KR20220152270A - Compositions and methods for inhibiting the expression of transthyretin (TTR) - Google Patents
Compositions and methods for inhibiting the expression of transthyretin (TTR) Download PDFInfo
- Publication number
- KR20220152270A KR20220152270A KR1020227034708A KR20227034708A KR20220152270A KR 20220152270 A KR20220152270 A KR 20220152270A KR 1020227034708 A KR1020227034708 A KR 1020227034708A KR 20227034708 A KR20227034708 A KR 20227034708A KR 20220152270 A KR20220152270 A KR 20220152270A
- Authority
- KR
- South Korea
- Prior art keywords
- ser
- glu
- leu
- rnai agent
- ttr
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/713—Double-stranded nucleic acids or oligonucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering nucleic acids [NA]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/321—2'-O-R Modification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/322—2'-R Modification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/344—Position-specific modifications, e.g. on every purine, at the 3'-end
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/352—Nature of the modification linked to the nucleic acid via a carbon atom
- C12N2310/3521—Methyl
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/353—Nature of the modification linked to the nucleic acid via an atom other than carbon
- C12N2310/3533—Halogen
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Saccharide Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
관련 출원related application
본 출원은 2020년 3월 6일자로 출원된 미국 가출원 제62/985,950호에 대한 우선권을 주장하며, 이의 전문은 본원에 참조로 인용된다.This application claims priority to U.S. Provisional Application No. 62/985,950, filed March 6, 2020, the entirety of which is incorporated herein by reference.
서열 목록sequence listing
본 출원은 ASCII 형식으로 전자적으로 제출된 서열 목록을 포함하고, 이는 그 전체가 참조로 인용된다. 2021년 2월 26일자로 생성된 상기 ASCII 복사본은 파일명이 121301_12320_SL.txt이며, 크기가 44,455 바이트이다. This application contains a sequence listing submitted electronically in ASCII format, which is incorporated by reference in its entirety. Said ASCII copy, created on February 26, 2021, has the file name 121301_12320_SL.txt and is 44,455 bytes in size.
트랜스티레틴 (TTR) (또한 전구알부민으로서 공지된)은 혈청 및 뇌척수액 (CSF) 중에서 발견된다. TTR은 레티놀-결합 단백질 (RBP) 및 티록신 (T4)을 수송하고 또한 혈액 및 CSF 중에서 RBP와의 연합을 통해 레티놀 (비타민 A)의 운반체로서 작용한다. 트랜스티레틴은 티록신 및 레티놀의 이의 수송 (transport of thyroxine and retinol)때문에 이름이 붙여졌다. TTR은 또한 프로테아제로서 기능하고, apoA-I (주요 HDL 아포지질단백질), 아밀로이드 β-펩타이드, 및 뉴로펩타이드 Y를 포함하는 단백질을 절단할 수 있다. 문헌(Liz, M.A. et al. (2010) IUBMB Life, 62(6):429-435)을 참조한다.Transthyretin (TTR) (also known as proalbumin) is found in serum and cerebrospinal fluid (CSF). TTR transports retinol-binding protein (RBP) and thyroxine (T4) and also acts as a carrier of retinol (vitamin A) through association with RBP in blood and CSF. Transthyretin is so named because of its transport of thyroxine and retinol. TTR also functions as a protease and can cleave proteins including apoA-I (the major HDL apolipoprotein), amyloid β-peptide, and neuropeptide Y. See Liz, MA et al. (2010) IUBMB Life , 62(6):429-435.
TTR은 베타 시트 구조가 풍부한 4개의 동일한 127개 아미노산 서브유닛(단량체)의 사량체이다. 각 단량체는 2개의 4가닥 베타 시트와 프롤레이트 타원체 모양을 갖는다. 역평행 베타 시트 상호작용은 단량체를 이량체에 연결한다. 각 단량체로부터의 짧은 루프는 주요 이량체-이량체 상호작용을 형성한다. 이들 2개 쌍의 루프는 이량체의 반대되는 볼록 베타 시트를 분리하여 내부 채널을 형성한다.TTR is a tetramer of four identical 127 amino acid subunits (monomers) enriched in beta sheet structures. Each monomer has the shape of a prolate ellipsoid with two four-stranded beta sheets. Antiparallel beta sheet interactions link monomers to dimers. A short loop from each monomer forms the main dimer-dimer interaction. These two pairs of loops separate the opposite convex beta sheets of the dimer to form an internal channel.
간은 TTR 발현의 주요 부위이다. 다른 중요한 발현 부위는 맥락총, 망막(특히 망막 색소 상피) 및 췌장을 포함한다.The liver is a major site of TTR expression. Other important sites of expression include the choroid plexus, the retina (particularly the retinal pigment epithelium) and the pancreas.
트랜스티레틴은 아밀로이드 원섬유 형성의 전구체 단백질인 적어도 27개의 독특한 유형의 단백질 중 하나이다. 문헌(Guan, J. et al. (Nov. 4, 2011) Current perspectives on cardiac amyloidosis, Am J Physiol Heart Circ Physiol, doi:10.1152/ajpheart.00815.2011)을 참조한다. 기관 및 조직에서 아밀로이드 원섬유의 세포외 침착은 아밀로이드증의 특징이다. 아밀로이드 원섬유는 잘못 폴딩된 단백질 응집체로 구성되고, 이는 전구체 단백질의 과잉 생산 또는 특정 돌연변이로 인해 발생할 수 있다. TTR의 아밀로이드 생성 가능성은 이의 광범위한 베타 시트 구조와 관련이 있을 수 있고; X선 결정학 연구는 특정 아밀로이드 생성 돌연변이가 단백질의 4량체 구조를 불안정하게 한다는 것을 지적한다. 예를 들어, 문헌(Saraiva M.J.M. (2002) Expert Reviews in Molecular Medicine, 4(12):1-11)을 참조한다.Transthyretin is one of at least 27 distinct types of proteins that are precursor proteins for the formation of amyloid fibrils. See Guan, J. et al . (Nov. 4, 2011) Current perspectives on cardiac amyloidosis, Am J Physiol Heart Circ Physiol , doi:10.1152/ajpheart.00815.2011. Extracellular deposition of amyloid fibrils in organs and tissues is a hallmark of amyloidosis. Amyloid fibrils are composed of misfolded protein aggregates, which can result from overproduction or specific mutations of the precursor protein. The amyloidogenic potential of TTR may be related to its extensive beta sheet structure; X-ray crystallography studies indicate that certain amyloidogenic mutations destabilize the protein's tetrameric structure. See, eg, Saraiva MJM (2002) Expert Reviews in Molecular Medicine , 4(12):1-11.
아밀로이드증은 아밀로이드 침착물을 특징으로 하는 아밀로이드 질환의 그룹에 대한 일반적인 용어이다. 아밀로이드 질환은 이들의 전구체 단백질을 기준으로 분류되고; 예를 들어 명칭은 아밀로이드 때문에 "A"로 시작하고 이어서 전구체 단백질, 예를 들어, 아밀로이드 생성 트랜스티레틴 (amloidogenic transthyretin)에 대한 ATTR이 뒤따른다. Ibid. Amyloidosis is a general term for a group of amyloid diseases characterized by amyloid deposits. Amyloid diseases are classified based on their precursor proteins; For example, the name starts with "A" for amyloid followed by an ATTR for a precursor protein, eg, amyloidogenic transthyretin . Ibid.
수많은 TTR 관련 질환이 있고, 이의 대부분은 아밀로이드 질환이다. 정상 서열 TTR은 노인의 심장 아밀로이드증과 관련이 있고, 노인성 전신 아밀로이드증(SSA)(노인성 심장 아밀로이드증(SCA) 또는 심장 아밀로이드증이라고도 함)이라고 호칭된다. SSA는 흔히 다른 많은 기관에 미세한 침착물을 동반한다. TTR 아밀로이드증은 다양한 형태로 나타난다. 말초 신경계가 더 두드러지게 영향을 받는 경우, 이 질환은 가족성 아밀로이드성 다발신경병증(FAP)으로 호칭된다. 심장이 주로 관련되지만 신경계가 관여하지 않는 경우, 이 질환은 가족성 아밀로이드성 심근병증(FAC)으로 호칭된다. TTR 아밀로이드증의 세 번째 주요 유형은 연수막 또는 수막뇌혈관 아밀로이드증, 중추신경계(CNS) 아밀로이드증 또는 아밀로이드증 VII 형태로도 공지된 연수막 아밀로이드증이다. TTR의 돌연변이는 또한 아밀로이드성 유리체 혼탁, 수근관 증후군 및 정상갑상선 고티록신혈증을 유발할 수 있고, 이는 티록신에 대한 친화성이 증가된 돌연변이 TTR 분자로 인해 티록신과 TTR의 증가된 연관성으로 인해 2차적인 것으로 사료되는 비-아밀로이드성 질환인 것으로 사료된다. 예를 들어, 문헌(Moses et al.(1982) J. Clin. Invest., 86, 2025-2033)을 참조한다.There are numerous TTR-related diseases, most of which are amyloid diseases. Normal sequence TTR is associated with cardiac amyloidosis in the elderly and is called senile systemic amyloidosis (SSA) (also called senile cardiac amyloidosis (SCA) or cardiac amyloidosis). SSA is often accompanied by microscopic deposits in many other organs. TTR amyloidosis presents in various forms. When the peripheral nervous system is more prominently affected, the disease is called familial amyloidogenic polyneuropathy (FAP). When the heart is primarily involved but the nervous system is not involved, the disease is called familial amyloidogenic cardiomyopathy (FAC). The third major type of TTR amyloidosis is leptomeningeal amyloidosis, also known as leptomeningeal or meningocerebrovascular amyloidosis, central nervous system (CNS) amyloidosis or form amyloidosis VII. Mutations in TTR can also cause amyloidotic vitreous opacity, carpal tunnel syndrome, and normothyroid hyperthyroxinemia, which have been shown to be secondary to increased association of TTR with thyroxine due to mutant TTR molecules with increased affinity for thyroxine. It is believed to be a non-amyloidic disease. See, eg, Moses et al . (1982) J. Clin. Invest. , 86, 2025-2033.
비정상적인 TTR 대립유전자는 유전되거나 체세포 돌연변이를 통해 획득될 수 있다. Guan, J. et al. (Nov. 4, 2011) Current perspectives on cardiac amyloidosis, Am J Physiol Heart Circ Physiol, doi:10.1152/ajpheart.00815.2011. 트랜스티레틴 연합된 ATTR은 가장 흔한 형태의 유전성 전신 아밀로이드증이다. Lobato, L. (2003) J. Nephrol., 16:438-442. TTR 돌연변이는 TTR 아밀로이드 형성 과정을 가속화하고 ATTR 발병에 대해 가장 중요한 위험 인자이다. 85개 초과의 아밀로이드 생성 TTR 변이체는 전신 가족성 아밀로이드증을 유발하는 것으로 공지되어 있다. 일부 돌연변이는 심근병증 또는 유리체 혼탁과 관련이 있지만, TTR 돌연변이는 일반적으로 말초 신경계의 특히 침범과 함께 전신 아밀로이드 침착물을 유발한다. Ibid. Abnormal TTR alleles may be inherited or acquired through somatic mutation. Guan, J. et al . (Nov. 4, 2011) Current perspectives on cardiac amyloidosis, Am J Physiol Heart Circ Physiol , doi:10.1152/ajpheart.00815.2011. Transthyretin-associated ATTR is the most common form of hereditary systemic amyloidosis. Lobato, L. (2003) J. Nephrol. , 16:438-442. TTR mutation accelerates the process of TTR amyloidogenesis and is the most important risk factor for the development of ATTR. More than 85 amyloidogenic TTR variants are known to cause systemic familial amyloidosis. While some mutations are associated with cardiomyopathy or vitreous opacity, TTR mutations generally cause systemic amyloid deposits with particular involvement of the peripheral nervous system. Ibid.
V30M 돌연변이는 가장 만연된 TTR 돌연변이다. 예를 들어, 문헌(Lobato, L. (2003) J Nephrol, 16:438-442)을 참조한다. V122I 돌연변이는 아프리카계 미국인 인구의 3.9%가 갖고 있고 FAC의 가장 흔한 원인이다. 문헌(Jacobson, D.R. et al. (1997) N. Engl. J. Med.336(7):466-73)을 참조한다. SSA는 80세 이상 인구의 25% 이상에 영향을 미치는 것으로 추정된다. 문헌(Westermark, P. et al. (1990) Proc. Natl. Acad. Sci. U.S.A.87 (7): 2843-5)을 참조한다.The V30M mutation is the most prevalent TTR mutation. See, eg, Lobato, L. (2003) J Nephrol , 16:438-442. The V122I mutation is carried by 3.9% of the African American population and is the most common cause of FAC. See Jacobson, DR et al. (1997) N. Engl. J. Med. 336(7):466-73. SSA is estimated to affect more than 25% of the population over the age of 80. See Westermark, P. et al. (1990) Proc. Natl. Acad. Sci. USA 87 (7): 2843-5.
따라서, TTR 관련 질환에 대한 효과적인 치료가 당업계에 필요하다.Thus, there is a need in the art for effective treatments for TTR-related diseases.
발명의 개요Summary of the Invention
본 발명은 TTR의 발현을 억제하기 위한 조성물 및 방법, 및 TTR 유전자를 표적화하는, 이중 가닥 RNAi 제제를 사용하여 사람 대상체에서 트랜스티레틴-(TTR-) 관련 질환을 치료 또는 예방하는 방법을 제공한다. The present invention provides compositions and methods for inhibiting expression of TTR, and methods for treating or preventing transthyretin- (TTR-) related diseases in human subjects using double-stranded RNAi agents targeting the TTR gene. .
본 발명은 센스 가닥 및 안티센스 가닥을 포함하는 이중 가닥 RNAi 제제를 제공하고, 여기서: 센스 가닥 및 안티센스 가닥 각각은 독립적으로 길이가 30개 이하의 뉴클레오타이드이고; 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고; 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)을 포함하고, 여기서, a, c, g, 및 u는 각각 2'-O-메틸아데노신-3’-포스페이트, 2'-O-메틸시티딘-3’-포스페이트, 2'-O-메틸구아노신-3’-포스페이트, 및 2'-O-메틸우리딘-3’-포스페이트이고; Af, Cf, Gf, 및 Uf는 각각 2’-플루오로아데노신-3’-포스페이트, 2’-플루오로시티딘-3’-포스페이트, 2’-플루오로구아노신-3’-포스페이트, 및 2’-플루오로우리딘-3’-포스페이트이고; (Tgn)은 티미딘-글리콜 핵산 (GNA) S-이성체이고; s는 포스포로티오에이트 링커이다.The present invention provides a double-stranded RNAi agent comprising a sense strand and an antisense strand, wherein: each of the sense strand and the antisense strand is independently 30 nucleotides or less in length; the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6); The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7), where a, c, g, and u are each 2'-O-methyladenosine-3'- phosphate, 2'-O-methylcytidine-3'-phosphate, 2'-O-methylguanosine-3'-phosphate, and 2'-O-methyluridine-3'-phosphate; Af, Cf, Gf, and Uf are 2'-fluoroadenosine-3'-phosphate, 2'-fluorocytidine-3'-phosphate, 2'-fluoroguanosine-3'-phosphate, and 2, respectively. '-fluorouridine-3'-phosphate; (Tgn) is the thymidine-glycol nucleic acid (GNA) S-isomer; s is a phosphorothioate linker.
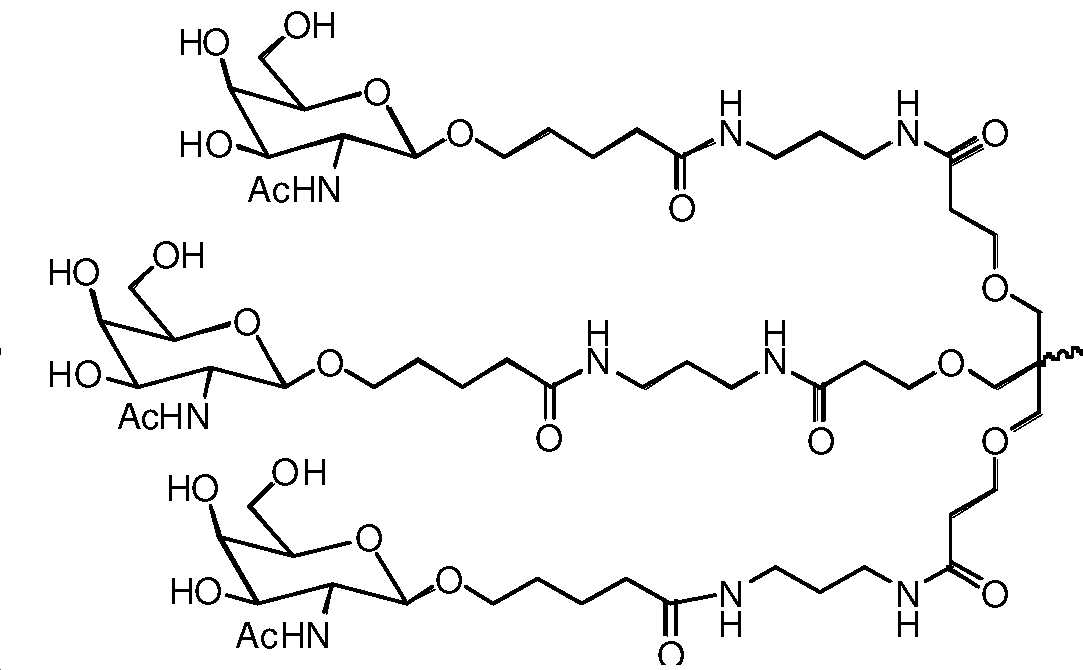
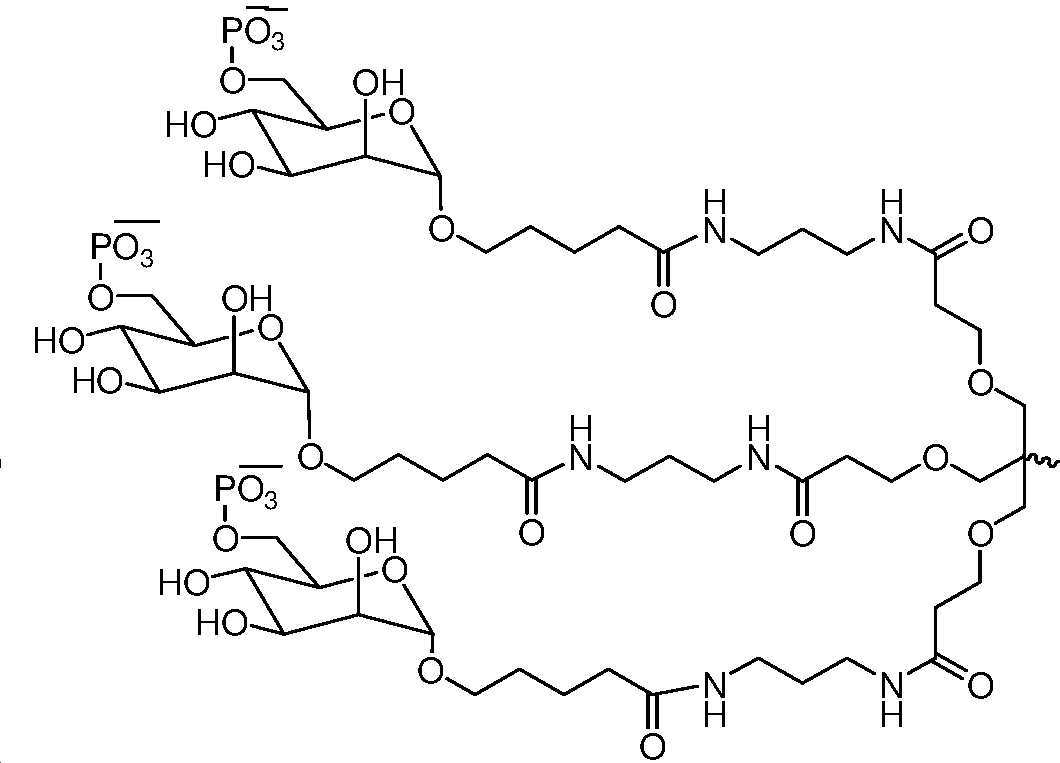
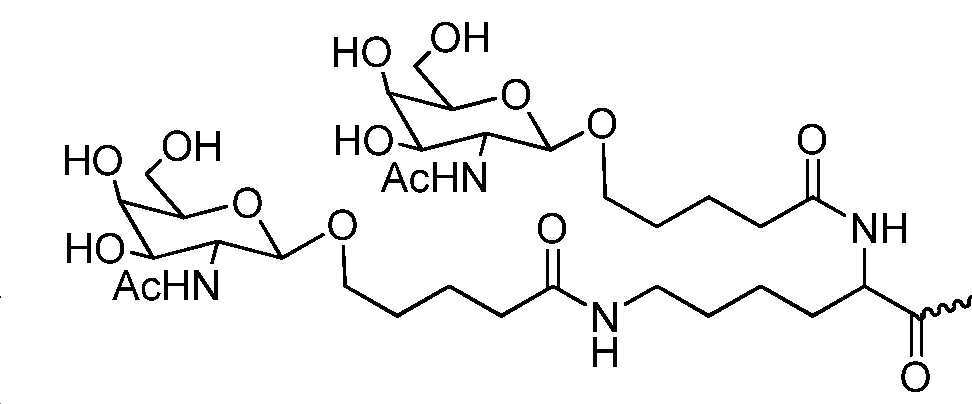
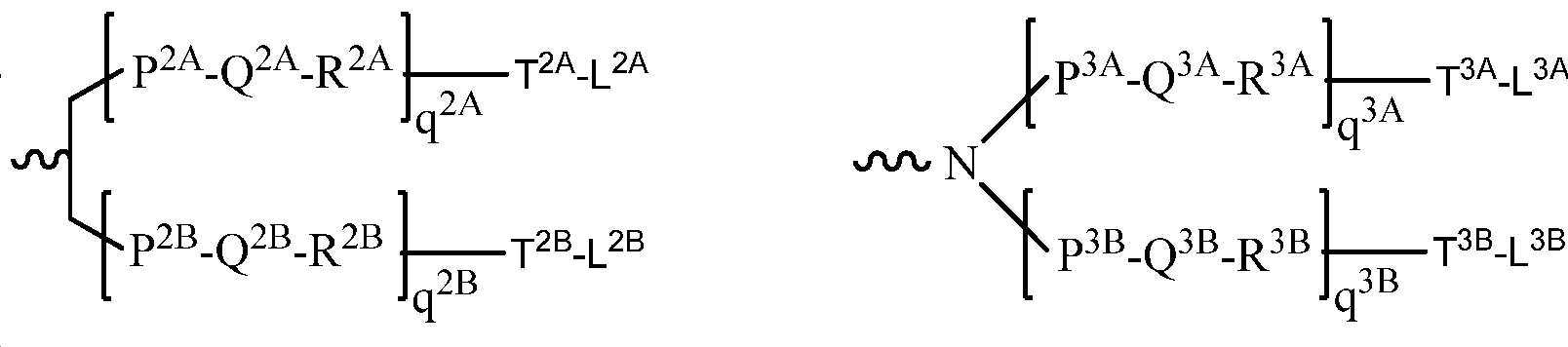
특정 구현예에서, 이중 가닥 RNAi제제의 센스 가닥은 적어도 하나의 리간드에 접합된다. 특정 구현예에서, 리간드는 2가 또는 3가 측쇄 링커를 통해 부착된 하나 이상의 GalNAc 유도체이다. 특정 구현예에서, 리간드는In certain embodiments, the sense strand of the double-stranded RNAi agent is conjugated to at least one ligand. In certain embodiments, the ligand is one or more GalNAc derivatives attached through a divalent or trivalent side chain linker. In certain embodiments, the ligand is
이다. to be.
특정 구현예에서, 리간드는 센스 가닥의 3' 말단에 부착된다.In certain embodiments, the ligand is attached to the 3' end of the sense strand.
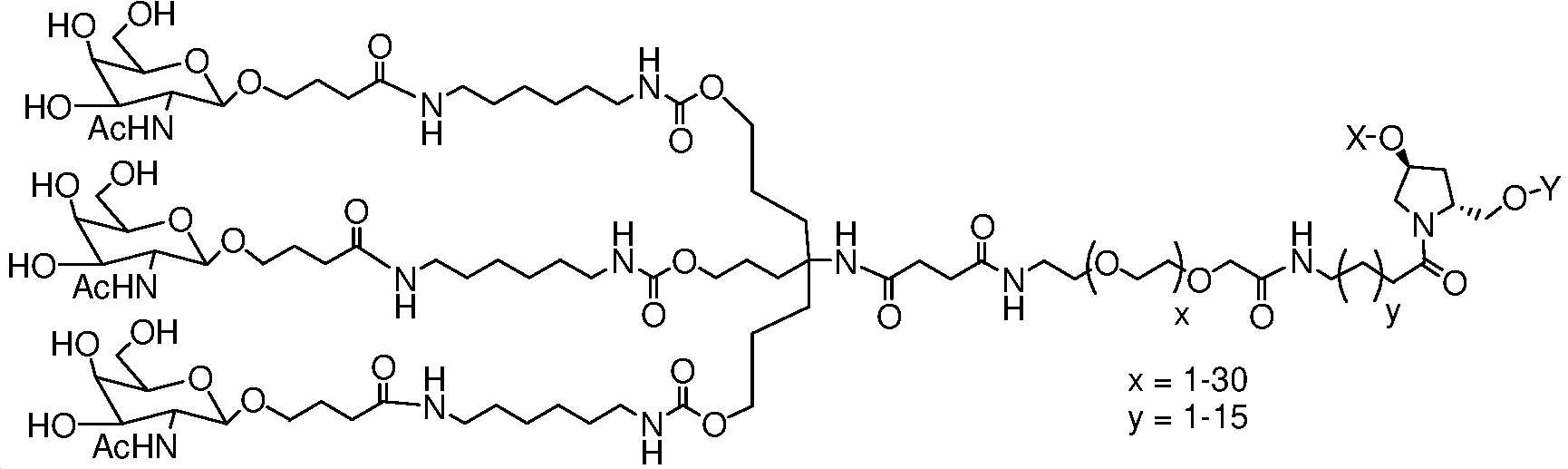
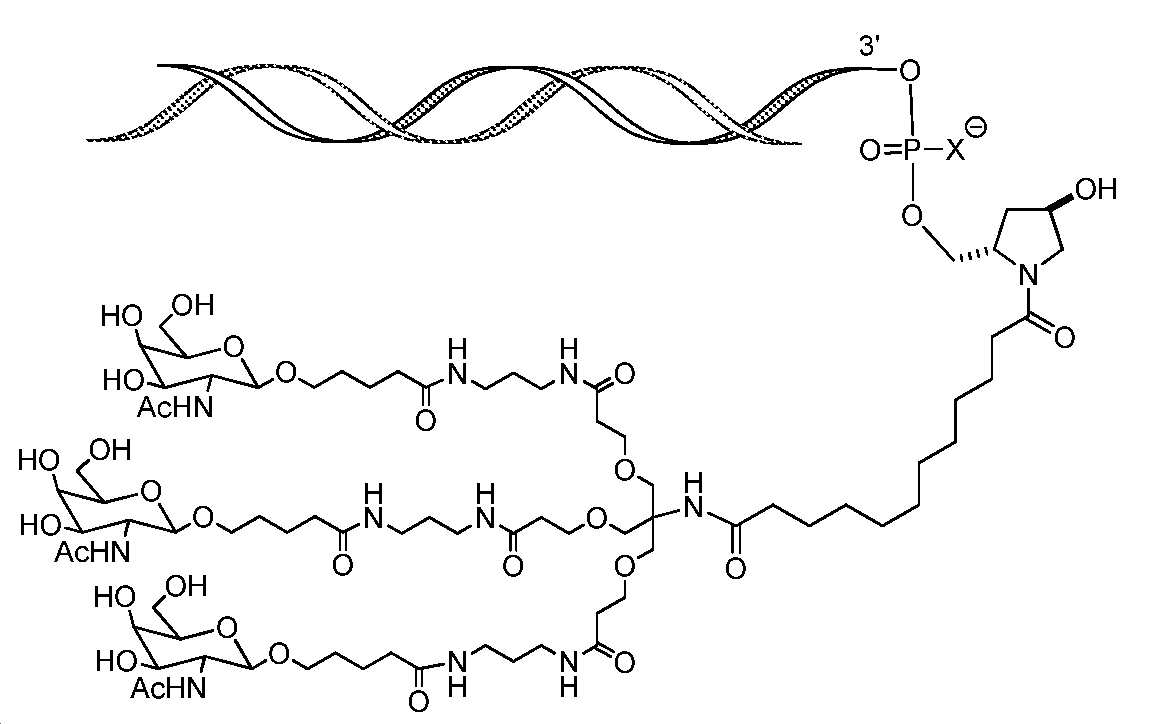
특정 구현예에서, 이중 가닥 RNAi 제제는 하기의 도식에 나타낸 바와 같이 리간드에 접합되고, In certain embodiments, the double-stranded RNAi agent is conjugated to a ligand as shown in the scheme below;
여기서, X는 O 또는 S이다. Here, X is O or S.
특정 구현예에서, 센스 가닥은 길이가 21개 뉴클레오타이드이고, 안티센스 가닥은 길이가 23개 뉴클레오타이드이다. In certain embodiments, the sense strand is 21 nucleotides in length and the antisense strand is 23 nucleotides in length.
본 발명은 이중 가닥 RNAi 제제의 약 25 mg 내지 약 1000 mg의 고정된 용량의 투여를 포함하는, TTR 관련 질환을 앓는 사람 대상체를 치료하는 방법에서 이중 가닥 RNAi 제제의 용도를 제공하고, 여기서, 센스 가닥 및 안티센스 가닥 각각은 독립적으로 길이가 30개 이하의 뉴클레오타이드이고; 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고; 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)을 포함하고, 여기서, a, c, g, 및 u는 각각 2'-O-메틸아데노신-3’-포스페이트, 2'-O-메틸시티딘-3’-포스페이트, 2'-O-메틸구아노신-3’-포스페이트, 및 2'-O-메틸우리딘-3’-포스페이트이고; Af, Cf, Gf, 및 Uf는 각각 2’-플루오로아데노신-3’-포스페이트, 2’-플루오로시티딘-3’-포스페이트, 2’-플루오로구아노신-3’-포스페이트, 및 2’-플루오로우리딘-3’-포스페이트이고; (Tgn)은 티미딘-글리콜 핵산 (GNA) S-이성체이고; s는 포스포로티오에이트 링커이다.The present invention provides the use of a double-stranded RNAi agent in a method of treating a human subject suffering from a TTR-associated disease comprising administration of a fixed dose of about 25 mg to about 1000 mg of the double-stranded RNAi agent, wherein the sense Each strand and antisense strand is independently 30 nucleotides or less in length; the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6); The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7), where a, c, g, and u are each 2'-O-methyladenosine-3'- phosphate, 2'-O-methylcytidine-3'-phosphate, 2'-O-methylguanosine-3'-phosphate, and 2'-O-methyluridine-3'-phosphate; Af, Cf, Gf, and Uf are 2'-fluoroadenosine-3'-phosphate, 2'-fluorocytidine-3'-phosphate, 2'-fluoroguanosine-3'-phosphate, and 2, respectively. '-fluorouridine-3'-phosphate; (Tgn) is the thymidine-glycol nucleic acid (GNA) S-isomer; s is a phosphorothioate linker.
본 발명은 또한 이중 가닥 RNAi 제제의 약 25 mg 내지 약 1000 mg의 고정된 용량의 투여를 포함하는, TTR 관련 질환의 진단학적 기준을 충족하지 않는 사람 대상체에서 TTR의 발현을 억제하는 방법에서 이중 가닥 RNAi 제제의 용도를 제공하고, 여기서, 센스 가닥 및 안티센스 가닥 각각은 독립적으로 길이가 30개 이하의 뉴클레오타이드이고; 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고; 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)을 포함하고, 여기서, a, c, g, 및 u는 각각 2'-O-메틸아데노신-3’-포스페이트, 2'-O-메틸시티딘-3’-포스페이트, 2'-O-메틸구아노신-3’-포스페이트, 및 2'-O-메틸우리딘-3’-포스페이트이고; Af, Cf, Gf, 및 Uf는 각각 2’-플루오로아데노신-3’-포스페이트, 2’-플루오로시티딘-3’-포스페이트, 2’-플루오로구아노신-3’-포스페이트, 및 2’-플루오로우리딘-3’-포스페이트이고; (Tgn)은 티미딘-글리콜 핵산 (GNA) S-이성체이고; s는 포스포로티오에이트 링커이다.The present invention also relates to a double-stranded method of inhibiting the expression of TTR in a human subject not meeting diagnostic criteria for a TTR-related disease comprising administration of a fixed dose of about 25 mg to about 1000 mg of a double-stranded RNAi agent. Provided is the use of an RNAi agent, wherein each of the sense strand and the antisense strand is independently 30 nucleotides or less in length; the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6); The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7), where a, c, g, and u are each 2'-O-methyladenosine-3'- phosphate, 2'-O-methylcytidine-3'-phosphate, 2'-O-methylguanosine-3'-phosphate, and 2'-O-methyluridine-3'-phosphate; Af, Cf, Gf, and Uf are 2'-fluoroadenosine-3'-phosphate, 2'-fluorocytidine-3'-phosphate, 2'-fluoroguanosine-3'-phosphate, and 2, respectively. '-fluorouridine-3'-phosphate; (Tgn) is the thymidine-glycol nucleic acid (GNA) S-isomer; s is a phosphorothioate linker.
특정 구현예에서, 이중 가닥 RNAi 제제의 센스 가닥은 적어도 하나의 리간드에 접합된다. 특정 구현예에서, 리간드는 2가 또는 3가 측쇄 링커를 통해 부착된 하나 이상의 GalNAc 유도체이다. 특정 구현예에서, 리간드는In certain embodiments, the sense strand of a double-stranded RNAi agent is conjugated to at least one ligand. In certain embodiments, the ligand is one or more GalNAc derivatives attached through a divalent or trivalent side chain linker. In certain embodiments, the ligand is
이다. to be.
특정 구현예에서, 리간드는 센스 가닥의 3' 말단에 부착된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 하기의 도식에 나타낸 바와 같이 리간드에 접합되고, In certain embodiments, the ligand is attached to the 3' end of the sense strand. In certain embodiments, the double-stranded RNAi agent is conjugated to a ligand as shown in the scheme below;
여기서, X는 O 또는 S이다. Here, X is O or S.
특정 구현예에서, 센스 가닥은 길이가 21개 뉴클레오타이드이고, 안티센스 가닥은 길이가 23개 뉴클레오타이드이다. In certain embodiments, the sense strand is 21 nucleotides in length and the antisense strand is 23 nucleotides in length.
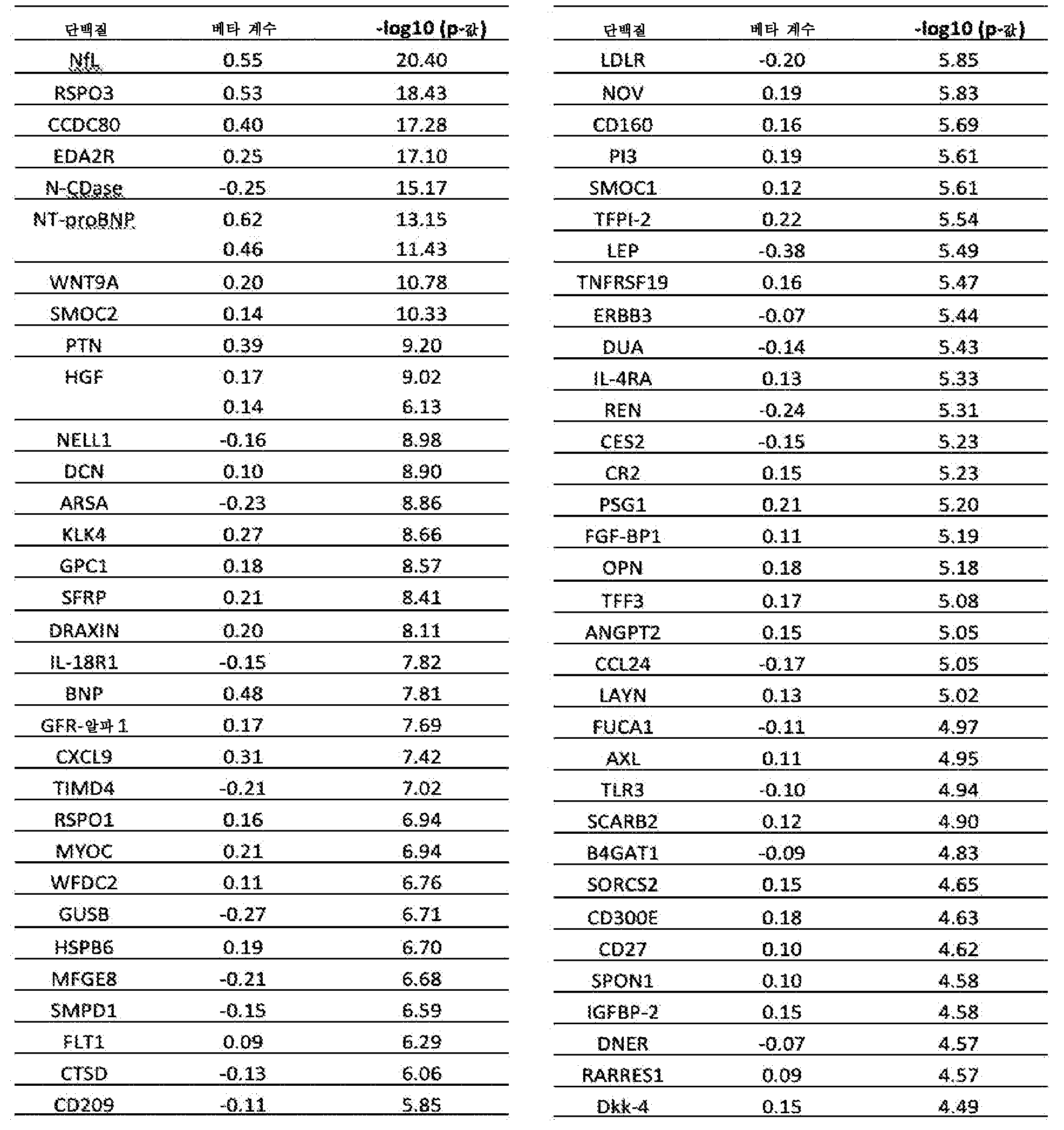
특정 구현예에서, 본 발명의 용도는 신경학적 손상, 삶의 질, 신경 손상, 심혈관 건강의 적어도 하나의 지표를 개선하는 것을 포함한다. 특정 구현예에서, 평가된 지표는 예를 들어 신경병증 손상(NIS) 스코어 또는 변형된 NIS(mNIS+7) 스코어를 사용하는 신경학적 손상이다. 특정 구현예에서, 지표는 예를 들어, SF-36®건강 조사 스코어, 노퍽(Norfolk) 삶의 질-당뇨병성 신경병증(Norfolk QOL-DN) 스코어, NIS-W 스코어, Rasch-구축된 전체 불구 스케일(R-ODS) 스코어, 복합 자율신경계 증상 스코어(COMPASS-31), 메디안 체질량 지수(mBMI) 스코어, 6분 걷기 시험(6MWT) 스코어 및 10미터 걷기 시험 스코어를 사용하여 평가된 삶의 질 지표이다. 특정 구현예에서, 지표는 평가된 신경 손상, 예를 들어 신경필라멘트 경쇄(NfL), RSPO3, CCDC80, EDA2R, NT-proBNP, 및 N-CDase 그룹으로부터 선택된 하나 이상의 단백질 수준의 변화, 예를 들어, 사람 혈액 샘플, 또는 그로부터 유래된 혈청 또는 혈장에서의 변화로 평가된 신경 손상이다. 특정 구현예에서, 신경 손상의 지표는 신경필라멘트 경쇄(NfL) 단백질 수준의 기준선으로부터의 변화이다. 특정 구현예에서, 심혈관 손상의 지표는 더 나은 건강 상태, 심장초음파 평가에 의한 평균 좌심실(LV) 벽 두께의 기준선으로부터의 변화, 심장초음파 평가에 의한 전체적인 종방향 긴장의 기준선으로부터의 변화, 및 N-말단 프로호르몬 B형 나트륨이뇨 펩타이드(NTproBNP)의 기준선으로부터의 변화를 나타내는 증가된 스코어와 함께 캔자스시티 심근병증 설문지 전체 요약(KCCQ-OS)을 사용한 심혈관 입원이다.In certain embodiments, uses of the present invention include improving at least one indicator of neurological impairment, quality of life, neurological impairment, or cardiovascular health. In certain embodiments, the assessed index is neurological impairment using, for example, a neuropathic impairment (NIS) score or a modified NIS (mNIS+7) score. In certain embodiments, the indicator is, for example, the SF-36® Health Survey score, the Norfolk Quality of Life-Diabetic Neuropathy (Norfolk QOL-DN) score, the NIS-W score, the Rasch-constructed total disability Quality of life indicators assessed using scale (R-ODS) score, composite autonomic symptom score (COMPASS-31), median body mass index (mBMI) score, 6-minute walk test (6MWT) score, and 10-meter walk test score to be. In certain embodiments, the indicator is an assessed neuronal injury, e.g., a change in the level of one or more proteins selected from the group of neurofilament light chain (NfL), RSPO3, CCDC80, EDA2R, NT-proBNP, and N-CDase, e.g., Neuronal damage assessed by changes in human blood samples, or serum or plasma derived therefrom. In certain embodiments, the indicator of nerve damage is a change from baseline in neurofilament light chain (NfL) protein levels. In certain embodiments, the indicator of cardiovascular damage is better health, change from baseline in mean left ventricular (LV) wall thickness by echocardiographic assessment, change from baseline in global longitudinal tension by echocardiographic assessment, and N Cardiovascular admissions using the Kansas City Cardiomyopathy Questionnaire Overall Summary (KCCQ-OS) with an increased score representing change from baseline in terminal prohormone type B natriuretic peptide (NTproBNP).
특정 구현예에서, 사람 대상체는 TTR 관련 질환, 예를 들어 노인성 전신성 아밀로이드증(SSA), 전신성 가족성 아밀로이드증, 가족성 아밀로이드성 다발신경병증(FAP), 연수막/중추 신경계(CNS) 아밀로이드증, 및 고티록신혈증의 발병과 관련된 TTR 유전자 돌연변이를 보유한다.In certain embodiments, the human subject has a TTR-related disease, eg, senile systemic amyloidosis (SSA), familial systemic amyloidosis, familial amyloidogenic polyneuropathy (FAP), leptomeningeal/central nervous system (CNS) amyloidosis, and hyperthyroxine. Carrying a TTR gene mutation associated with the development of hyperemia.
특정 구현예에서, 사람 대상체는 트랜스티레틴-매개 아밀로이드증(ATTR 아밀로이드증)을 갖고 이중 가닥 RNAi 제제의 사용은 사람 대상체에서 아밀로이드 TTR 침착물을 감소시킨다. 특정 구현예에서, ATTR 아밀로이드증은 유전성 ATTR(h-ATTR) 아밀로이드증이다. 특정 구현예에서, ATTR 아밀로이드증은 비-유전성 ATTR(wt ATTR) 아밀로이드증이다.In certain embodiments, the human subject has transthyretin-mediated amyloidosis (ATTR amyloidosis) and the use of a double-stranded RNAi agent reduces amyloid TTR deposits in the human subject. In certain embodiments, the ATTR amyloidosis is hereditary ATTR (h-ATTR) amyloidosis. In certain embodiments, the ATTR amyloidosis is non-hereditary ATTR (wt ATTR) amyloidosis.
특정 구현예에서, 이중 가닥 RNAi 제제는 피하 또는 정맥내로 사람 대상체에게 투여된다. 특정 구현예에서, 피하 투여는 자가 투여이다. 특정 구현예에서, 자가-투여는 사전 충전된 주사기 또는 자동-주사기 장치를 통한다.In certain embodiments, the double-stranded RNAi agent is administered subcutaneously or intravenously to a human subject. In certain embodiments, subcutaneous administration is self-administration. In certain embodiments, self-administration is via a pre-filled syringe or auto-injector device.
특정 구현예에서, 용도는 사람 혈액 샘플, 또는 이로부터 유래된 혈청 또는 혈장과 같은 사람 대상체로부터 유래된 샘플에서 TTR mRNA 발현 또는 TTR 단백질 발현의 수준을 평가하는 것을 추가로 포함한다.In certain embodiments, the use further comprises assessing the level of TTR mRNA expression or TTR protein expression in a sample derived from a human subject, such as a human blood sample, or serum or plasma derived therefrom.
특정 구현예에서, 이중 가닥 RNAi 제제는 매달 1회, 격월 1회, 3개월마다 1회, 4개월마다 1회, 5개월마다 1회, 또는 6개월마다 1회 사람 대상체에게 투여된다. 특정 구현예에서, 고정 용량의 이중 가닥 RNAi 제제는 사람 대상체에게 약 3개월마다 1회 투여된다. 특정 구현예에서, 고정 용량의 이중 가닥 RNAi 제제는 사람 대상체에게 약 6개월마다 1회 투여된다.In certain embodiments, the double-stranded RNAi agent is administered to a human subject once monthly, once every other month, once every 3 months, once every 4 months, once every 5 months, or once every 6 months. In certain embodiments, a fixed dose of a double-stranded RNAi agent is administered to a human subject about once every 3 months. In certain embodiments, a fixed dose of a double-stranded RNAi agent is administered to a human subject about once every 6 months.
특정 구현예에서, 이중 가닥 RNAi 제제는 사람 대상체에게 만성적으로 투여된다.In certain embodiments, the double-stranded RNAi agent is administered chronically to a human subject.
특정 구현예에서, 이중 가닥 RNAi 제제는 분기별 약 1회 내지 연간 약 1회로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 분기별 약 1회, 약 6개월마다 1회, 또는 연간 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject from about once per quarter to about once per year. In certain embodiments, the double-stranded RNAi agent is administered to a human subject about once per quarter, about once every 6 months, or about once per year.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 300 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 75 mg 내지 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 50 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 75 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 100 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 300 mg; 약 25 mg 내지 약 200 mg; 약 75 mg 내지 약 200 mg; 약 25 mg; 약 50 mg; 약 75 mg; 약 100 mg; 약 200mg; 또는 약 300 mg의 고정 용량으로 분기별 1회, 즉, 3개월 마다 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg to about 300 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg to about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 75 mg to about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 50 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 75 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 100 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is about 25 mg to about 300 mg; about 25 mg to about 200 mg; about 75 mg to about 200 mg; about 25 mg; about 50 mg; about 75 mg; about 100 mg; about 200 mg; or a fixed dose of about 300 mg is administered to a human subject once quarterly, ie, about once every 3 months.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 내지 약 600 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 또는 약 600 mg의 고정 용량으로 6개월 마다 약 1회,내지 연간 약 1회 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 또는 약 600 mg의 고정 용량으로 6개월마다 약 1회, 또는 연간 약 1회 사람 대상체에게 투여된다.In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg to about 600 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg or about 600 mg about once every 6 months, to about once a year. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg or about 600 mg about once every 6 months, or about once a year.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 700 mg 내지 약 1000 mg 또는 약 700 mg 내지 약 900 mg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 700 mg, 약 800 mg, 약 900 mg 또는 약 1000 mg의 고정된 용량으로 연간 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 700 mg to about 1000 mg or about 700 mg to about 900 mg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 700 mg, about 800 mg, about 900 mg, or about 1000 mg about once per year.
특정 구현예에서, 용도는 추가 치료학적 제제, 예를 들어, TTR 사량체 안정화제 또는 비스테로이드성 항염증제를 사람 대상체에게 투여하는 것을 추가로 포함한다.In certain embodiments, the use further comprises administering to the human subject an additional therapeutic agent, eg, a TTR tetramer stabilizer or a non-steroidal anti-inflammatory agent.
본 발명은 또한 본 발명의 임의의 방법을 수행하기 위한 키트를 제공한다. 키트는 이중 가닥 RNAi 제제; 및 사용 설명서를 포함하는 표지를 포함할 수 있다.The invention also provides kits for performing any of the methods of the invention. The kit includes a double-stranded RNAi agent; and a cover including instructions for use.
본 발명은 추가로 하기의 상세한 설명 및 도면에 의해 추가로 설명된다.The invention is further explained by the following detailed description and drawings.
도 1은 0일에 지적된 이중 가닥 RNAi 제제의 단일 1 mg/kg 용량을 투여한 후 V30M 유전자전이 마우스(그룹당 n=3)에서 상대적인 혈청 TTR 단백질 수준을 도시하는 그래프이다.
도 2는 0일에 지적된 이중 가닥 RNAi 제제의 단일 1 mg/kg 용량 또는 3 mg/kg 용량을 투여한 후 시노몰구스 몽키 (그룹당 n=3)에서 상대적인 혈청 TTR 단백질 수준을 도시하는 그래프이다. 결과는 3개의 독립적인 연구로부터 기원한다. Figure 1 is a graph depicting relative serum TTR protein levels in V30M transgenic mice (n=3 per group) after administration of a single 1 mg/kg dose of the indicated double-stranded RNAi preparations on day 0.
Figure 2 is a graph depicting relative serum TTR protein levels in cynomolgus monkeys (n=3 per group) after administration of a single 1 mg/kg dose or 3 mg/kg dose of the indicated double-stranded RNAi preparations on day 0. . Results originate from three independent studies.
본 발명은 트랜스티레틴-(TTR-) 관련 질환의 진단 기준을 충족하지 못하는 사람 대상체에서 TTR 발현을 억제함을 포함하는 TTR의 발현을 억제하는 방법, 및 TTR 유전자를 표적화하는 이중 가닥 RNAi 제제를 사용하여 트랜스티레틴-(TTR-) 관련 질환을 갖는 사람 대상체를 치료하는 방법을 제공하고, 여기서, 상기 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)을 포함하고; 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)을 포함한다. The present invention provides a method for inhibiting TTR expression, comprising inhibiting TTR expression in a human subject who does not meet criteria for diagnosis of a transthyretin- (TTR-) related disease, and a double-stranded RNAi agent targeting the TTR gene Provided is a method of treating a human subject having a transthyretin- (TTR-) related disease using the method, wherein the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6); The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7).
하기의 상세한 설명은 TTR 유전자의 발현을 선택적으로 억제하기 위한 RNAi 제제를 함유하는 조성물을 제조하고 사용하는 방법, 및 TTR 유전자의 발현의 억제 또는 감소가 이득이 되는 질환 및 장애를 갖는 대상체를 치료하기 위한 조성물, 용도 및 방법을 기재한다. The detailed description below describes methods of making and using compositions containing RNAi agents to selectively inhibit expression of the TTR gene, and methods for treating subjects having diseases and disorders that would benefit from inhibition or reduction of expression of the TTR gene. Compositions, uses and methods for
I. 정의I. Definition
본 발명이 보다 용이하게 이해될 수 있도록 하기 위해, 특정 용어를 먼저 정의한다. 또한, 파라미터의 값 또는 값의 범위가 인용될 때마다, 인용된 값의 중간 값 및 범위도 본 발명의 일부인 것으로 의도된다는 점에 유의해야 한다.In order that the present invention may be more readily understood, certain terms are first defined. Also, whenever a value or range of values for a parameter is recited, it should be noted that intermediate values and ranges of the recited values are also intended to be part of the invention.
단수형 관사 (“a” 및 “an”)는 본원에서 하나 또는 하나 이상 (즉, 적어도 하나)의 해당 관사의 문법적 대상을 지칭하는데 사용된다. 예를 들어, “요소”는 하나의 요소 또는 하나 초과의 요소, 예를 들어, 다수의 요소를 의미한다.The singular articles (“a” and “an”) are used herein to refer to one or more than one (ie, at least one) of the grammatical objects of that article. For example, “element” means one element or more than one element, eg, a plurality of elements.
용어 "포함하는"은 문구 “을 포함하지만 이에 제한되지 않는”을 의미하기 위해 본원에 사용되고 이와 상호교환적으로 사용된다.The term "comprising" is used herein to mean the phrase "including but not limited to" and is used interchangeably with it.
용어 "또는"은 달리 명백하게 지적되지 않는 경우, 용어 “및/또는”을 의미하기 위해 본원에 사용되고 이와 상호교환적으로 사용된다. The term “or” is used herein to mean the term “and/or” and is used interchangeably with it, unless expressly indicated otherwise.
용어 "약"은 당업계의 전형적인 관용성 범위 내, 예를 들어 용량 사이 시간에서 허용 가능한 변동, 투여 단위 양의 허용 가능한 변동을 의미하는 데 사용된다. 예를 들어, “약”은 평균으로부터 약 2 표준 편차 이내로서 이해될 수 있다. 특정 구현예에서, 약은 +10%를 의미한다. 특정 구현예에서, 약은 +5%를 의미한다. 약이 일련의 숫자 또는 범위 앞에 존재하는 경우, “약”은 일련의 또는 범위내 숫자 각각을 수식할 수 있는 것으로 이해된다. The term "about" is used to mean an acceptable variation in dosage unit amount, eg, an acceptable variation in the time between doses, within the normal tolerance range in the art. For example, “about” can be understood as within about 2 standard deviations from the mean. In certain embodiments, about means +10%. In certain embodiments, about means +5%. When about is preceded by a series of numbers or ranges, it is understood that “about” can modify each number in the series or range.
숫자 또는 일련의 숫자 앞의 "적어도", “이상”, 또는 “초과”라는 용어는 "적어도"라는 용어에 인접한 숫자와 문맥상 분명한 바와 같이 논리적으로 포함될 수 있는 모든 후속 숫자 또는 정수를 포함하는 것으로 이해된다. 예를 들어, 핵산 분자 내 뉴클레오타이드의 수는 정수이어야 한다. 예를 들어, “21개 뉴클레오타이드 핵산 분자의 적어도 18개 뉴클레오타이드”는 18, 19, 20, 또는 21개 뉴클레오타이드가 지적된 성질을 가짐을 의미한다. 적어도가 일련의 숫자 또는 범위 앞에 존재하는 경우, “적어도”는 일련의 또는 범위내 숫자 각각을 수식할 수 있는 것으로 이해된다. The terms "at least", "more than", or "more than" in front of a number or sequence of numbers are intended to include the number adjacent to the term "at least" and any subsequent number or whole number that may logically be included as is clear from the context. I understand. For example, the number of nucleotides in a nucleic acid molecule must be an integer. For example, “at least 18 nucleotides of a 21 nucleotide nucleic acid molecule” means that 18, 19, 20, or 21 nucleotides have the indicated property. Where at least precedes a series of numbers or ranges, it is understood that “at least” can modify each number in the series or range.
본원에 사용된 바와 같은 “이하” 또는 “미만”은 구문에 인접한 값으로 이해되고, 문맥상 논리적으로 0까지 논리적으로 낮은 값 또는 정수로서 이해된다. 예를 들어, “2개 이하의 뉴클레오타이드”의 오버행을 갖는 듀플렉스는 2, 1, 또는 0개의 뉴클레오타이드 오버행을 갖는다. “이하”가 일련의 숫자 또는 범위 앞에 존재하는 경우, “이하”는 일련의 또는 범위내 숫자 각각을 수식할 수 있는 것으로 이해된다.As used herein, "less than" or "less than" is understood to be a value adjacent to a phrase and, in context, as a logically low value or integer up to and including zero. For example, a duplex with an overhang of “less than 2 nucleotides” has an overhang of 2, 1, or 0 nucleotides. When "less than" is preceded by a series of numbers or ranges, it is understood that "less than" can modify each number in the series or range.
본원에 사용된 바와 같이, 검출 방법은 존재하는 분석물의 양이 상기 방법의 검출 수준 미만인 결정을 포함할 수 있다. As used herein, a detection method may include determining that the amount of an analyte present is below the detection level of the method.
본원에 사용된 바와 같은 “트랜스티레틴” (“TTR”)은 널리 공지된 유전자 및 단백질을 지칭한다. TTR은 또한 전구알부민, HsT2651, PALB, 및 TBPA로서 공지되어 있다. TTR은 레티놀 결합 단백질(RBP), 티록신(T4) 및 레티놀의 수송체로서 기능하고 이것은 또한 프로테아제로서 작용한다. 간은 TTR을 혈액으로 분비하고 맥락총은 TTR을 뇌척수액으로 분비한다. TTR은 또한 췌장 및 망막 색소 상피에서 발현된다. TTR의 가장 큰 임상적 관련성은 정상(야생형) 및 돌연변이 TTR 단백질 둘다가 아밀로이드 원섬유를 형성하여 세포외 침착물로 응집되어 아밀로이드증을 유발할 수 있다는 것이다. 예를 들어, 검토를 위해 문헌(Saraiva M.J.M. (2002) Expert Reviews in Molecular Medicine, 4(12):1-11)을 참조한다. 래트 트랜스티레틴의 분자 클로닝 및 뉴클레오타이드 서열, 및 mRNA 발현의 분포는 문헌(참조: Dickson, P.W. et al. (1985) J. Biol. Chem. 260(13)8214-8219)에 기재되어 있다. 사람 TTR의 X-선 결정 구조는 문헌(참조: Blake, C.C. et al. (1974) J Mol Biol 88, 1-12)에 기재되어 있다. 사람 TTR mRNA 전사체의 서열은 센터(National Center for Biotechnology Information (NCBI) RefSeq 승인 번호 NM_000371 (예를 들어, 서열번호 1 및 5)에서 찾을 수 있다. 마우스 TTR mRNA의 서열은 RefSeq 승인 번호 Nm_013697.2에서 찾을 수 있고, 래트 TTR mRNA의 서열은 RefSeq 승인 번호 Nm_012681.1에서 찾을 수 있다. TTR mRNA 서열의 추가의 예는 대중에게 가용한 데이터베이스, 예를 들어, GenBank, UniProt, 및 OMIM을 사용하여 용이하게 가용하다. “Transthyretin” (“TTR”) as used herein refers to well-known genes and proteins. TTR is also known as proalbumin, HsT2651, PALB, and TBPA. TTR functions as a transporter for retinol binding protein (RBP), thyroxine (T4) and retinol and it also acts as a protease. The liver secretes TTR into the blood and the choroid plexus secretes TTR into the cerebrospinal fluid. TTR is also expressed in the pancreas and retinal pigment epithelium. The greatest clinical relevance of TTR is that both normal (wild-type) and mutant TTR proteins can form amyloid fibrils that aggregate into extracellular deposits and cause amyloidosis. See, eg, Saraiva MJM (2002) Expert Reviews in Molecular Medicine , 4(12):1-11 for a review. The molecular cloning and distribution of nucleotide sequence and mRNA expression of rat transthyretin is described by Dickson, PW et al. (1985) J. Biol. Chem. 260(13)8214-8219. The X-ray crystal structure of human TTR has been described by Blake, CC et al. (1974) J Mol Biol 88 , 1-12. The sequence of the human TTR mRNA transcript can be found at the National Center for Biotechnology Information (NCBI) RefSeq Accession No. NM_000371 (eg , SEQ ID NOs: 1 and 5). The sequence of the mouse TTR mRNA is RefSeq Accession No. Nm_013697.2 and the sequence of rat TTR mRNA can be found under RefSeq Accession No. Nm_012681.1 Additional examples of TTR mRNA sequences are readily available using publicly available databases such as GenBank, UniProt, and OMIM. reasonably available
본원에 사용된 바와 같은 “TTR 관련 질환”은 TTR 유전자 또는 단백질과 관련된 임의의 질환을 포함하는 것으로 의도된다. 이러한 질환은 예를 들어 TTR 단백질의 과잉 생산, TTR 유전자 돌연변이, TTR 단백질의 비정상적인 절단, TTR 사량체의 불안정성, TTR과 다른 단백질 또는 기타 내인성 또는 외인성 물질 간의 비정상적인 상호작용에 의해 유발될 수 있다. "TTR 관련 질환"은 TTR이 비정상적인 세포외 응집체 또는 아밀로이드 침착물의 형성에 역할을 하는 임의의 유형의 트랜스티레틴 매개 아밀로이드증(ATTR 아밀로이드증), 예를 들어 유전성 ATTR(h-ATTR) 아밀로이드증 또는 비-유전성 ATTR(ATTR) 아밀로이드증을 포함한다. TTR 관련 질환은 노인성 전신성 아밀로이드증(SSA), 전신성 가족성 아밀로이드증, 가족성 아밀로이드성 다발신경병증(FAP), 가족성 아밀로이드성 심근병증(FAC), 연수막/중추신경계(CNS) 아밀로이드증, 아밀로이드성 유리체 혼탁, 수근관 증후군 및 고티록신혈증을 포함한다. TTR 아밀로이드증의 증상은 감각 신경병증(예를 들어, 감각 이상, 말단 사지의 감각 감퇴), 자율 신경병증(예를 들어, 위궤양 또는 기립성 저혈압과 같은 위장 기능부전), 운동 신경병증, 발작, 치매, 골수병증, 다발신경병증, 수근관 증후군, 자율신경 부전, 심근병증, 유리체 혼탁, 신부전, 신장병증, 실질적으로 감소된 mBMI(변형된 체질량 지수), 뇌신경 기능부전 및 각막 격자 이영양증을 포함한다.As used herein, "TTR-related disease" is intended to include any disease associated with the TTR gene or protein. These disorders can be caused, for example, by overproduction of the TTR protein, mutations in the TTR gene, abnormal cleavage of the TTR protein, instability of the TTR tetramer, or abnormal interactions between TTR and other proteins or other endogenous or exogenous substances. "TTR-related disease" means any type of transthyretin-mediated amyloidosis in which TTR plays a role in the formation of abnormal extracellular aggregates or amyloid deposits (ATTR amyloidosis), including hereditary ATTR (h-ATTR) amyloidosis or non-hereditary ATTR amyloidosis. ATTR (ATTR) amyloidosis. TTR-related diseases include senile systemic amyloidosis (SSA), systemic familial amyloidosis, familial amyloidogenic polyneuropathy (FAP), familial amyloidogenic cardiomyopathy (FAC), leptomeningeal/central nervous system (CNS) amyloidosis, and amyloidotic vitreous opacity. , carpal tunnel syndrome and hyperthyroxinemia. Symptoms of TTR amyloidosis include sensory neuropathy (e.g., paresthesia, decreased sensation in the extremities), autonomic neuropathy (e.g., gastrointestinal dysfunction such as gastric ulcer or orthostatic hypotension), motor neuropathy, seizures, and dementia. , myelopathy, polyneuropathy, carpal tunnel syndrome, autonomic dysfunction, cardiomyopathy, vitreous opacity, renal failure, nephropathy, substantially reduced mBMI (modified body mass index), cranial nerve dysfunction, and corneal lattice dystrophy.
본원에 사용된 용어 "서열을 포함하는 가닥"은 표준 뉴클레오타이드 명명법을 사용하여 언급된 서열에 의해 기재된 뉴클레오타이드 쇄를 포함하는 올리고뉴클레오타이드를 지칭한다.As used herein, the term “strand comprising a sequence” refers to an oligonucleotide comprising a nucleotide chain described by a stated sequence using standard nucleotide nomenclature.
본원에서 상호교환적으로 사용되는 "iRNA", "RNAi 제제", "iRNA 제제", "RNA 간섭 제제"라는 용어는 본원에 정의된 바와 같은 RNA를 함유하고 RNA 유도된 사일런싱 복합체(RISC) 경로를 통한 RNA 전사체의 표적화된 절단을 매개하는 제제를 지칭한다. iRNA는 RNA 간섭 (RNAi)으로서 공지된 공정을 통해 mRNA의 서열 특이적 분해를 지시한다. iRNA는 예를 들어, 세포에서, 예를 들어, 포유동물 대상체와 같은 대상체 내 세포에서 TTR 유전자의 발현을 조절, 예를 들어, 억제한다.The terms "iRNA," "RNAi agent," "iRNA agent," "RNA interference agent," as used interchangeably herein, refer to an RNA-induced silencing complex (RISC) pathway that contains RNA as defined herein and refers to agents that mediate targeted cleavage of RNA transcripts via iRNAs direct sequence-specific degradation of mRNA through a process known as RNA interference (RNAi). An iRNA regulates, eg, inhibits, the expression of a TTR gene in a cell, eg, in a cell in a subject, such as a mammalian subject.
본원에 사용된 바와 같은, 본 발명의 조성물, 용도 및 방법에 사용하기 위한 "iRNA"는 이중 가닥 RNA이고 본원에서 "이중 가닥 RNA 제제", "이중 가닥 RNA(dsRNA) 분자", "dsRNA 제제" 또는 "dsRNA"로서 지칭된다. 용어 "dsRNA"는 표적 RNA, 즉, TTR 유전자에 대해 "센스" 및 "안티센스" 배향을 갖는 것으로 지칭되는 2개의 역평행 및 실질적으로 상보적인 핵산 가닥을 포함하는 듀플렉스 구조를 갖는 리보핵산 분자의 복합체를 지칭한다. 이중 가닥 RNAi 제제는 본원에서 RNA 간섭 또는 RNAi로 지칭되는 전사후 유전자 사일런싱 기전을 통해 표적 RNA, 예를 들어 mRNA의 분해를 촉발한다.As used herein, "iRNA" for use in the compositions, uses and methods of the present invention is a double-stranded RNA and is herein referred to as a "double-stranded RNA preparation", "double-stranded RNA (dsRNA) molecule", "dsRNA preparation" or "dsRNA". The term "dsRNA" refers to a target RNA, i.e., a complex of ribonucleic acid molecules having a duplex structure comprising two anti-parallel and substantially complementary nucleic acid strands, referred to as having a "sense" and "antisense" orientation relative to the TTR gene. refers to Double-stranded RNAi agents trigger degradation of a target RNA, eg mRNA, through a post-transcriptional gene silencing mechanism referred to herein as RNA interference or RNAi.
본원에 사용된 용어 "변형된 뉴클레오타이드"는 독립적으로 변형된 당 모이어티, 변형된 뉴클레오타이드 간 연결, 또는 변형된 뉴클레오염기를 갖는 뉴클레오타이드를 지칭한다. 따라서, 용어 변형된 뉴클레오타이드는 뉴클레오사이드 간 연결, 당 모이어티 또는 뉴클레오염기에 대한 예를 들어 기능성 그룹 또는 원자의 치환, 추가 또는 제거를 포함한다. 본 발명의 제제에 사용하기에 적합한 변형은 본원에 기재되거나 당업계에 공지된 모든 유형의 변형을 포함한다. siRNA 유형의 분자에 사용된 바와 같은 임의의 상기 변형은 본원 명세서 및 청구범위의 목적을 위해 “RNAi 제제”에 의해 포괄된다.As used herein, the term "modified nucleotide" independently refers to a nucleotide having a modified sugar moiety, modified internucleotide linkage, or modified nucleotide group. Thus, the term modified nucleotide includes substitution, addition or removal of, for example, functional groups or atoms to internucleoside linkages, sugar moieties or nucleobases. Modifications suitable for use in the formulations of the present invention include all types of modifications described herein or known in the art. Any of the above modifications, as used in siRNA type molecules, are encompassed by "RNAi agents" for purposes of this specification and claims.
듀플렉스 영역은 RISC 경로를 통해 목적하는 표적 RNA의 특이적 분해를 허용하는 임의의 길이일 수 있고, 길이는 약 21 내지 36개 염기쌍, 예를 들어 약 21-30개 염기쌍, 예를 들어 약 21-30, 21-29, 21-28, 21-27, 21-26, 21-25, 21-24, 21-23, 또는 21-22개 염기쌍 길이의 범위일 수 있다. 하나의 구현예에서, 본 발명의 RNAi 제제는 dsRNA 제제이고, 이의 각각의 가닥은 21-23개 뉴클레오타이드를 포함하고, 이는 TTR mRNA 서열과 상호작용하여 표적 mRNA의 절단을 지시한다. 이론에 얽매이고자 하는 것 없이 세포 내로 도입된 긴 이중 가닥 RNA는 다이서(Dicer)로 공지된 III형 엔도뉴클레아제에 의해 siRNA로 분해된다(문헌참조: Sharp et al.(2001) Genes Dev.15:485).리보뉴클레아제 III형 효소인 다이서는 dsRNA를 특징적인 2개의 염기 3’ 오버행을 갖는 19-23개 염기쌍의 짧은 간섭 RNA로 가공한다(문헌참조: Bernstein, et al.,(2001) Nature 409:363).이어서 siRNA는 하나 이상의 헬리카제가 siRNA 듀플렉스를 푸는 RNA 유도된 사일런싱 복합체(RISC)에 통합되어 상보적 안티센스 가닥이 표적 인지를 안내할 수 있게 한다(문헌참조: Nykanen, et al.,(2001) Cell 107:309). 적절한 표적 mRNA에 결합하면 RISC 내의 하나 이상의 엔도뉴클레아제는 표적을 절단하여 사일런싱을 유도한다(문헌참조: Elbashir, et al.,(2001) Genes Dev.15:188). 하나의 구현예에서, 본 발명의 RNAi 제제는 24-30개 뉴클레오타이드의 dsRNA이고 이는 TTR mRNA 서열과 상호작용하여 표적 RNA의 절단을 지시한다. The duplex region can be of any length that allows specific degradation of the target RNA of interest via the RISC pathway, and is about 21 to 36 base pairs in length, such as about 21-30 base pairs, such as about 21-36 base pairs in length. 30, 21-29, 21-28, 21-27, 21-26, 21-25, 21-24, 21-23, or 21-22 base pairs in length. In one embodiment, the RNAi agent of the invention is a dsRNA agent, each strand of which comprises 21-23 nucleotides, which interacts with the TTR mRNA sequence to direct cleavage of the target mRNA. Without wishing to be bound by theory, long double-stranded RNA introduced into cells is digested into siRNA by a type III endonuclease known as Dicer (Sharp et al . (2001) Genes Dev . 15:485). Dicer, a type III ribonuclease enzyme, processes dsRNA into short interfering RNAs of 19-23 base pairs with a characteristic two base 3' overhang (Bernstein, et al . ,( 2001) Nature 409:363). The siRNA is then incorporated into an RNA-induced silencing complex (RISC) in which one or more helicases unwind the siRNA duplex, allowing the complementary antisense strand to guide target recognition (Nykanen , et al . , (2001) Cell 107:309). Upon binding to the appropriate target mRNA, one or more endonucleases within RISC cleave the target, leading to silencing (Elbashir, et al . , (2001) Genes Dev . 15:188). In one embodiment, the RNAi agent of the invention is a dsRNA of 24-30 nucleotides, which interacts with the TTR mRNA sequence to direct cleavage of the target RNA.
본원에 사용된 용어 "뉴클레오타이드 오버행"은 iRNA의 듀플렉스 구조, 예를 들어, dsRNA로부터 돌출된 적어도 하나의 쌍을 형성하지 않은 뉴클레오타이드를 지칭한다. 예를 들어, dsRNA의 한 가닥의 3'-말단이 다른 가닥의 5'-말단을 넘어 확장되거나 그 반대의 경우 뉴클레오타이드 오버행이 있다. dsRNA는 적어도 하나의 뉴클레오타이드의 오버행을 포함할 수 있고; 대안적으로 오버행은 적어도 2개의 뉴클레오타이드, 적어도 3개의 뉴클레오타이드, 적어도 4개의 뉴클레오타이드, 적어도 5개의 뉴클레오타이드 또는 그 이상을 포함할 수 있다. 뉴클레오타이드 오버행은 데옥시뉴클레오타이드/뉴클레오사이드를 포함하는 뉴클레오타이드/뉴클레오사이드 유사체를 포함하거나 이로 이루어질 수 있다. 오버행(들)은 센스 가닥, 안티센스 가닥, 또는 이들의 임의의 조합 상에 있을 수 있다. 또한, 오버행의 뉴클레오타이드(들)는 dsRNA의 안티센스 또는 센스 가닥의 5'-말단, 3'-말단 또는 양쪽 말단 상에 존재할 수 있다. dsRNA의 하나의 구현예에서, 적어도 하나의 가닥은 적어도 1개 뉴클레오타이드의 3’ 오버행을 포함한다. 또 다른 구현예에서, 적어도 하나의 가닥은 적어도 2개의 뉴클레오타이드, 예를 들어, 2, 3, 4, 5, 6, 7, 8 또는 9개 뉴클레오타이드의 3’ 오버행을 포함한다. 다른 구현예에서, RNAi 제제의 적어도 하나의 가닥은 적어도 1개 뉴클레오타이드의 5’ 오버행을 포함한다. 특정 구현예에서, 적어도 하나의 가닥은 적어도 2개 뉴클레오타이드, 예를 들어, 2, 3, 4, 5, 6, 7, 8 또는 9개 뉴클레오타이드의 5’ 오버행을 포함한다. 여전히 다른 구현예에서, RNAi 제제의 하나의 가닥의 3’ 및 5’ 말단 둘다는 적어도 1개 뉴클레오타이드의 오버행을 포함한다.As used herein, the term “nucleotide overhang” refers to at least one unpaired nucleotide protruding from a duplex structure of an iRNA, eg, a dsRNA. For example, there is a nucleotide overhang when the 3'-end of one strand of a dsRNA extends beyond the 5'-end of the other strand or vice versa. A dsRNA may contain an overhang of at least one nucleotide; Alternatively, the overhang may comprise at least 2 nucleotides, at least 3 nucleotides, at least 4 nucleotides, at least 5 nucleotides or more. Nucleotide overhangs may comprise or consist of nucleotide/nucleoside analogs, including deoxynucleotides/nucleosides. The overhang(s) may be on the sense strand, the antisense strand, or any combination thereof. In addition, the nucleotide(s) of the overhang may be present on the 5'-end, 3'-end or both ends of the antisense or sense strand of the dsRNA. In one embodiment of the dsRNA, at least one strand comprises a 3' overhang of at least 1 nucleotide. In another embodiment, at least one strand comprises a 3' overhang of at least 2 nucleotides, eg, 2, 3, 4, 5, 6, 7, 8 or 9 nucleotides. In another embodiment, at least one strand of the RNAi agent comprises a 5' overhang of at least 1 nucleotide. In certain embodiments, at least one strand comprises a 5' overhang of at least 2 nucleotides, e.g., 2, 3, 4, 5, 6, 7, 8 or 9 nucleotides. In yet another embodiment, both the 3' and 5' ends of one strand of the RNAi agent comprise an overhang of at least 1 nucleotide.
하나의 구현예에서, dsRNA의 안티센스 가닥은 3’-말단 또는 5’-말단에 1-9개 뉴클레오타이드, 예를 들어, 0-3, 1-3, 2-4, 2-5, 4-9, 5-9개, 예를 들어, 1, 2, 3, 4, 5, 6, 7, 8 또는 9개 뉴클레오타이드 오버행을 갖는다. 하나의 구현예에서, dsRNA의 센스 가닥은 3’-말단 또는 5’-말단에 1-9개 뉴클레오타이드, 예를 들어, 1, 2, 3, 4, 5, 6, 7, 8 또는 9개 뉴클레오타이드를 갖는다. 또 다른 구현예에서, 상기 오버행에서 하나 이상의 뉴클레오타이드는 뉴클레오사이드 티오포스페이트로 대체된다.In one embodiment, the antisense strand of the dsRNA is 1-9 nucleotides at the 3'-end or 5'-end, e.g., 0-3, 1-3, 2-4, 2-5, 4-9 , 5-9, eg, 1, 2, 3, 4, 5, 6, 7, 8 or 9 nucleotide overhangs. In one embodiment, the sense strand of the dsRNA is 1-9 nucleotides at the 3'-end or 5'-end, e.g. , 1, 2, 3, 4, 5, 6, 7, 8 or 9 nucleotides have In another embodiment, one or more nucleotides in the overhang are replaced with the nucleoside thiophosphate.
“평활(blunt)" 또는 "평활 말단(blunt end)"은 이중 가닥 RNAi 제제의 말단에 쌍을 형성하지 않는 뉴클레오타이드가 없고, 즉 뉴클레오타이드 오버행이 없음을 의미한다. “평활 말단화된” RNAi 제제는 이의 전체 길이 상에서 이중 가닥이고, 즉 분자의 어느 한 말단에서도 뉴클레오타이드 오버행이 없는 dsRNA이다. 본 발명의 RNAi 제제는 한 말단에 뉴클레오타이드 오버행을 갖는 RNAi 제제(즉, 하나의 오버행 및 하나의 평활 말단을 갖는 제제) 또는 양 말단에 뉴클레오타이드 오버행을 갖는 RNAi 제제를 포함한다. "blunt" or "blunt ends" means that there are no unpaired nucleotides at the ends of the double-stranded RNAi preparation, i.e. there are no nucleotide overhangs. A "blunt ended" RNAi preparation is It is a dsRNA that is double-stranded over its entire length, that is, there is no nucleotide overhang at either end of the molecule.The RNAi preparation of the present invention has a nucleotide overhang at one end (i.e., has one overhang and one blunt end). preparations) or RNAi preparations with nucleotide overhangs at both ends.
용어 "안티센스 가닥" 또는 "가이드 가닥"은 표적 서열, 예를 들어, TTR mRNA에 실질적으로 상보적인 영역을 포함하는 iRNA, 예를 들어, dsRNA의 가닥을 지칭한다. 본원에 사용된 용어 "상보성 영역"은 본원에 정의된 바와 같은 서열, 예를 들어 표적 서열, 예를 들어, TTR 뉴클레오타이드 서열에 실질적으로 상보적인 안티센스 가닥 상의 영역을 지칭한다. 상보성 영역이 표적 서열에 완전히 상보적이지 않은 경우, 미스매치는 분자의 내부 또는 말단 영역에 있을 수 있다. 일반적으로 가장 허용되는 미스매치는 말단 영역, 예를 들어 iRNA의 5'- 또는 3'-말단의 5, 4, 3, 2 또는 1개 뉴클레오타이드 내에 있다. 하나의 구현예에서, 본 발명의 이중 가닥 RNAi 제제는 안티센스 가닥 내에 뉴클레오타이드 미스매치를 포함한다. 또 다른 구현예에서, 본 발명의 이중 가닥 RNAi 제제는 센스 가닥 내에 뉴클레오타이드 미스매치를 포함한다. 하나의 구현예에서, 뉴클레오타이드 미스매치는 예를 들어 iRNA의 3'-말단으로부터 5, 4, 3, 2 또는 1개의 뉴클레오타이드 내에 있다. 또 다른 구현예에서, 뉴클레오타이드 미스매치는 예를 들어, iRNA의 3’-말단 뉴클레오타이드 내에 있다. The term “antisense strand” or “guide strand” refers to the strand of an iRNA, eg, a dsRNA, that includes a region substantially complementary to a target sequence, eg, TTR mRNA. As used herein, the term “region of complementarity” refers to the region on the antisense strand that is substantially complementary to a sequence as defined herein, eg, a target sequence, eg, a TTR nucleotide sequence. If the region of complementarity is not completely complementary to the target sequence, the mismatch may be in an internal or terminal region of the molecule. Generally, the most permissible mismatches are within 5, 4, 3, 2 or 1 nucleotides of the terminal region, eg the 5'- or 3'-end of the iRNA. In one embodiment, the double-stranded RNAi agent of the invention comprises a nucleotide mismatch within the antisense strand. In another embodiment, the double-stranded RNAi agent of the invention comprises a nucleotide mismatch in the sense strand. In one embodiment, the nucleotide mismatch is eg within 5, 4, 3, 2 or 1 nucleotides from the 3'-end of the iRNA. In another embodiment, the nucleotide mismatch is within, for example, the 3'-terminal nucleotide of the iRNA.
본원에 사용된 용어 "센스 가닥" 또는 "패신저 가닥"은 용어가 본원에 정의된 바와 같은 안티센스 가닥의 영역에 실질적으로 상보적인 영역을 포함하는 iRNA의 가닥을 지칭한다.As used herein, the term "sense strand" or "passenger strand" refers to the strand of an iRNA comprising a region substantially complementary to a region of the antisense strand, as the terms are defined herein.
본원에 사용된 바와 같이, 용어 "절단 영역"은 절단 부위에 바로 인접하여 위치하는 영역을 지칭한다. 절단 부위는 절단이 일어나는 표적 상의 부위이다. 일부 구현예에서, 절단 영역은 절단 부위의 어느 하나의 말단 상에 및 이에 바로 인접하여 3개의 염기를 포함한다. 일부 구현예에서, 절단 영역은 절단 부위의 어느 하나의 말단 상에 및 이에 바로 인접하여 2개의 염기를 포함한다. 일부 구현예에서, 절단 부위는 구체적으로 안티센스 가닥의 뉴클레오타이드 10 및 11에 의해 결합된 부위에 존재하고, 절단 영역은 뉴클레오타이드 11, 12 및 13을 포함한다.As used herein, the term "cleavage region" refers to the region immediately adjacent to the cleavage site. A cleavage site is the site on the target at which cleavage occurs. In some embodiments, the cleavage region comprises three bases on and immediately adjacent to either end of the cleavage site. In some embodiments, the cleavage region comprises two bases on and immediately adjacent to either end of the cleavage site. In some embodiments, the cleavage site is specifically at the site bound by nucleotides 10 and 11 of the antisense strand, and the cleavage region includes
본원에 사용된 바와 같고, 달리 지적되지 않는 경우, 용어 “상보성”은 제2 뉴클레오타이드 서열과 관련하여 제1 뉴클레오타이드 서열을 기재하기 위해 사용되는 경우, 당업자에 의해 이해되는 바와 같이 제1 뉴클레오타이드 서열을 포함하는 올리고뉴클레오타이드 또는 폴리뉴클레오타이드와 특정 조건하에서 하이드리드화하여 듀플렉스 구조를 형성하는 능력을 지칭한다. 상기 조건은 예를 들어, “엄중 조건”일 수 있고, 여기서, 엄중 조건은 다음을 포함할 수 있다: 400 mM NaCl, 40 mM PIPES pH 6.4, 1 mM EDTA, 12 내지 16시간 동안 50℃ 또는 70℃, 이어서 세척(문헌참조: 예를 들어, “Molecular Cloning: A Laboratory Manual, Sambrook, et al. (1989) Cold Spring Harbor Laboratory Press). 유기체 내부에서 접할 수 있는 바와 같은 생리학적 관련 조건과 같은 다른 조건을 적용할 수 있다. 당업자는 하이브리드화된 뉴클레오타이드의 궁극적인 적용에 따라 2개의 서열의 상보성 시험에 가장 적합한 조건 세트를 결정할 수 있을 것이다.As used herein, and unless otherwise indicated, the term "complementarity" when used to describe a first nucleotide sequence in relation to a second nucleotide sequence includes the first nucleotide sequence as understood by one of ordinary skill in the art. It refers to the ability of an oligonucleotide or polynucleotide to form a duplex structure by hybridizing under certain conditions. The conditions may be, for example, “stringent conditions,” wherein stringent conditions may include: 400 mM NaCl, 40 mM PIPES pH 6.4, 1 mM EDTA, 50° C. or 70° C. for 12 to 16 hours. °C, followed by washing (see, eg, “Molecular Cloning: A Laboratory Manual, Sambrook, et al. (1989) Cold Spring Harbor Laboratory Press). Other conditions may apply, such as physiologically relevant conditions as may be encountered inside an organism. One skilled in the art will be able to determine the most appropriate set of conditions for complementarity testing of two sequences depending on the ultimate application of the hybridized nucleotides.
iRNA 내, 예를 들어, 본원에 기재된 dsRNA 내 상보성 서열은제1 뉴클레오타이드 서열을 포함하는 올리고뉴클레오타이드 또는 폴리뉴클레오타이드와 하나 또는 둘다의 뉴클레오타이드 서열의 전체 길이에 걸쳐 제2 뉴클레오타이드 서열을 포함하는 올리고뉴클레오타이드 또는 폴리뉴클레오타이드의 염기쌍 형성을 포함한다. 상기 서열은 본원에서 서로에 대해 “완전한 상보성”으로서 언급될 수 있다. 그러나, 제1 서열이 본원의 제2 서열과 관련하여 “실질적으로 상보성”으로서 언급되는 경우, 2개의 서열은 완전히 상보성일 수 있거나, 이들은 30개 이하의 염기쌍의 듀플렉스에 대한 하이브리드화 시 하나 이상, 그러나 일반적으로 5, 4, 3, 또는 2개 이하의 미스매칭된 염기쌍을 형성할 수 있고, 이들의 궁극적인 적용, 예를 들어, 시험관내 또는 생체내 유전자 발현의 억제와 가장 관련된 조건하에서 하이브리드화하는 능력을 보유한다. 그러나, 2개의 올리고뉴클레오타이드가 하이브리드화시 하나 이상의 단일 가닥 오버행을 형성하도록 디자인된 경우, 상기 오버행은 상보성 결정과 관련하여 미스매치로서 간주되지 않는다. 예를 들어, 보다 긴 올리고뉴클레오타이드가 보다 짧은 올리고뉴클레오타이드에 완전히 상보적인 21개 뉴클레오타이드의 서열을 포함하는, 길이가 21개 뉴클레오타이드인 하나의 올리고뉴클레오타이드 및 길이가 23개 뉴클레오타이드인 또 다른 올리고뉴클레오타이드를 포함하는 dsRNA는 본원에 기재된 목적을 위해 “완전히 상보성”으로서 여전히 언급될 수 있다.A complementary sequence within an iRNA, e.g., within a dsRNA described herein, is an oligonucleotide or polynucleotide comprising a first nucleotide sequence and an oligonucleotide or polynucleotide comprising a second nucleotide sequence over the entire length of one or both nucleotide sequences. It involves base pairing of nucleotides. The sequences may be referred to herein as "perfect complementarity" to each other. However, when a first sequence is referred to as "substantially complementary" with respect to a second sequence herein, the two sequences may be completely complementary, or they may hybridize to a duplex of 30 base pairs or less, at least one; However, they are generally capable of forming no more than 5, 4, 3 , or 2 mismatched base pairs and hybridize under conditions most relevant to their ultimate application, e.g., inhibition of gene expression in vitro or in vivo. have the ability to However, if two oligonucleotides are designed to form one or more single-stranded overhangs upon hybridization, the overhangs are not considered as mismatches with respect to complementarity determination. For example, the longer oligonucleotide comprises one oligonucleotide of 21 nucleotides in length and another oligonucleotide of 23 nucleotides in length, wherein the longer oligonucleotide comprises a sequence of 21 nucleotides that is completely complementary to the shorter oligonucleotide. A dsRNA may still be referred to as “fully complementary” for purposes described herein.
본원에 사용된 바와 같은 "상보성" 서열은 또한 하이브리드화하는 이들의 능력과 관련하여 상기 요건이 충족되는 한, 비-왓슨-클릭 염기쌍 또는 비-천연 및 변형된 뉴클레오타이드로부터 형성된 염기쌍을 포함하거나 이들로부터 전적으로 형성될 수 있다. 상기 비-왓슨-클릭 염기쌍은 G:U 워블 또는 후그슈타인 염기쌍 형성을 포함하지만 이에 제한되지 않는다.As used herein, "complementary" sequences also include or from non-Watson-click base pairs or base pairs formed from non-natural and modified nucleotides, so long as the above requirements with respect to their ability to hybridize are met. can be completely formed. The non-Watson-click base pairing includes, but is not limited to, G:U wobble or Hoogstein base pairing.
본원에서 용어 “상보성”, “완전히 상보성” 및 “실질적으로 상보성”은 dsRNA의 센스 가닥과 안티센스 가닥 간의 염기 매칭 또는 이들의 사용과 관련된 내용으로부터 이해되는 바와 같이 iRNA 제제의 안티센스 가닥과 표적 서열과 같은 2개의 올리고뉴클레오타이드 또는 폴리뉴클레오타이드 간의 염기 매칭과 관련하여 사용될 수 있다.As used herein, the terms “complementarity,” “complete complementarity,” and “substantially complementarity,” as understood from references to base matching between the sense strand and the antisense strand of a dsRNA or their use, include the antisense strand of an iRNA preparation and a target sequence, such as It can be used in connection with base matching between two oligonucleotides or polynucleotides.
본원에 사용된 바와 같은, 전령 RNA (mRNA)의 “적어도 일부와 실질적으로 상보성”인 폴리뉴클레오타이드는 관심 대상의 mRNA (예를 들어, TTR 유전자를 암호화하는 mRNA)의 연속 부분에 실질적으로 상보성인 폴리뉴클레오타이드를 지칭한다. 예를 들어, 폴리뉴클레오타이드는 서열이 실질적으로 TTR 유전자를 암호화하는 mRNA의 비-중단 부분에 실질적으로 상보성인 경우 TTR mRNA의 적어도 일부에 상보성이다. As used herein, a polynucleotide that is “substantially complementary to at least a portion” of a messenger RNA (mRNA) is a polynucleotide that is substantially complementary to a contiguous portion of an mRNA of interest (eg, an mRNA encoding a TTR gene). refers to nucleotides. For example, a polynucleotide is complementary to at least a portion of a TTR mRNA if the sequence is substantially complementary to a non-interrupting portion of the mRNA encoding the TTR gene.
따라서, 일부 구현예에서, 본원에 기재된 안티센스 폴리뉴클레오타이드는 표적 TTR 서열에 완전히 상보성이다. 다른 구현예에서, 본원에 기재된 안티센스 폴리뉴클레오타이드는 서열번호 8 (5’- UGGGAUUUCAUGUAACCAAGA -3’)에 완전히 상보성이다. 하나의 구현예에서, 안티센스 폴리뉴클레오타이드 서열은 5’- UCUUGGUUACAUGAAAUCCCAUC -3’ (서열번호 9)이고, 여기서, 안티센스 가닥의 위치 7에서 U는 T일 수 있다. Thus, in some embodiments, an antisense polynucleotide described herein is fully complementary to a target TTR sequence. In another embodiment, the antisense polynucleotides described herein are fully complementary to SEQ ID NO: 8 (5'- UGGGAUUUCAUGUAACCAAGA -3'). In one embodiment, the antisense polynucleotide sequence is 5'- UCUUGGUUACAUGAAAUCCCAUC -3' (SEQ ID NO: 9), wherein U at
본원에 사용된 "참조 수준"은 검정에서 수득된 수준, 예를 들어, 바이오마커 수준, 예를 들어, 단백질 바이오마커 수준이 비교되는 미리 결정된 수준으로 이해된다. 특정 구현예에서, 참조 수준은 건강한 집단, 예를 들어, 바이오마커의 변경된 수준과 관련된 질병 또는 병태를 갖지 않고 소인, 예를 들어, 변화된 수준의 바이오마커와 관련된 질병 또는 병태에 대한 유전적 소인을 갖지 않는 집단에 대해 결정된 대조군 수준일 수 있다. 특정 구현예에서, 집단은 특정 기준, 예를 들어 연령, 성별에 대해 매칭되어야 한다. 특정 구현예에서, 바이오마커의 참조 수준은 더 이른 시간, 예를 들어, 증후성 질환의 발병 전 또는 치료 시작 전의 동일한 대상체로부터의 수준이다. 전형적으로, 샘플은 임상적으로 관련된 간격, 예를 들어 바이오마커의 변화가 관찰될 수 있는 시간상 충분히 분리된 간격, 예를 들어, 적어도 3개월 간격, 적어도 6개월 간격, 또는 적어도 9개월 간격에서 수득된다. 시간이 경과함에 따라 대상체로부터 2개 초과의 샘플이 수득되는 경우, 이전 샘플 중 어느 하나가 참조 수준으로 작용할 수 있는 것으로 이해된다. As used herein, a “reference level” is understood to be a predetermined level to which a level obtained in an assay, eg, a biomarker level, eg, a protein biomarker level, is compared. In certain embodiments, a reference level is a predisposition, eg, a genetic predisposition to a disease or condition associated with an altered level of a biomarker, without a healthy population, eg, a disease or condition associated with an altered level of the biomarker. It may be a control level determined for a population without. In certain implementations, populations must be matched for certain criteria, eg age, gender. In certain embodiments, the reference level of a biomarker is a level from the same subject at an earlier time, eg, before the onset of the symptomatic disease or before the start of treatment. Typically, samples are obtained at clinically relevant intervals, e.g., intervals sufficiently separated in time that changes in the biomarker can be observed, e.g., at least 3 months apart, at least 6 months apart, or at least 9 months apart. do. It is understood that if more than two samples are obtained from a subject over time, any of the previous samples may serve as the reference level.
본원에 사용된 바와 같이, "참조 수준과 비교한 변화" 등은 바이오마커 수준의 통계적으로 또는 임상적으로 유의적인 변화, 예를 들어 참조 수준과 비교하여 단백질 바이오마커 수준의 변화가 검정 방법의 전형적인 표준 편차보다 더 큰 것으로 이해된다. 더욱이 상기 변화는 임상적으로 관련되어야만 한다. 참조 수준과 비교되는 상기 변화는 퍼센트 변화로서 결정될 수 있다. 예를 들어, 참조 수준이 바이오마커 X에 대해 100 pg/ml이고 대상체에서 바이오마커 X의 수준이 150 pg/ml인 경우, 상기 수준은 ((150 pg/ml -100 pg/ ml)/100 pg/ml) X 100% = 50%에 의해 계산되는 50%까지 증가된다. 상기 대상체에서 바이오마커 X의 수준이 300 pg/ml인 경우, 상기 수준은 300%까지 증가된다. 상기 대상체에서 바이오마커 X의 수준이 50 pg/ml인 경우, 상기 수준은 50%까지 감소된다. 특정 구현예에서, 참조 수준과 비교하여 상기 변화는 적어도 50%까지 증가된다. 특정 구현예에서, 참조 수준과 비교하여 상기 변화는 적어도 100%, 적어도 200% 또는 적어도 300%까지 증가된다. 특정 구현예에서, 참조 샘플과 비교하여 상기 변화는 적어도 25%까지 감소된다. 특정 구현예에서, 참조 샘플과 비교하여 상기 변화는 적어도 50%까지 감소된다. As used herein, "change compared to reference level" and the like means a statistically or clinically significant change in biomarker level, e.g., a change in protein biomarker level compared to a reference level, typical of an assay method. It is understood to be greater than the standard deviation. Moreover, the change must be clinically relevant. The change compared to the reference level can be determined as a percent change. For example, if the reference level is 100 pg/ml for biomarker X and the level of biomarker X in the subject is 150 pg/ml, then the level is ((150 pg/ml -100 pg/ml)/100 pg /ml) X 100% = 50%. When the level of biomarker X in the subject is 300 pg/ml, the level is increased by 300%. When the level of biomarker X in the subject is 50 pg/ml, the level is reduced by 50%. In certain embodiments, the change compared to the reference level is increased by at least 50%. In certain embodiments, the change compared to the reference level is increased by at least 100%, at least 200% or at least 300%. In certain embodiments, the change compared to a reference sample is reduced by at least 25%. In certain embodiments, the change compared to a reference sample is reduced by at least 50%.
본원에 사용된 "대상체로부터의 생물학적 샘플" 또는 "대상체로부터의 샘플"은 대상체로부터 단리된 하나 이상의 체액, 세포 또는 조직을 포함한다. 생물학적 체액의 예는 혈액, 혈청 및 장액, 혈장, 뇌척수액, 안액, 림프, 소변, 타액 등을 포함한다. 조직 샘플은 조직, 기관 또는 국소 영역으로부터의 샘플을 포함할 수 있다. 예를 들어, 샘플은 특정 기관, 기관의 일부 또는 해당 기관 내의 체액이나 세포로부터 유래할 수 있다. 특정 구현예에서, 샘플은 간 조직일 수 있거나 간으로부터 유래될 수 있다. 일부 구현예에서, “대상체로부터의 생물학적 샘플"은 대상체로부터의 혈액 또는 혈액 유래된 혈청 또는 혈장을 지칭할 수 있다. 일부 구현예에서, 체액은 세포가 실질적으로 없고, 예를 들어 세포가 없다.As used herein, a “biological sample from a subject” or “sample from a subject” includes one or more bodily fluids, cells or tissues isolated from a subject. Examples of biological body fluids include blood, serum and intestinal fluid, plasma, cerebrospinal fluid, eye fluid, lymph, urine, saliva and the like. A tissue sample may include a sample from a tissue, organ or localized area. For example, a sample may be from a particular organ, part of an organ, or a body fluid or cell within that organ. In certain embodiments, the sample may be liver tissue or may be derived from the liver. In some embodiments, a “biological sample from a subject” may refer to blood or blood derived serum or plasma from a subject. In some embodiments, a bodily fluid is substantially free of cells, e.g., free of cells.
본원에 사용된 바와 같이, "임상적으로 관련된 차이"는 평가에 대한 전형적인 관찰자간 변동보다 적어도 더 큰 차이로 이해되고, 여기서 상기 관찰자는 동일한 개체가 거의 동시에, 예를 들어, 연속된 날과 같이 일주일 이내에 동일한 평가를 수행하는 숙련된 의료 전문가, 간병인 또는 환자일 수 있다. 특정 환자 관찰은 주관적이고, 짧은 시간 프레임내에 다른 관찰자가 수행할 때 거의 동일해야하는 것(예를 들어, 체중, 심박수)으로 이해된다. mNIS+7의 일부 양상(예를 들어, 터치 압력, 진동, 관절 위치 및 동작에 대한 반응) 및 노퍽(Norfolk)-삶의 질(예를 들어, 통증 수준, 뜨겁거나 차가운 손과 발, 서 있는 동안의 안정성)과 같은 기타 정성적 측정은 매일 그리고 관찰자마다 다양할 수 있다. 따라서 혼성 스코어는 관찰을 집계하는 데 사용되고, 관찰자 간의 더 큰 변동은 임상적으로 관련된 변화의 임의의 징후 없이 예상된다. 바이오마커 수준에 대한 검정은 샘플 내 및 샘플 간의 변동의 공지된 수준을 갖는다. 임상적으로 관련된 차이의 결정은 당업자, 예를 들어 TTR 관련 질환을 갖는 환자를 치료한 경험이 있는 건강 의료 전문가, 임상 실험실 전문가의 능력 범위 내에 있다. As used herein, "clinically relevant difference" is understood to be a difference that is at least greater than the typical inter-observer variability for an assessment, wherein the observers are the same subject at approximately the same time, e.g., on consecutive days. It could be a trained healthcare professional, caregiver or patient performing the same evaluation within a week. It is understood that certain patient observations are subjective and should be approximately the same (eg weight, heart rate) when performed by other observers within a short time frame. Some aspects of the mNIS+7 (e.g., response to touch pressure, vibration, joint position and motion) and Norfolk-quality of life (e.g., level of pain, hot/cold hands and feet, standing Other qualitative measures, such as stability over time, may vary from day to day and from observer to observer. Thus, a composite score is used to aggregate observations, and greater variability between observers is expected without any indication of clinically relevant changes. Assays for biomarker levels have a known level of variation within and between samples. Determination of clinically relevant differences is well within the capabilities of those skilled in the art, eg, health care professionals, clinical laboratory professionals experienced in treating patients with TTR-related disorders.
본원에 사용된 "만성적으로 투여되는"은 무기한 간격 동안, 예를 들어, 간 이식까지의 대상체의 남은 생애 동안 투여로서 이해된다. As used herein, "chronically administered" is understood as administration for indefinite intervals, eg, for the remainder of the subject's life up to liver transplantation.
본원에 사용된 바와 같은 "TTR을 안정화하는 치료학적 제제" 또는 "TTR 사량체를 안정화하는 치료학적 제제"는 TTR 사량체의 서브유닛의 해리, 예를 들어, 단량체로의 해리를 감소시키거나 방지하는 제제이다. 일부 구현예에서, 제제는 예를 들어 TTR 아밀로이드 플라크를 형성하는 TTR 단량체 또는 TTR 단량체의 단백질용해 단편의 수준을 감소시킴으로써 TTR 아밀로이드 플라크의 형성을 감소시킨다. 상기 제제는 타파미디스, 디플루니살 및 Ag10을 포함하지만 이에 제한되지 않는다.As used herein, "therapeutic agent stabilizing TTR" or "therapeutic agent stabilizing TTR tetramer" means to reduce or prevent dissociation of subunits of TTR tetramers, e.g., into monomers. It is a drug that In some embodiments, the agent reduces the formation of TTR amyloid plaques, for example by reducing the level of TTR monomers or proteolytic fragments of TTR monomers that form TTR amyloid plaques. Such agents include, but are not limited to, tafamidis, diflunisal, and Ag10.
본원에 사용된 용어 "치료학적 제제의 투여"는 대상체에게 치료학적 제제를 제공하는 것으로서 이해된다. 구현예에서, 치료학적 제제는, 예를 들어 치료학적 제제의 표지에 의해 제공된 바와 같은 제제에 대한 적절한 용량에서 및 투여 경로에 의해 제공된다.As used herein, the term "administration of a therapeutic agent" is understood as providing a therapeutic agent to a subject. In an embodiment, the therapeutic agent is provided at a dose appropriate for the agent and by route of administration, eg, as provided by the label of the therapeutic agent.
II. TTR 관련 질환을 표적화하기 위한 방법II. Methods for targeting TTR-related diseases
본 발명은 이중 가닥 RNAi 제제 및 이중 가닥 RNAi 제제 및 사람 대상체에서 TTR 관련 질환, 예를 들어 트랜스티레틴-매개 아밀로이드증(ATTR 아밀로이드증), 예를 들어 유전성 ATTR(h-ATTR) 아밀로이드증 또는 비-유전성 ATTR(wt ATTR) 아밀로이드증을 치료하기 위한; 또는 TTR 관련 질환의 진단 기준을 아직 충족하지 않지만 TTR 관련 질환이 발병할 위험에 처한 대상체, 예를 들어 TTR 아밀로이드증과 관련된 TTR 돌연변이를 갖는 대상체, TTR 아밀로이드증의 진단 기준을 아직 충족하지 않는 TTR 아밀로이드증의 일부 징후를 갖는 대상체, TTR 아밀로이드증과 관련된 변경된 바이오마커 수준을 갖는 대상체에서 TTR의 발현을 억제하기 위한 방법에서 이들의 용도를 제공한다. 방법은 본 발명의 치료학적 유효량의 RNAi 제제를 대상체에게 투여하는 것을 포함한다.The present invention relates to double-stranded RNAi preparations and TTR-related diseases in human subjects, such as transthyretin-mediated amyloidosis (ATTR amyloidosis), such as hereditary ATTR (h-ATTR) amyloidosis or non-hereditary ATTR (wt ATTR) for treating amyloidosis; or subjects who do not yet meet the diagnostic criteria for a TTR-related disease but are at risk of developing a TTR-related disease, e.g., those who have a TTR mutation associated with TTR amyloidosis, a subset of TTR amyloidosis that does not yet meet the diagnostic criteria for TTR amyloidosis Provided are their use in a method for inhibiting the expression of TTR in a subject with symptoms, a subject with altered biomarker levels associated with TTR amyloidosis. The method comprises administering to a subject a therapeutically effective amount of an RNAi agent of the present invention.
하나의 양상에서, 본 발명은 TTR 관련 질환을 앓고 있거나 TTR 관련 질환이 발병할 위험에 처한 사람 대상체를 치료하는 방법을 제공한다. 방법은 약 25 mg 내지 약 1000 mg의 고정된 용량의 이중 가닥 RNAi 제제를 사람 대상체에게 투여함을 포함하고, 여기서, 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고; 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)을 포함하고, 여기서, a, c, g, 및 u는 각각 2'-O-메틸아데노신-3’-포스페이트, 2'-O-메틸시티딘-3’-포스페이트, 2'-O-메틸구아노신-3’-포스페이트, 및 2'-O-메틸우리딘-3’-포스페이트이고; Af, Cf, Gf, 및 Uf는 각각 2’-플루오로아데노신-3’-포스페이트, 2’-플루오로시티딘-3’-포스페이트, 2’-플루오로구아노신-3’-포스페이트, 및 2’-플루오로우리딘-3’-포스페이트이고; (Tgn)은 티미딘-글리콜 핵산 (GNA) S-이성체이고; s는 포스포로티오에이트 링커이다.In one aspect, the invention provides a method of treating a human subject suffering from or at risk of developing a TTR-related disorder. The method comprises administering to a human subject a fixed dose of about 25 mg to about 1000 mg of a double-stranded RNAi preparation, wherein the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6). contain; The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7), where a, c, g, and u are each 2'-O-methyladenosine-3'- phosphate, 2'-O-methylcytidine-3'-phosphate, 2'-O-methylguanosine-3'-phosphate, and 2'-O-methyluridine-3'-phosphate; Af, Cf, Gf, and Uf are 2'-fluoroadenosine-3'-phosphate, 2'-fluorocytidine-3'-phosphate, 2'-fluoroguanosine-3'-phosphate, and 2, respectively. '-fluorouridine-3'-phosphate; (Tgn) is the thymidine-glycol nucleic acid (GNA) S-isomer; s is a phosphorothioate linker.
또 다른 양상에서, 본 발명은 TTR 관련 질환을 앓고 있거나 TTR 관련 질환이 발병할 위험에 처한 사람 대상체에서 신경학적 손상 또는 삶의 질의 적어도 하나의 지표를 개선시키는 방법을 제공한다. 방법은 약 25 mg 내지 약 1000 mg의 고정된 용량의 이중 가닥 RNAi 제제를 사람 대상체에게 투여함을 포함하고, 여기서, 상기 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고; 상기 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)를 포함한다.In another aspect, the invention provides a method for improving at least one indicator of neurological impairment or quality of life in a human subject suffering from or at risk of developing a TTR-related disorder. The method comprises administering to a human subject a fixed dose of about 25 mg to about 1000 mg of a double-stranded RNAi preparation, wherein the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6) contains; The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7).
또 다른 측면에서, 본 발명은 TTR 관련 질환을 앓거나 TTR 관련 질환을 발병할 위험에 처한 사람 대상에서 신경병증 손상 스코어(NIS) 또는 변형된 NIS(mNIS+7)를 감소, 감속 또는 정지시키는 방법을 제공한다. 방법은 약 25 mg 내지 약 1000 mg의 고정된 용량의 이중 가닥 RNAi 제제를 사람 대상체에게 투여함을 포함하고, 여기서, 상기 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고; 상기 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)를 포함한다.In another aspect, the invention provides a method for reducing, slowing or arresting the Neuropathic Impairment Score (NIS) or Modified NIS (mNIS+7) in a human subject suffering from or at risk of developing a TTR-related disorder. provides The method comprises administering to a human subject a fixed dose of about 25 mg to about 1000 mg of a double-stranded RNAi preparation, wherein the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6) contains; The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7).
또 다른 양상에서, 본 발명은 TTR 관련 질환을 앓고 있거나 TTR 관련 질환이 발병할 위험에 처한 사람 대상체에서 6분 걷기 시험 (6MWT)을 증가시키는 방법을 제공한다. 방법은 약 25 mg 내지 약 1000 mg의 고정된 용량의 이중 가닥 RNAi 제제를 사람 대상체에게 투여함을 포함하고, 여기서, 상기 센스 가닥은 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고; 상기 안티센스 가닥은 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)를 포함한다.In another aspect, the invention provides a method of increasing the 6 Minute Walk Test (6MWT) in a human subject suffering from or at risk of developing a TTR-related disorder. The method comprises administering to a human subject a fixed dose of about 25 mg to about 1000 mg of a double-stranded RNAi preparation, wherein the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6) contains; The antisense strand contains the modified nucleotide sequence 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (SEQ ID NO: 7).
특정 구현예에서, 이중 가닥 RNAi 제제는 분기별 약 1회 내지 연간 약 1회로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 분기별 약 1회, 약 6개월마다 1회, 또는 연간 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject from about once per quarter to about once per year. In certain embodiments, the double-stranded RNAi agent is administered to a human subject about once per quarter, about once every 6 months, or about once per year.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 300 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 75 mg 내지 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 50 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 75 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 100 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 300 mg; 약 25 mg 내지 약 200 mg; 약 50 mg 내지 약 300 mg; 약 25 mg; 약 50 mg; 약 100 mg; 약 200mg; 또는 약 300 mg의 고정 용량으로 분기별 1회, 즉, 3개월 마다 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg to about 300 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg to about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 75 mg to about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 50 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 75 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 100 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is about 25 mg to about 300 mg; about 25 mg to about 200 mg; about 50 mg to about 300 mg; about 25 mg; about 50 mg; about 100 mg; about 200 mg; or a fixed dose of about 300 mg is administered to a human subject once quarterly, ie, about once every 3 months.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 내지 약 600 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 또는 약 600 mg의 고정 용량으로 6개월 마다 약 1회,내지 연간 약 1회 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 또는 약 600 mg의 고정 용량으로 6개월마다 약 1회, 또는 연간 약 1회 사람 대상체에게 투여된다.In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg to about 600 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg or about 600 mg about once every 6 months, to about once a year. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg or about 600 mg about once every 6 months, or about once a year.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 700 mg 내지 약 1000 mg 또는 약 700 mg 내지 약 900 mg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 700 mg, 약 800 mg, 약 900 mg 또는 약 1000 mg의 고정된 용량으로 연간 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 700 mg to about 1000 mg or about 700 mg to about 900 mg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 700 mg, about 800 mg, about 900 mg, or about 1000 mg about once per year.
하나의 구현예에서, 대상체는 TTR 유전자 발현의 감소가 이득이 되는 질환, 장애 또는 병태에 대해 치료되거나 평가되는 사람이고; TTR 유전자 발현의 감소가 이득이 되는 질환, 장애 또는 병태에 대한 위험이 있는 사람, 예를 들어 TTR 관련 질병의 진단 기준을 충족하지 않지만 TTR 관련 질환의 적어도 하나의 징후 또는 증상을 나타내거나 TTR 관련 질환의 적어도 하나의 위험 인자를 갖는 사람; TTR 유전자 발현의 감소가 이득이 되는 질환, 장애 또는 병태를 갖는 사람; 또는 본원에 기재된 바와 같이 TTR 유전자 발현의 감소가 이득이 되는 질환, 장애 또는 병태에 대해 치료받는 사람이다. In one embodiment, the subject is a person being treated or evaluated for a disease, disorder or condition for which a reduction in TTR gene expression would benefit; A person at risk for a disease, disorder, or condition for which a decrease in TTR gene expression would benefit, e.g., who does not meet criteria for a diagnosis of a TTR-related disease but exhibits at least one sign or symptom of a TTR-related disease or who has a TTR-related disease people with at least one risk factor for; people with a disease, disorder or condition that would benefit from a reduction in TTR gene expression; or a person being treated for a disease, disorder or condition for which a reduction in TTR gene expression would benefit, as described herein.
일부 구현예에서, 사람 대상체는 TTR-관련 질환을 앓고 있다. 다른 구현예에서, 대상체는 TTR 관련 질환의 발병 위험에 처한 대상체, 예를 들어, TTR 관련 질병의 발병과 관련된 TTR 유전자 돌연변이를 갖는 대상체, TTR 관련 질환의 가족력이 있는 대상체 또는 TTR 관련 질환에 대한 진단 기준을 충족시키지 않으면서 TTR 관련 질환의 발병을 암시하는 징후 또는 증상을 갖는 대상체이다.In some embodiments, the human subject is suffering from a TTR-related disease. In another embodiment, the subject is at risk of developing a TTR-related disease, eg, a subject having a TTR gene mutation associated with developing a TTR-related disease, a subject with a family history of a TTR-related disease, or a diagnosis of a TTR-related disease. A subject who does not meet the criteria and has signs or symptoms suggestive of developing a TTR-related disease.
본원에 사용된 "TTR 관련 질환"은 원섬유 전구체가 변이체 또는 야생형 TTR 단백질로 이루어진 아밀로이드 침착물의 형성에 의해 야기되거나 이와 관련된 임의의 질환을 포함한다. 돌연변이 및 야생형 TTR은 다양한 형태의 아밀로이드 침착(아밀로이드증)을 유발한다. 아밀로이드증은 잘못 폴딩된 단백질의 형성 및 응집을 수반하여 장기 기능을 손상시키는 세포외 침착물을 초래한다. TTR 응집과 관련된 임상적 증상은 예를 들어, 노인성 전신성 아밀로이드증(SSA); 전신성 가족성 아밀로이드증; 가족성 아밀로이드성 다발신경병증(FAP); 가족성 아밀로이드성 심근병증(FAC); 및 연수막 또는 수막뇌혈관성 아밀로이드증, 중추신경계 (CNS) 아밀로이드증 또는 아밀로이드증 VII 형태로도 공지된 연수막 아밀로이드증을 포함한다.As used herein, "TTR-related disease" includes any disease caused by or associated with the formation of amyloid deposits in which fibrillar precursors consist of variant or wild-type TTR protein. Mutant and wild-type TTR cause various forms of amyloid deposits (amyloidosis). Amyloidosis involves the formation and aggregation of misfolded proteins resulting in extracellular deposits that impair organ function. Clinical conditions associated with TTR aggregation include, for example, senile systemic amyloidosis (SSA); systemic familial amyloidosis; Familial Amyloidosis Polyneuropathy (FAP); Familial Amyloid Cardiomyopathy (FAC); and leptomeningeal amyloidosis, also known as leptomeningeal or meningocerebrovascular amyloidosis, central nervous system (CNS) amyloidosis or form of amyloidosis VII.
하나의 구현예에서, 본 발명의 RNAi 제제는 가족성 아밀로이드성 심근병증(FAC)을 앓고 있는 대상체에게 투여된다. 또 다른 구현예에서, 본 발명의 RNAi 제제는 혼합 표현형을 갖는 FAC를 앓고 있는 대상체, 즉 심장 및 신경계 손상 둘 다를 갖는 대상체에게 투여된다. 여전히 또 다른 구현예에서, 본 발명의 RNAi 제제는 혼합 표현형을 갖는 FAP를 앓고 있는 대상체, 즉 신경계 및 심장 손상 둘 다를 갖는 대상체에게 투여된다. 하나의 구현예에서, 본 발명의 RNAi 제제는 동소 간 이식(OLT(orthotopic liver transplantation))으로 치료된 FAP를 앓고 있는 대상체에게 투여된다. In one embodiment, an RNAi agent of the invention is administered to a subject suffering from familial amyloidogenic cardiomyopathy (FAC). In another embodiment, an RNAi agent of the invention is administered to a subject suffering from FAC with a mixed phenotype, ie, a subject with both cardiac and nervous system damage. In yet another embodiment, an RNAi agent of the invention is administered to a subject suffering from FAP with a mixed phenotype, ie, a subject with both nervous system and cardiac damage. In one embodiment, an RNAi agent of the invention is administered to a subject suffering from FAP treated with orthotopic liver transplantation (OLT).
또 다른 구현예에서, 본 발명의 RNAi 제제는 노인성 전신성 아밀로이드증(SSA)을 앓고 있는 대상체에게 투여된다. 본 발명의 방법의 다른 구체예에서, 본 발명의 RNAi 제제는 가족성 아밀로이드성 심근병증(FAC) 및 노인성 전신성 아밀로이드증(SSA)을 앓고 있는 대상체에게 투여된다. 정상 서열 TTR은 노인의 심장 아밀로이드증을 유발하고, 노인성 전신성 아밀로이드증(SSA)(노인성 심장 아밀로이드증(SCA) 또는 심장 아밀로이드증이라고도 함)이라고 호칭된다. SSA는 흔히 다른 많은 기관에 미세한 침착물을 동반한다. TTR 돌연변이는 TTR 아밀로이드 형성 과정을 촉진시키고 임상적으로 유의적인 TTR 아밀로이드증(또한 ATTR (아밀로이드증 트랜스티레틴 유형)으로 호칭됨)의 발병에 대해 가장 중요한 위험 인자이다. 85개 초과의 아밀로이드 생성 TTR 변이체는 전신 가족성 아밀로이드증을 유발하는 것으로 공지되어 있다.In another embodiment, an RNAi agent of the invention is administered to a subject suffering from senile systemic amyloidosis (SSA). In another embodiment of the methods of the invention, an RNAi agent of the invention is administered to a subject suffering from familial amyloidogenic cardiomyopathy (FAC) and senile systemic amyloidosis (SSA). Normal sequence TTR causes cardiac amyloidosis in the elderly and is called senile systemic amyloidosis (SSA) (also called senile cardiac amyloidosis (SCA) or cardiac amyloidosis). SSA is often accompanied by microscopic deposits in many other organs. TTR mutations promote the process of TTR amyloidogenesis and are the most important risk factor for the development of clinically significant TTR amyloidosis (also called ATTR (transthyretin type amyloidosis)). More than 85 amyloidogenic TTR variants are known to cause systemic familial amyloidosis.
본 발명의 방법의 일부 구현예에서, 본 발명의 RNAi 제제는 트랜스티레틴(TTR) 관련 가족성 아밀로이드성 다발신경병증 (FAP)를 앓고 있는 대상체에게 투여된다. 이러한 대상체는 유리체 혼탁 및 녹내장과 같은 안구 징후를 앓을 수 있다. 망막 색소 상피(RPE)에 의해 합성된 아밀로이드 생성 트랜스티레틴(ATTR)이 안구 아밀로이드증의 진행에서 중요한 역할을 한다는 것은 당업자에게 알려져 있다. 이전 연구에 따르면 RPE 세포를 감소시키는 범망막 레이저 광응고가 유리체에서 아밀로이드 침착의 진행을 방지하여 RPE에서 ATTR 발현의 효과적인 억제가 안구 아밀로이드증에 대한 새로운 치료요법이 될 수 있음을 보여주었다(문헌참조: 예를 들어, Kawaji, T., et al., Ophthalmology. (2010) 117: 552-555). 또 다른 TTR 관련 질환은 "이상트랜스트레틴혈증성 고티록신혈증" 또는 "이상전구알부민혈증성 고티록신혈증"로도 알려진 고티록신혈증이다. 이러한 유형의 고티록신혈증은 티록신에 대한 친화도가 증가된 돌연변이체 TTR 분자로 인해 티록신과 TTR의 증가된 연관성에 이차적일 수 있다. 예를 들어, 문헌(Moses et al.(1982)J.Clin.Invest.,86,2025-2033)을 참조한다.In some embodiments of the methods of the invention, an RNAi agent of the invention is administered to a subject suffering from transthyretin (TTR) associated familial amyloidogenic polyneuropathy (FAP). Such subjects may suffer from ocular conditions such as vitreous opacity and glaucoma. It is known to those skilled in the art that amyloidogenic transthyretin (ATTR) synthesized by the retinal pigment epithelium (RPE) plays an important role in the development of ocular amyloidosis. Previous studies have shown that panretinal laser photocoagulation to reduce RPE cells prevents the progression of amyloid deposits in the vitreous, suggesting that effective inhibition of ATTR expression in RPE could represent a novel therapy for ocular amyloidosis (Ref. For example, Kawaji, T., et al., Ophthalmology. (2010) 117: 552-555). Another TTR-related disorder is hyperthyroxinemia, also known as “dystranslettinemia hyperthyroxinemia” or “dysproalbuminemia hyperthyroxinemia”. This type of hyperthyroxinemia may be secondary to increased association of thyroxine with TTR due to mutant TTR molecules having increased affinity for thyroxine. See, eg, Moses et al . (1982) J. Clin. Invest. , 86, 2025-2033.
본 발명의 RNAi 제제는 피하, 정맥내 및 근육내 주사, 및 이들의 임의의 조합을 포함하지만 이에 제한되지 않는 당업계에 공지된 임의의 투여 방식을 사용하여 대상체에게 투여될 수 있다. The RNAi agents of the present invention can be administered to a subject using any mode of administration known in the art, including but not limited to subcutaneous, intravenous and intramuscular injection, and any combination thereof.
일부 구현예에서, 제제는 피하로 대상체에게 투여된다. In some embodiments, the formulation is administered subcutaneously to the subject.
일부 구현예에서, 대상체는 피하 주사, 예를 들어 복부, 대퇴부 또는 상완 주사를 통해 단일 용량의 RNAi 제제를 투여받는다. 다른 구현예에서, 대상체는 피하 주사를 통해 분할 용량의 RNAi 제제를 투여받는다. 하나의 구현예에서, 분할 용량의 RNAi 제제는 대상체 상의 2개의 상이한 해부학적 위치에서 피하 주사를 통해 대상체에게 투여된다. 예를 들어, 대상체는 25 mg 내지 1000 mg의 용량으로 피하로 주사될 수 있다. 본 발명의 일부 구현예에서, 피하 투여는 예를 들어 미리 충전된 주사기 또는 자동주사 주사기를 통한 자가 투여이다. 일부 구현예에서, 피하 투여를 위한 RNAi 제제의 용량은 예를 들어, 약제학적으로 허용되는 담체의 1 ml 이하의 용적에 함유된다. 일부 구현예에서, RNAi 제제는 비-발열성 제형 중에 있다. In some embodiments, the subject is administered a single dose of the RNAi agent via subcutaneous injection, eg, abdominal, femoral, or brachial injection. In another embodiment, the subject receives divided doses of the RNAi agent via subcutaneous injection. In one embodiment, split doses of the RNAi agent are administered to the subject via subcutaneous injection at two different anatomical locations on the subject. For example, a subject can be injected subcutaneously at a dose of 25 mg to 1000 mg. In some embodiments of the invention, subcutaneous administration is self-administration, eg via a pre-filled syringe or auto-injecting syringe. In some embodiments, a dose of an RNAi agent for subcutaneous administration is contained in a volume of eg, 1 ml or less of a pharmaceutically acceptable carrier. In some embodiments, the RNAi agent is in a non-pyrogenic formulation.
일부 구현예에서, RNAi 제제는 대상체 내의 세포에서 TTR 발현을 억제하기에 효과적인 양으로 대상체에게 투여된다. 대상체 내 세포에서 TTR 발현을 억제하는 데 효과적인 양은 TTR mRNA, TTR 단백질, 또는 아밀로이드 침착물과 같은 관련 변수의 억제를 포함하는 방법을 포함하는 하기 논의된 방법을 사용하여 평가할 수 있다.In some embodiments, an RNAi agent is administered to a subject in an amount effective to inhibit TTR expression in cells within the subject. An amount effective to inhibit TTR expression in cells in a subject can be assessed using the methods discussed below, including methods involving inhibition of related variables such as TTR mRNA, TTR protein, or amyloid deposits.
일부 구현예에서, RNAi 제제는 치료학적 유효량으로 대상체에게 투여된다.In some embodiments, an RNAi agent is administered to a subject in a therapeutically effective amount.
본원에 사용된 "치료학적 유효량"은 TTR 관련 질환을 치료하기 위해 환자에게 투여될 때 질환의 치료에 영향을 미치기에 충분한 RNAi 제제의 양을 포함하는 것으로 의도된다(예를 들어, 적당한 대조군과 비교하여 기존의 질환의 진행을 감소시키거나, 유지하거나, 감속시키거나; 적절한 대조군과 비교하여 질환의 하나 이상의 증상을 감소시키거나, 유지하거나 감속시킴에 의해). “치료학적 유효량"은 RNAi 제제, 제제가 투여되는 방식, 질환 및 이의 중증도 및 병력, 연령, 체중, 가족력, 유전학적 구성, TTR 발현에 의해 매개되는 병리학적 과정의 단계, 경우에 따라 선행 또는 병용 치료의 유형 및 치료될 환자의 기타 개별적인 특징에 의존하여 다양할 수 있다. TTR 아밀로이드증, 다발신경병증 및 심근병증에 대한 진단 기준은 하기에서 추가로 논의된다. As used herein, "therapeutically effective amount" is intended to include an amount of an RNAi agent sufficient to effect treatment of a disease when administered to a patient to treat a TTR-associated disease (e.g., compared to an appropriate control). reducing, maintaining or slowing the progression of an existing disease by reducing, maintaining or slowing down one or more symptoms of the disease compared to an appropriate control). "Therapeutically effective amount" refers to the RNAi agent, the manner in which the agent is administered, the disease and its severity and history, age, weight, family history, genetic makeup, stage of the pathological process mediated by TTR expression, preceding or concomitant use as the case may be. Depending on the type of treatment and other individual characteristics of the patient being treated, diagnostic criteria for TTR amyloidosis, polyneuropathy and cardiomyopathy are further discussed below.
본원에 사용된 바와 같은 "치료학적 유효량"은 TTR 관련 질환의 진단 기준을 아직 충족하지 않는 대상체, 예를 들어, hTTR 아밀로이드증 다발신경병증으로 진단되지 않은 대상체; 단계 1 FAP의 진단 기준을 충족하지 않지만 상기 질환에 걸리기 쉬운 대상체, 예를 들어, TTR 아밀로이드증과 관련된 TTR 돌연변이가 있는 대상체, 기립성 저혈압, 심부전, 심장 부정맥, 좌심실 벽 두께, 심실 중격 벽 두께, 심장 후벽 두께 설사, 변비, 발기 부전, 녹내장, 유리체내 침착, 가리비 동공; 수근관 증후군, 요추 척추관 협착증 및 이두박근 건 파열; 기준 샘플과 비교하여 상승된 신경섬유 경쇄(NfL) 수준, 예를 들어, 혈청 내 적어도 37 pg/ml의 Nfl 수준을 갖는 대상체에 투여되는 경우 질환 또는 질환의 하나 이상의 증상을 예방하거나 개선하기에 충분한, RNAi 제제의 양을 포함하는 것으로 의도된다. 개선될 수 있는 증상은 감각 신경병증(예를 들어, 감각 이상, 말단 사지의 감각 이상), 자율 신경병증(예를 들어, 위궤양 또는 기립성 저혈압과 같은 위장 기능부전), 운동 신경병증, 발작, 치매, 척수병증, 다발신경병증, 수근관 증후군, 자율신경계 부전, 심근병증, 유리체 혼탁, 신부전, 신장병증, 실질적으로 감소된 mBMI(변형된 체질량 지수), 뇌신경 기능부전, 각막 격자 이영양증, 심장초음파 평가에 의한 좌심실(LV) 벽 비후, 심장초음파 평가에 의한 증가된 전체 종방향 긴장 증가 평가, 증가된 N-말단 프로호르몬 B형 나트륨이뇨 펩타이드(NTproBNP) 및 심장 사건으로 인한 입원을 포함한다. 질환의 감소는 질환 과정을 서행시키거나 후기 발병 질환의 중증도를 감소시킴을 포함한다. “용량"은 RNAi 제제, 제제가 투여되는 방식, 질환 위험 정도, 병력, 연령, 체중, 가족력, 유전적 구성, 경우에 따라 선행 또는 병용 치료의 유형 및 치료될 환자의 기타 개별적인 특징에 따라 다양할 수 있다.As used herein, “therapeutically effective amount” refers to subjects who do not yet meet diagnostic criteria for a TTR-related disease, eg, subjects who have not been diagnosed with hTTR amyloidosis polyneuropathy; Subjects who do not meet the diagnostic criteria for stage 1 FAP but are predisposed to the disease, eg, those with a TTR mutation associated with TTR amyloidosis, orthostatic hypotension, heart failure, cardiac arrhythmias, left ventricular wall thickness, ventricular septal wall thickness, cardiac posterior wall thickness diarrhea, constipation, impotence, glaucoma, intravitreal deposition, scallop pupil; carpal tunnel syndrome, lumbar spinal canal stenosis and biceps tendon rupture; sufficient to prevent or ameliorate a disease or one or more symptoms of a disease when administered to a subject having an elevated neurofibrillary tangle (NfL) level compared to a reference sample, eg, an Nfl level of at least 37 pg/ml in serum. , the amount of the RNAi agent. Symptoms that can be ameliorated include sensory neuropathy (e.g., paresthesia, paresthesia of distal limbs), autonomic neuropathy (e.g., gastrointestinal insufficiency such as gastric ulcer or orthostatic hypotension), motor neuropathy, seizures, Dementia, myelopathy, polyneuropathy, carpal tunnel syndrome, autonomic dysfunction, cardiomyopathy, vitreous opacity, renal failure, nephropathy, substantially reduced mBMI (modified body mass index), cranial nerve dysfunction, corneal lattice dystrophy, echocardiographic evaluation left ventricular (LV) wall thickening by echocardiography, assessment of increased total longitudinal tension by echocardiography, increased N-terminal prohormone type B natriuretic peptide (NTproBNP), and hospitalization for cardiac events. Reduction of a disease includes slowing the disease process or reducing the severity of a late onset disease. "Dosage" may vary depending on the RNAi agent, the way the agent is administered, the degree of disease risk, medical history, age, weight, family history, genetic makeup, type of prior or concomitant treatment as the case may be, and other individual characteristics of the patient to be treated. can
“치료학적 유효량"은 또한 임의의 치료에 적용할 수 있는 합리적인 이득/위험 비율로 일부 목적하는 국소 또는 전신 효과를 생성하는 RNAi 제제의 양을 포함한다. 본 발명의 방법에 사용되는 RNAi 제제는 그러한 치료에 적용할 수 있는 합리적인 이득/위험 비율을 생성하기에 충분한 양으로 투여될 수 있다."Therapeutically effective amount" also includes an amount of an RNAi agent that produces some desired local or systemic effect at a reasonable benefit/risk ratio applicable to any treatment. The RNAi agent used in the methods of the present invention is such It can be administered in an amount sufficient to produce a reasonable benefit/risk ratio applicable to treatment.
본원에 사용된 "치료학적 유효량"이라는 문구는 또한 TTR 발현에 의해 매개되는 병리학적 과정 또는 병리학적 과정의 증상(들)의 치료, 예방 또는 관리에 이득을 제공하는 양을 포함한다. TTR 아밀로이드증의 증상은 감각 신경병증(예를 들어, 감각 이상, 말단 사지의 감각 이상), 자율 신경병증(예를 들어, 위궤양 또는 기립성 저혈압과 같은 위장 기능부전), 운동 신경병증, 발작, 치매, 척수병증, 다발신경병증, 수근관 증후군, 자율신경계 부전, 심근병증, 유리체 혼탁, 신부전, 신장병증, 실질적으로 감소된 mBMI(변형된 체질량 지수), 뇌신경 기능부전, 각막 격자 이영양증, 심장초음파 평가에 의한 좌심실(LV) 벽 비후, 심장초음파 평가에 의한 증가된 전체 종방향 긴장 증가 평가, 증가된 N-말단 프로호르몬 B형 나트륨이뇨 펩타이드(NTproBNP) 및 심장 사건으로 인한 입원을 포함한다. As used herein, the phrase “therapeutically effective amount” also includes an amount that provides benefit in the treatment, prevention, or management of a pathological process or symptom(s) of a pathological process mediated by TTR expression. Symptoms of TTR amyloidosis include sensory neuropathy (e.g. paresthesia, paresthesia of distal limbs), autonomic neuropathy (e.g. gastrointestinal dysfunction such as gastric ulcer or orthostatic hypotension), motor neuropathy, seizures, and dementia. , myelopathy, polyneuropathy, carpal tunnel syndrome, autonomic dysfunction, cardiomyopathy, vitreous opacity, renal failure, nephropathy, substantially reduced mBMI (modified body mass index), cranial nerve dysfunction, corneal lattice dystrophy, by echocardiographic evaluation Left ventricular (LV) wall thickening, assessment of increased total longitudinal tension by echocardiographic evaluation, increased N-terminal prohormone type B natriuretic peptide (NTproBNP), and hospitalization for cardiac events.
하나의 구현예에서, 예를 들어, 대상체가 FAP, 혼합 표현형을 갖는 FAP, 혼합 표현형을 갖는 FAC, 또는 FAP를 갖고 OLT를 갖는 경우, 본 발명의 dsRNA 제제를 사용한 대상체의 치료는 신경병증의 진행을 서행시킨다. 또 다른 구현예에서, 예를 들어, 대상체가 FAP, 혼합 표현형을 갖는 FAP, 혼합 표현형을 갖는 FAC, 또는 FAP를 갖고 OLT를 갖는 경우, 본 발명의 dsRNA 제제를 사용한 대상체의 치료는 신경병증 및 심근병증의 진행을 서행시킨다. 또 다른 구현예에서, 예를 들어, 대상체가 심장 침범을 갖는 경우, 본 발명의 방법은 심장 구조 및 기능을 개선하고, 예를 들어, 상기 방법은 평균 좌심실 벽 두께 및 종방향 긴장을 감소시키고 심장 스트레스 바이오마커, N-말단 프로 b-형 나트륨이뇨 펩타이드(NT-proBNP)의 발현 수준을 감소시킨다.In one embodiment, treatment of a subject with a dsRNA agent of the present invention prevents progression of neuropathy, e.g., if the subject has FAP, FAP with a mixed phenotype, FAC with a mixed phenotype, or FAP and has an OLT. slow down In another embodiment, treatment of a subject with a dsRNA agent of the present invention may treat neuropathy and myocardial slow the progression of the disease. In another embodiment, eg, where the subject has cardiac involvement, the methods of the present invention improve cardiac structure and function, eg, the method reduces mean left ventricular wall thickness and longitudinal strain and reduces cardiac Reduces the expression level of the stress biomarker, N-terminal pro b-type natriuretic peptide (NT-proBNP).
치료학적 또는 예방학적 유효량의 본 발명의 RNAi 제제의 투여는 또한 TTR 관련 질환을 앓고 있거나 발병할 위험이 있는 대상체에서 신경학적 손상 또는 삶의 질에 대한 적어도 하나의 지표를 개선시키는 방법에 유용하다. Administration of a therapeutically or prophylactically effective amount of an RNAi agent of the invention is also useful in methods of improving at least one indicator of neurological impairment or quality of life in a subject suffering from or at risk of developing a TTR-related disease.
예를 들어, 하나의 구현예에서, 본 발명의 방법은 적어도 대상체에서 신경학적 손상의 지표를 개선시킨다. 대상체에서 "신경학적 손상의 적어도 하나의 지표를 개선하는 것"은 신경학적 손상을 서행시키거나, 감소시키거나 정지시키거나, 신경학적 손상과 관련된 임의의 증상을 개선하는 본 발명의 방법의 능력을 지칭한다. 신경계 손상의 임의의 적절한 척도를 사용하여 대상체가 신경계 손상, 또는 신경계 손상과 관련된 증상의 개선을 감소, 서행 또는 정지시켰는지의 여부를 결정할 수 있다. For example, in one embodiment, a method of the invention improves an indicator of neurological impairment in at least a subject. "Improving at least one indicator of neurological impairment" in a subject refers to the ability of a method of the present invention to slow, reduce or halt neurological impairment, or ameliorate any symptoms associated with neurological impairment. refers to Any suitable measure of nervous system damage can be used to determine whether a subject has reduced, slowed, or halted improvement in nervous system damage, or symptoms associated with nervous system damage.
하나의 적합한 척도는 신경병증 손상 스코어(NIS)이다. NIS는 특히 말초 신경병증과 관련하여 쇠약, 감각 및 반사를 측정하는 스코어링 시스템을 지칭한다. NIS 스코어는 쇠약에 대한 근육의 표준 그룹(1은 25% 쇠약, 2는 50% 쇠약, 3은 75% 쇠약, 3.25는 중력에 대항하는 움직임, 3.5는 제거된 중력과 함께 움직임, 3.75는 움직임이 없는 근육 깜박임, 및 4는 마비됨), 근육 스트레치 반사의 표준 그룹(0은 정상, 1은 감소, 2는 부재), 터치 압력, 진동, 관절 위치 및 운동, 핀프릭(모두 검지 및 엄지 발가락으로 등급이 매겨짐: 0은 정상, 1은 감소, 2는 부재)을 평가한다. 평가는 연령, 성별 및 체력에 대해 보정된다. One suitable measure is the Neuropathic Impairment Score (NIS). NIS refers to a scoring system that measures weakness, sensation, and reflexes, particularly in relation to peripheral neuropathy. The NIS score is the standard group of muscles for weakness (1 = 25% weakness, 2 = 50% weakness, 3 = 75% weakness, 3.25 is movement against gravity, 3.5 is movement with gravity removed, 3.75 is no movement). no muscle blink, and 4 paralyzed), standard group of muscle stretch reflexes (0 normal, 1 reduced, 2 absent), touch pressure, vibration, joint position and movement, pin prick (all with index and big toe) Graded: 0 normal, 1 reduced, 2 absent). Assessments are corrected for age, sex and fitness.
하나의 구현예에서, 본 발명의 방법은 투여 시작으로부터 18개월에 NIS를 적어도 5점까지 감소시킨다. 다른 구현예에서, 본 발명의 방법은 본원에 제공된 RNAi 제제로 치료를 개시한 지 18개월째에 NIS를 안정화시킨다. 다른 구현예에서, 방법은 질환의 자연력을 나타내는 적절한 대조군 그룹, 예를 들어 문헌 [참조: Adams et al., N Engl J Med 2018;379]에 제공된 바와 같은 위약 대조군 그룹과 비교하여 증가하는 NIS 스코어를 서행시킨다. 질병 진행 속도는 치료 개시 시 대상체의 질병 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.In one embodiment, the methods of the invention reduce NIS by at least 5 points at 18 months from start of dosing. In another embodiment, the methods of the invention stabilize NIS at 18 months of initiation of treatment with an RNAi agent provided herein. In another embodiment, the method increases NIS scores compared to an appropriate control group indicative of a natural history of disease, eg, a placebo control group as provided in Adams et al., N Engl J Med 2018;379. slow down The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
사람 대상체에서 NIS를 결정하기 위한 방법은 당업자에게 널리 공지되어 있고, 예를 들어, 문헌(참조: Dyck, PJ et al.,(1997) Neurology 1997. 49(1):pgs.229-239);Dyck PJ.(1988) Muscle Nerve. Jan;ll(l):21-32)에 찾을 수 있다.Methods for determining NIS in human subjects are well known to those skilled in the art and are described, for example, in Dyck, PJ et al . , (1997) Neurology 1997. 49(1): pgs.229-239; Dyck PJ. (1988) Muscle Nerve. Jan;ll(l):21-32).
신경학적 손상의 또 다른 적합한 측정은 변형된 신경병증 손상 스코어(mNIS+7)이다. 당업자에게 공지된 바와 같이, mNIS+7은 작고 큰 신경 섬유 기능(NCS 및 QST)의 전기생리학적 측정 및 자율 기능 측정(체위 혈압)과 조합된 신경학적 손상(NIS)의 임상 시험 기반 평가를 지칭한다. mNIS+7 스코어는 NIS+7 스코어(NIS + 7개 시험을 나타냄)의 변형이다. NIS+7은 쇠약 및 근육 스트레치 반사를 분석한다. 7개 시험 중 5개는 신경 전도 특성을 포함한다. 이들 특성은 비골 신경 복합 근육 활동 전위 진폭, 운동 신경 전도 속도 및 운동 신경 원위 잠복기(MNDL), 경골 MNDL 및 비복 감각 신경 활동 전위 진폭이다. 이들 값은 연령, 성별, 키 및 체중의 변수에 대해 보정된다. 7개 시험 중 나머지 2개는 진동 검출 임계값과 심호흡에 따른 심박수 감소를 포함한다. Another suitable measure of neurological impairment is the modified neuropathic impairment score (mNIS+7). As known to those skilled in the art, mNIS+7 refers to a clinical trial-based assessment of neurological impairment (NIS) combined with electrophysiological measures of small and large nerve fiber function (NCS and QST) and measures of autonomic function (postural blood pressure). do. The mNIS+7 score is a variant of the NIS+7 score (representing NIS+7 tests). NIS+7 analyzes weakness and muscle stretch reflexes. Five of the seven tests involved nerve conduction properties. These characteristics are peroneal nerve complex muscle action potential amplitude, motor nerve conduction velocity and motor nerve distal latency (MNDL), tibial MNDL and splenic sensory nerve action potential amplitudes. These values are corrected for the variables of age, sex, height and weight. The other two of the seven trials involved vibration detection thresholds and heart rate reduction following deep breathing.
mNIS+7 스코어는 NIS+7을 변형하여 스마트 체성감각 정량적 감지 시험(Smart Somatotopic Quantitative Sensation Testing), 새로운 자율 평가의 사용, 척골 신경, 비골 신경 및 경골 신경의 진폭의 복합 근육 활동 전위 및 척골 신경 및 비복 신경의 감각 신경 활동 전위의 사용을 고려한다 (문헌참조: Suanprasert, N. et al.,(2014)J.Neurol.Sci., 344(1-2): pgs. 121-128). The mNIS+7 score is a modification of the NIS+7 using the Smart Somatotopic Quantitative Sensation Testing, the use of novel autonomic assessments, compound muscle action potentials of the amplitudes of the ulnar, peroneal and tibial nerves and ulnar and ulnar nerves. Consider using sensory nerve action potentials of the splenic nerve (see Suanprasert, N. et al . , (2014) J. Neurol. Sci ., 344(1-2): pgs. 121-128).
하나의 구현예에서, 본 발명의 방법은 투여 시작으로부터 18개월에 mNIS+7을 적어도 5점까지 감소시킨다. 다른 구현예에서, 본 발명의 방법은 본원에 제공된 RNAi 제제로 치료를 개시한 지 18개월째에 mNIS+7을 안정화시킨다. 다른 구현예에서, 방법은 질환의 자연력을 나타내는 적절한 대조군 그룹, 예를 들어 문헌 [참조: Adams et al., N Engl J Med 2018;379]에 제공된 바와 같은 위약 대조군 그룹과 비교하여 증가하는 mNIS+7 스코어를 서행시킨다. 질병 진행 속도는 치료 개시 시 대상체의 질병 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.In one embodiment, the methods of the invention reduce mNIS+7 by at least 5 points at 18 months from start of dosing. In another embodiment, the methods of the invention stabilize mNIS+7 at 18 months after initiation of treatment with an RNAi agent provided herein. In another embodiment, the method comprises an increase in mNIS+ compared to a suitable control group indicative of a natural history of the disease, eg, a placebo control group as provided in Adams et al., N Engl J Med 2018;379. 7 Slow down the score. The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
또 다른 구현에에서, 본 발명의 방법은 적어도 대상체에서 삶의 질의 적어도 하나의 지표를 개선시킨다. 대상체에서 “삶의 질의 적어도 하나의 지표를 개선하는“은 삶의 질 악화를 서행시키거나 정지시키거나 삶의 질을 개선시키는 본 발명의 방법의 능력을 지칭한다. 삶의 질의 임의의 적합한 측정은 대상체가 서행되거나 정지된 삶의 질 악화 또는 개선된 삶의 질을 갖는지의 여부를 결정하는 데 사용될 수 있다.In another embodiment, the methods of the present invention improve at least one indicator of quality of life in at least a subject. “Improving at least one indicator of quality of life” in a subject refers to the ability of a method of the present invention to slow or halt deterioration in quality of life or improve quality of life. Any suitable measure of quality of life can be used to determine whether a subject has a slow or stationary deterioration in quality of life or an improved quality of life.
예를 들어, SF-36®건강 조사는 신체 기능, 신체 건강 문제로 인한 역할 제한, 신체 통증, 일반적인 건강, 활력(에너지 및 피로), 사회적인 기능, 정서적 문제로 인한 역할 제한, 및 정신 건강 (심리적 고통 및 심리적 안녕)의 8개 건강 파라미터를 측정하는 자가 보고 다수 항목 스케일을 제공한다. 각각의 스케일은 각 질문이 동일한 가중치를 갖는다는 가정 하에 0-100 스케일로 직접 변환된다. 스코어가 낮을 수록 기능장애가 많다. 스코어가 높을수록 기능장애가 적은 것이고, 즉, 제로 스코어는 최대 기능장애에 해당하고 100의 스코어는 기능장애가 없는 것과 동일하다. 설문 조사는 또한 물리적 구성 요소 요약 및 정신적 구성 요소 요약을 제공한다. For example, the SF-36® Health Survey covers physical functioning, role limitations due to physical health problems, body pain, general health, vitality (energy and fatigue), social functioning, role limitations due to emotional problems, and mental health (psychological It provides a self-reported multi-item scale that measures eight health parameters (e.g., pain and psychological well-being). Each scale is directly converted to a 0-100 scale under the assumption that each question has equal weight. The lower the score, the more dysfunction. Higher scores indicate less dysfunction, i.e., a score of zero corresponds to maximum dysfunction and a score of 100 equates to no dysfunction. The survey also provides a physical component summary and a mental component summary.
하나의 구현예에서, 본 발명의 방법은 대상체에게 SF-36 신체 건강 관련 파라미터(신체 건강, 역할-신체적, 신체 통증 또는 일반 건강) 중 적어도 하나 또는 SF-36 정신 건강 관련 매개변수(활력, 사회적 기능, 역할-정서적 또는 정신 건강)의 적어도 하나에서 기준선 대비 개선을 제공한다. 상기 개선은 투여 시작으로부터 9개월째에 임의의 하나 이상의 파라미터에 대한 스케일에서, 예를 들어 적어도 2 또는 적어도 3점의 증가의 형태를 취할 수 있다.In one embodiment, the methods of the present invention provide a subject with at least one of the SF-36 physical health related parameters (physical health, role-physical, body pain or general health) or the SF-36 mental health related parameters (vitality, social function, role-emotional or mental health). The improvement may take the form of, for example, an increase of at least 2 or at least 3 points on a scale for any one or more parameters at 9 months from start of dosing.
다른 구현예에서, 본 발명의 방법은 임의의 하나 이상의 파라미터에 대한 투여 시작으로부터 9개월째에 감소하는 SF-36 파라미터 스코어를 정지시키고, 예를 들어, 상기 방법은 예를 들어, SF-36 평가를 수행하는 개체에 대해 관찰된 변동 내에서 SF-36의 임상적으로 유의적인 변화를 유도하지 않는다. 또 다른 구현예에서, 본 발명의 방법은 투여 개시로부터 9개월째에 SF-36 스코어가 감소하는 속도, 질환의 자연력을 보여주는 적당한 대조군 그룹, 예를 들어, 문헌 (참조: Adams et al., N Engl J Med 2018;379:11-21)에 제공된 바와 같은 위약 대조군 그룹과 비교하여 SF-36 스코어의 감소 속도에 비해 본 발명의 RNAi 제제로 처리된 대상체에서 SF-36 스코어의 감소 속도를 서행시킨다. 질병 진행 속도는 치료 개시 시 대상체의 질병 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.In another embodiment, the method of the present invention stops a decreasing SF-36 parameter score at 9 months from the start of dosing for any one or more parameters, e.g., the method comprises an SF-36 assessment does not induce clinically significant changes in SF-36 within the variability observed for individuals performing In another embodiment, the method of the present invention is directed to a suitable control group showing the rate of decline in the SF-36 score at 9 months from the start of administration, a natural history of the disease, e.g., as described in Adams et al., N Engl J Med 2018;379:11-21) slows the rate of decrease in SF-36 score in subjects treated with an RNAi agent of the invention compared to the rate of decrease in SF-36 score compared to a placebo control group . The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
삶의 질에 대한 또 다른 적합한 측정은 Norfolk 삶의 질-당뇨병성 신경병증(Norfolk QOL-DN) 설문지이다. Norfolk QOL-DN은 기존 도구에서 포착되지 않은 대형 섬유, 소형 섬유 및 자율 신경병증과 관련된 DN의 전체 스펙트럼을 포착하도록 디자인된 검증된 종합 설문지이다. Another suitable measure of quality of life is the Norfolk Quality of Life-Diabetic Neuropathy (Norfolk QOL-DN) questionnaire. The Norfolk QOL-DN is a validated comprehensive questionnaire designed to capture the full spectrum of DN associated with large fibers, small fibers and autonomic neuropathy not captured by existing tools.
하나의 구현예에서, 본 발명의 방법은 기준선으로부터 대상체의 Norfolk QOL-DN 스코어, 예를 들어 본원에 제공된 RNAi 제제를 사용한 치료 개시로부터 9개월째에 약 -2.5, -3.0, -3.5, -4.0, -4.5, 또는 -5.0의 변화를 개선한다. 다른 구현예에서, 방법은 증가하는 Norfolk QOL-DN 스코어를 정지시키고, 예를 들어, 방법은 예를 들어 QOL-DN 평가를 수행하는 개체 간에 관찰된 변동 내에서 Norfolk QOL-DN 스코어의 임상적으로 유의적인 변화를 초래하지 않는다. 또 다른 구현예에서, 본 발명의 방법은 QOL-DN 스코어가 증가하는 속도, 예를 들어 질환의 자연력을 보여주는 적당한 대조군 그룹, 예를 들어, 문헌 (참조: Adams et al., N Engl J Med 2018;379:11-21)에 제공된 바와 같은 위약 대조군 그룹과 비교하여 QOL-DN 스코어의 증가 속도에 비해 본 발명의 RNAi 제제로 처리된 대상체에서 QOL-DN 스코어의 증가 속도를 서행시킨다. 질병 진행 속도는 치료 개시 시 대상체의 질병 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.In one embodiment, the methods of the invention measure the subject's Norfolk QOL-DN score from baseline, e.g., about -2.5, -3.0, -3.5, -4.0 at 9 months from initiation of treatment with an RNAi agent provided herein. , -4.5, or -5.0 changes. In another embodiment, the method halts an increasing Norfolk QOL-DN score, eg, the method clinically monitors the Norfolk QOL-DN score within observed variability among individuals performing the QOL-DN assessment. does not cause significant change. In another embodiment, the methods of the present invention can be performed on a suitable control group showing the rate at which the QOL-DN score increases, eg, a natural history of the disease, eg, Adams et al., N Engl J Med 2018 ;379:11-21) slows the rate of increase in QOL-DN scores in subjects treated with the RNAi agents of the present invention relative to the rate of increase in QOL-DN scores compared to a placebo control group. The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
삶의 질에 대한 또 다른 적합한 측정은 예를 들어 NIS-W 스코어에 의한 평가시 운동 강도이다. NIS-W 스코어는 머리, 몸통 및 사지 근육의 쇠약을 합산한 종합 스코어이다. NIS(W)(쇠약을 측정하는 스케일의 부분 참조)를 사용하여 근력은 중간 등급과 함께 정상(0) 또는 완전 마비(4)로 평가되고; 1은 임상 강도 시험에서 25% 쇠약한 것으로 간주되는 근육을 나타내고, 2는 50%, 3은 75%, 3.25는 중력에 대항하는 움직임, 3.50은 제거된 중력과 함께 움직임, 3.75는 근육 깜박임이다.Another suitable measure of quality of life is exercise intensity, as assessed, for example, by the NIS-W score. The NIS-W score is a composite score summing the weakness of the muscles of the head, trunk and extremities. Using the NIS(W) (see the part of the scale that measures weakness) strength is rated as normal (0) or completely paralyzed (4) with a moderate rating; 1 represents muscles considered 25% weak in the clinical strength test, 2 is 50%, 3 is 75%, 3.25 is movement against gravity, 3.50 is movement with gravity removed, and 3.75 is muscle blink.
하나의 구현예에서, 본 발명의 방법은 NIS-W 스코어에서 기준선 대비 개선을 대상체에게 제공한다. 이러한 개선은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 대상체의 NIS-W 스코어의 적어도 5, 6, 7, 8, 9 또는 10점의 감소 형태를 취할 수 있다. 다른 구현예에서, 방법은 NIS-W 스코어의 감소를 정지시키고, 예를 들어, 상기 방법은 질환의 자연력을 보여주는 적당한 대조군 그룹, 예를 들어, 문헌 (참조: Adams et al., N Engl J Med 2018;379:11-21)에 제공된 바와 같은 위약 대조군 그룹과 비교하여 NIS-W 스코어의 임상적으로 유의적인 증가를 유도하지 않거나 NIS-W 스코어의 증가 속도의 서행을 유도하지 않는다. 질병 진행 속도는 치료 개시 시 대상체의 질병 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.In one embodiment, the methods of the invention provide a subject with an improvement from baseline in NIS-W score. Such improvement may take the form of a reduction of at least 5, 6, 7, 8, 9 or 10 points in the subject's NIS-W score at 18 months of initiation of treatment with an RNAi agent provided herein. In another embodiment, the method halts the decrease in NIS-W score, eg, the method can be performed on a suitable control group showing natural history of the disease, eg, as described in Adams et al., N Engl J Med. 2018;379:11-21) does not induce a clinically significant increase in NIS-W score or a slowdown in the rate of increase in NIS-W score compared to a placebo control group. The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
삶의 질에 대한 또 다른 적절한 지표는 라쉬(Rasch)가 구축한 전체 기능장애 스케일(R-ODS)로, 이는 환자의 활동 및 사회 참여 제한을 포착하도록 디자인된 환자 설문지이다. 하나의 구현예에서, 본 발명의 방법은 R-ODS 스코어에서 기준선 대비 개선을 대상체에게 제공한다. 이러한 개선은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 대상체의 R-ODS 스코어의 적어도 2, 예를 들어, 적어도 2, 3, 4 또는 5점의 증가 형태를 취할 수 있다. 다른 구현예에서, 방법은 감소하는 R-ODS 스코어를 정지시키고, 예를 들어 방법은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 R-ODS 점수의 임상적으로 유의한 감소를 초래하지 않는다. 또 다른 구현예에서, 본 발명의 방법은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월째에 R-ODS 스코어가 감소하는 속도, 예를 들어, 질환의 자연력을 보여주는 적당한 대조군 그룹, 예를 들어, 문헌 (참조: Adams et al., N Engl J Med 2018;379:11-21)에 제공된 바와 같은 위약 대조군 그룹과 비교하여 R-ODS 스코어의 감소 속도에 비해 본 발명의 RNAi 제제로 처리된 대상체에서 R-ODS 스코어의 감소 속도를 서행시킨다. 질병 진행 속도는 치료 개시 시 대상체의 질병 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.Another relevant indicator of quality of life is the Overall Dysfunction Scale (R-ODS) constructed by Rasch, which is a patient questionnaire designed to capture the patient's activity and social participation limitations. In one embodiment, the methods of the invention provide a subject with an improvement from baseline in R-ODS score. Such improvement may take the form of an increase of at least 2, eg, at least 2, 3, 4 or 5 points in the subject's R-ODS score at 18 months of initiation of treatment with an RNAi agent provided herein. In another embodiment, the method stops a decreasing R-ODS score, e.g., the method does not result in a clinically significant decrease in R-ODS score at 18 months of initiation of treatment with an RNAi agent provided herein. don't In another embodiment, the method of the invention is performed on a suitable control group, e.g., showing the rate at which the R-ODS score declines, e.g., a natural history of the disease, at 18 months of initiation of treatment with an RNAi agent provided herein. For example, as provided in the literature (Adams et al., N Engl J Med 2018;379:11-21) compared to the rate of decrease in R-ODS scores compared to a placebo control group treated with an RNAi agent of the present invention Slow the rate of decline in the R-ODS score in the subject. The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
0에서 100까지의 증상 스코어를 제공하는 자율신경실조증의 증상을 평가하는 환자 설문지인 복합 자율신경계 증상 스코어(COMPASS-31)는 삶의 질에 대한 또 다른 적합한 지표이다. 하나의 구현예에서, 본 발명의 방법은 COMPASS-31 스코어에서 기준선 대비 개선을 대상체에게 제공한다. 이러한 개선은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 대상체의 COMPASS-31 스코어의 적어도 5, 예를 들어, 적어도 5, 6, 7, 8, 9 또는 10점의 증가 형태를 취할 수 있다. 다른 구현예에서, 방법은 감소하는 COMPASS-31 스코어를 정지시키고, 예를 들어 방법은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 COMPASS-31 스코어의 임상적으로 관련된 변화를 초래하지 않는다. 또 다른 구현예에서, 본 발명의 방법은 COMPASS-31 스코어가 감소하는 속도, 예를 들어 질환의 자연력을 보여주는 적당한 대조군 그룹, 예를 들어, 문헌 (참조: Adams et al., N Engl J Med 2018;379:11-21)에 제공된 바와 같은 위약 대조군 그룹과 비교하여 COMPASS-31 스코어의 감소 속도에 비해 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 COMPSS-31 스코어의 감소 속도를 서행시킨다. 질환 진행 속도는 치료 개시 시 대상체의 질환 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.The Composite Autonomic Symptom Score (COMPASS-31), a patient questionnaire assessing symptoms of dysautonomia providing a symptom score from 0 to 100, is another suitable indicator of quality of life. In one embodiment, the methods of the invention provide a subject with an improvement from baseline in a COMPASS-31 score. Such improvement may take the form of an increase in the subject's COMPASS-31 score of at least 5, eg, at least 5, 6, 7, 8, 9 or 10 points, at 18 months of initiation of treatment with an RNAi agent provided herein. have. In another embodiment, the method stops a decreasing COMPASS-31 score, eg, the method does not result in a clinically relevant change in the COMPASS-31 score at 18 months of initiation of treatment with an RNAi agent provided herein. . In another embodiment, the method of the present invention can be performed on a suitable control group showing the rate at which the COMPASS-31 score decreases, eg, a natural history of the disease, such as Adams et al., N Engl J Med 2018 ;379:11-21) slows the rate of decrease in COMPSS-31 score at 18 months of initiation of treatment with an RNAi agent provided herein compared to the rate of decrease in COMPASS-31 score compared to a placebo control group . The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
다른 삶의 질 지표는 예를 들어, 메디안 체질량 지수 (mBMI)에서 변화에 의해 평가된 바와 같이 영양 상태를 포함할 수 있다. 하나의 구현예에서, 본 발명의 방법은 mBMI에서 기준선 대비 개선을 대상체에게 제공한다. 상기 개선은 본원에 제공된 RNAi 제제를 사용한 치료 개시한지 18개월에 적어도 2, 3, 4, 5 이상의 mBMI 스코어 증가 형태를 취할 수 있다. 다른 구현예에서, 방법은 감소하는 mBMI 지수 스코어를 정지시키고, 예를 들어 방법은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 mBMI 스코어의 임상적으로 유의적인 변화를 초래하지 않는다. 또 다른 구현예에서, 본 발명의 방법은 mBMI 스코어가 감소하는 속도, 예를 들어 질환의 자연력을 보여주는 적당한 대조군 그룹, 예를 들어, 문헌 (참조: Adams et al., N Engl J Med 2018;379:11-21)에 제공된 바와 같은 위약 대조군 그룹과 비교하여 대상체에서 mBMI 스코어의 감소 속도에 비해 본 발명의 RNAi 제제로 처리된 대상체에서 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 mBMI 스코어의 감소 속도를 서행시킨다. 질환 진행 속도는 치료 개시 시 대상체의 질환 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.Other quality-of-life indicators may include nutritional status as assessed, for example, by change in median body mass index (mBMI). In one embodiment, the methods of the invention provide a subject with an improvement from baseline in mBMI. Such improvement may take the form of an increase in mBMI score of at least 2, 3, 4, 5 or more at 18 months of initiation of treatment with an RNAi agent provided herein. In another embodiment, the method stops a decreasing mBMI index score, eg, the method does not result in a clinically significant change in mBMI score at 18 months of initiation of treatment with an RNAi agent provided herein. In another embodiment, the method of the present invention is performed on a suitable control group showing the rate at which the mBMI score decreases, eg, the natural history of the disease, eg, Adams et al., N Engl J Med 2018;379 : 11-21) mBMI score at 18 months of initiation of treatment with an RNAi agent provided herein in subjects treated with an RNAi agent of the present invention relative to the rate of decrease in mBMI score in subjects compared to a placebo control group as provided in 11-21). slow down the rate of decrease of The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
또 다른 삶의 질 지표는 운동 능력 평가를 포함한다. 운동 능력의 한 가지 적합한 측정은 6분 걷기 시험(6MWT)이고, 이는 대상체가 6분 동안 얼마나 멀리 걸을 수 있는지, 즉 6분 도보 거리(6MWD)를 측정한다. 하나의 구현예에서, 본 발명의 방법은 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 6MWD에서 기준선으로부터 적어도 10미터, 예를 들어, 적어도 10, 15, 20, 또는 약 30미터 증가를 대상체에게 제공한다. Another quality-of-life indicator includes assessment of exercise capacity. One suitable measure of exercise capacity is the 6-minute walking test (6MWT), which measures how far a subject can walk in 6 minutes, ie the 6-minute walking distance (6MWD). In one embodiment, the methods of the invention achieve an increase from baseline of at least 10 meters, e.g., at least 10, 15, 20, or about 30 meters, at 6MWD at 18 months of initiation of treatment with an RNAi agent provided herein. provided to the subject.
또 다른 적합한 측정은 보행 속도를 측정하는 10미터 걷기 시험이다. 하나의 구현예에서, 본 발명의 방법은 10미터 걷기 시험에서 본원에 제공된 RNAi 제제를 사용한 치료를 개시한지 18개월에 기준선으로부터 적어도 0.025미터/초, 예를 들어, 적어도 0.025, 0.03, 0.04, 0.05, 0.06, 0.07, 0.08, 0.09, 1.0, 1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5 또는 약 5.0 미터/초로의 증가를 제공한다.Another suitable measurement is the 10-meter walk test, which measures walking speed. In one embodiment, a method of the invention measures at least 0.025 meters/second from baseline, e.g., at least 0.025, 0.03, 0.04, 0.05 , 0.06, 0.07, 0.08, 0.09, 1.0, 1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, or about 5.0 meters/sec.
일부 구현예에서, 혈장 바이오마커 수준의 변화는 ATTR 아밀로이드증에서 진행 중인 신경 손상 또는 다발신경병증의 진행의 감소의 지표이다. 예를 들어, 치료 시작 시 NfL 수준과 비교하여 9개월째 신경필라멘트 경쇄(NfL) 수준의 감소는 ATTR 아밀로이드증에서 진행 중인 신경 손상 또는 다발신경병증 진행의 감소의 지표일 수 있다. 특정 구현예에서, 다른 단백질, 특히 RSPO3, CCDC80, EDA2R 및 NT-proBNP의 수준의 감소는 단독으로 또는 치료 시작 시에 이의 상응하는 수준과 비교하여 치료 시작으로부터 9개월째에 NfL 수준의 감소와 조합하여 ATTR 아밀로이드증에서 진행 중인 신경 손상의 감소 또는 다발신경병증의 진행의 감소의 지표일 수 있다. 특정 구현예에서, 치료 시작 시의 상응하는 수준과 비교하여 치료 시작으로부터 9개월째에 단독으로 또는 상기 열거된 다른 마커와 조합하여 N-CDase 수준의 증가는 ATTR 아밀로이드증에서 진행 중인 신경 손상 또는 다발신경병증의 진행의 감소의 지표일 수 있다. 예를 들어 본원에서 제공되는 RNAi 제제를 사용한 치료 개시로부터 9개월째에서와 같이 ATTR 아밀로이드증에서 신경 손상 또는 다발신경병증의 감소의 지표로 작용할 수 있는 추가 바이오마커는 표 1에 제공된다. ATTR 아밀로이드증에서 진행 중인 신경 손상 또는 다발신경병증의 진행의 감소는 양의 베타 계수를 갖는 단백질의 감소와 상관관계가 있다. ATTR 아밀로이드증에서 진행 중인 신경 손상 또는 다발신경병증의 진행의 감소는 음의 베타 계수를 갖는 단백질의 증가와 상관관계가 있다. 바이오마커 수준의 변화는 통계적으로 유의적인 변화, 즉 검정의 고유한 변동성보다 큰 변화인 것으로 이해된다. In some embodiments, changes in plasma biomarker levels are indicative of ongoing nerve damage in ATTR amyloidosis or reduction in progression of polyneuropathy. For example, a decrease in neurofilament light chain (NfL) levels at 9 months compared to NfL levels at the start of treatment may be indicative of a reduction in ongoing nerve damage or polyneuropathy progression in ATTR amyloidosis. In certain embodiments, a decrease in the level of other proteins, particularly RSPO3, CCDC80, EDA2R and NT-proBNP, alone or in combination with a decrease in NfL levels at 9 months from the start of treatment compared to their corresponding levels at the start of treatment Thus, it may be an indicator of a reduction in ongoing nerve damage in ATTR amyloidosis or a reduction in the progression of polyneuropathy. In certain embodiments, an increase in N-CDase level, alone or in combination with the other markers listed above, at 9 months from the start of treatment compared to the corresponding level at the start of treatment is an increase in ongoing nerve damage or polyneuropathy in ATTR amyloidosis. It may be an indicator of a decrease in the progression of the condition. Additional biomarkers that can serve as indicators of reduction in nerve damage or polyneuropathy in ATTR amyloidosis, such as, for example, at 9 months from initiation of treatment with an RNAi agent provided herein, are provided in Table 1. Decreased progression of ongoing nerve damage or polyneuropathy in ATTR amyloidosis correlates with a decrease in proteins with positive beta coefficients. Decreased progression of ongoing nerve damage or polyneuropathy in ATTR amyloidosis correlates with increases in proteins with negative beta coefficients. Changes in biomarker levels are understood to be statistically significant changes, i.e., changes greater than the inherent variability of the test.
특정 구현예에서, 본 발명의 방법은 심혈관 지표의 개선, 예를 들어 캔자스시티 심근병증 설문지 전체 요약(KCCQ-OS)의 증가, 기준선과 비교하여 심장초음파 평가에 의한 좌심실(LV) 벽 비후 감소, 기준선과 비교하여 심장초음파 평가에 의한 감소된 전체적인 종방향 긴장, 기준선과 비교하여 N-말단 프로호르몬 B형 나트륨이뇨 펩타이드(NTproBNP) 감소, 및 심장 사건으로 인한 입원 감소를 제공한다.In certain embodiments, the methods of the present invention provide an improvement in a cardiovascular parameter, e.g., an increase in the Kansas City Cardiomyopathy Questionnaire Overall Summary (KCCQ-OS), a decrease in left ventricular (LV) wall thickening by echocardiographic evaluation compared to baseline, Reduced global longitudinal tension by echocardiographic assessment compared to baseline, decreased N-terminal prohormone type B natriuretic peptide (NTproBNP) compared to baseline, and reduced hospitalizations due to cardiac events.
본 발명의 방법은 또한 치료되는 대상체의 예후를 개선할 수 있다. 예를 들어, 본 발명의 방법은 질환의 자연력을 보여주는 적당한 대조군 그룹, 예를 들어, 문헌 (참조: Adams et al., N Engl J Med 2018;379:11-21)에 제공된 바와 같은 위약 대조군 그룹과 비교하여 치료 기간 동안에 임상적 악화 사건의 가능성의 감소 또는 감소된 병원입원을 대상체에 제공한다. 특정 구현예에서, 치료 동안에 임상적 악화 사건의 가능성의 감소는 예를 들어, 문헌 (참조: Maurer et al., N Engl J Med 2018:379:11-21)에 제공된 적당한 대조군 그룹과 비교하여, 예를 들어, 핑켈슈타인-쇼엔펠트 방법(Finkelstein-Schoenfeld method)에 따른 평가시 모든 원인의 사망률 또는 심혈관 관련 병원입원의 감소를 포함할 수 있다. 질환 진행 속도는 치료 개시 시 대상체의 질환 중증도, 치료 기간, 이전 치료 및 경우에 따라 존재하는 특정 TTR 돌연변이를 포함하지만 이에 제한되지 않는 다수의 인자에 의존한다.The methods of the present invention may also improve the prognosis of the subject being treated. For example, the methods of the present invention can be performed using a suitable control group showing a natural history of the disease, such as a placebo control group as provided in the literature (Adams et al., N Engl J Med 2018;379:11-21). Provides the subject with a reduced likelihood of a clinically deteriorating event or reduced hospital admission during the treatment period compared to In certain embodiments, a reduction in the likelihood of a clinically deteriorating event during treatment is compared to an appropriate control group, eg, provided in the literature (Maurer et al., N Engl J Med 2018:379:11-21), For example, an assessment according to the Finkelstein-Schoenfeld method may include a reduction in all-cause mortality or cardiovascular-related hospitalizations. The rate of disease progression depends on a number of factors including, but not limited to, the severity of the subject's disease at initiation of treatment, the duration of treatment, previous treatment, and the specific TTR mutation present, if any.
대상체에게 투여되는 RNAi 제제의 용량은 예를 들어, TTR 유전자 발현의 목적하는 수준의 억제(예를 들어, TTR mRNA 발현, TTR 단백질 발현, 또는 상기 정의된 바와 같은 아밀로이드 침착물의 감소에 기초하여 평가된 바와 같이) 또는 목적하는 치료학적 효과를 달성하고, 이와 동시에 바람직하지 않은 부작용을 피하기 위해 특정 용량의 위험과 이득의 균형을 이루도록 조정될 수 있다.The dose of an RNAi agent administered to a subject is, for example, a desired level of inhibition of TTR gene expression (e.g., TTR mRNA expression, TTR protein expression, or a reduction in amyloid deposits as defined above). as) or adjusted to balance the risks and benefits of a particular dose to achieve the desired therapeutic effect and at the same time avoid undesirable side effects.
하나의 구현예에서, 본 발명의 iRNA 제제가 "고정 용량"(예를 들어, mg 단위의 용량)으로서 대상체에게 투여된다는 것은 iRNA 제제의 1회 용량이 체중과 같은 임의의 특정 대상체-관련 인자에 관계없이 모든 대상체에 대해 사용됨을 의미한다. In one embodiment, administration of an iRNA agent of the invention to a subject as a “fixed dose” (eg, a dose in mg) means that a single dose of the iRNA agent is dependent on any particular subject-related factor, such as body weight. This means that it is used for all objects regardless of
일부 구현예에서, RNAi 제제는 약 25 mg 내지 약 1000 mg, 예를 들어, 약 25 mg, 약 50 mg, 약 100 mg, 약 200 mg, 약 300 mg, 약 400 mg, 약 500 mg, 약 600 mg, 약 700 mg, 약 800 mg, 약 900 mg, 또는 약 1000 mg의 고정 용량으로서 투여된다.In some embodiments, the RNAi agent is about 25 mg to about 1000 mg, e.g., about 25 mg, about 50 mg, about 100 mg, about 200 mg, about 300 mg, about 400 mg, about 500 mg, about 600 mg, about 700 mg, about 800 mg, about 900 mg, or about 1000 mg is administered as a fixed dose.
특정 구현예에서, 이중 가닥 RNAi 제제는 분기별 약 1회 내지 연간 약 1회로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 분기별 약 1회, 약 6개월마다 1회, 또는 연간 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject from about once per quarter to about once per year. In certain embodiments, the double-stranded RNAi agent is administered to a human subject about once per quarter, about once every 6 months, or about once per year.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 300 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 75 mg 내지 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 50 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 75 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 100 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 200 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 25 mg 내지 약 300 mg; 약 25 mg 내지 약 200 mg; 약 75 mg 내지 약 200 mg; 약 25 mg; 약 50 mg; 약 100 mg; 약 200mg; 또는 약 300 mg의 고정 용량으로 분기별 1회, 즉, 3개월 마다 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg to about 300 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg to about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 75 mg to about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 25 mg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 50 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 75 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 100 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 200 mg/kg. In certain embodiments, the double-stranded RNAi agent is about 25 mg to about 300 mg; about 25 mg to about 200 mg; about 75 mg to about 200 mg; about 25 mg; about 50 mg; about 100 mg; about 200 mg; or a fixed dose of about 300 mg is administered to a human subject once quarterly, ie, about once every 3 months.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 내지 약 600 mg/kg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 또는 약 600 mg의 고정 용량으로 6개월 마다 약 1회,내지 연간 약 1회 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 400 mg 또는 약 600 mg의 고정 용량으로 6개월마다 약 1회, 또는 연간 약 1회 사람 대상체에게 투여된다.In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg to about 600 mg/kg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg or about 600 mg about once every 6 months, to about once a year. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 400 mg or about 600 mg about once every 6 months, or about once a year.
특정 구현예에서, 이중 가닥 RNAi 제제는 약 700 mg 내지 약 1000 mg 또는 약 700 mg 내지 약 900 mg의 고정 용량으로 사람 대상체에게 투여된다. 특정 구현예에서, 이중 가닥 RNAi 제제는 약 700 mg, 약 800 mg, 약 900 mg 또는 약 1000 mg의 고정된 용량으로 연간 약 1회 사람 대상체에게 투여된다. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 700 mg to about 1000 mg or about 700 mg to about 900 mg. In certain embodiments, the double-stranded RNAi agent is administered to a human subject at a fixed dose of about 700 mg, about 800 mg, about 900 mg, or about 1000 mg about once per year.
특정 구현예에서, 투여는 피하 투여, 예를 들어 미리 충전된 주사기 또는 자동주사 주사기를 통한 자가 투여이다. 일부 구현예에서, 피하 투여를 위한 RNAi 제제의 용량은 예를 들어, 약제학적으로 허용되는 담체의 1 ml 이하의 용적에 함유된다. In certain embodiments, the administration is subcutaneous administration, eg, self-administration via a pre-filled syringe or autoinjector syringe. In some embodiments, a dose of an RNAi agent for subcutaneous administration is contained in a volume of eg, 1 ml or less of a pharmaceutically acceptable carrier.
이들 임의의 일정은 임의로 1회 이상 반복으로 반복될 수 있다. 반복 수는 목적하는 효과의 달성, 예를 들어, TTR 유전자의 억제, 레티놀 결합 단백질 수준, 비타민 A 수준 또는 치료 효과의 달성, 예를 들어, 아밀로이드 침착물 감소 또는 TTR 관련 질환의 증상 감소에 따라 다양할 수 있다. 특정 구현예에서, iRNA 제제는 무기한 기간 동안, 예를 들어 환자의 일생 동안 만성적으로 투여된다. Any of these schedules may optionally be repeated in one or more iterations. The number of repetitions varies depending on the achievement of a desired effect, eg, inhibition of the TTR gene, retinol binding protein levels, vitamin A levels, or achievement of a therapeutic effect, eg, reduction of amyloid deposits or reduction of symptoms of a TTR-related disease. can do. In certain embodiments, the RNAi agent is administered chronically for an indefinite period of time, eg, for the lifetime of the patient.
일부 구현예에서, RNAi 제제는 다른 치료학적 제제 또는 다른 치료학적 용법과 함께 투여된다. 예를 들어, TTR 관련 질환을 치료하기에 적합한 다른 제제 또는 다른 치료학적 용법은 간 이식, 심장 이식, 심박조율기 이식, 체내에서 단량체 TTR 수준을 감소시킬 수 있는 제제; TTR 아밀로이드 생성에 필요한 사량체 해리를 방지하는 TTR 사량체를 동력학적으로 안정화시키는 타파미디스(Vyndaqel®또는 Vyndamax®또는 AG10; 예를 들어, 심장 침범이 있는 TTR 아밀로이드증에서 부종을 감소시키기 위해 사용될 수 있는 디플루니살 및 이뇨제와 같은 비스테로이드성 항염증 약물(NSAIDS)을 포함할 수 있다.In some embodiments, the RNAi agent is administered in conjunction with other therapeutic agents or other therapeutic regimens. For example, other agents or other therapeutic regimens suitable for treating TTR-related disorders include liver transplantation, heart transplantation, pacemaker implantation, agents capable of reducing monomeric TTR levels in the body; tafamidis (Vyndaqel® or Vyndamax® or AG10), which kinetically stabilizes TTR tetramers, preventing tetramer dissociation required for TTR amyloidogenesis; may be used, for example, to reduce edema in TTR amyloidosis with cardiac involvement nonsteroidal anti-inflammatory drugs (NSAIDS) such as diflunisal and diuretics.
하나의 구현예에서, 대상체는 RNAi 제제의 초기 용량 및 1회 이상의 유지 용량을 투여받는다. 유지 용량 또는 용량들은 초기 용량, 예를 들어 초기 용량의 절반과 같거나 더 낮을 수 있다. 치료 후 환자는 환자의 조건에서의 변화에 대해 모니터링될 수 있다. In one embodiment, the subject receives an initial dose and one or more maintenance doses of the RNAi agent. The maintenance dose or doses may be less than or equal to the initial dose, eg half the initial dose. After treatment, the patient may be monitored for changes in the patient's condition.
본 발명의 방법의 일부 구현예에서, 혈청 또는 혈장 TTR 수준에 의해 평가되는 TTR 유전자의 발현은 적어도 85%, 일부 실시양태에서는 적어도 90%까지 억제된다. 본원에 제공된 iRNA 제제를 사용한 TTR 발현의 억제는 간에서 TTR의 발현을 억제하고 다른 조직, 예를 들어 눈에서의 TTR 발현을 실질적으로 억제하지 않는 것으로 이해된다. In some embodiments of the methods of the invention, expression of the TTR gene as assessed by serum or plasma TTR levels is inhibited by at least 85%, and in some embodiments by at least 90%. It is understood that inhibition of TTR expression using the iRNA preparations provided herein inhibits expression of TTR in the liver and does not substantially inhibit TTR expression in other tissues, such as the eye.
본원에 사용된 바와 같은 용어 “억제하는”은 “감소시키는”, “사일런싱”, “하향조절하는”, “억제하는 (suppressing)”, 및 기타 유사 용어와 상호교환적으로 사용되고, 임의의 억제 수준을 포함한다. 일부 구현예에서, 억제는 통계학적으로 유의적이거나 임상적으로 유의적인 억제를 포함한다. As used herein, the term "inhibiting" is used interchangeably with "reducing", "silencing", "downregulating", "suppressing", and other similar terms, and any inhibition include the level In some embodiments, inhibition comprises statistically significant or clinically significant inhibition.
"TTR의 발현을 억제하는"이라는 문구는 TTR 유전자의 변이체 또는 돌연변이체를 포함하는 임의의 TTR 유전자의 발현 억제를 지칭하는 것으로 의도된다. 따라서, TTR 유전자는 야생형 TTR 유전자, 돌연변이 TTR 유전자(예를 들어, 아밀로이드 침착을 일으키는 돌연변이 TTR 유전자)일 수 있다.The phrase “inhibiting expression of TTR” is intended to refer to inhibition of expression of any TTR gene, including variants or mutants of the TTR gene. Thus, the TTR gene can be a wild-type TTR gene, a mutant TTR gene (eg, a mutant TTR gene that causes amyloid deposits).
억제는 대조군 수준과 비교하여 TTR 발현과 관련된 하나 이상의 변수의 절대적 또는 상대적 수준의 감소에 의해 평가될 수 있다. 대조군 수준은 당업계에서 사용되는 임의의 유형의 대조군 수준, 예를 들어, 투여 전 수준, 처리되지 않거나 대조군(예를 들어, 완충제만의 대조군 또는 불활성 제제 대조군)으로 처리된 유사 대상체, 세포 또는 샘플로부터 결정된 수준일 수 있다. 본원에 사용된 바와 같이, TTR 발현의 억제는 전형적으로 적절한 샘플(예를 들어, 과거 대조군 샘플, 정상 샘플 또는 임상 시험에서 결정된 수준)에서 TTR 수준을 결정함으로써 또는 본원 또는 PCT 공개 WO2010048228, WO2013075035, 및 WO2017023660에 제공된 것들, 또는 TTR의 발현을 억제하는 다른 제제, 예를 들어 안티센스 올리고뉴클레오타이드 제제, 다이서 기질 제제(예를 들어 WO20118139917 및 WO20118139917 참조)를 사용한 대상체의 치료 전; 및 본원에 제공된 iRNA 제제로 치료한 후 평가된다. 본원에서 제공되는 iRNA 제제는 내구성이 있지만 느리게 작용하는 것으로 이해된다. 따라서, 녹다운 수준은 최저점에 도달하기에 충분한 시간 후, 예를 들어 사람 대상체에서 iRNA 제제의 첫 번째 투여 후 적어도 3주 후 또는 TTR 녹다운의 정상 상태가 달성되었을 때, 예를 들어 본원에서 제공되는 iRNA 제제를 사용한 다중 투여 후 결정된다. Inhibition can be assessed by a decrease in absolute or relative levels of one or more variables associated with TTR expression compared to control levels. A control level is any type of control level used in the art, eg, a pre-administration level, a similar subject, cell or sample that is untreated or treated with a control (eg, a buffer only control or an inactive agent control). It may be a level determined from As used herein, inhibition of TTR expression is typically achieved by determining the level of TTR in an appropriate sample (e.g., a historical control sample, a normal sample, or a level determined in a clinical trial) or as described herein or in PCT publications WO2010048228, WO2013075035, and Prior to treatment of a subject with those provided in WO2017023660, or other agents that inhibit expression of TTR, such as antisense oligonucleotide preparations, dicer substrate preparations (see, eg WO20118139917 and WO20118139917); and after treatment with an iRNA formulation provided herein. It is understood that the iRNA preparations provided herein are durable but slow acting. Thus, the level of knockdown is determined after a time sufficient to reach a nadir, e.g., at least 3 weeks after the first administration of an iRNA agent in a human subject, or when a steady state of TTR knockdown is achieved, e.g., an iRNA provided herein. determined after multiple administrations with the formulation.
TTR 유전자의 발현의 억제는 TTR 유전자가 전사되고, 처리된 (예를 들어, 세포 또는 세포들과 본원 개시내용의 iRNA를 접촉시킴에 의해 또는 본 발명의 RNAi 제제를 세포가 존재하거나 존재했던 대상체에게 투여함에 의해) 제1 세포 또는 세포들 그룹 (상기 세포는 예를 들어, 대상체로부터 유래된 샘플 중에 존재할 수 있다)에 의해 발현되는 mRNA의 양의 감소에 의해 나타나 TTR 유전자의 발현은 제1 세포 또는 세포들 그룹과 실질적으로 동일하지만 그와 같이 처리되지 않은 제2 세포 또는 세포들 그룹 (대조군 세포(들))과 비교하여 억제된다. 일부 구현예에서, 퍼센트 억제는 하기 식을 사용하여 대조군 세포에서 mRNA 수준의 퍼센트로서 처리된 세포에서 mRNA 수준을 표현함에 의해 평가된다:Inhibition of the expression of the TTR gene can be achieved by contacting a cell or cells with an iRNA of the present disclosure or by administering an RNAi agent of the present invention to a subject in which the TTR gene is or has been transcribed and treated (e.g., a cell or cells). Expression of the TTR gene is indicated by a decrease in the amount of mRNA expressed by a first cell or group of cells (which may be present, for example, in a sample derived from a subject) by administration) of the first cell or group of cells; substantially the same as the group of cells, but inhibited compared to a second cell or group of cells that have not been so treated (control cell(s)). In some embodiments, percent inhibition is assessed by expressing mRNA levels in treated cells as a percentage of mRNA levels in control cells using the formula:
발현의 퍼센트 억제를 결정하기 위해, 예를 들어 대상체로부터 수득된 혈액 샘플에서 혈청 TTR 단백질 농도에 대해 유사한 계산을 수행할 수 있다. 치료 후 혈청 또는 혈장 샘플에서 TTR이 검출되지 않은 경우, 존재하는 TTR의 양이 사용된 검정의 검출 하한치에 있는 것으로 고려된다. Similar calculations can be performed for serum TTR protein concentrations in blood samples obtained, for example, from a subject to determine percent inhibition of expression. If TTR is not detected in the serum or plasma sample after treatment, the amount of TTR present is considered to be at the lower detection limit of the assay used.
일부 구현예에서, 퍼센트 억제는 검증되고 임상적으로 허용되는 방법을 사용하여 결정된다. In some embodiments, percent inhibition is determined using validated and clinically accepted methods.
대안적으로, TTR 유전자의 발현 억제는 TTR 유전자 발현, 예를 들어 TTR 단백질 발현, 레티놀 결합 단백질 수준, 비타민 A 수준 또는 TTR을 포함하는 아밀로이드 침착물의 존재와 기능적으로 연계된 파라미터의 감소 측면에서 평가될 수 있다. TTR 유전자 사일런싱은 TTR을 발현하는 임의의 세포에서 항시성으로, 또는 게놈 가공에 의해 및 당업계에 공지된 임의의 검정에 의해 결정될 수 있다. 간은 TTR 유전자 발현의 주요 부위이다. 발명의 다른 유의적인 부위는 망막 및 맥락총을 포함한다.Alternatively, inhibition of expression of the TTR gene can be assessed in terms of a reduction in TTR gene expression, eg TTR protein expression, retinol binding protein levels, vitamin A levels or parameters functionally linked to the presence of amyloid deposits comprising TTR. can TTR gene silencing can be determined constitutively in any cell expressing TTR, or by genome engineering and any assay known in the art. The liver is the major site of TTR gene expression. Other significant sites of interest include the retina and choroid plexus.
III. 본 발명의 iRNA III. iRNAs of the present invention
본 발명의 방법에 사용하기 위해 적합한 iRNA는 대상체, 예를 들어 포유류, 예를 들어, TTR 관련 질환을 갖는 사람 내의 세포와 같은 세포에서 TTR 유전자의 발현을 억제하기 위한 이중 가닥 리보핵산(dsRNA) 분자를 포함한다. dsRNA는 TTR 유전자의 발현에서 형성된 mRNA의 적어도 일부에 상보성인 상보성 영역을 갖는 안티센스 가닥을 포함한다. 상보성 영역은 길이가 약 21개 내지 30개 이하의 뉴클레오타이드(예를 들어, 길이가 약 30, 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, 또는 21개 뉴클레오타이드)이다. TTR 유전자를 발현하는 세포와의 접촉시, iRNA는 Hep3B 세포가 본원에 제공된 방법을 사용하여 10nM의 iRNA 제제로 형질감염되는 경우 TTR 유전자(예를 들어, 사람, 비-사람 영장류, 또는 비-영장류 포유류 TTR 유전자)의 발현을 예를 들어, WO2013075035의 실시예 4에 제공된 방법을 사용한 실시간 PCR에 의한 평가시 적어도 약70%까지 선택적으로 억제한다. Suitable iRNAs for use in the methods of the invention are double-stranded ribonucleic acid (dsRNA) molecules for inhibiting the expression of the TTR gene in a cell, such as a cell in a subject, eg, a mammal, eg, a human with a TTR-related disease. includes The dsRNA includes an antisense strand having a region of complementarity that is complementary to at least a portion of the mRNA formed in expression of the TTR gene. The region of complementarity is between about 21 and no more than 30 nucleotides in length (e.g., about 30, 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, or 21 nucleotides in length). . Upon contact with a cell expressing the TTR gene, the iRNA is capable of expressing the TTR gene (e.g. , human, non-human primate, or non-primate) when Hep3B cells are transfected with 10 nM of the iRNA preparation using the methods provided herein. mammalian TTR gene) by at least about 70% as assessed by real-time PCR using, for example, the method provided in Example 4 of WO2013075035.
dsRNA는 상보성인 2개의 RNA 가닥을 포함하고, 하이브리드화하여 dsRNA가 사용되는 조건하에서 듀플렉스 구조를 형성한다. dsRNA의 하나의 가닥(안티센스 가닥)은 표적 서열과 실질적으로 상보적이고 일반적인 완전히 상보적인 상보성 영역을 포함한다. 표적 서열은 TTR 유전자의 발현 동안에 형성된 mRNA의 서열로부터 유래할 수 있다. 다른 가닥 (안티센스 가닥)은 안티센스 가닥에 상보적인 영역을 포함하여, 2개의 가닥은 적합한 조건하에서 조합되는 경우 하이브리드화하여 듀플렉스 구조를 형성한다. 본원 다른 곳에 기재되고 당업계에 공지된 바와 같이, dsRNA의 상보성 서열은 또한 별개의 올리고뉴클레오타이드 상에 존재하는 것과는 대조적으로 단일 핵산 분자의 자가-상보성 영역으로서 포함될 수 있다. A dsRNA comprises two RNA strands that are complementary and hybridize to form a duplex structure under the conditions in which the dsRNA is used. One strand of the dsRNA (the antisense strand) contains a region of complementarity that is substantially complementary to the target sequence and is usually fully complementary. The target sequence may be derived from the sequence of mRNA formed during expression of the TTR gene. The other strand (the antisense strand) contains a region complementary to the antisense strand so that the two strands hybridize to form a duplex structure when combined under suitable conditions. As described elsewhere herein and known in the art, complementary sequences of dsRNAs can also be included as self-complementary regions of a single nucleic acid molecule, as opposed to being on separate oligonucleotides.
일반적으로, 듀플렉스 구조는 길이가 21 내지 30개 염기쌍이다. 유사하게, 표적 서열과 상보성 영역의 길이는 22개 및 30개 뉴클레오타이드이다. Generally, duplex structures are 21 to 30 base pairs in length. Similarly, the length of the region of complementarity with the target sequence is 22 and 30 nucleotides.
dsRNA는 하기에서 추가로 논의되는 바와 같이 당업계에 공지된 표준 방법에 의해 합성될 수 있다. dsRNA can be synthesized by standard methods known in the art, as discussed further below.
본 발명의 iRNA 화합물은 2단계 과정을 사용하여 제조될 수 있다. 첫번째로, 이중 가닥 RNA 분자의 개별 가닥은 별도로 제조된다. 이어서, 성분 가닥은 어닐링된다. siRNA 화합물의 개별 가닥은 용액상 또는 고체상 유기 합성 또는 둘다를 사용하여 제조될 수 있다. 유기 합성은 비천연 또는 변형된 뉴클레오타이드를 포함하는 올리고뉴클레오타이드 가닥을 용이하게 제조할 수 있다는 이점을 제공한다. 본 발명의 단일 가닥 올리고뉴클레오타이드는 용액상 또는 고체상 유기 합성 또는 둘다를 사용하여 제조될 수 있다. iRNA compounds of the invention can be prepared using a two-step process. First, the individual strands of a double-stranded RNA molecule are prepared separately. The component strands are then annealed. Individual strands of siRNA compounds can be prepared using either solution phase or solid phase organic synthesis or both. Organic synthesis offers the advantage of being able to easily prepare oligonucleotide strands comprising unnatural or modified nucleotides. The single-stranded oligonucleotides of the present invention can be prepared using either solution-phase or solid-phase organic synthesis or both.
IV. 본 발명의 변형된 iRNAIV. Modified iRNAs of the present invention
본 발명의 방법에 사용하기 위한 iRNA 제제는 센스 및 안티센스 가닥에서 한정된 화학적 변형을 포함한다. 어느 한 가닥의 길이가 23개 초과의 뉴클레오타이드의 안티센스 가닥 및 21개 초과의 뉴클레오타이드의 센스 가닥을 제공하도록 연장되는 경우, 뉴클레오타이드는 당 변형, 백본 변형 및 염기 변형을 포함하지만 이에 제한되지 않는 변형을 포함할 수 있다.변형은 예를 들어, 말단 변형, 예를 들어, 5’-말단 변형 (인산화, 접합, 역위 연결) 또는 3’-말단 변형(접합, DNA 뉴클레오타이드, 역위 연결 등); 염기 변형, 예를 들어, 안정화 염기, 또는 파트너의 확장된 레퍼토리와 염기쌍을 형성하는 염기로의 대체, 염기의 제거(무염기 뉴클레오타이드), 또는 접합된 염기; 당 변형(예를 들어, 2’-위치 또는 4’-위치에서) 또는 당의 대체; 또는 포스포디에스테르 연결의 변형 또는 대체를 포함하는 백본 변형을 포함한다. 본원에 기재된 구현예에 유용한 iRNA 화합물의 특정 예는 변형된 백본을 함유하거나 어떠한 천연 뉴클레오타이드 간 연결을 함유하지 않는 RNA를 포함하지만 이에 제한되지 않는다. 변형된 골격을 갖는 RNA는 무엇 보다 골격 내 인 원자를 갖지 않는 것들을 포함한다. 본 명세서의 목적을 위해서 및 당업계에서 때로 언급되는 바와 같이, 이들의 뉴클레오타이드 간 골격 내 인 원자를 갖지 않는 변형된 RNA는 또한 올리고뉴클레오타이드인 것으로 고려될 수 있다. 일부 구현예에서, 변형된 iRNA는 이의 뉴클레오사이드 간 백본 내 인 원자를 갖는다. RNAi preparations for use in the methods of the invention include defined chemical modifications in the sense and antisense strands. When the length of either strand is extended to provide an antisense strand of greater than 23 nucleotides and a sense strand of greater than 21 nucleotides, the nucleotides include modifications, including but not limited to sugar modifications, backbone modifications and base modifications Modifications may include, for example, terminal modifications such as 5'-end modifications (phosphorylation, conjugation, inverted ligation) or 3'-end modifications (conjugation, DNA nucleotides, inverted ligation, etc.); base modifications, eg, replacement of stabilizing bases or bases that form base pairs with an expanded repertoire of partners, removal of bases (baseless nucleotides), or conjugated bases; sugar modifications ( eg , at the 2'-position or 4'-position) or replacement of sugars; or backbone modifications including modification or replacement of phosphodiester linkages. Specific examples of iRNA compounds useful in the embodiments described herein include, but are not limited to, RNAs that contain modified backbones or do not contain any natural internucleotide linkages. RNAs with modified backbones include, among others, those that do not have a phosphorus atom in the backbone. For purposes herein and as sometimes referred to in the art, modified RNAs that do not have a phosphorus atom in their internucleotide backbone may also be considered oligonucleotides. In some embodiments, a modified iRNA has a phosphorus atom in its internucleoside backbone.
변형된 RNA 골격은 예를 들어, 포스포로티오에이트, 키랄 포스포로티오에이트, 포스포로디티오에이트, 포스포트리에스테르, 아미노알킬포스포트리에스테르, 3’-알킬렌 포스포네이트 및 키랄 포스포네이트를 포함하는 메틸 및 다른 알킬 포스포네이트, 포스피네이트, 3’-아미노 포스포르아미데이트 및 아미노알킬포스포르아미데이트를 포함하는 포스포르아미데이트, 티오노포스포르아미데이트, 티오노알킬포스포네이트, 티오노알킬포스포트리에스테르, 및 정상 3’-5’ 연결을 갖는 보라노포스페이트, 이들의 2'-5’ 연결된 유사체, 및 뉴클레오사이드 유닛의 인접한 쌍이 3'-5’에서 5’-3’로 연결되거나, 2’-5'에서 5’-2'로 연결된 역위 극성을 갖는 것들을 포함한다. 다양한 염, 혼합 염 및 유리된 산 형태가 또한 포함된다. Modified RNA backbones include, for example, phosphorothioates, chiral phosphorothioates, phosphorodithioates, phosphotriesters, aminoalkylphosphotriesters, 3'-alkylene phosphonates and chiral phosphonates. methyl and other alkyl phosphonates, including phosphinates, phosphoramidates including 3'-amino phosphoramidates and aminoalkylphosphoramidates, thionophosphoramidates, thionoalkylphosphonates , thionoalkylphosphotriesters, and boranophosphates with normal 3'-5' linkages, their 2'-5' linked analogs, and adjacent pairs of nucleoside units from 3'-5' to 5'-3 ', or those with reverse polarity connected from 2'-5' to 5'-2'. Various salts, mixed salts and free acid forms are also included.
본원에서 인 원자를 포함하지 않는 변형된 RNA 골격은 단쇄 알킬 또는 사이클로알킬 뉴클레오사이드 간 연결, 혼합 헤테로원자 및 알킬 또는 사이클로알킬 뉴클레오사이드 간 연결, 또는 하나 이상의 단쇄 헤테로원자 또는 헤테로사이클릭 뉴클레오사이드 간 연결에 의해 형성된 골격을 갖는다. 이들은 모르폴리노 연결 (부분적으로 뉴클레오사이드의 당 부분으로부터 형성된); 실록산 골격; 설파이드, 설폭사이드 및 설폰 골격; 포름아세틸 및 티오포름아세틸 골격; 메틸렌 포름아세틸 및 티오포름아세틸 골격; 알켄 함유 골격; 설파메이트 골격; 메틸렌이미노 및 메틸렌하이드라지노 골격; 설포네이트 및 설폰아미드 골격; 아미드 골격; 및 혼합 N, O, S 및 CH2성분 부분을 갖는 기타의 것들을 갖는 것들을 포함한다. Modified RNA backbones herein that do not contain a phosphorus atom include short-chain alkyl or cycloalkyl internucleoside linkages, mixed heteroatoms and alkyl or cycloalkyl internucleoside linkages, or one or more short-chain heteroatomic or heterocyclic nucleoside linkages. It has a skeleton formed by side-to-side connections. These include morpholino linkages (formed in part from the sugar portion of a nucleoside); siloxane backbone; sulfide, sulfoxide and sulfone backbones; formacetyl and thioformacetyl backbones; methylene formacetyl and thioformacetyl backbones; alkene-containing backbones; sulfamate backbone; methyleneimino and methylenehydrazino backbones; sulfonate and sulfonamide backbones; amide backbone; and others having mixed N, O, S and CH 2 component parts.
다른 구현예에서, 적합한 RNA 모사체는 당 및 뉴클레오사이드 간 연결 둘다, 즉, 뉴클레오타이드 유닛의 백본이 신규 그룹으로 대체된 iRNA에 사용하기 위해 고려된다. 염기 유닛은 적당한 핵산 표적 화합물과의 하이브리드화를 위해 유지된다. 우수한 하이브리드화 성질을 갖는 것으로 나타난 RNA 모사체인 하나의 상기 올리고머 화합물은 펩타이드 핵산 (PNA)으로서 언급된다. PNA 화합물에서, RNA의 당 골격은 아미드 함유 골격, 특히 아미노에틸글라이신 골격으로 대체된다. 뉴클레오염기는 보유되고 직접적으로 또는 간접적으로 골격의 아미드 부분의 아자 질소 원자에 결합된다.In other embodiments, suitable RNA mimetics are contemplated for use in iRNAs in which both sugar and internucleoside linkages, i.e., the backbone of nucleotide units are replaced by new groups. Base units are retained for hybridization with an appropriate nucleic acid target compound. One such oligomeric compound, which is an RNA mimetic that has been shown to have good hybridization properties, is referred to as a peptide nucleic acid (PNA). In PNA compounds, the sugar backbone of RNA is replaced with an amide-containing backbone, particularly an aminoethylglycine backbone. The nucleobases are retained and bonded directly or indirectly to the aza nitrogen atom of the amide portion of the backbone.
본원 개시내용에서 특징으로 하는 일부 구현예는 포스포로티오에이트 백본, 및 헤테로원자 백본 및 특히 미국 특허 제5,489,677호의 --CH2--NH--CH2-, --CH2--N(CH3)--O--CH2--[메틸렌 (메틸이미노) 또는 MMI 백본으로서 공지된], --CH2--O--N(CH3)--CH2--, --CH2--N(CH3)--N(CH3)--CH2-- 및 --N(CH3)--CH2--CH2-- 및 상기 언급된 미국 특허 제5,602,240호의 아미드 백본을 갖는 올리고뉴클레오타이드를 갖는 RNA를 포함한다. 일부 구현예에서, 본원에 특징으로 하는 RNA는 상기 언급된 미국 특허 제5,034,506호의 모르폴리노 골격 구조를 갖는다. 고유 포스포디에스테르 백본은 O-P(O)(OH)-OCH2-로서 나타낼 수 있다.Some embodiments featured in the present disclosure include phosphorothioate backbones, and heteroatom backbones and particularly --CH 2 --NH--CH 2 -, --CH 2 --N(CH of US Pat. No. 5,489,677). 3 )--O--CH 2 --[known as methylene (methylimino) or MMI backbone], --CH 2 --O--N(CH 3 )--CH 2 --, --CH 2 --N(CH 3 )--N(CH 3 )--CH 2 -- and --N(CH 3 )--CH 2 --CH 2 -- and the amide backbone of the aforementioned US Pat. No. 5,602,240 It includes RNA having an oligonucleotide having a. In some embodiments, the RNA featured herein has the morpholino backbone structure of the aforementioned U.S. Patent No. 5,034,506. The native phosphodiester backbone can be represented as OP(O)(OH)-OCH2-.
변형된 RNA는 또한 하나 이상의 치환된 당 모이어티를 함유할 수 있다. iRNA, 예를 들어, 본원에서 특징으로 하는 dsRNA는 2’-위치에서 OH; F; O-, S-, 또는 N-알킬; O-, S-, 또는 N-알케닐; O-, S- 또는 N-알키닐; 또는 O-알킬-O-알킬 중 하나를 포함할 수 있고, 여기서, 알킬, 알케닐 및 알키닐은 치환되거나 치환되지 않은 C1내지 C10알킬 또는 C2내지 C10알케닐 및 알키닐일 수 있다. 예시적인 적합한 변형은 O[(CH2)nO]mCH3, O(CH2).nOCH3, O(CH2)nNH2, O(CH2)nCH3, O(CH2)nONH2,및 O(CH2)nON[(CH2)nCH3)]2,를 포함하고, 여기서, n 및 m은 1 내지 약 10이다. 다른 구현예에서, dsRNA는 2’ 위치에서 하기 중 하나를 포함한다: C1내지 C10저급 알킬, 치환된 저급 알킬, 알크아릴, 아르알킬, O-알크아릴 또는 O-아르알킬, SH, SCH3, OCN, Cl, Br, CN, CF3, OCF3, SOCH3, SO2CH3, ONO2, NO2, N3, NH2, 헤테로사이클로알킬, 헤테로사이클로알크아릴, 아미노알킬아미노, 폴리알킬아미노, 치환된 실릴, RNA 절단 그룹, 리포터 그룹, 삽입제, iRNA의 약동학 성질을 개선시키기 위한 그룹, 또는 iRNA의 약력학 성질을 개선시키기 위한 그룹, 및 유사한 성질을 갖는 기타 치환체. 일부 구현예에서, 변형은 2'-메톡시에톡시 (2'-O--CH2CH2OCH3, 또한 2'-O-(2-메톡시에틸) 또는 2'-MOE로서 공지된) (문헌참조: Martin et al.,Helv.Chim.Acta,1995,78:486-504),즉, 알콕시-알콕시 그룹을 포함한다. 또 다른 예시적인 변형은 하기에서 본원의 실시예에 기재된 바와 같이 2'-DMAOE로서도 공지된 2'-디메틸아미노옥시에톡시, 즉, O(CH2)2ON(CH3)2그룹, 및 2'-디메틸아미노에톡시에톡시(또한 당업계에서 2'-O-디메틸아미노에톡시에틸 또는 2'-DMAEOE로서 공지된), 즉, 2'-O--CH2--O--CH2--N(CH3)2이다. 추가의 예시적인 변형은 다음을 포함한다: 5’-Me-2’-F 뉴클레오타이드, 5’-Me-2’-OMe 뉴클레오타이드, 5’-Me-2’-데옥시뉴클레오타이드, (이들 3개의 계열 중 R 및 S 이성체 둘다); 2’-알콕시알킬; 및 2’-NMA (N-메틸아세트아미드). Modified RNAs may also contain one or more substituted sugar moieties. An iRNA, e.g., a dsRNA featured herein, has an OH at the 2'-position;F; O-, S-, or N-alkyl; O-, S-, or N-alkenyl; O-, S- or N-alkynyl; or O-alkyl-O-alkyl, wherein alkyl, alkenyl and alkynyl can be substituted or unsubstituted C 1 to C 10 alkyl or C 2 to C 10 alkenyl and alkynyl. . An exemplary suitable variant is O[(CH 2 ) n O] m CH 3 , O(CH 2 ). n OCH 3 , O(CH 2 ) n NH 2 , O(CH 2 ) n CH 3 , O(CH 2 ) n ONH 2 , and O(CH 2 ) n ON[(CH 2 ) n CH 3 )] 2 , wherein n and m are from 1 to about 10. In other embodiments, the dsRNA comprises one of the following at the 2' position: C 1 to C 10 lower alkyl, substituted lower alkyl, alkaryl, aralkyl, O-alkaryl or O-aralkyl, SH , SCH 3 , OCN, Cl, Br, CN, CF 3 , OCF 3 , SOCH 3 , SO 2 CH 3 , ONO 2 , NO 2 , N 3 , NH 2 , heterocycloalkyl, heterocycloalkaryl, aminoalkyl Amino, polyalkylamino, substituted silyl, RNA cleavage groups, reporter groups, intercalants, groups for improving the pharmacokinetic properties of iRNA, or groups for improving the pharmacodynamic properties of iRNA, and other substituents with similar properties. In some embodiments, the modification is 2'-methoxyethoxy (2'-O--CH 2 CH 2 OCH 3 , also known as 2'-O-(2-methoxyethyl) or 2'-MOE) (Reference: Martin et al . , Helv. Chim. Acta, 1995, 78: 486-504 ), that is, it contains an alkoxy-alkoxy group. Another exemplary modification is 2'-dimethylaminooxyethoxy, also known as 2'-DMAOE, ie, O(CH 2 ) 2 ON(CH 3 ) 2 groups, and 2 as described in the Examples herein below. '-dimethylaminoethoxyethoxy (also known in the art as 2'-O-dimethylaminoethoxyethyl or 2'-DMAEOE), i.e., 2'-O--CH 2 --O--CH 2 --N(CH 3 ) 2 . Additional exemplary modifications include: 5'-Me-2'-F nucleotides, 5'-Me-2'-OMe nucleotides, 5'-Me-2'-deoxynucleotides, (these three series of both R and S isomers); 2'-alkoxyalkyl; and 2'-NMA (N-methylacetamide).
기타 변형은 2'-메톡시(2'-OCH3),2'-아미노프로폭시 (2'-OCH2CH2CH2NH2) 및 2'-플루오로 (2'-F)를 포함한다. 유사한 변형은 또한 iRNA의 RNA 상의 다른 위치, 특히 3' 말단 뉴클레오타이드 상의 당의 3' 위치 또는 2'-5' 연결된 dsRNA 및 5' 말단 뉴클레오타이드의 5' 위치에서 이루어질 수 있다. iRNA는 또한 펜토푸라노실 당 대신에 사이클로부틸 모이어티와 같은 당 모방체를 가질 수 있다.Other modifications include 2'-methoxy (2'-OCH 3 ), 2'-aminopropoxy (2'-OCH 2 CH 2 CH 2 NH 2 ) and 2'-fluoro (2'-F). . Similar modifications can also be made at other positions on the RNA of the iRNA, particularly at the 3' position of the sugar on the 3' terminal nucleotide or at the 5' position of the 2'-5' linked dsRNA and 5' terminal nucleotide. An iRNA may also have a sugar mimetic such as a cyclobutyl moiety in place of a pentofuranosyl sugar.
본 발명의 iRNA의 RNA는 또한 뉴클레오염기(흔히 단순히 “염기”로서 언급되는) 변형 또는 치환을 포함할 수 있다. 본원에 사용된 바와 같은 “비변형된” 또는 “천연” 뉴클레오염기는 퓨린 염기 아데닌 (A) 및 구아닌(G), 및 피리미딘 염기 티민(T), 시토신 (C) 및 우라실 (U)을 포함한다. 변형된 뉴클레오염기는 데옥시티미딘(dT), 5-메틸시토신(5-me-C), 5-하이드록시메틸 시토신, 크산틴, 하이포산틴, 2-아미노아데닌, 아데닌 및 구아닌의 6-메틸 및 기타 알킬 유도체, 아데닌 및 구아닌의 2-프로필 및 기타 알킬 유도체, 2-티오우라실, 2-티오티민 및 2-티오시토신, 5-할로우라실 및 시토신, 5-프로피닐 우라실 및 시토신, 6-아조 우라실, 시토신 및 티민, 5-우라실(슈도우라실), 4-티오우라실, 8-할로, 8-아미노, 8-티올, 8-티오알킬, 8-히드록실 및 기타 8-치환된 아데닌 및 구아닌, 5-할로, 특히 5-브로모, 5-트리플루오로메틸 및 기타 5-치환된 우라실 및 시토신, 7-메틸구아닌 및 7-메틸아데닌, 8-아자구아닌 및 8-아자아데닌, 7-데아자구아닌 및 7-다아자아데닌 및 3-데아자구아닌 및 3-데아자아데닌과 같은 다른 합성 및 천연 뉴클레오염기를 포함한다. 특정 이들 뉴클레오염기는 특히 본 발명에서 특성화된 올리고머 화합물의 결합 친화성을 증가시키기 위해 유용하다. 이들은 2-아미노프로필아데닌, 5-프로필우라실 및 5-프로피닐시토신을 포함하는, 5-치환된 피리미딘, 6-아자피리미딘 및 N-2, N-6 및 0-6개 치환된 퓨린을 포함한다. 5-메틸시토신 치환은 0.6-1.2°C까지 핵산 듀플렉스 안정성을 증가시키는 것으로 나타났고(문헌참조: Sanghvi, Y. S., Crooke, S. T. and Lebleu, B., Eds., dsRNA Research and Applications, CRC Press, Boca Raton, 1993, pp. 276-278) 예시적으로 염기 치환이며, 보다 더 특히2'-O-메톡시에틸 당 변형과 조합되는 경우이다. The RNA of an iRNA of the invention may also contain nucleobase (commonly referred to simply as a “base”) modification or substitution. As used herein, “unmodified” or “natural” nucleobases include the purine bases adenine (A) and guanine (G), and the pyrimidine bases thymine (T), cytosine (C) and uracil (U). include The modified nucleobases are deoxythymidine (dT), 5-methylcytosine (5-me-C), 5-hydroxymethyl cytosine, xanthine, hypoxanthine, 2-aminoadenine, adenine, and 6 guanine. -methyl and other alkyl derivatives, 2-propyl and other alkyl derivatives of adenine and guanine, 2-thiouracil, 2-thiothymine and 2-thiocytosine, 5-haluracil and cytosine, 5-propynyluracil and cytosine, 6 -azouracil, cytosine and thymine, 5-uracil (pseudouracil), 4-thiouracil, 8-halo, 8-amino, 8-thiol, 8-thioalkyl, 8-hydroxyl and other 8-substituted adenines and Guanine, 5-halo, especially 5-bromo, 5-trifluoromethyl and other 5-substituted uracil and cytosine, 7-methylguanine and 7-methyladenine, 8-azaguanine and 8-azaadenine, 7- deazaguanine and other synthetic and natural nucleobases such as 7- and 3-deazaguanine and 3-deazaadenine. Certain of these nucleobases are particularly useful for increasing the binding affinity of the oligomeric compounds featured in the present invention. These include 5-substituted pyrimidines, 6-azapyrimidines and N-2, N-6 and 0-6 substituted purines, including 2-aminopropyladenine, 5-propyluracil and 5-propynylcytosine. include 5-methylcytosine substitution has been shown to increase nucleic acid duplex stability by 0.6-1.2 °C (see Sanghvi, Y. S., Crooke, S. T. and Lebleu, B., Eds., dsRNA Research and Applications, CRC Press, Boca Raton, 1993, pp. 276-278) exemplarily base substitutions, even more particularly in combination with modifications per 2'-O-methoxyethyl.
본원 개시내용의 RNAi 제제는 또한 하나 이상의 바이사이클릭 당 모이어티를 포함하도록 변형될 수 있다. “바이사이클릭 당"은 인접하거나 인접하지 않은 원자에 관계없이 2개의 탄소의 브릿징에 의해 형성된 환에 의해 변형된 푸라노실 환이다. “바이사이클릭 뉴클레오사이드” (“BNA”)는 인접하거나 인접해 있지 않든 상관 없이 당 환의 2개의 탄소 원자를 연결하여 바이사이클릭 환 시스템을 형성하는 브릿지를 포함하는 브릿징에 의해 형성된 환을 포함하는 당 모이어티를 갖는 뉴클레오사이드이다. 특정 구현예에서, 브릿지는 당 환의 4’-탄소 및 2’-탄소를 2’-비사이클릭 (acyclic) 산소 원자를 통해 연결한다. 따라서, 일부 구현예에서, 본원 개시내용의 제제는 하나 이상의 잠김 핵산 (LNA)를 포함할 수 있다. 잠김 핵산은 변형된 리보스 모이어티를 갖는 뉴클레오타이드이고, 여기서, 상기 리보스 모이어티는 2’ 및 4’ 탄소를 연결하는 여분의 브릿지를 포함한다. 다른 말로, LNA는 4'-CH2-O-2' 브릿지를 포함하는 바이사이클릭 당 모이어티를 포함하는 뉴클레오타이드이다. 상기 구조는 3’-엔도 구조 형태에서 리보스를 효과적으로 잠군다. siRNA로의 잠김 핵산의 첨가는 혈청에서 siRNA 안정성을 증가시키고 오프-표적 효과를 감소시키는 것으로 나타났다(문헌참조: Elmen, J. et al.,(2005) Nucleic Acids Research 33(1):439-447; Mook,OR.et al.,(2007) Mol Canc Ther6(3):833-843; Grunweller, A.et al.,(2003) Nucleic Acids Research 31(12):3185-3193). 본원 개시내용의 폴리뉴클레오타이드에 사용하기 위한 바이사이클릭 뉴클레오사이드의 예는 4'와 2' 리보실 고리 원자 사이에 브릿지를 포함하는 뉴클레오사이드를 제한 없이 포함한다. 특정 구현예에서, 본원 개시내용의 안티센스 폴리뉴클레오타이드 제제는 4′에서 2′로의 브릿지를 포함하는 하나 이상의 바이사이클릭 뉴클레오사이드를 포함한다. RNAi agents of the present disclosure may also be modified to include one or more bicyclic sugar moieties. A “bicyclic sugar” is a furanosyl ring modified by a ring formed by the bridging of two carbons, regardless of adjacent or non-adjacent atoms. A “bicyclic nucleoside” (“BNA”) is an adjacent A nucleoside having a sugar moiety comprising a ring formed by bridging, including a bridge connecting two carbon atoms of the sugar ring, whether contiguous or not, to form a bicyclic ring system. In, the bridge connects the 4'-carbon and the 2'-carbon of the sugar ring through a 2'-acyclic oxygen atom. Thus, in some embodiments, an agent of the present disclosure comprises one or more locked nucleic acids ( LNA). A locked nucleic acid is a nucleotide having a modified ribose moiety, wherein said ribose moiety contains an extra bridge connecting the 2' and 4' carbons. In other words, an LNA is a 4 A nucleotide comprising a bicyclic sugar moiety comprising a '-CH2-O-2' bridge. This structure effectively locks ribose in the 3'-endo conformational form. Addition of the locked nucleic acid to siRNA is siRNA It has been shown to increase stability and reduce off-target effects (see Elmen, J. et al . , (2005) Nucleic Acids Research 33(1):439-447; Mook, OR. et al . , (2007 ) Mol Canc Ther 6(3):833-843 Grunweller, A. et al . , (2003) Nucleic Acids Research 31(12):3185-3193 Bicyclics for Use in Polynucleotides of the Disclosure Examples of nucleosides include, but are not limited to, nucleosides comprising bridges between 4' and 2' ribosyl ring atoms. One or more bicyclic nucleosides containing bridges.
잠긴 뉴클레오사이드는 구조(입체화학 생략)로 나타낼 수 있고, 여기서 B는 핵염기 또는 변형된 핵염기이고 L은 2'-탄소를 리보스 환의 4'-탄소에 연결하는 연결 그룹이다. A locked nucleoside can be represented by a structure (stereochemistry omitted), where B is a nucleobase or modified nucleobase and L is a linking group connecting the 2'-carbon to the 4'-carbon of the ribose ring.
상기 4′에서 2′로 브릿지된 바이사이클릭 뉴클레오사이드의 예는 4′-(CH2)-O-2′ (LNA); 4′-(CH2)-S-2′; 4′-(CH2)-O-2′ (ENA); 4′-CH(CH3)-O-2′ (또한 “속박된 에틸” 또는 “cEt”로서 언급되는) 및 4′-CH(CH2OCH3)-O-2′ (및 이의 유사체; 예를 들어, 미국 특허 제7,399,845호를 참조한다); 4′-C(CH3)(CH3)-O-2′ (및 이의 유사체; 예를 들어, 미국 특허 제8,278,283호를 참조한다); 4′-CH2-N(OCH3)-2′ (및 이의 유사체; 예를 들어, 미국 특허 제8,278,425호를 참조한다); 4′-CH2-O-N(CH3)-2′ (예를 들어,미국 특허 공개 공보 제2004/0171570호 참조); R이 H, C1-C12 알킬 또는 보호 그룹인 4′-CH2-N(R)-O-2′(예를 들어, 미국 특허 제7,427,672호를 참조한다); 4′-CH2-C(H)(CH3)-2′ (예를 들어, Chattopadhyaya et al., J. Org. Chem.,2009,74,118-134를 참조한다); 및 4′-CH2-C(=CH2)-2′(및 이의 유사체; 예를 들어 미국 특허 제8,278,426호를 참조한다). 이전 문헌의 각각의 전체 내용은 본원에 참조로 인용된다. Examples of the above 4' to 2' bridged bicyclic nucleosides include 4'-(CH2)-O-2'(LNA);4′-(CH2)-S-2′; 4′-(CH2)-O-2′ (ENA); 4'-CH(CH3)-O-2' (also referred to as "bound ethyl" or "cEt") and 4'-CH(CH2OCH3)-O-2' (and analogs thereof; see, e.g., the United States See Patent No. 7,399,845); 4'-C(CH3)(CH3)-O-2' (and analogs thereof; see, eg, US Pat. No. 8,278,283); 4'-CH2-N(OCH3)-2' (and analogs thereof; see, eg, US Pat. No. 8,278,425); 4′-CH2-ON(CH3)-2′ (see, eg, US Patent Publication No. 2004/0171570); 4'-CH2-N(R)-O-2' where R is H, C1-C12 alkyl or a protecting group (see, eg, US Pat. No. 7,427,672); 4′-CH2-C(H)(CH3)-2′ ( see, eg , Chattopadhyaya et al ., J. Org. Chem ., 2009, 74, 118-134); and 4'-CH2-C(=CH2)-2' (and analogues thereof; see eg US Pat. No. 8,278,426). The entire contents of each of the foregoing documents are incorporated herein by reference.
잠김 핵산 뉴클레오타이드의 제조를 교시하는 추가의 대표적인 미국 특허 및 미국 특허 공개 공보는 하기를 포함하지만 이에 제한되지 않는다: 이들 각각의 전문이 본원에 참조로 인용되는 미국 특허 제6,268,490호; 제6,525,191호; 제6,670,461호; 제6,770,748호; 제6,794,499호; 제6,998,484호; 제7,053,207호; 제7,034,133호; 제7,084,125호; 제7,399,845호; 제7,427,672호; 제7,569,686호; 제7,741,457호; 제8,022,193호; 제8,030,467호; 제8,278,425호; 제8,278,426호; 제8,278,283호; 미국 공개 공보 제2008/0039618호; 및 미국 공개 공보 제2009/0012281호. Additional representative US patents and US patent publications that teach the preparation of locked nucleic acid nucleotides include, but are not limited to: US Patent Nos. 6,268,490, each of which is incorporated herein by reference in its entirety; 6,525,191; 6,670,461; 6,770,748; 6,794,499; 6,998,484; 7,053,207; 7,034,133; 7,084,125; 7,399,845; 7,427,672; 7,569,686; 7,741,457; 8,022,193; 8,030,467; 8,278,425; 8,278,426; 8,278,283; US Publication No. 2008/0039618; and US Publication No. 2009/0012281.
임의의 전술한 바이사이클릭 뉴클레오사이드는 예를 들어 α-L-리보푸라노스 및 β-D-리보푸라노스를 포함하는 하나 이상의 입체화학적 당 배열을 갖도록 제조될 수 있다(WO 99/14226 참조). Any of the foregoing bicyclic nucleosides can be prepared with one or more stereochemical sugar configurations including, for example, α-L-ribofuranose and β-D-ribofuranose (see WO 99/14226). ).
본원 개시내용의 RNAi 제제는 또한 하나 이상의 속박된 에틸 뉴클레오타이드를 포함하도록 변형될 수 있다. 본원에 사용된 바와 같은 "속박된 에틸 뉴클레오타이드" 또는 "cEt"는 4'-CH(CH3)-O-2' 브릿지(즉, 이전 구조에서 L)를 포함하는 바이사이클릭 당 모이어티를 포함하는 잠김 핵산이다. 하나의 구현예에서, 속박된 에틸 뉴클레오타이드는 본원에서 "S-cEt"로 지칭되는 S 형태로 있다.RNAi agents of the present disclosure may also be modified to include one or more constrained ethyl nucleotides. As used herein, "tethered ethyl nucleotide" or "cEt" refers to a bicyclic sugar moiety comprising a 4'-CH(CH3)-O-2' bridge (i.e., L in the previous structure). It is a locked nucleic acid. In one embodiment, the constrained ethyl nucleotides are in the S form, referred to herein as "S-cEt".
본 발명의 iRNA는 또한 하나 이상의 “형태적으로 제한된 뉴클레오타이드” (“CRN”)를 포함할 수 있다. CRN은 리보스의 C2' 및 C4' 탄소 또는 리보스의 C3 및 -C5' 탄소를 연결하는 링커를 갖는 뉴클레오타이드 유사체이다. CRN은 리보스 환을 안정한 형태로 잠그고 mRNA에 대한 하이브리드화 친화성을 증가시킨다. 링커는 안정성과 친화성을 위한 최적의 위치에 산소를 배치하여 리보스 환 퍼커링(puckering)을 감소시키는 데 충분한 길이이다. An iRNA of the invention may also contain one or more “conformationally restricted nucleotides” (“CRNs”). CRN is a nucleotide analog with a linker connecting the C2' and C4' carbons of ribose or the C3 and -C5' carbons of ribose. CRN locks the ribose ring into a stable conformation and increases the hybridization affinity for mRNA. The linker is of sufficient length to reduce ribose ring puckering by positioning the oxygen in an optimal position for stability and affinity.
본 발명의 iRNA의 하나 이상의 뉴클레오타이드는 또한 하이드록시메틸 치환된 뉴클레오타이드를 포함할 수 있다. “하이드록시메틸 치환된 뉴클레오타이드”는 또한 “잠금 해제된” (“UNA”) 변형으로서 지칭되는 비사이클릭 2’-3’-세코-뉴클레오타이드이다.One or more nucleotides of an iRNA of the invention may also include hydroxymethyl substituted nucleotides. A "hydroxymethyl substituted nucleotide" is an acyclic 2'-3'-seco-nucleotide also referred to as an "unlocked" ("UNA") variant.
RNA 분자의 말단으로 잠재적으로 안정화된 변형은 N- (아세틸아미노카프로일)-4-하이드록시프롤리놀 (Hyp-C6-NHAc), N-(카프로일-4-하이드록시피롤리놀 (Hyp-C6), N-(아세틸-4-하이드록시프롤리놀 (Hyp-NHAc), 티미딘-2'-0-데옥시티미딘 (에테르), N-(아미노카프로일)-4-하이드록시프롤리놀 (Hyp-C6-아미노), 2-도코사노일-우리딘-3’-포스페이트, 역위 염기 dT(idT) 등을 포함할 수 있다. 상기 변형의 개시내용은 WO 2011/005861에서 찾을 수 있다.Potentially stabilizing modifications to the ends of RNA molecules include N-(acetylaminocaproyl)-4-hydroxyprolinol (Hyp-C6-NHAc), N-(caproyl-4-hydroxypyrrolinol (Hyp-C6-NHAc), -C6), N-(acetyl-4-hydroxyprolinol (Hyp-NHAc), thymidine-2'-0-deoxythymidine (ether), N-(aminocaproyl)-4-hydroxy prolinol (Hyp-C6-amino), 2-docosanoyl-uridine-3'-phosphate, inverted base dT (idT), etc. The disclosure of such modifications can be found in WO 2011/005861 can
본 발명의 iRNA의 뉴클레오타이드의 기타 변형은 RNAi 제제의 안티센스 가닥 상의 5’ 포스페이트 또는 5’ 포스페이트 모사체, 예를 들어, 5’-말단 포스페이트 또는 포스페이트 모사체를 포함한다. 적합한 포스페이트 모사체는 예를 들어, 미국 특허 공개 공보 제2012/0157511호에 기재되어 있고, 이의 전문은 본원에 참조로 인용된다. Other modifications of the nucleotides of an iRNA of the invention include a 5' phosphate or 5' phosphate mimetic on the antisense strand of an RNAi agent, eg , a 5'-terminal phosphate or phosphate mimetic. Suitable phosphate mimetics are described, for example, in US Patent Publication No. 2012/0157511, incorporated herein by reference in its entirety.
V. 리간드에 접합된 iRNAV. iRNA conjugated to a ligand
본 발명의 iRNA의 RNA의 또 다른 변형은 iRNA의 활성, 세포 분포, iRNA의 세포 흡수를 증진시키는 하나 이상의 리간드, 모이어티 또는 접합체를 RNA에 화학적으로 연결하는 것을 포함한다. 상기 모이어티는 콜레스테롤 모이어티 (문헌참조: Letsinger et al., Proc. Natl. Acid. Sci. USA, 1989,86:6553-6556)와 같은 지질 모이어티, 콜산(문헌참조: Manoharan et al., Biorg. Med. Chem. Let., 1994,4:1053-1060), 티오에테르, 예를 들어, 베릴-S-트리틸티올(문헌참조: Manoharan et al., Ann. N.Y. Acad. Sci., 1992,660:306-309; Manoharanet al., Biorg. Med. Chem.Let., 1993,3:2765-2770),티오콜레스테롤 (문헌참조: Oberhauser et al., Nucl. Acids Res., 1992,20:533-538), 지방족 쇄, 예를 들어, 도데칸디올 또는 운데실 잔기 (문헌참조: Saison-Behmoaras et al.,EMBOJ, 1991, 10:1111-1118; Kabanovet et al., FEBS Lett., 1990, 259:327-330; Svinarchuk et al., Biochimie, 1993, 75:49-54), 인지질, 예를 들어, 디-헥사데실-rac-글리세롤 또는 트리에틸-암모늄 1,2-디-O-헥사데실-rac-글리세로-3-포스포네이트(문헌참조: Manoharan et al., Tetrahedron Lett., 1995,36:3651-3654; Shea et. al., Nucl. Acids Res., 1990, 18:3777-3783), 폴리아민 또는 폴리에틸렌 글리콜 쇄(문헌참조: Manoharan et al.,Nucleosides & Nucleotides, 1995,14:969-973),또는 아다만탄 아세트산(문헌참조: Manoharan et al.,Tetrahedron Lett., 1995,36:3651-3654),팔미틸 모이어티 (문헌참조: Mishra et al.,Biochim.Biophys.Acta,1995,1264:229-237),또는 옥타데실아민 또는 헥실아미노-카보닐옥시콜레스테롤 모이어티 (문헌참조: Crooke et al., J. Pharmacol. Exp. Ther.,1996, 277:923-937)를 포함하지만 이에 제한되지 않는다. Another modification of the RNA of the iRNA of the present invention involves chemically linking to the RNA one or more ligands, moieties or conjugates that enhance the activity of the iRNA, cellular distribution, or cellular uptake of the iRNA. Such moieties include lipid moieties such as cholesterol moieties (Letsinger et al., Proc. Natl. Acid. Sci. USA , 1989,86:6553-6556), cholic acid (Manoharan et al . , Biorg. Med. Chem. Let ., 1994, 4:1053-1060), thioethers such as beryl-S-tritylthiol (see Manoharan et al . , Ann. NY Acad. Sci ., 1992 , 660 : 306-309 ; 533-538), aliphatic chains such as dodecanediol or undecyl residues (see Saison-Behmoaras et al . , EMBOJ , 1991, 10:1111-1118; Kabanovet et al . , FEBS Lett ., 1990 Svinarchuk et al . , Biochimie , 1993, 75:49-54), phospholipids such as di-hexadecyl-rac-glycerol or triethyl-ammonium 1,2-di-O- Hexadecyl-rac-glycero-3-phosphonate (see Manoharan et al . , Tetrahedron Lett ., 1995, 36:3651-3654; Shea et. al. , Nucl. Acids Res ., 1990, 18: 3777-3783), polyamine or polyethylene glycol chains (see Manoharan et al . , Nucleosides & Nucleotides , 1995, 14:969-973), or adamantane acetic acid (see Manoharan et al . , Tetrahedron Lett ., 1995, 36:3651-3654), palmityl moiety (see Mishra et al . , Biochim.B iophys . Acta, 1995, 1264:229-237), or an octadecylamine or hexylamino-carbonyloxycholesterol moiety (see Crooke et al . , J. Pharmacol. Exp. Ther ., 1996, 277:923-937), but is not limited thereto.
하나의 구현예에서, 리간드는 이것이 도입되는 iRNA 제제의 분포, 표적화 또는 수명을 변경시킨다. 일부 구현예에서 리간드는 예를 들어, 리간드가 부재인 종과 비교하여 선택된 표적, 예를 들어 분자, 세포 또는 세포 유형, 구획, 예를 들어 세포 또는 기관 구획, 조직, 기관 또는 신체의 영역에 대해 증진된 친화성을 제공한다. 예시적인 리간드는 듀플렉스된 핵산에서 듀플렉스 쌍형성에 관여하지 않는다. In one embodiment, the ligand alters the distribution, targeting or longevity of the iRNA agent into which it is introduced. In some embodiments, a ligand is directed against a selected target, e.g., a molecule, cell or cell type, compartment, e.g., cell or organ compartment, tissue, organ, or region of the body, compared to a species in which the ligand is absent. Provides enhanced affinity. Exemplary ligands do not participate in duplex pairing in duplexed nucleic acids.
리간드는 또한 표적화 그룹, 예를 들어, 세포 또는 조직 표적화제, 예를 들어, 렉틴, 당단백질, 지질 또는 단백질, 예를 들어, 콩팥 세포와 같은 특정 세포 유형에 결합하는 항체를 포함할 수 있다. 표적화 그룹은 티로트로핀, 멜라노트로핀, 렉틴, 당단백질, 계면활성제 단백질 A, 뮤신 탄수화물, 다가 락토스, 1가 갈락토스, N-아세틸-갈락토스아민, N-아세틸-글루코스아민 다가 만노스, 다가 푸코스, 글리코실화된 폴리아미노산, 다가 갈락토스, 트랜스페린, 비스포스포네이트, 폴리글루타메이트, 폴리아스파르테이트, 지질, 콜레스테롤, 스테로이드, 담즙산, 폴레이트, 비타민 B12, 비타민 A, 비오틴, 또는 RGD 펩타이드 또는 RGD 펩타이드 모사체일 수 있다. 특정 구현예에서, 리간드는 1가 또는 다가의 갈락토스를 포함한다. 특정 구현예에서, 리간드는 콜레스테롤을 포함한다. A ligand may also include a targeting group, eg, a cell or tissue targeting agent, eg, a lectin, glycoprotein, lipid or protein, eg, an antibody that binds to a specific cell type, such as kidney cells. Targeting groups include thyrotropin, melanotropin, lectin, glycoprotein, surfactant protein A, mucin carbohydrate, polyvalent lactose, monovalent galactose, N-acetyl-galactosamine, N-acetyl-glucosamine polyvalent mannose, multivalent fu course, glycosylated polyamino acids, polyvalent galactose, transferrin, bisphosphonates, polyglutamates, polyaspartates, lipids, cholesterol, steroids, bile acids, folates, vitamin B12, vitamin A, biotin, or RGD peptides or RGD peptide mimetics can be In certain embodiments, the ligand comprises monovalent or polyvalent galactose. In certain embodiments, the ligand includes cholesterol.
본 발명의 리간드-접합된 올리고뉴클레오타이드는 (하기된) 올리고뉴클레오타이드 상으로 연결 분자의 부착으로부터 유래된 것과 같은 펜던트 반응성 관능기를 함유한 올리고뉴클레오타이드의 사용에 의해 합성될 수 있다. 상기 반응성 올리고뉴클레오타이드는 상업적으로 가용한 리간드, 임의의 다양한 보호기를 보유하는 합성된 리간드, 또는 이에 부착된 연결 모이어티를 갖는 리간드와 직접 반응할 수 있다. The ligand-conjugated oligonucleotides of the present invention can be synthesized by the use of oligonucleotides containing pendant reactive functional groups such as those derived from the attachment of a linking molecule onto the oligonucleotide (described below). The reactive oligonucleotides can react directly with commercially available ligands, synthetic ligands with any of a variety of protecting groups, or ligands with linking moieties attached thereto.
본 발명의 접합체에 사용되는 올리고뉴클레오타이드는 널리 공지된 고체상 합성 기술을 통해 편리하고 통상적으로 제조될 수 있다. 당업계에 공지된 상기 합성을 위한 임의의 다른 수단은 추가로 또는 대안적으로 사용될 수 있다. 또한 다른 올리고뉴클레오타이드, 예를 들어, 포스포로티오에이트 및 알킬화된 유도체를 제조하기 위한 유사한 기술을 사용하는 것이 공지되어 있다. The oligonucleotides used in the conjugates of the present invention can conveniently and routinely be prepared through well-known solid phase synthesis techniques. Any other means for such synthesis known in the art may additionally or alternatively be used. It is also known to use similar techniques to prepare other oligonucleotides, such as phosphorothioates and alkylated derivatives.
A. 탄수화물 접합체A. Carbohydrate Conjugates
본 발명의 조성물 및 방법의 일부 구현예에서, iRNA 올리고뉴클레오타이드는 추가로 탄수화물을 포함한다. 탄수화물 접합된 iRNA는 본원에 기재된 바와 같이 생체내 치료학적 사용을 위해 적합한 조성물 뿐만 아니라 핵산의 생체내 전달을 위해 유리하다. 본원에 사용된 바와 같은, “탄수화물”은 각각의 탄소 원자에 결합된 산소, 질소 또는 황 원자와 함께 적어도 6개의 탄소 원자를 갖는 하나 이상의 모노사카라이드 유닛 (선형, 측쇄 또는 사이클릭일 수 있는)으로 구성된 탄수화물 자체인 화합물; 또는 각각의 탄소원자에 결합된 산소, 질소 또는 황 원자와 함께 각각 어도 6개 탄소 원자를 갖는 하나 이상의 모노사카라이드 유닛(선형, 측쇄 또는 사이클릭일 수 있는)으로 구성된 탄수화물 모이어티를 일부로서 갖는 화합물을 언급한다. 대표적인 탄수화물은 당 (모노-, 디-, 트리-, 및 약 4, 5, 6, 7, 8 또는 9개의 모노사카라이드 유닛을 함유하는 올리고사카라이드) 및 폴리사카라이드, 예를 들어, 전분, 글리코겐, 셀룰로스 및 폴리사카라이드 검을 포함한다. 특이적 모노사카라이드는 C5 이상 (예를 들어, C5, C6, C7, 또는 C8) 당을 포함하고; 디사카라이드 및 트리사카라이드는 2개 또는 3개의 모노사카라이드 유닛(예를 들어, C5, C6, C7, 또는 C8)을 갖는 당을 포함한다. In some embodiments of the compositions and methods of the invention, the iRNA oligonucleotide further comprises a carbohydrate. Carbohydrate conjugated iRNAs are advantageous for in vivo delivery of nucleic acids as well as compositions suitable for therapeutic use in vivo as described herein. As used herein, “carbohydrate” refers to one or more monosaccharide units (which may be linear, branched or cyclic) having at least 6 carbon atoms with an oxygen, nitrogen or sulfur atom bonded to each carbon atom. A compound that is a carbohydrate itself composed of; or having as part a carbohydrate moiety consisting of one or more monosaccharide units (which may be linear, branched or cyclic) having at least 6 carbon atoms each with an oxygen, nitrogen or sulfur atom bonded to each carbon atom. mention the compound. Representative carbohydrates include sugars (mono-, di-, tri-, and oligosaccharides containing about 4, 5, 6, 7, 8 or 9 monosaccharide units) and polysaccharides such as starch, These include glycogen, cellulose and polysaccharide gums. Specific monosaccharides include C5 or higher (eg , C5, C6, C7, or C8) sugars; Disaccharides and trisaccharides include sugars having two or three monosaccharide units (eg , C5, C6, C7, or C8).
하나의 구현예에서, 본 발명의 조성물 및 방법에 사용하기 위한 탄수화물 접합체는 모노사카라이드이다. 또 다른 구현예에서, 본 발명의 조성물 및 방법에 사용하기 위한 탄수화물 접합체는 하기로 이루어진 그룹으로부터 선택된다:In one embodiment, carbohydrate conjugates for use in the compositions and methods of the present invention are monosaccharides. In another embodiment, the carbohydrate conjugate for use in the compositions and methods of the present invention is selected from the group consisting of:
화학식 II, formula II,
화학식 III, formula III,
화학식 IV, formula IV,
화학식 V, formula V,
화학식 VI, formula VI,
화학식 VII, formula VII,
화학식 VIII, formula VIII,
화학식 IX, formula IX,
화학식 X, formula X,
화학식 XI, formula XI,
화학식 XII, formula XII,
화학식 XIII, formula XIII,
화학식 XIV, formula XIV,
화학식 XV, formula XV,
화학식 XVI, formula XVI,
화학식 XVII, formula XVII,
화학식 XVIII, formula XVIII,
화학식 XIX, formula XIX,
화학식 XX, formula XX,
화학식 XXI, formula XXI,
화학식 XXII. Formula XXII.
하나의 구현예에서, 모노사카라이드는 N-아세틸갈락토사민, 예를 들어,In one embodiment, the monosaccharide is N-acetylgalactosamine, such as
화학식 II이다. Formula II.
본원에 기재된 구현예에 사용하기 위한 또 다른 대표적인 탄수화물 접합체는 다음을 포함하지만 이에 제한되지 않는다:Another representative carbohydrate conjugate for use in the embodiments described herein includes, but is not limited to:
(화학식 XXIII), X 또는 Y 중 하나가 올리고뉴클레오타이드인 경우, 다른 하나는 수소이다. (Formula XXIII), when one of X or Y is an oligonucleotide, the other is hydrogen.
본 발명의 특정 구현예에서, GalNAc 또는 GalNAc 유도체는 1가 링커를 통해 본 발명의 iRNA 제제에 부착된다. 일부 구현예에서, GalNAc 또는 GalNAc 유도체는 2가 링커를 통해 본 발명의 iRNA 제제에 부착된다. 본 발명의 또 다른 구현예에서, GalNAc 또는 GalNAc 유도체는 3가 링커를 통해 본 발명의 iRNA 제제에 부착된다. In certain embodiments of the invention, GalNAc or a GalNAc derivative is attached to an iRNA agent of the invention via a monovalent linker. In some embodiments, GalNAc or a GalNAc derivative is attached to an iRNA agent of the invention via a bivalent linker. In another embodiment of the present invention, GalNAc or a GalNAc derivative is attached to an iRNA agent of the present invention via a trivalent linker.
하나의 구현예에서, 본 발명의 이중 가닥 RNAi 제제는 iRNA 제제에 부착된 하나의 GalNAc 또는 GalNAc 유도체를 포함한다. 또 다른 구현예에서, 본 발명의 이중 가닥 RNAi 제제는 다수의 (예를 들어, 2, 3, 4, 5, 또는 6개) GalNAc 또는 GalNAc 유도체를 포함하고, 각각은 독립적으로 다수의 1가 링커를 통해 이중가닥 RNAi 제제의 다수의 뉴클레오타이드에 부착되어 있다.In one embodiment, the double-stranded RNAi agent of the present invention comprises one GalNAc or GalNAc derivative attached to the iRNA agent. In another embodiment, the double-stranded RNAi agent of the invention comprises multiple (e.g. , 2, 3, 4, 5, or 6) GalNAc or GalNAc derivatives, each independently containing multiple monovalent linkers. It is attached to a number of nucleotides of the double-stranded RNAi agent via.
일부 구현예에서, 예를 들어, 본 발명의 iRNA 제제의 2개의 가닥이 한 가닥의 3'-말단과 각각의 다른 가닥의 5'-말단 사이에 중단되지 않은 뉴클레오타이드 쇄에 의해 연결되어 다수의 쌍을 형성하지 않은 뉴클레오타이드를 포함하는 헤어핀 루프를 형성하는 하나의 더 큰 분자의 일부인 경우, 헤어핀 루프 내의 각각의 쌍을 형성하지 않은 뉴클레오타이드는 1가 링커를 통해 부착된 GalNAc 또는 GalNAc 유도체를 독립적으로 포함할 수 있다. 헤어핀 루프는 또한 듀플렉스의 하나의 가닥에 연장된 오버행에 의해 형성될 수 있다. In some embodiments, for example, the two strands of an RNAi agent of the invention are linked by uninterrupted nucleotide chains between the 3'-end of one strand and the 5'-end of each other strand to form multiple pairs. When part of one larger molecule that forms a hairpin loop containing nucleotides that do not form a nucleotide, each unpaired nucleotide within the hairpin loop may independently contain a GalNAc or GalNAc derivative attached via a monovalent linker. can A hairpin loop may also be formed by an extended overhang on one strand of the duplex.
일부 구현예에서, 탄수화물 접합체는 추가로 상기된 바와 같은 하나 이상의 추가의 리간드, 이에 제한되지 않지만 예를 들어, PK 조절제 또는 세포 투과 펩타이드를 포함한다.In some embodiments, the carbohydrate conjugate further comprises one or more additional ligands as described above, such as but not limited to, PK modulators or cell penetrating peptides.
본 발명에 사용하기 위해 적합한 추가의 탄수화물 접합체는 PCT 공개공보 WO 2014/179620 및 WO 2014/179627에 기재된 것들을 포함하고, 이의 각각의 전문은 본원에 참조로 인용된다.Additional carbohydrate conjugates suitable for use in the present invention include those described in PCT Publication Nos. WO 2014/179620 and WO 2014/179627, each of which is incorporated herein by reference in its entirety.
B. 링커B. linker
일부 구현예에서, 본원에 기재된 접합체 또는 리간드는 절단될 수 있거나 절단되지 않을 수 있는 다양한 링커를 사용하여 iRNA 올리고뉴클레오타이드에 부착될 수 있다. In some embodiments, a conjugate or ligand described herein may be attached to an iRNA oligonucleotide using a variety of linkers that may or may not be cleaved.
용어 "링커" 또는 "연결 그룹"은 화합물의 두 부분을 연결하는, 예를 들어 화합물의 두 부분을 공유적으로 부착시키는 유기 모이어티를 의미한다. 링커는 전형적으로 직접적인 결합 또는 산소 또는 황과 같은 원자, 유닛, 예를 들어 NR8, C(O), C(O)NH, SO, SO2,SO2NH또는 원자 쇄를 포함하고, 이제 제한되지 않지만 예를 들어, 치환되거나 비치환된 알킬, 치환되거나 비치환된 알케닐, 치환되거나 비치환된 알키닐, 아릴알킬, 아릴알케닐, 아릴알키닐, 헤테로아릴알킬, 헤테로아릴알케닐, 헤테로아릴알키닐, 헤테로사이클릴알킬, 헤테로사이클릴알케닐, 헤테로사이클릴알키닐, 아릴, 헤테로아릴, 헤테로사이클릴, 사이클로알킬, 사이클로알케닐, 알킬아릴알킬, 알킬아릴알케닐, 알킬아릴알키닐, 알케닐아릴알킬, 알케닐아릴알케닐, 알케닐아릴알키닐, 알키닐아릴알킬, 알키닐아릴알케닐, 알키닐아릴알키닐, 알킬헤테로아릴알킬, 알킬헤테로아릴알케닐, 알킬헤테로아릴알키닐, 알케닐헤테로아릴알킬, 알케닐헤테로아릴알케닐, 알케닐헤테로아릴알키닐, 알키닐헤테로아릴알킬, 알키닐헤테로아릴알케닐, 알키닐헤테로아릴알키닐, 알킬헤테로사이클릴알킬, 알킬헤테로사이클릴알케닐, 알킬헤테로사이클릴알키닐, 알케닐헤테로사이클릴알킬, 알케닐헤테로사이클릴알케닐, 알케닐헤테로사이클릴알키닐, 알키닐헤테로사이클릴알킬, 알키닐헤테로사이클릴알케닐, 알키닐헤테로사이클릴알키닐, 알킬아릴, 알케닐아릴, 알키닐아릴, 알킬헤테로아릴, 알케닐헤테로아릴, 알키닐헤테로아릴를 포함하고, 여기서 하나 이상의 메틸렌은 O, S, S(O), SO2, N(R8), C(O),치환되거나 비치환된 아릴, 치환되거나 비치환된 헤테로아릴, 또는 치환되거나 비치환된 헤테로사이클릭에 의해 중단되거나 말단화될 수 있고; 여기서, R8은 수소, 아실, 지방족 또는 치환된 지방족이다. 하나의 구현예에서, 링커는 약 1-24개 원자, 2-24, 3-24, 4-24, 5-24, 6-24, 6-18, 7-18, 8-18개 원자, 7-17, 8-17, 6-16, 7-17, 또는 8-16개 원자이다.The term “linker” or “linking group” means an organic moiety that connects two parts of a compound, eg, covalently attaches the two parts of a compound. Linkers typically include direct bonds or atoms, units such as oxygen or sulfur, such as NR8, C(O), C(O)NH, SO, SO 2 , SO 2 NH, or chains of atoms, and are now not limited to but for example, substituted or unsubstituted alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, arylalkyl, arylalkenyl, arylalkynyl, heteroarylalkyl, heteroarylalkenyl, heteroaryl Alkynyl, heterocyclylalkyl, heterocyclylalkenyl, heterocyclylalkynyl, aryl, heteroaryl, heterocyclyl, cycloalkyl, cycloalkenyl, alkylarylalkyl, alkylarylalkenyl, alkylarylalkynyl, al kenylarylalkyl, alkenylarylalkenyl, alkenylarylalkynyl, alkynylarylalkyl, alkynylarylalkenyl, alkynylarylalkynyl, alkylheteroarylalkyl, alkylheteroarylalkenyl, alkylheteroarylalkynyl, Alkenylheteroarylalkyl, alkenylheteroarylalkenyl, alkenylheteroarylalkynyl, alkynylheteroarylalkyl, alkynylheteroarylalkenyl, alkynylheteroarylalkynyl, alkylheterocyclylalkyl, alkylheterocyclylal kenyl, alkylheterocyclylalkynyl, alkenylheterocyclylalkyl, alkenylheterocyclylalkenyl, alkenylheterocyclylalkynyl, alkynylheterocyclylalkyl, alkynylheterocyclylalkenyl, alkynylheterocyclyl including alkynyl, alkylaryl, alkenylaryl, alkynylaryl, alkylheteroaryl, alkenylheteroaryl, alkynylheteroaryl, wherein one or more methylene is O, S, S(O), SO 2 , N(R8 ), C(O), substituted or unsubstituted aryl, substituted or unsubstituted heteroaryl, or substituted or unsubstituted heterocyclic; wherein R8 is hydrogen, acyl, aliphatic or substituted aliphatic. In one embodiment, the linker is about 1-24 atoms, 2-24, 3-24, 4-24, 5-24, 6-24, 6-18, 7-18, 8-18 atoms, 7 -17, 8-17, 6-16, 7-17, or 8-16 atoms.
절단가능한 연결 그룹은 세포 외부에서 충분히 안정할 수 있지만 표적 세포로 진입이 절단되어 링커가 함께 유지하고 있는 2개의 부분을 방출시키는 그룹이다. 하나의 구현예에서, 절단 가능한 연결 그룹은 대상체의 혈액에서 또는 제2 참조 조건 (예를 들어, 혈액 또는 혈청 중에서 발견되는 조건을 모방하거나 나타내는 것으로 선택될 수 있는)하에서 보다 표적 세포에서 또는 제1 참조 조건 (예를 들어, 세포내 조건을 모방하거나 나타내도록 선택될 수 있는)하에서 적어도 약 10배, 20배, 30배, 40배, 50배, 60배, 70배, 80배, 90배 이상 또는 적어도 약 100배 신속하게 절단된다.A cleavable linking group is a group that can be sufficiently stable outside the cell, but upon entry into the target cell is cleaved, releasing the two parts that the linker holds together. In one embodiment, the cleavable linking group is in the target cell or in a first, rather than in the subject's blood or under a second reference condition (eg, which can be selected to mimic or represent a condition found in blood or serum). at least about 10-fold, 20-fold, 30-fold, 40-fold, 50-fold, 60-fold, 70-fold, 80-fold, 90-fold or more under reference conditions (which may be selected to mimic or represent intracellular conditions, for example) or at least about 100 times faster.
절단가능한 연결 그룹은 절단제, 예를 들어, pH, 산화환원 전위 또는 분해 분자의 존재에 민감할 수 있다. 일반적으로, 절단제는 혈청 또는 혈액에서 보다 세포 내부에서 보다 높은 수준 또는 활성인 상태로 보다 만연되어 있거나 발견된다. 상기 분해제의 예는 다음을 포함한다: 특정 기질에 대해 선택되거나 어떠한 기질 특이성을 갖지 않는 산화환원제로서, 이는 예를 들어, 산화 또는 환원 효소 또는 환원제, 예를 들어, 환원에 의해 산화환원 절단가능한 연결 그룹을 분해시킬 수 있는 세포에 존재하는 머캅탄을 포함하는 산화환원제; 에스테라제; 엔도좀 또는 산성 환경을 생성시킬 수 있는 제제, 예를 들어, 5 이하의 pH를 유도하는 것들; 일반산으로서 작용함에 의해 산 절단가능한 연결 그룹을 가수분해시키거나 분해할 수 있는 효소, 펩티다제 (이는 기질 특이적일 수 있다), 및 포스파타제.A cleavable linking group may be sensitive to the presence of a cleavage agent, eg pH, redox potential or degrading molecule. Generally, cleavage agents are more prevalent or found at higher levels or activity inside cells than in serum or blood. Examples of such degradants include: redox agents selected for a particular substrate or having no substrate specificity, which are capable of redox cleavage, for example by oxidizing or reducing enzymes or reducing agents, for example reduction. redox agents including mercaptans present in cells capable of degrading linking groups; esterase; Agents that can create an endosome or an acidic environment, such as those that induce a pH of 5 or less; Enzymes capable of hydrolyzing or cleaving acid cleavable linking groups by acting as common acids, peptidases (which may be substrate specific), and phosphatases.
절단가능한 연결 그룹, 예를 들어, 디설파이드 결합은 pH에 민감할 수 있다. 사람 혈청의 pH는 7.4이고, 평균 세포내 pH는 약간 보다 낮아 약 7.1-7.3이다. 엔도좀은 5.5-6.0의 범위에서 보다 산성의 pH를 갖고, 리소좀은 약 5.0에서 심지어 보다 산성의 pH를 갖는다. 일부 링커는 선택된 pH에서 절단되어 세포 내부의 리간드로부터 양이온성 지질을 방출하거나 세포의 목적하는 구획으로 양이온성 지질을 방출하는 절단가능한 연결 그룹을 갖는다. A cleavable linking group, such as a disulfide bond, may be pH sensitive. The pH of human serum is 7.4, and the average intracellular pH is slightly lower, about 7.1-7.3. Endosomes have a more acidic pH in the range of 5.5-6.0, and lysosomes have an even more acidic pH at about 5.0. Some linkers have cleavable linking groups that are cleaved at a selected pH to release the cationic lipid from the ligand inside the cell or to the desired compartment of the cell.
링커는 특정 효소에 의해 절단될 수 있는 절단가능한 연결 그룹을 포함할 수 있다. 링커로 혼입된 절단가능한 연결 그룹의 유형은 표적화될 세포에 의존할 수 있다. 예를 들어, 간-표적화 리간드는 에스테르 그룹을 포함하는 링커를 통해 양이온성 지질에 연결될 수 있다. 간 세포에는 에스테라제가 풍부하고, 따라서 링커는 에스테라제가 풍부하지 않은 세포 유형에서 보다 간 세포에서 보다 효율적으로 절단된다. 에스테라제가 풍부한 다른 세포 유형은 폐, 신피질 및 고환의 세포를 포함한다.A linker can include a cleavable linking group that can be cleaved by a specific enzyme. The type of cleavable linking group incorporated into the linker may depend on the cell to be targeted. For example, a liver-targeting ligand can be linked to a cationic lipid via a linker comprising an ester group. Liver cells are rich in esterases and therefore linkers are cleaved more efficiently in liver cells than in cell types that are not rich in esterases. Other cell types rich in esterases include cells of the lung, neocortex and testis.
펩타이드 결합을 함유하는 링커는 간 세포 및 활막세포와 같은 펩티다제가 풍부한 세포 유형을 표적화하는 경우 사용될 수 있다. Linkers containing peptide bonds can be used when targeting peptidase-rich cell types such as liver cells and synovial cells.
일반적으로, 후보 절단가능한 연결 그룹의 적합성은 후보 연결 그룹을 절단하는 분해제(또는 조건)의 능력을 시험함으로써 평가될 수 있다. 또한 혈액 내에서 또는 다른 비표적 조직과 접촉할 때 절단에 저항하는 능력에 대해 후보 절단가능한 연결 그룹을 테스트하는 것이 바람직할 수 있다. 따라서, 당업자는 제1 조건과 제2 조건 사이의 절단에 대한 상대적인 감수성을 결정할 수 있고, 여기서 제1 조건은 표적 세포에서 절단을 나타내도록 선택되고, 제2 조건은 다른 조직 또는 생물학적 유체, 예를 들어 혈액 또는 혈청 내 절단을 나타내도록 선택된다. 평가는 무세포 시스템, 세포, 세포 배양물, 기관 또는 조직 배양물 또는 전체 동물에서 수행될 수 있다. 무세포 또는 배양 조건에서 초기 평가를 수행하고 전체 동물에서 추가의 평가에 의해 확인하기 위해 유용할 수 있다. 일부 구현예에서, 유용한 후보 화합물은 혈액 또는 혈청 (또는 세포외 조건을 모방하도록 선택된 시험관내 조건하에서)과 비교하여 세포(또는 세포내 조건을 모방하도록 선택된 시험관내 조건하에서)에서 적어도 약 2, 4, 10, 20, 30, 40, 50, 60, 70, 80, 90, 또는 약 100배 이상 신속하게 절단된다. In general, the suitability of a candidate cleavable linking group can be assessed by testing the ability of a degrading agent (or condition) to cleave the candidate linking group. It may also be desirable to test candidate cleavable linking groups for their ability to resist cleavage in blood or when in contact with other non-target tissues. Thus, one skilled in the art can determine the relative susceptibility to cleavage between a first condition and a second condition, wherein the first condition is selected to exhibit cleavage in the target cell and the second condition is selected to exhibit cleavage in another tissue or biological fluid, such as For example, it is selected to show cleavage in blood or serum. Assessments can be performed in cell-free systems, cells, cell cultures, organ or tissue cultures, or whole animals. It may be useful to perform initial assessments in cell-free or cultured conditions and to confirm by further assessments in whole animals. In some embodiments, useful candidate compounds have a concentration of at least about 2, 4 in cells (or under in vitro conditions selected to mimic intracellular conditions) compared to blood or serum (or under in vitro conditions selected to mimic extracellular conditions). , 10, 20, 30, 40, 50, 60, 70, 80, 90, or about 100 times more rapidly.
i. 산화환원 절단가능한 연결 그룹i. Redox cleavable linking group
하나의 구현예에서, 절단가능한 연결 그룹은 환원 또는 산화시 절단되는 산화환원 절단가능한 연결 그룹이다. 환원 절단가능한 연결 그룹의 예는 디설파이드 연결 그룹 (-S-S-)이다. 후보 절단 가능한 연결 그룹이 적합한 "환원적으로 절단가능한 연결 그룹"인지 또는 예를 들어 특정 iRNA 모이어티 및 특정 표적화제와 함께 사용하기에 적합한지의 여부를 결정하기 위해, 당업자는 본원에 기재된 방법을 살펴볼 수 있다. 예를 들어, 후보물은 세포, 예를 들어 표적 세포에서 관찰되는 절단 속도를 모방하는 당업계에 공지된 시약을 사용하여 디티오트레이톨(DTT) 또는 기타 환원제를 사용한 항온처리에 의해 평가될 수 있다. 후보물은 또한 혈액 또는 혈청 조건을 모방하도록 선택된 조건 하에서 평가될 수 있다. 하나에서, 후보 화합물은 혈액에서 최대 약 10%까지 절단된다. 다른 구현예에서, 유용한 후보 화합물은 혈액 (또는 세포외 조건을 모방하도록 선택된 시험관내 조건하에서)과 비교하여 세포(또는 세포내 조건을 모방하도록 선택된 시험관내 조건하에서)에서 적어도 약 2, 4, 10, 20, 30, 40, 50, 60, 70, 80, 90, 또는 약 100배 보다 신속하게 분해된다. 후보 화합물의 절단 속도는 세포내 배지를 모방하도록 선택된 조건 및 세포외 배지를 모방하도록 선택된 조건과 비교하여 표준 효소 동역학 검정을 사용하여 결정될 수 있다.In one embodiment, the cleavable linking group is a redox cleavable linking group that is cleaved upon reduction or oxidation. An example of a reductively cleavable linking group is a disulfide linking group (-S-S-). To determine whether a candidate cleavable linking group is a suitable "reductively cleavable linking group" or suitable for use with, for example, a specific iRNA moiety and a specific targeting agent, one skilled in the art will look to the methods described herein. can For example, candidates can be evaluated by incubation with dithiothreitol (DTT) or other reducing agents using reagents known in the art that mimic the cleavage rates observed in cells, eg, target cells. have. Candidates may also be evaluated under conditions selected to mimic blood or serum conditions. In one, the candidate compound is cleaved in the blood by up to about 10%. In another embodiment, a useful candidate compound has a concentration of at least about 2, 4, 10 in cells (or under in vitro conditions selected to mimic intracellular conditions) compared to blood (or under in vitro conditions selected to mimic extracellular conditions). , 20, 30, 40, 50, 60, 70, 80, 90, or about 100 times faster. The rate of cleavage of a candidate compound can be determined using standard enzyme kinetic assays by comparing conditions selected to mimic the intracellular medium and conditions selected to mimic the extracellular medium.
ii. 포스페이트 기반 절단가능한 연결 그룹ii. Phosphate-based cleavable linking groups
특정 구현예에서, 절단가능한 링커는 포스페이트 기반 절단가능한 연결 그룹을 포함한다. 표스페이트 기반 절단가능한 연결 그룹은 포스페이트 그룹을 분해하거나 가수분해하는 제제에 의해 절단된다. 세포에서 포스페이트 그룹을 절단하는 제제의 예는 세포 내 포스파타제와 같은 효소이다. 포스페이트 기반 연결 그룹의 예는 -O-P(O)(ORk)-O-, -O-P(S)(ORk)-O-, -O-P(S)(SRk)-O-, -S-P(O)(ORk)-O-, -O-P(O)(ORk)-S-, -S-P(O)(ORk)-S-, -O-P(S)(ORk)-S-, -S-P(S)(ORk)-O-, -O-P(O)(Rk)-O-, -O-P(S)(Rk)-O-, -S-P(O)(Rk)-O-, -S-P(S)(Rk)-O-, -S-P(O)(Rk)-S-, -O-P(S)(Rk)-S이고, 여기서 Rk는 각각 독립적으로 C1-C20 알킬, C1-C20 할로알킬, C6-C10 아릴, 또는 C7-C12 아르알킬일 수 있다. 예시적인 구현예는 -O-P(O)(OH)-O-, -O-P(S)(OH)-O-, -O-P(S)(SH)-O-, -S-P(O)(OH)-O-, -O-P(O)(OH)-S-, -S-P(O)(OH)-S-, -O-P(S)(OH)-S-, -S-P(S)(OH)-O-, -O-P(O)(H)-O-, -O-P(S)(H)-O-, -S-P(O)(H)-O, -S-P(S)(H)-O-, -S-P(O)(H)-S-, 및 -O-P(S)(H)-S-를 포함한다. 하나의 구현예에서, 포스페이트 기반 연결 그룹은 -O-P(O)(OH)-O-이다. 이들 후보물은 상기된 것들과 유사한 방법을 사용하여 평가될 수 있다.In certain embodiments, a cleavable linker comprises a phosphate-based cleavable linking group. Tablesphate-based cleavable linking groups are cleaved by agents that degrade or hydrolyze the phosphate group. Examples of agents that cleave phosphate groups in cells are enzymes such as intracellular phosphatases. Examples of phosphate-based linking groups are -O-P(O)(ORk)-O-, -O-P(S)(ORk)-O-, -O-P(S)(SRk)-O-, -S-P(O)(ORk) )-O-, -O-P(O)(ORk)-S-, -S-P(O)(ORk)-S-, -O-P(S)(ORk)-S-, -S-P(S)(ORk)- O-, -O-P(O)(Rk)-O-, -O-P(S)(Rk)-O-, -S-P(O)(Rk)-O-, -S-P(S)(Rk)-O- , -S-P(O)(Rk)-S-, -O-P(S)(Rk)-S, wherein each Rk is independently C1-C20 alkyl, C1-C20 haloalkyl, C6-C10 aryl, or C7- C12 aralkyl. Exemplary embodiments include -O-P(O)(OH)-O-, -O-P(S)(OH)-O-, -O-P(S)(SH)-O-, -S-P(O)(OH)- O-, -O-P(O)(OH)-S-, -S-P(O)(OH)-S-, -O-P(S)(OH)-S-, -S-P(S)(OH)-O- , -O-P(O)(H)-O-, -O-P(S)(H)-O-, -S-P(O)(H)-O, -S-P(S)(H)-O-, -S-P (O)(H)-S-, and -O-P(S)(H)-S-. In one embodiment, the phosphate based linking group is -O-P(O)(OH)-O-. These candidates can be evaluated using methods similar to those described above.
iii. 산 절단가능한 연결 그룹iii. acid cleavable linking group
특정 구현예에서, 절단가능한 링커는 산 절단가능한 연결 그룹을 포함한다. 산 절단가능한 연결 그룹은 산성 조건하에서 절단되는 연결 그룹이다. 일부 구현예에서, 산 절단가능한 연결 그룹은 pH가 약 6.5 이하 (예를 들어, 약 6.0, 5,75, 5.5, 5.25, 5.0 이하)인 산성 환경에서 또는 일반 산으로서 작용할 수 있는 효소와 같은 제제에 의해 절단된다. 세포에서 엔도좀 및 리소좀과 같은 특정 낮은 pH 기관은 산 절단 가능한 연결 그룹에 대한 절단 환경을 제공할 수 있다. 산 절단가능한 연결 그룹의 예는 하이드라존, 에스테르, 및 아미노산의 에스테르를 포함하지만 이에 제한되지 않는다. 산 절단가능한 그룹은 화학식 -C=NN-, C(O)O, 또는 -OC(O)를 가질 수 있다. 예시적인 구현예는 에스테르의 산소에 부착된 탄소 (알콕시 그룹)가 아릴 그룹, 치환된 알킬 그룹 또는 3급 알킬 그룹, 예를 들어, 디메틸 펜틸 또는 t-부틸인 경우이다. 이들 후보물은 상기된 것들과 유사한 방법을 사용하여 평가될 수 있다. In certain embodiments, a cleavable linker comprises an acid cleavable linking group. An acid cleavable linking group is a linking group that is cleaved under acidic conditions. In some embodiments, the acid cleavable linking group is an acidic environment with a pH of about 6.5 or less (e.g., about 6.0, 5,75, 5.5, 5.25, 5.0 or less) or an agent such as an enzyme that can act as a common acid. is cut by Certain low pH organelles in cells, such as endosomes and lysosomes, can provide a cleavage environment for acid cleavable linking groups. Examples of acid cleavable linking groups include, but are not limited to, hydrazones, esters, and esters of amino acids. An acid cleavable group can have the formula -C=NN-, C(O)O, or -OC(O). An exemplary embodiment is when the carbon (alkoxy group) attached to the oxygen of the ester is an aryl group, substituted alkyl group or tertiary alkyl group, such as dimethyl pentyl or t-butyl. These candidates can be evaluated using methods similar to those described above.
iv. 에스테르 기반 연결 그룹iv. Ester-based linking groups
또 다른 구현예에서, 절단가능한 링커는 에스테르 기반 절단가능한 연결 그룹을 포함한다. 에스테르 기반 절단가능한 연결 그룹은 세포내 에스테라제 및 아미다제와 같은 효소에 의해 절단된다. 에스테르 기반 절단가능한 연결 그룹의 예는 알킬렌, 알케닐렌 및 알키닐렌 그룹의 에스테르를 포함하지만 이에 제한되지 않는다. 에스테르 절단가능한 연결 그룹은 일반식 -C(O)O- 또는 -OC(O)-를 갖는다. 이들 후보물은 상기된 것들과 유사한 방법을 사용하여 평가될 수 있다.In another embodiment, a cleavable linker comprises an ester-based cleavable linking group. Ester-based cleavable linking groups are cleaved by enzymes such as intracellular esterases and amidases. Examples of ester-based cleavable linking groups include, but are not limited to, esters of alkylene, alkenylene, and alkynylene groups. Ester cleavable linking groups have the general formula -C(O)O- or -OC(O)-. These candidates can be evaluated using methods similar to those described above.
v. 펩타이드-기반 절단 그룹v. Peptide-based cleavage group
여전히 또 다른 구현예에서, 절단가능한 링커는 펩타이드 기반 절단가능한 연결 그룹을 포함한다. 펩타이드 기반 절단가능한 연결 그룹은 세포에서 펩티다제 및 프로테아제와 같은 효소에 의해 절단된다. 펩타이드 기반 절단가능한 연결 그룹은 아미노산 사이에 형성된 펩타이드 결합이고 올리고펩타이드 (예를 들어, 디펩타이드, 트리펩타이드 등) 및 폴리펩타이드를 생성한다. 펩타이드 기반 절단가능한 그룹은 아미드 그룹 (-C(O)NH-)을 포함하지 않는다. 아미드 그룹은 임의의 알킬렌, 알케닐렌 또는 알키넬렌 사이에 형성될 수 있다. 펩타이드 결합은 아미노산 사이에 형성된 특별한 유형의 아미드 결합이고 펩타이드 및 단백질을 생성한다. 펩타이드 기반 절단 그룹은 일반적으로 펩타이드 및 단백질을 생성하는 아미노산 사이에 형성된 펩타이드 결합 (즉, 아미드 결합)으로 제한되고, 전체 아미드 기능성 그룹을 포함하지 않는다. 펩타이드-기반 절단가능한 연결 그룹은 일반 화학식 - NHCHRAC(O)NHCHRBC(O)-을 갖고, 여기서, RA 및 Rb는 2개의 인접한 아미노산의 R 그룹이다. 이들 후보물은 상기된 것들과 유사한 방법을 사용하여 평가될 수 있다. In yet another embodiment, a cleavable linker comprises a peptide-based cleavable linking group. Peptide-based cleavable linking groups are cleaved by enzymes such as peptidases and proteases in cells. Peptide-based cleavable linking groups are peptide bonds formed between amino acids, resulting in oligopeptides (eg, dipeptides, tripeptides, etc.) and polypeptides. A peptide-based cleavable group does not contain an amide group (-C(O)NH-). Amide groups can be formed between any alkylene, alkenylene or alkynylene. A peptide bond is a special type of amide bond formed between amino acids, resulting in peptides and proteins. Peptide-based cleavage groups are generally limited to peptide bonds formed between the peptide and the amino acids that make up the protein (i.e., amide bonds), and do not include the entire amide functional group. Peptide-based cleavable linking groups have the general formula NHCHRAC(O)NHCHRBC(O)-, where RA and Rb are R groups of two adjacent amino acids. These candidates can be evaluated using methods similar to those described above.
하나의 구현예에서, 본 발명의 iRNA는 링커를 통해 탄수화물에 접합된다. 본 발명의 조성물 및 방법의 링커와 iRNA 탄수화물 접합체의 비제한적인 예는 다음을 포함하지만 이에 제한되지 않는다:In one embodiment, an iRNA of the invention is conjugated to a carbohydrate via a linker. Non-limiting examples of linker and iRNA carbohydrate conjugates of the compositions and methods of the present invention include, but are not limited to:
(화학식 XXIV), (Formula XXIV),
(화학식 XXV), (Formula XXV),
(화학식 XXVI), (formula XXVI),
(화학식 XXVII), (Formula XXVII),
(화학식 XXVIII), (Formula XXVIII),
(화학식 XXIX), (Formula XXIX),
(화학식 XXX), 및 (Formula XXX), and
(화학식 XXXI), (formula XXXI),
X 또는 Y 중 하나가 올리고뉴클레오타이드인 경우, 다른 하나는 수소이다.When either X or Y is an oligonucleotide, the other is hydrogen.
본 발명의 조성물 및 방법의 특정 구현예에서, 리간드는 2가 또는 3가 측쇄 링커를 통해 부착된 하나 이상의 “GalNAc” (N-아세틸갈락토사민) 유도체이다. In certain embodiments of the compositions and methods of the present invention, the ligand is one or more “GalNAc” (N-acetylgalactosamine) derivatives attached through a divalent or trivalent side chain linker.
하나의 구현예에서, 본 발명의 dsRNA는 임의의 화학식 (XXXII) - (XXXV)으로 나타낸 구조의 그룹으로부터 선택된 2가 또는 3가 측쇄 링커에 접합된다:In one embodiment, a dsRNA of the invention is conjugated to a divalent or trivalent side chain linker selected from the group of structures represented by any of Formulas (XXXII) - (XXXV):
화학식 XXXII 화학식 XXXIII Formula XXXII Formula XXXIII
화학식 XXXIV 화학식 XXXVFormula XXXIV Formula XXXV
여기서: here:
q2A, q2B, q3A, q3B, q4A, q4B, q5A, q5B 및 q5C는 독립적으로 각각 0 내지 20을 나타내고, 여기서, 반복 단위는 동일하거나 상이할 수 있고;q2A, q2B, q3A, q3B, q4A, q4B, q5A, q5B and q5C each independently represents 0 to 20, wherein the repeating units may be the same or different;
P2A, P2B, P3A, P3B, P4A, P4B, P5A, P5B, P5C, T2A, T2B, T3A, T3B, T4A, T4B, T4A, T5B, T5C는 각각 독립적으로 부재이거나 CO, NH, O, S, OC(O), NHC(O), CH2, CH2NH 또는 CH2O이고;P 2A , P 2B , P 3A , P 3B , P 4A , P 4B , P 5A , P 5B , P 5C , T 2A , T 2B , T 3A , T 3B , T 4A , T 4B , T 4A , T 5B , T 5C are each independently absent or CO, NH, O, S, OC(O), NHC(O), CH 2 , CH 2 NH or CH 2 O;
Q2A, Q2B, Q3A, Q3B, Q4A, Q4B, Q5A, Q5B, Q5C는 각각 독립적으로 부재이거나, 알킬렌, 치환된 알킬렌이고, 여기서 하나 이상의 메틸렌은 O, S, S(O), SO2, N(RN), C(R’)=C(R’’), C≡C 또는 C(O) 중 하나 이상에 의해 중단되거나 말단화될 있고;Q 2A , Q 2B , Q 3A , Q 3B , Q 4A , Q 4B , Q 5A , Q 5B , Q 5C are each independently absent, alkylene, substituted alkylene, wherein at least one methylene is O, S , S(O), SO 2 , N(R N ), C(R′)=C(R″), C≡C or C(O);
R2A, R2B, R3A, R3B, R4A, R4B, R5A, R5B, R5C은 각각 독립적으로 부재이거나, NH, O, S, CH2, C(O)O, C(O)NH, NHCH(Ra)C(O), -C(O)-CH(Ra)-NH-, CO, CH=N-O, , 또는 헤테로사이클릴이고;R 2A , R 2B , R 3A , R 3B , R 4A , R 4B , R 5A , R 5B , R 5C are each independently absent, or NH, O, S, CH 2 , C(O)O, C( O) NH, NHCH (R a ) C (O), -C (O) -CH (R a ) -NH-, CO, CH=NO, , or heterocyclyl;
L2A, L2B, L3A, L3B, L4A, L4B, L5A, L5B 및 L5C는 리간드, 즉, 각각 독립적으로 모노사카라이드 (예를 들어, GalNAc), 디사카라이드, 트리사카라이드, 테트라사카라이드, 올리고사카라이드 또는 폴리사카라이드이고; Ra는 H 또는 아미노산 측쇄이다.3가 접합 GalNAc 유도체는 특히 화학식 XXXVI의 것들과 같은 표적 유전자의 발현을 억제하기 위한 RNAi 제제와 함께 사용하기 위해 유용하다:L 2A , L 2B , L 3A , L 3B , L 4A , L 4B , L 5A , L 5B and L 5C are ligands, ie, each independently a monosaccharide (eg GalNAc), a disaccharide, a trisaccharide saccharides, tetrasaccharides, oligosaccharides or polysaccharides; R a is H or an amino acid side chain. Trivalent conjugated GalNAc derivatives are particularly useful for use with RNAi agents to inhibit expression of target genes, such as those of formula XXXVI:
화학식 XXXVIFormula XXXVI
여기서 L5A, L5B 및 L5C는 GalNAc 유도체와 같은 모노사카라이드를 나타낸다.Here, L 5A , L 5B and L 5C represent monosaccharides such as GalNAc derivatives.
GalNAc 유도체를 접합시키는 적합한 2가 및 3가 측쇄 링커 그룹의 예는 화학식 II, VII, XI, X, 및 XIII로서 상기된 구조를 포함하지만 이에 제한되지 않는다. Examples of suitable divalent and trivalent side chain linker groups for conjugating GalNAc derivatives include, but are not limited to, the structures set forth above as Formulas II, VII, XI, X, and XIII.
RNA 접합체의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제4,828,979호; 제4,948,882호; 제5,218,105호; 제5,525,465호; 제5,541,313호; 제5,545,730호; 제5,552,538호; 제5,578,717호, 제5,580,731호; 제5,591,584호; 제5,109,124호; 제5,118,802호; 제5,138,045호; 제5,414,077호; 제5,486,603호; 제5,512,439호; 제5,578,718호; 제5,608,046호; 제4,587,044호; 제4,605,735호; 제4,667,025호; 제4,762,779호; 제4,789,737호; 제4,824,941호; 제4,835,263호; 제4,876,335호; 제4,904,582호; 제4,958,013호; 제5,082,830호; 제5,112,963호; 제5,214,136호; 제5,082,830호; 제5,112,963호; 제5,214,136호; 제5,245,022호; 제5,254,469호; 제5,258,506호; 제5,262,536호; 제5,272,250호; 제5,292,873호; 제5,317,098호; 제5,371,241호, 제5,391,723호; 제5,416,203호, 제5,451,463호; 제5,510,475호; 제5,512,667호; 제5,514,785호; 제5,565,552호; 제5,567,810호; 제5,574,142호; 제5,585,481호; 제5,587,371호; 제5,595,726호; 제5,597,696호; 제5,599,923호; 제5,599,928호; 제5,688,941호; 제6,294,664호; 제6,320,017호; 제6,576,752호; 제6,783,931호; 제6,900,297호; 제7,037,646호; 및 제8,106,022호를 포함하지만 이에 제한되지 않고, 이들 각각의 전문은 본원에 참조로 인용된다. Representative U.S. patents that teach the preparation of RNA conjugates include U.S. Patent Nos. 4,828,979; 4,948,882; 5,218,105; 5,525,465; 5,541,313; 5,545,730; 5,552,538; 5,578,717; 5,580,731; 5,591,584; 5,109,124; 5,118,802; 5,138,045; 5,414,077; 5,486,603; 5,512,439; 5,578,718; 5,608,046; 4,587,044; 4,605,735; 4,667,025; 4,762,779; 4,789,737; 4,824,941; 4,835,263; 4,876,335; 4,904,582; 4,958,013; 5,082,830; 5,112,963; 5,214,136; 5,082,830; 5,112,963; 5,214,136; 5,245,022; 5,254,469; 5,258,506; 5,262,536; 5,272,250; 5,292,873; 5,317,098; 5,371,241; 5,391,723; 5,416,203; 5,451,463; 5,510,475; 5,512,667; 5,514,785; 5,565,552; 5,567,810; 5,574,142; 5,585,481; 5,587,371; 5,595,726; 5,597,696; 5,599,923; 5,599,928; 5,688,941; 6,294,664; 6,320,017; 6,576,752; 6,783,931; 6,900,297; 7,037,646; and 8,106,022, each of which is hereby incorporated by reference in its entirety.
주어진 화합물의 모든 위치가 균일하게 변형될 필요는 없고, 실제로 상기한 변형 중 하나 이상은 단일 화합물 또는 심지어 iRNA 내의 단일 뉴클레오시드에 도입될 수 있다. 본 발명은 또한 키메라 화합물인 iRNA 화합물을 포함한다.Not all positions of a given compound need be uniformly modified, and indeed one or more of the above modifications may be introduced into a single compound or even a single nucleoside within an iRNA. The present invention also includes iRNA compounds that are chimeric compounds.
VI. 본 발명의 iRNA의 전달VI. Delivery of the iRNA of the invention
세포, 예를 들어, 사람 대상체(예를 들어, 이를 필요로 하는 대상체, 예를 들어, 접촉 활성화 경로 유전자 발현과 관련된 질환, 장애 또는 병태를 갖는 대상체) 내 세포로의 본 발명의 iRNA의 전달은 다수의 상이한 방식으로 성취될 수 있다. 예를 들어, 전달은 세포를 본 발명의 iRNA와 시험관내 또는 생체내 접촉시킴에 의해 수행될 수 있다. 생체내 전달은 또한 iRNA, 예를 들어, dsRNA를 포함하는 조성물을 대상체에게 투여함에 의해 직접적으로 수행될 수 있다. 전달은 예를 들어 정맥내 투여 또는 피하 투여에 의해 수행될 수 있다. 특정 구현예에서, iRNA 제제는 피하 투여에 의해 전달된다. 특정 구현예에서, iRNA 제제는 사전 충전된 주사기 또는 자동-주사기 장치를 사용한 자가 투여에 의해 투여된다. Delivery of an iRNA of the invention to a cell, eg , a cell in a human subject (eg, a subject in need thereof, eg, a subject having a disease, disorder or condition associated with contact activation pathway gene expression) It can be accomplished in a number of different ways. For example, delivery can be performed by contacting a cell with an iRNA of the invention in vitro or in vivo. in vivo Delivery can also be performed directly by administering to a subject a composition comprising an iRNA, eg, a dsRNA. Delivery can be by, for example, intravenous or subcutaneous administration. In certain embodiments, iRNA preparations are delivered by subcutaneous administration. In certain embodiments, the iRNA preparation is administered by self-administration using a pre-filled syringe or auto-injector device.
일반적으로, 핵산 분자를 전달(시험관내 또는 생체내)하는 임의의 방법은 본 발명의 iRNA와 함께 사용하기 위해 채택될 수 있다(문헌참조: 예를 들어, Akhtar S. and Julian RL. (1992) Trends Cell.Biol.2(5):139-144및 WO9402595, 이의 전문은 본원에 참조로 인용된다). 생체내 전달을 위해, iRNA 분자를 전달하기 위해 고려할 인자들은 예를 들어, 전달된 분자의 생물학적 안정성, 비-특이적 효과의 예방, 및 표적 조직에서 전달된 분자의 축적을 포함한다. In general, any method of delivering nucleic acid molecules (in vitro or in vivo) can be adapted for use with the iRNAs of the present invention (see, eg, Akhtar S. and Julian RL. (1992)). Trends Cell. Biol.2 (5):139-144 and WO9402595, incorporated herein by reference in their entirety). For in vivo delivery, factors to consider for delivering an iRNA molecule include, for example, biological stability of the delivered molecule, prevention of non-specific effects, and accumulation of the delivered molecule in the target tissue.
VII. 본 발명의 약제학적 조성물 VII. Pharmaceutical composition of the present invention
본 발명은 또한 본 발명의 방법에 사용하기 위해 본원에 기재된 iRNA를 포함하는 약제학적 조성물 및 제형을 포함한다. 하나의 구현예에서, 본원에서는 본원에 기재된 바와 같은 iRNA 및 약제학적으로 허용되는 담체를 함유하는 약제학적 조성물이 제공된다. iRNA를 함유하는 약제학적 조성물은 TTR 유전자의 발현 또는 활성과 관련된 질환 또는 장애를 치료하기 위해 유용하다. 상기 약제학적 조성물은 전달 방식을 기준으로 제형화된다. 하나의 예는 비경구 전달을 통한, 예를 들어 피하(SC) 또는 정맥내(IV) 전달에 의한 전신 투여용으로 제형화된 조성물이다. 본 발명의 약제학적 조성물은 TTR 유전자의 발현을 억제하기에 충분한 용량으로 투여될 수 있다. 하나의 구현예에서, 본 발명의 iRNA 제제, 예를 들어 dsRNA 제제는 약제학적으로 허용되는 담체 중에서 피하 투여용으로 제형화된다.The invention also includes pharmaceutical compositions and formulations comprising the iRNAs described herein for use in the methods of the invention. In one embodiment, provided herein is a pharmaceutical composition containing an iRNA as described herein and a pharmaceutically acceptable carrier. Pharmaceutical compositions containing the iRNA are useful for treating diseases or disorders associated with the expression or activity of the TTR gene. The pharmaceutical composition is formulated based on the mode of delivery. One example is a composition formulated for systemic administration via parenteral delivery, eg, by subcutaneous (SC) or intravenous (IV) delivery. The pharmaceutical composition of the present invention can be administered in a dose sufficient to inhibit expression of the TTR gene. In one embodiment, an iRNA preparation, eg a dsRNA preparation, of the invention is formulated for subcutaneous administration in a pharmaceutically acceptable carrier.
다른 구현예에서, 약제학적 조성물의 단일 용량은 장기간 지속되어 후속 용량은 1개월 간격, 1, 2, 3, 또는 4개월 이하의 간격 또는 분기별 (약 3개월 마다) 간격으로 투여된다. 본 발명의 일부 구현예에서, 본 발명의 약제학적 조성물의 단일 용량은 1개월 마다 1회 투여된다. 본 발명의 다른 구현예에서, 본 발명의 약제학적 조성물의 단일 용량은 격월로 1회 투여된다. 다른 구현예에서, 본 발명의 약제학적 조성물의 단일 용량은 분기별로, 즉 3개월 마다 1회 투여된다. 다른 구현예에서, 본 발명의 약제학적 조성물의 단일 용량은 4개월 마다 1회 투여된다. 또 다른 구현예에서, 본 발명의 약제학적 조성물의 단일 용량은 5개월 마다 1회 투여된다. 다른 구현예에서, 본 발명의 약제학적 조성물의 단일 용량은 6개월 마다 1회 투여된다. 다른 구현예에서, 본 발명의 약제학적 조성물의 단일 용량은 12개월 마다 1회 투여된다.In another embodiment, a single dose of the pharmaceutical composition is sustained over an extended period of time such that subsequent doses are administered at 1-month intervals, 1, 2, 3, or 4-month intervals or quarterly (about every 3-monthly) intervals. In some embodiments of the invention, a single dose of the pharmaceutical composition of the invention is administered once per month. In another embodiment of the present invention, a single dose of the pharmaceutical composition of the present invention is administered once every other month. In another embodiment, a single dose of the pharmaceutical composition of the present invention is administered quarterly, ie once every 3 months. In another embodiment, a single dose of the pharmaceutical composition of the present invention is administered once every 4 months. In another embodiment, a single dose of the pharmaceutical composition of the present invention is administered once every 5 months. In another embodiment, a single dose of the pharmaceutical composition of the present invention is administered once every 6 months. In another embodiment, a single dose of the pharmaceutical composition of the present invention is administered once every 12 months.
VIII. 키트VIII. kit
본 발명은 또한 본 발명의 임의의 방법을 수행하기 위한 키트를 제공한다. 이러한 키트는 하나 이상의 이중 가닥 RNAi 제제(들) 및 본 발명의 경우 임의의 방법에서 사용하기 위한 이중 가닥 제제(들)의 사용 지침을 제공하는 표지를 포함한다. 키트는 임의로 세포를 RNAi 제제와 접촉시키기 위한 수단(예를 들어, 주사 장치 또는 주입 펌프), 또는 TTR의 억제를 측정하기 위한 수단(예를 들어, TTR mRNA 또는 TTR 단백질의 억제를 측정하기 위한 수단)을 추가로 포함할 수 있다. TTR의 억제를 측정하기 위한 상기 수단은 예를 들어 혈장 샘플과 같은 대상체로부터 샘플을 수득하기 위한 수단을 포함할 수 있다. 본 발명의 키트는 임의로 추가로 RNAi 제제(들)을 대상체에게 투여하기 위한 수단 또는 치료학적 유효량 또는 예방학적 유효량을 결정하기 위한 수단을 포함할 수 있다.The invention also provides kits for performing any of the methods of the invention. Such kits include one or more double-stranded RNAi agent(s) and a label providing instructions for use of the double-stranded agent(s) for use in any method for the present invention. The kit optionally includes means for contacting cells with the RNAi agent (eg, an injection device or infusion pump), or means for measuring inhibition of TTR (eg, means for measuring inhibition of TTR mRNA or TTR protein). ) may be further included. Such means for determining inhibition of TTR may include means for obtaining a sample from a subject, such as, for example, a plasma sample. Kits of the present invention may optionally further include means for administering the RNAi agent(s) to a subject or means for determining a therapeutically effective amount or a prophylactically effective amount.
RNAi 제제는 재현탁 및 주사를 위한 멸균수 용액 또는 기타 적절한 용액, 예를 들어 PBS, 생리 식염수, 5mM 포스페이트 완충액과 같은 임의의 편리한 형태로 제공될 수 있다. 예를 들어, RNAi 제제는 주사용 멸균수 중 물 또는 다른 적절한 용액과 함께 300 mg, 200 mg, 100 mg, 또는 50 mg 바이알로 제공될 수 있다. 특정 구현예에서, RNAi 제제는 적절한 용적의 투여용 부형제 중에 300mg, 200mg, 100mg, 또는 50mg의 RNAi 제제를 함유하는 사전 충전된 주사기 또는 자가주사기를 포함하는 자가 투여용 키트로 제공되며, 임의로 추가로 사용 지침서를 포함한다. 특정 구현예에서, RNAi 제제는 약 동일한 시간에, 예를 들어, 1주 이내, 1일 이내, 1시간 이내에 제공되는 다중 주사에 의한 용량의 투여를 위한 다중 바이알 또는 장치에 제공될 수 있다. The RNAi preparation may be provided in any convenient form, such as sterile water solution or other suitable solution for resuspension and injection, such as PBS, physiological saline, 5 mM phosphate buffer. For example, the RNAi preparation may be provided in a 300 mg, 200 mg, 100 mg, or 50 mg vial with water or other suitable solution in sterile water for injection. In certain embodiments, the RNAi agent is provided as a kit for self-administration comprising a pre-filled syringe or autoinjector containing 300 mg, 200 mg, 100 mg, or 50 mg of the RNAi agent in an appropriate volume of an excipient for administration, optionally further comprising: Instructions for use are included. In certain embodiments, the RNAi agent may be provided in multiple vials or devices for administration of doses by multiple injections given at about the same time, eg, within 1 week, within 1 day, within 1 hour.
IX. TTR 아밀로이드증 다발신경병증 진단 및 질환 부담 평가IX. TTR amyloidosis polyneuropathy diagnosis and disease burden assessment
TTR 아밀로이드증은 복잡한 다인성 질환이다. TTR-FAP의 진행을 모니터링하기 위해 기준의 확장 목록이 사용되었다: 신경병증 손상 스코어(NIS), NIS + 7, 및 변형된 NIS(mNIS) + 7 및 mNIS + 7Ionis. 이들 진단학적 기준은 당업계에 널리 공지되어 있고 기준의 주요 내용은 하기에 제공된다. 본원에 사용된 바와 같이, TTR-FAP의 진단 기준을 충족시키는 것은 유전성 TTR-FAP와 관련된 돌연변이의 존재 여부에 관계없이 FAP 단계 1 기준을 충족시키는 것으로 이해된다. 신경병증 지표의 진행은 변형된 신경병증 손상 스코어(mNIS) + 7에서 최소 2점의 증가로서 간주된다. TTR amyloidosis is a complex, multifactorial disease. An extended list of criteria was used to monitor the progression of TTR-FAP: Neuropathic Impairment Score (NIS), NIS + 7, and Modified NIS (mNIS) + 7 and mNIS + 7 Ionis . These diagnostic criteria are well known in the art and highlights of the criteria are provided below. As used herein, meeting the diagnostic criteria for TTR-FAP is understood to be fulfilling the FAP stage 1 criteria regardless of the presence or absence of a mutation associated with hereditary TTR-FAP. Progression of the neuropathic index is considered as an increase of at least 2 points in the modified neuropathic impairment score (mNIS) + 7.
가족성 아밀로이드 다발신경병증(FAP) 단계.Familial Amyloid Polyneuropathy (FAP) Stage.
문헌(참조: Coutinho et al.)은 hATTR(이전에는 가족성 아밀로이드 신경병증이라고 함)의 신경병증 증상에 대한 임상 병기(staging) 시스템을 개발하였다. 스케일은 다음과 같이 1 내지 3의 범위이다(문헌참조: Ando et al. Orphanet J Rare Dis. 2013;8:31): FAP 단계 1: 도움 없이 걷기, 하지의 경미한 신경병증(감각, 자율신경 및 운동). Coutinho et al. developed a clinical staging system for the neuropathic symptoms of hATTR (formerly called familial amyloid neuropathy). The scale ranges from 1 to 3 as follows (reference: Ando et al. Orphanet J Rare Dis. 2013;8:31): FAP stage 1: walking without assistance, mild neuropathy of the lower extremities (sensory, autonomic and Exercise).
FAP 단계 2: 도움을 받아 걷기, 하지, 몸통 및 상지의 중등도 장애. FAP Stage 2: Moderate impairment of assisted walking, lower extremities, trunk, and upper extremities.
FAP 단계 3: 휠체어 또는 침대에 의지, 중증 신경병증. FAP stage 3: wheelchair or bed-bound, severe neuropathy.
신경병증이 없는 대상체는 FAP 단계 0인 것으로 고려된다.Subjects without neuropathy are considered FAP stage 0.
신경병증 손상 스코어링 방법Neuropathic damage scoring method
신경병증을 평가하기 위한 방법은 당업계에 공지되어 있다. 예를 들어, 마요 클리닉 신경학적 조사 시트(Mayo Clinic Neurologic Examination Sheet)와 신경병증 손상 스코어(Neuropathy Impairment Score)(NIS)의 쇠약 서브스코어에서도 쇠약(NIS-W)은 1에서 4점까지 25% 감소율로 스코어링하고, 별도로 신체의 각 측면의 주요 근육 그룹에 대해 스코어링한다(문헌참조: Dyck et al., Quantitating overall neuropathic symptoms, impairments, and outcomes. In: Dyck PJ, Thomas PK, editors. Peripheral neuropathy. 4th ed. Philadelphia: Elsevier; 2005. p. 1031-52). 광범위한 그룹, 특히 두개골, 근위 및 말단 사지 근육은 NIS-W에서 최대 스코어 192점으로 평가된다. 주요 5개 근육 스트레치 반사의 감소는 일반적으로 신경과 전문의에 의해 평가되고, 발과 손의 촉각, 진동, 관절 운동 및 핀 찌르는 감각은 마요 클리닉 신경학적 조사 시트(Mayo Clinic Neurology Examination Sheet)에서 25% 감소율 및 1에서 4로 스코어링된다. 반사(NIS-R) 및 감각(NIS-S)의 NIS를 완료하기 위해 마요 클리닉 기록 스코어는 NIS 점수 스코어로 전환된다(즉, 마요 클리닉 스코어 1 또는 2는 NIS 점수 스코어 1에 부여되고 마요 클리닉 스코어 3 또는 4는 NIS 스코어 2에 부여된다). 따라서 신경과 전문의(NIS-R)가 평가하는 일반적인 반사의 최대 NIS 스코어는 5 × 2 × 2 = 20점이고 신경과 전문의(NIS-S)가 흔히 평가하는 4가지 감각 양식은 8 × 2 × 2 = 32점이다. 따라서, 최대 NIS 스코어는 192 + 20 + 32 =244점이다. NIS는 이전의 간행물에 기재되었다(문헌참조: Dyck et al. 2005 and Dyck et al., Neurol. 1997;49:229-39).Methods for assessing neuropathy are known in the art. For example, even in the Mayo Clinic Neurologic Examination Sheet and the Weakness subscore of the Neuropathy Impairment Score (NIS), Weakness (NIS-W) is a 25% decrease from 1 to 4 points. , and separately scored for major muscle groups on each side of the body (see Dyck et al., Quantitating overall neuropathic symptoms, impairments, and outcomes. In: Dyck PJ, Thomas PK, editors. Peripheral neuropathy. 4th ed. Philadelphia: Elsevier; 2005. p. 1031-52). A broad group, particularly the cranial, proximal and distal limb muscles, is rated for a maximum score of 192 on the NIS-W. Decreases in the major five muscle stretch reflexes are commonly assessed by neurologists, and foot and hand touch, vibration, joint motion, and pin prick sensation are 25% on the Mayo Clinic Neurology Examination Sheet. Decrease rate and scored from 1 to 4. To complete the NIS of reflexes (NIS-R) and sensory (NIS-S), Mayo Clinic record scores are converted to NIS score scores (i.e., a Mayo Clinic score of 1 or 2 is assigned to a NIS score score of 1 and a Mayo Clinic score of 3 or 4 is assigned an NIS score of 2). Thus, the maximum NIS score for common reflexes assessed by neurologists (NIS-R) is 5 × 2 × 2 = 20 points, and the four sensory modalities commonly assessed by neurologists (NIS-S) are 8 × 2 × 2 2 = 32 points. Thus, the maximum NIS score is 192 + 20 + 32 = 244 points. NIS has been described in previous publications (Dyck et al. 2005 and Dyck et al., Neurol. 1997;49:229-39).
NIS + 7은 당뇨병성 감각운동 다발신경병증, TTR FAP 및 기타 일반화된 감각운동 다발신경병증의 시험에서 1차 또는 공동 1차 결과 척도로 사용되었다(문헌참조: N. Suanprasert et al. J Neurol Sci 344 (2014) 121-128). NIS + 7은 단지 반사에 대한 천정 효과를 최소화하면서 근육 쇠약 및 근육 스트레치 반사 이상의 등급화된 중증도를 적절하게 평가한다. NIS + 7에서 7개 시험 중 5개는 신경 전도의 특성으로, 정상 편차(Ζ 스코어) 또는 점수로 표시된다. NIS + 7에 포함된 특성은 이들의 이상이 당뇨병성 감각운동 다발신경병증을 민감하게 검출하기 때문에 선택되었다(문헌참조: Dyck et al. Muscle Nerve 2003;27(2):202-10). 포함된 특성은 비골 신경 복합 근육 활동 전위 (CMAP) 진폭, 운동 신경 전도 속도(MNCV) 및 운동 신경 원위 잠복기(MNDL), 경골 MNDL 및 비복 감각 신경 활동 전위(SNAP) 진폭이다. 이들의 측정된 값은 대형의 건강한 대상체 참조 코호트에 대한 보다 이른 연구를 기반으로 하는 연령, 성별, 키 또는 체중의 해당 변수를 보정하는 퍼센트 값에서 정상 편차로 전환될 수 있다. 추가로, 이들 퍼센트 값은 수득된 퍼센트 값(즉, N5th = 0점, ≤5th-N 1st = 1점 및 ≤1st = 2점)에서 NIS 점수로 표현할 수 있다(이상이 정상적인 분포의 상부 테일에 있는 경우에도 유사하게).NIS + 7 has been used as the primary or co-primary outcome measure in trials of diabetic sensorimotor polyneuropathy, TTR FAP, and other generalized sensorimotor polyneuropathy (N. Suanprasert et al. J Neurol Sci). 344 (2014) 121-128). The NIS + 7 adequately assesses the graded severity of muscle weakness and muscle stretch reflex abnormalities with minimal ceiling effects on reflexes only. At NIS + 7, 5 out of 7 tests were characteristic of nerve conduction, expressed as normal deviations (Ζ scores) or scores. The features included in the NIS+7 were chosen because their abnormalities sensitively detect diabetic sensorimotor polyneuropathy (Dyck et al. Muscle Nerve 2003;27(2):202-10). Included characteristics were peroneal nerve complex muscle action potential (CMAP) amplitude, motor nerve conduction velocity (MNCV) and motor nerve distal latency (MNDL), tibial MNDL and sciatic sensory nerve action potential (SNAP) amplitudes. These measured values can be converted to normal deviations in percentage values correcting for the corresponding variables of age, sex, height or weight based on earlier studies of large healthy subject reference cohorts. Additionally, these percentage values can be expressed as NIS scores at the percentage values obtained (i.e., N5th = 0 points, ≤5th-N 1st = 1 point, and ≤1st = 2 points) (if the abnormality is in the upper tail of the normal distribution) similarly, if any).
쇠약 및 반사 이상 평가, 감각 상실 평가, 자율신경계 기능부전 및 신경 생리학적 시험 이상은 TTR FAP 시험에 사용하기 위해 NIS + 7에 의해 적절하게 평가되지 않는다. NIS + 7에서 감각 상실은 최적으로 평가되지 않는다: 1) 감각 상실의 신체 분포가 적절하게 고려되지 않고, 2) 소형 섬유에 비해 큰 감각 상실이 지나치게 강조되고, 3) 임상 평가보다 개선된 시험 방법 및 참조값과의 비교가 선호된다. 또한 심박수 심호흡(HRdb)만을 사용해서는 자율신경계 기능부전이 적절하게 평가되지 않는다. NIS + 7을 평가하기 위해 사용되는 신경 전도의 특성은 TTR FAP 연구에 이상적이지 않다.Weakness and dysreflexia assessment, sensory loss assessment, autonomic dysfunction and neurophysiological examination abnormalities are not adequately assessed by the NIS + 7 for use in the TTR FAP test. Sensory loss in the NIS + 7 is not optimally assessed: 1) body distribution of sensory loss is not adequately considered, 2) large sensory loss is overemphasized compared to small fibers, and 3) test method is improved over clinical evaluation. and comparisons with reference values are preferred. Also, using heart rate deep breathing (HRdb) alone does not adequately assess autonomic dysfunction. The properties of nerve conduction used to assess NIS+7 are not ideal for TTR FAP studies.
신경병증 손상 스코어 +7(mNIS+7) 및 NIS + 7의 업데이트 버전은 운동 강도, 반사, 감각, 신경 전도 및 자율 기능을 측정하는 복합 스코어이다. 상기 복합 측정의 2개의 버전은 다발신경병증이 있는 hATTR 아밀로이드증을 더 잘 반영하기 위해 NIS+7에서 조정되었고, 이노터센 및 파티시란 임상 시험에서 1차 결과로서 사용되었다. 이들 2개의 버전과 다른 신경병증 스코어링 시스템 간의 주요 차이점은 하기 표에 요약되어 있다(문헌참조: Adams et al., BMC Neurology, volume 17, Article number: 181 (2017)). 2개 스케일에서 점수가 낮을수록 신경계 기능이 더 우수함을 나타낸다(예를 들어, 스코어 증가는 신경계 손상의 악화를 반영한다).An updated version of the Neuropathic Impairment Score +7 (mNIS+7) and NIS+7 are composite scores that measure motor strength, reflexes, sensation, nerve conduction and autonomic function. Two versions of this composite measure were adjusted at NIS+7 to better reflect hATTR amyloidosis with polyneuropathy and were used as primary outcomes in the innotersen and patisiran clinical trial. The main differences between these two versions and other neuropathic scoring systems are summarized in the table below (Adams et al., BMC Neurology, volume 17, Article number: 181 (2017)). A lower score on either scale indicates better nervous system function (eg, an increase in score reflects worsening nervous system damage).
1. CMAP 화합물 근육 작용 전위; exam 검사; mNIS+7 변형된 NIS+7; NIS 신경병증1. CMAP compound muscle action potential; exam; mNIS+7 modified
손상 스코어; NIS-LL 하지만의 검사를 기준으로 하는 NIS; QST 정량적 감각 시험;damage score; NIS-LL but NIS based inspection; QST quantitative sensory test;
SNAP 감각 신경 작용 전위SNAP sensory nerve action potential
2. a건강한-대상체 파라미터를 기준으로 하는 정상 편차로서 표현되는 스코어(0-3.72)2. a Score (0-3.72) expressed as normal deviation based on the healthy-subject parameter
3. b한정된 카테고리에 따라 등급화된 스코어; 정상 (95 퍼센트) = 0점; 약간 감소된 (≥95 내지 <99 퍼센트)=1점; 및 매우 감소된 (≥99 퍼센트)= 2점3. b Scores graded according to defined categories; Normal (95 percent) = 0 points; slightly decreased (≥95 to <99 percent) = 1 point; and very reduced (≥99 percent) = 2 points
4. c또한 비골로서 지칭될 수 있음4. c may also be referred to as fibula
TTR 아밀로이드증 다발신경병증 (ATTR-CM)의 진단 및 질환 부담 평가Diagnosis and disease burden assessment of TTR amyloidotic polyneuropathy (ATTR-CM)
hATTR 아밀로이드증 및 심근병증을 갖는 환자는 전형적으로 심부전(HF) 및 심장 부정맥의 진행성 증상을 경험하고, 사망은 전형적으로 진단 후 2.5 내지 5년에 발생한다. TTR 아밀로이드 원섬유에 의한 세포외 매트릭스의 심장 침윤은 심실 벽 두께의 점진적인 증가 및 챔버 강성의 현저한 증가를 유발하여 이완기 기능 손상을 초래한다. 수축기 기능도 손상되고, 전형적으로 정상적인 박출률에도 불구하고 비정상적인 종방향 긴장에 의해 반영되고, 이는 질환의 말기까지 유지된다. ATTR 아밀로이드증 및 경쇄(AL) 심장 아밀로이드증을 갖는 환자에서 뇌 나트륨이뇨 펩타이드(NT-proBNP)의 종방향 긴장 및 N-말단 프로호르몬 둘다는 생존의 독립적인 예측 인자인 것으로 나타났다.Patients with hATTR amyloidosis and cardiomyopathy typically experience progressive symptoms of heart failure (HF) and cardiac arrhythmias, and death typically occurs 2.5 to 5 years after diagnosis. Cardiac infiltration of the extracellular matrix by TTR amyloid fibrils causes progressive increases in ventricular wall thickness and marked increases in chamber stiffness, resulting in impaired diastolic function. Systolic function is also impaired and is typically reflected by abnormal longitudinal tension despite a normal ejection fraction, which is maintained until the end of the disease. Both longitudinal tension of brain natriuretic peptide (NT-proBNP) and N-terminal prohormone have been shown to be independent predictors of survival in patients with ATTR amyloidosis and light chain (AL) cardiac amyloidosis.
심장초음파검사는 심장 구조와 기능을 평가하는 데 일상적으로 사용되고; 통계학적 분석 계획에 미리 특정된 파라미터는 평균 좌심실(LV) 벽 두께, LV 질량, 종방향 긴장 및 박출률을 포함한다. 심박출량, 좌심방 크기, LV 말단-확장기 용적(LVEDV) 및 LV 말기-수축기 용적(LVESV). 심장초음파는 심장 이미지화에 일상적으로 사용된다. 심근 긴장은 벤더 독립적인 소프트웨어를 사용하여 반점 추적으로 평가할 수 있다(TOMTEC, Munich, Germany). NT-proBNP 및 트로포닌 I 수준의 분석은 예를 들어 화학발광 검정을 사용하여 상업적으로 가용한 진단 시험을 사용하여 임상 실험실에서 일상적으로 수행된다(참조: Roche Diagnostic Cobas, Indianapolis, IN, USA for NT-proBNP; Siemens Centaur XP, Camberley, Surrey, UK for troponin I). 유사하게, 임상 수행은 일상적으로 예를 들어 신장 질환 연구 공식의 변형을 사용하여 크레아티닌 수준을 기반으로 하는 크레아티닌 수준 및 추정 사구체 여과율(eGFR)의 측정을 포함한다.Echocardiography is routinely used to evaluate heart structure and function; Parameters pre-specified in the statistical analysis plan include mean left ventricular (LV) wall thickness, LV mass, longitudinal tension and ejection fraction. Cardiac output, left atrial volume, LV end-diastolic volume (LVEDV) and LV end-systolic volume (LVESV). Echocardiography is routinely used for heart imaging. Myocardial tone can be assessed by speckle tracking using vendor-independent software (TOMTEC, Munich, Germany). Analysis of NT-proBNP and troponin I levels is routinely performed in clinical laboratories using commercially available diagnostic tests, e.g., using chemiluminescence assays (Roche Diagnostic Cobas, Indianapolis, IN, USA for NT -proBNP; Siemens Centaur XP, Camberley, Surrey, UK for troponin I). Similarly, clinical practices routinely include measurements of creatinine levels and estimated glomerular filtration rate (eGFR) based on creatinine levels, for example using a variation of the renal disease study formula.
ATTR-CM에 대한 스크리닝 및 진단 방법을 제공하는 리뷰는 문헌(참조: Witteles et al., 2019(JACC: Heart Failure, 2019. 7:709-716))에 의해 최근에 발표되었고, 이는 ATTR-CM의 존재를 시사하는 "적신호(red flag)" 목록을 포함하는 진단 방법 및 심장초음파검사, 심전도, 심장 자기 공명, 말초 또는 자율 신경계와 관련된 전신 증상의 존재와 하지에서 시작하여 상행하는 패턴에 따르는 양측 감각 운동 다발신경병증을 포함한 심장 기능부전을 포함한 스크리닝 방법, 기립성 저혈압, 설사/변비 및 발기 부전의 형태의 자율신경이상증, 및 녹내장, 유리체내 침착 및 가리비 동공과 같은 눈 침범; 수근관 증후군, 특히 양측 수근관 증후군, 요추 척추관 협착증 및 이두박근 건 파열을 포함한 스크리닝 방법에 대한 정보를 제공한다. 다른 진단 방법은 알려지지 않은 이유로 TTR 심장 아밀로이드 침착물에 국소화되는 테크네튬(Tc) 표지 비스포스포네이트를 사용한 골 신티그래피를 포함한다. 생검은 또한 심장에서 TTR 아밀로이드증의 존재를 확인하기 위해 사용된다.A review providing screening and diagnostic methods for ATTR-CM was recently published by Witteles et al., 2019 (JACC: Heart Failure, 2019. 7:709-716), which Diagnostic methods including a list of "red flags" suggesting the presence of echocardiography, electrocardiogram, cardiac magnetic resonance, presence of systemic symptoms related to the peripheral or autonomic nervous system and bilateral following an ascending pattern starting in the lower extremities screening methods including cardiac dysfunction including sensorimotor polyneuropathy, autonomic dystonia in the form of orthostatic hypotension, diarrhea/constipation and erectile dysfunction, and ocular involvement such as glaucoma, intravitreal deposition and scallop pupil; Provides information on screening methods for carpal tunnel syndromes, including bilateral carpal tunnel syndrome, lumbar spinal canal stenosis, and biceps tendon rupture. Other diagnostic methods include bone scintigraphy using technetium (Tc) labeled bisphosphonates, which for unknown reasons localize to TTR cardiac amyloid deposits. A biopsy is also used to confirm the presence of TTR amyloidosis in the heart.
상기 제공된 파라미터의 심장 기능의 평가 및 분류 방법은 당업계에 공지되어 있다. 본원에 사용된 바와 같이, 심장 기능의 평가 또는 분류의 특정 방법은 치료 표준이 의학적 개입, 예를 들어 약리학적 제제의 투여, 수술을 포함하도록 충분히 감소된 심장 기능을 입증하기 위해 임의의 임상적으로 허용되는 표준일 수 있다.Methods for assessment and classification of cardiac function of the parameters provided above are known in the art. As used herein, certain methods of assessment or classification of cardiac function refer to any clinically significant reduction in cardiac function such that standard of care includes medical intervention, e.g., administration of pharmacological agents, surgery. may be an acceptable standard.
신경 손상 및 TTR 아밀로이드증 진행의 지표로서 혈청 바이오마커Serum biomarkers as indicators of nerve damage and TTR amyloidosis progression
상기에서 설명한 진단 및 모니터링 방법은 복잡하고 종종 주관적이다. 또한, TTR 아밀로이드증은 드물고 상기 징후와 증상이 다수의 다른 질환에 나타날 수 있으므로 임상적으로 검증된 비침습성 혈장 바이오마커는 조기 진단을 용이하게 하고 질환 진행 모니터링을 촉진시킬 수 있다. 티카우 등 (Ticau et al., 2019) (참조: www.medrxiv.org/content/10.1101/19011155v2.full.pdf)에 의한 연구에서, >1000의 단백질들의 혈장 수준은 다발신경병증과 함께 hATTR 아밀로이드증을 갖고 단계 3 APOLLO 연구 (NCT01960348) 및 건강한 개체의 코호트에서 위약 또는 파티시란을 투여받은 환자에서 측정되었다. TTR의 간 발현을 억제하는 지질 제형화된 RNAi 제제인 파티시란을 사용한 치료가 각 단백질의 시간 프로필에 미치는 영향을 0, 9 및 18개월에 선형 혼합 모델에 의해 결정하였다. 신경필라멘트 경쇄(NfL) 단백질은 직교 정량적 접근을 사용하여 추가로 평가하였다. 66개 단백질 수준의 유의미한 변화는 위약 대비 파티시란에서 관찰되었고, 신경 손상의 지표인 NfL의 변화가 가장 두드러졌다. 단백질 수준의 변화 분석은 파티시란으로 치료받은 환자의 프로테옴이 18개월에 건강한 개체을 향한 경향이 있음을 입증하였다. 건강한 대조군에서 혈장 NfL 수준은 다발신경병증과 함께 TTR 아밀로이드증을 갖는 환자에서 보다 4배 낮았다(16.3 [SD 12.0] pg/mL 대 69.4 [SD 42.1] pg/mL, p<10-16).18개월에 NfL의 수준은 위약을 사용하면 증가하였고(99.5 [SD 60.1] pg/mL) 파티시란 처리를 사용하면 감소하였다(48.8 [SD 29.9] pg/mL). 18개월에, 파티시란 처리된 환자에서 변형된 신경병증 손상 스코어+7(mNIS+7)에서의 개선은 NfL 수준에서의 감소(R=0.43, p<10-7)와 유의적으로 상관관계가 있다. mNIS+7에서 개선과 상관관계가 있는 파티시란 처리를 사용한 NfL 감소는 이것이 TTR 아밀로이드증에서 신경 손상 및 다발신경병증의 바이오마커로서 작용할 수 있음을 시사한다. 상기 바이오마커는 hATTR 아밀로이드증을 갖는 환자에서 다발신경병증의 조기 진단을 가능하게 하고 질환 진행의 모니터링을 용이하게 할 수 있다.The diagnostic and monitoring methods described above are complex and often subjective. In addition, since TTR amyloidosis is rare and the signs and symptoms can be present in a number of other diseases, clinically validated non-invasive plasma biomarkers may facilitate early diagnosis and facilitate monitoring of disease progression. In a study by Ticau et al. (2019) (ref: www.medrxiv.org/content/10.1101/19011155v2.full.pdf), plasma levels of >1000 proteins were associated with hATTR amyloidosis with polyneuropathy. and in patients receiving placebo or patisiran in the Phase 3 APOLLO study (NCT01960348) and a cohort of healthy individuals. The effect of treatment with patisiran, a lipid formulated RNAi agent that inhibits hepatic expression of TTR, on the temporal profile of each protein was determined by a linear mixed model at 0, 9 and 18 months. Neurofilament light chain (NfL) protein was further evaluated using an orthogonal quantitative approach. Significant changes in the levels of 66 proteins were observed with patissiran compared to placebo, and the change in NfL, an indicator of nerve damage, was the most prominent. Analysis of changes in protein levels demonstrated that the proteome of patisiran-treated patients tended toward healthy individuals at 18 months. Plasma NfL levels in healthy controls were 4-fold lower than in patients with TTR amyloidosis with polyneuropathy (16.3 [SD 12.0] pg/mL vs. 69.4 [SD 42.1] pg/mL, p<10 -16 ). 18 months , levels of NfL increased with placebo (99.5 [SD 60.1] pg/mL) and decreased with patisiran treatment (48.8 [SD 29.9] pg/mL). At 18 months, improvement in modified neuropathic impairment score+7 (mNIS+7) in patisiran-treated patients significantly correlated with reduction in NfL level (R=0.43, p<10 -7 ) there is The reduction in NfL with patisiran treatment that correlated with improvement in
다른 단백질, 특히 RSPO3, CCDC80, EDA2R 및 NT-proBNP 수준의 감소는 mNIS+7의 개선과 상관관계가 있는 것으로 밝혀졌고, 이는 단독으로 또는 서로 또는 Nfl과 조합하여 이들이 ATTR 아밀로이드증에서 신경 손상 및 다발신경병증의 바이오마커로서 작용할 수 있음을 시사한다. N-CDase 수준의 증가는 mNIS+7의 개선과 상관관계가 있는 것으로 밝혀졌고, 이는 단독으로 또는 상기에 열거된 다른 마커와 조합하여 이들이 ATTR 아밀로이드증에서 신경 손상 및 다발신경병증의 바이오마커로서 작용할 수 있음을 시사한다. Decreased levels of other proteins, particularly RSPO3, CCDC80, EDA2R and NT-proBNP, have been found to correlate with improvements in
파티시란을 사용한 치료에 반응하여 변화하는 것으로 관찰된 추가 잠재적 바이오마커는 아래 표에 열거되어 있다. 대상체가 ATTR 아밀로이드증의 진행을 나타내는 참조 수준에 비해 양의 베타 계수를 갖는 단백질 수준이 증가하는 경우 및 대상체가 ATTR 아밀로이드증의 진행을 나타내는 참조 수준에 비해 음의 베타 계수를 갖는 단백질 수준이 감소한 경우. 이들 마커 중 하나 이상의 수준의 변화는 ATTR 아밀로이드증에서 진행 중인 신경 손상 및 다발신경병증 진행의 개선, 안정화 또는 감소를 나타낼 수 있다.Additional potential biomarkers observed to change in response to treatment with patisiran are listed in the table below. If the subject has an increase in protein level with a positive beta coefficient relative to the reference level indicative of progression of ATTR amyloidosis and if the subject has a decrease in protein level with a negative beta coefficient relative to the reference level indicative of progression of ATTR amyloidosis. Changes in the level of one or more of these markers may indicate amelioration, stabilization, or reduction of ongoing nerve damage and polyneuropathy progression in ATTR amyloidosis.
[표 1] [ Table 1 ]
파티시란 처리에 응답하는 변화된 수준을 갖는 바이오마커Biomarkers with altered levels in response to patisiran treatment
이들 바이오마커에 대한 서열은 서열번호 17-34로서 본원에 제공된다.Sequences for these biomarkers are provided herein as SEQ ID NOs: 17-34.
본 발명은 제한으로서 해석되지 말아야 하는 하기의 실시예로 추가로 설명된다. 본원에 전반에 걸쳐 인용된 모든 참고문헌, 공개된 특허 및 특허 출원의 내용과 서열 목록이 본원에 참조로 인용된다. The invention is further illustrated by the following examples which should not be construed as limiting. The contents and sequence listings of all references, published patents and patent applications cited throughout this application are hereby incorporated by reference.
실시예Example
본 발명의 방법에 사용하기 위한 예시적인 이중 가닥 RNAi 제제는 하기 표 3에 제공되어 있다. 하기 표 2는 핵산 서열 제공에 사용되는 뉴클레오타이드 단량체 및 리간드의 약어를 제공한다. 올리고뉴클레오타이드에 존재하는 경우 이들 단량체는 달리 지적되지 않는 경우 5'-3'-포스포디에스테르 결합에 의해 상호 연결되어 있는 것으로 이해된다.Exemplary double-stranded RNAi agents for use in the methods of the present invention are provided in Table 3 below. Table 2 below provides abbreviations for nucleotide monomers and ligands used to provide nucleic acid sequences. When present in an oligonucleotide, these monomers are understood to be interconnected by 5'-3'-phosphodiester linkages unless otherwise indicated.
[표 2][Table 2]
[표 3][Table 3]
실시예 1: V30M 유전자전이 마우스에서 RNAi 제제에 의한 TTR 단백질 녹다운Example 1: TTR protein knockdown by RNAi agents in V30M transgenic mice
V30M 돌연변이는 사람 TTR에서 흔한 아밀로이드 생성 돌연변이이다. 마우스 TTR이 없고 V30M 돌연변이를 갖는 사람 TTR을 발현하는 유전자전이 마우스가 연구에 사용되었다. 마우스(그룹당 n = 3)에게 이전에 WO2018112320에 기재된 RNAi 제제 AD-65492, 또는 안티센스 가닥의 단일 위치에서 화학적 변형이 상기 표 2에 나타낸 바와 같이 GNA 변형으로 변화된 AD-65942의 서열 및 화학을 기반으로 하는 다른 RNAi 제제의 단일 피하 1 mg/kg 용량을 투여하였다. 혈액 샘플은 0일 (투여 전), 3, 7, 10, 14, 21, 35, 및 49일에 수득하였다. 혈청을 준비하고 사람 TTR 수준을 ELISA 검정을 사용하여 결정하였다(문헌참조: 예를 들어, Coelho, et al.(2013)N Engl J Med 369:819). 0일째와 비교하여 상대적 TTR 수준은 도 1에 나타낸다. The V30M mutation is a common amyloidogenic mutation in human TTR. Transgenic mice lacking mouse TTR and expressing human TTR with the V30M mutation were used in the study. Based on the sequence and chemistry of AD-65492, the RNAi agent previously described in WO2018112320, or AD-65942 where the chemical modification at a single position of the antisense strand was changed to a GNA modification as shown in Table 2 above, mice (n = 3 per group) were injected. A single subcutaneous 1 mg/kg dose of different RNAi agents was administered. Blood samples were obtained on day 0 (pre-dose), 3, 7, 10, 14, 21, 35, and 49 days. Serum was prepared and human TTR levels were determined using an ELISA assay (see, eg , Coelho, et al . (2013) N Engl J Med 369:819). Relative TTR levels compared to day 0 are shown in FIG. 1 .
안티센스 가닥 내 7번 또는 8번 위치에서 GNA의 혼입은 관용성이 양호하였다(AD-87404 및 AD-87405). 유사한 동력학 및 최대 단백질 녹다운은 모 RNAi 제제 AD-65492와 유사하였다. AD-87404에 의한 녹다운의 내구성은 AD-65492와 유사하였다. 안티센스 가닥 내 3번 내지 6번 위치에서 GNA의 혼입은 관용성이 덜 양호하였다. Incorporation of GNA at
실시예 2: 비-사람 영장류에서 RNAi 제제에 의한 TTR 단백질 녹다운Example 2: TTR protein knockdown by RNAi agents in non-human primates
표 2의 iRNA 제제의 서열은 시노몰구스 몽키 TTR과 완전히 교차 반응성이다. AD-65492 (1 mg/kg) 또는 AD-87404 (1 mg/kg 또는 3 mg/kg)의 단일 피하 용량은 3개의 별도의 연구에서 0일에 시노몰구스 몽키 (그룹 당 n=3)에 투여하였다. 혈액 샘플은 도 2에 나타낸 바와 같이 전체 119일에 걸쳐 -7일 (투여 전 7일)에 다양하게 수거하였다. 혈청을 준비하고 시노몰구스 몽키 TTR 수준을 ELISA 검정을 사용하여 결정하였다(문헌참조: 예를 들어, Coelho, et al.(2013)N Engl J Med 369:819). 0일째와 비교하여 상대적 TTR 수준은 도 2에 나타낸다. TTR 녹다운은 1 mg/kg의 AD-65492 및 3 mg/kg의 AD-87404가 투여된 몽키에서 유사하였다.The sequences of the iRNA preparations in Table 2 are completely cross-reactive with Cynomolgus monkey TTR. A single subcutaneous dose of AD-65492 (1 mg/kg) or AD-87404 (1 mg/kg or 3 mg/kg) was not effective in cynomolgus monkeys on day 0 (n=3 per group) in three separate studies. administered. Blood samples were variously collected on day -7 (7 days prior to dosing) over a total of 119 days as shown in FIG. 2 . Serum was prepared and Cynomolgus monkey TTR levels were determined using an ELISA assay (see, eg , Coelho, et al . (2013) N Engl J Med 369:819). Relative TTR levels compared to day 0 are shown in FIG. 2 . TTR knockdown was similar in monkeys dosed with 1 mg/kg of AD-65492 and 3 mg/kg of AD-87404.
실시예 3: 건강한 사람 대상체에서 단일 용량의 AD-87404의 투여Example 3: Administration of a Single Dose of AD-87404 in Healthy Human Subjects
단계 I, 무작위 배정된, 단일 맹검, 위약 제어된 연구에서, AD-87404 (센스: 5’- usgsggauUfuCfAfUfguaaccaaga - 3’ (서열번호 6), 여기서, L96 리간드는 센스 가닥의 3’ 가닥에 접합된다); 안티센스: 5’- usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc - 3’ (서열번호 7))를 건강한 사람 지원자에게 25 mg, 75 mg, 100 mg, 200 mg, 또는 400 mg의 용량으로서 투여하고, 가능한 용량 그룹은 600 mg, 700 mg, 900 mg, 및 1000 mg이다. 연령, 성별, 체중과 같은 관련 인구통계학적 특징에 따라 그룹이 균형을 이룬다. In a phase I, randomized, single-blind, placebo-controlled study, AD-87404 (sense: 5'-usgsggauUfuCfAfUfguaaccaaga - 3' (SEQ ID NO: 6), wherein the L96 ligand is conjugated to the 3' strand of the sense strand) ; Antisense: 5′-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3′ (SEQ ID NO: 7)) is administered to healthy human volunteers at doses of 25 mg, 75 mg, 100 mg, 200 mg, or 400 mg, and the possible dose groups are 600 mg, 700 mg, 900 mg, and 1000 mg. Groups are balanced according to relevant demographic characteristics such as age, gender, and weight.
인구통계학적으로 매칭된 대조군 대상체에게도 단일 용량의 위약을 투여한다. Demographically matched control subjects will also receive a single dose of placebo.
혈장 샘플을 수거하고 위약 그룹의 대상체 및 모든 치료 그룹의 대상체로부터 샘플 중의 TTR 단백질 수준은 ELISA 분석을 사용하여 (문헌참조: 예를 들어, Coelho, et al.(2013) N Engl J Med 369:819) 미리 결정된 간격에서, 예를 들어, 1, 2, 3, 8, 15, 22, 29, 43, 57, 90일에, 이어서 활성 치료 그룹 대상체의 경우 28일마다 TTR 수준이 치료 전 수준의 80%로 회복될때까지(최대 투여 후 약 1년까지) 결정한다. 녹다운의 수준과 지속 시간이 결정된다. Plasma samples were collected and TTR protein levels in samples from subjects in the placebo group and subjects in all treatment groups were measured using an ELISA assay (see, e.g., Coelho, et al. (2013) N Engl J Med 369:819 ) at predetermined intervals, e.g., on
AD-87404 그룹 및 대조군 그룹 둘다에서 대상체는 또한 부작용에 대해 모니터링한다. 연구에서 모니터링된 예시적인 부작용은 주사 부위 홍반, 주사 부위 통증, 소양증, 기침, 메스꺼움, 피로 및 복통 및 신체 검사, ECG, 활력 징후 또는 임상 실험실 파라미터, 예를 들어, 신장 기능, 혈액학적 매개변수, 및 간 기능(예를 들어, 알라닌 아미노트랜스퍼라제(ALT), 아스파르테이트 아미노트랜스퍼라제(AST))의 임상적으로 유의적인 변화를 포함하지만 이에 제한되지 않는다.Subjects in both the AD-87404 group and the control group are also monitored for side effects. Exemplary side effects monitored in the study include injection site erythema, injection site pain, pruritus, cough, nausea, fatigue and abdominal pain and physical examination, ECG, vital signs or clinical laboratory parameters such as renal function, hematological parameters, and clinically significant changes in liver function (eg, alanine aminotransferase (ALT), aspartate aminotransferase (AST)).
상기 연구의 결과는 AD-87404의 단일 피하 용량이 용량 의존적 방식으로 TTR 단백질 수준을 강력하고 지속적으로 녹다운시킴을 입증한다. The results of this study demonstrate that a single subcutaneous dose of AD-87404 potently and consistently knocks down TTR protein levels in a dose dependent manner.
혈청 및 부작용에서 TTR 단백질 녹다운의 모니터링과 함께 다중 용량 연구 및 다중 상승 용량 연구도 고려된다. Multiple dose studies and multiple ascending dose studies with monitoring of TTR protein knockdown in serum and side effects are also contemplated.
등가물equivalent
당업자는 단지 통상의 실험, 본원에 기재된 개시내용의 특정 구현예 및 방법에 대한 많은 등가물을 인지하거나 이를 사용하여 확인할 수 있다. 이러한 균등물을 하기의 청구범위의 범위 내에 포함되는 것으로 의도된다. Those skilled in the art will recognize, or be able to ascertain using no more than routine experimentation, many equivalents to the specific embodiments and methods of the disclosure described herein. Such equivalents are intended to be included within the scope of the following claims.
SEQUENCE LISTING <110> ALNYLAM PHARMACEUTICALS, INC. <120> COMPOSITIONS AND METHODS FOR INHIBITING EXPRESSION OF TRANSTHYRETIN (TTR) <130> 121301-12320 <140> <141> <150> 62/985,950 <151> 2020-03-06 <160> 34 <170> PatentIn version 3.5 <210> 1 <400> 1 000 <210> 2 <400> 2 000 <210> 3 <400> 3 000 <210> 4 <400> 4 000 <210> 5 <400> 5 000 <210> 6 <211> 21 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 6 ugggauuuca uguaaccaag a 21 <210> 7 <211> 23 <212> DNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note="Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 7 ucuuggtuac augaaauccc auc 23 <210> 8 <211> 21 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 8 ugggauuuca uguaaccaag a 21 <210> 9 <211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 9 ucuugguuac augaaauccc auc 23 <210> 10 <211> 21 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 10 ugggauuuca uguaaccaag a 21 <210> 11 <211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 11 ucuugguuac augaaauccc auc 23 <210> 12 <211> 23 <212> DNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note="Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 12 uctugguuac augaaauccc auc 23 <210> 13 <211> 23 <212> DNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note="Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 13 ucutgguuac augaaauccc auc 23 <210> 14 <211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 14 ucuugguuac augaaauccc auc 23 <210> 15 <211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 15 ucuugguuac augaaauccc auc 23 <210> 16 <211> 23 <212> DNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note="Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 16 ucuuggutac augaaauccc auc 23 <210> 17 <211> 543 <212> PRT <213> Homo sapiens <400> 17 Met Ser Ser Phe Ser Tyr Glu Pro Tyr Tyr Ser Thr Ser Tyr Lys Arg 1 5 10 15 Arg Tyr Val Glu Thr Pro Arg Val His Ile Ser Ser Val Arg Ser Gly 20 25 30 Tyr Ser Thr Ala Arg Ser Ala Tyr Ser Ser Tyr Ser Ala Pro Val Ser 35 40 45 Ser Ser Leu Ser Val Arg Arg Ser Tyr Ser Ser Ser Ser Gly Ser Leu 50 55 60 Met Pro Ser Leu Glu Asn Leu Asp Leu Ser Gln Val Ala Ala Ile Ser 65 70 75 80 Asn Asp Leu Lys Ser Ile Arg Thr Gln Glu Lys Ala Gln Leu Gln Asp 85 90 95 Leu Asn Asp Arg Phe Ala Ser Phe Ile Glu Arg Val His Glu Leu Glu 100 105 110 Gln Gln Asn Lys Val Leu Glu Ala Glu Leu Leu Val Leu Arg Gln Lys 115 120 125 His Ser Glu Pro Ser Arg Phe Arg Ala Leu Tyr Glu Gln Glu Ile Arg 130 135 140 Asp Leu Arg Leu Ala Ala Glu Asp Ala Thr Asn Glu Lys Gln Ala Leu 145 150 155 160 Gln Gly Glu Arg Glu Gly Leu Glu Glu Thr Leu Arg Asn Leu Gln Ala 165 170 175 Arg Tyr Glu Glu Glu Val Leu Ser Arg Glu Asp Ala Glu Gly Arg Leu 180 185 190 Met Glu Ala Arg Lys Gly Ala Asp Glu Ala Ala Leu Ala Arg Ala Glu 195 200 205 Leu Glu Lys Arg Ile Asp Ser Leu Met Asp Glu Ile Ser Phe Leu Lys 210 215 220 Lys Val His Glu Glu Glu Ile Ala Glu Leu Gln Ala Gln Ile Gln Tyr 225 230 235 240 Ala Gln Ile Ser Val Glu Met Asp Val Thr Lys Pro Asp Leu Ser Ala 245 250 255 Ala Leu Lys Asp Ile Arg Ala Gln Tyr Glu Lys Leu Ala Ala Lys Asn 260 265 270 Met Gln Asn Ala Glu Glu Trp Phe Lys Ser Arg Phe Thr Val Leu Thr 275 280 285 Glu Ser Ala Ala Lys Asn Thr Asp Ala Val Arg Ala Ala Lys Asp Glu 290 295 300 Val Ser Glu Ser Arg Arg Leu Leu Lys Ala Lys Thr Leu Glu Ile Glu 305 310 315 320 Ala Cys Arg Gly Met Asn Glu Ala Leu Glu Lys Gln Leu Gln Glu Leu 325 330 335 Glu Asp Lys Gln Asn Ala Asp Ile Ser Ala Met Gln Asp Thr Ile Asn 340 345 350 Lys Leu Glu Asn Glu Leu Arg Thr Thr Lys Ser Glu Met Ala Arg Tyr 355 360 365 Leu Lys Glu Tyr Gln Asp Leu Leu Asn Val Lys Met Ala Leu Asp Ile 370 375 380 Glu Ile Ala Ala Tyr Arg Lys Leu Leu Glu Gly Glu Glu Thr Arg Leu 385 390 395 400 Ser Phe Thr Ser Val Gly Ser Ile Thr Ser Gly Tyr Ser Gln Ser Ser 405 410 415 Gln Val Phe Gly Arg Ser Ala Tyr Gly Gly Leu Gln Thr Ser Ser Tyr 420 425 430 Leu Met Ser Thr Arg Ser Phe Pro Ser Tyr Tyr Thr Ser His Val Gln 435 440 445 Glu Glu Gln Ile Glu Val Glu Glu Thr Ile Glu Ala Ala Lys Ala Glu 450 455 460 Glu Ala Lys Asp Glu Pro Pro Ser Glu Gly Glu Ala Glu Glu Glu Glu 465 470 475 480 Lys Asp Lys Glu Glu Ala Glu Glu Glu Glu Ala Ala Glu Glu Glu Glu 485 490 495 Ala Ala Lys Glu Glu Ser Glu Glu Ala Lys Glu Glu Glu Glu Gly Gly 500 505 510 Glu Gly Glu Glu Gly Glu Glu Thr Lys Glu Ala Glu Glu Glu Glu Lys 515 520 525 Lys Val Glu Gly Ala Gly Glu Glu Gln Ala Ala Lys Lys Lys Asp 530 535 540 <210> 18 <211> 284 <212> PRT <213> Homo sapiens <400> 18 Met Ser Ser Phe Ser Tyr Glu Pro Tyr Tyr Ser Thr Ser Tyr Lys Arg 1 5 10 15 Arg Tyr Val Glu Thr Pro Arg Val His Ile Ser Ser Val Arg Ser Gly 20 25 30 Tyr Ser Thr Ala Arg Ser Ala Tyr Ser Ser Tyr Ser Ala Pro Val Ser 35 40 45 Ser Ser Leu Ser Val Arg Arg Ser Tyr Ser Ser Ser Ser Gly Ser Leu 50 55 60 Met Pro Ser Leu Glu Asn Leu Asp Leu Ser Gln Val Ala Ala Ile Ser 65 70 75 80 Asn Asp Leu Lys Ser Ile Arg Thr Gln Glu Lys Ala Gln Leu Gln Asp 85 90 95 Leu Asn Asp Arg Phe Ala Ser Phe Ile Glu Arg Val His Glu Leu Glu 100 105 110 Gln Gln Asn Lys Val Leu Glu Ala Glu Leu Leu Val Leu Arg Gln Lys 115 120 125 His Ser Glu Pro Ser Arg Phe Arg Ala Leu Tyr Glu Gln Glu Ile Arg 130 135 140 Asp Leu Arg Leu Ala Ala Glu Asp Ala Thr Asn Glu Lys Gln Ala Leu 145 150 155 160 Gln Gly Glu Arg Glu Gly Leu Glu Glu Thr Leu Arg Asn Leu Gln Ala 165 170 175 Arg Tyr Glu Glu Glu Val Leu Ser Arg Glu Asp Ala Glu Gly Arg Leu 180 185 190 Met Glu Ala Arg Lys Gly Ala Lys Asn Thr Asp Ala Val Arg Ala Ala 195 200 205 Lys Asp Glu Val Ser Glu Ser Arg Arg Leu Leu Lys Ala Lys Thr Leu 210 215 220 Glu Ile Glu Ala Cys Arg Gly Met Asn Glu Ala Leu Glu Lys Gln Leu 225 230 235 240 Gln Glu Leu Glu Asp Lys Gln Asn Ala Asp Ile Ser Val Met Gln Asp 245 250 255 Thr Ile Asn Lys Leu Glu Asn Glu Leu Arg Thr Thr Lys Ser Glu Met 260 265 270 Ala Arg Tyr Leu Lys Glu Tyr Gln Asp Leu Leu Thr 275 280 <210> 19 <211> 272 <212> PRT <213> Homo sapiens <400> 19 Met His Leu Arg Leu Ile Ser Trp Leu Phe Ile Ile Leu Asn Phe Met 1 5 10 15 Glu Tyr Ile Gly Ser Gln Asn Ala Ser Arg Gly Arg Arg Gln Arg Arg 20 25 30 Met His Pro Asn Val Ser Gln Gly Cys Gln Gly Gly Cys Ala Thr Cys 35 40 45 Ser Asp Tyr Asn Gly Cys Leu Ser Cys Lys Pro Arg Leu Phe Phe Ala 50 55 60 Leu Glu Arg Ile Gly Met Lys Gln Ile Gly Val Cys Leu Ser Ser Cys 65 70 75 80 Pro Ser Gly Tyr Tyr Gly Thr Arg Tyr Pro Asp Ile Asn Lys Cys Thr 85 90 95 Lys Cys Lys Ala Asp Cys Asp Thr Cys Phe Asn Lys Asn Phe Cys Thr 100 105 110 Lys Cys Lys Ser Gly Phe Tyr Leu His Leu Gly Lys Cys Leu Asp Asn 115 120 125 Cys Pro Glu Gly Leu Glu Ala Asn Asn His Thr Met Glu Cys Val Ser 130 135 140 Ile Val His Cys Glu Val Ser Glu Trp Asn Pro Trp Ser Pro Cys Thr 145 150 155 160 Lys Lys Gly Lys Thr Cys Gly Phe Lys Arg Gly Thr Glu Thr Arg Val 165 170 175 Arg Glu Ile Ile Gln His Pro Ser Ala Lys Gly Asn Leu Cys Pro Pro 180 185 190 Thr Asn Glu Thr Arg Lys Cys Thr Val Gln Arg Lys Lys Cys Gln Lys 195 200 205 Gly Glu Arg Gly Lys Lys Gly Arg Glu Arg Lys Arg Lys Lys Pro Asn 210 215 220 Lys Gly Glu Ser Lys Glu Ala Ile Pro Asp Ser Lys Ser Leu Glu Ser 225 230 235 240 Ser Lys Glu Ile Pro Glu Gln Arg Glu Asn Lys Gln Gln Gln Lys Lys 245 250 255 Arg Lys Val Gln Asp Lys Gln Lys Ser Val Ser Val Ser Thr Val His 260 265 270 <210> 20 <211> 203 <212> PRT <213> Homo sapiens <400> 20 Met Lys Gln Ile Gly Val Cys Leu Ser Ser Cys Pro Ser Gly Tyr Tyr 1 5 10 15 Gly Thr Arg Tyr Pro Asp Ile Asn Lys Cys Thr Lys Cys Lys Ala Asp 20 25 30 Cys Asp Thr Cys Phe Asn Lys Asn Phe Cys Thr Lys Cys Lys Ser Gly 35 40 45 Phe Tyr Leu His Leu Gly Lys Cys Leu Asp Asn Cys Pro Glu Gly Leu 50 55 60 Glu Ala Asn Asn His Thr Met Glu Cys Val Ser Ile Val His Cys Glu 65 70 75 80 Val Ser Glu Trp Asn Pro Trp Ser Pro Cys Thr Lys Lys Gly Lys Thr 85 90 95 Cys Gly Phe Lys Arg Gly Thr Glu Thr Arg Val Arg Glu Ile Ile Gln 100 105 110 His Pro Ser Ala Lys Gly Asn Leu Cys Pro Pro Thr Asn Glu Thr Arg 115 120 125 Lys Cys Thr Val Gln Arg Lys Lys Cys Gln Lys Gly Glu Arg Gly Lys 130 135 140 Lys Gly Arg Glu Arg Lys Arg Lys Lys Pro Asn Lys Gly Glu Ser Lys 145 150 155 160 Glu Ala Ile Pro Asp Ser Lys Ser Leu Glu Ser Ser Lys Glu Ile Pro 165 170 175 Glu Gln Arg Glu Asn Lys Gln Gln Gln Lys Lys Arg Lys Val Gln Asp 180 185 190 Lys Gln Lys Ser Val Ser Val Ser Thr Val His 195 200 <210> 21 <211> 224 <212> PRT <213> Homo sapiens <400> 21 Met His Leu Arg Leu Ile Ser Trp Leu Phe Ile Ile Leu Asn Phe Met 1 5 10 15 Glu Tyr Ile Gly Ser Gln Asn Ala Ser Arg Gly Arg Arg Gln Arg Arg 20 25 30 Met His Pro Asn Val Ser Gln Gly Cys Gln Gly Gly Cys Ala Thr Cys 35 40 45 Ser Asp Tyr Asn Gly Cys Leu Ser Cys Lys Pro Arg Leu Phe Phe Ala 50 55 60 Leu Glu Arg Ile Gly Met Lys Gln Ile Gly Val Cys Leu Ser Ser Cys 65 70 75 80 Pro Ser Gly Tyr Tyr Gly Thr Arg Tyr Pro Asp Ile Asn Lys Cys Thr 85 90 95 Lys Cys Lys Ala Asp Cys Asp Thr Cys Phe Asn Lys Asn Phe Cys Thr 100 105 110 Lys Cys Lys Ser Gly Phe Tyr Leu His Leu Gly Lys Cys Leu Asp Asn 115 120 125 Cys Pro Glu Gly Leu Glu Ala Asn Asn His Thr Met Glu Cys Val Ser 130 135 140 Ile Val His Cys Glu Val Ser Glu Trp Asn Pro Trp Ser Pro Cys Thr 145 150 155 160 Lys Lys Gly Lys Thr Cys Gly Phe Lys Arg Gly Thr Glu Thr Arg Val 165 170 175 Arg Glu Ile Ile Gln His Pro Ser Ala Lys Gly Asn Leu Cys Pro Pro 180 185 190 Thr Asn Glu Thr Arg Lys Cys Thr Val Gln Arg Lys Lys Cys Gln Lys 195 200 205 Gly Glu Arg Gly Arg Thr Ser Arg Gly Asp Glu Arg Cys Phe Asn His 210 215 220 <210> 22 <211> 553 <212> PRT <213> Homo sapiens <400> 22 Met Thr Trp Arg Met Gly Pro Arg Phe Thr Met Leu Leu Ala Met Trp 1 5 10 15 Leu Val Cys Gly Ser Glu Pro His Pro His Ala Thr Ile Arg Gly Ser 20 25 30 His Gly Gly Arg Lys Val Pro Leu Val Ser Pro Asp Ser Ser Arg Pro 35 40 45 Ala Arg Phe Leu Arg His Thr Gly Arg Ser Arg Gly Ile Glu Arg Ser 50 55 60 Thr Leu Glu Glu Pro Asn Leu Gln Pro Leu Gln Arg Arg Arg Ser Val 65 70 75 80 Pro Val Leu Arg Leu Ala Arg Pro Thr Glu Pro Pro Ala Arg Ser Asp 85 90 95 Ile Asn Gly Ala Ala Val Arg Pro Glu Gln Arg Pro Ala Ala Arg Gly 100 105 110 Ser Pro Arg Glu Met Ile Arg Asp Glu Gly Ser Ser Ala Arg Ser Arg 115 120 125 Met Leu Arg Phe Pro Ser Gly Ser Ser Ser Pro Asn Ile Leu Ala Ser 130 135 140 Phe Ala Gly Lys Asn Arg Val Trp Val Ile Ser Ala Pro His Ala Ser 145 150 155 160 Glu Gly Tyr Tyr Arg Leu Met Met Ser Leu Leu Lys Asp Asp Val Tyr 165 170 175 Cys Glu Leu Ala Glu Arg His Ile Gln Gln Ile Val Leu Phe His Gln 180 185 190 Ala Gly Glu Glu Gly Gly Lys Val Arg Arg Ile Thr Ser Glu Gly Gln 195 200 205 Ile Leu Glu Gln Pro Leu Asp Pro Ser Leu Ile Pro Lys Leu Met Ser 210 215 220 Phe Leu Lys Leu Glu Lys Gly Lys Phe Gly Met Val Leu Leu Lys Lys 225 230 235 240 Thr Leu Gln Val Glu Glu Arg Tyr Pro Tyr Pro Val Arg Leu Glu Ala 245 250 255 Met Tyr Glu Val Ile Asp Gln Gly Pro Ile Arg Arg Ile Glu Lys Ile 260 265 270 Arg Gln Lys Gly Phe Val Gln Lys Cys Lys Ala Ser Gly Val Glu Gly 275 280 285 Gln Val Val Ala Glu Gly Asn Asp Gly Gly Gly Gly Ala Gly Arg Pro 290 295 300 Ser Leu Gly Ser Glu Lys Lys Lys Glu Asp Pro Arg Arg Ala Gln Val 305 310 315 320 Pro Pro Thr Arg Glu Ser Arg Val Lys Val Leu Arg Lys Leu Ala Ala 325 330 335 Thr Ala Pro Ala Leu Pro Gln Pro Pro Ser Thr Pro Arg Ala Thr Thr 340 345 350 Leu Pro Pro Ala Pro Ala Thr Thr Val Thr Arg Ser Thr Ser Arg Ala 355 360 365 Val Thr Val Ala Ala Arg Pro Met Thr Thr Thr Ala Phe Pro Thr Thr 370 375 380 Gln Arg Pro Trp Thr Pro Ser Pro Ser His Arg Pro Pro Thr Thr Thr 385 390 395 400 Glu Val Ile Thr Ala Arg Arg Pro Ser Val Ser Glu Asn Leu Tyr Pro 405 410 415 Pro Ser Arg Lys Asp Gln His Arg Glu Arg Pro Gln Thr Thr Arg Arg 420 425 430 Pro Ser Lys Ala Thr Ser Leu Glu Ser Phe Thr Asn Ala Pro Pro Thr 435 440 445 Thr Ile Ser Glu Pro Ser Thr Arg Ala Ala Gly Pro Gly Arg Phe Arg 450 455 460 Asp Asn Arg Met Asp Arg Arg Glu His Gly His Arg Asp Pro Asn Val 465 470 475 480 Val Pro Gly Pro Pro Lys Pro Ala Lys Glu Lys Pro Pro Lys Lys Lys 485 490 495 Ala Gln Asp Lys Ile Leu Ser Asn Glu Tyr Glu Glu Lys Tyr Asp Leu 500 505 510 Ser Arg Pro Thr Ala Ser Gln Leu Glu Asp Glu Leu Gln Val Gly Asn 515 520 525 Val Pro Leu Lys Lys Ala Lys Glu Ser Lys Lys His Glu Lys Leu Glu 530 535 540 Lys Pro Glu Lys Lys Lys Glu Lys Lys 545 550 <210> 23 <211> 331 <212> PRT <213> Homo sapiens <400> 23 Glu Gly Lys Arg Arg Leu Leu Leu Ile Thr Ala Pro Lys Ala Glu Asn 1 5 10 15 Asn Met Tyr Val Gln Gln Arg Asp Glu Tyr Leu Glu Ser Phe Cys Lys 20 25 30 Met Ala Thr Arg Lys Ile Ser Val Ile Thr Ile Phe Gly Pro Val Asn 35 40 45 Asn Ser Thr Met Lys Ile Asp His Phe Gln Leu Asp Asn Glu Lys Pro 50 55 60 Met Arg Val Val Asp Asp Glu Asp Leu Val Asp Gln Arg Leu Ile Ser 65 70 75 80 Glu Leu Arg Lys Glu Tyr Gly Met Thr Tyr Asn Asp Phe Phe Met Val 85 90 95 Leu Thr Asp Val Asp Leu Arg Val Lys Gln Tyr Tyr Glu Val Pro Ile 100 105 110 Thr Met Lys Ser Val Phe Asp Leu Ile Asp Thr Phe Gln Ser Arg Ile 115 120 125 Lys Asp Met Glu Lys Gln Lys Lys Glu Gly Ile Val Cys Lys Glu Asp 130 135 140 Lys Lys Gln Ser Leu Glu Asn Phe Leu Ser Arg Phe Arg Trp Arg Arg 145 150 155 160 Arg Leu Leu Val Ile Ser Ala Pro Asn Asp Glu Asp Trp Ala Tyr Ser 165 170 175 Gln Gln Leu Ser Ala Leu Ser Gly Gln Ala Cys Asn Phe Gly Leu Arg 180 185 190 His Ile Thr Ile Leu Lys Leu Leu Gly Val Gly Glu Glu Val Gly Gly 195 200 205 Val Leu Glu Leu Phe Pro Ile Asn Gly Gly Ser Val Val Glu Arg Glu 210 215 220 Asp Val Pro Ala His Leu Val Lys Asp Ile Arg Asn Tyr Phe Gln Val 225 230 235 240 Ser Pro Glu Tyr Phe Ser Met Leu Leu Val Gly Lys Asp Gly Asn Val 245 250 255 Lys Ser Trp Tyr Pro Ser Pro Met Trp Ser Met Val Ile Val Tyr Asp 260 265 270 Leu Ile Asp Ser Met Gln Leu Arg Arg Gln Glu Met Ala Ile Gln Gln 275 280 285 Ser Leu Gly Met Arg Cys Pro Glu Asp Glu Tyr Ala Gly Tyr Gly Tyr 290 295 300 His Ser Tyr His Gln Gly Tyr Gln Asp Gly Tyr Gln Asp Asp Tyr Arg 305 310 315 320 His His Glu Ser Tyr His His Gly Tyr Pro Tyr 325 330 <210> 24 <211> 85 <212> PRT <213> Homo sapiens <400> 24 Met Leu Leu Val Gly Lys Asp Gly Asn Val Lys Ser Trp Tyr Pro Ser 1 5 10 15 Pro Met Trp Ser Met Val Ile Val Tyr Asp Leu Ile Asp Ser Met Gln 20 25 30 Leu Arg Arg Gln Glu Met Ala Ile Gln Gln Ser Leu Gly Met Arg Cys 35 40 45 Pro Glu Asp Glu Tyr Ala Gly Tyr Gly Tyr His Ser Tyr His Gln Gly 50 55 60 Tyr Gln Asp Gly Tyr Gln Asp Asp Tyr Arg His His Glu Ser Tyr His 65 70 75 80 His Gly Tyr Pro Tyr 85 <210> 25 <211> 297 <212> PRT <213> Homo sapiens <400> 25 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His His Arg Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln Glu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Ala Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Gly Gly Leu Leu 165 170 175 Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val 180 185 190 Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu Asn Ile 195 200 205 Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys Ser Ser 210 215 220 Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser Cys Thr 225 230 235 240 Ser Glu Ser His Ser His Trp Val His Ser Pro Ile Glu Cys Thr Glu 245 250 255 Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr Thr Gly Ala Glu 260 265 270 Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu Glu Leu 275 280 285 Asn Val Pro Phe Glu Val Pro Ser Pro 290 295 <210> 26 <211> 318 <212> PRT <213> Homo sapiens <400> 26 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His His Arg Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln Glu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Ala Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Glu Lys Leu Ile 165 170 175 Ile Phe Ser Asp Pro Val Pro Ala Ser Leu Asn Leu Ile Pro Glu Phe 180 185 190 Ala Gly Gly Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu 195 200 205 Ser Leu Phe Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln 210 215 220 Val Ser Glu Asn Ile Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu 225 230 235 240 Asp Asp Cys Ser Ser Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr 245 250 255 Met Ala Ser Cys Thr Ser Glu Ser His Ser His Trp Val His Ser Pro 260 265 270 Ile Glu Cys Thr Glu Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser 275 280 285 Tyr Thr Gly Ala Glu Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly 290 295 300 Asp Arg Leu Glu Leu Asn Val Pro Phe Glu Val Pro Ser Pro 305 310 315 <210> 27 <211> 173 <212> PRT <213> Homo sapiens <400> 27 Met Ser Thr Gly Thr Asn Gly Asp Gly Val Ser Pro Ala Asn Gly Val 1 5 10 15 Val Leu Asp Arg Ser Tyr Pro Arg Cys Leu Pro Val Glu Leu Ser Gly 20 25 30 Gly Arg Tyr Thr His Ser Ala Pro Ser Gly Gly His Thr Cys Cys Thr 35 40 45 Gly Gly Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser 50 55 60 Leu Phe Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val 65 70 75 80 Ser Glu Asn Ile Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp 85 90 95 Asp Cys Ser Ser Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met 100 105 110 Ala Ser Cys Thr Ser Glu Ser His Ser His Trp Val His Ser Pro Ile 115 120 125 Glu Cys Thr Glu Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr 130 135 140 Thr Gly Ala Glu Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp 145 150 155 160 Arg Leu Glu Leu Asn Val Pro Phe Glu Val Pro Ser Pro 165 170 <210> 28 <211> 265 <212> PRT <213> Homo sapiens <400> 28 Met Ser Thr Gly Thr Asn Gly Asp Gly Val Ser Pro Ala Asn Gly Val 1 5 10 15 Val Leu Asp Arg Ser Tyr Pro Arg Ile Val Val Met Glu Arg Val Glu 20 25 30 Met Pro Thr Ala Gln Pro Ala Leu Leu Ala Gly Thr Lys Ala Ala Gly 35 40 45 Ala Thr Thr Asp Val Arg Val Ala Ser Pro Val Leu Ser Ser Ile Val 50 55 60 Phe Arg Arg Ser Thr Ala Gln Leu Pro Leu Met Leu Ser Val Gly Thr 65 70 75 80 Val Cys Pro Gly Ala Phe Gln Leu Ser Leu Val Glu Ala Asp Thr Pro 85 90 95 Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser Ser Leu 100 105 110 Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu Tyr Cys 115 120 125 Lys Gln Phe Phe Asn Arg His Cys Gln Arg Val Ala Gly Gly Leu Leu 130 135 140 Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val 145 150 155 160 Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu Asn Ile 165 170 175 Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys Ser Ser 180 185 190 Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser Cys Thr 195 200 205 Ser Glu Ser His Ser His Trp Val His Ser Pro Ile Glu Cys Thr Glu 210 215 220 Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr Thr Gly Ala Glu 225 230 235 240 Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu Glu Leu 245 250 255 Asn Val Pro Phe Glu Val Pro Ser Pro 260 265 <210> 29 <211> 107 <212> PRT <213> Homo sapiens <400> 29 Met Ser Thr Gly Thr Asn Gly Asp Gly Val Ser Pro Ala Asn Gly Val 1 5 10 15 Val Leu Asp Arg Ser Tyr Pro Arg Cys Leu Pro Val Glu Leu Ser Gly 20 25 30 Gly Arg Tyr Thr His Ser Ala Pro Ser Gly Gly His Thr Cys Cys Thr 35 40 45 Gly Gly Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser 50 55 60 Leu Phe Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val 65 70 75 80 Ser Trp Ala Pro Gly Ser Leu Ala Gln Leu Phe Ser Leu Asp Ser Val 85 90 95 Pro Ile Pro Gln Gln Gln Gln Gly Pro Glu Met 100 105 <210> 30 <211> 134 <212> PRT <213> Homo sapiens <400> 30 Met Gly Thr Val Cys His Leu Pro Thr Val Trp Ser Trp Thr Gly Ala 1 5 10 15 Ile Gln Gly Ala Phe Gln Leu Ser Leu Val Glu Ala Asp Thr Pro Thr 20 25 30 Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser Ser Leu Leu 35 40 45 Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu Tyr Cys Lys 50 55 60 Gln Phe Phe Asn Arg His Cys Gln Arg Val Ala Gly Gly Leu Leu Gln 65 70 75 80 Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val Pro 85 90 95 Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Trp Ala Pro Gly 100 105 110 Ser Leu Ala Gln Leu Phe Ser Leu Asp Ser Val Pro Ile Pro Gln Gln 115 120 125 Gln Gln Gly Pro Glu Met 130 <210> 31 <211> 132 <212> PRT <213> Homo sapiens <400> 31 Met Gly Thr Val Cys His Leu Pro Thr Val Trp Ser Trp Thr Gly Ala 1 5 10 15 Ile Gln Gly Ala Phe Gln Leu Ser Leu Val Glu Ala Asp Thr Pro Thr 20 25 30 Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser Ser Leu Leu 35 40 45 Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu Tyr Cys Lys 50 55 60 Gln Phe Phe Asn Arg His Cys Gln Arg Gly Gly Leu Leu Gln Phe Glu 65 70 75 80 Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val Pro Pro Ser 85 90 95 Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Trp Ala Pro Gly Ser Leu 100 105 110 Ala Gln Leu Phe Ser Leu Asp Ser Val Pro Ile Pro Gln Gln Gln Gln 115 120 125 Gly Pro Glu Met 130 <210> 32 <211> 299 <212> PRT <213> Homo sapiens <400> 32 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His His Arg Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln Glu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Thr Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Val Ala Gly Gly 165 170 175 Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe 180 185 190 Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu 195 200 205 Asn Ile Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys 210 215 220 Ser Ser Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser 225 230 235 240 Cys Thr Ser Glu Ser His Ser His Trp Val His Ser Pro Ile Glu Cys 245 250 255 Thr Glu Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr Thr Gly 260 265 270 Ala Glu Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu 275 280 285 Glu Leu Asn Val Pro Phe Glu Val Pro Ser Pro 290 295 <210> 33 <211> 297 <212> PRT <213> Homo sapiens <400> 33 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His His Arg Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln Glu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Thr Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Gly Gly Leu Leu 165 170 175 Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val 180 185 190 Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu Asn Ile 195 200 205 Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys Ser Ser 210 215 220 Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser Cys Thr 225 230 235 240 Ser Glu Ser His Ser His Trp Val His Ser Pro Ile Glu Cys Thr Glu 245 250 255 Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr Thr Gly Ala Glu 260 265 270 Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu Glu Leu 275 280 285 Asn Val Pro Phe Glu Val Pro Ser Pro 290 295 <210> 34 <211> 134 <212> PRT <213> Homo sapiens <400> 34 Met Asp Pro Gln Thr Ala Pro Ser Arg Ala Leu Leu Leu Leu Leu Phe 1 5 10 15 Leu His Leu Ala Phe Leu Gly Gly Arg Ser His Pro Leu Gly Ser Pro 20 25 30 Gly Ser Ala Ser Asp Leu Glu Thr Ser Gly Leu Gln Glu Gln Arg Asn 35 40 45 His Leu Gln Gly Lys Leu Ser Glu Leu Gln Val Glu Gln Thr Ser Leu 50 55 60 Glu Pro Leu Gln Glu Ser Pro Arg Pro Thr Gly Val Trp Lys Ser Arg 65 70 75 80 Glu Val Ala Thr Glu Gly Ile Arg Gly His Arg Lys Met Val Leu Tyr 85 90 95 Thr Leu Arg Ala Pro Arg Ser Pro Lys Met Val Gln Gly Ser Gly Cys 100 105 110 Phe Gly Arg Lys Met Asp Arg Ile Ser Ser Ser Ser Gly Leu Gly Cys 115 120 125 Lys Val Leu Arg Arg His 130 SEQUENCE LISTING <110> ALNYLAM PHARMACEUTICALS, INC. <120> COMPOSITIONS AND METHODS FOR INHIBITING EXPRESSION OF TRANSTHYRETIN (TTR) <130> 121301-12320 <140> <141> <150> 62/985,950 <151> 2020-03-06 <160> 34 <170> PatentIn version 3.5 <210> 1 <400> 1 000 <210> 2 <400> 2 000 <210> 3 <400> 3 000 <210> 4 <400> 4 000 <210> 5 <400> 5 000 <210> 6 <211> 21 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 6 ugggauuuca uguaaccaag a 21 <210 > 7 <211> 23 <212> DNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note= "Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 7 ucuuggtuac augaaauccc auc 23 <210> 8 <211> 21 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note= "Description of Artificial Sequence: Synthetic oligonucleotide" <400> 8 ugggauuuca uguaaccaag a 21 <210> 9 <211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 9 ucuugguuac augaaauccc auc 23 <210> 10 <211> 21 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 10 u gggauuuca uguaaccaag a 21 <210> 11 <211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 11 ucuugguuac augaaauccc auc 23 <210> 12 <211> 23 <212> DNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note="Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 12 uctugguuac augaaauccc auc 23 <210> 13 <211> 23 <212> DNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note="Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 13 ucutgguuac augaaauccc auc 23 <210> 14 < 211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 14 ucuugguuac augaaauccc auc 23 <210> 15 <211> 23 <212> RNA <213> Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <400> 15 ucuugguuac augaaauccc auc 23 <210> 16 <211> 23 <212> DNA <213 >Artificial Sequence <220> <221> source <223> /note="Description of Artificial Sequence: Synthetic oligonucleotide" <220> <221> source <223> /note="Description of Combined DNA/RNA Molecule: Synthetic oligonucleotide" <400> 16 ucuuggutac augaaauccc auc 23 <210> 17 <211> 543 <212> PRT <213> Homo sapiens <400> 17 Met Ser Ser Phe Ser Tyr Glu Pro Tyr Tyr Ser Thr Ser Tyr Lys Arg 1 5 10 15 Arg Tyr Val Glu Thr Pro Arg Val His Ile Ser Ser Val Arg Ser Gly 20 25 30 Tyr Ser Thr Ala Arg Ser Ala Tyr Ser Ser Tyr Ser Ala Pro Val Ser 35 40 45 Ser Ser Leu Ser Val Arg Arg Ser Tyr Ser Ser Ser Ser Gly Ser Leu 50 55 60 Met Pro Ser Leu Glu Asn Leu Asp Leu Ser Gln Val Ala Ala Ile Ser 65 70 75 80 Asn Asp Leu Lys Ser Ile Arg Thr Gln Glu Lys Ala Gln Leu Gln Asp 85 90 95 Leu Asn Asp Arg Phe Ala Ser Phe Ile Glu Arg Val His Glu Leu Glu 100 105 110 Gln Gln Asn Lys Val Leu Glu Ala Glu Leu Leu Val Leu Arg Gln Lys 115 120 125 His Ser Glu Pro Ser Arg Phe Arg Ala Leu Tyr Glu Gln Glu Ile Arg 130 135 140 Asp Leu Arg Leu Ala Ala Glu Asp Ala Thr Asn Glu Lys Gln Ala Leu 145 150 155 160 Gln Gly Glu Arg Glu Gly Leu Glu Glu Thr Leu Arg Asn Leu Gln Ala 165 170 175 Arg Tyr Glu Glu Glu Val Leu Ser Arg Glu Asp Ala Glu Gly Arg Leu 180 185 190 Met Glu Ala Arg Lys Gly Ala Asp Glu Ala Ala Leu Ala Arg Ala Glu 195 200 205 Leu Glu Lys Arg Ile Asp Ser Leu Met Asp Glu Ile Ser Phe Leu Lys 210 215 220 Lys Val His Glu Glu Glu Ile Ala Glu Leu Gln Ala Gln Ile Gln Tyr 225 230 235 240 Ala Gln Ile Ser Val Glu Met Asp Val Thr Lys Pro Asp Leu Ser Ala 245 250 255 Ala Leu Lys Asp Ile Arg Ala Gln Tyr Glu Lys Leu Ala Ala Lys Asn 260 265 270 Met Gln Asn Ala Glu Glu Trp Phe Lys Ser Arg Phe Thr Val Leu Thr 275 280 285 Glu Ser Ala Ala Lys Asn Thr Asp Ala Val Arg Ala Ala Lys Asp Glu 290 295 300 Val Ser Glu Ser Arg Arg Leu Leu Lys Ala Lys Thr Leu Glu Ile Glu 305 310 315 320 Ala Cys Arg Gly Met Asn Glu Ala Leu Glu Lys Gln Leu Gln Glu Leu 325 330 335 Glu Asp Lys Gln Asn Ala Asp Ile Ser Ala Met Gln Asp Thr Ile Asn 340 345 350 Lys Leu Glu Asn Glu Leu Arg Thr Thr Lys Ser Glu Met Ala Arg Tyr 355 360 365 Leu Lys Glu Tyr Gln Asp Leu Leu Asn Val Lys Met Ala Leu Asp Ile 370 375 380 Glu Ile Ala Ala Tyr Arg Lys Leu Leu Glu Gly Glu Glu Thr Arg Leu 385 390 395 400 Ser Phe Thr Ser Val Gly Ser Ile Thr Ser Gly Tyr Ser Gln Ser Ser Ser 405 410 415 Gln Val Phe Gly Arg Ser Ala Tyr Gly Gly Leu Gln Thr Ser Ser Tyr 420 425 430 Leu Met Ser Thr Arg Ser Phe Pro Ser Tyr Tyr Thr Ser His Val Gln 435 440 445 Glu Glu Gln Ile Glu Val Glu Glu Thr Ile Glu Ala Ala Lys Ala Glu 450 455 460 Glu Ala Lys Asp Glu Pro Pro Ser Glu Gly Glu Ala Glu Glu Glu Glu 465 470 475 480 Lys Asp Lys Glu Glu Ala Glu Glu Glu Glu Ala Ala Glu Glu Glu Glu Glu 485 490 495 Ala Ala Lys Glu Glu Glu Glu Glu Glu Ala Lys Glu Glu Glu Glu Gly Gly 500 505 510 Glu Gly Glu Glu Gly Glu Glu Thr Lys Glu Ala Glu Glu Glu Glu Lys 515 520 525 Lys Val Glu Gly Ala Gly Glu Glu Gln Ala Ala Lys Lys Lys Asp 530 535 540 <210> 18 <211> 284 <212> PRT <213> Homo sapiens <400> 18 Met Ser Ser Phe Ser Tyr Glu Tyr Ser Thr Ser Tyr Lys Arg 1 5 10 15 Arg Tyr Val Glu Thr Pro Arg Val His Ile Ser Ser Val Arg Ser Gly 20 25 30 Tyr Ser Thr Ala Arg Ser Ala Tyr Ser Ser Tyr Ser Ala Pro Val Ser 35 40 45 Ser Ser Leu Ser Val Arg Arg Ser Tyr Ser Ser Ser Ser Gly Ser Leu 50 55 60 Met Pro Ser Leu Glu Asn Leu Asp Leu Ser Gln Val Ala Ala Ile Ser 65 70 75 80 Asn Asp Leu Lys Ser Ile Arg Thr Gln Glu Lys Ala Gln Leu Gln Asp 85 90 95 Leu Asn Asp Arg Phe Ala Ser Phe Ile Glu Arg Val His Glu Leu Glu 100 105 110 Gln Gln Asn Lys Val Leu Glu Ala Glu Leu Leu Val Leu Arg Gln Lys 115 120 125 His Ser Glu Pro Ser Arg Phe Arg Ala Leu Tyr Glu Gln Glu Ile Arg 130 135 140 Asp Leu Arg Leu Ala Ala Glu Asp Ala Thr Asn Glu Lys Gln Ala Leu 145 150 155 160 Gln Gly Glu Arg Glu Gly Leu Glu Glu Thr Leu Arg Asn Leu Gln Ala 165 170 175 Arg Tyr Glu Glu Glu Val Leu Ser Arg Glu Asp Ala Glu Gly Arg Leu 180 185 190 Met Glu Ala Arg Lys Gly Ala Lys Asn Thr Asp Ala Val Arg Ala Ala 195 200 205 Lys Asp Glu Val Ser Glu Ser Arg Arg Leu Leu Lys Ala Lys Thr Leu 210 215 220 Glu Ile Glu Ala Cys Arg Gly Met Asn Glu Ala Leu Glu Lys Gln Leu 225 230 235 240 Gln Glu Leu Glu Asp Lys Gln Asn Ala Asp Ile Ser Val Met Gln Asp 245 250 255 Thr Ile Asn Lys Leu Glu Asn Glu Leu Arg Thr Thr Lys Ser Glu Met 260 265 270 Ala Arg Tyr Leu Lys Glu Tyr Gln Asp Leu Leu Thr 275 280 <210> 19 <211> 272 <212> PRT <213> Homo sapiens <400> 19 Met His Leu Arg Leu Ile Ser Trp Leu Phe Ile Il e Leu Asn Phe Met 1 5 10 15 Glu Tyr Ile Gly Ser Gln Asn Ala Ser Arg Gly Arg Arg Gln Arg Arg 20 25 30 Met His Pro Asn Val Ser Gln Gly Cys Gln Gly Gly Cys Ala Thr Cys 35 40 45 Ser Asp Tyr Asn Gly Cys Leu Ser Cys Lys Pro Arg Leu Phe Phe Ala 50 55 60 Leu Glu Arg Ile Gly Met Lys Gln Ile Gly Val Cys Leu Ser Ser Cys 65 70 75 80 Pro Ser Gly Tyr Tyr Gly Thr Arg Tyr Pro Asp Ile Asn Lys Cys Thr 85 90 95 Lys Cys Lys Ala Asp Cys Asp Thr Cys Phe Asn Lys Asn Phe Cys Thr 100 105 110 Lys Cys Lys Ser Gly Phe Tyr Leu His Leu Gly Lys Cys Leu Asp Asn 115 120 125 Cys Pro Glu Gly Leu Glu Ala Asn Asn His Thr Met Glu Cys Val Ser 130 135 140 Ile Val His Cys Glu Val Ser Glu Trp Asn Pro Trp Ser Pro Cys Thr 145 150 155 160 Lys Lys Gly Lys Thr Cys Gly Phe Lys Arg Gly Thr Glu Thr Arg Val 165 170 175 Arg Glu Ile Ile Gln His Pro Se r Ala Lys Gly Asn Leu Cys Pro Pro 180 185 190 Thr Asn Glu Thr Arg Lys Cys Thr Val Gln Arg Lys Lys Cys Gln Lys 195 200 205 Gly Glu Arg Gly Lys Lys Gly Arg Glu Arg Lys Arg Lys Lys Pro Asn 210 215 220 Lys Gly Glu Ser Lys Glu Ala Ile Pro Asp Ser Lys Ser Leu Glu Ser 225 230 235 240 Ser Lys Glu Ile Pro Glu Gln Arg Glu Asn Lys Gln Gln Gln Lys Lys 245 250 255 Arg Lys Val Gln Asp Lys Gln Lys Ser Val Ser Val Ser Thr Val His 260 265 270 <210> 20 <211> 203 <212> PRT <213> Homo sapiens <400> 20 Met Lys Gln Ile Gly Val Cys Leu Ser Ser Cys Pro Ser Gly Tyr Tyr 1 5 10 15 Gly Thr Arg Tyr Pro Asp Ile Asn Lys Cys Thr Lys Cys Lys Ala Asp 20 25 30 Cys Asp Thr Cys Phe Asn Lys Asn Phe Cys Thr Lys Cys Lys Ser Gly 35 40 45 Phe Tyr Leu His Leu Gly Lys Cys Leu Asp Asn Cys Pro Glu Gly Leu 50 55 6 0 Glu Ala Asn Asn His Thr Met Glu Cys Val Ser Ile Val His Cys Glu 65 70 75 80 Val Ser Glu Trp Asn Pro Trp Ser Pro Cys Thr Lys Lys Gly Lys Thr 85 90 95 Cys Gly Phe Lys Arg Gly Thr Glu Thr Arg Val Arg Glu Ile Ile Gln 100 105 110 His Pro Ser Ala Lys Gly Asn Leu Cys Pro Pro Thr Asn Glu Thr Arg 115 120 125 Lys Cys Thr Val Gln Arg Lys Lys Cys Gln Lys Gly Glu Arg Gly Lys 130 135 140 Lys Gly Arg Glu Arg Lys Arg Lys Lys Pro Asn Lys Gly Glu Ser Lys 145 150 155 160 Glu Ala Ile Pro Asp Ser Lys Ser Leu Glu Ser Ser Lys Glu Ile Pro 165 170 175 Glu Gln Arg Glu Asn Lys Gln Gln Gln Lys Lys Arg Lys Val Gln Asp 180 185 190 Lys Gln Lys Ser Val Ser Val Ser Thr Val His 195 200 <210> 21 <211> 224 <212> PRT <213> Homo sapiens <400> 21 Met His Leu Arg Leu Ile Ser Trp Leu Phe Ile Ile Leu Asn Phe Met 1 5 10 15 Glu Tyr Ile Gly Ser Gln Asn Ala Ser Arg Gly Arg Arg Gln Arg Arg 20 25 30 Met His Pro Asn Val Ser Gln Gly Cys Gln Gly Gly Cys Ala Thr Cys 35 40 45 Ser Asp Tyr Asn Gly Cys Leu Ser Cys Lys Pro Arg Leu Phe Phe Ala 50 55 60 Leu Glu Arg Ile Gly Met Lys Gln Ile Gly Val Cys Leu Ser Ser Cys 65 70 75 80 Pro Ser Gly Tyr Tyr Gly Thr Arg Tyr Pro Asp Ile Asn Lys Cys Thr 85 90 95 Lys Cys Lys Ala Asp Cys Asp Thr Cys Phe Asn Lys Asn Phe Cys Thr 100 105 110 Lys Cys Lys Ser Gly Phe Tyr Leu His Leu Gly Lys Cys Leu Asp Asn 115 120 125 Cys Pro Glu Gly Leu Glu Ala Asn Asn His Thr Met Glu Cys Val Ser 130 135 140 Ile Val His Cys Glu Val Ser Glu Trp Asn Pro Trp Ser Pro Cys Thr 145 150 155 160 Lys Lys Gly Lys Thr Cys Gly Phe Lys Arg Gly Thr Glu Thr Arg Val 165 170 175 Arg Glu Ile Ile Gln His Pro Ser Ala Lys Gly Asn Leu Cys Pro Pro 180 185 190 Thr Asn Glu Thr Arg Lys Cys Thr Val Gln Arg Lys Lys Cys Gln Lys 195 200 205 Gly Glu Arg Gly Arg Thr Ser Arg Gly Asp Glu Arg Cys Phe Asn His 210 215 220 <210> 22 <211> 553 <212> PRT <213> Homo sapiens <400> 22 Met Thr Trp Arg Met Gly Pro Arg Phe Thr Met Leu Leu Ala Met Trp 1 5 10 15 Leu Val Cys Gly Ser Glu Pro His Pro His Ala Thr Ile Arg Gly Ser 20 25 30 His Gly Gly Arg Lys Val Pro Leu Val Ser Pro Asp Ser Ser Arg Pro 35 40 45 Ala Arg Phe Leu Arg His Thr Gly Arg Ser Arg Gly Ile Glu Arg Ser 50 55 60 Thr Leu Glu Glu Pro Asn Leu Gln Pro Leu Gln Arg Arg Arg Ser Val 65 70 75 80 Pro Val Leu Arg Leu Ala Arg Pro Thr Glu Pro Pro Ala Arg Ser Asp 85 90 95 Ile Asn Gly Ala Ala Val Arg Pro Glu Gln Arg Pro Ala Ala Arg Gly 100 105 110 Ser Pro Arg Glu Met Ile Arg Asp Glu Gly Ser Ser Ala Arg Ser Arg 115 120 125 Met Leu Arg Phe Pro Ser Gly Ser Ser Ser Pro Asn Ile Leu Ala Ser 130 135 140 Phe Ala Gly Lys Asn Arg Val Trp Val Ile Ser Ala Pro His Ala Ser 145 150 155 160 Glu Gly Tyr Tyr Arg Leu Met Met Ser Leu Leu Lys Asp Asp Val Tyr 165 170 175 Cys Glu Leu Ala Glu Arg His Ile Gln Gln Ile Val Leu Phe His Gln 180 185 190 Ala Gly Glu Glu Gly Gly Lys Val Arg Arg Ile Thr Ser Glu Gly Gln 195 200 205 Ile Leu Glu Gln Pro Leu Asp Pro Ser Leu Ile Pro Lys Leu Met Ser 210 215 220 Phe Leu Lys Leu Glu Lys Gly Lys Phe Gly Met Val Leu Leu Lys Lys 225 230 235 240 Thr Leu Gln Val Glu Glu Arg Tyr Pro Tyr Pro Val Arg Leu Glu Ala 245 250 255 Met Tyr Glu Val Ile Asp Gln Gly Pro Ile Arg Arg Ile Glu Lys Ile 260 265 270 Arg Gln Lys Gly Phe Val Gln Lys Cys Lys Ala Ser Gly Val Glu Gly 275 280 285 Gln Val Val Ala Glu Gly Asn Asp Gly Gly Gly Gly Ala Gly Arg Pro 290 295 300 Ser Leu Gly Ser Glu Lys Lys Lys Glu Asp Pro Arg Arg Ala Gln Val 305 310 315 320 Pro Pro Thr Arg Glu Ser Arg Val Lys Val Leu Arg Lys Leu Ala Ala 325 330 335 Thr Ala Pro Ala Leu Pro Gln Pro Pro Ser Thr Pro Arg Ala Thr Thr 340 345 350 Leu Pro Pro Ala Pro Ala Thr Thr Val Thr Arg Ser Thr Ser Arg Ala 355 360 365 Val Thr Val Ala Ala Arg Pro Met Thr Thr Thr Ala Phe Pro Thr Thr Thr 370 375 380 Gln Arg Pro Trp Thr Pro Ser Pro Ser His Arg Pro Pro Thr Thr Thr 385 390 395 400 Glu Val Ile Thr Ala Arg Arg Pro Ser Val Ser Glu Asn Leu Tyr Pro 405 410 415 Pro Ser Arg Lys Asp Gln His Arg Glu Arg Pro Gln Thr Thr Arg Arg 420 425 430 Pro Ser Lys Ala Thr Ser Leu Glu Ser Phe Thr Asn Ala Pro Pro Thr 435 440 445 Thr Ile Ser Glu Pro Ser Thr Arg Ala Ala Gly Pro Gly Arg Phe Arg 450 455 460 Asp Asn Arg Met Asp Arg Arg Glu His Gly His Arg Asp Pro Asn Val 465 470 475 480 Val Pro Gly Pro Pro Lys Pro Ala Lys Glu Lys Pro Pro Lys Lys Lys 485 490 495 Ala Gln Asp Lys Ile Leu Ser Asn Glu Tyr Glu Glu Lys Tyr Asp Leu 500 505 510 Ser Arg Pro Thr Ala Ser Gln Leu Glu Asp Glu Leu Gln Val Gly Asn 515 520 525 Val Pro Leu Lys Lys Ala Lys Glu Ser Lys Lys His Glu Lys Leu Glu 530 535 540 Lys Pro Glu Lys Lys Lys Glu Lys Lys 545 550 <210> 23 <211> 331 <212> PRT <213> Homo sapiens <400> 23 Glu Gly Lys Arg Arg Leu Leu Leu Ile Thr Ala Pro Lys Ala Glu Asn 1 5 10 15 Asn Met Tyr Val Gln Gln Arg Asp Glu Tyr Leu Glu Ser Phe Cys Lys 20 25 30 Met Ala Thr Arg Lys Ile Ser Val Ile Thr Ile Phe Gly Pro Val Asn 35 40 45 Asn Ser Thr Met Lys Ile Asp His Phe Gln Leu Asp Asn Glu Lys Pro 50 55 60 Met Arg Val Val Asp Asp Glu Asp Leu Val Asp Gln Arg Leu Ile Ser 65 70 75 80 Glu Leu Arg Lys Glu Tyr Gly Met Thr Tyr Asn Asp Phe Phe Met Val 85 90 95 Leu Thr Asp Val Asp Leu Arg Val Lys Gln Tyr Tyr Glu Val Pro Ile 100 105 110 Thr Met Lys Ser Val Phe Asp Leu Ile Asp Thr Phe Gln Ser Arg Ile 115 120 125 Lys Asp Met Glu Lys Gln Lys Lys Glu Gly Ile Val Cys Lys Glu Asp 130 135 140 Lys Lys Gln Ser Leu Glu Asn Phe Leu Ser Arg Phe Arg Trp Arg Arg 145 150 155 160 Arg Leu Leu Val Ile Ser Ala Pro Asn Asp Glu Asp Trp Ala Tyr Ser 165 170 175 Gln Gln Leu Ser Ala Leu Ser Gly Gln Ala Cys Asn Phe Gly Leu Arg 180 185 190 His Ile Thr Ile Leu Lys Leu Leu Gly Val Gly Glu Glu Val Gly Gly 195 200 205 Val Leu Glu Leu Phe Pro Ile Asn Gly Gly Ser Val Val Glu Arg Glu 210 215 220 Asp Val Pro Ala His Leu Val Lys Asp Ile Arg Asn Tyr Phe Gln Val 225 230 235 240 Ser Pro Glu Tyr Phe Ser Met Leu Leu Val Gly Lys Asp Gly Asn Val 245 250 255 Lys Ser Trp Tyr Pro Ser Pro Met Trp Ser Met Val Ile Val Tyr Asp 260 265 270 Leu Ile Asp Ser Met Gln Leu Arg Arg Gln Glu Met Ala Ile Gln Gln 275 280 285 Ser Leu Gly Met Arg Cys Pro Glu Asp Glu Tyr Ala Gly Tyr Gly Tyr 290 295 300 His Ser Tyr His Gln Gly Tyr Gln Asp Gly Tyr Gln Asp Asp Tyr Arg 305 310 315 320 His His Glu Ser Tyr His His Gly Tyr Pro Tyr 325 330 <210> 24 <211> 85 <212> PRT <213> Homo sapiens <400> 24 Met Leu Leu Val Gly Lys Asp Gly Asn Val Lys Ser Trp Tyr Pro Ser 1 5 10 15 Pro Met Trp Ser Met Val Ile Val Tyr Asp Leu Ile Asp Ser Met Gln 20 25 30 Leu Arg Arg Gln Glu Met Ala Ile Gln Gln Ser Leu Gly Met Arg Cys 35 40 45 Pro Glu Asp Glu Tyr Ala Gly Tyr Gly Tyr His Ser Tyr His Gln Gly 50 55 60 Tyr Gln Asp Gly Tyr Gln Asp Asp Tyr Arg His His Glu Ser Tyr His 65 70 75 80 His Gly Tyr Pro Tyr 85 <210> 25 <211> 297 <212> PRT <213> Homo sapiens <400> 25 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His Ar g Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln Glu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Ala Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Gly Gly Leu Leu 165 170 175 Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val 180 185 190 Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu Asn Ile 195 200 205 Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys Ser Ser 210 215 220 Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser Cys Thr 225 230 235 240 Ser Glu Ser His Ser His Trp Val His Ser Pro Ile Glu Cys Thr Glu 245 250 255 Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr Thr Gly Ala Glu 260 265 270 Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu Glu Leu 275 280 285 Asn Val Pro Phe Glu Val Pro Ser Pro 290 295 <210 > 26 <211> 318 <212> PRT <213> Homo sapiens <400> 26 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His Arg Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln Glu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Ala Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Glu Lys Leu Ile 165 170 175 Ile Phe Ser Asp Pro Val Pro Ala Ser Leu Asn Leu Ile Pro Glu Phe 180 185 190 Ala Gly Gly Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu 195 200 205 Ser Leu Phe Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln 210 215 220 Val Ser Glu Asn Ile Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu 225 230 235 240 Asp Asp Cys Ser Ser Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr 245 250 255 Met Ala Ser Cys Thr Ser Glu Ser His Ser His Trp Val His Ser Pro 260 265 270 Ile Glu Cys Thr Glu Leu Asp Leu Gln Lys Phe Ser Ser Ser Ser Ala Ser 275 280 285 Tyr Thr Gly Ala Glu Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly 290 295 300 Asp Arg Leu Glu Leu Asn Val Pro Phe Glu Val Pro Ser Pro 305 310 315 <210> 27 <211> 173 <212> PRT <213> Homo sapiens <400> 27 Met Ser Thr Gly Thr Asn Gly Asp Gly Val Ser Pro Ala Asn Gly Val 1 5 10 15 Val Leu Asp Arg Ser Tyr Pro Arg Cys Leu Pro Val Glu Leu Ser Gly 20 25 30 Gly Arg Tyr Thr His Ser Ala Pro Ser Gly Gly His Thr Cys Cys Thr 35 40 45 Gly Gly Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser 50 5 5 60 Leu Phe Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val 65 70 75 80 Ser Glu Asn Ile Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp 85 90 95 Asp Cys Ser Ser Ser Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met 100 105 110 Ala Ser Cys Thr Ser Glu Ser His Ser His Trp Val His Ser Pro Ile 115 120 125 Glu Cys Thr Glu Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr 130 135 140 Thr Gly Ala Glu Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp 145 150 155 160 Arg Leu Glu Leu Asn Val Pro Phe Glu Val Pro Ser Pro 165 170 <210> 28 <211> 265 <212> PRT <213> Homo sapiens <400> 28 Met Ser Thr Gly Thr Asn Gly Asp Gly Val Ser Pro Ala Asn Gly Val 1 5 10 15 Val Leu Asp Arg Ser Tyr Pro Arg Ile Val Val Met Glu Arg Val Glu 20 25 30 Met Pro Thr Ala Gln Pro Ala Leu Leu Ala Gly Thr Lys Ala Ala Gly 35 40 45 Ala Thr Thr Asp Val Arg Val Ala Ser Pro Val Leu Ser Ser Ile Val 50 55 60 Phe Arg Arg Ser Thr Ala Gln Leu Pro Leu Met Leu Ser Val Gly Thr 65 70 75 80 Val Cys Pro Gly Ala Phe Gln Leu Ser Leu Val Glu Ala Asp Thr Pro 85 90 95 Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser Ser Leu 100 105 110 Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu Tyr Cys 115 120 125 Lys Gln Phe Phe Asn Arg His Cys Gln Arg Val Ala Gly Gly Leu Leu 130 135 140 Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val 145 150 155 160 Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu Asn Ile 165 170 175 Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys Ser Ser 180 185 190 Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser Cys Thr 195 200 205 Ser Glu Ser His Ser His Trp V al His Ser Pro Ile Glu Cys Thr Glu 210 215 220 Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr Thr Gly Ala Glu 225 230 235 240 Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu Glu Leu 245 250 255 Asn Val Pro Phe Glu Val Pro Ser Pro 260 265 <210> 29 <211> 107 <212> PRT <213> Homo sapiens <400> 29 Met Ser Thr Gly Thr Asn Gly Asp Gly Val Ser Pro Ala Asn Gly Val 1 5 10 15 Val Leu Asp Arg Ser Tyr Pro Arg Cys Leu Pro Val Glu Leu Ser Gly 20 25 30 Gly Arg Tyr Thr His Ser Ala Pro Ser Gly Gly His Thr Cys Cys Thr 35 40 45 Gly Gly Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser 50 55 60 Leu Phe Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val 65 70 75 80 Ser Trp Ala Pro Gly Ser Leu Ala Gln Leu Phe Ser Leu Asp Ser Val 85 90 95 Pro Ile Pro Gln Gln Gln Gln Gly Pro Glu Met 100 105 <210> 30 <211> 134 <212> PRT <213> Homo sapi ens <400> 30 Met Gly Thr Val Cys His Leu Pro Thr Val Trp Ser Trp Thr Gly Ala 1 5 10 15 Ile Gln Gly Ala Phe Gln Leu Ser Leu Val Glu Ala Asp Thr Pro Thr 20 25 30 Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser Ser Leu Leu 35 40 45 Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu Tyr Cys Lys 50 55 60 Gln Phe Phe Asn Arg His Cys Gln Arg Val Ala Gly Gly Leu Leu Gln 65 70 75 80 Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val Pro 85 90 95 Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Trp Ala Pro Gly 100 105 110 Ser Leu Ala Gln Leu Phe Ser Leu Asp Ser Val Pro Ile Pro Gln Gln 115 120 125 Gln Gln Gly Pro Glu Met 130 <210> 31 <211> 132 <212> PRT <213> Homo sapiens <400> 31 Met Gly Thr Val Cys His Leu Pro Thr Val Trp Ser Trp Thr Gly Ala 1 5 10 15 Ile Gln Gly Ala Phe Gln Leu Ser Leu Val Glu Ala Asp Thr Pro Thr 20 25 30 Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser Ser Leu Leu 35 40 45 Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu Tyr Cys Lys 50 55 60 Gln Phe Phe Asn Arg His Cys Gln Arg Gly Gly Leu Leu Gln Phe Glu 65 70 75 80 Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val Pro Pro Ser 85 90 95 Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Trp Ala Pro Gly Ser Leu 100 105 110 Ala Gln Leu Phe Ser Leu Asp Ser Val Pro Ile Pro Gln Gln Gln Gln 115 120 125 Gly Pro Glu Met 130 <210> 32 <211> 299 <212> PRT <213> Homo sapiens <400> 32 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His Arg Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln G lu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Thr Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Val Ala Gly Gly 165 170 175 Leu Leu Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe 180 185 190 Pro Val Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu 195 200 205 Asn Ile Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys 210 215 220 Ser Ser Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser 225 230 235 240 Cys Thr Ser G lu Ser His Ser His Trp Val His Ser Pro Ile Glu Cys 245 250 255 Thr Glu Leu Asp Leu Gln Lys Phe Ser Ser Ser Ala Ser Tyr Thr Gly 260 265 270 Ala Glu Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu 275 280 285 Glu Leu Asn Val Pro Phe Glu Val Pro Ser Pro 290 295 <210> 33 <211> 297 <212> PRT <213> Homo sapiens <400> 33 Met Asp Cys Gln Glu Asn Glu Tyr Trp Asp Gln Trp Gly Arg Cys Val 1 5 10 15 Thr Cys Gln Arg Cys Gly Pro Gly Gln Glu Leu Ser Lys Asp Cys Gly 20 25 30 Tyr Gly Glu Gly Gly Asp Ala Tyr Cys Thr Ala Cys Pro Pro Arg Arg 35 40 45 Tyr Lys Ser Ser Trp Gly His Arg Cys Gln Ser Cys Ile Thr Cys 50 55 60 Ala Val Ile Asn Arg Val Gln Lys Val Asn Cys Thr Ala Thr Ser Asn 65 70 75 80 Ala Val Cys Gly Asp Cys Leu Pro Arg Phe Tyr Arg Lys Thr Arg Ile 85 90 95 Gly Gly Leu Gln Asp Gln Glu Cys Ile Pro Cys Thr Lys Gln Thr Pro 100 105 110 Thr Ser Glu Val Gln Cys Ala Phe Gln Leu Ser Leu Val Glu Ala Asp 115 120 125 Thr Pro Thr Val Pro Pro Gln Glu Ala Thr Leu Val Ala Leu Val Ser 130 135 140 Ser Leu Leu Val Val Phe Thr Leu Ala Phe Leu Gly Leu Phe Phe Leu 145 150 155 160 Tyr Cys Lys Gln Phe Phe Asn Arg His Cys Gln Arg Gly Gly Leu Leu 165 170 175 Gln Phe Glu Ala Asp Lys Thr Ala Lys Glu Glu Ser Leu Phe Pro Val 180 185 190 Pro Pro Ser Lys Glu Thr Ser Ala Glu Ser Gln Val Ser Glu Asn Ile 195 200 205 Phe Gln Thr Gln Pro Leu Asn Pro Ile Leu Glu Asp Asp Cys Ser Ser Ser 210 215 220 Thr Ser Gly Phe Pro Thr Gln Glu Ser Phe Thr Met Ala Ser Cys Thr 225 230 235 240 Ser Glu Ser His Ser His Trp Val His Ser Pro Ile Glu Cys Thr Glu 245 250 255 Leu Asp Leu Gln Lys Phe Ser Ser Ser Ser Ala Ser Tyr Thr Gly Ala Glu 260 265 270 Thr Leu Gly Gly Asn Thr Val Glu Ser Thr Gly Asp Arg Leu Glu Leu 275 280 285 Asn Val Pro Phe Glu Val Pro Ser Pro 290 295 <210> 34 <211> 134 <212> PRT <213> Homo sapiens <400> 34 Met Asp Pro Gln Thr Ala Pro Ser Arg Ala Leu Leu Leu Leu Leu Leu Phe 1 5 10 15 Leu His Leu Ala Phe Leu Gly Gly Arg Ser His Pro Leu Gly Ser Pro 20 25 30 Gly Ser Ala Ser Asp Leu Glu Thr Ser Gly Leu Gln Glu Gln Arg Asn 35 40 45 His Leu Gln Gly Lys Leu Ser Glu Leu Gln Val Glu Gln Thr Ser Leu 50 55 60 Glu Pro Leu Gln Glu Ser Pro Arg Pro Thr Gly Val Trp Lys Ser Arg 65 70 75 80 Glu Val Ala Thr Glu Gly Ile Arg Gly His Arg Lys Met Val Leu Tyr 85 90 95 Thr Leu Arg Ala Pro Arg Ser Pro Lys Met Val Gln Gly Ser Gly Cys 100 105 110 Phe Gly Arg Lys Met Asp Arg Ile Ser Ser Ser Ser Gly Leu Gly Cys 115 120 125 Lys Val Leu Arg Arg His 130
Claims (51)
상기 센스 가닥 및 안티센스 가닥 각각이 독립적으로 30개 이하의 뉴클레오타이드 길이이고;
상기 센스 가닥이 변형된 뉴클레오타이드 서열 5'-usgsggauUfuCfAfUfguaaccaaga-3' (서열번호 6)를 포함하고;
상기 안티센스 가닥이 변형된 뉴클레오타이드 서열 5'-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3' (서열번호 7)을 포함하고,
여기서, a, c, g, 및 u는 각각 2'-O-메틸아데노신-3'-포스페이트, 2'-O-메틸시티딘-3'-포스페이트, 2'-O-메틸구아노신-3'-포스페이트, 및 2'-O-메틸우리딘-3'-포스페이트이고;
Af, Cf, Gf, 및 Uf는 각각 2'-플루오로아데노신-3'-포스페이트, 2'-플루오로시티딘-3'-포스페이트, 2'-플루오로구아노신-3'-포스페이트, 및 2'-플루오로우리딘-3'-포스페이트이고;
(Tgn)은 티미딘-글리콜 핵산 (GNA) S-이성체이고;
s는 포스포로티오에이트 링커인, RNAi 제제.A double-stranded RNAi agent comprising a sense strand and an antisense strand, wherein
wherein each of the sense strand and antisense strand is independently 30 nucleotides or less in length;
the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6);
wherein the antisense strand comprises the modified nucleotide sequence 5′-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3′ (SEQ ID NO: 7);
Here, a, c, g, and u are 2'-O-methyladenosine-3'-phosphate, 2'-O-methylcytidine-3'-phosphate, and 2'-O-methylguanosine-3', respectively. -phosphate, and 2'-O-methyluridine-3'-phosphate;
Af, Cf, Gf, and Uf are 2'-fluoroadenosine-3'-phosphate, 2'-fluorocytidine-3'-phosphate, 2'-fluoroguanosine-3'-phosphate, and 2, respectively. '-fluorouridine-3'-phosphate;
(Tgn) is the thymidine-glycol nucleic acid (GNA) S-isomer;
and s is a phosphorothioate linker.
인, RNAi 제제.4. The method of claim 3, wherein the ligand
Phosphorus, RNAi agent.
여기서, X가 O 또는 S인, RNAi 제제.6. The method of claim 5, wherein the double-stranded RNAi agent is conjugated to a ligand as shown in the scheme below,
wherein X is O or S.
상기 센스 가닥 및 안티센스 가닥 각각이 독립적으로 30개 이하의 뉴클레오타이드 길이이고;
상기 센스 가닥이 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고;
상기 안티센스 가닥이 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)을 포함하고,
여기서, a, c, g, 및 u는 각각 2'-O-메틸아데노신-3’-포스페이트, 2'-O-메틸시티딘-3’-포스페이트, 2'-O-메틸구아노신-3’-포스페이트, 및 2'-O-메틸우리딘-3’-포스페이트이고;
Af, Cf, Gf, 및 Uf는 각각 2’-플루오로아데노신-3’-포스페이트, 2’-플루오로시티딘-3’-포스페이트, 2’-플루오로구아노신-3’-포스페이트, 및 2’-플루오로우리딘-3’-포스페이트이고;
(Tgn)은 티미딘-글리콜 핵산 (GNA) S-이성체이고;
s는 포스포로티오에이트 링커인, 용도.Use of an RNAi agent in a method of treating a human subject suffering from a TTR-related disease, wherein the method comprises administering to the subject a fixed dose of 25 mg to 1000 mg of a double-stranded RNAi agent comprising a sense strand and an antisense strand. include, where
wherein each of the sense strand and antisense strand is independently 30 nucleotides or less in length;
the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6);
wherein the antisense strand comprises the modified nucleotide sequence 5′-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3′ (SEQ ID NO: 7);
Here, a, c, g, and u are 2'-O-methyladenosine-3'-phosphate, 2'-O-methylcytidine-3'-phosphate, and 2'-O-methylguanosine-3', respectively. -phosphate, and 2'-O-methyluridine-3'-phosphate;
Af, Cf, Gf, and Uf are 2'-fluoroadenosine-3'-phosphate, 2'-fluorocytidine-3'-phosphate, 2'-fluoroguanosine-3'-phosphate, and 2, respectively. '-fluorouridine-3'-phosphate;
(Tgn) is the thymidine-glycol nucleic acid (GNA) S-isomer;
s is a phosphorothioate linker.
상기 센스 가닥 및 안티센스 가닥 각각이 독립적으로 30개 이하의 뉴클레오타이드 길이이고;
상기 센스 가닥이 변형된 뉴클레오타이드 서열 5’-usgsggauUfuCfAfUfguaaccaaga-3’ (서열번호 6)를 포함하고;
상기 안티센스 가닥이 변형된 뉴클레오타이드 서열 5’-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3’ (서열번호 7)을 포함하고,
여기서, a, c, g, 및 u는 각각 2'-O-메틸아데노신-3’-포스페이트, 2'-O-메틸시티딘-3’-포스페이트, 2'-O-메틸구아노신-3’-포스페이트, 및 2'-O-메틸우리딘-3’-포스페이트이고;
Af, Cf, Gf, 및 Uf는 각각 2’-플루오로아데노신-3’-포스페이트, 2’-플루오로시티딘-3’-포스페이트, 2’-플루오로구아노신-3’-포스페이트, 및 2’-플루오로우리딘-3’-포스페이트이고;
(Tgn)은 티미딘-글리콜 핵산 (GNA) S-이성체이고;
s는 포스포로티오에이트 링커인, 용도. Use of an RNAi agent in a method of inhibiting the expression of TTR in a human subject who does not meet the criteria for diagnosis of a TTR-related disease, wherein the method comprises fixing 25 mg to 1000 mg of a double-stranded RNAi agent comprising a sense strand and an antisense strand administering the dose to the subject, wherein
wherein each of the sense strand and antisense strand is independently 30 nucleotides or less in length;
the sense strand comprises the modified nucleotide sequence 5'-usgsggauUfuCfAfUfguaaccaaga-3' (SEQ ID NO: 6);
wherein the antisense strand comprises the modified nucleotide sequence 5′-usCfsuugGf(Tgn)uAfcaugAfaAfucccasusc-3′ (SEQ ID NO: 7);
Here, a, c, g, and u are 2'-O-methyladenosine-3'-phosphate, 2'-O-methylcytidine-3'-phosphate, and 2'-O-methylguanosine-3', respectively. -phosphate, and 2'-O-methyluridine-3'-phosphate;
Af, Cf, Gf, and Uf are 2'-fluoroadenosine-3'-phosphate, 2'-fluorocytidine-3'-phosphate, 2'-fluoroguanosine-3'-phosphate, and 2, respectively. '-fluorouridine-3'-phosphate;
(Tgn) is the thymidine-glycol nucleic acid (GNA) S-isomer;
s is a phosphorothioate linker.
인, 용도.12. The method of claim 11, wherein the ligand
person, use.
여기서, X가 O 또는 S인, 용도.14. The method of claim 13, wherein the double-stranded RNAi agent is conjugated to a ligand as shown in the scheme below,
wherein X is O or S.
51. The use of claim 50, wherein the additional therapeutic agent is a TTR tetramer stabilizer or a non-steroidal anti-inflammatory agent.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202062985950P | 2020-03-06 | 2020-03-06 | |
| US62/985,950 | 2020-03-06 | ||
| PCT/US2021/021049 WO2021178778A1 (en) | 2020-03-06 | 2021-03-05 | Compositions and methods for inhibiting expression of transthyretin (ttr) |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220152270A true KR20220152270A (en) | 2022-11-15 |
Family
ID=75252841
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227034708A Pending KR20220152270A (en) | 2020-03-06 | 2021-03-05 | Compositions and methods for inhibiting the expression of transthyretin (TTR) |
Country Status (8)
| Country | Link |
|---|---|
| EP (1) | EP4114949A1 (en) |
| JP (1) | JP7802676B2 (en) |
| KR (1) | KR20220152270A (en) |
| CN (1) | CN115461460A (en) |
| AU (1) | AU2021232029A1 (en) |
| CA (1) | CA3174473A1 (en) |
| IL (1) | IL296106A (en) |
| WO (1) | WO2021178778A1 (en) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3222620A1 (en) | 2008-10-20 | 2010-04-29 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of transthyretin |
| JP6896703B2 (en) | 2015-07-31 | 2021-06-30 | アルナイラム ファーマシューティカルズ, インコーポレイテッドAlnylam Pharmaceuticals, Inc. | Transthyretin (TTR) iRNA composition for treating or preventing TTR-related diseases and how to use it |
| US11806360B2 (en) | 2017-09-19 | 2023-11-07 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for treating transthyretin (TTR) mediated amyloidosis |
| CN117795074A (en) | 2021-08-03 | 2024-03-29 | 阿尔尼拉姆医药品有限公司 | Transthyretin (TTR) iRNA compositions and methods of use |
| EP4634385A2 (en) * | 2022-12-16 | 2025-10-22 | Amgen Inc. | Rnai constructs for inhibiting ttr expression and methods of use thereof |
| WO2025077916A1 (en) * | 2023-10-13 | 2025-04-17 | 北京安龙生物医药有限公司 | Transthyretin-targeting oligonucleotide and use thereof |
| WO2025098117A1 (en) * | 2023-11-06 | 2025-05-15 | 成都倍特药业股份有限公司 | Rnai reagent and composition for inhibiting expression of transthyretin (ttr), and use |
Family Cites Families (84)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5927900A (en) | 1982-08-09 | 1984-02-14 | Wakunaga Seiyaku Kk | Oligonucleotide derivative and its preparation |
| FR2540122B1 (en) | 1983-01-27 | 1985-11-29 | Centre Nat Rech Scient | NOVEL COMPOUNDS COMPRISING A SEQUENCE OF OLIGONUCLEOTIDE LINKED TO AN INTERCALATION AGENT, THEIR SYNTHESIS PROCESS AND THEIR APPLICATION |
| US4605735A (en) | 1983-02-14 | 1986-08-12 | Wakunaga Seiyaku Kabushiki Kaisha | Oligonucleotide derivatives |
| US4948882A (en) | 1983-02-22 | 1990-08-14 | Syngene, Inc. | Single-stranded labelled oligonucleotides, reactive monomers and methods of synthesis |
| US4824941A (en) | 1983-03-10 | 1989-04-25 | Julian Gordon | Specific antibody to the native form of 2'5'-oligonucleotides, the method of preparation and the use as reagents in immunoassays or for binding 2'5'-oligonucleotides in biological systems |
| US4587044A (en) | 1983-09-01 | 1986-05-06 | The Johns Hopkins University | Linkage of proteins to nucleic acids |
| US5118802A (en) | 1983-12-20 | 1992-06-02 | California Institute Of Technology | DNA-reporter conjugates linked via the 2' or 5'-primary amino group of the 5'-terminal nucleoside |
| US5430136A (en) | 1984-10-16 | 1995-07-04 | Chiron Corporation | Oligonucleotides having selectably cleavable and/or abasic sites |
| US5258506A (en) | 1984-10-16 | 1993-11-02 | Chiron Corporation | Photolabile reagents for incorporation into oligonucleotide chains |
| US4828979A (en) | 1984-11-08 | 1989-05-09 | Life Technologies, Inc. | Nucleotide analogs for nucleic acid labeling and detection |
| US5034506A (en) | 1985-03-15 | 1991-07-23 | Anti-Gene Development Group | Uncharged morpholino-based polymers having achiral intersubunit linkages |
| US4762779A (en) | 1985-06-13 | 1988-08-09 | Amgen Inc. | Compositions and methods for functionalizing nucleic acids |
| US5317098A (en) | 1986-03-17 | 1994-05-31 | Hiroaki Shizuya | Non-radioisotope tagging of fragments |
| JPS638396A (en) | 1986-06-30 | 1988-01-14 | Wakunaga Pharmaceut Co Ltd | Poly-labeled oligonucleotide derivative |
| US4904582A (en) | 1987-06-11 | 1990-02-27 | Synthetic Genetics | Novel amphiphilic nucleic acid conjugates |
| US5585481A (en) | 1987-09-21 | 1996-12-17 | Gen-Probe Incorporated | Linking reagents for nucleotide probes |
| US5525465A (en) | 1987-10-28 | 1996-06-11 | Howard Florey Institute Of Experimental Physiology And Medicine | Oligonucleotide-polyamide conjugates and methods of production and applications of the same |
| DE3738460A1 (en) | 1987-11-12 | 1989-05-24 | Max Planck Gesellschaft | MODIFIED OLIGONUCLEOTIDS |
| US5082830A (en) | 1988-02-26 | 1992-01-21 | Enzo Biochem, Inc. | End labeled nucleotide probe |
| US5109124A (en) | 1988-06-01 | 1992-04-28 | Biogen, Inc. | Nucleic acid probe linked to a label having a terminal cysteine |
| US5262536A (en) | 1988-09-15 | 1993-11-16 | E. I. Du Pont De Nemours And Company | Reagents for the preparation of 5'-tagged oligonucleotides |
| US5512439A (en) | 1988-11-21 | 1996-04-30 | Dynal As | Oligonucleotide-linked magnetic particles and uses thereof |
| US5457183A (en) | 1989-03-06 | 1995-10-10 | Board Of Regents, The University Of Texas System | Hydroxylated texaphyrins |
| US5599923A (en) | 1989-03-06 | 1997-02-04 | Board Of Regents, University Of Tx | Texaphyrin metal complexes having improved functionalization |
| US5391723A (en) | 1989-05-31 | 1995-02-21 | Neorx Corporation | Oligonucleotide conjugates |
| US4958013A (en) | 1989-06-06 | 1990-09-18 | Northwestern University | Cholesteryl modified oligonucleotides |
| US5451463A (en) | 1989-08-28 | 1995-09-19 | Clontech Laboratories, Inc. | Non-nucleoside 1,3-diol reagents for labeling synthetic oligonucleotides |
| US5254469A (en) | 1989-09-12 | 1993-10-19 | Eastman Kodak Company | Oligonucleotide-enzyme conjugate that can be used as a probe in hybridization assays and polymerase chain reaction procedures |
| US5292873A (en) | 1989-11-29 | 1994-03-08 | The Research Foundation Of State University Of New York | Nucleic acids labeled with naphthoquinone probe |
| US5486603A (en) | 1990-01-08 | 1996-01-23 | Gilead Sciences, Inc. | Oligonucleotide having enhanced binding affinity |
| US7037646B1 (en) | 1990-01-11 | 2006-05-02 | Isis Pharmaceuticals, Inc. | Amine-derivatized nucleosides and oligonucleosides |
| US5578718A (en) | 1990-01-11 | 1996-11-26 | Isis Pharmaceuticals, Inc. | Thiol-derivatized nucleosides |
| US6783931B1 (en) | 1990-01-11 | 2004-08-31 | Isis Pharmaceuticals, Inc. | Amine-derivatized nucleosides and oligonucleosides |
| AU7579991A (en) | 1990-02-20 | 1991-09-18 | Gilead Sciences, Inc. | Pseudonucleosides and pseudonucleotides and their polymers |
| US5214136A (en) | 1990-02-20 | 1993-05-25 | Gilead Sciences, Inc. | Anthraquinone-derivatives oligonucleotides |
| DK0455905T3 (en) | 1990-05-11 | 1998-12-07 | Microprobe Corp | Dipsticks for nucleic acid hybridization assays and method for covalent immobilization of oligonucleotides |
| US5138045A (en) | 1990-07-27 | 1992-08-11 | Isis Pharmaceuticals | Polyamine conjugated oligonucleotides |
| US5218105A (en) | 1990-07-27 | 1993-06-08 | Isis Pharmaceuticals | Polyamine conjugated oligonucleotides |
| US5688941A (en) | 1990-07-27 | 1997-11-18 | Isis Pharmaceuticals, Inc. | Methods of making conjugated 4' desmethyl nucleoside analog compounds |
| US5489677A (en) | 1990-07-27 | 1996-02-06 | Isis Pharmaceuticals, Inc. | Oligonucleoside linkages containing adjacent oxygen and nitrogen atoms |
| US5602240A (en) | 1990-07-27 | 1997-02-11 | Ciba Geigy Ag. | Backbone modified oligonucleotide analogs |
| US5608046A (en) | 1990-07-27 | 1997-03-04 | Isis Pharmaceuticals, Inc. | Conjugated 4'-desmethyl nucleoside analog compounds |
| US5245022A (en) | 1990-08-03 | 1993-09-14 | Sterling Drug, Inc. | Exonuclease resistant terminally substituted oligonucleotides |
| US5512667A (en) | 1990-08-28 | 1996-04-30 | Reed; Michael W. | Trifunctional intermediates for preparing 3'-tailed oligonucleotides |
| ATE198598T1 (en) | 1990-11-08 | 2001-01-15 | Hybridon Inc | CONNECTION OF MULTIPLE REPORTER GROUPS ON SYNTHETIC OLIGONUCLEOTIDES |
| US5371241A (en) | 1991-07-19 | 1994-12-06 | Pharmacia P-L Biochemicals Inc. | Fluorescein labelled phosphoramidites |
| US5595726A (en) | 1992-01-21 | 1997-01-21 | Pharmacyclics, Inc. | Chromophore probe for detection of nucleic acid |
| US5565552A (en) | 1992-01-21 | 1996-10-15 | Pharmacyclics, Inc. | Method of expanded porphyrin-oligonucleotide conjugate synthesis |
| US5272250A (en) | 1992-07-10 | 1993-12-21 | Spielvogel Bernard F | Boronated phosphoramidate compounds |
| EP1251170A3 (en) | 1992-07-17 | 2002-10-30 | Ribozyme Pharmaceuticals, Inc. | Method and reagent for treatment of NF-kappaB dependent animal diseases |
| US5574142A (en) | 1992-12-15 | 1996-11-12 | Microprobe Corporation | Peptide linkers for improved oligonucleotide delivery |
| US6294664B1 (en) | 1993-07-29 | 2001-09-25 | Isis Pharmaceuticals, Inc. | Synthesis of oligonucleotides |
| US5597696A (en) | 1994-07-18 | 1997-01-28 | Becton Dickinson And Company | Covalent cyanine dye oligonucleotide conjugates |
| US5580731A (en) | 1994-08-25 | 1996-12-03 | Chiron Corporation | N-4 modified pyrimidine deoxynucleotides and oligonucleotide probes synthesized therewith |
| US6576752B1 (en) | 1997-02-14 | 2003-06-10 | Isis Pharmaceuticals, Inc. | Aminooxy functionalized oligomers |
| JP3756313B2 (en) | 1997-03-07 | 2006-03-15 | 武 今西 | Novel bicyclonucleosides and oligonucleotide analogues |
| US6770748B2 (en) | 1997-03-07 | 2004-08-03 | Takeshi Imanishi | Bicyclonucleoside and oligonucleotide analogue |
| US6794499B2 (en) | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| NZ503765A (en) | 1997-09-12 | 2002-04-26 | Exiqon As | Bi-cyclic and tri-cyclic nucleotide analogues |
| US6320017B1 (en) | 1997-12-23 | 2001-11-20 | Inex Pharmaceuticals Corp. | Polyamide oligomers |
| US7084125B2 (en) | 1999-03-18 | 2006-08-01 | Exiqon A/S | Xylo-LNA analogues |
| JP2002543214A (en) | 1999-05-04 | 2002-12-17 | エクシコン エ/エス | L-ribo-LNA analog |
| US6525191B1 (en) | 1999-05-11 | 2003-02-25 | Kanda S. Ramasamy | Conformationally constrained L-nucleosides |
| DE60119562T2 (en) | 2000-10-04 | 2007-05-10 | Santaris Pharma A/S | IMPROVED SYNTHESIS OF PURIN-BLOCKED NUCLEIC ACID ANALOGUE |
| AU2003290598A1 (en) | 2002-11-05 | 2004-06-03 | Isis Pharmaceuticals, Inc. | Modified oligonucleotides for use in rna interference |
| WO2004041889A2 (en) | 2002-11-05 | 2004-05-21 | Isis Pharmaceuticals, Inc. | Polycyclic sugar surrogate-containing oligomeric compounds and compositions for use in gene modulation |
| EP1661905B9 (en) | 2003-08-28 | 2012-12-19 | IMANISHI, Takeshi | Novel artificial nucleic acids of n-o bond crosslinkage type |
| CN102908630B (en) | 2006-01-27 | 2014-11-19 | Isis制药公司 | 6-modified bicyclic nucleic acid analogs |
| US7569686B1 (en) | 2006-01-27 | 2009-08-04 | Isis Pharmaceuticals, Inc. | Compounds and methods for synthesis of bicyclic nucleic acid analogs |
| US7547684B2 (en) | 2006-05-11 | 2009-06-16 | Isis Pharmaceuticals, Inc. | 5′-modified bicyclic nucleic acid analogs |
| WO2008150729A2 (en) | 2007-05-30 | 2008-12-11 | Isis Pharmaceuticals, Inc. | N-substituted-aminomethylene bridged bicyclic nucleic acid analogs |
| ES2386492T3 (en) | 2007-06-08 | 2012-08-21 | Isis Pharmaceuticals, Inc. | Carbocyclic bicyclic nucleic acid analogs |
| ATE538127T1 (en) | 2007-07-05 | 2012-01-15 | Isis Pharmaceuticals Inc | 6-DISUBSTITUTED BICYCLIC NUCLEIC ACID ANALOGUES |
| JP5635412B2 (en) | 2007-12-04 | 2014-12-03 | アルニラム ファーマスーティカルズ インコーポレイテッドAlnylam Pharmaceuticals, Inc. | Targeted lipid |
| CA3222620A1 (en) | 2008-10-20 | 2010-04-29 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of transthyretin |
| US8927513B2 (en) | 2009-07-07 | 2015-01-06 | Alnylam Pharmaceuticals, Inc. | 5′ phosphate mimics |
| WO2011005861A1 (en) | 2009-07-07 | 2011-01-13 | Alnylam Pharmaceuticals, Inc. | Oligonucleotide end caps |
| KR20180026798A (en) | 2010-04-29 | 2018-03-13 | 아이오니스 파마수티컬즈, 인코포레이티드 | Modulation of transthyretin expression |
| RU2678807C2 (en) | 2011-11-18 | 2019-02-01 | Элнилэм Фармасьютикалз, Инк. | Rnai agents, compositions and methods for use thereof for treating transthyretin (ttr) associated diseases |
| DK2991656T3 (en) | 2013-05-01 | 2020-03-23 | Ionis Pharmaceuticals Inc | COMPOSITIONS AND PROCEDURES FOR MODULATING APOLIPOPROTEIN C-III EXPRESSION |
| WO2015085158A1 (en) | 2013-12-06 | 2015-06-11 | Dicerna Pharmaceuticals, Inc. | Methods and compositions for the specific inhibition of transthyretin (ttr) by double-stranded rna |
| IL316808A (en) * | 2014-08-20 | 2025-01-01 | Alnylam Pharmaceuticals Inc | Modified double-stranded rna agents and uses thereof |
| JP6896703B2 (en) | 2015-07-31 | 2021-06-30 | アルナイラム ファーマシューティカルズ, インコーポレイテッドAlnylam Pharmaceuticals, Inc. | Transthyretin (TTR) iRNA composition for treating or preventing TTR-related diseases and how to use it |
| KR20190098181A (en) | 2016-12-16 | 2019-08-21 | 알닐람 파마슈티칼스 인코포레이티드 | How to Treat or Prevent TTR-Related Diseases Using Transthyretin (TTR) iRNA Compositions |
-
2021
- 2021-03-05 KR KR1020227034708A patent/KR20220152270A/en active Pending
- 2021-03-05 EP EP21714746.1A patent/EP4114949A1/en active Pending
- 2021-03-05 JP JP2022553196A patent/JP7802676B2/en active Active
- 2021-03-05 WO PCT/US2021/021049 patent/WO2021178778A1/en not_active Ceased
- 2021-03-05 CN CN202180030650.9A patent/CN115461460A/en active Pending
- 2021-03-05 IL IL296106A patent/IL296106A/en unknown
- 2021-03-05 AU AU2021232029A patent/AU2021232029A1/en active Pending
- 2021-03-05 CA CA3174473A patent/CA3174473A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| WO2021178778A1 (en) | 2021-09-10 |
| JP2023516748A (en) | 2023-04-20 |
| AU2021232029A1 (en) | 2022-10-06 |
| JP7802676B2 (en) | 2026-01-20 |
| IL296106A (en) | 2022-11-01 |
| EP4114949A1 (en) | 2023-01-11 |
| CN115461460A (en) | 2022-12-09 |
| CA3174473A1 (en) | 2021-09-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7802676B2 (en) | Compositions and methods for inhibiting transthyretin (TTR) expression | |
| ES2928500T3 (en) | Patisiran for use in the treatment of transthyretin-mediated amyloidosis | |
| US20260028631A1 (en) | KETOHEXOKINASE (KHK) iRNA COMPOSITIONS AND METHODS OF USE THEREOF | |
| US20210361692A1 (en) | Compositions and Methods for Treating Transthyretin (TTR) Mediated Amyloidosis | |
| JP2020502142A (en) | Method for treating or preventing a TTR-related disease using a transthyretin (TTR) iRNA composition | |
| US20240409929A1 (en) | Transthyretin (ttr) irna compositions and methods of use thereof | |
| US20240011032A1 (en) | Snca irna compositions and methods of use thereof for treating or preventing snca-associated neurodegenerative diseases | |
| AU2021232014A1 (en) | Ketohexokinase (KHK) IRNA compositions and methods of use thereof | |
| US20240309375A1 (en) | Compositions and methods for treating or preventing stargardt's disease and/or retinal binding protein 4 (rbp4)-associated disorders | |
| TW202328453A (en) | App irna compositions and methods of use thereof for treating or preventing diseases characterized by enlarged endosomes | |
| KR20220116520A (en) | Patatin-like phospholipase domain containing 3 (PNPLA3) iRNA compositions and methods of use thereof | |
| IL323871A (en) | Oligonucleotide delivery formulations | |
| US20250059541A1 (en) | Snca-targeting sirna compositions for treating snca-associated disease | |
| CN118215735A (en) | APP iRNA compositions and methods of use thereof for treating or preventing diseases characterized by enlarged endosomes | |
| NZ795574A (en) | Methods for treating or preventing TTR-associated diseases using transthyretin (TTR) iRNA compositions |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| A201 | Request for examination | ||
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| R18 | Changes to party contact information recorded |
Free format text: ST27 STATUS EVENT CODE: A-3-3-R10-R18-OTH-X000 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |