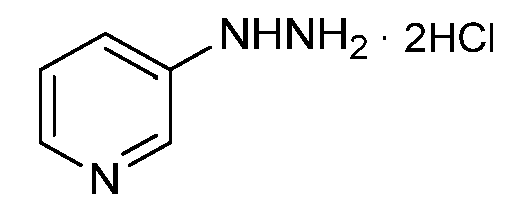KR20170042714A - 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 - Google Patents
3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 Download PDFInfo
- Publication number
- KR20170042714A KR20170042714A KR1020177007144A KR20177007144A KR20170042714A KR 20170042714 A KR20170042714 A KR 20170042714A KR 1020177007144 A KR1020177007144 A KR 1020177007144A KR 20177007144 A KR20177007144 A KR 20177007144A KR 20170042714 A KR20170042714 A KR 20170042714A
- Authority
- KR
- South Korea
- Prior art keywords
- chloro
- pyridin
- pyrazole
- carboxylate
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 238000002360 preparation method Methods 0.000 title claims description 12
- 238000000034 method Methods 0.000 title claims description 10
- JRNVHPAWUHSFAL-UHFFFAOYSA-N 3-(3-chloropyrazol-1-yl)pyridine Chemical compound N1=C(Cl)C=CN1C1=CC=CN=C1 JRNVHPAWUHSFAL-UHFFFAOYSA-N 0.000 title description 10
- -1 alkyl 3- (Pyridin-3-yl) -4,5-dihydro-1H-pyrazole-5-carboxylate Chemical compound 0.000 claims abstract description 40
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims abstract description 18
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 11
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 claims abstract description 10
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 claims abstract description 10
- QJFANABRDIUIEI-UHFFFAOYSA-N pyridin-3-ylhydrazine;dihydrochloride Chemical compound Cl.Cl.NNC1=CC=CN=C1 QJFANABRDIUIEI-UHFFFAOYSA-N 0.000 claims abstract description 9
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical group CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims description 33
- 239000003960 organic solvent Substances 0.000 claims description 12
- AFEVZFBTBLAWGB-UHFFFAOYSA-N 5-chloro-2-pyridin-3-ylpyrazole-3-carboxylic acid hydrochloride Chemical compound Cl.OC(=O)c1cc(Cl)nn1-c1cccnc1 AFEVZFBTBLAWGB-UHFFFAOYSA-N 0.000 claims description 11
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical group ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 claims description 10
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 8
- AMWRITDGCCNYAT-UHFFFAOYSA-L hydroxy(oxo)manganese;manganese Chemical group [Mn].O[Mn]=O.O[Mn]=O AMWRITDGCCNYAT-UHFFFAOYSA-L 0.000 claims description 8
- 239000012320 chlorinating reagent Substances 0.000 claims description 7
- 239000007800 oxidant agent Substances 0.000 claims description 7
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 claims description 5
- XNOUFJKTHFFXRS-UHFFFAOYSA-N 2-(3-chloropyrazol-1-yl)pyridine Chemical compound N1=C(Cl)C=CN1C1=CC=CC=N1 XNOUFJKTHFFXRS-UHFFFAOYSA-N 0.000 claims description 5
- 229910052783 alkali metal Inorganic materials 0.000 claims description 5
- 150000001340 alkali metals Chemical class 0.000 claims description 5
- 150000004703 alkoxides Chemical class 0.000 claims description 5
- IEPRKVQEAMIZSS-UHFFFAOYSA-N Di-Et ester-Fumaric acid Natural products CCOC(=O)C=CC(=O)OCC IEPRKVQEAMIZSS-UHFFFAOYSA-N 0.000 claims description 4
- IEPRKVQEAMIZSS-WAYWQWQTSA-N Diethyl maleate Chemical group CCOC(=O)\C=C/C(=O)OCC IEPRKVQEAMIZSS-WAYWQWQTSA-N 0.000 claims description 4
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical group CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 claims description 4
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical group [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 claims description 4
- 239000003880 polar aprotic solvent Substances 0.000 claims description 3
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 2
- JPVYNHNXODAKFH-UHFFFAOYSA-N Cu2+ Chemical compound [Cu+2] JPVYNHNXODAKFH-UHFFFAOYSA-N 0.000 claims description 2
- 238000012545 processing Methods 0.000 claims description 2
- 238000006114 decarboxylation reaction Methods 0.000 abstract description 6
- 150000002148 esters Chemical class 0.000 abstract description 4
- 230000007062 hydrolysis Effects 0.000 abstract description 3
- 238000006460 hydrolysis reaction Methods 0.000 abstract description 3
- 150000001735 carboxylic acids Chemical class 0.000 abstract 2
- ONSOCLDDNICHKA-UHFFFAOYSA-N 1H-pyrazole-5-carboxylic acid pyridine Chemical compound C1=CC=NC=C1.OC(=O)C=1C=CNN=1 ONSOCLDDNICHKA-UHFFFAOYSA-N 0.000 abstract 1
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 30
- 238000006243 chemical reaction Methods 0.000 description 28
- 241000196324 Embryophyta Species 0.000 description 19
- QPLDLSVMHZLSFG-UHFFFAOYSA-N Copper oxide Chemical compound [Cu]=O QPLDLSVMHZLSFG-UHFFFAOYSA-N 0.000 description 16
- 239000000203 mixture Substances 0.000 description 14
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- 150000001875 compounds Chemical class 0.000 description 9
- 239000007787 solid Substances 0.000 description 9
- BWSUFRYEIIZITF-UHFFFAOYSA-N ethyl 5-oxo-2-pyridin-3-ylpyrazolidine-3-carboxylate Chemical compound CCOC(=O)C1CC(=O)NN1c1cccnc1 BWSUFRYEIIZITF-UHFFFAOYSA-N 0.000 description 8
- 238000005481 NMR spectroscopy Methods 0.000 description 7
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 5
- 244000017020 Ipomoea batatas Species 0.000 description 5
- 235000002678 Ipomoea batatas Nutrition 0.000 description 5
- 239000002585 base Substances 0.000 description 5
- 238000003818 flash chromatography Methods 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 238000010561 standard procedure Methods 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- IJPFBRONCJOTTA-UHFFFAOYSA-N 5-chloro-1h-pyrazole Chemical compound ClC1=CC=NN1 IJPFBRONCJOTTA-UHFFFAOYSA-N 0.000 description 4
- 241001124076 Aphididae Species 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 4
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 4
- 235000013601 eggs Nutrition 0.000 description 4
- IOHOLHMGVQABTO-UHFFFAOYSA-N ethyl 5-chloro-2-pyridin-3-ylpyrazole-3-carboxylate Chemical compound CCOC(=O)c1cc(Cl)nn1-c1cccnc1 IOHOLHMGVQABTO-UHFFFAOYSA-N 0.000 description 4
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 4
- 239000011550 stock solution Substances 0.000 description 4
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 3
- LCPVQAHEFVXVKT-UHFFFAOYSA-N 2-(2,4-difluorophenoxy)pyridin-3-amine Chemical compound NC1=CC=CN=C1OC1=CC=C(F)C=C1F LCPVQAHEFVXVKT-UHFFFAOYSA-N 0.000 description 3
- 241000254123 Bemisia Species 0.000 description 3
- 240000007124 Brassica oleracea Species 0.000 description 3
- 235000003899 Brassica oleracea var acephala Nutrition 0.000 description 3
- 235000011301 Brassica oleracea var capitata Nutrition 0.000 description 3
- 235000001169 Brassica oleracea var oleracea Nutrition 0.000 description 3
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000012044 organic layer Substances 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- CHQMHPLRPQMAMX-UHFFFAOYSA-L sodium persulfate Substances [Na+].[Na+].[O-]S(=O)(=O)OOS([O-])(=O)=O CHQMHPLRPQMAMX-UHFFFAOYSA-L 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- XBDVJXXRYHXLCQ-UHFFFAOYSA-N 3-chloro-n,n-dimethylpyrazole-1-sulfonamide Chemical compound CN(C)S(=O)(=O)N1C=CC(Cl)=N1 XBDVJXXRYHXLCQ-UHFFFAOYSA-N 0.000 description 2
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- 235000011299 Brassica oleracea var botrytis Nutrition 0.000 description 2
- 240000003259 Brassica oleracea var. botrytis Species 0.000 description 2
- 235000007516 Chrysanthemum Nutrition 0.000 description 2
- 240000002024 Gossypium herbaceum Species 0.000 description 2
- 235000004341 Gossypium herbaceum Nutrition 0.000 description 2
- 235000007688 Lycopersicon esculentum Nutrition 0.000 description 2
- 241000721621 Myzus persicae Species 0.000 description 2
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 2
- 241000819999 Nymphes Species 0.000 description 2
- 229920001213 Polysorbate 20 Polymers 0.000 description 2
- 240000003768 Solanum lycopersicum Species 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 239000000908 ammonium hydroxide Substances 0.000 description 2
- 244000052616 bacterial pathogen Species 0.000 description 2
- 238000005660 chlorination reaction Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- KTPZOXXVMXIMJI-UHFFFAOYSA-N ethyl 5-chloro-2-pyridin-3-yl-3,4-dihydropyrazole-3-carboxylate Chemical compound CCOC(=O)C1CC(Cl)=NN1c1cccnc1 KTPZOXXVMXIMJI-UHFFFAOYSA-N 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 239000002917 insecticide Substances 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 230000017074 necrotic cell death Effects 0.000 description 2
- 150000002825 nitriles Chemical class 0.000 description 2
- PBDBXAQKXCXZCJ-UHFFFAOYSA-L palladium(2+);2,2,2-trifluoroacetate Chemical compound [Pd+2].[O-]C(=O)C(F)(F)F.[O-]C(=O)C(F)(F)F PBDBXAQKXCXZCJ-UHFFFAOYSA-L 0.000 description 2
- 239000000575 pesticide Substances 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 2
- 238000007363 ring formation reaction Methods 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 239000004071 soot Substances 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 1
- 0 *OC(c1cc(Cl)n[n]1-c1cnccc1)=O Chemical compound *OC(c1cc(Cl)n[n]1-c1cnccc1)=O 0.000 description 1
- OJTBJKFKQSZLFG-UHFFFAOYSA-N 1h-pyrazole-5-carboxylic acid;hydrochloride Chemical compound Cl.OC(=O)C1=CC=NN1 OJTBJKFKQSZLFG-UHFFFAOYSA-N 0.000 description 1
- NYPYPOZNGOXYSU-UHFFFAOYSA-N 3-bromopyridine Chemical compound BrC1=CC=CN=C1 NYPYPOZNGOXYSU-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 1
- 244000144730 Amygdalus persica Species 0.000 description 1
- 240000005528 Arctium lappa Species 0.000 description 1
- 235000003130 Arctium lappa Nutrition 0.000 description 1
- 235000008078 Arctium minus Nutrition 0.000 description 1
- 235000017647 Brassica oleracea var italica Nutrition 0.000 description 1
- 235000000981 Brassica parachinensis Nutrition 0.000 description 1
- 244000240551 Brassica parachinensis Species 0.000 description 1
- LVRCEUVOXCJYSV-UHFFFAOYSA-N CN(C)S(=O)=O Chemical compound CN(C)S(=O)=O LVRCEUVOXCJYSV-UHFFFAOYSA-N 0.000 description 1
- 235000002566 Capsicum Nutrition 0.000 description 1
- 240000006432 Carica papaya Species 0.000 description 1
- 235000009467 Carica papaya Nutrition 0.000 description 1
- 240000005250 Chrysanthemum indicum Species 0.000 description 1
- 244000189548 Chrysanthemum x morifolium Species 0.000 description 1
- CARFSMZWHGIXML-UHFFFAOYSA-N ClC1=NNC=C1.N1=CC=CC=C1 Chemical compound ClC1=NNC=C1.N1=CC=CC=C1 CARFSMZWHGIXML-UHFFFAOYSA-N 0.000 description 1
- 239000005751 Copper oxide Substances 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- ZAKOWWREFLAJOT-CEFNRUSXSA-N D-alpha-tocopherylacetate Chemical compound CC(=O)OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C ZAKOWWREFLAJOT-CEFNRUSXSA-N 0.000 description 1
- 244000000626 Daucus carota Species 0.000 description 1
- 235000002767 Daucus carota Nutrition 0.000 description 1
- 240000006497 Dianthus caryophyllus Species 0.000 description 1
- 235000009355 Dianthus caryophyllus Nutrition 0.000 description 1
- 240000002395 Euphorbia pulcherrima Species 0.000 description 1
- 244000299507 Gossypium hirsutum Species 0.000 description 1
- 240000008415 Lactuca sativa Species 0.000 description 1
- 235000003228 Lactuca sativa Nutrition 0.000 description 1
- 241000208467 Macadamia Species 0.000 description 1
- 235000017879 Nasturtium officinale Nutrition 0.000 description 1
- 240000005407 Nasturtium officinale Species 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 239000006002 Pepper Substances 0.000 description 1
- 235000016761 Piper aduncum Nutrition 0.000 description 1
- 240000003889 Piper guineense Species 0.000 description 1
- 235000017804 Piper guineense Nutrition 0.000 description 1
- 235000008184 Piper nigrum Nutrition 0.000 description 1
- 241000709769 Potato leafroll virus Species 0.000 description 1
- 241000723762 Potato virus Y Species 0.000 description 1
- 235000006040 Prunus persica var persica Nutrition 0.000 description 1
- 244000088415 Raphanus sativus Species 0.000 description 1
- 235000006140 Raphanus sativus var sativus Nutrition 0.000 description 1
- 241000109329 Rosa xanthina Species 0.000 description 1
- 235000004789 Rosa xanthina Nutrition 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- 241000208292 Solanaceae Species 0.000 description 1
- 244000061458 Solanum melongena Species 0.000 description 1
- 235000002597 Solanum melongena Nutrition 0.000 description 1
- 244000061456 Solanum tuberosum Species 0.000 description 1
- 235000002595 Solanum tuberosum Nutrition 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 150000004657 carbamic acid derivatives Chemical class 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 229910000431 copper oxide Inorganic materials 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 230000000911 decarboxylating effect Effects 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 244000013123 dwarf bean Species 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 239000012065 filter cake Substances 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 235000013312 flour Nutrition 0.000 description 1
- 230000012447 hatching Effects 0.000 description 1
- VHHHONWQHHHLTI-UHFFFAOYSA-N hexachloroethane Chemical compound ClC(Cl)(Cl)C(Cl)(Cl)Cl VHHHONWQHHHLTI-UHFFFAOYSA-N 0.000 description 1
- 230000000749 insecticidal effect Effects 0.000 description 1
- 230000009545 invasion Effects 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 230000001418 larval effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- RFYSRCRZAGKOIY-UHFFFAOYSA-N n,n-dimethylpyrazole-1-sulfonamide Chemical compound CN(C)S(=O)(=O)N1C=CC=N1 RFYSRCRZAGKOIY-UHFFFAOYSA-N 0.000 description 1
- JFCHSQDLLFJHOA-UHFFFAOYSA-N n,n-dimethylsulfamoyl chloride Chemical compound CN(C)S(Cl)(=O)=O JFCHSQDLLFJHOA-UHFFFAOYSA-N 0.000 description 1
- 235000012149 noodles Nutrition 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- UHZYTMXLRWXGPK-UHFFFAOYSA-N phosphorus pentachloride Chemical compound ClP(Cl)(Cl)(Cl)Cl UHZYTMXLRWXGPK-UHFFFAOYSA-N 0.000 description 1
- BZCGWAXQDLXLQM-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O.ClP(Cl)(Cl)=O BZCGWAXQDLXLQM-UHFFFAOYSA-N 0.000 description 1
- 230000029553 photosynthesis Effects 0.000 description 1
- 238000010672 photosynthesis Methods 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- VNUORQWNUXXHLX-UHFFFAOYSA-N pyrazolidine-3-carboxylic acid Chemical compound OC(=O)C1CCNN1 VNUORQWNUXXHLX-UHFFFAOYSA-N 0.000 description 1
- RCIGDGBXEMECGY-UHFFFAOYSA-N pyridin-3-ylhydrazine Chemical compound NNC1=CC=CN=C1 RCIGDGBXEMECGY-UHFFFAOYSA-N 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 230000005070 ripening Effects 0.000 description 1
- 235000015067 sauces Nutrition 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 239000012085 test solution Substances 0.000 description 1
- 210000005239 tubule Anatomy 0.000 description 1
- 244000000006 viral plant pathogen Species 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/34—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom
- A01N43/40—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom six-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/56—1,2-Diazoles; Hydrogenated 1,2-diazoles
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Plural Heterocyclic Compounds (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Agronomy & Crop Science (AREA)
- Pest Control & Pesticides (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Dentistry (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
3-히드라지노피리딘·디히드로클로라이드를 디알킬 말레에이트로 고리화하여 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트를 제공하고, 염소화하여 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트를 제공하고, 산화시켜 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트를 제공하고, 에스테르를 가수분해에 의해 카르복실산으로 전환시켜 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드를 제공하고, 카르복실산을 탈카르복실화 반응에 의해 제거함으로써 3-(3-클로로-1H-피라졸-1-일)피리딘을 제조한다.
Description
관련 출원에 대한 상호 참조
본 출원은 2014년 8월 19일에 출원된 미국 가출원 일련 번호 62/039,128을 우선권 주장하며, 이의 전체 개시내용은 이로써 명백히 본 출원에 참조로 포함된다.
기술분야
본 발명은 3-(3-클로로-1H-피라졸-1-일)피리딘을 제조하는 개선된 방법에 관한 것이다.
US 20130288893(A1)은 특히, 특정 (3-할로-1-(피리딘-3-일)-1H-피라졸-4-일)아미드 및 카르바메이트 및 살충제로서의 그의 용도를 기재하고 있다. 이러한 화합물을 제조하는 경로는 3-브로모피리딘을 3-클로로피라졸과의 직접 커플링에 의한 3-(3-클로로-1H-피라졸-1-일)피리딘의 제조를 수반하였다. 3-클로로피라졸은 a) 1H-피라졸을 2 디메틸술파모일 클로라이드 및 수소화나트륨으로 처리하여 N,N-디메틸-1H-피라졸-1-술폰아미드를 제공하고, b) N,N-디메틸-1H-피라졸-1-술폰아미드를 퍼클로로에탄 및 n-부틸 리튬으로 처리하여 3-클로로-N,N-디메틸-1H-피라졸-1-술폰아미드를 제공하고, c) 트리플루오로아세트산을 사용하여 3-클로로-N,N-디메틸-1H-피라졸-1-술폰아미드로부터 N,N-디메틸술폰아미드를 제거하여 3-클로로피라졸을 수득하는 것에 의해 제조하였다.
개시된 방법은 저수율을 초래하고, (3-클로로피라졸)을 제조하기에 어려운 출발 물질에 의존하며, 순수한 형태로 단리하기에 어려운 생성물을 제공한다. 이들 문제를 피하는 3-(3-클로로-1H-피라졸-1-일)피리딘을 제조 방법이 바람직할 것이다.
본 발명은 3-히드라지노피리딘-디히드로클로라이드를 디알킬 말레에이트로 고리화하여 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 제공하고, 염소화하여 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 제공하고, 산화시켜 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 제공하고, 에스테르를 가수분해에 의해 카르복실산으로 전환시켜 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)를 제공하고, 카르복실산을 탈카르복실화 반응에 의해 제거함으로써 이러한 대안을 제공한다. 따라서, 본 발명은 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)를 제조하는 방법이며,
a) 3-히드라지노피리딘·디히드로클로라이드를
디알킬 말레에이트로
(여기서 R은 (C1-C4) 알킬을 나타냄)
(C1-C4) 지방족 알콜 중에서 약 25℃ 내지 약 100℃의 온도에서 알칼리 금속 (C1-C4) 알콕시드의 존재 하에 처리하여 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 제공하고;
(여기서 R은 상기 정의된 바와 같음)
b) 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 염소화 시약으로 불활성 유기 용매 중에서 약 25℃ 내지 약 100℃의 온도에서 처리하여 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 제공하고;
(여기서 R은 상기 정의된 바와 같음)
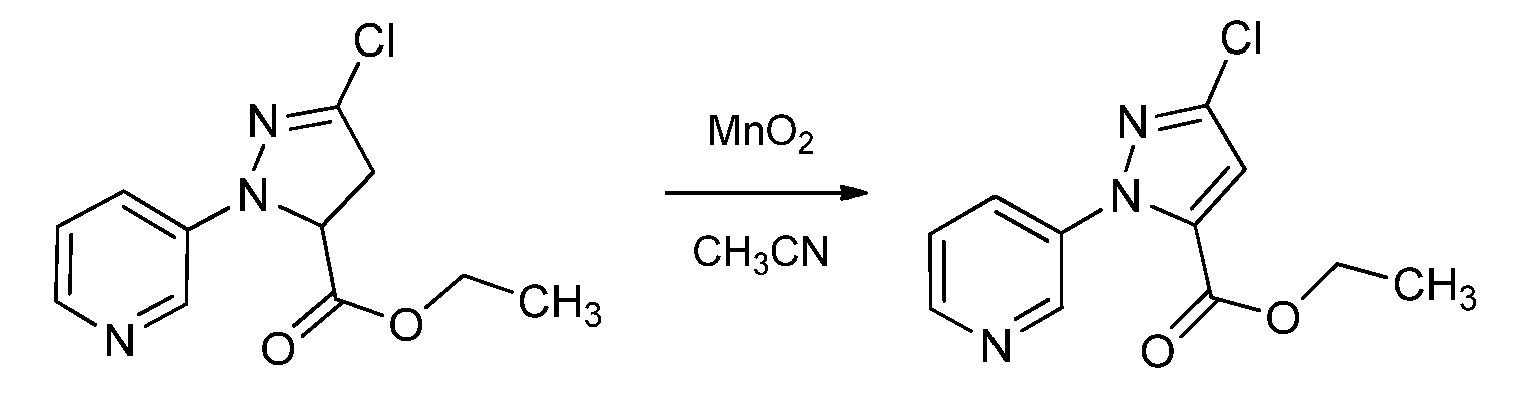
c) 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 산화제로 불활성 유기 용매 중에서 약 25℃ 내지 약 100℃의 온도에서 처리하여 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 제공하고;
(여기서 R은 상기 정의된 바와 같음)
d) 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 수성 염산으로 약 25℃ 내지 약 100℃의 온도에서 처리하여 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)를 제공하고;
e) 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드를 산화구리 (II)로 극성 비양성자성 용매 중에서 약 80℃ 내지 약 140℃의 온도에서 처리하는 것
을 포함하는, 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)를 제조하는 방법에 관한 것이다.
본 발명은 3-히드라지노피리딘·디히드로클로라이드를 디알킬 말레에이트로 고리화하여 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 제공하고, 염소화하여 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 제공하고, 산화시켜 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 제공하고, 에스테르를 가수분해에 의해 카르복실산으로 전환시켜 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)를 제공하고, 카르복실산을 탈카르복실화 반응에 의해 제거함으로써 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)를 제조하는 개선된 방법을 제공한다.
제1 단계에서, 3-히드라지노피리딘·디히드로클로라이드를 디알킬 말레에이트로 (C1-C4) 지방족 알콜 중에서 약 25℃ 내지 약 100℃의 온도에서 알칼리 금속 (C1-C4) 알콕시드의 존재 하에 처리하여 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 제공한다. 3-히드라지노피리딘·디히드로클로라이드 및 디알킬 말레에이트의 화학량론적 양이 요구되지만, 약 1.5배 내지 약 2배 과량의 디알킬 말레에이트를 사용하는 것이 종종 편리하다. 고리화는 알칼리 금속 (C1-C4) 알콕시드 염기의 존재 하에 실행한다. 약 2배 내지 약 5배 과량의 염기를 사용하는 것이 종종 편리하다. 고리화는 (C1-C4) 지방족 알콜 중에서 수행한다. 알콕시드 염기, 알콜 용매 및 말레에이트의 에스테르가 동일한 것, 예를 들어 디에틸 말레에이트와 함께 에탄올 중 소듐 에톡시드가 가장 편리하다.
바람직한 반응에서, 무수 에탄올 중에서 소듐 에톡시드를 반응 용기에 도입하고, 3-히드라지노피리딘·디히드로클로라이드를 첨가한다. 혼합물을 교반하고, 디에틸 말레에이트를 첨가한다. 혼합물을 약 60℃에서 대부분의 3-히드라지노피리딘이 반응할 때까지 가열한다. 혼합물을 냉각되도록 하고, 과량의 염기를 산으로 중화시킨다. 조 에틸 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 편리하게 표준 기술에 의해 단리하고 정제한다.
제2 단계에서, 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 염소화 시약으로 불활성 유기 용매 중에서 약 25℃ 내지 약 100℃의 온도에서 처리하여 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 제공한다. 적합한 염소화 시약은 포스포릴 클로라이드 (옥시염화인) 및 오염화인을 포함한다. 포스포릴 클로라이드가 바람직하다. 약 1.1배 내지 약 10배 과량의 염소화 시약을 사용하는 것이 종종 편리하다. 염소화는 염소화 시약에 대하여 불활성인 유기 용매 중에서 수행한다. 적합한 용매는 니트릴 예컨대 아세토니트릴을 포함한다. 염소화 시약으로서 포스포릴 클로라이드를 사용하며, 아세토니트릴이 바람직한 용매이다.
바람직한 반응에서, 에틸 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a) 및 아세토니트릴을 포스포릴 클로라이드와 혼합하고, 혼합물을 2시간 동안 약 60℃로 가열한다. 반응이 완결된 것으로 결정된 후에, 반응물을 실온으로 냉각시키고, 물로 희석한다. 이어서 반응 혼합물을 염기로 중화시키고 추출한다. 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 표준 기술에 의해 정제할 수 있다.
제3 단계에서, 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 산화제로 유기 용매 중에서 약 25℃ 내지 약 100℃의 온도에서 처리하여 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 제공한다. 적합한 산화제는 산화망가니즈 (IV) 및 과황산나트륨/황산을 포함한다. 약 1.5배 내지 약 15배 과량의 산화제를 사용하는 것이 종종 편리하다. 산화는 산화제에 대해 불활성인 유기 용매 중에서 수행한다. 적합한 용매는 니트릴 예컨대 아세토니트릴을 포함한다. 산화제로서 산화망가니즈 (IV) 또는 과황산나트륨/황산을 사용하며, 아세토니트릴이 바람직한 용매이다.
바람직한 반응에서, 에틸 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b) 및 아세토니트릴을 산화망가니즈 (IV)와 혼합하고, 혼합물을 반응이 완결될 때까지 약 60℃에서 가열한다. 에틸 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 편리하게 표준 기술에 의해 단리하고 정제한다.
제4 단계에서, 이어서 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 수성 염산 중에서 약 25℃ 내지 약 100℃의 온도에서 처리함으로써 목적하는 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)로 전환시킨다. 시약의 화학량론적 양이 요구되지만, 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)에 대하여 과량의 시약을 사용하는 것이 종종 편리하다. 따라서, 수성 염산은 반응 매질로서 매우 과량으로 사용한다.
바람직한 반응에서, 에틸 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c) 및 수성 염산의 혼합물을 혼합하고, 약 90℃로 가열한다. 반응의 완결 후에, 혼합물을 냉각시키고, 유기 용매로 희석한다. 생성된 용액을 농축시킨다. 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)를 표준 기술 예컨대 여과에 의해 정제할 수 있다.
3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)를 탈카르복실화에 의해 산화구리 (II)의 존재 하에 극성 용매 중에서 약 80℃ 내지 약 140℃의 온도에서 목적하는 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)으로 전환시킨다. 놀랍게도, 이러한 탈카르복실화가 단지 산화구리 (II)의 존재 하에서만 발생하는 것으로 밝혀졌다. 문헌 예컨대, 예를 들어, 염산 (실시예 4 참조), 황산 ("CE-5" 참조), 및 팔라듐(II) 트리플루오로아세테이트/트리플루오로아세트산 ("CE-5" 참조)으로부터의 여러 공지된 탈카르복실화제는 목적 생성물을 생성하지 않았다.
바람직한 반응에서, 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d) 및 산화구리 (II)의 혼합물을 유기 용매 중에서 혼합하고, 약 120℃로 가열한다. 화학량론적 양 미만의 산화구리 (II)를 사용하는 것이 종종 편리하다. 탈카르복실화는 극성 비양성자성 유기 용매 중에서 수행한다. 적합한 용매는 N,N'-디메틸포름아미드를 포함한다. 반응의 완결 후에, 혼합물을 냉각시키고, 수산화암모늄으로 희석, 및 추출한다. 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)를 표준 기술에 의해 정제할 수 있다.
하기 실시예는 본 발명을 예시하기 위해 제시된다.
실시예
1. 에틸 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)의 제조
4구 둥근 바닥 플라스크 (250 mL)에 소듐 에톡시드 (에탄올 중 21 중량%, 56 mL, 192 mmol)를 채웠다. 3-히드라지노피리딘·디히드로클로라이드 (10.0 g, 55.0 mmol)를 첨가하여, 20℃로부터 32℃로의 발열을 야기하였다. 반응물을 20℃로 냉각되도록 하고, 디에틸 말레에이트 (13.4 mL, 82.0 mmol)를 첨가하고, 반응물을 60℃에서 3시간 (h) 동안 가열하였다. 반응물을 20℃로 냉각시키고, 아세트산으로 켄칭하였다. 반응 혼합물을 물 (100 mL)로 희석하고, 에틸 아세테이트 (3 x 100 mL)로 추출하였다. 합한 유기물을 농축 건조시키고, 잔류물을 용리제로서 에틸 아세테이트를 사용하는 플래쉬 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 청색 오일 (6.60 g, 51%)로서 수득하였다:
1H NMR (400 MHz, DMSO-d6) δ 10.40 (s, 1H), 8.40 - 8.26 (m, 1H), 8.19 (dd, J = 4.4, 1.6 Hz, 1H), 7.47 - 7.21 (m, 2H), 4.77 (dd, J = 9.8, 2.1 Hz, 1H), 4.22 (qd, J = 7.1, 1.7 Hz, 2H), 3.05 (dd, J = 17.0, 9.8 Hz, 1H), 1.99 (s, 1H), 1.25 (t, J = 7.1 Hz, 3H); 13C NMR (101 MHz, DMSO-d6) δ 170.37, 146.60, 142.60, 137.28, 123.54, 121.94, 65.49, 61.32, 32.15, 20.72, 13.94; ESIMS m/z 236 ([M+H]+).
2. 에틸 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)의 제조
3구 둥근 바닥 플라스크 (100 mL)에 에틸 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (8.50 g, 36.1 mmol) 및 아세토니트릴 (40 mL)을 채웠다. 포스포릴 클로라이드 (4.05 mL, 43.4 mmol)를 채우고, 반응물을 60℃에서 2시간 동안 가열하였다. 반응물을 20℃로 냉각시키고, 물 (100 mL)을 첨가하였다. 탄산나트륨을 첨가하여 pH를 8로 조정하고, 혼합물을 에틸 아세테이트 (3 x 100 mL)로 추출하였다. 유기 층을 농축 건조시키고, 잔류물을 용리제로서 30-80% 에틸 아세테이트/헥산을 사용하는 플래쉬 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 황색 오일 (7.30 g, 79%)로서 수득하였다:
1H NMR (400 MHz, CDCl3) δ 8.30 (dd, J = 2.9, 0.8 Hz, 1H), 8.17 (dd, J = 4.7, 1.4 Hz, 1H), 7.38 (ddd, J = 8.4, 2.8, 1.4 Hz, 1H), 7.18 (ddd, J = 8.4, 4.7, 0.7 Hz, 1H), 4.79 (dd, J = 12.4, 6.9 Hz, 1H), 4.24 (qd, J = 7.1, 1.1 Hz, 2H), 3.55 (dd, J = 17.7, 12.4 Hz, 1H), 3.33 (dd, J = 17.8, 6.9 Hz, 1H), 1.25 (t, J = 7.1 Hz, 3H); 13C NMR (101 MHz, CDCl3) δ 169.65, 141.90, 141.33, 141.09, 135.13, 123.53, 120.37, 62.89, 62.35, 42.45, 14.03; ESIMS m/z 254 ([M+H]+).
3. 에틸 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)의 제조
3구 둥근 바닥 플라스크 (100 mL)에 에틸 3-클로로-1-(피리딘-3-일)-1H-디히드로피라졸-5-카르복실레이트 (2.00 g, 7.88 mmol) 및 아세토니트릴 (20 mL)을 채웠다. 산화망가니즈 (IV) (3.43 g, 39.4 mmol)를 첨가하였다. 반응물을 60℃에서 18시간 동안 교반하였다. 추가의 산화망가니즈 (IV) (3.43 g, 39.4 mmol)를 첨가하고, 반응물을 80℃에서 6시간 동안 교반하였다. 혼합물을 셀라이트(Celite)® 패드를 통해 여과하고, 패드를 에틸 아세테이트 (20 mL)로 헹구었다. 합한 여과액을 농축 건조시키고, 잔류물을 10-60% 에틸 아세테이트/헥산을 사용하는 플래쉬 칼럼 크로마토그래피에 의해 정제하였다. 순수한 분획을 농축 건조시켜 백색 고체 (1.84 g, 93%)를 건조 후에 수득하였다:
1H NMR (400 MHz, CDCl3) δ 8.75 - 8.64 (m, 2H), 7.79 (ddd, J = 8.2, 2.6, 1.5 Hz, 1H), 7.42 (ddd, J = 8.2, 4.8, 0.8 Hz, 1H), 6.98 (s, 1H), 4.27 (q, J = 7.1 Hz, 2H), 1.27 (t, J = 7.1 Hz, 3H); 13C NMR (101 MHz, CDCl3) δ 157.90, 149.88, 147.01, 141.41, 136.24, 135.27, 133.34, 123.11, 111.97, 61.87, 13.98; ESIMS m/z 252 ([M+H]+).
에틸 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)에 대한 대안적 합성 경로
바이알 (20 mL)에 에틸 3-클로로-1-(피리딘-3-일)-1H-디히드로피라졸-5-카르복실레이트 (0.500 g, 1.97 mmol) 및 아세토니트릴 (5 mL)을 채웠다. 과황산나트륨 (0.799 g, 2.96 mmol)에 이어서 황산 (0.733 g, 7.88 mmol)을 첨가하였다 (발열!). 반응물을 60℃에서 18시간 동안 가열하였다. 반응물을 20℃로 냉각시키고, 물 (20 mL)에 부었다. 혼합물을 탄산나트륨으로 처리하여 pH 9를 달성하고, 에틸 아세테이트 (2 x 20 mL)로 추출하였다. 유기 층을 잔류물로 농축시키고, 이를 용리제로서 50% 에틸 아세테이트/헥산을 사용하는 플래쉬 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 백색 고체 (0.280 g, 56%)로서 수득하였다.
4. 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)의 제조
3구 둥근 바닥 플라스크 (100 mL)에 에틸 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (0.200 g, 0.795 mmol) 및 염산 (37%, 4 mL)을 채웠다. 반응물을 90℃에서 18시간 동안 가열하고, 20℃로 냉각되도록 하였다. 디옥산 (5 mL)을 생성된 현탁액에 첨가하고, 농축 건조시켰다. 디옥산 (5 mL)을 첨가하고, 현탁액을 다시 농축시켜 백색 고체를 수득하였다. 디옥산 (5 mL)을 첨가하고, 생성된 현탁액을 1시간 동안 20℃에서 교반하였다. 고체를 여과하고, 고체를 디옥산 (2 mL)으로 헹구었다. 필터 케이크를 진공 하에 20℃에서 건조시켜 표제 화합물을 백색 고체 (0.218 g, 100%)로서 수득하였다:
1H NMR (400 MHz, DMSO-d 6) δ 9.05 (dd, J = 2.5, 0.7 Hz, 1H), 8.84 (dd, J = 5.3, 1.4 Hz, 1H), 8.41 (ddd, J = 8.3, 2.5, 1.4 Hz, 1H), 7.88 (ddd, J = 8.3, 5.2, 0.7 Hz, 1H), 7.26 (s, 1H); 13C NMR (101 MHz, DMSO-d 6) δ 158.71, 146.00, 143.44, 140.36, 137.76, 137.00, 136.83, 125.19, 111.71.
4. 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)의 제조
3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (1.00 g, 3.65 mmol)를 N,N'-디메틸포름아미드 (10 mL) 중에서 교반하였다. 산화구리 (II) (0.0580 mg, 0.730 mmol)를 첨가하고, 반응물을 120℃에서 16시간 동안 가열하고, 이 시점에서 반응이 ~20% 완결되었다. 추가의 산화구리 (II) (0.112 g, 1.46 mmol)를 첨가하고 반응물을 5시간 동안 교반하였다. 혼합물을 수산화암모늄 및 물로 희석하고, 에틸 아세테이트로 추출하였다. 유기 층을 염화리튬 (15%)으로 세척하고, 농축시켜 오렌지색 고체를 수득하였다. 잔류물을 용리제로서 에틸 아세테이트를 사용하는 플래쉬 칼럼 크로마토그래피에 의해 정제하고, 순수한 분획을 농축시켜 목적 생성물을 백색 고체 (0.481 g, 69.7%)로서 수득하였다; mp: 66-68℃;
1H NMR (400 MHz, CDCl3) δ 8.93 (d, J = 27 Hz, 1H), 8.57 (dd, J = 4.8, 1.4 Hz, 1H), 8.02 (ddd, J = 8.3, 2.7, 1.5 Hz, 1H), 7.91 (d, J = 2.6 Hz, 1H), 7.47-7.34 (m, 1H), 6.45 (d, J = 2.6 Hz, 1H); 13C NMR (101 MHz, CDCl3) δ 148.01, 142.72, 140.12, 135.99, 128.64, 126.41, 124.01, 108.0.
비교 실시예
실시예 CE-5 3-클로로-N-에틸-1-(피리딘-3-일)-1H-피라졸-아민 (5b):
황산을 사용한 시도된 탈카르복실화: 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (1.00 g, 2.50 mmol)를 따뜻한 술폴란 (12.5 mL) 중에 용해시켰다. 황산 (1.35 mL, 25.0 mmol)을 첨가하고, 반응 혼합물을 100℃로 가열하였다. 1시간 동안 교반한 후, LCMS는 반응이 발생하지 않은 것을 나타내었다. 반응물을 130℃에서 2시간 동안 추가로 가열하고, 이 시점에서 LCMS는 변화가 없는 것으로 나타내었다. 추가의 황산 (4 mL)을 첨가하고, 반응물을 150℃에서 2시간 동안 가열하였으며, 이 시점에서 LCMS는 목적 생성물에 해당하지 않는 새로운 주요 피크를 나타내었다.
팔라듐(II) 트리플루오로아세테이트/트리플루오로아세트산을 사용한 시도된 탈카르복실화: 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (1.00 g, 2.50 mmol)를 디메틸술폭시드 (0.625 mL) 및 N,N'-디메틸포름아미드 (11.9 mL)의 혼합물 중에 용해시켰다. 트리플루오로아세트산 (1.93 ml, 25.0 mmol)을 첨가한 후, 팔라듐(II) 트리플루오로아세테이트 (0.332 g, 1.00 mmol)를 첨가하였다. 반응물을 100℃에서 밤새 가열하고, 이 시점에서 LCMS는 반응이 발생하였으나, 목적 생성물은 형성되지 않았다는 것을 나타내었다.
생물학적 실시예
실시예 A 복숭아 혹 진딧물 (Green Peach Aphid) ("GPA") (미주스 페르시카에(Myzus persicae) (MYZUPE.)에 대한 생물학적 검정
GPA는 복숭아 나무의 가장 유의한 진딧물 해충이어서 감소된 성장, 잎의 시듦 및 다양한 조직의 괴사를 야기한다. 또한, 식물 바이러스, 예컨대 감자 바이러스 Y 및 감자 잎말림병 바이러스의 가지과/감자 과 솔라나세아에(Solanaceae)의 구성원으로의 수송 및 다양한 모자이크 바이러스의 다수의 다른 식용 작물로의 수송에 대한 벡터로서 작용하므로 유해하다. GPA는 다른 식물 중에서도 브로콜리, 우엉, 양배추, 당근, 콜리플라워, 무, 가지, 그린 빈, 상추, 마카다미아, 파파야, 페퍼, 고구마, 토마토, 물냉이 및 쥬키니와 같은 식물을 공격한다. GPA는 또한 다수의 관상 작물, 예컨대 카네이션, 국화, 꽃 흰양배추, 포인세티아 및 장미를 공격한다. GPA는 다수의 살충제에 대한 저항성이 발달되어 왔다.
본원에 개시된 여러 분자는 하기 기재된 절차를 사용하여 GPA에 대하여 시험하였다.
2-3개의 작은 (3-5 cm) 본엽을 갖는 3-인치 포트에서 성장한 양배추 묘목을 시험 기질로서 사용하였다. 화학물질 적용 1일 이전에 묘목에 20-5-GPA (날개 없는 성체 및 유충 단계)를 침입시켰다. 각 처리에 대해 개별 묘목을 갖는 4개의 화분을 사용하였다. 시험 화합물 (2 mg)을 2 mL의 아세톤/MeOH (1:1) 용매 중에 용해시켜 1000 ppm 시험 화합물의 원액을 형성하였다. 원액을 물 중 0.025% 트윈(Tween) 20으로 5X 희석하여 200 ppm 시험 화합물의 용액을 수득하였다. 핸드-헬드 흡인기 타입의 분무기를 사용하여 용액을 양배추 잎의 양면에 흘러넘칠 때까지 분무하였다. 대조 식물 (용매 체크)에 20 부피% 아세톤/MeOH (1:1) 용매만을 함유하는 희석제를 분무하였다. 처리한 식물을 등급화 전에 3일 동안 대략 25℃ 및 주위 상대 습도 (RH)에서 홀딩 룸에 두었다. 식물당 살아있는 진딧물의 수를 현미경 하에 계수함으로써 평가를 수행하였다. 하기와 같은 애보트 보정식 (W.S. Abbott, "A Method of Computing the Effectiveness of an Insecticide" J. Econ. Entomol 18 (1925), pp.265-267)을 사용하여 퍼센트 방제를 측정하였다.
보정된 % 방제율 = 100*(X-Y)/X
여기서
X = 용매 체크 식물 상의 살아있는 진딧물의 수 및
Y = 처리된 식물 상에 살아있는 진딧물의 수
결과는 하기 "표 1: GPA (MYZUPE) 및 고구마 가루이-약충 (BEMITA) 등급 표"라는 명칭의 표에 제시한다.
실시예 B 고구마 가루이 약충 (베미시아 타바시(Bemisia tabaci)) (BEMITA.)에 대한 생물검정
고구마 가루이, 베미시아 타바시 (겐나디우스(Gennadius))는 1800년대 후반 이래로 미국에서 기록되어 있다. 1986년 플로리다에서, 베미시아 타바시는 매우 경제적인 해충이 되었다. 가루이는 일반적으로 그의 숙주 식물의 잎의 하부면에서 먹고 산다. 알로부터, 현미경으로 보이는 가늘고 긴 구기를 꽂아서 수액을 체관부로부터 빨아 먹을 때까지 잎의 주위에서 움직이는 극히 작은 약충 단계로 부화된다. 성체 및 유충은 짙은 그을음병균이 자라는 끈적이는 점성 액체인 단물 (대개는 체관부에서의 먹이로부터의 식물당)을 분비한다. 성체 및 그의 자손이 심각한 침입은 간단히 수액 제거로 인하여 묘목 괴사 또는 더 큰 식물의 활력 및 수확량의 감소를 야기할 수 있다. 단물은 생면이 함께 붙게 하여 조면을 더 곤란하게 하여 그의 가치를 떨어뜨릴 수 있다. 그을음병균은 단물이 덮힌 기질 위에서 자라며, 잎을 우중충하게 하며, 광합성을 감소시키며, 과실의 품질 등급을 떨어뜨린다. 이는 중경 작물에 영향을 미치지 않았으며, 식물 생리적 질병, 예컨대 토마토의 불규칙한 숙성 및 은빛잎 질병을 유발하는 식물-병원성 바이러스를 전염시켰다. 가루이는 다수의 종래에 효과적인 살충제에 대하여 내성을 갖는다.
1개의 작은 (3-5 cm) 본엽을 갖는 3-인치 포트에서 성장한 목화 식물을 시험 기질로서 사용하였다. 식물을 가루이 성체가 있는 룸에 두었다. 성체가 2-3 일 동안 알을 낳게 하였다. 2-3 일 산란기 후, 식물을 성체 가루이 방으로부터 꺼내었다. 핸드-헬드 드빌블리스(Devilbliss) 분무기 (23 psi)를 사용하여 성체를 잎으로부터 날려보냈다. 알 침입 식물 (식물당 100-300개의 알)을 알 부화 및 약충 단계로 성장하게 하기 위하여 82℉ 및 50% RH에서 5-6 일 동안 홀딩 룸에 두었다. 4개의 목화 식물을 각각의 처리에 사용하였다. 화합물 (2 mg)을 1 mL의 아세톤 용매 중에 용해시켜 2,000 ppm의 원액을 형성하였다. 원액을 물 중의 0.025% 트윈 20으로 10X 희석하여 200 ppm에서의 시험 용액을 수득하였다. 핸드-헬드 드빌블리스 분무기를 사용하여 용액을 목화 잎의 양면에 흘러넘칠 때까지 분무하였다. 참조 식물 (용매 체크)은 희석제로만 분무하였다. 등급을 매기기 이전에, 처리한 식물을 8-9 일 동안 대략 82℉ 및 50% RH에서의 홀딩 룸에 두었다. 현미경 아래에서 식물 1개당 살아있는 유충의 수를 계수함으로써 평가를 수행하였다. 살충 활성은 애보트 보정식 (상기 참조)을 사용하여 측정하고, 하기 표 1에 제시하였다.
표 1: GPA (MYZUPE) 및 고구마 가루이-약충 (BEMITA) 등급 표
표 2
Claims (7)
- 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)를 제조하는 방법이며,
a) 3-히드라지노피리딘·디히드로클로라이드를
디알킬 말레에이트로
(여기서 R은 (C1-C4) 알킬을 나타냄)
(C1-C4) 지방족 알콜 중에서 약 25℃ 내지 약 100℃의 온도에서 알칼리 금속 (C1-C4) 알콕시드의 존재 하에 처리하여 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 제공하고;
(여기서 R은 상기 정의된 바와 같음)
b) 알킬 5-옥소-2-(피리딘-3-일)피라졸리딘-3-카르복실레이트 (10a)를 염소화 시약으로 불활성 유기 용매 중에서 약 25℃ 내지 약 100℃의 온도에서 처리하여 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 제공하고;
(여기서 R은 상기 정의된 바와 같음)
c) 알킬 3-클로로-1-(피리딘-3-일)-4,5-디히드로-1H-피라졸-5-카르복실레이트 (10b)를 산화제로 불활성 유기 용매 중에서 약 25℃ 내지 약 100℃의 온도에서 처리하여 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 제공하고;
(여기서 R은 상기 정의된 바와 같음)
d) 알킬 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실레이트 (10c)를 수성 염산으로 약 25℃ 내지 약 100℃의 온도에서 처리하여 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드 (10d)를 제공하고;
e) 3-클로로-1-(피리딘-3-일)-1H-피라졸-5-카르복실산 히드로클로라이드를 산화구리 (II)로 극성 비양성자성 용매 중에서 약 80℃ 내지 약 140℃의 온도에서 처리하는 것
을 포함하는, 3-(3-클로로-1H-피라졸-1-일)피리딘 (5b)를 제조하는 방법. - 제1항에 있어서, 단계 a)의 경우에 디알킬 말레에이트가 디에틸 말레에이트이고, (C1-C4) 지방족 알콜이 에탄올이고, 알칼리 금속 (C1-C4) 알콕시드가 소듐 에톡시드인 방법.
- 제1항에 있어서, 단계 b)의 경우에 염소화 시약이 포스포릴 클로라이드이고, 불활성 유기 용매가 아세토니트릴인 방법.
- 제1항에 있어서, 단계 c)의 경우에 산화제가 산화망가니즈 (IV)이고, 불활성 유기 용매가 아세토니트릴인 방법.
- 제1항에 있어서, 단계 e)의 경우에 극성 비양성자성 용매가 N,N'-디메틸포름아미드인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462039128P | 2014-08-19 | 2014-08-19 | |
| US62/039,128 | 2014-08-19 | ||
| PCT/US2014/061005 WO2016028328A1 (en) | 2014-08-19 | 2014-10-17 | Process for the preparation of 3-(3-chloro-1h-pyrazol-1-yl)pyridine |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170042714A true KR20170042714A (ko) | 2017-04-19 |
Family
ID=53001656
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177007144A Withdrawn KR20170042714A (ko) | 2014-08-19 | 2014-10-17 | 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 |
Country Status (11)
| Country | Link |
|---|---|
| US (6) | US9024031B1 (ko) |
| EP (1) | EP3183238A4 (ko) |
| JP (1) | JP2017525703A (ko) |
| KR (1) | KR20170042714A (ko) |
| CN (1) | CN107074774A (ko) |
| AR (1) | AR098112A1 (ko) |
| BR (1) | BR112017002735A2 (ko) |
| CA (1) | CA2958058A1 (ko) |
| IL (1) | IL250628A0 (ko) |
| TW (1) | TW201613894A (ko) |
| WO (1) | WO2016028328A1 (ko) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105636445B (zh) | 2013-10-17 | 2018-12-07 | 美国陶氏益农公司 | 制备杀虫化合物的方法 |
| EP3057426A4 (en) | 2013-10-17 | 2017-03-29 | Dow AgroSciences LLC | Processes for the preparation of pesticidal compounds |
| JP2016535010A (ja) | 2013-10-17 | 2016-11-10 | ダウ アグロサイエンシィズ エルエルシー | 有害生物防除性化合物の製造方法 |
| WO2015058021A1 (en) | 2013-10-17 | 2015-04-23 | Dow Agrosciences Llc | Processes for the preparation of pesticidal compounds |
| MX2016004940A (es) | 2013-10-17 | 2016-06-28 | Dow Agrosciences Llc | Proceso para la preparacion de compuestos plaguicidas. |
| CA2925595A1 (en) | 2013-10-17 | 2015-04-23 | Dow Agrosciences Llc | Processes for the preparation of pesticidal compounds |
| CA2925952A1 (en) | 2013-10-17 | 2015-04-23 | Dow Agrosciences Llc | Processes for the preparation of pesticidal compounds |
| KR20170039121A (ko) | 2014-07-31 | 2017-04-10 | 다우 아그로사이언시즈 엘엘씨 | 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 |
| JP2017523168A (ja) | 2014-07-31 | 2017-08-17 | ダウ アグロサイエンシィズ エルエルシー | 3−(3−クロロ−1h−ピラゾール−1−イル)ピリジンの製造方法 |
| CN106488909A (zh) | 2014-07-31 | 2017-03-08 | 美国陶氏益农公司 | 制备3‑(3‑氯‑1h‑吡唑‑1‑基)吡啶的方法 |
| KR20170042714A (ko) | 2014-08-19 | 2017-04-19 | 다우 아그로사이언시즈 엘엘씨 | 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 |
| JP2017528469A (ja) | 2014-09-12 | 2017-09-28 | ダウ アグロサイエンシィズ エルエルシー | 3−(3−クロロ−1h−ピラゾール−1−イル)ピリジンの調製方法 |
| BR112019008372B1 (pt) | 2016-12-29 | 2021-11-09 | Dow Agrosciences Llc | Processo para preparação de compostos pesticidas |
| WO2018125817A1 (en) | 2016-12-29 | 2018-07-05 | Dow Agrosciences Llc | Processes for the preparation of pesticidal compounds |
| TWI849253B (zh) * | 2019-11-11 | 2024-07-21 | 美商富曼西公司 | 用於製備3-溴-1- (3-氯吡啶-2-基) -1h-吡唑-5-羧酸乙酯的方法 |
| CN114163438A (zh) * | 2021-12-13 | 2022-03-11 | 无锡捷化医药科技有限公司 | 一种2-甲基-3-羰基吡唑并[4,3-c]吡啶-7-羧酸盐酸盐的制备方法 |
Family Cites Families (176)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3597341A (en) | 1968-09-11 | 1971-08-03 | Exxon Research Engineering Co | Selective addition of thiols to allylic isocyanates and isothiocyanates |
| CA962269A (en) | 1971-05-05 | 1975-02-04 | Robert E. Grahame (Jr.) | Thiazoles, and their use as insecticides |
| US4556671A (en) | 1979-07-13 | 1985-12-03 | Burroughs Wellcome Co. | Pharmaceutical formulations |
| US4347251A (en) | 1981-07-13 | 1982-08-31 | American Cyanamid Company | Novel 3-substituted amino-1-substituted heteroaryl-2-pyrazolines |
| US4407803A (en) | 1981-08-17 | 1983-10-04 | Abbott Laboratories | Antiinflammatory 1-(quinolinyl)-2-pyrazoline derivatives |
| FR2517176A1 (fr) | 1981-12-01 | 1983-06-03 | Rhone Poulenc Agrochimie | Association insecticide et acaricide a base de pyrethroide |
| US4528291A (en) | 1982-06-22 | 1985-07-09 | Schering Corporation | 2-(4'-Pyridinyl)-thiazole compounds and their use in increasing cardiac contractility |
| US4824953A (en) | 1983-11-15 | 1989-04-25 | Riker Laboratories, Inc. | Multi-step process for producing 5-hydroxy-N-(6-oxo-piperidyl-methyl)-2-(2,2,2-trifluoro-ethoxy)-benzamide and derivatives |
| EP0178035B1 (en) | 1984-05-12 | 1990-01-03 | FISONS plc | Anti-inflammatory 1,n-diarylpyrazol-3-amines, compositions containing them and processes for their preparation |
| IT1183181B (it) | 1985-02-07 | 1987-10-05 | Corvi Camillo Spa | Derivati del 3-metil-imidazo(4,5-c)pirazolo con attivita' terapeutica e procedimento per la loropreparazione |
| DE3520328A1 (de) | 1985-06-07 | 1986-12-11 | Bayer Ag, 5090 Leverkusen | 5-amino-4-heterocyclyl-1-pyridyl-pyrazole |
| GB8625897D0 (en) | 1986-10-29 | 1986-12-03 | Ici Plc | Insecticidal thioethers derivatives |
| JPS62153273A (ja) | 1985-12-26 | 1987-07-08 | Tokuyama Soda Co Ltd | ピラゾ−ル化合物 |
| DE3600950A1 (de) | 1986-01-15 | 1987-07-16 | Bayer Ag | 5-acylamido-1-aryl-pyrazole |
| JPS62153273U (ko) | 1986-03-19 | 1987-09-29 | ||
| DE3618717A1 (de) | 1986-06-04 | 1987-12-10 | Bayer Ag | 5- acylamino-pyrazol-derivate |
| JPH07106964B2 (ja) | 1987-01-14 | 1995-11-15 | 株式会社トクヤマ | 摘果剤 |
| DE3936622A1 (de) | 1989-11-03 | 1991-05-08 | Bayer Ag | Halogenierte sulfonylaminocarbonyltriazolinone |
| US5599944A (en) | 1987-03-24 | 1997-02-04 | Bayer Aktiengesellschaft | Intermediates for herbicidal sulphonylaminocarbonyltriazolinones having substituents which are bonded via sulphur |
| JPS63174905U (ko) | 1987-04-23 | 1988-11-14 | ||
| JPH089541B2 (ja) | 1988-03-07 | 1996-01-31 | 三井東圧化学株式会社 | ピラゾール類を主成分とする脳浮腫抑制剤 |
| US5300480A (en) | 1989-04-13 | 1994-04-05 | Bayer Aktiengesellschaft | Herbicidal sulphonylaminocarbonyltriazolinones having two substituents bonded via oxygen |
| US5541337A (en) | 1989-04-13 | 1996-07-30 | Bayer Aktiengesellschaft | Substituted 5-alkoxy-1,2,4-triazol-3-(thi)ones |
| US5241074A (en) | 1988-05-09 | 1993-08-31 | Bayer Aktiengesellschaft | Sulphonylaminocarbonyltriazolinones |
| US5220028A (en) | 1988-10-27 | 1993-06-15 | Nissan Chemical Industries, Ltd. | Halogeno-4-methylpyrazoles |
| US5534486A (en) | 1991-04-04 | 1996-07-09 | Bayer Aktiengesellschaft | Herbicidal sulphonylaminocarbonyl triazolinones having substituents bonded via oxygen |
| US5366987A (en) | 1991-08-22 | 1994-11-22 | Warner-Lambert Company | Isoxazolyl-substituted alkyl amide ACAT inhibitors |
| TW336932B (en) | 1992-12-17 | 1998-07-21 | Pfizer | Amino-substituted pyrazoles |
| JP3726306B2 (ja) | 1994-04-27 | 2005-12-14 | 日産化学工業株式会社 | ピラゾールカルボン酸誘導体および植物病害防除剤 |
| EP0858457A1 (de) | 1995-10-20 | 1998-08-19 | Dr. Karl Thomae GmbH | 5-gliedrige heterocyclen, diese verbindungen enthaltende arzneimittel und deren verwendung sowie verfahren zu ihrer herstellung |
| US5854265A (en) | 1996-04-03 | 1998-12-29 | Merck & Co., Inc. | Biheteroaryl inhibitors of farnesyl-protein transferase |
| JP2000507592A (ja) | 1996-04-03 | 2000-06-20 | メルク エンド カンパニー インコーポレーテッド | ファルネシル―タンパク質トランスフェラーゼ阻害剤 |
| TW430660B (en) | 1996-05-30 | 2001-04-21 | Mochida Pharm Co Ltd | Novel benzindole derivatives for neuron cell protection, processes for production, and the pharmaceutical compounds containing them |
| US5854264A (en) | 1996-07-24 | 1998-12-29 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| KR100390612B1 (ko) | 1997-04-25 | 2003-07-07 | 화이자 인코포레이티드 | 타입 5 시클릭 구아노신 3',5'-모노포스페이트포스포디에스테라제를 억제하는 성기능 장애 치료용피라졸로피리미디논 제조용 중간체의 제조 방법 |
| DE19725450A1 (de) | 1997-06-16 | 1998-12-17 | Hoechst Schering Agrevo Gmbh | 4-Haloalkyl-3-heterocyclylpyridine und 4-Haloalkyl-5-heterocyclylpyrimidine, Verfahren zu ihrer Herstellung, sie enthaltende Mittel und ihre Verwendung als Schädlingsbekämpfungsmittel |
| US6271237B1 (en) | 1997-12-22 | 2001-08-07 | Dupont Pharmaceuticals Company | Nitrogen containing heteromatics with ortho-substituted P1s as factor Xa inhabitors |
| US6506747B1 (en) | 1998-06-05 | 2003-01-14 | Boehringer Ingelheim Pharmaceuticals, Inc. | Substituted 1-(4-aminophenyl)pyrazoles and their use as anti-inflammatory agents |
| GB9827882D0 (en) | 1998-12-17 | 1999-02-10 | Smithkline Beecham Plc | Novel compounds |
| FR2789076B1 (fr) | 1999-02-02 | 2001-03-02 | Synthelabo | Derives de alpha-azacyclomethyl quinoleine, leur preparation et leur application en therapeutique |
| FR2789387B1 (fr) | 1999-02-04 | 2001-09-14 | Aventis Cropscience Sa | Nouveau procede de preparation d'intermediaires pesticides |
| EE200200065A (et) | 1999-08-12 | 2003-04-15 | Pharmacia Italia S.P.A. | 3-aminopürasooli derivaadid, nende valmistamine ja kasutamine vähivastaste toimeainetena ning neid sisaldav farmatseutiline kompositsioon |
| CA2382676A1 (en) | 1999-11-05 | 2001-05-17 | Warner-Lambert Company | Prevention of plaque rupture by acat inhibitors |
| KR100724676B1 (ko) | 2000-02-16 | 2007-06-07 | 이시하라 산교 가부시끼가이샤 | 페나실아민 유도체, 이들의 제조 방법 및 이들을 함유하는유해 생물 방제제 |
| GB0011095D0 (en) | 2000-05-08 | 2000-06-28 | Black James Foundation | astrin and cholecystokinin receptor ligands (III) |
| US6645990B2 (en) | 2000-08-15 | 2003-11-11 | Amgen Inc. | Thiazolyl urea compounds and methods of uses |
| AU2001280099A1 (en) | 2000-08-25 | 2002-04-02 | Sankyo Company Limited | 4-acylaminopyrazole derivatives |
| KR20030030029A (ko) | 2000-09-22 | 2003-04-16 | 니혼노야쿠가부시키가이샤 | N-(4-피라졸릴)아미드 유도체 및 농원예용 약제 그리고그 사용방법 |
| US20020134012A1 (en) | 2001-03-21 | 2002-09-26 | Monsanto Technology, L.L.C. | Method of controlling the release of agricultural active ingredients from treated plant seeds |
| KR100863659B1 (ko) | 2001-04-16 | 2008-10-15 | 미쓰비시 타나베 파마 코퍼레이션 | 질소-함유 헤테로시클릭 화합물 및 이를 포함하는 제약 조성물 |
| EP1256578B1 (en) | 2001-05-11 | 2006-01-11 | Pfizer Products Inc. | Thiazole derivatives and their use as cdk inhibitors |
| ATE298749T1 (de) | 2001-07-05 | 2005-07-15 | Pfizer Prod Inc | Heterocyclo-alkylsulfonyl pyrazole als entzündungshemmende/analgetische mittel |
| FR2827603B1 (fr) | 2001-07-18 | 2003-10-17 | Oreal | Composes derives de diaminopyrazole substitues par un radical heteroaromatique et leur utilisation en teinture d'oxydation des fibres keratiniques |
| TWI327566B (en) | 2001-08-13 | 2010-07-21 | Du Pont | Novel substituted ihydro 3-halo-1h-pyrazole-5-carboxylates,their preparation and use |
| GB0123589D0 (en) | 2001-10-01 | 2001-11-21 | Syngenta Participations Ag | Organic compounds |
| CN100532363C (zh) | 2001-12-20 | 2009-08-26 | 株式会社Sds生技 | 取代的吡唑衍生物及其制备方法以及含该衍生物的除草剂组合物 |
| US6936629B2 (en) | 2001-12-21 | 2005-08-30 | Virochem Pharma Inc. | Compounds and methods for the treatment or prevention of flavivirus infections |
| US6878196B2 (en) | 2002-01-15 | 2005-04-12 | Fuji Photo Film Co., Ltd. | Ink, ink jet recording method and azo compound |
| JP2003212864A (ja) | 2002-01-24 | 2003-07-30 | Sankyo Co Ltd | 5−(m−シアノベンジルアミノ)チアゾール誘導体 |
| DE60324898D1 (de) | 2002-02-25 | 2009-01-08 | Lilly Co Eli | Modulatoren von peroxisome proliferator-aktivierten rezeptoren |
| JP2004051628A (ja) | 2002-05-28 | 2004-02-19 | Ishihara Sangyo Kaisha Ltd | ピリジン系化合物又はその塩、それらの製造方法及びそれらを含有する除草剤 |
| AU2003254053A1 (en) * | 2002-07-23 | 2004-02-09 | Smithkline Beecham Corporation | Pyrazolopyrimidines as protein kinase inhibitors |
| MXPA05003337A (es) * | 2002-10-04 | 2005-07-05 | Du Pont | Insecticidas de antranilamida. |
| US6737382B1 (en) | 2002-10-23 | 2004-05-18 | Nippon Soda Co. Ltd. | Insecticidal aminothiazole derivatives |
| AU2003288956A1 (en) | 2002-10-30 | 2004-06-07 | Vertex Pharmaceuticals Incorporated | Compositions useful as inhibitors of rock and other protein kinases |
| EA011505B1 (ru) | 2002-12-03 | 2009-04-28 | Мириэл Лимитид | Пестициды на основе производных 5-(ациламино)пиразола |
| US7429581B2 (en) | 2002-12-23 | 2008-09-30 | Sanofi-Aventis Deutschland Gmbh | Pyrazole-derivatives as factor Xa inhibitors |
| JP4397615B2 (ja) | 2003-03-27 | 2010-01-13 | 富士フイルム株式会社 | インクジェット用インクおよびインクセット |
| GB0312654D0 (en) | 2003-06-03 | 2003-07-09 | Glaxo Group Ltd | Therapeutically useful compounds |
| EP1671937A4 (en) | 2003-09-19 | 2007-08-08 | Ube Industries | METHOD FOR PRODUCING A NITRILE COMPOUND, CARBOXYLIC COMPOUND OR CARBOXYLATE COMPOUND |
| CN100432038C (zh) * | 2003-09-19 | 2008-11-12 | 宇部兴产株式会社 | 腈化合物、羧酸化合物或羧酸酯化合物的制备方法 |
| US7514464B2 (en) | 2003-12-18 | 2009-04-07 | Pfizer Limited | Substituted arylpyrazoles |
| US7319108B2 (en) | 2004-01-25 | 2008-01-15 | Sanofi-Aventis Deutschland Gmbh | Aryl-substituted heterocycles, process for their preparation and their use as medicaments |
| DE102004003812A1 (de) | 2004-01-25 | 2005-08-11 | Aventis Pharma Deutschland Gmbh | Arylsubstituierte Heterozyklen, Verfahren ihrer Herstellung und ihre Verwendung als Arzneimittel |
| US7297168B2 (en) | 2004-02-02 | 2007-11-20 | The Procter & Gamble Company | Keratin dyeing compounds, keratin dyeing compositions containing them, and use thereof |
| CA2560510C (en) | 2004-03-18 | 2009-10-13 | Pfizer Inc. | N-(1-arylpyrazol-4yl) sulfonamides and their use as parasiticides |
| US20070167426A1 (en) | 2004-06-02 | 2007-07-19 | Schering Corporation | Compounds for the treatment of inflammatory disorders and microbial diseases |
| GT200500179AA (es) | 2004-07-01 | 2008-10-29 | Mezclas sinergistas de agentes de antranilamida para el control de plagas de invertebrados | |
| EP1784400B1 (en) | 2004-08-23 | 2015-01-14 | Eli Lilly And Company | Histamine h3 receptor agents, preparation and therapeutic uses |
| MX2007003377A (es) | 2004-09-23 | 2007-05-10 | Pfizer Prod Inc | Agonistas del receptor de trombopoyetina. |
| RU2007115900A (ru) | 2004-10-27 | 2008-11-10 | Дайити Санкио Компани, Лимитед (Jp) | Производные бензола, имеющие 2 или более заместителей |
| JP5197016B2 (ja) | 2004-12-23 | 2013-05-15 | デシファラ ファーマスーティカルズ, エルエルシー | 酵素モジュレータ及び治療 |
| CA2593439C (en) | 2005-01-14 | 2014-02-25 | F. Hoffmann-La Roche Ag | Thiazole-4-carboxamide derivatives as mglur5 antagonists |
| CA2602336A1 (en) | 2005-03-31 | 2006-10-05 | Ucb Pharma S.A. | Compounds comprising an oxazole or thiazole moiety, processes for making them, and their uses |
| CN101228134A (zh) | 2005-06-15 | 2008-07-23 | 辉瑞有限公司 | 用作杀寄生虫剂的取代芳基吡唑 |
| US7608592B2 (en) | 2005-06-30 | 2009-10-27 | Virobay, Inc. | HCV inhibitors |
| KR100654328B1 (ko) | 2005-08-26 | 2006-12-08 | 한국과학기술연구원 | 피페라지닐알킬피라졸계 t-타입 칼슘 채널 억제 화합물 및이의 제조방법 |
| CA2637530A1 (en) | 2006-01-18 | 2007-09-07 | Siena Biotech S.P.A. | Modulators of alpha7 nicotinic acetylcholine receptors and therapeutic uses thereof |
| WO2007087427A2 (en) | 2006-01-25 | 2007-08-02 | Synta Pharmaceuticals Corp. | Thiazole and thiadiazole compounds for inflammation and immune-related uses |
| EP2038272B8 (en) | 2006-06-30 | 2013-10-23 | Sunesis Pharmaceuticals, Inc. | Pyridinonyl pdk1 inhibitors |
| US20090325956A1 (en) | 2006-10-13 | 2009-12-31 | Takahiko Taniguchi | Aromatic amine derivative and use thereof |
| JO2754B1 (en) | 2006-12-21 | 2014-03-15 | استرازينكا ايه بي | Amylendazoleil derivatives for the treatment of glucocorticoid-mediated disorders |
| US7795249B2 (en) | 2006-12-22 | 2010-09-14 | Millennium Pharmaceuticals, Inc. | Certain pyrazoline derivatives with kinase inhibitory activity |
| GB0701426D0 (en) | 2007-01-25 | 2007-03-07 | Univ Sheffield | Compounds and their use |
| US20090069288A1 (en) | 2007-07-16 | 2009-03-12 | Breinlinger Eric C | Novel therapeutic compounds |
| CA2692713A1 (en) | 2007-07-17 | 2009-01-22 | Amgen Inc. | Heterocyclic modulators of pkb |
| ES2423181T3 (es) | 2007-07-17 | 2013-09-18 | F. Hoffmann-La Roche Ag | Inhibidores de la 11ß-hidroxiesteroide-deshidrogenasa |
| US8293919B2 (en) | 2007-07-23 | 2012-10-23 | Crestone, Inc. | Antibacterial sulfone and sulfoxide substituted heterocyclic urea compounds |
| JP2011502133A (ja) | 2007-11-02 | 2011-01-20 | メシルジーン インコーポレイテッド | ヒストンデアセチラーゼの阻害剤 |
| WO2009076454A2 (en) | 2007-12-12 | 2009-06-18 | Calcimedica, Inc. | Compounds that modulate intracellular calcium |
| MX2010008880A (es) | 2008-02-12 | 2010-09-24 | Dow Agrosciences Llc | Composiciones pesticidas. |
| CN101945905B (zh) | 2008-02-15 | 2013-06-26 | 旭化成电子材料株式会社 | 树脂组合物 |
| WO2010011375A2 (en) | 2008-04-21 | 2010-01-28 | Merck & Co., Inc. | Inhibitors of janus kinases |
| EP2725021A1 (de) | 2008-06-13 | 2014-04-30 | Bayer CropScience AG | Neue heteroaromatische Thioamide als Schädlingsbekämpfungsmittel |
| TW201004941A (en) | 2008-07-16 | 2010-02-01 | Wyeth Corp | Alpha7 nicotinic acetylcholine receptor inhibitors |
| EP2309857B1 (de) | 2008-07-17 | 2013-07-03 | Bayer CropScience AG | Heterocyclische verbindungen als schädlingsbekämpfungsmittel |
| JP2010030970A (ja) | 2008-07-31 | 2010-02-12 | Bayer Cropscience Ag | 殺虫性ベンゼンジカルボキサミド誘導体 |
| WO2010032874A1 (ja) | 2008-09-19 | 2010-03-25 | 住友化学株式会社 | 農業用組成物 |
| CA2737437A1 (en) | 2008-09-19 | 2010-03-25 | Absolute Science, Inc. | Methods of treating a botulinum toxin related condition in a subject |
| GB0817617D0 (en) | 2008-09-25 | 2008-11-05 | Ricardo Uk Ltd | Bearing for wind turbine |
| MX2011004125A (es) | 2008-10-21 | 2011-05-19 | Metabolex Inc | Agonistas del receptor gpr120 de arilo y usos de los mismos. |
| CN101747276B (zh) | 2008-11-28 | 2011-09-07 | 中国中化股份有限公司 | 具有含氮五元杂环的醚类化合物及其应用 |
| RU2505540C2 (ru) | 2008-12-23 | 2014-01-27 | Эббви Инк. | Антивирусные соединения |
| CA2750529C (en) | 2009-02-11 | 2016-10-11 | Dow Agrosciences Llc | Pesticidal compositions |
| US8785468B2 (en) | 2009-02-13 | 2014-07-22 | Amgen Inc. | Phenylalanine amide derivatives useful for treating insulin-related diseases and conditions |
| UA107791C2 (en) | 2009-05-05 | 2015-02-25 | Dow Agrosciences Llc | Pesticidal compositions |
| CN102438984A (zh) | 2009-05-19 | 2012-05-02 | 拜耳作物科学公司 | 杀虫用芳基吡咯啉 |
| FI20095678A0 (fi) | 2009-06-16 | 2009-06-16 | Biotie Therapies Oy | Ureasubstituoituja sulfoniamidijohdannaisia |
| UA110324C2 (en) | 2009-07-02 | 2015-12-25 | Genentech Inc | Jak inhibitory compounds based on pyrazolo pyrimidine |
| KR20120046765A (ko) | 2009-08-10 | 2012-05-10 | 스미또모 가가꾸 가부시끼가이샤 | (플루오로알킬티오)아세트산에스테르의 제조 방법 |
| JP2012254939A (ja) | 2009-10-07 | 2012-12-27 | Astellas Pharma Inc | オキサゾール化合物 |
| BR112012006239A2 (pt) | 2009-10-12 | 2015-09-08 | Bayer Cropscience Ag | amidas e tioamidas enquanto agentes pesticidas |
| CN103947645B (zh) | 2009-10-12 | 2016-07-06 | 拜尔农作物科学股份公司 | 作为杀虫剂的1-(吡啶-3-基)-吡唑和1-(嘧啶-5-基)-吡唑 |
| NZ601547A (en) | 2010-01-25 | 2014-04-30 | Chdi Foundation Inc | Certain kynurenine-3-monooxygenase inhibitors, pharmaceutical compositions, and methods of use thereof |
| PH12012501648A1 (en) | 2010-02-22 | 2017-08-23 | Syngenta Participations Ag | Dihydrofuran derivatives as insecticidal compounds |
| SG10201502484SA (en) | 2010-03-30 | 2015-05-28 | Verseon Corp | Multisubstituted aromatic compounds as inhibitors of thrombin |
| BR112012026530B1 (pt) | 2010-04-16 | 2018-03-20 | Bayer Intellectual Property Gmbh | Compostos heterocíclicos como pesticidas, composição os compreendendo e suas utilizações, bem como método para controle de pragas de pragas |
| EP2382865A1 (de) | 2010-04-28 | 2011-11-02 | Bayer CropScience AG | Synergistische Wirkstoffkombinationen |
| JP5868957B2 (ja) | 2010-05-05 | 2016-02-24 | バイエル・インテレクチュアル・プロパティ・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツングBayer Intellectual Property GmbH | 殺虫剤としてのチアゾール誘導体 |
| ES2700542T3 (es) | 2010-06-24 | 2019-02-18 | Gilead Sciences Inc | Composición farmacéutica que comprende un derivado de pirazolo[1,5-A]pirimidina como un agente antiviral |
| RU2013103422A (ru) | 2010-06-28 | 2014-08-10 | Байер Интеллектчуал Проперти Гмбх | Гетероарил-замещенные пиридиновые соединения для применения в качестве пестицидов |
| EP2590968A1 (en) | 2010-07-06 | 2013-05-15 | Novartis AG | Cyclic ether compounds useful as kinase inhibitors |
| BR112013000925A2 (pt) | 2010-07-15 | 2020-12-01 | Bayer Intellectual Property Gmbh | compostos heterocíclicos como pesticidas |
| PH12013500386A1 (en) | 2010-08-31 | 2013-04-22 | Dow Agrosciences Llc | Pesticidal compositions |
| JP2012082186A (ja) | 2010-09-15 | 2012-04-26 | Bayer Cropscience Ag | 殺虫性アリールピロリジン類 |
| BR112013009823A2 (pt) | 2010-10-22 | 2016-07-05 | Bayer Ip Gmbh | novos compostos heterocíclicos como pesticidas |
| CN105360132A (zh) | 2010-11-03 | 2016-03-02 | 陶氏益农公司 | 杀虫组合物和与其相关的方法 |
| WO2012061288A1 (en) | 2010-11-03 | 2012-05-10 | Dow Agrosciences Llc | Pesticidal compositions and processes related thereto |
| US9085501B2 (en) | 2010-11-17 | 2015-07-21 | China Petroleum & Chemical Corporation | Processes for increasing the yield of ethylene and propylene |
| WO2012070114A1 (ja) | 2010-11-24 | 2012-05-31 | 塩野義製薬株式会社 | Npy y5受容体拮抗作用を有するスルファミド誘導体 |
| WO2012102387A1 (ja) | 2011-01-27 | 2012-08-02 | 日産化学工業株式会社 | ピラゾール誘導体及び有害生物防除剤 |
| CN103347873A (zh) | 2011-02-09 | 2013-10-09 | 日产化学工业株式会社 | 吡唑衍生物和有害生物防除剂 |
| JP2012188418A (ja) | 2011-02-22 | 2012-10-04 | Nissan Chem Ind Ltd | トリアゾ−ル誘導体及び有害生物防除剤 |
| BR102012004142A2 (pt) | 2011-02-25 | 2015-04-07 | Dow Agrosciences Llc | Composições pesticidas e processos relacionados às mesmas |
| JP2013107867A (ja) | 2011-04-21 | 2013-06-06 | Nissan Chem Ind Ltd | ピラゾール誘導体及び有害生物防除剤 |
| WO2012147107A2 (en) | 2011-04-29 | 2012-11-01 | Msn Laboratories Limited | Novel & improved processes for the preparation of indoline derivatives and its pharmaceutical composition |
| EP2532661A1 (en) | 2011-06-10 | 2012-12-12 | Syngenta Participations AG | Novel insecticides |
| EP2540718A1 (en) | 2011-06-29 | 2013-01-02 | Syngenta Participations AG. | Novel insecticides |
| BR112014000688B8 (pt) | 2011-07-12 | 2022-10-11 | Dow Agrosciences Llc | Composições pesticidas, e processo para controle de pestes |
| MX2014000359A (es) | 2011-07-15 | 2014-05-01 | Basf Se | Metodos plaguicidas que utilizan compuestos de 3 - piridin tiazol sustituido y derivados para combatir las plagas de animales ii. |
| JP2013075871A (ja) | 2011-09-30 | 2013-04-25 | Nissan Chem Ind Ltd | チアゾール誘導体および有害生物防除剤 |
| JP2013082704A (ja) | 2011-09-30 | 2013-05-09 | Nissan Chem Ind Ltd | チアゾール誘導体および有害生物防除剤 |
| JP2013082699A (ja) | 2011-09-30 | 2013-05-09 | Nissan Chem Ind Ltd | ピラゾール誘導体および有害生物防除剤 |
| CN104093308A (zh) | 2011-10-26 | 2014-10-08 | 陶氏益农公司 | 杀虫组合物和与其相关的方法 |
| PH12014500930A1 (en) * | 2011-10-26 | 2014-06-09 | Dow Agrosciences Llc | Pesticidal compositions and processes related thereto |
| DE102011085492A1 (de) | 2011-10-31 | 2013-05-02 | Evonik Goldschmidt Gmbh | Neue aminogruppenhaltige Siloxane, Verfahren zu deren Herstellung und Anwendung |
| JP2013129651A (ja) | 2011-11-22 | 2013-07-04 | Nissan Chem Ind Ltd | チアゾール誘導体および有害生物防除剤 |
| JP2013129653A (ja) | 2011-11-22 | 2013-07-04 | Nissan Chem Ind Ltd | トリアゾ−ル誘導体および有害生物防除剤 |
| WO2013156431A1 (en) | 2012-04-17 | 2013-10-24 | Syngenta Participations Ag | Pesticidally active pyridyl- and pyrimidyl- substituted thiazole and thiadiazole derivatives |
| WO2013156433A1 (en) | 2012-04-17 | 2013-10-24 | Syngenta Participations Ag | Insecticidally active thiazole derivatives |
| US8901153B2 (en) | 2012-04-27 | 2014-12-02 | Dow Agrosciences, Llc. | Pesticidal compositions and processes related thereto |
| CN104540821B (zh) | 2012-06-04 | 2017-07-18 | 美国陶氏益农公司 | 制备某些2‑(吡啶‑3‑基)噻唑的方法 |
| PL2855467T3 (pl) | 2012-06-04 | 2017-06-30 | Dow Agrosciences Llc | Sposoby wytwarzania pewnych 2-(pirydyn-3-ylo)tiazoli |
| WO2014163932A1 (en) | 2013-03-13 | 2014-10-09 | Dow Agrosciences Llc | Preparation of haloalkoxyarylhydrazines and intermediates therefrom |
| CA2925595A1 (en) | 2013-10-17 | 2015-04-23 | Dow Agrosciences Llc | Processes for the preparation of pesticidal compounds |
| WO2015058021A1 (en) | 2013-10-17 | 2015-04-23 | Dow Agrosciences Llc | Processes for the preparation of pesticidal compounds |
| CN105636445B (zh) | 2013-10-17 | 2018-12-07 | 美国陶氏益农公司 | 制备杀虫化合物的方法 |
| EP3057426A4 (en) | 2013-10-17 | 2017-03-29 | Dow AgroSciences LLC | Processes for the preparation of pesticidal compounds |
| CA2925952A1 (en) | 2013-10-17 | 2015-04-23 | Dow Agrosciences Llc | Processes for the preparation of pesticidal compounds |
| JP2016535010A (ja) | 2013-10-17 | 2016-11-10 | ダウ アグロサイエンシィズ エルエルシー | 有害生物防除性化合物の製造方法 |
| MX2016004940A (es) | 2013-10-17 | 2016-06-28 | Dow Agrosciences Llc | Proceso para la preparacion de compuestos plaguicidas. |
| JP2017523168A (ja) | 2014-07-31 | 2017-08-17 | ダウ アグロサイエンシィズ エルエルシー | 3−(3−クロロ−1h−ピラゾール−1−イル)ピリジンの製造方法 |
| KR20170039121A (ko) | 2014-07-31 | 2017-04-10 | 다우 아그로사이언시즈 엘엘씨 | 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 |
| CN106488909A (zh) | 2014-07-31 | 2017-03-08 | 美国陶氏益农公司 | 制备3‑(3‑氯‑1h‑吡唑‑1‑基)吡啶的方法 |
| KR20170042714A (ko) | 2014-08-19 | 2017-04-19 | 다우 아그로사이언시즈 엘엘씨 | 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 |
| JP2017528469A (ja) | 2014-09-12 | 2017-09-28 | ダウ アグロサイエンシィズ エルエルシー | 3−(3−クロロ−1h−ピラゾール−1−イル)ピリジンの調製方法 |
-
2014
- 2014-10-17 KR KR1020177007144A patent/KR20170042714A/ko not_active Withdrawn
- 2014-10-17 CA CA2958058A patent/CA2958058A1/en not_active Abandoned
- 2014-10-17 US US14/517,344 patent/US9024031B1/en not_active Expired - Fee Related
- 2014-10-17 AR ARP140103918A patent/AR098112A1/es unknown
- 2014-10-17 CN CN201480082739.XA patent/CN107074774A/zh active Pending
- 2014-10-17 BR BR112017002735A patent/BR112017002735A2/pt not_active IP Right Cessation
- 2014-10-17 EP EP14900266.9A patent/EP3183238A4/en not_active Withdrawn
- 2014-10-17 WO PCT/US2014/061005 patent/WO2016028328A1/en not_active Ceased
- 2014-10-17 JP JP2017509654A patent/JP2017525703A/ja active Pending
-
2015
- 2015-03-24 US US14/666,812 patent/US9115115B1/en not_active Expired - Fee Related
- 2015-07-28 US US14/811,246 patent/US9522900B2/en not_active Expired - Fee Related
- 2015-08-14 TW TW104126570A patent/TW201613894A/zh unknown
-
2016
- 2016-10-27 US US15/335,809 patent/US9809570B2/en not_active Expired - Fee Related
-
2017
- 2017-02-15 IL IL250628A patent/IL250628A0/en unknown
- 2017-10-13 US US15/783,108 patent/US10005758B2/en not_active Expired - Fee Related
-
2018
- 2018-06-05 US US16/000,523 patent/US20180282298A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| EP3183238A4 (en) | 2018-01-10 |
| US9115115B1 (en) | 2015-08-25 |
| US9809570B2 (en) | 2017-11-07 |
| IL250628A0 (en) | 2017-05-29 |
| AR098112A1 (es) | 2016-05-04 |
| US20180282298A1 (en) | 2018-10-04 |
| US10005758B2 (en) | 2018-06-26 |
| US20170044134A1 (en) | 2017-02-16 |
| US9522900B2 (en) | 2016-12-20 |
| US9024031B1 (en) | 2015-05-05 |
| EP3183238A1 (en) | 2017-06-28 |
| US20160052908A1 (en) | 2016-02-25 |
| CN107074774A (zh) | 2017-08-18 |
| US20180037565A1 (en) | 2018-02-08 |
| WO2016028328A1 (en) | 2016-02-25 |
| BR112017002735A2 (pt) | 2017-12-19 |
| CA2958058A1 (en) | 2016-02-25 |
| JP2017525703A (ja) | 2017-09-07 |
| TW201613894A (en) | 2016-04-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20170042714A (ko) | 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 | |
| KR20160072154A (ko) | 살충성 화합물의 제조 방법 | |
| RU2088580C1 (ru) | Производные 1-(2-пиридил) пиразола или их кислотно-аддитивные соли, способ получения производных 1-(2-пиридил) пиразола или их кислотно-аддитивных солей (варианты), инсектоакарицидонематоцидная композиция и способ борьбы с насекомыми, клещами и нематодами | |
| JP5634504B2 (ja) | 殺線虫性スルホンアミド | |
| KR20160074541A (ko) | 살충성 화합물의 제조 방법 | |
| KR20160072155A (ko) | 살충성 화합물의 제조 방법 | |
| KR20160074540A (ko) | 살충성 화합물의 제조 방법 | |
| KR20170058388A (ko) | 3-(3-클로로-1h-피라졸-1-일)피리딘의 제조 방법 | |
| KR20160074542A (ko) | 살충성 화합물의 제조 방법 | |
| KR20160074543A (ko) | 살충성 화합물의 제조 방법 | |
| KR20160075565A (ko) | 살충성 화합물의 제조 방법 | |
| FI120396B (fi) | Pestisidiset 1-aryyli-5-(substituoidut alkylideeni-imino)pyratsolit | |
| JP2022527835A (ja) | 植物病原性真菌を制御または予防するための新規オキサジアゾール化合物 | |
| TW202226947A (zh) | 用於對抗植物病原真菌的新型雜環化合物 | |
| CN108349895A (zh) | 取代的2-二氟甲基-烟碱(硫代)甲酰苯胺衍生物及其作为杀真菌剂的用途 | |
| TW201641493A (zh) | 新穎三唑衍生物 | |
| JP2017522334A (ja) | 殺真菌性ピラゾール誘導体 | |
| CN111620867A (zh) | 介离子杀虫剂 | |
| JP2017512808A (ja) | 置換されているピラゾリル−ニコチン(チオ)アミド誘導体及び殺菌剤としてのそれらの使用 | |
| CN112794817A (zh) | 喹啉衍生物及其制备方法和应用 | |
| CN114249714B (zh) | 吡唑胺类化合物及其制备方法和应用 | |
| DE69117872T2 (de) | Pyrazolylacrylsäurederivate, deren Zwischenprodukte, und diese Derivate enthaltende Fungizide für Landwirtschaft und Gartenbau | |
| CN111925364A (zh) | 4-胺基呋喃-2(5h)酮衍生物及其制备方法和应用 | |
| CN112442026A (zh) | 介离子衍生物及其制备方法和应用 | |
| JP2022527836A (ja) | 植物病原性真菌を制御又は予防するための新規オキサジアゾール化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20170315 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |