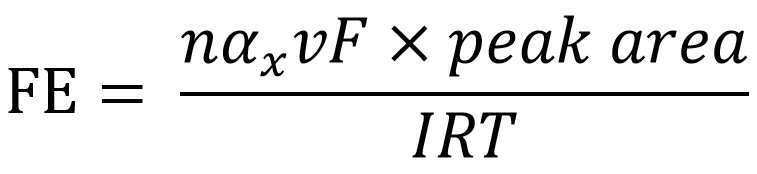KR102319109B1 - Hybrid sodium-carbon dioxide secondary battery capable of obtaining energy storage along with high value-added product by electrochemical carbon dioxide reduction and secondary battery system comprising the same - Google Patents
Hybrid sodium-carbon dioxide secondary battery capable of obtaining energy storage along with high value-added product by electrochemical carbon dioxide reduction and secondary battery system comprising the same Download PDFInfo
- Publication number
- KR102319109B1 KR102319109B1 KR1020200050877A KR20200050877A KR102319109B1 KR 102319109 B1 KR102319109 B1 KR 102319109B1 KR 1020200050877 A KR1020200050877 A KR 1020200050877A KR 20200050877 A KR20200050877 A KR 20200050877A KR 102319109 B1 KR102319109 B1 KR 102319109B1
- Authority
- KR
- South Korea
- Prior art keywords
- carbon dioxide
- secondary battery
- carbon
- sodium
- hybrid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M12/00—Hybrid cells; Manufacture thereof
- H01M12/08—Hybrid cells; Manufacture thereof composed of a half-cell of a fuel-cell type and a half-cell of the secondary-cell type
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25B—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES FOR THE PRODUCTION OF COMPOUNDS OR NON-METALS; APPARATUS THEREFOR
- C25B1/00—Electrolytic production of inorganic compounds or non-metals
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25B—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES FOR THE PRODUCTION OF COMPOUNDS OR NON-METALS; APPARATUS THEREFOR
- C25B3/00—Electrolytic production of organic compounds
- C25B3/20—Processes
- C25B3/25—Reduction
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25B—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES FOR THE PRODUCTION OF COMPOUNDS OR NON-METALS; APPARATUS THEREFOR
- C25B5/00—Electrogenerative processes, i.e. processes for producing compounds in which electricity is generated simultaneously
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/42—Methods or arrangements for servicing or maintenance of secondary cells or secondary half-cells
- H01M10/44—Methods for charging or discharging
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M14/00—Electrochemical current or voltage generators not provided for in groups H01M6/00 - H01M12/00; Manufacture thereof
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/134—Electrodes based on metals, Si or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/90—Selection of catalytic material
- H01M4/9041—Metals or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0002—Aqueous electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0002—Aqueous electrolytes
- H01M2300/0014—Alkaline electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
- H01M2300/0068—Solid electrolytes inorganic
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Metallurgy (AREA)
- Manufacturing & Machinery (AREA)
- Inorganic Chemistry (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
본 발명은 에너지 저장과 함께 이산화탄소의 전기화학적 환원반응으로 고부가가치 산물을 얻을 수 있는 하이브리드 소듐-이산화탄소 이차전지 및 이를 포함하는 이차전지 복합시스템에 관한 것으로, 보다 상세하게는 본 발명의 하이브리드 소듐-이산화탄소 이차전지는 음극에는 소듐 금속과 유기 전해액을 함유하고, 양극에는 금속-탄소 복합체 촉매와 수계 전해질을 함유한 구성으로 전지를 형성함으로써 방전 시 다양한 종류의 고부가가치 탄소 화합물과 전기에너지를 동시에 얻을 수 있다.
또한 본 발명의 이차전지 복합시스템은 에너지 저장 시스템과 상기 하이브리드 소듐-이산화탄소 이차전지를 포함함으로써 하나의 장치에서 방전 시 다양한 고부가가치의 탄소 화합물과 전기에너지를 동시에 얻을 수 있고, 생산된 전기에너지는 유연하게 저장 및 변환하여 에너지의 효율적 사용이 가능한 이점이 있다. The present invention relates to a hybrid sodium-carbon dioxide secondary battery capable of obtaining a high value-added product through an electrochemical reduction reaction of carbon dioxide with energy storage and a secondary battery composite system including the same, and more particularly, the hybrid sodium-carbon dioxide of the present invention In a secondary battery, the negative electrode contains sodium metal and an organic electrolyte and the positive electrode contains a metal-carbon composite catalyst and an aqueous electrolyte. .
In addition, the secondary battery composite system of the present invention includes an energy storage system and the hybrid sodium-carbon dioxide secondary battery, so that various high-value-added carbon compounds and electrical energy can be simultaneously obtained during discharging in one device, and the produced electrical energy is flexible It has the advantage of being able to efficiently use energy by storing and converting it.
Description
본 발명은 에너지 저장과 함께 이산화탄소의 전기화학적 환원반응으로 고부가가치 산물을 얻을 수 있는 하이브리드 소듐-이산화탄소 이차전지 및 이를 포함하는 이차전지 복합시스템에 관한 것이다.The present invention relates to a hybrid sodium-carbon dioxide secondary battery capable of obtaining a high value-added product through an electrochemical reduction reaction of carbon dioxide with energy storage and a secondary battery composite system including the same.
지구 온난화로 인한 이상 기후 문제가 심화됨에 따라, 그 원인 중 하나인 CO2 배출량을 감축하고자 하는 범세계적인 정책이 시행되고 있다. 대한민국에서는 2015년부터 온실가스 배출권 거래제가 시행되고 있으며, 특히 2015년 12월 12일 파리에서 체결된 신기후체제 파리 협정에 따라 대한민국은 2030년까지 BAU(배출전망치, Business AS Usual) 대비 37% 감축해야 할 의무가 있다.As the problem of abnormal climate due to global warming intensifies, a global policy to reduce CO 2 emission, which is one of the causes, is being implemented. In Korea, the greenhouse gas emission trading system has been in effect since 2015. In particular, in accordance with the Paris Agreement on the new climate regime signed in Paris on December 12, 2015, Korea will reduce its emissions by 37% compared to BAU (Business AS Usual) by 2030. have a duty to do
하지만 화석연료를 이용한 공정에서 CO2를 포함한 부생가스는 필연적으로 발생하며, 화석연료를 대체할 수 있는 국내 에너지사업은 매우 미비한 상태이다. 따라서 배출된 CO2를 포집, 저장 및 전환하는 기술에 관한 연구의 필요성이 강조되고 있다. However, in the process using fossil fuels, by-product gases including CO 2 are inevitably generated, and the domestic energy business that can replace fossil fuels is very insignificant. Therefore, the need for research on technologies to capture, store and convert the emitted CO 2 is emphasized.
현재 CO2를 고부가 가치의 탄소 화합물로 전환하는 기술은 높은 온도와 압력 등의 조건을 필요로 하므로 상용화에 어려움을 겪고 있다. 최근 학계에서는 CO2의 전기화학적 환원반응(CO2RR; CO2 reduction reaction)이 CO2 자원화 전략 중 하나로 각광받고 있다. CO2RR을 이용할 경우, 분해되기 어려운 CO2를 직접적으로 제거할 수 있다. 또한, CO2 제거 과정에서 발생하는 일산화탄소(CO), 포름산(HCOOH) 및 다양한 탄화수소 생성물에 의한 경제적 부가가치를 얻을 수 있다. 특히, 일산화탄소(CO) 및 포름산(HCOOH)의 경우 생산 가격 대비 높은 경제성을 보여줌으로써 전기화학적 CO2전환 사업의 주요 생산제품이 될 것으로 전망된다.Currently, the technology for converting CO 2 into a high-value-added carbon compound is difficult to commercialize because it requires conditions such as high temperature and pressure. In recent academic electrochemical reduction of CO 2 (CO 2 RR; CO 2 reduction reaction) is spotlighted as one of the CO 2 recycling strategy. When CO 2 RR is used, CO 2 that is difficult to decompose can be directly removed. In addition, it is possible to obtain economic value added by carbon monoxide (CO), formic acid (HCOOH) and various hydrocarbon products generated in the CO 2 removal process. In particular, carbon monoxide (CO) and formic acid (HCOOH) are expected to become major products in the electrochemical CO 2 conversion business by showing high economic feasibility compared to the production price.
그러나 CO2는 석유화학공정, 철강공정에서 연속적으로 배출되지만 기존의 CO2RR 시스템에서는 잉여 전기에너지가 불규칙적으로 생성되기 때문에 생성된 전기에너지를 유연하고 효율적으로 쓸 수가 없다. 또한 CO2를 전기화학적으로 환원시키기 위해선 고비용의 전기 에너지가 필요하다는 문제가 있다. 이러한 문제를 해결하기 위해서 CO2RR에 필요한 에너지를 효율적으로 운영할 수 있는 시스템에 대한 연구와 CO2RR에 대한 활성 및 선택도가 좋은 촉매 물질을 개발하는 연구가 동시에 이루어지고 있다.However, CO 2 is continuously emitted from petrochemical processes and steel processes, but in the existing CO 2 RR system, surplus electrical energy is generated irregularly, so the generated electrical energy cannot be used flexibly and efficiently. In addition, there is a problem that high-cost electrical energy is required to electrochemically reduce CO 2 . To solve this problem, a study on a system that can efficiently operate the energy required for CO 2 RR and a study on developing a catalyst material with good activity and selectivity for CO 2 RR are being conducted at the same time.
CO2를 활용할 수 있는 방법 중에 금속-CO2 배터리가 많은 주목을 받고 있다. 금속-CO2는 금속-공기 전지의 연구로부터 시작되었다. 금속-공기 전지는 높은 에너지 밀도를 가져 최근 몇 십년 동안 많은 연구가 이루어졌다. 하지만 금속-공기 전지는 실제 공기를 주입할 때 공기 속의 CO2로부터 카보네이트가 형성되면서 순수한 산소를 주입할 때와 비교하여 감쇄되는 용량과 안정성 문제가 있다. Among the methods that can utilize CO 2 , metal-CO 2 batteries are receiving a lot of attention. Metal-CO 2 started with the study of metal-air batteries. Metal-air batteries have a high energy density, so much research has been done in recent decades. However, the metal-air battery has problems with capacity and stability that are attenuated compared to when pure oxygen is injected as carbonate is formed from CO 2 in the air when actually air is injected.
금속-공기 전지에서 산소에 이산화탄소를 일정 부분 첨가하였을 때 용량이 3 배 증가한다는 것을 발견한 후에 Archer 그룹에서는 온도에 따라 용량이 변하는 일차 리튬-CO2 전지를 개발하였다. 방전 시에 CO2가 Li2CO3와 C로 고정되는 것을 확인하였다. 또한 Zhou 그룹은 Li2CO3의 분해를 촉진시킬 수 있는 양극을 활용하여 재충전이 가능한 리튬-CO2 전지를 개발하였다. 그 이후 많은 그룹들이 리튬-CO2로 대표되는 재충전이 가능한 금속-CO2 배터리에 집중하고 있다. After discovering that the capacity of a metal-air battery increased by a factor of three when carbon dioxide was added to oxygen in a certain portion, Archer's group developed a primary lithium-CO 2 battery whose capacity changes with temperature. It was confirmed that CO 2 was fixed to Li 2 CO 3 and C during discharge. In addition, Zhou group has developed a rechargeable lithium-CO 2 battery using an anode that can promote the decomposition of Li 2 CO 3 . Since then, many groups have focused on rechargeable metal-CO 2 batteries, represented by lithium-CO 2 .
현재 금속-CO2 배터리는 높은 작동전압, 높은 에너지 밀도와 수십 싸이클 이상 되는 수명을 보여주고 있다. 하지만 방전 시에 유기 전해질에서 양성자의 참여없이 CO2의 전기화학적 환원반응(CO2RR)이 일어나기 때문에 방전 생산물이 탄소(carbon), 카보네이트(carbonate), 옥실레이트(oxalate)에 국한되어 있다. 즉, 유기 전해질을 사용하는 금속-CO2 전지에서는 탄화수소, 산, 알코올과 같은 고부가가치의 탄소 화합물들은 생산이 불가능하다는 한계점을 가지고 있다.Currently, metal-CO 2 batteries exhibit high operating voltages, high energy density, and lifetimes of more than tens of cycles. However, there is a discharge product is limited to a carbon (carbon), carbonates (carbonate), oxylate (oxalate) due to occur without participation of the proton electrochemical reduction of CO 2 (CO 2 RR) in the organic electrolyte during discharging. That is, in a metal-CO 2 battery using an organic electrolyte, high value-added carbon compounds such as hydrocarbons, acids, and alcohols have a limitation in that it is impossible to produce them.
하기 비특허문헌 1 및 2는 양극부에서는 방전 시 CO2RR이 일어나지만 Zn 금속의 특성 상 0.5 V 이하의 낮은 전압을 보여 이차전지로서 효율적으로 충방전을 실시하는데 한계가 있다. The following
한편, 이론적으로 물은 CO2RR이 가능하도록 양성자를 제공하는데 완벽한 매개체이다. 실제로 많은 귀금속, 전이금속, 탄소 전기화학 촉매들이 물에서 CO2RR이 원활하게 이루어져 고부가가치의 생산물을 만들어 낼 수 있다는 것이 증명되었다. 추가로 물은 저비용이고 유기 전해질보다 친환경적이기 때문에 전해질로 적합한 이점이 있다.On the other hand, theoretically, water is the perfect medium to provide protons to enable CO 2 RR. In fact, it has been proven that many noble metals, transition metals, and carbon electrochemical catalysts can produce high value-added products by smoothly forming CO 2 RR in water. In addition, water has the advantage of being suitable as an electrolyte because it is less expensive and more environmentally friendly than organic electrolytes.
따라서 기존의 CO2RR 이차전지가 가진 전기에너지의 비효율성을 개선하고 다양한 생산물을 수득하기 위해 CO2RR에 대한 활성 및 선택도가 좋은 촉매 물질을 적용한 새로운 금속-이산화탄소 이차전지에 대한 연구개발이 필요하다.Therefore, in order to improve the inefficiency of electric energy of the existing CO 2 RR secondary battery and to obtain various products, research and development for a new metal-carbon dioxide secondary battery with good activity and selectivity for CO 2 RR has been applied. necessary.
상기와 같은 문제 해결을 위하여, 본 발명은 방전 시 다양한 고부가가치 산물을 얻을 수 있는 하이브리드 소듐-이산화탄소 이차전지를 제공하는 것을 그 목적으로 한다.In order to solve the above problems, an object of the present invention is to provide a hybrid sodium-carbon dioxide secondary battery capable of obtaining various high value-added products during discharge.
또한 본 발명은 에너지를 저장하는 동시에 고부가가치 산물을 얻을 수 있는 상기 하이브리드 소듐-이산화탄소 이차전지를 포함하는 이차전지 복합시스템을 제공하는 것을 그 목적으로 한다.Another object of the present invention is to provide a secondary battery composite system including the hybrid sodium-carbon dioxide secondary battery capable of storing energy and obtaining a high value-added product at the same time.
또한 본 발명은 상기 하이브리드 소듐-이산화탄소 이차전지를 이용하여 이산화탄소의 탄소 화합물을 제조하는 방법을 제공하는 것으로 그 목적으로 한다.Another object of the present invention is to provide a method for producing a carbon compound of carbon dioxide using the hybrid sodium-carbon dioxide secondary battery.
본 발명은 제1 집전체, 소듐 금속 및 유기 전해질을 함유하는 음극(anode)부; 제2 집전체, 금속-탄소 복합체 촉매 및 수계 전해질을 함유하는 양극(cathode)부; 및 상기 음극부와 양극부 사이에 위치하는 고체 전해질;을 포함하는 하이브리드 소듐-이산화탄소 이차전지를 제공한다.The present invention provides a first current collector, an anode comprising a sodium metal and an organic electrolyte; a second current collector, a metal-carbon composite catalyst, and a cathode containing an aqueous electrolyte; and a solid electrolyte positioned between the negative electrode part and the positive electrode part; hybrid sodium-carbon dioxide including a secondary battery.
상기 금속-탄소 복합체 촉매는 탄소지지체 상에 금속 나노입자가 1:9 내지 9:1 중량비로 결착된 것일 수 있다.The metal-carbon composite catalyst may be one in which metal nanoparticles are bound in a weight ratio of 1:9 to 9:1 on a carbon support.
상기 탄소지지체는 카본블랙, 케첸블랙, 아세틸렌블랙, 흑연, 탄소나노튜브, 탄소나노섬유, 산화그래핀 및 환원된 산화그래핀 중에서 선택된 1종 이상일 수 있다.The carbon support may be at least one selected from carbon black, Ketjen black, acetylene black, graphite, carbon nanotubes, carbon nanofibers, graphene oxide and reduced graphene oxide.
상기 금속 나노입자는 직경이 1~30 nm이고, 금, 은, 구리 및 주석 중에서 선택되는 1종 이상일 수 있다.The metal nanoparticles may have a diameter of 1 to 30 nm, and may be at least one selected from gold, silver, copper, and tin.
상기 수계 전해질은 탄산수소소듐(NaHCO3), 수산화소듐(NaOH), 황산소듐(Na2SO4), 질산소듐(NaNO3), 염화소듐(NaCl) 및 탄산소듐(Na2CO3) 중에서 선택되는 1종 이상일 수 있다.The aqueous electrolyte is selected from sodium hydrogen carbonate (NaHCO 3 ), sodium hydroxide (NaOH), sodium sulfate (Na 2 SO 4 ), sodium nitrate (NaNO 3 ), sodium chloride (NaCl) and sodium carbonate (Na 2 CO 3 ) There may be more than one type.
상기 양극의 수계 전해질 내에 이산화탄소를 주입하여 상기 하이브리드 소듐-이산화탄소 이차전지를 작동시키는 것일 수 있다.The hybrid sodium-carbon dioxide secondary battery may be operated by injecting carbon dioxide into the aqueous electrolyte of the positive electrode.
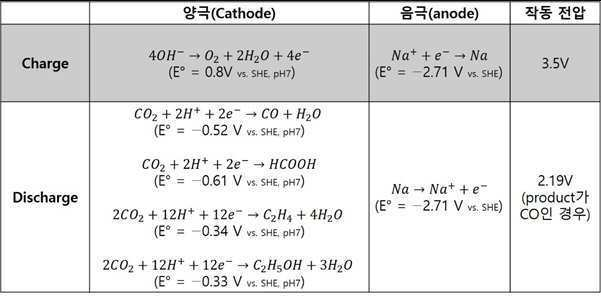
상기 하이브리드 소듐-이산화탄소 이차전지는 충전시 음극부에서는 하기 반응식 1과 같은 소듐화(sodiation) 반응이 일어나고, 양극부에서는 하기 반응식 2와 같은 산소발생반응(OER)이 일어날 수 있다.When the hybrid sodium-carbon dioxide secondary battery is charged, a sodiumization reaction as shown in
[반응식 1][Scheme 1]
Na+ + e- → NaNa + + e - → Na
[반응식 2][Scheme 2]
4OH- → O2 + 2H2O + 4e- 4OH - → O 2 + 2H 2 O + 4e -
상기 하이브리드 소듐-이산화탄소 이차전지는 방전시 음극부에서는 하기 반응식 3과 같은 탈소듐화(desodiation) 반응이 일어나고, 양극부에서는 하기 반응식 4 내지 반응식 7 중에서 선택된 하나 이상의 이산화탄소 환원반응(CO2RR)이 일어날 수 있다.When the hybrid sodium-carbon dioxide secondary battery is discharged, a desodium reaction as shown in
[반응식 3][Scheme 3]
Na → Na+ + e- Na → Na + + e -
[반응식 4][Scheme 4]
CO2 + 2H+ + 2e- → CO + H2OCO 2 + 2H + + 2e - → CO + H 2 O
[반응식 5][Scheme 5]
CO2 + 2H+ + 2e- → HCOOHCO 2 + 2H + + 2e - → HCOOH
[반응식 6][Scheme 6]
2CO2 + 12H+ + 12e- → C2H4 + 4H2O2CO 2 + 12H + + 12e - → C 2 H 4 + 4H 2 O
[반응식 7][Scheme 7]
2CO2 + 12H+ + 12e- → C2H5OH + 3H2O2CO 2 + 12H + + 12e - → C 2 H 5 OH + 3H 2 O
상기 이산화탄소 환원반응에 의해 일산화탄소(CO), 포름산(HCOOH), 에틸렌(C2H4) 및 에탄올(C2H5OH) 중에서 선택되는 1종 이상의 탄소 화합물이 생성될 수 있다.One or more carbon compounds selected from carbon monoxide (CO), formic acid (HCOOH), ethylene (C 2 H 4 ), and ethanol (C 2 H 5 OH) may be produced by the carbon dioxide reduction reaction.
상기 금속-탄소 복합체 촉매는 탄소지지체 상에 금속 나노입자가 4:6 내지 6:4 중량비로 결착된 것이고, 상기 탄소지지체는 카본블랙, 케첸블랙, 아세틸렌블랙, 흑연, 탄소나노튜브, 탄소나노섬유, 산화그래핀 및 환원된 산화그래핀 중에서 선택된 1종 이상이고, 상기 금속 나노입자는 직경이 1~30 nm이며, 금, 주석 또는 이들의 혼합물이고, 상기 수계 전해질은 탄산수소소듐(NaHCO3), 수산화소듐(NaOH) 및 염화소듐(NaCl) 중에서 선택되는 1종 이상이고, 상기 양극의 수계 전해질 내에 이산화탄소를 주입하여 상기 하이브리드 소듐-이산화탄소 이차전지를 작동시키는 것이고, 상기 하이브리드 소듐-이산화탄소 이차전지는 충전시 음극부에서는 하기 반응식 1과 같은 소듐화(sodiation) 반응이 일어나고, 양극부에서는 하기 반응식 2와 같은 산소발생반응(OER)이 일어나는 것이고,The metal-carbon composite catalyst is one in which metal nanoparticles are bound on a carbon support in a weight ratio of 4:6 to 6:4, and the carbon support is carbon black, Ketjen black, acetylene black, graphite, carbon nanotubes, carbon nanofibers. , graphene oxide and at least one selected from reduced graphene oxide, the metal nanoparticles have a diameter of 1 to 30 nm, gold, tin, or a mixture thereof, and the aqueous electrolyte is sodium hydrogen carbonate (NaHCO 3 ) , sodium hydroxide (NaOH) and at least one selected from sodium chloride (NaCl), and by injecting carbon dioxide into the aqueous electrolyte of the positive electrode to operate the hybrid sodium-carbon dioxide secondary battery, the hybrid sodium-carbon dioxide secondary battery is During charging, a sodiumization reaction as shown in
[반응식 1][Scheme 1]
Na+ + e- → NaNa + + e - → Na
[반응식 2][Scheme 2]
4OH- → O2 + 2H2O + 4e- 4OH - → O 2 + 2H 2 O + 4e -
상기 하이브리드 소듐-이산화탄소 이차전지는 방전시 음극부에서는 하기 반응식 3과 같은 탈소듐화(desodiation) 반응이 일어나고, 양극부에서는 하기 반응식 4 또는 반응식 5 중에서 선택된 하나 이상의 이산화탄소 환원반응(CO2RR)이 일어나는 것이고,When the hybrid sodium-carbon dioxide secondary battery is discharged, a desodium reaction as shown in
[반응식 3][Scheme 3]
Na → Na+ + e- Na → Na + + e -
[반응식 4][Scheme 4]
CO2 + 2H+ + 2e- → CO + H2OCO 2 + 2H + + 2e - → CO + H 2 O
[반응식 5][Scheme 5]
CO2 + 2H+ + 2e- → HCOOHCO 2 + 2H + + 2e - → HCOOH
상기 이산화탄소 환원반응에 의해 일산화탄소(CO) 또는 포름산(HCOOH) 중에서 선택되는 1종 이상의 탄소 화합물이 생성될 수 있다.At least one carbon compound selected from carbon monoxide (CO) and formic acid (HCOOH) may be produced by the carbon dioxide reduction reaction.
상기 금속-탄소 복합체 촉매는 탄소지지체 상에 금속 나노입자가 5:5 중량비로 결착된 것이고, 상기 탄소지지체는 카본블랙이고, 상기 금속 나노입자는 직경이 7~8 nm인 금이고, 상기 수계 전해질은 탄산수소소듐(NaHCO3)이고, 상기 양극의 수계 전해질 내에 이산화탄소를 주입하여 상기 하이브리드 소듐-이산화탄소 이차전지를 작동시키는 것이고, 상기 하이브리드 소듐-이산화탄소 이차전지는 충전시 음극부에서는 하기 반응식 1과 같은 소듐화(sodiation) 반응이 일어나고, 양극부에서는 하기 반응식 2와 같은 산소발생반응(OER)이 일어나는 것이고,In the metal-carbon composite catalyst, metal nanoparticles are bound on a carbon support in a weight ratio of 5:5, the carbon support is carbon black, the metal nanoparticles are gold having a diameter of 7 to 8 nm, and the aqueous electrolyte is sodium hydrogen carbonate (NaHCO 3 ), and by injecting carbon dioxide into the aqueous electrolyte of the positive electrode to operate the hybrid sodium-carbon dioxide secondary battery, the hybrid sodium-carbon dioxide secondary battery is charged in the negative electrode part as shown in
[반응식 1][Scheme 1]
Na+ + e- → NaNa + + e - → Na
[반응식 2][Scheme 2]
4OH- → O2 + 2H2O + 4e- 4OH - → O 2 + 2H 2 O + 4e -
상기 하이브리드 소듐-이산화탄소 이차전지는 방전시 음극부에서는 하기 반응식 3과 같은 탈소듐화(desodiation) 반응이 일어나고, 양극부에서는 하기 반응식 4와 같은 이산화탄소 환원반응(CO2RR)이 일어나는 것이고,When the hybrid sodium-carbon dioxide secondary battery is discharged, a desodium reaction as shown in
[반응식 3][Scheme 3]
Na → Na+ + e- Na → Na + + e -
[반응식 4][Scheme 4]
CO2 + 2H+ + 2e- → CO + H2OCO 2 + 2H + + 2e - → CO + H 2 O
상기 이산화탄소 환원반응에 의해 일산화탄소(CO)의 탄소 화합물이 생성될 수 있다.A carbon compound of carbon monoxide (CO) may be produced by the carbon dioxide reduction reaction.
한편, 본 발명은 상기 하이브리드 소듐-이산화탄소 이차전지를 포함하는 이차전지 복합시스템을 제공한다.On the other hand, the present invention provides a secondary battery composite system including the hybrid sodium-carbon dioxide secondary battery.
상기 하이브리드 소듐-이산화탄소 이차전지에 이산화탄소를 공급하는 이산화탄소 공급부; 상기 하이브리드 소듐-이산화탄소 이차전지로부터 생성된 전기에너지를 저장하는 에너지 저장 시스템(energy storage system, ESS); 및 상기 하이브리드 소듐-이산화탄소 이차전지로부터 생성된 이산화탄소의 탄소 화합물을 저장하는 반응 생성물 저장부;를 더 포함할 수 있다.a carbon dioxide supply unit for supplying carbon dioxide to the hybrid sodium-carbon dioxide secondary battery; an energy storage system (ESS) for storing electric energy generated from the hybrid sodium-carbon dioxide secondary battery; and a reaction product storage unit for storing a carbon compound of carbon dioxide generated from the hybrid sodium-carbon dioxide secondary battery.
또한, 본 발명은 음극(anode)부; 양극(cathode)부; 및 상기 음극부와 양극부 사이에 위치하는 고체 전해질;을 포함하는 상기 하이브리드 소듐-이산화탄소 이차전지를 이용하여 이산화탄소의 탄소 화합물을 제조하는 방법에 있어서, (a) 상기 양극부에 수계 전해질을 공급하는 단계; (b) 상기 수계 전해질이 공급된 양극부에 이산화탄소를 공급하는 단계; 및 (c) 상기 양극부 및 음극부 사이에 전류를 인가하여 상기 양극부에서 수소 이온(H+)을 형성시키고, 상기 수소 이온(H+)이 이산화탄소를 환원시켜 이산화탄소의 탄소 화합물을 생성시키는 단계;를 포함하는 이산화탄소의 탄소 화합물을 제조하는 방법을 제공한다.In addition, the present invention is a cathode (anode) portion; anode (cathode) part; and a solid electrolyte positioned between the negative electrode and the positive electrode; in the hybrid sodium-carbon dioxide secondary battery comprising: (a) supplying an aqueous electrolyte to the positive electrode in the method for producing a carbon compound of carbon dioxide step; (b) supplying carbon dioxide to the anode part to which the aqueous electrolyte is supplied; and (c) applying a current between the anode part and the cathode part to form hydrogen ions (H + ) in the anode part, and the hydrogen ions (H + ) reduce carbon dioxide to produce a carbon compound of carbon dioxide It provides a method for producing a carbon compound of carbon dioxide containing;
상기 (c) 단계는 상기 양극부 및 음극부 사이에 1 내지 3 mA의 전류를 인가하는 것일 수 있다.In step (c), a current of 1 to 3 mA may be applied between the anode part and the cathode part.
상기 이산화탄소의 탄소 화합물은 일산화탄소(CO), 포름산(HCOOH), 에틸렌(C2H4) 및 에탄올(C2H5OH) 중에서 선택되는 1종 이상일 수 있다.The carbon compound of carbon dioxide may be at least one selected from carbon monoxide (CO), formic acid (HCOOH), ethylene (C 2 H 4 ), and ethanol (C 2 H 5 OH).
상기 (c) 단계에서 생성되는 이산화탄소의 탄소 화합물은 1 내지 3 mA의 전류에서 55% 이상의 패러데이 효율(faradaic efficiency)로 생성될 수 있다.The carbon compound of carbon dioxide produced in step (c) may be produced with a faradaic efficiency of 55% or more at a current of 1 to 3 mA.
본 발명의 하이브리드 소듐-이산화탄소 이차전지는 음극에는 소듐 금속과 유기 전해액을 함유하고, 양극에는 금속-탄소 복합체 촉매와 수계 전해질을 함유한 구성으로 전지를 형성함으로써 방전 시 다양한 종류의 고부가가치 탄소 화합물과 전기에너지를 동시에 얻을 수 있다.The hybrid sodium-carbon dioxide secondary battery of the present invention contains sodium metal and an organic electrolyte in the negative electrode, and the positive electrode contains a metal-carbon composite catalyst and an aqueous electrolyte. Electrical energy can be obtained at the same time.
또한 본 발명의 하이브리드 소듐-이산화탄소 이차전지는 양극에 이산화탄소의 환원반응에 대한 활성 및 선택도가 우수한 금속-탄소 복합체 촉매를 함유함으로써 방전 시 생산되는 탄소 화합물의 수율을 향상시킬 수 있다.In addition, the hybrid sodium-carbon dioxide secondary battery of the present invention contains a metal-carbon composite catalyst having excellent activity and selectivity for the reduction reaction of carbon dioxide in the positive electrode, thereby improving the yield of carbon compounds produced during discharge.
또한 본 발명의 이차전지 복합시스템은 에너지 저장 시스템과 상기 하이브리드 소듐-이산화탄소 이차전지를 포함함으로써 하나의 장치에서 방전 시 다양한 고부가가치의 탄소 화합물과 전기에너지를 동시에 얻을 수 있고, 생산된 전기에너지는 유연하게 저장 및 변환하여 에너지의 효율적 사용이 가능한 이점이 있다. In addition, the secondary battery composite system of the present invention includes an energy storage system and the hybrid sodium-carbon dioxide secondary battery, so that various high-value-added carbon compounds and electrical energy can be simultaneously obtained during discharging in one device, and the produced electrical energy is flexible It has the advantage of being able to efficiently use energy by storing and converting it.
도 1은 본 발명의 하이브리드 소듐-이산화탄소 이차전지의 개략적인 구성도(a) 및 실제 구성된 사진(b)이다.
도 2는 본 발명의 실시예 1에서 제조된 금 나노입자-탄소지지체 복합체 촉매의 투과전자현미경(TEM) 이미지이다.
도 3은 본 발명의 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지에 대하여 전류별로 생성된 일산화탄소(CO) 및 수소(H2)의 패러데이 효율(Faradaic Efficiency)을 나타낸 그래프이다.
도 4는 본 발명의 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지의 방전 및 충전 전압 프로파일을 나타낸 그래프이다.
도 5는 본 발명의 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지에 대하여 1 mA 전류에서의 Galvanostatic 방전-충전 사이클링 곡선을 나타낸 그래프이다.
도 6은 본 발명의 실시예 2에서 제조된 하이브리드 소듐-이산화탄소 이차전지의 전류에 따른 방전전압 그래프(a)와 전류별로 생성된 포름산(HCOOH), 일산화탄소(CO) 및 수소(H2)의 패러데이 효율(Faradaic Efficiency)을 나타낸 그래프(b)이다. 1 is a schematic configuration diagram (a) and an actual configuration photograph (b) of a hybrid sodium-carbon dioxide secondary battery of the present invention.
2 is a transmission electron microscope (TEM) image of the gold nanoparticle-carbon support composite catalyst prepared in Example 1 of the present invention.
3 is a graph showing the Faradaic Efficiency of carbon monoxide (CO) and hydrogen (H 2 ) generated by current for the hybrid sodium-carbon dioxide secondary battery prepared in Example 1 of the present invention.
4 is a graph showing the discharge and charge voltage profiles of the hybrid sodium-carbon dioxide secondary battery prepared in Example 1 of the present invention.
5 is a graph showing a galvanostatic discharge-charge cycling curve at 1 mA current for the hybrid sodium-carbon dioxide secondary battery prepared in Example 1 of the present invention.
6 is a graph of the discharge voltage according to the current of the hybrid sodium-carbon dioxide secondary battery prepared in Example 2 of the present invention (a) and the Faradays of formic acid (HCOOH), carbon monoxide (CO) and hydrogen (H 2 ) It is a graph (b) showing the Faradaic Efficiency.
이하에서는 본 발명을 하나의 실시예로 더욱 상세하게 설명한다.Hereinafter, the present invention will be described in more detail by way of one embodiment.
본 발명에서 패러데이 효율(Faradaic Efficiency, FE)은 이산화탄소를 유기화합물로 전환하기 위해 사용한 에너지 중 실제 유기화합물 생성을 위해 사용된 에너지 비율을 의미한다.In the present invention, Faradaic Efficiency (FE) refers to a ratio of energy used to actually generate organic compounds among energy used to convert carbon dioxide into organic compounds.
본 발명은 에너지 저장과 함께 이산화탄소의 전기화학적 환원반응으로 고부가가치 산물을 얻을 수 있는 하이브리드 소듐-이산화탄소 이차전지 및 이를 포함하는 이차전지 복합시스템에 관한 것이다.The present invention relates to a hybrid sodium-carbon dioxide secondary battery capable of obtaining a high value-added product through an electrochemical reduction reaction of carbon dioxide with energy storage and a secondary battery composite system including the same.
기존의 이차전지 시스템은 양극 수용액에 이산화탄소를 흘려줌으로써 탄산수소소듐(NaHCO3) 형태로 이산화탄소를 수용액에 포집하고 양극에서 방전 시 수소를 생산하는 방식이었다. 그러나 본 발명은 기존 이차전지 시스템과 달리 양극에서 이산화탄소를 수용액에서 포집하여 수소를 생산하는 것이 아닌 이산화탄소의 직접적인 환원반응에 의해 일산화탄소(CO), 포름산(HCOOH), 에틸렌(C2H4) 또는 에탄올(C2H5OH)과 같은 고부가가치 산물을 수득할 수 있도록 설계한 것이다. The existing secondary battery system was a method of collecting carbon dioxide in the form of sodium bicarbonate (NaHCO 3 ) in the aqueous solution by flowing carbon dioxide into the anode aqueous solution and producing hydrogen when discharging from the anode. However, in the present invention, carbon monoxide (CO), formic acid (HCOOH), ethylene (C 2 H 4 ) or ethanol by a direct reduction reaction of carbon dioxide, rather than the production of hydrogen by capturing carbon dioxide in an aqueous solution at the positive electrode, unlike the conventional secondary battery system. It is designed to obtain high value-added products such as (C 2 H 5 OH).
즉, 본 발명의 하이브리드 소듐-이산화탄소 이차전지는 음극에는 소듐 금속과 유기 전해액을 함유하고, 양극에는 금속-탄소 복합체 촉매와 수계 전해질을 함유한 구성으로 전지를 형성함으로써 이산화탄소를 포집하는 것이 아닌 이산화탄소를 직접적으로 전환하여 고부가가치 산물을 수득할 수 있고, 나아가 산업적, 경제적으로 기여할 수 있다. That is, in the hybrid sodium-carbon dioxide secondary battery of the present invention, the negative electrode contains sodium metal and an organic electrolyte, and the positive electrode contains a metal-carbon composite catalyst and an aqueous electrolyte. A high value-added product can be obtained by direct conversion, and further industrial and economic contributions can be made.
구체적으로 본 발명은 제1 집전체, 소듐 금속 및 유기 전해질을 함유하는 음극(anode)부; 제2 집전체, 금속-탄소 복합체 촉매 및 수계 전해질을 함유하는 양극(cathode)부; 및 상기 음극부와 양극부 사이에 위치하는 고체 전해질;을 포함하는 하이브리드 소듐-이산화탄소 이차전지를 제공한다.Specifically, the present invention includes a first current collector, a negative electrode (anode) containing a sodium metal and an organic electrolyte; a second current collector, a metal-carbon composite catalyst, and a cathode containing an aqueous electrolyte; and a solid electrolyte positioned between the negative electrode part and the positive electrode part; hybrid sodium-carbon dioxide including a secondary battery.
도 1은 상기 하이브리드 소듐-이산화탄소 이차전지의 개략적인 구성도(a) 및 실제 구성된 사진(b)이다. 상기 도 1의 (a)를 참조하면, 상기 하이브리드 소듐-이산화탄소 이차전지는 음극(anode) 부분에는 coin-cell type으로 집전체, 소듐 금속 및 유기 전해질로 구성이 되며, 양극(cathode) 부분에는 집전체, 금속-탄소 복합체 촉매 및 수계 전해질로 구성된다. 상기 음극의 유기 전해질과 양극의 수계 전해질을 분리하고 Na+를 이동시킬 수 있는 NASICON 고체 전해질이 음극과 양극 사이에 위치한다. 1 is a schematic configuration diagram (a) and an actual configuration photograph (b) of the hybrid sodium-carbon dioxide secondary battery. Referring to (a) of FIG. 1, the hybrid sodium-carbon dioxide secondary battery is a coin-cell type in an anode part, and is composed of a current collector, sodium metal, and an organic electrolyte, and a house in the cathode part. It is composed of a whole, a metal-carbon composite catalyst and a water-based electrolyte. A NASICON solid electrolyte capable of separating the organic electrolyte of the negative electrode and the aqueous electrolyte of the positive electrode and moving Na + is positioned between the negative electrode and the positive electrode.
상기 하이브리드 소듐-이산화탄소 이차전지는 양극부의 수계 전해질에 이산화탄소(CO2) 기체를 흘러주면서 이차전지가 작동하게 되고, 작동된 상기 하이브리드 소듐-이산화탄소 이차전지는 방전 시 음극부에서는 탈소듐화 반응이 일어나고, 양극부에서는 이산화탄소의 환원반응이 일어나 탄소 화합물을 생성할 수 있음을 보여준다.In the hybrid sodium-carbon dioxide secondary battery , the secondary battery operates while flowing carbon dioxide (CO 2 ) gas to the aqueous electrolyte of the positive electrode part, and the operated hybrid sodium-carbon dioxide secondary battery causes a desodium reaction in the negative electrode part during discharge. , shows that the reduction reaction of carbon dioxide occurs in the anode part to produce carbon compounds.
상기 금속-탄소 복합체 촉매는 이산화탄소의 환원반응에 대한 활성 및 선택도가 우수하여 방전 시 생산되는 탄소 화합물의 수율을 향상시킬 수 있다. 상기 금속-탄소 복합체 촉매는 탄소지지체 상에 금속 나노입자가 1:9 내지 9:1 중량비, 바람직하게는 3:7 내지 7:3 중량비, 보다 바람직하게는 4:6 내지 6:4 중량비, 가장 바람직하게는 5:5 중량비로 결착된 것일 수 있다. 이때, 상기 금속 나노입자의 함량이 상기 탄소지지체 대비 1 중량비 미만이면 이산화탄소의 환원반응 활성을 저하시켜 탄소 화합물의 수율이 떨어질 수 있다. 반대로 상기 금속 나노입자의 함량이 9 중량비 초과이면 더 이상의 향상된 촉매 효율을 기대할 수 없으며, 이산화탄소의 환원반응에 대한 선택도가 저하될 수 있다.The metal-carbon composite catalyst has excellent activity and selectivity for the reduction reaction of carbon dioxide, thereby improving the yield of carbon compounds produced during discharge. The metal-carbon composite catalyst contains metal nanoparticles on the carbon support in a weight ratio of 1:9 to 9:1, preferably 3:7 to 7:3 by weight, more preferably 4:6 to 6:4 by weight, most Preferably, it may be bound in a weight ratio of 5:5. At this time, if the content of the metal nanoparticles is less than 1 weight ratio relative to the carbon support, the reduction reaction activity of carbon dioxide may be reduced, and thus the yield of the carbon compound may be reduced. Conversely, if the content of the metal nanoparticles exceeds 9 weight ratio, further improved catalytic efficiency cannot be expected, and the selectivity for the reduction reaction of carbon dioxide may be reduced.
상기 탄소지지체는 카본블랙, 케첸블랙, 아세틸렌블랙, 흑연, 탄소나노튜브, 탄소나노섬유, 산화그래핀 및 환원된 산화그래핀 중에서 선택된 1종 이상일 수 있다. 바람직하게는 상기 탄소지지체는 카본블랙, 케첸블랙 및 아세틸렌블랙 중에서 선택된 1종 이상일 수 있고, 가장 바람직하게는 카본블랙일 수 있다.The carbon support may be at least one selected from carbon black, Ketjen black, acetylene black, graphite, carbon nanotubes, carbon nanofibers, graphene oxide and reduced graphene oxide. Preferably, the carbon support may be at least one selected from carbon black, ketjen black and acetylene black, and most preferably carbon black.
상기 금속 나노입자는 직경이 1~30 nm이고, 금, 은, 구리 및 주석 중에서 선택되는 1종 이상일 수 있다. 바람직하게는 상기 금속 나노입자는 직경이 5~12 nm이고, 금, 주석 또는 이들의 혼합물일 수 있고, 가장 바람직하게는 상기 금속 나노입자는 직경이 7~8 nm인 금일 수 있다.The metal nanoparticles may have a diameter of 1 to 30 nm, and may be at least one selected from gold, silver, copper, and tin. Preferably, the metal nanoparticles have a diameter of 5 to 12 nm, and may be gold, tin, or a mixture thereof, and most preferably, the metal nanoparticles may be gold having a diameter of 7 to 8 nm.
상기 수계 전해질은 탄산수소소듐(NaHCO3), 수산화소듐(NaOH), 황산소듐(Na2SO4), 질산소듐(NaNO3), 염화소듐(NaCl) 및 탄산소듐(Na2CO3) 중에서 선택되는 1종 이상일 수 있다. 바람직하게는 상기 수계 전해질은 탄산수소소듐(NaHCO3), 수산화소듐(NaOH) 또는 이들의 혼합물일 수 있고, 가장 바람직하게는 탄산수소소듐(NaHCO3)일 수 있다. 상기 탄산수소소듐(NaHCO3)은 다른 수계 전해질에 비해 물에서 이온화가 잘 이루어져 이산화탄소와의 환원반응을 향상시킬 수 있다. 상기 수계 전해질은 충전 시 하기 반응식 2에서 생성된 물에 녹아 전해액 상태로 양극부에 존재할 수 있다. The aqueous electrolyte is selected from sodium hydrogen carbonate (NaHCO 3 ), sodium hydroxide (NaOH), sodium sulfate (Na 2 SO 4 ), sodium nitrate (NaNO 3 ), sodium chloride (NaCl) and sodium carbonate (Na 2 CO 3 ) There may be more than one type. Preferably, the aqueous electrolyte may be sodium hydrogen carbonate (NaHCO 3 ), sodium hydroxide (NaOH), or a mixture thereof, and most preferably sodium hydrogen carbonate (NaHCO 3 ). The sodium bicarbonate (NaHCO 3 ) is better ionized in water compared to other aqueous electrolytes, thereby improving the reduction reaction with carbon dioxide. The aqueous electrolyte may be dissolved in the water generated in
상기 양극의 수계 전해질 내에 이산화탄소를 주입하여 상기 하이브리드 소듐-이산화탄소 이차전지를 작동시킬 수 있다. 상기 이산화탄소의 주입에 의해 상기 하이브리드 소듐-이산화탄소 이차전지는 충전시 음극부에서는 하기 반응식 1과 같은 소듐화(sodiation) 반응이 일어나고, 양극부에서는 하기 반응식 2와 같은 산소발생반응(OER)이 일어날 수 있다. Carbon dioxide may be injected into the aqueous electrolyte of the positive electrode to operate the hybrid sodium-carbon dioxide secondary battery. When the hybrid sodium-carbon dioxide secondary battery is charged by the injection of carbon dioxide, a sodiumization reaction as shown in
[반응식 1][Scheme 1]
Na+ + e- → NaNa + + e - → Na
[반응식 2][Scheme 2]
4OH- → O2 + 2H2O + 4e- 4OH - → O 2 + 2H 2 O + 4e -
상기 하이브리드 소듐-이산화탄소 이차전지는 방전시 음극부에서는 하기 반응식 3과 같은 탈소듐화(desodiation) 반응이 일어나고, 양극부에서는 하기 반응식 4 내지 반응식 7 중에서 선택된 하나 이상의 이산화탄소 환원반응(CO2RR)이 일어날 수 있다.When the hybrid sodium-carbon dioxide secondary battery is discharged, a desodium reaction as shown in
[반응식 3][Scheme 3]
Na → Na+ + e- Na → Na + + e -
[반응식 4][Scheme 4]
CO2 + 2H+ + 2e- → CO + H2OCO 2 + 2H + + 2e - → CO + H 2 O
[반응식 5][Scheme 5]
CO2 + 2H+ + 2e- → HCOOHCO 2 + 2H + + 2e - → HCOOH
[반응식 6][Scheme 6]
2CO2 + 12H+ + 12e- → C2H4 + 4H2O2CO 2 + 12H + + 12e - → C 2 H 4 + 4H 2 O
[반응식 7][Scheme 7]
2CO2 + 12H+ + 12e- → C2H5OH + 3H2O2CO 2 + 12H + + 12e - → C 2 H 5 OH + 3H 2 O
특히 방전 시 상기 양극부에서는 상기 반응식 2를 통해 생성된 물과 자발적인 화학반응을 통해 하기 반응식 8과 같이 수소 양이온(H+)과 중탄산염(HCO3 -)이 생성될 수 있다. 생성된 수소 양이온(H+)은 상기 반응식 4 내지 반응식 7과 같이 이산화탄소 및 전자와 반응하여 탄소 생성물 또는 물을 생성할 수 있다. In particular, during discharge, hydrogen cations (H + ) and bicarbonate (HCO 3 − ) may be generated in the anode part through a spontaneous chemical reaction with water generated through
또한 방전 시 상기 양극부는 하기 반응식 9와 같이 일부는 수소가 생성되기도 하나, 1 내지 3 mA의 전류 범위에서 충방전을 수행함으로써 생성된 수소의 함량이 극히 낮다.In addition, during discharging, some of the hydrogen is generated as shown in Scheme 9 below, but the content of hydrogen generated by charging and discharging in a current range of 1 to 3 mA is extremely low.
[반응식 8][Scheme 8]
H2O(l) + CO2(g) → H+(aq) + HCO3 -(aq)H 2 O(l) + CO 2 (g) → H + (aq) + HCO 3 - (aq)
[반응식 9][Scheme 9]
2H++(aq) + 2e- → H2(g)2H + +(aq) + 2e - → H 2 (g)
이처럼 상기 이산화탄소 환원반응에 의해 일산화탄소(CO), 포름산(HCOOH), 에틸렌(C2H4) 및 에탄올(C2H5OH) 중에서 선택되는 1종 이상의 탄소 화합물이 생성될 수 있고, 바람직하게는 일산화탄소(CO) 또는 포름산(HCOOH) 중에서 선택되는 1종 이상일 수 있고, 가장 바람직하게는 일산화탄소(CO)일 수 있다.As such, one or more carbon compounds selected from carbon monoxide (CO), formic acid (HCOOH), ethylene (C 2 H 4 ) and ethanol (C 2 H 5 OH) may be produced by the carbon dioxide reduction reaction, preferably It may be at least one selected from carbon monoxide (CO) or formic acid (HCOOH), and most preferably carbon monoxide (CO).
하기 표 1은 상기 하이브리드 소듐-이산화탄소 이차전지의 작동(충방전) 메커니즘을 나타낸 것이다.Table 1 below shows the operation (charge/discharge) mechanism of the hybrid sodium-carbon dioxide secondary battery.
상기 표 1을 참조하면, 충전 시에 음극부에서는 소듐화(sodiation) 반응, 양극부에서는 OER 반응이 일어나게 되고, 방전 시에는 음극부에서는 탈소듐화(desodiation) 반응, 양극부에서는 고부가가치 화합물을 생산할 수 있는 CO2RR 반응이 일어나는 것을 보여준다. 이때, 충전 시 이론 3.5 V이고, 방전 시 생산물이 일산화탄소(CO)일 경우 이론 전압은 2.19 V가 된다. 또한 방전 시 생산물이 포름산(HCOOH)일 경우 이론 전압은 2.1 V가 된다. Referring to Table 1, during charging, a sodiumization reaction occurs in the negative electrode portion and an OER reaction occurs in the positive electrode portion, and during discharging, a desodium reaction occurs in the negative electrode portion and a high value-added compound is produced in the positive electrode portion. It shows that a CO 2 RR reaction that can produce occurs. At this time, when charging, the theoretical voltage is 3.5 V, and when discharging, when the product is carbon monoxide (CO), the theoretical voltage becomes 2.19 V. Also, when the product is formic acid (HCOOH) during discharge, the theoretical voltage becomes 2.1 V.
특히, 하기 실시예 또는 비교예 등에는 명시적으로 기재하지는 않았지만, 본 발명에 따른 하이브리드 소듐-이산화탄소 이차전지에 있어서, 상기 금속-탄소 복합체 촉매의 구성성분 및 그 혼합비, 수계 전해질의 종류, 이산화탄소의 주입 조건을 달리하여 제조된 하이브리드 소듐-이산화탄소 이차전지를 이용하여 300회 충방전을 실시하였다.In particular, although not explicitly described in the following Examples or Comparative Examples, in the hybrid sodium-carbon dioxide secondary battery according to the present invention, the components of the metal-carbon composite catalyst and its mixing ratio, the type of the aqueous electrolyte, and the amount of carbon dioxide A hybrid sodium-carbon dioxide secondary battery prepared under different injection conditions was charged and discharged 300 times.
그 결과, 다른 조건 및 다른 수치 범위에서와는 달리, 아래 조건을 모두 만족하였을 때 300회 충방전 후에도 음극부 또는 양극부가 소실되지 않아 전지의 수명이 우수함을 확인하였고, 이산화탄소의 탄소 화합물을 높은 패러데이 효율로 회수하였다. As a result, unlike other conditions and other numerical ranges, when all of the following conditions were satisfied, the battery life was excellent because the negative electrode or positive electrode did not disappear even after 300 charge/discharge cycles. recovered.
① 상기 금속-탄소 복합체 촉매는 탄소지지체 상에 금속 나노입자가 4:6 내지 6:4 중량비로 결착된 것이고, ② 상기 탄소지지체는 카본블랙, 케첸블랙 및 아세틸렌블랙 중에서 선택된 1종 이상이고, ③ 상기 금속 나노입자는 직경이 5~12 nm이며, 금, 주석 또는 이들의 혼합물이고, ④ 상기 수계 전해질은 탄산수소소듐(NaHCO3), 수산화소듐(NaOH) 또는 이들의 혼합물이고, ⑤ 상기 양극의 수계 전해질 내에 이산화탄소를 주입하여 상기 하이브리드 소듐-이산화탄소 이차전지를 작동시키는 것이고, ⑥ 상기 하이브리드 소듐-이산화탄소 이차전지는 충전시 음극부에서는 하기 반응식 1과 같은 소듐화(sodiation) 반응이 일어나고, 양극부에서는 하기 반응식 2와 같은 산소발생반응(OER)이 일어나는 것이고,① the metal-carbon composite catalyst is one in which metal nanoparticles are bound on a carbon support in a weight ratio of 4:6 to 6:4, ② the carbon support is at least one selected from carbon black, ketjen black, and acetylene black, ③ The metal nanoparticles have a diameter of 5 to 12 nm, gold, tin, or a mixture thereof, ④ the aqueous electrolyte is sodium hydrogen carbonate (NaHCO 3 ), sodium hydroxide (NaOH) or a mixture thereof, ⑤ of the positive electrode The hybrid sodium-carbon dioxide secondary battery is operated by injecting carbon dioxide into the aqueous electrolyte, and ⑥ the hybrid sodium-carbon dioxide secondary battery undergoes a sodiumization reaction as shown in the following
[반응식 1][Scheme 1]
Na+ + e- → NaNa + + e - → Na
[반응식 2][Scheme 2]
4OH- → O2 + 2H2O + 4e- 4OH - → O 2 + 2H 2 O + 4e -
⑦ 상기 하이브리드 소듐-이산화탄소 이차전지는 방전시 음극부에서는 하기 반응식 3과 같은 탈소듐화(desodiation) 반응이 일어나고, 양극부에서는 하기 반응식 4 또는 반응식 5 중에서 선택된 하나 이상의 이산화탄소 환원반응(CO2RR)이 일어나는 것이고,⑦ When the hybrid sodium-carbon dioxide secondary battery is discharged, a desodium reaction as shown in
[반응식 3][Scheme 3]
Na → Na+ + e- Na → Na + + e -
[반응식 4][Scheme 4]
CO2 + 2H+ + 2e- → CO + H2OCO 2 + 2H + + 2e - → CO + H 2 O
[반응식 5][Scheme 5]
CO2 + 2H+ + 2e- → HCOOHCO 2 + 2H + + 2e - → HCOOH
⑧ 상기 이산화탄소 환원반응에 의해 일산화탄소(CO) 또는 포름산(HCOOH) 중에서 선택되는 1종 이상의 탄소 화합물이 생성될 수 있다.⑧ One or more carbon compounds selected from carbon monoxide (CO) or formic acid (HCOOH) may be produced by the carbon dioxide reduction reaction.
다만, 상기 8가지 조건 중 어느 하나라도 충족되지 않는 경우에는 충방전 효율의 감소로 전지의 수명이 저하되었고, 방전 시 이산화탄소 환원반응에 의한 탄소 화합물이 제대로 생성되지 않거나, 반응이 충분히 일어나지 않아 생성된 탄소 화합물의 함량이 극히 소량이었다.However, if any one of the above eight conditions is not satisfied, the lifespan of the battery is reduced due to a decrease in the charging and discharging efficiency, and the carbon compound due to the carbon dioxide reduction reaction during discharge is not properly generated or the reaction does not occur sufficiently. The content of the carbon compound was very small.
특히, 하기 실시예 또는 비교예 등에는 명시적으로 기재하지는 않았지만, 본 발명에 따른 하이브리드 소듐-이산화탄소 이차전지에 있어서, 보다 바람직한 아래 조건들을 모두 만족하는 하이브리드 소듐-이산화탄소 이차전지를 제조하여 상온에서 200 시간 동안 충방전을 실시하였다.In particular, although not explicitly described in the following Examples or Comparative Examples, in the hybrid sodium-carbon dioxide secondary battery according to the present invention, a hybrid sodium-carbon dioxide secondary battery satisfying all of the following more preferable conditions was prepared and 200 at room temperature Charging and discharging was carried out for a period of time.
그 결과, 다른 조건 및 다른 수치 범위에서와는 달리, 아래 조건을 모두 만족하였을 때 전기에너지의 발생량이 현저하게 증가함과 동시에 이산화탄소의 탄소 화합물 생성량도 증가하였다. As a result, unlike in other conditions and in other numerical ranges, when all of the following conditions were satisfied, the amount of electrical energy generated remarkably increased and the amount of carbon compound production of carbon dioxide also increased.
① 상기 금속-탄소 복합체 촉매는 탄소지지체 상에 금속 나노입자가 5:5 중량비로 결착된 것이고, ② 상기 탄소지지체는 카본블랙이고, ③ 상기 금속 나노입자는 직경이 7~8 nm인 금이고, ④ 상기 수계 전해질은 탄산수소소듐(NaHCO3)이고, ⑤ 상기 양극의 수계 전해질 내에 이산화탄소를 주입하여 상기 하이브리드 소듐-이산화탄소 이차전지를 작동시키는 것이고, ⑥ 상기 하이브리드 소듐-이산화탄소 이차전지는 충전시 음극부에서는 하기 반응식 1과 같은 소듐화(sodiation) 반응이 일어나고, 양극부에서는 하기 반응식 2와 같은 산소발생반응(OER)이 일어나는 것이고,① The metal-carbon composite catalyst is a carbon support in which metal nanoparticles are bound in a 5:5 weight ratio, ② the carbon support is carbon black, ③ the metal nanoparticles are gold having a diameter of 7-8 nm, ④ The aqueous electrolyte is sodium hydrogen carbonate (NaHCO 3 ), ⑤ carbon dioxide is injected into the aqueous electrolyte of the positive electrode to operate the hybrid sodium-carbon dioxide secondary battery, ⑥ the hybrid sodium-carbon dioxide secondary battery is a negative electrode part when charging In the
[반응식 1][Scheme 1]
Na+ + e- → NaNa + + e - → Na
[반응식 2][Scheme 2]
4OH- → O2 + 2H2O + 4e- 4OH - → O 2 + 2H 2 O + 4e -
⑦ 상기 하이브리드 소듐-이산화탄소 이차전지는 방전시 음극부에서는 하기 반응식 3과 같은 탈소듐화(desodiation) 반응이 일어나고, 양극부에서는 하기 반응식 4와 같은 이산화탄소 환원반응(CO2RR)이 일어나는 것이고,⑦ When the hybrid sodium-carbon dioxide secondary battery is discharged, a desodiation reaction as shown in
[반응식 3][Scheme 3]
Na → Na+ + e- Na → Na + + e -
[반응식 4][Scheme 4]
CO2 + 2H+ + 2e- → CO + H2OCO 2 + 2H + + 2e - → CO + H 2 O
⑧ 상기 이산화탄소 환원반응에 의해 일산화탄소(CO)의 탄소 화합물이 생성될 수 있다.⑧ A carbon compound of carbon monoxide (CO) may be produced by the carbon dioxide reduction reaction.
다만, 상기 8가지 조건 중 어느 하나라도 충족되지 않는 경우에는 전기에너지 및 이산화탄소의 탄소 화합물 생성량이 낮았으며, 장시간의 충방전으로 인해 전극이 소실되어 전지의 수명이 저하되었다.However, when any one of the above eight conditions was not satisfied, the amount of carbon compound production of electric energy and carbon dioxide was low, and the electrode was lost due to long-time charging and discharging, thereby reducing the lifespan of the battery.
한편, 본 발명은 상기 하이브리드 소듐-이산화탄소 이차전지를 포함하는 이차전지 복합시스템을 제공한다.On the other hand, the present invention provides a secondary battery composite system including the hybrid sodium-carbon dioxide secondary battery.
상기 하이브리드 소듐-이산화탄소 이차전지에 이산화탄소를 공급하는 이산화탄소 공급부; 상기 하이브리드 소듐-이산화탄소 이차전지로부터 생성된 전기에너지를 저장하는 에너지 저장 시스템(energy storage system, ESS); 및 상기 하이브리드 소듐-이산화탄소 이차전지로부터 생성된 이산화탄소의 탄소 화합물을 저장하는 반응 생성물 저장부;를 더 포함할 수 있다.a carbon dioxide supply unit for supplying carbon dioxide to the hybrid sodium-carbon dioxide secondary battery; an energy storage system (ESS) for storing electric energy generated from the hybrid sodium-carbon dioxide secondary battery; and a reaction product storage unit for storing a carbon compound of carbon dioxide generated from the hybrid sodium-carbon dioxide secondary battery.
상기 에너지 저장 시스템은 전기에너지를 저장하였다가 필요에 따라 상기 하이브리드 소듐-이산화탄소 이차전지로 전기에너지를 공급하는 역할을 하여 에너지를 효율적으로 사용할 수 있다.The energy storage system stores electrical energy and, if necessary, serves to supply electrical energy to the hybrid sodium-carbon dioxide secondary battery to efficiently use energy.
상기 이차전지 복합시스템은 상기 하이브리드 소듐-이산화탄소 이차전지로부터 생성된 수소를 저장하는 수소 저장부와 상기 수소 저장부로부터 수소를 공급받는 연료전지를 더 포함할 수 있다.The secondary battery complex system may further include a hydrogen storage unit for storing hydrogen generated from the hybrid sodium-carbon dioxide secondary battery and a fuel cell receiving hydrogen from the hydrogen storage unit.
기존의 CO2RR 이차전지 시스템은 전기에너지를 소비만 해서 고부가가치의 생성물을 얻을 수 있는 구조였으나, 본 발명의 이차전지 복합시스템은 상기 하이브리드 소듐-이산화탄소 이차전지의 충방전에 의해 발생한 전기에너지를 에너지 저장 시스템에 저장함으로써 에너지를 유연하게 저장 및 변환하여 효율적으로 사용할 수 있다. 뿐만 아니라 이산화탄소의 환원반응에 의해 생성되는 다양한 고부가가치의 탄소 화합물을 수득할 수 있다.The conventional CO 2 RR secondary battery system has a structure that can obtain a high value-added product only by consuming electrical energy, but the secondary battery composite system of the present invention provides the electric energy generated by the charging and discharging of the hybrid sodium-carbon dioxide secondary battery. By storing it in an energy storage system, energy can be stored and converted flexibly and used efficiently. In addition, it is possible to obtain various high value-added carbon compounds produced by the reduction reaction of carbon dioxide.
또한, 본 발명은 음극(anode)부; 양극(cathode)부; 및 상기 음극부와 양극부 사이에 위치하는 고체 전해질;을 포함하는 상기 하이브리드 소듐-이산화탄소 이차전지를 이용하여 이산화탄소의 탄소 화합물을 제조하는 방법에 있어서, (a) 상기 양극부에 수계 전해질을 공급하는 단계; (b) 상기 수계 전해질이 공급된 양극부에 이산화탄소를 공급하는 단계; 및 (c) 상기 양극부 및 음극부 사이에 전류를 인가하여 상기 양극부에서 수소 이온(H+)을 형성시키고, 상기 수소 이온(H+)이 이산화탄소를 환원시켜 이산화탄소의 탄소 화합물을 생성시키는 단계;를 포함하는 이산화탄소의 탄소 화합물을 제조하는 방법을 제공한다.In addition, the present invention is a cathode (anode) portion; anode (cathode) part; and a solid electrolyte positioned between the negative electrode and the positive electrode; in the hybrid sodium-carbon dioxide secondary battery comprising: (a) supplying an aqueous electrolyte to the positive electrode in the method for producing a carbon compound of carbon dioxide step; (b) supplying carbon dioxide to the anode part to which the aqueous electrolyte is supplied; and (c) applying a current between the anode part and the cathode part to form hydrogen ions (H + ) in the anode part, and the hydrogen ions (H + ) reduce carbon dioxide to produce a carbon compound of carbon dioxide It provides a method for producing a carbon compound of carbon dioxide containing;
상기 (c) 단계는 상기 양극부 및 음극부 사이에 1 내지 3 mA, 바람직하게는 2 내지 3 mA, 가장 바람직하게는 2.4 내지 3 mA의 전류를 인가하는 것일 수 있다. 이때, 상기 전류의 세기가 1 mA 미만이면 탄소 화합물 생성량이 수소 생성량에 비해 상대적으로 현저하게 저하될 수 있고, 반대로 3 mA 초과이면 높은 전류로 인해 양극 또는 음극에서 전극의 열화가 발생할 수 있다.In step (c), a current of 1 to 3 mA, preferably 2 to 3 mA, and most preferably 2.4 to 3 mA may be applied between the anode part and the cathode part. At this time, if the intensity of the current is less than 1 mA, the amount of carbon compound produced may be significantly reduced relative to the amount of hydrogen produced, and if it is greater than 3 mA, deterioration of the electrode may occur at the anode or the cathode due to the high current.
상기 이산화탄소의 탄소 화합물은 일산화탄소(CO), 포름산(HCOOH), 에틸렌(C2H4) 및 에탄올(C2H5OH) 중에서 선택되는 1종 이상일 수 있고, 바람직하게는 일산화탄소(CO) 또는 포름산(HCOOH) 중에서 선택되는 1종 이상일 수 있고, 가장 바람직하게는 일산화탄소(CO)일 수 있다.The carbon compound of carbon dioxide may be at least one selected from carbon monoxide (CO), formic acid (HCOOH), ethylene (C 2 H 4 ) and ethanol (C 2 H 5 OH), preferably carbon monoxide (CO) or formic acid (HCOOH) may be at least one selected from, most preferably carbon monoxide (CO).
상기 (c) 단계에서 생성되는 이산화탄소의 탄소 화합물은 1 내지 3 mA의 전류에서 55% 이상의 패러데이 효율(faradaic efficiency)로 생성될 수 있다. 바람직하게는 상기 탄소 화합물은 2 내지 3 mA에서 69% 이상, 가장 바람직하게는 2.4 내지 3 mA에서 77% 이상의 패러데이 효율로 생성될 수 있다.The carbon compound of carbon dioxide produced in step (c) may be produced with a faradaic efficiency of 55% or more at a current of 1 to 3 mA. Preferably, the carbon compound can be produced with a Faraday efficiency of at least 69% at 2 to 3 mA, and most preferably at least 77% at 2.4 to 3 mA.
이상과 같이, 본 발명의 하이브리드 소듐-이산화탄소 이차전지는 음극에는 소듐 금속과 유기 전해액을 함유하고, 양극에는 금속-탄소 복합체 촉매와 수계 전해질을 함유한 구성으로 전지를 형성함으로써 방전 시 다양한 종류의 고부가가치 탄소 화합물과 전기에너지를 동시에 얻을 수 있다. 또한 상기 하이브리드 소듐-이산화탄소 이차전지는 양극에 이산화탄소의 환원반응에 대한 활성 및 선택도가 우수한 금속-탄소 복합체 촉매를 함유함으로써 방전 시 생산되는 탄소 화합물의 수율을 향상시킬 수 있다.As described above, in the hybrid sodium-carbon dioxide secondary battery of the present invention, the negative electrode contains sodium metal and an organic electrolyte, and the positive electrode contains a metal-carbon composite catalyst and an aqueous electrolyte. Value-added carbon compounds and electrical energy can be obtained at the same time. In addition, the hybrid sodium-carbon dioxide secondary battery contains a metal-carbon composite catalyst having excellent activity and selectivity for the reduction reaction of carbon dioxide in the positive electrode, thereby improving the yield of carbon compounds produced during discharge.
또한 본 발명의 이차전지 복합시스템은 에너지 저장 시스템과 상기 하이브리드 소듐-이산화탄소 이차전지를 포함함으로써 하나의 장치에서 방전 시 다양한 고부가가치의 탄소 화합물과 전기에너지를 동시에 얻을 수 있고, 생산된 전기에너지는 유연하게 저장 및 변환하여 에너지의 효율적 사용이 가능한 이점이 있다. In addition, the secondary battery composite system of the present invention includes an energy storage system and the hybrid sodium-carbon dioxide secondary battery, so that various high-value-added carbon compounds and electrical energy can be simultaneously obtained during discharging in one device, and the produced electrical energy is flexible It has the advantage of being able to efficiently use energy by storing and converting it.
이하 본 발명을 실시예에 의거하여 더욱 구체적으로 설명하겠는 바, 본 발명이 다음 실시예에 의해 한정되는 것은 아니다.Hereinafter, the present invention will be described in more detail based on examples, but the present invention is not limited by the following examples.
실시예 1 : 일산화탄소의 고부가가치 산물을 얻을 수 있는 하이브리드 소듐-이산화탄소 이차전지 제조Example 1: Preparation of a hybrid sodium-carbon dioxide secondary battery capable of obtaining a high value-added product of carbon monoxide
(1) 음극(anode) 제조(1) Preparation of anode
글러브박스 하에서 coin-type cell을 제작하였다. Na 금속을 제1 집전체에 붙인 후 유기 전해액을 주입시켜 주었다. 그 후 두께가 1 mm이고 직경이 16 mm인 NASICON(고체 전해질)이 붙여져 있는 뚜껑으로 밀봉시켜 주었다.A coin-type cell was produced under a glove box. After attaching the Na metal to the first current collector, an organic electrolyte was injected. Then, it was sealed with a lid attached with NASICON (solid electrolyte) having a thickness of 1 mm and a diameter of 16 mm.
(2) 금 나노입자-탄소지지체 복합체 촉매 제조(2) Preparation of Gold Nanoparticle-Carbon Support Composite Catalyst
본 시스템의 성능을 확인하기 위하여 합성한 gold nanoparticle은 기존의 알려진 문헌대로 합성을 하였다[Zhu, Wenlei, et al. "Monodisperse Au nanoparticles for selective electrocatalytic reduction of CO2 to CO." Journal of the American Chemical Society 135.45 (2013): 16833-16836.]. To confirm the performance of this system, the synthesized gold nanoparticles were synthesized according to the known literature [Zhu, Wenlei, et al. "Monodisperse Au nanoparticles for selective electrocatalytic reduction of CO 2 to CO." Journal of the American Chemical Society 135.45 (2013): 16833-16836.].
그 다음 200 mg HAuCl43H2O를 테트랄린(tetralin) 10 ml에 혼합하여 HAuCl43H2O 용액을 준비하였다. 또한 TBAB 0.5 mmol을 테트랄린 1 ml에 혼합하여 TBAB 용액을 준비하였다. 그 다음 HAuCl43H2O 용액을 ice bath에서 Ar flow와 함께 교반(stirring)을 하면서 TBAB 용액을 넣어준 뒤 1 시간 동안 교반하였다. 그 다음 케첸블랙(Ketjen black)을 헥산(hexane) 25 ml에 분산시키고, 금 나노입자(gold nanoparticle)을 1:1 중량비로 넣어주어 초음파처리(sonication) 하였다. 그 다음헥산(hexane)을 날려준 뒤 box furnace에서 180 ℃, 8 시간 조건으로 열처리를 진행함으로써 탄소지지체 상에 금 나노입자(7~8 nm)가 결착된 금 나노입자-탄소지지체 복합체 촉매를 제작하였다.Then, 200 mg of HAuCl 4 3H 2 O was mixed with 10 ml of tetralin to prepare a HAuCl 4 3H 2 O solution. In addition, 0.5 mmol of TBAB was mixed with 1 ml of tetralin to prepare a TBAB solution. Then , while stirring the HAuCl 4 3H 2 O solution with Ar flow in an ice bath, the TBAB solution was added and stirred for 1 hour. Then, Ketjen black was dispersed in 25 ml of hexane, and gold nanoparticles were added in a 1:1 weight ratio, followed by sonication. Then, after blowing hexane, heat treatment was performed in a box furnace at 180° C. for 8 hours to prepare a gold nanoparticle-carbon support composite catalyst in which gold nanoparticles (7-8 nm) were bound on a carbon support. did.
(3) 양극(cathode) 제조(3) Manufacturing of cathode
촉매 슬러리는 상기 금 나노입자-탄소지지체 복합체 촉매 10mg과 5% Nafion 45 ㎕ 및 IPA 1ml을 투입한 후 30 분 동안 초음파 처리하여 혼합하였다. 제2 집전체인 탄소페이퍼(carbon paper, Toray TGP-H-060)(0.25 cm2) 상에 상기 촉매 슬러리를 드롭-캐스팅(drop casting)(1 mg/cm2)하고 밤새(overnight) 건조시켰다.The catalyst slurry was mixed with 10 mg of the gold nanoparticle-carbon support composite catalyst, 45 μl of 5% Nafion, and 1 ml of IPA, followed by ultrasonication for 30 minutes. The second current collector is a carbon paper (carbon paper, Toray TGP-H -060) (0.25 cm 2) of the catalyst slurry on the drop-casting (drop casting) (1 mg / cm 2) and dried overnight (overnight) .
(4) 하이브리드 소듐-이산화탄소 이차전지 제조(4) Hybrid sodium-carbon dioxide secondary battery manufacturing
상기 음극과 양극은 NASICON(고체 전해질)을 사이에 두고 접합하여 하이브리드 소듐-이산화탄소 이차전지를 제조하였다. The negative electrode and the positive electrode were bonded with a NASICON (solid electrolyte) interposed therebetween to prepare a hybrid sodium-carbon dioxide secondary battery.
실시예 2 : 일산화탄소 및 포름산의 고부가가치 산물을 얻을 수 있는 하이브리드 소듐-이산화탄소 이차전지 제조Example 2: Preparation of hybrid sodium-carbon dioxide secondary battery capable of obtaining high value-added products of carbon monoxide and formic acid
양극 제조 시 금속촉매 물질로 금(Au) 나노입자 대신 직경이 7~8 nm인 주석(Sn) 나노입자를 사용한 것을 제외하고, 상기 실시예 1과 동일한 방법으로 하이브리드 소듐-이산화탄소 이차전지를 제조하였다. A hybrid sodium-carbon dioxide secondary battery was prepared in the same manner as in Example 1, except that tin (Sn) nanoparticles having a diameter of 7 to 8 nm were used instead of gold (Au) nanoparticles as a metal catalyst material during the preparation of the positive electrode. .
실험예 1: 상기 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지 충방전 평가Experimental Example 1: Evaluation of charging and discharging of the hybrid sodium-carbon dioxide secondary battery prepared in Example 1
상기 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지를 이용하여 충방전 성능을 평가하였으며, 그 결과는 도 2 내지 5에 나타내었다. Charging and discharging performance was evaluated using the hybrid sodium-carbon dioxide secondary battery prepared in Example 1, and the results are shown in FIGS. 2 to 5 .
상기 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지의 양극에 수계 전해질(0.5 M NaHCO3) 8 ml을 주입시킨 후 CO2 gas flow는 10 ml/min으로 주입시켰다. 이차전지의 성능은 실온에서 battery cycler(WBCS3000, WonAtech)을 사용하여 측정하였고 패러데이 효율(Faradic Efficiency, FE)은 기체 생산물(예컨대, H2, CO)일 경우, FID와 TCD로 구성되어 있는 Gas Chromatograph(GC)(Agilent 7890B)를 이용하여 측정하여 구하였다. 또한 액체 생산물(예컨대, HCOOH)일 경우 FE는 liquid Chromatograph(LC)(YL9100)를 이용하여 측정하였다. FE는 다음과 같은 수학식 1을 통해 구하였다. After injecting 8 ml of an aqueous electrolyte (0.5 M NaHCO 3 ) into the positive electrode of the hybrid sodium-carbon dioxide secondary battery prepared in Example 1, CO 2 gas flow was injected at 10 ml/min. The performance of the secondary battery was measured at room temperature using a battery cycler (WBCS3000, WonAtech), and the Faradic Efficiency (FE) is a Gas Chromatograph composed of FID and TCD in the case of gas products (eg, H 2 , CO). (GC) was determined using (Agilent 7890B). Also, in the case of a liquid product (eg, HCOOH), FE was measured using a liquid chromatography (LC) (YL9100). FE was obtained through
[수학식 1] [Equation 1]
상기 수학식 1에서 N은 CO2가 x로 전환하는데 필요한 전자 수, αx는 GC calibration으로 구해진 conversion factor, F는 Faraday constant, I는 전체 전류, R은 기체상수이다.In
도 2는 상기 실시예 1에서 제조된 금 나노입자-탄소지지체 복합체 촉매의 투과전자현미경(TEM) 이미지이다. 상기 도 2를 참조하면, 탄소지지체인 케첸블랙 상에 직경이 7~8 nm인 금 나노입자들이 고르게 결착되어 있는 것을 확인하였다.FIG. 2 is a transmission electron microscope (TEM) image of the gold nanoparticle-carbon support composite catalyst prepared in Example 1. FIG. Referring to FIG. 2 , it was confirmed that gold nanoparticles having a diameter of 7 to 8 nm were uniformly bound on the carbon support, Ketjen Black.
도 3은 상기 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지에 대하여 전류별로 생성된 일산화탄소(CO) 및 수소(H2)의 패러데이 효율(Faradaic Efficiency)을 나타낸 그래프이다. 상기 도 3을 참조하면, 0.5, 1, 1.5, 2, 2.25, 2.4, 및 2.9 mA의 전류에서 각각 CO 및 H2의 FE(Feradaic efficiency)는 하기 표 2와 같은 결과를 나타내었다.3 is a graph showing the Faradaic Efficiency of carbon monoxide (CO) and hydrogen (H 2 ) generated by current for the hybrid sodium-carbon dioxide secondary battery prepared in Example 1; Referring to FIG. 3, ferdaic efficiencies (FEs) of CO and H 2 at currents of 0.5, 1, 1.5, 2, 2.25, 2.4, and 2.9 mA, respectively, are shown in Table 2 below.
상기 표 2의 결과에 의하면, 전류의 세기가 증가할수록 일산화탄소(CO)의 페러데이 효율이 증가하였고, 이에 따라 상대적으로 수소(H2)의 패러데이 효율을 저하됨을 확인하였다. 특히 전류의 세기가 2.4 및 2.9 mA일 때 일산화탄소(CO)가 79% 이상의 패러데이 효율을 갖는 것을 확인하였다.According to the results of Table 2, as the intensity of the current increased, the Faraday efficiency of carbon monoxide (CO) increased, and thus it was confirmed that the Faraday efficiency of hydrogen (H 2 ) was relatively decreased. In particular, it was confirmed that carbon monoxide (CO) had a Faraday efficiency of 79% or more when the current strength was 2.4 and 2.9 mA.
도 4는 상기 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지의 방전 및 충전 전압 프로파일을 나타낸 그래프이다. 상기 도 4를 참조하면, 전류별로 충방전 전압 프로파일(profile)을 보았을 때 0.5 mA에서 방전 시 전압은 약 2 V, 충전 시 전압은 약 4 V였다. 1.5 mA에서는 방전 전압은 약 1.5 V, 충전 전압은 약 4.5 V 였다. 2 mA에서는 방전 전압은 약 1 V, 충전 전압은 4.8 V였다. 이를 통해 상기 하이브리드 소듐-이산화탄소 이차전지는 충방전 시 1V 이상의 전압을 안정적으로 구현함으로써 효율적인 이차전지 복합시스템으로 운영할 수 있음을 확인하였다.4 is a graph showing the discharge and charge voltage profiles of the hybrid sodium-carbon dioxide secondary battery prepared in Example 1. FIG. Referring to FIG. 4 , when the charging/discharging voltage profile for each current was viewed, the voltage during discharge at 0.5 mA was about 2 V, and the voltage during charging was about 4 V. At 1.5 mA, the discharge voltage was about 1.5 V and the charge voltage was about 4.5 V. At 2 mA, the discharge voltage was about 1 V and the charge voltage was 4.8 V. Through this, it was confirmed that the hybrid sodium-carbon dioxide secondary battery can be operated as an efficient secondary battery composite system by stably realizing a voltage of 1V or more during charging and discharging.
도 5는 상기 실시예 1에서 제조된 하이브리드 소듐-이산화탄소 이차전지에 대하여 1 mA 전류에서의 Galvanostatic 방전-충전 사이클링 곡선을 나타낸 그래프이다. 상기 도 5를 참조하면, 상기 하이브리드 소듐-이산화탄소 이차전지의 cyclability를 확인하기 위해 galvanostatic mode에서 충방전 곡선(curve)을 확인한 결과, 약 30 시간(90 싸이클) 이상 안정적으로 구동되는 것을 확인하였다.5 is a graph showing a galvanostatic discharge-charge cycling curve at a current of 1 mA for the hybrid sodium-carbon dioxide secondary battery prepared in Example 1; Referring to FIG. 5 , as a result of checking a charge/discharge curve in the galvanostatic mode in order to confirm the cyclability of the hybrid sodium-carbon dioxide secondary battery, it was confirmed that the hybrid battery was stably operated for more than about 30 hours (90 cycles).
실험예 2: 상기 실시예 2에서 제조된 하이브리드 소듐-이산화탄소 이차전지의 충방전 평가Experimental Example 2: Evaluation of charging and discharging of the hybrid sodium-carbon dioxide secondary battery prepared in Example 2
상기 실시예 2에서 제조된 하이브리드 소듐-이산화탄소 이차전지를 이용하여 상기 실험예 1과 동일한 방법으로 충방전 성능평가를 실시하였으며, 그 결과는 도 6 및 표 2에 나타내었다. The hybrid sodium-carbon dioxide secondary battery prepared in Example 2 was used for charging and discharging performance evaluation in the same manner as in Experimental Example 1, and the results are shown in FIGS. 6 and 2 .
도 6은 상기 실시예 2에서 제조된 하이브리드 소듐-이산화탄소 이차전지의 전류에 따른 방전전압 그래프(a)와 전류별로 생성된 포름산(HCOOH), 일산화탄소(CO) 및 수소(H2)의 패러데이 효율(Faradaic Efficiency)을 나타낸 그래프(b)이다. 6 is a graph of the discharge voltage according to the current of the hybrid sodium-carbon dioxide secondary battery prepared in Example 2 (a) and the Faraday efficiency of formic acid (HCOOH), carbon monoxide (CO) and hydrogen (H 2 ) Faradaic Efficiency) is a graph (b).
상기 표 3 및 도 6(a)의 경우 전류가 1, 2 및 3 mA에서 방전 전압은 각각 1.2, 0.9 및 0.4V를 나타내었다. 상기 도 6(b)의 경우, 전류가 1, 2, 3 mA에서 일산화탄소(CO) 및 포름산(HCOOH)이 동시에 생성되었으며, 전류의 세기가 증가함에 따라 각 생성물의 패러데이 효율도 증가한 것을 확인하였다. 이를 통해 금속-탄소 복합체 촉매에서 금속 나노입자로 직경이 7~8 nm인 주석 나노입자를 사용함으로써 일산화탄소(CO) 뿐만 아니라 포름산(HCOOH)도 동시에 생산된 것을 확인하였다. In the case of Table 3 and FIG. 6(a), the discharge voltages were 1.2, 0.9, and 0.4V at the currents of 1, 2, and 3 mA, respectively. In the case of FIG. 6(b), it was confirmed that carbon monoxide (CO) and formic acid (HCOOH) were simultaneously generated at a current of 1, 2, and 3 mA, and the Faraday efficiency of each product also increased as the intensity of the current increased. Through this, it was confirmed that carbon monoxide (CO) as well as formic acid (HCOOH) were simultaneously produced by using tin nanoparticles with a diameter of 7 to 8 nm as metal nanoparticles in the metal-carbon composite catalyst.
Claims (17)
제2 집전체, 금속-탄소 복합체 촉매 및 수계 전해질을 함유하는 양극(cathode)부; 및
상기 음극부와 양극부 사이에 위치하는 고체 전해질;
을 포함하고,
상기 금속-탄소 복합체 촉매는 탄소지지체 상에 금속 나노입자가 5:5 중량비로 결착된 것이고,
상기 탄소지지체는 카본블랙이고,
상기 금속 나노입자는 직경이 7~8 nm인 금이고,
상기 수계 전해질은 탄산수소소듐(NaHCO3)이고,
상기 양극의 수계 전해질 내에 이산화탄소를 주입하여 하이브리드 소듐-이산화탄소 이차전지를 작동시키는 것이고,
상기 하이브리드 소듐-이산화탄소 이차전지는 충전시 음극부에서는 하기 반응식 1과 같은 소듐화(sodiation) 반응이 일어나고,
[반응식 1]
Na+ + e- → Na
양극부에서는 하기 반응식 2와 같은 산소발생반응(OER)이 일어나는 것이고,
[반응식 2]
4OH- → O2 + 2H2O + 4e-
상기 하이브리드 소듐-이산화탄소 이차전지는 방전시 음극부에서는 하기 반응식 3과 같은 탈소듐화(desodiation) 반응이 일어나고,
[반응식 3]
Na → Na+ + e-
양극부에서는 하기 반응식 4와 같은 이산화탄소 환원반응(CO2RR)이 일어나는 것이고,
[반응식 4]
CO2 + 2H+ + 2e- → CO + H2O
상기 이산화탄소 환원반응에 의해 일산화탄소(CO)의 탄소 화합물이 생성되는 것을 특징으로 하는 하이브리드 소듐-이산화탄소 이차전지.
a first current collector, an anode portion containing sodium metal and an organic electrolyte;
a second current collector, a metal-carbon composite catalyst, and a cathode containing an aqueous electrolyte; and
a solid electrolyte positioned between the negative electrode and the positive electrode;
including,
The metal-carbon composite catalyst is one in which metal nanoparticles are bound in a weight ratio of 5:5 on a carbon support,
The carbon support is carbon black,
The metal nanoparticles are gold having a diameter of 7 to 8 nm,
The aqueous electrolyte is sodium hydrogen carbonate (NaHCO 3 ),
By injecting carbon dioxide into the aqueous electrolyte of the positive electrode, the hybrid sodium-carbon dioxide secondary battery is operated,
The hybrid sodium-carbon dioxide secondary battery undergoes a sodiumization reaction as shown in Scheme 1 below in the negative electrode part during charging,
[Scheme 1]
Na + + e - → Na
At the anode part, an oxygen evolution reaction (OER) as shown in Reaction Formula 2 below occurs,
[Scheme 2]
4OH - → O 2 + 2H 2 O + 4e -
The hybrid sodium-carbon dioxide secondary battery undergoes a desodium reaction as shown in Reaction Equation 3 below in the negative electrode portion during discharging,
[Scheme 3]
Na → Na + + e -
At the anode part, a carbon dioxide reduction reaction (CO 2 RR) as shown in the following Reaction Formula 4 occurs,
[Scheme 4]
CO 2 + 2H + + 2e - → CO + H 2 O
Hybrid sodium-carbon dioxide secondary battery, characterized in that a carbon compound of carbon monoxide (CO) is generated by the carbon dioxide reduction reaction.
The hybrid sodium-carbon dioxide of claim 1 secondary battery composite system comprising a secondary battery.
상기 하이브리드 소듐-이산화탄소 이차전지에 이산화탄소를 공급하는 이산화탄소 공급부;
상기 하이브리드 소듐-이산화탄소 이차전지로부터 생성된 전기에너지를 저장하는 에너지 저장 시스템(energy storage system, ESS); 및
상기 하이브리드 소듐-이산화탄소 이차전지로부터 생성된 이산화탄소의 탄소 화합물을 저장하는 반응 생성물 저장부;
를 더 포함하는 것을 특징으로 하는 이차전지 복합시스템.
13. The method of claim 12,
a carbon dioxide supply unit for supplying carbon dioxide to the hybrid sodium-carbon dioxide secondary battery;
an energy storage system (ESS) for storing electric energy generated from the hybrid sodium-carbon dioxide secondary battery; and
a reaction product storage unit for storing a carbon compound of carbon dioxide generated from the hybrid sodium-carbon dioxide secondary battery;
Secondary battery composite system, characterized in that it further comprises.
(a) 상기 양극부에 수계 전해질을 공급하는 단계;
(b) 상기 수계 전해질이 공급된 양극부에 이산화탄소를 공급하는 단계; 및
(c) 상기 양극부 및 음극부 사이에 전류를 인가하여 상기 양극부에서 수소 이온(H+)을 형성시키고, 상기 수소 이온(H+)이 이산화탄소를 환원시켜 이산화탄소의 탄소 화합물을 생성시키는 단계;
를 포함하는 이산화탄소의 탄소 화합물을 제조하는 방법.
anode (anode) part; anode (cathode) part; and a solid electrolyte positioned between the negative electrode part and the positive electrode part; in the hybrid sodium-carbon dioxide secondary battery of claim 1 , in a method for producing a carbon compound of carbon dioxide,
(a) supplying an aqueous electrolyte to the anode part;
(b) supplying carbon dioxide to the anode part to which the aqueous electrolyte is supplied; and
(c) applying a current between the anode part and the cathode part to form hydrogen ions (H + ) in the anode part, and the hydrogen ions (H + ) reduce carbon dioxide to produce a carbon compound of carbon dioxide;
A method for producing a carbon compound of carbon dioxide comprising a.
상기 (c) 단계는 상기 양극부 및 음극부 사이에 1 내지 3 mA의 전류를 인가하는 것을 특징으로 하는 이산화탄소의 탄소 화합물을 제조하는 방법.
15. The method of claim 14,
In step (c), a method for producing a carbon compound of carbon dioxide, characterized in that applying a current of 1 to 3 mA between the anode and the cathode.
상기 (c) 단계에서 생성되는 이산화탄소의 탄소 화합물은 1 내지 3 mA의 전류에서 55% 이상의 패러데이 효율(faradaic efficiency)로 생성되는 것을 특징으로 하는 이산화탄소의 탄소 화합물을 제조하는 방법.
15. The method of claim 14,
The method for producing a carbon compound of carbon dioxide, characterized in that the carbon compound of carbon dioxide produced in step (c) is generated with a faradaic efficiency of 55% or more at a current of 1 to 3 mA.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020190118973 | 2019-09-26 | ||
| KR20190118973 | 2019-09-26 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20210036789A KR20210036789A (en) | 2021-04-05 |
| KR102319109B1 true KR102319109B1 (en) | 2021-10-29 |
Family
ID=75461876
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020200050877A Active KR102319109B1 (en) | 2019-09-26 | 2020-04-27 | Hybrid sodium-carbon dioxide secondary battery capable of obtaining energy storage along with high value-added product by electrochemical carbon dioxide reduction and secondary battery system comprising the same |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102319109B1 (en) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102578353B1 (en) * | 2021-05-26 | 2023-09-15 | 울산과학기술원 | Sodium-carbon dioxide battery and its manufacturing method |
| JP7693598B2 (en) * | 2022-03-18 | 2025-06-17 | 株式会社東芝 | Electrode catalyst layer for electrolytic cell, electrode for electrolytic cell, and carbon dioxide electrolysis device |
| CN116154241A (en) * | 2023-02-17 | 2023-05-23 | 中国华能集团清洁能源技术研究院有限公司 | Metal-carbon dioxide battery power system coupled with carbon capture in power plants and method of operation thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009138270A (en) | 1997-05-07 | 2009-06-25 | George A Olah | Recycling of carbon dioxide into methyl alcohol and related oxygenates or hydrocarbons |
| KR101587445B1 (en) | 2014-08-25 | 2016-01-22 | 한국생산기술연구원 | Manufacturing method of a sodium rechargeable battery |
| US20180209054A1 (en) * | 2017-01-23 | 2018-07-26 | The Regents Of The University Of California | Copper nanoparticle structures for reduction of carbon dioxide to multicarbon products |
-
2020
- 2020-04-27 KR KR1020200050877A patent/KR102319109B1/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009138270A (en) | 1997-05-07 | 2009-06-25 | George A Olah | Recycling of carbon dioxide into methyl alcohol and related oxygenates or hydrocarbons |
| KR101587445B1 (en) | 2014-08-25 | 2016-01-22 | 한국생산기술연구원 | Manufacturing method of a sodium rechargeable battery |
| US20180209054A1 (en) * | 2017-01-23 | 2018-07-26 | The Regents Of The University Of California | Copper nanoparticle structures for reduction of carbon dioxide to multicarbon products |
Non-Patent Citations (2)
| Title |
|---|
| Changmin Kim et al. iScience. 2018, Vol. 9, pp. 278-285 |
| Jiafang Xie et al. Accounts of Chemical Research. 2019, Vol. 52, pp. 1721-1729 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20210036789A (en) | 2021-04-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Deng et al. | NiCo-doped CN nano-composites for cathodic catalysts of Zn-air batteries in neutral media | |
| Li et al. | Progress in research on Li–CO2 batteries: mechanism, catalyst and performance | |
| Chen et al. | Three-phases Co/Co9S8/MnS heterostructures engineering for boosted ORR/OER activities in Zn–air batteries | |
| KR102319109B1 (en) | Hybrid sodium-carbon dioxide secondary battery capable of obtaining energy storage along with high value-added product by electrochemical carbon dioxide reduction and secondary battery system comprising the same | |
| KR101197100B1 (en) | Fabrication method of air electrode using a-phase manganese oxide/carbon nanotube composite, and the air electorde thereby | |
| Xu et al. | A novel composite (FMC) to serve as a durable 3D-clam-shaped bifunctional cathode catalyst for both primary and rechargeable zinc-air batteries | |
| CN107565138B (en) | A kind of lithium carbon dioxide anode catalyst Mn2O3Preparation method | |
| Unnikrishnan et al. | Electrocatalytic behavior of carbon quantum dots in sustainable applications: a review | |
| Liu et al. | Carbon nanotube-encapsulated Co/Co3Fe7 heterojunctions as a highly-efficient bifunctional electrocatalyst for rechargeable zinc-air batteries | |
| Han et al. | Hierarchical core–shell heterostructure FeMoS@ CoFe LDH for multifunctional green applications boosting large current density water splitting | |
| Liu et al. | Carbon-based cathodes for sodium-air batteries | |
| CN116314871A (en) | A kind of preparation method of nickel cobalt selenide supported platinum catalyst | |
| Varshoy et al. | The dual capacity of the NiSn alloy/MWCNT nanocomposite for sodium and hydrogen ions storage using porous Cu foam as a current collector | |
| CN1901261A (en) | Novel high performance alkaline fuel cell | |
| CN110034319A (en) | A kind of zinc-water fuel cell and its application in power generation production hydrogen | |
| Dong et al. | Catalyzed carbon-based materials for CO2-battery utilization | |
| Wang et al. | Research status and perspectives of rechargeable Li-CO2 battery | |
| CN118198385A (en) | Oxygen electrocatalytic material and preparation and application thereof | |
| CN105576256A (en) | Nano lithium manganite loaded carbon material cathode catalyst used for oxygen reduction of air electrode as well as preparation method and application of nano lithium manganite loaded carbon material cathode catalyst | |
| CN117638329A (en) | Atomic-level dispersed nickel-based catalyst and preparation method and application thereof | |
| KR101282961B1 (en) | Fabrication method of λ-phase MnO2 electrode for air cathode using electron beam irradiation, and the λ-phase MnO2 electrode for air cathode | |
| Atri et al. | A Review of Water Electrolysis, Fuel Cells and Its Use in Energy Storage | |
| Wang et al. | Metallic cobalt encapsulated in N-doped carbon nanowires: a highly active bifunctional catalyst for oxygen reduction and evolution | |
| JP2002252002A (en) | Fuel cell | |
| CN114784424B (en) | A non-alkaline zinc-air battery based on zinc peroxide cathode |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| U11 | Full renewal or maintenance fee paid |
Free format text: ST27 STATUS EVENT CODE: A-4-4-U10-U11-OTH-PR1001 (AS PROVIDED BY THE NATIONAL OFFICE) Year of fee payment: 5 |