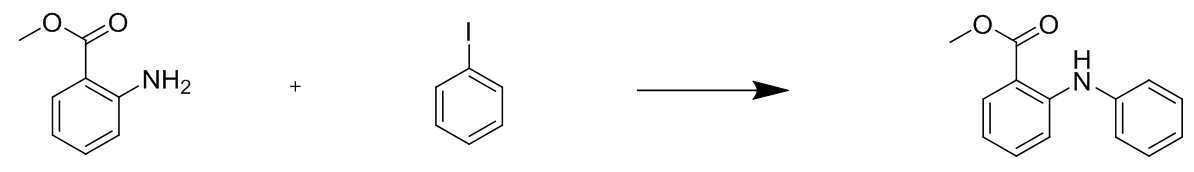KR102215780B1 - Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same - Google Patents
Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same Download PDFInfo
- Publication number
- KR102215780B1 KR102215780B1 KR1020140014005A KR20140014005A KR102215780B1 KR 102215780 B1 KR102215780 B1 KR 102215780B1 KR 1020140014005 A KR1020140014005 A KR 1020140014005A KR 20140014005 A KR20140014005 A KR 20140014005A KR 102215780 B1 KR102215780 B1 KR 102215780B1
- Authority
- KR
- South Korea
- Prior art keywords
- compound
- formula
- group
- substituted
- organic light
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02B—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO BUILDINGS, e.g. HOUSING, HOUSE APPLIANCES OR RELATED END-USER APPLICATIONS
- Y02B20/00—Energy efficient lighting technologies, e.g. halogen lamps or gas discharge lamps
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
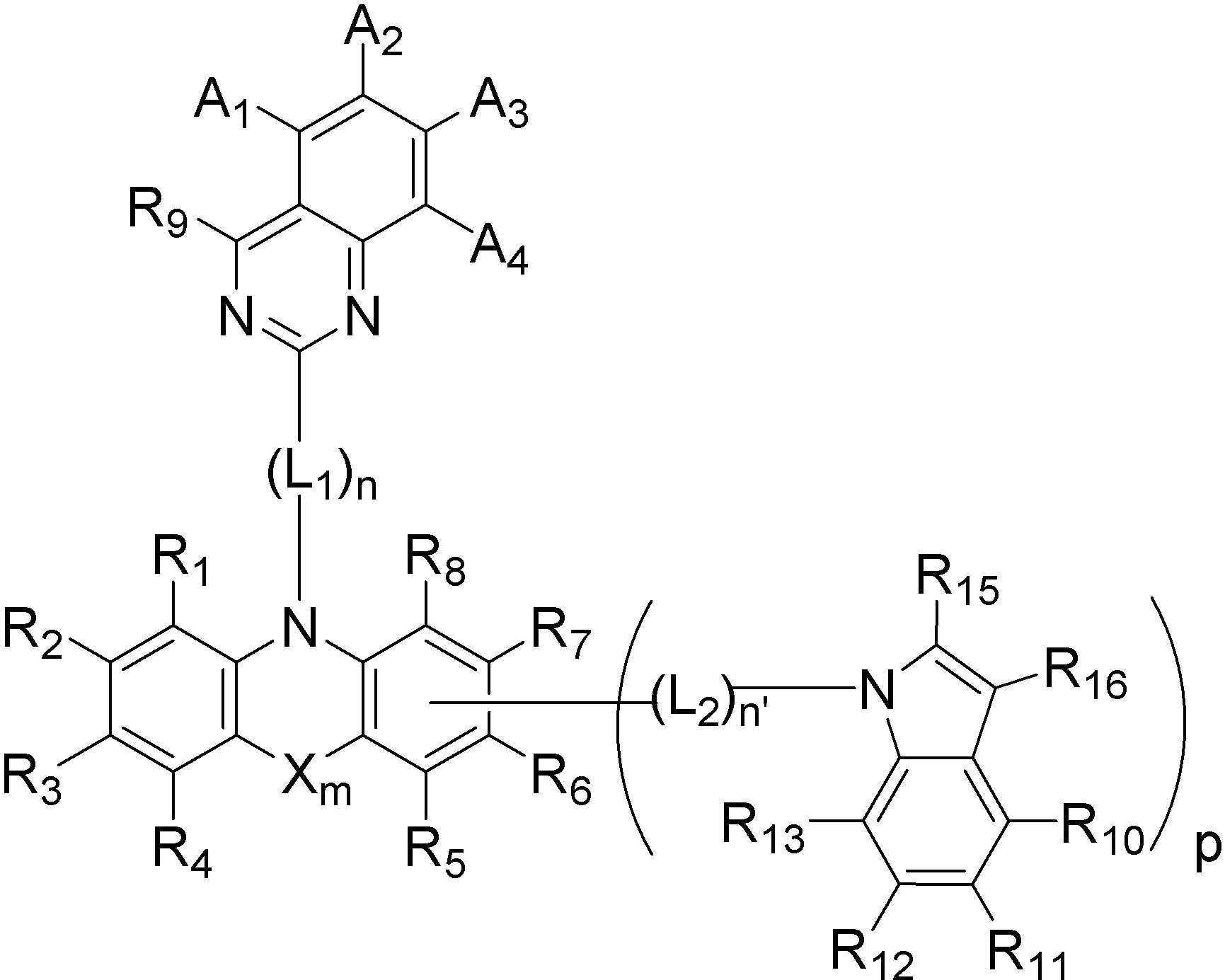
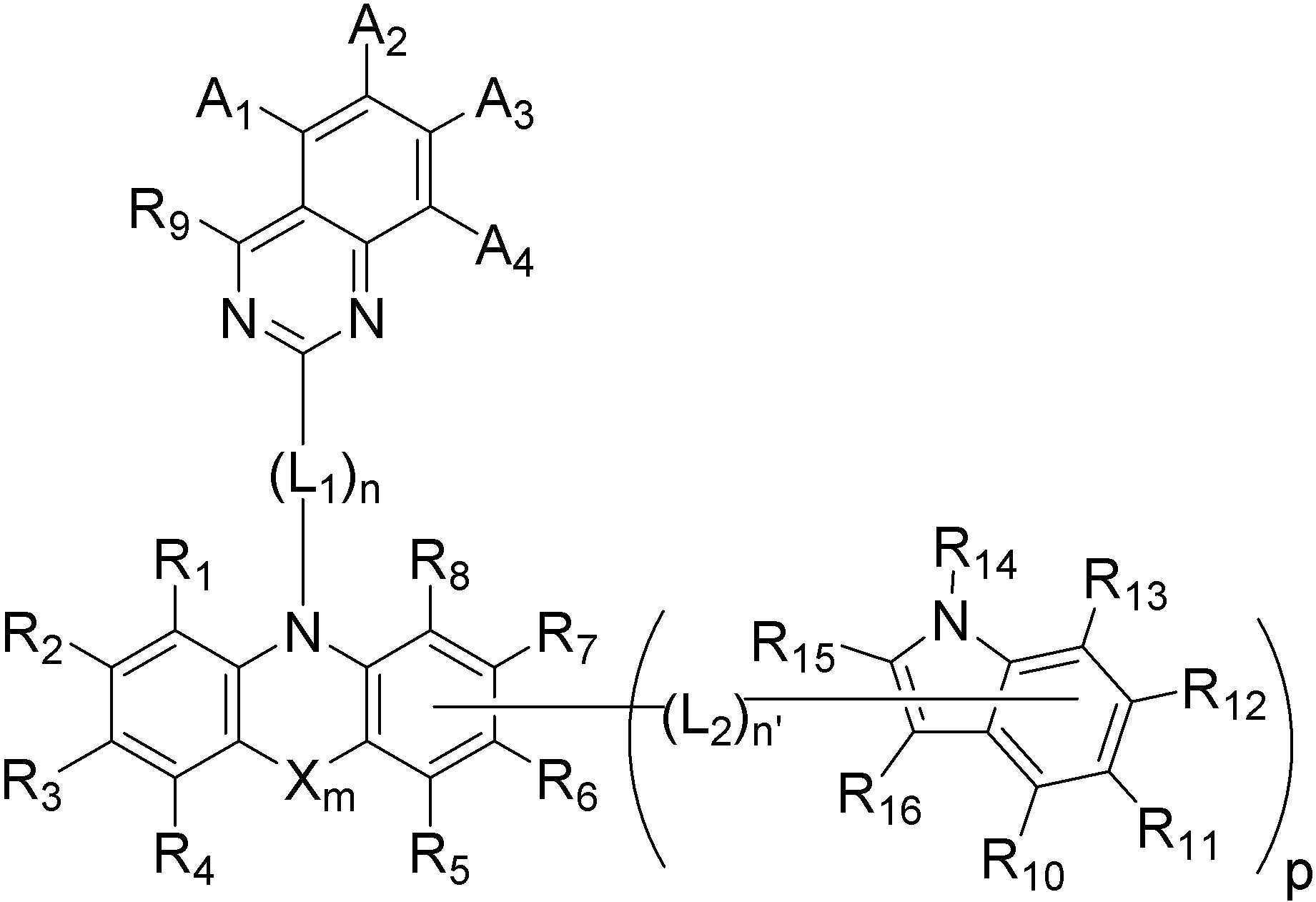
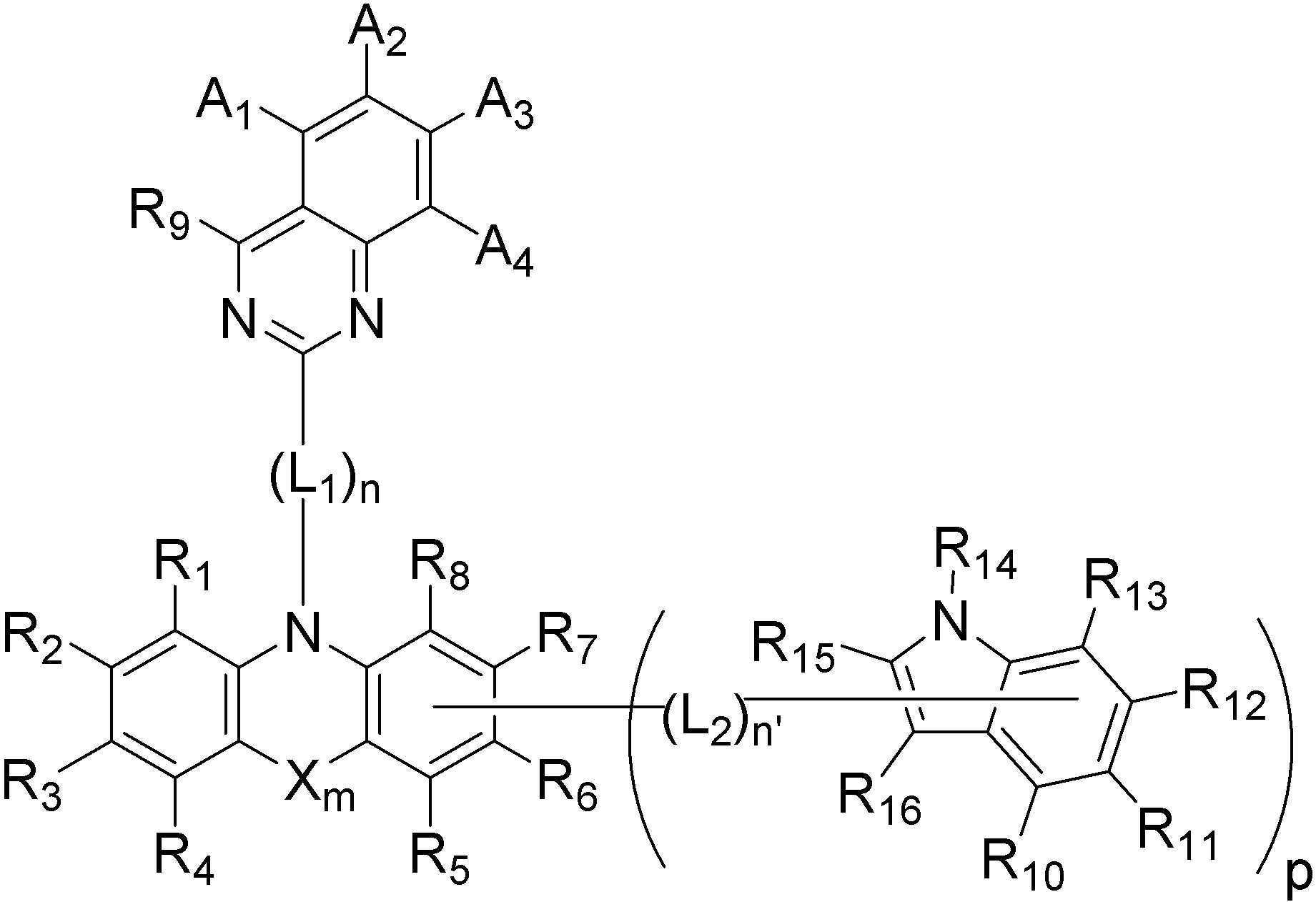
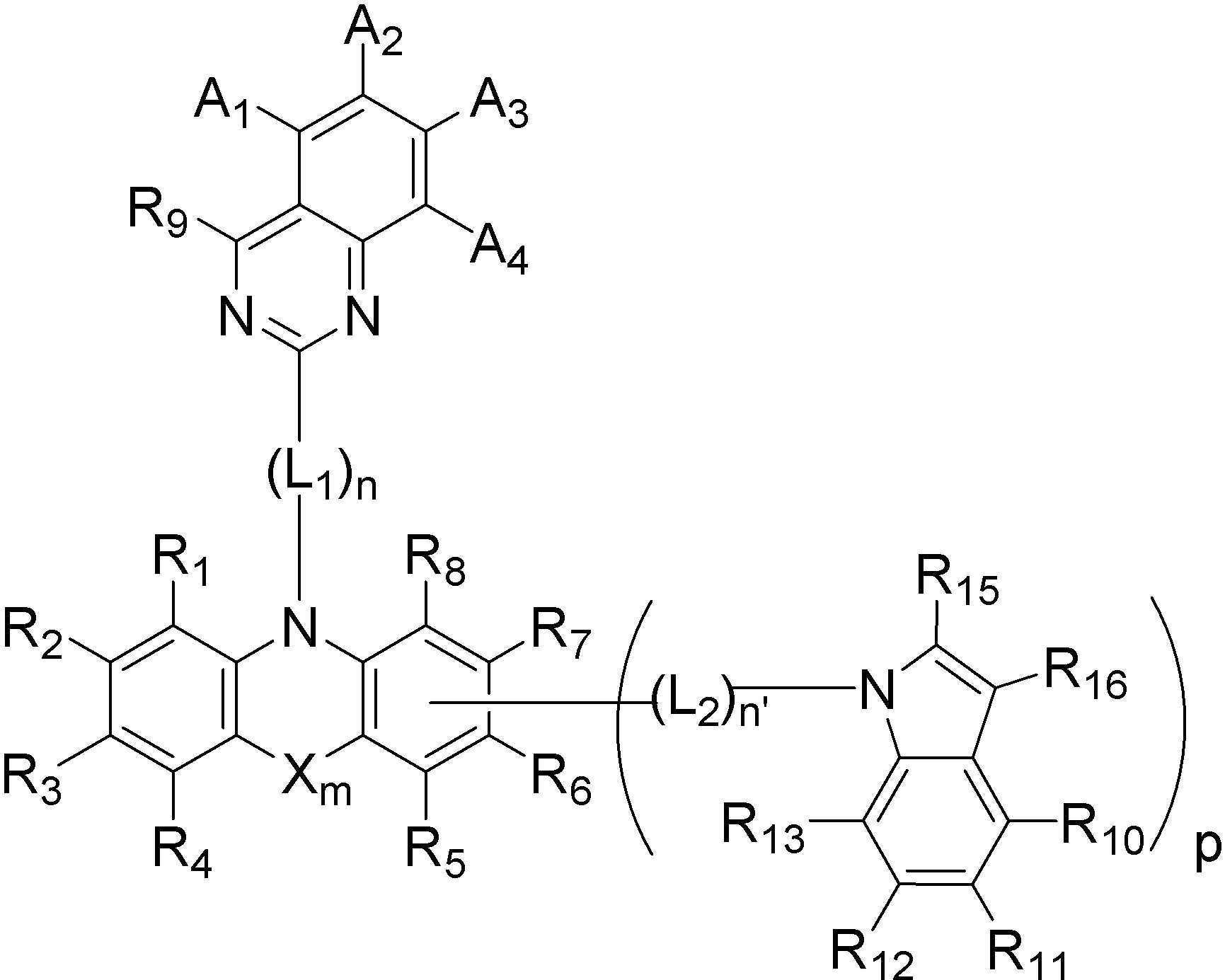
본 발명은 하기 [화학식 A] 또는 [화학식 B] 로 표시되는, 유기 발광 화합물 및 이를 포함하는 유기 발광 소자에 관한 것으로, 치환기 A1 내지 A4, R1 내지 R16, L1, L2, X, m, n, n' 및 p는 발명의 상세한 설명에 정의된 바와 동일하다.
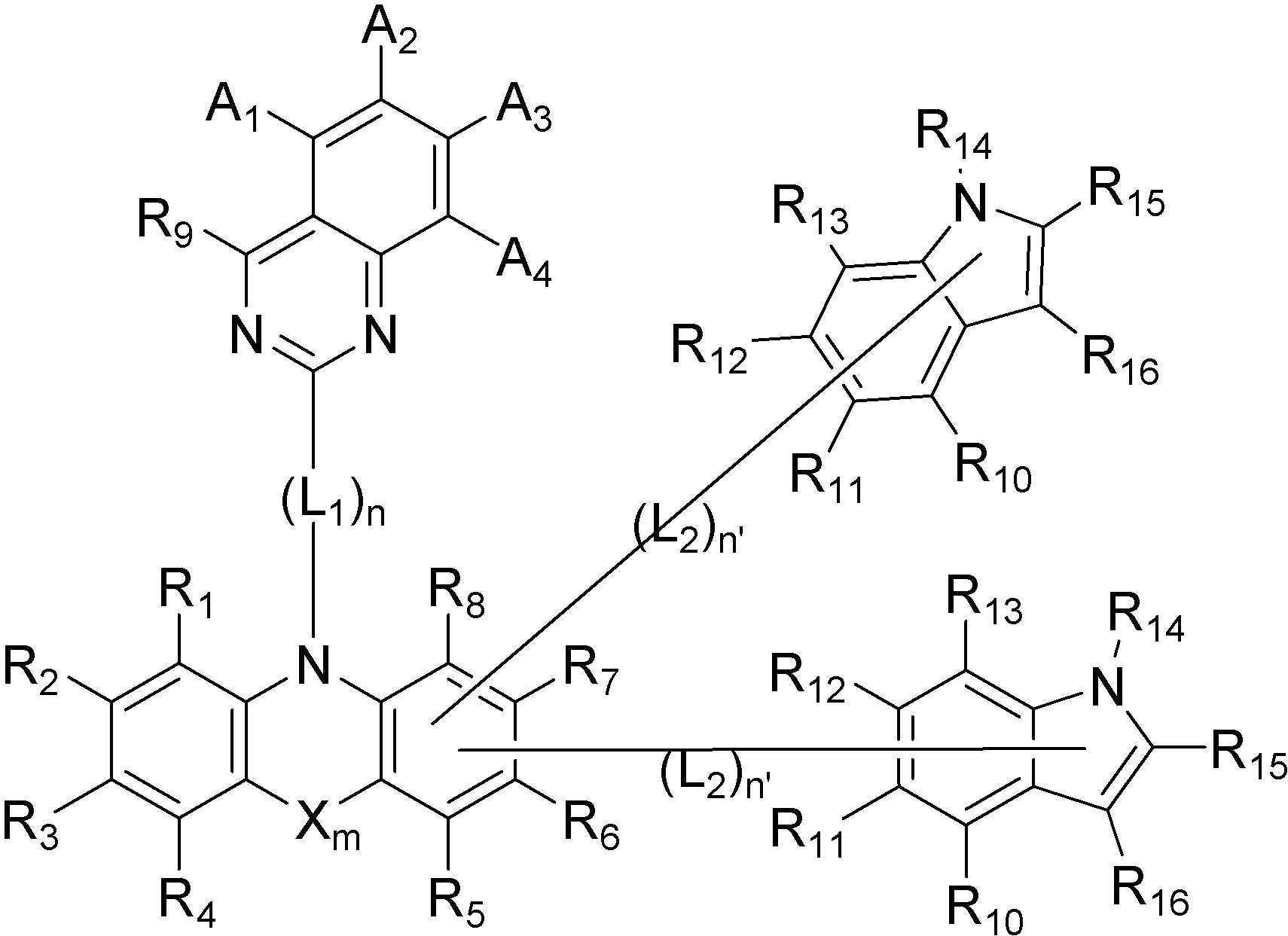
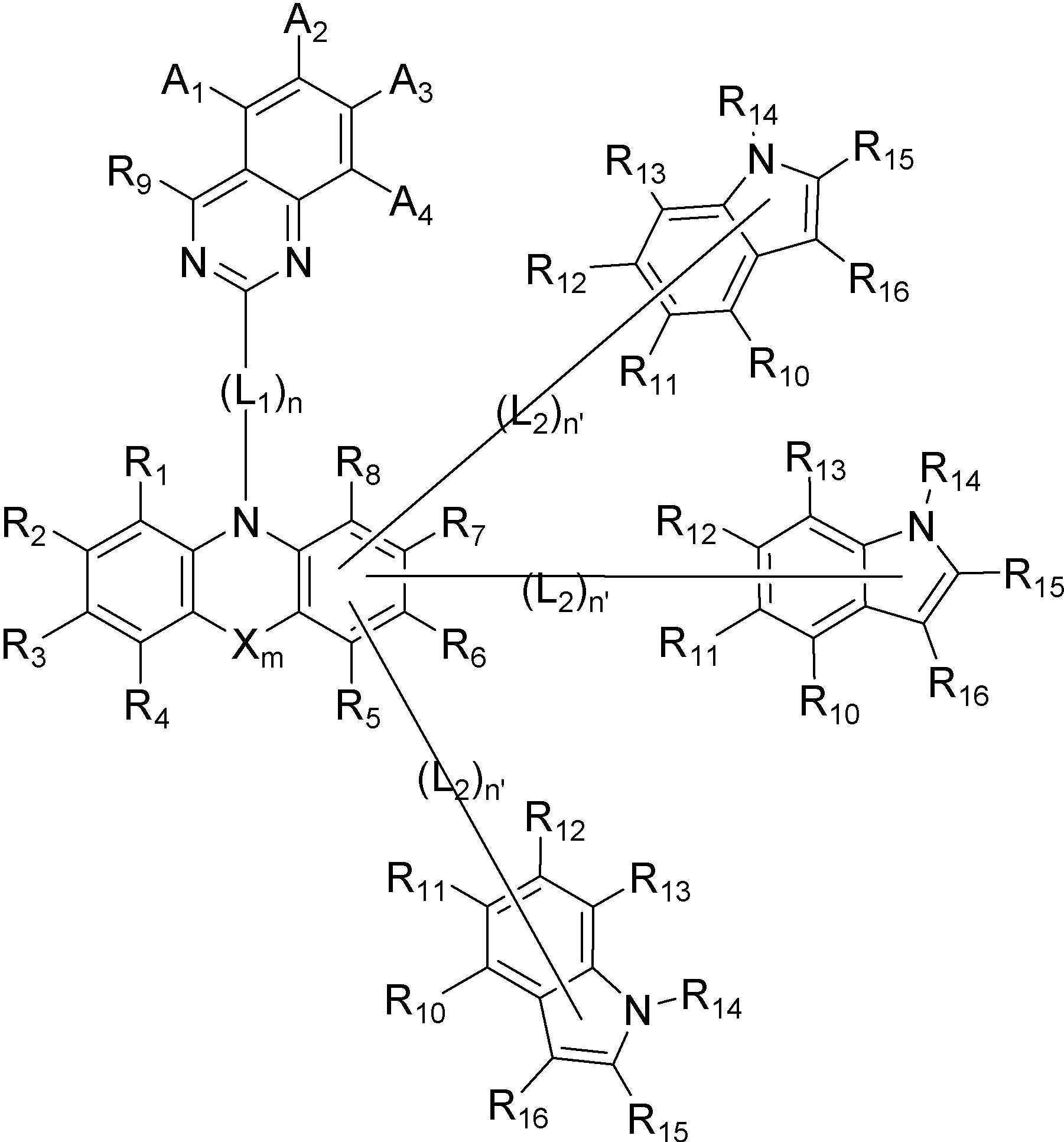
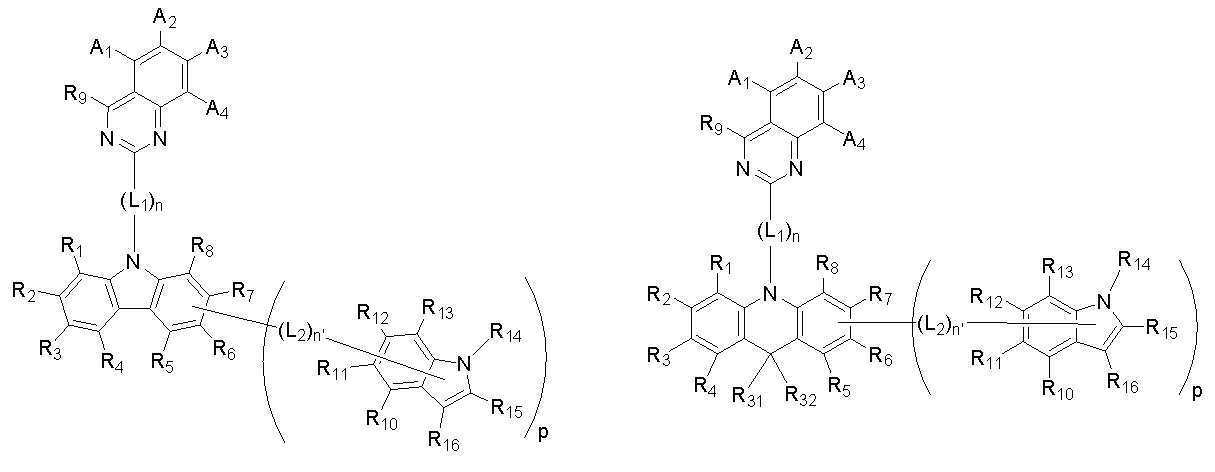
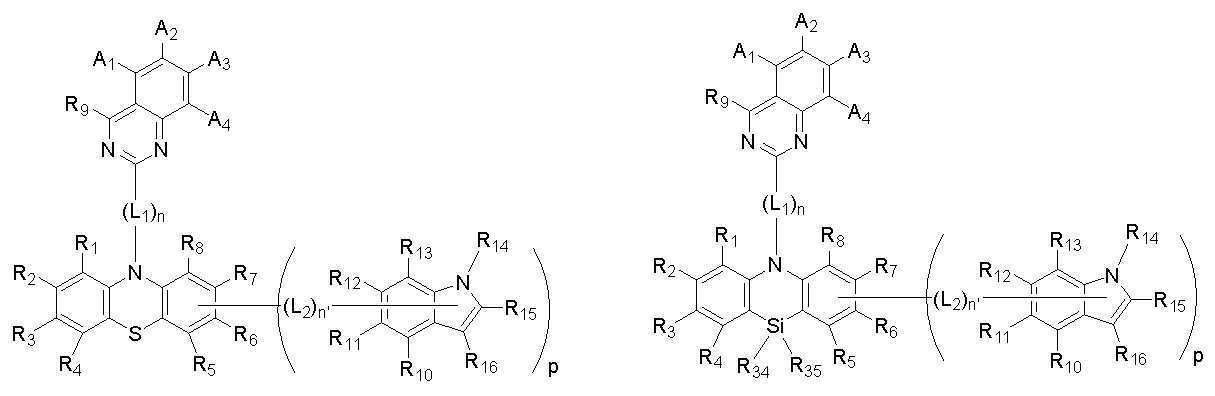
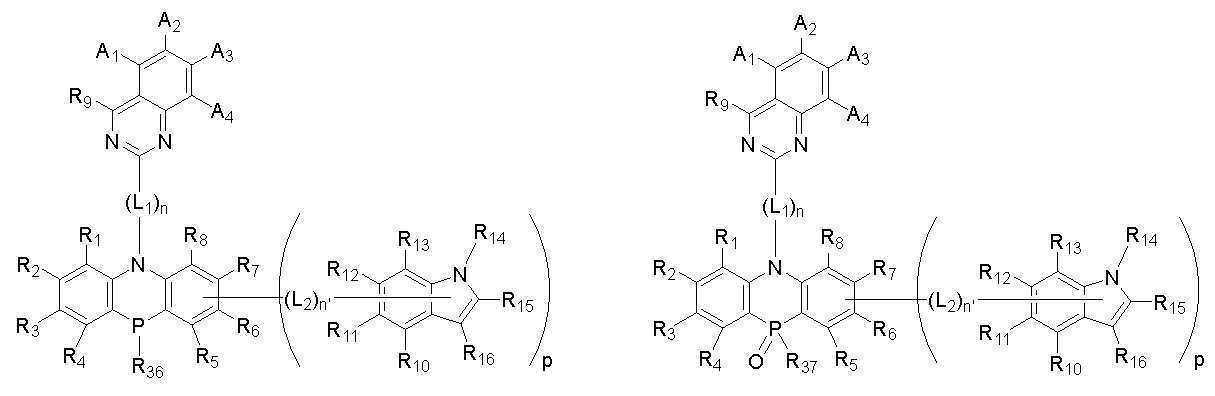
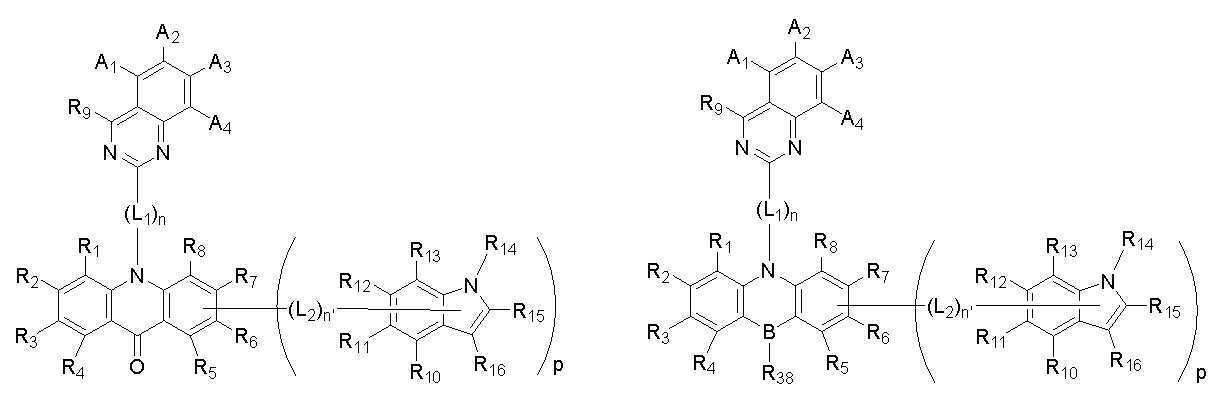
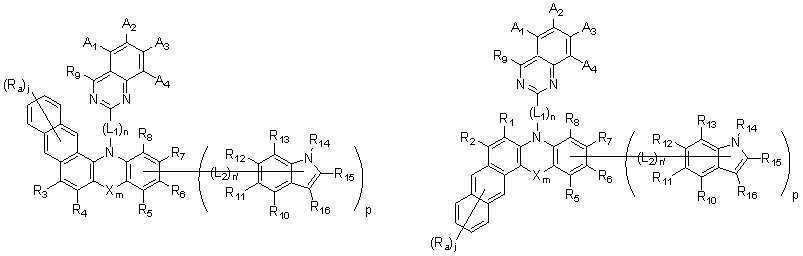
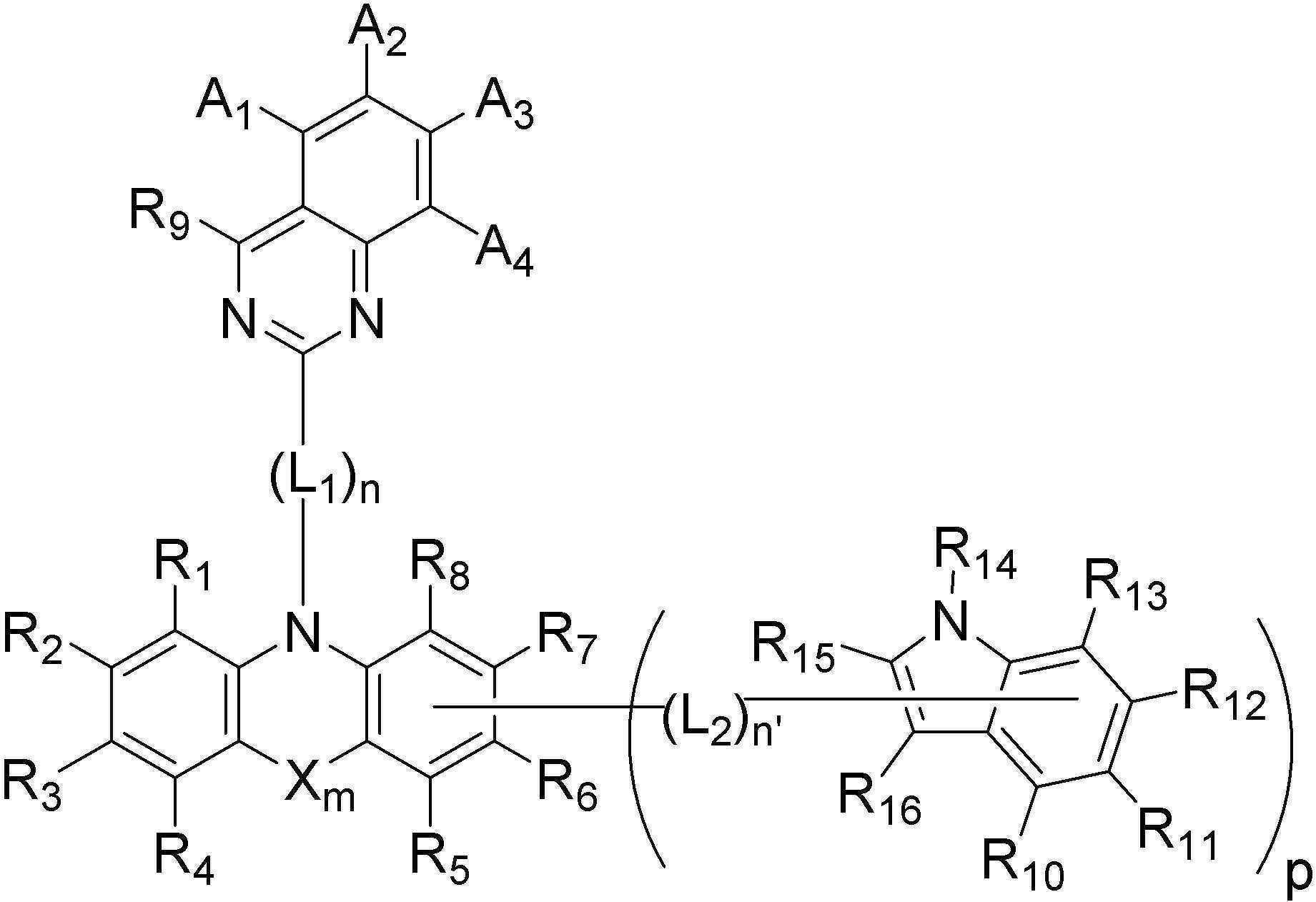
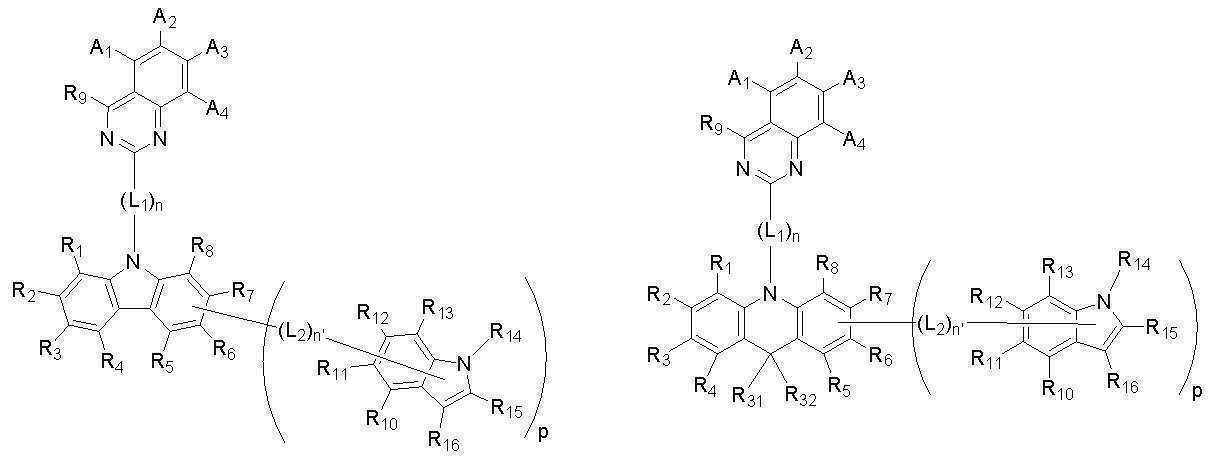
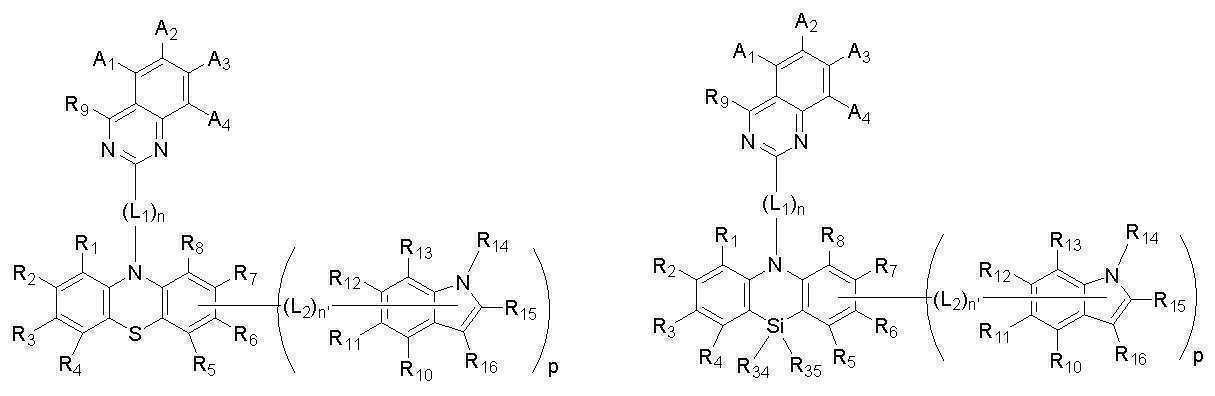
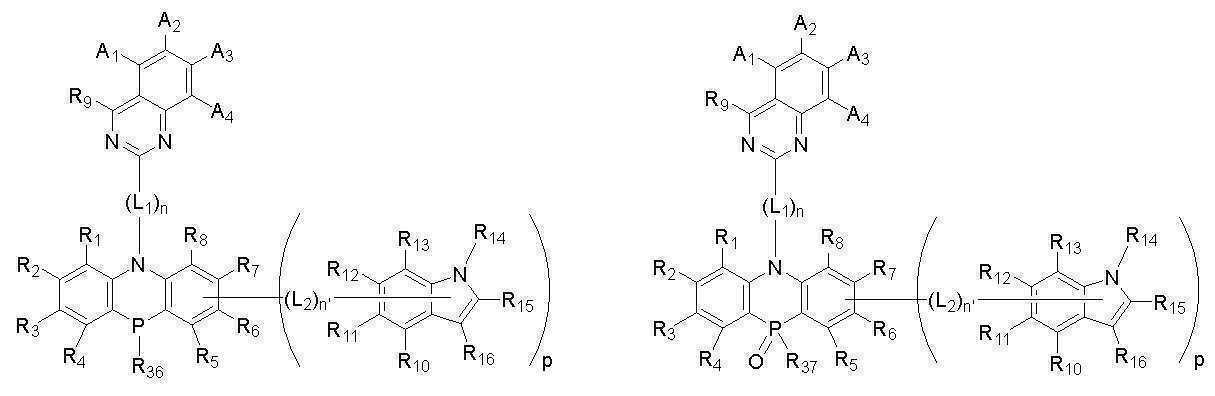
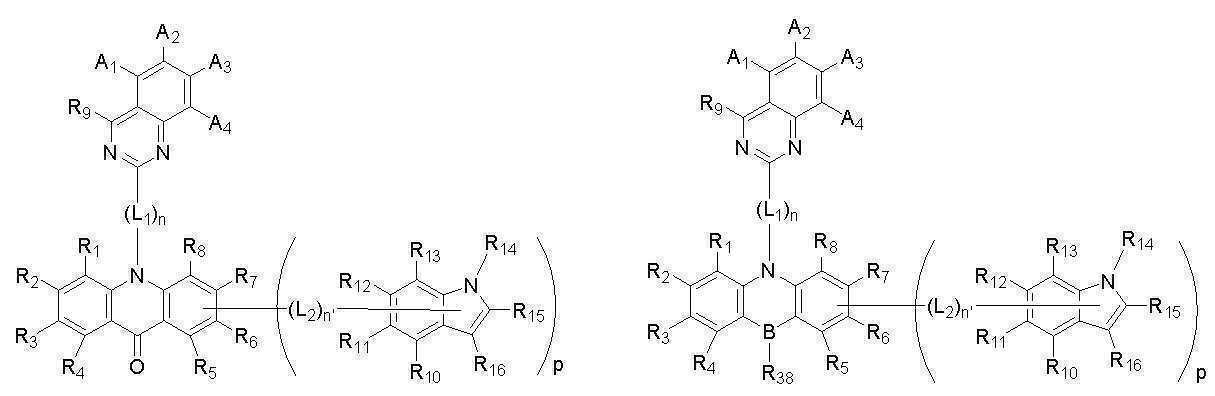
[화학식 A]
[화학식 B]
The present invention relates to an organic light-emitting compound and an organic light-emitting device including the same, represented by the following [Formula A] or [Formula B], substituents A1 to A4, R 1 to R 16 , L1, L2, X, m, n, n'and p are the same as defined in the detailed description of the invention.
[Formula A]
[Formula B]
Description
본 발명은 신규한 유기 화합물 및 이를 포함하는 유기 발광 소자에 관한 것으로서, 보다 상세하게는 구동전압을 낮출 수 있으며, 발광 효율이 우수한 소자특성을 보여줄 수 있는, 신규한 유기 화합물 및 이를 포함하는 유기 발광 소자에 관한 것이다. The present invention relates to a novel organic compound and an organic light-emitting device including the same, and in more detail, a novel organic compound capable of lowering a driving voltage and showing device characteristics excellent in luminous efficiency, and an organic light-emitting device including the same It relates to the device.
최근 표시장치의 대형화에 따라 평판구조에 의해 공간 점유가 적은 표시소자 또는 구부릴수 있는 표시소자의 요구가 증대되고 있는데, 대표적인 평면표시소자인 액정 디스플레이는 기존의 CRT(cathode ray tube)에 비해 경량화가 가능하다는 장점은 있으나, 시야각(viewing angle)이 제한되고 배면 광(back light)이 반드시 필요하다는 등의 단점을 갖고 있다. 이에 반하여, 새로운 평면표시소자인 유기 발광 소자(organic light emitting diode, OLED)는 자기 발광 현상을 이용한 디스플레이로서, 시야각이 크고, 액정 디스플레이에 비해 경박, 단소해질 수 있으며, 빠른 응답 속도 등의 장점을 가지고 있으며, 최근에는 풀-컬러(full-color) 디스플레이 또는 조명으로의 응용이 기대되고 있다.Recently, as display devices have become larger, there is an increasing demand for display devices that occupy less space or bendable display devices due to a flat panel structure, and liquid crystal displays, which are representative flat display devices, are lighter than conventional CRT (cathode ray tubes). Although there is an advantage that it is possible, it has disadvantages such as a limited viewing angle and a need for back light. On the other hand, organic light emitting diodes (OLEDs), which are new flat display devices, are displays using a self-luminous phenomenon, and have advantages such as a large viewing angle, lightness and compactness compared to liquid crystal displays, and fast response speed. And, in recent years, applications to full-color displays or lighting are expected.
일반적으로 유기 발광 현상이란 유기 물질을 이용하여 전기에너지를 빛에너지로 전환시켜주는 현상을 말한다.In general, the organic light emission phenomenon refers to a phenomenon in which electrical energy is converted into light energy using an organic material.
유기 발광 현상을 이용하는 유기 발광 소자는 통상 양극과 음극 및 이 사이에 유기물층을 포함하는 구조를 가진다. 여기서 유기물층은 유기 발광 소자의 효율과 안정성을 높이기 위하여 각기 다른 물질로 구성된 다층의 구조로 이루어진 경우가 많으며, 예컨대 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층 등으로 이루어질 수 있다. 이러한 유기 발광 소자의 구조에서 두 전극 사이에 전압을 걸어주게 되면 양극에서는 정공이, 음극에서는 전자가 유기물층에 주입되게 되고, 주입된 정공과 전자가 만났을 때 엑시톤(exciton)이 형성되며, 이 엑시톤이 다시 바닥상태로 떨어질 때 빛이 나게 된다. 이러한 유기 발광 소자는 자발광, 고휘도, 고효율, 낮은 구동전압, 넓은 시야각, 높은 콘트라스트, 고속 응답성 등의 특성을 갖는 것으로 알려져 있다.An organic light emitting device using the organic light emitting phenomenon has a structure including an anode, a cathode, and an organic material layer therebetween. Here, the organic material layer is often made of a multi-layered structure composed of different materials in order to increase the efficiency and stability of the organic light-emitting device.For example, it may be formed of a hole injection layer, a hole transport layer, a light emitting layer, an electron transport layer, an electron injection layer, and the like. In the structure of such an organic light-emitting device, when a voltage is applied between the two electrodes, holes are injected from the anode and electrons from the cathode are injected into the organic material layer, and excitons are formed when the injected holes and electrons meet. It glows when it falls back to the ground. These organic light-emitting devices are known to have characteristics such as self-luminescence, high luminance, high efficiency, low driving voltage, wide viewing angle, high contrast, and high-speed response.
유기 발광 소자에서 유기물층으로 사용되는 재료는 기능에 따라, 발광 재료와 전하수송 재료, 예컨대 정공주입 재료, 정공수송 재료, 전자수송 재료, 전자주입 재료 등으로 분류될 수 있다. 상기 발광 재료는 분자량에 따라 고분자형과 저분자형으로 분류될 수 있고, 발광 메커니즘에 따라 전자의 일중항 여기상태로부터 유래되는 형광 재료와 전자의 삼중항 여기상태로부터 유래되는 인광 재료로 분류될 수 있다. 또한, 발광 재료는 발광색에 따라 청색, 녹색, 적색 발광 재료와 보다 나은 천연색을 구현하기 위해 필요한 노란색 및 주황색 발광 재료로 구분될 수 있다.Materials used as the organic material layer in the organic light-emitting device can be classified into light-emitting materials and charge transport materials, such as hole injection materials, hole transport materials, electron transport materials, and electron injection materials, according to their functions. The light-emitting material may be classified into a high-molecular-type and a low-molecular-type according to its molecular weight, and may be classified into a fluorescent material derived from the singlet excited state of the electron and a phosphorescent material derived from the triplet excited state of the electron according to the light emitting mechanism . In addition, the light-emitting material may be classified into blue, green, and red light-emitting materials and yellow and orange light-emitting materials necessary for realizing a better natural color according to the light-emitting color.
한편, 발광 재료로서 하나의 물질만 사용하는 경우, 분자간 상호 작용에 의하여 최대 발광 파장이 장파장으로 이동하고 색순도가 떨어지거나 발광 감쇄 효과로 소자의 효율이 감소되는 문제가 발생하므로, 색순도의 증가와 에너지 전이를 통한 발광 효율을 증가시키기 위하여 발광 재료로서 호스트-도판트 시스템을 사용할 수 있다.On the other hand, when only one material is used as a light-emitting material, the maximum light-emitting wavelength shifts to a long wavelength due to the interaction between molecules, and the color purity decreases, or the efficiency of the device decreases due to the light-emitting attenuation effect. In order to increase the luminous efficiency through transition, a host-dopant system may be used as a light emitting material.
그 원리는 발광층을 형성하는 호스트보다 에너지 대역 간극이 작은 도판트를 발광층에 소량 혼합하면, 발광층에서 발생한 엑시톤이 도판트로 수송되어 효율이 높은 빛을 내는 것이다. 이때, 호스트의 파장이 도판트의 파장대로 이동하므로, 이용하는 도판트의 종류에 따라 원하는 파장의 빛을 얻을 수 있다.The principle is that when a small amount of a dopant having an energy band gap smaller than that of the host forming the light emitting layer is mixed in the light emitting layer, excitons generated in the light emitting layer are transported to the dopant to emit light with high efficiency. At this time, since the wavelength of the host moves to the wavelength of the dopant, light having a desired wavelength can be obtained according to the type of dopant used.
상기 유기 발광 소자가 전술한 우수한 특징들을 충분히 발휘하기 위해서는 소자 내 유기물층을 이루는 물질, 예컨대 정공주입 물질, 정공수송 물질, 발광 물질, 전자수송 물질, 전자주입 물질 등이 안정하고 효율적인 재료에 의하여 뒷받침되는 것이 선행되어야 한다.In order for the organic light-emitting device to fully exhibit the above-described excellent features, materials that form the organic material layer in the device, such as hole injection materials, hole transport materials, light-emitting materials, electron transport materials, electron injection materials, etc., are supported by stable and efficient materials. Things must precede.
유기발광소자에 전류를 가하면 양극과 음극으로부터 각각 정공과 전자가 주입되고, 주입된 정공과 전자는 각각의 정공수송층과 전자수송층을 거쳐 발광층에서 재결합하여 발광여기자를 형성한다. 이와 같이 형성된 발광여기자는 바닥상태로 전이하면서 빛을 방출한다. 상기 빛은 발광 메카니즘에 따라 단일항 여기자를 이용하는 형광과 삼중항 여기자를 이용하는 인광으로 나뉠 수 있고, 상기 형광 및 인광은 유기발광소자의 발광원으로 사용될 수 있다.When an electric current is applied to the organic light emitting device, holes and electrons are injected from the anode and the cathode, respectively, and the injected holes and electrons are recombined in the emission layer through the respective hole transport layer and electron transport layer to form emission excitons. The light-emitting excitons thus formed emit light while transitioning to the ground state. The light may be divided into fluorescence using singlet excitons and phosphorescence using triplet excitons according to an emission mechanism, and the fluorescence and phosphorescence may be used as a light emitting source of an organic light emitting device.
한편, 단일항 여기자만을 사용하는 형광은 단일항 여기자의 발생 확률이 25 %로서 발광 효율에 한계가 존재하는 반면에, 삼중항 여기자를 사용할 수 있는 인광은 발광 효율이 형광에 비해 월등하기 때문에 많은 연구가 계속되고 있다. On the other hand, fluorescence using only singlet excitons has a 25% probability of occurrence of singlet excitons, so there is a limit to the luminous efficiency, whereas phosphorescence that can use triplet excitons has superior luminous efficiency compared to fluorescence. Is going on.
상기 인광 발광체의 호스트 재료로는 현재까지 CBP가 가장 널리 알려져 있고, BCP 및 BAlq 등의 정공차단층을 적용한 유기발광소자가 공지되어 있다. CBP is the most widely known host material of the phosphorescent emitter so far, and an organic light emitting device to which a hole blocking layer such as BCP and BAlq is applied is known.
그러나 기존의 인광 발광 재료를 사용한 소자는 형광 발광 재료를 사용한 소자에 비해 효율은 높으나, 인광 발광 재료의 호스트로 사용되던 BAlq 또는 CBP와 같은 종래재료의 경우, 형광재료를 사용한 소자에 비해 구동 전압이 높아서 전력 효율(lm/w)면에서 큰 이점이 없고, 또한 수명 측면에서도 만족스럽지 못한 단점이 있다. 또한 이와 같은 인광재료를 이용하여 발광소자로 사용하기 위해, 공개특허공보 제10-2011-0013220호(2011.02.09)에서는 6원의 방향족 고리 또는 6원의 헤테로 방향족 고리의 골격에 방향족 헤테로고리가 도입된 유기 화합물에 관해 기재되어 있고, 일본공개특허공보 특개2010-166070호(2010.7.29)에서는 치환 또는 비치환된 피리미딘 또는 퀴나졸린 골격에 아릴 또는 헤테로아릴 고리가 결합된 유기화합물에 관해 기재되어 있다. However, a device using a conventional phosphorescent material is more efficient than a device using a fluorescent material, but in the case of a conventional material such as BAlq or CBP used as a host of a phosphorescent material, the driving voltage is higher than that of a device using a fluorescent material. As it is high, there is no big advantage in terms of power efficiency (lm/w), and there are disadvantages that are not satisfactory in terms of lifespan. In addition, in order to use such a phosphorescent material as a light-emitting device, Korean Patent Publication No. 10-2011-0013220 (2011.02.09) discloses an aromatic heterocycle in the skeleton of a 6-membered aromatic ring or a 6-membered heteroaromatic ring. Introduced organic compounds are described, and Japanese Laid-Open Patent Publication No. 2010-166070 (2010.7.29) describes organic compounds in which an aryl or heteroaryl ring is bonded to a substituted or unsubstituted pyrimidine or quinazoline skeleton. Has been.
그러나, 상기와 같은 유기 발광 소자용 재료를 제조하기 위한 노력에도 불구하고 아직까지 저구동전압 및 고발광 효율화를 위한 재료의 개발이 충분하다고는 할 수 없어, 저전압에서 구동이 가능하면서도 발광 효율이 우수한 발광 재료의 개발의 필요성은 지속적으로 요구되고 있는 실정이다.However, despite the efforts to manufacture the material for an organic light-emitting device as described above, it is not yet sufficient to develop materials for low driving voltage and high luminous efficiency, so that it is possible to drive at low voltage and has excellent luminous efficiency. The necessity of developing a light emitting material is a situation that is continuously required.
공개특허공보 제10-2011-0013220호 (2011.02.09)Patent Publication No. 10-2011-0013220 (2011.02.09)
일본공개특허공보 특개2010-166070호(2010.7.29)Japanese Unexamined Patent Application Publication No. 2010-166070 (2010.7.29)
따라서, 본 발명이 이루고자 하는 첫 번째 기술적 과제는 유기발광소자의 발광층에서 사용될 수 있으며, 장수명과 저전압구동 특성을 가지고 발광효율이 우수한 신규한 유기 화합물을 제공하는 것이다.Accordingly, the first technical problem to be achieved by the present invention is to provide a novel organic compound that can be used in an emission layer of an organic light emitting device, has a long lifespan, low voltage driving characteristics, and excellent luminous efficiency.
본 발명이 이루고자 하는 두 번째 기술적 과제는 상기 유기 화합물을 포함하는 유기 발광 소자를 제공하는 것이다. A second technical problem to be achieved by the present invention is to provide an organic light-emitting device including the organic compound.
본 발명은 상기 첫 번째 기술적 과제를 달성하기 위하여, 하기 [화학식 A] 또는 [화학식 B]로 표시되는 화합물을 제공한다. The present invention provides a compound represented by the following [Chemical Formula A] or [Chemical Formula B] in order to achieve the first technical problem.
[화학식 A] [Formula A]
[화학식 B][Formula B]
상기 [화학식 A] 또는 [화학식 B]에서, In the [Formula A] or [Formula B],
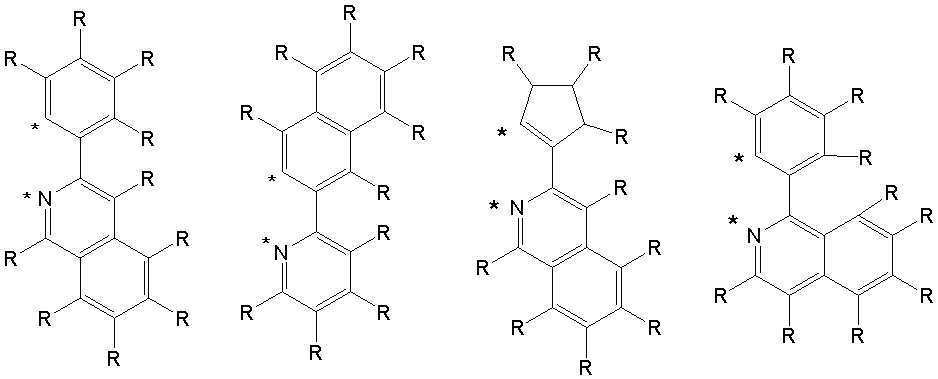
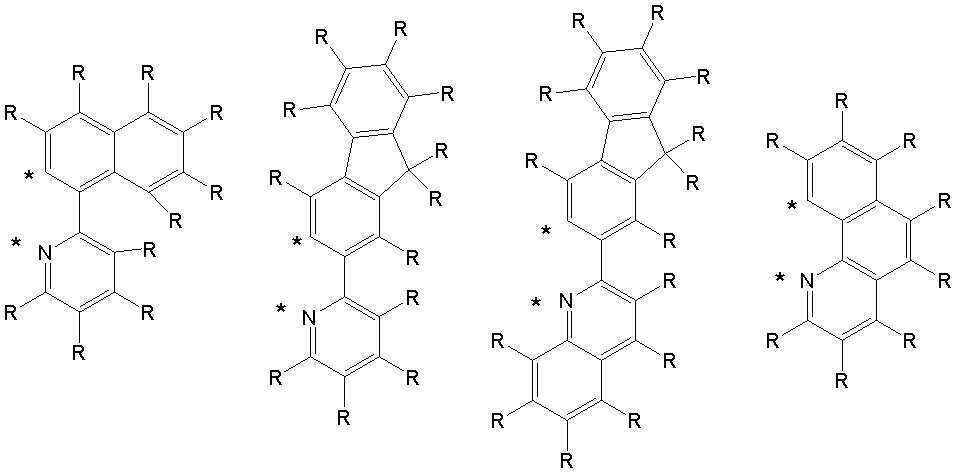
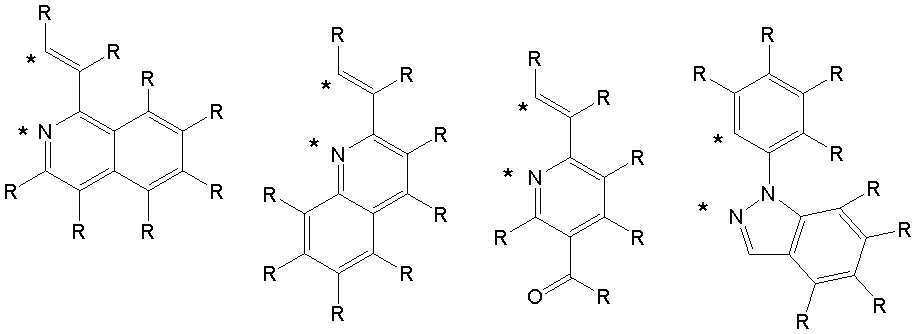
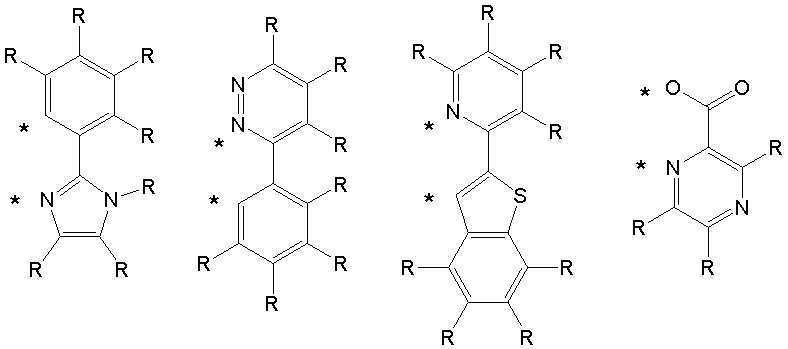
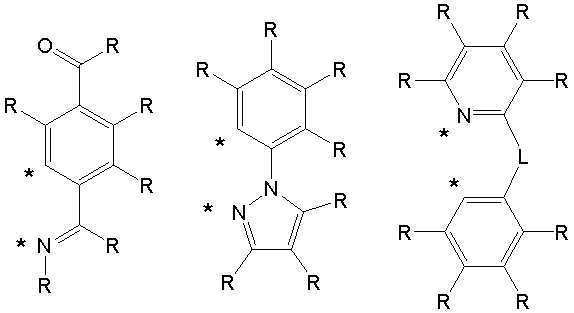
상기 A1 내지 A4 와 R1 내지 R16은 각각 동일하거나 상이하고, 서로 독립적으로 수소, 중수소, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 2 내지 20의 알키닐기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 시클로알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬티옥시기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴티옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아민기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 2 내지 50의 헤테로아릴기, 시아노기, 니트로기, 할로겐기 중에서 선택되는 어느 하나이고, 상기 A1 내지 A4 와 R1 내지 R8은 각각 서로 인접하는 치환기와 연결되어 지환족, 방향족의 단일환 또는 다환 고리를 형성할 수 있으며, 상기 형성된 지환족, 방향족의 단일환 또는 다환 고리의 탄소원자는 N, S, O 중에서 선택되는 어느 하나 이상의 헤테로원자로 치환될 수 있으며; The A 1 to A 4 and R 1 to R 16 are each the same or different, and independently of each other, hydrogen, deuterium, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted aryl group having 5 to 50 carbon atoms , A substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, a substituted or unsubstituted alkynyl group having 2 to 20 carbon atoms, a substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted carbon number of 5 to 30 Cycloalkenyl group, a substituted or unsubstituted alkoxy group having 1 to 30 carbon atoms, a substituted or unsubstituted aryloxy group having 6 to 30 carbon atoms, a substituted or unsubstituted alkylthioxy group having 1 to 30 carbon atoms, a substituted or unsubstituted An arylthioxy group having 5 to 30 carbon atoms, a substituted or unsubstituted alkylamine group having 1 to 30 carbon atoms, a substituted or unsubstituted arylamine group having 5 to 30 carbon atoms, a substituted or unsubstituted arylamine group having O, N or S as a hetero atom It is any one selected from a C2-C50 heteroaryl group, a cyano group, a nitro group, and a halogen group, and the A 1 to A 4 and R 1 to R 8 are each connected with a substituent adjacent to each other to be an alicyclic, aromatic Can form a monocyclic or polycyclic ring, and the carbon atoms of the formed alicyclic, aromatic monocyclic or polycyclic ring may be substituted with any one or more heteroatoms selected from N, S, and O ;
상기 L1 및 L2는 연결기로서, 단일 결합, 치환 또는 비치환된 탄소수 1 내지 60의 알킬렌기, 치환 또는 비치환된 탄소수 2 내지 60의 알케닐렌기, 치환 또는 비치환된 탄소수 2 내지 60의 알키닐렌기, 치환 또는 비치환된 탄소수 3 내지 60의 시클로알킬렌기, 치환 또는 비치환된 탄소수 2 내지 60의 헤테로시클로알킬렌기, 치환 또는 비치환된 탄소수 6 내지 60의 아릴렌기 또는 치환 또는 비치환된 탄소수 2 내지 60의 헤테로아릴렌기이며;The L 1 and L 2 is a linking group, a single bond, a substituted or unsubstituted alkylene group having 1 to 60 carbon atoms, a substituted or unsubstituted C 2 to
상기 X는 연결기로서, 단일결합이거나 -C(R31R32)-, NR33, O, S, SiR34R35, GeR36R37, PR38, PR39(=O), C=O, BR40 이며, X is a linking group, or a single bond or -C(R 31 R 32 )-, NR 33 , O, S, SiR 34 R 35 , GeR 36 R 37 , PR 38 , PR 39 (=O), C=O, BR 40 Is,
상기 R31 내지 R40은 상기 R1 내지 R16에서 정의한 바와 동일하며;R 31 to R 40 are the same as defined in R 1 to R 16 ;
상기 m, n, n'및 p는 각각 서로 독립적으로 1 내지 3의 정수이며, The m, n, n'and p are each independently an integer of 1 to 3,
상기 m, n, n'및 p가 각각 2이상인 경우에 각각의 연결기 및 인돌그룹은 서로 동일하거나 상이하며;When m, n, n'and p are each 2 or more, each linking group and indole group are the same or different from each other;
화학식 A에서 R5 내지 R8 중 p개와, R10 내지 R13 , R15 및 R16 중 하나는 각각 상기 L2 와 연결되는 단일결합이고, In formula A, p of R 5 to R 8 and R 10 to R 13 , R 15 and R 16 One of each is a single bond connected to the L 2 ,
화학식 B에서, R5 내지 R8 중 p개는 상기 L2 와 연결되는 단일결합이다. In Formula B, p of R 5 to R 8 is a single bond connected to L 2 .
또한 본 발명은 상기 두 번째 과제를 달성하기 위하여, 제1전극, 상기 제1전극에 대향된 제2전극 및 상기 제1전극과 상기 제2전극 사이에 개재된 유기층을 포함하고, 상기 유기층이 본 발명의 유기발광 화합물을 1종 이상 포함한, 유기 발광 소자를 제공한다.In addition, the present invention includes a first electrode, a second electrode facing the first electrode, and an organic layer interposed between the first electrode and the second electrode, and the organic layer is It provides an organic light-emitting device comprising at least one organic light-emitting compound of the invention.
본 발명에 따르면, [화학식 A] 내지 [화학식 B]로 표시되는 인광호스트용 유기발광 화합물은 기존 물질에 비하여 장수명 및 저 전압구동의 특성을 가지며 발광효율이 우수한 특성을 가지고 있어, 안정적이고 우수한 소자의 제조에 이용될 수 있다.According to the present invention, the organic light emitting compound for a phosphorescent host represented by [Chemical Formula A] to [Chemical Formula B] has characteristics of long life and low voltage driving compared to conventional materials, and has excellent luminous efficiency, so it is a stable and excellent device It can be used in the manufacture of.
도 1은 본 발명의 일 구체예에 따른 유기 발광 소자의 개략도이다.
도 2 는 본 발명의 비교예 2, 실시예 1, 실시예 8의 소자의 수명평가를 나타낸 그래프이다. 1 is a schematic diagram of an organic light-emitting device according to an embodiment of the present invention.
2 is a graph showing life evaluation of devices of Comparative Examples 2, 1 and 8 of the present invention.
이하, 본 발명을 더욱 상세하게 설명한다.Hereinafter, the present invention will be described in more detail.
본 발명은 유기 발광 소자의 발광층에 사용될 수 있는 유기발광 화합물로서, 하기 [화학식 A] 내지 [화학식 B]로 표시되는 유기발광 화합물이 종래기술에 의한 유기발광재료보다 유기발광소자의 장수명 및 저 전압구동의 특성과 양호한 발광효율을 보여 줄 수 있는 것으로 나타남으로써, 안정적이고 우수한 소자를 제조할 수 있음을 알게 되었다.The present invention is an organic light emitting compound that can be used in the light emitting layer of an organic light emitting device, and the organic light emitting compound represented by the following [Chemical Formula A] to [Chemical Formula B] has a longer life and lower voltage of the organic light emitting device than the organic light emitting material according to the prior art. It was found that a stable and excellent device can be manufactured by being shown to be capable of showing driving characteristics and good luminous efficiency.
보다 구체적으로 본 발명은 하기 [화학식 A] 내지 [화학식 B]에서 선택되는 어느 하나로 표시되는 화합물을 제공한다. More specifically, the present invention provides a compound represented by any one selected from the following [Formula A] to [Formula B].
[화학식 A] [Formula A]
[화학식 B][Formula B]
상기 [화학식 A] 또는 [화학식 B]에서, In the [Formula A] or [Formula B],
상기 A1 내지 A4 와 R1 내지 R16은 각각 동일하거나 상이하고, 서로 독립적으로 수소, 중수소, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 2 내지 20의 알키닐기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 시클로알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬티옥시기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴티옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아민기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 2 내지 50의 헤테로아릴기, 시아노기, 니트로기, 할로겐기 중에서 선택되는 어느 하나이고, 상기 A1 내지 A4 와 R1 내지 R8은 각각 서로 인접하는 치환기와 연결되어 지환족, 방향족의 단일환 또는 다환 고리를 형성할 수 있으며, 상기 형성된 지환족, 방향족의 단일환 또는 다환 고리의 탄소원자는 N, S, O 중에서 선택되는 어느 하나 이상의 헤테로원자로 치환될 수 있으며; The A 1 to A 4 and R 1 to R 16 are each the same or different, and independently of each other, hydrogen, deuterium, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted aryl group having 5 to 50 carbon atoms , A substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, a substituted or unsubstituted alkynyl group having 2 to 20 carbon atoms, a substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted carbon number of 5 to 30 Cycloalkenyl group, a substituted or unsubstituted alkoxy group having 1 to 30 carbon atoms, a substituted or unsubstituted aryloxy group having 6 to 30 carbon atoms, a substituted or unsubstituted alkylthioxy group having 1 to 30 carbon atoms, a substituted or unsubstituted An arylthioxy group having 5 to 30 carbon atoms, a substituted or unsubstituted alkylamine group having 1 to 30 carbon atoms, a substituted or unsubstituted arylamine group having 5 to 30 carbon atoms, a substituted or unsubstituted arylamine group having O, N or S as a hetero atom It is any one selected from a C2-C50 heteroaryl group, a cyano group, a nitro group, and a halogen group, and the A 1 to A 4 and R 1 to R 8 are each connected with a substituent adjacent to each other to be an alicyclic, aromatic Can form a monocyclic or polycyclic ring, and the carbon atoms of the formed alicyclic, aromatic monocyclic or polycyclic ring may be substituted with any one or more heteroatoms selected from N, S, and O ;
상기 L1 및 L2는 연결기로서, 단일 결합, 치환 또는 비치환된 탄소수 1 내지 60의 알킬렌기, 치환 또는 비치환된 탄소수 2 내지 60의 알케닐렌기, 치환 또는 비치환된 탄소수 2 내지 60의 알키닐렌기, 치환 또는 비치환된 탄소수 3 내지 60의 시클로알킬렌기, 치환 또는 비치환된 탄소수 2 내지 60의 헤테로시클로알킬렌기, 치환 또는 비치환된 탄소수 6 내지 60의 아릴렌기 또는 치환 또는 비치환된 탄소수 2 내지 60의 헤테로아릴렌기이며;The L 1 and L 2 is a linking group, a single bond, a substituted or unsubstituted alkylene group having 1 to 60 carbon atoms, a substituted or unsubstituted C 2 to
상기 X는 연결기로서, 단일결합이거나 -C(R31R32)-, NR33, O, S, SiR34R35, GeR36R37, PR38, PR39(=O), C=O, BR40 이며, X is a linking group, or a single bond or -C(R 31 R 32 )-, NR 33 , O, S, SiR 34 R 35 , GeR 36 R 37 , PR 38 , PR 39 (=O), C=O, BR 40 Is,
상기 R31 내지 R40은 상기 R1 내지 R16에서 정의한 바와 동일하며;R 31 to R 40 are the same as defined in R 1 to R 16 ;
상기 m, n, n'및 p는 각각 서로 독립적으로 1 내지 3의 정수이며, The m, n, n'and p are each independently an integer of 1 to 3,
상기 m, n, n'및 p가 각각 2이상인 경우에 각각의 연결기 및 인돌그룹은 서로 동일하거나 상이하며;When m, n, n'and p are each 2 or more, each linking group and indole group are the same or different from each other;
화학식 A에서 R5 내지 R8 중 p개와, R10 내지 R13 , R15 및 R16 중 하나는 각각 상기 L2 와 연결되는 단일결합이고, In Formula A, p of R 5 to R 8 and R 10 to R 13 , R 15 and R 16 One of each is a single bond connected to the L 2 ,
화학식 B에서, R5 내지 R8 중 p개는 상기 L2 와 연결되는 단일결합이며; In Formula B, p of R 5 to R 8 is a single bond connected to L 2 ;
상기 '치환 또는 비치환된'에서의 '치환'은 중수소, 시아노기, 할로겐기, 히드록시기, 니트로기, 탄소수 1 내지 24의 알킬기, 탄소수 1 내지 24의 할로겐화된 알킬기, 탄소수 1 내지 24의 알케닐기, 탄소수 1 내지 24의 알키닐기, 탄소수 1 내지 24의 헤테로알킬기, 탄소수 6 내지 24의 아릴기, 탄소수 6 내지 24의 아릴알킬기, 탄소수 2 내지 24의 헤테로아릴기 또는 탄소수 2 내지 24의 헤테로아릴알킬기, 탄소수 1 내지 24의 알콕시기, 탄소수 1 내지 24의 알킬아미노기, 탄소수 1 내지 24의 아릴아미노기, 탄소수 1 내지 24의 헤테로 아릴아미노기, 탄소수 1 내지 24의 알킬실릴기, 탄소수 1 내지 24의 아릴실릴기, 탄소수 1 내지 24의 아릴옥시기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환되는 것을 의미한다. 'Substituted' in the'substituted or unsubstituted' is deuterium, cyano group, halogen group, hydroxy group, nitro group, alkyl group having 1 to 24 carbon atoms, halogenated alkyl group having 1 to 24 carbon atoms, alkenyl group having 1 to 24 carbon atoms , C1-C24 alkynyl group, C1-C24 heteroalkyl group, C6-C24 aryl group, C6-C24 arylalkyl group, C2-C24 heteroaryl group, C2-C24 heteroarylalkyl group , C1-C24 alkoxy group, C1-C24 alkylamino group, C1-C24 arylamino group, C1-C24 hetero arylamino group, C1-C24 alkylsilyl group, C1-C24 arylsilyl It means substituted with one or more substituents selected from the group consisting of a group and an aryloxy group having 1 to 24 carbon atoms.
또한, 상기 "치환 또는 비치환된 탄소수 1 내지 30의 알킬기", "치환 또는 비치환된 탄소수 5 내지 50의 아릴기" 등에서의 상기 알킬기 또는 아릴기의 범위를 고려하여 보면, 상기 탄소수 1 내지 30의 알킬기 및 탄소수 5 내지 50의 아릴기의 탄소수의 범위는 각각 상기 치환기가 치환된 부분을 고려하지 않고 비치환된 것으로 보았을 때의 알킬 부분 또는 아릴 부분을 구성하는 전체 탄소수를 의미하는 것이다. 예컨대, 파라위치에 부틸기가 치환된 페닐기는 탄소수 4의 부틸기로 치환된 탄소수 6의 아릴기에 해당하는 것으로 보아야 한다. In addition, considering the range of the alkyl group or aryl group in the "substituted or unsubstituted alkyl group having 1 to 30 carbon atoms" and "substituted or unsubstituted aryl group having 5 to 50 carbon atoms", the carbon number is 1 to 30 The range of the number of carbon atoms of the alkyl group and the aryl group having 5 to 50 carbon atoms of each means the total number of carbon atoms constituting the alkyl moiety or aryl moiety when the substituent is considered to be unsubstituted without considering the substituted moiety. For example, a phenyl group substituted with a butyl group at the para position should be considered to correspond to an aryl group having 6 carbon atoms substituted with a butyl group having 4 carbon atoms.
한편, 본 발명의 화합물에서 사용되는 아릴기는 하나의 수소 제거에 의해서 방향족 탄화수소로부터 유도된 유기 라디칼로, 5 내지 7원, 바람직하게는 5 또는 6원을 포함하는 단일 또는 융합고리계를 포함하며, 또한 상기 아릴기에 치환기가 있는 경우 이웃하는 치환기와 서로 융합 (fused)되어 고리를 추가로 형성할 수 있다. On the other hand, the aryl group used in the compound of the present invention is an organic radical derived from an aromatic hydrocarbon by the removal of one hydrogen, and includes a single or fused ring system containing 5 to 7 members, preferably 5 or 6 members, In addition, when the aryl group has a substituent, it may be fused with neighboring substituents to further form a ring.
상기 아릴의 구체적인 예로 페닐, 나프틸, 비페닐, 터페닐, 안트릴, 인데닐(indenyl), 플루오레닐, 페난트릴, 트라이페닐레닐, 피렌일, 페릴렌일, 크라이세닐, 나프타세닐, 플루오란텐일 등을 포함하지만, 이에 한정되지 않는다.Specific examples of the aryl include phenyl, naphthyl, biphenyl, terphenyl, anthryl, indenyl, fluorenyl, phenanthryl, triphenylenyl, pyrenyl, peryleneyl, chrysenyl, naphthacenyl, fluorane. Including tenil, etc., but is not limited thereto.
상기 아릴기 중 하나 이상의 수소 원자는 중수소 원자, 할로겐 원자, 히드록시기, 니트로기, 시아노기, 실릴기, 아미노기 (-NH2, -NH(R), -N(R')(R''), R'과 R"은 서로 독립적으로 탄소수 1 내지 10의 알킬기이며, 이 경우 "알킬아미노기"라 함), 아미디노기, 히드라진기, 히드라존기, 카르복실기, 술폰산기, 인산기, 탄소수 1 내지 24의 알킬기, 탄소수 1 내지 24의 할로겐화된 알킬기, 탄소수 1 내지 24의 알케닐기, 탄소수 1 내지 24의 알키닐기, 탄소수 1 내지 24의 헤테로알킬기, 탄소수 6 내지 24의 아릴기, 탄소수 6 내지 24의 아릴알킬기, 탄소수 2 내지 24의 헤테로아릴기 또는 탄소수 2 내지 24의 헤테로아릴알킬기로 치환될 수 있다.At least one hydrogen atom in the aryl group is a deuterium atom, a halogen atom, a hydroxy group, a nitro group, a cyano group, a silyl group, an amino group (-NH 2 , -NH(R), -N(R')(R''), R'and R" are each independently an alkyl group having 1 to 10 carbon atoms, in this case referred to as an "alkylamino group"), an amidino group, a hydrazine group, a hydrazone group, a carboxyl group, a sulfonic acid group, a phosphoric acid group, an alkyl group having 1 to 24 carbon atoms , A halogenated alkyl group having 1 to 24 carbon atoms, an alkenyl group having 1 to 24 carbon atoms, an alkynyl group having 1 to 24 carbon atoms, a heteroalkyl group having 1 to 24 carbon atoms, an aryl group having 6 to 24 carbon atoms, an arylalkyl group having 6 to 24 carbon atoms, It may be substituted with a C2-C24 heteroaryl group or a C2-C24 heteroarylalkyl group.
본 발명의 화합물에서 사용되는 치환기인 헤테로아릴기는 상기 아릴기에서 각각의 고리 내에 N, O, P 또는 S 중에서 선택된 1 내지 4개의 헤테로 원자를 포함할 수 있는 탄소수 2 내지 24의 헤테로방향족 유기 라디칼을 의미하며, 상기 고리들은 융합(fused)되어 고리를 형성할 수 있다. 그리고 상기 헤테로아릴기 중 하나 이상의 수소 원자는 상기 아릴기의 경우와 마찬가지의 치환기로 치환가능하다.The heteroaryl group, which is a substituent used in the compound of the present invention, is a heteroaromatic organic radical having 2 to 24 carbon atoms which may contain 1 to 4 heteroatoms selected from N, O, P or S in each ring in the aryl group. It means, and the rings may be fused to form a ring. And at least one hydrogen atom in the heteroaryl group may be substituted with the same substituent as in the case of the aryl group.
본 발명에서 사용되는 치환기인 알킬기의 구체적인 예로는 메틸, 에틸, 프로필, 이소부틸, sec-부틸, tert-부틸, 펜틸, iso-아밀, 헥실 등을 들 수 있고, 상기 알킬기 중 하나 이상의 수소 원자는 원자는 상기 아릴기의 경우와 마찬가지의 치환기로 치환가능하다.Specific examples of the alkyl group as a substituent used in the present invention include methyl, ethyl, propyl, isobutyl, sec-butyl, tert-butyl, pentyl, iso-amyl, hexyl, and the like, and at least one hydrogen atom in the alkyl group is The atom may be substituted with the same substituent as in the case of the aryl group.
본 발명의 화합물에서 사용되는 치환기인 알콕시기의 구체적인 예로는 메톡시, 에톡시, 프로폭시, 이소부틸옥시, sec-부틸옥시, 펜틸옥시, iso-아밀옥시, 헥실옥시 등을 들 수 있고, 상기 알콕시기 중 하나 이상의 수소 원자는 상기 아릴기의 경우와 마찬가지의 치환기로 치환가능하다.Specific examples of the alkoxy group that is a substituent used in the compound of the present invention include methoxy, ethoxy, propoxy, isobutyloxy, sec-butyloxy, pentyloxy, iso-amyloxy, hexyloxy, and the like, At least one hydrogen atom in the alkoxy group may be substituted with the same substituent as in the case of the aryl group.
본 발명의 화합물에서 사용되는 치환기인 실릴기의 구체적인 예로는 트리메틸실릴, 트리에틸실릴, 트리페닐실릴, 트리메톡시실릴, 디메톡시페닐실릴, 디페닐메틸실릴, 실릴, 디페닐비닐실릴, 메틸사이클로뷰틸실릴, 디메틸퓨릴실릴 등을 들 수 있고, 상기 실릴기 중 하나 이상의 수소 원자는 상기 아릴기의 경우와 마찬가지의 치환기로 치환가능 하다. Specific examples of the silyl group as a substituent used in the compound of the present invention include trimethylsilyl, triethylsilyl, triphenylsilyl, trimethoxysilyl, dimethoxyphenylsilyl, diphenylmethylsilyl, silyl, diphenylvinylsilyl, methylcyclo Butylsilyl, dimethylfurylsilyl, and the like. At least one hydrogen atom in the silyl group may be substituted with the same substituent as in the case of the aryl group.
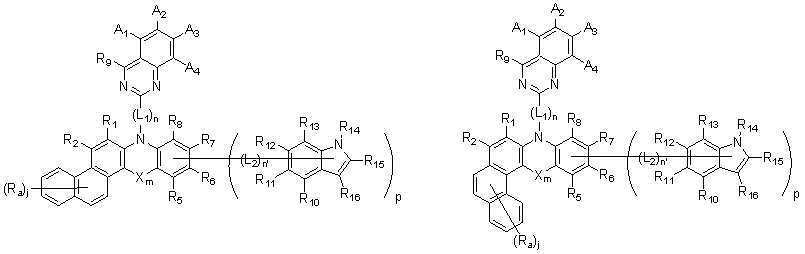
상기 [화학식 A]는 p가 1 내지 3인 경우에 따라서 하기 [화학식 101] 내지 [화학식 103] 중에서 선택되는 선택되는 하나의 화합물일 수 있다. [Chemical Formula A] may be one compound selected from the following [Chemical Formula 101] to [Chemical Formula 103] depending on the case where p is 1 to 3.
[화학식 101]
[Formula 101]
[화학식 102][Formula 102]
[화학식 103]
[Chemical Formula 103]
상기 [화학식 101] 내지 [화학식 103] 에서 치환기 A1 내지 A4 와 R1 내지 R16, X, L1, L2, m, n, n' 및 p는 각각 앞서 정의한 바와 동일하며, 치환되는 인돌그룹이 2 이상인 경우, 각각의 인돌그룹은 서로 동일하거나 상이할 수 있다. Substituents A 1 to A 4 and R 1 to R 16 , X, in the [Formula 101] to [Formula 103] L 1 , L 2 , m, n, n'and p are each the same as defined above, and when the indole group to be substituted is 2 or more, each indole group may be the same or different from each other.
또한 상기 [화학식 B]도 p가 1 내지 3인 경우에 따라, 인돌의 질소부분이 연결기 L2에 결합되는 것만을 제외하고는 상기 [화학식 101] 내지 [화학식 103]과 동일한 구조식에 의한 화합물로 나누어 질 수 있다. , In addition, the [Chemical Formula B] is divided into a compound according to the same structural formula as [Chemical Formula 101] to [Chemical Formula 103] except that the nitrogen portion of the indole is bonded to the linking group L2 depending on the case where p is 1 to 3 I can lose. ,
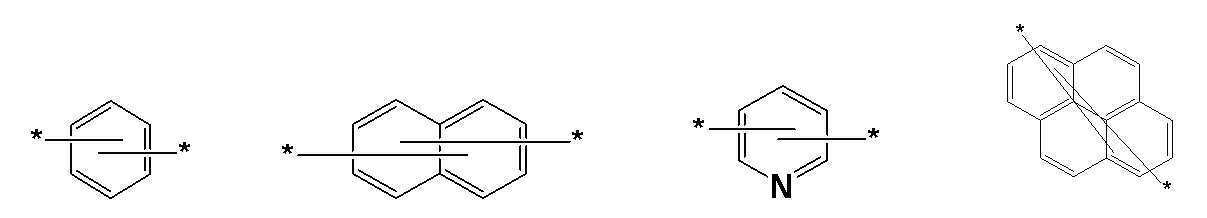
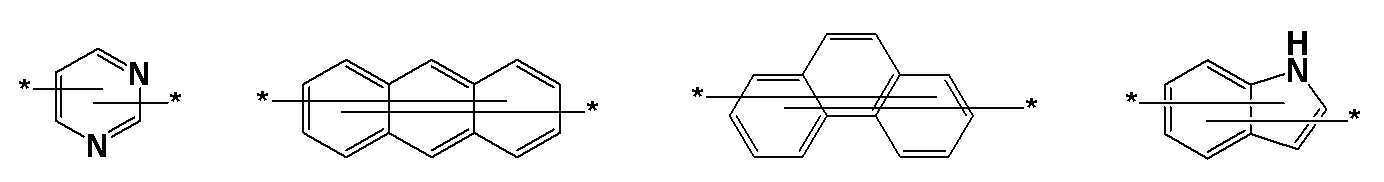
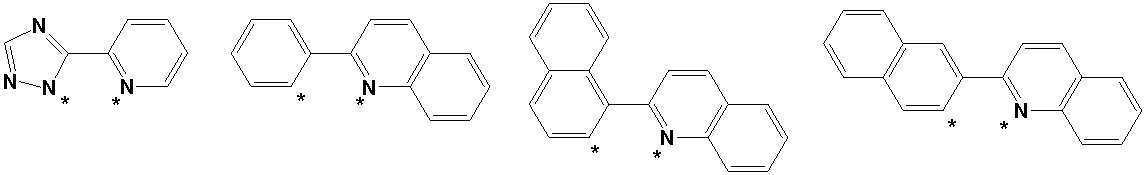
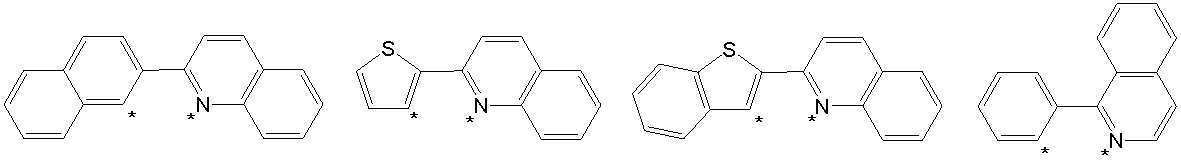
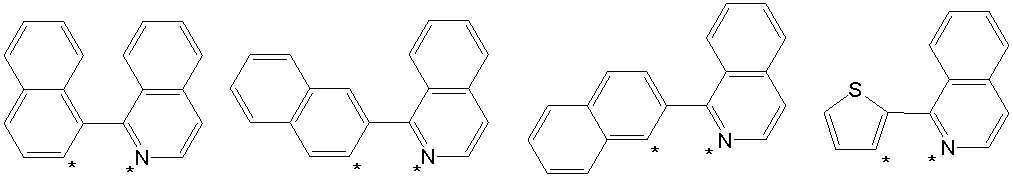
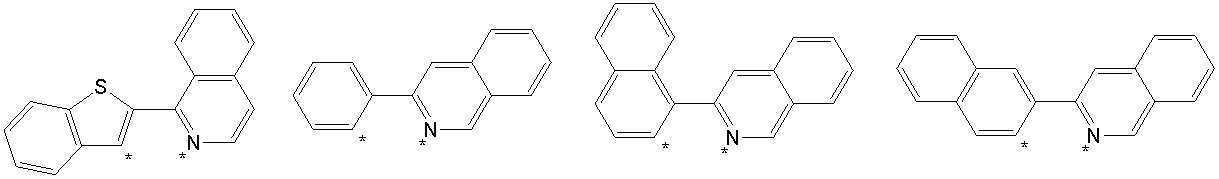
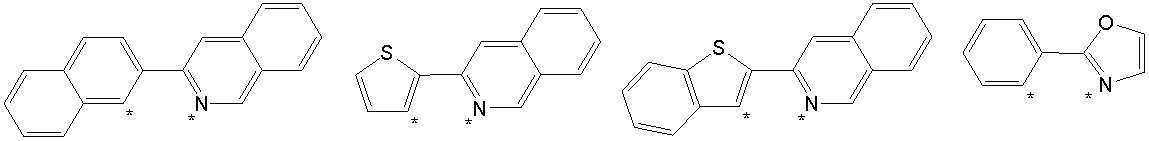
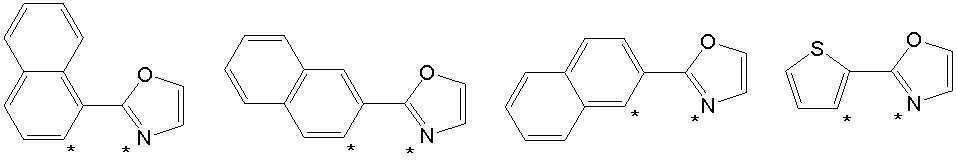
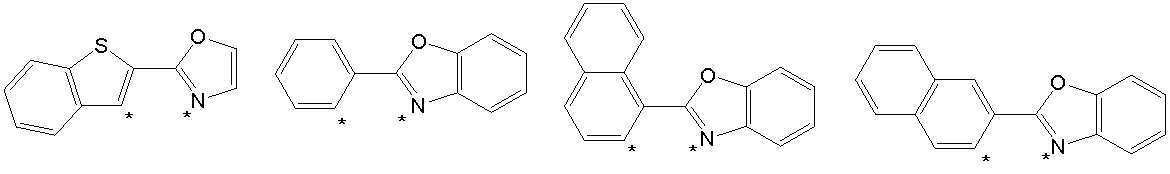
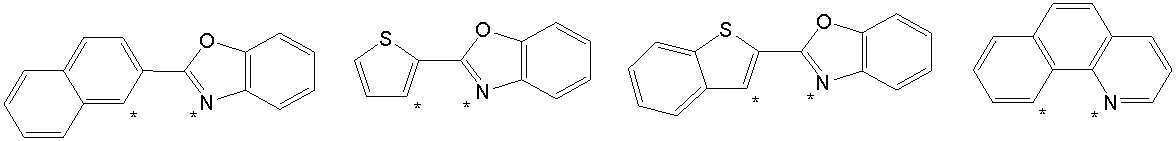
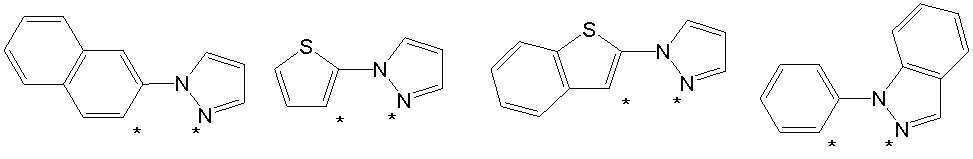
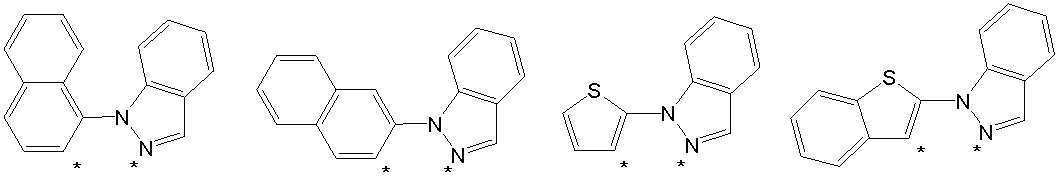
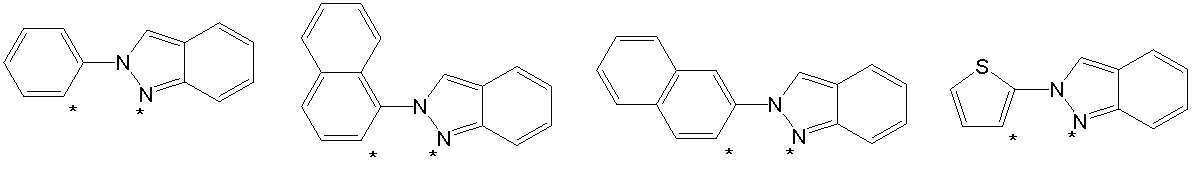
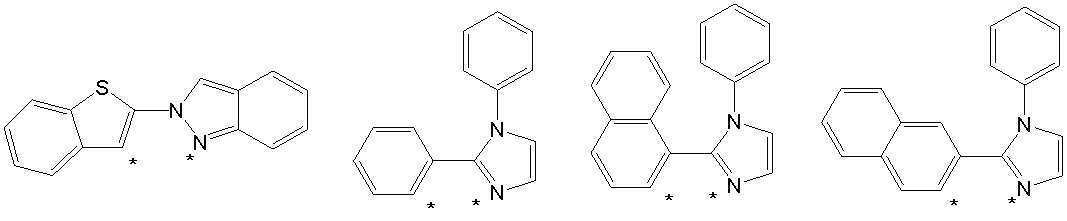
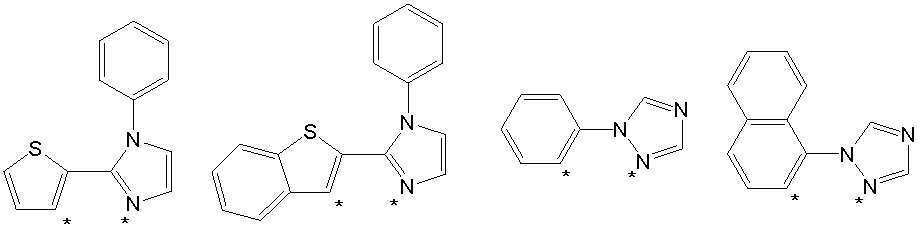
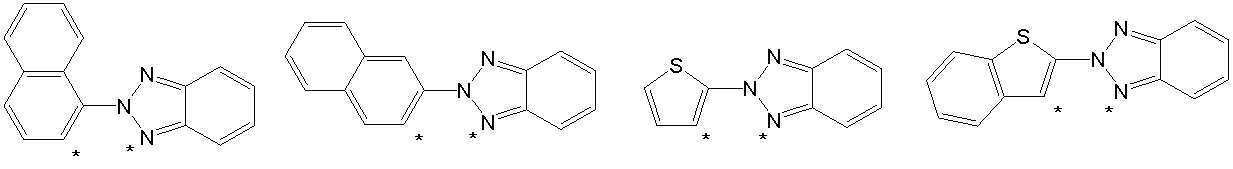
본 발명의 상기 [화학식 A] 및 [화학식 B] 에서 상기 연결기 L1 및 L2는 동일하거나 상이하며, 각각 독립적으로, 단일결합이거나, 아래 구조식 1 내지 구조식 8중에서 선택되는 어느 하나일 수 있다. In the [Formula A] and [Formula B] of the present invention, the linking groups L 1 and L 2 are the same or different, and each independently, may be a single bond, or may be any one selected from Structural Formulas 1 to 8 below.
[구조식 1] [구조식 2] [구조식 3] [구조식 4][Structural Formula 1] [Structural Formula 2] [Structural Formula 3] [Structural Formula 4]
[구조식 5] [구조식 6] [구조식 7] [구조식 8][Structural Formula 5] [Structural Formula 6] [Structural Formula 7] [Structural Formula 8]
여기서, 상기 치환기 L1 및 L2에서의 방향족 고리의 탄소자리는 수소 또는 중수소가 결합될 수 있다. Here, hydrogen or deuterium may be bonded to the carbon site of the aromatic ring in the substituents L 1 and L 2 .
또한, 본 발명에서 상기 [화학식 A] 및 [화학식 B]의 치환기 A1 내지 A4 와 R1 내지 R16은 각각 동일하거나 상이하고, 서로 독립적으로 수소, 중수소; 치환 또는 비치환된 탄소수 1 내지 20의 알킬기; 치환 또는 비치환된 탄소수 5 내지 20의 아릴기; 치환 또는 비치환된 탄소수 2 내지 20의 헤테로아릴기;중에서 선택되는 하나일 수 있으며, 상기 m, n, n'및 p는 1 또는 2일 수 있다. In addition, in the present invention, the substituents A 1 to A 4 and R 1 to R 16 of [Chemical Formula A] and [Chemical Formula B] are the same or different, respectively, and independently of each other, hydrogen and deuterium; A substituted or unsubstituted C1 to C20 alkyl group; A substituted or unsubstituted aryl group having 5 to 20 carbon atoms; A substituted or unsubstituted heteroaryl group having 2 to 20 carbon atoms; may be one selected from, and m, n, n'and p may be 1 or 2.
또한 본 발명에서는 상기 [화학식 A] 및 [화학식 B]의 화합물은 X의 변화에 따라 하기 [화학식 1] 내지 [화학식 10] 중에서 선택되는 하나일 수 있으나 이에 한정되는 것은 아니다. In addition, in the present invention, the compound of [Chemical Formula A] and [Chemical Formula B] may be one selected from the following [Chemical Formula 1] to [Chemical Formula 10] according to the change of X, but is not limited thereto.
[화학식 1] [화학식 2] [Formula 1] [Formula 2]
[화학식 3] [화학식 4] [Formula 3] [Formula 4]
[화학식 5] [화학식 6] [Formula 5] [Formula 6]
[화학식 7] [화학식 8] [Formula 7] [Formula 8]
[화학식 9] [화학식 10] [Formula 9] [Formula 10]
상기 [화학식 1] 내지 [화학식 10]에서 치환기 A1 내지 A4 와 R1 내지 R16, R33 내지 R38, L1, L2, n, n' 및 p는 각각 앞서 정의한 바와 동일하되, 상기 R10 내지 R16 중 하나는 상기 연결기 L2와 결합되는 단일결합이다.In the [Formula 1] to [Formula 10], substituents A 1 to A 4 and R 1 to R 16 , R 33 to R 38 , L 1 , L 2 , n, n'and p are each the same as defined above, but one of R 10 to R 16 is a single bond bonded to the linking group L 2 .
본 발명에서 상기 치환기 R1 내지 R8 은 각각 서로 인접하는 치환기와 연결되어 고리를 형성하지 않은 화합물일 수 있다. 즉, 본 발명에서 상기 [화학식 A] 및 [화학식 B]에서 선택되는 어느 하나로 표시되는 화합물은 상기 연결기 L1 과 L2 사이에 위치하는 연결그룹이 추가의 고리형성이 되지 않고 3개의 고리만으로 이루어지는 화합물인 것을 의미한다.In the present invention, the substituents R 1 to R 8 Each may be a compound that does not form a ring by being linked with a substituent adjacent to each other. That is, in the present invention, the compound represented by any one selected from [Chemical Formula A] and [Chemical Formula B] is composed of only three rings without additional ring formation in the linking group located between the linking groups L 1 and L 2 It means that it is a compound.
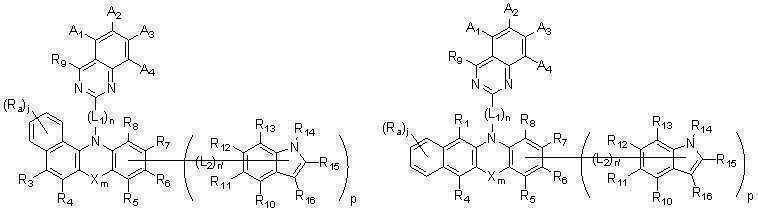
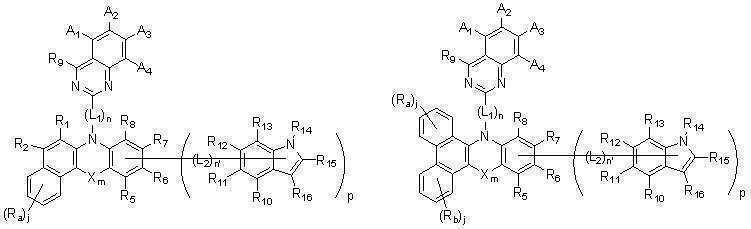
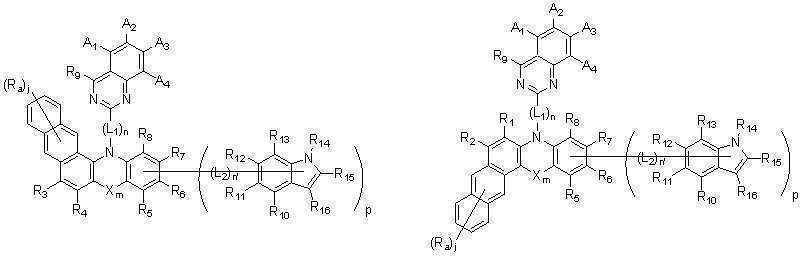
또한 본 발명에서, 상기 [화학식A] 및 [화학식 B]는 치환기 R1 내지 R4가 각각의 인접한 치환기와 서로 융합되어 단일환 또는 다환을 구성하여, 하기 [화학식 11] 내지 [화학식 22]로 표시되는 화합물로 나타낼 수 있으나, 이에 한정되는 것은 아니다.In addition, in the present invention, the [Chemical Formula A] and [Chemical Formula B] are represented by the following [Formula 11] to [Formula 22] by fusion of each of the substituents R 1 to R 4 to each other to form a monocyclic or polycyclic ring It may be represented by the compound to be displayed, but is not limited thereto.
[화학식 11] [화학식 12] [Formula 11] [Formula 12]
[화학식 13] [화학식 14] [Formula 13] [Formula 14]
[화학식 15] [화학식 16][Formula 15] [Formula 16]
[화학식 17] [화학식 18] [Formula 17] [Formula 18]
[화학식 19] [화학식 20] [Formula 19] [Formula 20]
[화학식 21] [화학식 22] [Formula 21] [Formula 22]
상기 [화학식 1] 내지 [화학식 22]에서 치환기 A1 내지 A4 와 R1 내지 R16, X, L1, L2, m, n, n' 및 p는 각각 앞서 정의한 바와 동일하되, 상기 R10 내지 R16 중 하나는 상기 연결기 L2와 결합되는 단일결합이며, Ra 및 Rb는 상기 R1 내지 R16에서 정의한 바와 동일하고, j는 1내지 6의 정수이며, j가 2이상인 경우 각각의 Ra는 동일하거나 상이할 수 있고 각각의 Rb도 동일하거나 상이할 수 있다. Substituents A 1 to A 4 and R 1 to R 16 , X, in the [Formula 1] to [Formula 22] L 1 , L 2 , m, n, n'and p are each the same as defined above, but one of the R 10 to R 16 is a single bond bonded to the linking group L 2, and Ra and Rb are the R 1 to Same as defined in R 16 , j is an integer from 1 to 6, and when j is 2 or more, each Ra can be the same or different and each Rb can be the same or different.
또한 본 발명에서 상기 [화학식 A] 및 [화학식 B] 의 치환기 R9는 중수소 또는 중수소를 포함하는 관능기일 수 있고, 상기 치환기 A1 내지 A4 는 중수소를 포함할 수 있다. 즉, 상기 치환기 R9및, 치환기 A1 내지 A4 은, 중수소, 중수소가 치환된 알킬기, 중수소가 치환된 아릴기, 중수소 치환된 헤테로아릴기 등의 관능기일 수 있다.In addition, in the present invention, the substituent R 9 of [Chemical Formula A] and [Chemical Formula B] may be a functional group including deuterium or deuterium, and the substituents A 1 to A 4 may include deuterium. That is, the substituent R 9 and the substituents A 1 to A 4 may be functional groups such as deuterium, an alkyl group substituted with deuterium, an aryl group substituted with deuterium, and a heteroaryl group substituted with deuterium.
또한 본 발명에서 상기 [화학식 A] 및 [화학식 B]의 치환기 A1 내지 A4 는 각각 수소 또는 중수소일 수 있다. In addition, in the present invention, the substituents A 1 to A 4 of [Chemical Formula A] and [Chemical Formula B] may be hydrogen or deuterium, respectively.
상기 중수소로 치환된 화합물은 수소와 결합된 화합물과 비교하여 중수소의 원자 질량이 수소보다 2배 커서 더 낮은 영점 에너지 및 더 낮은 진동 에너지 수준을 나타낸다. 또한, 중수소와 관련된 화학적 결합 길이 등의 물리화학적 특성은 수소와 상이하게 나타나며, 특히, C-H 결합에 비해 C-D 결합의 신장 진폭이 더 작아서, 중수소의 반데르발스 반경은 수소보다 작으며 일반적으로, C-D 결합이 C-H 결합보다 더 짧고 더 강함을 나타낸다. The deuterium-substituted compound exhibits a lower zero point energy and lower vibration energy level as the atomic mass of deuterium is twice that of hydrogen compared to the compound bound to hydrogen. In addition, the physicochemical properties, such as the length of chemical bonds related to deuterium, appear different from those of hydrogen, and in particular, the elongation amplitude of the CD bond is smaller than that of the CH bond, so the Van der Waals radius of deuterium is smaller than that of hydrogen, and in general, CD It indicates that the bond is shorter and stronger than the CH bond.
또한 중수소로 치환된 경우에는 바닥상태의 에너지가 낮아지며, 중수소, 탄소의 결합길이가 짧아짐에 따라, 분자 중심 부피(Molecular hardcore volume)가 줄어들고, 이에 따라 전기적 극성화도(Electroical polarizability)를 줄일 수 있으며, 분자간 상호작용(Intermolecular interaction)을 약하게 함으로써, 박막 부피를 증가시킬 수 있음이 알려지고 있다. 이러한 특성은 박막의 결정화도를 낮추는 효과 즉, 비결정질(Amorphous) 상태를 만들 수 있으며, 일반적으로 유기발광소자의 수명 및 구동특성을 높이기 위해 효과적일 수 있으며, 내열성이 보다 향상될 수 있다.In addition, when substituted with deuterium, the energy in the ground state is lowered, and as the bond length of deuterium and carbon is shortened, the molecular hardcore volume decreases, and accordingly, the electrical polarizability can be reduced. It is known that the volume of the thin film can be increased by weakening the intermolecular interaction. Such a characteristic may be effective in lowering the crystallinity of the thin film, that is, an amorphous state, and in general, it may be effective to increase the life and driving characteristics of the organic light emitting device, and the heat resistance may be further improved.
또한, 본 발명에서 상기 연결기 L1 및 L2는 동일하거나 상이하며, 각각 독립적으로, 단일결합이거나, 또는 이고, n, n'및 p 는 각각 1일 수 있다. In addition, in the present invention, the linking groups L 1 and L 2 are the same or different, and each independently, is a single bond, or And n, n'and p may each be 1.
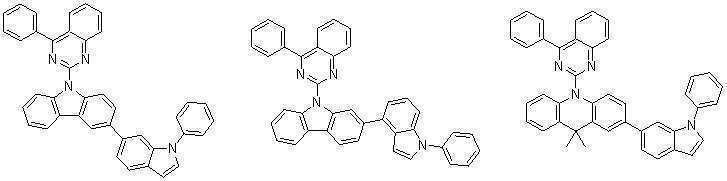
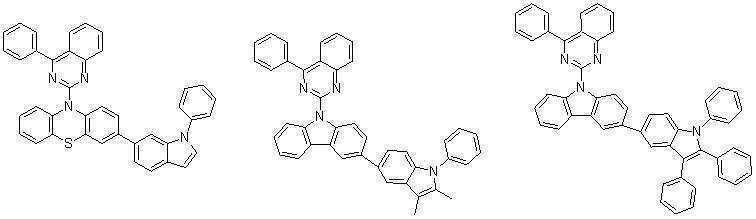
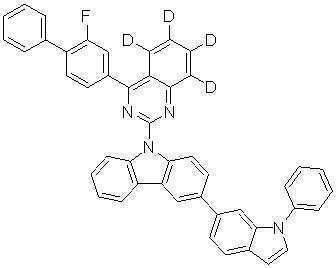
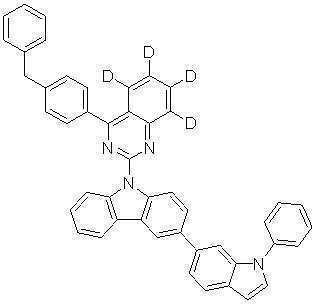
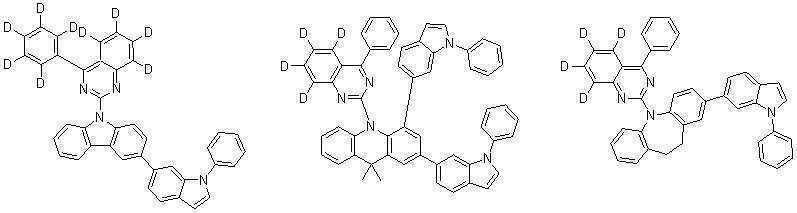
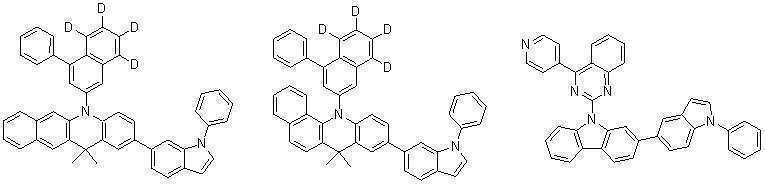
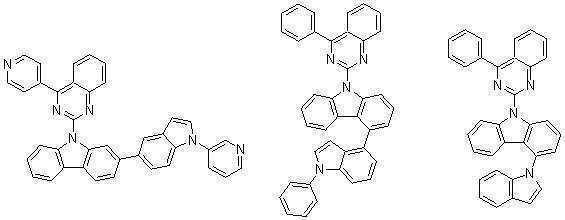
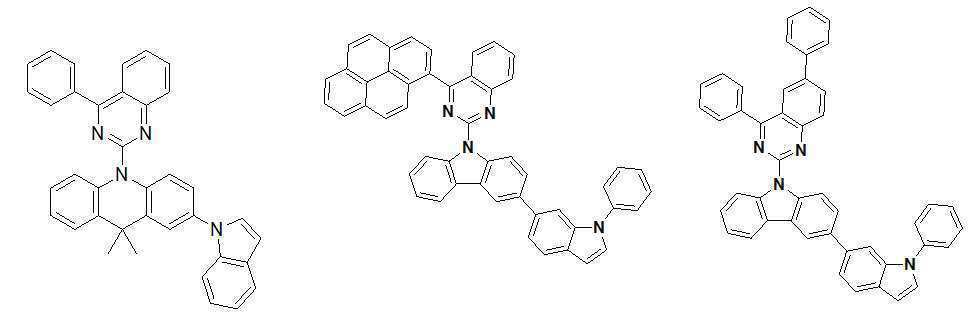
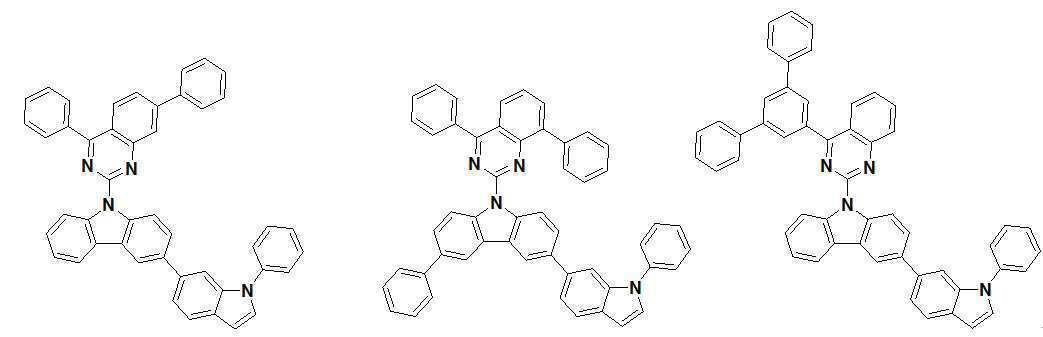
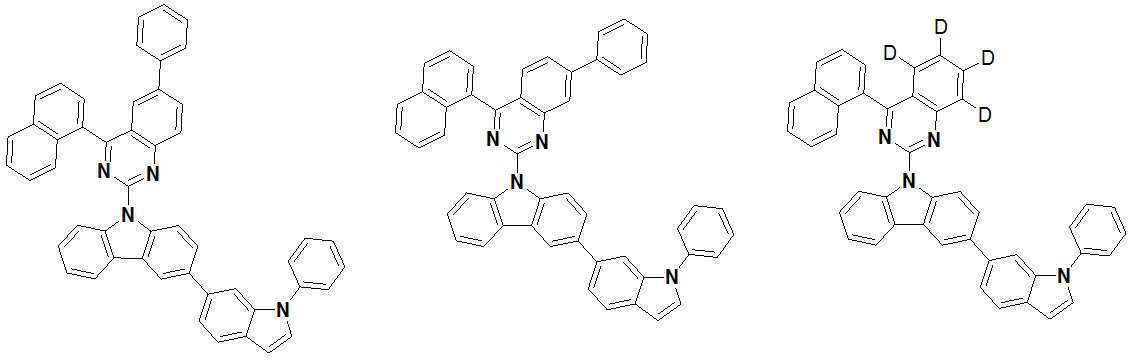
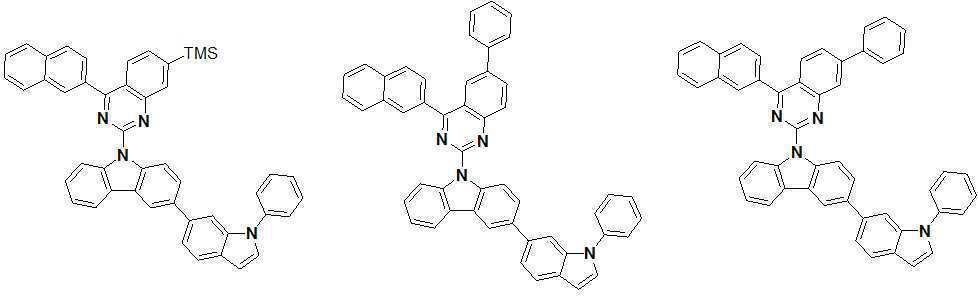
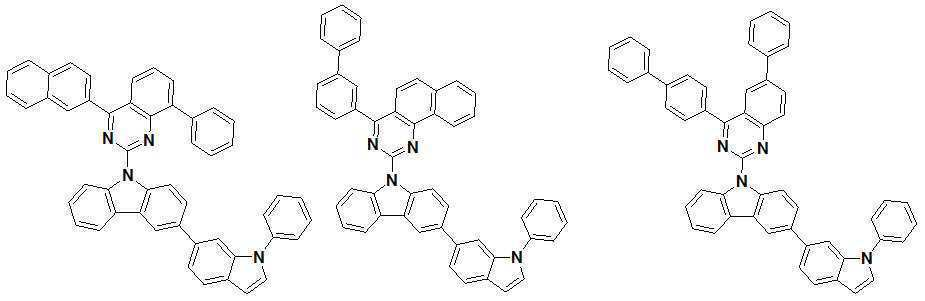
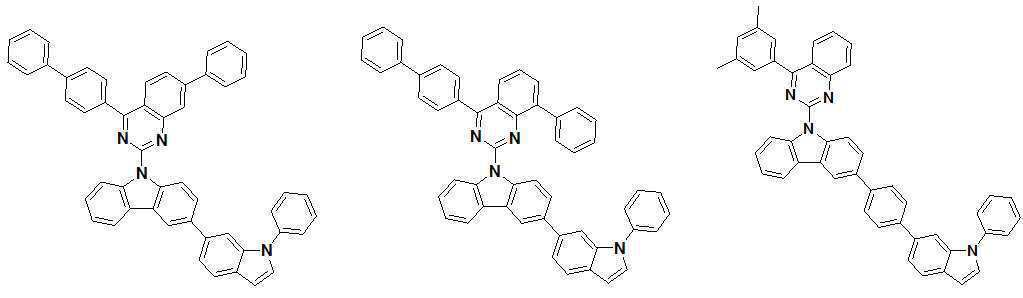
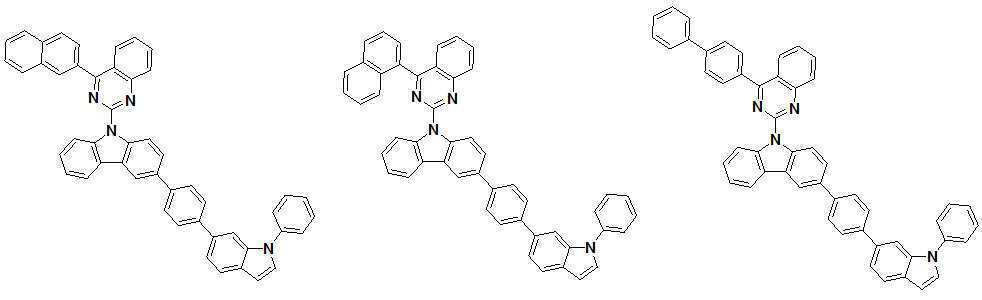
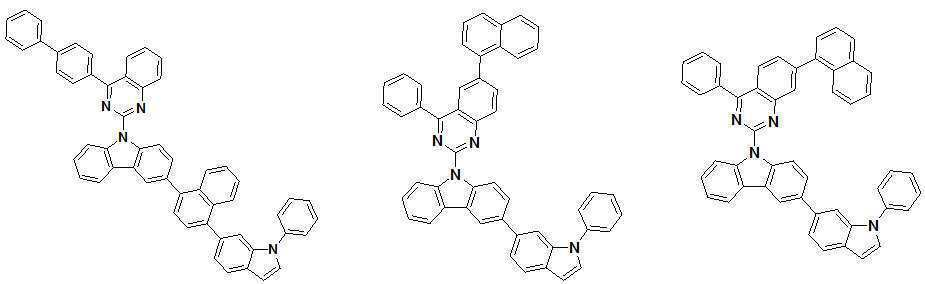
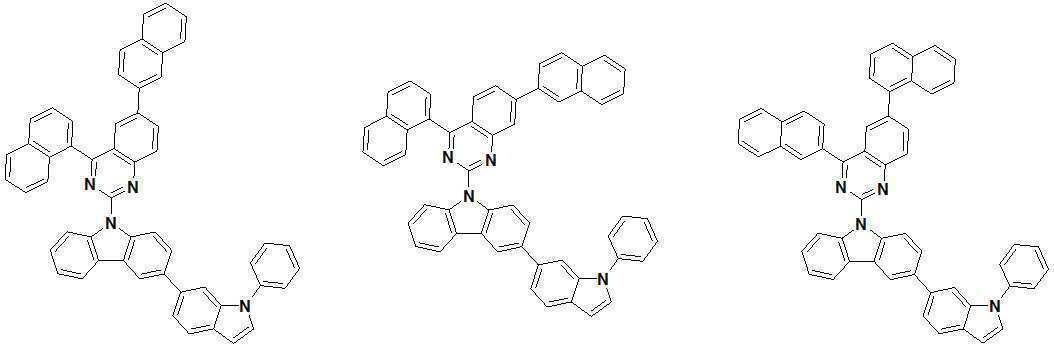
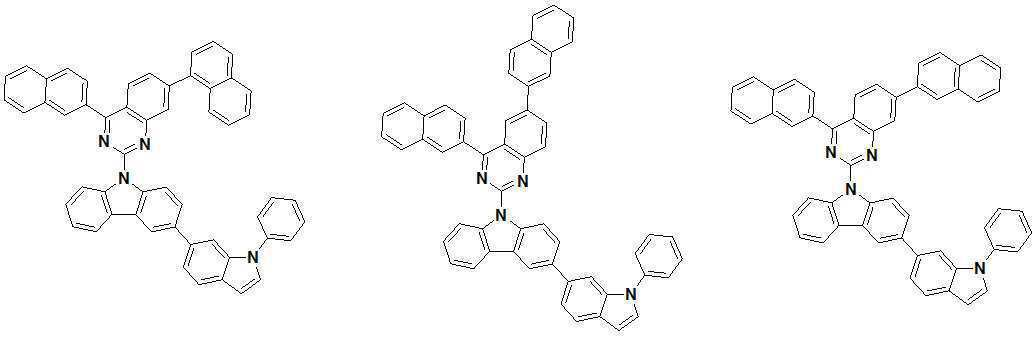
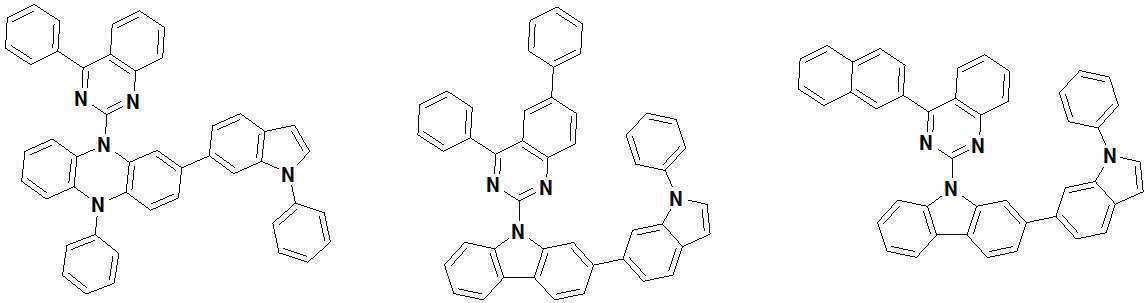
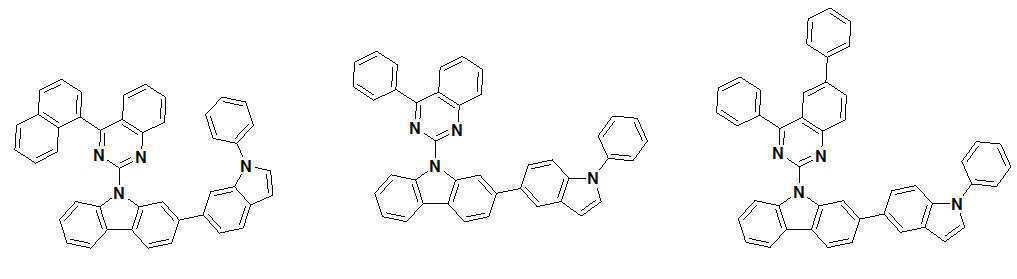
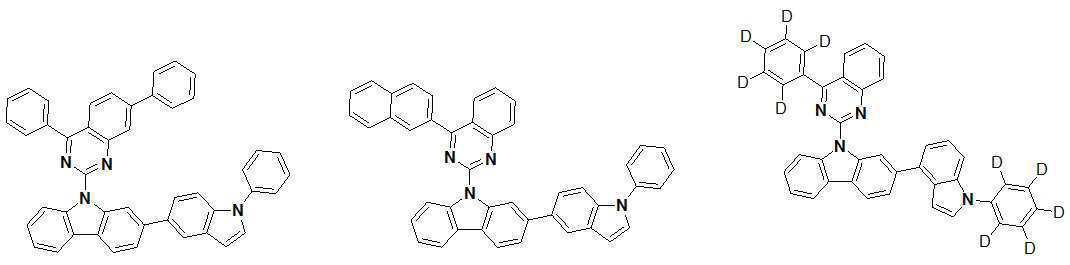
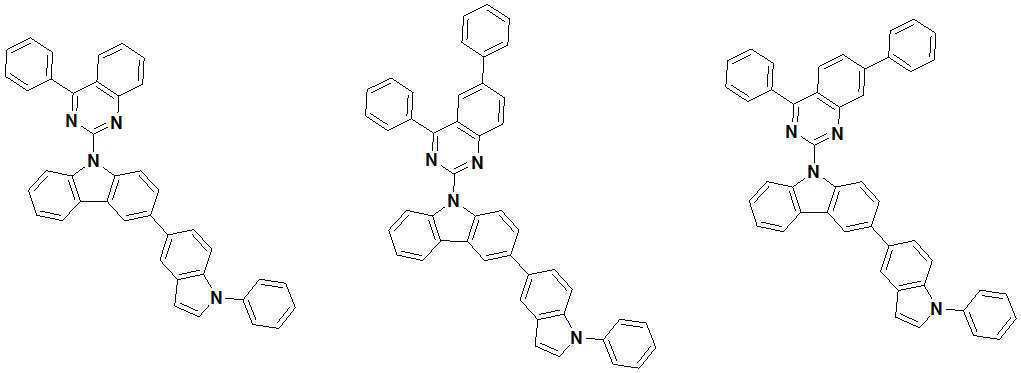
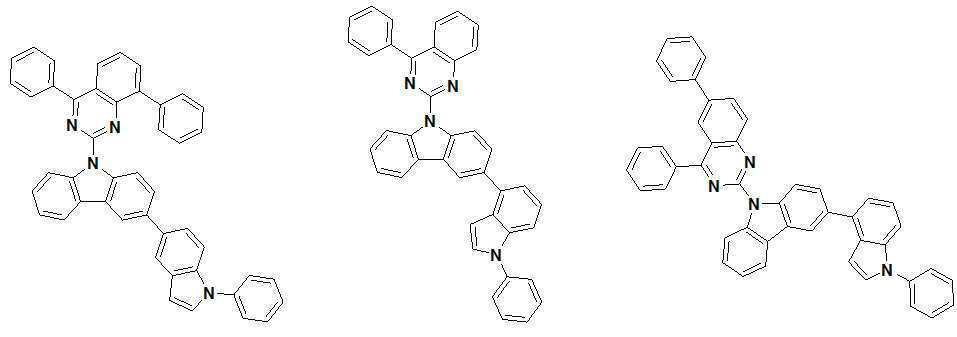
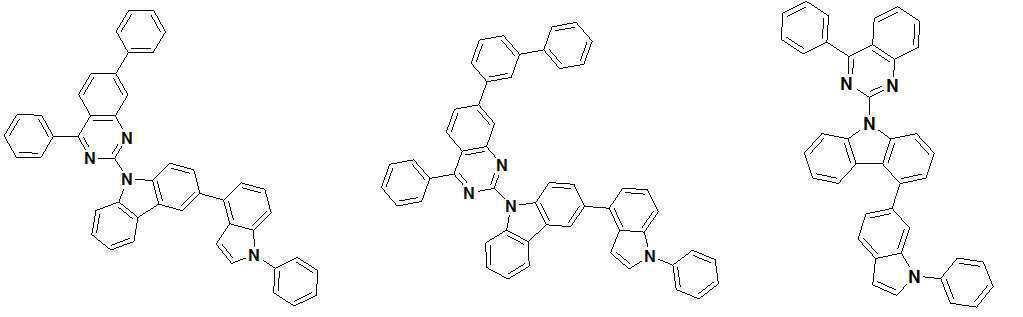
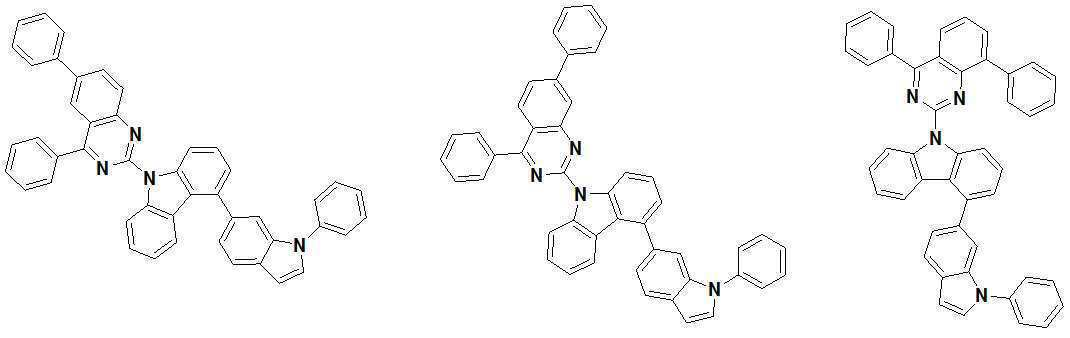
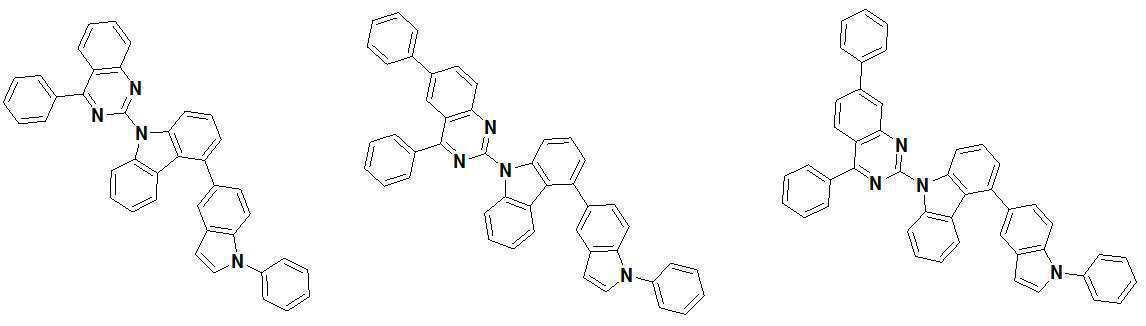
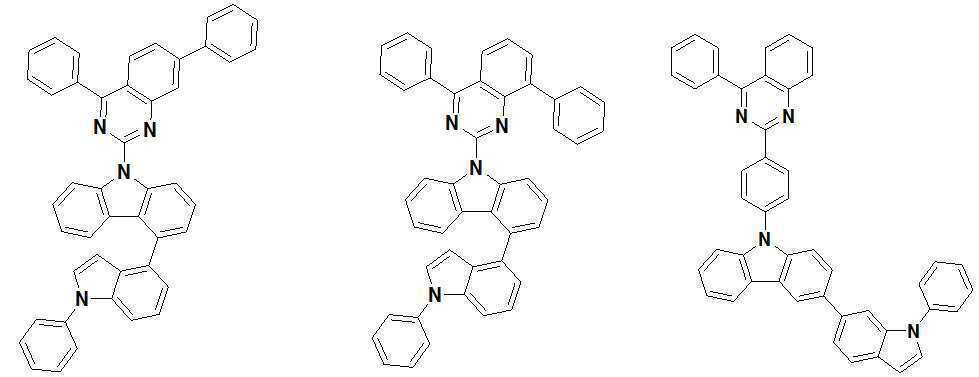
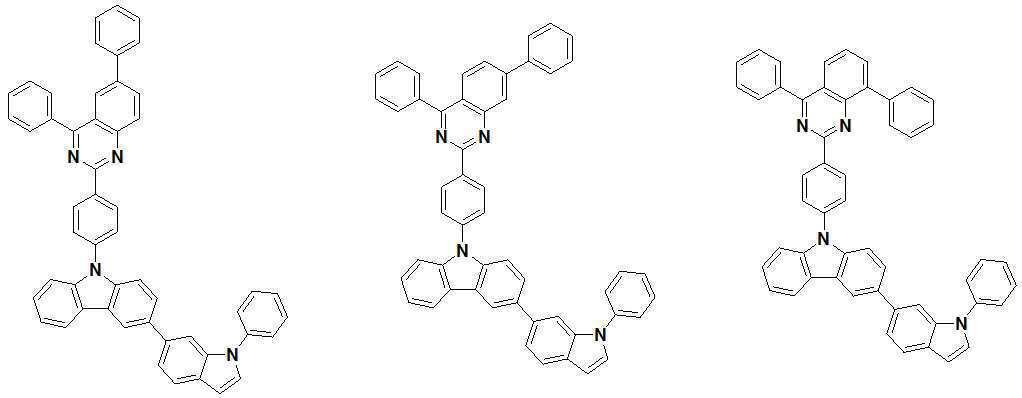
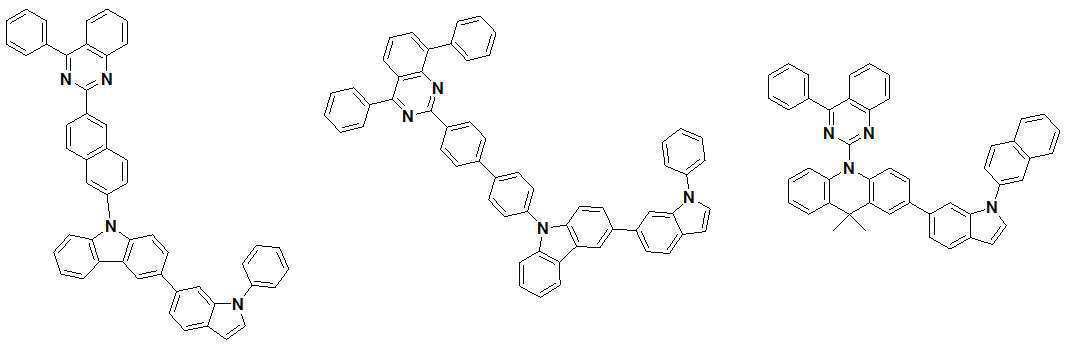
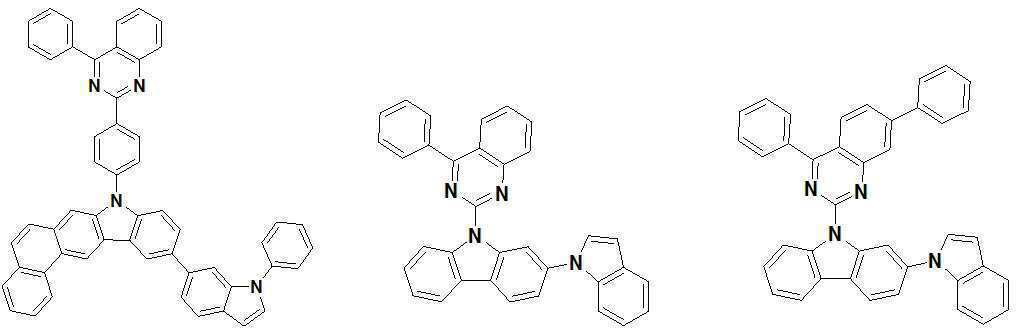
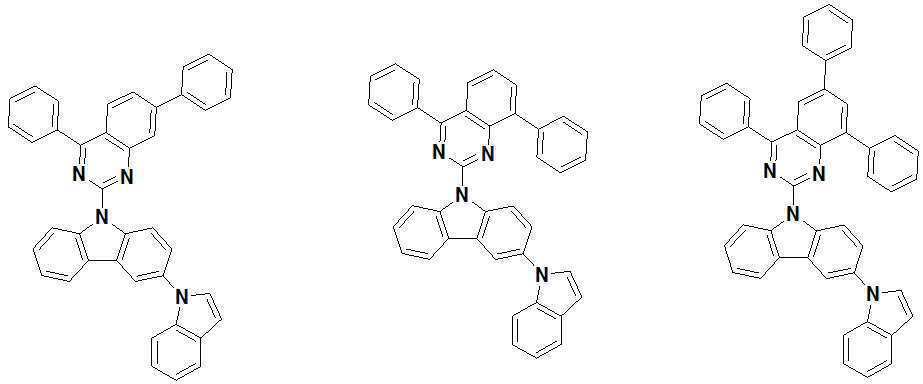
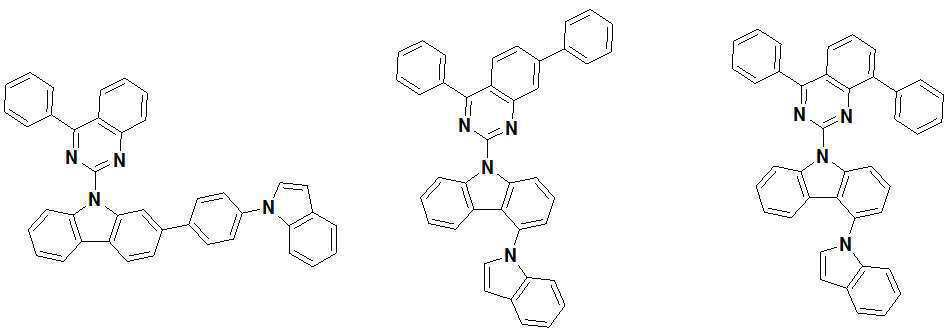
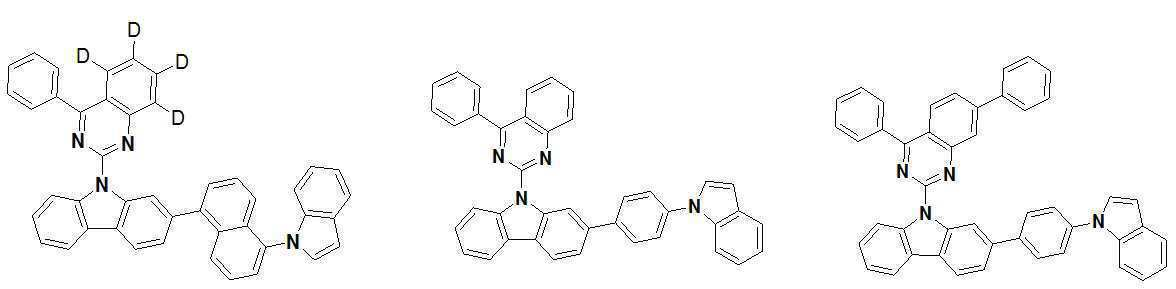
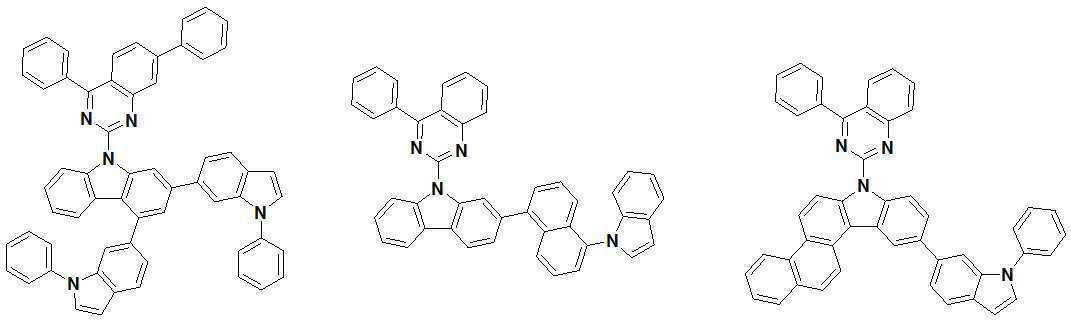
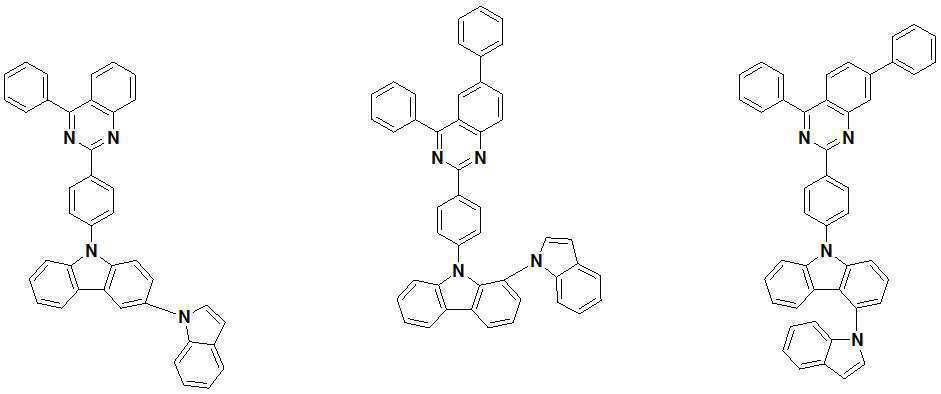
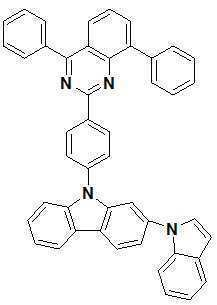
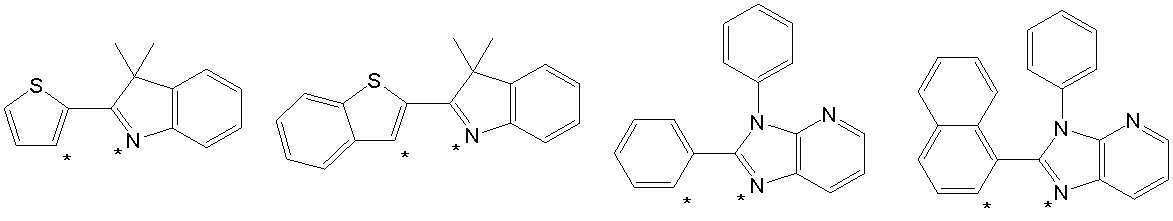
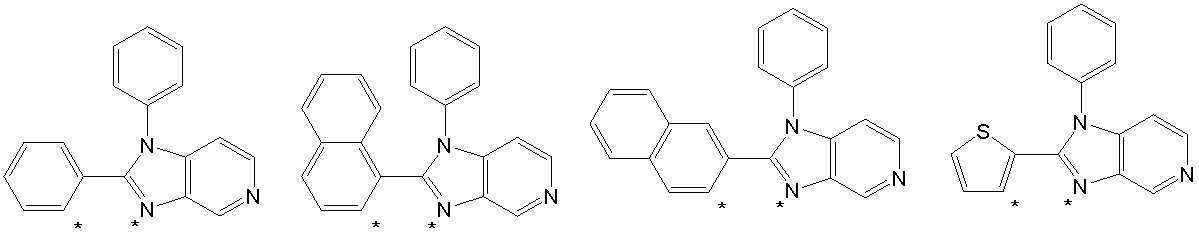
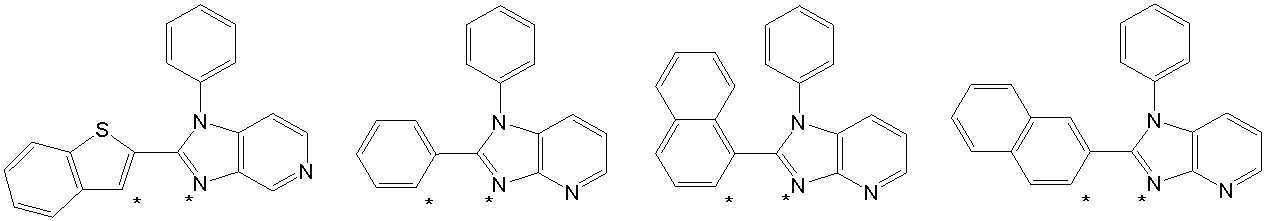
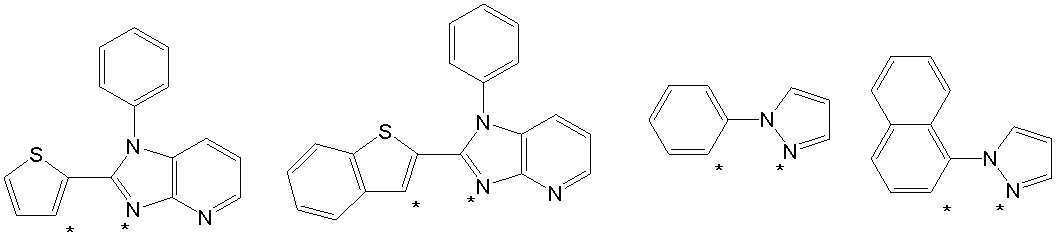
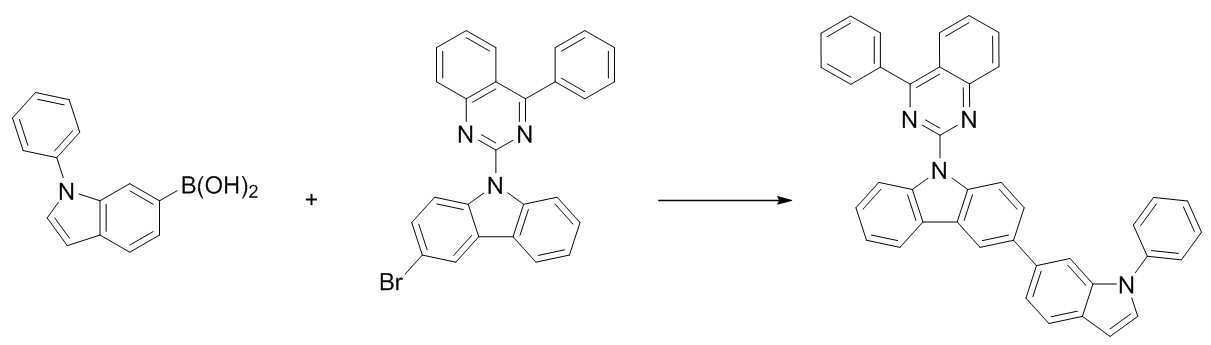
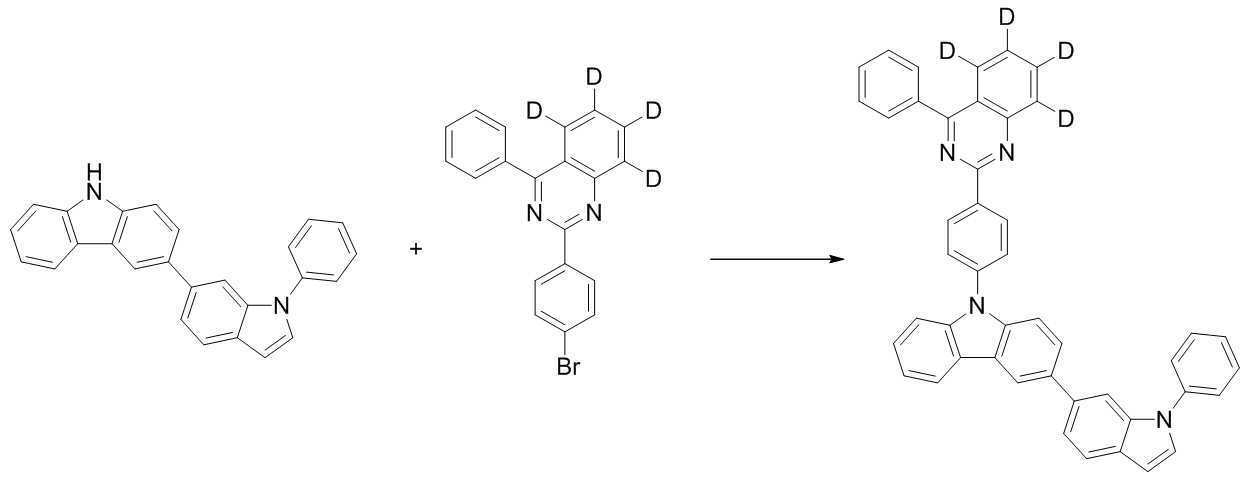
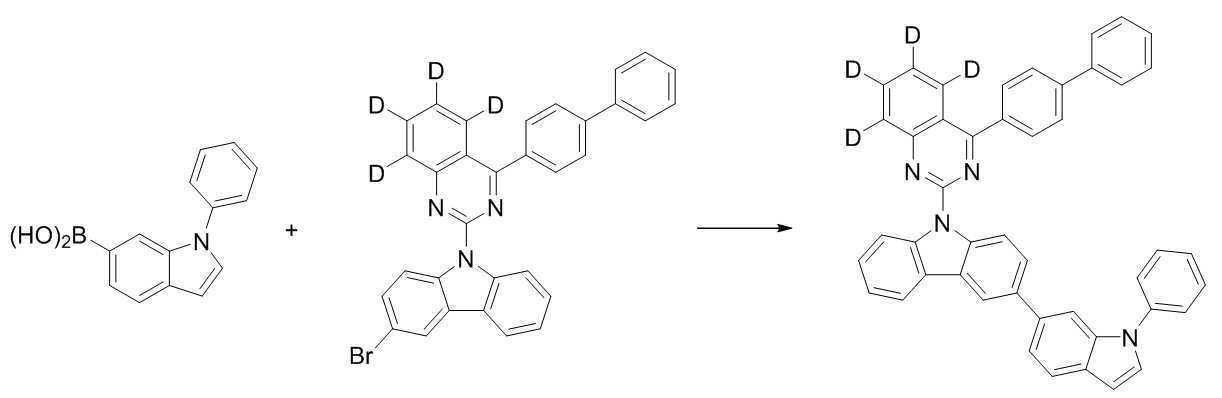
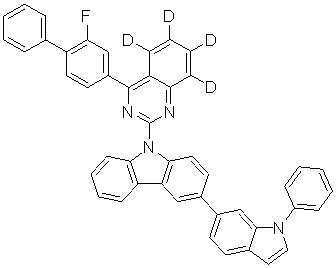
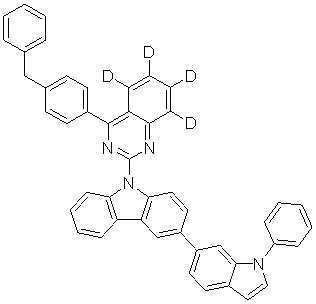
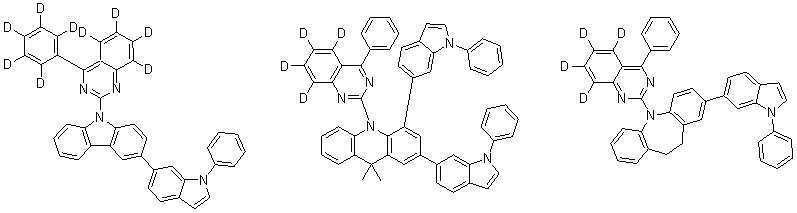
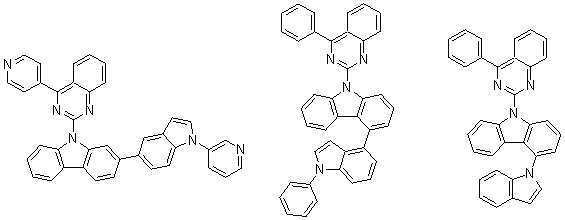
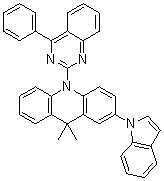
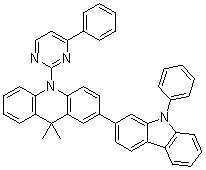
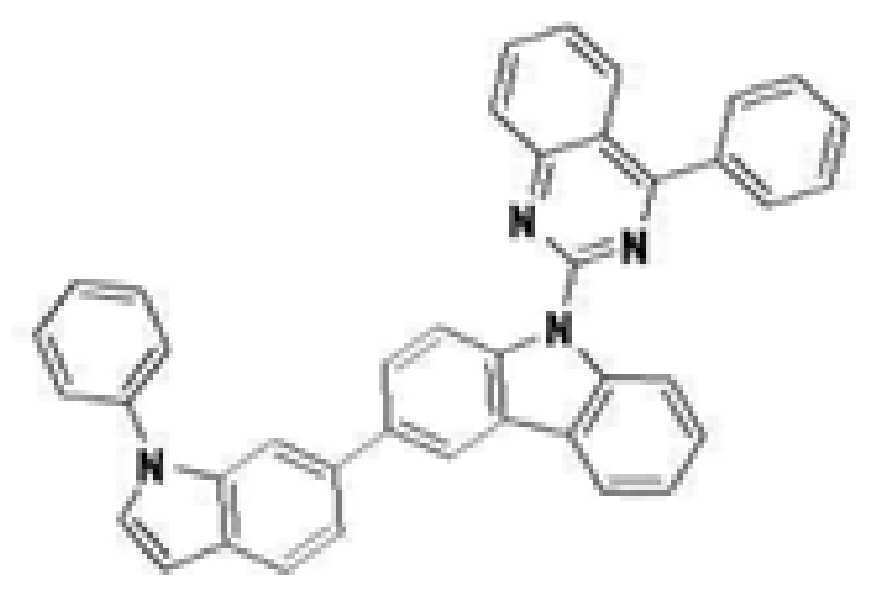
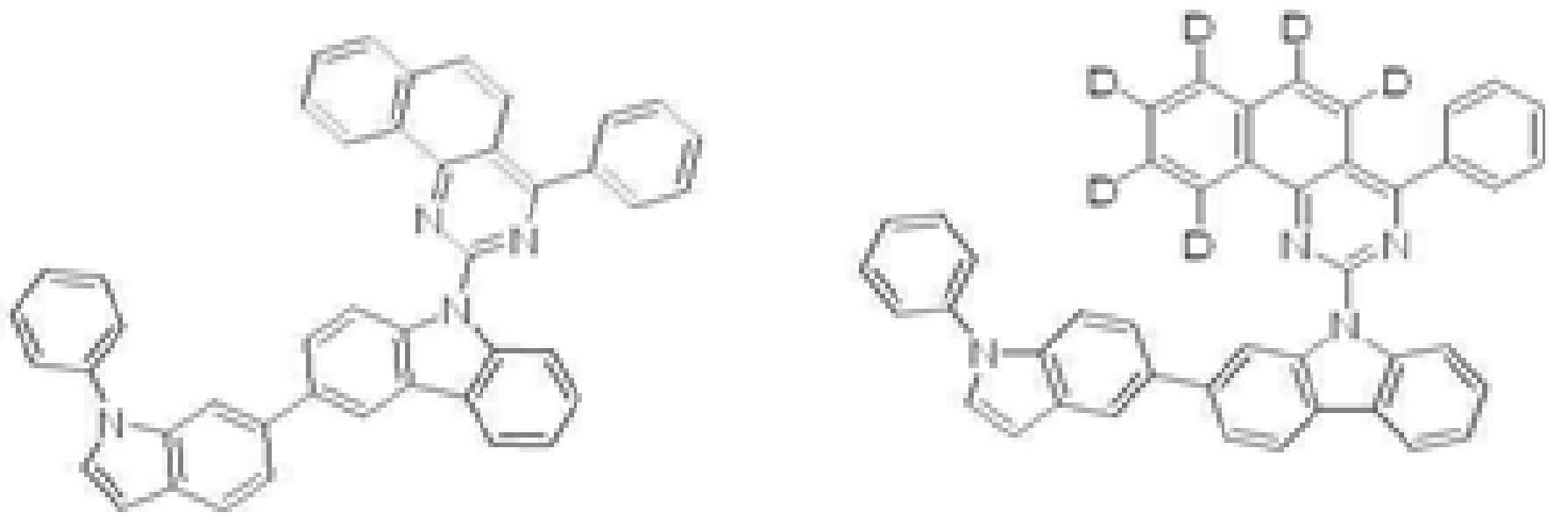
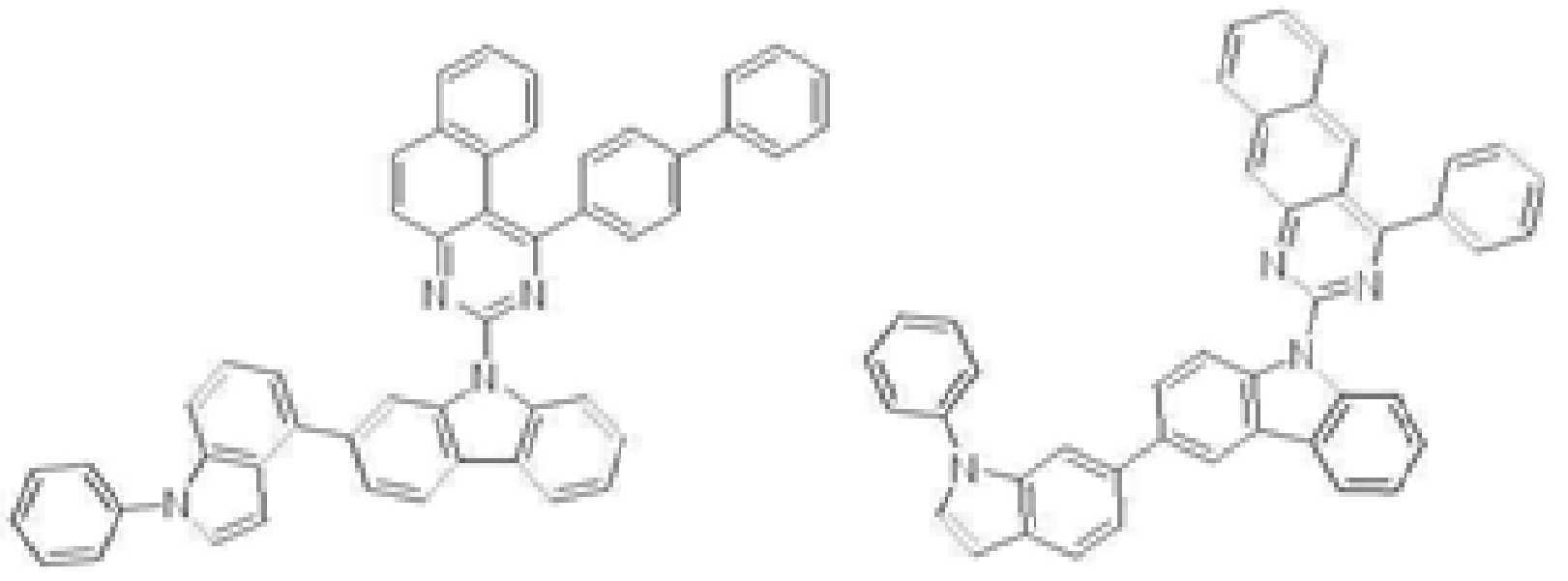
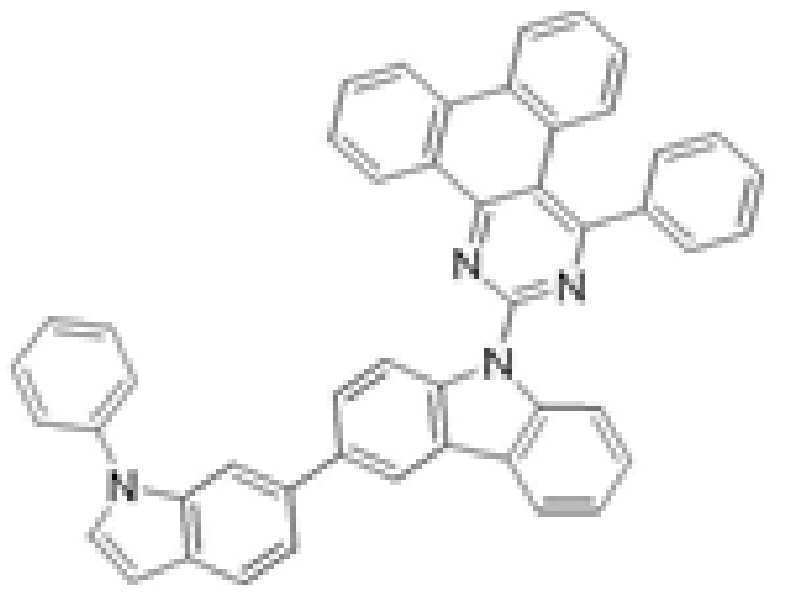
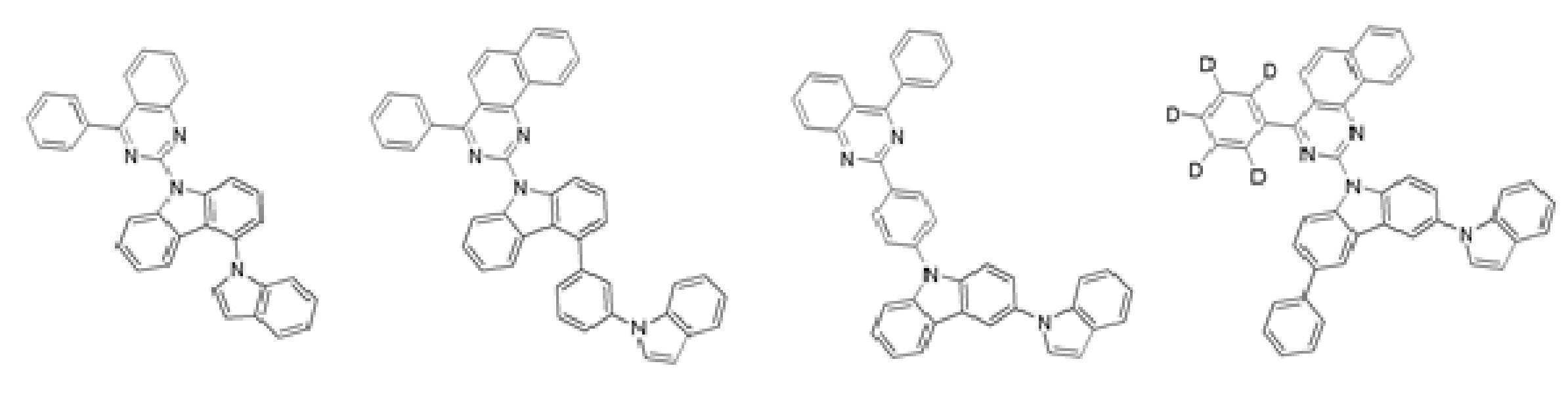
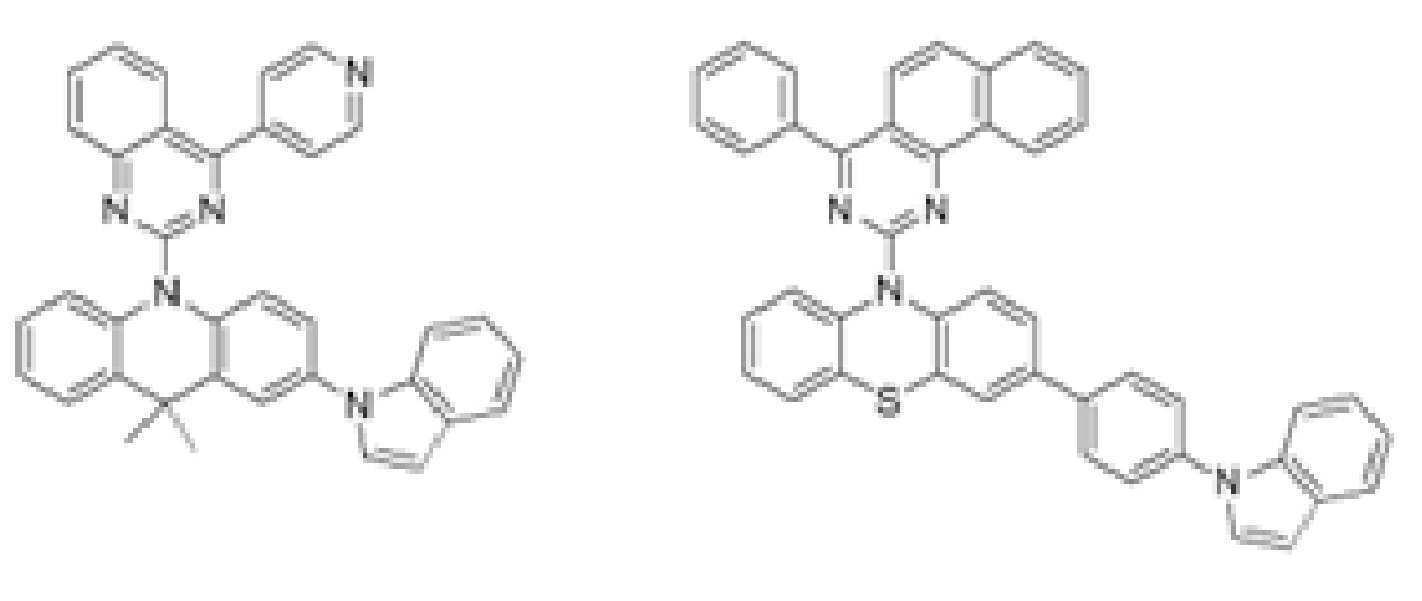
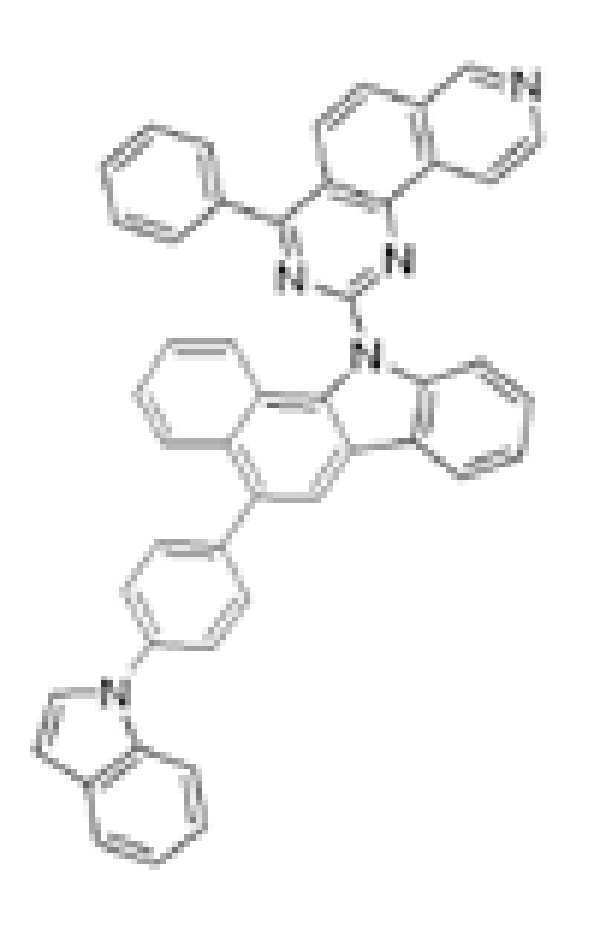
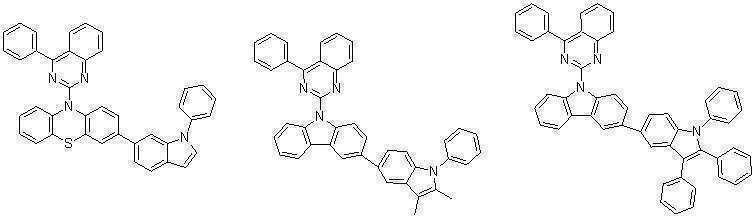
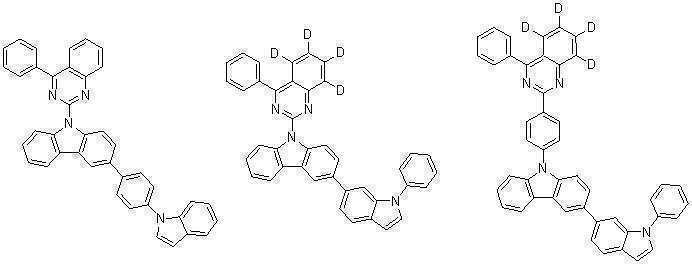
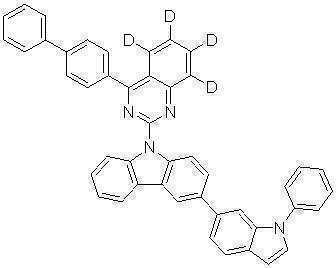
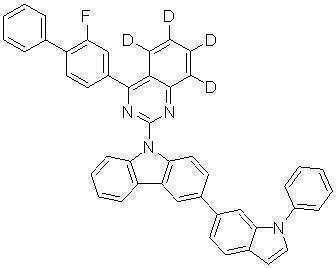
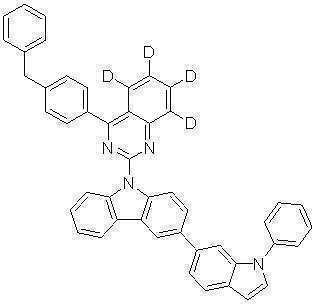
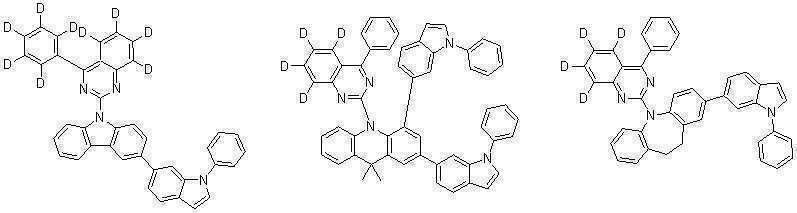
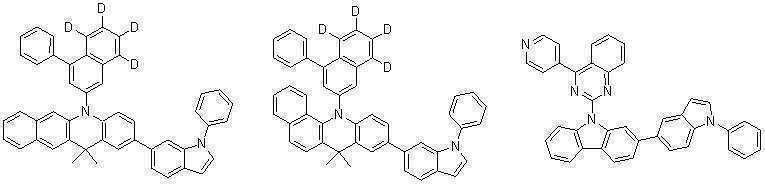
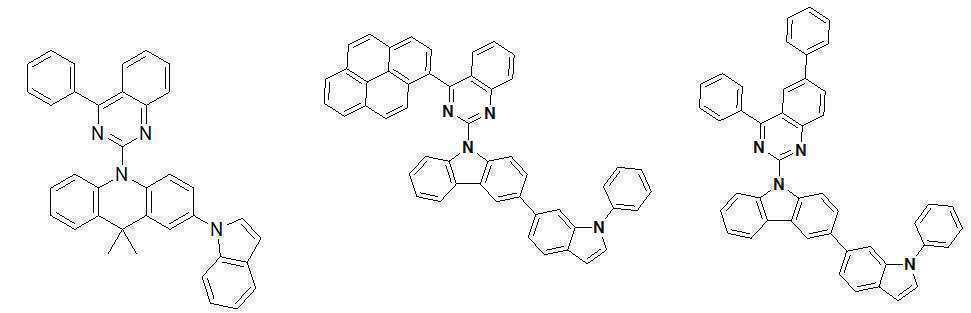
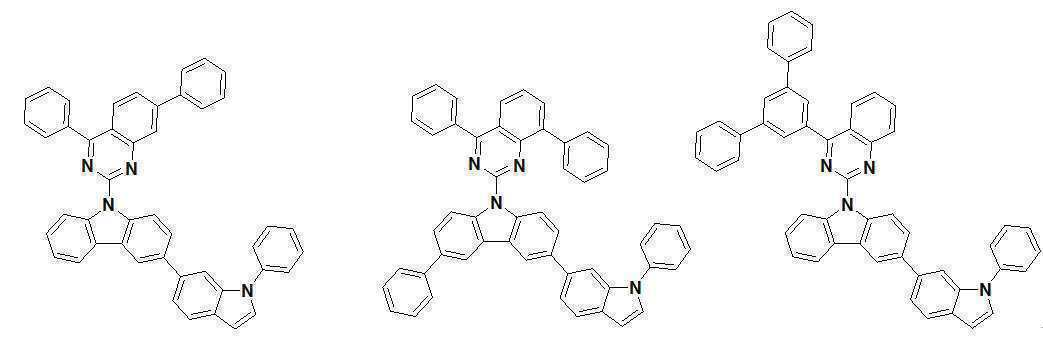
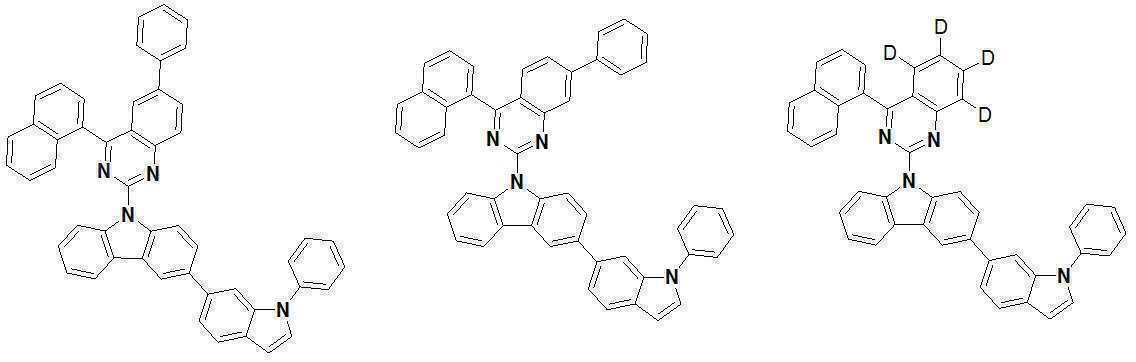
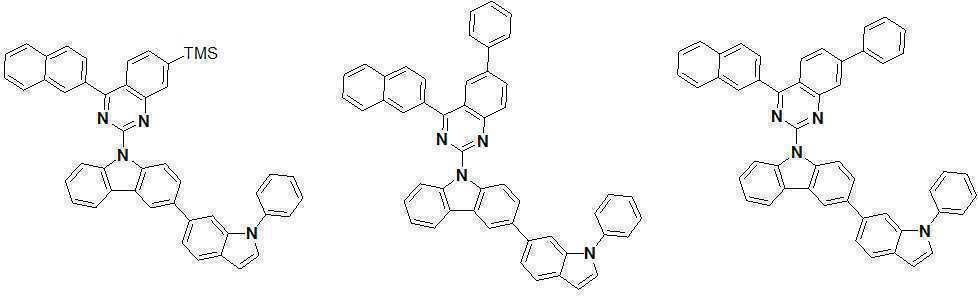
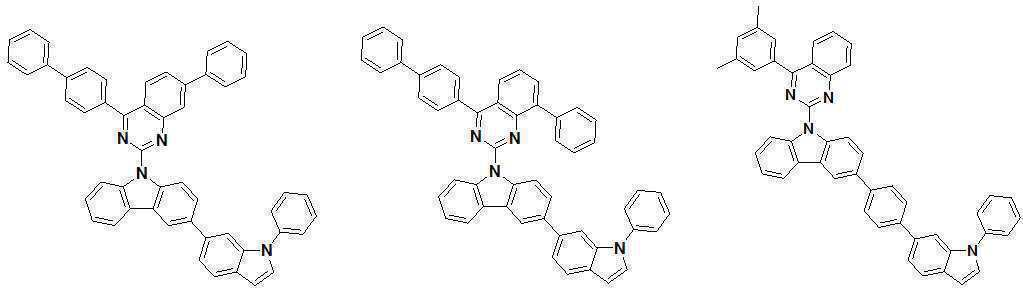
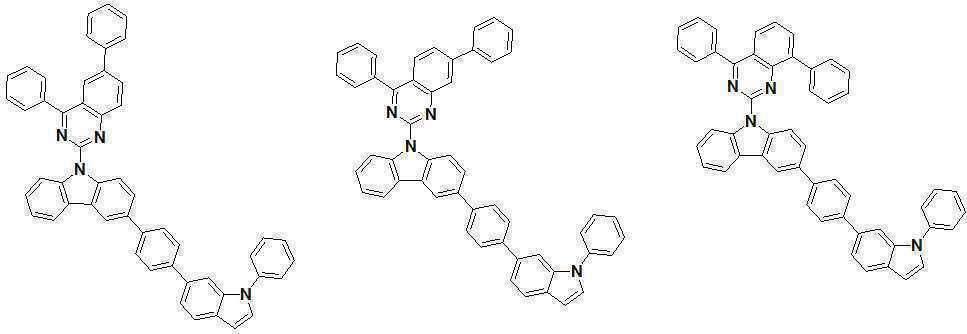
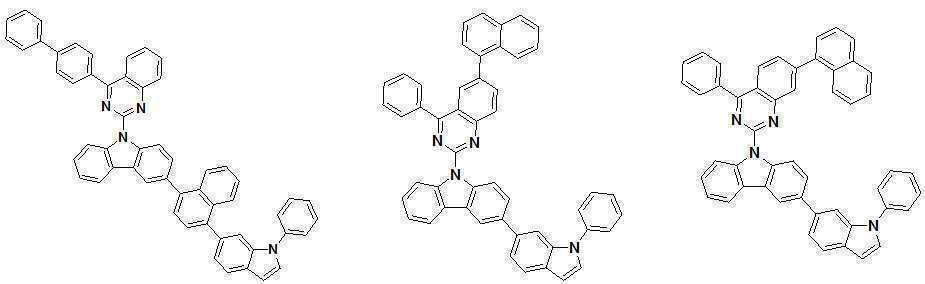
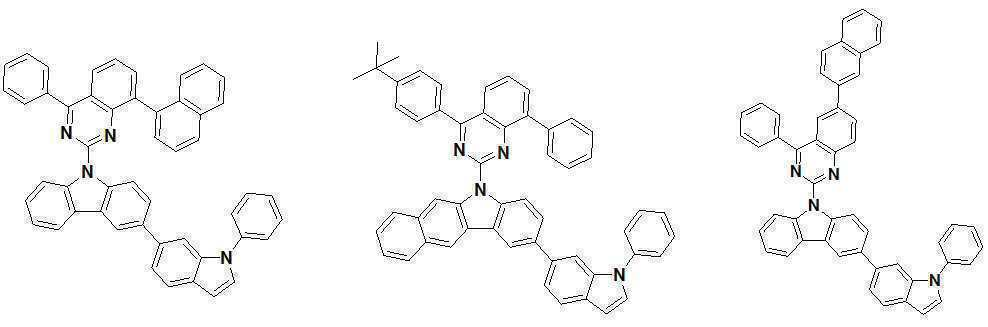
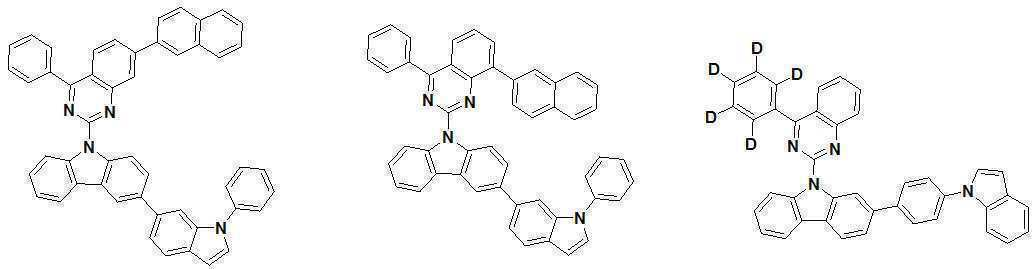
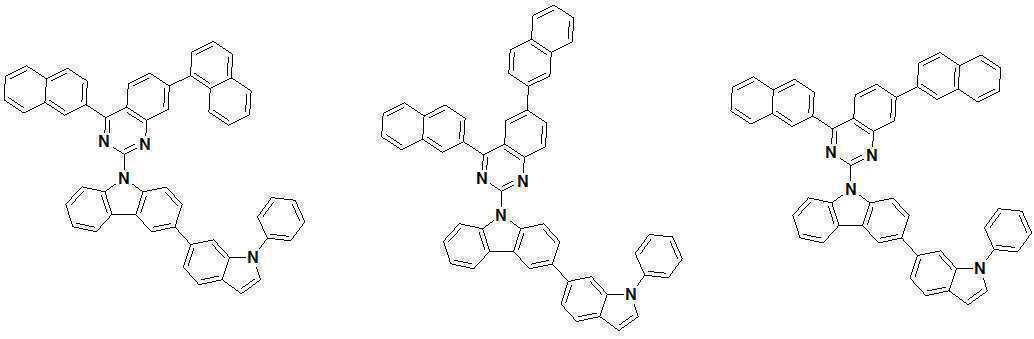
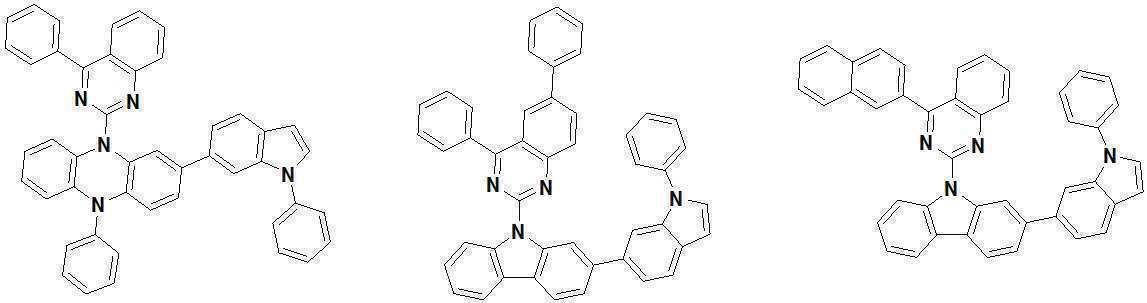
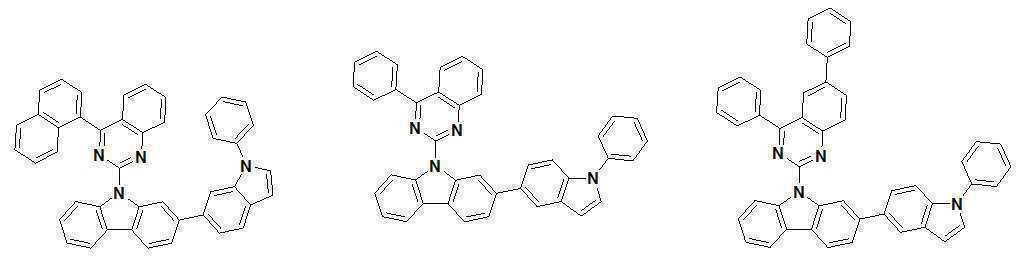
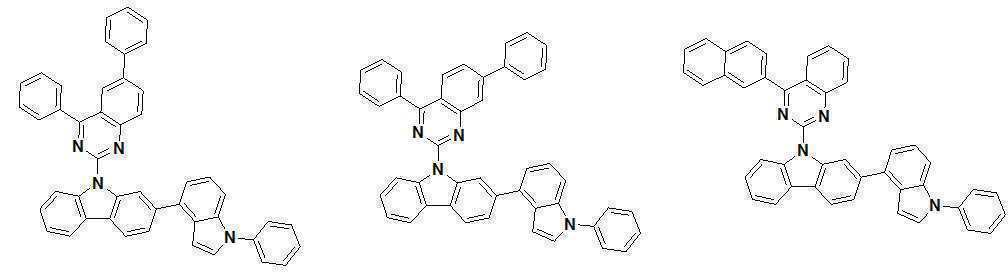
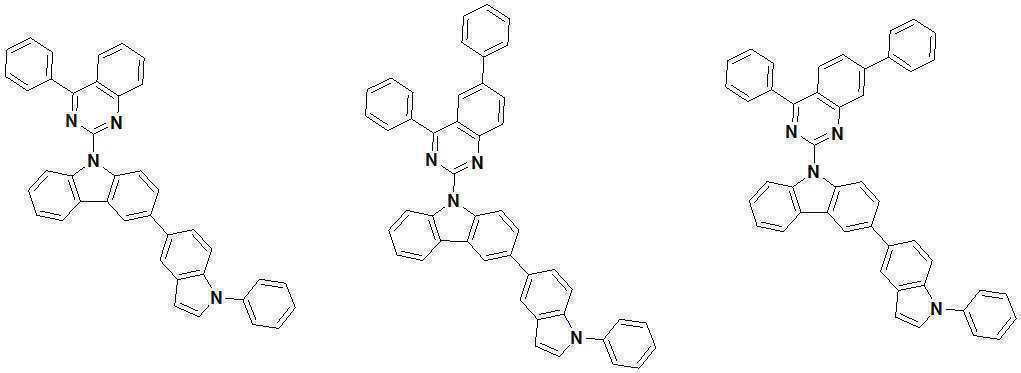
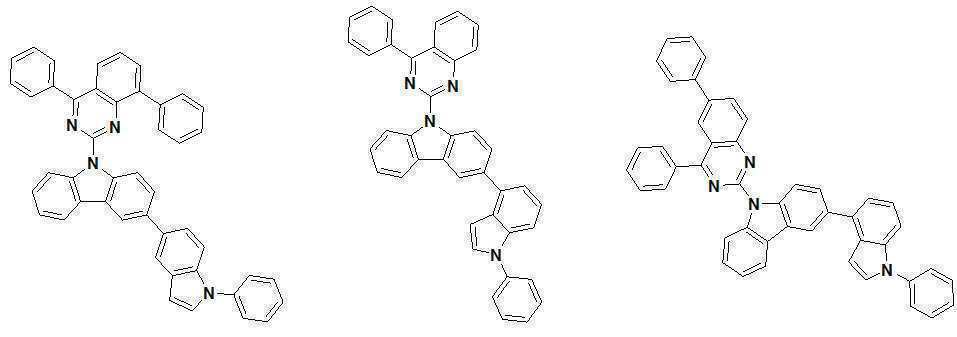
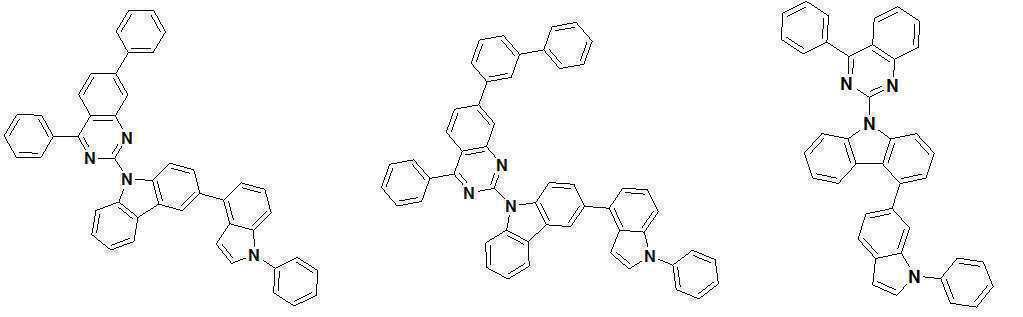
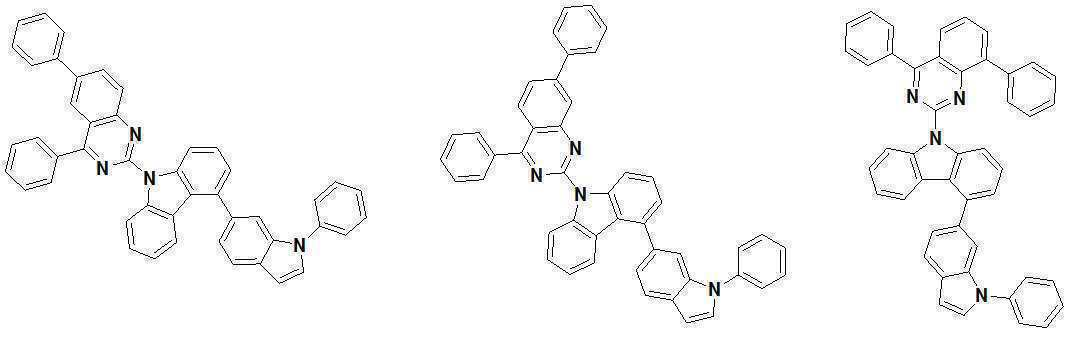
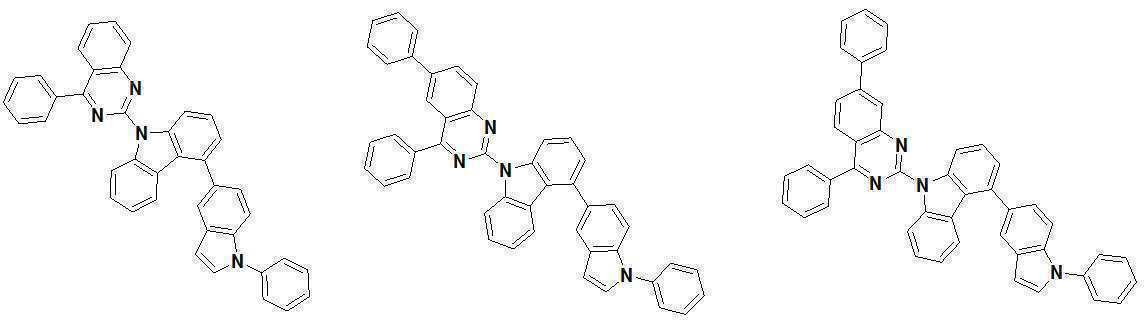
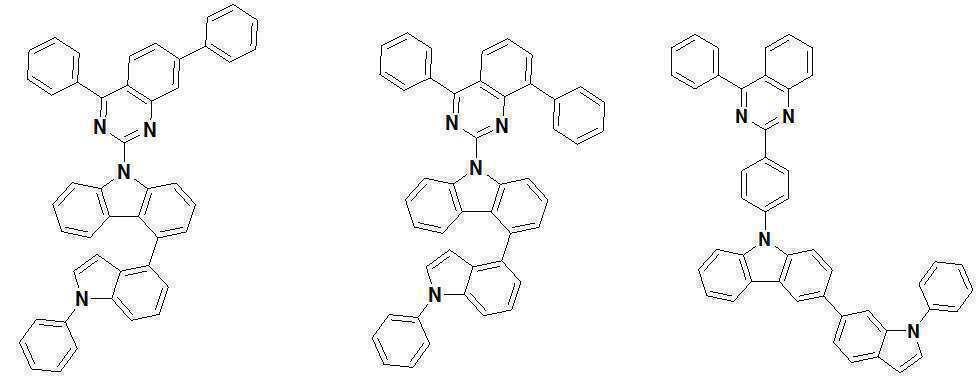
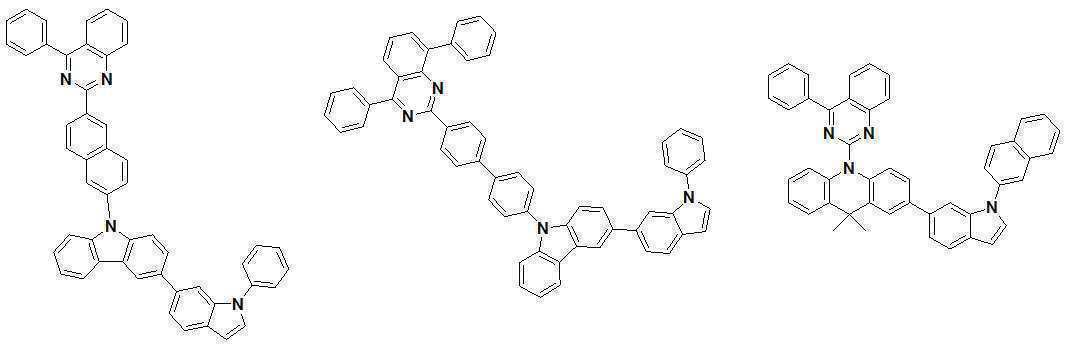
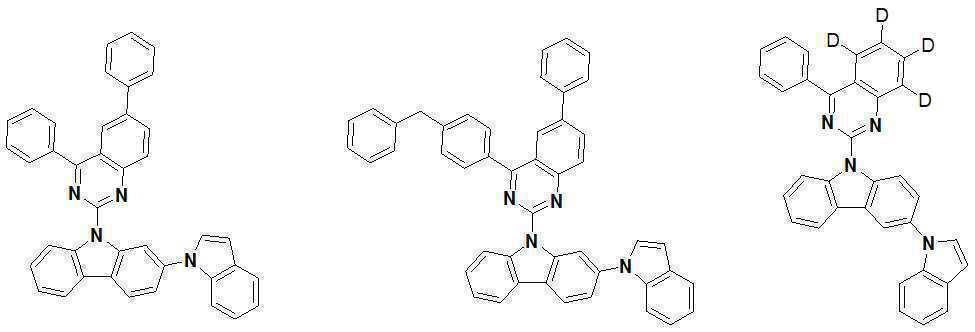
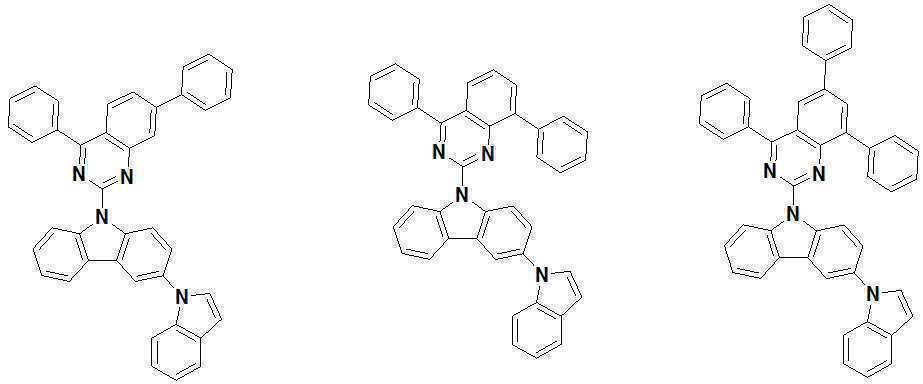
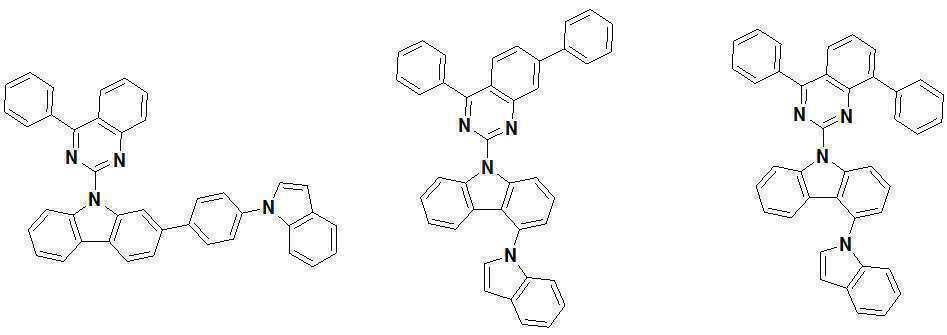
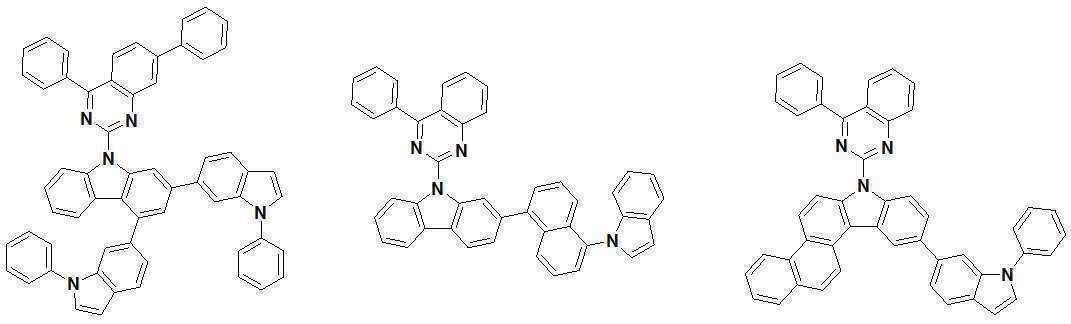
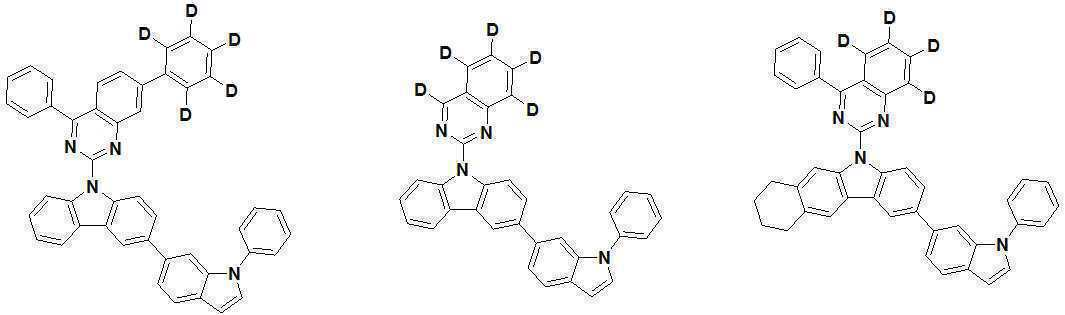
또한 본 발명에서 상기 [화학식 A] 또는 [화학식 B]로 표시되는 화합물은 하기 [화합물 1] 내지 [화합물 130] 중 어느 하나의 유기 발광 화합물일 수 있다. In addition, in the present invention, the compound represented by [Chemical Formula A] or [Chemical Formula B] may be any one of the following [Compound 1] to [Compound 130].
[화합물1] [화합물2] [화합물3][Compound 1] [Compound 2] [Compound 3]
[화합물4] [화합물5] [화합물6][Compound 4] [Compound 5] [Compound 6]
[화합물7] [화합물8] [화합물9][Compound 7] [Compound 8] [Compound 9]
[화합물10] [화합물11] [화합물12][Compound 10] [Compound 11] [Compound 12]
[화합물13] [화합물14] [화합물15][Compound 13] [Compound 14] [Compound 15]
[화합물16] [화합물17] [화합물18] [Compound 16] [Compound 17] [Compound 18]
[화합물19] [화합물20] [화합물21] [Compound 19] [Compound 20] [Compound 21]
[화합물22] [화합물23] [화합물24] [Compound 22] [Compound 23] [Compound 24]
[화합물25] [화합물26] [화합물27] [Compound 25] [Compound 26] [Compound 27]
[화합물28] [화합물29] [화합물30] [Compound 28] [Compound 29] [Compound 30]
[화합물31] [화합물32] [화합물33] [Compound 31] [Compound 32] [Compound 33]
[화합물34] [화합물35] [화합물36] [Compound 34] [Compound 35] [Compound 36]
[화합물37] [화합물38] [화합물39] [Compound 37] [Compound 38] [Compound 39]
[화합물40] [화합물41] [화합물42] [Compound 40] [Compound 41] [Compound 42]
[화합물43] [화합물44] [화합물45] [Compound 43] [Compound 44] [Compound 45]
[화합물46] [화합물47] [화합물48]
[Compound 46] [Compound 47] [Compound 48]
[화합물49] [화합물50] [화합물51] [Compound 49] [Compound 50] [Compound 51]
[화합물52] [화합물53] [화합물54] [Compound 52] [Compound 53] [Compound 54]
[화합물55] [화합물56] [화합물57] [Compound 55] [Compound 56] [Compound 57]
[화합물58] [화합물59] [화합물60] [Compound 58] [Compound 59] [Compound 60]
[화합물61] [화합물62] [화합물63] [Compound 61] [Compound 62] [Compound 63]
[화합물64] [화합물65] [화합물66] [Compound 64] [Compound 65] [Compound 66]
[화합물67] [화합물68] [화합물69] [Compound 67] [Compound 68] [Compound 69]
[화합물70] [화합물71] [화합물72] [Compound 70] [Compound 71] [Compound 72]
[화합물73] [화합물74] [화합물75] [Compound 73] [Compound 74] [Compound 75]
[화합물76] [화합물77] [화합물78] [Compound 76] [Compound 77] [Compound 78]
[화합물79] [화합물80] [화합물81] [Compound 79] [Compound 80] [Compound 81]
[화합물82] [화합물83] [화합물84] [Compound 82] [Compound 83] [Compound 84]
[화합물85] [화합물86] [화합물87] [Compound 85] [Compound 86] [Compound 87]
[화합물88] [화합물89] [화합물90] [Compound 88] [Compound 89] [Compound 90]
[화합물91] [화합물92] [화합물93] [Compound 91] [Compound 92] [Compound 93]
[화합물94] [화합물95] [화합물96] [Compound 94] [Compound 95] [Compound 96]
[화합물97] [화합물98] [화합물99] [Compound 97] [Compound 98] [Compound 99]
[화합물100] [화합물101] [화합물102] [Compound 100] [Compound 101] [Compound 102]
[화합물103] [화합물104] [화합물105] [Compound 103] [Compound 104] [Compound 105]
[화합물106] [화합물107] [화합물108] [Compound 106] [Compound 107] [Compound 108]
[화합물109] [화합물110] [화합물111] [Compound 109] [Compound 110] [Compound 111]
[화합물112] [화합물113] [화합물114] [Compound 112] [Compound 113] [Compound 114]
[화합물115] [화합물116] [화합물117] [Compound 115] [Compound 116] [Compound 117]
[화합물118] [화합물119] [화합물120] [Compound 118] [Compound 119] [Compound 120]
[화합물121] [화합물122] [화합물123] [Compound 121] [Compound 122] [Compound 123]
[화합물124] [화합물125] [화합물126] [Compound 124] [Compound 125] [Compound 126]
[화합물127] [화합물128] [화합물129] [Compound 127] [Compound 128] [Compound 129]
[화합물130] [Compound 130]
또한, 본 발명은 제1전극; 상기 제1전극에 대향된 제2전극; 및 상기 제1전극과 상기 제2전극 사이에 개재되는 유기층;을 포함하고, 상기 유기층이 본 발명에서의 본 발명에서의 상기 유기발광 화합물을 1종 이상 포함할 수 있다. In addition, the present invention is a first electrode; A second electrode facing the first electrode; And an organic layer interposed between the first electrode and the second electrode, wherein the organic layer may include one or more of the organic light emitting compounds in the present invention in the present invention.
본 발명에서 "(유기층이) 유기금속 화합물을 1종 이상 포함한다" 란, "(유기층이) 본 발명의 범주에 속하는 1종의 유기금속 화합물 또는 상기 유기금속 화합물의 범주에 속하는 서로 다른 2종 이상의 화합물을 포함할 수 있다"로 해석될 수 있다.In the present invention, "(organic layer) contains one or more organometallic compounds" means "(organic layer) one organometallic compound belonging to the scope of the present invention or two different kinds belonging to the organometallic compound It can be interpreted as "may include the above compounds.
또한, 상기 본 발명의 유기발광 화합물이 포함된 유기층은 정공 주입층, 정공 수송층, 정공 주입 기능 및 정공 수송 기능을 동시에 갖는 기능층, 발광층, 전자 수송층, 및 전자 주입층 중 적어도 하나를 포함할 수 있다. 이때, 상기 제1전극과 상기 제2전극 사이에 개재된 유기층이 발광층을 포함할 수 있으며, 상기 발광층은 호스트와 도판트로 이루어지고, 본 발명의 유기발광 화합물은 호스트로서 사용될 수 있다. In addition, the organic layer containing the organic light-emitting compound of the present invention may include at least one of a hole injection layer, a hole transport layer, a functional layer having a hole injection function and a hole transport function at the same time, a light emitting layer, an electron transport layer, and an electron injection layer. have. In this case, the organic layer interposed between the first electrode and the second electrode may include an emission layer, the emission layer is formed of a host and a dopant, and the organic emission compound of the present invention may be used as a host.
한편 본 발명에서 상기 발광층에는 호스트와 더불어, 도펀트 재료가 사용될 수 있다. 상기 발광층이 호스트 및 도펀트를 포함할 경우, 도펀트의 함량은 통상적으로 호스트 약 100 중량부를 기준으로 하여 약 0.01 내지 약 20 중량부의 범위에서 선택될 수 있으며, 이에 한정되는 것은 아니다.Meanwhile, in the present invention, a dopant material may be used in addition to a host for the emission layer. When the emission layer includes a host and a dopant, the content of the dopant may be generally selected in the range of about 0.01 to about 20 parts by weight based on about 100 parts by weight of the host, but is not limited thereto.
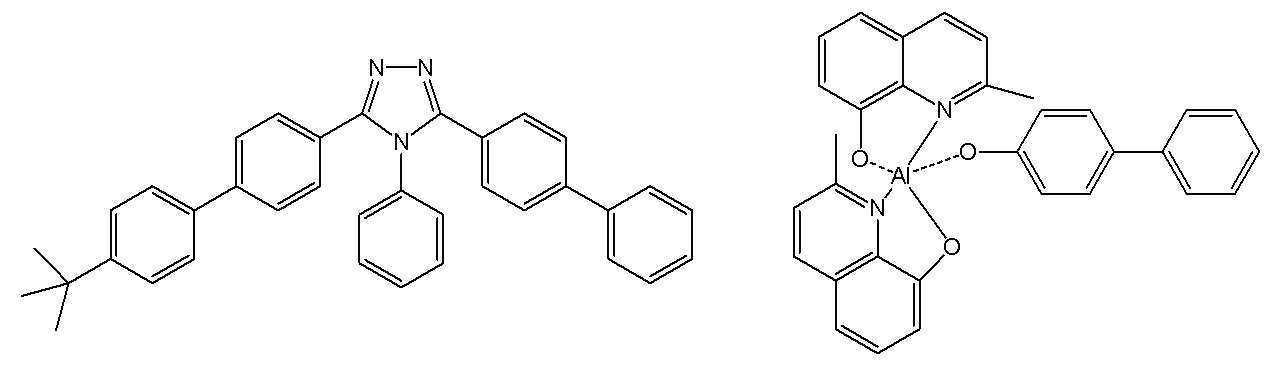
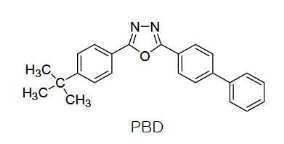
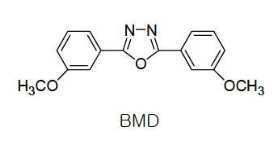
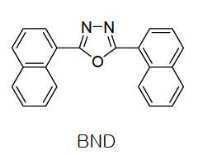
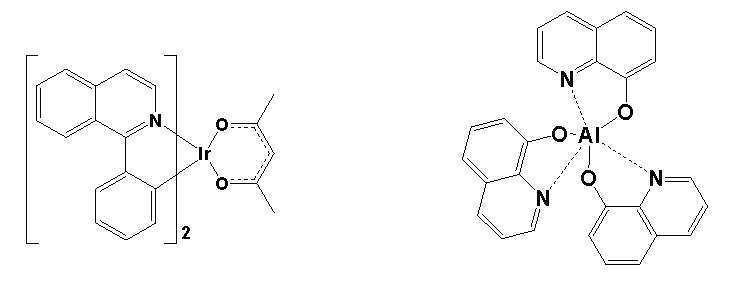
한편 본 발명에서 상기 전자 수송층 재료로는 전자주입전극(Cathode)로부터 주입된 전자를 안정하게 수송하는 기능을 하는 것으로서 공지의 전자 수송 물질을 이용할 수 있다. 공지의 전자 수송 물질의 예로는, 퀴놀린 유도체, 특히 트리스(8-퀴놀리노레이트)알루미늄(Alq3), TAZ, Balq, 베릴륨 비스(벤조퀴놀리-10-노에이트)(beryllium bis(benzoquinolin-10-olate: Bebq2), ADN, 화합물 201, 화합물 202, 옥사디아졸 유도체인 PBD, BMD, BND 등과 같은 재료를 사용할 수도 있으나, 이에 한정되는 것은 아니다.Meanwhile, in the present invention, a known electron transport material may be used as the material for the electron transport layer to stably transport electrons injected from an electron injection electrode (Cathode). Examples of known electron transport materials include quinoline derivatives, in particular tris(8-quinolinorate)aluminum (Alq3), TAZ, Balq, beryllium bis(benzoquinolin-10-noate) (beryllium bis(benzoquinolin-10-). olate: Bebq2), ADN, compound 201, compound 202, oxadiazole derivatives such as PBD, BMD, BND, etc. may be used, but the present invention is not limited thereto.
TAZ BAlqTAZ BAlq
화합물 201 화합물 202 BCPCompound 201 Compound 202 BCP
또한, 본 발명에서 사용되는 전자 수송층은 화학식 C로 표시되는 유기 금속 화합물이 단독 또는 상기 전자수송층 재료와 혼합으로 사용될 수 있다. In addition, as for the electron transport layer used in the present invention, an organometallic compound represented by Formula C may be used alone or in combination with the electron transport layer material.
[화학식 C] [Formula C]
상기 [화학식 C]에서, In [Chemical Formula C],
Y는 C, N, O 및 S에서 선택되는 어느 하나가 상기 M에 직접 결합되어 단일결합을 이루는 부분과, C, N, O 및 S에서 선택되는 어느 하나가 상기 M에 배위결합을 이루는 부분을 포함하며, 상기 단일결합과 배위결합에 의해 킬레이트된 리간드이고Y is a portion in which any one selected from C, N, O, and S is directly bonded to the M to form a single bond, and a portion in which any one selected from C, N, O, and S forms a coordination bond to the M. And is a ligand chelated by the single bond and the coordination bond
상기 M은 알카리 금속, 알카리 토금속, 알루미늄(Al) 또는 붕소(B)원자이고, 상기 OA는 상기 M과 단일결합 또는 배위결합 가능한 1가의 리간드로서,The M is an alkali metal, alkaline earth metal, aluminum (Al) or boron (B) atom, and the OA is a monovalent ligand capable of a single bond or coordination bond with the M,
상기 O는 산소이며,O is oxygen,
A는 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 2 내지 20의 알키닐기, 치환 또는 비치환된 탄소수 3 내지30의 시클로알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 시클로알케닐기 및 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 2 내지 50의 헤테로아릴기중에서 선택되는 어느 하나이고, A is a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted aryl group having 5 to 50 carbon atoms, a substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, a substituted or unsubstituted C2 to C20 An alkynyl group, a substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted cycloalkenyl group having 5 to 30 carbon atoms, and a substituted or unsubstituted hetero atom having O, N or S as a hetero atom and having 2 to 50 carbon atoms Is any one selected from aryl groups,
상기 M이 알카리 금속에서 선택되는 하나의 금속인 경우에는 m=1, n=0이고,When M is one metal selected from alkali metals, m = 1, n = 0,
상기 M이 알카리 토금속에서 선택되는 하나의 금속인 경우에는 m=1, n=1이거나, 또는 m=2, n=0이고, When M is one metal selected from alkaline earth metals, m=1, n=1, or m=2, n=0,
상기 M이 붕소 또는 알루미늄인 경우에는 m = 1 내지 3중 어느 하나이며, n은 0 내지 2 중 어느 하나로서 m +n=3을 만족하며;When M is boron or aluminum, m is any one of 1 to 3, and n is any one of 0 to 2, which satisfies m + n = 3;
상기 '치환 또는 비치환된'에서의 '치환'은 중수소, 시아노기, 할로겐기, 히드록시기, 니트로기, 알킬기, 알콕시기, 알킬아미노기, 아릴아미노기, 헤테로 아릴아미노기, 알킬실릴기, 아릴실릴기, 아릴옥시기, 아릴기, 헤테로아릴기, 게르마늄, 인 및 보론으로 이루어진 군에서 선택된 1개 이상의 치환기로 치환되는 것을 의미한다. 'Substituted' in the'substituted or unsubstituted' is deuterium, cyano group, halogen group, hydroxy group, nitro group, alkyl group, alkoxy group, alkylamino group, arylamino group, hetero arylamino group, alkylsilyl group, arylsilyl group, It means substituted with one or more substituents selected from the group consisting of aryloxy group, aryl group, heteroaryl group, germanium, phosphorus and boron.
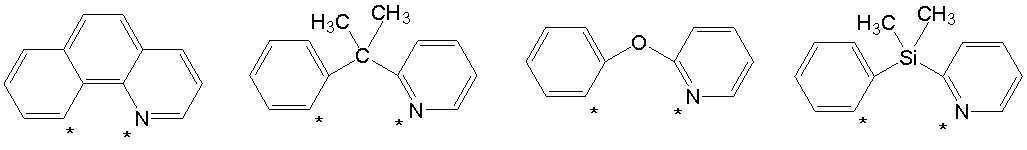
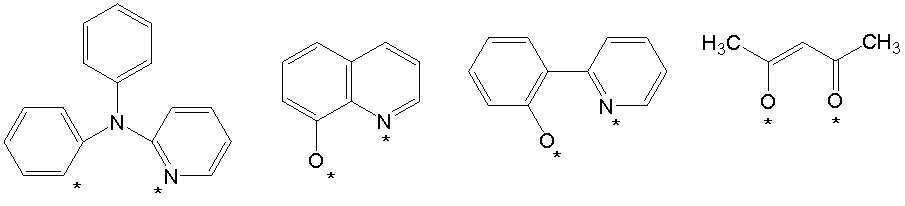
본 발명에서 Y 는 각각 동일하거나 상이하며, 서로 독립적으로 하기 [구조식 C1] 내지 [구조식 C39]부터 선택되는 어느 하나일 수 있으나, 이에 한정된 것은 아니다.In the present invention, Y is the same or different, and may be any one independently selected from the following [Structural Formula C1] to [Structure C39], but is not limited thereto.
[구조식 C1] [구조식 C2] [구조식 C3][Structural Formula C1] [Structural Formula C2] [Structural Formula C3]
[구조식 C4] [구조식 C5] [구조식 C6][Structural Formula C4] [Structural Formula C5] [Structural Formula C6]
[구조식 C7] [구조식 C8] [구조식 C9] [구조식 C10][Structural Formula C7] [Structural Formula C8] [Structural Formula C9] [Structural Formula C10]
[구조식 C11] [구조식 C12] [구조식 C13][Structural Formula C11] [Structural Formula C12] [Structural Formula C13]
[구조식 C14] [구조식 C15] [구조식 C16][Structural Formula C14] [Structural Formula C15] [Structural Formula C16]
[구조식 C17] [구조식 C18] [구조식 C19] [구조식 C20][Structural Formula C17] [Structural Formula C18] [Structural Formula C19] [Structural Formula C20]
[구조식 C21] [구조식 C22] [구조식 C23][Structural Formula C21] [Structural Formula C22] [Structural Formula C23]
[구조식 C24] [구조식 C25] [구조식 C26][Structural Formula C24] [Structural Formula C25] [Structural Formula C26]
[구조식 C27] [구조식 C28] [구조식 C29] [구조식 C30][Structural Formula C27] [Structural Formula C28] [Structural Formula C29] [Structural Formula C30]
[구조식 C31] [구조식 C32] [구조식 C33][Structural Formula C31] [Structural Formula C32] [Structural Formula C33]
[구조식 C34] [구조식 C35] [구조식 C36][Structural Formula C34] [Structural Formula C35] [Structural Formula C36]
[구조식 C37] [구조식 C38] [구조식 C39] [Structural Formula C37] [Structural Formula C38] [Structural Formula C39]
상기 [구조식 C1] 내지 [구조식 C39]에서,In the [Structural Formula C1] to [Structural Formula C39],
R은 서로 동일하거나 상이하며, 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴기, 치환 또는 비치환된 탄소수 3 내지 30의 헤테로아릴기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아미노기, 치환 또는 비치환된 탄소수 1 내지 30이 알킬실릴기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴아미노기 및 치환 또는 비치환된 탄소수 6 내지 30의 아릴실릴기 중에서 선택되고, 인접한 치환체와 알킬렌 또는 알케닐렌으로 연결되어 스피로고리 또는 융합고리를 형성할 수 있다. R is the same as or different from each other, and each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, substituted or unsubstituted aryl group having 6 to 30 carbon atoms, substituted or unsubstituted A heteroaryl group having 3 to 30 carbon atoms, a substituted or unsubstituted alkoxy group having 1 to 30 carbon atoms, a substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, a substituted or Unsubstituted C1-C30 alkylamino group, substituted or unsubstituted C1-C30 alkylsilyl group, substituted or unsubstituted C6-C30 arylamino group, and substituted or unsubstituted C6-C30 arylsilyl It is selected from groups, and may be connected to an adjacent substituent with alkylene or alkenylene to form a spiro ring or a fused ring.
이하 본 발명의 유기 발광 소자를 도 1을 통해 설명하고자 한다.Hereinafter, the organic light-emitting device of the present invention will be described with reference to FIG. 1.
도 1은 본 발명의 유기 발광 소자의 구조를 나타내는 단면도이다. 본 발명에 따른 유기 발광 소자는 애노드(20), 정공수송층(40), 유기발광층(50), 전자수송층(60) 및 캐소드(80)을 포함하며, 필요에 따라 정공주입층(30)과 전자주입층(70)을 더 포함할 수 있으며, 그 이외에도 1층 또는 2층의 중간층을 더 형성하는 것도 가능하며, 정공저지층 또는 전자저지층을 더 형성시킬 수도 있다. 1 is a cross-sectional view showing the structure of an organic light-emitting device of the present invention. The organic light emitting device according to the present invention includes an
도 1을 참조하여 본 발명의 유기 발광 소자 및 그 제조방법에 대하여 살펴보면 다음과 같다. 먼저 기판(10) 상부에 애노드 전극용 물질을 코팅하여 애노드(20)를 형성한다. 여기에서 기판(10)으로는 통상적인 유기 EL 소자에서 사용되는 기판을 사용하는데 투명성, 표면 평활성, 취급용이성 및 방수성이 우수한 유기 기판 또는 투명 플라스틱 기판이 바람직하다. 그리고, 애노드 전극용 물질로는 투명하고 전도성이 우수한 산화인듐주석(ITO), 산화인듐아연(IZO), 산화주석(SnO2), 산화아연(ZnO) 등을 사용한다.Referring to FIG. 1, an organic light-emitting device of the present invention and a method of manufacturing the same are as follows. First, an
상기 애노드(20) 전극 상부에 정공 주입층 물질을 진공열 증착, 또는 스핀 코팅하여 정공주입층(30)을 형성한다. 그 다음으로 상기 정공주입층(30)의 상부에 정공수송층 물질을 진공 열증착 또는 스핀 코팅하여 정공수송층(40)을 형성한다.The
상기 정공주입층 재료는 당업계에서 통상적으로 사용되는 것인 한 특별히 제한되지 않고 사용할 수 있으며, 예를 들어 2-TNATA [4,4',4"-tris(2-naphthylphenyl-phenylamino)-triphenylamine], NPD[N,N'-di(1-naphthyl)-N,N'-diphenylbenzidine)], TPD[N,N'-diphenyl-N,N'-bis(3-methylphenyl)-1,1'-biphenyl-4,4'-diamine], DNTPD[N,N'-diphenyl-N,N'-bis-[4-(phenyl-m-tolyl-amino)-phenyl]-biphenyl-4,4'-diamine] 등을 사용할 수 있다. 하지만 본 발명이 반드시 이에 한정되는 것은 아니다.The hole injection layer material is not particularly limited as long as it is commonly used in the art, and may be used, for example, 2-TNATA [4,4',4"-tris(2-naphthylphenyl-phenylamino)-triphenylamine] , NPD[N,N'-di(1-naphthyl)-N,N'-diphenylbenzidine)], TPD[N,N'-diphenyl-N,N'-bis(3-methylphenyl)-1,1'- biphenyl-4,4'-diamine], DNTPD[N,N'-diphenyl-N,N'-bis-[4-(phenyl-m-tolyl-amino)-phenyl]-biphenyl-4,4'-diamine ], etc. However, the present invention is not necessarily limited thereto.
또한 상기 정공수송층의 재료로서 당업계에 통상적으로 사용되는 것인 한 특별히 제한되지 않으며, 예를 들어, N,N'-비스(3-메틸페닐)-N,N'-디페닐 -[1,1-비페닐]-4,4'-디아민(TPD) 또는 N,N'-디(나프탈렌-1-일)-N,N'-디페닐벤지딘(a-NPD) 등을 사용할 수 있다. 하지만 본 발명이 반드시 이에 한정되는 것은 아니다.In addition, the material of the hole transport layer is not particularly limited as long as it is commonly used in the art, and for example, N,N'-bis(3-methylphenyl)-N,N'-diphenyl-[1,1 -Biphenyl]-4,4'-diamine (TPD) or N,N'-di(naphthalen-1-yl)-N,N'-diphenylbenzidine (a-NPD) and the like can be used. However, the present invention is not necessarily limited thereto.
이어서, 상기 정공수송층(40)의 상부에 유기발광층(50)을 적층하고 상기 유기발광층(50)의 상부에 선택적으로 정공저지층(미도시)을 진공 증착 방법, 또는 스핀 코팅 방법으로서 박막을 형성할 수 있다. 상기 정공저지층은 정공이 유기발광층을 통과하여 캐소드로 유입되는 경우에는 소자의 수명과 효율이 감소되기 때문에 HOMO(Highest Occupied Molecular Orbital) 레벨이 매우 낮은 물질을 사용함으로써 이러한 문제를 방지하는 역할을 한다. 이 때, 사용되는 정공 저지 물질은 특별히 제한되지는 않으나 전자수송능력을 가지면서 발광 화합물보다 높은 이온화 포텐셜을 가져야 하며 대표적으로 BAlq, BCP, TPBI 등이 사용될 수 있다.Subsequently, an organic light-emitting
상기 정공저지층에 사용되는 물질로써, BAlq, BCP, Bphen, TPBI, NTAZ, BeBq2, OXD-7, Liq 및 화학식 101 내지 화학식 107 중 에서 선택되는 어느 하나가 사용될 수 있으나, 이에 한정되는 것은 아니다.As the material used for the hole blocking layer, any one selected from BAlq, BCP, Bphen, TPBI, NTAZ, BeBq 2 , OXD-7, Liq, and Chemical Formulas 101 to 107 may be used, but is not limited thereto. .
BAlq BCP BphenBAlq BCP Bphen
TPBI NTAZ BeBq2 TPBI NTAZ BeBq 2
OXD-7 Liq OXD-7 Liq
화학식 101 화학식 102 화학식 103 Formula 101 Formula 102 Formula 103
화학식 104 화학식 105 화학식 106 Formula 104 Formula 105 Formula 106
화학식 107Chemical Formula 107
이러한 정공저지층 위에 전자수송층(60)을 진공 증착 방법, 또는 스핀 코팅 방법을 통해 증착한 후에 전자주입층(70)을 형성하고 상기 전자주입층(70)의 상부에 캐소드 형성용 금속을 진공 열증착하여 캐소드(80) 전극을 형성함으로써 유기 EL 소자가 완성된다. 여기에서 캐소드 형성용 금속으로는 리튬(Li), 마그네슘(Mg), 알루미늄(Al), 알루미늄-리듐(Al-Li), 칼슘(Ca), 마그네슘-인듐(Mg-In), 마그네슘-은(Mg-Ag) 등을 사용할 수 있으며, 전면 발광 소자를 얻기 위해서는 ITO, IZO를 사용한 투과형 캐소드를 사용할 수 있다.After depositing the
또한 상기 발광층은 호스트와 도펀트로 이루어질 수 있다.In addition, the emission layer may be formed of a host and a dopant.
또한, 본 발명의 구체적인 예에 의하면, 상기 발광층의 두께는 50 내지 2,000 Å인 것이 바람직하다. In addition, according to a specific example of the present invention, the thickness of the light emitting layer is preferably 50 to 2,000 Å.
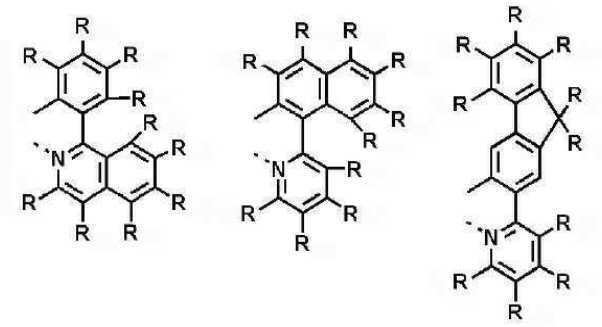
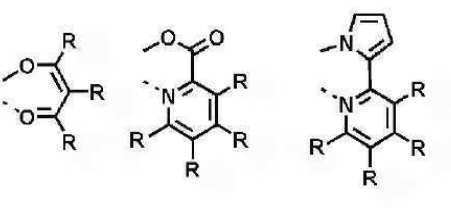
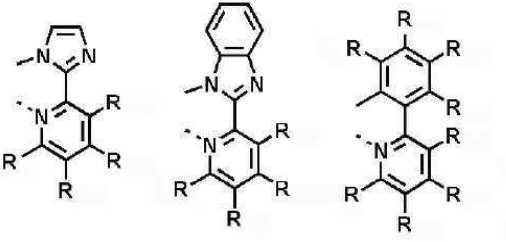
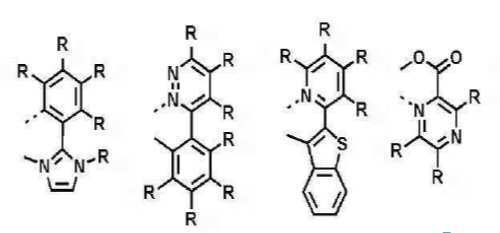
이때, 발광층에 사용되는 도펀트는 하기 일반식 (A-1) 내지 일반식 (J-1) 로 표시되는 화합물 중에서 선택되는 1종 이상의 화합물일 수 있다.In this case, the dopant used in the light emitting layer may be one or more compounds selected from compounds represented by the following general formulas (A-1) to (J-1).
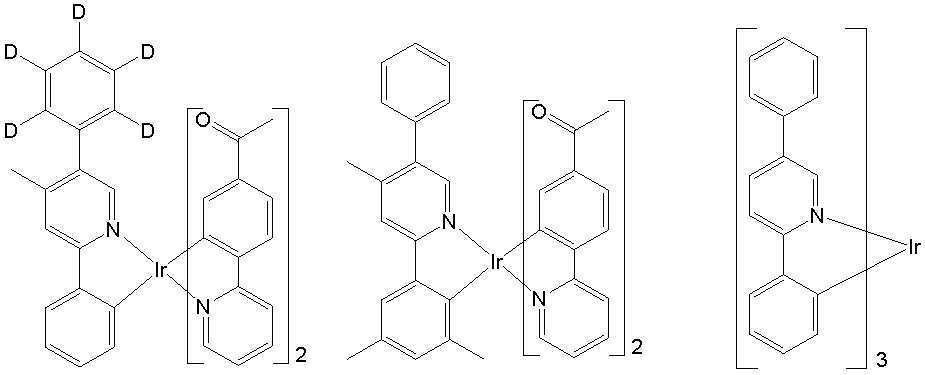
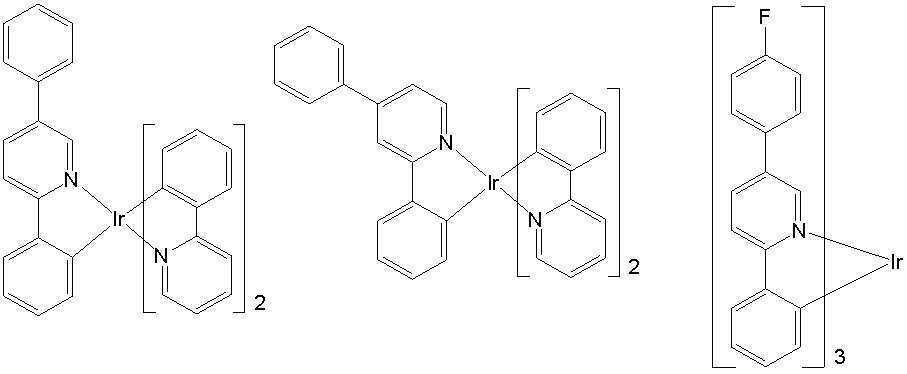
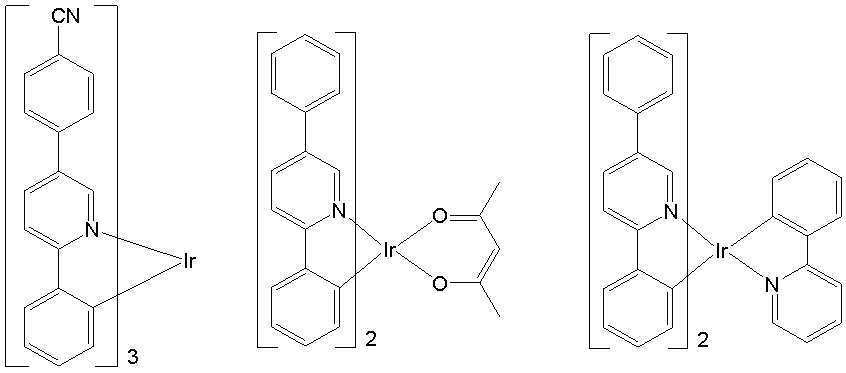
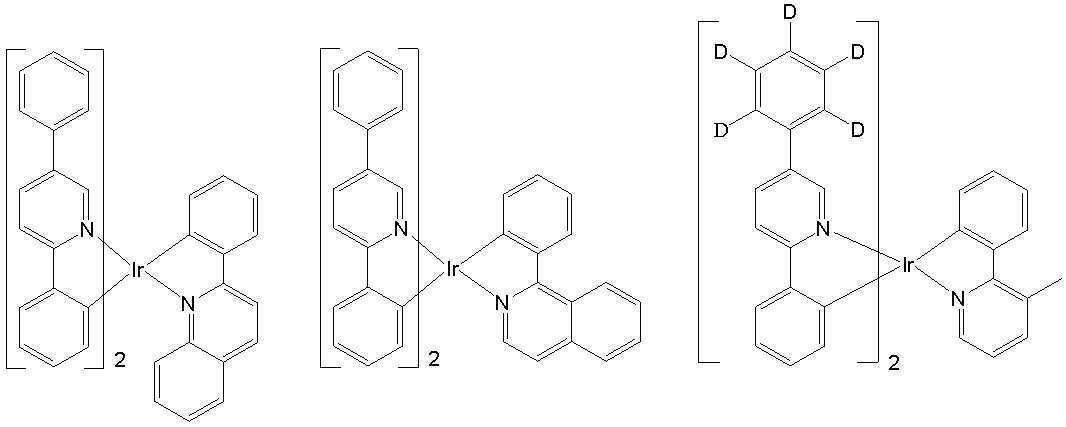
[일반식 A-1][General Formula A-1]
상기 M은 7족, 8족, 9족, 10족, 11족, 13족, 14족, 15족 및 16족의 금속으로 이루어진 군으로부터 선택되고, 바람직하게는 Ir, Pt, Pd, Rh, Re, Os, Tl, Pb, Bi, In, Sn, Sb, Te, Au 및 Ag로부터 선택된다. 또한, 상기 L1, L2 및 L3은 리간드로서 서로 동일하거나 상이하고 각각 독립적으로 하기 구조식D에서 선택되는 어느 하나를 들 수 있지만, 이에 한정되는 것은 아니다.The M is selected from the group consisting of metals of
또한, 하기 구조식 D내 「*」은 금속 이온 M에 배위하는 사이트(site)를 표현한다.Further, "*" in the following structural formula D represents a site coordinated with the metal ion M.
[구조식 D] [Structural Formula D]
상기 구조식 D에서 상기 R은 서로 상이하거나 동일하며 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 6 내지 50의 아릴기, 치환 또는 비치환된 탄소수 5 내지 50의 헤테로아릴기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아미노기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬실릴기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴아미노기 및 치환 또는 비치환된 탄소수 6 내지 30의 아릴실릴기 중에서 선택되는 어느 하나일수 있으며;In the structural formula D, R is different from or identical to each other, and each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, substituted or unsubstituted aryl group having 6 to 50 carbon atoms, substituted Or an unsubstituted C5-C50 heteroaryl group, a substituted or unsubstituted C1-C30 alkoxy group, a substituted or unsubstituted C3-C30 cycloalkyl group, a substituted or unsubstituted C2-C30 alke Nyl group, a substituted or unsubstituted alkylamino group having 1 to 30 carbon atoms, a substituted or unsubstituted alkylsilyl group having 1 to 30 carbon atoms, a substituted or unsubstituted arylamino group having 6 to 30 carbon atoms, and a substituted or unsubstituted C 6 to C atoms It may be any one selected from 30 arylsilyl groups;
상기 R은 각각 독립적으로 탄소수 1 내지 20의 알킬기, 탄소수 3 내지 20의 시클로알킬기, 탄소수 6 내지 40의 아릴기, 탄소수 3 내지 20의 헤테로아릴기, 시아노기, 할로겐기, 중수소 및 수소 중에서 선택되는 1종 이상의 치환기로 더 치환될 수 있고;Each of R is independently selected from an alkyl group having 1 to 20 carbon atoms, a cycloalkyl group having 3 to 20 carbon atoms, an aryl group having 6 to 40 carbon atoms, a heteroaryl group having 3 to 20 carbon atoms, a cyano group, a halogen group, deuterium and hydrogen May be further substituted with one or more substituents;
또한 상기 R은 각각의 인접한 치환기와 알킬렌 또는 알케닐렌으로 연결되어 지환족 고리 및 단일환 또는 다환의 방향족 고리를 형성할 수 있고;In addition, R may be connected to each of the adjacent substituents by alkylene or alkenylene to form an alicyclic ring and a monocyclic or polycyclic aromatic ring;
상기 L은 인접한 치환체와 알킬렌 또는 알케닐렌으로 연결되어 스피로고리 또는 융합고리를 형성할 수 있다.The L may be connected to an adjacent substituent with alkylene or alkenylene to form a spiro ring or a fused ring.
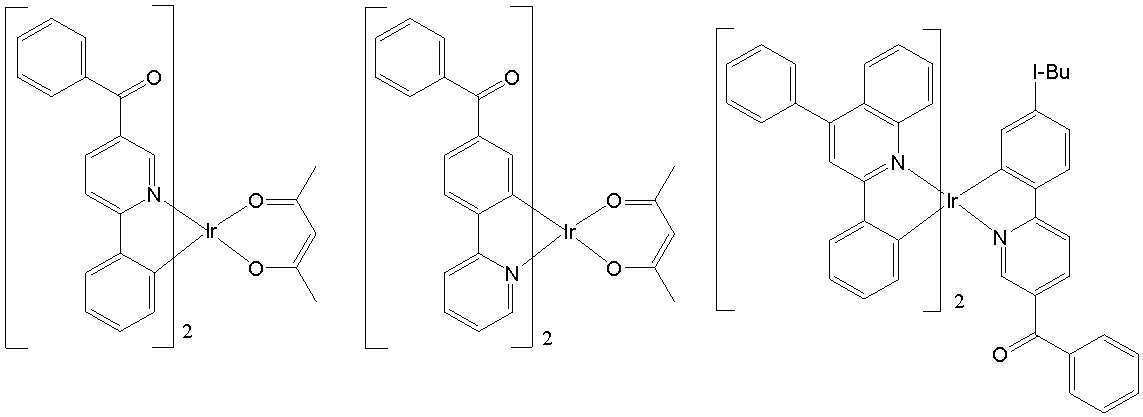
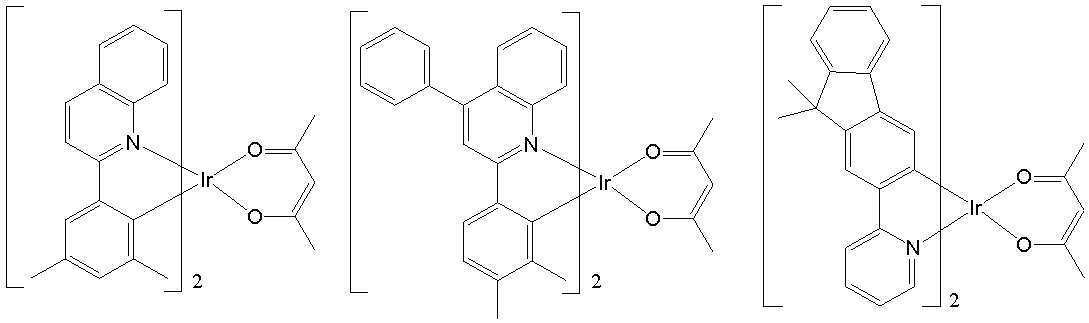
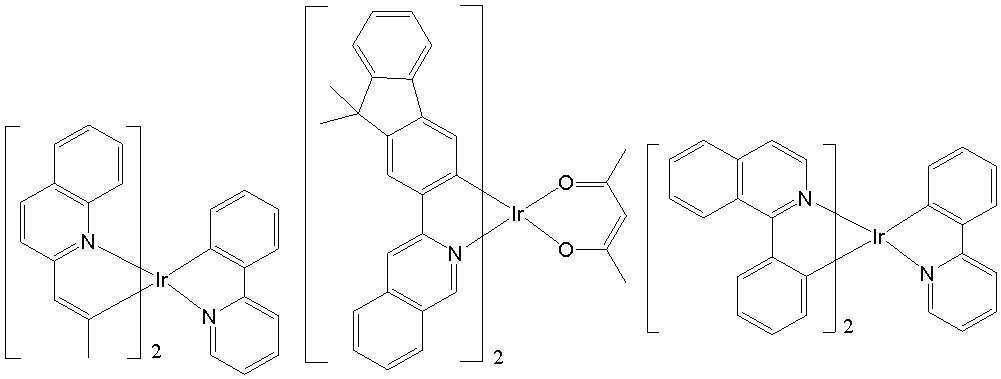
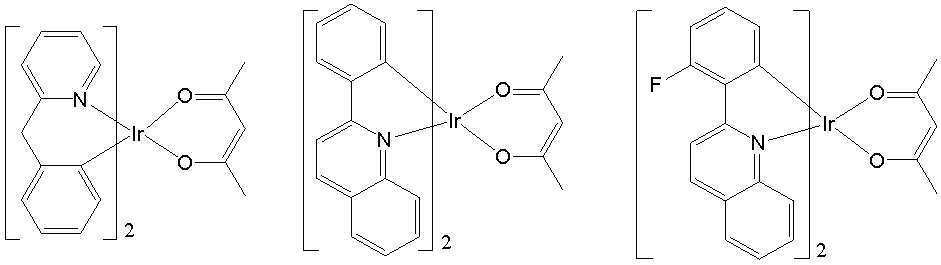
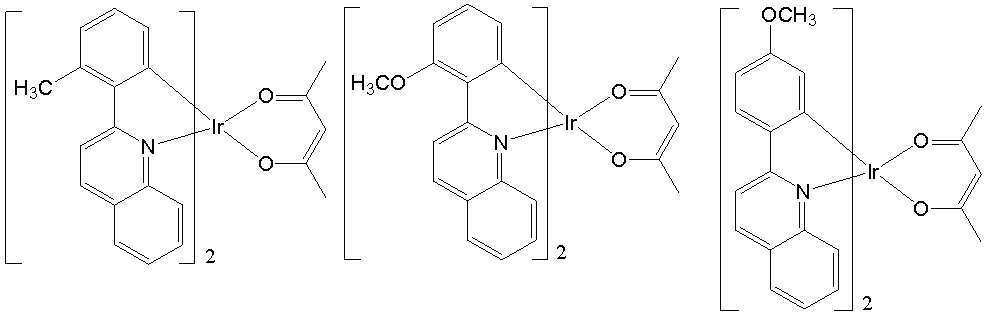
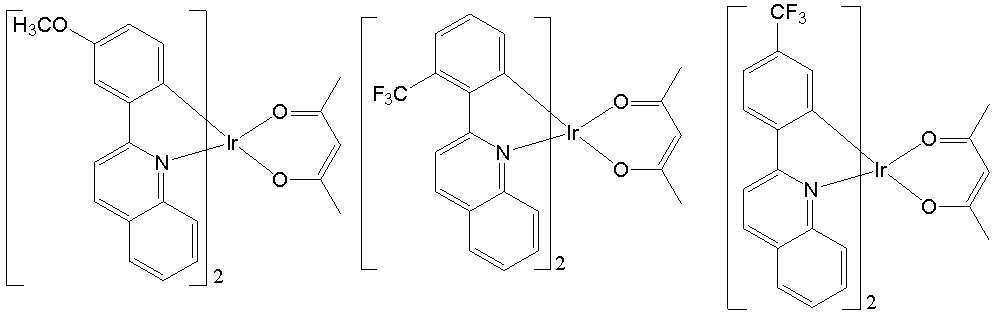
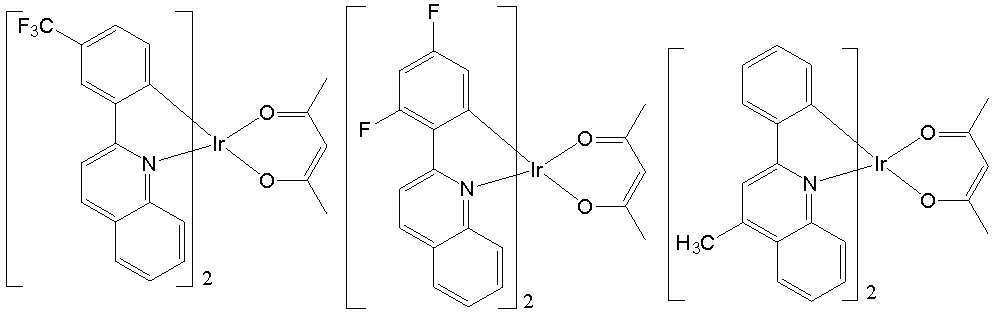
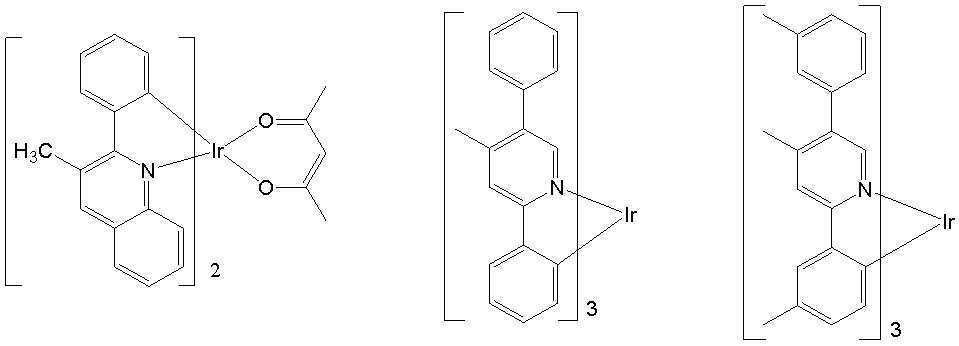
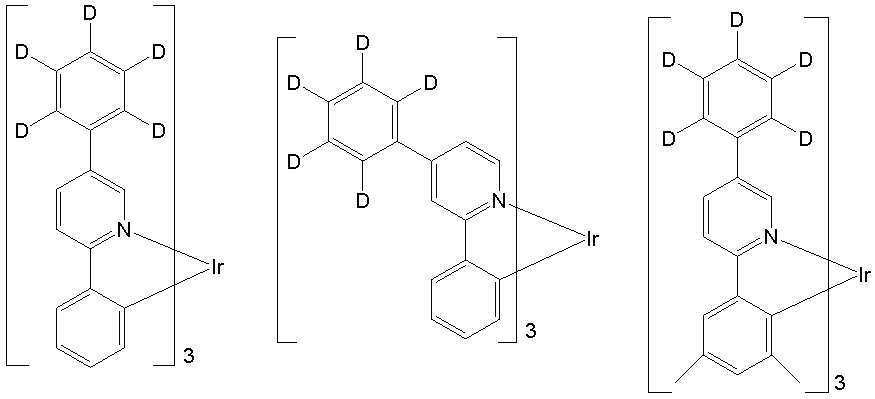
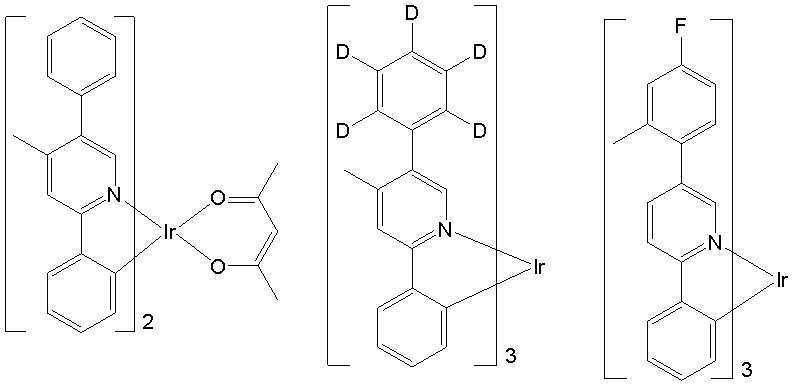
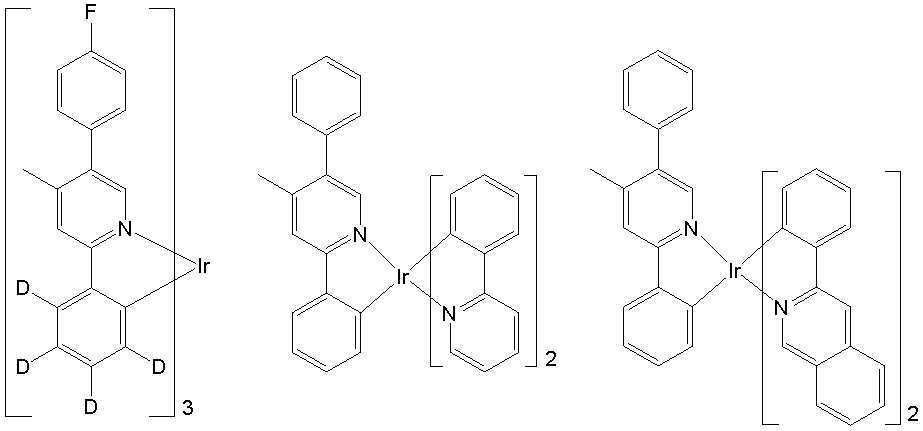
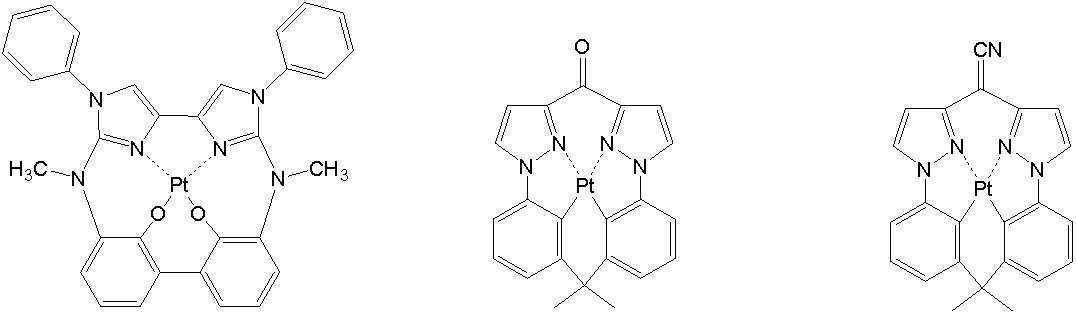
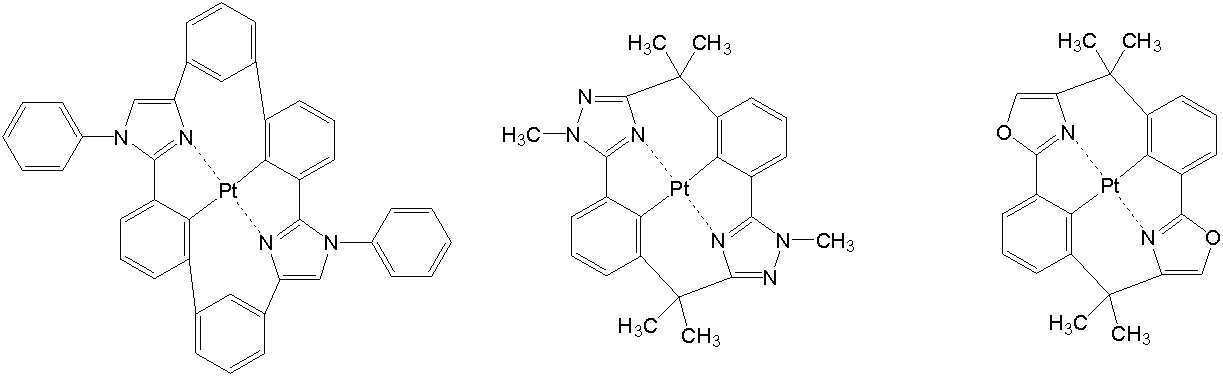
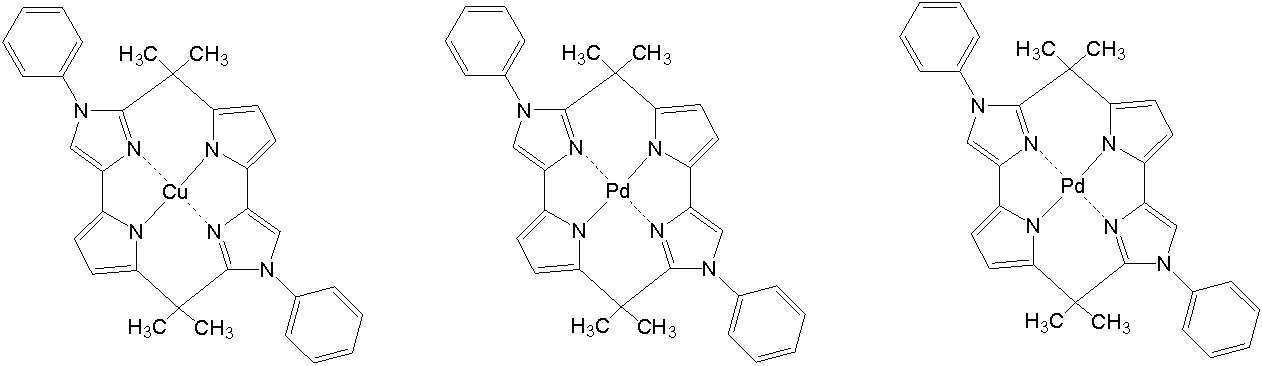
일 예로서, 상기 [일반식 A-1]으로 표시되는 도펀트는 하기 화합물 중에서 선택된 어느 하나일 수 있다. As an example, the dopant represented by [General Formula A-1] may be any one selected from the following compounds.
[일반식 B-1][General Formula B-1]
상기 일반식 B-1에서, In the general formula B-1,
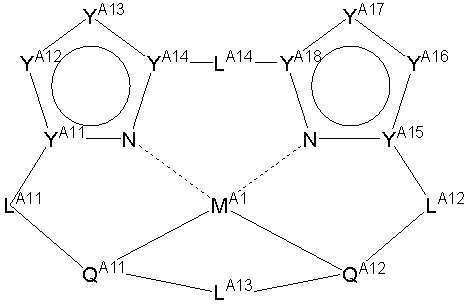
MA1은 일반식 (A-1)에서 정의한 바와 동일한 금속 이온을 나타내며, 또한, YA11 ,YA14 ,YA15 및 YA18 은 각각 독립적으로 탄소 원자 또는 질소 원자를 나타내며, YA12 ,YA13 ,YA16 및 YA17은 각각 독립적으로 치환 또는 무치환의 탄소 원자, 치환 또는 무치환의 질소원자, 산소원자, 황원자를 나타내고, LA11 ,LA12 ,LA13 ,LA14는 각각 앞서 정의한 바와 같은 연결기를 나타내며, QA11, QA12는 MA1에 결합하는 원자를 함유하는 부분 구조를 나타낸다.M A1 represents the same metal ion as defined in the general formula (A-1), and Y A11 and Y A14 ,Y A15 and Y A18 Each independently represents a carbon atom or a nitrogen atom, Y A12 , Y A13 ,Y A16 and Y A17 each independently represent a substituted or unsubstituted carbon atom, a substituted or unsubstituted nitrogen atom, an oxygen atom, and a sulfur atom, and L A11 ,L A12 ,L A13 ,L A14 represents a linking group as defined above, respectively, and Q A11 and Q A12 represent a partial structure containing an atom bonded to M A1 .
상기 일반식 B-1으로 표시되는 화합물의 예시적인 구조는 아래와 같으나, 이에 제한되지 않는다.An exemplary structure of the compound represented by the general formula B-1 is as follows, but is not limited thereto.
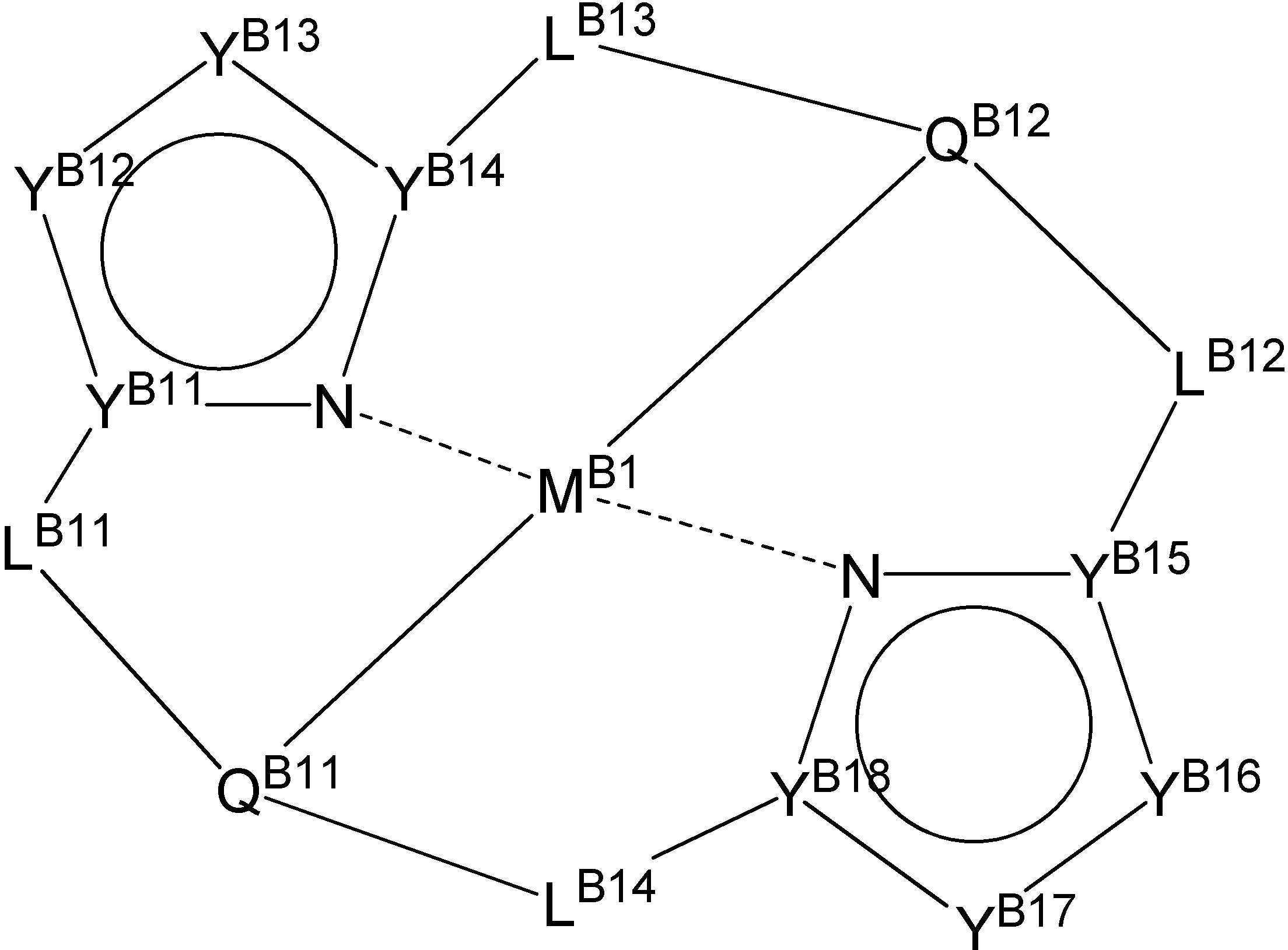
[일반식 C-1][General Formula C-1]
상기 일반식 C-1에서, In the general formula C-1,
MB1 은 일반식 A-1에서 정의한 바와 동일한 금속 이온을 나타내며, YB11 ,YB14 ,YB15 및 YB18은 각각 독립적으로 탄소 원자 또는 질소 원자를 나타내고, YB12, YB13, YB16 및 YB17은 각각 독립적으로 치환 또는 무치환의 탄소 원자,치환 또는 무치환의 질소원자, 산소원자, 황원자를 나타내며, LB11 ,LB12 ,LB13 ,LB14는 연결기를 나타내고, QB11 ,QB12는 MB1에 결합하는 원자를 함유하는 부분 구조를 나타낸다. M B1 represents the same metal ion as defined in the general formula A-1, Y B11 , Y B14 ,Y B15 and Y B18 each independently represent a carbon atom or a nitrogen atom, and Y B12 , Y B13 , Y B16 and Y B17 are each independently a substituted or unsubstituted carbon atom, a substituted or unsubstituted nitrogen atom, and oxygen Represents an atom or a sulfur atom, and L B11 ,L B12 ,L B13 ,L B14 represents a linking group, and Q B11 ,Q B12 represents a partial structure containing an atom bonded to M B1 .
상기 일반식 C-1으로 표시되는 화합물의 예시적인 구조는 아래와 같으나, 이에 제한되지 않는다.An exemplary structure of the compound represented by the general formula C-1 is as follows, but is not limited thereto.
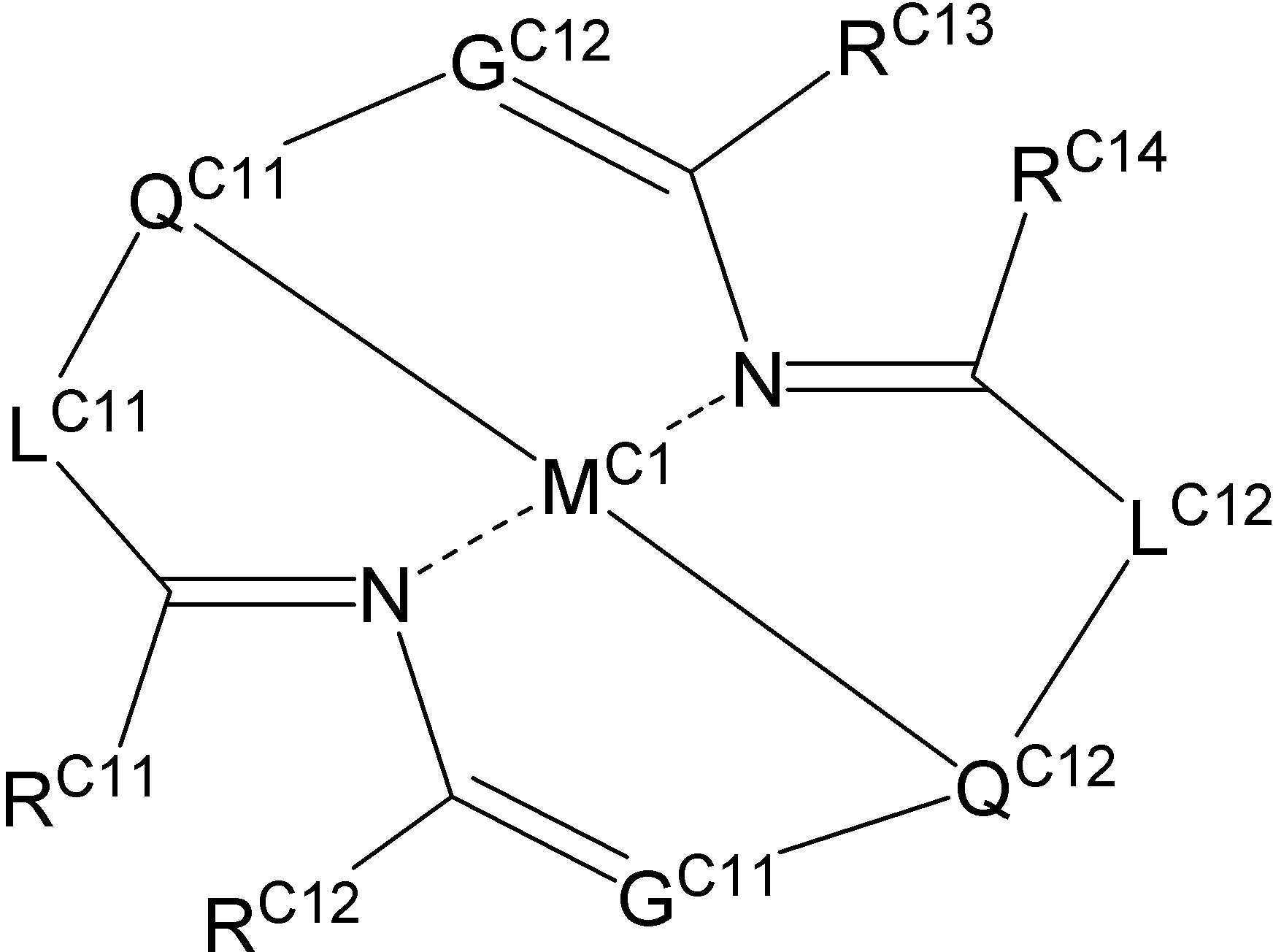
[일반식 D-1][General Formula D-1]
상기 일반식 D-1에서,In the general formula D-1,
MC1은 금속 이온을 일반식 A-1에서 정의한 바와 동일한 금속 이온을 나타내며, M C1 represents the same metal ion as the metal ion defined in the general formula A-1,
RC11,RC12는 각각 독립적으로 수소 원자, 서로 연결되어 5 원 고리를 형성하는 치환기, 서로 연결되지 않은 치환기를 나타내며,R C11 and R C12 each independently represent a hydrogen atom, a substituent that is connected to each other to form a 5-membered ring, and a substituent that is not connected to each other,
RC13,RC14는 각각 독립적으로 수소 원자, 서로 연결되어 5 원 고리를 형성하는 치환기,서로 연결되지 않은 치환기를 나타내며, GC11 ,GC12는 각각 독립적으로 질소 원자,치환 또는 무치환의 탄소 원자를 나타내며, LC11,LC12는 연결기를 나타내며, QC11,QC12는 MC1에 결합하는 원자를 함유하는 부분 구조를 나타낸다. R C13 and R C14 each independently represent a hydrogen atom, a substituent that is connected to each other to form a 5-membered ring, a substituent that is not connected to each other, and G C11 ,G C12 each independently represents a nitrogen atom, a substituted or unsubstituted carbon atom, L C11 and L C12 represent a linking group, and Q C11 and Q C12 represent a partial structure containing an atom bonded to M C1 .
상기 일반식 D-1으로 표시되는 화합물의 예시적인 구조는 아래와 같으나, 이에 제한되지 않는다.An exemplary structure of the compound represented by the general formula D-1 is as follows, but is not limited thereto.
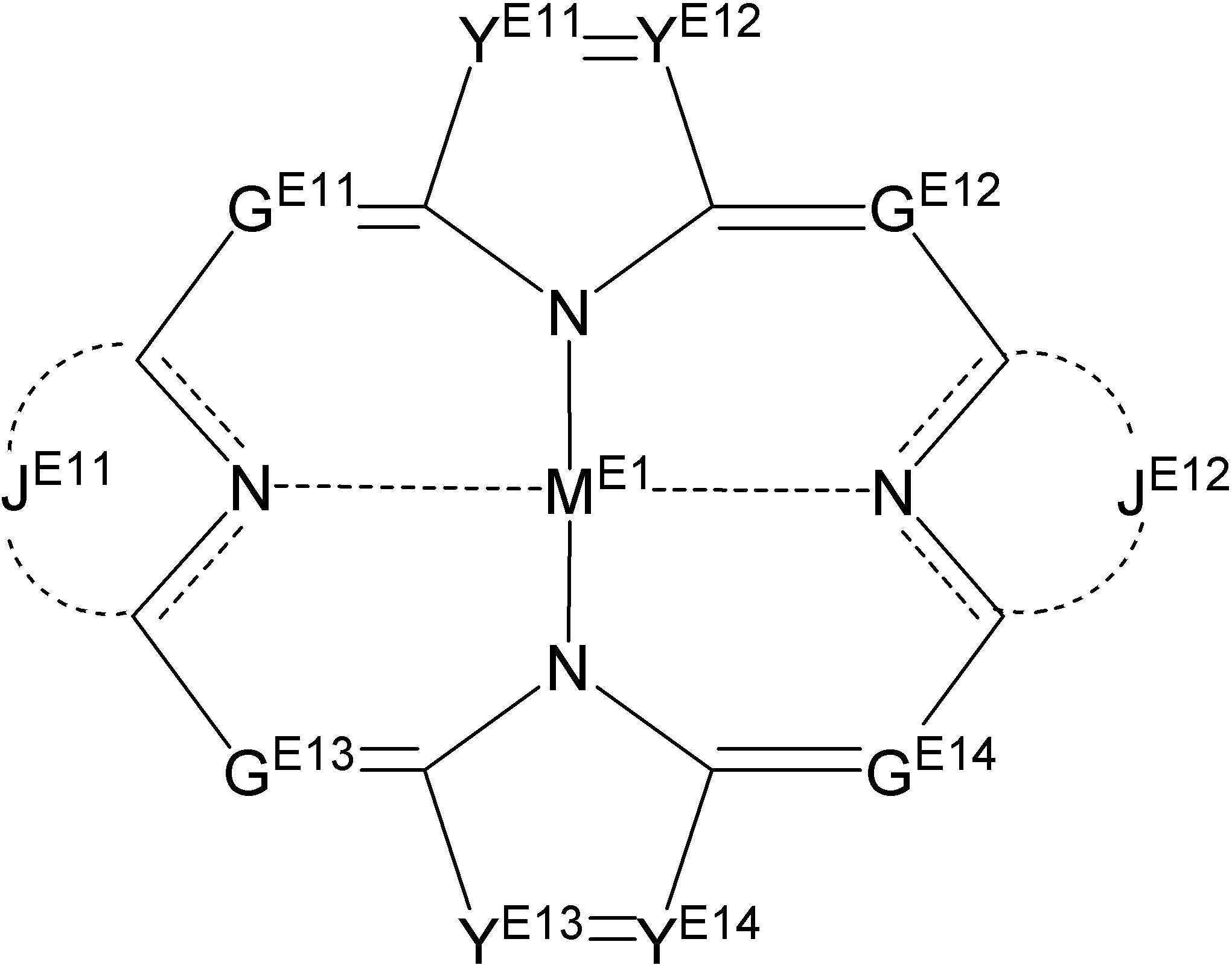
[일반식 E-1] [General Formula E-1]
상기 일반식 E-1에서,In the general formula E-1,
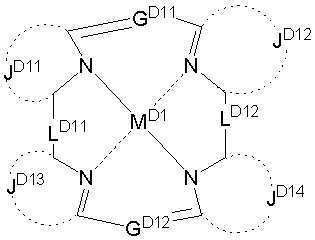
MD1은 일반식 (A-1)에서 정의한 바와 동일한 금속 이온을 나타내며, GD11,GD12는 각각 독립적으로 질소 원자,치환 또는 무치환의 탄소 원자를 나타내며, JD11,JD12,JD13 및 JD14는 각각 독립적으로 5원 고리를 형성하는데도 필요한 원자군을 나타내며, LD11,LD12는 연결기를 나타낸다. M D1 represents the same metal ion as defined in the general formula (A-1), G D11 , G D12 each independently represents a nitrogen atom, a substituted or unsubstituted carbon atom, J D11 , J D12 , J D13 and Each of J D14 independently represents an atomic group necessary to form a 5-membered ring, and L D11 and L D12 represent a linking group.
상기 일반식 E-1으로 표시되는 화합물의 예시적인 구조는 아래와 같으나, 이에 제한되지 않는다.An exemplary structure of the compound represented by the general formula E-1 is as follows, but is not limited thereto.
[일반식 F-1] [General Formula F-1]
상기 일반식 F-1에서, In the general formula F-1,
ME1은 일반식 A-1에서 정의한 바와 동일한 금속 이온을 나타내며, JE11,JE12는 각각 독립적으로 5 원 고리를 형성하는데도 필요한 원자군을 나타내며, GE11,GE12 ,GE13 및 GE14는 각각 독립적으로 질소 원자,치환 또는 무치환의 탄소 원자를 나타내며, YE11 ,YE12 ,YE13 및 YE14는 각각 독립적으로 질소 원자,치환 또는 무치환의 탄소원자를 나타낸다. M E1 represents the same metal ion as defined in General Formula A-1, J E11 and J E12 each independently represent a group of atoms required to form a five-membered ring, and G E11 , G E12 , G E13 and G E14 are Each independently represents a nitrogen atom, a substituted or unsubstituted carbon atom, and Y E11 ,Y E12 , Y E13 and Y E14 each independently represent a nitrogen atom, a substituted or unsubstituted carbon atom.
상기 일반식 F-1으로 표시되는 화합물의 예시적인 구조는 아래와 같으나, 이에 제한되지 않는다. An exemplary structure of the compound represented by the general formula F-1 is as follows, but is not limited thereto.
[일반식 G-1] [General Formula G-1]
상기 일반식 G-1에서,In the general formula G-1,
MF1은 일반식 A-1에서 정의한 바와 동일한 금속 이온을 나타내며, M F1 represents the same metal ion as defined in General Formula A-1,
LF11 ,LF12 및 LF13은 연결기를 나타내며, RF11,RF12,RF13 및 RF14는 치환기를 나타내고, RF11과 RF12,RF12 와 RF13, RF13과 RF14는 서로 연결되어 고리를 형성할 수 있고, 이때 RF1과 RF12,RF13과 RF14가 형성하는 고리는 5 원환이다. 또한 QF11, QF12는 MF1에 결합하는 원자를 함유하는 부분 구조를 나타낸다. L F11 ,L F12 and L F13 represent a linking group, R F11 ,R F12 ,R F13 and R F14 represent a substituent, and R F11 and R F12 ,R F12 And R F13 , R F13 and R F14 may be linked to each other to form a ring, wherein the ring formed by R F1 and R F12 , R F13 and R F14 is a 5-membered ring. Further, Q F11 and Q F12 represent a partial structure containing an atom bonded to M F1 .
상기 일반식 G-1으로 표시되는 화합물의 예시적인 구조는 아래와 같으나, 이에 제한되지 않는다. An exemplary structure of the compound represented by the general formula G-1 is as follows, but is not limited thereto.
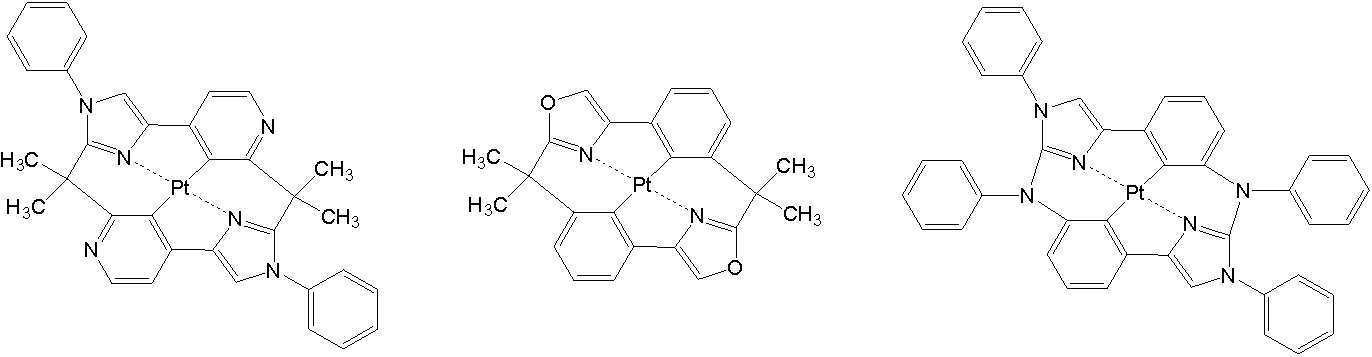
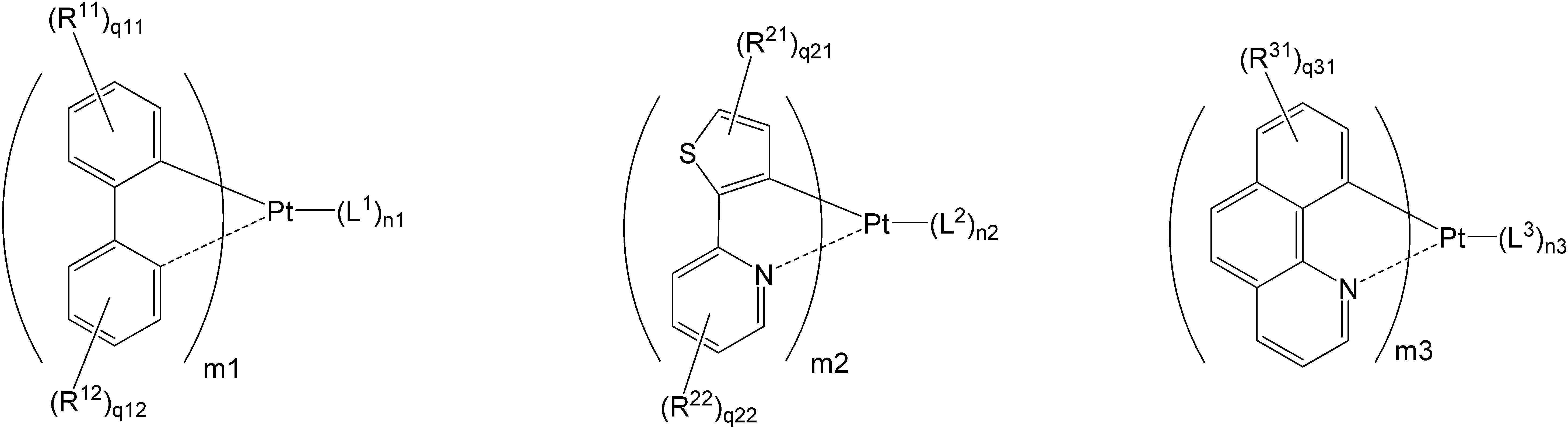
[일반식 H-1] [일반식 H-2] [일반식 H-3][General Formula H-1] [General Formula H-2] [General Formula H-3]
상기 일반식 H-1에서, In the general formula H-1,
R11, R12는 알킬, 아릴 또는 헤테로아릴의 치환기이며; 또한 서로 인접한 치환기와 융합고리를 형성할 수 있고, q11, q12는 0∼4의 정수로서, 바람직하게는 0∼2가 될 수 있다.R 11 , R 12 are substituents of alkyl, aryl or heteroaryl; In addition, a fused ring may be formed with a substituent adjacent to each other, and q11 and q12 are integers of 0 to 4, preferably 0 to 2.
또한 q11, q12가 2∼4의 경우, 복수개의 R11 및 R12는 각각 동일하거나 상이하며, In addition, when q11 and q12 are 2 to 4, a plurality of R11 and R12 are the same or different, respectively,
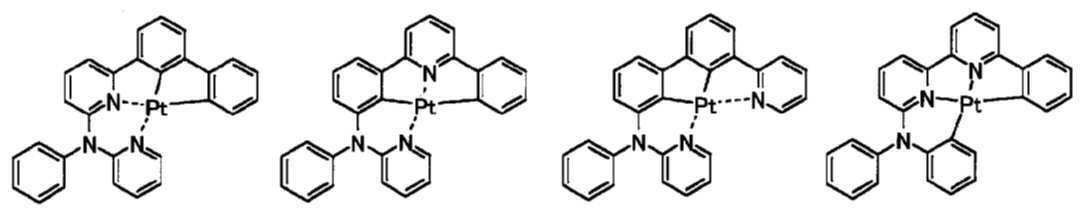
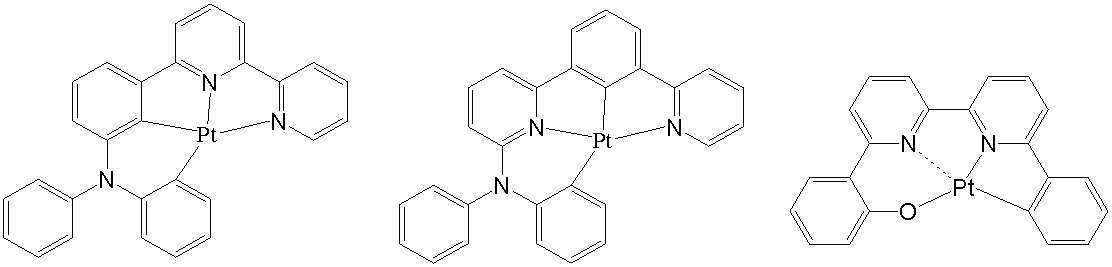
L1은 백금에 결합하는 리간드로서, 오르토 메탈(ortho metal)화 백금 착체를 형성할수 있는 리간드, 함질소헤테로환 리간드, 디케톤 리간드,할로겐 리간드가 바람직하고, 보다 바람직하게는 오르토 메탈(ortho metal)화 백금 착체를 형성하는 리간드, 비피리딜 리간드, 또는 페난트로린 리간드이다. L 1 is a ligand that binds to platinum, and is preferably a ligand capable of forming an ortho metalized platinum complex, a nitrogen-containing heterocyclic ligand, a diketone ligand, a halogen ligand, and more preferably an ortho metal. ) A ligand that forms a platinum complex, a bipyridyl ligand, or a phenanthroline ligand.
n1은 0 내지 3의 정수이며, 바람직하게는 0이고, m1은 1 또는 2이고 바람직하게는 2이다. n 1 is an integer of 0 to 3, preferably 0, and m 1 is 1 or 2, preferably 2.
또한, 상기 n1, m1 은 상기 일반식 H-1로 나타나는 금속 착체가 중성 착체가 되도록 하는 것이 바람직하다.In addition, it is preferable that n 1 and m 1 make the metal complex represented by the general formula H-1 become a neutral complex.
상기 일반식 H-2에서, R21, R22, n2, m2, q22, L2는 각각 상기 R11, R12, n1, m1, q12, L1과 동일하고, q21은 0 내지 2의 정수이며, 0이 바람직하다.In the general formula H-2, R 21 , R 22 , n 2 , m 2 , q 22 , L 2 are the same as the R 11 , R 12 , n 1 , m 1 , q 12 , L 1 , respectively, and q 21 is an integer of 0-2, and 0 is preferable.
상기 일반식 H-3에서, R31, n3, m3, L3 은 각각 상기 R11, n1, m1, L1과 동일하고, q31은 0 내지 8의 정수를 나타내고, 0 내지 2가 바람직하고, 0이 보다 바람직하다.In the general formula H-3, R 31 , n 3 , m 3 , L 3 are the same as R 11 , n 1 , m 1 , L 1 , respectively, and q 31 represents an integer of 0 to 8, and 0 to 2 is preferable and 0 is more preferable.
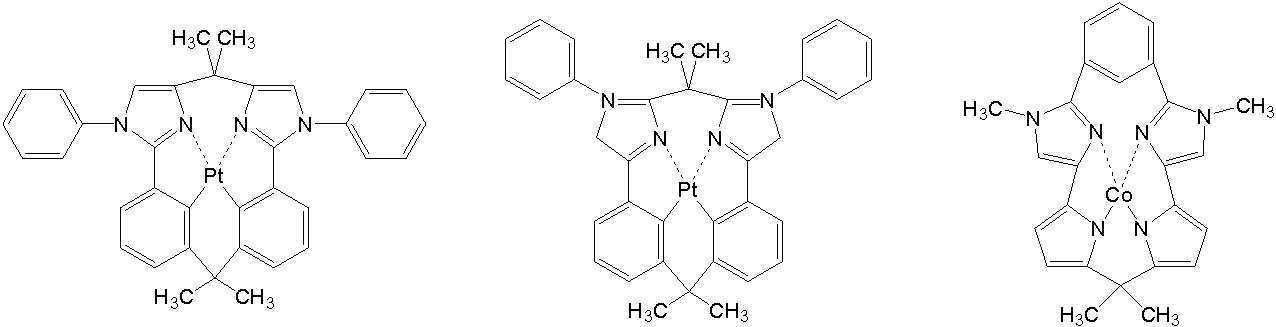
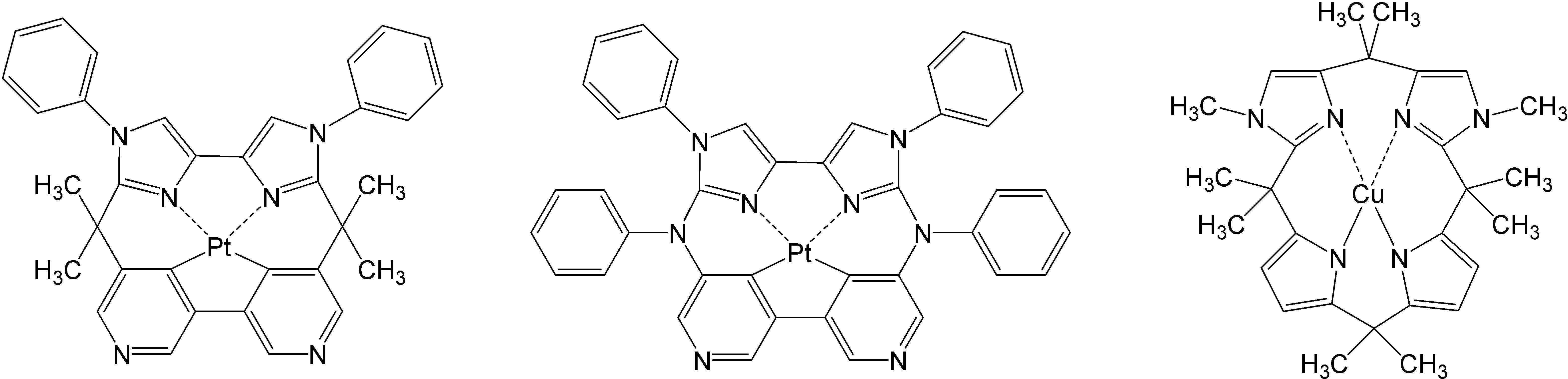
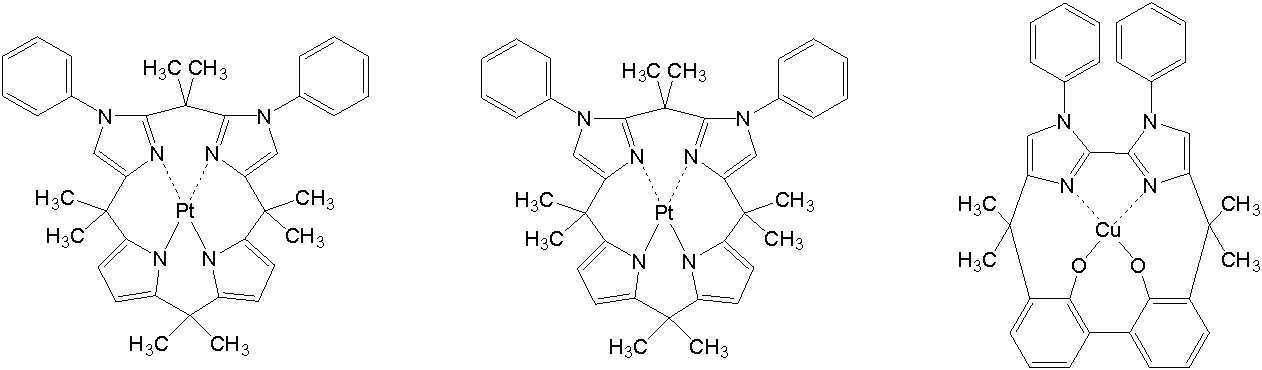
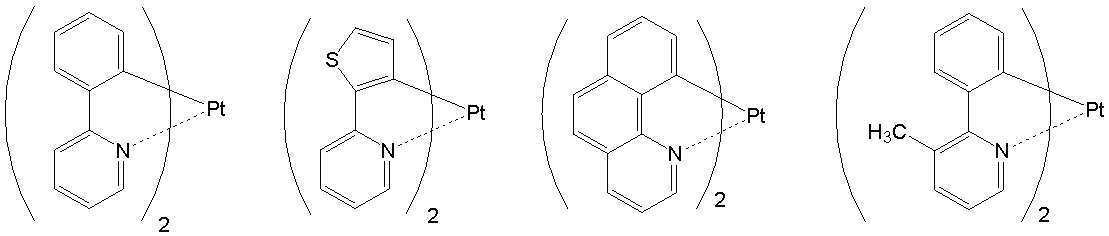
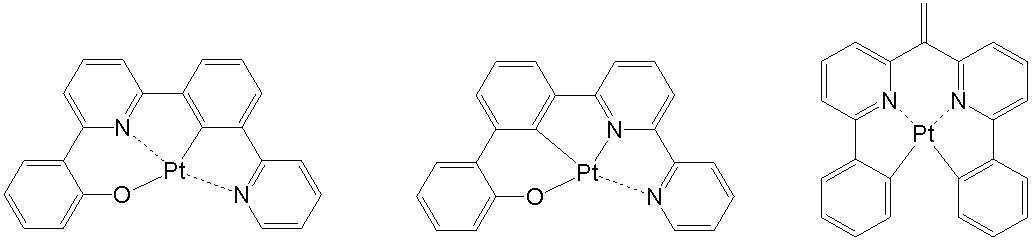
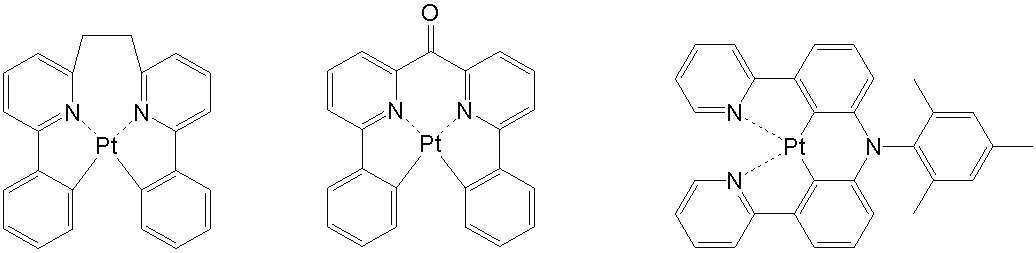
상기 일반식 H-1 내지 H-3의 구체적인 화합물의 예는 다음과 같으나, 이에 한정되는 것은 아니다.Examples of specific compounds of the general formulas H-1 to H-3 are as follows, but are not limited thereto.
[일반식 I-1][General Formula I-1]
상기 일반식 I-1에서, In the general formula I-1,
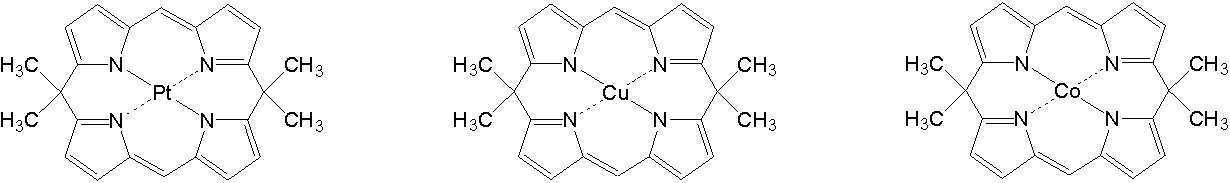
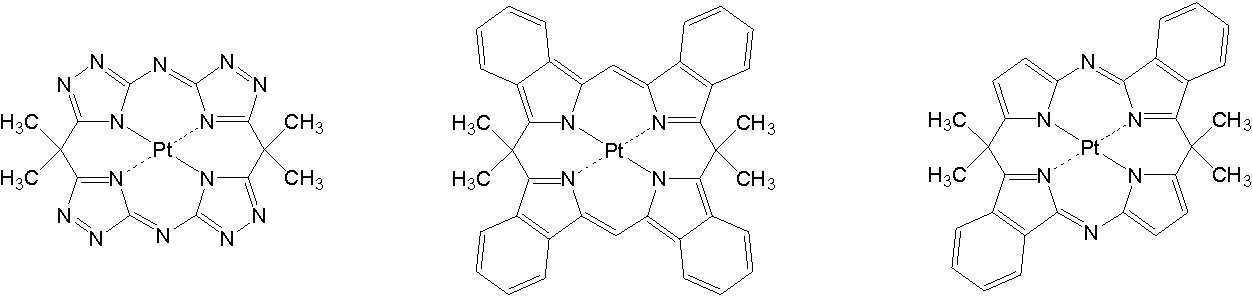
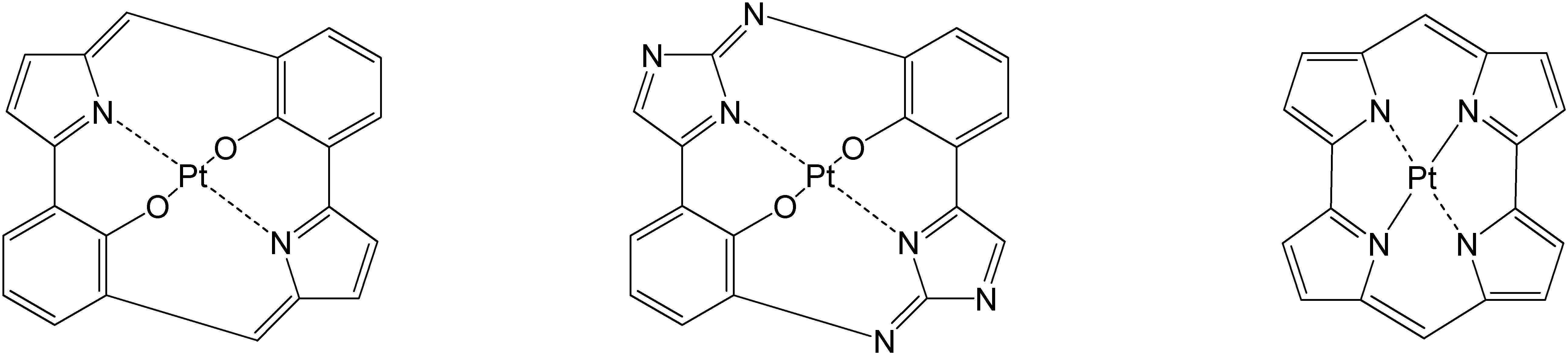
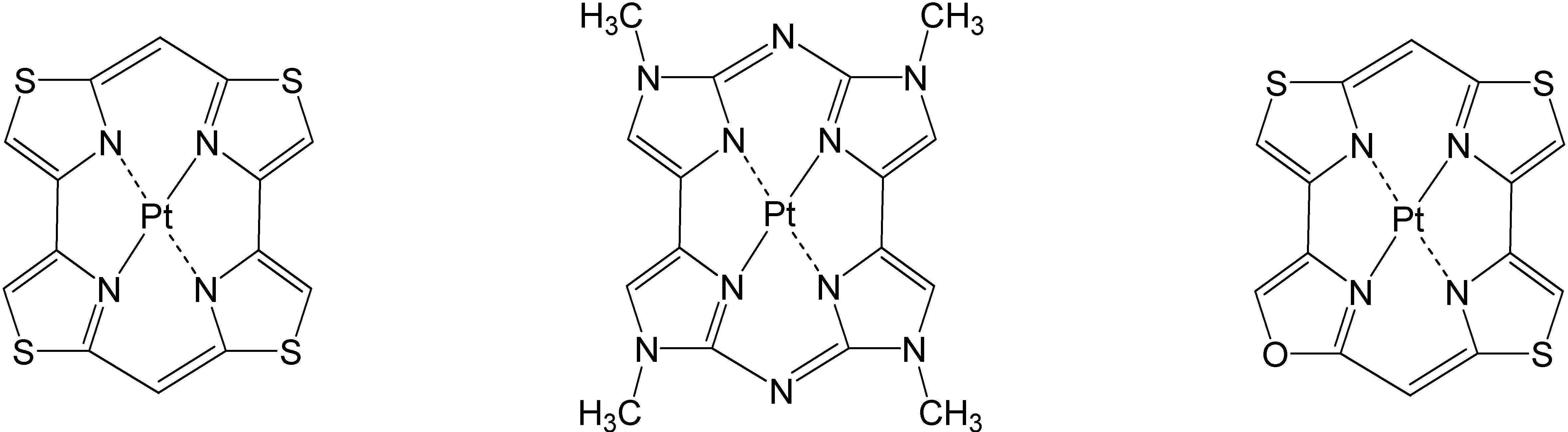
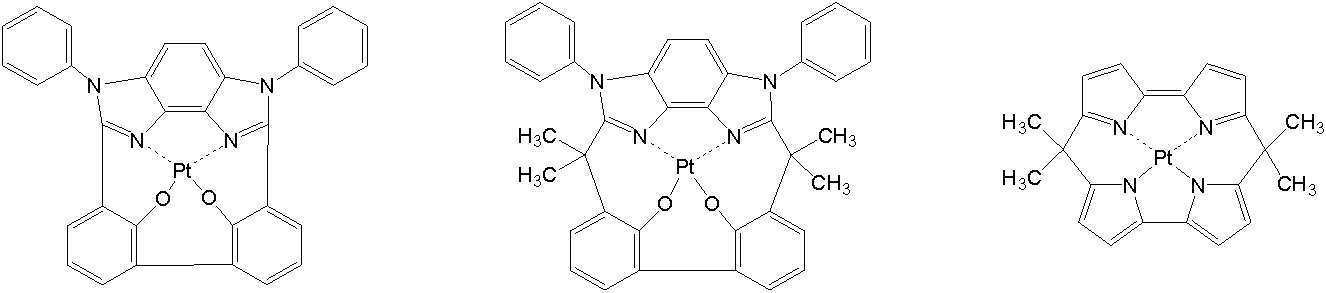
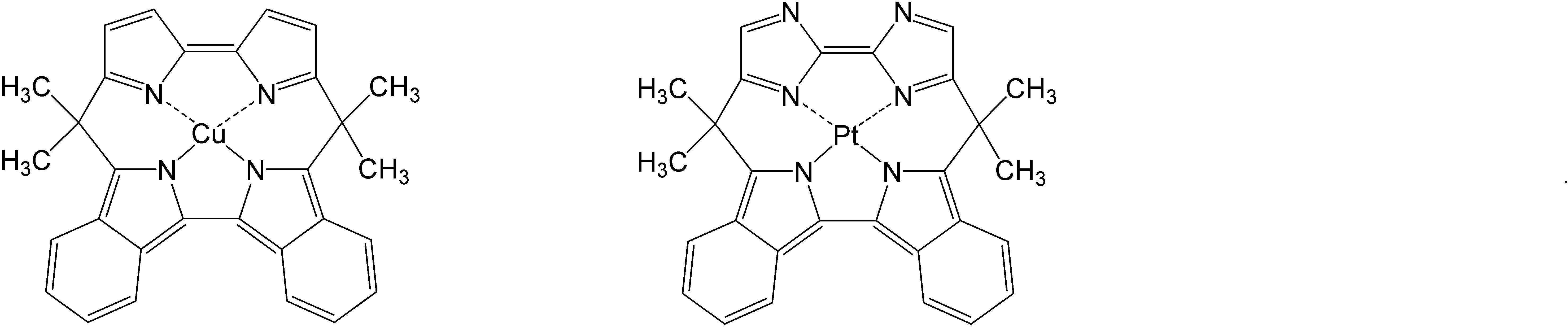
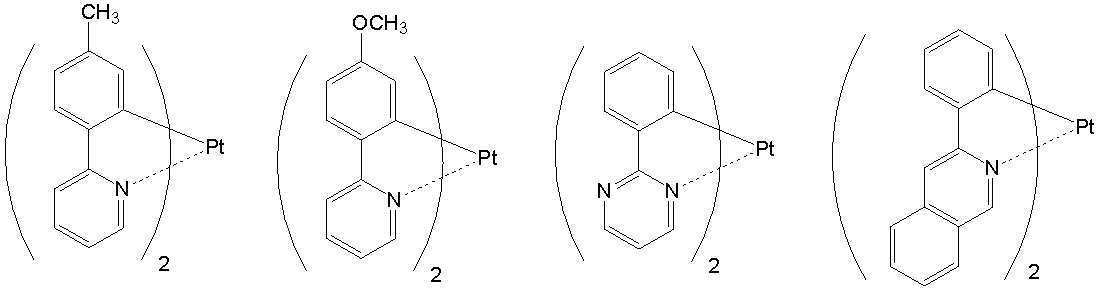
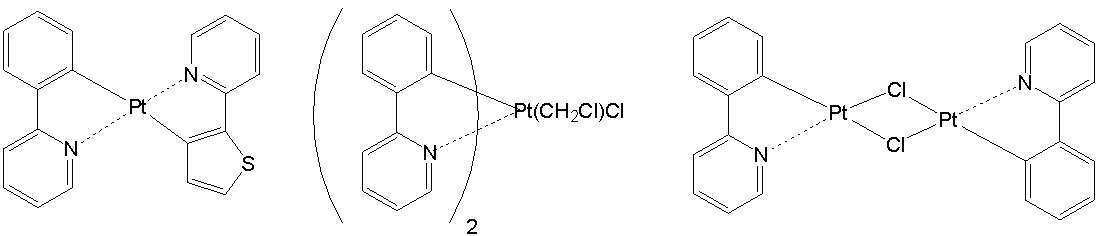
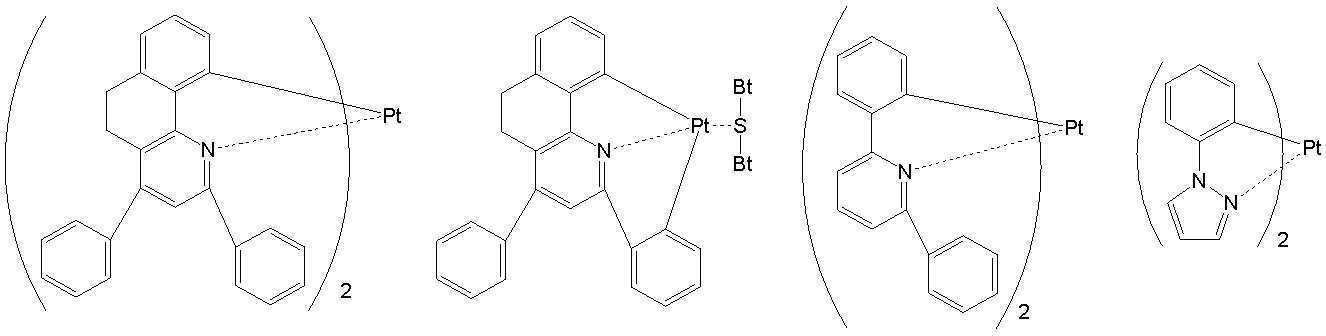
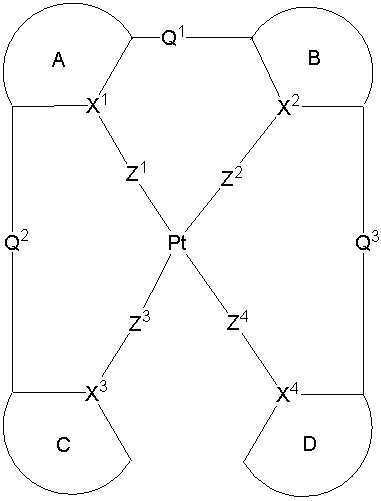
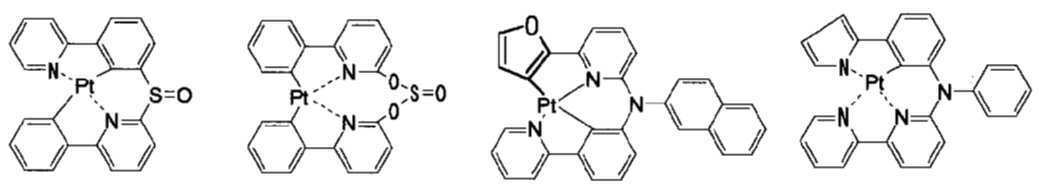
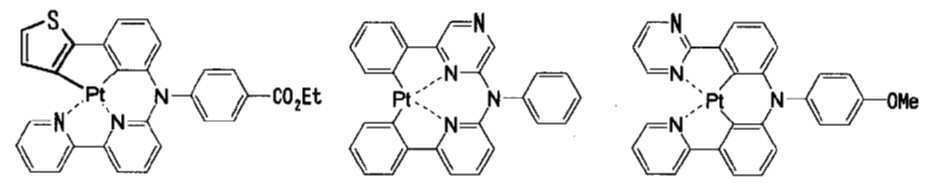
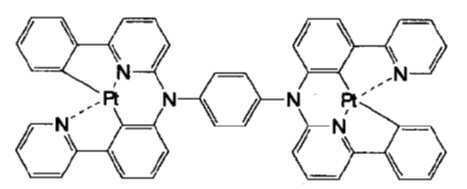
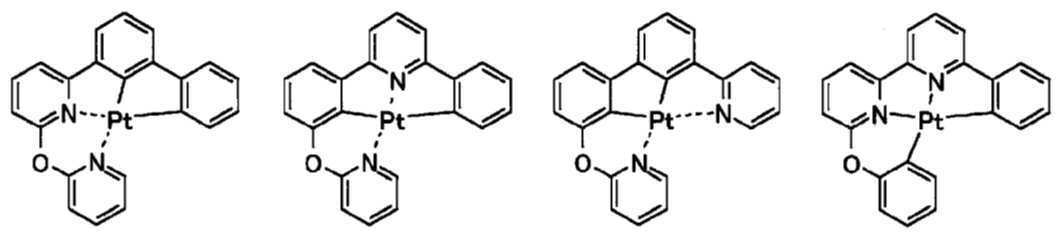
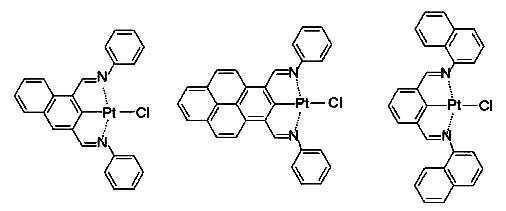
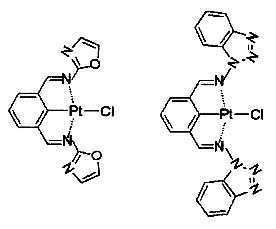
고리A, 고리B, 고리C 및 고리D는 상기 고리 A내지 D중의 어느 2개의 고리는 치환기를 가질 수 있는 질소 함유 헤테로고리를 나타내고, 나머지 2개의 고리는 치환기를 가질 수 있는 아릴고리 또는 헤테로아릴고리를 나타내고, 나타내며, 고리A와 고리B, 고리A와 고리C 및/또는 고리B와 고리D로 축합환을 형성할 수 있다. X1, X2, X3 및 X4는 이 중의 어느 2개가 백금원자에 배위결합하는 질소원자를 나타내고, 나머지 2개는 탄소원자 또는 질소원자를 나타낸다. Q1, Q2 및 Q3은 각각 독립적으로 2가의 원자(단) 또는 결합을 나타내지만, Q1, Q2 및 Q3이 동시에 결합을 나타내지는 않는다. Z1, Z2, Z3 및 Z4는 어느 2개가 배위결합을 나타내고, 나머지 2개는 공유결합, 산소원자 또는 황원자를 나타낸다.Ring A, Ring B, Ring C, and Ring D represent a nitrogen-containing heterocycle in which any two of the rings A to D may have a substituent, and the other two rings are an aryl ring or heteroaryl which may have a substituent. Represents and represents a ring, and a condensed ring can be formed by ring A and ring B, ring A and ring C, and/or ring B and ring D. X 1 , X 2 , X 3 and X 4 represent a nitrogen atom in which two of them are coordinated to a platinum atom, and the other two represent a carbon atom or a nitrogen atom. Q 1 , Q 2 and Q 3 each independently represent a divalent atom (term) or a bond, but Q 1 , Q 2 and Q 3 do not simultaneously represent a bond. Z 1 , Z 2 , Z 3 and Z 4 are any two representing a coordination bond, and the other two represent a covalent bond, an oxygen atom or a sulfur atom.
상기 일반식 I-1의 구체적인 화합물의 예는 다음과 같으나, 이에 한정되는 것은 아니다.Examples of specific compounds of the general formula I-1 are as follows, but are not limited thereto.
[일반식 J-1][General Formula J-1]
상기 일반식 J-1에 있어서, In the general formula J-1,
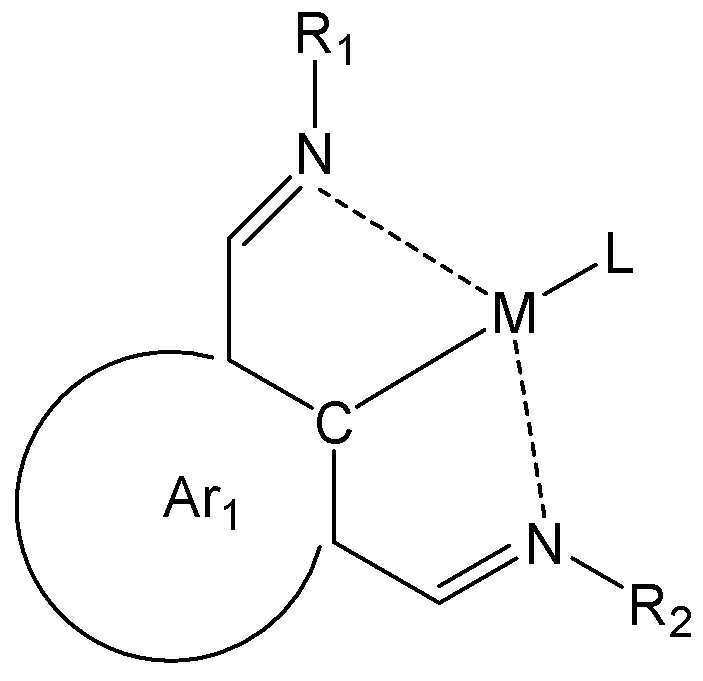
M은 일반식 A-1에서 정의한 바와 동일한 금속 이온을 나타내며, Ar1은 치환 또는 비치환의 고리구조를 표현하고, 상기 M에 결합하는 2개의 아조메틴(azomethine) 결합(-C=N-)에 있어서, 질소원자(N)는 각각 상기 M에 결합하고, 전체로서 상기 M에 3좌에서 결합되는 3좌 배위자를 형성하고 있다. M represents the same metal ion as defined in General Formula A-1, Ar1 represents a substituted or unsubstituted cyclic structure, and in the two azomethine bonds (-C=N-) bonded to the M , The nitrogen atom (N) is each bonded to the M, and as a whole, forms a tridentate ligand bonded to the M at three loci.
또한, Ar1에 있어서 C는 Ar1으로 표시되는 고리구조를 구성하는 탄소원자를 나타낸다. 또한 상기 R1 및 R2는, 서로 동일하거나 상이할 수 있고, 각각 치환 또는 비치환의 알킬기 또는 아릴기를 나타내며, L은 1좌 배위자를 표현한다.In addition, in Ar1, C represents a carbon atom constituting the ring structure represented by Ar1. In addition, R1 and R2 may be the same as or different from each other, and each represents a substituted or unsubstituted alkyl group or aryl group, and L represents a monodentate ligand.
상기 일반식J-1에 있어서, 상기 M은 Pt인 것이 바람직하다. 또한, 상기 Ar1으로서는,5원환, 6원환 및 이들의 축합환기부터 선택되는 것이 바람직하다.
In the general formula J-1, it is preferable that M is Pt. In addition, it is preferable that Ar1 is selected from a 5-membered ring, a 6-membered ring, and a condensed ring group thereof.
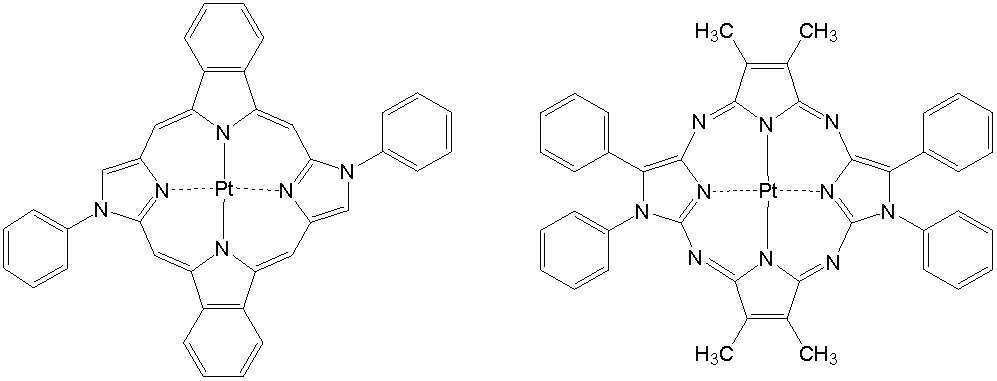
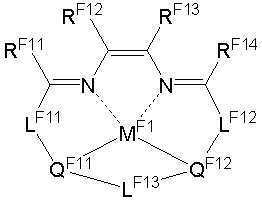
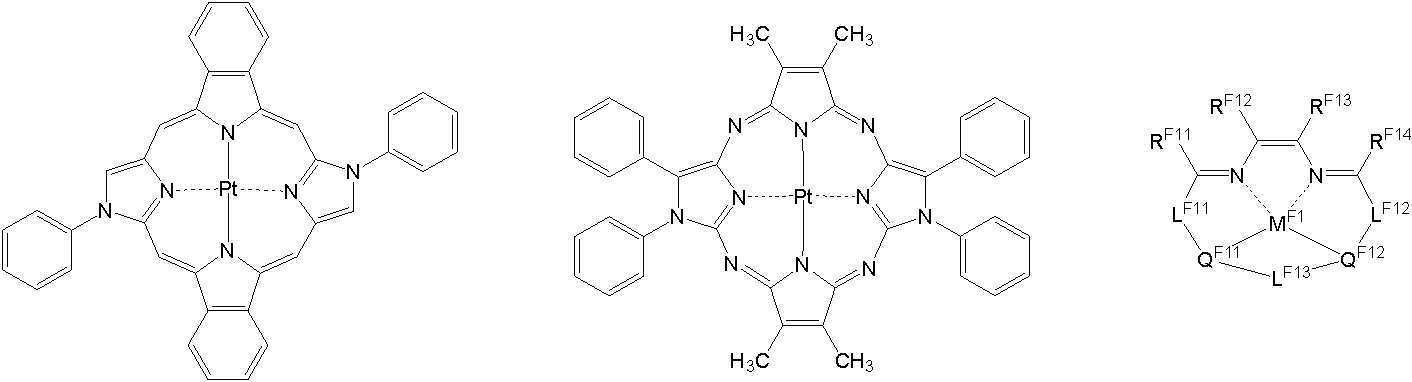
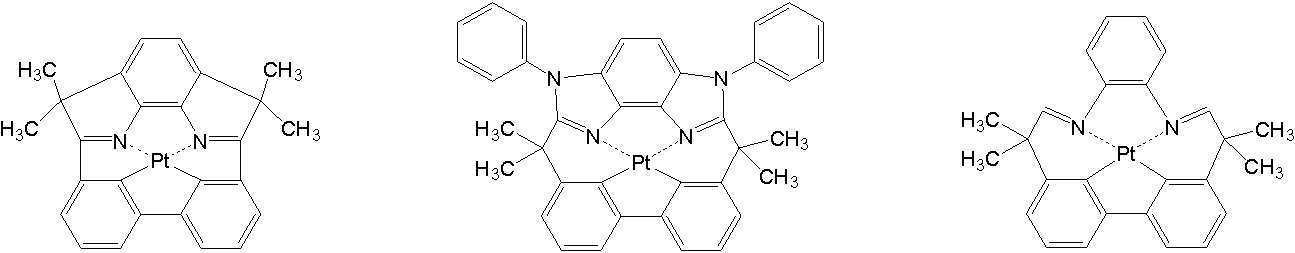
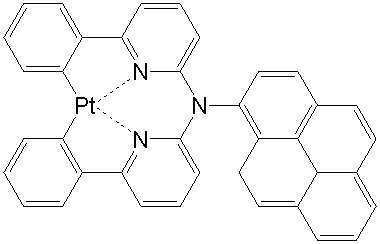
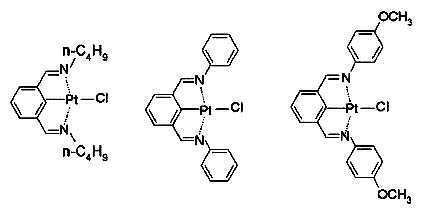
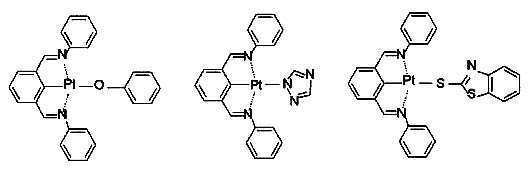
상기 일반식 J-1의 구체적인 화합물의 예는 다음과 같으나, 이에 한정되는 것은 아니다.Examples of specific compounds of the general formula J-1 are as follows, but are not limited thereto.
또한 상기 발광층은 상기 도판트와 호스트이외에도 다양한 호스트와 다양한 도펀트 물질을 추가로 포함할 수 있다.In addition, the emission layer may further include various hosts and various dopant materials in addition to the dopant and host.
또한, 본 발명에서 상기 정공주입층, 정공수송층, 전자저지층, 발광층, 정공저지층, 전자수송층 및 전자주입층으로부터 선택된 하나 이상의 층은 단분자 증착방식 또는 용액공정에 의하여 형성될 수 있다. 여기서 상기 증착 방식은 상기 각각의 층을 형성하기 위한 재료로 사용되는 물질을 진공 또는 저압상태에서 가열 등을 통해 증발시켜 박막을 형성하는 방법을 의미하고, 상기 용액공정은 상기 각각의 층을 형성하기 위한 재료로 사용되는 물질을 용매와 혼합하고 이를 잉크젯 인쇄, 롤투롤 코팅, 스크린 인쇄, 스프레이 코팅, 딥 코팅, 스핀 코팅 등과 같은 방법을 통하여 박막을 형성하는 방법을 의미한다. In addition, in the present invention, at least one layer selected from the hole injection layer, the hole transport layer, the electron blocking layer, the light emitting layer, the hole blocking layer, the electron transport layer and the electron injection layer may be formed by a single molecule deposition method or a solution process. Here, the deposition method refers to a method of forming a thin film by evaporating a material used as a material for forming each layer through heating in a vacuum or low pressure state, and the solution process is used to form each layer. It refers to a method of forming a thin film through a method such as inkjet printing, roll-to-roll coating, screen printing, spray coating, dip coating, spin coating, etc. by mixing a material used as a material for use with a solvent.
또한 본 발명에서의 상기 유기 발광 소자는 평판 디스플레이 장치; 플렉시블 디스플레이 장치; 단색 또는 백색의 평판 조명용 장치; 및 단색 또는 백색의 플렉시블 조명용 장치;에서 선택되는 어느 하나의 장치에 사용될 수 있다. In addition, the organic light emitting device in the present invention includes a flat panel display device; Flexible display device; Monochrome or white flat lighting devices; And a single color or white flexible lighting device; may be used in any one device selected from.
이하, 바람직한 실시예를 들어 본 발명을 더욱 상세하게 설명한다. 그러나, 이들 실시예는 본 발명을 보다 구체적으로 설명하기 위한 것으로, 본 발명의 범위가 이에 의하여 제한되지 않는다는 것은 당업계의 통상의 지식을 가진 자에게 자명할 것이다. Hereinafter, the present invention will be described in more detail with reference to preferred embodiments. However, these examples are for explaining the present invention in more detail, and it will be apparent to those of ordinary skill in the art that the scope of the present invention is not limited thereto.
(실시예)(Example)
합성예 1. [화합물1]의 합성Synthesis Example 1. Synthesis of [Compound 1]
합성예 1-1) [중간체 1-a]의 합성Synthesis Example 1-1) Synthesis of [Intermediate 1-a]
[반응식 1-1] [Reaction Scheme 1-1]
[중간체 1-a] [Intermediate 1-a]
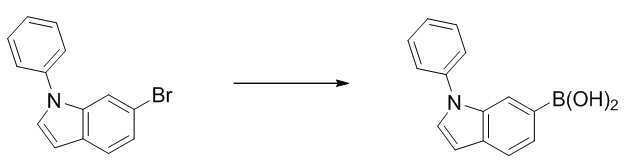
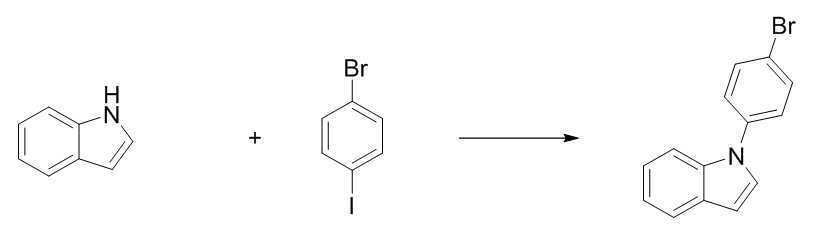
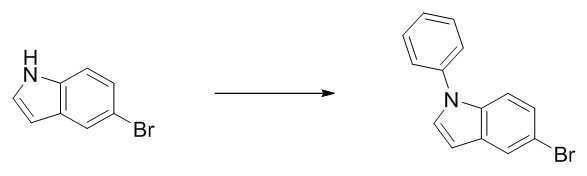
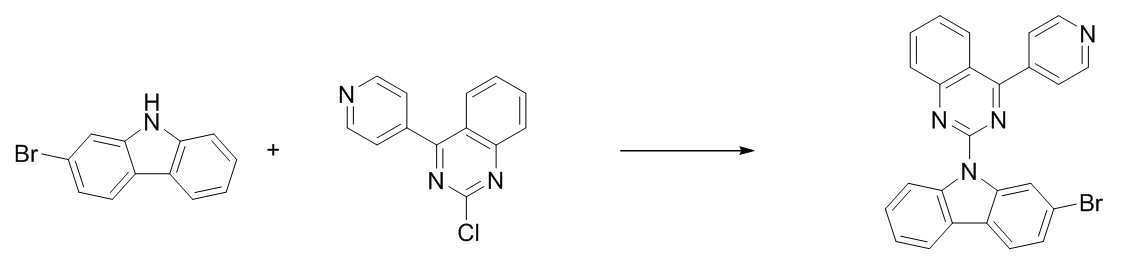
6-브로모인돌 50.0 g (255.0 mmol), 아이오도벤젠 10.4 g (510.0 mmol), 구리분말 32.4 g (510.0 mmol), 18-크라운-6 13.5 g (51.0 mmol), 탄산칼륨 105.7 g (765.0 mmol)을 순서대로 넣고, 1,2-디클로로벤젠 500 ml를 가한 후, 180 ℃에서 1일 동안 환류, 교반시킨다. 6-bromoindole 50.0 g (255.0 mmol), iodobenzene 10.4 g (510.0 mmol), copper powder 32.4 g (510.0 mmol), 18-crown-6 13.5 g (51.0 mmol), potassium carbonate 105.7 g (765.0 mmol) ) In order, 500 ml of 1,2-dichlorobenzene was added, and then refluxed and stirred at 180° C. for 1 day.
반응이 종료되면, 고온필터 후 용액을 감압농축하고 유기 층 용액을 헥산으로 컬럼 크로마토그래피를 하여 [중간체 1-a]를 57.6 g 얻었다. (수율 83 %)When the reaction was completed, the solution was concentrated under reduced pressure after high-temperature filtering, and the organic layer solution was subjected to column chromatography with hexane to obtain 57.6 g of [Intermediate 1-a]. (83% yield)
합성예 1-2) [중간체 1-b]의 합성 Synthesis Example 1-2) Synthesis of [Intermediate 1-b]
[반응식 1-2] [Scheme 1-2]
[중간체 1-a] [중간체 1-b][Intermediate 1-a] [Intermediate 1-b]
상기 [반응식 1-1]로부터 얻은 [중간체 1-a] 화합물 57.6 g (211.6 mmol)을 질소 기류하에서 테트라하이드로퓨란 600 ml에 녹인 후 -78 ℃에서 교반하면서 1.6M 노르말-부틸리튬159 ml (253.9 mmol)을 천천히 적가하고, 적가가 완료되면 -78 ℃를 유지하면서 1시간 동안 교반시킨다. 그 후 트리메틸보레이트 26.4 g (253.9 mmol)을 천천히 적가 한 후 상온으로 올려서 2시간 교반시킨다.After dissolving 57.6 g (211.6 mmol) of the [Intermediate 1-a] compound obtained from [Scheme 1-1] in 600 ml of tetrahydrofuran under a stream of nitrogen, and stirring at -78 °C, 159 ml of 1.6M normal-butyllithium (253.9 mmol) was slowly added dropwise, and when the dropwise addition was completed, the mixture was stirred for 1 hour while maintaining -78°C. After that, 26.4 g (253.9 mmol) of trimethylborate was slowly added dropwise, and then raised to room temperature and stirred for 2 hours.
반응이 종료되면 2M 염산수용액 300 ml를 상온에서 적가 한 후 30분간 교반시킨다. 그 후 에틸아세테이트와 물로 추출하고 유기층을 감압농축하고 디클로로메탄과 헥산으로 재결정하여 [중간체 1-b]를 28.6 g 얻었다. (수율 57 %)Upon completion of the reaction, 300 ml of a 2M aqueous hydrochloric acid solution was added dropwise at room temperature, followed by stirring for 30 minutes. Thereafter, extraction was performed with ethyl acetate and water, and the organic layer was concentrated under reduced pressure and recrystallized with dichloromethane and hexane to obtain 28.6 g of [Intermediate 1-b]. (Yield 57%)
합성예 1-3) [중간체 1-c]의 합성Synthesis Example 1-3) Synthesis of [Intermediate 1-c]
[반응식 1-3] [Scheme 1-3]
[중간체 1-c] [Intermediate 1-c]
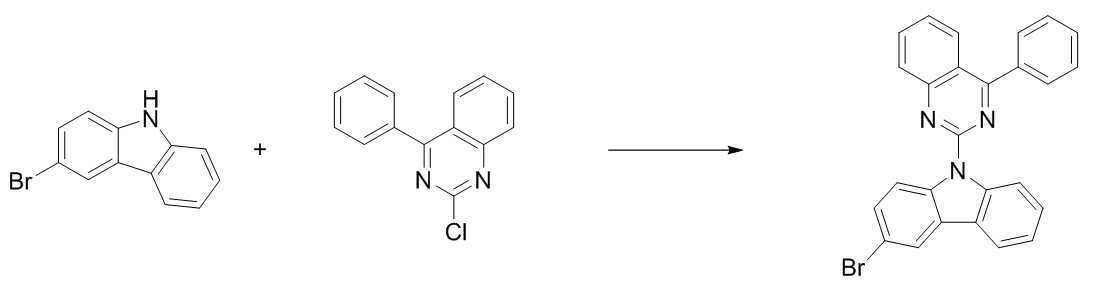
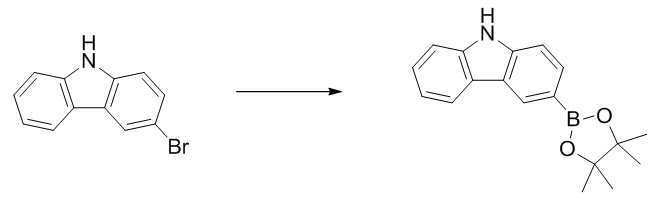
카바졸 150.0 g (762.6 mmol)을 디메틸포름아마이드1.0 L 에 녹인 후 0℃ 에서 교반시킨다. 그 후 N-브로모쑥신이미드 135.7 g (762.6 mmol)을 디메틸포름아마이드 0.5 L 녹여서 0℃ 를 유지하면서 1시간 동안 천천히 적가 시킨다. 적가가 완료되면 상온으로 올린 후 12시간 동안 교반시킨다.Carbazole 150.0 g (762.6 mmol) was dissolved in 1.0 L of dimethylformamide, and then stirred at 0°C. Thereafter, 135.7 g (762.6 mmol) of N-bromomucinimide was dissolved in 0.5 L of dimethylformamide, and then slowly added dropwise for 1 hour while maintaining 0°C. When the dropwise addition is complete, the mixture is raised to room temperature and stirred for 12 hours.
반응이 종료되면 증류수를 상온에서 적가 한 후 갈색 결정이 생기면 결정을 여과한 후 톨루엔, 메탄올로 재결정하여 [중간체 1-c] 110.0 g을 얻었다. (수율 58 %)When the reaction was completed, distilled water was added dropwise at room temperature, and when brown crystals were formed, the crystals were filtered and recrystallized with toluene and methanol to obtain 110.0 g of [Intermediate 1-c]. (Yield 58%)
합성예 1-4) [중간체 1-d]의 합성Synthesis Example 1-4) Synthesis of [Intermediate 1-d]
[반응식 1-4] [Scheme 1-4]
[중간체 1-d] [Intermediate 1-d]
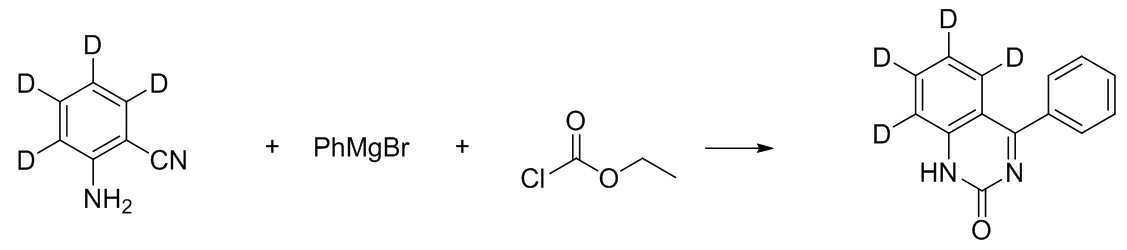
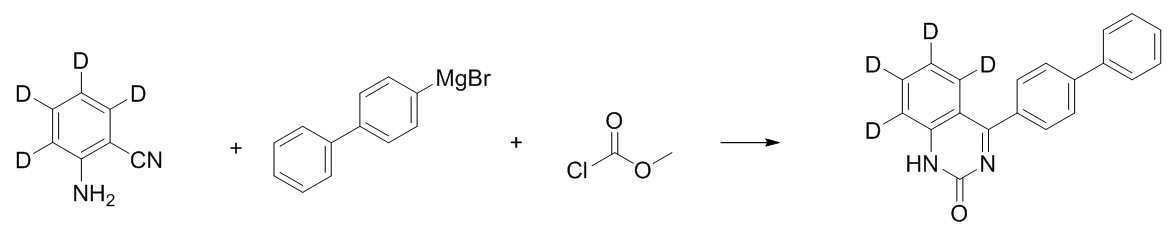
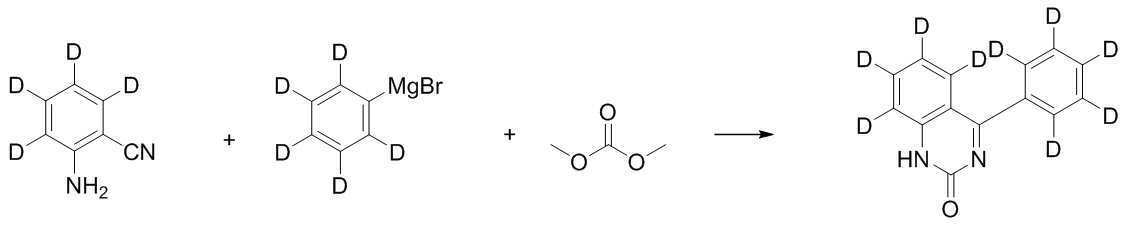
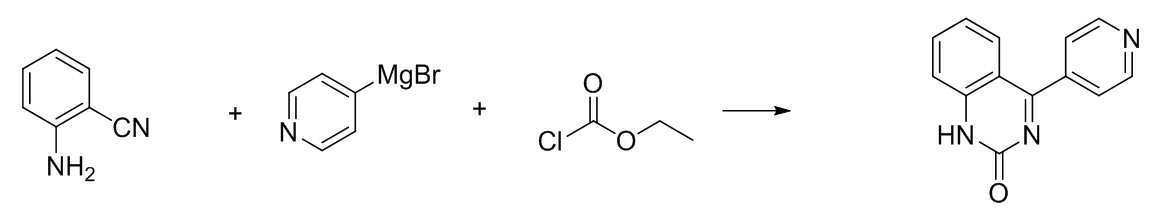
상온에서, 질소 기류하의 둥근 바닥 플라스크에 2-아미노벤조니트릴(20.0g, 169mmol), 테트라하이드로퓨란 140mL를 투입하고 교반하였다. 페닐마그네슘브로마이드(3.0M in Et2O)를 112.9mL(339mmol) 적하하였다. 1시간 정도 환류교반 후 온도를 0℃로 하였다. 에틸 클로로포메이트 (22.0g, 203mmol)를 적하한 후 약 1시간 정도 환류교반하였다. 암모늄클로라이드수용액을 약산성이 될 때까지 투입하고, 생성된 고체를 여과하여 물과 헵탄으로 씻어주어 [중간체 1-d]를 30.1g 얻었다. (수율 80%)At room temperature, 2-aminobenzonitrile (20.0 g, 169 mmol) and 140 mL of tetrahydrofuran were added to a round bottom flask under a nitrogen stream, followed by stirring. 112.9 mL (339 mmol) of phenyl magnesium bromide (3.0 M in Et 2 O) was added dropwise. After reflux stirring for about 1 hour, the temperature was set to 0°C. Ethyl chloroformate (22.0g, 203mmol) was added dropwise and stirred under reflux for about 1 hour. An aqueous ammonium chloride solution was added until it became slightly acidic, and the resulting solid was filtered and washed with water and heptane to obtain 30.1 g of [Intermediate 1-d]. (Yield 80%)
합성예 1-5) [중간체 1-e]의 합성Synthesis Example 1-5) Synthesis of [Intermediate 1-e]
[반응식 1-5] [Scheme 1-5]
[중간체 1-e] [Intermediate 1-e]
상온에서, 질소 기류하의 둥근 바닥 플라스크에 상기 합성한 [중간체 1-d](30.0g, 135mmol), 옥시염화인 약 80mL를 투입하고 교반하였다. 밤새 환류교반 후 다음날 온도를 -20℃로 냉각한 후 물을 약 400mL정도 천천히 적하하였다. 생성된 고체를 여과한 후 물, 메탄올, 헵탄으로 씻어주었다. 톨루엔과 헵탄으로 재결정하여 흰색 고체인 [중간체 1-e]를 14.6g 얻었다. (수율 44.9%)At room temperature, the synthesized [intermediate 1-d] (30.0 g, 135 mmol) and about 80 mL of phosphorus oxychloride were added to a round bottom flask under a nitrogen stream, followed by stirring. After reflux stirring overnight, the temperature was cooled to -20℃ the next day, and water was slowly added dropwise about 400mL. The resulting solid was filtered and washed with water, methanol, and heptane. Recrystallization from toluene and heptane gave 14.6 g of [Intermediate 1-e] as a white solid. (Yield 44.9%)
합성예 1-6) [중간체 1-f]의 합성Synthesis Example 1-6) Synthesis of [Intermediate 1-f]
[반응식 1-6] [Scheme 1-6]
[중간체 1-f] [Intermediate 1-f]
상온에서, 질소 기류하의 둥근 바닥 플라스크에 60% 소듐 하이드라이드 2.1 g (53 mmol)와 디메틸포름아마이드 50mL를 투입하고 약 30분간 교반하였다. 상기 [반응식 1-3]로부터 얻은 [중간체 1-c] 10.0 g (41 mmol)와 디메틸포름아마이드 100mL를 적하한 후 약 1시간 정도 더 교반하였다. 상기 합성한 [중간체 1-e] 12.7g (53 mmol)와 디메틸포름아마이드 100mL를 투입하고 밤새 교반하였다. 플라스크에 증류수 600mL를 넣어서 생긴 고체를 여과하였다. 톨루엔으로 재결정하여 [중간체 1-f] 14.3g을 얻었다. (수율 78.1 %)At room temperature, 2.1 g (53 mmol) of 60% sodium hydride and 50 mL of dimethylformamide were added to a round bottom flask under a flow of nitrogen, and the mixture was stirred for about 30 minutes. 10.0 g (41 mmol) of [Intermediate 1-c] obtained from [Scheme 1-3] and 100 mL of dimethylformamide were added dropwise, followed by stirring for about 1 hour. 12.7g (53 mmol) of the synthesized [Intermediate 1-e] and 100 mL of dimethylformamide were added, followed by stirring overnight. A solid formed by adding 600 mL of distilled water to the flask was filtered. Recrystallized from toluene to obtain 14.3 g of [Intermediate 1-f]. (Yield 78.1%)
합성예 1-7) [화합물 1]의 합성Synthesis Example 1-7) Synthesis of [Compound 1]
[반응식 1-7] [Scheme 1-7]
[화합물 1] [Compound 1]
상기 합성한 [중간체 1-f] 14.3 g(32 mmol), 상기 합성한 [중간체 1-b] 9.0 g(38 mmol), 테트라키스(트리페닐포스핀)팔라듐 0.7 g (0.64 mmol), 탄산칼륨 8.8 g(64 mmol), 1,4-다이옥산 80ml, 톨루엔 80ml, 증류수 30ml에 넣고 밤새 환류교반하였다. 반응이 종료되면 에틸아세테이트와 증류수를 사용하여 추출한다. 유기층을 감압농축하고 디클로로메탄과 아세톤으로 재결정하여 [화합물 1] 4.4 g을 얻었다. (수율 24.6 %)The synthesized [intermediate 1-f] 14.3 g (32 mmol), the synthesized [intermediate 1-b] 9.0 g (38 mmol), tetrakis (triphenylphosphine) palladium 0.7 g (0.64 mmol), potassium carbonate 8.8 g (64 mmol), 1,4-
MS(MALDI-TOF): m/z 563 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 563 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127.4,127.5,127.7,128.3,128.5,128.7,129.2,129.3,131.8,132.3,133,133.1,138.7,141.6,143.7,144.4,145.9,149.3,155.8,161 [40C]103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127.4,127.5,127.7,128.3,128.5,128.7,129.2,129.3,131.8,132.3,133,133.1,138.7, 141.6,143.7,144.4,145.9,149.3,155.8,161 [40C]
합성예 2. 화합물2의 합성Synthesis Example 2. Synthesis of Compound 2
상기 [반응식 1-1]에서 사용한 6-브로모인돌 대신 4-브로모인돌을 사용하여 상기 합성예 1-1 내지 1-2와 동일한 방법으로 제조하고, 상기 [반응식 1-6]에서 사용한 [중간체 1-c] 대신 2-브로모카바졸을 사용하여 상기 합성예 1-6 내지 1-7과 동일한 방법을 이용하여 [화합물2] 4.2g을 합성하였다. (수율 27%)It was prepared in the same manner as in Synthesis Examples 1-1 to 1-2 by using 4-bromoindole instead of 6-bromoindole used in [Scheme 1-1], and [ Using 2-bromocarbazole instead of the intermediate 1-c], 4.2 g of [Compound 2] was synthesized using the same method as in Synthesis Examples 1-6 to 1-7. (Yield 27%)
MS(MALDI-TOF): m/z 562 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 562 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
104.8,107.6,108.4,109.5,109.9,118.9,119.3,119.8,121.3,121.4,125.5,125.6,125.7,126.6,127.4,127.5,127.7,128.5,128.6,128.7,129.2,129.3,129.8,131.8,132.3,133,133.1,138.7,141.6,144.4,145.9,149.3,155.8,161 [40C]104.8,107.6,108.4,109.5,109.9,118.9,119.3,119.8,121.3,121.4,125.5,125.6,125.7,126.6,127.4,127.5,127.7,128.5,128.6,128.7,129.2,129.3,129.8,131.8,132.3, 133,133.1,138.7,141.6,144.4,145.9,149.3,155.8,161 [40C]
합성예 3. 화합물3의 합성Synthesis Example 3. Synthesis of Compound 3
합성예 3-1) [중간체 3-a]의 합성Synthesis Example 3-1) Synthesis of [Intermediate 3-a]
[반응식 3-1][Reaction Scheme 3-1]
[중간체 3-a] [Intermediate 3-a]
둥근 바닥 플라스크에 메틸 아미노벤조에이트 (50.0g, 330mmol), 아이오도 벤젠(56.3g, 276mmol), 팔라듐 아세테이트 (1.2g, 5.6mmol), 잔트포스 (6.4g, 11.02mmol), 탄산세슘 (126g, 386mmol), 톨루엔 1000mL을 넣고 24시간 환류교반하였다. 다음날 반응이 끝나면 상온으로 냉각시켜 여과하고 톨루엔을 감압 농축하여 용매를 제거하고 상기 농축액을 에틸아세테이트와 헥산을 전개용매로 하여 컬럼크로마토그래피를 한 결과 [중간체 3-a] 57g (수율 91.2%) 을 얻었다.In a round bottom flask, methyl aminobenzoate (50.0g, 330mmol), iodobenzene (56.3g, 276mmol), palladium acetate (1.2g, 5.6mmol), xantfos (6.4g, 11.02mmol), cesium carbonate (126g, 386mmol), toluene (1000 mL) was added and stirred under reflux for 24 hours. After the reaction was completed the next day, the reaction was cooled to room temperature, filtered, and toluene was concentrated under reduced pressure to remove the solvent, and the concentrate was subjected to column chromatography using ethyl acetate and hexane as developing solvents. As a result, 57g (yield 91.2%) of [Intermediate 3-a] Got it.
합성예 3-2) [중간체 3-b]의 합성Synthesis Example 3-2) Synthesis of [Intermediate 3-b]
[반응식 3-2] [Reaction Scheme 3-2]
[중간체 3-b] [Intermediate 3-b]
둥근 바닥 플라스크에 상기 [반응식 3-1] 로부터 얻은 [중간체 3-a] (57g, 250mmol), 아이소 프로필 에테르 800mL를 넣고 10℃로 냉각한 다음 메틸 마그네슘브로마이드(1.0M in 디에틸에테르 875mL, 875mmol) 을 1시간 동안 적하한 후 2시간 동안 환류교반 하였다. 상온으로 냉각한 후 10% 암모늄 클로라이드 수용액 400mL를 넣고 2시간 동안 교반 한 후 층분리 하여 유기층을 얻고 감압 농축하여 [중간체 3-b] 30g (수율 53%)을 얻었다.[Intermediate 3-a] (57g, 250mmol) obtained from [Scheme 3-1] and 800 mL of isopropyl ether were added to a round bottom flask, cooled to 10°C, and then methyl magnesium bromide (1.0M in diethyl ether 875 mL, 875 mmol) ) Was added dropwise for 1 hour, followed by reflux stirring for 2 hours. After cooling to room temperature, 400 mL of a 10% ammonium chloride aqueous solution was added and stirred for 2 hours. The layers were separated to obtain an organic layer and concentrated under reduced pressure to give 30 g (yield 53%) of [Intermediate 3-b].
합성예 3-3) [중간체 3-c]의 합성Synthesis Example 3-3) Synthesis of [Intermediate 3-c]
[반응식 3-3] [Reaction Scheme 3-3]
[중간체 3-c] [Intermediate 3-c]
둥근 바닥 플라스크에 [반응식 3-2]로부터 얻은 [중간체 3-b] (30g, 130mol)을 인산 60mL에 녹인 후 6시간 동안 반응한다. 반응종료 후 반응액을 과량의 물에 [중간체 3-c] 30g (수율 53%)을 얻었다.[Intermediate 3-b] (30g, 130mol) obtained from [Scheme 3-2] was dissolved in 60 mL of phosphoric acid in a round bottom flask and reacted for 6 hours. After completion of the reaction, the reaction solution was obtained in an excess of water to obtain 30 g of [Intermediate 3-c] (yield 53%).
합성예 3-4) [중간체 3-d]의 합성Synthesis Example 3-4) Synthesis of [Intermediate 3-d]
[반응식 3-4] [Scheme 3-4]
[중간체 3-d] [Intermediate 3-d]
둥근 바닥 플라스크에 [반응식 3-3]로부터 얻은 [중간체 3-c] (20g, 96mmol), 실리카겔 100g을 디클로로메탄 200mL 에 녹인 후 0℃ 로 냉각한 후 N-브로모쑥신이미드 (17.1g, 96mmol)을 디클로로메탄 200mL 에 녹인 것을 적가한 후 실온에서 5시간 교반하였다. 반응종료 후 물 600mL로 3번 씻어주고 용매 제거 하여 [중간체 3-d] 9.7g (수율 35.1%)를 얻었다.[Intermediate 3-c] (20g, 96mmol) obtained from [Scheme 3-3] and 100g of silica gel were dissolved in 200mL of dichloromethane in a round-bottom flask, cooled to 0℃, and then N-bromosaxinimide (17.1g, 96mmol) ) Dissolved in 200 mL of dichloromethane was added dropwise, followed by stirring at room temperature for 5 hours. After completion of the reaction, the mixture was washed 3 times with 600 mL of water, and the solvent was removed to obtain 9.7 g (yield 35.1%) of [Intermediate 3-d].
합성예 3-5) [화합물 3]의 합성Synthesis Example 3-5) Synthesis of [Compound 3]
[반응식 3-5][Scheme 3-5]
[화합물 3]
[Compound 3]
상기 [반응식 1-6]에서 사용한 [중간체 1-c] 대신 상기 합성한 [중간체 3-d]를 사용하여 제조된 것을 합성예 1-7)에서 사용된 [중간체 1-f] 대신 사용하여 상기 합성예 1-6 내지 합성예 1-7과 동일한 방법을 이용하여 [화합물 3] 3.9g (수율 35%)을 합성하였다.Instead of [Intermediate 1-c] used in [Scheme 1-6], the synthesized [Intermediate 3-d] was used instead of [Intermediate 1-f] used in Synthesis Example 1-7). 3.9 g (yield 35%) of [Compound 3] was synthesized using the same method as in Synthesis Examples 1-6 to 1-7.
MS(MALDI-TOF): m/z 605 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 605 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
22.6,30.9,104.8,109.9,111.7,112.2,118.5,118.7,118.9,119.3,120.1,121.3,122.9,125,125.4,125.5,125.8,126.3,127.5,128.3,128.7,129,129.2,129.3,130.5,130.9,131.4,131.7,131.8,136,137.1,138.7,141.6,145.9,149.2,155.6,160 [43C]22.6,30.9,104.8,109.9,111.7,112.2,118.5,118.7,118.9,119.3,120.1,121.3,122.9,125,125.4,125.5,125.8,126.3,127.5,128.3,128.7,129,129.2,129.3,130.5,130.9,131.4, 131.7,131.8,136,137.1,138.7,141.6,145.9,149.2,155.6,160 [43C]
합성예 4. [화합물 4]의 합성Synthesis Example 4. Synthesis of [Compound 4]
[반응식 4-1] [Reaction Scheme 4-1]
[화합물 4] [Compound 4]
상기 [반응식 1-6]에서 사용한 [중간체 1-c] 대신 3-브로모-10H-페노티아진을 사용하여 제조된 것을 합성예 1-7)에서 사용된 [중간체 1-f] 대신 사용하여 합성예 1-6 내지 1-7과 동일한 방법을 이용하여 [화합물 4] 3.4g (수율 33%)을 얻었다.Using 3-bromo-10H-phenothiazine instead of [intermediate 1-c] used in the above [Scheme 1-6] was used instead of [Intermediate 1-f] used in Synthesis Example 1-7) Using the same method as in Synthesis Examples 1-6 to 1-7, 3.4 g (yield 33%) of [Compound 4] was obtained.
MS(MALDI-TOF): m/z 595 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 595 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
104.8,109.9,112.7,118.2,118.5,118.7,118.9,119.3,120.2,121.3,122.2,122.9,125,125.5,125.8,126.6,127.2,127.3,127.5,128.1,128.3,128.7,129.2,129.3,130.8,131.4,131.8,138.7,141.6,144.3,145.4,145.9,149.2,155.6,160 [40C]104.8,109.9,112.7,118.2,118.5,118.7,118.9,119.3,120.2,121.3,122.2,122.9,125,125.5,125.8,126.6,127.2,127.3,127.5,128.1,128.3,128.7,129.2,129.3,130.8,131.4, 131.8,138.7,141.6,144.3,145.4,145.9,149.2,155.6,160 [40C]
합성예 5. [화합물 5]의 합성Synthesis Example 5. Synthesis of [Compound 5]
합성예 5-1. [중간체 5-a]의 합성Synthesis Example 5-1. Synthesis of [Intermediate 5-a]
[반응식 5-1] [Scheme 5-1]
[중간체 5-a] [Intermediate 5-a]
상기 [반응식 3-4]에서 사용된 [중간체 3-c] 대신 2,3-디메틸인돌을 사용한 것을 제외하고는 동일한 방법을 이용하여 [중간체 5-a]를 13.5 g (수율 72.8%) 얻었다.13.5 g (yield 72.8%) of [Intermediate 5-a] was obtained using the same method, except that 2,3-dimethylindole was used instead of [Intermediate 3-c] used in [Scheme 3-4].
합성예 5-2. [화합물 5]의 합성Synthesis Example 5-2. Synthesis of [Compound 5]
상기 [반응식 1-1]에서 사용한 6-브로모인돌 대신 상기 [반응식 5-1]에서 합성한 [중간체 5-a]를 사용한 것을 제외하고는 합성예 1-1) 내지 합성예 1-7)과 동일한 방법을 이용하여 [화합물 5] 5.1g (수율 28%)을 얻었다.Synthesis Example 1-1) to Synthesis Example 1-7), except that [intermediate 5-a] synthesized in [Scheme 5-1] was used instead of 6-bromoindole used in [Scheme 1-1] 5.1g (yield 28%) of [Compound 5] was obtained using the same method as described above.
MS(MALDI-TOF): m/z 591 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 591 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
9.5,10.7,103,109.5,109.9,110111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127.4,127.5,127.7,128.5,128.6,128.7,129.2,129.3,131.8,132.3,133,133.1,136.3,141.6,143.7,144.4,146.6,149.3,151,155.8,161 [42C]9.5,10.7,103,109.5,109.9,110111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127.4,127.5,127.7,128.5,128.6,128.7,129.2,129.3,131.8,132.3,133,133.1, 136.3,141.6,143.7,144.4,146.6,149.3,151,155.8,161 [42C]
합성예 6. [화합물 6]의 합성Synthesis Example 6. Synthesis of [Compound 6]
합성예 6-1. [중간체 6-a]의 합성Synthesis Example 6-1. Synthesis of [Intermediate 6-a]
[반응식 6-1][Scheme 6-1]
[중간체 6-a] [Intermediate 6-a]
둥근 바닥 플라스크에 4-브로모페닐히드라진하이드로클로라이드 (110g, 492mmol)와 벤질페닐케톤 (64g, 328mmol)과 에탄올 550mL를 모두 넣고 12시간 동안 환류시켰다. 염기로 중화과정을 거친 다음 물과 에틸아세테이트로 추출하였다. 유기물을 감압 농축 후 헥산으로 재결정하였다. 필터 후 건조하여 [중간체 6-a] 68.3g (수율 39.8%)를 얻었다. In a round-bottom flask, 4-bromophenylhydrazine hydrochloride (110g, 492mmol), benzylphenylketone (64g, 328mmol), and 550mL of ethanol were all added and refluxed for 12 hours. After neutralization with a base, it was extracted with water and ethyl acetate. The organic material was concentrated under reduced pressure and recrystallized from hexane. After the filter was dried, 68.3 g of [Intermediate 6-a] (yield 39.8%) was obtained.
합성예 6-2. [중간체 6-b]의 합성Synthesis Example 6-2. Synthesis of [Intermediate 6-b]
[반응식 6-2] [Scheme 6-2]
[중간체 6-b] [Intermediate 6-b]
둥근 바닥 플라스크에 [반응식 6-1]에서 합성한 [중간체 6-a] (25g, 72mmol)와 요오도벤젠 58.6g, 287mmol), 구리 (13.7g, 215mmol), 탄산칼륨 (49.6g, 359mmol), 18-크라운-6 (3.8g, 14mmol), 1,2-디클로로벤젠 125mL를 넣고 72시간 동안 환류시켰다. 반응종료 후 상온으로 냉각한 후 과량의 메탄올을 넣어주어 고체를 생성한 후 걸러주고 에틸아세테이트와 헥산을 전개용매로 하여 컬럼크로마토그래피를 한 결과 [중간체 6-b] 11.3g (수율 37%)를 얻었다.[Intermediate 6-a] (25g, 72mmol) synthesized in [Scheme 6-1], iodobenzene 58.6g, 287mmol), copper (13.7g, 215mmol), potassium carbonate (49.6g, 359mmol) in a round bottom flask , 18-crown-6 (3.8g, 14mmol) and 125mL of 1,2-dichlorobenzene were added and refluxed for 72 hours. After the reaction was completed, cooled to room temperature, an excess of methanol was added to generate a solid, filtered, and column chromatography was performed using ethyl acetate and hexane as developing solvents. As a result of [Intermediate 6-b] 11.3g (yield 37%) Got it.
합성예 6-3. [화합물 6]의 합성Synthesis Example 6-3. Synthesis of [Compound 6]
상기 [반응식 1-2]에서 사용한 [중간체 1-a] 대신 상기 [반응식 6-2]에서 합성한 [중간체 6-b]를 사용한 것을 제외하고는 합성예 1-2) 내지 합성예 1-7)과 동일한 방법을 이용하여 [화합물 6] 4.2g (수율 26%)을 얻었다.Synthesis Example 1-2) to Synthesis Example 1-7, except that [Intermediate 6-b] synthesized in [Scheme 6-2] was used instead of [Intermediate 1-a] used in [Scheme 1-2] ) Using the same method as [Compound 6] to obtain 4.2g (26% yield).
MS(MALDI-TOF): m/z 715 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 715 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
103,109.5,109.7,111.6,116.8,118.9,119.3,119.4,119.8,121.4,125.5,126.6,127.4,127.5,127.7,128.5,128.7,129.2,129.3,131.8,132.3,133,133.1,134.7,136.1,136.8,141.6,143.7,144.4,146.7,149.3,155.8,161 [52C]103,109.5,109.7,111.6,116.8,118.9,119.3,119.4,119.8,121.4,125.5,126.6,127.4,127.5,127.7,128.5,128.7,129.2,129.3,131.8,132.3,133,133.1,134.7,136.1,136.8,141.6, 143.7,144.4,146.7,149.3,155.8,161 [52C]
합성예 7. [화합물 7]의 합성
Synthesis Example 7. Synthesis of [Compound 7]
합성예 7-1. [중간체 7-a]의 합성Synthesis Example 7-1. Synthesis of [Intermediate 7-a]
[반응식 7-1][Scheme 7-1]
[중간체 7-a] [Intermediate 7-a]
상온에서, 질소 기류하의 둥근 바닥 플라스크에 인돌(16.8 g, 143 mmol), 1-브로모-4-아이오도벤젠 48.7 g (172 mmol), 트리스(디벤질리딘아세톤)디팔라듐(0) 2.6 g (2.87 mmol), 트리-터셔리-부틸포스포늄테트라플루오로보레이트 4.2 g (14.3 mmol), 소듐터셔리부톡사이드 27.6 g(287 mmol)및 자일렌 (300 mL)을 투입하고 24시간 동안 환류교반시켰다. 셀라이트를 사용하여 반응액을 여과한 후, 여액을 감압농축한 다음, 실리카겔컬럼크로마토그래피로 정제하여 [중간체 7-a] (29.1 g, 107 mmol)를 얻었다. (수율 74.9 %) At room temperature, in a round-bottom flask under a stream of nitrogen, indole (16.8 g, 143 mmol), 1-bromo-4-iodobenzene 48.7 g (172 mmol), tris(dibenzylidineacetone) dipalladium (0) 2.6 g (2.87 mmol), tri-tertiary-butylphosphonium tetrafluoroborate 4.2 g (14.3 mmol), sodium tertiary butoxide 27.6 g (287 mmol), and xylene (300 mL) were added and stirred under reflux for 24 hours. Made it. After the reaction solution was filtered using Celite, the filtrate was concentrated under reduced pressure, and then purified by silica gel column chromatography to obtain [Intermediate 7-a] (29.1 g, 107 mmol). (Yield 74.9%)
합성예 7-2. [중간체 7-b]의 합성Synthesis Example 7-2. Synthesis of [Intermediate 7-b]
[반응식 7-2]
[Reaction Scheme 7-2]
[중간체 7-b] [Intermediate 7-b]
상온에서, 질소 기류하의 둥근 바닥 플라스크에 3-브로모카바졸 (20.0 g, 81.3 mmol)과 비스(피나콜라토)다이보론(22.7 g, 89.4 mmol), 포타슘아세테이트(17.5 g, 179 mmol), PdCl2(dppf) [1,1'-비스(디페닐포스피노)페로센]디클로로팔라듐(Ⅱ) (1.8 g, 2.44 mmol) 및 톨루엔(200 mL)을 투입하고 12 시간 동안 환류교반시켰다. 셀라이트를 사용하여 반응액을 여과한 후, 여액을 감압농축한 다음, 실리카겔컬럼크로마토그래피로 정제하여 [중간체 7-b] (16.7 g, 57.0 mmol)를 얻었다. (수율 70.1 %)At room temperature, 3-bromocarbazole (20.0 g, 81.3 mmol), bis (pinacolato) diboron (22.7 g, 89.4 mmol), potassium acetate (17.5 g, 179 mmol), PdCl in a round bottom flask under a nitrogen stream. 2 (dppf) [1,1'-bis(diphenylphosphino)ferrocene]dichloropalladium(II) (1.8 g, 2.44 mmol) and toluene (200 mL) were added, followed by reflux stirring for 12 hours. After filtering the reaction solution using Celite, the filtrate was concentrated under reduced pressure and purified by silica gel column chromatography to obtain [Intermediate 7-b] (16.7 g, 57.0 mmol). (Yield 70.1%)
합성예 7-3. [중간체 7-c]의 합성Synthesis Example 7-3. Synthesis of [Intermediate 7-c]
[반응식 7-3][Scheme 7-3]
[중간체 7-a] [중간체 7-b] [중간체 7-c][Intermediate 7-a] [Intermediate 7-b] [Intermediate 7-c]
상온에서, 둥근 바닥 플라스크에 [반응식 7-1]로부터 얻은 [중간체 7-a] (7.5 g, 27.5 mmol) 와 [반응식 7-2]로부터 얻은 [중간체 7-b] (8.4 g, 30.2 mmol), 포타슘카보네이트(11.4 g, 82.4 mmol), 테트라키스트리페닐포스핀팔라듐(1.3 g, 1.10 mmol), 테트라하이드로퓨란(100 mL), 증류수(20mL)를 투입한 다음, 12시간 동안 환류교반시켰다. 반응액을 상온으로 냉각한 후, 에틸아세테이트와 증류수를 투입하여 층분리 시켰다. 유기층을 감압 농축한 후, 실리카겔컬럼크로마토그래피로 정제하여 [중간체 7-c] (7.8 g, 21.8 mmol)를 얻었다. (수율 79.2 %)At room temperature, [Intermediate 7-a] (7.5 g, 27.5 mmol) obtained from [Scheme 7-1] and [Intermediate 7-b] (8.4 g, 30.2 mmol) obtained from [Scheme 7-2] were placed in a round bottom flask at room temperature. , Potassium carbonate (11.4 g, 82.4 mmol), tetrakistriphenylphosphine palladium (1.3 g, 1.10 mmol), tetrahydrofuran (100 mL), and distilled water (20 mL) were added, followed by reflux stirring for 12 hours. After cooling the reaction solution to room temperature, ethyl acetate and distilled water were added to separate the layers. The organic layer was concentrated under reduced pressure and purified by silica gel column chromatography to obtain [Intermediate 7-c] (7.8 g, 21.8 mmol). (Yield 79.2%)
합성예 7-4. [화합물 7]의 합성Synthesis Example 7-4. Synthesis of [Compound 7]
[반응식 7-4][Scheme 7-4]
[화합물 7] [Compound 7]
상기 [반응식 1-6]에서 사용된 [중간체 1-c] 대신 [반응식 7-3]에서 합성한 [중간체 7-c]를 사용한 것을 제외하고는 상기 합성예 1-6과 동일한 방법을 이용하여 [화합물 7] 3.5g을 얻었다. (수율 34%)Using the same method as in Synthesis Example 1-6, except that [Intermediate 7-c] synthesized in [Scheme 7-3] was used instead of [Intermediate 1-c] used in [Scheme 1-6] [Compound 7] 3.5 g was obtained. (Yield 34%)
MS(MALDI-TOF): m/z 563 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 563 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
103,104.8,109.5,111.6,114.1,116.8,119.4,119.8,120.7,121.4,125.5,126.6,127.4,127.5,127.7,128.3,128.5,128.7,129.2,129.4,131.8,132.3,133,133.1,134.7,137.6,143.7,144.4,149.3,155.8,161 [40C]103,104.8,109.5,111.6,114.1,116.8,119.4,119.8,120.7,121.4,125.5,126.6,127.4,127.5,127.7,128.3,128.5,128.7,129.2,129.4,131.8,132.3,133,133.1,134.7,137.6,143.7, 144.4,149.3,155.8,161 [40C]
합성예 8. [화합물8]의 합성Synthesis Example 8. Synthesis of [Compound 8]
합성예 8-1) [중간체 8-a]의 합성Synthesis Example 8-1) Synthesis of [Intermediate 8-a]
[반응식 8-1] [Scheme 8-1]
[중간체 8-1-a] [중간체 8-a] [Intermediate 8-1-a] [Intermediate 8-a]
둥근 바닥 플라스크에 브로모벤젠-d5(500g, 3085mmol), 요오드화구리(117.5g, 615mmol), 트랜스-4-하이드록시-L-프롤린(162g, 1235mmol), 탄산칼륨(1279.5g, 9255mmol) 및 디메틸설폭사이드 2500mL를 넣고 교반하였다. 가스트랩을 장치한 후 암모니아수(28%) 2900mL를 천천히 적하하였다. 80℃에서 밤새 교반하였다. 반응 종료 후 에틸아세테이트와 증류수로 수회 추출하였다. 유기층을 감압농축 후 에틸아세테이트와 헵탄으로 컬럼크로마토그래피를 하여 액상의 [중간체 8-1-a]을 185g (수율 61.1%)을 얻었고, 둥근 바닥 플라스크에 상기 합성한 [중간체 8-1-a](185g, 1887mmol), 트리클로로아세토니트릴(326.6g, 2257mmol) 및 디클로로메탄 1850mL를 넣고, 염화주석(IV) (491.2g, 1887mmol)을 넣었다. 플라스크를 아이스-배스에 장치한 후 붕소삼염화물 1M in 디클로로메탄(243.3g, 2072mmol)을 천천히 적하하고, 24시간 환류교반하였다. 반응종료 후 플라스크를 아이스-배스에 장치한 후 탄산칼륨(3126.5g, 22616mmol)을 비커에서 메탄올에 녹인 것을 천천히 적하하였다. 모두 적하 후 가열하여 디클로로메탄을 제거하고 약 3시간 환류교반하였다. 상온으로 식혀준 후 녹지 않은 고체를 여과하고 여액을 감압농축하고, 에틸아세테이트에 녹인 후 2-노르말염산수용액과 물로 씻어주었다. 유기층을 황산마그네슘으로 처리하고 감압농축 후 에틸아세테이트와 헥산으로 컬럼크로마토그래피하여 [중간체 8-a]을 41.6g 얻었다. (수율 18.1%)In a round bottom flask, bromobenzene-d5 (500 g, 3085 mmol), copper iodide (117.5 g, 615 mmol), trans-4-hydroxy-L-proline (162 g, 1235 mmol), potassium carbonate (1279.5 g, 9255 mmol) and dimethyl 2500 mL of sulfoxide was added and stirred. After installing the gas trap, 2900 mL of aqueous ammonia (28%) was slowly added dropwise. Stir at 80° C. overnight. After the reaction was completed, the mixture was extracted several times with ethyl acetate and distilled water. The organic layer was concentrated under reduced pressure and then subjected to column chromatography with ethyl acetate and heptane to obtain 185 g (yield 61.1%) of the liquid [Intermediate 8-1-a], and the synthesized [Intermediate 8-1-a] in a round bottom flask (185g, 1887mmol), trichloroacetonitrile (326.6g, 2257mmol) and 1850mL dichloromethane were added, and tin (IV) chloride (491.2g, 1887mmol) was added. After the flask was installed in an ice-bath, boron trichloride 1M in dichloromethane (243.3 g, 2072 mmol) was slowly added dropwise, followed by reflux stirring for 24 hours. After completion of the reaction, the flask was installed in an ice-bath, and potassium carbonate (3126.5 g, 22616 mmol) dissolved in methanol in a beaker was slowly added dropwise. After dropping all, the mixture was heated to remove dichloromethane, followed by reflux stirring for about 3 hours. After cooling to room temperature, the insoluble solid was filtered, the filtrate was concentrated under reduced pressure, dissolved in ethyl acetate, and washed with an aqueous 2-normal hydrochloric acid solution and water. The organic layer was treated with magnesium sulfate, concentrated under reduced pressure, and then subjected to column chromatography with ethyl acetate and hexane to obtain 41.6 g of [Intermediate 8-a]. (Yield 18.1%)
합성예 8-2) [중간체 8-b]의 합성Synthesis Example 8-2) Synthesis of [Intermediate 8-b]
[반응식 8-2] [Scheme 8-2]
[중간체 8-b] [Intermediate 8-b]
상온에서, 질소 기류하의 둥근 바닥 플라스크에 [반응식 8-1]에서 얻은 [중간체 8-a](20.0g, 164mmol), 테트라하이드로퓨란 140mL를 투입하고 교반하였다. 페닐마그네슘브로마이드(3.0M in Et2O)를 109.1mL(327mmol) 적하하였다. 1시간 정도 환류교반 후 온도를 0℃로 하였다. 에틸 클로로포메이트 (15.5g, 143mmol)를 적하한 후 약 1시간 정도 환류교반하였다. 암모늄클로라이드수용액을 약산성이 될 때까지 투입하고, 생성된 고체를 여과하여 물과 헵탄으로 씻어주었다. 노란색 고체인 [중간체 8-b]를 30.2g 얻었다. (수율 81.5%)At room temperature, [Intermediate 8-a] (20.0 g, 164 mmol) obtained in [Scheme 8-1] and 140 mL of tetrahydrofuran were added to a round bottom flask under a nitrogen stream, followed by stirring. Phenyl magnesium bromide (3.0 M in Et 2 O) was added dropwise 109.1 mL (327 mmol). After stirring at reflux for about 1 hour, the temperature was set to 0°C. Ethyl chloroformate (15.5g, 143mmol) was added dropwise and stirred under reflux for about 1 hour. An aqueous ammonium chloride solution was added until it became slightly acidic, and the resulting solid was filtered and washed with water and heptane. 30.2 g of the yellow solid [Intermediate 8-b] was obtained. (Yield 81.5%)
합성예 8-3) [중간체 8-c]의 합성Synthesis Example 8-3) Synthesis of [Intermediate 8-c]
[반응식 8-3] [Scheme 8-3]
[중간체 8-c] [Intermediate 8-c]
상온에서, 질소 기류하의 둥근 바닥 플라스크에 [반응식 8-2]에서 얻은 [중간체 8-b](30.0g, 133mmol), 옥시염화인 약 80mL를 투입하고 교반하였다. 밤새 환류교반 후 다음날 온도를 -20℃로 냉각한 후 물을 약 400mL정도 천천히 적하하였다. 생성된 고체를 여과한 후 물, 메탄올, 헵탄으로 씻어주었다. 톨루엔과 헵탄으로 재결정하여 흰색 고체인 [중간체 8-c]를 15.2g 얻었다. (수율 46.8%)At room temperature, [Intermediate 8-b] (30.0 g, 133 mmol) obtained in [Scheme 8-2] and about 80 mL of phosphorus oxychloride were added to a round bottom flask under a nitrogen stream, followed by stirring. After reflux stirring overnight, the temperature was cooled to -20℃ the next day, and water was slowly added dropwise about 400mL. The resulting solid was filtered and washed with water, methanol, and heptane. Recrystallization from toluene and heptane gave 15.2 g of [Intermediate 8-c] as a white solid. (Yield 46.8%)
합성예 8-4) [중간체 8-d]의 합성Synthesis Example 8-4) Synthesis of [Intermediate 8-d]
[반응식 8-4] [Scheme 8-4]
[중간체 8-d] [Intermediate 8-d]
상온에서, 질소 기류하의 둥근 바닥 플라스크에 60% 소듐 하이드라이드 2.1 g (53 mmol)와 디메틸포름아마이드 50mL를 투입하고 약 30분간 교반하였다. 상기 [반응식 1-3]로부터 얻은 [중간체 1-c] 10.0 g (41 mmol)와 디메틸포름아마이드 100mL를 적하한 후 약 1시간 정도 더 교반하였다. 상기 [반응식 8-3]로부터 얻은 [중간체 8-c] 12.9g (53 mmol)와 디메틸포름아마이드 100mL를 투입하고 밤새 교반하였다. 플라스크에 증류수 600mL를 넣어서 생긴 고체를 여과하였다. 톨루엔으로 재결정하여 [중간체 8-d] 14.6g을 얻었다. (수율 79.1 %)At room temperature, 2.1 g (53 mmol) of 60% sodium hydride and 50 mL of dimethylformamide were added to a round bottom flask under a flow of nitrogen, and the mixture was stirred for about 30 minutes. 10.0 g (41 mmol) of [Intermediate 1-c] obtained from [Scheme 1-3] and 100 mL of dimethylformamide were added dropwise, followed by stirring for about 1 hour. 12.9g (53 mmol) of [Intermediate 8-c] obtained from [Scheme 8-3] and 100 mL of dimethylformamide were added, followed by stirring overnight. A solid formed by adding 600 mL of distilled water to the flask was filtered. Recrystallized from toluene to obtain 14.6 g of [Intermediate 8-d]. (Yield 79.1%)
합성예 8-5) [화합물 8]의 합성Synthesis Example 8-5) Synthesis of [Compound 8]
[반응식 8-5] [Scheme 8-5]
[화합물 8] [Compound 8]
상기 [반응식 8-4]로부터 얻은 [중간체 8-d]로 표시되는 화합물 14.6 g(32 mmol), 상기 [반응식 1-2]로부터 얻은 [중간체 1-b]로 표시되는 화합물 9.1 g(39 mmol), 테트라키스(트리페닐포스핀)팔라듐 0.7 g (0.64 mmol), 탄산칼륨 8.9 g(64 mmol), 1,4-다이옥산 80ml, 톨루엔 80ml, 증류수 30ml에 넣고 밤새 환류교반하였다. 반응이 종료되면 에틸아세테이트와 증류수를 사용하여 추출한다. 유기층을 감압농축하고 디클로로메탄과 아세톤으로 재결정하여 연노란색 고체인 [화합물 8] 4.6 g을 얻었다. (수율 25.3 %)14.6 g (32 mmol) of the compound represented by [Intermediate 8-d] obtained from [Scheme 8-4], 9.1 g (39 mmol) of the compound represented by [Intermediate 1-b] obtained from [Scheme 1-2] ), tetrakis (triphenylphosphine) palladium 0.7 g (0.64 mmol), potassium carbonate 8.9 g (64 mmol), 1,4-
MS(MALDI-TOF): m/z 567 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 567 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127,127.5,128,128.3,128.7,129,129.2,129.3,131.8,133,133.1,134,138.7,141.6,143.7,144.4,145.9,150,155.8,161 [40C]103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127,127.5,128,128.3,128.7,129,129.2,129.3,131.8,133,133.1,134,138.7,141.6,143.7,144.4,145.9, 150,155.8,161 [40C]
합성예 9. 화합물9의 합성Synthesis Example 9. Synthesis of Compound 9
합성예 9-1) [중간체 9-a]의 합성Synthesis Example 9-1) Synthesis of [Intermediate 9-a]
[반응식 9-1][Reaction Scheme 9-1]
[중간체 9-a] [Intermediate 9-a]
질소 기류하의 둥근 바닥 플라스크에 페닐마그네슘브로마이드(3.0M in Et2O) 110mL(331mmol)와 테트라하이드로퓨란 600mL를 넣고 45℃에서 약 30분간 교반하였다. 상기 [반응식 8-1]에서 얻은 [중간체 8-a] 19.6g (165mmol)과 테트라하이드로퓨란 175mL을 적하한 후 약 2시간 교반하였다. 0℃로 냉각 후 4-브로모 벤조일클로라이드 43.6g (199mmol)과 테트라하이드로퓨란 350mL을 적하한 후 45℃로 승온한 후 약 2시간 교반하였다. 0℃로 냉각 후 암모늄클로라이드수용액을 약산성이 될 때까지 투입하고, 상온에서 교반 후 생성된 고체를 여과하여 메탄올로 씻어주어 [중간체 9-a]를 29g 얻었다. (수율 48%)Phenylmagnesium bromide (3.0M in Et 2 O) 110 mL (331 mmol) and
합성예 9-2) [중간체 9-b]의 합성Synthesis Example 9-2) Synthesis of [Intermediate 9-b]
[반응식 9-2] [Scheme 9-2]
[중간체 9-b] [Intermediate 9-b]
둥근 바닥 플라스크에 상기 [반응식 1-3]로부터 얻은 [중간체 1-c] 8.3 g(34 mmol), 상기 [반응식 1-2]로부터 얻은 [중간체 1-b]로 표시되는 화합물 11.8 g(37 mmol), 테트라키스(트리페닐포스핀)팔라듐 1.6 g (1 mmol), 탄산칼륨 14.0 g(101 mmol), 1,4-다이옥산 45ml, 톨루엔 45ml, 증류수 20ml을 넣고 밤새 환류교반하였다. 반응이 종료되면 에틸아세테이트와 증류수를 사용하여 추출하였다. 유기층을 감압농축하고 실리카겔에 흡착하여 디클로로메탄과 아세톤을 이용하여 컬럼크로마트그래피로 분리하여 [중간체 9-b] 6.0 g을 얻었다. (수율 50 %)In a round-bottom flask, 8.3 g (34 mmol) of [Intermediate 1-c] obtained from [Scheme 1-3], 11.8 g (37 mmol) of a compound represented by [Intermediate 1-b] obtained from [Scheme 1-2] ), tetrakis (triphenylphosphine) palladium 1.6 g (1 mmol), potassium carbonate 14.0 g (101 mmol), 1,4-dioxane 45 ml, toluene 45 ml, distilled
합성예 9-3) [화합물 9]의 합성Synthesis Example 9-3) Synthesis of [Compound 9]
[반응식 9-3] [Reaction Scheme 9-3]
[화합물 9] [Compound 9]
둥근 바닥 플라스크에 상기 [반응식 9-2]로부터 얻은 [중간체 9-b] 5.4 g(15 mmol), 상기 [반응식 9-1]로부터 얻은 [중간체 9-a]로 표시되는 화합물 6.6 g(18 mmol), 트리스(디벤질리딘아세톤)디팔라듐(0) 0.3g (1 mmol), 트리-터셔리-부틸포스포늄테트라플루오로보레이트 0.4g (1 mmol), 소듐-터셔리-부톡사이드 0.4g (30mmol), 오르쏘-자일렌 30mL를 넣고 약 5시간 환류교반하였다. 반응액을 감압농축 후 메탄올을 넣어 생긴 결정을 여과하였다. 컬럼크로마토그래피로 분리하여 톨루엔과 메탄올로 재결정하여 [화합물 9] 2.7g을 얻었다. (수율 28%)In a round-bottom flask, 5.4 g (15 mmol) of [Intermediate 9-b] obtained from [Scheme 9-2] and 6.6 g (18 mmol) of the compound represented by [Intermediate 9-a] obtained from [Scheme 9-1] ), tris(dibenzylidineacetone)dipalladium (0) 0.3g (1 mmol), tri-tertiary-butylphosphonium tetrafluoroborate 0.4g (1 mmol), sodium-tertiary-butoxide 0.4g ( 30mmol), ortho-xylene 30mL was added and stirred under reflux for about 5 hours. The reaction solution was concentrated under reduced pressure, methanol was added, and the resulting crystals were filtered. Separated by column chromatography and recrystallized from toluene and methanol to obtain 2.7 g of [Compound 9]. (Yield 28%)
MS(MALDI-TOF): m/z 643 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 643 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
104.8,105.4,109.5,109.9,111.6,114.1,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127,127.5,128,128.1,128.3,128.7,129,129.2,129.3,131.5,131.8,134,135.5,136.8,138.7,141.6,143.7,145.4,145.9,150,155.8,161 [46C]
104.8,105.4,109.5,109.9,111.6,114.1,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127,127.5,128,128.1,128.3,128.7,129,129.2,129.3,131.5,131.8,134,135.5,136.8, 138.7,141.6,143.7,145.4,145.9,150,155.8,161 [46C]
합성예 10. 화합물10의 합성Synthesis Example 10. Synthesis of
합성예 10-1) [중간체 10-a]의 합성Synthesis Example 10-1) Synthesis of [Intermediate 10-a]
[반응식 10-1] [Scheme 10-1]
[중간체 10-a] [Intermediate 10-a]
상온에서, 질소 기류하의 둥근 바닥 플라스크 A에 마그네슘 14.3g(589mmol), 아이오딘 3알, 테트라하이드로퓨란 60mL를 투입하고 약 10분간 교반하였다. 물에 담겨진 플라스크에 4-브로모바이페닐 125.9g(540mmol), 테트라하이드로퓨란 240mL를 적하한 후 약 2시간 정도 환류교반하였다. 2시간 후 온도를 상온으로 하였다. 상온에서, 질소 기류하의 또 다른 둥근 바닥 플라스크 B에 상기 [반응식 8-1]에서 합성한 [중간체 8-a] 30.0g(246mmol), 테트라하이드로퓨란 150mL를 투입하고 교반하였다. 상온에서, 물에 담겨진 플라스크 B에 상기 플라스크 A에서 만들어진 반응액을 천천히 적하하였다. 그 후 1시간 정도 환류교반하였다. 온도를 0℃로 하고, 메틸 클로로포메이트 34.8g(368mmol)을 적하한 후 약 1시간 정도 환류교반하였다. 온도를 0℃로 하고, 암모늄클로라이드수용액을 약산성이 될 때까지 투입하고, 생성된 고체를 여과하여 물과 헵탄으로 씻어주었다. [중간체 10-a]를 51.2g 얻었다. (수율 69%)At room temperature, 14.3 g (589 mmol) of magnesium, 3 iodine, and 60 mL of tetrahydrofuran were added to a round-bottom flask A under a nitrogen stream, followed by stirring for about 10 minutes. In a flask immersed in water, 125.9 g (540 mmol) of 4-bromobiphenyl and 240 mL of tetrahydrofuran were added dropwise, followed by reflux stirring for about 2 hours. After 2 hours, the temperature was set to room temperature. At room temperature, 30.0 g (246 mmol) of [Intermediate 8-a] synthesized in [Scheme 8-1] and 150 mL of tetrahydrofuran were added to another round-bottom flask B under a flow of nitrogen and stirred. At room temperature, the reaction solution prepared in flask A was slowly added dropwise to flask B immersed in water. Then, it was stirred under reflux for about 1 hour. The temperature was set to 0° C., and 34.8 g (368 mmol) of methyl chloroformate was added dropwise, followed by reflux stirring for about 1 hour. The temperature was set to 0° C., an aqueous ammonium chloride solution was added until it became slightly acidic, and the resulting solid was filtered and washed with water and heptane. 51.2 g of [Intermediate 10-a] was obtained. (Yield 69%)
합성예 10-2) [중간체 10-b]의 합성Synthesis Example 10-2) Synthesis of [Intermediate 10-b]
[반응식 10-2] [Scheme 10-2]
[중간체 10-b] [Intermediate 10-b]
상기 [반응식 8-3]에서 사용한 [중간체 8-b] 대신 상기 [반응식 10-1]에서 합성한 [중간체 10-a]를 사용한 것을 제외하고는 합성예 8-3과 동일한 방법을 이용하여 [중간체 10-b]를 16.9g 얻었다. (수율 31.1%)Except for the use of [Intermediate 10-a] synthesized in [Scheme 10-1] instead of [Intermediate 8-b] used in [Scheme 8-3], and using the same method as Synthesis Example 8-3 [ Intermediate 10-b] was obtained 16.9g. (Yield 31.1%)
합성예 10-3) [중간체 10-c]의 합성Synthesis Example 10-3) Synthesis of [Intermediate 10-c]
[반응식 10-3] [Reaction Scheme 10-3]
[중간체 10-c] [Intermediate 10-c]
상기 [반응식 8-4]에서 사용한 [중간체 8-c] 대신 상기 [반응식 10-2]에서 합성한 [중간체 10-b]를 사용한 것을 제외하고는 합성예 8-4와 동일한 방법을 이용하여 [중간체 10-c]를 17.2g 얻었다. (수율 79.8%)Except for the use of [Intermediate 10-b] synthesized in [Scheme 10-2] instead of [Intermediate 8-c] used in [Scheme 8-4], and using the same method as in Synthesis Example 8-4 [ Intermediate 10-c] was obtained 17.2g. (Yield 79.8%)
합성예 10-4) [화합물 10]의 합성Synthesis Example 10-4) Synthesis of [Compound 10]
[반응식 10-4][Scheme 10-4]
[화합물 10] [Compound 10]
상기 합성예 8-5)에서 사용한 [중간체 8-d] 대신 상기 [반응식 10-3]에서 합성된 [중간체 10-c]를 사용한 것을 제외하고는 합성예 8-5와 동일한 방법을 이용하여 [화합물 10]을 5.2g 얻었다.(수율 25%)Using the same method as in Synthesis Example 8-5, except that [Intermediate 10-c] synthesized in [Scheme 10-3] was used instead of [Intermediate 8-d] used in Synthesis Example 8-5). Compound 10] was obtained 5.2g. (Yield 25%)
MS(MALDI-TOF): m/z 643 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 643 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127,127.2,127.6,127.9,128,128.3,129,129.2,129.3,130.7,133,133.1,134,138.7,140.8,141.6,143.7,144.4,145.9,150,155.8,161 [46C]103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127,127.2,127.6,127.9,128,128.3,129,129.2,129.3,130.7,133,133.1,134,138.7,140.8,141.6,143.7, 144.4,145.9,150,155.8,161 [46C]
합성예 11. 화합물11의 합성Synthesis Example 11. Synthesis of Compound 11
상기 합성예 8-2)의 [반응식 8-2]에서 사용한 페닐마그네슘브로마이드(3.0M in Et2O) 대신 (2-플루오로[1,1'-바이페닐]-4-)마그네슘브로마이드(0.5M in THF)를 사용한 것을 제외하고는 합성예 8-2) 내지 합성예 8-5)와 동일한 방법을 이용하여 [화합물11] 3.9g을 합성하였다. (수율 32%)Instead of phenyl magnesium bromide (3.0M in Et 2 O) used in [Scheme 8-2] of Synthesis Example 8-2), (2-fluoro[1,1'-biphenyl]-4-) magnesium bromide (0.5 Except for using M in THF), 3.9 g of [Compound 11] was synthesized using the same method as in Synthesis Example 8-2) to Synthesis Example 8-5). (Yield 32%)
MS(MALDI-TOF): m/z 661 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 661 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
103,104.8,109.5,109.9,111.6,116.4,116.8,118.9,119.3,119.4,119.8,121.3,121.4,123.6,125.5,126.6,127,127.6,127.9,128,128.3,129,129.2,129.3,130,133,133.1,133.5,134,136.5,138.7,141.6,143.7,144.4,145.9,150,155.8,159.2,161 [46C]103,104.8,109.5,109.9,111.6,116.4,116.8,118.9,119.3,119.4,119.8,121.3,121.4,123.6,125.5,126.6,127,127.6,127.9,128,128.3,129,129.2,129.3,130,133,133.1,133.5,134,136.5,138.7,141.6, 143.7,144.4,145.9,150,155.8,159.2,161 [46C]
합성예 12. 화합물12의 합성Synthesis Example 12. Synthesis of Compound 12
상기 합성예 8-2)의 [반응식 8-2]에서 사용한 페닐마그네슘브로마이드(3.0M in Et2O) 대신 (4-벤질페닐)마그네슘브로마이드(0.5M in 2-메틸테트라하이드로퓨란)를 사용한 것을 제외하고는 합성예 8-2) 내지 합성예 8-5)와 동일한 방법을 이용하여 [화합물12] 3.6g을 합성하였다. (수율 30%)Using (4-benzylphenyl) magnesium bromide (0.5M in 2-methyltetrahydrofuran) instead of phenyl magnesium bromide (3.0M in Et 2 O) used in [Scheme 8-2] of Synthesis Example 8-2) Except for Synthesis Example 8-2) to Synthesis Example 8-5) 3.6g of [Compound 12] was synthesized using the same method. (Yield 30%)
MS(MALDI-TOF): m/z 657 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 657 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
41.3,103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.2,126.3,126.6,127,128,128.2,128.3,128.7,129,129.2,129.3,133,133.1,134,138.7,141.5,141.6,143.7,144.4,145.9,150,155.8,161 [47C]41.3,103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.2,126.3,126.6,127,128,128.2,128.3,128.7,129,129.2,129.3,133,133.1,134,138.7,141.5,141.6, 143.7,144.4,145.9,150,155.8,161 [47C]
합성예 13. 화합물13의 합성Synthesis Example 13. Synthesis of Compound 13
합성예 13-1) [중간체 13-a]의 합성Synthesis Example 13-1) Synthesis of [Intermediate 13-a]
[반응식 13-1] [Scheme 13-1]
[중간체 13-a] [Intermediate 13-a]
상기 합성예 10-1)의 [반응식 10-1]에서 사용한 4-브로모바이페닐 대신 펜타듀테레오브로모벤젠을 사용하고, 메틸 클로로포메이트 대신 디메틸카보네이트를 사용한 것을 제외하고는 합성예 10-1과 동일한 방법을 이용하여 [중간체 13-a] 50g 을 얻었다. (수율 73%)Synthesis Example 10-1, except that pentadeutereobromobenzene was used instead of 4-bromobiphenyl used in [Scheme 10-1] of Synthesis Example 10-1), and dimethyl carbonate was used instead of methyl chloroformate. 50 g of [Intermediate 13-a] was obtained using the same method as described above. (Yield 73%)
합성예 13-2) [화합물 13]의 합성Synthesis Example 13-2) Synthesis of [Compound 13]
상기 [반응식 10-2]에서 사용한 [중간체 10-a] 대신 상기 합성예 13-1에서 합성된 [중간체 13-a]를 사용하여 제조된 것을 합성예 10-3)에 사용한 것을 제외하고는 합성예 10-2) 내지 합성예 10-4)와 동일한 방법을 이용하여 [화합물 13] 4.1g (수율 38%)을 얻었다.Synthesis except for those prepared using [Intermediate 13-a] synthesized in Synthesis Example 13-1 instead of [Intermediate 10-a] used in [Scheme 10-2], and used in Synthesis Example 10-3) Using the same method as in Example 10-2) to Synthesis Example 10-4), 4.1 g (yield 38%) of [Compound 13] was obtained.
MS(MALDI-TOF): m/z 572 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 572 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,125.6,126.6,127,127.5,128,128.3,129,129.3,133,133.1,134,134.4,138.7,141.6,143.7,144.4,145.9,150,155.8,161 [40C]103,104.8,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,125.6,126.6,127,127.5,128,128.3,129,129.3,133,133.1,134,134.4,138.7,141.6,143.7,144.4,145.9,150,155.8, 161 [40C]
합성예 14. [화합물 14]의 합성Synthesis Example 14. Synthesis of [Compound 14]
합성예 14-1. [중간체 14-a]의 합성Synthesis Example 14-1. Synthesis of [Intermediate 14-a]
[반응식 14-1] [Scheme 14-1]
[중간체 14-a] [Intermediate 14-a]
상기 [반응식 3-1]에서 사용한 메틸 아미노벤조에이트 대신 메틸 2-아미노-3,5-디브로모벤조에이트를 사용한 것을 제외하고는 합성예 3-1과 동일한 방법을 이용하여 [중간체 14-a] 78.8g (수율 62%)을 얻었다.[Intermediate 14-a] using the same method as in Synthesis Example 3-1, except that methyl 2-amino-3,5-dibromobenzoate was used instead of methyl aminobenzoate used in [Scheme 3-1] ] 78.8g (62% yield) was obtained.
합성예 14-2. [중간체 14-b]의 합성Synthesis Example 14-2. Synthesis of [Intermediate 14-b]
[반응식 14-2][Scheme 14-2]
[중간체 14-b] [Intermediate 14-b]
상기 [반응식 9-2]에서 사용한 [중간체 1-c] 대신 상기 [반응식 14-1]로부터 얻은 [중간체 14-a]를 사용하고, 상기 [반응식 1-2]로부터 얻은 [중간체 1-b]는 2배 양(2.2당량) 사용한 것을 제외하고는 합성예 9-2)와 동일한 방법을 이용하여 [중간체 14-b] 13.5 g을 얻었다. (수율 48 %)[Intermediate 1-b] obtained from [Scheme 14-1] was used instead of [Intermediate 1-c] used in [Scheme 9-2], and [Intermediate 1-b] obtained from [Scheme 1-2] [Intermediate 14-b] 13.5 g was obtained using the same method as in Synthesis Example 9-2), except that 2 times the amount (2.2 equivalents) was used. (Yield 48%)
합성예 14-3. [화합물 14]의 합성Synthesis Example 14-3. Synthesis of [Compound 14]
[반응식 14-3][Scheme 14-3]
[중간체 14-c] [중간체 14-d] [화합물14] [Intermediate 14-c] [Intermediate 14-d] [Compound 14]
상기 [반응식 3-2]에서 사용한 [중간체 3-a] 대신 상기 [반응식 14-2]에서 합성한 [중간체 14-b]을 사용하여 [중간체 14-c]를 합성하고, 상기 [반응식 3-3]에서 사용한 [중간체 3-b] 대신 [중간체 14-c]을 사용하여 [중간체 14-d]를 합성하고, 상기 [반응식 8-4]에서 사용된 [중간체 1-c] 대신 [중간체 14-d]를 사용한 것을 제외하고는 합성예 3-2) 내지 합성예 3-3) 및 합성예 8-4)와 동일한 방법을 이용하여 [화합물 14] 5.6g (수율 42%)을 얻었다.[Intermediate 14-c] was synthesized using [Intermediate 14-b] synthesized in [Scheme 14-2] instead of [Intermediate 3-a] used in [Scheme 3-2], and the [Scheme 3- [Intermediate 14-d] was synthesized using [Intermediate 14-c] instead of [Intermediate 3-b] used in [3], and [Intermediate 14] instead of [Intermediate 1-c] used in [Scheme 8-4] Except for using -d], 5.6 g (yield 42%) of [Compound 14] was obtained using the same method as in Synthesis Example 3-2) to Synthesis Example 3-3) and Synthesis Example 8-4).
MS(MALDI-TOF): m/z 800 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 800 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
22.9,30.9,104.8,109.9,111.7,112.7,118.5,118.7,118.9,119.3,121.3,122.7,123,124.6,125,125.4,125.5,126,127,127.5,128.3,128.7,129,129.2,129.3,129.8,130.5,131.8,133,137.1,138.7,140.9,141.6,145.9,149.9,155.6,160 [57C]22.9,30.9,104.8,109.9,111.7,112.7,118.5,118.7,118.9,119.3,121.3,122.7,123,124.6,125,125.4,125.5,126,127,127.5,128.3,128.7,129,129.2,129.3,129.8,130.5,131.8,133,137.1,138.7, 140.9,141.6,145.9,149.9,155.6,160 [57C]
합성예 15. [화합물 15]의 합성Synthesis Example 15. Synthesis of [Compound 15]
[반응식 15-1][Reaction Scheme 15-1]
[중간체 15-a] [화합물 15] [Intermediate 15-a] [Compound 15]
상기 [반응식 8-4]에서 사용한 [중간체 1-c] 대신 2-브로모-10,11-디하이드로-5H-디벤조[b,f]아제핀을 사용하여 [중간체 15-a]을 얻었고, 합성예 8-5)에서 사용된 [중간체 8-d] 대신 [중간체 15-a]을 사용한 것을 제외하고는 합성예 8-4) 내지 합성예 8-5)와 동일한 방법을 이용하여 [화합물 15] 3.6g (수율 30%)을 얻었다.[Intermediate 15-a] was obtained by using 2-bromo-10,11-dihydro-5H-dibenzo[b,f]azepine instead of [Intermediate 1-c] used in [Scheme 8-4]. [Compound] using the same method as in Synthesis Example 8-4) to Synthesis Example 8-5), except that [Intermediate 15-a] was used instead of [Intermediate 8-d] used in Synthesis Example 8-5). 15] 3.6g (30% yield) was obtained.
MS(MALDI-TOF): m/z 595 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 595 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
32.3,32.6,104.8,109.9,118.5,118.9,119.3,119.5,121.3,121.7,123,125,125.5,126,127.5,128.3,128.4,128.7,128.9,129.2,129.3,130.2,130.4,131.1,131.8,133,135.5,136.6,138.7,141.6,145.9,149.9,155.6,160 [42C]32.3,32.6,104.8,109.9,118.5,118.9,119.3,119.5,121.3,121.7,123,125,125.5,126,127.5,128.3,128.4,128.7,128.9,129.2,129.3,130.2,130.4,131.1,131.8,133,135.5,136.6,138.7, 141.6,145.9,149.9,155.6,160 [42C]
합성예 16. [화합물 16]의 합성Synthesis Example 16. Synthesis of [Compound 16]
[반응식 16-1][Scheme 16-1]
[중간체 16-a] [화합물 16] [Intermediate 16-a] [Compound 16]
상기 [반응식 3-1]에서 사용한 메틸 아미노벤조에이트 대신 메틸 3-아미노나프탈렌-2-카복실레이트를 사용한 것을 제외하고는 합성예 3-1)과 동일한 방법으로 제조하여 [중간체 16-a]을 얻었고, 이를 이용하여 합성예 3-2) 내지 합성예 3-5)와 동일한 방법을 이용하여 [화합물 16] 2.4g (수율 24%)을 얻었다.Except that methyl 3-aminonaphthalene-2-carboxylate was used instead of the methyl aminobenzoate used in [Scheme 3-1], it was prepared in the same manner as in Synthesis Example 3-1) to obtain [Intermediate 16-a]. , Using this, 2.4 g (yield 24%) of [Compound 16] was obtained using the same method as in Synthesis Example 3-2) to Synthesis Example 3-5).
MS(MALDI-TOF): m/z 657 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 657 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
23,30.9,104.8,107.6,109.9,113.1,115.8,118.9,119.3,121,121.2,121.3,122.7,123.7,124.1,124.2,125,125.5,125.8,125.9,126,126.3,126.7,126.8,127.6,127.9,128.3,129.2,129.3,130.9,131.7,134.3,134.4,136.5,136.6,138.7,141.6,142,143.1,144.6,145.9 [49C]23,30.9,104.8,107.6,109.9,113.1,115.8,118.9,119.3,121,121.2,121.3,122.7,123.7,124.1,124.2,125,125.5,125.8,125.9,126,126.3,126.7,126.8,127.6,127.9,128.3,129.2, 129.3,130.9,131.7,134.3,134.4,136.5,136.6,138.7,141.6,142,143.1,144.6,145.9 [49C]
합성예 17. [화합물 17]의 합성Synthesis Example 17. Synthesis of [Compound 17]
[반응식 17-1][Scheme 17-1]
[중간체 17-a] [화합물 17] [Intermediate 17-a] [Compound 17]
상기 [반응식 3-1]에서 사용한 메틸 아미노벤조에이트 대신 메틸 1-아미노나프탈렌-2-카복실레이트를 사용한 것을 제외하고는 합성예 3-1)과 동일한 방법으로 제조하여 [중간체 17-a]을 얻었고, 이를 이용하여 합성예 3-2) 내지 합성예 3-5)와 동일한 방법을 이용하여 [화합물 17] 2.7g (수율 26%)을 얻었다.Except for using methyl 1-aminonaphthalene-2-carboxylate instead of methyl aminobenzoate used in [Scheme 3-1], it was prepared in the same manner as in Synthesis Example 3-1) to obtain [Intermediate 17-a]. , Using this, 2.7 g (yield 26%) of [Compound 17] was obtained using the same method as in Synthesis Example 3-2) to Synthesis Example 3-5).
MS(MALDI-TOF): m/z 657 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 657 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
23,30.9,104.8,109.9,113.1,115.8,118.2,118.7,118.9,119.3,120.4,121,121.3,122.7,123.7,124.6,124.8,124.9,125,125.5,125.8,126,126.3,127.6,127.9,128.1,128.3,129.2,129.3,130.9,132.3,134.3,134.4,136.5,136.6,138.7,140.7,141.6,142,143.1,145.9 [49C]23,30.9,104.8,109.9,113.1,115.8,118.2,118.7,118.9,119.3,120.4,121,121.3,122.7,123.7,124.6,124.8,124.9,125,125.5,125.8,126,126.3,127.6,127.9,128.1,128.3,129.2, 129.3,130.9,132.3,134.3,134.4,136.5,136.6,138.7,140.7,141.6,142,143.1,145.9 [49C]
합성예 18. [화합물18]의 합성Synthesis Example 18. Synthesis of [Compound 18]
합성예 18-1) [중간체 18-a]의 합성Synthesis Example 18-1) Synthesis of [Intermediate 18-a]
[반응식 18-1] [Scheme 18-1]
[중간체 18-a] [Intermediate 18-a]
5-브로모인돌 50.0 g (255.0 mmol), 아이오도벤젠 10.4 g (510.0 mmol), 구리분말 32.4 g (510.0 mmol), 18-크라운-6 13.5 g (51.0 mmol), 탄산칼륨 105.7 g (765.0 mmol)을 순서대로 넣고, 1,2-디클로로벤젠 500 ml를 가한 후, 180 ℃에서 1일 동안 환류, 교반시켰다. 5-bromoindole 50.0 g (255.0 mmol), iodobenzene 10.4 g (510.0 mmol), copper powder 32.4 g (510.0 mmol), 18-crown-6 13.5 g (51.0 mmol), potassium carbonate 105.7 g (765.0 mmol) ) Was added in order, 500 ml of 1,2-dichlorobenzene was added, and then refluxed and stirred at 180° C. for 1 day.
반응이 종료되면, 고온필터 후 용액을 감압농축하고 유기 층 용액을 헥산으로 컬럼 크로마토그래피를 하여 [중간체 18-a]를 56.2 g 얻었다. (수율 81 %)When the reaction was completed, the solution was concentrated under reduced pressure after high-temperature filtering, and the organic layer solution was subjected to column chromatography with hexane to obtain 56.2 g of [Intermediate 18-a]. (Yield 81%)
합성예 18-2) [중간체 18-b]의 합성 Synthesis Example 18-2) Synthesis of [Intermediate 18-b]
[반응식 18-2] [Scheme 18-2]
[중간체 18-a] [중간체 18-b][Intermediate 18-a] [Intermediate 18-b]
상기 [반응식 18-1]로부터 얻은 [중간체 18-a] 화합물 56.2 g (206.5 mmol)을 질소 기류하에서 테트라하이드로퓨란 600 ml에 녹인 후 -78 ℃에서 교반하면서 1.6M 노르말-부틸리튬155 ml (247.8 mmol)을 천천히 적하하고, 적하 완료되면 -78 ℃를 유지하면서 1시간 동안 교반시켰다. 그 후 트리메틸보레이트 25.8 g (247.8 mmol)을 천천히 적하 한 후 상온으로 올려서 2시간 교반시켰다.After dissolving 56.2 g (206.5 mmol) of the [Intermediate 18-a] compound obtained from [Scheme 18-1] in 600 ml of tetrahydrofuran under a stream of nitrogen, 1.6M normal-butyllithium 155 ml (247.8 mmol) was slowly added dropwise, and when the dropping was completed, the mixture was stirred for 1 hour while maintaining -78°C. Thereafter, 25.8 g (247.8 mmol) of trimethylborate was slowly added dropwise, and the mixture was raised to room temperature and stirred for 2 hours.
반응이 종료되면 2M 염산수용액 300 ml를 상온에서 적하 한 후 30분간 교반시킨다. 그 후 에틸아세테이트와 물로 추출하고 유기층을 감압농축하고 디클로로메탄과 헥산으로 재결정하여 [중간체 18-b]를 17.9 g 얻었다. (수율 56 %)Upon completion of the reaction, 300 ml of a 2M aqueous hydrochloric acid solution was added dropwise at room temperature and stirred for 30 minutes. Thereafter, extraction was performed with ethyl acetate and water, the organic layer was concentrated under reduced pressure, and recrystallized with dichloromethane and hexane to obtain 17.9 g of [Intermediate 18-b]. (Yield 56%)
합성예 18-3) [중간체 18-d]의 합성Synthesis Example 18-3) Synthesis of [Intermediate 18-d]
[반응식 18-3-1] [Scheme 18-3-1]
[중간체 18-c-1] [Intermediate 18-c-1]
[반응식 18-3-2][Scheme 18-3-2]
[중간체 18-c-2] [Intermediate 18-c-2]
상기 합성예 1-4에서 사용한 페닐마그네슘브로마이드(3.0M in Et2O) 대신 4-피리디닐마그네슘브로마이드(0.25M in THF)를 사용한 것을 제외하고는 상기 합성예 1-4 내지 1-5와 동일한 방법을 이용하여 [중간체 18-c-2]를 얻었다. The same as in Synthesis Examples 1-4 to 1-5, except that 4-pyridinyl magnesium bromide (0.25M in THF) was used instead of phenyl magnesium bromide (3.0M in Et 2 O) used in Synthesis Example 1-4. [Intermediate 18-c-2] was obtained using the method.
합성예 18-4) [중간체 18-d]의 합성Synthesis Example 18-4) Synthesis of [Intermediate 18-d]
[반응식 18-4][Scheme 18-4]
[중간체 18-d] [Intermediate 18-d]
상기 [반응식 1-6]에서 사용된 [중간체 1-c] 대신 2-브로모-9H-카바졸을 사용하고 사용된 [중간체 1-e] 대신 상기 합성한 [중간체 18-c-2]를 사용한 것을 제외하고는 상기 합성예 1-6과 동일한 방법을 이용하여 [중간체 18-d] 15.8g을 얻었다. (수율 79%)Instead of [intermediate 1-c] used in [Scheme 1-6], 2-bromo-9H-carbazole was used, and [intermediate 18-c-2] synthesized above was used instead of [intermediate 1-e] 15.8g of [Intermediate 18-d] was obtained using the same method as in Synthesis Example 1-6, except that it was used. (79% yield)
합성예 18-5) [화합물 18]의 합성Synthesis Example 18-5) Synthesis of [Compound 18]
[반응식 18-5][Scheme 18-5]
[화합물 18] [Compound 18]
상기 [반응식 1-7]에서 사용된 [중간체 1-b] 대신 상기 합성한 [중간체 18-b], [중간체 1-f] 대신 상기 합성한 [중간체 18-d]를 사용한 것을 제외하고는 상기 합성예 1-7과 동일한 방법을 이용하여 [화합물 18] 4.6g을 얻었다. (수율 25%)Except for using the synthesized [intermediate 18-d] instead of the synthesized [intermediate 18-b] and [intermediate 1-f] instead of [intermediate 1-b] used in [Scheme 1-7] 4.6 g of [Compound 18] was obtained using the same method as in Synthesis Example 1-7. (Yield 25%)
MS(MALDI-TOF): m/z 564 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 564 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
104.8,107.6,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127.4,127.7,128.3,128.5,129.3,131.1,132.3,133,133.1,133.6,138.7,140.3,141.6,143.7,144.4,149.3,149.8,155.8,161 [39C]104.8,107.6,109.5,109.9,111.6,116.8,118.9,119.3,119.4,119.8,121.3,121.4,125.5,126.6,127.4,127.7,128.3,128.5,129.3,131.1,132.3,133,133.1,133.6,138.7,140.3, 141.6,143.7,144.4,149.3,149.8,155.8,161 [39C]
합성예 19. [화합물19]의 합성Synthesis Example 19. Synthesis of [Compound 19]
합성예 19-1) [중간체 19-a]의 합성Synthesis Example 19-1) Synthesis of [Intermediate 19-a]
[반응식 19-1] [Reaction Scheme 19-1]
[중간체 19-a] [Intermediate 19-a]
상기 [반응식 18-1]에서 사용된 아이오도벤젠 대신 3-아이오도피리딘을 사용한 것을 제외하고는 합성예 18-1과 동일한 방법으로 [중간체 19-a]를 57 g 얻었다. (수율 84 %)57 g of [Intermediate 19-a] was obtained in the same manner as in Synthesis Example 18-1, except that 3-iodopyridine was used instead of the iodobenzene used in [Scheme 18-1]. (Yield 84%)
합성예 19-2) [화합물 19]의 합성Synthesis Example 19-2) Synthesis of [Compound 19]
상기 [반응식 18-2]에서 사용된 [중간체 18-a] 대신 상기 합성한 [중간체 19-a]를 사용한 것을 제외하고는 합성예 18-2 내지 합성예 18-5와 동일한 방법을 이용하여 [화합물 19] 4.2g을 얻었다.(수율 24%)Except for using the synthesized [intermediate 19-a] instead of the [intermediate 18-a] used in [Scheme 18-2], using the same method as in Synthesis Example 18-2 to Synthesis Example 18-5 [ Compound 19] 4.2 g was obtained (yield 24%).
MS(MALDI-TOF): m/z 565 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 565 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
102.4,107.6,109.5,109.9,111.6,116.8,118.9,119.2,119.3,119.8,121.3,121.4,124.4,124.7,125.5,126.6,127.4,127.7,128.5,128.7,132.3,132.6,133,133.1,135.5,140.3,141.5,141.6,143.7,144.4,146.4,149.3,149.8,155.8,161 [38C]102.4,107.6,109.5,109.9,111.6,116.8,118.9,119.2,119.3,119.8,121.3,121.4,124.4,124.7,125.5,126.6,127.4,127.7,128.5,128.7,132.3,132.6,133,133.1,135.5,140.3, 141.5,141.6,143.7,144.4,146.4,149.3,149.8,155.8,161 [38C]
합성예 20. [화합물20]의 합성Synthesis Example 20. Synthesis of [Compound 20]
합성예 20-1) [중간체 20-a]의 합성Synthesis Example 20-1) Synthesis of [Intermediate 20-a]
[반응식 20-1] [Reaction Scheme 20-1]
[중간체 20-a] [Intermediate 20-a]
상기 [반응식 1-1]에서 사용한 6-브로모인돌 대신 4-브로모인돌을 사용하여 상기 합성예 1-1 내지 합성예 1-2와 동일한 방법으로 제조하여 [중간체 20-a]를 28g 얻었다. (수율 62%)Using 4-bromoindole instead of 6-bromoindole used in [Scheme 1-1], it was prepared in the same manner as in Synthesis Examples 1-1 to 1-2 to obtain 28g of [Intermediate 20-a] . (Yield 62%)
합성예 20-2) [중간체 20-b]의 합성Synthesis Example 20-2) Synthesis of [Intermediate 20-b]
[반응식 20-2] [Scheme 20-2]
[중간체 20-b] [Intermediate 20-b]
상기 [반응식 1-6]에서 사용된 [중간체 1-c] 대신 4-브로모-9H-카바졸을 사용하여 상기 합성예 1-6과 동일한 방법으로 [중간체 20-b]를 16g을 얻었다. (수율 79%)Using 4-bromo-9H-carbazole instead of [Intermediate 1-c] used in [Scheme 1-6], 16 g of [Intermediate 20-b] was obtained in the same manner as in Synthesis Example 1-6. (79% yield)
합성예 20-3) [화합물 20]의 합성Synthesis Example 20-3) Synthesis of [Compound 20]
[반응식 20-3] [Scheme 20-3]
[화합물 20] [Compound 20]
상기 [반응식 1-7]에서 사용된 [중간체 1-b] 대신 상기 합성한 [중간체 20-a]를 사용하고, [중간체 1-f] 대신 상기 합성한 [중간체 20-b]를 사용한 것을 제외하고는 상기 합성예 1-7과 동일한 방법을 이용하여 [화합물 20] 4.5g을 얻었다. (수율 26 %)Except for using the synthesized [intermediate 20-a] instead of [intermediate 1-b] used in [Scheme 1-7], and using the synthesized [intermediate 20-b] instead of [intermediate 1-f] Then, 4.5 g of [Compound 20] was obtained using the same method as in Synthesis Example 1-7. (Yield 26%)
MS(MALDI-TOF): m/z 563 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 563 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
104.8,108.4,109.5,117.6,118.9,119.8,121.3,121.4,125.5,125.6,125.7,126.6,127.4,127.5,127.7,128.5,128.6,128.7,129.2,129.3,129.8,131.8,132.3,133,138.7,144.4,145.9,149.3,155.8,161 [40C]104.8,108.4,109.5,117.6,118.9,119.8,121.3,121.4,125.5,125.6,125.7,126.6,127.4,127.5,127.7,128.5,128.6,128.7,129.2,129.3,129.8,131.8,132.3,133,138.7,144.4, 145.9,149.3,155.8,161 [40C]
합성예 21. [화합물21]의 합성Synthesis Example 21. Synthesis of [Compound 21]
[반응식 21-1][Scheme 21-1]
[화합물 21] [Compound 21]
둥근 바닥 플라스크에 [반응식 20-2]로부터 얻은 [중간체 20-b] 6.8 g(15.0 mmol), 인돌 3.7 g(32.0 mmol),트리스(디벤질리덴아세톤)디팔라듐 0.6 g(1.0 mmol), 1,1`-비스(디페닐포스피노)페로센 0.4 g(1.0 mmol), 소듐 터셔리 부톡사이드 6.2 g(65.0 mmol)과 톨루엔 120 mL를 투입 후 24시간 환류, 교반하였다. 반응이 종료되면 상온으로 온도를 조절한 후 결정을 여과하고. 그 결정을 디클로로메탄과 아세톤으로 재결정하여 [화합물 21] 3.8 g(수율 52%) 을 얻었다.[Intermediate 20-b] obtained from [Scheme 20-2] 6.8 g (15.0 mmol), indole 3.7 g (32.0 mmol), tris (dibenzylideneacetone) dipalladium 0.6 g (1.0 mmol), 1 ,1`-bis(diphenylphosphino)ferrocene 0.4 g (1.0 mmol), sodium tertiary butoxide 6.2 g (65.0 mmol) and toluene 120 mL were added, followed by refluxing and stirring for 24 hours. When the reaction is finished, the temperature is adjusted to room temperature and the crystal is filtered. The crystal was recrystallized from dichloromethane and acetone to obtain 3.8 g (yield 52%) of [Compound 21].
MS(MALDI-TOF): m/z 487 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 487 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
98.6,104.8,106.3,109.5,111.9,119.8,120.7,120.8,121.4,125.5,125.7,126.6,127.4,127.5,127.7,128.5,128.7,129.2,129.4,131.8,132.3,132.4,133,134.7,144.4,149.3,155.8,161 [34C]98.6,104.8,106.3,109.5,111.9,119.8,120.7,120.8,121.4,125.5,125.7,126.6,127.4,127.5,127.7,128.5,128.7,129.2,129.4,131.8,132.3,132.4,133,134.7,144.4,149.3, 155.8,161 [34C]
합성예 22. [화합물22]의 합성Synthesis Example 22. Synthesis of [Compound 22]
[반응식 22-1][Scheme 22-1]
[중간체 22-a] [화합물22] [Intermediate 22-a] [Compound 22]
상기 [반응식 21-1]에서 사용된 [중간체 20-b] 대신 상기 합성예 3에서 제조된 [중간체 22-a]를 사용한 것을 제외하고는 상기 합성예 21과 동일한 방법을 이용하여 [화합물 22] 4.3g을 얻었다. (수율 54%)[Compound 22] in the same manner as in Synthesis Example 21, except that [Intermediate 22-a] prepared in Synthesis Example 3 was used instead of [Intermediate 20-b] used in [Scheme 21-1]. I got 4.3 g. (Yield 54%)
MS(MALDI-TOF): m/z 529 [M]+ . 13C NMR(75MHz, CDCl3) δ: MS (MALDI-TOF): m/z 529 [M] + . 13 C NMR (75 MHz, CDCl 3 ) δ:
22.3,30.9,104.8,109.5,111.7,112.3,114.4,116,118.5,118.7,119.8,120.2,120.7,122.9,125,125.4,125.8,126.6,127.5,128.3,128.7,129,129.2,129.4,130.5,131.4,131.8,131.9,133.9,134.7,137.1,149.2,155.6,160 [37C]22.3,30.9,104.8,109.5,111.7,112.3,114.4,116,118.5,118.7,119.8,120.2,120.7,122.9,125,125.4,125.8,126.6,127.5,128.3,128.7,129,129.2,129.4,130.5,131.4,131.8,131.9, 133.9,134.7,137.1,149.2,155.6,160 [37C]
실시예Example 1 내지 22 1 to 22
유기 발광다이오드의 제조Fabrication of organic light emitting diodes
ITO 글래스의 발광 면적이 2 mm x 2 mm 크기가 되도록 패터닝한 후 세정하였다. 기판을 진공 챔버에 장착한 후 베이스 압력이 1x10-6 torr가 되도록 한 후 유기물을 상기 ITO위에 DNTPD(700Å), α-NPB (300Å), 본 발명에 의해 제조된 화합물 1 내지 22(90%) + (piq)2Ir(acac) (10%)(300Å), Alq3 (350Å), LiF(5Å), Al(1,000Å)의 순서로 성막하였으며, 0.4 mA에서 측정을 하였다.The ITO glass was patterned so that the light emitting area was 2 mm x 2 mm, and washed. After mounting the substrate in the vacuum chamber, the base pressure is 1x10 -6 torr, and then the organic material is placed on the ITO DNTPD (700Å), α-NPB (300Å), compounds 1 to 22 (90%) prepared by the present invention + (piq) 2 Ir(acac) (10%) (300Å), Alq 3 (350Å), LiF (5Å), and Al (1,000Å) were formed in the order, and the measurement was performed at 0.4 mA.
상기 DNTPD(700Å), α-NPB, (piq)2Ir(acac), Alq3 및 [화합물1] 내지 [화합물22]의 구조는 다음과 같다.The structures of the DNTPD (700Å), α-NPB, (piq) 2 Ir(acac), Alq 3 and [Compound 1] to [Compound 22] are as follows.
[DNTPD] [α-NPB] [DNTPD] [α-NPB]
[(piq)2Ir(acac)] [Alq3]
[(piq) 2 Ir(acac)] [Alq 3 ]
[화합물1] [화합물2] [화합물3][Compound 1] [Compound 2] [Compound 3]
[화합물4] [화합물5] [화합물6][Compound 4] [Compound 5] [Compound 6]
[화합물7] [화합물8] [화합물9][Compound 7] [Compound 8] [Compound 9]
[화합물10] [화합물11] [화합물12]
[Compound 10] [Compound 11] [Compound 12]
[화합물13] [화합물14] [화합물15][Compound 13] [Compound 14] [Compound 15]
[화합물16] [화합물17] [화합물18] [Compound 16] [Compound 17] [Compound 18]
[화합물19] [화합물20] [화합물21] [Compound 19] [Compound 20] [Compound 21]
[화합물22] [Compound 22]
실시예Example 23 23
상기 실시예 1 내지 22의 소자구조에서 발광층에 [화합물 1]을 사용하였으며, [(piq)2Ir(acac)] 대신 [PTOEP]를 사용한 점을 제외하고 동일하게 제작하였으며 [PTOEP]의 구조는 아래와 같다.In the device structures of Examples 1 to 22, [Compound 1] was used for the light emitting layer, and [PTOEP] was used instead of [(piq) 2 Ir(acac)], and the structure of [PTOEP] was It is as follows.
[PTOEP] [PTOEP]
비교예Comparative example 1 One
비교예를 위한 유기발광소자는 상기 실시예의 소자구조에서 본 발명에 의해 제조된 화합물 대신 일반적인 인광호스트 물질로 많이 사용되고 있는 CBP 를 사용한 점을 제외하고 동일하게 제작하였으며 상기 CBP 의 구조는 아래와 같다.The organic light emitting device for the comparative example was fabricated in the same manner, except that CBP, which is widely used as a general phosphorescent host material, was used instead of the compound prepared by the present invention in the device structure of the above example, and the structure of the CBP is as follows.
[CBP] [CBP]
비교예Comparative example 2 내지 5 2 to 5
비교예 2 내지 5를 위한 유기발광 소자는 상기 실시예1 내지 22의 소자구조에서 본발명에 의해 제조된 화합물 대신 하기의 [화합물 23] 내지 [화합물 26]을 사용한 점을 제외하고 동일하게 제작하였으며 그 구조는 아래와 같다.The organic light emitting devices for Comparative Examples 2 to 5 were fabricated in the same manner, except that the following [Compound 23] to [Compound 26] were used instead of the compound prepared by the present invention in the device structures of Examples 1 to 22. Its structure is as follows.
[화합물 23] [화합물 24] [화합물 25][Compound 23] [Compound 24] [Compound 25]
[화합물 26][Compound 26]
비교예Comparative example 6 6
비교예 6을 위한 유기발광 소자는 상기 실시예23의 소자구조에서 발명에 의해 제조된 [화합물 1] 대신 상기 [화합물 23]을 사용한 점을 제외하고 동일하게 제작하였다.
The organic light-emitting device for Comparative Example 6 was fabricated in the same manner, except that [Compound 23] was used instead of [Compound 1] prepared by the invention in the device structure of Example 23.
상기 실시예 1 내지 23, 비교예 1 내지 6에 따라 제조된 유기전계발광소자에 대하여, 전압, 전류밀도, 휘도, 색 좌표 및 수명을 측정하고 그 결과를 하기 [표 1]에 나타내었다. T90은 휘도가 초기휘도(5000nit)에서 90%로 감소되는데 소요되는 시간을 의미한다.For the organic electroluminescent devices manufactured according to Examples 1 to 23 and Comparative Examples 1 to 6, voltage, current density, luminance, color coordinates, and lifetime were measured, and the results are shown in Table 1 below. T90 refers to the time it takes for the luminance to decrease from the initial luminance (5000nit) to 90%.
[표 1][Table 1]
상기 표 1에서 보는 바와 같이 본 발명에 의하여 확보된 유기화합물은 인광 발광성 호스트 재료로 많이 쓰이는 호스트물질 중 CBP에 비하여 훨씬 낮은 구동전압과 높은 발광효율 그리고 장수명을 가진다. As shown in Table 1, the organic compound secured by the present invention has a much lower driving voltage, higher luminous efficiency, and a longer life than CBP among host materials commonly used as phosphorescent host materials.
또한 도 2에서는 상기 비교예 2, 실시예 1, 실시예 8의 수명평가(T90 값) 결과를 도시하였다. 표 1 및 도 2에서 볼 수 있듯이, 실시예 8 과 같이 중수소가 치환되는 경우에 중수소가 치환되지 않은 경우보다 훨씬더 수명이 추가적으로 개선됨을 알 수 있어, 장수명의 유기발광소자로서 응용가능성 높은 것을 나타내고 있다.
In addition, Fig. 2 shows the results of life evaluation (T90 value) of Comparative Example 2, Example 1, and Example 8. As can be seen in Table 1 and Figure 2, it can be seen that the lifespan is further improved even more than the case where deuterium is not substituted when deuterium is substituted as in Example 8, indicating high applicability as an organic light emitting device with a long life. have.
Claims (16)
[화학식 A]
[화학식 B]
상기 [화학식 A] 및 [화학식 B]에서,
상기 A1 내지 A4 와 R1 내지 R 16은 각각 동일하거나 상이하고, 서로 독립적으로 수소, 중수 소, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치 환된 탄소수 6 내지 50의 아릴기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴옥시기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 2 내지 50의 헤테로아릴기, 시아노기, 니트로기, 할로겐기 중에서 선택되는 어느 하나이고, 상기 A1 내지 A4 와 R1 내지 R8은 각각 서로 인접하는 치환기와 연결되어 지환족 , 방향족의 단일환 또는 다환 고리를 형성할 수 있으며, 상기 형성된 지환족, 방향족의 단일환 또는 다환 고리의 탄소원자는 N, S, O 중에 서 선택되는 어느 하나 이상의 헤테로원자로 치환될 수 있으며;
상기 L1 및 L2는 연결기로서, 단일 결합, 치환 또는 비치환된 탄소수 6 내지 60의 아릴렌기 또는 치환 또는 비치환된 탄소수 2 내지 60의 헤테로아릴렌기이며;
상기 X는 연결기로서, 단일결합이거나 -C(R31R32)-, NR33, O, S, SiR34R35, GeR36R37, PR38, PR39(=O), C=O, BR40 이며,
상기 R31 내지 R40은 상기 R1 내지 R16에서 정의한 바와 동일하며;
상기 m, n, n'및 p는 각각 서로 독립적으로 1 내지 2의 정수이며,
상 기 m, n, n'및 p가 각각 2인 경우에 각각의 연결기 및 인돌그룹은 서 로 동일하거나 상이하며;
화학식 A에서 R5 내지 R8 중 p개와, R10 내지 R13, R15 및 R16 중 하나는 각각 상기 L2 와 연결되는 단일결합이고,
화학식 B에서, R5 내지 R8 중 p개는 상기 L2 와 연결되는 단일결합이며;
상기 '치환 또는 비치환된'에서의 '치환'은 중수소, 시아노기, 할로겐기, 니트로기, 탄소수 1 내지 24의 알킬기, 탄소수 1 내지 24의 할로겐화된 알킬기, 탄소수 6 내지 24의 아릴기, 탄소수 7 내지 24의 아릴알킬기, 탄소수 2 내지 24의 헤테로아릴기, 탄소수 2 내지 24의 헤테로아릴알킬기, 탄소수 1 내지 24의 알콕시기, 탄소수 1 내지 24의 알킬실릴기, 탄소수 6 내지 24의 아릴실릴기, 탄소수 6 내지 24의 아릴옥시기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환되는 것을 의미한다.
단, 하기 구조로 표시되는 13개의 화합물은 제외한다.
An organic light-emitting compound represented by the following [Chemical Formula A] or [Chemical Formula B].
[Formula A]
[Formula B]
In the above [Formula A] and [Formula B],
The A 1 to A 4 and R 1 to R 16 are each the same or different, and independently of each other, hydrogen, deuterium, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted aryl group having 6 to 50 carbon atoms , A substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted alkoxy group having 1 to 30 carbon atoms, a substituted or unsubstituted aryloxy group having 6 to 30 carbon atoms, a substituted or unsubstituted and hetero atom O, It is any one selected from a C2-C50 heteroaryl group, a cyano group, a nitro group, and a halogen group having N or S, and the A 1 to A 4 and R 1 to R 8 are each connected with a substituent adjacent to each other Can form an alicyclic, aromatic monocyclic or polycyclic ring, and the formed alicyclic, aromatic monocyclic or polycyclic carbon atoms may be substituted with any one or more heteroatoms selected from N, S, and O;
L 1 and L 2 are a linking group, a single bond, a substituted or unsubstituted arylene group having 6 to 60 carbon atoms, or a substituted or unsubstituted heteroarylene group having 2 to 60 carbon atoms;
X is a linking group, or a single bond or -C(R 31 R 32 )-, NR 33 , O, S, SiR 34 R 35 , GeR 36 R 37 , PR 38 , PR 39 (=O), C=O, BR 40 ,
R 31 to R 40 are the same as defined in R 1 to R 16 ;
M, n, n'and p are each independently 1 to Is an integer of 2,
When m, n, n'and p are each 2, each linking group and indole group are the same or different from each other;
In Formula A, p of R 5 to R 8 and one of R 10 to R 13, R 15 and R 16 are each a single bond connected to L 2 ,
In Formula B, p of R 5 to R 8 is a single bond connected to L 2 ;
The'substituted' in the'substituted or unsubstituted' is deuterium, a cyano group, a halogen group, a nitro group, an alkyl group having 1 to 24 carbon atoms, a halogenated alkyl group having 1 to 24 carbon atoms, an aryl group having 6 to 24 carbon atoms, and 7 to 24 arylalkyl group, C 2 to C 24 heteroaryl group, C 2 to C 24 heteroarylalkyl group, C 1 to C 24 alkoxy group, C 1 to C 24 alkylsilyl group, C 6 It means substituted with one or more substituents selected from the group consisting of an arylsilyl group having 6 to 24 carbon atoms and an aryloxy group having 6 to 24 carbon atoms.
However, 13 compounds represented by the following structures are excluded.
상기 [화학식 A] 및 [화학식 B] 의 연결기 L1 및 L2는 동일하거나 상이하며, 각각 독립적으로, 단일결합이거나, 아래 구조식 1 내지 구조식 8 중에서 선택되는 어느 하나인 것을 특징으로 하는 유기 발광 화합물.
[구조식 1] [구조식 2] [구조식 3] [구조식 4]
[구조식 5] [구조식 6] [구조식 7] [구조식 8]
상기 치환기 L1 및 L2에서 방향족 고리의 탄소자리는 수소 또는 중수소가 결합된다.The method of claim 1,
The linking groups L 1 and L 2 of the [Chemical Formula A] and [Chemical Formula B] are the same or different, and each independently, a single bond, or an organic light-emitting compound, characterized in that any one selected from the following Structural Formulas 1 to 8 .
[Structural Formula 1] [Structural Formula 2] [Structural Formula 3] [Structural Formula 4]
[Structural Formula 5] [Structural Formula 6] [Structural Formula 7] [Structural Formula 8]
In the substituents L 1 and L 2 , hydrogen or deuterium is bonded to the carbon site of the aromatic ring.
상기 [화학식 A] 및 [화학식 B] 의 치환기 A1 내지 A4 와 R1 내지 R16은 각각 동일하거나 상이하고, 서로 독립적으로 수소, 중수소; 치환 또는 비치환된 탄소수 1 내지 20의 알킬기; 치환 또는 비치환된 탄소수 6 내지 20의 아릴기; 치환 또는 비치환된 탄소수 2 내지 20의 헤테로아릴기;중에서 선택되는 하나이며, 상기 m, n, n'및 p는 1인 것을 특징으로 하는 유기발광 화합물The method of claim 1,
The substituents A 1 to A 4 and R 1 to R 16 of [Chemical Formula A] and [Chemical Formula B] are the same or different, and independently of each other, hydrogen and deuterium; A substituted or unsubstituted C1 to C20 alkyl group; A substituted or unsubstituted aryl group having 6 to 20 carbon atoms; A substituted or unsubstituted heteroaryl group having 2 to 20 carbon atoms; one selected from among, and m, n, n'and p are 1
[화학식 A] 또는 [화학식 B]로 표시되는 유기발광 화합물은 [화학식 1] 내지 [화학식 10] 중에서 선택되는 어느 하나로 표시되는, 유기발광 화합물.
[화학식 1] [화학식 2]
[화학식 3] [화학식 4]
[화학식 5] [화학식 6]
[화학식 7] [화학식 8]
[화학식 9] [화학식 10]
상기 [화학식 1] 내지 [화학식 10]에서 치환기 A1 내지 A4 와 R1 내지 R16, R33 내지 R38, L1, L2, n, n' 및 p는 각각 제 1항에서 정의한 바와 동일하되, 상기 R10 내지 R16 중 하나는 상기 연결기 L2와 결합되는 단일결합이다. The method of claim 1,
The organic light-emitting compound represented by [Formula A] or [Formula B] is represented by any one selected from [Formula 1] to [Formula 10].
[Formula 1] [Formula 2]
[Formula 3] [Formula 4]
[Formula 5] [Formula 6]
[Formula 7] [Formula 8]
[Formula 9] [Formula 10]
In the [Formula 1] to [Formula 10], substituents A 1 to A 4 and R 1 to R 16 , R 33 to R 38 , L 1 , L 2 , n, n'and p are each the same as defined in claim 1, but one of R 10 to R 16 is a single bond bonded to the linking group L 2 .
상기 치환기 R1 내지 R8 은 각각 서로 인접하는 치환기와 연결되어 고리를 형성하지 않는 것을 특징으로 하는 유기발광 화합물 The method of claim 1,
The substituents R 1 to R 8 An organic light-emitting compound, characterized in that each is connected with a substituent adjacent to each other to form a ring
[화학식 A] 또는 [화학식 B]로 표시되는 유기발광 화합물은 [화학식 11] 내지 [화학식 22]에서 선택되는 어느 하나로 표시되는, 유기발광 화합물.
[화학식 11] [화학식 12]
[화학식 13] [화학식 14]
[화학식 15] [화학식 16]
[화학식 17] [화학식 18]
[화학식 19] [화학식 20]
[화학식 21] [화학식 22]
상기 [화학식 1] 내지 [화학식 22]에서 치환기 A1 내지 A4 와 R1 내지 R16, X, L1, L2, m, n, n' 및 p는 각각 제1항에서 정의한 바와 동일하되, 상기 R10 내지 R16 중 하나는 상기 연결기 L2와 결합되는 단일결합이며, Ra 및 Rb는 제1항에서의 R1 내지 R16에서 정의한 바와 동일하고, j는 1내지 6의 정수이며, j가 2이상인 경우 각각의 Ra는 동일하거나 상이할 수 있고 각각의 Rb도 동일하거나 상이할 수 있다. The method of claim 1,
The organic light emitting compound represented by [Formula A] or [Formula B] is represented by any one selected from [Formula 11] to [Formula 22].
[Formula 11] [Formula 12]
[Formula 13] [Formula 14]
[Formula 15] [Formula 16]
[Formula 17] [Formula 18]
[Formula 19] [Formula 20]
[Formula 21] [Formula 22]
Substituents A 1 to A 4 and R 1 to R 16 , X, in the [Formula 1] to [Formula 22] L 1 , L 2 , m, n, n'and p are each the same as defined in claim 1, but one of R 10 to R 16 is a single bond bonded to the linking group L 2, and Ra and Rb are the first The same as defined in R 1 to R 16 in item 1 , j is an integer of 1 to 6, and when j is 2 or more, each Ra can be the same or different and each Rb can be the same or different.
상기 [화학식 A] 및 [화학식 B] 의 치환기 R9 는 중수소 또는 중수소를 포함하는 관능기인 것을 특징으로 하는 유기발광 화합물The method of claim 1,
The substituent R 9 of the [Formula A] and [Formula B] is an organic light-emitting compound, characterized in that it is a functional group containing deuterium or deuterium
상기 [화학식 A] 및 [화학식 B] 의 치환기 A1 내지 A4 는 각각 수소 또는 중수소인 것을 특징으로 하는 유기발광 화합물The method of claim 1,
The organic light emitting compound, characterized in that the substituents A 1 to A 4 of [Chemical Formula A] and [Chemical Formula B] are each hydrogen or deuterium
상기 연결기 L1 및 L2는 동일하거나 상이하며, 각각 독립적으로, 단일결합이거나, 또는 이고, X는 단일결합이며, n, n' 및 p 는 각각 1인 것을 특징으로 하는, 유기발광 화합물The method of claim 8,
The linking groups L 1 and L 2 are the same or different, and each independently, is a single bond, or And, X is a single bond, n, n'and p are each 1, characterized in that the organic light-emitting compound
[화학식 A] 또는 [화학식 B]로 표시되는 화 합물은 하기 [화합물 2] 내지 [화합물 20], [화합물 22] 내지 [화합물 126], [화합물 128] 내지 [화합물 130] 중 어느 하나인 것을 특 징으로 하는 유기 발광 화합물
[화합물2] [화합물3]
[화합물4] [화합물5] [화합물6]
[화합물7] [화합물8] [화합물9]
[화합물10] [화합물11] [화합물12]
[화합물13] [화합물14] [화합물15]
[화합물16] [화합물17] [화합물18]
[화합물19] [화합물20]
[화합물22] [화합물23] [화합물24]
[화합물25] [화합물26] [화합물27]
[화합물28] [화합물29] [화합물30]
[화합물31] [화합물32] [화합물33]
[화합물34] [화합물35] [화합물36]
[화합물37] [화합물38] [화합물39]
[화합물40] [화합물41] [화합물42]
[화합물43] [화합물44] [화합물45]
[화합물46] [화합물47] [화합물48]
[화합물49] [화합물50] [화합물51]
[화합물52] [화합물53] [화합물54]
[화합물55] [화합물56] [화합물57]
[화합물58] [화합물59] [화합물60]
[화합물61] [화합물62] [화합물63]
[화합물64] [화합물65] [화합물66]
[화합물67] [화합물68] [화합물69]
[화합물70] [화합물71] [화합물72]
[화합물73] [화합물74] [화합물75]
[화합물76] [화합물77] [화합물78]
[화합물79] [화합물80] [화합물81]
[화합물82] [화합물83] [화합물84]
[화합물85] [화합물86] [화합물87]
[화합물88] [화합물89] [화합물90]
[화합물91] [화합물92] [화합물93]
[화합물94] [화합물95] [화합물96]
[화합물97] [화합물98] [화합물99]
[화합물100] [화합물101] [화합물102]
[화합물103] [화합물104] [화합물105]
[화합물106] [화합물107] [화합물108]
[화합물109] [화합물110] [화합물111]
[화합물112] [화합물113] [화합물114]
[화합물115] [화합물116] [화합물117]
[화합물118] [화합물119] [화합물120]
[화합물121] [화합물122] [화합물123]
[화합물124] [화합물125] [화합물126]
[화합물128] [화합물129] [화합물130]The method of claim 1,
The compound represented by [Formula A] or [Formula B] is any one of the following [Compound 2] to [Compound 20], [Compound 22] to [Compound 126], [Compound 128] to [Compound 130] Organic light-emitting compound as a feature
[Compound 2] [Compound 3]
[Compound 4] [Compound 5] [Compound 6]
[Compound 7] [Compound 8] [Compound 9]
[Compound 10] [Compound 11] [Compound 12]
[Compound 13] [Compound 14] [Compound 15]
[Compound 16] [Compound 17] [Compound 18]
[Compound 19] [Compound 20]
[Compound 22] [Compound 23] [Compound 24]
[Compound 25] [Compound 26] [Compound 27]
[Compound 28] [Compound 29] [Compound 30]
[Compound 31] [Compound 32] [Compound 33]
[Compound 34] [Compound 35] [Compound 36]
[Compound 37] [Compound 38] [Compound 39]
[Compound 40] [Compound 41] [Compound 42]
[Compound 43] [Compound 44] [Compound 45]
[Compound 46] [Compound 47] [Compound 48]
[Compound 49] [Compound 50] [Compound 51]
[Compound 52] [Compound 53] [Compound 54]
[Compound 55] [Compound 56] [Compound 57]
[Compound 58] [Compound 59] [Compound 60]
[Compound 61] [Compound 62] [Compound 63]
[Compound 64] [Compound 65] [Compound 66]
[Compound 67] [Compound 68] [Compound 69]
[Compound 70] [Compound 71] [Compound 72]
[Compound 73] [Compound 74] [Compound 75]
[Compound 76] [Compound 77] [Compound 78]
[Compound 79] [Compound 80] [Compound 81]
[Compound 82] [Compound 83] [Compound 84]
[Compound 85] [Compound 86] [Compound 87]
[Compound 88] [Compound 89] [Compound 90]
[Compound 91] [Compound 92] [Compound 93]
[Compound 94] [Compound 95] [Compound 96]
[Compound 97] [Compound 98] [Compound 99]
[Compound 100] [Compound 101] [Compound 102]
[Compound 103] [Compound 104] [Compound 105]
[Compound 106] [Compound 107] [Compound 108]
[Compound 109] [Compound 110] [Compound 111]
[Compound 112] [Compound 113] [Compound 114]
[Compound 115] [Compound 116] [Compound 117]
[Compound 118] [Compound 119] [Compound 120]
[Compound 121] [Compound 122] [Compound 123]
[Compound 124] [Compound 125] [Compound 126]
[Compound 128] [Compound 129] [Compound 130]
상기 제1전극에 대향된 제2전극; 및
상기 제1전극과 상기 제2전극 사이에 개재되는 유기층;을 포함하고, 상기 유기층이 제1항 내지 제10 항 중에서 선택되는 어느 한 항의 유기발광 화합물을 1종 이상 포함한, 유기 발광 소자.A first electrode;
A second electrode facing the first electrode; And
An organic light-emitting device comprising; an organic layer interposed between the first electrode and the second electrode, wherein the organic layer includes at least one organic light-emitting compound of any one selected from claims 1 to 10.
상기 유기층은 정공 주입층, 정공 수송층, 정공 주입 기능 및 정공 수송 기능을 동시에 갖는 기능층, 발광층, 전자 수송층, 및 전자 주입층 중 적어도 하나를 포함하는 것을 특징으로 하는 유기 발광 소자.The method of claim 11,
The organic layer is an organic light emitting device comprising at least one of a hole injection layer, a hole transport layer, a functional layer having a hole injection function and a hole transport function at the same time, a light emitting layer, an electron transport layer, and an electron injection layer.
상기 제1전극과 상기 제2전극 사이에 개재된 유기층이 발광층을 포함하며,
상기 발광층은 호스트와 도판트로 이루어지고, 상기 유기발광 화합물이 호스트로서 사용되는 것을 특징으로 하는 유기 발광 소자.The method of claim 12,
The organic layer interposed between the first electrode and the second electrode includes a light emitting layer,
The light-emitting layer is an organic light-emitting device comprising a host and a dopant, and the organic light-emitting compound is used as a host.
상기 유기층은 정공저지층 또는 전자저지층을 추가로 포함하는 것을 특징으로 하는 유기 발광 소자.The method of claim 13,
The organic layer is an organic light emitting device, characterized in that it further comprises a hole blocking layer or an electron blocking layer.
상기 각각의 층중에서 선택된 하나 이상의 층은 증착공정 또는 용액공정에 의해 형성되는 것을 특징으로 하는 유기 발광 소자The method of claim 12,
An organic light-emitting device, characterized in that at least one layer selected from each of the layers is formed by a deposition process or a solution process.
상기 유기발광소자는 평판 디스플레이 장치; 플렉시블 디스플레이 장치; 단색 또는 백색의 평판 조명용 장치; 및, 단색 또는 백색의 플렉시블 조명용 장치;에서 선택되는 어느 하나의 장치에 사용되는 것을 특징으로 하는 유기 발광 소자
The method of claim 11,
The organic light emitting device may include a flat panel display device; Flexible display device; Monochrome or white flat lighting devices; And, a single color or white flexible lighting device; organic light emitting device characterized in that used in any one device selected from
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20130016496 | 2013-02-15 | ||
| KR1020130016496 | 2013-02-15 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140103842A KR20140103842A (en) | 2014-08-27 |
| KR102215780B1 true KR102215780B1 (en) | 2021-02-17 |
Family
ID=51748008
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020140014005A Active KR102215780B1 (en) | 2013-02-15 | 2014-02-07 | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102215780B1 (en) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102118013B1 (en) * | 2013-02-22 | 2020-06-05 | 에스에프씨주식회사 | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same |
| WO2016079667A1 (en) | 2014-11-17 | 2016-05-26 | Idemitsu Kosan Co., Ltd. | Indole derivatives for electronic applications |
| CN107108570B (en) * | 2014-12-18 | 2021-04-13 | 东进世美肯株式会社 | Novel compounds and organic light-emitting devices comprising the same |
| WO2016099204A2 (en) * | 2014-12-18 | 2016-06-23 | 주식회사 동진쎄미켐 | Novel compound and organic light emitting element comprising same |
| WO2016153283A1 (en) * | 2015-03-24 | 2016-09-29 | 주식회사 엠비케이 | Organic light-emitting compound, ink composition, organic light-emitting diode, and electronic device |
| JP6701649B2 (en) * | 2015-09-10 | 2020-05-27 | コニカミノルタ株式会社 | Organic electroluminescence element, display device, lighting device, π-conjugated compound, and light-emitting thin film |
| KR102685450B1 (en) * | 2016-12-15 | 2024-07-16 | 솔루스첨단소재 주식회사 | Organic light-emitting compound and organic electroluminescent device using the same |
| CN106831743B (en) * | 2016-12-30 | 2020-03-17 | 上海天马有机发光显示技术有限公司 | Organic electroluminescent material and organic photoelectric device |
| CN109890810B (en) * | 2017-03-27 | 2021-08-20 | 株式会社Lg化学 | Benzocarbazole-based compound and organic light-emitting device comprising the same |
| KR102472171B1 (en) * | 2017-08-29 | 2022-11-30 | 삼성디스플레이 주식회사 | Polycyclic compound and organic electroluminescence device including the same |
| KR102767901B1 (en) | 2019-01-29 | 2025-02-18 | 삼성디스플레이 주식회사 | Organic electroluminescence device and polycyclic compound for organic electroluminescence device |
| KR102773699B1 (en) | 2019-03-05 | 2025-02-28 | 삼성디스플레이 주식회사 | Organic electroluminescence device and polycyclic compound for organic electroluminescence device |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20110013220A (en) | 2009-07-31 | 2011-02-09 | 다우어드밴스드디스플레이머티리얼 유한회사 | Novel organic light emitting compound and organic electroluminescent device comprising same |
| JP5120398B2 (en) | 2010-03-04 | 2013-01-16 | コニカミノルタホールディングス株式会社 | Organic electroluminescence element and display device |
| KR102191024B1 (en) * | 2012-04-10 | 2020-12-14 | 에스에프씨 주식회사 | Heterocyclic com pounds and organic light-emitting diode including the same |
| KR102191022B1 (en) * | 2012-04-18 | 2020-12-14 | 에스에프씨 주식회사 | Heterocyclic com pounds and organic light-emitting diode including the same |
| KR102191019B1 (en) * | 2012-12-26 | 2020-12-14 | 에스에프씨 주식회사 | An electroluminescent compound and an electroluminescent device comprising the same |
-
2014
- 2014-02-07 KR KR1020140014005A patent/KR102215780B1/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| KR20140103842A (en) | 2014-08-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102905139B1 (en) | An electroluminescent compound and an electroluminescent device comprising the same | |
| KR102444324B1 (en) | Novel heterocyclic compound and organic light emitting device comprising same | |
| KR102215780B1 (en) | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102758692B1 (en) | Organic light-emitting diode with long lifetime, low voltage and high efficiency | |
| KR102191778B1 (en) | Heterocyclic compounds and organic light-emitting diode including the same | |
| KR102084421B1 (en) | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102118013B1 (en) | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102169448B1 (en) | An electroluminescent compound and an electroluminescent device comprising the same | |
| KR102191024B1 (en) | Heterocyclic com pounds and organic light-emitting diode including the same | |
| KR102169444B1 (en) | Aromatic compound and organoelectro luminescent device comprising the compound | |
| KR20200116873A (en) | Aromatic compound and organoelectroluminescent device comprising the compound | |
| KR102215776B1 (en) | Novel heterocyclic compounds and organic light-emitting diode including the same | |
| KR102149450B1 (en) | Deuterated organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR20140000640A (en) | Aromatic compound and organoelectroluminescent device comprising the compound | |
| KR20240101527A (en) | Novel heterocyclic compounds and organic light-emitting diode including the same | |
| KR102084423B1 (en) | Deuterated organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102081617B1 (en) | Deuterated organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102169447B1 (en) | An organoelectro luminescent compounds and organoelectro luminescent device using the same | |
| KR102635131B1 (en) | Novel anthracene derivatives and organic light-emitting diode therewith | |
| KR102104633B1 (en) | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102127368B1 (en) | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102169446B1 (en) | An organoelectroluminescent compounds and organoelectroluminescent device using the same | |
| KR102197019B1 (en) | Novel organic compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR102191779B1 (en) | Aromatic compound and organoelectro luminescent device comprising the compound | |
| KR102154054B1 (en) | Heterocyclic compounds and organic light-emitting diode including the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| U11 | Full renewal or maintenance fee paid |
Free format text: ST27 STATUS EVENT CODE: A-4-4-U10-U11-OTH-PR1001 (AS PROVIDED BY THE NATIONAL OFFICE) Year of fee payment: 5 |