KR101996649B1 - Pyrene derivative compounds and organic light-emitting diode including the same - Google Patents
Pyrene derivative compounds and organic light-emitting diode including the same Download PDFInfo
- Publication number
- KR101996649B1 KR101996649B1 KR1020120038499A KR20120038499A KR101996649B1 KR 101996649 B1 KR101996649 B1 KR 101996649B1 KR 1020120038499 A KR1020120038499 A KR 1020120038499A KR 20120038499 A KR20120038499 A KR 20120038499A KR 101996649 B1 KR101996649 B1 KR 101996649B1
- Authority
- KR
- South Korea
- Prior art keywords
- chemical formula
- formula
- group
- substituted
- carbon atoms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
- H10K50/171—Electron injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
Landscapes
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
본 발명은 신규한 화합물 및 이를 발광물질로 포함하는 유기전계발광소자에 관한 것으로서, 구체적으로 하기 [화학식 1] 내지 [화학식 5]로 표시되는 신규한 화합물 및 이를 포함하는 유기전계발광소자인 것을 특징으로 하며, 본 발명에 따른 하기 [화학식 1] 내지 [화학식 5]의 발광 화합물을 포함하는 유기전계발광소자는 구동전압, 전류효율 등의 발광특성에 있어 우수한 효과가 있다.
[화학식 1] [화학식 2] [화학식 3]
[화학식 4] [화학식 5]
The present invention relates to a novel compound and an organic electroluminescent device comprising the same as a light emitting material, and more particularly to a novel compound represented by the following formulas (1) to (5) and an organic electroluminescent device including the novel compound , And the organic electroluminescent device comprising the light-emitting compounds of the following formulas (1) to (5) according to the present invention has an excellent effect on light emission characteristics such as driving voltage and current efficiency.
[Formula 3] < EMI ID =
[Chemical Formula 4]
Description
본 발명은 피렌 유도체 화합물 및 이를 발광물질로 포함하는 유기전계발광소자에 관한 것으로서, 보다 상세하게는 구동전압, 전류효율 등의 발광 특성이 우수하고, 보다 안정적인 피렌 유도체 화합물 및 이를 포함하는 유기전계발광소자에 관한 것이다.The present invention relates to a pyrene derivative compound and an organic electroluminescent device comprising the same as a light emitting material. More particularly, the present invention relates to a pyrene derivative compound having excellent emission characteristics such as a driving voltage and a current efficiency, Device.
최근 표시장치의 대형화에 따라 공간 점유가 작은 평면표시소자의 요구가 증대되고 있는데, 대표적인 평면표시소자인 액정 디스플레이는 기존의 CRT(cathode ray tube)에 비해 경량화가 가능하다는 장점은 있으나, 시야각(viewing angle)이 제한되고 배면 광(back light)이 반드시 필요하다는 등의 단점을 갖고 있다. 이에 반하여, 새로운 평면표시소자인 유기전계발광소자(organic light emitting diode, OLED)는 자기 발광 현상을 이용한 디스플레이로서, 시야각이 크고, 액정 디스플레이에 비해 경박, 단소해질 수 있으며, 빠른 응답 속도 등의 장점을 가지고 있으며, 최근에는 풀-컬러(full-color) 디스플레이 또는 조명으로의 응용이 기대되고 있다.In recent years, the demand for a flat display device having a small space occupation has been increasing due to the enlargement of a display device. The liquid crystal display, which is a typical flat display device, has an advantage of being lighter than a conventional CRT (cathode ray tube) angle is limited and a back light is necessarily required. On the other hand, an organic light emitting diode (OLED), which is a new flat display device, is a display using a self-luminous phenomenon and has a wide viewing angle and can be made thinner and thinner than a liquid crystal display, And in recent years, application to a full-color display or illumination is expected.
일반적으로 유기 발광 현상이란 유기 물질을 이용하여 전기에너지를 빛에너지로 전환시켜주는 현상을 말한다.In general, organic light emission phenomenon refers to a phenomenon in which an organic material is used to convert electric energy into light energy.
유기 발광 현상을 이용하는 유기전계발광소자는 통상 양극과 음극 및 이 사이에 유기물층을 포함하는 구조를 가진다. 여기서 유기물층은 유기전계발광소자의 효율과 안정성을 높이기 위하여 각기 다른 물질로 구성된 다층의 구조로 이루어진 경우가 많으며, 예컨대 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층 등으로 이루어질 수 있다. 이러한 유기전계발광소자의 구조에서 두 전극 사이에 전압을 걸어주게 되면 양극에서는 정공이, 음극에서는 전자가 유기물층에 주입되게 되고, 주입된 정공과 전자가 만났을 때 엑시톤(exciton)이 형성되며, 이 엑시톤이 다시 바닥상태로 떨어질 때 빛이 나게 된다. 이러한 유기전계발광소자는 자발광, 고휘도, 고효율, 낮은 구동전압, 넓은 시야각, 높은 콘트라스트, 고속 응답성 등의 특성을 갖는 것으로 알려져 있다.An organic electroluminescent device using an organic light emitting phenomenon usually has a structure including an anode, an anode, and an organic material layer therebetween. Here, in order to enhance the efficiency and stability of the organic electroluminescent device, the organic material layer may have a multi-layer structure composed of different materials and may include a hole injection layer, a hole transport layer, a light emitting layer, an electron transport layer, and an electron injection layer. When a voltage is applied between the two electrodes in the structure of the organic electroluminescent device, holes are injected into the anode, electrons are injected into the organic layer, and excitons are formed when injected holes and electrons meet. When it falls back to the ground state, the light comes out. Such an organic electroluminescent device is known to have properties such as self-emission, high luminance, high efficiency, low driving voltage, wide viewing angle, high contrast, and high speed response.
유기전계발광소자에서 유기물층으로 사용되는 재료는 기능에 따라, 발광 재료와 전하수송 재료, 예컨대 정공주입 재료, 정공수송 재료, 전자수송 재료, 전자주입 재료 등으로 분류될 수 있다. 상기 발광 재료는 분자량에 따라 고분자형과 저분자형으로 분류될 수 있고, 발광 메커니즘에 따라 전자의 일중항 여기상태로부터 유래되는 형광 재료와 전자의 삼중항 여기상태로부터 유래되는 인광 재료로 분류될 수 있다. 또한, 발광 재료는 발광색에 따라 청색, 녹색, 적색 발광 재료와 보다 나은 천연색을 구현하기 위해 필요한 노란색 및 주황색 발광 재료로 구분될 수 있다.A material used as an organic material layer in an organic electroluminescent device can be classified into a light emitting material and a charge transporting material such as a hole injecting material, a hole transporting material, an electron transporting material, and an electron injecting material depending on functions. The light emitting material may be classified into a polymer type and a low molecular type depending on the molecular weight and may be classified into a fluorescent material derived from singlet excited state of electrons and a phosphorescent material derived from the triplet excited state of electrons according to an emission mechanism . Further, the light emitting material can be classified into blue, green, and red light emitting materials and yellow and orange light emitting materials required to realize better natural color depending on the luminescent color.
한편, 발광 재료로서 하나의 물질만 사용하는 경우 분자간 상호 작용에 의하여 최대 발광 파장이 장파장으로 이동하고 색순도가 떨어지거나 발광 감쇄 효과로 소자의 효율이 감소되는 문제가 발생하므로, 색순도의 증가와 에너지 전이를 통한 발광 효율을 증가시키기 위하여 발광 재료로서 호스트-도판트 시스템을 사용할 수 있다.On the other hand, when only one material is used as a light emitting material, there arises a problem that the maximum light emission wavelength shifts to a long wavelength due to intermolecular interaction, the color purity decreases, or the efficiency of the device decreases due to the light emission attenuating effect. A host-dopant system can be used as a light-emitting material in order to increase the light-emitting efficiency through the light-emitting layer.
그 원리는 발광층을 형성하는 호스트보다 에너지 대역 간극이 작은 도판트를 발광층에 소량 혼합하면, 발광층에서 발생한 엑시톤이 도판트로 수송되어 효율이 높은 빛을 내는 것이다. 이때, 호스트의 파장이 도판트의 파장대로 이동하므로, 이용하는 도판트의 종류에 따라 원하는 파장의 빛을 얻을 수 있다.When the dopant having a smaller energy band gap than the host forming the light emitting layer is mixed with a small amount of the light emitting layer, the excitons generated in the light emitting layer are transported to the dopant to emit light with high efficiency. At this time, since the wavelength of the host is shifted to the wavelength band of the dopant, the light of the desired wavelength can be obtained according to the type of the dopant used.
유기전계발광소자가 전술한 우수한 특징들을 충분히 발휘하기 위해서는 소자 내 유기물층을 이루는 물질, 예컨대 정공주입 물질, 정공수송 물질, 발광 물질, 전자수송 물질, 전자주입 물질 등이 안정하고 효율적인 재료에 의하여 뒷받침되는 것이 선행되어야 하나, 아직까지 안정하고 효율적인 유기전계발광소자용 유기물층 재료의 개발이 충분히 이루어지지 않은 상태이다. 따라서, 당 기술분야에서는 새로운 재료의 개발이 계속 요구되고 있는 실정이다.In order for the organic electroluminescent device to sufficiently exhibit the above-described excellent characteristics, materials constituting the organic material layer in the device, such as a hole injecting material, a hole transporting material, a light emitting material, an electron transporting material, and an electron injecting material are supported by a stable and efficient material However, the development of a stable and efficient organic material layer material for an organic electroluminescence device has not been sufficiently developed yet. Therefore, there is a continuing need in the art for the development of new materials.
따라서, 본 발명이 이루고자 하는 첫 번째 기술적 과제는 구동전압이 낮고 발광효율이 우수한 특성을 갖는 피렌 유도체 화합물을 제공하는 것이다.Accordingly, a first technical object of the present invention is to provide a pyrene derivative compound having a low driving voltage and a high luminous efficiency.
본 발명이 이루고자 하는 두 번째 기술적 과제는 상기 피렌 유도체 화합물을 포함하는 유기전계발광소자를 제공하는 것이다.A second object of the present invention is to provide an organic electroluminescent device comprising the pyrene derivative compound.
본 발명은 상기 첫 번째 기술적 과제를 달성하기 위하여, 하기 [화학식 1] 내지 [화학식 5]로 표시되는 피렌 유도체 화합물을 제공한다.In order to accomplish the first technical object, the present invention provides a pyrene derivative compound represented by the following formulas (1) to (5).
[화학식 1] [화학식 2] [화학식 3][Formula 3] < EMI ID =
[화학식 4] [화학식 5][Chemical Formula 4]
상기 [화학식 1] 내지 [화학식 5]에서,In the above Chemical Formulas 1 to 5,
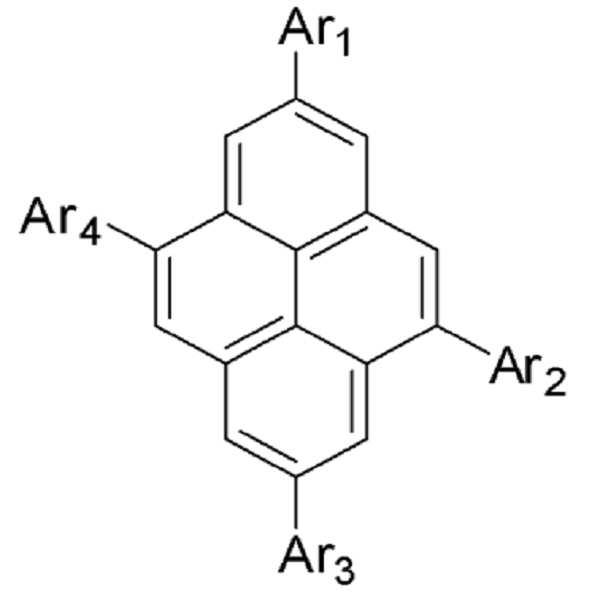
상기 Ar1 내지 Ar6는 서로 동일하거나 상이하고, 각각 독립적으로 수소 원자, 중수소 원자, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 시클로알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬티옥시기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴티옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아민기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기, 치환 또는 비치환된 실리콘기, 치환 또는 비치환된 붕소기, 치환 또는 비치환된 실란기, 카르보닐기, 포스포릴기, 아미노기, 니트릴기, 히드록시기, 니트로기, 할로겐기, 아미드기 및 에스테르기로 이루어진 군에서 선택되며, 서로 인접하는 기와 지방족, 방향족, 지방족헤테로 또는 방향족헤테로의 축합 고리를 형성할 수 있다.Ar 1 to Ar 6 are the same or different from each other and each independently represents a hydrogen atom, a deuterium atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, A substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted cycloalkenyl group having 5 to 30 carbon atoms, a substituted or unsubstituted alkoxy group having 1 to 30 carbon atoms, a substituted or unsubstituted aryloxy group having 6 to 30 carbon atoms , A substituted or unsubstituted alkylthio group having 1 to 30 carbon atoms, a substituted or unsubstituted arylthioxy group having 5 to 30 carbon atoms, a substituted or unsubstituted alkylamine group having 1 to 30 carbon atoms, a substituted or unsubstituted 5 A substituted or unsubstituted aryl group having 5 to 50 carbon atoms, a substituted or unsubstituted heteroaryl group having 3 to 50 carbon atoms having O, N or S, a substituted or unsubstituted hetero atom, a substituted Or a group selected from the group consisting of an unsubstituted silicon group, a substituted or unsubstituted boron group, a substituted or unsubstituted silane group, a carbonyl group, a phosphoryl group, an amino group, a nitrile group, a hydroxyl group, a nitro group, a halogen group, And may form a condensed ring of aliphatic, aromatic, aliphatic hetero or aromatic hetero with adjacent groups.
단, 상기 Ar1 내지 Ar6중 적어도 세 개 이상은 하기 [구조식 1]로 표시되는 구조이다.Provided that at least three or more of Ar 1 to Ar 6 have the structure represented by the following structural formula 1.
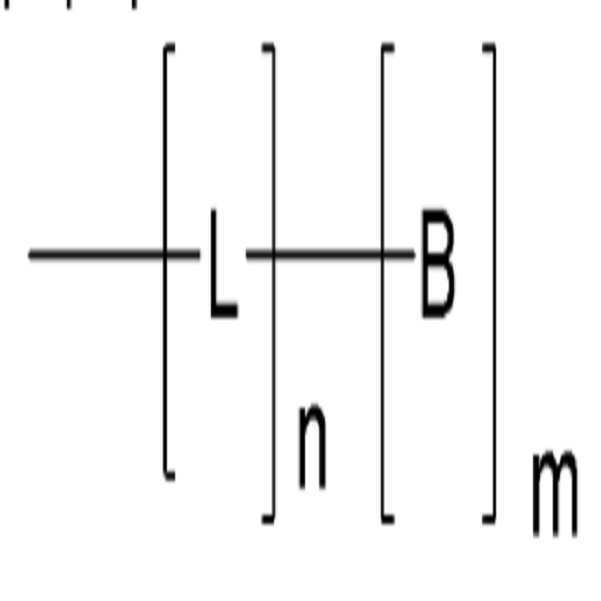
[구조식 1][Structural formula 1]
상기 [구조식 1]에서,In the above formula 1,
상기 n 및 m은 각각 독립적으로 0 또는 1의 정수이고, (단, n+m >1)And n and m are each independently an integer of 0 or 1 (provided that n + m > 1)
상기 L은 2가의 연결기로서 치환 또는 비치환된 탄소수 1 내지 30의 알킬렌기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐렌기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬렌기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴렌기, 치환 또는 비치환된 탄소수 3 내지 50의 헤테로아릴렌기로 이루어진 군에서 선택되며, n 또는 m이 0인 경우 1가의 치환기이며,L is a divalent linking group which is a substituted or unsubstituted alkylene group having 1 to 30 carbon atoms, a substituted or unsubstituted alkenylene group having 2 to 30 carbon atoms, a substituted or unsubstituted cycloalkylene group having 3 to 30 carbon atoms, A substituted or unsubstituted arylene group having 5 to 50 carbon atoms, a substituted or unsubstituted heteroarylene group having 3 to 50 carbon atoms, a monovalent substituent when n or m is 0,
상기 B는 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 시클로알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬티옥시기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴티옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아민기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기, 치환 또는 비치환된 실리콘기, 치환 또는 비치환된 붕소기, 치환 또는 비치환된 실란기, 카르보닐기, 포스포릴기, 아미노기, 니트릴기, 히드록시기, 니트로기, 할로겐기, 아미드기 및 에스테르기로 이루어진 군에서 선택되고, 서로 인접하는 기와 지방족, 방향족, 지방족헤테로 또는 방향족헤테로의 축합 고리를 형성할 수 있다.Wherein B represents a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, a substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted 5 to 30 carbon atoms A substituted or unsubstituted C1-C30 alkoxy group, a substituted or unsubstituted C6-C30 aryloxy group, a substituted or unsubstituted C1-C30 alkylthio group, a substituted or unsubstituted C1-C30 alkoxy group, A substituted or unsubstituted alkylamine group having 1 to 30 carbon atoms, a substituted or unsubstituted arylamine group having 5 to 30 carbon atoms, a substituted or unsubstituted aryloxy group having 5 to 50 carbon atoms, , A substituted or unsubstituted heteroaryl group having 3 to 50 carbon atoms having a hetero atom O, N or S, a substituted or unsubstituted silicon group, a substituted or unsubstituted boron group, a substituted or unsubstituted silane group, A condensed ring of an aliphatic, aromatic, aliphatic hetero or aromatic hetero ring selected from the group consisting of a carbonyl group, a phosphoryl group, an amino group, a nitrile group, a hydroxyl group, a nitro group, a halogen group, an amide group and an ester group, have.
본 발명의 일 실시예에 의하면, 상기 [구조식 1]의 B는 -NR1R2이고, 상기 R1 및 R2는 수소원자, 중수소원자, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기, 에스테르기로 이루어진 군에서 선택되고, 서로 인접하는 기와 지방족, 방향족, 지방족헤테로 또는 방향족헤테로의 축합 고리를 형성할 수 있다.
According to an embodiment of the present invention, B in the structural formula 1 is -NR 1 R 2 , R 1 and R 2 are each a hydrogen atom, a deuterium atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted Or an unsubstituted or substituted aryl group having 5 to 50 carbon atoms, a substituted or unsubstituted heteroaryl group having 3 to 50 carbon atoms having O, N or S, or an ester group, and an aliphatic, aromatic , Aliphatic heteroaromatic, or aromatic heteroaromatic rings.
본 발명은 상기 두 번째 과제를 달성하기 위하여,According to another aspect of the present invention,
애노드, 캐소드 및 상기 애노드와 상기 캐소드 사이에 개재되며, 상기 [화학식 1] 내지 [화학식 5]로 표시되는 피렌 유도체 화합물을 포함하는 유기전계발광소자를 제공한다.An organic electroluminescent device comprising an anode, a cathode, and a pyrene derivative compound interposed between the anode and the cathode and represented by the following Chemical Formulas 1 to 5:
본 발명에 따르면, [화학식 1] 내지 [화학식 5]로 표시되는 피렌 유도체 화합물은 기존 물질에 비하여 안정적이고 우수한 발광 특성을 가지므로 이를 포함하는 유기전계발광소자는 저전압 구동이 가능하고 발광효율을 개선시킬 수 있다.According to the present invention, the pyrene derivative compounds represented by the formulas (1) to (5) have stable and excellent luminescent characteristics as compared with the existing materials, and thus the organic electroluminescent device including the same can be operated at low voltage, .
도 1은 본 발명의 일 구체예에 따른 유기전계발광소자의 개략도이다.1 is a schematic view of an organic electroluminescent device according to one embodiment of the present invention.
이하, 본 발명을 더욱 상세하게 설명한다.Hereinafter, the present invention will be described in more detail.
본 발명은 유기전계소자의 발광층에 포함되는 피렌 유도체 화합물로서, 하기 [화학식 1] 내지 [화학식 5]로 표시되는 화합물인 것을 특징으로 하고, [화학식 1] 내지 [화학식 5]에서, 그 치환기를 보다 구체적으로 설명하면 하기와 같다.The present invention relates to a pyrene derivative compound contained in a light emitting layer of an organic electroluminescent device, which is a compound represented by the following formulas (1) to (5) More specifically, it is as follows.
[화학식 1] [화학식 2] [화학식 3][Formula 3] < EMI ID =
[화학식 4] [화학식 5][Chemical Formula 4]
상기 [화학식 1] 내지 [화학식 5]에서,In the above Chemical Formulas 1 to 5,
Ar1 내지 Ar6는 서로 동일하거나 상이하고, 각각 독립적으로 수소 원자, 중수소 원자, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 3 내지30의 시클로알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 시클로알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬티옥시기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴티옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아민기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기, 치환 또는 비치환된 실리콘기, 치환 또는 비치환된 붕소기, 치환 또는 비치환된 실란기, 카르보닐기, 포스포릴기, 아미노기, 니트릴기, 히드록시기, 니트로기, 할로겐기, 아미드기 및 에스테르기로 이루어진 군에서 선택되며, 서로 인접하는 기와 지방족, 방향족, 지방족헤테로 또는 방향족헤테로의 축합 고리를 형성할 수 있다.Ar 1 to Ar 6 are the same or different from each other and each independently represents a hydrogen atom, a deuterium atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, A substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted cycloalkenyl group having 5 to 30 carbon atoms, a substituted or unsubstituted alkoxy group having 1 to 30 carbon atoms, a substituted or unsubstituted aryloxy group having 6 to 30 carbon atoms, A substituted or unsubstituted alkylthio group having 1 to 30 carbon atoms, a substituted or unsubstituted arylthioxy group having 5 to 30 carbon atoms, a substituted or unsubstituted alkylamine group having 1 to 30 carbon atoms, A substituted or unsubstituted aryl group having 5 to 50 carbon atoms, a substituted or unsubstituted heteroaryl group having 3 to 50 carbon atoms having O, N or S, a substituted or unsubstituted heteroaryl group, a substituted or unsubstituted heteroaryl group having 1 to 30 carbon atoms, A substituted or unsubstituted silane group, a carbonyl group, a phosphoryl group, an amino group, a nitrile group, a hydroxyl group, a nitro group, a halogen group, an amide group and an ester group, , To form a condensed ring of aliphatic, aromatic, aliphatic hetero or aromatic hetero with adjacent groups.
단, 상기 Ar1 내지 Ar6중 적어도 세 개 이상은 하기 [구조식 1]로 표시되는 구조이다.Provided that at least three or more of Ar 1 to Ar 6 have the structure represented by the following structural formula 1.
[구조식 1][Structural formula 1]
상기 [구조식 1]에서,In the above formula 1,
n 및 m은 각각 독립적으로 0 또는 1의 정수이고, (단, n+m >1)n and m are each independently an integer of 0 or 1 (provided that n + m > 1)
L은 2가의 연결기로서 치환 또는 비치환된 탄소수 1 내지 30의 알킬렌기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐렌기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬렌기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴렌기, 치환 또는 비치환된 탄소수 3 내지 50의 헤테로아릴렌기로 이루어진 군에서 선택되며, n 또는 m이 0인 경우 1가의 치환기이며,L is a divalent linking group which is a substituted or unsubstituted alkylene group having 1 to 30 carbon atoms, a substituted or unsubstituted alkenylene group having 2 to 30 carbon atoms, a substituted or unsubstituted cycloalkylene group having 3 to 30 carbon atoms, A substituted or unsubstituted arylene group having 5 to 50 carbon atoms, a substituted or unsubstituted heteroarylene group having 3 to 50 carbon atoms, a monovalent substituent when n or m is 0,
B는 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 2 내지 30의 알케닐기, 치환 또는 비치환된 탄소수 3 내지 30의 시클로알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 시클로알케닐기, 치환 또는 비치환된 탄소수 1 내지 30의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 30의 아릴옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬티옥시기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴티옥시기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬아민기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기, 치환 또는 비치환된 실리콘기, 치환 또는 비치환된 붕소기, 치환 또는 비치환된 실란기, 카르보닐기, 포스포릴기, 아미노기, 니트릴기, 히드록시기, 니트로기, 할로겐기, 아미드기 및 에스테르기로 이루어진 군에서 선택되고, 서로 인접하는 기와 지방족, 방향족, 지방족헤테로 또는 방향족헤테로의 축합 고리를 형성할 수 있다.B represents a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted alkenyl group having 2 to 30 carbon atoms, a substituted or unsubstituted cycloalkyl group having 3 to 30 carbon atoms, a substituted or unsubstituted group having 5 to 30 carbon atoms A substituted or unsubstituted C1-C30 alkoxy group, a substituted or unsubstituted C6-C30 aryloxy group, a substituted or unsubstituted C1-C30 alkylthio group, a substituted or unsubstituted C1-C30 alkoxy group, A substituted or unsubstituted alkylamine group having 1 to 30 carbon atoms, a substituted or unsubstituted arylamine group having 5 to 30 carbon atoms, a substituted or unsubstituted aryl group having 5 to 50 carbon atoms, A substituted or unsubstituted heteroaryl group having 3 to 50 carbon atoms having a hetero atom O, N or S, a substituted or unsubstituted silicon group, a substituted or unsubstituted boron group, a substituted or unsubstituted silane group, A condensed ring of an aliphatic, aromatic, aliphatic hetero or aromatic hetero with an adjacent group selected from the group consisting of an alkyl group, an aryl group, a heteroaryl group, a heteroaryl group, a heteroaryl group, a heteroaryl group, .
상기 [구조식 1]의 B는 -NR1R2이고, 상기 R1 및 R2는 수소원자, 중수소원자, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기, 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기, 에스테르기로 이루어진 군에서 선택되고, 서로 인접하는 기와 지방족, 방향족, 지방족헤테로 또는 방향족헤테로의 축합 고리를 형성할 수 있다.B in the above formula 1 is -NR 1 R 2 , R 1 and R 2 are each a hydrogen atom, a deuterium atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted group having 5 to 50 carbon atoms An aryl group, a substituted or unsubstituted heteroaryl group having 3 to 50 carbon atoms having O, N or S as a hetero atom, an ester group, and a condensed ring of an aliphatic, aromatic, aliphatic hetero or aromatic hetero, Can be formed.
본 발명에 있어서, "치환 또는 비치환된"이라는 용어는 시아노기, 할로겐기, 히드록시기, 니트로기, 알킬기, 알콕시기, 알킬아미노기, 아릴아미노기, 헤테로 아릴아미노기, 알킬실릴기, 아릴실릴기, 아릴옥시기, 아릴기, 헤테로아릴기, 게르마늄, 인, 보론, 수소 및 중수소로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환되는 것을 의미한다.In the present invention, the term "substituted or unsubstituted" means a group selected from the group consisting of a cyano group, a halogen group, a hydroxyl group, a nitro group, an alkyl group, an alkoxy group, an alkylamino group, an arylamino group, a heteroarylamino group, an alkylsilyl group, Substituted or unsubstituted with at least one substituent selected from the group consisting of an oxygen atom, an aryl group, a heteroaryl group, germanium, phosphorus, boron, hydrogen and deuterium.
또한, 상기의 [화학식 1]에 따른 피렌 유도체 화합물에 대한 보다 구체적인 예에 의해서 본 발명의 범위가 이에 제한되는 것은 아니지만, 보다 구체적으로 하기 [화학식 1] 내지 [화학식 5]로 표시되는 화합물은 하기 [화학식 6] 내지 [화학식 97]으로 표시되는 군으로부터 선택되는 어느 하나일 수 있다.Further, although the range of the present invention is not limited by the more specific examples of the pyrene derivative compound according to the above formula (1), more specifically, the compounds represented by the following formulas (1) to (5) May be any one selected from the group consisting of formulas (6) to (97).
[화학식 6] [화학식 7] [화학식 8][Chemical Formula 7] < EMI ID =
[화학식 9] [화학식 10] [화학식 11][Chemical Formula 10] < EMI ID =
[화학식 12] [화학식 13][Chemical Formula 12]
[화학식 14] [화학식 15][Chemical Formula 14]
[화학식 16] [화학식 17][Chemical Formula 16]
[화학식 18] [화학식 19] [화학식 20][Chemical Formula 19] [Chemical Formula 20]
[화학식 21] [화학식 22] [화학식 23][Chemical Formula 21]
[화학식 24] [화학식 25] [화학식 26][Chemical Formula 25]
[화학식 27] [화학식 28] [화학식 29][Chemical Formula 27]
[화학식 30] [화학식 31] [화학식 32][Chemical Formula 32]
[화학식 33] [화학식 34][Chemical Formula 33]
[화학식 35] [화학식 36] [화학식 37][Chemical Formula 35]
[화학식 38] [화학식 39] [화학식 40][Chemical Formula 38] [Chemical Formula 39]
[화학식 41] [화학식 42] [화학식 43][Chemical Formula 41]
[화학식 44] [화학식 45] [화학식 46][Chemical Formula 45]
[화학식 47] [화학식 48] [화학식 49][Chemical Formula 48] [Chemical Formula 48]
[화학식 50] [화학식 51] [화학식 52] [화학식 53][Chemical Formula 51] [Chemical Formula 52] [Chemical Formula 53]
[화학식 54] [화학식 55] [화학식 56] [화학식 57][Chemical Formula 55] [Chemical Formula 55] [Chemical Formula 55]
[화학식 58] [화학식 59] [화학식 60] [화학식 61][Chemical Formula 60] [Chemical Formula 61]
[화학식 62] [화학식 63] [화학식 64] [화학식 65][Chemical Formula 62] [Chemical Formula 65] [Chemical Formula 65]
[화학식 66] [화학식 67] [화학식 68] [화학식 69][Chemical Formula 67] [Chemical Formula 68] [Chemical Formula 69]
[화학식 70] [화학식 71] [화학식 72] [화학식 73][Chemical Formula 71] [Chemical Formula 72] [Chemical Formula 73]
[화학식 74] [화학식 75] [화학식 76] [화학식 77][Chemical Formula 75] [Chemical Formula 76] [Chemical Formula 77]
[화학식 78] [화학식 79] [화학식 80] [화학식 81][Formula 79] [Formula 80] [Formula 81]
[화학식 82] [화학식 83] [화학식 84] [화학식 85] [Chemical Formula 82]
[화학식 86] [화학식 87] [화학식 88] [화학식 89] [Chemical Formula 88] [Chemical Formula 88] [Chemical Formula 89]
[화학식 90] [화학식 91] [화학식 92] [화학식 93][Chemical Formula 91] [Chemical Formula 92] [Chemical Formula 93]
[화학식 94] [화학식 95] [화학식 96] [화학식 97][Chemical Formula 95] [Chemical Formula 96] [Chemical Formula 97]
또한, 본 발명은 애노드, 캐소드 및 상기 애노드와 상기 캐소드 사이에 개재되며, 상기 [화학식 1] 내지 [화학식 5]로 표시되는 피렌 유도체 화합물을 포함하는 유기전계발광 소자를 제공한다.Also, the present invention provides an organic electroluminescent device comprising an anode, a cathode, and a pyrene derivative compound interposed between the anode and the cathode, and represented by the above Chemical Formulas 1 to 5.
이때, 상기 신규한 화합물이 포함된 층은 상기 애노드 및 캐소드 사이의 발광층인 것이 바람직하며, 애노드 및 캐소드 사이에는 정공주입층, 정공수송층, 전자저지층, 정공저지층, 전자수송층 및 전자주입층으로 이루어진 군으로부터 선택된 하나 이상의 층을 더 포함할 수 있다.In this case, the layer containing the novel compound is preferably a light emitting layer between the anode and the cathode, and a hole injecting layer, a hole transporting layer, an electron blocking layer, a hole blocking layer, an electron transporting layer and an electron injecting layer And at least one layer selected from the group consisting of
또한, 본 발명의 다른 일 실시예에 의하면, 상기 발광층의 두께는 50 내지 2,000 Å인 것이 바람직하고, 상기 발광층은 다양한 인광 호스트 물질을 추가로 포함할 수 있다.In addition, according to another embodiment of the present invention, the thickness of the light emitting layer is preferably 50 to 2,000 ANGSTROM, and the light emitting layer may further include various phosphorescent host materials.
구체적인 예로서, 정공수송층(HTL, Hole Transport Layer)이 추가로 적층되어 있고, 상기 캐소드와 상기 유기발광층 사이에 전자수송층(ETL, Electron Transport Layer)이 추가로 적층되어 있는 것일 수 있는데, 상기 정공수송층은 애노드로부터 정공을 주입하기 쉽게 하기 위하여 적층되는 것으로서, 상기 정공수송층의 재료로는 이온화 포텐셜이 작은 전자공여성 분자가 사용되는데, 주로 트리페닐아민을 기본 골격으로 하는 디아민, 트리아민 또는 테트라아민 유도체가 많이 사용되고 있다.As a specific example, a hole transport layer (HTL) may be further stacked, and an electron transport layer (ETL) may be further stacked between the cathode and the organic emission layer. An electron donor molecule having a low ionization potential is used as the material of the hole transport layer. A diamine, triamine or tetraamine derivative having a basic skeleton of triphenylamine is used as the hole transport layer. It is widely used.
본 발명에서도 상기 정공수송층의 재료로서 당업계에 통상적으로 사용되는 것인 한 특별히 제한되지 않으며, 예를 들어, N,N'-비스(3-메틸페닐)-N,N'-디페닐-[1,1-비페닐]-4,4'-디아민(TPD) 또는 N,N'-디(나프탈렌-1-일)-N,N'-디페닐벤지딘 (a-NPD) 등을 사용할 수 있다.In the present invention, the material for the hole transport layer is not particularly limited as long as it is commonly used in the art. For example, N, N'-bis (3-methylphenyl) -N, N'- , 1-biphenyl] -4,4'-diamine (TPD) or N, N'-di (naphthalene-1-yl) -N, N'-diphenylbenzidine (a-NPD).
상기 정공수송층의 하부에는 정공주입층(HIL, Hole Injecting Layer)을 추가적으로 더 적층할 수 있는데, 상기 정공주입층 재료 역시 당업계에서 통상적으로 사용되는 것인 한 특별히 제한되지 않고 사용할 수 있으며, 예를 들어 CuPc(copperphthalocyanine) 또는 스타버스트형 아민류인 TCTA(4,4',4"-tri(N-carbazolyl)triphenyl-amine), m-MTDATA(4,4',4"-tris-(3-methylphenylphenyl amino)triphenylamine) 등을 사용할 수 있다.A hole injection layer (HIL) may be additionally formed on the lower portion of the hole transport layer. The material for the hole injection layer is not particularly limited as long as it is commonly used in the art. For example, (4,4 ', 4 "-tri (N-carbazolyl) triphenylamine), m-MTDATA (4,4', 4" -tris- (3-methylphenylphenyl amino) triphenylamine) can be used.
또한, 본 발명에 따른 유기전계발광소자에 사용되는 상기 전자수송층은 캐소드로부터 공급된 전자를 유기발광층으로 원활히 수송하고 상기 유기발광층에서 결합하지 못한 정공의 이동을 억제함으로써 발광층 내에서 재결합할 수 있는 기회를 증가시키는 역할을 한다.In addition, the electron transport layer used in the organic electroluminescent device according to the present invention can transport electrons supplied from the cathode smoothly to the organic luminescent layer and inhibit the movement of holes which are not bonded in the organic luminescent layer, .
상기 전자수송층 재료로는 당 기술분야에서 통상적으로 사용되는 것이면 특별히 제한되지 않고 사용할 수 있음은 물론이며, 예를 들어 옥사디아졸 유도체인 PBD, BMD, BND 또는 Alq3 등을 사용할 수 있다.The material of the electron transport layer is not particularly limited as long as it is commonly used in the art. For example, oxadiazole derivative PBD, BMD, BND or Alq 3 can be used.
한편, 상기 전자수송층의 상부에는 캐소드로부터의 전자 주입을 용이하게 해주어 궁극적으로 파워효율을 개선 시키는 기능을 수행하는 전자주입층(EIL, Electron Injecting Layer)을 더 적층시킬 수도 있는데, 상기 전자주입층 재료 역시 당 기술분야에서 통상적으로 사용되는 것이면 특별한 제한없이 사용할 수 있으며, 예를 들어, LiF, NaCl, CsF, Li2O, BaO 등의 물질을 이용할 수 있다.Meanwhile, an electron injection layer (EIL) may be further formed on the electron transport layer to facilitate injection of electrons from the cathode to ultimately improve power efficiency. The electron injection layer material As long as it is commonly used in the art, it can be used without any particular limitation. For example, materials such as LiF, NaCl, CsF, Li 2 O, and BaO can be used.
본 발명에 따른 유기전계발광소자는 표시소자, 디스플레이 소자 및 단색 또는 백색 조명용 소자 등에 사용될 수 있다.The organic electroluminescent device according to the present invention can be used for a display device, a display device, an element for a single color or a white light, and the like.
도 1은 본 발명의 유기전계발광소자의 구조를 나타내는 단면도이다. 본 발명에 따른 유기전계발광소자는 애노드(20), 정공수송층(40), 유기발광층(50), 전자수송층(60) 및 캐소드(80)을 포함하며, 필요에 따라 정공주입층(30)과 전자주입층(70)을 더 포함할 수 있으며, 그 이외에도 1층 또는 2층의 중간층을 더 형성하는 것도 가능하며, 정공저지층 또는 전자저지층을 더 형성시킬 수도 있다.1 is a cross-sectional view showing the structure of an organic electroluminescent device of the present invention. The organic electroluminescent device according to the present invention includes an
도 1을 참조하여 본 발명의 유기전계발광소자 및 그 제조방법에 대하여 살펴보면 다음과 같다. 먼저 기판(10) 상부에 애노드 전극용 물질을 코팅하여 애노드(20)를 형성한다. 여기에서 기판(10)으로는 통상적인 유기 EL 소자에서 사용되는 기판을 사용하는데 투명성, 표면 평활성, 취급용이성 및 방수성이 우수한 유기 기판 또는 투명 플라스틱 기판이 바람직하다. 그리고, 애노드 전극용 물질로는 투명하고 전도성이 우수한 산화인듐주석(ITO), 산화인듐아연(IZO), 산화주석(SnO2), 산화아연(ZnO) 등을 사용한다.The organic electroluminescent device of the present invention and its manufacturing method will be described with reference to FIG. First, an anode electrode material is coated on the
상기 애노드(20) 전극 상부에 정공 주입층 물질을 진공열 증착, 또는 스핀 코팅하여 정공주입층(30)을 형성한다. 그 다음으로 상기 정공주입층(30)의 상부에 정공수송층 물질을 진공 열증착 또는 스핀 코팅하여 정공수송층(40)을 형성한다.A
이어서, 상기 정공수송층(40)의 상부에 유기발광층(50)을 적층하고 상기 유기발광층(50)의 상부에 선택적으로 정공저지층(미도시)을 진공 증착 방법, 또는 스핀 코팅 방법으로서 박막을 형성할 수 있다. 상기 정공저지층은 정공이 유기발광층을 통과하여 캐소드로 유입되는 경우에는 소자의 수명과 효율이 감소되기 때문에 HOMO(Highest Occupied Molecular Orbital) 레벨이 매우 낮은 물질을 사용함으로써 이러한 문제를 방지하는 역할을 한다. 이 때, 사용되는 정공 저지 물질은 특별히 제한되지는 않으나 전자수송능력을 가지면서 발광 화합물보다 높은 이온화 포텐셜을 가져야 하며 대표적으로 BAlq, BCP, TPBI 등이 사용될 수 있다.A hole blocking layer (not shown) is selectively formed on the organic
이러한 정공저지층 위에 전자수송층(60)을 진공 증착 방법, 또는 스핀 코팅 방법을 통해 증착한 후에 전자주입층(70)을 형성하고 상기 전자주입층(70)의 상부에 캐소드 형성용 금속을 진공 열증착하여 캐소드(80) 전극을 형성함으로써 유기 EL 소자가 완성된다. 여기에서 캐소드 형성용 금속으로는 리튬(Li), 마그네슘(Mg), 알루미늄(Al), 알루미늄-리듐(Al-Li), 칼슘(Ca), 마그네슘-인듐(Mg-In), 마그네슘-은(Mg-Ag) 등을 사용할 수 있으며, 전면 발광 소자를 얻기 위해서는 ITO, IZO를 사용한 투과형 캐소드를 사용할 수 있다.After the
또한, 본 발명의 다른 일실시예에 의하면, 상기 정공주입층, 정공수송층, 전자저지층, 발광층, 정공저지층, 전자수송층 및 전자주입층으로부터 선택된 하나 이상의 층은 단분자 증착방식 또는 용액공정에 의하여 형성될 수 있으며, 본 발명에 따른 유기전계발광소자는 표시소자, 디스플레이 소자 및 단색 또는 백색 조명용 소자에 사용될 수 있다.
According to another embodiment of the present invention, at least one layer selected from the hole injecting layer, the hole transporting layer, the electron blocking layer, the light emitting layer, the hole blocking layer, the electron transporting layer and the electron injecting layer is formed by a single molecular deposition method or a solution process And the organic electroluminescent device according to the present invention can be used for a display device, a display device, and a monochromatic or white illumination device.
이하, 바람직한 실시예를 들어 본 발명을 더욱 상세하게 설명한다. 그러나, 이들 실시예는 본 발명을 보다 구체적으로 설명하기 위한 것으로, 본 발명의 범위가 이에 의하여 제한되지 않는다는 것은 당업계의 통상의 지식을 가진 자에게 자명할 것이다.
Hereinafter, the present invention will be described in more detail with reference to preferred embodiments. It will be apparent, however, to those skilled in the art that these embodiments are for further explanation of the present invention and that the scope of the present invention is not limited thereby.
<실시예><Examples>
합성예 1. 중간체 합성Synthesis Example 1. Synthesis of intermediate
(1) 2,7,-다이아이오도-3,8-다이페닐-피렌의 합성(1) Synthesis of 2,7-diiodo-3,8-diphenyl-pyrene
(1-1) 2-브로모바이페닐아세틸렌의 합성(1-1) Synthesis of 2-bromobiphenylacetylene
2-브로모-아이오도-벤젠(10 g, 35 mmol), Pd(PPh3)4(0.8 g, 0.5 mmol), CuI(0.54 g, 1 mmol)을 트리에틸아민 50 mL에 넣고 상온에서 교반하며 잘 섞어 주었다.(반응은 질소 분위기에서 진행), 페닐아세틸렌(3.6 mL, 35 mmol)을 천천히 넣어 주었다.To a solution of 2-bromo-iodo-benzene (10 g, 35 mmol), Pd (PPh3) 4 (0.8 g, 0.5 mmol) and CuI (0.54 g, 1 mmol) in 50 mL of triethylamine was stirred at room temperature (Reaction proceeded in nitrogen atmosphere) and phenylacetylene (3.6 mL, 35 mmol) was slowly added.
상온에서 1 시간 정도 교반 후 헥산 300 mL를 넣어 반응을 종결하였으며, 용액 전체를 실리카켈에 통과시켜 생성물을 분리하고, 헥산 500 mL로 컬럼을 마저 내렸다. 용매를 제거하여 흰색의 생성물을 얻었다.(수율 98%)After stirring for about 1 hour at room temperature, 300 mL of hexane was added to terminate the reaction. The whole solution was passed through silica gel to separate the product, and the column was further drained with 500 mL of hexane. The solvent was removed to give a white product (yield: 98%).
MS(MALDI-TOF): m/z 257 [M]+
MS (MALDI-TOF): m / z 257 [M] < + &
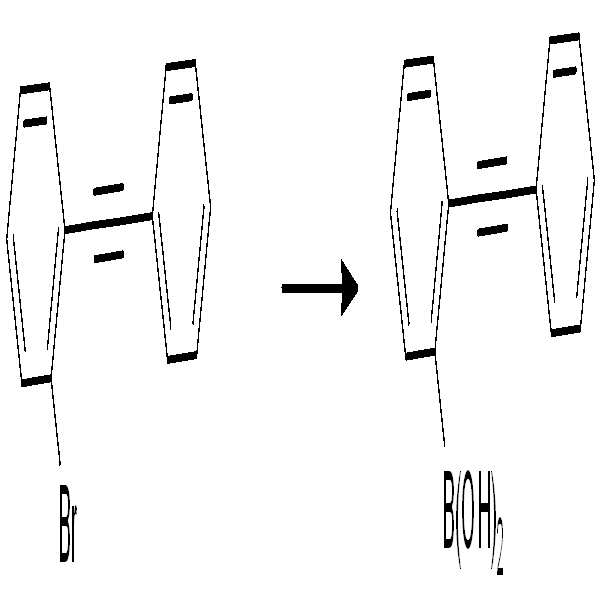
(1-2) 2-바이페닐아세틸렌 보로닉산의 합성(1-2) Synthesis of 2-biphenylacetylenevoronic acid
2-브로모바이페닐아세틸렌(10 g, 55 mmol)을 THF 100 mL에 녹였다. -78 ℃까지 냉각시킨 상태에서 n-BuLi(50 mL)를 천천히 넣어 주었다. 첨가가 끝나면 -78 ℃에서 1 시간 가량 교반 후 트리메틸 보레이트(6.57 g, 63 mmol)을 넣어 주었다. -78 ℃에서 1 시간 교반 후 2 시간 가량 상온에서 교반하고 2 N HCl을 넣어 산성을 맞추었다. EA로 추출 후 용매 제거하고 헥산에 희석시켜 -78 ℃에서 교반시켜 고체화하여 흰색 고체를 얻었다. (수율 70%)2-Bromobiphenylacetylene (10 g, 55 mmol) was dissolved in 100 mL of THF. The n-BuLi (50 mL) was added slowly while cooling to -78 ° C. After the addition, trimethylborate (6.57 g, 63 mmol) was added at -78 ° C for about 1 hour. After stirring at -78 ° C for 1 hour, the mixture was stirred at room temperature for 2 hours, and 2N HCl was added to adjust the acidity. After the extraction with EA, the solvent was removed, and the solution was diluted with hexane and stirred at -78 ° C to solidify to obtain a white solid. (70% yield)
MS(MALDI-TOF): m/z 257[M]+
MS (MALDI-TOF): m / z 257 [M] < + &
(1-3) 2,2'-다이페닐에티닐바이페닐의 합성(1-3) Synthesis of 2,2'-diphenylethynylbiphenyl
2-브로모바이페닐아세틸렌(10 g, 55 mmol), 2-바이페닐아세틸렌 보로닉산(9.5 g, 43 mmol), K2CO3(10.75 g, 78 mmol), Pd(PPh3)4(0.9 g, 1 mmol)을 toluene 100 mL, THF 100 mL, H2O 50 mL 혼합용액에 넣고 reflux시켰다. 반응이 끝나면 층분리하여 유기용매 제거하고, 컬럼분리로 생성물 분리(MC:Hx=1:9)하였다.(수율 70%)(9.5 g, 43 mmol), K2CO3 (10.75 g, 78 mmol) and Pd (PPh3) 4 (0.9 g, 1 mmol) were added to a solution of 2-bromobiphenylacetylene (10 g, 55 mmol) Was added to a mixed solution of 100 mL of toluene, 100 mL of THF, and 50 mL of H2O and refluxed. After the reaction was completed, the organic solvent was removed by layer separation, and the product was separated by column separation (MC: Hx = 1: 9) (yield 70%).
MS(MALDI-TOF): m/z 254[M]+
MS (MALDI-TOF): m / z 254 [M] < + &
(1-4) 2,7-다이아이오도-3,8-다이페닐-피렌(1-4) 2,7-diiodo-3,8-diphenyl-pyrene
2,2'-다이페닐에티닐바이페닐(10 g, 28 mmol)을 MC 100 mL에 녹였다. 상온에서 ICl (1M in MC)을 68 mL를 천천히 넣어 주었다. 상온에서 1 시간 교반 후 포화 Na2S2O3로 아이오딘을 제거하고 EA 추출하였다. Column(MC:Hx=1:9)으로 생성물 분리하였다.(수율 60%)2,2'-diphenylethynylbiphenyl (10 g, 28 mmol) was dissolved in 100 mL of MC. 68 mL of ICl (1M in MC) was slowly added at room temperature. After stirring at room temperature for 1 hour, iodine was removed with saturated Na2S2O3 and extracted with EA. The product was isolated by column (MC: Hx = 1: 9) (yield 60%).
MS(MALDI-TOF): m/z 606[M]+
MS (MALDI-TOF): m / z 606 [M] < + &
(2) 5,10-다이브로모-2,7-다이페닐-피렌의 합성(2) Synthesis of 5,10-dibromo-2,7-diphenyl-pyrene
(2-1) 4,4'-다이브로모-2,2'-다이니트로-바이페닐의 합성.(2-1) Synthesis of 4,4'-dibromo-2,2'-dinitro-biphenyl.
2,5-다이브로모니트로벤젠 250 g(0.890 mol), Copper powder 135.74 g(2.136 mol)과 DMF 1L를 넣었다. 반응기의 온도를 125 ℃로 승온하여 3 시간 동안 교반시켰다. 반응이 종료되면 온도를 실온으로 낮추고, Toluene 500 mL를 넣고 교반시켰다. 녹지않은 무기염을 celite filter하여 제거하고 여액을 건조시켰다. 건조된 여액에 Methanol 2 L를 넣고 강하게 교반시켰다. 생성된 결정을 여과하고 다시 Toluene 500 mL에 녹였다. 다시 남아있는 무기염을 celite filter하여 제거한 후, 여액을 건조시키고 다시 MeOH를 넣고 강하게 교반시켜 재결정여 4,4'-다이브로모-2,2'-다이니트로-바이페닐 139 g(77.7%)을 얻었다.250 g (0.890 mol) of 2,5-dibromonitrobenzene, 135.74 g (2.136 mol) of copper powder and 1 L of DMF were placed. The temperature of the reactor was raised to 125 캜 and stirred for 3 hours. When the reaction was completed, the temperature was lowered to room temperature, 500 mL of toluene was added, and the mixture was stirred. The insoluble inorganic salts were removed by celite filtration and the filtrate was dried. To the dried filtrate, 2 L of methanol was added and stirred vigorously. The resulting crystals were filtered and dissolved again in 500 mL of toluene. The remaining inorganic salts were removed by celite filtering, and the filtrate was dried. MeOH was added thereto and stirred vigorously to obtain 139 g (77.7%) of 4,4'-dibromo-2,2'-dinitro- .
MS(MALDI-TOF): m/z 402[M]+
MS (MALDI-TOF): m / z 402 [M] < + &
(2-2) 4,4'-다이브로모-2,2'-다이아미노바이페닐의 합성(2-2) Synthesis of 4,4'-dibromo-2,2'-diaminobiphenyl
4,4'-다이브로모-2,2'-다이니트로-바이페닐 139.7 g(0.347 mol)을 넣고 Ethanol 2 L을 넣었다. 그리고 12 M HCl 1 L를 넣고 교반시켰다. 반응기의 온도를 0 ℃로 낮추고 Tin powder 165 g(1.39 mol)을 20 분에 걸쳐서 천천히 넣었다. 반응기의 온도를 100 ℃로 승온하고 3 시간 동안 환류시켰다. 반응이 종료되면 반응기의 온도를 0 ℃로 낮추고 Sodium hydroxide 수용액 12 M 1 L를 천천히 넣어 반응액을 염기성으로 만들었다. Ethylacetate를 넣어 추출하여 유기층을 분리하고 유기층을 무수처리하여 농축하였다. 헥산과 메틸렌클로라이드를 전개용매로 사용하여 컬럼크로마토그래피로 분리하여 4,4'-다이브로모-2,2'-다이아미노바이페닐을 얻었다.(87.7 g, 73.8 %)139.7 g (0.347 mol) of 4,4'-dibromo-2,2'-dinitro-biphenyl was added and 2 L of ethanol was added. Then 1 L of 12 M HCl was added and stirred. The temperature of the reactor was lowered to 0 ° C and 165 g (1.39 mol) of Tin powder was added slowly over 20 minutes. The temperature of the reactor was raised to 100 ° C and refluxed for 3 hours. When the reaction was completed, the temperature of the reactor was lowered to 0 ° C. and 12 M 1 L of sodium hydroxide aqueous solution was slowly added to make the reaction solution basic. Ethylacetate was added to extract the organic layer, and the organic layer was dried and concentrated. (87.7 g, 73.8%) of 4,4'-dibromo-2,2'-diaminobiphenyl was obtained by separating by column chromatography using hexane and methylene chloride as eluent.
MS(MALDI-TOF): m/z 342[M]+
MS (MALDI-TOF): m / z 342 [M] < + &
(2-3) 4,4'-다이브로모-2,2'-다이아이오도바이페닐의 합성(2-3) Synthesis of 4,4'-dibromo-2,2'-diiodobiphenyl
4,4'-다이브로모-2,2'-다이아미노바이페닐 87.7 g(0.256 mol), 12 M HCl 380 mL, 물 380 mL를 넣었다. 반응기의 온도를 0 ℃로 낮추었다. Sodiumnitrite 44.2 g(0.641 mol)을 물 220 mL에 녹여 반응기에 천천히 적가하고, 적가가 완료되면 1 시간 동안 동일 온도에서 1 시간 동안 교반시켰다. Potassium iodide를 물 850 mL에 녹여 천천히 적가하고, 적가가 완료되면 상온에서 1 시간 동안 교반시켰다. 그리고 반응기의 온도를 60 ℃로 승온하여 3 시간 더 교반시켰다. 반응이 완료되면 실온으로 낮추고 Ethylacetate를 이용하여 추출하여 유기층을 분리하였다. 분리된 유기층을 무수처리하고 건조시킨 후 헥산을 전개용매로 사용하여 컬럼크로마토그래피로 분리하여 4,4'-다이브로모-2,2'-다이아이오도바이페닐을 42.1g (29.1 %)얻었다.87.7 g (0.256 mol) of 4,4'-dibromo-2,2'-diaminobiphenyl, 380 mL of 12 M HCl, and 380 mL of water. The temperature of the reactor was lowered to 0 ° C. Sodium nitrite (44.2 g, 0.641 mol) was dissolved in 220 mL of water and slowly added dropwise to the reactor. When the dropwise addition was completed, the mixture was stirred at the same temperature for 1 hour. Potassium iodide was dissolved in 850 mL of water and slowly added dropwise. When the dropwise addition was completed, the solution was stirred at room temperature for 1 hour. The temperature of the reactor was raised to 60 DEG C and stirred for 3 hours. When the reaction was complete, the mixture was cooled to room temperature and extracted with Ethylacetate to separate the organic layer. The separated organic layer was dried over anhydrous, dried and then subjected to column chromatography using hexane as a developing solvent to obtain 42.1 g (29.1%) of 4,4'-dibromo-2,2'-diiodobiphenyl.
MS(MALDI-TOF): m/z 563[M]+
MS (MALDI-TOF): m / z 563 [M] < + &
(2-4) 4,4'-다이브로모-2,2'-다이페닐에티닐바이페닐의 합성(2-4) Synthesis of 4,4'-dibromo-2,2'-diphenylethynylbiphenyl
500 mL 둥근 바닥 플라스크에 질소기류하에서 4,4'-다이브로모-2,2'-다이아이오도바이페닐 20 g(0.036 mol)과 Copper iodide 0.7 g(0.0035 mol), Pd(PPh3)4 1.6 g(0.0014 mol)을 넣고 Triethyl amine 200 mL에 녹였다. 반응기에 Phenylacetylene 9.3 g(0.085 mol)을 천천히 적가하고 1 시간 동안 교반시켰다. 반응이 종료되면 MC에 녹여 Celite와 Silica를 이용하여 filter하였다. 여액을 건조시키고 헥산을 전개용매로 사용하여 컬럼크로마토그래피로 분리하여 얻은 4,4'-다이브로모-2,2'-다이페닐에티닐바이페닐을 13.5 g (74.3 %) 얻었다.(0.036 mol) of 4,4'-dibromo-2,2'-diiodobiphenyl and 0.7 g (0.0035 mol) of copper iodide and 1.6 g (0.0014 mol) of Pd (PPh3) 4 in a 500 mL round- mol) was dissolved in 200 mL of triethyl amine. 9.3 g (0.085 mol) of phenylacetylene was slowly added dropwise to the reactor and stirred for 1 hour. After the reaction was completed, it was dissolved in MC and filtered using Celite and Silica. The filtrate was dried, and 13.5 g (74.3%) of 4,4'-dibromo-2,2'-diphenylethynylbiphenyl obtained by column chromatography using hexane as eluent was obtained.
MS(MALDI-TOF): m/z 512[M]+
MS (MALDI-TOF): m / z 512 [M] +
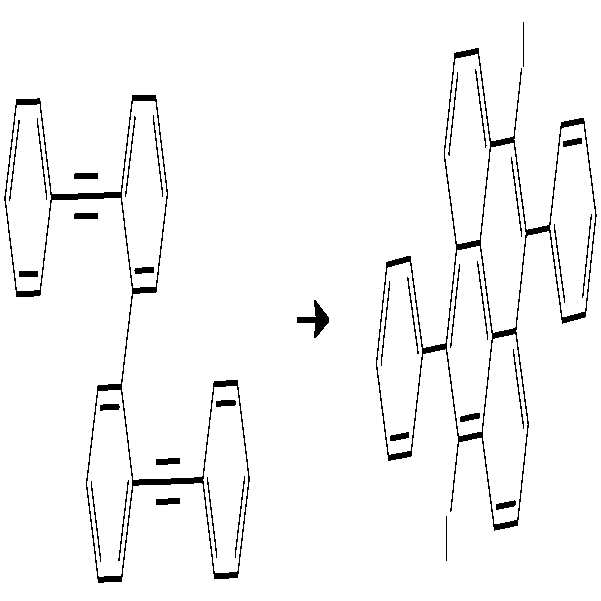
(2-5) 5,10-다이브로모-2,7-다이페닐-피렌의 합성(2-5) Synthesis of 5,10-dibromo-2,7-diphenyl-pyrene
250 mL 반응기에 질소 기류하에서 4,4'-다이브로모-2,2'-다이페닐에티닐바이페닐 12.3 g(0.024 mol)을 넣고 Dichloroethane 120 mL에 녹였다. Iron(III) trifluoro-methansulfonate 1.2 g(0.002 mol)을 넣고 12 시간 동안 환류시켰다. 반응이 종료되면 hotfilter하였다. 여액을 건조시키고 EA slurry하였다. 생성된 고체를 filter하고 재결정하여 5,10-다이브로모-2,7-다이페닐-피렌을 2.0 g (16.3 %) 얻었다.A 250 mL reactor was charged with 12.3 g (0.024 mol) of 4,4'-dibromo-2,2'-diphenylethynylbiphenyl in a nitrogen stream and dissolved in 120 mL of dichloroethane. Iron (III) trifluoro-methanesulfonate (1.2 g, 0.002 mol) was added and refluxed for 12 hours. After completion of the reaction, the mixture was hot-filtered. The filtrate was dried and EA slurried. The resulting solid was filtered and recrystallized to obtain 2.0 g (16.3%) of 5,10-dibromo-2,7-diphenyl-pyrene.
MS(MALDI-TOF): m/z 512[M]+
MS (MALDI-TOF): m / z 512 [M] +
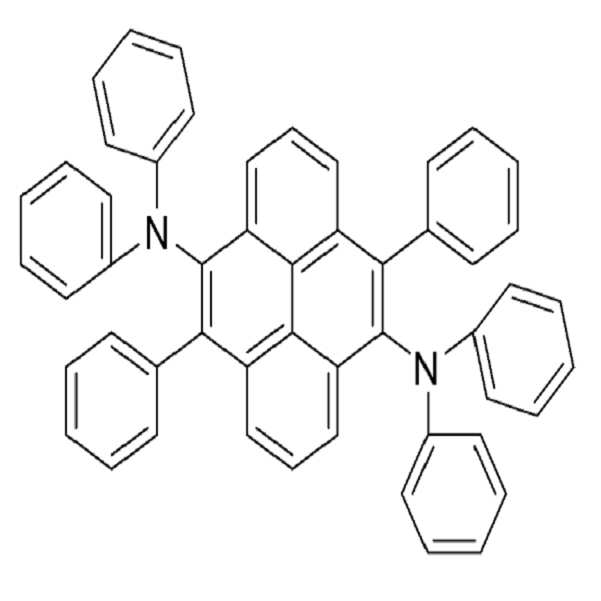
합성예 2. [화학식 14]의 합성Synthesis Example 2. Synthesis of [Formula 14]
2,7-diiodo-3,8-diphenyl-Pyrene(5 g, 8 mmol), diphenyl amine(3 g, 18 mmol),t-BuONa(3.49 g, 36 mmol), Pd(OAc)2 (0.15 g, 0.32 mmol) (t-Bu)3P (0.53 mL, 1.48 mmol)을 O-xylene 50 mL에 넣고 12 시간 이상 reflux시켰다. 반응이 끝나면 상온까지 식힌 후 용매를 제거하고 컬럼 분리(MC:Hx = 1:7)하여 생성물을 분리하였다.(수율 80%)Diphenylamine (3 g, 18 mmol), t-BuONa (3.49 g, 36 mmol), Pd (OAc) 2 (0.15 g, , 0.32 mmol) (t-Bu) 3P (0.53 mL, 1.48 mmol) was added to 50 mL of O-xylene and refluxed for 12 hours or more. After the reaction was completed, the reaction mixture was cooled to room temperature, the solvent was removed, and the product was isolated by column separation (MC: Hx = 1: 7) (yield 80%).
MS(MALDI-TOF): m/z 618[M]+
MS (MALDI-TOF): m / z 618 [M] < + &
합성예 3. [화학식 41]의 합성Synthesis Example 3. Synthesis of [Formula 41]
상기 합성예 2에서의 합성법과 같은 방법으로 하였으며, diphenyl amine대신 4,4'-di-tert-butylphenylamine을 사용하여 합성하였다.The synthesis was carried out in the same manner as in Synthesis Example 2, except that 4,4'-di-tert-butylphenylamine was used instead of diphenylamine.
MS(MALDI-TOF): m/z 913[M]+
MS (MALDI-TOF): m / z 913 [M] < + &
합성예 4. [화학식 50]의 합성Synthesis Example 4. Synthesis of [Formula 50]
상기 합성예 2에서의 합성법과 같은 방법으로 하였으며, diphenyl amine대신 4-phenyldiphenylamine을 사용하여 합성하였다.The synthesis was carried out in the same manner as in Synthesis Example 2, except that 4-phenyldiphenylamine was used instead of diphenyl amine.
MS(MALDI-TOF): m/z 841[M]+
MS (MALDI-TOF): m / z 841 [M] < + &
합성예 5. [화학식 35]의 합성Synthesis Example 5. Synthesis of [Formula 35]
2,7-diiodo-3,8-diphenyl-Pyrene (10 g, 17.2 mmol), Phenyl boronic acid (5.2 g, 43 mmol), K2CO3 (10.75 g, 78 mmol), Pd(PPh3)4 (0.9 g, 1 mmol)을 toluene 100 mL, THF 100 mL, H2O 50 mL 혼합용액에 넣고 reflux시켰다. 반응이 끝나면 층분리하여 유기용매를 제거하고, 컬럼분리로 생성물을 분리(MC:Hx=1:9)하였다.(수율 70%)(10 g, 17.2 mmol), Phenyl boronic acid (5.2 g, 43 mmol), K2CO3 (10.75 g, 78 mmol), Pd (PPh3) 4 (0.9 g, 1 mmol) was added to a mixed solution of 100 mL of toluene, 100 mL of THF and 50 mL of H 2 O and refluxed. After the reaction was completed, the organic solvent was removed by layer separation, and the product was separated by column separation (MC: Hx = 1: 9) (yield 70%).
MS(MALDI-TOF): m/z 506[M]+
MS (MALDI-TOF): m / z 506 [M] < + & gt ;
합성예 6. [화학식 36]의 합성Synthesis Example 6. Synthesis of [Formula 36]
상기 합성예 5와 같은 방법으로 합성하였고 Phenyl boronic acid 대신 3-pyridyl boronic acid을 사용하여 합성하였다.Was synthesized in the same manner as in Synthesis Example 5 and synthesized by using 3-pyridyl boronic acid instead of Phenyl boronic acid.
MS(MALDI-TOF): m/z 508[M]+
MS (MALDI-TOF): m / z 508 [M] < + & gt ;
합성예 7. [화학식 61]의 합성Synthesis Example 7. Synthesis of [Formula 61]
상기 합성예 2와 같은 방법으로 중간체를 5,10-Dibromo-2,7-Diphenyl-Pyrene로 바꾸고, amine을 4,4'-di-tert-butylphenylamine으로 하여 합성하였다The intermediate was changed to 5,10-Dibromo-2,7-diphenyl-Pyrene in the same manner as in Synthesis Example 2, and the amine was synthesized as 4,4'-di-tert-butylphenylamine
MS(MALDI-TOF): m/z 913[M]+
MS (MALDI-TOF): m / z 913 [M] < + &
합성예 8. [화학식 64]의 합성Synthesis Example 8. Synthesis of [Formula 64]
상기 합성예 2와 같은 방법으로 중간체를 5,10-Dibromo-2,7-Diphenyl-Pyrene로 바꾸고, amine을 4-Anilinobenzonitrile으로 하여 합성하였다.In the same manner as in Synthesis Example 2, the intermediate was changed to 5,10-Dibromo-2,7-Diphenyl-Pyrene and the amine was synthesized with 4-anilinobenzonitrile.
MS(MALDI-TOF): m/z 738[M]+
MS (MALDI-TOF): m / z 738 [M] < + &
합성예 9. [화학식 72]의 합성Synthesis Example 9. Synthesis of [Formula 72]
중간체를 5,10-Dibromo-2,7-Diphenyl-Pyrene로 바꾸고 boronic acid를 4-(N,N-diphenylamino)-1-phenylboronic acid로 바꾸어 합성하였다.The intermediate was synthesized by replacing boronic acid with 4- (N, N-diphenylamino) -1-phenylboronic acid by replacing 5,10-Dibromo-2,7-Diphenyl-Pyrene.
MS(MALDI-TOF): m/z 841[M]+
MS (MALDI-TOF): m / z 841 [M] < + &
실시예 2 내지 9Examples 2 to 9
ITO 글래스의 발광면적이 2 mm × 2 mm 크기가 되도록 패터닝한 후 세정하였다. 상기 ITO 글래스를 진공 챔버에 장착한 후 베이스 압력이 1×10-7 torr가 되도록 한 후 상기 ITO 위에 CuPc(800 Å), α-NPD(300 Å)순으로 성막한 후 본 발명에 따른 화합물을 성막(250 Å)한 다음 Alq3(350 Å), LiF(5 Å), Al(500 Å)의 순서로 성막하여 유기전계발광소자를 제조하였다.
The ITO glass was patterned to have a light emitting area of 2 mm x 2 mm and then cleaned. After the ITO glass was mounted in a vacuum chamber, the base pressure was adjusted to 1 × 10 -7 torr, and CuPc (800 Å) and α-NPD (300 Å) were sequentially deposited on the ITO. Alq 3 (350 ANGSTROM), LiF (5 ANGSTROM) and Al (500 ANGSTROM) were deposited in this order to form an organic electroluminescent device.
비교예Comparative Example
상기 실시예와 동일하게 제조하고, 다만, 발광층은 게스트 화합물로서, 하기 [화학식 98]로 표시되는 피렌계 화합물을 더 포함하고, 호스트물질은 [화학식 99] 화합물을 사용하였다.The light emitting layer further contains a pyrene compound represented by the following formula (98) as a guest compound, and the host material is a compound represented by the following formula (99).
[화학식 98] [화학식 99][Chemical Formula 98]
평가예Evaluation example
상기 실시예 2,3,4,7,8과 비교예 1에 따라 제조된 유기전계발광소자에 대하여, 전압, 전류밀도, 휘도, 색 좌표 및 수명을 측정하고 그 결과를 하기 [표 1]에 나타내었다. T97은 휘도가 초기휘도에 비해 97%로 감소되는데 소요되는 시간을 의미한다. The voltage, current density, luminance, color coordinates, and lifetime of the organic electroluminescent device manufactured according to Examples 2, 3, 4, 7, and 8 and Comparative Example 1 were measured and the results are shown in Table 1 Respectively. T97 means the time required for the luminance to be reduced to 97% of the initial luminance.
상기 [표 1]에서 보는 바와 같이, 본 발명에 따른 유기 발광 화합물을 포함하는 유기전계발광자는 구동 전압이 낮으며, 휘도 및 수명 등의 발광특성이 우수하여 다양한 디스플레이 소자에 활용할 수 있다.As shown in Table 1, the organic electroluminescent device including the organic electroluminescent compound according to the present invention has a low driving voltage and is excellent in light emission characteristics such as brightness and lifetime and can be utilized in various display devices.
10 : 기판 20 : 애노드
30 : 정공주입층 40 : 정공수송층
50 : 유기발광층 60 : 전자수송층
70 : 전자주입층 80 : 캐소드10: substrate 20: anode
30: Hole injection layer 40: Hole transport layer
50: organic light emitting layer 60: electron transporting layer
70: electron injection layer 80: cathode
Claims (8)
[화학식 1] [화학식 2] [화학식 3]
[화학식 4] [화학식 5]
상기 [화학식 1] 내지 [화학식 5]에서,
Ar1 내지 Ar6는 서로 동일하거나 상이하고, 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기 및 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기 중에서 선택되며 (단, [화학식 4]의 Ar3과 Ar6 및 [화학식 5]의 Ar2와 Ar4는 각각 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기인 경우는 제외함),
상기 Ar1 내지 Ar6 중 적어도 세 개 이상은 하기 [구조식 1]로 표시되고,
[구조식 1]
상기 [구조식 1]에서,
n 및 m은 각각 독립적으로 0 또는 1의 정수이고, (단, n+m ≥1)
L은 2가의 연결기로서 치환 또는 비치환된 탄소수 1 내지 30의 알킬렌기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴렌기 및 치환 또는 비치환된 탄소수 3 내지 50의 헤테로아릴렌기 중에서 선택되며,
단, 상기 m이 0인 경우에 L은 1가의 치환기이며, n이 0인 경우에는 L은 단일결합을 의미하며,
B는 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기, 치환 또는 비치환된 탄소수 5 내지 50의 아릴기 및 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기 중에서 선택된다 (단, [화학식 4]의 Ar3과 Ar6 및 [화학식 5]의 Ar2와 Ar4는 각각 상기 B가 치환 또는 비치환된 탄소수 5 내지 30의 아릴아민기인 경우는 제외함).A pyrene derivative compound represented by the following Chemical Formulas 1 to 5:
[Formula 3] < EMI ID =
[Chemical Formula 4]
In the above Chemical Formulas 1 to 5,
Ar 1 to Ar 6 are the same or different from each other and each independently represents hydrogen, deuterium, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted arylamine group having 5 to 30 carbon atoms, An aryl group having 5 to 50 carbon atoms, and a heteroaryl group having 3 to 50 carbon atoms having a substituted or unsubstituted heteroatom, O, N or S, with the proviso that Ar 3 and Ar 6 in the formula [4] ], Ar 2 and Ar 4 are each a substituted or unsubstituted arylamine group having 5 to 30 carbon atoms,
At least three of Ar 1 to Ar 6 are represented by the following structural formula 1,
[Structural formula 1]
In the above formula 1,
n and m are each independently an integer of 0 or 1 (provided that n + m > = 1)
L is a divalent linking group selected from a substituted or unsubstituted alkylene group having 1 to 30 carbon atoms, a substituted or unsubstituted arylene group having 5 to 50 carbon atoms, and a substituted or unsubstituted heteroarylene group having 3 to 50 carbon atoms,
Provided that when m is 0, L is a monovalent substituent, and when n is 0, L means a single bond,
B represents a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted arylamine group having 5 to 30 carbon atoms, a substituted or unsubstituted aryl group having 5 to 50 carbon atoms, and a substituted or unsubstituted heteroatom such as O, N or S, with the proviso that Ar 3 and Ar 6 in the formula (4) and Ar 2 and Ar 4 in the formula (5) each represent a substituted or unsubstituted heteroaryl group having 3 to 50 carbon atoms, An arylamine group having 5 to 30 carbon atoms is excluded).
상기 [구조식 1]의 B는 -NR1R2이고, 상기 R1 및 R2는 치환 또는 비치환된 탄소수 5 내지 50의 아릴기이거나, 또는 치환 또는 비치환되고 이종 원자로 O, N 또는 S를 갖는 탄소수 3 내지 50의 헤테로아릴기인 것을 특징으로 하는 피렌 유도체 화합물.The method according to claim 1,
B in the above structural formula 1 is -NR 1 R 2 , R 1 and R 2 are a substituted or unsubstituted aryl group having 5 to 50 carbon atoms, or a substituted or unsubstituted heteroatom such as O, N or S And R < 3 > is a heteroaryl group having 3 to 50 carbon atoms.
상기 [화학식 1] 내지 [화학식 5]는 하기 [화학식 6] 내지 [화학식 50], [화학식 53] 내지 [화학식 57], [화학식 60] 내지 [화학식 65], [화학식 67] 내지 [화학식 68], [화학식 70] 내지 [화학식 85], [화학식 87] 내지 [화학식 95] 및 [화학식 97]로 표시되는 군으로부터 선택되는 어느 하나인 것을 특징으로 하는 피렌 유도체 화합물:
[화학식 6] [화학식 7] [화학식 8]
[화학식 9] [화학식 10] [화학식 11]
[화학식 12] [화학식 13]
[화학식 14] [화학식 15]
[화학식 16] [화학식 17]
[화학식 18] [화학식 19] [화학식 20]
[화학식 21] [화학식 22] [화학식 23]
[화학식 24] [화학식 25] [화학식 26]
[화학식 27] [화학식 28] [화학식 29]
[화학식 30] [화학식 31] [화학식 32]
[화학식 33] [화학식 34]
[화학식 35] [화학식 36] [화학식 37]
[화학식 38] [화학식 39] [화학식 40]
[화학식 41] [화학식 42] [화학식 43]
[화학식 44] [화학식 45] [화학식 46]
[화학식 47] [화학식 48] [화학식 49]
[화학식 50] [화학식 53]
[화학식 54] [화학식 55] [화학식 56] [화학식 57]
[화학식 60] [화학식 61]
[화학식 62] [화학식 63] [화학식 64] [화학식 65]
[화학식 67] [화학식 68]
[화학식 70] [화학식 71] [화학식 72] [화학식 73]
[화학식 74] [화학식 75] [화학식 76] [화학식 77]
[화학식 78] [화학식 79] [화학식 80] [화학식 81]
[화학식 82] [화학식 83] [화학식 84] [화학식 85]
[화학식 87] [화학식 88] [화학식 89]
[화학식 90] [화학식 91] [화학식 92] [화학식 93]
[화학식 94] [화학식 95] [화학식 97]
The method according to claim 1,
[Formula 6] to [Formula 50], [Formula 53] to Formula [57], [Formula 60] to Formula [65], [Formula 67] Wherein the pyrene derivative compound is any one selected from the group consisting of the following formulas (70) to (85), (87) to (95)
[Chemical Formula 7] < EMI ID =
[Chemical Formula 10] < EMI ID =
[Chemical Formula 12]
[Chemical Formula 14]
[Chemical Formula 16]
[Chemical Formula 19] [Chemical Formula 20]
[Chemical Formula 21]
[Chemical Formula 25]
[Chemical Formula 27]
[Chemical Formula 32]
[Chemical Formula 33]
[Chemical Formula 35]
[Chemical Formula 38] [Chemical Formula 39]
[Chemical Formula 41]
[Chemical Formula 45]
[Chemical Formula 48] [Chemical Formula 48]
[Chemical Formula 50]
[Chemical Formula 55] [Chemical Formula 55] [Chemical Formula 55]
[Chemical Formula 60]
[Chemical Formula 62] [Chemical Formula 65] [Chemical Formula 65]
[Chemical Formula 67]
[Chemical Formula 71] [Chemical Formula 72] [Chemical Formula 73]
[Chemical Formula 75] [Chemical Formula 76] [Chemical Formula 77]
[Formula 79] [Formula 80] [Formula 81]
[Chemical Formula 82]
[Chemical Formula 88] [Chemical Formula 88]
[Chemical Formula 91] [Chemical Formula 92] [Chemical Formula 93]
[Chemical Formula 95] [Chemical Formula 95]
캐소드; 및
상기 애노드와 상기 캐소드 사이에 개재되며, 제 1 항 내지 제 3 항 중 어느 한 항의 화합물을 포함하는 유기전계발광소자.Anode;
Cathode; And
The organic electroluminescent device according to any one of claims 1 to 3, interposed between the anode and the cathode.
상기 화합물은 상기 애노드와 상기 캐소드 사이의 발광층 중에 포함되는 것을 특징으로 하는 유기전계발광소자.5. The method of claim 4,
Wherein the compound is contained in the light emitting layer between the anode and the cathode.
상기 애노드 및 캐소드 사이에 정공주입층, 정공수송층, 전자저지층, 정공저지층, 전자수송층 및 전자주입층으로 이루어진 군으로부터 선택된 하나 이상의 층을 더 포함하는 것을 특징으로 하는 유기전계발광소자.6. The method of claim 5,
Wherein at least one layer selected from the group consisting of a hole injecting layer, a hole transporting layer, an electron blocking layer, a hole blocking layer, an electron transporting layer and an electron injecting layer is further interposed between the anode and the cathode.
상기 정공주입층, 정공수송층, 전자저지층, 발광층, 정공저지층, 전자수송층 및 전자주입층으로부터 선택된 하나 이상의 층은 단분자 증착방식 또는 용액공정에 의하여 형성되는 것을 특징으로 하는 유기전계발광소자.The method according to claim 6,
Wherein at least one layer selected from the group consisting of the hole injection layer, the hole transport layer, the electron blocking layer, the light emitting layer, the hole blocking layer, the electron transport layer and the electron injection layer is formed by a single molecular deposition method or a solution process.
상기 유기전계발광소자는 표시소자, 디스플레이 소자, 또는 단색 또는 백색 조명용 소자에 사용되는 것을 특징으로 하는 유기전계발광소자.5. The method of claim 4,
Wherein the organic electroluminescent device is used in a display device, a display device, or a device for monochromatic or white illumination.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020110035226 | 2011-04-15 | ||
| KR20110035226 | 2011-04-15 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20120117675A KR20120117675A (en) | 2012-10-24 |
| KR101996649B1 true KR101996649B1 (en) | 2019-07-04 |
Family
ID=47285555
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020120038499A Active KR101996649B1 (en) | 2011-04-15 | 2012-04-13 | Pyrene derivative compounds and organic light-emitting diode including the same |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101996649B1 (en) |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW201213502A (en) | 2010-08-05 | 2012-04-01 | Idemitsu Kosan Co | Organic electroluminescent element |
| JP6005925B2 (en) * | 2011-11-18 | 2016-10-12 | ユー・ディー・シー アイルランド リミテッド | ORGANIC ELECTROLUMINESCENT ELEMENT, COMPOUND USED FOR THE ELEMENT, LIGHT EMITTING DEVICE, DISPLAY DEVICE AND LIGHTING DEVICE USING THE ELEMENT |
| KR101780855B1 (en) | 2011-11-25 | 2017-09-21 | 이데미쓰 고산 가부시키가이샤 | Aromatic amine derivative, material for organic electroluminescent element, and organic electroluminescent element |
| KR102002020B1 (en) * | 2012-10-15 | 2019-07-19 | 에스에프씨주식회사 | Pyrene derivatives having substituted cyclic amine groups and organic light-emitting diode including the same |
| KR102050484B1 (en) | 2013-03-04 | 2019-12-02 | 삼성디스플레이 주식회사 | Anthracene derivatives and organic light emitting diodes comprising the derivatives |
| KR102080738B1 (en) * | 2013-04-30 | 2020-02-24 | 에스에프씨 주식회사 | Pyrene derivatives and organic electro luminescent device comprising same |
| KR102107106B1 (en) | 2013-05-09 | 2020-05-07 | 삼성디스플레이 주식회사 | Styryl-based compound and organic light emitting diode comprising the same |
| KR102269131B1 (en) | 2013-07-01 | 2021-06-25 | 삼성디스플레이 주식회사 | Compound and organic light emitting device comprising same |
| US10062850B2 (en) | 2013-12-12 | 2018-08-28 | Samsung Display Co., Ltd. | Amine-based compounds and organic light-emitting devices comprising the same |
| KR20150132795A (en) | 2014-05-16 | 2015-11-26 | 삼성디스플레이 주식회사 | Organic light emitting device |
| KR102253440B1 (en) | 2014-06-02 | 2021-05-20 | 삼성디스플레이 주식회사 | Amine-based compounds and organic light- emitting device including the same |
| KR102327086B1 (en) | 2014-06-11 | 2021-11-17 | 삼성디스플레이 주식회사 | Organic light-emitting devices |
| KR102304716B1 (en) | 2014-06-13 | 2021-09-27 | 삼성디스플레이 주식회사 | Amine-based compounds and organic light-emitting device including the same |
| KR20160029962A (en) * | 2014-09-05 | 2016-03-16 | 에스케이케미칼주식회사 | Compound for organic electroluminescent device and organic electroluminescent device comprising the same |
| KR101780605B1 (en) | 2014-09-19 | 2017-09-21 | 이데미쓰 고산 가부시키가이샤 | Novel compound |
| WO2016111140A1 (en) * | 2015-01-09 | 2016-07-14 | 東レ株式会社 | Photoelectric conversion element and image sensor using same |
| KR102343145B1 (en) | 2015-01-12 | 2021-12-27 | 삼성디스플레이 주식회사 | Condensed compound and organic light-emitting device comprising the same |
| KR102606275B1 (en) | 2015-10-27 | 2023-12-05 | 삼성디스플레이 주식회사 | Organic light emitting device |
| KR101678134B1 (en) * | 2015-11-17 | 2016-11-21 | 가톨릭대학교 산학협력단 | Organic compound and organic optoelectric device including the same |
| KR102642605B1 (en) * | 2017-11-30 | 2024-03-04 | 엘지디스플레이 주식회사 | Organic compound, organic light emitting diode and organic light emiting device having the compound |
| CN109896920B (en) * | 2019-03-07 | 2021-06-01 | 南京邮电大学 | Synthetic method of phenanthrene and derivative thereof |
| DE102019106388A1 (en) * | 2019-03-13 | 2020-09-17 | Cynora Gmbh | ORGANIC MOLECULES FOR OPTOELECTRONIC DEVICES |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040076853A1 (en) * | 2002-04-24 | 2004-04-22 | Eastman Kodak Company | Organic light-emitting diode devices with improved operational stability |
| US20050031898A1 (en) | 2003-08-06 | 2005-02-10 | Canon Kabushiki Kaisha | Organic electroluminescent device based on pyrene derivatives |
| US20060033421A1 (en) | 2002-07-19 | 2006-02-16 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and organic light emitting medium |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1604974A4 (en) * | 2003-03-20 | 2007-11-14 | Idemitsu Kosan Co | AROMATIC AMINE DERIVATIVE AND ORGANIC ELECTROLUMINESCENT ELEMENT PRODUCED WITH THIS DERIVATIVE |
-
2012
- 2012-04-13 KR KR1020120038499A patent/KR101996649B1/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040076853A1 (en) * | 2002-04-24 | 2004-04-22 | Eastman Kodak Company | Organic light-emitting diode devices with improved operational stability |
| US20060033421A1 (en) | 2002-07-19 | 2006-02-16 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and organic light emitting medium |
| US20050031898A1 (en) | 2003-08-06 | 2005-02-10 | Canon Kabushiki Kaisha | Organic electroluminescent device based on pyrene derivatives |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20120117675A (en) | 2012-10-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101996649B1 (en) | Pyrene derivative compounds and organic light-emitting diode including the same | |
| KR101983991B1 (en) | Condensed aryl compound and organic light-diode including the same | |
| KR101216004B1 (en) | Anthracene derivatives and organic light-emitting diode including the same | |
| KR101771528B1 (en) | Spiro compound and organic electroluminescent devices comprising the same | |
| KR101825381B1 (en) | spiro compounds and organic light-emitting diode including the same | |
| KR102144446B1 (en) | Organic Compound for organic light emitting diode and an organic light emitting diode including the same with long life | |
| KR101759482B1 (en) | Heterocyclic compounds and organic light-emitting diode including the same | |
| KR101791022B1 (en) | spiro compounds and organic light-emitting diode including the same | |
| KR101861263B1 (en) | Anthracene deriva tives and organic light-emitting diode including the same | |
| KR102240004B1 (en) | Novel aromatic amine compounds for organic light-emitting diode and organic light-emitting diode including the same | |
| KR101996651B1 (en) | Fluorene derivatives and organic light-emitting diode including the same | |
| KR101825382B1 (en) | Heterocyclic com pounds and organic light-emitting diode including the same | |
| KR102017506B1 (en) | Phenanthridine Derivatives and organic light-emitting diode including the same | |
| KR102169273B1 (en) | Organic electroluminescent compound comprising acridine derivative and organic electroluminescent device comprising same | |
| KR101771529B1 (en) | Heterocyclic compounds and organic light-emitting diode including the same | |
| JP7181397B2 (en) | Novel boron compound and organic light-emitting device containing the same | |
| KR102143368B1 (en) | Antracene derivatives and organic light-emitting diode including the same | |
| KR101957902B1 (en) | New compounds and organic light-emitting diode including the same | |
| KR101793428B1 (en) | Condensed aryl compounds and organic light-diode including the same | |
| KR102184351B1 (en) | Organic Compound for organic light emitting diode and an organic light emitting diode including the same with long life | |
| KR101791023B1 (en) | Fused aromatic compound and organic electroluminescent devices comprising the same | |
| KR20140079306A (en) | An electroluminescent compound and an electroluminescent device comprising the same | |
| KR101794557B1 (en) | Amine-based compound and organic electroluminescent devices comprising the same | |
| KR20160107669A (en) | Novel organic light-emitting diode including antracene derivatives | |
| KR102423699B1 (en) | Novel compound and organic electroluminescent device comprising same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |