KR100812538B1 - Drug-controlled metformin-glymepiride combination - Google Patents
Drug-controlled metformin-glymepiride combination Download PDFInfo
- Publication number
- KR100812538B1 KR100812538B1 KR1020060102912A KR20060102912A KR100812538B1 KR 100812538 B1 KR100812538 B1 KR 100812538B1 KR 1020060102912 A KR1020060102912 A KR 1020060102912A KR 20060102912 A KR20060102912 A KR 20060102912A KR 100812538 B1 KR100812538 B1 KR 100812538B1
- Authority
- KR
- South Korea
- Prior art keywords
- metformin
- glymepiride
- drug
- layer
- release layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/155—Amidines (), e.g. guanidine (H2N—C(=NH)—NH2), isourea (N=C(OH)—NH2), isothiourea (—N=C(SH)—NH2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/64—Sulfonylureas, e.g. glibenclamide, tolbutamide, chlorpropamide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2027—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2072—Pills, tablets, discs, rods characterised by shape, structure or size; Tablets with holes, special break lines or identification marks; Partially coated tablets; Disintegrating flat shaped forms
- A61K9/2086—Layered tablets, e.g. bilayer tablets; Tablets of the type inert core-active coat
- A61K9/209—Layered tablets, e.g. bilayer tablets; Tablets of the type inert core-active coat containing drug in at least two layers or in the core and in at least one outer layer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Obesity (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Medicinal Preparation (AREA)
Abstract
본 발명은 약물 제어방출형 메트포르민-글리메피리드 복합제제에 관한 것으로서, 더욱 상세하게는 수용해성이 높고 단위 투여량이 큰 메트포르민의 방출이 24 시간동안 지속적으로 이루어지도록 방출제어물질을 특이성 있게 선택설계하여 서방층을 구성하고, 수용해성이 낮고 단위 투여량이 적은 글리메피리드의 함량이 균일하게 유지되면서 빠르게 방출되도록 속방층을 구성하며, 특히 상기 서방층을 구성하는 부형제가 글리메피리드의 빠른 방출에 영향을 줄 수 없도록 서방층과 속방층의 방출층을 완전히 차단시키는 다층정 형태의 제형을 구현하여 메트포르민과 글리메피리드가 위치하는 상을 완전히 분리함으로써 각 약물의 상호 작용이 최소화되며 각 약물의 효과가 상호 보완적으로 지속되므로 특히 2형 당뇨병에 효과적인 경구 투여용 약물 제어방출형 메트포르민-글리메피리드 복합제제에 관한 것이다.The present invention relates to a drug-controlled metformin-glymepiride combination formulation, and more particularly, to a sustained release layer by specifically selecting and designing a release controlling substance so that the release of metformin having a high water solubility and a high unit dosage is continuously performed for 24 hours. And the immediate release layer so that the content of glymepiride with low water solubility and low unit dose is maintained uniformly, and the rapid release layer is configured so that the excipient constituting the sustained release layer cannot affect the rapid release of glymepiride. By implementing a multi-layered formulation that completely blocks the release layer of the immediate release layer, the phase separation between metformin and glymepiride is minimized, minimizing the interaction of each drug and the effects of each drug are complementary. Drugs for oral administration effective for type diabetes Air-release metformin relates to a combined preparation glimepiride.
Description
도 1은 실시예 1에 따라 제조된 다층정제 중 메트포르민층의 용출곡선과 대조약(글루코파지 엑스알)의 용출곡선을 나타낸 그래프이다.1 is a graph showing the dissolution curve of the metformin layer of the multilayer tablet prepared according to Example 1 and the dissolution curve of the reference drug (glucophage XAL).
도 2는 실시예 5에 따라 제조된 다층정제 중 메트포르민층의 용출곡선과 대조약(글루코파지 엑스알)의 용출곡선을 나타낸 그래프이다.Figure 2 is a graph showing the dissolution curves of the metformin layer of the multilayer tablet prepared according to Example 5 and the dissolution curve of the reference drug (glucophage XAL).
도 3는 실시예 1 에 따라 제조된 다층정제 중 글리메피리드층의 용출곡선과 대조약(아마릴)의 용출곡선을 나타내는 그래프이다.FIG. 3 is a graph showing an elution curve of the glymepiride layer and an elution curve of the reference drug (Amaryl) in the multilayer tablet prepared according to Example 1. FIG.
본 발명은 메트포르민과 글리메피리드의 각 약물 간의 상호 작용이 최소화되며, 이들 약물의 효과가 상호 보완적으로 지속되므로 특히 2형 당뇨병에 효과적인 경구 투여용 약물 제어방출형 메트포르민-글리메피리드 복합제제에 관한 것이다.The present invention relates to a drug controlled-release metformin-glymepiride combination for oral administration, which is particularly effective for type 2 diabetes since the interaction between metformin and each drug of glymepire is minimized and the effects of these drugs are complementary.
2형 당뇨병(Type 2 Diabetes; DM), 즉, 인슐린 비의존적 당뇨병은 유전이나 자가면역질환이 아닌 생활습관 등에 기인한 당뇨병이다. 이는 인슐린은 분비되지만 부족하거나, 제대로 활용을 하지 못하여 나타나는 질병으로서 주된 치료 방향은 인슐린 저항성 및 인슐린 분비 결함, 변질된 지질혈증, 글루코오스 대사 장애, 및 기타 인자의 교란에 기인하는 고혈당증을 조절하고, 약물 치료에 기인하는 저혈당증을 예방하는 것이다. Type 2 Diabetes (DM), or insulin-independent diabetes, is diabetes caused by lifestyle, not inherited or autoimmune diseases. It is a disease caused by insulin secretion but insufficient or poor use, and the main therapeutic direction is to control hyperglycemia due to insulin resistance and insulin secretion deficiency, altered lipidemia, glucose metabolism disorder, and disturbance of other factors, and It is to prevent hypoglycemia due to treatment.
이를 위하여 현재 다른 기전을 가지는 당뇨병조절약의 병용 요법이 약효의 상승효과를 가져오며, 또한 고용량의 단일 활성 성분을 사용하는 경우보다 더 유용한 조절을 달성할 수 있음이 임상적으로 입증되어 있다. To this end, it is currently clinically demonstrated that combination therapy of diabetic modulators with different mechanisms has a synergistic effect and can achieve more useful control than when using high doses of a single active ingredient.
이러한 당뇨병 치료제로서, 예전에는 설포닐우레아계(Sulfonyl urea; SU계) 약물들이 주류를 이루었다. As the anti-diabetic agent, sulfonyl urea (SU-based) drugs have been mainstream in the past.
설포닐우레아계의 약물학적 기전은 베타세포로부터 인슐린 분비를 점차적으로 늘리는 방법을 통해 고혈당증을 조절하는 것이다. 그러나, 당뇨병 치료제에 있어서, 설포닐우레아계 약물의 장기복용시에 저혈당 유발, 체중증가, 혈중지질상태 악화 등의 부작용이 발생하는 문제점이 있다. 뿐만 아니라 설포닐우레아계 약물 요법을 실시한 당뇨병 환자의 10 ∼ 20 %는 초기투여부터 치료 효과가 나타나지 않고, 이를 1 ∼ 2 년 정도 복용하면 5 ∼ 20 %의 빈도로 치료 효과가 나타나지 않으며, 복용기간이 10 년이 경과하게 되면 50 %의 빈도로 효과가 나타나지 않는 특징을 보인다. 그리하여 다른 치료제의 병용투여가 검토되었다. The pharmacologic mechanism of the sulfonylurea system is to control hyperglycemia by gradually increasing insulin secretion from beta cells. However, in the treatment of diabetes, there is a problem that side effects such as hypoglycemia, weight gain, deterioration of blood lipid status, etc. occur during long-term use of sulfonylurea-based drugs. In addition, 10-20% of diabetic patients who received sulfonylurea-based drug therapy did not show a therapeutic effect from the initial administration, and when it was taken for 1 to 2 years, there was no therapeutic effect at a frequency of 5-20%. At the end of this decade, there is a 50% frequency of ineffectiveness. Thus, co-administration of other therapeutic agents was considered.
설포닐우레아계 약물과 병용투여되는 다른 치료제로는 비구아니드계, 티아졸리딘디온계, 알파-글루코시다제 억제제로 대표되는 세 가지의 새로운 종류의 치료 제가 고려되었다.Other therapeutic agents in combination with sulfonylureas have been considered three new classes of treatments, represented by biguanides, thiazolidinediones, and alpha-glucosidase inhibitors.
상기 병용투여되는 치료제 중에서 비구아니드계는 간의 당 생성 억제 및 말초의 당흡수 증진에 의해 인슐린 내성을 감소시킴으로 고혈당증을 조절하는 기전을 나타낸다. Among the coadministered therapeutic agents, the biguanide system exhibits a mechanism for controlling hyperglycemia by reducing insulin resistance by inhibiting hepatic glucose production and enhancing peripheral glucose absorption.
근래에 들어 상기 설포닐우레아계 약물과, 비구아니드계 약물의 약물학적 기전의 차이로 인한 혈당조절 기능은 서로 상승적임을 확인하였고, 이러한 상승 효과를 이용하여 병용 투여하는 방법이 임상적으로 시행되었다. Recently, it has been confirmed that the glycemic control function due to the difference in the pharmacological mechanism of the sulfonylurea-based drug and the biguanide-based drug is synergistic with each other. .
비구아니드계 치료제로서 대표적인 것은 메트포르민이며, 설포닐우레아계 치료제 중 글리부라이드 또는 글리메피리드를 메트포르민과 병용투여하는 사례가 대표적이다. 그리고, 설포닐우레아계 치료제의 단독 치료로서 혈당 조절에 성공하지 못한 환자들에 대해 설포닐우레아계 약물과 함께 메트포르민을 병용투여할 경우 두 약제가 혈당 조절에 뛰어난 효과가 있다는 것이 밝혀졌다. A typical example of a biguanide-based therapeutic agent is metformin, and a typical case of using a combination of metformin with glyburide or glymepiride among sulfonylurea-based therapeutic agents is typical. In addition, the combination of sulfonylurea-based drugs with metformin in combination with sulfonylurea-based drugs in patients who failed to successfully control the sulfonylurea-based treatments was found to have an excellent effect on glycemic control.
따라서, 서로 다른 작용 기전을 통하여 상호 보완적으로 혈당 조절이 이루어지는 상기 두 약물의 복합사용 사례는 증가하는 경향이며, 처방 자료에 따르면 메트포르민 사용의 약 60 %가 설포닐우레아계 치료제와 복합사용하는 것으로 나와 있다. Therefore, the combined use of the two drugs that complement the blood glucose control through different mechanisms of action tends to increase, and according to prescription data, about 60% of metformin use is combined with sulfonylurea treatment It is out.
메트포르민과 설포닐우레아계 약물 중 글리부라이드의 복합사용의 사례는 다음의 문헌에서 잘 나타나 있다. 비그네리(Vigneri) 등은 [Treatment of NIDDM Patients with secondary failure to Glyburide : Comparison of the Addition of Either Metformin of Bed-Time NPH Insulin to Gluburide, Diabete & Metabolism, 1991, 17, 232-234)에서 15 mg/일 용량의 글리부라이드로 2차적 실패를 한 2형 당뇨병 환자를 치료하기 위해 1500 mg/일 메트포르민 및 15 mg/일 글리부라이드의 복합사용을 개시하고 있다. Examples of the combined use of glyburide in metformin and sulfonylureas are well illustrated in the following literature. Vigneri et al. Described 15 mg / l in Treatment of NIDDM Patients with secondary failure to Glyburide: Comparison of the Addition of Either Metformin of Bed-Time NPH Insulin to Gluburide, Diabete & Metabolism, 1991, 17, 232-234. A combination use of 1500 mg / day metformin and 15 mg / day glyburide is disclosed to treat patients with type 2 diabetes who have secondary failure with one dose of glyburide.
WO2001/32158 호는 투약 경험이 없는 환자에게 당뇨병의 1차 치료를 위한 메트포르민과 설포닐우레아계 약물인 글리부라이드의 저용량 제약 제제의 사용을 개시하고 있으며, 당뇨병 초기 환자에게 당뇨병의 1차 치료에서 일반적으로 승인된 의료 실무에서 처방되는 그러한 약물의 단일 복용량보다 적은 복용량을 복합 제제화하여 투약할 경우 실질적으로 감소된 부작용을 나타낸다고 개시하고 있다.WO2001 / 32158 discloses the use of low-dose pharmaceutical preparations of metformin and sulfonylurea-based drugs, glyburide, for the first treatment of diabetes in patients who do not have experience with medication, and in the first treatment of diabetes in patients with early diabetes. It is disclosed that when combined dosages of less than a single dose of such drugs generally prescribed in approved medical practice have substantially reduced side effects.
그러나, 상기 단일정의 조합물의 경우는 당뇨병의 1차 환자, 즉 염산메트포르민을 1일 3회 복용하는 환자 혹은 설포닐우레아계 약물을 1일 1회 복용하는 환자에게 적용하였을 때에 유용하지만, 2차 환자, 즉 당뇨병이 이미 진행되어 메트포르민과 설포닐우레아계 약물을 같이 복용하는 환자에게는 유용성을 주지 못한다.However, the combination of the above-mentioned single tablets is useful when applied to primary patients with diabetes, i.e., patients taking metformin hydrochloride three times a day or patients taking sulfonylurea-based drugs once a day. In other words, diabetes has already progressed and it is not useful for patients taking metformin and sulfonylureas.
한편, 실제 임상에서는 메트포르민과 글리메피리드를 병용해서 투여해야하는 경우에는 각각의 단일 제제로서 투여하고 있다. 이때, 일반적인 복용방법은 메트포르민의 경우 1일 3회씩 복용하며 작용 지속시간이 긴 글리메피리드의 경우 1일 1회씩 복용한다. 이러한 복용횟수의 차이로 인하여 혼란을 야기할 수 있다. 이러한 혼란을 막기 위하여 메트포르민과 글리메피리드를 1일 1회 투여 할 경우, 메트포르민은 체내에서 빠르게 소실되기 때문에 글리메피리드와의 지속적인 상승작용으로 혈당을 유지하기는 어렵다. In practice, when metformin and glymepiride are to be administered in combination, they are administered as each single agent. In this case, the general method of taking is metformin three times a day, and in the case of long-acting glymepiride is taken once a day. This difference in doses can cause confusion. When metformin and glymepiride are administered once a day to prevent such confusion, it is difficult to maintain blood sugar by sustained synergy with glymepiride because metformin is rapidly lost in the body.
한국공개특허 제2006-6469호는 메트포르민 및 글리메피리드의 혼합 단일정의 투여를 제시하고 있는데, 메트포르민과 글리메피리드를 복합 투여하여 환자에게 임상적인 상승 효과를 나타낸다. 그러나, 상기 특허에서 메트포르민의 용출형태는 제어 방출용 서방특성을 가진 것이 아닌 일반정제로 제형설계 되어 있으며, 이때 일반정의 용출패턴으로 방출되는 메트포르민이 혈중에서 비교적 빠르게 소실되어 복용 후 글리메피리드와의 지속적인 상승효과를 기대하기는 힘들다Korean Patent Laid-Open No. 2006-6469 proposes a mixed single-dose administration of metformin and glimepiride, which shows a clinical synergistic effect on a patient by a combination administration of metformin and glimepiride. However, the elution form of metformin in the patent is designed as a general tablet, not having controlled release sustained release properties, where metformin released in the general definition elution pattern disappears relatively rapidly in the blood and is continuously elevated with glycepiride after taking. Hard to expect effects
한국공개특허 제2004-79980호는 속방성 및 서방성 약물 모두를 송달하는 경구 투약 형태의 제조 방법에 관한 특허로써, 염산메트포르민을 포함하는 서방층과, 글리메피리드를 포함하는 속방층을 구성하되, 글리메피리드의 속방출을 유도하기 위하여 속방층을 구성하는 약물을 10 미크론 미만의 입자로 제제화하거나, 코팅층을 형성하는 기술을 언급하고 있다. 그러나, 상기와 같이 글리메피리드층으로 외부 코팅 층을 사용할 주성분의 양이 매우 적기 때문에 함량의 균일성을 맞추기 어렵다. 뿐만 아니라 서방층의 제어 방출도 8시간 이내의 용출형태만을 언급하고 있으므로 24시간 작용을 나타내는 글리메피리드와의 지속적인 상승효과를 유지하기 힘들다. Korean Patent Laid-Open No. 2004-79980 relates to a method for preparing an oral dosage form for delivering both immediate release and sustained release drugs, comprising a sustained release layer containing metformin hydrochloride and an immediate release layer containing glymepiride, In order to induce rapid release, the drug constituting the immediate release layer is formulated into particles of less than 10 microns, or a technique of forming a coating layer is mentioned. However, since the amount of the main component to use the outer coating layer as the glymepiride layer as described above is very small, it is difficult to match the uniformity of the content. In addition, controlled release of the sustained release layer only mentions the elution form within 8 hours, so it is difficult to maintain a sustained synergistic effect with glymepiride, which exhibits 24-hour action.
한편, 메트포르민은 1회 투여량이 250 ∼ 1000 mg이고, 글리메피리드는 1회 투여량이 1 ∼ 8 mg으로서 각 성분의 단위 투여량에는 큰 차이가 있다. 또한 물성에서도 큰 차이를 나타내는데, 메트포르민의 경우 높은 용해도와 낮은 약물 흡수도를 보이는 반면 글리메피리드의 경우 낮은 용해도와 높은 약물 흡수도를 보인다. On the other hand, metformin is 250-1000 mg per dose, and glymepyride is 1-8 mg per dose, and there is a big difference in the unit dose of each component. In addition, there is a big difference in physical properties. Metformin shows high solubility and low drug absorption, while glymepiride shows low solubility and high drug absorption.
이러한 각각의 약물의 특성으로 인해 메트포르민의 지속적인 제어 방출과 글 리메피리드의 신속한 방출을 통해 약효의 극대화를 유도하는 위해서는 고도의 제제기술이 요구된다. 즉, 용해도가 높고 1회 투여량이 매우 큰 메트포르민의 24시간 지속적인 방출을 유도하는 것 자체가 정제의 크기를 고려할 때 어려운 작업이다. 또한, 용해도가 낮고 작용 지속시간이 긴 글리메피리드의 신속한 방출을 유도하는 것도 어려운 작업이다. 일반적인 제제 기술로는 메트포르민의 제어 방출을 위하여 사용되어지는 부형제에 의하여 글리메피리드 성분이 포획되어 약물의 방출이 늦어질 수 있기 때문이다. Due to the characteristics of each of these drugs, high formulation technology is required to induce maximum drug efficacy through continuous controlled release of metformin and rapid release of glymepiride. In other words, inducing a 24-hour sustained release of metformin with high solubility and very high doses is a difficult task in view of the size of the tablet itself. It is also a difficult task to induce the rapid release of glymepiride with low solubility and long duration of action. The general formulation technique is that the excipients used for controlled release of metformin can be captured by the glymepiride component, which can slow the release of the drug.
즉, 상기와 같이 방출성에 큰 차이를 보이는 두 성분의 제형화를 위해서는 다음과 같은 점을 극복해야만 한다. That is, in order to formulate two components having a large difference in release properties as described above, the following points must be overcome.
메트포르민의 경우 단위 투여량이 매우 크기 때문에 경구로 투약 가능한 정도의 크기를 나타내면서, 24시간 지속적인 제어방출을 유지할 수 있는 제제가 설계되어야 한다. 그리고, 글리메피리드의 경우 단위 투여량이 매우 적기 때문에 함량 균일성 문제를 해결할 수 있는 제제가 설계되어야 한다. 또한, 상호 반대되는 약물의 방출 기전을 가지는 활성 성분으로 인해 상호 약물의 방출에 영향을 주지 않는 적합한 제형 설계, 글리메피리드의 방출이 메트포르민의 제어 방출에 의해 영향을 받지 않는 제형 설계가 필요하다. Since metformin has a very large unit dose, an agent that can be orally administered should be designed to maintain a sustained controlled release for 24 hours. In the case of glimepiride, since the unit dosage is very small, a formulation which can solve the problem of content uniformity should be designed. There is also a need for suitable formulation designs that do not affect the release of mutual drugs due to active ingredients having opposite mechanisms of release of drugs, and formulation designs where the release of glymepiride is not affected by the controlled release of metformin.
이에 본 발명의 발명자들은 상기와 같은 문제점을 해결하기 위하여 연구 노력하였다.The inventors of the present invention have tried to solve the above problems.
그 결과, 수용해성이 매우 높으면서 단위 투여량이 큰 메트포르민의 방출이 24 시간동안 지속적으로 이루어지도록 방출제어물질을 특이성 있게 선택설계하여 서방층을 구성하고, 수용해성이 낮고 단위 투여량이 적은 글리메피리드의 함량이 균일하게 유지되면서 빠르게 방출되도록 속방층을 구성하며, 특히 상기 서방층을 구성하는 부형제가 글리메피리드의 빠른 방출에 영향을 줄 수 없도록 서방층과 속방층의 방출층을 완전히 차단시키는 다층정 형태의 제형을 구현하여 메트포르민과 글리메피리드가 위치하는 상을 완전히 분리함으로써 각 약물의 상호 작용이 최소화된 복합제제를 완성하였다.As a result, the release control material was specifically designed and designed to sustain the release of metformin with high water solubility and high unit dose continuously for 24 hours, thereby forming a slow release layer, and having low water solubility and low unit dose of glymepiride. The rapid release layer is configured to be released quickly while maintaining uniformity. In particular, the excipient constituting the sustained release layer has a multi-layered formulation that completely blocks the release layer of the sustained release layer and the immediate release layer such that the excipient constituting the sustained release layer cannot be affected. This was achieved by completely separating the phase where metformin and glymepire were located, thus completing a combination formulation with minimal interaction between drugs.
즉, 메트포르민을 함유하는 서방층을 구성하는 방출제어물질을 선택함에 있어 친수성 고분자 혼합물과 소수성 물질을 혼합사용함으로써 기존의 메트포르민 서방정과는 달리 정제의 크기를 작게 구성할 수 있어 경구 투약이 가능할 정도의 크기로도 메트포르민이 24시간 동안 지속적으로 방출되면서 약효가 지속될 수 있도록 하였으며, 글리메피리드를 함유하는 속방층은 상기 서방층과 다층정을 구성함으로써 이들간의 접촉면이 최소화되어 메트포르민을 함유하는 서방층이 팽윤시 글리메피리드가 포획되지 않고 속붕해되어 약효를 발현할 수 있게 되는 것이다.That is, unlike the conventional metformin sustained-release tablets, by using a hydrophilic polymer mixture and a hydrophobic material in selecting the release control material constituting the sustained release layer containing metformin, the tablet size can be made small so that oral administration is possible. In addition, the size of metformin was continuously released for 24 hours, so that the medicinal effect could be continued.The immediate release layer containing glymepiride constitutes the sustained release layer and the multi-layered tablet so that the contact surface between them is minimized, so that the release layer containing metformin swells. Glymepiride is not trapped, but quickly disintegrates to express the drug.
이러한 본 발명에 의하면, 기존의 메트포르민 제제가 1일 3회 투여되던 것과는 달리 1일 1회 투여만으로도 유효한 혈중 농도를 24 시간동안 지속할 수 있으며, 이렇게 체내에서 지속적인 농도를 유지하는 메트포르민은 체내소실 속도가 느린 글리메피리드와 지속적인 상승 작용을 나타낼 수 있으므로, 글리메피리드로 인한 혈중 농도의 급격한 상승 혹은 저하가 나타나지 않으므로 저혈당같은 부작용 역 시 효과적이고 지속적으로 차단할 수 있다. According to the present invention, unlike the conventional metformin formulations administered three times a day, effective once-daily administration can maintain effective blood levels for 24 hours, and metformin, which maintains a constant concentration in the body, thus loses body velocity May have a sustained synergistic effect with slow glymepiride, and thus no side effects such as hypoglycemia can be effectively and continuously blocked since there is no sudden rise or decrease in blood levels due to glymepireid.
또한, 글리메피리드와 병용투여시 이들 약물을 각각의 제제를 투여하던 것과는 달리 메트포르민과 글리메피리드를 단일정으로 투여할 수 있어 복약지도가 용이하고, 환자 순응도와 고용량 다빈도 투여시 혈중 농도의 차이에 의한 부작용 발생 등의 문제점을 해결할 수 있다.In addition, unlike the administration of these drugs in combination with glymepiride, metformin and glymepireide can be administered in a single tablet, so it is easy to guide the medication, and side effects due to the difference in the patient's compliance and the blood concentration during high-dose frequency administration Problems such as occurrence can be solved.
따라서, 본 발명은 글리메피리드와 메트포르민의 병용요법을 실시하는 당뇨 환자들에게 1일 1회 용법을 가능하게 하여 유용한 혈당 조절이 가능하도록 하는 신규한 약물 제어방출형 메트포르민-글리메피리드 복합제제를 제공하는데 그 목적이 있다.Accordingly, the present invention provides a novel drug-controlled release of metformin-glymepiride combination that enables the use of glycepiide and metformin in combination with once-daily treatment for diabetic patients who have a combination therapy of glycepiride and metformin. There is this.
본 발명은 메트포르민과 글리메피리드를 활성성분으로 하고 약학적으로 허용가능한 부형제를 포함하는 복합제제에 있어서, 활성성분으로서 메트포르민 또는 이의 약학적으로 허용가능한 염을 함유하며, 약학적으로 허용가능한 친수성 고분자 혼합물과 소수성 물질을 방출제어물질로 포함하는 서방층과, 활성성분으로서 글리메피리드 또는 이의 약학적으로 허용가능한 염을 함유하는 속방층을 포함하여 구성되며, 상기 서방층과 속방층이 타정되어 이루어진 다층정인 약물 제어방출형 메트포르민-글리메피리드 복합제제를 그 특징으로 한다.The present invention provides a combination formulation comprising metformin and glymepiride as an active ingredient and a pharmaceutically acceptable excipient, wherein the active ingredient contains metformin or a pharmaceutically acceptable salt thereof, and a pharmaceutically acceptable hydrophilic polymer mixture. A sustained release layer comprising a hydrophobic substance as a release controlling substance, and an immediate release layer containing glymepiride or a pharmaceutically acceptable salt thereof as an active ingredient, wherein the sustained release layer and the immediate release layer are tablets formed of a multi-layered tablet. It is characterized by a release metformin-glymepiride co-formulation.
이하 본 발명을 상세하게 설명하면 다음과 같다.Hereinafter, the present invention will be described in detail.
본 발명은 수용해성이 높고 단위 투여량이 큰 메트포르민의 방출이 24 시간 동안 지속적으로 이루어지도록 방출제어물질을 특이성 있게 선택설계하여 서방층을 구성하고, 수용해성이 낮고 단위 투여량이 적은 글리메피리드의 함량이 균일하게 유지되면서 빠르게 방출되도록 속방층을 구성하며, 특히 상기 서방층을 구성하는 부형제가 글리메피리드의 빠른 방출에 영향을 줄 수 없도록 서방층과 속방층의 방출층을 완전히 차단시키는 다층정 형태의 제형을 구현하여 메트포르민과 글리메피리드가 위치하는 상을 완전히 분리함으로써 각 약물의 상호 작용이 최소화되며 각 약물의 효과가 상호 보완적으로 지속되므로 특히 2형 당뇨병에 효과적인 경구 투여용 약물 제어방출형 메트포르민-글리메피리드 복합제제에 관한 것이다.The present invention constitutes a sustained release layer by specifically designing a release control material so that the release of metformin having a high water solubility and a high unit dose continuously for 24 hours, and a low water solubility and a low unit dose of glymepiride are uniform. The immediate release layer is configured to be rapidly released while maintaining the release, and in particular, the excipient constituting the sustained release layer implements a multi-layered formulation to completely block the release layer of the sustained release layer and the immediate release layer so that the excipient constituting the sustained release layer cannot be affected. By completely separating the phase where metformin and glymepire are located, the interaction of each drug is minimized, and the effects of each drug are complementary to each other. Therefore, the drug controlled-release metformin-glymepiride complex for oral administration, particularly effective for type 2 diabetes, It is about.
이하 본 발명의 약물 제어방출형 메트포르민-글리메피리드 복합제제를 구성성분별로 구체적으로 설명하면 다음과 같다.Hereinafter, the drug controlled-release metformin-glymepiride complex preparation of the present invention will be described in detail by component.
본 발명은 물리적으로 분리되거나 구획되어 2개의 약물의 상이한 방출 속도를 얻을 수 있도록 지연 방출형 메트포르민 조성물 및 즉시 방출을 위한 글리메피리드 조성물을 포함하는 투여 형태를 포함한다. 본 발명의 신규한 조성물은 물리적으로 분리되거나 구획되어 각각의 활성성분이 상이한 방출 속도를 얻을 수 있도록 메트포르민, 그의 약학적으로 허용 가능한 그의 염 및 원하는 부형제로 이루어지는 서방층과, 글리메피리드 및 원하는 부형제로 이루어지는 속방층으로 이루어진다. 이런 물리적인 구획은 다층정 형태의 제형으로 구현 가능하다. The present invention encompasses dosage forms comprising delayed release metformin compositions and glymepiride compositions for immediate release so that they can be physically separated or partitioned to achieve different release rates of the two drugs. The novel composition of the present invention consists of a sustained release layer consisting of metformin, its pharmaceutically acceptable salts and the desired excipients so that each active ingredient can be physically separated or partitioned to obtain different release rates, and glymepiride and the desired excipients. It consists of immediate layers. Such physical compartments may be embodied in a multi-layered formulation.
상기 서방층과 속방층은 100 : 10 ∼ 30 중량비로 구성되는 것이 각각의 활성성분의 투입량과 타정 후 정제의 크기를 고려할 때 가장 바람직하다. 또한, 본 발명의 약물 제어방출형 메트포르민-글리메피리드 복합제제는 서방층과 속방층 이 2층으로 압축적층된 이층정으로 구성될 수 있으며, 서방층을 포함되는 약물의 방출속도가 서로 다르게 조절된 2층의 서방층과 단일 속방층이 압축적층된 것으로, 상기 속방층이 제제의 최외각층을 구성하는 3층정으로 구성될 수도 있다.The sustained release layer and the immediate release layer is most preferably composed of 100: 10 to 30% by weight in consideration of the dosage of each active ingredient and the size of the tablet after tableting. In addition, the drug-controlled release metformin-glymepiride complex preparation of the present invention may be composed of a bilayer tablet in which the sustained release layer and the immediate release layer are compressed and laminated into two layers, and the release rate of the drug including the sustained release layer is differently controlled. The sustained release layer and the single immediate release layer of the layer are compression laminated, and the immediate release layer may be composed of three-layered tablets constituting the outermost layer of the formulation.
상기 메트포르민은 메트포르민 또는 이의 약학적으로 허용가능한 염의 형태로 사용할 수 있으며, 바람직하기로는 메트포르민의 염산염을 사용할 수 있다.The metformin may be used in the form of metformin or a pharmaceutically acceptable salt thereof, and preferably hydrochloride salt of metformin.
상기 복합제제에서 메트포르민은 염산염으로 환산할 때 250 ∼ 1000 mg, 바람직하게는 500 ∼ 750 mg 사용할 수 있고, 글리메피리드는 1 ∼ 8 mg, 바람직하게는 1 ∼ 2 mg을 사용할 수 있다.Metformin in the co-formulation may be used in the amount of 250 to 1000 mg, preferably 500 to 750 mg, and glymepyride may be 1 to 8 mg, preferably 1 to 2 mg, in terms of hydrochloride.
이러한 메트포르민은 서방층 중 55 ∼ 75 중량% 포함되도록 구성되는 것이 메트포르민을 원하는 정도의 지연 방출을 나타내기에 가장 적합하며, 글리메피리드는 속방층 중 0.05 ∼ 10 중량% 포함되는 것이 서방층의 매트릭스 기제에 포획되지 않고 속방출을 나타내기에 가장 바람직하다.Such metformin is best suited to exhibit a desired delayed release of metformin to be comprised of 55 to 75% by weight of the sustained release layer, and glymepyride is contained in the matrix base of the slow release layer to contain 0.05 to 10% by weight of the immediate release layer. Most preferred to exhibit rapid release.
이하, 본 발명의 복합제제를 이층정을 위주로 설명한다.Hereinafter, the composite preparation of the present invention will be described based on two-layered tablets.
본 발명의 복합제제를 이층정으로 구성할 경우 서방층과 속방층이 평행하게 압착된 층구조를 구성할 수 있는데,When the composite preparation of the present invention is composed of two-layered tablets, the sustained-release layer and the immediate release layer may be configured to have a compressed layer structure in parallel.
상기 서방층은 활성성분으로서 메트포르민 또는 이의 약학적으로 허용가능한 염을 함유하며, 약학적으로 허용가능한 친수성 고분자 혼합물과 소수성 물질을 방출제어물질을 함유하여 구성된다. 이때, 통상적으로 당분야에서 허용되는 통상의 부형제를 혼합하여 사용할 수 있음은 자명하다. The sustained release layer contains metformin or a pharmaceutically acceptable salt thereof as the active ingredient, and is composed of a pharmaceutically acceptable hydrophilic polymer mixture and a hydrophobic substance containing a release controlling substance. At this time, it is obvious that can be used in combination with conventional excipients that are commonly accepted in the art.
본 발명에서는 서방층을 구성함에 있어서, 방출제어 물질을 서방층 전체 조 성물 중 10 ∼ 45 중량% 포함하는 것을 특징으로 하며, 친수성 고분자 혼합물과 소수성 물질을 혼합하여 사용한다.In the present invention, in the sustained release layer, the release control material comprises 10 to 45% by weight of the total composition of the sustained release layer, and a hydrophilic polymer mixture and a hydrophobic material are mixed and used.
즉, 상기 친수성 고분자의 선택으로 이의 수팽창에 의해 형성된 겔층의 공극 크기를 조절할 수 있어 약물 성분의 방출 속도를 1차적으로 조절할 수 있고, 상기 소수성 물질의 선택으로 겔층의 공극을 차단한 수 있어 약물 성분의 방출속도를 2차적으로 조절할 수 있으므로, 기존의 서방정보다 적은 양의 방출제어물질을 사용으로도 체내에서 일정한 속도로 약물 성분을 서서히 방출시킬 수 있는 우수한 용출 특성을 나타내므로 1일 1회 투여로 24 시간 동안 일정한 혈중 농도를 유지할 수 있다. 또한, 상기와 같이 방출제어물질을 선택사용함에 의해 속방층에 포함된 글리메피리드가 포획되어 방출이 지연되는 문제점을 해결할 수 있다.That is, by selecting the hydrophilic polymer can adjust the pore size of the gel layer formed by its water expansion can be controlled primarily the release rate of the drug component, by selecting the hydrophobic material can block the pores of the gel layer drug Since the rate of release of the ingredient can be controlled secondarily, it is superior to conventional western information, so it shows excellent dissolution characteristics that can slowly release the drug ingredient in the body at a constant rate even with the use of a small amount of release control substance. To maintain a constant blood level for 24 hours. In addition, it is possible to solve the problem that the release is delayed by trapping the glymepiride contained in the immediate release layer by the selective use of the emission control material as described above.
상기 친수성 고분자는 당류, 셀룰로오스 유도체, 검류, 단백질류, 폴리비닐 유도체, 폴리메타크릴레이트 공중합체, 폴리에칠렌 유도체 및 카르복시비닐폴리머 등 중에서 선택된 2 종 이상의 혼합물을 사용할 수 있다. 상기 친수성 고분자는 수팽창성 물질로서 용출액에 접하면 수팽창되어 겔화 과정이 진행된다. The hydrophilic polymer may be a mixture of two or more selected from sugars, cellulose derivatives, gums, proteins, polyvinyl derivatives, polymethacrylate copolymers, polyethylene derivatives, and carboxyvinyl polymers. The hydrophilic polymer is a water-expandable substance that is in contact with the eluate and expands in water to undergo gelation.
보다 구체적으로 상기 친수성 고분자는 덱스트린, 폴리덱스트린, 덱스트란, 펙틴 및 펙틴 유도체, 알긴산염, 폴리갈락투론산, 자일란, 아라비노자일란, 아라비노갈락탄, 전분, 히드록시프로필스타치, 아밀로오스 및 아밀로펙틴 등 중에서 선택된 당류; 히드록시프로필메칠셀룰로오스, 히드록시프로필셀룰로오스, 히드록시메칠셀룰로오스, 히드록시에칠셀룰로오스, 메칠셀룰로오스, 카르복시메칠셀룰로오스 나트륨, 셀룰로오스 아세테이트 프탈레이트, 히드록시프로필 메칠셀룰로오스 아세테 이트 숙시네이트 및 히드록시에칠메칠셀룰로오스 등 중에서 선택된 셀룰로오스 유도체; 구아검, 로커스트빈 검, 트라가칸타, 카라기난, 아카시아검, 아라비아검 및 젤란검 등 중에서 선택된 검류; 젤라틴, 카제인 및 제인 등 중에서 선택된 단백질류; 폴리비닐 알코올, 폴리비닐 피롤리돈 및 폴리비닐아세탈디에칠아미노아세테이트 등 중에서 선택된 폴리비닐 유도체; 폴리(부틸 메타크릴레이트,(2-디메틸아미노에틸)메타크릴레이트, 메틸메타크릴레이트) 공중합체, 폴리(메타크릴산, 메틸메타크릴레이트) 공중합체 및 폴리(메타크릴산, 에틸아크릴레이트) 공중합체 등 중에서 선택된 폴리메타크릴레이트 공중합체; 폴리에틸렌 글리콜 및 폴리에칠렌 옥사이드 등 중에서 선택된 폴리에칠렌 유도체; 카르복시비닐폴리머로서 카보머 등 중에서 선택된 1 종 또는 2 종 이상의 혼합물을 사용할 수 있다.More specifically, the hydrophilic polymer is dextrin, polydextrin, dextran, pectin and pectin derivatives, alginates, polygalacturonic acid, xylan, arabinoxylan, arabinogalactan, starch, hydroxypropylstarch, amylose and amylopectin Sugars selected from among others; Hydroxypropylmethylcellulose, hydroxypropylcellulose, hydroxymethylcellulose, hydroxyethylcellulose, methylcellulose, carboxymethylcellulose sodium, cellulose acetate phthalate, hydroxypropylmethylcellulose succinate and hydroxyethylmethyl Cellulose derivatives selected from cellulose and the like; Gum selected from guar gum, locust bean gum, tragacantha, carrageenan, acacia gum, arabic gum and gellan gum; Proteins selected from gelatin, casein, zein and the like; Polyvinyl derivatives selected from polyvinyl alcohol, polyvinyl pyrrolidone, polyvinyl acetal diethyl amino acetate, and the like; Poly (butyl methacrylate, (2-dimethylaminoethyl) methacrylate, methylmethacrylate) copolymer, poly (methacrylic acid, methylmethacrylate) copolymer and poly (methacrylic acid, ethylacrylate) Polymethacrylate copolymers selected from copolymers and the like; Polyethylene derivatives selected from polyethylene glycol, polyethylene oxide and the like; As the carboxyvinyl polymer, one or a mixture of two or more selected from carbomer and the like can be used.
상기 소수성 물질은 수불용성 중합체, 소수성 화합물 또는 이들의 혼합물을 사용한다.The hydrophobic material uses a water insoluble polymer, a hydrophobic compound or a mixture thereof.
상기 수불용성 중합체는 약학적으로 허용 가능한 폴리비닐 아세테이트; 폴리(에틸아크릴레이트, 메칠 메타크릴레이트) 공중합체, 폴리(에칠아크릴레이트, 메칠 메타크릴레이트, 트리메칠아미노에칠메타크릴레이트)공중합체 등 중에서 선택된 폴리메타크릴레이트 공중합체; 에칠셀룰로오스, 셀룰로오스 아세테이트 등 중에서 선택된 셀룰로오스 유도체 중에서 선택된 1 종 또는 2 종 이상의 혼합물을 사용할 수 있다.The water insoluble polymer may be a pharmaceutically acceptable polyvinyl acetate; Polymethacrylate copolymers selected from poly (ethyl acrylate, methyl methacrylate) copolymer, poly (ethyl acrylate, methyl methacrylate, trimethylamino ethyl methacrylate) copolymer and the like; One or a mixture of two or more selected from cellulose derivatives selected from ethylcellulose, cellulose acetate and the like can be used.
상기 소수성 화합물은 글리세릴 팔미토스테아레이트, 글리세릴 스테아레이트, 글리세릴 비헤네이트, 세틸 팔미테이트, 글리세릴 모노 올레이트 및 스레아린산 등 중에서 선택된 지방산 및 지방산 에스테르류; 세토스테아릴 알코올, 세틸알코올 및 스테아릴알코올 등 중에서 선택된 지방산 알코올류; 카르나우바왁스, 밀납 및 미결정왁스 등 중에서 선택된 왁스류; 탈크, 침강탄산칼슘, 인산일수소칼슘, 산화아연, 산화티탄, 카올린, 벤토나이트, 몬모릴로나이트 및 비검 등 중에서 선택된 무기물질 중에서 선택된 1 종 또는 2 종 이상의 혼합물을 사용할 수 있다.The hydrophobic compound may be selected from fatty acids and fatty acid esters selected from glyceryl palmitostearate, glyceryl stearate, glyceryl bihenate, cetyl palmitate, glyceryl monooleate and sleanic acid; Fatty acid alcohols selected from cetostearyl alcohol, cetyl alcohol and stearyl alcohol; Waxes selected from carnauba wax, beeswax and microcrystalline wax; One or a mixture of two or more selected from inorganic materials selected from talc, precipitated calcium carbonate, calcium dihydrogen phosphate, zinc oxide, titanium oxide, kaolin, bentonite, montmorillonite, and non-gum can be used.
상기 친수성 고분자와 소수성 물질은 2 : 1 ∼ 20 : 1 중량비 범위로 포함하는 것이 방출성 조절 측면에서 바람직하다.It is preferable that the hydrophilic polymer and the hydrophobic material be included in a weight ratio of 2: 1 to 20: 1 in terms of controlled release.
상기 속방층은 활성성분으로서 글리메피리드 또는 이의 약학적으로 허용가능한 염을 함유하여 구성된다. 이때, 통상적으로 당분야에서 허용되는 통상의 부형제를 혼합하여 사용할 수 있음은 자명하다. The immediate release layer consists of glymepiride or a pharmaceutically acceptable salt thereof as the active ingredient. At this time, it is obvious that can be used in combination with conventional excipients that are commonly accepted in the art.
본 발명의 복합제제는 약학적으로 허용되는 담체로서 부형제를 필요에 따라 적절히 배합할 수 있고, 이외에도 착색제, 향료 중에서 선택된 다양한 첨가제로서 약학적으로 허용 가능한 첨가제를 선택 사용할 수 있다. 유효성분 이외에 사용될 수 있는 부형제 또는 첨가제 성분은 각각 1종 이상을 사용하여도 된다.
상기 부형제로는 붕해제, 희석제, 결합제 및 활택제 중에서 선택될 수 있다.The co-formulation of the present invention can be appropriately blended excipients as necessary as a pharmaceutically acceptable carrier, and in addition to the pharmaceutically acceptable additives can be selected as various additives selected from colorants and flavorings. Excipients or additives that may be used in addition to the active ingredient may each be used one or more.
The excipient may be selected from disintegrants, diluents, binders and lubricants.
붕해제로는 전분글리콘산 나트륨, 옥수수전분, 감자전분 또는 예비젤라틴화 전분 등의 전분 또는 변성전분과, 벤토나이트, 몬모릴나이트, 비검 등의 클레이와, 미결정셀룰로오스, 히드록시프로필셀룰로오스 또는 알긴류와, 크로스카멜로스 나트륨등의 가교 셀룰로오스류와 구아검, 잔탄검 등의 검류와, 크로스포비돈 등의 가교 중합체와, 중탄산나트륨, 시트르산 등의 비등성 제제 등을 혼합사용할 수 있다. 붕해제로는 바람직하게는 전분글리콜산 나트륨이 사용된다. 상기 붕해제는 정제의 단위 중량에 기초하여 0.01 ∼ 40 중량% 까지의 범위 내에서 혼합되어 질 수 있다. As a disintegrant, starch or modified starch, such as sodium starch glycolate, corn starch, potato starch or pregelatinized starch, clays such as bentonite, montmorillonite, non-gum, microcrystalline cellulose, hydroxypropyl cellulose or algins And crosslinked celluloses such as croscarmellose sodium, gums such as guar gum and xanthan gum, crosslinked polymers such as crospovidone, and boiling agents such as sodium bicarbonate and citric acid. As the disintegrant, sodium starch glycolate is preferably used. The disintegrant may be mixed in the range of 0.01 to 40% by weight based on the unit weight of the tablet.
희석제로 옥수수전분, 변형된 옥수수 전분, 유당, 포도당, 만니톨, 솔비톨, 알기네이트, 알카리토류금속염, 클레이, 탄산 칼슘같은 무기염 및 또는 목질 셀룰로오스, 미세결정 셀룰로오스와 같은 셀룰로오스 유도체 폴리에틸렌글리콜 및 디칼슘 포스페이트 등을 하나 이상 포함할 수 있다. 상기 희석제는 정제의 단위 중량에 기초하여 0.1 ∼ 90 중량%까지의 범위 내에서 혼합되어 질 수 있으며, 바람직하게는 0.1 ∼ 50 중량%를 사용할 수 있다. Diluents include corn starch, modified corn starch, lactose, glucose, mannitol, sorbitol, alginate, alkaline earth metal salts, clays, inorganic salts such as calcium carbonate and / or cellulose derivatives such as wood cellulose, microcrystalline cellulose polyethylene glycol and dicalcium phosphate And one or more. The diluent may be mixed in the range of 0.1 to 90% by weight based on the unit weight of the tablet, preferably 0.1 to 50% by weight can be used.
결합제로는 전분, 고분산성 실리카, 만니톨, 유당, 카르나우바 왁스, 파라핀, 경납, 폴리에틸렌왁스 폴리에틸렌 글리콜, 폴리비닐피롤리돈, 카르복시메틸셀룰로오스, 히드록시프로필 메틸셀룰로오스, 히드록시프로필셀룰로오스, 천연검, 합성검, 코포비돈 및 젤라틴 등을 사용할 수 있다. 상기 결합제는 정제의 단위 중량에 기초하여 3∼ 30 중량%까지의 범위 내에서 혼합되어 질 수 있으며, 바람직하게는 3 ∼ 10 중량%의 양을 포함한다. As binders, starch, highly dispersible silica, mannitol, lactose, carnauba wax, paraffin, braze, polyethylene wax polyethylene glycol, polyvinylpyrrolidone, carboxymethyl cellulose, hydroxypropyl methyl cellulose, hydroxypropyl cellulose, natural gum , Synthetic gums, copovidone, gelatin and the like can be used. The binder may be mixed in the range of 3 to 30% by weight based on the unit weight of the tablet, and preferably includes an amount of 3 to 10% by weight.
활택제로서 탈크, 스테아린산 마그네슘 및 알카리토금속, 스테아린산 칼슘, 아연등, 라우릴 설페이트, 수소화 식물성 오일, 나트륨 벤조에이트, 나트륨 스테아릴 푸마레이트, 글리세릴 모노스테아레이트 및 폴리에틸렌 글리콜, 글리세릴 베헤네이트 등으로 이루어진 군에서 하나 이상을 선택하여 사용할 수 있다. 상기 활택제는 정제의 단위 중량에 기초하여 0.05 ∼ 20 중량%까지의 범위 내에서 혼합되어 질 수 있으며, 바람직하게는 0.05 ∼ 2 중량%의 양을 포함한다. As lubricant, talc, magnesium stearate and alkaline earth metal, calcium stearate, zinc, lauryl sulfate, hydrogenated vegetable oil, sodium benzoate, sodium stearyl fumarate, glyceryl monostearate and polyethylene glycol, glyceryl behenate, etc. One or more selected from the group consisting of can be used. The lubricant may be mixed in the range of 0.05 to 20% by weight based on the unit weight of the tablet, and preferably includes an amount of 0.05 to 2% by weight.
임의로 존재할 수 있는 통상적인 또 다른 성분으로 방부제, 안정제, 항점착제 또는 경질무수규산 또는 유동화제, 착색제 등을 포함할 수 있다. Other conventional ingredients that may optionally be present may include preservatives, stabilizers, anti-tackifiers or light silicic anhydrides or glidants, colorants, and the like.
본 발명의 조성물의 정제는 0.1 ∼ 15 중량%를 구성하는 코팅 층을 포함할 수도 있다. 내부 고상입자를 그 안에 매립할 수 있는 외부 고상 위에 적용된 코팅층은 통상적인 코팅제를 포함할 수 있다. Tablets of the compositions of the present invention may comprise a coating layer constituting 0.1 to 15% by weight. The coating layer applied on the outer solid phase capable of embedding the inner solid particles therein may comprise a conventional coating agent.
상기 코팅층은 피막제, 피막 보조제 또는 이들의 혼합물을 사용할 수 있는데, 구체적으로 상기 코팅층은 피막제로서 셀룰로오스 유도체, 당 유도체, 폴리비닐 유도체, 왁스류, 지방류 및 젤라틴 등을 사용할 수 있고, 피막 보조제로서 폴리에틸렌글리콜, 에틸셀룰로오스, 글리세라이드류, 산화티탄 및 디에틸프탈레이트 등 중에서 선택된 1종 또는 2종 이상의 혼합물을 사용할 수 있다.The coating layer may be a coating agent, a coating aid or a mixture thereof. Specifically, the coating layer may be used as a coating agent, cellulose derivatives, sugar derivatives, polyvinyl derivatives, waxes, fats and gelatin, and polyethylene glycol as coating aids. Or a mixture of one or more selected from ethyl cellulose, glycerides, titanium oxide, diethyl phthalate and the like can be used.
필름형성제에는 물, 메틸알코올, 에틸알코올 또는 이소프로필 알코올같은 알코올, 아세톤, 에틸메틸케톤 같은 케톤, 메틸렌 클로라이드, 디클로로에탄, 및 1,1,1-트리클로로에탄 같은 클로로화 탄화수소를 포함하는 하나 이상의 용매가 포함될 수 있다. 바람직하게는 장기 복용되는 본 제제에서 장기복용시 문제의 소지가 있는 잔류용매에 의한 영향을 최소화 하고자 수계코팅을 기본으로 한다. 히드록시프로필메틸셀룰로오스와 같은 친수성 중합체를 하나이상, 폴리에틸렌글리콜과 같은 가소제를 하나 이상 포함할 수 있다. 착색제가 이용되는 경우, 착색 제는 필름형성제, 가소제 및 용매조성물 등과 함께 응용될 수 있다.Film forming agents include water, alcohols such as methyl alcohol, ethyl alcohol or isopropyl alcohol, ketones such as acetone, ethyl methyl ketone, methylene chloride, dichloroethane, and chlorolated hydrocarbons such as 1,1,1-trichloroethane The above solvent may be included. Preferably based on water-based coating in order to minimize the effect of the residual solvent in the long-term use of the problem in the long-term use of the formulation. One or more hydrophilic polymers, such as hydroxypropylmethylcellulose, and one or more plasticizers, such as polyethylene glycol. When a colorant is used, the colorant may be applied with a film forming agent, a plasticizer, a solvent composition, and the like.
이하, 본 발명의 복합제제를 다층정으로 제조하는 방법을 구체적으로 설명한다.Hereinafter, the method for producing the multi-layered tablet of the present invention will be described in detail.
먼저, 서방층의 활성성분으로서 메트포르민 또는 그의 약학적으로 허용되는 염과, 상기 활성성분의 서방출을 위한 제어방출물질, 상기의 붕해제, 희석제, 부형제, 결합제 및 활택제 등을 포함하는 약학적 조성물을 혼합한다.First, a pharmaceutical composition comprising metformin or a pharmaceutically acceptable salt thereof as an active ingredient of a sustained release layer, a controlled release material for sustained release of the active ingredient, a disintegrant, a diluent, an excipient, a binder and a lubricant, and the like. Mix the composition.
기제 내에는 유효성분인 메트포르민과 친수성 고분자와 소수성물질이 제어 방출을 위한 메트릭스를 형성하고 있다. 친수성 고분자는 팽윤하는 특성을 가지므로 위장내 체류시간을 연장시켜주며, 메트릭스 내에 포접되어 있는 메트포르민을 서서히 제어 방출한다. 소수성 물질은 시간이 지나면서 메트릭스 층 내의 공극을 막아줌으로써 약물이 방출을 지연시킨다. In the base, metformin, a hydrophilic polymer, and a hydrophobic material, which are active ingredients, form a matrix for controlled release. Hydrophilic polymers have the property of swelling, thus prolonging gastrointestinal retention time and slowly controlling release of metformin entrapped in the matrix. Hydrophobic materials delay the release of the drug by blocking the voids in the matrix layer over time.
이와는 별도로, 속방층이 활성성분으로서 글리메피리드 또는 그의 약학적으로 허용되는 염과, 붕해제, 희석제, 부형제, 결합제 및 활택제 등을 포함하는 약학적 조성물을 혼합, 과립화하는 단계이다.Apart from this, the immediate release layer is a step of mixing and granulating a pharmaceutical composition comprising a glimepiride or a pharmaceutically acceptable salt thereof as an active ingredient and a disintegrant, a diluent, an excipient, a binder, a lubricant, and the like.
상기 제조된 서방층의 혼합물과, 속방층의 과립물을 타정기의 각각의 호퍼에 넣고 압축하여 정제층을 형성한다. 혼합물의 경우 유동성이 직접 타정이 가능할 경우 직타법으로 타정하고, 유동성이 좋지 않을 경우 압착, 제립 및 정립하여 타정할 수 있다.The mixture of the sustained release layer and the granules of the immediate release layer were put into each hopper of the tableting machine and compressed to form a tablet layer. In the case of the mixture, the fluidity can be tableted by direct hitting when it is possible to tablet, and when the fluidity is not good, it can be compressed by compression, granulation and formulation.
이상에서 2층정을 제조하는 방법을 설명하였으나, 상기 다층정은 약물의 방출속도가 서로 다르게 조절된 2층의 서방층과 단일 속방층이 압축적층된 3층정으로서, 상기 속방층이 제제의 최외각층을 구성하는 3층정으로 제형화할 수 있다.Although the method of manufacturing the two-layered tablet has been described above, the multilayered tablet is a three-layered tablet in which the sustained-release layer and the single-release layer in which the drug release rate is controlled differently are compressed and laminated, and the immediate-release layer forms the outermost layer of the formulation. It can be formulated into a three-layered tablet.
상기한 본 발명의 복합제제는 나정으로 구성될 수 있으며, 필요에 따라 상기 정제층의 외면에 필름상의 코팅층을 형성시킨 코팅정으로 구성될 수도 있는데, 코팅층을 형성하여 사용할 경우 활성 성분의 안정성을 더욱 확보할 수 있는 장점이 있다.The complex preparation of the present invention may be composed of uncoated tablets, and may be composed of a coated tablet in which a film-like coating layer is formed on the outer surface of the tablet layer as necessary. There is an advantage to be secured.
상기 코팅층을 형성하는 방법은 상기한 성분들을 사용하여 정제층의 표면에 필름상의 코팅층을 형성할 수 있는 방법 중에서 당업자의 선택에 의하여 적절히 선택할 수 있으며, 유동층 코팅법, 팬코팅법 등의 방법을 적용할 수 있다. 바람직하기로는 팬 코팅법을 사용하는 것이 좋다.The method of forming the coating layer can be appropriately selected by the choice of those skilled in the art from the method of forming a film-like coating layer on the surface of the tablet layer using the above-described components, applying a method such as fluidized bed coating method, fan coating method can do. It is preferable to use a pan coating method.
본 발명의 활성성분인 메트포르민과 글리메피리드의 바람직한 투여량은 각각 250 ∼ 1000 ㎎, 1 ∼ 8 ㎎ 범위이며, 환자의 상태 및 체중, 질병의 정도, 약물형태, 투여경로 및 기간에 따라 다른데, 이는 당업자에 의해 적절하게 선택될 수 있다. Preferred dosages of metformin and glymepiride, the active ingredients of the present invention, range from 250 to 1000 mg and 1 to 8 mg, respectively, depending on the condition and weight of the patient, the extent of the disease, the form of the drug, the route of administration and the duration of time. Can be appropriately selected.
이하 실시예를 통하여 본 발명을 구체적으로 설명하나, 본 발명이 이에 한정 되는 것은 아니다Hereinafter, the present invention will be described in detail with reference to Examples, but the present invention is not limited thereto.
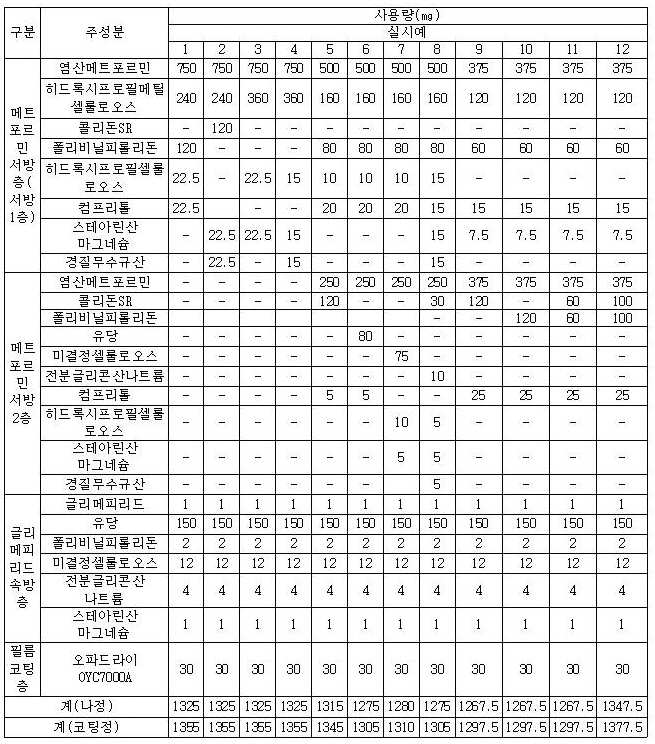
실시예Example 1 : 메트포르민 및 1: metformin and 글리메피리드의Glimepiride 이층정Two-story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방층 1) Metformin western layer
다음 표 1에 나타난 함량과 같이 더블콘믹서 내에 염산메트포르민, 히드록시프로필메틸셀룰로오스 및 폴리비닐필로리돈 및 히드록시프로필셀룰로오스를 넣고 혼합하였다. 상기 혼합물에 컴프리톨을 넣고 후혼합하였다.As shown in Table 1, metformin hydrochloride, hydroxypropylmethylcellulose and polyvinylpyrrolidone and hydroxypropyl cellulose were mixed and mixed in a double cone mixer. Compritol was added to the mixture and post-mixed.
2) 글리메피리드 속방층 2) Glymepyride Immediate Layer
다음 표 1에 나타난 함량과 같이 고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립화하였다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 이용해 활택 처리하였다.As shown in Table 1, it was mixed with glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate in a high speed mixer. The mixture was granulated with polyvinylpyrrolidone binding solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were lubricated with magnesium stearate.
3) 타정 및 코팅3) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 2개의 호퍼 내에 공급한 뒤, 이층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into two different hoppers of the tableting machine and then compressed into bilayer tablets. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 2 : 메트포르민 및 2: metformin and 글리메피리드의Glimepiride 이층정Two-story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방층 1) Metformin western layer
다음 표 1에 나타난 함량과 같이 더블콘믹서 내에 염산메트포르민, 히드록시프로필메틸셀룰로오스, 콜리돈SR 및 경질무수규산을 넣고 혼합하였다. 상기 혼합물에 컴프리톨을 넣고 후혼합하였다.As shown in Table 1, metformin hydrochloride, hydroxypropylmethylcellulose, collidone SR and hard silicic anhydride were added and mixed in a double cone mixer. Compritol was added to the mixture and post-mixed.
2) 글리메피리드 속방층 2) Glymepyride Immediate Layer
다음 표 1에 나타난 함량과 같이 고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립화 하였다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 이용해 활택 처리한다.As shown in Table 1, it was mixed with glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate in a high speed mixer. The mixture was granulated with polyvinylpyrrolidone binding solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules are lubricated with magnesium stearate.
3) 타정 및 코팅3) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 2개의 호퍼 내에 공급한 뒤, 이층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into two different hoppers of the tableting machine and then compressed into bilayer tablets. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예 3 : 메트포르민 및 글리메피리드의 이층정 형태의 제어 방출 제제Example 3 Controlled Release Formulations in Two-Layered Forms of Metformin and Glimepiride
1) 메트포르민 서방층 1) Metformin western layer
다음 표 1에 나타난 함량과 같이 더블콘믹서 내에 염산메트포르민, 히드록시프로필메틸셀룰로오스 및 히드록시프로필셀룰로오스을 넣고 혼합하였다. 상기 혼합물에 스테아린산 마그네슘을 넣고 후혼합한다.As shown in Table 1, metformin hydrochloride, hydroxypropylmethylcellulose and hydroxypropylcellulose were added and mixed in a double cone mixer. Magnesium stearate is added to the mixture and then mixed.
2) 글리메피리드 속방층 2) Glymepyride Immediate Layer
다음 표 1에 나타난 함량과 같이 고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립화 하였다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 이용해 활택 처리한다.As shown in Table 1, it was mixed with glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate in a high speed mixer. The mixture was granulated with polyvinylpyrrolidone binding solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules are lubricated with magnesium stearate.
3) 타정 및 코팅3) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 2개의 호퍼 내에 공급한 뒤, 혼입을 최소화 할 수 있는 이층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into two different hoppers of the tableting machine and then compressed into bilayer tablets to minimize incorporation. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 4 : 메트포르민 및 4: metformin and 글리메피리드의Glimepiride 이층정Two-story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방층 1) Metformin western layer
다음 표 1에 나타난 함량과 같이 더블콘믹서 내에 염산메트포르민, 히드록시프로필메틸셀룰로오스, 히드록시프로필셀룰로오스, 경질무수규산을 넣고 혼합하였다. 상기 혼합물에 스테아린산 마그네슘을 넣고 후혼합하였다.As shown in Table 1, metformin hydrochloride, hydroxypropylmethylcellulose, hydroxypropylcellulose, and hard silicic anhydride were mixed in a double cone mixer. Magnesium stearate was added to the mixture, followed by post-mixing.
2) 글리메피리드 속방층 2) Glymepyride Immediate Layer
다음 표 1에 나타난 함량과 같이 고속혼합기 내에 글리메피리드, 유당 및 미 결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립화 하였다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 이용해 활택 처리한다.As shown in Table 1, it was mixed with glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate in a high speed mixer. The mixture was granulated with polyvinylpyrrolidone binding solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules are lubricated with magnesium stearate.
3) 타정 및 코팅3) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 2개의 호퍼 내에 공급한 뒤, 혼입을 최소화 할 수 있는 조건으로 이층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into two different hoppers of the tableting machine and then compressed into bilayer tablets on conditions that minimize incorporation. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 5 : 메트포르민 및 5: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표 1에 나타난 의약품의 분량으로 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.To the amount of the drug shown in Table 1 was prepared in the same manner as the manufacturing method of the metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 콜리돈SR을 넣고 혼합하였다. 상기 혼합물에 컴프리톨을 넣고 후혼합하였다.Metformin hydrochloride and collidone SR were added and mixed in a double cone mixer. Compritol was added to the mixture and post-mixed.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립화 하였다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합한다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture was granulated with polyvinylpyrrolidone binding solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules are added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 혼입을 최소화 할 수 있는 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets to minimize incorporation. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 6 : 메트포르민 및 6: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표 1에 나타난 의약품의 분량으로 상기 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.Next, the amount of the drug shown in Table 1 was prepared in the same manner as in the preparation method of metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 유당을 넣고 혼합하였다. 상기 혼합물에 컴프리톨을 넣고 후혼합하였다.Metformin hydrochloride and lactose were added and mixed in a double cone mixer. Compritol was added to the mixture and post-mixed.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립화 하였다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합하였다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture was granulated with polyvinylpyrrolidone binding solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 혼입을 최소화 할 수 있는 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets to minimize incorporation. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 7 : 메트포르민 및 7: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표1에 나타난 의약품의 분량으로 상기 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.To the amount of the drug shown in Table 1 was prepared in the same manner as in the preparation method of the metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 미결정셀룰로오스, 히드록시프로필셀룰로오스를 넣고 혼합하였다. 상기 혼합물에 스테아린산 마그네슘을 넣고 후혼합하였다.Metformin hydrochloride, microcrystalline cellulose, and hydroxypropyl cellulose were placed in a double cone mixer and mixed. Magnesium stearate was added to the mixture, followed by post-mixing.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립화 하였다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합하였다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture was granulated with polyvinylpyrrolidone binding solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 혼입을 최소화 할 수 있는 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets to minimize incorporation. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 8 : 메트포르민 및 8: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표 1에 나타난 의약품의 분량으로 상기 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.Next, the amount of the drug shown in Table 1 was prepared in the same manner as in the preparation method of metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 콜리돈SR, 전분글리콘산 나트륨, 히드록시프로필셀룰로오스, 경질무수규산을 넣고 혼합하였다. 상기 혼합물에 스테아린산 마그네슘을 넣고 후혼합하였다.Metformin hydrochloride, collidone SR, sodium starch glycolate, hydroxypropyl cellulose, and hard silicic anhydride were added and mixed in a double cone mixer. Magnesium stearate was added to the mixture, followed by post-mixing.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립한다. 상기 과립을 60℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합하였다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture is granulated with polyvinylpyrrolidone binder solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 9 : 메트포르민 및 9: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표 1에 나타난 의약품의 분량으로 상기 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.Next, the amount of the drug shown in Table 1 was prepared in the same manner as in the preparation method of metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 콜리돈SR을 넣고 혼합하였다. 상기 혼합물에 콤프리톨을 넣고 후혼합하였다.Metformin hydrochloride and collidone SR were added and mixed in a double cone mixer. Compritol was added to the mixture, followed by post-mixing.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립한다. 상기 과립을 60℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합하였다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture is granulated with polyvinylpyrrolidone binder solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 10 : 메트포르민 및 10: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표 1에 나타난 의약품의 분량으로 상기 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.Next, the amount of the drug shown in Table 1 was prepared in the same manner as in the preparation method of metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 폴리비닐피롤리돈을 넣고 혼합하였다. 상기 혼합물에 콤프리톨을 넣고 후혼합하였다.Metformin hydrochloride and polyvinylpyrrolidone were added and mixed in a double cone mixer. Compritol was added to the mixture, followed by post-mixing.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립한다. 상기 과립을 60℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합하였다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture is granulated with polyvinylpyrrolidone binder solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 11 : 메트포르민 및 11: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표 1에 나타난 의약품의 분량으로 상기 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.Next, the amount of the drug shown in Table 1 was prepared in the same manner as in the preparation method of metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 콜리돈SR, 폴리비닐피롤리돈을 넣고 혼합하였다. 상기 혼합물에 콤프리톨을 넣고 후혼합하였다.Metformin hydrochloride, collidone SR, and polyvinylpyrrolidone were added and mixed in a double cone mixer. Compritol was added to the mixture, followed by post-mixing.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립한다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합하였다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture is granulated with polyvinylpyrrolidone binder solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실시예Example 12 : 메트포르민 및 12: metformin and 글리메피리드의Glimepiride 삼층정Three story 형태의 제어 방출 제제 Controlled release formulations in the form of
1) 메트포르민 서방 1층 1) Metformin West 1F
다음 표 1에 나타난 의약품의 분량으로 상기 실시예 1의 메트포르민 서방층의 제조방법과 동일하게 제조하였다.Next, the amount of the drug shown in Table 1 was prepared in the same manner as in the preparation method of metformin sustained layer of Example 1.
2) 메트포르민 서방 2층 2) Metformin West 2nd Floor
더블콘믹서 내에 염산메트포르민, 콜리돈SR, 폴리비닐피롤리돈을 넣고 혼합하였다. 상기 혼합물에 콤프리톨을 넣고 후혼합하였다.Metformin hydrochloride, collidone SR, and polyvinylpyrrolidone were added and mixed in a double cone mixer. Compritol was added to the mixture, followed by post-mixing.
3) 글리메피리드 속방층 3) Glymepyride Immediate Layer
고속혼합기 내에 글리메피리드, 유당 및 미결정셀룰로오스, 전분글리콘산 나트륨과 혼합하였다. 상기 혼합물을 폴리비닐피롤리돈 결합액을 이용해 과립한다. 상기 과립을 60 ℃의 온도 조건으로 건조하고, 18 메쉬 범위로 체과하였다. 상기 체과한 과립을 스테아린산 마그네슘을 넣고 최종혼합하였다.Glymepiride, lactose and microcrystalline cellulose and sodium starch glycolate were mixed in a high speed mixer. The mixture is granulated with polyvinylpyrrolidone binder solution. The granules were dried at a temperature of 60 ° C. and sieved to the 18 mesh range. The sieved granules were added with magnesium stearate and finally mixed.
4) 타정 및 코팅4) tableting and coating
다층정 타정기(MRC-37T : 세종)를 사용하여 타정하였다. 메트포르민 및 글리메피리드를 함유하는 상기 과립들을 타정기의 상이한 3개의 호퍼 내에 공급한 뒤, 삼층 정제로 타정하였다. 하이코터(SFC-30N, 세종 기계, 한국)로서 필름 코팅 층을 형성하여 제조하였다.It was compressed using a multi-layer tablet press (MRC-37T: Sejong). The granules containing metformin and glymepiride were fed into three different hoppers of the tableting machine and then compressed into three layer tablets. It was manufactured by forming a film coating layer as a high coater (SFC-30N, Sejong Machinery, Korea).
실험예 1. 비교용출시험Experimental Example 1. Comparative Dissolution Test
상기 실시예 1, 실시예 5에 의하여 제조된 메트포르민 서방정과 글리메피리드의 이층정 중에서 메트포르민의 비교용출시험을 진행하였다. 대조약은 미국에서 시판되어있는 제품을 사용하였다.(글루코파지750 엑스알, BMS)The comparative dissolution test of metformin was carried out in two-layered tablets of metformin sustained-release tablets and glymepiride prepared according to Examples 1 and 5. The control drug used was a product commercially available in the United States (glucophage 750 xal, BMS).
대한 약전 일반시험법 중 용출 시험항에 패들법으로 용출특성을 측정하였으며, 그 결과를 각각 도 1, 도 2와 같이 나타내었다. 시험결과에 따르면 메트포르민의 다층정 형태의 서방정을 만들때 일반 서방정과 유사한 용출특성을 나타내었다. The dissolution characteristics were measured by paddle method in the dissolution test term of the KEPCO general test method, and the results are shown as shown in FIGS. 1 and 2, respectively. According to the test results, the elution characteristics of metformin multi-layered sustained-release tablets were similar to those of general sustained-release tablets.
실험예Experimental Example 2. 비교용출시험 2. Comparative Dissolution Test
상기 실시예 1에 의하여 제조된 메트포르민 서방정과 글리메피리드의 이층정 중에서 글리메피리드의 비교용출시험을 진행하였다. 대조약은 시판되어있는 제품을 사용하였다.(아마릴, 한독아벤티스)The comparative dissolution test of glymepiride was carried out in a bilayer tablet of metformin sustained-release tablet and glymepiride prepared according to Example 1. The reference drug used was a commercially available product (Amaryl, Handok Aventis).
대한 약전 일반시험법 중 용출 시험항에 패들법으로 용출특성을 측정하였으며, 그 결과를 첨부도면 도 3과 같이 나타내었다. 시험결과에 따르면 본 발명의 이층정에서의 글리메피리드가 일반 글리메피리드 보다 빠른 용출특성을 나타내었다. The dissolution characteristics were measured by paddle method in the dissolution test term of the KEPCO general test method, and the results are shown in the accompanying drawings. According to the test results, glymepiride in the double-layered tablet of the present invention showed faster dissolution characteristics than general glymepiride.
상술한 바와 같이, 본 발명에 의하면 메트포르민과 글리메피리드의 다층정제는 메트포르민과 글리메피리드를 함께 복용하는 당뇨환자에게 각각의 약물의 복용방법차이(메트포르민 1일 3회, 글리메피리드 1일 1회)에 의한 환자의 혼란을 막고 복약 순응도를 높일 수 있다. As described above, according to the present invention, the multi-layered tablet of metformin and glymepiride is used in the diabetic patients taking metformin and glymepiride. This can prevent confusion and increase medication compliance.
또한 본 발명에 의하면 메트포르민 서방층과 글리메피리드 속방층의 다층정제는 메트포르민과 글리메피리드를 함께 복용하는 당뇨환자에게 기존제제에 비하여글리메피리드의 속방출로 인해 보다 빠른 약효를 기대할 수 있으며, 메트포르민의 서방출로 인해 보다 지속적인 약효를 기대할 수 있다.In addition, according to the present invention, the multi-layer tablet of metformin sustained-release layer and glymepiride immediate release layer can be expected to have a faster medicinal effect due to the rapid release of glymepiride compared to the conventional formulation to diabetic patients taking metformin and glymepiride together, and due to the sustained release of metformin. More sustainable effects can be expected.
또한 본 발명에 의한 메트포르민 서방층과 글리메피리드 속방층의 다층정제를 복용하는 경우 소실 속도가 느린 글리메피리드와 지속 방출되는 메트포르민은 약효유지시간동안 지속적인 약물상승효과를 기대할 수 있어 혈당의 조절에 보다 큰 유용성을 가질 수 있다.In addition, when taking multi-layered tablets of the metformin sustained-release layer and the glymepiride immediate release layer according to the present invention, the slow disappearing glymepiride and sustained-release metformin can be expected to have a sustained drug synergistic effect during the drug retention time, thereby increasing the usefulness of blood glucose control. Can have
또한 본 발명에 의하여 다층정을 구성하면 메트포르민 제어 방출의 팽윤 현상에 의해 글리메피리드층이 포획되는 것을 막을 수 있다. 포획되지 않고 빠르게 방출되는 글리메피리드층으로 투여 초기에 혈당관리에 보다 더 큰 유용함을 가진다. In addition, by constructing a multi-layered tablet according to the present invention, it is possible to prevent the glymepiride layer from being captured by the swelling phenomenon of metformin controlled release. The glymepiride layer, which is not captured and rapidly released, has greater utility in managing blood glucose at the beginning of administration.
또한 본 발명에 의하면 단일정제에서 많은 질량비율을 차지하는 메트포르민과 그렇지 않은 글리메피리드의 혼합에서 발생하는 함량불균일성을 다층정제를 구성함으로써 해결할 수 있다.In addition, according to the present invention, it is possible to solve the content non-uniformity caused by the mixing of metformin and glymepiride, which occupy a large mass ratio in a single tablet, by constructing a multilayer tablet.
Claims (22)
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020060102912A KR100812538B1 (en) | 2006-10-23 | 2006-10-23 | Drug-controlled metformin-glymepiride combination |
| PCT/KR2007/005197 WO2008050987A1 (en) | 2006-10-23 | 2007-10-23 | Combination formulation with controlled release comprising metformin and glimepiride |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020060102912A KR100812538B1 (en) | 2006-10-23 | 2006-10-23 | Drug-controlled metformin-glymepiride combination |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR100812538B1 true KR100812538B1 (en) | 2008-03-11 |
Family
ID=39324743
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020060102912A Expired - Fee Related KR100812538B1 (en) | 2006-10-23 | 2006-10-23 | Drug-controlled metformin-glymepiride combination |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR100812538B1 (en) |
| WO (1) | WO2008050987A1 (en) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010005257A3 (en) * | 2008-07-11 | 2010-04-01 | 주식회사 엘지생명과학 | Controlled-release pharmaceutical preparation containing nicorandil |
| WO2010071321A3 (en) * | 2008-12-15 | 2010-10-21 | 씨제이 제일제당(주) | ORAL FORMULATIONS CONTAINING METFORMIN AND α-GLYCOSIDASE INHIBITOR, AND PREPARATION METHOD THEREOF |
| KR101050076B1 (en) * | 2009-02-04 | 2011-07-19 | 한국유나이티드제약 주식회사 | Compositions of Oral Formulations Containing Controlled Release Aceclofenac and Methods for Making the Same |
| WO2011152652A3 (en) * | 2010-06-01 | 2012-03-08 | 한국유나이티드제약 주식회사 | Aceclofenac slow-release preparation providing an optimum pharmacological clinical effect when administered once a day |
| WO2013095042A3 (en) * | 2011-12-23 | 2013-08-15 | 씨제이제일제당(주) | Granule containing imatinib mesylate, immediate release oral tablet composition containing same, and preparation method thereof |
| WO2013169007A1 (en) * | 2012-05-11 | 2013-11-14 | 안국약품 주식회사 | Sustained-release complex preparations for treating diabetes with improved drug compliance and method for preparing same |
| KR20150068730A (en) * | 2013-12-12 | 2015-06-22 | 한미약품 주식회사 | Bilayered tablet composite formulation comprising metformin and losartan |
| WO2017073897A1 (en) * | 2015-10-28 | 2017-05-04 | Chong Kun Dang Pharmaceutical Corp. | Pharmaceutical composition comprising metformin and lobeglitazone |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2025674A1 (en) | 2007-08-15 | 2009-02-18 | sanofi-aventis | Substituted tetra hydro naphthalines, method for their manufacture and their use as drugs |
| WO2010045656A2 (en) * | 2008-10-17 | 2010-04-22 | Nectid, Inc. | Novel sglt2 inhibitor dosage forms |
| KR101076648B1 (en) * | 2008-12-04 | 2011-10-26 | 한국유나이티드제약 주식회사 | Controlled-release Aceclofenac Containing Oral Drug Preparations and it's Manufacturing Process |
| US20110009347A1 (en) | 2009-07-08 | 2011-01-13 | Yin Liang | Combination therapy for the treatment of diabetes |
| CN102740839B (en) | 2009-11-13 | 2015-05-06 | 阿斯利康(瑞典)有限公司 | immediate release tablet |
| WO2011107494A1 (en) | 2010-03-03 | 2011-09-09 | Sanofi | Novel aromatic glycoside derivatives, medicaments containing said compounds, and the use thereof |
| DE102010015123A1 (en) | 2010-04-16 | 2011-10-20 | Sanofi-Aventis Deutschland Gmbh | New benzylamidic diphenylazetidinone compounds, useful for treating lipid disorders, hyperlipidemia, atherosclerotic manifestations or insulin resistance, and for reducing serum cholesterol levels |
| NZ703128A (en) | 2010-05-11 | 2016-04-29 | Janssen Pharmaceutica Nv | Pharmaceutical formulations comprising 1 - (beta-d-glucopyranosyl) - 2 -thienylmethylbenzene derivatives as inhibitors of sglt |
| WO2011157827A1 (en) | 2010-06-18 | 2011-12-22 | Sanofi | Azolopyridin-3-one derivatives as inhibitors of lipases and phospholipases |
| US8530413B2 (en) | 2010-06-21 | 2013-09-10 | Sanofi | Heterocyclically substituted methoxyphenyl derivatives with an oxo group, processes for preparation thereof and use thereof as medicaments |
| TW201215388A (en) | 2010-07-05 | 2012-04-16 | Sanofi Sa | (2-aryloxyacetylamino)phenylpropionic acid derivatives, processes for preparation thereof and use thereof as medicaments |
| TW201215387A (en) | 2010-07-05 | 2012-04-16 | Sanofi Aventis | Spirocyclically substituted 1,3-propane dioxide derivatives, processes for preparation thereof and use thereof as a medicament |
| TW201221505A (en) | 2010-07-05 | 2012-06-01 | Sanofi Sa | Aryloxyalkylene-substituted hydroxyphenylhexynoic acids, process for preparation thereof and use thereof as a medicament |
| AU2011276332A1 (en) * | 2010-07-06 | 2013-01-17 | Janssen Pharmaceutica Nv | Formulation for co-therapy treatment of diabetes |
| WO2013037390A1 (en) | 2011-09-12 | 2013-03-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-styryl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| EP2567959B1 (en) | 2011-09-12 | 2014-04-16 | Sanofi | 6-(4-hydroxy-phenyl)-3-styryl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| EP2760862B1 (en) | 2011-09-27 | 2015-10-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-alkyl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| CN103505466B (en) * | 2012-06-20 | 2016-02-10 | 天津药物研究院 | Solid compound preparation containing metformin hydrochloride and glimepiride and its production and use |
| US8962020B2 (en) * | 2012-07-26 | 2015-02-24 | Glycadia Inc. | Long-acting and controlled release formulations of 2-[(3-chlorophenyl) amino] phenylacetic acid |
| CN103584083B (en) * | 2013-10-15 | 2015-11-11 | 中国科学院南海海洋研究所 | A kind of enteral nutrition preparation for gestational diabetes mellitus women and its production and use |
| GB201420300D0 (en) * | 2014-11-14 | 2014-12-31 | Bio Images Drug Delivery Ltd | Tablet |
| GB201420311D0 (en) | 2014-11-14 | 2014-12-31 | Bio Images Drug Delivery Ltd | Pharmaceutical processing |
| GB201420306D0 (en) | 2014-11-14 | 2014-12-31 | Bio Images Drug Delivery Ltd | Compositions |
| CN114469896B (en) * | 2020-10-26 | 2024-11-08 | 江苏万邦生化医药集团有限责任公司 | A kind of metformin hydrochloride sustained-release empagliflozin immediate-release micropill and preparation method thereof |
| EP4255495A4 (en) | 2020-12-03 | 2025-10-08 | Battelle Memorial Institute | POLYMER NANOPARTICLE AND DNA NANOSTRUCTURE COMPOSITIONS AND METHODS FOR NONVIRAL DELIVERY |
| WO2022216977A1 (en) | 2021-04-07 | 2022-10-13 | Batelle Memorial Institute | Rapid design, build, test, and learn technologies for identifying and using non-viral carriers |
| WO2025072751A1 (en) | 2023-09-29 | 2025-04-03 | Battelle Memorial Institute | Polymer nanoparticle compositions for in vivo expression of polypeptides |
| US12441996B2 (en) | 2023-12-08 | 2025-10-14 | Battelle Memorial Institute | Use of DNA origami nanostructures for molecular information based data storage systems |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4713248A (en) | 1984-02-10 | 1987-12-15 | A/S Alfred Benzon | Diffusion coated multiple-units dosage form |
| WO1999012524A1 (en) * | 1997-09-11 | 1999-03-18 | Nycomed Danmark A/S | MODIFIED RELEASE MULTIPLE-UNITS COMPOSITIONS OF NON-STEROID ANTI-INFLAMMATORY DRUG SUBSTANCES (NSAIDs) |
| WO2003103637A2 (en) * | 2002-01-10 | 2003-12-18 | Ranbaxy Laboratories Limited | Modified release, multiple unit drug delivery systems |
| KR20060051510A (en) * | 2004-09-23 | 2006-05-19 | 주식회사 한독약품 | Pharmaceutical combinations for the treatment of diabetes for oral administration |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9619757D0 (en) * | 1996-09-21 | 1996-11-06 | Knoll Ag | Chemical process |
| GB9715295D0 (en) * | 1997-07-18 | 1997-09-24 | Smithkline Beecham Plc | Novel method of treatment |
| SK287038B6 (en) * | 1998-11-12 | 2009-10-07 | Smithkline Beecham Plc | Pharmaceutical composition for modified release of 5-[4-[2-(N- methyl-N-(2-pyridyl)amino)ethoxy]benzyl]thiazolidine-2,4-dione and metformin and process for preparing thereof |
| US6682759B2 (en) * | 2002-02-01 | 2004-01-27 | Depomed, Inc. | Manufacture of oral dosage forms delivering both immediate-release and sustained-release drugs |
-
2006
- 2006-10-23 KR KR1020060102912A patent/KR100812538B1/en not_active Expired - Fee Related
-
2007
- 2007-10-23 WO PCT/KR2007/005197 patent/WO2008050987A1/en not_active Ceased
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4713248A (en) | 1984-02-10 | 1987-12-15 | A/S Alfred Benzon | Diffusion coated multiple-units dosage form |
| WO1999012524A1 (en) * | 1997-09-11 | 1999-03-18 | Nycomed Danmark A/S | MODIFIED RELEASE MULTIPLE-UNITS COMPOSITIONS OF NON-STEROID ANTI-INFLAMMATORY DRUG SUBSTANCES (NSAIDs) |
| WO2003103637A2 (en) * | 2002-01-10 | 2003-12-18 | Ranbaxy Laboratories Limited | Modified release, multiple unit drug delivery systems |
| KR20060051510A (en) * | 2004-09-23 | 2006-05-19 | 주식회사 한독약품 | Pharmaceutical combinations for the treatment of diabetes for oral administration |
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010005257A3 (en) * | 2008-07-11 | 2010-04-01 | 주식회사 엘지생명과학 | Controlled-release pharmaceutical preparation containing nicorandil |
| WO2010071321A3 (en) * | 2008-12-15 | 2010-10-21 | 씨제이 제일제당(주) | ORAL FORMULATIONS CONTAINING METFORMIN AND α-GLYCOSIDASE INHIBITOR, AND PREPARATION METHOD THEREOF |
| KR101050076B1 (en) * | 2009-02-04 | 2011-07-19 | 한국유나이티드제약 주식회사 | Compositions of Oral Formulations Containing Controlled Release Aceclofenac and Methods for Making the Same |
| WO2011152652A3 (en) * | 2010-06-01 | 2012-03-08 | 한국유나이티드제약 주식회사 | Aceclofenac slow-release preparation providing an optimum pharmacological clinical effect when administered once a day |
| CN102917696A (en) * | 2010-06-01 | 2013-02-06 | 韩国联合制药株式会社 | Aceclofenac slow-release preparation providing an optimum pharmacological clinical effect when administered once a day |
| CN102917696B (en) * | 2010-06-01 | 2015-04-01 | 韩国联合制药株式会社 | Aceclofenac slow-release preparation providing an optimum pharmacological clinical effect when administered once a day |
| WO2013095042A3 (en) * | 2011-12-23 | 2013-08-15 | 씨제이제일제당(주) | Granule containing imatinib mesylate, immediate release oral tablet composition containing same, and preparation method thereof |
| WO2013169007A1 (en) * | 2012-05-11 | 2013-11-14 | 안국약품 주식회사 | Sustained-release complex preparations for treating diabetes with improved drug compliance and method for preparing same |
| KR20150068730A (en) * | 2013-12-12 | 2015-06-22 | 한미약품 주식회사 | Bilayered tablet composite formulation comprising metformin and losartan |
| KR102229798B1 (en) | 2013-12-12 | 2021-03-19 | 한미약품 주식회사 | Bilayered tablet composite formulation comprising metformin and losartan |
| WO2017073897A1 (en) * | 2015-10-28 | 2017-05-04 | Chong Kun Dang Pharmaceutical Corp. | Pharmaceutical composition comprising metformin and lobeglitazone |
| KR101750690B1 (en) | 2015-10-28 | 2017-06-27 | 주식회사 종근당 | Pharmaceutical composition comprising metformin and lobeglitazone |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2008050987A1 (en) | 2008-05-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100812538B1 (en) | Drug-controlled metformin-glymepiride combination | |
| KR100858848B1 (en) | Metformin sustained-release tablet | |
| KR100949273B1 (en) | Combination | |
| JP4633329B2 (en) | Spaced drug delivery system | |
| EP1515701B1 (en) | Process for the manufacture of multilayer tablet compositions comprising thiazolidinedione and biguanide | |
| KR20090091085A (en) | Pharmaceutical Release Controlled Release | |
| MXPA01013047A (en) | Multilayered tablet for administration of a fixed combination of tramadol and diclofenac. | |
| KR20130032316A (en) | Time-delayed sustained release pharmaceutical composition comprising dapoxetine for oral administration | |
| KR20090114330A (en) | Pharmaceutical preparations | |
| KR101164300B1 (en) | Pharmaceutical Preparation | |
| WO2011098483A1 (en) | Pharmaceutical compositions comprising a combination of metformin and sitagliptin | |
| KR20170008923A (en) | Pharmaceutical compositions comprising celecoxib and tramadol | |
| KR100780553B1 (en) | Metformin sustained-release tablet and preparation method thereof | |
| KR101512386B1 (en) | METHYLGENIDID AND METHORPHIN COMPOSITION AND PROCESS FOR PRODUCING THE SAME | |
| KR101869406B1 (en) | Controlled Released Hard Capsule Preparation | |
| WO2014170770A1 (en) | Solid oral pharmaceutical compositions comprising fixed dose combination of metformin and sitagliptin or salts thereof | |
| KR101128891B1 (en) | Controlled release multiple layer tablet comprising loratadine and pseudoephedrine | |
| KR101265491B1 (en) | Dissolution rate controlled multilayered tablet for oral administration containing sarpogrelate hydrochloride and manufacturing method thereof | |
| WO2009134053A2 (en) | Pharmaceutical composition containing thiazide-based compound with controlled release and angiotensin-ii-receptor blocker | |
| KR20090047310A (en) | Multi-layered tablet containing dexibuprofen | |
| KR20160105662A (en) | Pharmaceutical composition comprising eperison and pelubiprofen | |
| KR20110129405A (en) | Pharmaceutical preparations | |
| EP4297733A1 (en) | Fixed-dose pharmaceutical compositions | |
| KR20170001545A (en) | Mosapride sustained-release formulation and Composite formulation comprising mosapride and rabeprazole | |
| KR101441355B1 (en) | Bilayered tablet comprising repaglinide and metformin and the preparation method thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| FPAY | Annual fee payment |
Payment date: 20130305 Year of fee payment: 6 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| FPAY | Annual fee payment |
Payment date: 20140303 Year of fee payment: 7 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| FPAY | Annual fee payment |
Payment date: 20150302 Year of fee payment: 8 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 8 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| LAPS | Lapse due to unpaid annual fee | ||
| PC1903 | Unpaid annual fee |
St.27 status event code: A-4-4-U10-U13-oth-PC1903 Not in force date: 20160306 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20160306 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| R18 | Changes to party contact information recorded |
Free format text: ST27 STATUS EVENT CODE: A-5-5-R10-R18-OTH-X000 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |