JP7514834B2 - 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 - Google Patents
抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 Download PDFInfo
- Publication number
- JP7514834B2 JP7514834B2 JP2021531103A JP2021531103A JP7514834B2 JP 7514834 B2 JP7514834 B2 JP 7514834B2 JP 2021531103 A JP2021531103 A JP 2021531103A JP 2021531103 A JP2021531103 A JP 2021531103A JP 7514834 B2 JP7514834 B2 JP 7514834B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- pharmaceutical composition
- amino acid
- antigen
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/07—Tetrapeptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/183—Amino acids, e.g. glycine, EDTA or aspartame
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/22—Heterocyclic compounds, e.g. ascorbic acid, tocopherol or pyrrolidones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/545—Heterocyclic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/68031—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being an auristatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6889—Conjugates wherein the antibody being the modifying agent and wherein the linker, binder or spacer confers particular properties to the conjugates, e.g. peptidic enzyme-labile linkers or acid-labile linkers, providing for an acid-labile immuno conjugate wherein the drug may be released from its antibody conjugated part in an acidic, e.g. tumoural or environment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Organic Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Dermatology (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Endocrinology (AREA)
- Gastroenterology & Hepatology (AREA)
- Inorganic Chemistry (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
本出願は、2018年12月3日に出願された米国仮特許出願第62/774,819号に対する優先権の恩典を主張し、その開示は参照によりその全体が本明細書に組み入れられる。
抗191P4D12抗体薬物コンジュゲートを含む薬学的組成物が本明細書で提供される。この薬学的組成物を使用する方法も本明細書で提供される。
原薬は、通常、様々な特殊化された薬学的機能を果たす1つまたは複数の他の剤と組み合わせて製剤の一部として投与される。薬学的賦形剤は、様々な機能を有し、多くの異なる方法で、例えば、可溶化、希釈、増粘、安定化、防腐、着色、着香などで薬学的製剤に寄与する。活性原薬を製剤化する場合に考慮され得る特性には、バイオアベイラビリティ、製造の容易さ、投与の容易さ、および剤形の安定性が含まれる。製剤化される活性原薬の様々な特性のために、剤形は、典型的には、有利な物理的および薬学的特性を達成するために、活性原薬に合わせて独自に調整された薬学的賦形剤を必要とする。
一局面では、(a)モノメチルアウリスタチンE(MMAE)の1つまたは複数の単位にコンジュゲートされた、191P4D12に結合する抗体またはその抗原結合断片を含む抗体薬物コンジュゲートであって、抗体またはその抗原結合断片が、SEQ ID NO:7に示される重鎖可変領域の相補性決定領域(CDR)のアミノ酸配列を含むCDRを含む重鎖可変領域と、SEQ ID NO:8に示される軽鎖可変領域のCDRのアミノ酸配列を含むCDRを含む軽鎖可変領域とを含む、抗体薬物コンジュゲートと、(b)L-ヒスチジン、ポリソルベート20(TWEEN-20(登録商標))、およびトレハロース二水和物とスクロースの少なくとも一方を含む、薬学的に許容される賦形剤と、を含む薬学的組成物が本明細書で提供される。
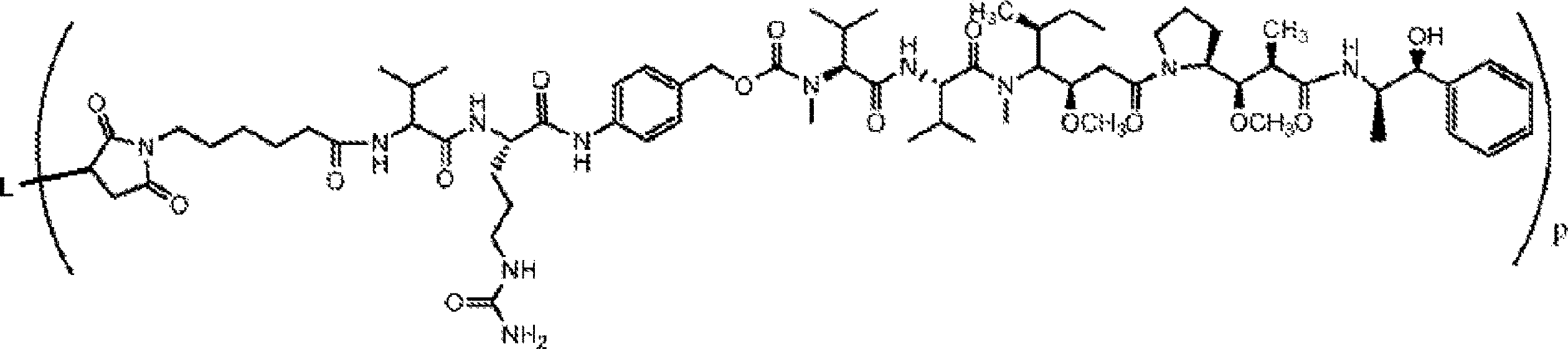
(a)以下の構造:
を有し、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、約5.5%(w/v)のトレハロース二水和物、およびHClを含む、薬学的に許容される賦形剤
を含み、pHは25℃で約6.0である。
(a)以下の構造:
を含み、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、約5.5%(w/v)のトレハロース二水和物、およびコハク酸を含む、薬学的に許容される賦形剤
を含み、pHは25℃で約6.0である。
(a)以下の構造:
を含み、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、約5.0%(w/v)のスクロース、およびHClを含む、薬学的に許容される賦形剤
を含み、pHは25℃で約6.0である。
[本発明1001]
(a)モノメチルアウリスタチンE(MMAE)の1つまたは複数の単位にコンジュゲートされた、191P4D12に結合する抗体またはその抗原結合断片を含む、抗体薬物コンジュゲートであって、該抗体またはその抗原結合断片が、SEQ ID NO:7に示される重鎖可変領域の相補性決定領域(CDR)のアミノ酸配列を含むCDRを含む重鎖可変領域と、SEQ ID NO:8に示される軽鎖可変領域のCDRのアミノ酸配列を含むCDRを含む軽鎖可変領域とを含む、抗体薬物コンジュゲート;ならびに
(b)L-ヒスチジン、ポリソルベート20(TWEEN-20(登録商標))、およびトレハロース二水和物とスクロースの少なくとも一方を含む、薬学的に許容される賦形剤
を含む、薬学的組成物。
[本発明1002]
抗体またはその抗原結合断片が、SEQ ID NO:9のアミノ酸配列を含むCDR H1、SEQ ID NO:10のアミノ酸配列を含むCDR H2、SEQ ID NO:11のアミノ酸配列を含むCDR H3、SEQ ID NO:12のアミノ酸配列を含むCDR L1、SEQ ID NO:13のアミノ酸配列を含むCDR L2、およびSEQ ID NO:14のアミノ酸配列を含むCDR L3を含む、本発明1001の薬学的組成物。
[本発明1003]
抗体またはその抗原結合断片が、SEQ ID NO:7の20番目のアミノ酸(グルタミン酸)から136番目のアミノ酸(セリン)までの範囲のアミノ酸配列を含む重鎖可変領域と、SEQ ID NO:8の23番目のアミノ酸(アスパラギン酸)から130番目のアミノ酸(アルギニン)までの範囲のアミノ酸配列を含む軽鎖可変領域とを含む、本発明1001の薬学的組成物。
[本発明1004]
抗体が、SEQ ID NO:7の20番目のアミノ酸(グルタミン酸)から466番目のアミノ酸(リジン)までの範囲のアミノ酸配列を含む重鎖と、SEQ ID NO:8の23番目のアミノ酸(アスパラギン酸)から236番目のアミノ酸(システイン)までの範囲のアミノ酸配列を含む軽鎖とを含む、本発明1001の薬学的組成物。
[本発明1005]
抗原結合断片がFab、F(ab') 2 、FvまたはscFv断片である、本発明1001~1004のいずれかの薬学的組成物。
[本発明1006]
抗体が完全ヒト抗体である、本発明1001~1005のいずれかの薬学的組成物。
[本発明1007]
抗体またはその抗原結合断片が組換え産生される、本発明1001~1006のいずれかの薬学的組成物。
[本発明1008]
抗体薬物コンジュゲートが以下の構造:
を有し、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、
本発明1001~1007のいずれかの薬学的組成物。
[本発明1009]
pが2~8である、本発明1008の薬学的組成物。
[本発明1010]
抗体または抗原結合断片が、リンカーを介してモノメチルアウリスタチンE(MMAE)の各単位に連結されている、本発明1001の薬学的組成物。
[本発明1011]
リンカーが、酵素切断可能なリンカーであり、抗体またはその抗原結合断片の硫黄原子と結合を形成する、本発明1010の薬学的組成物。
[本発明1012]
リンカーが-A a -W w -Y y -の式を有し、
式中、-A-は伸長単位であり、aは0または1であり、-W-はアミノ酸単位であり、wは0~12の範囲の整数であり、-Y-はスペーサ単位であり、yは0、1、または2である、
本発明1010の薬学的組成物。
[本発明1013]
伸長単位が以下の式(1)の構造を有し、アミノ酸単位がバリンシトルリンであり、スペーサ単位が以下の式(2)の構造を含むPAB基である、本発明1012の薬学的組成物:
。
[本発明1014]
伸長単位が抗体またはその抗原結合断片の硫黄原子と結合を形成し、スペーサ単位がカルバメート基を介してMMAEに連結されている、本発明1012の薬学的組成物。
[本発明1015]
抗体薬物コンジュゲートが、抗体またはその抗原結合断片当たり1~10単位のMMAEを含む、本発明1001の薬学的組成物。
[本発明1016]
抗体薬物コンジュゲートが、抗体またはその抗原結合断片当たり2~8単位のMMAEを含む、本発明1015の薬学的組成物。
[本発明1017]
1~20mg/mLの濃度の抗体薬物コンジュゲートを含む、本発明1001~1016のいずれかの薬学的組成物。
[本発明1018]
5~15mg/mLの濃度の抗体薬物コンジュゲートを含む、本発明1017の薬学的組成物。
[本発明1019]
8~12mg/mLの濃度の抗体薬物コンジュゲートを含む、本発明1017の薬学的組成物。
[本発明1020]
約10mg/mLの濃度の抗体薬物コンジュゲートを含む、本発明1017の薬学的組成物。
[本発明1021]
L-ヒスチジンが5~50mMの範囲で存在する、本発明1001~1020のいずれかの薬学的組成物。
[本発明1022]
L-ヒスチジンが10~40mMの範囲で存在する、本発明1001~1020のいずれかの薬学的組成物。
[本発明1023]
L-ヒスチジンが15~35mMの範囲で存在する、本発明1001~1020のいずれかの薬学的組成物。
[本発明1024]
L-ヒスチジンが15~30mMの範囲で存在する、本発明1001~1020のいずれかの薬学的組成物。
[本発明1025]
L-ヒスチジンが15~25mMの範囲で存在する、本発明1001~1020のいずれかの薬学的組成物。
[本発明1026]
L-ヒスチジンが約20mMで存在する、本発明1001~1020のいずれかの薬学的組成物。
[本発明1027]
TWEEN-20の濃度が0.001~0.1%(v/v)の範囲にある、本発明1001~1026のいずれかの薬学的組成物。
[本発明1028]
TWEEN-20の濃度が0.0025~0.075%(v/v)の範囲にある、本発明1001~1026のいずれかの薬学的組成物。
[本発明1029]
TWEEN-20の濃度が0.005~0.05%(v/v)の範囲にある、本発明1001~1026のいずれかの薬学的組成物。
[本発明1030]
TWEEN-20の濃度が0.01~0.03%(v/v)の範囲にある、本発明1001~1026のいずれかの薬学的組成物。
[本発明1031]
TWEEN-20の濃度が約0.02%(v/v)の範囲にある、本発明1001~1026のいずれかの薬学的組成物。
[本発明1032]
トレハロース二水和物を含む、本発明1001~1031のいずれかの薬学的組成物。
[本発明1033]
トレハロース二水和物が1~20%(w/v)の範囲で存在する、本発明1032の薬学的組成物。
[本発明1034]
トレハロース二水和物が2~15%(w/v)の範囲で存在する、本発明1032の薬学的組成物。
[本発明1035]
トレハロース二水和物が3~10%(w/v)の範囲で存在する、本発明1032の薬学的組成物。
[本発明1036]
トレハロース二水和物が4~6%(w/v)の範囲で存在する、本発明1032の薬学的組成物。
[本発明1037]
トレハロース二水和物が約5.5%(w/v)で存在する、本発明1032の薬学的組成物。
[本発明1038]
トレハロース二水和物が50mM~300mMの範囲で存在する、本発明1032の薬学的組成物。
[本発明1039]
トレハロース二水和物が75mM~250mMの範囲で存在する、本発明1032の薬学的組成物。
[本発明1040]
トレハロース二水和物が100mM~200mMの範囲で存在する、本発明1032の薬学的組成物。
[本発明1041]
トレハロース二水和物が130mM~150mMの範囲で存在する、本発明1032の薬学的組成物。
[本発明1042]
トレハロース二水和物が約146mMで存在する、本発明1032の薬学的組成物。
[本発明1043]
スクロースを含む、本発明1001~1031のいずれかの薬学的組成物。
[本発明1044]
スクロースが1~20%(w/v)の範囲で存在する、本発明1043の薬学的組成物。
[本発明1045]
スクロースが2~15%(w/v)の範囲で存在する、本発明1043の薬学的組成物。
[本発明1046]
スクロースが3~10%(w/v)の範囲で存在する、本発明1043の薬学的組成物。
[本発明1047]
スクロースが4~6%(w/v)の範囲で存在する、本発明1043の薬学的組成物。
[本発明1048]
スクロースが約5.5%(w/v)で存在する、本発明1043の薬学的組成物。
[本発明1049]
スクロースが50mM~300mMの範囲で存在する、本発明1043の薬学的組成物。
[本発明1050]
スクロースが75mM~250mMの範囲で存在する、本発明1043の薬学的組成物。
[本発明1051]
スクロースが100mM~200mMの範囲で存在する、本発明1043の薬学的組成物。
[本発明1052]
スクロースが130mM~150mMの範囲で存在する、本発明1043の薬学的組成物。
[本発明1053]
スクロースが約146mMで存在する、本発明1043の薬学的組成物。
[本発明1054]
5.5~6.5の範囲のpHを有する、本発明1001~1053のいずれかの薬学的組成物。
[本発明1055]
5.7~6.3の範囲のpHを有する、本発明1001~1053のいずれかの薬学的組成物。
[本発明1056]
約6.0のpHを有する、本発明1001~1053のいずれかの薬学的組成物。
[本発明1057]
pHが室温で測定される、本発明1054~1056のいずれかの薬学的組成物。
[本発明1058]
pHが15℃~27℃で測定される、本発明1054~1056のいずれかの薬学的組成物。
[本発明1059]
pHが4℃で測定される、本発明1054~1056のいずれかの薬学的組成物。
[本発明1060]
pHが25℃で測定される、本発明1054~1056のいずれかの薬学的組成物。
[本発明1061]
塩酸(HCl)を含む、本発明1001~1060のいずれかの薬学的組成物。
[本発明1062]
pHがHClによって調整される、本発明1001~1060のいずれかの薬学的組成物。
[本発明1063]
コハク酸を含む、本発明1001~1060のいずれかの薬学的組成物。
[本発明1064]
pHがコハク酸によって調整される、本発明1001~1060のいずれかの薬学的組成物。
[本発明1065]
約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、および約5.5%(w/v)のトレハロース二水和物または約5%(w/v)のスクロースの少なくとも一方を含む、本発明1001~1016のいずれかの薬学的組成物。
[本発明1066]
HClまたはコハク酸をさらに含む、本発明1065の薬学的組成物。
[本発明1067]
pHが室温で6.0である、本発明1065または本発明1066の薬学的組成物。
[本発明1068]
pHが25℃で6.0である、本発明1065または本発明1066の薬学的組成物。
[本発明1069]
(a)以下の構造:
を含み、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20(登録商標)、約5.5%(w/v)のトレハロース二水和物、およびHClを含む、薬学的に許容される賦形剤
を含み、pHが25℃で約6.0である、
薬学的組成物。
[本発明1070]
抗体薬物コンジュゲートが約10mg/mLの濃度である、本発明1069の薬学的組成物。
[本発明1071]
(a)以下の構造:
を含み、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20(登録商標)、約5.5%(w/v)のトレハロース二水和物、およびコハク酸を含む、薬学的に許容される賦形剤
を含み、pHが25℃で約6.0である、
薬学的組成物。
[本発明1072]
抗体薬物コンジュゲートが約10mg/mLの濃度である、本発明1071の薬学的組成物。
[本発明1073]
(a)以下の構造:
を含み、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20(登録商標)、約5.0%(w/v)のスクロース、およびHClを含む、薬学的に許容される賦形剤
を含み、pHが25℃で約6.0である、
薬学的組成物。
[本発明1074]
抗体薬物コンジュゲートが約10mg/mLの濃度である、本発明1073の薬学的組成物。
[本発明1075]
液体形態である、本発明1001~1074のいずれかの薬学的組成物。
[本発明1076]
凍結乾燥されている、本発明1001~1074のいずれかの薬学的組成物。
[本発明1077]
本発明1001~1074のいずれかの薬学的組成物を凍結乾燥することによって作製される凍結乾燥組成物。
[本発明1078]
-80℃、4℃、25℃または37℃で保存される、本発明1001~1074のいずれかの薬学的組成物。
[本発明1079]
有効量の本発明1001~1078のいずれかの薬学的組成物を対象に投与する工程を含む、対象の疾患または障害を予防または治療する方法。
[本発明1080]
対象がヒト対象である、本発明1079の方法。
[本発明1081]
癌が、結腸癌、膵臓癌、卵巣癌、肺癌、膀胱癌、尿路上皮癌、乳癌、食道癌、頭部癌、または頸部癌である、本発明1080の方法。
[本発明1082]
癌が結腸癌である、本発明1081の方法。
[本発明1083]
癌が膵臓癌である、本発明1081の方法。
[本発明1084]
癌が卵巣癌である、本発明1081の方法。
[本発明1085]
癌が肺癌であり、肺癌が任意で非小細胞肺癌である、本発明1081の方法。
[本発明1086]
癌が膀胱癌または尿路上皮癌である、本発明1081の方法。
[本発明1087]
膀胱癌が進行性膀胱癌または進行性尿路上皮癌である、本発明1086の方法。
[本発明1088]
膀胱癌が転移性膀胱癌または転移性尿路上皮癌である、本発明1086の方法。
[本発明1089]
癌が乳癌である、本発明1081の方法。
[本発明1090]
癌が食道癌である、本発明1081の方法。
[本発明1091]
癌が頭部癌である、本発明1081の方法。
[本発明1092]
癌が頸部癌である、本発明1081の方法。
[本発明1093]
癌が、191P4D12を発現する腫瘍細胞を有する、本発明1080の方法。
[本発明1094]
第2の治療薬を対象に投与する工程をさらに含む、本発明1079~1093のいずれかの方法。
[本発明1095]
第2の治療薬が免疫チェックポイント阻害剤である、本発明1094の方法。
[本発明1096]
免疫チェックポイント阻害剤がPD-1阻害剤またはPD-L1阻害剤である、本発明1095の方法。
[本発明1097]
免疫チェックポイント阻害剤がPD-1阻害剤である、本発明1096の方法。
[本発明1098]
PD-1阻害剤がニボルマブである、本発明1097の方法。
[本発明1099]
免疫チェックポイント阻害剤がPD-L1阻害剤である、本発明1096の方法。
[本発明1100]
PD-L1阻害剤が、アテゾリズマブ、アベルマブ、およびデュルバルマブからなる群より選択される、本発明1099の方法。
[本発明1101]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、1~10mg/kg対象体重の用量で投与される、本発明1079~1100のいずれかの方法。
[本発明1102]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、1~5mg/kg対象体重の用量で投与される、本発明1101の方法。
[本発明1103]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、1~2.5mg/kg対象体重の用量で投与される、本発明1101の方法。
[本発明1104]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、1~1.25mg/kg対象体重の用量で投与される、本発明1101の方法。
[本発明1105]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、約1mg/kg対象体重の用量で投与される、本発明1101の方法。
[本発明1106]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、約1.25mg/kg対象体重の用量で投与される、本発明1101の方法。
[本発明1107]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、静脈内(IV)注射または注入によって投与される、本発明1101~1106のいずれかの方法。
[本発明1108]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、3週間に2回のサイクルで、約30分かけて静脈内(IV)注射または注入によって投与される、本発明1107の方法。
[本発明1109]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、3週間のサイクルごとの第1日および第8日に約30分かけて静脈内(IV)注射または注入によって投与される、本発明1108の方法。
[本発明1110]
3週間のサイクルごとの第1日に静脈内(IV)注射または注入によって免疫チェックポイント阻害剤を投与する工程をさらに含む、本発明1109の方法。
[本発明1111]
免疫チェックポイント阻害剤が、約30分または60分かけて約100mg~約1500mgの量で投与される、本発明1110の方法。
[本発明1112]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、4週間に3回のサイクルで、約30分かけて静脈内(IV)注射または注入によって投与される、本発明1107の方法。
[本発明1113]
薬学的組成物へと製剤化された抗体薬物コンジュゲートが、4週間のサイクルごとの第1日、第8日および第15日に約30分かけて静脈内(IV)注射または注入によって投与される、本発明1112の方法。
[本発明1114]
静脈内(IV)注射または注入によって免疫チェックポイント阻害剤を投与する工程をさらに含む、本発明1113の方法。
本開示をさらに説明する前に、本開示は本明細書に記載される特定の態様に限定されないことが理解されるべきであり、また、本明細書で使用される用語は、特定の態様を説明することのみを目的としており、限定することを意図しないことも理解されるべきである。
本明細書に記載または参照される技術および手順には、例えば、Sambrook et al.,Molecular Cloning:A Laboratory Manual(3d ed.2001);Current Protocols in Molecular Biology(Ausubel et al.eds.,2003);Therapeutic Monoclonal Antibodies:From Bench to Clinic(An ed.2009);Monoclonal Antibodies:Methods and Protocols(Albitar ed.2010);およびAntibody Engineering Vols 1 and 2(Kontermann and Dubel eds.,2d ed.2010)に記載されている広く利用されている方法などの、当業者によって従来の方法論を使用して一般によく理解されているおよび/または一般に採用されているものが含まれる。
典型的な「-(C1~C8アルキレン)アリール」、「-(C2~C8アルケニレン)アリール」、「および-(C2~C8アルキニレン)アリール」基には、ベンジル、2-フェニルエタン-1-イル、2-フェニルエテン-1-イル、ナフチルメチル、2-ナフチルエタン-1-イル、2-ナフチルエテン-1-イル、ナフトベンジル、2-ナフトフェニルエタン-1-イルなどが含まれるが、これらに限定されるわけではない。
一局面では、本明細書で提供される抗体薬物コンジュゲートと、1つまたは複数の薬学的に許容されるまたは生理学的に許容される賦形剤とを含む「薬学的組成物」が、本明細書で提供される。特定の態様では、抗体薬物コンジュゲートは、1つもしくは複数のさらなる剤と組み合わせて、またはそれとは別個に提供される。そのような1つまたは複数のさらなる剤、および1つまたは複数の薬学的に許容されるまたは生理学的に許容される賦形剤を含む組成物も提供される。特定の態様では、抗体薬物コンジュゲートおよびさらなる剤(1つまたは複数)は、治療上許容される量で存在する。薬学的組成物は、本明細書で提供される方法および使用に従って使用され得る。したがって、例えば、薬学的組成物は、本明細書で提供される治療方法および使用を実施するために、対象にエクスビボまたはインビボで投与することができる。本明細書で提供される薬学的組成物は、意図される方法または投与経路と適合するように製剤化することができ、例示的な投与経路は本明細書に記載されている。
(a)以下の構造:
を有し、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、約5.5%(w/v)のトレハロース二水和物、およびHClを含む、薬学的に許容される賦形剤
を含み、ここで、抗体薬物コンジュゲートは約10mg/mLの濃度であり、pHは25℃で約6.0である。
(a)以下の構造:
を含み、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、約5.5%(w/v)のトレハロース二水和物、およびコハク酸を含む、薬学的に許容される賦形剤
を含み、ここで、抗体薬物コンジュゲートは約10mg/mLの濃度であり、pHは25℃で約6.0である。
(a)以下の構造:
を含み、ここで、L-は抗体またはその抗原結合断片を表し、pは1~10である、抗体薬物コンジュゲート;ならびに
(b)約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、約5.0%(w/v)のスクロース、およびHClを含む、薬学的に許容される賦形剤
を含み、ここで、抗体薬物コンジュゲートは約10mg/mLの濃度であり、pHは25℃で約6.0である。
本明細書で提供される薬学的組成物、製剤および剤形は、抗191P4D12抗体薬物コンジュゲートを含む。本明細書で提供される抗191P4D12抗体薬物コンジュゲートは、細胞傷害剤(または薬物単位)の1つまたは複数の単位にコンジュゲートされた、191P4D12に結合する抗体またはその抗原結合断片を含む。細胞傷害剤(または薬物単位)は、直接またはリンカー単位(LU)を介して共有結合され得る。
L-(LU-D)p (I)
式中、
Lは、抗体単位、例えば、下記のセクション5.3.1で提供される抗191P4D12抗体またはその抗原結合断片であり、
(LU-D)は、リンカー単位-薬物単位部分であり、
ここで、
LU-はリンカー単位であり、
Dは、標的細胞に対して細胞増殖抑制活性または細胞傷害活性を有する薬物単位であり、
pは1~20の整数である。
L-(Aa-Ww-Yy-D)p (II)
式中、
Lは、抗体単位、例えば、下記のセクション5.3.1で提供される抗191P4D12抗体またはその抗原結合断片であり;および
-Aa-Ww-Yy-はリンカー単位(LU)であり、ここで、
-A-は伸長単位であり、
aは0または1であり、
各-W-は独立してアミノ酸単位であり、
wは0~12の範囲の整数であり、
-Y-は自己犠牲スペーサ単位であり、
yは、0、1または2であり、
Dは、標的細胞に対する細胞増殖抑制活性または細胞傷害活性を有する薬物単位であり、
pは1~20の整数である。
一態様では、191P4D12関連タンパク質に結合する抗体またはその抗原結合断片は、SEQ ID NO:2のアミノ酸配列を含む191P4D12タンパク質に特異的に結合する抗体または抗原結合断片である(図5Aを参照)。191P4D12タンパク質をコードする対応するcDNAは、SEQ ID NO:1の配列を有する(図5Aを参照)。
(a)重鎖可変領域は、American Type Culture Collection(ATCC)アクセッション番号PTA-11267の下に寄託されたハイブリドーマによって産生される抗体に示される重鎖可変領域CDRのアミノ酸配列を含むCDRを含み;
(b)軽鎖可変領域は、American Type Culture Collection(ATCC)アクセッション番号PTA-11267の下に寄託されたハイブリドーマによって産生される抗体に示される軽鎖可変領域CDRのアミノ酸配列を含むCDRを含む。
(a)重鎖可変領域は、American Type Culture Collection(ATCC)アクセッション番号PTA-11267の下に寄託されたハイブリドーマによって産生される抗体の重鎖可変領域アミノ酸配列と少なくとも80%相同なアミノ酸配列を含み;および
(b)軽鎖可変領域は、American Type Culture Collection(ATCC)アクセッション番号PTA-11267の下に寄託されたハイブリドーマによって産生される抗体の軽鎖可変領域アミノ酸配列と少なくとも80%相同なアミノ酸配列を含む。
(a)重鎖は、American Type Culture Collection(ATCC)アクセッション番号PTA-11267の下に寄託されたハイブリドーマによって産生される抗体の重鎖アミノ酸配列と少なくとも80%相同なアミノ酸配列を含み;および
(b)軽鎖は、American Type Culture Collection(ATCC)アクセッション番号PTA-11267の下に寄託されたハイブリドーマによって産生される抗体の軽鎖アミノ酸配列と少なくとも80%相同なアミノ酸配列を含む。
いくつかの態様では、ADCは、ドラスタチンまたはドロスタチンのペプチド類似体および誘導体であるアウリスタチン(米国特許第5,635,483号;同第5,780,588号)にコンジュゲートされた抗体またはその抗原結合断片を含む。ドラスタチンおよびアウリスタチンは、微小管の動態、GTP加水分解、ならびに核および細胞分裂を妨げ(Woyke et al(2001)Antimicrob.Agents and Chemother.45(12):3580-3584)、抗癌活性(米国特許第5,663,149号)および抗真菌活性(Pettit et al(1998)Antimicrob.Agents Chemother.42:2961-2965)を有することが示されている。ドラスタチンまたはアウリスタチン薬物単位は、ペプチド性薬物単位のN(アミノ)末端またはC(カルボキシル)末端を介して抗体に結合され得る(国際公開公報第02/088172号)。
典型的には、抗体薬物コンジュゲートは、薬物単位(例えば、MMAE)と抗体単位(例えば、抗191P4D12抗体またはその抗原結合断片)との間にリンカー単位を含む。いくつかの態様では、リンカーは、リンカーの切断が細胞内環境で抗体から薬物単位を放出するように、細胞内条件下で切断可能である。さらに他の態様では、リンカー単位は切断可能ではなく、薬物は、例えば抗体分解によって放出される。
-Aa-Ww-Yy-
を有し、
式中、-A-は伸長単位であり、
aは0または1であり、
各-W-は独立してアミノ酸単位であり、
wは0~12の範囲の整数であり、
-Y-は自己犠牲スペーサ単位であり、
yは0、1または2である。
伸長単位(A)は、存在する場合、抗体単位を、アミノ酸単位(-W-)が存在する場合はアミノ酸単位(-W-)に、スペーサ単位(-Y-)が存在する場合はスペーサ単位(-Y-)に、または薬物単位(-D)に連結することができる。天然にまたは化学的操作を介して、抗191P4D12抗体またはその抗原結合断片(例えば、Ha22-2(2,4)6.1)上に存在することができる有用な官能基には、スルフヒドリル、アミノ、ヒドロキシル、炭水化物のアノマーヒドロキシル基、およびカルボキシルが含まれるが、これらに限定されるわけではない。適切な官能基は、スルフヒドリルおよびアミノである。一例では、スルフヒドリル基は、抗191P4D12抗体またはその抗原結合断片の分子内ジスルフィド結合の還元によって生成することができる。別の態様では、スルフヒドリル基は、抗191P4D12抗体または抗原結合断片のリジン部分のアミノ基と、2-イミノチオラン(トラウト試薬)または他のスルフヒドリル生成試薬との反応によって生成することができる。特定の態様では、抗191P4D12抗体またはその抗原結合断片は組換え抗体であり、1つまたは複数のリジンを担持するように操作される。特定の他の態様では、組換え抗191P4D12抗体は、さらなるスルフヒドリル基、例えばさらなるシステインを担持するように操作される。
アミノ酸単位(-W-)は、存在する場合、スペーサ単位が存在する場合は伸長単位をスペーサ単位に連結し、スペーサ単位が存在しない場合は伸長単位を薬物単位に連結し、伸長単位およびスペーサ単位が存在しない場合は抗体単位を薬物単位に連結する。
式中、R19は、水素、メチル、イソプロピル、イソブチル、sec-ブチル、ベンジル、p-ヒドロキシベンジル、-CH2OH、-CH(OH)CH3、-CH2CH2SCH3、-CH2CONH2、-CH2COOH、-CH2CH2CONH2、-CH2CH2COOH、-(CH2)3NHC(=NH)NH2、-(CH2)3NH2、-(CH2)3NHCOCH3、-(CH2)3NHCHO、-(CH2)4NHC(=NH)NH2、-(CH2)4NH2、-(CH2)4NHCOCH3、-(CH2)4NHCHO、-(CH2)3NHCONH2、-(CH2)4NHCONH2、-CH2CH2CH(OH)CH2NH2、2-ピリジルメチル-、3-ピリジルメチル-、4-ピリジルメチル-、フェニル、シクロヘキシル、
である。
式中、R20およびR21は以下の通りである:
式中、R20、R21およびR22は以下の通りである:
式中、R20、R21、R22およびR23は以下の通りである:
。
スペーサ単位(-Y-)は、存在する場合、アミノ酸単位が存在する場合はアミノ酸単位を薬物単位に連結する。あるいは、スペーサ単位は、アミノ酸単位が存在しない場合は伸長単位を薬物単位に連結する。スペーサ単位はまた、アミノ酸単位および伸長単位の両方が存在しない場合は、薬物単位を抗体単位に連結する。
スキーム1
スキーム2
スキーム3
式中、Qは、-C1~C8アルキル、-C1~C8アルケニル、-C1~C8アルキニル、-O-(C1~C8アルキル)、-O-(C1~C8アルケニル)、-O-(C1~C8アルキニル)、-ハロゲン、-ニトロまたは-シアノであり、mは0~4の範囲の整数である。アルキル基、アルケニル基およびアルキニル基は、単独でまたは別の基の一部としてのいずれでも、置換されていてもよい。
および
。
薬物負荷はpによって表され、分子中の抗体当たりの薬物単位の平均数である。薬物負荷は、抗体当たり1~20薬物単位(D)の範囲であり得る。本明細書で提供されるADCは、例えば1~20の範囲の薬物単位とコンジュゲートした抗体または抗原結合断片の集合を含む。コンジュゲーション反応からのADCの調製物中の抗体当たりの薬物単位の平均数は、質量分析およびELISAアッセイなどの従来の手段によって特徴付けることができる。pに関するADCの定量的分布も決定し得る。場合によっては、他の薬物負荷を有するADCからの、pが特定の値である均一なADCの分離、精製および特徴付けは、電気泳動などの手段によって達成し得る。
本明細書で提供される抗体薬物コンジュゲートの生成は、当業者に公知の任意の技術によって達成することができる。簡単に説明すると、抗体薬物コンジュゲートは、抗体単位としての抗191P4D12抗体またはその抗原結合断片、薬物、および任意で薬物と結合剤とを結合するリンカーを含む。いくつかの態様では、抗体は、上記のHa22-2(2,4)6.1と称される抗体のCDR領域を含む抗191P4D12抗体である。具体的な態様では、抗体は、上記のHa22-2(2,4)6.1と称される抗体の重鎖可変領域および軽鎖可変領域を含む抗191P4D12抗体である。具体的な態様では、抗体は、上記のHa22-2(2,4)6.1と称される抗体の重鎖および軽鎖を含む抗191P4D12抗体である。
スキーム5 vcMMAEの一般的な合成方法
ここで、AA1=アミノ酸1
AA2=アミノ酸2
AA5=アミノ酸5
DIL=ドライソロイン
DAP=ドラプロイン
リンカー=Val-Cit(vc)
一局面では、本明細書で提供される薬学的組成物の有効量を対象に投与する工程を含む、対象の疾患または障害を予防または治療する方法が本明細書で提供される。いくつかの態様では、対象はヒト対象である。
以下は、試験で使用された様々な方法および材料の説明であり、当業者に本発明を作成および使用する方法の完全な開示および説明を提供するために提示されており、本発明者らが自らの発明と見なすものの範囲を限定することを意図するものではなく、以下の実験が実施されたこと、および実施され得るすべての実験であることを表すことを意図するものでもない。現在形で書かれた例示的な説明は必ずしも実施されたわけではなく、むしろ、本発明の教示に関連するデータなどを生成するために説明が実施され得ることが理解されるべきである。使用される数(例えば、量、温度など)に関して正確性を確保するように努めてきたが、いくらかの実験誤差および偏差が考慮されるべきである。
AGS-22M6Eを14の候補緩衝液(すべて20mM;以下の表1に詳述されている)中10mg/mLで製剤化した。クエン酸でpH5.2およびpH5.7に滴定した20mMクエン酸ナトリウム緩衝液、ならびにHClでpH5.5、pH6.0およびpH6.5に滴定した20mMヒスチジン緩衝液を使用した製剤を評価した。さらに、3つの異なるアニオン、すなわち塩化物、リン酸塩およびコハク酸塩をヒスチジン緩衝系で評価した。液体製剤を、40℃の保存温度条件に2週間、室温(RT)で24時間の撹拌、ならびに凍結融解サイクル(-70℃で凍結および20℃~25℃で解凍を1、3および10サイクル)に供した。
それぞれ約50mlのAGS-22M6E(ロット番号AGS22M6-VCE-02)を含む4本のチューブ、合計約2.5グラムを凍結状態で受領した。AGS-22M6Eは、5%スクロースおよび0.02%ポリソルベート20を含む20mMヒスチジンpH6.0緩衝液中12.5mg/mLであった。材料は、使用するまで-70℃で保存した。
クエン酸(0.1M)、クエン酸ナトリウム(0.1M)およびL-ヒスチジン(0.2M)、コハク酸(0.25M)、トレハロース二水和物(40%)、スクロース(40%)、塩酸(2M)およびリン酸(2M)を含む原液を以下の表2に従って調製した。
1.0Lの各製剤を、以下の表3に従って透析およびプラセボバイアル充填のために調製した。
それぞれ50mlのAGS-22M6E(ロット番号AGS22M6-VCE-02)を含む4本のチューブを室温の水浴中で解凍し、次いで250mlボトル中で合わせた。11mlを各製剤に割り当て、透析カセットに添加した。カセットを、約40倍過剰の製剤緩衝液を含むビーカーに入れ、2℃~8℃で一晩撹拌した。緩衝液を廃棄し、新鮮な緩衝液を添加し、2℃~8℃で一晩撹拌した。材料をカセットから取り出し、50mlチューブに移し、濃度を決定し、最終濃度が10mg/mlになるように対応する製剤緩衝液で容量を調整した。プラセボは、生成物を製剤化するために使用された対応する緩衝液であった。
滅菌濾過および充填をBaker SG600層流フード内で行った。製剤およびプラセボを、無菌技術(Millipore Millex-GV 0.22μm PVDFシリンジフィルタ、No.SLGV033RS)を使用して滅菌濾過した。滅菌栓付きバイアル(Hollister-Stier 2ml滅菌栓付きバイアル、No.7505ZA)をフード内でデクリンプ(decrimp)し、無菌技術を用いて栓を取り外した。1.0mlの製剤化された生成物またはプラセボをバイアルに充填し、次いで再び栓をした。
材料要件および試料マップは以下の通りである。
時点およびアッセイは以下の表5の通りである。
製剤およびプラセボバイアルを40℃に設定したインキュベータ内に直立させた。各時点で、各製剤について1つの活性バイアルおよび1つのプラセボバイアルを試料マップに従って保存条件から取り出した。試料を-70℃で凍結させ、試験の最後にバッチ分析した。分析の前に、試料を室温で解凍した。各試料の3つのアリコートのセット(各試料について70μLのアリコート)を、0.22μmフィルタで濾過した後、-70℃で凍結させた。分析試験後、再試験が必要な場合に備えて、残りの材料を2℃~8℃で一晩保存した。すべてのアッセイが完了した後、残りの材料を-70℃で保存した。2つの凍結アリコートをcIEFおよび効力アッセイに使用した。
各製剤の1つのバイアル(1.0mL充填)を-70℃の冷凍庫に直立させて少なくとも4時間置き、凍結させた。解凍のために、各バイアルを保存場所から取り出し、氷が観察されなくなるまで室温で解凍し、次いでバイアルを穏やかに旋回させた。これは、1回の完全な凍結融解サイクルを構成した。各試験製剤試料バイアルについて、1回、3回および10回の凍結融解サイクルを完了した。最終凍結融解サイクルの後、すべての試料を分析試験によって評価した。各試料の3つのアリコートのセット(各試料について70μLのアリコート)を直ちに-70℃で凍結させた。分析試験後、再試験が必要な場合に備えて、残りの材料を2℃~8℃で一晩保存した。すべてのアッセイが完了した後、残りの材料を-70℃で保存した。2つの凍結アリコートをcIEFおよび効力アッセイに使用した。
各製剤について1つのバイアルを標準的な冷凍ボックス内で直立に固定した。次いで、ボックスを、500rpmに設定したIKA-VIBRAMAX-VXRオービタルシェーカに室温で24時間取り付けた。次いで、試料を取り出し、分析まで-70℃で保存した。
1.2mLのAGS-22M6E(ロット番号AGS22M6-VCE-02)出発物質(5%スクロースおよび0.02%ポリソルベート20を含む20mMヒスチジンpH6.0緩衝液中12.5mg/mL)を取り、200μl/バイアルでアリコートに分け、次いで、この試験の製剤標準として-70℃で保存した。
製剤F4、F9およびF14を上記のセクション6.1に記載されているように調製した。製剤F4、F9およびF14のそれぞれを、-20℃および-70℃の両方で1、3および10サイクルの凍結に供し、続いて20℃~25℃で解凍した。サンプルを目視検査、濃度(A280)測定、濁度(A330)測定、SE-HPLC、SDS-PAGE(R&NR)によって分析した。10サイクルの凍結融解試験については、試料をRP-HPLC NPIでも分析した。
注:
・バイアル:5mLの滅菌スクリューキャップポリカーボネートボトル(Nalgene 5ml、No.3500-05)
・BDS凍結/融解:5mLポリカーボネートボトルに1mLを充填。
・BDS振とう:5mLポリカーボネートボトルに3.5mLを充填。
滅菌濾過および充填をBaker SG600層流フード内で行った。製剤およびプラセボを、無菌技術(Millipore Millex-GV 0.22μm PVDFシリンジフィルタ、No.SLGV033RS)を使用して滅菌濾過した。滅菌チップ付きの5mL電子ピペットを使用して、濾過したAGS-22M6Eおよび濾過した製剤緩衝液(プラセボ)を滅菌スクリューキャップポリカーボネートボトル(Nalgene 5ml、No.3500-05)に移した。
製剤ごとに1つのバイアルを標準的な冷凍ボックス内で直立に固定した。次いで、ボックスを、500rpmに設定したIKA-VIBRAMAX-VXRオービタルシェーカに室温で24時間取り付けた。次いで、試料を取り出し、分析まで70℃で保存した。各試料の3つのアリコートのセット(各試料について70μLのアリコート)を、0.22μmフィルタで濾過した後、-70℃で凍結させた。分析試験後、再試験が必要な場合に備えて、残りの材料を2℃~8℃で一晩保存した。すべてのアッセイが完了した後、残りの材料を-70℃で保存した。2つの凍結アリコートをcIEFおよび効力アッセイに使用した。
製剤ごとに1バイアル(5mLのポリカーボネートボトルに1mlを充填)を-70℃および-20℃の冷凍庫に直立させて少なくとも4時間置き、凍結させた。解凍のために、各バイアルを保存場所から取り出し、氷が観察されなくなるまで室温(20~25℃)で解凍し、次いでバイアルを穏やかに旋回させた。これは、1回の完全な凍結融解サイクルを構成した。各試験製剤試料バイアルについて10回の凍結融解サイクルを完了した。最終凍結融解サイクルの後、すべての試料を分析試験によって評価した。試料を以下の方法によって分析した:外観、A280/A248、濁度(A330)、SE-HPLC、RP-HPLC-NPIおよびSDS-PAGE(R&NR)。各試料の3つのアリコートのセット(各試料について70μLのアリコート)を、0.22μmフィルタで濾過した後、-70℃で凍結させた。分析試験後、再試験が必要な場合に備えて、残りの材料を2℃~8℃で一晩保存した。すべてのアッセイが完了した後、残りの材料を-70℃で保存した。2つの凍結アリコートをcIEFおよび効力アッセイに使用した。
5.0%スクロース、0.02%Tween 20、pH6.0中12.8mg/mLのAGS-22M6E出発物質15mLを取り、500μl/バイアルでアリコートに分け、次いで、この試験の製剤標準として-70℃で保存した。
外観:すべての試料の外観をこの試験で分析し、振とうしても微粒子は見られなかった。
この試験は、上記のセクション6.2に記載されている試験と併せて実施された。この試験に使用された製剤組成物および材料は、セクション6.2に記載されているものと同じである。
注:試験の液体アームの試料は、凍結乾燥アームからの試料が調製されるまで-70℃で凍結された。次いで、試験の液体アームと凍結乾燥アームの両方についてt=0が同一になるように、凍結乾燥試料を条件に置くのと同時に凍結液体試料を条件に置いた。
製剤およびプラセボバイアルを、-70℃に設定した冷凍庫および2~8℃に設定したインキュベータ内に直立させた。各時点で、各製剤について1つの活性バイアルおよび1つのプラセボバイアルを、分析試験のための試料マップに従って保存条件から取り出した。分析試験後、再試験が必要な場合に備えて、残りの材料を2℃~8℃で保存した。アリコートを-70℃で保存し、cIEFおよび活性試験に使用した。
製剤およびプラセボバイアルを、2℃~8℃に設定したインキュベータ、25℃/60%RHに設定したインキュベータ、および40℃/75%RHに設定したインキュベータ内に直立させた。各時点で、各製剤について1つの活性バイアルおよび1つのプラセボバイアルを、分析試験のための試料マップに従って保存条件から取り出した。分析試験後、再試験が必要な場合に備えて、残りの材料を2℃~8℃で保存した。アリコートを-70℃で保存し、cIEFおよび活性試験に使用した。
上記のセクションで説明した製剤F4を、このさらなる凍結乾燥サイクル開発試験のために選択した。凍結乾燥サイクルのパラメータを以下の表に示す。凍結乾燥が完了した後、50mTの減圧下でバイアルに栓をした。バイアルのトレイを凍結乾燥機から取り出し、バイアルをアルミニウムシールで個別に圧着した。
各充填容量構成について、5つのプラセボバイアルに加えて5つの生成物バイアルを充填した。活性生成物およびプラセボのそれぞれからの2つのバイアルを、T=0で各充填容量について試験した(1つのバイアルは残留水分について試験し、1つのバイアルは再構成して、試験概要に記載されたアッセイを使用して試験した)。さらに、凍結乾燥工程中の温度監視のために、活性物質およびプラセボのそれぞれからの2つのバイアルを調べた。
凍結乾燥サイクル分析:総保存サイクル時間は2.6日間であり、これは5mLの充填容量について確立された4.7日間のサイクル時間よりも有意に短い(上記のセクション6.3を参照)。しかしながら、本試験の2.6日間のサイクル時間は、いずれかの充填容量についての最適化されたサイクル時間を表すものではない。サイクルに関連する個々の読み取り値を注意深く評価すると、いずれかの充填容量についての最適化されたサイクル時間の推定を行うことができる。露点モニタは両方の充填容量から発生する水分に応答するため、この試験では、3.0mLまたは1.5mLの充填容量のより最適な乾燥時間を推定するために使用しなかった。同様に、ピラニ真空計は、通常、一次乾燥時間の終点の優れた指標であるが、この場合は、棚のすべてのバイアルからの氷の昇華にも応答するので、指針を提供するだけである。代わりに、この試験の目的のために、生成物温度を監視することは、個々の充填容量ごとの乾燥時間を推定するための最も信頼できるツールを提供する。この試験では、熱電対プローブを活性バイアルとプラセボバイアルの両方に配置し、活性物質とプラセボの生成物温度プロフィール間の密接な一致が両方の充填容量で観察された。
本明細書は、配列表のコンピュータ可読形式(CRF)コピーと共に提出されている。2019年10月11日に作成された39,693バイトのサイズの「14369-244-228_SEQ_LISTING.txt」と題するCRFは、その全体が参照により本明細書に組み入れられる。
Claims (45)
- (a)モノメチルアウリスタチンE(MMAE)の1つまたは複数の単位にコンジュゲートされた、191P4D12に結合する抗体またはその抗原結合断片を含む、抗体薬物コンジュゲートであって、該抗体またはその抗原結合断片が、SEQ ID NO:7に示される重鎖可変領域の3つの相補性決定領域(CDR)のアミノ酸配列を含む重鎖可変領域と、SEQ ID NO:8に示される軽鎖可変領域の3つのCDRのアミノ酸配列を含む軽鎖可変領域とを含む、抗体薬物コンジュゲート;ならびに
(b)5~50mMの範囲のL-ヒスチジン、0.001~0.1%(v/v)の範囲のポリソルベート20(TWEEN-20(登録商標))、および4%~7%(w/v)の範囲のトレハロース二水和物、ならびにHClを含み、15℃~27℃で5.5~6.5の範囲のpHである、薬学的に許容される賦形剤
を含む、薬学的組成物。 - 抗体またはその抗原結合断片が、SEQ ID NO:9のアミノ酸配列を含むCDR H1、SEQ ID NO:10のアミノ酸配列を含むCDR H2、SEQ ID NO:11のアミノ酸配列を含むCDR H3、SEQ ID NO:12のアミノ酸配列を含むCDR L1、SEQ ID NO:13のアミノ酸配列を含むCDR L2、およびSEQ ID NO:14のアミノ酸配列を含むCDR L3を含む、請求項1記載の薬学的組成物。
- 抗体またはその抗原結合断片が、SEQ ID NO:7の20番目のアミノ酸(グルタミン酸)から136番目のアミノ酸(セリン)までの範囲のアミノ酸配列を含む重鎖可変領域と、SEQ ID NO:8の23番目のアミノ酸(アスパラギン酸)から130番目のアミノ酸(アルギニン)までの範囲のアミノ酸配列を含む軽鎖可変領域とを含む、請求項1記載の薬学的組成物。
- 抗体が、SEQ ID NO:7の20番目のアミノ酸(グルタミン酸)から466番目のアミノ酸(リジン)までの範囲のアミノ酸配列を含む重鎖と、SEQ ID NO:8の23番目のアミノ酸(アスパラギン酸)から236番目のアミノ酸(システイン)までの範囲のアミノ酸配列を含む軽鎖とを含む、請求項1記載の薬学的組成物。
- 抗原結合断片がFab、F(ab')2、FvまたはscFvである、請求項1~4のいずれか一項記載の薬学的組成物。
- 抗体が完全ヒト抗体である、請求項1~5のいずれか一項記載の薬学的組成物。
- 抗体またはその抗原結合断片が組換え産生される、請求項1~6のいずれか一項記載の薬学的組成物。
- pが2~8である、請求項8記載の薬学的組成物。
- pが3.8である、請求項8記載の薬学的組成物。
- 抗体または抗原結合断片が、リンカーを介してモノメチルアウリスタチンE(MMAE)の各単位に連結されている、請求項1記載の薬学的組成物。
- リンカーが、酵素切断可能なリンカーであり、抗体またはその抗原結合断片の硫黄原子と結合を形成する、請求項11記載の薬学的組成物。
- リンカーが-Aa-Ww-Yy-の式を有し、
式中、-A-は伸長単位であり、aは0または1であり、-W-はアミノ酸単位であり、wは0~12の範囲の整数であり、-Y-はスペーサ単位であり、yは0、1、または2である、
請求項11記載の薬学的組成物。 - 伸長単位が抗体またはその抗原結合断片の硫黄原子と結合を形成し、スペーサ単位がカルバメート基を介してMMAEに連結されている、請求項13記載の薬学的組成物。
- 1~20mg/mLの濃度の抗体薬物コンジュゲートを含む、請求項1~15のいずれか一項記載の薬学的組成物。
- 5~15mg/mLの濃度の抗体薬物コンジュゲートを含む、請求項16記載の薬学的組成物。
- 8~12mg/mLの濃度の抗体薬物コンジュゲートを含む、請求項16記載の薬学的組成物。
- 約10mg/mLの濃度の抗体薬物コンジュゲートを含む、請求項16記載の薬学的組成物。
- L-ヒスチジンが(i) 10~40mMの範囲で、(ii) 15~35mMの範囲で、(iii) 15~30mMの範囲で、(iv) 15~25mMの範囲で、または(v) 約20mMで存在する、請求項1~19のいずれか一項記載の薬学的組成物。
- TWEEN-20の濃度が(i) 0.0025~0.075%(v/v)の範囲、(ii) 0.005~0.05%(v/v)の範囲、(iii) 0.01~0.03%(v/v)の範囲、または(iv) 約0.02%(v/v)である、請求項1~20のいずれか一項記載の薬学的組成物。
- トレハロース二水和物を含み、前記トレハロース二水和物が4~6%(w/v)の範囲で、存在する、請求項1~21のいずれか一項記載の薬学的組成物。
- (i) 5.7~6.3の範囲、または(ii) 約6.0のpHを有する、請求項1~22のいずれか一項記載の薬学的組成物。
- pHが室温で測定される、請求項23記載の薬学的組成物。
- pHが25℃で測定される、請求項23記載の薬学的組成物。
- pHがHClによって調整される、請求項1~25のいずれか一項記載の薬学的組成物。
- 約20mMのL-ヒスチジン、約0.02%(w/v)のTWEEN-20、および約5.5%(w/v)のトレハロース二水和物を含む、請求項1~15のいずれか一項記載の薬学的組成物。
- pHが室温または25℃で6.0である、請求項27記載の薬学的組成物。
- 抗体薬物コンジュゲートが約10mg/mLの濃度である、請求項27または28記載の薬学的組成物。
- (a) 液体形態であるもしくは凍結乾燥形態である、または(b) -80℃、4℃、25℃または37℃で保存される、請求項1~29のいずれか一項記載の薬学的組成物。
- 凍結乾燥形態である、請求項1~29のいずれか一項記載の薬学的組成物。
- ヒト対象における癌を予防または治療するための医薬の調製における、請求項1~31のいずれか一項記載の薬学的組成物の使用。
- 癌が、結腸癌、膵臓癌、卵巣癌、肺癌、膀胱癌、尿路上皮癌、乳癌、食道癌、頭部癌、頸部癌、または非小細胞肺癌である、請求項32記載の使用。
- 膀胱癌が進行性膀胱癌、進行性尿路上皮癌、転移性膀胱癌、または転移性尿路上皮癌である、請求項33記載の使用。
- 癌が、191P4D12を発現する腫瘍細胞を有する、請求項32~34のいずれか一項記載の使用。
- 免疫チェックポイント阻害剤と組み合わせて投与される、請求項32~35のいずれか一項記載の使用。
- 免疫チェックポイント阻害剤が、(a) PD-1阻害剤またはPD-L1阻害剤である、(b) ニボルマブである、または(c) アテゾリズマブ、アベルマブ、およびデュルバルマブからなる群より選択される、請求項36記載の使用。
- 薬学的組成物へと製剤化された抗体薬物コンジュゲートが、(i) 1~10mg/kg対象体重、(ii) 1~5mg/kg対象体重、(iii) 1~2.5mg/kg対象体重、(iv) 1~1.25mg/kg対象体重、(v) 約1mg/kg対象体重、または(vi) 約1.25mg/kg対象体重の用量で投与される、請求項32~37のいずれか一項記載の使用。
- 薬学的組成物へと製剤化された抗体薬物コンジュゲートが、静脈内(IV)注射または注入によって投与される、請求項38記載の使用。
- 薬学的組成物へと製剤化された抗体薬物コンジュゲートが、3週間に2回のサイクルで、約30分かけて静脈内(IV)注射または注入によって投与される、請求項39記載の使用。
- 薬学的組成物へと製剤化された抗体薬物コンジュゲートが、3週間のサイクルごとの第1日および第8日に約30分かけて静脈内(IV)注射または注入によって投与される、請求項40記載の使用。
- 薬学的組成物が、3週間のサイクルごとの第1日に静脈内(IV)注射または注入によって投与される免疫チェックポイント阻害剤と組み合わせて投与され、免疫チェックポイント阻害剤が、約30分または60分かけて約100mg~約1500mgの量で投与される、請求項41記載の使用。
- 薬学的組成物へと製剤化された抗体薬物コンジュゲートが、4週間に3回のサイクルで、約30分かけて静脈内(IV)注射または注入によって投与される、請求項39記載の使用。
- 薬学的組成物へと製剤化された抗体薬物コンジュゲートが、4週間のサイクルごとの第1日、第8日および第15日に約30分かけて静脈内(IV)注射または注入によって投与される、請求項43記載の使用。
- 静脈内(IV)注射または注入によって免疫チェックポイント阻害剤が投与される、請求項36記載の使用。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024105882A JP7735490B2 (ja) | 2018-12-03 | 2024-07-01 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
| JP2025141148A JP2025170007A (ja) | 2018-12-03 | 2025-08-27 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862774819P | 2018-12-03 | 2018-12-03 | |
| US62/774,819 | 2018-12-03 | ||
| PCT/US2019/056214 WO2020117373A1 (en) | 2018-12-03 | 2019-10-15 | Pharmaceutical compositions comprising anti-191p4d12 antibody drug conjugates and methods of use thereof |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024105882A Division JP7735490B2 (ja) | 2018-12-03 | 2024-07-01 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2022513684A JP2022513684A (ja) | 2022-02-09 |
| JPWO2020117373A5 JPWO2020117373A5 (ja) | 2022-10-13 |
| JP7514834B2 true JP7514834B2 (ja) | 2024-07-11 |
Family
ID=70974767
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021531103A Active JP7514834B2 (ja) | 2018-12-03 | 2019-10-15 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
| JP2024105882A Active JP7735490B2 (ja) | 2018-12-03 | 2024-07-01 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
| JP2025141148A Pending JP2025170007A (ja) | 2018-12-03 | 2025-08-27 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024105882A Active JP7735490B2 (ja) | 2018-12-03 | 2024-07-01 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
| JP2025141148A Pending JP2025170007A (ja) | 2018-12-03 | 2025-08-27 | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 |
Country Status (17)
| Country | Link |
|---|---|
| US (2) | US12257340B2 (ja) |
| EP (1) | EP3890778A4 (ja) |
| JP (3) | JP7514834B2 (ja) |
| KR (1) | KR20210100671A (ja) |
| CN (1) | CN113677364B (ja) |
| AR (1) | AR117652A1 (ja) |
| AU (1) | AU2019392090A1 (ja) |
| BR (1) | BR112021010364A2 (ja) |
| CA (1) | CA3121573A1 (ja) |
| EA (1) | EA202191201A1 (ja) |
| IL (2) | IL283522B2 (ja) |
| MX (1) | MX2021006430A (ja) |
| PH (1) | PH12021551265A1 (ja) |
| SG (1) | SG11202105689XA (ja) |
| TW (1) | TWI894130B (ja) |
| WO (1) | WO2020117373A1 (ja) |
| ZA (1) | ZA202103719B (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102735988B1 (ko) | 2019-02-18 | 2024-12-03 | 일라이 릴리 앤드 캄파니 | 치료 항체 제제 |
| KR20220054321A (ko) * | 2019-08-13 | 2022-05-02 | 어젠시스 인코포레이티드 | 191p4d12 단백질에 결합하는 항체 약물 컨쥬게이트(adc)를 사용한 암의 치료 |
| MX2022016232A (es) * | 2020-06-19 | 2023-03-14 | Agensys Inc | Marcadores para uso en metodos para tratar canceres con conjugados de anticuerpo y farmaco (adc). |
| MX2023003059A (es) * | 2020-09-17 | 2023-06-02 | Agensys Inc | Métodos para tratar cáncer con conjugados de anticuerpo-fármaco (adc) que se unen a las proteínas 191p4d12. |
| WO2022076767A1 (en) * | 2020-10-11 | 2022-04-14 | Agensys, Inc. | Methods for treating cancers with antibody drug conjugates (adc) that bind to 191p4d12 proteins |
| CN115368447B (zh) * | 2022-07-19 | 2025-12-19 | 合肥天港免疫药物有限公司 | 双特异性抗体及其应用 |
| CN115368463B (zh) * | 2022-07-19 | 2025-12-19 | 合肥天港免疫药物有限公司 | 双特异性抗体及其应用 |
| CN115969986A (zh) * | 2022-12-30 | 2023-04-18 | 上海药明生物技术有限公司 | 羟丙基β环糊精稳定MMAE类抗体药物偶联物制剂的应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008521411A (ja) | 2004-11-30 | 2008-06-26 | キュラジェン コーポレイション | Gpnmbに対する抗体およびその使用 |
| JP2012514651A (ja) | 2009-01-09 | 2012-06-28 | シアトル ジェネティクス,インコーポレーテッド | 抗CD30vc−PAB−MMAE抗体−薬物コンジュゲートのウィークリー投与計画 |
| JP2013543498A (ja) | 2010-09-29 | 2013-12-05 | アジェンシス,インコーポレイテッド | 191p4d12タンパク質に結合する抗体薬物結合体(adc) |
Family Cites Families (152)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4179337A (en) | 1973-07-20 | 1979-12-18 | Davis Frank F | Non-immunogenic polypeptides |
| JPS6023084B2 (ja) | 1979-07-11 | 1985-06-05 | 味の素株式会社 | 代用血液 |
| US4640835A (en) | 1981-10-30 | 1987-02-03 | Nippon Chemiphar Company, Ltd. | Plasminogen activator derivatives |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4496689A (en) | 1983-12-27 | 1985-01-29 | Miles Laboratories, Inc. | Covalently attached complex of alpha-1-proteinase inhibitor with a water soluble polymer |
| DE3675588D1 (de) | 1985-06-19 | 1990-12-20 | Ajinomoto Kk | Haemoglobin, das an ein poly(alkenylenoxid) gebunden ist. |
| US4791192A (en) | 1986-06-26 | 1988-12-13 | Takeda Chemical Industries, Ltd. | Chemically modified protein with polyethyleneglycol |
| US4880935A (en) | 1986-07-11 | 1989-11-14 | Icrf (Patents) Limited | Heterobifunctional linking agents derived from N-succinimido-dithio-alpha methyl-methylene-benzoates |
| US5260203A (en) | 1986-09-02 | 1993-11-09 | Enzon, Inc. | Single polypeptide chain binding molecules |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| US5258498A (en) | 1987-05-21 | 1993-11-02 | Creative Biomolecules, Inc. | Polypeptide linkers for production of biosynthetic proteins |
| DE3853515T3 (de) | 1987-05-21 | 2005-08-25 | Micromet Ag | Multifunktionelle proteine mit vorbestimmter zielsetzung. |
| US5677425A (en) | 1987-09-04 | 1997-10-14 | Celltech Therapeutics Limited | Recombinant antibody |
| IL106992A (en) | 1988-02-11 | 1994-06-24 | Bristol Myers Squibb Co | Acylhydrazone derivatives of anthracycline and methods for their preparation |
| US6075181A (en) | 1990-01-12 | 2000-06-13 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US6150584A (en) | 1990-01-12 | 2000-11-21 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| WO1994004679A1 (en) | 1991-06-14 | 1994-03-03 | Genentech, Inc. | Method for making humanized antibodies |
| US6800738B1 (en) | 1991-06-14 | 2004-10-05 | Genentech, Inc. | Method for making humanized antibodies |
| JP4124480B2 (ja) | 1991-06-14 | 2008-07-23 | ジェネンテック・インコーポレーテッド | 免疫グロブリン変異体 |
| WO1993011161A1 (en) | 1991-11-25 | 1993-06-10 | Enzon, Inc. | Multivalent antigen-binding proteins |
| US5622929A (en) | 1992-01-23 | 1997-04-22 | Bristol-Myers Squibb Company | Thioether conjugates |
| AU4116793A (en) | 1992-04-24 | 1993-11-29 | Board Of Regents, The University Of Texas System | Recombinant production of immunoglobulin-like domains in prokaryotic cells |
| US5635483A (en) | 1992-12-03 | 1997-06-03 | Arizona Board Of Regents Acting On Behalf Of Arizona State University | Tumor inhibiting tetrapeptide bearing modified phenethyl amides |
| GB9225453D0 (en) | 1992-12-04 | 1993-01-27 | Medical Res Council | Binding proteins |
| DK0672142T3 (da) | 1992-12-04 | 2001-06-18 | Medical Res Council | Multivalente og multispecifikke bindingsproteiner samt fremstilling og anvendelse af disse |
| US5780588A (en) | 1993-01-26 | 1998-07-14 | Arizona Board Of Regents | Elucidation and synthesis of selected pentapeptides |
| US6214345B1 (en) | 1993-05-14 | 2001-04-10 | Bristol-Myers Squibb Co. | Lysosomal enzyme-cleavable antitumor drug conjugates |
| US7625697B2 (en) | 1994-06-17 | 2009-12-01 | The Board Of Trustees Of The Leland Stanford Junior University | Methods for constructing subarrays and subarrays made thereby |
| US5663149A (en) | 1994-12-13 | 1997-09-02 | Arizona Board Of Regents Acting On Behalf Of Arizona State University | Human cancer inhibitory pentapeptide heterocyclic and halophenyl amides |
| US5869046A (en) | 1995-04-14 | 1999-02-09 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US6121022A (en) | 1995-04-14 | 2000-09-19 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US6051227A (en) | 1995-07-25 | 2000-04-18 | The Regents Of The University Of California, Office Of Technology Transfer | Blockade of T lymphocyte down-regulation associated with CTLA-4 signaling |
| US5855887A (en) | 1995-07-25 | 1999-01-05 | The Regents Of The University Of California | Blockade of lymphocyte down-regulation associated with CTLA-4 signaling |
| US5811097A (en) | 1995-07-25 | 1998-09-22 | The Regents Of The University Of California | Blockade of T lymphocyte down-regulation associated with CTLA-4 signaling |
| WO1997023243A1 (en) | 1995-12-22 | 1997-07-03 | Bristol-Myers Squibb Company | Branched hydrazone linkers |
| US6207157B1 (en) | 1996-04-23 | 2001-03-27 | The United States Of America As Represented By The Department Of Health And Human Services | Conjugate vaccine for nontypeable Haemophilus influenzae |
| JP2001509679A (ja) | 1997-01-21 | 2001-07-24 | ヒューマン・ジェノム・サイエンシズ・インコーポレイテッド | レセプターをコードするポリヌクレオチドとポリペプチド |
| US6277375B1 (en) | 1997-03-03 | 2001-08-21 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| US20030065156A1 (en) | 1997-12-23 | 2003-04-03 | Williams Lewis T. | Novel human genes and gene expression products I |
| ES2272061T5 (es) | 1998-04-15 | 2012-02-24 | Merck Serono Biodevelopment | Secuencia genómica de la proteína activadora de 5-lipoxigenasa (flap), marcadores polimórficos de la misma y métodos para la detección de asma. |
| US6264949B1 (en) | 1998-09-29 | 2001-07-24 | Mount Sinai School Of Medicine Of New York University | Noninvasive agents for diagnosis and prognosis of the progression of fibrosis |
| US20020137160A1 (en) | 1998-12-17 | 2002-09-26 | Byatt John C | Nucleic acid and other molecules associated with lactation and muscle and fat deposition |
| US6682736B1 (en) | 1998-12-23 | 2004-01-27 | Abgenix, Inc. | Human monoclonal antibodies to CTLA-4 |
| US7160694B2 (en) | 1999-06-14 | 2007-01-09 | Millennium Pharmaceuticals, Inc. | Nucleic acids encoding TANGO405 and functional fragments and uses thereof |
| EP1194549A2 (en) | 1999-07-02 | 2002-04-10 | Chiron Corporation | Human genes and gene expression products |
| EP1074617A3 (en) | 1999-07-29 | 2004-04-21 | Research Association for Biotechnology | Primers for synthesising full-length cDNA and their use |
| US7605238B2 (en) | 1999-08-24 | 2009-10-20 | Medarex, Inc. | Human CTLA-4 antibodies and their uses |
| ATE354655T1 (de) | 1999-08-24 | 2007-03-15 | Medarex Inc | Humane antikörper gegen ctla-4 und deren verwendungen |
| CA2382161A1 (en) | 1999-09-03 | 2001-03-15 | Human Genome Sciences, Inc. | Immunoglobulin superfamily polynucleotides, polypeptides, and antibodies |
| EP1218392A4 (en) | 1999-09-10 | 2003-04-09 | Millennium Pharm Inc | GENE THE PROTEINS ENCODE WHICH PROGNOSTIC, DIAGNOSTIC, PREVENTIVE, THERAPEUTIC AND OTHER USE HAVE |
| AU7721500A (en) | 1999-09-29 | 2001-04-30 | Human Genome Sciences, Inc. | Colon and colon cancer associated polynucleotides and polypeptides |
| AU2001229340A1 (en) | 2000-01-14 | 2001-07-24 | Millennium Pharmaceuticals, Inc. | Genes compositions, kits, and methods for identification, assessment, prevention, and therapy of breast cancer |
| CA2397407A1 (en) | 2000-01-31 | 2001-08-02 | Human Genome Sciences, Inc. | Nucleic acids, proteins, and antibodies |
| US20030013649A1 (en) | 2000-01-31 | 2003-01-16 | Rosen Craig A. | Nucleic acids, proteins, and antibodies |
| US20020168711A1 (en) | 2000-01-31 | 2002-11-14 | Rosen Craig A. | Nucleic acids, proteins, and antibodies |
| AU2001243142A1 (en) | 2000-02-03 | 2001-08-14 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| AU2001241541A1 (en) | 2000-02-17 | 2001-08-27 | Millennium Predictive Medicine, Inc. | Novel genes, compositions, kits, and methods for identification, assessment, prevention, and therapy of human prostate cancer |
| CN1169954C (zh) | 2000-03-09 | 2004-10-06 | 上海市肿瘤研究所 | 编码具有抑制癌细胞生长功能的人蛋白的多核苷酸 |
| AU4592601A (en) | 2000-03-21 | 2001-10-03 | Millennium Predictive Medicine | Novel genes, compositions, kits, and method for identification, assessment, prevention, and therapy of ovarian cancer |
| US6436703B1 (en) | 2000-03-31 | 2002-08-20 | Hyseq, Inc. | Nucleic acids and polypeptides |
| WO2001090304A2 (en) | 2000-05-19 | 2001-11-29 | Human Genome Sciences, Inc. | Nucleic acids, proteins, and antibodies |
| WO2001094629A2 (en) | 2000-06-05 | 2001-12-13 | Avalon Pharmaceuticals | Cancer gene determination and therapeutic screening using signature gene sets |
| JP2004508019A (ja) | 2000-07-28 | 2004-03-18 | コンピュジェン インコーポレイテッド | トランスクリプトームの中に場所を占めるrna転写物及びスプライス変異体を検出するためのオリゴヌクレオチドライブラリー |
| MXPA03002479A (es) | 2000-10-05 | 2004-05-24 | Immunex Corp | Polipeptidos de nectina, polinucleotidos, metodos para elaborarlos y uso de los mismos. |
| WO2002059377A2 (en) | 2001-01-24 | 2002-08-01 | Protein Design Labs | Methods of diagnosis of breast cancer, compositions and methods of screening for modulators of breast cancer |
| US20040029114A1 (en) | 2001-01-24 | 2004-02-12 | Eos Technology, Inc. | Methods of diagnosis of breast cancer, compositions and methods of screening for modulators of breast cancer |
| AU2002251841A1 (en) | 2001-01-30 | 2002-08-12 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of pancreatic cancer |
| US7271240B2 (en) | 2001-03-14 | 2007-09-18 | Agensys, Inc. | 125P5C8: a tissue specific protein highly expressed in various cancers |
| AU2002338431A1 (en) | 2001-04-04 | 2002-11-05 | Quark Biotech, Inc. | Sequence characteristics of bladder cancer |
| JP2005527180A (ja) | 2001-04-18 | 2005-09-15 | プロテイン デザイン ラブス, インコーポレイテッド | 肺がんの診断方法、肺がんの修飾因子の組成及びスクリーニングの方法 |
| US20030083263A1 (en) | 2001-04-30 | 2003-05-01 | Svetlana Doronina | Pentapeptide compounds and uses related thereto |
| US6884869B2 (en) | 2001-04-30 | 2005-04-26 | Seattle Genetics, Inc. | Pentapeptide compounds and uses related thereto |
| US6794501B2 (en) | 2001-05-04 | 2004-09-21 | Ludwig Institute For Cancer Research | Colon cancer antigen panel |
| EP1572872A2 (en) | 2001-06-05 | 2005-09-14 | Exelixis, Inc. | Igs as modifiers of the p53 pathway and methods of use |
| CA2451465A1 (en) | 2001-06-18 | 2002-12-27 | Eos Biotechnology Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| US7171311B2 (en) | 2001-06-18 | 2007-01-30 | Rosetta Inpharmatics Llc | Methods of assigning treatment to breast cancer patients |
| US7189507B2 (en) | 2001-06-18 | 2007-03-13 | Pdl Biopharma, Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| US20040076955A1 (en) | 2001-07-03 | 2004-04-22 | Eos Biotechnology, Inc. | Methods of diagnosis of bladder cancer, compositions and methods of screening for modulators of bladder cancer |
| US20030099974A1 (en) | 2001-07-18 | 2003-05-29 | Millennium Pharmaceuticals, Inc. | Novel genes, compositions, kits and methods for identification, assessment, prevention, and therapy of breast cancer |
| KR101005130B1 (ko) | 2001-07-19 | 2011-01-04 | 니목스 코포레이션 | 종양 및 세포의 제거 또는 파괴를 필요로 하는 다른질환의 치료에 효과적인 펩티드 |
| EP2143438B1 (en) | 2001-09-18 | 2011-07-13 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumors |
| JP4200100B2 (ja) | 2001-11-07 | 2008-12-24 | アジェンシス,インコーポレイテッド | 癌の処置および検出において有用な161p2f10bと称される、核酸および対応タンパク質 |
| US20030232350A1 (en) | 2001-11-13 | 2003-12-18 | Eos Biotechnology, Inc. | Methods of diagnosis of cancer, compositions and methods of screening for modulators of cancer |
| EP1456652A4 (en) | 2001-11-13 | 2005-11-02 | Dana Farber Cancer Inst Inc | IMMUNOCELL ACTIVATION MODULATING SUBSTANCES AND USE METHOD THEREFOR |
| WO2003042661A2 (en) | 2001-11-13 | 2003-05-22 | Protein Design Labs, Inc. | Methods of diagnosis of cancer, compositions and methods of screening for modulators of cancer |
| IL149820A0 (en) | 2002-05-23 | 2002-11-10 | Curetech Ltd | Humanized immunomodulatory monoclonal antibodies for the treatment of neoplastic disease or immunodeficiency |
| AU2003245488A1 (en) | 2002-06-13 | 2003-12-31 | Regulome Corporation | Functional sites |
| EP2206517B1 (en) | 2002-07-03 | 2023-08-02 | Ono Pharmaceutical Co., Ltd. | Immunopotentiating compositions comprising anti-PD-L1 antibodies |
| EP2353611B1 (en) | 2002-07-31 | 2015-05-13 | Seattle Genetics, Inc. | Drug conjugates and their use for treating cancer, an autoimmune disease or an infectious disease |
| US20040081653A1 (en) | 2002-08-16 | 2004-04-29 | Raitano Arthur B. | Nucleic acids and corresponding proteins entitled 251P5G2 useful in treatment and detection of cancer |
| AU2008202217B2 (en) | 2002-08-16 | 2012-07-26 | Agensys, Inc. | Nucleic acids and corresponding proteins entitled 191PAD12(b) useful in treatment and detection of cancer |
| CA2496923A1 (en) | 2002-08-29 | 2004-03-11 | University Of Massachusetts | Utilization of emulsion interface engineering to produce oxidatively stable lipid delivery systems |
| JP4511943B2 (ja) | 2002-12-23 | 2010-07-28 | ワイス エルエルシー | Pd−1に対する抗体およびその使用 |
| EP2270051B1 (en) | 2003-01-23 | 2019-05-15 | Ono Pharmaceutical Co., Ltd. | Antibody specific for human PD-1 and CD3 |
| AR045563A1 (es) | 2003-09-10 | 2005-11-02 | Warner Lambert Co | Anticuerpos dirigidos a m-csf |
| PT2489364E (pt) | 2003-11-06 | 2015-04-16 | Seattle Genetics Inc | Compostos de monometilvalina conjugados com anticorpos |
| WO2005092380A2 (en) | 2004-03-26 | 2005-10-06 | Pfizer Products Inc | Uses of anti-ctla-4 antibodies |
| WO2005111076A1 (en) | 2004-05-12 | 2005-11-24 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | Nectin 4 (n4) as a marker for cancer prognosis |
| US7691962B2 (en) | 2004-05-19 | 2010-04-06 | Medarex, Inc. | Chemical linkers and conjugates thereof |
| NZ553500A (en) | 2004-09-23 | 2009-11-27 | Genentech Inc Genentech Inc | Cysteine engineered antibodies and conjugates withCysteine engineered antibodies and conjugates with a free cysteine amino acid in the heavy chain a free cysteine amino acid in the heavy chain |
| CN101500590A (zh) | 2005-03-31 | 2009-08-05 | 阿根西斯公司 | 与161p2f10b蛋白结合的抗体和相关分子 |
| WO2006105488A2 (en) | 2005-03-31 | 2006-10-05 | Agensys, Inc. | Antibodies and related molecules that bind to 161p2f10b proteins |
| PL2161336T5 (pl) | 2005-05-09 | 2017-10-31 | Ono Pharmaceutical Co | Ludzkie przeciwciała monoklonalne przeciwko białku Programmed Death 1 (PD-1) oraz sposoby leczenia raka z zastosowaniem samych przeciwciał anty-PD-1 lub w połączeniu z innymi środkami immunoterapeutycznymi |
| CN104356236B (zh) | 2005-07-01 | 2020-07-03 | E.R.施贵宝&圣斯有限责任公司 | 抗程序性死亡配体1(pd-l1)的人单克隆抗体 |
| US7612181B2 (en) | 2005-08-19 | 2009-11-03 | Abbott Laboratories | Dual variable domain immunoglobulin and uses thereof |
| EP2078732B1 (en) | 2006-07-10 | 2015-09-16 | Fujita Health University | Method of identifying a candidate diagnostic or therapeutic antibody using flow cytometry |
| LT2845866T (lt) | 2006-10-27 | 2017-07-10 | Genentech, Inc. | Antikūnai ir imunokonjugatai bei jų panaudojimas |
| JP5394246B2 (ja) | 2007-03-30 | 2014-01-22 | ジェネンテック, インコーポレイテッド | 抗体及びイムノコンジュゲートとこれらの使用方法 |
| CA2691357C (en) | 2007-06-18 | 2014-09-23 | N.V. Organon | Antibodies to human programmed death receptor pd-1 |
| DK2234600T3 (da) * | 2007-12-21 | 2014-09-08 | Hoffmann La Roche | Antistofformulering |
| US8168757B2 (en) | 2008-03-12 | 2012-05-01 | Merck Sharp & Dohme Corp. | PD-1 binding proteins |
| PL2350129T3 (pl) | 2008-08-25 | 2015-12-31 | Amplimmune Inc | Kompozycje antagonistów PD-1 i sposoby stosowania |
| CA2998281C (en) | 2008-09-26 | 2022-08-16 | Dana-Farber Cancer Institute, Inc. | Human anti-pd-1 antobodies and uses therefor |
| EP4331604B9 (en) | 2008-12-09 | 2025-07-23 | F. Hoffmann-La Roche AG | Anti-pd-l1 antibodies and their use to enhance t-cell function |
| ES2629337T3 (es) | 2009-02-09 | 2017-08-08 | Inserm - Institut National De La Santé Et De La Recherche Médicale | Anticuerpos contra PD-1 y anticuerpos contra PD-L1 y usos de los mismos |
| US20130017199A1 (en) | 2009-11-24 | 2013-01-17 | AMPLIMMUNE ,Inc. a corporation | Simultaneous inhibition of pd-l1/pd-l2 |
| WO2011082400A2 (en) | 2010-01-04 | 2011-07-07 | President And Fellows Of Harvard College | Modulators of immunoinhibitory receptor pd-1, and methods of use thereof |
| US8758758B1 (en) * | 2010-01-08 | 2014-06-24 | Seattle Genetics, Inc. | Post-relapse treatment of CD30 expressing lymphomas |
| CA2802344C (en) | 2010-06-18 | 2023-06-13 | The Brigham And Women's Hospital, Inc. | Bi-specific antibodies against tim-3 and pd-1 for immunotherapy in chronic immune conditions |
| US8907053B2 (en) | 2010-06-25 | 2014-12-09 | Aurigene Discovery Technologies Limited | Immunosuppression modulating compounds |
| WO2014009774A1 (en) | 2012-07-12 | 2014-01-16 | Hangzhou Dac Biotech Co., Ltd | Conjugates of cell binding molecules with cytotoxic agents |
| US20150231241A1 (en) | 2012-08-14 | 2015-08-20 | Ibc Pharmaceuticals, Inc. | Combination therapy for inducing immune response to disease |
| WO2014085666A1 (en) | 2012-11-27 | 2014-06-05 | Board Of Regents, The University Of Texas System | Methods of characterizing and treating molecular subset of muscle-invasive bladder cancer |
| US10023916B2 (en) | 2013-04-15 | 2018-07-17 | Regeneron Pharmaceuticals, Inc. | Markers of tumor cell response to anti-cancer therapy |
| HUE053069T2 (hu) | 2013-05-02 | 2021-06-28 | Anaptysbio Inc | Programozott halál-1 (PD-1) ellen irányuló ellenanyagok |
| CA2913977C (en) | 2013-05-31 | 2022-11-29 | Sorrento Therapeutics, Inc. | Antigen binding proteins that bind pd-1 |
| PT3702373T (pt) | 2013-09-13 | 2022-09-27 | Beigene Switzerland Gmbh | Anticorpos anti-pd1 e a sua utilização como agentes terapêuticos e de diagnóstico |
| SG10201804945WA (en) | 2013-12-12 | 2018-07-30 | Shanghai hengrui pharmaceutical co ltd | Pd-1 antibody, antigen-binding fragment thereof, and medical application thereof |
| TWI681969B (zh) | 2014-01-23 | 2020-01-11 | 美商再生元醫藥公司 | 針對pd-1的人類抗體 |
| JOP20200094A1 (ar) | 2014-01-24 | 2017-06-16 | Dana Farber Cancer Inst Inc | جزيئات جسم مضاد لـ pd-1 واستخداماتها |
| AU2015289533B2 (en) | 2014-07-18 | 2021-04-01 | Advaxis, Inc. | Combination of a PD-1 antagonist and a Listeria-based vaccine for treating prostate cancer |
| US20180030144A1 (en) * | 2014-10-10 | 2018-02-01 | Innate Pharma | Cd73 blockade |
| GB201419185D0 (en) | 2014-10-28 | 2014-12-10 | Adc Biotechnology Ltd | Method of synthesising ADCs using affinity resin |
| CA2985483A1 (en) | 2015-06-08 | 2016-12-15 | Genentech, Inc. | Methods of treating cancer using anti-ox40 antibodies |
| US10669338B2 (en) | 2016-06-17 | 2020-06-02 | Immunomedics, Inc. | Anti-PD-1 checkpoint inhibitor antibodies that block binding of PD-L1 to PD-1 |
| KR20190031246A (ko) * | 2016-07-20 | 2019-03-25 | 에르피오 세러퓨틱스 인코포레이티드 | VE-PTP (HPTP-β)를 표적으로 하는 인간화된 단클론성 항체 |
| WO2018110515A1 (ja) | 2016-12-12 | 2018-06-21 | 第一三共株式会社 | 抗体-薬物コンジュゲートと免疫チェックポイント阻害剤の組み合わせ |
| MX2019014318A (es) | 2017-06-05 | 2020-08-13 | Agensys Inc | Proteinas de union a nectina-4 y metodos de uso de las mismas. |
| MX420258B (es) | 2017-09-07 | 2025-02-10 | Dragonfly Therapeutics Inc | Proteínas de unión a nkg2d, cd16 y nectina 4. |
| MX2020009842A (es) | 2018-03-23 | 2020-10-15 | Seattle Genetics Inc | Uso de conjugados de anticuerpo-farmaco que comprenden agentes interruptores de tubulina para tratar tumor solido. |
| CA3111401A1 (en) | 2018-09-19 | 2020-03-26 | Genentech, Inc. | Therapeutic and diagnostic methods for bladder cancer |
| CN111423512B (zh) | 2019-01-10 | 2024-01-05 | 北京比洋生物技术有限公司 | 阻断血管内皮细胞生长且活化t细胞的多靶向融合蛋白和包含其的药物组合物 |
| WO2021022172A1 (en) | 2019-08-01 | 2021-02-04 | Incyte Corporation | A dosing regimen for an ido inhibitor |
| KR20220054321A (ko) | 2019-08-13 | 2022-05-02 | 어젠시스 인코포레이티드 | 191p4d12 단백질에 결합하는 항체 약물 컨쥬게이트(adc)를 사용한 암의 치료 |
| CA3162282A1 (en) | 2019-11-25 | 2021-06-03 | Agensys, Inc. | Treatment of cancers with antibody drug conjugates (adc) that bind to 191p4d12 proteins |
| MX2022016232A (es) | 2020-06-19 | 2023-03-14 | Agensys Inc | Marcadores para uso en metodos para tratar canceres con conjugados de anticuerpo y farmaco (adc). |
| MX2023003059A (es) | 2020-09-17 | 2023-06-02 | Agensys Inc | Métodos para tratar cáncer con conjugados de anticuerpo-fármaco (adc) que se unen a las proteínas 191p4d12. |
| WO2022076767A1 (en) | 2020-10-11 | 2022-04-14 | Agensys, Inc. | Methods for treating cancers with antibody drug conjugates (adc) that bind to 191p4d12 proteins |
| WO2023019236A1 (en) | 2021-08-13 | 2023-02-16 | Agensys, Inc. | Methods for treating non-muscle invasive bladder cancer (nmibc) with antibody drug conjugates (adc) that bind to 191p4d12 proteins |
| KR20240137135A (ko) | 2022-01-05 | 2024-09-19 | 어젠시스 인코포레이티드 | 191p4d12 단백질에 결합하는 항체 약물 접합체(adc)로 근육 침습성 요로상피암 또는 근육 침습성 방광함을 치료하는 방법 |
| TW202417052A (zh) | 2022-07-25 | 2024-05-01 | 美商艾澤西公司 | 以結合191p4d12蛋白質之抗體藥物結合物(adc)組合派姆單抗(pembrolizumab)治療局部晚期或轉移性尿路上皮癌之患者之方法 |
-
2019
- 2019-10-15 JP JP2021531103A patent/JP7514834B2/ja active Active
- 2019-10-15 SG SG11202105689XA patent/SG11202105689XA/en unknown
- 2019-10-15 KR KR1020217020866A patent/KR20210100671A/ko not_active Ceased
- 2019-10-15 CN CN201980091098.7A patent/CN113677364B/zh active Active
- 2019-10-15 AR ARP190102919A patent/AR117652A1/es unknown
- 2019-10-15 EA EA202191201A patent/EA202191201A1/ru unknown
- 2019-10-15 BR BR112021010364-3A patent/BR112021010364A2/pt unknown
- 2019-10-15 EP EP19892012.6A patent/EP3890778A4/en active Pending
- 2019-10-15 AU AU2019392090A patent/AU2019392090A1/en active Pending
- 2019-10-15 IL IL283522A patent/IL283522B2/en unknown
- 2019-10-15 MX MX2021006430A patent/MX2021006430A/es unknown
- 2019-10-15 CA CA3121573A patent/CA3121573A1/en active Pending
- 2019-10-15 WO PCT/US2019/056214 patent/WO2020117373A1/en not_active Ceased
- 2019-10-15 US US17/298,865 patent/US12257340B2/en active Active
- 2019-10-15 IL IL316135A patent/IL316135A/en unknown
- 2019-10-15 TW TW108137132A patent/TWI894130B/zh active
-
2021
- 2021-05-31 ZA ZA2021/03719A patent/ZA202103719B/en unknown
- 2021-05-31 PH PH12021551265A patent/PH12021551265A1/en unknown
-
2024
- 2024-07-01 JP JP2024105882A patent/JP7735490B2/ja active Active
-
2025
- 2025-02-19 US US19/057,775 patent/US20260000604A1/en active Pending
- 2025-08-27 JP JP2025141148A patent/JP2025170007A/ja active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008521411A (ja) | 2004-11-30 | 2008-06-26 | キュラジェン コーポレイション | Gpnmbに対する抗体およびその使用 |
| JP2012514651A (ja) | 2009-01-09 | 2012-06-28 | シアトル ジェネティクス,インコーポレーテッド | 抗CD30vc−PAB−MMAE抗体−薬物コンジュゲートのウィークリー投与計画 |
| JP2013543498A (ja) | 2010-09-29 | 2013-12-05 | アジェンシス,インコーポレイテッド | 191p4d12タンパク質に結合する抗体薬物結合体(adc) |
Also Published As
| Publication number | Publication date |
|---|---|
| US12257340B2 (en) | 2025-03-25 |
| IL316135A (en) | 2024-12-01 |
| TW202034956A (zh) | 2020-10-01 |
| TWI894130B (zh) | 2025-08-21 |
| WO2020117373A8 (en) | 2021-02-18 |
| IL283522A (en) | 2021-07-29 |
| SG11202105689XA (en) | 2021-06-29 |
| AR117652A1 (es) | 2021-08-25 |
| JP7735490B2 (ja) | 2025-09-08 |
| MX2021006430A (es) | 2021-09-14 |
| KR20210100671A (ko) | 2021-08-17 |
| US20260000604A1 (en) | 2026-01-01 |
| EP3890778A1 (en) | 2021-10-13 |
| IL283522B2 (en) | 2025-03-01 |
| JP2022513684A (ja) | 2022-02-09 |
| JP2024133544A (ja) | 2024-10-02 |
| IL283522B1 (en) | 2024-11-01 |
| JP2025170007A (ja) | 2025-11-14 |
| WO2020117373A1 (en) | 2020-06-11 |
| CN113677364A (zh) | 2021-11-19 |
| AU2019392090A1 (en) | 2021-06-17 |
| EA202191201A1 (ru) | 2022-01-26 |
| PH12021551265A1 (en) | 2021-10-25 |
| EP3890778A4 (en) | 2022-08-03 |
| BR112021010364A2 (pt) | 2021-08-24 |
| ZA202103719B (en) | 2025-09-25 |
| CN113677364B (zh) | 2024-07-05 |
| CA3121573A1 (en) | 2020-06-11 |
| US20220175950A1 (en) | 2022-06-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7735490B2 (ja) | 抗191p4d12抗体薬物コンジュゲートを含む薬学的組成物、およびその使用方法 | |
| JP7657774B2 (ja) | 191p4d12タンパク質に結合する抗体薬物コンジュゲート(adc)による癌の治療方法 | |
| JP2014516508A (ja) | 抗体−薬剤コンジュゲート | |
| US20230025600A1 (en) | Treatment of cancers with antibody drug conjugates (adc) that bind to 191p4d12 proteins | |
| CN116251196A (zh) | 抗-edb抗体和抗体-药物缀合物 | |
| HK40062231A (en) | Pharmaceutical compositions comprising anti-191p4d12 antibody drug conjugates and methods of use thereof | |
| EA048197B1 (ru) | Фармацевтические композиции, включающие конъюгаты анти-191p4d12 антитело-лекарственное средство, и способы их применения | |
| HK40062231B (zh) | 包含抗191p4d12抗体药物偶联物的药物组合物及其使用方法 | |
| HK40075918A (en) | Treatment of cancers with antibody drug conjugates (adc) that bind to 191p4d12 proteins |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221004 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20221004 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230720 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230721 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231019 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20231020 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240327 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20240409 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240604 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240701 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7514834 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |