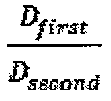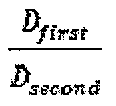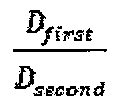JP7513799B2 - 療法薬を送達するためのデバイスおよび方法 - Google Patents
療法薬を送達するためのデバイスおよび方法 Download PDFInfo
- Publication number
- JP7513799B2 JP7513799B2 JP2023076521A JP2023076521A JP7513799B2 JP 7513799 B2 JP7513799 B2 JP 7513799B2 JP 2023076521 A JP2023076521 A JP 2023076521A JP 2023076521 A JP2023076521 A JP 2023076521A JP 7513799 B2 JP7513799 B2 JP 7513799B2
- Authority
- JP
- Japan
- Prior art keywords
- membrane
- polymer
- cells
- molecular weight
- electrospun
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/022—Artificial gland structures using bioreactors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/37—Digestive system
- A61K35/39—Pancreas; Islets of Langerhans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0024—Solid, semi-solid or solidifying implants, which are implanted or injected in body tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7007—Drug-containing films, membranes or sheets
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3804—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells characterised by specific cells or progenitors thereof, e.g. fibroblasts, connective tissue cells, kidney cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3804—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells characterised by specific cells or progenitors thereof, e.g. fibroblasts, connective tissue cells, kidney cells
- A61L27/3834—Cells able to produce different cell types, e.g. hematopoietic stem cells, mesenchymal stem cells, marrow stromal cells, embryonic stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/54—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/56—Porous materials, e.g. foams or sponges
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M31/00—Devices for introducing or retaining media, e.g. remedies, in cavities of the body
- A61M31/002—Devices for releasing a drug at a continuous and controlled rate for a prolonged period of time
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0676—Pancreatic cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0676—Pancreatic cells
- C12N5/0678—Stem cells; Progenitor cells; Precursor cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/20—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices containing or releasing organic materials
- A61L2300/252—Polypeptides, proteins, e.g. glycoproteins, lipoproteins, cytokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/43—Hormones, e.g. dexamethasone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2400/00—Materials characterised by their function or physical properties
- A61L2400/12—Nanosized materials, e.g. nanofibres, nanoparticles, nanowires, nanotubes; Nanostructured surfaces
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2537/00—Supports and/or coatings for cell culture characterised by physical or chemical treatment
- C12N2537/10—Cross-linking
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0613—Cells from endocrine organs
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Zoology (AREA)
- Cell Biology (AREA)
- Pharmacology & Pharmacy (AREA)
- Biotechnology (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Transplantation (AREA)
- Dermatology (AREA)
- Gastroenterology & Hepatology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Immunology (AREA)
- Developmental Biology & Embryology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Hematology (AREA)
- Heart & Thoracic Surgery (AREA)
- Urology & Nephrology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Botany (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Virology (AREA)
- Neurosurgery (AREA)
- Anesthesiology (AREA)
- Dispersion Chemistry (AREA)
Description
[0001] 本出願は、2017年6月14日に出願された米国仮出願第62/519,702号の利益を主張し、その出願は、参照により本明細書にそのまま援用される。
[0004] 一側面において、膜および非天然膵β細胞の集団を含むデバイスが、開示され、ここで、前記の非天然膵β細胞は、グルコース負荷に対してインビトログルコース刺激インスリン分泌(GSIS)反応を示し、ここで、前記の膜は、約2以上の
ゲン、プロカスパーゼ、パシファスチン、プロエラスターゼ、プロリパーゼおよびプロカルボキシポリペプチダーゼからなる群から選択される。ある場合には、前記の療法剤は、約0.01mg療法剤/mgポリマー~約0.5mg療法剤/mgポリマーの範囲で存在する。ある場合には、前記の療法剤は、少なくとも3日間前記の膜から放出されるように設計されている。ある場合には、前記の療法剤は、疎水性である。ある場合には、前記の療法剤は、親水性である。ある場合には、前記の療法剤は、微細化された微粒子の形態である。
は酵素である。ある場合には、前記の療法剤は、ホルモンである。ある場合には、前記の療法剤は、アミノ酸由来ホルモン、エイコサノイド、ペプチドホルモンまたはステロイドである。ある場合には、前記の療法剤は、グルカゴン、成長ホルモン、インスリン、膵臓ポリペプチド、副甲状腺ホルモン、ソマトスタチンおよびグルココルチコイドからなる群から選択される。ある場合には、前記の療法剤は、酵素である。ある場合には、前記の療法剤は、プロテアーゼ、リパーゼ、アミラーゼ、ホスホリパーゼA2、リゾホスホリパーゼまたはコレステロールエステラーゼである。ある場合には、前記の療法剤は、アンギオテンシノーゲン、トリプシノーゲン、キモトリプシノーゲン、ペプシノーゲン、フィブリノーゲン、プロカスパーゼ、パシファスチン、プロエラスターゼ、プロリパーゼおよびプロカルボキシポリペプチダーゼからなる群から選択される。ある場合には、前記の療法剤は、約0.01mg療法剤/mgポリマー~約0.5mg療法剤/mgポリマーの範囲で存在する。ある場合には、前記の療法剤は、少なくとも3日間前記の膜から放出されるように設計されている。ある場合には、前記の療法剤は、疎水性である。ある場合には、前記の療法剤は、親水性である。ある場合には、前記の療法剤は、微粉化された微粒子の形態である。
PHEMA、PCLまたはPLLAを含む。ある側面において、機能性ポリマーは、PEG、PEGMA、PEGDAまたはTEGDAを含む。さらなる側面において、ベースポリマーは、PANである。さらに別の側面において、機能性ポリマーは、PEGMAである。他の側面において、機能性ポリマーは、PEGDAである。さらに他の側面において、機能性ポリマーは、TEGDAである。
[0027] さらなる側面において、繊維は、約180~240nmの範囲内の直径を含む。他の側面において、繊維は、約520~560nmの範囲内の直径を含む。ある側面において、繊維は、約1000nm以下の直径を含む。ある側面において、膜は、約10~150μmの範囲内の厚さを含む。さらなる側面において、膜は、約80~120μmの範囲内の厚さを含む。
)プロピオニルヒドラジド、プロパルギル-N-ヒドロキシルスクシンイミジルエステル、PTAD-アジド、スルホ-NHS-ジアジリン、スルホスクシンイミジル4,4’-アジペンタノエート、4-(N-マレイミド)ベンゾフェノン、4-アジドフェナシルブロミド、5-アジド-2-ニトロ安息香酸N-ヒドロキシスクシンイミドエステル(5-azido-2-nitriobenzoic acid N-hydroxy succinimide ester)、スクシンイミジル-[4-(ソラレン-8-イルオキシ)]ブチレート、4-ベンゾイル安息香酸N-スクシンイミジルエステル、1,4-ビス[3-(2-ピリジルジチオ)プロピオンアミド]ブタン、ビス-マレイミドエタン、ジチオ-ビス-マレイミドエタンまたはそれらのあらゆる組合せを含む。
ースポリマーは、PAN、PET、PLG、PHEMA、PCLまたはPLLAを含む。
ゾインエチルエーテル、ベンゾインイソブチルエーテル、ベンゾインメチルエーテル、ベンゾフェノン、3,3’,4,4’-ベンゾフェノンテトラカルボン酸二無水物、4-ベンゾイルビフェニル、2-ベンジル-2-(ジメチルアミノ)-4’-モルホリノブチロフェノン、4,4’-ビス(ジエチルアミノ)ベンゾフェノン、カンファーキノン、2-クロロチオキサンテン-9-オン、(クメン)シクロペンタジエニル鉄(II)ヘキサフルオロホスフェート、ジベンゾスベレノン、2,2-ジエトキシアセトフェノン、4,4’-ジヒドロキシベンゾフェノン、2,2-ジメトキシ-2-フェニルアセトフェノン、4-(ジメチルアミノ)ベンゾフェノン、4,4’-ジメチルベンジル、2,5-ジメチルベンゾフェノン(2,5-dimethylbenzonphenone)、3,4-ジメチルベンゾフェノン、ジフェニル(2,4,6-トリメチルベンゾイル)ホスフィンオキシド、4’-エトキシアセトフェノン、2-エチルアントラキノン、フェロセン、3-ヒドロキシアセトフェノン、4-ヒドロキシアセトフェノン、1-ヒドロキシシクロヘキシルフェニルケトン、2-ヒドロキシ-2-メチルプロピオフェノン、2-メチルベンゾフェノン、3-メチルベンゾフェノン、メチルベンゾイルホルメート、2-メチル-4’-(メチルチオ)-2-モルホリノプロピオフェノン(2-methyl-4’-(methylthio)-2-morpholinoproiophenone)、フェナントレンキノン、4’-フェノキシアセトフェノン、チオキサンテン-9-オン、トリアリールスルホニウム、ヘキサフルオロアンチモネート塩類、トリアリールスルホニウムヘキサフルオロホスフェート塩類またはそれらのあらゆる組み合わせを含む。
クロヘキサンカルボニトリル)、2,2’-アゾビスイソブチロニトリル(2,2’-azobissobutyronitrile)、過酸化ベンゾイル、2,2’-ビス(tert-ブチルペルオキシ)ブタン、1,1-ビス(tert-ブチルペルオキシ)シクロヘキサン、2,5-ビス(tert-ブチルペルオキシ)-2,5-ジメチルヘキサン、2,5-ビス(tert-ブチルペルオキシ)-2,5-ジメチル-3-ヘキシン、ビス(1-(tert-ブチルペルオキシ)-1-メチルエチル)ベンゼン、1,1-ビス(tert-ブチルペルオキシ)-3,3,5-トリメチルシクロヘキサン、tert-ブチルヒドロペルオキシド、過酢酸tert-ブチル、tert-ブチルペルオキシド、tert-ブチルペルオキシベンゾエート、tert-ブチルペルオキシイソプロピルカーボネート、クメン、ヒドロペルオキシド、シクロヘキサノンペルオキシド、ジクミルペルオキシド、ラウロイルペルオキシド、2,4-ペンタンジオンペルオキシド、過酢酸、過硫酸カリウムまたはそれらのあらゆる組み合わせを含む。
0umの範囲内の厚さを含む。ある側面において、膜は、親水性である。ある側面において、ベースポリマーは、膜に構造的完全性を提供するように設計されている。ある側面において、ベースポリマーは、疎水性である。
[0058] 本明細書において言及される全ての刊行物、特許および特許出願は、それぞれの個々の刊行物、特許または特許出願が参照により援用されることが具体的かつ個々に示された場合と同程度まで参照により本明細書に援用される。
[0083] 別途示されない限り、本明細書中のいくつかの態様は、数値範囲を意図している。数値範囲が提供されている場合、別途示されない限り、範囲は、範囲の終点を含むことができる。別途示されない限り、数値範囲は、あたかも明示的に記載されたかのようにその中の全ての値および部分範囲を含むことができる。
るDfirst/Dsecond比を含むことができ、かつ/または提供するように設計されることができる。低分子量部分は、療法的部分であることができ、一方で高分子量部分は、宿主浸潤物または細胞である。ある場合には、本明細書に記載された膜の架橋は、膜に所望の特性、例えば上記で言及されたDfirst/Dsecond比を提供することができる。場合により、Dfirst/Dsecond比は、2以上であることができる。従って、本開示の架橋された機能性膜(例えば、電界紡糸ポリマー膜)は、より低い分子量の療法的部分の高い流動を可能にする一方で、より高い分子量の浸潤物の通過を制限するかまたは低分子量の療法的部分を分泌する操作された細胞がデバイスから出るのを防ぐことができる。ある場合には、機能性膜(例えば、電界紡糸ポリマー膜)の架橋された性質は、本明細書で開示される膜の機械的特性および構造的完全性をさらに増強し得る。
[0092] 本明細書で記載される膜は、ベースポリマーを含むことができるかまたはベースポリマーで作製されることができる。ベースポリマーは、ポリアクリロニトリル類、ポリアクリレート類、アクリルポリマー類、メタクリルポリマー類、ポリエーテル類、ポリエステル類、ポリウレタン類、乳酸ポリマー類、グリコール酸ポリマー類、セルロース、セルロイド、フルオロポリマー類、核酸、有機ケイ素ポリマー類、ペプチド類、ポリアミド、ポリアクリルアミド類、ポリカーボネート類、ポリアリールエーテルケトン、ポリオレフィン類、多糖類、タンパク質、タンニン類および/またはビニルポリマー類を含むがそれらに限定されない多くの異なるカテゴリーのポリマーを含むことができる。ベースポリマーは、生分解性または非生分解性であることができる。場合により、ベースポリマーは、生体適合性であることができる。本開示は、生体適合性であり対象への移植に適したベースポリマーを提供する。ある場合には、ベースポリマーは、コポリマー、例えばポリ(乳酸-コ-グリコール酸)(PLGA)、ポリ(フマル酸-セバシン酸無水物(pFASA)、ポリ(アクリロニトリル-コ-ブタジエン)、ポリ(アクリロニトリル-コ-ブチルメタクリレート)、ポリ(アクリロニトリル-コ-塩化ビニリデン)またはポリ(アクリルアミド)コポリマーであることができる。他の例では、ベースポリマーは、ジブロックまたはトリブロックポリマーであることができる。例えば、ジブロックまたはトリブロックポリマーは、ベースポリマーおよび別のベースポリマーの融合体であることができるであろう。別の例では、ジブロックまたはトリブロックポリマーは、ベースポリマーおよび機能性ポリマー(例えば、PLGA-PEG)の融合体であることができるであろう。
[0098] 本開示の膜は、ある場合には、機能性ポリマーを含むことができ、または機能性ポリマーから作製されることができる。機能性ポリマーは、膜に追加の特性を付与するためにさらなる合成操作を受けることができ得る。例えば、機能性ポリマーは、膜の架橋を可能にするように設計されることができる。あるいは、または加えて、機能性ポリマーは、療法剤の膜へのコンジュゲーションを可能にするように設計されることができる。場合により、機能性ポリマーは、改善された機械的強度および/またはデバイスの完全性のような特性を膜に付与することができる。本明細書で記載される機能性ポリマーは、ポリエチレングリコール(PEG)、ポリ(エチレングリコール)メタクリレート(poly(ethylene glycol) methacylate)(PEGMA)、ポリ(エチレングリコール)ジアシレート(PEGDA)、テトラエチレングリコールジアクリレート(TEGDA)またはそれらのあらゆる組み合わせを含むことができるが、それらに限定されない。
ゆる組み合わせによって架橋され得る。例えば、本開示の典型的な膜(例えば電界紡糸ポリマー膜)は、ベースポリマーとしてPANならびに機能性ポリマーとしてPEGMAまたはPEGMAおよびTEGDAを含むことができる。これらの膜(例えば電界紡糸ポリマー膜)は、膜の架橋を促進するために光開始剤の存在下でUV光にさらに曝露され、そうして機械的特性およびデバイスの完全性を向上させ、あらゆる装填された薬剤(例えば、細胞または薬物)の放出も調節することができる。
[0104] ある場合には、本明細書で記載される膜は、ベースポリマーおよび機能性ポリマーの両方を含むことができる。例えば、ベースポリマーおよび機能性ポリマーは、それぞれ本明細書で記載されるように所望の溶媒中で溶解させられ、電界紡糸の前に一緒に混合されることができる。膜は、ベースポリマー対機能性ポリマーの異なる質量比を含むことができ、または異なる質量比で作製されることができる。例えば、膜(例えば電界紡糸ポリマー膜)は、約5000対1、2000対1、1000対1、800対1、600対1、400対1、200対1、100対1、50対1、20対1、10対1、5対1、2対1、1対1、1対2、1対5、1対10、1対20、1対50、1対100、1対20
0、1対400、1対600、1対800、1対1000、1対2000、1対5000またはそれらの間のあらゆる値以上の質量比(w/w)を含むことができる。ある場合には、膜(例えば電界紡糸ポリマー膜)は、約0.001対1000、0.001対100、0.001対10、0.001対1、0.001対0.1、0.001対0.01、0.001対0.1、0.01対1000、0.01対100、0.01対10、0.01対1、0.01対0.1、0.1対1000、0.1対100、0.1対10、0.1対1、1対1000、1対100、1対10、10対1000、10対100または100対1000の範囲内の質量比(w/w)の機能性ポリマー対ベースポリマーを含むことができる。
す。図9Bにおいて示されるように、TEGDAなしでは、PEGMAの分子量の2kDaから480Daへの低下は、結果としてヤング率における低下をもたらす。しかし、TEGDAを有する架橋された機能性膜(例えば電界紡糸ポリマー膜)において、PEGMA分子量の低下は、ヤング率を増大させた。従って、機能性ポリマーの分子量は、引張強度およびヤング率の両方に影響を及ぼし得る。
[0112] 本明細書で記載されるポリマーのいずれか1種類またはいずれかの組合せを含有するポリマー溶液は、エミッターおよびコレクターを含む電界紡糸装置を使用して電界紡糸されることができる。収集されるあらゆる形態の繊維は、膜と呼ばれることができる。ポリマー溶液は、エミッターからコレクター上に噴霧され、エミッターおよびコレクターの間の電圧差によって集束される。紡糸されることができるポリマー溶液の最大濃度は、ポリマーの粘度および導電率に依存することができ、異なるベース/機能性ポリマーまたは異なる溶媒によって変動することもできる。順調な初期繊維形成の後、エミッタのx軸並進ステージは、反復線形パターンに設定されることができる。繊維は、回転ドラムコレクター上に収集されることができる。繊維は、平坦な表面上に収集されることもできる。繊維は、さらに、パターン化された構造上に繊維を収集することによって膜の形態で収集されることができる。結果として得られる膜は、パターン化された構造と同じ形状である形状を含むことができる。
[0119] 様々な架橋の方法が、本開示の機能性の架橋された膜(例えば電界紡糸ポリマー膜)を得るために利用されることができる。これらの方法は、光開始剤によるUV架橋、熱架橋開始剤による熱架橋、遷移金属および他の化学的架橋法を含むが、それらに限定されない。架橋剤は、機能性ポリマー上の反応性基間に新しい結合を形成するために、下記の架橋反応の1つにおいて使用され得るポリマー架橋剤または他の分子構造を含むことができる。言い換えれば、架橋剤は、本開示の膜(例えば電界紡糸ポリマー膜)中の機能性ポリマー上の反応性基を化学的に連結するために使用されることができる。これは、向上した機械的特性、より良好なデバイス完全性、多孔性の調節および結果として膜(例えば電界紡糸ポリマー膜)を通る様々な分子量部分の拡散速度の調節をもたらし得る。
例えば電界紡糸ポリマー膜)を光開始剤を含有する溶液中に浸漬することによって組み込まれることもできる。次いで、機能性膜(例えば電界紡糸ポリマー膜)は、乾燥させられ、架橋を開始するためにUV光の下に置かれる。本開示と適合し、機能性膜(例えば電界紡糸ポリマー膜)中に組み込まれることができる適切な光開始剤は、アセトフェノン、アニソイン、アントラキノン、ベンジル、ベンゾイン、ベンゼントリカルボニルクロム、ベンゾインエチルエーテル、ベンゾインイソブチルエーテル、ベンゾインメチルエーテル、ベンゾフェノン、3,3’,4,4’-ベンゾフェノンテトラカルボン酸二無水物、4-ベンゾイルビフェニル、2-ベンジル-2-(ジメチルアミノ)-4’-モルホリノブチロフェノン、4,4’-ビス(ジエチルアミノ)ベンゾフェノン、カンファーキノン、2-クロロチオキサンテン-9-オン、(クメン)シクロペンタジエニル鉄(II)ヘキサフルオロホスフェート、ジベンゾスベレノン、2,2-ジエトキシアセトフェノン、4,4’-ジヒドロキシベンゾフェノン、2,2-ジメトキシ-2-フェニルアセトフェノン、4-(ジメチルアミノ)ベンゾフェノン、4,4’-ジメチルベンジル、2,5-ジメチルベンゾフェノン(2,5-dimethylbenzonphenone)、3,4-ジメチルベンゾフェノン、ジフェニル(2,4,6-トリメチルベンゾイル)ホスフィンオキシド、4’-エトキシアセトフェノン、2-エチルアントラキノン、フェロセン、3-ヒドロキシアセトフェノン、4-ヒドロキシアセトフェノン、1-ヒドロキシシクロヘキシルフェニルケトン、2-ヒドロキシ-2-メチルプロピオフェノン、2-メチルベンゾフェノン、3-メチルベンゾフェノン、メチルベンゾイルホルメート、2-メチル-4’-(メチルチオ)-2-モルホリノプロピオフェノン(2-methyl-4’-(methylthio)-2-morpholinoproiophenone)、フェナントレンキノン、4’-フェノキシアセトフェノン、チオキサンテン-9-オン、トリアリールスルホニウム、ヘキサフルオロアンチモネート塩類、トリアリールスルホニウムヘキサフルオロホスフェート塩類等を含むが、それらに限定されない。
ことにより、全体の引張強度およびヤング率が、向上させられることができる。図9Cは、さらに、本明細書の架橋された機能性膜(例えば電界紡糸ポリマー膜)からの低分子量療法的部分の放出(例えば、低分子量療法的部分の所望のDfirst)の調節を示す。この図は、本明細書のDfirst係数における全体的な減弱がUVベースの架橋によって達成され得ることを図説している。
[0129] 本開示は、第1拡散係数(Dfirst)および第2拡散係数(Dsecond)の比によって特性付けられることができる膜(例えば電界紡糸ポリマー膜)を提供する。DfirstおよびDsecondは、第1分子量を有する第1部分および第2分子量部分を有する第2部分に対応する。ある場合には、第1部分は、膜内に配置されるかまたは含まれる部分(例えば療法的部分)であることができる。膜からのまたは膜を横切る第1部分の有効な放出または拡散を提供することができることが、望ましい可能性がある
。ある場合には、第2部分は、膜の外側(例えば宿主の体内)に配置されるかまたは含まれる部分であることができる。第2部分の膜中への、または膜を横切る拡散を防止する、または止めることができることが、望ましい可能性がある。一例として、第1部分は、インスリンであることができ、第2部分は、IgGであることができる。
00000Da、250000Da、300000Da、350000Da、400000Da、450000Da、500000Da、600000Da、700000Da、800000Da、900000Daまたは1000000Da。
は、所望の適用に基づいて設計されることができる。例えば、架橋された機能性膜(例えば電界紡糸ポリマー膜)を含む膜(例えば電界紡糸ポリマー膜)は、移植の目的のためおよび糖尿病を処置する目的のための対象への長期インスリン送達のために設計され得る。この例では、架橋された機能性膜(例えば電界紡糸ポリマー膜)は、インスリンを分泌する操作された幹細胞を封入するように設計され得る。従って、架橋された機能性膜(例えば電界紡糸ポリマー膜)は、膜からの分泌されるインスリン(Dfirst)の高い流束を提供し、特定のポリマー、架橋剤、架橋剤濃度、架橋時間、膜多孔性、繊維径またはそれらのあらゆる組合せを選択することによって封入細胞(Dsecond)もしくは宿主部分(Dsecond)、例えば宿主細胞もしくは宿主タンパク質、またはそれらのあらゆる組合せの拡散を制限するように設計されることができる。別の例では、架橋された機能性膜(例えば電界紡糸ポリマー膜)は、最初にインスリンを封入するように設計され得る。ここで、架橋された機能性膜(例えば電界紡糸ポリマー膜)は、膜からのインスリンの高流束(Dfirst)を提供する一方で宿主細胞または宿主タンパク質のような宿主部分の拡散(Dsecond)を制限するように設計されることができる。
[0137] 本明細書で開示される膜(例えば電界紡糸ポリマー膜)は、架橋されていてもいなくても、療法剤を装填され得る。本開示の療法剤は、間接的または直接的のいずれかで療法上の利益を示す部分を含むことができる。療法剤は、最初のポリマー溶液中への組み込みによって膜(例えば電界紡糸ポリマー膜)に埋め込まれることができ、それは、その後電界紡糸されて機能性膜(例えば電界紡糸ポリマー膜)になる。療法剤は、架橋された機能性膜(例えば電界紡糸ポリマー膜)を療法剤を含有する溶液中に浸漬することによって組み込まれることもできる。
側面(例えば遺伝子発現プロフィール)において著しく異なっていることを意味する。例えば、非天然膵β細胞は、ソマトスタチン、グルカゴンまたは両方を発現しない可能性がある。
ン、メラトニン、トリヨードチロニンおよびチロキシン)、エイコサノイド(例えばプロスタグランジン類、ロイコトリエン類、プロスタサイクリンおよびセロシス(therocis))、ペプチドホルモン(例えばアミリン、カルシトニン、エンケファリン、エリスロポエチン、ガラニン、グルカゴン、成長ホルモン、成長ホルモン放出ホルモン、インスリン、膵臓ポリペプチド、副甲状腺ホルモン、レニン、ソマトスタチンおよび血管作動性腸ペプチド)またはステロイド(例えばアンドロゲン、エストロゲン、グルココルチコイド、プロゲストーゲンおよびセコステロイド)であることができる。
[0151] 本開示の架橋された機能性膜(例えば電界紡糸ポリマー膜)を含む本明細書で開示される膜(例えば電界紡糸ポリマー膜)は、それを必要とする対象に療法的利益を与えるために利用されることができる。それを必要とする対象は、慢性疾患のような病気を有することができる。本明細書で開示される膜(例えば電界紡糸ポリマー膜)で処置され得る慢性疾患は、糖尿病を含み得る。膜(例えば電界紡糸ポリマー膜)は、対象において皮下、臓器実質中、腹腔中または筋内に移植され得る。
実施例1
膜の製造
[0155] この実施例は、膜(例えば電界紡糸ポリマー膜)の製造を記載する。膜製作プロセスは、6cmの直径を有する500rpmで動作する回転ドラムコレクターから5~17cm間隔を空けられた19ゲージ針を有する単一エミッターからなる環境制御電界紡糸装置(EC-CLI、IME Technologies)を使用して実施された。ポリマー溶液(6%w/v)を、湿度50%において23℃で、16.7μL/分の流速で0.8mm PTFE管を通過させてエミッター中に入れた。エミッターを15kV~18kVに設定し、収集ドラムを-4kVに保った。ファイバー形成が成功した後、エミッターのx軸並進ステージを、100mm/sの速度およびエッジにおける200msの遅延で、繰り返し線形パターンに設定した。並進ステージの起動後の総収集時間は、140分であった。膜(例えば電界紡糸ポリマー膜)は、パターン化された構造上に収集されることもできる。
様々な直径のPAN膜
[0157] この実施例は、走査型電子顕微鏡法および様々な直径のPAN膜(例えば電界紡糸ポリマー膜)からのタンパク質の累積放出を記載する。膜(例えば電界紡糸ポリマー膜)は、実施例1に従って製造された。PANポリマーを6%(w/v)PANポリマー溶
液で電界紡糸した。結果として得られた電界紡糸ポリマー膜中のフィラメントの直径を、ポリマー濃度および電圧を制御することによって変化させた。表1は、ポリマー溶液濃度(w/v)、正および負の電圧設定(kV)、供給速度、距離および電界紡糸の時間を含む、直径540nm、325nmおよび202nmの繊維フィラメントを有する50μm厚のポリマー膜を得るために使用される電界紡糸パラメーターを示す。
PAN電界紡糸ポリマー膜からのタンパク質放出
[0161] この実施例は、PAN電界紡糸ポリマー膜からの異なる分子量のタンパク質の放出を記載する。電界紡糸ポリマー膜を実施例1に従って製造した。PANポリマーを6%(w/v)ポリマー溶液中で電界紡糸した。放出試験を、上で実施例2において記載したように実施した。
マウスに移植された電界紡糸ポリマー膜の組織学的分析
[0163] この実施例は、マウスに移植された電界紡糸ポリマー膜の組織学的分析を記載する。PAN電界紡糸ポリマー膜を実施例1に従って製造した。PANポリマーを6%(w/v)ポリマー溶液中で溶解させ、実施例2で記載したように電界紡糸した。電界紡糸ポリマー膜を、NOD scidガンマ(NSG)マウスの精巣上体脂肪パッド中に60日間移植した。マウスを安楽死させ、電界紡糸ポリマー膜を含有する組織を剖検し、切片を作製し、ヘマトキシリンおよびエオシン(H&E)で染色した。
電界紡糸ポリマー膜の機械的強度
[0165] この実施例は、電界紡糸ポリマー膜の機械的強度を記載する。電界紡糸ポリマー膜を実施例1に従って製造した。エチレンカーボネート:PANおよびPAN:PEGの様々な配合物を、6%(w/v)ポリマー溶液中で電界紡糸した。引張特性は、所与の大きさの膜の細片を制御された方法の下で延伸することによって測定された。
架橋された機能性電界紡糸ポリマー膜の製造および試験
[0167] この実施例は、本開示の架橋された機能性電界紡糸ポリマー膜の製造および試
験を記載する。電界紡糸ポリマー膜を実施例1に従って製造した。PEGMA:PANポリマーを、6%(w/v)ポリマー溶液中で1:1~1:10の比のPEGMA:PANで電界紡糸した。SEMおよび放出試験のための膜の調製は、上記で実施例2において記載されている。別に、PAN:PEGMAポリマーを、2%TEGDAを含む6%(w/v)ポリマー溶液中で電界紡糸した。電界紡糸ポリマー膜を収集した後、膜をUV光下で照射して架橋を開始し、架橋された機能性電界紡糸ポリマー膜を得た。UV曝露を、UV架橋剤を用いて実施し、それは、上から照らすUVランプを有する密閉チャンバーである。光開始剤は、1%の濃度で存在し、UV曝露は、10分間実施される。
架橋された機能性電界紡糸ポリマー膜におけるインスリン分泌細胞送達
[0173] この実施例は、架橋された機能的電界紡糸ポリマー膜におけるインスリン分泌細胞の送達を記載する。膜(例えば電界紡糸ポリマー膜)は、実施例1に従って製造される。ベースポリマー、架橋剤および光開始剤は、適切な厚さの機能性電界紡糸ポリマー膜を得るための技術を用いて電界紡糸される。ベースポリマーは、PANおよびPEGMAを含み、架橋剤は、TEGDAを含み、光開始剤は、ジメトキシアセトフェノンを含む。ベースポリマー、架橋剤および光開始剤は、本明細書で記載されたポリマーおよび化合物のいずれであることもできる。機能性電界紡糸ポリマー膜をUV光で架橋して、架橋された機能性電界紡糸ポリマー膜を得る。細胞は、電界紡糸前のポリマー溶液中への組み込みにより架橋された機能性電界紡糸ポリマー膜中に装填され、または架橋された機能性電界紡糸ポリマー膜上にまかれる。細胞は、幹細胞、例えばインスリンを発現するように操作された幹細胞由来ベータ細胞である。
架橋された機能性電界紡糸ポリマー膜における薬物送達
[0174] この実施例は、架橋された機能性電界紡糸ポリマー膜における薬物の送達を記載する。電界紡糸ポリマー膜は、実施例1に従って製造される。ベースポリマー、架橋剤および光開始剤は、適切な厚さの機能性電界紡糸ポリマー膜を得るための技法を用いて電
界紡糸される。ベースポリマーは、PANおよびPEGMAを含み、架橋剤は、TEGDAを含み、光開始剤は、ジメトキシアセトフェノンを含む。ベースポリマー、架橋剤および光開始剤は、本明細書で記載されたポリマーおよび化合物のいずれであることもできる。機能性電界紡糸ポリマー膜をUV光で架橋して、架橋された機能性電界紡糸ポリマー膜を得る。薬物は、電界紡糸前のポリマー溶液中への組み込みにより架橋された機能性電界紡糸ポリマー膜中に装填され、または架橋された機能性電界紡糸ポリマー膜上にまかれる。薬物は、小分子、例えば疎水性薬物もしくは親水性薬物、または生物学的物質、例えばペプチドもしくはタンパク質を含む。特定の薬物は、免疫反応抑制剤または酸素生成試薬を含む。
糖尿病の処置
[0175] この実施例は、それを必要とする対象における糖尿病の処置を記載する。本開示のあらゆる架橋された機能性電界紡糸ポリマー膜は、実施例1に従って製造される。細胞または薬物を、実施例7および実施例8で記載されたように、架橋された機能的電界紡糸ポリマー膜に装填する。細胞は、インスリンを発現するように操作された幹細胞由来ベータ細胞である。薬物は、インスリンタンパク質である。これらの細胞または薬物を装填された架橋された機能性電界紡糸ポリマー膜を、それを必要とする対象中に移植する。対象は、マウス、ラット、ウサギ、非ヒト霊長類またはヒトのようなあらゆる動物である。それを必要とする対象は、病気を有する。病気は、糖尿病である。膜を移植すると、糖尿病の状態が改善される。膜は、6~36ヶ月までの間インスリンの放出によって糖尿病の状態を管理する。
平行フィラメントを有する電界紡糸ポリマー膜の製造
[0176] この実施例は、平行フィラメントを有する機能性電界紡糸ポリマーの製造を記載する。電界紡糸膜製作プロセスは、直径6cmを有する500rpmで作動する回転ドラムコレクターから5~17cm間隔を空けられた19ゲージ針を有する単一エミッターからなる環境制御電界紡糸装置(EC-CLI、IME Technologies)を使用して実施された。ポリマー溶液(6%w/v)を、湿度50%において23℃で、16.7μL/分の流速で0.8mm PTFE管を通過させてエミッター中に入れた。エミッターを15kV~18kVに設定し、収集ドラムを-4kVに保った。ファイバー形成が成功した後、エミッターのx軸並進ステージを、100mm/sの速度およびエッジにおける200msの遅延で、繰り返し線形パターンに設定した。並進ステージの起動後の総収集期間は、140分であった。電界紡糸ポリマー膜は、パターン化された構造上に収集されることもできる。
架橋された機能性電界紡糸ポリマー膜における細胞送達
[0179] この実施例は、架橋された機能性電界紡糸ポリマー膜における細胞の送達を記
載する。電界紡糸ポリマー膜は、実施例1に従って製造される。ベースポリマー、架橋剤および光開始剤は、適切な厚さの機能性電界紡糸ポリマー膜を得るための技術を用いて電界紡糸される。ベースポリマーは、PANおよびPEGMAを含み、架橋剤は、TEGDAを含み、光開始剤は、ジメトキシアセトフェノンを含む。ベースポリマー、架橋剤および光開始剤は、本明細書で記載されたポリマーおよび化合物のいずれであることもできる。機能性電界紡糸ポリマー膜をUV光で架橋して、架橋された機能性電界紡糸ポリマー膜を得る。細胞は、電界紡糸前のポリマー溶液中への組み込みにより架橋された機能性電界紡糸ポリマー膜中に装填され、または架橋された機能性電界紡糸ポリマー膜上にまかれる。細胞は、副甲状腺細胞、網膜色素上皮または心筋細胞である。
虚血性創傷の処置
[0180] この実施例は、それを必要とする対象における虚血性創傷の処置を記載する。本開示のあらゆる架橋された機能性電界紡糸ポリマー膜は、実施例1に従って製造される。細胞または薬物を、実施例7および実施例8において記載されたように、架橋された機能的電界紡糸ポリマー膜中に装填する。細胞は、虚血性創傷を処置するための適切な薬物、例えば血小板由来成長因子(PDGF)、結合組織成長因子(CTGF)、肝細胞成長因子(HGF)、幹細胞因子(SCF)、インスリン様成長因子(IGF-I)、形質転換成長因子ベータ-1(TGF-B1)等を発現するように操作される。これらの細胞または薬物を装填された架橋された機能性電界紡糸ポリマー膜は、それを必要とする対象中に移植される。対象は、マウス、ラット、ウサギ、非ヒト霊長類またはヒトのようなあらゆる動物である。それを必要とする対象は、病気を有する。病気は、虚血性創傷である。膜を移植すると、虚血性創傷状態は、改善される。
副甲状腺機能低下症の処置
[0181] この実施例は、それを必要とする対象における副甲状腺機能低下症の処置を記載する。本開示のあらゆる架橋された機能性電界紡糸ポリマー膜は、実施例1に従って製造される。細胞または薬物を、実施例7および実施例8において記載されたように、架橋された機能的電界紡糸ポリマー膜中に装填する。細胞は、副甲状腺機能低下症を処置するための適切な薬物、すなわち副甲状腺ホルモンを発現または分泌するように操作される。これらの細胞または薬物を装填された架橋された機能性電界紡糸ポリマー膜は、それを必要とする対象中に移植される。対象は、マウス、ラット、ウサギ、非ヒト霊長類またはヒトのようなあらゆる動物である。それを必要とする対象は、病気を有する。病気は、副甲状腺機能低下症である。膜を移植すると、副甲状腺機能低下症状態は、改善される。
[1]膜および非天然膵β細胞の集団を含むデバイスであって、
ここで、前記の非天然膵β細胞は、グルコース負荷に対してインビトログルコース刺激インスリン分泌(GSIS)反応を示し、
ここで、前記の膜は、約2以上の
あり、Dsecondは、第2分子量を含む第2分子に関する第2拡散係数であり、かつここで、前記の第1分子量に対する前記の第2分子量の比は、約10以上であるデバイス。
[2][1]に記載のデバイスであって、前記の非天然膵β細胞が前記のデバイス内に封入されているデバイス。
[3][1]または[2]に記載のデバイスであって、前記の非天然膵β細胞が、ソマトスタチン、グルカゴンまたは両方を発現しないデバイス。
[4][1]~[3]のいずれかに記載のデバイスであって、前記のデバイスが、対象中に移植された際にインスリンを産生し、放出するように設計されているデバイス。
[5][1]~[4]のいずれかに記載のデバイスであって、前記の非天然膵β細胞が、体積1μLあたり約104~約106細胞の範囲で前記のデバイス内に封入されているデバイス。
[6][1]~[5]のいずれかに記載のデバイスであって、前記の膜が、前記の非天然膵β細胞の通過を遮断するように設計されているデバイス。
[7]膜および細胞の集団を含むデバイスであって、
ここで、前記の細胞の集団の少なくとも1個の細胞が、第1分子量を含む第1分子を産生し、前記の細胞の集団の少なくとも1個の細胞が、第2分子量を含む第2分子を産生し、
ここで、前記のデバイスは、対象中に移植された際に、前記の第1分子を第1流動速度で放出し、前記の第2分子を第2流動速度で放出するように設計されており、
ここで、前記の第1流動速度は、前記の第2流動速度とは異なり、かつここで、前記の第2分子量に対する前記の第1分子量の比は、約1.0~約5.0であるデバイス。
[8][7]に記載のデバイスであって、前記の第1分子または前記の第2分子が療法剤を含むデバイス。
[9][7]または[8]に記載のデバイスであって、前記の第1分子が、インスリンであるデバイス。
[10][7]~[9]のいずれかに記載のデバイスであって、前記の第2分子が、グルカゴンであるデバイス。
[11][10]に記載のデバイスであって、前記の第1分子量対前記の第2分子量の前記の比が、約1.6であるデバイス。
[12][7]~[9]のいずれかに記載のデバイスであって、前記の第2分子が、ソマトスタチンであるデバイス。
[13][12]に記載のデバイスであって、前記の第1分子量対前記の第2分子量の前記の比が、約3.5であるデバイス。
[14][8]~[13]のいずれかに記載のデバイスであって、前記の療法剤が、ホルモンまたは酵素であるデバイス。
[15][14]に記載のデバイスであって、前記の療法剤が、ホルモンであるデバイス。
[16][15]に記載のデバイスであって、前記の療法剤が、アミノ酸由来ホルモン、エイコサノイド、ペプチドホルモンまたはステロイドであるデバイス。
[17][15]または[16]に記載のデバイスであって、前記の療法剤が、グルカゴン、成長ホルモン、インスリン、膵臓ポリペプチド、副甲状腺ホルモン、ソマトスタチンおよびグルココルチコイドからなる群から選択されるデバイス。
[18][14]に記載のデバイスであって、前記の療法剤が、酵素であるデバイス。
[19][18]に記載のデバイスであって、前記の療法剤が、プロテアーゼ、リパーゼ、アミラーゼ、ホスホリパーゼA2、リゾホスホリパーゼまたはコレステロールエステラーゼであるデバイス。
[20][18]または[19]に記載のデバイスであって、前記の療法剤が、アンギオテンシノーゲン、トリプシノーゲン、キモトリプシノーゲン、ペプシノーゲン、フィブリノーゲン、プロカスパーゼ、パシファスチン、プロエラスターゼ、プロリパーゼおよび
プロカルボキシポリペプチダーゼからなる群から選択されるデバイス。
[21][7]~[20]のいずれかに記載のデバイスであって、前記の細胞が、ホルモンまたは酵素分泌細胞を含むデバイス。
[22][7]~[21]のいずれかに記載のデバイスであって、前記の細胞が、非天然細胞を含むデバイス。
[23][7]~[22]のいずれかに記載のデバイスであって、前記の細胞が、幹細胞由来島細胞を含むデバイス。
[24][7]~[23]のいずれかに記載のデバイスであって、前記の細胞が、非天然膵β細胞を含むデバイス。
[25][7]~[24]のいずれかに記載のデバイスであって、前記の細胞が、グルコース負荷に対してインビトログルコース刺激インスリン分泌(GSIS)反応を示すデバイス。
[26][7]~[25]のいずれかに記載のデバイスであって、前記の細胞が、前記のデバイス内に封入されているデバイス。
[27][7]~[26]のいずれかに記載のデバイスであって、前記の細胞が、ソマトスタチン、グルカゴンまたは両方を発現しないデバイス。
[28][7]~[27]のいずれかに記載のデバイスであって、前記のデバイスが、前記の対象中に移植された際にインスリンを産生し、放出するように設計されているデバイス。
[29][7]~[28]のいずれかに記載のデバイスであって、前記の細胞が、体積1μLあたり約104~約106細胞の範囲で前記のデバイス内に封入されているデバイス。
[30][7]~[29]のいずれかに記載のデバイスであって、前記の膜が、前記の細胞の通過を遮断するように設計されているデバイス。
[31]膜および療法剤を含むデバイスであって、
ここで、前記の非天然膵β細胞は、前記のデバイス内に封入されており、
ここで、前記の膜は、約2以上の
[32][31]に記載のデバイスであって、前記の療法剤が、プロドラッグであるデバイス。
[33][31]または[32]に記載のデバイスであって、前記の療法剤が、10kDa未満であるデバイス。
[34][31]~[33]のいずれかに記載のデバイスであって、前記の療法剤が、小分子であるデバイス。
[35][31]~[33]のいずれかに記載のデバイスであって、前記の療法剤が、生物学的物質であるデバイス。
[36][35]に記載のデバイスであって、前記の生物学的物質が、ペプチドまたはタンパク質であるデバイス。
[37][31]~[36]のいずれかに記載のデバイスであって、前記の療法剤が、ホルモンまたは酵素であるデバイス。
[38][37]に記載のデバイスであって、前記の療法剤が、ホルモンであるデバイス。
[39][38]に記載のデバイスであって、前記の療法剤が、アミノ酸由来ホルモン
、エイコサノイド、ペプチドホルモンまたはステロイドであるデバイス。
[40][38]または[39]に記載のデバイスであって、前記の療法剤が、グルカゴン、成長ホルモン、インスリン、膵臓ポリペプチド、副甲状腺ホルモン、ソマトスタチンおよびグルココルチコイドからなる群から選択されるデバイス。
[41][37]に記載のデバイスであって、前記の療法剤が、酵素であるデバイス。
[42][41]に記載のデバイスであって、前記の療法剤が、プロテアーゼ、リパーゼ、アミラーゼ、ホスホリパーゼA2、リゾホスホリパーゼまたはコレステロールエステラーゼであるデバイス。
[43][41]または[42]に記載のデバイスであって、前記の療法剤が、アンギオテンシノーゲン、トリプシノーゲン、キモトリプシノーゲン、ペプシノーゲン、フィブリノーゲン、プロカスパーゼ、パシファスチン、プロエラスターゼ、プロリパーゼおよびプロカルボキシポリペプチダーゼからなる群から選択されるデバイス。
[44][31]~[43]のいずれかに記載のデバイスであって、前記の療法剤が、約0.01mg療法剤/mgポリマー~約0.5mg療法剤/mgポリマーの範囲で存在するデバイス。
[45][31]~[44]のいずれかに記載のデバイスであって、前記の療法剤が、少なくとも3日間前記の膜から放出されるように設計されているデバイス。
[46][31]~[45]のいずれかに記載のデバイスであって、前記の療法剤が、疎水性であるデバイス。
[47][31]~[45]のいずれかに記載のデバイスであって、前記の療法剤が、親水性であるデバイス。
[48][31]~[47]のいずれかに記載のデバイスであって、前記の療法剤が、微細化された微粒子の形態であるデバイス。
[49]膜を含むデバイスであって、
ここで、前記の膜が、細胞の集団または療法剤の前記の膜への封入を可能にするように設計されたポリマーを含み、
ここで、前記の膜が、以下:
a)約1000nm以下の平均繊維径;
b)約5μm以下の平均孔径;
c)約500μm以下の平均厚さ;
の少なくとも1つを含み、かつここで、前記の膜が、約2以上の
[50][49]に記載のデバイスであって、前記のポリマーが、前記の細胞の集団の封入を可能にするように設計されているデバイス。
[51][49]~[50]のいずれかに記載のデバイスであって、前記の細胞が、ホルモンまたは酵素分泌細胞を含むデバイス。
[52][49]~[51]のいずれかに記載のデバイスであって、前記の細胞が、療法剤を分泌するデバイス。
[53][52]に記載のデバイスであって、前記の療法剤が、ホルモンであるデバイス。
[54][53]に記載のデバイスであって、前記の療法剤が、アミノ酸由来ホルモン、エイコサノイド、ペプチドホルモンまたはステロイドであるデバイス。
[55][53]または[54]に記載のデバイスであって、前記の療法剤が、グルカ
ゴン、成長ホルモン、インスリン、膵臓ポリペプチド、副甲状腺ホルモン、ソマトスタチンおよびグルココルチコイドからなる群から選択されるデバイス。
[56][52]に記載のデバイスであって、前記の療法剤が、酵素であるデバイス。
[57][56]に記載のデバイスであって、前記の療法剤が、プロテアーゼ、リパーゼ、アミラーゼ、ホスホリパーゼA2、リゾホスホリパーゼまたはコレステロールエステラーゼであるデバイス。
[58][56]または[57]に記載のデバイスであって、前記の療法剤が、アンギオテンシノーゲン、トリプシノーゲン、キモトリプシノーゲン、ペプシノーゲン、フィブリノーゲン、プロカスパーゼ、パシファスチン、プロエラスターゼ、プロリパーゼおよびプロカルボキシポリペプチダーゼからなる群から選択されるデバイス。
[59][49]~[58]のいずれかに記載のデバイスであって、前記の細胞が、非天然細胞を含むデバイス。
[60][49]~[59]のいずれかに記載のデバイスであって、前記の細胞が、幹細胞由来島細胞を含むデバイス。
[61][49]~[60]のいずれかに記載のデバイスであって、前記の細胞が、非天然膵β細胞を含むデバイス。
[62][49]~[61]のいずれかに記載のデバイスであって、前記の細胞が、グルコース負荷に対してインビトログルコース刺激インスリン分泌(GSIS)反応を示すデバイス。
[63][49]~[62]のいずれかに記載のデバイスであって、前記の細胞が、前記のデバイス内に封入されているデバイス。
[64][49]~[63]のいずれかに記載のデバイスであって、前記の細胞が、ソマトスタチン、グルカゴンまたは両方を発現しないデバイス。
[65][49]~[64]のいずれかに記載のデバイスであって、前記のデバイスが、前記の対象中に移植された際にインスリンを産生し、放出するように設計されているデバイス。
[66][49]~[65]のいずれかに記載のデバイスであって、前記の細胞が、体積1μLあたり約104~約106細胞の範囲で前記のデバイス内に封入されているデバイス。
[67][49]~[66]のいずれかに記載のデバイスであって、前記の膜が、前記の細胞の通過を遮断するように設計されているデバイス。
[68][49]~[67]のいずれかに記載のデバイスであって、前記のポリマーが、前記の療法剤の封入を可能にするように設計されているデバイス。
[69][68]に記載のデバイスであって、前記の療法剤が、プロドラッグであるデバイス。
[70][68]または[69]に記載のデバイスであって、前記の療法剤が、10kDa未満であるデバイス。
[71][68]~[70]のいずれかに記載のデバイスであって、前記の療法剤が、小分子であるデバイス。
[72][68]~[70]のいずれかに記載のデバイスであって、前記の療法剤が、生物学的物質であるデバイス。
[73][72]に記載のデバイスであって、前記の生物学的物質が、ペプチドまたはタンパク質であるデバイス。
[74][72]~[73]のいずれかに記載のデバイスであって、前記の療法剤が、ホルモンまたは酵素であるデバイス。
[75][74]に記載のデバイスであって、前記の療法剤が、ホルモンであるデバイス。
[76][75]に記載のデバイスであって、前記の療法剤が、アミノ酸由来ホルモン、エイコサノイド、ペプチドホルモンまたはステロイドであるデバイス。
[77][75]または[76]に記載のデバイスであって、前記の療法剤が、グルカ
ゴン、成長ホルモン、インスリン、膵臓ポリペプチド、副甲状腺ホルモン、ソマトスタチンおよびグルココルチコイドからなる群から選択されるデバイス。
[78][74]に記載のデバイスであって、前記の療法剤が、酵素であるデバイス。
[79][78]に記載のデバイスであって、前記の療法剤が、プロテアーゼ、リパーゼ、アミラーゼ、ホスホリパーゼA2、リゾホスホリパーゼまたはコレステロールエステラーゼであるデバイス。
[80][78]または[79]に記載のデバイスであって、前記の療法剤が、アンギオテンシノーゲン、トリプシノーゲン、キモトリプシノーゲン、ペプシノーゲン、フィブリノーゲン、プロカスパーゼ、パシファスチン、プロエラスターゼ、プロリパーゼおよびプロカルボキシポリペプチダーゼからなる群から選択されるデバイス。
[81][68]~[80]のいずれかに記載のデバイスであって、前記の療法剤が、約0.01mg療法剤/mgポリマー~約0.5mg療法剤/mgポリマーの範囲で存在するデバイス。
[82][68]~[81]のいずれかに記載のデバイスであって、前記の療法剤が、少なくとも3日間前記の膜から放出されるように設計されているデバイス。
[83][68]~[82]のいずれかに記載のデバイスであって、前記の療法剤が、疎水性であるデバイス。
[84][68]~[82]のいずれかに記載のデバイスであって、前記の療法剤が、親水性であるデバイス。
[85][68]~[84]のいずれかに記載のデバイスであって、前記の療法剤が、微細化された微粒子の形態であるデバイス。
[86][1]~[85]のいずれかに記載のデバイスであって、前記の膜が、約1000nm以下の平均繊維径を含むデバイス。
[87][86]に記載のデバイスであって、前記の平均繊維径が、約800nm以下であるデバイス。
[88][87]に記載のデバイスであって、前記の平均繊維径が、約500nm以下であるデバイス。
[89][1]~[88]のいずれかに記載のデバイスであって、前記の膜が、約5μm以下の平均孔径を含むデバイス。
[90][89]に記載のデバイスであって、前記の平均孔径が、約2μm以下であるデバイス。
[91][90]に記載のデバイスであって、前記の平均孔径が、約1μm以下であるデバイス。
[92][1]~[91]のいずれかに記載のデバイスであって、前記の膜が、約800μm以下の平均厚さを含むデバイス。
[93][92]に記載のデバイスであって、前記の平均厚さが、約500μm以下であるデバイス。
[94][93]に記載のデバイスであって、前記の平均厚さが、約200μm以下であるデバイス。
[95][1]~[94]のいずれかに記載のデバイスであって、前記の第1分子量が、約10kDa未満であり、前記の第2分子量が、約100kDaより大きいデバイス。
[96][95]に記載のデバイスであって、前記の第1分子量が、約4kDaであり、前記の第2分子量が、約150kDaであるデバイス。
[97][1]~[6]および[31]~[96]のいずれかに記載のデバイスであって、前記の第1分子が、4kDaのFITC-デキストラン分子であり、前記の第2分子が、500kDaのFITC-デキストラン分子であるデバイス。
[98][1]~[97]のいずれかに記載のデバイスであって、前記の膜が、電界紡糸ポリマー膜であるデバイス。
[99][1]~[98]のいずれかに記載のデバイスであって、前記の膜が、さらにベースポリマーを含むデバイス。
[100][99]に記載のデバイスであって、前記のベースポリマーが、PAN、PET、PLG、PHEMA、PCLまたはPLLAを含むデバイス。
[101][100]に記載のデバイスであって、前記のベースポリマーが、PANであるデバイス。
[102][1]~[101]のいずれかに記載のデバイスであって、前記の膜が、さらに機能性ポリマーを含むデバイス。
[103][102]に記載のデバイスであって、前記の機能性ポリマーが、PEG、PEGMA、PEGDAまたはTEGDAを含むデバイス。
[104][103]に記載のデバイスであって、前記の機能性ポリマーが、PEGMAであるデバイス。
[105][103]に記載のデバイスであって、前記の機能性ポリマーが、TEGDAであるデバイス。
[106][102]~[105]のいずれかに記載のデバイスであって、前記の機能性ポリマーが、反応性官能基を含むデバイス。
[107][106]に記載のデバイスであって、前記の反応性官能基が、カルボキシレート基、ヒドロキシル基、アミド基、アジド基またはマレイミド基であるデバイス。
[108][102]~[107]のいずれかに記載のデバイスであって、前記の機能性ポリマーが、約400~4000Daの範囲内の分子量を含むデバイス。
[109][102]~[107]のいずれかに記載のデバイスであって、前記の機能性ポリマーが、約480Daの分子量を含むデバイス。
[110][102]~[107]のいずれかに記載のデバイスであって、前記の機能性ポリマーが、約1500~2500Daの範囲内の分子量を含むデバイス。
[111][102]~[107]のいずれかに記載のデバイスであって、前記の機能性ポリマーが、約2000Daの分子量を含むデバイス。
[112][1]~[111]のいずれかに記載のデバイスであって、前記の比が、約3以上であるデバイス。
[113][1]~[112]のいずれかに記載のデバイスであって、前記の比が、約5以上であるデバイス。
[114][1]~[113]のいずれかに記載のデバイスであって、前記の比が、約10以上であるデバイス。
[115][1]~[114]のいずれかに記載のデバイスであって、前記の膜が、約1MPa以上の引張強度を含むデバイス。
[116][1]~[115]のいずれかに記載のデバイスであって、前記の膜が、約5MPa以上のヤング率を含むデバイス。
[117][1]~[116]のいずれかに記載のデバイスであって、前記の膜が、親水性であるデバイス。
[118][1]~[116]のいずれかに記載のデバイスであって、前記の膜が、疎水性であるデバイス。
[119]病気を処置するための方法であって、以下の工程:
[1]~[118]のいずれかに記載の前記のデバイスを、それを必要とする対象中に配置する;
を含む方法。
[120][119]に記載の方法であって、前記のデバイスが、6ヶ月より長い期間の間前記の対象中に留まるように設計されている方法。
[121][119]または[120]に記載の方法であって、前記の病気が、慢性疾患である方法。
[122][121]に記載の方法であって、前記の慢性疾患が、糖尿病である方法。
[123][119]~[122]のいずれかに記載の方法であって、前記の方法が、さらに6ヶ月より長い前記の期間にわたって前記の対象のインスリンレベルをモニターすることを含む方法。
[124]細胞または療法剤の集団をそれを必要とする対象に送達するためのデバイスを作製する方法であって、以下の工程:
ポリマーを溶媒中で溶解させてポリマー溶液を提供し;
前記のポリマー溶液を用いて繊維を含む膜を形成し;そして
前記の膜を前記のデバイスへと組み立てる;
を含み、ここで、前記のデバイスが、[1]~[118]のいずれかに記載のデバイスである方法。
[125][124]に記載の方法であって、さらに前記の膜を架橋することを含む方法。
[126][125]に記載の方法であって、前記の膜の架橋が、前記の膜を光開始剤の存在下で紫外線(UV)光に曝露させることを含む方法。
[127][126]に記載の方法であって、前記の光開始剤が、アセトフェノン、アニソイン、アントラキノン、ベンジル、ベンゾイン、ベンゼントリカルボニルクロム、ベンゾインエチルエーテル、ベンゾインイソブチルエーテル、ベンゾインメチルエーテル、ベンゾフェノン、3,3’,4,4’-ベンゾフェノンテトラカルボン酸二無水物、4-ベンゾイルビフェニル、2-ベンジル-2-(ジメチルアミノ)-4’-モルホリノブチロフェノン、4,4’-ビス(ジエチルアミノ)ベンゾフェノン、カンファーキノン、2-クロロチオキサンテン-9-オン、(クメン)シクロペンタジエニル鉄(II)ヘキサフルオロホスフェート、ジベンゾスベレノン、2,2-ジエトキシアセトフェノン、4,4’-ジヒドロキシベンゾフェノン、2,2-ジメトキシ-2-フェニルアセトフェノン、4-(ジメチルアミノ)ベンゾフェノン、4,4’-ジメチルベンジル、2,5-ジメチルベンゾフェノン(2,5-dimethylbenzonphenone)、3,4-ジメチルベンゾフェノン、ジフェニル(2,4,6-トリメチルベンゾイル)ホスフィンオキシド、4’-エトキシアセトフェノン、2-エチルアントラキノン、フェロセン、3-ヒドロキシアセトフェノン、4-ヒドロキシアセトフェノン、1-ヒドロキシシクロヘキシルフェニルケトン、2-ヒドロキシ-2-メチルプロピオフェノン、2-メチルベンゾフェノン、3-メチルベンゾフェノン、メチルベンゾイルホルメート、2-メチル-4’-(メチルチオ)-2-モルホリノプロピオフェノン(2-methyl-4’-(methylthio)-2-morpholinoproiophenone)、フェナントレンキノン、4’-フェノキシアセトフェノン、チオキサンテン-9-オン、トリアリールスルホニウム、ヘキサフルオロアンチモネート塩類、トリアリールスルホニウムヘキサフルオロホスフェート塩類またはそれらのあらゆる組み合わせを含む方法。
[128][125]~[127]のいずれかに記載の方法であって、前記の膜の架橋が、前記の膜を熱開始剤の存在下で熱に曝露させることを含む方法。
[129][128]に記載の方法であって、前記の熱開始剤が、過硫酸アンモニア、tert-アミルペルオキシベンゾエート、4,4-アゾビス(4-シアノ吉草酸)、1,1’-アゾビス(シクロヘキサンカルボニトリル)、2,2’-アゾビスイソブチロニトリル(2,2’-azobissobutyronitrile)、過酸化ベンゾイル、2,2’-ビス(tert-ブチルペルオキシ)ブタン、1,1-ビス(tert-ブチルペルオキシ)シクロヘキサン、2,5-ビス(tert-ブチルペルオキシ)-2,5-ジメチルヘキサン、2,5-ビス(tert-ブチルペルオキシ)-2,5-ジメチル-3-ヘキシン、ビス(1-(tert-ブチルペルオキシ)-1-メチルエチル)ベンゼン、1,1-ビス(tert-ブチルペルオキシ)-3,3,5-トリメチルシクロヘキサン、tert-ブチルヒドロペルオキシド、過酢酸tert-ブチル、tert-ブチルペルオキシド、tert-ブチルペルオキシベンゾエート、tert-ブチルペルオキシイソプロピルカーボネート、クメン、ヒドロペルオキシド、シクロヘキサノンペルオキシド、ジクミルペルオキシド、ラウロイルペルオキシド、2,4-ペンタンジオンペルオキシド、過酢酸、過硫酸カリウムまたはそれらのあらゆる組み合わせを含む方法。
[130][125]~[129]のいずれかに記載の方法であって、前記の膜の架橋が、前記の膜を遷移金属に曝露させることを含む方法。
[131][130]に記載の方法であって、前記の遷移金属が、ベリリウム、マグネシウム、カルシウム、バリウム、マンガン、銅、鉄またはそれらのあらゆる組み合わせのイオンを含む方法。
[132][125]~[131]のいずれかに記載の方法であって、前記の膜の架橋が、さらに前記の膜を架橋剤に曝露させることを含む方法。
[133][132]に記載の方法であって、テトラ(エチレングリコール)ジアクリレート、ポリエチレングリコールジアクリレート(polyethylene glycol diacralte)、ビス(2-(スクシンイミジル-オキシカルボニルオキシル)エチル)スルホン、ジ(n-スクシンイミジル)グルタレート、ジスクシンイミジルタルタレート、3,3’-ジチオビス(スルホスクシンイミジル)プロピオネート、p-フェニレンジイソチオシアネート、セバシン酸ビス(N-スクシンイミジル)エステル、スベリン酸ビス(N-ヒドロキシスクシンイミドエステル)、APN-CHO、ブロモ酢酸N-ヒドロキシスクシンイミドエステル、CBTF、ヨード酢酸N-ヒドロキシスクシンイミドエステル、マレイミド-PEG-スクシンイミジルエステル、マレイミド酢酸N-ヒドロキシスクシンイミドエステル、アジピン酸ジヒドラジド、アルキン-PEG-マレイミド、APN-アミン、APN-アジド、APN-BCN、APN-COCl、ビオチン-ベンジル-テトラジン、ビオチン-PEG-TPG、1,11-ジアジド-3,6,9-トリオキサウンデカン、ジベンゾシクロオクチン-N-ヒドロキシスクシンイミジルエステル、ジベンゾシクロオクチン-マレイミド、ジベンゾシクロオクチン-PEG-マレイミド、4-(マレインイミド)フェニルイソシアネート(およそ95%純粋)、4,4’-メチレンビス(フェニルイソシアネート)、3-(2-ピリジルジチオ)プロピオニルヒドラジド、プロパルギル-N-ヒドロキシルスクシンイミジルエステル、PTAD-アジド、スルホ-NHS-ジアジリン、スルホスクシンイミジル4,4’-アジペンタノエート、4-(N-マレイミド)ベンゾフェノン、4-アジドフェナシルブロミド、5-アジド-2-ニトロ安息香酸N-ヒドロキシスクシンイミドエステル(5-azido-2-nitriobenzoic acid N-hydroxy succinimide ester)、スクシンイミジル-[4-(ソラレン-8-イルオキシ)]ブチレート、4-ベンゾイル安息香酸N-スクシンイミジルエステル、1,4-ビス[3-(2-ピリジルジチオ)プロピオンアミド]ブタン、ビス-マレイミドエタン、ジチオ-ビス-マレイミドエタンまたはそれらのあらゆる組合せを含む方法。
[134][124]~[133]のいずれかに記載の方法であって、さらに薬物を前記のポリマー溶液に添加することを含む方法。
[135][124]~[134]のいずれかに記載の方法であって、前記の溶媒が、混和性溶媒である方法。
[136][134]~[135]のいずれかに記載の方法であって、前記の薬物が、疎水性薬物である方法。
[137][134]~[135]のいずれかに記載の方法であって、前記の薬物が、親水性薬物である方法。
[138][134]~[137]のいずれかに記載の方法であって、前記の薬物が、微細化された微粒子の形態である方法。
[139][124]~[138]のいずれかに記載の方法であって、さらに前記のデバイス内に細胞を封入することを含む方法。
[140][124]~[139]のいずれかに記載の方法であって、前記の細胞が、非天然細胞である方法。
[141][124]~[140]のいずれかに記載の方法であって、前記の細胞が、幹細胞由来島細胞である方法。
[142][124]~[141]のいずれかに記載の方法であって、前記の細胞が、グルコース負荷に対してインビトログルコース刺激インスリン分泌(GSIS)反応を示す方法。
[143][124]~[142]のいずれかに記載の方法であって、さらに回転ドラ
ムコレクターを用いて前記の繊維を収集することを含む方法。
[144][124]~[143]のいずれかに記載の方法であって、さらに前記の繊維をパターン化された構造上に収集することを含む方法。
[145][144]に記載の方法であって、前記の膜が、前記のパターン化された構造の形状を含む方法。
[146][124]~[145]のいずれかに記載の方法であって、前記の溶媒が、DMF、アセトン、アセトニトリル、アニリン、酢酸n-ブチル、シクロヘキサノン、クロロホルム、ジアセトンアルコール、ジ(エチレングリコール)、ジメチルスルホキシド、ジクロロメタン、エタノール、酢酸エチル、二塩化エチレン、ギ酸、グリセロール、メタノール、酢酸メチル、モルホリン、2-ニトロプロパン、1-ペンタノール、n-プロパノール、ピリジン、トリフロロエタノール、テトラヒドロフラン、水またはそれらのあらゆる組み合わせを含む方法。
[147][124]~[146]のいずれかに記載の方法であって、前記のポリマーの前記の溶媒中での溶解が、ベースポリマーおよび機能性ポリマーを前記の溶媒中で溶解させることを含む方法。
[148][147]に記載の方法であって、前記のベースポリマーおよび前記の機能性ポリマーを約1:1(w/w)以下の比で前記の溶媒中で溶解させることを含む方法。
[149][148]に記載の方法であって、前記のベースポリマーおよび前記の機能性ポリマーを約1:5(w/w)以下の比で前記の溶媒中で溶解させることを含む方法。
[150][149]に記載の方法であって、前記のベースポリマーおよび前記の機能性ポリマーを約1:10(w/w)以下の比で前記の溶媒中で溶解させることを含む方法。
[151][150]に記載の方法であって、前記のベースポリマーおよび前記の機能性ポリマーを約1:20(w/w)以下の比で前記の溶媒中で溶解させることを含む方法。
[152][147]~[151]のいずれかに記載の方法であって、前記のベースポリマーおよび前記の機能性ポリマーが、約6重量%対体積パーセントで前記の溶媒と共に存在する方法。
[153][124]~[152]のいずれかに記載の方法であって、前記の膜が、コーティングを含まない方法。
Claims (15)
- 植え込み式デバイスを含む、糖尿病の処置において使用するための組成物であって、デバイスが:
1μm以下の平均孔径を有し、10μm~150μmの平均厚さを有し、1MPa以上の引張強度を有する多孔性ポリマー膜;および
膵前駆細胞、内分泌細胞、アルファ細胞、デルタ細胞、およびベータ細胞の群から選択される少なくとも1つを含む細胞集団;
を含み、
ここで、前記の膜は、2以上50以下のDfirst/Dsecondの比を示すように設計されており、ここで、Dfirstは、第1分子量を含む第1分子に関する第1拡散係数であり、第1分子量は50Da以上10kDa以下であり、Dsecondは、第2分子量を含む第2分子に関する第2拡散係数であり、第2分子量は50kDa以上500kDa以下であり、かつここで、前記の第1分子量に対する前記の第2分子量の比は、10以上である組成物。 - 前記膜が細胞集団を封入するように設計されている、請求項1に記載の組成物。
- 前記細胞集団が、1μLあたり104~106細胞の量で前記デバイス内に封入されている、請求項1または2に記載の組成物。
- 前記デバイスが対象中に移植された際にインスリンを産生し、放出するように設計されている請求項1~3のいずれか1項に記載の組成物。
- 前記の第1分子が、4kDaのFITC-デキストランであり、前記の第2分子が、500kDaのFITC-デキストランである、請求項1~4のいずれか1項に記載の組成物。
- 前記の第1分子が、4kDaのFITC-デキストランであり、前記の第2分子が、ペプシノーゲン、リパーゼ、プロリパーゼ、アンギオテンシノーゲン、アミラーゼ、またはコレステロールエステラーゼである、請求項1~4のいずれか1項に記載の組成物。
- 前記の膜が、1000nm以下の平均繊維径を有する、請求項1~6のいずれか1項に記載の組成物。
- 前記の膜が電界紡糸ポリマー膜である、請求項1~7のいずれか1項に記載の組成物。
- 前記の膜が、400Da以上1,500,000Da以下の分子量を有する機能性ポリマーを含む、請求項1~8のいずれか1項に記載の組成物。
- Dfirstが10-7cm2/秒以上である、請求項1~9のいずれか1項に記載の組成物。
- 前記の細胞が非天然ベータ細胞を含む、請求項1~10のいずれか1項に記載の組成物。
- 前記非天然ベータ細胞がグルコース負荷に対してインビトログルコース刺激インスリン分泌(GSIS)反応を示す、請求項11に記載の組成物。
- 前記膜が、ポリアクリロニトリル(PAN)、ポリスルホン(PSf)、ポリテトラフルオロエチレン(PTFE)、ポリウレタン(PU)、ポリフッ化ビニリデン(PVDF)、またはそれらの任意の組み合わせを含む、請求項1~12のいずれか1項に記載の組成物。
- 前記膜が60MPa以上のヤング率を有する、請求項1~13のいずれか1項に記載の組成物。
- 前記細胞集団がヒト細胞由来である、請求項1~14のいずれか1項に記載の組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024103857A JP2024123255A (ja) | 2017-06-14 | 2024-06-27 | 療法薬を送達するためのデバイスおよび方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762519702P | 2017-06-14 | 2017-06-14 | |
| US62/519,702 | 2017-06-14 | ||
| JP2020519004A JP7284948B2 (ja) | 2017-06-14 | 2018-06-14 | 療法薬を送達するためのデバイスおよび方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020519004A Division JP7284948B2 (ja) | 2017-06-14 | 2018-06-14 | 療法薬を送達するためのデバイスおよび方法 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024103857A Division JP2024123255A (ja) | 2017-06-14 | 2024-06-27 | 療法薬を送達するためのデバイスおよび方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023100847A JP2023100847A (ja) | 2023-07-19 |
| JP7513799B2 true JP7513799B2 (ja) | 2024-07-09 |
Family
ID=64660493
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020519004A Active JP7284948B2 (ja) | 2017-06-14 | 2018-06-14 | 療法薬を送達するためのデバイスおよび方法 |
| JP2023076521A Active JP7513799B2 (ja) | 2017-06-14 | 2023-05-08 | 療法薬を送達するためのデバイスおよび方法 |
| JP2024103857A Pending JP2024123255A (ja) | 2017-06-14 | 2024-06-27 | 療法薬を送達するためのデバイスおよび方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020519004A Active JP7284948B2 (ja) | 2017-06-14 | 2018-06-14 | 療法薬を送達するためのデバイスおよび方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024103857A Pending JP2024123255A (ja) | 2017-06-14 | 2024-06-27 | 療法薬を送達するためのデバイスおよび方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US11471398B2 (ja) |
| EP (1) | EP3638205A4 (ja) |
| JP (3) | JP7284948B2 (ja) |
| CN (1) | CN111565707A (ja) |
| AU (2) | AU2018285539B2 (ja) |
| CA (1) | CA3066055A1 (ja) |
| IL (3) | IL313825B2 (ja) |
| WO (1) | WO2018232180A1 (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2018285539B2 (en) | 2017-06-14 | 2024-10-31 | Vertex Pharmaceuticals Incorporated | Devices and methods for delivering therapeutics |
| CN111491617B (zh) | 2017-09-29 | 2024-12-31 | 沃泰克斯药物股份有限公司 | 细胞容纳装置 |
| CN112004523A (zh) | 2018-03-13 | 2020-11-27 | 沃泰克斯药物股份有限公司 | 植入装置、系统和方法 |
| US12194159B2 (en) | 2018-10-01 | 2025-01-14 | The Electrospinning Company Ltd | Multilayer porous membrane |
| CN113710198B (zh) | 2019-04-03 | 2024-11-15 | 沃泰克斯药物股份有限公司 | 大胶囊装置 |
| US20230310712A1 (en) | 2020-03-18 | 2023-10-05 | Takeda Pharmaceutical Company Limited | Implantable cell chamber device and uses thereof |
| US20230404765A1 (en) * | 2020-12-07 | 2023-12-21 | University Of Connecticut | A system and method for osteoarthritis treatment |
| EP4419676A1 (en) | 2021-10-21 | 2024-08-28 | Vertex Pharmaceuticals Incorporated | Hypoimmune cells |
| AU2022377078A1 (en) | 2021-11-01 | 2024-04-04 | Vertex Pharmaceuticals Incorporated | Stem cell derived pancreatic islet differentiation |
| WO2025024244A1 (en) | 2023-07-21 | 2025-01-30 | Vertex Pharmaceutials Incorporated | Macroencapsulation device implantation and transport system and methods |
| WO2025064982A1 (en) * | 2023-09-21 | 2025-03-27 | Northwestern University | Platform of hybrid advanced molecular manufacturing regulator and applications thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100150984A1 (en) | 2007-03-09 | 2010-06-17 | The University Of Akron | Bio-artificial pancreas and a procedure for preparation of same |
| JP2012520107A (ja) | 2009-03-11 | 2012-09-06 | ザ・ユニヴァーシティ・オヴ・シェフィールド | スカフォールド |
| WO2016052504A1 (ja) | 2014-09-30 | 2016-04-07 | 富士フイルム株式会社 | 組成物、細胞構造体、膵島移植キット、膵島細胞移植治療剤及び血糖低下剤、膵島を含む組成物、膵島を含むキット、並びに膵島移植治療剤及び血糖低下剤 |
Family Cites Families (90)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US670317A (en) | 1900-10-13 | 1901-03-19 | Eugene Friedlaender | Tongs-actuating apparatus. |
| US798204A (en) | 1903-05-04 | 1905-08-29 | Forest City Knitting Mills | Stocking-pressing machine. |
| US2984599A (en) | 1956-06-29 | 1961-05-16 | George D Edwards | Process for bonding teflon sheet to prepared surfaces |
| US4980060A (en) | 1987-07-13 | 1990-12-25 | Asahi Kasei Kogyo Kabushiki Kaisha | Hollow fiber membranes with fusion-bonded end portions |
| US5320512A (en) | 1992-09-24 | 1994-06-14 | E. I. Du Pont De Nemours And Company | Apparatus for spinning multicomponent hollow fibers |
| US6703017B1 (en) * | 1994-04-28 | 2004-03-09 | Ixion Biotechnology, Inc. | Reversal of insulin-dependent diabetes by islet-producing stem cells, islet progenitor cells and islet-like structures |
| WO1996032076A1 (en) | 1995-04-11 | 1996-10-17 | Baxter Internatonal Inc. | Tissue implant systems |
| IE77523B1 (en) | 1995-09-11 | 1997-12-17 | Elan Med Tech | Medicament delivery device |
| US5997900A (en) * | 1996-04-17 | 1999-12-07 | Wang; Taylor G. | Encapsulation system for the immunoisolation of living cells |
| US6051428A (en) | 1997-03-21 | 2000-04-18 | Sloan-Kettering Institute For Cancer Research | Rapid production of autologous tumor vaccines |
| US7615373B2 (en) * | 1999-02-25 | 2009-11-10 | Virginia Commonwealth University Intellectual Property Foundation | Electroprocessed collagen and tissue engineering |
| US6365385B1 (en) | 1999-03-22 | 2002-04-02 | Duke University | Methods of culturing and encapsulating pancreatic islet cells |
| US20050265977A1 (en) | 1999-04-30 | 2005-12-01 | Elliott Robert B | Xenotransplant for CNS therapy |
| WO2003016075A1 (en) | 2001-08-15 | 2003-02-27 | Florida State University | Method of manufacturing and design of microreactors, including microanalytical and separation devices |
| GB2399823B (en) | 2001-12-07 | 2006-02-15 | Geron Corp | Islet cells from primate pluripotent stem cells |
| US20040029941A1 (en) | 2002-05-06 | 2004-02-12 | Jennings Julianne E. | Zonisamide use in obesity and eating disorders |
| JP2004043749A (ja) * | 2002-07-12 | 2004-02-12 | Mebiol Kk | ハイドロゲル、ゲル体および物質の拡散制御方法 |
| US7407703B2 (en) | 2002-09-20 | 2008-08-05 | Bha Group, Inc. | Composite membrane having oleophobic properties |
| US8647873B2 (en) | 2004-04-27 | 2014-02-11 | Viacyte, Inc. | PDX1 expressing endoderm |
| KR101221302B1 (ko) | 2003-12-23 | 2013-01-11 | 비아싸이트, 인크. | 완전 내배엽 |
| US8586357B2 (en) | 2003-12-23 | 2013-11-19 | Viacyte, Inc. | Markers of definitive endoderm |
| US7625753B2 (en) | 2003-12-23 | 2009-12-01 | Cythera, Inc. | Expansion of definitive endoderm cells |
| US7985585B2 (en) | 2004-07-09 | 2011-07-26 | Viacyte, Inc. | Preprimitive streak and mesendoderm cells |
| US20050266554A1 (en) | 2004-04-27 | 2005-12-01 | D Amour Kevin A | PDX1 expressing endoderm |
| US7541185B2 (en) | 2003-12-23 | 2009-06-02 | Cythera, Inc. | Methods for identifying factors for differentiating definitive endoderm |
| EP2377922B1 (en) | 2004-04-27 | 2020-04-08 | Viacyte, Inc. | PDX1 expressing endoderm |
| WO2006016999A1 (en) | 2004-07-09 | 2006-02-16 | Cythera, Inc. | Methods for identifying factors for differentiating definitive endoderm |
| EP1791952A4 (en) | 2004-08-13 | 2008-06-11 | Univ Georgia Res Found | COMPOSITIONS AND METHODS OF SELF-RENEWAL AND DIFFERENTIATION IN HUMAN EMBRYONAL STEM CELLS |
| US20060167468A1 (en) | 2004-11-12 | 2006-07-27 | Shlomo Gabbay | Implantation system and method for loading an implanter with a prosthesis |
| NZ536009A (en) | 2005-04-18 | 2007-01-26 | Neurotrophincell Pty Ltd | Choroid plexus preparation and uses thereof |
| WO2007046719A2 (en) | 2005-10-21 | 2007-04-26 | Living Cell Products Pty Limited | Encapsulation system |
| DK2674485T3 (da) | 2005-10-27 | 2019-08-26 | Viacyte Inc | Pdx-1 udtrykkende dorsal og ventral fortarm endoderm |
| US7704230B2 (en) | 2005-12-29 | 2010-04-27 | Ethicon, Inc. | Pressurized fluid reservoir for an infusion system |
| KR20080109775A (ko) | 2006-02-23 | 2008-12-17 | 노보셀, 인크 | 분화가능한 세포를 배양하는데 유용한 조성물 및 방법 |
| US7695965B2 (en) | 2006-03-02 | 2010-04-13 | Cythera, Inc. | Methods of producing pancreatic hormones |
| EP1999253B1 (en) | 2006-03-02 | 2019-05-22 | Viacyte, Inc. | Endocrine precursor cells, pancreatic hormone-expressing cells and methods of production |
| US7989204B2 (en) | 2006-04-28 | 2011-08-02 | Viacyte, Inc. | Hepatocyte lineage cells |
| US9175254B2 (en) * | 2006-07-07 | 2015-11-03 | University Of Miami | Enhanced oxygen cell culture platforms |
| WO2008011518A2 (en) * | 2006-07-19 | 2008-01-24 | Diakine Therapeutics, Inc. | Encapsulation system |
| EP2056759B1 (en) | 2006-08-29 | 2015-01-14 | The University of Akron | Implantable devices for producing insulin |
| RU2009132949A (ru) | 2007-02-02 | 2011-03-10 | Юниверсити Оф Майами (Us) | Терапевтические гибридные имплантируемые устройства |
| DE102007006634B4 (de) | 2007-02-06 | 2010-12-16 | Laser-Laboratorium Göttingen e.V. | Verfahren zur PTFE-Oberflächenmodifizierung, Verfahren zum Verkleben einer Oberfläche aus PTFE sowie Bauteil mit einer Oberfläche aus PTFE |
| US7695963B2 (en) | 2007-09-24 | 2010-04-13 | Cythera, Inc. | Methods for increasing definitive endoderm production |
| US20090105811A1 (en) * | 2007-10-18 | 2009-04-23 | Medtronic, Inc. | Intravascular Devices for Cell-Based Therapies |
| US8623650B2 (en) | 2007-10-19 | 2014-01-07 | Viacyte, Inc. | Methods and compositions for feeder-free pluripotent stem cell media containing human serum |
| US8338170B2 (en) | 2008-04-21 | 2012-12-25 | Viacyte, Inc. | Methods for purifying endoderm and pancreatic endoderm cells derived from human embryonic stem cells |
| US20110305672A1 (en) | 2008-07-25 | 2011-12-15 | University Of Georgia Research Foundation, Inc. | COMPOSITIONS FOR MESODERM DERIVED ISL1+ MULTIPOTENT CELLS (IMPs), EPICARDIAL PROGENITOR CELLS (EPCs) AND MULTIPOTENT CD56C CELLS (C56Cs) AND METHODS OF PRODUCING AND USING SAME |
| US8008075B2 (en) | 2008-11-04 | 2011-08-30 | Viacyte, Inc. | Stem cell aggregate suspension compositions and methods of differentiation thereof |
| US8895300B2 (en) | 2008-11-04 | 2014-11-25 | Viacyte, Inc. | Scalable primate pluripotent stem cell aggregate suspension culture and differentiation thereof |
| EP2356227B1 (en) | 2008-11-14 | 2018-03-28 | Viacyte, Inc. | Encapsulation of pancreatic cells derived from human pluripotent stem cells |
| US9109245B2 (en) | 2009-04-22 | 2015-08-18 | Viacyte, Inc. | Cell compositions derived from dedifferentiated reprogrammed cells |
| FR2960783B1 (fr) | 2010-06-04 | 2012-07-27 | Ass Pour Les Transferts De Technologies Du Mans | Membrane fonctionnalisee pour chambre d'encapsulation de cellules produisant au moins une substance d'interet therapeutique et organe bioartificiel comprenant une telle membrane |
| US10617557B2 (en) * | 2010-08-05 | 2020-04-14 | Forsight Vision4, Inc. | Combined drug delivery methods and apparatus |
| WO2012115619A1 (en) | 2011-02-21 | 2012-08-30 | Viacyte, Inc. | Loading system for an encapsulation device |
| US10660987B2 (en) | 2011-04-29 | 2020-05-26 | Converge Biotech Inc. | Conformal coating of cells for immunoisolation |
| WO2014105246A2 (en) | 2012-10-05 | 2014-07-03 | Massachusetts Institute Of Technology | Nanofluidic sorting system for gene synthesis and pcr reaction products |
| AU2013248265B2 (en) | 2012-11-08 | 2018-11-01 | Viacyte, Inc. | Scalable primate pluripotent stem cell aggregate suspension culture and differentiation thereof |
| US20150298388A1 (en) | 2012-12-04 | 2015-10-22 | The Boeing Company | Joining Composite Components Using Low Temperature Thermoplastic Film Fusion |
| HK1218139A1 (zh) | 2013-02-06 | 2017-02-03 | Viacyte, Inc. | 去分化的重新編程細胞所衍生的細胞組合物 |
| US10160950B2 (en) | 2013-03-01 | 2018-12-25 | Wisconsin Alumni Research Foundation | Methods of maintaining, expanding and differentiating neuronal subtype specific progenitors |
| CN116212115A (zh) | 2013-03-07 | 2023-06-06 | 韦尔赛特公司 | 三维大容量细胞包封装置组件 |
| WO2014138671A2 (en) | 2013-03-08 | 2014-09-12 | Viacyte, Inc. | Cryopreservation, hibernation and room temperature storage of encapulated pancreatic endoderm cell aggregates |
| US8859286B2 (en) | 2013-03-14 | 2014-10-14 | Viacyte, Inc. | In vitro differentiation of pluripotent stem cells to pancreatic endoderm cells (PEC) and endocrine cells |
| US10172791B2 (en) | 2013-03-14 | 2019-01-08 | Massachusetts Institute Of Technology | Multi-layer hydrogel capsules for encapsulation of cells and cell aggregates |
| US9555007B2 (en) | 2013-03-14 | 2017-01-31 | Massachusetts Institute Of Technology | Multi-layer hydrogel capsules for encapsulation of cells and cell aggregates |
| JP6325649B2 (ja) | 2013-04-24 | 2018-05-16 | ネステク ソシエテ アノニム | カプセル化デバイス |
| EP3569694A1 (en) | 2013-06-11 | 2019-11-20 | President and Fellows of Harvard College | Sc-beta cells and compositions and methods for generating the same |
| JP6209393B2 (ja) | 2013-08-21 | 2017-10-04 | 日東電工株式会社 | フィルター濾材 |
| EP3049020B1 (en) | 2013-09-24 | 2022-06-15 | Giner Life Sciences, Inc. | System for gas treatment of a cell implant |
| KR20160134761A (ko) | 2014-03-19 | 2016-11-23 | 세키스이가가쿠 고교가부시키가이샤 | 시트 적층형 리튬 이온 2차 전지 및 시트 적층형 리튬 이온 2차 전지의 제조 방법 |
| US11051900B2 (en) | 2014-04-16 | 2021-07-06 | Viacyte, Inc. | Tools and instruments for use with implantable encapsulation devices |
| DK3131497T3 (da) | 2014-04-16 | 2023-11-06 | Viacyte Inc | Instrumenter til anvendelse med implanterbare indkapslingsindretninger |
| US20150374637A1 (en) * | 2014-06-27 | 2015-12-31 | Taylor Gun-Jin Wang | Semi-permeable capsular membrane with tapered conduits for diabetes functional cure |
| EP3169425B1 (en) | 2014-07-18 | 2022-08-31 | Sartorius Stedim Biotech GmbH | Membrane with increased surface area |
| US20160031054A1 (en) | 2014-07-31 | 2016-02-04 | Lee-Cheng Chang | Dust collector for collecting sawdust and wood chips |
| US20160036923A1 (en) | 2014-08-03 | 2016-02-04 | Microsoft Corporation | Efficient Migration of Application State Information |
| WO2016080943A1 (en) | 2014-11-20 | 2016-05-26 | Viacyte, Inc. | Instruments and methods for loading cells into implantable devices |
| US10443042B2 (en) | 2014-12-18 | 2019-10-15 | President And Fellows Of Harvard College | Serum-free in vitro directed differentiation protocol for generating stem cell-derived beta cells and uses thereof |
| EP3273949A4 (en) | 2015-03-23 | 2018-12-12 | The Regents of The University of California | Thin film cell encapsulation devices |
| US20160365556A1 (en) | 2015-06-11 | 2016-12-15 | Nano And Advanced Materials Institute Limited | Nonwoven nanofiber separator and method of improving physical stability of battery separator |
| JP2017086313A (ja) | 2015-11-06 | 2017-05-25 | 国立大学法人東北大学 | 細胞移植治療用の皮下埋め込みデバイス |
| US20190282624A1 (en) | 2015-11-30 | 2019-09-19 | Beihao Stem Cell And Regenerative Medicine Research Institute Co., Ltd. | Improved methods for reprograming non-pluripotent cells into pluripotent stem cells |
| AU2017205194A1 (en) | 2016-01-08 | 2018-07-19 | Massachusetts Institute Of Technology | Production of differentiated enteroendocrine cells and insulin producing cells |
| MA45502A (fr) | 2016-06-21 | 2019-04-24 | Janssen Biotech Inc | Génération de cellules bêta fonctionnelles dérivées de cellules souches pluripotentes humaines ayant une respiration mitochondriale glucose-dépendante et une réponse en sécrétion d'insuline en deux phases |
| JP7125398B2 (ja) | 2016-12-13 | 2022-08-24 | ミレニアム ファーマシューティカルズ, インコーポレイテッド | 生体表面のコンフォーマルコーティング |
| AU2018285539B2 (en) | 2017-06-14 | 2024-10-31 | Vertex Pharmaceuticals Incorporated | Devices and methods for delivering therapeutics |
| US20200208093A1 (en) | 2017-06-14 | 2020-07-02 | Takeda Pharmaceutical Company Limited | Cell-sealing device |
| CN111491617B (zh) | 2017-09-29 | 2024-12-31 | 沃泰克斯药物股份有限公司 | 细胞容纳装置 |
| CA3081762A1 (en) | 2017-11-15 | 2019-05-23 | Semma Therapeutics, Inc. | Islet cell manufacturing compositions and methods of use |
| CA3092842A1 (en) | 2018-03-02 | 2019-09-06 | Vertex Pharmaceuticals Incorporated | Methods of enhancing stem cell differentiation into beta cells |
-
2018
- 2018-06-14 AU AU2018285539A patent/AU2018285539B2/en active Active
- 2018-06-14 WO PCT/US2018/037637 patent/WO2018232180A1/en not_active Ceased
- 2018-06-14 IL IL313825A patent/IL313825B2/en unknown
- 2018-06-14 EP EP18816938.7A patent/EP3638205A4/en active Pending
- 2018-06-14 IL IL271195A patent/IL271195B2/en unknown
- 2018-06-14 CA CA3066055A patent/CA3066055A1/en active Pending
- 2018-06-14 JP JP2020519004A patent/JP7284948B2/ja active Active
- 2018-06-14 IL IL308120A patent/IL308120B2/en unknown
- 2018-06-14 CN CN201880052922.3A patent/CN111565707A/zh active Pending
-
2019
- 2019-03-06 US US16/294,631 patent/US11471398B2/en active Active
-
2022
- 2022-05-04 US US17/736,579 patent/US12194138B2/en active Active
-
2023
- 2023-05-08 JP JP2023076521A patent/JP7513799B2/ja active Active
-
2024
- 2024-06-27 JP JP2024103857A patent/JP2024123255A/ja active Pending
- 2024-11-26 US US18/960,798 patent/US20250161203A1/en active Pending
-
2025
- 2025-01-16 AU AU2025200324A patent/AU2025200324A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100150984A1 (en) | 2007-03-09 | 2010-06-17 | The University Of Akron | Bio-artificial pancreas and a procedure for preparation of same |
| JP2012520107A (ja) | 2009-03-11 | 2012-09-06 | ザ・ユニヴァーシティ・オヴ・シェフィールド | スカフォールド |
| WO2016052504A1 (ja) | 2014-09-30 | 2016-04-07 | 富士フイルム株式会社 | 組成物、細胞構造体、膵島移植キット、膵島細胞移植治療剤及び血糖低下剤、膵島を含む組成物、膵島を含むキット、並びに膵島移植治療剤及び血糖低下剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| IL271195B2 (en) | 2024-04-01 |
| IL308120B1 (en) | 2024-08-01 |
| US12194138B2 (en) | 2025-01-14 |
| AU2018285539A1 (en) | 2020-02-06 |
| US20220331234A1 (en) | 2022-10-20 |
| JP7284948B2 (ja) | 2023-06-01 |
| AU2018285539B2 (en) | 2024-10-31 |
| IL313825A (en) | 2024-08-01 |
| US20250161203A1 (en) | 2025-05-22 |
| CA3066055A1 (en) | 2018-12-20 |
| US20190201323A1 (en) | 2019-07-04 |
| US11471398B2 (en) | 2022-10-18 |
| IL308120A (en) | 2023-12-01 |
| IL308120B2 (en) | 2024-12-01 |
| EP3638205A1 (en) | 2020-04-22 |
| JP2024123255A (ja) | 2024-09-10 |
| IL313825B2 (en) | 2025-07-01 |
| AU2025200324A1 (en) | 2025-02-13 |
| NZ760829A (en) | 2025-05-02 |
| JP2020523415A (ja) | 2020-08-06 |
| IL271195B1 (en) | 2023-12-01 |
| JP2023100847A (ja) | 2023-07-19 |
| WO2018232180A1 (en) | 2018-12-20 |
| IL271195A (en) | 2020-01-30 |
| NZ800904A (en) | 2025-08-29 |
| EP3638205A4 (en) | 2021-03-17 |
| IL313825B1 (en) | 2025-03-01 |
| CN111565707A (zh) | 2020-08-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7513799B2 (ja) | 療法薬を送達するためのデバイスおよび方法 | |
| US11185498B2 (en) | Multilayer thin film drug delivery device and methods of making and using the same | |
| US10668106B2 (en) | Chamber for encapsulating secreting cells | |
| Khalf et al. | Modeling the permeability of multiaxial electrospun poly (ε-caprolactone)-gelatin hybrid fibers for controlled doxycycline release | |
| US20040049268A1 (en) | Artificial cornea | |
| Shalaby et al. | Polymers of biological and biomedical significance | |
| CN107349471A (zh) | 一种载药缓释的复合组织修复材料及其制备方法 | |
| US20130089594A1 (en) | Macroporous bioengineered scaffolds for cell transplantation | |
| JP2023534774A (ja) | 多層細胞カプセル及びその使用 | |
| HK40036584A (en) | Devices and methods for delivering therapeutics | |
| US20230173141A1 (en) | Nanofiber-enabled encapsulation devices and uses thereof | |
| CN220327790U (zh) | 一种人工耳蜗载药电极 | |
| US20150010611A1 (en) | Matrix for the Infiltration with Cells | |
| CN117545448A (zh) | 制造包含多个细胞的治疗装置和系统 | |
| WO2025106977A1 (en) | Drug-eluting anti-fibrotic macroencapsulation (dream) devices for delivery of therapeutic cells | |
| CN119013055A (zh) | 用于工程化血管网络的连续纤维支撑屏障 | |
| WO2022172930A1 (ja) | 移植デバイス | |
| WO2018227550A1 (zh) | 一种载药缓释的复合组织修复材料及其制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230607 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230607 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240529 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240627 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7513799 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |