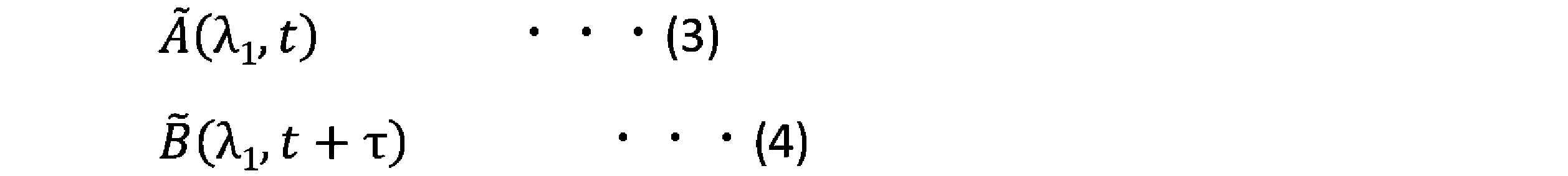JP7499503B2 - Method, device and program for evaluating protein structural changes - Google Patents
Method, device and program for evaluating protein structural changes Download PDFInfo
- Publication number
- JP7499503B2 JP7499503B2 JP2020104065A JP2020104065A JP7499503B2 JP 7499503 B2 JP7499503 B2 JP 7499503B2 JP 2020104065 A JP2020104065 A JP 2020104065A JP 2020104065 A JP2020104065 A JP 2020104065A JP 7499503 B2 JP7499503 B2 JP 7499503B2
- Authority
- JP
- Japan
- Prior art keywords
- spectrum
- fluorescence
- correlation
- changes
- protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims description 26
- 230000006333 protein structural change Effects 0.000 title description 2
- 102000004169 proteins and genes Human genes 0.000 claims description 127
- 108090000623 proteins and genes Proteins 0.000 claims description 127
- 238000001228 spectrum Methods 0.000 claims description 109
- 238000002189 fluorescence spectrum Methods 0.000 claims description 60
- 230000008859 change Effects 0.000 claims description 58
- 238000001142 circular dichroism spectrum Methods 0.000 claims description 54
- 238000005259 measurement Methods 0.000 claims description 52
- 238000011156 evaluation Methods 0.000 claims description 31
- 230000003595 spectral effect Effects 0.000 claims description 21
- 238000004364 calculation method Methods 0.000 claims description 12
- 230000036962 time dependent Effects 0.000 claims description 12
- 238000000513 principal component analysis Methods 0.000 claims description 8
- 230000005684 electric field Effects 0.000 claims description 3
- 239000000523 sample Substances 0.000 description 61
- 238000010586 diagram Methods 0.000 description 11
- 238000012545 processing Methods 0.000 description 9
- 238000012937 correction Methods 0.000 description 8
- 102000016943 Muramidase Human genes 0.000 description 7
- 108010014251 Muramidase Proteins 0.000 description 7
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 7
- 230000005284 excitation Effects 0.000 description 7
- 229960000274 lysozyme Drugs 0.000 description 7
- 235000010335 lysozyme Nutrition 0.000 description 7
- 239000004325 lysozyme Substances 0.000 description 7
- 125000000430 tryptophan group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C2=C([H])C([H])=C([H])C([H])=C12 0.000 description 7
- 238000013500 data storage Methods 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 5
- 230000007423 decrease Effects 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 5
- 229920002643 polyglutamic acid Polymers 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- OUYCCCASQSFEME-UHFFFAOYSA-L tyrosinate(2-) Chemical compound [O-]C(=O)C(N)CC1=CC=C([O-])C=C1 OUYCCCASQSFEME-UHFFFAOYSA-L 0.000 description 4
- QCVGEOXPDFCNHA-UHFFFAOYSA-N 5,5-dimethyl-2,4-dioxo-1,3-oxazolidine-3-carboxamide Chemical compound CC1(C)OC(=O)N(C(N)=O)C1=O QCVGEOXPDFCNHA-UHFFFAOYSA-N 0.000 description 3
- 229920000742 Cotton Polymers 0.000 description 3
- 102000002322 Egg Proteins Human genes 0.000 description 3
- 108010000912 Egg Proteins Proteins 0.000 description 3
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 3
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 3
- 229960000074 biopharmaceutical Drugs 0.000 description 3
- 238000002983 circular dichroism Methods 0.000 description 3
- 230000002596 correlated effect Effects 0.000 description 3
- 238000005314 correlation function Methods 0.000 description 3
- 238000004925 denaturation Methods 0.000 description 3
- 230000036425 denaturation Effects 0.000 description 3
- 235000014103 egg white Nutrition 0.000 description 3
- 239000007850 fluorescent dye Substances 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 230000001360 synchronised effect Effects 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 2
- 239000013566 allergen Substances 0.000 description 2
- 229940024606 amino acid Drugs 0.000 description 2
- 150000001413 amino acids Chemical group 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 229940125644 antibody drug Drugs 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 210000000969 egg white Anatomy 0.000 description 2
- 238000001506 fluorescence spectroscopy Methods 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 230000010287 polarization Effects 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 238000003908 quality control method Methods 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- 238000012356 Product development Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- -1 aromatic amino acids Chemical class 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000000991 chicken egg Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000005100 correlation spectroscopy Methods 0.000 description 1
- 230000000875 corresponding effect Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000009509 drug development Methods 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 238000010191 image analysis Methods 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 229940125730 polarisation modulator Drugs 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Landscapes
- Investigating Or Analysing Materials By Optical Means (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
Description
本発明は蛋白質の構造変化の評価方法に関し、蛋白質の産業利用分野に属する。 The present invention relates to a method for evaluating structural changes in proteins, and belongs to the field of industrial use of proteins.
円二色性スペクトルや蛍光スペクトルは、蛋白質の高次構造の変化を鋭敏に反映することが知られており、バイオ医薬品をはじめとする蛋白質の産業利用分野において、これらの測定が蛋白質の構造変化を評価する手法として重要な役割を担っている。 Circular dichroism and fluorescence spectra are known to sensitively reflect changes in the higher-order structure of proteins, and these measurements play an important role as methods for evaluating structural changes in proteins in the industrial application of proteins, including biopharmaceuticals.
蛋白質の構造は、大きく一次、二次、三次構造、四次構造に区分され、
一次構造は、蛋白質のアミノ酸配列を指し、
二次構造は、蛋白質一次構造の部分的な立体構造(αヘリックスやβシート)を指し、
三次構造は、蛋白質二次構造が空間的にまとまってできた蛋白質1分子がとる立体構造(コンフォメーション)を指し、
四次構造は、複数のポリペプチド鎖が集まって複合蛋白質を形成している状態を指す、
とされている。以下、CDスペクトルや蛍光スペクトルを用いて蛋白質の高次構造の変化を評価する既存の手法(文献1から3)について説明する。
Protein structures are broadly divided into primary, secondary, tertiary, and quaternary structures.
Primary structure refers to the amino acid sequence of a protein.
Secondary structure refers to the partial three-dimensional structure (alpha helix and beta sheet) of the primary protein structure.
Tertiary structure refers to the three-dimensional conformation that a protein molecule takes when the protein secondary structures are spatially organized.
Quaternary structure refers to the state in which multiple polypeptide chains are assembled to form a complex protein.
In the following, existing methods for evaluating changes in the higher-order structure of proteins using CD spectra and fluorescence spectra (References 1 to 3) will be described.
<円二色性測定>
文献1は、ポリ-L-グルタミン酸のCDスペクトルの測定例である。ポリ-L-グルタミン酸は、水溶液中でのpHの変化に伴って、その二次構造が「αヘリックス-ランダムコイル転移」することが知られている。文献1の図3(ポリペプチドのCD)を見ると、pH4.3及びpH11におけるポリ-L-グルタミン酸のCDスペクトルが400~200nmの波長範囲で表示されている。
<Circular dichroism measurement>
Reference 1 is an example of measuring the CD spectrum of poly-L-glutamic acid. It is known that poly-L-glutamic acid undergoes an "α-helix-random coil transition" in its secondary structure as the pH changes in an aqueous solution. Looking at Figure 3 (CD of polypeptide) in Reference 1, the CD spectra of poly-L-glutamic acid at pH 4.3 and pH 11 are displayed in the wavelength range of 400 to 200 nm.
文献1のCDスペクトルによると、pH4.3において、225nm付近に負のコットン効果が表れ、そのピークの大きさがαヘリックス含量の目安とされている。また、200nm以下の短波長領域に、強い正のコットン効果が表れている。一方、pH11の方は、ポリ-L-グルタミン酸がランダムコイルの状態で存在するため、上記のコットン効果が著しく変化している。 According to the CD spectrum in Reference 1, at pH 4.3, a negative Cotton effect appears around 225 nm, and the magnitude of this peak is used as an indicator of the α-helix content. Also, a strong positive Cotton effect appears in the short wavelength region below 200 nm. On the other hand, at pH 11, poly-L-glutamic acid exists in a random coil state, so the above Cotton effect changes significantly.
このように、CDスペクトル中の特定の波長域のCD強度の変化に基づいて、蛋白質の二次構造の変化を推定できることが説明されている。 In this way, it has been explained that changes in the secondary structure of a protein can be estimated based on changes in the CD intensity in a specific wavelength range in the CD spectrum.
<蛍光測定>
蛍光測定は、蛋白質の三次構造の変化を評価する方法として用いることができる。例えば、蛋白質分子に内在する芳香族アミノ酸(トリプトファン、チロシン、フェニルアラニン)を蛍光プローブとすることが多い。
<Fluorescence measurement>
Fluorescence measurement can be used as a method for evaluating changes in the tertiary structure of proteins. For example, aromatic amino acids (tryptophan, tyrosine, and phenylalanine) present in protein molecules are often used as fluorescent probes.
文献2には、このようなアミノ酸由来の蛍光スペクトルに基づいて、pHや圧力などの物理パラメータを変化させた際の蛋白質の立体構造の変性過程を評価する手法が紹介されている。文献2の図1(左)は、卵白アレルゲン蛋白質のpH条件を「4→10.4→12」の順に変えて測定した蛍光スペクトルを示している。この図では、蛍光スペクトルのピーク波長が304nm(チロシン由来の蛍光)から340nm(チロシネート由来の蛍光)へとシフトしている。このことから、塩基性側へのpH変化に伴って、チロシンの側鎖OH基からH+が解離し、チロシネートの濃度が上がった、と評価している。
また、文献2の図1(右)は、卵白アレルゲン蛋白質の圧力条件を「50気圧から7000気圧まで段階的に加圧」して測定した蛍光スペクトルを示している。圧力変化に伴って、蛍光スペクトルの波長304nmの蛍光強度(チロシン由来)が大幅に減少し、同時に波長340nmの蛍光強度(チロシネート由来)が増加している。このことから、加圧に伴う三次構造の転移が生じて、チロシンを含む構造状態の割合が減少し、チロシネートを含む構造状態の割合が増加したものと、評価している。
Figure 1 (right) of
<CDと蛍光>
文献3は、リゾチームの立体構造とリゾチーム内のトリプトファン残基の微環境が温度変化に伴ってどのように変化するかを、CDスペクトル及び蛍光スペクトルに基づいて評価した例である。この手法は、リゾチーム(鶏卵白)の水溶液(0.05mg/ml)を試料にして、5mmセルにてCDスペクトルを、10mmセルにて蛍光スペクトルを、20℃から90℃までの5℃間隔の温度インターバルで、それぞれのCDスペクトルを測定している。
<CD and Fluorescence>
文献3の図1は、190~260nmの波長範囲のCDスペクトルの温度変化測定の結果である。測定条件は、走査速度100nm/min、レスポンス2sec、バンド幅1nm、データ間隔0.1nm、積算2回としている。文献3の図2は、波長220nmのCD強度の温度変化測定の結果である。
Figure 1 in
文献3の図4は、300~400nmの波長範囲の蛍光スペクトルの温度変化測定の結果である。測定条件は、励起波長280nm、励起光バンド幅2nm、データ間隔1nm、レスポンス1secとしている。文献3の図5は、波長339nmの蛍光強度と波長349nmの蛍光強度との比をとって、温度変化に伴うその比の変化を示している。
Figure 4 in
文献3の図1のCDスペクトルによれば、200nm以下の波長領域に見られたピークの強度が、温度上昇に伴って、大幅に減少しており、20℃において波長207.7nmにあった負のピークが、90℃では波長202.8nmまで短波長側にシフトしている。このことから、文献3では、温度上昇によってリゾチームのαヘリックス構造が解けて、ランダムコイル構造に変化したものと評価している。そして、文献3の図2のαヘリックス構造に由来する波長220nmのCD強度の変化から、70~80℃の温度域で急激な減少が認められ、変性温度が73.9℃とされている。
According to the CD spectrum in Figure 1 of
また、文献3の図4の蛍光スペクトルによれば、20℃において波長339nmにあった蛍光ピーク(吸収極大)が、温度上昇に伴って長波長側へシフトし、90℃では波長348nmに生じている。一般に、蛋白質の蛍光をモニターすることにより、トリプトファン残基の置かれた微環境についての知見が得られる。トリプトファン残基の蛍光ピークは、その周辺環境の極性に敏感に反応し、例えば、トリプトファン残基が蛋白質の内部に埋まった状態(非極性の環境)では、330nm付近にピークを示す。立体構造が変化して、トリプトファン残基が蛋白質の表面で水に接触した状態(極性の高い環境)になると、ピークが350nm付近までシフトすると言われている。そのため、文献3では、図4の蛍光スペクトルの変化から、リゾチームの熱変性によって蛋白質内部に埋まっていたトリプトファン残差が蛋白質表面に現れた、と評価している。
According to the fluorescence spectrum in Figure 4 of
さらに、文献3の図5では、図2と同様に、70~75℃の温度域でピーク比がもっとも大きく変化していることから、リゾチームの二次構造(αヘリックスの構造)の変化も、三次構造(トリプトファン残差を含む立体構造)の変化も、同じ温度域で生じていると評価している。
Furthermore, in Figure 5 of
特許文献1から3に示される通り、従来の評価方法では、CD測定や蛍光測定によってそれぞれのスペクトルを観察し、特定の波長域でのスペクトル形状の変化に着目することで、蛋白質の高次構造がどのように変化したかどうかを評価している。しかしながら、蛋白質全体の中で異なる構造変化(二次と三次構造の各々の変化など)が相対的にどのようなタイミングで生じているのかや、蛋白質全体が何ら構造変化していないことなどを評価するには、個々のスペクトルデータの観察だけでは不十分であり、専門的な知識や多くの経験に基づく判断が必要になってしまう。 As shown in Patent Documents 1 to 3, conventional evaluation methods observe the respective spectra by CD measurement or fluorescence measurement, and evaluate whether or not the higher-order structure of the protein has changed by focusing on changes in the spectral shape in specific wavelength ranges. However, to evaluate the relative timing of different structural changes (such as changes in secondary and tertiary structures) occurring within the entire protein, or whether the entire protein has not undergone any structural changes, observing individual spectral data alone is insufficient, and judgment based on specialized knowledge and extensive experience is required.
発明者らは、蛋白質全体の中で異なる構造変化が相対的にどのようなタイミングで生じているのか、蛋白質全体が何ら構造変化を起こしていないこと等を、簡易に評価できる手法があれば、バイオ医薬品をはじめとする蛋白質の産業利用分野の発展に非常に役立つのでは、と考えた。 The inventors believed that if there was a method for easily evaluating the relative timing of different structural changes occurring within the entire protein, or whether the entire protein is not undergoing any structural changes, it would be extremely useful for the development of industrial applications of proteins, including biopharmaceuticals.
本発明の目的は、外部刺激が変化した際に生じる蛋白質の複数の構造変化を簡易に評価することができる評価方法、評価装置および評価プログラムを提供することにある。 The object of the present invention is to provide an evaluation method, an evaluation device, and an evaluation program that can easily evaluate multiple structural changes in a protein that occur when an external stimulus changes.
すなわち、本発明に係る蛋白質の構造変化の評価方法は、
蛋白質試料に対する外部刺激を経時的に変化させる手順と、
前記外部刺激の変化中の複数のタイミングにおいて蛍光スペクトル測定およびCDスペクトル測定を実行する手順と、
蛍光スペクトルの測定波長をX軸とし、CDスペクトルの測定波長をY軸として、測定された蛍光スペクトルおよびCDスペクトルの各々の経時的変化についての二次元相関スペクトルである同時相関スペクトルおよび異時相関スペクトルを演算する手順と、
前記同時相関スペクトルおよび異時相関スペクトルを画像データとして表示手段に表示する手順と、
前記同時相関スペクトルおよび異時相関スペクトルに現れる正または負のピークに基づいて、蛋白質試料の二次構造および三次構造の変化の相関を評価する手順と、を含むことを特徴とする。
That is, the method for evaluating a structural change of a protein according to the present invention comprises the steps of:
A procedure for changing an external stimulus to a protein sample over time;
performing fluorescence spectrum measurement and CD spectrum measurement at a plurality of timings during a change in the external stimulus;
a step of calculating a simultaneous correlation spectrum and an anti-chronic correlation spectrum, which are two-dimensional correlation spectra for the time-dependent changes of the measured fluorescence spectrum and CD spectrum, with the measurement wavelength of the fluorescence spectrum as the X-axis and the measurement wavelength of the CD spectrum as the Y-axis;
displaying the simultaneous correlation spectrum and the cross-time correlation spectrum as image data on a display means;
and a step of evaluating the correlation between changes in the secondary structure and the tertiary structure of the protein sample based on positive or negative peaks appearing in the simultaneous correlation spectrum and the different time correlation spectrum .
前記蛍光スペクトル測定では、蛋白質の三次構造の変化に反応する波長域が少なくとも含まれるように測定波長範囲を設定し、CDスペクトル測定では、蛋白質の二次構造の変化に反応する波長域が少なくとも含まれるように測定波長範囲を設定するとよい。 In the above-mentioned fluorescence spectrum measurement, the measurement wavelength range is set so as to include at least the wavelength range that responds to changes in the tertiary structure of the protein, and in the CD spectrum measurement, the measurement wavelength range is set so as to include at least the wavelength range that responds to changes in the secondary structure of the protein.
蛋白質への外部刺激としては、温度、pH、圧力、電場、磁場、光、応力、蛋白濃度、バッファーの種類、バッファー濃度のいずれかであることが好ましい。また、蛋白質試料の二次構造および三次構造の変化の相関を次表のように評価することが好ましい。
――――――――――――――――――――――――――――――――――――――――
同時相関Φ 異時相関Ψ λ1とλ2の交差ピークにおける各スペクトル変化
――――――――――――――――――――――――――――――――――――――――
正 ほぼゼロ 蛍光とCDの変化は同方向で同時に起こる
正 正 蛍光とCDの変化は同方向で蛍光はCDより先に起こる
正 負 蛍光とCDの変化は同方向で蛍光はCDより後に起こる
負 ほぼゼロ 蛍光とCDの変化は異方向で同時に起こる
負 正 蛍光とCDの変化は異方向で蛍光はCDより後に起こる
負 負 蛍光とCDの変化は異方向で蛍光はCDより先に起こる
――――――――――――――――――――――――――――――――――――――――
λ1:蛋白質の三次構造の変化に反応する蛍光スペクトルの波長
λ2:蛋白質の二次構造の変化に反応するCDスペクトルの波長
The external stimulus to the protein is preferably any one of temperature, pH, pressure, electric field, magnetic field, light, stress, protein concentration, type of buffer, and buffer concentration. It is also preferable to evaluate the correlation between the changes in the secondary structure and tertiary structure of the protein sample as shown in the following table.
----------------------------------------------------------------------------------
Simultaneous correlation Φ Cross-correlation Ψ Spectral changes at the cross peaks of λ1 and λ2
----------------------------------------------------------------------------------
Positive almost zero fluorescence and CD changes occur simultaneously in the same direction
The changes in fluorescence and CD are in the same direction, and fluorescence occurs before CD.
The positive and negative fluorescence and CD changes are in the same direction, and fluorescence occurs after CD.
Negative near-zero fluorescence and CD changes occur simultaneously in different directions
The changes in negative and positive fluorescence and CD are in opposite directions, and fluorescence occurs after CD.
The changes in fluorescence and CD are in opposite directions, and fluorescence occurs before CD .
----------------------------------------------------------------------------------
λ1: wavelength of the fluorescence spectrum that responds to changes in the tertiary structure of the protein
λ2: wavelength of the CD spectrum that responds to changes in the secondary structure of the protein
さらに、複数の蛋白質試料について、試料毎に前記二次元相関スペクトルを画像データとして取得し、これらの画像データに対して、画像用の主成分分析を実行することが好ましい。複数の蛋白質試料を、主成分にもとづいてグループ分けすることができる。 Furthermore, it is preferable to obtain the two-dimensional correlation spectrum for each of a plurality of protein samples as image data, and perform image principal component analysis on the image data. The plurality of protein samples can be grouped based on the principal components.
次に、本発明に係る蛋白質の構造変化の評価装置は、
蛋白質試料に対する外部刺激を経時的に変化させながら、当該外部刺激の変化中の複数のタイミングにおいて測定された蛍光スペクトルおよびCDスペクトルをデータとして受信する受信手段と、
蛍光スペクトルの測定波長をX軸とし、CDスペクトルの測定波長をY軸として、前記蛍光スペクトルおよび前記CDスペクトルの各々のデータの経時的変化についての二次元相関スペクトルである同時相関スペクトルおよび異時相関スペクトルを演算する演算手段と、
前記同時相関スペクトルおよび異時相関スペクトルを画像データとして表示手段に表示させる表示指令手段と、
前記同時相関スペクトルおよび異時相関スペクトルに現れる正または負のピークに基づいて、蛋白質試料の二次構造および三次構造の変化の相関を評価する評価手段と、を備えることを特徴とする。
Next, the apparatus for evaluating a structural change in a protein according to the present invention comprises:
a receiving means for receiving, as data, fluorescence spectra and CD spectra measured at a plurality of timings during the change in an external stimulus applied to a protein sample over time;
a calculation means for calculating a simultaneous correlation spectrum and an intertemporal correlation spectrum, which are two-dimensional correlation spectra regarding the time-dependent changes in data of the fluorescence spectrum and the CD spectrum, with the measurement wavelength of the fluorescence spectrum being the X-axis and the measurement wavelength of the CD spectrum being the Y- axis;
a display command means for causing a display means to display the simultaneous correlation spectrum and the cross-time correlation spectrum as image data;
and an evaluation means for evaluating the correlation between changes in the secondary structure and the tertiary structure of the protein sample based on positive or negative peaks appearing in the simultaneous correlation spectrum and the different time correlation spectrum .
また、本発明に係る蛋白質の構造変化の評価プログラムは、
蛋白質試料に対する外部刺激を経時的に変化させながら、当該外部刺激の変化中の複数のタイミングにおいて測定された蛍光スペクトルおよびCDスペクトルをデータとして受信する受信手段と、
蛍光スペクトルの測定波長をX軸とし、CDスペクトルの測定波長をY軸として、測定された前記蛍光スペクトルおよび前記CDスペクトルの各々の経時的変化についての二次元相関スペクトルである同時相関スペクトルおよび異時相関スペクトルを演算する演算手段と、
前記同時相関スペクトルおよび異時相関スペクトルを画像データとして表示手段に表示させる表示指令手段と、
前記同時相関スペクトルおよび異時相関スペクトルに現れる正または負のピークに基づいて、蛋白質試料の二次構造および三次構造の変化の相関を評価する評価手段と、してコンピュータを機能させることを特徴とする。
The program for evaluating a structural change in a protein according to the present invention further comprises:
a receiving means for receiving, as data, fluorescence spectra and CD spectra measured at a plurality of timings during the change in an external stimulus applied to a protein sample over time;
a calculation means for calculating a simultaneous correlation spectrum and an intertemporal correlation spectrum, which are two-dimensional correlation spectra regarding the time-dependent changes of the measured fluorescence spectrum and the measured CD spectrum, with the measurement wavelength of the fluorescence spectrum being the X-axis and the measurement wavelength of the CD spectrum being the Y-axis ;
a display command means for causing a display means to display the simultaneous correlation spectrum and the cross-time correlation spectrum as image data;
The present invention is characterized in that the computer functions as an evaluation means for evaluating the correlation between changes in the secondary structure and tertiary structure of a protein sample based on positive or negative peaks appearing in the simultaneous correlation spectrum and the different time correlation spectrum .
蛋白質の安定性評価(製造工程の評価を含む)においては、外部刺激の経時的変化に対する蛋白質の動的な構造変化、例えば、蛋白質の二次構造変化および三次構造変化についてのタイムラグを適切に把握できれば、より信頼性のある評価が可能になると言える。本発明では、外部刺激の変化を伴う蛋白質の蛍光スペクトル測定およびCDスペクトル測定によって得られたそれぞれのスペクトルデータから二次元相関スペクトルを演算し、それを例えば二次元画像データとしてモニターなどに表示する。 In evaluating protein stability (including evaluation of the manufacturing process), it can be said that more reliable evaluation is possible if the dynamic structural changes of the protein in response to changes in external stimuli over time, for example, the time lag in secondary and tertiary structural changes of the protein, can be properly understood. In the present invention, a two-dimensional correlation spectrum is calculated from the respective spectral data obtained by measuring the fluorescence spectrum and the CD spectrum of a protein accompanied by changes in external stimuli, and the two-dimensional correlation spectrum is displayed on a monitor, for example, as two-dimensional image data.
二次元相関スペクトルの算出方法自体は、公知の算出方法を用いる。本発明では、二次元相関スペクトルの算出方法を使って、蛍光スペクトルのある波長(λ1)の蛍光強度の変化状態と、CDスペクトルのある波長(λ2)のCD強度の変化状態と、の相関をとる。二次元マップ状にすべての又は選択された所定の波長(λ1,λ2)の組合せについて、上記の相関をとる。二次元相関スペクトルは、その相関結果を、X軸に蛍光スペクトルの波長をとり、Y軸にCDスペクトルの波長をとった二次元マトリックス状に表現させたものである。通常、二次元相関スペクトルは、同時相関スペクトルおよび異時相関スペクトルがセットで算出される。 The calculation method for the two-dimensional correlation spectrum itself uses a known calculation method. In the present invention, the calculation method for the two-dimensional correlation spectrum is used to obtain a correlation between the change in fluorescence intensity at a certain wavelength (λ1) of the fluorescence spectrum and the change in CD intensity at a certain wavelength (λ2) of the CD spectrum. The above correlation is obtained for all or selected combinations of predetermined wavelengths (λ1, λ2) in a two-dimensional map. The two-dimensional correlation spectrum is a representation of the correlation results in a two-dimensional matrix with the wavelength of the fluorescence spectrum on the X-axis and the wavelength of the CD spectrum on the Y-axis. Usually, the two-dimensional correlation spectrum is calculated as a set of simultaneous correlation spectrum and different-time correlation spectrum.
ユーザーは、その二次元相関スペクトル(同時相関スペクトルおよび異時相関スペクトル)の画像データを観察することにより、その二次元相関スペクトルに表れた正または負のピークに基づいて、蛋白質に同時に生じる構造変化やタイムラグのある複数の構造変化を視覚的にかつ網羅的に把握することができる。言い換えると、蛋白質の複合的な構造変化を一目で把握して評価できるようになった。このような評価方法は、蛋白質の産業利用分野における研究・製造・品質管理などの現場に極めて有用な分析法として貢献できる。 By observing the image data of the two-dimensional correlation spectra (simultaneous correlation spectra and different-time correlation spectra), users can visually and comprehensively grasp simultaneous structural changes or multiple structural changes with a time lag that occur in a protein based on the positive or negative peaks that appear in the two-dimensional correlation spectra. In other words, it is now possible to grasp and evaluate complex structural changes in a protein at a glance. This type of evaluation method can contribute as an extremely useful analytical method in research, production, quality control, and other fields in the industrial use of proteins.
第一実施形態
図1は、本発明の一実施形態に係る評価装置の機能ブロック図であり、この評価装置を用いて蛋白質の構造変化を評価する。本実施形態では、評価装置10は、コンピュータで構成され、コンピュータが記憶媒体に記憶された評価プログラムを読み取って実行することにより、例えば、データ受信部12、データ保持部14、補正部16、演算部18、表示指令部20、及び、評価部22などとして機能する。
1 is a functional block diagram of an evaluation device according to one embodiment of the present invention, which is used to evaluate structural changes in a protein. In this embodiment, the
データ受信部12は、外部から蛋白質試料の蛍光スペクトルデータおよびCDスペクトルデータを受信する。データ保持部14は、メモリー等からなり、スペクトルデータを保持する。補正部16は、二次元相関スペクトルデータの演算が適切に実行されるようにデータ保持部14から読み取ったスペクトルデータを補正する。演算部18は、蛍光スペクトルデータおよびCDスペクトルデータに基づいて二次元相関スペクトルデータを演算する。表示指令部20は、二次元相関スペクトルデータをデータ保持部14に保持させるとともに、当該二次元相関スペクトルデータを表示装置(液晶ディスプレイ等)24に画像表示させる。また、表示指令部20は、適宜、蛍光スペクトルデータおよびCDスペクトルデータを表示装置24に画像表示させてもよい。
The
評価部22は、二次元相関スペクトルデータに表れている蛋白質試料の構造変化の評価情報を、文字または図形を使って表示装置24に表示させる。
The
表示装置24には、その評価情報が、二次元相関スペクトルデータ、蛍光スペクトルデータ又はCDスペクトルデータと共に表示される。或いは、これらのスペクトルデータとは独立して表示される。表示装置24には、少なくとも二次元相関スペクトルデータを二次元画像データとして表示可能な公知の手段を採用できる。ここで、表示装置24は、評価装置10と一体でも、又は別体でもよい。
On the
図2は、評価装置10とCD/蛍光測定機30からなるシステムの全体構成図である。CD/蛍光測定機30の構成を図2を用いて簡単に説明する。CD/蛍光測定機30は、蛋白質試料を測定対象として、外部刺激を経時的に変化させた際の、その変化中の複数のタイミングにおいて、CDスペクトルデータおよび蛍光スペクトルデータを繰り返し測定する装置であり、図2に示すように、光源ランプ31、分光器32、偏光変調子(PEM)33、試料部34、CD用の光検出器35、蛍光用の分光器36、蛍光用の光検出器37、及び、両光検出器35,37からの信号を処理する信号処理部38を備える。信号処理部38では、測定機の動作条件の設定および測定条件の設定も行われる。信号処理部38は、設定された条件に従って、PEM33の駆動制御、各分光器32,36の波長走査制御、試料部34の温調制御やセル交換制御などを実行する。
Figure 2 is an overall configuration diagram of a system consisting of the
光源ランプ31、分光器32、PEM33の順で構成された照射光学系によって、PEM33の変調周波数fで偏光状態が周期的に変化する単波長光が形成されるとともに、分光器32の選択波長が所定の波長範囲内で変更される。本実施形態では、選択波長毎に、PEM33の変調周波数で決まる周期で左/右に交替する円偏光が形成され、試料部34を照射する。
The irradiation optical system, which is composed of the
図3は、試料部34に配置される温調セルホルダー39および試料セル40の平面図である。温調セルホルダー39は、例えば、ペルチェ素子などの温度制御素子を内蔵した水冷式のセルホルダーであり、セルホルダー内の試料セル40の温度を調整し、また、温度を経時的に変化させることができる。試料セル40は、例えば、断面が矩形である内部空間を有したミクロ石英セルである。試料セル40は、蛋白質試料の状態(通常は、液体等の媒質と蛋白質との混合状態)に応じて、蛋白質試料をセル内部に保持する構成や、蛋白質試料を連続的に流す構成から適宜選択される。
Figure 3 is a plan view of the temperature-controlled cell holder 39 and sample cell 40 arranged in the
PEM33からの単波長光は、試料セル40の一方の窓板から入射し、内部の蛋白質試料を通過して、他方の窓板から出射した後、CD用の光検出器35にて検出される。
The single-wavelength light from the
<CDスペクトルの測定>
左右に交替する円偏光状態の単波長光が、蛋白質試料に含まれる円二色性の部位を透過すると、透過光の左円偏光の吸光度と右円偏光の吸光度とに差が生じる。この差は、光検出器35からの光強度信号に交流成分として表れる。信号処理部38は、PEM3の変調周波数fの参照信号を使って、光強度信号から交流成分を検知し、CD強度信号を得る。また、分光器32を駆動させて単波長光の波長を走査すると、波長に応じたCD強度信号が得られ、これによって信号処理部38はCDスペクトルデータを取得することができる。図3に、蛋白質試料のCDスペクトルデータの模式図を示す。
<Measurement of CD spectrum>
When single-wavelength light with alternating left-right circular polarization passes through a circular dichroism site contained in a protein sample, a difference occurs between the absorbance of the left-handed circularly polarized light and the absorbance of the right-handed circularly polarized light that passes through the protein sample. This difference appears as an AC component in the light intensity signal from the
試料セル40は、さらに上記の一対の窓板に直角である第三の窓板を有する。 The sample cell 40 further has a third window plate that is perpendicular to the pair of windows described above.
<蛍光スペクトルの測定>
図2のシステム構成であれば、蛍光測定において、試料部の前段の分光器32が励起光の波長を固定し、蛋白質試料からの蛍光を後段の分光器36が波長を走査することによって、蛍光スペクトルデータ(励起光波長一定)を測定することができる。また、前段の分光器32が励起光の波長を走査し、後段の分光器36が蛋白質試料から発する蛍光から一定波長の成分を選択することによって、蛍光スペクトルデータ(蛍光波長一定)を測定することもできる。
<Measurement of fluorescence spectrum>
2, in the fluorescence measurement, the
どちらの蛍光スペクトルデータを用いてもよい。ここでは、前者の場合について説明する。PEM33からの単波長光(励起光)の波長が一定、例えば280nmの状態で、その単波長光が蛋白質試料に含まれる蛍光の部位(例えば蛍光プローブ)を励起すると、蛋白質試料は蛍光を発する。その蛍光は、試料セル40の第三の窓板から出射して、蛍光用の分光器36に入って波長毎の蛍光に分散された後、光検出器37で検出される。蛍光用の分光器36を駆動させて選択波長を走査することによって、信号処理部38は、光検出器37から選択波長毎の蛍光強度信号を得て、蛍光スペクトルデータを取得することができる。図3に、蛋白質試料の蛍光スペクトルデータの模式図を示す。
Either type of fluorescence spectrum data may be used. Here, the former case will be described. When the wavelength of the single-wavelength light (excitation light) from the
なお、蛍光スペクトル測定中、PEM33を変調駆動させたままでも、変調駆動を停止させてもよい。 During fluorescence spectrum measurement, the PEM33 may be kept modulated or the modulation may be stopped.
従来、独立したCD測定機と分光蛍光測定機を使って個別にスペクトル測定する場合や、1台のCD測定機であっても、その試料部にCD用セルと蛍光用セルを独立に配置してスペクトル測定する場合などでは、2つの試料セル内の蛋白質試料の外部刺激(特に、温度)の経時的な変化を同期させることが極めて難しかった。 Conventionally, when measuring spectra separately using independent CD and spectrofluorometers, or when measuring spectra using a single CD measurement instrument with a CD cell and a fluorescence cell separately placed in the sample section, it was extremely difficult to synchronize the changes over time in external stimuli (especially temperature) of the protein sample in the two sample cells.
本実施形態では、図3の構成の試料部34を採用することで、同一の試料セル内の蛋白質試料からCDスペクトルと蛍光スペクトルの両方が測定される。つまり、1つの試料セル40によって、それぞれのスペクトルを同時に測定することができるため、2つの試料セルでの測定時のような外部刺激の「ずれ」を排除することができる。加えて、1回の測定で2つのスペクトルデータが得られるので、測定に必要な試料量を少なくすることができる。
In this embodiment, by adopting the
図4のフローチャートは、図2のシステム構成を用いた蛋白質の構造変化の評価手順(S1~S8)を示す。 The flowchart in Figure 4 shows the procedure (S1 to S8) for evaluating protein structural changes using the system configuration in Figure 2.
手順S1では、CD/蛍光測定機30の動作条件を設定する。例えば、蛍光測定では、蛋白質の三次構造の変化に反応する波長域が少なくとも含まれるように測定波長範囲を設定する。CD測定では、蛋白質の二次構造の変化に反応する波長域が少なくとも含まれるように測定波長範囲を設定する。
In step S1, the operating conditions of the CD/
手順S2では、蛋白質試料に対する外部刺激の経時的変化の条件を設定する。外部刺激として、蛋白質の温度、pH、圧力、電場、磁場、光、応力、蛋白濃度、バッファーの種類、バッファー濃度などの物理パラメータから選択可能である。本実施形態では、一例として、温調セルホルダー39を用いて、試料セル40の蛋白質試料の温度を20℃から90℃まで経時的に変化させる条件に設定する。 In step S2, the conditions for the time-dependent change of the external stimulus to the protein sample are set. The external stimulus can be selected from physical parameters such as the protein temperature, pH, pressure, electric field, magnetic field, light, stress, protein concentration, buffer type, and buffer concentration. In this embodiment, as an example, the temperature-controlled cell holder 39 is used to set the conditions for changing the temperature of the protein sample in the sample cell 40 from 20°C to 90°C over time.
手順S3では、温調セルホルダー39を上記の条件で駆動させて、外部刺激の経時的変化を発生させる。そして、蛋白質試料の温度を20℃から90℃まで経時的に変化させつつ、例えば5℃間隔の温度インターバルで、蛍光スペクトルとCDスペクトルの両方を繰り返し測定する。5℃間隔の各温度において、信号処理部38は、各光検出器35,37からの強度信号を処理し、CDスペクトルデータおよび蛍光スペクトルデータを得て、これらのデータを評価装置10に出力する。手順S3までの実行の結果、20℃、25℃、・・・、90℃の各温度で、蛍光スペクトルおよびCDスペクトルが同時に得られる。
In step S3, the temperature-controlled cell holder 39 is driven under the above conditions to generate a change in the external stimulus over time. Then, while changing the temperature of the protein sample over time from 20°C to 90°C, both the fluorescence spectrum and the CD spectrum are repeatedly measured at temperature intervals of, for example, 5°C. At each temperature interval of 5°C, the
手順S4からS8までは、コンピュータ(評価装置10)によるスペクトルデータ処理の流れを示し、手順S3まで完了した後、続けて処理を開始してもよい。或いは、外部刺激の経時的変化を共通条件にして、別のCD測定機で測定したCDスペクトルデータと、別の分光蛍光測定機で測定した蛍光スペクトルデータとをデータ保持部14に保存しておき、ユーザーの必要に応じて、コンピュータがこれらのスペクトルデータに対して評価プログラムを実行するようにしてもよい。
Steps S4 to S8 show the flow of spectral data processing by the computer (evaluation device 10), and processing may be started continuously after step S3 is completed. Alternatively, the CD spectral data measured by a different CD measuring device and the fluorescence spectral data measured by a different spectrofluorometer may be stored in the
ここでは、手順S3に続く一連の動作として、手順S4からS8までを説明する。まず、コンピュータは、信号処理部38からの各々のスペクトルデータを受信し、メモリーなどのデータ保持部14に保持する(手順S4)。ここで、コンピュータは、二次元相関スペクトルデータの適切な演算のために、データ保持部14から読み取った各スペクトルデータに対して事前に補正を加えることができる(手順S5)。
Here, steps S4 to S8 will be described as a series of operations following step S3. First, the computer receives each piece of spectral data from the
<スペクトルデータの補正内容>
蛍光スペクトルデータに対しては、励起光の高次光カット処理、ダーク補正、スペクトル補正を適宜実行する。また、CDスペクトルデータに対しては、ベースライン補正、滴定測定のときの濃度補正を適時実行する。
<Spectral data correction details>
For the fluorescence spectrum data, a high-order light cut process for the excitation light, dark correction, and spectrum correction are appropriately performed, and for the CD spectrum data, baseline correction and concentration correction during titration measurement are appropriately performed.
次に、コンピュータは、蛍光スペクトルデータの測定波長をX軸とし、CDスペクトルの測定波長をY軸として、蛍光スペクトルデータの変化およびCDスペクトルデータの変化についての二次元相関スペクトルデータを演算する(手順S6)。 Next, the computer calculates two-dimensional correlation spectrum data for the changes in the fluorescence spectrum data and the changes in the CD spectrum data, with the measurement wavelength of the fluorescence spectrum data on the X-axis and the measurement wavelength of the CD spectrum on the Y-axis (step S6).
<二次元相関スペクトルの演算>
二次元相関スペクトルは、スペクトルの経時的な変化(「動的スペクトル」とも呼ばれる。)を解析する手法として知られている。一般的な動的スペクトルデータから単に二次元相関スペクトルを演算するだけであれば、市販のソフトウェアを用いることができる。
<Calculation of two-dimensional correlation spectrum>
Two-dimensional correlation spectroscopy is known as a method for analyzing time-dependent changes in a spectrum (also called "dynamic spectrum"). If you simply need to calculate a two-dimensional correlation spectrum from general dynamic spectrum data, you can use commercially available software.
ここで、スペクトルデータの波長をλとして、動的蛍光スペクトルを(1)で表し、動的CDスペクトルを(2)で表す。 Here, the wavelength of the spectral data is λ, the dynamic fluorescence spectrum is represented by (1), and the dynamic CD spectrum is represented by (2).
任意の波長λ1,λ2で、一定の相関時間τを置いて動的蛍光スペクトル(3)と動的CDスペクトル(4)が測定されるならば、次式(5)の相互相関関数「X(τ)」を求めることができる。 If the dynamic fluorescence spectrum (3) and the dynamic CD spectrum (4) are measured at arbitrary wavelengths λ1 and λ2 with a certain correlation time τ, the cross-correlation function "X(τ)" of the following equation (5) can be obtained.
この相関関数「X(τ)」は、当該相関関数を複素数で表した際の実数部に相当する同時相関強度Φと、虚数部に相当する異時相関強度Ψとを用いて表現することもできる。同時相関強度Φと異時相関強度Ψは、2つの独立した波長λ1,λ2によって決定される二次元スペクトルである。 This correlation function "X(τ)" can also be expressed using a simultaneous correlation intensity Φ, which corresponds to the real part when the correlation function is expressed as a complex number, and an intertemporal correlation intensity Ψ, which corresponds to the imaginary part. The simultaneous correlation intensity Φ and the intertemporal correlation intensity Ψ are two-dimensional spectra determined by two independent wavelengths λ1 and λ2.
コンピュータは、最も基本的な二次元相関スペクトルである、同時相関スペクトルと異時相関スペクトルを演算し(手順S6)、演算した二次元相関スペクトルを液晶ディスプレイ等の表示手段に表示させる(手順S7)。 The computer calculates the simultaneous correlation spectrum and the different time correlation spectrum, which are the most basic two-dimensional correlation spectra (step S6), and displays the calculated two-dimensional correlation spectra on a display means such as an LCD display (step S7).
図5(A),(B)は、モニター等に表示される同時相関スペクトルΦ(λ1,λ2)と異時相関スペクトルΨ(λ1,λ2)の一例をそれぞれ模式的に示したものである。各々の相関スペクトルのピークを、その高さに応じた色の変化によって表現しているが、等高線での表示や三次元立体表示にしてもよい。 Figures 5 (A) and (B) are schematic diagrams showing examples of a simultaneous correlation spectrum Φ(λ1, λ2) and an anti-chronic correlation spectrum Ψ(λ1, λ2) displayed on a monitor or the like. The peaks of each correlation spectrum are represented by changing colors according to their height, but they may also be displayed as contour lines or in a three-dimensional display.
最後に、コンピュータは、二次元相関スペクトルに現れた正または負の交差ピークに基づいて、蛋白質試料の二次構造および三次構造の変化を評価する(手順S9)。 Finally, the computer evaluates changes in the secondary and tertiary structures of the protein sample based on the positive or negative cross peaks that appear in the two-dimensional correlation spectrum (step S9).
ここで、蛋白質試料の構造変化の評価について簡単に説明する。 Here, we briefly explain how to evaluate structural changes in protein samples.
図5(A)の同時相関スペクトルΦ(λ1,λ2)には、蛍光の波長λ11(330nm付近)とCDの波長λ21(200nm付近)との交点に正の交差ピークP11が生じている。つまり、蛍光の波長λ11とCDの波長λ21の各強度が正の方向に同時相関している。 In the simultaneous correlation spectrum Φ(λ1, λ2) in FIG. 5(A), a positive cross peak P11 occurs at the intersection of the fluorescence wavelength λ11 (near 330 nm) and the CD wavelength λ21 (near 200 nm). In other words, the intensities of the fluorescence wavelength λ11 and the CD wavelength λ21 are simultaneously correlated in the positive direction.
正の方向の同時相関(交差ピークP11)は、蛍光信号およびCD信号がいずれも減少(又は増加)する場合であり、それぞれのスペクトル強度の変化の方向性が同じであると言える。そして、330nm付近における蛍光データからはトリプトファン由来の三次構造変化が読み取られ、200-230nmにおけるCDデータからはαヘリックスの二次構造変化が読み取られる。この例では、蛋白質の二次構造(例えばαヘリックスの構造)と三次構造(例えば蛍光プローブを含んだ立体構造)がどちらも崩壊している、或いは、二次構造と三次構造がどちらも生成していることの根拠となり得る。 Positive simultaneous correlation (cross peak P11) occurs when both the fluorescence signal and the CD signal decrease (or increase), and it can be said that the direction of change in the respective spectral intensities is the same. Fluorescence data at around 330 nm indicates a tryptophan-induced tertiary structure change, while CD data at 200-230 nm indicates an α-helix secondary structure change. In this example, this can be evidence that both the protein's secondary structure (e.g., the α-helix structure) and tertiary structure (e.g., a three-dimensional structure containing a fluorescent probe) have collapsed, or that both secondary and tertiary structures have been formed.
なお、同時相関スペクトルに負の交差ピークが生じていて、蛍光スペクトルおよびCDスペクトルの各強度が負の方向に同時相関(反相関とも呼ぶ。)している場合は、蛍光信号およびCD信号の一方が減少し、同時に他方が増加する場合であり、例えば、蛋白質の二次構造と三次構造のうちの一方には変化がないが、他方には崩壊または生成といった変化が起きているということの根拠になり得る。 When a negative cross peak appears in the simultaneous correlation spectrum and the intensities of the fluorescence spectrum and CD spectrum are simultaneously correlated in the negative direction (also called anti-correlation), one of the fluorescence signal and the CD signal decreases while the other increases. This can be evidence that, for example, there is no change in one of the secondary and tertiary structures of a protein, but a change such as collapse or formation has occurred in the other.
このように、同時相関スペクトルにおける交差ピークの存在は、外部刺激の経時的変化に対する蛋白質の二次構造の変化と三次構造の変化との相互作用の可能性を示すものとして、重要な意味をもたらす。 Thus, the presence of cross peaks in the simultaneous correlation spectrum is significant as it indicates the possible interaction between changes in the secondary and tertiary structures of a protein in response to time-dependent changes in external stimuli.
一方、図5(B)の異時相関スペクトルΨ(λ1,λ2)にも、蛍光の波長λ12(330nm付近)とCDの波長λ21(200nm付近)との交点に正の交差ピークP21が生じている。つまり、蛍光の波長λ12とCDの波長λ21の各強度が正の方向に異時相関している。 On the other hand, the anisochronic correlation spectrum Ψ(λ1, λ2) in FIG. 5(B) also has a positive cross peak P21 at the intersection of the fluorescence wavelength λ12 (near 330 nm) and the CD wavelength λ21 (near 200 nm). In other words, the intensities of the fluorescence wavelength λ12 and the CD wavelength λ21 are anisochronically correlated in the positive direction.
図5(A),(B)のように、ある波長の組合せ(λ1,λ2)において、正の方向の同時相関(交差ピークP11)と正の方向の異時相関(交差ピークP21)とが生じる場合は、蛍光およびCDの変化の方向性が同じで、蛍光強度の変化が先に生じ、CD強度の変化が遅れて生じることになる。例えば、蛋白質の三次構造の変化が先に進み、これに遅れて二次構造の変化が始まることの根拠となり得る。 As shown in Figures 5 (A) and (B), when a positive synchronous correlation (cross peak P11) and a positive asymmetric correlation (cross peak P21) occur for a certain wavelength combination (λ1, λ2), the directionality of the changes in fluorescence and CD is the same, with the change in fluorescence intensity occurring first and the change in CD intensity occurring later. For example, this could be evidence that the change in the tertiary structure of a protein proceeds first, followed by the start of a change in the secondary structure.
なお、正の方向の同時相関と負の方向の異時相関とが生じる場合は、蛍光およびCDの変化の方向性が同じであるが、CD強度の変化が先に生じ、蛍光強度の変化が遅れて生じることになる。例えば、蛋白質の二次構造の変化が先に進み、これに遅れて三次構造の変化が始まることの根拠となり得る。 When positive simultaneous correlation and negative asymmetric correlation occur, the directionality of the changes in fluorescence and CD is the same, but the change in CD intensity occurs first, followed by the change in fluorescence intensity. For example, this could be the basis for the fact that changes in the secondary structure of a protein occur first, followed by changes in the tertiary structure.
つまり、蛋白質への外部刺激の経時的変化に対して、先に、蛍光の330nm付近の強度変化(三次構造の変化)が生じ、その後に、CDの200nm付近の強度変化(二次構造の変化)が生じる、という、それぞれの構造変化のタイムラグを把握することができる。外部刺激の経時的変化に対する蛋白質の二次構造、三次構造がそれぞれどのような順序で変化するのかを知ることができ、蛋白質の熱安定性評価が容易になった。 In other words, in response to a time-dependent change in an external stimulus to a protein, a change in the fluorescence intensity around 330 nm (a change in the tertiary structure) occurs first, followed by a change in the CD intensity around 200 nm (a change in the secondary structure); this allows us to grasp the time lag between these structural changes. It is now possible to determine the order in which the secondary and tertiary structures of a protein change in response to a time-dependent change in an external stimulus, making it easier to evaluate the thermal stability of a protein.
また、異時相関スペクトルにおいて交差ピークが現れていない波長の組合せは、信号強度の変化が同期している、つまり、構造変化の速さが同じであるか、又は、両方とも構造変化が生じていないことを示している。 Furthermore, combinations of wavelengths that do not show cross peaks in the cross-chronological correlation spectrum indicate that the changes in signal intensity are synchronized, meaning that the speed of structural changes is the same, or that no structural changes are occurring in both.
コンピュータの評価部72による評価内容の表示例を図5(A),(B)に示す。その他、表形式での表示や、文章での表示でもよい。 Examples of the display of the evaluation contents by the computer's evaluation unit 72 are shown in Figures 5 (A) and (B). Alternatively, the display may be in a table format or in text.
次表に、二次元相関スペクトル(Φ、Ψ)の読み取り方の一例を示す。λ1は蛍光スペクトルの波長、λ2はCDスペクトルの波長を示す。表1に基づけば、図5の二次元相関スペクトル画像を読み取れば、同じ温度変化状況において、蛋白質試料は、αヘリックスの二次構造変化(CDの変化)よりも、トリプトファン由来の三次構造変化(蛍光の変化)が先に生じたことが分かる。表1に基づく評価内容を図5の二次元相関スペクトルの画像に表示してもよい。 The following table shows an example of how to read a two-dimensional correlation spectrum (Φ, Ψ). λ1 indicates the wavelength of the fluorescence spectrum, and λ2 indicates the wavelength of the CD spectrum. Based on Table 1, by reading the two-dimensional correlation spectrum image in Figure 5, it can be seen that under the same temperature change conditions, the protein sample experienced a tryptophan-derived tertiary structure change (change in fluorescence) before a secondary structure change in the α-helix (change in CD). The evaluation results based on Table 1 may be displayed on the two-dimensional correlation spectrum image in Figure 5.
[表1]
――――――――――――――――――――――――――――――――――――――――
同時相関Φ 異時相関Ψ λ1とλ2の交差ピークにおける各スペクトル変化
――――――――――――――――――――――――――――――――――――――――
正 ほぼゼロ 蛍光とCDの変化は同方向で同時に起こる
正 正 蛍光とCDの変化は同方向で蛍光はCDより先に起こる
正 負 蛍光とCDの変化は同方向で蛍光はCDより後に起こる
負 ほぼゼロ 蛍光とCDの変化は異方向で同時に起こる
負 正 蛍光とCDの変化は異方向で蛍光はCDより後に起こる
負 負 蛍光とCDの変化は異方向で蛍光はCDより先に起こる
――――――――――――――――――――――――――――――――――――――――
[Table 1]
----------------------------------------------------------------------------------
Simultaneous correlation Φ Antichronic correlation Ψ Spectral changes at the cross peaks of λ1 and λ2 ------------------------------------------------
Positive Almost zero The changes in fluorescence and CD occur simultaneously in the same direction. Positive Positive The changes in fluorescence and CD occur in the same direction, with fluorescence occurring before CD. Positive Negative The changes in fluorescence and CD occur in the same direction, with fluorescence occurring after CD. Negative Almost zero The changes in fluorescence and CD occur simultaneously in different directions. Negative Positive The changes in fluorescence and CD occur in different directions, with fluorescence occurring after CD. Negative Negative The changes in fluorescence and CD occur in different directions, with fluorescence occurring before CD.------------------------------------------------
抗体医薬開発などの分野では、蛋白質の温度変化依存の構造変化を適切に把握することが、製品開発、製造工程の確立および品質管理の上で、重要な事項になっている。本実施形態では、蛋白質の二次構造と三次構造の変化をモニタリングして、蛋白質の構造変化の評価が簡易になったため、蛋白質に付与される機能部位の効果の確認や変異の有無の把握をする上での重要な情報が容易に得られるようになった。昨今の目的部位をデザインするという抗体医薬分野での幅広い活用が期待される。 In fields such as antibody drug development, properly understanding temperature-dependent structural changes in proteins is an important issue in product development, establishment of manufacturing processes, and quality control. In this embodiment, changes in the secondary and tertiary structures of proteins are monitored, making it easy to evaluate structural changes in proteins, and therefore important information for confirming the effects of functional sites imparted to proteins and determining the presence or absence of mutations can be easily obtained. This is expected to be widely used in the field of antibody drugs, where target sites are designed these days.
第二実施形態
図6は、複数の蛋白質試料の二次元相関スペクトルデータを画像として、コンピュータが画像用の主成分分析を実行することを示した図である。本実施形態では、第一実施形態のシステム(図2)を用いており、図3の温調セルホルダー39として、6連温調セルチェンジャー(水冷ペルチェ素子内蔵)を用いることで、6検体のスペクトル測定を同時に実行、または順次実行できるように構成されている。また、評価装置10が画像用の主成分分析を実行する。
Second embodiment Fig. 6 is a diagram showing that a computer performs principal component analysis for images using two-dimensional correlation spectrum data of a plurality of protein samples as images. In this embodiment, the system of the first embodiment (Fig. 2) is used, and a six-stage temperature-controlled cell changer (with built-in water-cooled Peltier element) is used as the temperature-controlled cell holder 39 in Fig. 3, so that spectrum measurements of six samples can be performed simultaneously or sequentially. In addition, the
例えば、バイオ医薬品の開発段階で、ネイティブの蛋白質からなる1検体と、何らかの機能基がそれぞれ異なる条件で付与された5検体とを用いて、蛋白質に機能基を付与したことによる影響の有無を確認するケースについて説明する。 For example, we will explain a case in which, during the development stage of a biopharmaceutical, one sample consisting of a native protein and five samples to which some functional group has been added under different conditions are used to confirm whether or not there is any effect due to the addition of a functional group to the protein.
まず、温度変化条件の下、本実施形態のシステムを用いて、これら6検体の蛍光スペクトルデータおよびCDスペクトルデータを取得し、6セットの二次元相関スペクトルデータを得る(図6(A))。そして、これら6セットの二次元相関スペクトル(同時相関スペクトル,異時相関スペクトル)を画像データとして、これらの画像の主成分分析を実行する。この画像分析には、市販の画像用の主成分分析ソフトウェアを用いることができる。 First, under temperature change conditions, the system of this embodiment is used to acquire the fluorescence spectrum data and CD spectrum data of these six samples, and six sets of two-dimensional correlation spectrum data are obtained (FIG. 6(A)). Then, these six sets of two-dimensional correlation spectra (synchronous correlation spectrum, different-time correlation spectrum) are used as image data to perform principal component analysis of these images. For this image analysis, commercially available principal component analysis software for images can be used.
画像についての主成分分析の結果、6検体をグループ分けすることができる。図6(B)は、画像データの第1主成分(PC1)と画像データの第2主成分(PC2)を用いた例である。例えば、ネイティブの蛋白質の異時相関スペクトル画像に対する、他の検体の異時相関スペクトル画像の一致性/不一致性の結果から、6検体をグルーピングすることができる。異時相関スペクトル画像について、同じグループに属することになった検体を、さらに、同時相関スペクトル画像の主成分分析結果に基づいて、細かくグループ分けすることもできる。 As a result of the principal component analysis of the images, the six samples can be divided into groups. FIG. 6(B) shows an example using the first principal component (PC1) of the image data and the second principal component (PC2) of the image data. For example, the six samples can be grouped based on the results of the match/mismatch between the metachronic correlation spectral image of a native protein and the metachronic correlation spectral image of another sample. Samples that belong to the same group in the metachronic correlation spectral image can also be further divided into finer groups based on the results of the principal component analysis of the simultaneous correlation spectral image.
図6(B)の例では、グループ1にはネイティブの検体(No.1)を含む複数の検体が含まれている。これらの検体は、ネイティブとの一致性が高く、蛋白質の構造変化が起こっていないことを示す判断の根拠に使える。 In the example of Figure 6 (B), group 1 contains multiple samples, including a native sample (No. 1). These samples are highly consistent with the native sample and can be used as a basis for determining that no structural changes have occurred in the protein.
なお、温度変化条件のケースでは、図3のような試料セルを用いて、2種類のスペクトル測定を同時に行うことで、2種類のスペクトル測定の実行時に蛋白質試料の温度条件を一致させることができるというメリットがある。しかし、蛍光測定およびCD測定を別々に実行する場合でも、それぞれの蛋白質試料の温度変化を一致させることが可能であれば、2種類のスペクトルの同時測定は必須にはならない。 In the case of temperature change conditions, using a sample cell like that shown in Figure 3 to simultaneously perform two types of spectrum measurements has the advantage that the temperature conditions of the protein sample can be matched when performing the two types of spectrum measurements. However, even if fluorescence measurement and CD measurement are performed separately, simultaneous measurement of two types of spectra is not essential as long as it is possible to match the temperature changes of each protein sample.
CD測定機と蛍光測定機を用いて、2種類のスペクトルを測定する場合にも、本発明の評価手法を適用できる。 The evaluation method of the present invention can also be applied when measuring two types of spectra using a CD measuring device and a fluorescence measuring device.
10 評価装置(コンピュータ)
12 データ受信部(受信手段)
18 演算部(二次元相関スペクトルの演算手段)
20 表示指令部(表示指令手段)
22 評価部(蛋白質試料の構造変化を評価する評価手段)
24 表示装置(表示手段)
30 CD/蛍光測定機
34 試料部
38 信号処理部
39 温調セルホルダー(6連温調セルチェンジャー)
40 試料セル
10 Evaluation device (computer)
12 Data receiving unit (receiving means)
18 Calculation unit (means for calculating two-dimensional correlation spectrum)
20 Display command unit (display command means)
22 Evaluation unit (evaluation means for evaluating structural changes in a protein sample)
24 Display device (display means)
30 CD/
40 Sample cell
Claims (6)
前記外部刺激の変化中の複数のタイミングにおいて蛍光スペクトル測定およびCDスペクトル測定を実行する手順と、
蛍光スペクトルの測定波長をX軸とし、CDスペクトルの測定波長をY軸として、測定された蛍光スペクトルおよびCDスペクトルの各々の経時的変化についての二次元相関スペクトルである同時相関スペクトルおよび異時相関スペクトルを演算する手順と、
前記同時相関スペクトルおよび異時相関スペクトルを画像データとして表示手段に表示する手順と、
前記同時相関スペクトルおよび異時相関スペクトルに現れる正または負のピークに基づいて、蛋白質試料の二次構造および三次構造の変化の相関を評価する手順と、
を含むことを特徴とする蛋白質の構造変化の評価方法。 A procedure for changing an external stimulus to a protein sample over time;
performing fluorescence spectrum measurement and CD spectrum measurement at a plurality of timings during a change in the external stimulus;
a step of calculating a simultaneous correlation spectrum and an anti-chronic correlation spectrum, which are two-dimensional correlation spectra for the time-dependent changes of the measured fluorescence spectrum and CD spectrum, with the measurement wavelength of the fluorescence spectrum as the X-axis and the measurement wavelength of the CD spectrum as the Y-axis;
displaying the simultaneous correlation spectrum and the cross-time correlation spectrum as image data on a display means;
evaluating correlations of changes in the secondary and tertiary structures of the protein sample based on positive or negative peaks appearing in the simultaneous correlation spectrum and the different time correlation spectrum ;
A method for evaluating a structural change of a protein, comprising:
前記外部刺激としては、温度、pH、圧力、電場、磁場、光、応力、蛋白濃度、バッファーの種類、バッファー濃度のいずれかであることを特徴とする蛋白質の構造変化の評価方法。 The method for evaluating a structural change of a protein according to claim 1,
The method for evaluating a structural change of a protein, wherein the external stimulus is any one of temperature, pH, pressure, an electric field, a magnetic field, light, stress, protein concentration, a type of buffer, and a buffer concentration.
[表1]
――――――――――――――――――――――――――――――――――――――――
同時相関Φ 異時相関Ψ λ1とλ2の交差ピークにおける各スペクトル変化
――――――――――――――――――――――――――――――――――――――――
正 ほぼゼロ 蛍光とCDの変化は同方向で同時に起こる
正 正 蛍光とCDの変化は同方向で蛍光はCDより先に起こる
正 負 蛍光とCDの変化は同方向で蛍光はCDより後に起こる
負 ほぼゼロ 蛍光とCDの変化は異方向で同時に起こる
負 正 蛍光とCDの変化は異方向で蛍光はCDより後に起こる
負 負 蛍光とCDの変化は異方向で蛍光はCDより先に起こる
――――――――――――――――――――――――――――――――――――――――
λ1:蛋白質の三次構造の変化に反応する蛍光スペクトルの波長
λ2:蛋白質の二次構造の変化に反応するCDスペクトルの波長 3. The method for evaluating a structural change in a protein according to claim 1, wherein the correlation between the changes in the secondary structure and the tertiary structure of the protein sample is evaluated as shown in Table 1.
[Table 1]
----------------------------------------------------------------------------------
Simultaneous correlation Φ Cross-correlation Ψ Spectral changes at the cross peaks of λ1 and λ2
----------------------------------------------------------------------------------
Positive almost zero fluorescence and CD changes occur simultaneously in the same direction
The changes in fluorescence and CD are in the same direction, and fluorescence occurs before CD.
The positive and negative fluorescence and CD changes are in the same direction, and fluorescence occurs after CD.
Negative near-zero fluorescence and CD changes occur simultaneously in different directions
The changes in negative and positive fluorescence and CD are in opposite directions, and fluorescence occurs after CD.
The changes in fluorescence and CD are in opposite directions, and fluorescence occurs before CD .
----------------------------------------------------------------------------------
λ1: wavelength of the fluorescence spectrum that responds to changes in the tertiary structure of the protein
λ2: wavelength of the CD spectrum that responds to changes in the secondary structure of the protein
複数の蛋白質試料について、試料毎に前記二次元相関スペクトルを画像データとして取得し、これらの画像データに対して、画像用の主成分分析を実行することを特徴とする蛋白質の構造変化の評価方法。 The method for evaluating a structural change of a protein according to any one of claims 1 to 3 ,
A method for evaluating structural changes in a protein, comprising obtaining the two-dimensional correlation spectrum as image data for each of a plurality of protein samples, and performing image principal component analysis on the image data.
蛍光スペクトルの測定波長をX軸とし、CDスペクトルの測定波長をY軸として、前記蛍光スペクトルおよび前記CDスペクトルの各々のデータの経時的変化についての二次元相関スペクトルである同時相関スペクトルおよび異時相関スペクトルを演算する演算手段と、
前記同時相関スペクトルおよび異時相関スペクトルを画像データとして表示手段に表示させる表示指令手段と、
前記同時相関スペクトルおよび異時相関スペクトルに現れる正または負のピークに基づいて、蛋白質試料の二次構造および三次構造の変化の相関を評価する評価手段と、
を備えることを特徴とする蛋白質の構造変化の評価装置。 a receiving means for receiving, as data, fluorescence spectra and CD spectra measured at a plurality of timings during the change in an external stimulus applied to a protein sample over time;
a calculation means for calculating a simultaneous correlation spectrum and an intertemporal correlation spectrum, which are two-dimensional correlation spectra regarding the time-dependent changes in data of the fluorescence spectrum and the CD spectrum, with the measurement wavelength of the fluorescence spectrum being the X-axis and the measurement wavelength of the CD spectrum being the Y- axis;
a display command means for causing a display means to display the simultaneous correlation spectrum and the cross-time correlation spectrum as image data;
an evaluation means for evaluating the correlation between changes in the secondary structure and the tertiary structure of the protein sample based on positive or negative peaks appearing in the simultaneous correlation spectrum and the different time correlation spectrum ;
An apparatus for evaluating a structural change in a protein, comprising:
蛍光スペクトルの測定波長をX軸とし、CDスペクトルの測定波長をY軸として、測定された前記蛍光スペクトルおよび前記CDスペクトルの各々の経時的変化についての二次元相関スペクトルである同時相関スペクトルおよび異時相関スペクトルを演算する演算手段と、
前記同時相関スペクトルおよび異時相関スペクトルを画像データとして表示手段に表示させる表示指令手段と、
前記同時相関スペクトルおよび異時相関スペクトルに現れる正または負のピークに基づいて、蛋白質試料の二次構造および三次構造の変化の相関を評価する評価手段と、してコンピュータを機能させることを特徴とする蛋白質の構造変化の評価プログラム。 a receiving means for receiving, as data, fluorescence spectra and CD spectra measured at a plurality of timings during the change in an external stimulus applied to a protein sample over time;
a calculation means for calculating a simultaneous correlation spectrum and an intertemporal correlation spectrum, which are two-dimensional correlation spectra regarding the time-dependent changes of the measured fluorescence spectrum and the measured CD spectrum, with the measurement wavelength of the fluorescence spectrum being the X-axis and the measurement wavelength of the CD spectrum being the Y-axis ;
a display command means for causing a display means to display the simultaneous correlation spectrum and the cross-time correlation spectrum as image data;
A program for evaluating structural changes in proteins, which causes a computer to function as an evaluation means for evaluating the correlation between changes in the secondary structure and tertiary structure of a protein sample based on positive or negative peaks appearing in the simultaneous correlation spectrum and the different time correlation spectrum.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020104065A JP7499503B2 (en) | 2020-06-16 | 2020-06-16 | Method, device and program for evaluating protein structural changes |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020104065A JP7499503B2 (en) | 2020-06-16 | 2020-06-16 | Method, device and program for evaluating protein structural changes |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021196301A JP2021196301A (en) | 2021-12-27 |
| JP7499503B2 true JP7499503B2 (en) | 2024-06-14 |
Family
ID=79198200
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020104065A Active JP7499503B2 (en) | 2020-06-16 | 2020-06-16 | Method, device and program for evaluating protein structural changes |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7499503B2 (en) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4162851A (en) | 1978-03-29 | 1979-07-31 | Akiyoshi Wada | Simultaneous photometering method and assembly for multi-dimensional measurements concerning biologically related materials |
| JP2006507481A (en) | 2002-08-16 | 2006-03-02 | ファルマシア・アンド・アップジョン・カンパニー・エルエルシー | Isoform-specific interaction of apolipoprotein E with the intermediate conformation of Alzheimer Aβ peptide |
| JP2008512349A (en) | 2004-06-25 | 2008-04-24 | ピーディーエル バイオファーマ,インコーポレイティド | Stable liquid and lyophilized formulations of proteins |
| JP2010248266A (en) | 2001-11-27 | 2010-11-04 | Board Of Trustees Of The Univ Of Illinois | Materials and methods for producing improved micelle compositions |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5342790A (en) * | 1976-09-29 | 1978-04-18 | Akimitsu Wada | Simultaneous photometry system for multiidimensional measurement of living substance |
-
2020
- 2020-06-16 JP JP2020104065A patent/JP7499503B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4162851A (en) | 1978-03-29 | 1979-07-31 | Akiyoshi Wada | Simultaneous photometering method and assembly for multi-dimensional measurements concerning biologically related materials |
| JP2010248266A (en) | 2001-11-27 | 2010-11-04 | Board Of Trustees Of The Univ Of Illinois | Materials and methods for producing improved micelle compositions |
| JP2006507481A (en) | 2002-08-16 | 2006-03-02 | ファルマシア・アンド・アップジョン・カンパニー・エルエルシー | Isoform-specific interaction of apolipoprotein E with the intermediate conformation of Alzheimer Aβ peptide |
| JP2008512349A (en) | 2004-06-25 | 2008-04-24 | ピーディーエル バイオファーマ,インコーポレイティド | Stable liquid and lyophilized formulations of proteins |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021196301A (en) | 2021-12-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8526002B2 (en) | Two-dimensional fourier transform spectrometer | |
| Saudagar et al. | Advanced spectroscopic methods to study biomolecular structure and dynamics | |
| Gratton et al. | Multiphoton fluorescence microscopy | |
| Miles et al. | Circular dichroism spectroscopy for protein characterization: biopharmaceutical applications | |
| JP5057377B2 (en) | Method and apparatus for measuring biological components or their functions | |
| JPH10332533A (en) | Birefringence evaluation system | |
| JP7057349B2 (en) | Methods and equipment for detecting process parameters in liquid media | |
| Clarke | Circular dichroism in protein folding studies | |
| Quaroni | Infrared microscopy in the study of cellular biochemistry | |
| JP7499503B2 (en) | Method, device and program for evaluating protein structural changes | |
| US20080106733A1 (en) | Methods for visualizing crystals and distinguishing crystals from other matter within a biological sample | |
| Mendonça et al. | Comparative study of the folding/unfolding dynamics of poly (glutamic acid) in light and heavy water | |
| JP2011203097A (en) | Analysis method and analyzer | |
| JPS6127703B2 (en) | ||
| WO2006085606A1 (en) | Circular dichroic thermal lens microscope | |
| Lakowicz et al. | Fluorescence lifetime imaging of Ca2+ using visible wavelength excitation and emission | |
| WO2016009548A1 (en) | Optical analysis device | |
| Ohba et al. | Microscopic imaging of phase separation in giant liposome by using laurdan at video rate | |
| WO2011050760A1 (en) | A method for obtaining structural and functional information on proteins, based on polarization fluorescence microscopy, and a device implementing said method | |
| Horvath et al. | Toll-like receptor interactions imaged by FRET microscopy and GFP fragment reconstitution | |
| Vinogradov et al. | Two-Dimensional Infrared Spectroscopy of Nitrile Labels as a Tool to Probe Dynamics and Interactions in Lipid Membranes | |
| Gordon | Anisotropy Resolved Multidimensional Emission Spectroscopy (ARMES) as a tool for biophysical analysis | |
| Demeler et al. | Integrative biophysical characterization of molecular interactions: A case study with the sfGFP–nanobody complex | |
| Kerian | Polarization-dependent nonlinear optical microscopy methods for the analysis of crystals and biological tissues | |
| How | How to Analyze Protein Structure Using Circular Dichroism Spectroscopy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230526 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240305 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240425 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240514 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240528 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7499503 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |