本出願は、2018年7月20日に出願された米国特許出願第62/701,313号に対する優先権を主張するものであり、その開示は参照によりその全体が本明細書に組み込まれている。
定義
本開示において使用される以下の用語は、別段の記載がない限り、以下の意味を有するものと理解すべきである。用語が欠落している場合、当業者に公知の従来の用語が優先される。
また、本明細書の本文、スキーム、実施形態、及び表に記載されている炭素及びヘテロ原子は、原子価を満足するのに十分な数の水素原子を有すると仮定されていることにも注意すべきである。
本明細書に記載されるように、本開示の化合物は、本明細書に一般的に例示されるような、又は本開示の特定のクラス、サブクラス、及び種によって例示されるような、1つ以上の置換基で任意に置換されていてもよい。一般に、「置換された」という用語は、所定の構造中の水素原子を所定の置換基で置換することを意味する。本開示によって想起される置換基の組み合わせは、典型的には、安定な化合物又は化学的に実行可能な化合物の形成をもたらすものである。
本明細書で使用されるように、「含む」、「含有する」、及び「構成する」という用語は、その開放的で非限定的な意味で使用される。
本開示で使用されるような冠詞「a」及び「an」は、冠詞の文法的対象の1つ又は複数(すなわち、少なくとも1つ)を指すことができる。一例として、「ある要素」は、1つの要素を意味してもよいし、1つ以上の要素を意味してもよい。
本開示で使用される「及び/又は」という用語は、特に記載がない限り、「及び」又は「又は」のいずれかを意味する場合がある。
より簡潔な説明を提供するために、本明細書で与えられた量的表現のいくつかは、「約」という用語で修飾されていない。「約」という用語が明示的に使用されているか否かにかかわらず、本明細書で与えられるすべての量は、実際の与えられた値を指すことを意味し、また、そのような与えられた値についての実験及び/又は測定条件による等価物及び近似値を含む、当技術分野の通常の熟練度に基づいて合理的に推論され、そのような与えられた値への近似値を指すことを意味することが理解される。収率が百分率として与えられる場合は常に、そのような収率は、特定の化学量論的条件下で得ることができる同じ実体の最大量に関してその収率が与えられる実体の質量を指す。濃度がパーセンテージで示されているものは、別段の表示がない限り、質量比を示している。
「患者」又は「被験者」は、哺乳類及び非哺乳類の両方を包含することができる。哺乳類の例としては、マンマリアクラスの任意のメンバーを含むことができるが、これらに限定されない:ヒト;チンパンジー、サル、ヒヒ、又はアカゲザルのような非ヒト霊長類、及び他の類人猿及びサルの種;ウシ、ウマ、ヒツジ、ヤギ、及びブタのような農場動物;ウサギ、イヌ、及びネコのようなコンパニオン動物;ラット、マウス、及びモルモットのような齧歯類を含む実験動物;及びそのようなものが挙げられる。非哺乳類の例としては、鳥類、魚類などが挙げられるが、これらに限定されない。「患者」又は「被験者」は、ヒト及び動物の両方を含むことができる。いくつかの実施形態において、患者又は被験者はヒトである。
用語「阻害剤」は、特定の生物学的活性を阻害する、又はそうでなければ妨害する化合物、薬剤、酵素、又はホルモンなどの分子を指す場合がある。
1つ以上の化合物又は医薬組成物に関連して使用される場合、「有効量」又は「処置上有効量」という用語は、所望の生物学的結果を提供するのに十分な量の1つ以上の化合物又は医薬組成物を指すことができる。その結果は、疾患の徴候、症状、又は原因の減少及び/又は緩和、又は生物学的システムの他の任意の所望の改変であり得る。例えば、処置的使用のための「有効量」は、臨床的に有意な疾患の減少を提供するために必要な、本明細書に開示されているような、1種以上の化合物、又は薬学的に許容される塩、プロドラッグ、溶媒和物、水和物、異性体、プロドラッグ、及びそれらの互変異性体からなる医薬組成物の量であってもよい。個々の場合における適切な「有効量」は、日常的な実験を用いて当業者が決定し得る。したがって、「有効量」という表現は、一般に、活性物質が処置効果を有する量を指すことができる。本実施形態では、活性物質は、インフラマソームの阻害剤であってもよい。
本明細書で使用されるように、用語「処置」又は「処置」は、疾患の発症を延期すること、疾患の発症を防止すること、及び/又は発症するか又は発症すると予想されるそのような症状の重症度を軽減することを意味する。したがって、これらの用語は、既存の疾患の症状を改善すること;追加の症状を予防すること;症状の根本的な原因を改善又は予防すること;疾患を抑制すること、例えば、疾患の発生を阻止すること;疾患を緩和すること;疾患の退行を引き起こすこと;疾患によって引き起こされた症状を緩和すること;又は疾患の症状を停止又は緩和することを含み得る。
「薬学的に許容される」又は「薬理学的に許容される」という用語は、生物学的に、又はそうでなければ望ましくないものではない材料を指すことがあり、材料は、実質的に望ましくない生物学的効果を引き起こすことなく、又はそれが含まれる組成物のいずれかの成分と劇症的な方法で相互作用することなく、個人に投与することができ、その材料は、その組成物のいずれかの成分と相互作用してもよい。
本開示で使用されるように、「担体」という用語は、担体、賦形剤、及び希釈剤を包含し、材料、組成物又はビヒクル(液体又は固体充填剤など)、希釈剤、賦形剤、溶媒、又はカプセル化材料を意味し得る。本開示の医薬製剤(例えば、1種以上の化合物)、又は薬学的に許容される塩、プロドラッグ、水和物、水和物、異性体、プロドラッグ、及びそれらの互変異性体であり、1つの器官又は体の一部分から、被験体の別の器官又は体の一部分へ運ぶこと、又は輸送することに関与する。担体は、適合性及び所望の投与形態の放出プロファイル特性に基づいて選択されるべきである。例示的な担体材料は、例えば、結合剤、懸濁剤、崩壊剤、充填剤、界面活性剤、可溶化剤、安定化剤、滑沢剤、湿潤剤、希釈剤、噴霧乾燥分散液などを含むことができる。例えば、Hoover,John E.,Remington’s Pharmaceutical Sciences,Mack Publishing Co.,Easton,Paを参照のこと。
本明細書で使用される「IC50」という用語は、測定可能な活性、表現型又は応答、例えば腫瘍細胞などの細胞の増殖又は増殖が50%阻害される濃度を指すことができる。IC50値は、適切な用量反応曲線から、例えば目視によって、又は適切なカーブフィッティングもしくは統計ソフトウェアを使用することによって推定することができる。より正確には、IC50値は、非線形回帰分析を用いて決定されてもよい。
本開示で使用される「投与される」、「投与」、又は「投与する」という用語は、1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、又は本開示の医薬組成物を被験体に直接投与することのいずれかを指すことができる。
本明細書で使用されるように、「アルキル」は、1-10個の炭素原子を有する直鎖又は分岐飽和鎖を意味してもよい。代表的な飽和アルキル基としては、以下が挙げられるが、これらに限定されない:メチル、エチル、n-プロピル、イソプロピル、2-メチル-1-プロピル、2-メチル-2-プロピル、2-メチル-1-ブチル、3-メチル-1-ブチル、2-メチル-3-ブチル、2,2-ジメチル-1-プロピル、2-メチル-1-ペンチル、3-メチル-1-ペンチル、4-メチル-1-ペンチル、2-メチル-2-ペンチル、3-メチル-2-ペンチル、4-メチル-2-ペンチル、2,2-ジメチル-1-ブチル、3,3-ジメチル-1-ブチル、2-エチル-1-ブチル、ブチル、イソブチル、t-ブチル、n-ペンチル、イソペンチル、ネオペンチル、n-ヘキシル等の長鎖アルキル基や、ヘプチル、オクチル等の長鎖アルキル基。アルキル基は、非置換型又は置換型であり得る。3個以上の炭素原子を含有するアルキル基は、直鎖又は分枝鎖であり得る。本明細書中で使用する場合、「低級アルキル」とは、1~6個の炭素原子を有するアルキルを意味する。
本明細書で使用されるように、「アルケニル」は、2-12個の炭素原子を含む非分枝状又は分岐状の炭化水素鎖を含むことができる。「アルケニル」基は、少なくとも1つの二重結合を有する。アルケニル基の二重結合は、非共役であるか、又は他の不飽和基に共役することができる。アルケニル基の例としては、エチレン、ビニル、アリル、ブテニル、ペンテニル、ヘキセニル、ブタジエニル、ペンタジエニル、ヘキサジエニル、2-エチルヘキセニル、2-プロピル-2-ブテニル、4-(2-メチル-3-ブテン)-ペンテニル等を挙げることができるが、これらに限定されるものではない。アルケニル基は、非置換型又は置換型であり得る。本明細書中で定義するアルケニルはまた、分枝鎖又は直鎖であり得る。
本明細書で使用されるように、「アルキニル」は、2-12個の炭素原子を含む、分岐していない又は分岐した不飽和炭化水素鎖を含むことができる。「アルキニル」基は少なくとも1つの三重結合を有する。アルキニル基の三重結合は、非共役であるか、又は他の不飽和基に共役することができる。アルキニル基の例として、エチニル、プロピニル、ブチニル、ペンチニル、ヘキシニル、メチルプロピニル、4-メチル-1-ブチニル、4-プロピル-2-ペンチニル、4-ブチル-2-ヘキシニルなどが挙げられるが、これらに限定されない。アルキニル基は、非置換型又は置換型であり得る。
「ハロ」又は「ハロゲン」という用語は、フッ素、塩素、臭素、又はヨウ素を指す。
用語「ハロアルキル」とは、前記で定義されているように、1つ以上のハロラジカルによって置換されているアルキルラジカルを指す:例えばトリフルオロメチル、ジフルオロメチル、フルオロメチル、トリクロロメチル、2,2,2,2-トリフルオロエチル、1,2-ジフルオロエチル、3-ブロモ-2-フルオロプロピル。
1,2-ジブロモエチルなど。
本明細書に記載された環系(例えば、シクロアルキル、シクロアルケニル、アリール、ヘテロシクリル、及びヘテロアリール)に関連する用語と併せて使用される「環原子(annular atoms)」という用語は、系内に存在する環内原子(ring atoms)の総数を指す。したがって、「環原子」には、環に結合している置換基に存在する原子は含まれない。したがって、「環原子」の数は、縮合環に存在するすべての原子を含む。例えば、2-インドリル環
は、5員ヘテロアリールと考えられるが、9個の環原子を含むヘテロアリールでもある。別の例では、ピリジンは、6員ヘテロアリールと考えられ、6個の環原子を含むヘテロアリールである。
「シクロアルキル」とは、例えば3-20個の環炭素原子(すなわち、C
3-C
20シクロアルキル)を有する単一の飽和全炭素環を意味し、例えば3-15個の環炭素原子、例えば3-15個の環炭素原子を有する。いくつかの実施形態において、シクロアルキル基は、単環式(「単環式シクロアルキル」)であるか、又は二環式システム(「二環式シクロアルキル」)のような縮合環系、架橋環系又はスピロ環系を含み、飽和していてもよい。「シクロアルキル」は、前記で定義されているように、シクロアルキル環が、1つ以上のシクロアルキル基、シクロアルケニル基、ヘテロシクリル基、アリール基又はヘテロアリール基と融合している環系を含み、ここで、付着点がシクロアルキル環上にあり、そのような実施形態では、言及されている炭素原子の数は、付着点を含むシクロアルキル環中の炭素数を指定し続ける。シクロアルキル基の例としては、シクロヘキシル、シクロヘプチル、2-アダマンチル
2-(2,3-ジヒドロ-1H-インデン)
9-フルオレニル
等が挙げられる。上述したように、シクロアルキル環は、環原子の数によってさらに特徴付けることができる。例えば、シクロヘキシル環は環原子が6個のC
6シクロアルキル環であり、2-(2,3-ジヒドロ-1H-インデン)は環原子が9個のC
5シクロアルキル環である。また、例えば、9-フルオレニルは環原子数13のC
5シクロアルキル環であり、2-アダマンチルは環原子数10のC
6シクロアルキル環である。
いくつかの実施形態において、C3-C10シクロアルキルは、3-14個の環原子を有する。いくつかの実施形態において、C3-C10シクロアルキルは、3-10個の環原子を有する。いくつかの実施形態において、
C3-C10シクロアルキルは、3-12個の環原子を有する。いくつかの実施形態において、C3-C7シクロアルキルは
3-7個の環原子を有する。いくつかの実施形態において、C3-C9シクロアルキルは、3-14個の環原子を有する。いくつかの実施形態において、C3-C9シクロアルキルは、3-10個の環原子を有する。いくつかの実施形態において、
C3-C9シクロアルキルは、3-9個の環原子を有する。いくつかの実施形態において、C3-C8シクロアルキルは
3-8個の環原子を有する。いくつかの実施形態において、C3-C8シクロアルキルは、3-14個の環原子を有する。いくつかの実施形態において、C3-C7シクロアルキルは、3-14個の環原子を有する。いくつかの実施形態において、
C3-C7シクロアルキルは、3-10個の環原子を有する。いくつかの実施形態において、C3-C7シクロアルキルは3-7個の環原子を有する。
本明細書で使用されるように、用語「シクロアルケニル」は、部分的に飽和した、単環式、融合した、又はスピロ多環式の、環当たり3-18個の炭素原子を有する全炭素環を指してもよく、少なくとも1つの二重結合を含む。「シクロアルケニル」は、前記で定義されているように、シクロアルケニル環が、1つ以上のシクロアルキル基、シクロアルケニル基、ヘテロシクリル基、アリール基又はヘテロアリール基と融合している環系を含み、ここで、付着点がシクロアルケニル環上にあり、そのような実施形態において、言及されている炭素原子の数は、付着点を含むシクロアルケニル環中の炭素の数を指定し続ける。シクロアルケニル環は、環原子の数によってさらに特徴付けることができる。シクロアルケニルの例としては、1-シクロヘキサ-1-エニル、シクロペンタ-1-エニル等が挙げられる。
いくつかの実施形態において、シクロアルケニルは3-14個の環原子を有する。いくつかの実施形態において、シクロアルケニルは3-10個の環原子を有する。いくつかの実施形態において、シクロアルケニルは3-9個の環原子を有する。いくつかの実施形態において、シクロアルケニルは3-7個の環原子を有する。いくつかの実施形態において、C3-C10シクロアルケニルは、3-14個の環原子を有する。いくつかの実施形態において、C3-C10シクロアルケニルは、3-10個の環原子を有する。いくつかの実施形態において、C3-C9シクロアルケニルは、3-9個の環原子を有する。いくつかの実施形態において、C3-C8シクロアルケニルは、3-8個の環原子を有する。いくつかの実施形態において、C3-C8シクロアルケニルは、3-14個の環原子を有する。いくつかの実施形態において、C3-C7シクロアルケニルは、3-14個の環原子を有する。いくつかの実施形態において、C3-C7シクロアルケニルは、3-10個の環原子を有する。いくつかの実施形態において、C3-C7シクロアルケニルは、3-7個の環原子を有する。
本明細書で使用される「アリール」という用語は、単一の全炭素芳香環又は環の少なくとも1つが芳香族である複数の縮合全炭素環系を指す。例えば、いくつかの実施形態において、アリール基は、5-20個の環炭素原子、5-14個の環炭素原子、又は5-12個の環炭素原子を有する。アリールは、少なくとも1つの環が芳香族であり、他の環が芳香族であっても、芳香族でなくてもよい(すなわち、炭素環)、約9~20個の炭素原子を有する多重縮合環系(例えば、2、3又は4つの環を含む環系)も含む。「アリール」は、前記で定義されているように、アリール環が、1つ以上のシクロアルキル基、シクロアルケニル基、ヘテロシクリル基、アリール基又はヘテロアリール基と融合している環系を含み、ここで、付着点がアリール環上にあり、そのような実施形態において、言及されている炭素原子の数は、付着点を含むアリール環中の炭素原子の数を指定し続ける。アリール基の例としては、以下が挙げられる:フェニル、5-(2,3-ジヒドロ-1H-インデン):
上述したように、アリール環は、環原子の数によってさらに特徴付けることができる。例えば、フェニルは6個の環原子を有するC
6アリールであり、5-(2,3-ジヒドロ-1H-インデン)は9個の環原子を有するC
6アリールである。
いくつかの実施形態において、アリール環は、6-14個の環原子を有するC6-アリールである。いくつかの実施形態において、アリール環は、6-10個の環原子を有するC6アリールである。いくつかの実施形態において、アリール環は、6-12個の環原子を有するC6アリールである。いくつかの実施形態において、アリール環は、6個の環原子を有するC6アリールである。
本明細書で使用される「ヘテロシクリル」とは、単一の飽和又は部分的に不飽和の非芳香族環又は非芳香族多重環系であって、環内に少なくとも1つのヘテロ原子(酸素、窒素及び硫黄から選択される少なくとも1つの環ヘテロ原子)を有するものを意味する。特に指定しない限り、ヘテロシクリル基は、5個から約20個の環原子、例えば5個から約15個の環原子、例えば5個から約10個の環原子を有する。したがって、用語は、約1から約6個の環炭素原子を有する単一の飽和又は部分的に不飽和の環(例えば、3、4、5、6、又は7員環)と、環中の酸素、窒素、及び硫黄からなる群から選択される約1から約3個の環ヘテロ原子とを含む。本用語はまた、約4から約9個の環炭素原子と、環中の酸素、窒素及び硫黄からなる群から選択される約1から約3個の環ヘテロ原子とを有する単一の飽和又は部分的に不飽和の環(例えば、5、6、7、8、9、又は10員環)を含む。前記で定義されているようなヘテロシクリル環が、1つ以上のシクロアルキル基、シクロアルケニル基、ヘテロシクリル基、アリール基又はヘテロアリール基と融合されており、ここで、付着点がヘテロシクリル環上にあり、そのような実施形態において、言及されている環状部材の数は、付着点を含むヘテロシクリル環中の環原子の数を指定し続けている。複素環は、環原子の数によってさらに特徴付けることができる。複素環基の例としては、ピペリジニル(6員環原子を有する6員環複素環)、アゼパニル(7員環原子を有する7員環複素環)、3-クロマニル(6員環原子を有する10員環複素環)などが挙げられる。
いくつかの実施形態において、3-7員ヘテロシクリルは、3-7個の環原子を有する。いくつかの実施形態において、3-6員ヘテロシクリルは、3-6個の環原子を有する。いくつかの実施形態において、3-5員ヘテロシクリルは、3-5個の環原子を有する。いくつかの実施形態において、3-5員ヘテロシクリルは、3-9個の環原子を有する。いくつかの実施形態において、3-7員ヘテロシクリルは、3-14個の環原子を有する。いくつかの実施形態において、3-7員ヘテロシクリルは、3-12個の環原子を有する。いくつかの実施形態において、3-7員ヘテロシクリルは、3-10個の環原子を有する。
本明細書で使用される「ヘテロアリール」という用語は、酸素、窒素及び硫黄からなる群から選択される、環中に炭素以外の少なくとも1つの原子を有する単一の芳香族環を意味し、この用語はまた、少なくとも1つのそのような芳香族環を有する複数の縮合環系をも含む。したがって、用語は、約1-約6個の環炭素原子と、環中の酸素、窒素及び硫黄からなる群から選択される約1-4個の環ヘテロ原子とからなる単一のヘテロアリール環を含む。硫黄及び窒素原子は、酸化形態でも存在することができるが、但し、環が芳香族であることを条件とする。「ヘテロアリール」は、前記で定義されているように、ヘテロアリール環が、1つ以上のシクロアルキル基、シクロアルケニル基、ヘテロシクロアリール基、アリール基又はヘテロアリール基と融合している環系を含み、ここで、付着点がヘテロアリール環上にあり、そのような場合、付点を含むヘテロアリール環内の環状部材の数を指定し続けている。ヘテロアリール環は、環原子の数によってさらに特徴付けることができる。例えば、ピリジンは、6個の環原子を有する6員ヘテロアリールである。
いくつかの実施形態において、ヘテロアリール環は、5-15個の環原子を有する5-6員ヘテロアリールである。いくつかの実施形態において、ヘテロアリール環は、5-6員環のヘテロアリールであり
5-10個の環原子を有する。いくつかの実施形態において、ヘテロアリール環は、5-6員環原子を有する5-6員環ヘテロアリールである。いくつかの実施形態において、ヘテロアリール環は、5-12個の環原子を有する5-6員ヘテロアリールである。いくつかの実施形態において、ヘテロアリール環は、5-15個の環原子を有する5員ヘテロアリールである。いくつかの実施形態において、5員ヘテロアリールは、5個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-8個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-9個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-10個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-12個の環原子を有する。いくつかの実施形態において、ヘテロアリール環は、6-15個の環原子を有する6員ヘテロアリールである。いくつかの実施形態において、ヘテロアリール環は、6-10個の環原子を有する6員ヘテロアリールである。いくつかの実施形態において、ヘテロアリール環は、6-14個の環原子を有する6員ヘテロアリールである。いくつかの実施形態において、6員ヘテロアリールは、6-13個の環原子を有する。いくつかの実施形態において、6員ヘテロアリールは、6個の環原子を有する。いくつかの実施形態において、6員ヘテロアリールは、6-9個の環原子を有する。いくつかの実施形態において、6員ヘテロアリールは、6-10個の環原子を有する。いくつかの実施形態において、6員ヘテロアリールは、6-12個の環原子を有する。
本明細書で使用されるような数値範囲は、連続した整数を含むことができる。例えば、「0から5まで」と表される範囲は、0、1、2、3、4及び5を含むであろう。
本明細書で使用されるように、用語「不置換」は、指定された基が、記載された部位(例えば、水素によって価数が満たされる部位)を超えて置換基を持たないことを意味してもよい。
本明細書で使用される「オキソ」という用語は、「=O」基を意味する。また、本明細書では、C(O)又はC=Oと略記することもできる。
本開示は、本明細書に記載されているような化合物、及びそれらの薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及び互変異性体、ならびに本明細書に記載されているような1種以上の化合物、及びそれらの薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及び互変異性体からなる医薬組成物に向けられている。
本開示は、本明細書に記載されているような化合物、及びそれらの薬学的に許容される塩、エナンチオマー、水和物、溶媒和物、プロドラッグ、異性体、プロドラッグ、又は互変異性体に向けられている。「塩」、「水和物」、「溶媒和物」、「プロドラッグ」、「エステル」などの用語の使用は、開示された化合物のエナンチオマー、異性体、プロドラッグ、回転異性体、互変異性体、位置異性体、又はラセミ体の塩、水和物、溶媒和物、プロドラッグ、又はエステルに等しく適用されることを意図している。
すべての異性体の形態が、それらの混合物を含む本開示の範囲内に含まれることが理解されるべきである。用語「異性体」は、同じ組成及び分子量を有するが、物理的及び/又は化学的特性が異なる化合物を指す場合がある。構造的な違いは、構成(幾何学的異性体又は位置的異性体)又は偏光の平面を回転させる能力(立体異性体)にある場合がある。立体異性体に関して、本開示の化合物は、1つ以上の不斉炭素原子を有していてもよく、ラセミ体、ラセミ混合物、及び個々のエナンチオマー又はジアステレオマーとして存在してもよい。本開示の化合物の個々の異性体は、例えば、他の異性体から実質的に遊離していてもよく、又は、例えば、ラセミ体として、又は他のすべての、又は他の選択された異性体と、アドミックスされていてもよい。化合物が二重結合を含む場合、置換基は、EもしくはZ配置、又はシスもしくはトランス配置、又は前記のいずれかの混合物であってもよい。開示されたアッセイ結果は、ラセミ体、エナンチオマー的に純粋な形態、又は立体化学又は構成(例えば、幾何学的又は位置的異性体)の点で他の形態のために収集されたデ-タを反映してもよい。
本開示の化合物は、不斉中心又はキラル中心を含んでもよく、したがって、異なる立体異性体の形態で存在する。「立体異性体」という用語は、同じ数及び種類の原子を有し、それらの原子間で同じ結合結合連結性を共有するが、三次元構造が異なる化合物の集合を指す場合がある。用語「立体異性体」は、この化合物のセットの任意のメンバ-を指すことができる。例えば、立体異性体は、エナンチオマー又はジアステレオマーであってもよい。本開示の化合物のすべての立体異性体の形態、及びラセミ混合物を含むその混合物が、本開示の一部を形成することが意図される。
用語「エナンチオマー」は、互いの非スーパーインポーズ可能な鏡像である一対の立体異性体を指す場合がある。用語「エナンチオマー」は、この一対の立体異性体の単一のメンバーを指すことができる。用語「ラセミ」は、一対のエナンチオマーの1:1混合物を意味してもよい。本明細書に開示される各化合物は、立体化学が特に示されない限り、化合物の一般構造に適合するすべてのエナンチオマー(不斉炭素が存在しない場合でも存在し得る)を含んでいてもよい。化合物は、ラセミ体又はエナンチオマー的に純粋な形態、又は立体化学に関する任意の他の形態であってもよい。本開示のキラルセンターは、IUPAC1974年勧告で定義されているようなS又はR構成を有していてもよい。提示されたいくつかの例では、合成経路は、単一のエナンチオマー又はエナンチオマーの混合物を生成してもよい。本開示のいくつかの実施形態において、本開示の化合物はエナンチオマーである。いくつかの実施形態において、本開示の化合物は、(S)エナンチオマーである。いくつかの実施形態において、本開示の化合物は、(R)-エナンチオマーである。いくつかの実施形態において、本開示の化合物は、(+)又は(-)エナンチオマーであってもよい。
用語「ジアステレオマー」は、単結合を中心とした回転によって重ね合わせることができない立体異性体の集合を指す場合がある。例えば、シス二重結合及びトランス二重結合、二環式環系上でのエンド置換及びエクソ置換、及び相対配置が異なる複数の立体形成中心を含む化合物は、ジアステレオマーであると考えてよい。用語「ジアステレオマー」は、この化合物のセットの任意のメンバーを指すことができる。提示されたいくつかの例において、合成ルートは、単一のジアステレオマー又はジアステレオマーの混合物を生成してもよい。本開示は、本明細書に記載された化合物のジアステレオマーを含んでもよい。
いくつかの実施形態において、本開示の医薬組成物は、本明細書に記載された化合物の優勢に1つのエナンチオマーを提供するために濃縮されてもよい。エナンチオマーが濃縮された混合物は、例えば、1つのエナンチオマーの少なくとも60モル%、より好ましくは少なくとも75、少なくとも80、少なくとも85、少なくとも90、少なくとも95、少なくとも96、少なくとも97、少なくとも98、少なくとも99、少なくとも99.5、又はさらに好ましくは100モル%のエナンチオマーを含んでいてもよい。いくつかの実施形態において、1つのエナンチオマーを濃縮した本明細書に記載の組成物は、他のエナンチオマーを実質的に含まないものであってもよく、ここで実質的に含まないということは、問題の物質が、他のエナンチオマーの量と比較して、例えば医薬組成物又は化合物混合物中で、10%未満、又は5%未満、又は4%未満、又は3%未満、又は2%未満、又は1%未満を構成することを意味してもよい。例えば、医薬組成物又は化合物混合物が、98グラムの第1のエナンチオマー及び2グラムの第2のエナンチオマーを含む場合、98モルパーセントの第1のエナンチオマー及び2モルパーセントの第2のエナンチオマーのみを含むと言われる。
いくつかの実施形態において、本開示の医薬組成物は、本明細書に開示された化合物の1種のジアステレオマーを優勢に提供するために濃縮されてもよい。ジアステレオマーが濃縮された混合物は、例えば、1つのジアステレオマーの少なくとも60モル%、より好ましくは少なくとも75、少なくとも80、少なくとも85、少なくとも90、少なくとも95、少なくとも96、少なくとも97、少なくとも98、少なくとも99、少なくとも99.5、又はさらに好ましくは100モル%のジアステレオマーを含んでいてもよい。いくつかの実施形態において、1つのジアステレオマーを濃縮した本明細書に記載の組成物は、他のジアステレオマーを実質的に含まないものであってもよく、ここで実質的に含まないということは、問題の物質が、例えば医薬組成物又は化合物混合物中の他のジアステレオマーの量と比較して、10%未満、又は5%未満、又は4%未満、又は3%未満、又は2%未満、又は1%未満を構成していることを意味してもよい。
ジアステレオマー混合物は、例えばクロマトグラフィー及び/又は分画結晶化などの当業者に周知の方法によって、それらの物理的化学的差異に基づいて、それらの個々のジアステレオマーに分離することができる。エナンチオマーは、適切な光学活性化合物(例えば、キラルアルコール又はモッシャー酸塩化物などのキラル補助剤)との反応によりエナンチオマー混合物をジアステレオマー混合物に変換し、ジアステレオマーを分離し、個々のジアステレオマーを対応する純粋なエナンチオマーに変換(例えば加水分解)することによって分離できる。エナンチオマーはまた、キラルHPLCカラムを使用して分離することもできる。また、本開示の化合物の一部は、アトロプ異性体又はロタメリック形態であってもよく、本開示の一部とみなされる。
本開示の化合物は、それらの互変異性体の形態(例えば、アミド又はイミノエーテルとして)で存在してもよい。全てのそのような互変異性型は、本開示の一部として本明細書中で企図される。また、例えば、化合物の全てのケト-エノール及びイミン-エナミン形態は、本開示に含まれる。また、ここに記載のスルホンイミドアミジルウレアは互変異性体を有することにも留意すべきである。本明細書では、構造が一つの形態として図示されているが、互変異性体は平衡状態で存在し得ることに留意されたい。例えば、
は互変異性体である。各化合物についてのすべての互変異性体の形態が包含されるが、各化合物について1つの互変異性体の形態のみが表現されてもよく、それは大互変異性体の形態又は小互変異性体の形態であってもよい。
本開示は、本明細書に開示された化合物の薬学的に許容される塩を含むことができる。「薬学的に許容される塩」は、ヒト又は家畜における使用が許容され、生物学的に又は他の方法では望ましくない遊離形態の生物学的有効性及び特性を保持するそれらの塩を指すことができる。代表的な「薬学的に許容される塩」には、例えば、以下のものが含まれ得る:水溶性及び水不溶性の塩、例えば、アセテート、アムソネート(4,4-ジアミノスチルベン-2,2-ジスルホン酸塩)、ベンゼンスルホン酸塩、ベンゾネート、重炭酸塩、重硫酸塩、ビタルトレート、ホウ酸塩、臭化物、酪酸塩、カルシウム、エデテートカルシウム、カムシル酸塩、炭酸塩、塩化物、クエン酸塩などが挙げられる。クラブラリ酸塩、ジヒドロクロライド、エデテート、エジシル酸塩、エストレート、エシル酸塩、フィウナレート、グルセプテート、グルコン酸塩、グルタミン酸塩、グリコールアルサニル酸塩、ヘキサフルオロリン酸塩、ヘキシルレゾルシン酸塩、ヒドラバミン、臭化水素酸塩、塩酸塩、ヒドロキシナフトエート、ヨウ化物、セチオネート、乳酸塩。ラクトビオン酸塩、ラウリン酸塩、マグネシウム、リンゴ酸塩、マレイン酸塩、マンデラート、メシル酸塩、臭化メチル、硝酸メチル、硫酸メチル、ムカテート、ナプシル酸塩、硝酸塩、N-メチルグルカミンアンモニウム塩、3-ヒドロキシ-2-ナフトエート、オレイン酸塩、シュウ酸塩、パルミチン酸塩、パモエート、1,1-メチレンビス-2-ヒドロキシ-3-ナフトエート。アインボネート、パントテン酸塩、リン酸/二リン酸塩、ピクレート、ポリガラクツロン酸塩、プロピオン酸塩、p-トルエンスルホン酸塩、サリチル酸塩、ステアレート、サブアセテート、コハク酸塩、硫酸塩、スルホサリチル酸塩、スラメート、タンニン酸塩、タルトレート、テオクレート、トシル酸塩、トリエチヨード、及びバレレートの塩。
薬学的に許容される塩は、酸付加塩と塩基付加塩の両方を含んでもよい。「薬学的に許容される酸付加塩」とは、遊離塩基の生物学的有効性及び特性を保持する塩であって、生物学的に又は他の方法では好ましくないもの、例えば、無機酸で形成されていてもよいが、これらに限定されない以下のものを指すことができる:塩酸、臭化水素酸、硫酸、硝酸、リン酸等の有機酸、及び酢酸、2,2-ジクロロ酢酸、アジピン酸、アルギン酸、アスコルビン酸、アスパラギン酸、ベンゼンスルホン酸、安息香酸、4-アセトアミド安息香酸、樟脳酸、樟脳-10-スルホン酸等の有機酸が挙げられるが、これらに限定されるものではない。カプリン酸、カプロン酸、カプリル酸、炭酸、桂皮酸、クエン酸、シクラム酸、ドデシル硫酸、エタン-1,2-ジスルホン酸、エタンスルホン酸、2-ヒドロキシエタンスルホン酸、ギ酸、フマル酸、ガラクタル酸、ゲンチジン酸、グルコヘプトン酸、グルコン酸、グルクロン酸、グルタミン酸、グルタル酸、2-オキソ-グルタル酸、グリセロリン酸、グリコール酸、ヒプール酸、イソ酪酸、乳酸、ラクトビオン酸、ラウリン酸、マレイン酸、リンゴ酸、マロン酸、マンデル酸、メタンスルホン酸、ムチン酸、ナフタレン-L、5-ジスルホン酸、ナフタレン-2-スルホン酸、L-ヒドロキシ-2-ナフトエ酸。ニコチン酸、オレイン酸、オロチン酸、シュウ酸、パルミチン酸、パーム酸、プロピオン酸、ピログルタミン酸、ピルビン酸、サリチル酸、4-アミノサリチル酸、セバシン酸、ステアリン酸、コハク酸、酒石酸、チオシアン酸、p-トルエンスルホン酸、トリフルオロ酢酸、ウンデシレン酸など。
「薬学的に許容される塩基付加塩」とは、遊離酸の生物学的有効性及び特性を保持する塩を意味してもよく、生物学的に又は他の方法では好ましくない。これらの塩は、遊離酸に無機塩基又は有機塩基を添加して調製してもよい。無機塩基に由来する塩としては、ナトリウム塩、カリウム塩、リチウム塩、アンモニウム塩、カルシウム塩、マグネシウム塩、鉄塩、亜鉛塩、銅塩、マンガン塩、アルミニウム塩等が挙げられるが、これらに限定されるものではない。無機塩としては、例えば、アンモニウム塩、ナトリウム塩、カリウム塩、カルシウム塩、マグネシウム塩等が挙げられるが、これらに限定されるものではない。有機塩基に由来する塩としては、第一級アミン、第二級アミン、第三級アミンの塩、天然に存在する置換アミンを含む置換アミン、環状アミン、塩基性イオン交換樹脂、例えばアンモニア、イソプロピルアミン、トリメチルアミン、ジエチルアミン、トリエチルアミン、トリプロピルアミン、ジエタノールアミン、エタノールアミン等が挙げられるが、これらに限定されるものではない。デアノール、2-ジメチルアミノエタノール、2-ジエチルアミノエタノール、ジシクロヘキシルアミン、リジン、アルギニン、ヒスチジン、カフェイン、プロカイン、ヒドラバミン、コリン、ベタイン、ベンズアミン、エチレンジアミン、グルコサミン、メチルグルカミン、テオブロミン、トリエタノールアミン、トロメタミン、プリン、ピペラジン、ピペリジン、N-エチルピペリジン、ポリアミン樹脂等がある。
本開示は、本明細書に開示された化合物の双性イオンを含んでもよい。「双性イオン」とは、正の電荷を持つ基と負の電荷を持つ基の両方を持つが、全体的には電荷を持たない、すなわち、分子内で+と-の電荷が均衡している分子を指す場合がある。例として、本開示の化合物は、プロトン化されたアミノ基及び脱プロトン化された硫酸基を含んでいてもよい。
本開示の化合物は、溶媒和物として存在してもよい。「溶媒和物」という用語は、溶質と溶媒によって形成される可変化学量論の複合体を指す場合がある。本開示の目的のためのそのような溶媒は、溶質の生物学的活性を妨げないものであってもよい。好適な溶媒の例としては、水、MeOH、EtOH、AcOHなどが挙げられるが、これらに限定されない。水が溶媒分子である溶媒和物は、一般的に水和物と呼ばれる。水和物は、可変量の水を含む組成物と同様に、化学量論的量の水を含む組成物を含んでもよい。
本明細書に記載の化合物は、さらに、薬学的に許容されるすべての同位体標識化合物を含む。「同位体的に」又は「放射標識された」化合物は、1つ又は複数の原子が、自然界に通常見られる(すなわち、天然に存在する)原子質量又は質量数とは異なる原子質量又は質量数を有する原子で置換又は置換された化合物であってもよい。例えば、いくつかの実施形態において、本明細書に記載された化合物において、水素原子は、1つ以上の重水素又はトリチウムで置換又は置換されている。本開示の特定の同位体標識化合物、例えば放射性同位体を組み込んだ化合物は、薬物及び/又は基質の組織分布研究において有用であり得る。放射性同位体のトリチウム、すなわち3Hと炭素14、すなわち14Cは、それらの組み込みの容易さと検出手段の準備ができているという観点から、この目的のために特に有用である可能性がある。重水素、すなわち2Hのようなより重い同位体で置換することは、より高い代謝安定性、例えば、生体内半減期の増加、又は用量要件の減少などの結果として、ある種の処置上の利点をもたらす可能性があり、したがって、いくつかの状況では好ましいかもしれない。いくつかの実施形態において、化合物は、少なくとも1つの重水素原子からなる。例えば、本開示の化合物における1つ以上の水素原子を、重水素で置き換えるか、又は置換してもよい。いくつかの実施形態において、化合物は、2つ以上の重水素原子を含む。いくつかの実施形態において、化合物は、1、2、3、4、5、6、7、8、9、10、11又は12個の重水素原子を含む。本明細書に記載された化合物に組み込まれ得る適切な同位体は、2H(重水素を表すDとも記載される)、3H(トリチウムを表すTとも記載される)、11C、13C、14C、13N、15N、15O、17O、18O、18F、35S、36Cl、82Br、75Br、76Br、77Br、123I、124I、125I、及び131Iを含むが、これらに限定されない。11C、18F、15O、13Nなどの陽電子放射性同位体の置換は、陽電子放射トポグラフィ(PET)研究に有用である。
本明細書に開示された化合物の同位体標識化合物は、一般に、本明細書に開示されたスキーム及び/又は実施形態に開示されたものと類似した手順に従って、適切な同位体標識試薬を非同位体標識試薬に置換することによって調製することができる。
化合物
本開示は、式(I)
(式中、置換基は、本明細書に記載されている通りである(例えば、式(I-1)、(I-2)、(I-3)、(I-4)、(I-5)、及び(I-6)に関して記載されているようなもの)) の構造を有する化合物、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を提供する。
一態様においては、式(I)
(式中:
R
1は、下記(i)又は(ii):
(i):R
1は、下記式
の単環ピラゾールであって、
ここで、R
1wは、H、D、-CN、-C(O)R
5b、-S(O)
2R
5b、-S(O)R
5b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
5a、-C(O)R
5b、-P(O)R
5bR
6b、-S(O)
2R
5b、-S(O)R
5b、-NR
5aR
6a、-NR
5aC(O)R
6a、-NR
5aC(O)OR
6a、-NR
5aC(O)NR
6a、-NR
5aS(O)
2R
6a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1x及びR
1yは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、 C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;又は
(ii):R
1は、式
の縮合ピラゾールであり、
ここで、(ii-a)は:R
1w及びR
1yは、それらが結合している原子とともに、3-7員ヘテロシクリル又は5-6員ヘテロアリールを形成していてもよく;前記3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、1つ又は複数の置換基、又は存在する場合には2つの置換基で置換され、それらが結合している原子とともに環を形成していてもよく;そして
R
1xは、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-Or7a
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
(ii-b):R
1x及びR
1yは、それらが結合している原子とともに、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、又は5-6員アリール又はヘテロアリールを形成するしていてもよく;前記C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5-6員アリール又はヘテロアリールは、それぞれ独立して、非置換であるか、又は
R
1wは、H、D、-CN、-C(O)R
5b、-S(O)
2R
5b、-S(O)R
5b、
C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリール;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
5a、-C(O)R
5b、-P(O)R
5bR
6b、-S(O)
2R
5b、-S(O)R
5b、-NR
5aR
6a、-NR
5aC(O)R
6a、-NR
5aC(O)OR
6a、-NR
5aC(O)NR
6a、-NR
5aS(O)
2R
6a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている;
であり、
R
100は、H、Cl、D、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)
2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、C
6アリール、及び-NR
2gR
2hからなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、及びC
6アリールは、それぞれ独立して、非置換であるか、又は1つ以上の置換基で置換されており、又は、存在する場合には、場合により、2つの置換基が、それらが結合している原子とともに環を形成していてもよく;
各R
2g及びR
2hは、それぞれ独立して、H、D、C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
5a、R
6a、R
7a、R
8a、R
9a、R
10a、R
21a及びR
22aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
5b、R
6b、R
7b、R
8b、R
9b、R
10b、R
21b、及びR
22bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールでる;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
の構造を有する化合物、又はその薬学的に許容される塩、溶媒和物、異性体又は互変異性体が提供される。
いくつかの実施形態において、化合物は、表1Xの化合物及びその薬学的に許容される塩、溶媒和物、異性体及び互変異性体以外のものである。いくつかの実施形態において、式(I)の化合物などの本明細書の化合物は、表1Xの化合物Nos.1x-30xの1種又は2種以上から選択される化合物、及びそれらの薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体以外のものである。いくつかの実施形態において、本開示の化合物、及び本明細書に記載の化合物を使用する方法は、表1Xに記載の化合物、及びそれらの薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を含む、式(I)の化合物のいずれかを包含する。
一態様においては、R2が、本明細書で定義される通りであり、R1が、場合により本明細書で詳細に記載される通りに置換された単環ピラゾールである、式(I)の化合物、又はその塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、プロドラッグ、代謝物又は誘導体が提供される。一変形例において、化合物は、表1Xの化合物Nos.1x-30x、及びそれらの薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体から選択される1つ以上の化合物以外のものである。いくつかの実施形態において、R2は、場合により本明細書で詳述するように置換された4-ピラゾリルである(ただし、R1は、1,3-ジメチルピラゾール-4-イル以外のものである)。いくつかの実施形態において、R2は、本明細書で詳細に記載されるように任意に置換されている4-ピラゾリルである(ただし、化合物は、表1の化合物1x、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体以外のものである)。いくつかの実施形態において、R2は、場合により本明細書で詳述するように置換された3-ピラゾリルである(ただし、化合物は、表1Xの化合物Nos.2x-30x、及びそれらの薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体から選択される1つ以上の化合物以外のものである)。
いくつかの実施形態において、R100は、H、-CN、-C(O)R3b、又はC1-C6アルキルであり;前記C1-C6アルキルは、非置換であるか、又はC6アリールで置換されている。一変形例において、R100はHである。
いくつかの実施形態において、R2は、C1-C6アルキル、C3-C10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、C6アリール、及び-NR2gR2hからなる群から選択され;前記C1-C6アルキル、C3-C10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、及びC6アリールは、それぞれ独立して、非置換であるか、又はD、CN、ハロゲン、C1-C6アルキル、C1-C6ハロアルキル、C2-C6アルケニル、オキソ、-OR23a、-C(O)R23b、-P(O)R23bR24b、-S(O)2R23b、-S(O)R23b、-NR23aR24a、-NR23aC(O)R24a、-NR23aC(O)OR24a、-NR23aC(O)NR24a、-NR23aS(O)2R24a、-(CH2)1-4C3-C10シクロアルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R23a及びR24aは、それぞれ独立して、H、D、C1-C8アルキル、C2-C8アルケニル、C2-C8アルキニル、C3-C10シクロアルキル、C4-C8シクロアルケニル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C1-C8アルキル、C2-C8アルケニル、C2-C8アルキニル、C3-C10シクロアルキル、C4-C8シクロアルケニル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、-OH、-O-C1-C6アルキル、-NH2、-NH(C1-C6アルキル)、-N(C1-C6アルキル)2、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R23b、及びR24bは、それぞれ独立して、H、D、-OH、-O(C1-C6アルキル)、-NH2、-NH(C1-C6アルキル)、-N(C1-C6アルキル)2、-NHS(O)2CH3、C1-C8アルキル、C2-C8アルケニル、C2-C8アルキニル、C3-C10シクロアルキル、C4-C8シクロアルケニル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C1-C8アルキル、C2-C8アルケニル、C2-C8アルキニル、C3-C10シクロアルキル、C4-C8シクロアルケニル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、-OH、-O-C1-C6アルキル、-NH2、-NH(C1-C6アルキル)、-N(C1-C6アルキル)2、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
いくつかの実施形態において、R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、-NR
2gR
2h、
からなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
X
2は、N又はCR
2aであり;
X
3は、N又はCR
2cであり;
X
4は、N又はCR
2dであり;
X
5は、N又はCR
2eであり;
X
6及びX
7は、それぞれ独立してN又はCR
2nであり、前記X
6及びX
7のうちの少なくとも1つはNであり;
R
2aは、H、D、ハロゲン、-CN、-OR
15a、C
1-C
6アルキル、C
3-C
10シクロアルキル、-C(O)NR
15aR
16a、-C(O)OR
15a、-P(O)R
15bR
16b、-NR
15aR
16a、-NR
15aC(O)R
16a、-NR
15aC(O)OR
16a、-NR
15aC(O)NR
16a、又は-NR
15aS(O)
2R
16aであり、前記C
1-C
6アルキル及びC
3-C
10シクロアルキルは、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR
15a、-C(O)R
15b、-P(O)R
15bR
16b、-NR
15aR
16a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5~6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
2b、R
2c、R
2d、R
2e、及びR
2fは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2b、R
2c、R
2d、R
2e及びR
2fは、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2j、R
2k、R
2m及びR
2nは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2j、R
2k、R
2m及びR
2nは、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
R
15a、R
16a、R
17a、R
18a、R
19a及びR
20aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
15b、R
16b、R
17b、及びR
18bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルケニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
これらの実施形態のいくつかにおいて、R2aは、H、D、ハロゲン、-CN、-OR15a、C1-C6アルキル、C3-C10シクロアルキル、-C(O)NR15aR16a、-C(O)OR15a;-NR15aR16a、-NR15aC(O)R16a、-NR15aC(O)OR16a、-NR15aC(O)NR16a又は-NR15aS(O)2R16aであり、前記C1-C6アルキル及びC3-C10シクロアルキルは、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR15a、-C(O)R15b、-NR15aR16a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
これらの実施形態のいくつかにおいて、R2aは、H、ハロゲン、-CN、-OR15a、-C(O)OR15a、又はC1-C6アルキルであり;前記C1-C6アルキルは、非置換であるか、又はD、ハロゲン、-CN、-OR15a、-C(O)R15b、-P(O)R15bR16b、-NR15aR16a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
これらの実施形態のいくつかにおいて、R2aは、H、ハロゲン、-CN、-OR15a、-C(O)OR15a又はC1-C6アルキルであり;前記C1-C6アルキルは、非置換であるか、又はD、ハロゲン、-CN、-OR15a、-C(O)R15b、-NR15aR16a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。一変形例において、R2aはH又はFである。別の変形例において、R2aはHである。別の変形例において、R2aはFである。
いくつかの実施形態において、R
2は
であり、以下:
からなる群から選択される。
いくつかの実施形態において、R
2は
である。これらの実施形態のいくつかにおいて、X
3はCR
2cであり;X
4はCR
2dであり;X
5はCR
2eである。一変形例において、各R
2b、R
2c、R
2d、R
2e及びR
2fは、それぞれ独立して、H、D、ハロゲン、C
1-C
6アルキル、C
3-C
10シクロアルキル、及び-CNからなる群から選択される。これらの実施形態のいくつかでは、R
2は、
からなる群から選択される。
これらの実施形態のいくつかでは、X
3はCR
2cであり;X
4はCR
2dであり;X
5はCR
2eであり:
R
2bとR
2cは、それらが結合した原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく;前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2d、R
2e、及びR
2fは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
これらの実施形態のいくつかでは、R
2は、
からなる群から選択される。
これらの実施形態のいくつかでは、X3はCR2cであり;X4はCR2dであり;X5はCR2eであり:
R2bとR2cは、それらが結合した原子とともに、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく;前記C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C1-C6アルキル、-OR19a、及びNR19aR20aからなる群から選択される1つ以上の置換基で置換されており;
R2eとR2fは、それらが結合した原子とともに、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく;前記C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C1-C6アルキル、-OR19a、NR19aR20aからなる群から選択される1つ以上の置換基で置換されており;
R2dは、H、D、ハロゲン、-CN、-NO2、-SR17a、-OR17a、-C(O)R17b、-P(O)R17bR18b、-S(O)2R17b、-S(O)R17b、-NR17aR18a、-NR17aC(O)R18a、-NR17aC(O)R18a、-NR17aC(O)OR18a、-NR17aC(O)NR18a、-NR17aS(O)2R18a、C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR17a、-C(O)R17b、-P(O)R17bR18b、-S(O)2R17b、-S(O)R17b、-NR17aR18a、-NR17aC(O)R18a、-NR17aC(O)OR18a、-NR17aC(O)NR18a、-NR17aS(O)2R18a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
これらの実施形態のいくつかでは、R
2は、
からなる群から選択される。これらの実施形態のいくつかでは、R
2は、
からなる群から選択される。
いくつかの実施形態において、R
2は
であり、X
3はCR
2cであり;X
4はCR
2dであり;X
5はCR
2eであり;R
2は、
からなる群から選択される。
いくつかの実施形態において、R
2は
であり、X
3はNであり、X
4はCR
2dである。これらの実施形態のいくつかでは、X
5はCR
2eである。これらの実施形態のいくつかでは、X
5はNである。これらの実施形態のいくつかでは、R
2は、
からなる群から選択される。
一様態においては、R
2が、本明細書で定義される通りであり、R
1が、下記式:
(式中、R
1w、R
1x及びR
1yは、離散的な置換基である) の単環ピラゾールである、式(I)の化合物、又はその塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、プロドラッグ、代謝物又は誘導体が提供される。これらの実施形態のいくつかにおいて、R
1wは、H、D、-CN、-C(O)R
5b、-S(O)
2R
5b、-S(O)R
5b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
5a、-C(O)R
5b、-P(O)R
5bR
6b、-S(O)
2R
5b、-S(O)R
5b、-NR
5aR
6a、-NR
5aC(O)R
6a、-NR
5aC(O)OR
6a、-NR
5aC(O)NR
6a、-NR
5aS(O)
2R
6a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;各R
1x及びR
1yは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
一態様においては、R
2が、本明細書で定義される通りであり、R
1が、式
(式中、R
1w及びR
1yが、それらが結合している原子とともに縮合環を形成しているか、又はR
1x及びR
1yが、それらが結合している原子とともに縮合環を形成しているかのいずれであってもよい)
の縮合ピラゾールである、式(I)の化合物、又はその塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、プロドラッグ、代謝物又は誘導体が提供される。
これらの実施形態のいくつかにおいて、R1w及びR1yは、それらが結合している原子とともに、3-7員ヘテロシクリル又は5-6員ヘテロアリールを形成していてもよく;前記3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又は1つ以上の置換基で置換されており、又は、場合により、存在する場合には、置換基のうちの2つが、それらが結合している原子とともに、環を形成していてもよく;R1xは、H、D、ハロゲン、-CN、-NO2、-SR7a、-OR7a、-C(O)R7b、-P(O)R7bR8b、-S(O)2R7b、-S(O)R7b、-NR7aR8a、-NR7aC(O)R8a、-NR7aC(O)OR8a、-NR7aC(O)NR8a、-NR7aS(O)2R8a、C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、CN、ハロゲン、C1-C6アルキル、-OR7a、-C(O)R7b、-P(O)R7bR8b、-S(O)2R7b、-S(O)R7b、-NR7aR8a、-NR7aC(O)R8a、-NR7aC(O)OR8a、-NR7aC(O)NR8a、-NR7aS(O)2R8a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1w及びR1yは、それらが結合している原子とともに、3-7員ヘテロシクリル又は5-6員ヘテロアリールを形成していてもよく;前記3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、CN、ハロゲン、C1-C6アルキル、-OR9a、-C(O)R9b、-P(O)R9bR10b、-S(O)2R9b、-S(O)R9b、-NR9aR10a、-NR9aC(O)R10a、-NR9aC(O)OR10a、-NR9aC(O)NR10a、及び-NR9aS(O)2R10aからなる群から選択される1つ以上の置換基で置換されている。
これらの実施形態のいくつかにおいて、R1x及びR1yは、それらが結合している原子とともに、C3-C10シクロアルキル、3-7員ヘテロシクリル、又は5-6員アリール又はヘテロアリールを形成していてもよく;前記C3-C10シクロアルキル、3-7員ヘテロシクリル、及び5-6員アリール又はヘテロアリールは、それぞれ独立して、非置換であるか、又は1つ以上の置換基で置換されており、又は、場合により、存在する場合には、置換基のうちの2つが、それらが結合している原子とともに、環を形成していてもよく;R1wは、H、D、-CN、-C(O)R5b、-S(O)2R5b、-S(O)R5b、C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、OR5a、-C(O)R5b、-P(O)R5bR6b、-S(O)2R5b、-S(O)R5b、-NR5aR6a、-NR5aC(O)R6a、-NR5aC(O)OR6a、-NR5aC(O)NR6a、-NR5aS(O)2R6a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1x及びR1yは、それらが結合している原子と共に、C3-C10シクロアルキル、3-7員ヘテロシクリル、又は5-6員アリール又はヘテロアリールを形成していてもよく;前記C3-C10シクロアルキル、3-7員ヘテロシクリル、及び5-6員アリール又はヘテロアリールは、それぞれ独立して、非置換であるか、又はD、CN、ハロゲン、C1-C6アルキル、-OR9a、-C(O)R9b、-P(O)R9bR10b、-S(O)2R9b、-S(O)R9b、-NR9aR10a、-NR9aC(O)R10a、-NR9aC(O)OR10a、-NR9aC(O)NR10a、及び-NR9aS(O)2R10aからなる群から選択される1つ又は複数の置換基で置換されている。
いくつかの実施形態においては、R
2が、本明細書で定義される通りであり、R
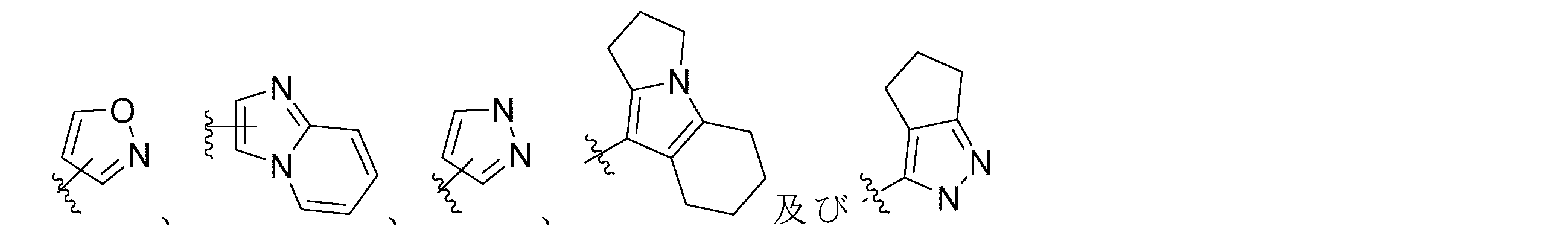
1が、以下:
(式中、
R
1zは、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-Or7a
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hは、それぞれ独立して、H、D、ハロゲン、CN、-NO
2、-SR
11a、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールから選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR7a
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hのうちの2つの基は、存在する場合、それらが結合している原子と共に、C
3-C
10シクロアルキル又は3-7員ヘテロシクリルを形成していてもよく;前記C
3-C
10シクロアルキル及び3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
13a、-C(O)R
13b、-P(O)R
13bR
14b、-S(O)
2R
13b、-S(O)R
13b、-NR
13aR
14a、-NR
13aC(O)R
14a、-NR
13aC(O)OR
14a、-NR
13aC(O)NR
14a、及び-NR
13aS(O)
2R
14aからなる群から選択される1つ以上の置換基で置換されているか、;又は
2つのジェミナルな基R
1a及びR
1b;R
1c及びR
1d;R
1e及びR
1f;またR
1g及びR
1hが、存在する場合、オキソ基を形成していてもよく;
R
7a、R
8a、R
11a、R
12a、R
13a及びR
14aは、それぞれ独立して、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5~6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
7b、R
8b、R
11b、R
12b、R
13b及びR
14bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-NH(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルケニル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
からなる群から選択される、式(I)の化合物、又はその塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、プロドラッグ、代謝物又は誘導体が提供される。
本開示は、式(I-1)
(式中:
R
100は、H、Cl、D、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)
2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
1は、
(式中、
R
1wは、H、D、-CN、-C(O)R
5b、-S(O)
2R
5b、-S(O)R
5b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
5a、-C(O)R
5b、-P(O)R
5bR
6b、-S(O)
2R
5b、-S(O)R
5b、-NR
5aR
6a、-NR
5aC(O)R
6a、-NR
5aC(O)OR
6a、-NR
5aC(O)NR
6a、-NR
5aS(O)
2R
6a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1x及びR
1yは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-Cアルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1w及びR
1yは、それらが結合している原子とともに、3-7員ヘテロシクリル又は5-6員ヘテロアリールを形成していてもよく;前記3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1x及びR
1yは、それらが結合している原子とともに、C
3-C
10-シクロアルキル、3-7員ヘテロシクリル、又は5-6員アリール又はヘテロアリールを形成していてもよく;前記C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5-6員アリール又はヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a、及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されている)
からなる群から選択され;
R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、C
6アリール、及び-NR
2gR
2hからなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、及びC
6アリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
2g及びR
2hは、それぞれ独立して、H、D、C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6ハロアルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
5a、R
6a、R
7a、R
8a、R
9a、R
10a、R
21a、R
22a、R
23a及びR
24aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
5b、R
6b、R
7b、R
8b、R
9b、R
10b、R
21b、R
22b、R
23b及びR
24bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル
)2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
の構造を有する化合物、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を提供する。
本開示は、式(I-2)
(式中:
R
100は、H、Cl、D、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)
2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
1は、
からなる群から選択され、
R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、-NR
2gR
2h、及び以下
からなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
X
2は、N又はCR
2aであり;
X
3は、N又はCR
2cであり;
X
4は、N又はCR
2dであり;
X
5は、N又はCR
2eであり;
X
6及びX
7は、それぞれ独立してN又はCR
2nであり、前記X
6及びX
7のうちの少なくとも1つはNであり;
R
1wは、H、D、-CN、-C(O)R
5b、-S(O)
2R
5b、-S(O)R
5b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
5a、-C(O)R
5b、-P(O)R
5bR
6b、-S(O)
2R
5b、-S(O)R
5b、-NR
5aR
6a、-NR
5aC(O)R
6a、-NR
5aC(O)OR
6a、-NR
5aC(O)NR
6a、-NR
5aS(O)
2R
6a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1x及びR
1yは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1w及びR
1yは、それらが結合している原子とともに、3-7員ヘテロシクリル又は5-6員ヘテロアリールを形成していてもよく;前記3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1x及びR
1yは、それらが結合している原子とともに、C
3-C
10-シクロアルキル、3-7員ヘテロシクリル、又は5-6員アリール又はヘテロアリールを形成していてもよく;前記C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5-6員アリール又はヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a、及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されており;
R
2aは、H、D、ハロゲン、-CN、-OR
15a、C
1-C
6アルキル、C
3-C
10シクロアルキル、-C(O)NR
15aR
16a、-C(O)OR
15a;-NR
15aR
16a、-NR
15aC(O)R
16a、-NR
15aC(O)OR
16a、-NR
15aC(O)NR
16a、又は-NR
15aS(O)
2R
16aであり、前記C
1-C
6アルキル及びC
3-C
10シクロアルキルは、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR
15a、-C(O)R
15b、-NR
15aR
16a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1以上の置換基で置換されており;
各R
2b、R
2c、R
2d、R
2e、及びR
2fは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2b、R
2c、R
2d、R
2e及びR
2fは、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2j、R
2k、R
2m及びR
2nは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2j、R
2k、R
2m及びR
2nは、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2g及びR
2hは、それぞれ独立して、H、D、C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
5a、R
6a、R
7a、R
8a、R
9a、R
10a、R
15a、R
16a、R
17a、R
18a、R
19a、R
20a、R
21a、R
22a、R
23a、及びR
24aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
5b、R
6b、R
7b、R
8b、R
9b、R
10b、R
15b、R
17b、R
18b、R
21b、R
22b、R
23b、及びR
24bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
の構造を有する化合物、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を提供する。
本開示は、式(I-3)
(式中:
R
100は、H、D、-Cl、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)
2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
1は、
からなる群から選択され、
R
2は、
X
2は、N又はCR
2aであり;
X
3は、N又はCR
2cであり;
X
4は、N又はCR
2dであり;
X
5は、N又はCR
2eであり;
R
1wは、H、D、-CN、C(O)R
5b、-S(O)
2R
5b、-S(O)R
5b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
5a、-C(O)R
5b、-P(O)R
5bR
6b、-S(O)
2R
5b、-S(O)R
5b、-NR
5aR
6a、-NR
5aC(O)R
6a、-NR
5aC(O)OR
6a、-NR
5aC(O)NR
6a、-NR
5aS(O)
2R
6a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1x及びR
1yは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1w及びR
1yは、それらが結合している原子とともに、3-7員ヘテロシクリルを形成していてもよく;前記3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a、及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1x及びR
1yは、それらが結合している原子とともに、C
3-C
10-シクロアルキル、3-7員ヘテロシクリル、又は5-6員アリール又はヘテロアリールを形成していてもよく;前記C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5-6員アリール又はヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a、及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されており;
R
2aは、H、D、ハロゲン、-CN、-OR
15a、C
1-C
6アルキル、C
3-C
10シクロアルキル、-C(O)NR
15aR
16a、-C(O)OR
15a;-NR
15aR
16a、-NR
15aC(O)R
16a、-NR
15aC(O)OR
16a、-NR
15aC(O)NR
16a、又は-NR
15aS(O)
2R
16aであり、前記C
1-C
6アルキル及びC
3-C
10シクロアルキルは、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR
15a、-C(O)R
15b、-NR
15aR
16a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1以上の置換基で置換されており;
各R
2b、R
2c、R
2d、R
2e、及びR
2fは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2b、R
2c、R
2d、R
2e及びR
2fは、それらが結合している原子と共に、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
5a、R
6a、R
7a、R
8a、R
9a、R
10a、R
15a、R
16a、R
17a、R
18a、R
19a及びR
20aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
5b、R
6b、R
7b、R
8b、R
9b、R
10b、R
15b、R
17b及びR
18bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
の構造を有する化合物、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を提供する。
本開示は、式(I-4)
(式中:
R
100は、H、Cl、D、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-Cアルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
1は、以下:
からなる群から選択され:
R
1zは、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hは、それぞれ独立して、H、D、ハロゲン、CN、-NO
2、-SR
11a、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールから選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hのうちの2つの基は、存在する場合、それらが結合している原子とともに、C
3-C
10シクロアルキル又は3-7員ヘテロシクリルを形成していてもよく;前記C
3-C
10シクロアルキル及び3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
13a、-C(O)R
13b、-P(O)R
13bR
14b、-S(O)
2R
13b、-S(O)R
13b、-NR
13aR
14a、-NR
13aC(O)R
14a、-NR
13aC(O)OR
14a、-NR
13aC(O)NR
14a、及び-NR
13aS(O)
2R
14aからなる群から選択される1つ以上の置換基で置換されているか;又は
2つのジェミナルな基R
1a及びR
1b;R
1c及びR
1d;R
1e及びR
1f;又はR
1g及びR
1hは、存在する場合、オキソ基を形成していてもよく;
R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、C
6アリール、及び-NR
2gR
2hからなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、及びC
6アリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
2g及びR
2hは、それぞれ独立して、H、D、C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
7a、R
8a、R
11a、R
12a、R
13a、R
14a、R
21a、R
22a、R
23及びR
24aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
7b、R
8b、R
11b、R
12b、R
13b、R
14b、R
21b、R
22b、R
23b及びR
24bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル
)2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
の構造を有する化合物、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を提供する。
本開示は、式(I-5)
(式中:
R
100は、H、Cl、D、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)
2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
1は、以下:
からなる群から選択され:
R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、-NR
2gR
2h、及び以下
からなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
X
2は、N又はCR
2aであり;
X
3は、N又はCR
2cであり;
X
4は、N又はCR
2dであり;
X
5は、N又はCR
2eであり;
X
6及びX
7は、それぞれ独立してN又はCR
2nであり、前記X
6及びX
7のうちの少なくとも1つはNであり;
R
1zは、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hは、それぞれ独立して、H、D、ハロゲン、CN、-NO
2、-SR
11a、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールから選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hのうちの2つの基は、存在する場合、それらが結合している原子とともに、C
3-C
10シクロアルキル又は3-7員ヘテロシクリルを形成していてもよく;前記C
3-C
10シクロアルキル及び3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
13a、-C(O)R
13b、-P(O)R
13bR
14b、-S(O)
2R
13b、-S(O)R
13b、-NR
13aR
14a、-NR
13aC(O)R
14a、-NR
13aC(O)OR
14a、-NR
13aC(O)NR
14a、及び-NR
13aS(O)
2R
14aからなる群から選択される1つ以上の置換基で置換されているか;又は
2つのジェミナルな基R
1a及びR
1b;R
1c及びR
1d;R
1e及びR
1f;又はR
1g及びR
1hは、存在する場合、オキソ基を形成していてもよく;
R
2aは、H、D、ハロゲン、-CN、-OR
15a、C
1-C
6アルキル、C
3-C
10シクロアルキル、-C(O)NR
15aR
16a、-C(O)OR
15a;-NR
15aR
16a、-NR
15aC(O)R
16a、-NR
15aC(O)OR
16a、-NR
15aC(O)NR
16a、又は-NR
15aS(O)
2R
16aであり、前記C
1-C
6アルキル及びC
3-C
10シクロアルキルは、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR
15a、-C(O)R
15b、-NR
15aR
16a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
2b、R
2c、R
2d、R
2e、及びR
2fは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2b、R
2c、R
2d、R
2e及びR
2fは、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2j、R
2k、R
2m及びR
2nは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2j、R
2k、R
2m及びR
2nは、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2g及びR
2hは、それぞれ独立して、H、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、C
6アリール、又は5員ヘテロアリールであり、前記3-7員ヘテロシクリル及び5員ヘテロアリールは、3-7員ヘテロシクリル又は5員ヘテロアリール上の炭素において窒素と結合しており、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、C
6アリール、又は5員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6アルキル、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
7a、R
8a、R
11a、R
12a、R
13a、R
14a、R
15a、R
16a、R
17a、R
18a、R
21a、R
22a、R
23a及びR
24aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
7b、R
8b、R
11b、R
12b、R
13b、R
14b、R
15b、R
17b、R
18b、R
21b、R
22b、R
23b及びR
24bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、D、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか、又は非置換である)
の構造を有する化合物、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を提供する。
本開示は、式(I-6)
(式中:
R
100は、H、Cl、D、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)
2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
1は、以下:
からなる群から選択され:
R
2が、
であり;
X
2は、N又はCR
2aであり;
X
3は、N又はCR
2cであり;
X
4は、N又はCR
2dであり;
X
5は、N又はCR
2eであり;
R
1zは、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hは、それぞれ独立して、H、D、ハロゲン、CN、-NO
2、-SR
11a、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールから選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hのうちの2つの基は、存在する場合、それらが結合している原子とともに、C
3-C
10シクロアルキル又は3-7員ヘテロシクリルを形成していてもよく;前記C
3-C
10シクロアルキル及び3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
13a、-C(O)R
13b、-P(O)R
13bR
14b、-S(O)
2R
13b、-S(O)R
13b、-NR
13aR
14a、-NR
13aC(O)R
14a、-NR
13aC(O)OR
14a、-NR
13aC(O)NR
14a、及び-NR
13aS(O)
2R
14aからなる群から選択される1つ以上の置換基で置換されているか;又は
2つのジェミナルな基R
1a及びR
1b;R
1c及びR
1d;R
1e及びR
1f;又はR
1g及びR
1hは、存在する場合、オキソ基を形成していてもよく;
R
2aは、H、D、ハロゲン、-CN、-OR
15a、C
1-C
6アルキル、C
3-C
10シクロアルキル、-C(O)NR
15aR
16a、-C(O)OR
15a;-NR
15aR
16a、-NR
15aC(O)R
16a、-NR
15aC(O)OR
16a、-NR
15aC(O)NR
16a、又は-NR
15aS(O)
2R
16aであり、前記C
1-C
6アルキル及びC
3-C
10シクロアルキルは、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR
15a、-C(O)R
15b、-NR
15aR
16a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
2b、R
2c、R
2d、R
2e、及びR
2fは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2b、R
2c、R
2d、R
2e及びR
2fは、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
7a、R
8a、R
11a、R
12a、R
13a、R
14a、R
15a、R
16a、R
17a及びR
18aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
7b、R
8b、R
11b、R
12b、R
13b、R
14b、R
15b、R
17b及びR
18bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
の構造を有する化合物、及びその薬学的に許容される塩、溶媒和物、異性体、プロドラッグ、及び互変異性体を提供する。
いくつかの実施形態において、R
1は、以下:
からなる群から選択され:
R
1zは、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hは、それぞれ独立して、H、D、ハロゲン、CN、-NO
2、-SR
11a、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールから選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g及びR
1hのうちの2つの基は、存在する場合、それらが結合している原子とともに、C
3-C
10シクロアルキル又は3-7員ヘテロシクリルを形成していてもよく;前記C
3-C
10シクロアルキル及び3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
13a、-C(O)R
13b、-P(O)R
13bR
14b、-S(O)
2R
13b、-S(O)R
13b、-NR
13aR
14a、-NR
13aC(O)R
14a、-NR
13aC(O)OR
14a、-NR
13aC(O)NR
14a、及び-NR
13aS(O)
2R
14aからなる群から選択される1つ以上の置換基で置換されているか;又は
2つのジェミナルな基R
1a及びR
1b;R
1c及びR
1d;R
1e及びR
1f;又はR
1g及びR
1hは、存在する場合、オキソ基を形成していてもよく;
R
7a、R
8a、R
11a、R
12a、R
13a及びR
14aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
7b、R
8b、R
11b、R
12b、R
13b及びR
14bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-NH(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルケニル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、以下からなる群から選択される1つ以上の置換基で置換されているか、又は非置換である;D、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
いくつかの実施形態において、R100はHである。いくつかの実施形態において、R100はC1-C6アルキルであり、前記C1-C6アルキルは、非置換であるか、又はC3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R100は、C1-C6アルキルであり、前記C1-C6アルキルは、非置換であるか、又はC6アリールで置換されている。
前記のように、R2は、C1-C6アルキル、C3-C10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、C6アリール、及び-NR2gR2hからなる群から選択され;前記C1-C6アルキル、C3-C10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、及びC6アリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、C1-C6ハロアルキル、C2-C6アルケニル、オキソ、-OR23a、-C(O)R23b、-P(O)R23bR24b、-S(O)2R23b、-S(O)R23b、-NR23aR24a、-NR23aC(O)R24a、-NR23aC(O)OR24a、-NR23aC(O)NR24a、-NR23aS(O)2R24a、-(CH2)1-4C3-C10シクロアルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
いくつかの実施形態において、R2は6員ヘテロアリールである。いくつかの実施形態において、6員ヘテロアリールは、6-10個の環原子を有する。いくつかの実施形態において、6員ヘテロアリールは、6-9個の環原子を有する。いくつかの実施形態において、6員ヘテロアリールは、6個の環原子を有する。
いくつかの実施形態において、R2は、1又は2個の窒素を含む6員ヘテロアリールである。いくつかの実施形態において、R2は、1個の窒素を含む6員ヘテロアリールである。いくつかの実施形態において、R2は、2個の窒素を含む6員ヘテロアリールである。
いくつかの実施形態において、6員ヘテロアリールは
(式中、X
3は、N又はCR
2cであり;X
4は、N又はCR
2dであり;X
5は、N又はCR
2eであり;X
6及びX
7は、それぞれ独立してN又はCR
2nである)
である。
いくつかの実施形態において、R
2は、非置換又は置換の6員ヘテロアリールであり、前記6員ヘテロアリールは、
からなる群から選択される。いくつかの実施形態において、R
2は、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
6アリール、-OR
23a、C
3-C
10シクロアルキル、C
2-C
6アルケニル、-CN、及び-NR
23aR
24aからなる群から選択される1つ以上の置換基で置換されている6員ヘテロアリールである。
いくつかの実施形態において、R2は、C6アリールである。いくつかの実施形態において、アリール環は、6-14個の環原子を有するC6-アリールである。いくつかの実施形態において、アリール環は、6-10個の環原子を有するC6アリールである。いくつかの実施形態において、アリール環は、6-12個の環原子を有するC6アリールである。いくつかの実施形態において、アリール環は、6個の環原子を有するC6アリールである。
いくつかの実施形態において、R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、-NR
2gR
2h、
からなる群から選択される。
いくつかの実施形態において、R
2は
(式中、X
3は、N又はCR
2cであり;X
4は、N又はCR
2dであり;X
5は、N又はCR
2eであり;X
6及びX
7は、それぞれ独立して、N又はCR
2nである)
である。
いくつかの実施形態において、R2は、C1-C6アルキルである。いくつかの実施形態において、R2は、C1アルキル、C2アルキル、C3アルキル、C4アルキル、C5アルキル、又はC6アルキルである。いくつかの実施形態において、R2は、1つ以上のC6アリールで置換されたC1-C6アルキルである。
いくつかの実施形態において、R2は、C3-C10シクロアルキルである。いくつかの実施形態において、C3-C10シクロアルキルは、3-14個の環原子を有する。いくつかの実施形態において、C3-C10シクロアルキルは、3-12個の環原子を有する。いくつかの実施形態において、C3-C10シクロアルキルは、3-10個の環原子を有する。いくつかの実施形態において、R2は、3-9個の環原子を有するC3-C9シクロアルキルである。いくつかの実施形態において、R2は、3-14個の環原子を有するC3-C9シクロアルキルである。いくつかの実施形態において、R2は、3-9個の環原子を有するC3-C9シクロアルキルである。いくつかの実施形態において、R2は、3-8個の環原子を有するC3-C8シクロアルキルである。いくつかの実施形態において、R2は、3-14個の環原子を有するC3-C8シクロアルキルである。いくつかの実施形態において、R2は、3-14個の環原子を有するC3-C7シクロアルキルである。いくつかの実施形態において、R2は、3-10個の環原子を有するC3-C7シクロアルキルである。いくつかの実施形態において、R2は、3-7個の環原子を有するC3-C7シクロアルキルである。
いくつかの実施形態において、R2は、C5シクロアルキル、C6シクロアルキル、又はC7シクロアルキルである。
シクロアルキル基の例としては、シクロヘキシル、シクロヘプチル、2-アダマンチル
2-(2,3-ジヒドロ-1H-インデン)、及び
9-フルオレニル
等が挙げられる。上述したように、シクロアルキル環は、環原子の数によってさらに特徴付けることができる。例えば、シクロヘキシル環は、環原子が6個のC
6シクロアルキル環であり、2-(2,3-ジヒドロ-1H-インデン)は、環原子が9個のC
5シクロアルキル環である。また、例えば、9-フルオレニルは、環原子が13個のC
5シクロアルキル環であり、2-アダマンチルは、環原子が10個のC
6シクロアルキル環である。
いくつかの実施形態において、R
2は、非置換又は置換のC
3-C
10シクロアルキルであり、前記C
3-C
10シクロアルキルは、
からなる群から選択される。いくつかの実施形態において、R
2は、C
1-C
6アルキル及びC
6アリールからなる群から選択される1つ以上の置換基で置換されたC
3-C
10シクロアルキルである。
いくつかの実施形態において、R2は、3-7員ヘテロシクリルである。いくつかの実施形態において、3-7員ヘテロシクリルは、3-7個の環原子を有する。いくつかの実施形態において、3-7員ヘテロシクリルは、3-14個の環原子を有する。いくつかの実施形態において、3-7員ヘテロシクリルは、3-12個の環原子を有する。いくつかの実施形態において、3-7員ヘテロシクリルは、3-10個の環原子を有する。いくつかの実施形態において、R2は、3-6員ヘテロシクリルである。いくつかの実施形態において、3-6員ヘテロシクリルは、3-6個の環原子を有する。いくつかの実施形態において、R2は、3-5員ヘテロシクリルである。いくつかの実施形態において、3-5員ヘテロシクリルは、3-5個の環原子を有する。いくつかの実施形態において、3-5員ヘテロシクリルは、3-9個の環原子を有する。
いくつかの実施形態において、R
2は、非置換又は置換の3-7員ヘテロシクリルであり、前記3-7員ヘテロシクリルは、
からなる群から選択される。いくつかの実施形態において、R
2は、1つ以上のC
1-C
6アルキルで置換された3-7員ヘテロシクリルである。
いくつかの実施形態において、R2は5員ヘテロアリールである。いくつかの実施形態において、5員ヘテロアリールは、5個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-8個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-9個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-10個の環原子を有する。いくつかの実施形態において、5員ヘテロアリールは、5-12個の環原子を有する。
いくつかの実施形態において、R2は、1又は2個の窒素を含む5員ヘテロアリールである。いくつかの実施形態において、R2は、1個の窒素を含む5員ヘテロアリールである。いくつかの実施形態において、R2は、2個の窒素を含む5員ヘテロアリールである。
いくつかの実施形態において、R
2は、非置換又は置換の5員ヘテロアリールであり、前記5員ヘテロアリールは、
からなる群から選択される。いくつかの実施形態において、R
2は、C
1-C
6アルキル、C
6アリール、オキソ、及び-(CH
2)
1-4C
3-C
10シクロアルキルからなる群から選択される1つ以上の置換基で置換された5員ヘテロアリールである。
いくつかの実施形態において、R
2は、下記
からなる群から選択される5員ヘテロアリールである。
いくつかの実施形態において、R
2は
であり、X
6及びX
7は、それぞれ独立してN又はCR
2nであり、前記X
6及びX
7のうちの少なくとも1つがNである。いくつかの実施形態において、X
6及びX
7のうちの1つはNである。いくつかの実施形態において、X
6及びX
7はNである。
いくつかの実施形態において、R2は、-NR2gR2hである。前記のように、各R2g及びR2hは、それぞれ独立して、H、D、C1-C6アルキル、C3-C1シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、C1-C6ハロアルキル、C2-C6アルケニル、オキソ、-OR21a、-C(O)R21b、-P(O)R21bR22b、-S(O)2R21b、-S(O)R21b、-NR21aR22a、-NR21aC(O)R22a、-NR21aC(O)OR22a、-NR21aC(O)NR22a、-NR21aS(O)2R22a、-(CH2)1-4C3-C10シクロアルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R2gはHであり、R2hはD、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである。
いくつかの実施形態において、R
2は
(式中、X
2は、N又はCR
2aであり;X
3は、N又はCR
2cであり;X
4は、N又はCR
2dであり;X
5は、N又はCR
2eである)
である。
いくつかの実施形態において、R2は、CR2aである。いくつかの実施形態において、R2は、Nである。
いくつかの実施形態において、R2aは、H、ハロゲン、C1-C6アルキル、又は-COR3bである。いくつかの場合において、R2aは、H、フルオロ、クロロ、メチル、又は-COOHである。
いくつかの実施形態において、R
2は、
である。いくつかの実施形態において、R
2は、
である。
いくつかの実施形態において、X3は、CR2cであり、X4は、CR2dであり、X5はCR2dである。
いくつかの実施形態において、各R2b、R2c、R2d、R2e及びR2fは、それぞれ独立して、H、D、ハロゲン、C1-C6アルキル、C3-C10シクロアルキル、及び-CNからなる群から選択される。いくつかの場合において、各R2b、R2c、R2d、R2e及びR2fは、それぞれ独立して、H、ハロゲン、及びC1-C6アルキルからなる群から選択される。いくつかの場合において、R2b、R2c、R2d、R2e及びR2fのうちの2個は、それぞれ独立して、ハロゲン及びC1-C6アルキルからなる群から選択される。いくつかの場合において、R2b、R2c、R2d、R2e及びR2fのうちの3個は、それぞれ独立して、ハロゲン及びC1-C6アルキルからなる群から選択される。
いくつかの実施形態において、R
2は、
である。いくつかの場合において、R
2b及びR
2fは、C
1-C
6アルキルである。いくつかの場合において、R
2dは、ハロゲンである。
いくつかの実施形態において、X3は、Nであり、X4は、CR2dであり、X5は、CR2dである。いくつかの実施形態において、X3は、CR2cであり、X4は、Nであり、X5は、CR2dである。いくつかの実施形態において、X3は、CR2cであり、X4は、CR2dであり、X5は、Nである。
上述のように、R
1は、
からなる群から選択される。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。
いくつかの実施形態において、R1w及びR1yは、それらが結合している原子と一緒になって3-7員ヘテロシクリルを形成することはない。
いくつかの実施形態において、R1x及びR1yは、それらが結合している原子と一緒になってC3-C10シクロアルキル又は3-7員ヘテロシクリルを形成することはない。
いくつかの実施形態において、R1y及びそれが結合している原子は、R1x、R1wのいずれか、又はそれらが結合している原子と一緒になって、C3-C10シクロアルキル又は
3-7員ヘテロシクリルを形成することはない。
いくつかの実施形態において、R1w、R1x及びR1yのうち少なくとも1つは、H以外である。いくつかの実施形態において、R1w、R1x及びR1yのうちの1つは、H以外である。いくつかの実施形態において、R1w、R1x及びR1yは、H以外である。いくつかの実施形態において、R1w、R1x及びR1yは、Hである。
いくつかの実施形態において、R1wは、H、D、-CN、-C(O)R5b、-S(O)2R5b、-S(O)R5b、C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、-OR5a、-C(O)R5b、-P(O)R5bR6b、-S(O)2R5b、-S(O)R5b、-NR5aR6a、-NR5aC(O)R6a、-NR5aC(O)OR6a、-NR5aC(O)NR6a、-NR5aS(O)2R6a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
いくつかの実施形態において、各R1x及びR1yは、それぞれ独立して、H、D、ハロゲン、OH、-NO2、-SR7a、-OR7a、-C(O)R7b、-P(O)R7bR8b、-S(O)2R7b、-S(O)R7b、-NR7aR8a、-NR7aC(O)R8a、-NR7aC(O)OR8a、-NR7aC(O)NR8a、-NR7aS(O)2R8a、C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C1-C6アルキル、C2-C6アルケニル、C4-C8シクロアルケニル、C2-C6アルキニル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、-OR7a、-C(O)R7b、-P(O)R7bR8b、-S(O)2R7b、-S(O)R7b、-NR7aR8a、-NR7aC(O)R8a、-NR7aC(O)OR8a、-NR7aC(O)NR8a、-NR7aS(O)2R8a、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている。
いくつかの実施形態において、R1wは、H又はC1-C6アルキルである。いくつかの実施形態において、R1xは、H又はC1-C6アルキルである。いくつかの実施形態において、R1yは、H又はC1-C6アルキルである。
いくつかの実施形態において、R1w及びR1yは、それらが結合している原子とともに、3-7員ヘテロシクリルを形成していてもよく;前記3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、OR9a、-C(O)R9b、-P(O)R9bR10b、-S(O)2R9b、-S(O)R9b、-NR9aR10a、-NR9aC(O)R10a、-NR9aC(O)OR10a、-NR9aC(O)NR10a、及び-NR9aS(O)2R10aからなる群から選択される1つ以上の置換基で置換されている
いくつかの実施形態において、R1w及びR1yが、それらが結合している原子とともに、3-7員ヘテロシクリルを形成するとき、R1w及びR1yは隣接している。
いくつかの実施形態において、R1x及びR1yは、それらが結合している原子とともに、C3-C10シクロアルキル又は3-7員ヘテロシクリルを形成していてもよく;前記C3-C10-シクロアルキル及び3-7員ヘテロシクリルは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C1-C6アルキル、-OR9a、-C(O)R9b、-P(O)R9bR10b、-S(O)2R9b、-S(O)R9b、-NR9aR10a、-NR9aC(O)R10a、-NR9aC(O)OR10a、-NR9aC(O)NR10a、及び-NR9aS(O)2R10aからなる群から選択される1つ以上の置換基で置換されている。
いくつかの実施形態において、R1xとR1yが、それらが結合している原子とともに、C3-C10-シクロアルキル又は3-7員ヘテロシクリルを形成するとき、R1xとR1yは隣接している。
いくつかの実施形態において、R1xとR1yが、それらが結合している原子とともに、5-6員環のアリール又はヘテロアリールを形成するとき、R1xとR1yは隣接している。
いくつかの実施形態において、R1zはHである。
上述したように、いくつかの実施形態では、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。
いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。
いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。いくつかの実施形態において、R
1は、
である。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R
1は、以下:
からなる群から選択される。
いくつかの実施形態において、R1a及びR1bは、それぞれ独立して、H、ハロゲン、 -OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである。いくつかの実施形態において、R1a及びR1bのうち少なくとも1つがH以外である。いくつかの実施形態において、R1a及びR1bのうちの1つはH以外である。いくつかの実施形態において、R1a及びR1bの両方がH以外である。いくつかの実施形態において、R1a及びR1bはHである。
いくつかの実施形態において、R1c及びR1dは、それぞれ独立して、H、ハロゲン、-OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである。いくつかの実施形態において、R1c及びR1dのうち少なくとも1つはH以外である。いくつかの実施形態において、R1c及びR1dのうちの1つはH以外である。いくつかの実施形態において、R1c及びR1dの両方がH以外である。いくつかの実施形態において、R1c及びR1dはHである。
いくつかの実施形態において、R1e及びR1fは、それぞれ独立して、H、ハロゲン、-OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである。いくつかの実施形態において、R1e及びR1fのうち少なくとも1つはH以外である。いくつかの実施形態において、R1e及びR1fのうちの1つはH以外である。いくつかの実施形態において、R1e及びR1fの両方がH以外である。いくつかの実施形態において、R1e及びR1fはHである。
いくつかの実施形態において、R1g及びR1hは、それぞれ独立して、H、ハロゲン、-OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである。いくつかの実施形態において、R1g及びR1hのうち少なくとも1つはH以外である。いくつかの実施形態において、R1g及びR1hのうちの1つはH以外である。いくつかの実施形態において、R1g及びR1hの両方がH以外である。いくつかの実施形態において、R1g及びR1hはHである。
本開示の化合物は、塩基性アミノ基を含むことができる。酸性部分も有することができる本開示の化合物への塩基性アミノ基の組み込みは、正味のゼロ電荷を有する双性イオンとして存在すると予想される。双性イオン性化合物は、弱有機酸とは異なる物理化学的特性を有することができる。特に、in vivoでの分布容積の増加ならびに血漿タンパク質結合の低下があり得る。
いくつかの実施形態において、R1a、R1b、R1c、R1d、R1e、R1f、R1g及びR1hのうちの少なくとも1つは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12a以下からなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。
いくつかの実施形態において、R1a、R1b、R1c、R1d、R1e、R1f、R1g及びR1hのうち少なくとも1つは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは、窒素を含む。
いくつかの実施形態において、R1a及びR1bは、それぞれ独立して、H、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1aはHであり、R1bは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1a及びR1bのうち少なくとも1つがH以外である。いくつかの実施形態において、R1a及びR1bのうちの1つはH以外である。いくつかの実施形態において、R1a及びR1bの両方がH以外である。
いくつかの実施形態において、R1a及びR1bは、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12a以下からなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1aはHであり、R1bは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、および-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1a及びR1bのうち少なくとも1つがH以外である。いくつかの実施形態において、R1a及びR1bのうちの1つはH以外である。いくつかの実施形態において、R1a及びR1bの両方がH以外である。いくつかの実施形態において、R1a及びR1bはHである。
いくつかの実施形態において、R1c及びR1dは、それぞれ独立して、H、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1cはHであり、R1dは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1c及びR1dのうち少なくとも1つはH以外である。いくつかの実施形態において、R1c及びR1dのうちの1つはH以外である。いくつかの実施形態において、R1c及びR1dの両方がH以外である。
いくつかの実施形態において、R1c及びR1dは、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1cはHであり、R1dは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、および-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1c及びR1dのうち少なくとも1つはH以外である。いくつかの実施形態において、R1c及びR1dのうちの1つはH以外である。いくつかの実施形態において、R1c及びR1dの両方がH以外である。
いくつかの実施形態において、R1e及びR1fは、それぞれ独立して、H、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1eはHであり、R1fは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1e及びR1fのうち少なくとも1つはH以外である。いくつかの実施形態において、R1e及びR1fのうちの1つはH以外である。いくつかの実施形態において、R1e及びR1fの両方がH以外である。
いくつかの実施形態において、R1e及びR1fは、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1eはHであり、R1fは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、および-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1e及びR1fのうち少なくとも1つはH以外である。いくつかの実施形態において、R1e及びR1fのうちの1つはH以外である。いくつかの実施形態において、R1e及びR1fの両方がH以外である。
いくつかの実施形態において、R1g及びR1hは、それぞれ独立してH、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1gはHであり、R1hは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1g及びR1hのうち少なくとも1つがH以外である。いくつかの実施形態において、R1g及びR1hのうちの1つはH以外である。いくつかの実施形態において、R1g及びR1hの両方がH以外である。
いくつかの実施形態において、R1g及びR1hは、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、R1gはHであり、R1hは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルは、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、および-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルは、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている。いくつかの実施形態において、3-7員ヘテロシクリルは窒素を含む。いくつかの実施形態において、R1g及びR1hのうち少なくとも1つがH以外である。いくつかの実施形態において、R1g及びR1hのうちの1つはH以外である。いくつかの実施形態において、R1g及びR1hの両方がH以外である。
本開示は、式が式(I):
(例えば、式(I-1)、(I-2)、(I-3)、(I-4)、(I-5)、及び(I-6)である化合物、及びその薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体を提供する。
本開示は、式が式(Ia):
である化合物、及びその薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体を提供する。
本開示は、式(Ib):
である化合物、及びその薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体を提供する。
いくつかの実施形態において、本開示は、以下の特徴:
a)R
100は、Hである;
b)R
1は、
である;
c)R
2は、
である;及び
d)X
2はCH又はCFである
のうちの1つ、2つ、又は3つを有する、式(I)、(Ia)、又は(Ib)の化合物を提供する。
いくつかの実施形態において、本開示は、以下の特徴:
a)R
100は、Hである;
b)R
1は、
である;
c)R
2は、
である;及び
d)X
3はCR
2cであり、X
4はCR
2dであり、X
5はCR
2dである
のうちの1つ、2つ、又は3つを有する、式(I)、(Ia)、又は(Ib)の化合物を提供する。
代表的な化合物を表1に示す。個々のエナチオマ-及びジアステレオマーは、化合物番号及び化合物名によって下の表に含まれており、それらの対応する構造は、それらから容易に決定することができることが理解される。場合によっては、エナンチオマー又はジアステレオマーは、それぞれの特性、たとえば、キラルHPLCでの保持時間又はその生物活性によって識別され、キラル中心の絶対立体配置は任意に割り当てられる。
いくつかの実施形態において、提供されるのは、表1の化合物番号1-210から選択される化合物、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体である。いくつかの実施形態において、提供されるのは、表1の化合物番号1-158から選択される化合物、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体である。いくつかの実施形態では、表1の化合物番号159-158から選択される化合物、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体が提供される。いくつかの実施形態において、化合物は、表1の化合物番号1-158、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体から選択される。いくつかの実施形態において、化合物は、表1の化合物番号1-39、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体から選択される。いくつかの実施形態において、化合物は、表1の化合物番号37、60、68-69、72-73、102-103及び159-170、又は塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、その異性体、又は互変異性体。いくつかの実施形態において、化合物は、表1の化合物番号171-189、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体から選択される。いくつかの実施形態において、化合物は、表1の化合物番号190-202、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体から選択される。いくつかの実施形態において、化合物は、表1の化合物番号203-210、又はそれらの塩(例えば、薬学的に許容される塩)、溶媒和物(例えば、水和物)、異性体、又は互変異性体から選択される。
いくつかの実施形態では、本開示は、以下からなる群から選択される化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、及びそれらの互変異性体を提供する:
いくつかの実施形態では、本開示は、以下からなる群から選択される化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、及びそれらの互変異性体を提供する:
本開示は、以下からなる群から選択される化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、及びそれらの互変異性体を提供する:
本開示は、以下からなる群から選択される化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、及びそれらの互変異性体を提供する:
本開示は、以下からなる群から選択される化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、及びそれらの互変異性体を提供する:
本開示は、以下からなる群から選択される化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、及びそれらの互変異性体を提供する:
化合物の合成方法
本開示の化合物は、標準化学を含む様々な方法で製造することができる。適切な合成経路は、本明細書に与えられたスキームに示されている。
本明細書に開示された化合物は、以下の合成スキームによって部分的に記載されているように、有機合成の技術分野で知られている方法によって調製することができる。本明細書に記載されたスキームにおいて、一般的な原理又は化学に基づいて、必要に応じて、敏感な基又は反応性基のための保護基が採用されることは、よく理解される。保護基は、有機合成の標準的な方法に従って操作される(T.W.Greene 及び P.G.M.Wuts,“Protective Groups in Organic Synthesis,” Third edition,Wiley,New York 1999).これらの群は、当技術に熟練した者には容易に明らかな方法を用いて、化合物合成の都合の良い段階で除去される。選択工程、反応条件及びその実行順序は、本明細書に開示されている化合物の調製と一致しているものとする。
当業者であれば、本明細書に開示された化合物に立体中心が存在するかどうかを認識するであろう。いくつかの実施形態では、本開示の化合物は、エナンチオマー又はジアステレオマーの立体異性体として存在することができる。したがって、本開示は、両方の可能な立体異性体(合成において特定されない限り)を含み、ラセミ化合物だけでなく個々のエナンチオマー及び/又はジアステレオマーも含む。化合物が単一のエナンチオマー又はジアステレオマーとして望まれる場合、立体特異的合成によって又は最終生成物もしくは任意の都合のよい中間体の分解によってそれを取得してもよい。例えば、本開示のエナンチオマー的に純粋な化合物は、エナンチオマー的に純粋なキラルビルディングブロックを用いて調製することができる。或いは、最終化合物のラセミ混合物又は高度中間体のラセミ混合物は、所望のエナンチオマー的に純粋な中間体又は最終化合物を得るために、本明細書に記載されているようなキラル精製を受けることができる。高度な中間体がその個々のエナンチオマーに精製される実施形態では、各個々のエナンチオマーは、本開示の最終的なエナンチオマー的に純粋な化合物を得るために別々に実施することができる。最終製品、中間体、又は出発物質の分解は、当技術分野で知られている任意の適切な方法によって影響を受けることができる。例えば、E.L.Eliel,S.H.Wilen,及びL.N.Manderによる”Stereochemistry of Organic Compounds”(Wiley-lnterscience,1994)を参照のこと。
本明細書に記載の化合物は、市販の出発物質から作られてもよいし、公知の有機、無機、及び/又は酵素プロセスを用いて合成されてもよい。
化合物の調製
一例として、本開示の化合物は、本開示の化合物を組み立てるシーケンスの例を含む一般スキーム1及び2に概説される工程に従うことによって合成することができる。出発物質は、市販されているか、又は報告されている文献中の公知の手順によってもしくは説明の通りに製造する。好ましい方法は、本明細書に記載された方法を含むが、これらに限定されない。
一般スキーム1
式I(化合物F)は、一般的なスキーム1に概説された一般的な手順に従って調製することができる。一般スキーム1において、PG
G1は保護基である。スルホンアミド(A)を保護して、保護されたスルホンアミド(B)を得る。保護されたスルホンアミド(B)は、活性化(すなわち、デオキシクロロ化又は触媒作用)及びアンモニア源(又はアミンでR
100-を得ることができる-図示せず)との反応による処理を経て、保護されたスルホンイミド(C)に変換される。保護されたスルホンイミド(C)をイソシアネート(D)と反応させ、化合物(E)を得る。次いで、化合物(E)を脱保護して化合物(F)を得る。
一般スキーム2
式I(化合物L)はまた、一般的なスキーム2に概説された一般的な手順に従って調製することができる。一般スキーム2において、PGG2は保護基であり、LG1は離脱基(通常、反応性種として活性化され得るハロゲン、すなわちリチウム-ハロゲン交換を介して)である。化合物(G)及び化合物(H)の反応に続いて、活性化及びアンモニア源(図示)又は第一級アミン(置換N-R100については、図示せず)での処理を行うと、保護されたスルホンイミド(I)が得られる。次いで、化合物(K)を脱保護して化合物(L)を得る。
一般的なスキーム3は、R
1部位の代表的な合成を示す。
一般スキーム3
一般的なスキーム3は、化合物(R)又はその塩もしくは溶媒和物の調製を示す。一般スキーム3において、X1は、ハロゲン(例えば、クロロ、ブロモ、ヨード、又はフルオロ)、スルホネート(例えば、ノシル酸塩、トシル酸塩、又はメシル酸塩)、硝酸塩、リン酸塩、又は他の適当な離脱基であり、PGN1は、アミノ保護基である。
化合物(M)を保護して化合物(N)を得る。次いで、化合物(N)をアルキル化して化合物(O)を形成し、例えば光延反応を行う。化合物(O)は脱保護と環化を経て化合物(P)を形成する。次いで、化合物(P)をスルホン化試薬と反応させて化合物(Q)を生成させる。次いで、化合物(Q)を酸化(すなわち塩素化を介して)し、次いでアンモニア源と反応させて化合物(R)を形成する。或いは、化合物(P)を臭素化して、一般スキーム2の化合物(G)のような出発物質を与えてもよい。
一般スキーム4
式I(化合物X)は、一般的なスキーム4に概説された一般的な手順に従って調製することができる。塩化スルホニル(S)は、還元を経てスルフィン酸メチルエステル(T)に変換され、次いで塩化スルフィニルが形成され、その後エステル化される。スルフィン酸メチルエステル(T)は、アミン源(soure)(LiHMDSなど)との反応を経てスルフィンアミド(U)に変換され、次いで加水分解される。スルフィンアミド(U)をイソシアネート(V)と反応させて化合物(W)を得る。次いで、化合物(W)を酸化的塩素化を経てスルホンイミド(X)に変換し、次いでアミン源又はアンモニア源と反応させて、化合物(W)をスルホンイミド(X)に変換する。
医薬品組成物
開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びその互変異性体は、それ自体を独立して使用することができるが、一般に、1種以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びその互変異性体(有効成分)が、薬学的に許容されるアジュバント又は担体と関連している医薬組成物の形態で投与される。適切な医薬組成物の選択及び調製のための従来の手順は、例えば、”Pharmaceutical-The Science of Dosage Form Designs,M.E.Aulton,Churchill Livingstone,1988”に記載されており、その全体が参照により本明細書に組み込まれている。いくつかの実施形態において、化合物、又はそれらの薬学的に許容される塩、異性体、プロドラッグ、及び互変異性体は、水和物の形態である。
投与形態に応じて、医薬組成物は、約0.05から約99重量%(重量%)、より具体的に約0.05から約80重量%、さらに具体的に約0.10から約70重量%、よりさらに具体的に約0.10から約50重量%の、1つ又は複数の開示された化合物、及び薬学的に許容される塩、水和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体からなり、すべての重量%は組成物の総量に基づく。
本開示はまた、1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体からなる医薬組成物を、薬学的に許容される担体と関連させて、本明細書で定義されているように提供する。
本開示はさらに、本開示の医薬組成物を調製するためのプロセスを提供し、このプロセスは、1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を、薬学的に許容されるアジュバント又は担体と本明細書で定義されているように混合することからなる。本開示の医薬組成物はまた、従来の混合、造粒又はコーティングの方法に従って調製することができる。
本開示の医薬組成物は、1つ又は複数の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を、1つ又は複数の薬学的に許容される担体と一緒に製剤化した、処置上有効な量からなることができる。また、以下の薬学的に許容される担体として機能し得る材料の例としては、製剤化者の判断により、医薬組成物中に存在し得る:乳糖、グルコース、ショ糖等の糖類;コーンスターチ、馬鈴薯澱粉等の澱粉類;カルボキシメチルセルロースナトリウム、エチルセルロース、酢酸セルロース等のセルロース及びその誘導体;粉末状のトラガカンス;麦芽;ゼラチン;タルク;ココアバター、座薬用ワックス等の賦形剤;ピーナッツ油、綿実油、ベニバナ油、ゴマ油、オリーブ油、コーン油、大豆油等の油類;プロピレングリコール等のグリコール類、オレイン酸エチル、ラウリン酸エチルなどのエステル類;寒天;水酸化マグネシウム、水酸化アルミニウムなどの緩衝剤;アルギン酸;ピロゲンフリー水;等張生理食塩水;リンガー溶液;エチルアルコール;及びリン酸緩衝液、ならびにラウリル硫酸ナトリウム、ステアリン酸マグネシウムなどの他の非毒性の互換性のある潤滑剤、着色剤、離型剤、コーティング剤、甘味料、香料、防腐剤、及び酸化防止剤。
意図された投与様式に応じて、開示された医薬組成物は、固体、半固体又は液体の投与形態、例えば、注射剤、錠剤、坐薬、丸薬、時間放出カプセル、エリキシル、チンキ剤、エマルジョン、シロップ、粉末、液体、懸濁液、又はそれらのような形態であり得、時に単位用量で、従来の医薬慣行と一致している。これらのモードは、経口投与、経鼻投与、非経口投与(静脈内投与(ボーラス及び輸液の両方)、筋肉内投与、又は皮下注射による)、経皮投与、膣投与、頬部投与、直腸投与、又は局所投与(粉末、軟膏、又は滴下による)のような全身投与又は局所投与を含むことができる。これらのモードはまた、膀胱内、腹腔内、経口又は鼻腔内スプレーとして、又は吸入のための液体エアロゾル又は乾燥粉末医薬組成物としてもよい。いくつかの実施形態において、1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体からなる開示の医薬組成物は、経口投与のためのものである。いくつかの実施形態において、1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体からなる開示の医薬組成物は、静脈内投与のためのものである。
経口投与用の固形製剤としては、カプセル剤、錠剤、錠剤、粉末、顆粒剤などが挙げられる。このような固形剤形において、1種以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体は、以下のような少なくとも1種の不活性で薬学的に許容される賦形剤又は担体と混合されてもよい:希釈剤、充填剤又は拡張剤、結合剤、湿潤剤、崩壊剤、溶液遅延剤、吸収促進剤、湿潤剤、吸収剤、滑沢剤、乳化剤又は分散剤、及び/又は1種以上の開示された化合物の吸収を促進する剤、ならびにそれらの薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体、カプセル、錠剤、丸薬の場合、剤形は緩衝剤を含んでいてもよい。
また、乳糖や乳糖、高分子量ポリエチレングリコールなどの賦形剤を用いて、軟包装や硬包装のゼラチンカプセルの充填剤として、同様のタイプの固形医薬組成物を使用してもよい。
錠剤、ドラージ剤、カプセル剤、錠剤、顆粒剤の固形剤形は、医薬製剤化技術においてよく知られている腸溶性コーティング剤などのコーティング剤やシェルを用いて調製することができる。それらは、任意に不透明化剤を含んでいてもよく、また、それらは、1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を、腸管の特定の部分でのみ、又は優先的に、任意に、遅延的に放出する組成物であってもよい。使用することができる埋め込み組成物の例としては、高分子物質及びワックスが挙げられる。
開示された1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体は、また、本明細書に記載されているように、1種以上の賦形剤とマイクロカプセル化された形態であってもよい。錠剤、ドラージ剤、カプセル剤、錠剤、顆粒剤の固形剤形は、腸溶性コーティング、放出制御コーティング、及び薬学的製剤化技術でよく知られている他のコーティングのようなコーティング及びシェルで調製することができる。このような固形剤形において、1種以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体は、ショ糖、ラクトース又はデンプンのような少なくとも1種の不活性希釈剤と混合されてもよい。そのような剤形はまた、通常の慣行として、不活性希釈剤以外の追加の物質、例えば、ステアリン酸マグネシウム及び微結晶セルロースのような打錠潤滑剤及び他の打錠補助剤を含んでいてもよい。カプセル、錠剤、丸薬の場合、剤形はまた、緩衝剤を含んでいてもよい。それらは、任意に不透明化剤を含んでいてもよく、また、それらは、1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を、腸管の特定の部分でのみ、又は優先的に、任意に、遅延的に放出する組成物であってもよい。使用することができる埋め込み組成物の例は、高分子物質及びワックスを含むことができる。
経口投与用の液体製剤は、薬学的に許容されるエマルジョン、マイクロエマルジョン、溶液、懸濁液、シロップ及びエリキシルを含むことができる。開示された1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体に加えて、液体製剤は、例えば、以下のような当技術分野で一般的に使用される不活性希釈剤を含んでもよい:水又は他の溶媒、可溶化剤及び乳化剤、例えばエチルアルコール、イソプロピルアルコール、炭酸エチル、酢酸エチル、ベンジルアルコール、安息香酸ベンジル、プロピレングリコール、1,3-ブチレングリコール、ジメチルホルムアミド、油(特に綿実油、落花生油、コーン油、胚芽油、オリーブ油、ヒマシ油及びゴマ油)、グリセロール、テトラヒドロフルフリルアルコール、ポリエチレングリコール及びソルビタンの脂肪酸エステル、及びそれらの混合物、また、口腔用医薬組成物には、不活性希釈剤の他に、湿潤剤、乳化剤、懸濁剤、甘味料、香料などのアジュバントを含有させることができる。
注射可能な医薬組成物、例えば、1種以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体からなる無菌注射可能な水性懸濁液は、適切な分散剤又は湿潤剤及び懸濁剤を使用して、公知の技術に従って処方することができる。本発明の無菌注射可能な医薬組成物はまた、例えば1,3-ブタンジオール中の溶液として、非毒性の非経口的に許容される希釈剤又は溶媒中の無菌注射可能な溶液、懸濁液又はエマルジョンであってもよい。採用することができる許容可能なビヒクル及び溶媒としては、水、リンゲル溶液、1%リドカイン、U.S.P.及び等張性塩化ナトリウム溶液が挙げられる。加えて、減菌済みの不揮発性油が、溶媒又は懸濁媒として従来通り採用される。この目的のために、合成モノグリセリド又は合成ジグリセリドを含むいかなる無刺激の不揮発性油も採用することができる。また、注射剤組成物には、オレイン酸等の脂肪酸が使用される。
注射可能な医薬組成物は、例えば、細菌保持フィルターを介して濾過することによって、又は使用前に滅菌水又は他の滅菌可能な注射媒体に溶解又は分散させることができる滅菌可能な固形医薬組成物の形態で滅菌剤を組み込むことによって滅菌することができる。
1つ以上の開示された化合物、及びその薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体の効果を延長するために、1つ以上の開示された化合物、及びその薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体の皮下注射又は筋肉内注射からの吸収を遅らせることが望ましい場合がある。このことは、水難溶性の結晶質又は非晶質材料の液体懸濁液の使用によって達成することができる。開示された1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の吸収率は、次いで、その溶解率に依存し、それは、結晶サイズ及び結晶形態に依存してもよい。或いは、非経口的に投与された1種以上の開示された化合物及びその薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及び互変異性体の吸収の遅延は、1種以上の開示された化合物及びその薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及び互変異性体を油性ビヒクル中に溶解又は懸濁させることによって達成されてもよい。注射可能なデポ形態は、ポリラクチド-ポリグリコリドのような生分解性ポリマー中に、1種以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体のマイクロカプセルマトリックスを形成することによって製造される。1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及び互変異性体とポリマーとの比率、及び採用される特定のポリマーの性質に応じて、1つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及び互変異性体の放出速度を制御することができる。他の生分解性重合体の例としては、ポリ(オルトエステル)及びポリ(無水物)が挙げられる。デポ注射可能な医薬組成物はまた、1種以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を、体組織に適合するリポソーム又はマイクロエマルジョン中に巻き込むことによって調製されてもよい。
直腸又は膣投与のための医薬組成物は、1種以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を、以下のような適切な非刺激性賦形剤又は担体と混合することによって調製することができる坐薬であってもよい:ココアバター、ポリエチレングリコール又は坐剤用ワックスであって、常温では固体であるが体温では液体であり、したがって直腸又は膣腔内で溶融し、開示されている1つ以上の化合物を放出するもの、及びそれらの薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及び互変異性体。
開示された1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体は、脂肪性エマルジョン又は懸濁液から調製することができる坐剤としても製剤化することができ;担体としてプロピレングリコールのようなポリアルキレングリコールを使用する。
開示された1種以上の化合物の局所又は経皮投与のための投与形態、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体は、軟膏、ペースト、クリーム、ローション、ゲル、粉末、溶液、スプレー、吸入剤又はパッチを含む。開示された1種以上の化合物、及びそれらの薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及び互変異性体は、薬学的に許容される担体、及び必要に応じて必要とされる防腐剤又は緩衝剤と無菌条件下で混合される。眼科用医薬組成物、点耳薬などもまた、本開示の範囲内であると考えられる。
軟膏、ペースト、クリーム及びゲルは、開示された1種又は2種以上の化合物に加えて、薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ及びそれらの互変異性体、動物性及び植物性の油脂、油脂、ワックス、パラフィン、デンプン、トラガカンス、セルロース誘導体、ポリエチレングリコール、シリコーン、ベントナイト、ケイ酸、タルク及び酸化亜鉛などの賦形剤、又はそれらの混合物を含んでいてもよい。
一つ以上の開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体はまた、一つ以上の開示された化合物、及び薬学的に許容される塩、溶解物(例えば、水和物)、異性体、プロドラッグ及びそれらの互変異性体、乳糖、タルク、ケイ酸、水酸化アルミニウム、ケイ酸カルシウム及びポリアミド粉末などの賦形剤、又はこれらの物質の混合物に加えて、含有することができる外用粉体及びスプレーとしての使用のために処方されてもよい。スプレーはさらに、クロロフルオロ炭化水素などの慣用的な推進剤を含むことができる。
経皮吸収型パッチには、体内への化合物の制御された送達を提供するという付加的な利点がある。このような剤形は、化合物を適切な媒体に溶解又は分注することにより製造することができる。吸収増強剤はまた、開示された1つ以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の皮膚を横切るフラックスを増加させるために使用することができる。速度は、速度制御膜を提供することによって、又は開示された1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体をポリマーマトリックス又はゲル中に分散させることによって制御することができる。
本開示の医薬組成物はまた、液体エアロゾル又は吸入可能な乾燥粉末として送達されるように製剤化されてもよい。液体エアロゾル医薬組成物は、末端気管支及び呼吸器気管支に送達され得る粒子サイズに主にネブリングされてもよい。液体エアロゾル及び吸入可能な乾燥粉末医薬組成物は、末梢気管支に至るまで、そして最終的には実質組織に送達されてもよい。
本開示のエアロゾル化された医薬組成物は、ジェット、振動多孔質プレート又は超音波ネブライザーのようなエアロゾル形成装置を用いて送達されてもよく、このような装置は、1-5μmの間に優勢に質量媒体平均直径を有するエアロゾル粒子の形成を可能にするように選択される。さらに、医薬組成物は、バランスのとれた浸透圧イオン強度及び塩化物濃度を有していてもよく、開示された1種以上の化合物の有効量を送達することができる最小のエアロゾル化可能な体積、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を有していてもよい。さらに、エアロゾル化された医薬組成物は、気道の機能を否定的に損なうことがなく、望ましくない副作用を引き起こすこともない。
本開示のエアロゾル医薬組成物の投与に適したエアロゾル化装置としては、例えば、ジェット式、振動多孔板式、超音波ネブライザー、及び通電式乾燥粉末吸入器が挙げられ、これらの装置は、本開示の医薬組成物を1-5pmの範囲の大きさのエアロゾル粒子径に優勢にネブレーションすることができる。本出願において優勢とは、生成された全てのエアロゾル粒子の少なくとも70%、しかし任意に90%以上が1-5μmの範囲であることを意味する。ジェットネブライザは、空気圧で液体をエアゾール状の液滴に分解するものである。振動多孔質プレートネブライザーは、急速に振動する多孔質プレートによって生成されたソニック真空を使用して、多孔質プレートを介して溶媒の液滴を押し出すために動作する。超音波ネブライザーは、圧電結晶が液体を小さなエアゾール液滴にせん断することで動作する。次のようなさまざまな適切なデバイスを利用できる:例えば、AeroNeb及びAeroDose振動多孔質プレートネブライザー(AeroGen,Inc.,Sunnyvale,Califolnia),Sidestream7ネブライザー(Medic-Aid Ltd.,West Sussex,England),PariLC7及びPariLC Star7ジェットネブライザー(Pari Respiratory Equipment,Inc.,Richmond,Virginia)、エアロソニック(DeVilbiss Medizinische Produkte(Deutschland)GmbH,Heiden,Germany)及びμLtraAire7(Omron Healthcare,Inc.,Vernon Hills,Ill.)超音波ネブライザー。
使用方法
開示された化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、ならびに組成物は、本明細書で論じられるように、医薬品として有用であり得る。
本開示は、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の有効量を投与する工程を含む、疾患を処置するための方法を提供し、それにより、疾患を必要とする対象の疾患を処置する方法を提供する。
本開示は、本開示の1つ以上の医薬組成物の有効量を投与する工程を含む、疾患を処置するための方法を提供し、それにより、疾患を必要としている対象において疾患を処置する方法を提供する。
本開示は、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、その異性体、プロドラッグ、及び互変異性体、又はそれらの1種以上の医薬組成物を提供し、それらを必要とする対象の疾患の処置に使用するための本開示の医薬組成物を提供する。
本開示は、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の、それを必要とする対象における疾患の処置のための使用を提供する。本開示はまた、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の使用を、必要とする対象における疾患の処置のために提供し、ここで、疾患は、インフラマソーム阻害に応答性である。
本開示は、それを必要とする対象における疾患の処置のための本開示の1種以上の組成物の使用を提供する。本開示はまた、本開示の1つ以上の組成物を、その必要とする対象における疾患の処置のために使用することを提供し、ここで、疾患は、インフラマソーム阻害に応答性である。
本開示は、本開示の1種又は2種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の、疾患の処置のための医薬の製造における使用を提供する。本開示はまた、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の使用を、インフラマソーム阻害に応答性のある疾患の処置のための医薬の製造において提供する。
本開示は、疾患の処置のための医薬の製造における本開示の1つ以上の組成物の使用を提供する。本開示はまた、本開示の1種以上の組成物を、インフラマソーム阻害に応答性のある疾患の処置のための医薬の製造において使用することを提供する。
本開示は、本開示の1種又は2種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の、疾患の処置のための医薬としての使用を提供する。
本開示は、疾患の処置のための医薬としての本開示の1種又は2種以上の組成物の使用を提供する。
いくつかの実施形態では、疾患は、インフラマソームの活性化の阻害に応答するものである。いくつかの実施形態において、疾患は、NLRP3インフラマソームの活性化の阻害に応答するものである。
いくつかの実施形態によれば、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、又は医薬組成物は、NLRP3の特定の阻害剤として有用である。
いくつかの実施形態において、疾患は、IL-6、IL-1β、IL-17、IL-18、IL-1α、IL-37、IL-22、IL-33、及びTh17細胞のうちの1つ以上の調節に応答性である。いくつかの実施形態において、疾患は、IL-1β及びIL-18の1つ以上の調節に応答性である。
いくつかの実施形態において、調節は、IL-6、IL-1β、IL-17、IL-18、IL-1α、IL-37、IL-22、及びIL-33のうちの1つ以上の阻害である。いくつかの実施形態において、調節は、IL-1β及びIL-18のうちの1つ以上の阻害である。
いくつかの実施形態において、Th17細胞の調節は、IL-17の産生及び/又は分泌の阻害によるものである。
いくつかの実施形態において、疾患は、免疫系、心血管系、内分泌系、胃腸管、腎臓系、呼吸器系、中枢神経系の疾患、疾患又は病態であり、がん又は他の悪性病変であり、及び/又は病原体によって引き起こされるか、又はそれと関連している。
疾患の広範なカテゴリに従って定義された一般的な実施形態は、相互に排他的ではないことが理解されるであろう。この点において、任意の特定の疾患は、本明細書に開示された一般的な実施形態のうちの1つ以上に従って分類され得る。非限定的な例としては、自己免疫疾患であり、内分泌系の疾患であるI型糖尿病がある。
いくつかの実施形態において、疾患は免疫系のものである。いくつかの実施形態において、疾患は、炎症性疾患又は自己免疫性疾患である。
いくつかの実施形態において、疾患は肝臓のものである。
いくつかの実施形態において、疾患は肺のものである。
いくつかの実施形態において、疾患は皮膚のものである。
いくつかの実施形態において、疾患は心臓血管系のものである。
いくつかの実施形態において、疾患は、癌、腫瘍又は他の悪性腫瘍である。本明細書で使用されるように、癌、腫瘍、及び悪性腫瘍は、異常又は異常な細胞増殖、分化、及び/又は移動を特徴とする、異常又は異常な細胞増殖、分化、及び/又は移動を伴う疾患、又は疾患に関連する細胞又は組織を指し、この疾患は、しばしば、腫瘍形成、腫瘍マーカーの発現、腫瘍抑制剤発現又は活性の損失、及び/又は異常又は異常な細胞表面マーカーの発現に関連する1つ以上の遺伝子変異又は他の遺伝的変化を含む異常又は異常な分子表現型を伴うことを特徴とする。いくつかの実施形態において、癌、腫瘍、及び悪性腫瘍は、これらに限定されないが、肉腫、リンパ腫、白血病、固形腫瘍、芽球腫、グリオーマ、癌、メラノーマ、及び転移性癌を含むことができる。がん、腫瘍及び悪性病変のより包括的なリストは、その全体を参照として本明細書に援用する、国立がん研究所のウェブサイトhttp://www.cancer.gov/cancertopics/types/alphalistに見出され得る。
いくつかの実施形態において、疾患は腎系のものである。
いくつかの実施形態において、疾患は胃腸管の疾患である。
いくつかの実施形態において、疾患は呼吸器系のものである。
いくつかの実施形態において、疾患は内分泌系のものである。
いくつかの実施形態において、疾患、疾患は、中枢神経系(CNS)の疾患である。
いくつかの実施形態において、疾患は病原体によって引き起こされるか、又は病原体と関連している。病原体は、ウイルス、細菌、原生生物、寄生虫もしくは真菌、又は哺乳類に感染することができる任意の他の生物であり得るが、これらに限定されない。
ウイルスの非限定的な例としては、インフルエンザウイルス、サイトメガロウイルス、エプスタインバーウイルス、ヒト免疫不全ウイルス(HIV)、チクングニアウイルス、ロス川ウイルスなどのアルファウイルス、デングウイルス、ジカウイルス、パピローマウイルスなどのフラビウイルスなどが挙げられるが、これらに限定されるものではない。
病原性細菌の非限定的な例としては、これらに限定されないが、以下が挙げられる:黄色ブドウ球菌、ヘリコバクターピロリ、アントラシス菌、百日咳菌、コリネバクテリウム ディプテリア、クロストリジウム テタニ、クロストリジウム ボツリヌス菌、肺炎球菌、膿疱性連鎖球菌、リステリア モノサイトゲネス、ヘモフィラス インフルエンザ、パスツレイア マルチシダ、赤痢症重症菌、結核菌、レプラエ菌 肺炎マイコプラズマ、マイコプラズマ ホミニス、ミネンチス菌、淋菌、リケッチア リケッチイ、レジオネラ ニューモフィラ、肺炎クレブシエラ、緑膿菌 プロピオンバクテリウム アクネス、トレポネーマ パリダム、クラミジア トラコマティス、ビブリオ コレラ、サルモネラ チフス、サルモネラ チフス、ボレリア ブルグドルフェリ、イエシニア ペスティス。
原生生物の非限定的な例としては、これらに限定されないが、マラリア原虫、バベシア、ジアルジア、エントアメーバ、リーシュマニア、及びトリパノソーマが挙げられる。
蠕虫の非限定的な例としては、これらに限定されるものではないが、システィサイム、ラウンドワーム、サナダムシ及びフリュークを含む蠕虫類が挙げられる。
菌類の非限定的な例としては、これらに限定されないが、カンジダ種及びアスペルギルス種が挙げられる。
疾患は、以下からなるグループから選択される:クリオピリン関連周期症候群(CAPS)を含む構成的炎症、マックルウェルズ症候群(MWS)、家族性寒冷自己炎症性症候群(FCAS)、新生児発症多系統炎症性疾患(NOMID);自己炎症性疾患、家族性地中海熱(FMF)、TNF受容体関連周期性症候群(TRAPS)、メバロネートキナーゼ欠損症(MKD)、高免疫グロブリン血症D及び周期性発熱症候群(H IDS)、インターロイキン1受容体(DIRA)アンタゴニストの欠損症、マジェド症候群、化膿性関節炎、壊疽性膿皮症及びニキビ(PAPA)、A20のハプロイン不全(HA20)、小児肉芽腫性関節炎(PGA)、PLCG2-関連抗体欠損及び免疫異常(PLAID)、PLCG2-関連自己炎症、抗体欠損及び免疫異常(APLAID)、B細胞免疫不全を伴うシデロバティック貧血、周期的発熱、及び発育遅延(SIFD)、スウィート症候群;慢性非細菌性骨髄炎(CNO)、慢性再発性多巣性骨髄炎(CRMO)及び滑膜炎、にきび、膿疱症、骨粗鬆症、骨炎症候群(SAPHO)、多発性硬化症(MS)、1型糖尿病、乾癬、関節リウマチ、ベーチェット病、シェーグレン症候群及びシュニッツラー症候群を含む自己免疫疾患、特発性肺線維症(IPF)、慢性閉塞性肺疾患(COPD)、ステロイド抵抗性喘息、アスベスト症、珪肺症、嚢胞性線維症を含む呼吸器疾患、パーキンソン病、アルツハイマー病、運動ニューロン病、ハンチントン病、脳マラリア、肺炎球菌性髄膜炎による脳損傷を含む中枢神経系疾患、代謝性疾患(2型糖尿病、動脈硬化症、肥満、痛風、偽痛風など)、眼球上皮疾患、加齢黄斑変性症(AMD)、角膜感染症、ぶどう膜炎、ドライアイなどの眼疾患、腎臓疾患(慢性腎臓病、シュウ酸腎症、糖尿病性腎症など)、非アルコール性脂肪肝炎、アルコール性肝疾患を含む肝臓疾患;接触過敏症、日焼けを含む皮膚の炎症反応;変形性関節症、全身性若年性特発性関節炎、成人型スティル病、再発性多発性軟骨炎を含む関節の炎症反応、アルファウイルス(チクングニア、ロス川)、フラビウイルス(デング熱、ジカウイルス)、インフルエンザ、HIVを含むウイルス感染症;膿疱性ヒドラデン炎(HS)及びその他の嚢胞を引き起こす皮膚疾患;肺がん転移、膵臓がん、胃がん、骨髄異形成症候群、白血病を含むがん。多発性筋炎;脳卒中;心筋梗塞;移植片対宿主病;高血圧;大腸炎;蠕虫感染症;細菌感染症;腹部大動脈瘤;創傷治癒;うつ病、心理的ストレス;ドレスラー症候群を含む心膜炎;虚血再灌流傷害、よびNLRP3の生殖細胞変異又は体細胞性非サイレント変異を有することが決定されている任意の疾患。
いくつかの実施形態において、疾患は、クライオピリン関連周期性症候群(CAPS)である。
いくつかの実施形態において、疾患はアテローム性動脈硬化症である。
記載されたそれらの非限定的な一例において、処置されている疾患は、NASHである。NLRP3のインフラマソーム活性化は、NASHにおける炎症性リクルートの中心であり、NLRP3の阻害は肝線維化の予防と逆転の両方の可能性がある。本開示の1種以上の化合物、又は薬学的に許容される塩、プロドラッグ、溶媒和物、水和物、異性体、プロドラッグ、及びそれらの互変異性体、又は本開示の医薬組成物は、肝臓組織におけるNLRP3インフラマソームの機能を遮断することにより、肝臓炎症の組織学的な減少、マクロファージ及び好中球のリクルートの減少、及びNF-κΒ活性化の抑制を引き起こすことができる。NLRP3の阻害は、プロIL-1βの肝発現を低下させ、肝及び循環IL-1β、IL-6及びMCP-1レベルを正常化し、それによって疾患の処置を補助することができる。
記載されたもののさらなる非限定的な例では、処置される疾患は、重度のステロイド抵抗性(SSR)喘息である。呼吸器感染症は、SSL喘息を促進するNLRP3インフラマソーム/カスパーゼ-1/IL-1βシグナル伝達軸を肺内で誘導する。NLRP3インフラマソームは、プロカスパーゼ-1を動員し、活性化して、IL-1β応答を誘導する。したがって、NLRP3インフラマソームにより誘導されるIL-β応答は感染の制御において重要ではあるが、過剰な活性化は異常な炎症をもたらし、SSR喘息及びCOPDの病因と関連している。特定の疾患プロセスを標的とする1種以上の化合物、又は薬学的に許容される塩、プロドラッグ、水和物、水和物、異性体、プロドラッグ、及び互変異性体、又は本開示の医薬組成物の投与は、ステロイド又はIL-1βを用いて炎症反応を非特異的に阻害するよりも処置的に魅力的である。NLRP3インフラマソーム/カスパーゼ-1 /IL-1βシグナル伝達軸を、1つ以上の化合物、又は薬学的に許容される塩、プロドラッグ、水和物、水和物、異性体、プロドラッグ、及びそれらの互変異性体、又は本開示の医薬組成物で標的化することは、したがって、SSR喘息及び他のステロイド抵抗性炎症状態の処置に有用であるかもしれない。
記載されたもののさらなる非限定的な例では、処置されている疾患はパーキンソン病である。パーキンソン病は最も一般的な神経変性運動疾患であり、疾患の病理学的特徴である、誤って折り畳まれたα-シヌクレイン(Syn)のレビー小体への蓄積を伴う、ドーパミン作動性ニューロンの選択的喪失を特徴とする。この疾患の初期には慢性ミクログリア神経炎症を見出すことができ、これが病理を推進すると提唱されている。
パーキンソン病の進行にはミクログリアのNLRP3が中心的な役割を果たしていることが示唆されている。NLRP3インフラナソームは、Sykキナーゼ依存性のメカニズムを介してフィブリラーSynによって活性化され、また、ドーパミン変性の初期段階でSyn病理が存在しない場合にも発生し、神経細胞の損失を駆動する。本開示の1種以上の化合物、又は薬学的に許容される塩、プロドラッグ、溶媒和物、水和物、その異性体、プロドラッグ、及び互変異性体、又は本開示の医薬組成物は、フィブリラーSyn又はミトコンドリア機能不全によるNLRP3インフラマソーム活性化をブロックし、それにより、ニグロストリアドーパミン系の効果的な神経保護を付与し、パーキンソン病の処置を補助することができる。
いくつかの実施形態において、方法は、以下を含むがこれらに限定されない疾患を処置する:細菌感染症、ウイルス感染症、真菌感染症、炎症性腸疾患、セリアック病、大腸炎、腸管過形成、がん、メタボリックシンドローム、肥満、関節リウマチ、肝臓病、肝線維症、肝性ステアトーシス、脂肪肝疾患、痛風、狼瘡、狼瘡腎炎、クローン病、IBD(炎症性腸疾患)、骨髄異形成症候群(MDS)、骨髄増殖性新生物(MPN)、非アルコール性脂肪肝疾患(NAFLD)、非アルコール性脂肪肝炎(NASH)。
いくつかの実施形態において、疾患は、以下からなる群から選択される:NASH(非アルコール性脂肪肝炎);骨髄異形成症候群(MDS);骨髄増殖性新生物(MPN);CAPS(クリオピリン関連周期性症候群);IPF(特発性肺線維症);MI(R/I)(心筋梗塞及び再灌流傷害);痛風;I/O(免疫腫瘍学);喘息;IBD(炎症性腸疾患)、腎線維症;成人発症スティル病;全身性若年性特発性関節炎;腫瘍壊死因子受容体関連周期症候群(TRAPS);コルキシン抵抗性家族性地中海熱(FMF);高IgD症候群(HIDS)/メバロネートキナーゼ欠乏症(MKD);外傷性脳損傷;パーキンソン病、中等度から重度の炎症性にきび;急性非直腸性非感染性ぶどう膜炎(NIU);AD(アルツハイマー病);COPD(慢性閉塞性肺疾患);セプシス;MS(多発性硬化症);ベーチェット病;クローン病;RA(関節リウマチ);びらん性変形性関節炎;T1D(1型糖尿病);T2D(2型糖尿病)、肥満;骨粗鬆症;嚢胞性線維症;アルコール性肝疾患;老化;HCC(肝細胞癌);うつ病;子宮内膜症;稀な潰瘍性皮膚疾患である壊疽性膿皮症(「PG」);狼瘡、狼瘡性腎炎;てんかん;虚血性脳卒中;難聴;鎌状赤血球症;SLE(全身性狼瘡エリテマトーデス);及び脊髄損傷。
いくつかの実施形態において、疾患は、狼瘡、狼瘡性腎炎、クライオピリン関連周期性症候群(CAPS)、骨髄異形成症候群(MDS)、痛風、骨髄増殖性新生物(MPN)、アテローム性動脈硬化症、クローン病、及び炎症性腸疾患(IBD)からなる群から選択される。
いくつかの実施形態において、疾患は痛風である。
いくつかの実施形態において、疾患は狼瘡である。
いくつかの実施形態において、疾患は腎炎である。
いくつかの実施形態において、疾患はクローン病である。
いくつかの実施形態において、疾患はIBD(炎症性腸疾患)である。
いくつかの実施形態において、疾患は、MDS(骨髄異形成症候群)である。
いくつかの実施形態において、疾患はMPN(骨髄増殖性新生物)である。
本明細書に記載された処置的用途のために、投与される投与量は、もちろん、1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、又は採用される医薬組成物、投与様式、所望の処置及び示された疾患によって異なるであろう。例えば、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体の1日投与量は、吸入した場合、体重1キログラム(μg/kg)あたり約0.05マイクログラムから体重1キログラム(μg/kg)あたり約100マイクログラムまでの範囲であり得る。代替的に、本開示の1つ以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体を経口投与する場合、本開示の1つ以上の化合物の1日投与量は、体重1キログラム(μg/kg)あたり約0.01マイクログラムから体重1キログラム(mg/kg)あたり約100ミリグラムの範囲であってもよい。
しかしながら、本開示の1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、ならびに本開示の医薬組成物の1日の総使用量は、健全な医学的判断の範囲内で主治医によって決定されることが理解されるであろう。任意の特定の患者のための特定の処置上有効な用量レベルは、処置されている疾患及び疾患の重症度;採用された特定の化合物の活性;採用された特定の医薬組成物;患者の年齢、体重、一般的な健康状態、性別及び食事;採用された特定の化合物の投与時間、投与経路、及び排泄率;処置の持続時間;採用された特定の化合物との組み合わせ又は偶然に使用される薬物;及び医療技術でよく知られているような要因を含む様々な要因に依存するであろう。当技術分野における通常の技術を有する医師又は獣医師は、1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、又は本明細書に開示された医薬組成物の処置的に有効な量を容易に決定し、処方することができ、疾患の進行を処置し、対抗し、又は阻止するために必要である。
併用療法
いくつかの実施形態において、本明細書に記載された1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、又は医薬組成物は、独立して使用されてもよく、又は公知の処置剤又は医薬組成物と一緒に、又は結合して投与されてもよく、又は組み合わせて使用されてもよい。接合投与又は併用投与は、先に投与された化合物又は医薬組成物が体内で有効である間に、第2の化合物又は医薬組成物が投与されるような、2つ以上の異なる化合物又は医薬組成物の投与の任意の形態を指すことができる。例えば、異なる化合物又は医薬組成物は、同一の剤形で、又は別個の剤形で、同時に、順次、又は処置の個々の成分を別々に投与することによって投与することができる。いくつかの実施形態において、異なる化合物又は医薬組成物は、互いに1時間、12時間、24時間、36時間、48時間、72時間、又は1週間以内に投与することができる。したがって、そのような処置を受ける個人は、異なる化合物又は医薬組成物の複合効果から利益を得ることができる。
いくつかの実施形態において、本開示の方法又は用途において、1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、その異性体、プロドラッグ、及び互変異性体、又は本開示の医薬組成物が、1種以上の他の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、その異性体、プロドラッグ、及び互変異性体、又は本開示の医薬組成物と組み合わされて使用される。特定のそのような実施形態において、本明細書に記載された1つ以上の疾患を処置するための方法において、1つ以上の他の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、それらの異性体、プロドラッグ、及び互変異性体、又は本開示の医薬組成物の組み合わせが使用される。
いくつかの実施形態において、1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、その異性体、プロドラッグ、及び互変異性体、又は本明細書で提供される医薬組成物、又は他の公知の医薬又は医薬組成物と1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、その異性体、プロドラッグ、及び互変異性体、又は本明細書で提供される医薬組成物との組み合わせは、本開示の方法及び用途において有用な医薬組成物及び医薬組成物に製剤化されている。本開示はまた、本明細書に記載された1つ以上の疾患を処置するためのそのような組み合わせの使用を提供する。
本開示のいくつかの実施形態において、1種以上の化合物、及び薬学的に許容される塩、溶媒和物(例えば、水和物)、異性体、プロドラッグ、及びそれらの互変異性体、又は本開示の医薬組成物は、処置下投与量で投与され、ここで、処置下投与量とは、独立して投与された場合には、本明細書に記載された疾患の1つを処置するのに不十分であろう量のことである。
例示的な実施形態
本開示のいくつかの実施形態において、以下の実施形態Iである:
実施形態I-1。式(I)
(式中:
R
100は、H、Cl、D、-CN、-NO
2、-OR
3a、-C(O)R
3b、-S(O)
2R
3b、-S(O)R
3b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、OR
3a、-C(O)R
3b、-P(O)R
3bR
4b、-S(O)
2R
3b、-S(O)R
3b、-NR
3aR
4a、-NR
3aC(O)R
4a、-NR
3aC(O)OR
4a、-NR
3aC(O)NR
4a、-NR
3aS(O)
2R
4a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
1は、
(式中、
R
1wは、H、D、-CN、-C(O)R
5b、-S(O)
2R
5b、-S(O)R
5b、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
5a、-C(O)R
5b、-P(O)R
5bR
6b、-S(O)
2R
5b、-S(O)R
5b、-NR
5aR
6a、-NR
5aC(O)R
6a、-NR
5aC(O)OR
6a、-NR
5aC(O)NR
6a、-NR
5aS(O)
2R
6a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1x及びR
1yは、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1w及びR
1yは、それらが結合している原子とともに、3-7員ヘテロシクリル又は5-6員ヘテロアリールを形成していてもよく;前記3-7員ヘテロシクリル及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a、及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1x及びR
1yは、それらが結合している原子と共に、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、又は5-6員アリール又はヘテロアリールを形成してもよく;前記C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5-6員アリール又はヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
9a、-C(O)R
9b、-P(O)R
9bR
10b、-S(O)
2R
9b、-S(O)R
9b、-NR
9aR
10a、-NR
9aC(O)R
10a、-NR
9aC(O)OR
10a、-NR
9aC(O)NR
10a、及び-NR
9aS(O)
2R
10aからなる群から選択される1つ以上の置換基で置換されている)
からなる群から選択され;
R
2は、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、C
6アリール、及び-NR
2gR
2hからなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、6員ヘテロアリール、及びC
6アリールは、それぞれ独立して、非置換であるか、又はD、CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
2g及びR
2hは、それぞれ独立して、H、D、C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3a、R
4a、R
5a、R
6a、R
7a、R
8a、R
9a、R
10a、R
21a、R
22a、R
23a、及びR
24aは、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
3b、R
4b、R
5b、R
6b、R
7b、R
8b、R
9b、R
10b、R
21b、R
22b、R
23b、及びR
24bは、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)である。-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルケニル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
2-C
8アルキニル、C
3-C
10シクロアルケニル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールは、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)
2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている)
の構造を有する化合物、又はその薬学的に許容される塩、溶媒和物、異性体又は互変異性体。
実施形態I-2。R
2が、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、-NR
2gR
2h、
からなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
X
2が、N又はCR
2aであり;
X
3が、N又はCR
2cであり;
X
4が、N又はCR
2dであり;
X
5が、N又はCR
2eであり;
X
6及びX
7が、それぞれ独立してN又はCR
2nであり、前記X
6及びX
7のうちの少なくとも1つがNであり;
R
2aが、H、D、ハロゲン、-CN、-OR
15a、C
1-C
6アルキル、C
3-C
10シクロアルキル、-C(O)NR
15aR
16a、-C(O)OR
15a;-NR
15aR
16a、-NR
15aC(O)R
16a、-NR
15aC(O)OR
16a、-NR
15aC(O)NR
16a、又は-NR
15aS(O)
2R
16aであり、前記C
1-C
6アルキル及びC
3-C
10シクロアルキルが、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR
15a、-C(O)R
15b、-NR
15aR
16a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
2b、R
2c、R
2d、R
2e、及びR
2fが、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2b、R
2c、R
2d、R
2e、及びR
2fが、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2j、R
2k、R
2m及びR
2nが、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2j、R
2k、R
2m及びR
2nが、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2g及びR
2hが、それぞれ独立して、H、D、C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
15a、R
16a、R
17a、R
18a、R
19a、R
20a、及びR
21aが、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)
2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
15b、R
17b、R
18b、及びR
21bが、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)
2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-3。R
1が、
である、実施形態I-1~I-2のいずれかの化合物、又はその薬学的に許容される塩、プロドラッグ、溶媒和物、水和物、異性体、もしくは互変異性体。
実施形態I-4。R
1が、以下:
からなる群から選択され:
R
1zが、H、D、ハロゲン、-CN、-NO
2、-SR
7a、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
7a、-C(O)R
7b、-P(O)R
7bR
8b、-S(O)
2R
7b、-S(O)R
7b、-NR
7aR
8a、-NR
7aC(O)R
8a、-NR
7aC(O)OR
8a、-NR
7aC(O)NR
8a、-NR
7aS(O)
2R
8a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
各R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g、及びR
1hが、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
11a、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールから選択され;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
11a、-C(O)R
11b、-P(O)R
11bR
12b、-S(O)
2R
11b、-S(O)R
11b、-NR
11aR
12a、-NR
11aC(O)R
12a、-NR
11aC(O)OR
12a、-NR
11aC(O)NR
12a、-NR
11aS(O)
2R
12a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
R
1a、R
1b、R
1c、R
1d、R
1e、R
1f、R
1g、及びR
1hのうちの2つの基が、存在する場合、それらが結合している原子と共に、C
3-C
10シクロアルキル又は3-7員ヘテロシクリルを形成していてもよく;前記C
3-C
10シクロアルキル及び3-7員ヘテロシクリルが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OR
13a、-C(O)R
13b、-P(O)R
13bR
14b、-S(O)
2R
13b、-S(O)R
13b、-NR
13aR
14a、-NR
13aC(O)R
14a、-NR
13aC(O)OR
14a、-NR
13aC(O)NR
14a、及び-NR
13aS(O)
2R
14aからなる群から選択される1つ以上の置換基で置換されているか;又は
2つのジェミナルな基R
1a及びR
1b;R
1c及びR
1d;R
1e及びR
1f;又はR
1g及びR
1hが、存在する場合、オキソ基を形成していてもよく;
R
7a、R
8a、R
11a、R
12a、R
13a、及びR
14aが、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)
2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
7b、R
8b、R
11b、R
12b、R
13b及びR
14bが、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)
2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-5。R
2が、C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、5員ヘテロアリール、-NR
2gR
2h、
からなる群から選択され;前記C
1-C
6アルキル、C
3-C
10シクロアルキル、3-7員ヘテロシクリル、及び5員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
23a、-C(O)R
23b、-P(O)R
23bR
24b、-S(O)
2R
23b、-S(O)R
23b、-NR
23aR
24a、-NR
23aC(O)R
24a、-NR
23aC(O)OR
24a、-NR
23aC(O)NR
24a、-NR
23aS(O)
2R
24a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
X
2が、N又はCR
2aであり;
X
3が、N又はCR
2cであり;
X
4が、N又はCR
2dであり;
X
5が、N又はCR
2eであり;
X
6及びX
7が、それぞれ独立してN又はCR
2nであり、前記X
6及びX
7のうちの少なくとも1つがNであり;
R
2aが、H、D、ハロゲン、-CN、-OR
15a、C
1-C
6アルキル、C
3-C
10シクロアルキル、-C(O)NR
15aR
16a、-C(O)OR
15a;-NR
15aR
16a、-NR
15aC(O)R
16a、-NR
15aC(O)OR
16a、-NR
15aC(O)NR
16a、又は-NR
15aS(O)
2R
16aであり、前記C
1-C
6アルキル及びC
3-C
10シクロアルキルが、それぞれ独立して、非置換であるか、又はD、ハロゲン、-CN、-OR
15a、-C(O)R
15b、-NR
15aR
16a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1以上の置換基で置換されており;
各R
2b、R
2c、R
2d、R
2e、及びR
2fが、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されているか;又は
隣接する2つのR
2b、R
2c、R
2d、R
2e、及びR
2fが、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2j、R
2k、R
2m及びR
2nが、それぞれ独立して、H、D、ハロゲン、-CN、-NO
2、-SR
17a、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
6アルキル、C
2-C
6アルケニル、C
4-C
8シクロアルケニル、C
2-C
6アルキニル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、-OR
17a、-C(O)R
17b、-P(O)R
17bR
18b、-S(O)
2R
17b、-S(O)R
17b、-NR
17aR
18a、-NR
17aC(O)R
18a、-NR
17aC(O)OR
18a、-NR
17aC(O)NR
18a、-NR
17aS(O)
2R
18a、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリール;又は
隣接する2つのR
2j、R
2k、R
2m及びR
2nが、それらが結合している原子とともに、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、5-6員ヘテロアリールを形成していてもよく、前記C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はハロゲン、D、-CN、C
1-C
6アルキル、-OR
19a、及びNR
19aR
20aからなる群から選択される1つ以上の置換基で置換されており;
各R
2g及びR
2hが、それぞれ独立して、H、D、C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり、前記C
1-C
6アルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、C
1-C
6ハロアルキル、C
2-C
6アルケニル、オキソ、-OR
21a、-C(O)R
21b、-P(O)R
21bR
22b、-S(O)
2R
21b、-S(O)R
21b、-NR
21aR
22a、-NR
21aC(O)R
22a、-NR
21aC(O)OR
22a、-NR
21aC(O)NR
22a、-NR
21aS(O)
2R
22a、-(CH
2)
1-4C
3-C
10シクロアルキル、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
15a、R
16a、R
17a、R
18a、R
19a、R
20a、及びR
21aが、それぞれ独立して、各出現において、H、D、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)
2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されており;
R
15b、R
17b、R
18b、及びR
21bが、それぞれ独立して、各出現において、H、D、-OH、-O(C
1-C
6アルキル)、-NH
2、-NH(C
1-C
6アルキル)、-N(C
1-C
6アルキル)
2、-NHS(O)
2CH
3、C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールであり;前記C
1-C
8アルキル、C
2-C
8アルケニル、C
2-C
8アルキニル、C
3-C
10シクロアルキル、C
4-C
8シクロアルケニル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールが、それぞれ独立して、非置換であるか、又はD、-CN、ハロゲン、C
1-C
6アルキル、-OH、-O-C
1-C
6アルキル、-NH
2、-NH(C
1-C
6アルキル)
2、-N(C
1-C
6アルキル)
2、C
3-C
10シクロアルキル、C
6アリール、3-7員ヘテロシクリル、及び5-6員ヘテロアリールからなる群から選択される1つ以上の置換基で置換されている、実施形態I-4の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-6。R
2が、
である、実施形態I-4又はI-5の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-7。R100がHである、実施形態I-1~I-6のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-8。R
2が
である、実施形態I-1~I-7のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-9。X2がCR2aである、実施形態I-1~I-8のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-10。X2がNである、実施形態I-1~I-8のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-11。R2aが、H、ハロゲン、C1-C6アルキル、又は-C(O)R3bである、実施形態I-1~I-9のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-12。R2aが、H、フルオロ、クロロ、メチル、又は-COOHである、実施形態I-1~I-9のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-13。R
2が
である、実施形態I-1~I-9及びI-11~I-12のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-14。R
2が
である、実施形態I-1~I-9及びI-11~I-12のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-15。R
2が
である、実施形態I-1~I-7のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-16。X3がCR2cであり、X4がCR2dであり、X5がCR2dである、実施形態I-15の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-17。各R2b、R2c、R2d、R2e、及びR2fが、それぞれ独立して、H、D、ハロゲン、C1-C6アルキル、C3-C10シクロアルキル、及び-CNからなる群から選択される、実施形態I-15~I-16のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-18。R
2が
である、実施形態I-15~I-17のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-19。R
2が
である、実施形態I-15~I-18のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-20。X3がNであり、X4がCR2dであり、X5がCR2dである、実施形態I-15の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-21。X3がCR2cであり、X4がNであり、X5がCR2dである、実施形態I-15の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-22。X3がCR2cであり、X4がCR2dであり、X5がNである、実施形態I-15の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-23。R
1が
である、実施形態I-1~I-22のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-24。R
1が
である、実施形態I-1~I-22のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-25。R
1が
である、実施形態I-1~I-22のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-26。R
1が
である、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-27。R
1が
である、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-28。R
1が
である、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-29。R
1が
である、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-30。R
1が、
からなる群から選択される、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-31。R
1が、
からなる群から選択される、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-32。R
1が、
からなる群から選択される、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体
実施形態I-33。R1zがHである、実施形態I-1~I-32のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-34。R
1が、
からなる群から選択される、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-35。R
1が、
からなる群から選択される、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-36。R
1が、
からなる群から選択される、実施形態I-1~I-23のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-37。R1a及びR1bが、それぞれ独立して、H、ハロゲン、-OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである、実施形態I-1~I-25、I-27及びI-30~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-38。R1c及びR1dが、それぞれ独立して、H、ハロゲン、-OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである、実施形態I-1~I-25及びI-29~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-39。R1e及びR1fが、それぞれ独立して、H、ハロゲン、-OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである、実施形態I-1~I-23、I-25、I-28、及びI-30~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-40。R1g及びR1hが、それぞれ独立して、H、ハロゲン、-OR11a、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、C3-C10シクロアルキル、C6アリール、3-7員ヘテロシクリル、又は5-6員ヘテロアリールである、実施形態I-1~I-22、I-25、及びI-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-41。R1a及びR1bが、それぞれ独立して、H、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1~I-25、I-27及びI-30~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-42。R1a及びR1bが、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、および-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1~I-25、I-27及びI-30~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-43。R1c及びR1dが、それぞれ独立して、H、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1~I-25及びI-29~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-44。R1c及びR1dが、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、および-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1~I-25及びI-29~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-45。R1e及びR1fが、それぞれ独立して、H、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている実施形態I-1~I-23、I-25、I-28、及びI-30~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-46。R1e及びR1fが、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1~I-23、I-25、I-28、及びI-30~I-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-47。R1g及びR1hが、それぞれ独立して、H、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12aからなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-C(O)R11b、-P(O)R11bR12b、-S(O)2R11b、-S(O)R11b、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ以上の置換基で置換されている、実施形態I-1~I-22、I-25、及びI-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-48。R1g及びR1hが、それぞれ独立して、H、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、-NR11aS(O)2R12a、C1-C6アルキル、又は3-7員ヘテロシクリルであり;前記C1-C6アルキルが、-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12a以下からなる群から選択される1つ以上の置換基で置換されており;前記3-7員ヘテロシクリルが、非置換であるか、又は-NR11aR12a、-NR11aC(O)R12a、-NR11aC(O)OR12a、-NR11aC(O)NR12a、及び-NR11aS(O)2R12aからなる群から選択される1つ又は複数の置換基で置換されている、実施形態I-1~I-22、I-25、及びI-33のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-49。3-7員ヘテロシクリルが窒素を含む、実施形態I-41~I-48のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-50。化合物が下記式:
のものである、実施形態I-1~I-49のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-51。化合物が下記式:
のものである、実施形態I-1~I-49のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-52。化合物が以下:
からなる群から選択される、実施形態I-1の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-53。化合物が以下:
からなる群から選択される、実施形態I-1の化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-54。実施形態I-1~I-53のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、互変異性体、及び薬学的に許容される担体からなる医薬組成物。
実施形態I-55。インフラマソームの阻害に応答する疾患を処置する方法であって、前記疾患を必要とする被験者に、実施形態I-1~I-53のいずれかの化合物の有効量を投与し、それによって前記疾患を処置することからなる方法。
実施形態I-56。実施形態I-55の方法であって、前記疾患が、NLRP3インフラマソームの活性化の阻害に応答するものである方法。
実施形態I-57。実施形態I-54~I-55のいずれかの方法であって、前記疾患が、IL-6、IL-1β、IL-17、IL-18、IL-1α、IL-37、IL-22、IL-33、及びTh17細胞の1つ以上の調節に応答する方法。
実施形態I-58。実施形態I-54~I-55のいずれかの方法であって、前記疾患が、IL-1β及びIL-18の1つ以上の調節に応答する方法。
実施形態I-59。実施形態I-55~I-58のいずれかの方法であって、前記疾患が免疫系の疾患である方法。
実施形態I-60。実施形態I-55~I-58のいずれかの方法であって、疾患が、炎症性の疾患、疾患又は病態であるか、又は自己免疫性の疾患、疾患又は病態である方法。
実施形態I-61。実施形態I-55~I-58のいずれかの方法であって、疾患が肝臓の疾患である方法。
実施形態I-62。実施形態I-55~I-58のいずれかの方法であって、前記疾患が肺の疾患である方法。
実施形態I-63。実施形態I-55~I-58のいずれかの方法であって、前記疾患が皮膚の疾患である方法。
実施形態I-64。実施形態I-55~I-58のいずれかの方法であって、前記疾患が心臓血管系の疾患である方法。
実施形態I-65。実施形態I-55~I-58のいずれかの方法であって、前記疾患が癌、腫瘍又は他の悪性腫瘍である方法。
実施形態I-66。実施形態I-55~I-58のいずれかの方法であって、前記疾患が腎系の疾患である方法。
実施形態I-67。実施形態I-55~I-58のいずれかの方法であって、前記疾患が胃腸管の疾患である方法。
実施形態I-68。実施形態I-55~I-58のいずれかの方法であって、前記疾患が呼吸器系の疾患である方法。
実施形態I-69。実施形態I-55~I-58のいずれかの方法であって、前記疾患が内分泌系の疾患である方法。
実施形態I-70。実施形態I-55~I-58のいずれかの方法であって、前記疾患が中枢神経系(CNS)の疾患である方法。
実施形態I-71。実施形態I-55~I-58のいずれかの方法であって、疾患が、構成性炎症、クライオピリン関連周期性症候群(CAPS)、マックルウェルズ症候群(MWS)、家族性寒冷自己炎症性症候群(FCAS)、新生児発症多系統炎症性疾患(NOMID)、自己炎症性疾患、家族性地中海熱(FMF)、TNF受容体関連周期性症候群(TRAPS)、メバロネートキナーゼ欠乏症(MKD)、高免疫グロブリン血症D、周期性発熱症候群(HIDS)、インターロイキン1受容体(DIRA)アンタゴニスト欠損症、マジェド症候群、化膿性関節炎、壊疽性膿皮症及びにきび(PAPA)、A20のハプロイン不全症(HA20)、小児肉芽腫性関節炎(PGA)、PLCG2関連抗体欠損症及び免疫異常症(PLAID)、PLCG2関連自己炎症、抗体欠乏及び免疫異常(APLAID)、B細胞免疫不全を伴う筋芽球性貧血、周期的発熱、発達遅延(SIFD)、スウィート症候群、慢性非細菌性骨髄炎(CNO)、慢性再発性多巣性骨髄炎(CRMO)及び滑膜炎、にきび、膿疱症、骨粗鬆症、骨炎症候群(SAPHO)、多発性硬化症(MS)、1型糖尿病、乾癬、関節リウマチ、ベーチェット病、シェーグレン症候群、シュニッツラー症候群、呼吸器疾患、特発性肺線維症(IPF)、慢性閉塞性肺疾患(COPD)、ステロイド抵抗性喘息、アスベスト症、珪肺症などの自己免疫疾患、嚢胞性線維症、中枢神経系疾患、パーキンソン病、アルツハイマー病、運動ニューロン病、ハンチントン病、脳マラリア、肺炎球菌性髄膜炎による脳損傷、代謝性疾患、2型糖尿病、動脈硬化症、肥満、痛風、疑似痛風、眼疾患、眼球上皮の疾患、加齢黄斑変性症(AMD)角膜感染症、ぶどう膜炎、ドライアイ、腎臓病、慢性腎臓病、シュウ酸塩腎症、糖尿病性腎症、肝臓病、非アルコール性脂肪肝炎、アルコール性肝疾患、皮膚の炎症反応、接触過敏症、日焼け、関節の炎症反応、変形性関節症、全身性若年性特発性関節炎 成人発症スティル病、再発性多発性軟骨炎、ウイルス感染症、アルファウイルス感染症、チクングンヤウイルス感染症、ロス川ウイルス感染症、フラビウイルス感染症、デングウイルス感染症、ジカウイルス感染症、インフルエンザ、HIV感染症、汗腺炎膿瘍(HS)、嚢胞性皮膚疾患、がん、肺がん転移、膵臓がん、胃がん、骨髄異形成症候群、白血病、多発性筋炎、脳卒中、心筋梗塞、移植片対宿主病、高血圧、大腸炎、蠕虫感染症、細菌感染症、腹部大動脈瘤、創傷治癒、うつ病、心理的ストレス、心膜炎、ドレスラー症候群、虚血性再灌流疾患、及びNLRP3における生殖細胞系列又は体細胞非サイレント変異が個体にあると判断された任意の疾患からなる群から選択される方法。
実施形態I-72。実施形態I-55~I-58のいずれかの方法であって、疾患が、細菌感染症、ウイルス感染症、真菌感染症、炎症性腸疾患、セリアック病、大腸炎、腸管過形成、癌、メタボリックシンドローム、肥満、関節リウマチ、肝臓病、肝性ステアトーシス、脂肪肝疾患、肝線維症、非アルコール性脂肪性肝疾患(NAFLD)、非アルコール性脂肪性肝炎(NASH)からなる群から選択される方法。
実施形態I-73。実施形態I-68の方法であって、疾患が、非アルコール性脂肪性肝炎(NASH)である方法。
実施形態I-74。実施形態I-55~I-58のいずれかの方法であって、疾患が、狼瘡、狼瘡性腎炎、クライオピリン関連周期性症候群(CAPS)、骨髄異形成症候群(MDS)、痛風、骨髄増殖性新生物(MPN)、アテローム性動脈硬化症、クローン病、及び炎症性腸疾患(IBD)からなる群から選択される方法。
実施形態I-75。医薬として使用するための、実施形態I-1~I-53のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-76。インフラマソームの阻害に応答する疾患の処置に使用するための、実施形態I-1~I-53のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体。
実施形態I-77。インフラマソームの阻害に応答する疾患を処置するための医薬の製造における、実施形態I-1~I-53のいずれかの化合物、又はその薬学的に許容される塩、溶媒和物、異性体、又は互変異性体の使用。
実施形態I-78。医薬として使用するための、実施形態I-54の医薬組成物。
実施形態I-79。インフラマソームの阻害に応答する疾患の処置に使用するための、実施形態I-54の医薬組成物。
実施形態I-80。インフラマソームの阻害に応答する疾患を処置するための医薬の製造における、実施形態I-54の医薬組成物の使用。
実施例
以下の実施例は、本開示を例示するために提供され、それらを限定するものとして解釈されるべきではない。これらの実施例において、他に別段の記載がない限り、全ての部及び百分率は、重量部及び重量百分率である。実施例中の略語を以下に記す。
略語:
キラルHPLC分析法:
方法A-
カラム:キラルセル OD-3 50×4.6mm I.D.,3μm
移動相:A:CO2 B:メタノール(0.05% DEA)
勾配:Bを2分で5%から40%まで上げ、1.2分で40%をキープし、その後0.8分でBの5%をキープする。
流量:4 mL/min
カラム温度:35℃
ABPR:1500 psi
方法B-
カラム:キラルパック AD-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05% DEA)
アイソクラティック:40% B
流量:2.5 mL/min
カラム温度:40℃
ABPR:100バール
方法C-
カラム:キラルパック AS-3 100×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05% DEA)
勾配:Bを4分で5%から40%まで上げ、2.5分で40%をキープし、その後1.5分でBの5%をキープする。
流量:2.8mL/min
カラム温度:35℃
ABPR:1500 psi
方法D-
カラム:キラルパック IC-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05% DEA)
勾配:Bを5分で5%から40%まで上げ、2.5分で40%をキープし、その後2.5分でBの5%をキープする。
流量:2.5mL/min
カラム温度:35℃
ABPR:1500 psi
方法E-
カラム:キラルパック AD-3 50×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05% DEA)
勾配:Bを2分で5%から40%まで上げ、1.2分で40%をキープし、その後0.8分でBの5%をキープする。
流量:4mL/min
カラム温度:35℃
ABPR:1500 psi
方法F-
カラム:キラルパック IC-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05% DEA)
アイソクラティック:40% B
流量:2.5 mL/min
カラム温度:40℃
ABPR:100バール
方法G-
カラム:セルロース 2 150×4.6mm I.D.,5μm
移動相:A:CO2 B:メタノール(0.05% DEA)
アイソクラティック:40% B
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法H-
カラム:キラルパック AD-3 150×4.6mm I.D.,3μm
移動相:CO2中で40%のメタノール(0.05%DEA)
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法I-
カラム:キラルパック AD-3 150×4.6mm I.D.,3μm
移動相:CO2中で40%のエタノール(0.05%DEA)
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法J-
カラム:キラルセル OJ-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05% DEA)
勾配:Bを5分で5%から40%まで上げ、0.5分で40%をキープし、その後1.5分でBの5%をキープする。
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法K-
カラム:キラルセル OD-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:メタノール(0.05%DEA)
勾配:Bを5分で5%から40%まで上げ、2.5分で40%をキープし、その後2.5分でBの5%をキープする。
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法L-
カラム:キラルパック IC-3 150×4.6 mm I.D.,3μm
移動相:CO2中で40%のエタノール(0.05%DEA)
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法M-
カラム:キラルセル OD-3 150×4.6 mm I.D.,3μm
移動相:A:CO2 B:メタノール(0.05% DEA)
勾配:Bを5.5分で5%から40%まで上げ、3分で40%をキープし、その後1.5分でBの5%をキープする。
流量:2.5 mL/min
カラム温度:40℃
ABPR:100バール
方法N-
カラム:キラルパック AD-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05% DEA)
勾配:Bを5分で5%から40%まで上げ、2.5分で40%をキープし、その後2.5分でBの5%をキープする。
流量:2.5mL/min
カラム温度:35℃
ABPR:1500 psi
方法O-
カラム:キラルパック AD-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:メタノール(0.05% DEA)
勾配:Bを5.5分で5%から40%まで上げ、3分で40%をキープし、その後1.5分でBの5%をキープする。
流量:2.5 mL/min
カラム温度:40℃
背圧:100バール
方法P-
カラム:セルロース 2 150×4.6mm I.D.,5μm
移動相:A:CO2 B:エタノール(0.05% DEA)
アイソクラティック:40% B
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法Q-
カラム:キラルセル OD-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:メタノール(0.05%DEA)
勾配:Bを5分で5%から40%まで上げ、0.5分で40%から5%まで下げ、その後1.5分でBの5%をキープする。
流量:2.5 mL/min
カラム温度:35℃
ABPR:1500 psi
方法R-
カラム:キラルセル OJ-H150×4.6mmI.D.,5μm
移動相:A:CO2 B:IPA(0.05% DEA)
アイソクラティック:40% B
流量:2.5 mL/min
カラム温度:40℃
ABPR:100バール
方法S-
カラム:キラルパック AD-3 150×4.6mm I.D.,3μm
移動相:A:CO2 B:エタノール(0.05%DEA)
勾配:Bを5.5分で5%から40%まで上げ、3分で40%をキープし、その後1.5分でBの5%をキープする。
流量:2.5 mL/min
カラム温度:40℃
ABPR:100バール
方法T-
カラム:シラセルOX、50x4.6mm、内径3μm
移動相:A:CO2 B:メタノール(0.1%NH4OH)
勾配:30%Bでアイソクラティック
流量:4 mL/min
カラム温度:40℃
ABPR:120バール
方法U-
カラム:Chiralpak IA、50x4.6 mm、I.D.3μm
移動相:A:CO2 B:メタノール(0.1%NH4OH)
勾配:35%Bでアイソクラティック
流量:4 mL/min
カラム温度:40℃
ABPR:120バール
方法V-
カラム:シラセルOX、50x4.6mm、内径3μm
移動相:A:CO2 B:メタノール(0.1%NH4OH)
勾配:40%Bでアイソクラティック
流量:4 mL/min
カラム温度:40℃
ABPR:120バール
方法W-
コラム:WhelkO-1(s,s)、100x4.6 mm、I.D.3μm
移動相:A:CO2 B:エタノール(0.1%NH4OH)
勾配:30%Bでアイソクラティック
流量:4 mL/min
カラム温度:40℃
ABPR:125バール
合成例
実施例A
臭素化ピラゾロ[5,1-b][1,3]オキサジンの合成:(S)-3-ブロモ-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン
工程1-1-アセチル-1,2-ジヒドロ-ピラゾール-3-オンの合成:
ピリジン(300 mL)中の1,2-ジヒドロピラゾール-3-オン(50.0 g、600 mmol)の溶液を95℃に加熱した。この溶液に、ピリジン(100 mL)中の無水酢酸(61.2 g、600 mmol)の溶液を0.5時間かけてゆっくりと加えた。反応物を95℃でさらに1時間加熱した。反応混合物を濃縮して空冷し、暗赤色の油を得、これを MeOH(150 mL)で濾過して 1-アセチル-1,2-ジヒドロピラゾール-3-オン(54.0 g、収率71%)を白色の固体として得た。1H NMR(300 MHz、DMSO-d6):δ=10.92(s,1H),8.08(s,1H),5.96(s,1H),2.45(オーバーラップ、3H).
工程2-(S)-1-(3-(オキシラン-2-イルメトキシ)-1H-ピラゾール-1-イル)エタン-1-オンの合成:
THF(400 mL)中の1-アセチル-1,2-ジヒドロピラゾール-3-オン(34.7 g、280 mmol)とPPh3(24.9 g、420 mmol)の混合物を、N2の雰囲気下で0℃まで冷却した。混合物にDIAD(84.8 g、420 mmol)をゆっくりと加えた。0℃で1時間撹拌した後、(R)-オキシラン-2-イルメタノール(25.2g、340mmol)をゆっくりと加えた。次いで反応物を室温で一晩撹拌した。反応混合物をブクオで濃縮し、残渣をシリカゲルカラム(PE/EtOAc=10/1)で精製し、白色固体として(S)-1-(3-(3-(オキシラン-2-イルメトキシ)-1H-ピラゾール-1-イル)エタン-1-オン(34.8 g、収率68%)を得た。68%)を得た。1H NMR(400 MHz,CDCl3):δ=8.06(d,J=2.8 Hz,1H),6.00(d,J=3.2 Hz,1H),4.55(dd,J=12.0,3.2 Hz,1H),4.20(dd,J=12.0,3.2 Hz,1H),3.39(q,J=3.2 Hz,1H),2.92(t,J=4.4 Hz,1H),2.76(dd,J=4.4,2.4 Hz,1H),2.57(s,3H).
工程3-(R)-1-(3-(3-(3-クロロ-2-ヒドロキシプロポキシ)-1H-ピラゾール-1-イル)エタン-1-オンの合成:
AcOH(34.2g,570mmol)及びTHF(200mL)中の(S)-1-(3-(オキシラン-2-イルメチル)-1H-ピラゾール-1-イル)エタン-1-オン(34.8g,190mmol)の溶液に、LiCl(13.1g,310mmol)を室温で加えた。反応物をEtOAc(200 mL)と水(200 mL)の間で分割し、室温で一晩撹拌した。有機層を飽和水性NaHCO3(100 mL)、ブライン(100 mL)で洗浄し、Na2SO4上で乾燥させ、空中で濃縮して、粗(R)-1-(3-(3-クロロ-2-ヒドロキシプロポキシ)-1H-ピラゾール-1-イル)エタン-1-オンを無色油として得て、これを精製することなく、次の工程で直接使用した。1H NMR(300 MHz,DMSO-d6):δ=8.25(d,J=2.7 Hz,1H),6.23(d,J=3.0 Hz,1H),5.59(brs,1H),4.24-4.19(m,2H),4.07-4.04(m,1H),3.75-3.62(m,2H),2.50(オーバーラップ、3H).MS:m/z 219.4(M+H+).
工程4-(S)-6,7-ジヒドロ-5H-ピラゾロ[5,1-bs[1,3]オキサジン-6-オールの合成:
(R)-1-(3-(3-クロロ-2-ヒドロキシプロポキシ)-1H-ピラゾール-1-イル)エタン-1-オン(粗製、190ミリモル)とK2CO3(78.7g,570ミリモル)の混合物 DMF(400 mL)中、135℃で一晩撹拌した。溶媒を減圧下で除去した。残渣をシリカゲルカラム(EtOAc)で精製し、白色固体として(S)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-オール(12.8 g、収率48%)を得た。1H NMR(400 MHz,DMSO-d6):δ=7.21(d,J=1.6 Hz,1H),5.51(d,J=3.2 Hz,1H),5.44(d,J=1.6 Hz,1H),4.24-4.13(m,4H),3.92(d,J=12.4 Hz,1H).
工程5-(S)-3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-オールの合成:
MeCN(200 mL)中の(S)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-オール(12.8 g,91.4 mmol)の溶液に、N2の雰囲気下、0℃でNBS(17.9 g,100.6 mmol)を2回に分けて加えた。反応物を室温まで温め、1時間撹拌した。反応物をEtOAc(200mL)と水(200mL)との間で分配した。有機層を飽和水性NaHCO3(100 mL)、ブライン(100 mL)で洗浄し、Na2SO4上で乾燥させ、真空中で濃縮した。粗残渣をEtOAc(50 mL)でトリツアレートし、濾過して(S)-3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-オール(11.3 g、収率 57%)を白色固体として得た。MS:m/z 219.3(M+H+).
工程6-(S)-3-ブロモ-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジンの合成:
(S)-3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-オール(12.2 g,55.7 mmol)のDMF(60 mL)中の溶液に、室温でN2雰囲気下でNaH(鉱油60%,2.7 g,66.8 mmol)を加えた。1時間後、MeI(9.5g,66.8mmol)を加えた。反応物を室温でさらに2時間撹拌した。次いで、反応物を水(200 mL)に注ぎ、EtOAc(100 mL×2)で抽出した。有機層を水(100 mL)、食塩水(100 mL)で洗浄し、Na2SO4上で乾燥し、濃縮した。粗残渣をMeOH/H2O(2/1,100 mL)でトリツアレートし、濾過して(S)-3-ブロモ-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン(9.5 g、収率 73%)を白色固体として得た。MS:m/z 233.3(M+H+).
実施例1
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-N-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミドの合成:
6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(1.0 g,4.9 mmol)の乾燥THF(20 mL)溶液に、n-BuLi(ヘキサン中2.5 M,2.4 mL,5.9 mmol)を-78℃でN2の下でゆっくりと加えた。2時間冷却しながら撹拌した後、TBSOTf(1.6 g,5.9 mmol)をゆっくりと加えた。冷却浴を除去し、反応混合物を室温で16時間撹拌した。反応混合物を飽和水性NH4Cl(10 mL)で急冷し、得られた溶液を逆相カラム(MeCN/H2O)で直接精製してN-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(610 mg、収率38%)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=7.42(s,1H),7.36(s,1H),4.40(t,J=5.2 Hz,2H),4.11(t,J=6.0 Hz,2H),2.20-2.15(m,2H),0.87(s,9H),0.11(s,6H).MS:m/z 318.3(M+H+).
工程2-N’-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
乾燥CHCl3(3.0 mL)中のPh3PCl2(363 mg,1.1 mmol)の撹拌懸濁液に、N2雰囲気下でトリエチルアミン(125 mg,1.5 mmol)を加えた。混合物を室温で10分間撹拌し、直ちに黄色の懸濁液を形成した。反応混合物を0℃に冷却し、N-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(316mg)の溶液を加えた。乾燥CHCl3(3mL)中の1.0ミリモル)を加えた。0℃で20分間撹拌した後、NH3ガスを0℃で10分間バブリングした。その後、得られた溶液を室温で30分間撹拌し、その時点で濃縮して乾燥させた。残渣を逆相カラム(MeCN/H2O)で精製し、N’-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(Ph3P=Oと混合)を得て、これをさらに精製することなく、次の工程で直接使用した。MS:m/z 317.3(M+H+).
工程3-N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
N’-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(~1.0 mmol)のMeOH(10 mL)中の懸濁液を80℃で撹拌し、透明な溶液を得た。MeONa(54mg,1.0mmol)を加え、混合物を5分間撹拌した。溶液を濃縮して乾燥させ、残渣をMeCN(5mL)と共蒸発させた。残留固体をMeCN(5 mL)に懸濁し、室温で4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(199 mg,1.0 mmol)を加えた。16時間後、反応物を濾過した。この固体を乾燥して、N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを白色固体として得て、これをさらに精製することなく次の工程で使用した。
工程4-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例1)
N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(40 mg,0.08 mmol)のDCM(5 mL)中の溶液に、室温でHCl/ジオキサン(2 M,2 mL)を添加した。2時間後、反応物を逆相カラム(MeCN/H2O)でまず精製し、粗生成物を得た。次いで、粗生成物をprep-HPLC(NH3.H2O)で精製し、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(4.6 mg、収率 15%、エナンチオマーの混合物)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=8.18(brs,1H),7.50(s,1H),7.23(brs,2H),6.85(s,1H),4.39(t,J=6.4 Hz,2H),4.12(t,J=6.0 Hz,2H),2.79(t,J=7.2 Hz,4H),2.70(t,J=7.2 Hz,4H),2.20-2.15(m,2H),1.96-1.89(m,4H).MS:m/z 402.1(M+H+).
実施例2
(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5、1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-(S)-N-(tert-ブチルジメチルシリル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミドの合成:
(S)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(2.0 g,8.6 mmol)のTHF(20 mL)中の懸濁液に、室温でEt3N(2.1 g,21.5 mmol)及びTBSOTf(3.0 g,11.2 mmol)を加えた。50℃で16時間撹拌した後、反応混合物を室温まで冷却し、濃縮し、逆相カラム(5% ~ 95% MeCN in H2O)で精製し、黄色固体として(S)-N-(tert-ブチルジメチルシリル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(2.6 g、収率87%)を得た。MS:m/z 348.3(M+H+).
工程2-(6S)-N’-(tert-ブチルジメチルシリル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
CHCl3(15 mL)中のPh3PCl2(1.8 g,5.5 mmol)の懸濁液に室温でEt3N(860 mg,8.6 mmol)を加えた。混合物を室温で0.5時間撹拌した後、CHCl3(5 mL)中の(S)-N-(tert-ブチルジメチルシリル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(1.6 g,4.6 mmol)を0℃で添加した。反応混合物を室温でさらに2時間撹拌し、次いでNH3(ガス)を5分間バブリングした。得られた溶液を室温で30分間撹拌し、濃縮して乾燥させた。残渣をシリカゲルカラム(DCM/MeOH=20/1)で精製し、(6S)-N’-(tert-ブチルジメチルシリル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(920mg,Ph3POと混合)を黄色固体として得た。MS:m/z 347.3(M+H+).
工程3-(6S)-N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
(6S)-N’-(tert-ブチルジメチルシリル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(110 mg,Ph3POと混合)のTHF(2 mL)中の懸濁液に、MeONa(19 mg,0.35 mmol)を加え、混合物を室温で20分間撹拌した。次に、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(75 mg,0.4 mmol)を加え、得られた混合物を室温で16時間撹拌した。その後、前記懸濁液に水(0.5 mL)を加えた。沈殿物を濾過により回収し、逆相カラム(MeCN/H2O)で精製して、(6S)-N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(45mg、純度:62%)を白色固体として得た。MS:m/z 546.4(M+H+).
工程4-(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例2)の合成:
(6S)-N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(45 mg、純度:62%)の懸濁液にMeOH(0.5 mL)を加えた。5 mL)を室温でHCl/ジオキサン(2 M,2 mL)を加えた。室温で16時間撹拌した後、反応混合物を濃縮し、逆相カラム(H2O中5-95%MeCN)で精製して、(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(7mg、収率21%、立体異性体の混合物)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=8.22(brs,1H),7.56(d,J=5.2 Hz,1H),7.31(brs,2H),6.89(s,1H),4.63(d,J=7.2 Hz,1H),4.37-4.19(m,3H),4.07(s,1H),3.38(overlap,3H),2.86-2.67(m,8H),2.02-1.91(m,4H).MS:m/z 432.2(M+H+).
実施例3
N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
表題化合物を、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(実施例1)の一般的手順を使用して調製した。具体的には、N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの調製のために記載された一般的な手順を用いて、エナンチオマーの混合物としてN’-((1,2,3.5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例1)を、工程3で4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを5-フルオロ-2-イソシアナト-1,3-ジイソプロピルベンゼンに置換することにより、実施例1と同様の方法で製造した。1H NMR(400 MHz,DMSO-d6):δ=8.01(s,1H),7.49(s,1H),7.23(s,2H),6.87(s,1H),6.85(s,1H),4.40-4.35(m,2H),4.10(t,J=6.0 Hz,2H),3.14-3.08(m,2H),2.18-2.15(m,2H),1.16-1.07(m,12H).MS:m/z 424.2(M+H+).
実施例4
N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順を用いて、表題化合物を調製した。N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの調製のために記載された一般的な手順を用いて、エナンチオマーの混合物としてN’-((1,2,3,5,6.7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例1)を、工程3で4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを4-フルオロ-8-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンに置換することにより、実施例1と同様の方法で製造することができる。1H NMR(400 MHz,DMSO-d6):δ=8.22(brs,1H),7.50(s,1H),7.23(s,2H),4.40-4.35(m,2H),4.10(t,J=6.0 Hz,2H),2.82(t,J=7.2 Hz,4H),2.70(t,J=7.2 Hz,4H),2.20-2.17(m,2H),2.01-1.96(m,4H).MS:m/z 420.1(M+H+).
実施例5
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-4-スルホンイミドアミド
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-4-スルホンイミドの調製のために記載された一般的な手順を用いて、エナンチオマーの混合物としてN’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6を調製した。7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例6)は、工程1で6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを1-メチル-1H-ピラゾール-4-スルホンイミドに置き換えることにより、立体異性体の混合物として表題化合物を得ることができた。MS:m/z 360(M+H+).
実施例6
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-N-(tert-ブチルジメチルシリル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミドの合成:
THF(28 mL)中の6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(1.5 g,6.5 mmol)を0℃で窒素下で撹拌した溶液を、水素化ナトリウム(60%,0.31 g,7.8 mmol)で処理した。20分後、tert-ブチルジメチルシリルトリフルオロメタンスルホン酸(2.3 g,8.4 mmol)を5分間かけて滴下添加した。次いで冷却浴を除去し、反応混合物を室温で13時間撹拌した。反応混合物を飽和NH4Cl溶液(10 mL)を添加して急冷した。水性混合物をEtOAc(3×20 mL)で抽出した。合わせた有機層を水、ブラインで洗浄し、Na2SO4上で乾燥させ、濃縮して無色の半固体残渣を得た。得られた残渣をシリカゲルカラム(DCM中の0-30%EtOAc)で精製した。クリ-ンな画分を組み合わせて、N-(tert-ブチルジメチルシリル)-6,6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(1.15 g,51 %)を白色固体として得た。MS:m/z 346(M+H+).
工程2-N’-(tert-ブチルジメチルシリル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
窒素下、0℃でCHCl3(12 mL)中で撹拌したトリフェニルホスフィンジクロリド(1.16 g,3.5 mmol)の懸濁液を、Et3N(0.52 mL,3.8 mmol)で5分間処理した。氷浴を除去し、混合物を15分間撹拌した(白色の懸濁液が形成された).混合物を0℃まで冷却した後、N-(tert-ブチルジメチルシリル)-6,6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(1g,2.9mmol)のCHCl3(12mL)中の溶液を加えた。混合物を20分間撹拌した後、氷浴を除去し、混合物を20分間撹拌した。混合物を0℃に冷却し、1,4ジオキサン中のアンモニア(20mL,11.6mmol)の0.5M溶液で処理した。混合物を30分間撹拌した後、氷浴を除去し、混合物をさらに1時間撹拌した。混合物を水(50mL)で処理した後、混合物を水のみが残るまで濃縮した;得られた水性混合物をEtOAc(3×30mL)で抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥し、濾過し、濃縮した。得られた固体をシリカゲルカラム(0-100%,DCM中のEtOAc)で精製した。所望の生成物を含む画分は、トリフェニルホスフィンオキシドで汚染されていた。画分を合わせ、濃縮して白色の固体を得た。この固体をヘキサン(20 mL)中の20%EtOAcの溶液で処理し、超音波処理し、沈殿物が形成される前に20分間静置した。懸濁液を濾過し(固体はトリフェニルホスフィンオキシドと判定された)、濾液を濃縮して乾燥させ、N’-(tert-ブチジメチルシリル)-6,6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(850 mg)をトリフェニルホスフィンオキシドで汚染して得た。これ以上の精製を行うことなく、材料を進めた。MS:m/z 345(M+H+).
工程3-N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
N’-(tert-ブチルジメチルシリル)-6,6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(400.0 mg,0.35 mmol,30% w/w)をDMF(4 mL)中で窒素下0℃で撹拌した溶液をNaH(60%,18 mg,0.45 mmol)で処理した。15分後、混合物を4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(76mg,0.38mmol)で処理した。氷浴を除去し、混合物をさらに2時間撹拌した。混合物を飽和NH4Cl溶液で処理し、EtOAc(3 X 20 mL)で抽出した。合わせた有機層を食塩水で洗浄し、硫酸ナトリウム上で乾燥し、濾過し、濃縮した。得られた残渣をMeOHで希釈し、超音波処理し、2時間静置した。懸濁液を濾過した後、濾過ケーキを追加のMeOHで洗浄した。濾液を蒸発させて乾燥させ、N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(180 mg)をトリフェニルホスフィンオキサイドで汚染して得た。これ以上の精製を行うことなく、材料を進めた。MS:m/z 544(M+H+).
工程4-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例6):
N’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(180 mg,0.07 mmol)の溶液を1,4ジオキサン(2 mL,6.6 mmol)中で撹拌した。07 mmol)を1,4ジオキサン(2 mL)中で撹拌した後、4N塩酸(2 mL,6.6 mmol)の溶液で処理した。氷浴を除去し、混合物を15分間撹拌した後、濃縮した。得られた固体をMeOH(30 mL)で希釈し、超音波をかけ、30分間静置した後、ろ過した。濾液を濃縮して乾燥させた後、得られた固体をエチルエーテル(20 mL)に懸濁させ、超音波処理して濾過した。白いフィルターケーキはトリフェニルホスフィンオキシドであり、濾液は残りのトリフェニルホスフィンオキシド及び他の副生成物と共に所望の生成物を含んでいた).濾液を濃縮した後、エチルエーテルトリチュレーションをさらに2回繰り返した。最後のトリチュレーションの濾液を濃縮した。得られた固体をMeOH(5 mL)で希釈し、わずかな懸濁液を得た。懸濁液を0.45Aシリンジフィルターで濾過し、濾液をPrep-LCMS(05-95%ACN,0.1% NH4Cl)で精製した。画分を回収し、濃縮してN-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを白色固体として得た(6 mg、立体異性体の混合物).MS:m/z 430(M+H+).
実施例7及び実施例8
(S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1と工程2.これら2つの工程は、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順と同様であった。
(S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(80 mg,0.2 mmol)をキラル分取HPLCで分離し、未知の絶対立体化学の2つの異性体を白色固体として得た。
ピーク1,21.4 mg、収率27% 1H NMR(400 MHz,DMSO-d6):δ=7.99(s,1H),7.49(s,1H),7.23(brs,2H),6.86(s,1H),6.84(s,1H),4.40-4.35(m,2H),4.10(t,J=6.0 Hz,2H),3.14-3.08(m,2H),2.18-2.15(m,2H),1.16-1.07(m,12H).MS:m/z 424.2(M+H+).
ピーク2,18.1mg、収率23% 1H NMR(400 MHz,DMSO-d6):δ=7.99(s,1H),7.49(s,1H),7.24(brs,2H),6.87(s,1H),6.84(s,1H),4.40-4.35(m,2H),4.10(t,J=6.0 Hz,2H),3.14-3.08(m,2H),2.18-2.15(m,2H),1.16-1.07(m,12H).MS:m/z 424.2(M+H+).
実施例9
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-N’-(tert-ブチルジメチルシリル)-N-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
N2雰囲気下、乾燥CHCl3(4.5 mL)中のトリフェニルホスフィンジクロリド(1.2 g,3.5 mmol)の撹拌懸濁液にトリエチルアミン(0.42 g,4.2 mmol)を加えた.反応混合物を室温で10分間撹拌した(白色の懸濁液が形成された).次いで、反応混合物を0℃に冷却し、乾燥CHCl3(3.5 mL)中のN-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンアミド(0.44 g,1.4 mmol)の溶液を滴下添加した。反応混合物を1時間かけて10℃まで温め、0℃まで冷却し、THF中のメタナミン(3 mL,6.9 mmol)の2M溶液を滴下添加した。反応混合物を0℃で20分間撹拌した後、室温まで2時間かけて暖めた。次いで、反応混合物を濃縮して乾燥させ、残渣をシリカゲルクロマトグラフィー(ヘキサン中30-100%EtOAc,DCM中0-10%MeOH)で精製して、トリフェニルホスフィンオキシド不純物を有するN’-(tert-ブチルジメチルシリル)-N-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(0.25 g,-85% w/w)を得た。この材料は、追加の精製を行わずに次の工程で使用した。MS:m/z 331(M+H+).
工程2-N’-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
N’-(tert-ブチルジメチルシリル)-N-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(0.25 g,~0.64 mmol,~85% w/w)のCH3CN(3 mL)中の溶液を10℃に冷却した溶液に、1,4-ジオキサン中の4N HCl(0.9 mL,3.8 mmol)の溶液を加え、1,4-ジオキサン中の4N HCl(0.9 mL,3.8 mmol)を加えた。反応混合物を2時間かけて室温まで温めた。次いで、反応混合物を濃縮して乾燥させ、残渣を分取HPLC(CH3CN/H2O/10mM aq.NH3)により精製して、N’-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(78mg、収率)を得た:48%)を無色油として得た。1H NMR(500 MHz,DMSO-d6):δ=7.44(s,1H),6.32(br.s,1H),4.41-4.35(m,2H),4.11(t,J=6.1 Hz,2H),3.71(br.s,1H),2.41(s,3H),2.22-2.17(m,2H).MS:m/z 217(M+H+).
工程3-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例9):
0℃に冷却したDMF(1 mL)中のN’-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(44 mg,0.20 mmol)の溶液に、N2雰囲気下で水素化ナトリウム(60%,8.1 mg,0.20 mmol)を加え、反応混合物を10分間撹拌した。次いで、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(41 mg,0.20 mmol)を1部添加し、氷水浴を除去した。反応混合物を室温で62時間撹拌した。反応混合物をMeOHで急冷し、ろ過し、分取HPLC(CH3CN/H2O/10 mM aq.NH3)で精製した。NH3)にN-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-メチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(9.2 mg、収率11 %、立体異性体の混合物)を白色固体として得た。1H NMR(500 MHz,DMSO-d6):δ=8.26(br.s,1H),7.50(s,1H),7.11(br.s,1H),6.87(s,1H),4.45-4.36(m,2H),4.13(t,J=6.1 Hz,2H),2.79(t,J=7.3 Hz,4H),2.71(t,J=7.3 Hz,4H),2.49(s,3H),2.25-2.17(m,2H),1.98-1.92(m,4H).MS:m/z 416(M+H+).
実施例10
1-(シクロプロピルメチル)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1H-ピラゾール-4-スルホンイミドアミド
1-(シクロプロピルメチル)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1H-ピラゾール-4-スルホンイミドを、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6の調製のために記載された一般的な手順を用いて、エナンチオマーの混合物として調製した。7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例6)は、工程1で6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを1-(シクロプロピルメチル)-1H-ピラゾール-4-スルホンイミドに置き換えることにより、立体異性体の混合物として表題化合物を得ることができた。MS:m/z 400(M+H+).
実施例11及び実施例12
N’-ベンジル-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルホンイミド及びN-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルホンイミド)
工程1-メチル-1H-ピラゾール-3-スルフィネートの合成
水(6 mL)に亜硫酸ナトリウム(1.4 g,2 Eq.11 mmol)と炭酸水素ナトリウム(0.93 g,2 Eq.11 mmol)の溶液を80℃に加熱し、1,4-ジオキサン(6 mL)に1-メチル-1H-ピラゾール-3-スルホニルクロリド(1.0 g,1 Eq.5.5 mmol)の溶液をゆっくりと加えた。反応混合物を同温度で1時間撹拌した後、減圧下で濃縮した。エタノール(100mL)を加え、反応混合物を1時間還流させた後、反応混合物が熱いうちに上清を分離した。残渣にエタノール(100 mL)を加え、室温で30分間撹拌した後、ろ過した。濾液を合わせ、減圧下でエタノールを除去して白色の固体を得た。
得られた固体をクロロホルム(10 mL)に懸濁し、塩化チオニル(0.86 g,0.53 mL,1.3 Eq.7.2 mmol)をN2下0 oCで滴下添加した。添加が完了した後、反応混合物を室温まで温め、1時間撹拌した(溶液A).別のフラスコに、THF(10 mL)中のTEA(1.7 g,2.3 mL,3 Eq.16 mmol)、メタノール(0.89 g,1.1 mL,5 Eq.28 mmol)を-78℃に冷却し、溶液AをN2下でゆっくりと添加した。反応混合物を0℃に温め、1時間撹拌した。TLC(10%MeOH/DCM)により反応の完了を示した。混合物をEtOAcで希釈し、水、食塩水で洗浄し、Na2SO4上で乾燥し、減圧下で濃縮し、シリカゲルクロマトグラフィー(0-100%EtOAc/Hex)で精製して、メチル-1-メチル-1H-ピラゾール-3-スルフィネート(503mg,56%、立体異性体の混合物)を白色固体として得た。1H NMR(400 MHz,DMSO-d6)σ 7.93(s,1H),6.68(s,1H),3.93(s,3H),3.52(s,3H).(ESI,m/z):161 [M+H]+.
工程2及び3-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルフィンアミドの合成:
無水THF(3 mL)中のメチル-1-メチル-1H-ピラゾール-3-スルフィネート(400 mg,1 Eq.2.5 mmol)の溶液に、N2の下でLHMDS(627 mg,3.7 mmol,1.5 Eq.3.75 mmol,THF中の1 M)を加えた。反応物を室温に温め、2時間撹拌した後、飽和NH4Cl溶液1mLを加え、さらに1時間撹拌した。その後、EtOAc(50 mL)を加え、得られた溶液をNa2SO4上で乾燥させた。混合物を濾過し、溶媒を留去して、粗1-メチル-1H-ピラゾール-3-スルフィンアミド(363mg,100%)を白色固体として得た。生成物は、追加の精製を行わずに次の工程で使用した。
前記のようにして得られた1-メチル-1H-ピラゾール-3-スルフィンアミド(363mg,1当量2.5mmol)を無水DMF(3mL)に溶かした。この溶液に4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(495 mg,1 Eq.2.5 mmol)を加え、次いでNaH(0.2 g,2 Eq.5.00 mmol,60%重量)を室温で加えた。混合物を1時間撹拌した後、1 mL MeOHで急冷した。混合物を分取HPLCにより精製し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルフィンアミド(190mg,22%)を白色固体として得た。1H NMR(400 MHz,DMSO-d6)σ 7.76(s,1H),6.85(s,1H),6.62(s,1H),3.88(s,3H),2.80(t,4H),2.73(t,4H),1.95(t,4H).LCMS:m/z=367 [M+Na]+.
N’-ベンジル-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルホンイミドの合成
工程4-N-ベンジル-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルホンイミドの合成
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルフィンアミド(50.0 mg,1 Eq.145 μmol)の無水アセトニトリル(1 mL)中の溶液に、NCS(29.1 mg,1.5 Eq.218 μmol)を0℃で加えた。反応物を室温まで温め、1時間撹拌した後、ベンジルアミン(31.1 mg 32 μL,2 Eq.290 μmol)をN2下で滴下添加した。反応混合物を室温で1時間撹拌した後、水(10 mL)を加えた。混合物をEtOAc(3×10 mL)で抽出し、結合した有機抽出物を水、ブラインで洗浄し、Na2SO4上で乾燥し、濃縮した。シリカゲルクロマトグラフィー(EtOAc/Hex 0-100%,MeOH/DCM 0-10%)で精製し、N’-ベンジル-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルホンイミド(35 mg,54%、立体異性体の混合物)を白色固体として得た。(ESI,m/z):450 [M+H]+.
工程5-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルホンイミドの合成
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルフィンアミド(50.0 mg,1 Eq.145 μmol)の無水アセトニトリル(1 mL)中の溶液に、NCS(29.1 mg,1.5 Eq.218 μmol)を0℃で加えた。反応混合物を室温まで温め、1時間撹拌した後、HMDS(46.9 mg,61 μL,2 Eq.290 μmol)をN2下で滴下添加した。反応物を室温で1時間撹拌し、粗混合物を分取HPLCにより精製し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-1-メチル-1H-ピラゾール-3-スルホンイミド(4mg,8%、立体異性体の混合物)を白色固体として得た。(ESI,m/z):360 [M+H]+.
実施例13及び実施例14
(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(S)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン(1.1 g,5.4 mmol)のTHF(20 mL)溶液に、n-BuLi(2.4 mL,5.9 mmol,2.5 M in hexane)を-78℃で滴下添加し、この温度で1時間撹拌した。THF(10 mL)中のTrtNSO(1.8 g,5.9 mmol)の溶液を滴下添加し、混合物を-78℃で20分間撹拌した後、氷浴に入れた。さらに10分間撹拌した後、次亜塩素酸tert-ブチル(650 mg,5.9 mmol)を加え、20分間撹拌した。次いで、NH3ガスを5分間バブリングし、得られた溶液を室温で16時間撹拌した。反応混合物を濃縮して乾燥させ、残渣を逆相カラム(MeCN/H2O)で精製して、N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(716mg、収率30%)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=7.43-7.41(m,6H),7.20-7.15(m,6H),7.11-7.07(m,3H),6.99(s,1H),6.20(brs,2H),4.20-4.19(m,2H),3.97-3.89(m,2H),2.10-2.07(m,2H).
工程2-N-(((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
THF(10 mL)中のN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(716 mg,1.6 mmol)の溶液に、MeONa(96 mg,1.8 mmol)を加え、室温で30分間撹拌した。次いで、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(375mg,1.7mmol)を加え、室温で16時間撹拌した。反応混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(370mg、収率36%)を白色固体として得た。MS:m/z 644.3(M+H+).
工程3-(R)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(S)-N-((1.2,3,5,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(350 mg,0.5 mmol)をキラル分取HPLCで分離し、白色固体として未知の絶対立体化学の2つの異性体R)-N-(((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S)-N-(((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを得た(ピーク1,80mg、収率23%、ピーク2,150mg、収率43%).
工程4-(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例13及び実施例14):
ピーク1から採取した材料(80 mg,0.1 mmol)のDCM(5 mL)溶液に、2滴のメチルスルホン酸を加えた。室温で0.5時間撹拌した後、反応液を飽和NaHCO
3でpH=8に調整し、濃縮して乾燥させ、逆相カラム(MeCN/H
2O)で精製して粗生成物を得た。粗生成物をさらに分取HPLC(NH
3.H
2O)で精製し、(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(2.2mg、収率5%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
1H NMR(400 MHz,DMSO-d
6):δ=8.01(s,1H),7.43(s,1H),6.82(s,1H),6.71(brs,1H),4.35(t,J=4.4 Hz,2H),4.08(t,J=6.0 Hz,2H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.17-2.15(m,2H),1.96-1.89(m,4H).MS:m/z 402.1(M+H
+).
ピーク2から採取した材料(80 mg,0.1 mmol)のDCM(4 mL)溶液に、2滴のメチルスルホン酸を加えた。室温で0.5時間撹拌した後、飽和NaHCO3を添加してpH=8に調整した。沈殿物を濾取し、乾燥して、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(10mg、収率23%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.17(s,1H),7.50(s,1H),7.21(s,2H),6.85(s,1H),4.41(t,J=3.2 Hz,2H),4.10(t,J=5.6 Hz,2H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.19-2.15(m,2H),1.96-1.89(m,4H).MS:m/z 402.1(M+H+).
実施例15
(6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成
THF(10 mL)中の(S)-3-ブロモ-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン(1.0 g,4.3 mmol)の溶液に、-78℃でn-BuLi(1.8 mL,4.3 mmol,2.5 M in hexane)を滴下添加し、この温度で0.5時間撹拌した。THF(5 mL)中のTrtNSO(1.3 g,4.3 mmol)の溶液を滴下添加し、混合物を-78℃で30分間撹拌した後、氷浴に入れた。さらに10分間撹拌した後、次亜塩素酸tert-ブチル(480 mg,4.5 mmol)を加え、20分間撹拌した。この混合物にNH3ガスを10分間バブリングし、得られた溶液を室温で16時間撹拌した。反応混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して、(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(400mg、収率20 %)を得た.
工程2-(6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(100 mg,0.2 mmol)のTHF(2 mL)中の溶液に、MeONa(13 mg,0.2 mmol)を加えた。反応混合物を室温で20分間撹拌し、ナトリウム塩懸濁液を得た。
別のフラスコに、THF(3 mL)中の4-フルオロ-2,6-ジイソプロピルアニリン(49 mg,0.3 mmol)の溶液に、トリエチルアミン(75 mg,0.8 mmol)及びトリホスゲン(29 mg,0.1 mmol)を0℃で1部ずつ加えた。N2下で室温で10分間撹拌した後、反応混合物を濾過した。この濾液を前記ナトリウム塩懸濁液に添加した。新しい反応混合物を室温で16時間撹拌した後、濃縮し、逆相カラム(MeCN/H2O)で精製して、(6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(49mg,33%)を黄色固体として得た。MS:m/z 696.4(M+H+).
工程3-(6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例15):
(6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(80 mg,0.1 mmol)のTHF(1.5 mL)中の溶液に、0℃でMeSO3H(6滴)を加えた。この温度で0.5時間撹拌した後、反応混合物を濃縮し、逆相カラム(MeCN/H2O)で精製して、(6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(32 mg,59 %、混合ジアステレオマー)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=7.99(s,1H),7.52-7.49(m,1H),7.13(brs,2H),6.88(s,1H),6.85(s,1H),4.64-4.50(m,1H),4.31-4.14(m,3H),4.04(s,1H),3.37(overlap,3H),3.20-3.06(m,2H),1.15-1.02(m,12H).MS:m/z 454.1(M+H+).
実施例16
(6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.
(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順を用いて表題化合物を調製し、混合物の立体異性体を得た。(6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの調製のために記載された一般的な手順を用いて、ジアステレオマーの混合物として(6S)-N’-((1,2,3.5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例17)を、工程2で4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを5-フルオロ-2-イソシアナト-1,3-ジイソプロピルベンゼンに置き換えることにより、実施例1と同様の方法で製造した。1H NMR(400 MHz,DMSO-d6):δ=8.03(d,J=10.0 Hz,1H),7.50(s,1H),7.23(brs,2H),6.86(s,1H),6.84(s,1H),4.40-4.19(m,3H),3.92-3.90(m,1H),3.15-3.10(m,3H),2.33(s,3H),1.07(s,12H).MS:m/z 453.2(M+H+).
実施例17
(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-tert-ブチルメチル((6S)-3-(N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)カルバメートの合成:
(S)-tert-ブチル(3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメート(570 mg,1.7 mmol)のTHF(15 mL)中の溶液に、n-BuLi(0.8 mL,1.9 mmol,2.5 M in hexanes)を-78℃で滴下添加し、この温度で1時間撹拌した。THF(5 mL)中のTrNSO(573 mg,1.9 mmol)の溶液を滴下添加し、混合物を-78℃で20分間撹拌した後、氷浴に入れた。さらに10分間撹拌した後、次亜塩素酸tert-ブチル(206mg,1.9mmol)を加え、20分間撹拌した。この混合物にNH3ガスを5分間バブリングし、得られた溶液を室温で16時間撹拌した。反応混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して、tert-ブチルメチル((6S)-3-(N’-トリチルスルファミミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)カルバメート(420mg、収率43%)を黄色固体として得た。MS:m/z 574.5(M+H+).
工程2-tert-ブチル((6S)-3-(N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメートの合成:
tert-ブチルメチル((6S)-3-(N’-トリチルスルファミミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)カルバメート(200 mg,0.3 mmol)のTHF(10 mL)中の溶液にMeONa(21 mg,0.4 mmol)を加え、室温で30分間撹拌した。次に、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(375 mg,1.7ミリモル)を加えた。室温で16時間撹拌した後、混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して、tert-ブチル((6S)-3-(N-(1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメート(110 mg、収率42%)を白色固体として得た。
工程3-(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例17)の合成:
DCM(5 mL)中の(((6S)-3-(N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメート(110 mg,0.1 mmol)の溶液に、メタンスルホン酸2滴を加えた。室温で0.5時間撹拌した後、反応液を飽和NaHCO4でpH=8に調整した。混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して粗生成物を得た。粗生成物をさらに分取HPLC(NH4HCO3)で精製し、((6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(3,8mg、収率6%、ジアステレオ異性体の混合物)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=8.18(brs,1H),7.51(d,J=5.2 Hz,1H),7.24(brs,2H),6.86(s,1H),4.30-4.20(m,3H),3.94(d,J=12.8 Hz,1H),3.15-3.14(m,1H),2.79(t,J=7.2 Hz,4H),2.70(t,J=7.2 Hz,4H),2.33(d,J=2.0 Hz,3H)1.96-1.83(m,4H).MS:m/z 431.2(M+H+).実施例18
実施例18
(6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-(6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成:
(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(83 mg,0.2 mmol)のTHF(3 mL)中の溶液に、MeONa(28 mg,0.5 mmol)を加えた。反応混合物を45℃で20分間撹拌し、ナトリウム塩懸濁液を得た。
別のフラスコに、THF(5 mL)中の8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(191 mg,1.0 mmol)の溶液に、Et3N(0.2 mL,1.1 mmol)及びトリホスゲン(100 mg,0.4 mmol)をアイスバスで1部ずつ加えた。反応混合物を70℃でN2下で1時間撹拌した。反応混合物を濾過し、濾液を前記ナトリウム塩懸濁液に加えた。新しい反応混合物を室温で16時間撹拌し、濃縮して、(6S)-N’-(tert-ブチルジメチルシリル)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(粗製)を得て、これをそのまま次の工程に使用した。MS:m/z 692.4(M+H+).
工程2-(6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例18):
(6S)-N’-(tert-ブチルジメチルシリル)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(粗)のDCM(2 mL)溶液に、MeSO3H(0.88 mmol)を0℃で加えた。05 mL,0.88 mmol)を 0℃で加えた。この温度で5分間撹拌した後、反応液を飽和NaHCO3でpH=8に調整した。得られた混合物を濃縮し、MeCN(3 mL)で希釈し、濾過した。濾液を分取HPLCにより精製し、(6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(3mg、収率2%、ジアステレオ異性体の混合物)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=8.23(brs,1H),7.53(s,1H),7.23(brs,1H),4.59(d,J=12.0 Hz,1H),4.31-4.17(m,3H),4.03(s,1H),3.36(overlap,3H),2.80(t,J=6.4 Hz,4H),2.72(t,J=6.0 Hz,4H),2.02-1.97(m,4H);MS:m/z 450.1(M+H+).
実施例19及び実施例20
(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(200 mg,0.4ミリモル)の溶液に THF(3mL)中のMeONa(25mg,0.5mmol)を加え、混合物を室温で20分間撹拌した。次に、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(75 mg,0.4 mmol)を加えた。t得られた混合物を室温で16時間撹拌し、濃縮し、逆相により精製した。カラム(MeCN / H2O)で(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(240 mg、収率85%)を黄色固体として得た。MS:m/z 674.5(M+H+).
工程2-(S,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
(S,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(460 mg,0.7 mmol)をキラル分取HPLCで分離し、絶対立体化学が不明な2つの異性体(ピーク1,200mg;ピーク2,227mg)を黄色固体として得た。MS:m/z 674.4(M+H+).
工程3-(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成(実施例19及び実施例20):
前記ピーク1の材料(100 mg,0.2 mmol)のTHF(2 mL)溶液に、0℃で MeSO3Hを加えた。この温度で0.5時間撹拌した後、反応混合物を飽和NaHCO3でpH=8に調整した。析出物を濾過で回収し、水(2mL),THF(2mL)で洗浄し、乾燥して、(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(27mg、収率42%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.19(s,1H),7.54(s,1H),7.29(s,2H),6.86(s,1H),4.59(d,J=12 Hz,1H),4.35-4.15(m,3H),4.03(s,1H),3.40(s,3H),2.77(t,J=6.8 Hz,4H),2.69(t,J=6.4 Hz,4H),2.01-1.88(m,4H).MS:m/z 432.2(M+H+).
ピーク2からの材料を同様に脱保護して単離し、白色の固体を得た。(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.16(s,1H),7.51(s,1H),7.18(s,2H),6.85(s,1H),4.59(d,J=11.6 Hz,1H),4.31-4.15(m,3H),4.03(s,1H),3.36(s,3H),2.77(t,J=7.2 Hz,4H),2.69(t,J=7.2 Hz,4H),1.98-1.88(m,4H).MS:m/z 432.2(M+H+).
実施例21及び実施例22
(S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((8-フルオロ-1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
(S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順を用いて表題化合物を調製し、混合物の立体異性体を得た。工程2で4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを4-フルオロ-8-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンに置き換えることにより、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例13及び実施例14)の調製に記載された一般的な手順を用いて、(S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及びR)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを調製した。キラル分取PLC精製後、絶対立体化学が不明な2つの異性体が単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.03(brs,1H),7.45(s,1H),6.86(brs,2H),4.36(t,J=3.6 Hz,2H),4.10(t,J=6.0 Hz,2H),2.82(t,J=7.2 Hz,4H),2.72(t,J=7.2 Hz,4H),2.20-2.15(m,2H),2.01-1.96(m,4H).MS:m/z 420.1(M+H+).化合物22
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.20(brs,1H),7.50(s,1H),7.23(s,2H),4.40-4.35(m,2H),4.10(t,J=6.0 Hz,2H),2.82(t,J=7.2 Hz,4H),2.72(t,J=7.2 Hz,4H),2.21-2.17(m,2H),2.01-1.96(m,4H).MS:m/z 420.1(M+H+).化合物21
実施例23及び実施例24
(S,6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R.6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-(S,6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R.6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
(6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(280 mg,0.4 mmol)をキラル分取HPLCで分離し、未知の絶対立体化学の2つの異性体(ピーク1,135 mg;ピーク2,80 mg)を黄色固体として得た;(S,6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R.6S)-N-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.
工程-(S,6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R.6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例23及び実施例24):
前記ピーク1から採取した材料の溶液(135 mg,0.2 mmol)に、THF(2 mL)中のMeSO3H(6滴)を0℃で加えた。この温度で0.5時間撹拌した後、反応混合物を濃縮し、逆相カラム(MeCN/H2O)で精製して、(S,6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(40 mg、収率46%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.01(s,1H),7.52(m,1H),7.33(s,2H),6.86(s,1H),6.84(s,1H),4.60-4.56(m,1H),4.33-4.18(m,3H),4.04(s,1H),3.36(s,3H),3.20-3.06(m,2H),1.17-1.02(m,12H).MS:m/z 454.2(M+H+).
ピーク2についても同様にして、白色の固体を得た。ピーク2からの材料を同様の方法で脱保護し、単離して、(R,6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.02(s,1H),7.50(s,1H),7.28(s,2H),6.87(s,1H),6.84(s,1H),4.60-4.56(m,1H),4.33-4.18(m,3H),4.04(s,1H),3.36(s,3H),3.20-3.06(m,2H),1.17-1.02(m,12H).MS:m/z 454.2(M+H+).
実施例25及び実施例26
(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-tert-ブチル((S)-3-((R)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1.3]オキサジン-6-イル)(メチル)カルバメート及びtert-ブチル((S)-3-((S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメート:
tert-ブチル((S)-3-((R)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメート及びtert-ブチル((S)-3-((R)-N-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメ-ト:tert-ブチル((6S)-3-(N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-6-イル)(メチル)カルバメート(1.0 g,1.3 mmol)をキラル分取HPLCで分離し、絶対立体化学的に未知の2つの異性体を白色固体として得た(ピーク1,410 mg、収率41%;ピーク2,450 mg、収率45%).
工程2-(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例25及び実施例26):
メタンスルホン酸(3滴)の添加 前記ピーク1の材料(200 mg,0.3 mmol)の DCM(3 mL)溶液にメタンスルホン酸を3滴添加した。室温で0.5時間撹拌した後、反応液を飽和NaHCO3でpH=8に調整した。沈殿物を濾取し、乾燥して(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(17.0 mg,収率15%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.21(brs,1H),7.51(s,1H),7.26(brs,2H),6.86(s,1H),4.36-4.20(m,3H),3.95-3.91(m,1H),3.16-3.15(m,1H),2.77(t,J=6.8 Hz,4H),2.68(t,J=6.8 Hz,4H),2.33(s,3H),2.15(brs,1H),1.96-1.89(m,4H).MS:m/z 431.1(M+H+).
前記ピーク2からの材料を同様の方法で脱保護し、単離して白色固体を得た。(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.16(brs,1H),7.51(s,1H),7.23(brs,2H),6.86(s,1H),4.36-4.20(m,3H),3.95-3.91(m,1H),3.16-3.14(m,1H),2.77(t,J=7.2 Hz,4H),2.69(t,J=6.8 Hz,4H),2.33(s,3H),2.07(brs,1H),1.98-1.89(m,4H).MS:m/z 431.1(M+H+).
実施例27及び実施例28
R,6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
(R,6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((4-フルオロ-2,6-ジイソプロピルフェニル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを、(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの調製に記載された一般的な手順を用いて調製した(実施例25及び実施例26).キラル分取HPLC後、絶対立体化学が不明な2つの異性体が白色固体として単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=7.99(s,1H),7.48(s,1H),7.23(brs,2H),6.86(s,1H),6.84(s,1H),4.33-4.19(m,3H),3.92-3.89(m,1H),3.15-3.10(m,3H),2.13(s,3H),2.06(brs,1H),1.07(s,12H).MS:m/z 453.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.03(s,1H),7.50(s,1H),7.23(s,2H),6.86(s,1H),6.84(s,1H),4.36-4.19(m,3H),3.93-3.86(m,1H),3.11-3.08(m,3H),2.34(s,3H),2.32(s,1H),0.99(s,12H).MS:m/z 453.2(M+H+).
実施例29
N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド
工程1-7-ブロモ-2,3-ジヒドロピラゾロ[5,1-b]オキサゾールの合成:
2,3-ジヒドロピラゾロ[5,1-b]オキサゾール(2.0 g,18.2 mmol)のMeCN(40 mL)溶液にNBS(3.9 g,21.8 mmol)を0℃で分量添加し、反応混合物を室温で2時間撹拌した。混合物を濾過し、濾液を逆相カラム(MeCN/H2O)で精製し、白色固体として3 7-ブロモ-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール(2.4 g、収率 71%)を得た。
1H NMR(400 MHz,CDCl3):δ=7.30(s,1H),5.12(t,J=8.0 Hz,2H),4.35(t,J=8.0 Hz,2H).
工程2-4-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成(実施例29):
これらの3つの工程は、(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順と同様であり、表題化合物を白色固体として得ることができた。
N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドは、工程1において、(S)-tert-ブチル(3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメートを7-ブロモ-2,3-ジヒドロピラゾロ[5,1-b]オキサゾールに置き換えることにより、(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例17)の調製に記載された一般的な手順を用いて、エナンチオマーの混合物として調製された。1H NMR(400 MHz,DMSO-d6):δ=8.06(brs,H),7.50(s,1H),7.01(brs,2H),5.17(t,J=8.4 Hz,2H),4.31(t,J=8.4 Hz,2H),2.80(t,J=7.2 Hz,4H),2.72(t,J=7.2 Hz,4H),1.96-1.89(m,4H).MS:m/z 406.1(M+H+).
実施例30
N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド:
(R,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順を用いて表題化合物を調製し、混合物の立体異性体を得た。工程1で(S)-tert-ブチル(3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメートを3-ブロモ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンに置き換えることにより、(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例17)の調製に記載された一般的な手順を用いて、エナンチオマーの混合物としてN’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドを調製した。1H NMR(400 MHz,DMSO-d6):δ=8.08(brs,1H),7.43(s,1H),6.91(brs,2H),4.15(t,J=5.2 Hz,2H),4.10(t,J=4.8 Hz,2H),2.80(t,J=7.2 Hz,4H),2.71(t,J=7.2 Hz,4H),2.03-1.93(m,6H),1.78-1.71(m,2H).MS:m/z 434.1(M+H+).
実施例31及び実施例32
(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-(6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成:
(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(720 mg,1.5 mmol)の溶液に THF(15mL)中、MeONa(81mg,1.5mmol)を加えた。反応混合物を45℃で20分間撹拌して、ナトリウム塩懸濁液を得た。
次に、THF(15mL)中の4-フルオロ-8-イソシアネート-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(粗製、約1.5ミリモル)の溶液を前記のナトリウム塩懸濁液に加えた.新しい反応混合物を室温で16時間撹拌し、濃縮して、(6S)-N’-(tert-ブチルジメチルシリル)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(粗製)を得て、これを次の工程に直接使用した。
工程2-(R,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
(S,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
(6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(210 mg,0.3 mmol)をキラル分取HPLCで分離し、絶対立体化学的に未知の2つの異性体を黄色固体として得た(ピーク1,60 mg;ピーク2,120 mg).
工程3-(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成(実施例31及び実施例32):
(S,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
前記ピーク1の材料(60 mg,0.09 mmol)の DCM(4 mL)中の溶液に MeSO3H(3滴)を 0℃で加えた。この温度で0.5時間撹拌した後、反応混合物を飽和NaHCO3でpH=8に調整した。析出物を濾過により回収し、水(2 mL),DCM(2 mL)で洗浄し、乾燥させて白色固体(16 mg、収率42%)を得た。1H NMR(400 MHz,DMSO-d6):δ=8.19(brs,1H),7.52(s,1H),7.26(s,2H),4.59(d,J=12.0 Hz,1H),4.31-4.17(m,3H),4.03(s,1H),3.34(overlap,3H),2.80(t,J=6.4 Hz,4H),2.73(t,J=6.4 Hz,4H),2.01-1.97(m,4H).MS:m/z 450.1(M+H+).
前記ピーク2からの材料を同様の方法で脱保護し、単離して白色固体を得た。1H NMR(400 MHz,DMSO-d6):δ=8.25(brs,1H),7.52(s,1H),7.26(s,2H),4.59(d,J=12.0 Hz,1H),4.31-4.17(m,3H),4.03(s,1H),3.34(overlap,3H),2.80(t,J=6.4 Hz,4H),2.68(t,J=6.4 Hz,4H),2.01-1.97(m,4H).MS:m/z 450.1(M+H+).
実施例33及び実施例34
(R,6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1及び工程2-(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミンの合成:
ピリジン(40 mL)中の(R)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-オール(5.0 g,35.7 mmol)及びDMAP(44 mg,0.4 mmol)の溶液に、Tf2O(20.2 g,71.4 mmol)をN2雰囲気下、-10 oCでゆっくりと加えた。混合物を-10℃で2時間撹拌した。次いで、MeOH(20mL)中のジメチルアミン(20mL、水中33%)の溶液を添加し、得られた反応混合物を室温でさらに2時間撹拌した。反応混合物を濃縮し、逆相カラム(MeCN/H2O)で精製して、(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(850mg、収率14%)を黄色固体として得た。
工程3-(6S)-6-(ジメチルアミノ)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
NBS(1.1 g,6.1 mmol)をMeCN(40 mL)中の(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(850 mg,5.1 mmol)の溶液に0℃で部分的に添加し、反応混合物を室温で2時間撹拌した。混合物を濾過し、逆相カラム(MeCN/H2O)で精製して、(S)-3-ブロモ-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(770mg、収率59%)を黄色固体として得た。
工程4-(6S)-6-(ジメチルアミノ)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
THF(15 mL)中の(S)-3-ブロモ-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(570 mg,2.3 mmol)の溶液に、-78℃でn-BuLi(ヘキサン中2.5 M,1.0 mL,2.5 mmol)を滴下添加し、同温度で1時間撹拌した。THF(15 mL)中のTrtNSO(780 mg,2.6 mmol)の溶液を滴下添加し、混合物を-78℃で20分間撹拌した後、0℃の氷浴に入れた。さらに 10 分間撹拌した後、次亜塩素酸tert-ブチル(278 mg,2.6 mmol)を加え、混合物を 20 分間撹拌した。この混合物をNH3ガスで5分間バブリングし、得られた混合物を室温で16時間撹拌した。反応混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して、(6S)-6-(ジメチルアミノ)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(330mg、収率30%)を黄色固体として得た。MS:m/z 488.5(M+H+).
工程5-7-(R,6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例33及び実施例34):
(S,6S)-6-(ジメチルアミノ)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R.6S)-6-(ジメチルアミノ)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:これら3つの工程は、(S,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順と同様であった。
(R,6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドは、工程1で(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを(6S)-6-(ジメチルアミノ)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドに、4-フルオロ-8-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-インダセンに置き換えることにより、(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例31及び実施例32)の調製に記載された一般的な手順を用いて調製した。分取HPLC後、絶対立体化学が不明な2つの異性体が白色固体として単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.19(brs,1H),7.52(s,1H),7.28(s,2H),6.86(s,1H),4.45-4.41(m,2H),4.23-4.13(m,2H),2.91-2.87(m,1H),2.77(t,J=7.2 Hz,4H),2.70-2.67(m,4H),2.26(s,6H),1.98-1.87(m,4H).MS:m/z 445.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.19(brs,1H),7.52(s,1H),7.25(s,2H),6.86(s,1H),4.45-4.40(m,2H),4.23-4.13(m,2H),2.91-2.87(m,1H),2.77(t,J=7.2 Hz,4H),2.68(t,J=7.2 Hz,4H),2.27(s,6H),1.93-1.89(m,4H).MS:m/z 445.1(M+H+).
実施例35及び実施例36
(R,6S)-6-(((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-tert-ブチル(S)-(6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(2-フルオロエチル)カルバメ-トの合成
(S)-tert-ブチル(6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-6-イル)カルバメート(5.0 g,20.9ミリモル)のDMF(30mL)を、N 2の雰囲気下、0℃で、NaH(鉱油中60%,1.0g,25.1mmol)を少しずつ加えた。混合物を0℃で30分間撹拌した。次に、1-ブロモ-2-フルオロエタン(3.2g,25.1mmol)を0℃で滴下して加えた。室温で2時間撹拌した後、反応混合物を水(120mL)に注ぎ、EtOAc(100mL×3)で抽出した。合わせた有機層をブライン(100 mLx3)で洗浄し、Na2SO4上で乾燥し、濃縮した。残渣をシリカフラッシュカラム(PE/EtOAc)で精製し、(S)-tert-ブチル(6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(2-フルオロエチル)カルバメート(4.0 g、収率 66%)を白色固体として得た。
工程2-6-(R,6S)-6-((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例35及び実施例36):
(R,6S)-6-(((2-フルオロエチル)アミノ)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-((2-フルオロエチル)アミノ)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:これら5工程は、(S,6S)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの一般的な手順と同様であった。
工程2において、(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミンをtert-ブチル(S)-(6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(2-フルオロエチル)カルバメートに置き換えることにより、(R,6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例33及び実施例34)の調製に記載された一般的な手順で(R,6S)-6-(((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを調製した。分取HPLCの後、未知の絶対立体化学の2つの異性体が単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.16(brs,1H),7.52(s,1H),7.26(s,2H),6.85(s,1H),4.52(t,J=4.8 Hz,1H),4.40-4.37(m,2H),4.27-4.20(m,2H),3.94(dd,J=12.0,5.2 Hz,1H),3.34(overlap,1H),2.97-2.93(m,1H),2.90-2.86(m,1H),2.79(t,J=7.2 Hz,4H),2.70(t,J=7.2 Hz,4H),2.29-2.26(m,1H),1.97-1.89(m,4H).MS:m/z 463.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.16(brs,1H),7.52(s,1H),7.24(s,2H),6.85(s,1H),4.52(t,J=4.8 Hz,1H),4.41-4.367(m,2H),4.27-4.23(m,2H),3.94(dd,J=12.0,5.2 Hz,1H),3.34(overlap,1H),2.95(t,J=5.2 Hz,1H),2.89(t,J=5.2 Hz,1H),2.77(t,J=7.2 Hz,4H),2.70(t,J=7.2 Hz,4H),2.33-2.31(m,1H),1.97-1.89(m,4H).MS:m/z 463.1(M+H+).
実施例37
8-(3-(6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボン酸
工程1-8-ブロモ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミンの合成
1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(500 mg,2.9 mmol)のDCM(15 mL)溶液にNBS(530 mg,3.0 mmol)を0℃で1部ずつ加えた。室温で16時間撹拌した後、反応混合物をDCM(50 mL)で希釈し、H2O(40 mL)で洗浄し、Na2SO4上で乾燥し、濃縮した。残渣をシリカゲルカラム(PE中の0-20%EtOAc)で精製して、8-ブロモ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(570mg、収率78%)を赤色の固形物として得た。1H NMR(400 MHz,CDCl3):δ=3.44(brs,2H),2.90(t,J=7.2 Hz,4H),2.79(t,J=7.2 Hz,4H),2.17-2.09(m,4H).
工程2-メチル-8-アミノ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボキシレートの合成:
8-ブロモ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(570 mg,2.3 mmol),TEA(460 mg,4.5 mmol)及びPd(dppf)Cl2(160 mg,0.2 mmol)のMeOH(25 mL)中の混合物を、CO雰囲気下、75℃で16時間撹拌した(バル-ン).反応混合物を濃縮し、シリカフラッシュカラム(PE中0%-20%EtOAc)で精製し、赤色固体としてメチル-8-アミノ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボキシレート(410mg、収率78%)を得た。1H NMR(400 MHz,CDCl3):δ=3.82(s,5H),3.22(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.16-2.07(m,4H).
工程3-メチル8-(3-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボキシレートの合成:
N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(300 mg,0.7 mmol)のTHF(15 mL)溶液に、MeONa(41 mg,0.8 mmol)を加えた。反応混合物を室温で20分間撹拌し、ナトリウム塩懸濁液を得た。
別のフラスコに、THF(15 mL)中のメチル-8-アミノ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボキシレート(157 mg,0.7 mmol)の溶液に、トリエチルアミン(137 mg,1.4 mmol)とトリホスゲン(62 mg,0.2 mmol)を0℃で1回に分けて加えた。N2の下で室温で10分間撹拌した後、反応混合物を濾過した。この濾液を前記ナトリウム塩懸濁液に添加した。新しい反応混合物を室温で16時間撹拌した後、濃縮し、逆相カラム(MeCN/H2O)で精製し、メチル8-(3-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボキシレート(310mg、収率65%)を白色固体として得た。
工程4-8-(3-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボン酸の合成:
DMSO(5 mL)中のメチル8-(3-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボキシレート(200 mg,0.3 mmol)の溶液に、t-BuOK(160 mg,1.4 mmol)を添加した。室温で16時間撹拌した後、反応混合物をH2O(20 mL)に注ぎ、2 M aq.HClでpH=6に酸性化し、EtOAc(15 mLx2)で抽出した。合わせたEtOAcをブライン(20 mL)で洗浄し、Na2SO4上で乾燥し、濃縮して8-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボン酸(190 mg、粗)を白色固体として得た。MS:m/z 688.6(M+H+).
工程5-8-(3-(3-(アミノ(6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-イル)(オキソ)-λ6-スルファネイリデン)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボン酸の合成(実施例37):
8-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボン酸(190 mg、粗)のDCM(5 mL)溶液に、室温でMeSO3Hを2滴加えた。この温度で5分間撹拌した後、反応液をH2O(15mL)に注ぎ、飽和NaHCO3でpH=8に塩基性化した。得られた溶液をDCM(10 mL x2)で洗浄し、水相を2 M aq.HClでpH=6に酸性化した。沈殿物を濾過により回収し、次いで分取HPLC(TFA)により精製し、8-(3-(3-(6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-カルボン酸(26mg、収率20%、立体異性体の混合物)を白色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=12.46(brs,1H),8.39(s,1H),7.52(s,1H),7.25(s,2H),4.44-4.39(m,2H),4.11(t,J=6.0 Hz,2H),3.05(t,J=7.2 Hz,4H),2.71(t,J=7.2 Hz,4H),2.20-2.15(m,2H),1.96-1.89(m,4H).MS:m/z 446.1(M+H+).
実施例38及び実施例39
(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-(S)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジンの合成:
(S)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミンを、(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミンと同様にして、ジメチルアミンの代わりに3-メトキシアゼチジンを置換して調製した。
工程2-(S)-3-ブロモ-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジンの合成:
(S)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン(335 mg,1.6 mmol)のDCM(5 mL)溶液にNBS(300 mg,1.7 mmol)を1分位添加し、室温で1時間撹拌した。反応混合物をDCM(15 mL)で希釈し、飽和NaHCO3(15 mL)で洗浄した。有機層をNa2SO4で乾燥し、濃縮して乾燥させ、(S)-3-ブロモ-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン(440mg、収率95%)を黄色固体として得た。MS:m/z 290.3(M+H+).
工程3-(6S)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
(S)-3-ブロモ-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン(440 mg,1.5 mmol)のTHF(5 mL)溶液に、n-BuLi(0.6 mL,1.5 mmol,2.5 M in hexane)を-78℃で滴下添加し、この温度で30分間撹拌した。THF(2 mL)中のTrtNSO(466 mg,1.5 mmol)の溶液を滴下添加し、混合物を-78℃で20分間撹拌した後、氷浴に入れた。さらに10分間撹拌した後、次亜塩素酸tert-ブチル(181mg,1.7mmol)を加え、20分間撹拌した。この混合物にNH3ガスを5分間バブリングし、得られた溶液を室温で16時間撹拌した。反応混合物をH2O(1 mL)で急冷し、濃縮して乾燥させた。残渣を逆相カラム(MeCN/H2O)で精製し、(6S)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(336mg、収率35%)を白色固体として得た。MS:m/z 530.5(M+H+).
工程4-(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
(6S)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(276 mg,0.5 mmol)のTHF(10 mL)中の溶液に、MeONa(42 mg,0.8 mmol)を加え、混合物を室温で30分間撹拌した。次に、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(104 mg,0.5 mmol)を加え、混合物を室温で16時間撹拌した。反応混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して、(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(283mg、収率60%)を白色固体として得た。MS:m/z 729.6(M+H+).
工程5-(S,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
(6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(330 mg)をキラル分取HPLCで分離し、絶対立体化学的に未知の2つの異性体を白色固体として得た(ピーク1,132 mg、収率40 %;ピーク2,171 mg、収率51 %).ピーク1,132 mg、収率40 %;ピーク2,171 mg、収率51 %).
工程6-(R,6S)-N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例38及び実施例39):
前記ピーク1の材料(132 mg,0.2 mmol)の DCM(3 mL)中の溶液に、メタンスルホン酸を 2 滴加えた。室温で10分間撹拌した後、反応液を飽和NaHCO3でpH=8に調整した。得られた混合物を濃縮して乾燥させ、逆相カラム(MeCN/H2O)で精製して、白色固体(単一の未知の立体異性体)として(72mg、収率83%)を得た。1H NMR(400 MHz,DMSO-d6):δ=8.16(brs,1H),7.51(s,1H),7.28(s,2H),6.86(s,1H),4.35-4.22(m,2H),4.14(dd,J=13.2,4.4 Hz,1H),3.94-3.90(m,1H),3.85(d,J=13.2 Hz,1H),3.53(t,J=6.4 Hz,2H),3.14(s,3H),3.02-2.95(m,3H),2.77(t,J=7.2 Hz,4H),2.69(t,J=7.2 Hz,4H),1.97-1.89(m,4H).MS:m/z 487.2(M+H+).
前記ピーク2からの材料を同様に脱保護して単離し、白色固体(単一の未知の立体異性体)(72mg、収率63%)を得た。1H NMR(400 MHz,DMSO-d6):δ=8.17(brs,1H),7.48(s,1H),7.24(s,2H),6.86(s,1H),4.30-4.20(m,2H),4.14(dd,J=12.8,4.0 Hz,1H),3.96-3.90(m,1H),3.85(d,J=12.8 Hz,1H),3.57-3.52(m,2H),3.14(s,3H),3.02-2.95(m,3H),2.77(t,J=7.2 Hz,4H),2.69(t,J=7.2 Hz,4H),1.97-1.90(m,4H).MS:m/z 487.2(M+H+).
実施例40及び実施例41
(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドは、工程1で(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドをtert-ブチルメチル((6S)-3-(N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-6-イル)カルバメ-トに置き換えて(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例31及び実施例32)の調製に記載した一般的な手順で調製した。分取HPLC後、絶対立体化学が不明な2つの異性体が白色固体として単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.20(brs,1H),7.50(s,1H),7.24(s,2H),4.35-4.20(m,3H),3.95-3.91(m,1H),3.15-3.14(m,1H),2.81(t,J=7.2 Hz,4H),2.71(t,J=7.2 Hz,4H),2.33(s,3H)2.03-1.96(m,4H).MS:m/z 449.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.18(brs,1H),7.51(s,1H),7.24(s,2H),4.36-4.20(m,3H),3.93(dd,J=12.4,4.0Hz,1H),3.16-3.15(m,1H),2.81(t,J=7.6 Hz,4H),2.71(t,J=7.2 Hz,4H),2.33(s,3H)2.03-1.96(m,4H).MS:m/z 449.1(M+H+).
実施例42及び実施例43
(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドは、工程1で(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを(6S)-6-(3-メトキシアゼチジン-1-イル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドに置き換えて(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例31及び実施例32)の調製に記載した一般的な手順で調製した。分取HPLCの後、未知の絶対立体化学の2つの異性体が単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.20(brs,1H),7.51(s,1H),7.28(s,2H),4.27-4.17(m,2H),4.15-4.12(m,1H),3.93-3.83(m,2H),3.54-3.51(m,2H),3.14(s,3H),3.02-2.96(m,3H),2.80(t,J=7.6 Hz,4H),2.75-2.50(m,4H),2.03-1.96(m,4H).MS:m/z 505.1(M+H+).化合物43
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.12(brs,1H),7.47(s,1H),7.12(s,2H),4.27-4.19(m,3H),3.94-3.83(m,2H),3.56-3.51(m,2H),3.14(s,3H),3.02-2.96(m,3H),2.80(t,J=7.2 Hz,4H),2.74(t,J=7.2 Hz,4H),2.03-1.96(m,4H).MS:m/z 505.2(M+H+).化合物42
実施例44及び実施例45
(R,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-(R)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イルトリフルオロメタンスルホン酸の合成:
Tf2O(40.4 g,142.8 mmol)をピリジン/DCM(20 mL/80 mL)中の(R)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-オール(10.0 g,71.4 mmol)及びDMAP(88 mg,0.7 mmol)の溶液に滴下添加し、-10℃でN2の雰囲気下で行った。2時間後、混合物をシリカカラム(PE/EtOAc=3/1)で精製し、(R)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イルトリフルオロメタンスルホン酸塩(12.1 g、収率62%)を黄色油として得た。
工程2-(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミンの合成:
(R)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イルトリフルオロメタンスルホン酸(12.1 g,44.5 mmol)とジメチルアミン(33% in water,20 mL)のMeOH(20 mL)中の溶液を室温で16時間撹拌した。反応混合物を濃縮し、粗残渣を逆相カラム(0-60%MeCN in H2O)で精製し、(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(1,1g、収率15%)を黄色固体として得た。
工程3-(S)-3-ブロモ-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミンの合成:
NBS(1.7 g,11.2 mmol)をMeCN(40 mL)中の(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(1.7 g,10.2 mmol)の溶液に、0℃で室温で部分的に添加した。2時間後、反応物を濾過し、濾液を逆相カラム(5%-95%MeCN in H2O)で精製し、(S)-3-ブロモ-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(1,9g、収率76%)を黄色の固体として得た。
工程4-(6S)-6-(ジメチルアミノ)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
n-BuLi(ヘキサン中2.5M,3.0mL,7.4mmol)をTHF(15 mL)中の(S)-3-ブロモ-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-アミン(1.4 g,5.7 mmol)の溶液に滴下添加し、-78℃で反応させた。1時間後、THF(10 mL)中のTrtNSO(2.3 g,7.4 mmol)の溶液を滴下添加した。反応物を20分間撹拌した後、0℃の氷浴に入れた。さらに10分間撹拌した後、次亜塩素酸tert-ブチル(807mg,7.4mmol)を加えた。反応物を20分間撹拌した後、NH3ガスを5分間バブリングした。得られた溶液を室温まで温め、さらに16時間撹拌した。反応物を濃縮して乾燥させ、粗残渣を逆相カラム(5%-95%MeCN in H2O)で精製して、(6S)-6-(ジメチルアミノ)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(1,1g、収率:39%)を黄色固体として得た。MS:m/z 488.6(M+H+).
工程5-(6S)-6-(ジメチルアミノ)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
MeONa(73mg,1.4mmol)を室温でTHF(10 mL)中の(6S)-6-(ジメチルアミノ)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(600mg,1.2mmol)の溶液に添加した。5分後、反応物を45℃で20分間加熱し、ナトリウム塩懸濁液を得た。反応物を室温まで冷却し、THF(15 mL)中の4-フルオロ-8-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(粗製、-1.4 mmol)の溶液を加えた。16時間後、反応物を濃縮し、粗残渣を逆相カラム(5%-95%MeCN in H2O)で精製し、(6S)-6-(ジメチルアミノ)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(450mg、収率52%)を黄色の固体として得た。MS:m/z 705.7(M+H+).
工程6-(S,6S)-6-(ジメチルアミノ)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R.6S)-6-(ジメチルアミノ)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
(6S)-6-(ジメチルアミノ)-N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(450 mg,0.6 mmol)をキラル分取HPLCで分離して、未知の絶対立体化学的異性体を得た。6 mmol)をキラル分取HPLCで分離し、絶対立体化学的に未知の2つの異性体を白色固体として得た(ピーク1,160 mg;ピーク2,210 mg).
工程7-(R,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例44及び実施例45):
ピーク1の材料(160mg,0.2mmol)のDCM(4 mL)中の溶液にメタンスルホン酸(3滴)を0℃で添加した。30分後、飽和水性NaHCO3を加えてpH=8に調整した。得られた沈殿物を濾過により回収し、水(2mL),DCM(2mL)で洗浄し、乾燥して、(R,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(68mg、収率:64%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.17(brs,1H),7.52(s,1H),7.27(s,2H),4.45-4.41(m,2H),4.24-4.13(m,2H),2.91-2.87(m,1H),2.80(t,J=7.6 Hz,4H),2.70-2.66(m,4H),2.26(s,6H),2.03-1.95(m,4H).MS:m/z 463.1(M+H+).
ピーク2からの材料を同様の方法で脱保護し、単離して、(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを送達した。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.12(brs,1H),7.50(s,1H),7.15(s,2H),4.44-4.42(m,2H),4.25-4.13(m,2H),2.90-2.88(m,1H),2.80(t,J=7.6 Hz,4H),2.73(t,J=7.6 Hz,4H),2.29(s,6H),2.03-1.96(m,4H).MS:m/z 463.1(M+H+).
実施例46及び実施例47
(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-フルオロエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-フルオロエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-フルオロエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-フルオロエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3] オキサジン-3-スルホンイミドアミドは、工程3で(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-6-アミンをtert-ブチル(S)-(6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-6-イル)(2-フルオロエチル)カルバメ-トに置き換えて(R,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例44及び実施例 45)の調製に記載された一般的な手順で調製した。分取HPLCの後、未知の絶対立体化学の2つの異性体が単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.21(brs,1H),7.57(s,1H),7.23(s,2H),4.70-4.21(m,7H),2.83-2.62(m,10H),2.04-1.97(m,5H).MS:m/z 481.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.22(brs,1H),7.61(s,1H),7.32(s,2H),4.72-4.45(m,5H),4.28-4.22(m,1H),3.95-3.92(m,1H),2.83-2.67(m,10H),2.08-1.97(m,5H).MS:m/z 481.1(M+H+).
実施例48及び実施例49
(R,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程4において、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジンに置き換えることにより、(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例38及び実施例39)の調製に記載された一般的な手順を用いて、(R,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを調製した。分取HPLCの後、未知の絶対立体化学の2つの異性体が単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.02(s,1H),7.51(s,1H),7.33(s,2H),6.45(s,1H),4.26-4.20(m,2H),4.13(dd,J=12.8,4.0 Hz,1H),3.96-3.91(m,1H),3.88-3.83(m,1H),3.81(s,3H),3.57-3.51(m,2H),3.20-3.18(m,1H),3.15(s,3H),3.03-2.97(m,4H),1.18-1.06(m,12H).MS:m/z 522.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.00(s,1H),7.47(s,1H),7.26(s,2H),6.45(s,1H),4.30-4.28(m,1H),4.20-4.10(m,2H),3.96-3.91(m,1H),3.88-3.85(m,1H),3.81(s,3H),3.58-3.52(m,2H),3.20-3.18(m,1H),3.15(s,3H),3.03-2.97(m,4H),1.18-1.06(m,12H).MS:m/z 522.2(M+H+)
実施例50及び実施例51
(R,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-tert-ブチル((6S)-3-(N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメ-トの合成:
MeONa(81 mg,1.5 mmol)をTHF(10 mL)中のtert-ブチルメチル((6S)-3-(N’-トリチルスルファミジモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)カルバメ-ト(573 mg,1.0 mmol)の溶液に室温で添加した。30分後、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(234mg,1.0mmol)を加え、混合物をさらに16時間撹拌した。反応物を濃縮し、粗残渣を逆相カラム(5-95%MeCN in H2O)で精製し、tert-ブチル((6S)-3-(N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N’-トリチルスルファミジモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバミン酸塩(500mg、収率62%)を黄色固体として得た。
工程2-tert-ブチル(((S)-3-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1.3]オキサジン-6-イル)(メチル)カルバメ-ト及びtert-ブチル((S)-3-((R)-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメ-ト:
tert-ブチル((6S)-3-(N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N’-トリチルスルファミドイミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメ-ト(500mg,0.6 mmol)をキラル分取HPLCで分離し、白色固体として未知の絶対立体化学の2つの異性体を得た(ピーク1,201mg、収率40%;ピーク2,200mg、収率44%).
工程3-(R,6S)-N’-{(2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル}-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(S.6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例50及び実施例51):
ピーク1の材料(200mg,0.25mmol)のDCM(5 mL)中の溶液にメタンスルホン酸(5滴)を室温で加えた。30分後、飽和水性NaHCO3を添加して反応物をpH=8に調整した。反応混合物を濃縮し、粗残渣を逆相カラム(0-95%MeCN in H2O)で精製し、粗生成物を得た。粗物質をさらに分取HPLC(NH4HCO3)により精製し、(R,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(60mg、収率52%)を白色固体として送達した。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=7.99(s,1H),7.49(s,1H),7.25(s,2H),6.45(s,1H),4.32-4.20(m,3H),3.93(dd,J=12.4,4.4 Hz,1H),3.80(s,3H),3.21-3.16(m,2H),3.05-2.98(m,1H),2.35(s,3H),1.10-1.06(m,12H).MS:m/z 466.1(M+H+).
ピーク2の材料(171 mg,0.24 mmol)のDCM(4 mL)中の溶液にメタンスルホン酸(2滴)を室温で加えた。10分後、飽和水性NaHCO3を添加してpH=8に調整した。沈殿物を濾過により回収し、乾燥して、(S,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(86 mg,収率67%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.02(s,1H),7.51(s,1H),7.27(s,2H),6.45(s,1H),4.37-4.20(m,3H),3.93(dd,J=12.4,4.8 Hz,1H),3.80(s,3H),3.21-3.16(m,2H),3.05-2.97(m,1H),2.35(s,3H),1.10-1.06(m,12H).MS:m/z 466.2(M+H+).
実施例52及び実施例53
(R,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(S.6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成
n-BuLi(2.5 M in hexane,1.5 mL,3.8 mmol)を、THF(18 mL)中の(S)-3-ブロモ-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン(900 mg,3.8 mmol)の溶液に、-78℃で滴下添加した。30分後、THF(5 mL)中のTrtNSO(1.2 g,3.8 mmol)の溶液を滴下添加した。反応物を30分間撹拌した後、0℃の氷浴に入れた。さらに10分間撹拌した後、次亜塩素酸tert-ブチル(453 mg,4.2 mmol)を加えた。反応物を20分間撹拌した後、NH3ガスを5分間バブリングした。得られた溶液を室温まで温め、さらに16時間撹拌した。反応混合物を濃縮して乾燥させ、粗残渣を逆相カラム(0-95%MeCN in H2O)で精製して、(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(800mg、収率:44%)を黄色の固体として得た。MS:m/z 475.5(M+H+).
工程2-(6S)-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成
MeONa(43mg,0.8mmol)を、THF(10 mL)中の(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(250mg,0.5mmol)の溶液に室温で添加した。20分間撹拌した後、ナトリウム塩の懸濁液が形成されていた。
別のフラスコに、2,4-ジイソプロピル-6-メトキシピリジン-3-アミン(208 mg,1.0 mmol)及びトリエチルアミン(152 mg,1.5 mmol)のTHF(10 mL)中の溶液に、トリホスゲン(98 mg,0.3 mmol)を1部ずつ加え、N2の雰囲気下、0℃で反応させた。5分後、反応物を室温まで温め、10分間撹拌した。反応混合物を濾過し、濾液をナトリウム塩懸濁液に加えた。16時間後、反応物を濃縮し、粗残渣を逆相カラム(5-95%MeCN in H2O))で精製し、(6S)-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(244mg、収率:65%)を黄色の固体として得た。MS:m/z 709.7(M+H+).
工程3-(S,6S)-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R.6S)-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
(6S)-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(244 mg,0.3 mmol)をキラル分取HPLCで分離し、黄色固体として未知の絶対立体化学の2つの異性体を得た(ピーク1,140 mg;ピーク2,120 mg).
工程4-(R,6S)-N’-{(2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル}-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(S.6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例52及び実施例53):
メタンスルホン酸(6滴)を、0℃でTHF(2mL)中のピーク1(140mg,0.2mmol)からの材料の溶液に加えた。30分後、飽和NaHCO3水溶液を加えて反応物をpH=8に調整した。反応混合物を濃縮し、粗残渣を逆相カラム(0-95%MeCN in H2O)で精製し、(R,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(63mg、収率68%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.06(s,1H),7.56(s,1H),7.35(s,2H),6.48(s,1H),4.64-4.60(m,1H),4.33-4.22(m,3H),4.07(s,1H),3.84(s,3H),3.39(s,3H),3.24-3.19(m,1H),3.06-3.01(m,1H),1.22-1.09(m,12H).MS:m/z 467.1(M+H+).
ピーク2からの材料を同様に脱保護し、単離して、(S,6S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.06(s,1H),7.53(s,1H),7.32(s,2H),6.48(s,1H),4.66-4.62(m,1H),4.30-4.21(m,3H),4.08-4.05(m,1H),3.84(s,3H),3.40(s,3H),3.27-3.18(m,1H),3.09-3.02(m,1H),1.17-1.09(m,12H).MS:m/z 467.1(M+H+).
実施例54及び実施例55
(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-メトキシエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-メトキシエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-メトキシエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-((2-メトキシエチル)アミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドは、工程1で1-ブロモ-2-フルオロエタンを1-ブロモ-2-メトキシエタンに置き換えて(R,6S)-6-(((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例35及び実施例36)の調製に記載した一般的な手順で調製した。分取HPLCの後、未知の絶対立体化学の2つの異性体が単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.17(brs,1H),7.51(s,1H),7.24(s,2H),6.86(s,1H),4.39(dd,J=11.6,2.8 Hz,1H),4.24(dd,J=12.0,5.2 Hz,2H),3.95(dd,J=12.4,5.2 Hz,1H),3.37(t,J=5.6 Hz,2H),3.31(overlap,1H),3.23(s,3H),2.77(t,J=7.2 Hz,6H),2.70(t,J=7.2 Hz,4H),2.09-2.01(m,1H),2.00-1.89(m,4H).MS:m/z 475.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.16(brs,1H),7.52(s,1H),7.24(s,2H),6.86(s,1H),4.39(dd,J=9.6,2.0 Hz,1H),4.25-4.19(m,2H),3.94(dd,J=12.0,4.8 Hz,1H),3.37(t,J=5.6 Hz,2H),3.31(overlap,1H),3.23(s,3H),2.77(t,J=5.6 Hz,6H),2.70(t,J=7.2 Hz,4H),2.10-2.00(m,1H),1.97-1.89(m,4H).MS:m/z 475.1(M+H+).
実施例56及び実施例57
(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(2-(メチルアミノ)エトキシ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(2-(メチルアミノ)エトキシ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-tert-ブチル(S)-(2-((6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)オキシ)エチル)(メチル)カルバメ-トの合成:
ジオキサン(8 mL)中の(S)-2-((6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)オキシ)-N-メチルエタナミン(900 mg,4.6 mmol)の溶液に、H2O(8 mL)中のNaOH(910 mg,22.8 mmol)とBoc2O(1.1 g,5.0 mmol)の溶液を0℃で加えた。5分後、反応物を室温に温め、さらに3時間撹拌した。反応物をH2O(30 mL)で希釈し、EtOAc(30 mL)で抽出した。有機層をNa2SO4上で乾燥し、濃縮し、粗残渣をシリカゲルカラム(PE/EtOAc=1/2-100%EtOAc)で精製し、tert-ブチル(S)-(2-((6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)オキシ)エチル)(メチル)カルバミン酸塩(1.0 g、収率79%)を無色油として得た。MS:m/z 298.4(M+H+).
工程2-6-(R,6S)-N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-6-(2-(メチルアミノ)エトキシ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(2-(メチルアミノ)エトキシ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例56及び実施例57):
(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(2-(メチルアミノ)エトキシ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(2-(メチルアミノ)エトキシ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドは、工程2で(S)-N,N-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-6-アミンをtert-ブチル(S)-(2-((6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-6-イル)オキシ)エチル)(メチル)カルバメ-トに置き換えて(R,6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S.6S)-6-(ジメチルアミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例33及び実施例34)の調製に記載した一般的な手順で調製した。prep-HPLCの後、絶対立体化学が未知の2つの異性体が分離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.17(brs,1H),7.54(s,1H),6.86(s,1H),4.58-4.54(m,1H),4.32-4.24(m,2H),4.19-4.15(m,2H),3.65-3.59(m,2H),2.78(t,J=7.2 Hz,4H),2.69(t,J=7.2 Hz,4H),2.60-2.58(m,2H),2.25(s,3H),1.97-1.90(m,4H).MS:m/z 475.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.15(brs,1H),7.52(s,1H),6.85(s,1H),4.58-4.54(m,1H),4.29-4.25(m,2H),4.19-4.15(m,2H),3.62-3.59(m,2H),2.78(t,J=7.2 Hz,4H),2.70(t,J=7.2 Hz,4H),2.58(t,J=5.6 Hz,2H),2.24(s,3H),1.97-1.90(m,4H).MS:m/z 475.1(M+H+).
実施例58及び実施例59
(R,6S)-6-アミノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-6-アミノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
(R,6S)-6-アミノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S,6S)-6-アミノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドは、工程1で1-ブロモ-2-フルオロエタンをブロモ(メトキシ)メタンに置き換えて(R,6S)-6-(((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S.6S)-6-((2-フルオロエチル)アミノ)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例35及び実施例36)の調製に記載した一般的な手順で調製した。分取HPLCの後、未知の絶対立体化学の2つの異性体が単離された。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.19(brs,1H),7.52(s,1H),7.25(brs,2H),6.86(s,1H),4.32(dd,J=10.8,2.4 Hz,1H),4.21(dd,J=12.8,4.8 Hz,1H),4.04-4.00(m,1H),3.79-3.74(m,1H),3.45-3.40(m,1H),2.79(t,J=7.2 Hz,4H),2.70(t,J=7.2 Hz,4H),2.32-1.89(m,4H).MS:m/z 417.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.16(brs,1H),7.52(s,1H),7.24(brs,2H),6.86(s,1H),4.30(d,J=5.6 Hz,1H),4.21(dd,J=12.0,4.4 Hz,1H),4.04-4.00(m,1H),3.77(dd,J=12.0,6.0 Hz,1H),3.47-3.40(m,1H),2.77(t,J=6.8 Hz,4H),2.70(t,J=7.2 Hz,4H),2.07-1.91(m,4H).MS:m/z 417.1(M+H+).
実施例60
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド:
工程1-N-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルフィンアミドの合成:
3-ブロモ-4,5,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン(300 mg,1.49 mmol)の無水THF(2 mL)中の溶液にn-BuLi(ヘキサン中2.5 M,0.72 mL,1.79 mmol)を-78℃で滴下添加した。1時間後、THF(2 mL)中のTrtNSO(547 mg,1.79 mmol)の溶液を滴下添加した。反応物を25分間撹拌した後、0℃の氷浴に入れた。20分後、水(20mL)を加えた。混合物をEtOAc(3x20 mL)で抽出した。合わせた有機層を水、食塩水で洗浄し、Na2SO4上で乾燥し、濃縮し、粗残渣をシリカクロマトグラフィー(EtOAc/Hex 0-100%)で精製し、N-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルフィンアミド(130 mg,20.4%)を白色固体として得た。LCMS:m/z 428(M+H+).
工程2-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドの合成:
0℃でTHF(1 mL)中のN-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルフィンアミド(130 mg,0.304 mmol)の溶液に、tert-ブチルヒドロペルオキシド(38 μL,0.395 mmol)を加えた。1時間後、アンモニア(1M in THF,1.3 mL)を加えた。反応物を室温まで温め、さらに3時間撹拌した。水(20 mL)を加え、水層をEtOAc(3x15 mL)で抽出した。合わせた有機層をブラインで洗浄し、Na2SO4上で乾燥し、減圧下で濃縮して、N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド(135 mg,100 %)を白色固体として得、これをさらに精製することなく次の工程で使用した。
工程3-4-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドの合成(実施例60):
N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドアミド(135 mg,0.305 mmol)と4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(60.8 mg,0.305 mmol)のTHF(2 mL)中の溶液にNaH(鉱油中60%,18 mg,0.458 mmol)を0℃で加え、反応を開始した。5分後、反応物を室温に温め、さらに1時間撹拌した。MeOH(5 mL)を加え、溶媒を減圧下で留去し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドを得、これをさらに精製することなく、次の工程で使用した。
粗物質を無水DCM(2 mL)に溶解し、0℃でメタンスルホン酸(58.6 mg,39.6 μL,0.610 mmol)を滴下添加した。30分後、トルエン(10 mL)を加え、減圧下で溶媒を留去した。粗残渣をMeOHに溶解し、分取HPLCにより精製して、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド(16mg、収率:13%-エナンチオマーの混合物として)を白色固体として得た。LCMS:m/z 400(M+H+).
実施例61及び実施例62
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7,8-ジヒドロ-4H,6H-ピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミド、及び(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7,8-ジヒドロ-4H,6H-ピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミド:
工程1-エチル-1-(3-ヒドロキシプロピル)-1H-ピラゾール-5-カルボキシレートの合成:
DMF(35 mL)中の1H-ピラゾール-5-カルボキシレートエチル(5.0 g,35.7 mmol)の溶液に、3-ブロモ-1-プロパノール(9.9 g,71.3 mmol)及びK2CO3(14.8 g,107 mmol)を加えた。混合物を60℃で16時間撹拌した。室温まで冷却した後、反応混合物を濾過し、濃縮した。残渣をシリカゲルクロマトグラフィー(石油エーテル中0-35%EtOAc)で精製して、1-(3-ヒドロキシプロピル)-1H-ピラゾール-5-カルボン酸エチル(4g、収率56%)を無色の油状物として得た。位置異性体は精製中に廃棄された。1H NMR(400 MHz,CDCl3)δ=7.49(d,J=1.6 Hz,1H),6.83(d,J=1.6 Hz,1H),4.71(t,J=6.4 Hz,2H),4.34(q,J=7.2 Hz,2H),3.55-3.49(m,2H),2.11-2.04(m,2H),1.42-1.31(m,1H),1.37(t,J=6.8 Hz,3H).MS:m/z 198.9(M+H+).
工程2- 3-(5-(ヒドロキシメチル)-1H-ピラゾール-1-イル)プロパン-1-オールの合成:
THF(80mL)中のLiAlH4(1.2g,30.3mmol)の溶液に、窒素雰囲気下、0℃で、エチル1-(3-ヒドロキシプロピル)-1H-ピラゾール-5-カルボキシレート(4.0g,20.2mmol)を加えた。1時間後、反応物をNa2SO4・10H2Oで急冷した。反応物を室温に温め、10分間撹拌した後、固形物を濾過により除去した。濾液を濃縮して3-(5-(ヒドロキシメチル)-1H-ピラゾール-1-イル)プロパン-1-オール(3g、収率95%)を無色油として得て、これをさらに精製することなく次の工程で使用した。MS:m/z 156.8(M+H+).
工程3-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピンの合成:
3-(5-(ヒドロキシメチル)-1H-ピラゾール-1-イル)プロパン-1-オール(1.7 g,10.9 mmol)のリン酸(30 mL,54.4 mmol)中の溶液を130℃で20時間撹拌した。室温まで冷却した後、水(40 mL)で反応物を急冷した。得られた混合物を飽和水性NaHCO3でpH=8に調整し、DCM(30mL×2)で抽出した。合わせた有機層をブライン(30mL×2)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮して4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン(400mg粗)を無色油として得て、これをさらに精製することなく次の工程で使用した。MS:m/z 139.0(M+H+).
工程4-3-ブロモ-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピンの合成:
4,6,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン(650 mg,4.7 mmol)のMeCN(10 mL)溶液に、0℃でNBS(921 mg,5.2 mmol)を加えた。室温で16時間撹拌した後、反応物を水(20 mL)で急冷し、DCM(2×20 mL)で抽出した。合わせた有機層をブライン(20mL×2)で洗浄し、無水Na2SO4上で乾燥し、濾過し、濃縮した。粗残渣をシリカゲルカラム(石油エーテル中0-50%EtOAc)で精製し、白色固体として3-ブロモ-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン(900mg、収率88%)を得た。1H NMR(400 MHz,CDCl3)δ=7.33(s,1H),4.66(s,2H),4.46(t,J=5.2 Hz,2H),4.05(t,J=5.2 Hz,2H),2.05-1.96(m,2H).MS:m/z 216.9(M+H+).
工程5-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミドの合成:
3-ブロモ-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン(200 mg,0.9 mmol)のTHF(5 mL)溶液に、n-BuLi(ヘキサン中2.5 M,0.4 mL,1.0 mmol)を窒素雰囲気下、-78℃で滴下添加した。78℃で0.5時間撹拌した後、THF(2 mL)中のTrtNSO(310 mg,1.0 mmol)の溶液を滴下添加した。混合物を-78℃で30分間撹拌した後、氷浴に入れた。反応物を水(5 mL)で急冷した。水層をDCM(2×10mL)で抽出した。合わせた有機層をブライン(20 mL)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮した。粗残渣をPrep-TLC(シリカ、DCM中5%メタノール)で精製し、N-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン-3-スルフィンアミド(180 mg、収率44%)を白色固体として得た。MS:m/z 466.1(M+Na+).
N-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン-3-スルフィンアミド(180 mg,0.4 mmol)のTHF(4 mL)溶液に、次亜塩素酸tert-ブチル(49 mg,0.4 mmol)を窒素雰囲気下、0 ℃で滴下添加した。0℃で30分間撹拌した後、NH3ガスを10分間バブリングし、得られた混合物を室温で16時間撹拌した。混合物を濃縮し、残渣をシリカゲルカラム(石油エーテル中の0-50%EtOAc)で精製して、N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミド(160mg、収率86%)を白色固体として得た。MS:m/z 481.1(M+Na+).
工程6-N-(((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミドの合成:
N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミド(160 mg,0.3 mmol)のTHF(5 mL)溶液に、0℃でMeONa(23 mg,0.4 mmol)を加えた。15分間撹拌した後、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(84mg,0.4mmol)を加えた。反応混合物を室温で16時間撹拌した。反応物をMeOH(1mL)で急冷し、混合物を濃縮した。粗残渣をシリカゲルカラム(DCM中0-5%メタノール)で精製し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミド(160mg、収率70%)を白色固体として得た。1H NMR(400 MHz,CDCl3)δ=10.72(s,1H),7.48-7.39(m,6H),7.24-7.16(m,10H),7.02(s,1H),6.51(s,1H),4.79(d,J=15.2 Hz,1H),4.42-4.18(m,3H),4.06-3.81(m,2H),2.91(d,J=5.6 Hz,8H),2.14-2.07(m,4H),2.00-1.90(m,2H).
工程7-(S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ [5,1-c] [1,4]オキサゼピン-3-スルホンイミドアミド及び(R)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c] [1,4]オキサゼピン-3-スルホンイミドアミド:
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c] [1,4]オキサゼピン-3-スルホンイミドアミド(160 mg,0.2 mmol)はキラルSFC(Chiralpak OD(250 mm * 30 mm,10 um),Supercritical CO2 / MeOH+0.1%NH4OH=55/45;50 mL / min)を用いて精製し、共に(R)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c] [1,4]オキサゼピン-3-スルホンイミドアミド(ピーク1,80 mg、収率50%)と(S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,6,7,8-テトラヒドロピラゾロ[5,1-c] [1,4]オキサゼピン-3-スルホンイミドアミド(ピーク2,65 mg、収率40%)を薄黄色の固体とし得た。各立体異性体には、任意に立体化学を割り当てた。MS:m/z 680.1(M+Na+).
工程8-(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7,8-ジヒドロ-4H,6H-ピラゾロ[5,1-c] [1,4]オキサゼピン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7,8-ジヒドロ-4H,6H-ピラゾロ[5,1-c] [1,4]オキサゼピン-3-スルホンイミドアミドの合成(実施例61及び実施例62):
ピーク1の材料(80 mg,0.1 mmol)のDCM(5 mL)溶液に、室温でMeSO3H(59 mg,0.6 mmol)を加えた。20分後、反応混合物を飽和水性NaHCO3でpH=8に調整し、濃縮した。粗残渣を逆相クロマトグラフィー(MeCN 35-65% /(0.04% NH4OH+0.1% NH4HCO3)を水に溶かして)に(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7,8-ジヒドロ-4H,6H-ピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミド(方法A,1.55分、5.1mg、収率10%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.21(s,1H),7.62(s,1H),7.30(s,2H),6.85(s,1H),4.99(d,J=15.2 Hz,1H),4.81(d,J=15.2 Hz,1H),4.46(t,J=5.2 Hz,2H),4.04-3.89(m,2H),2.76(t,J=7.2 Hz,4H),2.69-2.61(m,4H),1.95-1.85(m,6H).MS:m/z 416.0(M+H+).
前記ピーク2からの材料を同様の方法で脱保護し、単離して、(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7,8-ジヒドロ-4H,6H-ピラゾロ[5,1-c][1,4]オキサゼピン-3-スルホンイミド(方法A,1.69分、14.4mg、収率35%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。1H NMR(400 MHz,DMSO-d6):δ=8.21(s,1H),7.62(s,1H),7.30(s,2H),6.85(s,1H),4.99(d,J=15.2 Hz,1H),4.81(d,J=15.2 Hz,1H),4.46(t,J=5.2 Hz,2H),4.04-3.89(m,2H),2.76(t,J=7.2 Hz,4H),2.69-2.61(m,4H),1.95-1.85(m,6H).MS:m/z 416.1(M+H+).
実施例63
(R,6S)-N-シアノ-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、アンモニア:
工程1-(R,6S)-N-シアノ-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、アンモニアの合成(実施例63):
(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(10 mg,0.02 mmol)をDMF(0.5 mL)に溶解し、トリエチルアミン(DMF中の1M,60 μL)及びシアノゲンブロマイド(CH2Cl2中1M,30 μL)を室温で荷電した。30分後、飽和水性NaHCO3 50 mLを添加した。混合物を逆相HPLC(0.1%水性NH4OH中の5%-50%ACN)で直接精製し、所望の化合物(4.5 mg、収率45%)を得た。1H NMR(400 MHz,DMSO-d6)δ 7.78(s,1H),7.38(s,1H),7.07(t,J=72 Hz,3H),4.40 - 4.20(m,4H),4.10 - 3.90(m,2H),3.16(s,3H),2.78(t,J=7.2 Hz,4H),2.72(t,J=7.2 Hz,4H),2.05 - 1.95(m,4H).MS:m/z 530.2(M+H+).
実施例64、実施例65、実施例66及び実施例67
(S,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[ 5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド、(R,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド、(R,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド及び(S,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ [5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド:
Step 1 - Synthesis of 2-methylbutane-1,4-diol:
THF(200 mL)中のLiAlH4(8.9 g,234.6 mmol)の懸濁液にTHF(200 mL)中の2-メチルコハク酸(10 g,75.7 mmol)の溶液を滴下添加し、反応混合物を70℃で24時間撹拌した。室温まで冷却した後、Na2SO4の飽和水溶液をゆっくりと加えて反応物を急冷した。混合物を濾過し、有機相を濃縮して粗生成物を得て、これをシリカゲルクロマトグラフィー(石油エーテル中の0-100%EtOAc)で精製して、2-メチルブタン-1,4-ジオール(6.5 g、収率82%)を無色油として得た。1H NMR(400 MHz,DMSO-d6)δ=4.43(t,J=5.2 Hz,1H),4.36(t,J=5.2 Hz,1H),3.50-3.38(m,2H),3.29-3.22(m,1H),3.21-3.13(m,1H),1.63-1.47(m,2H),1.22-1.10(m,1H),0.82(d,J=6.8 Hz,3H).
工程2-2-メチルブタン-1,4-ジイルジメタンスルホン酸の合成:
2-メチルブタン-1,4-ジオール(6 g,57.6 mmol)とトリエチルアミン(40 mL,288 mmol)のDCM(120 mL)中の溶液に、0℃でMsCl(11.5 mL,148 mmol)を滴下して加えた。反応物を室温まで温めた。16時間後、反応物をDCM(150 mL)で希釈した。有機層を水(50 mL×2)、食塩水(100 mL)で洗浄し、Na2SO4上で乾燥し、ろ過し、濃縮して2-メチルブタン-1,4-ジイルジメタンスルホン酸塩(14.6 g、収率97%)を無色油として得た。1H NMR(400 MHz,DMSO-d6):δ=4.33-4.20(m,2H),4.14-4.02(m,2H),3.19(s,6H),2.03-1.93(m,1H),1.88-1.75(m,1H),1.62-1.47(m,1H),0.96(d,J=6.8 Hz,3H).
工程3-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン及び6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピンの合成:
DMF(52 mL)中の1H-ピラゾール-5-オール(1.3 g,15.6 mmol)の撹拌溶液にK2CO3(7.5 g,54.1 mmol)を加えた。混合物を窒素雰囲気下で100℃で1時間撹拌した。次いで、2-メチルブタン-1,4-ジイルジメタンスルホン酸塩(4.8g,18.5mmol)を加え、混合物を100℃でさらに12時間撹拌し続けた。合物を濃縮し、残渣をシリカゲルクロマトグラフィー(石油エーテル中30%EtOAc)で精製し、7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(300mg、収率13%)及び6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(190mg、収率8%)を共に無色油として得た。1H NMR(400 MHz,CDCl3):δ=7.24(d,J=2.0 Hz,1H),5.68(d,J=2.0 Hz,1H),4.31-4.22(m,2H),3.91-3.81(m,2H),2.04-1.96(m,2H),1.90-1.79(m,1H),1.04(d,J=6.4 Hz,3H).1H NMR(400 MHz,CDCl3):δ=7.24(d,J=2.0 Hz,1H),5.68(d,J=2.0 Hz,1H),4.37-4.20(m,1H),4.22-4.16(m,1H),4.14-4.03(m,1H),3.49-3.44(m,1H),2.26-2.12(m,1H),2.01-1.93(m,1H),1.57-1.43(m,1H),0.99(d,J=6.8 Hz,3H).
工程4-3-ブロモ-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンの合成:
7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(1.2 g,7.9 mmol)のMeCN(26 mL)溶液にNBS(1.4 g,7.9 mmol)を加えた。混合物を室温で16時間撹拌した。溶媒を留去し、混合物をフラッシュクロマトグラフィー(シリカ、石油エーテル中の0-30%EtOAc)で精製し、白色固体として3-ブロモ-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(1.6 g、収率:88%)を得た。MS:m/z 230.9(M+H
+).
工程5-7-メチル-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
3-ブロモ-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(200 mg,0.87 mmol)のTHF(3 mL)溶液に、n-BuLi(ヘキサン中2.5M,0.4 mL,0.95 mmol)を-78℃で滴下添加した。この温度で30分間撹拌した。THF(1 mL)中のTrtNSO(291 mg,0.95 mmol)の溶液を滴下添加し、混合物を-78℃で30分間撹拌した後、0℃の氷浴に入れた。次いで、次亜塩素酸tert-ブチル(0.11mL,0.95mmol)を加え、0℃で0.5時間撹拌した。NH3ガスを0℃で10分間バブリングし、得られた溶液を室温で16時間撹拌した。混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(溶媒勾配)で精製した。石油エーテル中の0-80%EtOAc)を用いて、白色固体として7-メチル-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(250mg、収率61%)を得た。1H NMR(400 MHz,DMSO-d6):δ=7.48-7.41(m,6H),7.21-7.17(m,6H),7.14-7.08(m,3H),7.04(d,J=12.0 Hz,1H),6.20(d,J=12.8 Hz,2H),4.32-4.18(m,1H),4.11-4.04(m,1H),3.94-3.75(m,2H),2.06-1.99(m,1H),1.91-1.86(m,1H),1.84-1.69(m,1H),0.94(d,J=6.4 Hz,3H).
工程6-N-(((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
7-メチル-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミド(150 mg,0.32 mmol)のTHF(5 mL)中の撹拌溶液に、0℃でMeONa(34 mg,0.63 mmol)を加えた。15分後、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(76 mg,0.38 mmol)を加えた。反応混合物を室温まで温め、16時間撹拌を続けた。反応物をMeOH(1mL)で急冷した。混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(DCM中0-5%MeOH)で精製し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(200mg、収率94%)を白色固体として得た。
工程7- N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5、1-b] [1,3]オキサゼピン-3-スルホンイミドアミド:
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(200 mg,0.30 mmol)のDCM(15 mL)中の溶液に、室温でMeSO3H(10滴)を加えた。0.5時間後、反応混合物を飽和水性NaHCO3でpH=8に調整した。反応物を濃縮して乾燥させ、粗残渣をフラッシュクロマトグラフィー(シリカ、DCM中0-1%MeOH)で精製し、N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(100mg、収率78%)を白色固体として得た。MS:m/z 430.1(M+H+).
工程7-(S,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(R.7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(R,7R)-N’-((1,2,3,5.6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、及び(S,7R)-N’-((1,2,3,5,6.7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(実施例64、実施例65、実施例66及び実施例67):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(160 mg,0.37 mmol)をSFC(Chiralpak ad(250 mm*50 mm,10 um));超臨界 CO2/EtOH(0.1% NH4OH)=40/40,80 mL/min))で分離し、ピーク1(方法B,3.04分、17mg、収率:11%)、ピーク2(方法B,3.45分、16.1mg、収率:10%)を得た;及び、ピーク3とピーク4の50mg混合物をSFC(セルロース-2(250 mm * 30 mm,10 um);超臨界 CO2/EtOH(0.1% NH4OH)=40/40,70 mL/min)で分離し、ピーク3(方法B,4.63分、22.3mg、収率14%)とピーク4(方法B,4.66分、23.8mg、収率15%)を得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)::δ=8.23(s,1H),7.50(s,1H),7.30(s,2H),6.85(s,1H),4.34-4.30(m,1H),4.21-4.17(m,1H),4.01-3.87(m,2H),2.77(t,J=7.2 Hz,4H),2.68-2.64(m,4H),2.08-1.99(m,1H),1.97-1.87(m,5H),1.85-1.75(m,1H),0.94(d,J=6.8 Hz,3H).MS:m/z 430.1(M+H+).化合物64
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.20(s,1H),7.50(s,1H),7.31(s,2H),6.85(s,1H),4.32-4.27(s,1H),4.20-4.17(m,1H),4.05-3.87(m,2H),2.77(t,J=7.2 Hz,4H),2.75-2.66(m,4H),2.05-2.01(m,1H),1.98-1.86(m,5H),1.86-1.73(m,1H),0.94(d,J=6.8 Hz,3H).化合物66
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.20(s,1H),7.49(s,1H),7.25(s,2H),6.85(s,1H),4.32-4.27(s,1H),4.20-4.17(m,1H),3.97-3.87(m,2H),2.77(t,J=7.2 Hz,4H),2.70-2.60(m,4H),2.05-2.01(m,1H),1.98-1.86(m,5H),1.86-1.73(m,1H),0.94(d,J=7.2 Hz,3H).MS:m/z 430.1(M+H+).化合物65
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.16(s,1H),7.48(s,1H),7.19(s,2H),6.84(s,1H),4.31-4.27(m,1H),4.19-4.16(m,1H),4.02-3.88(m,2H),2.76(t,J=7.2 Hz,4H),2.70-2.60(m,4H),2.04-1.99(m,1H),1.98-1.86(m,5H),1.85-1.72(m,1H),0.94(d,J=6.8 Hz,3H).MS:m/z 430.1(M+H+).化合物67
実施例68
R)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、アンモニア:
工程1で(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドに置き換えて(R,6S)-N-シアノ-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例63).の調製に記載された一般的な手順でR)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアンモニアを調製した。1H NMR(400 MHz,DMSO-d6)δ 7.78(s,1H),7.41(s,1H),7.07(t,J=72 Hz,3H),6.82(s,1H),4.43 - 4.25(m,2H),4.08(t,J=6.1 Hz,2H),2.76(t,J=7.4 Hz,4H),2.72 - 2.60(m,4H),2.17(h,J=6.1 Hz,2H),1.92(p,J=7.4 Hz,4H).MS:m/z 427.2(M+H+).
実施例69
(S)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミドアンモニア
(S)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドは、工程1で(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドに置き換えて(R,6S)-N-シアノ-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(3-メトキシアゼチジン-1-イル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例63)の調製に記載した一般的な手順で調製した。1H NMR(400 MHz,DMSO-d6)δ 7.72(s,1H),7.36(s,1H),6.79(s,1H),6.51(s,1H),4.42 - 4.21(m,2H),4.07(t,J=6.1 Hz,2H),2.76(t,J=7.4 Hz,4H),2.70 - 2.60(m,4H),2.20 - 2.10(m,2H),2.00 - 1.79(m,4H).MS:m/z 427.2(M+H+).
実施例70及び実施例71
(S)-N’-((2,4-ジイソプロピル-6-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R)-N’-((2.4-ジイソプロピル-6-(2-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド::
工程1-2-((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)オキシ)-N-メチルタナミンの合成:
THF(20 mL)中のNaH(鉱油中60%,660 mg,16.48 mmol)の混合物に、THF(10 mL)中のtert-ブチル(2-ヒドロキシエチル)(メチル)カルバメ-ト(1.59 g,9.06 mmol)を窒素雰囲気下で室温で滴下して加えた。混合物を70℃で0.5時間撹拌した。室温まで冷却した後、THF(10 mL)中の6-クロロ-2,4-ジイソプロピル-3-ニトロピリジン(2 g,8.24 mmol)を滴下添加した。得られた混合物を70℃で16時間撹拌した。室温まで冷却した後、反応物を水(50mL)でクエンチし、EtOAc(50mL×2)で抽出した。合わせた有機層をブライン(30mL)で洗浄し、無水Na2SO4で乾燥させ、濾過し、そして濃縮した。粗残渣をシリカゲルカラム(DCM中0-10%MeOH)で精製し、2-((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)オキシ)-N-メチルエタナミン(380mg、収率17%)を無色油として得た。MS:m/z 282.1(M+H+).
工程2-tert-ブチル(2-((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)オキシ)エチル)(メチル)カルバメ-トの合成:
2-((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)オキシ)-N-メチルエタナミン(380 mg,1.35 mmol)及びトリエチルアミン(273 mg,2.7 mmol)のDCM(5.4 mL)中の溶液にジ-tert-ブチルカ-ボネート(354 mg,1.62 mmol)を室温で加えた。16時間後、反応物を濃縮した。粗残渣をTLC(シリカ、石油エーテル中20%EtOAc)で精製し、tert-ブチル(2-((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)オキシ)エチル)(メチル)カルバメ-ト(385mg、収率75%)を無色油として得た。1H NMR(400 MHz,CDCl3)δ=6.59(s,1H),4.52(t,J=5.2 Hz,2H),3.05(t,J=5.2 Hz,2H),2.98-2.92(m,1H),2.87-2.80(m,1H),2.56(s,3H),1.30-1.10(m,21H)
工程3-tert-ブチル(2-((5-アミノ-4,6-ジイソプロピルピリジン-2-イル)オキシ)エチル)(メチル)カルバメ-トの合成:
tert-ブチル(2-((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)オキシ)エチル)(メチル)カルバメ-ト(385 mg,1.01 mmol)のEtOH(16 mL)中の溶液に、炭素上の10% Pd(118 mg,1.11 mmol)を加えた。混合物を水素雰囲気下(15psi)で16時間室温で撹拌した。混合物を濾過し、濾液を濃縮して、無色の液体としてtert-ブチル(2-((5-アミノ-4,6-ジイソプロピルピリジン-2-イル)オキシ)エチル)(メチル)カルバメ-ト(335mg、収率:94%)を得た。1H NMR(400 MHz,CDCl3)δ=6.40(s,1H),4.44-4.34(m,2H),3.62-3.56(m,2H),3.32(s,2H),3.06-3.01(m,1H),2.96(s,3H),2.94-2.86(m,1H),1.40(s,9H),1.27-1.22(m,12H)
工程4-tert-ブチル(2-((5-イソシアナト-4,6-ジイソプロピルピリジン-2-イル)オキシ)エチル)(メチル)カルバメ-トの合成:
無水THF(3.7 mL)中のtert-ブチル(2-((5-アミノ-4,6-ジイソプロピルピリジン-2-イル)オキシ)エチル)(メチル)カルバメ-ト(260 mg,0.74 mmol)及びトリエチルアミン(0.15 mL,1.11 mmol)の溶液に、室温でトリホスゲン(110 mg,0.37 mmol)を加えた。混合物を70℃で1時間撹拌した。室温まで冷却した後、混合物を濾過し、濾液を濃縮して、白色固体としてtert-ブチル(2-((5-イソシアナト-4,6-ジイソプロピルピリジン-2-イル)オキシ)エチル)カルバメ-ト(メチル)(279mg、収率99%)を得た。
工程5-tert-ブチル(2-((4,6-ジイソプロピル-5-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)ピリジン-2-イル)オキシ)エチル)(メチル)カルバメートの合成:
THF(13 mL)中のN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(219 mg,0.49 mmol)の溶液に、窒素雰囲気下、0℃でMeONa(40 mg,0.74 mmol)を加えた。20分間撹拌した後、THF(8 mL)中のtert-ブチル(2-((5-イソシアナト-4,6-ジイソプロピルピリジン-2-イル)オキシ)エチル)(メチル)カルバメート(279 mg,0.74 mmol)の溶液を0℃で滴下添加した。反応混合物を室温で16時間撹拌した。混合物を濃縮し、残渣を分取TLC(シリカ、DCM中5%メタノール)で精製して、tert-ブチル(2-((4,6-ジイソプロピル-5-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)ピリジン-2-イル)オキシ)エチル)(メチル)カルバミン酸塩(226mg、収率56%)を白色固体として得た。MS:m/z 844.3(M+Na+)
工程6-N’-((2,4-ジイソプロピル-6-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
DCM(13 mL)中のtert-ブチル(2-((4,6-ジイソプロピル-5-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)ピリジン-2-イル)オキシ)エチル)(メチル)カルバミン酸塩(226 mg,0.27 mmol)の溶液に、室温でMeSO3H(10滴)を加えた。1時間後、反応液を飽和水性NaHCO3でpH=8に調整した。反応物を濾過し、濃縮した。粗残渣をTLC(シリカ、DCM中10%MeOH)で精製し、N’-((2,4-ジイソプロピル-6-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(104mg、収率79%)を白色固体として得た。MS:m/z 480.1(M+H+).
工程7-(S)-N’-((2,4-ジイソプロピル-6-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((2.4-ジイソプロピル-6-(2-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例70及び実施例71):
N’-((2,4-ジイソプロピル-6-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(104 mg,0.22 mmol)をキラルSFC(Chiralpak AD,(250 mm * 30 mm,10 um),Supercritical CO2 / EtOH+0.1% NH4OH=65/35;80 mL/min)で分離し、(S)-N’-((2,4-ジイソプロピル-6-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法S,5.92分、ピーク1,28.8mg、収率27%)と(R)-N’-((2,4-ジイソプロピル-6-(2-(メチルアミノ)エトキシ)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法S,6.51分、ピーク2,27.4mg、収率26%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=7.97(s,1H),7.47(s,1H),6.43(s,1H),4.41-4.32(m,2H),4.26(t,J=5.6 Hz,2H),4.08(m,J=6.0 Hz,2H),3.24-3.11(m,1H),3.07-2.93(m,1H),2.78(t,J=5.6 Hz,2H),2.30(s,3H),2.20-2.12(m,2H),1.12-1.00(m,12H).MS:m/z 480.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=7.98(s,1H),7.48(s,1H),6.43(s,1H),4.42-4.33(m,2H),4.26(t,J=6.0 Hz,2H),4.10(t,J=6.0 Hz,2H),3.25-3.10(m,1H),3.06-2.91(m,1H),2.79(t,J=5.6 Hz,2H),2.31(s,3H),2.21-2.14(m,2H),1.12-1.00(m,12H).MS:m/z 480.2(M+H+).
実施例72及び実施例73
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a] ピリミジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[ 1,5-a]ピリミジン-3-スルホンイミドアミド:
工程-tert-ブチル3-(N’-トリチルスルファミドイル)-6,7-ジヒドロピラゾロ[1,5-a]ピリミジン-4(5H)-カルボキシレートの合成:
THF(32 mL)中のtert-ブチル3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[1,5-a]ピリミジン-4-カルボキシレート(2.0 g,6.62 mmol)の溶液に、窒素雰囲気下、-78℃で滴下してn-BuLi(ヘキサン中0.5M,2.91 mL,7.28 mmol)を添加した。78℃で0.5時間撹拌した後、THF(14 mL)中のTrtNSO(2.22 g,7.28 mmol)の溶液を滴下添加した。この混合物を-78℃で20分間撹拌した後、0℃で10分間撹拌した。次いで、次亜塩素酸tert-ブチル(0.8 mL,7.07 mmol)を0℃で滴下添加し、0℃で0.5時間撹拌した。NH3ガスを0℃で10分間バブリングし、得られた混合物を室温で16時間撹拌した。混合物を濃縮し、DCM/MeOH(20/1,15mL)を加えた。得られた混合物を濾過し、固体を水(20mL)に溶解し、DCM/MeOH(9/1,100mL×3)で抽出した。合わせた有機層を無水Na2SO4上で乾燥し、濾過し、濃縮して、tert-ブチル3-(N’-トリチルスルファミドイル)-6,7-ジヒドロピラゾロ[1,5-a]ピリミジン-4(5H)-カルボキシレート(1.9 g、収率:54%)を白色固体として得た。MS:m/z 566.1(M+Na+).
工程2-tert-ブチル3-(N-(((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロピラゾロ[1,5-a]ピリミジン-4(5H)-カルボキシレートの合成:
THF(5 mL)中のtert-ブチル3-(N’-トリチルスルファミミドイル)-6,7-ジヒドロピラゾロ[1,5-a]ピリミジン-4(5H)-カルボキシレート(120 mg,0.22 mmol)の溶液に、窒素雰囲気下、0℃でCH3ONa(18 mg,0.33 mmol)を加えた。0℃で20分間撹拌した後、THF(2 mL)中の4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(88 mg,0.44 mmol)の溶液を加えた。反応混合物を室温で16時間撹拌した。MeOH(5mL)を加え、混合物を濾過した。濾液を濃縮し、残渣をシリカゲルカラムクロマトグラフィー(0-1.5% メタノール in DCM)を用いて、tert-ブチル 3-(N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロピラゾロ[1,5-a]ピリミジン-4(5H)-カルボキシレート(120 mg、収率73%)を白色固体として得た。MS:m/z 743.4(M+H+).
工程3-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドの合成:
DCM(9 mL)中のtert-ブチル3-(N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロピラゾロ[1,5-a]ピリミジン-4(5H)-カルボキシレート(120 mg,0.16 mmol)の溶液に、MeSO3H(78 mg,0.81 mmol)を添加した。この混合物を室温で1時間撹拌した。反応液を飽和水性NaHCO3でpH=8に調整し、Na2SO4上で乾燥し、濾過し、濃縮した。残渣を分取TLC(シリカ、DCM中10%メタノール)で精製し、N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド(65mg、収率91%)を白色固体として得た。MS:m/z 401.2(M+H+).
工程4-(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドアミド(実施例72及び実施例73)
キラルSFC(Chiralpak AS(250 mm * 30 mm,10 um),Supercritical CO2 / EtOH+0.1% NH4OH=75/25;60 mL/min)を用いてN’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド(65 mg,0.16 mmol)を分離し、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド(方法C,3.65分、ピーク1,29.1mg、収率44%)と(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a] ピリミジン-3-スルホンイミドアミド(方法C,4.47分、ピーク2,31.4 mg、収率47%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.24(s,1H),7.38(s,1H),7.09(s,2H),6.88(s,1H),6.43(s,1H),3.96(t,J=6.0 Hz,2H),3.29-3.10(m,2H),2.79(t,J=7.2 Hz,4H),2.71(t,J=7.2 Hz,4H),2.04-1.86(m,6H).MS:m/z 401.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ 8.23(s,1H),7.37(s,1H),7.09(s,1H),6.88(d,MS:m/z 401.2(M+H+).J=9.2 Hz,1H),6.37(d,J=2.4 Hz,1H),3.96(dd,J=16.7,6.0 Hz,1H),3.25-3.15(m,2H),2.79(dd,J=16.7,7.2 Hz,1H),2.71(s,2H),5.75(dd,J=10.4,7.2 Hz,1H),2.03-1.89(m,6H).MS:m/z 401.2(M+H+).
実施例74、実施例75、実施例78及び実施例79
(S,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[ 5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド、(R,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド、(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド 及び(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ [5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミド:
工程1-4-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
工程4で7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピンを6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピンに置き換えることにより、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(実施例64、実施例65、実施例66及び実施例67)の調製に記載された一般的な手順でN’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミドを調製した。
工程5-(S,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.(R,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.(R,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド及び(S.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.(実施例74、実施例75、実施例78、実施例79)
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(150 mg,0.35 mmol)をSFC(daicel chiralpak AD(250 mm * 30 mm,10 um);超臨界 CO2/MeOH(0.1%NH3H2O)=70 mL/minで50/50)で分離し、ピーク3(方法B,5.32分、21.1mg、収率14%)、ピーク4(方法B,7.55分、22.5mg、収率15%)及びピーク1とピーク2の混合物50mg(SFC(regis(s,s)whelk-o1(250 mm * 30 mm,5 um);超臨界 CO2/IPA(0.1%NH3H2O)=70 mL/minで40/40)で分離してピーク1(方法B,3.32分、20.2mg、収率13%)とピーク2(方法B,3.49分、18.7mg、収率12%)の混合物を得た。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.22(s,1H),7.49(s,1H),7.28(s,2H),6.86(s,1H),4.36-4.19(m,2H),4.14-4.00(m,1H),3.60-3.55(m,1H),2.77(t,J=7.6 Hz,4H),2.70-2.66(m,4H),2.23-2.13(m,1H),1.97-1.90(m,5H),1.43-1.35(m,1H),0.92(d,J=6.8 Hz,3H).m/z 430.1(M+H+).化合物75
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.21(s,1H),7.51(s,1H),7.31(s,2H),6.85(s,1H),4.34-4.17(m,2H),4.13-4.02(m,1H),3.66-3.61(m,1H),2.77(t,J=7.2 Hz,4H),2.68-2.66(m,4H),2.20-2.13(m,1H),1.96-1.89(m,5H),1.44-1.35(m,1H),0.93(d,J=6.8 Hz,3H).m/z 430.1(M+H+).化合物74
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.21(s,1H),7.51(s,1H),7.31(s,2H),6.85(s,1H),4.33-4.20(m,2H),4.11-4.00(m,1H),3.66-3.61(m,1H),2.77(t,J=7.2 Hz,4H),2.70-2.66(m,4H),2.21-2.13(m,1H),1.98-1.89(m,5H),1.44-1.35(m,1H),0.93(d,J=6.8 Hz,3H).MS:m/z 430.1(M+H+).化合物78
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.19(s,1H),7.48(s,1H),7.22(s,2H),6.85(s,1H),4.34-4.20(m,2H),4.13-4.02(m,1H),3.60-3.55(m,1H),2.77(t,J=7.2 Hz,4H),2.70-2.64(m,4H),2.23-2.14(m,1H),1.96-1.89(m,5H),1.45-1.34(m,1H),0.93(d,J=6.8 Hz,3H).m/z 430.1(M+H+).化合物79
実施例76及び実施例77
R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S)-N’-((2.4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-3-ブロモ-6,6-ジメチル-5,7-ジヒドロピラゾロ[5,1-b][1,3]オキサジンの合成:
6,6-ジメチル-5,7-ジヒドロピラゾロ[5,1-b][1,3]オキサジン(1.27 g,8.34 mmol)のMeCN(25 mL)溶液に、0℃でNBS(1.49 g,8.34 mmol)を1部ずつ加えた。混合物を室温で3時間撹拌した後、濃縮した。残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中の0-50%EtOAc)で精製し、3-ブロモ-6,6-ジメチル-5,7-ジヒドロピラゾロ[5,1-b][1,3]オキサジン(1.63 g、収率85%)を淡黄色固体として得た。1H NMR(400 MHz,CDCl3):δ=7.33(s,1H),3.96(s,2H),3.84(s,2H),1.15(s,6H).
工程2-6,6-ジメチル-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
3-ブロモ-6,6-ジメチル-5,7-ジヒドロピラゾロ[5,1-b][1,3]オキサジン(1.0 g,4.33 mmol)のTHF溶液(15 mL)に、n-BuLi(2.5 M in hexane,1.9 mL,4.76 mmol)を窒素雰囲気下、-78℃で滴下添加した。1時間後、THF(15 mL)中のTrtNSO(1.45 g,4.76 mmol)の溶液を滴下添加した。混合物を-78℃で30分間撹拌した後、0℃の氷浴に入れた。次亜塩素酸tert-ブチル(0.54 mL,4.76 mmol)を加えた。30分後、NH3ガスを0℃で10分間バブリングした。得られた混合物を室温まで温め、16時間撹拌した。混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中の0-100%EtOAc)で精製し、白色固体として6,6-ジメチル-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(960mg、収率:47%)を得た。1H NMR(400 MHz,DMSO-d6):δ=7.43(d,J=7.6 Hz,6H),7.20-7.14(m,6H),7.12-7.06(m,3H),6.98(s,1H),6.25(s,2H),3.98-3.87(m,2H),3.74-3.63(m,2H),1.01(s,3H),0.99(s,3H).
工程3-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
THF(8 mL)中の2,4-ジイソプロピル-6-メトキシピリジン-3-アミン(400 mg,1.92 mmol)とトリエチルアミン(0.4 mL,2.88 mmol)の撹拌混合物にトリホスゲン(170 mg,0.57 mmol)を加えた。反応混合物を70℃で1時間撹拌した。室温まで冷却後、反応混合物を濾過し、濾液を濃縮して、3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジン(400mg、収率89%)を黄色油として得た。
6,6-ジメチル-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(400 mg,0.85 mmol)のTHF(16 mL)溶液に、MeONa(69 mg,1.27 mmol)を窒素雰囲気下0℃で加えた。15分後、3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジン(397 mg,1.69 mmol)を加えた。反応混合物を室温で16時間撹拌した。混合物を濃縮し、残渣をPrep-TLC(シリカ、石油エーテル中の50%酢酸エチル)で精製し、N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(430 mg、収率72%)を白色固体として得た。1H NMR(400 MHz,MeOD):δ=7.46-7.37(m,6H),7.25-7.19(m,9H),6.86(s,1H),6.52(s,1H),4.00(s,2H),3.91-3.85(m,3H),3.73-3.62(m,2H),3.42-3.34(m,1H),3.20(m,1H),1.30-1.18(m,1H),1.30-1.18(m,10H),1.12-1.03(m,7H).
工程4-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(380 mg,0.54 mmol)のTHF(30 mL)中の溶液に、0℃でMeSO3H(0.17 mL,2.69 mmol)を加えた。この混合物を室温で1時間撹拌した。反応液を飽和水性NaHCO3でpH=8に調整し、濃縮した。残渣をPrep-TLCで精製し、N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(300 mg crude,purity:80%)を白色固体として得た。MS:m/z 465.1(M+H+).
工程5-(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと、(S)-N’-((2.4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例76及び実施例77):
N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(240 mg,0.52 mmol)はキラルSFC(Chiralpak IC(250 mm * 30 mm,5 um),Supercritical CO2 / EtOH+0.1% NH4OH=30/70;65 mL/min)を用いて分離し、(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法D,4.07分、ピーク1,36.4mg、収率15%)と(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法D,4.46分、ピーク2,39.2mg、収率16%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=7.98(s,1H),7.52(s,1H),7.26(s,2H),6.44(s,1H),4.11-3.98(m,2H),3.85(s,2H),3.80(s,3H),3.21-3.12(m,1H),3.05-2.94(m,1H),1.15-0.96(m,18H)MS:m/z 465.1(M+H+).化合物76
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=7.98(s,1H),7.52(s,1H),7.26(s,2H),6.44(s,1H),4.09-3.98(m,2H),3.84(s,2H),3.79(s,3H),3.20-3.13(m,1H),3.03-2.93(m,1H),1.15-0.94(m,18H)MS:m/z 465.1(M+H+).化合物77
実施例80及び実施例81
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドは、2つの所望の異性体ピーク1(方法U,0.60分)及びピーク2(方法U,1.17分)を白色固体として送達するために、キラル分取HPLC(TBS保護基の脱保護が精製プロセス中に起こる)によってN’-(tert-ブチルジメチルシリル)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドのラセミ混合物を分離することによって調製された。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ 8.13(bs,1H),7.54(s,1H),7.24(bs,2H),6.85(s,1H),4.11 - 4.02(m,2H),3.86(s,2H),2.77(t,J=7.4 Hz,4H),2.68(t,J=7.4 Hz,4H),1.99 - 1.86(m,4H),1.04(s,3H),1.03(s,3H).MS:m/z 430.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ 8.08(bs,1H),7.51(s,1H),7.11(bs,2H),6.84(s,1H),4.08 - 4.02(m,2H),3.85(s,2H),2.77(t,J=7.4 Hz,4H),2.68(t,J=7.4 Hz,4H),1.98 - 1.86(m,4H),1.04(s,3H),1.03(s,3H).MS:m/z 430.2(M+H+).
実施例82及び実施例83
(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R.6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-tert-ブチル((6S)-3-(N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメ-トの合成:
tert-ブチルメチル((6S)-3-(N’-トリチルスルファミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)カルバメ-ト(1.2 g,2.09 mmol)のTHF(30 mL)中の撹拌溶液に、0℃の氷浴中でMeONa(226 mg,4.18 mmol)を添加した。15分後、4-フルオロ-8-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(1.02 g,4.70 mmol)の溶液を加えた。反応混合物を室温で16時間撹拌した。反応をMeOH(5mL)で急冷し、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(ジクロロメタン中、0-9%メタノール)で精製し、tert-ブチル((6S)-3-(N-(8-フルオロ-1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバメ-ト(610 mg、収率53%)を白色固体として得た。1H NMR(400 MHz,DMSO-d6)δ=8.29-8.13(m,1H),7.58-7.57(m,1H),7.29-7.28(m,2H),4.55-4.25(m,5H),2.82-2.79(m,4H),2.76-2.65(m,7H),2.13-1.88(m,4H),1.42(s,9H).MS:m/z 571.1(M+H+).
工程2-(6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
tert-ブチル((6S)-3-(N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-6-イル)(メチル)カルバミン酸塩(150 mg,0.27 mmol)の撹拌溶液に、0℃でMeSO3H(0.06 mL,0.94 mmol)を添加した。27 mmol)をDCM(6.4 mL)に0℃でMeSO3H(0.06 mL,0.94 mmol)を加えた。30分後、反応液が塩基性になるまでNaHCO3(固体)とH2O(0.1ml)を加えた。混合物を濃縮し、粗残渣を分取TLC(シリカ、DCM中10%MeOH,1%NH3・H2O)で精製し、(6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(44mg、収率.白色固体として36%)を得た。
MS:m/z 449.0(M+H+).
工程3-(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R.6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例82及び実施例83):
(6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(110 mg,0.25 mmol)はキラルSFC(Chiralpak AD(250 mm*30 mm,10 um),Supercritical CO2 / EtOH+0.1% NH4OH=40/60;60 mL/min)により分離され、(S,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法E,2.16分、ピーク1,37.8mg、収率32%)と(R,6S)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法E,2.32分、ピーク2,30.9mg、収率:26%)を用いて、(方法E,2.32分、ピーク2,30.9mg、収率26%)は白色固体となった。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ=8.16(s,1H),7.47(s,1H),7.21(s,2H),4.33-4.30(m,1H),4.24-4.16(m,2H),3.91-3.87(m,1H),3.20-3.13(m,1H),2.77(t,J=7.2 Hz,4H),2.69(t,J=7.2 Hz,4H),2.30(s,3H),2.01-1.92(m,4H).MS:m/z 449.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ=8.20(s,1H),7.50(s,1H),7.24(s,2H),4.36-4.20(m,3H),3.96-3.92(m,1H),3.20-3.13(m,1H),2.81(t,J=7.2 Hz,4H),2.74(t,J=6.8 Hz,4H),2.34(s,3H),2.04-1.97(m,4H),MS:m/z 449.1(M+H+).
実施例84及び実施例85
(S)-N’-((2,4-ジイソプロピル-6-(((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((2.4-ジイソプロピル-6-((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-tert-ブチル((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)メチル)(メチル)カルバメ-トの合成:
6-クロロ-2,4-ジイソプロピル-3-ニトロピリジン(500 mg,2.06 mmol),tert-ブチルメチル((4,4,5,5-テトラメチル-1,3,2-ジオキサボラン-2-イル)メチル)カルバメ-ト(726 mg,2.68 mmol),K3PO4(1.3 g,6.18 mmol)を1,4-ジオキサン(5 mL)及び水(0.5 mL)に加え、窒素雰囲気下でCataCXium A Pd G2(138 mg,0.21 mmol)を加えた。混合物を80℃で16時間撹拌した。室温まで冷却後、反応混合物を水(50 mL)で希釈し、EtOAc(50 mL×2)で抽出した。合わせた有機層をブライン(50mL×2)で洗浄し、無水Na2SO4上で乾燥し、濾過し、濃縮した。残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-10%EtOAc)で精製し、黄色固体としてtert-ブチル((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)メチル)カルバメ-ト(440mg、収率61%)を得た。1H NMR(400 MHz,CDCl3)δ=7.08-7.00(m,1H),4.55-4.45(m,2H),3.07-2.94(m,4H),2.91-2.81(m,1H),1.46-1.41(m,9H),1.29-1.23(m,12H).
工程2-tert-ブチル((5-アミノ-4,6-ジイソプロピルピリジン-2-イル)メチル)(メチル)カルバメ-トの合成:
EtOH(10 mL)中のtert-ブチル((4,6-ジイソプロピル-5-ニトロピリジン-2-イル)メチル)(メチル)カルバメ-ト(440 mg,1.25 mmol)の溶液に、炭素上の10%パラジウム(133 mg,0.13 mmol)を加えた。混合物を水素雰囲気下(15psi)で室温で撹拌した。2時間後、混合物を濾過し、濾液を濃縮してtert-ブチル((5-アミノ-4,6-ジイソプロピルピリジン-2-イル)メチル)カルバメ-ト(300mg、収率75%)を黄色油として得た。1H NMR(400 MHz,CDCl3)δ=6.88-6.80(m,1H),4.45-4.34(m,2H),3.60(s,2H),3.07-3.02(m,1H),2.96-2.83(m,4H),1.57-1.46(m,9H),1.29-1.20(m,12H).
工程3-tert-ブチル((5-イソシアナト-4,6-ジイソプロピルピリジン-2-イル)メチル)(メチル)カルバメ-トの合成:
tert-ブチル((5-アミノ-4,6-ジイソプロピルピリジン-2-イル)メチル)(メチル)カルバメ-ト(300 mg,0.93 mmol)及びトリエチルアミン(0.26 mL,1.87 mmol)のTHF(6 mL)中の溶液に、0℃でトリホスゲン(70 mg,0.24 mmol)を添加した。反応混合物を50℃で1時間撹拌した。室温まで冷却した後、混合物を濾過し、濾液を濃縮して、tert-ブチル((5-イソシアナト-4,6-ジイソプロピルピリジン-2-イル)メチル)カルバメ-ト(300mg、収率93%)を黄色油として得た。
工程4-tert-ブチル((4,6-ジイソプロピル-5-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)ピリジン-2-イル)メチル)カルバメ-トの合成:
N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(300 mg,0.67 mmol)のTHF(12 mL)中の撹拌溶液に、MeONa(73 mg,1.35 mmol)を窒素雰囲気下0℃で加えた。15分後、tert-ブチル((5-イソシアナト-4,6-ジイソプロピルピリジン-2-イル)メチル)(メチル)カルバメ-ト(281mg,0.81mmol)を得た。反応混合物を室温で16時間撹拌した。反応物をMeOH(1mL)で急冷し、得られた混合物を濃縮した。残渣をシリカゲルカラムクロマトグラフィー(DCM中0-5%メタノール)で精製し、tert-ブチル((4,6-ジイソプロピル-5-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)ピリジン-2-イル)メチル)カルバミン酸メチル(260mg、収率49%)を淡黄色固体として得た。MS:m/z 792.3(M+H+).
工程5-N’-((2,4-ジイソプロピル-6-((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
tert-ブチル((4,6-ジイソプロピル-5-(3-(N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)ウレイド)ピリジン-2-イル)メチル)カルバミン酸メチル(200mg,0.25mmol)のDCM(12mL)中の溶液に、室温でMeSO3H(121mg,1.26mmol)を加えた。2時間後、反応物を飽和水性NaHCO3でpH=8に調整し、濃縮した。粗残渣を分取TLC(シリカ、10%メタノールinDCM)で精製し、N’-((2,4-ジイソプロピル-6-((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(90mg、収率:79%)を淡黄色固体として得た。MS:m/z 450.2(M+H+).
工程6-(S)-N’-((2,4-ジイソプロピル-6-(((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと、(R)-N’-((2.4-ジイソプロピル-6-((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例84及び実施例85):
N’-((2,4-ジイソプロピル-6-((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(105 mg,0.23 mmol)はキラルSFC(Chiralpak IC(250 mm * 30 mm,10 um),Supercritical CO2 / EtOH+0.1% NH4OH=50/50;70 mL/min)を用いて精製し、(S)-N’-((2,4-ジイソプロピル-6-((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法F,5.43分、ピーク1,19mg、収率17%)と(R)-N’-((2,4-ジイソプロピル-6-((メチルアミノ)メチル)ピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法F,7.26分、ピーク2,17.3mg、収率15%)を薄黄色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.10(s,1H),7.46(s,1H),7.06(s,1H),4.37-4.25(m,2H),4.10-4.01(m,2H),3.63(s,2H),3.22-3.15(m,1H),3.08-2.99(m,1H),2.29(s,3H),2.20-2.10(m,2H),1.10-1.00(m,12H).MS:m/z 450.3(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.11(s,1H),7.49(s,1H),7.09(s,1H),4.46-4.30(m,2H),4.10(t,J=6.0 Hz,2H),3.63(s,2H),3.25-3.15(m,1H),3.13-3.01(m,1H),2.30(s,3H),2.20-2.10(m,2H),1.12-1.00(m,12H).MS:m/z 450.3(M+H+).
実施例88、実施例89、実施例90及び実施例91
(S,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.R,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.S,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、及び(R.7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド:
工程1-2-(ベンジルオキシ)コハク酸ジエチルの合成:
EtOAc(460 mL)中のリンゴ酸ジエチル(35 g,184 mmol)とAg2O(85.3 g,368.1 mmol)の混合物に、BnBr(31.5 g,184.0 mmol)を0℃で滴下添加した。暗い環境下で室温で12時間撹拌しながら反応を行った。反応混合物をセライトの短いパッド上で濾過した。濾液を濃縮し、無色油として2-(ベンジルオキシ)コハク酸ジエチル(50g、収率97%)を得た。1H NMR(400 MHz,CDCl3)δ=7.39-7.28(m,5H),4.83-4.49(m,2H),4.41-4.38(m,1H),4.29-4.09(m,4H),2.88-2.71(m,2H),1.33-1.22(m,6H).
工程2-2-ベンジルオキシブタン-1,4-ジオールの合成:
THF(381 mL)中のLiAlH4(10.2 g,267.6 mmol)の混合物に、THF(96 mL)中のジエチル2-(ベンジルオキシ)コハク酸(30 g,107.0 mmol)の溶液を、窒素雰囲気下、0℃で加えた。反応混合物を室温まで温め、12時間撹拌した。混合物を0℃まで冷却し、水(12 mL),15%水性NaOH(12 mL)、最後に追加の水(36 mL)で連続的に急冷した。混合物を濾過し、濃縮して2-ベンジルオキシブタン-1,4-ジオール(15g、収率71%)を無色油として得た。1H NMR(400 MHz,CDCl3)δ=7.40-7.28(m,5H),4.61(d,J=2.0 Hz,2H),3.81-3.68(m,4H),3.65-3.58(m,1H),2.63(s,2H),1.94-1.77(m,2H)
工程3-2-(ベンジルオキシ)ブタン-1,4-ジイルジメタンスルホン酸の合成:
2-ベンジルオキシブタン-1,4-ジオール(10 g,50.9 mmol)とトリエチルアミン(24.mL,173.1 mmol)のDCM(108 mL)中の溶液に、0℃でMsCl(9.6 mL,124.0 mmol)を滴下して加えた。反応混合物を室温で1時間撹拌した。反応物を水(80 mL)で急冷した。水層をDCM(50mL×2)で抽出した。合わせた有機層を無水Na2SO4上で乾燥し、濾過し、濃縮して2-(ベンジルオキシ)ブタン-1,4-ジイルジメタンスルホン酸塩(17.5g、収率97%)を褐色油として得た。1H NMR(400 MHz,CDCl3)δ=7.41-7.29(m,5H),4.75-4.54(m,2H),4.44-4.31(m,3H),4.24-4.20(m,1H),3.92-3.85(m,1H),3.02(s,3H),2.96(s,3H),2.10-1.97(m,2H).
工程4-7-ベンジルオキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン及び6-ベンジルオキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンの合成:
DMF(200 mL)中の1H-ピラゾール-5-オール(55 g,65.4 mmol)の撹拌溶液にK2CO3(31.6 g,229 mmol)を加え、130℃で30分間撹拌した。次いで、DMF(50 mL)中の2-(ベンジルオキシ)ブタン-1,4-ジイルジメタンスルホン酸(27.7 g,78.5 mmol)の溶液を加え、混合物を130℃でさらに16時間撹拌した。室温まで冷却した後、混合物を濾過し、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中10%EtOAc)で精製し、7-ベンジルオキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(5,7g、収率36%)と6-ベンジルオキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(720mg、収率5%)を無色油として得た。
7-ベンジルオキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン:1H NMR(400 MHz,CDCl3)δ=7.37-7.29(m,6H),5.71(d,J=2.0 Hz,1H),4.72(d,J=12 Hz,1H),4.55-4.52(m,2H),4.29-4.19(m,2H),4.13-4.05(m,1H),3.82-3.78(m,1H),2.23-2.18(m,2H).
6-ベンジルオキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン:1H NMR(400 MHz,CDCl3)δ=7.41-7.29(m,5H),7.24(d,J=2.0 Hz,1H),5.71(d,J=2.0 Hz,1H),4.68(s,2H),4.53-4.44(m,1H),4.16-4.07(m,2H),4.07-4.02(m,1H),3.86-3.80(m,1H),2.11-2.04(m,2H).
工程5- 5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-7-オールの合成:
EtOH(30mL)中の7-ベンジルオキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン(3g,12.3mmol)の撹拌溶液に、10%湿ったパラジウムを加えた。(1.5 g,1.4 mmol)炭素上で、混合物をH2雰囲気(45 psi)下で50℃で撹拌した。12時間後、反応物を室温に冷却し、セライトの短いパッドで濾過した。濾液を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中50%EtOAc)で精製し、白色固体として5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-オール(1.4 g、収率75%)を得た。MS:m/z 154.8(M+H+).
工程6-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンの合成:
5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-オール(1.5 g,9.7 mmol)のMeCN(30 mL)溶液に、MeI(1.8 mL,28.9 mmol)及びAg2O(4.5 g,19.5 mmol)を室温で加えた。16時間後、反応混合物をセライトの短いパッドの上で濾過した。セライトパッドをEtOH(2mL×3)で洗浄した。濾液を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中40%EtOAc)で精製し、7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(1.25 g、収率76%)を黄色油として得た。1H NMR(400 MHz,CDCl3)δ=7.30-7.26(m,1H),5.69(d,J=2.0 Hz,1H),4.50-4.45(m,1H),4.25-4.07(m,3H),3.64-3.58(m,1H),3.41(s,3H),2.22-2.16(m,2H).
工程7-3-ブロモ-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンの合成:
7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(1.13 g,6.7 mmol)のMeCN(24 mL)溶液にNBS(1.2 g,6.7 mmol)を加えた。得られた溶液を室温で12時間撹拌した。反応混合物を濃縮し、粗残渣をフラッシュカラムクロマトグラフィー(シリカ、石油エーテル中30%EtOAc)で精製し、黄色固体として3-ブロモ-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(1.38 g、収率83%)を得た。1H NMR(400 MHz,CDCl3)δ=7.28(s,1H),4.53-4.48(m,1H),4.24-4.17(m,3H),3.65-3.61(m,1H),3.39(s,3H),2.24-2.20(m,2H).
工程8-7-メトキシ-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
3-ブロモ-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(600 mg,2.4 mmol)のTHF(20 mL)溶液に、n-BuLi(2.5 M in hexane,1.2 mL,3.0 mmol)を-78℃で滴下した。1 時間後、TrtNSO(890 mg,2.9 mmol)の THF(2 mL)溶液を滴下した。反応物は-78℃で20分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。20分後、NH3ガスを混合物に10分間バブリングした。反応物を室温まで温め、さらに16時間撹拌した。反応混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中50%EtOAc)で精製し、7-メトキシ-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(200mg、収率33%)を白色固体として得た。MS:m/z 511.1(M+H+).
工程9-N-(((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
7-メトキシ-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミド(657 mg,1.3 mmol)のTHF(10 mL)中の撹拌溶液に、窒素雰囲気下、0℃でMeONa(109 mg,2.0 mmol)を加えた。20分後、THF(2 mL)中の4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(536 mg,2.7 mmol)の溶液を加えた。反応混合物を室温で16時間撹拌した。反応混合物を濾過し、濾液を濃縮した。粗残渣をカラムクロマトグラフィー(シリカ、石油エーテル中50%EtOAc)で精製し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(605mg、収率65%)を白色固体として得た。MS:m/z 710.1(M+H+).
工程10-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-N’-トリチル-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(605 mg,0.9 mmol)のDCM(46 mL)中の撹拌溶液に、室温でMeSO3H(0.06 mL,0.9 mmol)を加えた。1時間後、水(1mL)を加え、NaHCO3(固体)でpH=8になるように反応物を塩基化した。混合物を濾過し、MeOH(20mL)で洗浄した。濾液を濃縮し、粗残渣を分取TLC(シリカ、DCM中5%MeOH)で精製し、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(191mg、収率:49%)を白色固体として得た。MS:m/z 446.0(M+H+).
工程11-(S,7S)-N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド,(R.7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド,(S,7R)-N’-((1,2,3.5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド及び(R,7R)-N’-((1,2,3,5,6.7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(実施例88、実施例89、実施例90、実施例91):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(212 mg,0.48 mmol)をSFC(Chiralpak AD(250 mm * 30 mm,10 um,Supercritical CO2 / MeOH+0.1% NH4OH=60/40;80 mL/min)で分離し、ピーク3(方法G,4.71分、331.5 mg、収率15%)、ピーク4(方法G,7.64分、34.8 mg、収率16%)を得た;及び、ピーク1とピーク2の84mg混合物をSFC(セルロース-2(250 mm * 30 mm,10 um,Supercritical CO2 / MeOH+0.1% NH4OH=45/55;80 mL/min)で分離し、ピーク1(方法H,3.68分、35mg、収率17%)とピーク2(方法H,4.78分、30.4mg、収率14%)を得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ=8.19(s,1H),7.52(s,1H),7.33(s,2H),6.86(s,1H),4.52-4.48(m,1H),4.28-4.20(m,2H),4.12-4.05(m,1H),3.70-3.67(m,1H),3.26(s,3H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.20-2.12(m,2H),1.96-1.89(m,4H).MS:m/z 446.1(M+H+).化合物90
ピーク2:1H NMR(400 MHz,DMSO-d6)δ=8.23(s,1H),7.50(s,1H),7.31(s,2H),6.86(s,1H),4.52-4.48(m,1H),4.28-4.21(m,2H),4.07-4.02(m,1H),3.69-3.66(m,1H),3.26(s,3H),2.78(t,J=7.2 Hz,4H),2.69-2.62(m,4H),2.19-2.13(m,2H),1.97-1.89(m,4H).MS:m/z 446.1(M+H+).化合物91
ピーク3:1H NMR(400 MHz,DMSO-d6)δ=8.22(s,1H),7.50(s,1H),7.30(s,2H),6.86(s,1H),4.52-4.47(m,1H),4.28-4.20(m,2H),4.07-4.02(m,1H),3.70-3.66(m,1H),3.26(s,3H),2.77(t,J=7.2 Hz,4H),2.70-2.60(m,4H),2.20-2.11(m,2H),1.96-1.89(m,4H),MS:m/z 446.1(M+H+).化合物88
ピーク4:1H NMR(400 MHz,DMSO-d6)δ=8.18(s,1H),7.52(s,1H),7.32(s,2H),6.86(s,1H),4.53-4.48(m,1H),4.27-4.20(m,2H),4.11-4.06(m,1H),3.70-3.66(m,1H),3.26(s,3H),2.77(t,J=7.2 Hz,4H),2.67-2.61(m,4H),2.20-2.12(m,2H),1.96-1.91(m,4H),MS:m/z 446.1(M+H+).化合物89
実施例86、実施例87、実施例92及び実施例93
(S,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.(R,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.(S,6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド及び(R.6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド:
工程1-6-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミドは、工程5において、7-(ベンジルオキシ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンを6-(ベンジルオキシ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンに置き換えることにより、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(実施例86、実施例87、実施例92及び実施例93)の調製のために記載された一般的な手順を用いて調製した。
工程7-(S,6R)-N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(R.6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(S,6S)-N’-((1,2,3,5.6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド及び(R,6S)-N’-((1,2,3,5,6.7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(実施例86、実施例87、実施例92及び実施例93):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(103 mg,0.23 mmol)をキラルSFC(Chiralpak AD(250 mm * 30 mm,10 um),Supercritical CO2 / EtOH+0.1% NH4OH=50/50;70 mL/min)を用いて分離し、ピーク1(方法I,2.95分、14.9mg、収率:14%)、ピーク2(方法I,3.69分、14mg、収率:13%)、ピーク3(方法I,4.59分、15.9mg、収率:14%)及びピーク4(方法I,8.46分、18mg、収率:17%)をすべて白色固体とし得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ=8.22(s,1H),7.50(s,1H),7.29(s,2H),6.85(s,1H),4.27-4.22(m,2H),4.12-4.04(m,2H),3.73-3.67(m,1H),3.32(s,3H),2.76(t,J=6.8 Hz,4H),2.71-2.66(m,4H),1.96-1.90(m,6H).MS:m/z 446.1(M+H+).化合物86
ピーク2:1H NMR(400 MHz,DMSO-d6)δ=8.14(s,1H),7.47(s,1H),7.27(s,2H),6.82(s,1H),4.23-4.18(m,2H),4.07-4.04(m,2H),3.67-3.66(m,1H),3.32(s,3H),2.73(t,J=7.2 Hz,4H),2.62-2.52(m,4H),1.92-1.84(m,6H).MS:m/z 446.1(M+H+).化合物87
ピーク3:1H NMR(400 MHz,DMSO-d6)δ=8.13(s,1H),7.46(s,1H),7.22(s,2H),6.81(s,1H),4.24-4.18(m,2H),4.15-4.05(m,2H),3.69-3.66(m,1H),3.32(s,3H),2.73(t,J=7.2 Hz,4H),2.60(t,J=7.2 Hz,4H),1.92-1.80(m,6H).MS:m/z 446.1(M+H+).化合物92
ピーク4:1H NMR(400 MHz,DMSO-d6)δ=8.19(s,1H),7.50(s,1H),7.25(s,1H),6.85(s,1H),4.27-4.21(m,2H),4.13-4.02(m,4H),3.72-3.68(m,1H),3.35(s,3H),2.76(t,J=7.2 Hz,4H),2.69-2.60(m,4H),1.96-1.88(m,6H).MS:m/z 446.1(M+H+).化合物93
実施例94
N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1(エナンチオマーの混合物)で(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを(N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドに置き換えることにより、(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例104)の調製に記載された一般的な手順を用いてN-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを調製した。1H NMR(400 MHz,DMSO-d6)δ 7.71(s,1H),7.38(s,1H),6.79(s,1H),4.05 - 3.94(m,2H),3.82(s,2H),2.79-2.61(m,8H),1.90(p,J=7.3 Hz,4H),1.03(s,3H),1.02(s,3H).MS:m/z 455.2(M+H+).
実施例95
(S)-N-(N-(((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミド:
工程1-(S)-N-(N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミドの合成(実施例95):
塩化アセチル(2.1 mg,1.9 μL,26 μmol)をピリジン(1.0 mL)中の(R)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(10 mg,24 μmol)の溶液に滴下添加し、0℃で行った。1時間後、トルエン(10 mL)を加え、混合物を減圧下で濃縮した。粗残渣をMeOH(1mL)に溶解し、分取HPLCにより精製して、(S)-N-(N-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミドを得た(2.0 mg、収率18%-未知の立体異性体として)を白色固体として得た。MS:m/z 462(M+H+).
実施例96及び実施例97
(R)-N’-((1-(2,2-ジフルオロエチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S)-N’-((1-(2.2-ジフルオロエチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程3において、ヨ-ドエタンを1,1-ジフルオロ-2-ヨ-ドエタンに置き換えることにより、(S)-N’-((1-エチル-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((1-エチル-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例98及び実施例99)の調製のために記載された一般的な手順を用いて、(R)-N’-((1-(2,2-ジフルオロエチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及びS)-N’-((1-(2,2-ジフルオロエチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを調製した。分取HPLC及びキラル分取SFC(工程6)の後、絶対立体化学未知の2つの異性体を、ピーク1(方法T,0.49分)及びピーク2(方法T,0.78分)を単離した。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ 7.61(s,1H),7.48(s,1H),7.21(s,2H),6.52 - 5.98(m,1H),4.56 - 4.21(m,4H),4.09(t,J=6.1 Hz,2H),2.96(q,J=7.0 Hz,1H),2.79 - 2.65(m,1H),2.17(q,J=4.8 Hz,2H),1.27 - 0.96(m,12H).MS:m/z 460.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ 7.61(s,1H),7.48(s,1H),7.24(d,J=19.3 Hz,2H),6.46 - 6.03(m,1H),4.56 - 4.21(m,4H),4.09(t,J=6.1 Hz,2H),2.97(p,J=7.0 Hz,1H),2.73(p,J=6.9 Hz,1H),2.25 - 2.07(m,2H),1.32 - 0.88(m,12H).MS:m/z 460.2(M+H+).
実施例98及び実施例99
(S)-N’-((1-エチル-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R)-N’-((1-エチル-3.5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1:3,5-ジイソプロピル-1H-ピラゾールの合成:
ヒドラジン(330 mg,10 mmol)をエタノール(40 mL)中の2,6-ジメチルヘプタン-3,5-ジオン(1.6 g,10 mmol)の溶液に室温で加えた。2時間後、反応物をブクオで濃縮し、3,5-ジイソプロピル-1H-ピラゾール(1.5 g,10 mmol、収率100%)を得、これをさらに精製することなく次の工程で使用した。MS:m/z 153.1(M+H+).
工程2:3,5-ジイソプロピル-4-ニトロ-1H-ピラゾールの合成:
3,5-ジイソプロピル-1H-ピラゾール(1.5 g,10.0 mmol)を濃硝酸(3.2 mL)及び濃硫酸(2.4 mL)に溶解し、溶液を100℃で加熱した。10時間後、反応物を酢酸エチルで希釈した。有機層を水(2x)で洗浄し、ブライン、硫酸マグネシウム上で乾燥し、濾過し、そして空中で濃縮して、3,5-ジイソプロピル-4-ニトロ-1H-ピラゾール(1.6 g,8.4 mmol、収率:84%)を得、これをさらに精製することなく、次の工程で使用した。MS:m/z 198.1(M+H+).
工程3:1-エチル-3,5-ジイソプロピル-4-ニトロ-1H-ピラゾールの合成:
DMF(30 mL)中の3,5-ジイソプロピル-4-ニトロ-1H-ピラゾール(1.2 g,6.2 mmol)とK2CO3(940 mg,6.8 mmol)の混合物にヨードエタン(1.1 g,6.8 mmol)を加え、50℃で加熱して反応させた。4時間後、反応物を酢酸エチルで希釈した。有機物を水(3×)で洗浄し、無水硫酸マグネシウム上で乾燥し、濾過し、濃縮して空孔で1-エチル-3,5-ジイソプロピル-4-ニトロ-1H-ピラゾール(1.5 g,6.0 mmol、収率96%)を得、これをさらに精製することなく次の工程で使用した。MS:m/z 226.1(M+H+).
工程4:1-エチル-3,5-ジイソプロピル-1H-ピラゾール-4-アミンの合成:
酢酸(80 mL)中の1-エチル-3,5-ジイソプロピル-4-ニトロ-1H-ピラゾール(1.5 g,6.0 mmol)と亜鉛(1.2 g,18.0 mmol)の混合物に、濃縮塩酸(1.5 mL)を室温で加えた。15分後、反応物を酢酸エチルで希釈した。有機物を飽和水性炭酸水素ナトリウム水溶液で洗浄し、真空中で濃縮した。粗残渣をフラッシュカラムクロマトグラフィー(シリカ、DCM中1-10%MeOH)で精製し、1-エチル-3,5-ジイソプロピル-1H-ピラゾール-4-アミン(1.1 g,5.0 mmol、収率:83%)を得た。MS:m/z 1961.2(M+H+).
工程5:1-エチル-4-イソシアナト-3,5-ジイソプロピル-1H-ピラゾールの合成:
THF(8 mL)中の1-エチル-3,5-ジイソプロピル-1H-ピラゾール-4-アミン(361 mg,1.7 mmol)及びトリエチルアミン(201 mg,2.0 mmol)の溶液にトリホスゲン(177 mg,0.6 mmol)を加え、混合物を80℃で加熱した。1時間後、反応物を濾過し、そして空中で濃縮し、1-エチル-4-イソシアナト-3,5-ジイソプロピル-1H-ピラゾール(375 mg,1.7 mmol,100%収率)を得、それ以上の精製を行わずに次の工程で直ちに使用した。MS:m/z 222.1(M+H+).
工程6:(S)-N’-((1-エチル-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R)-N’-((1-エチル-3.5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例98及び実施例99):
室温で、NaH(鉱油中60%,46 mg,1.8 mmol)を、N’-(tert-ブチルジメチルシリル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(397 mg,0.9 mmol)及び1-エチル-4-イソシアナト-3,5-ジイソプロピル-1H-ピラゾール(200 mg,0.9 mmol)のTHF(3 mL)中の溶液に加えた。10分後、反応物を0℃まで冷却した。水(0.5 mL)を加え、反応物をブクオで濃縮した。粗残渣にHCl(ジオキサン中4M,2mL)を加え、室温で30分間撹拌した。混合物を真空中で濃縮した。粗残渣をジオキサン(2x)で共蒸発させ、逆相HPLC(0.1%NH4OH:ACN)及びキラルSFC(キラルセルOX(150 x 21 mm,5 um)、メタノール/w/0.1%NH4OH)で精製し、ピーク1((方法V,0.45分、20 mg、収率:5.2%)及びピーク2((方法V,0.67分、20 mg、収率5.2%)を得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ 7.53(s,1H),7.48(s,1H),7.21(s,2H),4.44 - 4.29(m,2H),4.09(t,J=6.1 Hz,2H),3.93(q,J=7.1 Hz,2H),2.93(p,J=7.0 Hz,2H),2.73(h,J=7.1 Hz,2H),2.17(q,J=4.6 Hz,2H),1.24(t,J=7.1 Hz,3H),1.17(d,J=7.0 Hz,6H),1.09(dd,J=6.9,2.1 Hz,6H).MS:m/z 424.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ 7.53(s,1H),7.47(s,1H),7.21(s,2H),4.44 - 4.29(m,2H),4.09(t,J=6.1 Hz,2H),3.93(q,J=7.1 Hz,2H),2.92(h,J=7.1 Hz,1H),2.73(h,J=7.1 Hz,1H),2.17(q,J=4.6 Hz,2H),1.24(t,J=7.1 Hz,3H),1.17(d,J=7.1 Hz,5H),1.08(dd,J=7.0,2.1 Hz,6H).MS:m/z 424.2(M+H+).
実施例100及び実施例101
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドと(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミド:
工程1-3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジンの合成;
MeCN(6 mL)中の6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン(190 mg,1.36 mmol)の溶液に、0℃でNBS(241 mg,1.36 mmol)を加えた。反応物は室温で16時間撹拌した。混合物を濃縮して乾燥させ、粗残渣をシリカゲルカラムクロマトグラフィー(PE中0-9%EtOAc)で精製し、白色固体として3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン(260 mg、収率87%)を得た。1H NMR(400 MHz,CDCl3):δ=7.45(s,1H),4.23(t,J=6.0 Hz,2H),3.12(t,J=5.6 Hz,2H),2.45-2.35(m,2H).MS:m/z 219.0(M+H+).
工程2-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドの合成:
3-ブロモ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン(260 mg,1.19 mmol)のTHF(5 mL)溶液に、n-BuLi(ヘキサン中2.5 M,0.5 mL,1.31 mmol)を-78℃でN2雰囲気下で滴下で添加した。30分後、THF(1 mL)中のTrtNSO(400 mg,1.31 mmol)の溶液を滴下添加した。反応物は-78℃で30分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。次亜塩素酸tert-ブチル(0.15 mL,1.31 mmol)を0℃で滴下添加した。30分後、NH3ガスを混合物に10分間バブリングした。反応物を室温まで温め、さらに16時間撹拌した。反応物を濃縮して乾燥させ、粗残渣をシリカゲルカラムクロマトグラフィー(PE中、0-80%EtOAc)で精製し、N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミド(300mg、収率54%)を白色固体として得た。1H NMR(400MHz,DMSO-d6)δ 7.47-7.40(m,7H),7.20-7.11(m,6H),7.10-7.05(m,3H),6.32(s,2H),4.11-3.95(m,2H),2.99(t,J=5.6 Hz,2H),2.24-2.11(m,2H).
工程3-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドの合成:
N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド(200 mg,0.43 mmol)のTHF(6 mL)中の撹拌溶液に、0℃でMeONa(26 mg,0.48 mmol)を加えた。15分後、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(104mg,0.52mmol)を加えた。反応混合物を室温で16時間撹拌した。反応物をMeOH(1mL)で急冷し、濃縮して乾燥させ、粗残渣をシリカゲルカラムクロマトグラフィー(DCM中の0-5%MeOH)で精製し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドを白色固体として得た(220mg,収率77%)を白色固体として得た。
工程4-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドの合成:
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド(220 mg,0.33 mmol)のDCM(12 mL)溶液に、0℃でMeSO3H(6滴)を加えた。反応物を室温まで温めた。1時間後、反応物を飽和水性NaHCO3で塩基性化し、濃縮して乾燥させ、粗残渣をシリカゲルカラムクロマトグラフィー(0-1% MeOH in DCM)で精製し、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミド(80 mg,収率40%)を白色固体として得た。MS:m/z 418.2(M+H+).
工程5-(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミド、及び(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドの合成(実施例100及び実施例101):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3 ]チアジン-3-スルホンイミドアミド(80 mg,0.19ミリモル)をキラルSFC(キラルパック AS(250 mm*30 mm,10 um);超臨界 CO2 / EtOH+0.1% NH4OH=65/35;70 mL/min)により分離し、白色固体として(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]チアジン-3-スルホンイミドアミド(ピーク1,25 mg、純度70%)を得て、(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミド(方法C,4.21分、ピーク2,17.2mg、収率22%)を得た。ピーク1をキラルSFC(キラルパック AD(250 mm*30 mm,10 um);超臨界 CO2 / EtOH+0.1% NH4OH=40/40;80 mL/min)でさらに精製して、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]チアジン-3-スルホンイミドアミド(方法C,3.97分、ピーク1,14.4 mg、収率18%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.17(s,1H),7.70(s,1H),7.33(s,2H),6.85(s,1H),4.19(t,J=6.0 Hz,2H),3.12(t,J=5.2 Hz,2H),2.77(t,J=7.2 Hz,4H),2.70-2.65(m,4H),2.28-2.21(m,2H),1.96-1.85(m,4H).MS:m/z 418.0(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.18(s,1H),7.71(s,1H),7.36(s,2H),6.86(s,1H),4.20(t,J=5.6 Hz,2H),3.12(t,J=5.6 Hz,2H),2.77(t,J=7.6 Hz,4H),2.73-2.65(m,4H),2.28-2.21(m,2H),1.96-1.85(m,4H).MS:m/z 418.0(M+H+).
実施例102及び実施例103
(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3] オキサジン-3-スルホンイミドアミド:
工程1-N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(200 mg,0.45 mmol)のTHF(12 mL)溶液に、窒素雰囲気下、0℃でMeONa(37 mg,0.67 mmol)を加えた。20分後、3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジン(159 mg,0.68 mmol)のTHF(8 mL)中の溶液を加えた。反応混合物を室温で16時間撹拌した。反応物をMeOH(5mL)で急冷し、濾過し、濃縮して乾燥させた。粗残渣をPrep-TLC(EtOAc)で精製し、N-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(99 mg、収率32%)を白色固体として得た。MS:m/z 679.3(M+H+).
工程2-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-N-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(99 mg,0.15 mmol)のDCM(8 mL)中の撹拌溶液に、0℃でMeSO3H(0.01 mL,0.15 mmol)を加えた。1時間後、反応混合物を飽和水性NaHCO3と希釈DCM(10 mL)で塩基性化した。この有機層を、Na2SO4上で乾燥させ、フィルタにかけ、濃縮した。粗残渣を分取TLC(ジクロロメタン中5%MeOH)で精製し、N’-{(2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル}-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(60mg、収率94%)を白色固体として得た。MS:m/z 437.1(M+H+).
工程3-(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((2.4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例102及び実施例103):
N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(60 mg,0.14 mmol)をキラルSFC(キラルパック OJ(250 mm * 30 mm,5 um)、超臨界 CO2 / EtOH+0.1% NH4OH=40/60;60 mL/min)で分離し、(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法J,2.57分、ピーク1,9mg、収率15%)と(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法J,2.74分、ピーク2,15.7 mg、収率26%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ=8.00(s,1H),7.49(s,1H),7.24(s,2H),6.45(s,1H),4.42-4.34(m,2H),4.09(t,J=5.6 Hz,2H),3.80(s,3H),3.21-3.15(m,1H),3.04-2.97(m,1H),2.19-2.11(m,2H),1.10-1.00(m,12H).MS:m/z 437.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ=8.00(s,1H),7.49(s,1H),7.24(s,2H),6.45(s,1H),4.42-4.33(m,2H),4.10(t,J=5.6 Hz,2H),3.80(s,3H),3.21-3.15(m,1H),3.00-2.95(m,1H),2.19-2.11(m,2H),1.10-1.00(m,12H).MS:m/z 437.1(M+H+).
実施例104:
(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、アンモニア:
工程1-(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-)の合成 イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、アンモニア(実施例104):
臭化シアノゲン(ジクロロメタン中1M,30μL,30μmol)をDMF(0.5 mL)中の(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミド(10 mg,0.02 mmol)の溶液に室温で添加した。30分後、飽和炭酸水素ナトリウム水溶液(50 mL)を加え、得られた溶液を逆相HPLC(5-50% ACN in 0.1% NH4OH(aq)で直接精製した。1% NH4OH(aq))で精製し、(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、アンモニア(4.5 mg、収率45%)を得た。1H NMR(400 MHz,DMSO-d6)δ=7.87(s,1H),7.43(s,1H),7.20(s,1H),7.07(s,1H),6.98(s,1H),6.51(s,1H),4.72 - 4.08(m,4H),2.74(ddd,J=30.2,15.2,7.9 Hz,8H),2.10 - 1.84(m,4H).MS:m/z 488.2(M+H+).
実施例105、実施例106、実施例109及び実施例110
(S,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.R,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド.S,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、及び(R.7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド:
工程1-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-オールの合成:
7-(ベンジルオキシ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン(7.2 g,29.47 mmol)のEtOH(72 mL)中の溶液に、炭素上の10%Pd(3.6 g,3.38 mmol)を加えた。この混合物を水素雰囲気下(45psi)で50℃で96時間撹拌した。室温まで冷却した後、反応混合物を濾過し、濾液を濃縮して、白色固体として5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-オール(4.11 g、収率:91%)を得て、これをさらに精製することなく次の工程で使用した.1H NMR(400 MHz,CDCl3)δ=7.27(d,J=2.0 Hz,1H),5.73(d,J=2.0 Hz,1H),4.72(s,1H),4.43-4.30(m,1H),4.28-4.12(m,4H),2.25-2.07(m,2H).MS:m/z 154.8(M+H+).
工程2-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イルメタンスルホン酸の合成:
5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-オール(3.81 g,24.71 mmol)のピリジン(38 mL)溶液に、窒素雰囲気下、室温でMsCl(3.94 g,34.4 mmol)を加えた。4時間後、反応物を濃縮し、水(50 mL)を加えた。水層をEtOAc(100mL×2)で抽出した。合わせた有機層をブライン(30 mL×2)で洗浄し、Na2SO4上で死滅させ、濃縮して5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イルメタンスルホン酸塩(5.7 g、収率:99%)を白色固体として得て、これをさらに精製することなく次の工程で使用した。MS:m/z 232.9(M+H+).
工程3-tert-ブチル(5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-トの合成:
DMF(25 mL)中の5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イルメタンスルホン酸塩(2.36 g,10.16 mmol)とNaN3(1.88 g,28.89 mmol)の混合物を窒素雰囲気下120℃で2時間撹拌した。室温まで冷却した後、反応混合物をそのまま次の工程で使用した。MS:m/z 179.9(M+H+).
反応混合物に、炭素上の10%Pd(1.39g,13.04ミリモル),Boc2O(3.33g,15.24ミリモル)及びMeOH(25mL)を室温で加えた。反応混合物を水素雰囲気下(50psi)で16時間撹拌した。反応物を濾過し、濾液を濃縮した。粗残渣に水(10 mL)を加えた。水層をEtOAc(100 mL x2)で抽出した。合わせた有機層をブライン(30 mL×2)で洗浄し、Na2SO4上で乾燥し、濃縮し、粗残渣をシリカゲルカラム(0-50% EtOAc in petrolumn ether)で精製し、tert-ブチル(5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバミン酸塩(2.45 g、収率95%)を白色固体として得た。MS:m/z 197.9(M-56+H+).
工程4-tert-ブチル(3-ブロモ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-トの合成:
MeCN(50 mL)中のtert-ブチル(5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-ト(2.45 g,9.67 mmol)の溶液に、0℃でNBS(2.07 g,11.61 mmol)を加えた。反応混合物を室温で16時間撹拌した。混合物を濃縮して乾燥させ、残渣をシリカゲルカラム(石油エーテル中の0-50%EtOAc)で精製して、黄色固体としてtert-ブチル(3-ブロモ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-ト(2,78g、収率86%)を得た。MS:m/z 276.8(M-56+H+).
工程5-tert-ブチル(3-ブロモ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)(メチル)カルバメ-トの合成:
DMF(25 mL)中のtert-ブチル(3-ブロモ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-ト(2.78 g,8.35 mmol)の溶液に、窒素雰囲気下、0℃でNaH(鉱油中60%,0.67 g,16.71 mmol)を加えた。1時間後、MeI(2.6 mL,41.77 mmol)を滴下添加した。得られた混合物を室温まで温め、さらに16時間撹拌した。反応物を水(100 mL)に注いだ。水層を酢酸エチル(50mL×3)で抽出した。合わせた有機層をブライン(50mL×3)で洗浄し、Na2SO4上で乾燥し、濃縮して乾燥させた。粗残渣をシリカゲルカラム(石油エーテル中0-33%EtOAc)で精製し、白色固体としてtert-ブチル(3-ブロモ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)(メチル)カルバミン酸塩(2.25 g、収率:78%)を得た。MS:m/z 289.8(M+H+).
工程6-tert-ブチルメチル(3-(N’-トリチルスルファミミドイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-トの合成:
THF(10 mL)中のtert-ブチル(3-ブロモ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)(メチル)カルバメ-ト(740 mg,2.14 mmol)の溶液に、窒素雰囲気下、-78℃でn-BuLi(ヘキサン中2.5 M,1.06 mL,2.64 mmol)を滴下して加えた。1時間後、THF(1.84 mL)中のTrtNSO(783 mg,2.56 mmol)を滴下添加した。反応物は-78℃で20分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。次亜塩素酸tert-ブチル(0.29 mL,2.57 mmol)を0℃で滴下添加した。20分後、NH3ガスを10分間バブリングした。反応物を室温まで温め、さらに16時間撹拌した。反応混合物を濃縮して乾燥させ、残渣をシリカゲルカラム(石油エーテル中の0-70%EtOAc)で精製して、tert-ブチルメチル(3-(N’-トリチルスルファミミドイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-ト(430 mg、収率35%)を黄色固体として得た。MS:m/z 610.1(M+Na+).
工程7-tert-ブチル(3-(N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)(メチル)カルバメ-トの合成:
MF(3 mL)及びTHF(15 mL)中のtert-ブチルメチル(3-(N’-トリチルスルファミミドイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)カルバメ-ト(330 mg,0.56 mmol)の溶液に、窒素雰囲気下、0℃でMeONa(46 mg,0.84 mmol)を添加した。20分後、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(224 mg,1.12 mmol)の溶液をTHF(9 mL)に滴下添加した。反応混合物を室温まで温めた。16時間後、反応物を濃縮して乾燥させ、粗残渣を分取TLC(50%EtOAc in Petrolamunneter)で精製して、tert-ブチル(3-(N-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)(メチル)カルバメ-ト(316mg、収率.72%)を白色固体として得た。MS:m/z 809.3(M+Na+).
工程8-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
DCM(20 mL)中のtert-ブチル(3-(N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチルスルファミミドイル)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-7-イル)(メチル)カルバミン酸塩(320 mg,0.41 mmol)の溶液に、0℃でMeSO3H(16滴)を添加した。反応物を室温まで温めた。1時間後、反応混合物を飽和水性NaHCO3の添加によりpH=8に調整した。反応物を濃縮して乾燥させ、粗残渣を分取TLC(DCM中10%MeOH)で精製し、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(117mg、収率:65%)を黄色固体として得た。MS:m/z 445.1(M+H+).
工程9-(S,7S)-N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(R.7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(S,7R)-N’-((1,2,3,5,6.7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド及び(R,7R)-N’-((1,2,3,5,6.7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(実施例105、実施例106、実施例109、実施例110):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(154 mg,0.35 mmol)をキラルSFC(Chiralpak AD(250 mm * 30mm,10 um);Supercritical CO2 / 0.1% EtOH+NH4OH=55/45;80 mL/min)で分離して(S,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(方法I,2.96分、ピーク1,22.4mg、収率14%)を白色固体、(R,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(方法I,4.76分、ピーク4,15.9mg、収率10%)を白色固体、(7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(ピーク2と3の混合物、76mg、収率50%)を白色固体として得た。(7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(ピーク2と3の混合物、76mg,0.17mmol)はキラルSFC(キラルパック OD(250 mm * 30 mm,5 um);超臨界 CO2 / 0.1% MeOH+NH4OH=70/30;50 mL/min)により分離され、(S,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(方法K,4.75分、ピーク2,15.6mg、収率21%)と(R,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(方法K,4.91分、ピーク3,11mg、収率14%)は白色固体となった。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.19(s,1H),7.48(s,1H),7.27(s,2H),6.85(s,1H),4.38-4.02(m,4H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.26(s,3H),2.20-2.09(m,1H),2.02-1.75(m,6H).MS:m/z 445.1(M+H+).化合物105
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.20(s,1H),7.47(s,1H),7.23(s,1H),6.85(s,1H),4.43-4.05(m,4H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.26(s,3H),2.20-2.10(m,1H),1.99-1.89(m,6H).MS:m/z 445.1(M+H+).化合物109
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.22(s,1H),7.52(s,1H),7.33(s,2H),6.86(s,1H),4.40-4.30(m,2H),4.26-4.04(m,2H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.39(s,3H),2.22-2.14(m,1H),2.13-1.87(m,6H).MS:m/z 445.1(M+H+).化合物110
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.18(s,1H),7.47(s,1H),7.21(s,2H),6.85(s,1H),4.30-4.03(m,4H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.26(s,3H),2.19-2.08(m,1H),1.99-1.72(m,6H).MS:m/z 445.1(M+H+).化合物106
実施例107及び実施例108
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドと(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド:
工程1-3-ブロモ-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジンの合成:
DCM(33 mL)中のtert-ブチル3-ブロモ-6,7-ジヒドロピラゾロ[1,5-a]ピリミジン-4(5H)-カルボキシレート(3.0 g,9.93 mmol)の撹拌溶液に、室温でTFA(6.6 mL,88.56 mmol)を加えた。1時間後、反応混合物をコンセト化して乾燥させた。飽和水性NaHCO3(20 mL)を粗残渣に加えた。水層をEtOAc(20 mL)で抽出した。合わせた有機層を水(50 mL)、食塩水(30 mL)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮して3-ブロモ-4,5,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン(1.67 g、収率:83%)を黄色油として得て、これをさらに精製することなく次の工程で使用した。1H NMR(400 MHz,CDCl3):δ=7.24(s,1H),4.11(t,J=6.0 Hz,2H),4.03(s,1H),3.38(t,J=6.0 Hz,2H),2.20-2.13(m,2H).
工程2-3-ブロモ-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジンの合成:
DMF(21 mL)中のNaH(60%鉱油、554 mg,13.86 mmol)の溶液に3-ブロモ-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン(1.4 g,6.93 mmol)を窒素雰囲気下、0 ℃で加えた。30分後、MeI(0.86 mL,13.86 mmol)を滴下添加した。反応物を室温まで温めた。16時間後、飽和水性NH4Cl(50ml)とEtOAc(100ml)を添加した。水層をEtOAcで抽出した。合わせた有機層を水(100 mL)、食塩水(50 mL)で洗浄し、Na2SO4上で乾燥し、ろ過し、濃縮して、黄色の固体として3-ブロモ-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン(1.3 g、収率:87%)を得た。1H NMR(400 MHz,CDCl3):δ=7.22(s,1H),4.07(t,J=6.0 Hz,2H),3.15-3.10(m,5H),2.19-2.09(m,2H).
工程3-4-メチル-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドの合成:
3-ブロモ-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン(1.1 g,5.09 mmol)のTHF(24 mL)溶液に、n-BuLi(ヘキサン中2.5 M,2.5 mL,6.29 mmol)を窒素雰囲気下、-78℃で滴下して加えた。1時間後、THF(4 mL)中のTrtNSO(1.86 g,6.11 mmol)を滴下添加した。反応物は-78℃で20分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。次亜塩素酸tert-ブチル(0.7 mL,6.19)を0℃で滴下添加した。20分後、NH3ガスを10分間バブリングした。反応物を室温まで温め、さらに16時間撹拌した。反応混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中50%EtOAc)で精製し、4-メチル-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド(480mg、収率:21%)を白色固体として得た。1H NMR(400 MHz,DMSO-d6)δ=7.46-7.41(m,6H),7.16-7.10(m,6H),7.07-7.02(m,3H),6.73(s,1H),6.41(s,2H),3.80-3.70(m,2H),3.27(s,3H),3.02-2.99(m,2H),1.94-1.85(m,2H).
工程4-5-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドの合成:
工程3でN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドを4-メチル-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドに置き換えることにより、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド(実施例100及び実施例101)の調製に記載された一般的な手順を用いてN’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドアミドを調製した。
工程6-(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドと、(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドの合成(実施例107及び実施例108):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミドアミド(100 mg,0.24 mmol)をキラルSFC(Chiralpak AS(250 mm * 50 mm,10 um),Supercritical CO2 / MeOH+0.1% NH4OH=70/30;70 mL/min)で分離し、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド(方法C,3.20分、ピーク1,27.2mg、収率27%)と(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4-メチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリミジン-3-スルホンイミド(方法C,3.37分、ピーク2,30.4mg、収率30%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.23(s,1H),7.43(s,1H),7.27(s,2H),6.86(s,1H),3.96(t,J=6.0 Hz,2H),3.27-3.21(m,5H),2.78(t,J=7.2 Hz,4H),2.68(t,J=7.6 Hz,4H),2.04-1.99(m,2H),1.97-1.88(m,4H).MS:m/z 415.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.23(s,1H),7.43(s,1H),7.27(s,2H),6.85(s,1H),3.95(t,J=6.0 Hz,2H),3.27-3.20(m,5H),2.77(t,J=7.2 Hz,4H),2.67(t,J=7.6 Hz,4H),2.04-1.98(m,2H),1.96-1.87(m,4H).MS:m/z 415.1(M+H+).
実施例111
(S,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミドアンモニア:
工程1の(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを(R,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドに置き換えることにより、(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例104)の調製に記載された一般的な手順を用いて(S,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドアミドアンモニアを調製した(単一の未知の立体異性体).1H NMR(400 MHz,DMSO-d6)δ 7.76(s,1H),7.43(s,1H),7.20(s,1H),7.07(s,1H),6.94(s,1H),6.51(s,1H),4.72 - 4.08(m,4H),2.74(ddd,J=30.2,15.2,7.9 Hz,8H),2.10 - 1.84(m,4H).MS:m/z 488.2(M+H+).
実施例112
(R,7S)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミドアンモニア:
工程1で(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを(S,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドに置き換えて(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例104)の調製に記載された一般的な手順で(R,7S)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミドアンモニアを調製した。単一の未知の立体異性体.1H NMR(400 MHz,DMSO-d6)δ 7.85(s,1H),7.37(s,1H),7.20(s,1H),7.07(s,1H),6.95(s,1H),6.81(s,1H),4.43(ddd,J=14.5,5.5,1.4 Hz,1H),4.31 - 4.11(m,2H),4.01(ddd,J=12.4,10.2,2.4 Hz,1H),3.64(m,1H),2.86 - 2.59(m,8H),2.16(m,2H),1.91(p,J=7.5 Hz,4H).MS:m/z 471.2(M+H+).
実施例113及び実施例114
(S)-N’-(1-(1-(シクロプロピルメチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1.3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((1-(シクロプロピルメチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程3において、ヨードエタンを(ブロモメチル)シクロプロパンで置換することにより、(R)-N’-((1-(2,2-ジフルオロエチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S)-N’-((1-(2,2-ジフルオロエチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例96及び実施例97)の調製に記載された一般的な手順を用いて、(S)-N’-((1-(シクロプロピルメチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((1-(シクロプロピルメチル)-3,5-ジイソプロピル-1H-ピラゾール-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを調製した。分取HPLC及び分取SFC(工程6)の後、絶対立体化学未知の2つの異性体を、ピーク1(方法T,1.02分)及びピーク2(方法T,1.74分)を単離した。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ 7.52(s,1H),7.48(s,1H),7.22(s,2H),4.50 - 4.21(m,2H),4.09(t,J=6.1 Hz,2H),3.79(d,J=6.7 Hz,2H),2.82 - 2.64(m,2H),2.28 - 2.08(m,2H),1.17(d,J=7.1 Hz,6H),1.09(dt,J=6.9,3.1 Hz,7H),0.56 - 0.38(m,2H),0.38 - 0.22(m,2H).MS:m/z 450.3(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ 7.52(s,1H),7.48(s,1H),7.21(s,2H),4.45 - 4.29(m,2H),4.09(t,J=6.1 Hz,2H),3.79(d,J=6.7 Hz,2H),2.80 - 2.63(m,2H),2.17(m,2H),1.18(m,6H),1.16 - 0.99(m,7H),0.54 - 0.38(m,2H),0.30(dt,J=4.9,2.9 Hz,2H).MS:m/z 450.2(M+H+).
実施例115及び実施例116
N-((S,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミドとN-((R.6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミド:
工程1-N-((S,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミドとN-((R.6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミドの合成(実施例115及び実施例116):
(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(180 mg,0.4171 mmol)の溶液にジクロロメタン(8 mL)を加えた。4171mmol)をジクロロメタン(8 mL)に加え、0℃でトリエチルアミン(1.16 mL,8.343mmol)と無水酢酸(0.39 mL,4.171mmol)を加えた。添加後、反応物を室温までゆっくりと温めた。1.5時間後、トリメチルアミン(1.16 mL,8.343 mmol)及び無水酢酸(0.39 mL,4.171 mmol)を追加添加した。1.5時間撹拌した後、所望の生成物を提供するために、反応混合物を直接フラッシュカラムクロマトグラフィー(シリカ、100%ジクロロメタン、その後、DCM/MeOH/H2O/NH4OH(90/10/0.6/0.6))の勾配)に供した。この材料をさらにキラルSFC(Regis Technologies(Morton Grove,IL)カラムからの2.1 x 25.0 cm(S,S)Whelk0-1、及び100バ-ル、25℃で0.25%水酸化アンモニウムを含むCO2及び45%エタノールからなるアイソクラティック法)で精製してN-((R,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミド(ピーク1、方法W,1,3分、32mg、収率16%).とN-((S,6S)-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-メトキシ-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドイル)アセトアミド(ピーク2、方法W,2.分、13mg、収率7%).を得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ 8.12(s,1H),7.57 - 7.51(m,1H),7.46(dd,J=6.7,4.0 Hz,1H),6.84(s,1H),4.54(d,J=11.5 Hz,1H),4.29(d,J=11.5 Hz,1H),4.23(dd,J=13.2,3.7 Hz,1H),4.14(d,J=13.2 Hz,1H),4.01(s,1H),3.35(d,J=1.4 Hz,4H),2.77(t,J=7.4 Hz,4H),2.69(t,J=7.2 Hz,4H),1.99 - 1.89(m,4H),1.86(d,J=2.9 Hz,3H).MS:m/z 474.2(M+H+).化合物116
ピーク2:1H NMR(400 MHz,DMSO-d6)δ 11.70(s,1H),8.33(s,1H),7.79 - 7.51(m,1H),6.88(s,1H),4.61(d,J=11.8 Hz,1H),4.33(d,J=11.7 Hz,1H),4.26(dd,J=13.3,3.5 Hz,1H),4.18(d,J=13.4 Hz,1H),4.05(s,1H),3.36(s,3H),2.79(t,J=7.4 Hz,4H),2.69(d,J=7.9 Hz,4H),2.03 - 1.88(m,7H).MS:m/z 474.2(M+H+).化合物115
実施例117及び実施例118
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド、及び(R)-N’-((1.2,3,5,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド:
工程1-エチル2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-5-イル)アセテートとエチル2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-3-イル)アセテートの合成:
DCM(300 mL)中のエチル2-(1H-ピラゾール-5-イル)アセテート(10.0 g,64.86 mmol)の溶液に、室温で3,4-ジヒドロ-2H-ピラン(11 g,129.73 mmol)とTsOH(3.21 g,16.86 mmol)を加えた。16時間後、反応混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-50%EtOAc)で精製し、エチル2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-5-イル)アセテートとエチル2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-3-イル)アセテート(12 g、収率77.6%)の混合物を無色油として得た。MS:m/z 239.2(M+H+).
工程2-2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-5-イル)エタノールと2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-3-イル)エタノールの合成
THF(100 mL)中のLiAlH4(5.2 g,151.08 mmol)の懸濁液に、THF(100 mL)中のエチル2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-5-イル)アセテート及びエチル2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-3-イル)アセテート(12 g,50.36 mmol)の溶液を0℃で滴下して添加した。添加後、反応混合物を室温まで温めた。3時間後、反応物を0℃まで冷却し、飽和水性Na2SO4をゆっくりと添加して反応物を急冷した。混合物をNa2SO4上で乾燥させた。濾過により固形物を除去し、濾液を濃縮して乾燥させ、2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-5-イル)エタノールと2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-3-イル)エタノールの混合物を得て、これをさらに精製することなく次の工程で使用した(7gの粗製).MS:m/z 197.0(M+H+).
工程3-1-(テトラヒドロ-2H-ピラン-2-イル)-5-(2-(2-(2-((テトラヒドロ-2H-ピラン-2-イル)オキシ)エトキシ)エトキシ)エチル)-1H-ピラゾールと、1-(テトラヒドロ-2H-ピラン-2-イル)-3-(2-(2-((テトラヒドロ-2H-ピラン-2-イル)オキシ)エトキシ)エチル)-1H-ピラゾールの合成:
2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-5-イル)エタノールと2-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-3-イル)エタノール(7 g,35.67 mmol)のDMF(150 mL)中の溶液に、0℃でNaH(鉱油60%,2.1 g,53.5 mmol)を加え、1-(1-(テトラヒドロ-2H-ピラン-2-イル)-1H-ピラゾール-5-イル)エタノールを加えた。30分後、2-(2-ブロモエトキシ)テトラヒドロピラン(22.3 g,107.01 mmol)を加えた。反応物を室温まで温めた。32時間後、反応物を飽和水性NH4Cl(50 mL)で急冷した。水層をDCM(3×300mL)で抽出した。合わせた有機層をNa2SO4上で乾燥させ、濾過し、濃縮して乾燥させた。粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-30% EtOAc)で精製し、1-(テトラヒドロ-2H-ピラン-2-イル)-5-(2-(2-((テトラヒドロ-2H-ピラン-2-イル)オキシ)エトキシ)エチル)-1H-ピラゾールと1-(テトラヒドロ-2H-ピラン-2-イル)-3-(2-(2-((テトラヒドロ-2H-ピラン-2-イル)オキシ)エトキシ)エチル)-1H-ピラゾール(4.8g、収率41%)の混合物を無色油として得た。MS:m/z 325.1(M+H+).
工程4-2-(2-(2-(1H-ピラゾール-5-イル)エトキシ)エタノールの合成:
1-(テトラヒドロ-2H-ピラン-2-イル)-5-(2-(2-(2-((テトラヒドロ-2H-ピラン-2-イル)オキシ)エトキシ)エチル)-1H-ピラゾール及び1-(テトラヒドロ-2H-ピラン-2-イル)-3-(2-(2-((テトラヒドロ-2H-ピラン-2-イル)オキシ)エトキシ)エチル)-1H-ピラゾール(4.8 g,7.4 mmol)の溶液に、0℃で濃縮HCl(7.0 mL,84 mmol)を加えた。8 g,7.4 mmol)をEtOH(80 mL)中に0℃で濃縮HCl(7.0 mL,84 mmol)を加えた。添加後、反応物を30℃まで温めた。16時間後、反応物を濃縮して乾燥させた。粗残渣に飽和水性NaHCO3を加え、溶液をpH=8に調整した。得られた混合物をDCM(50mL×3)で抽出した。合わせた有機層をNa2SO4上で乾燥させ、濾過し、濃縮して乾燥させた。粗残渣をシリカゲルカラムクロマトグラフィー(MeOH/DCM=1:10)で精製し、2-(2-(1H-ピラゾール-5-イル)エトキシ)エタノール(2g、収率86%)を無色油として得た。1H NMR(400 MHz,DMSO-d6):δ=12.45(s,1H),7.50-7.20(m,1H),6.07(s,1H),4.62(s,1H),3.61(t,J=7.2 Hz,2H),3.52-3.46(m,2H),3.44-3.40(m,2H),2.83-2.74(m,2H).
工程5-2-(2-(2-(1H-ピラゾール-5-イル)エトキシ)エチル)メタンスルホン酸エステルの合成:
DCM(60 mL)中の2-(2-(1H-ピラゾール-5-イル)エトキシ)エタノール(2.0 g,12.81 mmol)及びトリエチルアミン(5.3 mL,38.42 mmol)の撹拌溶液に、0℃でMsCl(1.0 mL,12.81 mmol)を加えた。1時間後、水(2 mL)を加えた。水層をDCM(50mL×3)で抽出した。合わせた有機層をNa2SO4上で乾燥させ、濾過し、濃縮して乾燥させた。粗残渣をシリカゲルカラムクロマトグラフィー(0-5% MeOH in DCM)で精製し、2-(2-(1H-ピラゾール-5-イル)エトキシ)エチルメタンスルホン酸塩(1.1 g、収率:26%)を無色油として得た。MS:m/z 234.9(M+H+).
工程6-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピンの合成:
DMF(18 mL)中の2-(2-(1H-ピラゾール-5-イル)エトキシ)エチルメタンスルホン酸塩(1.1 g,4.7 mmol)の溶液に、0℃でNaH(鉱油中60%,226 mg,5.63 mmol)を加えた。反応混合物を室温に温めた。12時間後、反応物を0℃まで冷却し、飽和NH4Cl水溶液(3 mL)を加えた。反応混合物を濃縮して乾燥させ、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-20%EtOAc)で精製して、4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン(480mg、収率70%)を無色油として得た。1H NMR(400 MHz,CDCl3):δ=7.33(d,J=1.6 Hz,1H),6.05(d,J=1.6Hz,1H),4.45-4.42(m,2H),3.90-3.87(m,2H),3.86-3.83(m,2H),3.01-2.98(m,2H).
工程7-3-ブロモ-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピンの合成:
4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン(480 mg,3.47 mmol)のMeCN(15 mL)溶液にNBS(618 mg,3.47 mmol)を0℃で加えた。反応物を室温まで温めた。1時間後、反応混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中、0-30%EtOAc)で精製し、白色固体として3-ブロモ-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン(420mg、収率:56%)を得た。1H NMR(400 MHz,CDCl3):δ=7.35(s,1H),4.43(t,J=4.0Hz,2H),3.90-3.84(m,4H),2.99(t,J=4.8 Hz,2H).
工程8- N’-トリチル-4,5,7,8-テトラヒドロピラゾロ[1,5-d] [1,4]オキサゼピン-3-スルホンイミドアミドの合成:
3-ブロモ-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン(200 mg,0.92 mmol)のTHF(4 mL)溶液に、n-BuLi(ヘキサン中2.5 M,0.41 mL,1.01 mmol)を窒素雰囲気下、-78℃で滴下して加えた。1時間後、THF(1 mL)中のTrtNSO(310 mg,1.01 mmol)を滴下添加した。反応物は-78℃で30分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。次亜塩素酸tert-ブチル(0.11 mL,0.99 mmol)を0℃で滴下添加した。30分後、NH3ガスを混合物に10分間バブリングした。反応物を室温まで温め、さらに16時間撹拌した。反応液を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-80%EtOAc)で精製し、N’-トリチル-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド(200mg,収率34%)を白色固体として得た。1H NMR(400 MHz,DMSO-d6)δ=7.42-7.30(m,6H),7.18-7.12(m,6H),7.10-7.07(m,4H),6.5(s,2H),4.25-4.19(m,2H),3.71-3.59(m,4H),3.08-3.03(m,2H).
工程9-N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミドの合成:
N’-トリチル-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミドアミド(100 mg,0.22 mmol)のTHF(5 mL)中の撹拌溶液に、0℃でMeONa(24 mg,0.44 mmol)を加えた。15分後、4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(52 mg,0.26 mmol)を加え、反応混合物を室温まで温めた。16時間後、MeOH(1 mL)を加え、反応物を濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(DCM中0-5%MeOH)で精製し、N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド(100mg、収率:70%)を白色固体として得た。
工程10-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミドの合成:
N-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-N’-トリチル-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド(200 mg,0.3 mmol)のDCM(10 mL)中の溶液に、0℃でMeSO3H(6滴)を加えた。添加後、反応物を室温まで温めた。1時間後、飽和水性NaHCO3を添加して反応物をpH=8に調整した。反応物を濃縮して乾燥させ、粗残渣をシリカゲルカラムクロマトグラフィー(DCM中0-2%MeOH)で精製し、N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド(100mg、収率:79%)を白色固体として得た。MS:m/z 416.1(M+H+).
工程11-(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミドと、(R)-N’-((1.2,3,5,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミドの合成(実施例117及び実施例118):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド(100 mg,0.24 mmol)はキラルSFC(キラルパック AD(250 mm * 50 mm,10 um);超臨界 CO2/EtOH+0.1% NH4OH=45/55;80 mL/min)により分離され、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド(方法E,2.30分、ピーク1,12.9mg、収率12%)と(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,7,8-テトラヒドロピラゾロ[1,5-d][1,4]オキサゼピン-3-スルホンイミド(方法E,2.92分、ピーク2,11.8mg、収率11%)は白色固体として得られた。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.17(s,1H),7.62(s,1H),7.32(s,2H),6.85(s,1H),4.47-4.38(m,2H),3.78-3.66(m,4H),3.21-3.16(m,2H),2.76(t,J=7.2 Hz,4H),2.64(t,J=7.2 Hz,4H),1.96-1.88(m,4H).MS:m/z 416.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.20(s,1H),7.63(s,1H),7.38(s,2H),6.85(s,1H),4.43(t,J=4.0 Hz,2H),3.80-3.64(m,4H),3.29-3.28(m,1H),3.23-3.14(m,1H),2.76(t,J=7.2 Hz,4H),2.64(t,J=6.8 Hz,4H),1.99-1.86(m,4H).MS:m/z 416.1(M+H+).
実施例119及び実施例120
(S)-N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1.3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-4-(5-フルオロ-2-イソシアナト-3-イソプロピルフェニル)-2-メトキシピリジンの合成:
4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)アニリン(WO2019008025で報告されているように合成、240 mg,0.92 mmol)とトリエチルアミン(0.35 mL,2.49 mmol)のTHF(12 mL)中の溶液に、窒素雰囲気下、室温でトリホスゲン(109 mg,0.37 mmol)を加えた。混合物を70℃に加熱した。1時間後、反応物を室温まで冷却し、シリカゲルのパッドを通して濾過した。シリカゲルパッドをTHF(5mL×3)で洗浄した。4-(5-フルオロ-2-イソシアナト-3-イソプロピルフェニル)-2-メトキシピリジンを含む濾液を、次の工程でTHF溶液として直接使用した。
工程2-N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドは、工程1で3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジンを4-(5-フルオロ-2-イソシアナト-3-イソプロピルフェニル)-2-メトキシピリジンに置き換えることにより、(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例102及び実施例103)の調製に記載された一般的な手順を用いて調製した。
工程3-(S)-N’-{(4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル}-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1.3]オキサジン-3-スルホンイミドアミド、及び(R)-N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例119及び実施例120):
N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(107 mg,0.22 mmol)をキラルSFC(Chiralpak IC(250 mm * 30 mm,10 um),CO2 / EtOH+0.1% NH4OH=40/60;80 mL/min)で分離し、(S)-N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [ 1,3]オキサジン-3-スルホンイミドアミド(方法L,3.63分、ピーク1,32 mg、収率29%)と(R)-N’-((4-フルオロ-2-イソプロピル-6-(2-メトキシピリジン-4-イル)フェニル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [ 1,3]オキサジン-3-スルホンイミドアミド(方法L,6.88分、ピーク2,38 mg、収率34%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.18-8.10(m,2H),7.27(s,1H),7.18-7.12(m,3H),7.00-6.90(m,2H),6.79(s,1H),4.36-4.30(m,2H),4.09(t,J=6.4 Hz,2H),3.87(s,3H),3.15-3.08(m,1H),2.20-2.12(m,2H),1.11-1.05(m,6H).MS:m/z 489.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.16-8.08(m,2H),7.27(s,1H),7.20-7.10(m,3H),7.00-6.90(m,2H),6.79(s,1H),4.38-4.31(m,2H),4.10(t,J=6.4 Hz,2H),3.87(s,3H),3.15-3.06(m,1H),2.20-2.12(m,2H),1.13-1.06(m,6H).MS:m/z 489.1(M+H+).
実施例121
(S,7R)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミドアンモニア:
工程1で(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを(R,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[ 5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミドに置き換えることにより、(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例104)の調製について説明した一般的な手順を使用して(S,7R)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミドアンモニアを調製した(単一の未知の立体異性体).1H NMR(400 MHz,DMSO-d6)δ 7.86(s,1H),7.39(s,1H),7.21(s,1H),7.08(s,1H),6.96(s,1H),6.82(s,1H),4.44(ddd,J=14.5,5.5,1.4 Hz,1H),4.27 - 4.13(m,2H),4.02(ddd,J=12.4,10.2,2.4 Hz,1H),3.65(q,J=4.3,3.1 Hz,1H),3.27(s,3H),2.87 - 2.61(m,8H),2.15(ddd,J=16.7,7.9,3.7 Hz,2H),2.03 - 1.81(m,4H).MS:m/z 471.2(M+H+).
実施例122
(R,7R)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミドアンモニア:
工程1で(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを(S,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[ 5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミドに置き換えることにより、(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例104)の調製について説明した一般的な手順を使用して(R,7R)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b] [1,3]オキサゼピン-3-スルホンイミドアミドアンモニアを調製した(単一の未知の立体異性体).1H NMR(400 MHz,DMSO-d6)δ 7.83(s,1H),7.41(s,1H),7.20(s,1H),7.07(s,1H),6.94(s,1H),6.82(s,1H),4.51 - 4.37(m,1H),4.28 - 4.15(m,2H),4.10(ddd,J=12.3,8.4,4.0 Hz,1H),3.65(q,J=4.5 Hz,1H),3.27(s,3H),2.76(m,4H),2.72 - 2.57(m,4H),2.14(dt,J=8.3,3.8 Hz,2H),2.01 - 1.84(m,4H).MS:m/z 471.2(M+H+).
実施例123
(S,7S)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアンモニア:
工程1の(S,6S)-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを(R,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドに置き換えることにより、(R,6S)-N-シアノ-6-(ジメチルアミノ)-N’-((8-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例104)の調製に記載された一般的な手順を用いて(S,7S)-N-シアノ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-メトキシ-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミドアンモニアを調製した(単一の未知の立体異性体).1H NMR(400 MHz,DMSO-d6)δ 7.80(s,1H),7.39(s,1H),7.20(s,1H),7.07(s,1H),6.94(s,1H),6.81(s,1H),4.44 - 4.37(m,1H),4.26 - 4.15(m,2H),4.09(ddd,J=12.3,8.6,3.9 Hz,1H),3.27(s,3H),2.76(m,4H),2.68(m,4H),2.14(dt,J=8.9,4.1 Hz,2H),2.02 - 1.80(m,4H).MS:m/z 471.2(M+H+).
実施例124及び実施例125
(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド、及び(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド:
工程1-N’-トリチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成:
7-ブロモ-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール(200 mg,1.06 mmol)のTHF(6 mL)中の撹拌溶液に、n-BuLi(ヘキサン中2.5 M,0.51 mL,1.27 mmol)を滴下し、-78℃でN2雰囲気下で加えた。1時間後、THF(1 mL)中のTrtNSO(388 mg,1.27 mmol)の溶液を滴下添加した。反応物は-78℃で20分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。次亜塩素酸tert-ブチル(0.15 mL,1.33 mmol)を0℃で滴下添加した。20分後、NH3ガスを混合物に10分間バブリングした。反応物を室温まで温め、さらに16時間撹拌した。反応混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(DCM中、0-2%MeOH)で精製し、N’-トリチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(140mg、収率31%)を黄色固体として得た。1H NMR(400 MHz,DMSO-d6)δ=7.43(d,J=7.6 Hz,6H),7.22-7.13(m,6H),7.13-7.06(m,3H),7.04(s,1H),6.38(s,2H),5.03(t,J=8.0 Hz,2H),4.18-4.07(m,2H).
工程2-3-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成:
工程3でN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドをN’-トリチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミドに置き換えることにより、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド(実施例100及び実施例101)の調製に記載された一般的な手順を用いてN’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミドを調製した。
工程4-(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド、及び(S)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成(実施例124及び実施例125):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(53 mg,0.14 mmol)をキラルSFC(キラルセル OD(250 mm * 30 mm,5 um);超臨界 CO2 / MeOH+0.1% NH4OH=40/60;50 mL/min)で分離し、(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(方法M,5.71分、ピーク1,4.8mg、収率9%)と(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(方法M,6.07分、ピーク2,6.3mg、収率 11%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.21(s,1H),7.54(s,1H),7.33(s,2H),6.86(s,1H),5.23-5.16(m,2H),4.34(t,J=8.4 Hz,2H),2.78(t,J=7.2 Hz,4H),2.72-2.66(m,4H),1.99-1.89(m,4H).MS:m/z 388.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.20(s,1H),7.54(s,1H),7.33(s,2H),6.86(s,1H),5.23-5.16(m,2H),4.33(t,J=8.4 Hz,2H),2.77(t,J=7.2 Hz,4H),2.70-2.64(m,4H),1.99-1.89(m,4H).MS:m/z 388.0(M+H+).
実施例126、実施例127、実施例128及び実施例129
(S)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.(S)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.(R)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドと(R)-N’-(((S)-3-メチル-1.5-イル)カルバモイル)との混合物.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-メチレン-8-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンの合成:
臭化メチルトリフェニルホスホニウム(18.5 g,51.8 mmol)のTHF(180mL)中の溶液に、t-BuOK(1.0 M in THF,41.4 mL,41.48 mmol)の溶液を窒素雰囲気下、0℃で滴下して加えた。2時間後、8-ニトロ-3,5,5,6,7-テトラヒドロ-2H-s-インダセン-1-オン(4.5 g,20.7 mmol)の溶液をTHF(27 mL)に滴下添加した。添加後、反応物を室温まで温めた。16時間後、反応物を水(80 mL)で急冷した。水層をEtOAc(100mL×2)で抽出した。合わせた有機層を食塩水(80mL×2)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中2%EtOAc)で精製し、黄色固体としてメチレン-8-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(2.1g、収率47%)を得た。1H NMR(400 MHz,CDCl3):δ=7.23(s,1H),5.24(s,1H),5.20(s,1H),2.97-2.91(m,6H),2.89-2.83(m,2H),2.21-2.10(m,2H).
工程2-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミンの合成:
EtOH(147 mL)中のメチレン-8-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(2.1 g,9.76 mmol)及び10% Pd/C on carbon(1.04 g,0.98 mmol)の混合物を、水素雰囲気下(15 psi)で室温で撹拌した。16時間後、反応混合物をセライトのパッドを通して濾過した。濾液を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中の0-10%EtOAc)で精製し、黄色固体として3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(800mg、収率44%)を得た。1H NMR(400 MHz,CDCl3):δ=6.61(s,1H),3.53(s,2H),3.24-3.14(m,1H),3.06-2.93(m,1H),2.91-2.83(m,2H),2.80-2.62(m,3H),2.35-2.23(m,1H),2.17-2.06(m,2H),1.83-1.73(m,1H),1.21(d,J=6.8 Hz,3H).
工程3-8-イソシアナト-1-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンの合成:
3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(306 mg,1.63 mmol)及びトリエチルアミン(0.61 mL,4.41 mmol)のTHF(20 mL)中の溶液に、トリホスゲン(194 mg,0.65 mmol)を窒素雰囲気下で室温で加えた。反応物を70℃で1時間加熱した。室温まで冷却した後、反応混合物をシリカゲルのパッドを通して濾過した。シリカゲルパッドをTHF(5mL×3)で洗浄した。8-イソシアナト-1-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを含む濾液を、次の工程でTHF溶液として直接使用した。
工程4-5-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
工程1で3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジンを8-イソシアナト-1-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンに置き換えることにより、(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例102及び実施例103)の調製に記載された一般的な手順を用いてN’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを調製した。
工程6-(S)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.(S)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、(R)-N’-((R)-3-メチル-1。2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ [5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-(((S)-3-methyl-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例126、実施例127、実施例128及び実施例129):
N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(116 mg,0.28 mmol)はキラルSFC(キラルパック AD(250 mm * 50 mm,10 um)、超臨界 CO2 / EtOH+0.1% NH4OH=65/35;70 mL/min)により分離され、(S)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法I,2.58分、ピーク1,7 mg、収率6%)、ミド(方法I,2.58分、ピーク1,7 mg、収率6%),(S)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法I,3.30分、ピーク2,7 mg、収率6%),(R)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法I,3.86分、ピーク3,9 mg、収率7%)、及び(R)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法I,4.32分、ピーク4,8 mg、収率6%)はすべて白色固体として得られた。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.08(s,1H),7.49(s,1H),7.19(s,2H),6.83(s,1H),4.40-4.33(m,2H),4.09(t,J=6.0 Hz,2H),2.88-2.60(m,7H),2.18-2.05(m,3H),1.97-1.85(m,2H),1.60-1.52(m,1H),1.03(d,J=6.8 Hz,3H).MS:m/z 416.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.10(s,1H),7.49(s,1H),7.18(s,2H),6.84(s,1H),4.40-4.35(m,2H),4.10(t,J=6.0 Hz,2H),2.85-2.60(m,7H),2.19-2.06(m,3H),1.95-1.85(m,2H),1.58-1.52(m,1H),1.04(d,J=6.8 Hz,3H).MS:m/z 416.2(M+H+).
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.09(s,1H),7.49(s,1H),7.18(s,2H),6.84(s,1H),4.40-4.33(m,2H),4.10(t,J=6.0 Hz,2H),2.85-2.60(m,7H),2.19-2.09(m,3H),1.95-1.85(m,2H),1.60-1.52(m,1H),1.04(d,J=6.8 Hz,3H).MS:m/z 416.1(M+H+).
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.09(s,1H),7.49(s,1H),7.22(s,2H),6.84(s,1H),4.40-4.34(m,2H),4.09(t,J=6.0 Hz,2H),2.86-2.60(m,7H),2.16-2.07(m,3H),1.97-1.89(m,2H),1.58-1.52(m,1H),1.1.03(d,J=6.8 Hz,3H).MS:m/z 416.1(M+H+).
実施例130、実施例131、及び実施例132
(S,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1.3]オキサゼピン-3-スルホンイミド、(R,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5.6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、及び(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド:
工程1-8-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成:
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドは、(S,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(R,7S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、(S,7R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドアミド、及び(R,7R)-N’-{(1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル}-7-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(実施例105、実施例106、実施例109及び実施例110)の調製のために記載された一般的な手順を用いて、工程1において、7-(ベンジルオキシ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンを6-(ベンジルオキシ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピンに置換することにより調製した。
工程9-(S,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5.1-b][1,3]オキサゼピン-3-スルホンイミド、(R,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7.8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド、及び(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミドの合成(実施例130、実施例131、及び実施例132):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(72 mg,0.16 mmol)はキラルSFC(Chiralpak AD(250 mm*30 mm,5 um),により分離され、(S,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(方法N,6.56分、ピーク1,11.2mg、収率16%),(R,6R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(方法N,7.11分、ピーク2,2.9mg、収率4%)、及び(6S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6-(メチルアミノ)-5,6,7,8-テトラヒドロピラゾロ[5,1-b][1,3]オキサゼピン-3-スルホンイミド(方法N,7.37分、ピーク3,4.3mg、収率6%)をすべて白色固体として得られた。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.23(s,1H),7.50(s,1H),7.31(s,2H),6.85(s,1H),4.39-4.29(m,1H),4.20-4.14(m,1H),4.11-4.01(m,1H),3.94-3.82(m,1H),2.92-1.86(s,1H),2.77(t,J=7.2 Hz,4H),2.68-2.65(m,4H),2.33(s,3H),1.97-1.85(m,5H),1.74-1.60(m,1H).MS:m/z 445.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.24(s,1H),7.51(s,1H),7.32(s,2H),6.86(s,1H),4.41-4.32(m,1H),4.26-4.19(m,1H),4.14-4.03(m,1H),3.97-3.85(m,1H),2.95-2.90(m,1H),2.78(t,J=7.2 Hz,4H),2.69-2.66(m,4H),2.37(s,3H),1.98-1.88(m,5H),1.77-1.64(m,1H).MS:m/z 445.3(M+H+).
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.25(s,1H),7.50(s,1H),7.31(s,2H),6.85(s,1H),4.41-4.30(m,1H),4.23-4.13(m,1H),4.10-4.00(m,1H),3.91-3.77(m,1H),2.92-1.86(s,1H),2.78(t,J=7.2 Hz,4H),2.68-2.64(m,4H),2.33(s,3H),1.99-1.87(m,5H),1.76-1.62(m,1H).MS:m/z 445.2(M+H+).
実施例133及び実施例134
(S)-4,4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド、及び(R)-4.4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド:
工程1-6’,7’-ジヒドロ-5’H-スピロ[[[1,3]ジチオラン-2,4’-ピラゾロ[1,5-a]ピリジン]の合成:
DCM(168 mL)中の6,7-ジヒドロ-5H-ピラゾロ[1,5-a]ピリジン-4-オン(4.0 g,29.4 mmol)の溶液に、室温で1,2-エタンジチオール(3.7 mL,44.0 mmol)と三フッ化ホウ素酢酸錯体(6.1 mL,43.8 mmol)を加えた。48時間後、反応物を水(200 mL)で急冷した。水層をDCM(200mL×3)で抽出した。合わせた有機層を水(200mL)、食塩水(200mL)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中の0-20%EtOAc)で精製し、6’,7’-ジヒドロ-5’H-スピロ[[1,3]ジチオラン-2,4’-ピラゾロ[1,5-a]ピリジン]を得た。4.2 g、収率67%)を淡黄色のオイルとして使用した。1H NMR(400 MHz,CDCl3)δ=7.43(d,J=2.0 Hz,1H),6.40(d,J=2.0 Hz,1H),4.18(t,J=6.0 Hz,2H),3.58-3.53(m,2H),3.48-3.34(m,2H),2.42(t,J=6.0 Hz,2H),2.28-2.22(m,2H).MS:m/z 212.9(M+H+).
工程2-3-ブロモ-4,4-ジフルオロ-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジンの合成:
DCM(46 mL)中の1,3-ジブロモ-5,5-ジメチル-2,4-イミダゾリジンジオン(23.0 g,80.4 mmol)の溶液に、-78℃でHF-ピリジン滴下(38 mL,421.8 mmol)を加え、次いで6’,7’-ジヒドロ-5’H-スピロ[[1,3]ジチオラン-2,4’-ピラゾロ[1,5-a]ピリジン](4.2 g,19.8 mmol)を添加した。4時間後、反応物を0℃に温め、さらに1時間撹拌した。反応物を水(100 mL)で急冷した。水層をDCM(2×100mL)で抽出した。合わせた有機層を水(100mL)、食塩水(100mL)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-20%EtOAc)で精製し、3-ブロモ-4,4-ジフルオロ-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン(3,13g、収率:67%)を黄色油として得た。1H NMR(400 MHz,CDCl3)δ=7.48(s,1H),4.20(t,J=6.0 Hz,2H),2.43-2.34(m,2H),2.27-2.21(m,2H).MS:m/z 236.9(M+H+).
工程3-4,4-ジフルオロ-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドの合成:
3-ブロモ-4,4-ジフルオロ-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジニン(400 mg,1.69 mmol)のTHF(8 mL)溶液に、n-BuLi(ヘキサン中2.5 M,0.84 mL,2.1 mmol)を窒素雰囲気下、-78℃で滴下添加した。1時間後、THF(8 mL)中のTrtNSO(618 mg,2.02 mmol)の溶液を滴下添加した。反応物は-78℃で20分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。次亜塩素酸tert-ブチル(0.24 mL,2.12 mmol)を0℃で添加した。20分後、NH3ガスを10分間バブリングした。得られた溶液を室温まで温め、さらに16時間撹拌した。反応物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中の0-70%EtOAc)で精製し、4,4-ジフルオロ-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド(315 mg、収率39%)を黄色固体として得た。1H NMR(400 MHz,DMSO-d6):δ=7.43-7.39(m,6H),7.18-7.15(m,6H),7.14-7.08(m,3H),6.33(s,2H),4.16-4.09(m,2H),2.40-2.32(m,2H),2.10-2.04(m,2H).MS:m/z 501.1(M+Na+).
工程4-5 - 4,4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7の合成-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドアミド:
工程3でN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドを4,4-ジフルオロ-N’-トリチル-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドに置き換えることにより、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド(実施例100及び実施例101)の調製に記載された一般的な手順を用いて4,4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドを調製した。
工程6-(S)-4,4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド、及び(R)-4.4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミドの合成(実施例133及び実施例134):
4,4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド(78 mg,0.18 mmol)をキラルSFC(キラルパック AS(250 mm * 30 mm,10 um)、超臨界 CO2 / EtOH+0.1% NH4OH=65/35;70 mL/min)で分離し、(S)-4,4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド(方法C,3.31分、ピーク1,11.1mg、収率14%)と(R)-4,4-ジフルオロ-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-4,5,6,7-テトラヒドロピラゾロ[1,5-a]ピリジン-3-スルホンイミド(方法C,3.55分、ピーク2,14.5mg、収率18%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.21(s,1H),7.85(s,1H),7.41(s,2H),6.85(s,1H),4.26(t,J=6.0 Hz,2H),2.76(t,J=7.2 Hz,4H),2.67(t,J=7.2 Hz,4H),2.48-2.40(m,2H),2.17-2.10(m,2H),1.95-1.88(m,4H).MS:m/z 436.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.21(s,1H),7.85(s,1H),7.41(s,2H),6.85(s,1H),4.26(t,J=6.0 Hz,2H),2.76(t,J=7.2 Hz,4H),2.67(t,J=6.8 Hz,4H),2.48-2.40(m,2H),2.17-2.10(m,2H),1.96-1.86(m,4H).MS:m/z 436.1(M+H+).
実施例135、実施例136、実施例137及び実施例138
(S)-6,6-ジメチル-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.(S)-6,6-ジメチル-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド.R)-6,6-ジメチル-N’-((((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(R)-6.6-ジメチル-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド:
工程1-2-6,6-ジメチル-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
工程3で3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジンを8-イソシアナト-1-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンに置き換えることにより、(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例76及び実施例77)の調製に記載された一般的な手順を用いて6,6-ジメチル-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを調製した。
工程3-(S)-6,6-ジメチル-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(S)-6,6-ジメチル-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(R)-6,6-ジメチル-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-6,6-ジメチル-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成(実施例135、実施例136、実施例137及び実施例138):
6,6-ジメチル-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(95 mg,0.21 mmol)をキラルSFC(Chiralpak AD(250 mm*30 mm,10 um),Supercritical CO2 / MeOH+0.1% NH4OH=40/60;70 mL/min)で分離し、(S)-6,6-ジメチル-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法O,5.58分、ピーク1,17.8 mg、収率19%),(S)-6,6-ジメチル-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法O,6.28分、ピーク2,12.9 mg、収率13%),(R)-6,6-ジメチル-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法O,7.67分、ピーク3,18.4 mg、収率19%),(R)-6,6-ジメチル-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法O,8.39分、ピーク4,12.7 mg、収率13%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.04(s,1H),7.52(s,1H),7.24(s,2H),6.83(s,1H),4.05(s,2H),3.85(s,2H),2.89-2.73(m,4H),2.70-2.55(m,3H),2.17-2.05(m,1H),1.98-1.85(m,2H),1.60-1.49(m,1H),1.05-1.01(m,9H).MS:m/z 444.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.06(s,1H),7.52(s,1H),7.26(s,2H),6.84(s,1H),4.06(s,2H),3.86(s,2H),2.89-2.73(m,4H),2.70-2.55(m,3H),2.17-2.05(m,1H),1.98-1.85(m,2H),1.60-1.49(m,1H),1.06-1.01(m,9H).MS:m/z 444.1(M+H+).
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.06(s,1H),7.52(s,1H),7.25(s,2H),6.83(s,1H),4.08(s,2H),3.83(s,2H),2.89-2.73(m,4H),2.70-2.55(m,3H),2.17-2.07(m,1H),1.99-1.84(m,2H),1.60-1.50(m,1H),1.06-1.00(m,9H).MS:m/z 444.1(M+H+).
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.07(s,1H),7.52(s,1H),7.25(s,2H),6.84(s,1H),4.05(s,2H),3.86(s,2H),3.28-3.25(m,1H),2.87-2.72(m,4H),2.70-2.51(m,2H),2.15-2.07(m,1H),1.99-1.85(m,2H),1.61-1.53(m,1H),1.06-1.01(m,9H).MS:m/z 444.1(M+H+).
実施例139及び実施例140
(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド:
工程1-tert-ブチル3-ヒドロキシ-1H-ピラゾール-1-カルボキシレートの合成:
DCM(300 mL)中の1H-ピラゾール-3(2H)-オン(20.0 g,238 mmol)の溶液に、0℃でトリエチルアミン(37 mL,267 mmol)を加えた。10分後、DCM(100 mL)中のBoc2O(57.11 g,262 mmol)を滴下添加した。添加後、反応物を室温まで温め、16時間撹拌した。反応物を減圧下で濃縮し、粗残渣を水(100mL)に溶解した。水層をEtOAc(200mL×2)で抽出した。合わせた有機層を、Na2SO4上で乾燥させ、フィルタにかけ、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(0-5%MeOH in DCM)で精製し、黄色固体としてtert-ブチル3-ヒドロキシ-1H-ピラゾール-1-カルボキシレート(2.8 g、収率6%)を得た。1H NMR(400 MHz,DMSO-d6):δ=10.92(s,1H),7.97(d,J=3.2 Hz,1H),5.89(d,J=2.8 Hz,1H),1.53(s,9H).
工程2-tert-ブチル3-((1-エトキシ-2-メチル-1-オキソプロパン-2-イル)オキシ)-1H-ピラゾール-1-カルボキシレートの合成:
MeCN(56 mL)中のtert-ブチル3-ヒドロキシ-1H-ピラゾール-1-カルボキシレート(2.8 g,15.2 mmol)の溶液に、窒素雰囲気下、室温でK2CO3(4.2 g,30.4 mmol)を加えた。反応物を80℃で加熱した。1時間後、2-ブロモ-2-メチルプロパノエートエチル(3.0g,15.2mmol)を加え、混合物を80℃で16時間撹拌した。室温まで冷却した後、反応混合物を濾過し、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中20%EtOAc)で精製し、tert-ブチル3-((1-エトキシ-2-メチル-1-オキソプロパン-2-イル)オキシ)-1H-ピラゾール-1-カルボキシレート(3.1 g、収率:68%)を黄色油として得た。1H NMR(400 MHz,CDCl3):δ=7.84(d,J=2.8 Hz,1H),5.87(d,J=3.2 Hz,1H),4.22(q,J=6.8 Hz,2H),1.70(s,6H),1.59(s,9H),1.23(t,J=7.2 Hz,3H).
工程3-2-((1H-ピラゾール-5-イル)オキシ)-2-メチルプロパン-1-オールの合成:
THF(90 mL)中のLiAlH4(1.2 g,31.17 mmol)の懸濁液に、THF(20 mL)中のtert-ブチル3-((1-エトキシ-2-メチル-1-オキソプロパン-2-イル)オキシ)-1H-ピラゾール-1-カルボキシレート(3.1 g,10.39 mmol)の溶液を0℃で滴下し、窒素雰囲気下で添加した。添加後、反応混合物を室温まで温め、さらに30分間撹拌した。飽和水性Na2SO4を添加して反応物を急冷した。得られた混合物をNa2SO4上で乾燥させた。固形物を濾過により除去し、濾液を濃縮して2-((1H-ピラゾール-5-イル)オキシ)-2-メチルプロパン-1-オール(1.5 g、収率92%)を得て、これをさらに精製することなく次の工程で使用した。1H NMR(400 MHz,CDCl3):δ=9.45(s,1H),7.39(d,J=2.4 Hz,1H),5.80(d,J=2.4 Hz,1H),4.85(s,1H),3.63(s,2H),1.37(s,6H).
工程4- 2-((1H-ピラゾール-5-イル)オキシ)-2-メチルプロピルメタンスルホン酸の合成:
2-((1H-ピラゾール-5-イル)オキシ)-2-メチルプロパン-1-オール(1.1 g,7.04 mmol)及びトリエチルアミン(2.93 mL,21.13 mmol)のDCM(33 mL)中のスチリル溶液に、MsCl(0.5 mL,7.04 mmol)を窒素雰囲気下、0℃で加えた。1時間後、水(10 mL)を加えた。水層をDCM(50mL×3)で抽出した。合わせた有機層を、Na2SO4上で乾燥させ、フィルタにかけ、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(DCM中0-5%MeOH)で精製し、2-((1H-ピラゾール-5-イル)オキシ)-2-メチルプロピルメタンスルホン酸塩(600mg、収率14%)を黄色油として得た。MS:m/z 234.9(M+H+).
工程5-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾールの合成:
2-((1H-ピラゾール-5-イル)オキシ)-2-メチルプロピルメタンスルホン酸塩(500 mg,0.79 mmol)のDMF(10 mL)中の溶液に、窒素雰囲気下、0℃でNaH(鉱油中60%,38 mg,0.95 mmol)を加えた。添加後、反応物を室温まで温め、さらに12時間撹拌した。反応物を0℃まで冷却し、飽和水性NH4Cl(3 mL)を加えた。反応混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-20%EtOAc)で精製し、2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール(180mg、収率50%)を無色油として得た。1H NMR(400 MHz,CDCl3):δ=7.36(d,J=2.0 Hz,1H),5.30(d,J=1.6 Hz,1H),4.03(s,2H),1.63(s,6H).
工程6-7-ブロモ-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾールの合成:
2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール(150 mg,1.09 mmol)のMeCN(5 mL)溶液に、0℃でNBS(193 mg,1.09 mmol)を加えた。添加後、反応物を室温まで温めた。1時間後、反応混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中の0-30%EtOAc)で精製し、白色固体として7-ブロモ-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール(120mg、収率:51%)を得た。1H NMR(400 MHz,CDCl3):δ=7.32(s,1H),4.07(s,2H),1.67(s,6H).
工程7-2,2-ジメチル-N’-トリチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成:
7-ブロモ-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール(120 mg,0.55 mmol)のTHF(5 mL)溶液に、n-BuLi(ヘキサン中2.5 M,0.3 mL,0.61 mmol)を窒素雰囲気下、-78℃で滴下して加えた.30分後、THF(1 mL)中のTrtNSO(186 mg,0.61 mmol)の溶液を滴下添加した。反応物は-78℃で30分間撹拌した後、0℃の氷浴に入れ、さらに10分間撹拌した。次亜塩素酸tert-ブチル(0.1mL,0.6mmol)を0℃で加えた。30分後、NH3ガスを10分間バブリングした。得られた溶液を室温まで温め、さらに16時間撹拌した。混合物を濃縮し、粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中0-80%EtOAc)で精製し、白色固体として2,2-ジメチル-N’-トリチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(120mg,収率50%)を得た。MS:m/z 481.1(M+Na+).
工程8-9-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成:
工程3でN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドを2,2-ジメチル-N’-トリチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミドに置き換えることにより、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]チアジン-3-スルホンイミドアミド(実施例100及び実施例101)の調製に記載された一般的な手順を用いてN’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドを調製した。
工程10-(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド、及び(R)-N’-((1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成(実施例139及び実施例140):
N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(60 mg,0.14 mmol)をキラルSFC(Phenomenex セルロース 2(250 mm*30 mm,10 um),Supercritical CO2 / EtOH+0.1% NH4OH=60/40;70 mL/min)で分離し、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド(方法P,4.31分、ピーク1,21.5 mg、収率36%)と(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,2-ジメチル-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド(方法P,4.91分、ピーク2,17.5 mg、収率29%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.17(s,1H),7.54(s,1H),7.31(s,2H),6.85(s,1H),4.15(s,2H),2.77(t,J=6.8 Hz,4H),2.68(t,J=6.8 Hz,4H),1.96-1.86(m,4H),1.60(d,J=5.6 Hz,6H).MS:m/z 416.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.17(s,1H),7.54(s,1H),7.29(s,2H),6.85(s,1H),4.15(s,2H),2.77(t,J=7.2 Hz,4H),2.68(t,J=6.8 Hz,4H),1.96-1.88(m,4H),1.60(d,J=5.6 Hz,6H).MS:m/z 416.1(M+H+).
実施例141及び実施例142
(R)-N’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S)-N’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
工程1-3-イソシアナト-2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデンの合成:
2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-アミン(WO2019023147,20 mg,0.13 mmol)とトリエチルアミン(0.03 mL,0.19 mmol)のTHF(0.5 mL)中の溶液に、トリホスゲン(19 mg,0.06 mmol)を室温で加えた。1時間後、反応混合物をセライトの短いパッド上で濾過した。セライトパッドをTHF(2mL)で洗浄した。濾液を濃縮し、3-イソシアナト-2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン(20mg、収率86%)を淡黄色油として得た。
工程2-3-N’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成.:
工程1で3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジンを3-イソシアナト-2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデンに置き換えることにより、(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(実施例102及び実施例103)の調製に記載された一般的な手順を用いてN’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドを調製した。MS:m/z 388.0(M+H+).
工程4-(R)-N’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド、及び(S)-N’-((2.4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成(実施例141及び実施例142):
N’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドをキラル(Chiralpak AS(250 mm * 30mm,10 um);Supercritical CO2 / EtOH+0.1% NH4OH=65/35;70 mL/min)で精製し、(R)-N’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法C,3.65分、ピーク1,1mg、収率9%)と(S)-N’-((2,4,5,6-テトラヒドロ-1H-シクロブタ[f]インデン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法C,3.87分、ピーク2,1.1mg、収率10%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,CDCl3):δ=7.68(s,1H),6.72(s,2H),4.48-4.44(m,2H),4.18-4.14(m,2H),3.25-3.20(m,2H),2.98-2.95(m,2H),2.91-2.87(m,2H),2.75-2.70(m,2H),2.33-2.28(m,2H),2.06-2.00(m,2H).MS:m/z 388.0(M+H+).
ピーク2:1H NMR(400 MHz,CDCl3):δ=7.68(s,1H),6.72(s,1H),6.69(s,1H),4.48-4.44(m,2H),4.20-4.15(m,2H),3.25-3.20(m,2H),3.00-2.95(m,2H),2.90(t,J=7.2 Hz,2H),2.75(t,J=7.2 Hz,2H),2.35-2.29(m,2H),2.08-2.02(m,2H).MS:m/z 388.0(M+H+).
実施例143、実施例144、実施例145、及び実施例146
(S)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド.(S)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド.R)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド、及び(R)-N’-((S)-3-メチル-1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド:
工程1-2-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミドの合成:
工程2で4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを8-イソシアナト-1-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンに置き換えることにより、(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド及び(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド(実施例124及び実施例125)の調製に記載された一般的な手順でN’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミドを調製した。
工程3-(S)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド.(S)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド、(R)-N’-((R)-3-メチル-1.2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド、及び(R)-N’-(((S)-3-メチル-1,2,3,5,6.7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドの合成(実施例143、実施例144、実施例145及び実施例146):
N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(200 mg,0.50 mmol)はキラルSFC(キラルセル AD(250 mm*30 mm,5 um),Supercritical CO2 / MeOH+0.1% NH4OH=65/35;50 mL/min)により分離され、(S)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミドアミド(方法Q,5.25分、ピーク1,4mg、収率2%),(S)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(方法Q,5.38分、ピーク2,5mg、収率2.5%).,((R)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(方法Q,5.53分、ピーク3,3mg、収率1.5%)及び(R)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-2,3-ジヒドロピラゾロ[5,1-b]オキサゾール-7-スルホンイミド(方法Q,5.67分、ピーク4,5mg、収率2.5%)はすべて白色固体として得られた。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.12(s,1H),7.52(s,1H),7.32(s,2H),6.84(s,1H),5.22-5.12(m,2H),4.33(t,J=8.0 Hz,2H),2.89-2.72(m,5H),2.70-2.55(m,2H),2.16-2.06(m,1H),1.98-1.88(m,2H),1.62-1.54(m,1H),1.04(d,J=6.8 Hz,3H).MS:m/z 402.2(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.10(s,1H),7.52(s,1H),7.32(s,2H),6.84(s,1H),5.21-5.15(m,2H),4.32(t,J=8.0 Hz,2H),2.86-2.72(m,5H),2.70-2.55(m,2H),2.14-2.05(m,1H),1.98-1.89(m,2H),1.62-1.55(m,1H),1.03(d,J=6.8 Hz,3H)MS:m/z 402.2(M+H+).
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.11(s,1H),7.52(s,1H),7.32(s,2H),6.84(s,1H),5.21-5.15(m,2H),4.32(t,J=8.4 Hz,2H),2.87-2.74(m,5H),2.70-2.60(m,2H),2.14-2.05(m,1H),1.98-1.86(m,2H),1.62-1.53(m,1H),1.03(d,J=6.4 Hz,3H).MS:m/z 402.1(M+H+).
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.12(s,1H),7.52(s,1H),7.32(s,2H),6.84(s,1H),5.23-5.16(m,2H),4.33(t,J=8.4 Hz,2H),2.89-2.73(m,5H),2.70-2.55(m,2H),2.14-2.06(m,1H),1.98-1.88(m,2H),1.62-1.54(m,1H),1.04(d,J=6.8 Hz,3H).MS:m/z 402.2(M+H+).
実施例147、実施例148、実施例149、及び実施例150
(S,6S)-6-メトキシ-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(S,6S)-6-メトキシ-N’-(((S)-3-メチル-1 2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(R,6S)-6-メトキシ-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-6-メトキシ-N’-(((S)-3-メチル-1 2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-2 -(6S)-6-メトキシ-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6の合成,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド:
(6S)-6-メトキシ-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドは、(S)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(S)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(R)-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例126、実施例127、実施例128及び実施例129)の調製に記載された一般的な手順を用いて、工程4においてN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドに置き換えて調製した。
工程3-(S,6S)-6-メトキシ-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(S,6S)-6-メトキシ-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(R,6S)-6-メトキシ-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-6-メトキシ-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成(実施例147、実施例148、実施例149及び実施例150):
(6S)-6-メトキシ-N’-((3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(80 mg,0.18 mmol)はキラルSFC(Chiralpak AD(250 mm * 30 mm,10 um),Supercritical CO2 / EtOH+0.1% NH4OH=55/45;70 mL/min)により分離され、(S,6S)-6-メトキシ-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法I,3.06分、ピーク1,13.7mg、収率17%),(S,6S)-6-メトキシ-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法I,4.19分、ピーク2,6.5 mg、収率8%),(R,6S)-6-メトキシ-N’-(((R)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法I,4.90分、ピーク3,5.5 mg、収率7%)、及び(R,6S)-6-メトキシ-N’-(((S)-3-メチル-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法I,6.08分、ピーク4,14 mg、収率18%)はすべて白色固体として得られた。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.11(s,1H),7.52(s,1H),7.29(s,2H),6.84(s,1H),4.60-4.56(m,1H),4.30-4.15(m,3H),4.04-4.01(m,1H),3.28-3.24(s,3H),2.86-2.75(m,4H),2.71-2.66(m,1H),2.64-2.55(m,2H),2.18-2.06(m,1H),1.96-1.87(m,2H),1.59-1.54(m,1H),1.03(d,J=6.8 Hz,3H).MS:m/z 446.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.12(s,1H),7.51(s,1H),7.29(s,2H),6.84(s,1H),4.60-4.56(m,1H),4.31-4.16(m,3H),4.04-4.01(m,1H),3.28-3.24(m,3H),2.90-2.74(m,4H),2.71-2.65(m,1H),2.64-2.53(m,2H),2.15-2.06(m,1H),1.99-1.85(m,2H),1.59-1.54(m,1H),1.04(d,J=6.8 Hz,3H).MS:m/z 446.2(M+H+).
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.12(s,1H),7.50(s,1H),7.27(s,2H),6.84(s,1H),4.60-4.56(m,1H),4.31-4.15(m,3H),4.04-4.01(m,1H),3.28-3.24(m,3H),2.89-2.74(m,4H),2.71-2.64(m,1H),2.61-2.52(m,2H),2.16-2.07(m,1H),2.00-1.84(m,2H),1.61-1.53(m,1H),1.05(d,J=6.8 Hz,3H).MS:m/z 446.2(M+H+).
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.11(s,1H),7.50(s,1H),7.24(s,2H),6.84(s,1H),4.60-4.56(m,1H),4.26-4.16(m,3H),4.04-4.01(m,1H),3.32-3.31(m,3H),2.86-2.75(m,4H),2.73-2.67(m,1H),2.63-2.55(m,2H),2.18-2.06(m,1H),1.98-1.87(m,2H),1.60-1.54(m,1H),1.05(d,J=6.8 Hz,3H).MS:m/z 446.2(M+H+).
実施例151及び実施例152
(S,6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-N-(2,3-ジヒドロ-1H-インデン-4-イル)ピバルアミドの合成:
DCM(30mL)中の2,3-ジヒドロ-1H-インデン-4-アミン(3 g 22.5 mmol)及びトリエチルアミン(4.7 mL,33.8 mmol)の溶液に、室温でピバロイルクロリド(3.1 mL,24.8 mmol)を滴下して加えた。1時間後、水(50 mL)を加えた。水層をDCM(50mL×3)で抽出した。合わせた有機層をNa2SO4上で乾燥し、濾過し、濃縮して、N-(2,3-ジヒドロ-1H-インデン-4-イル)ピバルアミド(4.8 g、収率:98%)を白色固体として得て、これをさらに精製することなく次の工程で使用した。1H NMR(400 MHz,CDCl3):δ 7.82(d,J=8.0 Hz,1H),7.23(s,1H),7.16(t,J=8.0 Hz,1H),7.02(d,J=7.6 Hz,1H),2.96(t,J=7.2 Hz,2H),2.81(t,J=7.6 Hz,2H),2.26-2.05(m,2H),1.33(s,9H).MS:m/z 218.2(M+H+).
工程2-N-(7-ブロモ-2,3-ジヒドロ-1H-インデン-4-イル)ピバルアミドの合成:
MeCN(40 mL)中のN-(2,3-ジヒドロ-1H-インデン-4-イル)ピバルアミド(4.8 g,22.1 mmol)の溶液に、室温でNBS(4.7 g,26.5 mmol)を加えた。15時間後、反応物を減圧下で濃縮し、粗残渣をDCM(50mL)に溶解した。有機層を飽和水性Na2CO3(50 mL×3)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮してN-(7-ブロモ-2,3-ジヒドロ-1H-インデン-4-イル)ピバルアミド(6.5 g、収率:99%)を白色固体として得て、これをさらに精製することなく次の工程で使用した。MS:m/z 296.1(M+H+).
工程3-7-ブロモ-2,3-ジヒドロ-1H-インデン-4-アミンの合成:
N-(7-ブロモ-2,3-ジヒドロ-1H-インデン-4-イル)ピバルアミド(6.5 g,21.9 mmol)を濃塩酸(100 mL)に溶解し、100℃で36時間加熱した。室温まで冷却した後、水(50 mL)を加え、混合物を濾過した。この固体をEtOAc(20 mL×3)で洗浄し、茶色の固体として7-ブロモ-2,3-ジヒドロ-1H-インデン-4-アミン(3.44 g、収率:74%)を得て、これをさらに精製することなく次の工程で使用した。1H NMR(400 MHz,DMSO-d6):δ 7.41(d,J=8.4 Hz,1H),7.11(d,J=8.0 Hz,1H),3.06(t,J=7.6 Hz,2H),2.90(t,J=7.2 Hz,2H),2.13-1.99(m,2H).MS:m/z 212.0(M+H+).
工程4-7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-アミンの合成:
H2O(5 mL)及び1,4-ジオキサン(40 mL)中の7-ブロモ-2,3-ジヒドロ-1H-インデン-4-アミン(2.7 g,12.7 mmol)の溶液に、窒素雰囲気下で(2-メトキシピリジン-4-イル)ボロン酸(2.3 g,15.3 mmol),K2CO3(5.3 g,38.2 mmol)及びPd(dppf)Cl2(0.9 g,1.3 mmol)を添加した。混合物を80℃で2時間撹拌した。室温まで冷却した後、反応物をH2O(50 mL)で希釈した。水層をEtOAc(50mL×3)で抽出した。合わせた有機層を食塩水(50 mL x 2)で洗浄し、Na2SO4上で乾燥し、ろ過し、濃縮した。粗残渣をシリカゲルカラム(石油エーテル中0-30%EtOAc)で精製し、7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-アミンを黄色固体として得た。1H NMR(400 MHz,CDCl3):δ 8.15(d,J=5.2 Hz,1H),7.11(d,J=8.4 Hz,1H),6.95(d,J=2.0,5.2 Hz,1H),6.78(s,1H),6.62(d,J=8.0 Hz,1H),3.97(s,3H),3.74(s,2H),3.03(t,J=7.6 Hz,2H),2.78(t,J=7.2 Hz,2H),2.17-2.04(m,2H).MS:m/z 241.0(M+H+).
工程5-4-(7-イソシアナト-2,3-ジヒドロ-1H-インデン-4-イル)-2-メトキシピリジンの合成:
THF(5 mL)中の7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-アミン(150 mg,0.6 mmol)及びトリエチルアミン(0.1 mL,0.7 mmol)の溶液に、室温でトリホスゲン(67 mg,0.2 mmol)を加えた。1時間後、混合物をシリカゲルのプラグを通して濾過し、トリエチルアミンヒドロキオン化物を除去した。濾液を濃縮して、4-(7-イソシアナト-2,3-ジヒドロ-1H-インデン-4-イル)-2-メトキシピリジン(135mg,81%)を黄色固体として得て、これをさらに精製することなく次の工程で使用した。
工程6-7-(6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
工程3でN’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]チアジン-3-スルホンイミドアミド及び4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンを(6S)-6-メトキシ-N’-トリチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び4-(7-イソシアナト-2,3-ジヒドロ-1H-インデン-4-イル)-2-メトキシピリジンに置き換えることにより、(S)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]チアジン-3-スルホンイミドアミド及び(R)-N’-((1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]チアジン-3-スルホンイミドアミド(実施例100及び実施例101)の調製に記載された一般的な手順を用いて(6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを調製した。
工程8-(S,6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R,6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成(実施例151及び実施例152):
(6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(60 mg,0.12 mmol)をキラルSFC(キラルセル OJ(250 mm * 30 mm,5 um),Supercritical CO2 / IPA+0.1% NH4OH=60/40;60 mL/min)で分離し、(S,6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法R,1.84分、ピーク1,4 mg、収率5%)と(R,6S)-6-メトキシ-N’-((7-(2-メトキシピリジン-4-イル)-2,3-ジヒドロ-1H-インデン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(方法R,2.25分、ピーク2,5 mg、収率5%)を両方とも白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.24(s,1H),8.17(d,J=5.6 Hz,1H),7.64-7.60(m,2H),7.36(s,2H),7.16(d,J=8.4 Hz,1H),7.05(d,J=4.8 Hz,1H),6.81(s,1H),4.62-4.58(m,1H),4.32-4.18(m,3H),4.05-4.01(m,1H),3.87(s,3H),3.41-3.37(m,3H),2.94(t,J=7.6 Hz,2H),2.85-2.80(m,2H),1.99-1.91(m,2H).MS:m/z 499.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.25(s,1H),8.16(d,J=5.2 Hz,1H),7.65-7.60(m,2H),7.40(s,2H),7.16(d,J=8.4 Hz,1H),7.05(d,J=5.6 Hz,1H),6.81(s,1H),4.62-4.58(m,1H),4.34-4.18(m,3H),4.05-4.01(m,1H),3.87(s,3H),3.37-3.36(m,3H),2.94(t,J=7.6 Hz,2H),2.85-2.80(m,2H),1.99-1.90(m,2H).MS:m/z 499.1(M+H+).
実施例153、実施例154、実施例155、及び実施例156
(S)-N’-(((S)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(R)-N’-(((S)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(S)-N’-(((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-(((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド
工程1-8-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-1-オールの合成:
8-ニトロ-3,5,5,6,7-テトラヒドロ-2H-s-インダセン-1-オン(7.9 g,36.37 mmol)のMeOH(100 mL)溶液にNaBH4(6.9 g,181.84 mmol)を窒素雰囲気下0℃で加えた。添加後、反応物を室温まで温めた。1時間後、溶媒をブクオで留去し、粗残渣にH2O(10 mL)を加えた。水層をEtOAc(20mL×2)で抽出した。合わせた有機層をブライン(40 mL)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮した。粗残渣をシリカゲルカラムクロマトグラフィー(石油エーテル中15%EtOAc)で精製し、8-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-1-オール(7.5g、収率94%)を淡黄色油として得た。
工程2-8-ニトロ-1,2,3,5-テトラヒドロ-s-インダセンの合成:
8-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-1-オール(7.5 g,34.21 mmol)のトルエン(100 mL)中の溶液を入れたディ-ン-スタ-クトラップを備えたフラスコに、TsOH(3.3 g,17 mmol)を加えた。反応物を110℃で2時間加熱した。室温まで冷却した後、混合物をEtOAc(50 mL)で希釈した。有機層を飽和水性NaHCO3(100 mL×2)、ブライン(100 mL)で洗浄し、無水Na2SO4上で乾燥し、ろ過し、濃縮した。粗残渣をヘキサンでトリチュレ-ションし、淡黄色固体として8-ニトロ-1,2,3,5-テトラヒドロ-s-インダセン(5.9 g、収率86%)を得た。1H NMR(400 MHz,CDCl3)δ=7.53(s,1H),7.49(d,J=6.0 Hz,1H),6.79-6.77(m,1H),3.45(s,2H),3.35(t,J=7.6 Hz,2H),3.02(t,J=7.6 Hz,2H),2.21-2.16(m,2H).
工程3-2-ニトロ-1a,3,4,5,7,7a-ヘキサヒドロ-s-インダセノ[1,2-b]オキシレンの合成:
8-ニトロ-1,2,3,5-テトラヒドロ-s-インダセン(5.9 g,29.32 mmol)のDCM(80 mL)溶液に、窒素雰囲気下0℃で85% m-CPBA(9.7 g,38.12 mmol)を加えた。添加後、反応物を室温まで温めた。12時間後、反応混合物を飽和NaHCO3水溶液(80 mL)とNa2S2O3水溶液(80 mL)で洗浄した。有機層を無水Na2SO4上で乾燥し、濾過し、濃縮した。粗残渣をシリカゲルカラム(石油エーテル中10%EtOAc)で精製し、白色固体として2-ニトロ-1a,3,4,5,7,7a-ヘキサヒドロ-s-インダセノ[1,2-b]オキシレン(4.2 g、収率66%)を得た。
工程4-4-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-2-オールの合成:
2-ニトロ-1a,3,4,5,7,7a-ヘキサヒドロ-s-インダセノ[1,2-b]オキシレン(4.0 g,18.41 mmol)のDCE(60 mL)溶液に、室温でZnI2(8.8 g,27.62 mmol)及びNaBH3CN(9.3 g,147.32 mmol)を加えた。反応物を80℃まで4時間加熱した。室温まで冷却した後、混合物を水性6 N HCl(10 mL)に注いだ。水層をDCM(50mL×3)で抽出した。合わせた有機層をNa2SO4上で乾燥し、濾過し、濃縮した。残渣をシリカゲルカラム(石油エーテル中20%EtOAc)で精製し、白色固体として4-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-2-オール(3.4 g、収率84%)を得た。1H NMR(400 MHz,DMSO-d6)δ=7.43(s,1H),4.94(s,1H),4.51(s,1H),3.29-3.25(m,1H),3.18-3.05(m,4H),2.89(t,J=7.6 Hz,2H),2.83-2.75(m,1H),2.10-2.04(m,2H).
工程5-2-フルオロ-4-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンの合成:
4-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-2-オール(800 mg,3.65 mmol)のDCM(20 mL)溶液に、DAST(1.50 mL,10.95 mmol)を窒素雰囲気下、0℃で滴下添加した。1時間後、飽和水性Na2CO3(5 mL)を慎重に添加した。有機層をブライン(50 mL)で洗浄し、Na2SO4上で乾燥し、濾過し、濃縮した。残渣をシリカゲルカラム(石油エーテル中15%EtOAc)で精製し、黄色油として2-フルオロ-4-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(370mg、収率46%)を得た。1H NMR(400 MHz,CDCl3)δ=7.39(s,1H),5.63-5.45(m,1H),3.70-3.63(m,2H),3.58-3.25(m,4H),3.21-2.98(m,2H),2.18-2.13(m,2H).
工程6-2-フルオロ-1,2,3,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミンの合成:
2-フルオロ-4-ニトロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン(370 mg,1.67 mmol)と10% Pd on carbon(178 mg,1.67 mmol)のEtOH(8 mL)中の混合物を、水素雰囲気下で室温で撹拌した(15 psi).2時間後、反応混合物をセライトのパッドを通して濾過した。2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(原油350mg)を黄色油として得て、これをさらに精製することなく次の工程で使用した。1H NMR(400 MHz,CDCl3)δ=6.65(s,1 H),5.60-5.44(m,1 H),3.52(s,2H),3.23-3.13(m,2 H),3.07-2.95(m,2H),2.88(t,J=7.6 Hz,2H),2.71(t,J=7.6 Hz,2H),2.15-2.05(m,2H).MS:m/z 192.1(M+H+).
工程7-2-フルオロ-4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンの合成:
2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-アミン(150 mg,0.78 mmol)及びトリエチルアミン(0.11 mL,0.78 mmol)の無水THF(9 mL)中の溶液に、室温でトリホスゲン(93 mg,0.31 mmol)を加えた。反応物を70℃で2時間加熱した。室温まで冷却した後、混合物をシリカゲルのプラグを通して濾過し、トリエチルアミン塩酸塩を除去した。濾液を次の工程で直接使用した。
工程8-9-N’-((2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
工程3で3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジンを2-フルオロ-4-イソシアナト-1,2,3,5,6,7-ヘキサヒドロ-s-インダセンに置き換えることにより、(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ [5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(実施例76及び実施例77)の調製に記載された一般的な手順でN’-((2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミドを調製した。
工程10-(S)-N’-(((S)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(R)-N’-(((S)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド、(S)-N’-(((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-(((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成(実施例153、実施例154、実施例155、及び実施例156):
N’-((2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[ 5,1-b] [1,3]オキサジン-3-スルホンイミドアミド(180 mg,0.40 mmol)をキラルSFC(Chiralpak AD(250 mm * 30 mm,10 um);Supercritical CO2 / EtOH+0.1% NH4OH=55/45;60 mL/min)で精製し、(S)-N’-((((S)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法G,4.97分,ピーク 3,ピーク 3,21.3 mg,収率12%),(R)-N’-(((S)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法G,5.27分、ピーク4,10.8 mg、収率6%)及びN’-(((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(ピーク1とピーク2の混合物、44 mg、収率24%)を全て白色固体として得た。N’-(((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(ピーク1とピーク2の混合物、44mg)をキラルSFC(キラルセル OJ(250 mm * 30 mm,5 um);超臨界 CO2 / IPA+0.1% NH4OH=75/25,60 mL/min)で精製して(S)-N’-((((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法G,4,14分、ピーク1,11.2 mg、収率25%)、及び(R)-N’-(((R)-2-フルオロ-1,2,3,5,6,7-ヘキサヒドロ-s-インダセン-4-イル)カルバモイル)-6,6-ジメチル-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法G,4.73分、ピーク2,14 mg、収率32%)を白色固体として得た。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6):δ=8.30(s,1H),7.55(s,1H),7.26(s,2H),6.91(s,1H),5.53-5.33(m,1H),4.07(s,2H),3.87(s,2H),3.23-2.84(m,4H),2.84-2.63(m,4H),1.99-1.88(m,2H),1.04(s,6H).MS:m/z 448.1(M+H+).化合物155
ピーク2:1H NMR(400 MHz,DMSO-d6):δ=8.28(s,1H),7.55(s,1H),7.27(s,2H),6.91(s,1H),5.55-5.33(m,1H),4.07(s,2H),3.86(s,2H),3.25-2.85(m,4H),2.84-2.60(m,4H),2.01-1.87(m,2H),1.03(d,J=6.8 Hz,6H).MS:m/z 448.1(M+H+).化合物156
ピーク3:1H NMR(400 MHz,DMSO-d6):δ=8.27(s,1H),7.55(s,1H),7.27(s,2H),6.91(s,1H),5.55-5.30(m,1H),4.10(s,2H),3.86(s,2H),3.24-2.83(m,4H),2.81-2.65(m,4H),2.00-1.87(m,2H),1.03(d,J=6.8 Hz,6H).MS:m/z 448.1(M+H+).化合物153
ピーク4:1H NMR(400 MHz,DMSO-d6):δ=8.29(s,1H),7.55(s,1H),7.26(s,2H),6.91(s,1H),5.55-5.30(m,1H),4.07(s,2H),3.87(s,2H),3.23-2.85(m,4H),2.84-2.60(m,4H),1.99-1.90(m,2H),1.04(s,6H).MS:m/z 448.1(M+H+).化合物154
実施例157及び実施例158
(S)-N’-(5-(5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1.3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド
工程1-N-(2,3-ジヒドロベンゾフラン-4-イル)アセトアミドの合成:
無水酢酸(40 mL,59.2 mmol)中の2,3-ジヒドロベンゾフラン-4-アミン(4.0 g,29.6 mmol)の混合物を室温で撹拌した。16時間後、反応混合物を濃縮してN-(2,3-ジヒドロベンゾフラン-4-イル)アセトアミド(3.4g、収率65%)を白色固体として得て、これをさらに精製することなく次の工程で使用した。MS:m/z 178.0(M+H+).
工程2-N-(5-ブロモ-2,3-ジヒドロベンゾフラン-4-イル)アセトアミドの合成:
DCM(70 mL)中のN-(2,3-ジヒドロベンゾフラン-4-イル)アセトアミド(3.4 g,19.2 mmol)の溶液に、窒素雰囲気下、0℃でNBS(3.76 g,21.1 mmol)を部分的に添加した。添加後、反応物を室温まで温めた。16時間後、反応混合物を濃縮し、粗残渣をシリカゲルカラム(1%MeOH in DCM)で精製し、N-(5-ブロモ-2,3-ジヒドロベンゾフラン-4-イル)アセトアミド(3.3 g、収率:67%)を白色固体として得た。1H NMR(400 MHz,CDCl3)δ 7.30(d,J=8.4 Hz,1H),7.15(s,1H),6.58(d,J=8.4 Hz,1H),4.61(t,J=8.8 Hz,2H),3.22(t,J=8.8 Hz,2H),2.23(s,3H).
工程3-5-ブロモ-2,3-ジヒドロベンゾフラン-4-アミンの合成:
N-(5-ブロモ-2,3-ジヒドロベンゾフラン-4-イル)アセトアミド(3.3g,12.9mmol)とNaOH(5.15g,128.9mmol)の水(500mL)とEtOH(100mL)の混合物を窒素雰囲気下で90℃で加熱した。80時間後、反応混合物を濃縮してEtOHを除去した。残渣をろ過し、白色固体を酢酸エチル(60 mL)及び水(10 mL)に溶解した。濃縮HClを添加してpHを2.0に調整した。得られた固体を濾過して、5-ブロモ-2,3-ジヒドロベンゾフラン-4-アミン(1.7 g、収率:62%)を白色固体として得て、これをさらに精製することなく次の工程で使用した。1H NMR(400 MHz,DMSO-d6)δ 7.06(d,J=8.4 Hz,1 H),6.00(d,J=8.4 Hz,1 H),4.50(t,J=8.8 Hz,2 H),3.01(t,J=8.8 Hz,2 H).
工程4-5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-アミンの合成:
1,4-ジオキサン(95 mL)及び水(15 mL)中の5-ブロモ-2,3-ジヒドロベンゾフラン-4-アミン(1.7 g,7.94 mmol)の溶液に、窒素雰囲気下で2-メトキシピリジン-4-ボロン酸(1.46 g,9.53 mmol),Pd(dppf)Cl2(581 mg,0.79 mmol)及びNa2CO3(2.52 g,23.8 mmol)を加えた。得られた混合物を80℃で3時間加熱した。室温まで冷却した後、混合物を濾過し、濾液を濃縮した。粗残渣をシリカゲルカラム(石油エーテル中10-20%EtOAc)で精製し、白色固体として5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-アミン(1.8 g、収率94%)を得た。1H NMR(400 MHz,DMSO-d6)δ 8.15(d,J=5.2 Hz,1H),7.00-6.98(m,1H),6.83(d,J=8.0 Hz,1H),6.77(s,1H),6.13(d,J=8.0 Hz,1H),4.92(s,2H),4.53(t,J=8.8 Hz,2H),3.86(s,3H),3.00(t,J=8.8 Hz,2H).
工程5-4-(4-イソシアナト-2,3-ジヒドロベンゾフラン-5-イル)-2-メトキシピリジンの合成:
THF(30 mL)中の5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-アミン(150 mg,0.62 mmol)とトリエチルアミン(0.26 mL,1.86 mmol)の溶液に、トリホスゲン(74 mg,0.25 mmol)を窒素雰囲気下、0℃で1部添加した。1時間後、反応混合物をシリカゲルのプラグを通して濾過し、トリエチルアミン塩酸塩を除去した。この濾液に4-(4-イソシアナト-2,3-ジヒドロベンゾフラン-5-イル)-2-メトキシピリジンを含有させたものを次の工程で直接使用した。
工程6-7-N’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミドの合成:
工程1で3-イソシアナト-2,4-ジイソプロピル-6-メトキシピリジンを4-(4-イソシアナト-2,3-ジヒドロベンゾフラン-5-イル)-2-メトキシピリジンに置き換えて(S)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((2,4-ジイソプロピル-6-メトキシピリジン-3-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3] オキサジン-3-スルホンイミドアミド(実施例102及び実施例103)の調製に記載された一般的な手順でN’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3 ]オキサジン-3-スルホンイミドアミドを調製した。MS:m/z 471.2(M+H+).
工程8-(S)-N’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミド及び(R)-N’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b] [1,3]オキサジン-3-スルホンイミドアミドの合成(実施例157及び実施例158):
N’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(95 mg,0.20 mmol)はキラルSFC(Phenomenex セルロース-2(250 mm * 30 mm,10 um);超臨界 CO2 / MeOH+0.1% NH4OH=45/55;70 mL/min)により分離され、(S)-N’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法G,8.4 mg、収率26%)及び(R)-N’-((5-(2-メトキシピリジン-4-イル)-2,3-ジヒドロベンゾフラン-4-イル)カルバモイル)-6,7-ジヒドロ-5H-ピラゾロ[5,1-b][1,3]オキサジン-3-スルホンイミドアミド(方法G,10.22分、ピーク2,30.8 mg、収率31%)は両方とも白色固体として得られた。各立体異性体には、任意に立体化学を割り当てた。
ピーク1:1H NMR(400 MHz,DMSO-d6)δ=8.19(s,1H),8.09(d,J=5.2 Hz,1H),7.41(s,1H),7.23(s,2H),7.07(d,J=8.4 Hz,1H),6.92(d,J=5.2 Hz,1H),6.74(s,1H),6.70(d,J=8.0 Hz,1H),4.56(t,J=8.8 Hz,2H),4.37(t,J=4.8 Hz,2H),4.11(t,J=6.0 Hz,2H),3.86(s,3H),3.11-3.06(m,2H),2.22-2.13(m,2H).MS:m/z 471.1(M+H+).
ピーク2:1H NMR(400 MHz,DMSO-d6)δ=8.18(s,1H),8.09(d,J=5.2 Hz,1H),7.41(s,1H),7.22(s,2H),7.07(d,J=8.0 Hz,1H),6.92(d,J=5.2 Hz,1H),6.74(s,1H),6.70(d,J=8.0 Hz,1H),4.56(t,J=8.8 Hz,2H),4.37(t,J=4.4 Hz,2H),4.11(t,J=6.0 Hz,2H),3.86(s,3H),3.11-3.06(m,2H),2.24-2.11(m,2H).MS:m/z 471.1(M+H+).
生物学的試験方法
略語:
PBMC:末梢血単核球
KCs:クッパ-細胞
FBS:ウシ胎仔血清
LPS:リポ多糖
NLRP3活性化及び阻害アッセイ
以下のアッセイのいくつかは、一般的な炎症酵素活性化刺激であるナイゲリシンを用いて、NLRP3炎症酵素に対する化合物の阻害活性を決定するために使用した。
実施例B1:細胞培養
リンパ球(T細胞、B細胞、NK細胞)、単球、樹状細胞からなるヒト末梢血単核細胞(PBMC)は、健康なドナ-からヒト末梢血から新鮮に単離されたものである。細胞は、iXCells BiotechnologiesによるIRB承認ドナ-プログラムを通して取得され、そこでは細菌及びウイルス感染について全てのドナ-が試験された。細胞は、フィコ-ル勾配遠心分離を用いて末梢血から精製した。
Disseの空間に存在する特殊な肝臓マクロファ-ジであるヒトクッパ-細胞(クッパ-cell:KCs)は、サムサラサイエンス社が死後に採取した肝臓標本から勾配分離することにより得られた。細胞は、Samsara SciencesによるIRB承認ドナ-プログラムを通して取得し、細菌及びウイルス感染に関して全てのドナ-が陰性であることを試験で確認した。
生物学的実施例 B2:NLRP3インフラマソーム活性化アッセイ
新鮮又は凍結保存されたPMBCをV底96ウェルプレートに0.5-1x10細胞/ウェルで播種し、GlutaMAXサプリメント、4.5g/L D-グルコ-ス、10%ウシ胎児血清(FBS),100mMピルビン酸ナトリウム、1%ペニシリン/ストレプトマイシン、10mM HEPES及び0.05mMのβ-メルカプトエタノールを添加したRPMI 1640培地で5%CO2で37℃で一晩インキュベートした。新鮮に単離された又は凍結保存されたKCs細胞を、0.6-1.5x10cells/wellで平底96ウェルプレートに播種し、GlutaMAXサプリメント、FBS,1%ペニシリン/ストレプトマイシン及び10mM HEPESとRPMI 1640培地中の37℃,5%CO2で一晩インキュベートした。翌日、細胞を100 ng/mLのリポ多糖類(LPS;Sigma Aldrich)でFBSフリ-のRPMI 1640中で3時間プライミングした。プライミング工程の後、培地を除去し、PBMCsを、NLRP3活性化剤の添加に先立ち、FBSフリーの培地中で30分間、試験化合物(0.00017-10uM)又はビヒクル(DMSO)のシリアル濃度でプレインキュベートした。細胞を10uMナイジェリシン(Sigma Aldrich;InvivoGen)で1.5時間刺激し、プレートを1,500rpmで3分間遠心分離して細胞をペレット化し、上清を新しいプレートに移し、その後の実験に使用した。
サイトカインの測定/NLRP3インフラマソーム活性の評価
ELISAアッセイのために、細胞を96ウェルプレートに播種した。試験後、上清を除去し、成熟したIL-1β,IL18及びTNFα(Quantikine ELISA,R&Dシステムズ社製)のレベルを、製造者の指示に従ってELISAにより細胞調整培地中で測定した。
実施例B3:CTG(CellTitre-Glo)アッセイ
化合物で処理した細胞の生存率は、ウェル内の生細胞の数に比例する細胞のATP含有量を測定するCellTiter-Glo(登録商標)アッセイ(Promega,Madison,WI)を用いて測定した。これは、LPS及びナイジェリシンで刺激し、化合物で処理した細胞におけるIL-1βレベルの減少が、細胞傷害性によるものではなく、インフラマソーム経路の阻害によるものであることを立証するためのカウンタ-スクリ-ニングである。NRLP3インフラマソーム活性化を阻害する化合物は、そうでなければ細胞溶解をもたらすであろうNLRP3媒介性ピロプト-シスを遮断することによって、LPS及びナイジェリシン刺激細胞の生存率を最終的に増加させる。
実施例B4:TNF-α
LPS及びニゲリシン刺激細胞のTNFαレベルをHTRFアッセイ(Cisbio,Bedford,MA)により測定した。インフラマソーム経路選択的化合物は、TNFα産生を阻害せず、これはLPS刺激にのみ依存し、TLR4/NFκB経路を介して進行する。TNFα産生の測定はまた、HTRF試薬を妨げる化合物を排除するための技術的なカウンタースクリーニングとしても役立つ。したがって、IL-1β及びTNFαレベルの両方を阻害する化合物は、インフラマソームに対して非選択的であるか、又はHTRFの読み出しを妨害するかのいずれかについてトリア-ジされる。
アッセイ結果
特定の化合物の結果を以下に示す。下表については、A:<100nM;B:100nM-1μM;C:1-10μM;D:>10μM。
実施例B5:PMBC IL-1β HTRFアッセイ
細胞培養及びNLRP3インフラマソーム活性化アッセイ:
ヒト凍結PBMCはStemCells Technologiesから購入した。細胞を37℃のウォーターバスで急速に解凍し、1%ピルビン酸ナトリウム、10mM HEPES,2.5g/Lグルコース及び55μM 2-メルカプトエタノールを含むRPMI 1640培地からなる新鮮なアッセイ培地に再懸濁した。細胞密度は8.1 x 105細胞/mLに調整した。細胞懸濁液中に最終濃度100ng / mLのリポ多糖(E.coli由来のInvivogen Ultrapureリポ多糖、tlrl-3pelps)を添加することにより、細胞をプライミングした。LPSを添加した細胞懸濁液37μLを384ウェルプレートのウェルあたりに播種し、37℃,5%CO2で3時間インキュベートした。プライミング後、PBMCを、37℃及び5%CO2のアッセイ培地中で30分間、20点曲線又はビヒクル(DMSO)のために、40μMの開始濃度に続いて2倍希釈した試験化合物で連続的に希釈したものでプレインキュベートした。次いで、細胞を10μMニゲリシン(Invivogen,tllll-nig-5)で37℃,5%CO2で90分間刺激し、細胞培養上清中のNLRP3依存性インフラマソーム経路及びIL-1β放出を活性化させた。細胞を1200rpmで1分間遠心分離し、40μLの上清を新鮮なプレートに移し、IL-1β分析まで-80℃で保存した。
IL-1β HTRFアッセイ:
16μLの上清を白色384ウェルHTRFプレートに添加し、次いで各ウェルに4μLのHTRFカクテルを添加した。プレートを素早く遠心分離し、密封し、室温で一晩インキュベートした。翌日、HTRFシグナルをPherastarで読み取り、細胞培養上清中のIL-1βの濃度を得るために、メーカーのプロトコルに基づいて665/620の比率を算出した。
実施例B6:THP-1 ASC-GFPスペックアッセイ
細胞培養:
THP-1 ASC-GFP細胞株は、インフラマソーム活性化アッセイのためにInvivogen,San Diegoから購入した。THP-1 ASC-GFP細胞は、37.6kDaのASC::GFP融合タンパク質を安定的に発現しており、NLRP3依存性インフラマソーム経路の活性化後、顕微鏡によるスペック形成のモニタリングを可能にする。細胞は、RPMI1640,2mM L-グルタミン、25mM HEPES及び10%熱不活化ウシ胎児血清からなる増殖培地中で、37℃及び5%CO2で600,000細胞/mLの密度で維持した。細胞を3-4日ごとにパサージュし、最大20パサージュまでのアッセイに使用した。
NLRP3 インフラマソーム活性化アッセイ:
THP-1 ASC-GFP細胞を800rpmで5分間遠心分離して回収した。細胞培養上清を除去し、RPMI1640,2mM L-グルタミン、25mM HEPES及び10%熱不活化ウシ胎児血清からなるアッセイ用培地に1x106細胞/mLの密度で新鮮な培地に細胞を再懸濁した。Phorbol12-ミリステート13-アセテート(PMA)(Invivogen,tlrl-pma)を最終濃度500ng/mlの細胞懸濁液に添加し、十分に混合した。384ウェルプレートのウェルあたり40,000個の細胞を添加し、37℃,5%CO2で一晩マクロファ-ジに分化させた。細胞を1μg/mLのリポ多糖(大腸菌由来のInvivogen超高純度リポ多糖、tlrl-3pelps)をアッセイ培地中で37℃及び5%CO2で3時間プライミングした。プライミング後、培地を除去し、THP-1 ASC-GFP細胞を、40μMの開始濃度で連続的に希釈した試験化合物でプレインキュベ-トし、次いで、20点曲線又はビヒクル(DMSO)を2倍希釈して、37℃及び5%CO2のアッセイ培地中で30分間、20点曲線又はビヒクル(DMSO)を調製した。次いで、細胞を10μMニゲリシン(Invivogen,tlrl-nig-5)で37℃,5%CO2で90分間刺激し、NLRP3依存性インフラマソーム経路とスペック形成を活性化させた。刺激後、細胞を4.8%パラホルムアルデヒド(Electron Microscopy Sciences#15710-S)で固定し、室温で15分間インキュベートした。次に、細胞を100 μLのリン酸緩衝生理食塩水で3回洗浄し、前処理/ブロックバッファ-の存在下で室温で20分間透過処理しました。次に、細胞を100 μLのリン酸緩衝生理食塩水で3回洗浄し、ヘキストの存在下、室温で1時間インキュベートした。ヘキストで染色した後、細胞を100 μLのリン酸緩衝生理食塩水で3回洗浄し、ASCスペック形成のために画像化した。
ASC-GFPスペックのイメージング:
THP-1 ASC-GFP細胞を488及びヘキストチャンネルで画像化した。細胞数にはヘキストチャンネルを使用し、画像化されたフィールド内のGFP ASCスペッククの数を識別するために488チャンネルを使用した。スペックを有する細胞の割合は、GFP陽性スポット数を総細胞数で割って算出した。
追加のアッセイ結果を表B1-a、表B1-b、及び表B1-cに示す。
同等物
本開示は、本明細書に記載されたいくつかの実施形態と関連して記載されているが、その多くの代替案、修正、及び他のバリエ-ションは、当技術分野の通常の当業者には明らかである。そのようなすべての代替案、修正案及び変形案は、本開示の精神及び範囲内に収まるように意図されている。