JP5618038B2 - エリスロポエチン応答性の診断方法 - Google Patents
エリスロポエチン応答性の診断方法 Download PDFInfo
- Publication number
- JP5618038B2 JP5618038B2 JP2007130756A JP2007130756A JP5618038B2 JP 5618038 B2 JP5618038 B2 JP 5618038B2 JP 2007130756 A JP2007130756 A JP 2007130756A JP 2007130756 A JP2007130756 A JP 2007130756A JP 5618038 B2 JP5618038 B2 JP 5618038B2
- Authority
- JP
- Japan
- Prior art keywords
- erythropoietin
- erythropoietin receptor
- antibody
- receptor
- subject
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
Description
前述したように、エリスロポエチンは主に腎臓で生成される165アミノ酸からなる造血ホルモンで、赤血球をつくる骨髄細胞のエリスロポエチン受容体を刺激し、赤血球の産生を増加させる。ちなみにエリスロポエチン受容体は、2つの部分からなり、エリスロポエチンはこれら2つの受容体分子を橋渡しするように結合することで、受容体を刺激し赤血球産生を促す。
発明者らは、エリスロポエチン不応性あるいは低応答性の患者から単離した血清中に、ヒトエリスロポエチン受容体の細胞外ドメインに特異的に結合する物質が共通して存在することを見出した。さらに、エリスロポエチン受容体を発現しているヒト前赤芽球性白血病細胞株(AS-E2)のエリスロポエチン依存性増殖が、この物質の添加によって、濃度依存的に抑制されることを明らかにした。これらの結果から、この物質がエリスロポエチン受容体と特異的に結合し、エリスロポエチン受容体を介したエリスロポエチンの作用を中和する活性を有するものと推定した。そして、血清中におけるこの物質のレベル(あるいは有無)と臨床的特徴や治療経過との関係を解析することにより、当該物質が被験者のエリスロポエチン応答性を予測する指標となりうることを実証した。以下、この物質を「エリスロポエチン阻害物質」と呼ぶ。
3.1 試料の調製
本発明の検査方法は、被験者から採取した末梢血、尿、組織抽出液等のサンプルを用いて非侵襲的に行われる。検体が血液の場合は、必要に応じて高速遠心を行うことにより不溶性の物質を除去した後、その後の検出方法に応じて適宜調製される。
指標とするエリスロポエチン阻害物質のレベルは、エリスロポエチン受容体との特異的結合を利用した生化学的方法を用いて検出することができる。ここで「レベル」とは当該エリスロポエチン阻害物質の量に限定されず、これを間接的に示す力価(抗体価等)も含む。
被験者から単離したサンプル中からエリスロポエチン受容体あるいはその断片と特異的に結合する物質が検出された場合、当該被験者はエリスロポエチン投与に対して、低応答性あるいは不応答性である可能性が高いと判定・評価できる。
本発明はまた、エリスロポエチン応答性の診断用キットを提供する。本発明のキットは、必須の構成要素としてエリスロポエチン受容体又はその断片(あるいはエリスロポエチン受容体の細胞外ドメイン又はその断片)を含む。このエリスロポエチン受容体の細胞外ドメイン又はその断片は、前項の記載に基づき、遺伝子組換え法により調製することができる。
実施例:
1.材料
(1)ヒトエリスロポエチン受容体
ヒトエリスロポエチンの細胞外ドメインのcDNA配列(配列番号1)を発現ベクター(Invitrogen)に組み込み、CHO細胞に導入して発現させ組換えヒトエリスロポエチン細胞外ドメイン(rhEPO細胞外ドメイン)を得た。
(2)抗ヒトエリスロポエチン抗体および抗ヒトエリスロポエチン受容体抗体
ウサギ抗ヒトエリスロポエチン(EPO)ポリクローナル抗体は、遺伝子組換えヒトEPO(中外製薬)を常法に従ってウサギに感作して作製した。マウス抗ヒトEPO受容体モノクローナル抗体は、遺伝子組換え可溶型ヒトEPO受容体をマウスに感作し、常法に従って樹立したハイブリドーマより作製した。
(3)EPO受容体発現細胞 AS-E2
EPO受容体発現細胞 AS-E2は中外製薬より供与されたものを用いた(文献:Miyazaki Y. Kuriyama K. Higuchi M. Tsushima H. Sohda H. Imai N. Saito M. Kondo T. Tomonaga M. Establishment and characterization of a new erythropoietin-dependent acute myeloid leukemia cell line, AS-E2. Leukemia. 11(11):1941-9, 1997 Nov.:受託番号FERM BP-04819)。このAS-E2細胞はEPO阻害物質の存在により増殖阻害を受ける。
(1)患者背景
金沢大学医学部附属病院血液浄化療法部に入院あるいは通院した患者のうち、腎不全、SLEと診断された107例(腎不全9例(男性7例、女性2例)、SLE患者41例(男性2例、女性39例))、抗好中球細胞質抗体陽性血管炎23例(男性8例、女性15例)他の膠原病34例(男性8例、女性26例)、及びネガティブコントロールとして健常人プール血清(Chemicon International Inc.製)を対象とした。なお、被験者からは、金沢大学倫理委員会の承認のもと、あらかじめインフォームドコンセントを得ている。
(2)血清の採取
常法にしたがい被験者の末梢血を採取し、遠心して血清を調製した。
(1)ELISA
・固相化プレートの作成
1) 可溶性ヒトEPO受容体(sEpoR)又はEPOを0.2M 炭酸水素ナトリウム緩衝液(pH9.5)で5μg/mLに希釈し、0.1mL/wellになるよう96 well Plate(Nunc社) に分注。
2) 4℃で24時間インキュベート。
3) Plate内の溶液を除去した後、0.3mL/wellの0.05% Tween 20/TBSで1回Washし、1%BSA/PBSを0.3mL/wellになるよう添加して4℃保存(Blocking)。
1) Plateを0.3mL/wellの 0.05% Tween 20/TBSで1回洗浄したのち、1% BSA/PBSで1000倍希釈した血清サンプルを100μg/well添加し、4℃で20時間インキュベート。
2) Plate内の溶液を除去したのち、ウェル当たり0.3mLの0.05% Tween 20/TBSを加えてPlateを洗浄。同じ操作を4回反復。
3) Plate内の溶液を除去したのち、1% BSA/PBSで5000倍希釈したHRP標識抗ヒトIg(Zymed社)又はウサギIgG抗体(Zymed社)あるいは10000倍希釈したHRP標識抗マウスIgG抗体(Zymed社)を0.1mL/well添加し、室温で1.5時間攪拌しながらインキュベート(480 rpm)。
4) Plate内の溶液を除去したのち、ウェル当たり0.3mLの0.05% Tween 20/TBSを加えてPlateを洗浄。同じ操作を4回反復。
5) Plate内の溶液を除去したのち、TMB基質(DAKO社)0.1mL/well添加し、室温で15分間発色。
6) 2N硫酸(0.1mL/well)で反応を停止し、450nmの吸光度を測定
・判定基準
ネガティブコントロール(健常人プール血清)で得られた吸光度の1.5倍以上の吸光度が得られた場合に抗体陽性と判断した。
Iodogen法(Fraker PJ, Speck JC Jr. Protein and cell membrane iodinations with a sparingly soluble chloroamide, 1,3,4,6-tetrachloro-3a,6a-diphrenylglycoluril. Biochem Biophys Res Commun. 1978; 80 (4): 849-857.)によってヨード125で標識した可溶性エリスロポエチンレセプター(sEpoR)100 μL(約100,000 cpm),血清20 μL及び検体希釈液((150 mmol/L NaCl,0.02 w/v% NaN3,0.1 w/v% BSA,0.1 vol% Tween 20含有10 mmol/L Tris-HCl buffer,pH 7.4)80μLあるいはcold(非標識体)sEpoR(2μg/Assay)を含有した検体希釈液80μLを添加・撹拌(計200μL)し、4℃で24時間静置した。検体希釈液で洗浄したProtein G Sepharose 4FF(GEヘルスケア)懸濁液50μLを添加し、振とう機を用いて4℃で1時間攪拌した。攪拌後、冷却した検体希釈液2 mLを添加・攪拌し、遠心分離[1,500×g,5分間,4℃]し、上清を除去した。この沈渣に再度冷却した検体希釈液2 mLを添加・攪拌・遠心分離[1,500×g,5分間,4℃]し、上清を除去した。沈渣の放射能量(cpm)をガンマーカウンターを用いて5分間測定した。
・判定基準
Cold sEpoRを添加して測定した際の放射能量(cpm)がCold sEpoR非添加時に比して50%以下に低下した場合、エリスロポエチン受容体に対する特異抗体(sEpoR)陽性と判断した。
抗EpoR抗体によるEPO阻害活性は、EPO依存性ヒト白血病細胞株(AS-E2細胞、文献:Leukemia. 11(11):1941-9, 1997)の増殖阻害を指標に測定した。96ウェルプレート(Costar社)を用いてAS-E2細胞(10000 cells/well)をEPO(1ng/ml)及び種々の濃度の患者血清存在下にIMDM培地中で培養し、5-7日間培養後の生細胞数をWST-1試薬(Takara社)によるミトコンドリア活性で数値化した。なお、培養系の血清濃度(total)はウシ胎児血清を用いて常に20%となるよう調整した。
(1)ELISA
107例のうち、11例で陽性であった。このうち10例がSLE患者であった。他の1例はその他の膠原病(シェーグレン症候群)であった。
(2)放射免疫沈降法
107例のうち、16例(男性3例、女性13例、SLE 7例、抗好中球細胞質抗体陽性血管炎4例、腎不全2例)に放射免疫沈降法を施行した。その結果、SLE患者ならびに抗好中球細胞質抗体陽性血管炎患者の2例において陽性であった。
最も陽性例が多くみられたSLE患者(11例/41例=26.8%)に対して臨床的特徴を検討した。表1に示すとおり、上記のいずれかの方法によるエリスロポエチン受容体結合性物質の有無(陽性/陰性)により、SLE患者は2群(陽性11例、陰性30例)に分けて解析した。その結果、両群間には網赤血球減少(Reticulocytopenia)及び骨髄赤芽球系の低形成(Erythroblastopenia)において有意な差(p<0.05)がみられた。
図1に示されるよう、健常血清ではいずれの濃度においても細胞の増殖は阻害されなかったが、患者血清(症例I:SLE患者(陽性)APSを合併したSLE女性)では添加した血清濃度依存的にAS-ES細胞の増殖が抑制された。
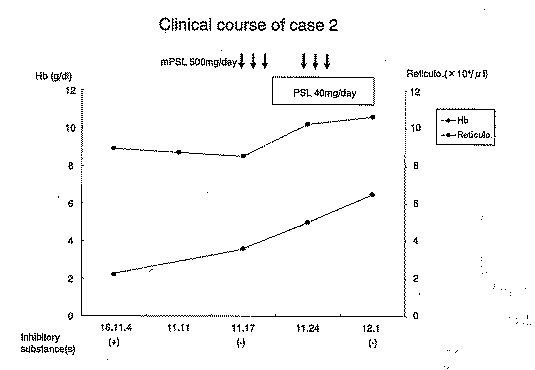
(4)治療経過と抗sEpoR抗体量の推移
さらに、プレドニン投与による治療経過と抗体量の推移を観察した(図2)。その結果、治療前に検出された抗sEpoR抗体はプレドニン治療により検出感度以下となり、それに伴って網赤血球数が増加し、貧血が軽快した。
以上の結果から、今回ELISA及び放射免疫沈降法によって患者血清から検出された抗sEpoR抗体は、エリスロポエチン阻害作用を有する新規物質(エリスロポエチン阻害物質)であると判断された。
したがって、この物質を膠原病、慢性腎不全等の貧血を呈する患者で検出することにより、エリスロポエチン不応性/低反応性を投与前に予測し、より安全で効果的な治療を行なうことができる。また、本結果は、貧血の成因と病態機序の解明とともに、貧血の新規分類につながる可能性がある。
Claims (7)
- 被験者から単離されたサンプル中にエリスロポエチン受容体と特異的に結合し、エリスロポエチン受容体を介したエリスロポエチンの作用を中和するエリスロポエチン受容体抗体の存在が確認された場合に前記被験者はエリスロポエチン不応性あるいは低応答性と診断する、被験者のエリスロポエチン応答性の診断のために、被験者から単離したサンプル中における、エリスロポエチン受容体と特異的に結合し、エリスロポエチン受容体を介したエリスロポエチンの作用を中和するエリスロポエチン受容体抗体のレベルを検出することを含む、エリスロポエチン受容体抗体の検出方法。
- 前記エリスロポエチン受容体抗体のレベルが免疫学的方法によって測定されることを特徴とする、請求項1に記載の検出方法。
- 前記免疫学的方法が、免疫沈降法、ならびにウエスタンブロット法、ドットブロット法、スロットブロット法、ELISA法、及びRIA法を含む固相免疫法あるいはこれらの変法から選ばれる少なくとも1つ以上である、請求項2に記載の検出方法。
- 前記免疫学的方法が免疫沈降法及び/又はELISA法である、請求項3に記載の検出方法。
- エリスロポエチン受容体又はその断片を構成要素として含み、被験者から単離したサンプル中に前記エリスロポエチン受容体又はその断片と特異的に結合するエリスロポエチン受容体抗体が検出された場合、当該被験者はエリスロポエチン投与に対して、不応性あるいは低応答性である可能性が高いと判定できる、エリスロポエチン応答性の診断用キット。
- 前記エリスロポエチン受容体又はその断片の少なくとも一部が固相に固定化されていることを特徴とする、請求項5に記載のキット。
- さらに、二次抗体、抗体固定用固相支持体、検出試薬、反応用緩衝液、酵素、及び基質から選ばれる少なくとも1つ以上を含む、請求項5又は6に記載のキット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007130756A JP5618038B2 (ja) | 2007-05-16 | 2007-05-16 | エリスロポエチン応答性の診断方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007130756A JP5618038B2 (ja) | 2007-05-16 | 2007-05-16 | エリスロポエチン応答性の診断方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008286599A JP2008286599A (ja) | 2008-11-27 |
| JP5618038B2 true JP5618038B2 (ja) | 2014-11-05 |
Family
ID=40146462
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007130756A Active JP5618038B2 (ja) | 2007-05-16 | 2007-05-16 | エリスロポエチン応答性の診断方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5618038B2 (ja) |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008544746A (ja) * | 2005-05-12 | 2008-12-11 | ザイモジェネティクス, インコーポレイテッド | 免疫応答を調節するための組成物および方法 |
-
2007
- 2007-05-16 JP JP2007130756A patent/JP5618038B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2008286599A (ja) | 2008-11-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2620770B1 (en) | Novel testing method for angiitis | |
| EP2754672B1 (en) | Antibody capable of binding to specific region of periostin, and method of measuring periostin using the same | |
| EP3077815B1 (en) | Methods and reagents for the assessment of gestational diabetes | |
| JPWO2008120684A1 (ja) | 急性中枢神経障害の予後判定方法 | |
| JP5783909B2 (ja) | 悪性腫瘍の診断方法 | |
| WO2012175602A2 (en) | Elisa for calprotectin | |
| JPWO2010024089A1 (ja) | 皮膚筋炎の診断方法および診断キット | |
| JP2012058048A (ja) | ペリオスチン測定の正確性の改善方法 | |
| JP5924502B2 (ja) | リンパ球性漏斗下垂体後葉炎のバイオマーカー及びその用途 | |
| EP2883057B1 (en) | Diagnostic of heart failure | |
| JP5618038B2 (ja) | エリスロポエチン応答性の診断方法 | |
| US20130040325A1 (en) | Enzyme Linked Immunosorbent Assay (ELISA) Method and Kit for Detecting Soluble Programmed Cell Death Protein 5 (PDCD5) | |
| CN112763716A (zh) | 检测血清lum表达的肝病纤维化检测试剂、检测试剂盒和检测方法 | |
| EP3732486A1 (en) | Methods of quantifying cftr protein expression | |
| WO2008012941A1 (fr) | Méthode de diagnostic d'une insuffisance cardiaque | |
| WO2024014426A1 (ja) | 筋炎/皮膚筋炎に伴うリスクを検出する方法 | |
| JP2024009473A (ja) | 筋炎/皮膚筋炎やそれに併発する間質性肺炎を発症するモデル動物 | |
| WO2016186173A1 (ja) | 劇症肝不全の診断方法、及び予防又は治療剤 | |
| JP6672168B2 (ja) | 肉腫の転移を検出するための方法およびバイオマーカー | |
| CN120927976A (zh) | 检测抗dlat自身抗体的试剂在制备检测和/或诊断免疫介导的坏死性肌病的产品中的应用 | |
| JP2021073435A (ja) | 試料に含まれるペリオスチン測定の感度の改善方法 | |
| WO2017094837A1 (ja) | 心疾患または筋疾患の診断薬 | |
| JP2019082329A (ja) | 慢性腎臓病患者における高リン血症の発症のしやすさを試験する方法 | |
| JP2016035448A (ja) | 難治性血管炎の病態を特定する新規なmpo−anca検査法 | |
| HK1229004A1 (en) | Methods and reagents for the assessment of gestational diabetes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100513 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20111109 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130108 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130311 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131217 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140210 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140812 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140902 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5618038 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |