JP3795072B2 - Transition metal compound, catalyst for olefin polymerization, and method for producing olefin polymer using the catalyst - Google Patents
Transition metal compound, catalyst for olefin polymerization, and method for producing olefin polymer using the catalyst Download PDFInfo
- Publication number
- JP3795072B2 JP3795072B2 JP51434595A JP51434595A JP3795072B2 JP 3795072 B2 JP3795072 B2 JP 3795072B2 JP 51434595 A JP51434595 A JP 51434595A JP 51434595 A JP51434595 A JP 51434595A JP 3795072 B2 JP3795072 B2 JP 3795072B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- carbon atoms
- molecular weight
- olefin
- catalyst
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F17/00—Metallocenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F10/00—Homopolymers and copolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/619—Component covered by group C08F4/60 containing a transition metal-carbon bond
- C08F4/61912—Component covered by group C08F4/60 containing a transition metal-carbon bond in combination with an organoaluminium compound
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/619—Component covered by group C08F4/60 containing a transition metal-carbon bond
- C08F4/6192—Component covered by group C08F4/60 containing a transition metal-carbon bond containing at least one cyclopentadienyl ring, condensed or not, e.g. an indenyl or a fluorenyl ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Transition And Organic Metals Composition Catalysts For Addition Polymerization (AREA)
Description
技術分野
本発明は遷移金属化合物,該遷移金属化合物を含有するオレフィン重合用触媒及びこの触媒を用いたオレフィン系重合体の製造方法に関するものである。さらに詳しくは、本発明は、オレフィン重合用触媒成分として有用な特定の置換インデニル基をπ配位子として有する遷移金属化合物、この遷移金属化合物を含有する高活性のオレフィン重合用触媒、及びこの触媒を用いて残留金属量の少ない品質の良好な通常のオレフィン系単独重合体や共重合体、あるいは弾性率と弾性回復率のバランスに優れる上、低温物性が改善され、かつ成形加工性が向上したオレフィン/環状オレフィン共重合体,エラストマーなどとして有用な分子量分布の狭い非晶性高分子量プロピレン系重合体及びマクロモノマーなどとして有用なビニル基含有量の高い低分子量オレフィン系重合体、更にそれを効率よく製造する方法に関するものである。
背景技術
ポリエチレン類やポリプロピレン類などのオレフィン系重合体は、汎用樹脂として多くの分野において幅広く用いられている。このオレフィン系重合体は、チーグラー・ナッタ触媒を基本とする触媒系で製造されることが知られているが、近年一つのπ配位子をもち、該π配位子と中心金属元素とが任意の基を介して結合してなる遷移金属化合物を触媒成分とする重合用触媒を用いて、オレフィン系重合体を製造することが試みられている。
例えば、ヨーロッパ公開特許第420436号、国際特許公開92−00333号、ヨーロッパ公開特許第418044号、同第416815号、同第468651号、同495375号、同514828号、同520732号などにおいて、上記の一つのπ配位子をもち、該π配位子と中心金属元素とが任意の基を介して結合してなる遷移金属化合物を触媒成分とするオレフィン重合用触媒及び該触媒を用いたオレフィン系重合体の製造方法が開示されている。
しかしながら、これらの中で、π配位子がインデニル基であるものは、すべて未置換であって、その活性については必ずしも充分に満足しうるものではなかった。
一方、α−オレフィンと環状オレフィンとの共重合体、あるいはα−オレフィンと環状オレフィンと環状ジエン化合物との共重合体などの環状オレフィン系共重合体は(特開平5−230144号公報,特開平5−261875号公報など)、透明性などの光学特性,柔軟性,弾性回復性などに優れることから、医療,包装,食料品分野などの種々の分野におけるフィルムやシートなどとして利用可能である。また、エチレンと特定の環状オレフィンとを共重合することによって、機械的特性、光学特性、耐熱性などがバランスよく優れた環状オレフィン系ランダム共重合体も知られている(特開昭60−168708号公報,特開平61−98780号公報など)。
ところで、オレフィン系重合体の成形方法は多岐にわたり、代表的な成形方法としては、射出成形,押出し成形,ブロー成形,インフレーション成形,圧縮成形,真空成形などが知られている。このような成形方法においては、加工特性を向上して加工コストを低下させるために、高速成形性の付与や成形加工の低エネルギー化の試みが長年にわたって行われてきており、それぞれの用途に合った最適な物性を付与し、最適な加工特性でもって成形することが重要な課題となっている。
また、近年、均一系メタロセン系触媒は、オレフィン間の共重合性に優れ、得られるポリマーの分子量分布が狭く、かつ従来のバナジウム系触媒と比較して極めて高い触媒活性を示すことが明らかにされた。したがって、このような特徴を生かして様々な用途分野への展開が期待されている。しかしながら、一方メタロセン系触媒により得られたポリオレフィンは、その成形加工特性に問題が多く、ブロー成形やインフレーション成形の際には制限を免れないという欠点を有している。
環状オレフィン系共重合体の成形性を向上させるために、特開平5−271485号公報では特定のガラス転移温度(Tg)を有する環状オレフィン系共重合体のうち、極限粘度〔η〕が異なるもの二種類を用いて組成物を形成することにより、溶融粘度が下がり、メルトフラクチャーが生じにくく、成形加工性に優れる環状オレフィン系共重合体組成物が得られることが開示されている。しかしながら、極限粘度〔η〕が異なるもの二種類を用いて組成物を形成すると、分子量分布が広くなり、フィルムの機械物性、特にフィルム強度が低下したり、透明性が低下するなどの問題が生じる。
したがって、機械物性に優れ、かつ溶融流動性が向上し、成形加工性の良好な環状オレフィン系共重合体を効率よく製造する方法の開発が望まれていた。
一方、高分子量アタクチックポリプロピレン(高分子量非晶性ポリプロピレン)は、単品でエラストマーなどとして利用でき、また熱可塑性オレフィン系エラストマー(TPO)の一成分としても利用が可能であり、特に分子量分布の狭い高分子量アタクチックポリプロピレンの利用価値は高い。しかしながら、従来の触媒系で得られるアタクチックポリプロピレンは分子量が低く、現在工業的に生産されているアイソタクチックポリプロピレンの副生成物として得られているにすぎない。また、米国特許第5026798号明細書には、未置換のインデニル基をπ配位子とする本発明と類似の触媒系を用いてプロピレンを単独重合する技術が開示されているが、この場合、生成するポリマーは、結晶性のアイソタクチックポリプロピレン(融点147℃,ペンタッド分率74.7モル%)である上、触媒活性が低く、低分子量体(重量平均分子量で71,300)である。したがって、分子量分布の狭い高分子量アタクチックポリプロピレンを効率よく製造する方法の開発が望まれていた。
他方、末端ビニル基含有量の高い低分子量オレフィン系重合体は、マクロモノマーとして利用可能である。例えば、オレフィン系共重合体のコモノマーとして利用することにより、ゲル化反応を伴うことなく容易に長鎖分岐を導入することができ、成形加工特性に優れるオレフィン系共重合体や、エラストマー,相溶化剤などとしての性能を有するオレフィン系共重合体を与えることができる。また、該末端ビニル基含有量の高い低分子量オレフィン系重合体を水添処理することにより、ワックスなどとして利用することができる。さらに、各種反応試剤で処理することにより、末端修飾マクロモノマーとして、例えば縮合系共重合体のコモノマーに用いられ、接着剤,表面改質剤,相溶化剤,コンポジット材料などに利用できる。
発明の開示
本発明の目的は、オレフィン重合用触媒成分として有用な遷移金属化合物、この遷移金属化合物を含有する高活性のオレフィン重合用触媒、及びこの触媒を用いて残留金属量の少ない品質の良好な通常のオレフィン系単独重合体や共重合体、あるいは機械物性に優れ、かつ成形加工性の良好なオレフィン/環状オレフィン共重合体,エラストマーなどとして有用な分子量分布の狭い非晶性高分子量プロピレン系重合体及びマクロモノマーなどとして有用なビニル基含有量の高い低分子量オレフィン系重合体、更にはこれを効率よく製造する方法を提供することである。
そこで、本発明者らは、前記目的を達成するために鋭意研究を重ねた結果、特定の構造の置換インデニル基を、π配位子として有する遷移金属化合物がオレフィン重合用触媒成分として有用であること、そしてこの遷移金属化合物と有機硼素化合物やアルミノキサンや特定のイオン性化合物と、場合により用いられるルイス酸との組合せからなる触媒が高活性を有し、この触媒を用いることにより、残留金属量の少ない品質の良好なオレフィン系単独重合体や共重合体を経済的に効率よく製造できることを見出した。さらに、該遷移金属化合物を適当に選ぶことにより、前記の好ましい性質を有するオレフィン/環状オレフィン共重合体,非晶性高分子量プロピレン系重合体及びビニル基含有量が高い低分子量オレフィン系重合体が経済的に効率よく得られることを見出した。本発明は、かかる知見に基づいて完成したものである。
すなわち、本発明は、
(1)五員環側に遷移金属元素と結合している置換基以外に少なくとも一つの置換基をもつ置換インデニル基をπ配位子として有することを特徴とする遷移金属化合物、
(2)五員環側に遷移金属元素と結合している置換基以外に少なくとも一つの置換基をもつ置換インデニル基をπ配位子として有する遷移金属化合物を含有してなるオレフィン重合用触媒、
(3)(A)一般式(II)
及び一般式(III)
〔式中、R1,R2,R3及びR4はそれぞれ水素原子,ハロゲン原子,炭素数1〜20の脂肪族炭化水素基,炭素数6〜20の芳香族炭化水素基,炭素数1〜20のアルコキシ基,炭素数6〜20のアリーロキシ基,炭素数1〜20のチオアルコキシ基,炭素数6〜20のチオアリーロキシ基,アミノ基,アミド基,カルボキシル基又はアルキルシリル基を示し、R1及びR3は、それぞれにおいて少なくとも一つが水素原子以外の基であり、複数のR1,複数のR2,複数のR3及び複数のR4は、それぞれにおいて同一でも異なっていてもよい。M2及びM3は、それぞれ周期律表3〜10族又はランタノイド系列の金属元素、X2及びX3は、それぞれσ配位子、L2及びL3は、それぞれルイス塩基、Q1及びQ2は、それぞれ炭素数1〜6の脂肪族炭化水素基,炭素数6〜20の芳香族炭化水素基,珪素数1〜5のシリレン基又はゲルマニウム数1〜5のゲルミレン基,J1及びJ2は、それぞれアミド基,フォスフィド基,酸素原子,硫黄原子又はアルキリデン基を示し、複数のX2,複数のX3,複数のL2及び複数のL3は、それぞれにおいて同一でも異なっていてもよい。c及びeは、それぞれM2及びM3の価数を示し、d及びfは0,1又は2である。〕
で表される遷移金属化合物の中から選ばれた少なくとも一種と、(B)(a)有機硼素化合物,(b)アルミノキサン及び(c)非配位性アニオンとカチオンとからなるイオン性化合物の中から選ばれた少なくとも一種との組合せからなるオレフィン重合用触媒、
(4)(A)上記一般式(II)及び(III)で表される遷移金属化合物の中から選ばれた少なくとも一種と、(B)(a)有機硼素化合物,(b)アルミノキサン及び(c)非配位性アニオンとカチオンとからなるイオン性化合物の中から選ばれた少なくとも一種と(C)ルイス酸との組合せからなるオレフィン重合用触媒、
及び
(5)上記(2)〜(4)の触媒の存在下、オレフィン類を単独重合、二種以上のオレフィン類を共重合又はオレフィン類と他の重合性不飽和化合物とを共重合させることを特徴とするオレフィン系重合体の製造方法を提供するものである。
さらに、本発明は、
(6)▲1▼ゲルパーミエーションクロマトグラフィー法により測定された重量平均分子量(Mw)と数平均分子量(Mn)との比Mw/Mnが6以下で、▲2▼環状オレフィン単位含有量が0.1〜95モル%であり、かつ▲3▼デカリン中,135℃で測定した極限粘度〔η〕と荷重2.16kgで測定したメルトインデックス(MI2.16)との関係が、式
〔η〕≦1.333−0.620×logMI2.16
を満たすオレフィン/環状オレフィン共重合体、
及び
(7)▲1▼デカリン中,135℃で測定した極限粘度〔η〕が1.0デシリットル/gより大きく、▲2▼ゲルパーミエーションクロマトグラフィー法により測定した重量平均分子量(Mw)と数平均分子量(Mn)との比Mw/Mnが3未満であり、かつ▲3▼融点(Tm)を有さず、ガラス転移点(Tg)が10℃未満のものであるプロピレン系重合体をも提供するものである。
なお、本発明の好適な実施態様は、
(8)オレフィン類と環状オレフィン類とを共重合させて、オレフィン/環状オレフィン共重合体を製造する上記(5)の方法、
(9)オレフィン/環状オレフィン共重合体が、▲1▼ゲルパーミエーションクロマトグラフィー法により測定された重量平均分子量(Mw)と数平均分子量(Mn)との比Mw/Mnが6以下で、▲2▼環状オレフィン単位含有量が0.1〜95モル%であり、かつ▲3▼デカリン中,135℃で測定した極限粘度〔η〕と荷重2.16kgで測定したメルトインデックス(MI2.16)との関係が、式
〔η〕≦1.333−0.620×logMI2.16
を満たすものである上記(8)の方法、
(10)(A)成分の遷移金属化合物において、一般式(II)及び(III)におけるM2及びM3が、それぞれチタニウムである上記(3),(4)の重合用触媒、
(11)(A)成分の遷移金属化合物において、一般式(II)及び(III)におけるM2及びM3が、それぞれジルコニウム又はハフニウムである上記(3),(4)の重合用触媒、
(12)上記(10)の触媒の存在下、プロピレンを単独重合、又はプロピレンと、炭素数2〜20の他のオレフィン類及び炭素数2〜20の他の重合性不飽和化合物の中から選ばれた少なくとも一種とを共重合させて、非晶性高分子量プロピレン系重合体を製造する上記(5)の方法、
(13)非晶性高分子量プロピレン系重合体が、▲1▼デカリン中、135℃で測定した極限粘度〔η〕が1.0デシリットル/gより大きく、▲2▼ゲルパーミエーションクロマトグラフィー法により測定した重量平均分子量(Mw)と数平均分子量(Mn)との比Mw/Mnが3未満であり、かつ▲3▼融点(Tm)を有さず、ガラス転移点(Tg)が10℃未満のものである上記(12)の方法、
(14)上記(11)の触媒の存在下、炭素数2〜20のオレフィン類を単独重合、炭素数2〜20のオレフィン類二種以上を共重合又は炭素数2〜20のオレフィン類と炭素数2〜20の他の重合性不飽和化合物とを共重合させて、ビニル基含有量の高い低分子量オレフィン系重合体を製造する上記(5)の方法、
(15)ビニル基含有量の高い低分子量オレフィン系重合体が、エチレン単独重合体、又はエチレンと、炭素数3〜20のオレフィン類及び炭素数2〜20の他の重合性不飽和化合物の中から選ばれた少なくとも一種との共重合体であって、▲1▼ゲルパーミエーションクロマトグラフィー法により測定したポリエチレン換算重量平均分子量(Mw)が200〜10,000で、▲2▼密度が0.925g/cm3以上であり、かつ▲3▼全不飽和基に占めるビニル基の割合が70モル%以上で、赤外線分光分析で測定したビニル基含有量が1000炭素当たり、1.5個以上である上記(14)の方法、
である。
発明を実施するための最良の形態
本発明の遷移金属化合物は、五員環側に遷移金属元素と結合している置換基以外に少なくとも一つの置換基をもつ置換インデニル基をπ配位子として有する新規な遷移金属化合物であって、該遷移金属化合物としては様々なものがある。例えば、一般式(I)
RM1X1 a-1L1 b ・・・(I)
で表されるπ配位子を一個もち、π配位子と金属とが任意の基を介して結合した遷移金属化合物、具体的には、一般式(II)
で表される化合物、一般式(III)
で表される化合物などが挙げられる。
上記一般式(I)において、Rはπ配位子で、五員環側に遷移金属元素と結合している置換基以外に少なくとも一つの置換基をもつ置換インデニル基を示す。一般式(II)及び(III)において、R1,R2,R3及びR4は、それぞれ水素原子,ハロゲン原子,炭素数1〜20の脂肪族炭化水素基,炭素数6〜20の芳香族炭化水素基,炭素数1〜20のアルコキシ基,炭素数6〜20のアリーロキシ基,炭素数1〜20のチオアルコキシ基,炭素数6〜20のチオアリーロキシ基,アミノ基,アミド基,カルボキシル基又はアルキルシリル基を示すが、R1及びR3は、それぞれにおいて少なくとも一つが水素原子以外の基である。また、複数のR1、複数のR2、複数のR3及び複数のR4は、それぞれにおいて同一であっても異なっていてもよい。
さらに、一般式(I),(II)及び(III)において、M1,M2及びM3は、それぞれ周期律表3〜10族又はランタノイド系列の金属元素、具体的にはチタン,ジルコニウム,ハフニウム,ランタノイド系金属,ニオブ,タンタルなどの遷移金属元素を示すが、これらの中でチタン,ジルコニウム及びハフニウムが好適である。また、X1,X2及びX3は、それぞれσ配位子を示し、具体的には水素原子,ハロゲン原子,炭素数1〜20の脂肪族炭化水素基,炭素数6〜20の芳香族炭化水素基,炭素数1〜20のアルコキシ基,炭素数6〜20のアリーロキシ基,炭素数1〜20のチオアルコキシ基,炭素数6〜20のチオアリーロキシ基,アミノ基,アミド基,カルボキシル基,アルキルシリル基などが挙げられる。複数のX1、複数のX2及び複数のX3は、それぞれにおいて同一でも異なっていてもよく、またたがいに任意の基を介して結合していてもよい。L1,L2及びL3はそれぞれルイス塩基を示し、複数のL1、複数のL2及び複数のL3は、それぞれにおいて同一でも異なっていてもよい。a,c及びeは、それぞれM1,M2及びM3の価数、b,d及びfは、0,1又は2である。
一般式(II)及び(III)において、Q1及びQ2は、それぞれ炭素数1〜6の脂肪族炭化水素基,炭素数6〜20の芳香族炭化水素基,珪素数1〜5のシリレン基又はゲルマニウム数1〜5のゲルミレン基を示す。J1及びJ2は、それぞれアミド基,フォスフィド基,酸素原子,硫黄原子又はアルキリデン基を示す。
置換インデニル基〔遷移金属元素に結合している置換基(Q1,Q2)は含まず。〕の具体例としては、2−メチルインデニル基;3−メチルインデニル基;3−トリメチルシリルインデニル基;2−t−ブチルインデニル基;2,3−ジメチルインデニル基;1,3−ジメチルインデニル基;2,4,7−トリメチルインデニル基;1,3,4,7−テトラメチルインデニル基;2,3,4,7,−テトラメチルインデニル基;3,4,5,6,7−ペンタメチルインデニル基;2,4,5,6,7−ペンタメチルインデニル基;2,3,4,5,6,7−ヘキサメチルインデニル基;1,3,4,5,6,7−ヘキサメチルインデニル基;2,3−ジメチル−4,7−ジメトキシインデニル基;2,3−ジメチル−4,7−ジフルオロインデニル基などが挙げられる。また、該X1(X2,X3)の具体例としては、水素原子,塩素原子,臭素原子,ヨウ素原子,メチル基,ベンジル基,フェニル基,トリメチルシリルメチル基,メトキシ基,エトキシ基,フェノキシ基,チオメトキシ基,チオフェノキシ基,ジメチルアミノ基,ジイソプロピルアミノ基などが挙げられる。
本発明の遷移金属化合物としては、上記例示の置換インデニル基及びX1(X2,X3)の中から、それぞれ任意の選択されたものを含む化合物を好ましく挙げることができる。
該遷移金属化合物の具体例としては、(t−ブチルアミド)(2,3−ジメチルインデニル)−1,2−エタンジイルチタニウムジクロリド;(t−ブチルアミド)(2,3−ジメチルインデニル)−1,2−エタンジイルチタニウムジメチル;(t−ブチルアミド)(2,3−ジメチルインデニル)−ジメチルシリルチタニウムジクロリド;(t−ブチルアミド)(2,3−ジメチルインデニル)−ジメチルシリルチタニウムジメチル;(t−ブチルアミド)(1,3−ジメチルインデニル)−ジメチルシリルチタニウムジクロリド;(t−ブチルアミド)(1,3−ジメチルインデニル)−ジメチルシリルチタニウムジメチル;(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド;(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジメチル;(t−ブチルアミド)(1,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド;(t−ブチルアミド)(1,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジメチル;(2,3−ジメチルインデニル)−1−エタン−2−オキサチタニウムジクロリド;(2,3−ジメチルインデニル)−1−エタン−2−オキサチタニウムジメチル;(フェニルアミド)(2,3−ジメチルインデニル)−1,2−エタンジイルジルコニウムジクロリド;(t−ブチルアミド)(2,3−ジメチルインデニル)−1,2−エタンジイルジルコニウムジメチル;(t−ブチルアミド)(2,3−ジメチルインデニル)−ジメチルシリルジルコニウムジクロリド;(t−ブチルアミド)(2,3−ジメチルインデニル)−ジメチルシリルジルコニウムジメチル;(t−ブチルアミド)(1,3−ジメチルインデニル)−ジメチルシリルジルコニウムジクロリド;(t−ブチルアミド)(1,3−ジメチルインデニル)−ジメチルシリルジルコニウムジメチル;(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルジルコニウムジクロリド;(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)ジメチルシリルジルコニウムジメチル;(t−ブチルアミド)(1,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルジルコニウムジクロリド;(t−ブチルアミド)(1,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルジルコニウムジメチル;(2,3−ジメチルインデニル)−1−エタン−2−オキサジルコニウムクロリド;(2,3−ジメチルインデニル)−1−エタン−2−オキサジルコニウムジメチルなど、及びこれらの化合物におけるチタニウムやジルコニウムをハフニウムに置換したものを挙げることができる。もちろん、これらに限定されるものではない。また、他の族又はランタノイド系列の金属元素の類似化合物であってもよい。
本発明のオレフィン重合用触媒は、上記の五員側に遷移金属元素と結合している置換基以外に、少なくとも一つの置換基をもつ置換インデニル基をπ配位子として有する遷移金属化合物を含有するものであり、特に(A)前記一般式(II)及び(III)で表される遷移金属化合物の中から選ばれた少なくとも一種と、(B)(a)有機硼素化合物、(b)アルミノキサン及び(c)非配位性アニオンとカチオンとからなるイオン性化合物の中から選ばれた少なくとも一種との組合せからなる触媒、並びに(A)前記一般式(II)及び(III)で表される遷移金属化合物の中から選ばれた少なくとも一種と、(B)(a)有機硼素化合物、(b)アルミノキサン及び(c)非配位性アニオンとカチオンとからなるイオン性化合物の中から選ばれた少なくとも一種と、(C)ルイス酸との組合せからなる触媒が好適である。
上記(B)成分における(a)成分の有機硼素化合物としては、一般式(IV)
R5 3BL4 v ・・・(IV)
で表される化合物が挙げられる。
上記一般式(IV)において、R5は水素原子,ハロゲン原子,炭素数1〜20の脂肪族炭化水素基,炭素数6〜20の芳香族炭化水素基,置換芳香族炭化水素基,炭素数1〜20のアルコキシ基,炭素数6〜20のアリーロキシ基,置換アリーロキシ基,アルミノキシ基,ボロキシ基,シロキシ基,ゲルミノキシ基などを示し、たがいに同一であっても異なっていてもよい。該R5の具体例としては、フェニル基,トルイル基,フルオロフェニル基,トリフルオロメチルフェニル基,トリメチルシリルテトラフルオロフェニル基,ペンタフルオロフェニル基,フッ素原子,塩素原子,臭素原子,ヨウ素原子,ジメチルアルミノキシ基,ジイソブチルアルミノキシ基などが挙げられる。L4はルイス塩基を示し、具体的にはジエチルエーテル,テトラヒドロフランなどのエーテル化合物、ピリジンなどのアミン化合物などが挙げられる。vは0〜3の整数である。
また、該(B)成分における(b)成分のアルミノキサンは、有機アルミニウム化合物と縮合剤とを接触させることにより得られるものであって、一般式(V)
〔式中、R6は炭素数1〜20のアルキル基、pは0〜50、好ましくは0〜30の数を示す。〕
で表される鎖状アルミノキサンや、一般式(VI)
〔式中、R6は前記と同じであり、qは2〜50、好ましくは2〜30の数を示す。〕
で表される環状アルミノキサンなどが挙げられる。
このアルミノキサンの原料として用いられる有機アルミニウム化合物としては、例えばトリメチルアルミニウム,トリエチルアルミニウム,トリイソブチルアルミニウムなどのトリアルキルアルミニウム及びその混合物などが挙げられる。また、縮合剤としては、典型的なものとして水が挙げられるが、この他に該トリアルキルアルミニウムが縮合反応する任意のもの、例えば無機物などの吸着水やジオールなどが挙げられる。
一方、(B)成分における(c)成分の非配位性アニオンとカチオンとからなるイオン性化合物としては、一般式(VII)
(〔L5−H〕g+)h(〔M4Y1Y2・・・Yn〕(n-m)-)i ・・・(VII)
又は一般式(VIII)
(〔L6〕g+)h(〔M5Y1Y2・・・Yn〕(n-m)-)i ・・・(VIII)
〔ただし、L6は後述のM6、R7R8M7又はR9 3Cである。〕
で表される化合物が挙げられる。
上記一般式(VII),(VIII)において、L5はルイス塩基を示し、M4及びM5は、周期律表の5族〜15族から選ばれる元素、具体的にはB,Al,P,As,Sbなどを示す。M6は周期律表の8族〜12族から選ばれる元素、具体的にはAg,Cuなどを示し、M7は周期律表の8族〜10族から選ばれる元素、具体的にはFe,Co,Niなどを示す。Y1〜Ynは、それぞれ水素原子,ジアルキルアミノ基,アルコキシ基,アリーロキシ基,炭素数1〜20のアルキル基,炭素数6〜20のアリール基,アリールアルキル基,アルキルアリール基,置換アルキル基,有機メタロイド基,ハロゲン原子などを示す。このY1〜Ynの具体例としては、ジメチルアミノ基,ジエチルアミノ基,メトキシ基,エトキシ基,ブトキシ基,フェノキシ基,2,6−ジメチルフェノキシ基,メチル基,エチル基,プロピル基,ブチル基,オクチル基,フェニル基,トルイル基,キシリル基,メシチル基,ベンジル基,ペンタフルオロフェニル基,3,5−ジ(トリフルオロメチル)基,4−t−ブチルフェニル基,F,Cl,Br,I,五メチルアンチモン基,トリメチルシリル基,トリメチルゲルミル基,ジフェニル硼素基などが挙げられる。
また、R7及びR8は、それぞれシクロペンタジエニル基,置換シクロペンタジエニル基,インデニル基,置換インデニル基,フルオレニル基などを示し、具体的にはメチルシクロペンタジエニル基,ペンタメチルシクロペンタジエニル基などが挙げられる。R9はアルキル基,アリール基,置換アリール基で、たがいに同一でも異なっていてもよく、具体的には、フェニル基,4−メトキシフェニル基,4−メチルフェニル基などが挙げられる。mはM4,M5の原子価で1〜7の整数、nは2〜8の整数、gは〔L5−H〕,〔L6〕のイオン価数で1〜7の整数、hは1以上の整数、i=(h×g)/(n−m)である。
該イオン性化合物における非配位性アニオンとしては、例えばテトラ(フェニル)ボレート;テトラ(フルオロフェニル)ボレート;テトラキス(ジフルオロフェニル)ボレート;テトラキス(トリフルオロフェニル)ボレート;テトラキス(テトラフルオロフェニル)ボレート;テトラキス(ペンタフルオロフェニル)ボレート;テトラキス(トリフルオロメチルフェニル)ボレート;テトラ(トルイル)ボレート;テトラ(キシリル)ボレート;(トリフェニル,ペンタフルオロフェニル)ボレート;〔トリス(ペンタフルオロフェニル),フェニル〕ボレート;トリデカハイドライド−7,8−ジカルバウンデカボレートなどが挙げられる。一方、カチオンとしては、例えばトリ(エチル)アンモニウム;トリ(ブチル)アンモニウム;N,N−ジメチルアニリニウム;N,N−ジエチルアニリニウム;トリフェニルフォスフィニウム;ジメチルフェニルフォスフィニウム;1,1’−ジメチルフェロセン;デカメチルフェロセン;銀(I);トリ(フェニル)カルベニウム;トリ(トルイル)カルベニウム;トリ(メトキシフェニル)カルベニウム;〔ジ(トルイル),フェニル〕カルベニウム;〔ジ(メトキシフェニル),フェニル〕カルベニウム;〔メトキシフェニル,ジ(フェニル)〕カルベニウムなどが挙げられる。
該イオン性化合物は、上記で例示した非配位性アニオン及びカチオンの中から、それぞれ任意に選択して組み合わせたものを好ましく用いることができる。
本発明の触媒においては、上記(B)成分として、(a)成分の有機硼素化合物を一種用いてもよいし、二種以上を組み合わせて用いてもよく、(b)成分のアルミノキサンを一種用いてもよいし、二種以上を組み合わせて用いてもよい。また、(c)成分のイオン性化合物を一種用いてもよいし、二種以上を組み合わせて用いてもよい。さらに、該(a)成分、(b)成分及び(c)成分を適当に組み合わせて用いてもよい。
本発明の触媒において、所望に応じて用いられる(C)成分のルイス酸としては、例えば有機アルミニウム化合物,マグネシウム化合物,亜鉛化合物,リチウム化合物などを挙げることができる。
該有機アルミニウム化合物としては、一般式(IX)
R10 rAl(OR11)sHtZ1 u ・・・(IX)
で表される化合物を用いることができる。
上記一般式(IX)において、R10及びR11は、それぞれ炭素数1〜8のアルキル基を示し、それらはたがいに同一でも異なっていてもよい。Z1はハロゲン原子を示し、r,s,t及びuは0<r≦3、0<s≦3、0≦t<3、0≦u<3、r+s+t+u=3の関係を満たす数である。
上記一般式(IX)で表される有機アルミニウム化合物の具体例としては、t=u=0、r=3の化合物としてトリメチルアルミニウム,トリエチルアルミニウム,トリイソプロピルアルミニウム,トリイソブチルアルミニウム,トリオクチルアルミニウムなどを、t=u=0、1.5≦r<3の化合物としてジエチルアルミニウムエトキシド,ジブチルアルミニウムブトキシド,ジエチルアルミニウムセスキエトキシド,ジブチルアルミニウムセスキブトキシド、さらには部分的にアルコキシ化されたアルキルアルミニウムなどを、s=t=0の化合物としてジエチルアルミニウムジクロリド,ジブチルアルミニウムジクロリドなど(r=2)、エチルアルミニウムセスキクロリド,ブチルアルミニウムセスキクロリドなど(r=1.5)、エチルアルミニウムジクロリド,ブチルアルミニウムジクロリドなど(r=1)を、s=u=0の化合物としてジエチルアルミニウムハイドライド,ジイソブチルアルミニウムハイドライドなど(r=2)、エチルアルミニウムジハイドライド,ブチルアルミニウムジハイドライドなど(r=1)を挙げることができる。
また、マグネシウム化合物としては、例えばメチルマグネシウムブロミド,エチルマグネシウムブロミド,フェニルマグネシウムブロミド,ベンジルマグネシウムブロミドなどのグリニア化合物、ジエトキシマグネシウム,エチルブチルマグネシウムなどの有機マグネシウム化合物、塩化マグネシウムなどの無機マグネシウム化合物などが挙げられる。さらに、亜鉛化合物やリチウム化合物としては、例えばジエチル亜鉛などの有機亜鉛化合物、メチルリチウムなどの有機リチウム化合物などを挙げることができる。
本発明の触媒においては、上記(C)成分のルイス酸は一種用いてもよく、二種以上を組み合わせて用いてもよい。
本発明の触媒は、上記(A)及び(B)成分、あるいは(A),(B)及び(C)成分からなるものであるが、このほかにさらに他の触媒成分を加えることも可能である。各触媒成分の配合割合は、各種条件により異なり、一義的には定められないが、通常、(B)成分が有機硼素化合物の場合、(A)成分と(B)成分とのモル比は、好ましくは1:0.1〜1:103、より好ましくは1:1〜1:103の範囲で選ばれ、(B)成分がアルミノキサンの場合、(A)成分と(B)成分とのモル比は、好ましくは1:1〜1:10,000、(B)成分がイオン性化合物の場合、(A)成分と(B)成分とのモル比は、好ましくは1:0.1〜1:100の範囲で選ばれる。また、(C)成分を用いる場合は、(A)成分と(C)成分とのモル比は、好ましくは1:0.1〜1:10,000の範囲で選ばれる。
また、(A)成分と(B)成分と所望により用いられる(C)成分との接触方法としては、例えば▲1▼(A)成分と(B)成分との接触混合物に、(C)成分を加えて触媒とし、重合すべきモノマーと接触させる方法、▲2▼(B)成分と(C)成分との接触混合物に(A)成分を加えて触媒とし、重合すべきモノマーと接触させる方法、▲3▼(A)成分と(C)成分との接触混合物に(B)成分を加えて触媒とし、重合すべきモノマーと接触させる方法、▲4▼重合すべきモノマー成分に(A),(B),(C)成分を別々に接触させる方法、▲5▼重合すべきモノマー成分と(C)成分との接触混合物に、上記の▲1▼〜▲3▼で調製した触媒を接触させる方法などがある。
上記(A)成分と(B)成分と所望により用いられる(C)成分との接触は、重合温度下で行えることはもちろん、−20〜200℃の範囲で行うことも可能である。
本発明はオレフィン重合用触媒においては、特に該(A)成分として用いられる一般式(II),(III)の遷移金属化合物におけるM2及びM3が、それぞれチタニウム,ジルコニウム又はハフニウムであるものが好適である。
本発明のオレフィン系重合体の製造方法においては、上述した重合用触媒の存在下、オレフィン類を単独重合、オレフィン類二種以上を共重合又はオレフィン類と他の重合性不飽和化合物とを共重合させて、オレフィン系単独重合体又は共重合体を製造する。
該オレフィン類としては、例えばエチレン;プロピレン;ブテン−1;ペンテン−1;ヘキセン−1;ヘプテン−1;オクテン−1;ノネン−1;デセン−1;4−フェニルブテン−1;6−フェニルヘキセン−1;3−メチルブテン−1;4−メチルペンテン−1;3−メチルペンテン−1;3−メチルヘキセン−1;4−メチルヘキセン−1;5−メチルヘキセン−1;3,3−ジメチルペンテン−1;3,4−ジメチルペンテン−1;4,4−ジメチルペンテン−1;ビニルシクロヘキサン;ビニルトリメチルシランなどのα−オレフィン、ヘキサフルオロプロペン;テトラフルオロエチレン;2−フルオロプロペン;フルオロエチレン;1,1−ジフルオロエチレン;3−フルオロプロペン;トリフルオロエチレン;3,4−ジクロロブテン−1などのハロゲン置換α−オレフィン、シクロペンテン;シクロヘキセン;ノルボルネン;5−メチルノルボルネン;5−エチルノルボルネン;5−プロピルノルボルネン;5,6−ジメチルノルボルネン;1−メチルノルボルネン;7−メチルノルボルネン;5,5,6−トリメチルノルボルネン;5−フェニルノルボルネン;5−ベンジルノルボルネンなどの環状オレフィンなどを挙げることができる。これらのオレフィンは一種用いてもよく、二種以上を組み合わせて用いてもよい。二種以上のオレフィンの共重合を行う場合、上記オレフィン類を任意に組み合わせることができる。
また、本発明においては、上記オレフィン類と他の重合性不飽和化合物とを共重合させてもよく、この際用いられる他の重合性不飽和化合物としては、スチレン、p−メチルスチレン;o−メチルスチレン;m−メチルスチレン;2,4−ジメチルスチレン;2,5−ジメチルスチレン;3,4−ジメチルスチレン;3,5−ジメチルスチレン;p−t−ブチルスチレンなどのアルキルスチレン、p−クロロスチレン;m−クロロスチレン;o−クロロスチレン;p−ブロモスチレン;m−ブロモスチレン;o−ブロモスチレン;p−フルオロスチレン;m−フルオロスチレン;o−フルオロスチレン;o−メチル−p−フルオロスチレンなどのハロゲン化スチレン、さらには有機珪素スチレン,ビニル安息香酸エステル,ジビニルベンゼンなどの芳香族ビニル化合物、ブタジエン;イソプレン;1,5−ヘキサジエンなどの鎖状ジエン化合物、ノルボルナジエン;5−エチリデンノルボルネン;5−ビニルノルボルネン;ジシクロペンタジエンなどの環状ジエン化合物、アセチレン;メチルアセチレン;フェニルアセチレン;トリメチルシリルアセチレンなどのアセチレン類などが挙げられる。これらの他の単量体は一種用いてもよいし、二種以上を組み合わせて用いてもよい。
このような本発明のオレフィン系重合体の製造方法は、例えばオレフィン類と環状オレフィン類とを共重合させてオレフィン/環状オレフィン共重合体を製造するのに適している。この際、オレフィン類としては、前記例示したものの中から一種だけを選び用いてもよく、二種以上を選び混合して用いてもよい。また、環状オレフィン類としては、前記例示したものの中から一種だけを選び用いてもよく、二種以上を選び混合して用いてもよい。本発明の方法によると、オレフィン/環状オレフィン共重合体として、特に次の性状を有するものを効率よく製造することができる。
すなわち、(1)ゲルパーミエーションクロマトグラフィー法(GPC法)により測定された重量平均分子量(Mw)と数平均分子量(Mn)との比Mw/Mnが6以下であり、分子量分布が狭く、(2)環状オレフィン単位含有量が0.1〜95モル%の範囲にある。また、(3)デカリン中、135℃で測定した極限粘度〔η〕と、荷重2.16kgで測定したメルトインデックス(MI2.16)との関係が、式
〔η〕≦1.333−0.620×logMI2.16
を満たし、非ニュートン性を示すため成形加工特性に優れる。さらに、(4)分子量が大きく、デカリン中、135℃で測定した極限粘度〔η〕が、通常1.0デシリットル/g以上である。このような性状を有するオレフィン/環状オレフィン共重合体は、弾性率と弾性回復率とのバランスに優れ、低温物性が改善されるとともに、前記したように成形加工特性に優れるなどの特徴を有している。
上記の性状を有するオレフィン/環状オレフィン共重合体は、本発明以外の方法により製造してもよいが、本発明の方法を用いることにより、経済的に効率よく製造することができる。
また、本発明のオレフィン系重合体の製造方法は、例えばプロピレン単独重合、又はプロピレンと、炭素数2〜20の他のオレフィン類及び炭素数2〜20の他の重合性不飽和化合物の中から選ばれた少なくとも一種と共重合させて、非晶性高分子量プロピレン系単独重合体や共重合体を製造するのに適している。この際、触媒としては、(A)成分の一般式(II),(III)で表される遷移金属化合物がチタニウム化合物であるものが用いられる。また、プロピレンと共重合させる単量体としては前記例示したオレフィン類及び重合性不飽和化合物の中から、プロピレン以外のものを一種だけ選び用いてもよく、二種以上を選び混合して用いてもよい。本発明の方法によると、非晶性高分子量プロピレン系重合体として、特に次の性状を有するものを効率よく製造することができる。
すなわち、(1)デカリン中、135℃で測定した極限粘度〔η〕が1.0デシリットル/gより大きく、高分子量であり、(2)GPC法により測定した重量平均分子量(Mw)と数平均分子量(Mn)との比Mw/Mnが3未満で、分子量分布が狭く、かつ(3)融点(Tm)を有さず、ガラス転移点(Tg)が10℃未満である。このような性状を有する非晶性高分子量プロピレン系重合体は、単品でエラストマーなどとして利用でき、また熱可塑性オレフィン系エラストマー(TPO)の一成分としても利用価値が高い。
上記の性状を有する非晶性高分子量プロピレン系重合体は、本発明以外の方法により製造してもよいが、本発明の方法を用いることにより、経済的に効率よく製造することができる。
さらに、本発明のオレフィン系重合体の製造方法は、例えば炭素数2〜20のオレフィン類を単独重合,炭素数2〜20のオレフィン類二種以上を共重合又は炭素数2〜20のオレフィン類と炭素数2〜20の他の重合性不飽和化合物とを共重合させて、ビニル基含有量の高い低分子量オレフィン系重合体を製造するのに適している。この際、触媒としては、(A)成分の一般式(II),(III)で表される遷移金属化合物がジルコニウム又はハフニウム化合物であるものが用いられる。本発明の方法によると、ビニル基含有量の高い低分子量オレフィン系重合体として、特に次の性状を有するエチレン単独重合体、又はエチレンと、炭素数3〜20のオレフィン類及び炭素数2〜20の他の重合性不飽和化合物の中から選ばれた少なくとも一種との共重合体を効率よく製造することができる。
すなわち、(1)GPC法により測定したポリエチレン換算重量平均分子量(Mw)が200〜10,000で、かつ重量平均分子量(Mw)と数平均分子量(Mn)との比Mw/Mnが好ましくは5以下、より好ましくは3以下であり、(2)密度勾配管法で測定した密度が0.925g/cm3以上である。また、(3)全不飽和基に占めるビニル基の割合が70モル%以上で、赤外線分光分析で測定したビニル基含有量が1000炭素当たり1.5個以上である。不飽基としては、トランスビニレン基が963cm-1,末端ビニル基が910cm-1,ビニリデン基が888cm-1であることが知られており、これらの不飽和基は温度190℃でのプレスシート〔厚み(t)が0.1mm程度〕を作成し、赤外線分光分析により同定及び定量が可能である。該不飽和基の含有量の算出に当たっては、次式を用いることができる。ここで、nは1000炭素当たりの不飽和結合数である。
トランスビニレン基:n=0.83A963/(d×t)
末端ビニル基 :n=1.14A910/(d×t)
ビニリデン基 :n=1.09A888/(d×t)
〔A:吸光度,d:密度(g/cm3),t:試料厚さ(mm)〕
エチレン系重合体の場合、エチレンと共重合させる単量体は、前記例示したオレフィン類及び重合性不飽和化合物の中から、エチレン以外のものを一種だけ選び用いてもよく、二種以上を選び混合して用いてもよい。
このようなビニル基含有量の高い低分子量オレフィン系重合体はマクロモノマーとして利用可能であり、例えばオレフィン系共重合体のコモノマーとして利用することにより、ゲル化反応を伴うことなく容易に長鎖分岐を導入することができ、成形加工特性に優れるオレフィン系共重合体や、エラストマー,相溶化剤などとしての性能を有するオレフィン系共重合体を与えることができる。また、該末端ビニル基含有量の高い低分子量オレフィン系重合体を水添処理することにより、ワックスなどとして利用することができる。さらに、各種反応試剤で処理することにより、末端修飾マクロモノマーとして、例えば縮合系共重合体のコモノマーに用いられ、接着剤,表面改質剤,相溶化剤,コンポジット材料などに利用できる。
上記の性状を有するビニル基含有量の高い低分子量オレフィン系重合体は、本発明以外の方法により製造してもよいが、本発明の方法を用いることにより、経済的に効率よく製造することができる。
本発明のオレフィン系重合体の製造方法における重合形式については、特に制限はなく、塊状重合でもよく、また、ペンタン,ヘキサン,ヘプタンなどの脂肪族炭化水素、シクロヘキサンなどの脂環式炭化水素、あるいはベンゼン,トルエン,キシレン,エチルベンゼンなどの芳香族炭化水素溶媒中で行ってもよい。また、適当な担体の上に触媒を担持して、溶媒中又は気相中で重合を行ってもよい。
重合温度は一般に0〜200℃であり、また、気体状モノマーを使用する際の気体状モノマーの分圧は、一般には300気圧以下、好ましくは30気圧以下である。また、分子量の調節,活性向上などの目的で水素などを加えることもできる。
次に、実施例により本発明をさらに詳細に説明するが、本発明はこれらの例によってなんら限定されるものではない。
なお、実施例1及び実施例2における反応は、特に記載のない場合、不活性ガス下又は気流下で行った。また、ポリマーの極限粘度〔η〕は、135℃,デカリン中で測定した値である。
実施例1
(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕の製造
(1)2,3,4,5,6,7−ヘキサメチル−1−オンの合成
三塩化アルミニウム58.7g(440ミリモル)を乾燥二硫化炭素(水素化カルシウム上より乾燥蒸留)300ミリリットルに懸濁して氷冷温度に置いた。チグロイルクロリド47.4g(400ミリモル)とテトラメチルベンゼン53.7g(400ミリモル)とを混合し、上記二硫化炭素溶液に滴下したのち、室温で攪拌を続けることにより、褐色から赤褐色の溶液が生成した。2時間攪拌後、さらに還流下に2時間反応を行うことにより、溶液はオレンジ色へ変化した。
反応混合物を室温に戻したのち、500gの水と500ミリリットルの濃塩酸との混合物上へ注ぎ、1時間程度攪拌後、エーテル400ミリリットルで2回、200ミリリットルでさらに2回抽出、分離操作を行い、エーテル相を合わせて無水塩化カルシウムで乾燥した。乾燥剤をろ別後、エーテルを留去し、得られた褐色の粘稠固体をヘキサンに溶かして再結晶した。室温飽和溶液を−20℃で放置し、析出物をろ取する操作を繰り返し、赤黄色固体として2,3,4,5,6,7−ヘキサメチルインダン−1−オン75.9gを得た。
(2)1,2,4,5,6,7−ヘキサメチルインデンの合成
リチウムアルミニウムハイドライド(LAH)3.09g(81ミリモル)を乾燥エーテル(金属ナトリウム上より蒸留)に懸濁した。上記(1)で合成した2,3,4,5,6,7−ヘキサメチルインダン−1−オン38.7g(180ミリモル)を200ミリリットルの乾燥エーテルに溶解し、上記LAH懸濁液に緩やかな還流が起こる程度の速度で滴下した。1.5時間で滴下を終了したのち、加熱還流下に2.5時間攪拌を続けた。氷冷下、水20ミリリットル、次いでINの塩化アンモニウム水溶液200ミリリットルでクエンチし、有機相を分離したのち、エーテル100ミリリットルで2回抽出分離操作を行い、有機相を合わせて、飽和塩化ナトリウム水溶液で洗浄後、無水硫酸マグネシウムで乾燥した。乾燥剤をろ別し、エーテル溶液を窒素置換して、ヨウ素小片を加えて脱水反応を行ったのち、窒素下に一晩放置後、3時間加熱還流し、反応を完結させた。
次いで、0.2Nのハイドロサルファイトナトリウム水溶液150ミリリットルで2回、飽和塩化ナトリウム水溶液150ミリリットルで2回洗浄後、無水硫酸マグネシウムで乾燥した。乾燥剤をろ別し、エーテルを除去して、黄色の粗1,2,4,5,6,7−ヘキサメチルインデンを得たのち、これを再度ヘキサン300ミリリットルに溶解し、無水硫酸マグネシウムで乾燥することにより、黄色の溶液が得られた。乾燥剤をろ別し、ヘキサンを留去して黄色の固体を得たのち、これを20gのシリカゲルにヘキサン溶液から吸着させ、80gのシリカゲルカラムより、ヘキサンで流し出し、目的の1,2,4,5,6,7−ヘキサメチルインデン28.8g(144ミリモル)を黄白色固体として得た。収率80.4%。
(3)1−(クロロジメチルシリル)−2,3,4,5,6,7−ヘキサメチルインデンの合成
1,2,4,5,6,7−ヘキサメチルインデン14.4g(72ミリモル)を乾燥テトラヒドロフラン150ミリリットルに溶解したのち、氷冷下、t−ブチルリチウム(1.7M/ペンタン溶液)47ミリリットルを滴下して室温で2時間攪拌後、揮発分を減圧留去し、次いで、ヘキサン不溶分をろ取、ヘキサン洗浄後乾燥して黄白色固体を得た。これを脱水テトラヒドロフラン150ミリリットルに溶解(赤色溶液)し、−78℃で単蒸留したジメチルクロロシラン10.9g(85ミリモル,10.3ミリリットル)を加えて室温に戻し、終夜放置したのち、得られた黄色の溶液から揮発分を減圧下で除き、次いで、ヘキサン不溶分をろ過により除き、ヘキサン可溶分より揮発分を減圧により留去させることにより、1−(クロロジメチリシリル)−2,3,4,5,6,7−ヘキサメチルインデン19.8gを白色固体として回収した。
(4)1−(t−ブチルアミノ−ジメチルシリル)−2,3,4,5,6,7−ヘキサメチルインデンの合成
1−(クロロジメチルシリル)−2,3,4,5,6,7−ヘキサメチルインデン19.8gを脱水エーテル150ミリリットルに溶解し、氷冷下、t−ブチルアミン13.2gを加え、室温に戻して二昼夜攪拌した。揮発分を減圧下に留去したのち、ヘキサン300ミリリットルで抽出し、不溶の塩をろ別後、ヘキサン溶液から溶媒を減圧留去することにより、淡黄色のオイルが得られ、室温で放置して白色の固体22.0gを得た。
(5)(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリドの合成
1−(t−ブチルアミノ−ジメチルシリル)−2,3,4,5,6,7−ヘキサメチルインデン10.1gを脱水エーテル150ミリリットルに溶解し、氷冷下1.6Mのn−ブチルリチウム/ヘキサン溶液31ミリリットルを滴下し、室温で二昼夜攪拌したのち、得られた赤色の溶液から溶媒を減圧留去し、ヘキサン不溶部をろ取後、さらにヘキサンで洗浄することにより黄色の固体を得た。この黄色のリチウム塩とTiCl3(thf)311.5gとを固体で混ぜ、乾燥テトラヒドロフラン200ミリリットルを加えて1時間攪拌したのち、塩化銀4.7gを加えてさらに2時間攪拌後、揮発分を減圧留去し、エーテル不溶分をろ別した。溶液からエーテルを留去したのち、トルエン/ヘキサン溶液から再結晶することにより、純粋な(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリドが得られた。
この化合物は、重クロロホルム溶媒中での1H−NMRより、2.70ppm(3水素),2.575ppm(3水素),2.452ppm(3水素),2.338ppm(3水素),2.305ppm(3水素),2.266ppm(3水素),1.372ppm(9水素),0.853ppm(3水素),0.735ppm(3水素)のシグナルを与える。
実施例2
(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルジルコニウムジクロリド
〔Me2Si(Me6Ind)(t−BuN)ZrCl2〕の製造
実施例1−(4)で得られた1−(t−ブチルアミノ−ジメチルシリル)−2,3,4,5,6,7−ヘキサメチルインデン10.0gを脱水エーテル150ミリリットルに溶解し、氷冷下1.6Mのn−ブチルリチウム/ヘキサン溶液(和光純薬社製)50ミリリットルを滴下し、室温で一昼夜攪拌した。得られた溶液から、室温で揮発分を減圧留去し、ヘキサン100ミリリットルに溶媒置換した。次いで、ヘキサン不溶部をろ取し、ヘキサン洗浄後減圧乾燥することにより、1−(t−ブチルアミド−ジメチルシリル)−2,3,4,5,6,7−ヘキサメチルインデニルジリチウムを黄色の固体として得た。
次に、この固体を脱水エーテル50ミリリットルに溶解し、ドライアイス/エタノール浴で冷却した。別容器で、四塩化ジルコニウム7.2gを脱水トルエンに懸濁し、ドライアイス/エタノール浴で冷却して脱水エーテル70ミリリットルを加え、この懸濁液に上記1−(t−ブチルアミド−ジメチルシリル)−2,3,4,5,6,7−ヘキサメチルインデニルジリチウム/エーテル溶液を加え、冷却したまま1時間混合攪拌した。この後、徐々に室温まで昇温し、室温で二昼夜攪拌した。得られた溶液から、室温で揮発分を減圧留去したのち、これに脱水トルエン240ミリリットルを加え、可溶分を抽出した。次いで、抽出相を減圧濃縮により全量を30ミリリットルにしたのち、これにヘキサン120ミリリットルを加え、ろ過し、ろ液より溶媒を減圧留去することにより、粘度の高いオイルが得られた。
このオイルにヘキサン50ミリリットルを加え、−60℃で不溶物をろ取し、さらに冷ヘキサン30ミリリットルで洗浄することにより、(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルジルコニウムジクロリド5.06gが得られた。
この化合物は、重クロロホルム溶媒中での1H−NMRより、2.70ppm(3H,s)、2.64ppm(3H,s)、2.49ppm(3H,s)、2.34ppm(3H,s)、2.28ppm(3H,s)、2.25ppm(3H,s)、1.34ppm(9H,s)、0.80ppm(3H,s)、0.76ppm(3H,s)のシグナルを与える。
実施例3
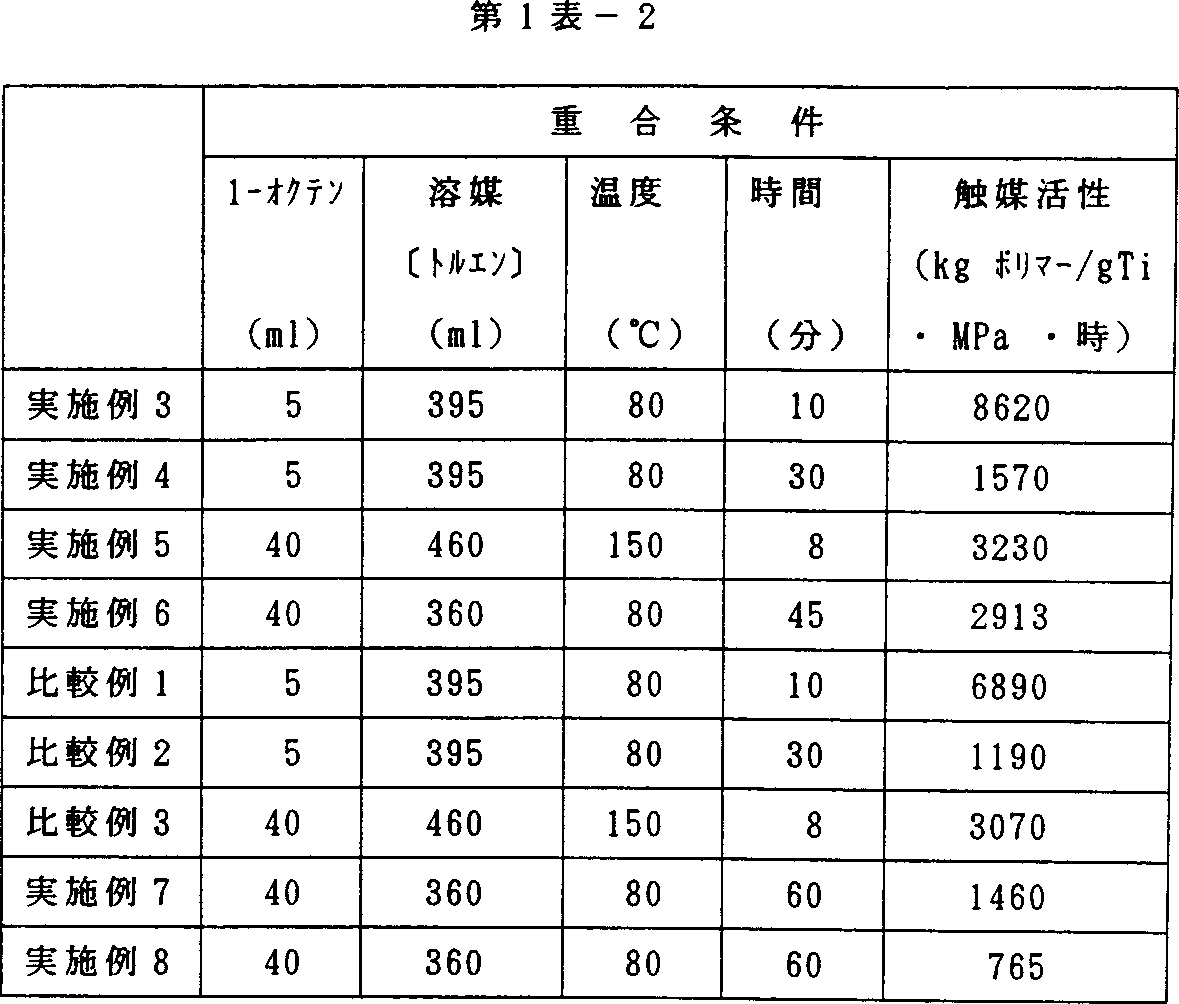
1リットルのオートクレーブにトルエン395ミリリットル及び1−オクテン5ミリリットルを加え80℃に加温したのち、これにアルミニウム換算で1モル/リットルのメチルアルミノキサン(MAO)3ミリリットルと1ミリモル/リットルの実施例1で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me2Ind)(t−BuN)TiCl2〕0.5ミリリットル(いずれもトルエン溶液)を加え、エチレンを導入し、全圧0.8MPa,80℃に維持して10分間重合した。未反応のガスを脱圧し、少量のメタノールを加えて反応を停止して、降温後、内容物をメタノール5リットルで洗浄した。
得られたエチレン/1−オクテン共重合体の乾燥重量は27.5gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
実施例4
1リットルのオートクレーブにトルエン395ミリリットル及び1−オクテン5ミリリットルを加え80℃に加温したのち、これに1モル/リットルのトリイソブチルアルミニウム(TIBA)1ミリリットルと1ミリモル/リットルの実施例1で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕0.5ミリリットルと1ミリモル/リットルのN,N−ジメチルアニリニウムテトラキス(ペンタフルオロフェニル)ボレート(〔N,N−Me2PhNH〕〔B(C6F5)4〕)0.5ミリリットル(いずれもトルエン溶液)を加え、エチレンを導入し、全圧0.8MPa,80℃に維持して30分間重合した。未反応のガスを脱圧し、少量のメタノールを加えて反応を停止して、降温後、内容物をメタノール5リットルで洗浄した。
得られたエチレン/1−オクテン共重合体の乾燥重量は15.0gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
実施例5
1リットルのオートクレーブにトルエン460ミリリットル及び1−オクテン40ミリリットルを加え150℃に加温し、エチレンを全圧2.4MPaで導入した。これに、アルミニウム換算で1モル/リットルのメチルアルミノキサン(MAO)6ミリリットルと1ミリモル/リットルの実施例1で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕1.0ミリリットル(いずれもトルエン溶液)を加え、150℃に維持して8分間重合した。未反応のガスを脱圧し、少量のメタノールを加えて反応を停止して、降温後、内容物をメタノール5リットルで洗浄した。
得られたエチレン/1−オクテン共重合体の乾燥重量は49.5gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
実施例6
実施例3において、トルエン360ミリリットル、1−オクテン40ミリリットル、メチルアルミノキサン(MAO)をアルミニウム換算で0.2ミリモル、(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕1.0マイクロモル、さらにトリイソブチルアルミニウム1.5ミリモルを使用した以外は、実施例3と同様に重合し、45分で重合反応を停止した。
得られたエチレン/1−オクテン共重合体の乾燥重量は83.7gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
比較例1
実施例3において、(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕の代わりに(t−ブチルアミド)(2,3,4,5−テトラメチルシクロペンタジエニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me4Cp)(t−BuN)TiCl2〕を用いた以外は、実施例3と同様にしてエチレン/1−オクテン共重合体を製造した。
得られたエチレン/1−オクテン共重合体の乾燥重量は22.0gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
比較例2
実施例4において、(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕の代わりに(t−ブチルアミド)(2,3,4,5−テトラメチルシクロペンタジエニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me4Cp)(t−BuN)TiCl2〕を用いた以外は、実施例4と同様にしてエチレン/1−オクテン共重合体を製造した。
得られたエチレン/1−オクテン共重合体の乾燥重量は11.4gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
比較例3
実施例5において、(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕の代わりに(t−ブチルアミド)(2,3,4,5−テトラメチルシクロペンタジエニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me4Cp)(t−BuN)TiCl2〕を用いた以外は、実施例5と同様にしてエチレン/1−オクテン共重合体を製造した。
得られたエチレン/1−オクテン共重合体の乾燥重量は47.1gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
実施例7
実施例6において、メチルアルミノキサン(MAO)の代わりにテトライソブチルアルミノキサン(iBu2AlOAliBu2)をアルミニウム換算で3.0ミリモル用い、かつ、トリイソブチルアルミニウム(TIBA)を用いなかったこと以外は、実施例6と同様に重合し、60分で重合反応を停止した。
得られたエチレン/1−オクテン共重合体の乾燥重量は56.0gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
実施例8
実施例6において、メチルアルミノキサン(MAO)の代わりにトリス(ジメチルアルミノ)ボロキサン〔B(OAlMe2)3〕をアルミニウム換算で3.0ミリモル使用し、かつ、トリイソブチルアルミニウム(TIBA)を1.0ミリモル用いた以外は、実施例6と同様に重合し、60分で重合反応を停止した。
得られたエチレン/1−オクテン共重合体の乾燥重量は29.3gであった。重合条件、触媒活性、ポリマーの物性を第1表に示す。
実施例9
1リットルのオートクレーブにトルエン400ミリリットルを入れ、50℃に加温したのち、これにアルミニウム換算1モル/リットルのメチルアルミノキサン(MAO)3ミリリットルと1ミリモル/リットルの実施例1で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕5ミリリットル(いずれもトルエン溶液)を加え、プロピレンを全圧0.8MPaで導入し続け、50℃に維持し15分間重合した。未反応のガスを脱圧し、少量のメタノールを加えて反応を停止して、降温後、内容物をメタノール5リットルで洗浄した。
得られたポリマーの乾燥重量は71.5gであった。このポリマーは、示差走査熱量分析(DSC)では融点(Tm)は観測されず、非晶性であり、ガラス転移点(Tg)は0℃であった。また、同位体炭素核磁気共鳴(13C−NMR)スペクトルの測定か、メソトライアッド〔mm〕が18モル%、ラセミトライアッド〔rr〕が34モル%のアタクチックポリプロピレンであった。重合条件、触媒活性、ポリマーの物性を第2表に示す。
実施例10
実施例9において、メチルアルミノキサン(MAO)(エチル社製)のトルエン溶液をアルミニウム換算で3.0ミリモル、トリイソブチルアルミニウム(TIBA)を0.5ミリモル、(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕を2.0マイクロモル使用し、60分間重合した以外は、実施例9と同様に実施した。
得られたポリマーの乾燥重量は72.9gであった。このポリマーは、実施例9と同様に融点(Tm)は観測されず、非晶性でガラス転移点(Tg)は0℃あり、メソペンタッド分率〔mmmm〕が2モル%,メソトライアッド〔mm〕が16モル%,ラセミトライアッド〔rr〕が37モル%のアタクチックポリプロピレンであった。重合条件、触媒活性、ポリマーの物性を第2表に示す。
実施例11
攪拌機を備えた内容積500ミリリットルのステンレス製耐圧反応器を減圧乾燥し、窒素置換したのち、トルエン160ミリリットル,1−オクテン5ミリリットル,トリイソブチルアルミニウム(TIBA)0.3ミリモル,メチルアルミノキサン(MAO)(東ソー・アグソ社製)をアルミニウム換算で1.5ミリモル,実施例1で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕1.0マイクロモルを入れ、50℃でプロピレンを連続的に供給し、内圧を0.8MPaに保ち、1時間重合を行った。重合反応終了後、過剰のプロピレンを脱圧して除き、メタノール5ミリリットルを加えて反応を停止させた。内容物を酸性メタノール1500ミリリットル中で2時間攪拌し、不溶物をろ取した。不溶物を、再度メタノール1500ミリリットル中で洗浄し、得られたポリマーを80℃で減圧乾燥した。
ポリマーの乾燥重量は16.6gであった。このポリマーは、実施例9と同様に融点(Tm)は観測されず、非晶性でガラス転移点(Tg)が−1℃であった。重合条件、触媒活性、ポリマーの物性を第2表に示す。
実施例12
攪拌機を備えた内容積500ミリリットルのステンレス製耐圧反応器を減圧乾燥し、窒素置換したのち、トルエン200ミリリットル、メチルアルミノキサン(MAO)(東ソー・アグソ社製)をアルミニウム換算で1.0ミリモル、実施例2で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルジルコニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)ZrCl2〕1.0マイクロモルを入れ、80℃でエチレンを連続的に供給し、内圧を0.8MPaに保ち、1時間重合を行った。重合反応終了後、過剰のエチレンを脱圧して除き、メタノール5ミリリットルを加えて反応を停止させた。内容物を酸性メタノール1500ミリリットル中で2時間攪拌し、不溶物をろ取した。不溶物を再度メタノール1500ミリリットル中で洗浄し、得られたポリマーを80℃で減圧乾燥し、ポリエチレン4.74gを得た。
このポリエチレンは、赤外線分光分析(IR)で観測できた不飽和結合は910cm-1の末端ビニル基のみであり、このビニル基の含有量は1000炭素当たり7.87個であった。重合条件、ポリマー収量、ポリマー物性を第3表に示す。
実施例13
実施例12において、メチルアルミノキサン(MAO)の量のアルミニウム換算で6.0ミリモルに変えた以外は、実施例12と同様に実施した。重合条件、ポリマー収量、ポリマー物性を第3表に示す。
実施例14
実施例12において、さらにトリイソブチルアルミニウム(TIBA)0.4ミリモルを用いた以外は、実施例12と同様にして実施した。重合条件、ポリマー収量、ポリマー物性を第3表に示す。
比較例4
攪拌機を備えた内容積500ミリリットルのステンレス製耐圧反応器を減圧乾燥し、窒素置換したのち、トルエン200ミリリットル,トリイソブチルアルミニウム(TIBA)0.2ミリモル,メチルアルミノキサン(MAO)(東ソー・アグソ社製)をアルミニウム換算で1.0ミリモル、(t−ブチルアミド)(テトラメチルシクロペンタジエニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me4Cp)(t−BuN)TiCl2〕1.0マイクロモルを入れ、80℃でエチレンを連続的に供給し、内圧を0.4MPaに保ち、1時間重合を行った。重合反応終了後、過剰のエチレンを脱圧して除き、メタノール5ミリリットルを加えて反応を停止させた。内容物を酸性メタノール1500ミリリットル中で2時間攪拌し、不溶物をろ取した。不溶物を再度メタノール1500ミリリットル中で洗浄し、得られたポリマーを80℃で減圧乾燥し、ポリエチレン31.7gを得た。
このポリエチレンは、IR分析で不飽和結合は観測されなかった。重合条件、ポリマー収量、ポリマーの物性を第3表に示す。
実施例15
窒素雰囲気下、150℃に昇温した2リットルのオートクレーブに、乾燥ヘキサン640ミリリットル,メチルアルミノキサン(MAO)をアルミニウム換算で1.5ミリモル,2−ノルボルネン70重量%を含有するヘキサン溶液300ミリリットル(2−ノルボルネンとして1.74モル)を、この順番に仕込んだ。次いで、触媒投入管に乾燥ヘキサン120ミリリットル,メチルアルミノキサン(MAO)1.5ミリモル(アルミニウム換算),実施例1で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me6Ind)(t−BuN)TiCl2〕6マイクロモルをこの順番に加えた。
次に、エチレン分圧が3.0MPaになるようにエチレンを導入したのち、触媒投入管より触媒溶液を投入し、エチレン分圧が3.0MPaになるように連続的にエチレンを導入しながら、5分間反応を行った。反応終了後、イソプロピルアルコールにより重合を停止し、フラッシュドラムにフラッシュさせて粉末状のエチレン/2−ノルボルネン共重合体65.6gを得た。触媒活性は229kg/gTiであった。
また、この共重合体は2−ノルボルネン単位含有量5.6モル%、極限粘度〔η〕2.83デシリットル/g、融点(Tm)83℃(ブロード)であり、GPC法により測定した分子量は、重量平均分子量(Mw)が196,000、数平均分子量(Mn)が60,500で、Mw/Mnが3.24であった。また、メルトインデックスは、MI21.6(荷重21.6kg)が0.34g/10分,MI2.16(荷重2.16kg)が0.007g/10分であった。
重合条件,触媒活性,ポリマーの物性を第4表に示す。
実施例16
予め乾燥ヘキサン120ミリリットル,メチルアルミノキサン(MAO)1.5ミリモル(アルミニウム換算)及び実施例1で得られた(t−ブチルアミド)(2,3,4,5,6,7−ヘキサメチルインデニル)−ジメチルシリルチタニウムジクロリド6マイクロモルを混合し、窒素下、室温で24時間放置したものを触媒投入管に加え、重合温度を170℃とした以外は実施例15と同様の操作を行った。
重合条件,触媒活性,ポリマーの物性を第4表に示す。
実施例17〜19
第4表に示す重合条件にて、実施例15と同様にしてエチレン/2−ノルボルネン共重合体を製造した。
重合条件,触媒活性,ポリマーの物性を第4表に示す。
比較例5
(A)成分の触媒として、(t−ブチルアミド)(テトラメチルシクロペンタジエニル)−ジメチルシリルチタニウムジクロリド〔Me2Si(Me4Cp)(t−BuN)TiCl2〕6マイクロモルを用い、第4表に示す重合条件にて、実施例15と同様にしてエチレン/2−ノルボルネン共重合体を製造した。重合条件,触媒活性,ポリマーの物性を第4表に示す。
溶媒としてヘキサン640ml使用し、重合時間は5分間である。
産業上の利用の可能性
本発明の遷移金属化合物は、五員環側に遷移金属元素と結合する置換基以外に、少なくとも一つの置換基をもつ置換インデニル基をπ配位子として有する新規な遷移金属化合物であって、オレフィン重合用触媒成分として有用である。この遷移金属化合物を含有する本発明のオレフィン重合用触媒は、高活性を有し、残留金属量の少ない品質の良好な通常のオレフィン系単独重合体や共重合体、あるいは弾性率と弾性回復率のバランスに優れる上、低温物性が改善され、かつ成形加工性が向上したオレフィン/環状オレフィン共重合体,エラストマーなどとして有用な分子量分布の狭い非晶性高分子量プロピレン系重合体及びマクロモノマーなどとして有用なビニル基含有量の高い低分子量オレフィン系重合体を、経済的に効率よく与えることができる。 Technical field
The present invention relates to a transition metal compound, an olefin polymerization catalyst containing the transition metal compound, and a method for producing an olefin polymer using the catalyst. More specifically, the present invention relates to a transition metal compound having a specific substituted indenyl group as a π ligand useful as an olefin polymerization catalyst component, a highly active olefin polymerization catalyst containing the transition metal compound, and the catalyst. Using ordinary olefin homopolymers and copolymers with low residual metal content and good quality, or excellent balance between elastic modulus and elastic recovery rate, improved low-temperature properties and improved moldability A low molecular weight olefin polymer with a high vinyl group content useful as an amorphous high molecular weight propylene polymer having a narrow molecular weight distribution useful as an olefin / cyclic olefin copolymer, elastomer, etc., and a macromonomer, etc. It relates to a method of manufacturing well.
Background art
Olefin polymers such as polyethylenes and polypropylenes are widely used in many fields as general-purpose resins. This olefin polymer is known to be produced by a catalyst system based on a Ziegler-Natta catalyst, but in recent years it has one π ligand, and the π ligand and the central metal element are Attempts have been made to produce an olefin polymer using a polymerization catalyst having a transition metal compound bonded through an arbitrary group as a catalyst component.
For example, in European Publication No. 420436, International Patent Publication No. 92-00333, European Publication No. 418044, No. 416815, No. 468651, No. 495375, No. 514828, No. 520732, etc. Olefin polymerization catalyst comprising a transition metal compound having one π ligand and the π ligand and a central metal element bonded via an arbitrary group, and an olefin system using the catalyst A method for producing a polymer is disclosed.
However, among these, those in which the π ligand is an indenyl group are all unsubstituted, and their activities are not always satisfactory.
On the other hand, cyclic olefin copolymers such as copolymers of α-olefins and cyclic olefins, or copolymers of α-olefins, cyclic olefins and cyclic diene compounds are disclosed in Japanese Patent Laid-Open Nos. 5-230144 and JP-A No. 5-261875, etc.), and is excellent in optical properties such as transparency, flexibility, elastic recovery, and the like, it can be used as films and sheets in various fields such as medical, packaging, and food products. In addition, a cyclic olefin random copolymer having a good balance of mechanical properties, optical properties, heat resistance and the like by copolymerizing ethylene with a specific cyclic olefin is also known (Japanese Patent Laid-Open No. 60-168708). No., JP-A 61-98780, etc.).
By the way, there are a wide variety of molding methods for olefin polymers, and typical molding methods include injection molding, extrusion molding, blow molding, inflation molding, compression molding, and vacuum molding. In such molding methods, attempts have been made for many years to impart high-speed moldability and lower energy in the molding process in order to improve the processing characteristics and reduce the processing cost. Therefore, it is an important issue to impart optimal physical properties and to perform molding with optimal processing characteristics.
In recent years, it has been clarified that homogeneous metallocene catalysts are excellent in copolymerization between olefins, have a narrow molecular weight distribution of the resulting polymer, and exhibit extremely high catalytic activity compared to conventional vanadium catalysts. It was. Therefore, it is expected to expand into various application fields by utilizing such characteristics. However, polyolefins obtained with metallocene-based catalysts have many problems in their molding process characteristics, and have the disadvantage that they are subject to restrictions during blow molding and inflation molding.
In order to improve the moldability of the cyclic olefin copolymer, JP-A-5-271485 discloses a cyclic olefin copolymer having a specific glass transition temperature (Tg) having a different intrinsic viscosity [η]. It is disclosed that by forming a composition using two types, a cyclic olefin copolymer composition having a low melt viscosity, less melt fracture, and excellent molding processability can be obtained. However, when two types of compositions having different intrinsic viscosities [η] are used to form a composition, the molecular weight distribution becomes wider, causing problems such as a decrease in mechanical properties of the film, particularly a decrease in film strength and a decrease in transparency. .
Therefore, it has been desired to develop a method for efficiently producing a cyclic olefin copolymer having excellent mechanical properties, improved melt fluidity, and good moldability.
On the other hand, high molecular weight atactic polypropylene (high molecular weight amorphous polypropylene) can be used alone as an elastomer or as a component of a thermoplastic olefin elastomer (TPO), and has a particularly narrow molecular weight distribution. The utility value of high molecular weight atactic polypropylene is high. However, atactic polypropylene obtained with conventional catalyst systems has a low molecular weight and is only obtained as a by-product of isotactic polypropylene currently produced industrially. In addition, US Pat. No. 5,026,798 discloses a technique for homopolymerizing propylene using a catalyst system similar to the present invention in which an unsubstituted indenyl group is a π ligand. In this case, The polymer produced is crystalline isotactic polypropylene (melting point 147 ° C., pentad fraction 74.7 mol%), has low catalytic activity, and is a low molecular weight substance (71,300 in weight average molecular weight). Therefore, development of a method for efficiently producing a high molecular weight atactic polypropylene having a narrow molecular weight distribution has been desired.
On the other hand, a low molecular weight olefin polymer having a high terminal vinyl group content can be used as a macromonomer. For example, by using it as a comonomer of an olefin copolymer, long chain branching can be easily introduced without a gelation reaction, and the olefin copolymer, elastomer, and compatibilization with excellent molding process characteristics. An olefin copolymer having performance as an agent or the like can be provided. Further, the low molecular weight olefin polymer having a high terminal vinyl group content can be used as a wax or the like by hydrogenation treatment. Further, by treating with various reaction reagents, it is used as a terminal-modified macromonomer, for example, as a comonomer of a condensation copolymer, and can be used as an adhesive, a surface modifier, a compatibilizing agent, a composite material, and the like.
Disclosure of the invention
An object of the present invention is to provide a transition metal compound useful as a catalyst component for olefin polymerization, a highly active olefin polymerization catalyst containing the transition metal compound, and a normal quality of good quality with a small amount of residual metal using the catalyst. An olefin homopolymer or copolymer, or an amorphous high molecular weight propylene polymer having a narrow molecular weight distribution useful as an olefin / cyclic olefin copolymer, an elastomer, etc. having excellent mechanical properties and good moldability It is to provide a low molecular weight olefin polymer having a high vinyl group content useful as a macromonomer and a method for efficiently producing the same.
Therefore, as a result of intensive studies to achieve the above object, the present inventors have found that a transition metal compound having a substituted indenyl group having a specific structure as a π ligand is useful as a catalyst component for olefin polymerization. In addition, a catalyst comprising a combination of the transition metal compound, an organoboron compound, an aluminoxane, a specific ionic compound, and an optional Lewis acid has a high activity. It has been found that good quality olefin homopolymers and copolymers with low quality can be produced economically and efficiently. Furthermore, by appropriately selecting the transition metal compound, an olefin / cyclic olefin copolymer having the above preferred properties, an amorphous high molecular weight propylene polymer, and a low molecular weight olefin polymer having a high vinyl group content are obtained. It was found that it can be obtained economically and efficiently. The present invention has been completed based on such findings.
That is, the present invention
(1) A transition metal compound having a substituted indenyl group having at least one substituent other than a substituent bonded to a transition metal element on the five-membered ring side as a π ligand,
(2) an olefin polymerization catalyst comprising a transition metal compound having, as a π ligand, a substituted indenyl group having at least one substituent other than the substituent bonded to the transition metal element on the five-membered ring side;
(3) (A) General formula (II)
And general formula (III)
[In the formula, R1, R2, RThreeAnd RFourAre each a hydrogen atom, a halogen atom, an aliphatic hydrocarbon group having 1 to 20 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, an alkoxy group having 1 to 20 carbon atoms, an aryloxy group having 6 to 20 carbon atoms, A thioalkoxy group having 1 to 20 carbon atoms, a thioaryloxy group having 6 to 20 carbon atoms, an amino group, an amide group, a carboxyl group or an alkylsilyl group;1And RThreeAre each a group other than a hydrogen atom, and a plurality of R1, Multiple R2, Multiple RThreeAnd multiple RFourMay be the same or different from each other. M2And MThreeAre each a group 3-10 of the periodic table or a lanthanoid series metal element,2And XThreeAre respectively σ ligand, L2And LThreeAre respectively Lewis base and Q1And Q2Are each an aliphatic hydrocarbon group having 1 to 6 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, a silylene group having 1 to 5 silicon atoms, or a germylene group having 1 to 5 germanium atoms, J1And J2Each represents an amide group, a phosphide group, an oxygen atom, a sulfur atom or an alkylidene group, and a plurality of X2, Multiple XThree, Multiple L2And multiple LThreeMay be the same or different from each other. c and e are M2And MThreeWhere d and f are 0, 1 or 2. ]
And (B) (a) an organoboron compound, (b) an aluminoxane, and (c) an ionic compound consisting of a non-coordinating anion and a cation. An olefin polymerization catalyst comprising a combination with at least one selected from
(4) (A) at least one selected from the transition metal compounds represented by the general formulas (II) and (III), (B) (a) an organoboron compound, (b) an aluminoxane, and (c ) An olefin polymerization catalyst comprising a combination of (C) a Lewis acid and at least one selected from ionic compounds comprising non-coordinating anions and cations;
as well as
(5) In the presence of the catalyst of the above (2) to (4), homopolymerizing olefins, copolymerizing two or more olefins, or copolymerizing olefins and other polymerizable unsaturated compounds. A feature of the present invention is to provide a method for producing an olefin polymer.
Furthermore, the present invention provides
(6) (1) The ratio Mw / Mn of the weight average molecular weight (Mw) to the number average molecular weight (Mn) measured by gel permeation chromatography is 6 or less, and (2) the content of cyclic olefin units is 0. 1 to 95 mol%, and (3) an intrinsic viscosity [η] measured at 135 ° C. in decalin and a melt index (MI2.16) Is an expression
[Η] ≦ 1.333−0.620 × logMI2.16
Olefin / Cyclic olefin copolymer satisfying
as well as
(7) Intrinsic viscosity [η] measured at 135 ° C. in (1) decalin is greater than 1.0 deciliter / g, (2) Weight average molecular weight (Mw) and number average measured by gel permeation chromatography method Also provided is a propylene polymer having a molecular weight (Mn) ratio Mw / Mn of less than 3 and (3) having no melting point (Tm) and a glass transition point (Tg) of less than 10 ° C. To do.
A preferred embodiment of the present invention is as follows.
(8) The method of (5) above, wherein an olefin / cyclic olefin copolymer is produced by copolymerizing an olefin and a cyclic olefin,
(9) The ratio Mw / Mn of the weight average molecular weight (Mw) and the number average molecular weight (Mn) measured by gel permeation chromatography method is 6 or less when the olefin / cyclic olefin copolymer is: 2) The cyclic olefin unit content is 0.1 to 95 mol%, and 3) the melt viscosity (MI) measured with decaline at an intrinsic viscosity [η] measured at 135 ° C. and a load of 2.16 kg.2.16) Is an expression
[Η] ≦ 1.333−0.620 × logMI2.16
The method of (8), which satisfies
(10) In the transition metal compound of component (A), M in the general formulas (II) and (III)2And MThreeIs a catalyst for polymerization according to the above (3) and (4), each of which is titanium,
(11) In the transition metal compound of component (A), M in the general formulas (II) and (III)2And MThreeAre the catalyst for polymerization according to the above (3) and (4), each of which is zirconium or hafnium,
(12) In the presence of the catalyst of (10) above, propylene is homopolymerized, or selected from propylene, other olefins having 2 to 20 carbon atoms, and other polymerizable unsaturated compounds having 2 to 20 carbon atoms The method of (5) above, wherein an amorphous high molecular weight propylene-based polymer is produced by copolymerizing at least one kind of
(13) The amorphous high molecular weight propylene-based polymer has (1) intrinsic viscosity [η] measured at 135 ° C. in decalin is greater than 1.0 deciliter / g, and (2) by gel permeation chromatography. The ratio Mw / Mn of the measured weight average molecular weight (Mw) and number average molecular weight (Mn) is less than 3, and (3) no melting point (Tm), and the glass transition point (Tg) is less than 10 ° C. The method of (12) above,
(14) In the presence of the catalyst of the above (11), olefins having 2 to 20 carbon atoms are homopolymerized, two or more olefins having 2 to 20 carbon atoms are copolymerized, or olefins having 2 to 20 carbon atoms and carbon The method of (5) above, wherein a low molecular weight olefin polymer having a high vinyl group content is produced by copolymerizing with other polymerizable unsaturated compounds of formula 2 to 20.
(15) The low molecular weight olefin polymer having a high vinyl group content is an ethylene homopolymer, or ethylene, olefins having 3 to 20 carbon atoms, and other polymerizable unsaturated compounds having 2 to 20 carbon atoms. A copolymer with at least one selected from (1) a polyethylene-converted weight average molecular weight (Mw) of 200 to 10,000 measured by gel permeation chromatography, and (2) a density of 0.00. 925 g / cmThree(3) The proportion of vinyl groups in all unsaturated groups is 70 mol% or more, and the vinyl group content measured by infrared spectroscopy is 1.5 or more per 1000 carbons (14 )the method of,
It is.
BEST MODE FOR CARRYING OUT THE INVENTION
The transition metal compound of the present invention is a novel transition metal compound having, as a π ligand, a substituted indenyl group having at least one substituent other than a substituent bonded to a transition metal element on the five-membered ring side. There are various transition metal compounds. For example, the general formula (I)
RM1X1 a-1L1 b ... (I)
A transition metal compound in which a π ligand and a metal are bonded via an arbitrary group, specifically, a general formula (II)
A compound represented by the general formula (III)
The compound etc. which are represented by these are mentioned.
In the general formula (I), R is a π ligand and represents a substituted indenyl group having at least one substituent other than the substituent bonded to the transition metal element on the five-membered ring side. In the general formulas (II) and (III), R1, R2, RThreeAnd RFourAre respectively a hydrogen atom, a halogen atom, an aliphatic hydrocarbon group having 1 to 20 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, an alkoxy group having 1 to 20 carbon atoms, and an aryloxy group having 6 to 20 carbon atoms. , A thioalkoxy group having 1 to 20 carbon atoms, a thioaryloxy group having 6 to 20 carbon atoms, an amino group, an amide group, a carboxyl group, or an alkylsilyl group,1And RThreeAre each a group other than a hydrogen atom. Also, multiple R1, Multiple R2, Multiple RThreeAnd multiple RFourMay be the same or different in each.
Further, in the general formulas (I), (II) and (III), M1, M2And MThreeRepresents a transition metal element such as titanium, zirconium, hafnium, lanthanoid-based metal, niobium, tantalum, etc., among these metal elements of groups 3 to 10 or lanthanoid series of the periodic table. And hafnium are preferred. X1, X2And XThreeEach represents a σ ligand, specifically a hydrogen atom, a halogen atom, an aliphatic hydrocarbon group having 1 to 20 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, or an alkyl group having 1 to 20 carbon atoms. Examples thereof include an alkoxy group, an aryloxy group having 6 to 20 carbon atoms, a thioalkoxy group having 1 to 20 carbon atoms, a thioaryloxy group having 6 to 20 carbon atoms, an amino group, an amide group, a carboxyl group, and an alkylsilyl group. Multiple X1, Multiple X2And multiple XThreeMay be the same as or different from each other, and may be bonded via any group. L1, L2And LThreeEach represents a Lewis base and a plurality of L1, Multiple L2And multiple LThreeMay be the same or different from each other. a, c and e are respectively M1, M2And MThreeThe valences, b, d and f are 0, 1 or 2.
In the general formulas (II) and (III), Q1And Q2Respectively represent an aliphatic hydrocarbon group having 1 to 6 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, a silylene group having 1 to 5 silicon atoms, or a germanylene group having 1 to 5 germanium atoms. J1And J2Each represents an amide group, a phosphide group, an oxygen atom, a sulfur atom or an alkylidene group.
Substituted indenyl group [substituent bonded to transition metal element (Q1, Q2) Is not included. Specific examples of 2-methylindenyl group; 3-methylindenyl group; 3-trimethylsilylindenyl group; 2-t-butylindenyl group; 2,3-dimethylindenyl group; Dimethylindenyl group; 2,4,7-trimethylindenyl group; 1,3,4,7-tetramethylindenyl group; 2,3,4,7, -tetramethylindenyl group; 2,4,5,6,7-pentamethylindenyl group; 2,3,4,5,6,7-hexamethylindenyl group; 1,3,4 , 5,6,7-hexamethylindenyl group; 2,3-dimethyl-4,7-dimethoxyindenyl group; 2,3-dimethyl-4,7-difluoroindenyl group and the like. In addition, the X1(X2, XThreeSpecific examples of hydrogen), chlorine atom, bromine atom, iodine atom, methyl group, benzyl group, phenyl group, trimethylsilylmethyl group, methoxy group, ethoxy group, phenoxy group, thiomethoxy group, thiophenoxy group, dimethylamino Group, diisopropylamino group and the like.
Examples of the transition metal compound of the present invention include the substituted indenyl groups exemplified above and X1(X2, XThree), A compound containing each arbitrarily selected compound can be preferably exemplified.
Specific examples of the transition metal compound include (t-butylamide) (2,3-dimethylindenyl) -1,2-ethanediyltitanium dichloride; (t-butylamide) (2,3-dimethylindenyl) -1 , 2-ethanediyltitanium dimethyl; (t-butylamide) (2,3-dimethylindenyl) -dimethylsilyltitanium dichloride; (t-butylamide) (2,3-dimethylindenyl) -dimethylsilyltitanium dimethyl; -Butylamide) (1,3-dimethylindenyl) -dimethylsilyltitanium dichloride; (t-butylamide) (1,3-dimethylindenyl) -dimethylsilyltitaniumdimethyl; (t-butylamide) (2,3,4, 5,6,7-hexamethylindenyl) -dimethylsilyltitanium di (T-butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dimethyl; (t-butylamide) (1,3,4,5,6,7-hexa (Methylindenyl) -dimethylsilyltitanium dichloride; (t-butylamide) (1,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitaniumdimethyl; (2,3-dimethylindenyl) -1 -Ethane-2-oxatitanium dichloride; (2,3-dimethylindenyl) -1-ethane-2-oxatitanium dimethyl; (phenylamido) (2,3-dimethylindenyl) -1,2-ethanediylzirconium Dichloride; (t-Butylamide) (2,3-dimethylindenyl) -1,2-ethanediylzirconium dimethyl (T-Butylamide) (2,3-dimethylindenyl) -dimethylsilylzirconium dichloride; (t-Butylamide) (2,3-dimethylindenyl) -dimethylsilylzirconium dimethyl; (t-Butylamide) (1,3- (Dimethylindenyl) -dimethylsilylzirconium dichloride; (t-butylamide) (1,3-dimethylindenyl) -dimethylsilylzirconium dimethyl; (t-butylamide) (2,3,4,5,6,7-hexamethyl Indenyl) -dimethylsilylzirconium dichloride; (t-butylamide) (2,3,4,5,6,7-hexamethylindenyl) dimethylsilylzirconium dimethyl; (t-butylamide) (1,3,4,5 , 6,7-Hexamethylindenyl) -dimethylsilylzirconi (T-Butylamide) (1,3,4,5,6,7-hexamethylindenyl) -dimethylsilylzirconium dimethyl; (2,3-dimethylindenyl) -1-ethane-2-oxazirconium Examples include chloride; (2,3-dimethylindenyl) -1-ethane-2-oxazirconium dimethyl and the like, and titanium and zirconium in these compounds substituted with hafnium. Of course, it is not limited to these. Moreover, the analogous compound of the metal element of another group or a lanthanoid series may be sufficient.
The catalyst for olefin polymerization of the present invention contains a transition metal compound having a substituted indenyl group having at least one substituent as a π ligand in addition to the substituent bonded to the transition metal element on the five-membered side. In particular, (A) at least one selected from the transition metal compounds represented by the general formulas (II) and (III), (B) (a) an organoboron compound, (b) an aluminoxane And (c) a catalyst comprising a combination of at least one selected from an ionic compound comprising a non-coordinating anion and a cation, and (A) represented by the general formulas (II) and (III). At least one selected from transition metal compounds and (B) (a) an organic boron compound, (b) an aluminoxane, and (c) an ionic compound composed of a non-coordinating anion and a cation. Small And one with a suitable catalyst comprising a combination of (C) a Lewis acid.
The organoboron compound of the component (a) in the component (B) is represented by the general formula (IV)
RFive ThreeBLFour v ... (IV)
The compound represented by these is mentioned.
In the general formula (IV), RFiveIs a hydrogen atom, a halogen atom, an aliphatic hydrocarbon group having 1 to 20 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, a substituted aromatic hydrocarbon group, an alkoxy group having 1 to 20 carbon atoms, or 6 carbon atoms. -20 aryloxy groups, substituted aryloxy groups, aluminoxy groups, boroxy groups, siloxy groups, germanoxy groups, and the like, which may be the same or different. RFiveSpecific examples of are: phenyl group, toluyl group, fluorophenyl group, trifluoromethylphenyl group, trimethylsilyltetrafluorophenyl group, pentafluorophenyl group, fluorine atom, chlorine atom, bromine atom, iodine atom, dimethylaluminoxy group, Examples include diisobutylaluminoxy group. LFourRepresents a Lewis base, and specific examples include ether compounds such as diethyl ether and tetrahydrofuran, and amine compounds such as pyridine. v is an integer of 0-3.
The aluminoxane of the component (b) in the component (B) is obtained by bringing an organoaluminum compound and a condensing agent into contact with each other, and is represented by the general formula (V)
[In the formula, R6Represents an alkyl group having 1 to 20 carbon atoms, and p represents a number of 0 to 50, preferably 0 to 30. ]
A chain aluminoxane represented by the general formula (VI)
[In the formula, R6Is the same as described above, and q represents a number of 2 to 50, preferably 2 to 30. ]
The cyclic aluminoxane represented by these is mentioned.
Examples of the organoaluminum compound used as a raw material for the aluminoxane include trialkylaluminums such as trimethylaluminum, triethylaluminum, triisobutylaluminum, and mixtures thereof. Moreover, as a condensing agent, water is typically used, but in addition to this, any agent that undergoes a condensation reaction of the trialkylaluminum, for example, adsorbed water such as an inorganic substance, diol, and the like can be used.
On the other hand, as the ionic compound comprising the non-coordinating anion and cation of the component (c) in the component (B), the general formula (VII)
([LFive-H]g +)h([MFourY1Y2... Yn](nm)-)i ... (VII)
Or general formula (VIII)
([L6]g +)h([MFiveY1Y2... Yn](nm)-)i ... (VIII)
[However, L6M6, R7R8M7Or R9 ThreeC. ]
The compound represented by these is mentioned.
In the general formulas (VII) and (VIII), LFiveRepresents a Lewis base, MFourAnd MFiveRepresents an element selected from Groups 5 to 15 of the periodic table, specifically B, Al, P, As, Sb, and the like. M6Represents an element selected from groups 8 to 12 of the periodic table, specifically Ag, Cu, etc., and M7Represents an element selected from Groups 8 to 10 of the periodic table, specifically Fe, Co, Ni and the like. Y1~ YnAre each a hydrogen atom, a dialkylamino group, an alkoxy group, an aryloxy group, an alkyl group having 1 to 20 carbon atoms, an aryl group having 6 to 20 carbon atoms, an arylalkyl group, an alkylaryl group, a substituted alkyl group, an organic metalloid group, A halogen atom or the like is shown. This Y1~ YnSpecific examples of dimethylamino group, diethylamino group, methoxy group, ethoxy group, butoxy group, phenoxy group, 2,6-dimethylphenoxy group, methyl group, ethyl group, propyl group, butyl group, octyl group, phenyl group , Toluyl group, xylyl group, mesityl group, benzyl group, pentafluorophenyl group, 3,5-di (trifluoromethyl) group, 4-t-butylphenyl group, F, Cl, Br, I, pentamethylantimony group , Trimethylsilyl group, trimethylgermyl group, diphenylboron group and the like.
R7And R8Represents a cyclopentadienyl group, a substituted cyclopentadienyl group, an indenyl group, a substituted indenyl group, a fluorenyl group, and the like, specifically, a methylcyclopentadienyl group, a pentamethylcyclopentadienyl group, and the like. It is done. R9Are alkyl groups, aryl groups, and substituted aryl groups, which may be the same or different, and specific examples include phenyl group, 4-methoxyphenyl group, 4-methylphenyl group and the like. m is MFour, MFiveThe integer of 1-7, n is an integer of 2-8, g is [LFive-H], [L6] Is an integer of 1 to 7, h is an integer of 1 or more, and i = (h × g) / (nm).
Examples of the non-coordinating anion in the ionic compound include tetra (phenyl) borate; tetra (fluorophenyl) borate; tetrakis (difluorophenyl) borate; tetrakis (trifluorophenyl) borate; tetrakis (tetrafluorophenyl) borate; Tetrakis (pentafluorophenyl) borate; Tetrakis (trifluoromethylphenyl) borate; Tetra (toluyl) borate; Tetra (xylyl) borate; (Triphenyl, pentafluorophenyl) borate; [Tris (pentafluorophenyl), phenyl] borate Tridecahydride-7,8-dicarboundeborate and the like. On the other hand, examples of cations include tri (ethyl) ammonium; tri (butyl) ammonium; N, N-dimethylanilinium; N, N-diethylanilinium; triphenylphosphinium; dimethylphenylphosphinium; Decamethylferrocene; silver (I); tri (phenyl) carbenium; tri (toluyl) carbenium; tri (methoxyphenyl) carbenium; [di (toluyl), phenyl] carbenium; [di (methoxyphenyl), Phenyl] carbenium; [methoxyphenyl, di (phenyl)] carbenium and the like.
As the ionic compound, those arbitrarily selected and combined from the non-coordinating anions and cations exemplified above can be preferably used.
In the catalyst of the present invention, as the component (B), one type of the organic boron compound of the component (a) may be used, or two or more types may be used in combination, and one type of the aluminoxane of the component (b) is used. It may also be used in combination of two or more. Moreover, the ionic compound of (c) component may be used 1 type, and may be used in combination of 2 or more type. Furthermore, you may use combining (a) component, (b) component, and (c) component suitably.
In the catalyst of the present invention, examples of the Lewis acid used as component (C) include organoaluminum compounds, magnesium compounds, zinc compounds, lithium compounds, and the like.
Examples of the organoaluminum compound include those represented by the general formula (IX)
RTen rAl (OR11)sHtZ1 u ... (IX)
The compound represented by these can be used.
In the general formula (IX), RTenAnd R11Each represents an alkyl group having 1 to 8 carbon atoms, which may be the same or different. Z1Represents a halogen atom, and r, s, t, and u are numbers satisfying the relationships of 0 <r ≦ 3, 0 <s ≦ 3, 0 ≦ t <3, 0 ≦ u <3, and r + s + t + u = 3.
Specific examples of the organoaluminum compound represented by the general formula (IX) include trimethylaluminum, triethylaluminum, triisopropylaluminum, triisobutylaluminum, trioctylaluminum and the like as t = u = 0, r = 3 compounds. , T = u = 0, 1.5 ≦ r <3, such as diethylaluminum ethoxide, dibutylaluminum butoxide, diethylaluminum sesquiethoxide, dibutylaluminum sesquibutoxide, and partially alkoxylated alkylaluminum , S = t = 0 as diethylaluminum dichloride, dibutylaluminum dichloride, etc. (r = 2), ethylaluminum sesquichloride, butylaluminum sesquichloride, etc. (r = 1.5), ethyl Rualuminum dichloride, butylaluminum dichloride, etc. (r = 1), diethylaluminum hydride, diisobutylaluminum hydride, etc. (r = 2), s = u = 0 compounds, ethylaluminum dihydride, butylaluminum dihydride, etc. (r = 1).
In addition, examples of magnesium compounds include Grineer compounds such as methylmagnesium bromide, ethylmagnesium bromide, phenylmagnesium bromide, and benzylmagnesium bromide, organic magnesium compounds such as diethoxymagnesium and ethylbutylmagnesium, and inorganic magnesium compounds such as magnesium chloride. Can be mentioned. Furthermore, examples of the zinc compound and the lithium compound include an organic zinc compound such as diethyl zinc and an organic lithium compound such as methyl lithium.
In the catalyst of the present invention, the Lewis acid of the component (C) may be used singly or in combination of two or more.
The catalyst of the present invention is composed of the above components (A) and (B) or the components (A), (B) and (C), but other catalyst components can be further added. is there. The blending ratio of each catalyst component varies depending on various conditions and is not uniquely determined. Usually, when the component (B) is an organoboron compound, the molar ratio of the component (A) to the component (B) is: Preferably 1: 0.1 to 1:10Three, More preferably 1: 1 to 1:10ThreeWhen the component (B) is an aluminoxane, the molar ratio of the component (A) to the component (B) is preferably 1: 1 to 1: 10,000, and the component (B) is an ionic compound. In this case, the molar ratio between the component (A) and the component (B) is preferably selected in the range of 1: 0.1 to 1: 100. Moreover, when using (C) component, the molar ratio of (A) component and (C) component becomes like this. Preferably it is chosen in the range of 1: 0.1-1: 10,000.
In addition, as a method for contacting the component (A), the component (B) and the component (C) used as desired, for example, (1) the contact mixture of the component (A) and the component (B), the component (C) To make the catalyst into contact with the monomer to be polymerized (2) Method to add the component (A) to the contact mixture of component (B) and component (C) to make the catalyst contact with the monomer to be polymerized (3) A method in which the component (B) is added to the contact mixture of the component (A) and the component (C) to make a catalyst and contact with the monomer to be polymerized, and (4) the monomer component to be polymerized (A), (B), (C) component contacting method, (5) contacting the catalyst prepared in the above (1) to (3) to the contact mixture of the monomer component to be polymerized and (C) component There are methods.
The contact between the component (A), the component (B) and the component (C) used as desired can be carried out at a polymerization temperature or in the range of -20 to 200 ° C.
In the olefin polymerization catalyst, the present invention is particularly applicable to M in the transition metal compounds of the general formulas (II) and (III) used as the component (A).2And MThreeAre preferably titanium, zirconium or hafnium, respectively.
In the method for producing an olefin polymer of the present invention, olefins are homopolymerized, two or more olefins are copolymerized, or olefins and other polymerizable unsaturated compounds are copolymerized in the presence of the polymerization catalyst described above. Polymerize to produce an olefin homopolymer or copolymer.
Examples of the olefins include ethylene, propylene, butene-1, pentene-1, hexene-1, heptene-1, octene-1, nonene-1, decene-1, 4-phenylbutene-1, 6-phenylhexene. -1; 3-methylbutene-1; 4-methylpentene-1; 3-methylpentene-1; 3-methylhexene-1; 4-methylhexene-1; 5-methylhexene-1; 3,3-dimethylpentene 3, 4-dimethylpentene-1; 4,4-dimethylpentene-1; vinylcyclohexane; α-olefins such as vinyltrimethylsilane, hexafluoropropene; tetrafluoroethylene; 2-fluoropropene; fluoroethylene; 1 , 1-difluoroethylene; 3-fluoropropene; trifluoroethylene; 3,4-dichloro Halogen-substituted α-olefins such as butene-1, cyclopentene; cyclohexene; norbornene; 5-methylnorbornene; 5-ethylnorbornene; 5-propylnorbornene; 5,6-dimethylnorbornene; 1-methylnorbornene; , 5,6-trimethylnorbornene; 5-phenylnorbornene; cyclic olefins such as 5-benzylnorbornene. These olefins may be used alone or in combination of two or more. When copolymerizing two or more olefins, the olefins can be arbitrarily combined.
In the present invention, the olefins and other polymerizable unsaturated compounds may be copolymerized. Examples of other polymerizable unsaturated compounds used in this case include styrene, p-methylstyrene; o- M-methylstyrene; 2,4-dimethylstyrene; 2,5-dimethylstyrene; 3,4-dimethylstyrene; 3,5-dimethylstyrene; alkyl styrene such as pt-butylstyrene, p-chloro M-chlorostyrene; o-chlorostyrene; p-bromostyrene; m-bromostyrene; o-bromostyrene; p-fluorostyrene; m-fluorostyrene; o-fluorostyrene; o-methyl-p-fluorostyrene Halogenated styrene such as organosilicon styrene, vinyl benzoate, divinylbenzene Any aromatic vinyl compound, butadiene; isoprene; linear diene compounds such as 1,5-hexadiene, norbornadiene; 5-ethylidenenorbornene; 5-vinylnorbornene; cyclic diene compounds such as dicyclopentadiene, acetylene; methyl acetylene; phenylacetylene Acetylenes such as trimethylsilylacetylene; These other monomers may be used alone or in combination of two or more.
Such a method for producing an olefin polymer of the present invention is suitable for producing an olefin / cyclic olefin copolymer by copolymerizing olefins and cyclic olefins, for example. In this case, as the olefins, only one kind may be selected and used from those exemplified above, or two or more kinds may be selected and used in combination. Further, as the cyclic olefins, only one kind may be selected and used from those exemplified above, or two or more kinds may be selected and mixed for use. According to the method of the present invention, an olefin / cyclic olefin copolymer having particularly the following properties can be efficiently produced.
That is, (1) The ratio Mw / Mn of the weight average molecular weight (Mw) and the number average molecular weight (Mn) measured by gel permeation chromatography (GPC method) is 6 or less, the molecular weight distribution is narrow ( 2) The cyclic olefin unit content is in the range of 0.1 to 95 mol%. (3) Intrical viscosity [η] measured at 135 ° C. in decalin and melt index (MI) measured at a load of 2.16 kg2.16) Is an expression
[Η] ≦ 1.333−0.620 × logMI2.16
And excellent non-Newtonian properties due to non-Newtonian properties. Furthermore, (4) the molecular weight is large, and the intrinsic viscosity [η] measured at 135 ° C. in decalin is usually 1.0 deciliter / g or more. The olefin / cyclic olefin copolymer having such properties has an excellent balance between elastic modulus and elastic recovery rate, improved low-temperature properties, and excellent molding process characteristics as described above. ing.
The olefin / cyclic olefin copolymer having the above properties may be produced by a method other than the present invention, but can be produced economically and efficiently by using the method of the present invention.
Moreover, the manufacturing method of the olefin polymer of this invention is, for example, from propylene homopolymerization, or propylene, other olefins having 2 to 20 carbon atoms, and other polymerizable unsaturated compounds having 2 to 20 carbon atoms. It is suitable for producing an amorphous high molecular weight propylene homopolymer or copolymer by copolymerization with at least one selected. In this case, a catalyst in which the transition metal compound represented by the general formulas (II) and (III) of the component (A) is a titanium compound is used as the catalyst. In addition, as a monomer to be copolymerized with propylene, from the above-exemplified olefins and polymerizable unsaturated compounds, only one type other than propylene may be selected and used, or two or more types may be selected and used in combination. Also good. According to the method of the present invention, an amorphous high molecular weight propylene-based polymer can be efficiently produced particularly having the following properties.
That is, (1) The intrinsic viscosity [η] measured at 135 ° C. in decalin is higher than 1.0 deciliter / g, and has a high molecular weight. (2) Weight average molecular weight (Mw) and number average measured by GPC method The ratio Mw / Mn to the molecular weight (Mn) is less than 3, the molecular weight distribution is narrow, (3) it does not have a melting point (Tm), and the glass transition point (Tg) is less than 10 ° C. The amorphous high molecular weight propylene-based polymer having such properties can be used as a single product as an elastomer or the like, and has a high utility value as a component of a thermoplastic olefin-based elastomer (TPO).
The amorphous high molecular weight propylene polymer having the above properties may be produced by a method other than the present invention, but can be produced economically and efficiently by using the method of the present invention.
Furthermore, the method for producing the olefin polymer of the present invention includes, for example, homopolymerizing olefins having 2 to 20 carbon atoms, copolymerizing two or more olefins having 2 to 20 carbon atoms, or olefins having 2 to 20 carbon atoms. And other polymerizable unsaturated compounds having 2 to 20 carbon atoms are suitable for producing a low molecular weight olefin polymer having a high vinyl group content. In this case, a catalyst in which the transition metal compound represented by the general formulas (II) and (III) of the component (A) is a zirconium or hafnium compound is used. According to the method of the present invention, as a low molecular weight olefin polymer having a high vinyl group content, an ethylene homopolymer having the following properties, or ethylene, an olefin having 3 to 20 carbon atoms, and 2 to 20 carbon atoms. A copolymer with at least one selected from other polymerizable unsaturated compounds can be efficiently produced.
That is, (1) The weight average molecular weight (Mw) in terms of polyethylene measured by the GPC method is 200 to 10,000, and the ratio Mw / Mn between the weight average molecular weight (Mw) and the number average molecular weight (Mn) is preferably 5 Or less, more preferably 3 or less. (2) The density measured by the density gradient tube method is 0.925 g / cm.ThreeThat's it. Moreover, (3) The ratio of the vinyl group which occupies for all unsaturated groups is 70 mol% or more, and the vinyl group content measured by infrared spectroscopy is 1.5 or more per 1000 carbons. As an unsaturated group, a trans vinylene group is 963 cm-1, Terminal vinyl group is 910cm-1, Vinylidene group is 888cm-1These unsaturated groups are known to produce a press sheet (thickness (t) of about 0.1 mm) at a temperature of 190 ° C., and can be identified and quantified by infrared spectroscopic analysis. In calculating the content of the unsaturated group, the following formula can be used. Here, n is the number of unsaturated bonds per 1000 carbons.
Transvinylene group: n = 0.83A963/ (D × t)
Terminal vinyl group: n = 1.14A910/ (D × t)
Vinylidene group: n = 1.09A888/ (D × t)
[A: absorbance, d: density (g / cmThree), T: sample thickness (mm)]
In the case of an ethylene-based polymer, the monomer to be copolymerized with ethylene may be selected from one or more of the olefins and polymerizable unsaturated compounds exemplified above, and two or more may be selected. You may mix and use.
Such a low molecular weight olefin polymer having a high vinyl group content can be used as a macromonomer. For example, by using it as a comonomer of an olefin copolymer, long chain branching can be easily carried out without causing a gelation reaction. Thus, it is possible to provide an olefin copolymer having excellent molding process characteristics and an olefin copolymer having performance as an elastomer, a compatibilizing agent, and the like. Further, the low molecular weight olefin polymer having a high terminal vinyl group content can be used as a wax or the like by hydrogenation treatment. Further, by treating with various reaction reagents, it is used as a terminal-modified macromonomer, for example, as a comonomer of a condensation copolymer, and can be used as an adhesive, a surface modifier, a compatibilizing agent, a composite material, and the like.
The low molecular weight olefin polymer having a high vinyl group content having the above-mentioned properties may be produced by a method other than the present invention, but can be produced economically and efficiently by using the method of the present invention. it can.
The polymerization mode in the method for producing an olefin polymer of the present invention is not particularly limited, and may be bulk polymerization. In addition, aliphatic hydrocarbons such as pentane, hexane, and heptane, alicyclic hydrocarbons such as cyclohexane, or You may carry out in aromatic hydrocarbon solvents, such as benzene, toluene, xylene, and ethylbenzene. Further, the polymerization may be carried out in a solvent or in a gas phase by loading a catalyst on a suitable carrier.
The polymerization temperature is generally 0 to 200 ° C., and the partial pressure of the gaseous monomer when using the gaseous monomer is generally 300 atm or less, preferably 30 atm or less. Further, hydrogen or the like can be added for the purpose of adjusting the molecular weight or improving the activity.
EXAMPLES Next, although an Example demonstrates this invention further in detail, this invention is not limited at all by these examples.
In addition, the reaction in Example 1 and Example 2 was performed under an inert gas or an air stream unless otherwise specified. The intrinsic viscosity [η] of the polymer is a value measured at 135 ° C. in decalin.
Example 1
(T-Butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2〕Manufacturing of
(1) Synthesis of 2,3,4,5,6,7-hexamethyl-1-one
58.7 g (440 mmol) of aluminum trichloride was suspended in 300 ml of dry carbon disulfide (dry distillation over calcium hydride) and placed at ice-cooled temperature. After mixing 47.4 g (400 mmol) of tigloyl chloride and 53.7 g (400 mmol) of tetramethylbenzene and adding dropwise to the above carbon disulfide solution, stirring is continued at room temperature, whereby a brown to reddish brown solution is obtained. Generated. After stirring for 2 hours, the solution was further changed to orange by reacting for 2 hours under reflux.
After returning the reaction mixture to room temperature, the mixture was poured onto a mixture of 500 g of water and 500 ml of concentrated hydrochloric acid, stirred for about 1 hour, extracted twice with 400 ml of ether, and further extracted twice with 200 ml. The ether phases were combined and dried over anhydrous calcium chloride. After filtering off the desiccant, ether was distilled off, and the resulting brown viscous solid was dissolved in hexane and recrystallized. The operation of allowing the room temperature saturated solution to stand at −20 ° C. and collecting the precipitate by filtration was repeated to obtain 75.9 g of 2,3,4,5,6,7-hexamethylindan-1-one as a red yellow solid. .
(2) Synthesis of 1,2,4,5,6,7-hexamethylindene
Lithium aluminum hydride (LAH) (3.09 g, 81 mmol) was suspended in dry ether (distilled over metal sodium). 38.7 g (180 mmol) of 2,3,4,5,6,7-hexamethylindan-1-one synthesized in (1) above was dissolved in 200 ml of dry ether, and gently dissolved in the LAH suspension. The solution was added dropwise at such a rate that a proper reflux occurred. After completion of the dropwise addition in 1.5 hours, stirring was continued for 2.5 hours under heating and reflux. Quench with 20 ml of water and then 200 ml of IN ammonium chloride solution under ice-cooling, and after separating the organic phase, extract and separate twice with 100 ml of ether. After washing, it was dried over anhydrous magnesium sulfate. The desiccant was removed by filtration, the ether solution was purged with nitrogen, and small pieces of iodine were added to perform a dehydration reaction. After standing overnight under nitrogen, the mixture was heated to reflux for 3 hours to complete the reaction.
Subsequently, it was washed twice with 150 ml of a 0.2 N aqueous sodium hydrosulfite solution and twice with 150 ml of a saturated aqueous sodium chloride solution and then dried over anhydrous magnesium sulfate. The desiccant was filtered off and the ether was removed to give crude yellow 1,2,4,5,6,7-hexamethylindene, which was again dissolved in 300 ml of hexane and dried over anhydrous magnesium sulfate. A yellow solution was obtained by drying. The desiccant was filtered off and hexane was distilled off to obtain a yellow solid, which was then adsorbed from 20 g of silica gel from the hexane solution and poured out of the 80 g silica gel column with hexane to obtain the desired 1,2, There were obtained 28.8 g (144 mmol) of 4,5,6,7-hexamethylindene as a pale yellow solid. Yield 80.4%.
(3) Synthesis of 1- (chlorodimethylsilyl) -2,3,4,5,6,7-hexamethylindene
After dissolving 14.4 g (72 mmol) of 1,2,4,5,6,7-hexamethylindene in 150 ml of dry tetrahydrofuran, 47 ml of t-butyllithium (1.7 M / pentane solution) is cooled with ice. Was added dropwise and the mixture was stirred at room temperature for 2 hours, and then the volatile component was distilled off under reduced pressure. Then, the hexane-insoluble component was collected by filtration, washed with hexane and dried to obtain a yellowish white solid. This was dissolved in 150 ml of dehydrated tetrahydrofuran (red solution), and 10.9 g (85 mmol, 10.3 ml) of dimethylchlorosilane which was simply distilled at −78 ° C. was added to return to room temperature and left to stand overnight. Volatile components are removed from the yellow solution under reduced pressure, then hexane-insoluble components are removed by filtration, and volatile components are distilled off from the hexane-soluble components under reduced pressure to give 1- (chlorodimethylsilyl) -2,3 , 4,5,6,7-Hexamethylindene was recovered as a white solid.
(4) Synthesis of 1- (t-butylamino-dimethylsilyl) -2,3,4,5,6,7-hexamethylindene
19.8 g of 1- (chlorodimethylsilyl) -2,3,4,5,6,7-hexamethylindene is dissolved in 150 ml of dehydrated ether, and 13.2 g of t-butylamine is added under ice cooling to room temperature. Returned and stirred for two days. After distilling off the volatile components under reduced pressure, extraction with 300 ml of hexane was carried out. After insoluble salts were filtered off, the solvent was removed from the hexane solution under reduced pressure to obtain a pale yellow oil, which was allowed to stand at room temperature. 22.0 g of a white solid was obtained.
(5) Synthesis of (t-butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride
10.1 g of 1- (t-butylamino-dimethylsilyl) -2,3,4,5,6,7-hexamethylindene was dissolved in 150 ml of dehydrated ether, and 1.6 M n-butyllithium was added under ice cooling. / 31 ml of hexane solution was added dropwise and stirred at room temperature for two days and nights, then the solvent was distilled off from the resulting red solution under reduced pressure, and the hexane insoluble part was collected by filtration and further washed with hexane to obtain a yellow solid. Obtained. This yellow lithium salt and TiClThree(Thf)Three11.5 g was mixed with solid, 200 ml of dry tetrahydrofuran was added and stirred for 1 hour, and then 4.7 g of silver chloride was added and stirred for another 2 hours. The volatiles were distilled off under reduced pressure, and ether insolubles were filtered off. did. The ether is distilled off from the solution and then recrystallized from a toluene / hexane solution to give pure (t-butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride. was gotten.
This compound is1From H-NMR, 2.70 ppm (3 hydrogen), 2.575 ppm (3 hydrogen), 2.452 ppm (3 hydrogen), 2.338 ppm (3 hydrogen), 2.305 ppm (3 hydrogen), 2.266 ppm (3 Hydrogen), 1.372 ppm (9 hydrogen), 0.853 ppm (3 hydrogen), 0.735 ppm (3 hydrogen).
Example 2
(T-Butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilylzirconium dichloride
[Me2Si (Me6Ind) (t-BuN) ZrCl2〕Manufacturing of
10.0 g of 1- (t-butylamino-dimethylsilyl) -2,3,4,5,6,7-hexamethylindene obtained in Example 1- (4) was dissolved in 150 ml of dehydrated ether, Under ice cooling, 50 ml of a 1.6 M n-butyllithium / hexane solution (manufactured by Wako Pure Chemical Industries, Ltd.) was added dropwise, and the mixture was stirred overnight at room temperature. From the obtained solution, volatile components were distilled off under reduced pressure at room temperature, and the solvent was replaced with 100 ml of hexane. Next, the hexane-insoluble part is collected by filtration, washed with hexane and dried under reduced pressure to give 1- (t-butylamido-dimethylsilyl) -2,3,4,5,6,7-hexamethylindenyldilithium in yellow As a solid.
This solid was then dissolved in 50 ml of dehydrated ether and cooled in a dry ice / ethanol bath. In a separate container, 7.2 g of zirconium tetrachloride was suspended in dehydrated toluene, cooled in a dry ice / ethanol bath, 70 ml of dehydrated ether was added, and 1- (t-butylamide-dimethylsilyl)-was added to this suspension. 2,3,4,5,6,7-Hexamethylindenyldilithium / ether solution was added and mixed and stirred for 1 hour with cooling. Thereafter, the temperature was gradually raised to room temperature and stirred at room temperature for two days and nights. From the obtained solution, volatiles were distilled off under reduced pressure at room temperature, and 240 ml of dehydrated toluene was added thereto to extract soluble components. Next, the extraction phase was concentrated under reduced pressure to a total volume of 30 ml, and 120 ml of hexane was added thereto, followed by filtration. The solvent was distilled off from the filtrate under reduced pressure to obtain an oil having a high viscosity.
50 ml of hexane was added to this oil, and insoluble matters were collected by filtration at −60 ° C., and further washed with 30 ml of cold hexane to obtain (t-butylamide) (2,3,4,5,6,7-hexa 5.06 g of methylindenyl) -dimethylsilylzirconium dichloride was obtained.
This compound is1From H-NMR, 2.70 ppm (3H, s), 2.64 ppm (3H, s), 2.49 ppm (3H, s), 2.34 ppm (3H, s), 2.28 ppm (3H, s), Signals of 2.25 ppm (3H, s), 1.34 ppm (9H, s), 0.80 ppm (3H, s), and 0.76 ppm (3H, s) are given.
Example 3
After adding 395 ml of toluene and 5 ml of 1-octene to a 1 liter autoclave and heating to 80 ° C., 3 ml of 1 mol / liter of methylaluminoxane (MAO) in terms of aluminum and 1 mmol / liter of Example 1 (T-Butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me2Ind) (t-BuN) TiCl2] 0.5 ml (both toluene solutions) was added, ethylene was introduced, and polymerization was carried out for 10 minutes while maintaining the total pressure at 0.8 MPa and 80 ° C. Unreacted gas was depressurized, and a small amount of methanol was added to stop the reaction. After the temperature was lowered, the contents were washed with 5 liters of methanol.
The dry weight of the obtained ethylene / 1-octene copolymer was 27.5 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Example 4
After adding 395 ml of toluene and 5 ml of 1-octene to a 1 liter autoclave and heating to 80 ° C., 1 ml of 1 mol / liter triisobutylaluminum (TIBA) and 1 mmol / liter of Example 1 were obtained. (T-Butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2] 0.5 ml and 1 mmol / l N, N-dimethylanilinium tetrakis (pentafluorophenyl) borate ([N, N-Me2PhNH] [B (C6FFive)Four] 0.5 ml (both toluene solutions) was added, ethylene was introduced, and polymerization was carried out for 30 minutes while maintaining the total pressure at 0.8 MPa and 80 ° C. Unreacted gas was depressurized, and a small amount of methanol was added to stop the reaction. After the temperature was lowered, the contents were washed with 5 liters of methanol.
The dry weight of the obtained ethylene / 1-octene copolymer was 15.0 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Example 5
To a 1 liter autoclave, 460 ml of toluene and 40 ml of 1-octene were added and heated to 150 ° C., and ethylene was introduced at a total pressure of 2.4 MPa. To this, 6 ml of 1 mol / liter of methylaluminoxane (MAO) in terms of aluminum and (t-butylamide) (2,3,4,5,6,7-hexa) obtained in Example 1 of 1 mmol / liter were added. Methylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2] 1.0 ml (both toluene solutions) was added, and the temperature was maintained at 150 ° C. for 8 minutes for polymerization. Unreacted gas was depressurized, and a small amount of methanol was added to stop the reaction. After the temperature was lowered, the contents were washed with 5 liters of methanol.
The dry weight of the obtained ethylene / 1-octene copolymer was 49.5 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Example 6
In Example 3, 360 ml of toluene, 40 ml of 1-octene, 0.2 mmol of methylaluminoxane (MAO) in terms of aluminum, (t-butylamide) (2,3,4,5,6,7-hexamethylindene Nyl) dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2The polymerization was carried out in the same manner as in Example 3 except that 1.0 micromol and 1.5 mmol of triisobutylaluminum were used, and the polymerization reaction was stopped in 45 minutes.
The dry weight of the obtained ethylene / 1-octene copolymer was 83.7 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Comparative Example 1
In Example 3, (t-butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2] Instead of (t-butylamide) (2,3,4,5-tetramethylcyclopentadienyl) -dimethylsilyltitanium dichloride [Me2Si (MeFourCp) (t-BuN) TiCl2An ethylene / 1-octene copolymer was produced in the same manner as in Example 3, except that
The dry weight of the obtained ethylene / 1-octene copolymer was 22.0 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Comparative Example 2
In Example 4, (t-butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2] Instead of (t-butylamide) (2,3,4,5-tetramethylcyclopentadienyl) -dimethylsilyltitanium dichloride [Me2Si (MeFourCp) (t-BuN) TiCl2An ethylene / 1-octene copolymer was produced in the same manner as in Example 4, except that
The dry weight of the obtained ethylene / 1-octene copolymer was 11.4 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Comparative Example 3
In Example 5, (t-butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2] Instead of (t-butylamide) (2,3,4,5-tetramethylcyclopentadienyl) -dimethylsilyltitanium dichloride [Me2Si (MeFourCp) (t-BuN) TiCl2An ethylene / 1-octene copolymer was produced in the same manner as in Example 5, except that
The dry weight of the obtained ethylene / 1-octene copolymer was 47.1 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Example 7
In Example 6, tetraisobutylaluminoxane (iBu) was used instead of methylaluminoxane (MAO).2AlOAliBu2) Was used in the same manner as in Example 6 except that 3.0 mmol in terms of aluminum was used and triisobutylaluminum (TIBA) was not used, and the polymerization reaction was stopped in 60 minutes.
The dry weight of the obtained ethylene / 1-octene copolymer was 56.0 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Example 8
In Example 6, instead of methylaluminoxane (MAO), tris (dimethylalumino) boroxan [B (OAlMe2)Three] Was used in the same manner as in Example 6 except that 3.0 mmol in terms of aluminum and 1.0 mmol of triisobutylaluminum (TIBA) were used, and the polymerization reaction was stopped in 60 minutes.
The dry weight of the obtained ethylene / 1-octene copolymer was 29.3 g. The polymerization conditions, catalyst activity, and polymer properties are shown in Table 1.
Example 9
400 ml of toluene was put in a 1 liter autoclave and heated to 50 ° C., and then obtained in Example 1 with 3 ml of methylaluminoxane (MAO) at 1 mol / liter in terms of aluminum and 1 mmol / liter (t -Butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl25 ml (both toluene solutions) were added, and propylene was continuously introduced at a total pressure of 0.8 MPa, and the temperature was maintained at 50 ° C. and polymerized for 15 minutes. Unreacted gas was depressurized, and a small amount of methanol was added to stop the reaction. After the temperature was lowered, the contents were washed with 5 liters of methanol.
The dry weight of the obtained polymer was 71.5 g. This polymer had no melting point (Tm) observed by differential scanning calorimetry (DSC), was amorphous, and had a glass transition point (Tg) of 0 ° C. In addition, isotope carbon nuclear magnetic resonance (13C-NMR) spectrum measurement or mesotriad [mm] was 18 mol% and racemic triad [rr] was 34 mol% atactic polypropylene. Table 2 shows the polymerization conditions, catalyst activity, and polymer properties.
Example 10
In Example 9, a toluene solution of methylaluminoxane (MAO) (manufactured by Ethyl Co., Ltd.) in terms of aluminum was 3.0 mmol, triisobutylaluminum (TIBA) was 0.5 mmol, and (t-butylamide) (2,3,4) , 5,6,7-hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2] Was used in the same manner as in Example 9 except that the polymerization was performed for 60 minutes.
The dry weight of the obtained polymer was 72.9 g. This polymer had no melting point (Tm) as in Example 9, was amorphous, had a glass transition point (Tg) of 0 ° C., a mesopentad fraction [mmmm] of 2 mol%, and a mesotriad [mm]. Was atactic polypropylene with 16 mol% and racemic triad [rr] of 37 mol%. Table 2 shows the polymerization conditions, catalyst activity, and polymer properties.
Example 11
A stainless steel pressure-resistant reactor having an internal volume of 500 ml equipped with a stirrer was dried under reduced pressure and purged with nitrogen, and then 160 ml of toluene, 5 ml of 1-octene, 0.3 mmol of triisobutylaluminum (TIBA), methylaluminoxane (MAO) (Tosoh Aguso) 1.5 mmol in terms of aluminum, (t-butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilyltitanium obtained in Example 1 Dichloride [Me2Si (Me6Ind) (t-BuN) TiCl21.0 micromol was added, propylene was continuously supplied at 50 ° C., and the internal pressure was maintained at 0.8 MPa, and polymerization was carried out for 1 hour. After completion of the polymerization reaction, excess propylene was depressurized and removed, and 5 ml of methanol was added to stop the reaction. The contents were stirred in 1500 ml of acidic methanol for 2 hours, and insolubles were collected by filtration. The insoluble material was washed again in 1500 ml of methanol, and the resulting polymer was dried at 80 ° C. under reduced pressure.
The dry weight of the polymer was 16.6 g. This polymer had no melting point (Tm) as in Example 9, was amorphous, and had a glass transition point (Tg) of -1 ° C. Table 2 shows the polymerization conditions, catalyst activity, and polymer properties.
Example 12
A stainless steel pressure-resistant reactor with an internal volume of 500 ml equipped with a stirrer was dried under reduced pressure and purged with nitrogen, and then 200 ml of toluene and 1.0 mmol of methylaluminoxane (MAO) (manufactured by Tosoh Aguso) were converted into aluminum. (T-Butylamide) (2,3,4,5,6,7-hexamethylindenyl) -dimethylsilylzirconium dichloride obtained in Example 2 [Me2Si (Me6Ind) (t-BuN) ZrCl2] 1.0 micromol was added, ethylene was continuously supplied at 80 ° C., and the internal pressure was maintained at 0.8 MPa, and polymerization was carried out for 1 hour. After completion of the polymerization reaction, excess ethylene was depressurized and removed, and 5 ml of methanol was added to stop the reaction. The contents were stirred in 1500 ml of acidic methanol for 2 hours, and insolubles were collected by filtration. The insoluble material was washed again in 1500 ml of methanol, and the resulting polymer was dried under reduced pressure at 80 ° C. to obtain 4.74 g of polyethylene.
This polyethylene has an unsaturated bond of 910 cm which can be observed by infrared spectroscopy (IR).-1The vinyl group content was 7.87 per 1000 carbons. Table 3 shows the polymerization conditions, polymer yield, and polymer properties.
Example 13
In Example 12, it carried out like Example 12 except having changed to 6.0 mmol in the aluminum conversion of the quantity of methylaluminoxane (MAO). Table 3 shows the polymerization conditions, polymer yield, and polymer properties.
Example 14
The same procedure as in Example 12 was performed, except that 0.4 mmol of triisobutylaluminum (TIBA) was used. Table 3 shows the polymerization conditions, polymer yield, and polymer properties.
Comparative Example 4
A stainless steel pressure-resistant reactor having an internal volume of 500 ml equipped with a stirrer was dried under reduced pressure and purged with nitrogen, and then 200 ml of toluene, 0.2 mmol of triisobutylaluminum (TIBA), methylaluminoxane (MAO) (manufactured by Tosoh Axo) ) 1.0 mmol in terms of aluminum, (t-butylamide) (tetramethylcyclopentadienyl) -dimethylsilyltitanium dichloride [Me2Si (MeFourCp) (t-BuN) TiCl2] 1.0 micromol was added, ethylene was continuously supplied at 80 ° C., and the internal pressure was kept at 0.4 MPa, and polymerization was carried out for 1 hour. After completion of the polymerization reaction, excess ethylene was depressurized and removed, and 5 ml of methanol was added to stop the reaction. The contents were stirred in 1500 ml of acidic methanol for 2 hours, and insolubles were collected by filtration. The insoluble material was washed again in 1500 ml of methanol, and the obtained polymer was dried under reduced pressure at 80 ° C. to obtain 31.7 g of polyethylene.
In this polyethylene, no unsaturated bond was observed by IR analysis. Table 3 shows the polymerization conditions, polymer yield, and polymer properties.
Example 15
In a 2 liter autoclave heated to 150 ° C. in a nitrogen atmosphere, 640 ml of dry hexane, 1.5 ml of methylaluminoxane (MAO) in terms of aluminum and 300 ml of hexane solution containing 70% by weight of 2-norbornene (2 -1.74 mol as norbornene) were charged in this order. Then, 120 ml of dry hexane, 1.5 mmol of methylaluminoxane (MAO) (as aluminum), (t-butylamide) obtained in Example 1 (2,3,4,5,6,7- Hexamethylindenyl) -dimethylsilyltitanium dichloride [Me2Si (Me6Ind) (t-BuN) TiCl2] 6 micromoles were added in this order.
Next, after introducing ethylene so that the ethylene partial pressure becomes 3.0 MPa, the catalyst solution is introduced from the catalyst introduction pipe, while continuously introducing ethylene so that the ethylene partial pressure becomes 3.0 MPa, The reaction was performed for 5 minutes. After completion of the reaction, the polymerization was stopped with isopropyl alcohol and flushed to a flash drum to obtain 65.6 g of a powdery ethylene / 2-norbornene copolymer. The catalytic activity was 229 kg / g Ti.
This copolymer has a 2-norbornene unit content of 5.6 mol%, an intrinsic viscosity [η] of 2.83 deciliter / g, a melting point (Tm) of 83 ° C. (broad), and the molecular weight measured by the GPC method is The weight average molecular weight (Mw) was 196,000, the number average molecular weight (Mn) was 60,500, and Mw / Mn was 3.24. The melt index is MI21.6(Load 21.6kg) is 0.34g / 10min, MI2.16(Load 2.16 kg) was 0.007 g / 10 min.
Table 4 shows the polymerization conditions, catalyst activity, and polymer properties.
Example 16
120 ml of dry hexane in advance, 1.5 mmol of methylaluminoxane (MAO) (as aluminum) and (t-butylamide) obtained in Example 1 (2,3,4,5,6,7-hexamethylindenyl) -The same operation as in Example 15 was performed except that 6 micromol of dimethylsilyltitanium dichloride was mixed and allowed to stand at room temperature under nitrogen for 24 hours was added to the catalyst charging tube, and the polymerization temperature was 170 ° C.
Table 4 shows the polymerization conditions, catalyst activity, and polymer properties.
Examples 17-19
An ethylene / 2-norbornene copolymer was produced in the same manner as in Example 15 under the polymerization conditions shown in Table 4.
Table 4 shows the polymerization conditions, catalyst activity, and polymer properties.
Comparative Example 5
As a catalyst for the component (A), (t-butylamide) (tetramethylcyclopentadienyl) -dimethylsilyltitanium dichloride [Me2Si (MeFourCp) (t-BuN) TiCl2An ethylene / 2-norbornene copolymer was produced in the same manner as in Example 15 using 6 micromol under the polymerization conditions shown in Table 4. Table 4 shows the polymerization conditions, catalyst activity, and polymer properties.
640 ml of hexane is used as a solvent, and the polymerization time is 5 minutes.
Industrial applicability
The transition metal compound of the present invention is a novel transition metal compound having, as a π ligand, a substituted indenyl group having at least one substituent other than the substituent bonded to the transition metal element on the five-membered ring side, It is useful as a catalyst component for olefin polymerization. The catalyst for olefin polymerization of the present invention containing this transition metal compound has high activity, low residual metal content and good quality normal olefin homopolymer or copolymer, or elastic modulus and elastic recovery rate. As a non-crystalline high molecular weight propylene polymer having a narrow molecular weight distribution and a macromonomer useful as an olefin / cyclic olefin copolymer, elastomer, etc. with improved low temperature properties and improved moldability A useful low molecular weight olefin polymer having a high vinyl group content can be provided economically and efficiently.
Claims (13)
及び一般式(III)
〔式中、R1、R2、R3及びR4は、それぞれ水素原子,ハロゲン原子,炭素数1〜20の脂肪族炭化水素基、炭素数6〜20の芳香族炭化水素基、炭素数1〜20のアルコキシ基、炭素数6〜20のアリーロキシ基、炭素数1〜20のチオアルコキシ基、炭素数6〜20のチオアリーロキシ基、アミノ基、アミド基、カルボキシル基又はアルキルシリル基を示し、R1及びR3は、それぞれにおいて少なくとも一つが水素原子以外の基であり、複数のR1、複数のR2、複数のR3及び複数のR4は、それぞれにおいて同一でも異なっていてもよい。M2及びM3は、それぞれ周期率表3〜10族又はランタノイド系列の金属元素、X2及びX3は、それぞれσ配位子、L2及びL3は、それぞれルイス塩基、Q1及びQ2は、それぞれ炭素数1〜6の脂肪族炭化水素基、炭素数6〜20の芳香族炭化水素基、珪素数1〜5のシリレン基又はゲルマニウム数1〜5のゲルミレン基、J1及びJ2は、それぞれアミド基,フォスフィド基,酸素原子,硫黄原子又はアルキリデン基を示し、複数のX2、複数のX3、複数のL2及び複数のL3は、それぞれにおいて同一でも異なっていてもよい。c及びeは、それぞれM2及びM3の価数を示し、d及びfは0、1又は2である。〕
で表される遷移金属化合物の中から選ばれた少なくとも一種と、(B)(a)有機硼素化合物、(b)アルミノキサン及び(c)非配位性アニオンとカチオンとからなるイオン性化合物の中から選ばれた少なくとも一種との組合せからなるオレフィン重合用触媒。(A) General formula (II)
And general formula (III)
[Wherein R 1 , R 2 , R 3 and R 4 are each a hydrogen atom, a halogen atom, an aliphatic hydrocarbon group having 1 to 20 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, or the number of carbon atoms. An alkoxy group having 1 to 20 carbon atoms, an aryloxy group having 6 to 20 carbon atoms, a thioalkoxy group having 1 to 20 carbon atoms, a thioaryloxy group having 6 to 20 carbon atoms, an amino group, an amide group, a carboxyl group or an alkylsilyl group; R 1 and R 3 each represent at least one group other than a hydrogen atom, and a plurality of R 1 , a plurality of R 2 , a plurality of R 3, and a plurality of R 4 may be the same or different in each case. Also good. M 2 and M 3 are each a periodic group 3-10 group metal element or a lanthanoid series metal element, X 2 and X 3 are σ ligands, L 2 and L 3 are respectively Lewis bases, Q 1 and Q 3 2 is an aliphatic hydrocarbon group having 1 to 6 carbon atoms, an aromatic hydrocarbon group having 6 to 20 carbon atoms, a silylene group having 1 to 5 silicon atoms, or a germanylene group having 1 to 5 germanium atoms, J 1 and J 2 represents an amide group, a phosphido group, an oxygen atom, a sulfur atom or an alkylidene group, and the plurality of X 2 , the plurality of X 3 , the plurality of L 2 and the plurality of L 3 may be the same or different from each other. Good. c and e represent the valences of M 2 and M 3 , respectively, and d and f are 0, 1 or 2. ]
And (B) (a) an organic boron compound, (b) an aluminoxane, and (c) an ionic compound comprising a non-coordinating anion and a cation. An olefin polymerization catalyst comprising a combination with at least one selected from the group consisting of:
〔η〕≦1.333−0.620×logMI2.16
を満たすものである請求項4記載の方法。The olefin / cyclic olefin copolymer is (1) a ratio Mw / Mn of weight average molecular weight (Mw) and number average molecular weight (Mn) measured by gel permeation chromatography method is 6 or less, and (2) cyclic The olefin unit content is 0.1 to 95 mol%, and (3) the relationship between the intrinsic viscosity [η] measured at 135 ° C. in decalin and the melt index (MI 2.16 ) measured at a load of 2.16 kg. [Η] ≦ 1.333−0.620 × log MI 2.16
The method according to claim 4 , wherein:
〔η〕≦1.333−0.620×logMI2.16
を満たすオレフィン/環状オレフィン共重合体。 Has been produced using the claim 1 or 2 wherein the catalyst (1) gel permeation weight average molecular weight as measured by chromatography (Mw) to number-average molecular weight (Mn) of the ratio Mw / Mn Is 6 or less, (2) the cyclic olefin unit content is 0.1 to 95 mol%, and (3) melt measured in decalin at 135 ° C. with an intrinsic viscosity [η] and a load of 2.16 kg. The relationship with the index (MI 2.16 ) is the formula [η] ≦ 1.333−0.620 × log MI 2.16
An olefin / cyclic olefin copolymer satisfying the above requirements.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP5-289289 | 1993-11-18 | ||
| JP28928993 | 1993-11-18 | ||
| PCT/JP1994/001939 WO1995014024A1 (en) | 1993-11-18 | 1994-11-17 | Transition metal compound, olefin polymerization catalyst, and process for producing olefin polymer by using said catalyst |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO1995014024A1 JPWO1995014024A1 (en) | 1996-04-30 |
| JP3795072B2 true JP3795072B2 (en) | 2006-07-12 |
Family
ID=17741255
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP51434595A Expired - Fee Related JP3795072B2 (en) | 1993-11-18 | 1994-11-17 | Transition metal compound, catalyst for olefin polymerization, and method for producing olefin polymer using the catalyst |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP3795072B2 (en) |
| WO (1) | WO1995014024A1 (en) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20190135953A1 (en) * | 2016-06-15 | 2019-05-09 | Scg Chemicals Co., Ltd. | Olefin polymerisation catalysts |
| US20190135954A1 (en) * | 2016-06-15 | 2019-05-09 | Scg Chemicals Co., Ltd. | Catalytic compositions |
| US10773246B2 (en) | 2015-01-06 | 2020-09-15 | Scg Chemicals Co., Ltd. | SiO2-layered double hydroxide microspheres and methods of making them |
| WO2020204188A1 (en) * | 2019-04-04 | 2020-10-08 | ポリプラスチックス株式会社 | Production method for cyclic olefin copolymer |
| US11053269B2 (en) | 2016-05-12 | 2021-07-06 | Scg Chemicals Co., Ltd. | Unsymmetrical metallocene catalysts and uses thereof |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL186283B1 (en) * | 1995-10-27 | 2003-12-31 | Dow Chemical Co | Metal complexes containing substituted indenyl and method of polymerising olefins |
| AU1685597A (en) * | 1996-01-26 | 1997-08-20 | Dow Chemical Company, The | Improved olefin addition polymerization catalyst composition |
| WO1998006727A1 (en) | 1996-08-08 | 1998-02-19 | The Dow Chemical Company | 3-heteroatom substituted cyclopentadienyl-containing metal complexes and olefin polymerization process |
| US6015868A (en) * | 1996-10-03 | 2000-01-18 | The Dow Chemical Company | Substituted indenyl containing metal complexes and olefin polymerization process |
| US5965756A (en) * | 1996-12-19 | 1999-10-12 | The Dow Chemical Company | Fused ring substituted indenyl metal complexes and polymerization process |
| ID21507A (en) * | 1996-12-19 | 1999-06-17 | Dow Chemical Co | METAL COMPLEX CONTAINING SUBSTITUTED INDENYL IN 3-ARYL AND ITS POLYMERIZATION PROCESS |
| EP1582525B1 (en) * | 1996-12-20 | 2014-12-17 | Sumitomo Chemical Company, Limited | Boron compound in the form of fine particles, component of catalyst for olefin polymerization comprising the same and method for producing the same |
| US6420507B1 (en) | 1997-05-01 | 2002-07-16 | The Dow Chemical Company | Olefin polymers prepared with substituted indenyl containing metal complexes |
| AR012645A1 (en) * | 1997-05-01 | 2000-11-08 | Dow Global Technologies Inc | ALPHA-OLEPHINE POLYMERS PREPARED BY POLYMERIZATION IN THE PRESENCE OF METAL COMPLEXES CONTAINING INDENILO GROUPS |
| DE19733017A1 (en) * | 1997-07-31 | 1999-02-04 | Hoechst Ag | Chemical compound |
| ES2666708T3 (en) | 1998-11-02 | 2018-05-07 | Dow Global Technologies Llc | Ethylene / alpha-olefin re-fluidizing interpolymers and their preparation |
| US6369176B1 (en) | 1999-08-19 | 2002-04-09 | Dupont Dow Elastomers Llc | Process for preparing in a single reactor polymer blends having a broad molecular weight distribution |
| JP4542657B2 (en) * | 2000-02-21 | 2010-09-15 | 日本ポリオレフィン株式会社 | Polysubstituted indene derivative and method for producing the same |
| US6455638B2 (en) | 2000-05-11 | 2002-09-24 | Dupont Dow Elastomers L.L.C. | Ethylene/α-olefin polymer blends comprising components with differing ethylene contents |
| TWI315314B (en) * | 2002-08-29 | 2009-10-01 | Ineos Europe Ltd | Polymerisation process |
| CA2680334C (en) | 2007-03-15 | 2016-03-29 | Union Carbide Chemicals & Plastics Technology Llc | Cable insulation with reduced electrical treeing |
| US8080735B2 (en) | 2007-09-25 | 2011-12-20 | Dow Global Technologies Llc | Styrenic polymers as blend components to control adhesion between olefinic substrates |
| WO2009058545A2 (en) | 2007-11-01 | 2009-05-07 | Dow Global Technologies Inc. | In situ moisture generation and use of polyfunctional alcohols for crosslinking of silane-functionalized resins |
| CA2726607C (en) | 2008-06-05 | 2016-10-04 | Union Carbide Chemicals & Plastics Technology Llc | Method for producing water tree-resistant, trxlpe-type cable sheath |
| JP5723372B2 (en) | 2009-09-16 | 2015-05-27 | ユニオン カーバイド ケミカルズ アンド プラスティックス テクノロジー エルエルシー | Method for producing a cross-linked melt-formed product |
| WO2011034833A2 (en) | 2009-09-18 | 2011-03-24 | Union Carbide Chemicals & Plastics Technology Llc | Process for making crosslinked injection molded articles |
| WO2011102957A1 (en) | 2010-02-16 | 2011-08-25 | Dow Global Technologies Llc | Adhesion reduction between a metal conductor and an insulation sheath |
| US8991039B2 (en) | 2010-09-30 | 2015-03-31 | Dow Global Technologies Llc | Method for manufacturing flexible multilayer electrical articles with improved layer adhesion |
| CA2861113C (en) | 2012-01-31 | 2020-03-24 | Dow Global Technologies Llc | Thermoplastic, semiconductive compositions |
| JP6785657B2 (en) | 2013-09-20 | 2020-11-18 | ダウ グローバル テクノロジーズ エルエルシー | How to degas a bridged power cable |
| WO2018044414A1 (en) | 2016-08-30 | 2018-03-08 | Dow Global Technologies Llc | Method for thermally insulating subsea structures |
| JP6921563B2 (en) * | 2017-03-07 | 2021-08-18 | 出光興産株式会社 | Method for Producing Transition Metal Compounds and Olefin Polymers |
| EP3688082B1 (en) | 2017-09-26 | 2023-11-08 | Dow Global Technologies LLC | Compositions comprising a tin-based catalyst and titanium dioxide for moisture cure of silane-functionalized ethylenic polymers |
| BR112022012371A2 (en) | 2019-12-26 | 2022-08-30 | Dow Global Technologies Llc | CROSS-LINKED POLYOLEFIN FOAM AND PROCESS TO PRODUCE IT |
| BR112022012559A2 (en) | 2019-12-30 | 2022-09-06 | Dow Global Technologies Llc | COMPOSITION AND COATED CONDUCTOR |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NZ235032A (en) * | 1989-08-31 | 1993-04-28 | Dow Chemical Co | Constrained geometry complexes of titanium, zirconium or hafnium comprising a substituted cyclopentadiene ligand; use as olefin polymerisation catalyst component |
| ATE147761T1 (en) * | 1990-06-22 | 1997-02-15 | Exxon Chemical Patents Inc | ALUMINUM-FREE MONOCYCLOPENTADIENYL METALLOCENE CATALYSTS FOR OLEFIN POLYMERIZATION |
| DE59210001D1 (en) * | 1991-10-15 | 2005-02-17 | Basell Polyolefine Gmbh | Process for the preparation of an olefin polymer using metallocenes with specifically substituted indenyl ligands |
| JP3205384B2 (en) * | 1991-12-03 | 2001-09-04 | 昭和電工株式会社 | Method for producing polyolefin |
-
1994
- 1994-11-17 JP JP51434595A patent/JP3795072B2/en not_active Expired - Fee Related
- 1994-11-17 WO PCT/JP1994/001939 patent/WO1995014024A1/en not_active Ceased
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10773246B2 (en) | 2015-01-06 | 2020-09-15 | Scg Chemicals Co., Ltd. | SiO2-layered double hydroxide microspheres and methods of making them |
| US11643331B2 (en) | 2015-01-06 | 2023-05-09 | Scg Chemicals Co., Ltd. | SiO2-layered double hydroxide microspheres and methods of making them |
| US11053269B2 (en) | 2016-05-12 | 2021-07-06 | Scg Chemicals Co., Ltd. | Unsymmetrical metallocene catalysts and uses thereof |
| US20190135953A1 (en) * | 2016-06-15 | 2019-05-09 | Scg Chemicals Co., Ltd. | Olefin polymerisation catalysts |
| US20190135954A1 (en) * | 2016-06-15 | 2019-05-09 | Scg Chemicals Co., Ltd. | Catalytic compositions |
| WO2020204188A1 (en) * | 2019-04-04 | 2020-10-08 | ポリプラスチックス株式会社 | Production method for cyclic olefin copolymer |
Also Published As
| Publication number | Publication date |
|---|---|
| WO1995014024A1 (en) | 1995-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3795072B2 (en) | Transition metal compound, catalyst for olefin polymerization, and method for producing olefin polymer using the catalyst | |
| JPWO1995014024A1 (en) | Transition metal compound, catalyst for olefin polymerization, and method for producing olefin polymer using said catalyst | |
| JP7238135B2 (en) | Olefin polymerization catalyst and olefin polymer prepared using the same | |
| JP3363904B2 (en) | Branched ethylene macromonomer and polymer using the same | |
| KR100244381B1 (en) | Method for producing alpha-olefin polymers | |
| JP3219277B2 (en) | Method for producing olefin-based polymer and ethylene-based polymerization | |
| EP0683184A1 (en) | Polyethylene, thermoplastic resin composition containing the same, and process for producing polyethylene | |
| KR20020030085A (en) | Branched olefinic macromonomer, olefin graft copolymer, and olefin resin composition | |
| JP3216748B2 (en) | Catalyst for producing aromatic vinyl compound polymer composition and method for producing aromatic vinyl compound polymer composition using the same | |
| CN100396706C (en) | polyolefin block copolymer | |
| JPWO1995011931A1 (en) | Branched ethylene macromonomer and polymer using same | |
| JPWO1995018158A1 (en) | Method for producing olefin polymer and ethylene polymer | |
| JPWO2003014166A1 (en) | Method for producing polymer | |
| JPH08512063A (en) | Process for producing amorphous poly-α-olefins by monocyclopentadienyl transition metal catalyst system | |
| CA2374007A1 (en) | Thermoplastic compositions of isotactic propylene polymers and flexible propylene polymers having reduced isotacticity and a process for the preparation thereof | |
| JP3301455B2 (en) | Catalyst for producing aromatic vinyl compound polymer and method for producing aromatic vinyl compound polymer using the same | |
| US5596054A (en) | Transition metal compound, polymerization catalyst using same and process for producing styrenic polymer using said polymerization catalyst | |
| NO310874B1 (en) | Metallocene compound and process for its use in the production of olefin polymer | |
| Kashiwa et al. | Recent progress on olefin polymerization catalysts | |
| JPH0733812A (en) | Styrene-based polymer production catalyst and method for producing styrene-based polymer using the same | |
| JP3233225B2 (en) | Method for producing olefin-based graft copolymer and olefin-based graft copolymer | |
| JP2002003553A (en) | Cross copolymer containing polyene in cross chain and method for producing the same | |
| JP3506147B2 (en) | Ethylene / α-olefin copolymer and thermoplastic resin composition containing the same | |
| JPH08325333A (en) | Ethylene-alpha-olefin copolymer | |
| CA2327781A1 (en) | Propylene copolymers containing styrene units |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20040622 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20040819 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20060328 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20060412 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| RD01 | Notification of change of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7426 Effective date: 20060413 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20090421 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120421 Year of fee payment: 6 |
|
| LAPS | Cancellation because of no payment of annual fees |