JP2024082217A - Tetracarboxylic dianhydrides, polyesterimides, and polyesterimide films - Google Patents
Tetracarboxylic dianhydrides, polyesterimides, and polyesterimide films Download PDFInfo
- Publication number
- JP2024082217A JP2024082217A JP2023079533A JP2023079533A JP2024082217A JP 2024082217 A JP2024082217 A JP 2024082217A JP 2023079533 A JP2023079533 A JP 2023079533A JP 2023079533 A JP2023079533 A JP 2023079533A JP 2024082217 A JP2024082217 A JP 2024082217A
- Authority
- JP
- Japan
- Prior art keywords
- film
- polyesterimide
- group
- tetracarboxylic dianhydride
- reaction
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 229920003055 poly(ester-imide) Polymers 0.000 title claims abstract description 167
- GTDPSWPPOUPBNX-UHFFFAOYSA-N ac1mqpva Chemical compound CC12C(=O)OC(=O)C1(C)C1(C)C2(C)C(=O)OC1=O GTDPSWPPOUPBNX-UHFFFAOYSA-N 0.000 claims abstract description 86
- 125000006158 tetracarboxylic acid group Chemical group 0.000 claims abstract description 66
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 52
- 238000010521 absorption reaction Methods 0.000 claims abstract description 36
- 125000003118 aryl group Chemical group 0.000 claims description 34
- 125000001931 aliphatic group Chemical group 0.000 claims description 22
- 239000000758 substrate Substances 0.000 claims description 19
- 238000004891 communication Methods 0.000 claims description 11
- 230000009477 glass transition Effects 0.000 claims description 9
- 238000004458 analytical method Methods 0.000 claims description 8
- 230000000930 thermomechanical effect Effects 0.000 claims description 6
- 239000010408 film Substances 0.000 description 168
- 239000002904 solvent Substances 0.000 description 90
- 239000002243 precursor Substances 0.000 description 61
- 238000006243 chemical reaction Methods 0.000 description 54
- 238000000034 method Methods 0.000 description 51
- 239000003795 chemical substances by application Substances 0.000 description 35
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 34
- 239000000243 solution Substances 0.000 description 33
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 31
- 238000006116 polymerization reaction Methods 0.000 description 31
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 30
- 239000000047 product Substances 0.000 description 30
- 229920001721 polyimide Polymers 0.000 description 29
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 27
- 125000004185 ester group Chemical group 0.000 description 27
- 229930185605 Bisphenol Natural products 0.000 description 26
- 239000002253 acid Substances 0.000 description 24
- 239000002966 varnish Substances 0.000 description 24
- 239000007788 liquid Substances 0.000 description 22
- -1 tetracarboxylic acid dianhydride Chemical class 0.000 description 21
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 18
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 18
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 18
- HLBLWEWZXPIGSM-UHFFFAOYSA-N 4-Aminophenyl ether Chemical compound C1=CC(N)=CC=C1OC1=CC=C(N)C=C1 HLBLWEWZXPIGSM-UHFFFAOYSA-N 0.000 description 17
- 150000004985 diamines Chemical class 0.000 description 17
- 238000005886 esterification reaction Methods 0.000 description 17
- 239000000543 intermediate Substances 0.000 description 16
- 238000004519 manufacturing process Methods 0.000 description 16
- 239000000203 mixture Substances 0.000 description 16
- CBCKQZAAMUWICA-UHFFFAOYSA-N 1,4-phenylenediamine Chemical compound NC1=CC=C(N)C=C1 CBCKQZAAMUWICA-UHFFFAOYSA-N 0.000 description 15
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 15
- 150000001875 compounds Chemical class 0.000 description 15
- 239000000178 monomer Substances 0.000 description 15
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 14
- 239000012320 chlorinating reagent Substances 0.000 description 14
- 239000000126 substance Substances 0.000 description 14
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 14
- 239000002585 base Substances 0.000 description 13
- 238000011156 evaluation Methods 0.000 description 13
- NJMOHBDCGXJLNJ-UHFFFAOYSA-N trimellitic anhydride chloride Chemical compound ClC(=O)C1=CC=C2C(=O)OC(=O)C2=C1 NJMOHBDCGXJLNJ-UHFFFAOYSA-N 0.000 description 13
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 12
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 12
- 239000004642 Polyimide Substances 0.000 description 12
- 239000000463 material Substances 0.000 description 12
- MNZMMCVIXORAQL-UHFFFAOYSA-N naphthalene-2,6-diol Chemical compound C1=C(O)C=CC2=CC(O)=CC=C21 MNZMMCVIXORAQL-UHFFFAOYSA-N 0.000 description 12
- 238000002360 preparation method Methods 0.000 description 12
- 238000000862 absorption spectrum Methods 0.000 description 11
- 239000006227 byproduct Substances 0.000 description 11
- 238000010438 heat treatment Methods 0.000 description 11
- 125000005462 imide group Chemical group 0.000 description 11
- 239000002244 precipitate Substances 0.000 description 11
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 10
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 10
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 10
- 230000015572 biosynthetic process Effects 0.000 description 10
- 230000001965 increasing effect Effects 0.000 description 10
- 238000001556 precipitation Methods 0.000 description 10
- 239000010409 thin film Substances 0.000 description 10
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 9
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- 238000005033 Fourier transform infrared spectroscopy Methods 0.000 description 9
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- 238000006460 hydrolysis reaction Methods 0.000 description 9
- 238000002844 melting Methods 0.000 description 9
- 230000008018 melting Effects 0.000 description 9
- 229920005575 poly(amic acid) Polymers 0.000 description 9
- 230000008569 process Effects 0.000 description 9
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 9
- VLDPXPPHXDGHEW-UHFFFAOYSA-N 1-chloro-2-dichlorophosphoryloxybenzene Chemical compound ClC1=CC=CC=C1OP(Cl)(Cl)=O VLDPXPPHXDGHEW-UHFFFAOYSA-N 0.000 description 8
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 8
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 8
- 238000009833 condensation Methods 0.000 description 8
- 230000005494 condensation Effects 0.000 description 8
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 8
- BGTOWKSIORTVQH-UHFFFAOYSA-N cyclopentanone Chemical compound O=C1CCCC1 BGTOWKSIORTVQH-UHFFFAOYSA-N 0.000 description 8
- 229920000642 polymer Polymers 0.000 description 8
- 238000001953 recrystallisation Methods 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 7
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 7
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 7
- 150000001408 amides Chemical class 0.000 description 7
- 229910052757 nitrogen Inorganic materials 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- BDNKZNFMNDZQMI-UHFFFAOYSA-N 1,3-diisopropylcarbodiimide Chemical compound CC(C)N=C=NC(C)C BDNKZNFMNDZQMI-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- JLTDJTHDQAWBAV-UHFFFAOYSA-N N,N-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1 JLTDJTHDQAWBAV-UHFFFAOYSA-N 0.000 description 6
- 238000005660 chlorination reaction Methods 0.000 description 6
- 238000007334 copolymerization reaction Methods 0.000 description 6
- 239000011889 copper foil Substances 0.000 description 6
- GGSUCNLOZRCGPQ-UHFFFAOYSA-N diethylaniline Chemical compound CCN(CC)C1=CC=CC=C1 GGSUCNLOZRCGPQ-UHFFFAOYSA-N 0.000 description 6
- 238000010790 dilution Methods 0.000 description 6
- 239000012895 dilution Substances 0.000 description 6
- 239000003759 ester based solvent Substances 0.000 description 6
- 238000001879 gelation Methods 0.000 description 6
- 150000004820 halides Chemical class 0.000 description 6
- 229910052739 hydrogen Inorganic materials 0.000 description 6
- 230000007062 hydrolysis Effects 0.000 description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 6
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 6
- 239000012299 nitrogen atmosphere Substances 0.000 description 6
- FDPIMTJIUBPUKL-UHFFFAOYSA-N pentan-3-one Chemical compound CCC(=O)CC FDPIMTJIUBPUKL-UHFFFAOYSA-N 0.000 description 6
- 150000003512 tertiary amines Chemical class 0.000 description 6
- GEWWCWZGHNIUBW-UHFFFAOYSA-N 1-(4-nitrophenyl)propan-2-one Chemical compound CC(=O)CC1=CC=C([N+]([O-])=O)C=C1 GEWWCWZGHNIUBW-UHFFFAOYSA-N 0.000 description 5
- 238000005160 1H NMR spectroscopy Methods 0.000 description 5
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 5
- 150000004984 aromatic diamines Chemical class 0.000 description 5
- 150000001718 carbodiimides Chemical class 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 230000018044 dehydration Effects 0.000 description 5
- 238000006297 dehydration reaction Methods 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 230000000704 physical effect Effects 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- 230000009257 reactivity Effects 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 5
- 150000003457 sulfones Chemical class 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 5
- LOCTYHIHNCOYJZ-UHFFFAOYSA-N (4-aminophenyl) 4-aminobenzoate Chemical compound C1=CC(N)=CC=C1OC(=O)C1=CC=C(N)C=C1 LOCTYHIHNCOYJZ-UHFFFAOYSA-N 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- KAUQJMHLAFIZDU-UHFFFAOYSA-N 6-Hydroxy-2-naphthoic acid Chemical compound C1=C(O)C=CC2=CC(C(=O)O)=CC=C21 KAUQJMHLAFIZDU-UHFFFAOYSA-N 0.000 description 4
- NFTLBCXRDNIJMI-UHFFFAOYSA-N 6-acetyloxynaphthalene-2-carboxylic acid Chemical compound C1=C(C(O)=O)C=CC2=CC(OC(=O)C)=CC=C21 NFTLBCXRDNIJMI-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 4
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 4
- 230000005540 biological transmission Effects 0.000 description 4
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical compound C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 4
- BGRWYRAHAFMIBJ-UHFFFAOYSA-N diisopropylcarbodiimide Natural products CC(C)NC(=O)NC(C)C BGRWYRAHAFMIBJ-UHFFFAOYSA-N 0.000 description 4
- 238000000921 elemental analysis Methods 0.000 description 4
- 239000004210 ether based solvent Substances 0.000 description 4
- 239000005453 ketone based solvent Substances 0.000 description 4
- AOJFQRQNPXYVLM-UHFFFAOYSA-N pyridin-1-ium;chloride Chemical compound [Cl-].C1=CC=[NH+]C=C1 AOJFQRQNPXYVLM-UHFFFAOYSA-N 0.000 description 4
- SQGYOTSLMSWVJD-UHFFFAOYSA-N silver(1+) nitrate Chemical compound [Ag+].[O-]N(=O)=O SQGYOTSLMSWVJD-UHFFFAOYSA-N 0.000 description 4
- 150000000000 tetracarboxylic acids Chemical class 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- CBGOEJZZFABRGB-UHFFFAOYSA-N (4-amino-2-methylphenyl) 4-aminobenzoate Chemical compound Cc1cc(N)ccc1OC(=O)c1ccc(N)cc1 CBGOEJZZFABRGB-UHFFFAOYSA-N 0.000 description 3
- CYSGHNMQYZDMIA-UHFFFAOYSA-N 1,3-Dimethyl-2-imidazolidinon Chemical compound CN1CCN(C)C1=O CYSGHNMQYZDMIA-UHFFFAOYSA-N 0.000 description 3
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical compound CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 3
- 238000005481 NMR spectroscopy Methods 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- BHTRKEVKTKCXOH-UHFFFAOYSA-N Taurochenodesoxycholsaeure Natural products OC1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(=O)NCCS(O)(=O)=O)C)C1(C)CC2 BHTRKEVKTKCXOH-UHFFFAOYSA-N 0.000 description 3
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 239000003513 alkali Substances 0.000 description 3
- 150000008064 anhydrides Chemical group 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- VKIRRGRTJUUZHS-UHFFFAOYSA-N cyclohexane-1,4-diamine Chemical compound NC1CCC(N)CC1 VKIRRGRTJUUZHS-UHFFFAOYSA-N 0.000 description 3
- 238000004821 distillation Methods 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 230000032050 esterification Effects 0.000 description 3
- 230000001771 impaired effect Effects 0.000 description 3
- 239000011261 inert gas Substances 0.000 description 3
- 150000007529 inorganic bases Chemical class 0.000 description 3
- YKYONYBAUNKHLG-UHFFFAOYSA-N n-Propyl acetate Natural products CCCOC(C)=O YKYONYBAUNKHLG-UHFFFAOYSA-N 0.000 description 3
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 3
- 229940090181 propyl acetate Drugs 0.000 description 3
- 239000002994 raw material Substances 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 229910000679 solder Inorganic materials 0.000 description 3
- AWDRATDZQPNJFN-VAYUFCLWSA-N taurodeoxycholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCCS(O)(=O)=O)C)[C@@]2(C)[C@@H](O)C1 AWDRATDZQPNJFN-VAYUFCLWSA-N 0.000 description 3
- 229950005578 tidiacic Drugs 0.000 description 3
- 230000001988 toxicity Effects 0.000 description 3
- 231100000419 toxicity Toxicity 0.000 description 3
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 3
- SRPWOOOHEPICQU-UHFFFAOYSA-N trimellitic anhydride Chemical compound OC(=O)C1=CC=C2C(=O)OC(=O)C2=C1 SRPWOOOHEPICQU-UHFFFAOYSA-N 0.000 description 3
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 3
- NQPDZGIKBAWPEJ-UHFFFAOYSA-N valeric acid Chemical compound CCCCC(O)=O NQPDZGIKBAWPEJ-UHFFFAOYSA-N 0.000 description 3
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 2
- XUSNPFGLKGCWGN-UHFFFAOYSA-N 3-[4-(3-aminopropyl)piperazin-1-yl]propan-1-amine Chemical compound NCCCN1CCN(CCCN)CC1 XUSNPFGLKGCWGN-UHFFFAOYSA-N 0.000 description 2
- KMKWGXGSGPYISJ-UHFFFAOYSA-N 4-[4-[2-[4-(4-aminophenoxy)phenyl]propan-2-yl]phenoxy]aniline Chemical compound C=1C=C(OC=2C=CC(N)=CC=2)C=CC=1C(C)(C)C(C=C1)=CC=C1OC1=CC=C(N)C=C1 KMKWGXGSGPYISJ-UHFFFAOYSA-N 0.000 description 2
- CQMIJLIXKMKFQW-UHFFFAOYSA-N 4-phenylbenzene-1,2,3,5-tetracarboxylic acid Chemical compound OC(=O)C1=C(C(O)=O)C(C(=O)O)=CC(C(O)=O)=C1C1=CC=CC=C1 CQMIJLIXKMKFQW-UHFFFAOYSA-N 0.000 description 2
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- JRNVZBWKYDBUCA-UHFFFAOYSA-N N-chlorosuccinimide Chemical compound ClN1C(=O)CCC1=O JRNVZBWKYDBUCA-UHFFFAOYSA-N 0.000 description 2
- 229910021607 Silver chloride Inorganic materials 0.000 description 2
- RAHZWNYVWXNFOC-UHFFFAOYSA-N Sulphur dioxide Chemical compound O=S=O RAHZWNYVWXNFOC-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 239000002318 adhesion promoter Substances 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N ammonia Natural products N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- WKDNYTOXBCRNPV-UHFFFAOYSA-N bpda Chemical compound C1=C2C(=O)OC(=O)C2=CC(C=2C=C3C(=O)OC(C3=CC=2)=O)=C1 WKDNYTOXBCRNPV-UHFFFAOYSA-N 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- 239000003431 cross linking reagent Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 2
- 150000002009 diols Chemical class 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000003063 flame retardant Substances 0.000 description 2
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 150000002430 hydrocarbons Chemical class 0.000 description 2
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 2
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 2
- 239000011256 inorganic filler Substances 0.000 description 2
- 229910003475 inorganic filler Inorganic materials 0.000 description 2
- 238000010295 mobile communication Methods 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- 239000012454 non-polar solvent Substances 0.000 description 2
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 2
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 2
- IWDCLRJOBJJRNH-UHFFFAOYSA-N p-cresol Chemical compound CC1=CC=C(O)C=C1 IWDCLRJOBJJRNH-UHFFFAOYSA-N 0.000 description 2
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 2
- 239000003504 photosensitizing agent Substances 0.000 description 2
- 230000010287 polarization Effects 0.000 description 2
- 229920003223 poly(pyromellitimide-1,4-diphenyl ether) Polymers 0.000 description 2
- 239000003505 polymerization initiator Substances 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 description 2
- 229910001961 silver nitrate Inorganic materials 0.000 description 2
- WBHQBSYUUJJSRZ-UHFFFAOYSA-M sodium bisulfate Chemical compound [Na+].OS([O-])(=O)=O WBHQBSYUUJJSRZ-UHFFFAOYSA-M 0.000 description 2
- 229910000342 sodium bisulfate Inorganic materials 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 230000003068 static effect Effects 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- ARCGXLSVLAOJQL-UHFFFAOYSA-N trimellitic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C(C(O)=O)=C1 ARCGXLSVLAOJQL-UHFFFAOYSA-N 0.000 description 2
- XFNJVJPLKCPIBV-UHFFFAOYSA-N trimethylenediamine Chemical compound NCCCN XFNJVJPLKCPIBV-UHFFFAOYSA-N 0.000 description 2
- 239000012855 volatile organic compound Substances 0.000 description 2
- 230000004580 weight loss Effects 0.000 description 2
- NAWXUBYGYWOOIX-SFHVURJKSA-N (2s)-2-[[4-[2-(2,4-diaminoquinazolin-6-yl)ethyl]benzoyl]amino]-4-methylidenepentanedioic acid Chemical compound C1=CC2=NC(N)=NC(N)=C2C=C1CCC1=CC=C(C(=O)N[C@@H](CC(=C)C(O)=O)C(O)=O)C=C1 NAWXUBYGYWOOIX-SFHVURJKSA-N 0.000 description 1
- GQAXSRIBRIMFIT-UHFFFAOYSA-N (6-carbonochloridoylnaphthalen-2-yl) acetate Chemical group C1=C(C(Cl)=O)C=CC2=CC(OC(=O)C)=CC=C21 GQAXSRIBRIMFIT-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- FQYTUPYMTLWOOF-UHFFFAOYSA-N 1,3,4,6-tetramethylcyclohex-4-ene-1,3-diamine Chemical compound CC1C=C(C)C(C)(N)CC1(C)N FQYTUPYMTLWOOF-UHFFFAOYSA-N 0.000 description 1
- YRIZYWQGELRKNT-UHFFFAOYSA-N 1,3,5-trichloro-1,3,5-triazinane-2,4,6-trione Chemical compound ClN1C(=O)N(Cl)C(=O)N(Cl)C1=O YRIZYWQGELRKNT-UHFFFAOYSA-N 0.000 description 1
- KEQGZUUPPQEDPF-UHFFFAOYSA-N 1,3-dichloro-5,5-dimethylimidazolidine-2,4-dione Chemical compound CC1(C)N(Cl)C(=O)N(Cl)C1=O KEQGZUUPPQEDPF-UHFFFAOYSA-N 0.000 description 1
- SBHHKGFHJWTZJN-UHFFFAOYSA-N 1,3-dimethylcyclobutane-1,2,3,4-tetracarboxylic acid Chemical compound OC(=O)C1(C)C(C(O)=O)C(C)(C(O)=O)C1C(O)=O SBHHKGFHJWTZJN-UHFFFAOYSA-N 0.000 description 1
- WZCQRUWWHSTZEM-UHFFFAOYSA-N 1,3-phenylenediamine Chemical compound NC1=CC=CC(N)=C1 WZCQRUWWHSTZEM-UHFFFAOYSA-N 0.000 description 1
- 125000001140 1,4-phenylene group Chemical group [H]C1=C([H])C([*:2])=C([H])C([H])=C1[*:1] 0.000 description 1
- PWGJDPKCLMLPJW-UHFFFAOYSA-N 1,8-diaminooctane Chemical compound NCCCCCCCCN PWGJDPKCLMLPJW-UHFFFAOYSA-N 0.000 description 1
- XOXIOEOLTILAQF-UHFFFAOYSA-N 1-phenoxy-2-[2-(2-phenoxyphenyl)propan-2-yl]benzene Chemical group C=1C=CC=C(OC=2C=CC=CC=2)C=1C(C)(C)C1=CC=CC=C1OC1=CC=CC=C1 XOXIOEOLTILAQF-UHFFFAOYSA-N 0.000 description 1
- RNFJDJUURJAICM-UHFFFAOYSA-N 2,2,4,4,6,6-hexaphenoxy-1,3,5-triaza-2$l^{5},4$l^{5},6$l^{5}-triphosphacyclohexa-1,3,5-triene Chemical compound N=1P(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP=1(OC=1C=CC=CC=1)OC1=CC=CC=C1 RNFJDJUURJAICM-UHFFFAOYSA-N 0.000 description 1
- RDMFEHLCCOQUMH-UHFFFAOYSA-N 2,4'-Diphenyldiamine Chemical group C1=CC(N)=CC=C1C1=CC=CC=C1N RDMFEHLCCOQUMH-UHFFFAOYSA-N 0.000 description 1
- VOZKAJLKRJDJLL-UHFFFAOYSA-N 2,4-diaminotoluene Chemical compound CC1=CC=C(N)C=C1N VOZKAJLKRJDJLL-UHFFFAOYSA-N 0.000 description 1
- 229940075142 2,5-diaminotoluene Drugs 0.000 description 1
- HOLGXWDGCVTMTB-UHFFFAOYSA-N 2-(2-aminophenyl)aniline Chemical group NC1=CC=CC=C1C1=CC=CC=C1N HOLGXWDGCVTMTB-UHFFFAOYSA-N 0.000 description 1
- ZGDMDBHLKNQPSD-UHFFFAOYSA-N 2-amino-5-(4-amino-3-hydroxyphenyl)phenol Chemical compound C1=C(O)C(N)=CC=C1C1=CC=C(N)C(O)=C1 ZGDMDBHLKNQPSD-UHFFFAOYSA-N 0.000 description 1
- WDRFYIPWHMGQPN-UHFFFAOYSA-N 2-chloroisoindole-1,3-dione Chemical compound C1=CC=C2C(=O)N(Cl)C(=O)C2=C1 WDRFYIPWHMGQPN-UHFFFAOYSA-N 0.000 description 1
- JJKWHOSQTYYFAE-UHFFFAOYSA-N 2-methoxyacetyl chloride Chemical compound COCC(Cl)=O JJKWHOSQTYYFAE-UHFFFAOYSA-N 0.000 description 1
- OBCSAIDCZQSFQH-UHFFFAOYSA-N 2-methyl-1,4-phenylenediamine Chemical compound CC1=CC(N)=CC=C1N OBCSAIDCZQSFQH-UHFFFAOYSA-N 0.000 description 1
- JRBJSXQPQWSCCF-UHFFFAOYSA-N 3,3'-Dimethoxybenzidine Chemical compound C1=C(N)C(OC)=CC(C=2C=C(OC)C(N)=CC=2)=C1 JRBJSXQPQWSCCF-UHFFFAOYSA-N 0.000 description 1
- NUIURNJTPRWVAP-UHFFFAOYSA-N 3,3'-Dimethylbenzidine Chemical compound C1=C(N)C(C)=CC(C=2C=C(C)C(N)=CC=2)=C1 NUIURNJTPRWVAP-UHFFFAOYSA-N 0.000 description 1
- BDSPLIQKGRTNCG-UHFFFAOYSA-N 3,4-dimethylcyclohexa-1,5-diene-1,3-diamine Chemical group CC1C=CC(N)=CC1(C)N BDSPLIQKGRTNCG-UHFFFAOYSA-N 0.000 description 1
- LXJLFVRAWOOQDR-UHFFFAOYSA-N 3-(3-aminophenoxy)aniline Chemical compound NC1=CC=CC(OC=2C=C(N)C=CC=2)=C1 LXJLFVRAWOOQDR-UHFFFAOYSA-N 0.000 description 1
- LJGHYPLBDBRCRZ-UHFFFAOYSA-N 3-(3-aminophenyl)sulfonylaniline Chemical compound NC1=CC=CC(S(=O)(=O)C=2C=C(N)C=CC=2)=C1 LJGHYPLBDBRCRZ-UHFFFAOYSA-N 0.000 description 1
- ZBMISJGHVWNWTE-UHFFFAOYSA-N 3-(4-aminophenoxy)aniline Chemical compound C1=CC(N)=CC=C1OC1=CC=CC(N)=C1 ZBMISJGHVWNWTE-UHFFFAOYSA-N 0.000 description 1
- RNLHGQLZWXBQNY-UHFFFAOYSA-N 3-(aminomethyl)-3,5,5-trimethylcyclohexan-1-amine Chemical compound CC1(C)CC(N)CC(C)(CN)C1 RNLHGQLZWXBQNY-UHFFFAOYSA-N 0.000 description 1
- DKKYOQYISDAQER-UHFFFAOYSA-N 3-[3-(3-aminophenoxy)phenoxy]aniline Chemical compound NC1=CC=CC(OC=2C=C(OC=3C=C(N)C=CC=3)C=CC=2)=C1 DKKYOQYISDAQER-UHFFFAOYSA-N 0.000 description 1
- LBPVOEHZEWAJKQ-UHFFFAOYSA-N 3-[4-(3-aminophenoxy)phenoxy]aniline Chemical compound NC1=CC=CC(OC=2C=CC(OC=3C=C(N)C=CC=3)=CC=2)=C1 LBPVOEHZEWAJKQ-UHFFFAOYSA-N 0.000 description 1
- WCXGOVYROJJXHA-UHFFFAOYSA-N 3-[4-[4-(3-aminophenoxy)phenyl]sulfonylphenoxy]aniline Chemical compound NC1=CC=CC(OC=2C=CC(=CC=2)S(=O)(=O)C=2C=CC(OC=3C=C(N)C=CC=3)=CC=2)=C1 WCXGOVYROJJXHA-UHFFFAOYSA-N 0.000 description 1
- HORNXRXVQWOLPJ-UHFFFAOYSA-N 3-chlorophenol Chemical compound OC1=CC=CC(Cl)=C1 HORNXRXVQWOLPJ-UHFFFAOYSA-N 0.000 description 1
- WECDUOXQLAIPQW-UHFFFAOYSA-N 4,4'-Methylene bis(2-methylaniline) Chemical compound C1=C(N)C(C)=CC(CC=2C=C(C)C(N)=CC=2)=C1 WECDUOXQLAIPQW-UHFFFAOYSA-N 0.000 description 1
- YBRVSVVVWCFQMG-UHFFFAOYSA-N 4,4'-diaminodiphenylmethane Chemical compound C1=CC(N)=CC=C1CC1=CC=C(N)C=C1 YBRVSVVVWCFQMG-UHFFFAOYSA-N 0.000 description 1
- XTEBLARUAVEBRF-UHFFFAOYSA-N 4-(1,1,1,3,3,3-hexafluoropropan-2-yl)aniline Chemical compound NC1=CC=C(C(C(F)(F)F)C(F)(F)F)C=C1 XTEBLARUAVEBRF-UHFFFAOYSA-N 0.000 description 1
- OBBOXORQYKYQJP-UHFFFAOYSA-N 4-[(4-amino-2,6-diethylphenyl)methyl]-3,5-diethylaniline Chemical compound CCC1=CC(N)=CC(CC)=C1CC1=C(CC)C=C(N)C=C1CC OBBOXORQYKYQJP-UHFFFAOYSA-N 0.000 description 1
- QUACYTKJOFAODG-UHFFFAOYSA-N 4-[(4-amino-2,6-dimethylphenyl)methyl]-3,5-dimethylaniline Chemical compound CC1=CC(N)=CC(C)=C1CC1=C(C)C=C(N)C=C1C QUACYTKJOFAODG-UHFFFAOYSA-N 0.000 description 1
- MWMISNKGHLBGLC-UHFFFAOYSA-N 4-[(4-amino-2-ethylcyclohexyl)methyl]-3-ethylcyclohexan-1-amine Chemical compound CCC1CC(N)CCC1CC1C(CC)CC(N)CC1 MWMISNKGHLBGLC-UHFFFAOYSA-N 0.000 description 1
- BNJLZTIXDDRDCF-UHFFFAOYSA-N 4-[(4-amino-2-ethylphenyl)methyl]-3-ethylaniline Chemical compound CCC1=CC(N)=CC=C1CC1=CC=C(N)C=C1CC BNJLZTIXDDRDCF-UHFFFAOYSA-N 0.000 description 1
- NTGJOYPFNABNES-UHFFFAOYSA-N 4-[(4-amino-2-methylcyclohexyl)methyl]-3-methylcyclohexan-1-amine Chemical compound CC1CC(N)CCC1CC1C(C)CC(N)CC1 NTGJOYPFNABNES-UHFFFAOYSA-N 0.000 description 1
- YFKPQCYLWJULME-UHFFFAOYSA-N 4-[(4-amino-2-methylphenyl)methyl]-3-methylaniline Chemical compound CC1=CC(N)=CC=C1CC1=CC=C(N)C=C1C YFKPQCYLWJULME-UHFFFAOYSA-N 0.000 description 1
- NWIVYGKSHSJHEF-UHFFFAOYSA-N 4-[(4-amino-3,5-diethylphenyl)methyl]-2,6-diethylaniline Chemical compound CCC1=C(N)C(CC)=CC(CC=2C=C(CC)C(N)=C(CC)C=2)=C1 NWIVYGKSHSJHEF-UHFFFAOYSA-N 0.000 description 1
- OMHOXRVODFQGCA-UHFFFAOYSA-N 4-[(4-amino-3,5-dimethylphenyl)methyl]-2,6-dimethylaniline Chemical compound CC1=C(N)C(C)=CC(CC=2C=C(C)C(N)=C(C)C=2)=C1 OMHOXRVODFQGCA-UHFFFAOYSA-N 0.000 description 1
- CBEVWPCAHIAUOD-UHFFFAOYSA-N 4-[(4-amino-3-ethylphenyl)methyl]-2-ethylaniline Chemical compound C1=C(N)C(CC)=CC(CC=2C=C(CC)C(N)=CC=2)=C1 CBEVWPCAHIAUOD-UHFFFAOYSA-N 0.000 description 1
- DZIHTWJGPDVSGE-UHFFFAOYSA-N 4-[(4-aminocyclohexyl)methyl]cyclohexan-1-amine Chemical compound C1CC(N)CCC1CC1CCC(N)CC1 DZIHTWJGPDVSGE-UHFFFAOYSA-N 0.000 description 1
- FLDONXPDUZAKQB-UHFFFAOYSA-N 4-[2-(4-aminocyclohexyl)-1,1,1,3,3,3-hexafluoropropan-2-yl]cyclohexan-1-amine Chemical compound C1CC(N)CCC1C(C(F)(F)F)(C(F)(F)F)C1CCC(N)CC1 FLDONXPDUZAKQB-UHFFFAOYSA-N 0.000 description 1
- BDBZTOMUANOKRT-UHFFFAOYSA-N 4-[2-(4-aminocyclohexyl)propan-2-yl]cyclohexan-1-amine Chemical compound C1CC(N)CCC1C(C)(C)C1CCC(N)CC1 BDBZTOMUANOKRT-UHFFFAOYSA-N 0.000 description 1
- BEKFRNOZJSYWKZ-UHFFFAOYSA-N 4-[2-(4-aminophenyl)-1,1,1,3,3,3-hexafluoropropan-2-yl]aniline Chemical compound C1=CC(N)=CC=C1C(C(F)(F)F)(C(F)(F)F)C1=CC=C(N)C=C1 BEKFRNOZJSYWKZ-UHFFFAOYSA-N 0.000 description 1
- WUPRYUDHUFLKFL-UHFFFAOYSA-N 4-[3-(4-aminophenoxy)phenoxy]aniline Chemical compound C1=CC(N)=CC=C1OC1=CC=CC(OC=2C=CC(N)=CC=2)=C1 WUPRYUDHUFLKFL-UHFFFAOYSA-N 0.000 description 1
- JCRRFJIVUPSNTA-UHFFFAOYSA-N 4-[4-(4-aminophenoxy)phenoxy]aniline Chemical compound C1=CC(N)=CC=C1OC(C=C1)=CC=C1OC1=CC=C(N)C=C1 JCRRFJIVUPSNTA-UHFFFAOYSA-N 0.000 description 1
- QBSMHWVGUPQNJJ-UHFFFAOYSA-N 4-[4-(4-aminophenyl)phenyl]aniline Chemical compound C1=CC(N)=CC=C1C1=CC=C(C=2C=CC(N)=CC=2)C=C1 QBSMHWVGUPQNJJ-UHFFFAOYSA-N 0.000 description 1
- HYDATEKARGDBKU-UHFFFAOYSA-N 4-[4-[4-(4-aminophenoxy)phenyl]phenoxy]aniline Chemical group C1=CC(N)=CC=C1OC1=CC=C(C=2C=CC(OC=3C=CC(N)=CC=3)=CC=2)C=C1 HYDATEKARGDBKU-UHFFFAOYSA-N 0.000 description 1
- UTDAGHZGKXPRQI-UHFFFAOYSA-N 4-[4-[4-(4-aminophenoxy)phenyl]sulfonylphenoxy]aniline Chemical compound C1=CC(N)=CC=C1OC1=CC=C(S(=O)(=O)C=2C=CC(OC=3C=CC(N)=CC=3)=CC=2)C=C1 UTDAGHZGKXPRQI-UHFFFAOYSA-N 0.000 description 1
- NVKGJHAQGWCWDI-UHFFFAOYSA-N 4-[4-amino-2-(trifluoromethyl)phenyl]-3-(trifluoromethyl)aniline Chemical compound FC(F)(F)C1=CC(N)=CC=C1C1=CC=C(N)C=C1C(F)(F)F NVKGJHAQGWCWDI-UHFFFAOYSA-N 0.000 description 1
- GDBUZIKSJGRBJP-UHFFFAOYSA-N 4-acetoxy benzoic acid Chemical compound CC(=O)OC1=CC=C(C(O)=O)C=C1 GDBUZIKSJGRBJP-UHFFFAOYSA-N 0.000 description 1
- XPAQFJJCWGSXGJ-UHFFFAOYSA-N 4-amino-n-(4-aminophenyl)benzamide Chemical compound C1=CC(N)=CC=C1NC(=O)C1=CC=C(N)C=C1 XPAQFJJCWGSXGJ-UHFFFAOYSA-N 0.000 description 1
- WXNZTHHGJRFXKQ-UHFFFAOYSA-N 4-chlorophenol Chemical compound OC1=CC=C(Cl)C=C1 WXNZTHHGJRFXKQ-UHFFFAOYSA-N 0.000 description 1
- VQVIHDPBMFABCQ-UHFFFAOYSA-N 5-(1,3-dioxo-2-benzofuran-5-carbonyl)-2-benzofuran-1,3-dione Chemical compound C1=C2C(=O)OC(=O)C2=CC(C(C=2C=C3C(=O)OC(=O)C3=CC=2)=O)=C1 VQVIHDPBMFABCQ-UHFFFAOYSA-N 0.000 description 1
- HHFPIFZYUXLOQA-UHFFFAOYSA-N C(C1C(CC(CC1C)N)C)C1C(CC(CC1C)N)C Chemical compound C(C1C(CC(CC1C)N)C)C1C(CC(CC1C)N)C HHFPIFZYUXLOQA-UHFFFAOYSA-N 0.000 description 1
- JNWPTDYJLGBDSO-UHFFFAOYSA-N C(C1C(CC(CC1CC)N)CC)C1C(CC(CC1CC)N)CC Chemical compound C(C1C(CC(CC1CC)N)CC)C1C(CC(CC1CC)N)CC JNWPTDYJLGBDSO-UHFFFAOYSA-N 0.000 description 1
- ZPAKUZKMGJJMAA-UHFFFAOYSA-N Cyclohexane-1,2,4,5-tetracarboxylic acid Chemical compound OC(=O)C1CC(C(O)=O)C(C(O)=O)CC1C(O)=O ZPAKUZKMGJJMAA-UHFFFAOYSA-N 0.000 description 1
- MQJKPEGWNLWLTK-UHFFFAOYSA-N Dapsone Chemical compound C1=CC(N)=CC=C1S(=O)(=O)C1=CC=C(N)C=C1 MQJKPEGWNLWLTK-UHFFFAOYSA-N 0.000 description 1
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 1
- 229910021578 Iron(III) chloride Inorganic materials 0.000 description 1
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 description 1
- 235000002597 Solanum melongena Nutrition 0.000 description 1
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical class [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 1
- 229920001646 UPILEX Polymers 0.000 description 1
- 239000012963 UV stabilizer Substances 0.000 description 1
- KEUCYUPOICDBOG-UHFFFAOYSA-N [2-(aminomethyl)-5-bicyclo[2.2.1]heptanyl]methanamine Chemical compound C1C2C(CN)CC1C(CN)C2 KEUCYUPOICDBOG-UHFFFAOYSA-N 0.000 description 1
- OTKFKCIRTBTDKK-UHFFFAOYSA-N [3-(aminomethyl)-5-bicyclo[2.2.1]heptanyl]methanamine Chemical compound C1C(CN)C2C(CN)CC1C2 OTKFKCIRTBTDKK-UHFFFAOYSA-N 0.000 description 1
- DVZXBSMBMDKMPP-UHFFFAOYSA-N [4-(4-carbonochloridoylphenyl)phenyl] acetate Chemical compound C1=CC(OC(=O)C)=CC=C1C1=CC=C(C(Cl)=O)C=C1 DVZXBSMBMDKMPP-UHFFFAOYSA-N 0.000 description 1
- OXIKYYJDTWKERT-UHFFFAOYSA-N [4-(aminomethyl)cyclohexyl]methanamine Chemical compound NCC1CCC(CN)CC1 OXIKYYJDTWKERT-UHFFFAOYSA-N 0.000 description 1
- AMNPXXIGUOKIPP-UHFFFAOYSA-N [4-(carbamothioylamino)phenyl]thiourea Chemical compound NC(=S)NC1=CC=C(NC(N)=S)C=C1 AMNPXXIGUOKIPP-UHFFFAOYSA-N 0.000 description 1
- 230000021736 acetylation Effects 0.000 description 1
- 238000006640 acetylation reaction Methods 0.000 description 1
- 125000004018 acid anhydride group Chemical group 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 239000003377 acid catalyst Substances 0.000 description 1
- 229920000800 acrylic rubber Polymers 0.000 description 1
- FOLJMFFBEKONJP-UHFFFAOYSA-N adamantane-1,3-diamine Chemical compound C1C(C2)CC3CC1(N)CC2(N)C3 FOLJMFFBEKONJP-UHFFFAOYSA-N 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000005456 alcohol based solvent Substances 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 239000002518 antifoaming agent Substances 0.000 description 1
- 239000000010 aprotic solvent Substances 0.000 description 1
- 238000010533 azeotropic distillation Methods 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- HFACYLZERDEVSX-UHFFFAOYSA-N benzidine Chemical compound C1=CC(N)=CC=C1C1=CC=C(N)C=C1 HFACYLZERDEVSX-UHFFFAOYSA-N 0.000 description 1
- XQBSPQLKNWMPMG-UHFFFAOYSA-N bicyclo[2.2.2]octane-2,3,5,6-tetracarboxylic acid Chemical compound C1CC2C(C(O)=O)C(C(=O)O)C1C(C(O)=O)C2C(O)=O XQBSPQLKNWMPMG-UHFFFAOYSA-N 0.000 description 1
- VCCBEIPGXKNHFW-UHFFFAOYSA-N biphenyl-4,4'-diol Chemical compound C1=CC(O)=CC=C1C1=CC=C(O)C=C1 VCCBEIPGXKNHFW-UHFFFAOYSA-N 0.000 description 1
- TUQQUUXMCKXGDI-UHFFFAOYSA-N bis(3-aminophenyl)methanone Chemical compound NC1=CC=CC(C(=O)C=2C=C(N)C=CC=2)=C1 TUQQUUXMCKXGDI-UHFFFAOYSA-N 0.000 description 1
- XSQRYCPTYSGRJK-UHFFFAOYSA-N bis(4-amino-2-methylphenyl) benzene-1,4-dicarboxylate Chemical compound NC1=CC(=C(C=C1)OC(C1=CC=C(C(=O)OC2=C(C=C(C=C2)N)C)C=C1)=O)C XSQRYCPTYSGRJK-UHFFFAOYSA-N 0.000 description 1
- CFTXGNJIXHFHTH-UHFFFAOYSA-N bis(4-aminophenyl) benzene-1,4-dicarboxylate Chemical compound C1=CC(N)=CC=C1OC(=O)C1=CC=C(C(=O)OC=2C=CC(N)=CC=2)C=C1 CFTXGNJIXHFHTH-UHFFFAOYSA-N 0.000 description 1
- ZLSMCQSGRWNEGX-UHFFFAOYSA-N bis(4-aminophenyl)methanone Chemical compound C1=CC(N)=CC=C1C(=O)C1=CC=C(N)C=C1 ZLSMCQSGRWNEGX-UHFFFAOYSA-N 0.000 description 1
- 238000005282 brightening Methods 0.000 description 1
- YHASWHZGWUONAO-UHFFFAOYSA-N butanoyl butanoate Chemical compound CCCC(=O)OC(=O)CCC YHASWHZGWUONAO-UHFFFAOYSA-N 0.000 description 1
- VHRGRCVQAFMJIZ-UHFFFAOYSA-N cadaverine Chemical compound NCCCCCN VHRGRCVQAFMJIZ-UHFFFAOYSA-N 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 239000007810 chemical reaction solvent Substances 0.000 description 1
- QQVDYSUDFZZPSU-UHFFFAOYSA-M chloromethylidene(dimethyl)azanium;chloride Chemical compound [Cl-].C[N+](C)=CCl QQVDYSUDFZZPSU-UHFFFAOYSA-M 0.000 description 1
- 229920000891 common polymer Polymers 0.000 description 1
- CURBACXRQKTCKZ-UHFFFAOYSA-N cyclobutane-1,2,3,4-tetracarboxylic acid Chemical compound OC(=O)C1C(C(O)=O)C(C(O)=O)C1C(O)=O CURBACXRQKTCKZ-UHFFFAOYSA-N 0.000 description 1
- WOSVXXBNNCUXMT-UHFFFAOYSA-N cyclopentane-1,2,3,4-tetracarboxylic acid Chemical compound OC(=O)C1CC(C(O)=O)C(C(O)=O)C1C(O)=O WOSVXXBNNCUXMT-UHFFFAOYSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000000113 differential scanning calorimetry Methods 0.000 description 1
- HBGGXOJOCNVPFY-UHFFFAOYSA-N diisononyl phthalate Chemical group CC(C)CCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCC(C)C HBGGXOJOCNVPFY-UHFFFAOYSA-N 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical group C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- BXKDSDJJOVIHMX-UHFFFAOYSA-N edrophonium chloride Chemical compound [Cl-].CC[N+](C)(C)C1=CC=CC(O)=C1 BXKDSDJJOVIHMX-UHFFFAOYSA-N 0.000 description 1
- 238000010292 electrical insulation Methods 0.000 description 1
- 239000003822 epoxy resin Substances 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- PWSKHLMYTZNYKO-UHFFFAOYSA-N heptane-1,7-diamine Chemical compound NCCCCCCCN PWSKHLMYTZNYKO-UHFFFAOYSA-N 0.000 description 1
- 239000012456 homogeneous solution Substances 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 239000011810 insulating material Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- RBTARNINKXHZNM-UHFFFAOYSA-K iron trichloride Chemical compound Cl[Fe](Cl)Cl RBTARNINKXHZNM-UHFFFAOYSA-K 0.000 description 1
- LSACYLWPPQLVSM-UHFFFAOYSA-N isobutyric acid anhydride Chemical compound CC(C)C(=O)OC(=O)C(C)C LSACYLWPPQLVSM-UHFFFAOYSA-N 0.000 description 1
- 125000000654 isopropylidene group Chemical group C(C)(C)=* 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 229940018564 m-phenylenediamine Drugs 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000002808 molecular sieve Substances 0.000 description 1
- DOBFTMLCEYUAQC-UHFFFAOYSA-N naphthalene-2,3,6,7-tetracarboxylic acid Chemical compound OC(=O)C1=C(C(O)=O)C=C2C=C(C(O)=O)C(C(=O)O)=CC2=C1 DOBFTMLCEYUAQC-UHFFFAOYSA-N 0.000 description 1
- YTVNOVQHSGMMOV-UHFFFAOYSA-N naphthalenetetracarboxylic dianhydride Chemical compound C1=CC(C(=O)OC2=O)=C3C2=CC=C2C(=O)OC(=O)C1=C32 YTVNOVQHSGMMOV-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- SXJVFQLYZSNZBT-UHFFFAOYSA-N nonane-1,9-diamine Chemical compound NCCCCCCCCCN SXJVFQLYZSNZBT-UHFFFAOYSA-N 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- XPMMKCKFOUDICN-UHFFFAOYSA-N oxolane-2,4-dicarboxylic acid Chemical compound OC(=O)C1COC(C(O)=O)C1 XPMMKCKFOUDICN-UHFFFAOYSA-N 0.000 description 1
- 125000005740 oxycarbonyl group Chemical group [*:1]OC([*:2])=O 0.000 description 1
- YNWDKZIIWCEDEE-UHFFFAOYSA-N pantoprazole sodium Chemical compound [Na+].COC1=CC=NC(CS(=O)C=2[N-]C3=CC=C(OC(F)F)C=C3N=2)=C1OC YNWDKZIIWCEDEE-UHFFFAOYSA-N 0.000 description 1
- UHZYTMXLRWXGPK-UHFFFAOYSA-N phosphorus pentachloride Chemical compound ClP(Cl)(Cl)(Cl)Cl UHZYTMXLRWXGPK-UHFFFAOYSA-N 0.000 description 1
- FAIAAWCVCHQXDN-UHFFFAOYSA-N phosphorus trichloride Chemical compound ClP(Cl)Cl FAIAAWCVCHQXDN-UHFFFAOYSA-N 0.000 description 1
- 238000000206 photolithography Methods 0.000 description 1
- LGRFSURHDFAFJT-UHFFFAOYSA-N phthalic anhydride Chemical group C1=CC=C2C(=O)OC(=O)C2=C1 LGRFSURHDFAFJT-UHFFFAOYSA-N 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 239000009719 polyimide resin Substances 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 239000002861 polymer material Substances 0.000 description 1
- 230000000379 polymerizing effect Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- WYVAMUWZEOHJOQ-UHFFFAOYSA-N propionic anhydride Chemical compound CCC(=O)OC(=O)CC WYVAMUWZEOHJOQ-UHFFFAOYSA-N 0.000 description 1
- KIDHWZJUCRJVML-UHFFFAOYSA-N putrescine Chemical compound NCCCCN KIDHWZJUCRJVML-UHFFFAOYSA-N 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- 238000007614 solvation Methods 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical compound ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 1
- 229950009390 symclosene Drugs 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- OAXARSVKYJPDPA-UHFFFAOYSA-N tert-butyl 4-prop-2-ynylpiperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC#C)CC1 OAXARSVKYJPDPA-UHFFFAOYSA-N 0.000 description 1
- 238000001757 thermogravimetry curve Methods 0.000 description 1
- ZCPSWAFANXCCOT-UHFFFAOYSA-N trichloromethanesulfonyl chloride Chemical compound ClC(Cl)(Cl)S(Cl)(=O)=O ZCPSWAFANXCCOT-UHFFFAOYSA-N 0.000 description 1
- 239000000326 ultraviolet stabilizing agent Substances 0.000 description 1
Landscapes
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
Abstract
【課題】低吸水率かつ低誘電正接であるポリエステルイミドの製造に使用できるテトラカルボン酸二無水物を提供すること。【解決手段】下記一般式(1):TIFF2024082217000030.tif27161で表され、前記一般式(1)中、Ar1が、2,6-ナフタレン構造を含む、テトラカルボン酸二無水物。【選択図】なしThe present invention provides a tetracarboxylic dianhydride that can be used to produce polyesterimide having low water absorption and low dielectric tangent. The tetracarboxylic dianhydride is represented by the following general formula (1): TIFF2024082217000030.tif27161, in which Ar1 in the general formula (1) contains a 2,6-naphthalene structure. [Selected Figure] None
Description
本発明の実施形態は、テトラカルボン酸二無水物、ポリエステルイミド、ポリエステル
イミドフィルム、高速通信用フレキシブルプリント配線基板、および耐熱絶縁基板に関す
る。
TECHNICAL FIELD The present invention relates to a tetracarboxylic dianhydride, a polyesterimide, a polyesterimide film, a flexible printed wiring board for high-speed communication, and a heat-resistant insulating substrate.
軽量で繰り返しの曲げおよび展開や複雑な形状に折り曲げて実装可能な電子回路基板、
並びに、フレキシブルプリント配線基板(FPC)は、近年、パーソナルコンピューター
、携帯電話、デジタルカメラ、プリンター、ハードディスク、医療用機器、自動車電装部
品等で広く用いられている。
Lightweight electronic circuit boards that can be repeatedly bent and unfolded, and can be folded into complex shapes for implementation;
In addition, flexible printed circuit boards (FPCs) have recently come to be widely used in personal computers, mobile phones, digital cameras, printers, hard disks, medical equipment, automotive electrical components, and the like.
FPCは、通常、ハンダ耐熱性を有するポリイミドからなる電気絶縁フィルム(ベース
フィルム材)上に銅回路が形成されたものである。FPCは、例えば、回路とポリイミド
フィルムとの強固な密着力を確保するため、エポキシ樹脂/アクリルゴム系等の強力な接
着剤を用いてポリイミドフィルムと銅箔を貼り合わせ、銅張積層板を作製しておき、これ
をフォトリソグラフィーとFeCl3水溶液により銅箔をエッチング処理(サブトラクテ
ィブ法)することにより製造される。
FPCs are usually made by forming a copper circuit on an electrical insulating film (base film material) made of polyimide having solder heat resistance. For example, in order to ensure strong adhesion between the circuit and the polyimide film, the polyimide film and copper foil are bonded together using a strong adhesive such as an epoxy resin/acrylic rubber system to prepare a copper-clad laminate, and then the copper foil is etched (subtractive method) using photolithography and an FeCl3 aqueous solution to produce the FPC.
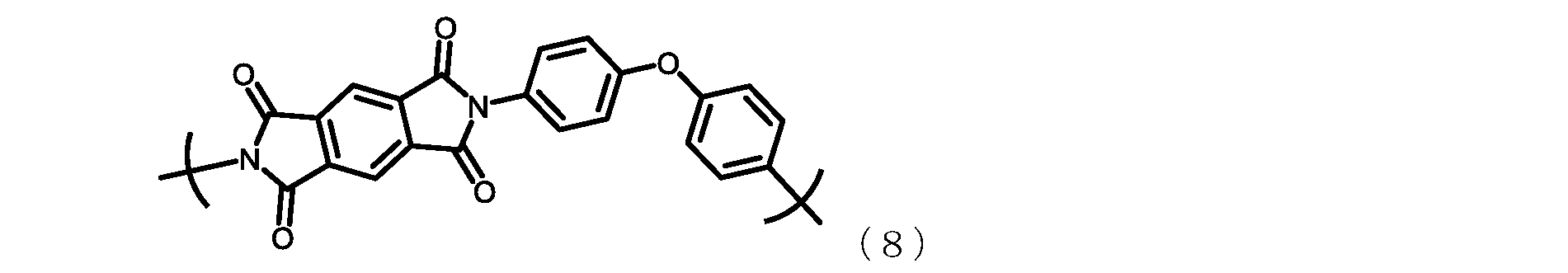
FPCのベースフィルム材として現在最も需要の多いポリイミドフィルムは、テトラカ
ルボン酸二無水物成分としてピロメリット酸二無水物(PMDA)とジアミン成分として
4,4’-オキシジアニリン(4,4’-ODA)から得られる下記式(8):
スフィルム材に求められる基本的特性、即ち、短期耐熱性(ガラス転移温度:Tg)、電
気絶縁信頼性、膜純度、機械的特性、耐薬品性、銅箔密着性および難燃性を全て満足して
いる。
The polyimide film, which is currently in the highest demand as a base film material for FPCs, is obtained from pyromellitic dianhydride (PMDA) as a tetracarboxylic dianhydride component and 4,4'-oxydianiline (4,4'-ODA) as a diamine component, represented by the following formula (8):
近年、FPCの高精細化に伴い回路の位置ずれ許容制限が厳しくなり、デバイス製造時
の熱サイクルに対するベースフィルム材の寸法安定性(XY方向の熱寸法安定性)が重視
されている。熱寸法安定性を確保するためには、ベースフィルム材のTgがハンダリフロ
ー温度(260℃)よりもずっと高いことに加えて、Tg以下のガラス領域でXY方向の
線熱膨張係数(CTE)が十分に低いことが望まれる。
In recent years, as FPCs become more highly precise, the tolerance for misalignment of circuits has become stricter, and emphasis has been placed on the dimensional stability of the base film material (thermal dimensional stability in the XY directions) against the thermal cycle during device manufacturing. In order to ensure thermal dimensional stability, it is desirable that the Tg of the base film material is much higher than the solder reflow temperature (260°C), and that the coefficient of linear thermal expansion (CTE) in the XY directions is sufficiently low in the glass region below Tg .
殆どの一般的な高分子フィルムは、耐熱性が不十分で、Tgがハンダリフロー温度に比
べてずっと低いのに加え、回路材である銅箔のCTE(17~18ppm/K)よりもず
っと高いCTE(50~100ppm/K)を示すため、熱寸法安定性も低い。一方、K
apton(R)Hフィルムは一般的な高分子フィルムよりは低いCTEを有しているが
、銅箔のCTEに比べると依然として高い値であり、熱寸法安定性の点では改善の余地が
ある。
Most common polymer films have insufficient heat resistance, and their Tg is much lower than the solder reflow temperature. In addition, their CTE (50-100 ppm/K) is much higher than the CTE (17-18 ppm/K) of the copper foil used as the circuit material, resulting in poor thermal dimensional stability.
Although the apton® H film has a lower CTE than general polymer films, it is still higher than the CTE of copper foil, and there is room for improvement in terms of thermal dimensional stability.
熱寸法安定性を改良したポリイミドフィルムも上市されている。例えば、銅箔に近いC
TEを示すKapton(R)ENや、3,3’、4,4’-ビフェニルテトラカルボン
酸二無水物(s-BPDA)とp-フェニレンジアミン(p-PDA)より得られ、銅箔
より低いCTEを示す、下記式(9):
る。
Polyimide films with improved thermal dimensional stability are also available on the market.
and Kapton® EN, which is made from 3,3′,4,4′-biphenyltetracarboxylic dianhydride (s-BPDA) and p-phenylenediamine (p-PDA) and has a lower CTE than copper foil, represented by the following formula (9):
また最近、スマートフォン等の移動体通信機器の高速、大容量、および低遅延通信を可
能にする新通信規格:5Gへの移行に伴い、移動体通信機器のアンテナ部とメイン基板を
接続するFPC部品では、従来よりも高い動作周波数(≧3.6GHz)における電気絶
縁基板由来の誘電損失を大幅に低減することが喫緊の課題となっている。
Furthermore, with the recent shift to 5G, a new communications standard that enables high-speed, large-capacity, and low-latency communications for mobile communications devices such as smartphones, it has become an urgent task to significantly reduce the dielectric loss originating from electrically insulating substrates at higher operating frequencies (≧3.6 GHz) than conventional ones for FPC components that connect the antenna unit and main circuit board of mobile communications devices.
FPCの絶縁層で生ずる誘電損失を抑制するために、ベースフィルム材であるポリイミ
ドフィルム自身の誘電正接(tan δ)を低く抑えることが有効である。しかしながら
、現行のポリイミドフィルムでは、マイクロ波域での誘電正接を劇的に低減することは原
理的に困難であるという問題があった。例えば、PMDAと4,4’-ODAより実験室
的に作製されたポリイミドフィルムは、高い誘電正接(10GHzで0.0140)を示
すことが報告されている(例えば、非特許文献1を参照。)。これはポリイミドの分子構
造中に高含有率で存在する分極したイミド基(O=C-N-C=O)によるものであると
考えられる。したがって、ベースフィルム材としてイミド基を多く含むポリイミドフィル
ムを選択する限り、低誘電正接化は困難であり、上記低いCTEを示すポリイミドフィル
ムも同様な理由からも高速通信FPC用途には好適ではない。
In order to suppress the dielectric loss occurring in the insulating layer of the FPC, it is effective to keep the dielectric loss tangent (tan δ) of the polyimide film itself, which is the base film material, low. However, with the current polyimide film, there is a problem that it is difficult in principle to dramatically reduce the dielectric loss tangent in the microwave range. For example, it has been reported that a polyimide film produced in a laboratory from PMDA and 4,4'-ODA exhibits a high dielectric loss tangent (0.0140 at 10 GHz) (see, for example, Non-Patent Document 1). This is thought to be due to the polarized imide group (O=C-N-C=O) that exists at a high content in the molecular structure of the polyimide. Therefore, as long as a polyimide film containing a large amount of imide groups is selected as the base film material, it is difficult to reduce the dielectric loss tangent, and for the same reason, the polyimide film showing the above-mentioned low CTE is not suitable for high-speed communication FPC applications.
しかしながら、イミド基は双極子-双極子相互作用に基づく強い分子間力の起源であり
、ポリイミドの耐熱性(極めて高いTg)を支える不可欠な基であるため、イミド基を安
易に排除するとポリイミドの最大の特徴である優れた物理的耐熱性(短期耐熱性)が大き
く損なわれる恐れがある。
However, since the imide group is the source of strong intermolecular forces based on dipole-dipole interactions and is an essential group supporting the heat resistance (extremely high T g ) of polyimides, there is a risk that the excellent physical heat resistance (short-term heat resistance), which is the greatest feature of polyimides, will be significantly impaired if the imide group is simply eliminated.
また従来のポリイミドフィルムでは、吸水率が高いことも重大な問題になることがある
。これは、上記誘電正接増大の要因と同様に、ポリイミド構造中に高い含有率で含まれる
分極したイミド基の存在によるものであると考えられる。吸水率が大きいと、吸湿により
許容を上回るフィルムの寸法変化が生じる恐れがある。また水の誘電損失は非常に大きい
ため、フィルムに吸着または吸収された水によって、ポリイミドフィルムの誘電正接増大
に拍車がかかることになる。
In addition, high water absorption can be a serious problem in conventional polyimide films. This is believed to be due to the presence of polarized imide groups contained in a high content in the polyimide structure, as is the cause of the increase in the dielectric tangent mentioned above. If the water absorption is high, there is a risk that the film will undergo dimensional changes that exceed the allowable range due to moisture absorption. In addition, the dielectric loss of water is very large, so that water adsorbed or absorbed into the film will accelerate the increase in the dielectric tangent of the polyimide film.
上記のように、従来のポリイミドフィルムに元来備わっている優れた特性を維持しなが
ら、高い熱寸法安定性(低CTE)、低吸水率、および低誘電正接をより高いレベルで実
現することは、FPCのベースフィルム材としてポリイミド樹脂を選択する限り原理的に
困難である。そこで、ポリイミドの代わりに変性ポリイミド、具体的にはポリエステルイ
ミドを用いることで、上記の問題を解決可能とする方法が提案されている(例えば、非特
許文献2を参照。)。ポリエステルイミドは、ポリマー骨格にエステル基(エステル結合
)とイミド基(イミド結合)とを有するポリマーである。
As described above, it is theoretically difficult to achieve high thermal dimensional stability (low CTE), low water absorption, and low dielectric tangent at a higher level while maintaining the excellent properties inherent to conventional polyimide films, as long as polyimide resin is selected as the base film material for FPCs. Therefore, a method has been proposed that uses modified polyimide, specifically polyesterimide, instead of polyimide to solve the above problem (see, for example, Non-Patent Document 2). Polyesterimide is a polymer having an ester group (ester bond) and an imide group (imide bond) in the polymer skeleton.
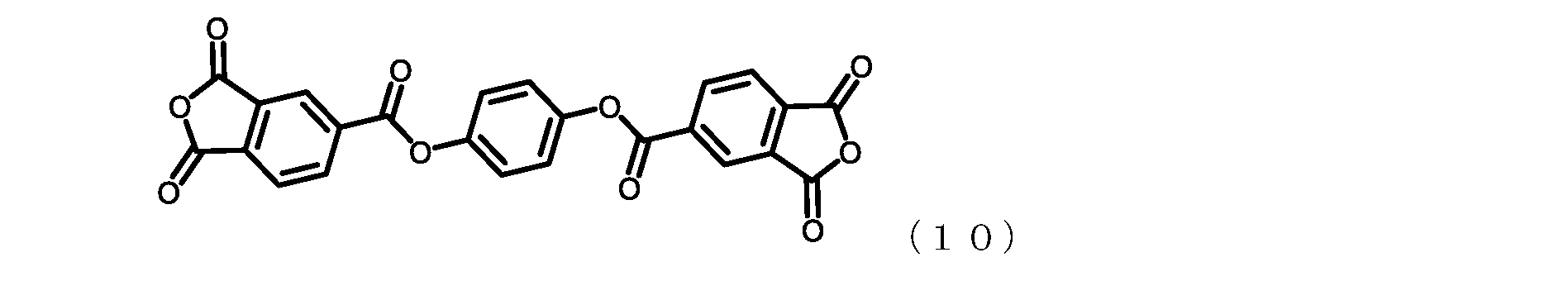
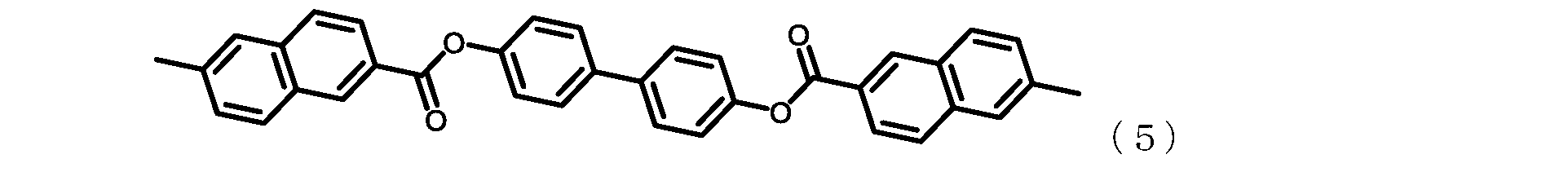
この技術によれば、エステル基を介して芳香環をパラまたはそれに類する結合位置で連
結したモノマー、例えば下記式(10):
汎用ジアミン(例えばp-PDA)を組み合わせることで、低熱膨張性を確保しながら、
従来のテトラカルボン酸二無水物(PMDA、s-BPDA等)を用いた場合に比べて吸
水率の低い耐熱性フィルムが得られる。
According to this technique, a monomer having an aromatic ring linked at a para or similar bonding position via an ester group, such as a monomer represented by the following formula (10):
A heat-resistant film having a lower water absorption rate can be obtained as compared to the case where a conventional tetracarboxylic dianhydride (PMDA, s-BPDA, etc.) is used.
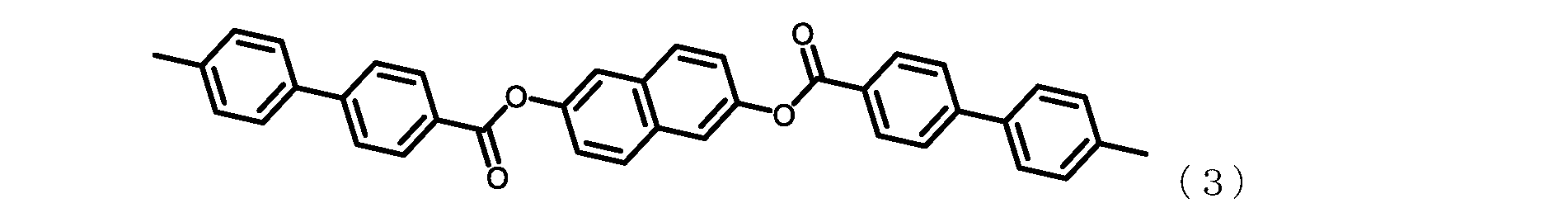
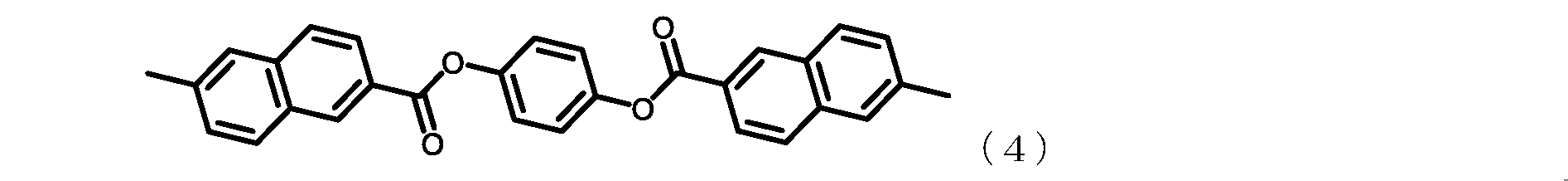
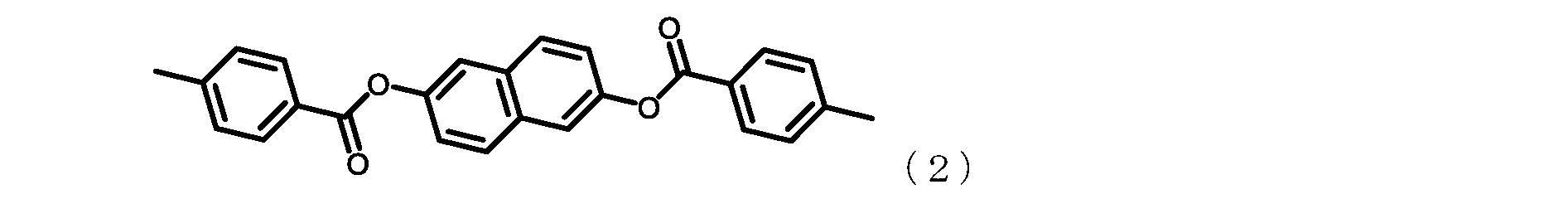
また、優れた物理的耐熱性(高Tg)および優れた熱寸法安定性(低CTE)を維持し
ながら更に吸水率を低減するには、エステル連結基を介してTA-HQよりも更に分子の
長手方向に芳香環を増環および延長した、下記式(11)~(13)で表されるテトラカ
ルボン酸二無水物を用いることが有効である。
例えば、芳香環を6環まで増環した上記式(13)で表されるテトラカルボン酸二無水
物を用い、これと適切な比率で剛直構造のジアミン(p-PDA)および屈曲構造のジア
ミン(4,4’-ODA)を併用(共重合)することで、沈殿析出やゲル化することなく
均一で粘稠なポリエステルイミドの前駆体ワニスが得られる。これを基板上に塗布し乾燥
させた後、高温で加熱して脱水閉環反応(熱イミド化)することで、極めて高いTg、超
低CTE、低い吸水率、十分な可撓性、および10GHzで非常に低い誘電正接を有する
ポリエステルイミドフィルムを得ることができる。
For example, by using a tetracarboxylic dianhydride represented by the above formula (13) in which the aromatic rings have been increased to six rings, and by co-polymerizing this with a diamine having a rigid structure (p-PDA) and a diamine having a bent structure (4,4'-ODA) in an appropriate ratio, a uniform and viscous precursor varnish of polyesterimide can be obtained without precipitation or gelation. This is applied to a substrate, dried, and then heated at a high temperature to cause a dehydration ring-closing reaction (thermal imidization), thereby obtaining a polyesterimide film having an extremely high Tg , an ultralow CTE, a low water absorption rate, sufficient flexibility, and an extremely low dielectric tangent at 10 GHz.
テトラカルボン酸二無水物構造を分子の長手方向への増環および延長することで得られ
た効果(吸水率と誘電正接が共に徐々に低下)は、ポリエステルイミド構造中、モル分極
の大きなイミド基の含有率が相対的に減少したことに起因していると考えられる。そのた
め、上記式(13)で表されるテトラカルボン酸二無水物に留まらず、更に増環および延
長したテトラカルボン酸二無水物を用いれば、吸水率と誘電正接を更に低減可能である。
しかしながら、更なる増環策は、ポリイミド前駆体の溶媒への溶解性(本明細書において
溶媒への溶解性を「溶媒溶解性」という場合がある。)を支配するポリイミド前駆体構造
中のカルボキシ基の含有率の低下をもたらす。これによりポリイミド前駆体の重合の際、
生成したポリイミド前駆体の溶媒和が不十分となって沈殿析出やゲル化が起こり、次の製
膜工程が実施困難になる恐れがある。
The effect obtained by increasing the number of rings and extending the tetracarboxylic dianhydride structure in the longitudinal direction of the molecule (both the water absorption coefficient and the dielectric loss tangent are gradually decreased) is considered to be due to the relative decrease in the content of imide groups, which have large molar polarization, in the polyesterimide structure. Therefore, by using not only the tetracarboxylic dianhydride represented by the above formula (13) but also a tetracarboxylic dianhydride that has been further increased in number and extended, the water absorption coefficient and the dielectric loss tangent can be further reduced.
However, further ring-increasing measures result in a decrease in the content of carboxy groups in the polyimide precursor structure, which governs the solubility of the polyimide precursor in a solvent (solubility in a solvent may be referred to as "solvent solubility" in this specification). This results in a decrease in the content of carboxy groups in the polyimide precursor structure, which governs the solubility of the polyimide precursor in a solvent (solubility in a solvent may be referred to as "solvent solubility"
If the solvation of the resulting polyimide precursor becomes insufficient, precipitation or gelation may occur, which may make it difficult to carry out the subsequent film formation step.
テトラカルボン酸二無水物の更なる増環策はまた、以下に示す、より顕在化した障害に
より実施困難になるという問題があった。
例えば、上記式(13)で表されるテトラカルボン酸二無水物は、一般的には下記反応
式(14)に従い、酸受容剤の存在下、非プロトン性溶媒中、室温以下でトリメリット酸
無水物クロリド(反応式(14)中、(a)、トリメリット酸(TMAC))とあらかじ
め合成しておいた分子の長手方向に増環および延長したビスフェノール(反応式(14)
中、(b))を反応させて得られる。
For example, the tetracarboxylic dianhydride represented by the above formula (13) is generally reacted with trimellitic anhydride chloride ((a), trimellitic acid (TMAC) in reaction formula (14)) at room temperature or lower in an aprotic solvent in the presence of an acid acceptor according to the following reaction formula (14), to form a bisphenol (reaction formula (14):
In the above, (b)) can be reacted to obtain the above-mentioned compound.
その際、上記ビスフェノール(b)は、ポリエステルイミドフィルムの低熱膨張性発現
を意図して、剛直で直線状の構造に設定されているため、溶媒溶解性があまり高くない。
予想されるように、ビスフェノール(b)を更に増環および延長すると、得られるビスフ
ェノールはもはや溶媒溶解性を失い、これをあらかじめ合成すること自体困難になるとい
う、更なる増環策を阻む大きな障害があった。
In this case, the bisphenol (b) is designed to have a rigid and linear structure in order to impart low thermal expansion to the polyesterimide film, and therefore does not have very high solubility in solvents.
As expected, when the bisphenol (b) is further ring-multiplied and extended, the resulting bisphenol no longer has solubility in a solvent, and it is difficult to synthesize the bisphenol in advance. This is a major obstacle that prevents further ring-multiplication.
本発明の課題は、低吸水率かつ低誘電正接であるポリエステルイミドの製造に使用でき
るテトラカルボン酸二無水物を提供することである。本発明の他の課題は、低吸水率かつ
低誘電正接であるポリエステルイミドを提供することである。本発明の更に他の課題は、
信頼性に優れ、誘電損失が低減された高速通信用フレキシブルプリント配線基板および耐
熱絶縁基板を提供することである。
An object of the present invention is to provide a tetracarboxylic dianhydride that can be used for producing a polyesterimide having low water absorption and low dielectric tangent. Another object of the present invention is to provide a polyesterimide having low water absorption and low dielectric tangent. Still another object of the present invention is to provide
The present invention provides a flexible printed wiring board and a heat-resistant insulating board for high-speed communication, which are highly reliable and have reduced dielectric loss.
本発明者らによる前述の知見および考察に基づき、本発明者らは更なる鋭意検討を重ね
た結果、分子の長手方向に芳香環を増環および延長する際に、2位および6位に結合位置
を持つナフタレン構造(2,6-ナフタレン構造)を導入することで、ビスフェノール構
造の剛直性および直線性を維持したまま、十分な溶媒溶解性を確保することができるよう
になり、これを用いて従来にない大きく増環された対称性エステル基含有テトラカルボン
酸二無水物を簡便で効率的な方法で合成できることを見出した。さらに、これを用いて特
性上、極めて有益な高速通信FPC用絶縁材料に適したポリエステルイミドフィルムが得
られることを見出し、本発明を完成するに至った。本明細書において、ポリエステルイミ
ドは、ポリマー骨格にエステル基(エステル結合)とイミド基(イミド結合)とを有する
ポリマーである。
Based on the above findings and considerations, the present inventors have further intensively studied and found that, when the aromatic rings are multiplied and extended in the longitudinal direction of the molecule, a naphthalene structure having bonding positions at the 2- and 6-positions (2,6-naphthalene structure) can be introduced to ensure sufficient solvent solubility while maintaining the rigidity and linearity of the bisphenol structure, and that this structure can be used to synthesize a symmetric ester group-containing tetracarboxylic acid dianhydride with a large number of rings that has not been seen before in a simple and efficient manner. Furthermore, the present inventors have found that this structure can be used to obtain a polyesterimide film that is suitable as an insulating material for high-speed communication FPCs, which is extremely useful in terms of its characteristics, and have completed the present invention. In this specification, polyesterimide is a polymer having an ester group (ester bond) and an imide group (imide bond) in the polymer skeleton.
本発明は以下に示す実施形態を含む。本発明は以下の実施形態に限定されない。
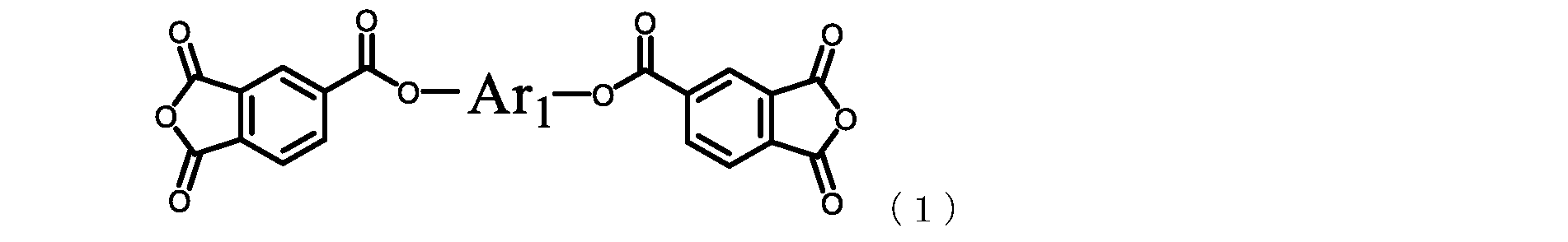
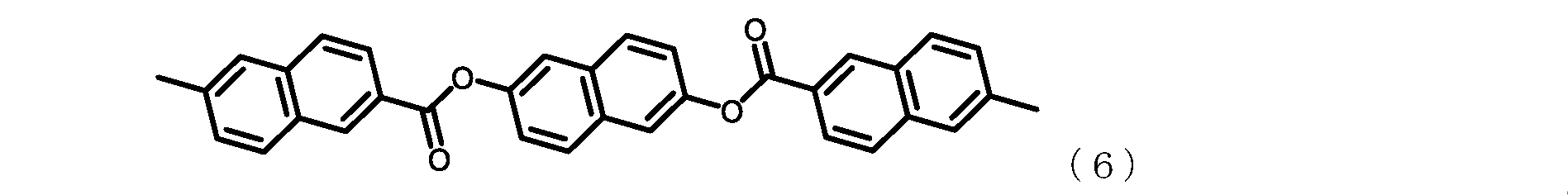
[1] 下記一般式(1):
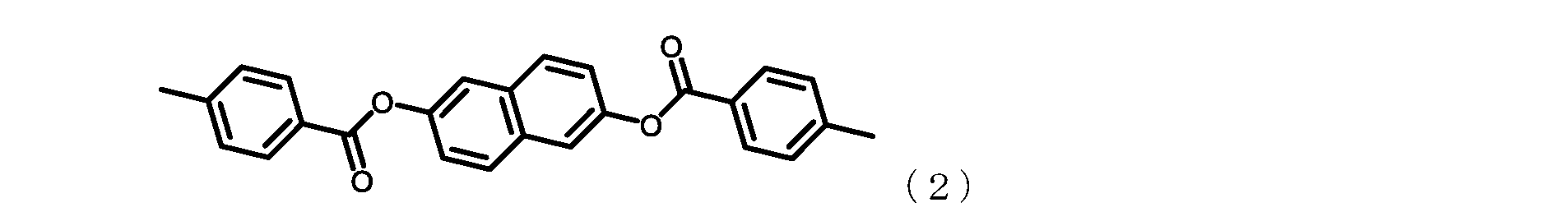
前記一般式(1)中、Ar1が、下記式(2)~(6):
テトラカルボン酸二無水物。
[2] 下記一般式(7):
前記一般式(7)中、Ar1は前記式(2)~(6)のいずれかで表され、Ar2は2
価の芳香族基、2価の脂肪族基、または芳香族基と脂肪族基の少なくとも一方を含む2価
の基である、
ポリエステルイミド。
[3] 上記[2]に記載のポリエステルイミドを含む、フィルム(本明細書において、
「ポリエステルイミドフィルム」という場合がある。)。
[4] 熱機械分析によって測定された100~200℃の間の平均線熱膨張係数が、3
0ppm/K以下である、上記[3]に記載のフィルム。
[5] 動的粘弾性分析により測定されたガラス転移温度が、300℃以上であるかまた
は検出されない、上記[3]に記載のフィルム。
[6] 吸水率が、0.5%以下である、上記[3]に記載のフィルム。
[7] 動作周波数10GHzにおける誘電正接が、0.003以下である、上記[3]に記載のフィルム。
[8] 上記[3]~[7]のいずれか1項に記載のフィルムを含む、高速通信用フレキ
シブルプリント配線基板。
[9] 上記[3]~[7]のいずれか1項に記載のフィルムを含む、耐熱絶縁基板。
The present invention includes the following embodiments, but is not limited to the following embodiments.
[1] The following general formula (1):
In the general formula (1), Ar 1 is represented by the following formulas (2) to (6):
Tetracarboxylic dianhydride.
[2] The following general formula (7):
In the general formula (7), Ar 1 is represented by any one of the formulas (2) to (6), and Ar 2 is
a divalent aromatic group, a divalent aliphatic group, or a divalent group containing at least one of an aromatic group and an aliphatic group,
Polyesterimide.
[3] A film comprising the polyesterimide according to [2] above (in the present specification,
It is sometimes called "polyesterimide film."
[4] The average linear thermal expansion coefficient between 100 and 200 ° C. measured by thermomechanical analysis is 3
The film according to the above [3], wherein the film has a viscosity of 0 ppm/K or less.
[5] The film according to the above [3], which has a glass transition temperature of 300° C. or higher or not detectable as measured by dynamic viscoelastic analysis.
[6] The film according to the above [3], having a water absorption rate of 0.5% or less.
[7] The film according to the above [3], having a dielectric loss tangent of 0.003 or less at an operating frequency of 10 GHz.
[8] A flexible printed circuit board for high-speed communication, comprising the film according to any one of [3] to [7] above.
[9] A heat-resistant insulating substrate comprising the film according to any one of the above [3] to [7].
本発明の実施形態によれば、低吸水率かつ低誘電正接であるポリエステルイミドの製造
に使用できるテトラカルボン酸二無水物を提供することができる。本発明の他の実施形態
によれば、低吸水率かつ低誘電正接であるポリエステルイミドを提供することができる。
本発明の更に他の実施形態によれば、信頼性に優れ、誘電損失が低減された高速通信用フ
レキシブルプリント配線基板および耐熱絶縁基板を提供することができる。
According to an embodiment of the present invention, a tetracarboxylic dianhydride that can be used for producing a polyesterimide having low water absorption and low dielectric loss tangent can be provided. According to another embodiment of the present invention, a polyesterimide having low water absorption and low dielectric loss tangent can be provided.
According to still another embodiment of the present invention, it is possible to provide a flexible printed wiring board and a heat-resistant insulating substrate for high-speed communication, which are highly reliable and have reduced dielectric loss.
本明細書中に段階的に記載されている数値範囲において、ある数値範囲で記載された上
限値又は下限値は、別の数値範囲の上限値又は下限値に置き換えてもよい。また、本明細
書中に記載されている数値範囲の上限値又は下限値は、実施例に示されている値に置き換
えてもよい。本明細書中に段階的に記載されている上限の数値と下限の数値とから、それ
ぞれある数値を選択し、段階的な数値範囲としてもよい。また、本明細書中に記載されて
いる上限の数値と下限の数値は、実施例に示されている値に置き換えてもよい。
本明細書において、各成分には、該当する物質が複数種含まれていてもよい。組成物中
に各成分に該当する物質が複数種存在する場合、各成分の含有率又は含有量は、特に断ら
ない限り、組成物中に存在する当該複数種の物質の合計の含有率又は含有量を意味する。
本明細書において「工程」の語には、他の工程から独立した工程に加え、他の工程と明
確に区別できない工程であってもその工程の初期の作用が達成されれば、当該工程も含ま
れる。
本明細書において「膜」には、連続する膜と不連続な膜とが含まれる。「膜」の厚さは
、均一であっても不均一であってもよい。「膜」の面方向の外縁及び厚さ方向の外縁は、
それぞれ、明確である場合と不明確である場合があり得る。「層」についても同様である。
In the numerical ranges described in stages in this specification, the upper limit or lower limit described in a certain numerical range may be replaced with the upper limit or lower limit of another numerical range. In addition, the upper limit or lower limit of the numerical range described in this specification may be replaced with a value shown in an example. A certain numerical value may be selected from the upper limit numerical value and the lower limit numerical value described in stages in this specification to form a stepped numerical range. In addition, the upper limit numerical value and the lower limit numerical value described in this specification may be replaced with a value shown in an example.
In the present specification, each component may contain multiple types of the corresponding substance. When multiple types of substances corresponding to each component are present in the composition, the content or amount of each component means the total content or amount of the multiple substances present in the composition, unless otherwise specified.
In this specification, the term "process" includes not only a process that is independent of other processes, but also a process that cannot be clearly distinguished from other processes, as long as the initial effect of the process is achieved.
In this specification, the term "film" includes a continuous film and a discontinuous film. The thickness of the "film" may be uniform or non-uniform. The outer edge in the plane direction and the outer edge in the thickness direction of the "film" are
Each of these can be either clear or unclear. The same goes for "layers."
本発明の実施形態は、一連のエステル連結基を介して分子の長手方向に増環および延長
した新規なテトラカルボン酸二無水物およびこれらを用いて得られたポリエステルイミド
フィルムを提供するものである。まず、新規なテトラカルボン酸二無水物とその製造方法
について以下に説明する。ただし、新規なテトラカルボン酸二無水物の製造方法は以下に
限定されない。
The present invention provides a novel tetracarboxylic dianhydride having a ring length increased and extended in the longitudinal direction of the molecule through a series of ester linking groups, and a polyesterimide film obtained by using the same. First, the novel tetracarboxylic dianhydride and a method for producing the same are described below. However, the method for producing the novel tetracarboxylic dianhydride is not limited to the following.
<テトラカルボン酸二無水物およびその製造方法>
本発明の一実施形態であるテトラカルボン酸二無水物は、上記一般式(1)で表される
。一般式(1)中、Ar1は、上記式(2)~(6)のいずれかである。
<Tetracarboxylic acid dianhydride and its production method>
The tetracarboxylic dianhydride according to one embodiment of the present invention is represented by the above general formula (1). In the general formula (1), Ar 1 is any one of the above formulas (2) to (6).
一般式(1)で表されるテトラカルボン酸二無水物は、2,6-ナフタレン構造を含む
従来にない大きく増環された対称性エステル基含有テトラカルボン酸二無水物であり、剛
直性および直線性を維持しつつ溶媒への十分な溶媒溶解性を有する。
The tetracarboxylic acid dianhydride represented by the general formula (1) is a symmetric ester group-containing tetracarboxylic acid dianhydride having an unprecedented large ring extension containing a 2,6-naphthalene structure, and has sufficient solubility in a solvent while maintaining rigidity and linearity.
Ar1は、式(3)~(6)のいずれかであってよく、式(4)~(6)のいずれかであることが好ましく、式(4)又は(6)であることがより好ましく、式(6)であることが更に好ましい。 Ar 1 may be any one of formulas (3) to (6), preferably any one of formulas (4) to (6), more preferably formula (4) or (6), and even more preferably formula (6).
以下に一般式(1)で表されるテトラカルボン酸二無水物の製造方法について説明する
が、これに限定されるものではない。以下の製造方法では、分子の長手方向に増環および
延長する際に2,6-ナフタレン構造を導入することで、溶媒への十分な溶媒溶解性を確
保できるため、一般式(1)で表されるテトラカルボン酸二無水物を簡便かつ効率的に合
成することが可能である。
A method for producing the tetracarboxylic dianhydride represented by the general formula (1) will be described below, but the method is not limited thereto. In the following production method, sufficient solubility in a solvent can be ensured by introducing a 2,6-naphthalene structure during ring growth and elongation in the longitudinal direction of the molecule, so that the tetracarboxylic dianhydride represented by the general formula (1) can be synthesized simply and efficiently.
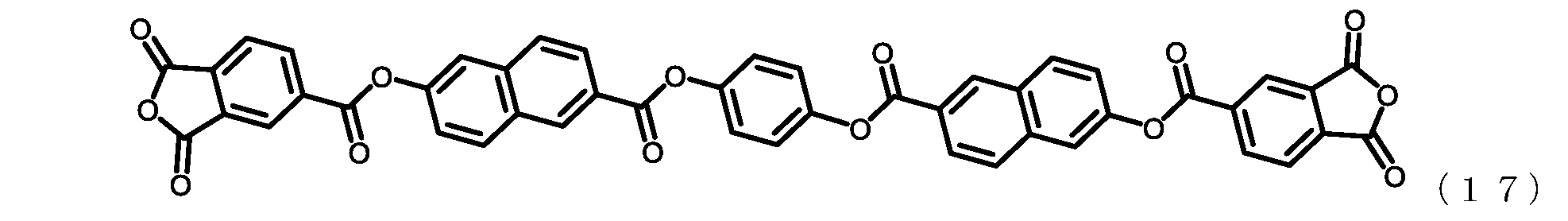
一般式(1)で表されるテトラカルボン酸二無水物のうち、一例として下記式(15)
で表されるテトラカルボン酸二無水物の製造方法を以下に説明する。
A method for producing the tetracarboxylic dianhydride represented by the formula (I) is described below.
上記式(15)で表されるテトラカルボン酸二無水物は下記反応式(16)で表される
経路で合成される。
まず、触媒として強酸の存在下、無水酢酸(Ac2O)で出発原料である6-ヒドロキ
シ-2-ナフタレンカルボン酸(上記反応式(16)中、(d))のヒドロキシ基を、ア
セチル化して保護し、6-アセトキシ-2-ナフタレンカルボン酸(反応式(16)中、
(e))を得る。
具体的には、反応容器に出発原料(d)、過剰量の無水酢酸および触媒量の酸(例えば
濃硫酸)を入れ、窒素雰囲気中、80~140℃で1~5時間還流して均一溶液を得る。
これを室温まで冷却して生成物を析出させる。析出物を濾過により回収し、洗浄し、50
~150℃で1~24時間にわたり真空乾燥するとアセチル化物(e)が得られる。
First, in the presence of a strong acid catalyst, the hydroxy group of the starting material, 6-hydroxy-2-naphthalenecarboxylic acid ((d) in the above reaction formula (16)) is acetylated and protected with acetic anhydride (Ac 2 O) to give 6-acetoxy-2-naphthalenecarboxylic acid ((c) in the above reaction formula (16)).
(e)) is obtained.
Specifically, the starting material (d), an excess amount of acetic anhydride, and a catalytic amount of acid (eg, concentrated sulfuric acid) are placed in a reaction vessel, and refluxed in a nitrogen atmosphere at 80 to 140° C. for 1 to 5 hours to obtain a homogeneous solution.
This is cooled to room temperature to precipitate the product. The precipitate is collected by filtration, washed, and
Drying in vacuum at .about.150.degree. C. for 1-24 hours gives the acetylated product (e).
次にアセチル化物(e)と2,6-ジヒドロキシナフタレン(g)をエステル化反応さ
せて、エステル基含有ジアセトキシ体(h)を得る工程について説明する。エステル化反
応の際、アセチル化物(e)のカルボキシ基を変換して酸クロリド(f)を得ておき、こ
れと2,6-ジヒドロキシナフタレン(g)を反応させる方法(酸ハライド法)の他、縮
合剤を用いてエステル化する方法が適用できる。以下に酸ハライド法について説明する。
Next, a process for obtaining an ester group-containing diacetoxy compound (h) by esterification of an acetylated compound (e) with 2,6-dihydroxynaphthalene (g) will be described. In the esterification reaction, the carboxyl group of the acetylated compound (e) is converted to obtain an acid chloride (f), which is then reacted with 2,6-dihydroxynaphthalene (g) (acid halide method), or a method of esterification using a condensing agent can be used. The acid halide method will be described below.
上記アセチル化物(e)を塩素化する反応の際に用いる塩素化剤は特に限定されないが
、例えば塩化チオニル、塩化スルフリル、塩化オキサリル、N-クロロコハク酸イミド、
ホスゲン、メタンスルホニルクロリド、メトキシアセチルクロリド、三塩化リン、五塩化
リン、オキシ塩化リン、N-クロロフタルイミド、トリクロロイソシアヌル酸、トリクロ
ロメタンスルホニルクロリド、1,3-ジクロロ-5,5-ジメチルヒダントイン等が挙
げられる。上記塩素化剤に触媒量のN,N-ジメチルホルムアミド(DMF)やピリジン
を加えて反応系中でビルスマイヤー試薬を発生させることで反応性を高めてもよい。安全
性、経済性、過剰量加えた場合の塩素化剤除去のしやすさおよび副生成物の除去のしやす
さの観点から塩化チオニルが好適に用いられる。
The chlorinating agent used in the chlorination reaction of the acetylated compound (e) is not particularly limited, and examples thereof include thionyl chloride, sulfuryl chloride, oxalyl chloride, N-chlorosuccinimide,
Examples of the chlorinating agent include phosgene, methanesulfonyl chloride, methoxyacetyl chloride, phosphorus trichloride, phosphorus pentachloride, phosphorus oxychloride, N-chlorophthalimide, trichloroisocyanuric acid, trichloromethanesulfonyl chloride, and 1,3-dichloro-5,5-dimethylhydantoin. The reactivity may be increased by adding a catalytic amount of N,N-dimethylformamide (DMF) or pyridine to the chlorinating agent to generate a Vilsmeier reagent in the reaction system. Thionyl chloride is preferably used from the viewpoints of safety, economy, ease of removal of the chlorinating agent when an excessive amount is added, and ease of removal of by-products.
使用する塩素化剤が塩化チオニルのように液体の場合は、溶媒を用いずに、塩素化剤を
塩素化剤兼溶媒として利用できる。液状塩素化剤の留去が容易な場合、塩素化剤は基質に
対して大過剰量となるように添加してもよい。過剰な塩素化剤を留去する際、共沸剤を用
いてもよい。例えば反応終了後、過剰な塩化チオニルを留去する場合は、トルエンまたは
ベンゼンを共沸剤として用いることで留去の効率を高めることもできる。
When the chlorinating agent used is liquid, such as thionyl chloride, it is possible to use the chlorinating agent as both the chlorinating agent and the solvent without using a solvent. When the liquid chlorinating agent is easy to remove by distillation, the chlorinating agent may be added in a large excess amount relative to the substrate. When removing the excess chlorinating agent by distillation, an azeotropic agent may be used. For example, when removing the excess thionyl chloride after the reaction is completed, the efficiency of the removal by distillation can be improved by using toluene or benzene as an azeotropic agent.
また上記塩素化の際、必要に応じて溶媒を用いてもよい。使用可能な溶媒は、塩素化剤
と反応せず、アセチル化物(e)を溶解するものであればよく、特に限定されないが、例
えばジクロロメタン、クロロホルム、トルエン、ベンゼン、N,N-ジメチルホルムアミ
ド、テトラヒドロフラン等が挙げられる。これらは脱水処理されていることが望ましい。
これらは2種類以上混合して使用してもよい。溶媒を用いる場合、添加する塩素化剤量は
アセチル化物(e)の1モルに対してモル比が、例えば1.1~10、好ましくは2~5
である。塩素化の際の反応温度は、塩素化剤の沸点や用いた溶媒の沸点にもよるが、例え
ば20~150℃、好ましくは50~100℃である。反応時間は例えば30分~6時間
、好ましくは1~4時間である。
In the above chlorination, a solvent may be used as necessary. The solvent that can be used is not particularly limited as long as it does not react with the chlorinating agent and dissolves the acetylated product (e). Examples of the solvent include dichloromethane, chloroform, toluene, benzene, N,N-dimethylformamide, and tetrahydrofuran. It is preferable that these solvents are dehydrated.
These may be used in combination of two or more kinds. When a solvent is used, the amount of the chlorinating agent added is, for example, 1.1 to 10, preferably 2 to 5, per mole of the acetylated compound (e).
The reaction temperature during chlorination varies depending on the boiling point of the chlorinating agent and the boiling point of the solvent used, but is, for example, 20 to 150° C., preferably 50 to 100° C. The reaction time is, for example, 30 minutes to 6 hours, preferably 1 to 4 hours.
塩素化反応終了後、過剰な塩素化剤や溶媒および副生成物を除去することで、目的とす
る酸クロリド(f)がほぼ定量的に得られる。例えば、DMFを触媒として塩化チオニル
で塩素化する場合は、副生成物は気体(二酸化硫黄)であるため、反応終了後、反応溶液
にベンゼンまたはトルエンを加えて過剰な液体を共沸留去するだけで、高純度の酸クロリ
ド(f)を得ることができるが、適当な溶媒から再結晶を行って酸クロリド(f)を精製
してもよい。その際、使用可能な溶媒は、酸クロリド(f)と反応せず且つ再結晶操作が
行えればよく、特に限定されない。例えば、n-ヘキサン、シクロヘキサン、ベンゼン、
トルエン等の無極性炭化水素系溶媒、酢酸メチル、酢酸エチル、酢酸プロピル、γ-ブチ
ロラクトン等のエステル系溶媒、アセトン、メチルエチルケトン、ジエチルケトン、シク
ロペンタノン、シクロヘキサノン等のケトン系溶媒、テトラヒドロフラン、1,4-ジオ
キサン、ジエチルエーテル等のエーテル系溶媒、N,N-ジメチルホルムアミド、N,N
-ジメチルアセトアミド、N-メチルピロリドン、1,3-ジメチル-2-イミダゾリジ
ノン等のアミド溶媒、ジメチルスルホキシド、スルホラン等のスルホン系溶媒などが挙げ
られる。これらを2種類以上混合して用いてもよい。これらの溶媒は十分に脱水処理され
ていることが望ましい。溶媒中の含水量および再結晶効率の観点から、シクロヘキサン、
ベンゼン、トルエン等の炭化水素系溶媒が好適に用いられる。
After the chlorination reaction is completed, the excess chlorinating agent, solvent, and by-products are removed to obtain the target acid chloride (f) almost quantitatively. For example, when chlorination is performed with thionyl chloride using DMF as a catalyst, the by-product is a gas (sulfur dioxide), so that after the reaction is completed, high-purity acid chloride (f) can be obtained simply by adding benzene or toluene to the reaction solution and azeotropically removing the excess liquid. However, the acid chloride (f) may be purified by recrystallization from a suitable solvent. In this case, the solvent that can be used is not particularly limited as long as it does not react with the acid chloride (f) and allows the recrystallization operation to be performed. For example, n-hexane, cyclohexane, benzene,
non-polar hydrocarbon solvents such as toluene; ester solvents such as methyl acetate, ethyl acetate, propyl acetate, and γ-butyrolactone; ketone solvents such as acetone, methyl ethyl ketone, diethyl ketone, cyclopentanone, and cyclohexanone; ether solvents such as tetrahydrofuran, 1,4-dioxane, and diethyl ether; N,N-dimethylformamide, N,N
Examples of suitable solvents include amide solvents such as N-dimethylacetamide, N-methylpyrrolidone, and 1,3-dimethyl-2-imidazolidinone, and sulfone solvents such as dimethylsulfoxide and sulfolane. Two or more of these may be mixed and used. It is preferable that these solvents are sufficiently dehydrated. From the viewpoint of the water content in the solvent and the recrystallization efficiency, cyclohexane,
Hydrocarbon solvents such as benzene and toluene are preferably used.
酸クロリド(f)と2,6-ジヒドロキシナフタレン(g)の反応では、よく乾燥した
反応容器中、所定量の2,6-ジヒドロキシナフタレン(g)および酸受容剤を脱水処理
済みの溶媒に溶かし、セプタムキャップで密封してA液とする。次に所定量の酸クロリド
(f)を脱水処理済みの溶媒に溶かし、セプタムキャップで密封してB液とする。B液を
所定の温度に設定して撹拌しながら、B液にA液をシリンジにて徐々に加える。その際、
A液添加後の全溶質濃度は例えば5~50質量%、好ましくは7~30質量%である。反
応は例えば-20~70℃、好ましくは0~50℃で、例えば1~72時間、好ましくは
2~48時間行う。
In the reaction of acid chloride (f) with 2,6-dihydroxynaphthalene (g), a predetermined amount of 2,6-dihydroxynaphthalene (g) and an acid acceptor are dissolved in a dehydrated solvent in a well-dried reaction vessel, and the vessel is sealed with a septum cap to obtain liquid A. Next, a predetermined amount of acid chloride (f) is dissolved in a dehydrated solvent, and the vessel is sealed with a septum cap to obtain liquid B. Liquid B is set to a predetermined temperature and stirred, while liquid A is gradually added to liquid B with a syringe. During this process,
The total solute concentration after addition of Solution A is, for example, 5 to 50% by mass, preferably 7 to 30% by mass. The reaction is carried out, for example, at −20 to 70° C., preferably 0 to 50° C., for example, for 1 to 72 hours, preferably 2 to 48 hours.
上記反応に用いるA液とB液の溶媒は同一なものを用いても異なっていてもよい。使用
可能な溶媒は、添加した酸クロリド(f)、2,6-ジヒドロキシナフタレン(g)およ
び酸受容剤と反応せず、これらをよく溶解するものであればよく、特に限定されない。例
えば、酢酸メチル、酢酸エチル、酢酸プロピル、γ-ブチロラクトン(GBL)等のエス
テル系溶媒、N,N-ジメチルホルムアミド、N,N-ジメチルアセトアミド、N-メチ
ルピロリドン、1,3-ジメチル-2-イミダゾリジノン等のアミド溶媒、ジメチルスル
ホキシド、スルホラン等のスルホン系溶媒、テトラヒドロフラン、1,4-ジオキサン等
のエーテル系溶媒、アセトン、メチルエチルケトン、ジエチルケトン、シクロペンタノン
、シクロヘキサノン等のケトン系溶媒等が挙げられる。これらを2種類以上混合して用い
てもよい。これらの溶媒は十分に脱水処理されていることが望ましい。溶解力の観点から
GBLが好適に用いられる。
The solvents of the A solution and the B solution used in the above reaction may be the same or different. The solvent that can be used is not particularly limited as long as it does not react with the added acid chloride (f), 2,6-dihydroxynaphthalene (g) and acid acceptor and dissolves them well. For example, ester solvents such as methyl acetate, ethyl acetate, propyl acetate, and γ-butyrolactone (GBL) and the like, amide solvents such as N,N-dimethylformamide, N,N-dimethylacetamide, N-methylpyrrolidone, and 1,3-dimethyl-2-imidazolidinone, sulfone solvents such as dimethylsulfoxide and sulfolane, ether solvents such as tetrahydrofuran and 1,4-dioxane, and ketone solvents such as acetone, methyl ethyl ketone, diethyl ketone, cyclopentanone, and cyclohexanone, and the like can be mentioned. Two or more of these may be mixed and used. It is preferable that these solvents are sufficiently dehydrated. GBL is preferably used from the viewpoint of dissolving power.
上記エステル化反応の際、目的外のモノエステル体の生成を避けるため、酸クロリド(
f)の使用量はジオールに対して当量(2倍モル量)よりもやや過剰に設定することが望
ましく、ジオールを1モルとすると、モル比は例えば2.01~5であり、好ましくは2
.05~3である。経済性および分離効率の点からは、酸クロリド(f)を過剰に用いる
ことなく、モル比5以下であることが好ましい。
In the above esterification reaction, in order to avoid the production of undesired monoesters,
The amount of f) used is preferably set to be slightly more than the equivalent amount (2 times the molar amount) of the diol. When the diol is taken as 1 mole, the molar ratio is, for example, 2.01 to 5, preferably 2.01 to 5.
From the standpoint of economy and separation efficiency, it is preferable that the acid chloride (f) is not used in excess, and that the molar ratio is 5 or less.
上記エステル化反応の際、添加される酸受容剤として有機3級アミンが使用可能であり
、特に限定されないが、例えば、ピリジン、ピコリン、キノリン、N,N-ジメチルアニ
リン、N,N-ジエチルアニリン、トリエチルアミン、トリプロピルアミン、トリブチル
アミン等が用いられる。毒性、経済性、過剰分に加えられた酸受容剤や副生成物である塩
酸塩の分離のしやすさの観点からピリジンが好適に使用される。また、酸受容剤の添加量
は発生する理論塩化水素量(モル)に対して例えば1~10倍モル量、好ましくは2~5
倍モル量である。
In the above esterification reaction, an organic tertiary amine can be used as an acid acceptor to be added, and although there is no particular limitation, examples that can be used include pyridine, picoline, quinoline, N,N-dimethylaniline, N,N-diethylaniline, triethylamine, tripropylamine, and tributylamine. Pyridine is preferably used from the viewpoints of toxicity, economy, and ease of separation of the acid acceptor added in excess and the by-product hydrochloride. The amount of the acid acceptor to be added is, for example, 1 to 10 times the molar amount, preferably 2 to 5 times the theoretical amount (mol) of hydrogen chloride to be generated.
It is double the molar amount.
エステル化反応後、析出した沈殿物をまずトルエン等の無極性溶媒で洗浄して過剰の酸
クロリド(f)を除去し、次いで少量の反応溶媒で洗浄する。更に水で洗浄して副生成物
である塩酸塩を除去するが、1%硝酸銀水溶液を用いて、洗浄液に塩化銀の白色沈殿の生
成の観察されなくなるまで、繰り返し水で洗浄する。
After the esterification reaction, the precipitate is first washed with a non-polar solvent such as toluene to remove excess acid chloride (f), then washed with a small amount of the reaction solvent, and then washed with water to remove the by-product hydrochloride, and is repeatedly washed with water using a 1% aqueous silver nitrate solution until no white precipitate of silver chloride is observed in the wash.
エステル化反応は、上記の酸ハライド法の他、脱水縮合剤を用いる方法も適用できる。
使用可能な縮合剤は特に限定されないが、例えば、ジシクロヘキシルカルボジイミド(D
CC)、ジイソプロピルカルボジイミド(DIC)、1-エチル-3-(3-ジメチルア
ミノプロピル)カルボジイミド(EDC)等のカルボジイミド系縮合剤が挙げられる。こ
れらと4-ジメチルアミノピリジンや1-ヒドロキシベンゾトリアゾール等とを添加して
併用してもよい。カルボジイミド系縮合剤以外にもN,N’-カルボニルジイミダゾール
等のイミダゾール系縮合剤、4-(4,6-ジメトキシ-1,3,5-トリアジン-2-
イル)-4-メチルモルホリニウムクロリドn水和物等のトリアジン系縮合剤も使用可能
である。反応効率、経済性、副生成物の除去のしやすさの観点から、縮合剤として1-エ
チル-3-(3-ジメチルアミノプロピル)カルボジイミドやN,N’-ジイソプロピル
カルボジイミド等が好適に用いられる。
The esterification reaction can be carried out by the acid halide method described above, or by a method using a dehydration condensation agent.
Usable condensation agents are not particularly limited, but examples thereof include dicyclohexylcarbodiimide (D
Examples of the carbodiimide-based condensing agent include carbodiimide-based condensing agents such as diisopropylcarbodiimide (DIC) and 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide (EDC). These may be used in combination with 4-dimethylaminopyridine or 1-hydroxybenzotriazole. In addition to the carbodiimide-based condensing agents, imidazole-based condensing agents such as N,N'-carbonyldiimidazole, 4-(4,6-dimethoxy-1,3,5-triazine-2-
In terms of reaction efficiency, economic efficiency, and ease of removing by-products, 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide, N,N'-diisopropylcarbodiimide, and the like are preferably used as the condensation agent.
次に、上記のようにして得られたエステル基含有ジアセトキシ体(h)の末端アセトキ
シ基をアルカリで加水分解して脱保護することで、エステル基含有ビスフェノール(i)
が得られる。上記反応は、具体的には以下のようにして行う。エステル基含有ジアセトキ
シ体(h)を溶媒に溶かし、これに塩基を加え、例えば0~50℃で5分~3時間撹拌し
て末端のアセトキシ基の加水分解を完結する。反応の完結は薄層クロマトグラフィー(T
LC)で追跡することができる。その後、酸を加えて中和することでビスフェノール(i
)を析出させ、濾過、洗浄、および真空乾燥により、ほぼ定量的にビスフェノール(i)
が得られる。
Next, the terminal acetoxy group of the ester group-containing diacetoxy compound (h) obtained as described above is hydrolyzed with an alkali to deprotect the compound, thereby obtaining an ester group-containing bisphenol (i).
The above reaction is specifically carried out as follows: The ester group-containing diacetoxy compound (h) is dissolved in a solvent, a base is added thereto, and the mixture is stirred, for example, at 0 to 50° C. for 5 minutes to 3 hours to complete the hydrolysis of the terminal acetoxy group. The completion of the reaction is confirmed by thin layer chromatography (T
The reaction can then be monitored by LC. After that, the reaction is neutralized by adding acid to obtain bisphenol (i
) was precipitated, filtered, washed, and vacuum dried to obtain bisphenol (i) in an almost quantitative yield.
is obtained.
上記加水分解の際、溶媒にジアセトキシ体(h)溶解しておいて、これにアルカリ水溶
液を添加してもよい。その際に使用可能な溶媒は、塩基に対して安定で、アルカリ水溶液
とよく混和し、ジアセトキシ体(h)を溶解するものであればよく、特に限定されないが
、例えば、N,N-ジメチルホルムアミド、N,N-ジメチルアセトアミド、N-メチル
-2-ピロリドン等のアミド系溶媒、ジメチルスルホオキシド、スルホラン等のスルホン
系溶媒、γ-ブチロラクトン等の環状エステル系溶媒、テトラヒドロフラン、1,4-ジ
オキサン等のエーテル系溶媒、メタノール、エタノール等のアルコール系溶媒、エチレン
グリコール等のグリコール系溶媒等が挙げられる。これらを2種類以上混合して使用して
もよい。
During the hydrolysis, the diacetoxy body (h) may be dissolved in a solvent, and an aqueous alkali solution may be added to the solution. The solvent that can be used in this case is not particularly limited as long as it is stable to bases, is miscible with an aqueous alkali solution, and dissolves the diacetoxy body (h). Examples of the solvent include amide solvents such as N,N-dimethylformamide, N,N-dimethylacetamide, and N-methyl-2-pyrrolidone, sulfone solvents such as dimethylsulfoxide and sulfolane, cyclic ester solvents such as γ-butyrolactone, ether solvents such as tetrahydrofuran and 1,4-dioxane, alcohol solvents such as methanol and ethanol, and glycol solvents such as ethylene glycol. Two or more of these may be mixed and used.
加水分解の際、加水分解により生成するビスフェノール(i)の末端ヒドロキシル基の
酸化を抑制するために、硫酸水素ナトリウムを添加してもよい。この際硫酸水素ナトリウ
ムの添加量は特に制限はないが、例えば全容質量に対して0.1~1質量%程度である。
During the hydrolysis, sodium hydrogen sulfate may be added to suppress oxidation of the terminal hydroxyl groups of bisphenol (i) produced by the hydrolysis. The amount of sodium hydrogen sulfate added is not particularly limited, but is, for example, about 0.1 to 1% by mass based on the total volume.
加水分解反応の際、塩基として、濃アンモニア水(28質量%)が好適に用いられるが
、水酸化ナトリウムおよび水酸化カリウム等無機強塩基の希薄溶液も使用可能である。無
機強塩基水溶液の濃度は特に制限はなく、例えば0.1~2Nである。加水分解反応は例
えば-20~50℃、好ましくは0~30℃で、例えば5分~12時間、好ましくは10
分~4時間撹拌して行う。塩基として無機強塩基を用いる場合、水溶液の濃度や反応温度
が高すぎたり、反応時間が長すぎたりしないように調節することで、エジアセトキシ体(
h)の末端アセトキシ基だけでなく、エステル基まで加水分解されること防止できる。
In the hydrolysis reaction, concentrated aqueous ammonia (28% by mass) is preferably used as the base, but dilute solutions of strong inorganic bases such as sodium hydroxide and potassium hydroxide can also be used. The concentration of the aqueous solution of strong inorganic base is not particularly limited, and is, for example, 0.1 to 2N. The hydrolysis reaction is carried out, for example, at -20 to 50°C, preferably 0 to 30°C, for example, for 5 minutes to 12 hours, preferably 10 minutes to 20 minutes.
When using a strong inorganic base as the base, it is possible to obtain the ethoxylated form (
Not only the terminal acetoxy group of h) but also the ester group can be prevented from being hydrolyzed.
加水分解反応後の中和反応で用いる酸は特に制限されず、塩酸等の無機酸水溶液や酢酸
等の有機酸が使用可能である。用いる酸の濃度は特に制限はなく、例えば0.1~2Nで
ある。加水分解後、ビスフェノール(i)を析出させるため、反応溶液が弱酸性になるよ
うに酸を添加するが、溶液のpHは特に制限はなく、例えばpH2~5、好ましくはpH
3~4に調節する。
The acid used in the neutralization reaction after the hydrolysis reaction is not particularly limited, and an aqueous solution of an inorganic acid such as hydrochloric acid or an organic acid such as acetic acid can be used. The concentration of the acid used is not particularly limited, and is, for example, 0.1 to 2N. After the hydrolysis, in order to precipitate bisphenol (i), an acid is added so that the reaction solution becomes weakly acidic. The pH of the solution is not particularly limited, and is, for example, pH 2 to 5, preferably pH 5.
Adjust to 3-4.
上記のようにして得られたビスフェノール(i)を用いて一般式(1)で表されるテト
ラカルボン酸二無水物を得るエステル化工程について以下に説明する。この反応にはトリ
メリット酸無水物クロリド(TMAC)を用いる酸ハライド法の他、トリメリット酸無水
物(TMA)のカルボキシ基とビスフェノール(i)のヒドロキシ基を、縮合剤を用いて
直接エステル化する方法が適用可能である。TMACが安価に入手可能であることから、
経済性、反応効率の観点から酸ハライド法が好適に用いられる。以下に酸ハライド法につ
いて説明する。
The esterification step for obtaining the tetracarboxylic dianhydride represented by the general formula (1) using the bisphenol (i) obtained as described above will be described below. In addition to the acid halide method using trimellitic anhydride chloride (TMAC), a method of directly esterifying the carboxy group of trimellitic anhydride (TMA) and the hydroxy group of bisphenol (i) using a condensing agent can be applied to this reaction. Since TMAC is available at low cost,
From the viewpoints of economy and reaction efficiency, the acid halide method is preferably used, and will be described below.
よく乾燥した反応容器中、所定量のビスフェノール(i)および酸受容剤を脱水処理済
みの溶媒に溶かし、セプタムキャップで密封してA液とする。次に所定量のTMACを脱
水処理済みの溶媒に溶かし、セプタムキャップで密封してB液とする。B液を所定の温度
に設定して撹拌しながら、B液にA液をシリンジにて徐々に加える。その際、A液添加後
の全溶質濃度は例えば5~50質量%、好ましくは7~30質量%である。反応は例えば
-20~70℃、好ましくは0~50℃で、例えば1~72時間、好ましくは2~48時
間行う。反応終了後、析出物を濾過、洗浄、および乾燥することで、目的とするテトラカ
ルボン酸二無水物(j)が得られる。
In a well-dried reaction vessel, a predetermined amount of bisphenol (i) and an acid acceptor are dissolved in a dehydrated solvent, and the vessel is sealed with a septum cap to obtain liquid A. Next, a predetermined amount of TMAC is dissolved in a dehydrated solvent, and the vessel is sealed with a septum cap to obtain liquid B. Liquid B is set to a predetermined temperature and stirred, while liquid A is gradually added to liquid B with a syringe. At that time, the total solute concentration after the addition of liquid A is, for example, 5 to 50 mass%, preferably 7 to 30 mass%. The reaction is carried out, for example, at -20 to 70°C, preferably 0 to 50°C, for example, for 1 to 72 hours, preferably 2 to 48 hours. After the reaction is completed, the precipitate is filtered, washed, and dried to obtain the desired tetracarboxylic dianhydride (j).
上記反応に用いるA液とB液の溶媒は同一なものを用いても異なっていてもよい。使用
可能な溶媒は、添加したTMAC、ビスフェノール(i)および酸受容剤と反応せず、こ
れらをよく溶解するものであればよく、特に限定されないが、例えば、N,N-ジメチル
ホルムアミド、N,N-ジメチルアセトアミド(DMAc)、N-メチルピロリドン(N
MP)、1,3-ジメチル-2-イミダゾリジノン等のアミド溶媒、ジメチルスルホキシ
ド、スルホラン等のスルホン系溶媒、酢酸メチル、酢酸エチル、酢酸プロピル、γ-ブチ
ロラクトン(GBL)等のエステル系溶媒、テトラヒドロフラン、1,4-ジオキサン等
のエーテル系溶媒、アセトン、メチルエチルケトン、ジエチルケトン、シクロペンタノン
、シクロヘキサノン等のケトン系溶媒等が挙げられる。これらを2種類以上混合して用い
てもよい。これらの溶媒は十分に脱水処理されていることが望ましい。溶解力、経済性、
安全性、処理のしやすさの観点からNMPやGBLが好適に用いられる。
The solvents for the A and B solutions used in the above reaction may be the same or different. The solvents that can be used are not particularly limited as long as they do not react with the added TMAC, bisphenol (i) and acid acceptor and dissolve them well. Examples of suitable solvents include N,N-dimethylformamide, N,N-dimethylacetamide (DMAc), N-methylpyrrolidone (N
Examples of suitable solvents include amide solvents such as dimethylsulfoxide and sulfolane, ester solvents such as methyl acetate, ethyl acetate, propyl acetate and γ-butyrolactone (GBL), ether solvents such as tetrahydrofuran and 1,4-dioxane, and ketone solvents such as acetone, methyl ethyl ketone, diethyl ketone, cyclopentanone and cyclohexanone. Two or more of these may be mixed and used. It is preferable that these solvents are sufficiently dehydrated. Solubility, economy,
From the viewpoints of safety and ease of processing, NMP and GBL are preferably used.
上記エステル化反応の際、目的外のモノエステル体の生成を避けるため、また、TMA
Cが安価に入手でき、除去もしやすいことを考慮して、TMACの使用量はビスフェノー
ル(i)に対して当量(2倍モル量)よりも過剰に設定することが望ましく、ビスフェノ
ール(i)を1モルとすると、モル比は例えば2.05~5であり、好ましくは2.1~
3である。
In the above esterification reaction, in order to avoid the formation of undesired monoesters, and in order to avoid the formation of TMA
Considering that C is inexpensively available and easy to remove, it is desirable to set the amount of TMAC used to be in excess of the equivalent amount (2 times the molar amount) to bisphenol (i). When bisphenol (i) is taken as 1 mole, the molar ratio is, for example, 2.05 to 5, and preferably 2.1 to 1.
The answer is 3.
上記エステル化反応の際、添加される酸受容剤として有機3級アミンが使用可能であり
、特に限定されないが、例えば、ピリジン、ピコリン、キノリン、N,N-ジメチルアニ
リン、N,N-ジエチルアニリン、トリエチルアミン、トリプロピルアミン、トリブチル
アミン等が用いられる。これらはあらかじめ脱水されていることが望ましい。毒性、経済
性、過剰分に加えられた酸受容剤や副生成物である塩酸塩の分離のしやすさの観点からピ
リジンが好適に使用される。また、酸受容剤の添加量は発生する理論塩化水素量(モル)
に対して例えば1~10倍モル量、好ましくは2~5倍モル量である。
In the above esterification reaction, an organic tertiary amine can be used as the acid acceptor to be added, and although there is no particular limitation, examples that can be used include pyridine, picoline, quinoline, N,N-dimethylaniline, N,N-diethylaniline, triethylamine, tripropylamine, and tributylamine. It is preferable that these are dehydrated in advance. From the viewpoints of toxicity, economy, and ease of separation of the excess acid acceptor added and the by-product hydrochloride, pyridine is preferably used. The amount of acid acceptor to be added is determined based on the theoretical amount (mol) of hydrogen chloride to be generated.
The molar amount is, for example, 1 to 10 times, and preferably 2 to 5 times, that of the above.
エステル化反応後、析出した沈殿物をまずトルエン等の無極性溶媒で洗浄して過剰のT
MACを除去し、次いで水で洗浄して副生成物である塩酸塩を除去するが、1%硝酸銀水
溶液を用いて、洗浄液に塩化銀の白色沈殿の生成の観察されなくなるまで、繰り返し水で
洗浄する。水で洗浄した際、末端酸無水物基の一部が加水分解をして開環する。これを例
えば150~250℃、好ましくは170~220℃で、例えば1~24時間、好ましく
は2~12時間真空で乾燥することで、一部の開環物を完全に閉環することができる。
After the esterification reaction, the precipitate was first washed with a non-polar solvent such as toluene to remove excess T.
The MAC is removed, and then the by-product hydrochloride is removed by washing with water, using a 1% aqueous silver nitrate solution and repeatedly washing with water until no white precipitate of silver chloride is observed in the washings. When washing with water, some of the terminal acid anhydride groups are hydrolyzed and ring-opened. This can be dried in a vacuum at, for example, 150 to 250°C, preferably 170 to 220°C, for example, for 1 to 24 hours, preferably 2 to 12 hours, to completely close the ring of some of the ring-opened groups.
上記エステル化反応は、上記の酸ハライド法の他、脱水縮合剤を用いる方法も適用でき
る。使用可能な縮合剤は特に限定されないが、例えば、ジシクロヘキシルカルボジイミド
(DCC)、ジイソプロピルカルボジイミド(DIC)、1-エチル-3-(3-ジメチ
ルアミノプロピル)カルボジイミド(EDC)等のカルボジイミド系縮合剤が挙げられる
。これらと4-ジメチルアミノピリジンや1-ヒドロキシベンゾトリアゾール等とを添加
して併用してもよい。カルボジイミド系縮合剤以外にもN,N’-カルボニルジイミダゾ
ール等のイミダゾール系縮合剤、4-(4,6-ジメトキシ-1,3,5-トリアジン-
2-イル)-4-メチルモルホリニウムクロリドn水和物等のトリアジン系縮合剤も使用
可能である。反応効率、経済性、副生成物の除去のしやすさの観点から、縮合剤として1
-エチル-3-(3-ジメチルアミノプロピル)カルボジイミドやN,N’-ジイソプロ
ピルカルボジイミド等が好適に用いられる。
In addition to the acid halide method, the above esterification reaction can also be carried out using a method using a dehydration condensation agent. The condensation agent that can be used is not particularly limited, and examples thereof include carbodiimide-based condensation agents such as dicyclohexylcarbodiimide (DCC), diisopropylcarbodiimide (DIC), and 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide (EDC). These may be added in combination with 4-dimethylaminopyridine, 1-hydroxybenzotriazole, or the like. In addition to carbodiimide-based condensation agents, imidazole-based condensation agents such as N,N'-carbonyldiimidazole, 4-(4,6-dimethoxy-1,3,5-triazine-
A triazine-based condensing agent such as 1-(2-yl)-4-methylmorpholinium chloride n-hydrate can also be used. From the viewpoints of reaction efficiency, economy, and ease of removing by-products, 1-(2-yl)-4-methylmorpholinium chloride n-hydrate is preferably used as the condensing agent.
N,N'-ethyl-3-(3-dimethylaminopropyl)carbodiimide, N,N'-diisopropylcarbodiimide, and the like are preferably used.
上記のようにして得られたテトラカルボン酸二無水物(j)は十分高純度であり、後述
するポリエステルイミド前駆体の製造方法にそのまま供することができるが、適当な溶媒
から再結晶して更に高純度化することもできる。その際、再結晶溶媒は、テトラカルボン
酸二無水物(j)と反応せず且つ再結晶操作が行えればよく、特に限定されないが、例え
ば、γ-ブチロラクトン(GBL)等の環状エステル系溶媒、N,N-ジメチルホルムア
ミド、N,N-ジメチルアセトアミド、N-メチルピロリドン等のアミド溶媒、ジメチル
スルホキシド等のスルホン系溶媒等が挙げられる。これらを2種類以上混合して用いても
よい。溶媒は十分に脱水処理されていることが望ましい。溶解力、安全性および再結晶効
率の観点から、NMP等のアミド系溶媒やGBLが好適に用いられる。
The tetracarboxylic dianhydride (j) obtained as described above has a sufficiently high purity and can be directly used in the method for producing a polyesterimide precursor described later, but can also be further purified by recrystallization from a suitable solvent. In this case, the recrystallization solvent is not particularly limited as long as it does not react with the tetracarboxylic dianhydride (j) and can perform the recrystallization operation, and examples of the recrystallization solvent include cyclic ester solvents such as γ-butyrolactone (GBL), amide solvents such as N,N-dimethylformamide, N,N-dimethylacetamide, and N-methylpyrrolidone, and sulfone solvents such as dimethylsulfoxide. Two or more of these may be mixed and used. It is preferable that the solvent is sufficiently dehydrated. From the viewpoints of dissolving power, safety, and recrystallization efficiency, amide solvents such as NMP and GBL are preferably used.
<ポリエステルイミド前駆体の製造方法>
一般式(7)で表される構造単位を含むポリエステルイミドは、ポリエステルイミド前
駆体を脱水閉環させることで得られる。ポリエステルイミド前駆体は、2,6-ナフタレ
ン構造が導入された式(2)~(6)のいずれかで表される構造を含むため、沈殿の析出
及びゲル化を回避しながらポリエステルイミド前駆体を作製することが可能である。
<Method of producing polyesterimide precursor>
A polyesterimide containing a structural unit represented by general formula (7) can be obtained by dehydrating and ring-closing a polyesterimide precursor. Since the polyesterimide precursor contains a structure represented by any one of formulas (2) to (6) into which a 2,6-naphthalene structure has been introduced, it is possible to prepare the polyesterimide precursor while avoiding precipitation and gelation.
以下にポリエステルイミド前駆体を製造する方法について説明するが、これに限定され
ず、公知の方法を適用することができる。
まずジアミンを重合溶媒に溶解し、これに一般式(1)で表されるテトラカルボン酸二
無水物の粉末を添加し、密封して例えば0~100℃、好ましくは20~60℃で、例え
ば1~100時間、好ましくは2~72時間撹拌する。
A method for producing a polyesterimide precursor will be described below, but the method is not limited thereto and any known method can be used.
First, a diamine is dissolved in a polymerization solvent, and then a powder of a tetracarboxylic dianhydride represented by the general formula (1) is added thereto. The mixture is sealed and stirred at, for example, 0 to 100° C., preferably 20 to 60° C., for example, for 1 to 100 hours, preferably 2 to 72 hours.
上記の重合反応の際、反応容器に仕込むジアミンとテトラカルボン酸二無水物とのモル
比は、ジアミン1に対して、テトラカルボン酸二無水物0.8~1.1であり、好ましく
は0.9~1.1、更に好ましくは0.95~1.05である。ジアミンとテトラカルボ
ン酸二無水物は実質的に等モルで仕込むと、ポリエステルイミド前駆体の重合度を高める
ことができる。
In the above polymerization reaction, the molar ratio of diamine to tetracarboxylic dianhydride charged in a reaction vessel is 0.8 to 1.1, preferably 0.9 to 1.1, and more preferably 0.95 to 1.05, per 1 part of diamine. When the diamine and tetracarboxylic dianhydride are charged in substantially equimolar amounts, the degree of polymerization of the polyesterimide precursor can be increased.
また、重合開始時の原料モノマー(固形分)濃度は、例えば5~50質量%、好ましく
は10~40質量%である。ポリエステルイミド前駆体の重合度の増加により、重合溶液
の粘度が高くなり効果的な撹拌に支障が生じた場合は、適宜同一の脱水処理済み溶媒で希
釈してもよい。原料モノマーは、一般式(1)で表されるテトラカルボン酸無水物と、ジ
アミンとを少なくとも含む。
The raw material monomer (solid content) concentration at the start of polymerization is, for example, 5 to 50 mass %, preferably 10 to 40 mass %. When the viscosity of the polymerization solution increases due to an increase in the degree of polymerization of the polyesterimide precursor, causing an impediment to effective stirring, the polymerization solution may be appropriately diluted with the same dehydrated solvent. The raw material monomer contains at least a tetracarboxylic acid anhydride represented by the general formula (1) and a diamine.
上記重合反応に用いる溶媒は、原料モノマーと生成するポリエステルイミド前駆体が十
分に溶解し、且つこれらと反応しなければよく、特に限定されない。例えばN,N-ジメ
チルホルムアミド、N,N-ジメチルアセトアミド、N-メチルピロリドン(NMP)、
1,3-ジメチル-2-イミダゾリジノン、ヘキサメチルホスホルトリアミド等のアミド
溶媒、γ-プチロラクトン(GBL)等の環状エステル溶媒、ジメチルスルホキシド、ス
ルホラン等のスルホン系溶媒、シクロペンタノン、シクロへキサノン等ケトン系溶媒、m
-クレゾール、p-クレゾール、3-クロロフェノール、4-クロロフェノール等のフェ
ノール系溶媒等が使用可能である。また、これらを2種類以上混合して用いてもよい。溶
解力、安全性、経済性の観点からNMPが好適に用いられる。
The solvent used in the polymerization reaction is not particularly limited as long as it sufficiently dissolves the raw material monomers and the polyesterimide precursor produced and does not react with them. For example, N,N-dimethylformamide, N,N-dimethylacetamide, N-methylpyrrolidone (NMP),
Amide solvents such as 1,3-dimethyl-2-imidazolidinone and hexamethylphosphortriamide, cyclic ester solvents such as γ-butyrolactone (GBL), sulfone solvents such as dimethylsulfoxide and sulfolane, ketone solvents such as cyclopentanone and cyclohexanone, m
Phenol-based solvents such as 1-cresol, p-cresol, 3-chlorophenol, 4-chlorophenol, etc. can be used. Two or more of these may be mixed and used. NMP is preferably used from the viewpoints of dissolving power, safety, and economy.
上記重合反応の際、重合反応性、反応溶液の均一性およびポリエステルイミドフィルム
の要求特性を損なわない範囲で使用可能な芳香族ジアミンを選択することが望ましい。本
明細書において、芳香族ジアミンは、分子内に、少なくとも芳香族基を含み、芳香族基と
脂肪族基とを含んでもよい。使用可能な芳香族ジアミンとして、特に限定されないが、例
えば、p-フェニレンジアミン、m-フェニレンジアミン、2,4-ジアミノトルエン、
2,5-ジアミノトルエン、2,4-ジアミノキシレン、2,4-ジアミノデュレン、4
,4’-メチレンジアニリン、4,4’-メチレンビス(3-メチルアニリン)、4,4
’-メチレンビス(3-エチルアニリン)、4,4’-メチレンビス(2-メチルアニリ
ン)、4,4’-メチレンビス(2-エチルアニリン)、4,4’-メチレンビス(3,
5-ジメチルアニリン)、4,4’-メチレンビス(3,5-ジエチルアニリン)、4,
4’-メチレンビス(2,6-ジメチルアニリン)、4,4’-メチレンビス(2,6-
ジエチルアニリン)、4,4’-ジアミノジフェニルエーテル、3,4’-ジアミノジフ
ェニルエーテル、3,3’-ジアミノジフェニルエーテル、2,4’-ジアミノジフェニ
ルエーテル、2,2’-ジアミノジフェニルエーテル、4,4’-ジアミノ-2,2’-
ビス(トリフルオロメチル)ジフェニルエーテル、4,4’-ジアミノジフェニルスルホ
ン、3,3’-ジアミノジフェニルスルホン、4,4’-ジアミノベンゾフェノン、3,
3’-ジアミノベンゾフェノン、4,4’-ジアミノベンズアニリド、ベンジジン、3,
3’-ジヒドロキシベンジジン、3,3’-ジメトキシベンジジン、o-トリジン、m-
トリジン、2,2’-ビス(トリフルオロメチル)ベンジジン、1,4-ビス(4-アミ
ノフェノキシ)ベンゼン、1,4-ビス(3-アミノフェノキシ)ベンゼン、1,3-ビ
ス(4-アミノフェノキシ)ベンゼン、1,3-ビス(3-アミノフェノキシ)ベンゼン
、4,4’-ビス(4-アミノフェノキシ)ビフェニル、ビス(4-(3-アミノフェノ
キシ)フェニル)スルホン、ビス(4-(4-アミノフェノキシ)フェニル)スルホン、
2,2-ビス(4-(4-アミノフェノキシ)フェニル)プロパン、2,2-ビス(4-
(4-アミノフェノキシ)フェニル)ヘキサフルオロプロパン、2,2-ビス(4-アミ
ノフェニル)ヘキサフルオロプロパン、p-ターフェニレンジアミン、4-アミノフェニ
ル4-アミノベンゾエート、4-アミノ-2-メチルフェニル4-アミノベンゾエート、ハイドロキノンビス(4-アミノベンゾエート)、メチルハイドロキノンビス(4-アミノベンゾエート)、メトキシハイドロキノンビス(4-アミノベンゾエート)、フェニルハイドロキノンビス(4-アミノベンゾエート)、ビス(4-アミノフェニル)テレフタレート、ビス(4-アミノ-2-メチルフェニル)テレフタレート等が挙げられる。これらを2種類以上併用(共重合)してもよい。
In the above polymerization reaction, it is desirable to select an aromatic diamine that can be used within a range that does not impair the polymerization reactivity, the uniformity of the reaction solution, and the required properties of the polyesterimide film. In this specification, the aromatic diamine contains at least an aromatic group in the molecule, and may contain an aromatic group and an aliphatic group. Usable aromatic diamines are not particularly limited, but examples thereof include p-phenylenediamine, m-phenylenediamine, 2,4-diaminotoluene,
2,5-diaminotoluene, 2,4-diaminoxylene, 2,4-diaminodurene, 4
, 4'-methylenedianiline, 4,4'-methylenebis(3-methylaniline), 4,4
'-methylenebis(3-ethylaniline), 4,4'-methylenebis(2-methylaniline), 4,4'-methylenebis(2-ethylaniline), 4,4'-methylenebis(3,
5-dimethylaniline), 4,4'-methylenebis(3,5-diethylaniline), 4,
4'-methylenebis(2,6-dimethylaniline), 4,4'-methylenebis(2,6-
diethylaniline), 4,4'-diaminodiphenyl ether, 3,4'-diaminodiphenyl ether, 3,3'-diaminodiphenyl ether, 2,4'-diaminodiphenyl ether, 2,2'-diaminodiphenyl ether, 4,4'-diamino-2,2'-
Bis(trifluoromethyl)diphenyl ether, 4,4'-diaminodiphenyl sulfone, 3,3'-diaminodiphenyl sulfone, 4,4'-diaminobenzophenone, 3,
3'-Diaminobenzophenone, 4,4'-diaminobenzanilide, benzidine, 3,
3'-Dihydroxybenzidine, 3,3'-dimethoxybenzidine, o-tolidine, m-
tolidine, 2,2'-bis(trifluoromethyl)benzidine, 1,4-bis(4-aminophenoxy)benzene, 1,4-bis(3-aminophenoxy)benzene, 1,3-bis(4-aminophenoxy)benzene, 1,3-bis(3-aminophenoxy)benzene, 4,4'-bis(4-aminophenoxy)biphenyl, bis(4-(3-aminophenoxy)phenyl)sulfone, bis(4-(4-aminophenoxy)phenyl)sulfone,
2,2-bis(4-(4-aminophenoxy)phenyl)propane, 2,2-bis(4-
Examples of such an aminophenyl ester include 4-aminophenyl hexafluoropropane, 2,2-bis(4-aminophenyl)hexafluoropropane, p-terphenylenediamine, 4-aminophenyl 4-aminobenzoate, 4-amino-2-methylphenyl 4-aminobenzoate, hydroquinone bis(4-aminobenzoate), methylhydroquinone bis(4-aminobenzoate), methoxyhydroquinone bis(4-aminobenzoate), phenylhydroquinone bis(4-aminobenzoate), bis(4-aminophenyl)terephthalate, and bis(4-amino-2-methylphenyl)terephthalate. Two or more of these may be used in combination (copolymerized).
上記重合反応の際、重合反応性、反応溶液の均一性およびポリエステルイミドフィルム
の要求特性を損なわない範囲で使用可能な脂肪族ジアミンを選択することが望ましい。本
明細書において、脂肪族ジアミンは、分子内に、少なくとも脂肪族基を含み、芳香族基を
含まない。使用可能な脂肪族ジアミンとして、特に限定されないが、例えば、トランス-
1,4-シクロヘキサンジアミン(t-CHDA)、シス-1,4-シクロヘキサンジア
ミン、4,4’-メチレンビス(シクロヘキシルアミン)、4,4’-メチレンビス(3
-メチルシクロヘキシルアミン)、4,4’-メチレンビス(3-エチルシクロヘキシル
アミン)、4,4’-メチレンビス(3,5-ジメチルシクロヘキシルアミン)、4,4
’-メチレンビス(3,5-ジエチルシクロヘキシルアミン)、イソホロンジアミン、1
,4-シクロヘキサンビス(メチルアミン)、2,5-ビス(アミノメチル)ビシクロ〔
2.2.1〕ヘプタン、2,6-ビス(アミノメチル)ビシクロ〔2.2.1〕ヘプタン
、3,8-ビス(アミノメチル)トリシクロ〔5.2.1.0〕デカン、1,3-ジアミ
ノアダマンタン、2,2-ビス(4-アミノシクロヘキシル)プロパン、2,2-ビス(
4-アミノシクロヘキシル)ヘキサフルオロプロパン、1,3-プロパンジアミン、1,
4-テトラメチレンジアミン、1,5-ペンタメチレンジアミン、1,6-ヘキサメチレ
ンジアミン、1,7-ヘプタメチレンジアミン、1,8-オクタメチレンジアミン、1,
9-ノナメチレンジアミン、シロキサン含有ジアミン等が挙げられる。これらを2種類以
上併用(共重合)してもよい。また、これらの脂肪族ジアミンと前述の芳香族ジアミンを
併用してもよい。
In the polymerization reaction, it is desirable to select an aliphatic diamine that can be used within a range that does not impair the polymerization reactivity, the uniformity of the reaction solution, and the required properties of the polyesterimide film. In this specification, the aliphatic diamine contains at least an aliphatic group and does not contain an aromatic group in the molecule. The usable aliphatic diamine is not particularly limited, but for example, trans-
1,4-cyclohexanediamine (t-CHDA), cis-1,4-cyclohexanediamine, 4,4'-methylenebis(cyclohexylamine), 4,4'-methylenebis(3
-methylcyclohexylamine), 4,4'-methylenebis(3-ethylcyclohexylamine), 4,4'-methylenebis(3,5-dimethylcyclohexylamine), 4,4
'-Methylenebis(3,5-diethylcyclohexylamine), isophoronediamine, 1
, 4-cyclohexanebis(methylamine), 2,5-bis(aminomethyl)bicyclo[
2.2.1]heptane, 2,6-bis(aminomethyl)bicyclo[2.2.1]heptane, 3,8-bis(aminomethyl)tricyclo[5.2.1.0]decane, 1,3-diaminoadamantane, 2,2-bis(4-aminocyclohexyl)propane, 2,2-bis(
4-aminocyclohexyl)hexafluoropropane, 1,3-propanediamine, 1,
4-Tetramethylenediamine, 1,5-Pentamethylenediamine, 1,6-Hexamethylenediamine, 1,7-Heptamethylenediamine, 1,8-Octamethylenediamine, 1,
9-nonamethylenediamine, siloxane-containing diamine, etc. Two or more of these may be used in combination (copolymerization). Furthermore, these aliphatic diamines may be used in combination with the aromatic diamines described above.
上記重合反応の際、重合反応性、反応溶液の均一性およびポリエステルイミドフィルム
の要求特性を損なわない範囲で、一般式(1)で表されるテトラカルボン酸二無水物以外
の芳香族テトラカルボン酸二無水物を共重合成分として併用することができる。その際に
使用可能な芳香族テトラカルボン酸二無水物としては、特に限定されないが、例えば、ピ
ロメリット酸二無水物、3,3’,4,4’-ビフェニルテトラカルボン酸二無水物、1
,4-フェニレンビス(トリメリテート アンハイドライド)、2-メチル-1,4-フ
ェニレンビス(トリメリテート アンハイドライド)、2-メトキシ-1,4-フェニレ
ンビス(トリメリテート アンハイドライド)、3,3’,4,4’-ベンゾフェノンテ
トラカルボン酸二無水物、3,3’,4,4’-ビフェニルエーテルテトラカルボン酸二
無水物、3,3’,4,4’-ビフェニルスルホンテトラカルボン酸二無水物、2,2’
-ビス(3,4-ジカルボキシフェニル)ヘキサフルオロプロパン酸二無水物、2,2’
-ビス(3,4-ジカルボキシフェニル)プロパン酸二無水物、1,4,5,8-ナフタ
レンテトラカルボン酸二無水物、2,3,6,7-ナフタレンテトラカルボン酸二無水物
等が挙げられる。また、これらを2種類以上用いてもよい。また、これらの共重合成分の
使用量は、全テトラカルボン酸二無水物中、例えば0.1~50mol%、好ましくは1
~40mol%の範囲である。
In the above polymerization reaction, aromatic tetracarboxylic dianhydrides other than the tetracarboxylic dianhydride represented by the general formula (1) can be used as a copolymerization component in the range that does not impair the polymerization reactivity, the uniformity of the reaction solution, and the required properties of the polyesterimide film. The aromatic tetracarboxylic dianhydride that can be used in this case is not particularly limited, but examples thereof include pyromellitic dianhydride, 3,3',4,4'-biphenyltetracarboxylic dianhydride, 1,2,3',4,4'-biphenyltetracarboxylic dianhydride, 1,2,3',4,4'-biphenyltetracarboxylic dianhydride, 1,3,4',5 ...
,4-phenylenebis(trimellitate anhydride), 2-methyl-1,4-phenylenebis(trimellitate anhydride), 2-methoxy-1,4-phenylenebis(trimellitate anhydride), 3,3',4,4'-benzophenonetetracarboxylic dianhydride, 3,3',4,4'-biphenylethertetracarboxylic dianhydride, 3,3',4,4'-biphenylsulfonetetracarboxylic dianhydride, 2,2'
-bis(3,4-dicarboxyphenyl)hexafluoropropanoic dianhydride, 2,2'
Examples of the copolymerizable components include 1,4,5,8-naphthalenetetracarboxylic dianhydride, 2,3,6,7-naphthalenetetracarboxylic dianhydride, and the like. Two or more of these may be used. The amount of these copolymerizable components used is, for example, 0.1 to 50 mol %, preferably 1.0 to 50 mol %, based on the total amount of tetracarboxylic dianhydride.
The range is 40 mol %.
上記重合反応の際、重合反応性、反応溶液の均一性およびポリエステルイミドフィルム
の要求特性を損なわない範囲で、一般式(1)で表されるテトラカルボン酸二無水物以外
に脂肪族テトラカルボン酸二無水物を共重合成分として併用することができる。その際に
使用可能な脂肪族テトラカルボン酸二無水物としては、特に限定されないが、例えば、例
えば、ビシクロ[2.2.2]オクト-7-エン-2,3,5,6-テトラカルボン酸二
無水物、ビシクロ[2.2.2]オクタン-2,3,5,6-テトラカルボン酸二無水物
、ビシクロ[2.2.2]ヘプタンテトラカルボン酸二無水物、テトラヒドロフラン-2
,3,4,5-テトラカルボン酸二無水物、3c-カルボキシメチルシクロペンタンー1
r,2c,4c-トリカルボン酸1,4:2,3-二無水物、ビシクロ-3,3’,4,
4’-テトラカルボン酸二無水物、1,2,4,5-シクロヘキサンテトラカルボン酸二
無水物(、1,2,3,4-シクロブタンテトラカルボン酸二無水物、1,3-ジメチル
-1,2,3,4-シクロブタンテトラカルボン酸二無水物、1,2,3,4-シクロペ
ンタンテトラカルボン酸二無水物等が挙げられる。これらを2種類以上用いてもよい。ま
た、脂肪族テトラカルボン酸二無水物(共重合成分)の使用量は、全テトラカルボン酸二
無水物中、例えば0.1~40mol%、好ましくは1~30mol%の範囲である。ま
た、の脂肪族テトラカルボン酸二無水物(共重合成分)と前述の芳香族テトラカルボン酸
二無水物(共重合成分)とを併用してもよい。
In the above polymerization reaction, aliphatic tetracarboxylic dianhydrides can be used in combination as copolymerization components in addition to the tetracarboxylic dianhydride represented by the general formula (1) within the scope of not impairing the polymerization reactivity, the uniformity of the reaction solution, and the required properties of the polyesterimide film. The aliphatic tetracarboxylic dianhydrides that can be used in this case are not particularly limited, but examples thereof include bicyclo[2.2.2]oct-7-ene-2,3,5,6-tetracarboxylic dianhydride, bicyclo[2.2.2]octane-2,3,5,6-tetracarboxylic dianhydride, bicyclo[2.2.2]heptane tetracarboxylic dianhydride, tetrahydrofuran-2,4-dicarboxylic dianhydride, and the like.
, 3,4,5-tetracarboxylic dianhydride, 3c-carboxymethylcyclopentane-1
r,2c,4c-tricarboxylic acid 1,4:2,3-dianhydride, bicyclo-3,3',4,
Examples of the dianhydride include 4'-tetracarboxylic acid dianhydride, 1,2,4,5-cyclohexanetetracarboxylic acid dianhydride (1,2,3,4-cyclobutanetetracarboxylic acid dianhydride, 1,3-dimethyl-1,2,3,4-cyclobutanetetracarboxylic acid dianhydride, and 1,2,3,4-cyclopentanetetracarboxylic acid dianhydride. Two or more of these may be used. The amount of the aliphatic tetracarboxylic acid dianhydride (copolymerization component) used is, for example, in the range of 0.1 to 40 mol %, and preferably 1 to 30 mol %, of the total tetracarboxylic acid dianhydrides. The aliphatic tetracarboxylic acid dianhydride (copolymerization component) and the aromatic tetracarboxylic acid dianhydride (copolymerization component) may be used in combination.
ポリエステルイミド前駆体ワニスのハンドリングおよびポリエステルイミドフィルムの
物性の観点から、ポリエステルイミド前駆体の固有粘度は0.5~5.0dL/gの範囲
であることが好ましく、1.0~3.0dL/gの範囲であることがより好ましい。ポリ
エステルイミド前駆体の固有粘度は、固形分濃度0.5質量%に調整したポリエステルイ
ミド前駆体の溶液を用い、オストワルド粘度計を用いて30℃で測定して得られる値であ
る。
From the viewpoint of handling of the polyesterimide precursor varnish and the physical properties of the polyesterimide film, the intrinsic viscosity of the polyesterimide precursor is preferably in the range of 0.5 to 5.0 dL/g, and more preferably in the range of 1.0 to 3.0 dL/g. The intrinsic viscosity of the polyesterimide precursor is a value obtained by measuring a solution of the polyesterimide precursor adjusted to a solids concentration of 0.5 mass % at 30° C. with an Ostwald viscometer.
上記の製造方法により得られたポリエステルイミド前駆体ワニスを、例えばキャスト製
膜工程のための適切な溶液粘度に調整する等の目的で、溶媒で適度に希釈してもよい。希
釈には前述の重合溶媒が使用可能である。通常、重合に用いたものと同一の溶媒で希釈す
るが、ワニスの均一性が損なわれなければ異なった溶媒で希釈してもよい。また、希釈溶
媒として2種類以上の溶媒を混合して用いてもよい。これらの希釈溶媒はあらかじめ脱水
処理されていることが望ましい。
The polyesterimide precursor varnish obtained by the above-mentioned production method may be appropriately diluted with a solvent, for example, for the purpose of adjusting the solution viscosity to an appropriate level for the cast film-forming process. The above-mentioned polymerization solvents can be used for dilution. Usually, the varnish is diluted with the same solvent as that used for polymerization, but it may be diluted with a different solvent as long as the uniformity of the varnish is not impaired. In addition, two or more types of solvents may be mixed and used as the dilution solvent. It is preferable that these dilution solvents are dehydrated in advance.
上記の製造方法により得られたポリエステルイミド前駆体ワニスとしてそのまま用いる
ことができ、または、前述の希釈溶媒で適度に希釈後、大量の水やメタノール等の貧溶媒
中に滴下して繊維状の粉末として析出させ、濾過、洗浄、及び乾燥してポリエステルイミ
ド前駆体を単離することもできる。更に単離した粉末を再度、溶媒に溶解して均一なワニ
スとすることができる。その際、再溶解には前述の重合溶媒が使用可能である。通常、重
合に用いたものと同一の溶媒に溶解させるが、ワニスの均一性が損なわれなければ異なっ
た溶媒に溶解させてもよい。また、再溶解用の溶媒(本明細書において「再溶解溶媒」と
いう場合がある。)として2種類以上の溶媒を混合して用いてもよい。これらの再溶解溶
媒はあらかじめ脱水処理されていることが望ましい。再溶解を促進するため、溶液を例え
ば30~120℃、好ましくは40~80℃で、例えば1分~4時間、好ましくは5分~
1時間加熱してもよい。
The polyesterimide precursor varnish obtained by the above-mentioned manufacturing method can be used as it is, or after being appropriately diluted with the above-mentioned dilution solvent, it can be dropped into a large amount of poor solvent such as water or methanol to precipitate as a fibrous powder, and then filtered, washed, and dried to isolate the polyesterimide precursor. The isolated powder can be dissolved again in a solvent to obtain a uniform varnish. In this case, the above-mentioned polymerization solvent can be used for redissolution. Usually, it is dissolved in the same solvent as that used in polymerization, but it may be dissolved in a different solvent as long as the uniformity of the varnish is not impaired. In addition, two or more types of solvents may be mixed and used as the solvent for redissolution (sometimes referred to as "redissolution solvent" in this specification). It is desirable that these redissolution solvents have been dehydrated in advance. In order to promote redissolution, the solution is heated, for example, at 30 to 120°C, preferably 40 to 80°C, for example, for 1 minute to 4 hours, preferably for 5 minutes to 120°C.
May be heated for 1 hour.
重合して得られたポリエステルイミド前駆体ワニスの粘度を安定化するため、またはポ
リエステルイミド前駆体の分子量を適度に下げること等を目的とし、重合して得られたポ
リエステルイミド前駆体ワニスをそのまま、希釈後、または再溶解後に、例えば50~1
30℃、好ましくは70~120℃で、例えば10分~6時間、好ましくは30分~4時
間加熱してもよい。
In order to stabilize the viscosity of the polyesterimide precursor varnish obtained by polymerization or to appropriately lower the molecular weight of the polyesterimide precursor, the polyesterimide precursor varnish obtained by polymerization is diluted or redissolved, and then diluted with water to a concentration of, for example, 50 to 100 ml.
It may be heated at 30° C., preferably 70 to 120° C., for example, for 10 minutes to 6 hours, preferably 30 minutes to 4 hours.
ポリエステルイミド前駆体を部分的にイミド化することを目的として、沈殿析出または
ゲル化を生じないように注意しながら、重合により得られたポリエステルイミド前駆体ワ
ニスをそのまま、希釈後、または再溶解後に、例えば70~160℃、好ましくは80~
150℃で、例えば10分~6時間、好ましくは30分~4時間加熱してもよい。
For the purpose of partially imidizing the polyesterimide precursor, the polyesterimide precursor varnish obtained by polymerization is heated, either directly or after dilution or after redissolution, at, for example, 70 to 160° C., preferably 80 to 100° C., while taking care not to cause precipitation or gelation.
The mixture may be heated at 150° C. for, for example, 10 minutes to 6 hours, preferably 30 minutes to 4 hours.
ポリエステルイミド前駆体を部分的にイミド化することを目的として、沈殿析出または
ゲル化を生じないように注意しながら、重合により得られたポリエステルイミド前駆体ワ
ニスをそのまま、希釈後、または再溶解後に、有機3級アミンと脱水閉環剤とを含む化学
イミド化剤を添加し、例えば0~100℃、好ましくは20~60℃で、例えば1~48
時間、好ましくは2~24時間撹拌してもよい。
For the purpose of partially imidizing the polyesterimide precursor, a chemical imidization agent containing an organic tertiary amine and a dehydrating ring-closing agent is added to the polyesterimide precursor varnish obtained by polymerization, either directly or after dilution or after redissolution, while taking care not to cause precipitation or gelation, and the mixture is heated at, for example, 0 to 100° C., preferably 20 to 60° C., for example, at 1 to 48° C.
The mixture may be stirred for a period of time, preferably for 2 to 24 hours.
化学イミド化剤中の有機3級アミンとして、特に限定されないが、例えばピリジン、ピ
コリン、N,N-ジメチルアニリン、N,N-ジエチルアニリン、トリエチルアミン、ト
リプロピルアミン、トリブチルアミン等が使用可能である。毒性や経済性の観点からピリ
ジンが好適に使用される。また、化学イミド化剤中の脱水閉環剤として、特に限定されな
いが、例えば無水酢酸、無水プロピオン酸、無水酪酸、無水イソ酪酸等の酸無水物が使用
可能である。除去の容易さや経済性の観点から無水酢酸が好適に用いられる。
The organic tertiary amine in the chemical imidization agent is not particularly limited, but for example, pyridine, picoline, N,N-dimethylaniline, N,N-diethylaniline, triethylamine, tripropylamine, tributylamine, etc. can be used. From the viewpoints of toxicity and economy, pyridine is preferably used. Furthermore, the dehydration ring-closing agent in the chemical imidization agent is not particularly limited, but for example, acid anhydrides such as acetic anhydride, propionic anhydride, butyric anhydride, isobutyric anhydride, etc. can be used. From the viewpoints of ease of removal and economy, acetic anhydride is preferably used.
化学イミド化剤中の脱水閉環剤と有機3級アミンの混合比(質量比)は特に限定されな
いが、脱水閉環剤の質量を1gとすると、有機3級アミンは例えば0.1~2gの範囲で
あり、好ましくは0.2~1gの範囲である。
The mixing ratio (mass ratio) of the dehydrating ring-closing agent and the organic tertiary amine in the chemical imidization agent is not particularly limited. When the mass of the dehydrating ring-closing agent is 1 g, the mass of the organic tertiary amine is, for example, in the range of 0.1 to 2 g, and preferably in the range of 0.2 to 1 g.
ポリエステルイミド前駆体を部分的にイミド化する際に添加する化学イミド化剤量は、
その中に含まれる脱水閉環剤が、ポリエステルイミド前駆体中のカルボキシ基量即ち理論
脱水量(モル)の0.05~0.2倍モル量の範囲になるように添加する。これにより、
反応溶液から沈殿が析出したり、ゲル化が生じたりすることを防ぐことができる。
The amount of the chemical imidizing agent added when partially imidizing the polyesterimide precursor is
The amount of the dehydrating ring-closing agent contained therein is added in a molar amount in the range of 0.05 to 0.2 times the amount of carboxy groups in the polyesterimide precursor, i.e., the theoretical amount of dehydration (molar amount).
This can prevent precipitation from occurring in the reaction solution and prevent gelation from occurring.
ポリエステルイミドフィルムの要求特性を損なわない範囲で、上記のようにして得られ
たポリエステルイミド前駆体のワニスに、ポリエステルイミド以外のポリマー、無機フィ
ラー、接着促進剤、剥離剤、難燃剤、紫外線安定剤、界面活性剤、レベリング剤、消泡剤
、蛍光増白剤、架橋剤、重合開始剤、感光剤等各種添加剤を添加してもよい。
Various additives, such as a polymer other than polyesterimide, an inorganic filler, an adhesion promoter, a release agent, a flame retardant, an ultraviolet stabilizer, a surfactant, a leveling agent, an antifoaming agent, a fluorescent brightening agent, a crosslinking agent, a polymerization initiator, and a photosensitizer, may be added to the varnish of the polyesterimide precursor obtained as described above, so long as the additives do not impair the required properties of the polyesterimide film.
<ポリエステルイミドおよびその製造方法>
本発明の一実施形態であるポリエステルイミドは、上記一般式(7)で表される構造単
位を含む。一般式(7)中、Ar1は前記式(2)~(6)のいずれかで表され、Ar2
は2価の芳香族基、2価の脂肪族基、または芳香族基と脂肪族基の少なくとも一方を含む
2価の基である。芳香族基と脂肪族基の少なくとも一方を含む2価の基は、芳香族基を含
む基、脂肪族基を含む基、または芳香族基と脂肪族基とを含む基であってよい。芳香族基
と脂肪族基の少なくとも一方を含む2価の基は、任意の基を更に含んでよい。「芳香族基と脂肪族基の少なくとも一方を含む2価の基」は、「2価の芳香族基」及び「2価の脂肪族基」以外の基であってよい。
<Polyesterimide and its manufacturing method>
A polyesterimide according to one embodiment of the present invention contains a structural unit represented by the above general formula (7). In the general formula (7), Ar 1 is represented by any one of the above formulas (2) to (6), and Ar 2 is
is a divalent aromatic group, a divalent aliphatic group, or a divalent group containing at least one of an aromatic group and an aliphatic group. The divalent group containing at least one of an aromatic group and an aliphatic group may be a group containing an aromatic group, a group containing an aliphatic group, or a group containing an aromatic group and an aliphatic group. The divalent group containing at least one of an aromatic group and an aliphatic group may further contain any group. The "divalent group containing at least one of an aromatic group and an aliphatic group" may be a group other than a "divalent aromatic group" and a "divalent aliphatic group".
一般式(7)で表される構造単位を含むポリエステルイミドは、エステル基を導入する
ことでイミド基の濃度が低減されているために低吸水率であり、かつ、2,6-ナフタレ
ン構造によりポリマー鎖に沿って芳香環が増環された構造単位を含むために低誘電正接で
ある。
A polyesterimide containing a structural unit represented by general formula (7) has a low water absorption rate because the concentration of imide groups is reduced by introducing an ester group, and also has a low dielectric tangent because it contains a structural unit in which aromatic rings are increased along the polymer chain by a 2,6-naphthalene structure.
Ar1は、式(3)~(6)のいずれかであってよく、式(4)~(6)のいずれかであることが好ましく、式(4)又は(6)であることがより好ましく、式(6)であることが更に好ましい。Ar1は、一般式(1)で表されるテトラカルボン酸二無水物に由来する構造であってよい。 Ar 1 may be any of formulas (3) to (6), preferably any of formulas (4) to (6), more preferably formula (4) or (6), and even more preferably formula (6). Ar 1 may be a structure derived from a tetracarboxylic dianhydride represented by general formula (1).
Ar2は、低吸水率、低誘電正接、低熱膨張性、及び高弾性のポリエステルイミドフィルムを得る観点から、2価の芳香族基であることが好ましく、フェニレン基であることがより好ましい。Ar2は、誘電正接が特に低いポリエステルイミドフィルムを得る観点から、芳香族基とオキシ基(エーテル結合)とを含む2価の基であることが好ましく、ジフェニルエーテル基(-Ph-O-Ph-基(Phはフェニレン基))であることがより好ましい。Ar2は、吸水率と誘電正接とが特に低いポリエステルイミドフィルムを得る観点から、芳香族基とオキシカルボニル基(エステル結合)とを含む2価の基であることが好ましい。Ar2は、誘電率を低下させる観点から、芳香族基とオキシ基(エーテル結合)とイソプロピリデン基とを含む2価の基であることが好ましく、ビス(フェノキシフェニル)プロパン基(-Ph-O-Ph-C3H6-Ph-O-Ph-基(Phはフェニレン基))であることが更に好ましい。2価の芳香族基、2価の脂肪族基、または芳香族基と脂肪族基の少なくとも一方を含む2価の基における芳香族基および脂肪族基は、それぞれ、置換又は非置換であってよい。Ar2である、2価の芳香族基、2価の脂肪族基、または芳香族基と脂肪族基の少なくとも一方を含む2価の基は、それぞれ、上記の芳香族ジアミンまたは脂肪族ジアミンに由来する構造であってよい。 From the viewpoint of obtaining a polyesterimide film having low water absorption, low dielectric tangent, low thermal expansion, and high elasticity, Ar 2 is preferably a divalent aromatic group, and more preferably a phenylene group. From the viewpoint of obtaining a polyesterimide film having a particularly low dielectric tangent, Ar 2 is preferably a divalent group containing an aromatic group and an oxy group (ether bond), and more preferably a diphenyl ether group (-Ph-O-Ph- group (Ph is a phenylene group)). From the viewpoint of obtaining a polyesterimide film having a particularly low water absorption and dielectric tangent, Ar 2 is preferably a divalent group containing an aromatic group and an oxycarbonyl group (ester bond). From the viewpoint of reducing the dielectric constant, Ar 2 is preferably a divalent group containing an aromatic group, an oxy group (ether bond), and an isopropylidene group, and more preferably a bis(phenoxyphenyl)propane group (-Ph-O-Ph-C 3 H 6 -Ph-O-Ph- group (Ph is a phenylene group)). The aromatic group and the aliphatic group in the divalent aromatic group, the divalent aliphatic group, or the divalent group containing at least one of an aromatic group and an aliphatic group may each be substituted or unsubstituted. The divalent aromatic group, the divalent aliphatic group, or the divalent group containing at least one of an aromatic group and an aliphatic group, which is Ar2 , may each have a structure derived from the above-mentioned aromatic diamine or aliphatic diamine.
ポリエステルイミドは、一般式(1)で表されるテトラカルボン酸二無水物以外の芳香
族テトラカルボン酸二無水物に由来する構造を含む構造単位、脂肪族テトラカルボン酸二
無水物に由来する構造を含む構造単位、またはこれらの両方の構造単位を更に含むことが
できる。
The polyesterimide may further include a structural unit including a structure derived from an aromatic tetracarboxylic dianhydride other than the tetracarboxylic dianhydride represented by general formula (1), a structural unit including a structure derived from an aliphatic tetracarboxylic dianhydride, or both of these structural units.
一般式(7)で表されるポリエステルイミドは、上記のポリエステルイミド前駆体を脱
水閉環させることにより製造することができる。脱水閉環させる方法は特に限定されず、
熱イミド化法、化学イミド化法等の公知の方法を適用できる。簡便であることから、熱イ
ミド化法が好ましく、加熱温度は例えば230~400℃、好ましくは250~370℃
である。
The polyesterimide represented by the general formula (7) can be produced by dehydrating and ring-closing the polyesterimide precursor. The method for dehydrating and ring-closing the polyesterimide precursor is not particularly limited.
Known methods such as thermal imidization and chemical imidization can be applied. The thermal imidization is preferred because it is simple, and the heating temperature is, for example, 230 to 400° C., preferably 250 to 370° C.
It is.
<ポリエステルイミドフィルム>
本発明の一実施形態であるポリエステルイミドフィルムは、少なくともポリエステルイ
ミドを含む。ポリエステルイミドフィルムは、用途に応じて、ポリエステルイミド以外の
ポリマー、無機フィラー、接着促進剤、剥離剤、難燃剤、紫外線安定剤、界面活性剤、レ
ベリング剤、消泡剤、蛍光増白剤、架橋剤、重合開始剤、感光剤等各種添加剤などを含ん
でもよい。
<Polyesterimide film>
The polyesterimide film according to one embodiment of the present invention contains at least polyesterimide, and may contain various additives such as polymers other than polyesterimide, inorganic fillers, adhesion promoters, release agents, flame retardants, UV stabilizers, surfactants, leveling agents, defoamers, fluorescent brighteners, crosslinking agents, polymerization initiators, and photosensitizers depending on the application.
以下にポリエステルイミドフィルムの製造方法について例示するが、これに限定されな
い。ポリエステルイミドフィルムの製造には、キャスト製膜法を好ましく用いることがで
きる。上記のように得られたポリエステルイミド前駆体の均一なワニスを様々な材質、例
えばガラス、銅、アルミニウム、ステンレス、シリコン等の支持体(基板)上に塗工し、
熱風乾燥器中、例えば40~150℃、好ましくは50~130℃で、例えば10分~4
時間、好ましくは30分~2時間乾燥し、ポリエステルイミド前駆体のフィルムを得る。
The following is an example of a method for producing a polyesterimide film, but the method is not limited thereto. A cast film-forming method can be preferably used for producing a polyesterimide film. A uniform varnish of the polyesterimide precursor obtained as described above is applied onto a support (substrate) made of various materials, such as glass, copper, aluminum, stainless steel, silicon, etc., and
In a hot air dryer, for example, at 40 to 150° C., preferably 50 to 130° C., for example, for 10 minutes to 4
The film is dried for a period of time, preferably 30 minutes to 2 hours, to obtain a film of the polyesterimide precursor.
上記のようにして得られたポリエステルイミド前駆体のフィルムを基板上で真空中また
は窒素等の不活性ガス中、例えば230~400℃、好ましくは250~370℃で加熱
することでポリエステルイミドフィルムを製造することができる。また、昇温は段階的に
行ってもよい。熱イミド化は真空中あるいは不活性ガス中で行うことが望ましいが、イミ
ド化温度が高すぎなければ空気中で行ってもよい。
A polyesterimide film can be produced by heating the polyesterimide precursor film obtained as described above on a substrate in vacuum or in an inert gas such as nitrogen at, for example, 230 to 400° C., preferably 250 to 370° C. The temperature may be raised stepwise. Thermal imidization is preferably carried out in vacuum or in an inert gas, but may be carried out in air as long as the imidization temperature is not too high.
ポリエステルイミド前駆体のフィルムのイミド化は通常、上記のように高温で加熱して
行うが、ポリエステルイミド前駆体フィルムを前述の化学イミド化剤浴中に浸漬すること
によっても行うことができる。浸漬したフィルムを洗浄および乾燥後、更に熱処理しても
よい。
The imidization of the polyesterimide precursor film is usually carried out by heating at a high temperature as described above, but it can also be carried out by immersing the polyesterimide precursor film in a bath of the above-mentioned chemical imidization agent. The immersed film may be washed and dried, and then further heat-treated.
熱イミド化工程後、ポリエステルイミドフィルムと基板との積層体を水やアルコール浴
等に浸漬し、ポリエステルイミドフィルムを基板から剥離して自立フィルムとし、これを
残留歪を除く等の目的で真空中、不活性ガス中または空気中で更に熱処理してもよい。そ
の際ポリエステルイミドフィルムの変形や配向緩和によるCTEの増加等の悪影響を抑制
するため、熱処理の温度条件を適宜選択することができる。
After the thermal imidization step, the laminate of the polyesterimide film and the substrate may be immersed in a water or alcohol bath, etc., and the polyesterimide film may be peeled off from the substrate to form a free-standing film, which may then be further heat-treated in vacuum, in an inert gas, or in air for the purpose of removing residual strain, etc. In this case, the temperature conditions of the heat treatment may be appropriately selected in order to suppress adverse effects such as deformation of the polyesterimide film and an increase in CTE due to relaxation of orientation.
ポリエステルイミドフィルムは、熱機械分析によって測定された100~200℃の間
の平均線熱膨張係数が、例えば60ppm/K以下、好ましくは30ppm/K以下、よ
り好ましくは10ppm/K以下である。下限は特に限定されない。平均線熱膨張係数は
、熱機械分析装置を用いて、試験片(例えば、長さ:20mm、幅:5mm、チャック間
長さ:15mm)に膜厚1μm当たり静荷重0.5gをかけて、昇温速度5℃/分におけ
る試験片の伸びより、100~200℃の範囲での平均値として求められるポリエステル
イミドフィルム(25μm厚)のフィルム面(XY)方向の値である。
The polyesterimide film has an average linear thermal expansion coefficient between 100 and 200°C measured by thermomechanical analysis of, for example, 60 ppm/K or less, preferably 30 ppm/K or less, more preferably 10 ppm/K or less. The lower limit is not particularly limited. The average linear thermal expansion coefficient is a value in the film surface (XY) direction of a polyesterimide film (25 μm thick) obtained as an average value in the range of 100 to 200°C from the elongation of a test piece (e.g., length: 20 mm, width: 5 mm, chuck length: 15 mm) at a temperature increase rate of 5°C/min, with a static load of 0.5 g per 1 μm of film thickness applied to the test piece using a thermomechanical analyzer.
ポリエステルイミドフィルムは、動的粘弾性分析により測定されたガラス転移温度が、
例えば300℃以上であるかまたは検出されないことが好ましく、より好ましくは340
℃以上、更に好ましくは350℃以上である。ガラス転移温度は、動的粘弾性測定装置を
用い、窒素雰囲気中、周波数0.1Hz、昇温速度5℃/分、室温~450℃の温度範囲
で測定した損失弾性率曲線のピーク温度から求めることができる。
The polyesterimide film has a glass transition temperature measured by dynamic viscoelastic analysis of:
For example, it is preferable that the temperature is 300° C. or higher or not detected, and more preferably 340° C. or higher.
The glass transition temperature is preferably 350° C. or higher, and more preferably 350° C. or higher. The glass transition temperature can be determined from the peak temperature of a loss modulus curve measured using a dynamic viscoelasticity measuring device in a nitrogen atmosphere, at a frequency of 0.1 Hz, at a heating rate of 5° C./min, and in a temperature range of room temperature to 450° C.
ポリエステルイミドフィルムは、吸水率が、例えば1.0%以下、好ましくは0.5%
以下、より好ましくは0.3%以下である。下限は特に限定されない。吸水率は、JIS
K 7209に従い、50℃で24時間真空乾燥したポリエステルイミドフィルムの質
量(W0)を秤量し、次にそのフィルムを23℃の水に24時間浸漬した後、余分の水分
を拭き取り質量(W)を秤量し、計算式:WA=(W-W0)/W0×100(%)より
求めることができる。
The polyesterimide film has a water absorption rate of, for example, 1.0% or less, preferably 0.5% or less.
The water absorption is preferably 0.3% or less, more preferably 0.3% or less. The lower limit is not particularly limited.
According to the method of Example 1, K 7209, the mass (W 0 ) of a polyesterimide film that has been vacuum dried at 50° C. for 24 hours is weighed, and the film is then immersed in water at 23° C. for 24 hours, after which excess water is wiped off and the mass (W) is weighed, and the mass can be calculated from the formula: W A =(W−W 0 )/W 0 ×100(%).
ポリエステルイミドフィルムは、動作周波数10GHzにおける誘電正接が、例えば0
.004以下、好ましくは0.003以下、より好ましくは0.002以下である。下限
は特に限定されない。誘電正接は、ポリエステルイミドフィルムを23℃、50%RH(
相対湿度)の環境に24時間置いた後、同一の温度および湿度条件下で、空洞共振器摂動
法により測定することができる。
The polyesterimide film has a dielectric loss tangent of, for example, 0.05% at an operating frequency of 10 GHz.
The dielectric loss tangent is 0.004 or less, preferably 0.003 or less, and more preferably 0.002 or less. There is no particular lower limit.
After placing it in an environment of 100 MPa (relative humidity) for 24 hours, it can be measured by the cavity resonator perturbation method under the same temperature and humidity conditions.
ポリエステルイミドフィルムは、高速伝送FPC用基板、耐熱絶縁基板、高速伝送FP
C用耐熱絶縁基板(ベースフィルム)等に好適に用いることができる。高速伝送FPCの
動作周波数は、例えば、3.6GHz以上である。これらの基板は、ポリエステルイミド
フィルムが低吸水率かつ低誘電正接であるために、信頼性の向上と誘電損失の低減とを両
立することができ、特性上極めて有益である。フィルムの厚さは、特に限定されず、適宜
調節することができる。FPC用耐熱絶縁基板として用いる場合、フィルム厚は10~6
0μmが好適な範囲である。
Polyesterimide film is used for high-speed transmission FPC substrates, heat-resistant insulating substrates, high-speed transmission FP
The film can be suitably used as a heat-resistant insulating substrate (base film) for C, etc. The operating frequency of high-speed transmission FPC is, for example, 3.6 GHz or more. These substrates are extremely beneficial in terms of characteristics, since the polyesterimide film has low water absorption and low dielectric tangent, and can simultaneously improve reliability and reduce dielectric loss. The thickness of the film is not particularly limited and can be adjusted as appropriate. When used as a heat-resistant insulating substrate for FPC, the film thickness is 10 to 6
The preferred range is 0 μm.
以下に本発明を実施例により具体的に説明するが、これらの実施例に限定されるもので
はない。なお、実施例中の物性値は、次の方法により測定した。
The present invention will be described in detail below with reference to examples, but is not limited to these examples. The physical properties in the examples were measured by the following methods.
<赤外線吸収(FT-IR)スペクトル>
合成したモノマー(テトラカルボン酸無水物)およびその中間体の赤外線吸収スペクト
ルは、フーリエ変換赤外分光光度計(日本分光社製FT-IR4100)を用い、KBr
プレート法にて測定した。また、透過法にてポリエステルイミド前駆体およびポリエステ
ルイミド薄膜(約5μm厚)の赤外線吸収スペクトルを測定した。
<Infrared absorption (FT-IR) spectrum>
The infrared absorption spectra of the synthesized monomer (tetracarboxylic anhydride) and its intermediates were measured using a Fourier transform infrared spectrophotometer (FT-IR4100 manufactured by JASCO Corporation) with KBr.
The infrared absorption spectra of the polyesterimide precursor and a thin film (about 5 μm thick) of polyesterimide were measured by a transmission method.
<1H-NMRスペクトル>
合成したモノマーおよびその中間体の1H-NMRスペクトルは、日本電子社製NMR
分光光度計(ECP400)を用い、重水素化ジメチルスルホキシド(DMSO-d6)
または重水素化クロロホルム(CDCl3)を溶媒として測定した。
< 1H -NMR spectrum>
The 1 H-NMR spectra of the synthesized monomers and their intermediates were measured using a JEOL NMR spectrometer.
Using a spectrophotometer (ECP400), deuterated dimethyl sulfoxide (DMSO-d 6 )
Alternatively, the measurements were performed using deuterated chloroform (CDCl 3 ) as a solvent.
<元素分析>
有機微量元素分析装置(ジェイ・サイエンス・ラボ社製MICRO CORDER J
M10)を用い、合成したモノマーおよびその中間体のC、H、Nの化学組成分析を行っ
た。
<Elemental analysis>
Organic trace elemental analyzer (MICRO CORDER J manufactured by J Science Labs)
M10) was used to analyze the C, H, and N chemical composition of the synthesized monomer and its intermediates.
<示差走査熱量分析(融点)>
合成したモノマーおよびその中間体の融点は、ネッチ・ジャパン社製示差走査熱量分析
装置(DSC3100)またはネッチ・ジャパン社製熱重量分析装置(TG-DTA20
00S)を用い、窒素雰囲気中、昇温速度5℃/分で測定したサーモグラムのピーク温度
から求めた。
<Differential scanning calorimetry (melting point)>
The melting points of the synthesized monomers and their intermediates were measured using a differential scanning calorimeter (DSC3100, manufactured by Netsch Japan) or a thermogravimetric analyzer (TG-DTA20, manufactured by Netsch Japan).
00S) in a nitrogen atmosphere at a heating rate of 5° C./min. The peak temperature of the thermogram was determined.
<固有粘度(ηinh)>
ポリエステルイミド前駆体の還元粘度(ηred)は、ポリエステルイミド前駆体であ
るポリアミド酸を重合により得た後のワニスを重合溶媒で希釈して、固形分濃度0.5質
量%の溶液とし、オストワルド粘度計を用いて30℃で測定した。この値は実質的に固有
粘度(ηinh)と見なすことができ、この値が高いほどポリアミド酸の分子量が高いこ
とを表す。通常、この条件で測定された還元粘度が1.0dL/g以上であると、十分高
分子量であると見なすことができる。
<Intrinsic Viscosity (η inh )>
The reduced viscosity (η red ) of the polyesterimide precursor was measured at 30° C. using an Ostwald viscometer after diluting a varnish obtained by polymerization of a polyamic acid, which is a polyesterimide precursor, with a polymerization solvent to prepare a solution with a solid content concentration of 0.5% by mass. This value can be regarded as substantially the intrinsic viscosity (η inh ), and the higher this value, the higher the molecular weight of the polyamic acid. Usually, if the reduced viscosity measured under these conditions is 1.0 dL/g or more, it can be regarded as a sufficiently high molecular weight.
<ガラス転移温度(Tg)>
TAインスツルメント社製動的粘弾性測定装置(Q800)を用い、窒素雰囲気中、周
波数0.1Hz、昇温速度5℃/分、室温~450℃の温度範囲で測定した損失弾性率曲
線のピーク温度からポリエステルイミドフィルム(25μm厚)のガラス転移温度(Tg
)を求めた。Tgが高いほど、物理的耐熱性(短期耐熱性)に優れていることを表す。
<Glass transition temperature ( Tg )>
The glass transition temperature (T g ) of the polyesterimide film (25 μm thick) was calculated from the peak temperature of the loss modulus curve measured in a nitrogen atmosphere at a frequency of 0.1 Hz, a heating rate of 5° C./min, and a temperature range of room temperature to 450° C. using a dynamic viscoelasticity measuring device ( Q800 ) manufactured by TA Instruments.
A higher Tg indicates better physical heat resistance (short-term heat resistance).
<線熱膨張係数(CTE)>
ネッチ・ジャパン社製熱機械分析装置(TMA4000)またはリガク社製熱機械分析
装置(TMA8311)を用いて、試験片(長さ:20mm、幅:5mm、チャック間長
さ:15mm)に膜厚1μm当たり静荷重0.5gをかけて、昇温速度5℃/分における
試験片の伸びより、100~200℃の範囲での平均値としてポリエステルイミドフィル
ム(25μm厚)のフィルム面(XY)方向のCTEを求めた。この値が低いほど、ガラ
ス状温度領域における熱寸法安定性に優れていることを表す。
<Coefficient of Linear Thermal Expansion (CTE)>
Using a thermomechanical analyzer (TMA4000) manufactured by Netzsch Japan or a thermomechanical analyzer (TMA8311) manufactured by Rigaku Corporation, a static load of 0.5 g per 1 μm of film thickness was applied to a test piece (length: 20 mm, width: 5 mm, chuck length: 15 mm), and the CTE in the film plane (XY) direction of the polyesterimide film (25 μm thick) was determined as the average value in the range of 100 to 200° C. from the elongation of the test piece at a heating rate of 5° C./min. The lower this value, the more excellent the thermal dimensional stability in the glassy temperature range.
<5%重量減少温度(Td
5)>
ネッチ・ジャパン社製熱重量分析装置(TG-DTA2000S)を用いて、窒素中お
よび空気気流中、昇温速度10℃/分での昇温過程におけるポリエステルイミドフィルム
(25μm厚)の重量が初期重量の5%減少した時の温度を測定した。窒素中で測定した
Td
5の値が高いほど化学的耐熱性(熱安定性)が高く、より高温まで揮発性有機化合物
(VOC)の発生が抑制されていることを表す。
<5% weight loss temperature (T d 5 )>
Using a thermogravimetric analyzer (TG-DTA2000S) manufactured by Netsch Japan, the temperature at which the weight of a polyesterimide film (25 μm thick) lost 5% of its initial weight during heating in nitrogen and air flow at a heating rate of 10° C./min was measured. The higher the T d 5 value measured in nitrogen, the higher the chemical heat resistance (thermal stability) and the more the generation of volatile organic compounds (VOCs) is suppressed up to higher temperatures.
<機械的特性:引張弾性率(E)、破断伸び(εb)、破断強度(σb)>
ポリエステルイミドフィルム(試験片:30mm長×3mm幅×25μm厚)の機械的
特性は、エー・アンド・デイ社製引張試験機(テンシロンUTM-2)を用い、延伸速度
8mm/分で測定した。応力-歪曲線の初期の勾配から引張弾性率(E)、フィルムが破
断した時の伸び率および応力から破断伸び(εb)および破断強度(σb)をそれぞれ求
めた。
<Mechanical properties: tensile modulus (E), breaking elongation (ε b ), breaking strength (σ b )>
The mechanical properties of the polyesterimide film (test piece: 30 mm long × 3 mm wide × 25 μm thick) were measured at a stretching speed of 8 mm/min using a tensile tester (Tensilon UTM-2) manufactured by A&D Co., Ltd. The tensile modulus (E) was calculated from the initial gradient of the stress-strain curve, and the breaking elongation (ε b ) and breaking strength (σ b ) were calculated from the elongation and stress at the time the film broke.
<吸水率(WA)>
JIS K 7209に従い、50℃で24時間真空乾燥したポリエステルイミドフィ
ルム(膜厚20~30μm)の質量(W0)を秤量し、次にそのフィルムを23℃の水に
24時間浸漬した後、余分の水分を拭き取り、質量(W)を秤量し、WA=(W-W0)
/W0×100(%)より吸水率(WA)を求めた。
<Water absorption rate ( WA )>
According to JIS K 7209, the mass (W 0 ) of a polyesterimide film (film thickness 20 to 30 μm) that had been vacuum dried at 50° C. for 24 hours was weighed, and the film was then immersed in water at 23° C. for 24 hours, after which excess water was wiped off and the mass (W) was weighed. W A =(W −W 0 ).
The water absorption rate ( WA ) was calculated from the following equation:/ W0 ×100(%).
<高周波誘電特性:誘電率(εr)、誘電正接(tan δ)>
ポリエステルイミドフィルムの高周波誘電特性(10GHz)は、フィルムを23℃、
50%RH(相対湿度)の環境に24時間置いた後、同一の温度および湿度条件で空洞共
振器摂動法(IEC62810準拠、キーサイト・テクノロジー社製PNAネットワーク
アナライザN5222B、関東電子応用開発社製空洞共振器10GHz用CP531)に
て、測定した。
<High-frequency dielectric properties: dielectric constant (ε r ), dielectric tangent (tan δ)>
The high frequency dielectric properties (10 GHz) of polyesterimide film are as follows:
After placing it in an environment of 50% RH (relative humidity) for 24 hours, it was measured under the same temperature and humidity conditions by a cavity resonator perturbation method (compliant with IEC62810, PNA network analyzer N5222B manufactured by Keysight Technologies, and cavity resonator for 10 GHz CP531 manufactured by Kanto Electronics Application Development Co., Ltd.).
<テトラカルボン酸二無水物の合成>
[実施例1:8環型テトラカルボン酸二無水物(TDCA)モノマーの合成]
実施例1のテトラカルボン酸二無水物は、以下の反応式(16’)に従い、以下に示す
手順で合成した。
[Example 1: Synthesis of 8-ring tetracarboxylic dianhydride (TDCA) monomer]
The tetracarboxylic dianhydride of Example 1 was synthesized according to the following reaction formula (16') and the procedure shown below.
[アセチル化]
まず、6-ヒドロキシ-2-ナフタレンカルボン酸(反応式(16’)中、(d))を
以下のようにしてアセチル化した。
300mL三口フラスコに6-ヒドロキシ-2-ナフタレンカルボン酸(17.11g
、912mmol)、無水酢酸(70mL)および濃硫酸3滴を入れ、マグネチックスタ
ーラーで撹拌しながら窒素雰囲気中、100℃で3時間リフラックスし、褐色透明溶液を
得た。これを室温に冷却して沈殿を析出させ、沈殿を濾別して水、次いでトルエンで洗浄
後、120℃で12時間真空乾燥しクリーム色の生成物を得た(収率78%)。
[Acetylation]
First, 6-hydroxy-2-naphthalenecarboxylic acid ((d) in reaction formula (16')) was acetylated as follows.
In a 300 mL three-neck flask, 6-hydroxy-2-naphthalenecarboxylic acid (17.11 g
The mixture was stirred with a magnetic stirrer under nitrogen atmosphere at 100°C for 3 hours to obtain a brown transparent solution. The solution was cooled to room temperature to separate a precipitate, which was then filtered and washed with water and then with toluene, and then vacuum dried at 120°C for 12 hours to obtain a cream-colored product (yield 78%).
この生成物の分析結果を以下に示す。FT-IR(KBrプレート法、cm-1):3
053(芳香族C-H伸縮)、2987/2845(脂肪族C-H伸縮)、2684(水
素結合性カルボキシ基、O-H伸縮)、1761(アセトキシ基、C=O伸縮)、168
0(水素結合性カルボキシ基、C=O伸縮)、1223(アセトキシ基、C-O伸縮)。
1H-NMR(400MHz、DMSO-d6、δ、ppm):13.11(s、1H(
相対積分強度:0.90H)、COOH)、8.64(s、1H(1.15H)、6-ア
セトキシ-2-ナフタレンカルボン酸ユニット(6A2NA)の1-プロトン)、8.1
8(d、1H(1.07H)、J=8.9Hz、6A2NAの8-プロトン)、8.03
-7.99(m、2H(2.27H)、6A2NAの3-プロトン+4-プロトン)、7
.77(sd、1H(1.15H)、J=2.2Hz、6A2NAの5-プロトン)、7
.42(dd、1H(1.09H)、J=8.9、2.2Hz,6A2NAの7-プロト
ン)、2.34(s、3H(3.00H)、CH3)。融点(TG-DTA):203℃
。これらの分析結果より、生成物は目的とするアセチル化物(反応式(16’)中、(e
))であることが確認された。
The analytical results of this product are as follows: FT-IR (KBr plate method, cm −1 ): 3
053 (aromatic C-H stretch), 2987/2845 (aliphatic C-H stretch), 2684 (hydrogen bonded carboxyl group, O-H stretch), 1761 (acetoxy group, C=O stretch), 168
0 (hydrogen-bonded carboxy group, C=O stretch), 1223 (acetoxy group, C-O stretch).
1H -NMR (400MHz, DMSO- d6 , δ, ppm): 13.11 (s, 1H(
Relative integrated intensity: 0.90H), COOH), 8.64 (s, 1H (1.15H), 1-proton of 6-acetoxy-2-naphthalene carboxylic acid unit (6A2NA), 8.1
8 (d, 1H (1.07H), J = 8.9 Hz, 8-proton of 6A2NA), 8.03
-7.99 (m, 2H (2.27H), 3-proton + 4-proton of 6A2NA), 7
.77 (sd, 1H (1.15H), J = 2.2 Hz, 5-proton of 6A2NA), 7
.42 (dd, 1H (1.09H), J=8.9, 2.2Hz, 7-proton of 6A2NA), 2.34 (s, 3H (3.00H), CH 3 ). Melting point (TG-DTA): 203°C
From these analytical results, it was found that the product was the desired acetylated product (in reaction formula (16'), (e
)) was confirmed.
[塩素化]
次に、上記のようにして得られたアセチル化物(e)を以下のようにして塩素化した。
300mLナス型フラスコにアセチル化物(e)15.37g(49mmol)、塩化チ
オニル(30mL、300mmol)および触媒としてN,N-ジメチルホルムアミド(
DMF)5滴を入れ、窒素雰囲気中、80℃で3時間リフラックスして黄色透明溶液を得
た。反応後、共沸剤としてベンゼンを加え、塩化チオニルを共沸留去し、黄色粉末を析出
させた。これをシクロヘキサンから再結晶し、結晶を濾別して60℃で12時間真空乾燥
して黄色結晶を得た(収率78%)。
[Chlorination]
Next, the acetylated product (e) obtained as above was chlorinated as follows.
In a 300 mL eggplant-shaped flask, 15.37 g (49 mmol) of the acetylated product (e), thionyl chloride (30 mL, 300 mmol), and N,N-dimethylformamide (
The mixture was refluxed at 80°C for 3 hours in a nitrogen atmosphere to obtain a yellow transparent solution. After the reaction, benzene was added as an azeotropic agent to remove thionyl chloride by azeotropic distillation to precipitate a yellow powder. This was recrystallized from cyclohexane, and the crystals were filtered and dried in vacuum at 60°C for 12 hours to obtain yellow crystals (yield 78%).
この生成物の分析結果を以下に示す。FT-IR(KBrプレート法、cm-1):3
063(芳香族C-H伸縮)、1741(アセトキシ基+酸クロリド、C=O伸縮)。1
H-NMR(400MHz、CDCl3、δ、ppm):8.74(s、1H(1.04
H)、6-アセトキシ-2-ナフタレンカルボン酸クロリドユニット(6A2NC)の1
-プロトン)、8.08-8.02(m、2H(2.18H)、6A2NCの8-プロト
ン+3-プロトン)、7.88(d、1H(1.09H)、J=8.7Hz、6A2NC
の4-プロトン)、7.65(sd、1H(1.04H)、6A2NCの5-プロトン、
J=2.0Hz)、7.37(dd、1H(1.06H)、J=8.9、2.2Hz,6
A2NCの7-プロトン)、2.38(s、3H(3.00H)、CH3)。融点(TG
-DTA):127℃。これらの分析結果より、生成物は目的とする酸クロリド(反応式
(16’)中、(f))であることが確認された。
The analytical results of this product are as follows: FT-IR (KBr plate method, cm −1 ): 3
063 (aromatic C-H stretch), 1741 (acetoxy group + acid chloride, C=O stretch).
H-NMR (400 MHz, CDCl 3 , δ, ppm): 8.74 (s, 1H (1.04
H), 6-acetoxy-2-naphthalenecarboxylic acid chloride unit (6A2NC)
-proton), 8.08-8.02 (m, 2H (2.18H), 8-proton + 3-proton of 6A2NC), 7.88 (d, 1H (1.09H), J = 8.7 Hz, 6A2NC
4-proton of 6A2NC), 7.65 (sd, 1H (1.04H), 5-proton of 6A2NC,
J = 2.0 Hz), 7.37 (dd, 1H (1.06H), J = 8.9, 2.2 Hz, 6
A2NC 7-proton), 2.38 (s, 3H (3.00H), CH 3 ). Melting point (TG
-DTA): 127° C. From these analytical results, it was confirmed that the product was the desired acid chloride ((f) in reaction formula (16′)).
[ビスエステル化]
次に、上記のようにして得られた酸クロリド(f)と2,6-ジヒドロキシナフタレン
(g)よりエステル化反応を行った。
100mLナス型フラスコ中、2,6-ジヒドロキシナフタレン(g)4.80g(2
9.9mmol)を脱水処理済みのγ-ブチロラクトン(GBL)20mLに溶かし、こ
れに酸受容剤としてピリジン8mL(100mmol)を添加して、セプタムキャップで
密封してA液とした。次に500mLナス型フラスコ中、酸クロリド(f)16.93g
(68mmol)をGBL210mLに溶かし、セプタムキャップで密封してB液とした
。室温でB液を撹拌しながら、B液にA液をシリンジにて徐々に加え、12時間撹拌を続
けた。析出した沈殿物を濾別し、トルエン、次いでGBLで洗浄して過剰の酸クロリドを
除去し、最後に水で十分洗浄して副生成物であるピリジン塩酸塩を完全に除去した。これ
を160℃で12時間真空乾燥し、クリーム色の生成物を得た(収率82%)。
[Bisesterification]
Next, an esterification reaction was carried out using the acid chloride (f) obtained as described above and 2,6-dihydroxynaphthalene (g).
In a 100 mL eggplant-shaped flask, 4.80 g (2
9.9 mmol) was dissolved in 20 mL of dehydrated γ-butyrolactone (GBL), and 8 mL (100 mmol) of pyridine was added as an acid acceptor, and the mixture was sealed with a septum cap to obtain solution A. Next, in a 500 mL eggplant-shaped flask, 16.93 g of acid chloride (f) was added.
(68 mmol) was dissolved in 210 mL of GBL and sealed with a septum cap to obtain liquid B. While stirring liquid B at room temperature, liquid A was gradually added to liquid B using a syringe, and stirring was continued for 12 hours. The precipitate was filtered off, washed with toluene and then with GBL to remove excess acid chloride, and finally washed thoroughly with water to completely remove the by-product pyridine hydrochloride. This was vacuum dried at 160°C for 12 hours to obtain a cream-colored product (yield 82%).
上記反応の際、2,6-ジヒドロキシナフタレンの2つの末端ヒドロキシ基のうち、片
側のみ酸クロリドと反応したモノエステル化中間体(モノアセトキシ体)の溶媒溶解性が
著しく低い場合、目的とするビスエステル化体の生成と並行して、目的外のモノエステル
化中間体(モノアセトキシ体)の沈殿析出が同時に起こり、純粋なビスエステル化体(ジ
アセトキシ体)が得られなくなる。しかしながら、実際には、TLCで調べたところ、析
出した生成物中にモノエステル化中間体は含まれていなかった。これよりモノエステル化
中間体、ビスエステル化体共に十分な溶媒溶解性が確保されていたことが示唆される。こ
れは、2,6-ナフタレン構造の導入による予想外に大きな溶解性の促進効果によるもの
と考えられる。
In the above reaction, if the solvent solubility of the monoesterified intermediate (monoacetoxy body) in which only one of the two terminal hydroxy groups of 2,6-dihydroxynaphthalene has reacted with the acid chloride is extremely low, the precipitation of the unintended monoesterified intermediate (monoacetoxy body) occurs in parallel with the production of the desired bisesterified body, and a pure bisesterified body (diacetoxy body) cannot be obtained. However, in reality, when examined by TLC, the precipitated product did not contain the monoesterified intermediate. This suggests that both the monoesterified intermediate and the bisesterified body had sufficient solvent solubility. This is thought to be due to the unexpectedly large solubility-promoting effect of the introduction of the 2,6-naphthalene structure.
得られた生成物の分析結果を以下に示す。FT-IR(KBrプレート法、cm-1)
:3068(芳香族C-H伸縮)、1757(アセトキシ基+酸クロリド、C=O伸縮)
、1736(芳香族エステル基、C=O伸縮)。1H-NMR(400MHz、DMSO
-d6、δ、ppm):8.97(sd、2H(2.00H)、J=0.84Hz、末端
6-アセトキシ-2-ナフタレンカルボキシレートユニット(末端6A2NCE)の1,
1’-プロトン)、8.32(d、2H(1.97H)、J=9.2Hz、末端6A2N
CEの8,8’-プロトン)、8.22(dd、2H(1.91H)、J=8.6、1.
7Hz、末端6A2NCEの3,3’-プロトン)、8.15-8.10(m、4H(4
.04H)、末端6A2NCEの4,4’-プロトン+中央2,6-ナフタレンユニット
(中央26NA)の4,8-プロトン)、8.02(sd、2H(1.97H)、J=2
.4Hz、末端6A2NCEの5,5’-プロトン)、7.86(sd、2H(2.01
H)、J=2.4Hz、中央26NAの1,5-プロトン)、7.62(dd、2H(1
.95H)、J=8.9、2.4Hz,末端6A2NCEの7,7’-プロトン)、7.
50(dd、2H(1.97H)、J=8.8、2.3Hz、中央26NAの3,7-プ
ロトン)、2.37(s、6H(5.94H)、CH3)。融点(TG-DTA):22
0℃。これらの分析結果より、生成物は目的とする純粋なエステル基含有ジアセトキシ体
(反応式(16’)中、(h))であることが確認された。
The analytical results of the product obtained are shown below: FT-IR (KBr plate method, cm -1 )
: 3068 (aromatic C-H stretch), 1757 (acetoxy group + acid chloride, C=O stretch)
, 1736 (aromatic ester group, C=O stretch). 1 H-NMR (400 MHz, DMSO
-d 6 , δ, ppm): 8.97 (sd, 2H (2.00H), J = 0.84 Hz, 1 of terminal 6-acetoxy-2-naphthalenecarboxylate unit (terminal 6A2NCE),
1'-proton), 8.32 (d, 2H (1.97H), J = 9.2 Hz, terminal 6A2N
CE 8,8'-protons), 8.22 (dd, 2H (1.91H), J = 8.6, 1.
7 Hz, 3,3'-protons of terminal 6A2NCE), 8.15-8.10 (m, 4H(4
.04H), 4,4'-protons of terminal 6A2NCE + 4,8-protons of central 2,6-naphthalene unit (central 26NA), 8.02 (sd, 2H (1.97H), J = 2
.4 Hz, 5,5'-protons of terminal 6A2NCE), 7.86 (sd, 2H (2.01
H), J = 2.4 Hz, 1,5-proton at the center of 26 NA), 7.62 (dd, 2H (1
95H), J = 8.9, 2.4 Hz, 7,7'-protons of terminal 6A2NCE), 7.
50 (dd, 2H (1.97H), J=8.8, 2.3 Hz, 3,7-protons at the center of 26 NA), 2.37 (s, 6H (5.94H), CH 3 ). Melting point (TG-DTA): 22
0° C. From these analytical results, it was confirmed that the product was the desired pure ester group-containing diacetoxy compound ((h) in reaction formula (16′)).
[末端ジアセトキシ基の加水分解]
次に、上記のようにして得られたエステル基含有ジアセトキシ体(h)の末端ジアセト
キシ基を加水分解してビスフェノールを得る反応を以下のようにして行った。
[Hydrolysis of terminal diacetoxy groups]
Next, the terminal diacetoxy group of the ester group-containing diacetoxy compound (h) obtained as above was hydrolyzed to obtain bisphenol, as follows.
500mLナス型フラスコにエステル基含有ジアセトキシ体(h)4.55g(8.4
mmol)とN-メチル-2-ピロリドン(NMP)50mLを入れ、150℃に加熱し
て完全に溶解した。次にこれを0℃に冷却し、撹拌しながらこの溶液に濃アンモニア水(
28質量%)40mLをゆっくり加え、0℃で20分撹拌を続けた。反応終了後、この溶
液に1N塩酸60mLを加えて弱酸性とし、沈殿を析出させた。これを濾別し、水で十分
洗浄後。160℃で12時間真空乾燥してクリーム色の生成物を得た(収率94%)。
In a 500 mL eggplant-shaped flask, 4.55 g (8.4
The mixture was heated to 150°C and completely dissolved. The mixture was then cooled to 0°C and concentrated aqueous ammonia (
40 mL of 1N hydrochloric acid (28% by mass) was slowly added and the mixture was stirred at 0° C. for 20 minutes. After the reaction was completed, 60 mL of 1N hydrochloric acid was added to the solution to make it weakly acidic, causing a precipitate to form. The precipitate was separated by filtration and thoroughly washed with water. The mixture was vacuum-dried at 160° C. for 12 hours to obtain a cream-colored product (yield 94%).
この生成物の分析結果を以下に示す。FT-IR(KBrプレート法、cm-1):3
419(末端ヒドロキシ基、O-H伸縮)、3069(芳香族C-H伸縮)、1717(
エステル基、C=O伸縮)。1H-NMR(400MHz、DMSO-d6、δ、ppm
):10.33(s、2H(2.00H)、OH)、8.79(sd、2H(1.95H
)、J=1.4Hz、末端6-ヒドロキシ-2-ナフタレンカルボキシレートユニット(
末端6H2NCE)の1,1’-プロトン)、8.10-8.05(m、6H(5.94
H)、末端6H2NCEの8,8’-プロトン+3,3’-プロトン+4,4’-プロト
ン)、7.97(sd、2H(1.87H)、J=2.4Hz、末端6H2NCEの5,
5’-プロトン)、7.88(d、2H(1.99H)、J=8.8Hz、中央26NA
の4,8-プロトン)、7.58(dd、2H(1.98H)、J=8.5、2.5Hz
、末端6H2NCEの7,7’-プロトン)、7.27-7.22(m、4H(4.06
H)、中央26NAの1,5-プロトン+3,7-プロトン)。融点(TG-DTA):
328℃。これらの分析結果より、生成物は目的とするエステル基含有ビスフェノール(
反応式(16’)中、(i))であることが確認された。
The analytical results of this product are as follows: FT-IR (KBr plate method, cm −1 ): 3
419 (terminal hydroxyl group, O-H stretch), 3069 (aromatic C-H stretch), 1717 (
Ester group, C=O stretch). 1H -NMR (400MHz, DMSO- d6 , δ, ppm
): 10.33 (s, 2H (2.00H), OH), 8.79 (sd, 2H (1.95H)
), J = 1.4 Hz, terminal 6-hydroxy-2-naphthalenecarboxylate unit (
1,1'-protons of terminal 6H2NCE), 8.10-8.05 (m, 6H (5.94
H), 8,8'-protons + 3,3'-protons + 4,4'-protons of the terminal 6H2NCE), 7.97 (sd, 2H (1.87H), J = 2.4 Hz, 5,
5'-proton), 7.88 (d, 2H (1.99H), J = 8.8 Hz, central 26 NA
4,8-protons), 7.58 (dd, 2H (1.98H), J = 8.5, 2.5 Hz
, 7,7'-protons of terminal 6H2NCE), 7.27-7.22 (m, 4H (4.06
H), 1,5-proton + 3,7-proton of central 26NA). Melting point (TG-DTA):
From these analytical results, it was determined that the product was the desired ester group-containing bisphenol (
It was confirmed that the reaction was (i) in reaction formula (16').
[エステル基含有ビスフェノールとTMACとのエステル化反応]
次に、上記のようにして得られたエステル基含有ビスフェノール(i)とトリメリット
酸無水物クロリド(TMAC)のエステル化反応により、テトラカルボン酸二無水物を得
る反応を以下のようにして行った。
[Esterification reaction of ester group-containing bisphenol with TMAC]
Next, the ester group-containing bisphenol (i) obtained as above was subjected to an esterification reaction with trimellitic anhydride chloride (TMAC) to obtain a tetracarboxylic dianhydride, as described below.
100mLナス型フラスコ中、エステル基含有ビスフェノール(i)3.58g(7.
16mmol)を脱水処理済みのNMP20mLに溶かし、これに酸受容剤としてピリジ
ン5mL(63mmol)を添加して、セプタムキャップで密封してA液とした。次に2
00mLナス型フラスコ中、TMAC6.34g(30mmol)をNMP20mLに溶
かし、セプタムキャップで密封してB液とした。室温でB液を撹拌しながら、B液にA液
をシリンジにて徐々に加え、12時間撹拌を続けた。析出した沈殿物を濾別し、トルエン
、次いでGBLで洗浄して過剰の酸クロリドを除去し、最後に水で十分洗浄して副生成物
であるピリジン塩酸塩を完全に除去した。これを200℃で12時間真空乾燥し、薄茶色
の生成物を得た(収率68%)。
In a 100 mL eggplant-shaped flask, 3.58 g (7.
16 mmol) was dissolved in 20 mL of dehydrated NMP, and 5 mL (63 mmol) of pyridine was added as an acid acceptor. The mixture was sealed with a septum cap to obtain solution A.
In a 100 mL eggplant flask, 6.34 g (30 mmol) of TMAC was dissolved in 20 mL of NMP and sealed with a septum cap to obtain liquid B. While stirring liquid B at room temperature, liquid A was gradually added to liquid B using a syringe, and stirring was continued for 12 hours. The precipitate was filtered off, washed with toluene and then with GBL to remove excess acid chloride, and finally washed thoroughly with water to completely remove the by-product pyridine hydrochloride. This was vacuum dried at 200°C for 12 hours to obtain a light brown product (yield 68%).
上記反応に用いたエステル基含有ビスフェノールの溶媒溶解性が著しく低い場合、低濃
度でビスエステル化反応を行わざるを得なくなり、反応の効率、生成物の収率および純度
が著しく悪化する。しかし実際には、用いたエステル基含有ビスフェノールは十分に高い
溶媒溶解性を保持していたため、十分に高い濃度で上記反応を実施することが可能であっ
た。また、エステル基含有ビスフェノールの2つの末端ヒドロキシ基のうち、片側のみT
MACと反応したモノエステル化中間体の溶媒溶解性が著しく低い場合、目的とするビス
エステル化体の生成と同時にモノエステル化中間体の沈殿析出が起こり、純粋な目的物が
得られなくなる。しかし実際には、生成物中にモノエステル化中間体は含まれていなかっ
た。これより、モノエステル化中間体は十分に高い溶媒溶解性を保持していたことが示唆
される。これは、2,6-ナフタレン構造の導入による予想外に大きな溶解性の促進効果
によるものと考えられる。
When the ester group-containing bisphenol used in the above reaction has a significantly low solvent solubility, the bisesterification reaction must be carried out at a low concentration, which significantly reduces the reaction efficiency, product yield, and purity. However, in reality, the ester group-containing bisphenol used had a sufficiently high solvent solubility, so the above reaction could be carried out at a sufficiently high concentration. In addition, only one of the two terminal hydroxyl groups of the ester group-containing bisphenol was T.
When the solvent solubility of the monoesterified intermediate reacted with MAC is extremely low, precipitation of the monoesterified intermediate occurs simultaneously with the production of the desired bisesterified product, making it impossible to obtain a pure target product. However, in reality, the product did not contain the monoesterified intermediate. This suggests that the monoesterified intermediate retained sufficiently high solvent solubility. This is thought to be due to the unexpectedly large solubility enhancing effect of the introduction of the 2,6-naphthalene structure.
得られた生成物の分析結果を以下に示す。FT-IR(KBrプレート法、cm-1)
:3065(芳香族C-H伸縮)、1858/1784(酸無水物基、C=O伸縮)、1
737(エステル基、C=O伸縮)。1H-NMR(400MHz、DMSO-d6、δ
、ppm):9.04(sd、2H(2.00H)、J=1.8Hz、6H2NCEの1
,1’-プロトン)、8.73-8.70(m、4H(4.17H)、末端無水フタル酸
ユニット(PAn)の3,3’-プロトン+6,6’-プロトン)、8.42(d、2H
(1.83H)、J=8.6Hz、6H2NCEの8,8’-プロトン)、8.33(d
d、2H(1.65H)、J=7.7、0.8Hz、PAnの5,5’-プロトン)、8
.27(dd、2H(2.37H)、J=8.4、1.7Hz、6H2NCEの3,3’
-プロトン)、8.21(d、2H(2.18H)、J=8.6Hz、6H2NCEの4
,4’-プロトン)、8.14-8.12(m、4H(3.88H)、6H2NCEの5
,5’-プロトン+中央26NAの1,5-プロトン)、8.04(d、2H(2.14
H)、J=8.6Hz、中央26NAの4,8-プロトン)、7.77(dd、2H(1
.74H)、J=8.7、2.1Hz、6H2NCEの7,7’-プロトン)、7.65
(dd、2H(2.38H)、J=8.6、2.1Hz、中央26NAの3,7-プロト
ン)。元素分析(C50H24O14、分子量848.73):推定値C;70.76%
、H;2.85%、分析値C;70.61%、H;3.06%。融点(TG-DTA):
284℃。これらの分析結果より、生成物は下記式(15)で表される目的とするテトラ
カルボン酸二無水物(反応式(16’)中、(j))であることが確認された。
: 3065 (aromatic C-H stretch), 1858/1784 (anhydride group, C=O stretch), 1
737 (ester group, C=O stretch). 1 H-NMR (400 MHz, DMSO-d 6 , δ
, ppm): 9.04 (sd, 2H (2.00H), J = 1.8 Hz, 6H2NCE
, 1'-proton), 8.73-8.70 (m, 4H (4.17H), 3,3'-proton + 6,6'-proton of terminal phthalic anhydride unit (PAn), 8.42 (d, 2H
(1.83H), J = 8.6 Hz, 8,8'-protons of 6H2NCE), 8.33 (d
d, 2H (1.65H), J = 7.7, 0.8 Hz, 5,5'-protons of PAn), 8
. 27 (dd, 2H (2.37H), J = 8.4, 1.7 Hz, 6H2NCE 3,3'
-proton), 8.21 (d, 2H (2.18H), J = 8.6 Hz, 6H2NCE 4
, 4'-proton), 8.14-8.12 (m, 4H (3.88H), 6H2NCE 5
, 5'-proton + 1,5-proton of central 26NA), 8.04 (d, 2H (2.14
H), J = 8.6 Hz, 4,8-protons at the center of 26 NA), 7.77 (dd, 2H (1
. 74H), J = 8.7, 2.1 Hz, 7,7'-protons of 6H2NCE), 7.65
(dd, 2H (2.38H), J=8.6, 2.1 Hz, 3,7-protons at center 26 NA). Elemental analysis (C 50 H 24 O 14 , molecular weight 848.73): Estimated C; 70.76%
, H; 2.85%, Analysis value C; 70.61%, H; 3.06%. Melting point (TG-DTA):
284° C. From these analytical results, it was confirmed that the product was the target tetracarboxylic dianhydride represented by the following formula (15) ((j) in reaction formula (16′)).
[実施例2:7環型TCDAモノマーの合成]
2,6-ジヒドロキシナフタレン(g)の代わりに、ハイドロキノンを用いた以外は、
上記反応式(16’)に準じて、実施例2のテトラカルボン酸二無水物を合成した。実施
例2においても、エステル基含有ビスフェノールを合成する工程や、これとTMACと反
応させてテトラカルボン酸二無水物を合成する工程において、好ましくないモノエステル
化中間体の沈殿析出は見られなかった。これは実施例1の場合と同様に、2,6-ナフタ
レン構造導入による予想外に大きな溶解性の促進効果によるものと考えられる。
[Example 2: Synthesis of 7-ring TCDA monomer]
Except for using hydroquinone instead of 2,6-dihydroxynaphthalene (g),
The tetracarboxylic dianhydride of Example 2 was synthesized according to the above reaction formula (16'). In Example 2, too, no undesirable precipitation of monoesterified intermediates was observed in the step of synthesizing the ester group-containing bisphenol or in the step of reacting the bisphenol with TMAC to synthesize the tetracarboxylic dianhydride. This is thought to be due to the unexpectedly large solubility enhancing effect of the introduction of the 2,6-naphthalene structure, as in the case of Example 1.
得られた生成物の分析結果を以下に示す。FT-IR(KBrプレート法、cm-1)
:3072(芳香族C-H伸縮)、1853/1779(酸無水物基、C=O伸縮)、1
742(エステル基、C=O伸縮)。1H-NMR(400MHz、DMSO-d6、δ
、ppm):8.99(s、2H(2.13H)、6H2NCEの1,1’-プロトン)
、8.73-8.69(m、4H(3.86H)、PAnの3,3’-プロトン+6,6
’-プロトン)、8.41(d、2H(2.07H)、J=9.0Hz、6H2NCEの
8,8’-プロトン)、8.33(dd、2H(2.22H)、J=7.8、0.7Hz
、PAnの5,5’-プロトン)、8.25-8.2(m、4H(4.19H)、6H2
NCEの3,3’-プロトン+4,4’-プロトン)、8.14(sd、2H(2.12
H)、J=1.9Hz、6H2NCEの5,5’-プロトン)、7.76(dd、2H(
2.11H)、J=8.7、2.3Hz、6H2NCEの7,7’-プロトン)、7.5
2(s、4H(4.00H)、中央ハイドロキノンユニットの2,3,5,6-プロトン
)。元素分析(C46H22O14、分子量798.67):推定値C;69.18%、
H;2.78%、分析値C;68.78%、H;3.13%。融点(DSC):306℃
。これらの分析結果より、生成物は下記式(17)で表される目的とするテトラカルボン
酸二無水物であることが確認された。
: 3072 (aromatic C-H stretch), 1853/1779 (anhydride group, C=O stretch), 1
742 (ester group, C=O stretch). 1 H-NMR (400 MHz, DMSO-d 6 , δ
, ppm): 8.99 (s, 2H (2.13H), 1,1'-protons of 6H2NCE)
, 8.73-8.69 (m, 4H (3.86H), 3,3'-protons of PAn + 6,6
'-protons), 8.41 (d, 2H (2.07H), J = 9.0 Hz, 8,8'-protons of 6H2NCE), 8.33 (dd, 2H (2.22H), J = 7.8, 0.7 Hz
, 5,5'-protons of PAn), 8.25-8.2 (m, 4H (4.19H), 6H2
3,3'-protons + 4,4'-protons of NCE), 8.14 (sd, 2H (2.12
H), J = 1.9 Hz, 5,5'-protons of 6H2NCE), 7.76 (dd, 2H(
2.11H), J = 8.7, 2.3 Hz, 7,7'-protons of 6H2NCE), 7.5
2 (s, 4H (4.00H), 2,3,5,6-protons of the central hydroquinone unit). Elemental analysis (C 46 H 22 O 14 , molecular weight 798.67): Estimated value C; 69.18%,
H: 2.78%, Analysis C: 68.78%, H: 3.13%. Melting point (DSC): 306°C
From these analytical results, it was confirmed that the product was the desired tetracarboxylic dianhydride represented by the following formula (17).
[比較例1:2,6-ナフタレン構造を有しない8環型TCDAモノマーの合成]
4,4’-ビフェノールと4-(4-アセトキシフェニル)安息香酸クロリドより、ビ
スエステル化反応により6環の芳香環を有するエステル基含有ジアセトキシ体を合成し、
次いでこの末端ジアセトキシ基を加水分解してビスフェノールに変換した後、これとTM
ACより、全8環のテトラカルボン酸二無水物を合成することを試みた。しかしながら、
最初のビスエステル化反応の際、析出した生成物は、目的外の片側モノエステル化中間体
(モノアセトキシ体)が主成分であり、目的とする6環のエステル基含有ビスアセトキシ
体を得ることは困難であった。これは片側モノエステル化中間体(モノアセトキシ体)の
溶媒溶解性が著しく低いためである。
[Comparative Example 1: Synthesis of 8-ring TCDA monomer not having a 2,6-naphthalene structure]
A diacetoxy compound containing an ester group and a six-ring aromatic ring is synthesized by a bis-esterification reaction of 4,4'-biphenol and 4-(4-acetoxyphenyl)benzoic acid chloride.
The terminal diacetoxy group is then hydrolyzed to convert it into bisphenol, which is then mixed with TM
We attempted to synthesize a tetracarboxylic dianhydride having eight rings from AC. However,
In the first bis-esterification reaction, the precipitated product was mainly composed of an undesired one-side monoesterified intermediate (monoacetoxy compound), and it was difficult to obtain the desired bis-acetoxy compound containing a six-ring ester group, because the one-side monoesterified intermediate (monoacetoxy compound) has extremely low solubility in solvents.
<ポリエステルイミド前駆体の重合、熱イミド化およびポリエステルイミドフィルム特性
評価>
[実施例3:8環型TCDA/p-PDA系ポリエステルイミドフィルムの作製および評価]
実施例1に記載の上記式(15)で表されるテトラカルボン酸二無水物とp-フェニレ
ンジアミン(p-PDA)より以下のようにしてポリエステルイミド前駆体を重合した。
<Polymerization of polyesterimide precursor, thermal imidization, and evaluation of polyesterimide film properties>
[Example 3: Preparation and evaluation of 8-ring TCDA/p-PDA-based polyesterimide film]
A polyesterimide precursor was polymerized from the tetracarboxylic dianhydride represented by the above formula (15) described in Example 1 and p-phenylenediamine (p-PDA) in the following manner.
よく乾燥した密閉反応容器中、p-PDA(2mmol)をモレキュラーシーブス4A
で脱水処理済みのNMPに溶かし、マグネチックスターラーで撹拌しながら、この溶液に
実施例1に記載のテトラカルボン酸二無水物粉末(2mmol)を加え撹拌を続けた(初
期全固形分濃度:30質量%)。重合が進むにつれて溶液粘度が増加し、十分に撹拌でき
なくなったため、適宜NMPを追加し、最終的に室温で141時間撹拌して均一で粘稠な
ポリエステルイミド前駆体ワニスを得た(最終全固形分濃度:15.9質量%)。NMP
中、30℃、0.5質量%の濃度でオストワルド粘度計にて測定したポリエステルイミド前駆体の還元粘度は1.24dL/gであり、十分に高分子量体のポリエステルイミド前駆体が得られた。
In a well-dried sealed reaction vessel, p-PDA (2 mmol) was filtered through molecular sieves 4A.
The tetracarboxylic dianhydride powder (2 mmol) described in Example 1 was added to this solution while stirring with a magnetic stirrer, and stirring was continued (initial total solids concentration: 30% by mass). As the polymerization proceeded, the viscosity of the solution increased and it became impossible to stir sufficiently, so NMP was added appropriately, and finally, the solution was stirred at room temperature for 141 hours to obtain a uniform and viscous polyesterimide precursor varnish (final total solids concentration: 15.9% by mass).
The reduced viscosity of the polyesterimide precursor measured at 30° C. and a concentration of 0.5% by mass using an Ostwald viscometer was 1.24 dL/g, and a polyesterimide precursor with a sufficiently high molecular weight was obtained.
このポリエステルイミド前駆体ワニスをガラス基板に塗布し、熱風乾燥器中80℃で3
時間乾燥してポリエステルイミド前駆体のキャストフィルムを得た。これをガラス基板ご
と電気炉に入れ、250℃で1時間、更に350℃で1時間、真空中で段階的に昇温し加
熱して熱イミド化を行った。残留応力を除去するため、フィルムをガラス基板から剥がし
て更に真空中350℃で1時間熱処理を行い、膜厚25μmの濁りのない可撓性のポリエ
ステルイミドフィルムを得た。上述の方法に従い、得られたフィルムの物性値を測定した
。
This polyesterimide precursor varnish was applied to a glass substrate and dried in a hot air dryer at 80° C. for 3 hours.
The film was then dried for 1 hour to obtain a cast film of polyesterimide precursor. The film was placed together with the glass substrate in an electric furnace and heated in a vacuum at 250°C for 1 hour and then at 350°C for 1 hour to perform thermal imidization. To remove residual stress, the film was peeled off from the glass substrate and further heat-treated in a vacuum at 350°C for 1 hour to obtain a clear, flexible polyesterimide film with a thickness of 25 μm. The physical properties of the obtained film were measured according to the above-mentioned methods.
別途、薄膜試料を用いて熱イミド化前後の赤外線吸収スペクトルを測定した。熱イミド
化処理により、ポリエステルイミド前駆体由来の1680および1530cm-1付近の
アミド基C=O伸縮振動吸収バンドが完全に消えていることから、この加熱条件で熱イミ
ド化反応が完結することが確認された。
Separately, infrared absorption spectra were measured for the thin film sample before and after thermal imidization. The thermal imidization treatment completely eliminated the amide group C=O stretching vibration absorption bands at around 1680 and 1530 cm -1 derived from the polyesterimide precursor, confirming that the thermal imidization reaction was completed under these heating conditions.
実施例3のポリエステルイミドフィルム(膜厚25μm)は非常に高いガラス転移温度
(371℃)に加え、極めて低い線熱膨張係数(3.8pm/K)を有していた。機械的
特性を評価した結果、引張弾性率(ヤング率)は7.70GPaであり、超高弾性率を示
した。観測された超低熱膨張性と高弾性は、テトラカルボン酸二無水物、ジアミン共に剛
直な構造のモノマーを用いたことによるポリエステルイミド主鎖の剛直かつ直線性と熱イ
ミド化によって誘起された主鎖の高度な面内配向によるものと考えられる。5%重量減少
温度は窒素中で467℃であり、十分に高い化学的耐熱性(長期耐熱性)も保持していた
。また、実施例3のポリエステルイミドフィルムは非常に低い吸水率(0.26%)を示
した。これは、2,6-ナフタレン構造を導入して長手方向に増環および延長した新規な
テトラカルボン酸二無水物を用いたことで、ポリエステルイミド構造中に含まれるモル分
極の高いイミド基の含有率が劇的に減少したことによるものと考えられる。更に10GH
zにおける誘電率は3.20、誘電正接は0.00246であった。この誘電正接は、液
晶ポリエステルに匹敵するほど、低い値であった。表1に物性値をまとめる。このように
、実施例3のポリエステルイミドフィルムは高速通信FPC用耐熱絶縁フィルム材に適し
た特性を有していた。なお、表1中、評価が行われなかった項目は空欄とした。
The polyesterimide film of Example 3 (film thickness 25 μm) had a very high glass transition temperature (371° C.) and an extremely low linear thermal expansion coefficient (3.8 pm/K). As a result of evaluating the mechanical properties, the tensile modulus (Young's modulus) was 7.70 GPa, indicating an ultra-high modulus of elasticity. The observed ultra-low thermal expansion and high elasticity are believed to be due to the rigidity and linearity of the polyesterimide main chain due to the use of monomers with rigid structures, both the tetracarboxylic dianhydride and the diamine, and the high degree of in-plane orientation of the main chain induced by thermal imidization. The 5% weight loss temperature was 467° C. in nitrogen, and the film also retained sufficiently high chemical heat resistance (long-term heat resistance). In addition, the polyesterimide film of Example 3 showed a very low water absorption rate (0.26%). This is believed to be due to the use of a novel tetracarboxylic dianhydride in which the ring is increased and extended in the longitudinal direction by introducing a 2,6-naphthalene structure, dramatically reducing the content of imide groups with high molar polarization contained in the polyesterimide structure. Furthermore, the 10 GH
The dielectric constant at z was 3.20, and the dielectric loss tangent was 0.00246. This dielectric loss tangent was a low value comparable to that of liquid crystal polyester. The physical properties are summarized in Table 1. Thus, the polyesterimide film of Example 3 had properties suitable for use as a heat-resistant insulating film material for high-speed communication FPC. In Table 1, items that were not evaluated are left blank.
[実施例4:8環型TCDA/4,4’-ODA系ポリエステルイミドフィルムの作製および評価]
ジアミンとしてp-PDAの代わりに4,4’-オキシジアニリン(4,4’-ODA
)を用いた以外は、実施例3に記載した方法と同様にして、ポリエステルイミド前駆体を
重合、キャスト製膜、熱イミド化してポリエステルイミドフィルムを作製し、フィルム特
性を評価した。実施例3に記載のポリエステルイミドフィルムと同様に非常に低い吸水率
(0.27%)を有していた。また、誘電正接は実施例3に記載のポリエステルイミドフ
ィルムよりも更に減少した極めて低い値(0.00170)であった。
[Example 4: Preparation and evaluation of 8-ring TCDA/4,4'-ODA based polyesterimide film]
As a diamine, 4,4'-oxydianiline (4,4'-ODA) was used instead of p-PDA.
A polyesterimide film was prepared by polymerization of the polyesterimide precursor, cast film formation, and thermal imidization in the same manner as in Example 3, except that a polyesterimide precursor was used, and the film properties were evaluated. The polyesterimide film had a very low water absorption (0.27%) like the polyesterimide film described in Example 3. The dielectric loss tangent was an extremely low value (0.00170), which was even lower than that of the polyesterimide film described in Example 3.
[実施例5:7環型TCDA/p-PDA系ポリエステルイミドフィルムの作製および評価]
実施例1に記載の上記式(15)で表されるテトラカルボン酸二無水物の代わりに、実
施例2に記載の上記式(17)で表されるテトラカルボン酸二無水物を用いた以外は、実
施例3に記載した方法と同様にして、ポリエステルイミド前駆体を重合、キャスト製膜、
熱イミド化してポリエステルイミドフィルムを作製し、フィルム特性を評価した。実施例
3に記載のポリエステルイミドフィルムと同様に優れた特性を有していた。図1に熱イミ
ド化前の薄膜試料(ポリエステルイミド前駆体のフィルム)の赤外線吸収スペクトルを、
図2に熱イミド化後の薄膜試料(ポリエステルイミドフィルム)の赤外線吸収スペクトル
を示す。
[Example 5: Preparation and evaluation of 7-ring TCDA/p-PDA-based polyesterimide film]
A polyesterimide precursor was polymerized and cast into a film in the same manner as in Example 3, except that the tetracarboxylic dianhydride represented by the formula (17) in Example 2 was used instead of the tetracarboxylic dianhydride represented by the formula (15) in Example 1.
A polyesterimide film was prepared by thermal imidization, and the film properties were evaluated. The film had excellent properties similar to those of the polyesterimide film described in Example 3. FIG. 1 shows the infrared absorption spectrum of the thin film sample (film of polyesterimide precursor) before thermal imidization.
FIG. 2 shows the infrared absorption spectrum of the thin film sample (polyesterimide film) after thermal imidization.
[実施例6:7環型TCDA/4,4’-ODA系ポリエステルイミドフィルムの作製および評価]
テトラカルボン酸二無水物として実施例2に記載の上記式(17)で表されるテトラカ
ルボン酸二無水物、ジアミンとして4,4’-ODAを用いた以外は、実施例3に記載し
た方法と同様にして、ポリエステルイミド前駆体を重合、キャスト製膜、熱イミド化して
ポリエステルイミドフィルムを作製し、フィルム特性を評価した。実施例4に記載のポリ
エステルイミドフィルムと同様に、低吸水率、低誘電正接の点で優れた特性を有していた
。
[Example 6: Preparation and evaluation of 7-ring TCDA/4,4′-ODA-based polyesterimide film]
A polyesterimide film was prepared by polymerization of a polyesterimide precursor, cast film formation, and thermal imidization in the same manner as in Example 3, except that the tetracarboxylic dianhydride represented by the above formula (17) described in Example 2 was used as the tetracarboxylic dianhydride and 4,4'-ODA was used as the diamine, and the film properties were evaluated. As with the polyesterimide film described in Example 4, the film had excellent properties in terms of low water absorption and low dielectric loss tangent.
[比較例2:TA-HQ/p-PDA系ポリエステルイミドフィルムの作製および評価]
テトラカルボン酸二無水物として、全3環型のエステル基含有テトラカルボン酸二無水
物:1,4-フェニレンビス(トリメリテート アンハイドライド)(TA-HQ)、ジ
アミンとしてp-PDAを用いた以外は、実施例3に記載した方法と同様にして、ポリエ
ステルイミド前駆体を重合、キャスト製膜、熱イミド化してポリエステルイミドフィルム
を作製し、いくつかのフィルム特性を測定した。比較例2のフィルムの吸水率は、Kap
ton(R)Hフィルムの値(2.5%)よりは低かったが、依然として高い値であった
。これは用いたTA-HQの増環が不十分で芳香環数が少ない上、2,6-ナフタレン構
造を含んでいないため、得られたポリエステルイミド構造中のイミド基含有率が依然とし
て高いためである。
Comparative Example 2: Preparation and Evaluation of TA-HQ/p-PDA-Based Polyesterimide Film
A polyesterimide film was prepared by polymerizing a polyesterimide precursor, casting the precursor, and thermally imidizing the precursor in the same manner as in Example 3, except that a tetracarboxylic dianhydride containing ester groups having a total of three rings, 1,4-phenylenebis(trimellitate anhydride) (TA-HQ), was used as the tetracarboxylic dianhydride, and p-PDA was used as the diamine. Some of the film properties were measured. The water absorption rate of the film in Comparative Example 2 was Kap
Although the value was lower than that of the ton (R) H film (2.5%), it was still high. This is because the ring multiplication of the TA-HQ used was insufficient, resulting in a small number of aromatic rings, and because it did not contain a 2,6-naphthalene structure, the imide group content in the obtained polyesterimide structure was still high.
[実施例2a:6環型TCDAモノマーの合成]
アセチル化物(e)(6-アセトキシ-2-ナフタレンカルボン酸)の代わりに、4-アセトキシ安息香酸を用いた以外は、上記反応式(16’)に準じて、実施例2aのテトラカルボン酸二無水物を合成した。実施例2aにおいても、実施例1および2と同様に、好ましくないモノエステル化中間体の沈殿析出は見られなかった。
[Example 2a: Synthesis of 6-ring TCDA monomer]
The tetracarboxylic dianhydride of Example 2a was synthesized according to the above reaction formula (16'), except that 4-acetoxybenzoic acid was used instead of the acetylated compound (e) (6-acetoxy-2-naphthalenecarboxylic acid). In Example 2a, as in Examples 1 and 2, no undesirable precipitation of monoesterified intermediates was observed.
得られた生成物の分析結果を以下に示す。FT-IR(KBrプレート法、cm-1):3111/3068(芳香族C-H伸縮)、1860/1781(酸無水物基、C=O伸縮)、1747/1736(エステル基、C=O伸縮)、1509(1,4-フェニレン)。1H-NMR(400MHz、DMSO-d6、δ、ppm):8.70-8.68(m、4H(4.04H)、PAnの3,3’-プロトン+6,6’-プロトン)、8.35(d、4H(3.92H)、J=8.9Hz、オキシベンゾエート(OBA)ユニットの2,2’,6,6’-プロトン)、8.31(dd、2H(2.11H)、J=7.6、1.0Hz、PAnの5,5’-プロトン)、8.10(d、2H(2.13H)、J=8.8Hz、中央ナフタレン(NA)の4,8-プロトン)、7.98(sd、2H(2.00H)、J=2.4Hz、NAの1,5-プロトン)、7.70(d、4H(3.86H)、J=8.8Hz、OBAの3,3’,5,5’-プロトン)、7.60(dd、2H(1.93H)、J=8.8、2.6Hz、NAの3,7-プロトン)。元素分析(C42H20O14、分子量748.61):推定値C;67.39%、H;2.69%、分析値C;67.71%、H;2.89%。融点(DSC):283℃。これらの分析結果より、生成物は下記式(18)で表される目的とするテトラカルボン酸二無水物であることが確認された。
[比較例3:PMDA/4,4’-ODA系ポリイミドフィルムの作製および評価]
汎用のモノマーであるピロメリット酸二無水物(PMDA)と4,4’-オキシジアニリン(4,4’-ODA)を用いた以外は、実施例3に記載の方法に準じて重合し、ポリアミド酸の均一なワニスを得た後、これをキャスト製膜し、熱イミド化してポリイミドフィルムを作製し、いくつかのフィルム特性を測定した。10GHzにおける誘電率は3.17、誘電正接は0.01140であった。このように非常に高い誘電正接値を示したことから、比較例3に示したような従来のポリイミドフィルムは、高速通信FPC用耐熱絶縁フィルム材に適していないことがわかる。
Comparative Example 3: Preparation and Evaluation of PMDA/4,4'-ODA-Based Polyimide Film
Except for using pyromellitic dianhydride (PMDA) and 4,4'-oxydianiline (4,4'-ODA), which are general-purpose monomers, polymerization was performed in accordance with the method described in Example 3 to obtain a uniform varnish of polyamic acid, which was then cast into a film and thermally imidized to produce a polyimide film, and several film properties were measured. The dielectric constant at 10 GHz was 3.17 and the dielectric loss tangent was 0.01140. Since such a very high dielectric loss tangent value was shown, it can be seen that the conventional polyimide film shown in Comparative Example 3 is not suitable as a heat-resistant insulating film material for high-speed communication FPCs.
[実施例7:8環型TDCA/APAB系ポリエステルイミドフィルムの作製および評価]
上記式(15)で表される実施例1に記載のテトラカルボン酸二無水物と、ジアミンとして4-アミノフェニル4-アミノベンゾエート(APAB)を用い、実施例3に記載の方法に従って重合し、ポリアミド酸の均一なワニスを得た後、これをキャスト製膜し、熱イミド化してポリエステルイミドフィルムを作製し、フィルム特性を評価した。このポリエステルイミドフィルムは実施例3~6に記載のポリエステルイミドフィルムと同様に、高耐熱性、低吸水率、低誘電正接の点で非常に優れた特性を有していた。表2に物性値をまとめる。なお、表2中、評価が行われなかった項目は空欄とした。
[Example 7: Preparation and evaluation of 8-ring TDCA/APAB-based polyesterimide film]
The tetracarboxylic dianhydride described in Example 1, represented by the above formula (15), and 4-aminophenyl 4-aminobenzoate (APAB) as a diamine were polymerized according to the method described in Example 3 to obtain a uniform varnish of polyamic acid, which was then cast into a film and thermally imidized to produce a polyesterimide film, and the film properties were evaluated. This polyesterimide film had very excellent properties in terms of high heat resistance, low water absorption, and low dielectric tangent, similar to the polyesterimide films described in Examples 3 to 6. Table 2 summarizes the physical properties. In Table 2, items that were not evaluated are left blank.
[実施例8:8環型TDCA/ATAB系ポリエステルイミドフィルムの作製および評価]
上記式(15)で表される実施例1に記載のテトラカルボン酸二無水物と、ジアミンとして4-アミノ-2-メチルフェニル4-アミノベンゾエート(ATAB)を用い、実施例3に記載の方法に従って重合し、ポリアミド酸の均一なワニスを得た後、これをキャスト製膜し、熱イミド化してポリエステルイミドフィルムを作製し、フィルム特性を評価した。このポリエステルイミドフィルムは実施例3~7に記載のポリエステルイミドフィルムと同様に、高耐熱性、低吸水率、低誘電正接の点で非常に優れた特性を有していた。図3に熱イミド化前の薄膜試料(ポリエステルイミド前駆体のフィルム)の赤外線吸収スペクトルを、図4に熱イミド化後の薄膜試料(ポリエステルイミドフィルム)の赤外線吸収スペクトルを示す。
[Example 8: Preparation and evaluation of 8-ring TDCA/ATAB-based polyesterimide film]
The tetracarboxylic dianhydride described in Example 1, represented by the above formula (15), and 4-amino-2-methylphenyl 4-aminobenzoate (ATAB) as a diamine were polymerized according to the method described in Example 3 to obtain a uniform varnish of polyamic acid, which was then cast into a film and thermally imidized to produce a polyesterimide film, and the film properties were evaluated. This polyesterimide film had excellent properties in terms of high heat resistance, low water absorption, and low dielectric tangent, similar to the polyesterimide films described in Examples 3 to 7. Figure 3 shows the infrared absorption spectrum of the thin film sample (film of polyesterimide precursor) before thermal imidization, and Figure 4 shows the infrared absorption spectrum of the thin film sample (polyesterimide film) after thermal imidization.
[実施例9:8環型TCDA/ATAB(70);BAPP(30)コポリマー系ポリエステルイミドフィルムの作製および評価]
上記式(15)で表される実施例1に記載のテトラカルボン酸二無水物と、ジアミンとして4-アミノ-2-メチルフェニル4-アミノベンゾエート(ATAB)(70mol%)および2,2-ビス[4-(4-アミノフェノキシ)フェニル]プロパン(BAPP)(30mol%)を用い、実施例3に記載の方法に従って重合し、ポリアミド酸の均一なワニスを得た後、これをキャスト製膜し、熱イミド化してポリエステルイミドフィルムを作製し、フィルム特性を評価した。このポリエステルイミドフィルムは実施例3~8に記載のポリエステルイミドフィルムと同様に、高耐熱性、低吸水率、低誘電正接の点で非常に優れた特性を有していた。
[Example 9: Preparation and evaluation of 8-ring TCDA/ATAB(70);BAPP(30) copolymer-based polyesterimide film]
The tetracarboxylic dianhydride described in Example 1, represented by the above formula (15), and 4-amino-2-methylphenyl 4-aminobenzoate (ATAB) (70 mol%) and 2,2-bis[4-(4-aminophenoxy)phenyl]propane (BAPP) (30 mol%) as diamines were polymerized according to the method described in Example 3 to obtain a uniform varnish of polyamic acid, which was then cast into a film and thermally imidized to produce a polyesterimide film, and the film properties were evaluated. This polyesterimide film had excellent properties in terms of high heat resistance, low water absorption, and low dielectric tangent, similar to the polyesterimide films described in Examples 3 to 8.
[実施例10:6環型TCDA/p-PDA系ポリエステルイミドフィルムの作製および評価]
上記式(18)で表される実施例2aに記載のテトラカルボン酸二無水物と、p-フェニレンジアミン(p-PDA)を用い、実施例3に記載の方法に従って重合し、ポリアミド酸の均一なワニスを得た後、これをキャスト製膜し、熱イミド化してポリエステルイミドフィルムを作製し、フィルム特性を評価した。このポリエステルイミドフィルムは実施例3~9に記載のポリエステルイミドフィルムと同様に、高耐熱性、低吸水率、低誘電正接の点で非常に優れた特性を有していた。
[Example 10: Preparation and evaluation of 6-ring TCDA/p-PDA-based polyesterimide film]
The tetracarboxylic dianhydride described in Example 2a, represented by the above formula (18), and p-phenylenediamine (p-PDA) were polymerized according to the method described in Example 3 to obtain a uniform varnish of polyamic acid, which was then cast into a film and thermally imidized to produce a polyesterimide film, and the film properties were evaluated. This polyesterimide film had excellent properties in terms of high heat resistance, low water absorption, and low dielectric tangent, similar to the polyesterimide films described in Examples 3 to 9.
[実施例11:6環型TCDA/4,4’-ODA系ポリエステルイミドフィルムの作製および評価]
上記式(18)で表される実施例2aに記載のテトラカルボン酸二無水物と、4,4’-ODAを用い、実施例3に記載の方法に従って重合を行い、ポリアミド酸の均一なワニスを得た後、これをキャスト製膜し、熱イミド化してポリエステルイミドフィルムを作製し、フィルム特性を評価した。このポリエステルイミドフィルムは実施例3~10に記載のポリエステルイミドフィルムと同様に、高耐熱性、低吸水率、低誘電正接の点で非常に優れた特性を有していた。
[Example 11: Preparation and evaluation of 6-ring TCDA/4,4'-ODA based polyesterimide film]
The tetracarboxylic dianhydride represented by formula (18) and described in Example 2a and 4,4'-ODA were polymerized according to the method described in Example 3 to obtain a uniform varnish of polyamic acid, which was then cast into a film and thermally imidized to produce a polyesterimide film, and the film properties were evaluated. This polyesterimide film had excellent properties in terms of high heat resistance, low water absorption, and low dielectric tangent, similar to the polyesterimide films described in Examples 3 to 10.
[実施例12:6環型TCDA/p-PDA(75);4,4’-ODA(25)コポリマー系ポリエステルイミドフィルムの作製および評価]
上記式(18)で表される実施例2aに記載のテトラカルボン酸二無水物と、p-PDA(75mol%)および4,4’-ODA(25mol%)を用い、実施例3に記載の方法に従って重合を行い、ポリアミド酸の均一なワニスを得た後、これをキャスト製膜し、熱イミド化してポリエステルイミドフィルムを作製し、フィルム特性を評価した。このポリエステルイミドフィルムは実施例3~11に記載のポリエステルイミドフィルムと同様に、高耐熱性、低吸水率、低誘電正接の点で非常に優れた特性を有していた。
[Example 12: Preparation and evaluation of 6-ring TCDA/p-PDA (75); 4,4′-ODA (25) copolymer-based polyesterimide film]
The tetracarboxylic dianhydride described in Example 2a, represented by the above formula (18), p-PDA (75 mol%) and 4,4'-ODA (25 mol%) were used to polymerize in accordance with the method described in Example 3 to obtain a uniform varnish of polyamic acid, which was then cast into a film and thermally imidized to produce a polyesterimide film, whose film properties were evaluated. This polyesterimide film had excellent properties in terms of high heat resistance, low water absorption and low dielectric tangent, similar to the polyesterimide films described in Examples 3 to 11.
Claims (9)
前記一般式(1)中、Ar1が、下記式(2)~(6):
テトラカルボン酸二無水物。 The following general formula (1):
In the general formula (1), Ar 1 is represented by the following formulas (2) to (6):
Tetracarboxylic dianhydride.
前記一般式(7)中、Ar1は前記式(2)~(6)のいずれかで表され、Ar2は2
価の芳香族基、2価の脂肪族基、または芳香族基と脂肪族基の少なくとも一方を含む2価
の基である、
ポリエステルイミド。 The following general formula (7):
In the general formula (7), Ar 1 is represented by any one of the formulas (2) to (6), and Ar 2 is
a divalent aromatic group, a divalent aliphatic group, or a divalent group containing at least one of an aromatic group and an aliphatic group,
Polyesterimide.
m/K以下である、請求項3に記載のフィルム。 The average linear thermal expansion coefficient between 100 and 200°C measured by thermomechanical analysis is 30pp.
4. The film of claim 3, wherein the viscosity is less than or equal to m/K.
されない、請求項3に記載のフィルム。 4. The film of claim 3, which has a glass transition temperature of 300° C. or more or not detectable as measured by dynamic viscoelastic analysis.
フィルム。 The film of claim 3, having a dielectric loss tangent of 0.003 or less at an operating frequency of 10 GHz.
ト配線基板。 A flexible printed wiring board for high-speed communication, comprising the film according to any one of claims 3 to 7.
A heat-resistant insulating substrate comprising the film according to any one of claims 3 to 7.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022195875 | 2022-12-07 | ||
| JP2022195875 | 2022-12-07 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2024082217A true JP2024082217A (en) | 2024-06-19 |
Family
ID=91523933
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023079533A Pending JP2024082217A (en) | 2022-12-07 | 2023-05-12 | Tetracarboxylic dianhydrides, polyesterimides, and polyesterimide films |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2024082217A (en) |
-
2023
- 2023-05-12 JP JP2023079533A patent/JP2024082217A/en active Pending
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5727795B2 (en) | Ester group-containing tetracarboxylic dianhydride, polyester polyimide precursor, polyesterimide, and methods for producing them | |
| JP6996609B2 (en) | Polyimide resin, polyimide varnish and polyimide film | |
| JPWO2019188305A1 (en) | Polyimide resin, polyimide varnish and polyimide film | |
| JP7666507B2 (en) | Imide-amic acid copolymer, method for producing same, varnish, and polyimide film | |
| JP2009286854A (en) | Polyesterimide precursor and polyesterimide | |
| JPWO2019188306A1 (en) | Polyimide resin, polyimide varnish and polyimide film | |
| KR102781850B1 (en) | Polyimide resin, polyimide varnish and polyimide film | |
| JP2007091701A (en) | Tetracarboxylic acids containing fluorenyl group and ester group, fluorenyl group-containing polyesterimide precursor, fluorenyl group-containing polyesterimide, and methods for producing them | |
| WO2016148150A1 (en) | Novel tetracarboxylic dianhydride, and polyimide and polyimide copolymer obtained from said acid dianhydride | |
| JP2023164495A (en) | Polyimide and polyimide film | |
| TWI878418B (en) | Polyimide resin, varnish and polyimide film | |
| JP7666506B2 (en) | Imide-amic acid copolymer, method for producing same, varnish, and polyimide film | |
| JP2011148901A (en) | Phosphorus-containing diamine and phosphorus-containing polyimide obtained therefrom | |
| JP7621923B2 (en) | Tetracarboxylic acid dianhydride, polyesterimide precursor and method for producing same, and polyesterimide and method for producing same | |
| TWI865714B (en) | Polyimide resin, polyimide varnish, and polyimide film | |
| JP2024082217A (en) | Tetracarboxylic dianhydrides, polyesterimides, and polyesterimide films | |
| CN111133034B (en) | Polyimide resin, polyimide varnish, and polyimide film | |
| JP2008163088A (en) | Ester group-containing alicyclic tetracarboxylic anhydride and process for producing the same | |
| JP6765093B2 (en) | Polyimide | |
| JP2008163090A (en) | Tetracarboxylic dianhydride, method for producing the same, and polymer | |
| TWI858133B (en) | Polyimide resin composition, polyimide varnish, and polyimide film | |
| JP2024165222A (en) | Polyimide Film | |
| JP2012012559A (en) | Ester group-containing tetracarboxylic acid dianhydride having asymmetrical structure, polyesterimide precursor, polyesterimide and laminate with metal obtained from the same, and method for producing these | |
| JP7726200B2 (en) | Polyimide film manufacturing method | |
| CN111936554B (en) | Polyimide resin, polyimide varnish and polyimide film |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AA64 | Notification of invalidation of claim of internal priority (with term) |
Free format text: JAPANESE INTERMEDIATE CODE: A241764 Effective date: 20230606 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230807 |