JP2023535024A - 抗aベータ抗体 - Google Patents
抗aベータ抗体 Download PDFInfo
- Publication number
- JP2023535024A JP2023535024A JP2023504285A JP2023504285A JP2023535024A JP 2023535024 A JP2023535024 A JP 2023535024A JP 2023504285 A JP2023504285 A JP 2023504285A JP 2023504285 A JP2023504285 A JP 2023504285A JP 2023535024 A JP2023535024 A JP 2023535024A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- fragment
- subject
- disease
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2887—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against CD20
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/461—Igs containing Ig-regions, -domains or -residues form different species
- C07K16/462—Igs containing a variable region (Fv) from one specie and a constant region (Fc) from another
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/734—Complement-dependent cytotoxicity [CDC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/02—Fusion polypeptide containing a localisation/targetting motif containing a signal sequence
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/40—Fusion polypeptide containing a tag for immunodetection, or an epitope for immunisation
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Neurosurgery (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Engineering & Computer Science (AREA)
- Neurology (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
本出願は、2020年7月23日出願の米国仮特許出願第63/055,813号、2020年10月1日出願の米国仮特許出願第63/086,589号、2021年5月11日出願の米国仮特許出願第63/187,379号および2021年7月8日出願の米国仮特許出願第63/219,611号の利益を主張し、これらは全て、その全体が参照によって本明細書に組み込まれる。
コンピューター可読形態の配列表が、電子的提出によって本出願と共に提出されており、その全体が参照によって本出願に組み込まれる。配列表は、2021年7月22日に作成されたファイル中に含有され、ファイル名「20-1030-WO_Sequence-Listing_ST25.txt」を有し、サイズは155kbである。
本開示は、抗アミロイドベータ(Aβ)抗体ならびに組成物およびそれらの使用の方法に関する。
アルツハイマー病(AD)は、老人性認知症を生じる進行性の疾患である。この疾患は、一般に、老齢(65+歳)において生じる遅発型、および老人期のかなり前、即ち、35歳と60歳との間に発症する若年性として分類される。疾患病変は、両方の型の疾患について同じように見えるが、異常は、若年に開始する症例においてより重症であり、より広い範囲に及ぶ傾向がある。この疾患は、脳における少なくとも2つの型の病変:神経原線維変化および老人斑によって特徴付けられる。神経原線維変化は、互いに対になって巻き付いた2つのフィラメントからなる微小管関連タウタンパク質の細胞内沈着物である。老人斑(即ち、アミロイド斑)は、脳組織の切片の顕微鏡解析によって可視できる、中心に細胞外アミロイド沈着物を有する最大150μmにわたる不規則な神経網の領域である。脳内のアミロイド斑の蓄積は、ダウン症候群および他の認知障害にも関連している。
本開示は、Aβに特異的に結合する抗体(および抗体断片)、かかる抗体および抗体断片ならびに関連の核酸を産生する方法、Aβ関連の神経学的障害を有する患者の処置の方法、例えば、アミロイド原性疾患を処置する、アミロイド原性疾患のリスクを低減させる、またはアミロイド原性疾患の発生を遅延させるため、アミロイド原性疾患のマーカー、例えば、Aβ斑を予防する、低減させるまたは阻害するため、および認知を改善するための予防的および/または治療的使用のための、Aβに対して高い親和性の結合を示す抗体の医薬製剤および組成物に関する。本開示は、アミロイド斑を検出する方法、およびアミロイド原性疾患に関して処置されている患者において処置の有効性を測定する方法にさらに関する。本開示は、Aβペプチドに特異的に結合し、斑負荷を低減させ、アミロイド原性障害に関連する可溶性Aβ種を中和するのに有効なモノクローナル抗体の同定および特徴付けに、少なくとも一部基づく。
重鎖CDR1は、配列番号16、19または20のうち1つを含み、
重鎖CDR2は、配列番号20、21、22または23のうち1つを含み、
重鎖CDR3は、配列番号18、24または25のうち1つを含み、
軽鎖CDR1は、配列番号26、29、31または32のうち1つを含み、
軽鎖CDR2は、配列番号33、34、35または36のうち1つを含み、
軽鎖CDR3は、配列番号28、38または39のうち1つを含む。
重鎖CDR1が、アミノ酸配列GFTFSNX1GMSを含み、式中、X1はYまたはFであり(配列番号88);
重鎖CDR2が、アミノ酸配列SX1RSGSGRTYYSDNVKGを含み、式中、X1はIまたはVであり(wherein is X1 is I or V)(配列番号89);
重鎖CDR3が、アミノ酸配列YDHYX1GX2SDYを含み、式中、X1はSまたはTであり、X2はSまたはTであり(配列番号90);
軽鎖CDR1が、アミノ酸配列KSSQSLLDYDGKTYLN(配列番号91)を含み;
軽鎖CDR2が、アミノ酸配列X1VX2NRDX3を含み、式中、X1はKまたはRであり、X2はSまたはTであり、X3はSまたはTであり(配列番号92);
軽鎖CDR3が、アミノ酸配列WQGTHFPRX1を含み、式中、X1はSまたはTである(配列番号93)
を有する、抗体またはその断片に関する。
重鎖CDR1が、アミノ酸配列GFTFX1NX2GMSを含み、式中、X1はSまたはAであり、X2はYまたはFであり(配列番号95);
重鎖CDR2が、アミノ酸配列SX1RSGX2X3RTYYSDNVKGを含み、式中、X1はIまたはVであり、X2はSまたはGであり、X3はSまたはGであり(配列番号96);
重鎖CDR3が、アミノ酸配列YDHYX1GX2SDYを含み、式中、X1はSまたはTであり、X2はSまたはTであり(配列番号90);
軽鎖CDR1が、アミノ酸配列X1SSQSLX2DX3DGKTYLNを含み、式中、X1はKまたはRであり、X2はV、MまたはLであり、X3はY、TまたはSであり(配列番号97);
軽鎖CDR2が、アミノ酸配列X1VX2NRX3X4を含み、式中、X1はKまたはRであり、X2はSまたはTであり、X3はEまたはDであり、X4はSまたはTであり(X4 i S or T)(配列番号98);
軽鎖CDR3が、アミノ酸配列WQGX1HFPRX2を含み、式中、X1はSまたはTであり、X2はSまたはTである(配列番号99)
を有する、抗体またはその断片に関する。
(a)請求項1から18のいずれか一項に記載の抗体またはその断片を対象に投与することによる処置の前の対象におけるアミロイド斑の第1のレベルを測定し、対象におけるAβに結合した抗体またはその断片の第1の量を検出するステップ、
(b)処置を対象に投与するステップ、
(c)抗体またはその断片を対象に投与することによる処置の後の対象におけるアミロイド斑の第2のレベルを測定し、対象におけるAβに結合した抗体またはその断片を検出するステップ
を含み、アミロイド斑のレベルにおける減少が、処置に対する肯定的応答を示す、方法。
アミロイドベータ(Aβ)のN末端を標的化するモノクローナル抗体(mAb)は、アミロイド斑負荷を低減させることが臨床的に実証されており、1つのかかる抗体であるアデュカヌマブは、斑負荷における有意な低減が、アルツハイマー病(AD)における認知低下の減速に関連したことを示した。前臨床研究は、AβのN末端エピトープを標的化するモノクローナル抗体(mAb)が、in vitroおよびin vivoの両方で、抗体依存的なミクログリア媒介性のAβ斑クリアランスおよび可溶性毒性Aβオリゴマーの中和を惹起することも示している。N末端Aβ標的化mAbの投与が、ADを有する患者におけるAβ斑のクリアランスおよび可溶性Aβ凝集体の中和を介して疾患進行を減速させると仮説が立てられる。
CDR-L1:S32Y(32位におけるSerからTyr)、および
CDR-H2:G55S(54位におけるGlyからSer)。
重鎖CDR1は、アミノ酸配列GFTFSNX1GMSを含み、式中、X1はYまたはFである(配列番号88);
重鎖CDR2は、アミノ酸配列SX1RSGSGRTYYSDNVKGを含み、式中、X1はIまたはVである(配列番号89);
重鎖CDR3は、アミノ酸配列YDHYX1GX2SDYを含み、式中、X1はSまたはTであり、X2はSまたはTである(配列番号90);
軽鎖CDR1は、アミノ酸配列KSSQSLLDYDGKTYLNを含む(配列番号91);
軽鎖CDR2は、アミノ酸配列X1VX2NRDX3を含み、式中、X1はKまたはRであり、X2はSまたはTであり、X3はSまたはTである(配列番号92);
軽鎖CDR3は、アミノ酸配列WQGTHFPRX1を含み、式中、X1はSまたはTである(配列番号93)。
重鎖CDR1は、アミノ酸配列GFTFX1NX2GMSを含み、式中、X1はSまたはAであり、X2はYまたはFである(配列番号95);
重鎖CDR2は、アミノ酸配列SX1RSGX2X3RTYYSDNVKGを含み、式中、X1はIまたはVであり、X2はSまたはGであり、X3はSまたはGである(配列番号96);
重鎖CDR3は、アミノ酸配列YDHYX1GX2SDYを含み、式中、X1はSまたはTであり、X2はSまたはTである(配列番号90);
軽鎖CDR1は、アミノ酸配列X1SSQSLX2DX3DGKTYLNを含み、式中、X1はKまたはRであり、X2はV、MまたはLであり、X3はY、TまたはSである(配列番号97);
軽鎖CDR2は、アミノ酸配列X1VX2NRX3X4を含み、式中、X1はKまたはRであり、X2はSまたはTであり、X3はEまたはDであり、X4はSまたはTである(配列番号98);
軽鎖CDR3は、アミノ酸配列WQGX1HFPRX2を含み、式中、X1はSまたはTであり、X2はSまたはTである(配列番号99)。
DAEFRHDSGYEVHHQKLVFFAEDVGSNKGAIIGLMVGGVVIA
Aβ抗体設計
競合ELISAアッセイによるIC50比決定
競合ELISAによるモノクローナル抗体効力決定
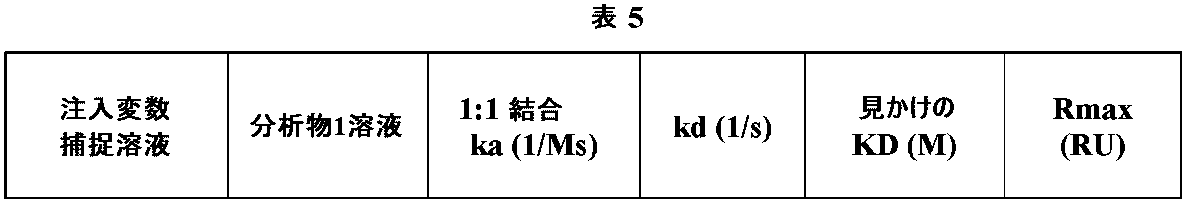
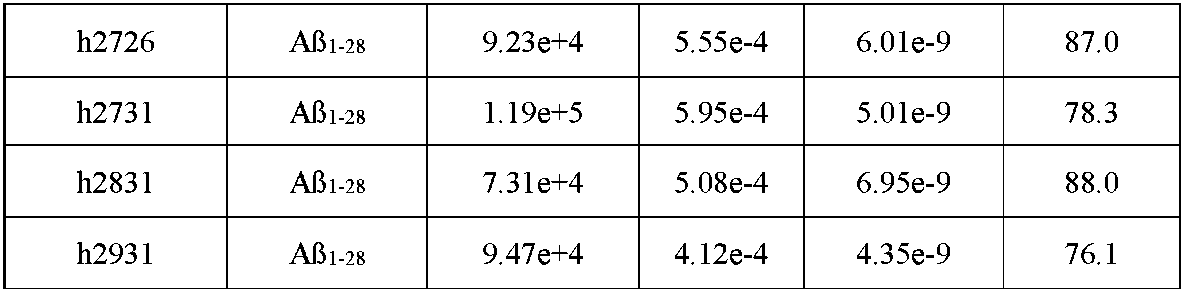
BIAcoreによるヒト化mAbまたはFabの特徴付け
BIAcoreによる見かけのヒト化mAb親和性の特徴付け
BIAcoreによる見かけのヒト化mAb親和性の特徴付け
ELISAによるAβ原線維結合
ELISAによるAβオリゴマーのh2931結合
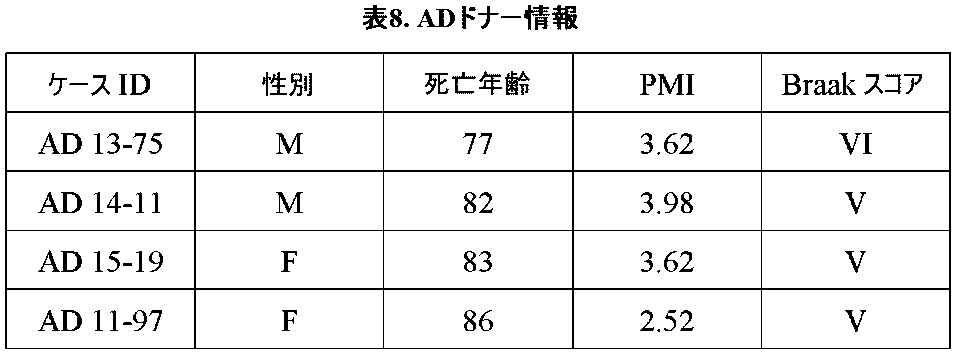
AD脳における抗Aβ抗体結合
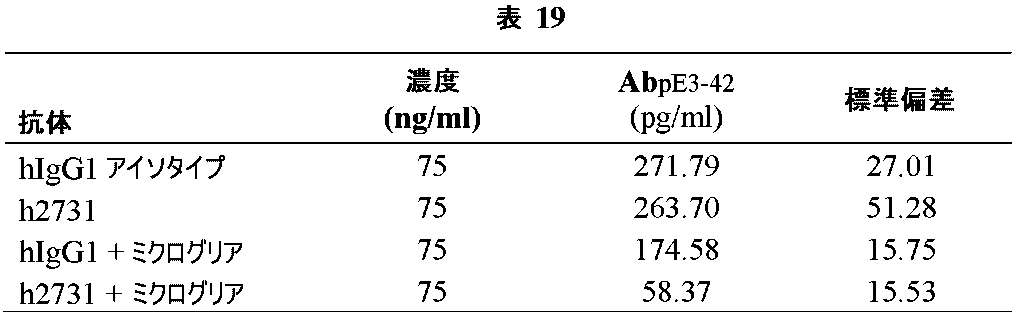
(Aβ1-42およびAβpE3-42)斑クリアランスの決定のためのex vivoファゴサイトーシスアッセイ
海馬結合アッセイにおけるオリゴマー遮断
ネイティブAβ種および改変されたAβ種への抗Aβ抗体の結合
in vitroファゴサイトーシス媒介性クリアランス - Aβ1-42前原線維のTHP-1ヒト単球媒介性取込み
進行したAD患者からの脳組織中の、総Aβおよびピログルタメート改変されたAβの分布
抗Aβ抗体h2731は、AD脳においてAβpE3-42と共局在する
本発明の抗Aβ抗体は、アデュカヌマブよりも高い有効性で、用量依存的様式でAD脳組織からのAβpE3-42クリアランスをex vivoで促進する
h2731標的係合
CDR-L1:S32Y(32位におけるSerからTyr)、および
CDR-H2:G55S(55位におけるGlyからSer)。
特定の実施形態では、例えば以下の項目が提供される。
(項目1)
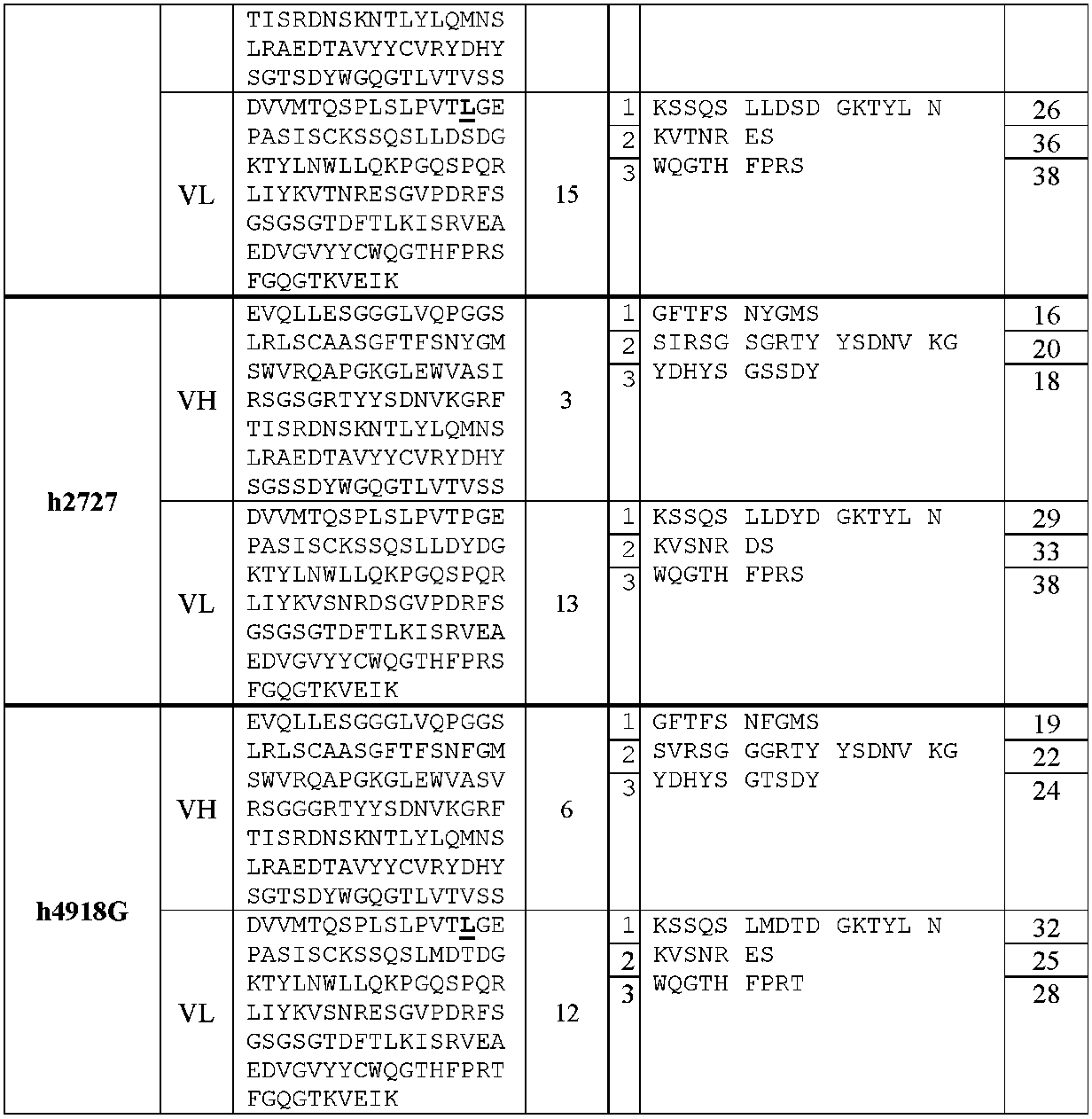
重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、前記重鎖CDR1、CDR2およびCDR3ならびに前記軽鎖CDR1、CDR2およびCDR3が、表1Aおよび表1B中の抗体のうち1つについて示される通りである、抗体またはその断片。
(項目2)
前記重鎖可変領域が、表1Aおよび表1B中の抗体のうち1つについて示される通りである、項目1に記載の抗体またはその断片。
(項目3)
前記軽鎖可変領域が、表1Aおよび表1B中の抗体のうち1つについて示される通りである、項目1に記載の抗体またはその断片。
(項目4)
重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、
重鎖CDR1が、配列番号16、19または20のうち1つを含み、
重鎖CDR2が、配列番号20、21、22または23のうち1つを含み、
重鎖CDR3が、配列番号18、24または25のうち1つを含み、
軽鎖CDR1が、配列番号26、29、31または32のうち1つを含み、
軽鎖CDR2が、配列番号33、34、35または36のうち1つを含み、
軽鎖CDR3が、配列番号28、38または39のうち1つを含む、
抗体またはその断片。
(項目5)
前記CDRを除く前記重鎖可変領域が、配列番号3、4、5、6および7から選択されるアミノ酸配列と少なくとも95%同一であり、前記CDRを除く前記軽鎖可変領域が、配列番号8、9、10、11、12、13、14および15から選択されるアミノ酸配列と少なくとも95%同一である、項目1または項目4に記載の抗体またはその断片。
(項目6)
前記CDRを除く重鎖可変領域が、配列番号3、4、5、6および7から選択されるアミノ酸配列と少なくとも98%同一であり、前記CDRを除く前記軽鎖可変領域が、配列番号8、9、10、11、12、13、14および15から選択されるアミノ酸配列と少なくとも98%同一である、項目5に記載の抗体またはその断片。
(項目7)
重鎖可変領域が、配列番号3、4、5、6および7から選択され、前記軽鎖可変領域が、配列番号8、9、10、11、12、13、14および15から選択される、項目6に記載の抗体またはその断片。
(項目8)
重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、
重鎖CDR1が、アミノ酸配列GFTFSNX 1 GMSを含み、式中、X 1 はYまたはFであり(配列番号88);
重鎖CDR2が、アミノ酸配列SX 1 RSGSGRTYYSDNVKGを含み、式中、X 1 はIまたはVであり(配列番号89);
重鎖CDR3が、アミノ酸配列YDHYX 1 GX 2 SDYを含み、式中、X 1 はSまたはTであり、X 2 はSまたはTであり(配列番号90);
軽鎖CDR1が、アミノ酸配列KSSQSLLDYDGKTYLNを含み(配列番号91);
軽鎖CDR2が、アミノ酸配列X 1 VX 2 NRDX 3 を含み、式中、X 1 =KまたはRであり、X 2 はSまたはTであり、X 3 はSまたはTであり(配列番号92);
軽鎖CDR3が、アミノ酸配列WQGTHFPRX 1 を含み、式中、X 1 はSまたはTである(配列番号93)、
抗体またはその断片。
(項目9)
軽鎖CDR3がWQGTHFPRX 1 FX 2 を含み、式中、X 1 はSまたはTであり、X 2 はFまたはYである(配列番号94)、項目8に記載の抗体またはその断片。
(項目10)
重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、
重鎖CDR1が、アミノ酸配列GFTFX 1 NX 2 GMSを含み、式中、X 1 はSまたはAであり、X 2 はYまたはFであり(配列番号95);
重鎖CDR2が、アミノ酸配列SX 1 RSGX 2 X 3 RTYYSDNVKGを含み、式中、X 1 はIまたはVであり、X 2 はSまたはGであり、X 3 はSまたはGであり(配列番号96);
重鎖CDR3が、アミノ酸配列YDHYX 1 GX 2 SDYを含み、式中、X 1 はSまたはTであり、X 2 はSまたはTであり(配列番号90);
軽鎖CDR1が、アミノ酸配列X 1 SSQSLX 2 DX 3 DGKTYLNを含み、式中、X 1 はKまたはRであり、X 2 はV、MまたはLであり、X 3 はY、TまたはSであり(配列番号97);
軽鎖CDR2が、アミノ酸配列X 1 VX 2 NRX 3 X 4 を含み、式中、X 1 =KまたはRであり、X 2 はSまたはTであり、X 3 はEまたはDであり、X 4 はSまたはTであり(配列番号98);
軽鎖CDR3が、アミノ酸配列WQGX 1 HFPRX 2 を含み、式中、X 1 はSまたはTであり、X 2 はSまたはTである(配列番号99)、
抗体またはその断片。
(項目11)
軽鎖CDR3が、WQGTHFPRX 1 FX 2 X 3 を含み、式中、X 1 はSまたはTであり、X 2 はSまたはTであり、X 3 はFまたはYである(配列番号100)、項目10に記載の抗体またはその断片。
(項目12)
前記抗体がヒト化されている、項目1から11の一項に記載の抗体またはその断片。
(項目13)
前記抗体がヒトIgG1である、項目1から11の一項に記載の抗体またはその断片。
(項目14)
前記抗体が、完全抗体、キメラ抗体、CDRグラフト抗体または組換え抗体である、項目1から11の一項に記載の抗体またはその断片。
(項目15)
前記断片が、Fab、Fab’、F(ab’)2、FabcまたはFvである、項目1から11の一項に記載の抗体またはその断片。
(項目16)
配列番号40と少なくとも95%同一なアミノ酸配列を含む重鎖定常領域をさらに含む、項目1から11の一項に記載の抗体またはその断片。
(項目17)
配列番号41と少なくとも95%同一なアミノ酸配列を含む軽鎖定常領域をさらに含む、項目1から11の一項に記載の抗体またはその断片。
(項目18)
前記抗体が、Aβのアミノ酸1~7からの3つまたはそれよりも多くのアミノ酸位置を含むアミノ酸配列を有するエピトープに特異的に結合する、項目1から17の一項に記載の抗体またはその断片。
(項目19)
項目1から18のいずれか一項に記載の抗体または断片の前記重鎖および/または軽鎖をコードする核酸。
(項目20)
項目1から19の一項に記載の抗体またはその断片と薬学的に許容される担体または希釈剤とを含む医薬組成物。
(項目21)
項目1から18の一項に記載の抗体またはその断片を産生する方法であって、
(a)前記抗体またはその断片の前記重鎖および軽鎖をコードする核酸で形質転換された細胞が前記抗体またはその断片を分泌するように、前記細胞を培養するステップ;ならびに
(b)前記抗体またはその断片を細胞培養物から精製するステップ
を含む、方法。
(項目22)
項目1から18の一項に記載の抗体またはその断片を産生する細胞系を産生する方法であって、
(a)前記抗体またはその断片の重鎖および軽鎖と選択可能なマーカーとをコードするベクターを、細胞中に導入するステップ;
(b)増加したコピー数の前記ベクターを有する細胞について選択する条件下で、前記細胞を拡大増殖させるステップ;
(c)前記選択された細胞から単一の細胞を単離するステップ;ならびに
(d)抗体またはその断片の収量に基づいて選択された単一の細胞からクローニングされた細胞をバンキングするステップ
を含む、方法。
(項目23)
選択条件下で前記細胞を拡大増殖させるステップ、ならびに少なくとも100mg/L/10 6 細胞/24時間を天然に発現および分泌する細胞系についてスクリーニングするステップをさらに含む、項目22に記載の方法。
(項目24)
患者においてアミロイド原性疾患を予防または処置する方法であって、項目1から18の一項に記載の抗体または断片の有効投与量を前記患者に投与するステップを含む、方法。
(項目25)
前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、項目24に記載の方法。
(項目26)
アルツハイマー病と診断された患者を処置する方法であって、前記疾患を処置するのに有効なレジメンにおいて、項目1から18の一項に記載の抗体またはその断片を、前記疾患を有する患者に投与するステップを含む、方法。
(項目27)
遺伝的または生化学的マーカーからアルツハイマー病のリスクが決定されている患者において、前記アルツハイマー病のリスクを低減させるまたはその発生を遅延させる方法であって、前記アルツハイマー病のリスクを低減させるまたはその発生を遅延させるのに有効なレジメンにおいて、項目1から18の一項に記載の抗体またはその断片を患者に投与するステップを含む、方法。
(項目28)
状態または疾患関連アミロイド原性疾患を有する対象において認知の改善をもたらすための方法であって、項目1から18の一項に記載の抗体またはその断片の有効量を前記対象に投与するステップを含む、方法。
(項目29)
前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、項目28に記載の方法。
(項目30)
ヒト対象においてダウン症候群または臨床的もしくは前臨床的アルツハイマー病を処置する方法であって、項目1から18の一項に記載の抗体または断片の有効量を前記ヒト対象に投与するステップを含む、方法。
(項目31)
ヒト対象においてアミロイド斑の形成を阻害する方法であって、項目1から18の一項に記載の抗体または断片の有効量を前記ヒト対象に投与するステップを含む、方法。
(項目32)
ヒト対象の脳においてアミロイド斑を低減させる方法であって、項目1から18の一項に記載のヒト化抗体または断片の有効量を前記ヒト対象に投与するステップを含む、方法。
(項目33)
アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象においてアミロイド斑を阻害するまたは低減させる方法であって、項目1から18のいずれか一項に記載の抗体の有効なレジメンを前記対象に投与し、それにより、前記対象においてアミロイド斑を阻害するまたは低減させるステップを含む、方法。
(項目34)
前記アミロイド斑が、Aβ 1-42 、Aβのピログルタメート種(例えば、Aβ pE3-42 )、またはそれらの組合せを含む、項目31から33のいずれか一項に記載の方法。
(項目35)
アミロイド原性疾患を有する対象またはアミロイド原性疾患のリスクがある対象においてアミロイド斑を検出する方法であって、項目1から18のいずれか一項に記載の抗体またはその断片を対象に投与するステップ、および前記対象におけるAβに結合した前記抗体またはその断片を検出するステップを含む、方法。
(項目36)
前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、項目35に記載の方法。
(項目37)
前記抗体またはその断片が標識されている、項目35に記載の方法。
(項目38)
前記抗体またはその断片が、蛍光標識、常磁性標識または放射性標識で標識されている、項目35に記載の方法。
(項目39)
前記放射性標識が、ポジトロン放出断層撮影(PET)または単光子放出コンピューター断層撮影(SPECT)を使用して検出される、項目38に記載の方法。
(項目40)
アミロイド原性疾患に関して処置されている対象において処置の有効性を測定する方法であって、
(a)項目1から18のいずれか一項に記載の抗体またはその断片を対象に投与することによる処置の前の前記対象におけるアミロイド斑の第1のレベルを測定し、前記対象におけるAβに結合した前記抗体またはその断片の第1の量を検出するステップ、
(b)前記処置を前記対象に投与するステップ、
(c)前記抗体またはその断片を対象に投与することによる処置の後の前記対象におけるアミロイド斑の第2のレベルを測定し、前記対象におけるAβに結合した前記抗体またはその断片を検出するステップ
を含み、アミロイド斑の前記レベルにおける減少が、処置に対する肯定的応答を示す、方法。
(項目41)
アミロイド原性疾患に関して処置されている対象において処置の有効性を測定する方法であって、
(a)項目1から18のいずれか一項に記載の抗体またはその断片を対象に投与することによる処置の前の前記対象におけるアミロイド斑の第1のレベルを測定し、前記対象におけるAβに結合した抗体またはその断片の第1の量を検出するステップ、
(b)前記処置を前記対象に投与するステップ、
(c)前記抗体またはその断片を対象に投与することによる処置の後の前記対象におけるアミロイド斑の第2のレベルを測定し、前記対象におけるAβに結合した抗体またはその断片の第2の量を検出するステップ
を含み、アミロイド斑の前記レベルにおける変化なしまたはアミロイド斑における小さい増加が、処置に対する肯定的応答を示す、方法。
(項目42)
ヒト対象においてAβのクリアランスを促進する方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
(項目43)
前記Aβが、前記対象の脳組織中に存在する、項目42に記載の方法。
(項目44)
ヒト対象においてAβを取り除く方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
(項目45)
前記Aβが、前記対象の脳組織中に存在する、項目44に記載の方法。
(項目46)
ヒト対象においてAβを低減させる方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
(項目47)
前記Aβが、前記対象の脳組織中に存在する、項目46に記載の方法。
(項目48)
ヒト対象においてAβの蓄積または凝集を低減させる方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
(項目49)
前記Aβが、前記対象の脳組織中に存在する、項目48に記載の方法。
(項目50)
ヒト対象においてAβの蓄積または凝集を阻害する方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
(項目51)
前記Aβが、前記対象の脳組織中に存在する、項目50に記載の方法。
(項目52)
アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβのクリアランスを促進する方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβのクリアランスを促進するステップを含む、方法。
(項目53)
アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβを取り除く方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβを取り除くステップを含む、方法。
(項目54)
アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβを低減させる方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβを低減させるステップを含む、方法。
(項目55)
アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβの蓄積または凝集を低減させる方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβの蓄積または凝集を低減させるステップを含む、方法。
(項目56)
アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβの蓄積または凝集を阻害する方法であって、項目1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβの蓄積または凝集を阻害するステップを含む、方法。
(項目57)
前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、項目52から56のいずれか一項に記載の方法。
(項目58)
前記Aβが、Aβ 1-42 、Aβのピログルタメート種(例えば、Aβ pE3-42 )、またはそれらの組合せを含む、項目42から57のいずれか一項に記載の方法。
(項目59)
前記抗体または断片が、末梢投与によって投与される、項目24から58のいずれか一項に記載の方法。
(項目60)
前記末梢投与が、静脈内または皮下である、項目59に記載の方法。
Claims (60)
- 重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、前記重鎖CDR1、CDR2およびCDR3ならびに前記軽鎖CDR1、CDR2およびCDR3が、表1Aおよび表1B中の抗体のうち1つについて示される通りである、抗体またはその断片。
- 前記重鎖可変領域が、表1Aおよび表1B中の抗体のうち1つについて示される通りである、請求項1に記載の抗体またはその断片。
- 前記軽鎖可変領域が、表1Aおよび表1B中の抗体のうち1つについて示される通りである、請求項1に記載の抗体またはその断片。
- 重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、
重鎖CDR1が、配列番号16、19または20のうち1つを含み、
重鎖CDR2が、配列番号20、21、22または23のうち1つを含み、
重鎖CDR3が、配列番号18、24または25のうち1つを含み、
軽鎖CDR1が、配列番号26、29、31または32のうち1つを含み、
軽鎖CDR2が、配列番号33、34、35または36のうち1つを含み、
軽鎖CDR3が、配列番号28、38または39のうち1つを含む、
抗体またはその断片。 - 前記CDRを除く前記重鎖可変領域が、配列番号3、4、5、6および7から選択されるアミノ酸配列と少なくとも95%同一であり、前記CDRを除く前記軽鎖可変領域が、配列番号8、9、10、11、12、13、14および15から選択されるアミノ酸配列と少なくとも95%同一である、請求項1または請求項4に記載の抗体またはその断片。
- 前記CDRを除く重鎖可変領域が、配列番号3、4、5、6および7から選択されるアミノ酸配列と少なくとも98%同一であり、前記CDRを除く前記軽鎖可変領域が、配列番号8、9、10、11、12、13、14および15から選択されるアミノ酸配列と少なくとも98%同一である、請求項5に記載の抗体またはその断片。
- 重鎖可変領域が、配列番号3、4、5、6および7から選択され、前記軽鎖可変領域が、配列番号8、9、10、11、12、13、14および15から選択される、請求項6に記載の抗体またはその断片。
- 重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、
重鎖CDR1が、アミノ酸配列GFTFSNX1GMSを含み、式中、X1はYまたはFであり(配列番号88);
重鎖CDR2が、アミノ酸配列SX1RSGSGRTYYSDNVKGを含み、式中、X1はIまたはVであり(配列番号89);
重鎖CDR3が、アミノ酸配列YDHYX1GX2SDYを含み、式中、X1はSまたはTであり、X2はSまたはTであり(配列番号90);
軽鎖CDR1が、アミノ酸配列KSSQSLLDYDGKTYLNを含み(配列番号91);
軽鎖CDR2が、アミノ酸配列X1VX2NRDX3を含み、式中、X1=KまたはRであり、X2はSまたはTであり、X3はSまたはTであり(配列番号92);
軽鎖CDR3が、アミノ酸配列WQGTHFPRX1を含み、式中、X1はSまたはTである(配列番号93)、
抗体またはその断片。 - 軽鎖CDR3がWQGTHFPRX1FX2を含み、式中、X1はSまたはTであり、X2はFまたはYである(配列番号94)、請求項8に記載の抗体またはその断片。
- 重鎖CDR1、CDR2およびCDR3を含む重鎖可変領域ならびに軽鎖CDR1、CDR2およびCDR3を含む軽鎖可変領域を含む、Aβペプチドに特異的に結合する抗体またはその断片であって、
重鎖CDR1が、アミノ酸配列GFTFX1NX2GMSを含み、式中、X1はSまたはAであり、X2はYまたはFであり(配列番号95);
重鎖CDR2が、アミノ酸配列SX1RSGX2X3RTYYSDNVKGを含み、式中、X1はIまたはVであり、X2はSまたはGであり、X3はSまたはGであり(配列番号96);
重鎖CDR3が、アミノ酸配列YDHYX1GX2SDYを含み、式中、X1はSまたはTであり、X2はSまたはTであり(配列番号90);
軽鎖CDR1が、アミノ酸配列X1SSQSLX2DX3DGKTYLNを含み、式中、X1はKまたはRであり、X2はV、MまたはLであり、X3はY、TまたはSであり(配列番号97);
軽鎖CDR2が、アミノ酸配列X1VX2NRX3X4を含み、式中、X1=KまたはRであり、X2はSまたはTであり、X3はEまたはDであり、X4はSまたはTであり(配列番号98);
軽鎖CDR3が、アミノ酸配列WQGX1HFPRX2を含み、式中、X1はSまたはTであり、X2はSまたはTである(配列番号99)、
抗体またはその断片。 - 軽鎖CDR3が、WQGTHFPRX1FX2X3を含み、式中、X1はSまたはTであり、X2はSまたはTであり、X3はFまたはYである(配列番号100)、請求項10に記載の抗体またはその断片。
- 前記抗体がヒト化されている、請求項1から11の一項に記載の抗体またはその断片。
- 前記抗体がヒトIgG1である、請求項1から11の一項に記載の抗体またはその断片。
- 前記抗体が、完全抗体、キメラ抗体、CDRグラフト抗体または組換え抗体である、請求項1から11の一項に記載の抗体またはその断片。
- 前記断片が、Fab、Fab’、F(ab’)2、FabcまたはFvである、請求項1から11の一項に記載の抗体またはその断片。
- 配列番号40と少なくとも95%同一なアミノ酸配列を含む重鎖定常領域をさらに含む、請求項1から11の一項に記載の抗体またはその断片。
- 配列番号41と少なくとも95%同一なアミノ酸配列を含む軽鎖定常領域をさらに含む、請求項1から11の一項に記載の抗体またはその断片。
- 前記抗体が、Aβのアミノ酸1~7からの3つまたはそれよりも多くのアミノ酸位置を含むアミノ酸配列を有するエピトープに特異的に結合する、請求項1から17の一項に記載の抗体またはその断片。
- 請求項1から18のいずれか一項に記載の抗体または断片の前記重鎖および/または軽鎖をコードする核酸。
- 請求項1から19の一項に記載の抗体またはその断片と薬学的に許容される担体または希釈剤とを含む医薬組成物。
- 請求項1から18の一項に記載の抗体またはその断片を産生する方法であって、
(a)前記抗体またはその断片の前記重鎖および軽鎖をコードする核酸で形質転換された細胞が前記抗体またはその断片を分泌するように、前記細胞を培養するステップ;ならびに
(b)前記抗体またはその断片を細胞培養物から精製するステップ
を含む、方法。 - 請求項1から18の一項に記載の抗体またはその断片を産生する細胞系を産生する方法であって、
(a)前記抗体またはその断片の重鎖および軽鎖と選択可能なマーカーとをコードするベクターを、細胞中に導入するステップ;
(b)増加したコピー数の前記ベクターを有する細胞について選択する条件下で、前記細胞を拡大増殖させるステップ;
(c)前記選択された細胞から単一の細胞を単離するステップ;ならびに
(d)抗体またはその断片の収量に基づいて選択された単一の細胞からクローニングされた細胞をバンキングするステップ
を含む、方法。 - 選択条件下で前記細胞を拡大増殖させるステップ、ならびに少なくとも100mg/L/106細胞/24時間を天然に発現および分泌する細胞系についてスクリーニングするステップをさらに含む、請求項22に記載の方法。
- 患者においてアミロイド原性疾患を予防または処置する方法であって、請求項1から18の一項に記載の抗体または断片の有効投与量を前記患者に投与するステップを含む、方法。
- 前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、請求項24に記載の方法。
- アルツハイマー病と診断された患者を処置する方法であって、前記疾患を処置するのに有効なレジメンにおいて、請求項1から18の一項に記載の抗体またはその断片を、前記疾患を有する患者に投与するステップを含む、方法。
- 遺伝的または生化学的マーカーからアルツハイマー病のリスクが決定されている患者において、前記アルツハイマー病のリスクを低減させるまたはその発生を遅延させる方法であって、前記アルツハイマー病のリスクを低減させるまたはその発生を遅延させるのに有効なレジメンにおいて、請求項1から18の一項に記載の抗体またはその断片を患者に投与するステップを含む、方法。
- 状態または疾患関連アミロイド原性疾患を有する対象において認知の改善をもたらすための方法であって、請求項1から18の一項に記載の抗体またはその断片の有効量を前記対象に投与するステップを含む、方法。
- 前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、請求項28に記載の方法。
- ヒト対象においてダウン症候群または臨床的もしくは前臨床的アルツハイマー病を処置する方法であって、請求項1から18の一項に記載の抗体または断片の有効量を前記ヒト対象に投与するステップを含む、方法。
- ヒト対象においてアミロイド斑の形成を阻害する方法であって、請求項1から18の一項に記載の抗体または断片の有効量を前記ヒト対象に投与するステップを含む、方法。
- ヒト対象の脳においてアミロイド斑を低減させる方法であって、請求項1から18の一項に記載のヒト化抗体または断片の有効量を前記ヒト対象に投与するステップを含む、方法。
- アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象においてアミロイド斑を阻害するまたは低減させる方法であって、請求項1から18のいずれか一項に記載の抗体の有効なレジメンを前記対象に投与し、それにより、前記対象においてアミロイド斑を阻害するまたは低減させるステップを含む、方法。
- 前記アミロイド斑が、Aβ1-42、Aβのピログルタメート種(例えば、AβpE3-42)、またはそれらの組合せを含む、請求項31から33のいずれか一項に記載の方法。
- アミロイド原性疾患を有する対象またはアミロイド原性疾患のリスクがある対象においてアミロイド斑を検出する方法であって、請求項1から18のいずれか一項に記載の抗体またはその断片を対象に投与するステップ、および前記対象におけるAβに結合した前記抗体またはその断片を検出するステップを含む、方法。
- 前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、請求項35に記載の方法。
- 前記抗体またはその断片が標識されている、請求項35に記載の方法。
- 前記抗体またはその断片が、蛍光標識、常磁性標識または放射性標識で標識されている、請求項35に記載の方法。
- 前記放射性標識が、ポジトロン放出断層撮影(PET)または単光子放出コンピューター断層撮影(SPECT)を使用して検出される、請求項38に記載の方法。
- アミロイド原性疾患に関して処置されている対象において処置の有効性を測定する方法であって、
(a)請求項1から18のいずれか一項に記載の抗体またはその断片を対象に投与することによる処置の前の前記対象におけるアミロイド斑の第1のレベルを測定し、前記対象におけるAβに結合した前記抗体またはその断片の第1の量を検出するステップ、
(b)前記処置を前記対象に投与するステップ、
(c)前記抗体またはその断片を対象に投与することによる処置の後の前記対象におけるアミロイド斑の第2のレベルを測定し、前記対象におけるAβに結合した前記抗体またはその断片を検出するステップ
を含み、アミロイド斑の前記レベルにおける減少が、処置に対する肯定的応答を示す、方法。 - アミロイド原性疾患に関して処置されている対象において処置の有効性を測定する方法であって、
(a)請求項1から18のいずれか一項に記載の抗体またはその断片を対象に投与することによる処置の前の前記対象におけるアミロイド斑の第1のレベルを測定し、前記対象におけるAβに結合した抗体またはその断片の第1の量を検出するステップ、
(b)前記処置を前記対象に投与するステップ、
(c)前記抗体またはその断片を対象に投与することによる処置の後の前記対象におけるアミロイド斑の第2のレベルを測定し、前記対象におけるAβに結合した抗体またはその断片の第2の量を検出するステップ
を含み、アミロイド斑の前記レベルにおける変化なしまたはアミロイド斑における小さい増加が、処置に対する肯定的応答を示す、方法。 - ヒト対象においてAβのクリアランスを促進する方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
- 前記Aβが、前記対象の脳組織中に存在する、請求項42に記載の方法。
- ヒト対象においてAβを取り除く方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
- 前記Aβが、前記対象の脳組織中に存在する、請求項44に記載の方法。
- ヒト対象においてAβを低減させる方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
- 前記Aβが、前記対象の脳組織中に存在する、請求項46に記載の方法。
- ヒト対象においてAβの蓄積または凝集を低減させる方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
- 前記Aβが、前記対象の脳組織中に存在する、請求項48に記載の方法。
- ヒト対象においてAβの蓄積または凝集を阻害する方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与するステップを含む、方法。
- 前記Aβが、前記対象の脳組織中に存在する、請求項50に記載の方法。
- アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβのクリアランスを促進する方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβのクリアランスを促進するステップを含む、方法。
- アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβを取り除く方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβを取り除くステップを含む、方法。
- アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβを低減させる方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβを低減させるステップを含む、方法。
- アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβの蓄積または凝集を低減させる方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβの蓄積または凝集を低減させるステップを含む、方法。
- アミロイド原性疾患を有する対象またはアミロイド原性疾患を発症するリスクがある対象の脳組織においてAβの蓄積または凝集を阻害する方法であって、請求項1から18のいずれか一項に記載の抗体または断片の有効なレジメンを前記対象に投与し、それにより、前記対象の脳組織においてAβの蓄積または凝集を阻害するステップを含む、方法。
- 前記アミロイド原性疾患が、全身性アミロイドーシス、アルツハイマー病、成人発症型糖尿病、パーキンソン病、ハンチントン病、前頭側頭葉型認知症、ダウン症候群または軽度認知障害である、請求項52から56のいずれか一項に記載の方法。
- 前記Aβが、Aβ1-42、Aβのピログルタメート種(例えば、AβpE3-42)、またはそれらの組合せを含む、請求項42から57のいずれか一項に記載の方法。
- 前記抗体または断片が、末梢投与によって投与される、請求項24から58のいずれか一項に記載の方法。
- 前記末梢投与が、静脈内または皮下である、請求項59に記載の方法。
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063055813P | 2020-07-23 | 2020-07-23 | |
| US63/055,813 | 2020-07-23 | ||
| US202063086589P | 2020-10-01 | 2020-10-01 | |
| US63/086,589 | 2020-10-01 | ||
| US202163187379P | 2021-05-11 | 2021-05-11 | |
| US63/187,379 | 2021-05-11 | ||
| US202163219611P | 2021-07-08 | 2021-07-08 | |
| US63/219,611 | 2021-07-08 | ||
| PCT/US2021/042900 WO2022020680A1 (en) | 2020-07-23 | 2021-07-23 | Anti-abeta antibodies |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023535024A true JP2023535024A (ja) | 2023-08-15 |
| JPWO2022020680A5 JPWO2022020680A5 (ja) | 2024-10-15 |
Family
ID=79728984
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023504285A Pending JP2023535024A (ja) | 2020-07-23 | 2021-07-23 | 抗aベータ抗体 |
Country Status (15)
| Country | Link |
|---|---|
| US (8) | US12435129B2 (ja) |
| EP (1) | EP4185612A4 (ja) |
| JP (1) | JP2023535024A (ja) |
| KR (1) | KR20230039734A (ja) |
| CN (1) | CN116348487A (ja) |
| AU (1) | AU2021310926A1 (ja) |
| BR (1) | BR112023001061A2 (ja) |
| CA (1) | CA3186614A1 (ja) |
| CL (3) | CL2023000216A1 (ja) |
| IL (1) | IL300059A (ja) |
| MX (1) | MX2023000949A (ja) |
| PH (1) | PH12023550178A1 (ja) |
| TW (1) | TW202216760A (ja) |
| UY (1) | UY39337A (ja) |
| WO (1) | WO2022020680A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023535024A (ja) | 2020-07-23 | 2023-08-15 | オター プロシーナ リミテッド | 抗aベータ抗体 |
| CN120513256A (zh) * | 2023-01-20 | 2025-08-19 | 迈威(美国)生物治疗有限公司 | 抗淀粉样蛋白β原纤丝/低聚物抗体和其用途 |
| TW202434629A (zh) * | 2023-01-26 | 2024-09-01 | 愛爾蘭商歐薩爾普羅席納有限公司 | 以抗類澱粉β (ABETA)抗體治療神經病症之方法 |
| WO2025015254A2 (en) * | 2023-07-12 | 2025-01-16 | Lloyd Tran | Therapeutic agent composition and method of use of combination therapy for treatment of mild cognitive impairment |
| TW202541846A (zh) * | 2024-01-05 | 2025-11-01 | 愛爾蘭商歐薩爾普羅席納有限公司 | 以抗類澱粉蛋白β (ABETA)抗體治療神經病症之方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003517461A (ja) * | 1999-05-28 | 2003-05-27 | ニユーララブ・リミテツド | アミロイド形成疾患の予防および処置 |
| JP2010534650A (ja) * | 2007-07-27 | 2010-11-11 | ヤンセン アルツハイマー イミュノセラピー | アミロイド原性疾患の処置 |
Family Cites Families (123)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3003097A (en) | 1958-07-17 | 1961-10-03 | Gen Electric | Sequence control system for timing motor |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| ATE420178T1 (de) | 1992-08-21 | 2009-01-15 | Univ Bruxelles | Immunoglobuline ohne leichtkette |
| US5834597A (en) | 1996-05-20 | 1998-11-10 | Protein Design Labs, Inc. | Mutated nonactivating IgG2 domains and anti CD3 antibodies incorporating the same |
| US8173127B2 (en) | 1997-04-09 | 2012-05-08 | Intellect Neurosciences, Inc. | Specific antibodies to amyloid beta peptide, pharmaceutical compositions and methods of use thereof |
| US6905686B1 (en) | 1997-12-02 | 2005-06-14 | Neuralab Limited | Active immunization for treatment of alzheimer's disease |
| US7179892B2 (en) | 2000-12-06 | 2007-02-20 | Neuralab Limited | Humanized antibodies that recognize beta amyloid peptide |
| US6761888B1 (en) | 2000-05-26 | 2004-07-13 | Neuralab Limited | Passive immunization treatment of Alzheimer's disease |
| US6750324B1 (en) | 1997-12-02 | 2004-06-15 | Neuralab Limited | Humanized and chimeric N-terminal amyloid beta-antibodies |
| US6518011B1 (en) | 1999-01-13 | 2003-02-11 | Bristol-Myers Squibb Company | Method for screening compounds to identify beta-amyloid production modulators |
| DE60036082T2 (de) | 1999-02-05 | 2008-06-12 | Samsung Electronics Co., Ltd., Suwon | Verfahren und vorrichtung zur wiederauffindung von texturbildern |
| US7629311B2 (en) | 1999-02-24 | 2009-12-08 | Edward Lewis Tobinick | Methods to facilitate transmission of large molecules across the blood-brain, blood-eye, and blood-nerve barriers |
| US6787637B1 (en) | 1999-05-28 | 2004-09-07 | Neuralab Limited | N-Terminal amyloid-β antibodies |
| DE1257584T1 (de) | 2000-02-24 | 2003-05-28 | Lilly Co Eli | Humanisierte antikörper, die amyloid beta peptid demarkieren |
| PE20020574A1 (es) | 2000-12-06 | 2002-07-02 | Wyeth Corp | Anticuerpos humanizados que reconocen el peptido amiloideo beta |
| US7700751B2 (en) | 2000-12-06 | 2010-04-20 | Janssen Alzheimer Immunotherapy | Humanized antibodies that recognize β-amyloid peptide |
| AU2002258808A1 (en) | 2001-04-30 | 2002-11-11 | Eli Lilly And Company | Humanized antibodies |
| MY139983A (en) | 2002-03-12 | 2009-11-30 | Janssen Alzheimer Immunotherap | Humanized antibodies that recognize beta amyloid peptide |
| WO2004029629A1 (en) | 2002-09-27 | 2004-04-08 | Janssen Pharmaceutica N.V. | N-11 truncated amyloid-beta nomoclonal antibodies, compositions, methods and uses |
| US20050129695A1 (en) | 2003-03-28 | 2005-06-16 | Marc Mercken | Anti-amyloid antibodies, compositions, methods and uses |
| PE20050627A1 (es) | 2003-05-30 | 2005-08-10 | Wyeth Corp | Anticuerpos humanizados que reconocen el peptido beta amiloideo |
| US20080050357A1 (en) | 2003-08-01 | 2008-02-28 | Claes Gustafsson | Systems and Methods for Antibody Engineering |
| US8005620B2 (en) | 2003-08-01 | 2011-08-23 | Dna Twopointo Inc. | Systems and methods for biopolymer engineering |
| WO2005018424A2 (en) | 2003-08-18 | 2005-03-03 | Research Foundation For Mental Hygiene, Inc. | Antibodies specific for fibrillar amyloid and a procedure to detect fibrillar amyloid deposits |
| SE0401601D0 (sv) | 2004-06-21 | 2004-06-21 | Bioarctic Neuroscience Ab | Protofibril specific antibodies and uses thereof |
| AU2005290250A1 (en) | 2004-07-30 | 2006-04-06 | Rinat Neuroscience Corp. | Antibodies directed against amyloid-beta peptide and methods using same |
| TWI374935B (en) | 2004-08-27 | 2012-10-21 | Pfizer Ireland Pharmaceuticals | Production of α-abeta |
| AU2005294131A1 (en) | 2004-10-05 | 2006-04-20 | Wyeth | Methods and compositions for improving recombinant protein production |
| BRPI0518151A2 (pt) | 2004-10-13 | 2009-06-16 | Ablynx Nv | polipetìdeos contra amiloide-beta, ácido nucléico que codifica tal polipetìdeo, composição compreendendo tal polipetìdeo, método para produzir um polipetìdeo e uso do mesmo |
| TW200635608A (en) | 2004-12-15 | 2006-10-16 | Neuralab Ltd | Aβ antibodies for use in improving cognition |
| GT200600031A (es) | 2005-01-28 | 2006-08-29 | Formulacion anticuerpo anti a beta | |
| NZ565044A (en) | 2005-06-17 | 2010-05-28 | Elan Pharma Int Ltd | Methods of purifying anti A beta antibodies with calcium chloride |
| JP5475994B2 (ja) | 2005-11-30 | 2014-04-16 | アッヴィ・インコーポレイテッド | 抗Aβグロブロマー抗体、その抗原結合部分、対応するハイブリドーマ、核酸、ベクター、宿主細胞、前記抗体を作製する方法、前記抗体を含む組成物、前記抗体の使用及び前記抗体を使用する方法。 |
| CA2632828C (en) | 2005-12-12 | 2012-07-10 | F. Hoffmann-La Roche Ag | Antibodies against amyloid beta with glycosylation in the variable region |
| EA015654B9 (ru) | 2006-03-30 | 2012-01-30 | Глаксо Груп Лимитед | Антитела против бета-амилоидного пептида |
| US8784810B2 (en) | 2006-04-18 | 2014-07-22 | Janssen Alzheimer Immunotherapy | Treatment of amyloidogenic diseases |
| AR062065A1 (es) | 2006-07-14 | 2008-10-15 | Ac Immune Sa | Anticuerpo humanizado |
| WO2008030251A1 (en) | 2006-09-08 | 2008-03-13 | Georgetown University | Deglycosylated anti-amyloid beta antibodies |
| HUE033466T2 (en) | 2006-10-02 | 2017-12-28 | Ac Immune Sa | Humanized antibody to beta-amyloid |
| EP3239174A1 (en) | 2007-01-05 | 2017-11-01 | University of Zurich | Anti-beta-amyloid antibody and uses thereof |
| HRP20140049T1 (hr) | 2007-01-05 | 2014-02-28 | University Of Zürich | Anti beta-amiloid antitijela i njihova upotreba |
| US8003097B2 (en) | 2007-04-18 | 2011-08-23 | Janssen Alzheimer Immunotherapy | Treatment of cerebral amyloid angiopathy |
| CN101970000A (zh) | 2007-04-18 | 2011-02-09 | 杨森阿尔茨海默氏症免疫治疗公司 | 脑淀粉样血管病的预防和治疗 |
| SG182192A1 (en) | 2007-06-12 | 2012-07-30 | Ac Immune Sa | Humanized antibodies to amyloid beta |
| SG178809A1 (en) | 2007-10-05 | 2012-03-29 | Genentech Inc | Use of anti-amyloid beta antibody in ocular diseases |
| JO3076B1 (ar) | 2007-10-17 | 2017-03-15 | Janssen Alzheimer Immunotherap | نظم العلاج المناعي المعتمد على حالة apoe |
| US20100291071A1 (en) | 2008-08-01 | 2010-11-18 | Immunas Pharma, Inc. | Antibody Specific Binding to A-Beta Oligomer and the Use |
| JPWO2009051220A1 (ja) | 2007-10-19 | 2011-03-03 | イムナス・ファーマ株式会社 | Aβオリゴマーに特異的に結合する抗体およびその利用 |
| EP2207568B1 (en) | 2007-11-16 | 2017-05-31 | The Rockefeller University | Antibodies specific for the protofibril form of beta-amyloid protein |
| WO2009099176A1 (ja) | 2008-02-08 | 2009-08-13 | Immunas Pharma, Inc. | Aβオリゴマーに特異的に結合する抗体およびその利用 |
| US9109026B2 (en) | 2008-06-03 | 2015-08-18 | Abbvie, Inc. | Dual variable domain immunoglobulins and uses thereof |
| US7561973B1 (en) | 2008-07-31 | 2009-07-14 | Dna Twopointo, Inc. | Methods for determining properties that affect an expression property value of polynucleotides in an expression system |
| US8126653B2 (en) | 2008-07-31 | 2012-02-28 | Dna Twopointo, Inc. | Synthetic nucleic acids for expression of encoded proteins |
| JP5674654B2 (ja) | 2008-07-08 | 2015-02-25 | アッヴィ・インコーポレイテッド | プロスタグランジンe2二重可変ドメイン免疫グロブリンおよびその使用 |
| US20110182809A1 (en) | 2008-07-09 | 2011-07-28 | University Of Zurich | Method of Promoting Neurogenesis |
| WO2010030203A1 (en) | 2008-09-09 | 2010-03-18 | Biocodex - Incubação De Empresas De Ciências Da Vida, S.A. | Monoclonal antibody to human amyloidogenic and modified forms of transthyretin and its use in the detection and treatment of fap and pathologies presenting modified ttr |
| US9067981B1 (en) | 2008-10-30 | 2015-06-30 | Janssen Sciences Ireland Uc | Hybrid amyloid-beta antibodies |
| DK2419447T3 (en) | 2009-04-17 | 2017-09-25 | Immunas Pharma Inc | ANTIBODIES THAT SPECIFICALLY BIND TO A BETA OLIGOMER AND USE THEREOF |
| WO2010129276A2 (en) | 2009-04-27 | 2010-11-11 | Case Western Reserve University | PYRO-GLUTAMATE Aβ TARGETING AGENTS |
| TW201116624A (en) | 2009-05-01 | 2011-05-16 | Abbott Lab | Dual variable domain immunoglobulin and uses thereof |
| JP5932642B2 (ja) | 2009-07-02 | 2016-06-08 | アンジオケム インコーポレーテッド | 多量体ペプチドコンジュゲートおよびその使用 |
| ES2624835T3 (es) | 2009-08-06 | 2017-07-17 | Immunas Pharma, Inc. | Anticuerpos que se unen específicamente a los oligómeros A beta y uso de los mismos |
| WO2011031720A1 (en) | 2009-09-11 | 2011-03-17 | Arizona Board Of Regents Acting For And On Behalf Of Arizona State University | Bispecific nanobodies as a therapeutic for alzheimer's disease |
| CA2788275A1 (en) | 2010-03-03 | 2011-09-09 | Boehringer Ingelheim International Gmbh | Biparatopic abeta binding polypeptides |
| ES2684475T3 (es) | 2010-04-15 | 2018-10-03 | Abbvie Inc. | Proteínas que se unen a beta amiloide |
| US9320793B2 (en) | 2010-07-14 | 2016-04-26 | Acumen Pharmaceuticals, Inc. | Method for treating a disease associated with soluble, oligomeric species of amyloid beta 1-42 |
| MX341369B (es) | 2010-07-30 | 2016-08-17 | Genentech Inc * | Anticuerpo anti-beta-amiloide humanizado seguro y funcional. |
| PT3042917T (pt) | 2010-08-12 | 2018-05-02 | Lilly Co Eli | Anticorpos do péptido beta amilóide anti-n3pglu e seus usos |
| WO2012021475A2 (en) | 2010-08-12 | 2012-02-16 | Eli Lilly And Company | ANTI-N3pGlu AMYLOID BETA PEPTIDE ANTIBODIES AND USES THEREOF |
| WO2012136552A1 (en) | 2011-04-08 | 2012-10-11 | H. Lundbeck A/S | ANTIBODIES SPECIFIC TO PYROGLUTAMATED Αβ |
| US9534016B2 (en) | 2011-11-28 | 2017-01-03 | Buck Institute For Research On Aging | Netrin loop peptide mimetics and uses thereof |
| JP6342333B2 (ja) * | 2012-01-27 | 2018-06-13 | プロセナ バイオサイエンシーズ リミテッド | α−シヌクレインを認識するヒト化抗体 |
| ITRM20120383A1 (it) | 2012-03-20 | 2013-09-21 | Uni Degli Studi Di Milano B Icocca | Metodo e kit per la rivelazione di anticorpi. |
| KR20150036163A (ko) | 2012-07-03 | 2015-04-07 | 얀센 알츠하이머 이뮤노테라피 | C―말단 및 중심 에피토프 a―베타 항체 |
| HK1215673A1 (zh) | 2012-12-07 | 2016-09-09 | Biogen International Neuroscience Gmbh | 一個使用抗ab抗體減少腦部澱粉蛋白質斑的方法 |
| US20140314741A1 (en) * | 2013-04-18 | 2014-10-23 | Developmen Center For Biotechnology | Human Antibody against Interleukin-20 and Treatment for Inflammatory Diseases |
| US9486559B2 (en) | 2013-05-07 | 2016-11-08 | Abbott Cardiovascular Systems Inc. | Methods of treatment with a bioresorbable scaffold for neurologic drug delivery |
| US10513555B2 (en) | 2013-07-04 | 2019-12-24 | Prothena Biosciences Limited | Antibody formulations and methods |
| US20160355573A1 (en) | 2013-09-05 | 2016-12-08 | Cornell University | Gene therapy for alzheimer's and other neurodegenerative diseases and conditions |
| DK3083681T3 (da) | 2013-12-20 | 2020-08-24 | Neurimmune Holding Ag | Antistofbaseret terapi af transthyretin- (ttr) amyloidose og human-afledte antistoffer dertil |
| CN106456729A (zh) | 2014-02-08 | 2017-02-22 | 豪夫迈·罗氏有限公司 | 治疗阿尔茨海默氏病的方法 |
| CA2944402A1 (en) | 2014-04-08 | 2015-10-15 | Prothena Biosciences Limited | Blood-brain barrier shuttles containing antibodies recognizing alpha-synuclein |
| WO2015165961A1 (en) | 2014-04-29 | 2015-11-05 | Affiris Ag | Treatment and prevention of alzheimer's disease (ad) |
| US20170152306A1 (en) | 2014-05-16 | 2017-06-01 | Universitat Autonoma De Barcelona | Single chain variable fragment (scfv) elongation mutants |
| WO2015191934A2 (en) * | 2014-06-11 | 2015-12-17 | Abbvie Inc. | Blood-brain barrier (bbb) penetrating dual specific binding proteins for treating brain and neurological diseases |
| JP6628786B2 (ja) | 2014-07-10 | 2020-01-15 | バイオアークティック アーベー | 改善されたAβプロトフィブリル結合抗体 |
| MX391037B (es) | 2014-07-29 | 2025-03-21 | Neurimmune Holding Ag | Anticuerpos anti-huntingtina (htt) derivados de humano y usos de los mismos. |
| WO2016040903A1 (en) | 2014-09-11 | 2016-03-17 | Board Of Regents Of The University Of Texas System | Detection of misfolded amyloid beta protein |
| MA41115A (fr) | 2014-12-02 | 2017-10-10 | Biogen Int Neuroscience Gmbh | Procédé de traitement de la maladie d'alzheimer |
| JP2018501482A (ja) | 2014-12-19 | 2018-01-18 | プロビオドルグ エージー | pGlu−Abetaペプチドの検出のための新規の方法 |
| WO2016137947A1 (en) | 2015-02-24 | 2016-09-01 | Rpeptide, Llc | Anti-amyloid-beta antibodies |
| EP3322723A2 (en) | 2015-07-16 | 2018-05-23 | Probiodrug AG | Anti-pyroglutamated amyloid beta humanized antibodies |
| CR20180365A (es) | 2015-12-16 | 2018-09-28 | Amgen Inc | PROTEÍNAS DE UNIÓN AL ANTÍGENO BISPECÍFICO DE ANTI-TL1A/ANTI-TNF-a Y SUS USOS |
| JOP20170004B1 (ar) | 2016-01-15 | 2022-09-15 | Lilly Co Eli | الأجسام المضادة لببتيد بيتا النشوي مضاد N3pGlu واستخداماته |
| BR112018014762A2 (pt) | 2016-01-20 | 2018-12-26 | Genentech Inc | método de tratamento da doença de alzheimer (da) precoce |
| DK3430397T3 (da) | 2016-03-14 | 2022-05-02 | Biogen Int Neuroscience Gmbh | Antistofafhængig cellemedieret fagocytoseassay til pålidelig måling af optagelse af aggregerede proteiner |
| WO2017186928A1 (en) | 2016-04-29 | 2017-11-02 | Curevac Ag | Rna encoding an antibody |
| CA3026598A1 (en) | 2016-06-07 | 2017-12-14 | Biogen International Neuroscience Gmbh | Methods for treating alzheimer's disease |
| CA3030872A1 (en) | 2016-07-19 | 2018-01-25 | Annexon, Inc. | Compositions and methods for treating frontotemporal dementia |
| CN117244056A (zh) | 2016-10-27 | 2023-12-19 | 卫材研究发展管理有限公司 | 用于治疗阿尔茨海默病的含有抗Aβ初原纤维抗体和β-分泌酶BACE1抑制剂的组合物 |
| TW201827467A (zh) | 2016-11-03 | 2018-08-01 | 比利時商健生藥品公司 | 焦穀胺酸類澱粉蛋白-β之抗體及其用途 |
| JP7217229B2 (ja) | 2016-11-15 | 2023-02-02 | ハー・ルンドベック・アクチエゼルスカベット | シヌクレイノパチーの治療のための薬剤、使用および方法 |
| WO2018119001A1 (en) | 2016-12-19 | 2018-06-28 | Fred Hutchinson Cancer Research Center | Peptide-antibody compositions and methods of use thereof |
| EP3354278A1 (en) | 2017-01-31 | 2018-08-01 | Sanofi | Neuronal cell protective effect of antibodies specific for the protofibrillar form of the beta-amyloid peptide |
| WO2018204408A1 (en) | 2017-05-02 | 2018-11-08 | Sanford Burnham Prebys Medical Discovery Institute | Methods of diagnosing and treating alzheimer's disease |
| EP3431496A1 (en) | 2017-07-19 | 2019-01-23 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Anti- isoasp7 amyloid beta antibodies and uses thereof |
| WO2019040612A1 (en) | 2017-08-22 | 2019-02-28 | Biogen Ma Inc. | PHARMACEUTICAL COMPOSITIONS CONTAINING ANTI-BETA-AMYLOID ANTIBODIES |
| US20190153102A1 (en) | 2017-09-28 | 2019-05-23 | Prothena Biosciences Limited | Dosing regimes for treatment of synucleinopathies |
| CA3076313A1 (en) | 2017-09-28 | 2019-04-04 | Prothena Biosciences Limited | Dosing regimes for treatment of synucleinopathies |
| US20200330592A1 (en) | 2017-10-09 | 2020-10-22 | Keith Black | Compositions and methods of treating alzheimer's and other amyloid related diseases |
| WO2019157440A1 (en) | 2018-02-09 | 2019-08-15 | The Trustees Of Dartmouth College | Chimeric antigen receptors for treatment of neurodegenerative diseases and disorders |
| US12325741B2 (en) | 2018-07-17 | 2025-06-10 | Jiangsu Hengrui Medicine Co., Ltd. | Anti-Aβ antibodies and antigen-binding fragments thereof |
| WO2020023530A2 (en) | 2018-07-24 | 2020-01-30 | Eisai R&D Management Co., Ltd. | Methods of treatment and prevention of alzheimer's disease |
| CN112584863B (zh) | 2018-08-17 | 2025-10-28 | Ab工作室有限公司 | 催化抗体和其使用方法 |
| US20200140533A1 (en) | 2018-11-02 | 2020-05-07 | Annexon, Inc. | Compositions and methods for treating brain injury |
| KR20210143752A (ko) | 2019-02-12 | 2021-11-29 | 프로테나 바이오사이언시즈 리미티드 | 항체-생산 세포 및 기타 면역 세포 상의 cd38 세포 막 분자 및 면역글로불린 경쇄에 대한 단일클론 항체들의 조합을 이용한 al 아밀로이드증의 치료 |
| BR112021019107A2 (pt) | 2019-03-26 | 2021-11-30 | Janssen Pharmaceutica Nv | Anticorpos contra amiloide-beta piroglutamato e usos dos mesmos |
| WO2020198866A1 (en) | 2019-04-04 | 2020-10-08 | The Royal Institution For The Advancement Of Learning / Mcgill University | USE OF Aß34 TO ASSESS ALZHEIMER'S DISEASE PROGRESSION |
| JP2022544640A (ja) | 2019-06-21 | 2022-10-20 | ユニバーシティ オブ カンザス | 脳疾患の治療に有用な組成物および方法 |
| ES2821599A1 (es) | 2019-10-24 | 2021-04-26 | Univ Del Pais Vasco / Euskal Herriko Unibertsitatea | Compuestos y metodos para el tratamiento de la enfermedad de alzheimer |
| WO2021113899A1 (en) | 2019-12-11 | 2021-06-17 | Ambetex Pty Ltd | Therapeutic compositions comprising an amyloid beta antibody or vaccine for prevention and treatment of diastolic dysfunction |
| PL4121007T3 (pl) | 2020-03-20 | 2025-11-03 | Eisai R&D Management Co., Ltd. | Formulacje o wysokim stężeniu przeciwciała przeciwko protofibrilom peptydu beta-amyloidowego i sposoby ich zastosowania |
| JP2023535024A (ja) | 2020-07-23 | 2023-08-15 | オター プロシーナ リミテッド | 抗aベータ抗体 |
-
2021
- 2021-07-23 JP JP2023504285A patent/JP2023535024A/ja active Pending
- 2021-07-23 BR BR112023001061A patent/BR112023001061A2/pt unknown
- 2021-07-23 US US17/383,765 patent/US12435129B2/en active Active
- 2021-07-23 PH PH1/2023/550178A patent/PH12023550178A1/en unknown
- 2021-07-23 MX MX2023000949A patent/MX2023000949A/es unknown
- 2021-07-23 WO PCT/US2021/042900 patent/WO2022020680A1/en not_active Ceased
- 2021-07-23 KR KR1020237005881A patent/KR20230039734A/ko active Pending
- 2021-07-23 UY UY0001039337A patent/UY39337A/es unknown
- 2021-07-23 IL IL300059A patent/IL300059A/en unknown
- 2021-07-23 CN CN202180063472.XA patent/CN116348487A/zh active Pending
- 2021-07-23 AU AU2021310926A patent/AU2021310926A1/en active Pending
- 2021-07-23 EP EP21847155.5A patent/EP4185612A4/en active Pending
- 2021-07-23 CA CA3186614A patent/CA3186614A1/en active Pending
- 2021-07-23 TW TW110127255A patent/TW202216760A/zh unknown
- 2021-10-25 US US17/510,140 patent/US11434283B2/en active Active
- 2021-10-25 US US17/510,160 patent/US20220089762A1/en not_active Abandoned
- 2021-10-25 US US17/510,170 patent/US11434285B2/en active Active
- 2021-10-25 US US17/510,150 patent/US11434284B2/en active Active
-
2022
- 2022-04-20 US US17/725,363 patent/US11440953B2/en active Active
- 2022-09-12 US US17/931,386 patent/US20230331828A1/en not_active Abandoned
-
2023
- 2023-01-23 CL CL2023000216A patent/CL2023000216A1/es unknown
-
2024
- 2024-04-01 CL CL2024000953A patent/CL2024000953A1/es unknown
- 2024-12-05 US US18/970,569 patent/US20250179161A1/en active Pending
-
2025
- 2025-01-10 CL CL2025000063A patent/CL2025000063A1/es unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003517461A (ja) * | 1999-05-28 | 2003-05-27 | ニユーララブ・リミテツド | アミロイド形成疾患の予防および処置 |
| JP2010534650A (ja) * | 2007-07-27 | 2010-11-11 | ヤンセン アルツハイマー イミュノセラピー | アミロイド原性疾患の処置 |
Non-Patent Citations (1)
| Title |
|---|
| PNAS, vol. 79, JPN6025032885, 1982, pages 1979 - 1983, ISSN: 0005660551 * |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2021310926A1 (en) | 2023-03-23 |
| US20220242940A1 (en) | 2022-08-04 |
| KR20230039734A (ko) | 2023-03-21 |
| EP4185612A1 (en) | 2023-05-31 |
| BR112023001061A2 (pt) | 2023-04-04 |
| UY39337A (es) | 2022-02-25 |
| CA3186614A1 (en) | 2022-01-27 |
| CL2023000216A1 (es) | 2023-10-20 |
| US20220089762A1 (en) | 2022-03-24 |
| IL300059A (en) | 2023-03-01 |
| US20230331828A1 (en) | 2023-10-19 |
| US20220041700A1 (en) | 2022-02-10 |
| US11434285B2 (en) | 2022-09-06 |
| US12435129B2 (en) | 2025-10-07 |
| MX2023000949A (es) | 2023-02-22 |
| US20220041701A1 (en) | 2022-02-10 |
| PH12023550178A1 (en) | 2023-12-04 |
| TW202216760A (zh) | 2022-05-01 |
| US11434283B2 (en) | 2022-09-06 |
| US11440953B2 (en) | 2022-09-13 |
| CL2024000953A1 (es) | 2024-07-26 |
| US20250179161A1 (en) | 2025-06-05 |
| EP4185612A4 (en) | 2024-12-25 |
| US20220041699A1 (en) | 2022-02-10 |
| WO2022020680A1 (en) | 2022-01-27 |
| US11434284B2 (en) | 2022-09-06 |
| CL2025000063A1 (es) | 2025-05-16 |
| US20220049009A1 (en) | 2022-02-17 |
| CN116348487A (zh) | 2023-06-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11440953B2 (en) | Anti-abeta antibodies | |
| CA2690435C (en) | Humanized antibodies to amyloid beta | |
| JP5765857B2 (ja) | Aβオリゴマーに特異的に結合する抗体およびその利用 | |
| AU2008311365B2 (en) | Humanized antibody | |
| EP2468770A1 (en) | Humanized antibody against amyloid beta | |
| CA2590337A1 (en) | Humanized amyloid beta antibodies for use in improving cognition | |
| JPWO2009051220A1 (ja) | Aβオリゴマーに特異的に結合する抗体およびその利用 | |
| US12351623B2 (en) | Antibody compositions targeting non-phosphorylated alpha-synuclein aggregates | |
| RS53160B (sr) | Humanizovana antitela na beta amiloid | |
| JP2026503664A (ja) | 抗aベータ抗体を用いた神経障害の治療方法 | |
| HK1140433B (en) | Humanized antibodies to amyloid beta |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230324 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240722 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20240722 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241004 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20250808 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20251107 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20251224 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20260115 |