ES2861507T3 - Procedimiento para la preparación de 5-fluoro-1H-pirazoles - Google Patents
Procedimiento para la preparación de 5-fluoro-1H-pirazoles Download PDFInfo
- Publication number
- ES2861507T3 ES2861507T3 ES14802882T ES14802882T ES2861507T3 ES 2861507 T3 ES2861507 T3 ES 2861507T3 ES 14802882 T ES14802882 T ES 14802882T ES 14802882 T ES14802882 T ES 14802882T ES 2861507 T3 ES2861507 T3 ES 2861507T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- formula
- compound
- methyl
- cyano
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 76
- WNDHCIJGEKNYNF-UHFFFAOYSA-N 5-fluoro-1h-pyrazole Chemical class FC=1C=CNN=1 WNDHCIJGEKNYNF-UHFFFAOYSA-N 0.000 title claims abstract description 8
- 238000002360 preparation method Methods 0.000 title description 32
- -1 CF2Cl Chemical group 0.000 claims abstract description 123
- 238000006243 chemical reaction Methods 0.000 claims abstract description 70
- 229910052731 fluorine Inorganic materials 0.000 claims abstract description 45
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims abstract description 25
- 239000012038 nucleophile Substances 0.000 claims abstract description 21
- 230000015572 biosynthetic process Effects 0.000 claims abstract description 17
- 238000003786 synthesis reaction Methods 0.000 claims abstract description 14
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims abstract description 11
- 150000003573 thiols Chemical class 0.000 claims abstract description 11
- 150000001298 alcohols Chemical group 0.000 claims abstract description 10
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 7
- 125000001153 fluoro group Chemical group F* 0.000 claims abstract description 7
- 150000002429 hydrazines Chemical class 0.000 claims abstract description 6
- 150000001336 alkenes Chemical class 0.000 claims abstract description 5
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 claims abstract description 4
- 150000003335 secondary amines Chemical class 0.000 claims abstract description 4
- 125000004953 trihalomethyl group Chemical group 0.000 claims abstract description 4
- 150000001875 compounds Chemical class 0.000 claims description 177
- 239000000460 chlorine Substances 0.000 claims description 57
- 229910052801 chlorine Inorganic materials 0.000 claims description 53
- 229910052739 hydrogen Inorganic materials 0.000 claims description 52
- 239000001257 hydrogen Substances 0.000 claims description 52
- 230000008569 process Effects 0.000 claims description 48
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 45
- 125000000217 alkyl group Chemical group 0.000 claims description 43
- 150000002431 hydrogen Chemical class 0.000 claims description 43
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 41
- 229910052794 bromium Inorganic materials 0.000 claims description 40
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 39
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 39
- 239000011737 fluorine Substances 0.000 claims description 38
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical group CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 claims description 33
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 30
- 229910052736 halogen Inorganic materials 0.000 claims description 28
- 150000002367 halogens Chemical class 0.000 claims description 28
- 125000001424 substituent group Chemical group 0.000 claims description 26
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical group OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 24
- 125000003545 alkoxy group Chemical group 0.000 claims description 21
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 16
- 229910052757 nitrogen Inorganic materials 0.000 claims description 16
- 150000002148 esters Chemical class 0.000 claims description 12
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 11
- UOCLXMDMGBRAIB-UHFFFAOYSA-N 1,1,1-trichloroethane Chemical compound CC(Cl)(Cl)Cl UOCLXMDMGBRAIB-UHFFFAOYSA-N 0.000 claims description 11
- 125000003118 aryl group Chemical group 0.000 claims description 11
- 230000007062 hydrolysis Effects 0.000 claims description 11
- 238000006460 hydrolysis reaction Methods 0.000 claims description 11
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 claims description 10
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 10
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 claims description 10
- 229910052799 carbon Inorganic materials 0.000 claims description 9
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 9
- 125000001997 phenyl group Chemical class [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 9
- 125000004769 (C1-C4) alkylsulfonyl group Chemical group 0.000 claims description 8
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 8
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims description 8
- 125000006727 (C1-C6) alkenyl group Chemical group 0.000 claims description 7
- 125000004739 (C1-C6) alkylsulfonyl group Chemical group 0.000 claims description 7
- 125000005115 alkyl carbamoyl group Chemical group 0.000 claims description 7
- 229910052740 iodine Inorganic materials 0.000 claims description 7
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims description 6
- 150000007529 inorganic bases Chemical class 0.000 claims description 6
- 239000011630 iodine Chemical group 0.000 claims description 6
- 125000004738 (C1-C6) alkyl sulfinyl group Chemical group 0.000 claims description 5
- 125000004916 (C1-C6) alkylcarbonyl group Chemical group 0.000 claims description 5
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 5
- 125000004414 alkyl thio group Chemical group 0.000 claims description 5
- 125000000623 heterocyclic group Chemical group 0.000 claims description 5
- 125000006239 protecting group Chemical group 0.000 claims description 5
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 claims description 4
- 125000004768 (C1-C4) alkylsulfinyl group Chemical group 0.000 claims description 3
- 150000001540 azides Chemical class 0.000 claims description 3
- 150000002222 fluorine compounds Chemical group 0.000 claims description 3
- 150000007522 mineralic acids Chemical class 0.000 claims description 3
- 238000010534 nucleophilic substitution reaction Methods 0.000 claims description 3
- GJVFBWCTGUSGDD-UHFFFAOYSA-L pentamethonium bromide Chemical compound [Br-].[Br-].C[N+](C)(C)CCCCC[N+](C)(C)C GJVFBWCTGUSGDD-UHFFFAOYSA-L 0.000 claims description 3
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 claims description 2
- MEKOFIRRDATTAG-UHFFFAOYSA-N 2,2,5,8-tetramethyl-3,4-dihydrochromen-6-ol Chemical compound C1CC(C)(C)OC2=C1C(C)=C(O)C=C2C MEKOFIRRDATTAG-UHFFFAOYSA-N 0.000 claims description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims 3
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 abstract description 16
- 125000000172 C5-C10 aryl group Chemical group 0.000 abstract 1
- 125000001188 haloalkyl group Chemical group 0.000 abstract 1
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 46
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 36
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 35
- 239000002904 solvent Substances 0.000 description 35
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 30
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 26
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 25
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 25
- 239000002253 acid Substances 0.000 description 23
- 239000002585 base Substances 0.000 description 22
- 239000000203 mixture Substances 0.000 description 22
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 21
- 239000000543 intermediate Substances 0.000 description 20
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 18
- 150000001412 amines Chemical class 0.000 description 17
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 16
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 15
- 230000035484 reaction time Effects 0.000 description 15
- 239000003153 chemical reaction reagent Substances 0.000 description 13
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 12
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 12
- 150000003839 salts Chemical group 0.000 description 12
- FAEGGADNHFKDQX-UHFFFAOYSA-N 1,1,1,3,4,4,5,5,5-nonafluoro-2-(trifluoromethyl)pent-2-ene Chemical compound FC(F)(F)C(C(F)(F)F)=C(F)C(F)(F)C(F)(F)F FAEGGADNHFKDQX-UHFFFAOYSA-N 0.000 description 11
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 11
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 11
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 description 10
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 10
- WLZXOARVJYAXQK-UHFFFAOYSA-N 5-fluoro-1-methyl-3-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole Chemical compound CN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1F WLZXOARVJYAXQK-UHFFFAOYSA-N 0.000 description 10
- 0 CCCOC(*)(C(C(F)(F)F)C(F)(F)F)F Chemical compound CCCOC(*)(C(C(F)(F)F)C(F)(F)F)F 0.000 description 10
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 10
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 10
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 10
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 10
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 10
- 239000011541 reaction mixture Substances 0.000 description 10
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 9
- 235000019439 ethyl acetate Nutrition 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 8
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 8
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 8
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 8
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 8
- 239000012074 organic phase Substances 0.000 description 7
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 6
- 125000001309 chloro group Chemical group Cl* 0.000 description 6
- 230000008878 coupling Effects 0.000 description 6
- 238000010168 coupling process Methods 0.000 description 6
- 238000005859 coupling reaction Methods 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- UAEPNZWRGJTJPN-UHFFFAOYSA-N methylcyclohexane Chemical compound CC1CCCCC1 UAEPNZWRGJTJPN-UHFFFAOYSA-N 0.000 description 6
- 150000003217 pyrazoles Chemical class 0.000 description 6
- FIARMZDBEGVMLV-UHFFFAOYSA-N 1,1,2,2,2-pentafluoroethanolate Chemical group [O-]C(F)(F)C(F)(F)F FIARMZDBEGVMLV-UHFFFAOYSA-N 0.000 description 5
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 5
- 238000005160 1H NMR spectroscopy Methods 0.000 description 5
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 5
- 150000007513 acids Chemical class 0.000 description 5
- 125000004644 alkyl sulfinyl group Chemical group 0.000 description 5
- 238000009835 boiling Methods 0.000 description 5
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 5
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 5
- 125000006216 methylsulfinyl group Chemical group [H]C([H])([H])S(*)=O 0.000 description 5
- 150000002825 nitriles Chemical class 0.000 description 5
- 150000007530 organic bases Chemical class 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 description 5
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 4
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 4
- 229910052783 alkali metal Inorganic materials 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 4
- 239000003054 catalyst Substances 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 4
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 4
- 229940117389 dichlorobenzene Drugs 0.000 description 4
- 239000003085 diluting agent Substances 0.000 description 4
- 150000002170 ethers Chemical class 0.000 description 4
- 125000000896 monocarboxylic acid group Chemical group 0.000 description 4
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 4
- 230000020477 pH reduction Effects 0.000 description 4
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 125000003226 pyrazolyl group Chemical group 0.000 description 4
- LFAGQMCIGQNPJG-UHFFFAOYSA-N silver cyanide Chemical compound [Ag+].N#[C-] LFAGQMCIGQNPJG-UHFFFAOYSA-N 0.000 description 4
- 229910052938 sodium sulfate Inorganic materials 0.000 description 4
- 235000011152 sodium sulphate Nutrition 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 3
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
- FJVPSOPCFRAJEF-UHFFFAOYSA-N 5-(4-bromopyrazol-1-yl)-1-methyl-3-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole Chemical compound CN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1N1N=CC(Br)=C1 FJVPSOPCFRAJEF-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 3
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 3
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 3
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 3
- 238000005481 NMR spectroscopy Methods 0.000 description 3
- 239000007832 Na2SO4 Substances 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 3
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 3
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 3
- KVNRLNFWIYMESJ-UHFFFAOYSA-N butyronitrile Chemical compound CCCC#N KVNRLNFWIYMESJ-UHFFFAOYSA-N 0.000 description 3
- 229950005499 carbon tetrachloride Drugs 0.000 description 3
- 239000012043 crude product Substances 0.000 description 3
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 150000008282 halocarbons Chemical class 0.000 description 3
- 125000001072 heteroaryl group Chemical group 0.000 description 3
- 150000004702 methyl esters Chemical class 0.000 description 3
- GYNNXHKOJHMOHS-UHFFFAOYSA-N methyl-cycloheptane Natural products CC1CCCCCC1 GYNNXHKOJHMOHS-UHFFFAOYSA-N 0.000 description 3
- HDZGCSFEDULWCS-UHFFFAOYSA-N monomethylhydrazine Chemical compound CNN HDZGCSFEDULWCS-UHFFFAOYSA-N 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- HKOOXMFOFWEVGF-UHFFFAOYSA-N phenylhydrazine Chemical compound NNC1=CC=CC=C1 HKOOXMFOFWEVGF-UHFFFAOYSA-N 0.000 description 3
- 229940067157 phenylhydrazine Drugs 0.000 description 3
- NNFCIKHAZHQZJG-UHFFFAOYSA-N potassium cyanide Chemical compound [K+].N#[C-] NNFCIKHAZHQZJG-UHFFFAOYSA-N 0.000 description 3
- 238000007363 ring formation reaction Methods 0.000 description 3
- 238000010898 silica gel chromatography Methods 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 3
- 238000005292 vacuum distillation Methods 0.000 description 3
- RHUYHJGZWVXEHW-UHFFFAOYSA-N 1,1-Dimethyhydrazine Chemical compound CN(C)N RHUYHJGZWVXEHW-UHFFFAOYSA-N 0.000 description 2
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 2
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 2
- 238000004293 19F NMR spectroscopy Methods 0.000 description 2
- OBTZDIRUQWFRFZ-UHFFFAOYSA-N 2-(5-methylfuran-2-yl)-n-(4-methylphenyl)quinoline-4-carboxamide Chemical compound O1C(C)=CC=C1C1=CC(C(=O)NC=2C=CC(C)=CC=2)=C(C=CC=C2)C2=N1 OBTZDIRUQWFRFZ-UHFFFAOYSA-N 0.000 description 2
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 2
- OZOWZLKSWCTNRI-UHFFFAOYSA-N 2-methyl-5-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole-3-carbonitrile Chemical compound CN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1C#N OZOWZLKSWCTNRI-UHFFFAOYSA-N 0.000 description 2
- VGWPBTQRGBEZPD-UHFFFAOYSA-N 2-methyl-5-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole-3-carbonyl chloride Chemical compound CN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1C(Cl)=O VGWPBTQRGBEZPD-UHFFFAOYSA-N 0.000 description 2
- NQACFNIHDULWSY-UHFFFAOYSA-N 2-methyl-5-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole-3-carboxylic acid Chemical compound CN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1C(O)=O NQACFNIHDULWSY-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- 125000006414 CCl Chemical group ClC* 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 2
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- IEDBVGZXRBRHED-UHFFFAOYSA-N FC=1C(C(F)(F)F)=C(C(F)(F)C(F)(F)F)N(N=1)C1=CC=CC=C1 Chemical compound FC=1C(C(F)(F)F)=C(C(F)(F)C(F)(F)F)N(N=1)C1=CC=CC=C1 IEDBVGZXRBRHED-UHFFFAOYSA-N 0.000 description 2
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 2
- LELOWRISYMNNSU-UHFFFAOYSA-N Hydrocyanic acid Natural products N#C LELOWRISYMNNSU-UHFFFAOYSA-N 0.000 description 2
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 2
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical group C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- SPEUIVXLLWOEMJ-UHFFFAOYSA-N acetaldehyde dimethyl acetal Natural products COC(C)OC SPEUIVXLLWOEMJ-UHFFFAOYSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 125000002723 alicyclic group Chemical group 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- HUCVOHYBFXVBRW-UHFFFAOYSA-M caesium hydroxide Chemical compound [OH-].[Cs+] HUCVOHYBFXVBRW-UHFFFAOYSA-M 0.000 description 2
- 150000003857 carboxamides Chemical class 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- 238000000105 evaporative light scattering detection Methods 0.000 description 2
- 229960004285 fomepizole Drugs 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 2
- 229910052500 inorganic mineral Inorganic materials 0.000 description 2
- 230000000749 insecticidal effect Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- 229940098779 methanesulfonic acid Drugs 0.000 description 2
- 235000010755 mineral Nutrition 0.000 description 2
- 239000011707 mineral Substances 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 239000003208 petroleum Substances 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 229910000027 potassium carbonate Inorganic materials 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- PPASLZSBLFJQEF-RKJRWTFHSA-M sodium ascorbate Substances [Na+].OC[C@@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RKJRWTFHSA-M 0.000 description 2
- 235000010378 sodium ascorbate Nutrition 0.000 description 2
- 229960005055 sodium ascorbate Drugs 0.000 description 2
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 2
- 229910000104 sodium hydride Inorganic materials 0.000 description 2
- PPASLZSBLFJQEF-RXSVEWSESA-M sodium-L-ascorbate Chemical compound [Na+].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RXSVEWSESA-M 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- VDZOOKBUILJEDG-UHFFFAOYSA-M tetrabutylammonium hydroxide Chemical compound [OH-].CCCC[N+](CCCC)(CCCC)CCCC VDZOOKBUILJEDG-UHFFFAOYSA-M 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 2
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 2
- 239000002699 waste material Substances 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- 125000006274 (C1-C3)alkoxy group Chemical group 0.000 description 1
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 1
- 125000006763 (C3-C9) cycloalkyl group Chemical group 0.000 description 1
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 1
- PBVZTJDHQVIHFR-UHFFFAOYSA-N 1,1,2,3,3,3-hexafluoroprop-1-ene Chemical compound FC(F)=C(F)C(F)(F)F.FC(F)=C(F)C(F)(F)F PBVZTJDHQVIHFR-UHFFFAOYSA-N 0.000 description 1
- SSUJUUNLZQVZMO-UHFFFAOYSA-N 1,2,3,4,8,9,10,10a-octahydropyrimido[1,2-a]azepine Chemical compound C1CCC=CN2CCCNC21 SSUJUUNLZQVZMO-UHFFFAOYSA-N 0.000 description 1
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical compound CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 description 1
- CYSGHNMQYZDMIA-UHFFFAOYSA-N 1,3-Dimethyl-2-imidazolidinon Chemical compound CN1CCN(C)C1=O CYSGHNMQYZDMIA-UHFFFAOYSA-N 0.000 description 1
- MSICZUYYRQISRC-UHFFFAOYSA-N 1-ethyl-5-fluoro-3-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole Chemical compound CCN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1F MSICZUYYRQISRC-UHFFFAOYSA-N 0.000 description 1
- JIFSQOOKYJPGKL-UHFFFAOYSA-N 1-methyl-3-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole Chemical compound CN1C=C(C(F)(F)F)C(C(F)(F)C(F)(F)F)=N1 JIFSQOOKYJPGKL-UHFFFAOYSA-N 0.000 description 1
- WITMXBRCQWOZPX-UHFFFAOYSA-N 1-phenylpyrazole Chemical compound C1=CC=NN1C1=CC=CC=C1 WITMXBRCQWOZPX-UHFFFAOYSA-N 0.000 description 1
- BNYCHCAYYYRJSH-UHFFFAOYSA-N 1h-pyrazole-5-carboxamide Chemical class NC(=O)C1=CC=NN1 BNYCHCAYYYRJSH-UHFFFAOYSA-N 0.000 description 1
- JVSFQJZRHXAUGT-UHFFFAOYSA-N 2,2-dimethylpropanoyl chloride Chemical compound CC(C)(C)C(Cl)=O JVSFQJZRHXAUGT-UHFFFAOYSA-N 0.000 description 1
- 125000001917 2,4-dinitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C(=C1*)[N+]([O-])=O)[N+]([O-])=O 0.000 description 1
- XSJVWZAETSBXKU-UHFFFAOYSA-N 2-ethoxypropane Chemical compound CCOC(C)C XSJVWZAETSBXKU-UHFFFAOYSA-N 0.000 description 1
- SMUKODJVMQOSAB-UHFFFAOYSA-N 2-ethylbutanoyl chloride Chemical compound CCC(CC)C(Cl)=O SMUKODJVMQOSAB-UHFFFAOYSA-N 0.000 description 1
- YOETUEMZNOLGDB-UHFFFAOYSA-N 2-methylpropyl carbonochloridate Chemical compound CC(C)COC(Cl)=O YOETUEMZNOLGDB-UHFFFAOYSA-N 0.000 description 1
- WVGCPEDBFHEHEZ-UHFFFAOYSA-N 4-bromo-1h-pyrazole Chemical compound BrC=1C=NNC=1 WVGCPEDBFHEHEZ-UHFFFAOYSA-N 0.000 description 1
- GTBFGUQRWWDFAV-UHFFFAOYSA-N 5-amino-n-benzyl-2-chlorobenzamide Chemical compound NC1=CC=C(Cl)C(C(=O)NCC=2C=CC=CC=2)=C1 GTBFGUQRWWDFAV-UHFFFAOYSA-N 0.000 description 1
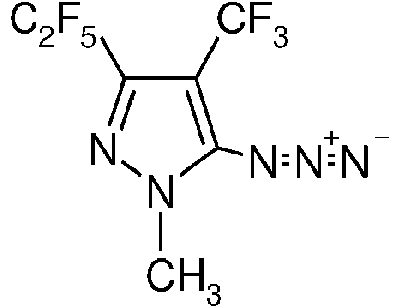
- WZHIPICREBZVHV-UHFFFAOYSA-N 5-azido-1-methyl-3-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole Chemical compound CN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1N=[N+]=[N-] WZHIPICREBZVHV-UHFFFAOYSA-N 0.000 description 1
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 1
- AGSHMPGZWFVZOL-UHFFFAOYSA-N CC(OC)=C(C(F)(F)F)C(F)(F)F Chemical compound CC(OC)=C(C(F)(F)F)C(F)(F)F AGSHMPGZWFVZOL-UHFFFAOYSA-N 0.000 description 1
- KLXDWYWDIFEEOC-UHFFFAOYSA-N CCOC(C)(C(C(F)(F)F)C(F)(F)F)F Chemical compound CCOC(C)(C(C(F)(F)F)C(F)(F)F)F KLXDWYWDIFEEOC-UHFFFAOYSA-N 0.000 description 1
- VLVMZUCSGZJHJZ-UHFFFAOYSA-N Cc1n[n](C)c(C(O)=O)c1C(F)(F)F Chemical compound Cc1n[n](C)c(C(O)=O)c1C(F)(F)F VLVMZUCSGZJHJZ-UHFFFAOYSA-N 0.000 description 1
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- WOEYQBUTVGYDLU-UHFFFAOYSA-N FC(C(F)(F)F)(c(c(C(F)(F)F)c1F)n[n]1-c1ccccc1)F Chemical compound FC(C(F)(F)F)(c(c(C(F)(F)F)c1F)n[n]1-c1ccccc1)F WOEYQBUTVGYDLU-UHFFFAOYSA-N 0.000 description 1
- 102000004961 Furin Human genes 0.000 description 1
- 229910013594 LiOAc Inorganic materials 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 229910021607 Silver chloride Inorganic materials 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- NARLZLCXFUDITJ-UHFFFAOYSA-N [2,3,5,6-tetrafluoro-4-(2,3,5,6-tetrafluoro-4-hydrazinylphenyl)phenyl]hydrazine Chemical group FC1=C(F)C(NN)=C(F)C(F)=C1C1=C(F)C(F)=C(NN)C(F)=C1F NARLZLCXFUDITJ-UHFFFAOYSA-N 0.000 description 1
- TVSDZBUZBHRNBV-UHFFFAOYSA-N [2,3,5,6-tetrafluoro-4-(trifluoromethyl)phenyl]hydrazine Chemical compound NNC1=C(F)C(F)=C(C(F)(F)F)C(F)=C1F TVSDZBUZBHRNBV-UHFFFAOYSA-N 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 238000005903 acid hydrolysis reaction Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910000288 alkali metal carbonate Inorganic materials 0.000 description 1
- 150000008041 alkali metal carbonates Chemical class 0.000 description 1
- 229910000102 alkali metal hydride Inorganic materials 0.000 description 1
- 150000008046 alkali metal hydrides Chemical class 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- 125000005119 alkyl cycloalkyl group Chemical group 0.000 description 1
- 125000005907 alkyl ester group Chemical group 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 125000000852 azido group Chemical group *N=[N+]=[N-] 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- AOGYCOYQMAVAFD-UHFFFAOYSA-N chlorocarbonic acid Chemical class OC(Cl)=O AOGYCOYQMAVAFD-UHFFFAOYSA-N 0.000 description 1
- 229910000365 copper sulfate Inorganic materials 0.000 description 1
- ARUVKPQLZAKDPS-UHFFFAOYSA-L copper(II) sulfate Chemical compound [Cu+2].[O-][S+2]([O-])([O-])[O-] ARUVKPQLZAKDPS-UHFFFAOYSA-L 0.000 description 1
- JZCCFEFSEZPSOG-UHFFFAOYSA-L copper(II) sulfate pentahydrate Chemical compound O.O.O.O.O.[Cu+2].[O-]S([O-])(=O)=O JZCCFEFSEZPSOG-UHFFFAOYSA-L 0.000 description 1
- DOBRDRYODQBAMW-UHFFFAOYSA-N copper(i) cyanide Chemical compound [Cu+].N#[C-] DOBRDRYODQBAMW-UHFFFAOYSA-N 0.000 description 1
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 1
- 239000007822 coupling agent Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- WHRIKZCFRVTHJH-UHFFFAOYSA-N ethylhydrazine Chemical compound CCNN WHRIKZCFRVTHJH-UHFFFAOYSA-N 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 238000002290 gas chromatography-mass spectrometry Methods 0.000 description 1
- 230000002140 halogenating effect Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 239000008241 heterogeneous mixture Substances 0.000 description 1
- HCDGVLDPFQMKDK-UHFFFAOYSA-N hexafluoropropylene Chemical compound FC(F)=C(F)C(F)(F)F HCDGVLDPFQMKDK-UHFFFAOYSA-N 0.000 description 1
- GNOIPBMMFNIUFM-UHFFFAOYSA-N hexamethylphosphoric triamide Chemical compound CN(C)P(=O)(N(C)C)N(C)C GNOIPBMMFNIUFM-UHFFFAOYSA-N 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- GPRLSGONYQIRFK-UHFFFAOYSA-N hydron Chemical compound [H+] GPRLSGONYQIRFK-UHFFFAOYSA-N 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Substances C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 1
- 239000012442 inert solvent Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- XIXADJRWDQXREU-UHFFFAOYSA-M lithium acetate Chemical compound [Li+].CC([O-])=O XIXADJRWDQXREU-UHFFFAOYSA-M 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- DPLHJUQFGXECAS-UHFFFAOYSA-N n-[3-(benzylcarbamoyl)-4-chlorophenyl]-2-methyl-5-(1,1,2,2,2-pentafluoroethyl)-4-(trifluoromethyl)pyrazole-3-carboxamide Chemical compound CN1N=C(C(F)(F)C(F)(F)F)C(C(F)(F)F)=C1C(=O)NC1=CC=C(Cl)C(C(=O)NCC=2C=CC=CC=2)=C1 DPLHJUQFGXECAS-UHFFFAOYSA-N 0.000 description 1
- JIKUXBYRTXDNIY-UHFFFAOYSA-N n-methyl-n-phenylformamide Chemical compound O=CN(C)C1=CC=CC=C1 JIKUXBYRTXDNIY-UHFFFAOYSA-N 0.000 description 1
- ISRXMEYARGEVIU-UHFFFAOYSA-N n-methyl-n-propan-2-ylpropan-2-amine Chemical compound CC(C)N(C)C(C)C ISRXMEYARGEVIU-UHFFFAOYSA-N 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 125000000636 p-nitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)[N+]([O-])=O 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- 125000000538 pentafluorophenyl group Chemical group FC1=C(F)C(F)=C(*)C(F)=C1F 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- FAIAAWCVCHQXDN-UHFFFAOYSA-N phosphorus trichloride Chemical compound ClP(Cl)Cl FAIAAWCVCHQXDN-UHFFFAOYSA-N 0.000 description 1
- 239000003880 polar aprotic solvent Substances 0.000 description 1
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 1
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- IVRIRQXJSNCSPQ-UHFFFAOYSA-N propan-2-yl carbonochloridate Chemical compound CC(C)OC(Cl)=O IVRIRQXJSNCSPQ-UHFFFAOYSA-N 0.000 description 1
- FVSKHRXBFJPNKK-UHFFFAOYSA-N propionitrile Chemical compound CCC#N FVSKHRXBFJPNKK-UHFFFAOYSA-N 0.000 description 1
- 239000003586 protic polar solvent Substances 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 150000003333 secondary alcohols Chemical group 0.000 description 1
- 229940098221 silver cyanide Drugs 0.000 description 1
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- MNWBNISUBARLIT-UHFFFAOYSA-N sodium cyanide Chemical compound [Na+].N#[C-] MNWBNISUBARLIT-UHFFFAOYSA-N 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- HVZJRWJGKQPSFL-UHFFFAOYSA-N tert-Amyl methyl ether Chemical compound CCC(C)(C)OC HVZJRWJGKQPSFL-UHFFFAOYSA-N 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- HFRXJVQOXRXOPP-UHFFFAOYSA-N thionyl bromide Chemical compound BrS(Br)=O HFRXJVQOXRXOPP-UHFFFAOYSA-N 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- 125000005270 trialkylamine group Chemical group 0.000 description 1
- GBXQPDCOMJJCMJ-UHFFFAOYSA-M trimethyl-[6-(trimethylazaniumyl)hexyl]azanium;bromide Chemical compound [Br-].C[N+](C)(C)CCCCCC[N+](C)(C)C GBXQPDCOMJJCMJ-UHFFFAOYSA-M 0.000 description 1
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 1
- 238000002424 x-ray crystallography Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/56—1,2-Diazoles; Hydrogenated 1,2-diazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D231/16—Halogen atoms or nitro radicals
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Dentistry (AREA)
- Wood Science & Technology (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Agronomy & Crop Science (AREA)
- General Health & Medical Sciences (AREA)
- Pest Control & Pesticides (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Un procedimiento para la síntesis de 5-fluoro-1H-pirazoles de la fórmula general (I) **(Ver fórmula)** haciendo reaccionar una olefina de la fórmula general (a) **(Ver fórmula)** con nucleófilos, y opcionalmente una base, seguido de reacción con hidrazinas de fórmula (b) R1-NH-NH2 (b), en la que R1 se selecciona entre alquilo C1-C6, cicloalquilo, arilo C5-C10; R2 es un resto trihalometilo con al menos un átomo de flúor; y R3 se selecciona entre haloalquilo C1-C5 como por ejemplo CF3, CF2Cl, C2F5, C3F7, CF2CF2Cl, CFClCF3, y el nucleófilo se selecciona entre alcoholes, tioles o aminas secundarias, y cuando el nucleófilo es un alcohol o un tiol, también en presencia de una base.
Description
DESCRIPCIÓN
Procedimiento para la preparación de 5-fluoro-1H-pirazoles
Descripción
Los 5-fluoro-1H-pirazoles, en particular el 5-fluoro-1-metil-3-pentafluoroetil-4-trifluorometil-1H-pirazol, son importantes unidades de construcción para la preparación de compuestos químicos para la protección de cultivos, como los descritos en WO 2010051926.
Estado de la técnica:
Se sabe que puede prepararse 5-fluoro-1-metil-3-pentafluoroetil-4-trifluorometil-1H-pirazol mediante el tratamiento del dímero de hexafluoropropeno con N,N-dimetilhidrazina libre de agua en dietiléter a -50 °C seguido por calentamiento del intermedio a 120 °C, I.L. Knunyants y col. Izv. Akad. Nauk SSSR, (1990) 2583-2589.
Sin embargo, esta transformación en dos pasos requiere bajas temperaturas para el primer paso y resulta en la formación de CH3F durante la eliminación térmica en el segundo paso, tornando costoso el procedimiento, desfavorable para el medio ambiente, y de particular dificultad para su aplicación industrial.
Comenzando a partir de perfluoro-2-metil-2-penteno y fenilhidrazina, en presencia de trietilamina a -50 °C, se demostró que el 1 -fenilpirazol puede obtenerse con 90 % de rendimiento (SU 1456419). Furin y col. J. Fluor. Chem.
98(1999) 29 informa que la reacción de perfluoro-2-metil-2-penteno con fenilhidrazina en CH3CN dio una mezcla de pirazoles isoméricos 3 y 4 en una relación 4:1.
Chi, Ki-Whan y col. “Synthesis of fluorinated A/-arylpyrazoles with perfluoro-2-methyl-2-pentene and arylhydrazines,” Journal of fluorine chemistry 98.1 (1999): 29-36 escribe que las reacciones de arilhidrazinas (fenilo, 2-nitrofenilo, 4-nitrofenilo, 2,4-dinitrofenilo, pentafluorofenilo, 4-trifluorometil-2,3,5,6-tetrafluorofenilhidrazina o 4,4'-dihidrazinooctafluorobifenilo) con perfluoro-2 -metil-2 -penteno en presencia de trietilamina han producido efectivamente 1 -aril-perfluoro-3-etil-4-metilpirazol y 1-aril-perfluoro-5-etil-4-metilpirazol en diversas proporciones dependiendo de las condiciones de reacción y de la arilhidrazina usada. Se han aislado en condiciones apropiadas sin- y anti-aminoiminas que podrían ser los intermediarios de pirazoles. Se han discutido las rutas de formación de estos productos y el papel de la trietilamina. La reacción de perfluoro-2-metil-2-penteno con fenilhidrazina se ha investigado en detalle. La estructura del 3-fluoro-5-pentafluoroetil-1-fenil-4-trifluorometilpirazol se ha dilucidado mediante cristalografía de rayos X.
Sin embargo, el uso de monoalquilhidrazinas disponibles comercialmente a bajo costo (especialmente en forma de sus soluciones acuosas) para la síntesis regioselectiva de dichos pirazoles no es conocido en el arte anterior. El problema a resolver por medio de esta invención era identificar un procedimiento simple y selectivo para preparar 5-fluoro-1 H-pirazoles a partir de fluoroalquenos y hidrazinas mono-sustituidas disponibles, que en particular debe ser adaptable a un procedimiento a escala industrial. Como ventaja adicional, este procedimiento debe tener un perfil favorable de seguridad y producción de desechos indeseados.
De manera sorprendente, los 5-fluoro-1H-pirazoles de la fórmula general (I)
pueden prepararse con alta pureza y por un procedimiento corto y simple haciendo reaccionar una olefina de la fórmula general (a)
con nucleófilos, y opcionalmente una base seguido de reacción con hidrazinas de fórmula (b)
R1-NH-NH2 (b),
en la que
R1 se selecciona entre alquilo C1-C6, cicloalquilo, arilo C5-C10;
R2 es un resto trihalometilo con al menos un átomo de flúor; y
R3 se selecciona entre haloalquilo C1-C5, como CF3, CF2G, C2F5 , C3F7 , CF2CF2G, CFGCF3, y
el nucleófilo se selecciona entre alcoholes, tioles o aminas secundarias, y en caso de que el nucleófilo sea un alcohol o un tiol, también en presencia de una base.
De manera sorprendente, se ha descubierto que la interacción de los fluoroalquenos de fórmula (a) en un primer paso con un nucleófilo seleccionado entre el grupo que consiste en alcoholes, tioles, aminas, y dependiendo de la alcalinidad del nucleófilo opcionalmente con una base, seguida por una reacción de los intermedios de fórmula (c) o (d) formados con hidrazinas de fórmula (b), ocurre en forma regioselectiva con alta especificidad para la formación de solo un pirazol isomérico de la fórmula (I) con altos rendimientos.
Los nucleófilos preferidos usados en la reacción de acuerdo con la invención pueden clasificarse de la siguiente manera:
Paso 1: Reacciones con alcoholes o tioles y una base
En la que Y puede ser oxígeno o azufre y los residuos R1, R2, R3 tienen los significados como se han definido anteriormente.
Algunos compuestos de fórmula (c’) y (c’’) pueden prepararse de acuerdo con V. Snegirev y col. Izvestiya Akademii Nauk SSR, Seriya Khimicheskaya, N. 1, pp. 106-119, 1986. Los compuestos preferidos de fórmula (c) se seleccionan entre:
I. Reacciones con aminas secundarias y opcionalmente una base:
en la que
R4 se selecciona en forma independiente entre alquilo C1-12, cicloalquilo C3-8, arilo C6-12 o aril C6-i2-alquilo C1-4, preferentemente alquilo C1-4 y ciclopropilo; o ambos R4 forman junto con el N al cual están unidos un anillo de cinco o seis miembros que contiene, además del N al cual ambos R4 se unen, átomos del anillo seleccionados entre el grupo que consiste en C, O, N y S, preferentemente seleccionados entre C y O, formando, por ejemplo una unidad piperidina, pirrolidina o morfolina, preferentemente una unidad morfolina. Los residuos R1, R2, R3 tienen los significados como se han definido anteriormente.
Los compuestos de fórmulas (d’) y (d’’) puede prepararse de acuerdo con V.Snegirev et al, Izestiya Akademii nauk, SSSR, Seriya Khimicheskaya, N 11, pp, 2561-2568, 1982. Los compuestos preferidos de fórmula V se seleccionan entre:
Preferentemente, los nucleófilos se seleccionan entre alquiUN OH, alcoholes (por ejemplo: metanol, etanol, isopropanol, alcohol bencílico), metilamina, etilamina, dimetilamina. También es posible la combinación de diferentes nucleófilos.
Para los nucleófilos como alcoholes o tioles que no son de naturaleza suficientemente básica, típicamente se añade una base a la reacción en el Paso 1. Para las aminas, preferentemente, no se añade una base adicional.
La reacción puede realizarse en presencia de bases orgánicas e inorgánicas. Las bases orgánicas preferidas para llevar a cabo la reacción son: trimetilamina, trietilamina, tripropilamina, tributilamina, metildiisopropilamina, N-metilmorfolina, piridina, alquilpiridinas, hidróxido de tiometilbencilamonio, hidróxido de tetrabutilamonio, base de Hünig. Preferentemente la base es trietilamina.
Las bases inorgánicas preferidas para llevar a cabo la reacción son: NaHCO3, K2CO3, NaOH, NaHCO3, KF, LiOH, CsOH, Cs2CO3.
La cantidad de base se encuentra en el intervalo desde 1 hasta 7 equivalentes, preferentemente desde 1,5 hasta 4 equivalentes, más preferentemente desde 1,5 hasta 3 equivalentes por cada equivalente del compuesto de fórmula (a).
Generalmente, el tiempo de reacción para la realización del paso 1 no es de importancia crítica y puede depender entre otros factores del volumen de reacción, la naturaleza de la base empleada, y la reactividad del alqueno de fórmula (a). Preferentemente se encuentra en el intervalo desde 1 hasta 5 h, más preferentemente en el intervalo desde 1 hasta 3 h.
De acuerdo con otra forma de realización preferida de la presente invención, la cantidad de nucleófilo usado en la reacción se encuentra en el intervalo desde 1 hasta 5 equivalentes, preferentemente en el intervalo desde 1,2 hasta 3 equivalentes, más preferentemente desde 1 hasta 3 equivalentes por cada equivalente del compuesto de fórmula (a).
La ciclización (paso 2) puede realizarse en diferentes disolventes seleccionados entre
a) alcanos, como hexanos por ejemplo ciclohexano o metilciclohexano;
b) haloalcanos, preferentemente diclorometano, dicloretano;
c) alcoholes, preferentemente metanol, etanol, o isopropanol;
d) nitrilos, preferentemente acetonitrilo, o butironitrilo;
e) amidas, preferentemente dimetilformamida, o dimetilacetamida;
f) éteres como dietiléter, metilferc-butiléter, dimetoxietano, diglima,
g) benceno, tolueno, diclorobenceno, clorobenceno.
Los disolventes particularmente preferidos para la ciclización son diclorometano, dicloroetano, acetonitrilo y butironitrilo, y los disolventes con preferencia máxima para esta reacción son diclorometano, acetonitrilo y butironitrilo De acuerdo con una forma de realización adicional de la presente invención, la ciclización se realiza a temperaturas en el intervalo desde -5 °C hasta 50 °C, más preferentemente a temperaturas en el intervalo desde 0 °C hasta 30 °C, con preferencia máxima desde 0 °C hasta temperatura ambiente. Generalmente, el tiempo de reacción no es de importancia crítica y puede depender del volumen de reacción, preferentemente se encuentra en el intervalo desde 3 hasta 20 h, más preferentemente en el intervalo desde 1 hasta 5 h.
La relación del compuesto de fórmula (III) y el compuesto de fórmula (c’, c’’) o (d’, d’’) puede variar dentro de un amplio intervalo, preferentemente se encuentra en el intervalo desde 0,9 hasta 5 equivalentes, más preferentemente desde 1 hasta 2,5 equivalentes, aún más preferentemente desde 1 hasta 1,5, y con preferencia máxima 1 equivalente de (b) por cada equivalente del compuesto de fórmula (c’, c’’) o (d’, d’’). Una forma de realización preferida de la presente invención se relaciona con un procedimiento para preparar pirazoles de fórmula (la),
en la que R1 se selecciona entre alquilo Ci-C6, preferentemente metilo, y que comprende la reacción de perfluoro-2-metil-2 -penteno
con una hidrazina de fórmula general (b).
R1-NH-NH2 (b)
Una forma de realización particularmente preferida de la presente invención se relaciona con un procedimiento para
preparar pirazoles de fórmula (Ib),
El perfluoro-2-metil-2-penteno está disponible comercialmente (Fa. Daikin y P&M Invest (Rusia)) o puede prepararse por dimerización de hexafluoropropeno, véase US 5.254.774; R.Haszeldiner et al, Journal of the Chemical Society [Section] D: Chemical Communications (1970), (21), 1444-5.
Las monoalquilhidrazinas y monoarilhidrazinas están disponibles comercialmente.
Preferentemente R1 se selecciona entre alquilo, con preferencia particular es metilo.
Preferentemente R2 se selecciona entre CF3, CF2Cl, con preferencia particular es CF3.
Preferentemente R3 se selecciona entre CF3, C2F5, C3F7, CF2CF2Cl, CFClCF3, con preferencia particular es C2F5. Se otorga preferencia máxima a la combinación de R1=metilo, R2=CF3, R3=C2F5.
Paso 3
En el Paso 3, el compuesto de fórmula (I), preferentemente el compuesto (Ia), puede transformarse en su análogo CN de fórmula (6 ) o (6 a), respectivamente
en la que R1 es alquilo (Ci-C4), preferentemente, el compuesto de fórmula (6 ) es un compuesto de fórmula (6 a):
haciendo reaccionar el compuesto (I), preferentemente el compuesto (Ia), con un donante de CN como por ejemplo cianuros alcalinos (por ejemplo, NaCN, KCN, CsCN, o CuCN).
Los disolventes típicos son acetonitrilo, DMF, DMA, N-metilpirrolidona (NMP), sulfolano, dimetoxietano, diglima. Los disolventes preferidos son acetonitrilo, DMF o DMA.
Típicamente, la temperatura para esta reacción es entre 30 °C y 120 °C, preferentemente entre 40 °C y 110 °C, más preferentemente superior a 60 °C como por ejemplo entre 60 °C y 120 °C o entre 60 °C y 100 °C.
Generalmente, el tiempo de reacción no es de importancia crítica y puede depender del volumen de reacción. Preferentemente, el tiempo de reacción es entre 2 h y 8 h, más preferentemente entre 4 y 8 h.
Paso 4
En el Paso 4, un compuesto de fórmula (6 ), preferentemente (6 a), puede transformarse en su análogo ácido carboxílico de fórmula (7), preferentemente de fórmula (7a), respectivamente, de acuerdo con pasos de hidrólisis conocidos en la técnica:
en la que R1 es alquilo C1-C4, preferentemente el compuesto de fórmula (7) es un compuesto de fórmula (7a):
La conversión de un grupo ciano (-CN) en un grupo carboxílico (-COOH) generalmente se lleva a cabo bajo condiciones ácidas o básicas.
Para la hidrólisis ácida, se otorga preferencia a ácidos minerales, por ejemplo H2SO4, HCl, HSO3Cl, HF, HBr, HI, H3PO4 o ácidos orgánicos, por ejemplo CF3COOH, ácido p-toluensulfónico, ácido metansulfónico, ácido trifluorometansulfónico. La reacción puede acelerarse por medio de la adición de catalizadores, por ejemplo FeCl3 , AlCl3 , BF3, SbCl3, NaH2PO4. La reacción también puede realizarse sin adición de ácido, solamente en agua.
La hidrólisis básica se efectúa en presencia de bases inorgánicas como por ejemplo hidróxidos de metales alcalinos, por ejemplo hidróxido de litio, hidróxido de sodio o hidróxido de potasio, carbonatos de metales alcalinos, por ejemplo Na2CO3, K2CO3 y acetatos de metales alcalinos, por ejemplo NaOAc, KOAc, LiOAc, y alcóxidos de metales alcalinos, por ejemplo NaOMe, NaOEt, NaOt-Bu, KOt-Bu o bases orgánicas como por ejemplo trialquilaminas, alquilpiridinas, fosfazenos y 1,8-diazabiciclo[5.4.0]undeceno (DBU). Se otorga preferencia a las bases inorgánicas, por ejemplo NaOH, KOH, Na2CO3 o K2CO3. Para generar la forma ácida protonada de fórmula (7) o (7a), respectivamente, luego debe realizarse un paso de acidificación.
Típicamente, un ácido inorgánico adecuado para realizar la acidificación después de completarse la hidrólisis básica es cualquier ácido que sea más fuerte que la forma desprotonada de un compuesto de fórmula (7) o (7a), respectivamente. Se otorga preferencia a ácidos minerales, por ejemplo H2SO4, HCl, HF, HBr, HI, H3PO4 o ácidos orgánicos, por ejemplo CF3COOH, ácido p-toluensulfónico, ácido metansulfónico, ácido trifluorometansulfónico. Los ácidos preferidos para esta acidificación son HCl o H2SO4.
El paso de reacción puede realizarse en forma pura o en un disolvente. Se otorga preferencia a realizar la reacción en un disolvente. Los disolventes adecuados se seleccionan, por ejemplo, entre el grupo que comprende agua, alcoholes como por ejemplo metanol, etanol, isopropanol o butanol, hidrocarburos alifáticos y aromáticos, por ejemplo n-hexano, benceno o tolueno, que pueden estar sustituidos con flúor y átomos de cloro, como por ejemplo cloruro de metileno, dicloroetano, clorobenceno o diclorobenceno; éteres, por ejemplo dietiléter, difeniléter, metil-ferc-butiléter, isopropiletiléter, dioxano, diglima, dimetilglicol, dimetoxietano (DME) o THF; nitrilos como por ejemplo metilo nitrilo, butilo nitrilo o fenilo nitrilo; amidas como dimetilformamida (DMF) o N-metilpirrolidona o mezclas de dichos disolventes, en la que se otorga preferencia particular a agua, acetonitrilo, diclorometano y alcoholes (etanol). Preferentemente, la reacción se lleva a cabo en agua. El paso de procedimiento de la invención generalmente se lleva a cabo bajo presión estándar. De manera alternativa, sin embargo, también es posible trabajar bajo vacío o bajo presión elevada (por ejemplo reacción en un autoclave con HCl acuoso).
El tiempo de reacción puede seleccionarse, de acuerdo con el tamaño del lote y la temperatura, dentro de un intervalo desde 1 hora hasta varias horas como por ejemplo entre 1 h y 30 h, preferentemente entre 3 h y 20 h.
Se otorga preferencia a la conversión por medio de hidrólisis básica seguida por acidificación.
El paso de procedimiento de la invención se realiza preferentemente dentro de un intervalo de temperatura desde 20 °C hasta 150 °C, más preferentemente a temperaturas desde 30 °C hasta 110 °C, con preferencia máxima desde 30 °C hasta 80 °C.
Generalmente el tiempo de reacción puede seleccionarse, de acuerdo con el tamaño del lote y la temperatura, dentro de un intervalo desde 1 hora hasta varias horas como por ejemplo entre 1 h y 30 h, preferentemente entre 3 h y 20 h.
Compuestos de fórmula (II)
La presente invención también hace referencia a un procedimiento para dar un compuesto insecticida de fórmula (II), preferentemente de fórmula (II’), más preferentemente de fórmula (IIa), basado en la preparación de los compuestos de fórmula (I), más preferentemente de fórmula (Ib). Los compuestos de fórmula (II) son conocidos, por ejemplo, de WO 2010/051926.
en la que
R1 es alquilo C i -C4 , preferentemente metilo; y
A i es C-R2; y
R2 es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo C1-C6 opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o N-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo); preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2 , metilo, etilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, n-propoxi, 1-metiletoxi, fluorometoxi, difluorometoxi, clorodifluorometoxi, diclorofluorometoxi, trifluorometoxi, 2,2,2-trifluoroetoxi, 2-cloro-2,2-difluoroetoxi, pentafluoroetoxi, metilsulfonilo, metilsulfinilo, trifluorometilsulfonilo, trifluorometilsulfinilo o N-ciclopropilaminocarbonilo, más preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2, metilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, o pentafluoroetoxi, preferentemente hidrógeno, flúor, cloro, bromo, con preferencia máxima cloro; y
A2 es C-R3 o nitrógeno; y
R3 es hidrógeno, metilo, flúor o cloro, preferentemente hidrógeno; y
Q es hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C6, aril C6-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3, aminoalquilo C1-C4, aminocarbonil-alquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4, los cuales están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco, preferentemente con uno o dos, más preferentemente con un sustituyente seleccionado en forma independiente entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3, ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoilo C1-C4, cicloalquilcarbamoilo C4-C6 y opcionalmente en forma independiente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoilo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2; preferentemente Q es cicloalquilo C3-C6, o cicloalquilo C3-C6 el cual está sustituido con al menos un sustituyente seleccionado entre el grupo que consiste en cloro, flúor, bromo, yodo, ciano y hidroxi, o aril C6-alquilo C1-C3; más preferentemente ciclopropilo, 1-ciano-ciclopropilo o bencilo (-CH2-C6H5);
preferentemente, el compuesto de fórmula (II) es un compuesto de fórmula (II’):
en la que A1 y A2 y Q son como se definen para el compuesto de fórmula (II), en la que el procedimiento se caracteriza porque comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030].
En una forma de realización preferida, el compuesto de fórmula (II) es el compuesto (IIa) definido por los siguientes sustituyentes:
El nuevo procedimiento de la invención para preparar un compuesto de fórmula (II), preferentemente (II’), más preferentemente (IIa), se caracteriza porque comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030]. En una forma de realización preferida, el procedimiento se caracteriza porque comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030]. En otra forma de realización preferida, el procedimiento comprende además de los pasos 1 y 2 como se describe en los párrafos [0006] a [0030], opcionalmente el Paso 3 y el Paso 4 como se describe en los párrafos [0031] a [0044] y opcionalmente el Paso 6 posterior descrito a continuación. Opcionalmente, el compuesto (8) en el Paso 6 puede prepararse por medio de la reacción indicada edn el Paso 5 que se describe a continuación:
en la que R1 y A 1 y A2 y Q tienen los significados descritos para los compuestos de fórmula (II). LG es cualquier grupo saliente deseado, por ejemplo halógeno o anhidrato.
Típicamente, un derivado amina de la fórmula (8) no hace referencia solamente a la amina sino también a su forma de sal (8)H+ W - en la que W- se selecciona entre -, Cl-, Br-, J-, HSO4-, CH3COO-, BF4-, CH3SO3-, ácido toluensulfónico,CF3COO- o CF3SO3-.
De este modo, una forma de realización preferida hace referencia a la reacción del paso 6 en la que el compuesto de fórmula (8) está presente en su forma de sal (8)H+ W-, en la que W se selecciona entre -, Cl-, Br , J-, HSO4-, CH3COO-, BF4-, CH3SO3-, ácido toluensulfónico,CF3COO- o CF3SO3-.
En una forma de realización más preferida, un compuesto de fórmula (8) es el compuesto (8a) y/o su sal (8a’):
en la que
W-(en el caso del compuesto (8a’)) se selecciona entre el grupo que consiste en F-, Cl-, Br, J-, HSO4-, CH3COO-, BF4-, CH3SO3-, ácido toluensulfónico,CF3COO- o CF3SO3-.
Paso 6
En el Paso 6, compuestos de acuerdo con la invención del tipo (II), preferentemente (II’), más preferentemente (IIa), pueden sintetizarse haciendo reaccionar aminas de la estructura general (8) (o sus sales) con el intermedio (7’) que es una forma activada del derivado ácido carboxílico de fórmula (7), preferentemente de fórmula (7a). La reacción puede llevarse a cabo con o sin disolventes. En este paso, también puede usarse una base adecuada.
en la que R1 es hidrógeno, alquilo Ci-C4 opcionalmente halogenado o ciclopropilo opcionalmente halogenado, preferentemente metilo.
Una forma activada del derivado ácido carboxílico de fórmula 7, preferentemente de fórmula (7a), que se indica en el esquema de reacción del paso 6 anterior con cualquier grupo saliente LG en el grupo -C(=O)LG, comprende a) análogos de fórmula (7) o (7a), respectivamente, en la que el Oh del grupo COOH se reemplaza por un grupo saliente adecuado como por ejemplo halógeno; b) anhidratos de compuestos de fórmula (7) o (7a), respectivamente; o c) compuestos de fórmula (7) o (7a), respectivamente en presencia de un agente de acoplamiento cuya presencia activa el compuesto de fórmula (7) o (7a), respectivamente, en el sentido de la presente invención, como por ejemplo diciclohexilcarbodiimida o 1-hidroxibenzotriazol. Los expertos en la materia conocerán los grupos salientes adecuados, la preparación de anhidratos de ácido carboxílico o reactivos de acoplamiento adecuados para reacciones de ácido / amina y la preparación de dichos compuestos. Los grupos salientes preferidos son haluros de ácido carboxílico como
por ejemplo cloruros o fluoruros de ácido carboxílico.
Los haluros de ácido carboxílico cíclicos, representados entre otros por la estructura general (7'), pueden prepararse simplemente haciendo reaccionar un ácido carboxílico heterocíclico del compuesto (7) con reactivos de halogenación como por ejemplo cloruro de tionilo, bromuro de tionilo, cloruro de fosforilo, cloruro de oxalilo, tricloruro de fósforo, etc. (Houben-Weyl (1952) vol. VIII, p,463 ff.).
Los derivados de amina de la fórmula (7) y sus sales son conocidos en la materia, están disponibles comercialmente o puede prepararse de manera conocida (véase, por ejemplo, WO 2010/051926).
La síntesis de carboxamidas representadas por la fórmula (II), preferentemente (II'), más preferentemente (IIa), sin embargo, puede llevarse a cabo usando reactivos de acoplamiento como por ejemplo diciclohexilcarbodiimida y aditivos como por ejemplo 1-hidroxibenzotriazol (Konig y col. Chem. Ber. (1970), 788-798). también es posible usar reactivos de acoplamiento como por ejemplo 1-etil-3-(3-dimetilaminopropil)carbodiimida, 1,1'-carbonil-1H-imidazol y compuestos similares.
Los reactivos de acoplamiento que se usan para llevar a cabo el procedimiento de síntesis son todos aquellos que son adecuados para la preparación de un enlace éster o amida (cf. por ejemplo Bodansky y col., Peptide Synthesis, 2da ed., Wiley & Sons, Nueva York, 1976; Gross, Meienhofer, The Peptide: Analysis, Synthesis, Biology (Academic Press, Nueva York, 1979).
Además, también pueden usarse anhídridos mixtos para la síntesis de (II), preferentemente (II'), más preferentemente (IIa) (véase, por ejemplo, Anderson et al, J. Am. Chem. Soc (1967), 5012-5017). En este procedimiento es posible usar diversos cloroformiatos, como por ejemplo cloroformiato de isobutilo, cloroformiato de isopropilo. De manera similar, puede usarse cloruro de dietilacetilo, cloruro de trimetilacetilo y similares.
En general, el Paso 6 puede llevarse a cabo opcionalmente, cuando sea apropiado, en presencia de un diluyente/disolvente adecuado y, opcionalmente, cuando sea apropiado, en presencia de un coadyuvante de reacción básico adecuado.
El procedimiento de acuerdo con la invención puede realizarse en presencia de un diluyente/disolvente. Los diluyentes útiles para este fin incluyen todos los disolventes orgánicos inertes, preferentemente hidrocarburos alifáticos, alicíclicos o aromáticos, por ejemplo éter de petróleo, hexano, heptano, ciclohexano, metilciclohexano, benceno, tolueno, xileno o decalina; hidrocarburos halogenados, por ejemplo clorobenceno, diclorobenceno, diclorometano, cloroformo, tetraclorometano, dicloroetano o tricloroetano; éteres como por ejemplo dietiléter, diisopropiléter, metil-t-butiléter, metilt-amiléter, dioxano, tetrahidrofurano, 1,2-dimetoxietano, 1,2-dietoxietano o anisol; cetonas como por ejemplo acetona, butanona, metilisobutilcetona o ciclohexanona; nitrilos como por ejemplo acetonitrilo, propionitrilo, n- o i-butironitrilo o benzonitrilo; amidas como por ejemplo N,N-dimetilformamida, N,N-dimetilacetamida, N-metilformanilida, N-metilpirrolidona o hexametilfosforamida, más preferentemente se usa clorobenceno y tolueno.
Los diluyentes preferidos son hidrocarburos alifáticos, alicíclicos o aromáticos, por ejemplo éter de petróleo, hexano, heptano, ciclohexano, metilciclohexano, benceno, tolueno, xileno o decalina; e hidrocarburos halogenados, por ejemplo clorobenceno, diclorobenceno, diclorometano, cloroformo, tetraclorometano, dicloroetano o tricloroetano; por ejemplo tolueno o clorbenceno.
El disolvente que puede usarse es cualquier disolvente que no afecte adversamente la reacción, como por ejemplo agua. Son adecuados los hidrocarburos aromáticos como por ejemplo benceno o tolueno; hidrocarburos halogenados como por ejemplo diclorometano, cloroformo o tetraclorometano, éteres de cadena abierta o cíclica como por ejemplo dietiléter, dioxano, tetrahidrofurano o 1,2-dimetoxietano; ésteres como por ejemplo acetato de etilo y acetato de butilo; cetonas como por ejemplo acetona, metilisobutilcetona y ciclohexanona; amidas como por ejemplo dimetilformamida y dimetilacetamida; nitrilos como por ejemplo acetonitrilo; y otros disolventes inertes como por ejemplo 1,3-dimetil-2-imidazolidinona; los disolventes puede usarse solos o en combinación de dos o más.
La base (coadyuvante de reacción básico) usada puede ser un aceptor de ácido como una base orgánica como por ejemplo trietilamina, etildiisopropilamina, tri-n-butilamina, piridina y 4-dimetilaminopiridina; además, pueden usarse las siguientes bases, por ejemplo: hidróxidos de metales alcalinos, como por ejemplo hidróxido de sodio e hidróxido de potasio; carbonatos como por ejemplo carbonato ácido de sodio y carbonato de potasio; fosfatos como por ejemplo fosfato ácido de dipotasio y fosfato de disodio; hidruros de metales alcalinos, como por ejemplo hidruro de sodio; alcoholatos de metales alcalinos, como por ejemplo metanolato de sodio y etanolato de sodio. Estas bases pueden usarse en relaciones desde 0,01 hasta 5,0 equivalentes molares en base a (8) y (7'). Además, también puede usarse cianuro de plata(I) como base y activador (véase, por ejemplo, Journal of Organic Chemistry. 1992, 57, 4394-4400; Journal of Medicinal Chemistry 1992, 35, 3905-3918; Journal of Organic Chemistry 2003, 68, 1843-1851).
Sin embargo, en una forma de realización preferida de la presente invención, el Paso 6 se lleva a cabo en ausencia de un aceptor de ácido y el grupo saliente es Cl o F, más preferentemente Cl.
En el contexto de la invención, “en ausencia de un aceptor de ácido” significa en ausencia de un aceptor de ácido distinto del reactivo amina (8) o, en otras palabras, “en ausencia de un aceptor de ácido adicional” en la que “adicional”
significa además del derivado amina de la fórmula (8) (o su sal (8')) que es parte de la reacción. Un “aceptor de ácido adicional” en el sentido de la presente invención puede ser una base además del compuesto amina de acuerdo con la invención o compuestos que reducen la fuerza de un ácido formado como por ejemplo sales, por ejemplo cianuro de plata (AgCN), que son capaces de transformar ácidos fuertes que se forman durante la reacción (anión de grupo saliente más catión hidrógeno) en sales insolubles y ácidos débiles (por ejemplo e1HCl formado (si el grupo saliente es cloro) reacciona con AgCN para dar AgCl insoluble y la base débil HCN).
De manera sorprendente, las carboxamidas de la fórmula (II) pueden prepararse en ausencia de un aceptor de ácido con buenos rendimientos con alta pureza y selectividad. Otra ventaja del procedimiento de acuerdo con la invención es que la preparación es más simple, dado que no es necesario un aceptor de ácido. Esto causa un desperdicio menor o nulo de agua, permite un procedimiento de purificación más fácil sin aislación previa mediante la adición de un alcohol alifático en el mismo recipiente de reacción, y la posibilidad de realizar el procedimiento a mayor concentración. Por lo tanto el producto resultante se obtuvo con un pureza sorprendente superior a 90 % o incluso cercana a 100 %, y con menor requerimiento de reactivos y esfuerzo, mientras que las condiciones previas en presencia de un aceptor de ácido generalmente conducen a una pureza cercana o menor a 90 % El procedimiento de acuerdo con la invención resulta más viable económicamente.
De este modo, una forma de realización preferida hace referencia a una reacción para la producción de compuestos de fórmula (IIa)
en la que el grupo saliente LG hace referencia a F, Cl, Br o I, preferentemente F o Cl, y
en ausencia de un aceptor de ácido adicional al compuesto (8a).
La temperatura de reacción adecuada se encuentra en el intervalo desde -20 °C hasta el punto de ebullición del disolvente particular. En general, la temperatura de reacción es entre 70 °C y 150 °C, preferentemente entre 80 °C y 140 °C, por ejemplo 100 °C o aproximadamente 100 °C como por ejemplo entre 80 °C y 130 °C o entre 80 °C y 120 °C. El tiempo de reacción es entre 1 min y 96 h dependiendo de la selección de volumen, reactivos, disolventes y temperatura de reacción.
Para el procedimiento del paso 6, generalmente se usa entre 0,8 y 1,5 mol, preferentemente entre 0,8 y 1,4 mol, entre 0,9 y 1,4 mol, cantidades equimolares o entre 1 y 1,2 mol de derivado amina de la fórmula (8) o su sal, preferentemente (8a) o (8a'), por cada mol del derivado pirazol-carboxamida (7').
Una forma de realización preferida hace referencia a una reacción del compuesto (8a) o su sal (8a'), respectivamente, con el compuesto (7'), en la que X es Cl y en la que la relación del compuesto (8a) (o su sal (8a')) y (7') en la que X es Cl es entre 1:1 y 1:1,3, preferentemente entre 1:1 y 1:2 como por ejemplo entre 1:1 y 1:1 o incluso 1:1.
Según la selección de volumen, reactivos, disolventes y temperatura de reacción, el tiempo de reacción puede variar entre un minuto y 96 h. Típicamente, el tiempo de reacción es hasta 15 horas, pero la reacción también puede terminarse aún más temprano en el caso de obtenerse una conversión completa. Se otorga preferencia a un tiempo de reacción de 5-10 horas.
La reacción del paso 6 generalmente se lleva a cabo bajo presión estándar. Sin embargo, es posible trabajar bajo presión elevada o reducida, generalmente se prefiere entre 0,1 Mpa y 1 MPa. Es preferible trabajar bajo presión reducida para eliminar el HCl del volumen de reacción.
La reacción del paso 6 generalmente puede llevarse a cabo bajo atmósfera normal. Sin embargo, se prefiere llevar a cabo el procedimiento bajo gas protector como por ejemplo argón. o nitrógeno.
Además los expertos comprenderán que también es posible hacer reaccionar un compuesto de fórmula (7') con un compuesto de fórmula (8*), en la que la unidad -C (=o )-NH-Q de los compuestos de fórmula (8) se reemplaza por una unidad C(=O)-OH o C(=O)-PG en un compuesto de fórmula (8*), en la que PG significa cualquier grupo protector de
grupo carboxílico (como un metiléster, por ejemplo PG representa -O-metilo). Los pasos de desprotección de la unidad carboxílica del compuesto (II*) resultante de una reacción con un compuesto (8*) y/o activación de la unidad carboxílica y/acoplamiento con una amina para dar un compuesto de fórmula (II) son conocidos por los expertos en la materia. Los compuestos de la estructura general (II*) pueden sintetizarse haciendo reaccionar una amina de la estructura general (7) con derivados de ácido carboxílico activados de la estructura general (8*). En este contexto, se aplican las mismas condiciones para la selección del disolvente, las condiciones de reacción, el tiempo de reacción y los reactivos que para la síntesis de (II), descrita anteriormente.
Paso 5
Los compuestos de la estructura general (8) pueden sintetizarse haciendo reaccionar una amina de la estructura general (10) con derivados de ácido carboxílico activados de la estructura general (9). En este contexto, se aplican las mismas condiciones para la selección del disolvente, las condiciones de reacción, el tiempo de reacción y los reactivos que para la síntesis de (II), preferentemente (II’), más preferentemente (IIa), descrita en el Paso 6 anterior.
Compuestos de fórmula (III)
La presente invención también hace referencia a un procedimiento para dar un compuesto insecticida de fórmula (III) o (III’) basado en la preparación de los compuestos de fórmula (I).
en la cual
R1 es alquilo (C1-C4), preferentemente metilo; y
A i es C-R2;
R2 es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo C1-C6 opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o N-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo); preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2, metilo, etilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, n-propoxi, 1-metiletoxi, fluorometoxi, difluorometoxi, clorodifluorometoxi, diclorofluorometoxi, trifluorometoxi, 2,2,2-trifluoroetoxi, 2-cloro-2,2-difluoroetoxi, pentafluoroetoxi, metilsulfonilo, metilsulfinilo, trifluorometilsulfonilo, trifluorometilsulfinilo o N-ciclopropilaminocarbonilo, más preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2, metilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, o pentafluoroetoxi, preferentemente hidrógeno, flúor, cloro, bromo, con preferencia máxima cloro; y
A2 es C-R3 o nitrógeno;
R3 es hidrógeno, metilo, flúor o cloro, preferentemente hidrógeno; y
Q es hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C1-C6 , C6-aril-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3, aminoalquilo C1-C4, aminocarbonil-alquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4, los cuales están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco, preferentemente con uno o dos, más preferentemente con un sustituyente seleccionado en forma independiente entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3, ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoilo C1-C4, cicloalquilcarbamoilo C4-C6 y opcionalmente en forma independiente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoilo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2;
preferentemente Q es cicloalquilo C3-C6, o cicloalquilo C3-C6 el cual está sustituido con al menos un sustituyente seleccionado entre el grupo que consiste en cloro, flúor, bromo, yodo, ciano y hidroxi, o aril C6-alquilo C1-C3 ; más preferentemente ciclopropilo, 1-ciano-ciclopropilo o bencilo (-CH2-C6H5);
T representa uno de los anillos heteroaromáticos de 5 miembros T1-T8 provistos a continuación, en la que el enlace al grupo pirazol principal se marca con un asterisco *,
en la que
R6 en forma independiente en cada caso representa halógeno, ciano, nitro, amino o alquilo C1-C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6, alquilsulfonilo C1-C6, y n representa los valores 0-2, preferentemente 0, con la condición de que n es 0 o 1 en T5, T6 y T8 y con la condición de que n es 0 en T7;
preferentemente, un compuesto de fórmula (III) es un compuesto de fórmula (III’)
en la que A1 y A2 y T y Q tienen los significados provistos anteriormente para el compuesto de fórmula (III) en la que el procedimiento se caracteriza porque comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030]. Debe comprenderse que si n en cualquier fórmula descrita en la presente es 0 (cero), entonces los átomos de carbono del anillo con una valencia libre están sustituidos con hidrógeno.
En una forma de realización preferida, el compuesto de fórmula (III) es el compuesto (IIIa) definido por los siguientes sustituyentes:
El nuevo procedimiento de la invención para preparar un compuesto de fórmula (III), preferentemente (III’), más preferentemente (IIIa), se caracteriza porque el procedimiento comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030]. En otra forma de realización preferida, el procedimiento comprende, además de los pasos 1 y 2 como se describe en los párrafos [0006] a [0030], el Paso 7 y el Paso 8 posteriores:
Los radicales A i , A2 , R1 y Q tienen los significados descritos para el compuesto (NI). Preferentemente, R1 es metilo. Los ciclos de cinco miembros de E1-E3, carbono y nitrógeno representan los heterociclos de 5 miembros definidos bajo T. U representa bromo, yodo o triflato si M representa un ácido borónico, éster borónico o trifluoroboronato. U representa un ácido borónico, éster borónico o trifluoroboronato si M representa bromo, yodo o triflato.
Paso 7
Los compuestos de la estructura general (12) puede prepararse por medio de procedimientos conocidos de la bibliografía por ejemplo por sustitución nucleofílica de F en el anillo aromático (WO2007-107470; Sakya y col., Tetrahedron Letters 2003, 44, 7629-7632) a partir de los materiales de partida de fórmula (I) apropiados, preferentemente (Ia), más preferentemente (Ib), y (11).
Paso 8
Los Compuestos de fórmula (III) o (III'), preferentemente el compuesto (IIIa), pueden prepararse usando reacciones catalizadas por paladio con las contrapartes de reacción (12) y (13) (véase, por ejemplo, WO 2005/040110 o WO 2009/089508). Los compuestos de la estructura general (13) están disponibles comercialmente o pueden prepararse por medio de procedimientos conocidos por los expertos en la materia.
Además, los expertos en la materia comprenderán que es posible como alternativa hacer reaccionar un compuesto de fórmula (12) con un compuesto de fórmula (13*), en la que la unidad -C(=O)-NH-Q de los compuestos de fórmula (13) se reemplaza por una unidad C(=O)-OH o C(=O)-PG en un compuesto de fórmula (13*), en la que PG significa cualquier grupo protector de grupo carboxílico (por ejemplo un alquiléster eomo metiléster, por ejemplo PG representa -O-metilo). Los expertos en la materia conocerán los pasos de desprotección de la unidad carboxílica del compuesto (III*) resultante de una reacción con un compuesto (13*) y/o activación de la unidad carboxílica y/acoplamiento con una amina para dar un compuesto de fórmula (III).
En conclusión, los compuestos de la estructura general (III) pueden sintetizarse haciendo reaccionar una amina de la estructura general (10) con derivados de ácido carboxílico activados de la estructura general (III*). En este contexto, se aplican las mismas condiciones para la selección del disolvente, las condiciones de reacción, el tiempo de reacción y los reactivos que para la síntesis de (II), descrita en el Paso 6 anterior.
En otra forma de realización preferida, la invención hace referencia a un procedimiento para preparar un compuesto de fórmula (III” ), preferentemente de fórmula (III'” ), por ejemplo, conocido de WO 2012/107434:
en la que R1, R6, n, A 1, A2, y Q son como se definen para el compuesto (III), preferentemente; preferentemente, el compuesto de fórmula (III” ) es un compuesto de fórmula (III” ')
en la que R6, n, Ai, A2 y Q son como se definen para el compuesto de fórmula (NI), preferentemente, en la que n es 0, en la que el procedimiento se caracteriza porque comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030].
En una forma de realización preferida, el compuesto de fórmula (NI’’’) es el compuesto (IIIb) definido por los siguientes sustituyentes:
El procedimiento para preparar un compuesto de fórmula (III’’), preferentemente (III’’’), más preferentemente (IIIb), se caracteriza porque comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030]. En otra forma de realización preferida, el procedimiento comprende, además de los pasos 1 y 2 como se describe en los párrafos [0006] a [0030], opcionalmente el Paso 3 y el Paso 4 como se describe en los párrafos [0031] a [004], opcionalmente el Paso 7 y el Paso 8 posteriores como se describe en los párrafos [0081] a [0084] u opcionalmente el Paso 9 y el Paso 10 posteriores. Los Pasos 11 y 12 son conocidos en la materia (véase, por ejemplo, WO 2012/107434).
Paso 9
En el Paso 9, un compuesto de fórmula (I), preferentemente de fórmula (Ia), puede transformarse en su análogo azido de fórmula (14) o (14a), respectivamente:
en la que R1 es hidrógeno, alquilo C1-C4 opcionalmente halogenado o ciclopropilo opcionalmente halogenado, preferentemente metilo,
preferentemente, el compuesto de fórmula (14) es el compuesto (14a)
(14a),
haciendo reaccionar el compuesto (I), preferentemente el compuesto (Ia), más preferentemente el compuesto (Ib), con un donante de azida como una azida de metal alcalino (por ejemplo, NaN3).
Preferentemente, la reacción se lleva a cabo en un disolvente aprótico polar como por ejemplo tetrahidrofurano (THF), acetato de etilo (EtOAc), acetona, dimetilformamida (DMF), acetonitrilo o dimetilsulfóxido (DMSO). Un disolvente preferido es DMSO.
Típicamente, la temperatura de reacción es entre 0°C y 60 °C, preferentemente entre 10 °C y 30 °C, más preferentemente entre 20 °C y 30 °C.
El tiempo de reacción puede depender, entre otros factores, del volumen de reacción y es usualmente entre 0,5 h y 30 h.
Paso 10
En el Paso 10, un intermedio de fórmula (14), preferentemente de fórmula (14a), se hace reaccionar con un intermedio de fórmula (15) para dar un intermedio de fórmula o preferentemente un compuesto de fórmula en la que R1 es metilo, respectivamente:
en la que R1, R6, A1, y A2 son como se definen para el compuesto (III), n es 0 o 1 y PG es cualquier grupo protector del grupo carboxílico como por ejemplo alquilo C1-C6 (por ejemplo, metilo). Preferentemente, R1 en un compuesto de fórmula (III’’*) es metilo (compuesto de fórmula ). Más preferentemente, R1 en la fórmula es metilo y n en la fórmula (III’’*) es 0.
Los compuestos de fórmula (15) están disponibles comercialmente o puede prepararse de acuerdo con procedimientos conocidos en la materia.
Típicamente, el disolvente para la reacción del paso 10 es un disolvente prótico polar como por ejemplo agua, ácido fórmico, n-butanol, isopropanol, nitrometano, etanol, metanol, ácido acético o combinaciones de los mismos. Preferentemente, el disolvente es n-butanol, isopropanol, etanol, agua o combinaciones de los mismos.
La reacción se lleva a cabo en presencia de cobre o un catalizador de cobre como por ejemplo sulfato de cobre o ioduro de cobre (I), opcionalmente en presencia de una base como por ejemplo N-etildiisopropilamina. Sin embargo, también son adecuadas otras bases orgánicas. En el caso de un catalizador de Cu(II), puede usarse un agente reductor como por ejemplo ascorbato de sodio. En el caso de un catalizador de Cu(0), como por ejemplo una sal de amina, puede usarse un agente oxidante (véase, por ejemplo, Angewandte Chemie, International Edition (2009), 48(27), 4900-4908 y referencias citadas, Lutz., Angew. Chem. Int. Ed. 2008, 47, 2182 - 2184 y referencias citadas, y Bock y col., Eur. J. Org. Chem.(2006), 51-68 y referencias citadas).
Comenzando a partir de un compuesto de fórmula (III’’*), pueden prepararse fácilmente los compuestos de fórmula (III), (III’), (III’’), (III’’’), (IIIb), (III’’’’), (IV) o (IV’) de acuerdo con procedimientos conocidos en la materia (véase, por ejemplo WO 2012/107434).
Paso 11
El compuesto de fórmula (III’’’’) puede prepararse por reacción de un compuesto de fórmula (III’’*) en la que O-PG es alcoxi C1-C6 por hidrólisis. Por ejemplo, en el caso en la que -O-PG es metoxi o etoxi, la hidrólisis puede realizarse con agua y una base, como por ejemplo hidróxido de potasio o hidróxido de litio, en ausencia o en presencia de un disolvente, como por ejemplo tetrahidrofurano o metanol. En el caso en la que R es, por ejemplo, ferc-butoxi, la hidrólisis se realiza en presencia de ácido, como por ejemplo ácido trifluoroacético o ácido clorhídrico. La reacción se lleva a cabo a una temperatura de entre -120 °C y 130 °C, preferentemente entre -100 °C y 100 °C.
en la que R1, R6, n, Ai, y A2 son como se definen para el compuesto (NI), preferentemente R1 es metilo y n es 0. Los compuestos de la estructura general (III) pueden sintetizarse haciendo reaccionar una amina de la estructura general (10) con derivados de ácido carboxílico activados de la estructura general (NI’’’’). En este contexto, se aplican las mismas condiciones para la selección del disolvente, las condiciones de reacción, el tiempo de reacción y los reactivos que para la síntesis de (II) descrita en el Paso 6 anterior.
Compuestos de fórmula (IV)
También se describe en el presente documento un procedimiento para la preparación de un compuesto de fórmula (IV), preferentemente de fórmula (IV’):
en la cual
R1 es alquilo C1-C4 , preferentemente metilo; y
A 1 es C-R2; y
R2 es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo C1-C6 opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o N-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo); preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2, metilo, etilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, n-propoxi, 1-metiletoxi, fluorometoxi, difluorometoxi, clorodifluorometoxi, diclorofluorometoxi, trifluorometoxi, 2,2,2-trifluoroetoxi, 2-cloro-2,2-difluoroetoxi, pentafluoroetoxi, metilsulfonilo, metilsulfinilo, trifluorometilsulfonilo, trifluorometilsulfinilo o N-ciclopropilaminocarbonilo, más preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2, metilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, o pentafluoroetoxi, preferentemente hidrógeno, flúor, cloro, bromo, con preferencia máxima cloro; y
A2 es C-R3 o nitrógeno; y
R3 es hidrógeno, metilo, flúor o cloro, preferentemente hidrógeno; y
T representa uno de los anillos heteroaromáticos de 5 miembros T1-T9 provistos a continuación, en la que el enlace al grupo pirazol principal se marca con un asterisco *,
T5 T6 T7 T8
o *-C(=O)-NH
T9 y
R6 en forma independiente en cada caso representa halógeno, ciano, nitro, amino o alquilo C i -C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6 , alquilsulfonilo n representa los valores 0-2, preferentemente 0, con la condición de que n es 0 o 1 en T5, T6 y T8 y con la condición de que n es 0 en T7.
Q es hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C6 , aril C6-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3, aminoalquilo C1-C4, aminocarbonil-alquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4, los cuales están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco, preferentemente con uno o dos, más preferentemente con un sustituyente seleccionado en forma independiente entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3 , ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4 , alquilcarbamoilo C1-C4 , cicloalquilcarbamoilo C4-C6 y opcionalmente en forma independiente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoilo C1-C2, alquilo C1-C2 , alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2; preferentemente Q es cicloalquilo C3-C6, o cicloalquilo C3-C6 el cual está sustituido con al menos un sustituyente seleccionado entre el grupo que consiste en cloro, flúor, bromo, yodo, ciano y hidroxi, o aril C6-alquilo C1-C3 ; más preferentemente ciclopropilo, 1-ciano-ciclopropilo o bencilo (-CH2-C6H5);
preferentemente, el compuesto de fórmula (IV) es un compuesto de fórmula (IV’):
en la que T, A 1, A2 y Q son como se definen para el compuesto de fórmula (IV), en la que preferentemente T se selecciona entre T3, T8 o T9, en la que el procedimiento se caracteriza porque comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030].
Una caso hace referencia a un procedimiento para la preparación del compuesto (IV) en la que R1, en todas las fórmulas descritas en la presente en la que R1 está presente, representa metilo.
Otro caso hace referencia a un procedimiento para la preparación del compuesto (IV) en la que n, en todas las fórmulas descritas en la presente en la que n está presente, representa 0.
Otro caso hace referencia a un procedimiento para la preparación del compuesto (IV) en la que A 1, en todas las fórmulas descritas en la presente en la que A1 está presente, representa C-R2 , en la que R2 representa hidrógeno, flúor, cloro o bromo, con preferencia máxima en la que R2 representa cloro.
Otro caso hace referencia a un procedimiento para la preparación del compuesto (IV) en la que A2 , en todas las fórmulas descritas en la presente en la que A2 está presente, representa C-R3 en la que R3 representa hidrógeno.
Otro caso hace referencia a un procedimiento para la preparación del compuesto (IV) en la que T, en la fórmula (IV) y todas las otras fórmulas descritas en la presente en la que T está presente, representa T3, T8 o T9.
Otro caso hace referencia a un procedimiento para la preparación del compuesto IV en la que Q, en todas las fórmulas descritas en la presente en la que Q está presente, representa cicloalquilo C3-C6 o aril C6-alquilo C1-C3 opcionalmente sustituido con ciano, aún más preferentemente Q representa C3-cicloalquilo o bencilo opcionalmente sustituido con ciano, aún más preferentemente, Q representa bencilo o ciclopropilo sustituido con ciano (por ejemplo, 1-cianociclopropilo).
Otro caso hace referencia a un procedimiento para la preparación del compuesto (IV) en la que R1, en todas las fórmulas descritas en la presente en la que R1 está presente, representa metilo y n, en todas las fórmulas descritas en la presente en la que n está presente, representa 0 y A 1 , en todas las fórmulas descritas en la presente en la que
Ai está presente, representa C-Cl y A2, en todas las fórmulas descritas en la presente en la que A2 está presente, representa C-H y en la que T, en la fórmula (IV) y todas las otras fórmulas descritas en la presente en la que T está presente, representa T3, T8 o T9, y Q en todas las fórmulas descritas en la presente en la que Q está presente representa cicloalquilo C3-C6 o aril C6-alquilo C1-C3 opcionalmente sustituido con ciano.
Otro caso hace referencia a un procedimiento para la preparación del compuesto IV en la que R1, en todas las fórmulas descritas en la presente en la que R1 está presente, representa metilo y T, en todas las fórmulas descritas en la presente en la que T está presente, representa T3, T8 o T9 y n, en todas las fórmulas descritas en la presente en la que n está presente, representa 0 y A1, en todas las fórmulas descritas en la presente en la que A1 está presente, representa C-Cl y A2, en todas las fórmulas descritas en la presente en la que A2 está presente, representa C-H y Q, en todas las fórmulas descritas en la presente en la que Q está presente, representa bencilo o ciclopropilo sustituido con ciano (por ejemplo 1-ciano-ciclopropilo).
La presente invención también hace referencia a un procedimiento para la preparación de un compuesto de fórmula (6), preferentemente de fórmula (6a), que comprende los pasos 1 y 2 como se describe en los párrafos[0006] a [0030], opcionalmente el Paso 3 y el Paso 4 como se describe en los párrafos [0031] a [0044].
La presente invención también hace referencia a un procedimiento para la preparación de un compuesto de fórmula (6) , preferentemente de fórmula (6a), que comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030], opcionalmente el Paso 3 y el Paso 4 como se describe en los párrafos [0031] a [0044], o que comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030] y el Paso 3 como se describe en los párrafos [0031] a [0034].
La presente invención también hace referencia a un procedimiento para la preparación de un compuesto de fórmula (7) , preferentemente de fórmula (7a), que comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030].
La presente invención también hace referencia a un procedimiento para la preparación de un compuesto de fórmula (7), preferentemente de fórmula (7a), que comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030]; o a un procedimiento para la preparación de un compuesto de fórmula (I), preferentemente de fórmula (7a) que comprende los pasos 1 y 2 como se describe en los párrafos [0006] a [0030] y el Paso 3 y el Paso 4 como se describe en los párrafos [0031] a [0044].
En un aspecto, la presente invención también hace referencia al uso de compuestos de fórmula (I) preparados por medio de un procedimiento que comprende al menos los pasos 1 y 2 como se describe en los párrafos [0006] a [0030] para preparar un compuesto de fórmula (II), preferentemente de fórmula (IIa).
Además, la presente invención también hace referencia al uso de compuestos de fórmula (1) preparados por medio de un procedimiento que comprende al menos los pasos 1 y 2 como se describe en los párrafos [0006] a [0030] para preparar un compuesto de fórmula (III), preferentemente de fórmula (III’), más preferentemente de fórmula (IIIa).
Además, la presente invención también hace referencia al uso de compuestos de fórmula (1) preparados por medio de un procedimiento que comprende al menos los pasos 1 y 2 como se describe en los párrafos [0006] a [0030] para preparar un compuesto de fórmula preferentemente de fórmula (III’’’), más preferentemente de fórmula (IIIb).
Además, la presente invención también hace referencia al uso de compuestos de fórmula (1) preparados por medio de un procedimiento que comprende al menos los pasos 1 y 2 como se describe en los párrafos [0006] a [0030] para preparar un compuesto de fórmula (IV), preferentemente de fórmula (IV’).
Resumen de la invención
Un aspecto de la presente invención hace referencia a un procedimiento para la síntesis de 5-fluoro-1H-pirazoles de la fórmula general (I)
haciendo reaccionar una olefina de la fórmula general (a)
con nucleófilos, y opcionalmente una base,
y seguido de reacción con hidrazinas de fórmula (b)
R1-NH-NH2 (b),
en la que
R1 se selecciona entre alquilo C1-C6 , cicloalquilo, arilo C5-C10;
R2 es un resto trihalometilo con al menos un átomo de flúor; y
R3 se selecciona entre haloalquilo C1-C5 como por ejemplo CF3 , CF2Cl, C2F5, C3F7, CF2CF2Cl, CFClCF3, y el nucleófilo se selecciona de alcoholes, tioles o aminas secundarias, y en caso de que el nucleófilo sea un alcohol o un tiol, también en presencia de una base.
Una forma de realización preferida hace referencia a un procedimiento de acuerdo con el párrafo 0, en la que R1 es metilo
R2 es CF3
R3 es C2F5 ,
Una forma de realización preferida hace referencia a un procedimiento de acuerdo con cualquiera de los párrafos 0 a 00, en la que el nucleófilo es metanol y la base es trietilamina.
También se describe en el presente documento un procedimiento para la preparación de un compuesto de fórmula (IV)
en la cual
R1 es alquilo C1-C4; y
A 1 es C-R2; y
R2 es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo C1-C6 opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o N-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo); preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2 , metilo, etilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, n-propoxi, 1-metiletoxi, fluorometoxi, difluorometoxi, clorodifluorometoxi, diclorofluorometoxi, trifluorometoxi, 2,2,2-trifluoroetoxi, 2-cloro-2,2-difluoroetoxi, pentafluoroetoxi, metilsulfonilo, metilsulfinilo, trifluorometilsulfonilo, trifluorometilsulfinilo o N-ciclopropilaminocarbonilo, más preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2 , metilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, o pentafluoroetoxi, preferentemente hidrógeno, flúor, cloro, bromo, con preferencia máxima cloro; y
A2 es C-R3 o nitrógeno; y
R3 es hidrógeno, metilo, flúor o cloro, preferentemente hidrógeno; y
T representa uno de los grupos T1-T9 provistos a continuación, en la que el enlace al grupo pirazol principal se marca con un asterisco *,
o *-C(=O)-NH-T9 y
R6 en forma independiente en cada caso representa halógeno, ciano, nitro, amino o alquilo Ci -C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6, alquilsulfonilo C1-C6, y n representa los valores 0-2, preferentemente 0, con la condición de que n es 0 o 1 en T5, T6 y T8 y con la condición de que n es 0 en T7; y
Q es hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo C1-C6 , alquenilo C3-C6 , alquinilo C3-C6 , cicloalquilo C3-C9 , heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C1-C6 , aril C6-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3, aminoalquilo C1-C4, aminocarbonil-alquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4, los cuales están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco, preferentemente con uno o dos, más preferentemente con un sustituyente seleccionado en forma independiente entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3 , ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoilo C1-C4, cicloalquilcarbamoilo C4-C6 y opcionalmente en forma independiente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoilo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2; preferentemente Q es cicloalquilo C3-C6, o cicloalquilo C3-C6 el cual está sustituido con al menos un sustituyente seleccionado entre el grupo que consiste en cloro, flúor, bromo, yodo, ciano y hidroxi, o aril C6-alquilo C1-C3; más preferentemente ciclopropilo, 1-ciano-ciclopropilo o bencilo (-CH2-C6H5);
que comprende los pasos de acuerdo con cualquiera de la reivindicaciones 1 a 4.
Un caso hace referencia a un procedimiento de acuerdo con el párrafo 0, en la que el compuesto de fórmula (IV) es un compuesto de fórmula (II), preferentemente de fórmula (II’).
Una forma de realización preferida hace referencia a un procedimiento de acuerdo con el párrafo 0 o el párrafo 0, en la que el compuesto de fórmula (IV) es el compuesto (IIa).
Un caso hace referencia a un procedimiento de acuerdo con cualquiera de los párrafos 0 a 0, que además comprende los pasos de:
- hacer reaccionar un compuesto (I) con un donante de ciano para preparar el intermedio de fórmula (6)
en la que R1 es alquilo (C1-C4); y
- hacer reaccionar un compuesto (6) con una base inorgánica fuerte en un primer paso de hidrólisis y después añadir un ácido inorgánico en un segundo paso de hidrólisis para preparar el intermedio de fórmula (7)
C 2F5 C F„
N
'
n
'
. .
N W / C O O H
R 1
(7),
en la que
R1 es alquilo (C1-C4); y
- hacer reaccionar un compuesto de fórmula (8) o su sal (8') con una forma activada (7') del compuesto (7)
en la que
R1 es alquilo C1-C4 y
A 1 es C-R2*; y
R2* es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo Ci -Ca opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o N-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo);
A2 es C-R3* o nitrógeno; y
R3* es hidrógeno, metilo, flúor o cloro;
Qes hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo Ci -Ca , alquenilo C3-Ca , alquinilo C3-Ca , cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo Ci -Ca, aril Ca-alquilo C1-C3, heteroaril C5-Ca-alquilo C1-C3, aminoalquilo C1-C4, aminocarbonilalquilo C1-C4 o alquil Ci -C4-amino-alquilo C1-C4, los cuales están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco, preferentemente con uno o dos, más preferentemente con un sustituyente seleccionado en forma independiente entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3, ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoilo C1-C4, cicloalquilcarbamoilo C4-Ca y opcionalmente en forma independiente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoilo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2 y
LG es un grupo saliente,
para preparar un compuesto de fórmula (II).
También se describe en el presente documento un procedimiento de acuerdo con el párrafo [0119], en el que el compuesto de fórmula (IV) es un compuesto de fórmula (III)
( iii)
en la cual
R1 es alquilo (C1-C4); y
A 1 es C-R2;
R2 es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo C1-C6 opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o N-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo); preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2, metilo, etilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, n-propoxi, 1-metiletoxi, fluorometoxi, difluorometoxi, clorodifluorometoxi, diclorofluorometoxi, trifluorometoxi, 2,2,2-trifluoroetoxi, 2-cloro-2,2-difluoroetoxi, pentafluoroetoxi, metilsulfonilo, metilsulfinilo, trifluorometilsulfonilo, trifluorometilsulfinilo o N-ciclopropilaminocarbonilo, más preferentemente hidrógeno, flúor, cloro, bromo, CN, NO2, metilo, fluorometilo, difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, metoxi, etoxi, o pentafluoroetoxi, preferentemente hidrógeno, flúor, cloro, bromo, con preferencia máxima cloro; y
A2 es C-R3 o nitrógeno;
R3 es hidrógeno, metilo, flúor o cloro, preferentemente hidrógeno; y
Q es hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C1-Ca , aril C6-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3, aminoalquilo C1-C4, aminocarbonil-alquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4, los cuales están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco, preferentemente con uno o dos, más preferentemente con un sustituyente seleccionado en forma independiente entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3, ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoilo C1-C4, cicloalquilcarbamoilo C4-Ca y opcionalmente en forma independiente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoilo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2; preferentemente Q es cicloalquilo C3-Ca, o cicloalquilo C3-Ca el cual está sustituido con al menos un sustituyente seleccionado entre el grupo que consiste en cloro, flúor, bromo, yodo, ciano y hidroxi, o aril Ca-alquilo C1-C3; más preferentemente ciclopropilo, 1-ciano-ciclopropilo o bencilo (-CH2-CaH5);
T representa uno de los anillos heteroaromáticos de 5 miembros T1-T8 provistos a continuación, en la que el enlace al grupo pirazol principal se marca con un asterisco *,
T7 T8
en las que
R6 en forma independiente en cada caso representa halógeno, ciano, nitro, amino o alquilo C1-C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6, alquilsulfonilo C1-C6, y n representa los valores 0-2, preferentemente 0, con la condición de que n es 0 o 1 en T5, T6 y T8 y con la condición de que n es 0 en T7.
También se describe en el presente documento un procedimiento de acuerdo con el párrafo 0, en el que el compuesto de fórmula (III) es el compuesto de fórmula (III'), más preferentemente el compuesto (IIIa) o el compuesto (IIIb). Una forma de realización preferida hace referencia a un procedimiento de acuerdo con uno cualquiera de los párrafos [0123] o [0124], que además comprende los pasos de
hacer reaccionar un compuesto de fórmula (I) con un intermedio de fórmula (11) por sustitución nucleofílica del anillo en la posición del fluoruro del compuesto de fórmula (I) (mencionado en la presente como Paso 9)
(I) (12)
en la que
R1 es alquilo (C1-C4) opcionalmente halogenado o ciclopropilo opcionalmente halogenado; y
U representa bromo, yodo, triflato, ácido borónico, éster borónico o trifluoroboronato; y los ciclos de cinco miembros de E1-E3, carbono y nitrógeno representan los heterociclos de 5 miembros seleccionados entre el grupo que consiste en
T5 T6 T7 T8
en las que
R6 en forma independiente en cada caso representa halógeno, ciano, nitro, amino o alquilo C1-C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6, alquilsulfonilo C1-C6, y
n representa los valores 0-2, preferentemente 0, con la condición de que n es 0 o 1 en T5, T6 y T8 y con la condición de que n es 0 en T7;
para preparar un intermedio de fórmula (12); y
- hacer reaccionar un compuesto de fórmula (12) y un compuesto de fórmula (13) (mencionado en la presente como Paso 10)
en las que
R1 es alquilo (C1-C4); y
A i es C-R2*; y
A2 es C-R3* o nitrógeno; y
R3* es hidrógeno. metilo. flúor o cloro;
Q es hidrógeno, ciano, hidroxi, formu lo o uno de los grupos alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C1-C6, aril C6-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3, aminoalquilo C1-C4, alquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4, los cuales están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco, preferentemente con uno o dos, más preferentemente con un sustituyente seleccionado en forma independiente entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3, ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoilo C1-C4, cicloalquilcarbamoilo C4-C6 y opcionalmente en forma independiente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoilo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2 y
U representa bromo, yodo, triflato, ácido borónico, éster borónico o trifluoroboronato; y los ciclos de cinco miembros de E1-E3, carbono y nitrógeno representan los heterociclos de 5 miembros seleccionados entre el grupo que consiste en
T5 T6 T7 T8
en las que
R6 en forma independiente en cada caso representa halógeno, ciano, nitro, amino o alquilo C1-C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6, alquilsulfonilo C1-C6, y
n representa los valores 0-2, preferentemente 0, con la condición de que n es 0 o 1 en T5, T6 y T8 y con la condición de que n es 0 en T7; y
M representa bromo, yodo o triflato cuando U representa un ácido borónico, éster borónico o trifluoroboronato; o
M representa un ácido borónico, éster borónico o trifluoroboronato cuando U representa bromo, yodo o triflato
para preparar un compuesto de fórmula (III).
Una forma de realización preferida hace referencia a un procedimiento de acuerdo con el párrafo 0, en la que el compuesto de fórmula (IV) es un compuesto de fórmula (III''), preferentemente de fórmula (III'” ).
Una forma de realización preferida se refiere a un proceso de acuerdo con el párrafo [0126] - [0118] que comprende además los pasos de
- hacer reaccionar un compuesto de fórmula (I) y un donante de azida para preparar el intermedio (14)
en la que R1 es como se define para un compuesto de fórmula (III); y
- hacer reaccionar el intermedio (14) con un intermedio de fórmula (15) para dar un intermedio (III”*) (mencionado en la presente como Paso 12)
en las que R1, R6, A1, y A2 son como se definen para el compuesto (III), n es 0 o 1 y PG es cualquier grupo protector del grupo carboxílico como por ejemplo alquilo C1-C6 (por ejemplo, metilo).
Procedimiento de acuerdo con uno cualquiera de los párrafos[0116] a [0127], en los que R1 es metilo.
Ejemplo 1 N-Metil-3-pentafluoroetil-4-trifluorometil-5-fluoro-1H-pirazol
En un recipiente de 3 bocas de 2 l equipado con condensador, termómetro, y un embudo de goteo se colocaron 1300 ml de cloruro de metileno y perfluoro-2-metil-2-penteno (197 g, 0,65 mol), y después se añadieron 25 g de metanol. La mezcla se enfrió a -0 °C y se añadió Et3N (164 g, 1,62 mol) a una temperatura de entre -5° y 5 °C. La mezcla se agitó a esta temperatura durante 15 min y se añadió lentamente a esta mezcla una solución de 100 ml de N-metilhidrazina en agua (40 % p.p. ) a 5 °C dentro de un período de 2 h. La mezcla de reacción se agitó durante 15 20 h a 20 °C. La mezcla se lavó con agua, la fase orgánica se secó sobre Na2SÜ4 y el disolvente se separó por destilación a presión atmosférica. El producto en bruto se purificó mediante destilación al vacío. El rendimiento de N-Metil-3-pentafluoroetil-4-trifluorometil-5-fluoro-1H-pirazol fue de 140 g (80 % de rendimiento). Punto de ebullición 62-67 °C a 1,5-2,0KPa.
RMN 19F 5; 53,7 (3F), 83,9 (3F), 112,1 (2F), 125,1 (1F) ppm.
Ejemplo 2 N-Metil-3-pentafluoroetil-4-trifluorometil-5-fluoro-1H-pirazol
En un recipiente de 3 bocas de 2 l equipado con condensador, termómetro, y un embudo de goteo se colocaron 1300 ml de cloruro de metileno y perfluoro-2-metil-2-penteno (197 g, 0,65 mol), y después se añadieron 46 g de etanol. La mezcla se enfrió a -0 °C y se añadió Et3N (164 g, 1,62 mol) a una temperatura de entre -5° y 5 °C. La mezcla se agitó a esta temperatura durante 15 min y se añadió lentamente a esta mezcla una solución de 100 ml N-metilhidrazina en agua (40 % p.p. ) a 5 °C dentro de un período de 2 h. La mezcla de reacción se agitó durante 15-20 ha 20 °C. La mezcla se lavó con agua, la fase orgánica se secó sobre Na2SÜ4 y el disolvente se separó por destilación a presión atmosférica. El producto en bruto se purificó mediante destilación al vacío. El rendimiento de N-Metil-3-pentafluoroetil-4-trifluorometil-5-fluoro-1H-pirazol fue de 139 g (75% de rendimiento). Punto de ebullición 62 67 °C a 1,5-2,0 kPa.
Ejemplo 3 N-Metil-3-pentafluoroetil-4-trifluorometil-5-fluoro-1H-pirazol
En un recipiente de 3 bocas de 2 l equipado con condensador, termómetro, y un embudo de goteo se colocaron 1300 ml de cloruro de metileno y perfluoro-2-metil-2-penteno (197 g, 0,65 mol), y después se añadieron 48 g de dietilamina. La mezcla se enfrió a -0 °C y se añadió Et3N (164 g, 1,62 mol) a una temperatura de entre -5° y 5 °C. La
mezcla se agitó a esta temperatura durante 15 min y se añadió lentamente a esta mezcla una solución de 100 ml de N-metilhidrazina en agua (40 % p.p. ) a 5 °C dentro de un período de 2 h. La mezcla de reacción se agitó durante 15 20 h a 20 °C. La mezcla se lavó con agua, la fase orgánica se secó sobre Na2SO4 y el disolvente se separó por destilación a presión atmosférica. El producto en bruto se purificó mediante destilación al vacío. El rendimiento de N-Metil-3-pentafluoroetil-4-trifluorometil-5-fluoro-1H-pirazol fue de 145 g (78 % de rendimiento). Punto de ebullición 62-67 °C a 1,5-2,0 kPa.
Ejemplo 4 N- Etil-3-pentafluoroetil-4-trifluorometil-5-fluoro-1H-pirazol
Se obtuvo a partir de perfluoro-2-metil-2-penteno y N-etilhidrazina de acuerdo con el ejemplo 2.
Rendimiento 83 %, punto de ebullición 70 °C a 1,8-2,0 kPa.
Ejemplo 5 (Paso 3)
Preparación de 5-Ciano-1-metil-3-pentafluoroetil-4-trifluorometil-1H-pirazol (intermedio (6a))
(6 a)
Se suspendieron 28,6 g (0,1 mol) de 5-fluoro-1-metil-3-pentafluoroetil-4-trifluorometilpirazol (compuesto (Ia)) y 9,7 g (0,15 mol) de cianuro de potasio en 150 ml de acetonitrilo y después se calentó a reflujo durante 5 h en una atmósfera de gas protectora. Después de enfriar, el precipitado (KCN, KF) se retiró por filtración, y el disolvente se retiró al vacío (30,0 kPa) para dar un aceite pardo (27,8 g, 95 % ) que se usó para el paso siguiente sin purificación alguna.
RMN 1H (400 MHz, ds-acetonitrilo): 5 = 4,11 (s, 3H, CH3) ppm
RMN 19F (400 MHz, CDCh): 5 = -56,7 (3F), -111,4 (3F), -111,6 (2F) ppm.
CG-EM: Tiempo de retención 2,67 min; masa (m/z): 224 (M)+.
Ejemplo 6 (Paso 4)
Preparación de ácido 1-Metil-3-pentafluoroetil-4-trifluorometil-1tf-pirazol-5-carboxílico (intermedio (7a))
Se calentaron 29,3 g (0,1 M) de 5-ciano-1-metil-3-pentafluoroetil-4-trifluorometilpirazol (compuesto (6a)) y 110 g de NaOH 10 % en un baño de aceite a 100 °C durante 6 h hasta que se formó una solución transparente. Después de enfriar a 5 °C, la mezcla de reacción se acidificó lentamente hasta pH 1 mediante la adición de HCl al 37 % para dar cristales blancos que se retiraron por filtración, se lavó con 40 ml agua fría y se secó para dar 28 g (7a) de ácido 1-metil-3-pentafluoroetil-4-trifluorometilpirazol-5- carboxílico) como un sólido blanco con p.f.120-122 °C.
RMN 1H (400 MHz, d3-acetonitrilo) 5 = 4,08 (s, 3H, CH3) ppm;
HPCL-EM a): logP = 1,86; masa (m/z): 313,0 (M+H)+.
Ejemplo 7 (Paso 7)
Preparación de 4-bromo-2'-metil-5'-(pentafluoroetil)-4'-(trifluorometil)-2'H-1,3'-bipirazol (intermedio (12)) Se suspendieron 2,00 g (6,99 mmol) de 5-fluoro-1-metil-3-(pentafluoroetil)-4-(trifluorometil)-1H-pirazol (compuesto (Ia)), 1,03 g (6,99 mmol) de 4-bromo-1H-pirazol (compuesto de fórmula (11)) y 1,93 g de carbonato de potasio en 50 ml de tetrahidrofurano p.a. La mezcla de reacción se calentó a reflujo durante 16 h. La mezcla de reacción enfriada se filtró y el disolvente se eliminó bajo presión reducida. El residuo se purificó mediante cromatografía de columna sobre gel de sílice.
Esto dio 0,69 g de 4-bromo-2'-metil-5'-(pentafluoroetil)-4'-(trifluorometil)-2'H-1,3'-bipirazol como un sólido incoloro. RMN 1H (400 MHz, d3-acetonitrilo): 5 = 8,00 (s, 1H), 7,91 (s, 1H), 3,71 (s, 3H).
HPCL-EMa): logP = 4,14, masa (m/z) = 413 [M+H]+.
Ejemplo 8 (Paso 8)
Preparación de 2-Cloro-N-1-ciano-ciclopropil-5-[2'-metN-5'-(pentafluoroetN)-4'-(trifluorometN)-2'H-1,3'-bipirazol-4-il]benzamida (compuesto (IIIa))
Se mezclaron 150 mg (0,36 mmol) 4-bromo-2'-metil-5'-(pentafluoroetil)-4'-(trifluorometil)-2'H-1,3'-bipirazol, 126 mg (0,36 mmol) 2-cloro-N-(1-c¡anoc¡cloprop¡l)-5-(4,4,5,5-tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)benzam¡da, 21 mg (0,01 mmol) tetrakis(trifenilfosfin)paladio y 1,1 ml de b¡carbonato de sod¡o acuoso 1M con 10,5 ml de ¡sopropanol y se calentó a reflujo durante 3 h. El d¡solvente se el¡m¡nó bajo pres¡ón reduc¡da y el res¡duo se d¡solv¡ó en acetato de et¡lo. La fase orgán¡ca se lavó dos veces con agua, se secó sobre Na2SO4, y se filtró. El d¡solvente se el¡m¡nó bajo pres¡ón reduc¡da. El res¡duo se purificó por med¡o de cromatografía de columna sobre gel de síl¡ce, para dar 98 mg de 2-cloro-N-(1-danoddoprop¡l)-5-[2'-mefil-5'-(pentafluoroefil)-4'-(trifluoromet¡l)-2'H-1,3'-b¡p¡razol-4-¡l]benzam¡da como un sól¡do ¡ncoloro.
RMN 1H (400 MHz, ds-Aceton¡tr¡lo): 5 = RMN 1H (400 MHz, d3-Aceton¡tr¡lo): 5 = 8,27 (s, 1H), 8,25 (s, 1H), 7,75 (d, 1H), 7,70 (dd, 1H), 7,62 (s, 1H), 7,51 (d, 1H), 3,75 (s, 3H), 1,56-1,60 (m, 2H), 1,33-1,36 (m, 2H).
HPCL-EMa): logP = 3,72, Masa (m/z) = 553,1 [M+H]+.
Ejemplo 9 (Paso 9)
Preparación de 5-Azido-1-metil-3-pentafluoroetil-4-trifluorometil-lH-pirazol (intermedio (14), R1 = metilo) Se añad¡ó 5-Fluoro-l-met¡l-3-pentafluoroet¡l-4-tr¡fluoromet¡l-lH-p¡razol (que se preparó de acuerdo con los pasos 1 to 4; 7 mmol) a una mezcla de d¡met¡lsulfóx¡do (DMSO) (10 ml). Después se añad¡ó az¡da de sod¡o (0,5 g; 7,7 mmol) a la mezcla, que se mantuvo a temperatura amb¡ente. La mezcla se ag¡tó durante la noche a temperatura amb¡ente. Después de haberse completado la reacc¡ón, se añad¡ó una mezcla de agua (100 ml) y d¡et¡léter (100 ml). Las fases se separaron y la fase acuosa se extrajo dos veces con d¡et¡léter. Este compuesto se ut¡l¡zó s¡n pur¡f¡cac¡ón ad¡c¡onal.
Ejemplo 10 (Paso 10)
Preparación de metiléster del ácido 2-Cloro-5-[l-(2- metM-5-pentafluoroetil-4-trifluorometM-2H-pirazol-3-M)-lH-[1.2.3] triazol-4-il]- benzoico (véase intermedio (MI’’*))
Se suspend¡ó met¡léster del ác¡do 2-Cloro-5-et¡n¡l-benzo¡co (1,13g, 5,8 mmol) y 5- Az¡do-l-met¡l-3-pentafluoroet¡l-4-tr¡fluoromet¡l-lH-p¡razol (1,80 g, 5,8 mmol) en una mezcla de agua y t-BuOH (30 ml). Se añad¡ó a la mezcla ascorbato de sod¡o (0,600 ml sol. 1M en agua, rec¡én preparado) segu¡do por sulfato de cobre (II) pentah¡drato (0,015 g). La mezcla heterogénea resultante se ag¡tó enérg¡camente durante 96 horas. La mezcla de reacc¡ón se d¡luyó con agua y el producto se extrajo con acetato de et¡lo. La fase orgán¡ca se lavó con salmuera, se secó sobre sulfato de magnes¡o y se evaporó. El res¡duo se somet¡ó a cromatografía de columna sobre gel de síl¡ce (c-HEX/EtOAc=3 : l) para dar el producto deseado met¡léster del ác¡do 2-Cloro-5-[l-(2- met¡l-5-pentafluoroet¡l-4-tr¡fluoromet¡l-2H-p¡razol-3-¡l)-lH-[1.2.3] tr¡azol-4-¡l]- benzo¡co (rend¡m¡ento 53 %).
RMN 1H (400 MHz, CDCls): 5 = 8,47(s, 1H), 8,12 (Es, 1H), 8,0 (d, 1H), 7,62 (d, 1H), 3,98 (s, 3H), 3,87 (s, 3H) ppm. CL-EM Tr 2,12, 504 (M+H+), 545 (M+CH3CN+H+)
Ejemplo 11 (Paso 11)
Preparación de ácido 2-Cloro-5-[l-(2-metil-5-pentafluoroetil-4-trifluorometil-2H- pirazol-3-il)-lH-[L2,3]triazol-4-il]-benzoico (véase compuesto de fórmula (III’’’’))
Se suspendió metilésterdel ácido 2-Cloro-5-[l-(2-metil-5-pentafluoroetil-4-trifluorometil-2H-pirazol-3-il)-lH- [l,2,3]triazol-4-il]-benzoico (1,53g, 3,0 mmol) en una mezcla de agua y se añadió tetrahidrofurano (1:3, 50 ml) e hidróxido de litio (0,22 g, 9,1 mmol). La mezcla resultante se agitó enérgicamente durante 5 horas a 60 °C. La mezcla de reacción se diluyó con agua y se acidificó con cloruro de hidrógeno (2N). La fase acuosa se extrajo dos veces con AcOEt, se secó sobre MgS04 y se concentró bajo vacío para dar el producto deseado ácido 2-Cloro-5-[l-(2-metil-5- pentafluoroetil-4-trifluorometil-2H-pirazol-3-il)-lH-[l,2,3]triazol-4-il]-benzoico. Este compuesto se usó sin purificación adicional.
RMN 1H (400 MHz, CDCls): 5 = 8,52(s, 1H), 8,18 (Es, 1H), 8,09 (d, 1H), 7,66 (d, 1H), 3,88 (s, 3H) ppm.
CL-EM Tr 2,08, 488 (M+H+).
Ejemplo 12 (Paso 6)
Preparación de N-[4-cloro-3-(bencNcarbamoN)feml]-1-metN-3-(pentafluoroetN)-4-(trifluorometN)-1H-pirazol-5-carboxamida (compuesto (IIa))
Se suspendieron 560 mg (1,79 mmol) de ácido 1-metil-3-pentafluoroetil-4-trifluorometilpirazol-5-carboxílico en 10 ml de diclorometano. La suspensión se enfrió a 0 °C y después se mezcló con 0,02 ml de N,N-dimetilformamida y 188 pl (2,15 mmol;1,2eq) de cloruro de oxalilo. La mezcla de reacción se agitó en primer lugar durante 0,5 h a 0 °Cy después durante 3 horas a temperatura ambiente. El disolvente se eliminó bajo presión reducida en un evaporador rotativo. El cloruro de 1-metil-3-(pentafluoroetil)-4-(trifluorometil)-1H-pirazol-5-carbonilo se usó para el paso de síntesis subsiguiente sin tratamiento ulterior.
Se disolvieron 88,7 mg (0,34 mmol) de 5-amino-N-bencil-2-clorobenzamida y 2,77 mg (0,02 mmol) de N,N-dimetilpiridin-4-amina (DMPA) en 2,5 ml de acetato de etilo. La solución se enfrió a 0 °C usando un baño de hielo y se mezcló con 119 pl (0,68 mmol) de N-etildiisopropilamina. Se suspendieron 75,0 mg (0,22 mmol) de cloruro de 1-metil-3-(pentafluoroetil)-4-(trifluorometil)-1H-pirazol-5-carbonilo en 2,5 ml de acetato de etilo y después se añadió a la solución de reacción enfriada. La mezcla de reacción se calentó durante cuatro horas a 50 °C y después se agitó durante 16 horas a temperatura ambiente. La solución de la reacción se diluyó con 10,0 ml de acetato de etilo. La fase orgánica se lavó tres veces con ácido clorhídrico 1M, dos veces con solución de hidróxido de sodio 1M y una vez con solución saturada de cloruro de sodio. La fase orgánica se secó sobre sulfato de sodio y se filtró y el disolvente se eliminó bajo presión reducida en un evaporador rotativo. Esto dio 140 mg (0,17 mmol) de N-[4-cloro-3-(bencilcarbamoil)fenil]-1-metil-3-(pentafluoroetil)-4-(trifluorometil)-1H-pirazol-5-carboxamida (97%) como un sólido blanco.
RMN 1H (400 MHz, ds-acetonitrilo): 5 = 9,29 (bs, 1H), 7,78 (d, 1H), 7,67 (dd, 1H), 7,48 (d, 1H), 7,21-7,52 (m, 6H), 4,54 (d, 2H), 3,97 (s, 3H) ppm.
1La masa indicada es el pico del patrón de isótopo del ión [M+H]+ ion con la máxima intensidad.
HPCL-EMa): logP = 3,90 masa (m/z) = 555,1 [M+H]+.
a) Nota referida a la determinación de los valores de logP y la detección de masa: Los valores de logP dados aquí se determinaron de acuerdo la Directiva EEC 79/831 Anexo V.A8 mediante HPLC (Cromatografía líquida de alto
rendimiento) en una columna en fase reversa C18. Sistema Agilent 1100 LC; 50*4,6 Zorbax Eclipse Plus C18 1,8 micrones; eluyente A: acetonitrilo (ácido fórmico 0,1 %); eluyente B: agua (ácido fórmico 0,09%); gradiente lineal desde acetonitrilo al 10 % hasta 95 % en 4,25 min, luego acetonitrilo 95 % durante otros 1,25 min; temperatura de la estufa 55 °C; flujo: 2,0 ml/min. La detección de masa se llevó a cabo mediante un sistema Agilent MSD.
Claims (9)
1. Un procedimiento para la síntesis de 5-fluoro-1H-pirazoles de la fórmula general (I)
haciendo reaccionar una olefina de la fórmula general (a)
con nucleófilos, y opcionalmente una base,
seguido de reacción con hidrazinas de fórmula (b)
R1-NH-NH2 (b),
en la que
R1 se selecciona entre alquilo C1-C6, cicloalquilo, arilo C5-C10;
R2 es un resto trihalometilo con al menos un átomo de flúor; y
R3 se selecciona entre haloalquilo C1-C5 como por ejemplo CF3 , CF2Cl, C2F5, C3 F7, CF2CF2Cl, CFClCF3, y el nucleófilo se selecciona entre alcoholes, tioles o aminas secundarias, y cuando el nucleófilo es un alcohol o un tiol, también en presencia de una base.
2. Procedimiento de acuerdo con la reivindicación 1, en la que
R1 es metilo
R2 es CF3
R3 es C2F5.
3. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 1 o 2, en las que el nucleófilo es metanol y la base es trietilamina.
4. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 1 a 3, que además comprende los pasos de: - hacer reaccionar un compuesto (I) con un donante de ciano para preparar el intermedio de fórmula (6 )
(6),
en la que R1 es alquilo (C1-C4); y
- hacer reaccionar un compuesto (6 ) con una base inorgánica fuerte en un primer paso de hidrólisis y después añadir un ácido inorgánico en un segundo paso de hidrólisis para preparar el intermedio de fórmula (7)
C 2F5 C F 3
N
'
n
'
. .
N W / C O O H
R '
(7),
en la que
R1 es alquilo (C1-C4); y
en la que
R1 es alquilo C1-C4; y
A i es C-R2*; y
R2* es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo C1-C6 opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o A/-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo);
A2 es C-R3* o nitrógeno; y
R3* es hidrógeno, metilo, flúor o cloro;
Q es hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C1-C6, aril C6-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3, aminoalquilo C1-C4, aminocarbonil-alquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4 que están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco sustituyentes independientemente seleccionado entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3, ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoílo C1-C4, cicloalquilcarbamoílo C4-C6 y de manera opcional, independientemente con uno, dos o tres sustituyentes seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoílo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2; y
LG es cualquier grupo saliente,
para preparar un compuesto de fórmula (II).
5. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 1 a 3, que además comprende los pasos de
- hacer reaccionar un compuesto de fórmula (I) con un intermedio de fórmula (11) mediante sustitución nucleófila del fluoruro en la posición del anillo de un compuesto de fórmula (I) (en el presente documento denominado Paso 9)
en la que
R1 es alquilo (Ci-C4) opcionalmente halogenado o ciclopropilo opcionalmente halogenado; y
U represents bromo, yodo, triflate, ácido borónico, éster borónico o trifluoroboronato; y los ciclos de cinco miembros de E1-E3, carbono y nitrógeno representan los heterociclos de 5 miembros seleccionados del grupo que consiste en
en las que
R6 independientemente entre sí representa halógeno, ciano, nitro, amino o alquilo C1-C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6, alquilsulfonilo C1-C6, y
n representa los valores 0-2, preferentemente 0, siempre que n sea 0 o 1 en T5, T6 y T8 y siempre que n sea 0 en T7;
para preparer un intermedio de formula (12); y
- hacer reaccionar un compuesto de fórmula (12) y un compuesto de fórmula (13) (en el presente documento denominado Paso 10)
en las que
R1 es alquilo (C1-C4); y
A 1 es C-R2*;
R2* es hidrógeno, flúor, cloro, bromo, CN, NO2, alquilo C1-C6 opcionalmente halogenado, alcoxi C1-C4 opcionalmente halogenado, alquilsulfonilo C1-C4 opcionalmente halogenado, alquilsulfinilo C1-C4 opcionalmente halogenado o N-ciclopropilaminocarbonilo (-C(=O)-NH-ciclopropilo; y
A2 es C-R3* o nitrógeno;
R3* es hidrógeno, metilo, flúor o cloro
Q es hidrógeno, ciano, hidroxi, formilo o uno de los grupos alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C9, heterocicloalquilo C3-C9, alcoxi C1-C4, alquilcicloalquilo C4-C15, cicloalquilalquilo C4-C15, hidroxialquilo C1-C6, aril C6-alquilo C1-C3, heteroaril C5-C6-alquilo C1-C3 , aminoalquilo C1-C4, aminocarbonilalquilo C1-C4 o alquil C1-C4-amino-alquilo C1-C4 que están opcionalmente sustituidos con uno, dos, tres, cuatro o cinco sustituyentes independientemente seleccionados entre el grupo que consiste en hidroxi, nitro, amino, halógeno, alcoxi C1-C3, ciano, hidroxicarbonilo, alcoxicarbonilo C1-C4, alquilcarbamoílo C1-C4, cicloalquilcarbamoílo C4-C6 y de manera opcional, independientemente con uno, dos o tres sustituyentes
seleccionados entre el grupo que consiste en halógeno, ciano, nitro, hidroxicarbonilo, alquilcarbamoílo C1-C2, alquilo C1-C2, alquilo C1-C2 halogenado y fenilo sustituido con alcoxi C1-C2; y
U represents bromo, yodo, triflato, ácido borónico, éster borónico o trifluoroboronate; y
los ciclos de cinco miembros de E1-E3, carbono y nitrógeno representan los heterociclos de 5 miembros seleccionados del grupo que consiste en
en las que
R6 independientemente entre sí representa halógeno, ciano, nitro, amino o alquilo C1-C6 opcionalmente sustituido, alquiloxi C1-C6, alquilcarbonilo C1-C6, alquilsulfanilo C1-C6, alquilsulfinilo C1-C6, alquilsulfonilo C1-C6, y
n n representa los valores 0-2, preferentemente 0, siempre que n sea 0 o 1 en T5, T6 y T8 y siempre que n sea 0 en T7; y
M representa bromo, yodo o triflato cuando U representa un ácido borónico, éster borónico o trifluoroboronato; o
M representa un ácido borónico, éster borónico o trifluoroboronato cuando U representa bromo, yodo o triflato para preparar un compuesto de formula (III).
7. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 1 a 3 que además comprende los pasos de - hacer reaccionar un compuesto de fórmula (I) y un donante de azida para preparar el intermedio (14)
en la que R1 es como se define para un compuesto de formula (III); y
- hacer reaccionar el intermedio (14) con un intermedio de fórmula (15) para dar un intermedio (III”*) (en el presente documento denominado Paso 12)
en las que R1, R6, Ai y A2 son como se definen para el compuesto (NI), n es 0 o 1 y PG es cualquier grupo protector del grupo carboxílico, tal como alquilo C1-C6 (por ejemplo, metilo).
8. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 4, 5, 6 y 7 en las que
R2* es cloro; y
R3* es hidrógeno.
9. Procedimiento de acuerdo con una cualquiera de las reivindicaciones precedentes, en las que R1 es metilo.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP13194560 | 2013-11-27 | ||
| PCT/EP2014/075491 WO2015078847A1 (en) | 2013-11-27 | 2014-11-25 | Process for the preparation of 5-fluoro-1h-pyrazoles |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2861507T3 true ES2861507T3 (es) | 2021-10-06 |
Family
ID=49674199
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14802882T Active ES2861507T3 (es) | 2013-11-27 | 2014-11-25 | Procedimiento para la preparación de 5-fluoro-1H-pirazoles |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US9845312B2 (es) |
| EP (1) | EP3083565B1 (es) |
| JP (1) | JP6613234B2 (es) |
| KR (1) | KR102367289B1 (es) |
| CN (1) | CN105934428B (es) |
| BR (1) | BR112016011899B1 (es) |
| ES (1) | ES2861507T3 (es) |
| IL (1) | IL245476B (es) |
| MX (1) | MX386134B (es) |
| TW (1) | TWI678362B (es) |
| WO (1) | WO2015078847A1 (es) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI2885277T1 (sl) * | 2012-07-19 | 2016-12-30 | Bayer Cropscience Ag | Postopek priprave 5-fluoro-1H-pirazolov |
| CN114698369A (zh) | 2019-08-14 | 2022-07-01 | 威隆股份公司 | 用于防治寄生虫的包含替戈拉纳的组合物 |
| EP4059927A4 (en) * | 2019-11-14 | 2023-10-04 | Unimatec Co., Ltd. | FLUORINE-CONTAINING PYRAZOLE COMPOUND AND PRODUCTION PROCESS THEREOF |
| JP7797419B2 (ja) | 2020-05-27 | 2026-01-13 | ヴェトキノール サ | 2-クロロ-n-(1-シアノシクロプロピル)-5-[2’-メチル-5’-(ペンタフルオロエチル)-4’-(トリフルオロメチル)-2’h-1,3’-ビピラゾール-4-イル]ベンズアミドを調製するための方法 |
| KR20230028268A (ko) | 2020-05-29 | 2023-02-28 | 뵈링거 잉겔하임 애니멀 헬스 유에스에이 인코포레이티드 | 구충성 헤테로시클릭 화합물 |
| EP4332092A4 (en) * | 2021-04-27 | 2025-07-16 | Unimatec Co Ltd | FLUORINE-CONTAINING PYRAZOLE COMPOUND AND PROCESS FOR PRODUCTION THEREOF |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1456419A1 (ru) | 1987-06-18 | 1989-02-07 | Институт элементоорганических соединений им.А.Н.Несмеянова | Способ получени 1-замещенных 3-пентафторэтил-4-трифторметил-5-фторпиразолов |
| JP2817863B2 (ja) * | 1992-02-21 | 1998-10-30 | 宇部興産株式会社 | 含フッ素ピラゾール化合物、その製法及び有害生物防除剤 |
| US5254774A (en) | 1992-12-28 | 1993-10-19 | Minnesota Mining And Manufacturing Company | Preparation of hexafluoropropene oligomers |
| ATE430729T1 (de) * | 2003-10-08 | 2009-05-15 | Lilly Co Eli | Pyrrol- und pyrazolderivate als potentiatoren von glutamatrezeptoren |
| GB0403155D0 (en) * | 2004-02-12 | 2004-03-17 | Vernalis Res Ltd | Chemical compounds |
| HUE026011T2 (en) | 2006-03-22 | 2016-05-30 | Hoffmann La Roche | Pyrazoles as 11-beta-HSD-1 |
| EP2184273A1 (de) | 2008-11-05 | 2010-05-12 | Bayer CropScience AG | Halogen-substituierte Verbindungen als Pestizide |
| EP2673270A1 (en) | 2011-02-09 | 2013-12-18 | Syngenta Participations AG | Insecticidal compounds |
| CN105934429B (zh) * | 2013-11-27 | 2022-03-04 | 拜耳动物保健有限责任公司 | 制备5-氟-1h-吡唑的方法 |
-
2014
- 2014-11-25 EP EP14802882.2A patent/EP3083565B1/en active Active
- 2014-11-25 WO PCT/EP2014/075491 patent/WO2015078847A1/en not_active Ceased
- 2014-11-25 MX MX2016006977A patent/MX386134B/es unknown
- 2014-11-25 KR KR1020167016012A patent/KR102367289B1/ko active Active
- 2014-11-25 ES ES14802882T patent/ES2861507T3/es active Active
- 2014-11-25 US US15/037,402 patent/US9845312B2/en active Active
- 2014-11-25 TW TW103140711A patent/TWI678362B/zh active
- 2014-11-25 BR BR112016011899-5A patent/BR112016011899B1/pt active IP Right Grant
- 2014-11-25 CN CN201480074147.3A patent/CN105934428B/zh active Active
- 2014-11-25 JP JP2016534656A patent/JP6613234B2/ja active Active
-
2016
- 2016-05-04 IL IL245476A patent/IL245476B/en active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| US9845312B2 (en) | 2017-12-19 |
| US20160289213A1 (en) | 2016-10-06 |
| CN105934428B (zh) | 2019-07-19 |
| MX386134B (es) | 2025-03-18 |
| BR112016011899B1 (pt) | 2021-03-23 |
| IL245476A0 (en) | 2016-06-30 |
| JP6613234B2 (ja) | 2019-11-27 |
| BR112016011899A2 (pt) | 2017-08-08 |
| IL245476B (en) | 2019-07-31 |
| EP3083565A1 (en) | 2016-10-26 |
| MX2016006977A (es) | 2016-09-07 |
| KR20160091355A (ko) | 2016-08-02 |
| EP3083565B1 (en) | 2020-12-23 |
| TWI678362B (zh) | 2019-12-01 |
| JP2016539945A (ja) | 2016-12-22 |
| WO2015078847A1 (en) | 2015-06-04 |
| KR102367289B1 (ko) | 2022-02-23 |
| TW201609663A (zh) | 2016-03-16 |
| CN105934428A (zh) | 2016-09-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2861507T3 (es) | Procedimiento para la preparación de 5-fluoro-1H-pirazoles | |
| ES2750353T3 (es) | Procedimiento de preparación de 5-fluoro-1H-pirazoles partiendo de hexafluoropropeno | |
| ES2939161T3 (es) | Proceso para la preparación de 5-fluoro-1H-pirazoles | |
| JP7013501B2 (ja) | ヘキサフルオロプロペンから出発する5-フルオロ-1h-ピラゾール類の調製のための方法 | |
| BR112016010413B1 (pt) | processo para preparação de derivados de 3,5-bis(haloalquil)pirazole a partir de a,a-dihaloaminas |