EP0000348B1 - Polyuret polyisocyanates, preparation thereof and their use in the preparation of polyurethanes. - Google Patents
Polyuret polyisocyanates, preparation thereof and their use in the preparation of polyurethanes. Download PDFInfo
- Publication number
- EP0000348B1 EP0000348B1 EP78100256A EP78100256A EP0000348B1 EP 0000348 B1 EP0000348 B1 EP 0000348B1 EP 78100256 A EP78100256 A EP 78100256A EP 78100256 A EP78100256 A EP 78100256A EP 0000348 B1 EP0000348 B1 EP 0000348B1
- Authority
- EP
- European Patent Office
- Prior art keywords
- diisocyanates
- reaction
- carbon atoms
- monoamines
- groups
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
- 0 C*(C)*[N+](**)[O-] Chemical compound C*(C)*[N+](**)[O-] 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/80—Masked polyisocyanates
- C08G18/8061—Masked polyisocyanates masked with compounds having only one group containing active hydrogen
- C08G18/807—Masked polyisocyanates masked with compounds having only one group containing active hydrogen with nitrogen containing compounds
- C08G18/808—Monoamines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C273/00—Preparation of urea or its derivatives, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups
- C07C273/18—Preparation of urea or its derivatives, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups of substituted ureas
- C07C273/1809—Preparation of urea or its derivatives, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups of substituted ureas with formation of the N-C(O)-N moiety
- C07C273/1818—Preparation of urea or its derivatives, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups of substituted ureas with formation of the N-C(O)-N moiety from -N=C=O and XNR'R"
- C07C273/1827—X being H
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C275/00—Derivatives of urea, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups
- C07C275/46—Derivatives of urea, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups containing any of the groups, X being a hetero atom, Y being any atom, e.g. acylureas
- C07C275/58—Y being a hetero atom
- C07C275/62—Y being a nitrogen atom, e.g. biuret
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/77—Polyisocyanates or polyisothiocyanates having heteroatoms in addition to the isocyanate or isothiocyanate nitrogen and oxygen or sulfur
- C08G18/78—Nitrogen
- C08G18/7806—Nitrogen containing -N-C=0 groups
- C08G18/7818—Nitrogen containing -N-C=0 groups containing ureum or ureum derivative groups
Definitions
- the present invention relates to new organic polyisocyanates containing polyurethane groups, a novel process for their preparation and the use of the new compounds as an isocyanate component in the production of polyurethane plastics.
- Polyisocyanates containing biuret groups are known and find practical use as raw materials for high-quality, lightfast coatings. You can, for example, from diisocyanates and water (DT-AS 1 101 394), hydrogen sulfide (DT-AS 1 165 580), formic acid (DT-AS 1 174760), tertiary alcohols (DT-AS 1 543 178, DT-AS 1 931 055, monoamines (DT-OS 2308015) or polyamines (DT-OS 2 261 065).
- diisocyanates and water DT-AS 1 101 394
- hydrogen sulfide DT-AS 1 165 580
- formic acid DT-AS 1 174760
- tertiary alcohols DT-AS 1 543 178
- DT-AS 1 931 055 monoamines
- DT-OS 2308015 monoamines
- polyamines DT-OS 2 261 065
- the isocyanate groups initially form amino groups, which react further with excess diisocyanate via the corresponding diisocyanate ureas to form biuret polyisocyanates.
- the conversion of the isocyanate groups into amino groups is always accompanied by the formation of gaseous by-products such as carbon dioxide, carbon monoxide, carbon sulfoxide or olefins, the removal of which can lead to exhaust gas problems.
- gaseous by-products such as carbon dioxide, carbon monoxide, carbon sulfoxide or olefins
- the present invention also relates to the use of the new compounds as an isocyanate component in the production of polyurethane plastics by the isocyanate polyaddition process.
- Suitable monoamines are: dimethylamine, diethylamine, dipropylamine, dibutylamine or piperidine.
- modified polyisocyanates containing triuret or higher polyuret groups are formed from the monoamines mentioned above and the diisocyanates mentioned below by way of example, in which the rest of the amine which is indifferent to the reaction is incorporated. This reaction takes place via the intermediate stages of the compounds having urea groups which form from the amines and the diisocyanates or the compounds which have urea groups and compounds having further diurayate-forming biuret groups.
- Intermediate stages are therefore the monourea monoisocyanates formed by the addition of one mole of amine and one mole of diisocyanate or also of bisheas formed from two moles of amine and one mole of diisocyanate, or the biuret polyisocyanates formed from these and further diisocyanate.
- a logical consequence of this fact is, of course, that as a starting material according to a modification of the process according to the invention, these can also be used, for example, in a separate operation from the intermediates prepared in the example of monoamines and the isocyanates mentioned below as examples.
- the type of manufacture of these intermediates is of no importance here.
- reaction product containing urea groups from one mole of hexamethylene-bis-carbamic acid chloride and 2 moles of a monoamine which corresponds to the reaction product containing urea groups from one mole of hexamethylene diisocyanate and 2 moles of the same monoamine.
- Ge for the inventive process - suitable diisocyanates are those having aliphatically and / or cycloaliphatically attached isocyanate groups, in particular those in which the two isocyanate groups are connected via aliphatic hydrocarbon radicals having 4-12 carbon atoms or cycloaliphatic hydrocarbon radicals having 4-15 carbon atoms, wherein the aliphatic or Cycloaliphatic hydrocarbon chains can be interrupted or substituted by ester groups, such as: 1,4-diisocyanatobutane, 1,6-diisocyanatohexane, 2,4,4-trimethyl-1,6-di-isocyanatohexane, 1,11-diisocyanatoundecane, 3-isocyanatomethyl -3,5,5-trimethylcydohexyl isocyanate, 4,4'-cydohexane diisocyanate, 4,4'-dicyclohexylmethane diisocyanate, 1,2-bis
- diisocyanate mixtures can also be used, e.g. a urea or a biuret are first produced from a diisocyanate with a monofunctional amine, which then form polyurets with another diisocyanate.
- the catalysts to be used in accordance with the invention are proton-releasing strong acids which react with isocyanates, in particular with aliphatic or cycloaliphatic isocyanates, to form a mixed acid anhydride, the carbamic acid corresponding to the isocyanate and the proton-releasing acid being the acids of the mixed acid anhydride.
- suitable acids are hydrogen halides such as e.g. Hydrogen fluoride, hydrogen chloride, hydrogen bromide or hydrogen iodine, chlorosulfonic acid, fluorosulfonic acid, sulfuric acid, alkanesulfonic acids such as e.g. Methanesulfonic acid or perhalogenated alkanesulfonic acids such as e.g. Trifluoromethanesulfonic acid.
- Hydrogen chloride is the preferred acid to be used in the process according to the invention.
- the ammonium salts corresponding to the acids with the amines used as starting material or the mixed carbamic acid anhydrides corresponding to the acids, in particular carbamic acid chlorides, the diisocyanates used as starting material or any other isocyanate can of course be used in the process according to the invention.
- the catalysts are used in amounts of 0.001-10, preferably 0.01-1.0% by weight, based on the total weight of the reactants.
- the process according to the invention can be carried out, in particular, using the acids mentioned as examples as catalysts at relatively low temperatures in the range from about 0-140 ° C., the reaction leading to triuret and polyuret groups having reaction products going beyond the stage of the biuret polyisocyanates in general Range between 90 and 140 ° C expires.
- the catalysis according to the invention with the acids mentioned by way of example thus permits, under mild reaction conditions, the preparation of isocyanate addition products containing polyurethane groups from organic diisocyanates and organic monoamines or urea groups or compounds having biuret groups formed from monoamines and diisocyanates.
- monoamines no volatile by-products arise due to the mild reaction conditions.
- the remainder of the monoamines which are indifferent to the implementation of the invention, thus always forms part of the process products of the invention.
- these and the diisocyanates are generally used in proportions which have an NCO / NH molar ratio of 5.5: 1 to 100: 1, preferably 6: 1 to 30: 1, correspond.
- starting materials containing urea groups i.e.
- Corresponding quantitative ratios of monourea monoisocyanates or bis-ureas formed from monoamines and diisocyanates are used, taking into account that monoamines and diisocyanates in a molar ratio of 1: 1 or 2: 1 are already present in the starting materials containing urea groups.
- the reaction is terminated. This is done simply by cooling the reaction mixture to 20-50 ° C.
- the reaction times required depend on the type of starting products, on the temperature and in particular on the type and amount of the catalyst used. They are generally 1-20, preferably 2-8, hours. After the reaction has ended, clear, colorless to slightly yellowish reaction solutions are obtained.
- the reactions are usually ended at a point in time when on average about 3 NCO groups have been consumed per amino group.
- the products then have an average functionality of 3.5, taking into account the polymer homologue.
- it is possible to achieve a higher "degree of polyuretization", i.e. implement 4 and more NCO groups per amino group.
- the viscosities of the products then increase quickly.
- the catalyst is generally removed by distilling the reaction mixture in vacuo. If hydrogen halides are used as catalysts, the removal, in particular in the case of smaller amounts of catalyst, can also be carried out by adding equimolar amounts of propylene oxide. It is also possible to remove the catalyst by e.g. Remove thin film evaporation if the crude isocyanate is freed from excess diisocyanate. The distillate from the thin-film distillation, which then contains the catalyst in addition to the diisocyanate, can be reused as the starting material.
- the removal of excess diisocyanate is usually done by thin-layer evaporation; however, it can also be extracted by extraction of the reaction mixture with suitable solvents, e.g. Hexane, heptane etc. can be achieved.
- suitable solvents e.g. Hexane, heptane etc.
- the crude isocyanates can be used as such. In most cases, however, they are preferably freed from monomeric isocyanate fractions by thin-layer evaporation or extraction.
- the monomer-free products are light yellow oils or solid resins; the NCO content is 10-22%.
- the process is ideal for continuous implementation. In these cases, several reaction vessels are cascaded together. In the first reaction vessel, the starting products diisocyanate and amine are mixed at approx. 60 ° C. The catalyst is added at about 80 ° C. in the second reaction vessel. In the third and optionally further reaction vessels, the further reaction to the polyisocyanate takes place at approx. 90-140 ° C., the desired degree of “polyurethaneisation” being set by controlling the temperature and the residence time.
- Excess diisocyanate and the catalyst are e.g. removed via a coiled tube evaporator combined with a downstream thin film evaporator.
- the distillates consisting of diisocyanate and catalyst are combined and returned to the process.
- the polyisocyanate is obtained as the residue of thin-film distillation.
- the properties of the modified polyisocyanates obtained, in particular their NCO functionality, NCO content, and the viscosity can be adjusted not only by selecting the suitable starting materials but also particularly simply by adjusting the "degree of polyuretization", i.e. the number of NCO groups converted per amino group can be controlled.
- the process products according to the invention can be used in particular as an isocyanate component in the production of polyurethane plastics by the isocyanate polyaddition process. They are both suitable for the production of poly. urethane foams, as well as for the production of elastomers, coatings or bonds. In particular when using the process products according to the invention for the first-mentioned area of application, it is often unnecessary to distill off the excess diisocyanate after the reaction according to the invention has ended.
- the monomer-free process products according to the invention are excellent raw materials for producing high-quality, weatherproof and lightfast coatings.
- the reaction solution was cooled to 50 ° C. and 11 g (0.19 mol) of propylene oxide were added to bind the hydrolyzable chlorine.
- Example 5 154 g of the polyester solution described in Example 5 were processed with 100 g of titanium dioxide (rutile type) to form a paste. In addition to the catalyst and leveling agent, 120 g of the solvent mixture already described were added to this paste. The mixture thus obtained was mixed with 135 g of a 75% solution of the polyisocyanate from Example 1 in ethyl glycol acetate / xylene (1: 1) and applied in a thin layer to steel sheets.
- the paint films containing pigment hardened completely at room temperature. They were characterized by scratch resistance and solvent resistance and had the following properties compared to the clear lacquer films:
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Polyurethanes Or Polyureas (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
Die vorliegende Erfindung betrifft neue, Polyuretgruppen aufweisende organische Polyisocyanate, ein neuartiges Verfahren zu deren Herstellung und die Verwendung der neuen Verbindungen als Isocyanat-Komponente bei der Herstellung von Polyurethankunststoffen.The present invention relates to new organic polyisocyanates containing polyurethane groups, a novel process for their preparation and the use of the new compounds as an isocyanate component in the production of polyurethane plastics.
Biuretgruppen enthaltende Polyisocyanate sind bekannt und finden als Rohstoffe für hochwertige, litchtechte Lackierungen praktische Verwendung. Sie können beispielsweise aus Diisocyanaten und Wasser (DT-AS 1 101 394), Schwefelwasserstoff (DT-AS 1 165 580), Ameisensäure (DT-AS 1 174760), tertiären Alkoholen (DT-AS 1 543 178, DT-AS 1 931 055, Monoaminen (DT-OS 2308015) oder Polyaminen (DT-OS 2 261 065) hergestellt werden.Polyisocyanates containing biuret groups are known and find practical use as raw materials for high-quality, lightfast coatings. You can, for example, from diisocyanates and water (DT-AS 1 101 394), hydrogen sulfide (DT-AS 1 165 580), formic acid (DT-AS 1 174760), tertiary alcohols (DT-AS 1 543 178, DT-AS 1 931 055, monoamines (DT-OS 2308015) or polyamines (DT-OS 2 261 065).
Diese Verfahren des Standes der Technik zur Herstellung von Biuretpolyisocyanaten weisen eine Reihe von Natchteilen auf.These prior art processes for the production of biuret polyisocyanates have a number of snap parts.
So entstehen bei den meisten der Verfahren aus einem Teil der Isocyanatgruppen zunächst Aminogruppen, die mit überschüssigem Diisocyanat über die entsprechenden Diisocyanatharnstoffe zu Biuretpolyisocyanaten weiterreagiern. Die Umwandlung der Isocyanatgruppen in Aminogruppen wird stets durch die Entstehung von gasförmigen Nebenprodukten wie Kohlendioxid, Kohlenmonoxid, Kohlensulfoxid oder Olefine begleitet, deren Beseitigung zu Abgasproblemen führen kann. Bei der heterogenen Reaktion von Diisocyanaten mit Wasser besteht zusätzlich die Gefahr der Bildung von unlöslichen Polyharnstoffen die nur schwer abzutrennen sind. Die Reaktion von Diisocyanaten mit tertiären Alkoholen, die zur Herstellung von Biuretpolyisocyanaten technisch genutzt wird, hat den weiteren Nachteil, daß für die Urethanspaltung zur Überführung der Isocyanatgruppen in Aminogruppen verhältnismäßig hohe Temperaturen notwendig sind. Von besonderem Nachteil ist jedoch# der Umstand, daß bei diesen Verfahren zunächst ein Teil der lsocyanatgruppen des als Ausgangsmaterial verwendeten Diisocyanats unter Aminbildung vernichtet werden muß.In most of the processes, some of the isocyanate groups initially form amino groups, which react further with excess diisocyanate via the corresponding diisocyanate ureas to form biuret polyisocyanates. The conversion of the isocyanate groups into amino groups is always accompanied by the formation of gaseous by-products such as carbon dioxide, carbon monoxide, carbon sulfoxide or olefins, the removal of which can lead to exhaust gas problems. In the heterogeneous reaction of diisocyanates with water, there is also the risk of the formation of insoluble polyureas which are difficult to separate. The reaction of diisocyanates with tertiary alcohols, which is used industrially for the production of biuret polyisocyanates, has the further disadvantage that relatively high temperatures are necessary for the urethane cleavage to convert the isocyanate groups into amino groups. Of particular disadvantage, however, is the fact that in these processes a part of the isocyanate groups of the diisocyanate used as the starting material must first be destroyed with the formation of amines.
Die direkte Umsetzung von Polyaminen mit Diisocyanaten führt zwar gemäß DT-OS 2 261 065 ohne Abspaltung von flüchtigen Nebenprodukten und ohne Umwandlung von Isocyanatgruppen in Aminogruppen zu Biuretpolyisocyanaten. Bei diesem Verfahren treten aber insbesondere bei Verwendung von technisch leicht zugänglichen Ausgangsmaterialien wie Hexamethylendiamin und Hexamethylen- diisocyanat erhebliche praktische Schwierigkeiten auf, da wegen der hohen Reaktivität der Aminogruppen gegenüber den Isocyanatgruppen die Tendenz zur Bildung von unlöslichen Polyharnstoffen sehr groß ist und so in den meisten Fällen zur Vervollständigung der Umsetzung unwirtschaftlich langes Nachheizen des Reaktionsgemisches bei hoher Temperatur notwendig ist, was zu einer starken Beeinträchtigung der Eigenschaften der Verfahrensprodukte, insbesondere deren Eigenfarbe, führt.According to DT-OS 2 261 065, the direct reaction of polyamines with diisocyanates leads to biuret polyisocyanates without elimination of volatile by-products and without conversion of isocyanate groups into amino groups. In this process, however, considerable practical difficulties arise, particularly when using technically easily accessible starting materials such as hexamethylene diamine and hexamethylene diisocyanate, since the tendency towards the formation of insoluble polyureas is very great because of the high reactivity of the amino groups with the isocyanate groups, and so in most cases To complete the implementation, uneconomically long reheating of the reaction mixture at high temperature is necessary, which leads to a severe impairment of the properties of the process products, in particular their inherent color.
Bei allen Verfahren des Standes der Technik findet unter den genannten Nachteilen der Übergang von Diisocyanaten zu Biuretpolyisocyanaten statt. Dabei wird die Weiterreaktion zu Polyuretpolyisocyanaten nicht beobachtet.In all of the prior art processes, the transition from diisocyanates to biuret polyisocyanates takes place under the disadvantages mentioned. The further reaction to polyurethane polyisocyanates is not observed.
Es war daher die Aufgabe der vorliegenden Erfindung, ein neues Verfahren zur Verfügung zu stellen, welches auf einfache Weise die Herstellung von hochwertigen modifizierten Polyisocyanaten gestattet, die die Vorteile der Biuretpolyisocyanate in sich vereinigen, ohne daß das Verfahren mit den genannten Nachteilen der Verfahren des Standes der Technik behaftet ist.It was therefore the object of the present invention to provide a new process which allows the preparation of high-quality modified polyisocyanates which combine the advantages of the biuret polyisocyanates in a simple manner without the process having the disadvantages of the processes of the prior art mentioned is affected by technology.
Diese Aufgabe konnte überraschenderweise dadurch gelöst werden, daß man bestimmte, nachstehend näher beschriebene organische Monoamine mit überschüssigen Mengen an bestimmten, nachstehend näher beschreibenen Diisocyanaten unter bestimmten nachstehend näher beschriebenen Reaktionsbedingungen umsetzt.This object was surprisingly achieved by reacting certain organic monoamines, described in more detail below, with excess amounts of certain diisocyanates, described in more detail below, under certain reaction conditions described in more detail below.
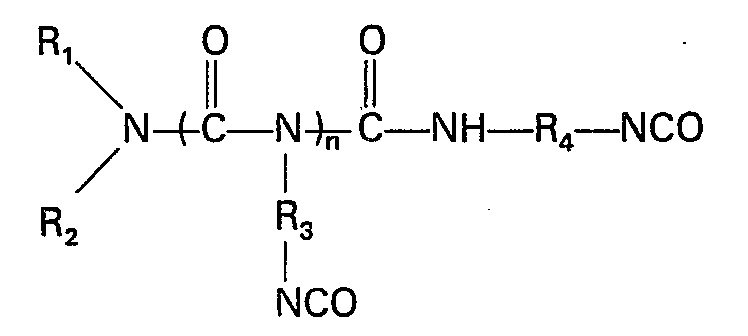
Gegenstand der vorliegenden Erfindung sind Verbindungen der Formel
- R1 und R2 für gleiche oder verschiedene Reste stehen und aliphatische Kohlenwasserstoff- reste mit 1-4 Kohlenstoffatomen bedeuten, wobei R1 und R2 zusammen mit dem Stickstoffatom auch einen Piperidinrest bilden können,
- R3 und R4 für gleiche oder verschiedene Reste stehen und aliphatische, gegebenenfalls durch Estergruppen unterbrochene Kohlenwasserstoffreste mit 4-12 Kohlenstoffatomen oder cycloaliphatische Kohlenwasserstoffreste mit 4-15 Kohlenstoffatomen bedeuten und eine Zahl von 2-8 bedeutet.
- R 1 and R 2 stand for identical or different radicals and mean aliphatic hydrocarbon radicals with 1-4 carbon atoms, where R 1 and R 2 together with the nitrogen atom can also form a piperidine radical,
- R 3 and R 4 represent identical or different radicals and are aliphatic hydrocarbon radicals with 4-12 carbon atoms, optionally interrupted by ester groups, or cycloaliphatic hydrocarbon radicals with 4-15 carbon atoms and represent a number from 2-8.
Gegenstand der vorliegenden Erfindung ist auch ein Verfahren zur Herstellung von Verbindungen der Formel
- a) aliphatische sekundäre Monoamine, deren aliphatische Kohlenwasserstoff-reste 1-4 Kohlenstoffatome aufweisen oder Piperidin oder
- b) Harnstoff- und/oder Biuretgruppen, sowie den bezüglich der Umsetzung indifferenten Rest der Amine aufweisende Umsetzungsprodukte der unter a) genannten Monoamine mit aliphatischen Diisocyanaten, deren aliphatischer Kohlenwasserstoffrest 4-12 Kohlenstoffatome aufweist und durch Estergruppen unterbrochen sein kann oder mit cycloaliphatischen Diisocyanaten, deren cycloaliphatischer Kohlenwasserstoffrest 4-15 Kohlenstoffatome aufweist
mit Diisocyanaten der unter b) genannten Art bei 0140°C in Gegenwart von starken, mit Isocyanaten ein gemischtes Carbamidsäureanhydrid bildenden Säuren umsetzt, wobei man die Menge der eingesetzten Diisocyanate so wählt, daß insgesamt ein NCO/NH-Molverhältnis, bezogen auf Diisocyanate und Monoamine von 5,5:1 bis 100:1 vorliegt.The present invention also relates to a process for the preparation of compounds of the formula
- a) aliphatic secondary monoamines whose aliphatic hydrocarbon radicals have 1-4 carbon atoms or piperidine or
- b) urea and / or biuret groups, and the reaction products of the monoamines mentioned under a) with aliphatic diisocyanates whose aliphatic hydrocarbon radical has 4-12 carbon atoms and which may be interrupted by ester groups or with cycloaliphatic diisocyanates, the reaction products of the amines mentioned under a) cycloaliphatic hydrocarbon radical has 4-15 carbon atoms
with diisocyanates of the type mentioned under b) at 0140 ° C in the presence of strong acids forming a mixed carbamic acid anhydride with isocyanates, the amount of diisocyanates used being chosen so that a total NCO / NH molar ratio, based on diisocyanates and monoamines from 5.5: 1 to 100: 1.
Gegenstand der vorliegenden Erfindung ist schließlich auch die Verwendung der neuen Verbindungen als Isocyanatkomponente bei der Herstellung von Polyurethankunststoffen nach dem Isocyanat-Polyadditionsverfahren.Finally, the present invention also relates to the use of the new compounds as an isocyanate component in the production of polyurethane plastics by the isocyanate polyaddition process.
Ausgangsmaterialien für das erfindungsgemäße Verfahren sind Monoamine der Formel
- R1 und R2 die bereits oben angegebene Bedeutung haben.
- R 1 and R 2 have the meaning already given above.
Beliebige Gemische der genannten Amine können ebenfalls eingesetzt werden. Konkrete Beispiele für geeignete Monoamine sind: Dimethylamin, Diäthylamin, Dipropylamin, Dibutylamin oder Piperidin.Any mixtures of the amines mentioned can also be used. Specific examples of suitable monoamines are: dimethylamine, diethylamine, dipropylamine, dibutylamine or piperidine.
Bei der Durchführung des erfindungsgemäßen Verfahrens entstehen aus den beispielhaft genannten Monoaminen und den nachstehend beispielhaft genannten Diisocyanaten Triuretoder höhere Polyuretgruppen aufweisende, modifizierte Polyisocyanate, in denen der bezüglich der Umsetzung indifferente Rest des Amins eingebaut ist. Diese Umsetzung verläuft über die Zwischenstufen der aus den Aminen und den Diisocyanaten sich bildenden Harnstoffgruppen aufweisenden Verbindungen bzw. sich den Harnstoffgruppen aufweisenden Verbindungen mit weiterem Diisocyanat bildenden Biuretgruppen aufweisenden Verbindungen. Zwischenstufen sind somit die sich durch Addition von einem Mol Amin und einem Mol Diisocyanat bildenden Monoharnstoff-Monoisocyanate oder auch aus zwei Mol Amin und einem Mol Diisocyanat entstehende Bisharnstoffe bzw. die sich aus diesen und weiterem Diisocyanat bildenden Biuretpolyisocyanate. Eine logische Konsequenz dieses Tatbestandes ist selbstverständlich, daß als Ausgangsmaterial gemäß einer Abänderung des erfindungsgemäßen Verfahrens auch diese beispielsweise in einem separaten Arbeitsgang aus den bei spielhaft genannten Monoaminen und den nachstehend beispielhaft genannten Isocyanaten hergestellte Zwischenprodukte eingesetzt werden können. Hierbei spielt selbstverständlich die Art der Herstellung dieser Zwischenprodukte keine Rolle. So wäre es selbstverständlich auch denkbar, als Ausgangsmaterials beim erfindungsgemäßen Verfahren das Harnstoffgruppen aufweisende Umsetzungsprodukt aus einem Mol Hexamethylen-bis-carbamidsäurechlorid und 2 Mol eines Monoamins einzusetzen, welches dem Harnstoffgruppen aufweisenden Umsetzungsprodukt aus einem Mol Hexamethylendiisocyanat und 2 Mol des gleichen Monoamins entspricht.When carrying out the process according to the invention, modified polyisocyanates containing triuret or higher polyuret groups are formed from the monoamines mentioned above and the diisocyanates mentioned below by way of example, in which the rest of the amine which is indifferent to the reaction is incorporated. This reaction takes place via the intermediate stages of the compounds having urea groups which form from the amines and the diisocyanates or the compounds which have urea groups and compounds having further diurayate-forming biuret groups. Intermediate stages are therefore the monourea monoisocyanates formed by the addition of one mole of amine and one mole of diisocyanate or also of bisheas formed from two moles of amine and one mole of diisocyanate, or the biuret polyisocyanates formed from these and further diisocyanate. A logical consequence of this fact is, of course, that as a starting material according to a modification of the process according to the invention, these can also be used, for example, in a separate operation from the intermediates prepared in the example of monoamines and the isocyanates mentioned below as examples. Of course, the type of manufacture of these intermediates is of no importance here. It would of course also be conceivable to use as the starting material in the process according to the invention the reaction product containing urea groups from one mole of hexamethylene-bis-carbamic acid chloride and 2 moles of a monoamine which corresponds to the reaction product containing urea groups from one mole of hexamethylene diisocyanate and 2 moles of the same monoamine.
Für das erfindungsgemäße Verfahren ge- eignete Diisocyanate sind solche mit aliphatisch und/oder cycloaliphatisch gebundenen Isocyanatgruppen, insbesondere solche in denen die beiden Isocyanatgruppen über aliphatische Kohlenwasserstoffreste mit 4-12 Kohlenstoffatomen oder über cycloaliphatische Kohlenwasserstoffreste mit 4-15 Kohlenstoffatomen verbunden sind, wobei die aliphatischen oder cycloaliphatischen Kohlenwasserstoffketten durch Estergruppen unterbrochen oder substituiert sein können, wie z.B.: 1,4-Diisocyanatobutan, 1,6-Diisocyanatohexan, 2,4,4-Trimethyl-1,6-di-isocyanatohexan, 1,11-Diisocyanatoundecan, 3-lsocyanatomethyl-3,5,5-trimethylcydo- hexylisocyanat, 4,4'-Cydohexandiisocyanat, 4,4'-Dicyclohexylmethan-diisocyanat, 1,2-Bis-(isocyanatomethyl)cyclobutan oder 6-lsocyanato- capronsäure-2-isocyanatoäthylester. Bevorzugt wird Hexamethylen-diisocyanat eingesetzt.Ge for the inventive process - suitable diisocyanates are those having aliphatically and / or cycloaliphatically attached isocyanate groups, in particular those in which the two isocyanate groups are connected via aliphatic hydrocarbon radicals having 4-12 carbon atoms or cycloaliphatic hydrocarbon radicals having 4-15 carbon atoms, wherein the aliphatic or Cycloaliphatic hydrocarbon chains can be interrupted or substituted by ester groups, such as: 1,4-diisocyanatobutane, 1,6-diisocyanatohexane, 2,4,4-trimethyl-1,6-di-isocyanatohexane, 1,11-diisocyanatoundecane, 3-isocyanatomethyl -3,5,5-trimethylcydohexyl isocyanate, 4,4'-cydohexane diisocyanate, 4,4'-dicyclohexylmethane diisocyanate, 1,2-bis (isocyanatomethyl) cyclobutane or 6-isocyanato-caproic acid 2-isocyanatoethyl ester. Hexamethylene diisocyanate is preferably used.
Selbstverständlich können auch Diisocyanatgemische verwendet werden, wobei z.B. zuerst aus einem Diisocyanat mit einem monofunktionellen Amin ein Harnstoff oder ein Biuret erzeugt werden, die dann mit einem anderen Diisocyanat Polyurete bilden.Of course, diisocyanate mixtures can also be used, e.g. a urea or a biuret are first produced from a diisocyanate with a monofunctional amine, which then form polyurets with another diisocyanate.
Während die Reaktion von Aminen mit Diisocyanaten zu den entsprechenden Harnstoffen bzw. Biureten zum vorbekannten Stand der Technik gehört, ist bislang noch kein technisch brauchbares Verfahren bekannt ge* worden, welches eine Weiterführung der zwischen Amin und Isocyanat ablaufenden Additionsreaktion über die Zwischenstufe der entsprechenden Biurete hinaus gestattet. Dies liegt an der Reaktionsträgheit der Biurete gegenüber organischen Diisocyanaten, die nur durch Verwendung geeigneter Katalysatoren überwunden werden kann. Erfindungsgemäß wird nun auch die Weiterreaktion von Monoaminen mit überschüssigem Diisocyanat über die Harnstoff- und Biuretstufe hinaus zu Polyureten in Gegenwart von Katalysatoren durchgeführt.While the reaction of amines with diisocyanates to the corresponding ureas or biurets belongs to the prior art, no technically usable process has been known to date, which would continue the addition reaction between amine and isocyanate beyond the intermediate stage of the corresponding biurets allowed. This is due to the inertia of the biurets with organic diisocyanates, which can only be overcome by using suitable catalysts. According to the invention the further reaction of monoamines with excess diisocyanate beyond the urea and biuret stage to give polyurets in the presence of catalysts is now also carried out.
Bei den erfindungsgemäß einzusetzenden Katalysatoren handelt es sich um protonenabspaltende starke Säuren, welche mit lsocyanaten, insbesondere mit aliphatischen oder cycloaliphatischen Isocyanaten, unter Bildung eines gemischten Säureanhydrids reagieren, wobei die dem Isocyanat entsprechende Carbamidsäure und die protonenabspaltende Säure die Säuren des gemischten Säureanhydrids darstellen. So reagieren derartige, für das erfindungsgemäße Verfahren geeignete Säuren HX (X = Säurerest nach Abspaltung des Protons) mit Isocyanaten Y-NCO zu Addukten der Formel Y-NH-C0-X, welche als gemischtes Anhydrid der Carbamidsäure Y-NH-COOH und der Säure HX anzusehen sind.The catalysts to be used in accordance with the invention are proton-releasing strong acids which react with isocyanates, in particular with aliphatic or cycloaliphatic isocyanates, to form a mixed acid anhydride, the carbamic acid corresponding to the isocyanate and the proton-releasing acid being the acids of the mixed acid anhydride. Such acids HX (X = acid residue after proton cleavage) suitable for the process according to the invention react with isocyanates Y-NCO to form adducts of the formula Y-NH-CO-X, which as a mixed anhydride of the carbamic acid Y-NH-COOH and Acid HX can be seen.
Beispiele geeigneter Säuren sind Halogenwasserstoffe wie z.B. Fluorwasserstoff, Chlorwasserstoff, Bromwasserstoff oder Jodwasserstoff, Chlorsulfonsäure, Fluorsulfonsäure, Schwefelsäure, Alkansulfonsäuren wie z.B. Methansulfonsäure oder perhalogenierte Alkansulfonsäuren wie z.B. Trifluormethansulfonsäure. Chlorwasserstoff ist die beim erfindungsgemäßen Verfahren bevorzugt einzusetzende Säure. Anstelle der Säuren können beim erfindungsgemäßen Verfahren selbstverständlich sowohl die den Säuren entsprechenden Ammoniumsalze mit den als Ausgangsmaterial eingesetzten Aminen oder die den Säuren entsprechenden gemischten Carbamidsäureanhydride, insbesondere Carbamidsäurechloride, der als Ausgangsmaterial eingesetzten Diisocyanate oder eines beliebigen anderen isocyanats eingesetzt werden. Im Allgemeinen werden die Katalysatoren in Mengen von 0,001-10, vorzugsweise 0,01-1,0 Gew.-%, bezogen auf das Gesamtgewicht der Reaktionspartner, eingesetzt.Examples of suitable acids are hydrogen halides such as e.g. Hydrogen fluoride, hydrogen chloride, hydrogen bromide or hydrogen iodine, chlorosulfonic acid, fluorosulfonic acid, sulfuric acid, alkanesulfonic acids such as e.g. Methanesulfonic acid or perhalogenated alkanesulfonic acids such as e.g. Trifluoromethanesulfonic acid. Hydrogen chloride is the preferred acid to be used in the process according to the invention. Instead of the acids, the ammonium salts corresponding to the acids with the amines used as starting material or the mixed carbamic acid anhydrides corresponding to the acids, in particular carbamic acid chlorides, the diisocyanates used as starting material or any other isocyanate can of course be used in the process according to the invention. In general, the catalysts are used in amounts of 0.001-10, preferably 0.01-1.0% by weight, based on the total weight of the reactants.
Die Durchführung des erfindungsgemäßen Verfahrens insbesondere unter Verwendung der beispielhaft genannten Säuren als Katalysatoren ist bei relativ niedrigen Temperaturen im Bereich von ca. 0-140°C möglich, wobei die über die Stufe der Biuretpolyisocyanate hinausführende Reaktion zu Triuret-und Polyuretgruppen aufweisenden Umsetzungsprodukten im allgemeinen im Bereich zwischen 90 und 140°C abläuft. Die erfindungsgemäße Katalyse mit den beispielhaft genannten Säuren gestattet somit unter milden Reaktionsbedingungen die Herstellung von Polyuretgruppen aufweisenden Isocyanat-Additionsprodukten aus organischen Diisocyanaten und organischen Monoaminen bzw. aus Monoaminen und Diisocyanaten entstehenden Harnstoffgruppen oder Biuretgruppen aufweisenden Verbindungen. Bei der Durchführung des erfindungsgemäßen Verfahrens unter Verwendung von Monoaminen als Ausgangsmaterialien entstehen wegen der milden Reaktionsbedingungen keine leicht flüchtigen Nebenproduktc. Der bezüglich der erfindungsgemäßen Umsetzung indifferente Rest der Monoamine bildet somit stets einen Bestandteil der erfindungsgemäßen Verfahrensprodukte.The process according to the invention can be carried out, in particular, using the acids mentioned as examples as catalysts at relatively low temperatures in the range from about 0-140 ° C., the reaction leading to triuret and polyuret groups having reaction products going beyond the stage of the biuret polyisocyanates in general Range between 90 and 140 ° C expires. The catalysis according to the invention with the acids mentioned by way of example thus permits, under mild reaction conditions, the preparation of isocyanate addition products containing polyurethane groups from organic diisocyanates and organic monoamines or urea groups or compounds having biuret groups formed from monoamines and diisocyanates. When the process according to the invention is carried out using monoamines as starting materials, no volatile by-products arise due to the mild reaction conditions. The remainder of the monoamines, which are indifferent to the implementation of the invention, thus always forms part of the process products of the invention.
Bei der Durchführung des erfindungsgemäßen Verfahrens unter Verwendung von Monoaminen als Ausgangsmaterialien werden diese und die Diisocyanate im allgemeinen in Mengenverhältnissen eingesetzt, die einem NCO/NH-Molverhältnis von 5,5:1 bis 100:1, vorzugsweise 6:1 bis 30:1, entsprechen. Bei Verwendung von Harnstoffgruppen aufweisenden Ausgangsmaterialien, d.h. von aus Monoaminen und Diisocyanaten gebildeten Monoharnstoff-Monoisocyanaten bzw. Bis-Harnstoffen kommen entsprechende Mengenverhältnisse zum Einsatz, wobei zu berücksichtigen ist, daß in den genannten Harnstoffgruppen aufweisenden Ausgangsmaterialien bereits Monoamine und Diisocyanate im Molverhältnis 1:1 bzw. 2:1 vorliegen. Diese in Form der Harnstoffgruppen aufweisenden Ausgangsmaterialien vorliegenden Monoamine und Diisocyanate gehen mit in die Berechnung des Mengenverhältnisses Amin:Diisocyanat ein. Sinngemäß die gleichen Ausführungen gelten bei Verwendung von Biuretgruppen aufweisenden Ausgangsmaterialien, wie sie durch Umsetzung der genannten Harnstoffgruppen aufweisenden Zwischenprodukte mit weiterem Diisocyanat entstehen.When carrying out the process according to the invention using monoamines as starting materials, these and the diisocyanates are generally used in proportions which have an NCO / NH molar ratio of 5.5: 1 to 100: 1, preferably 6: 1 to 30: 1, correspond. When using starting materials containing urea groups, i.e. Corresponding quantitative ratios of monourea monoisocyanates or bis-ureas formed from monoamines and diisocyanates are used, taking into account that monoamines and diisocyanates in a molar ratio of 1: 1 or 2: 1 are already present in the starting materials containing urea groups. These monoamines and diisocyanates, which are present in the form of the starting materials containing urea groups, are included in the calculation of the amine: diisocyanate ratio. The same statements apply mutatis mutandis when starting materials containing biuret groups are used, as they result from the reaction of the intermediate products containing urea groups with further diisocyanate.
Zur Durchführung des erfindungsgemäßen Verfahren wird im allgemeinen wie folgt verfahren:
- Man legt das Diisocyanat in einem geeigneten Reaktionsgefäß vor und gibt das Amin bei Temperaturen von 0-100°C zu. Dabei beträgt das NCO/NH-Molverhältnis im allgemeinen 6:1 bis 30:1. Feste Amine werden über einen beheitzten und flüssige Amine über einen normalen Tropftrichter dosiert. Gasförmige Amine werden eventuell zusammen mit einem Inertgasstrom in das Diisocyanat eingeleitet. Es bilden sich spontan die entsprechenden Hamstoffe. Bei Einsatz von sekundären Aminen bliebt die Reaktion bei Abwesenheit des Katalysators auf der Stufe der zumeist in überschüssigem Diisocyanat nicht vollständig löslichen Harnstoffe stehen. Die Katalysatorzugabe kann zu jedem Zeitpunkt der Reaktion erfolgen. Man kann ihn z.B. mit dem Diisocyanat vorlegen, ihn als Ammoniumsalz mit den Aminen eindosieren oder ihn erst nach Beendigung der Vorreaktion zu Harnstoff- oder Biuretisocyanaten zugeben. Danach wird das Reaktionsgemisch auf 90140°C erhitzt und der Reaktionsverlauf durch Kontrolle der NCO-Gehaltsabnahme verfolgt. Bei Verwendung von flüchtigen Katalysatoren, z.B. Chlorwasserstoff, kann zur Vermeidung von bei höheren Temperaturen möglichen Katalysatorverlusten unter Druck gearbeitet werden.
- The diisocyanate is placed in a suitable reaction vessel and the amine is added at temperatures of 0-100 ° C. The NCO / NH molar ratio is generally 6: 1 to 30: 1. Solid amines are dosed via a heated and liquid amine via a normal dropping funnel. Gaseous amines may be introduced into the diisocyanate together with an inert gas stream. The corresponding ureas form spontaneously. When secondary amines are used, the reaction remains in the absence of the catalyst at the stage of the ureas, which are usually not completely soluble in excess diisocyanate. The catalyst can be added at any time during the reaction. It can be introduced, for example, with the diisocyanate, metered in as the ammonium salt with the amines, or added to urea or biuret isocyanates only after the preliminary reaction has ended. The reaction mixture is then heated to 90140 ° C. and the course of the reaction is monitored by checking the decrease in NCO content. When using volatile catalysts, for example hydrogen chloride, it is possible to work under pressure to avoid possible catalyst losses at higher temperatures.
Wenn die NCO-Abnahme dem gewünschten "Polyuretisierungsgrad" entspricht: d.h., wenn pro Aminogruppe die gewünschte Menge an NCO-Gruppen umgesetzt ist, wird die Reaktion beendet. Dies geschieht einfach durch Abkühlen des Reaktionsgemisches auf 20-50°C. Die benötigten Reaktionszeiten hängen von der Art der Ausgangsprodukte, von der Temperatur und insbesondere von der Art und Menge des verwendeten Katalysators ab. Sie betragen im allgemeinen 1-20, vorzugsweise 2-8, Stunden. Nach Beendigung der Reaktion erhält man klare, farblose bis schwach gelblich gefärbte Reaktionslösungen.If the NCO decrease corresponds to the desired "degree of polyurethaneization": i.e., if the desired amount of NCO groups has been reacted per amino group, the reaction is terminated. This is done simply by cooling the reaction mixture to 20-50 ° C. The reaction times required depend on the type of starting products, on the temperature and in particular on the type and amount of the catalyst used. They are generally 1-20, preferably 2-8, hours. After the reaction has ended, clear, colorless to slightly yellowish reaction solutions are obtained.
Die Reaktionen werden meistens zu einem Zeitpunkt beendet, zu dem im Mittel pro Aminogruppe ca. 3 NCO-Gruppen verbraucht sind. Die Produkte haben dann unter Berücksichtigung der Polymerhomologen eine durchschnittliche Funktionalität von 3,5. Es ist jedoch möglich, einen höheren "Polyuretisierungsgrad" zu erreichen, d.h. pro Aminogruppe 4 und mehr NCO-Gruppen umzusetzen. Allerdings nehmen die Viskositäten der Produkte dann schnell zu.The reactions are usually ended at a point in time when on average about 3 NCO groups have been consumed per amino group. The products then have an average functionality of 3.5, taking into account the polymer homologue. However, it is possible to achieve a higher "degree of polyuretization", i.e. implement 4 and more NCO groups per amino group. However, the viscosities of the products then increase quickly.
Der Katalysator wird im allgemeinen durch Andestillieren des Reaktionsgemisches im Vakuum entfernt. Bei Verwendung von Halogenwasserstoffen als Katalysatoren kann die Beseitigung, insbesondere bei kleineren Kaalysatormengen auch durch Zugabe äquimolarer Mengen Propylenoxid erfolgen. Ferner ist es möglich, den Katalysator durch z.B. Dünnschichtverdampfung zu entfernern, falls das Rohisocyanat von überschüssigem Diisocyanat befreit wird. Das Destillat der Dünnschichtdestillation, das dann neben dem Diisocyanat den Katalysator enthält, kann als Ausgangsmaterial wiederverwendet werden.The catalyst is generally removed by distilling the reaction mixture in vacuo. If hydrogen halides are used as catalysts, the removal, in particular in the case of smaller amounts of catalyst, can also be carried out by adding equimolar amounts of propylene oxide. It is also possible to remove the catalyst by e.g. Remove thin film evaporation if the crude isocyanate is freed from excess diisocyanate. The distillate from the thin-film distillation, which then contains the catalyst in addition to the diisocyanate, can be reused as the starting material.
Ist die Entfernung von überschüssigem Diisocyanat vorgesehen, so erfolgt sie meistens durch Dünnschichtverdampfung; sie kann jedoch auch durch Extraktion des Reaktionsgemisches mit geeigneten Lösungsmitteln, wie z.B. Hexan, Heptan etc. erreicht werden.If the removal of excess diisocyanate is provided, it is usually done by thin-layer evaporation; however, it can also be extracted by extraction of the reaction mixture with suitable solvents, e.g. Hexane, heptane etc. can be achieved.
Die Rohisocyanate können als olche verwendet werden. In den meisten Fällen werden sie jedoch vorzugsweise durch Dünnschichtverdampfung oder Extraktion von monomeren lsocyanatanteilen befreit. Die monomerenfreien Produkte sind hellgelbe Öle oder auch feste Harze; der NCO-Gehalt beträgt 10-22%.The crude isocyanates can be used as such. In most cases, however, they are preferably freed from monomeric isocyanate fractions by thin-layer evaporation or extraction. The monomer-free products are light yellow oils or solid resins; the NCO content is 10-22%.
Das Verfahren eignet sich vorzüglich für eine kontinuierliche Durchführung. In diesen Fällen werden mehrere Reaktionsgefäße in Form einer Kaskade hinereinandergeschaltet. Im ersten Reaktionsgefäß werden die Ausgangsprodukte Diisocyanat und Amin bei ca. 60°C vermischt. Im zweiten Reaktionsgefäß wird bei ca. 80°C der Katalysator zugegeben. Im dritten und gegebenenfalls weiteren Reaktionsgefäßen findet bei ca. 90-140°C die Weiterreaktion zum Polyisocyanat statt, wobei durch Steuerung der Temperatur und der Verweilzeit der angestrebte "Polyuretisierungsgrad" eingestellt wird.The process is ideal for continuous implementation. In these cases, several reaction vessels are cascaded together. In the first reaction vessel, the starting products diisocyanate and amine are mixed at approx. 60 ° C. The catalyst is added at about 80 ° C. in the second reaction vessel. In the third and optionally further reaction vessels, the further reaction to the polyisocyanate takes place at approx. 90-140 ° C., the desired degree of “polyurethaneisation” being set by controlling the temperature and the residence time.
Überschüssiges Diisocyanat und der Katalysator werden z.B. über einen Schlangenrohrverdampfer kombiniert mit nachgeschaltetem Dünnschichtverdampfer entfernt. Die aus Diisocyanat und Katalysator bestehenden Destillate werden vereinigt und wieder in den Prozeß zurückgeführt. Das Polyisocyanat wird als Rüchstand der Dünnschichtdestillation gewonnen.Excess diisocyanate and the catalyst are e.g. removed via a coiled tube evaporator combined with a downstream thin film evaporator. The distillates consisting of diisocyanate and catalyst are combined and returned to the process. The polyisocyanate is obtained as the residue of thin-film distillation.
Eine Extraktion des erfindungsgemäßen Verfahrensprodukts mit geeigneten Lösungsmitteln wie z.B. n-Hexan ist nicht erforderlich, da eine Abspaltung von Monoisocyanat bei der Durchführung des erfindungsgemäßen Verfahrens, welches durch Extraktion entfernt werden müßte, ausgeschlossen ist.Extraction of the process product according to the invention with suitable solvents such as e.g. n-Hexane is not necessary since the elimination of monoisocyanate when carrying out the process according to the invention, which would have to be removed by extraction, is impossible.
Bei der Durchführung des erfindungsgemäßen Verfahrens können die Eigenschaften der erhaltenen modifizierten Polyisocyanate, insbesondere deren NCO-Funktionalität, NCO-Gehalt, sowie die Viskosität nicht nur durch Wahl der geeigneten Ausgangsmaterialien sondern besonders einfach durch Einstellung des "Polyuretisierungsgrades", d.h. der Zahl der pro Aminogruppe umgesetzten NCO-Gruppen gesteuert werden.When carrying out the process according to the invention, the properties of the modified polyisocyanates obtained, in particular their NCO functionality, NCO content, and the viscosity can be adjusted not only by selecting the suitable starting materials but also particularly simply by adjusting the "degree of polyuretization", i.e. the number of NCO groups converted per amino group can be controlled.
Bei Verwendung von sekundären Monoaminen mit aliphatisch bzw. cycloaliphatisch gebundenen Aminogruppen und aliphatischen bzw. cycloaliphatischen Diisocyanaten entstehen die erfindungsgemäßen Verfahrensprodukte der eingangs angegebenen Formel. Bei der besonders bevorzugten Verwendung von Dialkylaminen mit Cl-C47A1kylresten bzw. von Piperidin, sowie von Hexamethylendiisocyanat als Ausgangsmaterialien bei der Durchführung des erfindungsgemäßen Verfahrens entstehen die besonders bevorzugten erfindungsgemäßen Verfahrensprodukte der genannten allge-. meinen Formel, in welcher die Reste R1 und R2 die bereits genannte Bedeutung haben, R3 und R4 für Hexamethylenreste stehen und n für eine Zahl von 2 bis 8 steht.When secondary monoamines with aliphatically or cycloaliphatically bound amino groups and aliphatic or cycloaliphatic diisocyanates are used, the process products of the formula given at the outset are obtained. In the particularly preferred use of dialkyl amines with C l- C 47 A1kylresten or piperidine, and hexamethylene diisocyanate as starting materials in carrying out the process according to the invention are formed, the most preferred products of the process according to the invention of the above general. my formula in which the radicals R 1 and R 2 have the meaning already mentioned, R 3 and R 4 are hexamethylene radicals and n is a number from 2 to 8.
Die erfindungsgemäßen Verfahrensprodukte können insbesondere als Isocyanatkomponente bei der Herstellung von Polyurethankunststoffen nach dem Isocyanat-Polyadditionsverfahren eingesetzt werden. Sie eignen sich sowohol zur Herstellung von Poly-. urethan-Schaumstoffen, als auch zur Herstellung von Elastomeren, Beschichtungen oder Verklebungen. Insbesondere bei Verwendung der erfindungsgemäßen Verfahrensprodukte für das erstgenannte Einsatzgebeit erübrigt sich oft ein Abdestillieren des überschüssigen Diisocyanats nach Beendigung der erfindungsgemäßen Umsetzung. Die monomerenfreien erfindungsgemäßen Verfahrensprodukte stellen hervorragende Rohstoffe zur Herstellung hochwertiger, wetterfester und lichtechter Lackierungen dar.The process products according to the invention can be used in particular as an isocyanate component in the production of polyurethane plastics by the isocyanate polyaddition process. They are both suitable for the production of poly. urethane foams, as well as for the production of elastomers, coatings or bonds. In particular when using the process products according to the invention for the first-mentioned area of application, it is often unnecessary to distill off the excess diisocyanate after the reaction according to the invention has ended. The monomer-free process products according to the invention are excellent raw materials for producing high-quality, weatherproof and lightfast coatings.
Bezüglich der Verwendung der erfindungsgemäßen Verfahrensprodukte als "Lackiso- cyanate" ist insbesondere ihre ausgezeichnete Verträglichkeit mit handelsüblichen Polyhydroxy-Polyacrylaten hervorzuheben. Ein weiterer Vorteil der erfindungsgemäßen Verfahrensprodukte gegenüber bekannten Biuretpolyisocyanaten ist darin zu sehen, daß sie gegen Monomerenrückspaltung stabil sind, d.h. daß auch während der Lagerung bei erhöhter Temperatur (50°C) der Monomerengehalt der erfindungsgemäßen Polyisocyanate nicht ansteigt.Regarding the use of the process products according to the invention as "Lackiso - cyanates" is to be emphasized with commercially available polyhydroxy polyacrylates particular their excellent compatibility. A Another advantage of the process products according to the invention over known biuret polyisocyanates is that they are stable against monomer cleavage, ie that the monomer content of the polyisocyanates according to the invention does not increase even during storage at elevated temperature (50 ° C.).
In einem 4 I-Vierhalskolben mit Rührer, Rückflußkühler und Kontaktthermometer wurden in 3024 g (18 Mol) 1,6-Diisocyanatohexan unter Stickstoffüberlagerung 135 g (3 Mol) Dimethylamin eingeleitet, wobei die Temperatur im Reaktionsgefäß auf ca. 60°C anstieg. Es bildete sich der entsprechende Harnstoff, der bis auf geringe Restmengen nach Beendigung der Aminzugabe gelöst war. Nun wurden 7 g (0,19 Mol) Chlorwasserstoff in 100 g 1,6-Diisocyanatohexan dem Reaktionsgemisch zugefügt und die Temperatur auf 100°C erhöht. Der NCO-Gehalt der nun klaren Reaktionslösung betrug 44% (entsprechend einem Verbrauch von 1 NCO-Gruppe pro Aminogruppe). Nach 2 Stunden war der NCO-Gehalt auf 40% (entsprechend einem Verbrauch von 2 NCO-Gruppen pro Aminogruppe) und nach 4 Stunden auf 35% (entsprechend einem Verbrauch von 3,3 NCO-Gruppen pro Aminogruppe, entsprechend n = 2,3) gesunken. Die Reaktionslösung wurde auf 50°C abgekühlt und zur Bindung des hydrolysierbaren Chlors mitd 11 g (0,19 Mol) Propylenoxid versetzt. Die nachfolgende Dünnschichtdestillation ergab 1600 g 1,6-Diisocyanatohexan als Destillat und 1540 g Polyuretpolyisocyanat als Rückstand (NCO-Gehalt = 19,5%; Viskosität bei 25°C = 5000 mPa.s; Restgehalt an monomerem 1,6-Diisocyanatohexan = 0,60%).135 g (3 mol) of dimethylamine were introduced into 3024 g (18 mol) of 1,6-diisocyanatohexane under nitrogen blanket in a 4 l four-necked flask equipped with a stirrer, reflux condenser and contact thermometer, the temperature in the reaction vessel rising to approx. 60 ° C. The corresponding urea was formed, which, apart from small residual amounts, was dissolved after the amine addition had ended. 7 g (0.19 mol) of hydrogen chloride in 100 g of 1,6-diisocyanatohexane were then added to the reaction mixture and the temperature was raised to 100.degree. The NCO content of the now clear reaction solution was 44% (corresponding to a consumption of 1 NCO group per amino group). After 2 hours the NCO content was 40% (corresponding to a consumption of 2 NCO groups per amino group) and after 4 hours to 35% (corresponding to a consumption of 3.3 NCO groups per amino group, corresponding to n = 2.3 ) decreased. The reaction solution was cooled to 50 ° C. and 11 g (0.19 mol) of propylene oxide were added to bind the hydrolyzable chlorine. The subsequent thin-film distillation gave 1600 g of 1,6-diisocyanatohexane as the distillate and 1540 g of polyurethane polyisocyanate as the residue (NCO content = 19.5%; viscosity at 25 ° C = 5000 mPa.s; residual content of monomeric 1,6-diisocyanatohexane = 0 , 60%).
Anhand der Kontrolle des Monomerengehalts von Produktproben, die über längere Zeit bei 50°C gelagert wurden, zeigte sich, daß das Polyisocyanat gegen Monomerenrückspaltung stabil ist.
Analog Beispiel 1 wurden 3024 g (18 Mol) 1,6-Diisocyanatohexan unter Zusatz von 7 g (0,19 Mol) Chlorwasserstoff mit 225 g (5 Mol) Dimethylamin umgesetzt. Nach 7 Stunden betrug der NCO-Gehalt des Reaktionsgemisches 27,4% (entsprechend einem Verbrauch von 3 NCO-Gruppen pro Aminogruppe (n = 2)). Nach der Dünnschichtverdampfung erhielt man neben 1000 g 1,6-Diisocyanatohexan 2150 g Polyisocyanat (NCO-Gehalt = 16,2%; Viskosität bei 25°C = 30 000 mPa.s; Restmonomerengehalt = 0,3%).Analogously to Example 1, 3024 g (18 mol) of 1,6-diisocyanatohexane were reacted with 225 g (5 mol) of dimethylamine with the addition of 7 g (0.19 mol) of hydrogen chloride. After 7 hours, the NCO content of the reaction mixture was 27.4% (corresponding to a consumption of 3 NCO groups per amino group (n = 2)). After the thin-layer evaporation, 2150 g of polyisocyanate were obtained in addition to 1000 g of 1,6-diisocyanatohexane (NCO content = 16.2%; viscosity at 25 ° C. = 30,000 mPa.s; residual monomer content = 0.3%).
Analog Beispiel 1 wurden 1008 g (6 Mol) 1,6-Diisocyanatohexan unter Zusatz von 3 g (0,08 Mol) Chlorwasserstoff mit 45 g (1 Mol) Dimethylamin umgesetzt. Nach 6 Stunden war der NCO-Gehalt des Reaktionsgemisches auf 28% gesunken (entsprechend einem Umsetzungsgrad von 5 NCO-Gruppen pro Aminogruppe (n = 4)). Die Viskosität des Rohisocyanats betrug 200 mPa.s/25°C.
154 g einer 65%-igen Lösung eines stark verzweigten Polyesters auf Basis Phthalsäureanhydrid und Trimethylolpropan (Hydroxylgehalt 8%) in Äthylglycolacetat/Xylol (1:1) wurden nach Zugabe von 1 g eines tertiären Amins als Katalysator und 0,4 g Cellulosebutyrat-propionat als Verlaufmittel mit 220 g eines Lösungsmittelgemisches aus Methyläthylketon, Butylacetat, Äthylglycolacetat und Toluol (4:1:4:1) verdünnt. Hierzu wurden 135 g einer 75 %igen Lösung des Polyisocyanats aus Beispiel 1 in Äthylglycolacetat/Xylol (1:1) gegeben (NCO/OH-Molverhältnis = 1:1). Die fertige Lacklösung wurde dann auf Stahlbleche aufgetragen, wo die Lackfilme bei Raumtemperatur aushärteten. Die durchgehärteten Klarlackfilme waren kratzfest, elastisch und gegen Lösungsmittel wie Toluol, Äthylglycolacetat, Äthylacetat oder Aceton beständig. Sie hatten ferner folgende Eigenschaften:
Es wurden 154 g der im Beispiel 5 beschriebenen Polyesterlösung mit 100 g Titandioxid (Rutiltyp) zu einer Paste verarbeitet. Dieser Paste wurden neben Katalysator und Verlaufmittel 120 g des schon beschriebenen Lösungsmittelgemisches zugefügt. Die so erhaltene Mischung wurde mit 135 g einer 75 %igen Lösung des Polyisocyanats aus Beispiel 1 in Athylglycolacetat/Xylol (1:1) versetzt und in dünner Schicht auf Stahlbleche aufgetragen. Die pigmenthaltigen Lackfilme härteten bei Raumtemperatur durch. Sie zeichneten sich durch Kratzfestigkeit und Lösungsmittelresistenz aus und hatten verglichen mit den Klarlackfilmen folgende Eigenschaften:
Claims (4)
are reacted with diisocyanates of the kind mentioned under b), at 0140°C in the presence of strong acids which form a mixed carbamic acid anhydride with isocyanates; the quantity of diisocyanates used is chosen so that there is altogether an NCO/NH molar ratio of 5.5 : 1 to 100 : 1, related to the diisocyanates and and monoamines.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE2730513 | 1977-07-06 | ||
| DE19772730513 DE2730513A1 (en) | 1977-07-06 | 1977-07-06 | PROCESS FOR THE PREPARATION OF MODIFIED POLYISOCYANATES |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0000348A1 EP0000348A1 (en) | 1979-01-24 |
| EP0000348B1 true EP0000348B1 (en) | 1980-07-23 |
Family
ID=6013279
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP78100256A Expired EP0000348B1 (en) | 1977-07-06 | 1978-06-28 | Polyuret polyisocyanates, preparation thereof and their use in the preparation of polyurethanes. |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US4220749A (en) |
| EP (1) | EP0000348B1 (en) |
| JP (1) | JPS5414922A (en) |
| DE (2) | DE2730513A1 (en) |
| ES (1) | ES471506A1 (en) |
| IT (1) | IT7850153A0 (en) |
| NZ (1) | NZ187758A (en) |
Families Citing this family (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2856864A1 (en) * | 1978-12-30 | 1980-07-24 | Bayer Ag | NEW POLYISOCYANATES, A METHOD FOR THE PRODUCTION AND THEIR USE |
| DE2856826A1 (en) * | 1978-12-30 | 1980-07-17 | Bayer Ag | PROCESS FOR PRODUCING BIURET AND / OR HIGHER POLYURET GROUPS, THE COMPOUNDS OBTAINABLE BY THIS PROCESS AND THEIR USE AS COMPONENTS IN THE PRODUCTION OF POLYURETHANE |
| DE4405042A1 (en) * | 1994-02-17 | 1995-08-24 | Herberts Gmbh | Process for the preparation of blocked isocyanates, the blocked isocyanates obtained and their use |
| US5489704A (en) | 1994-08-29 | 1996-02-06 | Bayer Corporation | Polyisocyanate/polyamine mixtures and their use for the production of polyurea coatings |
| US5523376A (en) | 1994-12-21 | 1996-06-04 | Bayer Corporation | Coating compositions based on aldimines and polyisocyanates containing uretdione groups |
| US5561200A (en) | 1995-05-23 | 1996-10-01 | Bayer Corporation | Blocked polyisocyanates with improved thermal stability |
| DE10025301A1 (en) * | 2000-05-22 | 2001-11-29 | Bayer Ag | Process for the preparation of polyisocyanates with a biuret structure |
| US6852905B2 (en) | 2001-11-15 | 2005-02-08 | Paragon Trade Brands, Inc. | Fluid handling layers made from foam and absorbent articles containing same |
| US20050137374A1 (en) * | 2003-12-17 | 2005-06-23 | Roesler Richard R. | Two-component water-borne adhesive |
| US20050137322A1 (en) * | 2003-12-17 | 2005-06-23 | Roesler Richard R. | Silane modified two-component polyurethane coating |
| US20050158131A1 (en) * | 2004-01-20 | 2005-07-21 | Markusch Peter H. | Geotextile/polyurethane composites based on blocked isocyanate compositions |
| US20050277732A1 (en) * | 2004-06-14 | 2005-12-15 | Yu Poli C | Two-component coating composition |
| US20050288431A1 (en) * | 2004-06-25 | 2005-12-29 | Gindin Lyubov K | Polyurethane dispersion prepared from a high acid functional polyester |
| US20050288430A1 (en) * | 2004-06-25 | 2005-12-29 | Gindin Lyubov K | Polyurethane dispersions with high acid content |
| US20060011295A1 (en) * | 2004-07-14 | 2006-01-19 | Karsten Danielmeier | Aspartic ester functional compounds |
| US20060014890A1 (en) * | 2004-07-14 | 2006-01-19 | Zielinski David P | Polyisocyanates with improved compatibility with high hydroxyl content polyols |
| US20060089480A1 (en) * | 2004-10-21 | 2006-04-27 | Roesler Richard R | Biuretized isocyanates and blocked biuretized isocyanates |
| US20060089481A1 (en) * | 2004-10-21 | 2006-04-27 | Roesler Richard R | Blocked biuretized isocyanates |
| US7371807B2 (en) * | 2004-10-21 | 2008-05-13 | Bayer Materialscience Llc | Blocked biuretized isocyanates |
| US20090131581A1 (en) * | 2007-11-19 | 2009-05-21 | Wylie Amy S | Aqueous, stain-resistant coating compositions |
| US20090176907A1 (en) | 2008-01-08 | 2009-07-09 | Ramesh Subramanian | Direct-to-metal radiation curable compositions |
| CN102281998B (en) | 2009-01-14 | 2015-03-11 | 拜尔材料科学有限公司 | Long-fiber thermoset composite with low orange peel |
| US20110045219A1 (en) * | 2009-08-18 | 2011-02-24 | Bayer Materialscience Llc | Coating compositions for glass substrates |
| KR20120093158A (en) | 2009-09-26 | 2012-08-22 | 세게티스, 인코포레이티드. | Ketal lactones and stereospecific adducts of oxocarboxylic ketals with trimethylol compounds, polymers containing the same, methods of manufacture, and uses thereof |
| TWI418373B (en) * | 2009-12-01 | 2013-12-11 | Far Eastern New Century Corp | Platelet adhesion-resistant material |
| US9080074B2 (en) | 2010-03-19 | 2015-07-14 | Bayer Materialscience Llc | Low temperature curing polyuretdione compositions |
| US8343601B1 (en) | 2011-07-06 | 2013-01-01 | Bayer Materialscience Llc | Waterborne polyurethane coating compositions |
| US20140356561A1 (en) | 2011-07-06 | 2014-12-04 | Bayer Materialscience Ag | Free radical curable waterborne glass coating compositions |
| US8354151B1 (en) | 2011-07-06 | 2013-01-15 | Bayer Materialscience Llc | Waterborne polyurethane coating compositions |
| US20140199491A1 (en) | 2013-01-15 | 2014-07-17 | Allnex Ip S.À.R.L. | One-component, dual-cure conformal coating compositions |
| CN113698572B (en) * | 2021-09-15 | 2023-12-19 | 万华化学(宁波)有限公司 | Polyisocyanate composition, preparation method and application |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1227003B (en) * | 1962-11-29 | 1966-10-20 | Bayer Ag | Process for the preparation of polyisocyanates with a carbamylbiuret structure |
| DE1174759B (en) * | 1963-02-08 | 1964-07-30 | Bayer Ag | Process for the production of polyisocyanates with a biuret structure |
| DE1227004B (en) * | 1963-04-13 | 1966-10-20 | Bayer Ag | Process for the production of more than divalent isocyanates with a biuret structure or carbamyl biuret structure |
| DE1720711A1 (en) * | 1967-09-18 | 1971-07-08 | Bayer Ag | Process for the production of polyurethane plastics |
| GB1254574A (en) * | 1968-03-15 | 1971-11-24 | Bayer Ag | Process for the preparation of isocyanate group-containing compounds |
| US3862973A (en) * | 1970-03-07 | 1975-01-28 | Bayer Ag | Process for the preparation of polyisocyanates containing biuret groups |
| DE2308015B2 (en) * | 1973-02-17 | 1980-07-31 | Bayer Ag, 5090 Leverkusen | Process for the production of polyisocyanates with a biuret structure |
-
1977
- 1977-07-06 DE DE19772730513 patent/DE2730513A1/en not_active Withdrawn
-
1978
- 1978-06-21 US US05/917,765 patent/US4220749A/en not_active Expired - Lifetime
- 1978-06-28 DE DE7878100256T patent/DE2860054D1/en not_active Expired
- 1978-06-28 EP EP78100256A patent/EP0000348B1/en not_active Expired
- 1978-07-03 NZ NZ187758A patent/NZ187758A/en unknown
- 1978-07-04 IT IT7850153A patent/IT7850153A0/en unknown
- 1978-07-04 JP JP8060378A patent/JPS5414922A/en active Pending
- 1978-07-06 ES ES471506A patent/ES471506A1/en not_active Expired
Also Published As
| Publication number | Publication date |
|---|---|
| NZ187758A (en) | 1979-11-01 |
| US4220749A (en) | 1980-09-02 |
| DE2860054D1 (en) | 1980-11-13 |
| ES471506A1 (en) | 1979-01-16 |
| DE2730513A1 (en) | 1979-01-25 |
| JPS5414922A (en) | 1979-02-03 |
| IT7850153A0 (en) | 1978-07-04 |
| EP0000348A1 (en) | 1979-01-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0000348B1 (en) | Polyuret polyisocyanates, preparation thereof and their use in the preparation of polyurethanes. | |
| EP0339396B1 (en) | Process for producing polyisocyanates containing isocyanurate groups | |
| EP0456062B1 (en) | Process for preparation of isocyanuratepolyisocyanates, the compounds prepared according to this process, and their use | |
| EP0330966B1 (en) | Process for the preparation of polyisocyanates containing isocyanurate groups | |
| EP0682012B1 (en) | Process for the preparation of light stable polyisocyanates containing allophanate groups | |
| EP0478990B1 (en) | Polyisocyanate mixture, process for its preparation and its use in polyurethane lacquers | |
| EP0000194B1 (en) | Preparation of isocyanate-substituted allophanates and their use for the preparation of lacquers | |
| EP0178520B1 (en) | Process for the preparation of urethdione groups containing compounds, the compounds obtained with this process and their use in the preparation of polyurethanes | |
| EP0585835B1 (en) | Process for the preparation of low-viscosity polyisocyanate compositions having isocyanurate and urethane groups | |
| DE2308015B2 (en) | Process for the production of polyisocyanates with a biuret structure | |
| EP0056158A1 (en) | Process for the production of isocyanurate groups containing polyisocyanates, solutions useful as catalyst ingredients in this process and the use of the process products as isocyanate components in the production of polyurethanes | |
| EP0481318B1 (en) | Process for the preparation of polyisocyanates containing urethdione and isocyanate groups | |
| DE19523657A1 (en) | Process for the preparation of solutions of polyisocyanates containing isocyanurate groups with a reduced residual monomer content and their use | |
| EP0649866A1 (en) | Lacquer polyisocyanates and their use | |
| DE2725318A1 (en) | PROCESS FOR THE PRODUCTION OF ALLOPHANATE GROUPS POLYISOCYANATES | |
| EP0012973B1 (en) | Process for the preparation of bi- and/or polyuret-polyisocyanates; products obtained by this process and their use in the preparation of polyurethanes | |
| EP0150769A2 (en) | Process for the production of polyisocyanates with a biuret structure | |
| EP0744423A1 (en) | Blocked polyisocyanates as well as a process for their preparation | |
| EP0193828B1 (en) | Polyisocyanates containing isocyanurate groups, process for their production and their use as isocyanate components in the production of polyurethane lacquers | |
| EP0778303A1 (en) | Polyisocyanates containing allophanate groups based on diphenylmethanediisocyanate and having predominantly or completely blocked isocyanate groups | |
| EP0012970B1 (en) | Polyisocyanates, process for their preparation and their use | |
| DE3133865C2 (en) | Process for the preparation of an organic polyisocyanate composition and the use thereof | |
| EP0183150B1 (en) | Process for the preparation of modified polyisocyanates and theiruse in the preparation of polyurethane coatings | |
| DE19735043A1 (en) | Process for the production of light-colored uretdione polyisocyanates | |
| EP0325941A2 (en) | Process for the preparation of modified polyisocyanates, polyisocyanates so obtained and their use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Designated state(s): BE DE FR GB NL SE |
|
| 17P | Request for examination filed | ||
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Designated state(s): BE DE FR GB NL SE |
|
| REF | Corresponds to: |
Ref document number: 2860054 Country of ref document: DE Date of ref document: 19801113 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19810526 Year of fee payment: 4 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: NL Payment date: 19810630 Year of fee payment: 4 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: SE Payment date: 19810731 Year of fee payment: 4 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: BE Payment date: 19810930 Year of fee payment: 4 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: BE Effective date: 19820628 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Effective date: 19820629 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19830101 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee | ||
| GBPC | Gb: european patent ceased through non-payment of renewal fee | ||
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19830331 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19840526 Year of fee payment: 7 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19880301 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Effective date: 19881117 |
|
| EUG | Se: european patent has lapsed |
Ref document number: 78100256.3 Effective date: 19850612 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |