CN113614109A - 双功能抗pd-1/il-7分子 - Google Patents
双功能抗pd-1/il-7分子 Download PDFInfo
- Publication number
- CN113614109A CN113614109A CN201980092752.6A CN201980092752A CN113614109A CN 113614109 A CN113614109 A CN 113614109A CN 201980092752 A CN201980092752 A CN 201980092752A CN 113614109 A CN113614109 A CN 113614109A
- Authority
- CN
- China
- Prior art keywords
- seq
- antibody
- amino acid
- inhibitors
- bifunctional molecule
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2046—IL-7
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/30—Cellular immunotherapy characterised by the recombinant expression of specific molecules in the cells of the immune system
- A61K40/36—Immune checkpoint inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
- C07K14/5418—IL-7
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/74—Inducing cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/75—Agonist effect on antigen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmacology & Pharmacy (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Epidemiology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Toxicology (AREA)
- Microbiology (AREA)
- Endocrinology (AREA)
- Mycology (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本发明涉及包含抗PD‑1抗体和IL‑7的双功能分子及其用途。
Description
发明领域
本发明涉及免疫治疗领域。本发明提供了一种包含抗PD-1抗体或其抗体结合片段的双功能分子。
发明背景
靶向T细胞抑制检查点以使用治疗性抗体解除抑制的方法是一个深入研究的领域(有关评述,请参见Pardoll,Nat Rev Cancer,2012;12:253-264)。靶向适应性免疫的免疫检查点已显示出对抗多种癌症的巨大治疗功效,但其仅在有限比例的患者中显示。将免疫检查点疗法与其他免疫治疗策略相结合已在临床前模型中表现出很高的效率,但在临床上仍然是一个挑战。
免疫细胞激活由平衡共刺激和共抑制信号的整合控制。T细胞受体(TCR)介导的T细胞激活由共刺激和共抑制信号两者调节。抗原非依赖性第二信号修饰第一信号,其由抗原肽-MHC复合物与TCR的相互作用提供,从而赋予对应答的特异性。T细胞共刺激和共抑制途径具有广泛的免疫调节功能,控制效应子、记忆和调节T细胞以及初始T细胞。那些途径的治疗调节正在转化为用于治疗癌症的有效新策略(关于综述,请参见Schildberg等,44(5),Immunity,2016)。正在进行的关于免疫应答调节的研究已经确定了多种免疫途径,可以靶向所述途径以开发癌症疗法。那些分子在本文中称为免疫检查点共激活剂或共抑制剂(参见综述Sharma等,Cell,161(2),2015和Pardoll,Nature ReviewsCancer,12(4),2012)。
程序性细胞死亡蛋白1(PD-1,也称为CD279)是一种细胞表面蛋白分子,其属于免疫球蛋白超家族。PD-1在T和B淋巴细胞和巨噬细胞上表达,并在细胞命运和分化中发挥作用。已鉴定出PD-1的两种配体,即PD-L1和PD-L2,其已被证明在结合至PD-1后可下调T细胞激活(Freeman等,(2000)J Exp Med 192:1027-34;Latchman等,(2001)Nat Immunol 2:261-8;Carter等,(2002)Eur J Immunol 32:634-43)。PD-1与其配体之间的相互作用导致肿瘤浸润淋巴细胞减少、T细胞受体介导的增殖减少和癌细胞的免疫逃避。特别是,PD1连接减少T细胞上TCR刺激下游的信号,抑制T细胞应答并导致激活和细胞因子产生减少。
PD-1/PD-L1疗法已被FDA批准作为大范围广泛的血液学和实体癌的一线和二线疗法用于治疗,但基于如RECIST标准定义的肿瘤大小减少30%以上的客观响应在癌症亚型之间的差异很大。
在难治性霍奇金氏淋巴瘤(65-85%)(Borcherding N等,J Mol Biol.,2018年7月6日;430(14):2014-2029)中或具有高微卫星不稳定性结肠癌(MSI-H)(25%-80%)或梅克尔细胞癌(56%)的肿瘤中观察到高响应率。
在黑色素瘤(24%至44%)和非小细胞肺癌患者(12.8%至43.7%)中观察到中等客观响应率,其中抗PD-1疗法被用作一线治疗。尽管只有一部分患者受益于该疗法,PD-1/PD-L1疗法相比于旧标准护理化疗改善了总体生存。
在一些实体瘤中,观察到低或零临床响应,特别是在胰腺癌、非MSI结直肠癌、胃癌和一些乳腺癌中(Borcherding N等,J Mol Biol.,2018年7月6日;430(14):2014-2029)。
已经描述了多种机制,且可以解释这种不同的功效和对PD-1/PD-L1检查点疗法的抗性,特别是其中一些涉及T细胞生物学,例如(1)记忆T细胞的形成受损;(2)T细胞浸润受损;(3)肿瘤特异性T细胞生成不足;(4)T细胞功能不足;和(5)调节性T细胞诱导的免疫抑制微环境。通过靶向IL-7信号传导而进行的联合治疗可能是通过刺激T细胞浸润、维持T细胞效应能力和促进持久的记忆T细胞应答来解决抗PD-1抗性患者而不刺激调节性T细胞扩增和生存的良好策略。
Interleukin-7是IL-2超家族的免疫刺激细胞因子成员,其在适应性免疫系统中发挥重要作用,且促进B细胞和T细胞介导的免疫应答。这种细胞因子通过T细胞和B细胞的存活和分化,淋巴细胞的存活,自然杀伤(NK)细胞活性的刺激来激活免疫功能。IL-7还通过淋巴组织诱导(LTi)细胞来调节淋巴结的发育,并促进初始T细胞或记忆T细胞的存活和分裂。此外,IL-7通过促进IL-2和干扰素-γ的分泌来增强人的免疫反应。IL-7的受体是异源二聚体,且由IL-7Rα(CD127)和共有的γ链(CD132)组成。γ链在所有造血细胞类型上表达,而IL-7Rα主要由淋巴细胞表达(包括B和T淋巴前体、初始T细胞和记忆T细胞)。相比于表达更高水平的效应/初始T细胞,在调节性T细胞上观察到IL-7Rα的低表达,因此,将CD127用作表面标志物以区分这两个群体。IL-7Rα也在先天性淋巴细胞NK和肠道相关淋巴组织(GALT)衍生的T细胞上表达。IL-7Rα(CD127)链与TSLP(肿瘤基质淋巴细胞生成素)共享,CD132与IL-2、IL-4、IL-9、IL-15和白介素21共享。通过CD127/CD132的(1)Janus激酶/STAT通路(即Jak-Stat-3和5)和(2)磷酸肌醇-3激酶通路(即PI3K-Akt)来诱导两条主要信号传导通路。IL-7施用在患者中具有良好的耐受性,并导致CD8和CD4细胞扩增以及CD4+ T调节性细胞的相对减少。已在临床上测试了重组裸IL-7或与抗体Fc的N端结构域融合的IL-7,其基本原理是通过Fc结构域的融合来增加IL-7的半衰期并提高治疗的长期持续效率。靶向IL-7信号传导相比于IL-2信号传导应该更有希望,因为IL-2作用于Treg和T效应细胞两者,而IL-7选择性地激活T效应细胞。
为了提高抗PD1免疫疗法的功效并克服患者中潜在的抗PD-1抗性,开发靶向IL-7信号传导的联合治疗可能是刺激T细胞浸润、维持T细胞效应能力和促进持久的记忆T细胞应答,而不刺激调节性T细胞的扩增和存活的良好策略。确实,抗PD-1治疗增加了耗竭T细胞上CD127的表达,从而增加了其对IL-7应答的能力,并改善了干扰素-γ(IFN-γ)和肿瘤坏死因子-α(TNF-α)的共产生(Pauken等,Science,2016年12月2日;354(6316):1160-1165,Shi等,Nat Commun.,2016年8月8日;7:12335)。
然而,联合免疫疗法的验证和开发受到生物疗法成本和此类免疫疗法的有限获取的强烈限制。因此,本领域仍然非常需要用于安全免疫疗法的新的改善药剂,特别是针对癌症,靶向T细胞,并且对适应性免疫应答(特别是T细胞免疫应答)具有有效的积极影响的安全免疫疗法。本发明人已经用本文公开的发明向前迈出了重要的一步。
发明内容
本发明人提供了包含抗hPD-1抗体和人IL-7的双功能分子,其有望用于多种治疗应用,特别是用于治疗癌症。本发明基于特异性靶向人PD-1的抗体的开发,该抗体显示出对PD-1的高结合亲和性并与其配体PDL-1和/或PD-L2的强烈竞争。出人意料地,IL-7的N-端末端与抗hPD-1抗体Fc区的C-端末端的融合允许保留其对CD127(IL7受体)的高亲和力至与内源性IL-7相似的程度,这表明有效的IL-7R激活。Fc结构域与IL-7的融合也增加了产品的半衰期。此外,本文公开的双功能抗PD1/IL-7分子允许IL-7在PD-1+ T细胞浸润中的积累和IL-7在PD-1+ T细胞上的重定位。特别是,抗PD-1/IL-7双功能分子诱导由细胞因子(例如IFNγ)分泌和整联蛋白(例如α4和β7和LFA-1)表达反映的初始、部分耗竭和完全耗竭T细胞亚群的增殖和激活)。这种抗hPD-1/IL-7双功能分子具有克服相关抗性机制并提高抗PD-1免疫疗法的功效。
在第一个方面,本发明涉及一种双功能分子,其包含:
(a)抗人PD-1抗体或其抗原结合片段,其包含:
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域(VH),和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域(VL),和
(b)人白介素7(IL-7)或其片段或变体,
其中所述抗体或其片段,优选地通过肽接头,与所述人IL-7或其片段或变体共价连接作为融合蛋白。
特别地,所述人IL-7或其片段的N-端末端与所述抗人PD-1抗体或其抗原结合片段的的重链或轻链或两者的C-端末端连接。
在一个方面,所述抗体或其抗原结合片段是嵌合、人源化或人抗体。
在一个特定方面,本发明涉及一种双功能分子,其包含抗人PD-1抗体或其抗原结合片段,所述抗人抗体或其抗原结合片段包含以下或由以下组成:
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域(VH),和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域(VL),
其中:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成;
-所述重链CDR3(HCDR3)包含SEQ ID NO:3的氨基酸序列或由SEQ ID NO:3的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;
-所述轻链CDR1(LCDR1)包含SEQ ID NO:12的氨基酸序列或由SEQ ID NO:12的氨基酸序列组成,其中X是G或T;
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成。
特别地,所述抗人PD-1抗体或其抗原结合片段包含以下或由以下组成:(a)包含SEQ ID NO:17的氨基酸序列的VH或由SEQ ID NO:17的氨基酸序列组成的VH,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;(b)包含SEQ ID NO:26的氨基酸序列的VL或由SEQ ID NO:26的氨基酸序列组成的VL,其中X是G或T。
更特别地,本发明涉及一种双功能分子,其包含抗人PD-1抗体或其抗原结合片段,所述抗人PD-1抗体或其抗原结合片段包含以下或由以下组成:(i)包含SEQ ID NO:24的氨基酸序列的重链可变区(VH)或由SEQ ID NO:24的氨基酸序列组成的重链可变区(VH),和(ii)包含SEQ ID NO:28的氨基酸序列的轻链可变区(VL)或由SEQ ID NO:28的氨基酸序列组成的轻链可变区(VL)。
替代地,所述抗PD1抗体选自派姆单抗,纳武单抗,匹地利珠单抗,西米普利单抗,PDR001以及单克隆抗体5C4、17D8、2D3、4H1、4A11、7D3和5F4。
特别地,所述IL-7或其变体包含与野生型人IL-7(wth-IL-7)具有至少75%同一性的氨基酸序列或由与野生型人IL-7(wth-IL-7)具有至少75%同一性的氨基酸序列组成。在一个特定方面,所述IL-7包含SEQ ID NO:51中所示的氨基酸序列或由SEQ ID NO:51中所示的氨基酸序列组成。
替代地,所述IL-7是IL-7变体,其中所述IL-7变体呈现出与包含SEQ ID NO:51中所示的氨基酸序列或由SEQ ID NO:51中所示的氨基酸序列组成的野生型人IL-7(wth-IL-7)至少75%同一性,其中所述变体包含至少一个氨基酸突变,所述氨基酸突变i)相比于与wth-IL-7对IL-7R的亲和力减少了所述IL-7变体对IL-7受体的亲和力,并且ii)相比于包含IL-7的双功能分子改善了包含所述IL-7变体的所述双功能分子的药代动力学。
特别地,所述至少一个突变是选自以下的氨基酸置换或氨基酸置换组:(i)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S,(ii)W142H、W142F或W142Y,(iii)D74E、D74Q或D74N,(iv)Q11E、Y12F、M17L、Q22E和/或K81R;或其任何组合。
在一个方面,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、以及C47S-C92S和C34S-C129S。
在另一个方面,所述IL-7变体包含选自以下的氨基酸置换:W142H、W142F和W142Y。
在另一个方面,所述IL-7变体包含选自以下的氨基酸置换:D74E、D74Q和D74N。
优选地,所述IL-7变体包含SEQ ID NO:53-66中所示的氨基酸序列或由SEQ IDNO:53-66中所示的氨基酸序列组成。甚至更优选地,所述IL-7变体包含SEQ ID NO:54、56或63中所示的氨基酸序列或由SEQ ID NO:54、56或63中所示的氨基酸序列组成。
在一个特定方面,所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgGl、IgG2、IgG3或IgG4重链恒定结构域(优选地IgGl或IgG4重链恒定结构域)的重链恒定结构域。
在一个更特定的方面,所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgGl重链恒定结构域的重链恒定结构域,其任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A。
在另一个更特定的方面,所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgG4重链恒定结构域的重链恒定结构域,其任选地具有选自以下的置换或置换的组合:S228P;L234A/L235A,S228P+M252Y/S254T/T256E.17和K444A。
任选地,所述抗体或其片段通过接头序列与IL-7或其变体连接,所述接头序列优选地选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地选自(GGGGS)3或(GGGS)3。
在一个非常特定的方面,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、C47S-C92S和C34S-C129S、W142H、W142F、W142Y、D74E、D74Q和D74N;所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgGl重链恒定结构域的重链恒定结构域,其任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A;并且所述抗体或其片段通过接头(GGGGS)3与IL-7变体连接。
在另一个方面,本发明涉及一种分离的核酸分子或分离的核酸分子组,其编码本文公开的双功能分子;一种载体,其包含本文公开的核酸或核酸分子组;和/或一种宿主细胞,其包含本文公开的载体、核酸或核酸分子组。
在另一个方面,本发明涉及一种用于产生所述双功能分子的方法,其包括培养本文公开的宿主细胞的步骤和任选地分离所述双功能分子的步骤。
在另一个方面,本发明涉及一种药物组合物,其包含本文公开的双功能分子、核酸或核酸分子组、载体或宿主细胞和药学上可接受的载体。
任选地,所述药物组合物还包含另外的治疗剂,所述另外的治疗剂优选地选自以下:烷化剂、血管生成抑制剂、抗体、抗代谢物、抗有丝分裂剂、抗增殖剂、抗病毒剂、极光激酶抑制剂、凋亡促进剂(例如,Bcl-2家族抑制剂)、死亡受体通路激活剂、Bcr-Abl激酶抑制剂、BiTE(双特异性T细胞接合剂)抗体、抗体药物缀合物、生物应答调节剂、布鲁顿氏酪氨酸激酶(BTK)抑制剂、细胞周期蛋白依赖性激酶抑制剂、细胞周期抑制剂、环氧合酶-2抑制剂、DVD、白血病病毒癌基因同源物(ErbB2)受体抑制剂、生长因子抑制剂、热休克蛋白(HSP)-90抑制剂、组蛋白去乙酰化酶(HDAC)抑制剂、激素疗法、免疫药、凋亡蛋白抑制剂(IAP)的抑制剂、嵌入型抗生素、激酶抑制剂、驱动蛋白抑制剂、Jak2抑制剂、哺乳动物雷帕霉素靶蛋白抑制剂、microRNA、丝裂原激活的细胞外信号调节激酶抑制剂、多价结合蛋白、非甾体抗炎药(NSAID)、聚ADP(二磷酸腺苷)-核糖聚合酶(PARP)抑制剂、铂类化学治疗剂、polo样激酶(Plk)抑制剂、磷酸肌醇-3激酶(PI3K)抑制剂、蛋白酶体抑制剂、嘌呤类似物、嘧啶类似物、受体酪氨酸激酶抑制剂、类视黄醇/类维生素D植物生物碱(deltoids plant alkaloids)、小抑制性核糖核酸(siRNA)、拓扑异构酶抑制剂、泛素连接酶抑制剂、低甲基化剂、检查点抑制剂、肽疫苗等、来自肿瘤抗原的表位或新表位、以及这些试剂中的一种或多种的组合。
特别地,所述药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞用作药物。
本发明最终涉及本文公开的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞,其用作药物,优选地用于治疗选自以下的癌症的疾病:表达PD-1和/或PD-L1的血液系统恶性肿瘤或实体瘤,如选自以下的癌症:淋巴造血肿瘤、血管免疫母细胞性T细胞淋巴瘤、骨髓增生异常综合征和急性髓性白血病,由病毒诱发或与免疫缺陷相关的癌症,如选自以下的癌症:卡波西氏肉瘤(例如,与卡波西氏肉瘤疱疹病毒相关的);宫颈癌、肛门癌、阴茎癌和外阴鳞状细胞癌和口咽癌(例如,与人乳头瘤病毒相关的);B细胞非霍奇金氏淋巴瘤(NHL),包括弥漫性大B细胞淋巴瘤、伯基特氏淋巴瘤、浆母细胞淋巴瘤、原发性中枢神经系统淋巴瘤、HHV-8原发性渗出性淋巴瘤、经典霍奇金氏淋巴瘤和淋巴增生性病症(例如,与爱泼斯坦-巴尔病毒(EBV)和/或卡波西氏肉瘤疱疹病毒相关的);肝细胞癌(例如,与乙型肝炎和/或丙型肝炎病毒相关的);梅克尔细胞癌(例如,与梅克尔细胞多瘤病毒(MPV)相关的);和与人免疫缺陷病毒感染(HIV)相关的癌症;以及选自以下的癌症:转移性或非转移性、黑色素瘤、恶性间皮瘤、非小细胞肺癌、肾细胞癌、霍奇金氏淋巴瘤、头颈癌、尿道上皮癌、结直肠癌、肝细胞癌、小细胞肺癌、转移性梅克尔细胞癌、胃癌或食道癌和宫颈癌。
任选地,所述双功能分子、所述药物组合物、所述分离的核酸或所述分离的核酸分子组、所述载体、或所述宿主细胞,其用于与放射疗法或另外的治疗剂联合使用,所述另外的治疗剂优选地选自烷化剂、血管生成抑制剂、抗体、抗代谢剂、抗有丝分裂剂、抗增殖剂、抗病毒剂、极光激酶抑制剂、凋亡促进剂(例如,Bcl-2家族抑制剂)、死亡受体通路激活剂、Bcr-Abl激酶抑制剂、BiTE(双特异性T细胞接合剂)抗体、抗体药物缀合物、生物应答调节剂、布鲁顿氏酪氨酸激酶(BTK)抑制剂、细胞周期蛋白依赖性激酶抑制剂、细胞周期抑制剂、环氧合酶-2抑制剂、DVD、白血病病毒癌基因同源物(ErbB2)受体抑制剂、生长因子抑制剂、热休克蛋白(HSP)-90抑制剂、组蛋白去乙酰化酶(HDAC)抑制剂、激素疗法、免疫药、凋亡蛋白抑制剂(IAP)的抑制剂、嵌入型抗生素、激酶抑制剂、驱动蛋白抑制剂、Jak2抑制剂、哺乳动物雷帕霉素靶蛋白抑制剂、microRNA、丝裂原激活的细胞外信号调节激酶抑制剂、多价结合蛋白、非甾体抗炎症药物(NSAID)、聚ADP(二磷酸腺苷)-核糖聚合酶(PARP)抑制剂、铂类化学治疗剂、polo样激酶(Plk)抑制剂、磷酸肌醇-3激酶(PI3K)抑制剂、蛋白酶体抑制剂、嘌呤类似物、嘧啶类似物、受体酪氨酸激酶抑制剂、类视黄醇/类维生素D植物生物碱、小抑制性核糖核酸(siRNA)、拓扑异构酶抑制剂、泛素连接酶抑制剂、低甲基化剂、检查点抑制剂、肽疫苗等、来自肿瘤抗原的表位或新表位、以及这些试剂中的一种或多种的组合。
本文所述的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞用于抑制调节性T细胞的遏制活性,激活T效应细胞和/或刺激初始、部分耗竭和全部耗竭T细胞的增殖。
本文所述的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞还可用于治疗传染病、优选地慢性传染病、甚至更优选地慢性病毒感染。优选地,所述传染疾病由选自以下的病毒引起:HIV、肝炎病毒、疱疹病毒、腺病毒、流感病毒、黄病毒、埃可病毒、鼻病毒、柯萨奇病毒、冠状病毒、呼吸道合胞病毒、腮腺炎病毒、轮状病毒、麻疹病毒、风疹病毒、细小病毒、痘苗病毒、HTLV病毒、登革热病毒、乳头瘤病毒、软疣病毒、脊髓灰质炎病毒、狂犬病病毒、JC病毒和虫媒脑炎病毒。
附图说明
图1:结合PD-1的ELISA测定。固化人重组PD-1(rPD1)蛋白并添加不同浓度的抗体。使用与过氧化物酶偶联的抗人Fc抗体进行揭示。使用TMB底物,在450nm处确定比色法。A.比较抗PD1(■)、抗PD1VL-IL7(o)和抗PD1VH-IL7(●)与重组PD1(rPD1)的结合。B.在重链或/和轻链上与IL7融合的抗PD1抗体的嵌合Bicki(●)相比于人源化Bicki(■)形式的比较:抗PD1VH-IL7(左图)、抗PD1VL-IL7(中图)或抗PD1VH和VL-IL7(右图)。将不同浓度的分子添加到人PD1重组蛋白包被的板上。C.在人PD1重组蛋白包被的板上以不同浓度测试了用Keytruda(●)和Opdivo(■)骨架构建的Bicki抗PD-1/IL-7的PD-1结合。
图2:Bicki抗PD1-IL7分子阻断PD-1/PD-L1和PD1/PDL2相互作用的拮抗能力。A.ELISA测定:将PD-L1固化在Maxisorp板上,添加复合物抗体+生物素化重组人PD-1。用固定浓度的PD1(0.6μg/mL)生成该复合物,并测试不同浓度的抗PD1(■)、抗PD1VH-IL7(●)或抗PD1VL-IL7(o)抗体。B:通过Biacore对在人PD-L2重组蛋白上与抗PD1抗体、抗PD1VH-IL7或抗PD1VL-IL7抗体预孵育的的PD-1重组蛋白进行亲和力评估。将人重组PD-L2固化在CM5生物芯片上,并添加复合物抗体(200nM)+重组人PD-1(100nM)。用通过Biacore测量的相互作用的相对响应%来表示数据:100%=PD-1相对响应。
图3:Bicki抗PD1-IL7分子刺激如通过人PBMC中离体STAT5磷酸化而测量的IL-7R信号传导通路。将从健康志愿者的外周血中分离的PBMC与重组IL-7(rIL7)(灰色●)+/-抗PD1(灰色▽)、抗PD1VH-IL7(■)或抗PD1VL-IL7(●)一起孵育15分钟。然后将细胞固定、透化并用AF647标记的抗pSTAT5(克隆47/Stat5(pY694))染色。通过计算MFI pSTAT*%pSTAT5+群体并归一化(100%=rIL-7(57.5nM))来获得数据,并且其代表两个独立实验中3个不同供体的平均值。
图4:Bicki抗PD1-IL7增强体外T细胞激活。(A)Discover’x PD-1Path HunterBioassay:稳定表达与β-gal片段(ED)融合的工程化PD-1受体和与互补β-gal片段(EA)融合的工程化SHP1的Jurkat T细胞。抗PD1拮抗剂抗体的添加阻断PD-1信号传导,导致生物发光信号(RLU)丢失。在不同的摩尔浓度下测试抗PD1(■)或抗PD1VH-IL7(●)。数据以RLU(相对发光信号)表示。(B)Promega PD-1/PD-L1生物测定:将(1)效应T细胞(稳定表达PD-1、NFAT诱导的荧光素酶的Jurkat)与(2)激活靶细胞(稳定表达PDL1和设计为以抗原独立性方式激活同源TCR的表面蛋白的CHO K1细胞)共培养。在添加BioGloTM荧光素后,对发光进行定量,并且其反映了T细胞激活。测试了抗PD1抗体+/-重组IL-7(rIL-7)或Bicki抗PD1VH-IL7或抗PD1VL-IL7抗体的系列摩尔浓度。每个点代表一个实验的EC50。(C)用Keytruda或Opdivo骨架构建的Bicki抗PD-1/IL-7刺激NFAT的能力。还使用Promega PD-1/PD-L1生物测定测试了T细胞激活。在不同浓度下测试了单独的Keytruda或单独的Opdivo(●)相比于派姆单抗VHIL-7或纳武单抗VH IL-7(○)。
图5:Bicki抗PD1-IL7分子增强IFNg分泌。在同种型对照、抗PD1+/-rIL7、抗PD1VH-IL7、抗PD1VL-IL7、同种型VH-IL7(最终抗体浓度为5μg/ml)的存在下,用OKT3/PDL1包被的板(分别为2和5μg/ml)刺激从健康志愿者的外周血中分离的T细胞。刺激后第5天,通过夹心ELISA定量分泌的IFNγ。结果代表4个供体(n=2个实验)。
图6:Bicki抗PD1-IL7以与重组可溶性IL-7相似的程度增强T细胞增殖。用抗CD3/CD28刺激从健康志愿者的外周血中分离的PBMC细胞。刺激后20小时,收集PBMC,并在rIL-7或Bicki抗PD1VH-IL7的存在下,在OKT3/PDL1包被的板(分别为2和5μg/mL)上对其进行重刺激。测试了(A)固定剂量(29nM BiCKI或3,2nM rIL-7)或(B)多剂量的单独的rIL-7(□)抗PD1或抗PD1VH-IL7(●)或抗PD1VL-IL7(■)或同种型VH IL-7(▲)。刺激后第5天,通过3H胸苷掺入来评估T细胞增殖。数据被归一化(100%=rIL7 10nM)并代表在3个不同供体上获得的平均值。EC50(pM)是指达到50%T细胞增殖所需的浓度。
图7.Bicki抗PD1VH-IL7刺激T细胞表面上整联蛋白的表达。不用任何分子(灰色直方图)孵育人PBMC 3天,或将人PBMC与rIL-7/rIL-2或rIL-7(50ng/mL)或抗PD-1或抗PD1VH-IL7(5μg/mL)一起孵育3天。A.α4和β7整联蛋白细胞表面表达分析。通过LSR来分析FACS,并且数据表示为归一化至1的倍数变化,其对应于每个供体的对照(未处理)的荧光中值。B.通过FACS,使用LSR而进行的LFA-1细胞表面表达分析(CD11a和CD18)。结果表示为中值荧光。每个点代表3个独立实验的一个供体。
图8.导致T细胞耗竭的T细胞慢性抗原刺激的建模。每3天在CD3 CD28包被的板(3μg/mL OKT3和3μg/mL CD28.2抗体)上反复刺激人PBMC。(A)刺激后24小时,针对PD-1、Lag3和Tim3抑制性受体对T细胞进行染色。通过流式细胞术,使用荧光染料标记的抗体和FACSLSRII来分析表达。用3个供体的阳性细胞%来表示数据(一个供体=一条曲线)。(B)通过每次刺激后第5天的胸苷3H掺入来确定T细胞增殖能力。(C)每次刺激后24小时,通过ELISA(pg/ml)来分析上清液IFNg分泌。
图9.耗竭T细胞的IL7通路激活:耗竭T细胞对细胞与rIL-7或Bicki抗PD1VH-IL7的15分钟孵育的响应,其是通过在每次刺激48小时后测量STAT5的磷酸化而进行的。然后将细胞固定、透化并用AF647标记的抗pSTAT5(克隆47/Stat5(pY694))染色。A.灰色直方图表示用rIL7处理的细胞,和黑色直方图表示用Bicki抗PD1VH-IL7处理的细胞。数据被归一化(MFI pSTAT*%pSTAT5群体)并代表4个不同的供体。(B)确定每次刺激的pSTAT5的ED50(pM),并且其是指达到50%的pSTAT5激活所需的rIL-7(■灰色)或Bicki抗PD1VH-IL7(■黑色)的浓度。
图10:IL-7刺激后耗竭T细胞的增殖。在CD3 CD28包被的板(3μg/mL OKT3和3μg/mLCD28.2抗体)上反复刺激人PBMC。(A)每次刺激后24小时,在抗PD1、rIL-7或Bicki抗PD1-IL7(抗PD1VH-IL7或抗PD1VL-IL7)的存在下,在OKT3包被的板(2μg/mL)上重刺激T细胞。在第5天进行H3掺入测定以确定T细胞增殖。显示了一个供体在刺激(STIM)3、4和5后的原始增殖数据。(B)3次刺激后的T细胞不再受到刺激(无Stim)或在抗CD3(StimOKT3)、抗CD3+重组PDL1(Stim OKT3/PDL1)或抗CD3+重组PDL2(StimOKT3/PDL2)包被的板(分别为2和5μg/mL)上重刺激。在第5天进行H3掺入测定,并将数据归一化(1=使用同种型抗体的H3掺入)。n=4个供体和2个不同的实验。
图11.Treg对CD8效应T细胞增殖的遏制活性。
从健康供体的外周血中分离CD8+效应T细胞和CD4+ CD25高CD127低Treg,用细胞增殖染料(针对CD8+ T细胞使用CPDe450)染色。然后在存在或不存在rIL-7、抗PD-1、抗PD-1+rIL-7、抗PD1VH-IL7的情况下,在OKT3包被的板上以1:1的比率共培养Treg/CD8+Teff 5天。通过细胞荧光法分析效应T细胞的增殖。A.数据代表以下的增殖%:单独的Teff(黑色直方图)或与Treg共培养的Teff(灰色直方图)+/-SEM,基于CD8 T效应细胞群体中CPD标志物的丢失。(n=4个不同实验中的4个供体)。B.在与不同等摩尔剂量的IL-7(▲)、IL-2(●)、IL-15(■)或抗PD1VH-IL7(▼)孵育后,使用CPD增殖染料来评估Treg增殖。
图12:人源化小鼠模型中Bicki抗PD1-IL7抗体的体内功效。将人PBMC腹膜内注射到小鼠中。每两周用单独的抗PD1抗体或Bicki抗PD1VH-IL7(5mg/kg)处理小鼠。注射后第16天采血并处死小鼠。(A)在人CD45+细胞群体中,通过流式细胞术分析外周人CD3 T细胞的百分比。每个点代表一只小鼠。(B)通过ELISA定量血浆中的人IFNg。每个点代表一只小鼠。(C)通过免疫组织荧光法定量结肠、肝脏和肺中人CD3+细胞的浸润。近端和远端结肠、肝脏和肺被包埋在TissueOCT中,并针对Dapi和人CD3进行染色。每个点代表一只小鼠,并且对于结肠,每个点代表3个切片的CD3+计数的平均值。
图13:人肿瘤浸润淋巴细胞的免疫表型。从肾癌(△)(▽)、转移性结直肠癌(□)、胰腺癌(○)、肝细胞癌(●)(◇)中提取T细胞,并对CD3、CD4、CD8、PD-1、CD127和CD132进行染色。通过FACS LSRII分析免疫荧光。数据代表CD4+CD3+或CD8+CD3+群体。
图14:离体肿瘤中肿瘤内调节性T细胞或效应T细胞的STAT5激活。从神经鞘瘤(▼)、肾癌(○)、肝细胞癌(□)(■)、转移性结直肠癌(●)或胰腺癌(▲)患者的肿瘤中提取细胞,并用rIL-7或Bicki抗PD1VH-IL7(29nM)处理15分钟。然后将细胞固定、透化并针对pSTAT5(克隆47/Stat5(pY694))、CD3和Foxp3进行染色。直方图代表CD3+FoxP3+群体(调节性T细胞)或CD3+FoxP3-(效应T细胞)中的pSTAT5荧光中值。
图15.用Bicki抗PD1-IL7处理人癌症活检组织后IFNγ分泌的体外研究:将人肿瘤活检组织在完全培养基中捣碎以分离细胞。以5μg/mL的浓度将细胞重悬在含同种型对照、抗PD1、B12-IL7同种型对照抗体(同种型-VH IL-7)、抗PD-1+重组IL-7,或含抗Bicki抗PD1VH-IL7的完整介质中。48小时后,收集上清液并使用MSD技术(Meso scale Discovery)分析IFNγ分泌。A.代表结直肠癌细胞的结果,和B.个体肿瘤的结果(CC:结直肠癌活检组织,HCC:肝癌活检组织,KC:肾癌)。
图16.用Bicki抗PD1VH-IL7处理后肿瘤内调节性T细胞或效应T细胞的STAT5激活。(A)肿瘤内FoxP3 Treg细胞进入结直肠癌、神经鞘瘤、肾癌或肝细胞癌的肿瘤中的百分比。(B)针对用rIL7或用抗PD1VH-IL7(29nM)处理(15分钟孵育)后FoxP3-CD3+效应T细胞相比于FoxP3-CD3+ Treg细胞中的STAT5激活,分析来自结直肠癌(●)、神经鞘瘤(○)和胰腺癌(□)的细胞。然后将细胞固定、透化并针对pSTAT5(克隆47/Stat5(pY694))、CD3和Foxp3进行染色。
图17:bicki IL-7突变体的结合PD-1的ELISA测定。固化人重组PD-1(rPD1)蛋白并添加不同浓度的抗体。使用与过氧化物酶偶联的抗人Fc抗体进行揭示。使用TMB底物,在450nm处确定比色法。A.包含抗PD1抗体和在氨基酸D74、Q22、Y12F、M17、Q11、K81上突变的IL-7的双功能分子的PD-1结合。B.包含在氨基酸W142上突变的IL-7的双功能分子的PD-1结合。C.在IL-7(SS1、SS2和SS3突变体)的二硫键中突变的双功能分子的PD-1结合。该图中测试的所有分子是用IgG4m同种型以及Fc和IL-7结构域之间的GGGGSGGGGSGGGGS接头构建的。
图18:IgG融合的突变IL-7的结合CD127的ELISA测定。将PD-1重组蛋白固化在板上,然后将双功能抗PD-1 IL-7分子与CD127重组蛋白(组氨酸标签,Sino参考号10975-H08H)一起预孵育并加入孔中。使用与生物素偶联的抗组氨酸抗体+与过氧化物酶偶联的链霉亲和素的混合物进行揭示。使用TMB底物,在450nm处确定比色法。A.包含在氨基酸D74、Q22、M17、Q11、Y12F、K81上突变的IL-7的双功能分子的CD127结合。B.包含在氨基酸W142上突变的IL-7的双功能分子的CD127结合。
图19:如通过STAT5磷酸化测量的不同双功能分子的IL-7-7R信号传导通路。将从健康志愿者的外周血中分离的人PBMC与双功能抗PD-1 IL-7分子一起孵育15分钟。然后将细胞固定、透化并用AF647标记的抗pSTAT5(克隆47/Stat5(pY694))染色。通过计算CD3 T细胞中的MFI pSTAT5来获得数据。A.包含在氨基酸D74、Q22、M17、Y12F、Q11、K81上突变的IL-7的抗PD-1 IL-7双功能分子的pSTAT5激活。B.包含在氨基酸W142上突变的IL-7的抗PD-1IL-7双功能分子的pSTAT激活。C.相比于抗PD-1 IL-7 WT(●灰色),包含在IL-7的二硫键中突变的IL-7,SS2(●黑色)和SS3(▲)的的抗PD-1 IL-7双功能分子的pSTAT5激活。该图中测试的所有分子是用IgG4m同种型以及Fc和IL-7结构域之间的GGGGSGGGGSGGGGS接头构建的。
图20:抗PD-1 IL-7双功能分子在小鼠中的药代动力学。给小鼠静脉注射一剂IgG融合的IL-7野生型或突变IL-7。在注射后的多个时间点,通过ELISA来评估血清中分子的浓度。A.注射IgG4-G4S3 IL7 WT(■灰色);IgG4-G4S3 IL7 D74E(●黑色)。B.注射IgG4-G4S3IL7 WT(■灰色)或IgG4-G4S3 IL7 W142H(●黑色)。C.注射IgG4-G4S3 IL7 WT(■灰色);IgG4-G4S3 IL7 SS2(●)或IgG4-G4S3 IL7 SS3(▲)。D.从每个分子的PK相比于ED50pSTAT5(nM)计算的曲线下面积(AUC)之间的相关性。该图中测试的所有分子是用IgG4m同种型以及Fc和IL-7结构域之间的GGGGSGGGGSGGGGS接头构建的。
图21:在抗PD-1和IL-7之间添加二硫键降低pSTAT5激活,同时增加体内药物暴露。A.在用抗PD-1 IL-7双功能分子WT(灰色●)或具有额外二硫键的抗PD-1 IL-7双功能分子(黑色●)处理后,如通过人PBMC上pSTAT5激活而测量的IL7R信号传导。B.抗PD-1IL-7双功能分子WT(灰色●)或具有额外二硫键的抗PD-1 IL-7双功能分子(黑色●)分子在小鼠体内的药代动力学。向小鼠静脉注射一剂抗PD-1 IL7双功能分子。在注射后的多个时间点,通过ELISA来评估血清中分子的浓度。该图中测试的所有分子是用IgG4m同种型以及Fc和IL-7结构域之间的GGGGSGGGGSGGGGS接头构建的。
图22:结合PD-1的ELISA测定。固化人重组PD-1(rPD1)蛋白并添加不同浓度的抗体。使用与过氧化物酶偶联的抗人Fc抗体进行揭示。使用TMB底物,在450nm处确定比色法。A.具有IgG4m的抗PD-1 IL-7 WT双功能分子(●灰色)、具有IgG1m的抗PD-1 IL-7 WT双功能分子(▲黑色)、具有IgG1m同种型的抗PD-1 IL-7 D74E双功能分子(■)或具有IgG1m的抗PD-1 IL-7 W142H双功能分子(◇)的PD-1结合。B.在另一个实验中,测试了具有IgG4m同种型的抗PD-1 IL-7 SS2双功能分子(■)或具有IgG1m的抗PD-1 IL-7 SS2双功能分子(▲)的PD-1结合。
图23:用IgG1N298A或IgG4同种型构建的抗PD-1IL-7双功能分子的结合CD127的ELISA测定。固化抗体骨架靶向的重组蛋白,然后将与IL-7融合的抗体与CD127重组蛋白(组氨酸标签,Sino ref10975-H08H)一起预孵育。使用与生物素偶联的抗组氨酸抗体和与过氧化物酶偶联的链霉亲和素的混合物进行揭示。使用TMB底物,在450nm处确定比色法。A.具有IgG4m同种型的抗PD-1 IL-7 W142H双功能分子(●灰色)、具有IgG1m的抗PD-1 IL-7 W142H双功能分子(▲黑色)或具有IgG1m同种型的抗PD-1 IL-7 WT双功能分子(●黑色)的CD127结合。B.具有IgG4m同种型的抗PD-1 IL-7 SS2双功能分子(●灰色)、具有IgG1m的抗PD-1IL-7 SS2双功能分子(▲黑色)或具有IgG1m的抗PD-1 IL-7 WT双功能分子(●黑色)的CD127结合。C.具有IgG4m同种型的抗PD-1 IL-7 SS3双功能分子(●灰色)、具有IgG1m的抗PD-1 IL-7 SS3双功能分子(▲黑色)或具有IgG1m的抗PD-1 IL-7 WT双功能分子(●黑色)的CD127结合。D.具有同种型IgG1m(●黑色)或同种型IgG1m+YTE(●灰色)的抗PD-1W142H双功能分子的CD127结合。还测试了具有同种型IgG1m(▲黑色)或同种型IgG1m+YTE(▲灰色)的抗PD-1D74E双功能分子的CD127。该图中测试的所有分子是用Fc和IL-7结构域之间的GGGGSGGGGSGGGGS接头构建的。
图24:用IgG1N298A或IgG4同种型构建的抗PD-1 IL-7双功能分子的IL-7R信号传导分析。将人PBMC或jurkat PD1+ CD127+细胞与抗PD-1 IL7双功能分子一起孵育15分钟。然后将细胞固定、透化并用AF647标记的抗pSTAT5(克隆47/Stat5(pY694))染色。通过计算CD3 T细胞中pSTAT5的%来获得数据。A.用IgG4m同种型(●灰色)或IgG1m同种型(▲黑色)处理具有突变D74E的双功能分子抗PD-1 IL-7后人PBMC上的pSTAT5信号传导。B.用IgG4m同种型(●灰色)处理抗PD-1 IL-7 SS2或用IgG1m(▲黑色)处理抗PD-1 IL-7 SS2后人PBMC上的pSTAT5信号传导。C.用IgG4m同种型(●灰色)或IgG1m(▲黑色)处理抗PD-1 IL-7 SS3后人PBMC上的pSTAT5信号传导。D.(左图)处理用IgG4m(●灰色)或IgG1m(▲黑色)同种型构建的抗PD-1 IL-7 WT后jurkat PD1+CD127+细胞上的pSTAT5信号传导。D.(右图)用IgG4m同种型(●灰色)处理抗PD-1 IL-7 SS2或用IgG1m(▲黑色)处理抗PD-1 IL-7 SS2后的pSTAT5信号传导。
图25:抗PD-1 IL-7突变的双功能分子增强体外T细胞激活。Promega PD-1/PD-L1生物测定:将(1)效应T细胞(稳定表达PD-1、NFAT诱导的荧光素酶的Jurkat)和(2)激活靶细胞(稳定表达PDL1和设计为以抗原独立性方式激活同源TCR的表面蛋白的CHO K1细胞)共培养。添加BioGloTM荧光素后,对发光进行定量并反映T细胞激活。测试了抗PD1抗体+/-重组IL-7(rIL-7)或抗PD1IL7双功能分子的系列摩尔浓度。每个点代表一个实验。A.具有IgG4m同种型的抗PD-1 IL-7 WT双功能分子(●灰色)或抗PD-1(▲)或抗PD-1+rIL-7(○)的的NFAT激活。B.抗PD-1 IL-7 D74E IgG4m(●)、PD-1 IL-7 D74E IgG1m(▲虚线)和单独的抗PD-1(黑色▲)的NFAT激活。C.具有IgG4m的抗PD-1 IL-7 W142H双功能分子(●)、具有IgG1m的PD-1 IL-7 W142H双功能分子(▲虚线)、和单独的抗PD-1(黑色▲)的NFAT激活。D.具有IgG4m的抗PD-1 IL-7 SS2双功能分子(●)和单独的抗PD-1(黑色▲)的NFAT激活。
图26:用IgG1m或IgG4m同种型构建的抗PD-1 IL-7双功能分子的药代动力学。给小鼠静脉注射一剂与IL-7野生型或突变IL-7融合的IgG。在注射后的多个时间点,通过ELISA来评估血清中的药物浓度。A.具有IgG4m的抗PD-1 IL-7 WT双功能分子(●灰色素线)、具有IgG1m的抗PD-1 IL-7 WT双功能分子(●灰色虚线)、具有IgG1m的抗PD-1 IL-7 D74E双功能分子(▲黑色虚线)、具有IgG4m的抗PD-1 IL-7 W142H双功能分子(○黑色素线)、具有IgG1m的抗PD-1 IL-7 W142H双功能分子(○虚线黑色素线)、具有IgG4的抗PD-1 IL-7 SS3(■素线)和具有IgG1m的抗PD-1 IL-7 SS3(■虚线)的药代动力学。B.具有IgG1m的抗PD-1 IL-7D74E、D74Q、W142H、D74E+W142H突变双功能分子的药代动力学。
图27:用IgG1 N298A+K444A同种型构建的抗PD-1 IL-7双功能分子的药代动力学。给小鼠静脉注射一剂具有同种型IgG1N298A(■)或同种型IgG1m+K444A突变同种型(●)的抗PD-1 IL7 D74E双功能分子。在注射后的多个时间点,通过ELISA来评估抗体的浓度。
图28:接头的长度不显著影响药代动力学,但降低了对IL-7R信号传导的刺激。A.用不同接头((GGGGS)、(GGGGS)2、(GGGGS)3)构建的抗PD-1 IL-7 WT双功能分子的药代动力学。B.用不同接头((GGGGS)、(GGGGS)2、(GGGGS)3)构建的抗PD-1 IL-7 D74双功能分子的药代动力学。C.用不同接头((GGGGS)2、(GGGGS)3)构建的抗PD-1 IL-7 W142H双功能分子的药代动力学。给小鼠静脉注射一剂与IL-7野生型或突变IL-7融合的IgG。在注射后的多个时间点,通过ELISA来评估与IL-7融合的IgG的浓度。D.不使用接头或使用GGGGS、(GGGGS)2、(GGGGS)3接头构建的抗PD-1 IL-7双功能分子的pSTAT5信号传导。
图29:抗PD-1 IL-7突变体相对于PD-1-CD127+细胞,优先靶向PD-1+ CD127+细胞。用45nM抗PD-1 IL-7双功能分子对表达CD127+或共表达CD127+和PD-1+的Jurkat细胞进行染色,并用抗IgG-PE(Biolegend,克隆HP6017)揭示。数据代表PD-1+CD127+Jurkat细胞上的荧光中值与PD1-细胞CD127+Jurkat细胞上获得的荧光中值的比率。在本测定中,测试了抗PD-1 IL-7 WT双功能分子IgG1m、抗PD-1 IL-7 D74E双功能分子IgG1m、抗PD-1 IL-7 W142H双功能分子IgG1m、抗PD-1 IL-7 SS2双功能分子IgG4m、抗PD-1 IL-7 SS3双功能分子IgG1m。
图30:抗PD-1 IL-7分子增强T细胞增殖并在食蟹猴中显示了临床前安全性。c相对于PD-1-CD127+细胞,靶向PD-1+ CD127+细胞。给食蟹猴静脉注射一剂bicki抗PD-1 IL-7WT(6,87nM/kg(n=2)或34,35nM(n=1))。进行血液分析直至注射后第15天或4小时为止。A.在多个时间点评估外周血中的淋巴细胞计数,以6,87nM/kg注射Bicki抗PD-1 IL-7 WT(n=2)。B.通过流式细胞术,使用Ki67/CD4/CD8和CD19标志物,评估了CD4/CD8或B细胞的增殖,以6,87nM/kg注射Bicki抗PD-1 IL-7 WT(n=2)。C.通过FACS,在CD3+ T细胞中,在多个时间点分析pSTAT5,以6,87nM/kg注射Bicki抗PD-1 IL-7 WT(n=2)。D/E/F/G和H。在多个时间点评估生化和细胞血液分析。
图31:根据本发明所述的Bicki抗PD1-IL-7的作用机制的说明。
本发明具体实施方式
简介
本发明所述的抗体是双功能的,因为它们结合了特异性抗PD-1作用和与抗PD-1抗体融合的人白介素7的作用。实际上,本发明涉及包含抗PD-1抗体和IL-7的双功能分子,所述白介素与所述抗PD-1抗体的多肽链(所述抗体的轻链或重链或两者或其片段)共价连接。将所述抗PD-1抗体或其片段的链和所述IL-7制备为融合蛋白。在该特别的方面中,所述IL-7的N-端末端,任选地通过肽接头,与所述抗PD-1抗体的链或其片段的C-端末端连接。
如本领域技术人员所知,由于在许多癌症中观察到的称为T细胞耗竭的现象,T细胞可能无法充分清除肿瘤细胞。例如,如Jiang,Y.,Li,Y.和Zhu,B(Cell Death Dis 6,el792(2015))所述,肿瘤微环境中的耗竭T细胞可导致抑制性受体的过表达、效应细胞因子产生和细胞溶解活性的减少,导致癌症消除失败并通常导致癌症免疫逃避。恢复耗竭T细胞因此是针对癌症治疗设想的临床策略。
PD-1是调节T细胞耗竭的主要抑制性受体。事实上,具有高PD-1表达的T细胞清除癌细胞的能力下降。抗PD1治疗性化合物,尤其是抗PD1抗体,在临床上的癌症治疗中用于阻断PD1-PDL1相互作用的抑制作用(PD1对T细胞和PDL1对肿瘤细胞)和T细胞耗竭。然而,抗PD1抗体并不总是足够有效以允许耗竭T细胞的“重”激活。
申请人在本文中表明,根据本发明所述的双功能抗PD1-IL-7分子相比于单独的抗PD-1增强了T细胞(特别是耗竭T细胞)的激活(NFAT介导的激活)。特别是,所述抗PD1-IL-7双功能分子诱导初始、部分耗竭和完全耗竭T细胞亚群的增殖和激活,如细胞因子(例如IFNγ)分泌所反映的。这种抗PD1-IL-7双功能分子有能力克服相关的抗性机制并提高抗PD-1免疫疗法的功效。
申请人特别表明,所述抗PD1-IL-7双功能分子与表达i)PD1和ii)IL-7受体的单个T细胞的相互作用导致NFAT途径(TCR信号传导)的意外激活,对T细胞激活,特别是对耗竭T细胞激活有阳性作用,促进T细胞消除肿瘤细胞的能力。
这意味着,一方面,本发明所述的双功能分子的IL-7靶向IL-7受体,激活PSTAT5通路;另一方面,所述双功能分子的抗PD1部分阻断PD-1/PD-L1相互作用。BICKI分子在相同细胞上同时靶向IL-7和PD-1。这导致TCR(NFAT)信号传导的协同激活,这在单独使用抗PD1抗体和IL-7的组合(作为两种单独的化合物)时从未观察到。这种激活不能由靶向PD-L1的双功能分子提供。事实上,本领域已知PD-L1在肿瘤细胞上而不是在免疫细胞如T细胞上表达。
此外,所述双功能抗PD1/IL-7分子允许PD-1+ T细胞浸润中IL-7的积累和PD-1+ T细胞上IL-7的重定位。在需要高剂量IL-7来激活或重激活这些T细胞的耗竭T细胞的背景下,这种PD-1+ T细胞附近的IL-7积累尤其令人感兴趣。
不仅在本发明所述的特定抗PD-1抗体中,而且在其他两种抗PD-1参照(即Opdivo和Keytruda)中也观察到了对T细胞激活的协同作用。
此外,所述双功能抗PD1/IL-7分子具有促进T细胞浸润到肿瘤中的能力。考虑到肿瘤部位缺乏T细胞浸润是目前抗PD1抗体治疗效果的主要障碍,这种能力是优化抗PD-1抗体治疗的优势。
此外,所述双功能抗PD1/IL-7分子可阻断Treg介导的抑制作用。因此,所述双功能分子能够特异性激活T效应细胞而不是T reg细胞,而抗PD1抗体不能抑制T效应细胞上的Treg抑制活性。然后,发明人表明所述双功能抗PD1-IL7分子通过刺激效应T细胞增殖和存活并同时保留(spare)调节性T细胞而相对于T调节性免疫平衡偏向T细胞效应子。
此外,所述IL7抗PD-1双功能分子还有其他优点。
发明人表明IL7抗PD-1双功能分子主要激活T效应细胞(Teff)而不是T调节细胞(Treg)。所述IL7抗PD-1双功能分子具有不促进T Reg增殖、诱导T Reg失活和诱导T细胞(特别是耗竭T细胞)激活的优点。
此外,IL7抗PD-1双功能分子允许使用非常有利的剂量,表现出有利的治疗指数(致死剂量(DL50)与治疗有效剂量之间的比率)。特别地,对于患者,通常可以使用范围在10至1500μg/Kg、有利地200-1200μg/Kg的IL7;患者可以很好地耐受例如1200μg/Kg的高剂量。然后,IL7抗PD-1双功能分子允许以适当剂量的原始化合物和最终产品生产治疗性化合物。事实上,IL7的高剂量耐受性(例如约1.2mg/kg的IL7)对应于约2mg/kg的抗体量,这是令人满意的施用于患者的剂量。
IL7抗PD-1双功能分子的优点是可以基本上靶向仅部分耗竭的耗竭T祖细胞,这是满足上述医疗需求的关键目标。补充说,在与T细胞类似耗竭相关的病毒感染的情况下,慢性激活很重要,因此病毒病理学包括在本申请新产品所针对的病理学范围内。
最后,在一个具体方面,发明人设计了包含IL-7突变体或变体的双功能分子。IL-7突变体或变体的特征在于i)相比于野生型IL-7的亲和力对IL-7受体(IL-7R)的亲和力降低,和ii)相比于包含野生型IL-7的双功能分子改善了包含IL-7变体的双功能分子的药代动力学。首先,在双功能分子中使用IL-7变体对于增加双功能分子的体内药代动力学很重要。其次,通过降低IL-7变体对其受体的亲和力,其增加了双功能分子通过双功能分子的抗PD-1抗体部分优先结合靶向T细胞和显示出对这些细胞的特异性作用、并同时利用与相同T细胞上的双功能分子的两个部分的作用相关的协同作用的能力。具有IL-7变体的双功能分子对PD-1具有良好的结合和拮抗活性。此外,双功能分子在其对PD-1的亲和力和对IL-7R的亲和力之间呈现出合适的平衡。令人惊讶的是,发明人观察到,具有IgG1重链恒定结构域的双功能分子相比于具有IgG4重链恒定结构域的相同分子具有改善的IL-7变体活性(pStat5信号、协同作用和CD127结合)。此外,在抗体和IL-7之间使用接头(GGGGS)3可使IL-7变体(pStat5信号和CD127结合)的活性最大化。
本发明所述的双功能分子具有以下优点中的特定一个或多个:
-所述双功能分子诱导初始、部分耗竭和完全耗竭T细胞亚群的增殖,而不仅仅是像抗PD1/PDL1疗法那样仅诱导部分耗竭T细胞亚群的增殖。更特别地,其具有T细胞激活的协同作用。
-所述双功能分子允许将靠近或位于PD-1+耗竭T细胞上的IL-7特异性定位到肿瘤中,靶向需要更高浓度的IL-7的细胞。其特别诱导PD-1+ T细胞浸润中的IL-7积累和PD-1+T细胞上的IL-7重定位。
-虽然抗PD-1阻断剂无法将耗竭T细胞重新编程为具有活性的记忆T细胞,限制了肿瘤的长期清除,但所述双功能分子通过IL-7的存在促进记忆T细胞的形成、存活和增殖。然后,所述双功能分子通过持续和扩展的记忆T细胞应答诱导持久的抗肿瘤免疫。
-尽管抗PD1/PD-L1治疗功效与预先存在的T细胞浸润和T细胞效应功能相关,特别是IFNγ特征,但双功能分子增加效应T细胞的增殖及其分泌IFNγ的能力,具有协同作用。
-所述双功能分子可以通过减少T reg群体和抑制TGFβ(一种抑制性细胞因子)的分泌来减少免疫抑制微环境。更特别地,所述双功能分子特异性地刺激效应T细胞而不刺激T reg。
-所述双功能分子,其中IL-7可以与所述重链和/或轻链的C-端部分融合,并且其中IL7保留了对CD127的高亲和力,类似于裸/天然IL-7。所述双功能分子在IL-7R激活和半衰期方面可能更有效。
-其作为双功能分子以高产率生产。
-所述双功能分子通过减少T reg的数量来降低Treg细胞对肿瘤微环境的免疫抑制活性。更特别地,所述双功能分子特异性地刺激效应T细胞而不刺激T reg。
-所述双功能化合物相比于单独的抗PD1应答增加整联蛋白(即α4和/或β7和LFAT)的表达,促进T细胞浸润到组织和/或肿瘤中。特别是,所述双功能化合物促进T细胞迁移和肿瘤浸润。
-所述双功能分子可包含如本发明人识别的IL-7变体或突变体以最大化体内药代动力学,同时保持抗DP-1抗体的IL-7活性和拮抗剂活性,在IL-7和IL-7R与抗PD-1和PD-1之间具有合适的亲和力平衡。
定义
为了更容易理解本发明,以下定义了某些术语。在整个具体实施方式中阐述了另外的定义。
除非另有定义,本文中使用的所有技术术语、符号和其他科学术语旨在具有本发明所属领域的技术人员通常理解的含义。在一些情况下,为了清楚和/或便于参考,本文定义具有普遍理解的含义的术语,并且本文中包含的此类定义不应被解释为代表与本领域通常理解的差异。此处描述或引用的技术和程序通常是本领域技术人员使用常规方法学充分理解和普遍采用的。
如本文所用,术语“白介素-7”、“IL-7”和“IL-7”是指哺乳动物内源性分泌糖蛋白,特别是IL-7多肽、其衍生物和类似物,其例如在IL-7受体结合亲和力的标准生物测定或测定中,与野生型哺乳动物IL-7具有实质性氨基酸序列同一性并具有基本相等的生物活性。例如,IL-7是指具有以下氨基酸序列的重组或非重组多肽的氨基酸序列:i)IL-7多肽的天然或天然存在的等位基因变体,ii)IL-7多肽的生物活性片段,iii)IL-7多肽的生物活性多肽类似物,或iv)IL-7多肽的生物活性变体。IL-7可以包含其肽信号或不包含其肽信号。该分子的替代名称是“前体B细胞生长因子”和“淋巴细胞生成素-1”。优选地,术语“IL-7”是指人IL-7。例如,人IL-7氨基酸序列为约152个氨基酸(在不存在信号肽的情况下),并且其Genbank登录号为NP_000871.1,该基因位于染色体8q12-13上。在UniProtKB-P13232中描述了人IL-7。
如本文所用,术语“野生型白介素-7”、“wt-IL-7”和“wt-IL7”是指哺乳动物内源性分泌糖蛋白,特别是IL-7多肽、其衍生物和类似物,其例如在IL-7受体结合亲和力的标准生物测定或测定中,与野生型哺乳动物IL-7具有实质性氨基酸序列同一性并具有基本相等的生物活性。例如,IL-7是指具有以下氨基酸序列的重组或非重组多肽的氨基酸序列:i)IL-7多肽的天然或天然存在的等位基因变体,ii)IL-7多肽的生物活性片段,iii)IL-7多肽的生物活性多肽类似物,或iv)IL-7多肽的生物活性变体。IL-7wt可以包含其肽信号或不包含其肽信号。该分子的替代名称是“前体B细胞生长因子”和“淋巴细胞生成素-1”。优选地,术语“wt-IL-7”是指人IL-7(wth-IL7)。例如,人wt-IL-7氨基酸序列为约152个氨基酸(在不存在信号肽的情况下),并且其Genbank登录号为NP_000871.1,该基因位于染色体8q12-13上。在UniProtKB-P13232中描述了人IL-7。
如本文所用,术语“程序性死亡1”、“程序性细胞死亡1”、序PD1”、“PD-1”、“PDCD1”、“PD-1抗原”、“人PD-1”、“hPD-1”和“hPD1”可以互换使用,其指程序性死亡-1受体,也称为CD279,并且包括人PD-1的变体和亚型,以及与PD-1具有至少一个共同表位的类似物。PD-1是免疫应答阈值和外周免疫耐受的关键调节剂。其在激活的T细胞、B细胞、单核细胞和树突状细胞上表达,并与其配体PD-L1和PD-L2结合。人PD-1由PDCD1基因编码。举例而言,人PD-1的氨基酸序列在GenBank登录号NP_005009下公开。PD1具有四种在人类外周血单核细胞(PBMC)上表达的剪接变体。因此,PD-1蛋白包括全长PD-1,以及PD-1的替代剪接变体,如PD-1Aex2、PD-1Aex3、PD-1Aex2,3和PD-1Aex2,3,4。除非另有说明,否则术语包括天然由PBMC表达或由经PD-1基因转染的细胞表达的人PD-1的任何变体和亚型。
如本文所用,术语“抗体”描述了一种免疫球蛋白分子类型,并且以其最广泛的意义使用。特别地,抗体包括免疫球蛋白分子和免疫球蛋白分子的免疫活性片段,即,包含抗原结合位点的分子。免疫球蛋白分子可以是任何类型(例如,IgG、IgE、IgM、IgD、IgA和IgY)、类别(例如,IgG1、IgG2、IgG3、IgG4、IgA1和IgA2)或亚类。对应于不同类别免疫球蛋白的重链恒定结构域分别称为α、δ、ε、γ和μ。除非特定地指出,否则术语“抗体”包括完整免疫球蛋白以及“抗体片段”或体抗原结合片段”(例如Fab、Fab'、F(ab')2、Fv)、单链(scFv)、其突变体、包含抗体部分的分子、双体、线性抗体、单链抗体和包含具有所需特异性的抗原识别位点的免疫球蛋白分子的任何其他修饰构型,包括抗体的糖基化变体、抗体的氨基酸序列变体。优选地,术语“抗体”指人源化抗体。
如本文所用,抗体的“抗原结合片段”指展现对PD-1的抗原结合能力的抗体的一部分,亦即与本发明的抗体的结构的一部分对应的分子,可能呈其天然形式;与对应四链抗体的抗原结合特异性相比,此类片段尤其显示相同或基本上相同的对该抗原的抗原结合特异性。有利地,抗原结合片段具有与对应4链抗体类似的结合亲和性。然而,相对于相应的4链抗体具有降低的抗原结合亲和性的抗原结合片段也包括在本发明内。抗原结合能力可以通过测量抗体与目标片段之间的亲和性来确定。也可以将这些抗原结合片段称为抗体的“功能性片段”。抗体的抗原结合片段是包含其被称为CDR(互补决定区)或其包含抗原识别位点(即,PD1的胞外域)的部分的高变结构域的片段,从而定义抗原识别特异性。
“Fab”片段包含轻链的恒定结构域和重链的第一恒定结构域(CH1)。Fab'片段与Fab片段的不同之处在于在重链CH1结构域的羧基末端添加了几个残基,包括来自抗体铰链区的一个或多个半胱氨酸。F(ab')片段是通过在F(ab')2胃蛋白酶消化产物的铰链半胱氨酸处切割二硫键而产生的。抗体片段的其他化学偶联是本领域普通技术人员公知的。Fab和F(ab')2片段缺乏完整抗体的Fc片段,从动物循环中清除得更快,并且可能比完整抗体具有更少的非特异性组织结合(参见例如Wahl等,1983,J.Nucl.Med.24:316)。
“Fv”片段是包含完整靶点识别和结合位点的抗体的最小片段。该区域由一个重链可变结构域和一个轻链可变结构域紧密非共价结合的二聚体组成(VH-VL二聚体)。正是在这种构型中,每个可变结构域的三个CDR相互作用以定义VH-VL二聚体表面上的靶点结合位点。通常,六个CDR赋予抗体靶向结合特异性。然而,在一些情况下,即使单个可变结构域(或仅包含对靶点特异的三个CDR的Fv的一半)也可以具有识别和结合靶点的能力,尽管亲和性低于整个结合位点。
“单链Fv”或“scFv”抗体结合片段包含抗体的VH和VL结构域,其中这些结构域存在于单个多肽链中。通常,Fv多肽在VH和VL结构域之间还包含多肽接头,其使得scFv能够形成用于靶点结合的所需结构。
“单域抗体”由对PD-1表现出足够亲和性的单个VH或VL结构域组成。在一个特定实施方式中,单域抗体是骆驼源化抗体(参见,例如,Riechmann,1999,Journal ofImmunological Methods 231:25-38)。
就结构而言,抗体可具有通过二硫键互相连接的重链(H)和轻链(L)。有两种类型的轻链λ和κ。各重链和轻链含有恒定区和可变区(“结构域”)。轻链和重链可变区包含被三个高变区(也称为“互补决定区”或“CDR”)中断的“框架”区。已定义了框架区和CDR的范围(参见Kabat等,Sequences of Proteins of Immunological Interest,和U.S.Departmentof Health and Human Services,1991,其通过引用并入本文)。优选地,CDR根据Kabat方法定义。框架区起到形成支架的作用,通过链间非共价相互作用将CDR定位在正确的方向上。CDR主要负责结合抗原表位。每条链的CDR通常称为“互补决定区1”或“CDR1”、“CDR2”和“CDR3”,从N末端开始依次编号。根据本发明的抗体的VL和VH结构域可以包含四个框架区或“FR”,其在本领域中和本文中分别称为“框架区1”或“FR1”、“FR2”、“FR3”和“FR4”。这些框架区和互补决定区优选按以下顺序可操作地连接:FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4(从氨基末端到羧基末端)。如本文所用,术语“抗体框架”指可变结构域中的部分,VL和/或VH,其用作该可变结构域的抗原结合环(CDR)的支架。
如本文所用,“抗体重链”指抗体构象中存在的两种类型多肽链中较大的一种。抗体重链的CDR通常称为“HCDR1”、“HCDR2”和“HCDR3”。抗体重链的框架区通常称为“HFR1”、“HFR2”、“HFR3”和“HFR4”。
如本文所用,“抗体轻链”指抗体构象中存在的两种类型多肽链中较小的一种,κ和λ轻链指两种主要抗体的轻链同种型。抗体轻链的CDR通常称为“LCDR1”、“LCDR2”和“LCDR3”。抗体轻链的框架区通常称为“LFR1”、“LFR2”、“LFR3”和“LFR4”。
关于抗体与靶分子的结合,术语“结合(bind/binding)”指识别和接触抗原的肽、多肽、蛋白、融合蛋白、分子和抗体(包括抗体片段)。优选地,其指抗原-抗体类型相互作用。术语“特异性结合”、“特异性结合至”、“特异性针对”、“选择性结合”和“选择性针对”特定抗原(例如,PD-1)或特定抗原(例如,PD-1)上的表位"指抗体识别和结合特定抗原,但基本上不识别或结合样品中的其他分子。例如,特异性(或优先)结合至PD-1或PD-1表位的抗体是结合该PD-1表位的抗体,例如,以比结合至其他PD-1表位或非PD-1表位更高的亲和性、亲合力、更容易和/或更长的持续时间。优选地,术语“特异性结合”指抗体和抗原之间以等于或低于10-7M的结合亲和性接触。在某些方面中,抗体以等于或低于10-8M、10-9M或10-10M的亲和性结合。
如本文所用,“PD-1抗体”、“抗PD-1抗体”、“PD-1 Ab”、“PD-1 Ab”、“PD-1特异性抗体”、“抗PD-1 Ab”可以互换使用,并且指特异性结合至PD-1,特别地人PD-1的如本文所述的抗体。在一些实施方式中,所述抗体与PD-1的胞外域结合。特别地,抗PD-1抗体是能够结合至PD-1抗原的抗体,并抑制PD-1介导的信号传导通路,从而增强免疫应答,如T细胞激活。
如本文所用,术语“双功能分子”、“双功能化合物”、“双功能蛋白”、“Bicki”、“Bicki抗体”、“双功能抗体”和“双功能检查点抑制剂分子”具有相同含义并可互换使用。这些术语是指通过含有至少一个对一个抗原具有特异性的区域(例如来源于抗体的可变区)和至少为多肽的第二区域来识别该抗原的抗体。更具体地,所述双功能分子是抗体或其部分的融合蛋白,优选其抗原结合片段与另一多肽或其多肽片段。
如本文所用,术语“嵌合抗体”指抗体或抗原结合片段,其重链和/或轻链中的一部分来源于一个物种,而所述重链和/或所述轻链的其余部分来源于不同的物种。在说明性实例中,所述嵌合抗体可包含来源于人的恒定区和来源于非人物种(例如小鼠)的可变区。
如本文所用,术语“人源化抗体”旨在指其中来源于另一哺乳动物物种(例如小鼠)的种系的CDR序列已被移植到人框架序列的抗体(例如,包含来源于非人抗体的最少序列的嵌合抗体)。“人源化抗体”(例如,非人抗体)还指已经历人源化的抗体。人源化抗体通常是人免疫球蛋白(受体抗体),其中一个或多个CDR的残基被非人抗体(供体抗体)的至少一个CDR的残基置换,同时保持所需的特异性、亲和性和原始抗体的能力。供体抗体可以是任何适宜的非人抗体,如具有所需特异性、亲和性或生物学效应的小鼠、大鼠、兔、鸡或非人灵长类抗体。在一些情况下,受体抗体的选定框架区残基被来自供体抗体的框架区残基替代。或者,共同抗体的选定框架区残基被来自人或人源化抗体的框架区残基替代。可以在人框架序列内进行另外的框架区修饰。因此,人源化抗体还可以包含在受体抗体或供体抗体中均未发现的残基。可以进行此类氨基酸修饰以进一步完善抗体功能和/或增加人源化过程。本文中“氨基酸改变”或“氨基酸修饰”指在多肽的氨基酸序列中的改变。“氨基酸修饰”包括在多肽序列中的置换、插入和/或缺失。本文中的“氨基酸置换”或“置换”是指用另一个氨基酸置换亲本多肽序列中特定位置的氨基酸。“氨基酸插入”或“插入”是指在亲本多肽序列中的特定位置添加氨基酸。“氨基酸缺失”或“缺失”是指在亲本多肽序列中的特定位置除去氨基酸。氨基酸置换可以是保守的。保守性置换是给定的氨基酸残基被具有类似化学性质(例如,电荷、体积和/或疏水性)的侧链(“疏水基团”)的另一个残基置换。如本文所用,“氨基酸位置”或“氨基酸位置编号”可以互换使用,并且指在氨基酸序列中特定氨基酸的位置,通常用氨基酸的单字母代码指定。氨基酸序列中的第一个氨基酸(即,从N-端开始)应被视为具有位置1。
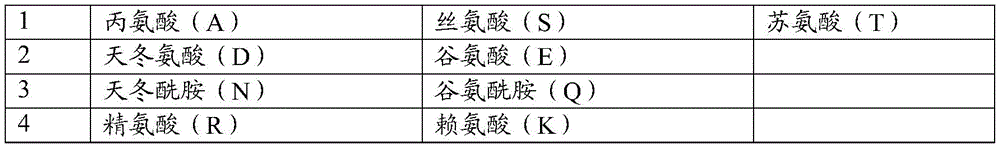
保守性置换是给定的氨基酸残基被具有类似化学性质(例如,电荷、体积和/或疏水性)的侧链(“R-基团”)的另一个残基置换。在通常情况下,保守性氨基酸置换将基本上不改变蛋白的功能性性质。保守性置换和相应规则在现有技术中有很好的描述。例如,保守性置换可以通过下表中反映的氨基酸组内的置换来定义:
表A–氨基酸残基
| 氨基酸基团 | 氨基酸残基 |
| 酸性残基 | ASP和GLU |
| 碱性残基 | LYS、ARG和HIS |
| 亲水性不带电残基 | SER、THR、ASN和GLN |
| 脂肪族不带电残基 | GLY、ALA、VAL、LEU和ILE |
| 非极性不带电残基 | CYS、MET和PRO |
| 芳香族残基 | PHE、TYR和TRP |
表B-替代保守性氨基酸残基置换组
表C–氨基酸残基的其他替代物理和功能分类
如本文所用,“分离的抗体”是从其自然环境的组分中分离和/或回收的抗体。分离的抗体包括重组细胞内的原位抗体,因为不存在抗体自然环境的至少一种组分。在一些实施方式中,如通过例如电泳(例如,SDS-PAG、等电聚焦(IEF)、毛细管电泳)或层析(例如,离子交换或反相HPLC)在还原或非还原条件下所确定的,抗体纯化至同质性和/或纯度90%、95%或99%。
如本文所用,术语“来源于(derive from/derived from)”指具有来源于母体化合物或蛋白结构的结构的化合物,并且其结构与本文公开的那些足够相似并且基于该相似性,本领域技术人员将预期其表现出与要求保护的化合物相同或相似的性质、活性和效用。例如,来源于小鼠抗体的人源化抗体指与该小鼠抗体共享相似性质,例如,识别相同表位、共享具有参与和/或增加抗体人源化的修饰的残基的相似VH和VL的抗体或抗体片段。
术语“治疗”指旨在改善患者健康状况的任何行为,如疾病或疾病症状的治疗、预防、预防和延缓。其指的是对疾病的治愈性治疗和/或预防性治疗。治愈性治疗被定义为导致治愈的治疗或减轻、改善和/或消除、减轻和/或稳定疾病或疾病的症状或其直接或间接引起的痛苦的治疗。预防性治疗包括导致疾病预防的治疗和减少和/或延迟疾病的进展和/或发生或其发生的风险的治疗。在某些实施方式中,该术语是指改善或根除疾病、病症、感染或与之相关的症状。在其他实施方式中,该术语指最小化癌症的播散或恶化。根据本发明的治疗不一定意味着100%或完全治疗。相反,存在不同程度的治疗,其中本领域普通技术人员认为具有潜在获益或治疗效果。优选地,术语“治疗”指将包含一种或多种活性剂的组合物应用或施用给患有病症/疾病的受试者,例如与由PD-1介导的信号传导途径相关的病症/疾病。
如本文所用,术语“病症”或“疾病”是指由于遗传或发育错误、感染、毒物、营养缺乏或失衡、毒性或不利环境因素的影响而导致身体功能不正常的器官、部分、结构或系统。优选地,这些术语指监控病症或疾病,例如,破坏正常身体或精神功能的疾病。更优选地,术语病症指影响动物和/或人的免疫和/或炎症疾病,如癌症。
如本文所用,术语“免疫疾病”指受试者的病况,其特征在于由受试者对其自身细胞、组织和/或器官的免疫反应引起的细胞、组织和/或器官损伤。术语“炎症疾病”指受试者中以炎症(例如,慢性炎症)为特征的病况。自身免疫性病症可能与炎症相关,也可能无关。据此,炎症可能是也可能不是由自身免疫性病症引起的。
如本文所用,术语“癌症”定义为特征在于异常细胞的快速且不受控制的生长的疾病。癌细胞可以局部扩散或通过血流和淋巴系统扩散到身体的其他部位。
如本文所用,术语“与PD-1相关联或相关的疾病”、“PD-1阳性癌症”或“PD-1阳性感染性疾病”旨在指由PD-1表达引起或具有PD-1表达的症状和/或特征的癌症或感染性疾病(例如,由病毒和/或细菌引起),即,由PD-1表达或活性增加或减少引起、引起加重或与其相关的任何病况。
如本文所用,术语“受试者”、“宿主”、“个体”或“患者”指人,包括成人或儿童。
如本文所用,“药物组合物”指一种或多种活性剂的制剂,如包含根据本发明所述的双功能分子与任选地其他化学组分,如生理学上适宜的载体和赋形剂。药物组合物的目的是促进将活性剂施用于生物体。本发明的组合物可以是适合于任何常规给药途径或使用的形式。在一个实施方式中,“组合物”通常指活性剂(例如,化合物或组合物)与天然存在或非天然存在的载体的组合,所述载体是惰性的(例如,检测剂或标签)或活性的,如佐剂、稀释剂、粘合剂、稳定剂、缓冲剂、盐、亲脂性溶剂、防腐剂、佐剂等,并且包括药学上可接受的载体。如本文所指,“可接受的载剂”或“可接受的载体”是本领域技术人员公知的可用于配制药物组合物的任何已知化合物或化合物的组合。
如本文所用,“有效量”或“治疗有效量”指单独或与一种或多种其他活性剂组合,赋予受试者治疗作用所需的活性剂的量,例如,治疗目标疾病或病症或产生所需作用所需的活性剂的量。“有效量”将根据以下而改变:一种或多种药剂、疾病及其严重程度、待治疗的受试者的特征,包括年龄、身体状态、体格、性别和体重、治疗持续时间、伴随疗法的性质(如果有的话)、具体的施用途径以及健康从业者知识和专业知识范围内的类似因素。这些因素是本领域普通技术人员众所周知的,并且可以通过常规实验解决。通常优选使用单个组分或其组合的最大剂量,即根据合理的医学判断的最高安全剂量。
如本文所用,术语“药物”指具有治愈或预防病症或疾病的性质的任何物质或组合物。
如本文所用,术语“联合”指使用一种以上的疗法(例如,预防剂和/或治疗剂)。术语“联合”的使用不限制向患有疾病或病症的受试者施用疗法(例如,预防剂和/或治疗剂)的顺序。
术语“多核苷酸”、“核酸”和“核酸序列”是等同的,并且指具有任何长度的核苷酸的聚合形式,例如RNA或DNA或其类似物。本发明的核酸(例如,核酸的组分或部分)可以是天然存在的、经修饰或经工程化的、分离的和/或非天然的。工程化的核酸包括重组核酸和合成核酸。
“编码抗PD1抗体的分离的核酸”指编码抗体重链和轻链(或其片段)的一种或多种核酸分子,包括单一载体或单独载体中的此类一个或多个核酸分子,以及存在于宿主细胞中的一个或多个位置处的此类一个或多个核酸分子。如本文所用,术语“核酸构建体”、“质粒”和“载体”是等同的,并且指用于将诸如DNA或RNA的乘客核酸序列转移至宿主细胞中的核酸分子。
如本文所用,术语“宿主细胞”旨在包括可以是或已经是载体、外源性核酸分子和编码本发明抗体构建体的多核苷酸的任何个体细胞或细胞培养物;和/或抗体构建体本身的受体。可通过转化、转染等方式将相应材料引入细胞。术语“宿主细胞”还旨在包括单个细胞的后代或可能后代。宿主细胞包括例如细菌、微生物、植物和动物细胞。
如本文所用,“免疫细胞”指与先天性免疫和适应性免疫相关的细胞,例如,比如来源于骨髓中产生的造血干细胞(HSC)的白血细胞(白细胞)、淋巴细胞(T细胞、B细胞、自然杀伤(NK)细胞和自然杀伤T细胞(NKT)和髓系来源的细胞(中性粒细胞、嗜酸性细胞、嗜碱性细胞、单核细胞、巨噬细胞、树突状细胞)。特别地,免疫细胞可以在包含B细胞、T细胞、特别是CD4+ T细胞和CD8+ T细胞、NK细胞、NKT细胞、APC细胞、树突状细胞和单核细胞的非详尽性列表中选择。如本文所用,“T细胞”包括例如CD4+ T细胞、CD8+ T细胞、T辅助1型T细胞、T辅助2型T细胞、T辅助17型T细胞和抑制性T细胞。
如本文所用,术语“T效应细胞”、“T eff”或“效应细胞”描述了一组免疫细胞,其包括若干种对刺激(例如共刺激)积极应答的T细胞类型。其特别包括具有消除抗原功能的T细胞(例如,通过产生调节其他细胞激活的细胞因子或通过细胞毒性活性)。其尤其包括CD4+、CD8+、Treg细胞、细胞毒性T细胞和辅助性T细胞(Th1和Th2)。
如本文所用,术语“调节性T细胞”、“Treg细胞”或“Treg”指调节免疫系统、维持对自身抗原的耐受性和预防自身免疫疾病的T细胞亚群体。Treg具有免疫抑制作用,通常抑制或下调效应T细胞的诱导和增殖。Treg表达生物标志物CD4、FOXP3和CD25,并且被认为来源于与初始CD4细胞相同的谱系。
术语“耗竭T细胞”指处于功能障碍状态(即“耗竭”)的T细胞群体。T细胞耗竭通过功能的逐渐丧失、转录谱的变化和抑制性受体的持续表达来表征。耗竭T细胞失去其细胞因子产生能力、其高增殖能力和其细胞毒性潜力,最终导致其缺失。耗竭T细胞通常指示较高的CD43、CD69和抑制性受体水平与较低的CD62L和CD127表达的组合。
术语“免疫应答”指例如淋巴细胞、抗原呈递细胞、吞噬细胞、粒细胞和由以上细胞或肝脏产生的可溶性大分子(包括抗体、细胞因子和补体)对侵入病原体、感染病原体的细胞或组织、癌细胞或在自身免疫性或病理性炎症的情况下正常人类细胞或组织进行选择性损害、破坏或使其从人体消除的作用。
如本文所用,术语“拮抗剂”指阻断或降低另一种物质的活性或功能的物质。特别地,该术语指作为参考物质(例如,PD-L1和/或PD-L2)的细胞受体(例如,PD-1)结合的抗体,阻止其产生全部或部分通常的生物学效应(例如,建立免疫抑制性微环境)。可以通过竞争性ELISA评估根据本发明所述的抗体的拮抗剂活性。
如本文所用,术语“分离的”表示所述材料(例如,抗体、多肽、核酸等)与其在自然界中一起存在的其他材料基本上分离或相对于其他材料富集。特别地,“分离的”抗体是一种已经从自然环境的组分鉴别出并分离和/或回收的抗体。例如,分离的抗体被纯化(1)通过Lowry法测定的大于75%的抗体重量,或(2)在还原或非还原条件下通过SDS-PAGE纯化。分离的抗体包括重组细胞内的原位抗体,因为将不存在抗体自然环境的至少一种组分。然而,通常分离的抗体将通过至少一个纯化步骤来制备。
如本文所用,术语“和/或”将被视为两个特定特征或组分中的每一个的具体公开,其中包含或不包含另一个。例如,“A和/或BA将被视为(i)A、(ii)B和(iii)A和B中的每一个的具体公开,就好像每一个都是单独列出的一样。
术语“一个/一种(a/an)”可以指其修饰的要素中的一个或多个(例如,“一种试剂”可以表示一种或多种试剂),除非上下文清楚地描述了要素的一个或多个要素。
如本文所用,联合任何和所有值(包括数值范围的下限和上限)的术语“约”指具有高达+/-10%偏差的可接受范围的任何值(例如,+/-0.5%、+/-1%、+/-1.5%、+/-2%、+/-2.5%、+/-3%、+/-3.5%、+/-4%、+/-4.5%、+/-5%、+/-5.5%、+/-6%、+/-6.5%、+/-7%、+/-7.5%、+/-8%、+/-8.5%、+/-9%、+/-9.5%)。在一串值开头的术语“约”的使用修饰所述值的每一个(即,“约1、2和3”指约1、约2和约3)。此外,当本文所述的是值的列表(例如,约50%、60%、70%、80%、85%或86%)使,所述列表包括其所有中间值和分数值(例如,54%、85.4%)。
抗PD-1抗体
根据本发明所述的双功能分子包含第一实体,所述第一实体包含抗hPD-1抗体或其抗原结合片段。
本文提供了一种特别结合至人PD-1的抗体。在一些方面中,所述抗体与人PD-1(优选地与人PD-1的胞外结构域)特异性地结合。在一些方面中,所述抗体与全长人PD-1、PD-1Aex2、PD-1Aex3、PD-1Aex2,3和PD-1Aex2,3,4的一个或多个选择性地结合。
在一些方面中,所述抗PD1抗体是分离的抗体,特别是非天然的分离的抗体。此类分离的抗PD1抗体可以通过至少一个纯化步骤制备。在一些实施方式中,所述分离的抗PD1抗体纯化至以重量计至少80%、85%、90%、95%或99%。在一些实施方式中,分离的抗PD1抗体以包含以重量计至少85%、90%、95%、98%、99%至100%抗体的溶液提供,所述重量的其余部分包含溶解在溶剂中的其他溶质的重量。
优选地,此类抗体具有阻断或抑制PD-1与至少一种其配体(例如,PD-L1和/或PD-L2)之间的相互作用。如本文所用,“阻断结合”或“阻断相互作用”或“抑制相互作用”的能力指抗体或抗原结合片段阻止两个分子(例如,PD-1和其配体PD-L1和/或PD-L2)之间的结合相互作用至任何可检测程度的能力。
优选地,所述抗PD1抗体或其抗原结合片段是人PD-L1和/或PD-L2结合至人PD-1的拮抗剂,更优选地人PD-L1和PD-L2结合至PD-1的拮抗剂。
在某些实施方式中,所述抗hPD1抗体或其抗原结合片段抑制PD-1和至少一种其配体(例如,PD-L1和/或PD-L2,优选地PD-L1和PD-L2)之间的结合相互作用至少50%。在某些实施方式中,该抑制可以大于60%、大于70%、大于80%或大于90%。
根据本发明所述的抗hPD1抗体可以包含任何类别的免疫球蛋白(例如IgD、IgE、IgG、IgA或IgM(或其亚类)),包含来源于靶向人PD-1的非人(例如,小鼠)免疫球蛋白的最小序列的免疫球蛋白链或其片段(例如Fv、Fab、Fab'、F(ab')2、scFv或抗体的其他抗原结合子序列)。优选地,根据本发明所述的抗hPD-1抗体来源于IgG1、IgG2、IgG3或IgG4,优选地来源于IgG4或IgG1。
在一个实施方式中,所述抗体的抗原结合片段包含重链,其包含重链可变结构域,所述重链可变结构域包含HCDR1、HCDR2和HCDR3;和轻链,其包含轻链可变结构域,所述轻链可变结构域包含LCDR1、LCDR2和LCDR3;和重链恒定结构域的片段。通过重链恒定结构域的片段,应理解所述抗原结合片段因此包含完整重链恒定结构域中的至少一部分。例如,重链恒定结构域可以包含以下或由以下组成:至少重链的CH1结构域,或至少重链的CH1和CH2结构域,或至少重链的至CH1、CH2和CH3结构域。重链恒定结构域的片段也可定义为包含所述重链的Fc结构域中的至少一部分。因此,抗体的抗原结合片段涵盖完整抗体的Fab部分、完整抗体的F(ab’)2部分、完整抗体的Fab’部分。所述重链恒定结构域还可以包含完整重链恒定结构域或由完整重链恒定结构域组成,例如在本说明书中说明的,其中描述了几个完整重链恒定结构域。在本发明的特别的实施方式中,并且当抗体的抗原结合片段包含重链恒定结构域的片段(所述片段包含完整重链恒定结构域中的一部分或存在于完整重链恒定结构域中的一部分中)时,所述重链恒定结构域片段可由至少10个氨基酸残基组成;或可由10至300个氨基酸残基、特别是210个氨基酸残基组成。
优选地,针对人PD-1的抗体是单克隆抗体。如本文所用,术语“单克隆抗体”是指从基本上同质的抗体群体中获得的抗体,即构成群体的个体抗体是相同的和/或结合相同的表位。优选地,此类单克隆抗体(mAb)来自哺乳动物,例如小鼠、啮齿动物、兔、山羊、灵长类动物、非人灵长类动物或人。制备此类单克隆抗体的技术可以在例如Stites等(编著),BASIC AND CLINICAL IMMUNOLOGY(第4版),Lange Medical Publications,Los Altos,CA,以及其中引用的参考文献;Harlow和Lane(1988),ANTIBODIES:ALABORATORY MANUAL CSHPress;Goding(1986)MONOCLONAL ANTIBODIES:PRINCIPLES AND PRACTICE(第2版),Academic Press,New York,NY中找到。
在某些实施方式中,本文提供的抗hPD1抗体是嵌合抗体。在一个实施例中,所述嵌合抗体包含非人可变区(例如,源自小鼠、大鼠、仓鼠、兔或非人灵长类动物(例如猴)的可变区)和人恒定区。在另一个实施例中,所述嵌合抗体是“类别转换”抗体,其中类别或亚类已从亲本抗体的类别或亚类改变。所述嵌合抗体包括其抗原结合片段。
在某些实施方式中,所述抗hPD1抗体是人源化抗体。人源化抗体通常包含一个或多个可变结构域,其中CDR(或其部分)来源于非人抗体,并且FR(或其部分)来源于人或人源化抗体序列。或者,可以替换一些FR残基以恢复或改善抗体特异性、亲和力和/或人源化。人源化抗体任选地还将包含人或人源化恒定区(Fc)中的至少一部分。抗体人源化的方法是本领域中众所周知的,参见例如Winter和Milstein,Nature,1991,349:293-299;Riechmann等,Nature,332,第323页(1988);Verhoeyen等,Science,239,第1534页(1988),Rader等,Proc.Nat.Acad.Sci.U.S.A.,1998,95:8910-8915;Steinberger等,J.Biol.Chem.,2000,275:36073-36078;Queen等,Proc.Natl.Acad.Sci.U.S.A.,1989,86:10029-10033;Almagro,J.C.和Fransson,J.,Front.Biosci.13(2008)1619-1633;Kashmiri,S.V.等,Methods 36(2005)25-34(描述SDR(a-CDR)移植);Padlan,E.A.,Mol.Immunol.28(1991)489-498(描述“表面重塑”);Dall’Acqua,W.F.等,Methods 36(2005)43-60(描述“FR重排”);和Osbourn,J.等,Methods 36(2005)61-68;和Klimka,A.等,Br.J.Cancer 83(2000)252-260(描述FR重排的“引导选择”方法);和美国专利号5,585,089,5,693,761,5,693,762,5,821,337、,7,527,791,6,982,321,和7,087,409;和6,180,370。
优选地,针对人PD-1的所述人源化抗体是单克隆抗体。
特别地,人源化抗体是具有至少80%或至少85%、更优选地至少88%、甚至更优选地至少90%的T20人源化评分,最优选地包含在85%和95%之间、优选地在88%和92%之间的T20人源化评分的人源化抗体。
如Gao S H、Huang K、Tu H、Adler A S.,BMC Biotechnology 2013:13:55中所述,通常使用T20评分分析仪来测量“人源化”以定量单克隆抗体可变区的人源化。T20人源化评分是抗体人源化领域中常用的参数,其由Gao等(BMC Biotechnol.,2013,13,55)首先公开。T20人源化评分通常用于在专利申请(例如,WO15161311、WO17127664、WO18136626、WO18190719、WO19060750或WO19170677)中定义人源化抗体的专利申请。
提供基于网络的工具,使用T20截止值人数据库http://abAnalyzer.lakepharma.com计算抗体序列的T20评分。在计算T20评分的过程中,首先给输入VH、VK或VL可变区蛋白序列分配Kabat编号,并鉴定CDR残基。使用blastp蛋白-蛋白BLAST算法比较全长序列或仅框架序列(已除去CDR残基)与相应抗体数据库中的每个序列。分离各配对比较之间的序列同一性,并在分析完数据库中的每个序列之后,基于与输入序列的序列同一性将序列从高到低排序。对前20个匹配序列的同一性百分比取平均值,以获得T20评分。
对于“全人类数据库”中的每种链类型(VH、VK、VL)和序列长度(全长或仅框架),使用T20评分分析仪用各抗体序列的相应数据库对其进行评分。在排除输入序列本身之后获得前20个匹配序列的T20评分(因为序列1始终是输入抗体本身,所以对序列2至21的同一性百分比取平均值)。将各组的T20评分从高到低排序。对于大部分序列而言,评分减少大致上是线性的;然而,最后~15%抗体的T20评分开始急剧下降。因此,除去最后15%的序列,并使剩余序列形成T20截止值人数据库,其中T20评分截止值表明在新数据库中序列的最低T20评分。
因此,包含于所述双功能分子中的根据本发明所述的人源化抗PD1抗体具有至少80%或至少85%、更优选地至少88%、甚至更优选地至少90%的T20人源化评分,最优选地介于85%与95%之间、优选地88%与92%之间的T20人源化评分。
在一个实施方式中,所述抗PD1抗体可以选自派姆单抗(也称为Keytruda兰博利珠单抗,MK-3475),纳武单抗(Opdivo,MDX-1106,BMS-936558,ONO-4538),匹地利珠单抗(CT-011),西米普利单抗(Libtayo),西米普利单抗,AUNP12,AMP-224,AGEN-2034,BGB-A317(替雷利珠单抗),PDR001(斯帕利珠单抗),MK-3477,SCH-900475,PF-06801591,JNJ-63723283,吉诺珠单抗(CBT-501),LZM-009,BCD-100,SHR-1201,BAT-1306,AK-103(HX-008),MEDI-0680(也称为AMP-514)MEDI0608,JS001(参见Si-Yang Liu等,J.Hematol.Oncol.10:136(2017)),BI-754091,CBT-501,INCSHR1210(也称为SHR-1210),TSR-042(也称为ANB011),GLS-010(也称为WBP3055),AM-0001(Armo),STI-1110(参见WO 2014/194302),AGEN2034(参见WO 2017/040790),MGA012(参见WO 2017/19846),或IBI308(参见WO 2017/024465、WO2017/025016、WO 2017/132825和WO 2017/133540),描述于WO 2006/121168中的单克隆抗体5C4、17D8、2D3、4H1、4A11、7D3和5F4。还已知靶向PD-1的双功能或双特异性分子,例如RG7769(Roche)、mAb20717(Xencor)、MEDI5752(AstraZeneca)、FS118(F-star)、SL-279252(Takeda)和mAb23104(Xencor)
在一个特定的实施方式中,所述抗PD1抗体可以是派姆单抗(也称为Keytruda兰博利珠单抗,MK-3475)或纳武单抗(Opdivo,MDX-1106,BMS-936558,ONO-4538)。
人源化抗hPD1抗体的一个具体实例在下文中通过其CDR、框架区以及Fc和铰链区来描述。
CDR
“互补决定区”或“CDR”是本领域公知的,指抗体可变区内氨基酸的不连续序列,其赋予抗原特异性和结合亲和性。给定CDR的准确氨基酸序列边界使用多种众所周知方案的任何一种能够容易地确定,包括Kabat等,(Sequences of Proteins of ImmunologicalInterest第5版(1991)“Kabat”编号方案);Al-Lazikani等,1997,J.Mol.Biol,273:927-948(“Chothia”编号方案);MacCallum等,1996,J.Mol.Biol.262:732-745(“Contact”编号方案);Lefranc等,Dev.Comp.Immunol.,2003,27:55-77(“IMGT”编号方案);和Honegge和Pluckthun,J.Mol.Biol,2001,309:657-70(“AHo”编号方案)所述的那些。除非另有说明,否则用于标识本文中特定CDR的编号方案是Kabat编号方案。
在一个实施方式中,所述双功能分子包含人源化抗hPD-1抗体或其抗原结合片段。所述人源化抗体的CDR区可来源于小鼠抗体并且已经优化以i)提供具有非常高的人源化水平(优于85%)的安全人源化抗体;并ii)提高抗体特性,尤其是在哺乳动物细胞中生产时更高的可制备性和在哺乳动物细胞(例如COS和HCO细胞)中的更高的产量,同时保留拮抗剂活性(即对人PD-L1与人PD-1结合的抑制),因为它们对人PD-1的结合亲和力(KD)小于10-7M,优选地小于10-8M。
在一个非常特别的实施方式中,所述双功能分子包含抗人PD-1抗体或其抗原结合片段,优选地包含以下的人源化抗人PD-1抗体或其抗原结合片段:
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域,和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域,
其中:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:3的氨基酸序列或由SEQ ID NO:3的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E;任选地具有一个、两个或三个选自SEQ ID NO:3的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR1(LCDR1)包含SEQ ID NO:12的氨基酸序列或由SEQ ID NO:12的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:12的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰任何组合;和
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在一个方面,所述双功能分子包含人源化抗hPD-1抗体或其抗原结合片段,其包含
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域,和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域,
其中:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:3的氨基酸序列或由SEQ ID NO:3的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E;任选地具有一个、两个或三个选自SEQ ID NO:3的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR1(LCDR1)包含SEQ ID NO:12的氨基酸序列或由SEQ ID NO:12的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:12的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰任何组合;和
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在另一个实施方式中,所述双功能分子包含人源化抗hPD-1抗体或其抗原结合片段,其包含
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域,和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域,
其中:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:4、5、6、7、8、9、10或11的氨基酸序列或由SEQ ID NO:4、5、6、7、8、9、10或11的氨基酸序列组成,任选地具有一个、两个或三个选自SEQID NO:4、5、6、7、8、9、10或11的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
-所述轻链CDR1(LCDR1)包含SEQ ID NO:13或SEQ ID NO:14的氨基酸序列或由SEQID NO:13或SEQ ID NO:14的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ IDNO:13或SEQ ID NO:14的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在另一个方面,所述双功能分子包含人源化抗hPD-1抗体或其抗原结合片段,其包含:
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域(VH),和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域(VL),
其中:
(a)所述轻链CDR1(LCDR1)包含SEQ ID NO:13的氨基酸序列或由SEQ ID NO:13的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:13的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(b)所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰任何组合;
(c)所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(d)所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(e)所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
(f)所述重链CDR3(HCDR3)包含SEQ ID NO:4的氨基酸序列或由SEQ ID NO:4的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:4的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:5的氨基酸序列或由SEQ ID NO:5的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:5的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:6的氨基酸序列或由SEQ ID NO:6的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:6的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:7的氨基酸序列或由SEQ ID NO:7的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:7的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:8的氨基酸序列或由SEQ ID NO:8的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:8的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:9的氨基酸序列或由SEQ ID NO:9的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:9的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:10的氨基酸序列或由SEQ ID NO:10的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:10的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:11的氨基酸序列或由SEQ ID NO:11的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:11的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在另一个方面,所述双功能分子包含人源化抗hPD-1抗体或其抗原结合片段,其包含:
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域(VH),和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域(VL),
其中:
(a)所述轻链CDR1(LCDR1)包含SEQ ID NO:14的氨基酸序列或由SEQ ID NO:14的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:14的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(b)所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(c)所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(d)所述重链CDR1(LCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(e)所述重链CDR2(LCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
(f)所述重链CDR3(LCDR3)包含SEQ ID NO:4的氨基酸序列或由SEQ ID NO:4的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:4的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:5的氨基酸序列或由SEQ ID NO:5的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:5的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:6的氨基酸序列或由SEQ ID NO:6的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:6的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:7的氨基酸序列或由SEQ ID NO:7的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:7的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:8的氨基酸序列或由SEQ ID NO:8的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:8的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:9的氨基酸序列或由SEQ ID NO:9的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:9的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:10的氨基酸序列或由SEQ ID NO:10的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:10的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
-所述重链CDR3(HCDR3)包含SEQ ID NO:11的氨基酸序列或由SEQ ID NO:11的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:11的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在特别的方面中,所述修饰是置换,特别是保守置换。
在一个实施方式中,所述抗人PD-1抗体或其抗原结合片段包含以下:(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:3的CDR3,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;和(ii)轻链,其包含SEQ ID NO:12的CDR1(其中X是G或T)、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3。
在一个实施方式中,所述抗人PD-1抗体或其抗原结合片段包含以下:(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:3的CDR3,其中X1是D,并且X2选自T、H、A、Y、N和E,优选地选自H、A、Y、N和E;或其中X1是E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E和S;和(ii)轻链,其包含SEQ ID NO:12的CDR1(其中X是G或T)、SEQ IDNO:15的CDR2和SEQ ID NO:16的CDR3。
在一个实施方式中,所述抗人PD-1抗体或其抗原结合片段包含以下:(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:3的CDR3,其中X1是D,并且X2选自T、H、A、Y、N和E,优选地选自H、A、Y、N和E;和(ii)轻链,其包含SEQ ID NO:12的CDR1(其中X是G或T)、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3。
在一个实施方式中,所述抗人PD-1抗体或其抗原结合片段包含以下:(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:3的CDR3,其中X1是E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E和S;和(ii)轻链,其包含SEQ ID NO:12的CDRl(其中X是G或T)、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3。
在另一个实施方式中,所述抗人PD-1抗体或其抗原结合片段包含以下或基本上由以下组成:(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:4、5、6、7、8、9、10或11的CDR3;和(ii)轻链,其包含SEQ ID NO:13或SEQ ID NO:14的CDR1、SEQ IDNO:15的CDR2和SEQ ID NO:16的CDR3。
在另一个实施方式中,所述抗人PD-1抗体或其抗原结合片段包含以下或基本上由以下组成:
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:4的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:5的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:6的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:7的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:8的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:9的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:10的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:11的CDR3;和(ii)轻链,其包含SEQ ID NO:13的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
在另一个实施方式中,所述抗人PD-1抗体或其抗原结合片段基本上包含以下或由以下组成:
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:4的CDR3;和(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:5的CDR3;和(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:6的CDR3;和(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:7的CDR3;(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:8的CDR3;和(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:9的CDR3;和(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:10的CDR3;和(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3;或者
(i)重链,其包含SEQ ID NO:1的CDR1、SEQ ID NO:2的CDR2和SEQ ID NO:11的CDR3;和(ii)轻链,其包含SEQ ID NO:14的CDR1、SEQ ID NO:15的CDR2和SEQ ID NO:16的CDR3。
框架
在一个实施方式中,根据本发明所述的抗PD1抗体或抗原结合片段包含框架区,特别是重链可变区框架区(HER)HFR1、HFR2、HFR3和HFR4,以及轻链可变区框架区(LFR)LFR1、LFR2、LFR3和LFR4。
优选地,根据本发明所述的抗PD1抗体或抗原结合片段包含人或人源化框架区。出于本文目的的“人受体框架”是包含来源于如以下所定义的人免疫球蛋白框架或人共有框架的轻链可变结构域(VL)框架或重链可变结构域(VH)框架的氨基酸序列的框架。来源于人免疫球蛋白框架或人共有框架的人受体框架可以包含其相同氨基酸序列,或其可以包含氨基酸序列变化。在一些实施方式中,氨基酸变化的数量是10个或更少、9个或更少、8个或更少、7个或更少、6个或更少、5个或更少、4个或更少、3个或更少或者2个或更少。在一些实施方式中,VL受体人框架在序列上等同于VL人免疫球蛋白框架序列或人共有框架序列。“人共有框架”是代表一系列人免疫球蛋白VL或VH框架序列中最常出现的氨基酸残基的框架。
特别地,所述抗PD1抗体或抗原结合片段包含重链可变区框架区(HFR)HFR1、HFR2、HFR3和HFR4,其分别包含SEQ ID NO:41、42、43和44的氨基酸序列,其任选地具有一个、两个或三个选自HFR3(即,SEQ ID NO:43)的位置27、29和32之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。优选地,所述抗PD1抗体或抗原结合片段包含SEQ ID NO:41的HFR1、SEQ ID NO:42的HFR2、SEQ ID NO:43的HFR3和SEQ IDNO:44的HFR4。
替代地或另外地,所述抗PD1抗体或抗原结合片段包含轻链可变区框架区(LFR)LFR1、LFR2、LFR3和LFR4,其分别包含SEQ ID NO:45、46、47和48的氨基酸序列,其任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。优选地,人源化抗PD1抗体或抗原结合片段包含SEQ ID NO:45的LFR1、SEQ ID NO:46的LFR2、SEQ ID NO:47的LFR3和SEQ ID NO:48的LFR4。
VH-VL
根据本发明所述的抗hPD1抗体的VL和VH结构域可以包含被三个互补决定区中断的四个框架区,优选按以下顺序可操作地连接:FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4(从氨基末端到羧基末端)。
在第一实施方式中,包含于双功能分子中的抗人PD-1人源化抗体或其抗原结合片段包含:
(a)重链可变区(VH),其包含SEQ ID NO:17的氨基酸序列或由SEQ ID NO:17的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;其任选地具有一个、两个或三个选自SEQ ID NO:17的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(b)轻链可变区(VL),其包含SEQ ID NO:26的氨基酸序列或由SEQ ID NO:26的氨基酸序列组成,其中X是G或T,其任选地具有一个、两个或三个选自SEQ ID NO:26的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在第二实施方式中,包含于所述双功能分子中的所述抗人PD-1人源化抗体或其抗原结合片段包含:
(a)重链可变区(VH),其包含SEQ ID NO:17的氨基酸序列或由SEQ ID NO:17的氨基酸序列组成,其中X1是D,并且X2选自T、H、A、Y、N,E,优选地选自H、A、Y、N、E;或者X1是E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E和S;任选地具有一个、两个或三个选自SEQ ID NO:17的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(b)轻链可变区(VL),其包含SEQ ID NO:26的氨基酸序列或由SEQ ID NO:26的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:26的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在第三实施方式中,包含于所述双功能分子中的所述抗人PD-1人源化抗体或其抗原结合片段包含:
(a)重链可变区(VH),其包含SEQ ID NO:17的氨基酸序列或由SEQ ID NO:17的氨基酸序列组成,其中X1是D,并且X2选自T、H、A、Y、N,E,优选地选自H、A、Y、N、E;任选地具有一个、两个或三个选自SEQ ID NO:17的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(b)轻链可变区(VL),其包含SEQ ID NO:26的氨基酸序列或由SEQ ID NO:26的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:26的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在另一个实施方式中,包含于所述双功能分子中的所述抗人PD-1人源化抗体或其抗原结合片段包含:
(a)重链可变区(VH),其包含SEQ ID NO:17的氨基酸序列或由SEQ ID NO:17的氨基酸序列组成,其中X1是E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E和S,任选地具有一个、两个或三个选自SEQ ID NO:17的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(b)轻链可变区(VL),其包含SEQ ID NO:26的氨基酸序列或由SEQ ID NO:26的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:26的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在另一个实施方式中,包含于所述双功能分子中的所述抗人PD-1人源化抗体或其抗原结合片段包含:
(a)重链可变区(VH),其包含SEQ ID NO:18、19、20、21、22、23、24或25的氨基酸序列或由SEQ ID NO:18、19、20、21、22、23、24或25的氨基酸序列组成,任选地具有一个、两个或三个分别选自SEQ ID NO:18、19、20、21、22、23、24或25的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(b)轻链可变区(VL),其包含SEQ ID NO:27或SEQ ID NO:28的氨基酸序列或由SEQID NO:27或SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ IDNO:27或SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在另一个实施方式中,包含于所述双功能分子中的所述抗人PD-1人源化抗体或其抗原结合片段包含:
(a)重链可变区(VH),其包含SEQ ID NO:18的氨基酸序列或由SEQ ID NO:18,任选地具有一个、两个或三个选自SEQ ID NO:18的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:19的氨基酸序列或由SEQ ID NO:19,任选地具有一个、两个或三个选自SEQ ID NO:19的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:20的氨基酸序列或由SEQ ID NO:20,任选地具有一个、两个或三个选自SEQ ID NO:20的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:21的氨基酸序列或由SEQ ID NO:21,任选地具有一个、两个或三个选自SEQ ID NO:21的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:22的氨基酸序列或由SEQ ID NO:22,任选地具有一个、两个或三个选自SEQ ID NO:22的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:23的氨基酸序列或由SEQ ID NO:23,任选地具有一个、两个或三个选自SEQ ID NO:23的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:24的氨基酸序列或由SEQ ID NO:24,任选地具有一个、两个或三个选自SEQ ID NO:24的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:25的氨基酸序列或由SEQ ID NO:25的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:25的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:27的氨基酸序列或由SEQ ID NO:27的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:27的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:18的氨基酸序列或由SEQ ID NO:18的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:18的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:19的氨基酸序列或由SEQ ID NO:19的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:19的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:20的氨基酸序列或由SEQ ID NO:20的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:20的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:21的氨基酸序列或由SEQ ID NO:21的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:21的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:22的氨基酸序列或由SEQ ID NO:22的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:22的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:23的氨基酸序列或由SEQ ID NO:23的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:23的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:24的氨基酸序列或由SEQ ID NO:24的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:24的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链可变区(VH),其包含SEQ ID NO:25的氨基酸序列或由SEQ ID NO:25的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:25的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在特别的方面中,所述修饰是置换,特别是保守置换。
CH-CL
在一个实施方式中,所述重链(CH)和轻链(CL)包含如上所述的VL和VH序列。
在特别的实施方式中,包含于所述双功能分子中的所述抗人PD-1抗体或其抗原结合片段包含:
(a)重链,其包含选自SEQ ID NO:29、30、31、32、33、34、35或36的氨基酸序列或由选自SEQ ID NO:29、30、31、32、33、34、35或36的氨基酸序列组成,任选地具有一个、两个或三个分别选自SEQ ID NO:29、30、31、32、33、34、35或36的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和
(b)轻链,其包含SEQ ID NO:37或SEQ ID NO:38的氨基酸序列或由SEQ ID NO:37或SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:37或SEQID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
在另一个实施方式中,包含于所述双功能分子中的所述抗人PD-1人源化抗体或其抗原结合片段包含:
(a)重链,其包含选自SEQ ID NO:29的氨基酸序列或由选自SEQ ID NO:29的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:29的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:30的氨基酸序列或由选自SEQ ID NO:30的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:30的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:31的氨基酸序列或由选自SEQ ID NO:31的氨基酸序列组成,其任选地具有一个、两个或三个选自SEQ ID NO:31的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,其任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:32的氨基酸序列或由选自SEQ ID NO:32的氨基酸序列组成,其任选地具有一个、两个或三个选自SEQ ID NO:32的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,其任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(a)重链,其包含选自SEQ ID NO:33的氨基酸序列或由选自SEQ ID NO:33的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:33的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:34的氨基酸序列或由选自SEQ ID NO:34的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:34的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:35的氨基酸序列或由选自SEQ ID NO:35的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:35的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:36的氨基酸序列或由选自SEQ ID NO:36的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:36的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:37的氨基酸序列或由SEQ ID NO:37的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:37的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:29的氨基酸序列或由选自SEQ ID NO:29的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:29的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:30的氨基酸序列或由选自SEQ ID NO:30的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:30的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、SEQ IDNO:38的33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:31的氨基酸序列或由选自SEQ ID NO:31的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:31的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:32的氨基酸序列或由选自SEQ ID NO:32的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:32的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:33的氨基酸序列或由选自SEQ ID NO:33的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:33的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:34的氨基酸序列或由选自SEQ ID NO:34的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:34的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:35的氨基酸序列或由选自SEQ ID NO:35的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:35的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;或者
(a)重链,其包含选自SEQ ID NO:36的氨基酸序列或由选自SEQ ID NO:36的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:36的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)轻链,其包含SEQ ID NO:38的氨基酸序列或由SEQ ID NO:38的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:38的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰。
优选地,所述修饰是置换,特别是保守置换。
Fc和铰链区
几项开发治疗性抗体的研究导致对Fc区进行工程化,以优化抗体特性,从而生成更适合其所需药理学活性的分子。抗体的Fc区介导其血清半衰期和效应功能,如补体依赖性细胞毒性(CDC)、抗体依赖性细胞的细胞毒性(ADCC)和抗体依赖性细胞的吞噬作用(ADCP)。位于CH2和CH3结构域之间的界面上的若干突变,如T250Q/M428L,和M252Y/S254T/T256E+H433K/N434F,已显示增加与FcRn结合的亲和性并增加IgG1在体内的半衰期。然而,增加FcRn结合与改善半衰期之间未必总是直接相关。改善治疗性抗体的有效性的一种方法是增加其血清持久性,从而允许更高的循环水平、减少施用频率和降低剂量。工程化Fc区可能是所需的,以降低或增加抗体的效应功能。对于靶向细胞表面分子(特别是免疫细胞上的那些)的抗体,需要消除效应功能。而相反的是,对于意欲用于肿瘤学用途的抗体,增加效应功能可改善治疗活性。四种人IgG同种型以不同亲和性结合激活Fcγ受体(FcγRI、FcγRIIa、FcγRIIIa)、抑制性FcγRIIb受体和补体的第一组分(C1q),产生极为不同的效应功能。IgG与FcγR或C1q的结合取决于位于铰链区和CH2结构域中的残基。CH2结构域的两个区对于FcγR和C1q结合而言是关键的,并在IgG2和IgG4中具有独特序列。
根据本发明所述的抗体任选地包含免疫球蛋白恒定区(Fc)、通常是哺乳动物免疫球蛋白的免疫球蛋白恒定区、甚至更优选地人或人源化免疫球蛋白的免疫球蛋白恒定区中的至少一部分。优选地,Fc区是本文所述的抗hPD-1抗体中的一部分。包含于本发明所述的双功能分子中的所述抗hPD1抗体或其抗原结合片段可包含免疫球蛋白的恒定区,或所述恒定区的片段、类似物、变体、突变体或衍生物。正如本领域技术人员所熟知的,重链恒定结构域的IgG同种型的选择集中在是否需要特定功能以及是否需要适宜的体内半衰期。例如,为选择性根除癌细胞而设计的抗体通常需要活性同种型,该同种型允许补体激活和通过抗体依赖性细胞介导的细胞毒性作用介导的效应物介导的细胞杀伤。人IgG1和IgG3(半衰期更短)同种型两者符合这些标准,特别是人IgG1同种型(野生型和变体)。特别地,取决于重链恒定结构域的IgG同种型(特别是人野生型和变体IgG1同种型),本发明所述的抗hPD1抗体可以通过CDC、ADCC和/或ADCP机制对表达PD-1的细胞是细胞毒性的。实际上,可结晶片段(Fc)区与多种辅助分子相互作用,以介导间接效应功能,如抗体依赖性细胞的细胞毒性(ADCC)、抗体依赖性细胞的吞噬作用(ADCP)和补体依赖性细胞毒性(CDC)。
在优选的实施方式中,所述恒定区来源于人免疫球蛋白重链,例如,例如,IgG1、IgG2、IgG3、IgG4或其他类别。在一个进一步的方面中,所述人恒定区选自以下:IgG1、IgG2、IgG2、IgG3和IgG4。优选地,所述抗PD1抗体包含IgG1或IgG4 Fc区。甚至更优选地,所述抗hPD1抗体包含IgG4 Fc区,其具有稳定所述IgG4的S228P。
在一个实施方式中,所述抗PD1抗体包含截短的Fc区或Fc区的片段。在一个实施方式中,所述恒定区包含CH2结构域。在另一个实施方式中,所述恒定区包含CH2和CH3结构域或包含铰链-CH2-CH3。或者,恒定区可以包含铰链区、CH2结构域和/或CH3结构域的全部或一部分。在一个优选的实施方式中,所述恒定区包含来源于人IgG4重链的CH2和/或CH3结构域。在一些实施方式中,所述恒定区包含来源于人IgG4重链的CH2和/或CH3结构域。
在另一个实施方式中,所述恒定区包含CH2结构域和铰链区的至少一部分。铰链区可以来源于免疫球蛋白重链,例如,IgG1、IgG2、IgG3、IgG4或其他类别。优选地,铰链区来源于人IgG1、IgG2、IgG3、IgG4或其他适宜类别,突变的或未突变的。更优选地,铰链区来源于人IgG1重链。在一个实施方式中,所述恒定区包含来源于第一抗体同种型的CH2结构域和来源于第二抗体同种型的铰链区。在一个特定实施方式中,CH2结构域来源于人IgG2或IgG4重链,而铰链区来源于改变的人IgG1重链。
在一个实施方式中,所述恒定区含有降低对Fc受体的亲和性减少Fc效应功能的突变。例如,恒定区可以含有消除IgG重链恒定区内的糖基化位点的突变。
在另一个实施方式中,所述恒定区包含CH2结构域和铰链区的至少一部分。铰链区可以来源于免疫球蛋白重链,例如,IgG1、IgG2、IgG3、IgG4或其他类别。优选地,铰链区来源于人IgG1、IgG2、IgG3、IgG4或其他适宜类别。IgG1铰链区具有三个半胱氨酸,其中两个参与免疫球蛋白两条重链之间的二硫键。这些相同的半胱氨酸允许在Fc部分之间形成有效且一致的二硫键。因此,本发明的优选铰链区来源于IgG1,更优选地,来源于人IgG1。在一些实施方式中,人IgG1铰链区内的第一半胱氨酸突变成另一氨基酸,优选丝氨酸。IgG2同种型铰链区具有四个二硫键,在重组系统的分泌过程中,这些二硫键往往会促进寡聚化和可能不正确的二硫键。适宜的铰链区可以来源于IgG2铰链;前两个半胱氨酸各自优选突变为另一种氨基酸。已知IgG4的铰链区无法有效地形成链间二硫键。然而,针对本发明的适宜的铰链区可以来源于IgG4铰链区,优选地含有增强来源于重链的部分之间的二硫键的正确形成的突变(Angal S,等,(1993)Mol.Immunol.,30:105-8)。更优选地,铰链区来源于人IgG4重链。
在一个实施方式中,所述恒定区包含来源于第一抗体同种型的CH2结构域和来源于第二抗体同种型的铰链区。在一个特定实施方式中,CH2结构域来源于人IgG4重链,而铰链区来源于改变的人IgG1重链。
根据本发明,恒定区可以含有CH2和/或CH3结构域和铰链区,其来源于不同抗体同种型,即,杂交恒定区。例如,在一个实施方式中,所述恒定区含有来源于IgG2或IgG4的CH2和/或CH3结构域和来源于IgG1的突变铰链区。或者,将来自另一IgG亚类的突变铰链区用于杂交恒定区中。例如,可以使用允许两个重链之间有效二硫键键合的IgG4铰链的突变形式。突变铰链还可以来源于IgG2铰链,其中前两个半胱氨酸各突变成另一氨基酸。已在美国专利公开号20030044423中描述了此类杂交恒定区的组装,其公开的内容通过引用并入本文。
在一个实施方式中,所述恒定区可以包含具有下表D所述的突变之一或其任何组合的CH2和/或CH3。
表D:抗体的适宜的人工程化Fc结构域。重链恒定区中残基的编号基于EU编号(Edelman,G.M.等,Proc.Natl.Acad.USA,63,78-85(1969);www.imgt.org/ IMGTScientificChart/Numbering/Hu_IGHGnber.html#refs)。
在特别的方面中,所述双功能分子(优选地所述结合部分)包含人IgG1重链恒定结构域或IgG1 Fc结构域,其任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A。
在另一个方面中,所述结合部分包含人IgG4重链恒定结构域或IgG4 Fc结构域,其任选地具有选自以下的置换或置换的组合:S228P;L234A/L235A,S228P+M252Y/S254T/T256E和K444A。甚至更优选地,所述双功能分子(优选地所述结合部分)包含IgG4 Fc区,其具有稳定所述IgG4的S228P。
在某些实施方式中,可以将氨基酸修饰引入本文提供的抗体的Fc区中以产生Fc区变体。在某些实施方式中,Fc区变体具有一些但并不是所有的效应功能。此类抗体可能是有用的,例如,在抗体的体内半衰期重要但某些效应功能不必要或有害的应用中。效应功能的实例包括补体依赖性细胞毒性(CDC)和抗体引导的补体介导的细胞毒性(ADCC)。改变效应功能的大量置换或置换或缺失是本领域公知的。
在一个实施方式中,所述恒定区包含降低对Fc受体的亲和性或降低Fc效应功能的突变。例如,所述恒定区可以包含消除IgG重链恒定区内糖基化位点的突变。优选地,CH2结构域包含消除CH2结构域内糖基化位点的突变。
在一个实施方式中,根据本发明所述的抗hPD1具有SEQ ID NO.39或52的重链恒定结构域和/或SEQ ID.40的轻链恒定结构域,特别是SEQ ID NO.39或52的重链恒定结构域和SEQ ID.40的轻链恒定结构域。
在另一个实施方式中,根据本发明所述的抗hPD1具有SEQ ID NO:52的重链恒定结构域和/或SEQ ID.40的轻链恒定结构域,特别是SEQ ID NO:52的重链恒定结构域和SEQID.40的轻链恒定结构域。
表E:适于根据本发明所述的人源化抗体的重链恒定结构域和轻链恒定结构域的实例。
靠近Fc部分与非Fc部分的结合处的氨基酸的改变可显著增加Fc融合蛋白的血清半衰期(PCT公开号WO 01/58957)。因此,本发明的蛋白或多肽的连接区可以包含相对于免疫球蛋白重链和促红细胞生成素的天然存在的序列优选位于连接点的约10个氨基酸内的改变。这些氨基酸变化能够引起疏水性增加。在一个实施方式中,所述恒定区来源于C-端赖氨酸残基被替代的IgG序列。优选地,IgG序列的C-端赖氨酸被非赖氨酸(例如丙氨酸或亮氨酸)替代,以进一步增加血清半衰期。
人IgG的所有亚类带有在循环中裂解的抗体重链的C-端赖氨酸残基(K444)。这种血液中裂解可通过释放IL-7来损害双功能分子的生物活性。为了规避这个问题,在IgG1或IgG4结构域中的K444氨基酸可以被丙氨酸置换以减少蛋白水解裂解,其为常用于抗体的突变。然后,在一个实施方式中,所述抗PD1抗体包含至少一个由K444A组成的其他氨基酸置换。
在一个实施方式中,所述抗PD1抗体在IgG的C-端结构域包含另外的半胱氨酸残基以产生另外的二硫键,并且潜在地限制双功能分子的灵活性。
在某些实施方式中,所述抗体可以改变以增加、降低或消除糖基化程度。
检查点抑制剂
发明人在本文中显示,根据本发明所述的双功能分子结合了IL-7变体或突变体对IL-7受体的作用和对PD-1抑制作用的阻断,并且适用于优化检查点抑制剂(例如抗PD-1抗体)的作用。特别是,已经显示出对T细胞(尤其是耗竭T细胞)激活、更特别地对TCR信号传导的协同作用。发明人特别显示了对相同细胞的激活,其由包含在相同免疫细胞上的双功能分子中的抗PD-1抗体与IL-7的结合所提供的。使用IL-7和抗PD-1抗体作为单独的化合物从未观察到这种协同作用。然后,可以设想在表达IL-7R的免疫细胞上表达的除PD-1之外的任何分子都可以被根据本发明所述的双功能构建体(特别是耗竭因子)触发。然后,在实施方式中,所述双功能分子包含针对在免疫细胞上表达的靶标(除PD-1之外)的抗体或其抗原结合片段。例如,所述靶标可以是在免疫细胞(尤其是T细胞)的表面上表达的受体。受体可以是抑制剂受体。替代地,所述受体可以是激活受体。
如本文所用,术语“靶标”是指在免疫细胞的外表面上表达的肽、多肽、蛋白、抗原或表位。关于免疫细胞表面上靶标的表达,术语“表达”是指存在于细胞外表面处或在细胞外表面处呈递的靶标。术语“特异性地表达”是指靶标在免疫细胞上表达,但基本上不被其他细胞类型表达,特别是例如肿瘤细胞。
在一个实施方式中,所述靶标由健康受试者中或患有疾病(特别是例如癌症)的受试者中的免疫细胞特异性地表达。这意味着所述靶标在免疫细胞中的表达水平高于在其他细胞中的表达水平,或者总的免疫细胞中表达所述靶标的免疫细胞的比率高于总的其他细胞中表达所述靶标的其他细胞的比率。优选地,表达水平或比率高2、5、10、20、50或100倍。更具体地,可以确定特定类型的免疫细胞,例如T细胞,更具体地CD8+T细胞、效应T细胞或耗竭T细胞,或在特定背景下,例如患有癌症或感染等疾病的受试者。
在一个方面,所述靶标是免疫检查点。优选地,所述靶标选自PD-1、CD28、CD80、CTLA-4、BTLA、TIG IT、CD160、CD40L、ICOS、CD27、0X40、4-1BB、GITR、HVEM、Tim-1、LFA-1、TIM3、CD39、CD30、NKG2D、LAG 3、B7-1、2B4、DR3、CD101、CD44、SIRPG、CD28H、CD38、CXCR5、CD3、PDL2、CD4和CD8。这类靶标在下表F中更具体地描述。
表F.感兴趣的靶标的实例。
然后,在该方面,包含在根据本发明所述的双功能分子中的抗体或其抗原片段结合选自CD28、CD80、CTLA-4、BTLA、TIGIT、CD160、CD40L、ICOS、CD27、OX40、4-1BB、GITR、HVEM、Tim-1、LFA-1、TIM3、CD39、CD30、NKG2D、LAG3、B7-1、2B4、DR3、CD101、CD44、SIRPG、CD28H、CD38、CXCR5、CD3、PDL2、CD4和CD8。
在优选方面,包含在根据本发明所述的双功能分子中的抗体或其抗原结合片段选自CTLA-4、BTLA、TIGIT、LAG3和TIM3。
还已知针对TIM3的抗体和靶向TIM3的双功能或双特异性分子,例如Sym023、TSR-022、MBG453、LY3321367、INCAGN02390、BGTB-A425、LY3321367、RG7769(Roche)。在一些实施方式中,TFM-3抗体如公开于国际专利申请公开号WO2013006490、WO2016/161270、WO 2018/085469、或WO 2018/129553、WO 2011/155607、U.S.8,552,156、EP 2581113和U.S 2014/044728。
还已知针对CTLA-4的抗体和靶向CTLA-4的双功能或双特异性分子,例如伊匹单抗、曲美木单抗、MK-1308、AGEN-1884、XmAb20717(Xencor)、MEDI5752(AstraZeneca)。也在WO18025178、WO19179388、WO19179391、WO19174603、WO19148444、WO19120232、WO19056281、WO19023482、WO18209701、WO18165895、WO18160536、WO18156250、WO18106862、WO18106864、WO18068182、WO18035710、WO18025178、WO17194265、WO17106372、WO17084078、WO17087588、WO16196237、WO16130898、WO16015675、WO12120125、WO09100140和WO07008463中公开了抗CTLA-4抗体。
还已知针对LAG-3的抗体和靶向LAG-3的双功能或双特异性分子,例如BMS-986016、IMP701、MGD012或MGD013(双特异性PD-1和LAG-3抗体)。也在WO2008132601、EP2320940、WO19152574中公开了抗LAG-3抗体。
针对BTLA的抗体也是本领域已知的,例如hu Mab8D5、hu Mab8A3、hu Mab21H6、huMab19A7或hu Mab4C7。针对BTLA的抗体TAB004目前正在晚期恶性肿瘤受试者中进行临床试验。抗BTLA抗体也在WO08076560、WO10106051(例如BTLA8.2)、WO11014438(例如4C7)、WO17096017和WO17144668(例如629)中公开。
针对TIGIT的抗体也是本领域已知的,例如,如在WO19232484中公开的BMS-986207或AB154、BMS-986207CPA.9.086、CHA.9.547.18、CPA.9.018、CPA.9.027、CPA.9.049、CPA.9.057、CPA.9.059、CPA.9.083、CPA.9.089、CPA.9.093、CPA.9.101、CPA.9.103、CHA.9.536.1、CHA.9.536.3、CHA.9.536.4、CHA.9.536.5、CHA.9.536.6、CHA.9.536.7、CHA.9.536.8、CHA.9.560.1、CHA.9.560.3、CHA.9.560.4、CHA.9.560.5、CHA.9.560.6、CHA.9.560.7、CHA.9.560.8、CHA.9.546.1、CHA.9.547.1、CHA.9.547.2、CHA.9.547.3、CHA.9.547.4、CHA.9.547.6、CHA.9.547.7、CHA.9.547.8、CHA.9.547.9、CHA.9.547.13、CHA.9.541.1、CHA.9.541.3、CHA.9.541.4、CHA.9.541.5、CHA.9.541.6、CHA.9.541.7、和CHA.9.541.8。还在WO16028656、WO16106302、WO16191643、WO17030823、WO17037707、WO17053748、WO17152088、WO18033798、WO18102536、WO18102746、WO18160704、WO18200430、WO18204363、WO19023504、WO19062832、WO19129221、WO19129261、WO19137548、WO19152574、WO19154415、WO19168382和WO19215728中公开了抗TIGIT抗体。
针对CD160的抗体也是本领域已知的,例如,如在WO06015886中公开的CL1-R2CNCM I-3204,或如在WO10006071、WO10084158、WO18077926中公开的其他抗体。
在特定方面,根据本发明所述的双功能分子包含抗CTLA-4抗体或其抗原结合片段,优选地人、人源化或嵌合抗CTLA-4抗体或其抗原结合片段。优选地,所述抗体是CTLA-4的拮抗剂。因此,所述双功能分子结合IL-7wt、其变体或突变体对所述IL-7受体的作用和对CTLA-4抑制作用的阻断,并且可能对T细胞(尤其是耗竭T细胞)的激活、更特别地是对TCR信号传导具有协同作用。
在另一个特别的方面,根据本发明所述的双功能分子包含抗BTLA抗体或其抗原结合片段,优选地人、人源化或嵌合抗BTLA抗体或其抗原结合片段。优选地,所述抗体是BTLA的拮抗剂。因此,所述双功能分子结合IL-7wt、其变体或突变体对所述IL-7受体的作用和对BTLA抑制作用的阻断,并且可能对T细胞(尤其是耗竭T细胞)的激活、更特别地是对TCR信号传导具有协同作用。
在另一个特别的方面,根据本发明所述的双功能分子包含抗TIGIT抗体或其抗原结合片段,优选地人、人源化或嵌合抗TIGIT抗体或其抗原结合片段。优选地,所述抗体是TIGIT的拮抗剂。因此,所述双功能分子结合IL-7wt、其变体或突变体对所述IL-7受体的作用和对TIGIT抑制作用的阻断,并且可能对T细胞(尤其是耗竭T细胞)的激活、更特别地是对TCR信号传导具有协同作用。
在另一个特别的方面,根据本发明所述的双功能分子包含抗LAG-3抗体或其抗原结合片段,优选地人、人源化或嵌合抗LAG-3抗体或其抗原结合片段。优选地,所述抗体是LAG-3的拮抗剂。因此,所述双功能分子结合IL-7wt、其变体或突变体对所述IL-7受体的作用和对LAG-3抑制作用的阻断,并且可能对T细胞(尤其是耗竭T细胞)的激活、更特别地是对TCR信号传导具有协同作用。
在另一个特别的方面,根据本发明所述的双功能分子包含抗TIM3抗体或其抗原结合片段,优选地人、人源化或嵌合抗TIM3抗体或其抗原结合片段。优选地,所述抗体是TIM3的拮抗剂。因此,所述双功能分子结合所述IL-7变体或突变体对所述IL-7受体的作用和对TIM3抑制作用的阻断,并且可能对T细胞(尤其是耗竭T细胞)的激活、更特别地是对TCR信号传导具有协同作用。
肽接头
本发明包括双功能分子,其可包含所述抗PD-1抗体或其片段与IL-7之间的肽接头。所述肽接头通常具有足够的长度和柔韧性以保证与其之间的接头相连的两个蛋白元件在空间上有足够的自由度以发挥其功能并避免α螺旋和β折叠的形成对所述重组双功能分子的稳定性的影响。
在本公开的一个方面中,所述抗hPD1抗体优选地通过肽接头与IL-7连接。换言之,本发明涉及一种双功能分子,其包含如本文详述的抗PD1抗体或其抗原结合片段的双功能分子,其链,例如轻链或重链或其片段,优选地重链或其片段,通过肽接头与IL-7连接。如本文所用,术语“接头”指连接IL-7和所述抗PD-1免疫球蛋白序列部分的至少一个氨基酸的序列。这种接头可用于防止空间位阻。所述接头的长度通常为3-44个氨基酸残基。优选地,所述接头具有3-30个氨基酸残基。在一些实施方式中,所述接头具有3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30个氨基酸残基。
在一个实施方式中,本发明涉及一种双功能分子,其包含如上定义的抗PD-1抗体或其抗原结合片段和IL-7,其中所述抗体的链,例如轻链或重链,优选地重链,甚至更优选地重链或轻链的C-端通过肽接头与IL-7连接,优选地与IL-7的N-端连接。
在一个特别的方面中,本发明涉及一种双功能分子,其包含如上定义的抗hPD-1抗体或其抗原结合片段,其中IL-7优选地通过肽接头与所述抗体的重链的C-端末端(例如,所述重链恒定结构域的C-端末端)连接。
在一个实施方式中,本发明涉及一种双功能分子,其包含如上定义的抗PD-1抗体或其抗原结合片段,其中IL-7优选地通过肽接头与所述抗体的轻链的C-端末端(例如,所述轻链恒定结构域的C-端末端)连接。
所述接头序列可以是天然存在的序列或非天然存在的序列。如果用于治疗目的,所述接头优选地在向其施用所述双功能分子的受试者中是非免疫原性的。一组有用的接头序列是来源于如WO 96/34103和WO 94/04678所述的重链抗体的铰链区的接头。其他实例是聚丙氨酸接头序列。接头序列的其他优选实例是不同长度的Gly/Ser接头,包括(Gly4Ser)4、(Gly4Ser)3、(Gly4Ser)2、Gly4Ser、Gly3Ser、Gly3、Gly2ser和(Gly3Ser2)3,特别是(Gly4Ser)3。优选地,所述接头选自(Gly4Ser)4、(Gly4Ser)3、和(Gly3Ser2)3。
在一个实施方式中,包含于所述双功能分子中的所述接头选自(Gly4Ser)4、(Gly4Ser)3、(Gly4Ser)2、Gly4Ser、Gly3Ser、Gly3、Gly2ser和(Gly3Ser2)3,优选是(Gly4Ser)3。优选地,所述接头选自(Gly4Ser)4、(Gly4Ser)3、和(Gly3Ser2)3。甚至更优选地,所述接头是(GGGGS)3。
在一个实施方式中,本发明涉及一种双功能分子,其包含如上定义的抗PD-1抗体或其片段,其中所述抗体或其片段通过接头序列与IL-7连接,所述接头序列优选地选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地选自(GGGGS)3。优选地,所述接头选自(GGGGS)3、(GGGGS)4、和(GGGS)3。
优选地,所述抗PD-1抗体的重链,优选地所述抗PD-1抗体的重链的C-端,通过柔性(Gly4Ser)3接头与IL-7的N-端遗传融合。在融合连接处,所述抗体重链的C-端赖氨酸残基可以突变为丙氨酸以减少蛋白水解裂解。
优选地,所述抗PD-1抗体的重链,优选地所述抗PD-1抗体的轻链的C-端,通过柔性(Gly4Ser)3接头与IL-7的N-端遗传融合。在融合连接处,所述抗体轻链的C-端赖氨酸残基可以突变为丙氨酸以减少蛋白水解裂解。
IL-7
根据本发明所述的双功能分子包含另外的或第二实体,其包含白介素7或其变体或片段。
优选地,所述IL-7蛋白是人IL-7或其变体。因此,所述IL-7或其变体具有与野生型IL-7、尤其是与SEQ ID No:51的蛋白具有至少75%同一性的氨基酸序列。
在一个实施方式中,所述双功能分子包含152个氨基酸(SEQ ID NO:51)的典型野生型IL-7人蛋白。优选地,所述IL-7蛋白是SEQ ID No:51的蛋白。所述IL-7蛋白可以包含其肽信号或不包含其肽信号。
IL-7蛋白的“变体”定义为被一个或多个氨基酸改变的氨基酸序列。变体可以具有“保守”修饰或“非保守”修饰。此类修饰可包括氨基酸置换、缺失和/或插入。可以使用本领域众所周知的计算机程序,例如用于分子建模或用于产生比对的软件,找到确定哪些和多少氨基酸残基可以被取代、插入或删除而不破坏生物特性(例如活性、结合能力和/或结构)的指导。在一个特定方面,本发明中包括的变体IL-7蛋白具体包括相比于野生型IL-7保留了基本相等的IL-7生物特性的IL-7蛋白。在另一个方面,本发明中包括的变体IL-7蛋白具体包括相比于野生型IL-7不保留基本相等的生物特性(例如活性、结合能力和/或结构)的IL-7蛋白。IL-7的变体还包括改变的IL-7多肽序列(例如氧化、还原、脱氨基化或截短形式)。特别地,保留与全长IL-7蛋白相当的生物特性的IL-7的截短形式或片段包括在本发明的范围内。在一个实施方式中,白介素7是其任何生物活性片段。IL-7的变体更优选地包括由天然多态性产生的天然等位基因变体,包括SNP、剪接变体等。
IL-7蛋白的生物活性可以使用体外细胞增殖测定来测量。优选地,根据本发明所述的IL-7变体相比于野生型人IL-7保持了至少1%、5%、10%、20%、30%、40%、50%、60%的生物活性,相比于野生型IL-7保持了优选地至少80%、90%、95%和甚至更优选地99%的生物活性。
变体IL-7蛋白还包括与野生型IL-7、特别是与SEQ ID No:51的蛋白具有至少约65%、70%、75%、80%、85%、90%、92%、95%、96%、97%、98%、99%或更多序列同一性的多肽。
根据本发明优选的IL-7是包含如SEQ ID No:51、EP 314 415或WO2004/018681A2中所述的氨基酸序列或由如SEQ ID No:51、EP 314 415或WO2004/018681 A2中所述的氨基酸序列组成的人IL-7多肽,以及其任何天然变体和同源物。
一方面,本发明中使用的IL-7多肽是重组IL-7。如本文所用,术语“重组”是指所述多肽是从重组表达系统,即从宿主细胞(例如,微生物或昆虫或植物或哺乳动物)的培养物或从经工程化已获得编码IL-7多肽的核酸分子的转基因植物或动物中获得的或来源的。优选地,所述重组IL-7是人重组IL-7(例如在重组表达系统中产生的人IL-7)。
本发明还提供包含相比于野生型IL-7蛋白具有增强的生物活性的IL-7蛋白的双功能分子。例如,如US7960514中所述,具有Cys2-Cys92、Cys34-Cys129和Cys47-141的二硫键模式的IL-7蛋白在体内比野生型重组IL-7蛋白更有活性。如EP1904635中所述,IL-7的高糖基化也提高了IL-7(如IL-7蛋白)生物活性,其中Asn116未经糖基化但Asn70和Asn91经糖基化。
替代地,本发明提供包含相比于野生型IL-7蛋白免疫原性降低的IL-7蛋白的双功能分子,特别是通过去除IL-7内可刺激免疫应答的T细胞表位。此类IL-7的实例在WO2006061219中有所描述。
在特定方面,本公开还提供了包含IL-7变体或突变体的双功能分子。术语“白介素-7突变体”、“突变IL-7”、“IL-7突变体”、“IL-7变体”、“IL-7m”或IL-7v”在本文中可互换使用。
在这种情况下,所述IL-7变体或突变体相比于野生型IL-7不保留基本相等的生物特性(例如活性、结合能力和/或结构)。所述IL-7突变体或变体包含至少一个突变。特别地,所述至少一个突变降低了所述IL-7变体或突变体对IL-7受体(IL-7R)的亲和力,但不会导致对IL-7R的识别丧失。因此,IL-7突变体或变体保留例如通过pStat5信号测量的激活IL-7R的能力(例如公开于Bitar等,Front.Immunol.,2019,第10卷中的)。可以使用体外细胞增殖测定或通过ELISA或FACS测量进入T细胞中的P-Stat5来测量IL-7蛋白的生物活性。优选地,根据本发明所述的IL-7变体相比于野生型IL-7、优选地wth-IL7,生物特性(例如活性、结合能力和/或结构)降低至少2、5、10、20、30、40、50、100、250、500、750、1000、2500、5000或8000倍。更优选地,所述IL-7变体与IL-7受体的结合降低但保留激活IL-7R的能力。例如,与IL-7受体的结合相比于野生型IL-7可以降低至少1%、5%、10%、20%、30%、40%、50%、60%,并且相比于野生型IL-7保留了激活IL-7R至少90%、80%、70%、60%、50%、40%、30%或20%的能力。
在一方面,所述IL-7变体或突变体与wt-IL-7有至少一个氨基酸突变的不同,其i)相比于wt-IL-7对IL-7R的亲和力降低了所述IL-7变体对IL-7受体(IL-7R)的亲和力,并ii)相比于wt-IL7改善了IL7变体的药代动力学。更特别地,所述IL-7变体或突变体进一步保留了激活IL-7R的能力,特别是通过pStat5信号传导。
在另一方面,包含IL-7变体或突变体的双功能分子与wt-IL-7有至少一个氨基酸突变的不同,其i)相比于包含wt-IL-7的双功能分子对IL-7R的亲和力降低了所述双功能分子对IL-7受体(IL-7R)的亲和力,并ii)相比于包含wt-IL7的双功能分子改善了包含IL7变体或其突变体的双功能分子的药代动力学。更特别地,包含IL7变体或其突变体的双功能分子进一步保留了激活IL-7R的能力,特别是通过pStat5信号传导。例如,包含IL-7变体或突变体的双功能分子与所述IL-7受体的结合相比于包含野生型IL-7的双功能分子可以降低至少10%、20%、30%、40%、50%、60%,并且相比于包含野生型IL-7的双功能分子保留激活IL-7R的能力至少90%、80%、70%、60%、50%、40%、30%或20%。
在特定方面,与wth-IL-7对IL-7R的亲和力相比,IL-7变体或突变体对IL-7受体(IL-7R)的亲和力降低。特别地,与wth-IL-7分别对CD127和/或CD132的亲和力相比,IL-7变体或突变体对CD127和/或CD132的亲和力降低。优选地,与wth-IL-7对CD127的亲和力相比,IL-7变体或突变体对CD127的亲和力降低。
优选地,所述至少一个氨基酸突变使IL-7变体或突变体对IL-7R、特别是CD132或CD127的亲和力相比于wt-IL-7对IL-7R的亲和力降低至少10、100、1000、10,000或100,000倍。这种亲和力比较可以通过本领域技术人员已知的任何方法进行,例如ELISA或Biacore。
优选地,与IL-7wt相比,所述至少一个氨基酸突变降低IL-7变体或突变体对IL-7R的亲和力,但不降低IL-7变体或突变体的生物学活性(特别是如通过pStat5信号测量的)。
替代地,与IL-7wt相比,所述至少一个氨基酸突变降低IL-7变体或突变体对IL-7R的亲和力,但不显著降低IL-7m的生物活性(特别是如通过pStat5信号测量的)。
另外地或替代地,IL-7变体或突变体相比于含野生型IL-7的双功能分子改善包含IL-7变体或突变体的双功能分子的药代动力学。特别地,根据本发明所述的IL-7变体或突变体相比于包含wth-IL-7的双功能分子将包含IL-7变体或突变体的双功能分子的药代动力学提高了至少10、100或1000倍。药代动力学曲线比较可以通过本领域技术人员已知的任何方法进行,例如体内药物注射和多个时间点的血清中药物剂量ELISA,例如如实施例9中所示。
如本文所用,术语“药代动力学”和“PK”可互换使用,指的是向活体施用化合物、物质或药物的归宿。药代动力学特别包括ADME或LADME方案,代表释放(即物质从组合物中释放)、吸收(即物质进入血液循环)、分布(即物质通过身体分散或散布)、代谢(即物质的转化或降解)和排泄(即物质从生物体中去除或清除)。代谢和排泄这两个阶段也可以在标题消除下归为一组。本领域技术人员可以监测不同的药代动力学参数,例如消除半衰期、消除恒定速率、清除率(即每单位时间清除药物的血浆体积)、Cmax(最大血清浓度)和药物暴露(由曲线下面积确定)(Scheff等,Pharm Res.,2011,28,1081-9)。
然后,通过使用IL-7变体或突变体改善药代动力学是指改善上述参数中的至少一个。优选地,其指的是双功能分子消除半衰期的改善,即半衰期持续时间或Cmax的增加。
在一个具体实施方式中,相比于包含IL-7wt的双功能分子,IL-7变体或突变体的至少一个突变提高了包含IL-7变体或突变体的双功能分子的消除半衰期。
在一个实施方式中,所述IL-7变体或突变体呈现出与例如SEQ ID NO:51中公开的152氨基酸的野生型人IL-7(wth-IL-7)蛋白至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少98%或至少99%同一性。优选地,所述IL-7变体或突变体呈现出与SEQID NO:51至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少98%或至少99%同一性。
特别地,所述至少一个突变发生在IL-7的氨基酸位置74和/或142处。另外地或替代地,所述至少一个突变发生在氨基酸位置2和141、34和129、和/或47和92处。这些位置是指SEQ ID NO:51中所示的氨基酸的位置。
特别地,所述至少一个突变是选自以下的氨基酸置换或氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、C47S-C92S和C34S-C129S、W142H、W142F、W142Y、Q11E、Y12F、M17L、Q22E、K81R、D74E、D74Q和D74N或其任何组合。这些突变是指SEQ ID NO:51中所示的氨基酸的位置。然后,例如突变W142H代表wth-IL7的色氨酸被置换成组氨酸以获得在氨基酸位置142中具有组氨酸的IL-7m。此类突变体例如描述于SEQ ID No:56中。
在一个实施方式中,所述IL-7变体或突变体包含置换的组以破坏C2和C141、C47和C92以及C34-C129之间的二硫键。特别地,所述IL-7变体或突变体包含两组置换以破坏C2和C141、和C47和C92、C2和C141、和C34-C129、或C47和C92、和C34-C129之间的二硫键。例如,半胱氨酸残基可以被丝氨酸置换以防止二硫键形成。因此,氨基酸置换可以选自C2S-C141S和C47S-C92S(称为“SS2”)、C2S-C141S和C34S-C129S(称为“SS1”)、和C47S-C92S和C34S-C129S(称为“SS3”)。这些突变是指SEQ ID NO:51中所示的氨基酸的位置。此类IL-7变体或突变体在SEQ ID No:53至55(分别为SS1、SS2和SS3)中所示的序列下特别描述。优选地,所述IL-7变体或突变体包含氨基酸置换C2S-C141S和C47S-C92S。甚至更优选地,所述IL-7变体或突变体呈现了SEQ ID NO:54中所示的序列。
在另一个实施方式中,所示IL-7变体或突变体包含至少一个突变,其选自W142H、W142F和W142Y。此类IL-7变体或突变体分别在SEQ ID NO:57至58中所示的序列下具体描述。优选地,所述IL-7变体或突变体包含突变W142H。甚至更优选地,所述IL-7变体或突变体呈现了SEQ ID NO:56中所示的序列。
在另一个实施方式中,所示IL-7变体或突变体包含至少一个突变,其选自D74E、D74Q和D74N,优选地D74E和D74Q。此类IL-7变体或突变体分别在SEQ ID NO:63至65中所示的序列下具体描述。优选地,所述IL-7变体或突变体包含突变D74E。甚至更优选地,所述IL-7变体或突变体呈现了SEQ ID NO:63中所示的序列。
在另一个实施方式中,所述IL-7变体或突变体包含至少一个突变,其选自Q11E、Y12F、M17L、Q22E和/或K81R。这些突变是指SEQ ID NO:51中所示的氨基酸的位置。此类IL-7变体或突变体分别在SEQ ID NO:59、60、61、62和66中所示的序列下具体描述。
在一个实施方式中,所述IL-7变体或突变体包含至少一个突变,其存在于以下中:i)W142H、W142F或W142Y和/或ii)D74E、D74Q或D74N,优选地D74E或D74Q和/或iii)C2S-C141S和/或C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
在一个实施方式中,所述IL-7变体或突变体包含W142H置换和至少一个突变,其由以下组成:i)D74E、D74Q或D74N,优选地D74E或D74Q和/或ii)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
在一个实施方式中,所述IL-7变体或突变体包含D74E置换和至少一个突变,其由以下组成:i)W142H、W142F或W142Y和/或ii)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
在一个实施方式中,所述IL-7变体或突变体包含突变C2S-C141S和C47S-C92S和至少一个置换,其由以下组成:i)W142H、W142F或W142Y和/或ii)D74E、D74Q或D74N,优选地D74E或D74Q。
在一个实施方式中,所述IL-7变体或突变体包含i)D74E和W142H置换和ii)突变C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
所述IL IL-7变体或突变体可包含其肽信号或不包含其肽信号。
在一个实施方式中,根据本发明所述的双功能分子包含IL-7变体,其包含SEQ IDNO:53-58或63-65中所示的氨基酸序列或由SEQ ID NO:53-58或63-65中所示的氨基酸序列组成。甚至更优选地,根据本发明所述的双功能分子包含IL-7变体,其包含SEQ ID NO 54、56或63中所示的氨基酸序列或由SEQ ID NO 54、56或63中所示的氨基酸序列组成。
双功能分子或“Bicki”
本发明特别提供了一种双功能分子,其包含如上公开地抗hPD1抗体或其抗体片段和IL-7,或存在于如上公开的抗hPD1抗体或其抗体片段和IL-7中,所述抗hPD1抗体或其抗体片段优选地通过如上公开的肽接头,与IL-7共价连接,特别是作为融合蛋白。
特别地,根据本发明所述的双功能分子包含两个实体:第一实体,其包含抗hPD1抗体或其片段,或基本上由抗hPD1抗体或其片段组成;第二实体,其包含白介素7(IL-7)、优选地人IL-7,或基本上由白介素7(IL-7)、优选地人IL-7组成,这两个实体任选地通过肽接头连接。
特别地,根据本发明所述的双功能分子包含一、二、三或四个IL-7的分子。特别地,所述双功能分子可仅包含一个仅与所述抗PD-1抗体的一条轻链或重链连接的IL-7的分子。所述双功能分子还可包含与所述抗PD-1抗体的轻链或重链连接的两个IL-7的分子。所述双功能分子还可包含两个IL-7的分子,第一分子与抗PD-1抗体的轻链连接,第二分子与所述抗PD-1抗体的重链连接。所述双功能分子还可以包含三个IL-7分子,其中两个与所述抗PD-1抗体的轻链或重链连接,最后一个与所述抗PD-1抗体的另一条链连接。最后,所述双功能分子还可以包含四个IL-7分子,两个分子与所述抗PD-1抗体的轻链连接,两个分子与所述抗PD-1抗体的重链连接。因此,所述双功能分子包含一至四个如本文公开的IL-7分子。
在一个实施方式中,仅一条轻链包含一个IL-7分子(例如所述双功能分子包含一个IL-7分子),仅一条重链包含一个IL-7分子(例如所述双功能分子包含一个IL-7分子),每条轻链包含一个IL-7分子(例如所述双功能分子包含两个IL-7分子),每条重链包含一个IL-7分子(例如所述双功能分子包含两个IL-7分子),仅一条轻链和仅一条重链包含一个IL-7分子(例如所述双功能分子包含两个IL-7分子),每条轻链包含一个IL-7分子,且仅一条重链包含一个IL-7分子(例如,所述双功能分子包含三个IL-7分子),每条重链包含一个IL-7分子,且仅一条轻链包含一个IL-7分子(例如所述双功能分子包含三个IL-7分子),或者轻链和重链两者均包含一个IL-7分子(例如所述双功能分子包含四个IL-7分子)。
在一个实施方式中,根据本发明所述的双功能分子包含以下或由以下组成:
(a)抗人PD-1抗体或其抗原结合片段,其包含(i)重链,和(ii)轻链;和
(b)人白介素(IL-7)或其片段或变体,
其中所述抗体重链和/或轻链或其片段通过肽接头,与IL-7共价连接,优选地作为融合蛋白。
优选地,根据本发明所述地双功能分子包含以下或由以下组成:
(a)人源化抗人PD-1抗体或其抗原结合片段,其包含(i)重链,和(ii)轻链;和
(b)人白介素(IL-7)或其变体或片段,
其中所述抗体重链或轻链或其片段通过肽接头,与IL-7共价连接,优选地作为融合蛋白。
优选地,这种双功能分子包含至少一个连接IL-7的N-端与所述抗人PD-1抗体的重链或轻链或两者的C-端的肽接头,所述肽接头优选地选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地是(GGGGS)3。
优选地,所述IL-7的N-端末端通过至少一个肽接头,与所述抗人PD-1抗体的重链或轻链或两者的C-端末端连接。替代地,IL-7的C-端末端通过至少一个肽接头,与所述抗人PD-1抗体的重链或轻链或两者的N-端末端连接。
在一个实施方式中,根据本发明所述的双功能分子包含以下或由以下组成:
(a)抗人PD-1抗体或其抗原结合片段,其包含(i)重链,和(ii)轻链,
(b)人白介素(IL-7)或其变体或片段,和
(c)连接IL-7的N-端末端与所述抗人PD-1抗体的重链或轻链或两者的C-端末端的肽接头,所述肽接头优选地选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地是(GGGGS)3。
在特别的实施方式中,根据本发明所述的双功能分子包含以下或由以下组成:
(a)抗人PD-1抗体或其抗原结合片段,其包含:
(i)重链可变结构域,其包含HCDR1、HCDR2和HCDR3,和
(ii)轻链可变结构域,其包含LCDR1、LCDR2和LCDR3,
其中:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:3的氨基酸序列或由SEQ ID NO:3的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;任选地具有一个、两个或三个选自SEQ ID NO:3的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR1(LCDR1)包含SEQ ID NO:12的氨基酸序列或由SEQ ID NO:12的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:12的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)SEQ ID No:51的人白介素7或其变体或片段,
其中所述抗体重链和/或轻链或其片段,优选地通过肽接头,与IL-7共价连接作为融合蛋白。
在另一个实施方式中,根据本发明所述的双功能分子包含以下或由以下组成:(a)抗人PD-1抗体或其抗原结合片段,其包含:
(i)重链可变结构域,其包含HCDR1、HCDR2和HCDR3,和
(ii)轻链可变结构域,其包含LCDR1、LCDR2和LCDR3,
其中:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:3的氨基酸序列或由SEQ ID NO:3的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;任选地具有一个、两个或三个选自SEQ ID NO:3的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR1(LCDR1)包含SEQ ID NO:12的氨基酸序列或由SEQ ID NO:12的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:12的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)SEQ ID No:51的人白介素7或其变体或片段,
其中所述抗体重链和/或轻链或其片段,优选地通过肽接头,与IL-7共价连接作为融合蛋白。
在另一个实施方式中,根据本发明所述的双功能分子包含以下或由以下组成:(a)人源化抗人PD-1抗体或其抗原结合片段,其包含:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:1的位置3之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:2的位置13、14和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述重链CDR3(HCDR3)包含SEQ ID NO:4、5、6、7、8、9、10或11的氨基酸序列或由SEQ ID NO:4、5、6、7、8、9、10或11的氨基酸序列组成,任选地具有一个、两个或三个选自SEQID NO:4、5、6、7、8、9、10或11的位置2、3、7和8之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR1(LCDR1)包含SEQ ID NO:13或SEQ ID NO:14的氨基酸序列或由SEQID NO:13或SEQ ID NO:14的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ IDNO:13或SEQ ID NO:14的位置5、6、10、11和16之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,任选地具有一个、两个或三个选自一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;并且
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成,任选地具有一个、两个或三个选自SEQ ID NO:16的位置1、4和6之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;和(b)SEQ ID No:51的人白介素7或其变体或片段,
其中所述抗体重链和/或轻链或其片段,优选地通过肽接头,与IL-7共价连接作为融合蛋白。
优选地,所述肽接头选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地为(GGGGS)3。
在另一个实施方式中,本发明涉及一种双功能分子,其包含:
(a)人源化抗人PD-1抗体或其抗原结合片段,其包含:
(i)重链可变区(VH),其包含SEQ ID NO:17的氨基酸序列或由SEQ ID NO:17的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E,任选地具有一个、两个或三个选自SEQ ID NO:17的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(ii)轻链可变区(VL),其包含SEQ ID NO:26的氨基酸序列或由SEQ ID NO:26的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:26的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰,和
(b)SEQ ID No:51的人白介素7或其变体或片段,
(c)在所述抗hPD1抗体的轻链和/或重链与所述人IL-7或其变体或片段之间的肽接头,其选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地为(GGGGS)3。
优选地,所述IL-7的N-端末端通过至少一个肽接头,与所述抗人PD-1抗体的重链或轻链或两者的C-端末端连接。替代地,IL-7的C-端末端通过至少一个肽接头,与所述抗人PD-1抗体的重链或轻链或两者的N-端末端连接。
在另一个实施方式中,本发明涉及一种双功能分子,其包含以下或由以下组成:
(a)人源化抗人PD-1抗体,其包含:
(i)重链可变区(VH),其包含SEQ ID NO:17的氨基酸序列或由SEQ ID NO:17的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E,任选地具有一个、两个或三个选自SEQ ID NO:17的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(ii)轻链可变区(VL),其包含SEQ ID NO:26的氨基酸序列或由SEQ ID NO:26的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:26的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰,和
(b)SEQ ID No:51的人白介素7或其变体或片段,
其中,所述抗体或其抗原结合片段的重链和/或轻链的C-端末端,优选地通过(GGGGS)3肽接头与IL-7的N-端末端共价连接。
在另一个实施方式中,本发明涉及一种双功能分子,其包含以下或由以下组成:a)人源化抗人PD-1抗体,其包含:
(i)重链可变区(VH),其包含SEQ ID NO:18、19、20、21、22、23、24或25的氨基酸序列或由SEQ ID NO:18、19、20、21、22、23、24或25的氨基酸序列组成,任选地具有一个、两个或三个分别选自SEQ ID NO:18、19、20、21、22、23、24或25的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(ii)轻链可变区(VL),其包含SEQ ID NO:27或SEQ ID NO:28的氨基酸序列或由SEQ ID NO:27或SEQ ID NO:28的氨基酸序列组成,任选地具有一个、两个或三个选自SEQID NO:27或SEQ ID NO:28的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰,
(b)SEQ ID No:51的人白介素7或其变体或片段,
其中所述抗体或其抗原结合片段的重链和/或轻链的C-端末端,优选地通过(GGGGS)3肽接头,与IL-7的N-端末端共价连接。
在优选的实施方式中,所述抗体或其抗原结合片段的重链的C-端末端与IL-7的N-端末端共价连接以形成融合蛋白。优选地,仅所述抗体或其抗原结合蛋白的重链与IL-7共价连接。
在另一个实施方式中,本发明涉及一种双功能分子,其包含以下或由以下组成:a)人源化抗人PD-1抗体,其包含:
(i)重链可变区(VH),其包含SEQ ID NO:17的氨基酸序列或由SEQ ID NO:17的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N、E,任选地具有一个、两个或三个选自SEQ ID NO:17的位置7、16、17、20、33、38、43、46、62、63、65、69、73、76、78、80、84、85、88、93、95、96、97、98、100、101、105、106和112之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰;
(ii)轻链可变区(VL),其包含SEQ ID NO:26的氨基酸序列或由SEQ ID NO:26的氨基酸序列组成,其中X是G或T,任选地具有一个、两个或三个选自SEQ ID NO:26的位置3、4、7、14、17、18、28、29、33、34、39、42、44、50、81、88、94、97、99和105之外的任何位置处的一个或多个置换、一个或多个添加、一个或多个缺失及其任何组合的修饰,和
(b)SEQ ID No:51的人白介素7或其变体或片段,
其中所述抗体或其抗原结合片段的重链的C-端末端,优选地通过(GGGGS)3肽接头,与IL-7的N-端末端共价连接以形成融合蛋白。
在另一个实施方式中,本发明涉及一种双功能分子,其包含以下或由以下组成:a)人源化抗人PD-1抗体,其包含:
(i)重链可变区(VH),其包含SEQ ID NO:24的氨基酸序列或由SEQ ID NO:24的氨基酸序列组成;
(ii)轻链可变区(VL),其包含SEQ ID NO:28的氨基酸序列或由SEQ ID NO:28的氨基酸序列组成,
(b)SEQ ID No:51的人白介素7或其变体或片段,
其中所述抗体或其抗原结合片段的重链的C-端末端,优选地通过(GGGGS)3肽接头,与IL-7的N-端末端共价连接以形成融合蛋白。
优选地,所述抗体或其抗原片段具有IgGl或IgG4 Fc结构域。
在一个方面,所述抗体或其抗原片段具有IgGl Fc结构域,任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A,甚至更优选地具有例如上文所述的突变N297A的IgGl Fc结构域。
在另一方面,所述抗体或其抗原片段具有IgG4 Fc结构域,任选地具有选自以下的置换或置换的组合:S228P;L234A/L235A,S228P+M252Y/S254T/T256E和K444A,甚至更优选地具有例如上文所述的突变S228P的IgG4 Fc结构域。
任选地,在以上指定的实施方式中的任一个中,所述IL-7是IL-7变体或突变体。
更特别地,所述IL-7变体或突变体呈现出与包含SEQ ID NO:51中所示的氨基酸序列或由SEQ ID NO:51中所示的氨基酸序列组成的野生型人IL-7(wth-IL-7)至少75%同一性,这种IL-7变体包含至少一个氨基酸突变,所述氨基酸突变i)相比于wth-IL-7对IL-7R的亲和力减少了所述IL-7变体对IL-7受体的亲和力,并且ii)相比于包含IL-7的双功能分子改善了包含所述IL-7变体的所述双功能分子的药代动力学。更优选地,这种突变i)相比于wth-IL-7对IL-7R的亲和力减少了所述IL-7变体对IL-7受体的亲和力,ii)保留了激活IL-7R的能力;并且iii)相比于包含IL-7的双功能分子改善了包含所述IL-7变体的所述双功能分子的药代动力学。
更具体地,所述IL-7变体或突变体可呈现出与包含SEQ ID NO:51中所示的氨基酸序列或由SEQ ID NO:51中所示的氨基酸序列组成的野生型人IL-7(wth-IL-7)至少75%同一性,这种IL-7变体包含至少一个氨基酸突变,所述氨基酸突变选自:(i)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S,(ii)W142H、W142F或W142Y,(iii)D74E、D74Q或D74N,优选地D74E或D74Q;(iv)Q11E、Y12F、M17L、Q22E和/或K81R;或其任何组合。
所述IL-7变体或突变体可以包含选自以下的至少一组置换:C2S-C141S和C47S-C92S(称为“SS2”)、C2S-C141S和C34S-C129S(称为“SS1”)、以及C47S-C92S和C34S-C129S(称为“SS3”)。这些突变是指SEQ ID NO:51中所示的氨基酸的位置。这种IL-7变体或突变体在SEQ ID No:53至55(分别为SS1、SS2和SS3)中所示的序列下特别描述。优选地,所述IL-7变体或突变体包含氨基酸置换C2S-C141S和C47S-C92S。甚至更优选地,所述IL-7变体或突变体呈现了SEQ ID NO:54中所示的序列。
所述IL-7变体或突变体可以包含选自以下的至少一个突变:W142H、W142F和W142Y。这种IL-7变体或突变体分别在SEQ ID NO:57至58中所示的序列下特别描述。优选地,所述IL-7变体或突变体包含突变W142H。甚至更优选地,所述IL-7变体或突变体呈现了SEQ ID NO:56中所示的序列。
所述IL-7变体或突变体可以包含选自以下的至少一个突变:D74E、D74Q和D74N,优选地D74E或D74Q。这种IL-7变体或突变体分别在SEQ ID NO:63至65中所示的序列下特别描述。优选地,所述IL-7变体或突变体包含突变D74E。甚至更优选地,所述IL-7变体或突变体呈现了SEQ ID NO:63中所示的序列。
所述IL-7变体或突变体可以包含选自以下的至少一个突变:Q11E、Y12F、M17L、Q22E和/或K81R。这些突变是指SEQ ID NO:51中所示的氨基酸的位置。这种IL-7变体或突变体分别在SEQ ID NO:59、60、61、62和66中所示的序列下特别描述。
所述IL-7变体或突变体可以包含存在于以下中的至少一个突变:i)W142H、W142F或W142Y和/或ii)D74E、D74Q或D74N,优选地D74E或D74Q和/或iii)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
所述IL-7变体或突变体可以包含W142H置换和由以下组成的至少一个突变:i)D74E、D74Q或D74N,优选地D74E或D74Q和/或ii)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
所述IL-7变体或突变体可以包含D74E置换和由以下组成的至少一个突变:i)W142H、W142F或W142Y和/或ii)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
所述IL-7变体或突变体可以包含突变C2S-C141S和C47S-C92S和由以下组成的至少一个置换:i)W142H、W142F或W142Y和/或ii)D74E、D74Q或D74N。
所述IL-7变体或突变体可以包含i)D74E和W142H置换和ii)突变C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S。
所述IL-7变体或突变体可以包含SEQ ID NO:53、54、55、56、57、58、63、64或65中所示的氨基酸序列或由SEQ ID NO:53、54、55、56、57、58、63、64或65中所示的氨基酸序列组成。
在一个特别的方面,所述IL-7是根据本发明所述的IL-7变体并且所述抗体或其抗体片段具有IgGl Fc结构域,任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A,甚至更优选地,具有例如上述的突变N297A的IgGl Fc结构域。优选地,所述抗体或其片段通过选自(GGGGS)3、(GGGGS)4和(GGGS)3的接头,甚至更优选地通过(GGGGS)3,与IL-7或其变体连接。优选地,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、C47S-C92S和C34S-C129S、W142H、W142F、W142Y、D74E、D74Q和D74N。更优选地,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、W142H、W142F、W142Y、D74E、D74Q和D74N。仍然更优选地,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、W142H和D74E。
在特别的方面,根据本发明所述的双功能分子是融合蛋白,其包含以下或由以下组成:
(a)如上所述的抗体或其抗体片段,其与免疫细胞表面上表达的靶标、优选地T细胞、更优选地选自以下的靶标特异性地结合:PD-1、CD28、CD80、CTLA-4、BTLA、TIGIT、CD160、CD40L、ICOS、CD27、OX40、4-1BB、GITR、HVEM、Tim-1、LFA-1、TIM3、CD39、CD30、NKG2D、LAG3、B7-1、2B4、DR3、CD101、CD44、SIRPG、CD28H、CD38、CXCR5、CD3、PDL2、CD4和CD8,更优选地PD-1、TIM3、CD244、LAG-3、BTLA、TIGIT和CD160。
(b)SEQ ID No:51的人白介素7或其变体或片段,和
(c)任选地肽接头,其选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGS、GGG、GGS和(GGGS)3,优选地(GGGGS)3。
上文针对所述双功能抗PD-1分子而公开的具体的特定方面和实施方式中的所有或任一个可以应用于这些替代的双功能分子。
在特别的方面,如上所述的所述抗体或其抗原片段,其与免疫细胞表面上表达的靶标、优选地T细胞、更优选地选自以下的靶标特异性地结合:PD-1、CD28、CD80、CTLA-4、BTLA、TIGIT、CD160、CD40L、ICOS、CD27、OX40、4-1BB、GITR、HVEM、Tim-1、LFA-1、TIM3、CD39、CD30、NKG2D、LAG3、B7-1、2B4、DR3、CD101、CD44、SIRPG、CD28H、CD38、CXCR5、CD3、PDL2、CD4和CD8,更优选地PD-1、TIM3、CD244、LAG-3、BTLA、TIGIT和CD160;所述IL-7是根据本发明所述的IL-7变体,并且所述抗体或其抗体片段具有IgG1 Fc结构域,任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A,甚至更优选地,具有例如上述的突变N297A的IgGl Fc结构域。优选地,所述抗体或其片段通过选自(GGGGS)3、(GGGGS)4和(GGGS)3的接头,甚至更优选地通过(GGGGS)3,与IL-7或其变体连接。优选地,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、C47S-C92S和C34S-C129S、W142H、W142F、W142Y、D74E、D74Q和D74N。更优选地,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、W142H、W142F、W142Y、D74E、D74Q和D74N。仍然更优选地,所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、W142H和D74E。
所述双功能分子与其特定靶标的结合可以通过例如酶联免疫吸附测定(ELISA)、放射免疫测定(RIA)、FACS分析、生物测定(例如生长抑制)或蛋白印迹测定来确认。这些测定中的每一个通常通过使用对感兴趣的复合物具有特异性的标记试剂(例如,抗体)来检测特别感兴趣的蛋白-抗体复合物的存在。例如,可以使用例如识别并特异性结合IL-7或IL-7受体的酶联抗体或抗体片段来检测所述抗hPD-1抗体/IL-7复合物。
在一些实例中,本文所述的双功能分子遏制所述PD-1信号传导通路至少20%、至少40%、至少50%、至少75%、至少90%、至少100%,或至少2倍、至少5倍、至少10倍、至少20倍、至少50倍、至少100倍、或至少1000倍。优选地,这种双功能分子具有阻断或抑制PD-1与其配体(例如PD-L1和/或PD-L2)之间的相互作用的能力。在某些实施方式中,所述双功能分子抑制PD-1与其配体(例如PD-L1和/或PD-L2)之间的相互作用至少50%。在某些实施方式中,该抑制可为大于60%、大于70%、大于80%、或大于90%。
在一些实施例中,本文所述的双功能分子遏制所述PD-1信号传导通路至少20%、至少40%、至少50%、至少75%、至少90%、至少100%,或至少2倍、至少5倍、至少10倍、至少20倍、至少50倍、至少100倍或至少1000倍。
在一些实例中,本文所述的双功能分子刺激IFNγ分泌和/或α4和β7。
在另一个实例中,本文所述的双功能分子促进肿瘤中T细胞浸润。
在一些实例中,本文所述的双功能分子刺激IL-7R信号传导通路至少10%、至少20%、至少40%、至少50%、至少75%、至少90%、至少100%,或至少2倍、至少5倍、至少10倍、至少20倍、至少50倍、至少100倍或至少1000倍。
在其他方面,本文所述的双功能分子相比于野生型IL-7保留了基本上相等的IL-7生物特性。例如,其保留了与全长IL-7蛋白相当的生物特性。可以使用体外细胞增殖测定或通过ELISA或FACS测量进入T细胞的P-Stat5来测量L-7蛋白的生物活性。优选地,本文所述的IL-7双功能分子相比于野生型人IL-7保持了至少10%、20%、30%、40%、50%、60%的生物活性,相比于野生型IL-7保持了优选地至少80%、90%、95%和甚至更优选地99%的生物活性。例如,可以通过测量本文所述的双功能分子与IL-7R结合的能力和/或与野生型IL-7竞争结合IL-7R的能力来评估生物活性。
在另一个实例中,本文所述的双功能分子诱导细胞因子分泌,和/或初始、部分耗竭和/或全部耗竭T细胞亚群的增殖。
双功能分子的制备-编码所述双功能分子的核酸分子、包含其的重组表达载体和宿主细胞
为了产生本发明所述的双功能分子,本发明所述的抗hPD1抗体与IL-7或其变体功能性连接。
所述双功能分子的两个实体都在同一载体中编码并作为融合蛋白产生。因此,本文还公开了编码本文所述的双功能分子中的任一个的核酸、载体(例如表达载体)或包含这些核酸的重组病毒、和包含所述核酸和/或载体的宿主细胞。
为了生产由哺乳动物细胞以稳定形式分泌的双功能融合蛋白,根据本发明,将编码所述双功能分子的核酸序列亚克隆到通常用于转染哺乳动物细胞的表达载体中。用于生产包含抗体序列的分子的一般技术描述于Coligan等(编著),Current protocols inimmunology,第10.19.1-10.19.11页(Wiley Interscience 1992)(其内容通过引用并入本文)中和来自W.H.Freeman和Company的“Antibody engineering:a practical guide”(1992)中,其中与分子生产相关的评述散布在各个文本中。
通常,该方法包括以下步骤:
(1)用编码本发明所述的重组双功能分子的多核苷酸或其变体或包含所述多核苷酸的载体来转染或转化合适的宿主细胞;
(2)在合适的培养基中培养所述宿主细胞;和
(3)任选地从所述培养基或宿主细胞中分离或纯化所述蛋白。
本发明进一步涉及编码上述双功能分子的核酸、包含本发明所述的核酸的载体(优选表达载体)、用本发明所述的载体或直接用编码所述重组双功能分子的序列来转化的基因工程化宿主细胞、和用于通过重组技术来生产本发明所述的蛋白的方法。
下文更具体地描述了所述核酸、所述载体和所述宿主细胞。
核酸序列
本发明还涉及一种核酸分子,其编码如上文定义的双功能分子;或一种核酸分子组,其编码如上文定义的双功能分子。
抗体DNA序列可以例如由合成免疫球蛋白的细胞的RNA扩增,使用PCR利用克隆的免疫球蛋白合成,或通过编码已知的信号肽氨基酸序列的寡核苷酸合成。优选地,对于VH和/或CH,信号肽包含选自SEQ ID NO:49的氨基酸序列或由选自SEQ ID NO:49的氨基酸序列组成;和/或对于VL和/或CL,信号肽包含选自SEQ ID NO:50的氨基酸序列或由选自SEQID NO:50的氨基酸序列组成。特别地,信号肽在CH、VH、CL和/或VL的N-端。
此类核酸可以编码包含抗体的VL的氨基酸序列和/或包含抗体的VH的氨基酸序列(例如,抗体的轻链和/或重链)。使用常规程序可以容易地分离和测序此类核酸。
特别地,编码如上文定义的双功能分子的所述核酸分子包含:
-编码如本文公开的抗hPD-1抗体的可变重链结构域的第一核酸分子,其任选地具有SEQ ID NO.49的肽信号,和
-编码如本文公开的抗hPD-1抗体的可变轻链结构域的第二核酸分子,其任选地具有SEQ ID NO:50的肽信号,和
-编码IL-7或其变体、优选地人IL-7或其变体的第三核酸,其通过编码肽接头的核酸,与所述第一核酸或所述第二核酸或两者可操作地连接。
优选地,编码如上文定义的双功能分子的所述核酸分子包含:
-第一核酸分子,其编码SEQ ID NO:17的可变重链结构域,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;任选地具有SEQ ID NO.49的肽信号,和
-第二核酸分子,其编码SEQ ID NO:26的可变轻链结构域,其中X是G或T;任选地具有SEQ ID NO:50的肽信号,和
-第三核酸分子,其编码SEQ ID No:51、53、54、55、56、57、58、59、60、61、62或63的人IL-7或其变体或片段,所述人IL-7或其变体或片段任选地通过编码肽接头的核酸,与所述第一核酸或所述第二核酸或两者可操作地连接。
优选地,编码如上定义的双功能分子的核酸分子包括:
-第一核酸分子,其编码SEQ ID NO:18、19、20、21、22、23、24或25中所示的氨基酸序列的可变重链结构域;任选地具有SEQ ID NO.49的肽信号,和
-第二核酸分子,其编码SEQ ID NO:27或SEQ ID NO:28中所示的氨基酸序列的可变轻链结构域;任选地具有SEQ ID NO.50的肽信号,和
-第三核酸分子,其编码SEQ ID No:51、53、54、55、56、57、58、59、60、61、62或63的人IL-7或其变体,所述人IL-7或其变体任选地通过编码肽接头的核酸,与所述第一核酸或所述第二核酸或两者可操作地连接。
在一个非常特别的实施方式中,编码可变重链结构域的所述核酸分子具有SEQ IDNO:73中所示的序列,和/或编码可变轻链结构域的所述核酸分子具有SEQ ID NO:74中所示的序列。
可操作地连接是指所述核酸编码包含可变重链或轻链结构域、任选的肽接头、和IL-7的蛋白融合体。优选地,所述接头选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地是(GGGGS)3。
在一个实施方式中,核酸分子是分离的、特别是非天然的核酸分子。
编码根据本发明所述的双功能分子的核酸分子或核酸分子组优选地包含在载体或载体组中。
载体
在另一个方面中,本发明涉及包含如上文定义的核酸分子或核酸分子组的载体。
如本文所用,“载体”是用作载剂的核酸分子,其将遗传物质转移至细胞中。术语“载体”包含质粒、病毒、粘粒和人工染色体。在通常情况下,工程化的载体包含复制原点、多克隆位点和选择性标志物。载体本身通常是一个核苷酸序列,通常是一个DNA序列,其包含一个插入片段(转基因)和一个更大的序列,作为载体的“骨架”。除了转基因插入物和骨架之外,现代载体可能还包含其他特征:启动子、遗传标志物、抗生素抗性、报告基因、靶向序列、蛋白纯化标签。称为表达载体(表达构建体)的载体特定用于在目标细胞中表达转基因,并且通常具有控制序列。
在一个实施方式中,所述抗PD1抗体的重链编码序列和轻链编码序列和/或恒定区包含在一个表达载体中。重链编码序列和轻链编码序列的每一者可以可操作地连接至适宜启动子,所述重链和/或所述轻链与本文发明所述的免疫治疗剂可操作地连接。或者,重链和轻链两者的表达可以由相同启动子驱动。在另一个实施方式中,所述抗体的重链和轻链中的每一者克隆至单独载体中,所述重链和轻链中的一者或两者,所述重链和/或所述轻链与根据本发明所述的免疫治疗剂可操作地连接。在后一种情况下,编码重链和轻链的表达载体可以共转染至一个宿主细胞中以表达这两条链,这两条链可以在体内或体外进行组装以形成完整抗体。或者,可以将编码重链和编码轻链的表达载体引入不同宿主细胞中以表达重链和轻链两者,然后可以将其在体外纯化和组装以形成完整抗体。
本领域技术人员可以将编码人源化抗PD-1抗体或其抗体片段的核酸分子克隆至载体中,然后转化进入宿主细胞。因此,本发明还提供了一种重组载体,其包含编码本发明的抗PD-1抗体或其片段的核酸分子。在一个优选的实施方式中,表达载体还包含启动子和编码分泌信号肽的核酸序列,以及任选地包含至少一种用于筛选的抗药基因。
适宜的表达载体通常包含(1)编码细菌复制原点和抗生素抗性标志物的原核DNA元件,以提供表达载体在细菌宿主中的生长和选择;(2)控制转录起始的真核DNA元件,如启动子;和(3)控制转录物加工的DNA元件,如转录终止/聚腺苷酸化序列。
可使用本领域技术人员公知的方法构建包含本文所述抗双功能分子的核酸序列和用于转录/翻译的适宜调控组分的表达载体。这些方法包括体外重组DNA技术、DNA合成技术、体内重组技术等。DNA序列与表达载体中的适当启动子有效连接,以指导mRNA的合成。表达载体还可以包含用于启动翻译、转录终止子等的核糖体结合位点。
可以使用多种技术将表达载体引入宿主细胞,包括磷酸钙转染、脂质体介导的转染、电穿孔等。优选地,对转染细胞进行选择和增殖,其中将表达载体稳定整合至宿主细胞基因组中以产生稳定的转化体。在以下中描述了用于将载体引入真核细胞中的技术和用于使用显性可选择标记物选择稳定转化体的技术:Sambrook,Ausubel,Bebbington,“Expression of Antibody Genes in Nonlymphoid Mammalian Cells,”2METHODS:Acompanion to methods in enzymology 136(1991),和Murray(编著),Gene transfer andexpression protocols(Humana Press 1991)。在以下中描述了适宜的克隆载体:Sambrook等(编著),MOLECULAR CLONING:A LABORATORY MANUAL,第二版(Cold Spring HarborPress 1989)(下文称为“Sambrook”);Ausubel等(编著),CURRENT PROTOCOLS INMOLECULAR BIOLOGY(Wiley Interscience 1987)(下文称为“Ausubel”);和Brown(编著),MOLECULAR BIOLOGY LABFAX(Academic Press 1991)。
宿主细胞
在另一个方面中,本发明涉及包含如上文定义地载体或核酸分子或核酸分子组的宿主细胞,其用于双功能分子产生目的。
如本文所用,术语“宿主细胞”旨在包括可以是或曾经是载体、外源核酸分子和编码本发明抗体构建体的多核苷酸和/或抗体构建体或双功能分子本身的受体的任何个体细胞或细胞培养物。可以通过转化、转染等方式将相应物质引入细胞。术语“宿主细胞”还旨在包括单个细胞的后代或可能后代。适宜宿主细胞包括原核细胞或真核细胞,并且还包括但不限于细菌、酵母细胞、真菌细胞、植物细胞和动物细胞,如昆虫细胞和哺乳动物细胞,例如,小鼠、家兔、猕猴或人。
在一个实施方式中,宿主细胞包含(例如,经转化具有):(1)包含核酸的载体,所述核酸编码包含抗体的VL的氨基酸序列和/或包含抗体的VH的氨基酸序列和/或抗体的恒定区,或(2)第一载体,其包含编码包含抗体的VL的氨基酸序列的核酸,和第二载体,其包含编码包含抗体的VH的氨基酸序列的核酸。
在另一个实施方式中,宿主细胞包含(例如,已用以下转化)载体,所述载体包含所述双功能分子的两个实体。优选地,宿主细胞包含(例如,已用以下转化)载体,所述载体包含编码如本文公开的抗hPD-1抗体的可变重链结构域的第一核酸分子和编码如本文公开的抗hPD-1抗体的可变轻链结构域的第二核酸分子,所述第一核酸分子和所述第二核酸分子与编码IL-7或其变体或突变体、优选地人IL-7或其变体的第三核酸可操作地连接。
本文还提供了一种人源化抗PD1抗体的生产方法。该方法包括在适于表达抗体的条件下培养如上文所提供的包含编码抗体的核酸的宿主细胞,并且任选地从宿主细胞(或宿主细胞培养基)回收抗体。特别地,为了重组生产人源化抗PD1抗体,分离编码抗体(例如,如上文所述的)的核酸,并插入一个或多个载体,以进一步在宿主细胞中克隆和/或表达。
本发明所述的双功能分子优选地在真核细胞(例如哺乳动物细胞、植物细胞、昆虫细胞或酵母细胞)中表达。哺乳动物细胞是特别优选的真核宿主,因为哺乳动物细胞提供适宜的翻译后修饰,如糖基化。优选地,此类适宜的真核宿主细胞可以是真菌,如毕赤酵母(Pichia pastoris)、酿酒酵母(Saccharomyces cerevisiae)、粟酒裂殖酵母(Schizosaccharomyces pombe);昆虫细胞,如东方粘虫(Mythimna separate);植物细胞,如烟草,和哺乳动物细胞,如BHK细胞、293细胞、CHO细胞、NSO细胞和COS细胞。有用的哺乳动物宿主细胞系的其他实例是具有SV40基因的CV-1来源细胞(COS细胞)、由SV40转化的猴肾CV1系(COS-7);人胚肾细胞系(293或293细胞,如例如在Graham,F.L.等,J.Gen Virol.36(1977)59-74中描述的);幼仓鼠肾细胞(BHK);小鼠塞尔托利细胞(TM4细胞,如例如在Mather,J.P.,Biol.Reprod.23(1980)243-252中描述的);人肾上皮细胞(HEK细胞);猴肾细胞(CV1);非洲绿猴肾细胞(VERO-76);人宫颈癌细胞(HELA);犬肾细胞(MDCK);水牛大鼠肝细胞(BRL 3A);人肺细胞(W138);人肝细胞(Hep G2);小鼠乳腺肿瘤(MMT 060562);TRI细胞,如例如在Mather,J.P.等,Annals N.Y.Acad.Sci.383(1982)44-68中描述的;MRC 5细胞;和FS4细胞。其他有用的哺乳动物宿主细胞系包括中国仓鼠卵巢(CHO)细胞,包括DHFR"CHO细胞(Urlaub,G.等,Proc.Natl.Acad.Sci.USA 77(1980)4216-4220);和骨髓瘤细胞系,如Y0、NSO和Sp2/0。对于适于生产抗体的某些哺乳动物宿主细胞系的综述,参见,例如,Yazaki,P.和Wu,A.M.,Methods in Molecular Biology,Vol.248,Lo,B.K.C.(编著),Humana Press,Totowa,NJ(2004),pp.255-268。例如,适于在悬液中生长的哺乳动物细胞系可能是有用的。
特别地,本发明的宿主细胞选自以下:CHO细胞、COS细胞、NSO细胞和HEK细胞。
对于哺乳动物宿主,表达载体的转录和翻译调控信号可以来源于病毒来源,如腺病毒、牛乳头瘤病毒、猿猴病毒等,其中调控信号与具有高表达水平的特定基因相关。适宜的转录和翻译调控序列也可以从哺乳动物基因获得,如肌动蛋白、胶原蛋白、肌球蛋白和金属硫蛋白基因。
可以使用多种方法鉴定生产根据本发明所述的双功能分子的稳定转化体。鉴定出分子生产细胞之后,将宿主细胞在适合其生长和双功能分子表达的条件(例如,温度、培养基)下培养。然后,通过本领域公知的任何方法分离和/或纯化人源化抗体。这些方法包括但不限于常规复性处理、蛋白沉淀剂(例如盐沉淀)处理、离心、通过渗透的细胞裂解、超声、超速离心、分子筛层析法或凝胶层析法、吸附层析法、离子交换层析法、HPLC、任何其他液相层析法及其组合。如例如Coligan所描述的,双功能分子分离技术可以特别地包括使用蛋白A琼脂糖的亲和层析法、体积排阻层析法和离子交换层析法。优选地将蛋白A用于分离本发明所述的双功能分子。
药物组合物及其施用方法
本发明还涉及一种药物组合物,其包含本文所述的双功能分子中的任一个,如上文所述的核酸分子、核酸分子组、载体和/或宿主细胞,优选地为活性成分或化合物。可以将制剂灭菌,且如有需要与如药学上可接受的载体和赋形剂的辅助剂混合,所述辅助剂不与本发明所述的双功能分子,本发明所述的核酸、载体和/或宿主细胞有害地相互作用。任选地,药物组合物还可以包含如下文详细描述的另外的治疗剂。
优选地,本发明所述的药物组合物可以包含如本文所述的双功能分子,如上文所述的核酸分子、核酸分子组、载体和/或宿主细胞,与一种或多种如下文所述的药学上或生理学上可接受的载体、稀释剂、赋形剂、盐和抗氧化剂组合。理想地,使用不会不利地影响根据本发明所述的双功能分子的所需免疫增强作用的药学上可接受的形式。为了便于施用,可以将如本文所述的双功能分子制成供体内施用的药物组合物。在本领域中已描述了制备此类组合物的方法(参见例如Remington:The Science and Practice of Pharmacy,Lippincott Williams&Wilkins,第21版(2005))。
特别地,可以将根据本发明所述的药物组合物制成任何常规施用途径,包括局部、肠内、口服、肠胃外、鼻内、静脉内、肌内、皮下或眼内施用等。优选地,将根据本发明所述的药物组合物配制成用于肠内或肠胃外施用途径。用于肠胃外施用的组合物和制剂可以包括无菌水溶液,其还可以包含缓冲剂、稀释剂和其他适宜的添加剂,例如但不限于渗透促进剂、载体(carder)化合物和其他药学上可接受的载体或赋形剂。
药物组合物可以通过将具有所需纯度的试剂与任选的药学上可接受的载体、赋形剂或稳定剂(Remington's Pharmaceutical Sciences第16版,Osol,A.编著(1980))混合来制备,其呈冻干制剂或水溶液形式。可接受的载体、赋形剂或稳定剂在所使用的剂量和浓度下对受体是无毒的,并且包括缓冲剂,如磷酸盐、柠檬酸盐和其他有机酸;抗氧化剂,包括抗坏血酸和甲硫氨酸;防腐剂(例如十八烷基二甲基苄基氯化铵;氯化六甲铵;苯扎氯铵,苄索氯铵;苯酚、丁醇或苯甲醇;如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯等烷基酯;儿茶酚;间苯二酚;环己醇;3-戊醇;和间甲酚);低分子量(小于约10个残基)多肽;蛋白,如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,如聚乙烯吡咯烷酮;氨基酸,如甘氨酸、谷氨酰胺、天冬酰胺、组氨酸、精氨酸或赖氨酸;单糖、二糖和其他碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,如EDTA;糖,如蔗糖、甘露醇、海藻糖或山梨糖醇;成盐抗衡离子,如钠;金属配合物(例如,Zn-蛋白配合物);和/或非离子表面活性剂,如TWEENTM、PLURONICSTM或聚乙二醇(PEG)。
固体药学上可接受的载剂可以包括一种或多种物质,其还可以作为调味剂、润滑剂、增溶剂、悬浮剂、染料、填充剂、助流剂、压缩助剂、惰性粘合剂、甜味剂、防腐剂、染料、包衣或片剂崩解剂。适宜的固体载剂包括例如磷酸钙、硬脂酸镁、滑石、糖、乳糖、糊精、淀粉、明胶、纤维素、聚乙烯吡咯烷、低熔点蜡和离子交换树脂。药学上可接受的载体包括无菌水溶液或分散液以及用于临时制备无菌可注射溶液或分散液的无菌粉末。除非任何常规介质或药剂与活性化合物不相容,否则考虑将其用于本发明所述的药物组合物中。
根据本发明所述的双功能分子可以溶解或混悬在药学上可接受的液体载剂中,如水、有机溶剂、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇)及其类似物、两者的混合物或药学上可接受的油或脂肪及其适宜混合物。液体载体可以包含其他适宜的药物添加剂,如增溶剂、乳化剂、缓冲剂、防腐剂、甜味剂、调味剂、悬浮剂、润湿剂、增稠剂、着色剂、粘度调节剂、稳定剂或渗透压调节剂。用于口服和肠内施用的液体载体的适宜实例包括水(部分包含上述添加剂,例如,纤维素衍生物,优选羧甲基纤维素钠溶液)、醇类(包括一元醇和多元醇,例如,二醇)及其衍生物和油(例如,分馏椰子油和花生油)。对于肠胃外施用而言,载剂还可以是油性酯,如油酸乙酯和肉豆蔻酸异丙酯。无菌液体载剂可用于经肠施用的无菌液体形式组合物。用于加压组合物的液体载剂可以是卤代烃或其他药学上可接受的推进剂。
本发明所述的药物组合物还可以包含一种或多种药学上可接受的盐。“药学上可接受的盐”指保留母体化合物的所需生物活性并且不产生任何不希望的毒理学作用的盐。此类盐的实例包括酸加成盐和碱加成盐。酸加成盐包括来源于无毒无机酸,如盐酸、硝酸、磷酸、硫酸、氢溴酸、氢碘酸、磷酸等,以及来源于无毒有机酸,如脂肪族一元和二元羧酸、苯基取代的链烷酸、羟基链烷酸、芳香酸、脂肪族和芳香族磺酸等。碱加成盐包括来源于碱金属或碱土金属的那些,如钠、钾、镁、钙等,以及来源于无毒有机胺,如Ν,Ν'-二苄基乙二胺、N-甲基葡糖胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、普鲁卡因等的那些。
本发明所述的药物组合物还可以包含药学上可接受的抗氧化剂。药学上可接受的抗氧化剂的实例包括:水溶性抗氧化剂,如抗坏血酸、盐酸半胱氨酸、硫酸氢钠、焦亚硫酸钠、亚硫酸钠等;油溶性抗氧化剂,如抗坏血酸棕榈酸酯、丁基羟基茴香醚(BHA)、丁基羟基甲苯(BHT)、卵磷脂、没食子酸丙酯、α-生育酚等;金属螯合剂,如柠檬酸、乙二胺四乙酸(EDTA)、山梨糖醇、酒石酸、磷酸等。
为了便于递送,可以将所述双功能分子中的任一个或其编码核酸与伴侣剂(chaperon agent)缀合。伴侣剂可以是天然存在的物质,如蛋白(例如,人血清白蛋白、低密度脂蛋白或球蛋白)、碳水化合物(例如,葡聚糖、支链淀粉、几丁质、壳聚糖、菊粉、环糊精或透明质酸)或脂质。其也可以是重组或合成分子,如合成聚合物,例如,合成聚氨基酸。聚氨基酸的实例包括聚赖氨酸(PLL)、聚L天冬氨酸、聚L谷氨酸、苯乙烯-马来酸酐共聚物、聚(L-丙交酯-共-乙二醇)共聚物、二乙烯基醚-马来酸酐共聚物、N-(2-羟丙基)甲基丙烯酰胺共聚物(HMPA)、聚乙二醇(PEG)、聚乙烯醇(PVA)、聚氨酯、聚(2-乙基丙烯酸)、N-异丙基丙烯酰胺聚合物和聚磷嗪。在一个实施方式中,所述伴侣剂是胶束、脂质、纳米颗粒或微球。用于制备此类胶束、脂质体、纳米颗粒或微球的方法是本领域众所周知的。参见例如美国专利5,108,921;5,354,844;5,416,016;和5,527,5285。
药物组合物在生产和贮存条件下通常必需是无菌和稳定的。可以将药物组合物制成溶液、微乳、脂质体或其他适合高药物浓度和/或适合注射的有序结构。可以保持适当的流动相,例如,通过使用包衣,如卵磷脂,在分散剂的情况下通过保持所需粒径和通过使用表面活性剂。
在一个实施方式中,药物组合物是可注射组合物,其可以包含各种载体,如植物油、二甲基乙酰胺、二甲基甲酰胺、乳酸乙酯、碳酸乙酯、肉豆蔻酸异丙酯、乙醇和多元醇(甘油、丙二醇、液态聚乙二醇等)。对于静脉内注射,水溶性抗体可以通过滴注法给药,由此输注含有抗体和生理学上可接受的赋形剂的药物制剂。生理学上可接受的赋形剂可以包含例如5%右旋糖、0.9%盐水、林格氏溶液或其他适宜赋形剂。肌内制剂,例如,抗体的适宜可溶性盐形式的无菌制剂,可以在药物赋形剂中溶解并施用,如注射用水、0.9%盐水或5%葡萄糖溶液。
无菌可注射溶液可以通过将所需量的活性化合物掺入适当的溶剂中制备,根据需要,将上述一种或多种成分组合,然后进行灭菌微滤。通常,分散剂是通过将活性化合物掺入无菌载体中来制备的,所述载体包含碱性分散介质和来自上文列举的那些所需的其他成分。在用于制备无菌可注射溶液的无菌粉末的情况下,优选的制备方法是真空干燥和冷冻干燥(冻干),从其先前无菌过滤的溶液中产生活性成分加上任何额外的所需成分的粉末。可注射组合物的延长吸收可以通过在组合物中包含延迟吸收的试剂例如单硬脂酸盐和明胶来实现。
可以通过灭菌程序和包含各种抗菌剂和抗真菌剂,例如氯丁醇、山梨酸苯酚等来确保防止微生物的存在。在组合物中包含等渗剂,如糖、氯化钠等也可能是所需的。此外,可注射药物形式的延长吸收可以通过包含延迟吸收的试剂如单硬脂酸铝和明胶来实现。
本领域技术人员将理解,本发明的制剂可以与人血液等渗,即本发明的制剂具有与人血液基本相同的渗透压。此类等渗制剂通常具有从约250mOSm至约350mOSm的渗透压。等渗性可以通过例如蒸汽压或冰冻型渗透压计来测量。通过使用张力调节剂来调节制剂的张力。“张力调节剂”是那些药学上可接受的惰性物质,其可以加入到制剂中以提供制剂的等渗性。适用于本发明的张力调节剂包括但不限于糖类、盐类和氨基酸。
可以配制根据本发明所述的药物组合物以在施用后基本上立即或在施用后的任何预定时间或时间段释放活性成分(例如,本发明所述的双功能分子)。在一些方面,药物组合物可以采用延时释放、延迟释放和持续释放递送系统,使得组合物的递送发生在待治疗部位的致敏之前并且有足够的时间引起待治疗部位的致敏。可以使用本领域公知的方法来防止或最小化组合物的释放和吸收,直到其到达靶组织或器官,或确保组合物的定时释放。这样的系统可以避免组合物的重复给药,从而增加受试者和医生的便利性。
可与载体材料组合以产生单一剂型的活性成分的量将根据所治疗的受试者和特定的给药方式而变化。可与载体材料组合以产生单一剂型的活性成分的量通常是产生治疗效果的组合物的量。
受试者、方案和施用
本发明涉及如本文所述的双功能分子;编码其的核酸或载体,宿主细胞或药物组合物,核酸,载体或宿主细胞,其用作药物,或用于治疗疾病或用于在受试者中施用或用作药物。其还涉及本发明的药物组合物、核酸、载体或宿主细胞或者包含抗PD1抗体或其抗体片段和IL-7或其变体的双功能分子在制备用于在受试者中治疗疾病的药物中的用途。最后,其涉及用于在受试者中治疗疾病或病症的方法,其包括向所述受试者施用治疗有效量的药物组合物或包含抗PD1抗体或其抗体片段和IL-7或其变体的双功能分子。在下文的“方法和用途”部分更具体地描述了治疗的实例。
待治疗的受试者可以是人,特别是处于产前阶段的人、新生儿、儿童、婴儿、青少年或成人、特别是至少30岁、40岁的成人、优选地至少50岁的成人、另外更优选地至少60岁的成人、甚至更优选地至少70岁的成人。
特别地,受试者患有可能涉及PD-1/PDL-1通路,特别是其中表达、特别是过表达PD-1的配体(例如,PDL-1和/或PDL-2)或PD-1中的至少一种的疾病。优选地,受试者患有癌症、甚至更优选地患有PD1、PD-L1和/或PD-L2阳性癌症或PD-1阳性癌症。疾病和癌症的实例在下文“方法和用途”部分更具体地描述。
在一个特别的实施方式中,在施用包含根据本发明所述的抗PD1抗体或其抗体片段和IL-7或其变体的双功能分子或根据本发明所述的药物组合物之前,受试者已接受至少一线治疗,优选地若干线治疗。
可使用本领域普通技术人员公知的常规方法向受试者施用双功能分子或本文公开的药物组合物,其取决于要质量的疾病类型或疾病部位。该组合物可以通过常规途径施用,例如,口服、肠胃外、肠内、通过吸入喷雾、局部、直肠、鼻腔、口腔、阴道或通过植入的储库施用。如本文所用,术语“肠胃外”包括皮下、皮内、静脉内、肌内、关节内、动脉内、滑膜内、肿瘤内、胸骨内、鞘内、病灶内和颅内注射或输液技术。当肠胃外给药时,本发明所述的药物组合物优选通过静脉内给药途径施用。当经肠施用时,本发明所述的药物组合物优选通过口服给药途径施用。该组合物也可以局部施用。
根据本发明所述的药物组合物或双功能分子的药物组合物的形式、施用途径和施用剂量可由本领域技术人员根据感染的类型和严重程度以及患者,特别是其年龄、体重、性别和一般身体状况进行调整。本发明的组合物可以多种方式给药,这取决于需要局部治疗还是全身治疗。
优选地,用所述双功能分子或用根据本发明所述的药物组合物进行的治疗定期施用,优选地,在每天、每周或每月之间,更优选地,在每天与每周、每两周、每三周或每四周之间。在一个特别的实施方式中,治疗一天施用若干次,优选地一天2次或3次。
用所述双功能分子或用根据本发明所述的药物组合物进行的治疗的持续时间优选地介于1天至20周之间、更优选地介于1天至10周之间、另外更优选地介于1天至4周之间、甚至更优选地介于1天至2周之间。或者,治疗可持续至与疾病持续一样长。
本文公开的双功能分子可以在约1ng/kg体重至约30mg/kg体重、1μg/kg至约20mg/kg、10μg/kg至约10mg/kg、或从100μg/kg至5mg/kg的范围内的有效剂量,任选地每一周、两周、三周或四周,优选地通过肠胃外或口服施用,特别是通过静脉内或皮内施用提供。
特别地,根据本发明所述的双功能分子可以低于治疗剂量施用。如本文所用,术语“亚治疗剂量”指低于通常用于治疗疾病的有效单一疗法剂量水平的剂量,或当前通常不用于使用抗hPD1抗体进行有效单一疗法的剂量。
方法和用途
在治疗疾病中的用途
本发明所述的双功能分子、核酸、载体、宿主细胞、组合物和方法具有多种体外和体内效用和应用。例如,本文所述的双功能分子、核酸、载体、宿主细胞和/或药物组合物可以用作治疗剂、诊断剂和医学研究。特别地,本文提供的任何双功能分子、核酸分子、核酸分子组、载体、宿主细胞或药物组合物可以用于治疗方法中和/或用于治疗目的。特别地,本文提供的双功能分子、核酸、载体或药物组合物可以用于治疗任何疾病或病况,所述疾病或病况优选地涉及PD-1,例如癌症、自身免疫疾病和感染,或者与免疫缺陷相关的其他疾病,例如T细胞功能障碍。
甚至更优选地,本发明涉及一种在有需要的受试者中治疗选自以下的疾病和/或病症的方法:癌症、感染性疾病和慢性病毒感染,所述方法包括向所述受试者施用有效量的如上文定义的双功能分子或药物组合物。在下文中更明确地描述了此类疾病的实例。
特别地,根据本发明所述的双功能分子被称为“双功能检查点抑制剂”,因为其靶向PD-1/PD-L1/PD-L2和IL7通路。
本发明特别涉及双功能分子,编码其的核酸、核酸组或载体,或者包含其的药物组合物用于治疗能够通过抑制PD-L1和/或PD-L2与PD-1的结合而预防或治疗的病变、疾病和/或病症。
根据本发明所述的双功能分子靶向CD127+免疫细胞,特别是CD127+T细胞。这种细胞可在以下特别感兴趣的区域中发现:淋巴结中的常驻淋巴细胞(主要在副皮质内,偶尔有细胞在滤泡中),扁桃体(滤泡间区域),脾脏(主要在白髓的小动脉周围淋巴鞘(PALS)和红髓中的一些分散细胞中),胸腺(主要在髓质中;也在皮质中),骨髓(分散分布),整个消化道(胃、十二指肠、空肠、回肠、盲肠结肠、直肠)的GALT(肠道相关淋巴组织,主要在毛囊间区域和固有层中)中,胆囊的MALT(粘膜相关淋巴组织)中。因此,本发明所述的双功能分子对于治疗位于或涉及这些区域的疾病(特别是癌症)具有特别的意义。
因此,本文公开了用于治疗特别与PD-1和/或PD-1/PD-L1和/或PD-1/PD-L2信号传导通路相关的疾病的方法,其包括向需要治疗的受试者施用有效量的本文所述的双功能分子或药物组合物中的任一个。还必须考虑患者的生理数据(例如,年龄、体型和体重)和施用途径来确定合适的剂量,以便给予患者治疗有效量。
在另一个方面中,可以例如在体内向受试者施用本文所述的双功能分子以增强免疫,优选地以治疗病症和/或疾病。因此,在一个方面中,本发明提供了一种改变受试者的免疫应答的方法,其包括向受试者施用本发明所述的双功能分子、核酸、载体或药物组合物,以使得在受试者中的免疫应答被改变。优选地,免疫应答被增强、增加、刺激或上调。所述双功能分子或药物组合物可以用于在需要治疗的受试者中增强免疫应答。如T细胞激活。免疫应答增强可以导致PD-L1和/或PD-L2与PD-1的结合抑制,从而减少免疫抑制环境,刺激人T细胞的增殖和/或激活和/或人PBMC的IFNγ分泌。
本发明特别地提供了一种在受试者中增强免疫应答的方法,其包括向所述受试者施用治疗有效量的本文所述的双功能分子、核酸、载体或包含其的药物组合物中的任一个,以使得在所述受试者中的免疫应答是增强的。
在一些实施方式中,本文所述的双功能分子的量在抑制PD-1信号传导中是有效的(例如,与对照相比,降低PD-1信号传导至少20%、30%、50%、80%、100%、200%、400%或500%)。在其他实施方式中,本文所述的双功能分子的量在激活免疫应答中是有效的(例如,与对照相比,激活至少20%、30%、50%、80%、100%、200%、400%或500%)。
在一些实施方式中,本文所述的双功能分子的量在抑制人PD-L1和/或PD-L2与人PD-1的结合中是有效的(例如,与对照相比,抑制结合至少20%、30%、50%、80%、100%、200%、400%或500%)。
在一些实施方式中,本文所述的双功能分子的量足以具有人PD-L1和/或PD-L2与人PD-1结合的拮抗剂活性(例如,与对照相比,抑制结合至少20%、30%、50%、80%、100%、200%、400%或500%)。
本发明还涉及如本文所述的用于在受试者中治疗病症和/或疾病和/或用作药物或疫苗的双功能分子、编码其的核酸或载体、或包含其的药物组合物。其还涉及如本文所述的双功能分子、编码其的核酸或载体、或包含其的药物组合物在制备用于在受试者中治疗病症和/或疾病的药物中的用途。最后,其涉及用于在受试者中治疗疾病或病症的方法,其包括向所述受试者施用治疗有效量的药物组合物或双功能分子。
本文公开了治疗患有疾病和/或病症的患者的方法,其包括:(a)识别需要治疗的患者;和(b)向所述患者施用治疗有效量的本文所述的双功能分子、核酸、载体或药物组合物中的任一个。
需要治疗的受试者可以是患有、有风险患有或怀疑患有与PD-1介导的信号传导途径相关的疾病的人。可以通过常规医学检查来识别这样的患者。例如,可以通过检查此类受试者是否携带PD-1、PD-L1和/或PD-L2阳性细胞来识别适合所述治疗的受试者。优选地,“PD-L1阳性细胞”或“PD-L2阳性肿瘤细胞”旨在指代肿瘤细胞群体,其中PD-L1或PD-L2分别在10%的肿瘤细胞,优选地至少20%、30%、40%或50%的肿瘤细胞中表达。
在一个实施方式中,需要治疗的受试者是患有、怀疑患有或有风险患有疾病的患者,所述疾病优选地为PD-1、PDL1和/或PDL2阳性疾病,甚至更优选为其中PD-1和/或至少一种PD-1配体过表达的疾病。在这样的受试者中,由于根据本发明所述的双功能分子或药物组合物的施用,PD-1/PD-L1和/或PD-1/PD-L2相互作用的破坏可以增强所述受试者的免疫应答。在一些实施方式中,本文所述的人源化抗PD-1抗体或药物组合物中的任一个可用于治疗PD-1阳性细胞。
-癌症
本领域公知,抗体对PD-1的阻断能够增强患者中针对癌细胞的免疫应答。因此,在一个方面中,本发明提供了一种双功能分子或药物组合物,其用于治疗患有癌症的受试者的用途,其包括向个体施用有效量的所述双功能分子或药物组合物,优选地以破坏或抑制PD1/PD-L1和/或PD1/PD-L2相互作用,和/或激活IL7受体。
在一个实施方式中,需要治疗的受试者是患有、疑似患有或处于疾病风险中的患者,优选地PD-1或PD-L1阳性癌症,甚至更优选地,其中PD-1表达或过表达的癌症。在一些实施方式中,本文所述的抗PD-1抗体或药物组合物中的任一个可以用于治疗PD-1阳性肿瘤细胞。例如,通过考察此类患者是否携带PD-1阳性肿瘤细胞能够鉴定适于治疗的患者。
在另一个实施方式中,受试者是患有、疑似患有或处于癌症进展风险中的患者,优选地PD-L1和/或PD-L2阳性癌症。在一些实施方式中,本文所述的双功能分子或药物组合物中的任一个能够用于治疗PD-L1和/或PD-L2阳性肿瘤。例如,通过考察是否此类患者携带PD-L1和/或PD-L2阳性癌细胞能够鉴定适于治疗的人类患者。
在其他方面中,提供了一种双功能分子或药物组合物,其用于治疗癌症、优选地PD-1、PD-L1和/或PD-L2阳性癌症、甚至更优选地其中PD-1、PD-L1和/或PD-L2过表达的癌症。
在另一个实施方式中,本发明提供了如本文公开的双功能分子或药物组合物在制备用于在受试者中治疗癌症(例如抑制肿瘤细胞(优选地PD-1、PD-L1或PD-L2阳性肿瘤细胞)生长)的药物中的用途。
在本公开内容的一个方面中,待治疗的癌症与耗竭T细胞相关。
因此,在一个实施方式中,本发明提供了一种治疗癌症(例如用于抑制受试者中肿瘤细胞生长)的方法,其包括向所述受试者施用治疗有效量的根据本发明所述的双功能分子或药物组合物。特别地,本发明涉及使用双功能分子治疗受试者从而抑制癌细胞的生长。
可以使用本文提供的双功能分子来治疗的任何适宜癌症可以是造血系统癌症或实体癌。此类癌症包括癌瘤、宫颈癌、结肠直肠癌、食管癌、胃癌、胃肠癌、头颈癌、肾癌、肝癌、肺癌、淋巴瘤、胶质瘤、间皮瘤、黑色素瘤、胃癌、尿道癌、环境诱发的癌症以及所述癌症的任何组合。本发明还用于治疗转移性癌症,特别是表达PD-L1的转移性癌症(Iwai等,(2005)Int.Immunol.17:133-144)。此外,本发明包括难治性或复发性恶性肿瘤。
优选地,待治疗或预防的癌症选自转移性或非转移性黑色素瘤、恶性间皮瘤、非小细胞肺癌、肾细胞癌、霍奇金氏淋巴瘤、头颈癌、尿道上皮癌、结直肠癌、肝细胞癌、小细胞肺癌、转移性梅克尔细胞癌、胃癌或食道癌和宫颈癌。
在一个特别的方面中,癌症是高表达PD-1和/或PD-L1的血液系统恶性肿瘤或实体瘤。此类癌症可以选自以下:淋巴造血系统肿瘤、血管免疫母细胞性T细胞淋巴瘤、骨髓增生异常综合征、急性髓性白血病。
在一个特别的方面中,癌症是由病毒诱导的或与免疫缺陷相关的癌症。此类癌症可以选自以下:卡波西氏肉瘤(例如,与卡波西氏肉瘤疱疹病毒相关);宫颈、肛门、阴茎和外阴鳞状细胞癌以及口咽癌(例如,与人乳头瘤病毒相关);B细胞非霍奇金氏淋巴瘤(NHL),包括弥漫性大B细胞淋巴瘤、伯基特氏淋巴瘤、浆母细胞淋巴瘤、原发性中枢神经系统淋巴瘤、HHV-8原发性渗出性淋巴瘤、经典霍奇金氏淋巴瘤和淋巴增生性病症(例如,与爱泼斯坦-巴尔病毒(EBV)和/或卡波西氏肉瘤疱疹病毒相关的);肝细胞癌(例如,与乙型肝炎和/或丙型肝炎病毒相关的);梅克尔细胞癌(例如,与梅克尔细胞多瘤病毒(MPV)相关的);和与人免疫缺陷病毒感染(HIV)相关的癌症。
优选的治疗癌症包括通常对免疫疗法起响应的癌症。或者,优选的治疗癌症是对免疫疗法无响应的癌症。
优选地,本文公开的双功能分子、核酸、载体、宿主细胞或组合物用于治疗患有预后不良的癌症的受试者。如本文所用,术语“不良预后”是指降低的受试者存活和/或早期癌症进展和/或增加的或早期癌症复发和/或增加的转移风险或增加的转移发生。特别是,不良预后与其中肿瘤中存在Treg细胞群体或其中肿瘤中Treg/Teff比率高的癌症相关(Chraa等,2018J Leukoc Biol.2018;1-13.)
举例而言且不希望受到理论束缚,用抗癌抗体或抗癌免疫缀合物或其他导致癌细胞死亡的当前抗癌疗法进行治疗将加强由PD-1介导的免疫应答。因此,过度增殖性疾病(例如,癌症肿瘤)的治疗可包括双功能分子与抗癌治疗的组合,同时或顺序或其任何组合,这可能会增强宿主的抗肿瘤免疫应答。优选地,可以将双功能分子与其他免疫原性药剂、标准癌症治疗或其他抗体联合使用。
-感染性疾病
本发明所述的双功能分子、核酸、核酸组、载体、宿主细胞或药物组合物用于治疗已暴露于特定毒素或病原体的患者。因此,本发明的一个方面提供了一种在受试者中治疗感染性疾病的方法,其包括向所述受试者施用根据本发明所述的双功能分子或包含其的药物组合物,优选地以使得所述受试者的感染性疾病得到治疗。
可以使用本文提供的根据本发明所述的双功能分子、核酸、核酸组、载体、宿主细胞或药物组合物来治疗任何适宜的感染。引起可由本发明方法治疗的感染的致病性病毒的一些实例包括HIV、肝炎(甲型、乙型或丙型)、疱疹病毒(例如,VZV、HSV-1、HAV-6、HSV-II和CMV、爱泼斯坦巴尔病毒)、腺病毒、流感病毒、黄病毒、埃可病毒、鼻病毒、柯萨奇病毒、冠状病毒、呼吸道合胞病毒、腮腺炎病毒、轮状病毒、麻疹病毒、风疹病毒、细小病毒、痘苗病毒、HTLV病毒、登革热病毒、乳头瘤病毒、软疣病毒、脊髓灰质炎病毒、狂犬病毒、JC病毒和虫媒脑炎病毒。
特别地,本发明所述的双功能分子或药物组合物用于治疗患有慢性病毒感染的患者,此类感染由选自以下的病毒引起:逆转录病毒、指环病毒、圆环病毒、疱疹病毒、水痘带状疱疹病毒(VZV)、巨细胞病毒(CMV)、爱泼斯坦-巴尔病毒(EBV)、多瘤病毒BK、多瘤病毒、腺相关病毒(AAV)、单纯疱疹1型(HSV-1)、腺病毒、单纯疱疹2型(HSV-2)、卡波西氏氏肉瘤疱疹病毒(KSHV)、乙型肝炎病毒(HBV)、GB病毒C、乳头瘤病毒、丙型肝炎病毒(HCV)、人类免疫缺陷病毒(HIV)、丁型肝炎病毒(HDV)、人T细胞白血病病毒1型(HTLV1)、异嗜性鼠白血病病毒相关病毒(XMLV)、风疹病毒、德国麻疹、细小病毒B19、麻疹病毒、柯萨奇病毒。
引起可由本发明方法治疗的感染的致病性细菌的一些实例包括衣原体、立克次体细菌、分枝杆菌、葡萄球菌、链球菌、肺炎球菌、脑膜炎球菌和链球菌、克雷伯菌、变形杆菌、沙雷氏菌、假单胞菌、军团菌、白喉、沙门氏菌、杆菌、霍乱、破伤风、肉毒杆菌、炭疽、鼠疫、钩端螺旋体病和莱姆病细菌。
引起可由本发明方法治疗的感染的致病性真菌的一些实例包括念珠菌属(白色念珠菌、克鲁斯念珠菌、光滑念珠菌、热带念珠菌等)、新型隐球菌、曲霉属(烟曲霉、黑曲霉等)、毛霉菌目(毛霉菌属、犁头霉属、根霉属)、申基孢子丝菌、皮炎芽生菌、巴西副球孢子菌、粗球孢子菌和荚膜组织胞浆菌。
引起可由本发明方法治疗的感染的致病性寄生虫的一些实例包括溶组织内阿米巴、大肠蠕虫、福氏耐格里阿米巴、棘阿米巴虫属、蓝氏贾弟鞭毛虫、隐孢子虫属、卡氏肺囊虫、间日疟原虫、小巴贝斯虫、布氏锥虫、克氏锥虫、多诺瓦利什曼原虫、刚地弓形虫和巴西日圆线虫。
在所有上述方法中,所述双功能分子可与诸如细胞因子治疗(例如,干扰素、GM-CSF、G-CSF、IL-2)的其他形式的免疫疗法或增强肿瘤抗原呈递的任何疗法联合。
联合疗法
特别地,根据本发明所述的双功能分子可以与一些其他潜在的策略相结合,以克服临床开发中或已经上市药物的免疫逃避机制(参见来自Antonia等,Immuno-oncologycombinations:a review of clinical experience and future prospects.Clin.CancerRes.Off.J.Am.Assoc.Cancer Res.20,6258–6268,2014的表1)。这种与根据本发明所述的双功能分子的组合可特别用于:
1-逆转适应性免疫的抑制(阻断T细胞检查点途径);
2-开启适应性免疫(使用激动剂分子(特别是抗体)促进T细胞共刺激受体信号传导);
3-改善先天性免疫细胞的功能;
4-激活免疫系统(增强免疫细胞效应功能),例如通过基于疫苗的策略。
因此,本文还提供了用于与如本文所述的PD-1信号传导相关的任何疾病的联合疗法,其使用如本文所述的双功能分子或包含其的药物组合物中的任一个以及合适的第二药剂。在一个方面中,所述双功能分子和所述第二药剂可存在于如上文所述的药物组合物中。或者,如本文所用,术语“联合疗法”或“联合的疗法”包括以顺序方式施用这些药剂(例如,如本文所述的双功能分子和另外或第二适宜治疗剂),即,其中每种治疗剂在不同时间施用,以及这些治疗剂或至少两种药剂以基本上同时的方式施用。顺序或基本上同时施用每种药剂可以通过任何适当途径实现。药剂可以通过相同途径或通过不同途径施用。例如,第一药剂(例如,双功能分子)可以口服施用,且另一治疗剂(例如,抗癌剂、抗感染剂或免疫调节剂)可以静脉内施用。或者,所选组合的药剂可以通过静脉内注射施用,而组合的其他药剂可以口服施用。
在另一个方面中,本发明涉及一种治疗手段,特别是组合产品手段,其包含作为活性成分的:如上文定义的双功能分子和另外的治疗剂,其中所述活性成分被配制用于单独、顺序或联合疗法,尤其是组合或顺序使用。
如本文所用,除非另有说明,否则术语“顺序”指以规则顺序或次序为特征,例如,如果给药方案包括施用双功能分子和另外的或第二药剂,则顺序给药方案可以包括在施用第二药剂之前、同时、基本同时或之后施用本发明所述的双功能分子,但两种药剂将以规则顺序或次序施用。除非另有说明,否则术语“单独”指将一个与另一个分开。除非另有说明,否则术语“同时”指同时发生或完成,即本发明所述的药剂同时施用。术语“基本上同时”指药剂在彼此相隔几分钟内(例如,彼此相隔15分钟内)施用,并且旨在包括联合施用和连续施用,但如果施用是连续的,但是,如果施用是连续的,则其在时间上只间隔很短的时间(例如,医生分别施用两种化合物所需的时间)。
应当理解,如本文所述的任何组合可以以任何顺序用于治疗本文所述的病症或疾病。可以基于多种因素来选择本文所述的组合,这些因素包括但不限于抑制或预防目标疾病进展的效用、减轻组合的另一种药剂的副作用的效用,或减轻与目标疾病相关的症状的效用。例如,本文所述的联合疗法可以降低与组合的每个单独成员相关的任何副作用。
本发明还涉及一种用于在受试者中治疗疾病的方法,其包括向所述受试者施用治疗有效量的本文所述的双功能分子或药物组合物和治疗有效量的另外的或第二治疗剂。
当本文所述的双功能分子或药物组合物与另外的治疗剂共同使用时,所述双功能分子、所述组合物或所述第二药剂的亚治疗剂量,或两者的亚治疗剂量,可用于治疗受试者,优选患有或有风险发生与由PD-1介导的细胞信号传导相关的疾病或病症的受试者。
在WO 2018/053106第36-43页上提供了另外的或第二治疗剂的具体实例。
在一个方面中,所述另外的或第二治疗剂可在包含以下的非详尽列表中选择:烷化剂、血管生成抑制剂、抗代谢物、抗有丝分裂剂、抗增殖剂、抗病毒剂、极光激酶抑制剂、凋亡促进剂(例如,Bcl-2家族抑制剂)、死亡受体通路激活剂、Bcr-Abl激酶抑制剂、BiTE(双特异性T细胞接合剂)抗体、抗体药物缀合物、生物应答调节剂、布鲁顿氏酪氨酸激酶(BTK)抑制剂、细胞周期蛋白依赖性激酶抑制剂、细胞周期抑制剂、环氧合酶-2抑制剂、DVD、白血病病毒癌基因同源物(ErbB2)受体抑制剂、生长因子抑制剂、热休克蛋白(HSP)-90抑制剂、组蛋白去乙酰化酶(HDAC)抑制剂、激素疗法、免疫药、凋亡蛋白抑制剂(IAP)的抑制剂、嵌入型抗生素、激酶抑制剂、驱动蛋白抑制剂、Jak2抑制剂、哺乳动物雷帕霉素靶蛋白抑制剂、microRNA、丝裂原激活的胞外信号调节激酶抑制剂、多价结合蛋白、非甾体抗炎药(NSAID)、聚ADP(二磷酸腺苷)-核糖聚合酶(PARP)抑制剂、铂类化学治疗剂、polo样激酶(Plk)抑制剂、磷酸肌醇-3激酶(PI3K)抑制剂、蛋白酶体抑制剂、嘌呤类似物、嘧啶类似物、受体酪氨酸激酶抑制剂、类视黄醇/类维生素D植物生物碱、小抑制性核糖核酸(siRNA)、拓扑异构酶抑制剂、泛素连接酶抑制剂、低甲基化剂、检查点抑制剂、肽疫苗等、来自肿瘤抗原的表位或新表位以及这些药剂的一种或多种的组合。例如,所述另外的治疗剂可以选自以下:化学疗法、放射疗法、靶向疗法、抗血管生成剂、低甲基化剂、癌症疫苗、来自肿瘤抗原的表位或新表位、骨髓检查点抑制剂、其他免疫疗法和HDAC抑制剂。
在一个优选的实施方式中,所述第二治疗剂选自以下:化学治疗剂、放射疗法药剂、免疫治疗剂、细胞疗法药剂(例如CAR-T细胞)、抗生素和益生菌。所述免疫治疗剂还可以是抗体靶向肿瘤抗原,特别地选自以下:抗Her2、抗EGFR、抗CD20、抗CD19、抗CD52。
在一个实施方式中,本发明涉及如上文定义的联合疗法,其中所述第二治疗剂特别地选自以下:治疗性疫苗、免疫检查点阻断剂或激活剂、特别是适应性免疫细胞(T和B淋巴细胞)和抗体-药物缀合物。优选地,用于与根据本发明所述的抗hPD-1抗体或其片段或者药物组合物共同使用的适宜药剂包括结合至共刺激受体(例如,OX40、CD40,、ICOS、CD27、HVEM或GITR)的抗体、诱导免疫原性细胞死亡的药剂(例如,化学治疗剂、放射性治疗剂、抗血管生成剂或用于靶向疗法的药剂)、抑制检查点分子(例如,CTLA4、LAG3、TIM3、B7H3、B7H4、BTLA或TIGIT)的药剂、癌症疫苗、调节免疫抑制酶(例如,IDO1或iNOS)的药剂、靶向Treg细胞的药剂、用于过继性细胞疗法的药剂或调节髓系细胞的药剂。
在一个实施方式中,本发明涉及如上文定义的联合疗法,其中所述第二治疗剂是选自以下的适应性免疫细胞(T和B淋巴细胞)的免疫检查点阻断剂或激活剂:抗CTLA4、抗CD2、抗CD28、抗CD40、抗HVEM、抗BTLA、抗CD160、抗TIGIT、抗TIM-1/3、抗LAG-3、抗2B4和抗OX40、抗CD40激动剂、CD40-L、TLR激动剂、抗ICOS、ICOS-L和B细胞受体激动剂。
在一个实施方式中,所述另外的或第二治疗剂是靶向肿瘤抗原的抗体,特别地选自以下:抗Her2、抗EGFR、抗CD20、抗CD19、抗CD52。
联合疗法还依赖于施用双功能分子与手术、化学疗法(例如,如多西他赛或达卡巴嗪)、放射疗法、免疫疗法(例如,如靶向CD40、CTLA-4的抗体)、基因靶向和调节和/或其他药剂(例如免疫调节剂、血管生成抑制剂)及其任何组合的组合。
试剂盒
本文所述的任何抗体或组合物可以包括在本发明提供的试剂盒中。本公开内容特别提供了用于增强免疫应答和/或治疗与PD-1信号传导或IL-7信号传导相关的疾病(例如,癌症和/或感染)的试剂盒。
在本发明的背景下,术语“试剂盒”指包装在容器(container/recipient)或其他中的两种或更多种组分(其中之一对应于本发明所述的双功能分子、核酸分子、载体或细胞)。因此,可以将试剂盒描述为足以达成某一目标的一组产品和/或用具,其可作为单个单元销售。
特别地,根据本发明所述的试剂盒可以包含:
-如上定义的双功能分子,
-与IL-7或其变体连接的抗hPD1抗体或其抗原结合片段
-编码所述双功能分子的核酸分子或核酸分子组,
-包含所述核酸分子或核酸分子组的载体,和/或
-包含所述载体或核酸分子或核酸分子组的细胞。
因此,在合适的容器手段中,所述试剂盒可以包含本发明所述的药物组合物和/或双功能分子和/或宿主细胞,和/或编码本发明所述的核酸分子和/或核酸分子的载体,和/或本发明所述的酸分子或相关试剂。在一些实施方式中,可以提供从个体获取样品和/或测定样品的手段。在某些实施方式中,所述试剂盒包含细胞、缓冲剂、细胞培养基、载体、引物、限制性酶、盐等。试剂盒还可以包含用于容纳无菌、药学上可接受的缓冲剂和/或其他稀释剂的构件。
所述容器可以是单位剂量、散装包装(例如,多剂量包装)或亚单位剂量。在一个实施方式中,本发明涉及如上文定义的用于单剂量施用单元的试剂盒。本发明所述的试剂盒可以包含包含干燥/冻干双功能分子的第一容器和包含水性制剂的第二容器。在本发明的某些实施方式中,提供了包含单室和多室预充式注射器(例如,液体注射器和冻干物注射器)的试剂盒。
本发明所述的试剂盒在适宜包装中。适宜包装包括单不限于小瓶、瓶子、罐、软包装(例如,密封的聚酯薄膜或塑料瓶)等。还涉及与特定装置如吸入器、鼻内施用装置(例如,雾化器)或输液装置如微型泵联合使用的包装。试剂盒可以具有无菌进入孔(例如,容器可以是静脉内溶液袋或具有皮下注射针可穿刺的塞子的小瓶)。容器也可以具有无菌进入孔(例如,容器可以是静脉内溶液袋或具有皮下注射针可穿刺的塞子的小瓶)。所述组合物中的至少一种活性剂是本文所述的双功能分子,其包含与IL-7或其变体、或IL-7m连接的抗hPD-1抗体。
还可以将在根据本发明所述的试剂盒中包含的组合物配制成注射器相容性组合物。在这种情况下,容器构件本身可以是注射器、吸管和/或其他此类设备,从这些装置可以将制剂施用于身体的感染区域,和/或甚至应用于和/或与试剂盒的其他组分混合。试剂盒的组分可替代地以干燥粉末的形式提供。当试剂和/或组分以干燥粉末形式提供时,可以通过添加适宜溶剂重构可溶性组分。设想溶剂也可以提供在另一种容器装置中并且适合于施用。
在一些实施方式中,所述试剂盒还包括用于治疗癌症或感染性疾病的另外的药剂,并且所述另外的药剂可以与所述双功能分子或本发明所述的试剂盒的其他组分联合使用,或者可以单独提供在试剂盒中。特别地,本文所述的试剂盒可以包含一种或多种另外的治疗剂,如在上文所述的“联合疗法”中所描述的那些。试剂盒可以针对个体的特定癌症进行定制,并且包含用于个体的如上文所描述的对应的第二癌症疗法。
与本文所述的双功能分子或药物组合物的使用相关的说明书通常包括关于剂量、给药方案、预期治疗的施用途径、用于重构所述双功能分子的手段和/或稀释本发明所述的双功能分子的手段的信息。在本发明所述的试剂盒中提供的说明书通常是标签或包装说明书上的书面说明(例如,以传单或说明书形式包含在试剂盒中的纸页)。在一些实施方式中,所述试剂盒可以包含根据本文所述的任何方法使用的说明书。所包含的说明书可以包括对施用包含所述双功能分子的药物组合物以增强免疫应答和/或治疗如本文所述的疾病的描述。该试剂盒还可以包含基于鉴定个体是否患有与PD-1信号传导相关的疾病(例如,本文所述的那些)来选择适合治疗的个体的描述。
实施例
下列附图和实施例旨在为本领域普通技术人员提供如何制作和使用本发明的完整公开和描述,并且不旨在限制发明人视为其发明的范围,也不旨在表示以下实验是全部或唯一进行的实验。虽然已经参照本发明的具体实施方式描述了本发明,但是本领域技术人员应当理解,在不脱离本发明的真实精神和范围的情况下,可以进行各种改变并且可以被等价物替换。此外,可以进行许多修改以使特定情况、材料、物质组成、工艺、一个或多个工艺步骤适应本发明的目的、精神和范围。所有这些修改都旨在在所附权利要求的范围内。
实施例1:Bicki抗hPD1-IL7分子与IL7R和PD1的结合
通过Biacore对重组IL-7细胞因子(rlL7)(Biorad PHP046)、与Fc结构域融合的IL-7(IL7-Fc、CHI-HF-22007Adipogen)、和在其重链(抗PDIVH-IL7,嵌合形式)或轻链(抗PD1VL-IL7,嵌合形式)上与IL-7融合的Bicki抗PD1抗体进行针对CD127(A)或CD132(B)的亲和力评估。将CD127(Sinobiological,10975-H03H-50)以20μg/ml固化在CM5生物芯片上,并以系列浓度(0.34;1.03;3.11;9.3;28nM)添加指定蛋白。使用二态反应模型和二价模型来分析亲和力,因为IL7-Fc和抗PD1-IL7具有二聚体形式。为了评估IL-7对CD132的亲和力,在生物芯片上进行复合物CD127/IL-7,然后以不同浓度(125、250、500、1000et 2000nM)添加CD132受体(Sinobiological 10555-H08B)。
使用Blitz(Forte Bio;USA;目录号C22-2 No 61010-1)进行Blitz方法。通过组氨酸尾巴将重组hPD1-His(Sino Biologicals,Beijing,China;目录号10377-H08H)以10μg/ml固化在Ni-NTA生物传感器(Forte Bio;USA;目录号18-0029)中30秒。然后,将抗PD1抗体以20μg/ml关联120秒。在动力学缓冲液中进行抗PD1抗体解离120秒。使用Blitz pro 1.2软件生成分析数据,该软件计算关联常数(ka)和解离常数(kd)并确定亲和力常数KD(ka/kd)。
表1:Bicki抗PD1-IL7与CD127和CD132受体的结合:通过Biacore对重组IL-7细胞因子、与Fc结构域融合的IL-7(IL7-Fc)、和在其重链(抗PDIVH-IL7)或轻链(抗PD1VL-IL7)上与IL-7融合的抗PD1抗体进行针对CD127(A)或CD132(B)的亲和力评估。稳态亲和力模型用于IL-7分析和二价模型用于融合蛋白。
| Blitz分析 | |
| 抗PD-1无融合 | 1.079nm |
| 抗PD-1 VH IL-7 | 1.776nM |
| 抗PD-1 VL IL-7 | 3.225nM |
| 抗PD-1 VH VL IL-7 | 1.848nM |
表2:Bicki抗PD1-IL7抗体与人重组PD-1蛋白的结合。
结果
发明人观察到IL-7与Fc部分的N-端部分的融合(IL7-Fc)减少了对CD127受体的亲和力(表1),而出乎意料地,IL-7与重链Fc区或轻链恒定结构域的C-端部分的融合保留其对CD127的亲和力至与rIL-7相似的程度。这些数据证明IL7与抗PD1抗体(在重链或轻链上)的C-端融合相比于常规IL7-Fc化合物在IL-7R激活通路方面将更有效,并且相比于用于治疗用途的IL7重组细胞因子在至患者体内的消除半衰期方面将更有效。
表2和图1A和B确认了Bicki抗PD1-IL7分子(嵌合或人源化)与人重组PD-1蛋白结合。抗PD-1抗体的人源化形式以与嵌合抗体相似的功效与PD-1重组蛋白结合。然而,图1A的部分A显示了相比于单独的抗PD1抗体,Bicki的结合功效降低。发明人已用其他抗PD-1骨架(派姆单抗或纳武单抗)构建了Bicki IL7分子。图1C显示了这些Bicki分子保留了与PD-1的良好结合。
此外,相比于IL7-Fc,双功能抗PD1/IL-7分子允许IL-7在PD-1+T细胞浸润中的积累和IL-7在PD-1+T细胞上的重定位。
实施例2:Bicki抗PD1-IL7分子阻断PD-1/PD-L1和PD1-PDL2相互作用的拮抗能力
将PD-L1固化在Maxisorp板上,并添加复合物抗PD1抗体+生物素化重组人PD-1。该复合物是用固定浓度的PD1(0.6μg/mL)产生的,并测试了不同浓度的抗PD-1抗体。在该测试中使用了PD-1抗体的嵌合形式。使用链霉亲和素过氧化物酶进行揭示以检测生物素化的PD1分子,并使用TMB底物在450nm处通过比色法揭示。通过Biacore对在人PD-L2重组蛋白上与抗PD1抗体、抗PD1VH-IL7或抗PD1VL-IL7抗体预孵育的PD-1重组蛋白进行亲和力评估。将人重组PD-L2固化在CM5生物芯片上,并添加复合抗体(200nM)+重组人PD-1(100nM)。数据以通过Biacore测量的相互作用的相对响应%表示:100%=PD-1相对响应。在本实验中使用了PD-1抗体的嵌合形式。
结果
如图2所示,Bicki抗PD1-IL7分子展现了非常好的阻断PD1与PD-L1以及PD-L2相互作用的能力。虽然在ELISA测定中,单独的抗PD1相比于Bicki分子展现了与PD1的最高结合,但出乎意料地,抗体和Bicki形式之间的PD1-PDL1或PD-1-PDL2相互作用抑制是可比的,这证实了本发明所述的Bicki抗PD1-IL7分子可以与抗PD1抗体一样有效。
实施例3:用Bicki抗PD1-IL7分子刺激后对人PBMC的离体IL-7R信号通路分析
将从健康的人类志愿者的外周血中分离的PBMC与重组IL-7、Bicki抗PD1-IL-7(PD-1VH-IL7/PD1VL-IL7)孵育15分钟。然后将细胞固定、透化并用AF647标记的抗pSTAT5(克隆47/Stat5(pY694))染色。通过计算MFI pSTAT*%pSTAT5+群体并归一化(100%=rIL-757.5nM)来获得数据,其代表两个独立实验中3个不同供体的平均值。
结果
在分析Bicki抗PD1-IL7分子与IL7R的结合后,通过流式细胞术对总人PBMC中或CD4+和CD8+T细胞上的STAT5磷酸化来测量IL7R激活。
图3显示,用在重链或轻链上融合的Bicki抗PD1-IL7分子相似地诱导STAT5磷酸化。Bicki抗PD1-IL7分子的最大活性与单独的重组IL-7相似,其EC50为约0.7nM。
实施例4:用Bicki抗PD1-IL7分子处理的T细胞激活和增殖的体外和离体分析
-进行了基于细胞的测定(Discover’x PD-1Path Hunter Bioassay试剂盒)。稳定表达与β-gal片段(ED)融合的工程化PD-1受体和与互补β-gal片段(EA)融合的工程化SHP1的Jurkat T细胞用于Jurkat细胞与PD-L1表达细胞的共培养,其导致PD-1磷酸化和工程化SHP-1的募集,迫使ED和EA片段的互补和活性β-gal酶的产生。添加底物后,βGal酶产生与PD-1信号传导激活成正比的化学发光信号。抗PD-1抗体的添加阻断了PD-1信号传导,导致生物发光信号(RLU)的丢失。在不同摩尔浓度下测试了抗PD-1抗体或Bicki抗PD1-IL7分子。
-进行了promega PD-1/PD-L1生物测定试剂盒。使用了两种细胞系:(1)效应T细胞(稳定表达PD-1、NFAT诱导的荧光素酶的Jurkat)和(2)激活靶细胞(稳定表达PDL1和设计用于以抗原独立性方式激活同源TCR的表面蛋白的CHO K1细胞)。当细胞共培养时,PD-L1/PD-1相互作用直接抑制TCR介导的激活,从而阻断NFAT激活和荧光素酶活性。抗PD1抗体的添加阻断了抑制信号,导致NFAT激活和荧光素酶合成。添加BioGloTM荧光素后,对发光进行定量,其反映了T细胞激活。测定了抗PD1抗体或Bicki抗PD1-IL7抗体的系列摩尔浓度。
-用抗CD3/CD28包被的板(分别为克隆OKT3和CD28.2,3μg/mL)来刺激从健康志愿者的外周血中分离的人PBMC细胞以诱导PD-1表达。刺激20次后,收集PBMC,并在重组IL7(rIL-7)或与IL-7融合的抗PD1抗体(在其重链(抗PD-1VH IL-7)或轻链(抗PD-1VL IL-7)上)的存在下,在OKT3/PDL1包被的板(分别为2和5μg/mL)上对其进行再刺激。在该测试中以抗体的固定剂量(5μg/ml)或以多剂量使用Bicki抗PD1-IL7抗体的嵌合形式。刺激后第5天,通过3H胸苷掺入来评估T细胞增殖,并且通过夹心ELISA来对分泌的IFN-γ进行定量。
结果
为了在基于细胞的测定中确定Bicki抗PD1-IL7分子阻断PD-1信号传导的能力,进行了Discover’x PD-1Path Hunter Bioassay试剂盒。结果如图4A所示,显示Bicki抗PD1VH-IL7能够在92.1μM的浓度下抑制50%的SHP1激活。该结果与单独使用抗PD1而获得的结果(80.66μM)非常相似,显示了对PD1/PDL1相互作用的良好抑制功效,从而导致PD1通路抑制。平行地,使用NFAT生物测定测量了通过PD1与T细胞表面的PDL1的相互作用而诱导的抑制信号的抑制。图4B显示了测试的每种抗体或治疗组合的EC50。以出乎意料的方式,发明人观察到测试的两种Bicki抗PD1-IL7分子的EC50显著优于抗PD1或抗PD1+rIL7组合(BickiVH-IL7和VL-IL7的平均值为0.41和0.33nM,而抗PD1和抗PD1+rIL7的平均值为3.6和6nM)。出乎意料的地,该结果突显了Bicki抗PD1-IL7比抗PD1+IL-7的组合更有效地诱导PD-1+ T淋巴细胞上的T细胞激活,证明了Bicki分子在PD1+ T细胞上的协同作用。图4C显示,这些用派姆单抗和纳武单抗构建的Bicki IL7分子相比于单独的抗PD-1具有相似的协同作用,表明本发明可以适用于其他抗PD-1骨架。
平行地,在用抗PD1抗体、rIL7或抗PD1+rIL7或Bicki抗PD1-IL7分子处理后,测试了离体T细胞激活和增殖。图5和图6显示的结果表明,与抗PD1融合的IL7能够以与单独的IL7细胞因子相当的方式诱导IFNg分泌和诱导T细胞增殖。然而,图6B显示,Bicki分子通过提供20pM的EC50(相比于IL7细胞因子,50pM)而有更好的诱导T细胞增殖的功效。
实施例5:Bicki抗PD1-IL7分子处理后细胞表面的整联蛋白表达
将人PBMC与IL-7(50ng/mL)或抗PD-1或抗PD1 VH-IL7(5μg/mL)孵育3天,并针对α4(BDbiosciences,Rungis,France,目录号559881)、β7(BDBiosciences,目录号555945)或LFA-1整联蛋白(CD11a/CD18)(BDBiosciences,CD11a目录号555380和CD18目录号557156)进行染色。通过LSR来分析FACS,并以每个标志物的中值荧光来表示。数据代表3个不同供体的3个独立实验。
结果
本发明人在图7中显示了bicki抗PD1-IL7分子刺激一些整联蛋白的过表达,例如α4和β7肠道归巢整联蛋白和LFA1整联蛋白(CD11a和CD18),与rIL7一样好。相比之下,IL-2和IL-5细胞因子没有显著改变这些整联蛋白(a4,β7)的表达或至少显著降低至IL-7和BiCki抗PD-1 IL-7的程度。这些数据支持将Bicki抗PD1-IL7分子用于治疗PD-1抗性结直肠癌的兴趣,因为其证明了其通过IL-7促进T细胞浸润到肿瘤部位中的能力。通过与其内皮细胞上的配体ICAM-1的结合,LFA-1介导炎症组织中的T细胞运输和外渗。其他研究表明,IL-7刺激LFA-1和VLA-4粘附分子的表达,促进T细胞向任何发炎组织迁移。该数据支持抗PD-1/IL-7双功能分子可促进多种癌症亚型中的T细胞浸润。肿瘤部位中T细胞浸润的缺失是目前对抗PD1功效的主要障碍。
实施例6:用Bicki抗PD1-IL7分子处理的初始(naive)、部分耗竭和完全耗竭的T细
胞子集的增殖和激活。
导致耗竭的T细胞慢性抗原刺激
每3天在CD3 CD28包被的板(3μg/mL OKT3和3μg/mL CD28.2抗体)上反复刺激人PBMC。刺激后24小时,针对PD-1、Lag3和Tim 3抑制性受体对T细胞进行染色以分析其在每次刺激后的耗竭状态。通过流式细胞术,使用荧光染料标记的抗体和FACS LSRII来分析表达。每次刺激后24小时,在CD3/PD-L2包被的板上重刺激T细胞,在每次刺激后第5天,通过胸苷3H掺入来测定增殖能力,并通过ELISA分析上清液中的IFNg分泌。在每次刺激后48小时,通过STAT5磷酸化来分析耗竭的T细胞对IL-7和Bicki抗PD1-IL7分子的应答。
使用序列稀释(从29nM开始至0.29fM的重组IL-7、与IL-7融合的抗PD-1(PD-1 VHIL-7/PD-1 VL IL-7)或与IL-7融合的同种型对照(B12 VH IL-7)孵育T细胞15分钟。然后将细胞固定、透化并用AF647标记的抗pSTAT5(克隆47/Stat5(pY694))染色。在每次刺激后用29nM IL-7或Bicki抗PD1VH-IL7分子处理后,分析pSTAT5+细胞的百分比。
在CD3 CD28包被的板(3μg/mL OKT3和3μg/mL CD28.2抗体)上反复刺激人PBMC。每次刺激后24小时,在抗PD-1、IL-7或与IL-7融合的抗PD-1(抗PD-1 VH IL7或抗PD-1 VL IL-7)的存在下,在OKT3包被的板(2μg/mL)上重刺激T细胞。在第5天进行H3掺入测定以测定T细胞增殖。刺激3次的T细胞在抗CD3、抗CD3+重组PDL1或抗CD3+重组PDL2包被的板(分别为2和5μg/mL)上重刺激。在第5天进行H3掺入测定。
结果
使用体外反复TCR刺激的模型,发明人概述了T细胞的慢性抗原刺激(例如在免疫原性肿瘤的背景下),并表征了T细胞在慢性抗原刺激诱导的T细胞耗竭后对IL-7应答的能力(图8和9)。在该模型中,T细胞在刺激后高度表达了抑制性受体(Tim 3、PD1、Lag3)并丧失了增殖和分泌细胞因子的能力,这是耗竭T细胞的一个关键特征(图8)。与之前在文献中公布的或基于耗竭T细胞上IL7R表达的强烈降低而预测的相反,发明人观察到,如通过pSTAT5激活所示,部分和完全耗竭的人T细胞仍然对IL-7有应答(图9),并且甚至当T细胞完全耗竭(5次刺激)时,IL-7也增加了T细胞增殖的能力(图10)。然而,当激活T细胞所需的IL-7的量增加时,对IL-7的敏感性随反复刺激而降低(图9B和图10A和B)。这些数据解释需要高IL-7浓度进入肿瘤微环境中以激活长期被刺激的耗竭T细胞。可以通过增加IL-7半衰期(例如通过与抗体或Fc片段重组蛋白融合)来达到IL-7的这种高局部浓度。将IL-7与单克隆抗体融合相比于Fc结构域(IL7-Fc)的另一个优点是,用本发明所述的抗PD1抗体靶向PD1将诱导靠近或直接在肿瘤内PD-1+耗竭T细胞上、恰好在需要更高浓度的IL-7的细胞上的IL-7细胞因子的特异性定位。此外,随着PD-1+ T细胞在肿瘤微环境中的积累,Bicki抗PD1-IL7分子将导致PD-1+细胞积累处的局部IL-7浓度增加。
实施例7:对效应T细胞的Treg遏制活性的离体分析
从健康供体的外周血中分离CD8+效应T细胞和CD4+CD25高CD127低Treg,用细胞增殖染料(针对CD8+ T细胞,用CPDe450)染色。然后在存在或不存在rIL-7(10ng/mL,0.58nM)、抗PD1(0.58nM)、抗PD1+rIL-7(0.58nM),bicki抗PD1VH-IL7(0.58nM)的情况下,以1:1的比率在OKT3包被的板(2μg/mL)上共培养Treg/CD8+Teff 5天。通过细胞荧光法来分析效应T细胞的增殖。
尽管抗PD1疗法刺激T细胞效应子功能,但免疫遏制分子(TGFB、IDO、IL-10……)和调节性细胞(Treg、MDSC、M2巨噬细胞)产生限制疗法的全部潜力的不利微环境。然后,通过测量效应T细胞的增殖来测试肿瘤内T reg反应对IL-7处理的敏感性(图11)。尽管Treg细胞表达低水平的IL-7R(CD127)),但其仍然能够在IL-7处理后刺激pSTAT5。在遏制测定中,通过共培养Treg和T效应细胞,发明人观察到图11:IL-7或bicki抗PD1-IL7处理阻断了Treg介导的抑制作用。抗PD1抗体不能抑制Treg对T效应细胞的遏制活性。已知IL7解除Treg遏制功能(A等,J.Immunol.,2015)。发明人在图11中显示了Bicki抗PD1-IL7分子解除Treg介导的抑制,导致与IL7细胞因子一样好的效应T细胞增殖。尽管Treg细胞表达低水平的IL-7受体,但已经很好地描述了IL-7直接影响Treg并消除其遏制功能(Liu W,等,J ExpMed.,2006年7月10日;Liu W等;Seddiki N等,J exp Med,2006年7月10日;Codarri L等,2007;Heninger AK等,J immuonl,2012年12月15日)。此外,图11B显示,靶向IL-7信号传导相比于IL-2和IL-15信号传导应该更有希望,因为相对于IL-7和Bicki抗PD-1/IL-7,IL-2和IL-15强烈刺激两种Treg的增殖。本发明人在该实验中显示,Bicki抗PD1-IL7分子将通过刺激效应T细胞增殖和存活而相对于T调节免疫平衡偏向T细胞效应细胞,同时保留调节性T细胞。与IL-2信号相比,靶向IL-7信号传导相比于IL-2信号传导应该更有希望,因为IL-2作用于Treg和T效应细胞两者上,而IL-7选择性激活T效应细胞。
实施例8:Bicki抗PD1-IL7分子在人源化小鼠模型中的功效和对来自肿瘤或离体
人肿瘤外植体培养物的人T细胞的离体功效。
人源化小鼠模型:
将1e6人PBMC腹膜内注射到小鼠中。每周用抗PD1抗体或Bicki抗PD1VH-IL7分子(5mg/kg)处理小鼠两次。注射后第16天,采血并处死小鼠。通过流式细胞术在人CD45细胞中分析人CD3 T细胞的百分比,通过ELISA在血浆中给药人IFNγ,并通过免疫组织荧光法定量小鼠结肠中人CD3+细胞的浸润。近端和远端结肠、肝脏和肺被包埋在TissueOCT中。针对Dapi和人CD3进行切片染色。对于肝脏和肺,以像素2/mm2对CD3浸润进行定量。对于结肠,对CD3+浸润的T细胞进行计数。
不同癌症的离体T细胞研究:
从肾癌、转移性结直肠癌、肝细胞癌、神经鞘瘤活检组织中提取T细胞,并针对CD3、CD4、CD8、PD-1、CD127和CD132进行染色。通过FACS LSRII来分析免疫荧光。分析了CD4+CD3+或CD8+CD3+群体。
用重组IL-7或抗PD1VH-IL7抗体(29nM)处理细胞15分钟。然后将细胞固定、透化并针对pSTAT5(克隆47/Stat5(pY694))、CD3、CD4和CD8进行染色。然后通过离心洗涤细胞并将其重悬于具有同种型对照、抗PD-1、与Il-7融合的B12同种型(同种型-VH IL-7)或具有与IL-7融合的抗PD-1(抗-PD-1 VH IL-7)(浓度为5μg/mL)的完整介质中。48小时后,收集上清液并使用MSD技术(Meso scale Discovery)对IFNγ分泌进行定量(dose)。
CD3+ T细胞群体中的肿瘤内FoxP3 Treg染色。用重组IL-7或抗PD-1VHIL7(29nM)处理(孵育15分钟)后,FoxP3-CD3+效应T细胞相比于FoxP3-CD3+ Treg细胞中pSTAT5的Facs分析。然后将细胞固定、透化并针对pSTAT5(克隆47/Stat5(pY694))、CD3和Foxp3进行染色。
结果
在人源化小鼠模型中(图12),发明人观察到,相比于抗PD1抗体和PBS阴性对照,用Bicki抗PD1-IL7分子处理后,外周血中CD3阳性细胞百分比增加,且IFNg分泌增加,在体内证实Bicki分子增加了人T细胞的扩增、存活和激活。此外,这种差异不仅与结肠中的高T细胞浸润有关,也与肝脏和肺中的高T细胞浸润有关,证实了Bicki分子的IL-7部分促进人发炎组织中的T细胞迁移。
对人肿瘤的T细胞表型分析表明,肿瘤内T细胞表达PD-1、IL-7R/γ共有链(CD127和CD132),表明Bicki抗PD1-IL7分子可能在局部有效刺激肿瘤内人T细胞,这与文献中的预测相反(图13)。确实,如通过pSTAT5染色所示,肿瘤内T细胞对IL-7和Bicki抗PD1-IL7分子有应答(图14),证实从肿瘤中纯化的人T细胞的离体Bicki抗PD1-IL7分子可促进各种肿瘤亚型的治疗。然后,使用包含肿瘤细胞以及所有肿瘤微环境(包括用抗PD1、同种型VH-IL7、Bicki抗PD1-IL7分子或IL-7处理的人免疫细胞和基质细胞)的人肿瘤外植体的离体培养模型(图15)。在上清液中分析IFNg分泌作为T细胞激活的特异性标志物和与各种临床试验中抗PD1应答相关的替代标志物。发明人观察到,bicki抗PD-1 IL7处理的人肿瘤培养物显著分泌更多的IFNg,证实IL7在肿瘤床中局部起作用并增加局部T细胞激活。有趣的是,用Bicki抗PD1-IL7分子处理的人肿瘤细胞培养物比单独的抗PD1或单独的IL7/同种型VHIL7分泌更多的IFNg,证明将抗PD-1与IL-7组合以激活肿瘤内T细胞的协同作用(图15B)。还分析了癌症(结直肠癌、神经鞘瘤、肾癌和肝细胞癌)患者的肿瘤内T reg(FoxP3+)的百分比。图16A呈现的结果表明,每种测试的癌症都存在Treg细胞,其可以是Bicki抗PD1-IL7分子的靶标以解除Treg细胞武装。然后,在用Bicki抗PD1-IL7分子处理后,分析了肿瘤内效应细胞(FoxP3-)和调节性T细胞(FoxP3+)中的STAT5激活(pSTAT5)。使用来自结肠直肠癌、神经鞘瘤和胰腺癌的细胞获得并示于图16B中的结果显示,Bicki分子能够激活肿瘤内效应和调节T细胞中的IL-7R通路。该结果强调了Bicki抗PD1-IL7分子是双刃剑,其偏向效应T细胞激活进入肿瘤中,同时消除Treg遏制活性。
实施例9.Fc融合IL-7的突变改变了与IL-7R和pSTAT5信号传导的结合并改善了体
内药代动力学。
为了获得IL-7突变体,用具有相似性质和特性的氨基酸置换IL7与CD127相互作用中涉及的氨基酸。产生了若干突变体,即Q11E、Y12F、M17L、Q22E、D74E、D74Q、D74N、K81R、W142H、W142F和W142Y。
通过用丝氨酸残基替换半胱氨酸残基来破坏IL-7二硫键,导致以下置换:C2S-C141S+C34S-C129S(名为“SS1”的突变体),或C2S-C141S+C47S-C92S(名为“SS2”的突变体),或C47S-C92S+C34S-C129S(名为“SS3”的突变体)。
| 样品 | EC50 ng/mL |
| IgG4 G4S3 IL7 WT | 18.4 |
| IgG4 G4S3 IL7 Q11E | 18.49 |
| IgG4 G4S3 IL7 Y12F | 22.27 |
| IGG4 G4S3 IL7 M17L | 20.96 |
| IGG4 G4S3 IL7 Q22E | 17.44 |
| IgG4 G4S3 IL7 D74E | 103.94 |
| IgG4 G4S3 IL7 K81R | 20.18 |
| IgG4 IL7 G4S3 W142F | 34.86 |
| IgG4 G4S3 IL7 W142H | 136.32 |
| IGG4 G4S3 IL7 W142Y | 44.6 |
表3.来自图17A、B和C的ED50测定指达到与CD127受体的结合的50%所需的浓度。每个表代表一个不同的实验,且可以与阳性对照IgG4 G4S3 IL7WT进行比较。
| 样品 | Ka(1/Ms) | Kd2(1/s) | KD(M) |
| IgG4 Fc G4S3 IL-7 WT | 5.76E+06 | 1.22E-04 | 4.14E-11 |
| IgG4 Fc G4S3 IL-7 W142H | 5.02E+05 | 2.56E-03 | 5,68E-08 |
| IgG4 Fc G4S3 Fc IL-7 SS2 | 6.11E+05 | 1.55E-03 | 7.22E-09 |
| IgG4 Fc G4S3 Fc IL-7 SS3 | 1962 | 6.02E-4 | 1,36E-6 |
表4.WT和突变的IL-7与CD127受体的结合。通过Biacore对融合抗PD-1 IL-7对CD127的亲和力进行的评估。使用二态反应模型进行分析。
表5.WT相比于突变的IL-7与CD132受体的结合。通过Biacore对CD132上复合物CD127+IgG融合IL-7进行亲和力评估。使用稳态反应模型进行分析。
表6.来自图18A、B和C的ED50测定指在该测定中针对每个抗PD-1 IL-7分子达到pSTAT5信号的50%所需的浓度。每个表代表使用不同供体的不同实验,并且每个表可以与阳性对照IgG4 G4S3 IL7WT进行比较。
| 样品 | 获得的Cmax(nM) | 曲线下面积(AUG) |
| IgG4 G4S3 IL7 WT | 13.22 | 121.4 |
| IgG4 G4S3 IL7D74E | 89.19 | 151.9 |
| IgG4 G4S3 IL7 W142F | 98 | 未测定 |
| IgG4 G4S3 IL7 W142H | 141 | 248.2 |
| IgG4 G4S3 IL7 W142Y | 70 | 未测定 |
| IgG4 G4S3 SS2 | 69.9 | 361.6 |
| IgG4 G4S3 SS3 | 140.6 | 466.5 |
表7.来自图19的Cmax、曲线下面积和半衰期测定。在抗PD-1 IL7注射后15分钟的时间点计算Cmax。在抗PD-1 IL-7注射后0至144小时计算AUC。
IL7序列中一个氨基酸的置换没有改变其结合PD-1受体的能力(图17A、B和C)。然而,如通过离体T细胞测定中的CD127结合和pSTAT5信号传导显示的,这些突变改变了其生物活性(图18和19和表3和6)。突变D74E和W142H是降低IL-7与CD127结合和T淋巴细胞中pStat5激活两者的最有效突变(图18A、18B和19A、19B和表3和7)。在另一个实验中,分析了二硫化物键破坏的影响(图18C)。在高浓度(10μg/ml)下,SS2或SS3能够激活T淋巴细胞中的pStat5,其与IL-7 WT的偏差未3log(图18C和表6)。
为了确认这些突变体的结合能力,进行了Biacore测定以测定KD(受体及其抗原之间的平衡解离常数,参见表4)。突变体SS2和W142H对CD127的亲和力较低,其KD接近7至57nM。SS3突变体对CD127的亲和力最低,其KD接近3μM。如表5所示,还评估了对CD132受体的亲和力。在该实验中,由于CD127在不存在IL-7的情况下与CD132二聚化,因此单独使用IgG4作为基线KD亲和力。IL-7突变体W142H与CD132结合,但其亲和力比IgG IL-7WT高5倍。如图18所示,该数据表明,突变W142H减少了与CD127的结合,并重新定向IL-7与CD132受体的结合,导致T细胞中pSTAT5激活的丧失。相反,发明人在测试的条件下观察到SS2突变体失去与CD132受体结合的能力,表明SS2突变体优先结合CD127而非CD132受体,导致T细胞中pSTAT5活性降低(图19)。
为了确定体内抗PD-1 IL-7的药代动力学/药效学,向小鼠静脉注射一剂IgG-IL-7(34.4nM/kg)。通过对人IgG具有特异性的ELISA来分析血浆药物浓度。图19和表7显示,IgG4IL-7 WT分子具有快速分布,因为获得的Cmax(注射后15分钟的最大浓度)比理论浓度低30倍。测试的所有W142Y、F、H突变体描绘了更好的分布曲线,其Cmax比IL-7 WT高5至10倍(图19A和表7)。W142H突变体呈现最佳Cmax。抗PD-1 IL-7 D74E突变体也表现出良好的Cmax。突变体SS2和SS3表现出最好的PK曲线,其Cmax比IL-7 WT高7至13倍,并且具有良好的线性曲线。同时,确定了AUC(曲线下面积)(表7和图20D),通过AUC可以了解药物暴露的程度及其从体内的清除率。这些数据表明AUC随IL-7突变体而增加,这意味着IL-7突变体具有改善的药物暴露。如图20D所示,发明人观察到药物暴露与突变体的IL-7效能(其通过pSTAT5 EC50测量)相关。总之,IL-7的亲和力与产品的药代动力学相关。降低IL-7与其受体CD127和CD132的亲和力可改善IL_7双功能分子在体内的吸收和分布。
实施例10:IgG的C-端结构域的C-端结构域处的半胱氨酸添加降低IL7分子的灵活
性并改善体内药代动力学
还测试了IgG的C-端结构域的C-端结构域处的半胱氨酸添加以产生额外的二硫键并潜在地限制IL-7分子的灵活性。该突变体被命名为“C-IL-7”。图21显示,IgG结构中的二硫键添加相比于抗PD-1 IL7 WT双功能分子降低了IL-7的pSTAT5活性(图21A),并增加了体内药代动力学分析中的Cmax(5倍)(图21B)。
实施例11:用IgG1N298A同种型构建的抗PD-1 IL-7突变体具有与IL-7R的更好的
结合、更高的pSTAT5信号传导和良好的体内药代动力学特征
用IgG4m(S228P)或IgG1m(N298A或N297A,取决于编号方法)测试了抗PD-1 IL-7双功能分子的不同的同种型。IgG4同种型包含S228P突变以防止体内Fab臂交换,而IgG1同种型包含消除IgG1同种型与可减少免疫细胞因子的非特异性结合的FcγR受体结合的N298A突变(名为“IgG4m”或“IgG1N298A”的突变体)。然后,用2种不同的同种型(N297A中突变的IgG1(称为IgG1m)同种型相比于IgG4 S288P同种型(称为IgG4m))构建抗PD-1 IL-7双功能分子以确定同种型结构是否改变了IL-7的生物活性及其药代动力学特征。
图22A和22B证明用IgG4m或IgG1m同种型构建的抗PD-1 IL7双功能分子对PD-1受体具有相同的结合特性,表明同种型不改变VH和VL的构象和抗PD-1抗体对PD-1的亲和力。然而,发明人观察到,出乎意料地,IgG1m同种型改善了IL-7 D74、SS2与CD127的结合并略微改善了SS3与CD127的结合(图23A、B、C和D),并改善了pSTAT5对人PBMC的激活(图24A、B和C)。pSTAT5信号传导的这种增加在另一种T细胞系(表达PD-1和CD127的Jurkat细胞,参见图24D)上的SS2突变体中得到证实,但令人惊讶的是,IgG1m同种型不改变抗PD-1 IL-7 WT双功能分子的pSTAT5活性,表明IgG1m同种型仅提高IL-7突变体的活性。为了确定包含抗PD1抗体和IL7突变体的双功能分子重新激活TCR介导的信号传导的能力,进行了NFAT生物测定。图25A呈现的结果显示,双功能分子比抗PD1或抗PD1+rIL7(作为单独的化合物)更好地激活TCR介导的信号传导(NFAT),证明双功能分子对PD1+T细胞的协同作用。发明人接下来评估了用IgG4m相比于IgG1m同种型构建的包含抗PD-1抗体和IL-7突变体(其具有突变D74E、W142H或SS2)的双功能分子的协同能力(图25B、C、D)。所有测试的突变体都对激活NFAT信号具有协同效应,其激活水平与其激活pSTAT5信号的能力相关,特别是对于具有IL-7 D74E和IgG4m的双功能分子。
小鼠中的药代动力学研究表明,IgG1同种型不会改变IL7WT和SS3分子的药物暴露,并且对W142H分子的影响最小(图26A)。总而言之,这些数据表明优化的同种型(IgG1m)足以增强突变体的生物活性,同时在体内保持产品的良好药代动力学。使用IgG1m同种型,测试了其他IL-7突变体:D74N、D74Q和D74E+W142H突变的组合。在pSTAT5激活(图25B)和药代动力学(图26B)方面没有观察到与抗PD-1 IL-7 D74E突变体的差异。双突变体D74E+W142H显示出与W124H IgG1相似的特征,而D74Q显示出与D74E突变体相似的特征。本发明人还构建了具有IgG1m同种型+YTE突变(M252Y/S254T/T256E)的双功能分子。该突变已被描述为通过增加与FcRn受体的结合来增加抗体的半衰期。如图23D所示,YTE突变不改变包含D74或W142H突变体的双功能分子的pSTAT5信号传导。
实施例12:K444A至C-端赖氨酸残基的突变不影响体内药代动力学
人IgG的所有亚类都带有抗体重链的C-端赖氨酸残基(K444),该残基可在循环中被裂解掉。血液中的这种裂解可潜在地通过将连接的IL-7释放至IgG来损害免疫细胞因子的生物活性。为了避免这个问题,IgG结构域中的K444氨基酸被丙氨酸置换以减少蛋白水解裂解(一种常用于抗体的突变)。如图27所示,在IgG WT IL-7与IgG K444A IL-7之间获得了相似的曲线,表明该突变不影响药物的药代动力学特征。
实施例13:IgG抗体之间的接头不改变体内药代动力学但改善pSTAT5信号传导的
激活
测试了IgG Fc结构域和IL-7m之间的不同接头以改变灵活性。测试了几种条件(例如无接头、GGGGS、GGGGSGGGS、GGGGSGGGGS、GGGGSGGGGSGGGGS)。
对于实施例1和2,Fc的C-端结构域和IL-7的N-端结构域之间的接头(G4S)3分别用于IgG4m-IL7和IgG1m-IL-7构建。该接头允许IL7激活信号的高度灵活性和改进。为了降低IL7对CD127的亲和力并改善药代动力学,使用不同长度的接头(无接头、G4S、(G4S)2或(G4S)3)测试了不同的结构。为了比较,还用各种接头产生了IgG1m或IgG4m Fc IL-7 WT。
药代动力学研究表明,接头的长度对以下测试的构建产品的分布、吸收和消除没有影响:抗PD-1 IL7 WT(图28A)、抗PD-1 IL-7 D74(图28B)和抗PD-1 IL-7 W142H(图28C)。然而,如图28D所示,接头的长度影响pStat5的激活。事实上,用接头(G4S)3构建的抗PD-1IL7相比于用(G4S)2或G4S3接头构建的抗PD-1 IL-7在激活pSTAT5信号传导方面更有效,甚至相比于不用接头构建的抗PD-1 IL-7更有效。这些数据强调了使用(G4S)3接头可以使IL-7具有灵活性,而不会损害药物的体内药代动力学。
实施例14:抗PD-1 IL-7突变体允许相对于PD-1-CD127+细胞优先结合PD-1+CD127
+细胞
接下来,发明人评估了抗PD-1 IL-7双功能分子靶向PD-1+ T细胞的能力。表达CD127+或共表达CD127+和PD-1+的Jurkat细胞用45nM的以下双功能分子染色:抗PD-1 IL-7WT、D74、W142H、SS2和SS3。用抗IgG-PE(Biolegend,克隆HP6017)检测结合并通过流式细胞术分析。
结果:图29显示抗PD-1 IL-7 WT和D74突变体以与PD-1-/CD127+细胞相似的功效结合PD-1+/CD127+细胞,而抗PD-1 IL-7突变体SS2、SS3以相比于PD-1-/CD127+细胞高2至3倍的功效与PD-1+/CD127+细胞结合。抗PD-1 IL-7 W142H双功能分子显示出中等作用,并且以高1,4倍的功效与PD-1+/CD127+细胞结合。总之,这些数据表明,IL-7突变不仅允许药物更好的药代动力学,而且允许IL-7优先结合PD-1+细胞,即药物靶向同一细胞。这方面对药物的体内生物活性有利,因为抗PD-1 IL-7会相对于CD127+初始T细胞将PD-1+CD127+耗竭的T细胞上的IL-7集中到肿瘤微环境中。
实施例15:bicki抗PD-1 IL-7分子允许CD4和CD8 T细胞的增殖,并在食蟹猴体内
证明了临床前安全性。
食蟹猴注射了6,87nM/kg(n=2)或34,35nM(n=1)(相当于1mg/kg或5mg/Kg)的抗体。进行血液分析直至注射后第15天或4小时为止。通过流式细胞术,使用Ki67标志物,在血液中评估了CD4/CD8 T细胞或B细胞的增殖。在细胞固定和透化后,通过FACS在CD3+T细胞中的多个时间点分析pSTAT5。
结果:图30A和B显示bicki抗PD-1 IL-7的单次注射诱导了CD4和CD8 T细胞的增殖,但不诱导B细胞的增殖。注射后,观察到pSTAT5的快速激活,其最大激活时间为1至24小时(如图30C所示)。该药物在该剂量下耐受性良好且安全,如图30D/E/F所示,临床参数(生化和血细胞计数)在注射该分子后处于或接近正常范围。这些数据表明该分子能够在体内激活T细胞并显示出临床前安全性。
结论
IL-7细胞因子与Fc部分的C-端结构域融合的Bicki抗PD1-IL7抗体形式保持与CD127受体的结合,而出乎意料的地,与Fc的N-端结构域融合的IL7(IL7-Fc)失去其结合能力。Bicki形式在患者的IL-7R激活和消除半衰期方面将更有效。此外,Bicki抗PD1-IL7抗体形式相比于IL7-Fc化合物允许IL-7在PD-1+ T细胞浸润中积累,并允许IL-7在PD-1+ T细胞上重新定位,Bicki的使用相比于抗PD1+ IL7重组蛋白的组合使用具有增加的T细胞激活。此外,Bicki抗PD1-IL7分子是一把双刃剑,其一方面通过体外和体内两种模型中IFNg细胞因子的分泌来增加效应T细胞的增殖及其激活,另一方面通过解除武装Treg对T细胞的遏制功能。这已在从各种肿瘤类型和适应症中分离的人T细胞上得到证实,表明Bicki抗PD1-IL7分子可用于各种肿瘤亚型。对PD-1疗法有抗性的肿瘤呈现T细胞排斥反应。众所周知,PD-1应答与肿瘤浸润T细胞的数量相关。Bicki抗PD1-IL7分子增加细胞表面的整联蛋白表达,表明本发明所述的双功能分子促进T细胞浸润到多种癌症亚型的肿瘤中。
材料和方法
结合PD1的ELISA
对于活性ELISA测定,将重组hPD1(Sino Biologicals,Beijing,China;目录号10377-H08H)在碳酸盐缓冲液(pH 9.2)中以0.5μg/ml固化在塑料上,并添加纯化抗体以测量结合。在孵育和洗涤后,添加过氧化物酶标记的驴抗人IgG(Jackson Immunoresearch;USA;目录号709-035-149),通过常规方法揭示。
使用Biacore方法进行的亲和力测量
通过Biacore对在其重链上与IL-7融合的IgG进行针对CD127(A)或CD132(B)的亲和力评估。CD127(Sinobiological,10975-H03H-50)以20μg/ml的浓度固化在CM5生物芯片上,并以系列浓度(0.35;1.1;3.3;10;30nM)添加指定蛋白。使用二态反应模型分析亲和力。为了评估IL-7对CD132的亲和力,将CD127固化在CM5生物芯片上,并以30nM的浓度注射每种IL-7构建。以不同的浓度(例如31.25、52.5、125、250、500nM)添加CD132受体(Sinobiological 10555-H08B)。使用稳态亲和力模型进行分析。
结合CD127的ELISA
通过夹心ELISA方法来评估CD127结合。固化抗体骨架靶向的重组蛋白,然后将与IL-7融合的抗体与CD127重组蛋白(组氨酸标记的,Sino目录号10975-H08H)预孵育。使用与生物素偶联的抗组氨酸抗体(MBL#D291-6)和与过氧化物酶(JI 016-030-084)偶联的链霉亲和素的混合物进行揭示。使用TMB底物在450nm处确定比色法。
体内pSTAT5分析
从健康的人类志愿者的外周血中分离的PBMC与重组IL-7或融合IgG的IL-7孵育15分钟。然后将细胞固定、透化并用AF647标记的抗pSTAT5(克隆47/Stat5(pY694))染色。通过计算CD3+ T细胞群体中的MFI pSTAT5来获得数据。
融合IgG的IL-7的体内药代动力学
为了分析IL-7免疫细胞因子的药代动力学,向BalbcRJ小鼠(雌性6-9周龄)眼眶内注射了单剂量的分子。通过ELISA,使用固化抗人轻链抗体(克隆NaM76-5F3),稀释血清(包含融合IgG的IL-7)来测定血浆药物浓度。使用过氧化物酶标记的驴抗人IgG(JacksonImmunoresearch;USA;目录号709-035-149)来进行检测,并通过常规方法揭示。
给食蟹猴静脉注射2个剂量的Bicki IL-7。在注射后的多个时间点(第15/30分钟、第1/2/4小时、第1/2/3/6/10/14天)采集血液以分析生化和细胞计数。
使用Promega的基于细胞的生物测定法进行的T细胞激活测定
使用Promega PD-1/PD-L1试剂盒(目录号J1250)测试了抗PD-1抗体恢复T细胞激活的能力。使用了两种细胞系:(1)效应T细胞(稳定表达PD-1、NFAT诱导的荧光素酶的Jurkat)和(2)激活靶细胞(稳定表达PDL1和设计用于以抗原独立性方式激活同源TCR的表面蛋白的CHO K1细胞)。当细胞共培养时,PD-L1/PD-1相互作用直接抑制TCR介导的激活,从而阻断NFAT激活和荧光素酶活性。抗PD1抗体的添加阻断了PD-1介导的抑制信号,导致NFAT激活和荧光素酶合成和生物发光信号的发射。按照制造商的建议进行实验。测试了PD-1抗体的序列稀释。在PD-L1+靶细胞、PD-1效应细胞和抗PD-1抗体共培养四小时后,将BioGloTM荧光素底物加入孔中,并使用TecanTM光度计来读取板。
抗体和双功能分子
以下抗体和双功能分子已用于本文公开的不同实验中:派姆单抗(Keytrudra,Merck)、纳武单抗(Opdivo,Bristol-Myers Squibb),并且本文公开的双功能分子包含抗PD1人源化抗体或抗PD1嵌合抗体,所述抗PD1人源化抗体包含如SEQ ID NO:19、22或24定义的重链和如SEQ ID NO:28定义的轻链,所述抗PD1嵌合抗体包含如SEQ ID NO:71定义的重链和如SEQ ID NO:72定义的轻链。
Claims (33)
1.一种双功能分子,其包含:
(a)抗人PD-1抗体或其抗原结合片段,其包含:
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域(VH),和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域(VL),和
(b)人白介素7(IL-7)或其片段或变体,
其中所述抗体或其片段,优选地通过肽接头,与所述人IL-7或其片段或变体共价连接作为融合蛋白。
2.根据权利要求1所述的双功能分子,其中所述人IL-7或其片段的N-端末端与所述抗人PD-1抗体或其抗原结合片段的的重链/或轻链或两者的C-端末端连接。
3.根据权利要求1-2中任一项所述的双功能分子,其中所述抗体或其抗原结合片段是嵌合、人源化或人抗体。
4.根据权利要求1-3所述的双功能分子,其中所述抗人PD-1抗体或其抗原结合片段包含:
(i)包含HCDR1、HCDR2和HCDR3的重链可变结构域(VH),和
(ii)包含LCDR1、LCDR2和LCDR3的轻链可变结构域(VL),
其中:
-所述重链CDR1(HCDR1)包含SEQ ID NO:1的氨基酸序列或由SEQ ID NO:1的氨基酸序列组成;
-所述重链CDR2(HCDR2)包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO:2的氨基酸序列组成;
-所述重链CDR3(HCDR3)包含SEQ ID NO:3的氨基酸序列或由SEQ ID NO:3的氨基酸序列组成,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;
-所述轻链CDR1(LCDR1)包含SEQ ID NO:12的氨基酸序列或由SEQ ID NO:12的氨基酸序列组成,其中X是G或T;
-所述轻链CDR2(LCDR2)包含SEQ ID NO:15的氨基酸序列或由SEQ ID NO:15的氨基酸序列组成,
-所述轻链CDR3(LCDR3)包含SEQ ID NO:16的氨基酸序列或由SEQ ID NO:16的氨基酸序列组成。
5.根据权利要求1-4所述的双功能分子,其中所述抗人PD-1抗体或其抗原结合片段包含以下或由以下组成:(a)包含SEQ ID NO:17的氨基酸序列的VH或由SEQ ID NO:17的氨基酸序列组成的VH,其中X1是D或E,并且X2选自T、H、A、Y、N、E和S,优选地选自H、A、Y、N和E;(b)包含SEQ ID NO:26的氨基酸序列的VL或由SEQ ID NO:26的氨基酸序列组成的VL,其中X是G或T。
6.根据权利要求1-5所述的双功能分子,其中所述抗人PD-1抗体或其抗原结合片段包含以下或由以下组成:(i)包含SEQ ID NO:24的氨基酸序列的重链可变区(VH)或由SEQ IDNO:24的氨基酸序列组成的重链可变区(VH),和(ii)包含SEQ ID NO:28的氨基酸序列的轻链可变区(VL)或由SEQ ID NO:28的氨基酸序列组成的轻链可变区(VL)。
7.根据权利要求1-3所述的双功能分子,其中所述抗PD1抗体选自派姆单抗,纳武单抗,匹地利珠单抗,西米普利单抗,PDR001以及单克隆抗体5C4、17D8、2D3、4H1、4A11、7D3和5F4。
8.根据权利要求1-7中任一项所述的双功能分子,其中所述IL-7或其变体包含与野生型人IL-7(wth-IL-7)具有至少75%同一性的氨基酸序列或由与野生型人IL-7(wth-IL-7)具有至少75%同一性的氨基酸序列组成。
9.根据权利要求1-8中任一项所述的双功能分子,其中所述IL-7包含SEQ ID NO:51中所示的氨基酸序列或由SEQ ID NO:51中所示的氨基酸序列组成。
10.根据权利要求1-8中任一项所述的双功能分子,其中所述IL-7是IL-7变体,其中所述IL-7变体呈现出与包含SEQ ID NO:51中所示的氨基酸序列或由SEQ ID NO:51中所示的氨基酸序列组成的野生型人IL-7(wth-IL-7)至少75%同一性,其中所述变体包含至少一个氨基酸突变,所述氨基酸突变i)相比于与wth-IL-7对IL-7受体(IL-7R)的亲和力减少了所述IL-7变体对IL-7R的亲和力,并且ii)相比于包含IL-7的双功能分子改善了包含所述IL-7变体的所述双功能分子的药代动力学。
11.根据权利要求10所述的双功能分子,其中所述至少一个突变是选自以下的氨基酸置换或氨基酸置换组:(i)C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、或C47S-C92S和C34S-C129S,(ii)W142H、W142F或W142Y,(iii)D74E、D74Q或D74N,(iv)Q11E、Y12F、M17L、Q22E和/或K81R;或其任何组合。
12.根据权利要求10所述的双功能分子,其中所述IL-7变体包含选自以下的氨基酸置换组:C2S-C141S和C47S-C92S、C2S-C141S和C34S-C129S、以及C47S-C92S和C34S-C129S。
13.根据权利要求10所述的双功能分子,其中所述IL-7变体包含选自以下的氨基酸置换:W142H、W142F和W142Y。
14.根据权利要求10所述的双功能分子,其中所述IL-7变体包含选自以下的氨基酸置换:D74E、D74Q和D74N。
15.根据权利要求1-8和10中任一项所述的双功能分子,其中所述IL-7变体包含SEQ IDNO:53-66中所示的氨基酸序列或由SEQ ID NO:53-66中所示的氨基酸序列组成。
16.根据权利要求1-8和10中任一项所述的双功能分子,其中所述IL-7变体包含SEQ IDNO:54、56或63中所示的氨基酸序列或由SEQ ID NO:54、56或63中所示的氨基酸序列组成。
17.根据权利要求1-16中任一项所述的双功能分子,其中所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgGl、IgG2、IgG3或IgG4重链恒定结构域(优选地IgGl或IgG4重链恒定结构域)的重链恒定结构域。
18.根据权利要求1-17中任一项所述的双功能分子,其中所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgGl重链恒定结构域的重链恒定结构域,其任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A。
19.根据权利要求1-17中任一项所述的双功能分子,其中所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgG4重链恒定结构域的重链恒定结构域,其任选地具有选自以下的置换或置换的组合:S228P;L234A/L235A,S228P+M252Y/S254T/T256E.17和K444A。
20.根据权利要求1-19中任一项所述的双功能分子,其中所述抗体或其片段通过接头序列与IL-7或其变体连接,所述接头序列优选地选自(GGGGS)3、(GGGGS)4、(GGGGS)2、GGGGS、GGGS、GGG、GGS和(GGGS)3,甚至更优选地选自(GGGGS)3。
21.根据权利要求12-16中任一项所述的双功能分子,其中所述抗体或其抗原结合片段包含来源于人κ轻链恒定结构域的轻链恒定结构域和来源于人IgGl重链恒定结构域的重链恒定结构域,其任选地具有选自以下的置换或置换的组合:T250Q/M428L;M252Y/S254T/T256E+H433K/N434F;E233P/L234V/L235A/G236A+A327G/A330S/P331S;E333A;S239D/A330L/I332E;P257I/Q311;K326W/E333S;S239D/I332E/G236A;N297A;L234A/L235A;N297A+M252Y/S254T/T256E;K322A和K444A,优选地选自以下:N297A,其任选地与M252Y/S254T/T256E组合,和L234A/L235A;并且所述抗体或其片段通过接头(GGGGS)3与IL-7变体连接。
22.一种分离的核酸分子或分离的核酸分子组,其编码根据权利要求1-21中任一项所述的双功能分子。
23.一种载体,其包含根据权利要求22所述的核酸或核酸分子组。
24.一种宿主细胞,其包含根据权利要求23所述的载体或根据权利要求22所述的核酸或核酸分子组。
25.一种用于产生根据权利要求1-21中任一项所述的双功能分子的方法,其包括培养根据权利要求24所述的宿主细胞的步骤和任选地分离所述双功能分子的步骤。
26.一种药物组合物,其包含根据权利要求1-21中任一项所述的双功能分子、根据权利要求22所述的核酸或核酸分子组、根据权利要求23所述的载体或根据权利要求24所述的宿主细胞和药学上可接受的载体。
27.根据权利要求26所述的药物组合物,其中其还包含另外的治疗剂,所述另外的治疗剂优选地选自以下:烷化剂、血管生成抑制剂、抗体、抗代谢物、抗有丝分裂剂、抗增殖剂、抗病毒剂、极光激酶抑制剂、凋亡促进剂(例如,Bcl-2家族抑制剂)、死亡受体通路激活剂、Bcr-Abl激酶抑制剂、BiTE(双特异性T细胞接合剂)抗体、抗体药物缀合物、生物应答调节剂、布鲁顿氏酪氨酸激酶(BTK)抑制剂、细胞周期蛋白依赖性激酶抑制剂、细胞周期抑制剂、环氧合酶-2抑制剂、DVD、白血病病毒癌基因同源物(ErbB2)受体抑制剂、生长因子抑制剂、热休克蛋白(HSP)-90抑制剂、组蛋白去乙酰化酶(HDAC)抑制剂、激素疗法、免疫药、凋亡蛋白抑制剂(IAP)的抑制剂、嵌入型抗生素、激酶抑制剂、驱动蛋白抑制剂、Jak2抑制剂、哺乳动物雷帕霉素靶蛋白抑制剂、microRNA、丝裂原激活的细胞外信号调节激酶抑制剂、多价结合蛋白、非甾体抗炎药(NSAID)、聚ADP(二磷酸腺苷)-核糖聚合酶(PARP)抑制剂、铂类化学治疗剂、polo样激酶(Plk)抑制剂、磷酸肌醇-3激酶(PI3K)抑制剂、蛋白酶体抑制剂、嘌呤类似物、嘧啶类似物、受体酪氨酸激酶抑制剂、类视黄醇/类维生素D植物生物碱、小抑制性核糖核酸(siRNA)、拓扑异构酶抑制剂、泛素连接酶抑制剂、低甲基化剂、检查点抑制剂、肽疫苗等、来自肿瘤抗原的表位或新表位、以及这些试剂中的一种或多种的组合。
28.根据权利要求26或27所述的药物组合物、根据权利要求1-21中任一项所述的双功能分子、根据权利要求22所述的核酸或核酸分子组、或根据权利要求23所述的载体、或根据权利要求24所述的宿主细胞,其用作药物。
29.根据权利要求28所述的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞,其用于治疗选自癌症的疾病。
30.根据权利要求29所述的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞,其中所述癌症选自以下:表达PD-1和/或PD-L1的血液系统恶性肿瘤或实体瘤,如选自以下的癌症:淋巴造血肿瘤、血管免疫母细胞性T细胞淋巴瘤、骨髓增生异常综合征和急性髓性白血病,由病毒诱发或与免疫缺陷相关的癌症,如选自以下的癌症:卡波西氏肉瘤(例如,与卡波西氏肉瘤疱疹病毒相关的);宫颈癌、肛门癌、阴茎癌和外阴鳞状细胞癌和口咽癌(例如,与人乳头瘤病毒相关的);B细胞非霍奇金氏淋巴瘤(NHL),包括弥漫性大B细胞淋巴瘤、伯基特氏淋巴瘤、浆母细胞淋巴瘤、原发性中枢神经系统淋巴瘤、HHV-8原发性渗出性淋巴瘤、经典霍奇金氏淋巴瘤和淋巴增生性病症(例如,与爱泼斯坦-巴尔病毒(EBV)和/或卡波西氏肉瘤疱疹病毒相关的);肝细胞癌(例如,与乙型肝炎和/或丙型肝炎病毒相关的);梅克尔细胞癌(例如,与梅克尔细胞多瘤病毒(MPV)相关的);和与人免疫缺陷病毒感染(HIV)相关的癌症;以及选自以下的癌症:转移性或非转移性、黑色素瘤、恶性间皮瘤、非小细胞肺癌、肾细胞癌、霍奇金氏淋巴瘤、头颈癌、尿道上皮癌、结直肠癌、肝细胞癌、小细胞肺癌、转移性梅克尔细胞癌、胃癌或食道癌和宫颈癌。
31.根据权利要求28-30中任一项所述的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞,其用于与放射疗法或另外的治疗剂联合使用,所述另外的治疗剂优选地选自烷化剂、血管生成抑制剂、抗体、抗代谢剂、抗有丝分裂剂、抗增殖剂、抗病毒剂、极光激酶抑制剂、凋亡促进剂(例如,Bcl-2家族抑制剂)、死亡受体通路激活剂、Bcr-Abl激酶抑制剂、BiTE(双特异性T细胞接合剂)抗体、抗体药物缀合物、生物应答调节剂、布鲁顿氏酪氨酸激酶(BTK)抑制剂、细胞周期蛋白依赖性激酶抑制剂、细胞周期抑制剂、环氧合酶-2抑制剂、DVD、白血病病毒癌基因同源物(ErbB2)受体抑制剂、生长因子抑制剂、热休克蛋白(HSP)-90抑制剂、组蛋白去乙酰化酶(HDAC)抑制剂、激素疗法、免疫药、凋亡蛋白抑制剂(IAP)的抑制剂、嵌入型抗生素、激酶抑制剂、驱动蛋白抑制剂、Jak2抑制剂、哺乳动物雷帕霉素靶蛋白抑制剂、microRNA、丝裂原激活的细胞外信号调节激酶抑制剂、多价结合蛋白、非甾体抗炎症药物(NSAID)、聚ADP(二磷酸腺苷)-核糖聚合酶(PARP)抑制剂、铂类化学治疗剂、polo样激酶(Plk)抑制剂、磷酸肌醇-3激酶(PI3K)抑制剂、蛋白酶体抑制剂、嘌呤类似物、嘧啶类似物、受体酪氨酸激酶抑制剂、类视黄醇/类维生素D植物生物碱、小抑制性核糖核酸(siRNA)、拓扑异构酶抑制剂、泛素连接酶抑制剂、低甲基化剂、检查点抑制剂、肽疫苗等、来自肿瘤抗原的表位或新表位、以及这些试剂中的一种或多种的组合。
32.根据权利要求28所述的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞,其用于治疗传染病、优选地慢性传染病、甚至更优选地慢性病毒感染。
33.根据权利要求32所述的药物组合物、双功能分子、核酸或核酸分子组、载体、或宿主细胞,其中所述传染病由选自以下的病毒引起:HIV、肝炎病毒、疱疹病毒、腺病毒、流感病毒、黄病毒、埃可病毒、鼻病毒、柯萨奇病毒、冠状病毒、呼吸道合胞病毒、腮腺炎病毒、轮状病毒、麻疹病毒、风疹病毒、细小病毒、痘苗病毒、HTLV病毒、登革热病毒、乳头瘤病毒、软疣病毒、脊髓灰质炎病毒、狂犬病病毒、JC病毒和虫媒脑炎病毒。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18306808.9 | 2018-12-21 | ||
| EP18306808 | 2018-12-21 | ||
| PCT/EP2019/085791 WO2020127377A1 (en) | 2018-12-21 | 2019-12-17 | Bifunctional anti-pd-1/il-7 molecule |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113614109A true CN113614109A (zh) | 2021-11-05 |
Family
ID=65628504
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980092752.6A Pending CN113614109A (zh) | 2018-12-21 | 2019-12-17 | 双功能抗pd-1/il-7分子 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20230071889A1 (zh) |
| EP (1) | EP3898677A1 (zh) |
| JP (1) | JP7807234B2 (zh) |
| KR (1) | KR20210108978A (zh) |
| CN (1) | CN113614109A (zh) |
| BR (1) | BR112021012037A2 (zh) |
| CA (1) | CA3123338A1 (zh) |
| IL (2) | IL284002B1 (zh) |
| TW (1) | TW202039572A (zh) |
| WO (1) | WO2020127377A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117050178A (zh) * | 2023-10-13 | 2023-11-14 | 北京百普赛斯生物科技股份有限公司 | 特异性检测il-7的抗体及应用 |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102577036B1 (ko) | 2017-01-25 | 2023-09-08 | 오제 이뮈노테라프틱스 | 펩티드 전달용 안정한 에멀젼을 제조하는 방법 |
| KR102371173B1 (ko) | 2018-12-21 | 2022-03-04 | 오제 이뮈노테라프틱스 | 인간화된 항-인간-pd-1 항체 |
| WO2020127369A1 (en) * | 2018-12-21 | 2020-06-25 | Ose Immunotherapeutics | Bifunctional molecule directed against human pd-1 |
| KR20220114637A (ko) * | 2019-12-17 | 2022-08-17 | 오제 이뮈노테라프틱스 | Il-7 변이체를 포함하는 이작용성 분자 |
| MX2022012541A (es) * | 2020-04-15 | 2022-11-07 | Hoffmann La Roche | Inmunoconjugados. |
| JP2023554097A (ja) * | 2020-12-17 | 2023-12-26 | オーエスイー・イミュノセラピューティクス | 二機能性抗pd1/il-7分子 |
| EP4320155A1 (en) | 2021-04-09 | 2024-02-14 | Ose Immunotherapeutics | New scaffold for bifunctional molecules with improved properties |
| WO2023281484A1 (en) * | 2021-07-09 | 2023-01-12 | Bright Peak Therapeutics Ag | Synthetic il-7 and il-7 immunocytokines |
| CN116867805A (zh) * | 2021-09-27 | 2023-10-10 | 盛禾(中国)生物制药有限公司 | 一种异源二聚体蛋白质及其应用 |
| CN118215674A (zh) | 2021-10-14 | 2024-06-18 | 豪夫迈·罗氏有限公司 | 新颖白细胞介素-7免疫缀合物 |
| WO2023062048A1 (en) | 2021-10-14 | 2023-04-20 | F. Hoffmann-La Roche Ag | Alternative pd1-il7v immunoconjugates for the treatment of cancer |
| AU2023226512A1 (en) | 2022-02-23 | 2024-08-29 | Bright Peak Therapeutics Ag | Immune antigen specific il-18 immunocytokines and uses thereof |
| JP7805983B2 (ja) | 2022-03-22 | 2026-01-26 | アッヴィ・インコーポレイテッド | ブルトン型チロシンキナーゼを分解するためのピリミジン |
| WO2025202147A1 (en) | 2024-03-27 | 2025-10-02 | F. Hoffmann-La Roche Ag | Interleukin-7 immunoconjugates |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014066834A1 (en) * | 2012-10-26 | 2014-05-01 | The University Of Chicago | Synergistic combination of immunologic inhibitors for the treatment of cancer |
| CN105828834A (zh) * | 2013-11-05 | 2016-08-03 | 同源生物服务股份有限公司 | 检查点抑制剂和治疗剂的组合以治疗癌症 |
| WO2018184964A1 (en) * | 2017-04-03 | 2018-10-11 | F. Hoffmann-La Roche Ag | Immunoconjugates of an anti-pd-1 antibody with a mutant il-2 or with il-15 |
| WO2019144945A1 (en) * | 2018-01-25 | 2019-08-01 | I-Mab | Anti-pd-l1 antibody and il-7 fusions |
| CN113557245A (zh) * | 2018-12-21 | 2021-10-26 | Ose免疫疗法公司 | 人源化的抗人pd-1抗体 |
| CN113573782A (zh) * | 2018-12-21 | 2021-10-29 | Ose免疫疗法公司 | 针对人pd-1的双功能分子 |
| CN114369167A (zh) * | 2020-10-15 | 2022-04-19 | 苏州泽璟生物制药股份有限公司 | 抗pd-l1抗体和il-7构成的双功能融合蛋白 |
| CN116848140A (zh) * | 2020-12-17 | 2023-10-03 | Ose免疫疗法公司 | 双功能抗pd1/il-7分子 |
Family Cites Families (105)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6548640B1 (en) | 1986-03-27 | 2003-04-15 | Btg International Limited | Altered antibodies |
| ZA887773B (en) | 1987-10-26 | 1989-07-26 | Immunex Corp | Interleukin-7 |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5354844A (en) | 1989-03-16 | 1994-10-11 | Boehringer Ingelheim International Gmbh | Protein-polycation conjugates |
| US5108921A (en) | 1989-04-03 | 1992-04-28 | Purdue Research Foundation | Method for enhanced transmembrane transport of exogenous molecules |
| JP4124480B2 (ja) | 1991-06-14 | 2008-07-23 | ジェネンテック・インコーポレーテッド | 免疫グロブリン変異体 |
| ATE420178T1 (de) | 1992-08-21 | 2009-01-15 | Univ Bruxelles | Immunoglobuline ohne leichtkette |
| US5275285A (en) | 1992-12-30 | 1994-01-04 | Clegg Industries | Business card holder with sound generating microchip |
| EP0739981A1 (en) | 1995-04-25 | 1996-10-30 | Vrije Universiteit Brussel | Variable fragments of immunoglobulins - use for therapeutic or veterinary purposes |
| WO1999029888A1 (en) | 1997-12-05 | 1999-06-17 | The Scripps Research Institute | Humanization of murine antibody |
| DE60122286T2 (de) | 2000-02-11 | 2007-08-02 | Merck Patent Gmbh | Steigerung der zirkulierenden halbwertzeit von auf antikörpern basierenden fusionsproteinen |
| BR0207854A (pt) | 2001-03-07 | 2004-08-24 | Merck Patent Gmbh | Tecnologia de expressão para proteìnas contendo uma porção de anticorpo de isotipo hìbrido |
| EP1391513A1 (en) | 2002-08-08 | 2004-02-25 | Cytheris | IL-7 drug substance, IL-7 comprising composition, preparation and uses thereof |
| BRPI0418286A (pt) | 2003-12-30 | 2007-05-02 | Merck Patent Gmbh | proteìnas de fusão de il-7 |
| MXPA06011199A (es) | 2004-03-31 | 2007-04-16 | Genentech Inc | Anticuerpos anti-tgf-beta humanizados. |
| EP1626059A1 (en) | 2004-08-09 | 2006-02-15 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | Angiogenic and immunologic applications of anti-CD160 specific compounds obtainable from mAb CL1-R2 |
| RU2437893C2 (ru) | 2004-12-09 | 2011-12-27 | Мерк Патент Гмбх | Варианты il-7 со сниженной иммуногенностью |
| WO2010006071A1 (en) | 2008-07-08 | 2010-01-14 | La Jolla Institute For Allergy And Immunology | Hvem/btla, hvem/cd160 and hvem/gd cis complexes and methods of use |
| PL2161336T5 (pl) | 2005-05-09 | 2017-10-31 | Ono Pharmaceutical Co | Ludzkie przeciwciała monoklonalne przeciwko białku Programmed Death 1 (PD-1) oraz sposoby leczenia raka z zastosowaniem samych przeciwciał anty-PD-1 lub w połączeniu z innymi środkami immunoterapeutycznymi |
| WO2007008463A2 (en) | 2005-07-07 | 2007-01-18 | Coley Pharmaceutical Group, Inc. | Anti-ctla-4 antibody and cpg-motif-containing synthetic oligodeoxynucleotide combination therapy for cancer treatment |
| EP1746161A1 (en) | 2005-07-20 | 2007-01-24 | Cytheris | Glycosylated IL-7, preparation and uses |
| AU2007334264A1 (en) | 2006-11-15 | 2008-06-26 | Medarex, Inc. | Human monoclonal antibodies to BTLA and methods of use |
| EP1987839A1 (en) | 2007-04-30 | 2008-11-05 | I.N.S.E.R.M. Institut National de la Sante et de la Recherche Medicale | Cytotoxic anti-LAG-3 monoclonal antibody and its use in the treatment or prevention of organ transplant rejection and autoimmune disease |
| US8263073B2 (en) | 2008-02-04 | 2012-09-11 | Medarex, Inc. | Anti-CTLA-4 antibodies with reduced blocking of binding of CTLA-4 to B7 and uses thereof |
| AR072999A1 (es) | 2008-08-11 | 2010-10-06 | Medarex Inc | Anticuerpos humanos que se unen al gen 3 de activacion linfocitaria (lag-3) y los usos de estos |
| EP2210903A1 (en) | 2009-01-21 | 2010-07-28 | Monoclonal Antibodies Therapeutics | Anti-CD160 monoclonal antibodies and uses thereof |
| EP2408818A1 (en) | 2009-03-17 | 2012-01-25 | Université de la Méditerranée | Btla antibodies and uses thereof |
| CA2769473A1 (en) | 2009-07-31 | 2011-02-03 | N.V. Organon | Fully human antibodies to btla |
| JP6158511B2 (ja) | 2010-06-11 | 2017-07-05 | 協和発酵キリン株式会社 | 抗tim−3抗体 |
| GB201103955D0 (en) | 2011-03-09 | 2011-04-20 | Antitope Ltd | Antibodies |
| WO2013006490A2 (en) | 2011-07-01 | 2013-01-10 | Cellerant Therapeutics, Inc. | Antibodies that specifically bind to tim3 |
| SG10201700698WA (en) * | 2012-05-15 | 2017-02-27 | Bristol Myers Squibb Co | Cancer immunotherapy by disrupting pd-1/pd-l1 signaling |
| KR20140025836A (ko) * | 2012-08-22 | 2014-03-05 | 한화케미칼 주식회사 | 항 HER2/Neu 단일클론항체와 IL-7가 연결된 융합 단일클론 항체 및 이를 포함하는 암 치료용 조성물 |
| CA2913977C (en) | 2013-05-31 | 2022-11-29 | Sorrento Therapeutics, Inc. | Antigen binding proteins that bind pd-1 |
| EP3131581B1 (en) | 2014-04-18 | 2020-09-23 | The Research Foundation of the State University of New York | Humanized anti-tf-antigen antibodies |
| CN105296433B (zh) | 2014-08-01 | 2018-02-09 | 中山康方生物医药有限公司 | 一种ctla4抗体、其药物组合物及其用途 |
| SG11201701161QA (en) | 2014-08-19 | 2017-03-30 | Merck Sharp & Dohme | Anti-tigit antibodies |
| MA40662B1 (fr) | 2014-12-23 | 2020-12-31 | Bristol Myers Squibb Co | Anticorps contre tigit |
| CA2976446A1 (en) | 2015-02-13 | 2016-08-18 | Sorrento Therapeutics, Inc. | Antibody therapeutics that bind ctla4 |
| SMT202400420T1 (it) | 2015-04-01 | 2024-11-15 | Anaptysbio Inc | Anticorpi diretti contro la proteina dell’immunoglobulina delle cellule t e della mucina 3 (tim-3) |
| TWI715587B (zh) | 2015-05-28 | 2021-01-11 | 美商安可美德藥物股份有限公司 | Tigit結合劑和彼之用途 |
| DK3303394T3 (da) | 2015-05-29 | 2020-07-06 | Agenus Inc | Anti-ctla-4-antistoffer og fremgangsmåder til anvendelse deraf |
| SG10201906059VA (en) | 2015-07-30 | 2019-08-27 | Macrogenics Inc | Pd-1-binding molecules and methods of use thereof |
| KR20180035906A (ko) * | 2015-08-07 | 2018-04-06 | 피어이스 파마슈티컬즈 게엠베하 | Lag-3 및 pd-1에 특이적인 신규 융합 폴리펩타이드 |
| WO2017024465A1 (en) | 2015-08-10 | 2017-02-16 | Innovent Biologics (Suzhou) Co., Ltd. | Pd-1 antibodies |
| CN105111314B (zh) * | 2015-08-13 | 2019-01-08 | 成都百世博生物技术有限公司 | 一种新型融合蛋白、药物组合物及其制备方法和用途 |
| CN115925931A (zh) | 2015-08-14 | 2023-04-07 | 默沙东公司 | 抗tigit抗体 |
| WO2017040790A1 (en) | 2015-09-01 | 2017-03-09 | Agenus Inc. | Anti-pd-1 antibodies and methods of use thereof |
| CN108137691B (zh) | 2015-09-02 | 2021-10-19 | 耶路撒冷希伯来大学伊萨姆研究发展有限公司 | 特异性针对人类t-细胞免疫球蛋白和itim结构域(tigit)的抗体 |
| NZ739750A (en) | 2015-09-25 | 2019-11-29 | Genentech Inc | Anti-tigit antibodies and methods of use |
| EA038179B1 (ru) | 2015-11-18 | 2021-07-20 | Мерк Шарп И Доум Корп. | Ctla4-связывающие вещества |
| CN107406504B (zh) | 2015-11-19 | 2021-04-30 | 蔡则玲 | Ctla-4抗体及其用途 |
| JP7227007B2 (ja) | 2015-12-02 | 2023-02-21 | ストサイエンシス, インコーポレイテッド | グリコシル化btla(b-及びt-リンパ球減弱因子)に特異的な抗体 |
| IL259988B2 (en) | 2015-12-15 | 2023-02-01 | Oncoimmune Inc | Chimeric and humanized monoclonal antibodies against ctla-4 and uses thereof |
| CN108848669B (zh) | 2016-01-20 | 2022-06-07 | 斯克利普斯研究所 | Ror1抗体组合物和相关方法 |
| CN111491362B (zh) | 2016-02-02 | 2023-10-24 | 华为技术有限公司 | 确定发射功率的方法、用户设备和基站 |
| WO2017132827A1 (en) | 2016-02-02 | 2017-08-10 | Innovent Biologics (Suzhou) Co., Ltd. | Pd-1 antibodies |
| EP3411414A4 (en) * | 2016-02-05 | 2019-10-23 | Washington University | COMPOSITIONS AND METHOD FOR TARGETED CYTOKINE RELIEF |
| JP7030704B2 (ja) * | 2016-02-05 | 2022-03-08 | オリオニス バイオサイエンシズ ビーブイ | 二重特異性シグナル伝達物質およびその使用 |
| CA3013333A1 (en) | 2016-02-26 | 2017-08-31 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Antibodies having specificity for btla and uses thereof |
| BR112018067458A2 (pt) | 2016-03-04 | 2019-01-02 | Abmuno Therapeutics Llc | anticorpos para tigit |
| SG10201603721TA (en) | 2016-05-10 | 2017-12-28 | Agency Science Tech & Res | Anti-CTLA-4 Antibodies |
| NL2017270B1 (en) | 2016-08-02 | 2018-02-09 | Aduro Biotech Holdings Europe B V | New anti-hCTLA-4 antibodies |
| KR20230145510A (ko) | 2016-08-17 | 2023-10-17 | 컴퓨젠 엘티디. | 항-tigit 항체, 항-pvrig 항체 및 이들의 조합 |
| WO2018035710A1 (en) | 2016-08-23 | 2018-03-01 | Akeso Biopharma, Inc. | Anti-ctla4 antibodies |
| MX2019002946A (es) | 2016-09-14 | 2019-09-26 | Abbvie Biotherapeutics Inc | Anticuerpos anti-pd-1 y sus usos. |
| JP6976322B2 (ja) | 2016-10-10 | 2021-12-08 | クラウン バイオサイエンス,インコーポレイテッド(タイツァン) | 新規抗ctla4抗体 |
| US11186635B2 (en) | 2016-10-25 | 2021-11-30 | Institut National De La Santé Et De La Recherché Médical (Inserm) | Monoclonal antibodies binding to the CD160 transmembrane isoform |
| KR20190098741A (ko) | 2016-11-01 | 2019-08-22 | 아납티스바이오, 아이엔씨. | T 세포 면역글로불린 및 뮤신 단백질 3(tim-3)에 대한 항체 |
| CN110662552A (zh) | 2016-11-30 | 2020-01-07 | 昂科梅德制药有限公司 | 包含tigit结合剂的癌症治疗方法 |
| WO2018102746A1 (en) | 2016-12-02 | 2018-06-07 | Rigel Pharmaceuticals, Inc. | Antigen binding molecules to tigit |
| AU2017373944B2 (en) | 2016-12-07 | 2022-02-03 | Agenus Inc. | Anti-CTLA-4 antibodies and methods of use thereof |
| MA50948A (fr) | 2016-12-07 | 2020-10-14 | Agenus Inc | Anticorps et procédés d'utilisation de ceux-ci |
| CN108250303B (zh) * | 2016-12-19 | 2023-01-03 | 南京金斯瑞生物科技有限公司 | 单域抗体融合蛋白及其应用 |
| MA47206A (fr) | 2017-01-09 | 2019-11-13 | Tesaro Inc | Méthodes de traitement du cancer au moyen d'anticorps anti-tim-3 |
| KR102697723B1 (ko) | 2017-01-18 | 2024-08-21 | 비스테라, 인크. | 항체 분자-약물 접합체 및 이의 용도 |
| US11319372B2 (en) | 2017-02-21 | 2022-05-03 | Remd Biotherapeutics, Inc. | Cancer treatment using antibodies that bind cytotoxic T-lymphocyte antigen-4 (CTLA-4) |
| SG11201907867TA (en) | 2017-02-28 | 2019-09-27 | Bristol Myers Squibb Co | Use of anti-ctla-4 antibodies with enhanced adcc to enhance immune response to a vaccine |
| SG11201907278VA (en) | 2017-02-28 | 2019-09-27 | Seattle Genetics Inc | Anti-tigit antibodies |
| WO2018165895A1 (zh) | 2017-03-15 | 2018-09-20 | 苏州银河生物医药有限公司 | Ctla4抗体、其药物组合物及其用途 |
| SG11201908813QA (en) | 2017-04-13 | 2019-10-30 | Aduro Biotech Holdings Europe B V | Anti-sirp alpha antibodies |
| CN110621341A (zh) | 2017-04-26 | 2019-12-27 | 百时美施贵宝公司 | 使二硫键还原最小化的抗体生产方法 |
| WO2018204363A1 (en) | 2017-05-01 | 2018-11-08 | Agenus Inc. | Anti-tigit antibodies and methods of use thereof |
| CA3060618A1 (en) | 2017-05-19 | 2018-11-22 | Wuxi Biologics (Shanghai) Co. Ltd. | Novel monoclonal antibodies to cytotoxic t-lymphocyte-associated protein 4 (ctla-4) |
| TWI799432B (zh) | 2017-07-27 | 2023-04-21 | 美商再生元醫藥公司 | 抗ctla-4抗體及其用途 |
| WO2019023504A1 (en) | 2017-07-27 | 2019-01-31 | Iteos Therapeutics Sa | ANTI-TIGIT ANTIBODIES |
| SI3661954T1 (sl) * | 2017-08-03 | 2022-05-31 | Amgen Inc. | Muteini interlevkina-21 in postopki zdravljenja |
| WO2019056281A1 (en) | 2017-09-21 | 2019-03-28 | Eucure (Beijing) Biopharma Co., Ltd | ANTI-CTLA4 ANTIBODIES AND USES THEREOF |
| CN111372590A (zh) | 2017-09-23 | 2020-07-03 | 纪念斯隆-凯特林癌症中心 | A33抗体组合物及在放射免疫疗法中使用其的方法 |
| CN111051347B (zh) | 2017-09-29 | 2021-12-21 | 江苏恒瑞医药股份有限公司 | Tigit抗体、其抗原结合片段及医药用途 |
| PL3710484T3 (pl) | 2017-12-20 | 2024-03-25 | Harbour Biomed (Shanghai) Co., Ltd | Przeciwciała wiążące ctla-4 i ich zastosowania |
| SG11202004158QA (en) | 2017-12-28 | 2020-06-29 | Nanjing Legend Biotech Co Ltd | Single-domain antibodies and variants thereof against tigit |
| TWI816729B (zh) | 2017-12-30 | 2023-10-01 | 英屬開曼群島商百濟神州有限公司 | 抗tigit抗體及其作為治療和診斷的用途 |
| TW201932489A (zh) | 2018-01-15 | 2019-08-16 | 大陸商南京傳奇生物科技有限公司 | 針對tigit之抗體及其變異體 |
| WO2019152574A1 (en) | 2018-02-01 | 2019-08-08 | Merck Sharp & Dohme Corp. | Methods for treating cancer or infection using a combination of an anti-pd-1 antibody, an anti-lag3 antibody, and an anti-tigit antibody |
| WO2019148444A1 (en) | 2018-02-02 | 2019-08-08 | Adagene Inc. | Anti-ctla4 antibodies and methods of making and using the same |
| SG11202004521QA (en) | 2018-02-06 | 2020-06-29 | I Mab Biopharma Us Ltd | Antibodies to t cell immunoreceptor with ig and itim domains (tigit) and uses thereof |
| MX2020008795A (es) | 2018-02-28 | 2020-10-08 | Yuhan Corp | Anti cuerpos anti tigit y usos de los mismos. |
| US20210024632A1 (en) | 2018-03-05 | 2021-01-28 | Etablissement Francais Du Sang | Recombinant single chain immunoglobulins |
| CN110272490B (zh) | 2018-03-14 | 2021-05-14 | 上海开拓者生物医药有限公司 | 靶向ctla-4抗体、其制备方法和用途 |
| CN112218892B (zh) | 2018-03-19 | 2023-04-25 | 上海药明生物技术有限公司 | 新型抗ctla-4抗体多肽 |
| WO2019179391A1 (en) | 2018-03-19 | 2019-09-26 | Wuxi Biologics (Shanghai) Co., Ltd. | Novel bispecific pd-1/ctla-4 antibody molecules |
| WO2019215728A1 (en) | 2018-05-09 | 2019-11-14 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Antibodies specific to human nectin4 |
| WO2019232484A1 (en) | 2018-06-01 | 2019-12-05 | Compugen Ltd | Anti-pvrig/anti-tigit bispecific antibodies and methods of use |
| JP7444889B2 (ja) * | 2018-12-20 | 2024-03-06 | コーセプト セラピューティクス, インコーポレイテッド | ソマトスタチン受容体陽性腫瘍のイメージング及び治療のための方法 |
-
2019
- 2019-12-17 CN CN201980092752.6A patent/CN113614109A/zh active Pending
- 2019-12-17 CA CA3123338A patent/CA3123338A1/en active Pending
- 2019-12-17 EP EP19818167.9A patent/EP3898677A1/en active Pending
- 2019-12-17 US US17/414,970 patent/US20230071889A1/en active Pending
- 2019-12-17 KR KR1020217022838A patent/KR20210108978A/ko active Pending
- 2019-12-17 WO PCT/EP2019/085791 patent/WO2020127377A1/en not_active Ceased
- 2019-12-17 BR BR112021012037A patent/BR112021012037A2/pt unknown
- 2019-12-17 JP JP2021536209A patent/JP7807234B2/ja active Active
- 2019-12-20 TW TW108147053A patent/TW202039572A/zh unknown
-
2021
- 2021-06-14 IL IL284002A patent/IL284002B1/en unknown
-
2025
- 2025-10-12 IL IL323895A patent/IL323895A/en unknown
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014066834A1 (en) * | 2012-10-26 | 2014-05-01 | The University Of Chicago | Synergistic combination of immunologic inhibitors for the treatment of cancer |
| CN105828834A (zh) * | 2013-11-05 | 2016-08-03 | 同源生物服务股份有限公司 | 检查点抑制剂和治疗剂的组合以治疗癌症 |
| WO2018184964A1 (en) * | 2017-04-03 | 2018-10-11 | F. Hoffmann-La Roche Ag | Immunoconjugates of an anti-pd-1 antibody with a mutant il-2 or with il-15 |
| WO2019144945A1 (en) * | 2018-01-25 | 2019-08-01 | I-Mab | Anti-pd-l1 antibody and il-7 fusions |
| CN113557245A (zh) * | 2018-12-21 | 2021-10-26 | Ose免疫疗法公司 | 人源化的抗人pd-1抗体 |
| CN113573782A (zh) * | 2018-12-21 | 2021-10-29 | Ose免疫疗法公司 | 针对人pd-1的双功能分子 |
| CN114369167A (zh) * | 2020-10-15 | 2022-04-19 | 苏州泽璟生物制药股份有限公司 | 抗pd-l1抗体和il-7构成的双功能融合蛋白 |
| CN116848140A (zh) * | 2020-12-17 | 2023-10-03 | Ose免疫疗法公司 | 双功能抗pd1/il-7分子 |
Non-Patent Citations (2)
| Title |
|---|
| YUICHIRO SHINDO: "Interleukin 7 and anti-programmed cell death 1 antibody have differing effects to reverse sepsis-induced immunosuppression", 《SHOCK》, vol. 43, no. 4, 30 April 2015 (2015-04-30), pages 334, XP055612000, DOI: 10.1097/SHK.0000000000000317 * |
| 王彦志: "程序性死亡分子1 /程序性死亡配体1 抗体 治疗人类癌症的研究进展", 《安徽医药》, vol. 21, no. 3, 31 March 2017 (2017-03-31), pages 395 - 399 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117050178A (zh) * | 2023-10-13 | 2023-11-14 | 北京百普赛斯生物科技股份有限公司 | 特异性检测il-7的抗体及应用 |
| CN117050178B (zh) * | 2023-10-13 | 2024-01-12 | 北京百普赛斯生物科技股份有限公司 | 特异性检测il-7的抗体及应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| IL284002A (en) | 2021-07-29 |
| IL284002B1 (en) | 2025-11-01 |
| TW202039572A (zh) | 2020-11-01 |
| CA3123338A1 (en) | 2020-06-25 |
| US20230071889A1 (en) | 2023-03-09 |
| JP2022514702A (ja) | 2022-02-14 |
| EP3898677A1 (en) | 2021-10-27 |
| WO2020127377A9 (en) | 2020-09-03 |
| WO2020127377A1 (en) | 2020-06-25 |
| KR20210108978A (ko) | 2021-09-03 |
| AU2019407814A1 (en) | 2021-07-22 |
| IL323895A (en) | 2025-12-01 |
| JP7807234B2 (ja) | 2026-01-27 |
| BR112021012037A2 (pt) | 2021-11-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7807234B2 (ja) | 二機能性抗pd-1/il-7分子 | |
| CN113573782B (zh) | 针对人pd-1的双功能分子 | |
| JP7404423B2 (ja) | ヒト化抗ヒトpd-1抗体 | |
| JP7675012B2 (ja) | 二機能性抗pd-1/sirpa分子 | |
| AU2020406083A1 (en) | Bifunctional molecules comprising an IL-7 variant | |
| US20240067727A1 (en) | Bifunctional anti-pd1/il-7 molecules | |
| JP2024515263A (ja) | 改善された特性を有する二機能性分子のための新規足場構造 | |
| US20230303648A1 (en) | Bifunctional molecules comprising an il-7 variant | |
| US20240182572A1 (en) | Scaffold for bifunctional molecules comprising pd-1 or cd28 and sirp binding domains | |
| AU2019407814B2 (en) | Bifunctional anti-PD-1/IL-7 molecule |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |