CN112505223B - 一种同时检测食品中毒黄素和米酵菌酸含量的方法 - Google Patents
一种同时检测食品中毒黄素和米酵菌酸含量的方法 Download PDFInfo
- Publication number
- CN112505223B CN112505223B CN202011354358.6A CN202011354358A CN112505223B CN 112505223 B CN112505223 B CN 112505223B CN 202011354358 A CN202011354358 A CN 202011354358A CN 112505223 B CN112505223 B CN 112505223B
- Authority
- CN
- China
- Prior art keywords
- mobile phase
- content
- sample
- acid
- methanol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
- G01N2030/8809—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample
- G01N2030/884—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample organic compounds
Landscapes
- Physics & Mathematics (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
本发明提供一种简单、高效的能同时检测毒黄素和米酵菌酸含量的方法同时检测食品中毒黄素和米酵菌酸含量的方法,包括如下步骤:1)对样品进行前处理,将样品进行两次提取处理,每次均用80%‑90%甲醇水溶液涡旋,超声,然后离心,吸取上清液至预装有dSPE EMR‑Lipid吸附剂的离心管中,涡旋,离心,取上清液;合并上清液,对所得上清液进行氮吹处理后,用甲醇定容并用滤膜过滤;2)对步骤1)所得处理后样品进行色谱分析,色谱条件包括:色谱柱为C18色谱柱;流动相包括流动相A和流动相B,其中流动相A为甲醇,流动相B为pH 2.5‑3.0的水;3)定量分析样品中毒黄素和米酵菌酸的含量。
Description
技术领域
本发明涉及毒黄素和米酵菌酸的定量分析检测技术,特别涉及一种同时检测食品中毒黄素和米酵菌酸含量的方法。
背景技术
近年来由椰毒假单胞菌酵米面亚种(Pseudomonas cocovenenanssubsp.farinofermentans,简称椰酵假单胞菌)引起的食物中毒事件时有发生,涉及食品种类包括谷类发酵制品、变质银耳及薯类制品等。在适宜温度、湿度等的条件下,椰酵假单胞菌会产生米酵菌酸(Bongkrekic acid,BA)和毒黄素(Toxofl avin,TF)两种毒素。毒理学研究表明,BA对小鼠静脉注射的LD50为1.14mg/kg、MED50为0.0562mg/kg,TF对小鼠静脉注射的LD50为1.7mg/kg,MED50为8.39mg/kg,其中,米酵菌酸耐热,且一般烹调方法不能去除,这也是由椰酵假单胞菌引起食物中毒导致病死率高的主要原因之一。
目前,针对由椰酵假单胞菌引起食物中毒事件调查,主要开展病原菌分离鉴定和毒素测定工作。病原菌椰毒假单胞菌酵米面亚种分离鉴定可参照GB/T4789.29-2003《食品卫生微生物学检验椰毒假单胞菌酵米面亚种检验》,毒素米酵菌酸含量测定参照GB5009.189-2016《食品安全国家标准食品中米酵菌酸的测定》,而毒黄素暂无国家标准方法。Suzuki等(Suzuki F,Sawada H,Azegami K,et al.Molecular characterization of thetox operon involved in toxoflavin biosynthesis of Burkholderia glumae.J GenPlant Pathol,2004,70:97-107)和Zhu等(Suzuki F,Sawada H,Azegami K,etal.Molecular characterization of the tox operon involved in toxoflavinbiosynthesis of Burkholderia glumae.J Gen Plant Pathol,2004,70:97-107)采用薄层色谱法进行定性分析;Buckle KA(Buckle KA,Kartadarma E.Inhibition of bongkrekacid and toxoflavin production in tempe bongkrek containing Pseudomonascocovenenans.J Appl Bacteriol,1990,68:571-6)和Fenwick MK(Fenwick MK,PhilmusB,Begley TP,et al.Toxoflavin lyase requires a novel 1-His-2-carboxylatefacial triad.Biochemistry,2011,50:1091-100)分别开发了高效液相色谱法和液相色谱质谱法测定培养液中毒黄素的浓度,不过适用的检验范围比较窄;近年李红艳;张东雷等(李红艳;张东雷;盛华栋,等.基于固相萃取-高效液相色谱法的复杂食品基质中细菌性毒素米酵菌酸和毒黄素检测方法研究[Z].国家科技成果;李红艳,金燕飞,黄海智,等.高效液相色谱-二极管阵列检测器结合固相萃取法快速测定食品中米酵菌酸残留[J].食品科学,2016,37(24):254-258.)开发了基于固相萃取-高效液相色谱法的复杂食品基质中细菌性毒素米酵菌酸和毒黄素检测方法采用混合型弱阴离子小柱(WAX)和多功能净化柱MycoSep226分别对米酵菌酸和毒黄素进行净化,再合并浓缩后测定,但该方法操作步骤繁琐,有机溶剂损耗大,对于米面制品等淀粉含量较大的食品,净化后合并的溶液量较大,浓缩时间较长。亟需开发一种快速的净化方法,缩短前处理时间,以及能实现同时检测毒黄素和米酵菌酸含量的方法,从而提高食品中毒黄素和米酵菌酸的检测分析效率。
发明内容
本发明目的在于提供一种简单、高效的能同时检测毒黄素和米酵菌酸含量的方法。
本发明为达到其目的,提供如下技术方案:
本发明提供一种同时检测食品中毒黄素和米酵菌酸含量的方法,包括如下步骤:
1)对样品进行前处理
将样品进行两次提取处理,每次均用80%-90%(体积百分比)甲醇水溶液涡旋2-5min,超声10-15min,然后离心,吸取上清液至预装有dSPE EMR-Lipid吸附剂(吸附剂的用量采用该吸附剂商品的预定用量)的离心管中,涡旋2-5min,离心,取上清液;
合并两次提取所得上清液,对所得上清液进行氮吹处理后,用甲醇定容并用滤膜过滤,获得处理后样品;
2)对步骤1)所得处理后样品进行色谱分析,色谱条件包括:色谱柱为C18色谱柱;流动相包括流动相A和流动相B,其中流动相A为甲醇,流动相B为pH 2.5-3.0的水;检测波长为258nm;梯度洗脱程序为:
0-5min,流动相A 20%,流动相B 80%;
5-6min,流动相A 20%→90%,流动相B 80%→10%;
6-14min,流动相A 90%,流动相B10%;
14-15min,流动相A 90%→20%,流动相B10%→80%;
15-20min,流动相A 20%,流动相B 80%;
以上百分比均指在流动相中的体积百分比;
3)根据预先绘制的标准曲线和步骤2)色谱分析所得检测结果(如色谱分析获得的响应峰面积),定量分析样品中毒黄素和米酵菌酸的含量。
优选实施方式中,步骤2)中,作为流动相B的水的pH为3.0。
优选实施方式中,步骤2)中,作为流动相B的水采用甲酸调节其pH为3.0。
优选实施方式中,步骤1)中,所述甲醇水溶液的浓度为80%。
一些实施方式中,步骤1)中,基于每2g样品,所述甲醇水溶液的用量为10ml。
一些实施方式中,,步骤2)中,色谱条件还包括:流速为1mL/min;柱温为30℃;进样量为10μL。
本发明的检测方法,所使用的食品样品可以为有检测毒黄素和米酵菌酸含量需要的各种食品样品,例如但不限于谷类发酵制品、薯类制品、银耳和/或黑木耳,例如玉米面、湿河粉等。
具体的,本发明采用外标法进行所述定量分析。
本发明提供的技术方案具有如下有益效果:
本发明提供的方法能简单、快速、灵敏度高的同时检测食品中毒黄素和米酵菌酸含量,可以简化检测过程,提高检测效率。
附图说明
图1为不同提取溶剂对毒黄素和米酵菌酸回收率的影响;
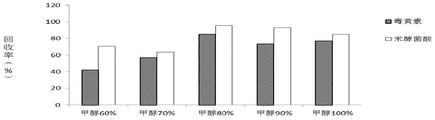
图2为不同浓度的甲醇溶液对毒黄素及米酵菌酸回收率的影响;
图3为以80%甲醇为溶剂不同提取次数对毒黄素及米酵菌酸回收率的影响;
图4-1和图4-2依次分别为毒黄素和米酵菌酸光谱图;
图5为不同流动相酸度调节剂的色谱图;
图6为不同pH的流动相色谱图。
具体实施方式
为了更好的理解本发明的技术方案,下面结合实施例进一步阐述本发明的内容,但本发明的内容并不仅仅局限于以下实施例。
以下实施例或对比例中,所用仪器、材料和试剂说明如下:
实验仪器:
Agilent 1260高效液相色谱仪配DAD检测器(G4212A 1260美国安捷伦公司);GT-2227QTS智能超声波清洗仪(广东固特超声股份有限公司);Fotector Plus高通量全自动固相萃取仪(厦门睿科集团股份有限公司)。
材料与试剂:
毒黄素(CAS号:84-82-2,纯度≥98%),米酵菌酸(CAS号:11076-19-0,纯度≥95%),甲醇、乙腈为色谱纯,QuEChERS dSPE EMR-Lipid(广州安捷伦科技有限公司)、Polish Tube-NaCl/MgSO4(广州安捷伦科技有限公司)、dSPE Cleaneup Tubes(300mgMgSO4,100mg PSA,100mg C18,15mL)(上海安谱实验科技股份有限公司)、Cleanert MAS-Q(PSA400mg,C18 400mg,MgSO4 1.2g,15mL)(天津博纳艾杰尔科技有限公司);其余试剂为分析纯;实验用水为超纯水。
绘制标准曲线所用标准溶液的配制:
米酵菌酸标准储备液(0.1mg/mL):准确称取米酵菌酸标准品1mg(精确至0.01mg),用甲醇溶解,转移至10mL容量瓶中,用甲醇定容。
毒黄素标准储备液(0.1mg/mL):准确称取毒黄素标准品1mg(精确至0.01mg),用甲醇溶解,转移至10mL容量瓶中,用甲醇定容。
线性关系、方法检出限及定量限:
分别以米酵菌酸标准储备液和毒黄素标准储备液为原液,依次分别配制成浓度为0.5、1.0、2.0、5.0、10.0、25.0μg/mL的系列标准溶液。按照和如下实施例1中相同的色谱条件进行分析,测定标准溶液的峰面积。以峰面积为纵坐标,毒黄素和米酵菌酸浓度为横坐标,绘制标准曲线,线性关系、方法检出限及定量限见表1。结果表明,毒黄素和米酵菌酸在0.5~25μg/ml范围内呈现良好的线性关系。
色谱条件:色谱柱:C18色谱柱(柱长250mm,内径4.6mm,粒度5μm);流动相:A:甲醇,B:水(甲酸调节pH至3.0);流速:1mL/min;检测波长:258nm;柱温:30℃;进样量:10μL,梯度洗脱程序见实施例1中的表2。
表1米酵菌酸和毒黄素的线性关系、方法检出限及定量限
实施例1
1.1、检测方法
样品前处理:称取粉碎/混匀的试样2g(精确至0.01g)于50mL塑料离心管中,加入80%甲醇水溶液(作为提取溶剂)10mL,涡旋2min,超声10min,5000r/min离心5min,吸取上清液至预装dSPE EMR-Lipid吸附剂(用量采用商品预定用量)的离心管中,涡旋2min,5000r/min离心5min,取上清液于氮吹管中;同时,重复上述提取、净化步骤,合并两次上清液于40℃水浴中氮吹至低于1ml,用甲醇定容至1ml,0.22μm滤膜过滤后进行色谱分析。
色谱条件:色谱柱:C18色谱柱(柱长250mm,内径4.6mm,粒度5μm);流动相:A:甲醇,B:水(用甲酸调节pH至3.0);流速:1mL/min;检测波长:258nm;柱温:30℃;进样量:10μL,梯度洗脱程序见表2。
外标法定量,根据绘制的标准曲线和色谱检测结果计算得到样品中毒黄素和米酵菌酸含量。
表2梯度洗脱程序(以下百分比为体积百分比)
1.2、检测方法的稳定性试验
按照实施例1的检测方法,以湿米粉作为样品,制备的供试品溶液室温放置,放置0、6、12、18、24、30h后各测定一次,共测定6次,毒黄素峰面积在18h内的RSD为4.79%,而后峰面积明显衰减,RSD远大于5%;米酵菌酸的峰面积在36h的RSD为0.83%,稳定性较好。
1.3、方法回收率与精密度
样品加标回收率:相同的样品取两份,其中一份加入定量的待测成分标准物质;两份同时按相同的分析步骤分析,加标的一份所得的结果减去未加标一份所得的结果,其差值同加入标准物质的理论值之比即为样品加标回收率。
加标回收率=(加标试样测定值-试样测定值)÷加标量×100%
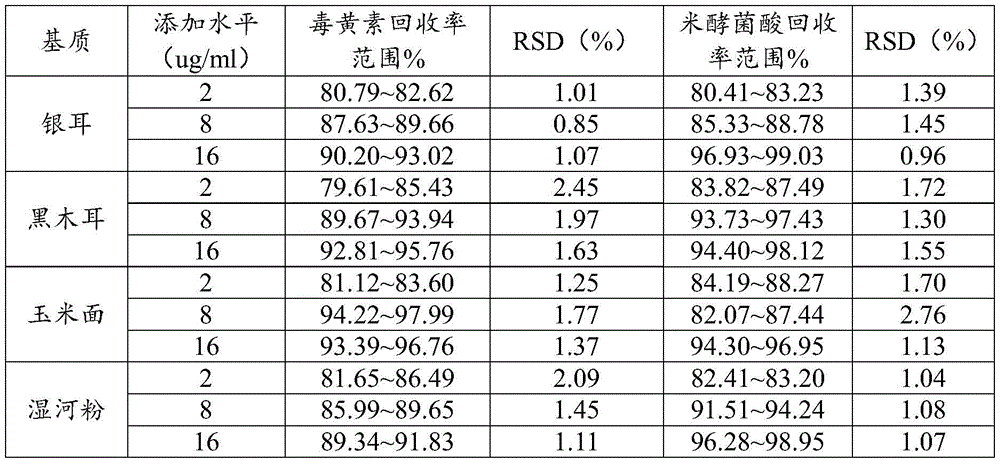
按照实施例1的检测方法,选取银耳、黑木耳、玉米面以及湿米粉4种不同基质进行3水平的添加回收率(加标回收率)实验和精密度实验,结果(表3)表明在2ug/mL、8ug/mL、16ug/mL,3个加标水平下,毒黄素的平均回收率(n=6)为88.94%,平均相对标准偏差(RSD,n=6)为1.50%;米酵菌酸的平均回收率(n=6)为90.43%,平均相对标准偏差(RSD,n=6)为1.43%;方法的准确度和精密度良好。
表3毒黄素和米酵菌酸的回收率结果(n=6)
实施例2
本实施例和实施例1的检测方法基本相同,不同在于,以湿米粉为样品,在样品前处理中,分别以甲醇、乙腈、80%甲醇、80%乙腈为提取溶剂,采用这四种不同溶剂的毒黄素和米酵菌酸的回收率对比结果见图1。
从图1可见,80%甲醇水溶液的提取效果优于甲醇、乙腈、80%乙腈,毒黄素和米酵菌酸的回收率分别为95.3%、87.1%。
实施例3
本实施例和实施例1的检测方法不同在于,以湿米粉为样品,在样品前处理中,分别以60%甲醇水溶液、70%甲醇水溶液、80%甲醇水溶液、90%甲醇水溶液、100%甲醇为提取溶剂,采用这四种不同浓度的甲醇溶液的回收率对比结果见图2。从图2可见,当选取80%甲醇时,毒黄素和米酵菌酸的回收率均最好,发明人发现,当水的比例较高时,氮吹困难,液体浑浊,不易吹干,导致结果误差较大。
实施例4
本实施例和实施例1的检测方法基本相同,不同在于,以湿米粉为样品,在样品前处理中,分别采用了dSPE、MAS-Q、dSPEEMR-Lipid以及dSPEEMR-Lipid+Nacl/MgSO4四种不同净化吸附剂,毒黄素和米酵菌酸的回收率结果见表4。其中dSPEEMR-Lipid+Nacl/MgSO4为QuEChERS dSPE EMR-Lipid(广州安捷伦科技有限公司)、Polish Tube-NaCl/MgSO4(广州安捷伦科技有限公司)两种吸附剂的组合,具体为在吸附剂处理环节先用QuEChERS dSPEEMR-Lipid处理,之后再用Polish Tube-NaCl/MgSO4处理;本实施例中涉及的各吸附剂均采用吸附剂商品的预定用量。
结果表明,dSPE和MAS-Q作为净化剂时,目标化合物的回收率均低于30%,dSPE和MAS-Q主要成分为PSA(N-丙基乙二胺)和C18(十八烷基键合硅胶),因为PSA吸附剂可去除样品基质中的有机酸、色素和糖类杂质,C18吸附剂可以去除脂肪和酯类等非极性干扰物,在净化过程中,PSA和C18会将目标化合物去除掉,降低了毒黄素和米酵菌酸的回收率。而dSPEEMR-Lipid和dSPEEMR-Lipid+Nacl/MgSO4做净化剂时,毒黄素和米酵菌酸的回收率均可达到80%以上,单独采用dSPE EMR-Lipid,操作简单,样品回收率更高。
表4不同净化剂组合对毒黄素和米酵菌酸回收率的影响
实施例5
本实施例和实施例1的检测方法基本相同,不同在于,以湿米粉为样品,在样品前处理中,分别采用提取次数1次、2次和3次。毒黄素和米酵菌酸的回收率结果见图3。实验发现,试样经两次提取后,回收率达到最佳。
实施例6
发明人利用二极管阵列检测器分析其对米酵菌酸和毒黄素最大吸收波长分别为258nm、267nm、300nm。
本实施例和实施例1的检测方法基本相同,不同在于,以湿米粉为样品,在色谱分析时分别采用258nm、267nm、300nm作为检测波长,光谱图如图4-1和图4-2。结果发现在258nm处米酵菌酸和毒黄素两种成分均具有较大吸收且色谱分离度均大于1.5,能很好的满足色谱分析要求。
实施例7
本实施例和实施例1的检测方法基本相同,不同在于,以湿米粉为样品,在色谱分析时,流动相B分别选择甲酸、乙酸、磷酸进行pH调节为3.0。色谱图见图5。发现甲酸作为酸度调节剂时,目标化合物的响应信号强,杂峰少,分离效果好。
实施例8
本实施例和实施例1的检测方法基本相同,不同在于,以湿米粉为样品,在色谱分析时,流动相B的pH分别调节为2.5、3.0、3.5,色谱图见图6。发现流动相B的pH为pH2.5和pH3.0时,目标物分离度均较好,而pH越低,对色谱柱和仪器的损害越大,且选择色谱柱的范围越窄。因此用甲酸调节pH至3.0的水溶液作为流动相B更佳。
综上可见,采用本发明的检测方法,一方面,可以解决在不同食品基质中杂质干扰的问题;另一方面,采用本发明特定的样品前处理工艺和色谱分析条件,可以实现毒黄素和米酵菌酸的有效分离,通过对线性方程、检出限、定量限、回收率等方法学指标进行验证,本发明方法灵敏度、精密度、准确度均较好,提供了一种准确、高效、简便的同时检测食品中毒黄素和米酵菌酸含量的方法。
本领域技术人员可以理解,在本说明书的教导之下,可对本发明做出一些修改或调整。这些修改或调整也应当在本发明权利要求所限定的范围之内。
Claims (7)
1.一种同时检测食品中毒黄素和米酵菌酸含量的方法,其特征在于,包括如下步骤:
1)对样品进行前处理
将样品进行两次提取处理,每次均用80%-90%甲醇水溶液涡旋2-5min,超声10-15min,然后离心,吸取上清液至预装有dSPE EMR-Lipid吸附剂的离心管中,涡旋2-5min,离心,取上清液;
合并两次提取所得上清液,对所得上清液进行氮吹处理后,用甲醇定容并用滤膜过滤,获得处理后样品;所述样品包括谷类发酵制品、薯类制品、银耳和/或黑木耳;
2)对步骤1)所得处理后样品进行色谱分析,色谱条件包括:色谱柱为C18色谱柱;流动相包括流动相A和流动相B,其中流动相A为甲醇,流动相B为pH 2.5-3.0的水;检测波长为258nm;梯度洗脱程序为:
0-5min,流动相A 20%,流动相B 80%;
5-6min,流动相A 20%→90%,流动相B 80%→10%;
6-14min,流动相A 90%,流动相B10%;
14-15min,流动相A 90%→20%,流动相B10%→80%;
15-20min,流动相A 20%,流动相B 80%;
以上百分比均指在流动相中的体积百分比;
3)根据预先绘制的标准曲线和步骤2)色谱分析所得检测结果,定量分析样品中毒黄素和米酵菌酸的含量。
2.根据权利要求1所述的同时检测食品中毒黄素和米酵菌酸含量的方法,其特征在于,步骤2)中,作为流动相B的水的pH为3.0。
3.根据权利要求1或2所述的同时检测食品中毒黄素和米酵菌酸含量的方法,其特征在于,步骤2)中,作为流动相B的水采用甲酸调节其pH为3.0。
4.根据权利要求3所述的同时检测食品中毒黄素和米酵菌酸含量的方法,其特征在于,步骤1)中,所述甲醇水溶液的浓度为80%。
5.根据权利要求1或2所述的同时检测食品中毒黄素和米酵菌酸含量的方法,其特征在于,步骤1)中,基于每2g样品,所述甲醇水溶液的用量为10ml。
6.根据权利要求1或2所述的同时检测食品中毒黄素和米酵菌酸含量的方法,其特征在于,步骤2)中,色谱条件还包括:流速为1mL/min;柱温为30℃;进样量为10μL。
7.根据权利要求1所述的同时检测食品中毒黄素和米酵菌酸含量的方法,其特征在于,采用外标法进行所述定量分析。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202011354358.6A CN112505223B (zh) | 2020-11-26 | 2020-11-26 | 一种同时检测食品中毒黄素和米酵菌酸含量的方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202011354358.6A CN112505223B (zh) | 2020-11-26 | 2020-11-26 | 一种同时检测食品中毒黄素和米酵菌酸含量的方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN112505223A CN112505223A (zh) | 2021-03-16 |
| CN112505223B true CN112505223B (zh) | 2022-10-28 |
Family
ID=74966705
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202011354358.6A Active CN112505223B (zh) | 2020-11-26 | 2020-11-26 | 一种同时检测食品中毒黄素和米酵菌酸含量的方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN112505223B (zh) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115508468A (zh) * | 2022-09-19 | 2022-12-23 | 九三食品股份有限公司 | 一种植物油中维生素a含量的检测方法 |
| CN115616116A (zh) * | 2022-11-11 | 2023-01-17 | 惠州市食品药品检验所(惠州市药品不良反应监测中心) | 三重四级杆液质联用法同时检测毒黄素和米酵菌酸的方法 |
| CN116162717A (zh) * | 2022-11-14 | 2023-05-26 | 惠州市食品药品检验所(惠州市药品不良反应监测中心) | 一种用于椰毒假单胞菌酵米面亚种鉴定的检测靶点和应用 |
| CN116593431B (zh) * | 2023-04-09 | 2025-11-07 | 湖南科技大学三亚研究院 | 一种基于亲和传感器法的米酵菌酸毒素便携式检测装置及检测方法 |
| CN117890494B (zh) * | 2023-12-11 | 2025-05-09 | 宁波市疾病预防控制中心(宁波市健康教育与促进中心) | 一种同时测定食品中米酵菌酸、异米酵菌酸和毒黄素的方法 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3942828B2 (ja) * | 2000-07-25 | 2007-07-11 | 独立行政法人科学技術振興機構 | ボンクレキン酸前駆化合物及びその製造方法 |
| AR080234A1 (es) * | 2010-02-25 | 2012-03-21 | Marrone Bio Innovations Inc | Cepa bacteriana aislada del genero burkholderia y metabolitos pesticidas del mismo |
| CN106018659A (zh) * | 2016-05-07 | 2016-10-12 | 浙江省质量检测科学研究院 | 一种食品中毒黄素的快速检测方法 |
-
2020
- 2020-11-26 CN CN202011354358.6A patent/CN112505223B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN112505223A (zh) | 2021-03-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN112505223B (zh) | 一种同时检测食品中毒黄素和米酵菌酸含量的方法 | |
| CN101315351B (zh) | 一种同时检测19种喹诺酮类药物的hplc-esi-ms/ms测定方法 | |
| CN109342632A (zh) | 微波萃取-固相萃取前处理结合液质联用技术同时检测水产养殖底泥中15种抗生素的方法 | |
| CN110887912B (zh) | 一种检测烟用香精或水基胶中邻苯二甲酸酯的方法 | |
| CN116124905B (zh) | 一种小鼠血浆、粪便或组织样本中短链脂肪酸的检测方法 | |
| CN108426965B (zh) | 黄酒中异麦芽糖、异麦芽三糖、麦芽糖、潘糖的检测方法 | |
| CN117890494B (zh) | 一种同时测定食品中米酵菌酸、异米酵菌酸和毒黄素的方法 | |
| CN105911172B (zh) | 一种快速检测高粱中塑化剂的方法 | |
| CN109061009B (zh) | 一种发酵液中衣康酸含量的测定方法 | |
| CN108918694B (zh) | 一种msx残留的hplc柱前衍生化检测方法 | |
| CN111474279B (zh) | 检测大环内酯抗生素化合物的方法和试剂盒 | |
| CN110426471B (zh) | 一种婴幼儿食品中生物素含量的测定方法 | |
| CN113866318A (zh) | 一种(6-氨基吡啶-2-基)(1-甲基哌啶-4-基)甲酮双盐酸盐的检测方法 | |
| CN112684018B (zh) | 一种检测动物源性食品中双酚s和双酚f含量的方法及其应用 | |
| CN107478752B (zh) | 一种小麦中脱氧雪腐镰刀菌烯醇的hplc定性方法 | |
| CN116148385B (zh) | 一种同时检测黑蒜中硒代蛋氨酸和硒甲基硒代半胱氨酸含量的方法 | |
| CN119595800B (zh) | 一种水产品中氯芬新、因灭汀、氟苯脲、二甲戊灵和甲霜灵的快速检测方法 | |
| CN111337611A (zh) | 水产品中孔雀石绿、隐色孔雀石绿、结晶紫、隐色结晶紫的检测方法 | |
| CN114414713B (zh) | 一种基于响应面法优化的茶叶中主要PAEs提取和检测方法 | |
| CN120801576B (zh) | 一种基于lc-ms测定生物样本中肉桂酰甘氨酸的方法 | |
| CN119375408B (zh) | 一种测定酵母培养物中n-乙酰谷氨酸含量的方法 | |
| CN114166985B (zh) | 一种海洋沉积物中多种类生物毒素的检测方法 | |
| Ying et al. | Determination of γ-aminobutyric acid and nucleosides in Chinese liquor by HPLC. | |
| CN116026968A (zh) | 一种检测酒糟中邻苯二甲酸酯类化合物的方法 | |
| CN109187798A (zh) | 检测去甲基卡波地那非、丙氧基艾地那非、n-乙基他达拉非和羟丙基去甲基他达拉非方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |