CN108918694B - 一种msx残留的hplc柱前衍生化检测方法 - Google Patents
一种msx残留的hplc柱前衍生化检测方法 Download PDFInfo
- Publication number
- CN108918694B CN108918694B CN201810410377.2A CN201810410377A CN108918694B CN 108918694 B CN108918694 B CN 108918694B CN 201810410377 A CN201810410377 A CN 201810410377A CN 108918694 B CN108918694 B CN 108918694B
- Authority
- CN
- China
- Prior art keywords
- solution
- msx
- mobile phase
- derivatization
- detected
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000001514 detection method Methods 0.000 title claims abstract description 46
- 238000001212 derivatisation Methods 0.000 title claims abstract description 40
- 238000004128 high performance liquid chromatography Methods 0.000 title claims abstract description 37
- 239000000243 solution Substances 0.000 claims abstract description 35
- 239000012086 standard solution Substances 0.000 claims abstract description 31
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 claims abstract description 27
- QKFJKGMPGYROCL-UHFFFAOYSA-N phenyl isothiocyanate Chemical compound S=C=NC1=CC=CC=C1 QKFJKGMPGYROCL-UHFFFAOYSA-N 0.000 claims abstract description 24
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 claims abstract description 22
- 238000000034 method Methods 0.000 claims abstract description 21
- 229940117953 phenylisothiocyanate Drugs 0.000 claims abstract description 12
- 238000002156 mixing Methods 0.000 claims abstract description 7
- 239000012528 membrane Substances 0.000 claims abstract description 6
- 239000000126 substance Substances 0.000 claims abstract description 6
- 238000001914 filtration Methods 0.000 claims abstract description 4
- 238000002347 injection Methods 0.000 claims abstract description 4
- 239000007924 injection Substances 0.000 claims abstract description 4
- 238000011068 loading method Methods 0.000 claims abstract description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims description 34
- 210000004978 chinese hamster ovary cell Anatomy 0.000 claims description 14
- 239000011550 stock solution Substances 0.000 claims description 12
- 108010025020 Nerve Growth Factor Proteins 0.000 claims description 8
- 102000015336 Nerve Growth Factor Human genes 0.000 claims description 8
- 229940053128 nerve growth factor Drugs 0.000 claims description 8
- 238000002360 preparation method Methods 0.000 claims description 8
- 238000010828 elution Methods 0.000 claims description 5
- 238000000825 ultraviolet detection Methods 0.000 claims description 4
- 230000035484 reaction time Effects 0.000 claims description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 3
- HRSIEGIETAEGEO-UHFFFAOYSA-M sodium;acetonitrile;acetate Chemical compound [Na+].CC#N.CC([O-])=O HRSIEGIETAEGEO-UHFFFAOYSA-M 0.000 claims 1
- 239000012085 test solution Substances 0.000 claims 1
- 239000003814 drug Substances 0.000 abstract description 5
- 238000004458 analytical method Methods 0.000 abstract description 4
- 238000004519 manufacturing process Methods 0.000 abstract description 4
- 238000003908 quality control method Methods 0.000 abstract description 2
- 238000012827 research and development Methods 0.000 abstract description 2
- QEFRNWWLZKMPFJ-YGVKFDHGSA-N L-methionine S-oxide Chemical group CS(=O)CC[C@H](N)C(O)=O QEFRNWWLZKMPFJ-YGVKFDHGSA-N 0.000 description 60
- QEFRNWWLZKMPFJ-UHFFFAOYSA-N L-methionine sulphoxide Natural products CS(=O)CCC(N)C(O)=O QEFRNWWLZKMPFJ-UHFFFAOYSA-N 0.000 description 50
- 239000000523 sample Substances 0.000 description 24
- FFEARJCKVFRZRR-UHFFFAOYSA-N L-Methionine Natural products CSCCC(N)C(O)=O FFEARJCKVFRZRR-UHFFFAOYSA-N 0.000 description 9
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 9
- 229930195722 L-methionine Natural products 0.000 description 9
- 229960004452 methionine Drugs 0.000 description 9
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 8
- 108090000623 proteins and genes Proteins 0.000 description 8
- 235000017281 sodium acetate Nutrition 0.000 description 8
- 239000001632 sodium acetate Substances 0.000 description 8
- 150000001413 amino acids Chemical class 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 102000005396 glutamine synthetase Human genes 0.000 description 5
- 108020002326 glutamine synthetase Proteins 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 239000012535 impurity Substances 0.000 description 4
- 239000011259 mixed solution Substances 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 229940079593 drug Drugs 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 230000010355 oscillation Effects 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- HNSDLXPSAYFUHK-UHFFFAOYSA-N 1,4-bis(2-ethylhexyl) sulfosuccinate Chemical compound CCCCC(CC)COC(=O)CC(S(O)(=O)=O)C(=O)OCC(CC)CCCC HNSDLXPSAYFUHK-UHFFFAOYSA-N 0.000 description 2
- 101150074355 GS gene Proteins 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- 238000009509 drug development Methods 0.000 description 2
- 239000013604 expression vector Substances 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 239000012488 sample solution Substances 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 230000001502 supplementing effect Effects 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- PBCJIPOGFJYBJE-UHFFFAOYSA-N acetonitrile;hydrate Chemical group O.CC#N PBCJIPOGFJYBJE-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000000855 fermentation Methods 0.000 description 1
- 230000004151 fermentation Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 125000001841 imino group Chemical group [H]N=* 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 231100000563 toxic property Toxicity 0.000 description 1
- 238000003260 vortexing Methods 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
Landscapes
- Physics & Mathematics (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Other Investigation Or Analysis Of Materials By Electrical Means (AREA)
Abstract
本发明公开了一种MSX残留的HPLC柱前衍生化检测方法。包括精密吸取标准溶液或待测溶液加入离心管中,加入三乙胺溶液和异硫氰酸苯酯溶液,混匀后室温反应,再加入正己烷混匀,静置,取下相滤膜过滤后得到衍生化标准品或衍生化待测样品;分别将衍生化标准品或衍生化待测样品上样到HPLC柱中检测;按照上述HPLC检测的色谱条件进样分析,以标准溶液的不同浓度梯度浓度x、峰面积y绘制标准曲线;再将待测溶液的MSX的峰面积代入所得的标准曲线,从而计算出待测溶液中MSX的含量。快速方便、准确度高、重复性好,成本低,适用性好,能满足不同MSX残留量水平的检测需要,在药物研发和生产的质量控制中具有极大的应用价值。
Description
技术领域
本发明涉及生化领域的检测方法,尤其涉及一种MSX残留的HPLC柱前衍生化检测方法。
背景技术
中国仓鼠卵巢细胞(Chinese Hamster Ovary,CHO)是使用最广泛的外源蛋白真核表达系统之一。其中CHO-GS细胞系统将外源蛋白的目的基因和谷氨酰胺合成酶(GS)基因标记的表达载体转染于CHO细胞,通过加入谷氨酰胺合成酶的抑制物L-蛋氨酸亚砜亚胺(L-Methionine Sulphoximine,MSX),可使GS基因及与之相连的目的蛋白基因一起扩增,达到提高目的蛋白基因表达水平的目的,从而提高目的蛋白产量。
但是,MSX的化学、物理和毒性性质尚未经完整的研究,其在重组蛋白质产品中的杂质残留可能对用药安全性有着影响。按照中国药典2015版《通则9102药品杂质分析指导原则》的要求,MSX属于工艺相关杂质,药品质量标准应严格规定毒性杂质含量。但MSX在紫外没有吸收峰,也缺乏相应的显色方法,导致目前MSX残留检测方法研究尚不完善,缺少通用性的检测方法。有报道指出采用高效液相色谱与质谱连用(HPLC-MS)可以检测MSX含量,但该方法所需设备昂贵,其成本很难为广大医药企业和研究机构所承受。因此,MSX残留检测很难在常规的药物研发和企业实际生产中进行推广。
发明内容
本发明的目的在于提供一种测定MSX残留的HPLC柱前衍生化检测方法,该方法简单可靠、重复性好,便于在药物研发和实际生产中使用。
为实现上述目的,本发明提供一种MSX残留的HPLC柱前衍生化检测方法,其特征在于,
样品前处理:精密吸取标准溶液或待测溶液加入离心管中,加入三乙胺溶液和异硫氰酸苯酯溶液,混合均匀后室温下反应,再加入正己烷混合均匀,静置,取下相滤膜过滤后得到衍生化标准品或衍生化待测样品;
HPLC检测:分别将衍生化标准品或衍生化待测样品上样到HPLC柱中检测;
获得结果:按照上述HPLC检测的色谱条件进样分析,以标准溶液的不同浓度梯度浓度为x、峰面积为y绘制标准曲线;再将待测溶液的MSX的峰面积,代入所得的标准曲线,从而计算出待测溶液中MSX的含量。
进一步,所述样品前处理步骤中,标准溶液或待测溶液:三乙胺溶液:异硫氰酸苯酯溶液:正己烷的体积用量比(1~3):(0.5~2):(0.5~2):(2~5);优选的,体积用量比为2:1:1:4。
进一步,所述样品前处理步骤中,所述室温下反应时间为0.5-1.5h;优选的,室温下反应时间为1h。
进一步,所述样品前处理步骤中,加入正己烷混合均匀为加入正己烷涡旋振荡;优选的,涡旋振荡的时间为5-15min;更优选的,涡旋振荡的时间为10min。
进一步,所述样品前处理步骤中,静置的时间为20-40min;优选的,静置的时间为30min。
进一步,所述样品前处理步骤中,滤膜采用的是0.45μm滤膜。
进一步,所述HPLC的条件为,流动相采用流动相A和流动相B;其中流动相A为pH6.5,0.1mol/L醋酸钠与乙腈的混合溶液,流动相B为80体积%乙腈水溶液;优选的,流动相A为93体积份的pH6.5,0.1mol/L醋酸钠与7体积份的乙腈的混合溶液;
进一步,所述HPLC的条件为,洗脱开始采用100%体积的流动相A;15分钟开始改为85体积%流动相A+15体积%流动相B;18分钟开始改为76体积%流动相A+24体积%流动相B;25分钟开始改为60体积%流动相A+40体积%流动相B;30分钟开始改为60体积%流动相A+40体积%流动相B;30.01分钟开始改为100体积%流动相B;40.01分钟开始改为100体积%流动相A。
进一步,所述HPLC的条件为,采用DIONEX UltiMate 3000高效液相色谱仪;
优选的,采用的色谱柱为反相C18色谱柱;更优选的,为Sepax AAA,规格为4.6mm×250mm×5μm;
任选的,色谱柱温度为36℃。
进一步,所述HPLC的条件为,流动相流速为1.0mL/min;
任选的,进样量为100μL;
任选的,UV检测波长为254nm。
对于MSX而言,尚无公开的文献资料表明衍生化适用于MSX或是具有合适的衍生化试剂。本发明通过对MSX的化学结构进行研究,认为其化学组成包括氨基酸类似结构与亚砜亚胺结构两个部分,其中氨基酸类似结构具有作为衍生化靶点的潜力。而异硫氰酸苯酯是一种与氨基酸和亚氨基酸均能反应的广谱衍生化试剂,异硫氰酸苯酯和游离氨基酸反应生成的硫氰酸苯酯-氨基酸衍生物可在紫外254nm下被检测到。因此,本发明创造性地使用异硫氰酸苯酯对MSX进行衍生化,使用通用高效液相色谱(HPLC)搭配紫外检测器对MSX进行检测,并配套使用检测小分子化合物常用的反相C18色谱柱,其操作简单、分离度良好,从而使MSX残留得到快速、准确的定量检测,取得了意想不到的技术效果。
本发明具有以下有益效果:
(1)本发明提供的检测方法操作简单、快速方便、准确度高、重复性好,可对待测样品MSX残留量进行定量判定,在药物研发和生产的质量控制中具有极大的应用价值。
(2)待测样品柱前衍生化与检测时间均较短,能快速对大批量样品进行检测,检测速度快、成本低,适用性良好。
(3)检测准确度高,MSX在1.5625μmol/L~50μmol/L范围内有良好的线性关系,能满足不同MSX残留量水平的检测需要。
(4)本发明提供的方法的通用性高,所需仪器、衍生化试剂等均为广大医药企业和研究机构常规配置,其操作简单、成本低廉,适于进行大规模的推广和使用。
附图说明
图1是1.5625μmol/L标准溶液HPLC检测图谱。1为MSX峰。
图2是3.1250μmol/L标准溶液HPLC检测图谱。1为MSX峰。
图3是6.2500μmol/L标准溶液HPLC检测图谱。1为MSX峰。
图4是12.5000μmol/L标准溶液HPLC检测图谱。1为MSX峰。
图5是25.0000μmol/L标准溶液HPLC检测图谱。1为MSX峰。
图6是37.5000μmol/L标准溶液HPLC检测图谱。1为MSX峰。
图7是50.0000μmol/L标准溶液HPLC检测图谱。1为MSX峰。
图8是MSX标准曲线图。x轴为MSX浓度(μmol/L),y轴为峰面积(mAU·min)。
图9是水衍生化后检测图谱。
图10是含12.5μmol/L MSX和12.5μmol/L MET混合样品HPLC检测图谱。1为MSX峰,2为MET峰。
图11是待测样品HPLC检测图谱。
具体实施方式
下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
实施例1:
1、标准溶液制备
50μmol/L MSX标准储备液配制:称取0.9012g MSX溶解于0.1mol/L醋酸钠(pH6.5):乙腈=93:7(V/V)溶液中,定容至1L。
25μmol/L MSX标准溶液配制:上述50μmol/L MSX标准储备液加入等体积的0.1mol/L醋酸钠(pH 6.5):乙腈=93:7(V/V)溶液即可。
不同浓度梯度标准溶液配制:分别吸取1000、750、500、250、125、62.5、31.25μL的50μmol/L MSX标准储备液,分别加入0、250、500、750、875、937.5、968.75μL的0.1mol/L醋酸钠(pH6.5):乙腈=93:7(V/V)溶液定容至1mL,得到浓度分别50、37.5、25、12.5、6.25、3.125、1.5625μmol/L的浓度梯度标准溶液。标准溶液浓度梯度配制方法如表1。
表1不同浓度梯度标准溶液配制表
2、衍生化试剂配制
三乙胺溶液:将14mL三乙胺和86mL乙腈混和均匀所得。
异硫氰酸苯酯溶液:配成12.5μL/mL的异硫氰酸苯酯的乙腈溶液。
3、柱前衍生化方法
精密吸取200μL标准溶液或待测溶液(CHO细胞重组人神经生长因子原液,批号L01,未名生物医药有限公司)加入1.5mL离心管中,加入100μL上述三乙胺溶液和100μL上述异硫氰酸苯酯溶液,混合,置于室温下反应1h,再加入400μL正己烷,涡旋振荡10min。静置30min,取下相用0.45μm滤膜过滤后得到衍生化待测样品。
所述CHO细胞重组人神经生长因子原液的制备方法为:使用含成熟118氨基酸的重组人神经生长因子编码DNA序列(成熟肽,118个氨基酸,GenBank No.V01511)和谷氨酰胺合成酶(GS)基因标记的表达载体转染于中国仓鼠卵巢细胞(CHO细胞),CHO细胞种子细胞于CDFortiCHO培养基(货号:A1148301,美国GIBCO公司)中培养10d后取重组人神经生长因子CHO细胞发酵液,4000rpm离心5min,取上清液进行纯化,纯化方法见中国专利申请文件CN106478801A,采用实施例1的方法纯化获得CHO细胞重组人神经生长因子原液。
4、HPLC-UV检测条件
检测条件为:
高效液相色谱仪:DIONEX UltiMate 3000高效液相色谱仪(包括在线脱气器,四元泵,自动上样器,柱温箱,配置DAD检测器Chromeleon 7工作站)。
色谱柱:Sepax AAA,规格为4.6mm×250mm×5μm,即内径4.6mm,柱长250mm,填料粒径5μm;
色谱柱温度:36℃;
流动相:流动相A为0.1mol/L醋酸钠(pH6.5)-乙腈=93:7(V/V),流动相B为80%(V/V)乙腈水溶液;
洗脱程序:流动相A与流动相B梯度洗脱比例见表2;
表2流动相A与流动相B梯度洗脱体积比例表
| 时间(min) | 流动相A(%) | 流动相B(%) |
| 0 | 100 | 0 |
| 15 | 85 | 15 |
| 18 | 76 | 24 |
| 25 | 60 | 40 |
| 30 | 60 | 40 |
| 30.01 | 0 | 100 |
| 40 | 0 | 100 |
| 40.01 | 100 | 0 |
| 45 | 100 | 0 |
流动相流速:1.0mL/min;
进样量:100μL;
UV检测波长:254nm;
5、标准曲线制备
不同浓度梯度标准溶液按上述衍生化条件进行衍生化后,按照上述色谱条件进样分析,以浓度为x、峰面积为y绘制标准曲线,结果见表4。不同浓度梯度标准溶液HPLC检测叠加图谱见图1-图7,标准曲线见图8。图1-7中,1为MSX峰,峰高从高到低分别为50、37.5、25、12.5、6.25、3.125、1.5625μmol/L的MSX标准溶液。从表3和图1-2可以看出,MSX在1.5625~50μmol/L范围内呈良好线性关系,回归方程为y=0.3339x-0.4705,R2=0.9986。
表3标准曲线检测结果表
| 标准溶液编号 | 浓度(μmol/L) | 峰面积(mAU·min) |
| 7 | 1.5625 | 0.2300 |
| 6 | 3.1250 | 0.5837 |
| 5 | 6.2500 | 1.6480 |
| 4 | 12.5000 | 3.6126 |
| 3 | 25.0000 | 7.4376 |
| 2 | 37.5000 | 12.3519 |
| 1 | 50.0000 | 16.2277 |
6、专属性实验
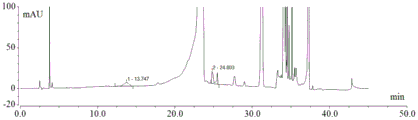
取上述制备得到的25μmol/L MSX标准溶液100μL,加入25μmol/L的L-蛋氨酸(MET)水溶液100μL,制备含12.5μmol/L MSX和12.5μmol/L L-蛋氨酸(MET)的混合溶液。分别取水、上述所得混合溶液各200μL,各按上述衍生化条件进行衍生化后,按上述检测条件测定。检测图谱见图9、图10。图10中1为MSX峰,2为MET峰。
从图9和图10可以看出,水衍生化样品在MSX位置无吸收峰;MSX的保留时间为13.747min,MET的保留时间为24.803min,两者之间的分离度为13.24,MET不影响MSX残留量的检测,说明本方法专属性达到要求。
7、准确度实验
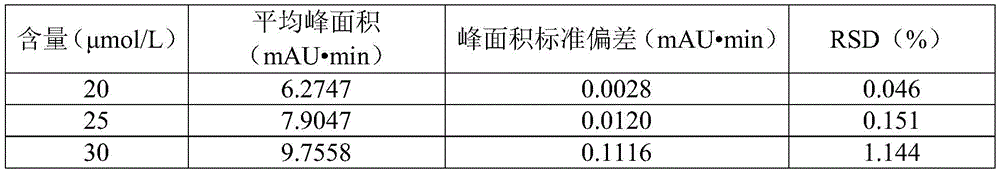
分别在50μL待测样品溶液中加入80、100、120μL的50μmol/L MSX标准储备液,再补加0.1mol/L醋酸钠(pH6.5):乙腈=93:7(V/V)溶液至200μL,制备得含20、25、30μmol/L MSX标准品的待测样品溶液,按上述衍生化条件进行衍生化后,按上述检测条件测定各3份待测样品的结果,计算回收率及相对标准偏差RSD,结果见表5。从表5可以看出,三个浓度水平的RSD均小于2%,说明本方法准确度高。
表4准确度实验结果表
8、中间精密度实验
取25μmol/L MSX标准溶液,经衍生化后,分别放置0、24h后按上述检测条件分别测定结果,记录峰面积,计算相对标准偏差RSD,结果见表5。从表5可以看出,不同时间检测的RSD为0.720%,小于2%,说明本方法中间精密度高。
表5中间精密度实验结果表
9、重复性实验
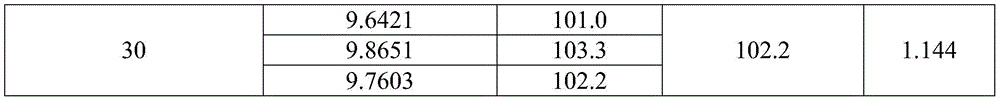
分别取80、100、120μL的50μmol/L MSX标准品储备液,再补加0.1mol/L醋酸钠(pH6.5):乙腈=93:7(V/V)溶液至200μL,制备20、25、30μmol/L MSX标准溶液,经衍生化后,按上述检测条件各测定3份样品的结果,计算平均峰面积、标准偏差及相对标准偏差,结果见表6。三个浓度水平的RSD均小于2%,说明本方法重复性好。
表6重复性实验结果表
10、待测样品中MSX残留的检测
取经步骤3衍生化后的待测样品液,按上述相同检测条件进行检测,计算待测样品中MSX的峰面积,代入所得的标准曲线,计算出待测样品中MSX的含量。结果见图11。从图11可以看出,待测样品HPLC检测图谱未在MSX位置出峰,表明CHO细胞重组人神经生长因子原液中MSX残留低于检测限,其安全性得到保证。
本发明的保护范围并不局限于对CHO细胞重组人神经生长因子原液中MSX残留的检测,针对其他类型的样品(如CHO细胞重组蛋白、抗体的原液和制剂等),本领域技术人员有能力选择与之相应的预处理方式得到待测样品,本实施例中的色谱条件及标准曲线对其也同样适用。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,优选的实施方式,不能理解为对本发明的限制,本领域的普通技术人员在不脱离本发明的原理和宗旨的情况下在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
Claims (5)
1.一种MSX残留的HPLC柱前衍生化检测方法,其特征在于,
样品前处理:精密吸取标准溶液或待测溶液加入离心管中,加入三乙胺溶液和异硫氰酸苯酯溶液,混合均匀后室温下反应0.5-1.5h,再加入正己烷混合均匀,静置20-40min,取下相0.45μm滤膜过滤后得到衍生化标准品或衍生化待测样品;其中待测溶液为CHO细胞重组人神经生长因子原液,抗体的原液和制剂;标准溶液或待测溶液:三乙胺溶液:异硫氰酸苯酯溶液:正己烷的体积用量比(1~3):(0.5~2):(0.5~2):(2~5);
HPLC检测:分别将衍生化标准品或衍生化待测样品上样到HPLC柱中检测;所述HPLC的条件为,采用Sepax AAA反相C18色谱柱,规格为4.6mm×250mm×5μm,色谱柱温度为36℃,流动相采用流动相A和流动相B;其中流动相A为0.1mol/L醋酸钠-乙腈=93:7(V/V),其pH=6.5,流动相B为80体积%乙腈水溶液;洗脱开始采用100%体积的流动相A;15分钟开始改为85体积%流动相A+15体积 %流动相B;18分钟开始改为76体积%流动相A+24体积 %流动相B;25分钟开始改为60体积%流动相A+40体积 %流动相B;30分钟开始改为60体积%流动相A+40体积 %流动相B;30.01分钟开始改为100体积 %流动相B;40.01分钟开始改为100体积%流动相A;流动相流速为1.0mL/min;进样量为100µL;UV检测波长为254 nm;
获得结果:按照上述HPLC检测的色谱条件进样分析,以标准溶液的不同浓度梯度浓度为x、峰面积为y绘制标准曲线;再将待测溶液的MSX的峰面积,代入所得的标准曲线,从而计算出待测溶液中MSX的含量。
2.如权利要求1所述MSX残留的HPLC柱前衍生化检测方法,其特征在于,所述样品前处理步骤中,标准溶液或待测溶液:三乙胺溶液:异硫氰酸苯酯溶液:正己烷的体积用量比为2:1:1:4。
3.如权利要求1所述MSX残留的HPLC柱前衍生化检测方法,其特征在于,所述样品前处理步骤中,所述室温下反应时间为1h。
4.如权利要求1所述MSX残留的HPLC柱前衍生化检测方法,其特征在于,所述样品前处理步骤中,加入正己烷混合均匀为加入正己烷涡旋振荡10min。
5.如权利要求1所述MSX残留的HPLC柱前衍生化检测方法,其特征在于,所述样品前处理步骤中,静置的时间为30min。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201810410377.2A CN108918694B (zh) | 2018-05-02 | 2018-05-02 | 一种msx残留的hplc柱前衍生化检测方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201810410377.2A CN108918694B (zh) | 2018-05-02 | 2018-05-02 | 一种msx残留的hplc柱前衍生化检测方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN108918694A CN108918694A (zh) | 2018-11-30 |
| CN108918694B true CN108918694B (zh) | 2021-05-25 |
Family
ID=64403263
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201810410377.2A Active CN108918694B (zh) | 2018-05-02 | 2018-05-02 | 一种msx残留的hplc柱前衍生化检测方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN108918694B (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN114166964A (zh) * | 2021-11-23 | 2022-03-11 | 上海臻格生物技术有限公司 | 一种蛋氨酸亚砜酰亚胺快速检测方法 |
| CN115718100B (zh) * | 2022-12-06 | 2025-07-25 | 绪必迪药业(沧州)有限公司 | 一种氨基乙腈残留的限度检测方法 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100936608B1 (ko) * | 2008-01-24 | 2010-01-13 | (주)아모레퍼시픽 | 액체크로마토그래피를 이용한 두 종 이상의 아미노산동시분석 방법 |
| CN103698453B (zh) * | 2013-12-16 | 2015-09-09 | 广州王老吉药业股份有限公司 | 小儿七星茶制剂氨基酸指纹图谱的检测方法及构建方法 |
| CN103837620A (zh) * | 2014-03-21 | 2014-06-04 | 上海硕源健标生物医学科技有限公司 | 一种同时检测人体血浆中多种氨基酸含量的方法 |
| CN105021729B (zh) * | 2015-07-16 | 2017-04-26 | 金花企业(集团)股份有限公司西安金花制药厂 | 一种健骨药物的质量检测方法 |
| CN106226428B (zh) * | 2016-07-20 | 2019-01-01 | 未名生物医药有限公司 | 一种快速检测cho细胞发酵液中重组人神经生长因子含量的方法 |
| CN106885856B (zh) * | 2017-03-14 | 2019-09-20 | 上海和黄药业有限公司 | 一种胃可宁片中氨基酸类成分指纹图谱的检测方法及其应用 |
-
2018
- 2018-05-02 CN CN201810410377.2A patent/CN108918694B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN108918694A (zh) | 2018-11-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109387587B (zh) | 一种l-2-氨基-5-胍基戊酸对映异构体的检测方法 | |
| CN111537648A (zh) | 一种超高效液相色谱串联质谱技术检测血清中抗结核病药物的试剂盒 | |
| CN111830153A (zh) | 一种检测血清中多粘菌素b1和多粘菌素b2浓度的方法 | |
| CN108918694B (zh) | 一种msx残留的hplc柱前衍生化检测方法 | |
| CN120084911A (zh) | 一种丙氨酰谷氨酰胺有关物质的测定方法 | |
| CN108072712B (zh) | 一种sd大鼠血浆中新化合物wsj-557的血药浓度定量分析方法 | |
| CN110208419B (zh) | 一种用于检测比伐卢定中杂质的方法 | |
| CN111665307A (zh) | 一种检测血清中多粘菌素b1和多粘菌素b2浓度的试剂盒 | |
| CN116858978B (zh) | 一种同时检测门冬胰岛素和德谷胰岛素的方法及其血浆样品处理方法 | |
| CN112362780A (zh) | 盐酸普萘洛尔的高效液相检测方法 | |
| CN111505182A (zh) | 衍生化气相色谱-质谱联用测定药物中硫酸二甲酯的方法 | |
| CN112903836A (zh) | 体外培育熊胆粉中异丙基-β-D-硫代吡喃半乳糖苷的测定方法 | |
| CN114264765A (zh) | 一种利用hplc测定格列美脲中间体中有关物质的分析方法 | |
| CN114689737B (zh) | 一种s-邻氯苯甘氨酸甲酯酒石酸盐有关物质的分析方法 | |
| CN111426760B (zh) | 一种多索茶碱原料药中基因毒性杂质的测定方法 | |
| CN114166964A (zh) | 一种蛋氨酸亚砜酰亚胺快速检测方法 | |
| CN111060612B (zh) | 一种液质联用测定血浆中泼尼松、醋酸泼尼松及其活性代谢产物泼尼松龙浓度的方法 | |
| CN111337611A (zh) | 水产品中孔雀石绿、隐色孔雀石绿、结晶紫、隐色结晶紫的检测方法 | |
| CN110231416B (zh) | 一种利用hplc测定2-碘酰基苯甲酸有关物质的方法 | |
| Xie et al. | Quantitative analysis of carbohydrate residues in dextran 40 from various sources: a comparative study using high-performance liquid chromatography coupled with a charged aerosol detector | |
| CN112326827A (zh) | 一种检测氯化胆碱含量的分析方法 | |
| CN114544839B (zh) | 一种抗人神经生长因子抗体的电荷变异体检测方法 | |
| CN113219097A (zh) | 基于超高效合相色谱的婴幼儿配方奶粉中肉碱对映体拆分和测定方法 | |
| CN116930368B (zh) | 一种司替戊醇异构体的检测方法 | |
| CN115128184B (zh) | 一种利用hplc外标法测定盐酸普拉克索原料中硫脲含量的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |