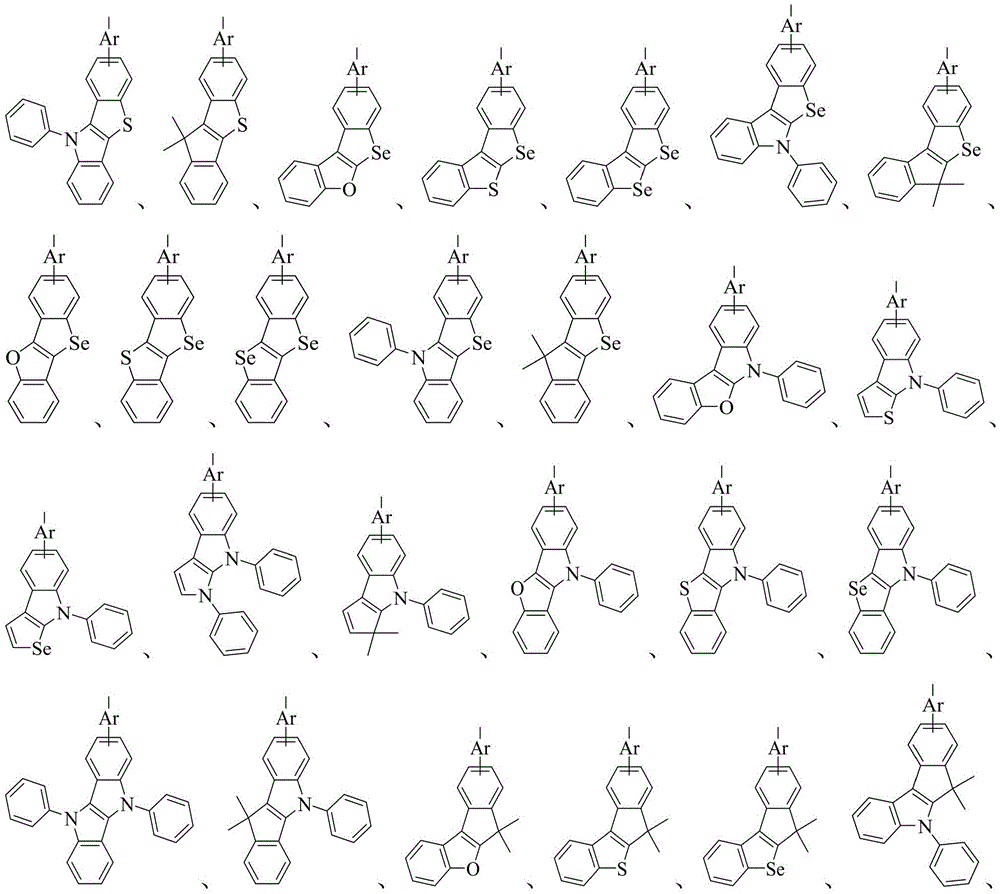CN110964007B - 一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用 - Google Patents
一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用 Download PDFInfo
- Publication number
- CN110964007B CN110964007B CN201811158821.2A CN201811158821A CN110964007B CN 110964007 B CN110964007 B CN 110964007B CN 201811158821 A CN201811158821 A CN 201811158821A CN 110964007 B CN110964007 B CN 110964007B
- Authority
- CN
- China
- Prior art keywords
- compound
- general formula
- organic electroluminescent
- substituted
- theoretical value
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 64
- LISFMEBWQUVKPJ-UHFFFAOYSA-N quinolin-2-ol Chemical class C1=CC=C2NC(=O)C=CC2=C1 LISFMEBWQUVKPJ-UHFFFAOYSA-N 0.000 title claims abstract description 15
- 239000010410 layer Substances 0.000 claims description 65
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 9
- 125000004076 pyridyl group Chemical group 0.000 claims description 6
- 125000002541 furyl group Chemical group 0.000 claims description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 5
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 4
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 4
- 229910052717 sulfur Inorganic materials 0.000 claims description 4
- 125000004434 sulfur atom Chemical group 0.000 claims description 4
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical group [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 claims description 3
- 229910052711 selenium Inorganic materials 0.000 claims description 3
- 125000001424 substituent group Chemical group 0.000 claims description 3
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 3
- 239000002346 layers by function Substances 0.000 claims description 2
- 229930185107 quinolinone Natural products 0.000 claims 2
- 125000000732 arylene group Chemical group 0.000 claims 1
- 239000000463 material Substances 0.000 abstract description 73
- 229910052757 nitrogen Inorganic materials 0.000 abstract description 19
- 125000005842 heteroatom Chemical group 0.000 abstract description 8
- 230000002035 prolonged effect Effects 0.000 abstract description 4
- 230000009286 beneficial effect Effects 0.000 abstract description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 abstract description 3
- 230000006798 recombination Effects 0.000 abstract description 3
- 238000005215 recombination Methods 0.000 abstract description 3
- 125000004429 atom Chemical group 0.000 abstract description 2
- 125000000623 heterocyclic group Chemical group 0.000 abstract description 2
- 239000000543 intermediate Substances 0.000 description 93
- 239000007858 starting material Substances 0.000 description 48
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 33
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 33
- 238000012360 testing method Methods 0.000 description 33
- 238000000921 elemental analysis Methods 0.000 description 32
- 230000015572 biosynthetic process Effects 0.000 description 22
- 238000003786 synthesis reaction Methods 0.000 description 22
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 19
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 18
- 238000002347 injection Methods 0.000 description 18
- 239000007924 injection Substances 0.000 description 18
- 238000006243 chemical reaction Methods 0.000 description 16
- 239000002994 raw material Substances 0.000 description 15
- 230000000903 blocking effect Effects 0.000 description 13
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 13
- 238000001816 cooling Methods 0.000 description 12
- 238000010438 heat treatment Methods 0.000 description 12
- 238000004128 high performance liquid chromatography Methods 0.000 description 12
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 10
- 238000001704 evaporation Methods 0.000 description 10
- 239000000741 silica gel Substances 0.000 description 10
- 229910002027 silica gel Inorganic materials 0.000 description 10
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 9
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 8
- 230000000052 comparative effect Effects 0.000 description 8
- 230000006872 improvement Effects 0.000 description 8
- 238000002360 preparation method Methods 0.000 description 8
- 238000010992 reflux Methods 0.000 description 8
- 238000002390 rotary evaporation Methods 0.000 description 8
- 238000005070 sampling Methods 0.000 description 8
- 239000000706 filtrate Substances 0.000 description 7
- 238000001914 filtration Methods 0.000 description 7
- 238000004770 highest occupied molecular orbital Methods 0.000 description 7
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- 230000005540 biological transmission Effects 0.000 description 6
- 230000005525 hole transport Effects 0.000 description 6
- 239000012046 mixed solvent Substances 0.000 description 6
- 239000007864 aqueous solution Substances 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- 238000001035 drying Methods 0.000 description 5
- 230000007935 neutral effect Effects 0.000 description 5
- 239000012074 organic phase Substances 0.000 description 5
- CDBYLPFSWZWCQE-UHFFFAOYSA-L sodium carbonate Substances [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 238000007738 vacuum evaporation Methods 0.000 description 5
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 4
- 125000003118 aryl group Chemical group 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical class C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 239000007772 electrode material Substances 0.000 description 4
- 230000009477 glass transition Effects 0.000 description 4
- 125000001072 heteroaryl group Chemical group 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 4
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- 230000002194 synthesizing effect Effects 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 4
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 4
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- 229940125782 compound 2 Drugs 0.000 description 3
- DKHNGUNXLDCATP-UHFFFAOYSA-N dipyrazino[2,3-f:2',3'-h]quinoxaline-2,3,6,7,10,11-hexacarbonitrile Chemical compound C12=NC(C#N)=C(C#N)N=C2C2=NC(C#N)=C(C#N)N=C2C2=C1N=C(C#N)C(C#N)=N2 DKHNGUNXLDCATP-UHFFFAOYSA-N 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 3
- 238000000034 method Methods 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 125000001624 naphthyl group Chemical group 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 238000007363 ring formation reaction Methods 0.000 description 3
- 239000011669 selenium Substances 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- 229910000029 sodium carbonate Inorganic materials 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 229910001868 water Inorganic materials 0.000 description 3
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 2
- YQOLEILXOBUDMU-KRWDZBQOSA-N (4R)-5-[(6-bromo-3-methyl-2-pyrrolidin-1-ylquinoline-4-carbonyl)amino]-4-(2-chlorophenyl)pentanoic acid Chemical compound CC1=C(C2=C(C=CC(=C2)Br)N=C1N3CCCC3)C(=O)NC[C@H](CCC(=O)O)C4=CC=CC=C4Cl YQOLEILXOBUDMU-KRWDZBQOSA-N 0.000 description 2
- QTMAZYGAVHCKKX-UHFFFAOYSA-N 2-[(4-amino-5-bromopyrrolo[2,3-d]pyrimidin-7-yl)methoxy]propane-1,3-diol Chemical compound NC1=NC=NC2=C1C(Br)=CN2COC(CO)CO QTMAZYGAVHCKKX-UHFFFAOYSA-N 0.000 description 2
- PYRKKGOKRMZEIT-UHFFFAOYSA-N 2-[6-(2-cyclopropylethoxy)-9-(2-hydroxy-2-methylpropyl)-1h-phenanthro[9,10-d]imidazol-2-yl]-5-fluorobenzene-1,3-dicarbonitrile Chemical compound C1=C2C3=CC(CC(C)(O)C)=CC=C3C=3NC(C=4C(=CC(F)=CC=4C#N)C#N)=NC=3C2=CC=C1OCCC1CC1 PYRKKGOKRMZEIT-UHFFFAOYSA-N 0.000 description 2
- RSIWALKZYXPAGW-NSHDSACASA-N 6-(3-fluorophenyl)-3-methyl-7-[(1s)-1-(7h-purin-6-ylamino)ethyl]-[1,3]thiazolo[3,2-a]pyrimidin-5-one Chemical compound C=1([C@@H](NC=2C=3N=CNC=3N=CN=2)C)N=C2SC=C(C)N2C(=O)C=1C1=CC=CC(F)=C1 RSIWALKZYXPAGW-NSHDSACASA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 229940126639 Compound 33 Drugs 0.000 description 2
- PNUZDKCDAWUEGK-CYZMBNFOSA-N Sitafloxacin Chemical compound C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 PNUZDKCDAWUEGK-CYZMBNFOSA-N 0.000 description 2
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 2
- YCOXTKKNXUZSKD-UHFFFAOYSA-N as-o-xylenol Natural products CC1=CC=C(O)C=C1C YCOXTKKNXUZSKD-UHFFFAOYSA-N 0.000 description 2
- 235000010290 biphenyl Nutrition 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- SISAYUDTHCIGLM-UHFFFAOYSA-N bromine dioxide Inorganic materials O=Br=O SISAYUDTHCIGLM-UHFFFAOYSA-N 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 229940125797 compound 12 Drugs 0.000 description 2
- 229940125844 compound 46 Drugs 0.000 description 2
- 125000004093 cyano group Chemical group *C#N 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- SNHMUERNLJLMHN-UHFFFAOYSA-N iodobenzene Chemical compound IC1=CC=CC=C1 SNHMUERNLJLMHN-UHFFFAOYSA-N 0.000 description 2
- 239000008204 material by function Substances 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- YGBMCLDVRUGXOV-UHFFFAOYSA-N n-[6-[6-chloro-5-[(4-fluorophenyl)sulfonylamino]pyridin-3-yl]-1,3-benzothiazol-2-yl]acetamide Chemical compound C1=C2SC(NC(=O)C)=NC2=CC=C1C(C=1)=CN=C(Cl)C=1NS(=O)(=O)C1=CC=C(F)C=C1 YGBMCLDVRUGXOV-UHFFFAOYSA-N 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- 229910000027 potassium carbonate Inorganic materials 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 230000000171 quenching effect Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 238000005303 weighing Methods 0.000 description 2
- JSRLURSZEMLAFO-UHFFFAOYSA-N 1,3-dibromobenzene Chemical compound BrC1=CC=CC(Br)=C1 JSRLURSZEMLAFO-UHFFFAOYSA-N 0.000 description 1
- LFZAGIJXANFPFN-UHFFFAOYSA-N N-[3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-thiophen-2-ylpropyl]acetamide Chemical compound C(C)(C)C1=NN=C(N1C1CCN(CC1)CCC(C=1SC=CC=1)NC(C)=O)C LFZAGIJXANFPFN-UHFFFAOYSA-N 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 125000006267 biphenyl group Chemical group 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 238000000113 differential scanning calorimetry Methods 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 125000005549 heteroarylene group Chemical group 0.000 description 1
- QWXYZCJEXYQNEI-OSZHWHEXSA-N intermediate I Chemical compound COC(=O)[C@@]1(C=O)[C@H]2CC=[N+](C\C2=C\C)CCc2c1[nH]c1ccccc21 QWXYZCJEXYQNEI-OSZHWHEXSA-N 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- UQPUONNXJVWHRM-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 UQPUONNXJVWHRM-UHFFFAOYSA-N 0.000 description 1
- 238000011056 performance test Methods 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/10—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D421/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having selenium, tellurium, or halogen atoms as ring hetero atoms
- C07D421/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having selenium, tellurium, or halogen atoms as ring hetero atoms containing two hetero rings
- C07D421/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having selenium, tellurium, or halogen atoms as ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D517/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having selenium, tellurium, or halogen atoms as ring hetero atoms
- C07D517/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having selenium, tellurium, or halogen atoms as ring hetero atoms in which the condensed system contains two hetero rings
- C07D517/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1096—Heterocyclic compounds characterised by ligands containing other heteroatoms
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
本发明公开了一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用,本发明化合物结构内包含喹啉酮衍生物作为电子受体,有利于电子在发光层中的传输。连接的杂环基团是电子给体,它有利于空穴在发光层中的传输。含杂原子苯并氮杂萘酮内部的氮原子是饱和原子,它不仅具有很强的刚性,还有利于提高母核化合物三重态能级,电子给体和电子受体的组合可以提高激子的复合效率,降低启动电压,提高器件性能。本发明化合物作为有机电致发光器件的发光层材料使用时,器件的电流效率,得到很大改善,同时对于器件寿命提升非常明显。
Description
技术领域
本发明涉及半导体技术领域,尤其涉及一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用。
背景技术
当前,OLED显示技术已经在智能手机,平板电脑等领域获得应用,进一步还将向电视等大尺寸应用领域扩展,但是,和实际的产品应用要求相比,OLED器件的发光效率和使用寿命等性能还需要进一步提升。
目前对OLED发光器件提高性能的研究包括:降低器件的驱动电压、提高器件的发光效率、提高器件的使用寿命等。为了实现OLED器件的性能的不断提升,不但需要从OLED器件结构和制作工艺的创新,更需要OLED光电功能材料不断研究和创新,创制出更高性能的OLED功能材料。
应用于OLED器件的OLED光电功能材料从用途上可划分为两大类,分别为电荷注入传输材料和发光材料。进一步,还可将电荷注入传输材料分为电子注入传输材料、电子阻挡材料、空穴注入传输材料和空穴阻挡材料,还可以将发光材料分为主体发光材料和掺杂材料。
为了制作高性能的OLED发光器件,要求各种有机功能材料具备良好的光电性能,譬如,作为电荷传输材料,要求具有良好的载流子迁移率,高玻璃化转化温度等,作为发光层的主体材料具有良好双极性,适当的HOMO/LUMO能阶等。
构成OLED器件的OLED光电功能材料膜层至少包括两层以上结构,产业上应用的OLED器件结构则包括空穴注入层、空穴传输层、电子阻挡层、发光层、空穴阻挡层、电子传输层、电子注入层等多种膜层,也就是说应用于OLED器件的光电功能材料至少包括空穴注入材料、空穴传输材料、发光材料、电子传输材料等,材料类型和搭配形式具有丰富性和多样性的特点。另外,对于不同结构的OLED器件搭配而言,所使用的光电功能材料具有较强的选择性,相同的材料在不同结构器件中的性能表现也可能完全迥异。
因此,针对当前OLED器件的产业应用要求以及OLED器件的不同功能膜层,器件的光电特性需求,必须选择更适合、性能更高的OLED功能材料或材料组合,才能实现器件的高效率、长寿命和低电压的综合特性。
发明内容
针对现有技术存在的上述问题,本申请人提供了一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用。本发明化合物以含杂原子苯并氮杂萘酮为核心,可以增加轨道重叠,具有较高的三重态能级,能使化合物三重态激子局限在发光层中,从而提高发光效率。
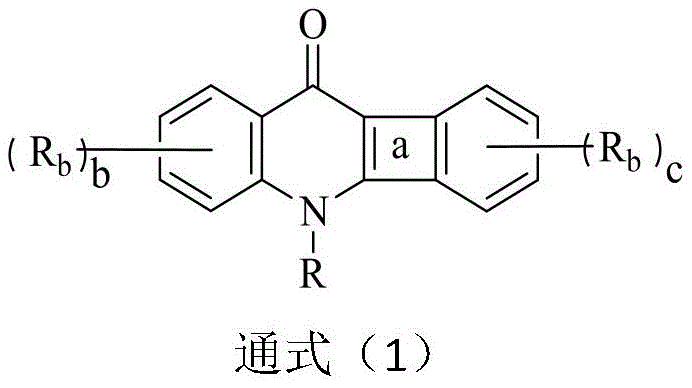
本发明解决上述技术问题的技术方案如下:一种以喹啉酮衍生物为核心的化合物,所述化合物结构如通式(1)所示:
R1~R5分别独立的表示为C1-10烷基、取代或未取代的C6-30芳基、含有一个或多个杂原子的取代或未取代的5-30元杂芳基中的一种;
其中,R表示为含有一个或多个杂原子的取代或未取代的5-30元杂芳基、取代或未取代的的C6-30芳基;
b和c分别独立地表示为0或1,且b+c=1;
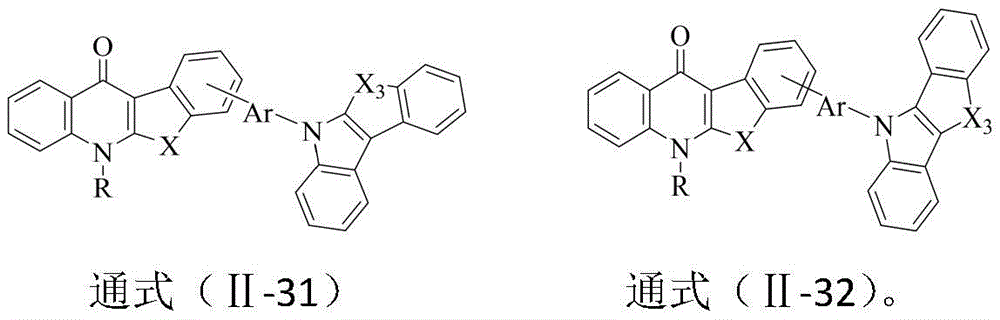
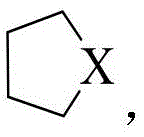
Rb表示为通式(2)或者通式(3)表示的结构:
所述通式(2)和通式(3)通过单键和通式(1)中苯环连接;
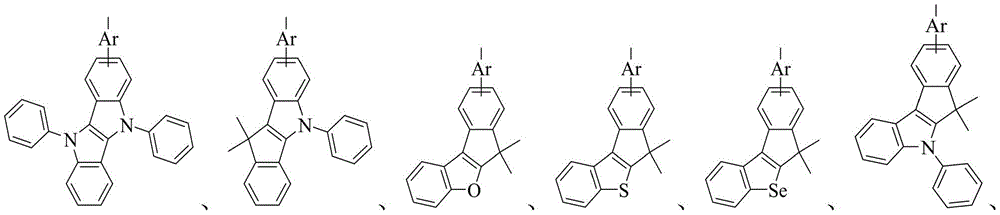
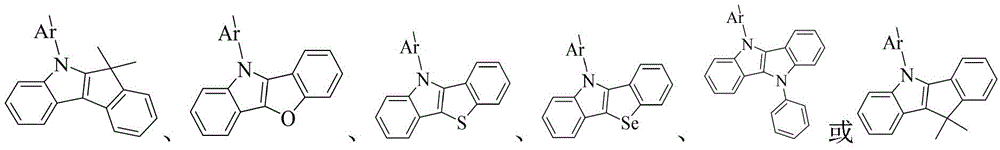
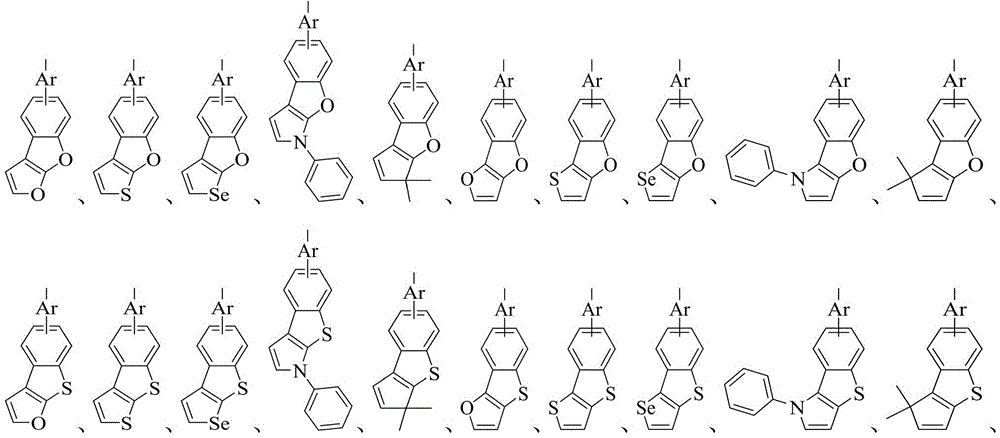
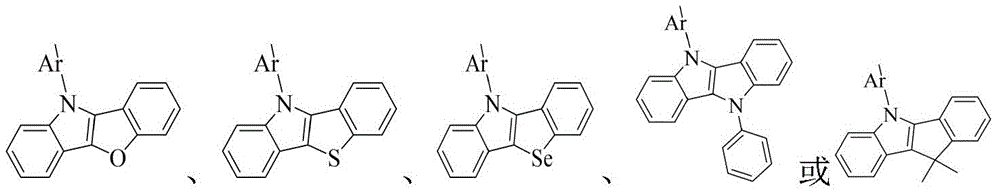
其中,R6、R7分别独立的表示为通式(4)或通式(5)所示结构;Ar表示为取代或者未被取代的C6-30亚芳基、含有一个或多个杂原子取代或者未被取代的5-30元亚杂芳基;
X1、X2、X3分别相同或不同地表示为氧原子、硫原子、硒原子、-C(R8)(R9)-或-N(R10)-;R8~R10分别独立的表示为C1-10烷基、取代或未取代的C6-30芳基、含有一个或多个杂原子的取代或未取代的5-30元杂芳基中的一种;
通式(4)或通式(5)通过*标记的两个相邻位置与通式(2)或通式(3)中*标记的两个相邻的位置稠合连接;
所述可被取代基团的取代基任选自卤素、氰基、C1-10烷基、C6-30芳基、5-30元杂芳基中的一种或几种;
所述杂原子任选自氧原子、硫原子或氮原子中的一种或几种。
作为本发明的进一步改进,所述R1~R5分别独立的表示为甲基、乙基、丙基、异丙基、叔丁基、戊基、取代或未取代的苯基、取代或未取代的萘基、取代或未取代的联苯基、取代或未取代的吡啶基、取代或未取代的呋喃基;
所述R表示为取代或未取代的苯基、取代或未取代的萘基、取代或未取代的联苯基、取代或未取代的吡啶基、取代或未取代的呋喃基;
所述R8~R10分别独立的表示甲基、乙基、丙基、异丙基、叔丁基、戊基、取代或未取代的苯基、取代或未取代的吡啶基、取代或未取代的呋喃基;
所述可取代基团的取代基任选自氟原子、氰基、甲基、乙基、丙基、异丙基、叔丁基、戊基、苯基、萘基、联苯基、萘啶基或吡啶基中的一种或多种。
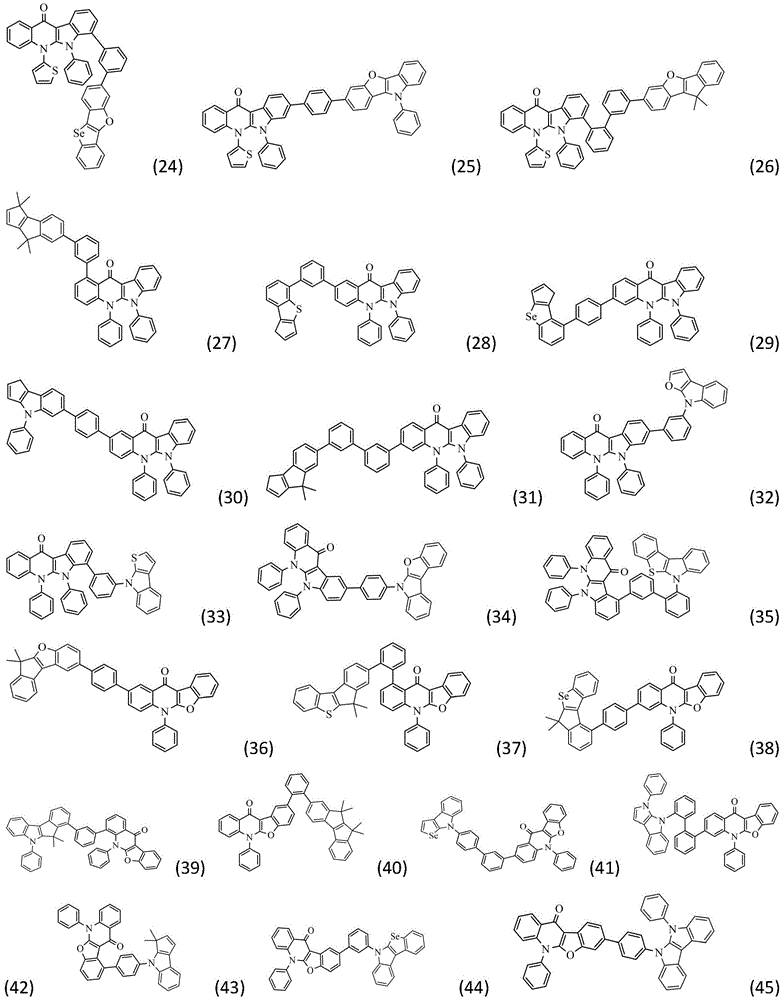
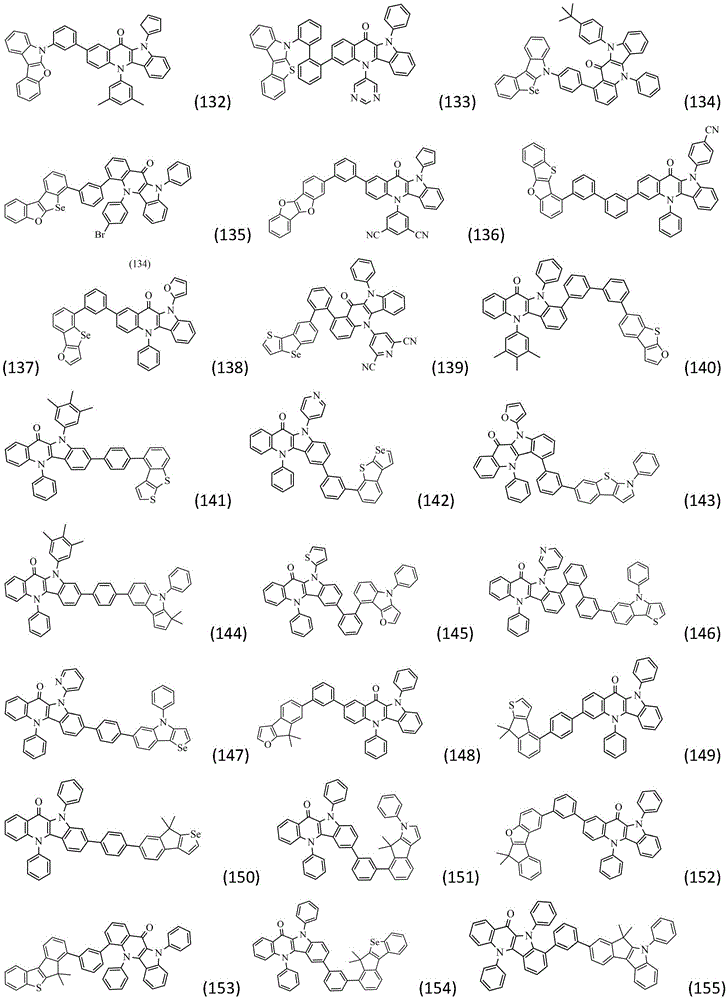
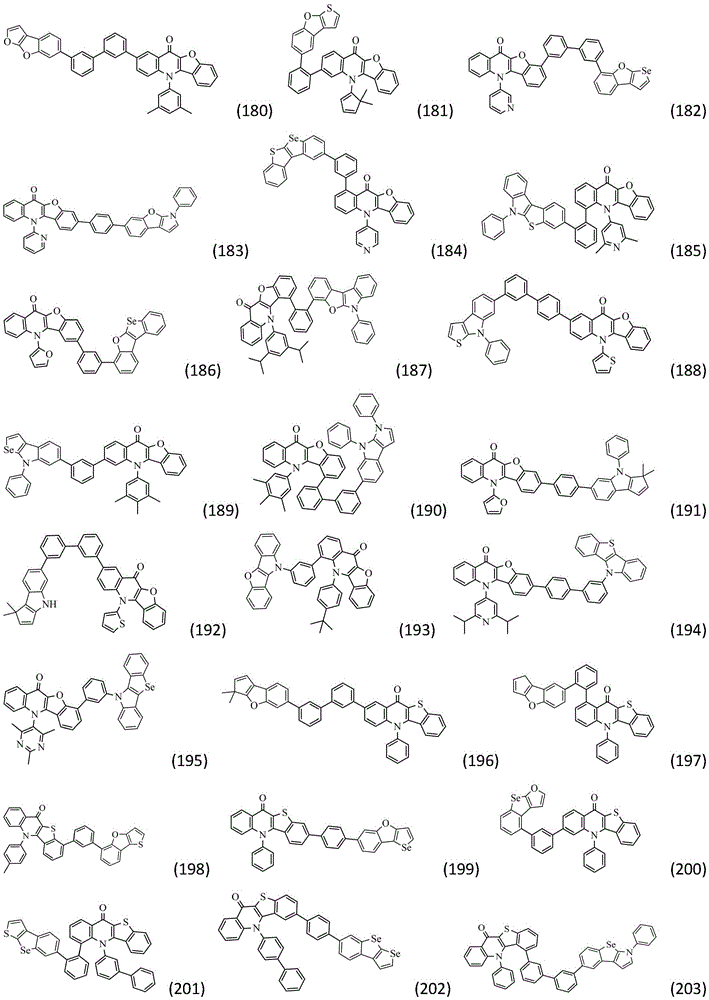
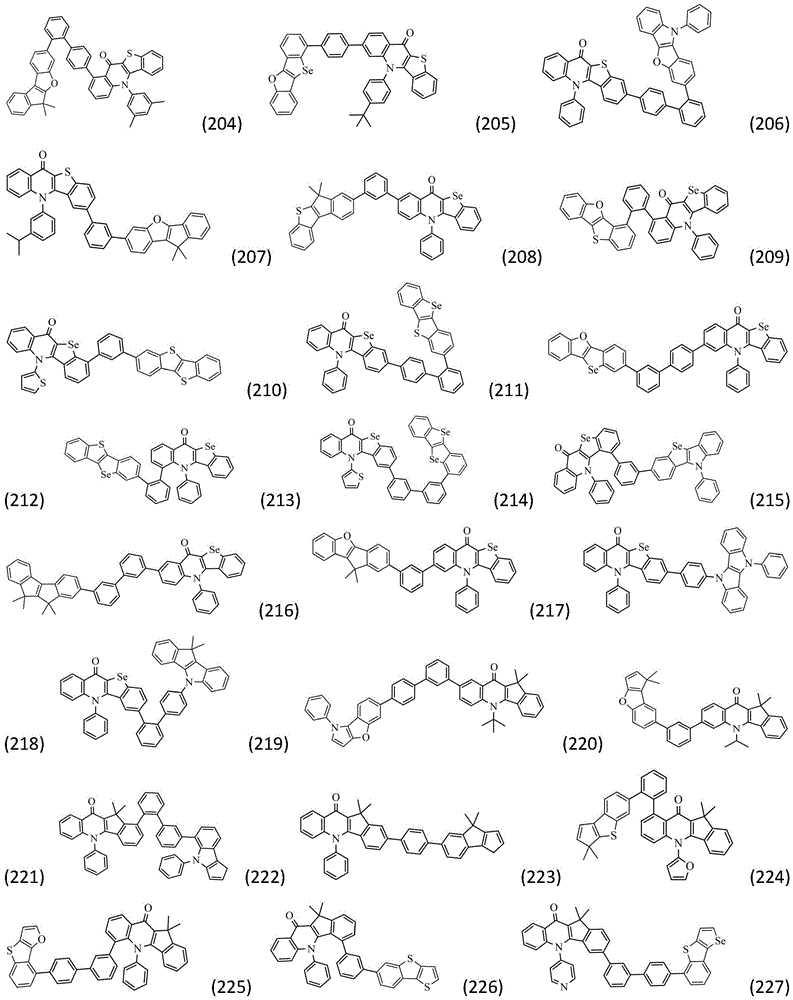
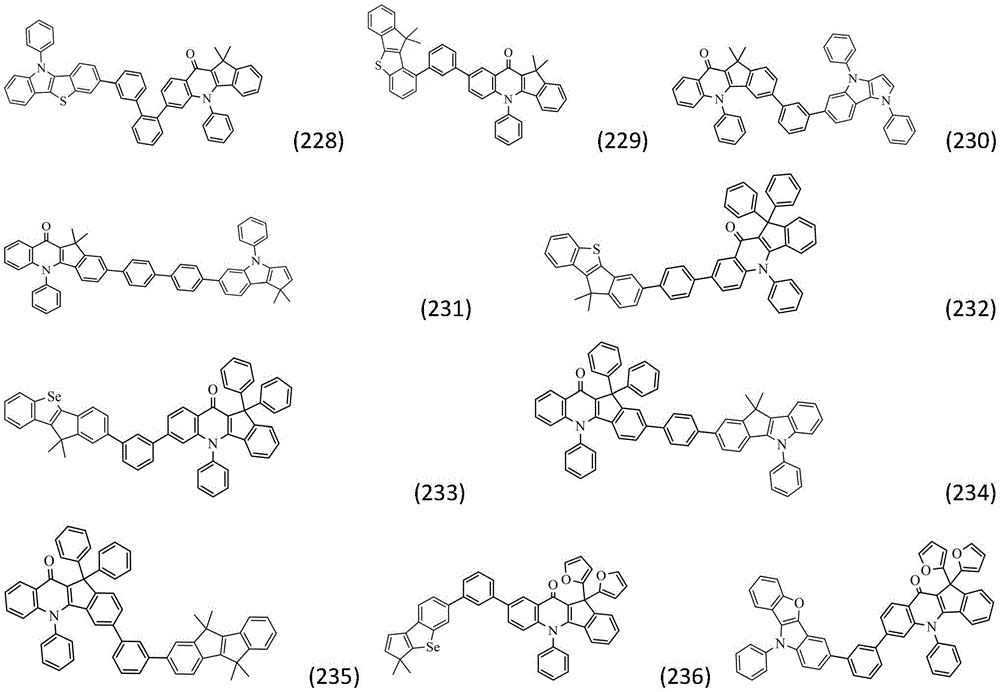
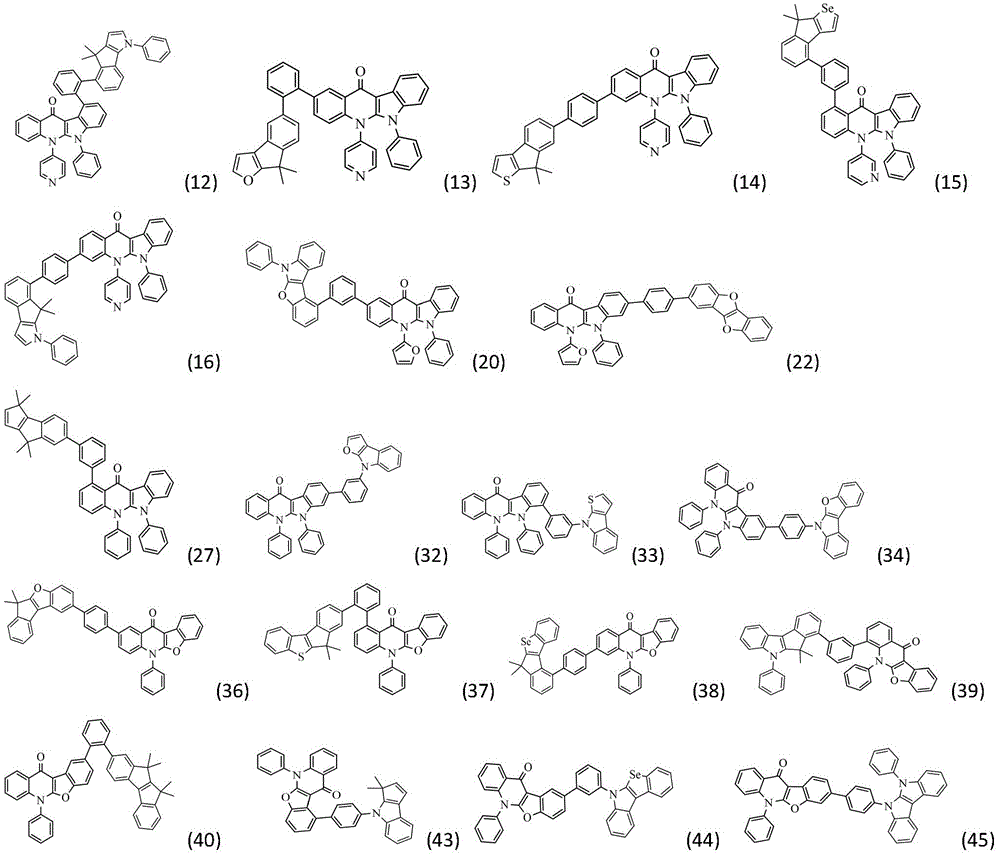
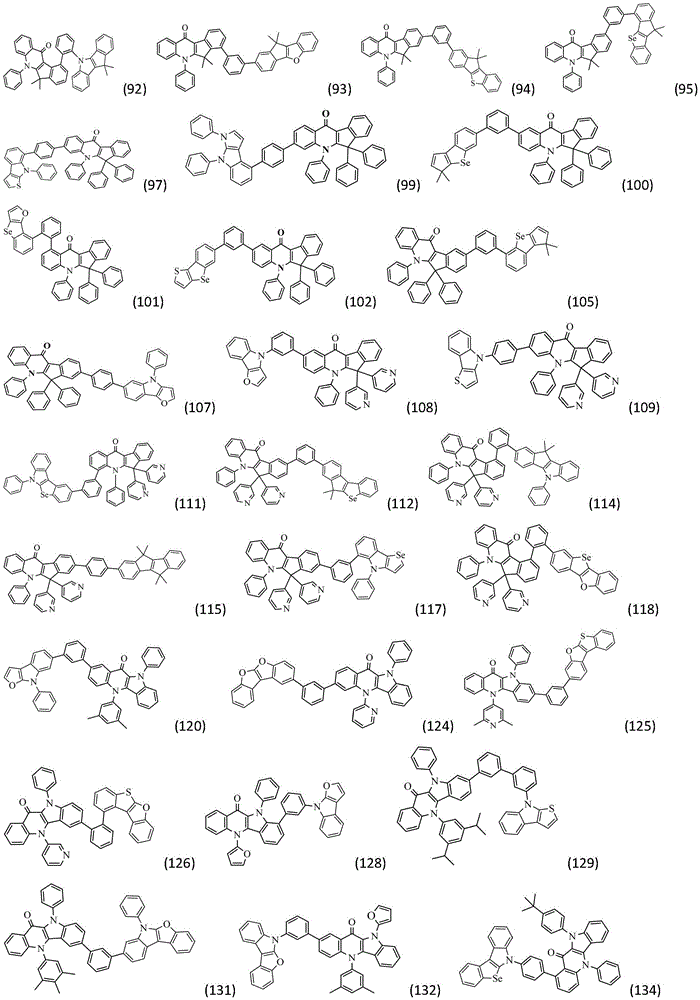
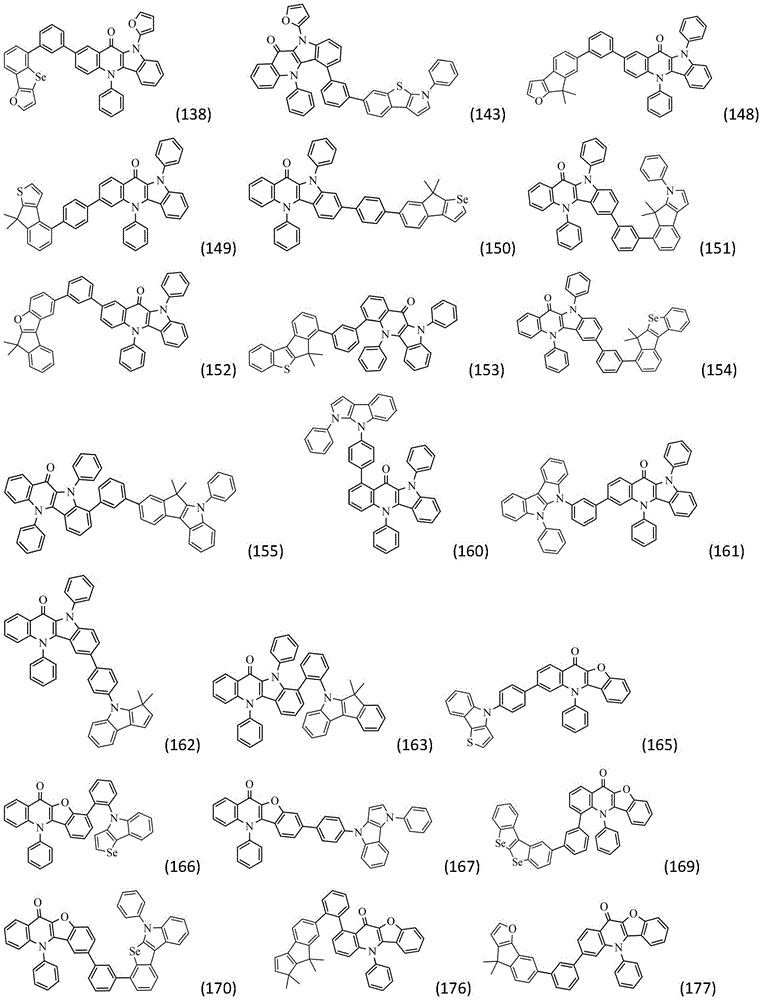
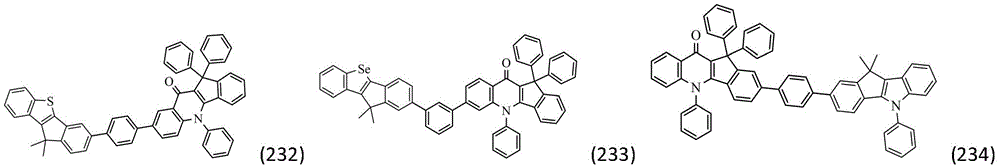
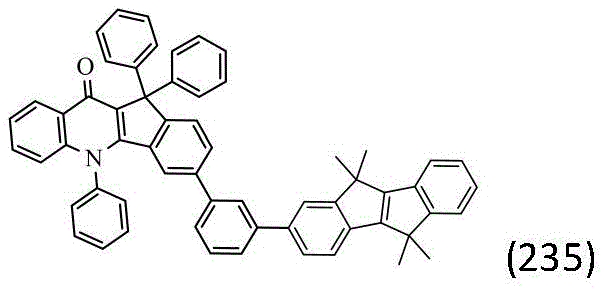
作为本发明的进一步改进,所述化合物结构通过通式(Ⅱ-1)~(Ⅱ-32)中的任一种表示:
作为本发明的进一步改进,所述通式(2)表示为:
作为本发明的进一步改进,所述通式(3)表示为:
作为本发明的进一步改进,所述通式(1)的具体结构式为:
一种制备以喹啉酮衍生物为核心的化合物的方法,合成步骤如下:
其中a、R和Rb如上述通式(1)中所定义;
称取原料A、中间体B,用体积比为2:1的甲苯与乙醇的混合溶剂溶解;在惰性气氛下,再加入Na2CO3水溶液、Pd(PPh3)4;将上述反应物的混合溶液于反应温度95-110℃,反应10-24小时,冷却并过滤反应溶液,滤液旋蒸,过硅胶柱,得到目标产物;所述原料A与中间体B的摩尔比为1:1.0-2.0;Na2CO3与原料A的摩尔比为1.0-3.0:1;Pd(PPh3)4与原料A的摩尔比为0.006-0.02:1。
一种有机电致发光器件,所述有机电致发光器件包括至少一层功能层含有所述的以喹啉酮衍生物为核心的化合物。
作为本发明的进一步改进,所述有机电致发光器件包括发光层,所述发光层含有所述的以喹啉酮衍生物为核心的化合物。
一种照明或显示元件,所述照明或显示元件包括所述的有机电致发光器件。
本发明有益的技术效果在于:
本发明化合物结构分子内包含电子给体(donor,D)与电子受体(acceptor,A)的组合,可以增加轨道重叠、提高发光效率,同时连接芳香杂环基团以获得HOMO、LUMO空间分离的电荷转移态材料,实现小的S1态和T1态的能级差,从而在热刺激条件下易于实现反向系间窜越。
本发明化合物以喹啉酮衍生物为母核,再连接芳香杂环基团,具备很强的刚性,破坏了分子对称性,从而破坏分子的结晶性,避免了分子间的聚集作用。所述化合物结构分子内包含喹啉酮衍生物作为电子受体(acceptor,A),有利于电子在发光层中的传输。连接的杂环基团是电子给体(donor,D),它有利于空穴在发光层中的传输。含杂原子苯并氮杂萘酮内部的氮原子是饱和原子,它不仅具有很强的刚性,还有利于提高母核化合物三重态能级,电子给体和电子受体的组合可以提高激子的复合效率,降低启动电压,提高器件性能。
母核为喹啉酮衍生物具有较高的三重态能级,使化合物三重态激子局限在发光层中,提高发光效率。
本发明所述化合物可作为发光层材料应用于OLED发光器件制作,作为发光层主体材料可以获得良好的器件表现,器件的电流效率,功率效率和外量子效率均得到很大改善;同时,对于器件寿命提升非常明显。
附图说明
图1为本发明所列举的材料应用于OLED器件的结构示意图;
图中:1为透明基板层,2为ITO阳极层,3为空穴注入层,4为空穴传输层,5为电子阻挡层,6为发光层,7为空穴阻挡/电子传输层,8为电子注入层,9为阴极反射电极层。
图2为本发明实施例中制备的OLED器件在不同温度下测量的电流效率曲线图。
具体实施方式
下面结合附图和实施例,对本发明进行具体描述。
中间体B的制备:
中间体Ⅰ-1的制备:
(1)500mL的三口瓶,在氮气保护下,加入0.05mol原料C-1,0.06mol原料D-1,用混合溶剂溶解(180ml甲苯,90ml乙醇),然后加入0.15mol Na2CO3水溶液(2M),通氮气搅拌1小时,然后加入0.0005mol Pd(PPh3)4,100℃加热回流15小时,取样点板,反应完全。自然冷却,过滤,滤液旋蒸,过硅胶柱,得到中间体L-1,HPLC纯度93.4%,收率64.2%。
元素分析结构(分子式C23H17BrS2):理论值C,63.16;H,3.92;Br,18.27;S,14.66;测试值:C,63.15;H,3.92;Br,18.27;S,14.67。ESI-MS(m/z)(M+):理论值为436.00,实测值为436.12。
(2)在氮气保护下,称0.01mol中间体L-1和0.012mol碳酸铯,用DMSO溶解,加热至140~150℃,反应8~12小时;取样点板,显示无中间体L-1剩余,反应完全;将反应体系冷却至室温,加入饱和的氯化钠溶液,用乙酸乙酯萃取,分液,有机相用无水硫酸钠干燥,减压旋蒸,所得粗产物过中性硅胶柱,得到中间体Ⅰ-1,HPLC纯度98.1%,收率88.3%;
元素分析结构(分子式C23H15BrS):理论值C,68.49;H,3.75;Br,19.81;S,7.95;测试值:C,68.48;H,3.75;Br,19.81;S,7.96。ESI-MS(m/z)(M+):理论值为402.01,实测值为402.08。
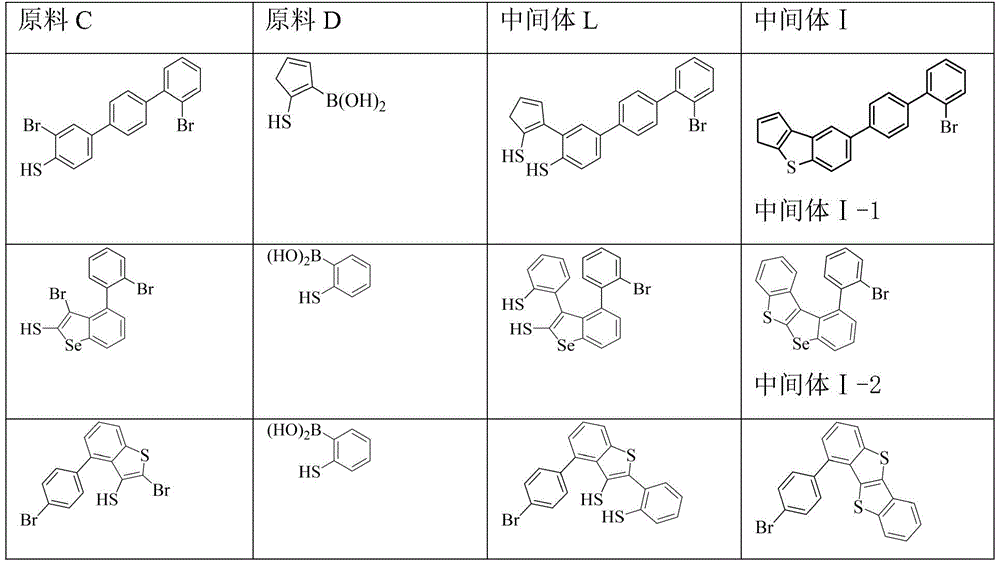
中间体Ⅰ-1的合成分为两步:由原料C-1和原料D-1合成中间体L-1;中间体L-1经成环反应形成中间体Ⅰ-1。其他中间体Ⅰ的制备方法与中间体Ⅰ-1的制备方法类似,本发明用到的中间体Ⅰ的具体结构以及制备原料如表1所示。
表1
原料C和原料D通过商业途径购买所得。
中间体Ⅱ-1的制备:
(1)在三口烧瓶中,加入原料E-1(0.1mol)、原料F-1(0.1mol)、碳酸钾(0.2mol)、四氢呋喃(300ml)、水(100ml)和三苯基膦化钯(1g),在氮气保护下,室温下回流10小时,取样点板,反应完全。自然冷却,用二氯甲烷萃取,有机相干燥,浓缩,经柱层析纯化得到中间体M-1-1;HPLC纯度97.5%,收率68.4%。
元素分析结构(分子式C19H16BrNO2):理论值C,61.64;H,4.36;Br,21.58;N,3.78;O,8.64;测试值:C,61.65;H,4.36;Br,21.57;N,3.77;O,8.65。ESI-MS(m/z)(M+):理论值为369.04,实测值为369.10。
(2)在三口烧瓶中,加入中间体M-1-1(0.03mol)、三苯基膦(0.24mol)和邻二氯苯(200ml),氮气保护下180℃加热回流5个小时,冷却,旋蒸除去溶剂,粗产品用四氢呋喃和乙醇重结晶得到中间体M-2-1;HPLC纯度96.4%,收率89.0%。
元素分析结构(分子式C19H16BrN):理论值C,67.47;H,4.77;Br,23.62;N,4.14;测试值:C,67.46;H,4.77;Br,23.63;N,4.14。ESI-MS(m/z)(M+):理论值为337.05,实测值为336.98。
(3)在250mL的三口瓶中,在氮气保护下,加入0.02mol中间体M-2-1、碘苯、0.05mol叔丁醇钠、0.2mmolPd2(dba)3、0.2mmol三叔丁基膦,用150mL甲苯搅拌混合,加热至110~~120℃,回流反应12-24小时,取样点板,显示无中间体M-2-1剩余,反应完全;自然冷却至室温,过滤,滤液减压旋蒸至无馏分,过中性硅胶柱,得到中间体Ⅱ-1;HPLC纯度95.6%,收率86.8%。
元素分析结构(分子式C25H20BrN):理论值C,72.47;H,4.87;Br,19.28;N,3.38;测试值:C,72.47;H,4.86;Br,19.28;N,3.39。ESI-MS(m/z)(M+):理论值为413.08,实测值为413.12。
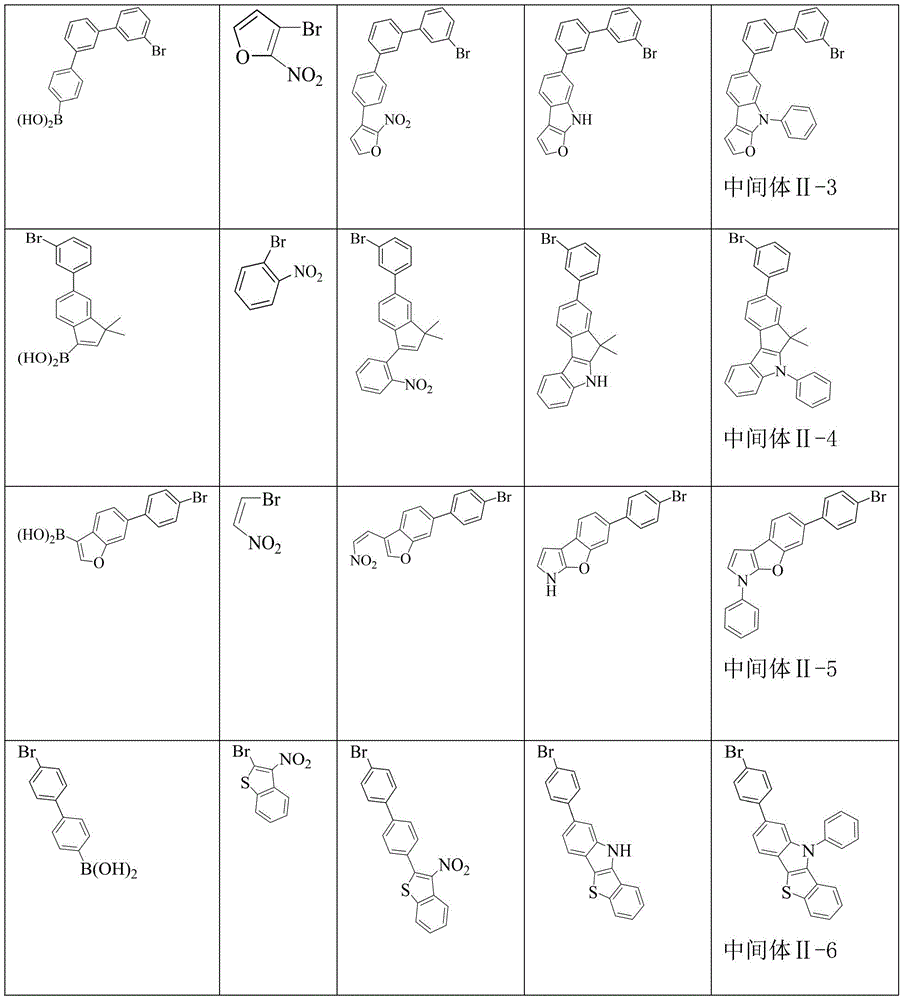
中间体Ⅱ-1的合成分为三步:由原料E-1和原料F-1合成中间体M-1-1;中间体M-1-1经成环反应形成中间体M-2-1;中间体M-2-1和碘苯合成中间体Ⅱ-1。其他中间体Ⅱ的制备方法与中间体Ⅱ-1的制备方法类似,本发明用到的中间体Ⅱ的具体结构以及制备原料如表2所示。
表2
原料E和原料F通过商业途径购买所得。
中间体Ⅲ-1的制备:
(1)在三口烧瓶中,加入原料G-1(0.1mol)、原料H-1(0.1mol)、碳酸钾(0.2mol)、四氢呋喃(300ml)、水(100ml)和四三苯基膦钯(1g),在氮气保护下,100℃加热回流10小时,取样点板,反应完全。自然冷却,用二氯甲烷萃取,有机相干燥,浓缩,经柱层析纯化得到中间体N-1-1;HPLC纯度98.3%,收率87.1%。
元素分析结构(分子式C10H7NO2S):理论值C,58.52;H,3.44;N,6.82;O,15.59;S,15.62;测试值:C,58.52;H,3.43;N,6.82;O,15.59;S,15.63。ESI-MS(m/z)(M+):理论值为205.02,实测值为205.13。
(2)在三口烧瓶中,加入中间体N-1-1(0.03mol)、三苯基膦(0.24mol)和邻二氯苯(200ml),氮气保护下180℃加热回流5个小时,冷却,旋蒸除去溶剂,粗产品用四氢呋喃和乙醇重结晶得到中间体N-2-1;HPLC纯度93.4%,收率88.6%。
元素分析结构(分子式C10H7NS):理论值C,69.33;H,4.07;N,8.09;S,18.51;测试值:C,69.32;H,4.07;N,8.10;S,18.51。ESI-MS(m/z)(M+):理论值为173.03,实测值为173.05。
(3)在250mL的三口瓶中,在氮气保护下,加入0.02mol中间体N-2-1、原料Q、0.05mol叔丁醇钠、0.2mmolPd2(dba)3、0.2mmol三叔丁基膦,用150mL甲苯搅拌混合,加热至110~~120℃,回流反应12-24小时,取样点板,显示无中间体N-2-1剩余,反应完全;自然冷却至室温,过滤,滤液减压旋蒸至无馏分,过中性硅胶柱,得到中间体Ⅲ-1;HPLC纯度97.2%,收率87.4%。
元素分析结构(分子式C16H10BrNS):理论值C,58.55;H,3.07;Br,24.34;N,4.27;S,9.77;测试值:C,58.55;H,3.07;Br,24.35;N,4.26;S,9.77。ESI-MS(m/z)(M+):理论值为326.97,实测值为327.10。
中间体Ⅲ-1的合成分为三步:由原料G-1和原料H-1合成中间体N-1-1;中间体N-1-1经成环反应形成中间体N-2-1;中间体N-2-1和间二溴苯合成中间体Ⅲ-1。其他中间体Ⅲ的制备方法与中间体Ⅲ-1的制备方法类似,本发明用到的中间体Ⅲ的具体结构以及制备原料如表3所示。
表3
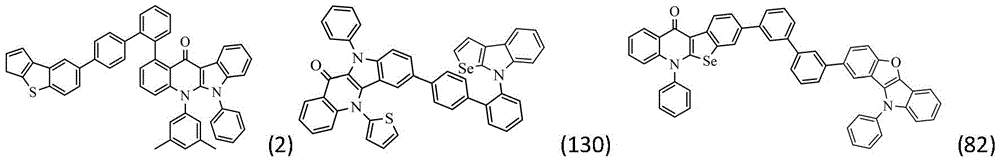
实施例1:化合物2的合成:
在250mL的三口瓶中,通入氮气,加入0.01mol原料A-1,0.015mol中间体Ⅰ-1,用甲苯和乙醇的混合溶剂溶解(其中甲苯90mL,乙醇45mL),然后加入0.03mol Na2CO3水溶液(2M),通氮气搅拌1h,然后加入0.0001mol Pd(PPh3)4,100℃加热回流15h,取样点板,反应完全。自然冷却、过滤、滤液旋蒸、残余物过硅胶柱,得到目标产物,纯度98.1%,收率84.9%。元素分析结构(分子式C52H36N2OS):理论值C,84.75;H,4.92;N,3.80;O,2.17;S,4.35;测试值:C,84.75;H,4.91;N,3.82;O,2.17;S,4.34。ESI-MS(m/z)(M+):理论值为736.25,实测值为736.19。
实施例2:化合物12的合成:
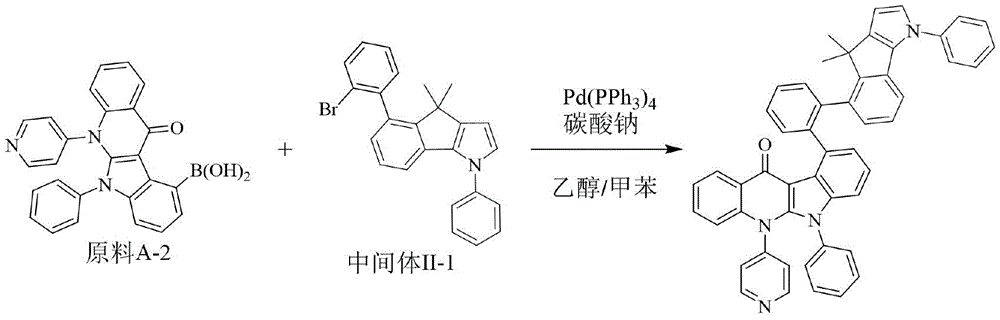
化合物12的制备方法同实施例1,不同之处在于采用原料A-2替换原料A-1,用中间体Ⅱ-1替换中间体Ⅰ-1。元素分析结构(分子式C51H36N4O):理论值C,84.97;H,5.03;N,7.77;O,2.22;测试值:C,84.96;H,5.03;N,7.77;O,2.23。HPLC-MS:材料分子量为720.29,实测分子量720.35。
实施例3:化合物33的合成:
化合物33的制备方法同实施例1,不同之处在于采用原料A-3替换原料A-1,用中间体Ⅲ-1替换中间体Ⅰ-1。元素分析结构(分子式C43H27N3OS):理论值C,81.49;H,4.29;N,6.63;O,2.52;S,5.06;测试值:C,81.48;H,4.29;N,6.63;O,2.53;S,5.06。HPLC-MS:材料分子量为633.19,实测分子量633.22。
实施例4:化合物44的合成:
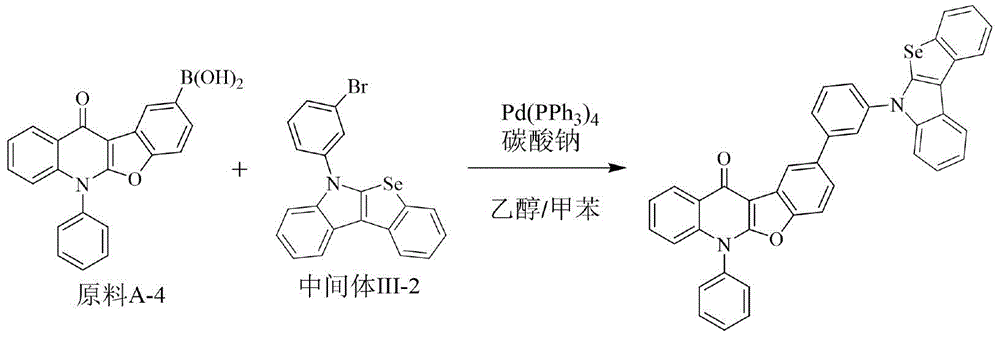
化合物44的制备方法同实施例1,不同之处在于采用原料A-4替换原料A-1,用中间体Ⅲ-2替换中间体Ⅰ-1。元素分析结构(分子式C41H24N2O2Se):理论值C,75.11;H,3.69;N,4.27;O,4.88;Se,12.04;测试值:C,75.12;H,3.69;N,4.27;O,4.87;Se,12.04。HPLC-MS:材料分子量为656.10,实测分子量656.16。
实施例5:化合物46的合成:
化合物46的制备方法同实施例1,不同之处在于采用原料A-5替换原料A-1,用中间体Ⅲ-3替换中间体Ⅰ-1。元素分析结构(分子式C46H34N2O2):理论值C,85.42;H,5.30;N,4.33;O,4.95;测试值:C,85.42;H,5.30;N,4.32;O,4.96。HPLC-MS:材料分子量为646.26,实测分子量646.29。
实施例6:化合物52的合成:
化合物52的制备方法同实施例1,不同之处在于采用原料A-6替换原料A-1,用中间体Ⅰ-2替换中间体Ⅰ-1。元素分析结构(分子式C40H22N2O2SSe):理论值C,71.32;H,3.29;N,4.16;O,4.75;S,4.76;Se,11.72;测试值:C,71.32;H,3.29;N,4.15;O,4.75;S,4.76;Se,11.73。HPLC-MS:材料分子量为674.06,实测分子量674.23。
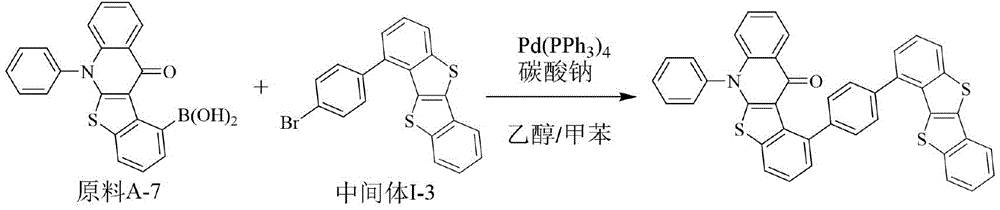
实施例7:化合物67的合成:
化合物67的制备方法同实施例1,不同之处在于采用原料A-7替换原料A-1,用中间体Ⅰ-3替换中间体Ⅰ-1。元素分析结构(分子式C41H23NOS3):理论值C,76.73;H,3.61;N,2.18;O,2.49;S,14.99;测试值:C,76.74;H,3.61;N,2.18;O,2.49;S,14.98。HPLC-MS:材料分子量为641.09,实测分子量640.95。
实施例8:化合物82的合成:
化合物82的制备方法同实施例1,不同之处在于采用原料A-8替换原料A-1,用中间体Ⅱ-2替换中间体Ⅰ-1。元素分析结构(分子式C53H32N2O2Se):理论值C,78.80;H,3.99;N,3.47;O,3.96;Se,9.77;测试值:C,78.80;H,3.99;N,3.46;O,3.97;Se,9.77。HPLC-MS:材料分子量为808.16,实测分子量808.07。
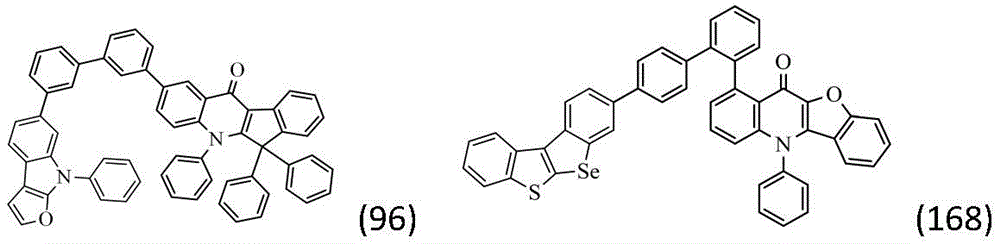
实施例9:化合物96的合成:
化合物96的制备方法同实施例1,不同之处在于采用原料A-9替换原料A-1,用中间体Ⅱ-3替换中间体Ⅰ-1。元素分析结构(分子式C62H40N2O2):理论值C,88.13;H,4.77;N,3.32;O,3.79;测试值:C,88.12;H,4.77;N,3.33;O,3.79。HPLC-MS:材料分子量为844.31,实测分子量844.23。
实施例10:化合物108的合成:
合成路线:
化合物108的制备方法同实施例1,不同之处在于采用原料A-10替换原料A-1,用中间体Ⅲ-4替换中间体Ⅰ-1。元素分析结构(分子式C48H30N4O2):理论值C,82.98;H,4.35;N,8.06;O,4.61;测试值:C,82.98;H,4.35;N,8.06;O,4.61。HPLC-MS:材料分子量为694.24,实测分子量694.26。
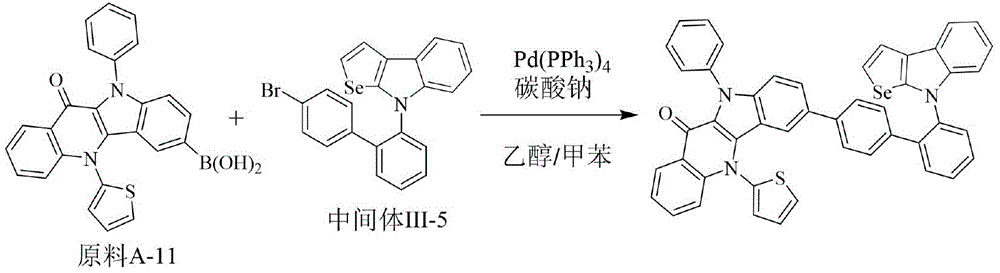
实施例11:化合物130的合成:
化合物130的制备方法同实施例1,不同之处在于采用原料A-11替换原料A-1,用中间体Ⅲ-5替换中间体Ⅰ-1。元素分析结构(分子式C47H29N3OSSe):理论值C,74.01;H,3.83;N,5.51;O,2.10;S,4.20;Se,10.35;测试值:C,74.02;H,3.83;N,5.52;O,2.10;S,4.20;Se,10.33。HPLC-MS:材料分子量为763.12,实测分子量763.04。
实施例12:化合物132的合成:
化合物132的制备方法同实施例1,不同之处在于采用原料A-12替换原料A-1,用中间体Ⅲ-6替换中间体Ⅰ-1。元素分析结构(分子式C47H31N3O3):理论值C,82.32;H,4.56;N,6.13;O,7.00;测试值:C,82.31;H,4.56;N,6.13;O,7.01。HPLC-MS:材料分子量为685.24,实测分子量685.36。
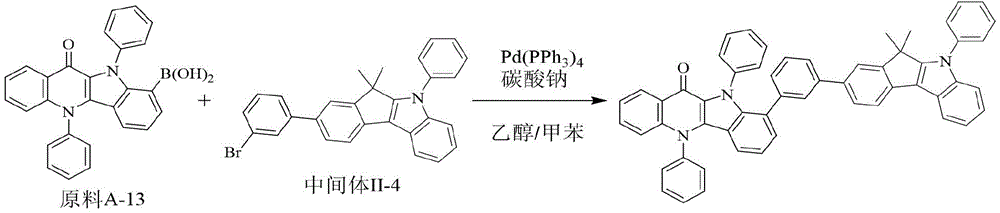
实施例13:化合物155的合成:
化合物155的制备方法同实施例1,不同之处在于采用原料A-13替换原料A-1,用中间体Ⅱ-4替换中间体Ⅰ-1。元素分析结构(分子式C56H39N3O):理论值C,87.36;H,5.11;N,5.46;O,2.08;测试值:C,87.37;H,5.11;N,5.45;O,2.08。HPLC-MS:材料分子量为769.31,实测分子量769.28。
实施例14:化合物168的合成:
化合物168的制备方法同实施例1,不同之处在于采用原料A-14替换原料A-1,用中间体Ⅰ-4替换中间体Ⅰ-1。元素分析结构(分子式C47H27NO2SSe):理论值C,75.39;H,3.63;N,1.87;O,4.27;S,4.28;Se,10.55;测试值:C,75.38;H,3.63;N,1.87;O,4.28;S,4.28;Se,10.55。HPLC-MS:材料分子量为749.09,实测分子量749.15。
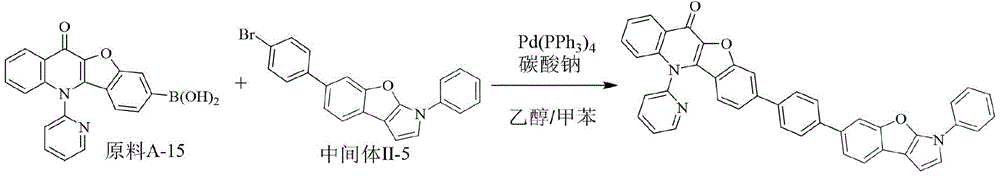
实施例15:化合物183的合成:
化合物183的制备方法同实施例1,不同之处在于采用原料A-15替换原料A-1,用中间体Ⅱ-5替换中间体Ⅰ-1。元素分析结构(分子式C42H25N3O3):理论值C,81.41;H,4.07;N,6.78;O,7.75;测试值:C,81.42;H,4.08;N,6.78;O,7.73。HPLC-MS:材料分子量为619.19,实测分子量619.23。
实施例16:化合物205的合成:
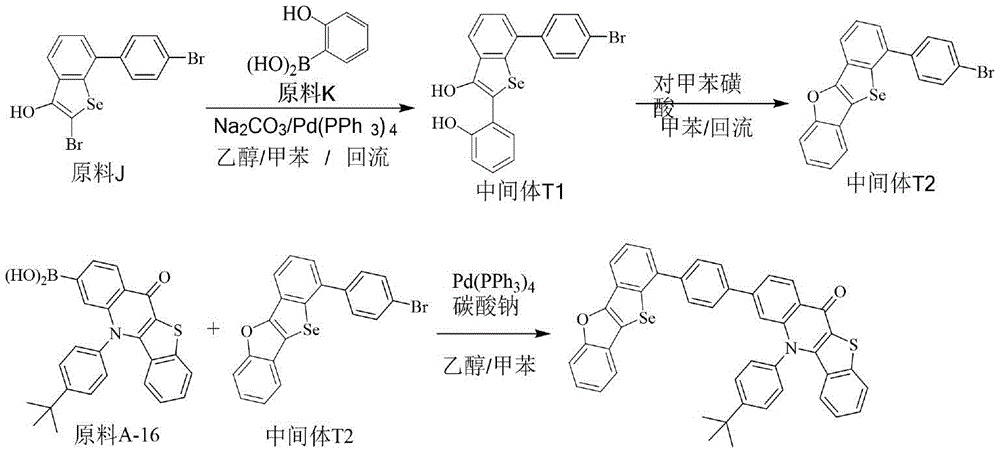
(1)500mL的三口瓶,在氮气保护下,加入0.05mol原料J,0.06mol原料K,用混合溶剂溶解(180ml甲苯,90ml乙醇),然后加入0.15mol Na2CO3水溶液(2M),通氮气搅拌1小时,然后加入0.0005mol Pd(PPh3)4,100℃加热回流15小时,取样点板,反应完全。自然冷却,过滤,滤液旋蒸,过硅胶柱,得到中间体T1,HPLC纯度94.8%,收率76.4%。元素分析结构(分子式C20H13BrO2Se):理论值C,54.08;H,2.95;Br,17.99;O,7.20;Se,17.78;测试值:C,54.08;H,2.96;Br,17.99;O,7.20;Se,17.77。ESI-MS(m/z)(M+):理论值为443.93,实测值为443.82。
(2)250mL的三口瓶,在氮气保护下,加入0.03mol中间体T1和0.036mol对甲苯磺酸,用100ml甲苯溶解,加热至100℃,反应15小时;取样点板,显示无中间体T1剩余,反应完全;反应结束后,向反应体系中加入饱和碳酸钠溶液淬灭,用乙酸乙酯萃取,分液,有机相用无水硫酸钠干燥后减压旋蒸至无馏分,所得粗产物过中性硅胶柱,得到中间体T2,HPLC纯度98.7%,收率88.2%。
元素分析结构(分子式C20H11BrOSe):理论值C,56.37;H,2.60;Br,18.75;O,3.75;Se,18.53;测试值:C,56.37;H,2.60;Br,18.74;O,3.75;Se,18.54。ESI-MS(m/z)(M+):理论值为425.92,实测值为425.87。
(3)化合物205的制备方法同实施例1,不同之处在于采用原料A-16替换原料A-1,用中间体T2替换中间体Ⅰ-1。元素分析结构(分子式C45H31NO2SSe):理论值C,74.17;H,4.29;N,1.92;O,4.39;S,4.40;Se,10.83;测试值:C,74.17;H,4.30;N,1.91;O,4.40;S,4.40;Se,10.82。HPLC-MS:材料分子量为729.12,实测分子量729.18。
实施例17:化合物213的合成:
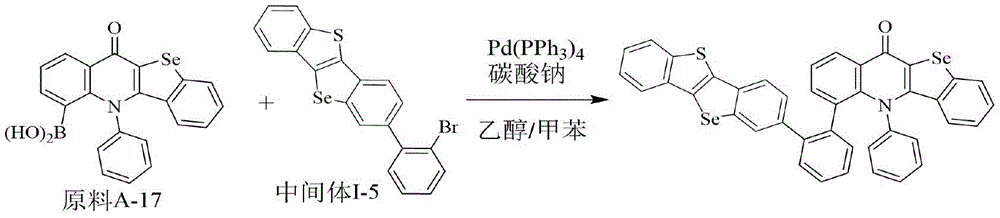
化合物213的制备方法同实施例1,不同之处在于采用原料A-17替换原料A-1,用中间体Ⅰ-5替换中间体Ⅰ-1。元素分析结构(分子式C41H23NOSSe2):理论值C,66.94;H,3.15;N,1.90;O,2.17;S,4.36;Se,21.47;测试值:C,66.95;H,3.15;N,1.90;O,2.17;S,4.36;Se,21.46。HPLC-MS:材料分子量为736.98,实测分子量737.05。
实施例18:化合物221的合成:
(1)500mL的三口瓶,在氮气保护下,加入0.05mol原料O,0.06mol原料P,用混合溶剂溶解(180ml甲苯,90ml乙醇),然后加入0.15mol Na2CO3水溶液(2M),通氮气搅拌1小时,然后加入0.0005mol Pd(PPh3)4,加热回流15小时,取样点板,反应完全。自然冷却,过滤,滤液旋蒸,过硅胶柱,得到中间体Q1,HPLC纯度95.4%,收率75.2%。元素分析结构(分子式C19H17BrO2):理论值C,63.88;H,4.80;Br,22.37;O,8.96;测试值:C,63.88;H,4.79;Br,22.37;O,8.97。ESI-MS(m/z)(M+):理论值为356.04,实测值为356.19。
(2)250mL的三口瓶,在氮气保护下,加入中间体0.03mol中间体Q1和0.036mol对甲苯磺酸,用100ml甲苯溶解,加热至100℃,反应15小时;取样点板,显示无中间体Q1剩余,反应完全;反应结束后,向反应体系中加入饱和碳酸钠溶液淬灭,用乙酸乙酯萃取,分液,有机相用无水硫酸钠干燥后减压旋蒸至无馏分,所得粗产物过中性硅胶柱,得到中间体Q2,HPLC纯度96.1%,收率86.8%。
元素分析结构(分子式C19H15BrO):理论值C,67.27;H,4.46;Br,23.55;O,4.72;测试值:C,67.27;H,4.46;Br,23.54;O,4.73。ESI-MS(m/z)(M+):理论值为338.03,实测值为337.94。
(3)化合物221的制备方法同实施例1,不同之处在于采用原料A-18替换原料A-1,用中间体Q2替换中间体Ⅰ-1。元素分析结构(分子式C40H35NO2):理论值C,85.53;H,6.28;N,2.49;O,5.70;测试值:C,85.52;H,6.28;N,2.49;O,5.71。HPLC-MS:材料分子量为561.27,实测分子量561.35。
实施例19:化合物224的合成:
化合物224的制备方法同实施例1,不同之处在于采用原料A-19替换原料A-1,用中间体Ⅰ-6替换中间体Ⅰ-1。元素分析结构(分子式C41H31NO2S):理论值C,81.83;H,5.19;N,2.33;O,5.32;S,5.33;测试值:C,81.83;H,5.20;N,2.33;O,5.32;S,5.32。HPLC-MS:材料分子量为601.21,实测分子量601.14。
实施例20:化合物238的合成:
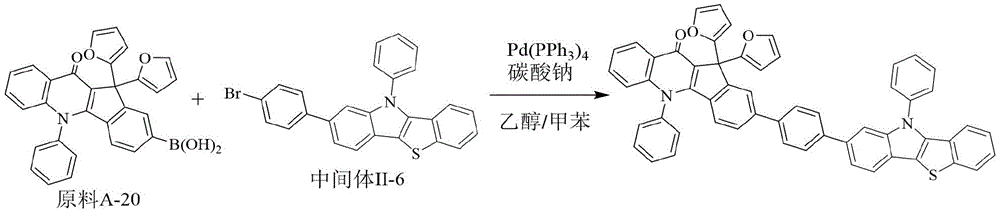
化合物238的制备方法同实施例1,不同之处在于采用原料A-20替换原料A-1,用中间体Ⅱ-6替换中间体Ⅰ-1。元素分析结构(分子式C56H34N2O3S):理论值C,82.53;H,4.21;N,3.44;O,5.89;S,3.93;测试值:C,82.53;H,4.22;N,3.44;O,5.89;S,3.92。HPLC-MS:材料分子量为814.23,实测分子量814.35。
本发明化合物在发光器件中使用,具有高的玻璃化转变温度(Tg)和三线态能级(T1),合适的HOMO、LUMO能级,可作为发光层主体材料使用。对本发明上述实施例制备的化合物分别进行热性能、T1能级以及HOMO能级测试,结果如表4所示。
表4
注:三线态能级T1是由日立的F4600荧光光谱仪测试,材料的测试条件为2*10- 5mol/L的甲苯溶液;玻璃化转变温度Tg由示差扫描量热法(DSC,德国耐驰公司DSC204F1示差扫描量热仪)测定,升温速率10℃/min;最高占据分子轨道HOMO能级是由电离能量测试系统(IPS-3)测试,测试为大气环境。
由上表数据可知,本发明的化合物具有高的玻璃化转变温度,可提高材料膜相态稳定性,进一步提高器件使用寿命;本发明化合物含有电子给体与电子受体,使得应用本发明化合物的OLED器件电子和空穴达到平衡状态,保证了电子和空穴的复合率,从而提升了OLED器件的效率和寿命。同时本发明材料具有合适的HOMO能级可以解决载流子的注入问题,可降低器件电压;因此,本发明的有机材料在应用于OLED器件的发光层后,可有效提高器件的发光效率及使用寿命。
器件的制备:
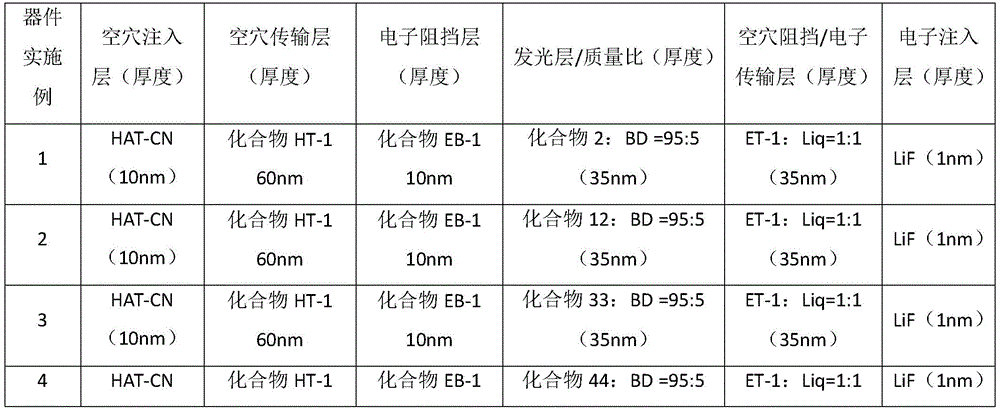
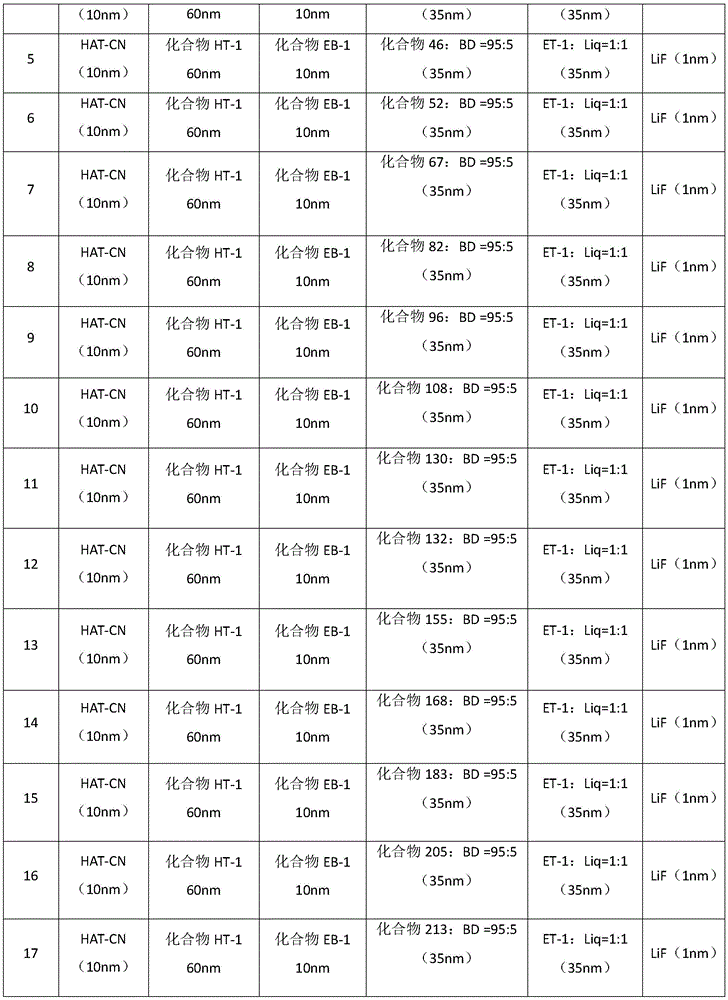
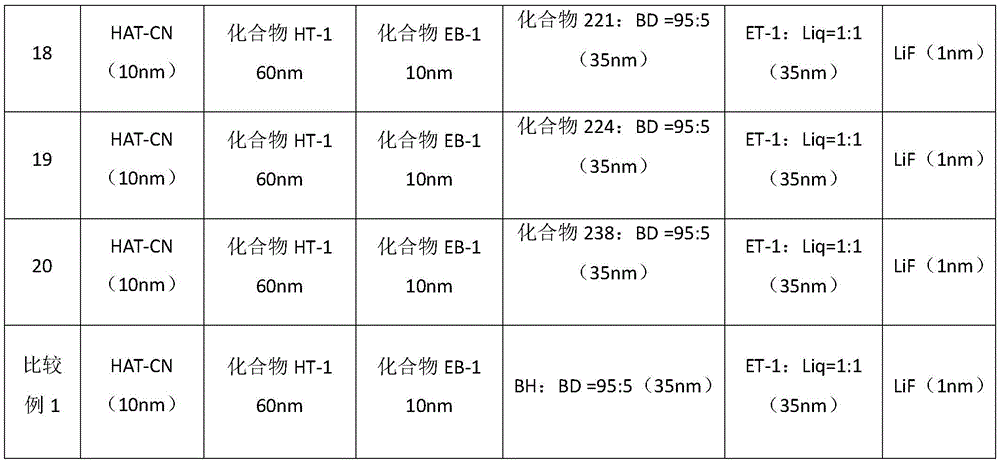
以下通过器件实施例1-20和器件比较例1详细说明本发明合成的化合物在器件中作为发光层材料的应用效果。器件实施例2-20以及器件比较例1与器件实施例1相比,所述器件的制作工艺完全相同,并且所采用了相同的基板材料和电极材料,电极材料的膜厚也保持一致,所不同的是器件中发光层材料发生了改变。器件叠层结构如表5所示,各器件的性能测试结果见表6和表7。
器件实施例1
如图1所示,一种电致发光器件,其具体的制作步骤如下:
a)清洗透明基板层1上的ITO阳极层2,分别用去离子水、丙酮、乙醇超声清洗各15分钟,然后在等离子体清洗器中处理2分钟;b)在ITO阳极层2上,通过真空蒸镀方式蒸镀空穴注入层材料HAT-CN,厚度为10nm,这层作为空穴注入层3;c)在空穴注入层3上,通过真空蒸镀方式蒸镀空穴传输层材料化合物HT-1,厚度为60nm,该层为空穴传输层4;d)在空穴传输层4上,通过真空蒸镀方式蒸镀化合物EB-1,厚度为10nm,该层为电子阻挡层5;e)在电子阻挡层5上,通过真空蒸镀方式蒸镀发光层6,主体材料为本发明化合物2,掺杂材料为BD,化合物2和BD的质量比为95:5厚度为35nm;f)在发光层6之上,通过真空蒸镀方式蒸镀空穴阻挡/电子传输材料ET-1和Liq,两者质量比为1:1,厚度为35nm,这层作为空穴阻挡/电子传输层7使用;g)在空穴阻挡/电子传输层7之上,真空蒸镀电子注入层LiF,厚度为1nm,该层为电子注入层8;h)在电子注入层8之上,真空蒸镀阴极Al(100nm),该层为阴极反射电极层9。
按照上述步骤完成电致发光器件的制作后,测量器件的IVL数据和光衰寿命,其结果见表6所示。相关材料的分子结构式如下所示:
器件实施例2-20和比较例1与器件实施例1的器件的制作工艺完全相同,并且所采用了相同的基板材料和电极材料,电极材料的膜厚也保持一致,不同之处在于发光层所用的材料不相同。具体的数据参见表5。
表5
各实施例和比较例器件的效率和寿命数据见表6所示。
表6
由表6的器件数据结果可以看出,本发明的有机发光器件无论是在效率还是寿命均相对于已知材料的OLED器件获得较大的提升。
为了比较不同器件在高电流密度下效率衰减的情况,定义效率衰减系数φ进行表示,它表示驱动电流为100mA/cm2时器件的最大效率μ100与器件的最大效率μm之差与最大效率之间的比值,φ值越大,说明器件的效率滚降越严重,反之,说明器件在高电流密度下快速衰降的问题得到了控制。对器件实施例1-20和比较例1分别进行效率衰减系数φ的测定,检测结果如表7所示:
表7
从表7的数据来看,通过实施例和比较例的效率衰减系数对比我们可以看出,本发明的有机发光器件能够有效地降低效率滚降。
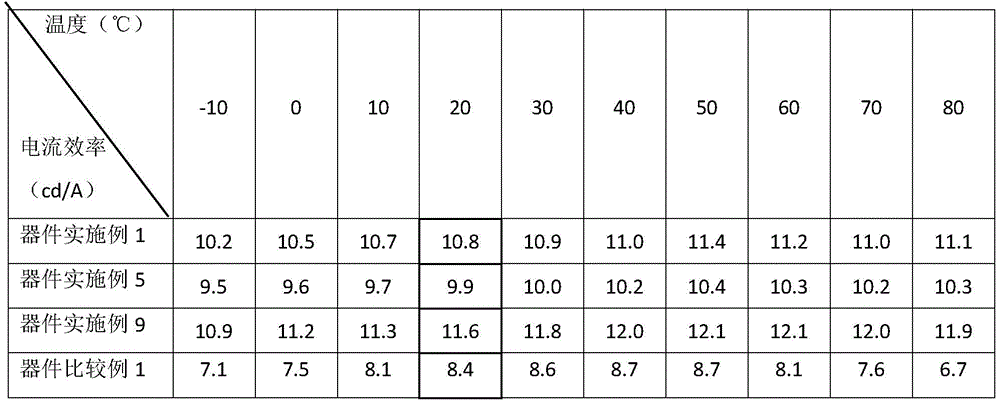
进一步的本发明材料制备的OLED器件在低温下工作时效率也比较稳定,将器件实施例1、5、9和器件比较例1在-10~80℃区间进行效率测试,所得结果如表8和图2所示。
表8
从表8和图2的数据可知,器件实施例1、5、9为本发明材料和已知材料搭配的器件结构,和器件比较例1相比,不仅低温效率高,而且在温度升高过程中,效率平稳升高。
Claims (6)
1.一种以喹啉酮衍生物为核心的化合物,其特征在于所述化合物结构如通式(1)所示:
所述R1~R2分别独立的表示为甲基、苯基或吡啶基中的一种;
所述R3表示为苯基或呋喃基中的一种;
其中,所述R表示为取代或未取代的苯基、取代或未取代的吡啶基、取代或未取代的呋喃基;
b和c分别独立地表示为0或1,且b+c=1;
Rb表示为通式(2)或者通式(3)表示的结构:
所述通式(2)表示为:
所述通式(3)表示为:
所述通式(2)和通式(3)通过单键和通式(1)中苯环连接;
其中,Ar表示为取代或者未被取代的C6亚芳基;
可取代基团的取代基任选自甲基、异丙基、叔丁基中的一种或多种。
4.一种有机电致发光器件,其特征在于,所述有机电致发光器件包括至少一层功能层含有权利要求1所述的以喹啉酮衍生物为核心的化合物。
5.根据权利要求4所述的有机电致发光器件,包括发光层,其特征在于,所述发光层含有权利要求1所述的以喹啉酮衍生物为核心的化合物。
6.一种照明或显示元件,其特征在于,所述照明或显示元件包括权利要求4或5所述的有机电致发光器件。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201811158821.2A CN110964007B (zh) | 2018-09-30 | 2018-09-30 | 一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201811158821.2A CN110964007B (zh) | 2018-09-30 | 2018-09-30 | 一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN110964007A CN110964007A (zh) | 2020-04-07 |
| CN110964007B true CN110964007B (zh) | 2021-10-22 |
Family
ID=70028977
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201811158821.2A Active CN110964007B (zh) | 2018-09-30 | 2018-09-30 | 一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN110964007B (zh) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12349592B2 (en) * | 2020-01-13 | 2025-07-01 | Samsung Electronics Co., Ltd. | Compound and photoelectric device, image sensor, and electronic device including the same |
| CN112979687B (zh) * | 2021-03-01 | 2023-07-18 | 深圳大学 | 一种热活化延迟荧光材料及其制备方法和应用 |
| CN113121560A (zh) * | 2021-03-29 | 2021-07-16 | 北京大学深圳研究生院 | 一种苯并噻吩并苯并五元杂环材料及其制备方法与应用 |
| CN114736212A (zh) * | 2022-04-29 | 2022-07-12 | 临沂大学 | 一种呋喃并[3,2-b]吲哚衍生物及其合成方法和应用 |
| CN114685517B (zh) * | 2022-05-05 | 2023-10-24 | 武汉天马微电子有限公司 | 一种含氮杂芳香环的有机化合物及其电致发光的应用 |
| CN119325755A (zh) | 2022-06-20 | 2025-01-17 | 默克专利有限公司 | 用于光电器件的有机杂环化合物 |
| CN119325756A (zh) | 2022-06-20 | 2025-01-17 | 默克专利有限公司 | 用于光电器件的杂环化合物 |
| CN121264197A (zh) | 2023-06-12 | 2026-01-02 | 默克专利有限公司 | 用于光电器件的有机杂环化合物 |
| WO2025021855A1 (de) | 2023-07-27 | 2025-01-30 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen und organische sensoren |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011160757A1 (de) * | 2010-06-22 | 2011-12-29 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| CN106699763A (zh) * | 2016-12-16 | 2017-05-24 | 江苏三月光电科技有限公司 | 一种以喹唑啉酮衍生物为核心的化合物及其应用 |
| CN106831825A (zh) * | 2017-01-20 | 2017-06-13 | 江苏三月光电科技有限公司 | 一种以含杂原子苯并芴酮为核心的化合物及其在有机电致发光器件上的应用 |
| CN107586299A (zh) * | 2017-09-29 | 2018-01-16 | 江苏三月光电科技有限公司 | 一种以氮杂苯为核心的有机化合物及其应用 |
-
2018
- 2018-09-30 CN CN201811158821.2A patent/CN110964007B/zh active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011160757A1 (de) * | 2010-06-22 | 2011-12-29 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| CN106699763A (zh) * | 2016-12-16 | 2017-05-24 | 江苏三月光电科技有限公司 | 一种以喹唑啉酮衍生物为核心的化合物及其应用 |
| CN106831825A (zh) * | 2017-01-20 | 2017-06-13 | 江苏三月光电科技有限公司 | 一种以含杂原子苯并芴酮为核心的化合物及其在有机电致发光器件上的应用 |
| CN107586299A (zh) * | 2017-09-29 | 2018-01-16 | 江苏三月光电科技有限公司 | 一种以氮杂苯为核心的有机化合物及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN110964007A (zh) | 2020-04-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110964007B (zh) | 一种以喹啉酮衍生物为核心的化合物及其在有机电致发光器件上的应用 | |
| CN111377937B (zh) | 一种以咔唑衍生物为核心的有机化合物及其在有机电致发光器件上的应用 | |
| JP2022514108A (ja) | 化合物およびこれを含む有機発光素子 | |
| CN113072568B (zh) | 一种含有双硼的有机电致发光材料及其应用 | |
| CN107586261B (zh) | 一种含有螺二苯并环庚烯芴的有机化合物及其应用 | |
| CN114057660B (zh) | 一种含双三嗪结构的化合物及其应用 | |
| CN110964021A (zh) | 一种以芴为核心的化合物、制备方法及其应用 | |
| CN110526825B (zh) | 一种以异屈与三芳胺结构为核心的化合物及其应用 | |
| CN111943941B (zh) | 一种以杂蒽酮为核心的化合物及其应用 | |
| CN113135928B (zh) | 一种有机化合物及包含其的有机电致发光器件 | |
| CN110903295A (zh) | 一种以苯并呋喃衍生物为核心的有机化合物及其应用 | |
| CN113121515B (zh) | 一种以二苯并五元杂环为核心的化合物及其应用 | |
| CN111233867A (zh) | 一种以咔唑衍生物为核心的有机化合物及其在有机电致发光器件上的应用 | |
| CN110835318B (zh) | 一种以氮杂芴为核心的有机化合物及其制备方法与应用 | |
| CN113004298B (zh) | 一种蒽酮并五元环有机化合物及其应用 | |
| CN107602542B (zh) | 一种含有二苯并六元环的有机化合物及其应用 | |
| KR20200126889A (ko) | 축합 다환 화합물 및 그 제조방법과 용도 | |
| CN110642732B (zh) | 一种含螺芴蒽酮结构的有机化合物及其应用 | |
| CN110577523B (zh) | 一种含三芳胺结构的化合物及其制备的有机电致发光器件 | |
| CN114369088B (zh) | 一种含三嗪结构的化合物及其应用 | |
| CN111362810B (zh) | 一种含二苯并环庚烯的化合物及其在有机电致发光器件上的应用 | |
| CN110835305B (zh) | 一种含二苯并环庚烯的有机化合物及其制备方法和其应用 | |
| CN114315775A (zh) | 一种含有双蒽结构的有机化合物及其在有机电致发光器件中的应用 | |
| KR20180044817A (ko) | 헤테로 고리 화합물 및 이를 포함하는 유기 발광 소자 | |
| CN112552225A (zh) | 一种以咔唑为核心的三芳胺类有机化合物及其应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| CB02 | Change of applicant information |
Address after: 214112 No. 210, Xinzhou Road, New District, Jiangsu, Wuxi Applicant after: Jiangsu March Technology Co., Ltd Address before: 214112 No. 210, Xinzhou Road, New District, Jiangsu, Wuxi Applicant before: JIANGSU SUNERA TECHNOLOGY Co.,Ltd. |
|
| CB02 | Change of applicant information | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |