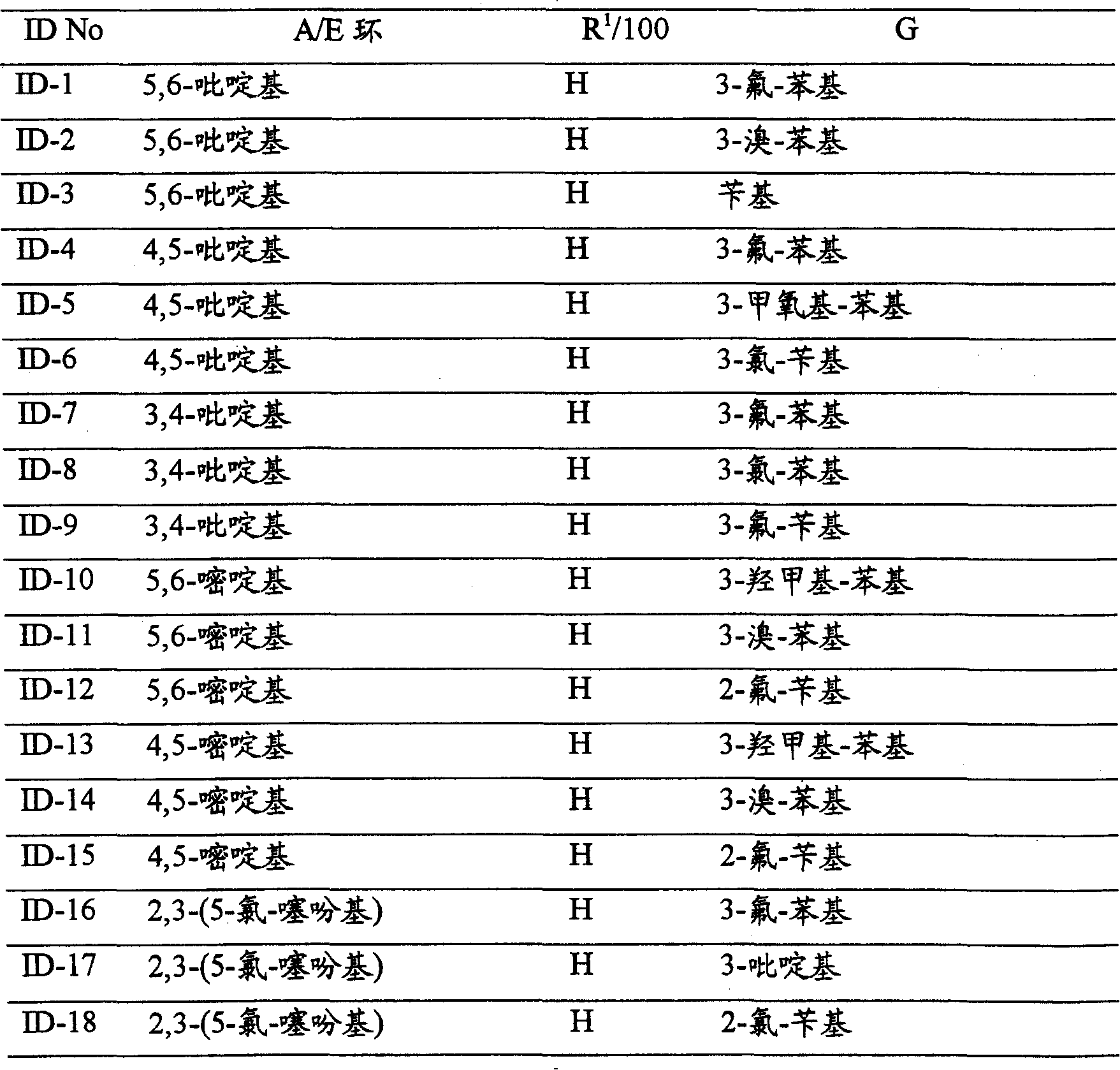
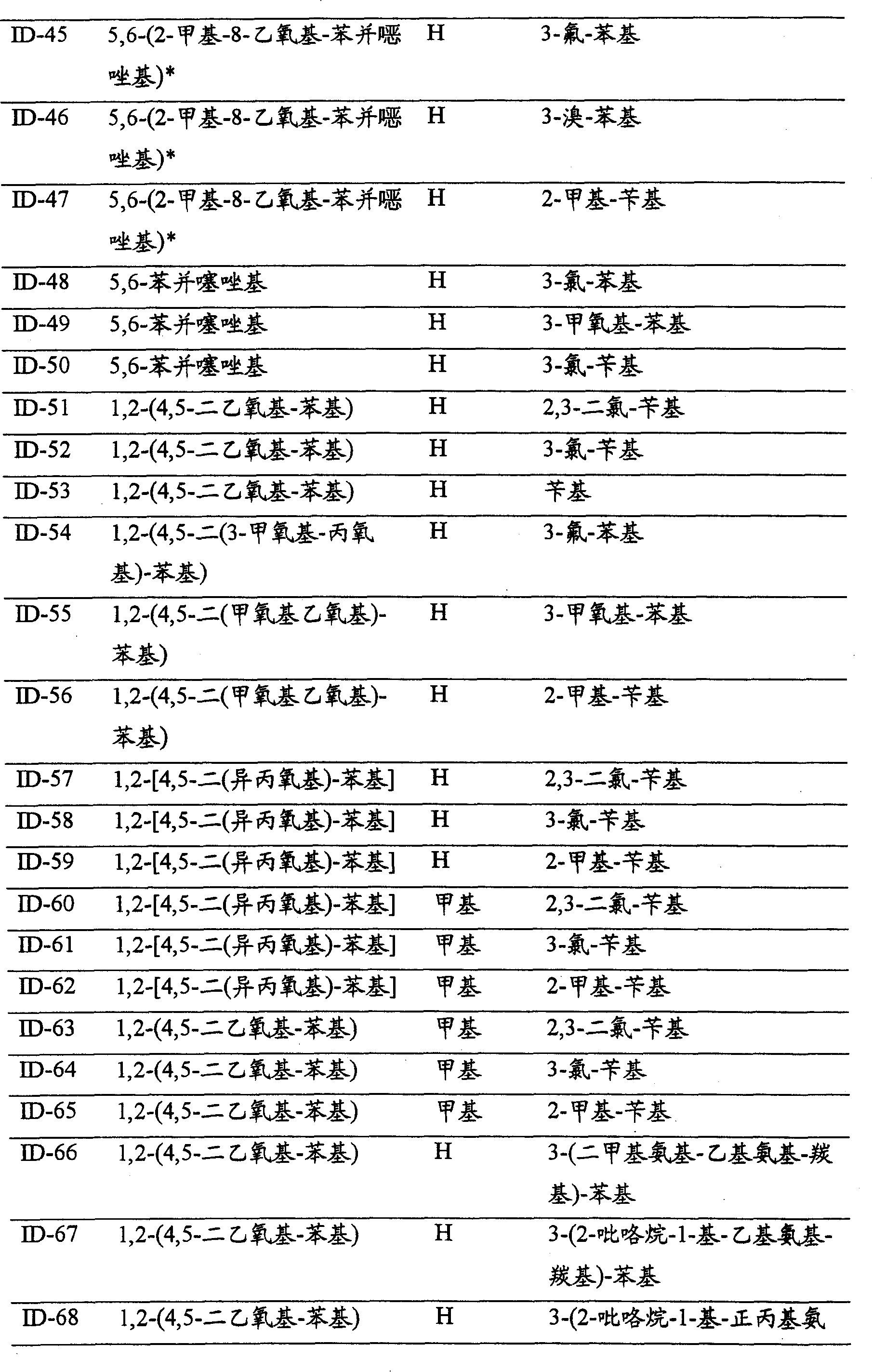
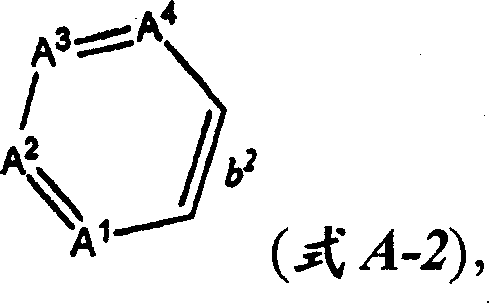CN100396670C - 作为pdfg受体抑制剂的n-取代的3-氨基苯并环戊二烯并吡唑及药用组合物和用途 - Google Patents
作为pdfg受体抑制剂的n-取代的3-氨基苯并环戊二烯并吡唑及药用组合物和用途 Download PDFInfo
- Publication number
- CN100396670C CN100396670C CNB038164884A CN03816488A CN100396670C CN 100396670 C CN100396670 C CN 100396670C CN B038164884 A CNB038164884 A CN B038164884A CN 03816488 A CN03816488 A CN 03816488A CN 100396670 C CN100396670 C CN 100396670C
- Authority
- CN
- China
- Prior art keywords
- alkyl
- nhc
- group
- compound
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- -1 N-substituted 3-aminobenzene-pyrazoles Chemical class 0.000 title claims description 238
- 239000008194 pharmaceutical composition Substances 0.000 title abstract 2
- 108091006082 receptor inhibitors Proteins 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims abstract description 539
- 108091008606 PDGF receptors Proteins 0.000 claims abstract description 36
- 102000011653 Platelet-Derived Growth Factor Receptors Human genes 0.000 claims abstract description 34
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 20
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 18
- 201000010099 disease Diseases 0.000 claims abstract description 16
- 125000000217 alkyl group Chemical group 0.000 claims description 2200
- 125000003545 alkoxy group Chemical group 0.000 claims description 240
- 229910052736 halogen Inorganic materials 0.000 claims description 169
- 150000002367 halogens Chemical class 0.000 claims description 169
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 85
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 70
- 238000002360 preparation method Methods 0.000 claims description 64
- 239000000203 mixture Substances 0.000 claims description 60
- 150000003839 salts Chemical class 0.000 claims description 53
- 230000004048 modification Effects 0.000 claims description 34
- 238000012986 modification Methods 0.000 claims description 34
- 230000003287 optical effect Effects 0.000 claims description 34
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 27
- 230000000694 effects Effects 0.000 claims description 25
- 125000001153 fluoro group Chemical group F* 0.000 claims description 25
- 208000035269 cancer or benign tumor Diseases 0.000 claims description 18
- 238000011282 treatment Methods 0.000 claims description 16
- 125000001246 bromo group Chemical group Br* 0.000 claims description 11
- 239000003814 drug Substances 0.000 claims description 10
- 230000015572 biosynthetic process Effects 0.000 claims description 9
- 108091000080 Phosphotransferase Proteins 0.000 claims description 8
- 102000020233 phosphotransferase Human genes 0.000 claims description 8
- 208000037803 restenosis Diseases 0.000 claims description 8
- 206010012689 Diabetic retinopathy Diseases 0.000 claims description 7
- 208000032839 leukemia Diseases 0.000 claims description 7
- 206010009944 Colon cancer Diseases 0.000 claims description 6
- 208000001333 Colorectal Neoplasms Diseases 0.000 claims description 6
- 201000010989 colorectal carcinoma Diseases 0.000 claims description 6
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 claims description 6
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 6
- 201000001320 Atherosclerosis Diseases 0.000 claims description 5
- 230000004663 cell proliferation Effects 0.000 claims description 5
- 208000005069 pulmonary fibrosis Diseases 0.000 claims description 5
- 206010006187 Breast cancer Diseases 0.000 claims description 4
- 208000026310 Breast neoplasm Diseases 0.000 claims description 4
- 208000017897 Carcinoma of esophagus Diseases 0.000 claims description 4
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 4
- 206010030155 Oesophageal carcinoma Diseases 0.000 claims description 4
- 206010060862 Prostate cancer Diseases 0.000 claims description 4
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims description 4
- 208000005718 Stomach Neoplasms Diseases 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 4
- 201000005619 esophageal carcinoma Diseases 0.000 claims description 4
- 201000005202 lung cancer Diseases 0.000 claims description 4
- 208000020816 lung neoplasm Diseases 0.000 claims description 4
- 201000000498 stomach carcinoma Diseases 0.000 claims description 4
- 206010010356 Congenital anomaly Diseases 0.000 claims description 3
- 208000026372 Congenital cystic kidney disease Diseases 0.000 claims description 3
- 206010058314 Dysplasia Diseases 0.000 claims description 3
- 206010018364 Glomerulonephritis Diseases 0.000 claims description 3
- 206010025323 Lymphomas Diseases 0.000 claims description 3
- 208000034578 Multiple myelomas Diseases 0.000 claims description 3
- 206010033128 Ovarian cancer Diseases 0.000 claims description 3
- 206010061535 Ovarian neoplasm Diseases 0.000 claims description 3
- 206010035226 Plasma cell myeloma Diseases 0.000 claims description 3
- 208000021045 exocrine pancreatic carcinoma Diseases 0.000 claims description 3
- 206010061989 glomerulosclerosis Diseases 0.000 claims description 3
- 201000001441 melanoma Diseases 0.000 claims description 3
- 208000030761 polycystic kidney disease Diseases 0.000 claims description 3
- 201000002793 renal fibrosis Diseases 0.000 claims description 3
- 208000019553 vascular disease Diseases 0.000 claims description 3
- 206010061218 Inflammation Diseases 0.000 claims description 2
- 238000007599 discharging Methods 0.000 claims description 2
- 206010020718 hyperplasia Diseases 0.000 claims description 2
- 230000004054 inflammatory process Effects 0.000 claims description 2
- 208000002780 macular degeneration Diseases 0.000 claims description 2
- 230000003313 weakening effect Effects 0.000 claims 4
- 208000031261 Acute myeloid leukaemia Diseases 0.000 claims 2
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 claims 2
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 claims 2
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 claims 2
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 claims 2
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 claims 1
- 206010016654 Fibrosis Diseases 0.000 claims 1
- 208000014767 Myeloproliferative disease Diseases 0.000 claims 1
- 201000007224 Myeloproliferative neoplasm Diseases 0.000 claims 1
- 206010029379 Neutrophilia Diseases 0.000 claims 1
- 230000001154 acute effect Effects 0.000 claims 1
- 230000005540 biological transmission Effects 0.000 claims 1
- 230000001684 chronic effect Effects 0.000 claims 1
- 230000004761 fibrosis Effects 0.000 claims 1
- 210000004072 lung Anatomy 0.000 claims 1
- 238000000034 method Methods 0.000 abstract description 202
- 239000003112 inhibitor Substances 0.000 abstract description 11
- 102000001253 Protein Kinase Human genes 0.000 abstract description 3
- 108060006633 protein kinase Proteins 0.000 abstract description 3
- JVVRJMXHNUAPHW-UHFFFAOYSA-N 1h-pyrazol-5-amine Chemical class NC=1C=CNN=1 JVVRJMXHNUAPHW-UHFFFAOYSA-N 0.000 abstract 1
- 230000002062 proliferating effect Effects 0.000 abstract 1
- 125000003118 aryl group Chemical group 0.000 description 204
- 125000004415 heterocyclylalkyl group Chemical group 0.000 description 188
- 125000004414 alkyl thio group Chemical group 0.000 description 136
- 125000001072 heteroaryl group Chemical group 0.000 description 134
- 239000002585 base Substances 0.000 description 130
- 125000000753 cycloalkyl group Chemical group 0.000 description 124
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 111
- 125000003342 alkenyl group Chemical group 0.000 description 97
- 238000006243 chemical reaction Methods 0.000 description 92
- 125000003368 amide group Chemical group 0.000 description 86
- 125000003282 alkyl amino group Chemical group 0.000 description 85
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 84
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 81
- 125000004093 cyano group Chemical group *C#N 0.000 description 79
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 74
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 72
- 150000002825 nitriles Chemical class 0.000 description 63
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 54
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 50
- 125000001188 haloalkyl group Chemical group 0.000 description 50
- 125000002837 carbocyclic group Chemical group 0.000 description 48
- 239000000543 intermediate Substances 0.000 description 48
- 125000004646 sulfenyl group Chemical group S(*)* 0.000 description 48
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 47
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 46
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 36
- 229910052799 carbon Inorganic materials 0.000 description 36
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 36
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical class OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 34
- 239000002904 solvent Substances 0.000 description 33
- 125000005647 linker group Chemical group 0.000 description 32
- 150000001721 carbon Chemical group 0.000 description 30
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 28
- 239000000243 solution Substances 0.000 description 28
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 27
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 27
- 239000011541 reaction mixture Substances 0.000 description 27
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 26
- 239000003513 alkali Substances 0.000 description 25
- 238000003756 stirring Methods 0.000 description 24
- 238000005406 washing Methods 0.000 description 23
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 22
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 22
- 229910052938 sodium sulfate Inorganic materials 0.000 description 22
- 235000011152 sodium sulphate Nutrition 0.000 description 22
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 21
- 238000005160 1H NMR spectroscopy Methods 0.000 description 21
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 21
- 239000002253 acid Substances 0.000 description 20
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 18
- 235000019439 ethyl acetate Nutrition 0.000 description 18
- 239000007787 solid Substances 0.000 description 18
- 239000000010 aprotic solvent Substances 0.000 description 17
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 16
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- 125000004043 oxo group Chemical group O=* 0.000 description 16
- 229910052760 oxygen Inorganic materials 0.000 description 16
- 239000000376 reactant Substances 0.000 description 16
- 238000010992 reflux Methods 0.000 description 16
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 15
- 239000007864 aqueous solution Substances 0.000 description 15
- 239000012043 crude product Substances 0.000 description 15
- 125000005843 halogen group Chemical group 0.000 description 15
- 239000000463 material Substances 0.000 description 15
- 239000001257 hydrogen Substances 0.000 description 14
- 229910052739 hydrogen Inorganic materials 0.000 description 14
- 239000003960 organic solvent Substances 0.000 description 14
- 125000001424 substituent group Chemical group 0.000 description 14
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 13
- 125000002757 morpholinyl group Chemical group 0.000 description 13
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 12
- 238000003810 ethyl acetate extraction Methods 0.000 description 12
- 238000004128 high performance liquid chromatography Methods 0.000 description 12
- 239000001301 oxygen Substances 0.000 description 12
- 125000004076 pyridyl group Chemical group 0.000 description 12
- 229910000104 sodium hydride Inorganic materials 0.000 description 12
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical compound S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 11
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 11
- 238000004440 column chromatography Methods 0.000 description 11
- 229910000037 hydrogen sulfide Inorganic materials 0.000 description 11
- 238000010898 silica gel chromatography Methods 0.000 description 11
- 150000001412 amines Chemical class 0.000 description 10
- 210000004027 cell Anatomy 0.000 description 10
- 125000002883 imidazolyl group Chemical group 0.000 description 10
- 125000000714 pyrimidinyl group Chemical group 0.000 description 10
- 229910052720 vanadium Inorganic materials 0.000 description 10
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 9
- 125000002877 alkyl aryl group Chemical group 0.000 description 9
- 125000005936 piperidyl group Chemical group 0.000 description 9
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 9
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 8
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 8
- QTBSBXVTEAMEQO-UHFFFAOYSA-N acetic acid Substances CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 8
- 238000004176 ammonification Methods 0.000 description 8
- 229910052786 argon Inorganic materials 0.000 description 8
- 125000003710 aryl alkyl group Chemical group 0.000 description 8
- 238000004108 freeze drying Methods 0.000 description 8
- 239000007789 gas Substances 0.000 description 8
- AFRJJFRNGGLMDW-UHFFFAOYSA-N lithium amide Chemical compound [Li+].[NH2-] AFRJJFRNGGLMDW-UHFFFAOYSA-N 0.000 description 8
- 229910052757 nitrogen Inorganic materials 0.000 description 8
- 239000000843 powder Substances 0.000 description 8
- 239000002994 raw material Substances 0.000 description 8
- 230000004044 response Effects 0.000 description 8
- 239000011734 sodium Substances 0.000 description 8
- 229910052708 sodium Inorganic materials 0.000 description 8
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 7
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 7
- 150000001335 aliphatic alkanes Chemical class 0.000 description 7
- 230000035578 autophosphorylation Effects 0.000 description 7
- 230000008859 change Effects 0.000 description 7
- 229940126543 compound 14 Drugs 0.000 description 7
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 7
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 7
- 239000012044 organic layer Substances 0.000 description 7
- 239000012312 sodium hydride Substances 0.000 description 7
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 description 6
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 239000000370 acceptor Substances 0.000 description 6
- 239000012267 brine Substances 0.000 description 6
- 230000003197 catalytic effect Effects 0.000 description 6
- 239000000284 extract Substances 0.000 description 6
- 238000000605 extraction Methods 0.000 description 6
- 125000002541 furyl group Chemical group 0.000 description 6
- 125000005842 heteroatom Chemical group 0.000 description 6
- NEXSMEBSBIABKL-UHFFFAOYSA-N hexamethyldisilane Chemical compound C[Si](C)(C)[Si](C)(C)C NEXSMEBSBIABKL-UHFFFAOYSA-N 0.000 description 6
- QNXSIUBBGPHDDE-UHFFFAOYSA-N indan-1-one Chemical compound C1=CC=C2C(=O)CCC2=C1 QNXSIUBBGPHDDE-UHFFFAOYSA-N 0.000 description 6
- 229910052740 iodine Inorganic materials 0.000 description 6
- 229910052744 lithium Inorganic materials 0.000 description 6
- HZVOZRGWRWCICA-UHFFFAOYSA-N methanediyl Chemical compound [CH2] HZVOZRGWRWCICA-UHFFFAOYSA-N 0.000 description 6
- 230000000630 rising effect Effects 0.000 description 6
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 6
- 238000003786 synthesis reaction Methods 0.000 description 6
- 230000004862 vasculogenesis Effects 0.000 description 6
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 5
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 5
- 102000053187 Glucuronidase Human genes 0.000 description 5
- 108010060309 Glucuronidase Proteins 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 5
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 5
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- 125000005037 alkyl phenyl group Chemical group 0.000 description 5
- 201000011510 cancer Diseases 0.000 description 5
- 239000000460 chlorine Substances 0.000 description 5
- 125000004803 chlorobenzyl group Chemical group 0.000 description 5
- 125000000068 chlorophenyl group Chemical group 0.000 description 5
- 125000000219 ethylidene group Chemical group [H]C(=[*])C([H])([H])[H] 0.000 description 5
- 150000002431 hydrogen Chemical class 0.000 description 5
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 5
- 239000011630 iodine Substances 0.000 description 5
- 125000004193 piperazinyl group Chemical group 0.000 description 5
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Substances [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 5
- 235000015320 potassium carbonate Nutrition 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 238000004007 reversed phase HPLC Methods 0.000 description 5
- 235000017557 sodium bicarbonate Nutrition 0.000 description 5
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 5
- 125000001544 thienyl group Chemical group 0.000 description 5
- FANCTJAFZSYTIS-IQUVVAJASA-N (1r,3s,5z)-5-[(2e)-2-[(1r,3as,7ar)-7a-methyl-1-[(2r)-4-(phenylsulfonimidoyl)butan-2-yl]-2,3,3a,5,6,7-hexahydro-1h-inden-4-ylidene]ethylidene]-4-methylidenecyclohexane-1,3-diol Chemical compound C([C@@H](C)[C@@H]1[C@]2(CCCC(/[C@@H]2CC1)=C\C=C\1C([C@@H](O)C[C@H](O)C/1)=C)C)CS(=N)(=O)C1=CC=CC=C1 FANCTJAFZSYTIS-IQUVVAJASA-N 0.000 description 4
- ZJSQZQMVXKZAGW-UHFFFAOYSA-N 2H-benzotriazol-4-ol hydrate Chemical compound O.OC1=CC=CC2=C1N=NN2 ZJSQZQMVXKZAGW-UHFFFAOYSA-N 0.000 description 4
- IHMQOBPGHZFGLC-UHFFFAOYSA-N 5,6-dimethoxy-2,3-dihydroinden-1-one Chemical compound C1=C(OC)C(OC)=CC2=C1C(=O)CC2 IHMQOBPGHZFGLC-UHFFFAOYSA-N 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- 238000005727 Friedel-Crafts reaction Methods 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- 125000002619 bicyclic group Chemical group 0.000 description 4
- 229910052794 bromium Inorganic materials 0.000 description 4
- 239000012141 concentrate Substances 0.000 description 4
- 235000008504 concentrate Nutrition 0.000 description 4
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 4
- RAFNCPHFRHZCPS-UHFFFAOYSA-N di(imidazol-1-yl)methanethione Chemical compound C1=CN=CN1C(=S)N1C=CN=C1 RAFNCPHFRHZCPS-UHFFFAOYSA-N 0.000 description 4
- 238000006073 displacement reaction Methods 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 125000004175 fluorobenzyl group Chemical group 0.000 description 4
- 125000001207 fluorophenyl group Chemical group 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 125000000842 isoxazolyl group Chemical group 0.000 description 4
- 150000002576 ketones Chemical class 0.000 description 4
- ZDNURMVOKAERHZ-UHFFFAOYSA-N n-(3-fluorophenyl)-6,7-dimethoxy-1,4-dihydroindeno[1,2-c]pyrazol-3-amine Chemical compound N=1NC=2C=3C=C(OC)C(OC)=CC=3CC=2C=1NC1=CC=CC(F)=C1 ZDNURMVOKAERHZ-UHFFFAOYSA-N 0.000 description 4
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- 238000010189 synthetic method Methods 0.000 description 4
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 4
- 230000004614 tumor growth Effects 0.000 description 4
- HBENZIXOGRCSQN-VQWWACLZSA-N (1S,2S,6R,14R,15R,16R)-5-(cyclopropylmethyl)-16-[(2S)-2-hydroxy-3,3-dimethylpentan-2-yl]-15-methoxy-13-oxa-5-azahexacyclo[13.2.2.12,8.01,6.02,14.012,20]icosa-8(20),9,11-trien-11-ol Chemical compound N1([C@@H]2CC=3C4=C(C(=CC=3)O)O[C@H]3[C@@]5(OC)CC[C@@]2([C@@]43CC1)C[C@@H]5[C@](C)(O)C(C)(C)CC)CC1CC1 HBENZIXOGRCSQN-VQWWACLZSA-N 0.000 description 3
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 description 3
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 3
- WGFNXGPBPIJYLI-UHFFFAOYSA-N 2,6-difluoro-3-[(3-fluorophenyl)sulfonylamino]-n-(3-methoxy-1h-pyrazolo[3,4-b]pyridin-5-yl)benzamide Chemical compound C1=C2C(OC)=NNC2=NC=C1NC(=O)C(C=1F)=C(F)C=CC=1NS(=O)(=O)C1=CC=CC(F)=C1 WGFNXGPBPIJYLI-UHFFFAOYSA-N 0.000 description 3
- HGINCPLSRVDWNT-UHFFFAOYSA-N Acrolein Chemical compound C=CC=O HGINCPLSRVDWNT-UHFFFAOYSA-N 0.000 description 3
- ZKHQWZAMYRWXGA-KQYNXXCUSA-N Adenosine triphosphate Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)[C@@H](O)[C@H]1O ZKHQWZAMYRWXGA-KQYNXXCUSA-N 0.000 description 3
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 3
- QGJOPFRUJISHPQ-UHFFFAOYSA-N Carbon disulfide Chemical compound S=C=S QGJOPFRUJISHPQ-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 3
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 3
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 3
- 150000003973 alkyl amines Chemical class 0.000 description 3
- 150000004982 aromatic amines Chemical class 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 3
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 3
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 229940125904 compound 1 Drugs 0.000 description 3
- 238000006352 cycloaddition reaction Methods 0.000 description 3
- 125000005265 dialkylamine group Chemical group 0.000 description 3
- 125000005594 diketone group Chemical group 0.000 description 3
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 3
- 239000006185 dispersion Substances 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 125000005241 heteroarylamino group Chemical group 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 3
- GRHBQAYDJPGGLF-UHFFFAOYSA-N isothiocyanic acid Chemical compound N=C=S GRHBQAYDJPGGLF-UHFFFAOYSA-N 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000002480 mineral oil Substances 0.000 description 3
- 235000010446 mineral oil Nutrition 0.000 description 3
- QKFJKGMPGYROCL-UHFFFAOYSA-N phenyl isothiocyanate Chemical compound S=C=NC1=CC=CC=C1 QKFJKGMPGYROCL-UHFFFAOYSA-N 0.000 description 3
- 239000002953 phosphate buffered saline Substances 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 229940002612 prodrug Drugs 0.000 description 3
- 239000000651 prodrug Substances 0.000 description 3
- 125000004353 pyrazol-1-yl group Chemical group [H]C1=NN(*)C([H])=C1[H] 0.000 description 3
- 150000003217 pyrazoles Chemical class 0.000 description 3
- 230000019491 signal transduction Effects 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 229960001866 silicon dioxide Drugs 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- 238000004809 thin layer chromatography Methods 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 230000002792 vascular Effects 0.000 description 3
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 2
- AEVBPXDFDKBGLT-YOUFYPILSA-N (2s,3s,4r,5r)-n-[2-[4-(diethoxyphosphorylmethyl)anilino]-2-oxoethyl]-5-(2,4-dioxopyrimidin-1-yl)-3,4-dihydroxyoxolane-2-carboxamide Chemical compound C1=CC(CP(=O)(OCC)OCC)=CC=C1NC(=O)CNC(=O)[C@@H]1[C@@H](O)[C@@H](O)[C@H](N2C(NC(=O)C=C2)=O)O1 AEVBPXDFDKBGLT-YOUFYPILSA-N 0.000 description 2
- VIMMECPCYZXUCI-MIMFYIINSA-N (4s,6r)-6-[(1e)-4,4-bis(4-fluorophenyl)-3-(1-methyltetrazol-5-yl)buta-1,3-dienyl]-4-hydroxyoxan-2-one Chemical compound CN1N=NN=C1C(\C=C\[C@@H]1OC(=O)C[C@@H](O)C1)=C(C=1C=CC(F)=CC=1)C1=CC=C(F)C=C1 VIMMECPCYZXUCI-MIMFYIINSA-N 0.000 description 2
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 2
- HDBACITVPQEAGG-UHFFFAOYSA-N 1-fluoro-3-isothiocyanatobenzene Chemical compound FC1=CC=CC(N=C=S)=C1 HDBACITVPQEAGG-UHFFFAOYSA-N 0.000 description 2
- XHLHPRDBBAGVEG-UHFFFAOYSA-N 1-tetralone Chemical compound C1=CC=C2C(=O)CCCC2=C1 XHLHPRDBBAGVEG-UHFFFAOYSA-N 0.000 description 2
- HBEDSQVIWPRPAY-UHFFFAOYSA-N 2,3-dihydrobenzofuran Chemical compound C1=CC=C2OCCC2=C1 HBEDSQVIWPRPAY-UHFFFAOYSA-N 0.000 description 2
- 125000006282 2-chlorobenzyl group Chemical group [H]C1=C([H])C(Cl)=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 125000004847 2-fluorobenzyl group Chemical group [H]C1=C([H])C(F)=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 125000006179 2-methyl benzyl group Chemical group [H]C1=C([H])C(=C(C([H])=C1[H])C([H])([H])*)C([H])([H])[H] 0.000 description 2
- QISAUDWTBBNJIR-UHFFFAOYSA-N 2-phenylmethoxyacetyl chloride Chemical compound ClC(=O)COCC1=CC=CC=C1 QISAUDWTBBNJIR-UHFFFAOYSA-N 0.000 description 2
- 125000006275 3-bromophenyl group Chemical group [H]C1=C([H])C(Br)=C([H])C(*)=C1[H] 0.000 description 2
- 125000003852 3-chlorobenzyl group Chemical group [H]C1=C([H])C(=C([H])C(Cl)=C1[H])C([H])([H])* 0.000 description 2
- 125000004179 3-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(Cl)=C1[H] 0.000 description 2
- 125000004180 3-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(F)=C1[H] 0.000 description 2
- 125000006180 3-methyl benzyl group Chemical group [H]C1=C([H])C(=C([H])C(=C1[H])C([H])([H])[H])C([H])([H])* 0.000 description 2
- WMDAUVLSCBKCBO-UHFFFAOYSA-N 5,6-dihydroxy-2,3-dihydroinden-1-one Chemical compound C1=C(O)C(O)=CC2=C1C(=O)CC2 WMDAUVLSCBKCBO-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 2
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 2
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 2
- 102000016354 Glucuronosyltransferase Human genes 0.000 description 2
- 108010092364 Glucuronosyltransferase Proteins 0.000 description 2
- 108010044467 Isoenzymes Proteins 0.000 description 2
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 2
- 102000007399 Nuclear hormone receptor Human genes 0.000 description 2
- 108020005497 Nuclear hormone receptor Proteins 0.000 description 2
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical class [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229960000583 acetic acid Drugs 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 2
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 2
- 238000011122 anti-angiogenic therapy Methods 0.000 description 2
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 235000011089 carbon dioxide Nutrition 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 230000012292 cell migration Effects 0.000 description 2
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 2
- 229940125878 compound 36 Drugs 0.000 description 2
- 238000009833 condensation Methods 0.000 description 2
- 230000005494 condensation Effects 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 238000011262 co‐therapy Methods 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 2
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- 150000002118 epoxides Chemical class 0.000 description 2
- LBAQSKZHMLAFHH-UHFFFAOYSA-N ethoxyethane;hydron;chloride Chemical compound Cl.CCOCC LBAQSKZHMLAFHH-UHFFFAOYSA-N 0.000 description 2
- 239000002024 ethyl acetate extract Substances 0.000 description 2
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- FVIZARNDLVOMSU-UHFFFAOYSA-N ginsenoside K Natural products C1CC(C2(CCC3C(C)(C)C(O)CCC3(C)C2CC2O)C)(C)C2C1C(C)(CCC=C(C)C)OC1OC(CO)C(O)C(O)C1O FVIZARNDLVOMSU-UHFFFAOYSA-N 0.000 description 2
- 229930182480 glucuronide Natural products 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- KTUFNOKKBVMGRW-UHFFFAOYSA-N imatinib Chemical compound C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 KTUFNOKKBVMGRW-UHFFFAOYSA-N 0.000 description 2
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 230000009878 intermolecular interaction Effects 0.000 description 2
- 125000005956 isoquinolyl group Chemical group 0.000 description 2
- 125000001786 isothiazolyl group Chemical group 0.000 description 2
- 229940043355 kinase inhibitor Drugs 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 239000002207 metabolite Substances 0.000 description 2
- UAEPNZWRGJTJPN-UHFFFAOYSA-N methylcyclohexane Chemical compound CC1CCCCC1 UAEPNZWRGJTJPN-UHFFFAOYSA-N 0.000 description 2
- GRVDJDISBSALJP-UHFFFAOYSA-N methyloxidanyl Chemical group [O]C GRVDJDISBSALJP-UHFFFAOYSA-N 0.000 description 2
- CMAOIURPBUCSJE-UHFFFAOYSA-N n-phenyl-1h-pyrazol-5-amine Chemical class C=1C=CC=CC=1NC=1C=CNN=1 CMAOIURPBUCSJE-UHFFFAOYSA-N 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 2
- 150000003053 piperidines Chemical class 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 235000019260 propionic acid Nutrition 0.000 description 2
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 2
- 125000005493 quinolyl group Chemical group 0.000 description 2
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 2
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 2
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000002390 rotary evaporation Methods 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 229940124530 sulfonamide Drugs 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 125000004149 thio group Chemical group *S* 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 description 2
- 239000005483 tyrosine kinase inhibitor Substances 0.000 description 2
- 230000029663 wound healing Effects 0.000 description 2
- OJZQOQNSUZLSMV-UHFFFAOYSA-N (3-aminophenyl)methanol Chemical compound NC1=CC=CC(CO)=C1 OJZQOQNSUZLSMV-UHFFFAOYSA-N 0.000 description 1
- MPDDTAJMJCESGV-CTUHWIOQSA-M (3r,5r)-7-[2-(4-fluorophenyl)-5-[methyl-[(1r)-1-phenylethyl]carbamoyl]-4-propan-2-ylpyrazol-3-yl]-3,5-dihydroxyheptanoate Chemical compound C1([C@@H](C)N(C)C(=O)C2=NN(C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C2C(C)C)C=2C=CC(F)=CC=2)=CC=CC=C1 MPDDTAJMJCESGV-CTUHWIOQSA-M 0.000 description 1
- NXLNNXIXOYSCMB-UHFFFAOYSA-N (4-nitrophenyl) carbonochloridate Chemical compound [O-][N+](=O)C1=CC=C(OC(Cl)=O)C=C1 NXLNNXIXOYSCMB-UHFFFAOYSA-N 0.000 description 1
- VUDZSIYXZUYWSC-DBRKOABJSA-N (4r)-1-[(2r,4r,5r)-3,3-difluoro-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-4-hydroxy-1,3-diazinan-2-one Chemical compound FC1(F)[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)N[C@H](O)CC1 VUDZSIYXZUYWSC-DBRKOABJSA-N 0.000 description 1
- CXWGKAYMVASWDQ-UHFFFAOYSA-N 1,2-dithiane Chemical compound C1CCSSC1 CXWGKAYMVASWDQ-UHFFFAOYSA-N 0.000 description 1
- DEOWHQAFPBKSMV-UHFFFAOYSA-N 1,5-dihydroxypentan-3-one Chemical compound OCCC(=O)CCO DEOWHQAFPBKSMV-UHFFFAOYSA-N 0.000 description 1
- SZCBDIVMCGFVPW-UHFFFAOYSA-N 1-[4-(aminomethyl)-2,6-di(propan-2-yl)phenyl]-3-[1-butyl-4-(3-methoxyphenyl)-2-oxo-1,8-naphthyridin-3-yl]urea;hydrochloride Chemical compound Cl.CC(C)C=1C=C(CN)C=C(C(C)C)C=1NC(=O)NC=1C(=O)N(CCCC)C2=NC=CC=C2C=1C1=CC=CC(OC)=C1 SZCBDIVMCGFVPW-UHFFFAOYSA-N 0.000 description 1
- XTIGGAHUZJWQMD-UHFFFAOYSA-N 1-chloro-2-methoxyethane Chemical compound COCCCl XTIGGAHUZJWQMD-UHFFFAOYSA-N 0.000 description 1
- WGXCKFMVBAOIFH-UHFFFAOYSA-N 1-chloro-3-isothiocyanatobenzene Chemical compound ClC1=CC=CC(N=C=S)=C1 WGXCKFMVBAOIFH-UHFFFAOYSA-N 0.000 description 1
- VZAWCLCJGSBATP-UHFFFAOYSA-N 1-cycloundecyl-1,2-diazacycloundecane Chemical compound C1CCCCCCCCCC1N1NCCCCCCCCC1 VZAWCLCJGSBATP-UHFFFAOYSA-N 0.000 description 1
- QDKWLJJOYIFEBS-UHFFFAOYSA-N 1-fluoro-4-$l^{1}-oxidanylbenzene Chemical group [O]C1=CC=C(F)C=C1 QDKWLJJOYIFEBS-UHFFFAOYSA-N 0.000 description 1
- VBOHCKYFZJZSJR-UHFFFAOYSA-N 2-amino-2-chloroethanol Chemical compound NC(Cl)CO VBOHCKYFZJZSJR-UHFFFAOYSA-N 0.000 description 1
- 125000000979 2-amino-2-oxoethyl group Chemical group [H]C([*])([H])C(=O)N([H])[H] 0.000 description 1
- 125000006280 2-bromobenzyl group Chemical group [H]C1=C([H])C(Br)=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000006276 2-bromophenyl group Chemical group [H]C1=C([H])C(Br)=C(*)C([H])=C1[H] 0.000 description 1
- UFKIPBAVGKSSTN-UHFFFAOYSA-N 2-chloroethyl ethyl hydrogen phosphate Chemical compound CCOP(O)(=O)OCCCl UFKIPBAVGKSSTN-UHFFFAOYSA-N 0.000 description 1
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 description 1
- HHURGDWHVFFYAU-UHFFFAOYSA-N 2-fluoro-4h-1,3-benzodioxine Chemical compound C1=CC=C2OC(F)OCC2=C1 HHURGDWHVFFYAU-UHFFFAOYSA-N 0.000 description 1
- 125000004198 2-fluorophenyl group Chemical group [H]C1=C([H])C(F)=C(*)C([H])=C1[H] 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- JJKWHOSQTYYFAE-UHFFFAOYSA-N 2-methoxyacetyl chloride Chemical compound COCC(Cl)=O JJKWHOSQTYYFAE-UHFFFAOYSA-N 0.000 description 1
- RXJJIFUOUWVKTA-UHFFFAOYSA-N 2-methyl-4-oxobutanoic acid Chemical compound OC(=O)C(C)CC=O RXJJIFUOUWVKTA-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- DGMOBVGABMBZSB-UHFFFAOYSA-N 2-methylpropanoyl chloride Chemical compound CC(C)C(Cl)=O DGMOBVGABMBZSB-UHFFFAOYSA-N 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000006479 2-pyridyl methyl group Chemical group [H]C1=C([H])C([H])=C([H])C(=N1)C([H])([H])* 0.000 description 1
- 125000006499 2-trifluoromethoxy benzyl group Chemical group [H]C1=C([H])C(OC(F)(F)F)=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000006494 2-trifluoromethyl benzyl group Chemical group [H]C1=C([H])C([H])=C(C(=C1[H])C([H])([H])*)C(F)(F)F 0.000 description 1
- 125000005809 3,4,5-trimethoxyphenyl group Chemical group [H]C1=C(OC([H])([H])[H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 description 1
- 125000003762 3,4-dimethoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 description 1
- 125000006185 3,4-dimethyl benzyl group Chemical group [H]C1=C(C([H])=C(C(=C1[H])C([H])([H])[H])C([H])([H])[H])C([H])([H])* 0.000 description 1
- QXDOFVVNXBGLKK-UHFFFAOYSA-N 3-Isoxazolidinone Chemical compound OC1=NOCC1 QXDOFVVNXBGLKK-UHFFFAOYSA-N 0.000 description 1
- HCLQARMRCPEALF-DNQXCXABSA-N 3-[[(2r)-2-[(1r)-2-[[1-(1-benzothiophen-2-yl)-2-methylpropan-2-yl]amino]-1-hydroxyethyl]pyrrolidin-1-yl]methyl]benzonitrile Chemical compound C([C@@H]1[C@H](O)CNC(C)(CC=2SC3=CC=CC=C3C=2)C)CCN1CC1=CC=CC(C#N)=C1 HCLQARMRCPEALF-DNQXCXABSA-N 0.000 description 1
- 125000000984 3-chloro-4-fluorobenzyl group Chemical group [H]C1=C(F)C(Cl)=C([H])C(=C1[H])C([H])([H])* 0.000 description 1
- QZVQQUVWFIZUBQ-UHFFFAOYSA-N 3-fluoroaniline Chemical compound NC1=CC=CC(F)=C1 QZVQQUVWFIZUBQ-UHFFFAOYSA-N 0.000 description 1
- 125000006284 3-fluorobenzyl group Chemical group [H]C1=C([H])C(=C([H])C(F)=C1[H])C([H])([H])* 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- BNPOTXLWPZOESZ-UHFFFAOYSA-N 4-(chloromethyl)-2,2-dimethyl-1,3-dioxolane Chemical compound CC1(C)OCC(CCl)O1 BNPOTXLWPZOESZ-UHFFFAOYSA-N 0.000 description 1
- 125000004800 4-bromophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Br 0.000 description 1
- 125000000242 4-chlorobenzoyl group Chemical group ClC1=CC=C(C(=O)*)C=C1 0.000 description 1
- 125000004176 4-fluorobenzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1F)C([H])([H])* 0.000 description 1
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 description 1
- 125000006181 4-methyl benzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000004863 4-trifluoromethoxyphenyl group Chemical group [H]C1=C([H])C(OC(F)(F)F)=C([H])C([H])=C1* 0.000 description 1
- 125000004199 4-trifluoromethylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C(F)(F)F 0.000 description 1
- GSAHFRQIQURXHP-UHFFFAOYSA-N 5,6-diethoxy-2,3-dihydroinden-1-one Chemical compound C1=C(OCC)C(OCC)=CC2=C1C(=O)CC2 GSAHFRQIQURXHP-UHFFFAOYSA-N 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- NXBUZUXNLSLTRN-UHFFFAOYSA-N CCBrCC Chemical compound CCBrCC NXBUZUXNLSLTRN-UHFFFAOYSA-N 0.000 description 1
- GPYKQOCYDCMGOA-UHFFFAOYSA-N CCCCCC[O] Chemical compound CCCCCC[O] GPYKQOCYDCMGOA-UHFFFAOYSA-N 0.000 description 1
- 229940126074 CDK kinase inhibitor Drugs 0.000 description 1
- QCMHGCDOZLWPOT-FMNCTDSISA-N COC1=C(CC[C@@H]2CCC3=C(C2)C=CC(=C3)[C@H]2CC[C@](N)(CO)C2)C=CC=C1 Chemical compound COC1=C(CC[C@@H]2CCC3=C(C2)C=CC(=C3)[C@H]2CC[C@](N)(CO)C2)C=CC=C1 QCMHGCDOZLWPOT-FMNCTDSISA-N 0.000 description 1
- 101100421901 Caenorhabditis elegans sos-1 gene Proteins 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 102100034770 Cyclin-dependent kinase inhibitor 3 Human genes 0.000 description 1
- 241000790917 Dioxys <bee> Species 0.000 description 1
- 101100015729 Drosophila melanogaster drk gene Proteins 0.000 description 1
- 241000709661 Enterovirus Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 108090000386 Fibroblast Growth Factor 1 Proteins 0.000 description 1
- 102100031706 Fibroblast growth factor 1 Human genes 0.000 description 1
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 description 1
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000945639 Homo sapiens Cyclin-dependent kinase inhibitor 3 Proteins 0.000 description 1
- 101000692455 Homo sapiens Platelet-derived growth factor receptor beta Proteins 0.000 description 1
- 206010020651 Hyperkinesia Diseases 0.000 description 1
- 208000000269 Hyperkinesis Diseases 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 239000005517 L01XE01 - Imatinib Substances 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 238000006086 Paal-Knorr synthesis reaction Methods 0.000 description 1
- 208000037273 Pathologic Processes Diseases 0.000 description 1
- 102000003993 Phosphatidylinositol 3-kinases Human genes 0.000 description 1
- 108090000430 Phosphatidylinositol 3-kinases Proteins 0.000 description 1
- 108010056751 Phospholipase C gamma Proteins 0.000 description 1
- 102000004422 Phospholipase C gamma Human genes 0.000 description 1
- 102100026547 Platelet-derived growth factor receptor beta Human genes 0.000 description 1
- KDCGOANMDULRCW-UHFFFAOYSA-N Purine Natural products N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 1
- 108091005682 Receptor kinases Proteins 0.000 description 1
- 208000015634 Rectal Neoplasms Diseases 0.000 description 1
- 206010039361 Sacroiliitis Diseases 0.000 description 1
- 102000013275 Somatomedins Human genes 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 239000005864 Sulphur Substances 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 102000014384 Type C Phospholipases Human genes 0.000 description 1
- 108010079194 Type C Phospholipases Proteins 0.000 description 1
- LSKFNBLMCNRDGE-UHFFFAOYSA-N [Cl].C(C)S(=O)(=O)N Chemical compound [Cl].C(C)S(=O)(=O)N LSKFNBLMCNRDGE-UHFFFAOYSA-N 0.000 description 1
- GLRAHDCHUZLKKC-UHFFFAOYSA-N acetonitrile;2,2,2-trifluoroacetic acid;hydrate Chemical compound O.CC#N.OC(=O)C(F)(F)F GLRAHDCHUZLKKC-UHFFFAOYSA-N 0.000 description 1
- 125000001539 acetonyl group Chemical group [H]C([H])([H])C(=O)C([H])([H])* 0.000 description 1
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 1
- 239000012346 acetyl chloride Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 150000001345 alkine derivatives Chemical class 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 125000002431 aminoalkoxy group Chemical group 0.000 description 1
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 230000036592 analgesia Effects 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 239000003472 antidiabetic agent Substances 0.000 description 1
- 210000000709 aorta Anatomy 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 150000008365 aromatic ketones Chemical class 0.000 description 1
- 125000001769 aryl amino group Chemical group 0.000 description 1
- 150000001500 aryl chlorides Chemical class 0.000 description 1
- 125000005110 aryl thio group Chemical group 0.000 description 1
- 125000005165 aryl thioxy group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 125000004619 benzopyranyl group Chemical group O1C(C=CC2=C1C=CC=C2)* 0.000 description 1
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical compound ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- DKEKURXRUXRNES-UHFFFAOYSA-N bis(1h-pyrrol-2-yl)methanone Chemical compound C=1C=CNC=1C(=O)C1=CC=CN1 DKEKURXRUXRNES-UHFFFAOYSA-N 0.000 description 1
- HMKCSFHWMJHMTG-UHFFFAOYSA-N bis(furan-2-yl)methanone Chemical compound C=1C=COC=1C(=O)C1=CC=CO1 HMKCSFHWMJHMTG-UHFFFAOYSA-N 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- OSVHLUXLWQLPIY-KBAYOESNSA-N butyl 2-[(6aR,9R,10aR)-1-hydroxy-9-(hydroxymethyl)-6,6-dimethyl-6a,7,8,9,10,10a-hexahydrobenzo[c]chromen-3-yl]-2-methylpropanoate Chemical compound C(CCC)OC(C(C)(C)C1=CC(=C2[C@H]3[C@H](C(OC2=C1)(C)C)CC[C@H](C3)CO)O)=O OSVHLUXLWQLPIY-KBAYOESNSA-N 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- 230000036952 cancer formation Effects 0.000 description 1
- MOIPGXQKZSZOQX-UHFFFAOYSA-N carbonyl bromide Chemical compound BrC(Br)=O MOIPGXQKZSZOQX-UHFFFAOYSA-N 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 230000035605 chemotaxis Effects 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- GLUYADGKGBGXRV-UHFFFAOYSA-N chloro dihydrogen phosphate Chemical compound OP(O)(=O)OCl GLUYADGKGBGXRV-UHFFFAOYSA-N 0.000 description 1
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 description 1
- 230000004087 circulation Effects 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 235000019628 coolness Nutrition 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 239000002875 cyclin dependent kinase inhibitor Substances 0.000 description 1
- 229940043378 cyclin-dependent kinase inhibitor Drugs 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- URYYVOIYTNXXBN-UPHRSURJSA-N cyclooctene Chemical compound C1CCC\C=C/CC1 URYYVOIYTNXXBN-UPHRSURJSA-N 0.000 description 1
- 239000004913 cyclooctene Substances 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 230000017858 demethylation Effects 0.000 description 1
- 238000010520 demethylation reaction Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- LGTLXDJOAJDFLR-UHFFFAOYSA-N diethyl chlorophosphate Chemical compound CCOP(Cl)(=O)OCC LGTLXDJOAJDFLR-UHFFFAOYSA-N 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 125000005879 dioxolanyl group Chemical group 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- LOZWAPSEEHRYPG-UHFFFAOYSA-N dithiane Natural products C1CSCCS1 LOZWAPSEEHRYPG-UHFFFAOYSA-N 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000036267 drug metabolism Effects 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- RIFGWPKJUGCATF-UHFFFAOYSA-N ethyl chloroformate Chemical compound CCOC(Cl)=O RIFGWPKJUGCATF-UHFFFAOYSA-N 0.000 description 1
- 125000006260 ethylaminocarbonyl group Chemical group [H]N(C(*)=O)C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008175 fetal development Effects 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 125000006332 fluoro benzoyl group Chemical group 0.000 description 1
- 150000002240 furans Chemical class 0.000 description 1
- JKFAIQOWCVVSKC-UHFFFAOYSA-N furazan Chemical compound C=1C=NON=1 JKFAIQOWCVVSKC-UHFFFAOYSA-N 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 229940080856 gleevec Drugs 0.000 description 1
- 229940097043 glucuronic acid Drugs 0.000 description 1
- 230000023611 glucuronidation Effects 0.000 description 1
- 150000008134 glucuronides Chemical class 0.000 description 1
- 101150098203 grb2 gene Proteins 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 239000003630 growth substance Substances 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- VKYKSIONXSXAKP-UHFFFAOYSA-N hexamethylenetetramine Chemical compound C1N(C2)CN3CN1CN2C3 VKYKSIONXSXAKP-UHFFFAOYSA-N 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 125000001183 hydrocarbyl group Chemical group 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 208000013403 hyperactivity Diseases 0.000 description 1
- 229940126904 hypoglycaemic agent Drugs 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 229960002411 imatinib Drugs 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- 125000002636 imidazolinyl group Chemical group 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000002584 immunomodulator Effects 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 1
- HOBCFUWDNJPFHB-UHFFFAOYSA-N indolizine Chemical compound C1=CC=CN2C=CC=C21 HOBCFUWDNJPFHB-UHFFFAOYSA-N 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- QWXYZCJEXYQNEI-OSZHWHEXSA-N intermediate I Chemical compound COC(=O)[C@@]1(C=O)[C@H]2CC=[N+](C\C2=C\C)CCc2c1[nH]c1ccccc21 QWXYZCJEXYQNEI-OSZHWHEXSA-N 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000006142 intramolecular cycloaddition reaction Methods 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- 150000002561 ketenes Chemical class 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M methanesulfonate group Chemical class CS(=O)(=O)[O-] AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- SRXOJMOGPYFZKC-UHFFFAOYSA-N methyl 4-chloro-4-oxobutanoate Chemical compound COC(=O)CCC(Cl)=O SRXOJMOGPYFZKC-UHFFFAOYSA-N 0.000 description 1
- HAMGRBXTJNITHG-UHFFFAOYSA-N methyl isocyanate Chemical compound CN=C=O HAMGRBXTJNITHG-UHFFFAOYSA-N 0.000 description 1
- JZMJDSHXVKJFKW-UHFFFAOYSA-M methyl sulfate(1-) Chemical compound COS([O-])(=O)=O JZMJDSHXVKJFKW-UHFFFAOYSA-M 0.000 description 1
- GYNNXHKOJHMOHS-UHFFFAOYSA-N methyl-cycloheptane Natural products CC1CCCCCC1 GYNNXHKOJHMOHS-UHFFFAOYSA-N 0.000 description 1
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 description 1
- MZVYSWVJXQYPOT-UHFFFAOYSA-N methylsulfanylimino(oxo)methane Chemical compound CSN=C=O MZVYSWVJXQYPOT-UHFFFAOYSA-N 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 239000003226 mitogen Substances 0.000 description 1
- 230000002073 mitogenetic effect Effects 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 230000037257 muscle growth Effects 0.000 description 1
- JFCHSQDLLFJHOA-UHFFFAOYSA-N n,n-dimethylsulfamoyl chloride Chemical compound CN(C)S(Cl)(=O)=O JFCHSQDLLFJHOA-UHFFFAOYSA-N 0.000 description 1
- GVOISEJVFFIGQE-YCZSINBZSA-N n-[(1r,2s,5r)-5-[methyl(propan-2-yl)amino]-2-[(3s)-2-oxo-3-[[6-(trifluoromethyl)quinazolin-4-yl]amino]pyrrolidin-1-yl]cyclohexyl]acetamide Chemical compound CC(=O)N[C@@H]1C[C@H](N(C)C(C)C)CC[C@@H]1N1C(=O)[C@@H](NC=2C3=CC(=CC=C3N=CN=2)C(F)(F)F)CC1 GVOISEJVFFIGQE-YCZSINBZSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- XGXNTJHZPBRBHJ-UHFFFAOYSA-N n-phenylpyrimidin-2-amine Chemical class N=1C=CC=NC=1NC1=CC=CC=C1 XGXNTJHZPBRBHJ-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004923 naphthylmethyl group Chemical group C1(=CC=CC2=CC=CC=C12)C* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000000324 neuroprotective effect Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 231100000956 nontoxicity Toxicity 0.000 description 1
- 125000003261 o-tolyl group Chemical group [H]C1=C([H])C(*)=C(C([H])=C1[H])C([H])([H])[H] 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- BHAAPTBBJKJZER-UHFFFAOYSA-N p-anisidine Chemical compound COC1=CC=C(N)C=C1 BHAAPTBBJKJZER-UHFFFAOYSA-N 0.000 description 1
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 description 1
- 125000001037 p-tolyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000009054 pathological process Effects 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- AHWALFGBDFAJAI-UHFFFAOYSA-N phenyl carbonochloridate Chemical compound ClC(=O)OC1=CC=CC=C1 AHWALFGBDFAJAI-UHFFFAOYSA-N 0.000 description 1
- DGTNSSLYPYDJGL-UHFFFAOYSA-N phenyl isocyanate Chemical compound O=C=NC1=CC=CC=C1 DGTNSSLYPYDJGL-UHFFFAOYSA-N 0.000 description 1
- 125000003884 phenylalkyl group Chemical group 0.000 description 1
- 125000004344 phenylpropyl group Chemical group 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- IVRIRQXJSNCSPQ-UHFFFAOYSA-N propan-2-yl carbonochloridate Chemical class CC(C)OC(Cl)=O IVRIRQXJSNCSPQ-UHFFFAOYSA-N 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- LVTJOONKWUXEFR-FZRMHRINSA-N protoneodioscin Natural products O(C[C@@H](CC[C@]1(O)[C@H](C)[C@@H]2[C@]3(C)[C@H]([C@H]4[C@@H]([C@]5(C)C(=CC4)C[C@@H](O[C@@H]4[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@@H](O)[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@H](CO)O4)CC5)CC3)C[C@@H]2O1)C)[C@H]1[C@H](O)[C@H](O)[C@H](O)[C@@H](CO)O1 LVTJOONKWUXEFR-FZRMHRINSA-N 0.000 description 1
- 230000001185 psoriatic effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000002755 pyrazolinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000005344 pyridylmethyl group Chemical group [H]C1=C([H])C([H])=C([H])C(=N1)C([H])([H])* 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 125000001422 pyrrolinyl group Chemical group 0.000 description 1
- 150000004728 pyruvic acid derivatives Chemical class 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 150000003252 quinoxalines Chemical class 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 206010038038 rectal cancer Diseases 0.000 description 1
- 201000001275 rectum cancer Diseases 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000013049 sediment Substances 0.000 description 1
- 239000000333 selective estrogen receptor modulator Substances 0.000 description 1
- 229940095743 selective estrogen receptor modulator Drugs 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- VGKDLMBJGBXTGI-SJCJKPOMSA-N sertraline Chemical compound C1([C@@H]2CC[C@@H](C3=CC=CC=C32)NC)=CC=C(Cl)C(Cl)=C1 VGKDLMBJGBXTGI-SJCJKPOMSA-N 0.000 description 1
- 229960002073 sertraline Drugs 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 210000000329 smooth muscle myocyte Anatomy 0.000 description 1
- 239000012279 sodium borohydride Substances 0.000 description 1
- 229910000033 sodium borohydride Inorganic materials 0.000 description 1
- MFBOGIVSZKQAPD-UHFFFAOYSA-M sodium butyrate Chemical compound [Na+].CCCC([O-])=O MFBOGIVSZKQAPD-UHFFFAOYSA-M 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 210000003518 stress fiber Anatomy 0.000 description 1
- RINCXYDBBGOEEQ-UHFFFAOYSA-N succinic anhydride Chemical compound O=C1CCC(=O)O1 RINCXYDBBGOEEQ-UHFFFAOYSA-N 0.000 description 1
- FDDDEECHVMSUSB-UHFFFAOYSA-N sulfanilamide Chemical compound NC1=CC=C(S(N)(=O)=O)C=C1 FDDDEECHVMSUSB-UHFFFAOYSA-N 0.000 description 1
- 150000003456 sulfonamides Chemical class 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- YJBKVPRVZAQTPY-UHFFFAOYSA-J tetrachlorostannane;dihydrate Chemical compound O.O.Cl[Sn](Cl)(Cl)Cl YJBKVPRVZAQTPY-UHFFFAOYSA-J 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000002769 thiazolinyl group Chemical group 0.000 description 1
- YUKQRDCYNOVPGJ-UHFFFAOYSA-N thioacetamide Chemical compound CC(N)=S YUKQRDCYNOVPGJ-UHFFFAOYSA-N 0.000 description 1
- DLFVBJFMPXGRIB-UHFFFAOYSA-N thioacetamide Natural products CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 1
- 125000004568 thiomorpholinyl group Chemical group 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000027 toxicology Toxicity 0.000 description 1
- 108091008578 transmembrane receptors Proteins 0.000 description 1
- 102000027257 transmembrane receptors Human genes 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 1
- 125000005034 trifluormethylthio group Chemical group FC(S*)(F)F 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 150000004917 tyrosine kinase inhibitor derivatives Chemical class 0.000 description 1
- 125000001493 tyrosinyl group Chemical group [H]OC1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
- 239000002676 xenobiotic agent Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/645—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having two nitrogen atoms as the only ring hetero atoms
- C07F9/6503—Five-membered rings
- C07F9/65031—Five-membered rings having the nitrogen atoms in the positions 1 and 2
- C07F9/65038—Five-membered rings having the nitrogen atoms in the positions 1 and 2 condensed with carbocyclic rings or carbocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/54—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/54—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings condensed with carbocyclic rings or ring systems
- C07D231/56—Benzopyrazoles; Hydrogenated benzopyrazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/64—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms, e.g. histidine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oncology (AREA)
- Rheumatology (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Biochemistry (AREA)
- Physical Education & Sports Medicine (AREA)
- Vascular Medicine (AREA)
- Pulmonology (AREA)
- Immunology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Ophthalmology & Optometry (AREA)
- Hematology (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Plural Heterocyclic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Saccharide Compounds (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Materials For Medical Uses (AREA)
Abstract
本发明涉及用作血小板-衍生的生长因子受体(PDGF-R)激酶的抑制剂的N-取代的三环3-氨基吡唑衍生物,以及制备所述衍生物的方法。本发明还涉及包含本发明化合物的药用组合物,以及治疗疾病(如肿瘤)和其它细胞增殖性疾病的方法。
Description
相互参照
本国际申请要求同时待审的美国专利申请系列号60/380,735(2002年5月15日提交)的优先权,其全部内容和全部目的通过引用结合到本文中。
发明领域
本发明涉及一系列新的N-取代的三环3-氨基吡唑化合物及此类化合物治疗细胞增殖性疾病,如肿瘤、再狭窄、类风湿性关节炎、糖尿病性视网膜病等的用途。更具体地说,所述化合物为PDGF受体酪氨酸激酶的抑制剂。
发明背景
累积的证据支持这样一个概念,即癌细胞的生长控制的丧失涉及信号途径的紊乱,所述信号途径在正常细胞中受生长调节因子的控制。血小板-衍生的生长因子(PDGF)为一种结缔组织细胞促细胞分裂剂,它与肿瘤发生有关(Ostman和Heldin,Adv.Can.Res.,80:1-38,2001,及其中的参考文献),并且是血管生成的复杂过程的一个重要参与者,而血管生成对肿瘤生长来说是极其重要的。
PDGF通过结合于其特异性受体(PDGF-R)发挥其细胞作用。
PDGF-R是一种跨膜受体酪氨酸激酶(RTK)。它由两种同工酶α和β组成。这些受体的每一种具有一个特征为5个免疫球蛋白-样结构域的细胞外部分和一个具有一个酪氨酸激酶结构域的细胞内部分。含有α和β两者的受体与促有丝分裂的活性、刺激细胞边缘波动并使其失去应力纤维有关。只有含β的受体与趋化性和肌动蛋白再组织有关(Heldin,C-H,EMBO Journal 11:4251-4259,1992)。
PDGF与PDGF-R的结合导致PDGF-R受体的两个亚单位的二聚作用,由此引起细胞质的结构域中的特异性酪氨酸残基上的每个亚单位的自磷酸化作用。自磷酸化作用引起激酶活性增加,并为大量具有SH2结构域的信号分子,如Grb2/Sos1、PLC-γ、GAP、PI-3激酶和Src产生停靠位点。(Heldin等,Biochem.Acta 1378:F79-113,1998,及其中的参考文献)。一旦结合于PDGF-R,这些含SH2结构域的信号分子启动信号转导途径,这些途径参与不同的细胞反应,如细胞增殖、细胞迁移、细胞渗透或细胞凋亡。
PDGF在体内具有几种重要的细胞作用。它在胚胎发育期间调节细胞生长、分化和迁移,并可能在神经保护和再生方面起作用。它也刺激成人的伤口愈合。此外,PDGF在血管系统以及在结缔组织的内环境稳定方面也具有特殊的功能(Ostman和Heldin,Adv.Can.Res.,80:1-38,2001及其中的参考文献)。
PDGF的活动过度与许多严重的疾病的发病机理有关,这些疾病包括癌症(神经胶质瘤、肺癌、乳腺癌、直肠癌、前列腺癌、胃癌和食管癌、白血病和淋巴瘤)以及其它细胞增殖性疾病,如动脉粥样硬化、移植-诱导的血管疾病、新生内膜形成、肺纤维化、再狭窄、肺的纤维变性、肾小球性肾炎、肾小球硬化症、先天性多囊性肾发育不良、肾纤维化和类风湿性关节炎(Ostman A,Heldin CH.,Adv.CancerRes,80:1-38,2001及其中的参考文献)。
大量的直接或间接的实验证据表明,肿瘤的持续生长和转移为血管生成-依赖性的(见例如,Hanahan,Science,277:48-50,1997)。血管生成是从先前存在的血管和/或循环的内皮干细胞中长出新的脉管系统的过程(见例如,Springer等,1998)。血管生成在许多生理学的过程中,如胚胎发生、伤口愈合和月经期间起着重要作用。血管生成在某些病理学过程,如实体瘤生长和转移、关节炎、银屑病和糖尿病性视网膜病方面也似乎是重要的(Hanahan和Folkman,Cell,86(3):353-364,1996)。
抗血管生成疗法目前作为一种干扰肿瘤生长的方法正在研究之中。的确,在动物模型中的大量研究已证实通过靶向血管生成生长因子如血管内皮生长因子(VEGF)、酸性和碱性成纤维细胞生长因子(aFGF,bFGF)和PDGF抑制肿瘤生长的惊人效果。VEGF和PDGF的受体属于受体酪氨酸激酶的一个超家族。
因此,除了在治疗其它细胞增殖性疾病中的作用外,临床上有用的PDGF-R酪氨酸激酶抑制剂还用于抗血管生成疗法和控制肿瘤细胞增殖。
受体酪氨酸激酶的小分子抑制剂构成一类新的强效药物(Druker和Lydon,J.Clin.Invest.,105:3-7,2000及其中的参考文献)。自1995年以来,已鉴定了许多对PDGF受体自磷酸化作用的小分子抑制剂。下面列出一些实例。
JP 06087834(Zimmermann)公开了具有肿瘤抑制活性的N-苯基-2-嘧啶-胺衍生物,因而用于治疗温血动物包括人的肿瘤。这组化合物的衍生物,化合物CGP53716(Buchdunger等,PNAS,92:2558-2562,1995)和化合物STI-571(Buchdunger等,Cancer Res,56:100-4,1996),已显示可抑制PDGF-R自磷酸化作用。
JP 11158149(Kubo等)公开了用于治疗诸如肿瘤和糖尿病性视网膜病的疾病的喹啉衍生物。这组化合物的衍生物,化合物Ki6783(Yagi等,Exp.Cell Res.243:285-292,1997)和化合物Ki6896(Yagi等,Gen.Pharmacol.31:765-773,1998),已显示可抑制PDGF-R自磷酸化作用。
US5932580(Levitzki等)公开了喹喔啉类的PDGF受体激酶抑制化合物,包括酪氨酸磷酸化抑制剂、所述受体激酶的ATP-竞争抑制剂。
US5409930(Spada等)公开双(一-和/或二环)芳基和/或杂芳基化合物显示蛋白酪氨酸激酶抑制活性。化合物RPR101511A,一种该类化合物的衍生物,显示抑制PDGF-R自磷酸化作用(Bilder等,Circulation.99(25):3292-9.1999)。
US 5563173(Yatsu等)公开了一种通过丁酸钠(其抑制PDGF-R激酶活性)抑制平滑肌细胞增殖的方法。
US5476851(Myers等)公开了作为PDGF受体蛋白酪氨酸激酶抑制剂的吡唑并[3,4-g]喹喔啉化合物。
已显示化合物SU-6668,一种ATP竞争抑制剂,可抑制PDGF-R自磷酸化作用(Laird等,Cancer Res.60:4152-4160,2000]。
WO01/79198(Reich等)公开了调节和/或抑制所述蛋白激酶活性的下式的氨基-吡唑化合物。
WO0212242(Fancelli等)公开了用于治疗与蛋白激酶失调有关的疾病的二环-吡唑化合物。
迄今为止,STI-571(GLEEVEC)为已经上市的惟一具有显著的PDGFR活性的化合物,虽然它不是该酶的选择性拮抗剂。因此,PDGF-R仍然是设计有效的和选择性小分子抑制剂的一个极其吸引人的目标,所述抑制剂将代表一类用于治疗肿瘤和其它细胞增殖性疾病的重要的新的治疗剂。
有关的一些取代的三环吡唑衍生物包括公开使用的那些衍生物:酪氨酸激酶活性的抑制剂(WO 99/17769,WO 99/17770);周期素依赖性激酶抑制剂(WO 99/54308);选择性雌激素受体调节剂(WO00/07996);镇痛剂(U.S.4,420,476);由鼻病毒引起的疾病的预防和治疗(U.S.4,220,776;U.S.4,140,785);镇痛/抗-炎活性(U.S.3,928,378;Schenone,Silvia等Farmaco(2000),55(5),383-388);照相用染料的氰基偶合剂(cyan couplers)(EP 0620489、JP 8022109);作为药物的喹啉和1,5-二氮杂萘(JP 6092963);免疫调节剂(JP 6100561);及降血糖药(Reddy,R.Raja等,Indian Journal of Heterocyclic Chemistry(1998),7(3),189-192)。
发明概述
本发明提供作为PDGF受体(PDGF-R)酪氨酸激酶的抑制剂的N-取代的三环3-氨基吡唑衍生物和此类化合物治疗细胞增殖性疾病或涉及(即,相关或涉及)血小板-衍生的生长因子受体(PDGF-R)有关的疾病如肿瘤、再狭窄、类风湿性关节炎、糖尿病性视网膜病等的用途。
本发明的实例是一种含有药学上可接受的载体及任何式(I)和(II)化合物的药用组合物。本发明的一个其它实例是一种制备药用组合物的方法,它包括将任何式(I)和(II)化合物与药学上可接受的载体混合。本发明的一个其它实例是一种通过将任何式(I)和(II)化合物与药学上可接受的载体混合而制备的药用组合物。
本发明还涉及式(I)和(II)的化合物在患者中治疗PDGF-R相关疾病或细胞增殖性疾病的用途,其包括给予所述患者治疗有效量的式(I)和(II)的化合物。与PDGF-R有关的疾病或细胞增殖性疾病选自瘤形成和其它细胞增殖性疾病。优选地,所述瘤形成疾病是一种选自以下的癌:神经胶质瘤、肺癌、乳腺癌、结肠直肠癌、前列腺癌、胃癌、食管癌、结肠癌、胰腺癌、卵巢癌、黑素瘤、脊髓发育不良、多发性骨髓瘤、白血病和淋巴瘤,而所述其它的细胞增殖性疾病选自动脉粥样硬化、移植诱导的血管疾病、新生内膜形成、肺纤维化、黄斑变性、再狭窄、肺的纤维变性、肾小球性肾炎、肾小球硬化症、先天性多囊性肾发育不良、肾纤维化、类风湿性关节炎和糖尿病性视网膜病。
本发明涉及一种在患者中抑制与PDGF-R有关的疾病或细胞增殖性疾病发作的方法,它包括给予所述患者预防有效量的式(I)和(II)的化合物。
本发明还包括在患者中治疗或抑制与PDGF-R有关的疾病或细胞增殖性疾病发作的联合疗法。所述联合疗法包括分别给予所述患者治疗或预防有效量的本发明的化合物以及采用一种或多种其它抗-细胞增殖疗法,所述疗法包括(但不限于)化学疗法、放射疗法、基因疗法和免疫疗法。
本发明也提供一种用于治疗细胞增殖性疾病(优选血管壁内再狭窄、内膜增生、炎症或动脉粥样硬化)的方法,该方法包括通过从管腔内医疗装置释放来控制本发明化合物以治疗有效量进行传递。
本发明还提供一种在患者中治疗细胞增殖性疾病的方法,所述疾病优选选自神经胶质瘤、肺癌、乳腺癌、结肠直肠癌、前列腺癌、胃癌、食管癌、结肠癌、胰腺癌、卵巢癌、黑素瘤、脊髓发育不良、多发性骨髓瘤、白血病和淋巴瘤的瘤形成疾病,该方法包括给予所述患者与靶向剂结合的有效量的本发明化合物。
本发明还提供一种在细胞中减弱或抑制PDGF-R或c-Abl的激酶活性的方法,它包括使所述细胞与式(I)或(II)化合物接触的步骤。本发明也提供一种在患者中抑制PDGF-R或c-Abl的激酶活性的方法,它包括给予所述患者式(I)或(II)化合物的步骤。本发明还提供在细胞中抑制细胞增殖的方法,它包括使所述细胞与式(I)或(II)化合物接触的步骤。
本发明还提供一种鉴定新的PDGF-R激酶抑制剂的方法。该方法包括以下的步骤:
(a)在包含PDGF-R激酶催化结构域的多肽的存在下或不存在下,确定式(I)或(II)化合物的三维结构;
(b)仅分析该化合物的三维结构或者分析所述化合物和PDGF-R的分子间的相互作用;
(c)选择仅模拟该化合物的结构或者结合预计的相互作用的某种化合物;
(d)合成所设计的化合物;及
(e)测定所述分子结合和抑制PDGF-R激酶活性的能力。
本发明还提供一种鉴定新的c-Abl激酶抑制剂的方法。该方法包括以下的步骤:
(a)在包含c-Abl激酶催化结构域的多肽的存在下或不存在下,确定式(I)或(II)化合物的三维结构;
(b)仅分析该化合物的三维结构或者分析所述化合物和c-Abl的分子间的相互作用;
(c)选择仅模拟该化合物的结构或者结合预计的相互作用的某种化合物;
(d)合成所设计的化合物;及
(e)测定所述分子结合和抑制c-Abl激酶活性的能力。
本发明还涉及制备式(I)化合物或式(II)化合物的方法。
从以下的本发明的详细描述及其权利要求书中应能清楚地了解本发明的其它特征和优点。
发明详述
本发明涉及新的N-取代的三环3氨基吡唑衍生物,它们的合成方法和所述化合物治疗和/或预防PDGF-R相关疾病,如肿瘤、再狭窄、类风湿性关节炎、糖尿病性视网膜病等的用途。
1.式(I)
本发明涉及用于治疗PDGF-R相关疾病的式(I)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐:
式(I)
其中,n为1-4的整数;
R1选自氢、低级烷基、-OH、烷氧基、-氧代基、-NH2、-NH(烷基)和-N(烷基)2;
选自芳基、5-6元单环杂芳基、9-10元苯并-稠合的杂芳基、9-10元苯并-稠合的杂环烷基和9-10元苯并-稠合的环烷基;其中所述苯并-稠合的杂芳基、苯并-稠合的杂环烷基或苯并-稠合的环烷基连接于该分子上,以使所述苯环直接连接于该分子的
部分;
p为0-2的整数;
X和Y各自独立不存在或选自-O-、-NH-、-N(烷基)-、-S-、-SO-、SO2-、-OC(=O)、-C(=O)O-、-NHC(=O)-、-N(烷基)C(=O)-、-C(=O)NH-、-C(=O)N(烷基)-、-OC(=O)O-、-NHC(=O)O-、-OC(=O)NH-、-N(烷基)C(=O)O-、-OC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)N(烷基)-、-NHSO2-、-SO2NH-、-N(烷基)SO2-和-SO2N(烷基)-;
A1不存在或选自烷基或链烯基;A2选自烷基、链烯基或H;其中,当A1或A2为烷基或链烯基时,所述烷基或链烯基可以由独立选自以下一个或多个基团任选取代:卤素、氰基、羟基、烷氧基、硫基、卤代烷氧基、-OC(=O)烷基、-OC(=O)O烷基、氨基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基、二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)NH2、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选被一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2,-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
q为0-4的整数;
R3选自卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2,-N(烷基)C(=O)N(烷基)2和-OC(=O)N(烷基)2;
前提是p和q的总和为0-4的整数;
L1不存在或选自烷基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基。
在式(I)中,当为9-10元苯并-稠合的杂芳基、9-10元苯并-稠合的杂环烷基或9-10元苯并-稠合的环烷基时,所述苯并-稠合的杂芳基、苯并-稠合的杂环烷基或苯并-稠合的环烷基连接于该分子上,以使苯环直接连接于该分子的部分中标明为”x”和”y”处的碳原子上。例如,其中为未取代的3,4-亚甲二氧基苯基,所述1,3-亚甲二氧基苯基可以连接于式(I)化合物的剩余部分以形成于式(Im)、(In)或(Ip)化合物:
其中准确的取向应可从制备的化合物的结构或命名中清楚地得知。
1.a式(1)的实施方案
在本发明的一个实施方案中,
选自苯基、噻吩基、吡啶基、嘧啶基、呋喃基、异噁唑基、咪唑基、吡唑基和3,4-亚甲二氧基苯基。优选选自苯基、噻吩基和3,4-亚甲二氧基苯基。在本发明的另一个实施方案中,选自5或6元杂芳基。在本发明的另一个实施方案中,选自9或10元苯并-稠合的杂芳基、9或10元苯并-稠合的环烷基和9或10元苯并-稠合的杂环烷基。
在本发明的一个优选实施方案中,R1选自氢、羟基、甲基和氧代基,优选R1为氢或甲基。
在本发明的一个实施方案中,n为1-2的整数。在本发明的另一个实施方案中,p为0且q为0-2的整数。在本发明的又一个实施方案中,p为1-2的整数且q为0-1的整数。
在本发明的一个实施方案中,R2为其中X、A1和如本文所定义。优选X为O。在本发明的另一个实施方案中,X为O,为杂环烷基或杂芳基,其中所述杂环烷基或杂芳基任选被1-3个独立选自以下的取代基取代:卤素、烷氧基、羟基、氨基、烷基氨基或二烷基氨基。
在本发明的另一个实施方案中,R2为-X-A1-Y-A2,其中X、A1、Y、A2如本文所定义。优选地,X和Y各自独立不存在或为O。
在本发明的一个实施方案中,R3选自烷氧基、卤素、氨基、二烷基氨基、低级烷基和羟基。优选R3为低级烷基或低级烷氧基。
在本发明的一个实施方案中,L1是低级烷基,优选为亚甲基。在本发明的另一个实施方案中,L1不存在。
本发明的一个实施方案是一种式(1a)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐:
式(1a)
本发明的另一个优选实施方案是一种式(I)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐,其中n为1-2的整数;
R1为氢;
p为0-2的整数;
其中A1选自低级烷基;其中所述低级烷基任选被1-2个独立选自以下的取代基取代:羟基、氨基、烷基氨基或二烷基氨基;
且其中选自5或6元杂芳基和5或6元杂环烷基;其中所述杂芳基或杂环烷基任选被1-2个独立选自以下的取代基取代:卤素、低级烷基、低级烷氧基、氨基、低级烷基氨基或二(低级烷基)氨基;优选R2选自3-二甲基氨基-丙氧基、3-甲氧基-丙氧基、2,3-二羟基-正丙氧基、3-羟基-丙氧基、2-羟基-3-吡咯烷-1-基-丙氧基和3-(4-甲基-哌嗪-1-基)-丙氧基;
q为0-2的整数;
R3选自低级烷基和低级烷氧基和卤素;优选R3选自甲基、甲氧基、乙氧基;
L1不存在或为低级烷基、优选L1不存在或为CH2;
选自苯基和5或6元杂芳基;其中所述苯基或杂芳基任选被1-2个独立选自以下的取代基取代:卤素、低级烷基、低级烷氧基或苄氧基;优选选自苯基和吡啶基;其中所述苯基任选被1-2个独立选自以下的取代基取代:氟代基、氯代基、甲基,甲氧基或苄氧基。
本发明的另一个实施方案是一种式(I)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐,其中R1选自氢和低级烷基;优选R1选自氢或甲基;
选自苯基、5-6元杂芳基和9-10元苯并-稠合的杂芳基;其中所述苯基、5-6元杂芳基或9-10元苯并-稠合的杂芳基任选被1-2个独立选自以下的取代基取代:卤素、低级烷基、低级烷氧基、三氟甲基,三氟甲氧基、二氟甲氧基或低级烷氧基-低级烷氧基;优选选自苯基、3,5-二甲氧基苯基、4,5-二乙氧基苯基、4,5-二(三氟甲氧基)-苯基、4,5-二(甲氧基乙氧基)-苯基、4,5-二(甲氧基丙氧基)-苯基、4,5-二(异丙氧基)-苯基、4,5-二(二氟甲氧基)-苯基、4-氯-5-甲氧基-苯基、4-甲氧基乙氧基-5-乙氧基-苯基、吡啶基,嘧啶基、呋喃基、5-氯-噻吩基、3-乙氧基-噻吩基、异噁唑基、3-甲基-异噁唑基、2-甲基-8-乙氧基-苯并噁唑基、苯并噻吩基,
L1不存在或选自低级烷基,优选L1不存在或选自甲基或乙基;
选自芳基、环烷基和5-6元杂芳基;其中所述芳基或杂芳基任选被1-2个独立选自以下的取代基取代:卤素、低级烷基、羟基取代的低级烷基、低级烷氧基、氨基磺酰基、(低级烷基)氨基、二(低级烷基)氨基、二(低级烷基)氨基-烷氧基羰基、低级烷氧基羰基、杂环烷基-低级烷基氨基羰基、二(低级烷基)氨基-低级烷基氨基羰基或杂芳基-低级烷基氨基羰基;其中所述杂环烷基-低级烷基氨基羰基或杂芳基-低级烷基氨基羰基取代基的所述杂芳基或杂环烷基部分任选被选自以下的取代基取代:低级烷基、羟基或羟基取代的低级烷基;
优选选自苯基、苄基、苯乙基、环己基、环己基-甲基,3-羟基环己基、4-羟基-环己基、2-氟代苄基、2-氯代苄基、3-氯代苄基、2,3-二氯苄基、2,6-二氯苄基、2-氟代苯乙基、3-氟代苯基、3-溴代苯基、3-氯代苯基、2-甲基苄基、3-甲基苄基、3-甲氧基苯基、4-甲氧基苯基、3-羟甲基苯基、2-羟甲基苄基、3-氯-4-氟-苄基、2-氨基磺酰基-苄基、2-氨基磺酰基-苯基、3-氨基磺酰基-苯基、4-氨基磺酰基-苯基、3-二甲基氨基苯基、3-(二甲基氨基-乙基氨基羰基)-苯基、3-乙氧基羰基-苯基、3-(2-吡咯烷-1-基-乙基氨基羰基)-苯基、3-(2-吡咯烷-1-基-正丙基氨基羰基)-苯基、3-(二甲基氨基-乙基氨基羰基)-苯基、3-(2-咪唑-1-基-乙基氨基羰基)-苯基、3-(2-(1-甲基-咪唑-2-基)乙基氨基羰基)-苯基、3-[3-(羟甲基-吡咯烷-1-基-丙基)-氨基羰基]-苯基、吡啶基-甲基、吡啶基-乙基、嘧啶基-甲基和3-甲基-咪唑基-甲基。
1.b.式(I)化合物的制备
本发明还涉及一种制备式(I)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐的方法,
式(I)
其中,n为1-4的整数;R1选自氢、低级烷基、-OH、烷氧基、-氧代基、-NH2、-NH(烷基)和-N(烷基)2;
选自芳基、5-6元单环杂芳基、9-10元苯并-稠合的杂芳基、9-10元苯并-稠合的杂环烷基和9-10元苯并-稠合的环烷基;其中所述苯并-稠合的杂芳基、苯并-稠合的杂环烷基或苯并-稠合的环烷基连接于该分子上,以使苯环直接连接于该分子的
p为0-2的整数;
X和Y各自独立不存在或选自-O-、-NH-、-N(烷基)-、-S-、-SO-、SO2-、-OC(=O)、-C(=O)O-、-NHC(=O)-、-N(烷基)C(=O)-、-C(=O)NH-、-C(=O)N(烷基)-、-OC(=O)O-、-NHC(=O)O-、-OC(=O)NH-、-N(烷基)C(=O)O-、-OC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)N(烷基)-、-NHSO2-、-SO2NH-、-N(烷基)SO2-和-SO2N(烷基)-;
A1不存在或选自烷基或链烯基;A2选自烷基、链烯基或H;其中,当A1或A2为烷基或链烯基时,所述烷基或链烯基可以由独立选自以下一个或多个基团任选取代:卤素、氰基、羟基、烷氧基、硫基、卤代烷氧基、-OC(=O)烷基、-OC(=O)O烷基、氨基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基、二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)NH2、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基,任选被一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2,-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
q为0-4的整数;
R3选自卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2,-N(烷基)C(=O)N(烷基)2和-OC(=O)N(烷基)2;
前提是p和q的总和为0-4的整数;
L1不存在或选自烷基;
该方法包括
在碱的存在下,在非质子溶剂中,使式(S1)化合物与1,1′-硫代羰基咪唑反应,得到相应的式(S5)化合物;
在非质子溶剂中,使式(S5)化合物与式(S6)化合物反应,得到相应的式(S3)化合物;
使式(S3)化合物与肼反应,得到相应的式(I)化合物。
2.式(II)
本发明还涉及式(II)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐:
其中:
其中式A-1在式A-1的b1边上连接于式(II)的L2环并任选由一个选自式A-1-a、A-1-b和A-1-c的基团取代:
其中式A-1-a在a1边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-b在a2边上连接于式A-1的d1或d2边上的相邻碳原子;及
其中式A-1-c在a6边上连接于式A-1的d1或d2边上的相邻碳原子;
其中R8为H或烷基;
其中式A-2在式A-2的b2边上连接于式(II)的L2环,且A1、A2、A3、A4为(i)-N-;或(ii)由H或烷氧基取代的-C-,其中所述烷氧基可以任选由烷氧基在末端碳原子或由最多可达3个卤原子在末端碳原子上进一步取代;前提是A1、A2、A3、A4中的至少一个但不多于两个为-N-;及
其中式A-3在式A-3的b3边上连接于式(II)的L2环,且B1、B2和B3独立为(i)任选由烷基、芳基、烷氧基或卤素取代的-CH-,(ii)-S-;(iii)-O-;或(iv)-N-;前提是B1、B2或B3中不超过一个为-S-或-O-,且前提是当B1、B2或B3其中之一为-S-或-O-时,则相邻的环成员不是-S-或-O-;
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基和烷硫基;
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R100选自:烷基、羟基、芳基、烷氧基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH;前提是当L2为-CH2CH2-时,R6或者R7不为-CH2-(C=O)NH烷基、-CH2-(C=O)N(烷基)2或-CH2C(=O)O烷基;前提是当L2为-OCH(R100)-时,R100为烷氧基、
其中X1和Y1各自独立不存在或选自:-(烷基)C(=O)N(烷基)-、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
A20不存在或选自烷基或链烯基;和
A21选自烷基、链烯基或H;
其中当A20或A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由独立选自以下的一个或多个取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
s为0-2的整数;
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(d)由H、甲基、乙基或苄基为端基的-C(=O)(CH2CH2O-)1-10;
(e)由H、甲基、乙基或苄基为端基的-C(=O)CH2O(CH2CH2O-)1-10;
(f)-C(=O)烷基或-C(=O)(C3-6)环烷基,其中所述-C(=O)烷基和-C(=O)(C3-6)环烷基可以由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基或-C(=O)杂芳基,其中所述-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基和-C(=O)杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基或-C(=O)O(C3-6)环烷基,其中所述-C(=O)O烷基和-C(=O)O(C3-6)环烷基可以由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基,其中所述-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基或-C(=O)N(烷基)2,其中所述-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基和-C(=O)N(烷基)2可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHCO)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基或-C(=O)NH杂芳基,其中所述-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基和-C(=O)NH杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(q)-C(=S)NH烷基;
(r)-C(=S)N(烷基)2;
(s)-SO2NH2;
(t)-SO2NH烷基;
(u)-SO2N(烷基)2;
(v)-P(=O)(OCH3)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在;
L3不存在或为选自烷二基、羰基或-SO2-的连接基团;
r为0-4的整数;及
R5独立选自:烷基、烷基氨基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH、-CH2OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代SO2-烷基、卤代烷硫基、羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、-SO2NH2,硫基、烷硫基、和-V-B10-W-B20;其中,
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
B10不存在或选自烷基或链烯基;
B20不存在或选自烷基、链烯基或H;
其中,当B10或B20为烷基或链烯基时,所述烷基或链烯基可以任选由一个或多个独立选自以下的基团取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
选自:芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基,其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基,任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
在式(II)中,″式(II)的L2环″指含有L2取代基的式(II)的环。
L2为-CH2CH2-和为苯基时,所述连接点如下所示:
2.a式(II)的实施方案
2.a.1
本发明的其它实施方案包括式II化合物,其中E、L2、R6、R7、R4、L3H和(R5)r的定义变化如以下对其单个变量或变量的组合所述。
本发明的一个实施方案包括式(II)化合物,其中:
其中式A-1在式A-1的b1边上连接于式(II)的L2环,并任选由一个选自式A-1-a、A-1-b和A-1-c的基团取代:
其中R8为H或低级烷基;
其中式A-2在式A-2的b2边上连接于式(II)的L2环,且A1、A2、A3、A4中的一个或两个为-N-;剩余的为由H或烷氧基取代的-C-,其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达3个的卤原子在末端碳原子上进一步取代;及
其中式A-3在式A-3的b3边上连接于式(II)的L2环,且B1、B2和B3独立为(i)任选由C1-4烷基、芳基、烷氧基或卤素取代的-CH-,(ii)-S-,(iii)-O-或(iv)-N-;前提是B1、B2或B3中不超过一个为-S-或-O-,且前提是当B1、B2或B3中的一个为-S-或-O-时,则相邻的环成员不是-S-或-O-。
本发明的一个实施方案包括式(II)化合物,其中:
其中式A-1在式A-1的b1边上连接于式(II)的L2环,并任选由一个选自式A-1-a、A-1-b和A-1-c的基团取代:
其中R8为H或低级烷基;
其中式A-2选自吡啶基和嘧啶基,在式A-2的b2边上连接于式(II)的L2环;且任选在碳环成员上由H或烷氧基取代,其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达3个的卤原子在末端碳原子上进一步取代;及
本发明的一个实施方案包括式(II)化合物,其中
其中式A-4在式A-4的b1边上连接于式(II)的L2环;
其中式A-5在式A-5的b1边上连接于式(II)的L2环;其中R8为氢和低级烷基;
其中式A-6在式A-6的b1边上连接于式(II)的L2环;及
其中式A-3-a在式A-3-a的b3边上连接于式(II)的L2环,其中R12独立选自H、甲基、苯基、乙氧基、氯代基或氟代基;及其中
本发明的一个实施方案包括式(II)化合物,其中
选自:
其中式A-4在式A-4的b1边上连接于式(II)的L2环;
其中式A-5在式A-5的b1边上连接于式(II)的L2环;其中R8为氢和低级烷基;及
其中式A-3-a在式A-3-a的b3边上连接于式(II)的L2环,其中R12独立选自H、甲基、苯基、乙氧基、氯代基或氟代基;及其中
本发明的一个实施方案包括式(II)化合物,其中
本发明的一个实施方案包括式(II)化合物,其中:
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2-烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基和硫烷基。
本发明的一个实施方案包括式(II)化合物,其中:
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、羟基、-NHC(=O)烷基、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基和硫烷基。
本发明的一个实施方案包括式(II)化合物,其中:
R9独立选自:烷氧基、烷基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、羟基和-NHC(=O)烷基。
本发明的一个实施方案包括式(II)化合物,其中:
R9独立选自:甲氧基、乙氧基、异丙氧基、甲基,氨基、氰基、N,N-二甲基-氨基、溴代基、氯代基、氟代基、三氟甲基,三氟甲氧基、羟基和N-(1-氧代-乙基)-氨基。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)-、-(CH2)3-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R200)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R200选自:烷基、羟基、芳基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)-、-(CH2)3-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O(CH2)1-4-、-OCH(R200)-、-OC(R100)2-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R200选自:烷基、羟基、芳基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-,-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-CH2CH2-时,R6或R7不是-CH2-(C=O)NH烷基。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-C(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-CH2CH2-时,R6或者R7不为-CH2-(C=O)NH烷基或-CH2-(C=O)N(烷基)2。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-CH2CH2-时,R6或R7不是-CH2C(=O)O烷基。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-,-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-CH2CH2-,R6或者R7不为-CH2-(C=O)NH烷基、-CH2-(C=O)N(烷基)2或-CH2C(=O)O烷基。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为OCH(R100)-,R100为烷氧基和为苯基时,R5不是-C(=O)NH-NH2。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-,-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-O-时,则R6或者R7不为-CH3。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-S-时,则R6或R7不是-CH3。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-O-或-S-时,则R6或R7不是-CH3。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-。
本发明的一个实施方案包括式(II)化合物,其中:
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-和-O(CH2)1-4-。
本发明的一个实施方案包括式(II)化合物,其中:R100选自:烷基、羟基、芳基、氧代或=N(OH)。
本发明的一个实施方案包括式(II)化合物,其中:R100选自:烷基、羟基、芳基或氧代。
本发明的一个实施方案包括式(II)化合物,其中:R100选自:甲基,羟基、苯基、氧代或=N(OH)。
本发明的一个实施方案包括式(II)化合物,其中:R100选自:甲基,羟基、苯基或氧代。
本发明的一个实施方案包括式(II)化合物,其中:
R10独立选自
-X1-A20-Y1-A21,-X1-A20-A21,-X1-A21,-A20-A21和-A21。
本发明的一个实施方案包括式(II)化合物,其中:
R10独立选自
-X1-A20-Y1-A21,
-X1-A20-A21和-X1-A21
本发明的一个实施方案包括式(II)化合物:其中X1和Y1各自独立不存在或选自:-C(=O)NH-、-C(=O)O-、-NH-、-NHC(=O)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、-SO2-和-SO2NH-。
本发明的一个实施方案包括式(II)化合物:其中X1和Y1各自独立不存在或选自:-NH-、-O-、-SO2-和-SO2NH-。
本发明的一个实施方案包括式(II)化合物,其中X1和Y1各自独立不存在或为-O-。
本发明的一个实施方案包括式(II)化合物,其中X1不存在或-O-。
本发明的一个实施方案包括式(II)化合物,其中Y1不存在。
本发明的一个实施方案包括式(II)化合物,其中:A20不存在或为烷基;及
其中当A20为烷基时,则烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基。
本发明的一个实施方案包括式(II)化合物,其中:
A20不存在或为烷基;及其中当A20为烷基时,则所述烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基、-NHC(=O)NH2、-NHSO2烷基、-SO2烷基或硫烷基。
本发明的一个实施方案包括式(II)化合物,其中:
A20不存在或选自甲基,乙基、丙基或异丙基;其中甲基,乙基、丙基或异丙基任选由独立选自以下的一个或多个基团取代:烷氧基、二烷基氨基或羟基。
本发明的一个实施方案包括式(II)化合物,其中:
A20不存在或选自甲基,乙基、丙基或异丙基;其中甲基,乙基、丙基或异丙基任选由一个或多个独立选自以下的基团取代:甲氧基、二甲基-氨基或羟基。
本发明的一个实施方案包括式(II)化合物,其中:
A21选自烷基、链烯基或H;及
其中当A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基。
本发明的一个实施方案包括式(II)化合物,其中:
A21选自烷基、链烯基或H;及
其中当A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基、-NHC(=O)NH2、-NHSO2烷基或硫烷基。
本发明的一个实施方案包括式(II)化合物,其中A21为H。
本发明的一个实施方案包括式(II)化合物,其中
选自芳基、环烷基、部分不饱和的碳环、杂芳基和杂环烷基,其任选由一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2。
本发明的一个实施方案包括式(II)化合物,其中
选自芳基、杂芳基和杂环烷基,其任选由一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2。
本发明的一个实施方案包括式(II)化合物,其中
选自苯基、咪唑基、吡咯烷基、哌啶基和吗啉基,其任选由一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2。
本发明的一个实施方案包括式(II)化合物,其中
选自苯基、咪唑基、吡咯烷基、哌啶基和吗啉基,其任选由一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硝基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、二烷基氨基、-NHSO2烷基或-SO2烷基。
本发明的一个实施方案包括式(II)化合物,其中
本发明的一个实施方案包括式(II)化合物,其中R9和R10独立选自:1-哌啶基,2-(吡咯烷-1-基)-乙氧基、2,3-二羟基-丙氧基、2-羟基-3-吡咯烷-1-基-丙氧基、3-(4-甲基-哌嗪-1-基)-丙氧基、3-(N,N-二甲基-氨基)-丙氧基、3-羟基-丙氧基、3-咪唑-1-基-丙氧基、3-甲氧基-丙氧基、3-吗啉-4-基-丙氧基、3-吡咯烷-1-基-2-羟基-丙氧基、3-吡咯烷-1-基-丙氧基、4-甲基-哌嗪-1-基,氨基、苄基、苄氧基、溴代基、氯代基、氰基、乙氧基、氟代基、H,羟基、异丙氧基、甲氧基、甲基,N-(1-氧代-乙基)-氨基和N,N-二甲基-氨基。
本发明的一个实施方案包括式(II)化合物,其中
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(d)由H为末端的-C(=O)(CH2CH2O-)1-10;
(e)由H为末端的-C(=O)CH2O(CH2CH2O-)1-10;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基或-C(=O)芳基,其中所述-C(=O)芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基、乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基或-N(烷基)2;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基或-C(=O)O芳基,其中所述-C(=O)O芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基、苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基或-C(=O)N(C1-20烷基)2,其中所述-C(=O)NH(C1-20)烷基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基或-C(=O)NH芳基,其中所述-C(=O)NH芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2-、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(q)-C(=S)NH烷基;
(r)-C(=S)N(烷基)2;
(s)-SO2NH2;
(t)-SO2NH烷基;
(u)-SO2N(烷基)2;
(v)-P(=O)(OCH3)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,其中
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-C(=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基或-C(=O)芳基,其中所述-C(=O)芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基或-N(烷基)2;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基或-C(=O)O芳基,其中所述-C(=O)O芳基可以任选由一个或多个独立选自以下的基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基或-C(=O)N(C1-20烷基)2,其中所述-C(=O)NH(C1-20)烷基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基或-C(=O)NH芳基,其中所述-C(=O)NH芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(u)-SO2N(烷基)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,
其中R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)-O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)芳基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基或-N(烷基)2;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O芳基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH(C1-20)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH芳基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2-OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(u)-SO2N(烷基)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,其中
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基-苯基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)芳基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或吡咯烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基或-N(烷基)2;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O芳基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH(C1-20)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、吡咯烷基、吗啉基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)苯基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)苯基的苯基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH芳基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)苯基;其中所述-C(=O)苯基的苯基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(u)-SO2N(烷基)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,其中
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-C(=O)O烷基、-(C=O)NH2、-C(=O)烷基或-苯基-OC(=O)烷基;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基-苯基或-OC(=O)烷基;
(g)-C(=O)苯基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈或-OC(=O)烷基;
(h)由-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或吡咯烷基为端基的-C(=O)(CH2)1-6C(=O)-;
(hh)由-O烷基为端基的-C(=O)烷基OC(=O)烷基-;
(i)由H或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)由一个或多个-O烷基任选取代的-C(=O)O烷基;
(k)-C(=O)O苯基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈或-OC(=O)烷基;
(l)由-H为端基的-C(=O)NH(CH2CH2O-)1-10;
(m)-C(=O)NH(C1-20)烷基,其由独立选自以下的一个或多个基团任选取代:-NH2、-NH烷基、-N(烷基)2、吡咯烷基、吗啉基、-NHC(=O)烷基、-OC(=O)链烯基、-NHC(=O)苯基或-C(=O)O烷基;且其中所述-NHC(=O)苯基的苯基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH苯基,其由独立选自以下的一个或多个任选基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基和-C(=O)苯基;其中所述-C(=O)苯基的苯基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素和腈;
(p)-C(=S)NH2;
(u)-SO2N(烷基)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,其中
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-C(=O)O烷基、-(C=O)NH2、-C(=O)烷基或-苯基-OC(=O)烷基;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基-苯基或-OC(=O)烷基;
(g)-C(=O)苯基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈和-OC(=O)烷基;
(h)由-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或吡咯烷基为端基的-C(=O)(CH2)1-6C(=O)-;
(hh)由-O烷基为端基的-C(=O)烷基OC(=O)烷基-;
(i)由H或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)由一个或多个-O烷基任选取代的-C(=O)O烷基;
(k)-C(=O)O苯基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈和-OC(=O)烷基;
(l)由-H为端基的-C(=O)NH(CH2CH2O-)1-10;
(m)-C(=O)NH(C1-20)烷基,其由独立选自以下的一个或多个基团任选取代:-NH2、-NH烷基、-N(烷基)2、吡咯烷基、吗啉基、-NHC(=O)烷基、-OC(=O)链烯基、-NHC(=O)苯基或-C(=O)O烷基;且其中所-NHC(=O)苯基的苯基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素和腈;
(n)-C(=O)NH苯基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、氯代基、氟代基、腈和-OC(=O)烷基;
(o)由-CH2CH2OH和-C(=O)苯基为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3;其中所述-C(=O)苯基的苯基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素和腈;
(p)-C(=S)NH2;
(u)-SO2N(烷基)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,其中
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-C(=O)O烷基、-(C=O)NH2、-C(=O)烷基或-苯基-OC(=O)烷基;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基-苯基或-OC(=O)烷基;
(g)-C(=O)苯基,其由独立选自以下的一个或多个基团任选取代:-O烷基、氯代基或氟代基,;
(h)由-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或吡咯烷基为端基的-C(=O)(CH2)1-6C(=O)-;
(hh)由-O烷基为端基的-C(=O)烷基OC(=O)烷基-;
(i)由H或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)由一个或多个-O烷基任选取代的-C(=O)O烷基;
(k)由一个或多个氯代基、氟代基任选取代的-C(=O)O苯基;
(l)由-H为端基的-C(=O)NH(CH2CH2O-)1-10;
(m)-C(=O)NH(C1-20)烷基,其由独立选自以下的一个或多个基团任选取代:-NH2、-NH烷基、-N(烷基)2、吡咯烷基、吗啉基、-NHC(=O)烷基、-OC(=O)链烯基、-NHC(=O)苯基或-C(=O)O烷基;且其中所述-NHC(=O)苯基的苯基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素和腈;
(n)由一个或多个氟代基任选取代的-C(=O)NH苯基;
(o)由-CH2CH2OH和-C(=O)苯基为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3;其中所述-C(=O)苯基的苯基部分可以任选由一个或多个-OH基团取代;
(p)-C(=S)NH2;
(u)-SO2N(烷基)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,其中
R6和R7独立选自:H,
1-甲氧基-1-氧代-乙基、1-甲基-乙氧基-羰基、1-氧代-丁氧基-甲基、
1-氧代-乙氧基-甲基、1-氧代-乙基、1-氧代-丙基、
2-(1-氧代-乙氧基)-1-氧代-乙基,2-(2-甲氧基-1-氧代-乙氧基)-1-氧代-乙基、
2-(2-甲基-1-氧代-丙氧基)-1-氧代-乙基、2-氨基-2-氧代-乙基、
2,2-二甲基-1-氧代-丙氧基-甲基、2-乙氧基-2-氧代-乙基、
2-甲氧基-2-氧代-乙基、2,6-二氟-苯甲酰基、
2-[2-(2-羟基-乙氧基)-乙氧基]-乙氧基-羰基、
2-苄氧基-1-氧代-乙基、2-苄氧基-乙氧基-羰基、
2-氯-苯氧基-羰基、2-氟-苯甲酰基、2-羟基-1-氧代-乙基、
2-羟基-乙基、2-羟基-丙基、2-甲氧基-1-氧代-乙基、
2-甲氧基-乙氧基-羰基、2-甲基-1-氧代-丙基、2-氧代-丙基、
3-(N,N-二乙基氨基)-1,3-二氧代-丙基、
3-1H-吡咯烷-1-基-1,3-二氧代-丙基、3-乙氧基-1,3-二氧代-丙基、
3-1H-吡咯烷-1-基-1,3-二氧代-丙基、4-(1-氧代-乙氧基)-苄基、
4-氨基-1,4-二氧代-正丁基、4-乙氧基-1,4-二氧代-正丁基、
4-羟基-1,4-二氧代-正丁基、4-甲氧基-1,4-二氧代-正丁基、
4-氯-苯甲酰基,4-氯-苯氧基-羰基、4-氟-苯甲酰基,
4-氟-苯氧基-羰基、4-甲氧基-苯甲酰基,
5-(N-甲基-氨基)-1,5-二氧代-戊基、5-甲氧基-1,5-二氧代-戊基、苯甲酰基,二乙氧基-氧膦基、乙氧基-羰基、甲氧基-羰基、甲氧基-甲基、甲基、N-(2-乙氧基-2-氧代-乙基)-氨基-羰基、
N-(2-1H-吡咯烷-1-基-乙基)-氨基-羰基、
N-(2-氨基-乙基)-氨基-羰基、
N-(2-吗啉-4-基-乙基)-氨基-羰基、
N-(3-乙氧基-3-氧代-丙基)-氨基-羰基、
N-(3-氟-苯基)-氨基-羰基、N-(十五烷基)-氨基-羰基、
N,N-二甲基-氨基-磺酰基、
N-[2-(2-次甲基-1-氧代-丙氧基)-乙基]-氨基-羰基、
N-[2-(3-甲基-1-甲氧基-1-氧代)-正丁基]-氨基-羰基、
N-[2-(4-甲基-1-甲氧基-1-氧代)-戊基]-氨基-羰基、
N-[2-(N,N-二甲基-氨基)-乙基]-氨基-羰基、
N-[2-(N-苯甲酰基-氨基-乙基]-氨基-羰基、
N-[2-(N-甲基-氨基)-乙基]-氨基-羰基、
N-[2-[2-(2-羟基-乙氧基)-乙氧基]-乙基]-氨基-羰基、
N-[2-[N-(1-氧代-乙基)-氨基]-乙基]-氨基-羰基、
N-[2-[N-(2-羟基-苯甲酰基)-氨基]-乙基]-氨基-羰基、
N-[2-[N-(2-羟基-乙基)-氨基]-乙基]-氨基-羰基、
N-[2-[N-(2-甲基-1-氧代-丙基)-氨基]-乙基]-氨基-羰基、
N-甲基-氨基-羰基、N-甲基-氨基-硫代羰基,和
苯氧基-羰基、前提是当R6存在时,则R7不存在;及
前提是当R7存在时,则R6不存在。
本发明的一个实施方案包括式(II)化合物,其中L3不存在或是选自亚甲基、亚乙基、羰基或-SO2的连接基团。
本发明的一个实施方案包括式(II)化合物,其中L3不存在或是选自亚甲基、亚乙基或羰基的连接基团。
本发明的一个实施方案包括式(II)化合物,其中
本发明的一个实施方案包括式(II)化合物,其中
本发明的一个实施方案包括式(II)化合物,其中
本发明的一个实施方案包括式(II)化合物,其中
R5独立选自:烷基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代烷硫基、羟基、羟基烷基、-NHC(=O)NH2、-NHSO2烷基、硝基、-SO2烷基、-SO2NH2,硫基、烷硫基、
本发明的一个实施方案包括式(II)化合物,其中
R5独立选自:烷基、烷基氧基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代烷硫基、羟基、羟基烷基、硝基、-SO2NH2、烷硫基、
和-V-B10-W-B20。
本发明的一个实施方案包括式(II)化合物,其中
R5独立选自:甲基、乙基、异丙基、叔丁基、甲氧基、乙氧基、-C(=O)NH2、-C(=O)O甲基、-C(=O)O乙基、-C(=O)OH、氰基、二甲基-氨基、溴代基、氯代基、氟代基、三氟甲基,三氟甲氧基、硫代-三氟甲基,羟基、羟甲基,羟基乙基、硝基、-SO2NH2、甲硫基、和-V-B10-W-B20。
本发明的一个实施方案包括式(II)化合物:其中
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-NH-、-NHC(=O)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-和-SO2NH-。
本发明的一个实施方案包括式(II)化合物:其中
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-NH-、-O-和-SO2-。
本发明的一个实施方案包括式(II)化合物,其中V不存在或选自:
-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-NH-、-O-和-SO2-。
本发明的一个实施方案包括式(II)化合物,其中V不存在或选自:
-C(=O)NH-、-C(=O)O-、-NH-、-O-和-SO2-。
本发明的一个实施方案包括式(II)化合物,其中W不存在。
本发明的一个实施方案包括式(II)化合物,其中:
B10不存在或为烷基;及
其中当B10为烷基时,所述烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基。
本发明的一个实施方案包括式(II)化合物,其中:B10不存在或为烷基;及其中当B10为烷基时,所述烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基、-NHC(=O)NH2、-NHSO2烷基、-SO2烷基或硫烷基。
本发明的一个实施方案包括式(II)化合物,其中:
B10不存在或选自甲基或乙基,;其中甲基或乙基任选由一个或多个独立选自以下的基团取代:二烷基氨基或羟基。
本发明的一个实施方案包括式(II)化合物,其中:
B10不存在或选自甲基或乙基,;其中甲基或乙基任选由一个或多个独立选自以下的基团取代:二甲基-氨基或羟基。
本发明的一个实施方案包括式(II)化合物,其中:
B20不存在或选自烷基、链烯基或H;其中,当B20为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基。
本发明的一个实施方案包括式(II)化合物,其中:
B20不存在或选自烷基、链烯基或H;其中,当B20为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基、-NHC(=O)NH2、-NHSO2烷基或硫烷基。
本发明的一个实施方案包括式(II)化合物,其中:B20不存在或为H。
本发明的一个实施方案包括式(II)化合物,其中:
选自芳基、环烷基、部分不饱和的碳环、杂芳基和杂环烷基,其任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
本发明的一个实施方案包括式(II)化合物,其中:
选自苯基、咪唑基、吡啶基、嘧啶基、吡咯烷基、吗啉基、哌嗪基和哌啶基,其任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
本发明的一个实施方案包括式(II)化合物,其中:
选自苯基、咪唑基、吡啶基、嘧啶基、吡咯烷基、吗啉基、哌嗪基和哌啶基,其任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、杂芳基,羟基、羟基烷基、-NHC(=O)NH2、-NHSO2烷基、硝基或-SO2烷基。
本发明的一个实施方案包括式(II)化合物,其中:
本发明的一个实施方案包括式(II)化合物,其中:
选自:1-(3-甲氧基-苯基)-(S*)乙基;2-(3-溴)-吡啶基;2-(3-甲基)-吡啶基;2-(3-甲基-5-溴)-吡啶基;2-(4,6-二甲基)-吡啶基;2-(4-溴代)-吡啶基;2-(哌啶-1-基)-乙基;2,2-二氟-1,3-苯并二氧杂环戊-4-基;2,3-二氯-苄基;2,3-二氯-苯基;2,3-二氢-1H-吲哚-1-基;2,3-二甲氧基-苄基;2,4,6-三氟-苯基;2,4-二氯-苯基;2,4-二氟-苄基;2,4-二甲氧基-苯基;2,4-二甲氧基-苯基;2,5-二氯-苄基;2,5-二氯-苯基;2,5-二氟-苄基;2,5-二氟-苯基;2,5-二甲氧基-苄基;2,5-二甲氧基-苯基;2,6-二氯-苄基;2,6-二氟-苄基;2,6-二氟-苯基;2-溴-3-氟-苯基;2-溴-苄基;2-溴-苯基;2-氯-苄基;2-氯-苯基;2-乙基-苯基;2-氟-苄基;2-氟-苯基;2-呋喃基;2-异丙基-苯基;2-甲氧基-苄基;2-甲氧基-苯基;2-甲基-苄基;2-甲基-苯基;2-吗啉-4-基-乙基;2-吡啶基;2-吡啶基-甲基;2-三氟甲氧基-苄基;2-三氟甲氧基-苯基;2-三氟甲基-4-溴-苯基;2-三氟甲基-苄基;2-三氟甲基-苯基;3-(1-羟基-乙基)-苯基;3-(2,4-二甲氧基)-吡啶基;3-(2-氯代)-吡啶基;3-(2-羟基-乙基-氨基-羰基)-苯基;3-(4-甲氧基)-吡啶基;3-(4-甲基-哌嗪基-羰基)-苯基;3-(4-三氟甲基)-吡啶基;3-(氨基-羰基)-苯基;3-(氨基-磺酰基)-苯基;3-(乙氧基-羰基)-苯基;3-(甲氧基-羰基)-苯基;3-(三氟甲硫基(trifluoromethyl-thio))-苯基;3,4,5-三甲氧基-苯基;3,4-二氯-苄基;3,4-二氯-苯基;3,4-二氟-苄基;3,4-二甲氧基-苯基;3,4-二甲基-苄基;3,4-亚甲二氧基-苯基;3,5-二(叔丁基)-苯基;3,5-二(三氟甲基)-苯基;3,5-二氯-苄基;3,5-二氯-苯基;3,5-二氟-苯基;3,5-二甲氧基-苯基;3,5-二甲基-苯基;3-[N-(3-吡咯烷-1-基-丙基)-氨基-羰基]-苯基;3-苄氧基-苯基;3-溴-苯基;3-羧基-苯基;3-氯-4-氟-苯基;3-氯-4-甲氧基-苯基;3-氯-4-甲基-苄基;3-氯-苄基;3-氯-苯基;3-氰基-苯基;3-乙氧基-苯基;3-乙基-苯基;3-氟-苄基;3-氟-苯基;3-羟甲基-苯基;3-羟基-苯基;3-异丙氧基-苯基;3-甲氧基-5-三氟甲基-苯基;3-甲氧基-苄基;3-甲基-苄基;3-甲基-苯基;3-甲硫基-苯基;3-吡啶基;3-吡啶基-甲基;3-三氟甲氧基-苯基;3-三氟甲基-苯基;4-(4-甲基-哌嗪-1-基)-苯基;4-(乙氧基-羰基)-苯基;4-(N,N-二甲基-氨基)-苯基;4-(哌啶-4-基-磺酰基)-苯基;4-苄氧基-苯基;4-溴-苯基;4-氯-3-甲基-苄基;4-氯-苯基;4-氰基-苯基;4-二甲基氨基-苯基;4-氟-3-氯-苯基;4-氟-3-硝基-苯基;4-氟-3-三氟甲基-苯基;4-氟-苄基;4-氟-苯基;4-甲氧基-苄基;4-甲基-3-[N-[4-(3-吡啶基)-嘧啶-2-基]氨基]-苯基;4-甲基-苄基;4-甲基-苯基;4-三氟甲氧基-苯基;4-三氟甲基-苯基;5-(苯基)-异噁唑-3-基-甲基;5-溴-2,3-二氢-1H-吲哚-1-基;5-氯-2-甲氧基-苯基;5-氯-2-甲基-苯基;5-茚满基;5-吲哚基;5-吲哚基;5-三氟甲基-2-氟-苯基;6-吲唑基;苄基;环己基;环己基-甲基;及苯基。
2.a.2
本发明的一个实施方案包括式(II)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐,其中:
选自式A-1、A-2和A-3:
其中R8为H或低级烷基;
其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达的3个的卤原子在末端碳原子上进一步取代;及
s为0-2的整数;及
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、羟基、-NHC(=O)烷基、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基和硫烷基;
L2是选自以下的连接基团:-(CH2)-、-(CH2)3-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;前提是当L2为-O-时,则R6或者R7不为-CH3;
R100选自:烷基、羟基、芳基、氧代或=N(OH);
R10独立选自
-X1-A20-Y1-A21,-X1-A20-A21,-X1-A21,-A20-A21和-A21,
其中
X1和Y1各自独立不存在或选自:-NH-、-O-、-SO2-和-SO2NH-;
A20不存在或为烷基;
其中当A20为烷基时,则所述烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
A21选自烷基、链烯基或H;
其中当A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
选自芳基、环烷基、部分不饱和的碳环、杂芳基和杂环烷基,其任选由一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
R6和R7独立选自:(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(d)由H为末端的-C(=O)(CH2CH2O-)1-10;
(e)由H为末端的-C(=O)CH2O(CH2CH2O-)1-10;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基或-C(=O)芳基,其中所述-C(=O)芳基可以任选由独立选自以下的一个或多个基因取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基或-N(烷基)2;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基或-C(=O)O芳基,其中所述-C(=O)O芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基或-C(=O)N(C1-20烷基)2,其中所述-C(=O)NH(C1-20)烷基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基或-C(=O)NH芳基,其中所述-C(=O)NH芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(q)-C(=S)NH烷基;
(r)-C(=S)N(烷基)2;
(s)-SO2NH2;
(t)-SO2NH烷基;
(u)-SO2N(烷基)2;
(v)-P(=O)(OCH3)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在;
L3不存在或是选自以下的连接基团:亚甲基、亚乙基、羰基或-SO2-;
r为0-4的整数;和
R5独立选自:烷基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代烷硫基、羟基、羟基烷基、-NHC(=O)NH2、-NHSO2烷基、硝基、-SO2烷基、-SO2NH2,硫基、烷硫基、
和-V-B10-W-B20;
其中
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-NH-、-NHC(=O)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-和-SO2NH-;
B10不存在或为烷基;
其中当B10为烷基时,所述烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
B20不存在或选自烷基、链烯基或H;
其中,当B20为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
选自芳基、环烷基、部分不饱和的碳环、杂芳基和杂环烷基,其任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
本发明的一个实施方案包括式(II)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐,其中
其中式A-5在式A-5的b1边上连接于式(II)的L2环;其中R8为氢和低级烷基;
s为0-2的整数;及
R9独立选自:烷氧基、烷基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、羟基和-NHC(=O)烷基;
L2是选自以下的连接基团:-(CH2)-、-(CH2)3-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;
R100选自:烷基、羟基、芳基、氧代或=N(OH);
R10独立选自
-X1-A20-A21和-X1-A21,其中
X1和Y1各自独立不存在或为-O-;
A20不存在或为烷基;
其中当A20为烷基时,则所述烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基、-NHC(=O)NH2、-NHSO2烷基、-SO2烷基或硫烷基;
A21选自烷基、链烯基或H;
其中当A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基、-NHCO(=O)NH2、-NHSO2烷基或硫烷基;及
选自芳基、杂芳基和杂环烷基,其任选由一个或多个独立选自以下的取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷硫基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(f)-C(=O)烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基或-C(=O)芳基,其中所述-C(=O)芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基、乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基或-N(烷基)2;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基,其由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基或-C(=O)O芳基,其中所述-C(=O)O芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基或-C(=O)N(C1-20烷基)2,其中所述-C(=O)NH(C1-20)烷基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基或-C(=O)NH芳基,其中所述-C(=O)NH芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(u)-SO2N(烷基)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在;
L3不存在或是选自亚甲基、亚乙基或羰基的连接基团;
r为0-4的整数;及
R5独立选自:烷基、烷基氧基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代烷硫基、羟基、羟基烷基、硝基、-SO2NH2,烷硫基、
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-NH-、-O-和-SO2-;
B10不存在或为烷基;
其中当B10为烷基时,所述烷基可以任选由独立选自以下的一个或多个基团取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基-NHC(=O)NH2、-NHSO2烷基、-SO2烷基或硫烷基;
B20不存在或选自烷基、链烯基或H;
其中,当B20为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、二烷基氨基、卤素、卤代烷氧基、羟基、-NHC(=O)NH2、-NHSO2烷基或硫烷基;及
选自苯基、咪唑基、吡啶基、嘧啶基、吡咯烷基、吗啉基、哌嗪基和哌啶基,其任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
2.b式(II-AA)至(II-JJ)
本发明还涉及式(II-AA)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐
其中:
R100选自:H和烷基;
RB和RC独立选自:烷氧基;及
R5选自:烷氧基和卤素。
本发明的一个优选实施方案包括式(II-AA)的化合物,其中R100选自:H、甲基、乙基;RB和RC独立选自:甲氧基和乙氧基;及R5选自:甲氧基、乙氧基、异丙氧基、氯代基、溴代基和氟代基。
本发明还涉及式(II-BB)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐
其中
RC为-O(CH2)3OH;
R100选自:H和烷基;
RB选自:烷氧基;及
R5选自:烷氧基和卤素。
本发明的一个优选实施方案包括式(II-BB)的化合物,其中R100选自:H、甲基、乙基;RB选自:甲氧基和乙氧基;及R5选自:甲氧基、乙氧基、异丙氧基、氯代基、溴代基和氟代基。
本发明还涉及式(II-CC)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐
其中
R100选自:H和烷基;
RB和RC独立选自:烷氧基;及
R5选自:烷基、氰基、羟基、烷氧基和卤素。
本发明的一个优选实施方案包括式(II-CC)的化合物,其中R100选自:H、甲基、乙基;RB和RC独立选自:甲氧基和乙氧基;及R5选自:甲氧基、乙氧基、异丙氧基、氯代基、甲基、氰基和羟基。
本发明还涉及式(II-DD)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐
其中
RC为-O(CH2)3OH;
R100选自:H和烷基;
RB选自:烷氧基;及
R5选自:烷基、氰基、羟基、烷氧基和卤素。
本发明的一个优选实施方案包括式(II-DD)的化合物,其中R100选自:H、甲基和乙基;RB选自:甲氧基和乙氧基;及R5选自:甲氧基、乙氧基、异丙氧基、氯代基、甲基、氰基和羟基。
本发明还涉及式(II-EE)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐
其中
R5选自:烷氧基和卤素;及
Rc选自:烷氧基、
在一个优选的实施方案中,本发明还涉及式(II-FF)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐
其中
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基和烷硫基;
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R100选自:烷基、羟基、芳基、烷氧基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH;前提是当L2为-CH2CH2-时,R6或者R7不为-CH2-(C=O)NH烷基、-CH2-(C=O)N(烷基)2或-CH2C(=O)O烷基;前提是当L2为-OCH(R100)-,R100为烷氧基,且为苯基时,R5不是-C(=O)NH-NH2;及前提是当L2为-O-或-S-时,R6或者R7不为-CH3;
其中X1和Y1各自独立不存在或选自:-(烷基)C(=O)N(烷基)-、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
A20不存在或选自烷基或链烯基;及
A21选自烷基、链烯基或H;
其中当A20或A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由独立选自以下的一个或多个取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
s为0-2的整数;
m为0-4的整数;前提是则m和s的总和为0-4的整数;
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(d)由H、甲基、乙基或苄基为端基的-C(=O)(CH2CH2O-)1-10;
(e)由H、甲基、乙基或苄基为端基的-C(=O)CH2O(CH2CH2O-)1-10;
(f)-C(=O)烷基或-C(=O)(C3-6)环烷基,其中所述-C(=O)烷基和-C(=O)(C3-6)环烷基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基或-C(=O)杂芳基,其中所述-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基和-C(=O)杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基或-C(=O)O(C3-6)环烷基,其中所述-C(=O)O烷基和-C(=O)O(C3-6)环烷基可以由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基,其中所述-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基或-C(=O)N(烷基)2,其中所述-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基和-C(=O)N(烷基)2可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基或-C(=O)NH杂芳基,其中所述-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基和-C(=O)NH杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2-CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(q)-C(=S)NH烷基;
(r)-C(=S)N(烷基)2;
(s)-SO2NH2;
(t)-SO2NH烷基;
(u)-SO2N(烷基)2;
(v)-P(=O)(OCH3)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在;
L3不存在或为选自烷二基、羰基或-SO2-的连接基团;
r为0-4的整数;及
R5独立选自:烷基、烷基氨基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH、-CH2OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代SO2-烷基、卤代烷硫基、羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、-SO2NH2,硫基、烷硫基、
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
B10不存在或选自烷基或链烯基;
B20不存在或选自烷基、链烯基或H;
其中,当R10或B20为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
选自:芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基,其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基,任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
本发明的其它实施方案包括式II-FF的化合物,其中L2、R4、R6、R7、L3H和(R5)r的定义变化如在以上2.a.1部分对式II和其变量的组合所述。
在一个优选的实施方案中,本发明还涉及式(II-GG)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐:
其中:
其中式A-1在式A-1的b1边上连接于式(II-GG)的L2环,并任选由一个选自式A-1-a、A-1-b和A-1-c的取代基取代:
其中式A-1-a在其a1边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-b在其a2边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-c在其a6边上连接于式A-1的d1或d2边上的相邻碳原子;
其中R8为氢或烷基;
其中式A-2在式A-2的b2边上连接于式(II-GG)的L2环,且A1、A2、A3、A4为(i)-N-;或(ii)由H或烷氧基取代的-C-,其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达3个的卤原子在末端碳原子上进一步取代;前提是A1、A2、A3、A4中的至少一个但不多于两个为-N-;及
其中式A-3在式A-3的b3边上连接于式(II-GG)的L2环,且B1、B2和B3独立为(i)任选由烷基、芳基、烷氧基或卤素取代的-CH-,
(ii)-S-;(iii)-O-;或(iv)-N-;前提是B1、B2或B3中不超过一个为-S-或-O-,且前提是当B1、B2或B3其中之一为-S-或-O-时,则相邻的环成员不为-S-或-O-;
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基和烷硫基;
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH--N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R100选自:烷基、羟基、芳基、烷氧基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH;前提是当L2为-OCH(R100)-,R100为烷氧基和为苯基时,R5不是-C(=O)NH-NH2;
R10独立选自和-X1-A20-Y1-A21;
其中X1和Y1各自独立不存在或选自:-(烷基)C(=O)N(烷基)-、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)- 、-N(烷基)C(=O)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
A20不存在或选自烷基或链烯基;及
A21选自烷基、链烯基或H;
其中当A20或A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由独立选自以下的一个或多个取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
s为0-2的整数;
R6和R7独立选自:
(a)H;
(c)烷基
(d)-C(=O)烷基OH;及
(e)-C(=O)CH2O烷氧基;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在;
L3不存在或为选自烷二基、羰基或-SO2-的连接基团;
r为0-4的整数;及
R5独立选自:烷基、烷基氨基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH、-CH2OH、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代SO2-烷基、卤代烷硫基、羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、-SO2NH2,硫基、烷硫基、
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
B10不存在或选自烷基或链烯基;
B20不存在或选自烷基、链烯基或H;
其中,当B10或B20为烷基或链烯基时,所述烷基或链烯基可以任选
由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
本发明的其它实施方案包括式II-GG的化合物,其中E、L2、R4、L3H和(R5)r,及上述E、L2、R4、L3H和(R5)r的变量的组合的定义变化如在以上2.a.1部分对式II的描述,而R6和R7的定义变化如下所述。
本发明的一个优选的实施方案为式II-GG的化合物,其中R7不存在,R6选自:
(a)H;
(c)甲基;
(d)-C(=O)CH2OH;及
(e)-C(=O)CH2O甲氧基。
在一个优选的实施方案中,本发明还涉及式(I1-HH)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐:
其中:
其中式A-1在式A-1的b1边上连接于式(II-HH)的L2环,并任选由一个选自式A-1-a、A-1-b和A-1-c的取代基取代:
其中式A-1-a在其a1边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-b在其a2边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-c在其a6边上连接于式A-1的d1或d2边上的相邻碳原子;
其中R8为H或烷基;
其中式A-2在式A-2的b2边上连接于式(II-HH)的L2环,且A1、A2、A3、A4为(i)-N-;或(ii)由H或烷氧基取代的-C-,其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达3个的卤原子在末端碳原子上进一步取代;前提是A1、A2、A3、A4中的至少一个但不多于两个为-N-;及
其中式A-3在式A-3的b3边上连接于式(II-HH)的L2环,且B1、B2和B3独立为(i)任选由烷基、芳基、烷氧基或卤素取代的-CH-,
(ii)-S-;(iii)-O-;或(iv)-N-;前提是B1、B2或B3中不超过一个为-S-或-O-,且前提是当B1、B2或B3之一为-S-或-O-时,则相邻的环成员不为-S-或-O;
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基和烷硫基;
L2是选自以下的连接基团:-(CH2)-、-CH(CH3)-、-CH(CH2CH3)-和-O-,前提是当L2为-O-时,则R6或者R7不为-CH3;
其中X1和Y1各自独立不存在或选自:-(烷基)C(=O)N(烷基)-、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
A20不存在或选自烷基或链烯基;及
A21选自烷基、链烯基或H;
其中当A20或A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由独立选自以下的一个或多个取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
s为0-2的整数;
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-(C=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(d)由H、甲基、乙基或苄基为末端的-C(=O)(CH2CH2O-)1-10;
(e)由H、甲基、乙基或苄基为端基的-C(=O)CH2O(CH2CH2O-)1-10;
(f)-C(=O)烷基或-C(=O)(C3-6)环烷基,其中所述-C(=O)烷基和-C(=O)(C3-6)环烷基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基或-C(=O)杂芳基,其中所述-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基和-C(=O)杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(l)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基或-C(=O)O(C3-6)环烷基,其中所述-C(=O)O烷基和-C(=O)O(C3-6)环烷基可以由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基,其中所述-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基,苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基或-C(=O)N(烷基)2,其中所述-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基和-C(=O)N(烷基)2可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基或-C(=O)NH杂芳基,其中所述-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基和-C(=O)NH杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(q)-C(=S)NH烷基;
(r)-C(=S)N(烷基)2;
(s)-SO2NH2;
(t)-SO2NH烷基;
(u)-SO2N(烷基)2;
(v)-P(=O)(OCH3)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在;
L3不存在或为选自烷二基、羰基或-SO2-的连接基团;
r为0-4的整数;及
R5独立选自:烷基、烷基氨基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH、-CH2OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代SO2-烷基、卤代烷硫基、羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、-SO2NH2,硫基、烷硫基、和-V-B10-W-B20;其中,
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
B10不存在或选自烷基或链烯基;
B20不存在或选自烷基、链烯基或H;
其中,当R10或B20为烷基或链烯基时,则所述烷基或链烯基可以任选由一个或多个独立选自以下的基团取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
本发明的其它实施方案包括式II-HH的化合物,其中E、R4、R6、R7、L3H和(R5)r,及上述E、R4、R6、R7、L3H和(R5)r的变量的组合的定义变化如在以上2.a.1部分对式II的描述,而L2的定义变化如下所述。
本发明的一个优选的实施方案为式II-HH的化合物,其中L2是选自以下的连接基团:-(CH2)-、-CH(CH3)-、-CH(CH2CH3)-。在一个优选的实施方案中,本发明还涉及式(II-JJ)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐:
其中
R6和R7独立选自:
(a)H;
(c)由选自以下的一个基团取代的-CH2-:-H、-甲基、-O烷基、-CH2OH、-CH(CH3)OH、-O(C=O)烷基、-(C=O)OH、-C(=O)O烷基、-C(=O)O芳基、-C(=O)O杂芳基、-C(=O)NH2、-(C=O)NH烷基、-(C=O)N(烷基)2、-C(=O)烷基、-苯基-OCH3或-苯基-OC(=O)烷基;
(d)由H、甲基、乙基或苄基为末端的-C(=O)(CH2CH2O-)1-10;
(e)由H、甲基、乙基或苄基为端基的-C(=O)CH2O(CH2CH2O-)1- 10;
(f)-C(=O)烷基或-C(=O)(C3-6)环烷基,其中所述-C(=O)烷基和-C(=O)(C3-6)环烷基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-O烷基芳基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基或-OC(=O)烷基;
(g)-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基或-C(=O)杂芳基,其中所述-C(=O)(CH2)1-3芳基、-C(=O)芳基、-C(=O)(CH2)1-3杂芳基和-C(=O)杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(h)由以下基团为端基的-C(=O)(CH2)1-6C(=O)-:甲基,乙基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(hh)由以下基团为端基的-C(=O)烷基OC(=O)烷基-:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2或杂环烷基;
(i)由H、甲基、乙基或苄基为端基的-C(=O)O(CH2CH2O-)1-10;
(j)-C(=O)O烷基或-C(=O)O(C3-6)环烷基,其中所述-C(=O)O烷基和-C(=O)O(C3-6)环烷基可以由独立选自以下的一个或多个基团任选取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;
(k)-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基,其中所述-C(=O)O(CH2)1-3芳基、-C(=O)O芳基、-C(=O)O(CH2)1-3杂芳基或-C(=O)O杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(l)由以下基团为端基的-C(=O)NH(CH2CH2O-)1-10:-H、甲基、乙基、苄基、-CH2CH2NH2、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基或-C(=O)烷基;
(m)-C(=O)NH2、-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基或-C(=O)N(烷基)2,其中所述-C(=O)NH(C1-20)烷基、-C(=O)NH(C3-6)环烷基和-C(=O)N(烷基)2可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)链烯基、-NHC(=O)芳基、-C(=O)OH、-C(=O)O烷基、-C(=O)NH2、-C(=O)NH烷基或-C(=O)N(烷基)2;且其中所述-NHC(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、卤素或腈;
(n)-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基或-C(=O)NH杂芳基,其中所述-C(=O)NH(CH2)1-3芳基、-C(=O)NH芳基、-C(=O)NH(CH2)1-3杂芳基和-C(=O)NH杂芳基可以任选由独立选自以下的一个或多个基团取代:-OH、-O烷基、-NH2、-NH烷基、-N(烷基)2、杂环烷基、-NHC(=O)烷基、-NHSO2烷基、卤素、腈或-OC(=O)烷基;
(o)由以下基团为端基的-C(=O)NHCH2CH2NH(CH2CH2NH-)0-3:H、甲基、乙基、-CH2CH2NH烷基、-CH2CH2N(烷基)2、-CH2CH2-1-吡咯烷基、-CH2CH2-1-哌啶基、-CH2CH2-4-吗啉基、-CH2CH2-1-哌嗪基、-CH2CH2-1-(4-CH3)-哌嗪基、-CH2CH2OH、-CH2CH2OCH3、-CH2CH2OCH2CH3、-CH2CH2OC(=O)烷基或-C(=O)芳基;其中所述-C(=O)芳基的芳基部分可以任选由独立选自以下的一个或多个基团取代:烷基、-OH、-O烷基、-NH2、NH烷基、-N(烷基)2、卤素或腈;
(p)-C(=S)NH2;
(q)-C(=S)NH烷基;
(r)-C(=S)N(烷基)2;
(s)-SO2NH2;
(t)-SO2NH烷基;
(u)-SO2N(烷基)2;
(v)-P(=O)(OCH3)2;及
(w)-P(=O)(OCH2CH3)2;
前提是当R6存在时,则R7不存在;及前提是当R7存在时,则R6不存在;
本发明的其它实施方案包括式II-JJ的化合物,其中R6和R7的定义变化如在以上2.a.1部分对式II的描述。
2.c优选的化合物
在一个优选的实施方案中,本发明还涉及选自以下的化合物:
在一个优选的实施方案中,本发明还涉及选自以下的化合物:
在一个优选的实施方案中,本发明还涉及下式的化合物:
在一个优选的实施方案中,本发明还涉及下式的化合物:
在一个优选的实施方案中,本发明还涉及下式的化合物:
在一个优选的实施方案中,本发明还涉及下式的化合物:
2.d.式(IIa)化合物的制备
本发明还涉及一种制备式(IIa)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐的方法:
其中:
其中式A-1在式A-1的b1边上连接于式(II)的L2环,并任选由一个选自式A-1-a、A-1-b和A-1-c的基团取代:
其中式A-1-a在其a1边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-b在其a2边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-c在其a6边上连接于式A-1的d1或d2边上的相邻碳原子;
其中R8为H或烷基;
其中式A-2在式A-2的b2边上连接于式(II)的L2环,且A1、A2、A3、A4为(i)-N-;或(ii)由H或烷氧基取代的-C-,其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达3个的卤原子在末端碳原子上进一步取代;前提是A1、A2、A3、A4中的至少一个且不超过两个为-N-;及
其中式A-3在式A-3的b3边上连接于式(II)的L2环,且B1、B2和B3独立为(i)由C1-4烷基、芳基、烷氧基或卤素任选取代的-CH-,(ii)-S-;(iii)-O-;或(iv)-N-;前提是B1、B2或B3中不超过一个为-S-或-O-,且前提是当B1、B2或B3之一为-S-或-O-时,则相邻的环成员不是-S-或-O-;
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基和烷硫基;
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R100选自:烷基、羟基、芳基、烷氧基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH;前提是当L2为-OCH(R100)-,R100为烷氧基和为苯基时,R5不是-C(=O)NH-NH2;
其中X1和Y1各自独立不存在或选自:-(烷基)C(=O)N(烷基)-、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
A20不存在或选自烷基或链烯基;及
A21选自烷基、链烯基或H;
其中当A20或A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由独立选自以下的一个或多个取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
s为0-2的整数;
L3不存在或为选自烷二基、羰基或-SO2-的连接基团;
选自芳基、环烷基、部分不饱和的碳环、芳烷基、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基、9-10元苯并-稠合的杂芳基和9-10元苯并-稠合的杂环烷基;
r为0-4的整数;及
R5独立选自:烷基、烷基氨基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH、-CH2OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代SO2-烷基、卤代烷硫基、羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、-SO2NH2,硫基、烷硫基、
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、-SO2-、-SO2N(烷基)-和-SO2NH-;
B10不存在或选自烷基或链烯基;
B20不存在或选自烷基、链烯基或H;
其中,当R10或B20为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基、羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基;
该方法包括
在碱的存在下,在非质子溶剂中,使式(T1)化合物与1,1′-硫代羰基二咪唑反应,得到相应的式(T5)化合物;
在非质子溶剂中,使式(T5)化合物与式(T6)化合物反应,得到相应的式(T3)化合物;
使式(T3)化合物与肼反应,得到相应的式(IIa)化合物。
本发明还涉及一种制备式(T5)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐的方法
其中:
其中式A-1在式A-1的b1边上连接于式(II)的L2环,并任选由一个选自式A-1-a、A-1-b和A-1-c的取代基取代:
其中式A-1-a在其a1边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-b在其a2边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-c在其a6边上连接于式A-1的d1或d2边上的相邻碳原子;
其中R8为H或烷基;
其中式A-2在式A-2的b2边上连接于式(II)的L2环,且A1、A2、A3、A4为(i)-N-;或(ii)由H或烷氧基取代的-C-,其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达的3个的卤原子在末端碳原子上进一步取代;前提是A1、A2、A2、A4中的至少一个但不多于两个为-N-;及
其中式A-3在式A-3的b3边上连接于式(II)的L2环,且B1、B2和B3独立为(i)任选由烷基、芳基、烷氧基或卤素取代的-CH-,(ii)-S-(iii)-O-;或(iv)-N-;前提是B1、B2或B3中不超过一个为-S-或-O-,且前提是当B1、B2或B3之一为-S-或-O-时,则相邻的环成员不是-S-或-O-;
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基和烷硫基;
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)-、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R100选自:烷基、羟基、芳基、烷氧基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH;
R10独立选自和-X1-A20-Y1-A21;
其中X1和Y1各自独立不存在或选自:-(烷基)C(=O)N(烷基)-、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
A20不存在或选自烷基或链烯基;及
A21选自烷基、链烯基或H;
其中当A20或A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由独立选自以下的一个或多个取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
s为0-2的整数;
该方法包括
在碱的存在下,在非质子溶剂中,使式(T1)化合物与1,1′-硫代羰基二咪唑反应,得到相应的式(T5)化合物。
本发明还涉及一种制备式(T3)化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐的方法,
其中:
选自式A-1、A-2和A-3:
其中式A-1在式A-1的b1边上连接于式(II)的L2环,并任选由一个选自式A-1-a、A-1-b和A-1-c的取代基取代:
其中式A-1-a在其a1边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-b在其a2边上连接于式A-1的d1或d2边上的相邻碳原子;
其中式A-1-c在其a6边上连接于式A-1的d1或d2边上的相邻碳原子;
其中R8为H或烷基;
其中式A-2在式A-2的b2边上连接于式(II)的L2环,且A1、A2、A3、A4为(i)-N-;或(ii)由H或烷氧基取代的-C-,其中所述烷氧基可以任选由烷氧基在末端碳原子上或由最多可达3个的卤原子在末端碳原子上进一步取代;前提是A1、A2、A3、A4中的至少一个但不多于两个为-N-;及
其中式A-3在式A-3的b3边上连接于式(II)的L2环,且B1、B2和B3独立为(i)任选由烷基、芳基、烷氧基或卤素取代的-CH-,(ii)-S-;(iii)-O-;或(iv)-N-;前提是B1、B2或B3中不超过一个为-S-或-O-,且前提是当B1、B2或B3其中之一为-S-或-O-时,则相邻的环成员不是-S-或-O-;
R9独立选自:烷氧基、烷基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基和烷硫基;
L2是选自以下的连接基团:-(CH2)1-4-、-CH(R100)-、-C(=R100)-、-C(R100)2-、-O-、-O(CH2)1-4-、-OCH(R100)、-OC(R100)2-、-S-、-NH-、-N(低级烷基)-、-N(CO烷基)-、-N(芳基)-、-N(CO2烷基)-、-N(CONH烷基)-、-N(SO2烷基)和-N(SO2芳基)-;其中R100选自:烷基、羟基、芳基、烷氧基、氧代基、-NH2、-NH(烷基)-N(烷基)2、=N(OH)或-NH2OH;前提是当L2为-OCH(R100)-,R100为烷氧基和为苯基时,R5不是-C(=O)NH-NH2;
其中X1和Y1各自独立不存在或选自:-(烷基)C(=O)N(烷基)-、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
A20不存在或选自烷基或链烯基;及
A21选自烷基、链烯基或H;
其中当A20或A21为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;
选自芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、9-10元苯并-稠合的环烷基和9-10元苯并-稠合的杂环烷基;其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由独立选自以下的一个或多个取代基取代:卤素、羟基、氨基、硫基、硝基、氰基、烷基、卤代烷基、烷氧基、卤代烷氧基、烷基氨基、-NHC(=O)烷基、-N(烷基)C(=O)烷基或二烷基氨基、-NHC(=O)NH2、-NHC(=O)NH烷基、-N(烷基)C(=O)NH烷基、-OC(=O)NH烷基、-NHC(=O)O烷基、-N(烷基)C(=O)O烷基、-NHSO2烷基、-N(烷基)SO2烷基、烷硫基、卤代烷硫基、-SO2烷基、卤代-SO2烷基、-NHC(=O)N(烷基)2、-N(烷基)C(=O)N(烷基)2或-OC(=O)N(烷基)2;
s为0-2的整数;
b或A-1-c之一取代时,则m和s的总和为0-2的整数;
L3不存在或为选自烷二基、羰基或-SO2-的连接基团;
r为0-4的整数;及
R5独立选自:烷基、烷基氨基、烷氧基、氨基、-C(=O)NH2、-C(=O)O烷基、-C(=O)OH、-CH2OH,氰基、二烷基氨基、卤素、卤代烷基、卤代烷氧基、卤代SO2-烷基、卤代烷硫基、羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、-SO2NH2,硫基、烷硫基、
和-V-B10-W-B20;其中,
V和W各自独立不存在或选自:-C(=O)、-C(=O)N(烷基)-、-C(=O)NH-、-C(=O)O-、-N(烷基)-、-N(烷基)C(=O)-、-N(烷基)C(=O)N(烷基)-、-N(烷基)C(=O)NH-、-N(烷基)C(=O)O-、-N(烷基)SO2-、-NH-、-NHC(=O)-、-NHC(=O)N(烷基)-、-NHC(=O)NH-、-NHC(=O)O-、-NHSO2-、-O-、-OC(=O)、-OC(=O)N(烷基)-、-OC(=O)NH-、-OC(=O)O-、-S-、-SO-、SO2-、-SO2N(烷基)-和-SO2NH-;
B10不存在或选自烷基或链烯基;
B20不存在或选自烷基、链烯基或H;
其中,当B10或B20为烷基或链烯基时,所述烷基或链烯基可以任选由独立选自以下的一个或多个取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代-SO2烷基、卤代烷硫基、羟基-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、-OC(=O)烷基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-OC(=O)O烷基、-SO2烷基、硫基或烷硫基;及
其中,所述芳基、环烷基、部分不饱和的碳环、杂芳基、杂环烷基、苯并-稠合的环烷基或苯并-稠合的杂环烷基任选由一个或多个独立选自以下的取代基取代:烷氧基、烷基氨基、氨基、氰基、二烷基氨基、卤素、卤代烷氧基、卤代烷基、卤代-SO2烷基、卤代烷硫基、杂芳基,羟基、羟基烷基、-N(烷基)C(=O)烷基、-N(烷基)C(=O)N(烷基)2、-N(烷基)C(=O)NH烷基、-N(烷基)C(=O)O烷基、-N(烷基)SO2烷基、-NHC(=O)烷基、-NHC(=O)N(烷基)2、-NHC(=O)NH2、-NHC(=O)NH烷基、-NHC(=O)O烷基、-NHSO2烷基、硝基、-OC(=O)N(烷基)2、-OC(=O)NH烷基、-SO2烷基、硫基或烷硫基。
该方法包括
在非质子溶剂中,使式(T5)化合物与式(T6)化合物反应,得到相应的式(T3)化合物。
代表性的化合物
本发明的一个实施方案为下面表1至13所列的化合物。由″MS″指明的分子量以m/z(M+H)+单位表示。已合成的化合物列于表1至5和表7至13中。
(参照式(I)和(II)的化合物,G表示在式(I)中的
在下面的表4和6中,环(A/E环)(在式(I)中表示(A环)和在式(II)中表示(E环))按照惯例以顺时针方向计数编号,除非依照特别指明,在前的编号表示连接于核心分子的剩余部分的碳原子。因此,例如,对于在下面的结构中的A/E环
取代基将被命名为4,5-(3-甲基-异噁唑基)。
指定的A/E环,后面带有*(星号)的取代基按照惯例以反时针方向编号。例如,在下面的A/E环结构中
取代基将被命名为5,6-(2-甲基-8-乙氧基-苯并噁唑基)*。
另外,当A/E环是苯基时,所述苯基被定义为连接于1,2位,且苯基环取代基以顺时针方向计数编号,如在上面的第一个结构(4,5-异噁唑基)中所示。
表1
表2
表3
表4
表5
表6
表7
表8
表9
表10
表11
表12
表13
除非另外指明,本文所用的术语″烷基″,无论是单独使用或是作为取代基的一部分使用时,包括具有1-10个碳原子或在此范围内的任何数目的直链或支链。例如,烷基包括甲基、乙基、正丙基、异丙基、正丁基,异丁基、仲丁基、叔丁基、正戊基、3-(2-甲基)丁基、2-戊基、2-甲基丁基、新戊基、正己基、2-己基、2-甲基戊基等。除非另外指明,低级烷基包括具有1-4个碳原子或在此范围内的任何数目的直链或支链。
除非另外指明,术语″烷氧基″或″烷基氧基″在本文中作为同义词使用,在此使用时,无论是单独使用或是作为取代基的一部分使用,指上述的直链或支链烷基的氧醚基。例如,烷氧基包括甲氧基、乙氧基、正丙氧基、仲丁氧基、叔丁氧基、正己基氧基等。与烷基部分有关的氧原子的具体位置以下列方式特别指明,″-O烷基″或″-烷基O-″分别描述-OCH3和-CH2O-(其中烷基的例子为甲基)。
除非另外指明,″芳基″单独或与其它术语结合使用(如,芳氧基、芳硫基(arylthioxy)、芳烷基)时,应指包括碳原子的芳环结构,例如,苯基、萘基、芴基等。
除非另外指明,本文所用的,″芳烷基″应指由芳基(如苯基、萘基等)取代的任何低级烷基,例如,苄基、苯乙基、苯基丙基、萘基甲基等。
除非另外指明,本文所用的术语″环烷基″,无论是单独使用或是作为取代基的一部分使用时,应指任何稳定的3-10元饱和环系,例如环丙基、环丁基、环戊基、环己基、环庚基和环辛基。
除非另外指明,本文所用的术语″部分不饱和的碳环″,无论是单独使用或是作为取代基的一部分使用时,应指任何稳定的5-10元部分不饱和的环系,其中所述碳环含有至少一个不饱和键,例如环戊烯基、环己烯基、环庚烯基等。
除非另外指明,如本文所用的术语″杂芳基″,无论是单独使用或是作为取代基的一部分使用时,应指任何5-10元单环或二环芳环结构,其包含碳原子和至少一个选自O、N和S的杂原子,任选含有1-4个独立选自O、N和S的另外的杂原子。所述杂芳基可以连接于所述环的任何杂原子或碳原子上,以便产生一种稳定的结构。合适的杂芳基的实例包括,但不限于,吡咯基、呋喃基、噻吩基、噁唑基、咪唑基、吡唑基、异噁唑基、异噻唑基、三唑基、噻二唑基、吡啶基,哒嗪基、嘧啶基,吡嗪基、吡喃基、呋咱基、中氮茚基、吲哚基、异吲哚基、吲唑基、苯并呋喃基、苯并噻吩基、苯并咪唑基,苯并噻唑基、嘌呤基、喹嗪基、喹啉基、异喹啉基、异噻唑基、肉啉基、2,3-二氮杂萘基、喹唑啉基、喹喔啉基、1,5-二氮杂萘基、蝶啶基等。
本文所用的术语″杂环烷基″应指任何5-10元单环或二环的、饱和或部分不饱和的环结构,其包含C原子和至少一个选自O、N和S的杂原子,任选含有1-4个独立选自O、N和S的另外的杂原子。所述单环或二环杂烷基基团可以连接于所述环的任何杂原子或碳原子上,以便产生一种稳定的结构。合适的单环或二环杂烷基的实例包括,但不限于,吡咯啉基、吡咯烷基、二氧戊环基、咪唑啉基、咪唑烷基、吡唑啉基、吡唑烷基、哌啶基、二氧六环基、吗啉基、二噻烷基、硫代吗啉基、哌嗪基、三噻烷基、二氢吲哚、苯并吡喃基、1,3-亚甲二氧基苯基(相当于苯并稠合的二氧杂环戊基),1,4亚乙基二氧基苯基(相当于苯并稠合的二氧六环基)、2,3-二氢苯并呋喃基等。
除非另外指明,本文所用的,术语″苯并-稠合的杂芳基″应指二环环结构,其中一个环为苯基,而另一个是5-6元杂芳基。苯并-稠合的杂芳基为杂芳基的一个子集。合适的实例包括,但不限于,吲哚基、异吲哚基、苯并呋喃基、苯并噻吩基、吲唑基、苯并噻唑基、喹啉基、异喹啉基、肉啉基、2,3-二氮杂萘基、喹唑啉基、蝶啶基等。
除非另外指明,本文所用的术语″苯并-稠合的杂环烷基″应指二环环结构,其中一个环为苯基,而另一个环是一个5-6元杂环烷基。所述苯并稠合的杂环烷基为杂环烷基的一个子集。合适的实例包括,但不限于,1,3-苯并二氧杂环戊基(也称作1,3-亚甲二氧基苯基),二氢吲哚基、1,4-苯并二氧戊环基(也称作1,4-亚乙基二氧基苯基)、苯并二氢呋喃基、苯并四氢吡喃基、苯并二氢噻吩等。
除非另外指明,本文所用的,术语″苯并-稠合的环烷基″应指二环环结构,其中一个环为苯基,而另一个环是3-8元环烷基。合适的实例包括,但不限于茚满基、1,2,3,4-四氢萘基、6,7,8,9-四氢-5H-苯并环庚烯基、5,6,7,8,9,10-六氢苯并环辛烯基等。
本文所用的术语″连接基团″意指例如从两个不同的原子的每一个中除去至少一个氢原子或从单个原子中除去两个氢原子所衍生的二价基团,从而使所述两个单价基团中心或单一的二价基团中心与不同的原子形成键。
本文所用的术语″烷二基″应包括1-10个碳原子的或在此范围内的任何数目的碳原子的直链和支链二价或单价烃基,所述烃基由两个不同的碳原子中的每一个除去一个氢原子或从单个碳原子除去两个氢原子所衍生。实例包括甲二基(methyldiyl)(在此也称为亚甲基)和乙二基(ethyldiyls)(在此也称为亚乙基),如乙-1,1-二基和乙-1,2-二基。
一般来说,IUAC命名法规则用于本公开全文之中。对于基团取代基的命名由第一个指定的具有连字符的连接点的官能团开始,继之以朝着侧链的末端部分的相邻官能团来推导,如下例中:
-(C1-10)烷基-C(O)NH-(C1-10)烷基-苯基或者,在不使用前导的连字符时,首先由描述侧链的末端部分开始,继之以朝向连接点的相邻官能团来推导,如在下例中:
苯基-(C1-10)烷基酰氨基(C1-10)烷基,或
苯基烷基酰氨基烷基
所有这三种均指下式的基团:
当存在两个连接点时,例如在连接基团中,或在环成员上,用前面的连字符和最后的连字符指示两个连接点。例如,具有两个单价基团中心的连接基团的连接点将被表示为-(CH2)2-或-O(CH2)2-等;具有一个单一二价基团中心的连接基团的连接点将被表示为-NH-或-N(C=O烷基)-等。芳环成员的连接点将被表示为例如-N-、-S-或-CH-等。
当使用短语″为端基″时,末端取代基的连接点用第二个短划线表示。例如,对于短语″由-H、甲基、乙基或苄基为端基的-C(=O)-(CH2CH2O-)1-10″,所选择的末端取代基的连接点为末端氧,例如,-C(=O)-(CH2CH2OH)或-C(=O)-(CH2CH2OCH2CH2OCH2CH2OCH3)。
当一个特定基团(如苯基、芳基、杂烷基、杂芳基)被″取代″时,该基团可具有一个或多个取代基,优选1-5个取代基,更优选1-3个取代基,最优选1-2个取代基,所述取代基独立选自取代基的表中。
对取代基而言,术语″独立地″意指当可能有一个以上的这样的取代基时,这样的取代基可以彼此相同或不同。
一个分子中具体位置上的任何取代基或变量的定义与该分子其它位置上的定义意欲是彼此独立的。应该理解,本领域普通技术人员可以选择本发明化合物上的取代基和取代类型,以提供化学上稳定的且可通过本领域已知的技术和本文提出的那些方法容易地合成的化合物。
本发明中举例说明的化合物可根据本领域熟知的命名法命名,或者采用Autonom 2.2版(由CambridgeSoft.Com上市的ChemDrawUltra7.0.1 Office Suite提供的命名法软件商标)命名。
本申请书(特别是流程和实施例)中所使用的缩写词如下:
Aq. = 水溶液
ATP = 三磷酸腺苷
DBU = 2,2′-二氮杂双环十一烷
DCM = 二氯甲烷
DME = 1,2-二甲氧基乙烷
DMF = N,N-二甲基甲酰胺
DMSO = 二甲亚砜
DTT = 二硫苏糖醇
EtOAc = 乙酸乙酯
HPLC = 高效液相色谱法
IprOH = 异丙醇
MeOH = 甲醇
PBS = 磷酸盐缓冲盐水
PLC = 磷脂酶C
RAR = 大鼠主动脉环
Sat. = 饱和的
SMGS = 平滑肌生长补充物
TFA = 三氟乙酸
THF = 四氢呋喃
TLC = 薄层层析
Tris HCI或tris-Cl = 三[羟甲基]氨基甲基盐酸盐
本发明的化合物可以通过如下所述任何数目的通用方法和在以下实施例中更明确地描述的方法制备。
在制备本文所述的本发明的化合物的任何方法中,保护所涉及的任何分子上的敏感的或反应性基团(例如羟基、氨基、硫基、氧代基或羰基)可能是必要的和/或需要的。这可通过常规保护基团的方法实现,如在Protective Groups in Organic Chemistry(有机化学中的保护基团),ed.J.F.W.McOmie,Plenum Press,1973;及T.W.Greene & P.G.M.Wuts,Protective Groups in Organic Synthesis(有机合成中的保护基团).John Wiley & Sons,1991中所述的那些基团。所述保护基团可通过采用本领域已知的方法在随后的方便的阶段中除去。
合成方法
合成本发明化合物的方法包括但不限于下述的方法。方法A至E中所用的起始原料通常为式(S1)的原料酮
其中R1、R2、R3、p、q和n如本文对式(I)中所述,式(S1)化合物或者是已知的或者是可市售获得的化合物,或者是可通过已知的化学方法由已知的化合物制备。
芳香酮可通过Friedel-Crafts反应制备(见Practical OrganicChemistry,由Vogel编辑,第三版,724-749页)。例如,如在该文献中所述,式(S1a)的取代的芳基丙酸或其衍生物的Friedel-Crafts酰化将得到取代的式(S1b)的茚满-1-酮。类似地,取代的芳基丁酸或其衍生物的Friedel-Crafts酰化将得到取代的α-四氢萘酮(例如,见Cho,H等,Heterocycles(1996),43(1),127-131;Baddeley等,J. Chem.Soc,(1956),4647;Reeve等,J. Amer.Chem.Soc.(1951),73,1371)
式(S1b)的原料酮还可通过采用各种已知的氧化剂,由式(S1c)的相应的醇或式(S1d)的链烷烃的氧化来制备(例如,见Mandal等,Tetrahedron Lett,(1996),37(21),3769-3772;Ishihara等,J.Org. Chem.(1997),62(17),5664-5665)。
原料吡啶基杂芳基酮可以通过式(S1e)的二酮或式(S1g)的烯胺酮(enaminones)分别与式(S1f)的丙二缩酮(propandiketals)或式(S1h)的丙烯醛(propenaldehydes)缩合来制备(实例见:Huang等,Synth.Commun.(1998),28(7),1197-1200;Reimann等,Pharmazie(1995),50(9),589-592)。
使用氯化铝、多磷酸或三氟乙酸等,通过杂芳基丙酸的Friedel-Crafts酰化,得到环化的酮可以制备原料噻吩基杂芳基酮。(例如见Cantrell等,Tetrahedron Lett(1967),4477;Muraro等,C R Hebd SeancesAcad Sci(1971),273,1362;Macdowell等,J.Org.Chem.(1967),32,1226;Binder等,Monatsh Chem(1998),129(8),887-896)。
式(S1)的原料呋喃基杂芳基酮也可以根据Kraus等,Synlett(1997),11,1259-1260;Hoye等,J.Org.Chem.(1990),55(15),4518;及Lee等,Bull Korean Chem.Soc.(1998),19(10),1080-1083中所述方法制备。
原料吡咯基酮可以通过酰胺内鎓盐(azomethide ylide)与如下所示的限制性的炔烃进行分子内的环加成反应而制备(Nayyar等,J.Org.Chem.(1997),62(4),982-991)。另外,原料吡咯酮可以通过二酮与α-溴代酮或α-溴代丙酮酸酯反应,然后用合适的取代的胺进行Paal-Knorr环化来制备(例如,见Stojanovic等,J. Serb.Chem.Soc.(1997),62(9),749-7530)。
噻唑基杂芳基酮可以按Maillard等,在Eur.J.Med. Chem.Ther(1984),19(5),451中所述,通过溴代酮与硫代乙酰胺的缩合制备。
噁唑酮和呋喃基酮可以通过铑催化的α-二氮杂-酮与腈或乙炔的环加成反应来制备。类似地,碘鎓内盐可以经历Rh2(OAc)4催化的与乙炔和腈的热[3+2]-环加成反应,分别形成相应的呋喃和噁唑。(例如见Lee等,Heterocycles(1998),48(5),875-883;及Gogonas等,Tetrahedron Lett.(2000),41(48),9299-9303)。
原料异噁唑酮可以通过如下所示的方法,通过N-氧化物与环二酮或烯酮的环加成,以一步反应制备(例如见Akhrem等,Khim.Geterotsikl.Soedin.(1974),7,901-4;Akhrem等,Synthesis(1978),1,43)。
本领域技术人员应该认识到,制备本发明的化合物的所述起始原料,即上述式(S1)化合物,为已知的化合物或为可以根据已知方法(例如,如上概述的方法)制备的化合物。原料式(S1)化合物,其中n选自2-4,为类似的已知化合物,或可根据已知方法类似地制备或通过修饰上述例举的方法而制备。
方法A
式(I)化合物可以根据方法A中概述的方法制备。
因此,在约-78至约100℃的温度范围内,在质子惰性有机溶剂如THF、二氧六环、DMF等中,在碱如二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,使式(S1)化合物(一种已知的化合物或由已知方法制备的化合物)与合适的取代的式(S2)化合物(一种已知的化合物或由已知方法制备的化合物)反应,可得到相应的式(S3)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(S3)化合物与肼反应,得到相应的式(I)化合物。
β-酮基硫代酰胺与肼环化(S3至1)形成苯胺基吡唑的实例类似于在以上方法A的第二步中描述的那些实例,它们已在文献中被报道(例如,见M.Suesse和S.John,J. Prakt.Chem.;(1986),328(4),635-9)。此外,一些酮基硫代酰胺在文献中有报道,例如Wesolowska等,Pol.J. Chem.(2001),75(3),387-400;Hansen等,J.Mol.Struct.(1996),378(1),45-59;Augustin等,J.Prakt.Chem.(1979),321(2),205-14;Schoen等,Rocz.Chem.(1971),45(1),73-60。
方法B
作为选择,式(I)化合物可以根据方法B中概述的方法制备。
因此,在约-78℃至约0℃范围的低温下,在质子惰性有机溶剂如THF、二氧六环、DMF等中,在强碱如氢化钠、二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,使式(S1)化合物(一种已知的化合物或由已知方法制备的化合物)与式(S4)化合物(1,1′-硫代羰基二咪唑)反应,得到相应的式(S5)化合物。
在质子惰性有机溶剂如THF、二氧六环、二氯甲烷、氯仿、DMF等中,使式(S5)的化合物与合适地取代的式(S6)的化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(S3)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(S3)化合物与肼反应,得到相应的式(I)化合物。
本发明还涉及一种制备式(I)化合物的方法(如在以上方法B中所详述)。在本发明的一个实施方案中,本发明涉及一种使用以上方法B制备式(S5)化合物的方法。在另一个实施方案中,本发明涉及一种使用以上方法B概述的过程制备式(S3)化合物的方法。
方法C
作为选择,式(I)化合物可以根据方法C中概述的方法制备。
更具体地说,在约0至约120℃的温度范围内,在质子惰性有机溶剂如THF,DMF等中,在氢化钠的存在下,使式(S1)化合物(一种已知的化合物或由已知方法制备的化合物)与合适地取代的式(S2)化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(S3)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(S3)化合物与肼反应,得到相应的式(I)化合物。
方法D
作为选择,式(I)化合物可以根据方法D中概述的方法制备。
因此,在碱如氢化钠、二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,在质子惰性有机溶剂如THF、DMF等中,在约25至约100℃范围的升高的温度下,使式(S1)化合物(一种已知的化合物或由已知方法制备的化合物)与二硫化碳和甲基碘反应,得到相应的式(S7)化合物。一些式(S7)化合物为已知的,例如在Villemin等,Synthesis(1991),(4),301-3;Augustin等,J.Prakt.Chem.(1979),321(2),215-25;及在WIPO公布号WO 95/07893中公开的那些。
在质子惰性有机溶剂如THF,DMF等中,在约25至约150℃范围的升高的温度下,在催化量的酸如乙酸、硫酸、对甲苯磺酸等的存在下,使式(S7)化合物与合适地取代的式(S6)的化合物反应(一种已知的化合物或由已知方法制备的化合物),得到相应的式(S8)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(S8)化合物与肼反应,得到相应的式(I)化合物。
方法E
作为选择,式(I)化合物可以根据方法E中概述的方法制备。
因此,在甲基碘和碱如DBU、NaH、二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,在质子惰性有机溶剂如乙腈、THF、DMF等中,在约0至约100℃范围的升高的温度下,使式(S1)化合物(一种已知的化合物或由已知方法制备的化合物)与合适地取代的式(S2)化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(S8)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(S8)化合物与肼反应,得到相应的式(I)化合物。
方法F
结构(IIa)的式(II)化合物可以根据方法F中概述的方法制备。
因此,在约-78至约100℃的温度范围内,在质子惰性有机溶剂如THF、二氧六环、DMF等中,在碱如二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,使式(T1)化合物(一种已知的化合物或由已知方法制备的化合物)与合适地取代的式(T2)化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(T3)化合物。
式(T1)化合物,其中L2包含氧、硫或氮原子,也可以通过已知的方法制备(例如,见A.R.Deshpande等,Synthetic Communications,(1990),20(6),809-816;W-S.Li等,Tetrahedron Letters,(2002),43,1923-1925;C.Brian等,Tetrahedron,(1987),43(1),69-76;H.Winfvoid等,Chemie,(1970),10(9),343:C.Mukerjee等,Synletters,(2002),(2),325-327;T.Sugasawa等,J.Org.Chem.,(1979),44(4),578-586:S;及Torii等,J.Org.Chem.,(1978),43(14),2882-2885)。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(T3)化合物与肼反应,得到相应的式(IIa)化合物。
β-酮基硫代酰胺与肼环化(T3至IIa)形成苯胺基吡唑的实例类似于在以上方法F的第二步中描述的那些实例,它们已在文献中被报道(例如,见M.Suesse和S.John,J.Prakt.Chem.;(1986),328(4),635-9)。此外,一些酮基硫代酰胺在文献中有报道,例如Wesolowska等,Pol.J.Chem.(2001),75(3),387-400;Hansen等,J.Mol.Struct.(1996),378(1),45-59;Augustin等,J.Prakt.Chem.(1979),321(2),205-14;Schoen等,Rocz.Chem.(1971),45(1),73-60。
方法G
结构(IIa)的式(II)化合物可以根据方法G中概述的方法制备。
因此,在约-78℃至约0℃范围的低温下,在质子惰性有机溶剂如THF、二氧六环、DMF等中,在强碱如氢化钠、二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,使式(T1)化合物(一种已知的化合物或由已知方法制备的化合物)与式(T4)化合物(1,1′-硫代羰基二咪唑)反应,得到相应的式(T5)化合物。
在质子惰性有机溶剂如THF、二氧六环、二氯甲烷、氯仿、DMF等中,使式(T5)化合物与合适地取代的式(T6)化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(T3)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(T3)化合物与肼反应,得到相应的式(IIa)化合物。
本发明还涉及一种制备式(IIa)化合物的方法(如在以上方法G中所详述)。在本发明的一个实施方案中,本发明涉及一种使用以上方法G制备式(T5)化合物的方法。在另一个实施方案中,本发明涉及一种使用以上方法G概述的过程制备式(T3)化合物的方法。
方法H
作为选择,结构(IIa)的式(II)化合物可以根据方法H中概述的方法制备。
更具体地说,在约0至约120℃的温度范围内,在质子惰性有机溶剂如THF,DMF等中,在氢化钠的存在下,使式(T1)化合物(一种已知的化合物或由已知方法制备的化合物)与合适地取代的式(T2)化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(T3)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(T3)化合物与肼反应,得到相应的式(IIa)化合物。
方法I
作为选择,结构(IIa)的式(II)化合物可以根据方法I中概述的方法制备。
因此,在碱如氢化钠、二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,在质子惰性有机溶剂如THF、DMF等中,在约25至约100℃范围的升高的温度下,使式(T1)化合物(一种已知的化合物或由已知方法制备的化合物)与二硫化碳和甲基碘反应,得到相应的式(T7)化合物。
在质子惰性有机溶剂如THF,DMF等中,在约25至约150℃范围的升高的温度下,在催化量的酸如乙酸、硫酸、对甲苯磺酸等的存在下,使式(T7)化合物与合适地取代的式(T6)化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(T8)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(T8)化合物与肼反应,得到相应的式(IIa)化合物。
方法J
作为选择,结构(IIa)的式(II)化合物可以根据方法J中概述的方法制备。
因此,在甲基碘和碱如DBU、NaH、二(三甲基硅烷基)氨化锂、二(三甲基硅烷基)氨化钠、二异丙基氨化锂等的存在下,在质子惰性有机溶剂如乙腈、THF、DMF等中,在约0至约100℃范围的升高的温度下,使式(T1)化合物(一种已知的化合物或由已知方法制备的化合物)与合适地取代的式(T2)化合物(一种已知的化合物或由已知方法制备的化合物)反应,得到相应的式(T8)化合物。
优选在约1当量的酸(如乙酸、盐酸等)存在下,在升高的温度下,优选在约回流的温度下,使式(T8)化合物与肼反应,得到相应的式(IIa)化合物。
本发明包括式(II)化合物,其中R6或R7之一存在且不为氢(即如下面的详细定义的式(IIb)、(IIc)、(IId)、(IId)、(IIe)、(IIf)、(IIg)、(IIh)、(IIj)、(IIk)、(IIm)(IIn)、(IIo)、(IIp)、(IIq)、(IIr)和(IIs)化合物)。所述化合物为式(I)和(II)的化合物的潜在的药物前体。本发明还包括所述式(IIb)、(IIc)、(IId)、(IId)、(IIe)、(IIf)、(IIg)、(IIh)、(IIj)、(IIk)、(IIm)(IIn)、(IIo)、(IIp)、(IIq)、(IIr)和(IIs)化合物的制备方法。
作为药物前体,式(II)化合物,其中R6或R7之一存在且不为氢,被认为是可在体内吸收的,然后经代谢或水解生成式(I)或(II)的相应的化合物。其中R6或R7之一存在且不为氢的式(II)化合物还可以具有与母体式(I)和/或(II)化合物类似的内在的生物学活性。
方法L
式(IIb)和(IIc)化合物,其中R6或R7之一选自式(II)的段落(c),可以根据方法L中概述的方法制备。
因此,在-70至100℃的温度范围内,在非质子溶剂中如THF、DMF等中;在碱如碳酸钾、碳酸铯、吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适取代的烷化剂,一种式(T9)化合物(一种已知的化合物,例如甲基碘、硫酸二甲酯、新戊酸氯代甲酯、环氧乙烷等;或者与通过已知的方法制备的化合物,例如卤化物、甲磺酸酯、对甲苯磺酸酯、环氧化物和三氟甲磺酸酯等)反应,得到式(IIb)和(IIc)的相应的区域异构体化合物的混合物。所述两种区域异构体的比率依赖于所用的碱和溶剂。两种区域异构体优选通过硅胶柱层析或反相柱层析分离,得到式(IIb)和(IIc)化合物。
方法M
式(IId)和(IIe)化合物,其中R6或R7之一选自式(II)的段落(d)、(e)、(f)、(g)、(h)和(hh),可以根据方法M中概述的方法制备。
因此,在约-70和约100℃之间的温度范围内,在非质子溶剂如THF、DMF、吡啶等中,在碱如吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适的酰化剂,式(T11)或(T12)化合物(一种已知的化合物或由已知方法制备的化合物,例如,乙酰氯、异丁酰氯、琥珀酸酐、甲氧基乙酰氯,苄氧基乙酰氯,苯甲酰氯等)反应,得到式(IId)和(IIe)的相应的区域异构体化合物的混合物。所述两种区域异构体的比率依赖于所用的碱和溶剂。优选两种区域异构体通过硅胶柱层析或反相柱层析分离,得到式(IId)和(IIe)化合物。
方法N
作为选择,式(IId)和(IIe)的化合物,其中R6或R7之一选自式(II)的段落(d)、(e)、(f)、(g)、(h)和(hh),可以根据方法N中概述的方法制备。
因此,在约-70和约100℃之间的温度范围内,在非质子溶剂中如THF、DMF等中,在碱如三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适取代的羧酸,式(T13)的化合物(一种已知的化合物或由已知方法制备的化合物例如,3-氧代-3-吡咯烷-1-丙酸等)反应,得到式(IId)和(IIe)的相应的区域异构体化合物的混合物。所述两种区域异构体的比率依赖于所用的碱和溶剂。优选两种区域异构体通过硅胶柱层析或反相柱层析分离,得到式(IId)和(IIe)的化合物。
本领域技术人员应该认识到,当式(T13)的羧酸为如苯甲酸、丙酸等时,所述反应在合适的肽偶合剂,如1-(3-二甲基氨基丙基)-3-乙基碳二亚胺(EDC)和羟基苯并三唑水合物(HOBT)等的存在下完成。
方法O
式(IIf)和(IIg)的化合物,其中R6或R7之一选自式(II)的段落(i)、(j)和(k),可以根据方法O中概述的方法制备。
因此,在约-70至约100℃的温度范围内,在非质子溶剂中如THF、DMF、DCM等中,在碱如吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适取代的氯代甲酸酯,式(T14)的化合物(一种已知的化合物或由已知方法制备的化合物),例如,氯代甲酸乙基酯、氯代甲酸2-甲氧基乙基酯、氯代甲酸异丙基酯、三(乙二醇)、双(氯代甲酸酯)等进行反应,得到式(IIf)和(IIg)的相应的区域异构体化合物的混合物。所述两种区域异构体的比率依赖于所用的碱和溶剂。优选两种区域异构体通过硅胶柱层析或反相柱层析分离,得到式(IIf)和(IIg)的化合物。
方法P
式(IIh)和(IIj)的化合物,其中R6或R7之一选自式(II)段落(l)、(m)、(n)和(o),可以根据方法P中概述的方法制备。
因此,在约-70和约100℃之间的温度范围内,在非质子溶剂如THF、DMF、DCM等中,在碱如吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适取代的芳基氯代甲酸酯,式(T15)的化合物(一种已知的化合物或由已知方法制备的化合物),例如,氯代甲酸苯基酯、氯代甲酸4-硝基苯基酯等进行反应,得到式(T16)和(T17)的相应的区域异构体化合物的混合物。式(T16)和(T17)的化合物通过硅胶柱层析或反相柱层析分离。
在非质子溶剂如DMF、DMSO、THF等中,在约-70°和约100℃之间的温度范围内,使式(T16)和(T17)的化合物分别与合适取代的胺,式(T18)的化合物(一种已知的化合物或由已知方法制备的化合物),例如,1-甲基-1-乙基-1,2-二胺、丙胺、3-(吗啉-4-基)-1-丙基胺等反应,得到相应的式(IIh)和(IIj)化合物。
作为选择,使作为混合物的式(T16)和(T17)的化合物与合适取代的胺,式(T18)的化合物反应,得到式(IIh)和(IIj)的化合物的混合物。然后通过已知的方法,例如经硅胶柱或反相柱层析,分离式(IIh)和(IIj)的化合物。
两种程序均得到所需的式(IIh)和(IIi)的化合物。通过使式(T16)和(T17)的化合物分别反应比通过使式(T16)和(T17)的化合物的混合物反应,然后分离,可以更有效地实现化合物库的制备。
方法Q
式(IIk)和(IIm)的化合物,其中R6或R7之一选自式(II)的段落(I)、(m)、(n)、(o)、(p)和(q),可以根据方法Q中概述的方法制备。
因此,在约-20°和约100℃之间的温度范围内,在非质子溶剂如THF、DMF、DCM等中,在碱如吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适取代的异氰酸酯(式(T19)的化合物)或合适取代的硫代异氰酸酯(式(T20)的化合物),例如,异氰酸苯酯,异氰酸甲酯,硫代异氰酸甲酯等反应,得到相应的式(IIk)和(IIm)的化合物的区域异构体的混合物。所述两种区域异构体的比率依赖于所用的碱和溶剂。优选两种区域异构体通过硅胶柱层析或反相柱层析分离,得到式(IIk)和(IIm)的化合物。
本领域技术人员应该认识到,当式(IIa)化合物与异氰酸酯反应时,则相应的式(IIk)和(IIm)的化合物将具有-C(O)NHR″″的R6或R7取代基。类似地,当式(IIa)化合物与硫代异氰酸酯反应时,则相应的式(IIk)和(IIm)的化合物将具有-C(S)NHR″″′的R6/或R7取代基。
方法R
式(IIn)和(IIo)的化合物,其中R6或R7之一选自式(II)的段落(s)、(t)和(u),可以根据方法R中概述的方法制备。
因此,在约-20°和约100℃之间的温度范围内,在非质子溶剂如THF、DMF、DCM等中,在碱如吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适取代的氨磺酰氯,式(T21)的化合物(一种已知的化合物,例如,二甲基氨磺酰氯,乙基氨磺酰氯等反应,或者与通过已知的方法制备的化合物)反应,得到相应的式(IIn)和(IIo)的化合物的区域异构体的混合物。所述两种区域异构体的比率依赖于所用的碱和溶剂。优选两种区域异构体通过硅胶柱层析或反相柱层析分离,得到式(IIn)和(IIo)的化合物。
本领域技术人员应该认识到,当式(IIa)化合物与氨磺酰化合物反应时,则式(IIo)和(IIp)的相应的化合物将具有-SO2NHR″″″和-SO2N(R””)2的R6或R7取代基。
方法S
式(IIp)和(IIq)的化合物,其中R6或R7之一选自式(II)的段落(v)和(w),可以根据方法S中概述的方法制备。
因此,在约-20°和约100℃之间的温度范围内,在非质子溶剂如THF、DMF、DCM等中,在碱如吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适的氯代磷酸烷基酯,式(T22)的化合物(一种已知的化合物,例如,氯代磷酸二甲酯、氯代磷酸二乙酯等反应,或者与通过已知的方法制备的化合物)反应,得到相应的式(IIp)和(II)的化合物的区域异构体的混合物。所述两种区域异构体的比率依赖于所用的碱和溶剂。优选两种区域异构体通过硅胶柱层析或反相柱层析分离,得到式(IIp)和(IIt)的化合物。
本领域技术人员应该认识到,当式(IIa)化合物与氯代磷酸二烷基酯反应时,则相应的式(IIp)和(IIq)化合物将具有-P(=O)(O(C1-3)烷基)2的R6或R7取代基。
方法T
式(IIr)和(IIs)的化合物,其中R6或R7之一选自式(II)的段落(r),可以根据方法T中概述的方法制备。
因此,在约-70°和约100℃之间的温度范围内,在非质子溶剂如THF、DMF、DCM等中,在碱如吡啶、三乙胺、二异丙基乙胺等的存在下,使合适取代的式(IIa)化合物与合适的取代的硫代氯甲酸-O-芳基酯,式(T23)的化合物(一种已知的化合物或由已知方法制备的化合物),例如,硫代氯甲酸-O-苯酯等反应,得到相应的式(T24)和(T25)的化合物的区域异构体的混合物。式(T24)和(T25)的化合物通过硅胶柱层析或反相柱层析分离。
在非质子溶剂如DMF、DMSO、THF等中,在约-70°和约100℃之间的温度范围内,使所述式(T24)和(T25)的化合物分别与合适取代的胺,式(T26)的化合物(一种已知的化合物或由已知方法制备的化合物),例如,哌啶、吗啉、二甲胺、吡咯烷等反应,得到相应的式(IIr)和(IIs)的化合物。
作为选择,使作为混合物的所述式(T24)和(T25)的化合物与合适取代的胺,式(T26)的化合物反应,得到式(IIr)和(IIs)的化合物的混合物。式(IIr))和(IIs)的化合物再通过已知的方法,例如经硅胶柱或反相柱层析分离。
两种程序均得到所需的式(IIr)和(IIs)的化合物。
通过使式(T24)和(T25)的化合物分别反应比通过使式(T24)和(T25)的化合物的混合物反应,然后分离,可以更有效地实现化合物库的制备。
N-葡糖苷酸的合成
本发明的各种化合物可以在体内通过UDP-葡糖醛酸基转移酶(glucuronosyl transferase)家族的各种内源性同工酶经受不同程度地N-葡糖醛酸化作用(glucuronidation)(Chiu,S-HL;Huskey,S-EW;1996ASPET N-glucuronidation of xenobiotics symposium:Species differencesin N-glucuronidation,Drug Metabolism and Disposition 1998,26(9):838-847)。
本领域技术人员应该理解,通过内源性β-葡糖醛酸糖苷酶的作用,式(I)和(II)的化合物的体内代谢产物可以容易地被还原为式(1)和(II)化合物。科学文献详述了肿瘤组织通常含有升高水平的内源性β-葡糖醛酸糖苷酶。通过内源性β-葡糖醛酸糖苷酶的作用,可以实现式(I)和(II)的化合物的原位再生成。这样,本发明的化合物被可逆性地葡糖醛酸化的能力使得本发明化合物靶向作用于肿瘤组织(Sperker,B;Backman,JT;Kroemer,HK,The role of β-glucuronidase in drugdisposition and drug targeting in humans,Clin.Pharmacokinet.,1997,33(1):18-31)。
此外,本领域技术人员也可以认识到,本发明化合物的可逆性的葡糖醛酸化作用为式(I)和(II)的化合物的解毒的一种有效方法(Caldwell,J;The significance of phase 11 conjugation reactions in drugdisposition and toxicity,Life Sci,1979,24:571-578),因此这就使得形成的N-葡糖苷酸代谢产物起到作为式(I)和(II)的化合物的有效的非毒性贮库的作用,而后式(I)和(II)的化合物可以通过与肿瘤有关的β-葡糖醛酸糖苷酶容易地原位形成完全生物学活性的式(I)和(II)的化合物。
式(I)和(II)的化合物的N-葡糖苷酸代谢产物将具有如下GLU A、GLU B和GLU C所示的结构:
式(I)的GLU A衍生物 式(I)的GLU B衍生物
式(I)的GLU C衍生物 式(II)的GLU A衍生物
式(II)的GLU B衍生物 式(II)的GLU C衍生物
通常,经葡糖醛酸化的化合物将具有在端基异构的碳原子附近的β-构型,特别是如果所述葡糖苷酸是通过本领域技术人员已知的经充分确证的酶促方法所产生(Luukkanen,L;Kilpelaeinen,l;Kangas,H;Ottoila,P;Elovaara,E;Taskinen,J,Enzyme-Assisted Synthesis andStructural Characterization of Nitrocatechol glucuronides,BioconjugateChemistry(1999),10(1),150-154)。
通过本领域技术人员已知的合成方法,使式(I)和(II)的化合物与适当保护的葡糖醛酸基卤化物反应,也可以经直接合成法制备N-葡糖苷酸(Upadhyaya,Pramod;Mclntee,Edward J.;Hecht,Stephen S.,Preparation of Pyridine-N-glucuronide of Tobacco-specificNitrosamines.,Chemical Research in Toxicology(2001),14(5),555-561)。
本领域技术人员应该认识到,式(I)和(II)化合物的GLU A、GLU B和GLU C衍生物可以通过已知的方法,通过上面引用的方法的修改方法制备。
可选择的方法
(I核心)
例如,如果一个或多个Z基团为羟基,则所述羟基可以根据已知方法与烷基卤反应,形成相应的-O-烷基取代基;与Cl-C(O)-烷基或Cl-C(O)-芳基反应,形成相应的-C(O)-烷基或-C(O)-芳基取代基;与Cl-C(O)O-烷基或Cl-C(O)O-芳基反应,形成相应的-C(O)O-烷基或-C(O)O-芳基取代基;或者与C(O)N(烷基)或C(O)C(芳基)反应,形成相应的OC(O)N(烷基)或-OC(O)N(芳基)取代基。
如果一个或多个Z基团为氨基,则所述氨基可以根据已知方法与HC(O)-烷基或HC(O)-芳基反应,形成相应的-NHCH2-烷基或-NHCH2-芳基取代基;与Cl-C(O)-烷基或Cl-C(O)-芳基反应,形成相应的-NHC(O)-烷基或-NHC(O)芳基取代基;与C(O)N-烷基或C(O)N-芳基反应,形成相应的NHC(O)NH-烷基或-NHC(O)NH-芳基取代基;与Cl-C(O)O-烷基或ClC(O)O-芳基反应,形成相应的-NHC(O)O-烷基或-NHC(O)O-芳基取代基;或者与CI-SO2-烷基或CI-SO2-芳基反应,形成相应的-NHSO2-烷基或-NHSO2-芳基取代基。本领域技术人员还应该认识到,如果Z基团为烷基氨基或芳基氨基,可以进行类似的化学反应,得到相应的其中直接连接于A或B环的N基团还可以被烷基或芳基取代的取代基。
如果一个或多个Z基团为硫代基,则所述硫代基团可以根据已知方法与烷基卤反应,形成相应的烷硫基取代基。如果一个或多个Z基团为烷硫基,则烷硫基可以根据已知方法反应,形成相应的烷基磺酰基取代基。
如果一个或多个Z基团为羧基,则所述羧基可以根据已知方法反应,形成相应的-C(O)Cl基团,后者又可以依次进一步反应,形成所需的R2和/或R3取代基。
如果一个或多个Z基团为-C(O)Cl,则-C(O)Cl基团可以根据已知方法与烷氧基反应,形成相应的C(O)O-烷基取代基;与-NH(烷基)或N(烷基)2反应,形成相应的C(O)NH(烷基)或-C(O)N(烷基)2取代基。
如果一个或多个Z基团是一种卤素(如碘或溴),则卤素可以根据已知方法与B(OH)2-烷基、B(OH)2-芳基或B(OH)2-杂芳基反应,用相应的-烷基、-芳基或-杂芳基置换卤素。
作为选择,如果一个或多个Z基团是卤素(如碘或溴),则卤素可以根据已知方法与烷基胺、二烷基胺、芳基胺、杂芳基胺或杂环烷基胺反应,用相应的-NH-烷基、-N(烷基)2、-N-芳基、-NH-杂芳基或-NH-杂环烷基置换卤素。
作为选择,如果一个或多个Z基团是一种卤素(如碘或溴),则卤素可以根据已知方法与HO-烷基、HO-芳基、HO-杂芳基或HO-杂环烷基反应,用相应的-O-烷基、-O-芳基、-O-杂芳基或-O-杂环烷基置换卤素。
作为选择,如果一个或多个Z基团是一种卤素(如碘或溴),则卤素可以根据已知方法与HS-烷基、HS-芳基、HS-杂芳基或HS-杂环烷基反应,用相应的-S-烷基、-S-芳基、-S-杂芳基或-S-杂环烷基置换卤素。
如果一个或多个Z基团为-O-SO2-芳基或-OSO2-烷基,则所述-O-SO2芳基或-OSO2-烷基可以根据已知方法与烷基胺、二烷基胺、芳基胺或杂芳基氨基反应,形成相应的-NH(烷基)、-N(烷基)2、-NH(芳基)或-NH(杂芳基)基团。
作为选择,如果一个或多个Z基团为-O-SO2-芳基或-OSO2-烷基,则所述-O-SO2芳基或-OSO2-烷基可以根据已知的方法反应,用卤素如Br或I置换-O-SO2基团,形成活性中间体,然后其可进一步反应形成所需的取代基。
如果一个或多个Z基团为-S-烷基、-S-芳基、-S-杂芳基或-S-杂环烷基,则所述S可以根据已知方法被氧化形成相应的-SO2-烷基、-SO2-芳基、-SO2-杂芳基或-SO2-杂环烷基取代基。
如果一个或多个Z基团含有末端不饱和键,则Z基团可以根据已知方法反应,形成相应的环氧化物,然后与取代的胺,如烷基氨基、二烷基胺、芳基胺、杂芳基胺、杂环烷基胺或环胺(如哌啶、吗啉、咪唑等)反应,形成相应的-CH(OH)CH2-NH-烷基、CH(OH)CH2-N(烷基)2、-CH(OH)CH2-NH-芳基、-CH(OH)CH2-NH-杂芳基、-CH(OH)CH2-NH-杂环烷基或-CH(OH)CH2-(通过N原子连接的环胺)取代基。
本领域技术人员还将认识到,类似于上述转化或反应的那些转化或反应可以用于(或应用于)制备式(II)化合物。更具体地说,上述用于在和/或环上引入R2和/或R3基团的方法可以用于将R5、R9和/或R10取代基引入到式(II)化合物的和/或环上。
本领域技术人员应该认识到,根据已知的方法,可将其中R1为氧代基(=O)的式(I)化合物,转化而形成其中R1为羟基的式(I)化合物(经还原)或转化为其中R1为=NHOH的中间体化合物(经与氢氧化铵反应)。然后,可以根据已知的方法将其中R1为=NHOH的中间体化合物还原为相应的胺,随后后者可以任选被进一步官能化为相应的取代的胺。
根据已知的方法,通过使中间体化合物与相应的Cl-SO2-芳基或Cl-SO2-烷基试剂反应,可以将其中R1为羟基的式(I)化合物转化而形成其中R1为-O-SO2-芳基或-O-SO2-烷基的中间体化合物。然后根据已知方法,可以使-O-SO2-芳基或-O-SO2-烷基R1基团任选进一步反应,形成胺(通过与NaN3反应,随后还原)。
作为选择,根据已知的方法,通过使其中R1为羟基的式(I)化合物与相应的烷基卤反应,而将前药转化形成其中R1为-O-烷基的式(I)化合物。
根据已知的方法,通过使其中R1为胺或烷基胺的式(I)化合物与HC(O)-烷基反应,形成其中R1为-NH-CH2-烷基或-NH-(CH2-烷基)2的式(I)化合物。
本领域技术人员还应该认识到,与上述那些转化或反应类似的转化或反应可以用于(或应用于)制备式(II)化合物。更具体地说,上述用于在式(I)化合物中引入R1基团或任选将R1基团转化的方法可以类似地应用于制备式(II)化合物,其中这样的转化在所需的L2基团的制备中是适宜的。
本领域技术人员还应该认识到,包含在所述式(I)化合物和/或式(II)化合物中所需取代基的实例并不意味着包括全部,而只是打算提供用于引入代表性的取代基的已知化学的实例。可以通过已知的方法将在此未特别描述的其它取代基引入到式(I)化合物和/或式(II)化合物中。
如下给出通过上述方法合成的本发明的代表性化合物。具体化合物的合成实例在下文中介绍。
给出以下实施例以举例说明本发明化合物的合成方法,但下列实施例并不以任何方式限制本发明。
实施例1
1-氧代-茚满-2-硫代甲酸苯酰胺,中间体A(方法A)
中间体A
在氩气下,将NaH(在矿物油中的60%分散液,0.25g,6mmol)和茚满-1-酮(化合物1a)(0.50g,3.79mmole)在THF(5mL)中混合。于室温下,将该混合物搅拌5分钟。然后,将异硫氰酸苯酯(化合物1b)(0.46mL,3.79mmole)加入到该混合物中。再过5分钟后,经TLC分析显示该反应完成,将该反应化合物倾入到NH4Cl溶液中,随后过滤。将1-氧代-茚满-2-硫代甲酸苯酰胺(中间体A)从乙腈中结晶,为黄色固体。MS m/z 268
(M+H)+;1HNMR(DMSO-d6):3.5 (dd,.3H),3.8(d,.15H),3.9(s,1.55H),4.3(dd,.3H),7.3(t,1H),7.4-7.8(m,7.4H),7.9(d,.6H),10.6(s,.7H),12.1(s,.3H),14.1(s,.7H).
实施例2
2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺,化合物1(方法A)
化合物1
在氩气下,将(中间体A)1-氧代-茚满-2-硫代甲酸苯酰胺(0.35g,1.31mmole)、乙醇(2mL)和肼(0.043mL 1.38mmole)在烧瓶中混合。将该反应化合物在蒸气浴中加热1小时,然后冷却,蒸发溶剂,得到一种棕色油状物。将该油状物溶于二氯甲烷中,用1N HCl,3NNaOH和盐水洗涤。干燥(硫酸钠)得到的有机物(0.31g),过滤,真空除去溶剂。经硅胶层析分离产物,用2%甲醇∶二氯甲烷洗脱。随后从甲基环己烷∶甲苯中结晶标题化合物(化合物1),为白色固体。
m,p.148-149℃;MS m/z 248(M+H)+;1HNMR(DMSO-d6):3.5(s,2H),6.75(t,1H),7.0-7.3(m,5H),7.35(t,1H),7.5(dd,2H),8.4(s,1H),12.3(s,1H).
实施例3
(3,5-二氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺,化
合物19(方法A)
化合物19
于室温、搅拌下,将5,6-二甲氧基茚满-1-酮,化合物3a,(4g,0.021mole)、异硫氰酸3,5-二氯苯酯,化合物3b,(4.45g,0.022mole)和THF(30mL)的混合物滴加到六甲基乙硅烷基锂(26.9mL,0.269mole)中。将肼(1.04mL,0.032mole)和乙酸(1.65mL)加入到反应混合物中,然后于室温下将其搅拌12小时。于75℃继续搅拌过夜。将得到的有机物先用乙酸乙酯(100mL)稀释,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。使该化学残留物从乙醇中重结晶。合并第一批和第二批收获的固体,然后将其溶于热乙腈中,向其中加入等体积的HCl-乙醚溶液,以沉淀出标题化合物(化合物19),收集,于60℃真空干燥。
mp>270℃;MS m/z 376 and 378(M+H)+;1HNMR(DMSO-d6):3.44(s,2H),3.83(s,3H),3.82(s,3H),6.93(s,1H),7.19(s,1H),7.21(s,1H),7.35(s,2H).
实施例4
(3-氟-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺,化合物
14(方法A)
化合物14
于室温、搅拌下,将5,6-二甲氧基茚满-1-酮,化合物3a,(3.0g,0.0154mole)、异硫氰酸3-氟-苯酯,化合物4a,(2.4g,0.0157mole)和THF(3.0mL)的混合物滴加到六甲基乙硅烷基锂(15.4mL,0.0154mole)中。搅拌反应混合物12小时。将肼(0.75mL,0.0154mole)和乙酸(0.96mL)加入到反应混合物中,然后将其在回流温度下加热24小时。将得到的混合物先加入水(30mL)中,然后用二氯甲烷提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。使残留物溶于热乙腈中。然后向该混合物中加入1当量HCl-乙醚溶液,得到标题化合物的沉淀物。使该沉淀物溶于乙腈中,用炭脱色,重结晶得到化合物14,为灰白色固体。
MS m/z 326(M+H)+;1HNMR(DMSO-d6):3.44(s,2H),3.80(s,3H),3.81(s,3H),6.58(t,1H),6.85(d,1H),7.1(d,1H),7.21(s,1H),7.23(s,1H),7.3(m,1H),9.2(br s,1H).
实施例5
2-(咪唑-1-硫代甲酰基(carbothioyl)-5,6-二甲氧基-茚满-1-酮.中间体B
(方法B)
在氮气、搅拌下,将在THF中的双(三甲基硅烷基)氨化锂(11mL,11mmol)和THF(20mL)在一干燥烧瓶中混合。将在15mL THF中的5,6-二甲氧基茚满-1-酮(1.92g,10mmol)加入到该烧瓶中。然后在干冰-丙酮浴中冷却反应混合物。于-78℃搅拌反应溶液,加入在15mLTHF中的硫代二咪唑(2.18g,11mmol)。于-78C搅拌反应混合物5小时,然后用40mL饱和氯化铵溶液猝灭,随后升温至室温。用乙酸乙酯提取该混合物的水溶液两次,得到在有机溶液中的标题化合物。用水和饱和氯化钠溶液洗涤该混合物,干燥(硫酸钠),真空除去溶剂。得到2-(咪唑-1-硫代甲酰基)-5,6-二甲氧基-茚满-1-酮,为黄色固体。HPLC分析显示该产物是纯的。
MS m/z 303(M+H)+;1HNMR(DMSO-d6):3.60(s,2H),3.70(s,3H),3.85(s,3H),6.90(s,1H),7.1(s,1H),7.51(s,1H),7.60(s,1H),9.1(s,1H).
实施例6
[3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯基]-甲醇,化
合物36(方法B)
将2-(咪唑-1-硫代甲酰基)-5,6-二甲氧基-茚满-1-酮,中间体B,(1.0g,3.3mmol)与3-氨基苄基醇(0.40g,3.3mmol)和30mL THF在一烧瓶中混合。于室温下搅拌反应混合物4小时后,得到5,6-二甲氧基-1-氧代-茚满-2-硫代甲酸(3-羟甲基-苯基)-酰胺。HPLC/MS m/z 358(M+H)+。不用分离中间体,将该混合物与肼(0.13mL,4mmol)和乙酸(2-3滴)混合。于78℃将该反应物加热12小时。然后用乙酸乙酯稀释反应溶液,用水洗涤,经硫酸钠干燥。除去溶剂,标题化合物经使用C-18反相柱的HPLC纯化,用乙腈-水-TFA作为梯度溶剂。得到标题化合物[3-(6,7-二甲氧基-2,4-二氢茚并[1,2-c]吡唑-3-基氨基)-苯基]-甲醇,化合物36,为固体TFA盐。
MS m/z 338(M+H)+;HPLC:100%(uv 214mu);1HNMR(DMSO-d6):3.40(s,2H),4.54(s,2H),6.81(d,1H),7.02(d,1H),7.14(s,1H),7.22(d,2H).
实施例7
N3-苯基-2,4-二氢-茚并[1,2-c]吡唑-3,6-二胺,化合物66(方法C)
化合物66
在氩气气氛下,将NaH(在矿物油中的60%分散液(0.25g,6mmol))和无水THF(25mL)在烧瓶中混合。然后在搅拌下,将5-氨基茚满-1-酮,化合物7a,(0.22g,15mmol)和异硫氰酸苯酯,化合物1b,(0.18mL,15mmol)加入到反应物。于室温下搅拌反应混合物1小时后,加入肼(0.45mL,75mmol),接着加入乙酸(0.070mL,2.25mmol)。于70℃、搅拌下继续反应过夜。用饱和碳酸氢钠水溶液稀释该反应物,用乙酸乙酯提取,用盐水洗涤,经硫酸钠干燥,真空除去溶剂。粗品物质经HPLC纯化,得到标题化合物(化合物66),为TFA盐。
MS m/z 263(M+H)+;1HNMR(DMSO-d6):3.50(s,2H),6.80(m,1H),6.98(m,1H),7.14(m,3H),7.24(m,2H),7.32(t,1H),7.49(d,1H),7.56(d,1H),8.80(bs,1H);HPLC:100%(uv 214).
实施例8
2-(双-甲硫基-亚甲基)-5,6-二甲氧基-茚满-1-酮,中间体D (方法D)
在氮气下,将NaH(在矿物油中的60%分散液;3.37g,44.3mmol)、二硫化碳(3.37g,44.3mmol)和THF(50mL)加入到一干燥烧瓶中。用冰水浴冷却反应烧瓶,然后加入在THF(50mL)中的5,6-二甲氧基-茚满-1-酮,化合物3a,(7.1g,37mmol)。搅拌反应混合物1小时。然后加入甲基碘(5.2mL,44.3mmol)。于室温下,将得到的反应溶液搅拌过夜,然后加入氯化铵水溶液(150mL),接着加入乙酸乙酯(150mL)。分离含水层,用乙酸乙酯提取两次。将有机溶液用水洗涤,加入饱和氯化钠溶液。经硫酸钠干燥该溶液,过滤并浓缩。用乙醇研磨得到的固体,得到2-(双-甲硫基-亚甲基)-5,6-二甲氧基-茚满-1-酮,中间体D,为黄色固体。
MS m/z 297(M+H)+;1HNMR(CDCl3):2.50(s,3H),2.58(s,3H),3.80(s,2H),3.90(s,3H),4.0(s,3H),7.20(s,1H),7.22(s,1H).
实施例9
(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苯基)-胺,化
合物6(方法D)
将50mg(0.17mmol)中间体D(如在以上实施例8中所述制备)、25mg 4-甲氧基苯胺(0.2mmol)和1mL乙酸置于一反应烧瓶中。于70℃将该混合物加热过夜。然后将该混合物倾入水中,用乙酸乙酯提取。洗涤该有机溶液,干燥并浓缩,得到深棕色残留物。使残留物悬浮于乙醇中,然后与0.050mL肼混合。然后于70℃将该反应化合物加热过夜,用乙酸乙酯稀释该混合物,然后用水洗涤,干燥并浓缩。粗产物经硅胶柱层析纯化,使用二氯甲烷和甲醇的混合物作为洗脱剂。收集纯净的部分,浓缩得到标题化合物(化合物6),(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苯基)-胺,为棕色固体。
MS m/z338(M+H)+;HPLC:99%pure(uv);1HNMR(CDCl3):3.29(s,2H),3.73(s,3H),3.80(s,3H),3.89(s,3H),6.80(d,2H),6.95(m,3H),7.3(s,1H).
实施例10
3-苯基氨基-2H-茚并[1,2-c]吡唑-4-酮,化合物35(方法E)
将1,3-茚二酮(indione)(5g,0.0342mol)和异硫氰酸苯酯,化合物1b,(4.1mL,0.0342mol)加入到冷却至0℃的乙腈(50mL)中。然后滴加入DBU(10.2mL,0.0684mol),于室温下搅拌反应混合物2小时。将该反应化合物冷却至0℃,然后缓慢加入甲基碘(3.2mL,0.051mol)。将该反应化合物于室温下搅拌4小时,然后用50/50乙酸/水溶液(300mL)猝灭。过滤沉淀,用水洗涤。
将沉淀物(0.50g,0.0017mol)、肼(0.08mL,0.0026mol)和乙酸(0.5mL,0.006mol)一起加入到乙腈(10mL)中,然后于75℃搅拌4小时。将该反应混合物用饱和碳酸氢钠水溶液猝灭,用乙酸乙酯提取,用盐水洗涤,经硫酸钠干燥。真空除去溶剂。将得到的粗品物质用二氯甲烷和甲醇研磨,得到标题化合物(化合物35),3-苯基氨基-2H-茚并[1,2c]吡唑-4-酮。
MS m/z 262(M+H)+;1HNMR(DMSO-d6):6.92(m,1H),7.11(m,2H),7.27(m,3H),7.48(m,3H)9.60(s,1H),12.3(s,1H).
实施例11
3-苯基氨基-2,4-二氢-茚并[1,2-c]吡唑-4-醇,化合物50(方法E)
将化合物35(如在实施例10中制备)(0.15g,0.00057mol)悬浮于50/50 DCM/MeOH(50mL)的混合物中,向其中加入硼氢化钠(800mg)。搅拌反应混合物2小时。然后用饱和碳酸氢钠水溶液猝灭该反应混合物,用乙酸乙酯提取,用盐水洗涤,经硫酸钠干燥。真空除去溶剂。将粗品物质用二氯甲烷和甲醇研磨,得到标题化合物,3-苯基氨基-2,4-二氢-茚并[1,2-c]吡唑-4-醇。
MS m/z 264(M+H)+;1HNMR(DMSO-d6):5.28(m,2H),6.70(m,1H),7.19(m,6H),7.34(m,1H),7.48(m,1H)8.32(s,1H),12.15(s,1H).
实施例12
5-羟基-6-甲氧基-茚满-1-酮,中间体H
将5,6-二甲氧基茚满-1-酮(25.0g,0.13mole)、氯化锂(20.0g,0.47mole)和DMF(200.0mL)的混合物于160℃搅拌60小时。加入水(400.0mL),用乙酸乙酯洗涤该混合物。用2N HCl酸化含水层,用乙酸乙酯提取(2×300.0mL)。将有机层用盐水洗涤,真空除去溶剂。粗品物质经硅胶柱纯化,使用DCM/MeOH(97/3)作为洗脱剂。真空除去溶剂,得到5-羟基-6-甲氧基-茚满-1-酮(中间体H),为淡黄色固体。MS m/z 179(M+H)+:179 m/z。标题化合物(中间体H)是一种已知的化合物,还可以于100℃,使用KCN/DMSO,通过使5,6-二甲氧基茚满-1-酮去甲基化制备(J.M.Saa等,J.Org.Chem.1992,57,589)。
实施例13
5-(2,2-二甲基-1,3-二氧戊环-4-基甲氧基)-6-甲氧基-茚满-1-酮,中间体
I
将5-羟基-6-茚满-1-酮,中间体H,(0.50g,0.0028mol)、4-氯甲基-2,2-二甲基-1,3-二氧戊环(0.766mL,0.0056mol)、碳酸钾(1.54g,0.011mol)和DMF(20.0mL)的混合物于95℃搅拌3天。加入水(150.0mL),将该混合物用乙酸乙酯提取(2×150mL)。将有机层用饱和碳酸氢钠、盐水洗涤,经硫酸钠干燥。然后真空除去溶剂,得到5-(2,2-二甲基-[1,3]二氧戊环-4-基甲氧基)-6-甲氧基-茚满-1-酮(中间体I),为浅棕色固体。MS m/z 293(M+H)+。
实施例14
3-[3-[(3-氯-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-
丙烷-1,2-二醇,化合物259(方法A)
化合物259
于室温、搅拌下,将5-(2,2-二甲基-[1,3]二氧戊环-4-基甲氧基)-6-甲氧基-茚满-1-酮(中间体I)(0.30g,0.001mole)、异硫氰酸3-氯-苯酯(化合物14a)(0.14mL,0.0011mole)和THF(1.5mL)的混合物滴加到六甲基乙硅烷基锂(1.2mL,0.0012mole)中。搅拌反应混合物4小时。将肼(0.070mL,0.0022mole)和乙酸(0.132mL,0.0022mole)加入加反应混合物中,然后将其在回流温度下加热18小时。先将得到的混合物加入到水(10mL)中,然后用二氯甲烷提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。粗品物质经反相HPLC纯化,然后在0.1%TFA溶液中静置后转化为所需的产物。冻干得到标题化合物,3-[3-[(3-氯-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇,为白色粉末。
MS m/z 402(M+H)+;1HNMR(DMSO-d6):3.41(s,2H),3.46(d,2H),3.78(s,4H),3.88(m,1H),4.00(m,1H),6.75(d,1H),7.15(m,4H),7.40(s,1H),8.80(br s,1H).
实施例15
5-(3-溴-丙氧基)-6-甲氧基-茚满-1-酮,中间体J
于室温、氩气下,将5-羟基-6-甲氧基-茚满-1-酮(中间体H)(5.0g,0.028mole)、1,3-二溴丙烷(5.7mL,0.056mole)和氢化钠(1.2g,0.028mole)在50mL DMF中的混合物搅拌过夜。将该反应混合物用水(150mL)猝灭,用乙酸乙酯提取,然后用1N HCl和盐水洗涤。提取物经硫酸钠干燥,真空除去溶剂,得到标题化合物,5-(3-溴-丙氧基)-6-甲氧基-茚满-1-酮。MS m/z 297(M+H)+。
实施例16
6-甲氧基-5-(3-吡咯烷-1-基-丙氧基)-茚满-1-酮,中间体K
于室温、氩气下,将5-(3-溴-丙氧基)-6-甲氧基-茚满-1-酮(中间体J)(2.0g,0.0066mole)和吡咯烷(1.7mL,0.02mole)的混合物在50mLDME(1,2-二甲氧基乙烷)中搅拌过夜。将该反应物用水(150mL)猝灭,用1N HCl(50mL)使呈酸性。将该水溶液用乙酸乙酯洗涤,用3NNaOH(25mL)使呈碱性,用乙酸乙酯提取。用盐水洗涤并经硫酸钠干燥后,真空除去溶剂,得到标题化合物。MS m/z 290(M+H)+。
实施例17
(3-氟-苯基)-[7-甲氧基-6-(3-吡咯烷-1-基-丙氧基)-2,4-二氢-茚并[1,2-c]
吡唑-3-基]-胺,化合物180(方法A)
于室温、搅拌下,将6-甲氧基-5-(3-吡咯烷-1-基-丙氧基)-茚满-1-酮(中间体K,0.45g,0.00155mole)、异硫氰酸3-氟-苯酯(化合物4a)(0.19mL,0.0017mole)和THF(1.5mL)的混合物滴加到六甲基乙硅烷基锂(1.8mL,0.0018mole)中。搅拌反应混合物4小时。将肼(0.095mL,0.003mole)和乙酸(0.180mL,0.003mole)加入到反应混合物中。然后将该反应混合物在回流温度下加热18小时。将得到的混合物先加入到水(10mL)中,然后用二氯甲烷提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。粗品物质经反相HPLC纯化。冻干得到标题化合物,(3-氟-苯基)-[7-甲氧基-6-(3-吡咯烷-1-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]胺,为白色粉末。
MS m/z 423(M+H)+;1HNMR(DMSO-d6):1.88(m,2H),2.00(m,2H),2.15(m,2H),3.02(m,2H),3.29(dd,2H),3.37(s,2H),3.61(m,2H),3.74(s,3H),4.04(t,2H),6.52(t,1H),6.93(d,1H),7.18(m,4H),8.8(br s,1H),9.7(br s,1H).
实施例18
6-甲氧基-5-[3-(四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮,中间体L
于80℃、氩气下,将5-羟基-6-甲氧基-茚满-1-酮(中间体H,2.98g,0.017mole)、2-(3-氯-丙氧基)-四氢-吡喃(化合物18a)(6.0g,0.034mole)和碳酸钾(10.0g,0.0725mole)的混合物在50mL DMF中搅拌过夜。然后用200mL乙酸乙酯稀释该反应混合物,用水洗涤3次。经硫酸钠干燥后,真空除去溶剂。粗品物质经放置后固化,得到标题化合物6-甲氧基-5-[3-(四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮。MS m/z 309(M+H)+。
实施例19
3-[7-甲氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧
基]-丙-1-醇,化合物266(方法A)
化合物266
于室温、搅拌下,将6-甲氧基-5-[3-(四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮(中间体L)(0.16g,0.0005mole)、异硫氰酸3-甲氧基-苯酯(化合物19a)(0.08mL,0.0006mole)和THF(1.5mL)的混合物滴加到六甲基乙硅烷基锂(0.7mL,0.0007mole)中。搅拌反应混合物4小时。将肼(0.035mL,0.0011mole)和乙酸(0.66mL,0.0011mole)加入反应混合物中,然后将其在回流温度下加热18小时。先向得到的混合物中加入水(10mL),然后用二氯甲烷提取反应混合物。合并有机层,用碳酸氢钠水溶液洗涤,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。粗品物质经反相HPLC纯化,然后在1%TFA的乙腈∶水溶液中静置转化为所需的产物。冻干得到标题化合物,3-[7-甲氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇,为白色粉末。
MS m/z382(M+H)+;1HNMR(DMSO-d6):1.88(m,2H),3.40(s,2H),3.57(t,2H),3.72(s,3H),3.78(s,3H),4.05(t,2H),6.38(d,1H),6.68(d,1H),6.77(s,1H),7.10(m,2H),7.25(s,1H),8.75(br s,1H).
实施例20
6-甲氧基-5-环氧乙烷基甲氧基-茚满-1-酮.中间体M
于70℃、氩气下,将5-羟基-6-甲氧基-茚满-1-酮(中间体H,5.0g,0.028mole)、2-氯代甲基-环氧乙烷(4.4mL,0.056mole)和碳酸钾(11.6g,0.084mole)的混合物在50mL DMF中搅拌过夜。然后用200mL乙酸乙酯稀释该反应物,用水洗涤3次。该乙酸乙酯溶液经硫酸钠干燥,真空除去溶剂,得到标题化合物(中间体M)。MS m/z 236(M+H)+。
实施例21
5-(2-羟基-3-吡咯烷-1-基-丙氧基)-6-甲氧基-茚满-1-酮,中间体N
于50℃、氩气下,将6-甲氧基-5-环氧乙烷基甲氧基-茚满-1-酮(中间体M,2.5g,0.0106mole)和吡咯烷(0.9mL,0.011mole)的混合物在50mL DME中搅拌5小时。然后,加入150mL乙酸乙酯,将所得溶液用水洗涤(2x)。用2N HCl提取后,用3N NaOH使酸性水溶液层呈碱性,用乙酸乙酯提取。将乙酸乙酯提取物用盐水洗涤,经硫酸钠干燥,真空除去溶剂。将得到的残留物用乙醚研磨,得到标题化合物。MS m/z 306(M+H)+。
实施例22
1-[7-甲氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧
基]-3-吡咯烷-1-基-丙-2-醇,化合物270(方法A)
于室温、搅拌下,向5-(2-羟基-3-吡咯烷-1-基-丙氧基)-6-甲氧基-茚满-1-酮(中间体N)(0.16g,0.0005mole)、异硫氰酸3-甲氧基-苯酯(化合物19a)(0.08mL,0.0006mole)和THF(1.5mL)的混合物中滴加入六甲基乙硅烷基锂(0.7mL,0.0007mole)。搅拌反应混合物4小时。将肼(0.035mL,0.0011mole)和乙酸(0.66mL,0.0011mole)加入到反应混合物中。然后将该反应混合物在回流温度下加热18小时。向得到的混合物中先加入水(10mL),然后用二氯甲烷提取反应混合物。合并有机层,用碳酸氢钠水溶液洗涤,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。粗品物质经反相HPLC纯化。冻干得到标题化合物,1-[7-甲氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇,为白色粉末。
MS m/z 451(M+H)+;1HNMR(DMSO-d6):1.89(m,2H),2.02(m,2H),3.12(m,2H),3.34(m,2H),3.45(s,2H),3.62(s,2H),3.70(s,3H),3.85(s,3H),4.00(m,2H),4.20(m,2H),6,37(d,1H),6.71(d,1H),6.78(s,1H),7.10(t,1H),7.25(s,1H),7.3(s,1H),8.68(br s,1H),9.60(br s,1H).
实施例23
5,6-二羟基-茚满-1-酮,中间体O
将5,6-二甲氧基茚满-1-酮(化合物3a)(19g,0.094mole)的200mL二氯甲烷溶液在用干冰/异丙醇浴的-78℃下冷却。然后向该溶液中滴加入200mL(0.2mole)的1M BBr3的二氯甲烷溶液。于-78℃,将得到的溶液搅拌1小时,然后于0℃搅拌1小时。然后将该溶液用干冰/异丙醇浴再冷却至-78℃,用50mL MeOH猝灭。将该溶液在旋转蒸发器上蒸发至干,使该固体再次溶解于MeOH中,然后浓缩,重复进行两次。红色固体,即标题化合物无须纯化而用于随后的反应。MSm/z 165(M+H)+。
实施例24
5,6-二乙氧基-茚满-1-酮,中间体P
于60℃,将5,6-二羟基-茚满-1-酮(中间体O)(24g,0.146mole)、碳酸钾(60g,0.43mole)和二乙基溴(56mL,0.75mole)的DMF(200mL)的混合物搅拌14小时。将水(150mL)加入到反应物中,然后用乙酸乙酯提取(2×150mL)反应混合物。将乙酸乙酯提取物用饱和碳酸氢钠、盐水洗涤,经硫酸钠干燥。然后真空除去溶剂,得到标题化合物,为棕色固体。MS m/z 221(M+H)+。
实施例26
4-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-4-氧代-
丁酸甲酯,化合物428(方法M)
化合物428
于室温、搅拌下,向(6,7-二甲氧基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺(化合物14)(0.50g,1.5mmol)、3-氯代羰基-丙酸甲基酯(化合物26a)(0.277g,1.8mmole)和DMF(1.5mL)的混合物中加入二异丙基乙胺(DIEA)(0.52mL,3.0mmole)。于室温下,将反应物搅拌过夜。将该反应物用水猝灭,用EtOAc提取。经旋转蒸发除去溶剂,粗品物质经反相HPLC纯化。冻干得到标题化合物,为白色粉末。MS m/z 439.9(M+H)+;
1HNMR(DMSO-d6):2.78(t,2H),3.32(t,2H),3.45(s,2H),3.62(s,3H),3.79(s,6H),6.64(m,1H),7.15(s,1H),7.30(m,2H),7.62(d,1H),7.70(s,1H),9.45(s,1H).
实施例27
1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-羟基-
乙酮,化合物432(方法M)
化合物432
于室温、搅拌下,向(6,7-二甲氧基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺(化合物14)(3.6g,10.0mmol)、苄氧基-乙酰氯(化合物27a)(2.2g,12.0mmole)和DMF(50mL)的混合物中加入二异丙基乙胺(5.2mL,30mmole)。于室温下将该反应物搅拌过夜。用水猝灭反应物,用EtOAc提取。经硫酸钠干燥,真空除去溶剂。然后使粗品物质溶于乙醇中,加入0.5gPd/C。将该反应物在氢化器上震摇过夜。通过Celite过滤反应物,真空除去溶剂。在少量的EtOAc中研磨。制备出3.2g约90%纯度的物质。将300mg该粗品物质在Gilson上纯化,冻干得到化合物432,为白色粉末。MS m/z 384(M+H)+。
1HNMR(DMSO-d6):3.55(s,2H),3.82(s,6H),4.87(s,2H),5.40(br s,1H),6.65(m,1H),7.24(m,3H),7.58(d,1H),7.92(s,1H),9.50(s,1H).
实施例28
1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-3-吡咯
烷-1-基-丙烷-1,3-二酮,化合物536(方法N)
化合物536
于室温下,将(6,7-二甲氧基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺(化合物14)(0.36,1.0mmol)、3-氧代-3-吡咯烷-1-基-丙酸(化合物28a)(0.157g,1.0mmole)、1-(3-二甲基氨基丙基)-3-乙基碳二亚胺(EDC)(0.24g,1.25mmol)、羟基苯并-三唑水合物(HOBT)(0.17g,1.25mmol)和DIEA(0.220mL,1.25mmol)的混合物在10mL DMF中搅拌过夜。用饱和碳酸氢钠猝灭反应物,用EtOAc提取。真空除去溶剂,粗品物质经Gilson纯化。冻干得到白色粉末。MS m/z 465.1(M+H)+。
1HNMR(DMSO-d6):1.82(m,2H),1.98(m,2H),3.34(s,2H),3.59(m,4H),3.79(s,3H),3.80(s,3H),4.09(s,2H),6.67(t,1H),7.27(m 3H),7.65(d,1H),8.89(s,1H),9.50(s,1H).
实施例29
1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-3-吡咯
烷-1-基-丙烷-1,3-二酮,化合物535(方法N)
化合物535
于室温下,将(6,7-二甲氧基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺(化合物14)(0.36,1.0mmol)、3-氧代-3-吡咯烷-1-基-丙酸(化合物28a)(0.157g,1.0mmole)、EDC(0.24g,1.25mmol)、HOBt(0.17g,1.25mol)和DIEA(0.220mL,1.25mmol)在10mL DMF中搅拌过夜。用饱和碳酸氢钠猝灭反应物,用EtOAc提取。真空除去溶剂,粗品物质经Gilson纯化。冻干得到化合物535,为白色粉末。MS m/z 465.1(M+H)+。
1HNMR(DMSO-d6):1.82(m,2H),1.98(m,2H),3.34(s,2H),3.59(m,4H),3.79(s,3H),3.80(s,3H),4.09(s,2H),6.67(t,1H),7.27(m 3H),7.65(d,1H),8.89(s,1H),9.50(s,1H).
实施例30
5-羟基-6-甲氧基-4-硝基-茚满-1-酮,中间体Q
中间体H是一种已知的化合物,根据在Jose M.Saa等,J.OrgChem.,57(2),589,1992中所描述的文献方法制备。将5-羟基-6-甲氧基-茚满-1-酮(中间体H)(3.0g. 0.017mol)溶于100mL乙醚中,滴加到7.5mL硝酸。于室温下,搅拌该反应物2小时。经HPLC显示反应完成。滤出沉淀物,用乙醚洗涤。得到3.2g黄色固体(中间体Q)。
MS m/z 224(M+H)+;1HNMR(DMSO-d6):2.64(m,2H),3.15(m,2H),3.92(s,3H),7.32(s,1H),11.75(s,1H)。
实施例31
4-氨基-5-羟基-6-甲氧基-茚满-1-酮,中间体R
中间体Q 中间体R
中间体Q是一种已知的化合物,根据在Jose M.Saa等,J.OrgChem.,57(2),589,1992中所描述的文献方法制备。将5-羟基-6-甲氧基-4-硝基-茚满-1-酮(中间体Q)(2.0g,9.0mmol)加入到在冰浴上的氯化锡二水合物(10.0g,44mmol)的30mL浓HCl溶液。于室温下将反应物搅拌过夜。经HPLC显示反应完成。将该反应物用水猝灭,用固体氢氧化钠颗粒使呈中性。通过Celite过滤除去形成的固体沉淀物。用EtOAc提取含水层,用盐水洗涤,经硫酸钠干燥。经旋转蒸发除去溶剂,得到1.5g中间体R,为黄色固体。MS m/z 194(M+H)+;
1HNMR(DMSO-d6):2.42(m,2H),2.76(m,2H),3.71(s,3H),6.50(s,1H)。
实施例32
4-甲氧基-2-甲基-7,8-二氢-茚并[4,5d]噁唑-6-酮,中间体S
中间体R是一种已知的化合物,根据在Jose M.Saa等,J.OrgChem.,57(2),589,1992中所描述的文献方法制备。将4-氨基-5-羟基-6-甲氧基-茚满-1-酮(中间体R)(1.5g,7.8mmol)溶于40mL冰醋酸中,温和回流过夜。经HPLC显示反应未完成,所以继续反应1天。用水猝灭,用3N NaOH使呈碱性,用EtOAc提取。用盐水洗涤,经硫酸钠干燥,真空除去溶剂。得到1.2g深色固体(中间体Q);MS m/z218(M+H)+。
实施例33
(3-氟-苯基)-(4-甲氧基-2-甲基-7,9-二氢-3-氧杂-1,6,7-三氮杂-环戊并
[b]-不对称引达省-8-基(as-indacen-8-yl))-胺,化合物605(方法A)
于室温、搅拌下,将4-甲氧基-2-甲基-7,8-二氢-茚并[4,5-d]噁唑-6-酮(化合物33a)(0.22g,0.001mole)、异硫氰酸3-氟-苯酯(化合物4a)(0.14mL,0.0011mole)和THF(1.5mL)的混合物滴加到六甲基乙硅烷基锂(1.2mL,0.0012mole)中。搅拌反应混合物4小时,以提供中间体产物(化合物33b),其无须分离。将肼(0.070mL,0.0022mole)和乙酸(0.132mL,0.0022mole)加入到反应混合物中,然后将其在回流温度下加热18小时。将得到的混合物先加入水(10mL),然后用EtOAc提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。粗品物质经反相HPLC纯化。冻干得到化合物605,为白色粉末。MS m/z 351.1(M+H)+。
1HNMR(DMSO-d6):2.62(s,3H),3.60(s,2H),4.05(s,3H),6.54(t,1H),6.98(d,1H),7.22(m,3H),8.87(br,1H).
实施例34
5,6-二甲氧基-4-硝基-茚满-1-酮,中间体T
中间体T
使5-羟基-6-甲氧基-4-硝基-茚满-1-酮(中间体Q)(4.4g,0.02mol)和碳酸钾(2.7g,0.02mol)溶于DMF。加入甲基碘(5.0mL,0.08mol),于室温下将反应物搅拌过夜。经HPLC显示只有15%转化,因此使反应在50℃继续4小时。用水猝灭该反应物,用EtOAc提取。用盐水洗涤,经硫酸钠干燥,真空除去溶剂。得到3.4g粗品物质(中间体T)。MS m/z 238(M+H)+。
实施例35
4-氨基-5,6-二甲氧基-茚满-1-酮,中间体U
中间体U
将5,6-二甲氧基-4-硝基-茚满-1-酮(中间体T)(2.0g,8.4mmol)加入到在冰浴上的氯化锡二水合物(10.0g,44mmol)的30mL浓HCl溶液中。于室温下将反应物搅拌过夜。经HPLC显示反应完成。将该反应物用水猝灭,用固体氢氧化钠颗粒使呈中性。通过Celite过滤除去形成的固体沉淀物。用EtOAc提取含水层,用盐水洗涤,经硫酸钠干燥。经旋转蒸发除去溶剂,得到1.2g黄色固体(中间体U)。MS m/z208(M+H)+。
1HNMR(CDCl3):2.69(m,2H),2.80(m,2H),3.84(s,3H),3.87(s,3H),4.02(s,2H),6.72(s,1H).
实施例36
N-(5,6-二甲氧基-1-氧代-茚满-4-基)-乙酰胺,中间体V
中间体V
使4-氨基-5,6-二甲氧基-茚满-1-酮(中间体U)(0.214g,1.0mmol)溶于5mL DMF中,加入乙酰氯(0.071mL,1.0mmol)和DIEA(0.18mL,1.0mmol)。于室温下将反应物搅拌过夜。用饱和碳酸氢钠猝灭该反应物,用EtOAc提取。将有机层用盐水洗涤,经硫酸钠干燥,真空除去。得到0.25g粗品物质(中间体V);MS m/z 250.1(M+H)+。
实施例37
N-[3-(3-氟-苯基氨基)-6,7-二甲氧基-2,4-二氢-茚并[1.2-c]吡唑-5-基]-乙
酰胺,化合物557(方法A)
于室温、搅拌下,将N-(5,6-二甲氧基-1-氧代-茚满-4-基)-乙酰胺(中间体V)(0.25g,0.001mole)、异硫氰酸3-氟-苯酯(化合物4a)(0.14mL,0.0011mole)和THF(1.5mL)的混合物滴加入六甲基乙硅烷基锂(1.2mL,0.0012mole)中。搅拌反应混合物4小时,以提供中间体产物(化合物37a),其无须分离。将肼(0.070mL,0.0022mole)和乙酸(0.132mL,0.0022mole)加入到反应混合物中然后于回流温度下加热18小时。先向得到的混合物加入水(10mL),然后用EtOAc提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水和盐水溶液洗涤,干燥(硫酸钠),真空除去溶剂。粗品物质经反相HPLC纯化。冻干得到一种白色粉末(化合物557)。MS m/z 383.1(M+H)+。
1HNMR(DMSO-d6):2.07(s,1H),3.32(s,1H),3.40(s,1H),3.72(s,3H),3.89(s,3H),6.51(t,1H),6.92(t,1H),7.18(m,3H),8.87(br,1H),9.62(s,1H).
实施例38
3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸异丙基
酯,化合物436(方法O)
搅拌(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺HCl(化合物14)(0.50g,0.0014mole)、THF(10mL)和二异丙基胺(0.512mL,0.00295mole)的溶液,直至固体完全溶解。于室温下缓慢加入氯代甲酸异丙基酯(1.5mL,0.0015mole)。将该反应化合物于室温下搅拌过夜。从得到的有机物真空除去溶剂。试图用反相层析法分离得到的异构体未获得成功。将包含异构体的各部分置于冰箱中。主要异构体的大部分被结晶出来。从溶液中过滤出白色结晶的标题化合物(化合物436)。MS m/z 412(M+H)+。
1H NMR(DMSO-d6):1.4(d,6H),3.55(s,2H),3.85(s,6H),5.25(sept,1H),6.65(t,1H),7.25(m,3H),7.65(d,1H),7.8(s,1H),9.4(s,1H).
实施例39
3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸2-甲氧基-
乙基酯,化合物438(方法O)
搅拌(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺HCl(化合物14)(0.50g,0.0014mole)、THF(10mL)和二异丙基胺(0.512mL,0.00295mole)的溶液,直至固体完全溶解。于室温下滴加入氯代甲酸2-甲氧基乙基酯(0.178mL,0.00154mole)。搅拌2小时后反应完成。真空除去溶剂,有机油状物经反相层析系统纯化,以分离异构体。分离是成功的。收集所需的部分,冻干得到淡黄色固体(化合物438)。NMR显示主要异构体是标题化合物。MS m/z 428(M+H)+。
1H NMR(DMSO-d6):3.35(s,3H),3.6(s,2H),3.75(t,2H),3.85(d,6H),4.6(t,2H),6.7(m,1H),7.3(m,3H),7.7(d,1H),7.8(s,1H),9.4(s,1H).
实施例40
3-(3-氟-苯基-氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸2-甲氧基
-乙基酯,化合物437(方法O)
搅拌(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺HCl(化合物14)(0.50g,0.0014mole)、THF(10mL)和二异丙基胺(0.512mL,0.00295mole)的溶液,直至固体完全溶解。于室温下滴加入氯代甲酸2-甲氧基乙基酯(0.178mL,0.00154mole)。搅拌2小时后反应完成。真空除去溶剂,有机油状物经反相层析系统纯化,以分离异构体。分离是成功的。收集所需的部分,冻干得到淡黄色固体(化合物437)。NMR显示较少的异构体是标题化合物。MS m/z 428(M+H)+。
1H NMR(DMSO-d6):3.35(s,3H),3.4(s,2H),3.7(t,2H),3.8(s,3H),3.9(s,3H),4.5(t,2H),6.85(t,1H),7.0(m,2H),7.2(s,1H),7.35(m,2H),8.9(s,1H).
实施例41
3-(3-氟-苯基-氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸2-[2-(2-
羟基-乙氧基)-乙氧基]-乙酯,化合物471(方法O)
装置两个烧瓶,使每个烧瓶各含50mL THF。向第一个烧瓶中加入(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺HCl(化合物14)(0.50g,00014mole)和二异丙基胺(0.512mL,0.00295mole),并在氩气下搅拌,直至固体完全溶解。将三(乙二醇)双(氯代甲酸酯)(1.134mL,0.0055mole)加入到第二个烧瓶中,并在氩气下置于干冰/异丙醇浴中。然后将第一个烧瓶中的内容物一次性加入到第二个烧瓶中。反应在10分钟内完成。使反应物回升至室温。真空除去溶剂。使得到的棕色油状物溶于乙酸乙酯和二氯甲烷中,用碳酸氢钠洗涤。干燥(硫酸钠)得到的有机物,过滤,真空除去溶剂。经反相层析将主要异构体(化合物471)和次要异构体分离。经1H NMR,将游离的氯代甲酸酯水解为在DMSO中的醇,以用于装填反相柱。收集各异构体的部分并冻干。MS m/z 502(M+H)+。
1H NMR(DMSO-d6):3.3-3.7(m,12H),3.85(d,6H),4.6(m,2H),6.7(m,1H),7.3(m,3H),7.7(d,1H),7.8(s,1H),9.4(s,1H).
实施例42
(6,7-二甲氧基-1-甲基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-
胺,化合物609(方法L)
将碘甲烷(0.141g,0.001mole)加入到(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]1-N-甲基-吡唑-3-基)-胺(化合物14)(321mg,0.001mole)、二异丙基乙胺(0.129g,0.001mole)和DCM(5mL)的混合物中。将该反应化合物于室温下搅拌18小时。先将得到的混合物加入到水(5mL)中,然后用二氯甲烷提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水洗涤,干燥(硫酸钠),真空除去溶剂。根据hplc/ms分析,该混合物含有两种异构体。将该混合物用C-18反相柱经HPLC分离,用乙腈-水-TFA作为梯度溶剂。得到标题化合物(化合物609;主要异构体),为固体TFA盐。
HPLC:100%(uv 214mμ);MS m/z 340(M+H)+;
1HNMR(CDCl3-d1):3.33(s,2H),3.84(s,3H),3.90(s,3H),3.95(s,3H),6.48(t,1H),6,.66(d 1H),6.57(d,1H),7.0(s,1H),7.1(t,2H).
实施例43
(6,7-二甲氧基-2-甲基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-
胺,化合物610(方法L)
将碘甲烷(0.141g,0.001mole)加入到(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]1-N-甲基-吡唑-3-基)-胺(化合物14)(321mg,0.001mole)、二异丙基乙胺(0.129g,0.001mole)和DCM(5mL)的混合物中。将该反应化合物于室温下搅拌18小时。先将得到的混合物加入到水(5mL)中,然后用二氯甲烷提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水洗涤,干燥(硫酸钠),真空除去溶剂。根据hplc/ms分析,该混合物含有两种异构体。将该混合物用C-18反相柱经HPLC分离,用乙腈-水-TFA作为梯度溶剂。得到标题化合物(化合物610;次要异构体),为固体TFA盐。MS m/z 340(M+H)+。
1HNMR(CDCl3-d1):3.33(s,2H),3.74(s,3H),3.84(s,3H),3.88(s,3H),6.37(d,1H),6,.46(d 1H),6.53(t,1H),7.0(s,1H),7.1(t,1H),7.2(s,1H).
实施例44
3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸(3-氟-苯
基)-酰胺,化合物395(方法Q)
化合物395
向(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]1-N-甲基-吡唑-3-基)-胺(化合物14)(321mg,0.001mole)、二异丙基乙胺(0.129g,0.001mole)和DCM(5mL)的混合物中加入3-氟代苯基异氰酸酯(化合物44a)(0.137g 0.001mole)。将该反应化合物于室温下搅拌18小时。先将得到的混合物加入到水(5mL)中,然后用二氯甲烷提取。合并有机层,用碳酸氢钠水溶液洗涤,然后用水洗涤,干燥(硫酸钠),真空除去溶剂。将标题化合物用C-18反相柱经HPLC纯化,用乙腈-水-TFA作为梯度溶剂。得到标题化合物,为固体TFA盐。MS m/z 463(M+H)+。
1HNMR(CDCl3-d1):3.33(s,2H),3.74(s,3H),3.84(s,3H),3.88(s,3H),6.377(m,1H),7.21(s 1H),7.33(m,3H),7.4(m,2H),7.6(d,1H),7.85(s,1H),7.9(m,1H),9.31(s,1H),9.54(s,1H).
实施例46
(2-氯-吡啶-3-基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)胺,化
合物377(方法B)
化合物377
将2-(咪唑-1-硫代甲酰基)-5,6-二甲氧基-茚满-1-酮(中间体B)(0.302g,0.001mole)(如实施例5中制备)的溶液与3-氨基-2-氯代吡啶(化合物46a)(0.128g,0.001mole)和10mL THF在一烧瓶中混合。于室温下搅拌该反应混合物4小时后,经HPLC/MS证实,得到5,6-二甲氧基-1-氧代-茚满-2-硫代甲酸(4-氯-N-甲基-苯基)-酰胺(化合物46b),HPLC/MS m/z 362(M+H)+。
无须分离中间体(化合物46b),随后用肼(0.04mL,1.3mmol)和乙酸(2滴)处理该混合物。于75℃将该反应物加热18小时。然后用二氯甲烷稀释反应溶液,用碳酸氢钠水溶液洗涤,然后用水洗涤,干燥(硫酸钠),真空除去溶剂。将标题化合物用C-18反相柱经HPLC纯化,用乙腈-水-TFA作为梯度溶剂。得到标题化合物(化合物529),为固体TFA盐。MS m/z 343(M+H)+。
1HNMR(CDCl3-d1):3.33(s,2H),3.84(s,3H),3.88(s,3H),6.77(t,1H),6,.86(d1H),7.6(d,1H),7.9(d,1H),8.23(s,1H).
实施例47
5,6-二甲氧基-3-乙基-茚满-1-酮,中间体W
中间体W
在氩气下,在冰浴中,将1,2-二甲氧基-苯(化合物47a)(21.9mL,0.170mole)和戊-3-烯酸(化合物47b)(25.5g,0.255mole)的混合物搅拌。缓慢加入多磷酸(230g,1.05mole)。加入完毕后,移去冰浴,于60℃将反应物加热16小时。将反应物加入冰水中,用二氯甲烷提取。将有机提取物用3N NaOH、水、盐水洗涤,经硫酸钠干燥。然后真空除去溶剂,得到包含粗品标题化合物的红色油状物。该粗品物质经硅胶柱纯化,使用二氯甲烷作为洗脱剂。合并纯净的各部分,浓缩得到标题化合物的外消旋混合物,为灰白色固体。MS m/z 221(M+H)+;
HPLC:99%纯度(UV);
1HNMR:0.9(t,3H),1.4(m,1H),2.0(m,1H),2.2(d of d,1H),2.7(d of d,1H),3.2(m,1H),3.8(s,1H),3.9(s,1H),7.0(s,1H),7.2(s,1H).
实施例48
*
R-5,6-二甲氧基-3-乙基-茚满-1-酮,中间体W(
*
R);
*
S-5,6-二甲氧基
-3-乙基-茚满-1-酮,中间体W(
*
S)
中间体W(*S) 中间体W(*R)
将实施例47中制备的外消旋混合物进行手性分离。在ChiralpackAD柱上(500g,5cm ID和41cm长度)进行分离,使用己烷/乙醇:88/12作为等度洗脱剂。收集纯对映体,真空除去溶剂,得到灰白色结晶的标题化合物。MS m/z 221(M+H)+;
HPLC:99%纯度(UV);
1HNMR:0.9(t,3H),1.4(m,1H),2.0(m,1H),2.2(d of d,1H),2.7(d of d,1H),3.2(m,1H),3.8(s,1H),3.9(s,1H),7.0(s,1H),7.2(s,1H).
*R和*S构型如图中所示。绝对构型未测定。
*R异构体有旋光性:α(MeOH)=-20.55
*S异构体有旋光性:α(MeOH)=+18.60
实施例49
5,6-二甲氧基-3-甲基-茚满-1-酮,中间体X
中间体X
在氩气下,在冰浴中,将1,2-二甲氧基-苯(化合物47a)(19.1mL,0.150mole)和丁-3-烯酸(化合物49a)(19.2mL,0.225mole)的混合物搅拌。缓慢加入多磷酸(230g,1.05mole)。加入完毕后,移去冰浴,于60℃将反应物加热16小时。将反应物加入冰水中,用乙醚提取。将有机提取物用3N NaOH、水、盐水洗涤,经硫酸钠干燥。然后真空除去溶剂,得到包含标题化合物的外消旋混合物的黄色固体。粗品物质经硅胶柱纯化,使用1∶2EtOAc∶己烷作为洗脱剂。合并纯净的各部分,浓缩得到标题化合物的外消旋混合物(中间体X),为灰白色固体。
MS m/z 207(M+H)+;
1HNMR:1.3(d,3H),2.1(d of d,1H),2.8(d of d,1H),3.3(m,1H),3.8(s,3H),3.9(s,3H),7.0(s,1H),7.2(s,1H).
实施例50
(3R)-(5,6-二甲氧基-3-甲基)-茚满-1-酮,中间体X(
*
R);(3S)-(5,6-二甲
氧基-3-甲基)-茚满-1-酮,中间体X(
*
S)
将实施例49中制备的外消旋混合物(中间体X)进行手性分离。在Chiralpack AD柱(500g,5cm ID和41cm长度)上进行分离,使用己烷/乙醇:88/12作为等度洗脱剂。收集纯对映体,真空除去溶剂,得到灰白色结晶的标题化合物。MS m/z 207(M+H)+;HPLC:97%纯度(UV);
1HNMR:1.3(d,3H),2.1(d of d,1H),2.8(d of d,1H),3.3(m,1H),3.8(s,3H),3.9(s,3H),7.0(s,1H),7.2(s,1H).
*R和*S构型如图中所示。绝对构型未测定。
*R异构体有旋光性:α(MeOH)=-5.85
*S异构体有旋光性:α(MeOH)=+6.00
实施例51
(4R)-N-(3-溴-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-
基)-胺,化合物553(方法A)
化合物553
在氩气下,将*R-5,6-二甲氧基-3-甲基-茚满-1-酮(中间体X(*R))(0.250g,0.0012mole)加入到一烧瓶中,在THF中搅拌直至溶解。滴加入六甲基乙硅烷基锂(1.22mL,0.00122mole)。将该溶液搅拌30分钟,直至其转变成深红色。加入3-Br-异硫氰酸酯(化合物51a)(0.261g,0.00122mole),反应物变成深红色。加入乙酸(0.076mL,0.00132mole)和肼水合物(0.059mL,0.00122mole)。于80℃将反应物回流18小时。完成后,将1mL水加入该反应物中。将该溶液倾到干燥柱上,用二氯甲烷从柱中提取。用氮气吹掉溶剂,使粗品物质溶于DMSO中,以便在反相HPLC上纯化。收集纯净的部分,冻干得到标题化合物(化合物553),为浅黄色固体。MS m/z 401(M+H)+;HPLC:100%纯度(UV)
1HNMR:1.2(d,3H),3.7(q,1H),3.8(d,6H),7.0(m,1H),7.1(s,1H),7.2(d,2H),7.25(s,1H),7.55(s,1H),8.8(s,1H).
*R异构体有旋光性:α(MeOH)=+62.85
绝对构型未测定。
实施例52
*
S-(3-溴-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-
胺,化合物568(方法A)
在氩气下,将*S-5,6-二甲氧基-3-甲基-茚满-1-酮(中间体X(*S))(0.250g,0.0012mole)加入到一烧瓶中,在THF中搅拌直至溶解。滴加入六甲基乙硅烷基锂(1.22mL,0.00122mole)。将该溶液搅拌30分钟,直至其转变成深红色。加入3-Br-异硫氰酸酯(化合物51a)(0.261g,0.00122mole),反应物变成深红色。加入乙酸(0.076mL,0.00132mole)和肼水合物(0.059mL,0.00122mole)。于80℃将反应物回流18小时。完成后,将1mL水加入到该反应物中。将该溶液倾到干燥柱上,用二氯甲烷从柱中提取。用氮气吹掉溶剂,使粗品物质溶于DMSO中,以便在反相HPLC上纯化。收集纯净的部分,冻干得到标题化合物(化合物568),为浅黄色固体。MS m/z 401(M+H)+;
HPLC:100%纯度(UV)
1HNMR:1.2(d,3H),3.7(q,1H),3.8(d,6H),7.0(m,1H),7.1(s,1H),7.2(d,2H),7.25(s,1H),7.55(s,1H),8.8(s,1H).
*S异构体有旋光性:α(MeOH)=-62.60
绝对构型未测定。
实施例53
*
R-(3-溴-苯基)-(6,7-二甲氧基-4-乙基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-
胺,化合物555(方法A)
在氩气下,将*R-5,6-二甲氧基-3-乙基-茚满-1-酮(中间体W(*R))(0.250g,0.0011mole)加入到一烧瓶中,在THF中搅拌直至溶解。滴加入六甲基乙硅烷基锂(1.2mL,0.0012mole)。将该溶液搅拌30分钟,直至其转变成深红色。加入3-Br-异硫氰酸酯(化合物51a)(0.257g,0.0012mole),反应物变成深红色。加入乙酸(0.069mL,0.00121mole)和肼水合物(0.058mL,0.0012mole)。于80℃将反应物回流18小时。完成后,将1mL水加入到该反应物中。将该溶液倾到干燥柱上,用二氯甲烷从柱中提取。用氮气吹掉溶剂,使粗品物质溶于DMSO中,以便在反相HPLC上纯化。收集纯净的部分,冻干得到标题化合物(化合物555),为浅黄色固体。MS m/z 415(M+H)+;
HPLC:100%纯度(UV);
1HNMR:0.5(t,3H),1.7(m,1H),1H),(m,1H),3.7(t,1H),3.8(d,6H),6.95(d,1H),7.1(d,1H),7.2(m,3H),7.3(s,1H),8.7(s,1H).
*R异构体有旋光性:α(MeOH)=+74.64
绝对构型未测定。
实施例54
*
S-(3-溴-苯基)-(6,7-二甲氧基-4-乙基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-
胺,化合物570(方法A)
在氩气下,将*S-5,6-二甲氧基-3-乙基-茚满-1-酮(中间体W(*S))(0.250g,0.0011mole)加入到一烧瓶中,在THF中搅拌直至溶解。滴加入六甲基乙硅烷基锂(1.2mL,0.0012mole)。将该溶液搅拌30分钟,直至其转变成深红色。加入3-Br-异硫氰酸酯(化合物51a)(0.257g,0.0012mole),反应物变成深红色。加入乙酸(0.069mL,0.00121mole)和肼水合物(0.058mL,0.0012mole)。于80℃将反应物回流18小时。完成后,将1mL水加入到该反应物中。将该溶液倾到干燥柱上,用二氯甲烷从柱中提取。用氮气吹掉溶剂,使粗品物质溶于DMSO中,以便在反相HPLC上纯化。收集纯净的部分,冻干得到标题化合物(化合物570),为浅黄色固体。MS m/z 415(M+H)+;
HPLC:100%纯度(UV);
1HNMR:0.5(t,3H),1.8(m,2H),3.7(t,1H),3.8(d,6H),6.95(d,1H),7.1(d,1H),7.2(m,3H),7.3(s,1H),8.7(s,1H).
*S异构体有旋光性:α(MeOH)=-53.85
绝对构型未测定。
实施例55
3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸苯基酯(方
法O),化合物433
于室温、搅拌下,向(6,7-二甲氧基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺(化合物14)(1.5g g,4.2mmol)、氯代甲酸苯基酯(化合物55a)(0.76mL,6.3mmole)和THF(10mL)的混合物中加入二异丙基乙胺(DIPEA)(1.4mL,8.4mmole)。于室温下将反应物搅拌过夜。用饱和碳酸氢钠猝灭反应物,用乙酸乙酯提取。溶剂经硫酸钠干燥,然后经旋转蒸发除去,得到粗品物质(化合物433)。MS m/z 446.1(M+H)+。
实施例56
3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-甲基氨
基-乙基)-酰胺,化合物524(方法P)
使3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸苯基酯(化合物433)(0.50g,1.12mmol)和N-1-甲基-乙烷-1,2-二胺(化合物56a)(0.12mL,1.3mmol)溶于5mL DMSO中。于室温下,将反应物搅拌过夜。用饱和碳酸氢钠猝灭反应物,用乙酸乙酯提取。溶剂经硫酸钠干燥并经旋转蒸发除去。粗品物质经Gilson HPLC制备,冻干得到标题化合物,为TFA盐。MS m/z 426.3(M+H)+;
1HNMR(DMSO-d6):2.60(s,3H),3.12(m,2H),3.24(s,2H),3.58(q,2H),3.78(s,3H),3.81(s,3H),6.55(t,1H),7.21(m,2H),7.32(d,1H),7.49(d,1H),7.90(s,1H),8.15(t,1H),8.60(s,1H),9.22(s,1H).
实施例57
(3-氟-苯基)-(2H-8-氧杂-2,3-二氮杂-环戊并[a]茚-1-基)-胺,化合物380
(方法A)
于室温、搅拌下,向苯并呋喃-3-酮(化合物57a)(0.150g,0.00112mol)、异硫氰酸3-氟-苯酯(化合物4a)(0.259g,0.00134mmol)和THF(2.00mL)的混合物中滴加入六甲基乙硅烷基锂(1.34mL,0.00134mol)。搅拌反应混合物12小时。将肼(0.084mL,0.00268mol)和乙酸(0.154mL,0.00268mol)加入到反应混合物中,然后将其在回流温度下加热48小时。然后用乙酸乙酯稀释反应溶液,用水洗涤,经硫酸镁干燥。真空除去溶剂,将标题化合物经使用C-18反相柱的HPLC纯化,用乙腈-水-TFA作为梯度溶剂。得到标题化合物,为一种TFA盐。MS m/z 268(M+H)+;
1HNMR(DMSO-d6):6.55(dt,1H),6.95(d,1H),7.05(d,1H),7.20(dd,1H),7.40(m,2H),7.65(d,1H),7.75(d,1H),9.00(br s,1H).
实施例58
2,2-二甲基-丙酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-
1-基甲基酯,化合物409(方法L)
将(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺(化合物14)(1.25g,0.00385mol)、二异丙基乙胺(1.00mL,0.00578mol)、新戊酸氯代甲酯(0.833mL,0.00578mol)和碘化钾(0.960g,0.00578mol)在THF(19mL)中的混合物加热至75℃12小时。将该混合物用乙酸乙酯稀释,用盐水洗涤,经硫酸镁干燥。用乙腈-水-TFA作为梯度溶剂,经使用C-18反相柱的HPLC纯化,首先分离出来的是标题化合物。然而,这种异构体混有起始原料(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺(化合物14)。标题化合物经硅胶柱层析进一步纯化(用1%三乙胺的己烷溶液预先洗涤),使用2∶1己烷∶乙酸乙酯作为洗脱剂。MS m/z 440.1(M+H)+;
1HNMR(DMSO-d6):1.20(s,9H),3.40(s,2H),3.90(s,3H),3.96(s,3H),6.20(s,2H),6.57(m,1H),6.82(d,1H),6.95(m,1H),7.03(s,1H),7.15(m,1H),7.27(s,1H).
实施例59
2,2-二甲基-丙酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-
2-基甲基酯,化合物408(方法L)
将(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺(化合物14)(1.25g,0.00385mol)、二异丙基乙胺(1.00mL,0.00578mol)、新戊酸氯代甲酯(0.833mL,0.00578mol)和碘化钾(0.960g,0.00578mol)在THF(19mL)中的混合物加热至75℃12小时。将该混合物用乙酸乙酯稀释,用盐水洗涤,经硫酸镁干燥。用乙腈-水-TFA作为梯度溶剂,经使用C-18反相柱的HPLC纯化,第二批分离出来的是标题化合物。然而,这种异构体混有起始原料(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺(化合物14)。标题化合物经硅胶柱层析进一步纯化(用1%三乙胺的己烷溶液预先洗涤),使用2∶1己烷∶乙酸乙酯作为洗脱剂。MS m/z 440.1(M+H)+;
1HNMR(DMSO-d6):1.22(s,9H),3.40(s,2H),3.90(s,3H),3.93(s,3H),5.94(s,2H),6.62(m,2H),6.72(d,1H),6.97(s,1H),7.21(m,1H),7.33(s,1H),7.56(bs,1H).
实施例60
5,6-双[3-四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮,中间体Y
于60℃,将5,6-二羟基-茚满-1-酮(中间体O)(2.00g,0.0122mole)、碳酸钾(4.22g,0.0305mol)、2-(3-氯-丙氧基)-四氢-吡喃(化合物18a)(4.36g,0.0244mol)和碘化钾(4.00g,0.0244mol)在DMF(20mL)中的混合物搅拌36小时。然后用乙酸乙酯稀释该反应混合物,用水洗涤,经硫酸镁干燥。真空除去溶剂,标题化合物经硅胶柱层析纯化,使用3∶1己烷∶乙酸乙酯作为洗脱剂。MS m/z 449(M+H)+;
1HNMR(CDCl3):1.60(m,12H),2.13(m,4H),2.70(t,2H),3.12(t,3H),3.52(m,4H),3.90(m,2H),4.20(m,4H),4.60(s,2H),6.90(s,1H),7.18(s,1H).
实施例61
3-[3-(3-氟-苯基氨基)-6-(3-羟基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-7-基
氧基]丙-1-醇,化合物398(方法A)
于室温、搅拌下,向5,6-二[3-四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮(中间体Y)(0.100g,0.00022mol)、异硫氰酸3-氟代苯酯(化合物4a)(0.031mL,0.00026mol)和THF(4mL)的混合物中滴加入六甲基乙硅烷基锂(0.260mL,0.00026mol)。搅拌反应混合物12小时。将肼(0.008mL,0.00026mol)和乙酸(0.015mL,0.00026mol)加入到反应混合物中,然后将其在回流温度下加热24小时。然后用乙酸乙酯稀释反应溶液,用水洗涤,经硫酸镁干燥。真空除去溶剂,标题化合物经使用C-18反相柱的HPLC纯化,用乙腈-水-TFA作为梯度溶剂。得到标题化合物,为固体TFA盐。
MS m/z 414.3(M+H)+;
1HNMR(MeOH-d4):2.05(m,4H),3.50(s,2H),3.83(m,4H),4.20(t,4H),6.76(m,1H),6.95(m,2H),7.26(s,1H),7.28(s,1H),7.36(m,1H).
实施例62
5-乙氧基-6-[3-(四氢-吡喃-2-基氧基)-丙氧基-茚满-1-酮,中间体Z
于室温下,将5,6-二羟基-茚满-1-酮(中间体O)(2.00g,0.0122mole)、碳酸钾(4.22g,0.0305mol)和乙基溴(0.911mL,0.0122mol)在DMF(20mL)中的混合物搅拌12小时。将该混合物用乙酸乙酯稀释,用水洗涤,经硫酸镁干燥。真空除去溶剂。得到的5-乙氧基-6-羟基-茚满-1-酮(化合物62a)经硅胶柱层析纯化,使用3∶1己烷∶乙酸乙酯作为洗脱剂。
于60℃,将5-乙氧基-6-羟基-茚满-1-酮(化合物62a)(0.520g,0.00271mol)、2-(3-氯-丙氧基)-四氢-吡喃(化合物18a)(0.938g,0.00542mol)、碳酸钾(0.936g,0.00678mol)和碘化钾(0.900g,0.00542mol)在DMF(5.5mL)中的混合物搅拌12小时。然后将反应混合物用乙酸乙酯稀释,用水洗涤,经硫酸镁干燥。真空除去溶剂,标题化合物经硅胶柱层析纯化,使用3∶1己烷∶乙酸乙酯作为洗脱剂。MS m/z 334.2(M+H)+;
1HNMR(CDCl3):1.60(m,9H),2.18(m,2H),2.65(t,2H),3.06(t,2H),3.48(m,2H),3.85(m,2H),4.18(m,4H),4.62(t,1H),6.84(s,1H),7.22(s,1H).
实施例63
3-[6-乙氧基-3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-丙
-1-醇,化合物365(方法A)
于室温、搅拌下,向5-乙氧基-6-[3-(四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮(中间体Z)(0.100g,0.0003mol)、异硫氰酸3-氟代苯酯(化合物4a)(0.043mL,0.00036mol)和THF(3mL)的混合物中滴加入六甲基乙硅烷基锂(0.360mL,0.00036mol)。搅拌反应混合物5小时。将肼(0.011mL,0.00036mol)和乙酸(0.021mL,0.00036mol)加入到反应混合物中,然后将其在回流温度下加热12小时。然后用乙酸乙酯稀释反应溶液,用水洗涤,经硫酸镁干燥。真空除去溶剂,粗品物质经反相HPLC纯化,然后在0.1%TFA溶液中静置后转化为所需的产物。冻干得到标题化合物,为白色粉末。MS m/z 384.4(M+H)+;
1HNMR(CDCl3):1.47(t,3H),2.12(m,2H),3.43(s,2H),3.90(t,2H),4.08(q,2H),4.22(t,2H),4.85(bs,1H),6.89(m,2H),6.97(s,1H),7.18(s,1H),7.32(m,2H),9.42(bs,1H).
实施例64
6-乙氧基-5-[3-(四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮,中间体AA
于60℃,将5,6-二羟基-茚满-1-酮(中间体O)(1.80g,0.01098mole)、碳酸钾(3.80g,0.02744mol)、2-(3-氯-丙氧基)-四氢-吡喃(化合物18a)(1.37g,0.00769mol)和碘化钾(1.28g,0.00769mol)在DMF(20mL)中的混合物搅拌4小时。然后向该混合物中加入乙基溴(1.64mL,0.02196mol),继续加热另外4小时。然后将该反应混合物用乙酸乙酯稀释,用水洗涤,经硫酸镁干燥。真空除去溶剂,标题化合物经硅胶柱层析纯化,使用3∶1己烷∶乙酸乙酯作为洗脱剂。MS m/z 334.2(M+H)+;
1HNMR(CDCl3):1.65(m,9H),2.20(m,2H),2.68(t,2H),3.15(t,2H),3.55(m,2H),4.10(m,6H),4.60(m,1H),6.92(s,1H),7.16(s,1H).
实施例65
3-[7-乙氧基-3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙
-1-醇,化合物382(方法A)
于室温、搅拌下,向6-乙氧基-5-[3-(四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮(中间体AA)(0.100g,0.0003mol)、异硫氰酸3-氟代苯酯(化合物4a)(0.043mL,0.00036mol)和THF(3mL)的混合物中滴加入六甲基乙硅烷基锂(0.360mL,0.00036mol)。搅拌反应混合物48小时。将肼(0.011mL,0.00036mol)和乙酸(0.021mL,0.00036mol)加入到反应混合物中,然后将其在回流温度下加热12小时。然后用乙酸乙酯稀释反应溶液,用水洗涤,经硫酸镁干燥。真空除去溶剂,粗品物质经反相HPLC纯化,然后在0.1%TFA溶液中静置后转化为所需的产物。冻干得到标题化合物,为白色粉末。MS m/z 384.2(M+H)+;
1HNMR(DMSO-d6):1.28(t,3H),2.90(m,2H),3.42(s,2H),3.60(t,2H),4.12(m,4H),6.54(m,1H),6.88(d,1H),7.20(m,4H),8.80(bs,1H).
实施例66
3-噻吩-2-基-丙烯酸,中间体AB
将噻吩-2-甲醛(化合物66a)(1.20g,0.0107mol)、丙二酸(1.11g,0.0107mol)和乙酸铵(0.825g,0.0107mol)在DMF(8.5mL)中的混合物加热至100℃3小时。将该系统用乙酸乙酯稀释,用水洗涤,经硫酸镁干燥。真空除去溶剂,标题化合物经硅胶柱层析纯化,使用3∶1己烷∶乙酸乙酯作为洗脱剂。
1HNMR(CDCl3):6.25(d,1H),7.08(m,1H),7.30(d,1H),7.42(d,1H),7.88(d,1H)。
实施例67
3-噻吩-2-基-丙酸,中间体AC
在氢气气氛(50PSI)下,将3-噻吩-2-基-丙烯酸(中间体AB)(2.00g,0.01299mol)、10%Pd/C(2.00g)在甲醇(200mL)中的混合物搅拌18小时。将得到的系统用N2吹洗,然后经硅藻土垫过滤。有机物经硫酸镁干燥,真空除去溶剂,得到3-噻吩-2-基-丙酸。
1HNMR(CDCl3):2.76(t,2H),3.20(t,2H),6.82(d,1H),6.95(m,1H),7.15(d,1H)。
实施例68
5,6-二氢-环戊并[b]噻吩-4-酮,中间体AD
于室温下,向3-噻吩-2-基-丙酸(中间体AC)(1.75g,0.01122mol)的二氯甲烷(50mL)溶液中加入SOCl2(1.67mL,0.02244mol),于室温下搅拌6小时。用45分钟,将该溶液滴加到AlCl3(2.98g,0.02244mol)在二氯甲烷(50mL)中的悬浮液中。于室温下搅拌得到的混合物12小时。通过滴加水(10mL)猝灭该系统,用二氯甲烷提取。经硫酸镁干燥有机物,真空除去溶剂。标题化合物经硅胶柱层析纯化,使用4∶1己烷∶乙酸乙酯作为洗脱剂。MS m/z 139.1(M+H)+;
1HNMR(CDCl3):3.01(t,2H),3.18(t,2H),7.15(d,1H),7.32(d,1H)。
实施例69
(5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-(3-乙氧基-苯
基)胺,化合物405(方法A)
于室温、搅拌下,向5,6-二氢-环戊并[b]噻吩-4-酮(中间体AD)(0.065g,0.00047mol)异硫氰酸3-乙氧基-苯酯(化合物69a)(0.108g,0.00056mol)和THF(2.5mL)的混合物中滴加入六甲基乙硅烷基锂(0.560mL,0.00056mol)。搅拌反应混合物3小时。将肼(0.036mL,0.00112mol)和乙酸(0.0032mL,0.00056mol)加入到反应混合物中,然后将其加热至50℃8小时。然后用乙酸乙酯稀释反应溶液,用水洗涤,经硫酸镁干燥。真空除去溶剂,标题化合物经使用C-18反相柱的HPLC纯化,用乙腈-水-TFA作为梯度溶剂。得到标题化合物,为固体TFA盐。MS m/z 298.2(M+H)+;
1HNMR(DMSO-d6):1.25(t,1H),3.52(s,2H),3.88(q,2H),5.80(bs,1H),6.28(m,1H),6.65(m,2H),7.05(t,1H),7.18(d,1H),7.58(d,1H),8.60(bs,1H).
实施例70
3-(6-乙氧基-3-(3-乙氧基-苯基氨基)-2,4-二氢-茚并{1,2-c}吡唑-7-基氧
基]-丙-1-醇,化合物388(方法A)
于室温、搅拌下,向5-乙氧基-6-[3-(四氢-吡喃-2-基氧基)-丙氧基]-茚满-1-酮(中间体Z)(0.100g,0.0003mol)、异硫氰酸3-乙氧基苯酯(化合物69a)(0.043mL,0.00036mol)和THF(3mL)的混合物中滴加入六甲基乙硅烷基锂(0.360mL,0.00036mol)。搅拌反应混合物5小时。将肼(0.011mL,0.00036mol)和乙酸(0.021mL,0.00036mol)加入到该反应混合物中,然后在回流温度下加热12小时。然后用乙酸乙酯稀释反应溶液,用水洗涤,经硫酸镁干燥。真空除去溶剂,粗品物质经反相HPLC纯化,然后在0.1%TFA溶液中静置后并转化为所需的产物。冻干得到标题化合物,为白色粉末。MS m/z 410.2(M+H)+;
1HNMR(DMSO-d6):8.65(bs,1H),7.14(m,3H),6.79(s,1H),6.71(d,1H),6.37(d,1H),4.03(m,6H),3.60(t,2H),3.40(s,1H),1.88(m,2H),1.30(m,6H).
生物学活性
本发明化合物的生物学活性
将本发明范围内的化合物进行各种生物学试验。这些试验的结果表明,本发明范围内的化合物抑制PDGF-R激酶活性。本发明范围内的化合物也显示针对c-Abl激酶的抑制活性。此外,在有或无PDGF刺激下,本发明范围内的化合物抑制细胞(包括正常组织细胞、肿瘤细胞和白血病细胞)增殖。其它研究证实本发明范围内的化合物抑制血管生成,且所述化合物显示具有抗-肿瘤活性。另外,本发明范围内的化合物使肿瘤细胞对放射治疗变得敏感。已证实本发明范围内的化合物的药物前体在体内可经转化重新变回母体化合物。
进行以下代表性的测定法,以测定本发明范围内的化合物的生物学活性。给出这些测定法是为了以非限制的方式阐明本发明。
1.PDGF-受体激酶活性的抑制
PDGF-R激酶活性通过其在无细胞系统中使它的靶蛋白之一,PLCγ,(特别是包含酪氨酸残基的PLC1肽)磷酸化的能力来测定,其中发生的磷酸化用于所述测定中。
材料
制备用于所述测定的以下试剂:10X激酶缓冲液(500mM Tris-HClpH=8,100mM MgCl2、1mM Na3 VO4);10mM DTT(在测定中的终浓度为1mM);10mM ATP(在测定中的终浓度为5μM);33P-γ-ATP(Cat.No.:NEG/602 H.2000-3000 Ci/mmol,购自NEN);包含酪氨酸激酶结构域(从GenBank Access NO:AAA36427的氨基酸545-1106)的0.4mg/mL纯化的、可溶解的重组PDGF-受体β酶;酶稀释缓冲液(50mM Tris-HCl pH=8.0,0.1%BSA);洗涤/终止缓冲液(PBS+100mMEDTA);NEN链霉抗生物素快速板(Cat.No.:SMP-103),其结合生物素化的PLC1肽,但并非PDGF-R酶;在50mM Tris-HCl中的1mMPLC1肽(Biotin-KHKKLAEGSAYEEV-酰胺),pH 8.0。
步骤
根据以下方案,先将试剂混合:
| (μl) | (μl) | |
| 10X激酶缓冲液 | 1100 | 10 |
| 10mMDTT | 1100 | 10 |
| 10mM冷的ATP | 5.5 | 0.05 |
| 1mM PLC1肽 | 2.75 | 0.025 |
| 33P-γ-ATP(10μCi/μl) | 8.8 | 0.08 |
| H<sub>2</sub>O | 5475 | 49.77 |
将以上的反应混合物以70μl/孔的量分配到快速板(Flashplate)每孔中。为测试化合物对PDGF-R激酶活性的效果,将试验化合物或者以在100%DMSO中的固定的浓度,或者以系列稀释的浓度加入到适当的各孔中,其量为1μl/孔。
将酶PDGF-R用酶稀释缓冲液如下稀释:
酶稀释缓冲液 3289μl
PDGF-R酶 100μl
通过向含有热的ATP和PLC1的Flashplate的各孔中加入30μl稀释的PDGF-R酶溶液启动激酶反应,第12列E至H排的各孔除外,这些孔被用于计算该测定板的背景值。将Flashplate旋转以便混合,于30℃温育60分钟。然后,弃去反应混合物,用洗涤/终止缓冲液洗涤Flashplate 3次,每次200μl。
随后,在Flashplate的各孔中加入200μl洗涤/终止缓冲液。在将所述板用透明板密封层密封后,用Packard TopCount测量保留在每孔中的33P的量。
当一种试验化合物抑制PDGF-R激酶活性时,含有这种化合物的孔与不含这种化合物的孔比较,其含有较低的33P的量。试验化合物对PDGF-R激酶活性的抑制百分率被定义为含有所述化合物的孔中所保留的33P的量除以不含所述化合物的孔中所保留的33P的量。在所述的测定条件下进行测试,本发明范围内的超过600个化合物在终浓度为10μM时已证实对PDGF-R激酶活性有抑制作用。
为了测试本发明化合物的抑制效力,用上述方法测量单一化合物的IC50。本文所用的对PDGF-R激酶活性的IC50指与不含抑制剂的反应物比较,使PDGF-R激酶的活性减少一半所需的抑制剂浓度。
采用上述测定法时,PDGF-R激酶活性的抑制作用优选指低于或等于约75μM的IC50。优选所述化合物具有低于或等于约10μM,更优选低于或等于约1μM,最优选低于或等于约0.1μM的IC50的抑制PDGF-R激酶活性。优选较低的IC50值,因为IC50给出了所述化合物的有效性的指征。对于治疗上的应用,还应考虑本领域已知的其它因素,如化合物的半衰期、生物-分布和毒性。这些因素可以使具有较高IC50的化合物比具有较低IC50的化合物在体内具有更大的功效。
对本发明的代表性化合物的PDGF-R激酶活性进行了测定,其%抑制率和/或IC50值的结果如表A中所列。
表A.化合物对PDGF-R激酶活性的IC50值和抑制百分率
| CPD | 命名 | 10μM时的抑制百分率 | IC50(μm) |
| 1 | (2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基胺 | 91 | 0.317 |
| 2 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基胺 | 91 | 0.006 |
| 3 | (4-氯-苯基)-(2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 90 | 0.157 |
| 4 | (3-氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 90 | 0.003 |
| 5 | (4-氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 91 | 0.659 |
| 6 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苯基)-胺 | 75 | 0.131 |
| 7 | (6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 92 | 0.217 |
| 8 | (5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 98 | 0.054 |
| 9 | (2-氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 89 | 0.11 |
| 10 | 4-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯甲酸乙酯 | 68 | 2.07 |
| 11 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯甲酸甲酯 | 97 | 0.0157 |
| 12 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-氟-苯基)-胺 | 76 | 0.056 |
| 13 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-苯基)-胺 | 91 | 0.0065 |
| 14 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 108 | 0.0017 |
| 15 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-2-(三氟甲氧基-苯基)-胺 | 79 | 1.92 |
| 16 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)- | 79 | 4 |
| 4-(三氟甲氧基-苯基)-胺 | |||
| 17 | (2,4-二氯-苯基)-(6,7-二甲氧基-2,4-二氢-7茚并[1,2-c]吡唑-3-基)胺 | 9 | 3.54 |
| 18 | (3,4-二氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 65 | 0.23 |
| 19 | (3,5-二氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 91 | 0.174 |
| 20 | (2,3-二氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 77 | 1.095 |
| 21 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 103 | 0.121 |
| 22 | (7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 96 | 0.045 |
| 23 | (5-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 87 | 1.94 |
| 24 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 71 | 0.084 |
| 25 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲基-苯基)-胺 | 62 | 4.766 |
| 26 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-三氟甲基-苯基)-胺 | 92 | 0.037 |
| 27 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-甲氧基-苯基)-胺 | 71 | 0.655 |
| 28 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-三氟甲基-苯基)-胺 | 96 | 19.14 |
| 29 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 99 | 0.01 |
| 30 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 107 | 0.016 |
| 31 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-邻-甲苯基-胺 | 59 | 0.115 |
| 32 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-间-甲苯基-胺 | 79 | 0.012 |
| 33 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)- | 59 | 1.415 |
| 对-甲苯基-胺 | |||
| 34 | (2,5-二氯-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 57 | 6.987 |
| 35 | 3-苯基氨基-2H-茚并[1,2-c]吡唑-4-酮 | 88 | 2.063 |
| 36 | [3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯基]-甲醇 | 85 | 0.033 |
| 37 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(1H-吲唑-6-基)-胺 | 80 | 1.978 |
| 38 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯酚 | 74 | 0.031 |
| 39 | (7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 92 | 0.018 |
| 40 | N-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-N′,N″-二甲基-苯-1,2-二胺 | 63 | 5.95 |
| 41 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3,5-二甲氧基-苯基)-胺 | 83 | 0.0336 |
| 42 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3,4,5-三甲氧基苯基)-胺 | 85 | 0.692 |
| 43 | (2-溴-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 60 | 0.195 |
| 44 | (3-溴-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 94 | 0.00054 |
| 45 | (4-溴-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 86 | 2.164 |
| 46 | (5-氯-2-甲基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 51 | 14.15 |
| 47 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2,4-二甲氧基-苯基)-胺 | 47 | NT |
| 48 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-2,5-二甲氧基-苯基)-胺 | 39 | NT |
| 49 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3,4-二甲氧基-苯基)-胺 | 72 | 3.066 |
| 50 | 3-苯基氨基-2,4-二氢-茚并[1,2-c]吡唑-4-醇 | 38 | 11.37 |
| 51 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-[4-(4-甲基-哌嗪-1-基)-苯基]-胺 | 30 | 26.75 |
| 52 | (4,5-二氢-2H-6-硫杂-1,2-二氮杂-不对称引达省-3-基)-苯基-胺 | 71 | 2.4 |
| 53 | (3-氯-4-氟-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 94 | 0.05859 |
| 54 | (3-苄氧基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 76 | 0.0348 |
| 55 | (2,5-二氟-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 76 | 0.636 |
| 56 | (5-氯-2-甲氧基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 36 | 8.402 |
| 57 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-异丙基-苯基)-胺 | 71 | 2.151 |
| 58 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-乙基-苯基)-胺 | 40 | 8.524 |
| 59 | 4-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯甲腈 | 71 | 1.818 |
| 61 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯甲腈 | 71 | 0.137 |
| 62 | 苯并[1,3]二氧杂环戊-5-基-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 85 | 0.313 |
| 63 | 苄基-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 94 | 0.1909 |
| 64 | [6-(4-甲基-哌嗪-1-基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]苯基-胺 | 118 | 0.449 |
| 65 | 苯基-(6-哌啶-1-基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 76 | 1.535 |
| 66 | N3-苯基-2,4-二氢-茚并[1,2-c]吡唑-3,6-二胺108 | 108 | 0.092 |
| 67 | 环己基-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 77 | 0.617 |
| 69 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-吗啉-4-基-乙基)-胺 | 18 | |
| 70 | (3,5-双-三氟甲基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 41.5 | 16.85 |
| 71 | [5-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-苯基-胺 | 110 | 0.185 |
| 72 | (3-氯-苯基)-[5-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 96 | 0.283 |
| 73 | [5-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(4-氟-苯基)-胺 | ~30 | >>50 |
| 74 | 5-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-甲氧基-苯基)-胺 | 102 | 0.424 |
| 75 | [5-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-吡啶-3-基-胺 | 115 | 0.575 |
| 76 | (4-溴-2-三氟甲基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 16 | >>50 |
| 77 | 3-[5-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基]-苯甲酸甲酯 | 108 | 0.217 |
| 78 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-呋喃-2-基-胺 | 85 | 1.291 |
| 79 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-茚满-5-基-胺 | 56 | 3.705 |
| 81 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-哌啶-1-基-乙基)-胺 | 29 | 85.95 |
| 82 | (4-氟-苯基)-(6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 79 | 0.273 |
| 83 | (3-溴-苯基)-(6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 93 | 0.0719 |
| 84 | (6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 86 | 0.71 |
| 85 | (2,5-二甲氧基-苯基)-(6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 61 | 5.823 |
| 86 | (3,4-二甲氧基-苯基)-(6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 57 | 2.532 |
| 87 | (2,5-二氟-苯基)-(6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 91 | 0.069 |
| 88 | (6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲氧基-苯基)-胺 | 42 | 20.8 |
| 89 | (6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲基-苯基)-胺 | 88 | 0.886 |
| 90 | [5-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-氟-苯基)-胺 | 97 | 0.0087 |
| 91 | (3-溴-苯基)-(6,7-二甲氧基-1-甲基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 76 | 2.969 |
| 92 | N6,N6-二甲基-N3-苯基-2,4-二氢-茚并[1,2-c]吡唑-3,6-二胺 | 75 | 0.383 |
| 93 | (4,5-二氢-2H-苯并[g]吲唑-3-基)-苯基-胺 | 88 | 1.027 |
| 94 | (5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-苯基-胺 | 95 | 0.415 |
| 95 | (3-溴-苯基)-(2,9-二氢-5,7-二氧杂-2,3-二氮杂-环戊并[a]-对称引达省-1-基(s-indacen-1-yl))-胺 | 91.0 | 0.063 |
| 96 | (2,9-二氢-5,7-二氧杂-2,3-二氮杂-环戊并[a]-对称引达省-1-基)-(3-氟-苯基)-胺 | 93.0 | 0.076 |
| 97 | (2,9-二氢-5,7-二氧杂-2,3-二氮杂-环戊并[a]-对称引达省-1-基)-(3-甲氧基-苯基)-胺 | 91.0 | 0.054 |
| 98 | (4-氟-苯基)-(5-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 26 | 30.69 |
| 99 | (3-氟-苯基)-(5-甲基-2,4-二氢-茚并1,2-c]吡唑-3-基)-胺 | 87.5 | 1468 |
| 100 | (5-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 81 | 1.723 |
| 101 | (2,5-二甲氧基-苯基)-(5-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 52 | 1.092 |
| 102 | (2,4-二甲氧基-苯基)-(5-甲基-2,4-二氢-茚并 | 50 | 3.404 |
| [1,2-c]吡唑-3-基)-胺 | |||
| 103 | (2,5-二氟-苯基)-(5-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 43 | 4.099 |
| 104 | (5-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲氧基-苯基)-胺 | 36 | 0.666 |
| 105 | (5-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲基-苯基)-胺 | 69 | 1.884 |
| 106 | (4-氟-苯基)-(4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 38 | 1.048 |
| 107 | (4-甲氧基-苯基)-(4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 56 | 1.275 |
| 108 | (3-氟-苯基)-(4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 82 | 0.3 |
| 109 | (4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 83 | 0.537 |
| 110 | (2,5-二甲氧基-苯基)-(4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 80 | 0.189 |
| 111 | (2,4-二甲氧基-苯基)-(4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 95 | 0.11 |
| 112 | (2,5-二氟-苯基)-(4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 72 | 0.083 |
| 113 | (4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲氧基-苯基)-胺 | 60 | 2.45 |
| 114 | (4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-三氟甲基-苯基)-胺 | 80 | 1.37 |
| 115 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯甲酸 | 82 | 3.056 |
| 116 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯甲酰胺 | 96 | 0.0053 |
| 117 | N3-(3-溴-苯基)-2,4-二氢-茚并[1,2-c]吡唑-3,6-二胺 | 98 | 0.13 |
| 118 | N3-(3-甲氧基-苯基)-2,4-二氢-茚并[1,2-c]吡唑- | 74 | 0.0213 |
| 3,6-二胺 | |||
| 119 | N3-(3-氯-苯基)-2,4-二氢-茚并[1,2-c]吡唑-3,6-二胺 | 90 | 0.0198 |
| 120 | 3-(6-氨基-2,4-二氢-茚并[1,2-c]吡唑-3-基-氨基-苯甲酸甲酯 | 87 | 0.308 |
| 121 | N3-(3-氟-苯基)-2,4-二氢-茚并[1,2-c]吡唑-3,6-二胺 | 92 | 0.143 |
| 122 | (3-溴-苯基)-[6-(4-甲基-哌嗪-1-基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 70 | 0.0162 |
| 123 | (3-甲氧基-苯基)-[6-(4-甲基-哌嗪-1-基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 87 | 0.228 |
| 124 | (3-氯-苯基)-[6-(4-甲基-哌嗪-1-基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 94 | 0.0163 |
| 125 | 3-(3-溴-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6,7-二醇 | 71 | 3.44 |
| 126 | (2,9-二氢-5,7-二氧杂-2,3-二氮杂-环戊并[a]-对称引达省-1-基)-吡啶-3-基-胺 | 65 | 0.1758 |
| 127 | 3-(2,9-二氢-5,7-二氧杂-2,3-二氮杂-环戊并[a]-对称引达省-1-基氨基)-苯甲酸甲酯 | 89 | 0.421 |
| 128 | (3-氯-苯基)-(2,9-二氢-5,7-二氧杂-2,3-二氮杂-环戊并[a]-对称引达省-1-基)-胺 | 88 | 0.05958 |
| 129 | [7-甲氧基-6-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-吡啶-3-基-胺 | 53.5 | 0.0367 |
| 130 | (3-溴-苯基)-[7-甲氧基-6-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 94.5 | 0.002148 |
| 131 | [7-甲氧基-6-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-甲氧基-苯基)-胺 | 97 | 0.01297 |
| 132 | (3-氯-苯基)-[7-甲氧基-6-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 79 | 0.00537 |
| 133 | 3-[7-甲氧基-6-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基]-苯甲酸甲酯 | 53 | 0.03789 |
| 134 | (3-氟-苯基)-[7-甲氧基-6-(3-吗啉-4-基-丙氧基)- | 96 | 0.01006 |
| 2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | |||
| 135 | (3-氯-苯基)-[6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 87 | 0.202 |
| 136 | (4-氟-苯基)-[6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 64.5 | 1.331 |
| 137 | 3-[6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基]-苯甲酸甲酯 | 71 | 2.11 |
| 138 | (3-氟-苯基)-[6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 79.5 | 0.3011 |
| 139 | (3-甲氧基-苯基)-[6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 80 | 0.09822 |
| 140 | [6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-苯基-胺 | 56.5 | 0.01366 |
| 141 | (3-溴-苯基)-[6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 83.5 | 0.3192 |
| 142 | [6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-吡啶-3-基-胺 | 82.5 | 0.4534 |
| 143 | (4-甲氧基-苯基)-[6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 67 | 8.124 |
| 144 | (4-氟-苯基)-(5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 96.5 | 0.8359 |
| 145 | (5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苯基)-胺 | 48.5 | 13.93 |
| 146 | (5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 78.5 | 0.1603 |
| 147 | (2,5-二甲氧基-苯基)-(5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 32 | 2.984 |
| 148 | (2,4-二甲氧基-苯基)-(5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 57 | 8.601 |
| 149 | (5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-三氟甲氧基-苯基)-胺 | 27.5 | 8.37 |
| 150 | (5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3- | 85 | 0.8226 |
| 三氟甲基-苯基)-胺 | |||
| 151 | (6-溴-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 79 | 0.09184 |
| 152 | (6-溴-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 80 | 0.1739 |
| 153 | (6-溴-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2,5-二氟-苯基)-胺 | 79 | 1.033 |
| 154 | (6-溴-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-三氟甲氧基-苯基)-胺 | 29 | 41.62 |
| 155 | (6-溴-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-三氟甲基-苯基)-胺 | 53 | 8.11 |
| 156 | (3-甲氧基-苯基)-[7-甲氧基-6-(3-吡咯烷-1-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 87.5 | 0.001 |
| 157 | 3-[7-甲氧基-6-(3-吡咯烷-1-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基]-苯甲酸甲酯 | 85 | 0.007 |
| 158 | (6-溴-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 87.5 | 0.1859 |
| 159 | [6-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(4-氟-苯基)-胺 | 92.5 | 0.09887 |
| 160 | [6-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-氟-苯基)-胺 | 94.5 | 0.05855 |
| 161 | [6-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-吡啶-3-基-胺 | 84 | 0.3825 |
| 162 | (2,5-二甲氧基-苯基)-[6-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 21.5 | 54.87 |
| 163 | (2,5-二氟-苯基)-[6-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 32 | 22.65 |
| 165 | [6-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-三氟甲基-苯基)-胺 | 92.5 | 0.1009 |
| 166 | (3-氯-4-氟-苯基)-[7-甲氧基-6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 88 | 0.085 |
| 167 | (3-氯-4-氟-苯基)-(6,7-二异丙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 92 | 0.5111 |
| 168 | (6,7-二异丙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 91 | 0.0688 |
| 169 | (6,7-二异丙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 89 | 0.036 |
| 170 | (4-氟-苯基)-(7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 95.5 | 0.02676 |
| 171 | (7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苯基)-胺 | 92.5 | 0.1232 |
| 172 | (3-氟-苯基)-(7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 55 | 0.0133 |
| 173 | (7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 87 | 0.2146 |
| 174 | (2,5-二甲氧基-苯基)-(7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 83 | 0.3459 |
| 175 | (2,4-二甲氧基-苯基)-(7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 71 | 3.929 |
| 176 | (2,5-二氟-苯基)-(7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 46.5 | 0.3183 |
| 177 | (7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲氧基-苯基)-胺 | 65.5 | 0.5226 |
| 178 | (7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-4-三氟甲基-苯基)-胺 | 98.5 | 0.1324 |
| 179 | (3-氯-4-氟-苯基)-[7-甲氧基-6-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 92 | 0.07124 |
| 180 | (3-氟-苯基)-[7-甲氧基-6-(3-吡咯烷-1-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 98.5 | 0.0133 |
| 181 | (3-氯-4-氟-苯基)-[7-甲氧基-6-(3-吡咯烷-1-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 74.5 | 0.01536 |
| 182 | (3-氟-苯基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 107 | 0.005 |
| 183 | (4-甲氧基-苯基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 53 | 0.5455 |
| 184 | (2,5-二甲氧基-苯基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 94 | 1.1 |
| 185 | (2,5-二氟-苯基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 84 | 0.05 |
| 186 | (7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲氧基-苯基)-胺 | 78 | 0.4141 |
| 187 | (7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-三氟甲基-苯基)-胺 | 35 | |
| 188 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 74 | 0.0437 |
| 189 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苯基)-胺 | 92 | 0.1989 |
| 190 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 80 | 0.04 |
| 191 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 88 | 0.0686 |
| 192 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2,5-二氟-苯基)-胺 | 67 | 0.103 |
| 193 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲基-苯基)-胺 | 49 | |
| 194 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲氧基-苯基)-胺 | 87 | 2.608 |
| 195 | (3,5-双-三氟甲基-苯基)-(6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 76 | 2.28 |
| 196 | N-(6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-N′,N′-二甲基-苯-1,4-二胺 | 70 | 1.293 |
| 197 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-间-甲苯基-胺 | 8 | |
| 198 | (6-氯-2,4-二氢-茚并[1,2-c]吡唑-3-基)-对-甲苯基-胺 | 72 | 0.1384 |
| 199 | [6-(3-二甲基氨基-丙氧基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基-(3-氟-苯基)-胺 | 83 | 0.0059 |
| 200 | (3-氯-4-氟-苯基)-[6-(3-二甲基氨基-丙氧基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 87 | 0.002 |
| 201 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-苯基)-胺 | 96 | 0.009 |
| 202 | (3-氯-4-氟-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 77 | 0.01238 |
| 203 | (2,5-二甲氧基-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 86 | 0.01595 |
| 204 | (3,5-二甲氧基-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 90 | 0.038 |
| 205 | (3,4-二甲氧基-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 86 | 0.047 |
| 206 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3,5-二甲基-苯基)-胺 | 63 | 0.6401 |
| 207 | (3,5-二氟-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 89 | 0.01 |
| 208 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲硫基-苯基)-胺 | 82 | 0.003 |
| 209 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-乙基-苯基)-胺 | 99 | 0.03281 |
| 210 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯甲酸乙酯 | 90 | 0.06723 |
| 211 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-三氟甲硫基-苯基)-胺 | 87 | 0.05 |
| 212 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-3-三氟甲基苯基)-胺 | 84 | 0.775 |
| 213 | (3-氯-苯基)-{7-甲氧基-6-[3-(4-甲基-哌嗪-1-基)-丙氧基]-2,4-二氢-茚并[1,2-c]吡唑-3-基}-胺 | 82 | 0.0027 |
| 214 | (3-氯-4-氟-苯基)-{7-甲氧基-6-[3-(4-甲基-哌嗪-1-基)-丙氧基]-2,4-二氢-茚并[1,2-c]吡唑-3-基}-胺 | 46 | |
| 215 | {7-甲氧基-6-[3-(4-甲基-哌嗪-1-基)-丙氧基]- | 99 | 0.0057 |
| 2,4-二氢-茚并[1,2-c]吡唑-3-基}-(3-甲氧基-苯基)-胺 | |||
| 216 | (3-氟-苯基)-{7-甲氧基-6-[3-(4-甲基-哌嗪-1-基)-丙氧基]-2,4-二氢-茚并[1,2-c]吡唑-3-基}-胺 | 100 | 0.0058 |
| 217 | [6-(3-二甲基氨基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(4-三氟甲氧基-苯基)-胺 | 51 | 3.479 |
| 218 | (4-苄氧基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基}-胺 | 81 | 2.01 |
| 219 | (3,4-二氯-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 39 | |
| 220 | 环己基甲基-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 73 | 3.29 |
| 221 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-[4-(哌啶-4-磺酰基)-苯基]-胺 | 71 | 1.598 |
| 222 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲基-苄基)-胺 | 70 | 0.806 |
| 223 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-甲基-苄基)-胺 | 97 | 0.04593 |
| 224 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-甲氧基-苄基)-胺 | 24 | |
| 225 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苄基)-胺 | 90 | 0.07443 |
| 226 | (3-氟-苯基)-[6-(3-咪唑-1-基-丙氧基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 102 | 0.003 |
| 227 | (3-氯-4-氟-苯基)-[6-(3-咪唑-1-基-丙氧基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 83.5 | 0.03487 |
| 230 | (2-氯-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 90 | 0.0019 |
| 231 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苄基)-胺 | 37 | |
| 232 | (5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-(3-甲氧基-苯基)-胺 | 102 | 0.0396 |
| 233 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-苯基)-胺 | 50 | 0.02759 |
| 234 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 101 | 0.3581 |
| 235 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 86 | 0.2114 |
| 236 | (2,5-二氟-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 82 | 0.005 |
| 237 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲基-苯基)-胺 | 88 | 0.05 |
| 238 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲氧基-苯基)-胺 | 87 | 0.4187 |
| 239 | (3,5-双-三氟甲基-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 91 | 0.138 |
| 240 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-间-甲苯基-胺 | 92 | 0.002 |
| 242 | (3-氟-苯基)-[7-甲氧基-6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 104 | 0.013 |
| 244 | [7-甲氧基-6-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-甲氧基-苯基)-胺 | 101 | 0.0002 |
| 245 | (6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 87 | 0.001 |
| 246 | (3-氯-4-氟-苯基)-(6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 77 | 0.0121 |
| 247 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 96 | 0.07 |
| 248 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-苯基)-胺 | 68 | 0.4099 |
| 249 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 96 | 0.006 |
| 250 | (3-氯-4-氟-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 88 | 0.2234 |
| 251 | (3,5-二氟-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 84 | 0.3222 |
| 252 | (2,5-二氟-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 16 | |
| 253 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 94 | 0.0165 |
| 254 | (3-苄氧基-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 89 | 0.1808 |
| 255 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲硫基-苯基)-胺 | 90 | 0.1615 |
| 256 | (3-溴-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 89 | 0.008 |
| 257 | (3-氯-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 35 | |
| 258 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2,5-二甲氧基-苯基)-胺 | 39 | |
| 259 | 3-[3-(3-氯-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 93 | 0.002045 |
| 260 | 3-[7-甲氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 91 | 0.0015 |
| 261 | 3-[3-(3-氯-4-氟-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 71 | 0.01 |
| 262 | 3-[3-(3-氟-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 90 | 0.001 |
| 263 | 3-[7-甲氧基-3-(吡啶-3-基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 103 | 0.046 |
| 264 | 苄基-(6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 86 | 0.08519 |
| 265 | 3-[3-(3-氟-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 63 | 0.005535 |
| 266 | 3-[7-甲氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 110 | 0.001534 |
| 267 | 3-[3-(3-氯-4-氟-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 93.5 | 0.01059 |
| 268 | 3-[3-(3-氯-苯基氨基)-7-甲氧基-2,4-二氢-[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 84 | 0.001134 |
| 269 | 1-[3-(3-氟-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 94 | 0.0005914 |
| 270 | 1-[7-甲氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 107 | 0.0004287 |
| 271 | (3,5-二氯-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 54.5 | 6.987 |
| 272 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲基-苄基)-胺 | 61 | 0.3888 |
| 273 | (3-氯-4-甲基-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 77 | 1.584 |
| 274 | 2,5-二甲氧基-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 57.5 | 2.61 |
| 275 | (3,4-二氟-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 80.5 | 0.5006 |
| 276 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-3-硝基-苯基)-胺 | 11 | 0.2874 |
| 277 | (3-氯-4-甲氧基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 88 | 1.361 |
| 278 | 1-[3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯基]-乙醇 | 97 | 0.02949 |
| 279 | (3,5-二-叔丁基-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 19.5 | 203.1 |
| 280 | 1-[3-(3-氯-4-氟-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 102 | 0.00172 |
| 281 | 1-[7-甲氧基-3-(吡啶-3-基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 67 | 0.002599 |
| 282 | 1-[3-(3-氯-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 99 | 0.000089 |
| 283 | [6,7-双-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-氟-苯基)-胺 | 86.5 | 0.004356 |
| 284 | [6,7-双-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-甲氧基-苯基)-胺 | 84.6 | 0.00509 |
| 285 | [6,7-双-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-氯-苯基)-胺 | 18.5 | 0.002779 |
| 286 | [6,7-双-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-吡啶-3-基-胺 | 95.5 | 001624 |
| 287 | [6,7-双-(3-甲氧基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-(3-氯-4-氟-苯基)-胺 | 92.5 | 0.02616 |
| 288 | (3-氯-4-甲氧基-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 88.5 | 0.2194 |
| 289 | 1-[3-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基-氨基)-苯基]-乙醇 | 93.5 | 0.01853 |
| 290 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-1H-吲哚-5-基)-胺 | 87.5 | 0.06142 |
| 291 | (6-苄氧基-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 95 | 0.2052 |
| 292 | (2-氯-苄基)-(6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 86.5 | 0.01822 |
| 293 | (6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-氟-苄基)-胺 | 96.5 | 0.06916 |
| 294 | (6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苄基)-胺 | 81 | 0.2637 |
| 295 | (2,6-二氯-苄基)-(6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 81.5 | 0.001645 |
| 296 | (6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-甲氧基-苄基)-胺 | 72.5 | 1.821 |
| 297 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-N-(2-羟基-乙基)-苯甲酰胺 | 90.5 | 0.2749 |
| 298 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基-N-(3-吡咯烷-1-基-丙基)-苯甲酰胺 | 92 | 0.4082 |
| 299 | (7-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 80 | 0.01928 |
| 300 | (6,7-二甲氧基-4-苯基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 40 | |
| 301 | (6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-三氟甲氧基-苄基)-胺 | 72 | |
| 302 | (6,7-二甲氧基-4-苯基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 47 | |
| 303 | (3,5-二-叔丁基-苯基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 50 | 9.338 |
| 304 | (3,5-二氯-苄基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 38 | 3.456 |
| 305 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲基-苄基)-胺 | 87 | 0.4577 |
| 306 | (3-氯-4-甲基-苄基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 47.5 | 8.589 |
| 307 | (2,5-二甲氧基-苄基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 59 | 3.401 |
| 308 | (3,4-二氟-苄基)-(6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 14 | 0.5108 |
| 309 | (3-氯-4-甲氧基-苯基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 92.5 | 0.03022 |
| 310 | 1-[3-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯基]-乙醇 | 95.5 | 0.0202 |
| 311 | (1H-吲哚-5-基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 68.5 | 0.07478 |
| 312 | (3,5-二-叔丁基-苯基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 56.5 | 5.672 |
| 313 | (3,5-二氯-苄基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 62.5 | 3.503 |
| 314 | (3-甲基-苄基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡 | 76 | 0.8944 |
| 唑-3-基)-胺 | |||
| 315 | (3-氯-4-甲基-苄基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 17.5 | 1.924 |
| 316 | (2,5-二甲氧基-苄基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 66 | 4.906 |
| 317 | (3,4-二氟-苄基)-(7-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 79 | 1.247 |
| 318 | (4,5-二氢-2H-6-氧杂-1,2-二氮杂-苯并[e]甘菊环-3-基)-苯基-胺 | 23 | 34.38 |
| 319 | [3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯基]-(4-甲基-哌嗪-1-基)-甲酮 | 80.5 | 2.201 |
| 320 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3,4-二甲基-苄基)-胺 | 70.5 | 1.958 |
| 321 | (2,6-二氟-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 77 | 0.007454 |
| 322 | (2,3-二甲氧基-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 22 | 0.05466 |
| 323 | (2,5-二氟-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 60.5 | 8.711 |
| 324 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-[1-(3-甲氧基-苯基)-乙基]-胺 | 74.5 | 1.325 |
| 325 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-氟-苄基)-胺 | 61 | 0.09669 |
| 326 | (2,3-二氯-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 82 | 0.2671 |
| 327 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苄基)-胺 | 52 | 10.62 |
| 328 | (2,4-二氟-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 78.5 | 0.6971 |
| 329 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-三氟甲基-苄基)-胺 | 58 | 0.0762 |
| 330 | (2,5-二氯-苄基)-(6,7-二甲氧基-2,4-二氢茚并 | 100 | 0.0162 |
| [1,2-c]吡唑-3-基)-胺 | |||
| 331 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-苄基)-胺 | 93 | 0.1886 |
| 332 | (5,8-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-苯基-胺 | 90 | 0.3716 |
| 333 | (3-氯-苄基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 73.5 | 2.55 |
| 334 | (7-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 99.5 | 0.008693 |
| 335 | (5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-(3-氟-苯基)-胺 | 100 | 0.1292 |
| 337 | (2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 100 | 0.008804 |
| 338 | (5-氯-2-甲基-苯基)-(2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 78.5 | 0.4512 |
| 339 | (2,5-二氟-苯基)-(2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 100 | 0.1174 |
| 340 | (2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-氟-5-三氟甲基-苯基)-胺 | 92.5 | 0.1046 |
| 341 | (2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2,5-二甲氧基-苯基)-胺 | 92.5 | 0.04118 |
| 342 | (5-氯-2-甲氧基-苯基)-(2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 56.5 | 0.02668 |
| 343 | (2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 99.5 | 0.008075 |
| 344 | (6,7-二乙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 100 | 0.06465 |
| 345 | (6,7-二乙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 88 | 0.0893 |
| 346 | (3-溴-苯基)-(6,7-二乙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 98 | 0.07392 |
| 347 | (3-氯-4-氟-苯基)-(6,7-二乙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 90.5 | 0.5453 |
| 348 | (6,7-二乙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 97.5 | 0.02529 |
| 349 | (6,7-二乙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-苯基)-胺 | 78 | 0.08089 |
| 350 | 3-苯基氨基-4,5-二氢-2H-苯并[g]吲唑-7-甲腈 | 91 | 0.6512 |
| 351 | (6,7-二异丙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 93 | 0.3998 |
| 352 | (6,7-二异丙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基-胺 | 86.5 | 0.7554 |
| 353 | (3-溴-苯基)-(6,7-二异丙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 88 | 0.3594 |
| 354 | (3-氯-4-氟-苯基)-(6,7-二异丙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 62 | 2.45 |
| 355 | (6,7-二异丙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 85 | 1.026 |
| 356 | (6,7-二异丙氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-苯基)-胺 | 70 | 1.953 |
| 357 | (6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 98.5 | 0.009417 |
| 358 | (3-溴-苯基)-(6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 92 | 0.00877 |
| 359 | (3-氯-4-氟-苯基)-(6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 98.5 | 0.04151 |
| 360 | (6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 98 | 0.007501 |
| 361 | (6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-氟-苯基)-胺 | 100 | 0.01156 |
| 362 | 3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6,7-二醇 | 80.5 | 0.7844 |
| 363 | 3-(3-氟-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-醇 | 76.5 | 0.005466 |
| 364 | (6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3- | 100 | 0.01506 |
| 基)-吡啶-3-基-胺 | |||
| 365 | 3-[6-乙氧基-3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-丙-1-醇 | 99.5 | 0.01131 |
| 366 | 3-[6-乙氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-丙-1-醇 | 100 | 0.01209 |
| 367 | 3-[3-(3-氯-苯基氨基)-6-乙氧基-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-丙-1-醇 | 97 | 0.00814 |
| 368 | 3-[3-(3-氯-4-氟-苯基氨基)-6-乙氧基-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-丙-1-醇 | 89.5 | 0.06293 |
| 369 | (6-溴-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 100 | 0.0187 |
| 370 | (6-溴-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 94 | 0.01218 |
| 371 | 3-[6-乙氧基-3-(吡啶-3-基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-丙-1-醇 | 100 | 0.0476 |
| 372 | 3-[7-(3-羟基-丙氧基)-3-(吡啶-3-基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 100 | 0.01553 |
| 373 | 3-[3-(3-氯-苯基氨基)-7-(3-羟基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 100 | 0.003772 |
| 374 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-乙氧基-苯基)-胺 | 100 | 0.01412 |
| 375 | (6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-乙氧基-苯基)-胺 | 96.5 | 0.1028 |
| 376 | 3-[3-(3-乙氧基-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 100 | 0.009096 |
| 377 | (2-氯-吡啶-3-基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 99 | 0.008572 |
| 378 | (6-氟-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-甲基-苄基)-胺 | 94.5 | 0.467 |
| 379 | 3-[3-(3-乙氧基-苯基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 100 | 0.008119 |
| 380 | (3-氟-苯基)-(2H-8-氧杂-2,3-二氮杂-环戊并[a] | 99.5 | 0.01533 |
| 茚-1-基)-胺 | |||
| 381 | (3-氯-4-氟-苯基)-(2H-8-氧杂-2,3-二氮杂-环戊并[a]茚-1-基)-胺 | 100 | 0.05492 |
| 382 | 3-[7-乙氧基-3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 100 | 0.01185 |
| 383 | 3-[7-乙氧基-3-(吡啶-3-基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 93 | 0.02533 |
| 384 | 3-[7-乙氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 100 | 0.005607 |
| 385 | 3-[3-(2-氯-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 98.5 | 0.004072 |
| 386 | 3-[3-(2-氟-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 95.5 | 0.01101 |
| 387 | 3-[3-(2-氟-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 100 | 0.01162 |
| 388 | 3-[6-乙氧基-3-(3-乙氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-丙-1-醇 | 96 | 0.03667 |
| 389 | 3-[3-(3-氯-4-氟-苯基氨基)-7-(3-羟基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基)-丙-1-醇 | 98 | 0.01511 |
| 390 | 1-[3-(2,6-二氯-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 99 | 0.002029 |
| 391 | 1-[3-(2,6-二氟-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 99 | 0.006796 |
| 392 | (3-氯-苯基)-[5-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 80 | 0.1528 |
| 393 | (3-氟-苯基)-[5-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 94.5 | 0.1737 |
| 394 | (3-乙氧基-苯基)-[5-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 91 | 0.3289 |
| 395 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸(3-氟-苯基)-酰胺 | 88 | 0.6861 |
| 396 | 1-[3-(2-氯-苄基氨基)-7-甲氧基-2,4-二氢-茚并 | 99.5 | 0.005129 |
| [1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | |||
| 397 | 1-[3-(2-氟-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 92 | 0.007701 |
| 398 | 3-[3-(3-氟-苯基氨基)-7-(3-羟基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 96 | 0.00682 |
| 400 | 3-[7-(3-羟基-丙氧基)-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 98.5 | 0.002918 |
| 401 | 3-[3-(3-乙氧基-苯基氨基)-7-(3-羟基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 98.5 | 0.02203 |
| 402 | (5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-吡啶-3-基-胺 | 90 | 0.1957 |
| 403 | (3-氯-苯基)-(5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-胺 | 96 | 0.08588 |
| 404 | (3-氯-4-氟-苯基)-(5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-胺 | 74.5 | 1.115 |
| 405 | (5,7-二氢-1-硫杂-4,5-二氮杂-环戊并[a]并环戊二烯-6-基)-(3-乙氧基-苯基)-胺 | 94.5 | 0.06354 |
| 406 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-乙酮 | 96 | 0.07502 |
| 407 | {[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-羰基]-氨基}-乙酸乙酯 | 39 | 9.883 |
| 408 | 2,2-二甲基-丙酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基甲酯 | 83 | 0.6866 |
| 409 | 2,2-二甲基-丙酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基甲酯 | 85.5 | 0.1076 |
| 410 | (2-溴-3-氟-苯基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 83.5 | 1.076 |
| 411 | 3-[(6,7-二甲氧基-3-苯基氨基-4H-茚并[1,2-c]吡唑-2-羰基)-氨基]-丙酸乙酯 | 14.5 | 0.08233 |
| 412 | 2-{[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-羰基]-氨基}-4-甲基-丙酸甲酯 | 44 | 12.72 |
| 413 | 2-{[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并 | 71 | 1.14 |
| [1,2-c]吡唑-2-羰基]-氨基}-3-甲基-丁酸甲酯 | |||
| 414 | (2,6-二氟-苄基)-[5-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 80.5 | 0.5639 |
| 415 | (2,6-二氯-苄基)-[5-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 98 | 0.02581 |
| 416 | (2-氟-苄基)-[5-(3-吗啉-4-基-丙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 72.5 | 1.185 |
| 417 | (5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-5-三氟甲基-苯基)-胺 | 27.5 | 12.2 |
| 418 | 3-(5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-苯磺酰胺 | 82.5 | 0.8916 |
| 419 | (3-氯-苯基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 100 | 0.06214 |
| 420 | (3-溴-苯基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 100 | 0.05236 |
| 421 | (4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 100 | 0.08219 |
| 422 | (3-氟-苯基)-(5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 83 | 0.02966 |
| 423 | (2,6-二氟-苄基)-(5-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 90 | 0.1815 |
| 424 | (3-氯-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 100 | 0.07912 |
| 425 | (6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2-甲基-苄基)-胺 | 96 | 0.002296 |
| 426 | (2-氟-苄基)-(6-氟-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 97 | 0.2415 |
| 427 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-苯基-甲酮 | 80 | 1.15 |
| 428 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-4-氧代-丁酸甲酯 | 85.5 | 0.432 |
| 429 | 4-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并 | 72 | 0.6706 |
| [1,2-c]吡唑-1-基]-4-氧代-丁酸乙酯 | |||
| 430 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-丙-1-酮 | 61.5 | 0.571 |
| 431 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-甲基-丙-1-酮 | 84.5 | 0.4437 |
| 432 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-羟基-乙酮 | 95.5 | 0.03804 |
| 433 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸苯基酯 | 71 | 0.5849 |
| 434 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸甲酯 | 86 | 0.503 |
| 435 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸乙酯 | 67 | 1.588 |
| 436 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸异丙基酯 | 9.5 | 0.9619 |
| 437 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸2-甲氧基-乙酯 | 83.5 | 0.2914 |
| 438 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸2-甲氧基-乙酯 | 77.5 | 0.9923 |
| 439 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸甲酯 | 69.5 | 0.6202 |
| 440 | 3-[3-(3-氯-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙-1-醇 | 895 | 0.04574 |
| 441 | 3-[3-(3-乙氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙-1-醇 | 96 | 0.2058 |
| 442 | 3-[3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙-1-醇 | 94.5 | 0.2048 |
| 443 | 3-(3-(2,6-二氟-苄基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙-1-醇 | 89.5 | 0.09795 |
| 444 | 3-[3-(2-氟-苄基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙-1-醇 | 79.5 | 0.5185 |
| 445 | 3-[3-(2-甲基-苄基氨基)-2,4-二氢-茚并[1,2-c]吡 | 95 | 0.02526 |
| 唑-5-基氧基]-丙-1-醇 | |||
| 446 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-膦酸二乙酯 | 93.5 | 0.2656 |
| 447 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-磺酸二甲基酰胺 | 7 | |
| 448 | 3-[3-(2,6-二氯-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 100 | 0.001767 |
| 449 | 3-[3-(2,6-二氟-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙-1-醇 | 98.5 | 0.004098 |
| 450 | 3-[3-(2,6-二氯-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 100 | 0.0009382 |
| 451 | 3-[3-(2-氯-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 99.5 | 0.002004 |
| 452 | N1-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-4-甲基-N3-(4-吡啶-3-基-嘧啶-2-基)-苯-1,3-二胺 | 72 | 1.096 |
| 453 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-甲氧基-吡啶-3-基)-胺 | 88 | 0.8294 |
| 454 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(2,4-二甲氧基-吡啶-3-基)-胺 | 99 | 0.2579 |
| 455 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(5-苯基-异恶唑-3-基甲基)-胺 | 95 | 0.1532 |
| 457 | 3-[3-(2,6-二氟-苄基氨基)-7-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-6-基氧基]-丙烷-1,2-二醇 | 100 | 0.003414 |
| 458 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-(4-甲氧基-苯基)-甲酮 | 70.5 | 6.998 |
| 459 | 3-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-3-氧代-丙酸乙酯 | 100 | 0.03654 |
| 460 | 1-[6-乙氧基-3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 97.5 | 0.00427 |
| 461 | 1-[6-乙氧基-3-(吡啶-3-基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 97.5 | 0.007552 |
| 462 | 1-[6-乙氧基-3-(3-甲氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 99 | 0.00215 |
| 463 | 1-[6-乙氧基-3-(3-乙氧基-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-7-基氧基]-3-吡咯烷-1-基-丙-2-醇 | 98.5 | 0.01095 |
| 464 | 5-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-5-氧代-戊酸甲酯 | 92 | 0.2446 |
| 465 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-甲氧基-乙酮 | 96 | 0.006728 |
| 466 | 4-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-4-氧代-丁酸 | 96 | 0.03113 |
| 467 | 乙酸2-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-氧代-乙酯 | 96.5 | 0.01763 |
| 468 | 3-[3-(3-溴-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙烷-1,2-二醇 | 95.5 | 0.04784 |
| 469 | 3-[3-(3-氟-苯基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙烷-1,2-二醇 | 96 | 0.1598 |
| 470 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸2-苄氧基-乙酯 | 96 | 0.197 |
| 471 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸2-[2-(2-羟基-乙氧基)-乙氧基]-乙酯 | 90.5 | 0.1347 |
| 472 | (6,7-二甲氧基-1-甲氧基甲基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 35 | |
| 473 | 甲氧基-乙酸2-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-氧代-乙酯 | 98.5 | 0.008962 |
| 474 | 异丁酸2-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-氧代-乙酯 | 91.5 | 0.06342 |
| 475 | (6,7-二甲氧基-2-甲氧基甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 65.5 | 5.035 |
| 476 | (2,6-二氟-苯基)-(6,7-二甲氧基-2,4-二氢-茚并 | 88.5 | 0.2495 |
| [1,2-c]吡唑-3-基)-胺 | |||
| 477 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-2,4,6-三氟-苯基)-胺 | 95 | 0.2293 |
| 478 | (3-溴-苯基)-[5-(2-吡咯烷-1-基-乙氧基)-2,4-二氢-茚并[1,2-c]吡唑-3-基]-胺 | 93.5 | 0.1617 |
| 479 | 3-[3-(2,6-二氯-苄基氨基)-2,4-二氢-茚并[1,2-c]吡唑-5-基氧基]-丙烷-1,2-二醇 | 94.5 | 0.6238 |
| 480 | (2,6-二氟-苯基)-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-甲酮 | 8 | |
| 481 | (2-氟-苯基)-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-甲酮 | 59 | 3.764 |
| 482 | (3-溴-苯基)-(4-乙基-6,7-二甲氧基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 100 | 0.03863 |
| 483 | (3-溴-苯基)-(4-乙基-6,7-二甲氧基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 78.5 | 4.97 |
| 484 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-丙-2-酮 | 87 | 0.218 |
| 485 | (3-溴-苯基)-(6,7-二甲氧基-4,4-二甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 32 | 59.03 |
| 486 | (3-氯-苯基)-(6,7-二甲氧基-4,4-二甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 34.5 | 15.76 |
| 487 | (6,7-二甲氧基-4,4-二甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 43 | 37.47 |
| 488 | (6,7-二甲氧基-4,4-二甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 33.5 | 39.29 |
| 489 | (6,7-二甲氧基-4,4-二甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-乙氧基-苯基)-胺 | 25.5 | |
| 490 | 丁酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c1吡唑-1-基甲酯 | 96 | 0.0285 |
| 491 | 丁酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基甲酯 | 92 | 0.3142 |
| 492 | (4-氟-苯基)-[3-(3-氟-苯基氨基)-6,7-二甲氧基- | 78 | 0.4716 |
| 4H-茚并[1,2-c]吡唑-1-基]-甲酮 | |||
| 494 | (4-氯-苯基)-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-甲酮 | 83 | 1.541 |
| 496 | 乙酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基甲酯 | 88.5 | 0.0136 |
| 497 | 乙酸3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基甲酯 | 97 | 0.07774 |
| 498 | 乙酸4-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基甲基]-苯基酯 | 51.5 | 8.326 |
| 499 | 乙酸4-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基甲基]苯基酯 | 87 | 1.743 |
| 500 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸4-氟-苯基酯 | 80.5 | 0.4923 |
| 501 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸4-氯-苯基酯 | 90 | 0.09598 |
| 502 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-丙-2-醇 | 60.5 | 54.02 |
| 503 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸4-氟-苯基酯 | 103 | 0.04509 |
| 504 | (6,7-二乙氧基-4-甲基-2,4-二氢-茚并[12-c]吡唑-3-基)-(3-乙氧基-苯基)-胺 | 101 | 0.1419 |
| 505 | (3-乙氧基-苯基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 97 | 0.134 |
| 506 | 5-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-5-氧代-戊酸甲基酰胺 | 97 | 0.0294 |
| 509 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-乙酸甲酯 | 30.5 | |
| 510 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-乙酸乙酯 | 57 | 26.62 |
| 511 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-乙酸乙酯 | 51 | 12.52 |
| 512 | (4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑 | 92 | 0.1834 |
| -3-基-(3-甲氧基-苯基)-胺 | |||
| 513 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸2-氯-苯基酯 | 86 | 0.7726 |
| 514 | 1-[3-(3-溴-苯基氨基)-4-乙基-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-2-甲氧基-乙酮 | 85 | 0.24 |
| 515 | 1-[3-(3-溴-苯基氨基)-4-乙基-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-2-甲氧基-乙酮 | 90 | 0.1357 |
| 516 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-氨基-乙基)-酰胺 | 68.5 | 10.04 |
| 517 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-二甲基氨基-乙基)-酰胺 | 75.5 | 1.793 |
| 518 | 2-苄氧基-1-[3-(3-溴-苯基氨基)-4-乙基-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-乙酮 | 92.5 | 0.1838 |
| 519 | 2-苄氧基-1-[3-(3-溴-苯基氨基)-4-乙基-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-乙酮 | 97.5 | 0.139 |
| 520 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-吡咯烷-1-基-乙基)-酰胺 | 100 | 0.06525 |
| 521 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-吗啉-4-基-乙基)-酰胺 | 97 | 0.05587 |
| 522 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸(2-吗啉-4-基-乙基)-酰胺 | 94 | 0.7909 |
| 523 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸[2-(2-羟基-乙基氨基)-乙基]-酰胺 | 98.5 | 0.1927 |
| 524 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-甲基氨基-乙基)-酰胺 | 78 | 2.482 |
| 525 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-异丁酰基氨基-乙基)-酰胺 | 33 | 43.16 |
| 526 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-乙酰基氨基-乙基)-酰胺 | 73 | 8.091 |
| 527 | 2-甲基-丙烯酸2-([3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-羰基]-氨基}-乙酯 | 46.5 | 17.47 |
| 528 | 2-甲基-丙烯酸2-{[3-(3-氟-苯基氨基)-6,7-二甲 | 93.5 | 0.196 |
| 氧基-4H-茚并[1,2-c]吡唑-2-羰基-氨基}-乙酯 | |||
| 529 | 6-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-3,4,5-三羟基-四氢-吡喃-2-甲酸 | 44 | 10.64 |
| 530 | 2-{[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-羰基]-氨基}-3-甲基-丁酸甲酯 | 71.5 | 4.151 |
| 531 | 4-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-4-氧代-丁酰胺 | 90 | 0.02404 |
| 532 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸(2-苯甲酰基氨基-乙基)-酰胺 | 42 | |
| 534 | 2-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-乙酰胺 | 94 | 0.9332 |
| 535 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-3-吡咯烷-1-基-丙烷-1,3-二酮 | 105 | 0.03224 |
| 536 | 1-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-3-吡咯烷-1-基-丙烷-1,3-二酮 | 88 | 0.4362 |
| 537 | N,N-二乙基-3-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-3-氧代-丙酰胺 | 104 | 0.3303 |
| 538 | (3-溴-苯基)-(4-异丙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 65 | |
| 540 | (3-氯-苯基)-(4-异丙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 47 | 14.68 |
| 541 | (4-异丙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲氧基-苯基)-胺 | 50 | 44.22 |
| 542 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸[2-(2-羟基-苯甲酰基氨基)-乙基]-酰胺 | 21 | |
| 544 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸{2-[2-(2-羟基-乙氧基-乙氧基)-乙基]-酰胺 | 60 | |
| 546 | [3-(3-溴-苯基氨基)-4-乙基-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-苯基)-甲酮 | 72.5 |
| 547 | 3-(3-溴-苯基氨基)-4-乙基-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸2-[2-(2-羟基-乙氧基)-乙氧基-乙酯 | 68.5 | |
| 548 | 3-(3-溴-苯基氨基)-6,7-二甲氧基-4-甲基-4H-茚并[1,2-c]吡唑-1-甲酸2-[2-(2-羟基-乙氧基)-乙氧基]-乙酯 | 82.5 | 0.2144 |
| 549 | (7-苄氧基-6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 106 | 0.09114 |
| 553 | (3-溴-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 99.5 | 0.006501 |
| 554 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-乙氧基-苯基)-胺 | 102 | 0.0208 |
| 555 | (3-溴-苯基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 97.5 | 0.02094 |
| 556 | (3-乙氧基-苯基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 98 | 0.0104 |
| 557 | N-[3-(3-氟-苯基氨基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-5-基]-乙酰胺 | 101.5 | 0.03248 |
| 558 | N3-(3-氟-苯基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3,5-二胺 | 102 | 0.01214 |
| 559 | (2-氯-吡啶-3-基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 102 | 0.03706 |
| 560 | (4-甲氧基-2-甲基-6,9-二氢-3-氧杂-1,6,7-三氮杂-环戊并[b]-不对称引达省-8-基)-(3-甲氧基-苯基)-胺 | 102 | 0.02471 |
| 562 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-2-基-胺 | 93.5 | 0.08399 |
| 563 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-2-基甲基-胺 | 89 | 1.449 |
| 564 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-吡啶-3-基甲基-胺 | 99.5 | 0.8864 |
| 565 | (2,2-二氟-苯并[1,3]二氧杂环戊-4-基)-(6,7-二甲 | 41.5 |
| 氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | |||
| 566 | 3-(2,3-二氢-吲哚-1-基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑 | 54 | |
| 567 | 3-(5-溴-2,3-二氢-吲哚-1-基)-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑 | 39.5 | |
| 568 | (3-溴-苯基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 78 | 0.7904 |
| 569 | (6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-乙氧基-苯基)-胺 | 64 | 5.098 |
| 570 | (3-溴-苯基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 77.5 | 2.048 |
| 571 | (3-乙氧基-苯基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 66 | 3.886 |
| 572 | 2-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-乙醇 | 67 | 7.332 |
| 573 | 2-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-乙醇 | 52 | |
| 574 | (2-氟-苄基)-(4-甲氧基-2-甲基-6,9-二氢-3-氧杂-1,6,7-三氮杂-环戊并[b]-不对称引达省-8-基)-胺 | 99 | 0.163 |
| 575 | (2-溴-苄基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 99.5 | 0.002129 |
| 576 | (5-溴-3-甲基-吡啶-2-基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基-胺 | 18 | 33.33 |
| 577 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4-三氟甲基-吡啶-3-基)-胺 | 19 | 361.5 |
| 578 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-甲酸甲基酰胺 | 80 | 4.023 |
| 579 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸甲基酰胺 | 28 | |
| 580 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-硫代甲酸甲基酰胺 | 93 | 0.1255 |
| 581 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2- | 90.5 | 1.139 |
| c]吡唑-1-硫代甲酸甲基酰胺 | |||
| 582 | (3-溴-吡啶-2-基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 82.5 | 1.247 |
| 583 | (5-溴-吡啶-2-基)-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 82 | 1.101 |
| 584 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-异丙氧基-苯基)-胺 | 109 | 0.01113 |
| 585 | (2,6-二氯-苄基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 101.5 | 0.4287 |
| 586 | (2,6-二氯-苄基)-(6,7-二甲氧基-4-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 100.5 | 0.02776 |
| 587 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-甲基-吡啶-2-基)-胺 | 86 | 1.704 |
| 588 | (6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(4,6-二甲基-吡啶-2-基)-胺 | 103 | 0.5564 |
| 591 | 6-[(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-氨基]-3,4,5-三羟基-四氢-吡喃-2-甲酸 | 96 | 0.6623 |
| 594 | (6,7-二乙氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 64 | 0.0156 |
| 595 | (7-甲氧基-2H-8-氧杂-2,3-二氮杂-环戊并[a]茚-1-基)-苯基-胺 | 71 | 0.02488 |
| 598 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸十五烷基酰胺 | 0 | 98.43 |
| 601 | 3-(6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基氨基)-N-{2-[2-(2-{2-[5-(2-氧代-六氢-噻吩并[3,4-d]咪唑-6-基)-戊酰基氨基]-乙氧基}-乙氧基)-乙氧基]-乙基}-苯甲酰胺 | 89 | 2.29 |
| 602 | [3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-基]-乙酸甲酯 | 40 | |
| 604 | 3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-2-甲酸{2-[2-(2-羟基-乙氧基)-乙氧基]- | 79.5 | 2.127 |
| 乙基}-酰胺 | |||
| 605 | (3-氟-苯基)-(4-甲氧基-2-甲基-8a,9-二氢-3-氧杂-1,6,7-三氮杂-环戊并[b]-不对称引达省-8-基)-胺 | 97.5 | 0.0051 |
| 606 | 8-苄基-3-(3-氟-苯基氨基)-6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-7-醇 | 53.5 | |
| 607 | (2-氯-吡啶-3-基)-(4-乙基-6,7-二甲氧基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-胺 | 78 | 0.5475 |
| 608 | 3-(3-氟-苯基氨基)-6-甲氧基-2,4-二氢-茚并[1,2-c]吡唑-7-醇 | 106 | 0.02596 |
| 609 | (6,7-二甲氧基-1-甲基-1,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 84 | 4.683 |
| 610 | (6,7-二甲氧基-2-甲基-2,4-二氢-茚并[1,2-c]吡唑-3-基)-(3-氟-苯基)-胺 | 51.5 | 9.377 |
| 611 | 6-[3-(3-氟-苯基氨基)-6,7-二甲氧基-4H-茚并[1,2-c]吡唑-1-基]-3,4,5-三羟基-四氢-吡喃-2-甲酸 |
2.c-Abl激酶活性的抑制
先前的研究已经表明选择性的PDGF-R激酶抑制剂ST1-571(同上)也是c-Abl激酶活性的选择性抑制剂,因此是对Bcr-Abl致癌基因产物的选择性抑制剂(对Bcr-Abl的治疗性介入的综述,见Kindler等,2002,Expert Opin Ther Targets;6(1):85-101)。各种不同的Bcr-Abl与不同类型的人白血病有关:如慢性骨髓性白血病(CML);急性淋巴细胞白血病(ALL);慢性嗜中性白血病(CNL);急性未分化白血病(AUL);及急性骨髓性白血病(AML)(Anjali等,2002,LeukemiaResearch,26(8):713-720)。本发明范围内的化合物对c-Abl激酶活性的抑制活性根据以下步骤测定。
材料
1.10X激酶缓冲液[500mM Tris-HCl pH=8,100mM MgCl2,1mMNa3VO4]
2.10mM DTT[终浓度1mM]
3.10mM ATP[终浓度5μM](Gibco,Cat No:18330-019,Carlsbad,CA)
4.33P-γ-ATP[NEG-602H;2000-3000Ci/mmol],每孔2μCuries,10μCi/μl(0.2μl/孔)
5.Abl酶(New England Biolabs,Cat No.P6050L,Beverly,MA),100单位/μl,使用10单位/孔(0.1μl/孔)
6.酶稀释缓冲液[50mM Tris-HCl pH=8.0,0.1%BSA]
7.洗涤/终止缓冲液[PBS+100mM EDTA]
8.NEN链霉抗生物素Flashplates(New England Nuclear,Cat No.SMP-103,Boston,MA)。
9.Abl肽底物(Biotin-EAIYAAPFAKKK-酰胺),1mM在50mM Tris-HCl中,pH=8.0。(使用1.0μM)。
步骤
先根据以下方案混合各试剂:
| 一测定板(ul) | 每孔(μl) | |
| 10X激酶缓冲液 | 1100 | 10 |
| 10mM DTT | 1100 | 10 |
| 10mM冷ATP | 5.5 | 0.05 |
| 1mM Abl肽 | 11 | 0.1 |
| 33P-γ-ATP,10Ci/μl | 22 | 0.2 |
| H<sub>2</sub>O | 5462 | 49.65 |
将上面的反应混合物以70μl/孔的浓度分配到Flashplate的每孔中。为测试化合物对Abl激酶活性的作用,将试验化合物或者以在100%DMSO中的固定的浓度或者以系列稀释浓度,按1μl/孔的量加入到适当的孔中。
将酶Abl在酶稀释缓冲液中稀释如下:
酶稀释缓冲液 3289μl
Abl酶(100单位/μl) 11μl
通过将30μl稀释的Abl酶溶液加入到包含热ATP(2μCi/孔)和Abl肽底物(1μM的终浓度)的Flashplate的各孔中,启动激酶反应,第12列E至H排的各孔除外,这些孔被用于计算该测定板的背景值。将Flashplate旋转以便混合,于30℃温育60分钟。然后,弃去反应混合物,用洗涤/终止缓冲液洗涤Flashplate 3次,每次200μl。随后,在Flashplate的各孔中加入200μl洗涤/终止缓冲液。在将所述板用透明板密封层密封后,用Packard TopCount测量保留在每孔中的33P的量。
当一种试验化合物抑制c-Abl激酶活性时,含有这种试验化合物的孔与不含这种化合物的孔比较,其含有较低的33P的量。在所述的测定条件下进行测试,本发明范围内的化合物显示对c-Abl激酶活性的抑制作用。
为了测试本发明化合物的抑制效力,用上述方法测量单一化合物的IC50。本文所用的对c-Abl激酶活性的IC50指与不含抑制剂的反应物比较,使c-Abl激酶的活性减少一半所需的抑制剂浓度。本发明的各代表性化合物对c-Abl激酶活性的IC50列于表B中。
表B.化合物对c-Abl激酶活性的IC50
| 化合物号 | IC<sub>50</sub>(μM) |
| 2 | 0.011 |
| 8 | 0.694 |
| 11 | 0.118 |
| 12 | 0.020 |
| 13 | 0.173 |
| 14 | 0.038 |
| 22 | 0.019 |
| 26 | 0.134 |
| 29 | 0.005 |
| 30 | 0.491 |
| 32 | 0.002 |
| 36 | 0.064 |
| 38 | 0.002 |
| 39 | 0.013 |
| 41 | 0.078 |
| 44 | 0.007 |
| 54 | 0.971 |
| 63 | 0.419 |
| 90 | 10.290 |
| 97 | 0.227 |
| 116 | 0.386 |
| 118 | 0.427 |
| 119 | 0.524 |
| 122 | 1.260 |
| 124 | 1.850 |
| 128 | 0.313 |
| 129 | 10.780 |
| 129 | 2.360 |
| 130 | 0.236 |
| 化合物号 | IC<sub>50</sub>(μM) |
| 132 | 0.665 |
| 133 | 0.498 |
| 134 | 1.160 |
| 140 | 1.410 |
| 156 | 0.089 |
| 157 | 0.371 |
| 160 | 1.020 |
| 170 | 0.075 |
| 172 | 0.084 |
| 179 | 0.870 |
| 180 | 0.082 |
| 181 | 0.056 |
| 182 | 0.093 |
| 185 | 0.666 |
| 188 | 1.400 |
| 190 | 0.069 |
| 199 | 0.027 |
| 200 | 0.020 |
| 201 | 0.217 |
| 202 | 2.650 |
| 203 | 0.160 |
| 204 | 0.165 |
| 205 | 0.328 |
| 207 | 0.062 |
| 208 | 0.009 |
| 209 | 0.007 |
| 218 | 0.439 |
| 226 | 0.245 |
| 227 | 0.641 |
| 247 | 0.033 |
| 249 | 0.035 |
| 253 | 0.03795 |
| 化合物号 | IC<sub>50</sub>(μM) |
| 256 | 0.055 |
| 260 | 0.013 |
| 261 | 0.064 |
| 262 | 0.027 |
| 263 | 0.512 |
| 265 | 0.085 |
| 266 | 0.015 |
| 267 | 0.326 |
| 268 | 0.020 |
| 269 | 0.101 |
| 270 | 0.036 |
| 280 | 0.363 |
| 281 | 1.580 |
| 282 | 0.043 |
| 283 | 0.340 |
| 284 | 0.069 |
| 286 | 2.950 |
| 287 | 3.450 |
| 289 | 2.400 |
| 292 | 0.001 |
| 299 | 0.198 |
| 309 | 0.822 |
| 310 | 1.471 |
| 330 | 0.091 |
| 334 | 3.300 |
| 337 | 2.742 |
| 339 | 2.180 |
| 341 | 0.350 |
| 348 | 0.011 |
| 358 | 0.338 |
| 359 | 0.143 |
| 360 | 0.077 |
| 化合物号 | IC<sub>50</sub>(μM) |
| 361 | 0.043 |
| 363 | 0.001 |
| 369 | 0.047 |
| 370 | 0.006 |
| 371 | 0.905 |
| 373 | 0.010 |
| 374 | 0.051 |
| 376 | 0.060 |
| 379 | 0.014 |
| 380 | 0.327 |
| 381 | 1.496 |
| 382 | 0.019 |
| 383 | 0.183 |
| 384 | 0.004 |
| 385 | 0.012 |
| 386 | 0.020 |
| 388 | 0.046 |
| 389 | 0.017 |
| 390 | 0.000 |
| 391 | 0.014 |
| 396 | 0.002 |
| 398 | 0.010 |
| 400 | 0.005 |
| 401 | 0.014 |
| 415 | 0.219 |
| 419 | 0.292 |
| 420 | 0.335 |
| 422 | 3.078 |
| 432 | 0.096 |
| 448 | 0.003 |
| 449 | 0.023 |
| 457 | 0.004 |
| 化合物号 | IC<sub>50</sub>(μM) |
| 459 | 0.070 |
| 460 | 0.004 |
| 461 | 0.337 |
| 462 | 0.000 |
| 463 | 0.008 |
| 465 | 0.051 |
| 466 | 0.191 |
| 467 | 0.244 |
| 468 | 0.603 |
| 469 | 0.027 |
| 490 | 0.038 |
| 595 | 0.460 |
3.抗-细胞增殖测定法
除了以上无细胞测定法外,也以基于细胞的测定法测定本发明化合物的生物学活性。一种这样的测定法是在PDGF刺激的存在或不存在下,在各种细胞类型中测定所述化合物对细胞增殖的作用。
3a.在PDGF刺激的存在下,在正常细胞中的抗-细胞增殖作用
在PDGF刺激的存在下,基于14C-胸腺嘧啶核苷结合到细胞的DNA中,测定本发明化合物在正常人原代细胞(特别是冷藏的人冠状动脉平滑肌细胞(HCASMC))中对细胞增殖的作用。
材料
以下材料分别从它们各自的来源处购得:重组人PDGF β同源二聚体,rhPDGF-BB(此后称为″PDGF-BB″)购自R&D System(Minneapolis,MN,Cat.No 220-BB);冷藏的人冠状动脉平滑肌细胞(HCASMC)、用于HCASMC的组织培养基以及平滑肌生长补充剂(SMGS)购自Cascade Biololcs(Portland,OR,HCASMC Cat.No:C-017-5C;Medium 231 Cat.No:M-231-500;及SMGS Cat.No:S-007-25);96-孔CytoStar组织培养物处理用液体闪烁微量滴定板购自Amersham(piscataway,NJ,Cat.No:RPNQ0160);甲基14C-胸腺嘧啶核苷(56mCi/mmol)(250μCi/2.5mL)购自NEN(Cat.No.:NEC568);DMSO购自Sigma(St.Louis,MO,Cat.No:D-5879);无菌试剂贮库购自Costar(VWR International,Inc.,West Chester,PA,Cat.No:4870);Dulbecco′s PBS购自Gibco(Cat.No:14190-136);用于CytoStar板的底部的白板背封板罩购自Packard(Cat.No:6005199)
步骤
将HCASMC以大约4000细胞/孔的量接种于100μl体积的包含SMGS的完全培养基231中。使细胞生长48个小时直至它们达到80%汇合。然后将它们在无SMGS的培养基231中静止24小时。以包含50ng/mL PDGF-BB的无SMGS的培养基231补充细胞培养基,使其总容量达到100μl/孔;将1μl在100%DMSO中的系列稀释浓度的待测化合物加入到每孔中。在最大生长的对照孔中,只加入1μl 100%DMSO;在最小生长(空白)的孔中,每孔中加入1μl 10mM环己酰亚胺。孵化24小时后,在每孔中加入20μl 14C-胸腺嘧啶核苷混合剂,该14C-胸腺嘧啶核苷混合剂按照以下配方配制:
| 试剂 | 一板(μl) | 一孔(μl) |
| 14C-胸腺嘧啶核苷 | 220 | 2 |
| 无SMGS的培养基231 | 1980 | 18 |
| 总混合剂 | 2200 | 20 |
将细胞在包含待测化合物、PDGF-BB和14C-胸腺嘧啶核苷的培养基中再孵化24小时。然后,将反应混合物弃去,并以每次200μl PBS洗涤滴定板3次。随后,将板上每孔注入200μl PBS。将板的顶部以透明封板罩(transparent plate sealer)封口,在板底应用白板背封板罩(white plate backing sealers)。用Packard TopCount测量每孔中14C的残留量。
14C在一孔中的残余量与该孔中细胞的增殖相关。当一种待测化合物抑制PDGF-BB诱导的HCASMC的增殖时,包含这种化合物的孔与无该化合物的最大生长的对照孔比较,其残留的14C较少。为了测试本化合物的抑制能力,应用上述程序测试单独一种化合物抑制PDGF-BB诱导的HCASMC增殖的IC50。本文中所述IC50指在与无该化合物的最大生长对照孔相比较时,使得PDGF-BB诱导的HCASMC增殖减少一半量时试验化合物的浓度。表C显示典型的本发明化合物的IC50实例。
3b.无PDGF刺激时在普通细胞中的抗细胞增殖作用
基于5-溴脱氧尿核苷(BrdU)参入细胞DNA,测试本发明化合物在普通人类原始细胞(特别是人类脐静脉内皮细胞(HUVEC))中无PDGF刺激时对细胞增殖的作用。
原料
以下原料均购于其各自来源:HUVEC细胞购自Cascade Biologics,产品编号:C-015-10C;培养基200购自Cascade Biologics,产品编号:M-200-500;低血清生长补充物(Low serum growth supplements,LSGS)购自Cascade Biololcs,产品编号:S-003-10;F12-K培养基购自Gibco/BRL,产品编号:21127-022; BrdU试剂盒购自Roche,产品编号:1647229;胰蛋白酶/EDTA溶液购自Cascade Biologics,产品编号:R-001-100。
步骤
在补充LSGS的M-200培养基中使HUVEC细胞生长以进行繁殖。为进行研究,以胰蛋白酶/EDTA溶液分离细胞,然后以10mLF-12K(LS,低血清)培养基洗涤三次,再以400×G离心5分钟。F-12K(LS)培养基是包含0.2%热处理的胎牛血清的F-12K培养基。
在F-12K(LS)培养基中调节细胞浓度至大约5×104细胞/mL,然后向一个96孔板的各孔中加入200μl(大约1×104个细胞)。然后在37℃95%空气/5%CO2下将细胞孵化16至24小时,以使细胞附着并静止。
通过在F-12K(LS)中加入50μL 1∶10的LSGS稀释液刺激细胞增殖。通过加入50μL 1∶10的LSGS稀释液而制备最大刺激对照孔。各零对照孔只是包含50μL F-12K(LS)培养基。加入2.5μL的量的待测化合物的100%DMSO溶液以达到所需的药物终浓度。每种条件重复测试八孔。在37℃孵化细胞过夜。于次日将25μLBrdU(在F-12K(LS)培养基中将储备液按1∶100稀释)加入到每孔中。
将细胞再孵化20-24小时。移除培养基,然后通过在每孔中加入200μLFixDent溶液(包含于BrdU试剂盒中)固定细胞,然后在室温下再孵化30分钟。轻弹板并用吸水纸吸附以除去FixDent,再在每孔中加入以1∶100比例稀释于一种抗体稀溶液(包含于BrdU试剂盒中)的100μL抗-BrdU-POD(包含于BrdU试剂盒中)。稀释的抗-BrdU-POD溶液于使用前即刻配制。将各板在室温下孵化90分钟。
以洗涤溶液(每次洗涤200μL)洗涤三次而移除未结合的抗体。洗涤溶液通过用蒸馏水按1∶10稀释洗涤缓冲储备液(包含于BrdU试剂盒中)而制备。在每孔中加入底物溶液(包含于BrdU试剂盒中)(100μL),再孵化30-40分钟。然后在一96孔板读取器上于405nm读取各孔板。
为了测试本化合物的抑制能力,应用上述程序测试单独一种化合物抑制无PDGF-BB刺激的HUVEC增殖的IC50。本文中所述IC50指在与无该化合物的最大生长对照孔相比较时使得HUVEC增殖减少一半量时所述试验化合物的浓度。表C显示典型的本发明化合物的IC50实例。
3c.在肿瘤细胞中的抗细胞增殖作用
基于14C-胸腺嘧啶脱氧核苷结合入细胞的DNA中,测试本发明化合物对不同肿瘤细胞的细胞增殖的作用。
原料
与在以上3a中所述相似,只是应用不同的细胞、细胞生长培养基和生长补充物。人类肿瘤细胞系来自不同的人类组织器官(LoVo来自结肠,H460来自肺,T47D来自乳腺,PC3来自前列腺,A375来自黑素瘤,AsPC1来自胰腺),由美国典型培养物保藏中心(AmericanType Culture Collection,ATCC)获得,并按ATCC提供的每种细胞类别所需的特定条件进行培养。完全培养基来自Cellgro:含有10%胎牛血清(FBS)的Iscove′s培养基(Mediatech,Inc.,Herndon,VA 20171,产品编号:10-016-CV)。
步骤
将肿瘤细胞以大约每孔3000-8000细胞接种于100μl体积的完全培养基中。在完全培养基中使细胞生长24小时,然后将1μl待测化合物序列稀释于100%DMSO中,然后加入每孔中。在作为最大生长对照的孔中,只加入1μl 100%DMSO。孵化24小时后,将20μl 14C-胸腺嘧啶核苷总合剂(master mix)加入到每孔中,14C-胸腺嘧啶核苷总合剂(master mix)按照以下配方配制:
| 试剂 | 一板(μl) | 一孔(μl) |
| 14C-胸腺嘧啶核苷 | 220 | 2 |
| 完全培养基 | 1980 | 18 |
| 全部合剂 | 2200 | 20 |
在37℃下,将细胞在包含待测化合物和14C-胸腺嘧啶核苷的培养基中再孵化24小时。然后,将反应混合物弃去,然后每次以200μlPBS洗涤板2次。随后,向板上每孔中注入200μl PBS。将板的顶部以透明封板罩封口,在板底应用白板背底封板。用Packard TopCount测量每孔中14C的残留量。
为了测试本化合物的抑制能力,应用上述程序测试单独一种化合物抑制肿瘤细胞系增殖的IC50。本文中所用的IC50指在与无该化合物的最大生长对照孔相比较时使得肿瘤细胞增殖减少一半时得测化合物的浓度。表C显示典型的本发明化合物的IC50实例。
表C.典型的化合物对于细胞增殖的IC
50
| 化合物编号 | HCASMC(PDGF-BB)(μM) | HUVEC(LSGS)(μM) | H460(μM) | LoVo(μM) | PC3(μM) | T47D(μM) | A375(μM) | AsPC1(μM) |
| 4 | 0.268 | 1.730 | 0.030 | 0.012 | 0.048 | 0.030 | 1.580 | 0.427 |
| 11 | 0.014 | 0.002 | 0.033 | 0.002 | 0.014 | 0.007 | 0.005 | 0.03 |
| 12 | 0.106 | 0.031 | 0.003 | 0.011 | 0.013 | 0.031 | 0.011 | 0.077 |
| 14 | 0.003 | 4.870 | 0.010 | 0.011 | 0.02 | 0.032 | 0.007 | 0.592 |
| 22 | 0.278 | 2.150 | 9.270 | 13.450 | 49.500 | 0.381 | 11.550 | >10 |
| 30 | 0.002 | >1.0 | 0.290 | 0.423 | 0.175 | 8.200 | 0.507 | >10 |
| 39 | 0.009 | 0.015 | 9.950 | 10.530 | >10 | >10 | >50 | >10 |
| 63 | 0.014 | 2.460 | 3.67 | 2.4 | 6.12 | 2.6 | 2.84 | 10.3 |
| 91 | 0.071 | 0.004 | ||||||
| 97 | 0.019 | 1.910 | 0.424 | 0.225 | 1.68 | 0.622 | 0.362 | 5.67 |
| 122 | 0.125 | 0.223 | 14.300 | 3.840 | 6.340 | 10.500 | 14.400 | >10 |
| 157 | 0.008 | 0.218 | 3.590 | 2.140 | 3.130 | 1.900 | 1.230 | >10 |
| 330 | 0.049 | 1.200 | 3.700 | 0.303 | 0.355 | 2.176 | 1.550 | |
| 388 | 0.006 | 0.018 | 0.004 | 0.003 | 0.002 | 0.155 | ||
| 432 | 0.035 | 0.012 | 0.006 | 0.002 | 0.040 | |||
| 420 | 4.100 | 3.800 | 0.276 | 0.822 | 0.214 | 4.300 |
3d.在白血病细胞中的抗细胞增殖作用
应用流式血细胞计和锥虫蓝排阻细胞计数分析法,测试本发明化合物对白血病细胞特别是人类慢性骨髓性白血病(CML)K562细胞系的细胞增殖的作用。已发现CML K562细胞系表达致癌基因bcr/abl,这是人类CML的基因学标志(Wu等,1995,Leukemia,9(5):858-862)。
原料和步骤
人类慢性骨髓性白血病(CML)K562细胞系来自美国典型培养物保藏中心(ATCC),并按ATCC指定的特定条件进行培养。应用一台Becton Dickinson FACSCalibur仪器进行流式细胞计数分析。在细胞染色的研究中应用Cycle TEST PLUS DNA试剂盒(产品编号:340242,Becton Dickinson)。按照Becton Dickinson的标准操作程序和CycleTEST PLUS DNA试剂盒的应用方案进行研究。简言之,对不同染色的CML K562细胞系进行24小时流式细胞计数分析而估测以不同浓度化合物处理的细胞其DNA信息(content)和细胞周期分期分布。经No.14化合物处理的CML K562细胞系首先被碘化丙锭染色,随后以荧光分析法确定细胞周期分布。应用ModFit LT细胞周期数据分析程序(Verity Software House,Topsham,Maine 04086,www.vsh.com)进行数据分析。依照本领域技术熟练人员周知的步骤,应用台盼蓝排除分析(Trypan Blue exclusion assay)(Trypan Blue来自Sigma,产品编号:T 0776)进行细胞成活力检验(Cell viability test)。
流式血细胞计光谱显示以化合物处理24小时后导致细胞在周期中G2/M期细胞积聚以及浓度依赖模式(concentration-dependentfashion)的人类CML K562细胞系的生长阻碍(表D)。
表D.化合物处理后细胞在不同生长分期的比例
| 化合物浓度(nM) | G0-G1(%) | S期(%) | G2/M(%) |
| 0 | 37 | 45 | 18 |
| 1 | 35 | 53 | 11 |
| 10 | 31 | 41 | 28 |
| 100 | 2 | 0 | 98 |
| 1000 | 3 | 4 | 93 |
| 10000 | 5 | 5 | 90 |
应用台盼蓝排除分析(Trypan Blue exclusion assay)进行的细胞成活力检验显示以No.14化合物处理K562细胞系24小时导致K562细胞系中细胞增殖的浓度依赖性降低。经台盼蓝排除分析(Trypan Blueexclusion assay)测量,No.14化合物对K562细胞系的IC50(即在与无该化合物的最大生长对照孔相比较时使得K562细胞增殖减少一半时待测化合物的浓度)为大约10nM。
应用类似的流式血细胞计方案和台盼蓝排除细胞计数分析,发现No.14化合物还阻碍其他细胞类型(如H460和LoVo)在G2/M细胞周期分期的生长。
可应用在此描述的各种方案测试本发明领域中任何化合物抑制细胞增殖的能力。
4.抗血管生成试验
本发明之化合物抑制血管生成的活性可通过血管生成的matrigel小鼠模型(MM分析)(Passaniti等,Laboratory Investigation,67:519-528,1992)进行体内测定。matrigel小鼠测试法是一种成熟的量化血管生成的方法(例如参见Capogrossi等,Methods in Molecular Medicine,Vascular Disease:Molecular Biology and Gene Therapy Protocols,A.H.Baker编辑,Humana PressInc.,Totowa,NJ,1999)。该模型最大的特点是恰当地模拟了血管生成的过程,并已经被广泛用于多种化合物/药剂的体内潜在的血管生成和抗血管生成活性的评估。在其他血管生成模型(例如RAR分析)中表现抗血管生成活性的化合物,在MM分析中已经显示其为血管生成的潜在的抑制剂,且在人类肿瘤异种移植模型中使肿瘤生长减少。所有涉及动物的步骤均在完全按照美国实验动物管理认证协会(AAALAC)认可的动物设施中进行,并遵从实验动物饲养管理及使用规范(NIH)。实验方案均经过RWJ-PRI国际实验动物管理与使用协会(IACUC)认可。
步骤
以加入一种单剂纯化的原血管生成生长因子(pro-angiogenicgrowth factor)(100-500ng/mL之rhPDGF-BB(同上)、重组人类碱性纤维母细胞生长因子(rhFGF-basic)(R&D System产品编号:233-FB)或重组人类血管内皮生长因子(rhVEGF,PanVera产品编号:R2951))和肝素(35U/mL))的1.0mL冷冻的matrigel经皮下(腹部肋骨架下腹中线上)注射入正常雄性小鼠(C57BL/6J)。将化合物制成在0.5%甲基纤维素中的0.1%悬浮液(终浓度1mg/mL)。在注射matrigel两小时后,开始通过管饲法将介质或待测化合物(每处理组8-10只小鼠)经口服给予小鼠。连续三天持续给药(即第1天1日1次,第2天1日2次,第3天1日2次)。在末次给予介质或药物大约18小时后,对小鼠施无痛致死术,将matrigel栓外科手术完整地取出(去除其上覆盖的皮肤,然后保留一些腹膜衬里作为衬托而将栓切出)。将该栓放入预先标记好的装有1.0mL蒸馏水的试管中,切碎,然后在37℃水浴及轻摇下,萃取血红蛋白(Hb)过夜。次日将试管以3000rpm离心20分钟。去除上清液,应用Drabkin’s分析法(Drabkin’s试剂盒525-A;SIGMA)并以Beckman DU 7400分光光度计读取,通过分光光度测量法测出栓萃出物中的血红蛋白浓度。应用栓中血红蛋白含量作为一个血管生成的间接性指标,栓中血红蛋白含量的降低指示体内的抗血管生成活性。将化合物抑制PDGF-BB刺激的体内血管生成的能力直接与介质处理的对照组小鼠相比较。应用Mann-Whitney检验对组间差异进行统计学分析,以p值0.05或更少而认定具有显著统计学意义。
可应用在此描述的体内MM分析方案对本发明领域中的任何化合物进行测试。表E显示在加入PDGF的体内MM测试中本发明的代表性化合物的结果。
表E.在补充PDGF-BB的体内MM测试中代表性化合物对血管
生成的抑制作用
| 化合物编号 | 以30mg/kg口服的抑制百分率(%) |
| 14 | 40 |
| 12 | 45 |
| 26 | 42 |
5.抗肿瘤测试
应用人类肿瘤裸鼠异种移植模型在体内评估化合物的抗肿瘤活性。所有涉及动物的步骤均在完全按照美国实验动物管理认证协会(AAALAC)认可的动物设施中进行,并遵从实验动物饲养管理及使用规范(NIH)。实验方案均经过RWJ-PRI国际实验动物管理与使用协会(IACUC)认可。
人类肿瘤细胞系(LoVo,MDA-MB-231,H460等)来自美国典型培养物保藏中心,并按照每种细胞系需要的特定条件进行培养。在第0天,于雌性无胸腺裸鼠(Charles River nu/nu)股部腹股沟区以0.1mL体积的1-2×106肿瘤细胞进行皮下注射。肿瘤接种后三天,开始以介质(对照组)或实验药物经口给小鼠喂服以进行生长延缓研究。在0.5%甲基纤维素中制备化合物,连续30-35天每天给药两次进行处理。处理期间每周两次以测径器测量肿瘤生长。肿瘤面积(mm2)以长度x宽度之乘积计算。每周测量两次体重,将体重的减轻作为大体毒性的估测。在研究终点,对小鼠施无痛致死术,将实性肿瘤外科手术完整地切离并称重。将最终肿瘤重量作为主要效能终点。以ANOVA和Dunnett′s t-检验对处理组和对照组小鼠的差异进行统计学分析。
可应用在此描述的人类肿瘤裸鼠异种移植模型对本发明领域内的任何化合物进行体内测试。在体内人类肿瘤裸鼠异种移植模型研究中,一种代表性化合物,化合物14,在以50mg/kg给药时,抑制肿瘤72%的生长。
6.与辐射结合的疗法
放射疗法是治疗多种癌症(包括人类前列腺癌和卵巢癌)的一种主要的治疗方式。结合辐射处理,测试了本发明范围的化合物的抗增殖活性。将辐射处理和一种本发明的典型化合物——化合物No.14的处理联合应用后,针对两种不同的人类癌症细胞系:DU145(前列腺癌)和MDAH2774(卵巢癌)进行克隆发生测试。
原料:
DU145(前列腺癌)和MDAH2774(卵巢癌)细胞均来自ATCC;在生长介质MEM培养基(Mediatech,Herndon,VA)中添加入8%FBS,50U/ml青霉素和50μg/ml链霉素(Hyclone,Logan,UT),2mM L-谷氨酰胺(Hyclone,Logan,UT),25mM HEPES(Hyclone,Logan,UT);在McCoy′s 5A培养基(Mediatech,Hemdon,VA)中添加入8%FBS,50U/ml青霉素和50μg/ml-链霉素(Hyclone,Logan,UT)和谷氨酰胺2mM L-谷氨酰胺(Hyclone,Logan,UT),137Cs γ-射线源是一部Gammacell 1000 Elite辐照器(MDS Nordion,Kanata,Ontario,Canada);DMSO;1X PBS;甲醇;0.25%结晶紫以及60mm组织培养皿。
步骤:
将所需细胞数量的DU145或MDAH2774细胞在早期对数增殖期(early log phase)分别地接种于(plated)添加入了8%FBS、青霉素、链霉素、L-谷氨酰胺的MEM培养基或是添加入了8%FBS、青霉素、链霉素和谷氨酰胺的McCoy′s培养基的60mm培养皿中。将细胞一式三份进行接种。接种14小时后,将不同浓度的化合物No.14加入到细胞中。在细胞培养基中该化合物的终浓度范围在1至100nM之间。与待测化合物一起孵育24小时后,将各板(plate)分成相等体积的两组。应用137Cs γ-射线源(剂量率3.32Gy/min)对第一组板以7.3Gy(含有DU145细胞的板)或5.4Gy(含有MDAH2774细胞的板)进行辐射。同样地处理第二组板,但不进行辐射。将细胞在含有待测化合物的培养基中再孵育24小时。然后,用新鲜的无化合物的同样的培养基补充给细胞,使其再生长11天。然后将细胞以甲醇固定,以0.25%结晶紫染色,对含有超过50个细胞的克隆进行计数。
这些研究的结果表明始于30nM浓度的化合物No.14在辐射存在或不存在下均对DU145和MDAH2774细胞的菌落形成有显著的抑制活性,但结合辐射后抑制效果明显的更强(表F)。该活性表现为浓度-依赖性,每种细胞系结合辐射后化合物(浓度)达100nM时效果都更为显著。该结果与化合物No.14在增殖的肿瘤细胞中导致其G2/M期生长阻碍的观察结果一致,因为人们认为G2/M期生长阻碍的细胞对附加损伤(如辐射)是更易损且更敏感的。
可应用在此描述的方案对本发明领域中的任何化合物进行测试其对放射治疗的细胞的敏感的能力。
表F.对结合辐射和化合物No.14处理的克隆发生的测试
该研究表明与单用化合物或辐射处理比较,将癌症细胞以低浓度的本发明化合物预处理后结合辐射处理可使集落形成更加减少。这些初步研究支持联合应用本发明化合物与放射疗法治疗癌症的重要性,而放射疗法已经是一种标准的治疗形式。
7.前体药物向母体化合物的转化
已证明就一种特别的生物空间来讲,活性药物的化学修饰可显著改变其化学-物理性质,如溶解性、稳定性、吸收、转运和生物-利用度(参见Bioreversible Carrier in Drug Design,Edward B.Roche著,Pergamon Press,1987)。前体药物是能够被酶(如酯酶)可逆地水解回活性药物的分子。通过体外和体内测试系统评估本发明领域化合物的前体药物在体内转化为母体化合物的可能性。
将本发明中的一种典型化合物——化合物No.14的各种前体药物在新鲜制备的大鼠血浆中孵育2小时。在血浆孵育之前和之后测定这些前体药物的PDGF-R激酶抑制活性。如上所述进行PDGF-R激酶抑制活性的测定。结果表明血浆中孵化2小时能显著提高前体药物的PDGF-R激酶抑制活性。这提示在大鼠血浆中大量的前体药物已经被转化成为母体药物。实际上,在与大鼠血浆孵育2小时后,通过HPLC分析已经检测出了大量的母体化合物(表G)。
另外,在药代动力学研究中,将前体药物通过口服给予大鼠(10mg/kg),然后通过HPLC/MS/MS分析测定了前体药物至母体化合物的转化。从药代动力学研究的大鼠血浆中检测母体化合物或母体化合物的葡糖苷酸共轭体(表G)。
表G:通过HPLC测定典型的前体药物向母体化合物No.14的转化
采用本文所述的方案,可以对本发明范围内的药物前体向任何母体化合物的转化进行测试。
应用本发明化合物的方法
本发明的化合物可以用于治疗/预防细胞增殖性疾病或与PDGF-R有关的疾病的方法中。它们也可以用于例如通过合理的设计鉴定新的PDGF-R抑制剂的方法中。
1.基于合理的设计鉴定新的PDGF-R激酶抑制剂的方法。
在本发明的一个方面,本发明化合物可以根据合理的设计,用于鉴定新的PDGF-R激酶抑制剂。
本文所用的″合理的设计″指设计PDGF-R激酶抑制剂基于PDGF-R激酶抑制剂的三维结构的方法,优选所述方法包括PDGF-R激酶抑制剂与PDGF-R蛋白的结合,优选与人PDGF-R蛋白,且更优选与人PDGF-R蛋白的激酶催化结构域结合的三维结构。本文所用″PDGF-R激酶催化结构域″指由用于PDGF-R激酶活性所需的最小限度的氨基酸序列组成的多肽,其中所述用于PDGF-R激酶活性所需的最小限度的氨基酸序列可以由本领域技术人员容易地确定。所述催化结构域可以是来自人或动物的PDGF-R的催化结构域。例如,所述″PDGF-R激酶催化结构域″可以包含GenBank Access NO:AAA36427的氨基酸545至1106。
基于合理的设计的结构可以成功地用于鉴定各种酶(如蛋白酶和蛋白酪氨酸磷酸酶)的新的小分子抑制剂。用于基于合理的设计鉴定新的PDGF-R激酶抑制剂的方法包括以下步骤:(a)在包括PDGF-R激酶催化结构域的多肽的存在或不存在下,确定式I或11的化合物的三维结构;(b)仅分析该化合物的三维结构或者分析所述化合物和PDGF-R的分子间的相互作用;(c)选择仅模拟该化合物的结构或者结合预计的相互作用的化合物;(d)合成所设计的化合物;及(e)测定所述分子结合和抑制PDGF-R激酶活性的能力。可以通过精细地调整相互作用的特征,重复这些步骤以获得最佳的化合物。
所述三维结构可以通过例如X-射线结晶学、核磁共振或同源性模拟(homology modeling)获得,所有这些都是熟知的方法。
本发明的一种具体方法包括分析所述化合物和PDGF-R(优选PDGF-R的活性激酶结构域)间分子的相互作用的三维结构。本发明包括在分子模拟软件系统中应用式I或11的化合物与PDGF-R的结合的三维结构的信息,以帮助分析分子间的相互作用。应该鉴定和分析在PDGF-R上的可能的结合位点以及在式(I)或(II)化合物上的关键残基,它们对于分子间的相互作用是关键的。
本发明的另一个具体方法包括设计参与以上鉴定的预计的相互作用的化合物。这种计算机-辅助模型和药物设计可以利用诸如化学构象分析、分子的静电电位、蛋白折叠效应等信息。因此,根据式(I)或(II)化合物和PDGF-R之间的分子间相互作用,将新的PDGF-R激酶抑制剂设计成为能使所设计的化合物特异性结合于PDGF-R。式(I)或(II)化合物可以用作初步设计的模板。
本发明的另一个具体方法包括合成参与以上鉴定的预计相互作用的所设计的化合物。此类化合物可以采用本领域已知的各种方法合成。例如,可以证明在此描述的合成方法或这些方法的修改方法对合成所设计的化合物是有用的。
本发明的又一个具体方法包括测定新的化合物结合和抑制PDGF-R活性的能力。化合物抑制PDGF-R激酶活性的能力可以采用任何上述的生物学测定法测定,所述方法包括无细胞的PDGF-R激酶测定法;PDGF-BB刺激的HCASMC细胞增殖和人肿瘤细胞增殖测定法;体内抗-血管生成MM测定法;及人肿瘤小鼠异种移植测定法。
因为本发明范围内的化合物还显示对c-Abl激酶的抑制活性,新的c-Abl激酶抑制剂可以通过合理的设计,采用类似于在此描述的步骤鉴定。这样的方法包括以下的步骤:
(a)在包含c-Abl激酶催化结构域的多肽的存在或不存在下,确定式I或11的化合物的三维结构;
(b)仅分析该化合物的三维结构或者分析所述化合物和c-Abl的分子间的相互作用;
(c)选择仅模拟该化合物的结构或者结合预计的相互作用的化合物;
(d)合成所设计的化合物;及
(e)测定所述分子结合和抑制c-Abl激酶活性的能力。
2.治疗/预防的方法
在本发明的另一个方面,本发明化合物可以用于在细胞或患者中抑制或减弱PDGF-R激酶或c-Abl激酶活性,或者用于在患者中治疗与PDGF-R或细胞增殖有关的疾病。
在该方面的一个实施方案中,本发明提供一种在细胞中减弱或抑制PDGF-R或c-Abl的激酶活性的方法,该方法包括使所述细胞与式(I)或(II)化合物接触的步骤。本发明也提供一种在患者中抑制PDGF-R或c-Abl的激酶活性的方法,该方法包括给予所述患者式(I)或(II)化合物的步骤。本发明还提供在细胞中抑制细胞增殖的方法,该方法包括使所述细胞与式(I)或(II)化合物接触的步骤。
在细胞或患者中的PDGF-R或c-Abl激酶活性可以通过本领域熟知的方法,如上述的PDGF-R激酶测定法或c-Abl激酶测定法进行测定。
本文所用的术语″患者″指已作为治疗、观察或试验对象的动物,优选哺乳动物,最优选人。
在该方面的其它实施方案中,本发明提供用于治疗具有发生(或易感)细胞增殖性疾病或与PDGF-R有关的疾病的危险的患者的预防和治疗方法。
在一个实例中,本发明提供在患者中通过给予所述患者预防有效量的药用组合物来预防细胞增殖性疾病或与PDGF-R有关的疾病的方法,所述药用组合物包括式(I)或(II)化合物和药学上可接受的载体。可以在细胞增殖性疾病或与PDGF-R有关的疾病的特征性症状的临床表现之前给予所述预防剂,以预防疾病或紊乱或者延缓病情的发展。
在另一个实例中,本发明涉及在患者中通过给予所述患者治疗有效量的药用组合物来治疗细胞增殖性疾病或与PDGF-R有关的疾病的方法,所述药用组合物包括式(I)或(II)化合物和药学上可接受的载体。可以在所述疾病的特征性症状的临床表现出现的同时给予所述治疗剂,以使所述治疗剂作为对细胞增殖性疾病或与PDGF-R有关的疾病的代偿的疗法起作用。
本文所使用的术语“预防有效量”表示由研究人员、兽医、医生或其它临床医生所寻找的在患者中抑制或延缓患者疾病的发生的活性化合物或药物的量。
本文所使用的术语“治疗有效量”表示由研究人员、兽医、医生或其它临床医生所探寻的在患者中可以引发生物或药物反应的活性化合物或药物的量,所述反应包括所治疗的疾病或紊乱的缓解。
用于确定本发明药用组合物的治疗或预防有效量的方法为本领域已知。
本文所使用的术语“组合物”意指包括含特定量的特定成分的产品,以及由特定量的各特定成分的组合直接或间接产生的任何产品。
本文所用的术语″与PDGF-R有关的疾病″或″与PDGF受体有关的疾病″或″与PDGF受体酪氨酸激酶有关的疾病″应包括涉及或与PDGF-R活性有关的疾病(例如,PDGF-R活性过高)和与这些疾病并发的病症。术语″PDGF-R活性过高″或者指1)PDGF-R在细胞中的表达(所述细胞正常不表达PDGF-R);或者指2)细胞表达的PDGF(所述细胞正常不表达PDGF);或者指3)PDGF-R表达增加导致不需要的细胞增殖;或者指4)PDGF表达的增加导致不需要的细胞增殖;或者指5)突变导致PDGF-R的成分激活(constitutive activation)。″与PDGF-R有关的疾病″的实例包括因PDGF异常高的量或PDGF的突变引起PDGF-R的过度刺激所致的病症或因PDGF-R异常高的量或PDGF-R的突变引起PDGF-R活性异常高的量所致的疾病。已知PDGF的活性过高与一些严重疾病的发病机理有关,所述疾病包括癌症(神经胶质瘤、肺癌、乳腺癌、直肠癌、前列腺癌、胃癌和食管癌、白血病和淋巴瘤)和其它细胞增殖性疾病,如动脉粥样硬化、移植-诱导的血管疾病、新生内膜形成、肺纤维化、再狭窄、肺的纤维变性、肾小球性肾炎、肾小球硬化症、先天性多囊性肾发育不良、肾纤维化和类风湿性关节炎(Ostman A,Heldin CH.,Adv.Cancer Res,80:1-38,2001,以及其中的参考文献)。
术语″细胞增殖性疾病″指多细胞有机体中的一个或多个细胞亚群的不需要的细胞增殖,所述增殖对多细胞有机体造成危害(即,不适或减少寿命)。细胞增殖性疾病可以发生于不同种类的动物和人中。例如,本文所用的″细胞增殖性疾病″包括瘤形成和其它细胞增殖性疾病。如本文所用的″瘤形成疾病″指不受控制的细胞过度生长所致的肿瘤。瘤形成疾病的实例包括但不限于癌症,如神经胶质瘤、肺癌、乳腺癌、直肠结肠癌、前列腺癌、胃癌、食管癌、结肠癌、胰腺癌、卵巢癌、脊髓发育不良、多发性骨髓瘤、白血病和淋巴瘤。白血病的实例包括但不限于:慢性骨髓性白血病(CML);急性淋巴细胞白血病(ALL);慢性嗜中性白血病(CNL);急性未分化白血病(AUL);及急性骨髓性白血病(AML)。其它的细胞增殖性疾病包括但不限于:动脉粥样硬化、移植诱导的血管疾病、新生内膜形成、肺纤维化、黄斑变性、再狭窄、肺的纤维变性、肾小球性肾炎、肾小球硬化症、先天性多囊性肾发育不良、肾纤维化、糖尿病性视网膜病和类风湿性关节炎。
在该方面的另一个实施方案中,本发明包括用联合疗法在患者中治疗或抑制细胞增殖性疾病或与PDGF-R有关的疾病的发病。所述联合疗法包括给予所述患者治疗或预防有效量的式(I)或(II)化合物和一种或多种其它抗-细胞增殖疗法(包括化学疗法、放射疗法、基因疗法和免疫疗法)。
在本发明的一个实施方案中,可以将本发明的化合物与化学疗法联合使用。本文所用的化学疗法指包括化学治疗剂的疗法。可以将各种化学治疗剂与本文公开的治疗方法联合应用。考虑作为实例的化学治疗剂包括(但不限于)阿霉素、更生霉素、自力霉素、洋红霉素、柔红霉素、多柔比星、他莫昔芬、紫杉醇、泰素帝、长春新碱、长春花碱、长春瑞滨、依托泊苷(VP-16)、5-氟尿嘧啶(5FU)、阿糖胞苷、环磷酰胺、塞替派、甲氨蝶呤、喜树碱、曲妥单抗、放线菌素-D、丝裂霉素C、顺铂(CDDP)、氨蝶宁、考步他汀及其衍生物和药物前体。
在本发明的另一个实施方案中,本发明的化合物可以与放射疗法联合使用。本文所用的″放射疗法″指包括使有此需要的患者暴露于辐射疗法。这种疗法是本领域技术人员已知的。放射疗法的合适的方案应当类似于已用于临床的那些疗法,其中所述放射疗法可以单独使用或与其它化学疗法联合使用。
在本发明的另一个实施方案中,本发明的化合物可以与基因疗法联合应用。本文所用的″基因疗法″指靶向涉及肿瘤发生的特定基因的疗法。可能的基因疗法策略包括缺陷性癌-抑制基因的恢复,细胞转导或用相应于生长因子及其受体的基因编码的反义DNA转染或用所谓的′自杀基因′转染。
在本发明的其它实施方案中,本发明的化合物可以与免疫疗法联合使用。本文所用的″免疫疗法″指通过对与肿瘤发生有关的特殊蛋白具有特异性的抗体靶向所述蛋白的疗法。例如,在癌症的治疗中已经使用针对血管内皮生长因子的单克隆抗体。
除了本发明化合物外,还使用第二种药物时,这两种药物可以以单一的组合物一起给予,或者根据分开的给药方案分别、顺序、基本同时给予。
本领域普通技术人员应该理解,化学治疗剂的适当剂量通常类似于或低于临床疗法中已经使用的那些剂量,其中所述化学治疗剂可以单独给予或与其它化学治疗剂联合给予。仅仅作为一个例子,药物如顺铂和其它DNA烷基化剂已广泛用于治疗癌症。临床应用的顺铂的有效剂量为每3周中的5天使用20mg/m2,总共进行3个疗程。顺铂不能口服吸收,因而必须通过静脉内、皮下、肿瘤内或腹膜内注射传递。
其它有用的药物包括可干扰DNA复制、有丝分裂和染色体分离的化合物。这类化学治疗剂化合物包括阿霉素(也称作多柔比星)、依托泊苷、维拉帕米、鬼臼毒素等,它们已广泛用于临床上治疗肿瘤。这些化合物通过静脉内大剂量注射给予,阿霉素的剂量为25-75mg/m2,间隔21天;依托泊苷静脉给予35-50mg/m2或者口服给予静脉内剂量的两倍。中断多核苷酸前体合成和复制(fidelity)的药物(如5-氟尿嘧啶(5-FU))优先用于靶向瘤形成细胞。虽然5-FU具有相当的毒性,但它通常通过静脉内给予,其剂量范围在3-15mg/kg/天之间。
本发明化合物可以向患者全身给药,例如,经静脉内、口服、皮下、肌内、真皮内或胃肠外给药。本发明化合物也可以向患者局部给药。局部传递系统的非限制性实例包括管腔内医疗装置的应用,所述装置包括血管内药物传递导管、导线(wires)、药物移植片固定模和内腔的铺料(endoluminal paving)。还可将本发明化合物与靶向剂联合给予患者,以达到所述化合物在靶位上的局部高浓度。此外,可将所述化合物制成为快速释放或缓慢释放的剂型,以便达到维持药物或药剂在数小时至数周的时间范围内与靶组织接触的目的。
本发明也提供药用组合物,它包括与药学上可接受的载体混合的式(I)或(II)化合物或其旋光异构体、对映体、非对映体、外消旋体或药学上可接受的盐。所述药用组合物可以含有约0.1mg-1000mg,优选约100-500mg的所述化合物,并可以构成适合所选择的给药方式的任何形式。短语″药学上可接受的″指如果需要而给予动物或人时,不会产生不利的、过敏的或其它不需要的反应的分子实体和成分。兽医的运用同样包括在本发明范围内,且″药学上可接受的″制剂包括用于临床和/或兽医用途的制剂。载体包括必需的和惰性的药用赋形剂,包括但不限于粘合剂、悬浮剂、润滑剂、调味剂、甜味剂、防腐剂、干燥剂和包衣材料。适合口服给药的组合物包括固体形式如丸剂、片剂、胶囊形片剂、胶囊(每一种包括立即释放、分时释放和缓慢释放剂型)、颗粒剂和粉末剂以及液体形式如溶液剂、糖浆剂、酏剂、乳剂和悬浮液。用于肠胃外给药的剂型包括无菌溶液剂、乳剂和悬浮液。
本发明的药用组合物也包括用于缓慢释放本发明化合物的药用组合物。所述组合物包括缓慢释放的载体(典型地为聚合物载体)和本发明化合物。缓慢释放的可生物降解的载体为本领域熟知的。这样的载体为可形成能将活性化合物截留于其中并在合适的环境(如,水性、酸性、碱性等)下缓慢降解/溶解的材料,由此其可在体液中降解/溶解并释放其中的活性化合物。所述颗粒优选为纳米颗粒(即,直径在约1-500nm,优选直径在约50-200nm,最优选直径在约100nm范围内)。
本发明还提供制备本发明的药用组合物的方法。根据常规的制药混合技术,将作为活性成分的式(I)或(II)化合物或其旋光异构体、对映体、酯、非对映体、外消旋体或外消旋混合物及其盐与药学上可接受的载体紧密地混合,依据所需给药的制剂形式,例如口服或胃肠外(如肌内)给药,所述载体可以采用多种多样的形式。在制备口服剂型的组合物中,可以使用任何有用的药用介质。因此,例如对于液体口服制剂,如悬浮液、酏剂和溶液剂而言,合适的载体和添加剂包括水、二醇类、油类、醇、调味剂、防腐剂、着色剂等;对于固体口服制剂,例如,散剂、胶囊、小胶囊剂、胶囊形片剂和片剂而言,合适的载体和添加剂包括淀粉、糖、稀释剂、成粒剂、润滑剂、粘合剂、崩解剂等。片剂和胶囊剂因其易于服用,因而代表最有利的口服剂量单位形式,其中显然可以采用固体药用载体。如果需要,片剂可以通过标准技术进行包糖衣或包肠衣。对于胃肠外制剂,所述载体将通常包含无菌水,虽然例如为了增加溶解度或者防腐的目的,可以包括其它成分。也可以制备可注射的悬浮液,其中可以使用适当的液体载体、悬浮剂等。在缓释制剂的制备中,先将缓慢释放的载体(通常为聚合物载体)和本发明化合物溶解或分散于有机溶剂中。然后将得到的有机溶液加入到含水的溶液中,以获得水包油类型的乳剂。所述含水的溶液优选包括表面活性剂。随后,从水包油类型的乳剂中蒸发有机溶剂,以获得包含缓慢释放的载体和本发明化合物的颗粒的胶体悬浮液。
本发明的药用组合物每剂量单位如片剂、胶囊、散剂、注射剂、茶匙剂等含有传递如上所述的有效剂量所必需量的活性成分。本发明的药用组合物每剂量单位如片剂、胶囊、散剂、注射剂、栓剂、茶匙剂等含有约0.01mg-200mg/kg体重/天。优选剂量范围为约0.03-约100mg/kg体重/天,最优选为约0.05-约10mg/kg体重/天。所述化合物可以根据每日1-5次的方案给药。然而可以根据患者的需要、所治疗疾病的严重程度和所用的具体化合物改变所述剂量。可以使用每日给药或后周期给药的用法。
优选这些组合物为单位剂型,如片剂、丸剂、胶囊剂、散剂、颗粒剂、无菌胃肠外溶液剂或悬浮液、计量气雾剂或液体喷雾剂、滴剂、安瓿剂、自动-注射装置或栓剂;以用于口服、胃肠外、鼻内、舌下或直肠给药,或通过吸入法或吹入法给药。另一方面,所述组合物可以以适合用于每周一次或每月一次给药的形式存在,例如,可将所述活性化合物的不溶性盐(如癸酸盐)制成适用于提供用于肌内注射的储存制剂。对于制备固体组合物,例如片剂,可将主要活性成分与药用载体混合,所述载体如常规制片成分,如玉米淀粉、乳糖、蔗糖、山梨醇、滑石粉、硬脂酸、硬脂酸镁、磷酸二钙或树胶以及其它药用稀释剂(如水),以形成含有本发明化合物或其药学上可接受盐的均匀混合物的固态药用组合物。当提及这些均质的预先制备的组合物时,指的是将这些活性成分均匀地分布在整个组合物中,以使所述组合物可以容易地分配到每一等效的剂量形式(例如片剂、丸剂和胶囊)中。然后,将该固体预先制备的组合物分配到以上所述类型的单位剂量形式中,其含有0.1至大约500mg本发明的活性成分。可将所述新组合物的片剂或丸剂包衣,或另外混合配制成以便提供具有延长活性优势的剂量形式。例如,所述片剂或丸剂可以含有内部剂量和外部剂量成分,后者可以是前者的包封物。可以通过肠溶衣层将两种成分分开,所述肠溶衣层可以阻止在胃内崩解并且使内部成分完整地进入十二指肠或延迟释放。可以使用多种原料作为所述肠溶衣层或包衣,该物质包括许多聚合酸以及如紫胶、鲸蜡醇和乙酸纤维素等的物质。
可用于口服或注射给药的式(I)或(II)化合物的液体形式包括水性溶液剂、适当调味的糖浆剂、水性或油性悬浮液、利用可食用油(如棉籽油、芝麻油、椰子油或花生油)的乳剂,以及酏剂和类似的药用形式。作为水性悬浮液的合适的分散剂或悬浮剂包括合成的和天然的树胶,如西黄蓍胶、阿拉伯胶、藻酸盐、葡聚糖、羧甲基纤维素钠、甲基纤维素、聚乙烯吡咯烷酮或明胶。为合适调味的悬浮剂或分散剂的液体形式也可以包括合成或天然树胶,例如黄蓍胶、阿拉伯树胶、甲基纤维素等。对于肠胃外给药,需要无菌悬浮液或溶液剂。当需要静脉给药时,应用通常含有合适的防腐剂的等渗制剂。
式(I)或(II)化合物可以优选以单一日剂量给药,或者将总日剂量以每天两次、三次或四次的分剂量给药。另外,可将本发明的化合物以鼻内剂型通过局部使用合适的鼻内载体给药,或通过本领域一般技术人员已熟知的透皮贴给药。当然,当以经皮释放系统形式给药时,通过所述剂量方案给药的剂量是连续的,而不是断续的。
例如,对于以片剂或胶囊形式的口服给药而言,可将所述活性药物成分与口服、无毒性药学上可接受的惰性载体(如乙醇、甘油、水等)相混合。此外,当需要或要求时,也可以将合适的粘合剂、润滑剂、崩解剂和着色剂掺入到所述混合物中。合适的粘合剂包括但不限于:淀粉、明胶、天然糖(如葡萄糖或β-乳糖)、玉米甜味剂、天然和合成树胶如阿拉伯树胶、黄蓍胶或油酸钠、硬脂酸钠、硬脂酸镁、苯甲酸钠、乙酸钠、氯化钠等。崩解剂包括但不限于:淀粉、甲基纤维素、琼脂、皂土、黄原胶等。
所述产品的日剂量可以在每个成人每日1-5000mg的宽范围内变化。对于口服给予,所述组合物优选以含有0.01、0.05、0.1、0.5,1.0,2.5、5.0、10.0、15.0、25.0、50.0、100、150、200、250和500毫克的活性成分的片剂形式,根据症状调整剂量以提供给待治疗的患者。有效量的药物通常以约0.01mg/kg-约200mg/kg体重/天的剂量水平供给。优选所述剂量范围为约0.03-约15mg/kg体重/天,且更优选所述剂量范围为约0.05-约10mg/kg体重/天。所述化合物可根据给药方案,以每日多至4次或更多次给予,优选每日1-2次。
给药的最佳剂量可以由本领域技术人员容易地确定,并且根椐所使用的具体化合物、给药的方法、制剂的剂量、给药方式以及疾病的进展情况而变化。另外,调整剂量需要考虑与所治疗的具体患者有关的因素,包括患者的年龄、体重、饮食和给药的时间。
本发明的化合物也可以以脂质体传递系统形式给药,例如小单层脂质体、大单层脂质体和多层脂质体。脂质体可以由各种脂类形成,包括但不限于亲水亲油性脂类如卵磷脂、鞘磷脂、磷脂酰基乙醇胺、磷脂酰胆碱、心磷脂、磷脂酰丝氨酸、磷脂酰基甘油酯、磷脂酸、磷脂酰肌醇、二酰基三甲基铵丙烷、二酰基二甲基铵丙烷和硬脂酰胺、中性脂类如甘油三酯及其组合。它们可以含有胆固醇或者可以不含胆固醇。
本发明的化合物也可以局部给予。可以使用任何传递装置,如血管内药物传递导管、导线、药物移植片固定模和内腔的铺料。优选传递装置包含包括包衣或鞘的移植片固定模,从中可以洗脱或释放所述化合物。用于这种装置的传递系统可以包含局部用的输入导管,其通过以给药者控制的速率从导管中传递所述化合物。
本发明提供一种药物传递装置,其包括管腔内医疗装置(优选移植片固定模)和治疗剂量的本发明化合物。
术语″移植片固定模″指任何能够通过导管传递的装置。移植片固定模通常用于预防因身体异常(如由于手术创伤所致的血管组织的不需要的向内生长)引起的血管闭塞。它往往具有适合于留在管腔内部的管状的、扩张的格子状-类型的结构,以减轻闭塞。所述移植片固定模具有腔壁充分接触的表面和腔壁暴露的表面。所述腔壁充分接触的表面是管腔的外表面,而所述腔壁暴露的表面是管腔的内表面。所述移植片固定模可以是聚合的、金属的或聚合并金属的,且它可以任选具有可生物降解性。
通常,移植片固定模以非膨胀的形式插入到管腔中,然后自发膨胀或借助于原位的第二种装置膨胀。典型的膨胀方法通过使用安装有导管的血管成形术气囊进行,它在狭窄的血管或体内通道内膨胀,以便切断和分裂与血管壁成分有关的闭塞物,获得扩张管腔。也可以使用自身-膨胀的移植片固定模(如在US 2002/0016625 A1(Falotico等,待审批)中所述)。移植片固定模与预防炎症和增殖的药物、药剂或化合物的组合使用可以对血管成形术后的再狭窄提供最有效的治疗。
可将本发明的化合物以多种方式以及使用任何数量的可生物相容的材料加入或附于移植片固定模上。在一个示例性实施方案中,所述化合物与聚合物基质(如高分子聚吡咯)直接结合,随后对移植片固定模的外表面进行包衣。本质上,所述化合物通过扩散到聚合物分子而从基质中脱出。移植片固定模及对移植片固定模上的药物包衣的方法在WIPO出版物WO9632907中有详细描述。在另一个示例性实施方案中,先对所述移植片固定模用含有所述化合物、亚乙基-共聚-乙烯基乙酸酯和聚丁基异丁烯酸酯的溶液作为基底层进行包衣。然后,再用仅包含聚丁基异丁烯酸酯的外层物对移植片固定模进一步包衣。所述外层用作扩散的阻挡层,以防止所述化合物过快地脱出而进入周围的组织。外层或外层包衣的厚度决定着所述化合物从基质中脱出的速率。移植片固定模和包衣的方法在U.S.公布号2002/0016625及其中公开的参考文献中有详细的讨论。
可将本发明化合物和生物可相容的材料/聚合物的溶液以多种方式结合到移植片固定模中或其之上。例如,可将所述溶液喷雾到移植片固定模上或将所述移植片固定模浸入到所述溶液中。在一个优选的实施方案中,所述溶液可喷洒到移植片固定模上,然后使之干燥。在另一个优选的实施方案中,可使所述溶液带有一极电荷,而使移植片固定模带有相反一极的电荷。在这种方式下,所述溶液和移植片固定模将相互吸引。采用这种类型的喷雾方法时,可以减少损耗,且可以实现对包衣厚度的更好的控制。化合物优选仅附于移植片固定模的外表面上,这将使其与一种组织亲密接触。然而,对于某些化合物来说,可以对全部移植片固定模包衣。施加于移植片固定模上的所述化合物和控制药物的释放的聚合物包衣中的联合剂量在所述药物的有效性方面是重要的。化合物优选保留在移植片固定模中至少3天至最多可达约6个月,优选在7-30天之间。
可将任何类型的非-腐蚀的生物可相容的聚合物与本发明化合物结合使用。重要的是应注意到不同的聚合物可以用于不同的移植片固定模。例如,上述亚乙基-共聚-乙烯基乙酸酯和聚丁基异丁烯酸酯基质与不锈钢移植片固定模组合效果良好。可利用其它聚合物更有效地与由其它材料(包括显示高弹性的材料,如镍和钛的合金)形成的移植片固定模组合使用。
本发明还提供一种用于治疗与PDGF-R有关的疾病,特别是血管壁的再狭窄、内膜增生或炎症的方法,该方法包括通过从管腔内医疗装置(如移植片固定模)释放治疗有效量的本发明化合物来控制传递。
将移植片固定模引入体内管腔的方法是本领域熟知的,本发明的化合物-包衣的移植片固定模优选使用导管引入。本领域普通技术人员应该理解,根据移植片固定模植入的部位,可将这些方法稍加修改。对于冠脉移植片固定模的植入,可将携带移植片固定模的气囊导管插入到冠状动脉中,并将该移植片固定模定位于所需的部位。气囊膨胀会使移植片固定模扩大。当移植片固定模膨胀时,移植片固定模接触腔壁。移植片固定模一旦定位,该气囊即放气并移出。携带所述化合物的移植片固定模遗留在接触管腔的表面的部位而直接与管腔壁表面接触。需要时,移植片固定模植入法可以与抗凝血疗法联合使用。
使用本发明的移植片固定模传递所述化合物的最佳条件可以随着所用的不同的局部传递系统以及所用所述化合物的特性和浓度而变化。可以最优化的条件包括,例如所述化合物的浓度、传递的量、传递速率、血管壁的渗透深度、邻近血管的舒张压、穿孔的数量和大小以及药物传递导管气囊的安装。可以使抑制损伤部位的平滑肌细胞增殖的条件最优化,以使因再狭窄所致的严重的动脉阻塞不再发生,例如,通过测定平滑肌细胞的增殖能力或通过测定血管再狭窄的变化或管腔直径即可得知。根据得自动物模型研究的数据,采用常规计算机方法,可以确定最佳条件效果。
本发明化合物可选择的另一种给药的方法可以是将所述化合物与靶向剂结合,所述靶向剂可以直接结合到其作用的预定位点,即结合于血管内皮细胞或结合于肿瘤细胞。可以使用抗体和非-抗体靶向剂。由于靶向剂和其相应的结合配体之间的特异性相互作用,可以以高的局部浓度将本发明的化合物给予靶向位点或其附近,由此可在靶位更有效地治疗疾病。
所述抗体靶向剂包括抗体或其抗原结合片段,它们结合于肿瘤细胞、肿瘤脉管系统或肿瘤基质的可靶向的或易接近的成分。肿瘤细胞、肿瘤脉管系统或肿瘤基质的″可靶向的或易接近的成分″优选为表面-表达的、表面-易接近的或表面-定位的成分。抗体靶向剂也包括抗体或或其抗原结合片段,它们结合于从坏死肿瘤细胞中释放的细胞内成分。这类抗体优选是单克隆抗体或其抗原结合片段,它们结合于细胞中存在的不溶性细胞内抗原,所述抗原可在几乎所有的肿瘤形成细胞和正常细胞中引起渗透,但不存在于或不能接近哺乳动物的正常活细胞的外部。
本文所用的术语“抗体”广义上意指任何免疫学结合物质,如IgG、IgM、IgA、IgE、F(ab′)2、单价片段如Fab’、Fab、Dab,及遗传工程抗体,如重组抗体、人源化抗体、双特异性抗体等。所述抗体可以是多克隆的或单克隆的,虽然优选为单克隆的。现在在本领域中存在已知的很宽序列的抗体,这些抗体实际上对任何实体瘤类型的细胞表面具有免疫学的特异性(参见Thorpe等的US 5855866中有关实体瘤的单克隆抗体的一览表)。生产和分离针对肿瘤的抗体的方法为本领域技术人员所熟知(见例如,Thorpe等的US 5855866和Thorpe等的US 6342219)。
所述非-抗体靶向剂包括生长因子,如PDGF、VEGF和FGF;肽,包括三肽R-G-D,其特异性结合于肿瘤脉管系统;及其它靶向成分,如膜联蛋白及相关配体。此外,也可以使用各种其它的有机分子作为肿瘤的靶向剂,实例有透明质酸寡糖(hyaluronanoligosaccharides),其特异性地识别透明质酸-结合蛋白,所述结合蛋白是一种在肿瘤细胞和内皮细胞迁移期间以及在毛细管-样细管形成(US 5902795,Toole等)期间表达的细胞表面蛋白,以及多阴离子化合物,特别是在US 5762918(Thorpe)中描述的多硫酸盐化(polysulphated)或多磺酸盐化(polysulphonated)的化合物,如N-和O-硫酸盐多阴离子多糖、聚苯乙烯磺酸盐和其它多阴离子化合物,它们选择性的结合于血管内皮细胞。
将治疗部分结合于抗体的技术是熟知的,见如Amon等,″Monoclonal Antibodies For Immunotargeting Of Drug In CancerTherapy″,in Monoclonal Antibodies And Cancer Therapy,Reisfeld等(eds.),第243-56页(Alan R.Liss,Inc.1985);Hellstrom等,″AntibodiesFor Drug Delivery″,in Controlled Drug Delivery(第二版),Robinson等(eds.),第623-53页(Marcel Dekker,Inc.1987);Thorpe,″AntibodyCarriers Of Cytotoxic Agents In Cancer Therapy:A Review″,inMonoclonal Antibodies′84:Biological And Clinical Applications,Pinchera等(eds.)第475-506页(1985)。相似的技术也可以应用于使本发明化合物附着于非-抗体靶向剂上。本领域的技术人员应该知道或者能够确定与非-抗体靶向剂(如小分子、寡肽、多糖或其它多阴离子化合物)形成轭合物的方法。
虽然在血液中相当稳定的任何连接部分均可以用于连接本发明化合物与靶向剂,但优选生物学上-可断开的键和/或选择性地可裂解的间隔键或连接键。″生物学上-可断开的键″和″选择性地可裂解的间隔键或连接键″在血液循环中仍有相当的稳定性,但仅在或优选在一定条件下,即在一定的环境下,或在与特殊的药物接触时进行,却是可断开的、可裂解的或可水解的。这样的键包括,例如,二硫(disulfide)键和三硫键(trisulfide bonds)以及酸-不稳定键(如在美国专利号5,474,765和5,762,918中所述)和酶-敏感键,包括肽键、酯键、酰胺键、磷酸二酯键和糖苷键(如在美国专利号5,474,765和5,762,918中所述)。这样的选择性-释放设计特征在于有助于在预订的靶位点使所述化合物从轭合物中缓慢释放出来。
本发明提供一种药用组合物,它包括上述的与靶向剂结合的有效量的本发明化合物和药学上可接受的载体。
本发明还提供一种治疗与PDGF-R有关的疾病(特别是肿瘤)的方法,它包括给予所述患者与靶向剂结合的治疗有效量的式(I)或(II)化合物。当将蛋白(如抗体或生长因子)或多糖用作靶向剂时,它们优选以可注射的组合物的形式给予。可用2分钟-约45分钟,优选10-20分钟的时间内,将可注射的抗体溶液给药进入静脉、动脉、脑脊液中。在某些情况下,真皮内和腔内给药对限制于封闭区域如皮肤的特定部位和/或特定的体腔的肿瘤是有利的。此外,鞘内给药可以用于位于脑部的肿瘤。
与靶向剂结合的本发明化合物的治疗有效量取决于患者个体、疾病类型、疾病状况、给药方法和其它临床变量。使用得自动物模型的数据可以容易地确定有效剂量。在转换为临床环境之前,频繁使用患有实体瘤的实验动物可以优化适合的治疗剂量。在判定有效的抗癌策略中,了解这类模型是非常可靠的。例如,带有实体瘤的小鼠已广泛用于临床前试验,用以确定治疗剂产生有益的抗肿瘤作用而毒性最小的应用范围。
本领域技术人员应该认识到,所述式(I)或(II)化合物在其结构中可具有一个或多个不对称碳原子。打算将所述化合物的立体化学纯的同分异构形式及其外消旋体均包括在本发明范围内。立体化学纯的同分异构形式可以通过应用本领域已知的原理获得。非对映异构体可以通过物理分离方法(如分级结晶和层析技术)分离,而对映体可以通过与光学活性酸或碱所成的非对映体盐进行选择性结晶或通过层析法彼此分离。纯立体异构体也可以由适当的立体化学纯的起始原料经合成制备或通过使用立体选择性反应制备。
本发明的某些化合物可具有反式和顺式异构体。此外,当采用制备本发明化合物的方法得到立体异构体的混合物时,这些异构体可以通过常规技术如制备型层析分离。可将所述化合物制备成为单一的立体异构体或者作为一些可能的立体异构体的混合物的外消旋形式。所述非外消旋形式可以通过合成或拆分得到。例如,所述化合物可通过标准技术,如通过形成非对映体对的盐而拆分成其组分对映体。所述化合物也可以通过共价键连接的手性辅料拆分,接着经层析分离和/或结晶分离,随后除去辅料来完成。作为选择,所述化合物可以采用手性层析来拆分。本发明的范围打算覆盖所有此类异构体或立体异构体本身,以及顺式和反式异构体的混合物,非对映体的混合物和对映体(光学异构体)的外消旋混合物。
尽管以上说明书用以说明目的提供的实施例的方式说明了本发明的原理,然而,应当理解:本发明的实施包括在以下说明书及其同等内容范围内常见的改变、调整和/或修正。
Claims (28)
1.一种具有式(II-AA)的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐:
其中:
R100选自:H和烷基;
RB和RC独立选自:烷氧基;及
R5选自:烷氧基和卤素。
2.一种权利要求1的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐,其中R100选自:H、甲基、乙基;RB和RC独立选自:甲氧基和乙氧基;及R5选自:甲氧基、乙氧基、异丙氧基、氯代基、溴代基和氟代基。
4.一种权利要求3的化合物或其光学异构体、对映体、非对映体、外消旋体或其药学上可接受的盐,其中R100选自:H、甲基、乙基;RB选自:甲氧基和乙氧基;及R5选自:甲氧基、乙氧基、异丙氧基、氯代基、溴代基和氟代基。
15.一种药用组合物,它包括药学上可接受的载体和权利要求1-14任一项的化合物。
16.权利要求1-14任一项的化合物在制备用于治疗有此需要的患者中与PDGF受体有关的疾病或细胞增殖性疾病的药物中的应用。
17.权利要求16的应用,其中所述细胞增殖性疾病是一种瘤形成疾病。
18.权利要求17的应用,其中所述瘤形成疾病是一种选自以下的癌症:神经胶质瘤、肺癌、乳腺癌、结肠直肠癌、前列腺癌、胃癌、食管癌、结肠癌、胰腺癌、卵巢癌、黑素瘤、骨髓增生异常、多发性骨髓瘤、淋巴瘤和白血病。
19.权利要求18的应用,其中所述白血病选自慢性骨髓性白血病(CML);急性淋巴细胞白血病(ALL);慢性嗜中性白血病(CNL);急性未分化性白血病(AUL);及急性骨髓性白血病(AML)。
20.权利要求16的应用,其中所述细胞增殖性疾病不是瘤形成疾病。
21.权利要求20的应用,其中所述细胞增殖性疾病选自动脉粥样硬化、移植-诱导的血管疾病、新生内膜形成、肺纤维化、黄斑变性、再狭窄、肺的纤维变性、肾小球性肾炎、肾小球硬化症、先天性多囊性肾发育不良、肾纤维化、糖尿病性视网膜病和类风湿性关节炎。
22.权利要求16的应用,其中所述药物通过从管腔内医疗装置释放来控制传递。
23.权利要求22的应用,其中所述细胞增殖性疾病或与PDGF-R有关的疾病为血管壁的再狭窄、内膜增生、动脉粥样硬化或炎症。
24.权利要求1-14任一项的化合物在制备用于在细胞中减弱或抑制PDGF-R激酶活性的药物中的应用。
25.权利要求1-14任一项的化合物在制备用于在患者中减弱或抑制PDGF-R激酶活性的药物中的应用。
26.权利要求1-14任一项的化合物在制备用于在细胞中减弱或抑制c-Abl激酶活性的药物中的应用。
27.权利要求1-14任一项的化合物在制备用于在患者中减弱或抑制c-Abl激酶活性的药物中的应用。
28.权利要求1-14任一项的化合物在制备用于在细胞中抑制细胞增殖的药物中的应用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US38073502P | 2002-05-15 | 2002-05-15 | |
| US60/380,735 | 2002-05-15 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1668601A CN1668601A (zh) | 2005-09-14 |
| CN100396670C true CN100396670C (zh) | 2008-06-25 |
Family
ID=29550005
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB038164884A Expired - Fee Related CN100396670C (zh) | 2002-05-15 | 2003-05-13 | 作为pdfg受体抑制剂的n-取代的3-氨基苯并环戊二烯并吡唑及药用组合物和用途 |
Country Status (29)
| Country | Link |
|---|---|
| US (2) | US7196110B2 (zh) |
| EP (1) | EP1506175B1 (zh) |
| JP (1) | JP2006502097A (zh) |
| KR (1) | KR20040106554A (zh) |
| CN (1) | CN100396670C (zh) |
| AR (1) | AR040079A1 (zh) |
| AT (1) | ATE427301T1 (zh) |
| AU (1) | AU2003234567A1 (zh) |
| BR (1) | BRPI0311179A2 (zh) |
| CA (1) | CA2486097A1 (zh) |
| CR (1) | CR7574A (zh) |
| DE (1) | DE60326950D1 (zh) |
| EA (1) | EA008770B1 (zh) |
| ES (1) | ES2323952T3 (zh) |
| HR (1) | HRP20041188A2 (zh) |
| IL (1) | IL165197A0 (zh) |
| MX (1) | MXPA04011320A (zh) |
| MY (1) | MY138268A (zh) |
| NO (1) | NO20045451L (zh) |
| NZ (1) | NZ548796A (zh) |
| PE (1) | PE20040758A1 (zh) |
| PL (1) | PL374062A1 (zh) |
| RS (1) | RS98804A (zh) |
| SA (1) | SA03240431A (zh) |
| TW (1) | TW200407311A (zh) |
| UA (1) | UA80820C2 (zh) |
| UY (1) | UY27811A1 (zh) |
| WO (1) | WO2003097609A1 (zh) |
| ZA (1) | ZA200410108B (zh) |
Families Citing this family (51)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN100396670C (zh) * | 2002-05-15 | 2008-06-25 | 詹森药业有限公司 | 作为pdfg受体抑制剂的n-取代的3-氨基苯并环戊二烯并吡唑及药用组合物和用途 |
| JP2007511514A (ja) * | 2003-11-13 | 2007-05-10 | ジヤンセン・フアーマシユーチカ・ナームローゼ・フエンノートシヤツプ | 生体分子標的同定用の固定化n置換三環状3−アミノピラゾール |
| AU2005204428A1 (en) * | 2004-01-07 | 2005-07-28 | Ambit Biosciences Corporation | Conjugated small molecules |
| ES2415665T3 (es) * | 2004-06-21 | 2013-07-26 | Proteome Sciences Plc | Procedimientos de cribado usando c-abl, fyn y sky en combinación con la proteína tau |
| CN101022803B (zh) * | 2004-07-09 | 2011-11-23 | 药物合成技术公司 | 治疗化合物和治疗 |
| EP2402323A3 (en) | 2004-10-13 | 2012-05-30 | PTC Therapeutics, Inc. | Pyrazole or triazole compounds and their use for the manufacture of a medicament for treating somatic mutation-related diseases |
| JP2006321724A (ja) * | 2005-05-17 | 2006-11-30 | Tokyo Univ Of Science | 抗腫瘍剤 |
| EP2037954A4 (en) * | 2006-06-20 | 2011-09-14 | Janssen Pharmaceutica Nv | METHOD FOR MODULATING PHARMACOKINETICS AND METABOLISM OF THERAPEUTIC USE |
| US20080031866A1 (en) * | 2006-06-20 | 2008-02-07 | Eichenbaum Gary M | Method for modulating the pharmacokinetics and metabolism of a therapeutic agent |
| EP2128138A1 (en) | 2007-01-29 | 2009-12-02 | Takeda Pharmaceutical Company Limited | Pyrazole compound |
| WO2008094896A1 (en) * | 2007-01-31 | 2008-08-07 | Janssen Pharmaceutica, N.V. | N-substituted tricyclic 3-aminopyrazoles as anti-mitotic tubulin polymerization inhibitors |
| US9220837B2 (en) | 2007-03-19 | 2015-12-29 | Insuline Medical Ltd. | Method and device for drug delivery |
| MX2009010000A (es) | 2007-03-19 | 2010-03-17 | Insuline Medical Ltd | Dispositivo para el suministro de farmaco. |
| US8622991B2 (en) | 2007-03-19 | 2014-01-07 | Insuline Medical Ltd. | Method and device for drug delivery |
| EP2231229A1 (en) | 2007-12-18 | 2010-09-29 | Insuline Medical Ltd. | Drug delivery device with sensor for closed-loop operation |
| KR20110086132A (ko) | 2008-11-07 | 2011-07-27 | 인슐린 메디컬 엘티디 | 약물 전달 장치 및 방법 |
| MX336881B (es) * | 2009-10-29 | 2016-02-04 | Bristol Myers Squibb Co | Compuestos heterociclicos triciclicos. |
| US8754114B2 (en) | 2010-12-22 | 2014-06-17 | Incyte Corporation | Substituted imidazopyridazines and benzimidazoles as inhibitors of FGFR3 |
| JPWO2012121168A1 (ja) * | 2011-03-04 | 2014-07-17 | 国立大学法人京都大学 | キナーゼ阻害剤 |
| TWI553010B (zh) * | 2012-04-12 | 2016-10-11 | 財團法人生物技術開發中心 | 雜環吡唑化合物,其製備方法及用途 |
| DK3176170T3 (en) | 2012-06-13 | 2019-01-28 | Incyte Holdings Corp | SUBSTITUTED TRICYCLIC RELATIONS AS FGFR INHIBITORS |
| US9388185B2 (en) | 2012-08-10 | 2016-07-12 | Incyte Holdings Corporation | Substituted pyrrolo[2,3-b]pyrazines as FGFR inhibitors |
| WO2014039831A1 (en) | 2012-09-07 | 2014-03-13 | Takeda Pharmaceutical Company Limited | SUBSTITUTED-1,4-DIHYDROPYRAZOLO[4,3-b]INDOLES |
| US9266892B2 (en) | 2012-12-19 | 2016-02-23 | Incyte Holdings Corporation | Fused pyrazoles as FGFR inhibitors |
| AU2014241079C1 (en) * | 2013-03-14 | 2017-07-06 | Newlink Genetics Corporation | Tricyclic compounds as inhibitors of immunosuppression mediated by tryptophan metabolization |
| CA3130452C (en) | 2013-04-19 | 2023-10-31 | Incyte Holdings Corporation | Bicyclic heterocycles as fgfr inhibitors |
| US10851105B2 (en) | 2014-10-22 | 2020-12-01 | Incyte Corporation | Bicyclic heterocycles as FGFR4 inhibitors |
| CN105884828A (zh) * | 2015-02-16 | 2016-08-24 | 上海迪诺医药科技有限公司 | 多环化合物、其药物组合物及应用 |
| MA41551A (fr) | 2015-02-20 | 2017-12-26 | Incyte Corp | Hétérocycles bicycliques utilisés en tant qu'inhibiteurs de fgfr4 |
| US9580423B2 (en) | 2015-02-20 | 2017-02-28 | Incyte Corporation | Bicyclic heterocycles as FGFR4 inhibitors |
| MX373169B (es) | 2015-02-20 | 2020-04-24 | Incyte Holdings Corp | Heterociclos bicíclicos como inhibidores de receptores del factor de crecimiento fibroblástico (fgfr). |
| US10633354B2 (en) | 2016-09-02 | 2020-04-28 | Bristol-Myers Squibb Company | Substituted tricyclic heterocyclic compounds |
| AR111960A1 (es) | 2017-05-26 | 2019-09-04 | Incyte Corp | Formas cristalinas de un inhibidor de fgfr y procesos para su preparación |
| US11046646B2 (en) | 2017-08-09 | 2021-06-29 | Bristol-Myers Squibb Company | Alkylphenyl compounds |
| WO2019032631A1 (en) | 2017-08-09 | 2019-02-14 | Bristol-Myers Squibb Company | OXIME ETHER COMPOUNDS |
| CN112867716B (zh) | 2018-05-04 | 2024-09-13 | 因赛特公司 | Fgfr抑制剂的固体形式和其制备方法 |
| AU2019262579B2 (en) | 2018-05-04 | 2024-09-12 | Incyte Corporation | Salts of an FGFR inhibitor |
| US11628162B2 (en) | 2019-03-08 | 2023-04-18 | Incyte Corporation | Methods of treating cancer with an FGFR inhibitor |
| WO2021007269A1 (en) | 2019-07-09 | 2021-01-14 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| TWI759829B (zh) | 2019-08-23 | 2022-04-01 | 財團法人生物技術開發中心 | 作為第iii型受體酪胺酸激酶抑制劑之雜環吡唑衍生物 |
| US12122767B2 (en) | 2019-10-01 | 2024-10-22 | Incyte Corporation | Bicyclic heterocycles as FGFR inhibitors |
| PH12022550892A1 (en) | 2019-10-14 | 2023-05-03 | Incyte Corp | Bicyclic heterocycles as fgfr inhibitors |
| US11566028B2 (en) | 2019-10-16 | 2023-01-31 | Incyte Corporation | Bicyclic heterocycles as FGFR inhibitors |
| CA3162010A1 (en) | 2019-12-04 | 2021-06-10 | Incyte Corporation | Derivatives of an fgfr inhibitor |
| CA3163875A1 (en) | 2019-12-04 | 2021-06-10 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| WO2021146424A1 (en) | 2020-01-15 | 2021-07-22 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| JP2024513575A (ja) | 2021-04-12 | 2024-03-26 | インサイト・コーポレイション | Fgfr阻害剤及びネクチン-4標的化剤を含む併用療法 |
| AR126102A1 (es) | 2021-06-09 | 2023-09-13 | Incyte Corp | Heterociclos tricíclicos como inhibidores de fgfr |
| EP4430047A1 (en) | 2021-11-08 | 2024-09-18 | Progentos Therapeutics, Inc. | Platelet-derived growth factor receptor (pdgfr) alpha inhibitors and uses thereof |
| CN114890987B (zh) * | 2022-04-13 | 2023-12-19 | 万华化学集团股份有限公司 | 一种硫酚-噻吩配体及其制备方法、烯烃聚合催化剂及其制备方法、应用 |
| CN114686427B (zh) * | 2022-05-23 | 2022-07-29 | 中国人民解放军总医院第一医学中心 | 一种脾脏调节型b淋巴细胞及其制备方法与应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999017769A1 (en) * | 1997-10-06 | 1999-04-15 | Basf Aktiengesellschaft | INDENO[1,2-c]-, NAPHTHO[1,2-c]- AND BENZO[6,7]CYCLOHEPTA[1,2-c]PYRAZOLE DERIVATIVES |
| WO2000059901A1 (en) * | 1999-04-06 | 2000-10-12 | Knoll Gesellschaft Mit Beschraenkter Haftung | Substituted 1,4-dihydroindeno[1,2-c]pyrazoles as inhibitors of tyrosine kinase |
| WO2001079198A1 (en) * | 2000-04-18 | 2001-10-25 | Agouron Pharmaceuticals, Inc. | Pyrazoles for inhibiting protein kinase |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3928378A (en) | 1974-01-30 | 1975-12-23 | Hoechst Co American | Fused bicyclic aminopyrazoles |
| US4220776A (en) | 1978-12-21 | 1980-09-02 | E. I. Du Pont De Nemours And Company | N-(Pyridothienopyrazol)amides |
| US4140785A (en) | 1978-05-08 | 1979-02-20 | E. I. Du Pont De Nemours And Company | N-(benzothienopyrazol)amide antirhinoviral agents |
| US4420476A (en) | 1982-05-24 | 1983-12-13 | Averst McKenna & Harrison, Inc. | Benzofuro[3,2-c]pyrazol-3-amine derivatives |
| ES2108120T3 (es) | 1991-05-10 | 1997-12-16 | Rhone Poulenc Rorer Int | Compuestos bis arilicos y heteroarilicos mono- y biciclicos que inhiben tirosina quinasa receptora de egf y/o pdgf. |
| CA2452130A1 (en) | 1992-03-05 | 1993-09-16 | Francis J. Burrows | Methods and compositions for targeting the vasculature of solid tumors |
| US5474765A (en) | 1992-03-23 | 1995-12-12 | Ut Sw Medical Ctr At Dallas | Preparation and use of steroid-polyanionic polymer-based conjugates targeted to vascular endothelial cells |
| JPH0622109A (ja) | 1992-07-03 | 1994-01-28 | Fujitsu Ltd | ファクシミリ装置およびファクシミリ情報サービス方式 |
| JPH06100561A (ja) | 1992-07-13 | 1994-04-12 | Otsuka Pharmaceut Factory Inc | ナフチリジン及びピリドピラジン誘導体 |
| JP2997828B2 (ja) | 1992-07-30 | 2000-01-11 | 株式会社大塚製薬工場 | キノリン及びナフチリジン誘導体 |
| JP3148960B2 (ja) | 1993-04-12 | 2001-03-26 | コニカ株式会社 | 写真用シアンカプラー |
| ATE174591T1 (de) | 1993-09-15 | 1999-01-15 | Merck Sharp & Dohme | Kondensierte tricyclische heteroaromatische derivate als liganden des dopamin-rezeptor- subtyps |
| US5364881A (en) | 1993-11-15 | 1994-11-15 | The Medical College Of Wisconsin Research Foundation, Inc. | S-alkyl-isothioureido-amino acids and use thereof |
| JP3245765B2 (ja) | 1994-07-05 | 2002-01-15 | コニカ株式会社 | 写真用シアンカプラー |
| US5476932A (en) | 1994-08-26 | 1995-12-19 | Hoffmann-La Roche Inc. | Process for producing N4-acyl-5'-deoxy-5-fluorocytidine derivatives |
| US5476851A (en) | 1994-09-08 | 1995-12-19 | Rhone-Poulenc Rorer Pharmaceuticals, Inc. | Pyrazolo[3,4-g]quinoxaline compounds which inhibit PDGF receptor protein tyrosine kinase |
| US5563173A (en) | 1994-12-22 | 1996-10-08 | Research Development Foundation | Anti-proliferative effects of sodium butyrate |
| DE69623455T2 (de) | 1995-04-19 | 2003-01-16 | Schneider (Usa) Inc., Plymouth | Beschichteter dilatator zur abgabe eines arzneistoffs |
| JP2001518502A (ja) | 1997-10-06 | 2001-10-16 | ビーエーエスエフ アクチェンゲゼルシャフト | チロシンキナーゼ活性を阻害するためのインデノ[1,2−c]ピラゾール誘導体 |
| JP4194678B2 (ja) | 1997-11-28 | 2008-12-10 | キリンファーマ株式会社 | キノリン誘導体およびそれを含む医薬組成物 |
| US5932580A (en) | 1997-12-01 | 1999-08-03 | Yissum Research And Development Company Of The Hebrew University Of Jerusalem | PDGF receptor kinase inhibitory compounds their preparation and compositions |
| IL138079A0 (en) | 1998-04-21 | 2001-10-31 | Du Pont Pharm Co | 5-aminoindeno (1,2-c) pyrazol-4-ones as anti-cancer and anti-proliferative agents |
| ES2281186T3 (es) | 1998-08-07 | 2007-09-16 | Novartis Vaccines And Diagnostics, Inc. | Pirazoles como moduladores de receptores de estrogenos. |
| ATE269357T1 (de) | 1999-04-28 | 2004-07-15 | Univ Texas | Zusammensetzungen und verfahren zur krebsbehandlung durch die selektive hemmung von vegf |
| US6824987B1 (en) * | 1999-05-11 | 2004-11-30 | President And Fellows Of Harvard College | Small molecule printing |
| US6776796B2 (en) | 2000-05-12 | 2004-08-17 | Cordis Corportation | Antiinflammatory drug and delivery device |
| NZ524475A (en) | 2000-08-10 | 2004-11-26 | Pharmacia Italia S | Bicyclo-pyrazoles active as kinase inhibitors, process for their preparation and pharmaceutical compositions comprising them |
| CN100396670C (zh) * | 2002-05-15 | 2008-06-25 | 詹森药业有限公司 | 作为pdfg受体抑制剂的n-取代的3-氨基苯并环戊二烯并吡唑及药用组合物和用途 |
-
2003
- 2003-05-13 CN CNB038164884A patent/CN100396670C/zh not_active Expired - Fee Related
- 2003-05-13 KR KR10-2004-7018454A patent/KR20040106554A/ko not_active Application Discontinuation
- 2003-05-13 DE DE60326950T patent/DE60326950D1/de not_active Expired - Fee Related
- 2003-05-13 MY MYPI20031800A patent/MY138268A/en unknown
- 2003-05-13 JP JP2004505342A patent/JP2006502097A/ja not_active Withdrawn
- 2003-05-13 NZ NZ548796A patent/NZ548796A/en unknown
- 2003-05-13 EP EP03728909A patent/EP1506175B1/en not_active Expired - Lifetime
- 2003-05-13 MX MXPA04011320A patent/MXPA04011320A/es active IP Right Grant
- 2003-05-13 CA CA002486097A patent/CA2486097A1/en not_active Abandoned
- 2003-05-13 PL PL03374062A patent/PL374062A1/xx not_active Application Discontinuation
- 2003-05-13 UA UA20041109391A patent/UA80820C2/uk unknown
- 2003-05-13 AU AU2003234567A patent/AU2003234567A1/en not_active Abandoned
- 2003-05-13 ES ES03728909T patent/ES2323952T3/es not_active Expired - Lifetime
- 2003-05-13 EA EA200401378A patent/EA008770B1/ru not_active IP Right Cessation
- 2003-05-13 WO PCT/US2003/015193 patent/WO2003097609A1/en active Application Filing
- 2003-05-13 RS YU98804A patent/RS98804A/sr unknown
- 2003-05-13 AT AT03728909T patent/ATE427301T1/de not_active IP Right Cessation
- 2003-05-13 BR BRPI0311179A patent/BRPI0311179A2/pt not_active IP Right Cessation
- 2003-05-14 US US10/438,152 patent/US7196110B2/en not_active Expired - Lifetime
- 2003-05-14 TW TW092113012A patent/TW200407311A/zh unknown
- 2003-05-15 UY UY27811A patent/UY27811A1/es not_active Application Discontinuation
- 2003-05-15 PE PE2003000466A patent/PE20040758A1/es not_active Application Discontinuation
- 2003-05-15 AR ARP030101696A patent/AR040079A1/es not_active Application Discontinuation
- 2003-12-07 SA SA03240431A patent/SA03240431A/ar unknown
-
2004
- 2004-11-14 IL IL16519704A patent/IL165197A0/xx unknown
- 2004-11-15 CR CR7574A patent/CR7574A/es not_active Application Discontinuation
- 2004-12-14 NO NO20045451A patent/NO20045451L/no unknown
- 2004-12-14 HR HR20041188A patent/HRP20041188A2/xx not_active Application Discontinuation
- 2004-12-14 ZA ZA200410108A patent/ZA200410108B/en unknown
-
2007
- 2007-01-25 US US11/657,912 patent/US7795440B2/en not_active Expired - Lifetime
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999017769A1 (en) * | 1997-10-06 | 1999-04-15 | Basf Aktiengesellschaft | INDENO[1,2-c]-, NAPHTHO[1,2-c]- AND BENZO[6,7]CYCLOHEPTA[1,2-c]PYRAZOLE DERIVATIVES |
| WO2000059901A1 (en) * | 1999-04-06 | 2000-10-12 | Knoll Gesellschaft Mit Beschraenkter Haftung | Substituted 1,4-dihydroindeno[1,2-c]pyrazoles as inhibitors of tyrosine kinase |
| WO2001079198A1 (en) * | 2000-04-18 | 2001-10-25 | Agouron Pharmaceuticals, Inc. | Pyrazoles for inhibiting protein kinase |
Also Published As
| Publication number | Publication date |
|---|---|
| NO20045451L (no) | 2005-02-09 |
| US20070142305A1 (en) | 2007-06-21 |
| PE20040758A1 (es) | 2005-01-01 |
| NZ548796A (en) | 2008-01-31 |
| WO2003097609A1 (en) | 2003-11-27 |
| EA200401378A1 (ru) | 2005-06-30 |
| IL165197A0 (en) | 2005-12-18 |
| CR7574A (es) | 2008-09-10 |
| US20040082639A1 (en) | 2004-04-29 |
| SA03240431A (ar) | 2005-12-03 |
| MXPA04011320A (es) | 2005-08-16 |
| ES2323952T3 (es) | 2009-07-28 |
| TW200407311A (en) | 2004-05-16 |
| CN1668601A (zh) | 2005-09-14 |
| AU2003234567A1 (en) | 2003-12-02 |
| CA2486097A1 (en) | 2003-11-27 |
| JP2006502097A (ja) | 2006-01-19 |
| DE60326950D1 (de) | 2009-05-14 |
| RS98804A (en) | 2006-10-27 |
| UA80820C2 (en) | 2007-11-12 |
| EP1506175A1 (en) | 2005-02-16 |
| EA008770B1 (ru) | 2007-08-31 |
| MY138268A (en) | 2009-05-29 |
| US7196110B2 (en) | 2007-03-27 |
| KR20040106554A (ko) | 2004-12-17 |
| AR040079A1 (es) | 2005-03-16 |
| PL374062A1 (en) | 2005-09-19 |
| BRPI0311179A2 (pt) | 2016-06-21 |
| ZA200410108B (en) | 2006-05-31 |
| US7795440B2 (en) | 2010-09-14 |
| EP1506175B1 (en) | 2009-04-01 |
| UY27811A1 (es) | 2003-10-31 |
| HRP20041188A2 (en) | 2007-03-31 |
| ATE427301T1 (de) | 2009-04-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN100396670C (zh) | 作为pdfg受体抑制剂的n-取代的3-氨基苯并环戊二烯并吡唑及药用组合物和用途 | |
| CN102399233B (zh) | PI3K和mTOR双重抑制剂类化合物 | |
| CN102686591B (zh) | 酞嗪酮类衍生物、其制备方法及其在医药上的应用 | |
| JP4845736B2 (ja) | プロテインキナーゼ阻害剤 | |
| KR101483215B1 (ko) | 단백질 키나아제 저해활성을 갖는 비시클릭 헤테로아릴 유도체 | |
| KR101099161B1 (ko) | 항암제로서 유용한 트라이아졸로피라진 유도체 | |
| CN103119035B (zh) | 杂环化合物和它们作为糖原合成酶激酶-3抑制剂的用途 | |
| CN109890822A (zh) | 细胞代谢过程的抑制剂 | |
| EP2581371B1 (en) | Pyrrolyl substituted dihydroindol-2-one derivatives, preparation methods and uses thereof | |
| CN103958497A (zh) | 作为AXL和c-MET激酶抑制剂的尿嘧啶衍生物 | |
| CN105037333A (zh) | 新的喹唑啉衍生物 | |
| CN101155807A (zh) | 具有tie2(tek)抑制活性的化合物 | |
| HUE030390T2 (en) | Triazolopyridazines as tyrosine kinase modulators | |
| CN103420977A (zh) | 具有抗肿瘤活性的乙炔衍生物 | |
| CN103974955A (zh) | 嘧啶并-哒嗪酮化合物及其用途 | |
| WO2008055233A1 (en) | Protein kinase inhibitors | |
| KR102169940B1 (ko) | 암, 바이러스성 감염 및 폐질환의 치료를 위한 인돌의 새로운 유도체 | |
| CN107151233B (zh) | 含腙的嘧啶类衍生物及其用途 | |
| CN101198602A (zh) | 具有tie2抑制活性的氨基嘧啶衍生物 | |
| CN101500562B (zh) | 噻吩并[3,2-c]吡啶-7-羧酸衍生物 | |
| Mohammadian et al. | Thienopyrimidine‐based agents bearing diphenylurea: Design, synthesis, and evaluation of antiproliferative and antiangiogenic activity | |
| CN105461708A (zh) | 喹唑啉类酪氨酸激酶抑制剂及其制备和应用 | |
| CN102002044A (zh) | 嘌呤-8-酮类及噻唑并嘧啶类衍生物及其制备方法和医药用途 | |
| TWI548637B (zh) | 酞嗪酮類衍生物、其製備方法及其在醫藥上的應用 | |
| KR20250030448A (ko) | Pi3k 억제제로서의 벤조피리미딘-4(3h)-온 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20080625 Termination date: 20100513 |