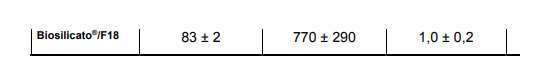BR102020017697A2 - Process of preparation of bone grafts and bone grafts obtained - Google Patents
Process of preparation of bone grafts and bone grafts obtained Download PDFInfo
- Publication number
- BR102020017697A2 BR102020017697A2 BR102020017697-8A BR102020017697A BR102020017697A2 BR 102020017697 A2 BR102020017697 A2 BR 102020017697A2 BR 102020017697 A BR102020017697 A BR 102020017697A BR 102020017697 A2 BR102020017697 A2 BR 102020017697A2
- Authority
- BR
- Brazil
- Prior art keywords
- bone
- biosilicate
- scaffold
- bioglass
- bone graft
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/02—Inorganic materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/12—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/18—Materials at least partially X-ray or laser opaque
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/28—Bones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2430/00—Materials or treatment for tissue regeneration
- A61L2430/02—Materials or treatment for tissue regeneration for reconstruction of bones; weight-bearing implants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/02—Inorganic materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/02—Inorganic materials
- A61L27/10—Ceramics or glasses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/56—Porous materials, e.g. foams or sponges
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B29—WORKING OF PLASTICS; WORKING OF SUBSTANCES IN A PLASTIC STATE IN GENERAL
- B29C—SHAPING OR JOINING OF PLASTICS; SHAPING OF MATERIAL IN A PLASTIC STATE, NOT OTHERWISE PROVIDED FOR; AFTER-TREATMENT OF THE SHAPED PRODUCTS, e.g. REPAIRING
- B29C67/00—Shaping techniques not covered by groups B29C39/00 - B29C65/00, B29C70/00 or B29C73/00
- B29C67/02—Moulding by agglomerating
- B29C67/04—Sintering
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C12/00—Powdered glass; Bead compositions
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C3/00—Glass compositions
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C4/00—Compositions for glass with special properties
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B35/00—Shaped ceramic products characterised by their composition; Ceramics compositions; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products
- C04B35/01—Shaped ceramic products characterised by their composition; Ceramics compositions; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products based on oxide ceramics
- C04B35/14—Shaped ceramic products characterised by their composition; Ceramics compositions; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products based on oxide ceramics based on silica
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B35/00—Shaped ceramic products characterised by their composition; Ceramics compositions; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products
- C04B35/01—Shaped ceramic products characterised by their composition; Ceramics compositions; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products based on oxide ceramics
- C04B35/16—Shaped ceramic products characterised by their composition; Ceramics compositions; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products based on oxide ceramics based on silicates other than clay
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B35/00—Shaped ceramic products characterised by their composition; Ceramics compositions; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products
- C04B35/622—Forming processes; Processing powders of inorganic compounds preparatory to the manufacturing of ceramic products
- C04B35/626—Preparing or treating the powders individually or as batches ; preparing or treating macroscopic reinforcing agents for ceramic products, e.g. fibres; mechanical aspects section B
- C04B35/63—Preparing or treating the powders individually or as batches ; preparing or treating macroscopic reinforcing agents for ceramic products, e.g. fibres; mechanical aspects section B using additives specially adapted for forming the products, e.g.. binder binders
- C04B35/632—Organic additives
- C04B35/634—Polymers
- C04B35/63404—Polymers obtained by reactions only involving carbon-to-carbon unsaturated bonds
- C04B35/63416—Polyvinylalcohols [PVA]; Polyvinylacetates
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B38/00—Porous mortars, concrete, artificial stone or ceramic ware; Preparation thereof
- C04B38/06—Porous mortars, concrete, artificial stone or ceramic ware; Preparation thereof by burning-out added substances by burning natural expanding materials or by sublimating or melting out added substances
- C04B38/0615—Porous mortars, concrete, artificial stone or ceramic ware; Preparation thereof by burning-out added substances by burning natural expanding materials or by sublimating or melting out added substances the burned-out substance being a monolitic element having approximately the same dimensions as the final article, e.g. a porous polyurethane sheet or a prepreg obtained by bonding together resin particles
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Ceramic Engineering (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Vascular Medicine (AREA)
- Heart & Thoracic Surgery (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Surgery (AREA)
- Structural Engineering (AREA)
- Manufacturing & Machinery (AREA)
- Inorganic Chemistry (AREA)
- Dermatology (AREA)
- Geochemistry & Mineralogy (AREA)
- General Chemical & Material Sciences (AREA)
- Cardiology (AREA)
- Biomedical Technology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Composite Materials (AREA)
- Dispersion Chemistry (AREA)
- Polymers & Plastics (AREA)
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Mechanical Engineering (AREA)
- Prostheses (AREA)
- Materials For Medical Uses (AREA)
Abstract
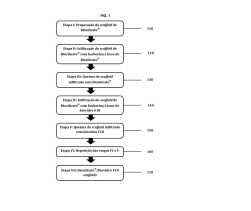
É descrito um processo de preparação de enxertos ósseos a partir da preparação de um Biosilicato® em (110), em (120) infiltrar barbotina de Biosilicato® no Biosilicato® de (110), em (130) queimar o Biosilicato® infiltrado de (120), em (140) infiltrar o Biosilicato® queimado de (130) com Biovidro F18, em (150) queimar o produto de (140), em (160) repetir a infiltração com Biovidro F18 de (140) e a queima de (150), e em (170) recuperar o produto Biosilicato®/Biovidro F18 com resistência aperfeiçoada à compressão. Os enxertos ósseos obtidos apresentam porosidade desde 83,0 ± 2%, tamanho médio de célula de 770 ± 290 μm e resistência à compressão de 1,0 ± 0,2MPa a porosidade 82,0 ± 1,3%, tamanho médio de célula de 525 ± 220 μm e resistência à compressão de 3,3 ± 0,3 MPa conforme forem preparados respectivamente a partir de espumas de PU com 35 ppi ou 45 ppi. Os enxertos ósseos obtidos são usados como substituintes do osso trabecular e proporcionam integridade mecânica consistente e porosidade para regeneração de tecidos ósseos funcionais. A process for preparing bone grafts is described from the preparation of a Biosilicate® in (110), in (120) infiltrating Biosilicate® slip into the Biosilicate® of (110), in (130) burning the infiltrated Biosilicate® from ( 120), in (140) infiltrate the Biosilicate® burnt from (130) with Bioglass F18, in (150) burn the product from (140), in (160) repeat the infiltration with Bioglass F18 of (140) and the firing of (150), and in (170) recover the Biosilicate®/Bioglass F18 product with improved compressive strength. The bone grafts obtained showed porosity from 83.0 ± 2%, average cell size of 770 ± 290 μm and compressive strength of 1.0 ± 0.2MPa at porosity of 82.0 ± 1.3%, average cell size of 525 ± 220 μm and compressive strength of 3.3 ± 0.3 MPa as prepared from 35 ppi or 45 ppi PU foams respectively. The bone grafts obtained are used as replacements for trabecular bone and provide consistent mechanical integrity and porosity for regeneration of functional bone tissues.
Description
[001] A presente invenção pertence ao campo dos enxertos ósseos sintéticos bioativos, mais particularmente, a enxertos ósseos sintéticos com propriedades de resistência mecânica melhorada em relação a enxertos ósseos similares.[001] The present invention pertains to the field of bioactive synthetic bone grafts, more particularly, to synthetic bone grafts with improved mechanical strength properties over similar bone grafts.
[002] Os biomateriais sintéticos para enxerto ósseo podem ser classificados como biomateriais de primeira, segunda e terceira geração e suas diferenças dependem da força da resposta que o implante mostra quando exposto a fluidos corporais. Os biomateriais de primeira geração foram criados em 1960 e, desde então, são utilizados em milhares de implantes. Em geral, são metais e ligas (Ti, aço inoxidável) e cerâmicas densas ou porosas (alumina, zircônia). Uma de suas características é o fato de serem bioinertes devido à sua pouca ou nenhuma interação com os tecidos circundantes.[002] Synthetic biomaterials for bone grafting can be classified as first, second and third generation biomaterials and their differences depend on the strength of the response that the implant shows when exposed to body fluids. First-generation biomaterials were created in the 1960s and have since been used in thousands of implants. In general, these are metals and alloys (Ti, stainless steel) and dense or porous ceramics (alumina, zirconia). One of their characteristics is the fact that they are bioinert due to their little or no interaction with the surrounding tissues.
[003] Os biomateriais de segunda geração são classificados como materiais bioativos ou reabsorvíveis, tais como novas composições de cerâmicas, vidros e vitrocerâmicas.[003] Second generation biomaterials are classified as bioactive or resorbable materials, such as new compositions of ceramics, glasses and glass-ceramics.
[004] Um material bioativo é aquele que provoca uma resposta biológica específica na interface do material, o que resulta na formação de uma ligação entre os tecidos. Por exemplo, quando os biovidros interagem com o tecido e os fluidos corporais, formam rapidamente uma camada de hidroxicarbonatoapatita (HCA) na interface entre o material e o tecido, aumentando a adesão interfacial do implante. Esse mecanismo permite criar uma interface estável e duradoura que aumenta a interação celular e controla o crescimento dos tecidos maduros.[004] A bioactive material is one that provokes a specific biological response at the interface of the material, which results in the formation of a bond between tissues. For example, when bioglasses interact with tissue and body fluids, they rapidly form a layer of hydroxycarbonateapatite (HCA) at the interface between the material and the tissue, increasing the interfacial adhesion of the implant. This mechanism makes it possible to create a stable and lasting interface that increases cellular interaction and controls the growth of mature tissues.
[005] Em 1980, materiais bioativos, como vidros bioativos, cerâmicas, vitrocerâmicas e compósitos passaram a ter diferentes aplicações ortopédicas e odontológicas. Materiais reabsorvíveis como fosfatos de cálcio cristalinos ou amorfos em contato com os fluidos corporais são rapidamente dissolvidos, e os espaços vazios formados na estrutura são gradualmente reabastecidos com tecido vivo. Quando o material se dissolve, o implante começa a perder força mecânica, gerando uma interface instável, causando imobilização do paciente por um longo tempo. O enxerto ideal deve ter uma taxa de degradação sincronizada com a formação do novo tecido ósseo.[005] In 1980, bioactive materials such as bioactive glasses, ceramics, glass-ceramics and composites began to have different orthopedic and dental applications. Resorbable materials such as crystalline or amorphous calcium phosphates in contact with body fluids are rapidly dissolved, and the voids formed in the structure are gradually replenished with living tissue. When the material dissolves, the implant begins to lose mechanical strength, generating an unstable interface, causing the patient to be immobilized for a long time. The ideal graft should have a rate of degradation that is synchronized with the formation of new bone tissue.
[006] Apesar de os biomateriais de primeira e segunda geração constituírem soluções importantes para diversos problemas clínicos, para algumas aplicações esses implantes podem falhar, normalmente após 10 a 25 anos, sendo necessária uma intervenção cirúrgica. Muitos esforços econômicos e científicos foram realizados para melhorar o desempenho desses biomateriais sem resultados ideais.[006] Although the first and second generation biomaterials constitute important solutions to several clinical problems, for some applications these implants can fail, usually after 10 to 25 years, requiring surgical intervention. Many economic and scientific efforts have been made to improve the performance of these biomaterials without optimal results.
[007] Os tecidos biológicos são capazes de reagir a cargas dinâmicas ou estímulos bioquímicos; esse recurso está ausente nos biomateriais de primeira e segunda geração, restringindo sua vida útil. Como é necessário produzir um método que gere uma resposta mais biológica, surgiu o interesse no desenvolvimento de biomateriais de terceira geração, que promovem respostas celulares específicas no nível molecular. Esses tipos de biomateriais são caracterizados por possuírem bioatividade e serem absorvíveis, além de apresentarem melhores resultados clínicos.[007] Biological tissues are capable of reacting to dynamic loads or biochemical stimuli; this feature is absent in first and second generation biomaterials, restricting their useful life. As it is necessary to produce a method that generates a more biological response, interest has arisen in the development of third-generation biomaterials, which promote specific cellular responses at the molecular level. These types of biomaterials are characterized by having bioactivity and being absorbable, in addition to presenting better clinical results.
[008] Os Biovidros de terceira geração permitem a ativação de genes que estimulam a regeneração dos tecidos vivos, conservando a arquitetura e as propriedades mecânicas do osso lesionado. Sua osteocondução e osteoindução estão relacionadas à liberação de produtos de dissolução iônica durante o processo de degradação que gera respostas intracelulares e extracelulares na interface. Este processo está ligado à diferenciação e proliferação dos osteoblastos. Quando os osteoblastos humanos primários estão em contato com os produtos de dissolução iônica, sete famílias de genes são ativadas e reguladas, facilitando a formação do novo tecido ósseo. No entanto, apesar de sua alta bioatividade, os Biovidros apresentam baixa resistência mecânica, sendo necessário encontrar novos métodos que permitam um incremento desta.[008] Third-generation Bioglasses allow the activation of genes that stimulate the regeneration of living tissues, conserving the architecture and mechanical properties of the injured bone. Its osteoconduction and osteoinduction are related to the release of ionic dissolution products during the degradation process that generates intracellular and extracellular responses at the interface. This process is linked to the differentiation and proliferation of osteoblasts. When primary human osteoblasts are in contact with ionic dissolution products, seven gene families are activated and regulated, facilitating the formation of new bone tissue. However, despite their high bioactivity, Bioglasses have low mechanical strength, being necessary to find new methods that allow an increase in this.
[009] O principal objetivo da engenharia de tecidos é reparar, substituir, preservar ou aprimorar a função de um tecido ou órgão específico. O enxerto ósseo ou scaffold ideal para engenharia de tecidos deve funcionar como um modelo para o crescimento de tecidos em três dimensões, fornecendo uma rede macroporosa interconectada com uma distribuição de tamanho de poros apropriada, o que promove a vascularização, a entrega de nutrientes e a descarga de resíduos metabólicos. Sua interação com as células deve incentivar a adesão, proliferação, migração e função celular diferenciada, mas também evitar o tecido cicatricial. Idealmente, o enxerto ósseo ou scaffold deve ser degradável e reabsorvido na mesma taxa que a regeneração do tecido. Além disso, ele deve ser forte o suficiente para evitar o colapso da estrutura porosa e a perda da nova estrutura tecidual. Finalmente, o enxerto ósseo ou scaffold deve ser não tóxico para as células e ter uma área superficial alta.[009] The main objective of tissue engineering is to repair, replace, preserve or enhance the function of a specific tissue or organ. The ideal bone graft or scaffold for tissue engineering should function as a model for tissue growth in three dimensions, providing an interconnected macroporous network with an appropriate pore size distribution, which promotes vascularization, nutrient delivery and discharge of metabolic waste. Their interaction with cells should encourage adhesion, proliferation, migration and differentiated cell function, but also prevent scar tissue. Ideally, the bone graft or scaffold should be degradable and resorbable at the same rate as tissue regeneration. In addition, it must be strong enough to prevent the collapse of the porous structure and the loss of new tissue structure. Finally, the bone graft or scaffold must be non-toxic to cells and have a high surface area.
[0010] Os vidros bioativos podem ser classificados como derivados por fusão e derivados de sol-gel. Os vidros derivados de fusão são principalmente quaternários, como o Biovidro 45S5 (24,4-Na2O-26,9%CaO46,1SiO2-2,6P2O5, mol%). O Biovidro 45S5 pode ser fundido em várias formas ou tamanhos de pó e é encontrado comercialmente como Novabone (USA). Esses materiais têm aplicações diferentes na engenharia de tecidos, pois são capazes de suportar a vascularização in vivo e in vitro; estimular adesão, crescimento e diferenciação de osteoblastos; induzir diferenciação de células mesenquimais em osteoblastos; possuem a capacidade de unir tecidos moles e tecidos duros; e em contato com o fluido biológico gerar uma camada de HCA, a qual é capaz de produzir uma forte ligação entre os Biovidros e os ossos humanos. Além disso, seus produtos de dissolução iônica, como Si4+ , Ca2+ e fosfato, promovem a expressão de diferentes genes de células osteoblásticas e outras respostas biológicas. O mecanismo de osteoindução não é totalmente elucidado. No entanto, alguns estudos mostraram que durante a degradação do Biovidro os íons silício, cálcio e sódio são liberados juntamente com grupos fosfato, que estimulam a formação do tecido ósseo.[0010] Bioactive glasses can be classified as melt-derived and sol-gel derivatives. Fusion-derived glasses are mainly quaternary, such as Bioglass 45S5 (24.4-Na2O-26.9%CaO46.1SiO2-2.6P2O5, mol%). Bioglass 45S5 can be melted into various powder shapes or sizes and is commercially available as Novabone (USA). These materials have different applications in tissue engineering as they are able to support vascularization in vivo and in vitro; stimulate adhesion, growth and differentiation of osteoblasts; inducing differentiation of mesenchymal cells into osteoblasts; have the ability to unite soft and hard tissues; and in contact with the biological fluid generate a layer of HCA, which is capable of producing a strong bond between Bioglass and human bones. Furthermore, its ionic dissolution products, such as Si4+ , Ca2+ and phosphate, promote the expression of different osteoblast cell genes and other biological responses. The mechanism of osteoinduction is not fully elucidated. However, some studies have shown that during the degradation of Bioglass, silicon, calcium and sodium ions are released together with phosphate groups, which stimulate the formation of bone tissue.
[0011] Apesar da alta bioatividade dos Biovidros, suas fracas propriedades mecânicas dificultam sua aplicação clínica. Uma solução para aumentar sua resistência é induzir a cristalização nesses materiais, mas foi observado que esse processo pode gerar uma perda de bioatividade. O vidro bioativo mais conhecido é o 45S5, que foi sintetizado pela primeira vez por Larry Hench no final da década de 1960 e foi o primeiro material que mostrou capacidade de formar uma ligação interfacial com o tecido hospedeiro em ratos. Sua composição específica fornece características especiais, como o mais alto índice de bioatividade (IB= 12,5), biocompatibilidade e biodegradabilidade. Sendo classificado como um material bioativo de classe A por ser osteogênico e osteocondutor, ao interagir com o fluido corporal a superfície do Biovidro 45S5 forma uma camada de HCA, o que aumenta a atividade dos osteoblastos. Os produtos de dissolução iônica do Biovidro 45S5 podem regular positivamente a expressão gênica, que governa a osteogênese, a produção de fatores de crescimento e a angiogênese. Quando tubos de silicone foram cobertos com Biovidro 45S5, foi observado um incremento da neovascularização em comparação com tubos de silicone que não foram recobertos com vidro.[0011] Despite the high bioactivity of Bioglasses, their poor mechanical properties make their clinical application difficult. A solution to increase its resistance is to induce crystallization in these materials, but it was observed that this process can generate a loss of bioactivity. The best-known bioactive glass is 45S5, which was first synthesized by Larry Hench in the late 1960s and was the first material that showed the ability to form an interfacial bond with host tissue in mice. Its specific composition provides special characteristics, such as the highest index of bioactivity (IB= 12.5), biocompatibility and biodegradability. Being classified as a class A bioactive material for being osteogenic and osteoconductive, when interacting with the body fluid, the surface of Bioglass 45S5 forms a layer of HCA, which increases the activity of osteoblasts. The ionic dissolution products of Bioglass 45S5 can upregulate gene expression, which governs osteogenesis, growth factor production, and angiogenesis. When silicone tubes were coated with Bioglass 45S5, an increase in neovascularization was observed compared to silicone tubes that were not coated with glass.
[0012] A porosidade e o tamanho dos poros dos enxertos ósseos desempenham um papel notável na formação óssea in vitro e in vivo. Verificou-se que a osteogênese in vivo é afetada pelo tamanho dos poros. O tamanho dos poros afeta processos como vascularização, recrutamento e penetração celular. Poros abertos e altamente interconectados são muito importantes para o desempenho dos enxertos ósseos, pois garantem a migração e a proliferação de osteoblastos e células mesenquimais, bem como o crescimento de vasos sanguíneos, o que facilita o suprimento de nutrientes, o fornecimento de oxigênio às células e a remoção de resíduos metabólicos. Poros maiores que 300 µm promovem a vascularização e alta oxigenação, enquanto poros menores que 150 µm produzem oclusão dos poros das células, o que dificulta a penetração celular, a produção de matriz extracelular e a neovascularização das áreas internas dos enxertos ósseos. Sabe-se que a microporosidade, ou seja, poros inferiores a 10 µm, é necessária para o crescimento capilar e as interações entre a matriz e as células. Portanto, a geometria dos poros e o controle do tamanho das células são necessários para imitar as características dos ossos, que podem mudar dependendo do tipo de osso. Além disso, a rugosidade da superfície melhora a fixação, proliferação e diferenciação das células.[0012] The porosity and pore size of bone grafts play a notable role in bone formation in vitro and in vivo. Osteogenesis in vivo was found to be affected by pore size. Pore size affects processes such as vascularization, recruitment and cell penetration. Open and highly interconnected pores are very important for the performance of bone grafts, as they ensure the migration and proliferation of osteoblasts and mesenchymal cells, as well as the growth of blood vessels, which facilitates the supply of nutrients, the supply of oxygen to the cells. and the removal of metabolic wastes. Pores larger than 300 µm promote vascularization and high oxygenation, while pores smaller than 150 µm produce occlusion of cell pores, which hinders cell penetration, production of extracellular matrix and neovascularization of the internal areas of bone grafts. It is known that microporosity, that is, pores smaller than 10 µm, is necessary for capillary growth and interactions between the matrix and cells. Therefore, pore geometry and cell size control are needed to mimic bone characteristics, which can change depending on bone type. In addition, surface roughness improves cell attachment, proliferation and differentiation.
[0013] Na engenharia de tecidos ósseos, os tamanhos adequados de poros para o crescimento do tecido ósseo estão na faixa de 150–900 μm. Poros maiores que 900 μm diminuem a relação superfície/volume, gerando neoformação lenta do tecido e poros menores que 150 μm inibem a migração e vascularização celular. A porosidade satisfatória e os tamanhos dos poros são influenciados por diversos fatores, como características ósseas in vivo, biomateriais específicos, células e citocinas utilizadas in vitro e in vivo.[0013] In bone tissue engineering, suitable pore sizes for bone tissue growth are in the range of 150–900 μm. Pores larger than 900 μm decrease the surface/volume ratio, generating slow tissue neoformation and pores smaller than 150 μm inhibit cell migration and vascularization. Satisfactory porosity and pore sizes are influenced by several factors, such as in vivo bone characteristics, specific biomaterials, cells and cytokines used in vitro and in vivo.
[0014] Embora o aumento da porosidade e o tamanho dos poros sejam essenciais para o crescimento ósseo adequado, estes podem afetar profundamente as propriedades mecânicas dos materiais devido à fraqueza estrutural dos enxertos ósseos. Consequentemente existe um limite superior para a porosidade e o tamanho dos poros para impedir que as propriedades mecânicas sejam severamente reduzidas. Por exemplo, os Biovidros são materiais que podem imitar a matriz extracelular (ECM) e sua troca iônica in vivo ajuda no crescimento da camada de HCA. Por esse motivo, são materiais promissores para a regeneração óssea, mas suas estruturas altamente porosas podem afetar suas propriedades mecânicas, o que pode dificultar sua ampla aplicação clínica. Uma opção para superar esse problema é revestir a superfície dos enxertos ósseos com um polímero para fabricar estruturas mecânicas resistentes.[0014] Although increased porosity and pore size are essential for proper bone growth, these can profoundly affect the mechanical properties of materials due to the structural weakness of bone grafts. Consequently, there is an upper limit to porosity and pore size to prevent the mechanical properties from being severely reduced. For example, Bioglasses are materials that can mimic the extracellular matrix (ECM) and their ion exchange in vivo helps the growth of the HCA layer. For this reason, they are promising materials for bone regeneration, but their highly porous structures can affect their mechanical properties, which can make their wide clinical application difficult. One option to overcome this problem is to coat the surface of bone grafts with a polymer to manufacture strong mechanical structures.
[0015] Os Biovidros têm sido utilizados em diferentes estudos relacionados à regeneração óssea, utilizando diferentes composições e porosidades. Assim, foram sintetizados enxertos ósseos com poros gigantes, macroporos e nanoporos usando vidro poli(ε-caprolactona) bioativo que exibia redes de poros bem interconectados em 3D. Esses biomateriais exerceram uma boa influência na bioatividade durante a formação do tecido ósseo e na atividade celular em testes in vitro. Também foi utilizado Biovidro 13-93 (6,0Na2O-7,9K2O-7,7MgO-22,1CaO-1,7P2O5- 54,6SiO2, mol%), cujos diâmetros de poros eram controláveis. Os enxertos ósseos de vidro 13-93 mostraram uma excelente microestrutura e resposta mecânica para possíveis aplicações no reparo de ossos que suportam altas cargas (load-bearing)[0015] Bioglasses have been used in different studies related to bone regeneration, using different compositions and porosities. Thus, bone grafts with giant pores, macropores and nanopores were synthesized using bioactive poly(ε-caprolactone) glass that exhibited well-interconnected 3D pore networks. These biomaterials exerted a good influence on bioactivity during bone tissue formation and on cellular activity in in vitro tests. Bioglass 13-93 (6.0Na2O-7.9K2O-7.7MgO-22.1CaO-1.7P2O5- 54.6SiO2, mol%), whose pore diameters were controllable, was also used. The 13-93 glass bone grafts showed excellent microstructure and mechanical response for possible applications in the repair of load-bearing bones.
[0016] Os enxertos ósseos biodegradáveis podem ser absorvidos pelo organismo e, após a cirurgia de implantação, não é necessária sua remoção cirúrgica, por esse motivo, têm sido intensamente investigados. Esse fator deve ser acompanhado da taxa de degradação apropriada; assim, enquanto o novo osso é formado, o enxerto ósseo ou scaffold temporário se degrada; em outras palavras, esses processos concomitantes garantem que, quando o tecido lesionado for completamente regenerado, o enxerto ósseo ou scaffold esteja completamente degradado. Isso evita a perda da função do enxerto ósseo ou scaffold devido à sua degradação prematura. A taxa de degradação é estabelecida dependendo da aplicação ou tipo específico de tecido.[0016] Biodegradable bone grafts can be absorbed by the body and, after implantation surgery, their surgical removal is not necessary, for this reason, they have been intensively investigated. This factor must be accompanied by the appropriate degradation rate; thus, while the new bone is formed, the bone graft or temporary scaffold degrades; in other words, these concomitant processes ensure that when the injured tissue is completely regenerated, the bone graft or scaffold is completely degraded. This prevents loss of bone graft or scaffold function due to premature degradation. The rate of degradation is established depending on the application or specific tissue type.
[0017] Em geral, a consolidação dos enxertos ósseos porosos à base de vidro requer tratamentos térmicos que induzem a desvitrificação. Como consequência, os Biovidros são utilizados principalmente na forma de partículas para preencher defeitos ósseos.[0017] In general, the consolidation of porous glass-based bone grafts requires heat treatments that induce devitrification. As a consequence, Bioglasses are mainly used in the form of particles to fill bone defects.
[0018] Quanto às propriedades mecânicas ideais, os enxertos ósseos têm sido utilizados na regeneração de tecidos para promover a formação e a maturação de novos tecidos ou órgãos, onde é essencial um equilíbrio entre suporte mecânico temporário e transporte de massa (degradação e crescimento celular). Portanto, os enxertos ósseos devem ter integridade mecânica suficiente para suportar o procedimento de implantação e as forças mecânicas que são geralmente experimentadas durante o processo de remodelação, bem como as atividades normais do paciente, para evitar o colapso da estrutura. Idealmente, os enxertos ósseos devem possuir resistência e rigidez iniciais adequadas que devem ser conservadas até a formação completa do novo tecido. Por esse motivo, preferencialmente, as propriedades mecânicas dos enxertos ósseos devem ser semelhantes às do tecido circundante, evitando a proteção de carga (stress shielding) ao redor do enxerto ósseo ou scaffold e, consequentemente, a perda óssea ou o afrouxamento do implante. Nesse sentido, esse processo de adaptação mecânica deve ser realizado especialmente para enxertos ósseos de estrutura de poros abertos, cujo processo de crescimento ósseo é realizado dentro do scaffold. Além disso, as propriedades mecânicas estão relacionadas à semeadura celular, uma vez que certas células-tronco mesenquimais (CTMs) se diferenciam se a rigidez for semelhante ao respectivo tecido[0018] As for the ideal mechanical properties, bone grafts have been used in tissue regeneration to promote the formation and maturation of new tissues or organs, where a balance between temporary mechanical support and mass transport (degradation and cell growth) is essential. ). Therefore, bone grafts must have sufficient mechanical integrity to withstand the implantation procedure and the mechanical forces that are generally experienced during the remodeling process, as well as the patient's normal activities, to prevent the structure from collapsing. Ideally, bone grafts should have adequate initial strength and stiffness, which should be conserved until new tissue is fully formed. For this reason, preferably, the mechanical properties of bone grafts should be similar to those of the surrounding tissue, avoiding load protection (stress shielding) around the bone graft or scaffold and, consequently, bone loss or loosening of the implant. In this sense, this process of mechanical adaptation must be performed especially for bone grafts with an open pore structure, whose bone growth process is carried out within the scaffold. Furthermore, the mechanical properties are related to cell seeding, as certain mesenchymal stem cells (MSCs) differentiate if the stiffness is similar to the respective tissue.
[0019] Os biomateriais metálicos têm sido amplamente utilizados na engenharia de tecidos duros. No entanto, materiais metálicos densos têm um valor de módulo de Young mais alto que o osso natural, o que pode causar a reabsorção dos tecidos ósseos ao redor, devido ao efeito de proteção de carga após o implante. Para superar essa desvantagem, é necessário o desenvolvimento de uma estrutura porosa que tenha uma rigidez semelhante à do osso natural. Os enxertos ósseos metálicos porosos são frequentemente usados para aplicação onde o tecido suporta altas cargas, devido às suas excelentes propriedades mecânicas, como resistência à fadiga superior, alta resistência à compressão e boa usinabilidade. Porém, esses enxertos ósseos apresentam certas deficiências: como suas superfícies não são bioativas, a maioria não é biodegradável e há a possibilidade de liberação de agentes tóxicos.[0019] Metallic biomaterials have been widely used in hard tissue engineering. However, dense metallic materials have a higher Young's modulus value than natural bone, which can cause resorption of surrounding bone tissues, due to the load-protecting effect after implantation. To overcome this disadvantage, it is necessary to develop a porous structure that has a rigidity similar to that of natural bone. Porous metallic bone grafts are often used for application where the tissue supports high loads due to their excellent mechanical properties such as superior fatigue strength, high compressive strength and good machinability. However, these bone grafts have certain deficiencies: as their surfaces are not bioactive, most are not biodegradable and there is the possibility of releasing toxic agents.
[0020] Fosfatos de cálcio, sulfatos de cálcio e vidro bioativo têm sido utilizados como materiais de regeneração óssea. O fosfato de cálcio e os vidros bioativos são capazes de induzir a formação, precipitação e deposição de fosfato de cálcio. Por outro lado, o uso de biovidro em aplicações médicas representa um grande desafio devido às suas baixas propriedades mecânicas.[0020] Calcium phosphates, calcium sulfates and bioactive glass have been used as bone regeneration materials. Calcium phosphate and bioactive glasses are capable of inducing the formation, precipitation and deposition of calcium phosphate. On the other hand, the use of bioglass in medical applications represents a great challenge due to its low mechanical properties.
[0021] A resistência à compressão do osso esponjoso natural está na faixa de 2 a 12 MPa, e seu módulo de Young é em torno de 22 MPa. Por esse motivo, muitos estudos foram desenvolvidos para fabricar biomateriais que atingem propriedades mecânicas em torno desses valores, um requisito para sua aplicação em engenharia de tecidos ósseos.[0021] The compressive strength of natural cancellous bone is in the range of 2 to 12 MPa, and its Young's modulus is around 22 MPa. For this reason, many studies have been developed to manufacture biomaterials that achieve mechanical properties around these values, a requirement for their application in bone tissue engineering.
[0022] Para diferentes enxertos ósseos vitrocerâmicos com porosidade inferior a 89%, foi encontrada uma relação linear entre a resistência à compressão e a porosidade, observando uma diminuição de 15 a 2 MPa no valor da resistência à compressão quando a porosidade do enxerto ósseo ou scaffold aumenta 10%.[0022] For different glass-ceramic bone grafts with porosity lower than 89%, a linear relationship was found between compressive strength and porosity, observing a decrease of 15 to 2 MPa in the value of compressive strength when the porosity of the bone graft or scaffold increases by 10%.
[0023] Algumas estratégias usadas para aumentar a baixa resistência mecânica dos enxertos ósseos ou scaffolds de cerâmica obtidos através da técnica de réplica incluem o revestimento da superfície dos enxertos ósseos ou scaffolds com diferentes materiais, como polímeros naturais e sintéticos, vidros e compósitos desses materiais. A resistência mecânica de enxertos ósseos ou scaffolds de silicato de cálcio apresentou incremento de 0,32 MPa para 1,45 MPa quando sua superfície foi coberta com uma camada de poli (D, L-ácido lático) (PDLLA). A diminuição da porosidade após o recobrimento foi muito baixa, mantendo uma porosidade superior a 80% com um incremento significativo da resistência á compressão. Um dos fatores que melhorou as propriedades mecânicas dos enxertos ósseos ou scaffolds foi que o polímero preencheu os microporos e as microfissuras sobre a superfície, conservando a interconectividade do enxerto ósseo ou scaffold.[0023] Some strategies used to increase the low mechanical strength of bone grafts or ceramic scaffolds obtained through the replica technique include coating the surface of bone grafts or scaffolds with different materials, such as natural and synthetic polymers, glasses and composites of these materials. . The mechanical strength of bone grafts or calcium silicate scaffolds increased from 0.32 MPa to 1.45 MPa when their surface was covered with a layer of poly(D, L-lactic acid) (PDLLA). The decrease in porosity after coating was very low, maintaining a porosity above 80% with a significant increase in compressive strength. One of the factors that improved the mechanical properties of bone grafts or scaffolds was that the polymer filled the micropores and microcracks on the surface, preserving the interconnectivity of the bone graft or scaffold.
[0024] O grupo de pesquisadores do LAMAV (Laboratório de Materiais Vítreos) da UFSCar, dentre os quais os inventores do presente pedido, desenvolvem, desde os anos 2000, pesquisas no sentido de obter materiais bioativos. Essas pesquisas resultaram na obtenção de proteção patentária para alguns produtos bioativos que serão elencados a seguir.[0024] The group of researchers from LAMAV (Laboratory of Vitreous Materials) at UFSCar, among which the inventors of the present application, have been developing, since the 2000s, research in order to obtain bioactive materials. These researches resulted in the obtaining of patent protection for some bioactive products that will be listed below.
[0025] Assim, a patente brasileira PI0300644B1 trata de um processo para preparar biosilicatos particulados, bioativos e reabsorvíveis a partir de placas vítreas ou fritas, o processo compreendendo tratar termicamente as placas vítreas ou fritas em uma ou duas etapas de tratamento térmico, moer o vidro cristalizado obtido e para obter pós de biosilicato cristalizado bioativo de bioatividade desejada, que em contato com fluidos corpóreos produz uma camada de HCA para restauração dos dentes ou pode ser gradualmente substituída por tecido dental e reabsorvida. Para diferentes condições de processo, diferentes fases cristalinas são obtidas de modo a preparar uma faixa de silicatos bioativos ou reabsorvíveis que podem ser usados como tal ou combinados no tratamento de diferentes problemas bucais como hipersensibilidade da dentina, fissuras dentais e xerostomia. A distribuição do tamanho de partícula está entre 0,1 e 30 microns. O produto é comercializado sob a marca Biosilicato®.[0025] Thus, the Brazilian patent PI0300644B1 deals with a process to prepare particulate, bioactive and resorbable biosilicates from glass or fritted plates, the process comprising thermally treating the glassy or fritted plates in one or two heat treatment steps, grinding the crystallized glass obtained and to obtain bioactive crystallized biosilicate powders of desired bioactivity, which in contact with body fluids produces a layer of HCA for restoration of teeth or can be gradually replaced by dental tissue and reabsorbed. For different process conditions, different crystalline phases are obtained in order to prepare a range of bioactive or resorbable silicates that can be used as such or combined in the treatment of different oral problems such as dentin hypersensitivity, dental fissures and xerostomia. The particle size distribution is between 0.1 and 30 microns. The product is marketed under the brand name Biosilicate®.
[0026] Ainda, a patente brasileira PI1003676B2, do mesmo grupo de pesquisa que elaborou o Biosilicato® e dos mesmos autores do presente pedido trata do processo de preparação de enxertos ósseos ou scaffolds através da técnica de réplica. Esta patente brasileira trata de suspensões à base de Biosilicato® para a preparação de enxertos ósseos ou scaffolds. As suspensões compreendem, em relação ao volume total da suspensão, de 10-50% de sólidos constituídos de 50 a 98% de agente porogênico, de 2 a 50% de Biosilicato® e de 50 a 90% de líquidos constituídos de 0,5-15% de ligante e de 85 a 99,5% de meio líquido. Em um processo de preparação, são misturados o ligante, meio líquido e Biosilicato®, formando uma suspensão, a suspensão é moída, é adicionado o agente porogênico, é feita mistura da suspensão com o agente porogênico, a mistura é seca em um pó, o pó obtido é peneirado, conformado em moldes de qualquer geometria, o produto conformado é queimado e recuperado o produto final enxerto ósseo ou scaffold. Os enxertos ósseos obtidos por este processo apresentam porosidade total variando entre 65 - 95% e tamanho médio de poros entre 100 e 600 µm.[0026] Also, the Brazilian patent PI1003676B2, from the same research group that developed the Biosilicate® and from the same authors of the present application, deals with the process of preparing bone grafts or scaffolds through the replica technique. This Brazilian patent deals with suspensions based on Biosilicate® for the preparation of bone grafts or scaffolds. The suspensions comprise, in relation to the total volume of the suspension, from 10-50% of solids consisting of 50 to 98% of porogenic agent, from 2 to 50% of Biosilicate® and from 50 to 90% of liquids consisting of 0.5 -15% of binder and from 85 to 99.5% of liquid medium. In a preparation process, the binder, liquid medium and Biosilicate® are mixed, forming a suspension, the suspension is ground, the porogenic agent is added, the suspension is mixed with the porogenic agent, the mixture is dried into a powder, the powder obtained is sieved, shaped in molds of any geometry, the shaped product is burned and the final bone graft or scaffold product is recovered. The bone grafts obtained by this process present total porosity varying between 65 - 95% and average pore size between 100 and 600 µm.
[0027] Ainda desenvolvida pelo mesmo grupo de pesquisa da UFSCar, o pedido brasileiro publicado BR102013020961 (e as patentes correspondentes europeia EP3034480B1 e norte-americana US9731994B1) trata de um produto vítreo denominado F18. Esta publicação trata de uma composição vítrea, fibras e tecidos vítreos bioativos e artigos. É descrita uma composição vítrea por quantidade em % peso SiO2 43-52; Na2O 4-9,5, K20 20,5-32; MgO 0,5-2,5; CaO 15-20; Au0,1-3,5; Ag 0,1-3,5; B203 1,5-4; P205 1-6; ZnO 0,1-3,5; SrO 0,1-3,5. Fibras vítreas contínuas são obtidas por downdrawing da dita composição fundida, com comprimento desde milímetros até quilômetros, e diâmetros entre 2 mm e 3 mm. As fibras são recobertas por colágeno e formam tecidos vítreos. Os tecidos formam artigos para várias aplicações médicas. O tecido vítreo obtido é altamente bioativo. A composição proposta neste pedido brasileiro publicado confere ao vidro elevada reatividade e baixa durabilidade química, como é esperado para um vidro altamente bioativo. Sua maior estabilidade vítrea permite que o vidro seja manipulado e que passe por tratamentos térmicos e/ou sinterização sem apresentar cristalização descontrolada, permitindo, portanto, que sejam utilizados processos simples, ao mesmo tempo em que exigem baixa tendência de cristalização.[0027] Still developed by the same research group at UFSCar, the published Brazilian application BR102013020961 (and the corresponding European patents EP3034480B1 and North American US9731994B1) deals with a vitreous product called F18. This publication deals with a vitreous composition, bioactive vitreous fibers and tissues and articles. A glass composition by amount in % weight SiO2 43-52 is described; Na2O 4-9.5, K20 20.5-32; MgO 0.5-2.5; CaO 15-20; Au0.1-3.5; Ag 0.1-3.5; B203 1.5-4; P205 1-6; ZnO 0.1-3.5; SrO 0.1-3.5. Continuous glass fibers are obtained by downdrawing said molten composition, with lengths from millimeters to kilometers, and diameters between 2 mm and 3 mm. The fibers are covered by collagen and form vitreous tissues. The fabrics form articles for various medical applications. The vitreous tissue obtained is highly bioactive. The composition proposed in this published Brazilian application gives the glass high reactivity and low chemical durability, as is expected for a highly bioactive glass. Its greater vitreous stability allows the glass to be manipulated and undergo heat treatments and/or sintering without uncontrolled crystallization, therefore allowing simple processes to be used, while requiring a low tendency to crystallization.
[0028] A publicação internacional WO2014044666A1 trata de implantes médicos sob forma de enxertos ósseos ou scaffolds de dióxido de titânio. Enxertos ósseos com resistência mecânica melhorada à compressão são obtidos pelo recozimento do enxerto ósseo ou scaffold com uma suspensão de dióxido de titânio de baixa viscosidade em um processo de infiltração a vácuo seguido de sinterização do enxerto ósseo ou scaffold. Embora esta publicação trate do aumento da resistência mecânica à compressão do enxerto ósseo através de infiltração a vácuo de uma suspensão, pelo fato de o dióxido de titânio (cerâmica formado por ligações covalentes entre um metal (Ti) e o Oxigênio) ser um pó, o efeito da infiltração de uma suspensão de dióxido de titânio no enxerto ósseo de dióxido de titânio é diverso daquele buscado na presente invenção. Com efeito, na invenção a infiltração sob vácuo de suspensão de vidro F18 (vidro formado por ligações covalentes entre um semimetal (Si) e o Oxigênio) se destina a preencher defeitos da estrutura do enxerto ósseo de Biosilicato® e reduzir a porosidade do mesmo fluindo entre os poros, porém sem cristalização. Portanto, o mecanismo de melhoria da resistência mecânica conforme a presente invenção é diverso daquele da publicação internacional WO2014044666A1.[0028] The international publication WO2014044666A1 deals with medical implants in the form of bone grafts or titanium dioxide scaffolds. Bone grafts with improved mechanical strength to compression are obtained by annealing the bone graft or scaffold with a low viscosity titanium dioxide suspension in a vacuum infiltration process followed by sintering the bone graft or scaffold. Although this publication deals with increasing the mechanical resistance to compression of the bone graft through vacuum infiltration of a suspension, due to the fact that titanium dioxide (a ceramic formed by covalent bonds between a metal (Ti) and Oxygen) is a powder, the effect of infiltrating a titanium dioxide suspension into the titanium dioxide bone graft is different from that sought in the present invention. Indeed, in the invention, the vacuum infiltration of F18 glass suspension (glass formed by covalent bonds between a semimetal (Si) and Oxygen) is intended to fill defects in the structure of the Biosilicate® bone graft and reduce the porosity of the same flowing between the pores, but without crystallization. Therefore, the mechanical strength improvement mechanism according to the present invention is different from that of the international publication WO2014044666A1.
[0029] De fato, na publicação internacional WO2014044666A1 é descrito um método para produzir enxertos ósseos ou scaffolds de dióxido de titânio que podem ser usados como enxertos ósseos e cuja resistência à compressão foi melhorada através de vários recobrimentos com dióxido de titânio. O dióxido de titânio é um material usado em implantes ortopédicos devido à sua estabilidade em ambientes biológicos e sua capacidade de suportar altas cargas físicas com mínima deformação. Além disso, possui alta resistência à corrosão e boa biocompatibilidade. Além de uma estrutura reticular altamente interconectada, é necessário um tamanho de célula médio superior a 300 µm para fornecer espaço e permeabilidade adequados para a formação do novo tecido ósseo em uma estrutura não reabsorvível como os enxertos ósseos ou scaffolds de dióxido de titânio. Inicialmente, os enxertos ósseos ou scaffolds de dióxido de titânio são sintetizados usando o método da réplica. Como molde de sacrifício foi usado espumas cilíndricas de poliuretano de 60 ppi com 10 mm de diâmetro e 10 mm de altura. Para controlar as propriedades reológicas das barbotinas, o pH das suspensões foi mantido a 1,5 e sob agitação por 2,5 horas a 5000 rpm. Primeiramente, uma barbotina de dióxido de titânio (por exemplo, 65 g de dióxido de titânio em 25 mL de água) é aplicada sobre o molde de sacrifício. Depois que a barbotina se solidifica, o molde poroso é queimado a uma temperatura de cerca de 400-550°C a uma taxa de 0,5°C/min por uma hora. Então, o enxerto ósseo ou scaffold é sinterizado a uma temperatura entre 1300–1500°C por 2–40 horas a uma taxa de 3°C/min. Este processo permite obter os enxertos ósseos ou scaffolds de dióxido de titânio. Em seguida, uma segunda barbotina de dióxido de titânio (por exemplo, 30–45 g de dióxido de titânio em 25 mL de água) é aplicada sobre os enxertos ósseos ou scaffolds de dióxido de titânio (sinterizado durante 40 horas) sob vácuo. Opcionalmente, o enxerto ósseo ou scaffold pode ser submetido à centrifugação para retirar o excesso de barbotina. Depois que a barbotina solidifica sobre o enxerto ósseo ou scaffold de dióxido de titânio, o enxerto ósseo ou scaffold é sinterizado a uma temperatura de 1500°C durante 40 horas a uma velocidade de 3°C/min. Este processo permite obter um enxerto ósseo ou scaffold de dióxido de titânio com dois recobrimentos de dióxido de titânio. Opcionalmente, outra infiltração a vácuo pode ser realizada no enxerto ósseo ou scaffold de dióxido de titânio com dois recobrimentos de dióxido de titânio. Uma terceira barbotina de dióxido de titânio de baixa viscosidade (10–20 g de dióxido de titânio em 25 mL de água) é aplicada ao enxerto ósseo ou scaffold de dióxido de titânio com dois recobrimentos de dióxido de titânio sob condições de vácuo (0,2 mbar por 5 minutos). Opcionalmente, o enxerto ósseo ou scaffold pode ser centrifugado para remover o excesso de barbotina. Depois que a barbotina solidifica, o enxerto ósseo ou scaffold é sinterizado a uma temperatura de 1500°C por 4 horas a uma taxa de 3°C/min. Através deste procedimento é obtido o enxerto ósseo ou scaffold de dióxido de titânio com três recobrimentos de dióxido de titânio. Alternativamente, a ordem do segundo e terceiro recobrimento com dióxido de titânio pode ser invertida. A resistência à compressão dos enxertos ósseos ou scaffolds de dióxido de titânio incrementou consideravelmente após os vários recobrimentos com dióxido de titânio. Foi verificado que o terceiro recobrimento com dióxido de titânio, levado a cabo através do processo de infiltração a vácuo incrementou consideravelmente a resistência à compressão dos enxertos ósseos ou scaffolds de dióxido de titânio (3,39 ± 0,77 MPa) em comparação com os enxertos ósseos ou scaffolds que foram recobertos só duas vezes com dióxido de titânio (1,78 ± 0,52 MPa). No entanto, a interconectividade das estruturas foi reduzida durante o segundo recobrimento, principalmente pela barbotina com menor teor de sólidos (30 g de dióxido de titânio em 25 mL de água). Portanto, este parâmetro foi controlado, pois determina a uniformidade e a interconectividade da rede de poros quando a integridade mecânica das espumas cerâmicas é incrementada através de infiltrações ao vácuo. Esses enxertos ósseos ou scaffolds apresentaram alta porosidade (88–90%) e tamanho de célula adequado (435-450µm). A estratégia usada no documento de patente internacional WO2014044666A1 para preencher a porosidade interna dos struts foi incrementar a consolidação dos enxertos ósseos ou scaffolds de dióxido de Titânio (enxertos ósseos ou scaffolds com só um recobrimento de dióxido de Titânio) através do incremento do tempo de sinterização (1500 °C). Esse processo permitiu que a porosidade interna dos struts de dióxido de Titânio fosse parcialmente preenchida através de uma melhor densificação do material. Assim foi verificado que a porosidade interna dos struts dos enxertos ósseos ou scaffolds de dióxido de Titânio foi consideravelmente reduzida após 20 horas de sinterização a 1500°C. No entanto, o incremento da resistência à compressão foi muito baixo (< 2 MPa, o valor mínimo para o osso trabecular).[0029] In fact, in the international publication WO2014044666A1 a method is described for producing bone grafts or titanium dioxide scaffolds that can be used as bone grafts and whose compressive strength has been improved through various titanium dioxide coatings. Titanium dioxide is a material used in orthopedic implants due to its stability in biological environments and its ability to withstand high physical loads with minimal deformation. In addition, it has high corrosion resistance and good biocompatibility. In addition to a highly interconnected reticular structure, an average cell size greater than 300 µm is required to provide adequate space and permeability for the formation of new bone tissue in a non-resorbable structure such as bone grafts or titanium dioxide scaffolds. Initially, bone grafts or titanium dioxide scaffolds are synthesized using the replica method. As a sacrificial mold, 60 ppi cylindrical polyurethane foams with 10 mm in diameter and 10 mm in height were used. To control the rheological properties of the slips, the pH of the suspensions was kept at 1.5 and under agitation for 2.5 hours at 5000 rpm. First, a slip of titanium dioxide (eg, 65 g of titanium dioxide in 25 mL of water) is applied over the sacrificial mold. After the slip has solidified, the porous mold is fired at a temperature of about 400-550°C at a rate of 0.5°C/min for one hour. Then, the bone graft or scaffold is sintered at a temperature between 1300–1500°C for 2–40 hours at a rate of 3°C/min. This process makes it possible to obtain bone grafts or titanium dioxide scaffolds. Then, a second slip of titanium dioxide (eg, 30–45 g of titanium dioxide in 25 mL of water) is applied over the bone grafts or titanium dioxide scaffolds (sintered for 40 hours) under vacuum. Optionally, the bone graft or scaffold can be subjected to centrifugation to remove excess slip. After the slip solidifies on the bone graft or titanium dioxide scaffold, the bone graft or scaffold is sintered at a temperature of 1500°C for 40 hours at a rate of 3°C/min. This process makes it possible to obtain a titanium dioxide bone graft or scaffold with two titanium dioxide coatings. Optionally, another vacuum infiltration can be performed on bone graft or titanium dioxide scaffold with two titanium dioxide overlays. A third low viscosity titanium dioxide slip (10–20 g titanium dioxide in 25 mL of water) is applied to the bone graft or titanium dioxide scaffold with two titanium dioxide overlays under vacuum conditions (0. 2 mbar for 5 minutes). Optionally, the bone graft or scaffold can be centrifuged to remove excess slip. After the slip solidifies, the bone graft or scaffold is sintered at a temperature of 1500°C for 4 hours at a rate of 3°C/min. Through this procedure, a bone graft or titanium dioxide scaffold with three titanium dioxide coatings is obtained. Alternatively, the order of the second and third titanium dioxide coatings can be reversed. The compressive strength of bone grafts or titanium dioxide scaffolds increased considerably after several titanium dioxide coatings. It was verified that the third coating with titanium dioxide, carried out through the vacuum infiltration process, considerably increased the compressive strength of bone grafts or titanium dioxide scaffolds (3.39 ± 0.77 MPa) in comparison with the bone grafts or scaffolds that were coated only twice with titanium dioxide (1.78 ± 0.52 MPa). However, the interconnectivity of the structures was reduced during the second coating, mainly due to the slip with lower solids content (30 g of titanium dioxide in 25 mL of water). Therefore, this parameter was controlled, as it determines the uniformity and interconnectivity of the pore network when the mechanical integrity of ceramic foams is increased through vacuum infiltration. These bone grafts or scaffolds showed high porosity (88–90%) and adequate cell size (435-450µm). The strategy used in the international patent document WO2014044666A1 to fill the internal porosity of the struts was to increase the consolidation of bone grafts or titanium dioxide scaffolds (bone grafts or scaffolds with only one titanium dioxide coating) by increasing the sintering time. (1500°C). This process allowed the internal porosity of the titanium dioxide struts to be partially filled through better densification of the material. Thus, it was verified that the internal porosity of the struts of bone grafts or titanium dioxide scaffolds was considerably reduced after 20 hours of sintering at 1500°C. However, the increase in compressive strength was very low (< 2 MPa, the minimum value for trabecular bone).
[0030] Portanto, os autores do referido documento de patente internacional. WO2014044666A1 recobriram os enxertos ósseos ou scaffolds de dióxido de titânio com várias barbotinas de dióxido de titânio para incrementar a resistência a compressão do material. Este processo foi realizado sob condições de vácuo para obter uma camada homogênea na superfície dos enxertos ósseos ou scaffolds e para evitar que a espessura dos struts aumentasse demais. Além disso, o vácuo facilitou a penetração da barbotina nas microtrincas e microporosidades na superfície dos struts, permitindo um incremento considerável da resistência à compressão. Com esse processo, foi aumentada a resistência à compressão do material sem gerar uma diminuição significativa da porosidade e da interconectividade da estrutura reticular. Outro fator que evitou a deposição de uma camada grossa na superfície dos enxertos ósseos ou scaffolds de dióxido de titânio foi que, após a segunda e terceira infiltração com dióxido de titânio, o material foi centrifugado para remover o excesso de barbotina.[0030] Therefore, the authors of said international patent document. WO2014044666A1 covered the bone grafts or titanium dioxide scaffolds with various titanium dioxide slips to increase the material's compressive strength. This process was carried out under vacuum conditions to obtain a homogeneous layer on the surface of the bone grafts or scaffolds and to prevent the struts thickness from increasing too much. In addition, the vacuum facilitated the penetration of the slip into the microcracks and microporosities on the surface of the struts, allowing a considerable increase in compressive strength. With this process, the compressive strength of the material was increased without generating a significant decrease in the porosity and interconnectivity of the reticular structure. Another factor that prevented the deposition of a thick layer on the surface of bone grafts or titanium dioxide scaffolds was that, after the second and third infiltration with titanium dioxide, the material was centrifuged to remove excess slip.
[0031] Já o principal objetivo da presente invenção foi incrementar a resistência à compressão dos enxertos ósseos ou scaffolds de Biosilicato através de vários recobrimentos com barbotinas de Biovidro F18 sob condições de vácuo. Este processo foi efetuado para forçar o vidro a penetrar na parte oca da estrutura. Para facilitar este processo, os enxertos ósseos ou scaffolds de Biosilicato foram obtidos usando partículas de Biosilicato com um tamanho médio de 45 µm. Assim, os enxertos ósseos ou scaffolds de Biosilicato apresentaram uma superfície muito porosa que facilitou a penetração das partículas de vidro. Diferentemente da invenção objeto da publicação internacional WO2014044666A1, onde a porosidade interna dos struts de dióxido de titânio foi reduzida principalmente pelo aumento do tempo de sinterização (20–40 horas), o qual incrementou a densificação dos enxertos ósseos ou scaffolds de dióxido de titânio, na presente invenção a porosidade interna dos struts de Biosilicato foi reduzida através de vários processos de infiltração a vácuo usando barbotinas de vidro F18, permitindo o preenchimento parcial da porosidade interna (ver Figura 2 da presente invenção) dos struts de Biosilicato.[0031] The main objective of the present invention was to increase the compressive strength of bone grafts or Biosilicate scaffolds through several coatings with F18 Bioglass slips under vacuum conditions. This process was carried out to force the glass to penetrate the hollow part of the structure. To facilitate this process, bone grafts or Biosilicate scaffolds were obtained using Biosilicate particles with an average size of 45 µm. Thus, the bone grafts or Biosilicate scaffolds presented a very porous surface that facilitated the penetration of the glass particles. Unlike the invention object of the international publication WO2014044666A1, where the internal porosity of titanium dioxide struts was reduced mainly by increasing the sintering time (20–40 hours), which increased the densification of bone grafts or titanium dioxide scaffolds, in the present invention the internal porosity of the Biosilicate struts was reduced through various vacuum infiltration processes using F18 glass slips, allowing partial filling of the internal porosity (see Figure 2 of the present invention) of the Biosilicate struts.
[0032] O principal objetivo da presente invenção foi aumentar a resistência à compressão de enxertos ósseos ou scaffolds de Biosilicato através de vários recobrimentos com uma barbotina de Biovidro F18.[0032] The main objective of the present invention was to increase the compressive strength of bone grafts or Biosilicate scaffolds through several coatings with an F18 Bioglass slip.
[0033] Na literatura são reportados diferentes tipos de recobrimentos usados para incrementar a resistência mecânica dos enxertos ósseos ou scaffolds cerâmicos. Em geral, polímeros sintéticos ou naturais são usados para realizar este tipo de recobrimento. Além disso, os enxertos ósseos ou scaffolds cerâmicos também podem ser recobertos usando somente vidros bioativos. O F18 é ideal para esse tipo de recobrimento, pois o Biovidro F18 é sinterizado a baixas temperaturas e pelo mecanismo de escoamento viscoso. A alta estabilidade deste biovidro frente à cristalização permite que o mesmo flua durante o processo, preenchendo poros pequenos e microtrincas. A estrutura oca do enxerto ósseo ou scaffold também é preenchida durante o processo de infiltração, tornando-se sólida após a sinterização. Além disso, obtém-se uma superfície lisa e isenta de defeitos. Tudo isso contribui para o aumento da resistência mecânica final dos enxertos ósseos ou scaffolds. Além disso, o vidro F18 forma uma camada de hidroxicarbonatoapatita na superfície do enxerto ósseo ou scaffold de Biosilicato, incrementando a bioatividade do biomaterial, o que é muito importante para incrementar o processo de osseointegração e osteogênese. Isso facilita o processamento do enxerto ósseo ou scaffold, em contraste com materiais como dióxido de titânio que, por serem materiais não bioativos, precisam de funcionalização da superfície para induzir a formação de uma camada de fosfato de cálcio na superfície do dióxido de titânio. Outra propriedade importante do vidro F18 e do Biosilicato é que eles são materiais reabsorvíveis que podem ser excretados pelo corpo, evitando uma segunda cirurgia para removê-los.[0033] In the literature, different types of coatings are reported used to increase the mechanical strength of bone grafts or ceramic scaffolds. In general, synthetic or natural polymers are used to perform this type of coating. In addition, bone grafts or ceramic scaffolds can also be covered using only bioactive glasses. The F18 is ideal for this type of coating, as the Bioglass F18 is sintered at low temperatures and by the viscous flow mechanism. The high stability of this bioglass against crystallization allows it to flow during the process, filling small pores and microcracks. The hollow structure of the bone graft or scaffold is also filled during the infiltration process, becoming solid after sintering. In addition, a smooth, defect-free surface is obtained. All of this contributes to increasing the final mechanical strength of bone grafts or scaffolds. In addition, the F18 glass forms a hydroxycarbonateapatite layer on the surface of the bone graft or Biosilicate scaffold, increasing the bioactivity of the biomaterial, which is very important to enhance the osseointegration and osteogenesis process. This facilitates the processing of the bone graft or scaffold, in contrast to materials such as titanium dioxide which, as they are non-bioactive materials, need surface functionalization to induce the formation of a calcium phosphate layer on the titanium dioxide surface. Another important property of F18 glass and Biosilicate is that they are resorbable materials that can be excreted by the body, avoiding a second surgery to remove them.
[0034] A patente US3090094 descreve o processo básico da réplica, que consiste na impregnação das espumas poliméricas ou naturais pela suspensão cerâmica seguida de tratamento térmico, que permite a queima da parte orgânica e a sinterização do material cerâmico, resultando na réplica da espuma original. A otimização das etapas do processo (escolha da espuma polimérica, preparação da suspensão cerâmica, impregnação, secagem e tratamento térmico) permite o desenvolvimento de materiais com características desejáveis para aplicações específicas. As espumas flexíveis de poliuretano (PU) são muito utilizadas, com diferentes tamanhos de células.[0034] The patent US3090094 describes the basic process of the replica, which consists of impregnating polymeric or natural foams by the ceramic suspension followed by heat treatment, which allows the burning of the organic part and the sintering of the ceramic material, resulting in the replica of the original foam . The optimization of the process steps (choice of polymeric foam, preparation of the ceramic suspension, impregnation, drying and heat treatment) allows the development of materials with desirable characteristics for specific applications. Flexible polyurethane (PU) foams are widely used, with different cell sizes.
[0035] O pedido publicado norte-americano US20130330537A1 trata de processo para produzir enxertos ósseos pelo método de revestimento de um molde de sacrifício ou molde de poliuretano (PU) para obter materiais cerâmicos porosos. A espuma usada como molde de sacrifício é tratada e uma suspensão é revestida no molde de sacrifício, que é sinterizado para formar o material cerâmico poroso. Uma segunda suspensão é preparada e usada para revestir o material cerâmico, quando então os poros bloqueados são liberados e o material é seco e sinterizado para formar um material poroso cerâmico sinterizado final. O material final é considerado similar à estrutura do osso trabecular e provê integridade mecânica consistente e porosidade para regeneração de tecidos ósseos funcionais.[0035] The US published application US20130330537A1 deals with a process for producing bone grafts by the method of coating a sacrificial mold or polyurethane (PU) mold to obtain porous ceramic materials. The foam used as the sacrificial mold is treated and a suspension is coated into the sacrificial mold, which is sintered to form the porous ceramic material. A second suspension is prepared and used to coat the ceramic material, whereupon the blocked pores are released and the material is dried and sintered to form a final sintered ceramic porous material. The final material is considered to be similar to the structure of trabecular bone and provides consistent mechanical integrity and porosity for regeneration of functional bone tissue.
[0036] As microtrincas e irregularidades na superfície dos enxertos ósseos ou scaffolds cerâmicos obtidos pela técnica da réplica são geradas por um recobrimento deficiente da barbotina na superfície da esponja de PU. Além disso, durante o tratamento térmico, a defasagem entre a expansão térmica da espuma de PU e o recobrimento cerâmico gera esses tipos de defeitos de superfície. Outro fator que contribui fortemente a redução das propriedades mecânicas das espumas cerâmicas ou scaffolds sintetizados pelo método da réplica é a presença de espaços vazios no interior das estruturas que corresponde ao espaço inicialmente ocupado pelo molde de sacrifício ou espuma de PU.[0036] The microcracks and irregularities on the surface of bone grafts or ceramic scaffolds obtained by the replica technique are generated by a poor coating of slip on the surface of the PU sponge. Furthermore, during heat treatment, the lag between the thermal expansion of the PU foam and the ceramic coating generates these types of surface defects. Another factor that strongly contributes to the reduction of the mechanical properties of ceramic foams or scaffolds synthesized by the replica method is the presence of voids inside the structures that correspond to the space initially occupied by the sacrificial mold or PU foam.
[0037] Dado que os enxertos ósseos ou scaffolds de cerâmicas obtidos através da técnica da réplica apresentam defeitos de superfície como microtrinca e microporosidades, técnicas como recobrimento de superfície dos enxertos ósseos ou scaffolds podem ser usadas para melhorar a estrutura da superfície dos struts.[0037] Given that bone grafts or ceramic scaffolds obtained through the replica technique have surface defects such as microcracks and microporosities, techniques such as surface covering of bone grafts or scaffolds can be used to improve the surface structure of the struts.
[0038] Deste modo, seria interessante que a técnica dispusesse de um processo de preparação de enxertos ósseos bioativos e reabsorvíveis à base de Biosilicato® e vidro F18, de modo que o enxerto ósseo obtido apresente resistência mecânica à compressão aperfeiçoada.[0038] Thus, it would be interesting if the technique had a process for preparing bioactive and resorbable bone grafts based on Biosilicate® and F18 glass, so that the bone graft obtained presents improved mechanical resistance to compression.
[0039] Em geral, o processo da invenção para preparação de enxertos ósseos ou scaffolds úteis para implantes de osso trabecular compreende impregnar, pelo processo de réplica, moldes de sacrifício de espumas de poliuretano (PU) com entre 35 e 55 ppi com suspensões ou barbotinas de Biosilicato®, sinterizar os moldes impregnados sob temperaturas controladas obtendo enxertos ósseos ou scaffolds e numa etapa posterior infiltrando sob vácuo e sinterizando repetidas vezes o produto obtido com suspensões de Biovidro F18. O produto obtido é um enxerto ósseo ou scaffold adequado para aplicação em odontologia, em lugares onde o tecido ósseo não suporta altas cargas.[0039] In general, the process of the invention for preparing bone grafts or scaffolds useful for trabecular bone implants comprises impregnating, by the replica process, sacrificial molds of polyurethane foams (PU) with between 35 and 55 ppi with suspensions or Biosilicate® slips, sinter the impregnated molds under controlled temperatures, obtaining bone grafts or scaffolds and, in a later step, infiltrating under vacuum and repeatedly sintering the product obtained with suspensions of Bioglass F18. The product obtained is a bone graft or scaffold suitable for application in dentistry, in places where the bone tissue does not support high loads.
[0040] O processo da invenção para a preparação de enxertos ósseos ou scaffolds de Biosilicato/Biovidro F18 compreende, portanto, várias Etapas, de I a VII:[0040] The process of the invention for the preparation of bone grafts or scaffolds of Biosilicate/Bioglass F18 therefore comprises several Steps, from I to VII:
[0041] Etapa I: Preparação do enxerto ósseo ou scaffold de Biosilicato®. Para tanto, parte-se do enxerto ósseo ou scaffold de Biosilicato® (objeto da patente PI0300644B1). Para a preparação deste enxerto ósseo ou scaffold, é utilizada uma esponja de PU com abertura de células média na faixa 35-55 ppi. Em seguida prepara-se uma barbotina ou suspensão de Biosilicato® e a espuma de PU é mergulhada na barbotina de Biosilicato®. A espuma infiltrada é removida da barbotina e o excesso de barbotina é removido; a espuma contendo partículas de Biosilicato® é seca à temperatura ambiente por 24 horas. Após a secagem, a espuma passa pelo primeiro processo de queima ou sinterização, em etapas, em temperaturas crescentes e com temperaturas máximas próximas a 1000°C. O material obtido é uma vitrocerâmica totalmente cristalina e não um biovidro. Ao final do processo pode haver microporos e trincas residuais. O enxerto ósseo ou scaffold de Biosilicato® obtido tem resistência mecânica inferior a 0,1 MPa.[0041] Step I: Preparation of the bone graft or Biosilicate® scaffold. For that, it starts with the bone graft or Biosilicate® scaffold (object of patent PI0300644B1). For the preparation of this bone graft or scaffold, a PU sponge with a medium cell opening in the range 35-55 ppi is used. Then a Biosilicate® slip or suspension is prepared and the PU foam is dipped in the Biosilicate® slip. The infiltrated foam is removed from the slip and excess slip is removed; the foam containing Biosilicate® particles is dried at room temperature for 24 hours. After drying, the foam undergoes the first firing or sintering process, in stages, at increasing temperatures and with maximum temperatures close to 1000°C. The material obtained is a fully crystalline glass-ceramic and not a bioglass. At the end of the process, there may be micropores and residual cracks. The obtained Biosilicate® bone graft or scaffold has a mechanical strength of less than 0.1 MPa.
[0042] Etapa II: Nesta Etapa, o enxerto ósseo ou scaffold de Biosilicato® da Etapa I é infiltrado sob vácuo (-400mmHg a -600mmHg) durante 5 a 10 minutos com a mesma barbotina de Biosilicato® da Etapa I. O enxerto ósseo obtido nesta etapa é seco à temperatura ambiente.[0042] Step II: In this Step, the bone graft or Biosilicate® scaffold from Step I is vacuum infiltrated (-400mmHg to -600mmHg) for 5 to 10 minutes with the same Biosilicate® slip as in Step I. The bone graft obtained in this step is dried at room temperature.
[0043] Etapa III: Nesta Etapa, o enxerto ósseo ou scaffold de Biosilicato® infiltrado na etapa II é submetido à queima, empregando-se o mesmo procedimento descrito na Etapa I.[0043] Step III: In this Step, the bone graft or Biosilicate® scaffold infiltrated in step II is submitted to firing, using the same procedure described in Step I.
[0044] Etapa IV: Na Etapa IV, o enxerto ósseo ou scaffold de Biosilicato® é infiltrado sob vácuo por uma barbotina à base de Biovidro F18 (objeto do pedido publicado brasileiro BR102013020961). O procedimento de infiltração do scaffold de Biosilicato® com a barbotina de Biovidro F18 é análogo ao descrito na Etapa II.[0044] Step IV: In Step IV, the bone graft or Biosilicate® scaffold is infiltrated under vacuum by a slip based on Bioglass F18 (object of Brazilian published application BR102013020961). The procedure for infiltrating the Biosilicate® scaffold with the Bioglass F18 slip is similar to that described in Step II.
[0045] Etapa V: Na Etapa V, o enxerto ósseo ou scaffold de Biosilicato® que foi infiltrado com a barbotina de Biovidro F18 é submetido à queima sob condições controladas.[0045] Stage V: In Stage V, the bone graft or Biosilicate® scaffold that was infiltrated with the Bioglass F18 slip is submitted to firing under controlled conditions.
[0046] Etapa VI: Na Etapa VI são repetidas as Etapas IV e V.[0046] Stage VI: In Stage VI, Stages IV and V are repeated.
[0047] Etapa VII: Na Etapa VII o produto enxerto ósseo scaffold de Biosilicato®/Biovidro F18 com resistência mecânica à compressão aperfeiçoada é recuperado.[0047] Step VII: In Step VII the Biosilicate®/Bioglass F18 scaffold bone graft product with improved mechanical resistance to compression is recovered.
[0048] Diferentemente do Biosilicato®, o Biovidro F18 sinteriza-se em baixas temperaturas e pelo mecanismo de escoamento viscoso. A alta estabilidade deste biovidro frente à cristalização permite que o mesmo flua durante o processo, preenchendo poros pequenos e microtrincas. A estrutura oca do enxerto ósseo ou scaffold também é preenchida durante o processo de infiltração, tornando-se sólida após a sinterização. Além disso, obtém-se uma superfície lisa e isenta de defeitos. Tudo isso contribui para o aumento da resistência mecânica final do enxerto ósseo ou scaffold.[0048] Unlike Biosilicate®, Bioglass F18 sinters at low temperatures and by the viscous flow mechanism. The high stability of this bioglass against crystallization allows it to flow during the process, filling small pores and microcracks. The hollow structure of the bone graft or scaffold is also filled during the infiltration process, becoming solid after sintering. In addition, a smooth, defect-free surface is obtained. All of this contributes to increasing the final mechanical strength of the bone graft or scaffold.
[0049] Desta forma, é obtido um enxerto ósseo ou scaffold de Biosilicato®/Biovidro F18, com resistência mecânica superior a 3 MPa, ou seja, compatível com os enxertos ósseos ou scaffolds na forma de pequenos blocos existentes no mercado. A presença do Biovidro F18 aumenta o efeito bactericida do enxerto ósseo ou scaffold.[0049] In this way, a bone graft or scaffold of Biosilicate®/Bioglass F18 is obtained, with mechanical strength greater than 3 MPa, that is, compatible with bone grafts or scaffolds in the form of small blocks on the market. The presence of Bioglass F18 increases the bactericidal effect of the bone graft or scaffold.
[0050] E os enxertos ósseos ou scaffolds preparados inicialmente a partir de uma esponja polimérica de porosidade 45 ppi (pores per inch) ao final do processo da invenção apresentam porosidade de 82,0 ± 1,3%, tamanho médio de célula de 525 ± 220 μm e resistência à compressão de 3,3 ± 0,3 MPa. Essa estrutura tridimensional altamente porosa e interconectada imita a morfologia do osso trabecular, promovendo migração, adesão, proliferação e diferenciação celular.[0050] And the bone grafts or scaffolds prepared initially from a polymeric sponge of
[0051] Já os enxertos ósseos ou scaffolds preparados inicialmente a partir de uma esponja de poliuretano (PU) de porosidade 35 ppi (pores per inch), obtidos ao final do processo da invenção apresentam porosidade de 83,0 ± 2%, tamanho médio de célula de 770 ± 290 μm e resistência à compressão de 1,0 ± 0,2 MPa. A esponja polimérica de 35 ppi apresenta um tamanho de célula maior o que reflete no resultado final da resistência à compressão[0051] On the other hand, bone grafts or scaffolds prepared initially from a polyurethane sponge (PU) of
[0052] A invenção provê, portanto, um processo para a preparação de enxertos ósseos ou scaffolds a partir de um enxerto ósseo de Biosilicato® que é submetido a tratamentos de revestimento sob vácuo com Biovidro F18 a fim de aumentar sua resistência à compressão de modo a tornar o mesmo aplicável como material de engenharia.[0052] The invention therefore provides a process for the preparation of bone grafts or scaffolds from a Biosilicate® bone graft that is subjected to vacuum coating treatments with Bioglass F18 in order to increase its compressive strength so to make the same applicable as engineering material.
[0053] A invenção provê ainda os enxertos ósseos ou scaffolds resultantes do processo, que apresentam porosidade de 82,0 ± 1,3%, tamanho médio de célula de 525 ± 220 μm e resistência à compressão de 3,3 ± 0,3 MPa.[0053] The invention also provides bone grafts or scaffolds resulting from the process, which have porosity of 82.0 ± 1.3%, average cell size of 525 ± 220 μm and compressive strength of 3.3 ± 0.3 MPa
[0054] Estas propriedades permitem ao enxerto ósseo ou scaffold imitar a estrutura do osso trabecular, facilitando o processo de osteogênese. Além disso, esse biomaterial possui não somente uma alta bioatividade (osteocondução e osteoindução), mas também uma resistência à compressão na faixa de valores do osso trabecular (2–12 MPa), sendo um biomaterial com alto potencial para ser usado na regeneração óssea da mandíbula, onde os enxertos ósseos ou scaffolds não estão sujeitos a forte tensões, provendo a resistência adequada ao tecido durante o processo de cicatrização.[0054] These properties allow the bone graft or scaffold to mimic the structure of trabecular bone, facilitating the osteogenesis process. In addition, this biomaterial has not only a high bioactivity (osteoconduction and osteoinduction), but also a compressive strength in the range of trabecular bone values (2–12 MPa), being a biomaterial with high potential to be used in bone regeneration of the trabecular bone. mandible, where bone grafts or scaffolds are not subjected to strong tensions, providing adequate tissue resistance during the healing process.
[0055] Deste modo, um objetivo da invenção é um processo de preparação de um enxerto ósseo ou scaffold útil na regeneração do osso trabecular. O enxerto ósseo ou scaffold deve ter uma estrutura com porosidade superior a 80%, com poros abertos e altamente interconectados que facilitem a migração, adesão, proliferação e diferenciação de células, estimulando a formação de novo tecido ósseo.[0055] Thus, an object of the invention is a process of preparing a bone graft or scaffold useful in the regeneration of trabecular bone. The bone graft or scaffold must have a structure with porosity greater than 80%, with open and highly interconnected pores that facilitate migration, adhesion, proliferation and differentiation of cells, stimulating the formation of new bone tissue.
[0056] Outro objetivo da invenção é um processo de preparação de um enxerto ósseo ou scaffold de alta bioatividade para facilitar o processo de osteogênese.[0056] Another objective of the invention is a process of preparing a bone graft or scaffold of high bioactivity to facilitate the osteogenesis process.
[0057] Outro objetivo da invenção é um processo de preparação de um enxerto ósseo ou scaffold com resistência à compressão entre 1,00 ± 0,2 MPa e 3,3 ± 0,3 MPa, a partir de moldes de sacrifício do tipo PU com entre 35 e 55 ppi (pores per inch).[0057] Another objective of the invention is a process for preparing a bone graft or scaffold with compressive strength between 1.00 ± 0.2 MPa and 3.3 ± 0.3 MPa, from PU-type sacrificial molds with between 35 and 55 ppi (pores per inch).
[0058] Outro objetivo da invenção é um enxerto ósseo ou scaffold compreendendo uma estrutura de Biosilicato® revestida com Biovidro F18 de modo que a porosidade final esteja compreendida entre 82% e 83%, e o tamanho de célula, entre 525 µm e 770 µm de modo a atingir resistência à compressão entre 1,00 ± 0,2 MPa e 3,3 ± 0,3 MPa.[0058] Another object of the invention is a bone graft or scaffold comprising a Biosilicate® structure coated with Bioglass F18 so that the final porosity is comprised between 82% and 83%, and the cell size, between 525 µm and 770 µm so as to achieve compressive strength between 1.00 ± 0.2 MPa and 3.3 ± 0.3 MPa.
[0059] Ainda outro objetivo da invenção é usar o Biovidro F18 como revestimento do enxerto ósseo ou scaffold. Isto porque o Biovidro F18 flui sem cristalizar em temperaturas acima de 600ºC, unindo as microtrincas nos struts do Biosilicato® reduzindo o tamanho dos poros porém sem que estes sejam obstruídos.[0059] Yet another object of the invention is to use Bioglass F18 as a bone graft coating or scaffold. This is because the Bioglass F18 flows without crystallizing at temperatures above 600ºC, joining the microcracks in the Biosilicate® struts, reducing the size of the pores, but without them being obstructed.
[0060] A FIGURA 1 anexa é um fluxograma ilustrativo das várias etapas do processo de preparação do enxerto ósseo ou scaffold de acordo com a invenção.[0060] The attached FIGURE 1 is an illustrative flowchart of the various steps of the bone graft or scaffold preparation process according to the invention.
[0061] A FIGURA 2 anexa ilustra através de micrografias MEV com ampliação de 500x o efeito de preenchimento de poros de um enxerto ósseo ou scaffold de Biosilicato® (Figura 2A) pela infiltração de Biovidro F18 (Figura 2B) a vácuo conforme o processo do fluxograma da Figura 1. A Figura 2C mostra nitidamente o preenchimento de uma microfissura com Biovidro F18, indicado pela seta azul.[0061] The attached FIGURE 2 illustrates through SEM micrographs with 500x magnification the effect of filling the pores of a bone graft or Biosilicate® scaffold (Figure 2A) by the infiltration of Bioglass F18 (Figure 2B) under vacuum according to the process of flowchart of Figure 1. Figure 2C clearly shows the filling of a microcrack with Bioglass F18, indicated by the blue arrow.
[0062] A FIGURA 3 anexa ilustra a curva de tensão-deformação para os enxertos ósseos ou scaffolds de Biosilicato® usando espuma de PU de 35 ppi.[0062] The attached FIGURE 3 illustrates the stress-strain curve for bone grafts or Biosilicate® scaffolds using 35 ppi PU foam.
[0063] A FIGURA 4 anexa ilustra a curva de tensão-deformação para os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 usando espuma de PU de 35 ppi.[0063] Attached FIGURE 4 illustrates the stress-strain curve for BioS-2P/Bioglass F18 bone grafts or scaffolds using 35 ppi PU foam.
[0064] A FIGURA 5 anexa é um Gráfico de barras comparando as forças à compressão entre os enxertos ósseos de Biosilicato ® e os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 usando espuma de PU de 35 ppi.[0064] Attached FIGURE 5 is a Bar Graph comparing compressive forces between Biosilicate ® bone grafts and BioS-2P/Bioglass F18 bone grafts or scaffolds using 35 ppi PU foam.
[0065] A FIGURA 6 anexa ilustra micrografias obtidas por MEV mostrando a superfície porosa dos enxertos ósseos ou scaffolds de Biosilicato ® obtidos por infiltração em espuma PU de 45 ppi de barbotinas preparadas usando as condições seguintes: FIGURA 6A moagem da barbotina de Biosilicato ® com esferas de ágata de 30 mm de diâmetro a 500 rpm por 10 minutos. Temperatura de sinterização 950°C. Amplificação 100x. FIGURA 6B moagem com esferas de ágata de 30 mm de diâmetro a 500 rpm por 10 minutos. Temperatura de sinterização: 925°C. Amplificação 100x. Para facilitar a penetração das partículas de vidro F18 durante os processos de infiltração a vácuo, struts com superfícies altamente porosas foram gerados. Diferentes tipos de moagem para preparar a barbotina de Biosilicato® foram testados para recobrir as espumas de PU. Além disso, a sinterização foi realizada em diferentes temperaturas, como pode ser observado nas figuras 6A e 6B, visando criar uma superfície altamente porosa.[0065] The attached FIGURE 6 illustrates micrographs obtained by SEM showing the porous surface of the bone grafts or Biosilicate ® scaffolds obtained by infiltration in 45 ppi PU foam of slips prepared using the following conditions: FIGURE 6A milling of the Biosilicate ® slip with 30 mm diameter agate spheres at 500 rpm for 10 minutes. Sintering temperature 950°C. 100x amplification. FIGURE 6B grinding with 30 mm diameter agate beads at 500 rpm for 10 minutes. Sintering temperature: 925°C. 100x amplification. To facilitate the penetration of F18 glass particles during vacuum infiltration processes, struts with highly porous surfaces were generated. Different types of grinding to prepare the Biosilicate® slip were tested to coat the PU foams. Furthermore, the sintering was carried out at different temperatures, as can be seen in Figures 6A and 6B, in order to create a highly porous surface.
[0066] A FIGURA 7 anexa ilustra micrografias MEV obtidas para enxertos ósseos ou scaffolds a partir de espumas de PU de 45 ppi, sob as seguintes condições: a FIGURA 7A mostra micrografia MEV (amplificação 50x) com estrutura porosa de enxerto ósseo ou scaffold altamente interconectada após a infiltração da espuma com a barbotina de Biosilicato® com tamanho de partícula de 45 µm; a FIGURA 7B mostra micrografia MEV (amplificação 50x) após infiltração da estrutura da FIGURA 7A com sucessivos revestimentos com Biovidro F18 com tamanho de partícula de 5 µm conforme o processo da invenção; a FIGURA 7C mostra micrografia MEV (amplificação 500x) mostrando a estrutura oca de enxerto ósseo ou scaffold enquanto a FIGURA 7D mostra a mesma estrutura (amplificação 500x) após sucessivos revestimentos com Biovidro F18, com redução do tamanho de poro, incrementando a resistência mecânica do enxerto obtido.[0066] Attached FIGURE 7 illustrates SEM micrographs obtained for bone grafts or scaffolds from 45 ppi PU foams under the following conditions: FIGURE 7A shows SEM micrograph (50x magnification) with highly porous bone graft or scaffold structure interconnected after infiltration of the foam with Biosilicate® slip with a particle size of 45 µm; FIGURE 7B shows SEM micrograph (50x magnification) after infiltration of the structure of FIGURE 7A with successive coatings with Bioglass F18 with particle size of 5 µm according to the process of the invention; FIGURE 7C shows SEM micrograph (500x amplification) showing the hollow structure of bone graft or scaffold while FIGURE 7D shows the same structure (500x amplification) after successive coatings with Bioglass F18, with pore size reduction, increasing the mechanical strength of the graft obtained.
[0067] A FIGURA 8 anexa são as curvas de tensão/deformação para os enxertos ósseos ou scaffolds de BioS-P2/F18 preparado conforme a invenção a partir de espumas de PU de 35 e 45 ppi.[0067] The attached FIGURE 8 is the stress/strain curves for the bone grafts or scaffolds of BioS-P2/F18 prepared according to the invention from PU foams of 35 and 45 ppi.
[0068] A FIGURA 9 anexa mostra um gráfico de barras comparando as resistências à compressão entre os enxertos ósseos ou scaffolds de BioS2P/Biovidro F18 sintetizados usando espuma de 45ppi e 35 ppi; e os enxertos ósseos ou scaffolds de Biosilicato® sintetizados usando espuma de 35 ppi e 45 ppi. P = porosidade e TC = tamanho da célula.[0068] Attached FIGURE 9 shows a bar graph comparing compressive strengths between BioS2P/Bioglass F18 bone grafts or scaffolds synthesized using 45ppi and 35ppi foam; and Biosilicate® bone grafts or scaffolds synthesized using 35 ppi and 45 ppi foam. P = porosity and TC = cell size.
[0069] A FIGURA 10 anexa é um gráfico que mostra a comparação entre os valores de resistência à compressão, obtidos pelos modelos de Ryshkewitch e Gibson & Ashby e o valor experimental obtido para os scaffolds de BioS2P/Biovidro F18(X = 3,3 MPa). Para uma porosidade = 82%, n = 5 e σo = 250 MPa.[0069] The attached FIGURE 10 is a graph that shows the comparison between the values of compressive strength, obtained by the Ryshkewitch and Gibson & Ashby models and the experimental value obtained for the BioS2P/Bioglass F18 scaffolds (X = 3.3 MPa). For porosity = 82%, n = 5 and σo = 250 MPa.
[0070] Conforme a invenção, os seguintes termos têm a acepção como segue:[0070] According to the invention, the following terms have the meaning as follows:
[0071] Espuma: é uma estrutura celular composta por uma rede de estruturas sólidas nomeadas struts. Os struts são as bordas e faces das células, são a parte sólida da espuma que se encontra nas junções (plateau borders). As espumas de células abertas (por exemplo, espumas reticulares) consistem de células interconectadas que permitem a passagem de um fluido.[0071] Foam: it is a cellular structure composed of a network of solid structures called struts. The struts are the edges and faces of the cells, they are the solid part of the foam that is found at the junctions (plateau borders). Open cell foams (eg reticular foams) consist of interconnected cells that allow a fluid to pass through.
[0072] Enxerto ósseo ou scaffold de Biosilicato®: É um enxerto ósseo ou scaffold preparado conforme os ensinamentos da patente brasileira BR0306444B1, da Requerente e aqui integralmente incorporada como referência.[0072] Biosilicate® bone graft or scaffold: It is a bone graft or scaffold prepared in accordance with the teachings of the Brazilian patent BR0306444B1, of the Applicant and fully incorporated herein by reference.
[0073] BioS-2P é um produto da família Biosilicato® e como tal será usado no presente relatório como equivalente ao Biosilicato®.[0073] BioS-2P is a product of the Biosilicate® family and as such will be used in this report as the equivalent of Biosilicate®.
[0074] Biovidro F18: Enxerto ósseo ou scaffold preparado segundo os ensinamentos do pedido brasileiro BR102013020961, da Requerente e aqui integralmente incorporado como referência.[0074] Bioglass F18: Bone graft or scaffold prepared according to the teachings of Brazilian application BR102013020961, by the Applicant and fully incorporated herein by reference.
[0075] Suspensões para preparação de enxertos ósseos ou scaffolds utilizados na obtenção dos produtos da presente invenção são conforme os ensinamentos da patente brasileira BR1003676B2, da Requerente e aqui integralmente incorporada como referência.[0075] Suspensions for preparing bone grafts or scaffolds used in obtaining the products of the present invention are in accordance with the teachings of the Brazilian patent BR1003676B2, of the Applicant and hereby fully incorporated by reference.
[0076] A presente invenção compreende preparar enxertos ósseos ou scaffolds a partir de revestimento e sinterização de moldes de sacrifício. Esses moldes são materiais comerciais, em geral espumas de poliuretano (PU) com poros por polegada (pores per inch) entre 35 e 55 ppi. Na presente invenção foram utilizadas espumas de PU com 35 ppi e 45 ppi.[0076] The present invention comprises preparing bone grafts or scaffolds from coating and sintering of sacrificial molds. These molds are commercial materials, typically polyurethane (PU) foams with pores per inch between 35 and 55 ppi. In the present invention PU foams with 35 ppi and 45 ppi were used.
[0077] De acordo com o processo de réplica utilizado na invenção, dependendo do tamanho de poros do molde de sacrifício o enxerto ósseo ou scaffold produzido terá poros maiores ou menores, o que é importante no sentido de que o produto final tenha resistência mecânica adequada para a aplicação desejada.[0077] According to the replica process used in the invention, depending on the pore size of the sacrificial mold, the bone graft or scaffold produced will have larger or smaller pores, which is important in the sense that the final product has adequate mechanical strength for the desired application.
[0078] A partir dos experimentos que conduziram ao presente pedido, a Requerente verificou que os poros de enxertos ósseos ou scaffolds obtidos após sinterização de moldes de sacrifício de PU com 35 ppi impregnados com suspensões de Biosilicato® apresentam resistência à compressão relativamente baixa (1,0 ± 0,2) e tamanho de célula (TC) de 770 µm, mesmo após sucessivas impregnações a vácuo com Biovidro F18, vide diagrama de blocos da Figura 9.[0078] From the experiments that led to the present application, the Applicant found that the pores of bone grafts or scaffolds obtained after sintering PU sacrificial molds with 35 ppi impregnated with Biosilicate® suspensions have relatively low compressive strength (1 .0 ± 0.2) and cell size (TC) of 770 µm, even after successive vacuum impregnations with Bioglass F18, see block diagram in Figure 9.
[0079] Já o processo da invenção utilizando como molde de sacrifício um produto PU de 45 ppi, por ter os poros menores (maior número de poros por polegada), estes são preenchidos mais facilmente na etapa de impregnação a vácuo de Biovidro F18, produzindo enxertos ósseos ou scaffolds com resistência à compressão (3,3 ± 0,3 ) e tamanho de célula (TC) de 525 µm, estas sendo faixas adequadas para aplicação do produto obtido como implante trabecular.[0079] On the other hand, the process of the invention using a 45 ppi PU product as a sacrificial mold, as it has smaller pores (greater number of pores per inch), these are filled more easily in the vacuum impregnation step of Bioglass F18, producing bone grafts or scaffolds with compressive strength (3.3 ± 0.3 ) and cell size (TC) of 525 µm, these being suitable ranges for application of the product obtained as a trabecular implant.
[0080] O processo da invenção para a preparação de enxertos ósseos ou scaffolds compreende as Etapas I a VII, que serão detalhadas a seguir. O processo está igualmente apresentado sob forma de fluxograma na Figura 1.[0080] The process of the invention for the preparation of bone grafts or scaffolds comprises Steps I to VII, which will be detailed below. The process is also presented in the form of a flowchart in Figure 1.
[0081] Conforme a Figura 1, na Etapa I, em (110), é feita a preparação do enxerto ósseo ou scaffold de Biosilicato® conforme a patente brasileira PI0300644B1. Para a preparação deste enxerto ósseo ou scaffold é utilizada uma esponja de poliuretano (PU) com abertura média de células na faixa 35-55 ppi (“pores per inch” ou poros por polegada). No caso, a esponja de PU pode apresentar formas geométricas diversas, a forma geométrica não sendo um aspecto limitativo da invenção. Em seguida prepara-se uma barbotina (ou “suspensão”) de Biosilicato®. A composição da barbotina de Biosilicato® é apresentada na Tabela 1. [0081] According to Figure 1, in Step I, in (110), the preparation of the bone graft or scaffold of Biosilicate® is made according to the Brazilian patent PI0300644B1. For the preparation of this bone graft or scaffold, a polyurethane sponge (PU) with an average cell opening in the range 35-55 ppi ("pores per inch" or pores per inch) is used. In this case, the PU sponge can have different geometric shapes, the geometric shape not being a limiting aspect of the invention. A slip (or “suspension”) of Biosilicate® is then prepared. The composition of Biosilicate® slip is shown in Table 1.
[0082] Para a preparação da barbotina, é empregado o Biosilicato® na forma de pó com tamanho médio de partículas de 45 μm (faixa de distribuição de tamanho de partículas: 1-100μm). Além do Biosilicato®, utiliza-se o polivinilbutiral (PVB) como ligante e o álcool etílico anidro como meio líquido. Eventualmente é possível igualmente utilizar outros ligantes como PVA (poli álcoolvinílico) e CMC (carboximetil celulose) e meios líquidos como o álcool isopropílico e até a água, tais aspectos não sendo críticos para o presente processo. Estes materiais são adicionados em um jarro de ágata contendo esferas também de ágata e misturados em moinho planetário a 500 rpm por 30-120 minutos.[0082] For the preparation of the slip, Biosilicate® is used in the form of a powder with an average particle size of 45 μm (particle size distribution range: 1-100μm). In addition to Biosilicate®, polyvinylbutyral (PVB) is used as a binder and anhydrous ethyl alcohol as a liquid medium. Eventually it is also possible to use other binders such as PVA (polyvinyl alcohol) and CMC (carboxymethyl cellulose) and liquid media such as isopropyl alcohol and even water, such aspects being not critical for the present process. These materials are added to an agate jar containing agate beads and mixed in a planetary mill at 500 rpm for 30-120 minutes.
[0083] Note-se que a mistura da barbotina eventualmente também pode ocorrer através de outros métodos de mistura, como por exemplo, em girador de jarros ou através de um agitador mecânico, tal aspecto não sendo crítico para o presente processo.[0083] It should be noted that the slip mixing may also occur through other mixing methods, such as, for example, in a pitcher spinner or through a mechanical stirrer, this aspect being not critical for the present process.
[0084] Em seguida, a espuma de PU é mergulhada na barbotina de Biosilicato®, permanecendo por 5-10 minutos. A espuma infiltrada é removida da barbotina e o excesso de barbotina é removido mecanicamente por compressão (“squeezing”); este procedimento é repetido mais uma vez.[0084] Then the PU foam is dipped in Biosilicate® slip, remaining for 5-10 minutes. The infiltrated foam is removed from the slip and the excess slip is removed mechanically by compression (“squeezing”); this procedure is repeated once more.
[0085] A espuma contendo partículas de Biosilicato® é seca à temperatura ambiente por 24 horas. Após a secagem, a espuma passa pelo primeiro processo de queima. A queima da espuma, por sua vez, é composta pelas seguintes etapas:
- a) Aquecimento a uma taxa de 1-5ºC/min até a temperatura de eliminação (“burn-out”) do ligante (PVB) e da espuma (PU), a 400-450ºC;
- b) Patamar de 4 horas na temperatura de 350-450ºC;
- c) Novo aquecimento a 1-5ºC/min até a temperatura de sinterização do Biosilicato® (900-1.100ºC);
- d) Patamar de 3-5horas na temperatura de 900-1.100ºC; e
- e) Resfriamento até a temperatura ambiente, a uma taxa de 1-5ºC/min.
- a) Heating at a rate of 1-5ºC/min until the burn-out temperature of the binder (PVB) and foam (PU), at 400-450ºC;
- b) Level of 4 hours at a temperature of 350-450ºC;
- c) Reheating at 1-5ºC/min until the Biosilicate® sintering temperature (900-1,100ºC);
- d) Level of 3-5 hours at a temperature of 900-1,100ºC; and
- e) Cooling to room temperature at a rate of 1-5°C/min.
[0086] O processo de sinterização do Biosilicato® ocorre em temperaturas altas (~ 1.000ºC) e pelo mecanismo de reação no estado sólido, pois este material é uma vitrocerâmica totalmente cristalina e não um biovidro. Portanto, a sinterização do Biosilicato® é um processo mais lento, podendo haver microporos e trincas residuais ao final do processo.[0086] The sintering process of Biosilicate® occurs at high temperatures (~ 1,000ºC) and by the reaction mechanism in the solid state, as this material is a fully crystalline glass-ceramic and not a bioglass. Therefore, the sintering of Biosilicate® is a slower process, and there may be micropores and residual cracks at the end of the process.
[0087] Através deste procedimento, obtém-se o enxerto ósseo ou scaffold de Biosilicato® (com resistência mecânica inferior a 0.1 MPa), a ser utilizado nas etapas posteriores. Devido à sua baixa resistência mecânica, o enxerto ósseo ou scaffold deve ser manuseado com extremo cuidado.[0087] Through this procedure, the bone graft or scaffold of Biosilicate® (with mechanical strength less than 0.1 MPa) is obtained, to be used in later stages. Due to its low mechanical strength, the bone graft or scaffold must be handled with extreme care.
[0088] Na Etapa II seguinte, em (120), o enxerto ósseo ou scaffold de Biosilicato® é infiltrado sob vácuo (-400mmHg a -600mmHg) com uma barbotina de Biosilicato® cuja composição (Tabela 1) foi descrita na Etapa I; entretanto utiliza-se um pó de Biosilicato® com tamanho médio de partículas de 5 μm (faixa de distribuição de tamanho de partículas: 0,1-20 μm).[0088] In the following Step II, in (120), the bone graft or Biosilicate® scaffold is infiltrated under vacuum (-400mmHg to -600mmHg) with a Biosilicate® slip whose composition (Table 1) was described in Step I; however, a Biosilicate® powder with an average particle size of 5 μm is used (particle size distribution range: 0.1-20 μm).
[0089] Para as finalidades da invenção foi construído um aparato especifico para a infiltração do enxerto ósseo ou scaffold sob vácuo (não representado); entretanto, outros dispositivos podem ser utilizados desde que a operação seja realizada sob vácuo. Em resumo, a infiltração sob vácuo compreende as seguintes operações:
- a) O enxerto ósseo ou scaffold é colocado dentro de um recipiente no interior de uma câmara de vácuo;
- b) O vácuo (-400mmHg a -600mmHg) é aplicado;
- c) A barbotina é vertida sobre o(s) enxerto(s) ósseo(s) ou scaffold(s);
- d) Após 5-10 minutos, o vácuo é removido;
- e) O enxerto ósseo ou scaffold é retirado da câmara de vácuo e o excesso de barbotina é removido dos macroporos com o auxílio de uma pistola de ar comprimido; e
- f) O enxerto ósseo ou scaffold é seco à temperatura ambiente por 12- 24 horas e está pronto para ser utilizado na etapa seguinte.
- a) The bone graft or scaffold is placed inside a container inside a vacuum chamber;
- b) Vacuum (-400mmHg to -600mmHg) is applied;
- c) The slip is poured over the bone graft(s) or scaffold(s);
- d) After 5-10 minutes, the vacuum is removed;
- e) The bone graft or scaffold is removed from the vacuum chamber and the excess slip is removed from the macropores with the aid of a compressed air gun; and
- f) The bone graft or scaffold is dried at room temperature for 12-24 hours and is ready to be used in the next step.
[0090] Na Etapa III, em (130), o enxerto ósseo ou scaffold de Biosilicato® que foi infiltrado novamente com a barbotina de Biosilicato® é submetido à queima, empregando-se o mesmo procedimento descrito na Etapa I acima no presente relatório.[0090] In Step III, in (130), the bone graft or Biosilicate® scaffold that was infiltrated again with the Biosilicate® slip is submitted to firing, using the same procedure described in Step I above in this report.
[0091] Na Etapa IV em (140), o enxerto ósseo ou scaffold de Biosilicato® é infiltrado sob vácuo por uma barbotina à base de Biovidro F18 (biovidro objeto da patente US9731994B2 correspondente ao pedido brasileiro BR102013020961).[0091] In Step IV in (140), the bone graft or Biosilicate® scaffold is infiltrated under vacuum by a slip based on Bioglass F18 (bioglass object of patent US9731994B2 corresponding to the Brazilian application BR102013020961).
[0092] A composição da barbotina de Biovidro F18 é apresentada na Tabela 2: [0092] The composition of Bioglass F18 slip is shown in Table 2:
[0093] Para a determinação do tamanho médio de partículas (PSD – particle size distribution) é utilizado o analisador de tamanho de partícula (Horiba-LA-93) em meio álcool isopropílico (99,5%-QHEMIS).[0093] To determine the particle size distribution (PSD) the particle size analyzer (Horiba-LA-93) is used in isopropyl alcohol (99.5%-QHEMIS).
[0094] A preparação da barbotina de Biovidro F18 é similar à preparação da barbotina de Biosilicato®: é empregado o Biovidro F18 na forma de pó com tamanho médio de partículas de 5 μm (faixa de distribuição de tamanho de partículas: 0,1-20 μm). Além do Biovidro F18, utiliza-se o polivinilbutiral (PVB) em pó como ligante, o álcool etílico anidro como meio líquido.[0094] The preparation of Bioglass F18 slip is similar to the preparation of Biosilicate® slip: Bioglass F18 is used in the form of a powder with an average particle size of 5 μm (particle size distribution range: 0.1- 20 μm). In addition to Bioglass F18, powdered polyvinylbutyral (PVB) is used as a binder and anhydrous ethyl alcohol as a liquid medium.
[0095] Eventualmente é possível utilizar outros ligantes como PVA (poliálcoolvinílico) e CMC (carboximetil celulose) e meios líquidos como o álcool isopropílico e até a água, esse aspecto não sendo crítico para o presente processo.[0095] Eventually it is possible to use other binders such as PVA (polyvinyl alcohol) and CMC (carboxymethyl cellulose) and liquid media such as isopropyl alcohol and even water, this aspect being not critical for the present process.
[0096] Estes materiais são adicionados em um jarro de ágata contendo esferas de ágata e misturados em moinho planetário a 500 rpm por 30-120 minutos.[0096] These materials are added to an agate jar containing agate beads and mixed in a planetary mill at 500 rpm for 30-120 minutes.
[0097] A mistura da barbotina eventualmente também pode ocorrer através de outros métodos de mistura, como por exemplo, em girador de jarros ou através de um agitador mecânico, esse aspecto não sendo crítico para o presente processo.[0097] The slip mixing may also occur through other mixing methods, such as, for example, in a pitcher spinner or through a mechanical stirrer, this aspect being not critical for the present process.
[0098] O procedimento de infiltração do enxerto ósseo ou scaffold de Biosilicato® com a barbotina de Biovidro F18 é análogo ao descrito na Etapa II acima no presente relatório.[0098] The procedure for infiltrating the bone graft or Biosilicate® scaffold with the Bioglass F18 slip is analogous to that described in Step II above in this report.
[0099] Na Etapa V, em (150), o enxerto ósseo ou scaffold de Biosilicato® que foi infiltrado com a barbotina de Biovidro F18 é submetido à queima, sendo empregado o seguinte procedimento:
- a) Aquecimento a uma taxa de 1-5ºC/min até a temperatura de eliminação (“burn-out”) do ligante (PVB), a 400-450ºC;
- b) Patamar de 4 horas na temperatura de 400-450ºC;
- c) Novo aquecimento a 1-5ºC/min até a temperatura de sinterização do Biovidro F18 (600-900ºC);
- d) Patamar de 3-5horas na temperatura de 600-900ºC; e
- e) Resfriamento até a temperatura ambiente, a uma taxa de 1-5ºC/min.
- a) Heating at a rate of 1-5ºC/min until the burn-out temperature of the binder (PVB), at 400-450ºC;
- b) Level of 4 hours at a temperature of 400-450ºC;
- c) Reheating at 1-5ºC/min until the sintering temperature of Bioglass F18 (600-900ºC);
- d) Level of 3-5 hours at a temperature of 600-900ºC; and
- e) Cooling to room temperature at a rate of 1-5°C/min.
[00100] Diferentemente do Biosilicato®, o Biovidro F18 é sinterizado em baixas temperaturas e pelo mecanismo de escoamento viscoso (ou “viscous flow”). A alta estabilidade deste biovidro frente à cristalização permite que o mesmo flua durante o processo, preenchendo poros pequenos e microtrincas. A estrutura oca do enxerto ósseo ou scaffold também é preenchida durante o processo de infiltração, tornando-se sólida após a sinterização. Além disso, obtém-se uma superfície lisa e isenta de defeitos. Tudo isso contribui para o aumento da resistência mecânica final do enxerto ósseo ou scaffold.[00100] Unlike Biosilicate®, Bioglass F18 is sintered at low temperatures and by the viscous flow mechanism (or “viscous flow”). The high stability of this bioglass against crystallization allows it to flow during the process, filling small pores and microcracks. The hollow structure of the bone graft or scaffold is also filled during the infiltration process, becoming solid after sintering. In addition, a smooth, defect-free surface is obtained. All this contributes to increasing the final mechanical strength of the bone graft or scaffold.
[00101] Na Etapa VI, em (160), são repetidas as Etapas IV (140), e V (150), acima no presente relatório. Opcionalmente, a Etapa VI pode ser repetida mais vezes, mais deve-se levar em conta que a porosidade do scaffold deve ser superior a 80% e o tamanho da célula superior a 300 µm.[00101] In Step VI, in (160), Steps IV (140) and V (150) above are repeated in this report. Optionally, Step VI can be repeated more times, taking into account that the porosity of the scaffold must be greater than 80% and the cell size greater than 300 µm.
[00102] Na Etapa VII em (170), é recuperado o produto da invenção, enxerto ósseo ou scaffold, Biosilicato®/Biovidro F18, com uma estrutura altamente porosa e interconectada e com resistência mecânica superior a 3 MPa, ou seja, compatível com os enxertos ósseos ou scaffolds na forma de pequenos blocos existentes no mercado. A presença do Biovidro F18 aumenta o efeito bactericida do enxerto ósseo ou scaffold.[00102] In Step VII in (170), the product of the invention is recovered, bone graft or scaffold, Biosilicate®/Biovidro F18, with a highly porous and interconnected structure and with mechanical strength greater than 3 MPa, that is, compatible with bone grafts or scaffolds in the form of small blocks available on the market. The presence of Bioglass F18 increases the bactericidal effect of the bone graft or scaffold.
[00103] O produto da invenção, enxerto ósseo ou scaffold de Biosilicato®/Biovidro F18 deve ser caracterizado com o auxílio de várias técnicas analíticas.[00103] The product of the invention, bone graft or Biosilicate®/Bioglass F18 scaffold must be characterized with the aid of several analytical techniques.
[00104] Análises de Microscopia Eletrônica de Varredura (MEV) permitiram observar as microestruturas das amostras sinterizadas obtidas pela técnica da réplica. Equipamentos: FEG Philips (XL-30) do laboratório de caracterização estrutural (LCE-DEMa/UFSCar) e o equipamento FEI (PHENOMTM) do laboratório de materiais vítreos (LaMaV/UFSCar). As amostras foram cobertas com ouro por 180 segundos.[00104] Scanning Electron Microscopy (SEM) analyzes allowed the observation of the microstructures of the sintered samples obtained by the replica technique. Equipment: Philips FEG (XL-30) from the structural characterization laboratory (LCE-DEMa/UFSCar) and the FEI equipment (PHENOMTM) from the vitreous materials laboratory (LaMaV/UFSCar). The samples were covered with gold for 180 seconds.
[00105] Já a porosidade foi calculada através da densidade geométrica. Primeiro, para os enxertos ósseos ou scaffolds com forma de prisma foi medido o comprimento, a altura e a largura do prisma em suas quatro faces e para as amostras cilíndricas foi medido o diâmetro e a altura, e o valor médio foi calculado. Com esses dados, calculou-se o volume médio dos diferentes corpos de prova e determinou-se a densidade de cada enxerto ósseo ou scaffold usando seu peso. Foi calculada a densidade média para cada tipo de enxerto ósseo ou scaffold. Finalmente, foi determinada a porosidade média de cada tipo de enxerto ósseo ou scaffold, usando a Equação 1, onde o valor da densidade do Biosilicato® é de 2,79 g.cm-3 [00105] The porosity was calculated through the geometric density. First, for bone grafts or prism-shaped scaffolds, the length, height and width of the prism on its four faces were measured, and for cylindrical samples, the diameter and height were measured, and the mean value was calculated. With these data, the average volume of the different specimens was calculated and the density of each bone graft or scaffold was determined using its weight. The mean density was calculated for each type of bone graft or scaffold. Finally, the average porosity of each type of bone graft or scaffold was determined, using Equation 1, where the Biosilicate® density value is 2.79 g.cm-3
[00106] O tamanho médio dos poros foi medido com auxílio do software Image-J.[00106] The average pore size was measured using Image-J software.
[00107] A Tabela 3 abaixo lista os valores de porosidade total, tamanho médio das células e resistência à compressão para os enxertos ósseos ou scaffolds de Biosilicato obtidos com espuma de 35 ppi antes e depois do revestimento com a barbotina de F18. [00107] Table 3 below lists the total porosity, average cell size and compressive strength values for bone grafts or Biosilicate scaffolds obtained with 35 ppi foam before and after coating with F18 slip.
[00108] Os testes mecânicos evidenciaram que as resistências à compressão dos enxertos ósseos ou scaffolds de Biosilicato são muito baixas (Figura 3 anexa), apresentando uma resistência à compressão média de 0,020 ± 0,005 MPa. Além da alta porosidade e um tamanho médio de célula elevado, outro dos fatores que contribuiu significativamente na diminuição da força mecânica dos enxertos ósseos ou scaffolds de Biosilicato foi a porosidade interna gerada pela queima da esponja durante a sinterização. Para os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18, foi observada uma resistência média à compressão de 1,0 ± 0,2 MPa (Figura 4 anexa), gerando um incremento de cerca de 50 vezes do valor encontrado para os enxertos ósseos ou scaffolds de Biosilicato® (Figura 5 anexa). Esse aumento da resistência à compressão está relacionado com os diversos revestimentos com a barbotina de Biovidro F18. Esta foi capaz de penetrar nos poros da superfície das estruturas e infiltrar parcialmente a estrutura oca dos enxertos ósseos ou scaffolds de Biosilicato®. Este aumento na resistência mecânica também está relacionado com a diminuição da porosidade total e do tamanho médio das células dos enxertos ósseos ou scaffolds de Biosilicato® (Figura 5 e Tabela 3 acima).[00108] The mechanical tests showed that the compressive strengths of bone grafts or Biosilicate scaffolds are very low (Figure 3 attached), with an average compressive strength of 0.020 ± 0.005 MPa. In addition to the high porosity and high average cell size, another factor that significantly contributed to the decrease in the mechanical strength of bone grafts or Biosilicate scaffolds was the internal porosity generated by the burning of the sponge during sintering. For bone grafts or BioS-2P/Bioglass F18 scaffolds, an average compressive strength of 1.0 ± 0.2 MPa was observed (Figure 4 attached), generating an increase of about 50 times the value found for the grafts. bones or Biosilicate® scaffolds (Figure 5 attached). This increase in compressive strength is related to the different coatings with Bioglass F18 slip. This was able to penetrate the surface pores of the structures and partially infiltrate the hollow structure of the bone grafts or Biosilicate® scaffolds. This increase in mechanical strength is also related to the decrease in total porosity and average cell size of bone grafts or Biosilicate® scaffolds (Figure 5 and Table 3 above).
[00109] As microtrincas e irregularidades na superfície dos scaffolds cerâmicos obtidos pela técnica da réplica são geradas por um recobrimento deficiente da barbotina na superfície da esponja de PU. Além disso, durante o tratamento térmico, a defasagem entre a expansão térmica da espuma de PU e o recobrimento cerâmico gera esses tipos de defeitos de superfície, o que diminui fortemente as propriedades mecânicas das espumas cerâmicas ou scaffolds. Quando o scaffold de Biosilicato® foi infiltrado com a barbotina de Biovidro F18, o vácuo permitiu que a barbotina conseguisse penetrar nas microtrincas e microporosidade sobre a superfície dos struts, o qual permitiu um incremento considerável da resistência à compressão e da uniformidade estrutural. A camada de Biovidro F18 depositada na superfície dos scaffolds de Biosilicato® aumentou a espessura dos struts diminuindo a porosidade total e o tamanho médio das células dos enxertos ósseos ou scaffolds de Biosilicato® (Figura 5 e Tabela 3 acima), que por sua vez incrementou sua integridade mecânica. Ademais, as partículas de Biovidro F18 foram capazes de penetrar nos poros da superfície dos scaffolds de Biosilicato® e infiltrar parcialmente os struts porosos dos enxertos ósseos ou scaffolds de Biosilicato®. Apesar do aumento considerável na resistência à compressão (50 vezes), o valor mínimo desejado não foi atingido, ou seja, valores na faixa de resistência à compressão do osso trabecular (2-12 MPa). Um valor mínimo de 2 MPa permite o uso desse tipo de biomateriais nos processos de regeneração óssea, em locais onde o osso não está sujeito a altas tensões, como a mandíbula. Além disso, apesar de serem necessário tamanhos de poros > 300 µm para a formação de tecido ósseo e vascularização, um tamanho de poros muito grande esta associado a uma baixa taxa de crescimento ósseo, além de comprometer consideravelmente as propriedades mecânicas do scaffold.[00109] The microcracks and irregularities on the surface of the ceramic scaffolds obtained by the replica technique are generated by a poor coating of the slip on the surface of the PU sponge. Furthermore, during the heat treatment, the lag between the thermal expansion of the PU foam and the ceramic coating generates these types of surface defects, which greatly diminish the mechanical properties of the ceramic foams or scaffolds. When the Biosilicate® scaffold was infiltrated with the F18 Bioglass slip, the vacuum allowed the slip to penetrate the microcracks and microporosity on the surface of the struts, which allowed a considerable increase in compressive strength and structural uniformity. The layer of Bioglass F18 deposited on the surface of the Biosilicate® scaffolds increased the thickness of the struts, decreasing the total porosity and the average cell size of the bone grafts or Biosilicate® scaffolds (Figure 5 and Table 3 above), which in turn increased its mechanical integrity. Furthermore, the Bioglass F18 particles were able to penetrate the surface pores of the Biosilicate® scaffolds and partially infiltrate the porous struts of the bone grafts or Biosilicate® scaffolds. Despite the considerable increase in compressive strength (50 times), the minimum desired value was not reached, ie, values in the range of compressive strength of trabecular bone (2-12 MPa). A minimum value of 2 MPa allows the use of this type of biomaterials in bone regeneration processes, in places where the bone is not subject to high stresses, such as the mandible. Furthermore, although pore sizes > 300 µm are required for bone tissue formation and vascularization, a very large pore size is associated with a low rate of bone growth, in addition to considerably compromising the mechanical properties of the scaffold.
[00110] A fim de obter resultados aperfeiçoados na infiltração da barbotina na estrutura oca dos enxertos ósseos, o processo da invenção contempla duas providências:
- a) Usar um pó de Biosilicato® grosso (45 µm) no primeiro procedimento de infiltração para aumentar a porosidade na superfície dos enxertos ósseos ou scaffolds, facilitando a penetração da barbotina nas subsequentes infiltrações; e
- b) Usar pós muito finos (5 µm) para a preparação das barbotinas usadas nas seguintes infiltrações, facilitando a penetração das barbotinas no interior da estrutura oca dos enxertos ósseos ou scaffolds.
- a) Use a coarse Biosilicate® powder (45 µm) in the first infiltration procedure to increase the porosity on the surface of the bone grafts or scaffolds, facilitating the penetration of the slip in the subsequent infiltrations; and
- b) Use very fine powders (5 µm) for the preparation of the slips used in the following infiltrations, facilitating the penetration of the slips inside the hollow structure of the bone grafts or scaffolds.
[00111] O tamanho médio de células para a espuma de PU (45 ppi) foi 590 ± 170 μm e para os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 foi 525 ± 220 μm. Além disso, as distribuições de tamanho de partícula foram encontradas na faixa de 310-1230 μm e 230-1140 μm, respectivamente.[00111] The mean cell size for the PU foam (45 ppi) was 590 ± 170 μm and for the bone grafts or BioS-2P/Bioglass F18 scaffolds it was 525 ± 220 μm. Furthermore, particle size distributions were found in the range of 310-1230 μm and 230-1140 μm, respectively.
[00112] A porosidade total dos enxertos ósseos ou scaffolds de BioS2P/Biovidro F18 sintetizados usando a espuma de 45 ppi foi de 82,0 ± 1,3% (Tabela 4). Esse valor é muito próximo ao apresentado por scaffolds de BioS-2P/ Biovidro F18 obtidos com a espuma de 35 ppi, 83%. Quando se compara o tamanho médio de célula da espuma de 45 ppi (590 μm) e o tamanho médio de célula dos scaffolds de BioS-2P/Biovidro F18 (525 μm) também obtidos com a espuma de 45 ppi pode-se observar que esses valores são semelhantes. Isso é devido a que o encolhimento linear durante o processo de sinterização foi pequeno.[00112] The total porosity of the BioS2P/Bioglass F18 bone grafts or scaffolds synthesized using the 45 ppi foam was 82.0 ± 1.3% (Table 4). This value is very close to that presented by BioS-2P/Bioglass F18 scaffolds obtained with 35 ppi foam, 83%. When comparing the average cell size of the 45 ppi foam (590 μm) and the average cell size of the BioS-2P/Bioglass F18 scaffolds (525 μm) also obtained with the 45 ppi foam, it can be observed that these values are similar. This is because the linear shrinkage during the sintering process was small.
[00113] Após os recobrimentos com Biovidro F18, o biovidro infiltrou-se nas microtrincas na superfície dos enxertos ósseos ou scaffolds de Biosilicato®, ajudando a consolidar a estrutura. Esta camada homogênea de Biovidro F18 na superfície dos scaffolds de Biosilicato® aumentou a espessura dos struts fortalecendo a estrutura. Além disso, o vidro penetrou no interior dos struts preenchendo parcialmente a porosidade interna da estrutura.[00113] After coatings with Bioglass F18, the bioglass infiltrated the microcracks on the surface of the bone grafts or Biosilicate® scaffolds, helping to consolidate the structure. This homogeneous layer of Bioglass F18 on the surface of the Biosilicate® scaffolds increased the thickness of the struts, strengthening the structure. In addition, the glass penetrated the interior of the struts, partially filling the internal porosity of the structure.
[00114] Outros fatores tais como menor tamanho de poros (525 μm) e menor porosidade (82%) do scaffold de Biosilicato® sintetizado com esponja de 45 ppi aumentaram a resistência à compressão do Biomaterial.[00114] Other factors such as smaller pore size (525 μm) and lower porosity (82%) of the Biosilicate® scaffold synthesized with a 45 ppi sponge increased the compressive strength of the Biomaterial.
[00115] Considerando que os struts da espuma de PU de 45 ppi são mais finos que os struts da espuma de PU de 35 ppi, a porosidade interna resultante nos struts durante a pirólise da espuma tem um volume menor, aumentando a estabilidade mecânica dos enxertos ósseos ou scaffolds.[00115] Considering that 45 ppi PU foam struts are thinner than 35 ppi PU foam struts, the resulting internal porosity in the struts during foam pyrolysis has a smaller volume, increasing the mechanical stability of the grafts bones or scaffolds.
[00116] Uma estrutura altamente porosa e interconectada com tamanho de célula de 525 μm e porosidade acima de 80% são essenciais para a penetração e a migração celular, crescimento do tecido, angiogênese e transporte de nutrientes, oxigênio e resíduos.[00116] A highly porous and interconnected structure with a cell size of 525 μm and porosity above 80% are essential for cell penetration and migration, tissue growth, angiogenesis and transport of nutrients, oxygen and waste.
[00117] Verifica-se igualmente que o enxerto ósseo ou scaffold obtido pelo processo da invenção a partir de espuma de PU de 45 ppi apresenta resistência à compressão útil para aplicações em regeneração de tecido ósseo em locais onde o enxerto ósseo ou scaffold não está sujeito a altas tensões como em cirurgia de elevação de seio ou de aumento vertical.[00117] It is also verified that the bone graft or scaffold obtained by the process of the invention from PU foam of 45 ppi presents compressive strength useful for applications in bone tissue regeneration in places where the bone graft or scaffold is not subject to to high tensions as in breast lift or vertical augmentation surgery.
[00118] Os resultados de porosidade total, tamanho médio de célula e resistência à compressão para produtos conforme a invenção, obtidos a partir de espuma de PU de 35 e 45 ppi respectivamente estão listados na Tabela 4 a seguir. [00118] The results of total porosity, average cell size and compressive strength for products according to the invention, obtained from PU foam of 35 and 45 ppi respectively are listed in Table 4 below.
[00119] A partir dos resultados expressos na Tabela 4 acima é nítida a influência do tamanho médio de célula no desempenho do produto obtido no que diz respeito à resistência à compressão. No caso da espuma de partida ter 35 ppi, menos poros por polegada, o enxerto ósseo ou scaffold apresenta tamanho médio de célula tal que a infiltração efetuada com barbotina de Biovidro F18 não atinge um preenchimento de poros e tamanho de célula do enxerto ósseo ou scaffold tal que o produto recuperado apresente resistência à compressão adequada para as aplicações desejadas. Ao contrário, o enxerto ósseo ou scaffold obtido com espuma de 45 ppi tem tamanho médio de célula menor, na faixa adequada para que, após infiltração com barbotina de Biovidro F18 apresente resistência à compressão adequada para a finalidade desejada.[00119] From the results expressed in Table 4 above, the influence of the average cell size on the performance of the product obtained with regard to compressive strength is clear. In case the starting foam has 35 ppi, less pores per inch, the bone graft or scaffold has an average cell size such that the infiltration performed with Bioglass F18 slip does not reach a pore filling and cell size of the bone graft or scaffold such that the recovered product has adequate compressive strength for the desired applications. On the contrary, the bone graft or scaffold obtained with 45 ppi foam has a smaller average cell size, in the appropriate range so that, after infiltration with Bioglass F18 slip, it presents adequate compressive strength for the desired purpose.
[00120] A Figura 8 é um gráfico que mostra o bom resultado da curva de tensão/deformação para o enxerto ósseo ou scaffold de BioS-2P/Biovidro F18 sintetizado usando uma espuma de PU de 45 ppi. Esta curva é comparada com a curva de tensão/deformação para o enxerto ósseo ou scaffold de BioS-2P/Biovidro F18 sintetizado usando uma espuma de PU de 35 ppi.[00120] Figure 8 is a graph showing the good stress/strain curve result for the BioS-2P/Bioglass F18 bone graft or scaffold synthesized using a 45 ppi PU foam. This curve is compared to the stress/strain curve for the BioS-2P/Bioglass F18 bone graft or scaffold synthesized using a 35 ppi PU foam.
[00121] A este respeito também a Figura 9 é interessante, mostrando não só os resultados da Tabela 4, mas adicionalmente, os mesmos parâmetros medidos para o enxerto ósseo ou scaffold de Biosilicato® sem infiltração de barbotina de Biovidro F18. A Figura 9 ilustra deste modo a influência do número de poros por polegada da espuma (35 ou 45 ppi), que se reflete no tamanho médio de célula do enxerto ósseo ou scaffold obtido, seja somente de Biosilicato® ou seja o produto final do presente processo, após infiltração do enxerto ósseo ou scaffold de Biosilicato® com barbotina de Biovidro F18. A combinação desses fatores determina então a resistência à compressão do produto.[00121] In this regard also Figure 9 is interesting, showing not only the results of Table 4, but additionally, the same parameters measured for the bone graft or scaffold of Biosilicate® without infiltration of slip of Bioglass F18. Figure 9 thus illustrates the influence of the number of pores per inch of the foam (35 or 45 ppi), which is reflected in the average cell size of the bone graft or scaffold obtained, whether only of Biosilicate® or the final product of the present process, after infiltration of the bone graft or Biosilicate® scaffold with Bioglass F18 slip. The combination of these factors then determines the compressive strength of the product.
[00122] Para demonstrar que os resultados obtidos durante as pesquisas da Requerente que conduziram ao presente pedido estavam de acordo com um modelo teórico, a Figura 10 mostra a comparação entre os valores calculados usando os modelos de Ryshkewitch e Gibson & Ashby e os dados experimentais obtidos para os scaffolds de BioS-2P/Biovidro F18 (espuma de 45 ppi), quando n = 5, σo = 250 MPa e a porosidade é 82%.[00122] To demonstrate that the results obtained during the Applicant's research that led to the present application were in accordance with a theoretical model, Figure 10 shows the comparison between the values calculated using the models of Ryshkewitch and Gibson & Ashby and the experimental data obtained for the BioS-2P/Bioglass F18 scaffolds (45 ppi foam), when n = 5, σo = 250 MPa and the porosity is 82%.
[00123] Como pode ser observado na Tabela 5, o valor experimental foi próximo do valor teórico. No entanto, foi menor, pois o modelo Ryshkewitch é para materiais densos e o modelo Gibson & Ashby modificado assume que a estrutura não é oca na região central dos struts. Por esses motivos, esperava-se que o valor experimental fosse menor. Além disso, o valor exato de n e σo para os scaffolds de BioS-2P/Biovidro F18 são desconhecidos. Parece que os dados experimentais se ajustaram bem a ambos os modelos quando n = 5 e σo = 250 MPa; apesar desse fato, seria necessário determinar os valores exatos dessas constantes para saber se os dados experimentais realmente se encaixam bem nos dois modelos. Por outro lado, uma possível estratégia para aumentar a resistência mecânica dos enxertos ósseos ou scaffolds seria usar uma espuma de 60 ppi que possuía um tamanho de strut menor. No momento da queima dos struts da espuma, a parte oca deixada pela esponja seria menor devido a que seu tamanho é mais reduzido. Embora a espuma de 60 ppi tenha um tamanho de célula médio próximo (tamanho médio = 370µm, distribuição de tamanho = 140–640µm) ao limite inferior (300 µm) necessário para aplicações em regeneração óssea, provavelmente a redução do tamanho da célula durante o processo de sinterização seria pequeno por causa do pouco encolhimento linear, conservando o tamanho de célula ideal para a regeneração óssea. Um comportamento similar foi observado quando o tamanho da célula de espuma diminuiu de 35 ppi para 45 ppi. Logo, espera-se que uma espuma com tamanho de célula menor (370µm) e pós moídos com moinho vibratório representem condições que reduzam a porosidade interna dos scaffolds após revestimentos a vácuo com a barbotina de Biovidro F18 de modo a aumentar sua resistência mecânica.[00123] As can be seen in Table 5, the experimental value was close to the theoretical value. However, it was smaller, as the Ryshkewitch model is for dense materials and the modified Gibson & Ashby model assumes that the structure is not hollow in the central region of the struts. For these reasons, the experimental value was expected to be lower. Furthermore, the exact value of n and σo for the BioS-2P/Bioglass F18 scaffolds are unknown. It seems that the experimental data fit both models well when n = 5 and σo = 250 MPa; despite this fact, it would be necessary to determine the exact values of these constants in order to know whether the experimental data really fit the two models well. On the other hand, a possible strategy to increase the mechanical strength of bone grafts or scaffolds would be to use a 60 ppi foam that had a smaller strut size. At the time of burning the foam struts, the hollow part left by the sponge would be smaller due to its smaller size. Although the 60 ppi foam has an average cell size close to (average size = 370µm, size distribution = 140–640µm) to the lower limit (300 µm) required for bone regeneration applications, probably the reduction in cell size during sintering process would be small because of little linear shrinkage, conserving the ideal cell size for bone regeneration. A similar behavior was observed when the foam cell size decreased from 35 ppi to 45 ppi. Therefore, it is expected that a foam with a smaller cell size (370µm) and powders ground with a vibrating mill represent conditions that reduce the internal porosity of the scaffolds after vacuum coatings with Bioglass F18 slip in order to increase their mechanical strength.
[00124] A Tabela 1 lista os valores da resistência à compressão determinados pelos modelos Ryshkewitch e Gibson & Ashby e os dados experimentais obtidos para os scaffolds de BioS-2P/Biovidro F18 sintetizados com esponja de 45 ppi. A porosidade para os dados calculados e experimentais foi de 82%. [00124] Table 1 lists the compressive strength values determined by the Ryshkewitch and Gibson & Ashby models and the experimental data obtained for the BioS-2P/Bioglass F18 scaffolds synthesized with a 45 ppi sponge. The porosity for the calculated and experimental data was 82%.
[00125] Portanto, o resultado obtido pela aplicação do presente processo está conforme com o modelo teórico de Ryshkewitch e Gibson & Ashby,[00125] Therefore, the result obtained by the application of the present process is in accordance with the theoretical model of Ryshkewitch and Gibson & Ashby,
[00126] A adequação do produto enxerto ósseo ou scaffold à utilização pretendida em humanos deve atender a certos critérios, pelo que foram efetuados testes in vitro tal como descrito a seguir.[00126] The suitability of the bone graft or scaffold product for its intended use in humans must meet certain criteria, so in vitro tests were performed as described below.
[00127] Para efetuar os testes in vitro foram usadas células-tronco mesenquimais derivadas de tecido adiposo humano (human adipose-derivated stem cells–hASCs) (Sciencell), as quais foram mantidas em atmosfera de Nitrogênio em recipiente criogênico (Thermo Scientific–model 316306). Todas as culturas celulares foram feitas em cabine de segurança biológicas (Microzone Corporation-model BK-2-4) sob condições esterilizadas.[00127] To perform the in vitro tests, mesenchymal stem cells derived from human adipose tissue (human adipose-derivated stem cells–hASCs) (Sciencell) were used, which were kept in a nitrogen atmosphere in a cryogenic container (Thermo Scientific–model 316306). All cell cultures were performed in a biological safety cabinet (Microzone Corporation-model BK-2-4) under sterile conditions.
[00128] As células foram passadas a placas de 6 poços para expansão usando meio de cultura para células-tronco mesenquimais (MSCM) (SciencellCanada). A expansão foi feita segundo as recomendações do fabricante do kit. As placas foram incubadas por 4 dias a 37 ºC com 5% de CO2 em incubadora de CO2 (ThermoScientific–Steri-Cycle) até atingir confluência completa. O MSCM foi trocado a cada dois dias. Para o processo de diferenciação foram usadas as células da segunda, terceira e quarta passagem, as quais foram subcultivadas usando MSCM e enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 com MSCM, como explicado abaixo.[00128] Cells were passaged to 6-well plates for expansion using Mesenchymal Stem Cell Culture Medium (MSCM) (SciencellCanada). The expansion was performed according to the kit manufacturer's recommendations. The plates were incubated for 4 days at 37°C with 5% CO2 in a CO2 incubator (ThermoScientific–Steri-Cycle) until complete confluence. The MSCM was changed every two days. Second, third and fourth passage cells were used for the differentiation process, which were subcultured using MSCM and bone grafts or BioS-2P/Bioglass F18 scaffolds with MSCM, as explained below.
[00129] Após completa confluência, as células foram subcultivadas em uma placa de 24 poços a uma densidade de 1 x 105 células.cm-2 , usando 0,5 mL de MSCM por poço e as placas foram incubadas a 37 °C com 5% de CO2 em incubadora por 4 dias até 95-100% de confluência. Estas células foram utilizadas como controles e outras como amostras nomeadas grupo dos íons. No grupo dos íons, o meio osteogênico usado para diferenciar as células foi colocado em contato como os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 por 48 horas a 37°C. Este processo permitiu extrair os íons dos enxertos ósseos ou scaffolds.[00129] After complete confluence, the cells were subcultured in a 24-well plate at a density of 1 x 105 cells.cm-2 , using 0.5 mL of MSCM per well and the plates were incubated at 37 °C with 5 % CO2 in incubator for 4 days until 95-100% confluence. These cells were used as controls and others as samples named ion group. In the ion group, the osteogenic medium used to differentiate the cells was placed in contact with bone grafts or BioS-2P/Bioglass F18 scaffolds for 48 hours at 37°C. This process allowed extracting ions from bone grafts or scaffolds.
[00130] Além disso, a passagem das hASCs também foi feita sobre os scaffolds de BioS-2P/Biovidro F18 (grupos dos enxertos ósseos ou scaffolds) e expandidas usando MSCM. Primeiramente, os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 foram previamente esterilizados em forno (ThermoScientificmodelo 6520) a 180ºC por três horas. Em seguida, o recipiente de vidro esterilizado com os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 foi coberto e armazenado até o uso. Antes de fazer a passagem celular, os enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 foram colocados em placas de 24 poços e deixados sob luz UV por 20 minutos. Em seguida, os enxertos ósseos ou scaffolds foram deixados 1 hora com solução de vitronectina para facilitar a adesão celular. Finalmente, a solução foi retirada e as hASCs foram subcultivadas sobre os enxertos ósseos ou scaffolds a uma densidade de 1 x 105 células.cm-2 usando 1 mL de MSCM para cobrir completamente os enxertos ósseos ou scaffolds. As placas foram incubadas a 37°C com 5% de CO2 em incubadora por 4 dias até 95- 100% de confluência. O MSCM foi trocado a cada dois dias. Todas as amostras e controles foram feitos em triplicatas.[00130] In addition, passage of hASCs was also performed on BioS-2P/Bioglass F18 scaffolds (bone graft groups or scaffolds) and expanded using MSCM. First, the bone grafts or BioS-2P/Bioglass F18 scaffolds were previously sterilized in an oven (ThermoScientific model 6520) at 180ºC for three hours. Then, the sterilized glass container with the BioS-2P/Bioglass F18 bone grafts or scaffolds was covered and stored until use. Prior to cell passage, the BioS-2P/Bioglass F18 bone grafts or scaffolds were placed in 24-well plates and left under UV light for 20 minutes. Then, the bone grafts or scaffolds were left for 1 hour with vitronectin solution to facilitate cell adhesion. Finally, the solution was removed and the hASCs were subcultured over the bone grafts or scaffolds at a density of 1 x 105 cells.cm-2 using 1 mL of MSCM to completely cover the bone grafts or scaffolds. The plates were incubated at 37°C with 5% CO2 in an incubator for 4 days until 95-100% confluence. The MSCM was changed every two days. All samples and controls were performed in triplicate.
[00131] Em relação à diferenciação osteogênica, o MSCM foi trocado em todos os grupos pelo meio de diferenciação osteogênico para células-tronco mesenquimais (MODM) (Sciencell-Canada). Este meio foi preparado e armazenado de acordo com as recomendações do fabricante. Foi colocado 0,5 mL em cada poço dos controles, 1 mL em cada poço no grupo dos enxertos ósseos ou scaffolds. Para o grupo dos íons, o meio osteogênico para diferenciar as células foi preparado da seguinte forma: 10 mL de MODM foram deixados com 1 g de enxertos ósseos ou scaffolds de BioS-2P/Biovidro F18 a 37°C durante 48 horas com 5% de CO2 em incubadora. Depois o meio foi filtrado com filtro de seringa esterilizado (VWR-Ø 0,2 µm) e foi adicionado MODM no meio filtrado até alcançar um volume final de 50 mL. Em cada poço do grupo dos íons foi colocado 0,5 mL deste meio. As células foram mantidas em cultura durante 21 dias. Nas células foram realizados diversos ensaios de viabilidade celular através do kit live/dead (Invitrogen-Life Technologies), análise da atividade fosfatase alcalina através da coloração de NBT/BCIP (Sigma-Aldrich) e do método colorimétrico do paranitrofenol (Abcam-Canada), avaliação da mineralização através de coloração e quantificação de vermelho de alizarina R (ARS) (Sigma-Aldrich) e expressão genica usando o kit RT2 Profiler PCR Arrays Formats C (Quiagen).[00131] Regarding osteogenic differentiation, MSCM was exchanged in all groups for osteogenic differentiation medium for mesenchymal stem cells (MODM) (Sciencell-Canada). This medium was prepared and stored according to the manufacturer's recommendations. 0.5 mL was placed in each well of the controls, 1 mL in each well in the bone grafts or scaffolds group. For the ion group, the osteogenic medium to differentiate the cells was prepared as follows: 10 mL of MODM were left with 1 g of bone grafts or BioS-2P/Bioglass F18 scaffolds at 37°C for 48 hours with 5% of CO2 in an incubator. Then the medium was filtered with a sterile syringe filter (VWR-Ø 0.2 µm) and MODM was added to the filtered medium until reaching a final volume of 50 ml. 0.5 mL of this medium was placed in each well of the ion group. Cells were maintained in culture for 21 days. Several cell viability assays were performed on the cells using the live/dead kit (Invitrogen-Life Technologies), analysis of alkaline phosphatase activity through NBT/BCIP staining (Sigma-Aldrich) and the colorimetric method of paranitrophenol (Abcam-Canada) , mineralization assessment by staining and quantification of alizarin red R (ARS) (Sigma-Aldrich) and gene expression using the RT2 Profiler PCR Arrays Formats C kit (Quiagen).
[00132] A concentração de íons cálcio foi determinada pelo método fotométrico, a concentração de grupos de fosfato foi determinada pelo método fotométrico UV e a concentração de íons sódio foi determinada por eletrodo íonseletivo no Laboratório Maricondi (São Carlos/SP-Brasil).[00132] The concentration of calcium ions was determined by the photometric method, the concentration of phosphate groups was determined by the UV photometric method and the concentration of sodium ions was determined by an ion-selective electrode at the Maricondi Laboratory (São Carlos/SP-Brazil).
[00133] O ALP é um marcador no estagio inicial da osteogênese, esta enzima catalisa a hidrólise de ésteres de fosfato, gerando os grupos fosfato necessários para a formação e deposição de hidroxiapatita durante o processo osteogênico. Os ensaios de coloração de NBT/BCIP confirmaram a formação de ALP nos controles, no grupo de íons e nos enxertos ósseos ou scaffolds nos dias 7 e 14. Estes resultados foram confirmados através da avaliação da atividade enzimática do ALP, através da qual foi constatado que a quantidade de ALP foi significativa maior nos controles do que no grupo de íons e nos scaffolds no dia 7. Nesse período, as células do grupo de íons e os enxertos ósseos ou scaffolds estavam em processo de adaptação, uma vez que o meio osteogênico sofreu saturação com os produtos de dissolução iônica dos enxertos ósseos ou scaffolds, afetando a produção da enzima. No dia 14, a quantidade de ALP foi significativamente maior para os enxertos ósseos ou scaffolds do que para os controles e o grupo de íons, o que pode ser atribuído à estrutura tridimensional altamente porosa e interconectada que favorece a migração, proliferação e diferenciação das células dentro dos enxertos ósseos ou scaffolds. Além disso, a superfície hidrofílica dos enxertos ósseos ou scaffolds favorece a adesão celular e os íons liberados pelos enxertos ósseos ou scaffolds ativam vários genes do processo osteogênico.[00133] ALP is a marker in the early stage of osteogenesis, this enzyme catalyzes the hydrolysis of phosphate esters, generating the phosphate groups necessary for the formation and deposition of hydroxyapatite during the osteogenic process. The NBT/BCIP staining assays confirmed the formation of ALP in the controls, in the ion group and in the bone grafts or scaffolds on days 7 and 14. These results were confirmed through the evaluation of the enzymatic activity of ALP, through which it was verified that the amount of ALP was significantly higher in the controls than in the ion group and in the scaffolds on day 7. During this period, the cells of the ion group and the bone grafts or scaffolds were in the process of adaptation, since the osteogenic medium suffered saturation with ionic dissolution products from bone grafts or scaffolds, affecting enzyme production. On day 14, the amount of ALP was significantly higher for bone grafts or scaffolds than for controls and the ion group, which can be attributed to the highly porous and interconnected three-dimensional structure that favors cell migration, proliferation and differentiation. within bone grafts or scaffolds. Furthermore, the hydrophilic surface of bone grafts or scaffolds favors cell adhesion and the ions released by bone grafts or scaffolds activate several genes of the osteogenic process.
[00134] Os ensaios de coloração com vermelho de alizarina R permitiram observar a formação dos nódulos calcificados nos controles, no grupo de íons e nos enxertos ósseos ou scaffolds nos dias 7, 14 e 21. A quantificação de ARS para os controles e o grupo de íons mostrou um depósito mais significativo de cálcio para o grupo de íons do que para os controles no dia 21. Este incremento pode ser atribuído aos íons liberados no meio pelos enxertos ósseos ou scaffolds, o que pode promover a expressão de vários genes relacionados à osteogênese.[00134] The alizarin red R staining assays allowed observing the formation of calcified nodules in the controls, in the ion group and in the bone grafts or scaffolds on days 7, 14 and 21. The quantification of ARS for the controls and the group of ions showed a more significant deposit of calcium for the ion group than for controls on day 21. This increment can be attributed to ions released into the medium by bone grafts or scaffolds, which can promote the expression of several genes related to osteogenesis.
[00135] Através da análise da expressão gênica foi verificado que os enxertos ósseos ou scaffolds promovem a diferenciação osteogênica de célulastronco derivadas de tecido adiposo humano. Observa-se que os grupos de íons e os enxertos ósseos ou scaffolds foram capazes de induzir a expressão de diferentes membros da superfamília BMP, receptor da superfamília TGF, fatores de transcrição, receptores de integrina e colágenos, todos essenciais para a osteogênese.[00135] Through the analysis of gene expression it was found that bone grafts or scaffolds promote osteogenic differentiation of stem cells derived from human adipose tissue. It is observed that ion groups and bone grafts or scaffolds were able to induce the expression of different members of the BMP superfamily, TGF superfamily receptor, transcription factors, integrin and collagen receptors, all essential for osteogenesis.
Claims (13)
a) Preparar em (110) um enxerto ósseo ou scaffold de Biosilicato® a partir da impregnação de espumas de poliuretano (PU) com 35-55 ppi (“pores per inch”) com barbotina de Biosilicato® preparada pela mistura em moinho planetário a 500 rpm por 30-120 minutos de 20- 40% em volume de Biosilicato® em pó com tamanho médio de partículas de 45 μm, 0-5% em volume de um ligante selecionado dentre PVB, PVA e CMC e 55-80% em volume de um solvente hidroxilado, seguido de secagem e queima da espuma e sinterização do Biosilicato® obtido a temperaturas ~ 1.000ºC, e separar o enxerto ósseo de Biosilicato® com resistência mecânica inferior a 0,1 MPa, dito processo sendo caracterizado por:
b) Infiltrar, em (120),sob vácuo (-400 mmHg a -600mmHg), por 5-10 minutos, o enxerto ósseo ou scaffold de Biosilicato® obtido em a) com a mesma barbotina de Biosilicato® de a) exceto por o tamanho médio de partículas do pó de Biosilicato® ser de 5 μm, e;
c) Em (130), efetuar, sob as mesmas condições de a), a sinterização do Biosilicato® infiltrado obtido em b);
d) Infiltrar, em (140)sob vácuo (-400 mmHg a -600mmHg), por 5-10 minutos, o enxerto ósseo ou scaffold de Biosilicato® da etapa c) com 15-35% em volume de uma barbotina de Biovidro F18 com tamanho médio de partículas de 5 μm, 0-5% em volume de um ligante selecionado dentre PVB, PVA e CMC e 60-85% em volume de um solvente hidroxilado, obtendo um enxerto ósseo ou scaffold infiltrado com Biovidro F18;
e) Queimar, em (150), sob escoamento viscoso do dito Biovidro F18, o enxerto ósseo infiltrado de d) sob as seguintes condições de queima:
- • Aquecimento a uma taxa de 1-5ºC/min até a temperatura de eliminação (“burn-out”) do ligante a 400-450ºC;
- • Patamar de 4 horas na temperatura de 400-450ºC;
- • Novo aquecimento a 1-5ºC/min até a temperatura de sinterização do Biovidro F18 (600-900ºC);
- • Patamar de 3-5horas na temperatura de 600-900ºC; e
- • Resfriamento até a temperatura ambiente, a uma taxa de 1- 5ºC/min, recuperando um enxerto ósseo de Biosilicato® infiltrado com Biovidro F18 com superfície lisa;
g) Recuperar, em (170), o enxerto ósseo ou scaffold de Biosilicato® e Biovidro F18 com resistência à compressão entre 1,0 ± 0,2MPa e 3,3 ±0,3 MPa.Bone graft preparation process comprising:
a) Prepare in (110) a bone graft or Biosilicate® scaffold from the impregnation of polyurethane foams (PU) with 35-55 ppi (“pores per inch”) with Biosilicate® slip prepared by mixing in a planetary mill at 500 rpm for 30-120 minutes of 20-40% by volume of Biosilicate® powder with an average particle size of 45 μm, 0-5% by volume of a binder selected from PVB, PVA and CMC and 55-80% in volume of a hydroxylated solvent, followed by drying and burning the foam and sintering the Biosilicate® obtained at temperatures ~ 1,000ºC, and separating the Biosilicate® bone graft with mechanical strength lower than 0.1 MPa, said process being characterized by:
b) Infiltrate, at (120), under vacuum (-400 mmHg to -600 mmHg), for 5-10 minutes, the bone graft or Biosilicate® scaffold obtained in a) with the same Biosilicate® slip as in a) except for the average particle size of the Biosilicate® powder is 5 μm, and;
c) In (130), carry out, under the same conditions as in a), the sintering of the infiltrated Biosilicate® obtained in b);
d) Infiltrate, in (140) under vacuum (-400 mmHg to -600mmHg), for 5-10 minutes, the bone graft or Biosilicate® scaffold from step c) with 15-35% by volume of a slip of Bioglass F18 with an average particle size of 5 μm, 0-5% by volume of a binder selected from PVB, PVA and CMC and 60-85% by volume of a hydroxylated solvent, obtaining a bone graft or scaffold infiltrated with Bioglass F18;
e) Burn, in (150), under viscous flow of said Bioglass F18, the infiltrated bone graft from d) under the following firing conditions:
- • Heating at a rate of 1-5ºC/min until the burn-out temperature of the binder at 400-450ºC;
- • Level of 4 hours at a temperature of 400-450ºC;
- • Reheating at 1-5ºC/min to the sintering temperature of Bioglass F18 (600-900ºC);
- • Level of 3-5 hours at a temperature of 600-900ºC; and
- • Cooling to room temperature, at a rate of 1-5ºC/min, recovering a Biosilicate® bone graft infiltrated with Bioglass F18 with a smooth surface;
g) Recover, in (170), the bone graft or scaffold of Biosilicate® and Bioglass F18 with compressive strength between 1.0 ± 0.2MPa and 3.3 ±0.3 MPa.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BR102020017697-8A BR102020017697A2 (en) | 2020-08-31 | 2020-08-31 | Process of preparation of bone grafts and bone grafts obtained |
| PCT/BR2021/050372 WO2022040771A1 (en) | 2020-08-31 | 2021-08-31 | Method for obtaining bone grafts and bone grafts obtained |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BR102020017697-8A BR102020017697A2 (en) | 2020-08-31 | 2020-08-31 | Process of preparation of bone grafts and bone grafts obtained |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| BR102020017697A2 true BR102020017697A2 (en) | 2022-03-15 |
Family
ID=80352338
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR102020017697-8A BR102020017697A2 (en) | 2020-08-31 | 2020-08-31 | Process of preparation of bone grafts and bone grafts obtained |
Country Status (2)
| Country | Link |
|---|---|
| BR (1) | BR102020017697A2 (en) |
| WO (1) | WO2022040771A1 (en) |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE320277T1 (en) * | 2000-06-29 | 2006-04-15 | Biosyntech Canada Inc | COMPOSITION AND METHOD FOR REPAIR AND REGENERATION OF CARTILAGE AND OTHER TISSUES |
| BRPI0300644B8 (en) * | 2003-02-20 | 2022-04-26 | Fundacao Univ Federal De Sao Carlos | Process of preparing particulate, bioactive and resorbable biosilicates, compositions for preparing said biosilicates and bioactive and resorbable particulate biosilicates. |
| BRPI1003676B1 (en) * | 2010-04-06 | 2018-12-26 | Fundacao Univ Federal De Sao Carlos | suspensions for the preparation of biosilicate-based bone scaffolds, obtained bone grafts and processes for obtaining them |
| KR20190102101A (en) * | 2013-03-06 | 2019-09-02 | 가부시끼가이샤 쓰리디 매트릭스 | Surgical methods employing purified amphiphilic peptide compositions |
| US9381274B2 (en) * | 2013-03-14 | 2016-07-05 | Prosidyan, Inc. | Bone graft implants containing allograft |
| BR102013020961A2 (en) * | 2013-08-12 | 2016-03-08 | Univ Fed De São Carlos | vitreous composition, bioactive vitreous fibers and tissues and articles |
| US9566368B2 (en) * | 2014-11-13 | 2017-02-14 | Bioventus, Llc | Moldable bone graft compositions |
-
2020
- 2020-08-31 BR BR102020017697-8A patent/BR102020017697A2/en unknown
-
2021
- 2021-08-31 WO PCT/BR2021/050372 patent/WO2022040771A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| WO2022040771A9 (en) | 2023-01-05 |
| WO2022040771A1 (en) | 2022-03-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Baino et al. | Bioceramics and scaffolds: a winning combination for tissue engineering | |
| Baino et al. | Three‐dimensional glass‐derived scaffolds for bone tissue engineering: current trends and forecasts for the future | |
| Bellucci et al. | A new hydroxyapatite-based biocomposite for bone replacement | |
| Fu et al. | Mechanical and in vitro performance of 13–93 bioactive glass scaffolds prepared by a polymer foam replication technique | |
| Hench et al. | Molecular control of bioactivity in sol-gel glasses | |
| Guo et al. | Biocompatibility and osteogenicity of degradable Ca-deficient hydroxyapatite scaffolds from calcium phosphate cement for bone tissue engineering | |
| JP5172795B2 (en) | Artificial stabilizing composition of calcium phosphate phase specifically tailored to support bone cell activity | |
| ES2367972T3 (en) | POROUS BIOVIDRIO AND PREPARATION PROCEDURE. | |
| Zhang et al. | Novel mesoporous hydroxyapatite/chitosan composite for bone repair | |
| CN104368047B (en) | High-strength multi-level micro-nano structure silicon-based bone repair scaffold material, its preparation method and application | |
| EP1305056A1 (en) | Porous synthetic bone graft and method of manufacture thereof | |
| AU2001275715A1 (en) | Porous synthetic bone graft and method of manufacture thereof | |
| CN103055352A (en) | Calcium phosphate/collagen composite biologic ceramic material and preparation method thereof | |
| WO2005007802A2 (en) | Fibrous composite for tissue engineering | |
| KR102567367B1 (en) | The manufacturing and implementation of microchanneled scaffold | |
| Mala et al. | Bioceramics in orthopaedics: A review | |
| Marin et al. | Competent F18 bioglass-Biosilicate® bone graft scaffold substitutes | |
| CN112190762B (en) | An injection-type magnesium-based composite fiber reinforced calcium phosphate biological bone adhesive and its preparation method and application | |
| BRPI1003676A2 (en) | suspensions for the preparation of biosilicate-based bone scaffolds, obtained bone grafts and processes for obtaining them | |
| Sugimori et al. | Effects of Apatite Foam Combined with Platelet-rich Plasma on Regeneration of Bone Defect | |
| BR102020017697A2 (en) | Process of preparation of bone grafts and bone grafts obtained | |
| CN113559326A (en) | Calcium silicate/magnesium silicate biological bone porous implant and preparation method and application thereof | |
| CN1493615A (en) | Inorganic/organic nanocomposite bioactive porous material and preparation method thereof | |
| CN112043873B (en) | Organic polymer bridging-containing bio-inorganic composite structure material and preparation method and application thereof | |
| CN110075349B (en) | A kind of bioactive glass composite stent and application |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B03A | Publication of a patent application or of a certificate of addition of invention [chapter 3.1 patent gazette] | ||
| B06W | Patent application suspended after preliminary examination (for patents with searches from other patent authorities) chapter 6.23 patent gazette] |