벤조퓨란
보이기
| |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
1-benzofuran[1] | |||
| 별칭 | |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 107704 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.005.439 | ||
| EC 번호 |
| ||
| 260881 | |||
| KEGG | |||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1993 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C8H6O | |||
| 몰 질량 | 118.135 g·mol−1 | ||
| 녹는점 | −18 °C (0 °F; 255 K) | ||
| 끓는점 | 173 °C (343 °F; 446 K) | ||
| 위험 | |||
| GHS 그림문자 |  
| ||
| 신호어 | 경고 | ||
| H226, H351, H412 | |||
| P201, P202, P210, P233, P240, P241, P242, P243, P273, P280, P281, P303+361+353, P308+313, P370+378, P403+235, P405, P501 | |||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose)
|
500 mg/kg (mice).[2] | ||
| 관련 화합물 | |||
관련 화합물
|
벤조싸이오펜, 인돌, 인덴 | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
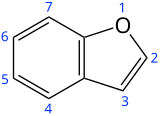
벤조퓨란(영어: benzofuran)은 벤젠 고리와 퓨란 고리가 융합된 두 개의 고리 구조를 특징으로 하는 분자식이 C8H6O인 헤테로고리 화합물이다. 벤조퓨란은 무색의 액체로 콜타르의 구성 성분이다. 벤조퓨란은 보다 복잡한 구조를 갖는 많은 관련 화합물들의 모체 화합물이다. 예를 들어, 솔라렌은 여러 식물들에서 생성되는 벤조퓨란 유도체이다.
생성
[편집]벤조퓨란은 콜타르에서 추출된다. 벤조퓨란은 또한 2-에틸페놀의 탈수소화에 의해 얻을 수 있다.[2]
실험실에서 제조 방법
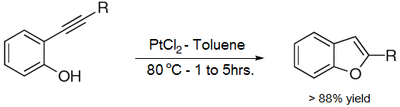
[편집]벤조퓨란은 실험실에서 다양한 방법으로 제조할 수 있다. 주목할 만한 예들은 다음과 같다.
 |
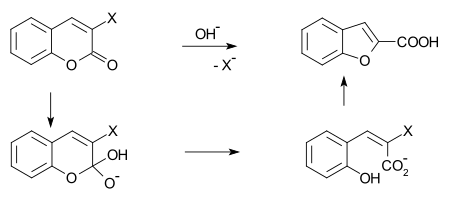 |
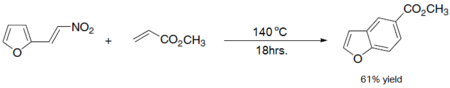 |
 |
같이 보기
[편집]- 치환된 벤조퓨란
- 퓨란 – 융합된 벤젠 고리가 없는 유사체.
- 인돌 – 산소 원자 대신 질소 원자를 가지고 있는 유사체.
- 벤조싸이오펜 – 산소 원자 대신 황 원자를 가지고 있는 유사체.
- 아이소벤조퓨란 – 2번 위치에 산소 원자를 가지고 있는 이성질체.
- 오론
- 툰베르기놀 F
각주
[편집]- ↑ 가 나 〈Front Matter〉. 《Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)》. Cambridge: The Royal Society of Chemistry. 2014. 218쪽. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ 가 나 Collin, G.; Höke, H. (2007). 〈Benzofurans〉. 《Ullmann's Encyclopedia of Industrial Chemistry》. Weinheim: Wiley-VCH. doi:10.1002/14356007.l03_l01. ISBN 978-3527306732.
- ↑ Burgstahler, A. W.; Worden, L. R. (1966). “Coumarone” (PDF). 《Organic Syntheses》 46: 28.; 《Collective Volume》 5, 251쪽
- ↑ Perkin, W. H. (1870). “XXIX. On some New Bromine Derivatives of Coumarin”. 《Journal of the Chemical Society》 23: 368–371. doi:10.1039/JS8702300368.
- ↑ Perkin, W. H. (1871). “IV. On some New Derivatives of Coumarin”. 《Journal of the Chemical Society》 24: 37–55. doi:10.1039/JS8712400037.
- ↑ Bowden, K.; Battah, S. (1998). “Reactions of Carbonyl Compounds in Basic Solutions. Part 32. The Perkin Rearrangement”. 《Journal of the Chemical Society, Perkin Transactions 2》 1998 (7): 1603–1606. doi:10.1039/a801538d.
- ↑ Kusurkar, R. S.; Bhosale, D. K. (1990). “Novel Synthesis of Benzosubstituted Benzofurans Via Diels-Alder Reaction”. 《Synthetic Communications》 20 (1): 101–109. doi:10.1080/00397919008054620.
- ↑ Fürstner, Alois & Davies, Paul (2005). “Heterocycles by PtCl2-Catalyzed Intramolecular Carboalkoxylation or Carboamination of Alkynes”. 《Journal of the American Chemical Society》 127 (43): 15024–15025. doi:10.1021/ja055659p. hdl:11858/00-001M-0000-0025-AA5A-1. PMID 16248631.