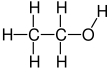
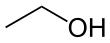
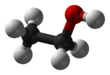
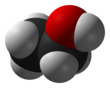
เอทานอล
| |||
| |||

| |||
| ชื่อ | |||
|---|---|---|---|
| Pronunciation | /ˈɛθənɒl/ | ||
| Preferred IUPAC name
Ethanol[1] | |||
ชื่ออื่น
| |||
| เลขทะเบียน | |||
3D model (JSmol)
|
|||
| 3DMet | |||
| 1718733 | |||
| ChEBI | |||
| ChEMBL | |||
| เคมสไปเดอร์ | |||
| ดรักแบงก์ | |||
| ECHA InfoCard | 100.000.526 | ||
| 787 | |||
| KEGG | |||
ผับเคม CID
|
|||
| UNII | |||
| UN number | UN 1170 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| คุณสมบัติ | |||
| C2H6O | |||
| มวลโมเลกุล | 46.069 g·mol−1 | ||
| ลักษณะทางกายภาพ | ของเหลวไม่มีสี | ||
| กลิ่น | ฉุนเหมือนไวน์[2] | ||
| ความหนาแน่น | 0.78945 g/cm3 (at 20 °C)[3] | ||
| จุดหลอมเหลว | −114.14 ± 0.03[3] องศาเซลเซียส (−173.45 ± 0.05 องศาฟาเรนไฮต์; 159.01 ± 0.03 เคลวิน) | ||
| จุดเดือด | 78.23 ± 0.09[3] องศาเซลเซียส (172.81 ± 0.16 องศาฟาเรนไฮต์; 351.38 ± 0.09 เคลวิน) | ||
| ผสมกันได้ | |||
| log P | −0.18 | ||
| ความดันไอ | 5.95 kPa (at 20 °C) | ||
| pKa | 15.9 (H2O), 29.8 (DMSO)[4][5] | ||
| −33.60·10−6 cm3/mol | |||
ดัชนีหักเหแสง (nD)
|
1.3611[3] | ||
| ความหนืด | 1.2 mPa·s (at 20 °C), 1.074 mPa·s (at 25 °C)[6] | ||
| 1.69 D[7] | |||
| ความอันตราย | |||
| GHS labelling: | |||
 
| |||
| อันตราย | |||
| H225, H319 | |||
| P210, P233, P240, P241, P242, P305+P351+P338 | |||
| NFPA 704 (fire diamond) | |||
| จุดวาบไฟ | 14 °C (Absolute)[9] | ||
| ปริมาณหรือความเข้มข้น (LD, LC): | |||
LD50 (median dose)
|
| ||
| NIOSH (US health exposure limits): | |||
PEL (Permissible)
|
TWA 1000 ppm (1900 mg/m3)[10] | ||
REL (Recommended)
|
TWA 1000 ppm (1900 mg/m3)[10] | ||
IDLH (Immediate danger)
|
N.D.[10] | ||
| เอกสารข้อมูลความปลอดภัย (SDS) | [8] | ||
| สารประกอบอื่นที่เกี่ยวข้องกัน | |||
สารประกอบที่เกี่ยวข้อง
|
|||
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |||
เอทานอล (อังกฤษ: ethanol) หรือ เอทิลแอลกอฮอล์ (อังกฤษ: ethyl alcohol) (สูตรเคมี C2H5OH) เป็นแอลกอฮอล์ชนิดหนึ่งซึ่งเกิดจากการนำเอาพืชมาหมักเพื่อเปลี่ยนแป้งเป็นน้ำตาล จากนั้นจึงเปลี่ยนจากน้ำตาลเป็นแอลกอฮอล์ โดยใช้เอนไซม์หรือกรดบางชนิดช่วยย่อย เมื่อทำให้เป็นแอลกอฮอล์บริสุทธิ์ 95% โดยการกลั่น ส่วนใหญ่ผลิตจากพืช สองประเภทคือ พืชประเภทน้ำตาล เช่นอ้อย บีตรูต และพืชจำพวกแป้งเช่น มันสำปะหลัง ข้าว ข้าวโพด เป็นต้น
อุตสาหกรรมเอทานอล
[แก้]บราซิลเป็นผู้ผลิตเอทานอลอันดับหนึ่งในโลก [11] ข้อมูลปี พ.ศ. 2551 ประเทศไทยมีโรงงานเอทานอล 11 แห่ง กำลังการผลิตรวม 1.75 ล้านลิตรต่อวัน ขณะที่ความต้องการใช้ในประเทศมีเพียง 800,000 ลิตรต่อวัน [12]
เอทานอลเป็นเชื้อเพลิงที่สะอาดและเผาไหม้ได้สมบูรณ์ช่วยลดการเกิดมลพิษในอากาศและเป็นผลดีต่อสภาวะแวดล้อมและมีฐานวัตถุดิบมาจากพืชซึ่งสามารถดูดซับปริมาณ แก๊สคาร์บอนไดออกไซค์ในบรรยากาศได้
เอทานอลเป็นพลังงานหมุนเวียน (Renewable Energy) ผลิตได้จากวัตถุดิบทางการเกษตรซึ่งแบ่งได้เป็น 3 ประเภท[13] 1. วัตถุดิบประเภทน้ำตาล ได้แก่ น้ำอ้อย น้ำตาลจากบีตรูต และกากน้ำตาลซึ่งยีสต์สามารถย่อยสลายวัตถุดิบประเภทนี้ได้เลยทันทีโดยไม่ต้องผ่านการย่อยเพื่อเป็นน้ำตาล (Pretreatment) 2. วัตถุดิบประเภทแป้ง ได้แก่ มันสำปะหลัง ธัญพืชและมันฝรั่งในการผลิตจะต้องย่อยแป้งในวัตถุดิบให้เป็นน้ำตาลกลูโคสซึ่งเป็นน้ำตาลโมเลกุลเดี่ยวเสียก่อนยีสต์จึงจะเปลี่ยนน้ำตาลเป็นเอทานอลได้ 3. วัตถุดิบประเภทที่เป็นผลพลอยได้จากอุตสาหกรรมเกษตร เช่น กากอ้อย ฟางข้าวซังข้าวโพด และของเสียจากอุตสาหกรรม เยื่อกระดาษ ฯลฯ
เอทานอลมีค่าออกเทนสูงนำไปผสมกับน้ำมันเบนซินเรียกว่าน้ำมันแก๊สโซฮอล์ได้ ถ้าผสมกับน้ำมันดีเซล เรียกว่าน้ำมันดีโซฮอล์ใช้เป็นเชื้อเพลิงได้ นอกจากนี้ยังสามารถใช้เอทานอล บริสุทธิ์เป็นเชื้อเพลิงได้โดยตรงโดยไม่ต้องผสมกับน้ำมันได้อีกด้วย ปัจจุบันไทยมีโรงงานเอทานอล 27 แห่ง กำลังการผลิตรวม 6.125 ล้านลิตร [14]
ดูเพิ่ม
[แก้]อ้างอิง
[แก้]- ↑ Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge, UK: The Royal Society of Chemistry. 2014. p. 30. doi:10.1039/9781849733069-00001. ISBN 978-0-85404-182-4.
- ↑ "Ethanol". PubChem. สืบค้นเมื่อ 29 December 2022.
- ↑ 3.0 3.1 3.2 3.3 Haynes, William M., บ.ก. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. p. 3.246. ISBN 1439855110.
- ↑ Ballinger P, Long FA (1960). "Acid Ionization Constants of Alcohols. II. Acidities of Some Substituted Methanols and Related Compounds1,2". Journal of the American Chemical Society. 82 (4): 795–798. doi:10.1021/ja01489a008.
- ↑ Arnett EM, Venkatasubramaniam KG (1983). "Thermochemical acidities in three superbase systems". J. Org. Chem. 48 (10): 1569–1578. doi:10.1021/jo00158a001.
- ↑ Lide DR, บ.ก. (2012). CRC Handbook of Chemistry and Physics (92 ed.). Boca Raton, FL: CRC Press/Taylor and Francis. pp. 6–232.
- ↑ Lide DR, บ.ก. (2008). CRC Handbook of Chemistry and Physics (89 ed.). Boca Raton, FL: CRC Press. pp. 9–55.
- ↑ "MSDS Ethanol". สืบค้นเมื่อ 2023-01-12.
- ↑ "Ethanol". webwiser.nlm.nih.gov (ภาษาอังกฤษ). สืบค้นเมื่อ 2021-06-25.
- ↑ 10.0 10.1 10.2 NIOSH Pocket Guide to Chemical Hazards. "#0262". National Institute for Occupational Safety and Health (NIOSH).
- ↑ http://www.ftawatch.org/news/view.php?id=11176[ลิงก์เสีย]
- ↑ http://www.thairath.co.th/news.php?section=economic&content=100548
- ↑ thai-ethanol.com/th/2013-04-06-13-53-49/what-is-ethanol.html
- ↑ "สำเนาที่เก็บถาวร". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-11-30. สืบค้นเมื่อ 2020-09-08.
อ่านเพิ่มเติม
[แก้]- Boyce JM, Pittet D (2003). "Hand Hygiene in Healthcare Settings". Atlanta, GA: Centers for Disease Control..
- Onuki S, Koziel JA, van Leeuwen J, Jenks WS, Grewell D, Cai L (June 2008). Ethanol production, purification, and analysis techniques: a review. 2008 ASABE Annual International Meeting. Providence, RI. สืบค้นเมื่อ 16 February 2013.
- "Explanation of US denatured alcohol designations". Sci-toys.
- Lange, Norbert Adolph (1967). John Aurie Dean (บ.ก.). Lange's Handbook of Chemistry (10th ed.). McGraw-Hill.
แหล่งข้อมูลอื่น
[แก้]- Alcohol (Ethanol) at The Periodic Table of Videos (University of Nottingham)
- International Labour Organization ethanol safety information
- National Pollutant Inventory – Ethanol Fact Sheet
- CDC – NIOSH Pocket Guide to Chemical Hazards – Ethyl Alcohol
- National Institute of Standards and Technology chemical data on ethanol
- Chicago Board of Trade news and market data on ethanol futures
- Calculation of vapor pressure, liquid density, dynamic liquid viscosity, surface tension of ethanol
- Ethanol History A look into the history of ethanol
- ChemSub Online: Ethyl alcohol
- Industrial ethanol production process flow diagram using ethylene and sulphuric acid