Индол
Индол је ароматично хетероциклично органско једињење. Он има бицикличну структуру, која се састоји од сесточланог бензеновог прстена спојеног са петочланим пироловим прстеном. Индол се често среће у мирисима и лековима. Једињења која садрже индолни прстен се називају индолима.[6] Индолна аминокиселина триптофан је прекурзор неуротрансмитера серотонина.[7]
| Индол | |||
|---|---|---|---|
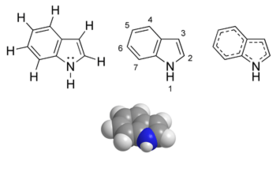
| |||
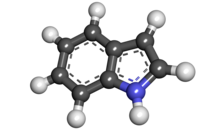
| |||
| ИУПАЦ име |
| ||
| Други називи | 2,3-Бензопирол, кетол, 1-бензазол | ||
| Идентификација | |||
| ЦАС регистарски број | 120-72-9 | ||
| ПубЦхем[1][2] | 798 | ||
| ЦхемСпидер[3] | 776 | ||
| УНИИ | 8724ФЈW4М5 | ||
| КЕГГ[4] | |||
| ЦхЕМБЛ[5] | ЦХЕМБЛ15844 | ||
| РТЕЦС регистарски број токсичности | НЛ2450000 | ||
| Јмол-3Д слике | Слика 1 | ||
| |||
| |||
| Својства | |||
| Молекулска формула | C8Х7Н | ||
| Моларна маса | 117.15 г/мол | ||
| Агрегатно стање | Бела чврста материја | ||
| Густина | 1.1747 г/цм3, чврсто стање | ||
| Тачка топљења |
52–54 °Ц | ||
| Тачка кључања |
253–254 °Ц (526 К) | ||
| Растворљивост у води | 0.19 г/100 мл (20 °Ц) Растворан у топлој води | ||
| пКа | 16.2 (21.0 у ДМСО) | ||
| Базност (пКб) | 17.6 | ||
| Структура | |||
| Кристална решетка/структура | Пна21 | ||
| Облик молекула (орбитале и хибридизација) | Планарна | ||
| Диполни момент | 2.11 D у бензену | ||
| Опасност | |||
| Подаци о безбедности приликом руковања (МСДС) | [1] | ||
| Р и С ознаке | Р: 21/22-37/38-41-50/53 С: 26-36/37/39-60-61 | ||
| Тачка паљења | 121 °Ц | ||
| Сродна једињења | |||
| Сродна ароматична једињења |
бензен, бензофуран, карбазол, карболин, инден, индолин, исатин, метилиндол, оксиндол, пирол, скатол | ||
|
Уколико није другачије напоменуто, подаци се односе на стандардно стање (25 °Ц, 100 кПа) материјала | |||
| Инфобоx референцес | |||
Генералне особине и распрострањеност
уредиИндол је чврст на собној температури. Индол могу да произведу бактерије као деградациони продукт аминокиселине триптофана. Он се природно јавља у људском измету и има интензивни фекални задах. У веома ниским концентрацијама, међутим, он има мирис цвећа,[8] и састојак је многих цветних мириса (суцх ас оранге блоссомс) и парфема. Он се такође јавља у катрану.
Кореспондирајући супституент се назива индолил.
Индол подлеже електрофилној супституцији, углавном на позицији 3. Супституисани индоли су структурни елементи (и за нека од једињења синтетички прекурзори) триптофанских-деривата триптаминских алкалоида попут неуротрансмитера серотонина, и мелатонина. У индолна једињења се исто тако уврштавају биљни хормон ауксин (индолил-3-сирћетна киселина), антиинфламаторни лек индомтацин, бета блокатор пиндолол, природни халуциноген диметилтриптамин (Н,Н-ДМТ).
Име индол је формирано од речи индиго и олеум, јер је индол први пут изолован третманом индиго боје олеумом.
Синтеза индола
уредиИндол је присутан у катрану у знатним количинама, и 220–260 °Ц дистилациона фракција је главни индустријски извор материала. Индол и његови деривати такође могу бити синтетисани различитим методама.[9][10][11] Главни индустријски путеви почињу од анилина.
Пример синтезе великих количина, је реакција у гасовитој фази у којој се индол (и супституисани деривати) формирају из анилина и етилен гликола у присуству катализатора:
Генерално, реакције се изводе на 200 до 500 °Ц. Приноси могу да буду и до 60%. Други прекурзори индола су формилтолуидин, 2-етиланилин, и 2-(2-нитрофенил)етанол. Они су сви подложни циклизацији.[12] Многи други методи су били развијени.
Хемијске реакције индола
уредиБазност
уредиЗа разлику од већине амина, индол није базан. У том погледу је аналоган са пиролом. Веома јаке киселине као што је хлороводонична киселина су потребне да би се протонисао индол. Протонисана форма има пКа од −3.6. Сенситивност многих индолних једињења (нпр., триптамина) у киселој средини је узрокована овом протонацијом.
Електрофилна супституција
уредиНајреактивнија позиција индола за електрофилну ароматичну супституцију је C-3, која је 1013 пута реактивнија него угљеник бензена. На пример, Вилсмеиер-Хакова формилација индола[13] се одвија на собној температури ексклузивн на C-3. Пошто је пиролни прстен најреактивнији део индола, со електрофилне супституције бензеновог прстена долази само након што су Н-1, C-2, и C-3 супституисани.
Грамин је користан синтетички интермедијар, који се производи Маничевом реакцијом индола са диметиламином и формалдехидом. Он је прекурзор индолне сирћетне киселине и синтетичког триптофана.
Киселост азотног водоника и органометалини индолни ањонски комплекси
уредиН-Х центер има пКа вредност 21 у ДМСО, тако да су веома јаке базе као што је натријум хидрид или бутил литијум и одсуство воде неоходни за комплетну депротонацију. Резултирајући деривати алкалних метала могу да реагују на два начина. Соли јонског карактера као што су једињења натријума или калијума реагују са електрофилима на азоту-1, док једињења магнезијума која су у већој мери ковалентна (индолни Григнард реагенси) и (посебно) цинкови комплекси теже да реагују на угљенику-3. Слично томе, поларни апротонски растварачи као што је ДМФ и ДМСО приоритизују напад на азот, док неполарни растварачи као што је толуен доприносе C-3 нападу.[14]
Референце
уреди- ↑ Ли Q, Цхенг Т, Wанг Y, Брyант СХ (2010). „ПубЦхем ас а публиц ресоурце фор друг дисцоверy.”. Друг Дисцов Тодаy 15 (23-24): 1052-7. ДОИ:10.1016/j.drudis.2010.10.003. ПМИД 20970519.
- ↑ Еван Е. Болтон, Yанли Wанг, Паул А. Тхиессен, Степхен Х. Брyант (2008). „Цхаптер 12 ПубЦхем: Интегратед Платформ оф Смалл Молецулес анд Биологицал Ацтивитиес”. Аннуал Репортс ин Цомпутатионал Цхемистрy 4: 217-241. ДОИ:10.1016/S1574-1400(08)00012-1.
- ↑ Хеттне КМ, Wиллиамс АЈ, ван Муллиген ЕМ, Клеињанс Ј, Ткацхенко V, Корс ЈА. (2010). „Аутоматиц вс. мануал цуратион оф а мулти-соурце цхемицал дицтионарy: тхе импацт он теxт мининг”. Ј Цхеминформ 2 (1): 3. ДОИ:10.1186/1758-2946-2-3. ПМИД 20331846.
- ↑ Јоанне Wиxон, Доуглас Келл (2000). „Wебсите Ревиеw: Тхе Кyото Енцyцлопедиа оф Генес анд Геномес — КЕГГ”. Yеаст 17 (1): 48–55. ДОИ:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Гаултон А, Беллис Љ, Бенто АП, Цхамберс Ј, Давиес M, Херсеy А, Лигхт Y, МцГлинцхеy С, Мицхаловицх D, Ал-Лазикани Б, Оверингтон ЈП. (2012). „ЦхЕМБЛ: а ларге-сцале биоацтивитy датабасе фор друг дисцоверy”. Нуцлеиц Ацидс Рес 40 (Датабасе иссуе): Д1100-7. ДОИ:10.1093/nar/gkr777. ПМИД 21948594.
- ↑ Катритзкy А.Р., Позхарскии А.Ф. (2000). Хандбоок оф Хетероцyцлиц Цхемистрy. Ацадемиц Пресс. ИСБН 0080429882.
- ↑ Цлаyден Јонатхан, Ницк Греевес, Стуарт Wаррен, Петер Wотхерс (2001). Органиц цхемистрy. Оxфорд, Оxфордсхире: Оxфорд Университy Пресс. ИСБН 0-19-850346-6.
- ↑ „Рецент Евентс ин Олфацторy Ундерстандинг”.
- ↑ Гриббле Г. W. (2000). „Рецент девелопментс ин индоле ринг сyнтхесис—метходологy анд апплицатионс”. Ј. Цхем. Соц. Перкин Транс. 1 (7): 1045. ДОИ:10.1039/a909834h.
- ↑ Цаццхи, С.; Фабризи, Г. (2005). „Сyнтхесис анд Фунцтионализатион оф Индолес Тхроугх Палладиум-цаталyзед Реацтионс”. Цхем. Рев. 105 (7): 2873. ДОИ:10.1021/cr040639b. ПМИД 16011327.
- ↑ Хумпхреy, Г. Р.; Куетхе, Ј. Т. (2006). „Працтицал Метходологиес фор тхе Сyнтхесис оф Индолес”. Цхем. Рев. 106 (7): 2875. ДОИ:10.1021/cr0505270. ПМИД 16836303.
- ↑ Герд Цоллин анд Хартмут Хöке “Индоле” Уллманн'с Енцyцлопедиа оф Индустриал Цхемистрy 2002, Wилеy-ВЦХ, Wеинхеим. ДОИ:10.1002/14356007.a14_167.
- ↑ Јамес, П. Н.; Снyдер, Х. Р. (1959). „Индоле-3-алдехyде”. Органиц Сyнтхесес 39: 30-.
- ↑ Хеанеy, Х.; Леy, С. V. (1974). „1-Бензyлиндоле”. Органиц Сyнтхесес 54: 58-.
Литература
уреди- Индолес Парт Оне, W. Ј. Хоулихан (ед.), Wилеy Интерсциенце, Неw Yорк, 1972.
- Сундберг, Р. Ј. (1996). Индолес. Сан Диего: Ацадемиц Пресс. ИСБН 0-12-676945-1.
- Јоуле, Ј. А.; Миллс, К. (2000). Хетероцyцлиц Цхемистрy. Оxфорд, УК: Блацкwелл Сциенце. ИСБН 0-632-05453-0.
- Јоуле, Ј., Ин Сциенце оф Сyнтхесис, Тхомас, Е. Ј., Ед.; Тхиеме: Стуттгарт, (2000); Вол. 10, пп. 361. ИСБН 3-13-112241-2 (ГТВ); ИСБН 0-86577-949-X (ТНY).