Oxidação de Swern
Esta página ou seção foi marcada para revisão devido a incoerências ou dados de confiabilidade duvidosa. |
A oxidação de Swern é uma reacção química onde um álcool primário ou secundário é oxidado por um aldeído ou uma cetona na presença de cloreto de oxilo, sulfóxido dimetílico (DMSO) e uma base orgânica, como a trietilamina.[1][2][3] A reacção é conhecida pelo seu carácter suave pela sua grande tolerância a grupos funcionais.[4][5][6][7]
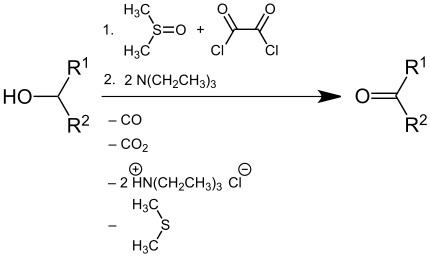
Os produtos da reacção são sulfito dimetílico (Me2S), monóxido de carbono (CO) e - caso a base usada seja a trietilamina - cloreto de trietilamónia (Et3NHCl). Dois dos produtos, sulfito dimetílico e monóxido de carbono, são compostos muito tóxicos e voláteis, pelo que a reacção deve ocorrer dentro de uma hotte. O sulfito dimetílico, um líquido volátil (ponto de fusão 37 °C), tem um cheiro desagradável. Um método conveniente para reduzir este odor é tratá-lo com uma solução de iões oxónio, que faz com que o sulfito se converta em sulfóxido dimetílico, que não tem cheiro.
Algumas análises ao tema foram publicados.[8][9][10]
Mecanismo
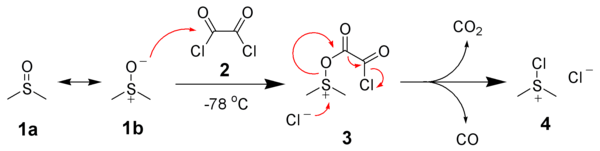
[editar | editar código-fonte]O primeiro requisito para a Oxidação de Swern é a reacção do sufóxido dimetílico (DMSO), 1a & 1b, com cloreto de oxalilo, 2. O primeiro intermédio, 3., decompõe-se facilmente libertando CO2 e CO e obtendo cloreto clorosulfodimetílico, 4.
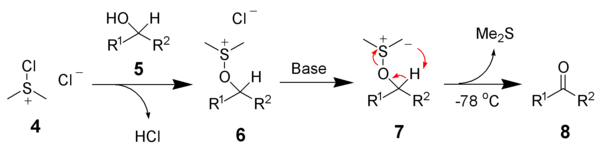
Após adição do álcool 5, o cloreto clorosulfodimetílico 4 reage com o álcool para dar o ião chave intermediário alcoxisulfureto, 6. A adição de pelo menos dois equivalentes de base - normalmente trimetilamina - vão dehidrogenar/deprotonar o ião alcoxisulfureto para fornecer o ylide sulfúrico(?) 7. Num estado de transição de anel de 5 membros, a ilida sulfúrica decompõe-se para originar sulfureto dimetílico e a cetona (ou aldeído) desejada 8.
Variações
[editar | editar código-fonte]Quando usando cloreto de oxilo como agente de desidrogenação, a reacção deve ser mantida abaixo dos -60 °C para evitar reacções paralelas. Com anidro trifluoroacético em vez do cloreto de oxilo, a reacção pode subir aos -30 °C sem reacções indesejadas. Em alguns casos, o uso de trimetilamina como base pode levar a uma epimerização envolvendo o recém-formado carbonilo. Usando uma base mais volumosa como, por exemplo, diisopropiletilamina (i-Pr2ENT, base de Hünig) pode-se atenuar esta reacção paralela.
- ↑ Omura, K.; Swern, D. Tetrahedron 1978, 34, 1651. (doi:10.1016/0040-4020(78)80197-5)
- ↑ Mancuso, A. J.; Huang, S.-L.; Swern, D. J. Org. Chem. 1978, 43, 2480–2482. (doi:10.1021/jo00406a041)
- ↑ Mancuso, A. J.; Brownfain, D. S.; Swern, D. J. Org. Chem. 1979, 44, 4148. (doi:10.1021/jo01337a028)
- ↑ Dondoni, A.; Perrone, D. Org. Syn., Coll. Vol. 10, p.320 (2004); Vol. 77, p.64 (2000). (Article)
- ↑ Bishop, R. Org. Syn., Coll. Vol. 9, p.692 (1998); Vol. 70, p.120 (1992). (Article)
- ↑ Leopold, E. J. Org. Syn., Coll. Vol. 7, p.258 (1990); Vol. 64, p.164 (1986). (Article)
- ↑ Gabriel Tojo and Marcos Fernández. Oxidation of Alkohols to Aldehydes and Ketones: A Guide to Current Common Practice. Springer, 2006.
- ↑ Mancuso, A. J.; Swern, D. Synthesis 1981, 165-185. (Review)
- ↑ Tidwell, T. T. Org. React. 1990, 39, 297-572. (Review)
- ↑ Tidwell, T. T. Synthesis 1990, 857-870. (Review) (doi:10.1055/s-1990-27036)