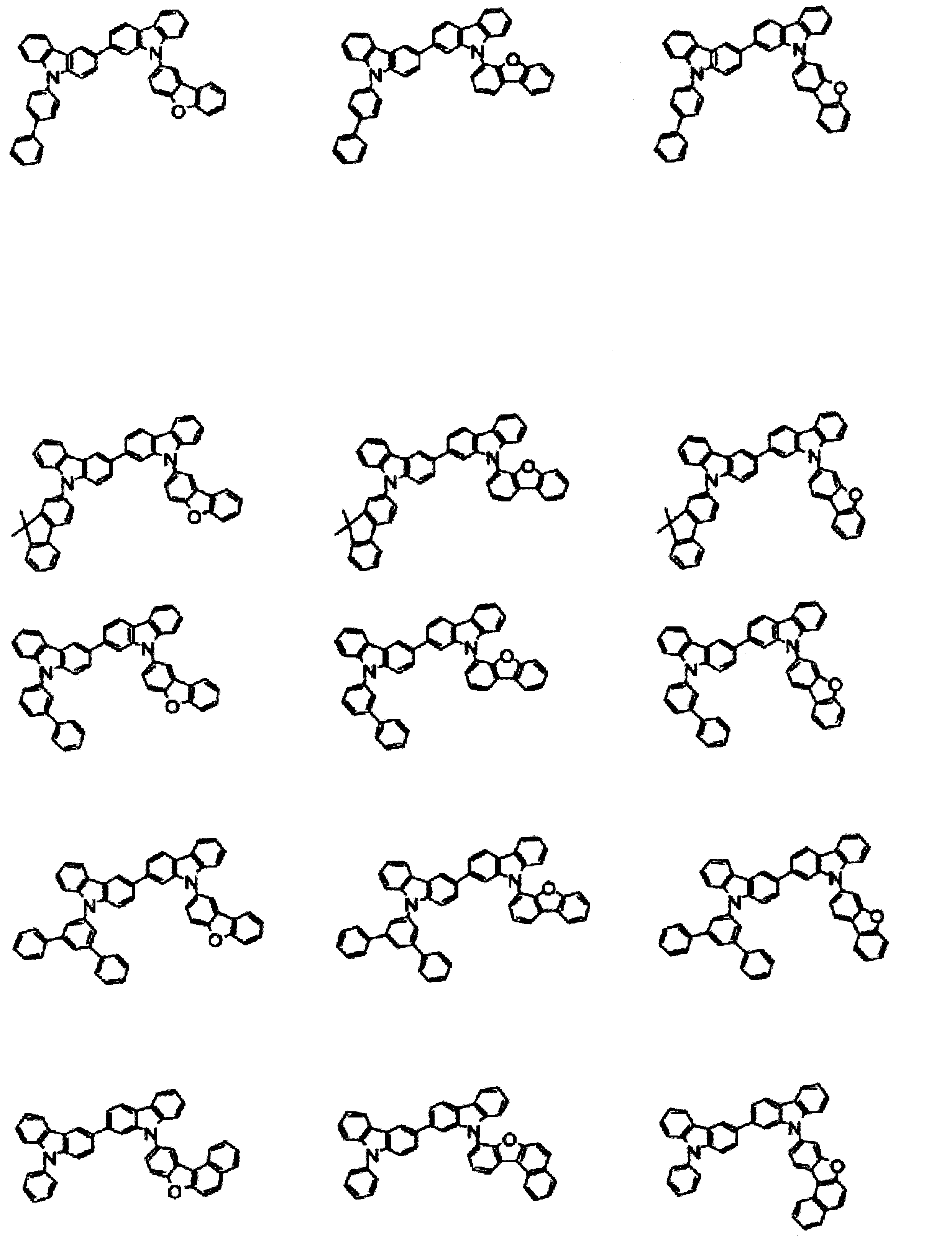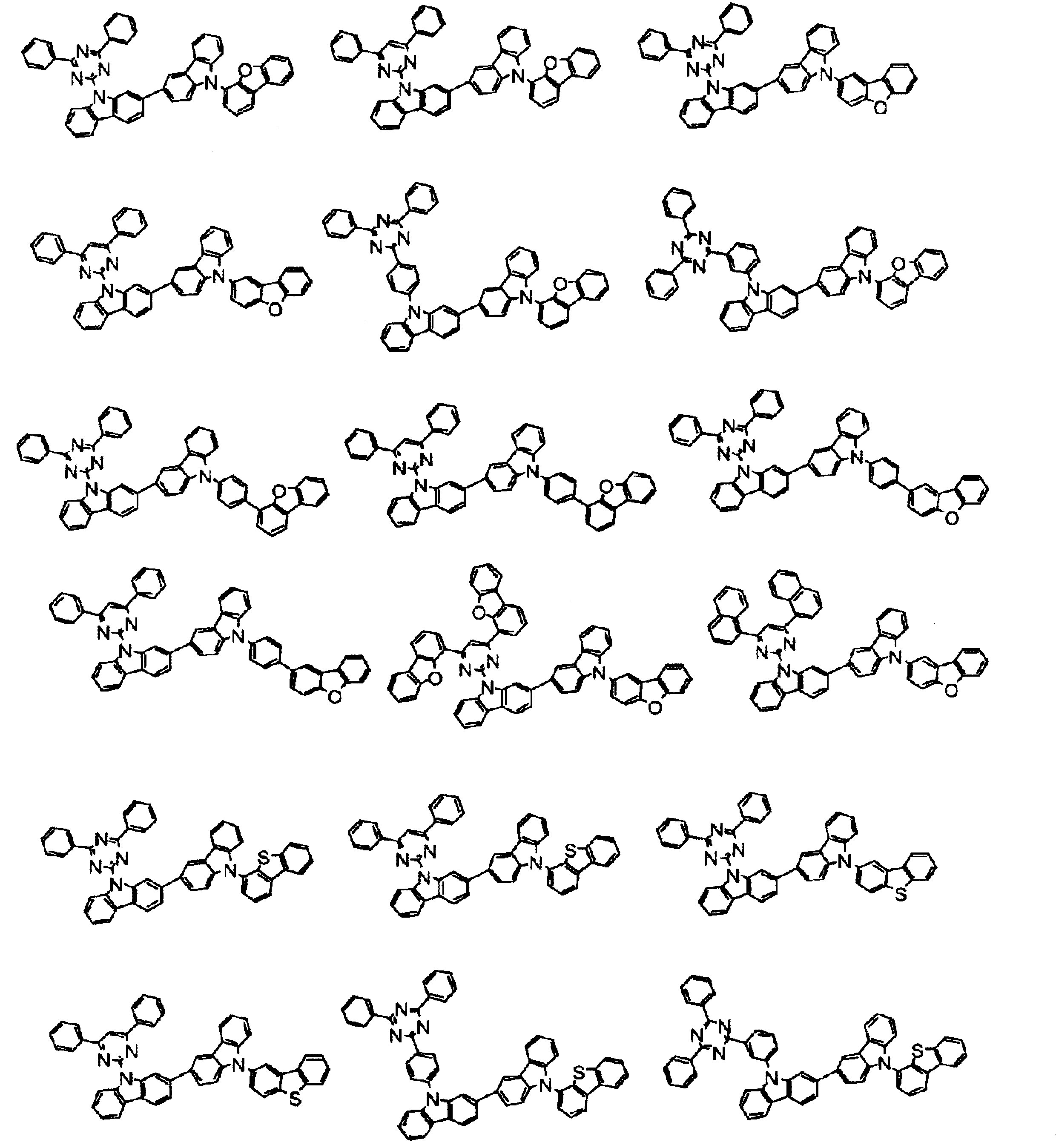WO2014057685A1 - 有機エレクトロルミネッセンス素子 - Google Patents
有機エレクトロルミネッセンス素子 Download PDFInfo
- Publication number
- WO2014057685A1 WO2014057685A1 PCT/JP2013/006063 JP2013006063W WO2014057685A1 WO 2014057685 A1 WO2014057685 A1 WO 2014057685A1 JP 2013006063 W JP2013006063 W JP 2013006063W WO 2014057685 A1 WO2014057685 A1 WO 2014057685A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- ring
- group
- atom
- organic
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 N*C1OCCC=C1 Chemical compound N*C1OCCC=C1 0.000 description 41
- WYLBQDVWWJMOBT-UHFFFAOYSA-N CC1=C(CCCCC2=CC=CCC2)C=CC1 Chemical compound CC1=C(CCCCC2=CC=CCC2)C=CC1 WYLBQDVWWJMOBT-UHFFFAOYSA-N 0.000 description 1
- PAFZNILMFXTMIY-UHFFFAOYSA-N NC1CCCCC1 Chemical compound NC1CCCCC1 PAFZNILMFXTMIY-UHFFFAOYSA-N 0.000 description 1
- AVKNGPAMCBSNSO-UHFFFAOYSA-N NCC1CCCCC1 Chemical compound NCC1CCCCC1 AVKNGPAMCBSNSO-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/20—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the material in which the electroluminescent material is embedded
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/22—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed systems contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains three hetero rings
- C07D487/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/22—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/12—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains three hetero rings
- C07D491/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/22—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D495/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/22—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
- C09K2211/1048—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms with oxygen
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
Definitions
- G 1 to G 4 and G 13 to G 16 are each independently N or> CR b1
- One of G 5 to G 8 is a single bond bonded to one of G 9 to G 12
- the other G 5 to G 8 are each independently N or> CR b1
- One of G 9 to G 12 is a single bond bonded to one of G 5 to G 8
- the other G 9 to G 12 are each independently N or> CR b1
- R b1 is independently a hydrogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, a substituted or unsubstituted cycloalkyl group having 3 to 30 ring carbon atoms, a substituted or unsubstituted ring forming carbon atom.
- alkyl group examples include methyl group, ethyl group, propyl group, isopropyl group, n-butyl group, s-butyl group, isobutyl group, t-butyl group, n-pentyl group, n-hexyl group, n- Heptyl, n-octyl, n-nonyl, n-decyl, n-undecyl, n-dodecyl, n-tridecyl, n-tetradecyl, n-pentadecyl, n-hexadecyl, n- And heptadecyl group, n-octadecyl group, neopentyl group, 1-methylpentyl group, 2-methylpentyl group, 1-pentylhexyl group, 1-butylpentyl group, 1-heptyloctyl group,
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Electroluminescent Light Sources (AREA)
Description
本発明は、有機エレクトロルミネッセンス素子に関する。
有機エレクトロルミネッセンス(EL)素子には、蛍光型及び燐光型があり、それぞれの発光メカニズムに応じ、最適な素子設計や材料が検討されている。一般に有機EL素子は、有機薄膜を複数層積層した構成を有し、各有機薄膜は数nm~数百nm程度ときわめて薄い。そのため、薄膜を形成する有機化合物の分子配置が素子の性能に影響することが知られている。
例えば、特許文献1は新規なアミン化合物を開示するとともに、アモルファス状態は分子の配置がランダムであり、分子が完全に配向している結晶状態と比較すると、電荷の輸送においては不利な分子配置であると教示している。また、分子の配向と電子移動度には相関があり、薄膜内での分子配向がアモルファス薄膜の電荷輸送性の向上に有効であることが示されている。
例えば、特許文献1は新規なアミン化合物を開示するとともに、アモルファス状態は分子の配置がランダムであり、分子が完全に配向している結晶状態と比較すると、電荷の輸送においては不利な分子配置であると教示している。また、分子の配向と電子移動度には相関があり、薄膜内での分子配向がアモルファス薄膜の電荷輸送性の向上に有効であることが示されている。
青色燐光を発する素子では、電流密度が高い場合に顕著な発光効率の低下(ロールオフ現象)が生じることが知られている。これは、燐光型有機EL素子では三重項励起子の寿命がマイクロ秒以上と長いため、三重項三重項対消滅が起きやすいためと考えられる。
本発明の目的は、電流密度が高い領域における発光効率の低下を抑制した有機EL素子を提供することである。
本発明の目的は、電流密度が高い領域における発光効率の低下を抑制した有機EL素子を提供することである。
本発明によれば、陽極と陰極の間に、第一有機薄膜層と第二有機薄膜層を互いに隣接して含み、前記第一有機薄膜層は、配向パラメータSが-0.2~-0.5である有機化合物を含み、前記第二有機薄膜層は、発光極大波長が550nm未満の発光材料を含む、有機エレクトロルミネッセンス素子が提供される。
本発明によれば、電流密度が高い領域における発光効率の低下を抑制した有機EL素子を提供できる。
本発明の有機EL素子の一実施形態は、陽極と陰極の間に、第一有機薄膜層と第二有機薄膜層を互いに隣接して含む。そして、第一有機薄膜層は、配向パラメータSが-0.2~-0.5である有機化合物を含み、第二有機薄膜層は、発光極大波長が550nm未満の発光材料を含むことを特徴とする。本発明では、それぞれ所定の化合物を含有する2層の有機薄膜を隣接して形成することにより、電流密度が高い領域、例えば、10~50mA/cm2の領域における発光効率の低下を抑制できる。
第一有機薄膜層は、配向パラメータSが-0.2~-0.5である有機化合物を含む。配向パラメータSは、すべての分子が基板と平行方向に配向した場合に-0.50となる。また、分子が配向せずにランダムである場合は0.00となる。本発明では、第一有機薄膜層に上記有機化合物を使用することにより、電流密度が高い領域における発光効率の低下を抑制できる。有機化合物の配向パラメータSは、-0.3~-0.5であることが好ましく、特に、-0.4~-0.5であることが好ましい。
薄膜内における配向パラメータSの評価方法は公知の手法であり、詳細はOrganic Electronics誌,2009年,第10巻,127頁に記載されている。基板上に形成した薄膜内における分子軸と基板法線方向のなす角をθ、薄膜の多入射角分光エリプソメトリー測定により得られる基板平行方向及び垂直方向の消衰係数をそれぞれko及びkeとした場合、配向パラメータSは下記式(A)で表される。
S=(1/2)<3cos2θ-1>=(ke-ko)/(ke+2ko)・・・(A)
尚、薄膜を形成する方法としては、真空蒸着法、スピンコート法、キャスト法等の公知の方法を適用することができる。
薄膜内における配向パラメータSの評価方法は公知の手法であり、詳細はOrganic Electronics誌,2009年,第10巻,127頁に記載されている。基板上に形成した薄膜内における分子軸と基板法線方向のなす角をθ、薄膜の多入射角分光エリプソメトリー測定により得られる基板平行方向及び垂直方向の消衰係数をそれぞれko及びkeとした場合、配向パラメータSは下記式(A)で表される。
S=(1/2)<3cos2θ-1>=(ke-ko)/(ke+2ko)・・・(A)
尚、薄膜を形成する方法としては、真空蒸着法、スピンコート法、キャスト法等の公知の方法を適用することができる。
配向パラメータSが-0.2~-0.5である有機化合物としては、例えば、6環以上の縮合環構造を有する化合物が好ましい。例えば、下記式(1)で表される構造を含む化合物が挙げられる。
(式中、環A~Fは、それぞれ独立に、炭素原子、窒素原子、酸素原子、及び硫黄原子から選択される少なくとも1種の原子から構成される、5員環又は6員環を表わす。
環Bの構成元素であるX1及びX2の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。
環Dの構成元素であるX3及びX4の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。
環Fの構成元素であるX5及びX6の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。)
環Bの構成元素であるX1及びX2の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。
環Dの構成元素であるX3及びX4の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。
環Fの構成元素であるX5及びX6の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。)
なかでも、式(1)の環B、環D及び環Fがすべて5員環であり、かつ環A、環C及び環Eがすべて6員環である構造を含む化合物であることが好ましい。例えば、下記式(2)で表される構造を含む化合物が挙げられる。
(式中、Y1~Y12は、それぞれ独立に、窒素原子又は炭素原子であり、X1~X3はそれぞれ独立に、窒素原子、炭素原子、酸素原子及び硫黄原子から選択される原子である。)
上記式(2)の構造を有する化合物は、中心骨格としてπ共役平面の広がった骨格である、ビスインドロジベンゾフラン骨格、ビスインドロジベンゾチオフェン骨格、又はビスインドロカルバゾール骨格を有し、梯子(ラダー)構造を構成していることからキャリア輸送性に優れる。また、配向パラメータSが-0.2~-0.5の範囲にある。キャリア輸送性に優れる化合物を、有機EL素子の材料として用いることで、素子内のキャリアバランスを整え、素子を高効率化させることができる。
式(2)で表される構造を有する有機化合物の例としては、式(2)において、Y1~Y12は、それぞれ独立に、N、又は、>CRaであり、
X1~X3は、それぞれ独立に、>NR1、>CR2R3、酸素原子又は硫黄原子であり、
Raは、水素原子、置換もしくは無置換の環形成炭素数6~18の芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の芳香族複素環基、置換もしくは無置換の炭素数1~12のアルキル基、シアノ基、又は炭素数1~12のハロアルキル基であり、
R1~R3は、それぞれ独立に、置換もしくは無置換の環形成炭素数6~18の芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の芳香族複素環基、又は置換もしくは無置換の炭素数1~12のアルキル基である化合物が挙げられる。
X1~X3は、それぞれ独立に、>NR1、>CR2R3、酸素原子又は硫黄原子であり、
Raは、水素原子、置換もしくは無置換の環形成炭素数6~18の芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の芳香族複素環基、置換もしくは無置換の炭素数1~12のアルキル基、シアノ基、又は炭素数1~12のハロアルキル基であり、
R1~R3は、それぞれ独立に、置換もしくは無置換の環形成炭素数6~18の芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の芳香族複素環基、又は置換もしくは無置換の炭素数1~12のアルキル基である化合物が挙げられる。
尚、式(2)においてRaが複数ある場合、Raはそれぞれ同一でも異なっていてもよい。また、R1~R3がそれぞれ複数ある場合、各R1、R2、及び各R3はそれぞれ同一でも異なっていてもよい、
また、例えば、基「>CRa」の「>C」は、C(炭素)が環を構成する原子であることを意味する。
また、例えば、基「>CRa」の「>C」は、C(炭素)が環を構成する原子であることを意味する。
式(2)のX1及びX3がそれぞれ独立に、>NRであり、X2が1酸素原子又は硫黄原子である化合物が、キャリア輸送性が向上するため、好ましい。
以下、式(2)で表わされる化合物の各基(Ra、R1~R3)の例について説明する。
尚、本発明において、「置換もしくは無置換の・・・」の「無置換」とは、水素原子が結合していることを意味する。また、水素原子とは、中性子数が異なる同位体、即ち、軽水素(protium)、重水素(deuterium)、三重水素(tritium)を包含する。
以下、式(2)で表わされる化合物の各基(Ra、R1~R3)の例について説明する。
尚、本発明において、「置換もしくは無置換の・・・」の「無置換」とは、水素原子が結合していることを意味する。また、水素原子とは、中性子数が異なる同位体、即ち、軽水素(protium)、重水素(deuterium)、三重水素(tritium)を包含する。
環形成炭素数6~18の芳香族炭化水素基としては、フェニル基、ビフェニル基、ターフェニル基、フルオレニル基が挙げられる。
尚、「環形成炭素」とは飽和環、不飽和環、又は芳香環を構成する炭素原子を意味する。
尚、「環形成炭素」とは飽和環、不飽和環、又は芳香環を構成する炭素原子を意味する。
環形成原子数5~14の芳香族複素環基としては、ピロリル基、ピラジニル基、ピリジニル基、ピリミジニル基、トリアジニル基、インドリル基、イソインドリル基、イミダゾリル基、フリル基、ベンゾフラニル基、イソベンゾフラニル基、ジベンゾフラニル基、ジベンゾチオフェニル基、アザジベンゾフラニル基、アザジベンゾチオフェニル基、ジアザジベンゾフラニル基、ジアザジベンゾチオフェニル基、キノリル基、イソキノリル基、キノキサリニル基、カルバゾリル基、フェナントリジニル基、アクリジニル基、フェナントロリニル基、フェナジニル基、フェノチアジニル基、フェノキサジニル基、オキサゾリル基、オキサジアゾリル基、フラザニル基、チエニル基、ベンゾチオフェニル基、ジヒドロアクリジニル基、アザカルバゾリル基、ジアザカルバゾリル基、キナゾリニル基等が挙げられる。好ましくは、ピリジニル基、ピリミジニル基、トリアジニル基、ジベンゾフラニル基、ジベンゾチオフェニル基、アザジベンゾフラニル基、アザジベンゾチオフェニル基、ジアザジベンゾフラニル基、ジアザジベンゾチオフェニル基、カルバゾリル基、アザカルバゾリル基、ジアザカルバゾリル基である。
炭素数1~12のアルキル基としては、直鎖状若しくは分岐状のアルキル基があり、具体的には、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基、n-ペンチル基、n-ヘキシル基、n-ヘプチル基、n-オクチル基等が挙げられ、好ましくは、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が挙げられ、より好ましくはメチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、sec-ブチル基、tert-ブチル基である。
炭素数1~12のアルキル基としては、直鎖状若しくは分岐状のアルキル基があり、具体的には、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基、n-ペンチル基、n-ヘキシル基、n-ヘプチル基、n-オクチル基等が挙げられ、好ましくは、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が挙げられ、より好ましくはメチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、sec-ブチル基、tert-ブチル基である。
炭素数1~12のハロアルキル基としては、上述したアルキル基に1つ以上のハロゲン原子(F,Cl,Br,I等)が置換した基が挙げられる。フルオロアルキル基が好ましく、具体的には、フルオロメチル基、ジフルオロメチル基、トリフルオロメチル基、フルオロエチル基、トリフルオロメチルメチル基、ペンタフルオロエチル基等が挙げられる。好ましくは、トリフルオロメチル基、ペンタフルオロエチル基が挙げられる。
上述した各基の「置換若しくは無置換の・・・」の置換基としては、上記のアルキル基、ハロアルキル基、芳香族炭化水素基、芳香族複素環基、その他に、シクロアルキル基、ハロゲン原子(フッ素、塩素、臭素、ヨウ素等が挙げられ、好ましくはフッ素原子である。)、ヒドロキシル基、ニトロ基、シアノ基、カルボキシ基、アリールオキシ基等が挙げられる。
式(2)で表わされる化合物の製造方法は特に限定されず、公知の方法により製造することができる。
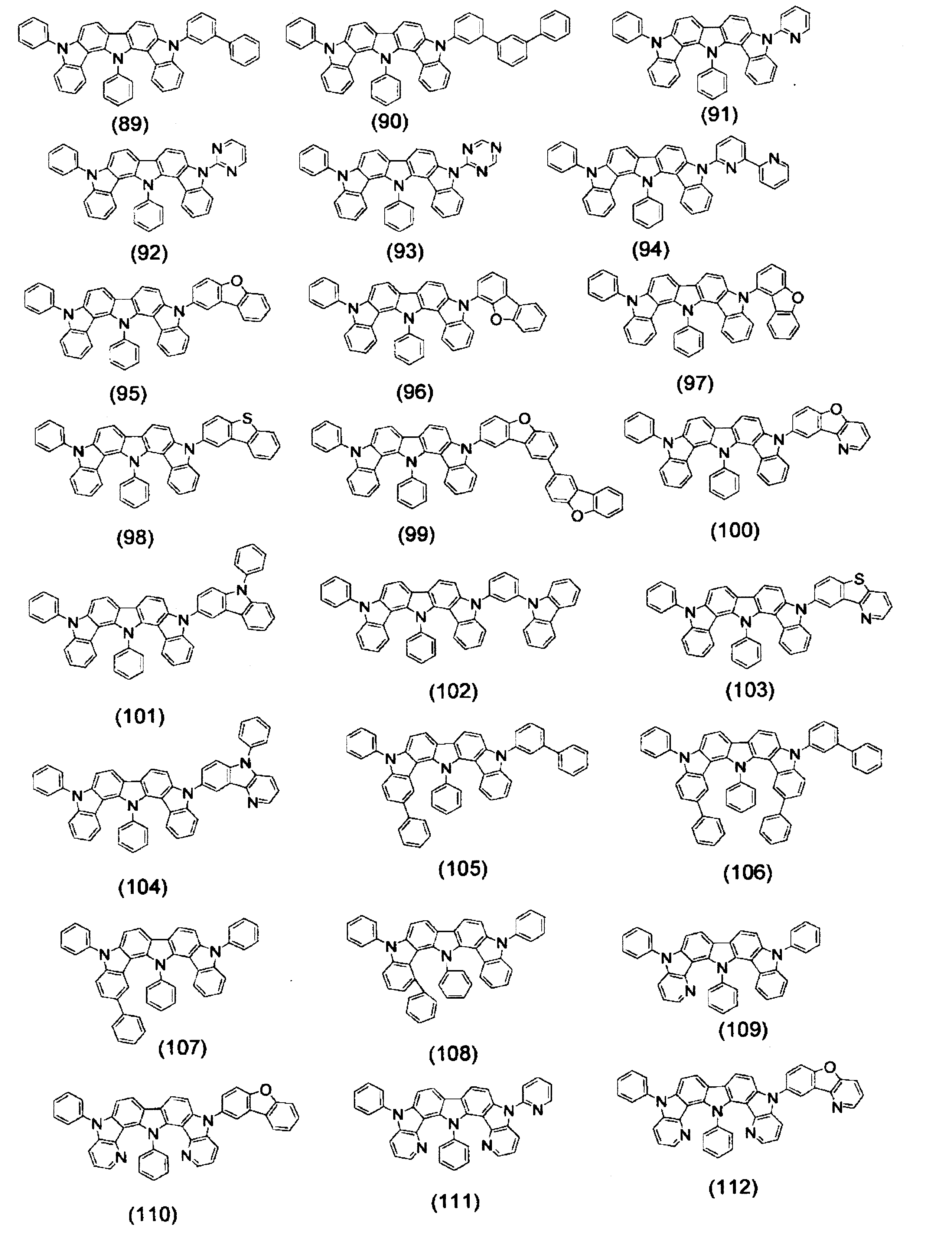
以下に、式(2)で表わされる化合物の具体例を示す。
式(2)で表わされる化合物の製造方法は特に限定されず、公知の方法により製造することができる。
以下に、式(2)で表わされる化合物の具体例を示す。
また、配向パラメータが-0.2~-0.5である有機化合物としては、例えば、下記式(3)で表される化合物が好ましい。
(式(3)中、A1及びA2は、それぞれ独立に、置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基、置換もしくは無置換の環形成原子数3~30の芳香族複素環基、-Si(Rc)3、又は-ORcであり、
L1及びL2は、それぞれ独立に、単結合、置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基、又は置換もしくは無置換の環形成原子数3~30の芳香族複素環基であり、
G1~G4及びG13~G16は、それぞれ独立に、N、又は、>CRb1であり、
G5~G8の1つはG9~G12の1つと結合する単結合であり、他のG5~G8は、それぞれ独立に、N、又は、>CRb1であり、
G9~G12の1つはG5~G8の1つと結合する単結合であり、他のG9~G12は、それぞれ独立に、N、又は、>CRb1であり、
Rb1は、それぞれ独立に、水素原子、置換もしくは無置換の炭素数1~30のアルキル基、置換もしくは無置換の環形成炭素数3~30のシクロアルキル基、置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基、置換もしくは無置換の環形成原子数3~30の芳香族複素環基、-Si(Rc)3、又は-ORcである。
Rcは、水素原子、置換もしくは無置換の炭素数1~30のアルキル基、又は置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基である。
複数のCRb1が存在する場合、複数のRb1は、それぞれ同一又は異なっていてもよい。
複数のNRb1が存在する場合、複数のRb1は、それぞれ同一又は異なっていてもよい。
複数のRcが存在する場合、複数のRcは、それぞれ同一又は異なっていてもよい。)
L1及びL2は、それぞれ独立に、単結合、置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基、又は置換もしくは無置換の環形成原子数3~30の芳香族複素環基であり、
G1~G4及びG13~G16は、それぞれ独立に、N、又は、>CRb1であり、
G5~G8の1つはG9~G12の1つと結合する単結合であり、他のG5~G8は、それぞれ独立に、N、又は、>CRb1であり、
G9~G12の1つはG5~G8の1つと結合する単結合であり、他のG9~G12は、それぞれ独立に、N、又は、>CRb1であり、
Rb1は、それぞれ独立に、水素原子、置換もしくは無置換の炭素数1~30のアルキル基、置換もしくは無置換の環形成炭素数3~30のシクロアルキル基、置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基、置換もしくは無置換の環形成原子数3~30の芳香族複素環基、-Si(Rc)3、又は-ORcである。
Rcは、水素原子、置換もしくは無置換の炭素数1~30のアルキル基、又は置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基である。
複数のCRb1が存在する場合、複数のRb1は、それぞれ同一又は異なっていてもよい。
複数のNRb1が存在する場合、複数のRb1は、それぞれ同一又は異なっていてもよい。
複数のRcが存在する場合、複数のRcは、それぞれ同一又は異なっていてもよい。)
以下、式(3)又は式(4)で表される各基(A1、A2、L1、L2、Rb1)の例について説明する。
芳香族炭化水素環基は、単環の芳香族炭化水素環基及び複数の炭化水素環が縮合した縮合芳香族炭化水素環基を含み、芳香族複素環基は、単環の芳香族複素環基、並びに複数の芳香族複素環が縮合した縮合芳香族複素環基、及び芳香族炭化水素環と芳香族複素環とが縮合した縮合芳香族複素環基を含む。
芳香族炭化水素環基は、単環の芳香族炭化水素環基及び複数の炭化水素環が縮合した縮合芳香族炭化水素環基を含み、芳香族複素環基は、単環の芳香族複素環基、並びに複数の芳香族複素環が縮合した縮合芳香族複素環基、及び芳香族炭化水素環と芳香族複素環とが縮合した縮合芳香族複素環基を含む。
アルキル基の具体例としては、メチル基、エチル基、プロピル基、イソプロピル基、n-ブチル基、s-ブチル基、イソブチル基、t-ブチル基、n-ペンチル基、n-ヘキシル基、n-ヘプチル基、n-オクチル基、n-ノニル基、n-デシル基、n-ウンデシル基、n-ドデシル基、n-トリデシル基、n-テトラデシル基、n-ペンタデシル基、n-ヘキサデシル基、n-ヘプタデシル基、n-オクタデシル基、ネオペンチル基、1-メチルペンチル基、2-メチルペンチル基、1-ペンチルヘキシル基、1-ブチルペンチル基、1-ヘプチルオクチル基、3-メチルペンチル基等が挙げられ、このうち炭素数1~6のものが好ましい。
シクロアルキル基の具体例としては、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、ノルボルニル基、アダマンチル基等が挙げられ、このうち環形成炭素数5又は6のものが好ましい。
A1、A2、L1、L2、Rb1、Rcが置換基を有する場合の当該置換基R’は、例えば、水素原子、炭素数1~20のアルキル基、環形成炭素数3~20のシクロアルキル基、炭素数1~20のアルコキシ基、環形成炭素数3~20のシクロアルコキシ基、環形成炭素数6~18の芳香族炭化水素環基、環形成炭素数6~18のアリールオキシ基、環形成原子数5~18のヘテロ芳香族環基、シリル基、フッ素原子、炭素数1~20のフルオロアルキル基、炭素数1~20のフルオロアルコキシ基又はシアノ基である。
式(3)で表される化合物の製造方法は特に限定されず、公知の方法により製造することができる。
A1、A2、L1、L2、Rb1、Rcが置換基を有する場合の当該置換基R’は、例えば、水素原子、炭素数1~20のアルキル基、環形成炭素数3~20のシクロアルキル基、炭素数1~20のアルコキシ基、環形成炭素数3~20のシクロアルコキシ基、環形成炭素数6~18の芳香族炭化水素環基、環形成炭素数6~18のアリールオキシ基、環形成原子数5~18のヘテロ芳香族環基、シリル基、フッ素原子、炭素数1~20のフルオロアルキル基、炭素数1~20のフルオロアルコキシ基又はシアノ基である。
式(3)で表される化合物の製造方法は特に限定されず、公知の方法により製造することができる。
有機化合物の三重項エネルギーは、2.8eV以上であることが好ましい。この場合、発光ドーパントから第一有機薄膜層へのエネルギー移動を抑制することが可能である。有機化合物の三重項エネルギーは、2.9eV以上であることがより好ましい。尚、上限は特に規定しないが、通常3.6eV以下となる。
第一有機薄膜層は、実質的に配向パラメータSが-0.2~-0.5である有機化合物のみからなっていてもよく、他の材料、例えば、正孔輸送層、電子輸送層、発光層等に使用される公知の有機化合物を含有していてもよい。第一有機薄膜層における配向パラメータSが-0.2~-0.5である有機化合物の含有量は、90重量%以上であることが好ましく、95重量%以上であることが特に好ましい。
第一有機薄膜層の膜厚は、好ましくは5~50nm、より好ましくは7~50nm、さらに好ましくは10~50nmである。5nm以上であると層形成が容易であり、50nm以下であると駆動電圧の上昇が避けられる。
第二有機薄膜層は、発光極大波長が550nm未満(好ましくは480nm未満)の発光材料を含む。発光材料としては、例えば、発光層のドーパントとして公知の燐光発光性材料又は蛍光発光性材料が使用できる。
燐光発光性材料は、三重項励状態から発光することのできる化合物であり、三重項励状態から発光する限り特に限定されないが、Ir、Pt、Os、Cu及びAuから選択される少なくとも一つの金属と配位子とを含む有機金属錯体であることが好ましい。前記配位子は、オルトメタル結合を有することが好ましい。燐光量子収率が高く、発光素子の外部量子効率をより向上させることができるという点で、Ir、Os及びPtから選ばれる金属原子を含有する金属錯体が好ましく、イリジウム錯体、オスミウム錯体、白金錯体等の金属錯体、特にオルトメタル化錯体がより好ましく、イリジウム錯体及び白金錯体がさらに好ましく、オルトメタル化イリジウム錯体が特に好ましい。
燐光発光性材料は、三重項励状態から発光することのできる化合物であり、三重項励状態から発光する限り特に限定されないが、Ir、Pt、Os、Cu及びAuから選択される少なくとも一つの金属と配位子とを含む有機金属錯体であることが好ましい。前記配位子は、オルトメタル結合を有することが好ましい。燐光量子収率が高く、発光素子の外部量子効率をより向上させることができるという点で、Ir、Os及びPtから選ばれる金属原子を含有する金属錯体が好ましく、イリジウム錯体、オスミウム錯体、白金錯体等の金属錯体、特にオルトメタル化錯体がより好ましく、イリジウム錯体及び白金錯体がさらに好ましく、オルトメタル化イリジウム錯体が特に好ましい。
燐光発光性材料の発光層における含有量は特に制限はなく目的に応じて適宜選択することができるが、例えば、0.1~70質量%が好ましく、1~30質量%がより好ましい。燐光発光性材料の含有量が0.1質量%以上であると十分な発光が得られ、70質量%以下であると濃度消光を避けることができる。
第二有機薄膜層は、例えば、上述した発光性材料に加えてホスト材料を含有する。ホスト材料としては、発光層で使用する公知のホスト材料が使用できる。
第二有機薄膜層は、例えば、上述した発光性材料に加えてホスト材料を含有する。ホスト材料としては、発光層で使用する公知のホスト材料が使用できる。
第二有機薄膜層の膜厚は、好ましくは5~50nm、より好ましくは7~50nm、さらに好ましくは10~50nmである。5nm以上であると層形成が容易であり、50nm以下であると駆動電圧の上昇が避けられる。
本発明の有機EL素子は、陽極と陰極の間に、上述した第一有機薄膜層と第二有機薄膜層を互いに隣接して含んであればよい。他の構成は特に限定されず、有機EL素子において公知の構成及び材料等を採用できる。
第一有機薄膜層は、例えば、電荷輸送や障壁(阻止)等の機能を有する。第二有機薄膜層は、例えば、発光層の機能を有する。
第一有機薄膜層は、例えば、電荷輸送や障壁(阻止)等の機能を有する。第二有機薄膜層は、例えば、発光層の機能を有する。
尚、障壁層(阻止層)とは、キャリアの移動障壁、又は励起子の拡散障壁の機能を有する層である。発光層から正孔輸送帯域へ電子が漏れることを防ぐための有機層を主に電子障壁層と定義し、発光層から電子輸送帯域へ正孔が漏れることを防ぐための有機層を正孔障壁層と定義することがある。また、発光層で生成された三重項励起子が、三重項エネルギーが発光層よりも低い準位を有する周辺層へ拡散することを防止するための有機層を励起子阻止層(トリプレット障壁層)と定義することがある。
図1は、本発明の有機EL素子の一実施形態の層構成を示す概略図である。
有機EL素子1は、基板10上に、陽極20、正孔輸送帯域30、燐光発光層40、電子輸送帯域50及び陰極60を、この順で積層した構成を有する。正孔輸送帯域30は、正孔輸送層、正孔注入層、電子阻止層等を意味する。同様に、電子輸送帯域50は、電子輸送層、電子注入層、正孔阻止層等を意味する。
本実施形態において、燐光発光層40が第二有機薄膜層に相当する。また、正孔輸送帯域30内の層であって燐光発光層40に隣接する層、及び、電子輸送帯域50内の層であって燐光発光層40に隣接する層のうち、少なくとも1層が第一有機薄膜層に相当する。
有機EL素子1は、基板10上に、陽極20、正孔輸送帯域30、燐光発光層40、電子輸送帯域50及び陰極60を、この順で積層した構成を有する。正孔輸送帯域30は、正孔輸送層、正孔注入層、電子阻止層等を意味する。同様に、電子輸送帯域50は、電子輸送層、電子注入層、正孔阻止層等を意味する。
本実施形態において、燐光発光層40が第二有機薄膜層に相当する。また、正孔輸送帯域30内の層であって燐光発光層40に隣接する層、及び、電子輸送帯域50内の層であって燐光発光層40に隣接する層のうち、少なくとも1層が第一有機薄膜層に相当する。
本実施形態では、陽極20、第一有機薄膜層、第二有機薄膜層及び陰極60を、この順に積層して含むことが好ましい。即ち、正孔輸送帯域30内に第一有機薄膜層があることが好ましい。
本発明の有機EL素子では、上述した本発明の有機EL素子用材料を使用した層以外の構成については、特に限定されず、公知の材料等を使用できる。以下、素子の構成要素について簡単に説明するが、本発明の有機EL素子に適用される材料は以下に限定されない。
(基板)
基板は、発光素子の支持体として用いられる。基板としては、例えば、ガラス、石英、プラスチックなどを用いることができる。また、可撓性基板を用いてもよい。可撓性基板とは、折り曲げることができる(フレキシブル)基板のことであり、例えば、ポリカーボネート、ポリ塩化ビニルからなるプラスチック基板等が挙げられる。
基板は、発光素子の支持体として用いられる。基板としては、例えば、ガラス、石英、プラスチックなどを用いることができる。また、可撓性基板を用いてもよい。可撓性基板とは、折り曲げることができる(フレキシブル)基板のことであり、例えば、ポリカーボネート、ポリ塩化ビニルからなるプラスチック基板等が挙げられる。
(陽極)
基板上に形成される陽極には、仕事関数の大きい(具体的には4.0eV以上)金属、合金、電気伝導性化合物、及びこれらの混合物などを用いることが好ましい。具体的には、例えば、酸化インジウム-酸化スズ(ITO:Indium Tin Oxide)、珪素若しくは酸化珪素を含有した酸化インジウム-酸化スズ、酸化インジウム-酸化亜鉛、酸化タングステン、及び酸化亜鉛を含有した酸化インジウム、グラフェン等が挙げられる。この他、金(Au)、白金(Pt)、又は金属材料の窒化物(例えば、窒化チタン)等が挙げられる。
基板上に形成される陽極には、仕事関数の大きい(具体的には4.0eV以上)金属、合金、電気伝導性化合物、及びこれらの混合物などを用いることが好ましい。具体的には、例えば、酸化インジウム-酸化スズ(ITO:Indium Tin Oxide)、珪素若しくは酸化珪素を含有した酸化インジウム-酸化スズ、酸化インジウム-酸化亜鉛、酸化タングステン、及び酸化亜鉛を含有した酸化インジウム、グラフェン等が挙げられる。この他、金(Au)、白金(Pt)、又は金属材料の窒化物(例えば、窒化チタン)等が挙げられる。
(正孔注入層)
正孔注入層は、正孔注入性の高い物質を含む層である。正孔注入性の高い物質としては、モリブデン酸化物、チタン酸化物、バナジウム酸化物、レニウム酸化物、ルテニウム酸化物、クロム酸化物、ジルコニウム酸化物、ハフニウム酸化物、タンタル酸化物、銀酸化物、タングステン酸化物、マンガン酸化物、芳香族アミン化合物、又は高分子化合物(オリゴマー、デンドリマー、ポリマー等)等も使用できる。
正孔注入層は、正孔注入性の高い物質を含む層である。正孔注入性の高い物質としては、モリブデン酸化物、チタン酸化物、バナジウム酸化物、レニウム酸化物、ルテニウム酸化物、クロム酸化物、ジルコニウム酸化物、ハフニウム酸化物、タンタル酸化物、銀酸化物、タングステン酸化物、マンガン酸化物、芳香族アミン化合物、又は高分子化合物(オリゴマー、デンドリマー、ポリマー等)等も使用できる。
(正孔輸送層)
正孔輸送層は、正孔輸送性の高い物質を含む層である。正孔輸送層には、芳香族アミン化合物、カルバゾール誘導体、アントラセン誘導体等を使用する事ができる。ポリ(N-ビニルカルバゾール)(略称:PVK)やポリ(4-ビニルトリフェニルアミン)(略称:PVTPA)等の高分子化合物を用いることもできる。但し、電子よりも正孔の輸送性の高い物質であれば、これら以外のものを用いてもよい。尚、正孔輸送性の高い物質を含む層は、単層のものだけでなく、上記物質からなる層が二層以上積層したものとしてもよい。
尚、「正孔輸送層」は、上述した第一有機薄膜層とは異なる層を意図しているが、本発明の有機EL素子の一実施形態では、正孔輸送層を設けずに、第一有機薄膜層が正孔輸送層としての機能を兼ね備えていてもよい。
正孔輸送層は、正孔輸送性の高い物質を含む層である。正孔輸送層には、芳香族アミン化合物、カルバゾール誘導体、アントラセン誘導体等を使用する事ができる。ポリ(N-ビニルカルバゾール)(略称:PVK)やポリ(4-ビニルトリフェニルアミン)(略称:PVTPA)等の高分子化合物を用いることもできる。但し、電子よりも正孔の輸送性の高い物質であれば、これら以外のものを用いてもよい。尚、正孔輸送性の高い物質を含む層は、単層のものだけでなく、上記物質からなる層が二層以上積層したものとしてもよい。
尚、「正孔輸送層」は、上述した第一有機薄膜層とは異なる層を意図しているが、本発明の有機EL素子の一実施形態では、正孔輸送層を設けずに、第一有機薄膜層が正孔輸送層としての機能を兼ね備えていてもよい。
(発光層のゲスト材料)
発光層は、発光性の高い物質を含む層であり、種々の材料を用いることができる。例えば、発光性の高い物質としては、蛍光を発光する蛍光性化合物や燐光を発光する燐光性化合物を用いることができる。蛍光性化合物は一重項励起状態から発光可能な化合物であり、燐光性化合物は三重項励起状態から発光可能な化合物である。
発光層に用いることができる青色系の蛍光発光材料として、ピレン誘導体、スチリルアミン誘導体、クリセン誘導体、フルオランテン誘導体、フルオレン誘導体、ジアミン誘導体、トリアリールアミン誘導体等が使用できる。発光層に用いることができる緑色系の蛍光発光材料として、芳香族アミン誘導体等を使用できる。発光層に用いることができる赤色系の蛍光発光材料として、テトラセン誘導体、ジアミン誘導体等が使用できる。
発光層に用いることができる青色系の燐光発光材料として、イリジウム錯体、オスミウム錯体、白金錯体等の金属錯体が使用される。発光層に用いることができる緑色系の燐光発光材料としてイリジウム錯体等が使用される。発光層に用いることができる赤色系の燐光発光材料として、イリジウム錯体、白金錯体、テルビウム錯体、ユーロピウム錯体等の金属錯体が使用される。
発光層は、発光性の高い物質を含む層であり、種々の材料を用いることができる。例えば、発光性の高い物質としては、蛍光を発光する蛍光性化合物や燐光を発光する燐光性化合物を用いることができる。蛍光性化合物は一重項励起状態から発光可能な化合物であり、燐光性化合物は三重項励起状態から発光可能な化合物である。
発光層に用いることができる青色系の蛍光発光材料として、ピレン誘導体、スチリルアミン誘導体、クリセン誘導体、フルオランテン誘導体、フルオレン誘導体、ジアミン誘導体、トリアリールアミン誘導体等が使用できる。発光層に用いることができる緑色系の蛍光発光材料として、芳香族アミン誘導体等を使用できる。発光層に用いることができる赤色系の蛍光発光材料として、テトラセン誘導体、ジアミン誘導体等が使用できる。
発光層に用いることができる青色系の燐光発光材料として、イリジウム錯体、オスミウム錯体、白金錯体等の金属錯体が使用される。発光層に用いることができる緑色系の燐光発光材料としてイリジウム錯体等が使用される。発光層に用いることができる赤色系の燐光発光材料として、イリジウム錯体、白金錯体、テルビウム錯体、ユーロピウム錯体等の金属錯体が使用される。
(発光層のホスト材料)
発光層としては、上述した発光性の高い物質(ゲスト材料)を他の物質(ホスト材料)に分散させた構成としてもよい。発光性の高い物質を分散させるための物質としては、各種のものを用いることができ、発光性の高い物質よりも最低空軌道準位(LUMO準位)が高く、最高被占有軌道準位(HOMO準位)が低い物質を用いることが好ましい。
発光性の高い物質を分散させるための物質(ホスト材料)としては、1)アルミニウム錯体、ベリリウム錯体、若しくは亜鉛錯体等の金属錯体、2)オキサジアゾール誘導体、ベンゾイミダゾール誘導体、若しくはフェナントロリン誘導体等の複素環化合物、3)カルバゾール誘導体、アントラセン誘導体、フェナントレン誘導体、ピレン誘導体、若しくはクリセン誘導体等の縮合芳香族化合物、3)トリアリールアミン誘導体、若しくは縮合多環芳香族アミン誘導体等の芳香族アミン化合物が使用される。
発光層としては、上述した発光性の高い物質(ゲスト材料)を他の物質(ホスト材料)に分散させた構成としてもよい。発光性の高い物質を分散させるための物質としては、各種のものを用いることができ、発光性の高い物質よりも最低空軌道準位(LUMO準位)が高く、最高被占有軌道準位(HOMO準位)が低い物質を用いることが好ましい。
発光性の高い物質を分散させるための物質(ホスト材料)としては、1)アルミニウム錯体、ベリリウム錯体、若しくは亜鉛錯体等の金属錯体、2)オキサジアゾール誘導体、ベンゾイミダゾール誘導体、若しくはフェナントロリン誘導体等の複素環化合物、3)カルバゾール誘導体、アントラセン誘導体、フェナントレン誘導体、ピレン誘導体、若しくはクリセン誘導体等の縮合芳香族化合物、3)トリアリールアミン誘導体、若しくは縮合多環芳香族アミン誘導体等の芳香族アミン化合物が使用される。
(電子輸送層)
電子輸送層は、電子輸送性の高い物質を含む層である。電子輸送層には、1)アルミニウム錯体、ベリリウム錯体、亜鉛錯体等の金属錯体、2)イミダゾール誘導体、ベンゾイミダゾール誘導体、アジン誘導体、カルバゾール誘導体、フェナントロリン誘導体等の複素芳香族化合物、3)高分子化合物を使用することができる。
電子輸送層は、電子輸送性の高い物質を含む層である。電子輸送層には、1)アルミニウム錯体、ベリリウム錯体、亜鉛錯体等の金属錯体、2)イミダゾール誘導体、ベンゾイミダゾール誘導体、アジン誘導体、カルバゾール誘導体、フェナントロリン誘導体等の複素芳香族化合物、3)高分子化合物を使用することができる。
(電子注入層)
電子注入層は、電子注入性の高い物質を含む層である。電子注入層には、リチウム(Li)、フッ化リチウム(LiF)、フッ化セシウム(CsF)、フッ化カルシウム(CaF2)、リチウム酸化物(LiOx)等のようなアルカリ金属、アルカリ土類金属、又はそれらの化合物を用いることができる。
電子注入層は、電子注入性の高い物質を含む層である。電子注入層には、リチウム(Li)、フッ化リチウム(LiF)、フッ化セシウム(CsF)、フッ化カルシウム(CaF2)、リチウム酸化物(LiOx)等のようなアルカリ金属、アルカリ土類金属、又はそれらの化合物を用いることができる。
(陰極)
陰極には、仕事関数の小さい(具体的には3.8eV以下)金属、合金、電気伝導性化合物、及びこれらの混合物などを用いることが好ましい。このような陰極材料の具体例としては、元素周期表の第1族又は第2族に属する元素、すなわちリチウム(Li)やセシウム(Cs)等のアルカリ金属、及びマグネシウム(Mg)等のアルカリ土類金属、及びこれらを含む合金(例えば、MgAg、AlLi)等の希土類金属及びこれらを含む合金等が挙げられる。
陰極には、仕事関数の小さい(具体的には3.8eV以下)金属、合金、電気伝導性化合物、及びこれらの混合物などを用いることが好ましい。このような陰極材料の具体例としては、元素周期表の第1族又は第2族に属する元素、すなわちリチウム(Li)やセシウム(Cs)等のアルカリ金属、及びマグネシウム(Mg)等のアルカリ土類金属、及びこれらを含む合金(例えば、MgAg、AlLi)等の希土類金属及びこれらを含む合金等が挙げられる。
本発明の有機EL素子は、発光素子として各種ディスプレイ等に使用されるパネルモジュールに使用できる。
また、本発明の有機EL素子は、テレビ、携帯端末、パーソナルコンピュータ等の表示装置や、照明等の電子機器に使用できる。
また、本発明の有機EL素子は、テレビ、携帯端末、パーソナルコンピュータ等の表示装置や、照明等の電子機器に使用できる。
三口フラスコにジベンゾフラン 20.0g(80.9mmol)、脱水テトラヒドロフラン 200mlを入れ、窒素雰囲気下にて反応器を-70℃に冷却した。反応器に1.68Mのs-ブチルリチウムへキサン溶液 96ml(161.8mmol)を滴下し、-70℃にて1時間撹拌した。これにさらにホウ酸トリイソプロピル 37.3ml(162mmol)を加え室温で6時間撹拌した。反応終了後、1NのHCl水溶液 100mlを加え30分撹拌した後、試料溶液を分液ロートに移し、ジクロロメタンにて数回抽出した。これを、無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをヘキサンにて分散洗浄し、白色の固体を得た。
収量は15.9g、収率は93%であった。
収量は15.9g、収率は93%であった。
三口フラスコに化合物(1-1)25.0g(97.7mmol)、2-ヨードニトロベンゼン74.7g(300mmol)、2M炭酸ナトリウム水溶液250mL、1,2-ジメトキシエタン500mL、テトラキス(トリフェニルホスフィン)パラジウム(0)[Pd(PPh3)4] 2.30g(1.95mmol)を入れ、窒素雰囲気下にて12時間還流させた。反応終了後、試料溶液をろ過し、得られた固体をメタノール、ヘキサンにて洗浄した。
収量は26.5g、収率は66%であった。
収量は26.5g、収率は66%であった。
三口フラスコに化合物(1-2)26.5g(64.6mmol)、亜リン酸トリエチル430mlを加え、170℃で16時間加熱撹拌した。
反応終了後、蒸留を行い、残った亜リン酸トリエチル、亜リン酸トリエチル残渣を除去し、得られた有機層をシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=10:1~5:1~1:1)で精製し、淡黄色の固体を得た。
収量は12.1g、収率は54%であった。
反応終了後、蒸留を行い、残った亜リン酸トリエチル、亜リン酸トリエチル残渣を除去し、得られた有機層をシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=10:1~5:1~1:1)で精製し、淡黄色の固体を得た。
収量は12.1g、収率は54%であった。
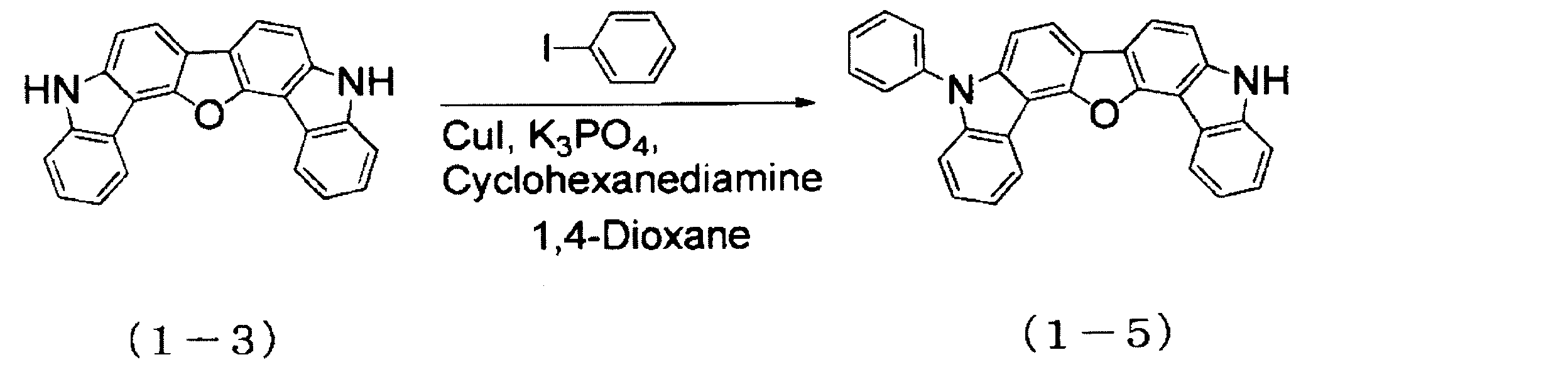
三口フラスコに化合物(1-3)3.46g(10mmol)、3-ブロモ-9-フェニルカルバゾール7.09g(22mmоl)、ヨウ化銅1.90g(10mmol)、リン酸三カリウム4.24g(20mmol)、1,2-シクロヘキサンジアミン2.28g(20mmol)、1,4-ジオキサン50mLを入れ、窒素雰囲気下にて24時間還流させた。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=10:1~5:1~2:1)で精製し、白色の固体を得た。
収量は5.6g、収率は67%であった。
FD-MS分析の結果、分子量828に対してm/e=828であった。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=10:1~5:1~2:1)で精製し、白色の固体を得た。
収量は5.6g、収率は67%であった。
FD-MS分析の結果、分子量828に対してm/e=828であった。
合成例2(化合物(151)の合成)
(1)化合物(1-4)の合成
三口フラスコに化合物(1-3)3.46g(10mmol)、3-ブロモ-9-フェニルカルバゾール3.22g(10mmоl)、ヨウ化銅1.90g(10mmol)、リン酸三カリウム4.24g(20mmol)、1,2-シクロヘキサンジアミン2.28g(20mmol)、1,4-ジオキサン50mLを入れ、窒素雰囲気下にて24時間還流させた。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=3:1~3:2)で精製し、白色の固体を得た。
収量は3.1g、収率は52%であった。
(1)化合物(1-4)の合成
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=3:1~3:2)で精製し、白色の固体を得た。
収量は3.1g、収率は52%であった。
三口フラスコに化合物(1-4)1.0g(1.70mmol)、2-(m-ブロモフェニル)ジベンゾフラン0.66g(2.04mmоl)、ヨウ化銅0.49g(2.55mmol)、リン酸三カリウム0.72g(3.40mmol)、1,2-シクロヘキサンジアミン0.39g(3.40mmol)、1,4-ジオキサン15mLを入れ、窒素雰囲気下にて12時間還流させた。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=4:1~3:2)で精製し、白色の固体を得た。
収量は1.2g、収率は85%であった。
FD-MS分析の結果、分子量829に対してm/e=829であった。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=4:1~3:2)で精製し、白色の固体を得た。
収量は1.2g、収率は85%であった。
FD-MS分析の結果、分子量829に対してm/e=829であった。
三口フラスコに化合物(1-3)3.46g(10mmol)、ヨードベンゼン2.04g(10mmоl)、ヨウ化銅1.90g(10mmol)、リン酸三カリウム4.24g(20mmol)、シクロヘキサンジアミン2.28g(20mmol)、1,4-ジオキサン30mLを入れ、窒素雰囲気下にて12時間還流させた。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=10:1~5:1)で精製し、白色の固体を得た。
収量は1.69g、収率は40%であった。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=10:1~5:1)で精製し、白色の固体を得た。
収量は1.69g、収率は40%であった。
三口フラスコに化合物(1-5)1.30g(3.08mmol)、2-(m-ブロモフェニル)ジベンゾフラン1.09g(3.38mmоl)、ヨウ化銅0.59g(3.08mmol)、リン酸三カリウム0.65g(3.08mmol)、1,2-シクロヘキサンジアミン0.35g(3.08mmol)、1,4-ジオキサン20mLを入れ、窒素雰囲気下にて18時間還流させた。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=4:1~1:1~1:4)で精製し、白色の固体を得た。
収量は0.95g、収率は46%であった。
FD-MS分析の結果、分子量664に対してm/e=664であった。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=4:1~1:1~1:4)で精製し、白色の固体を得た。
収量は0.95g、収率は46%であった。
FD-MS分析の結果、分子量664に対してm/e=664であった。
三口フラスコに化合物(1-3)2.50g(7.22mmol)、2-ブロモ-9,9-ジメチルフルオレン4.93g(18.0mmоl)、ヨウ化銅1.38g(7.22mmol)、リン酸三カリウム2.30g(10.1mmol)、1,2-シクロヘキサンジアミン0.82g(7.22mmol)、1,4-ジオキサン40mLを入れ、窒素雰囲気下にて15時間還流させた。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=3:1~7:3)で精製し、白色の固体を得た。
収量は3.75g、収率は71%であった。
FD-MS分析の結果、分子量730に対してm/e=730であった。
反応終了後、不溶物をセライトで濾別し、濾液を分液ロートに移し、ジクロロメタンにて数回抽出した。得られた有機層を無水硫酸マグネシウムで乾燥、ろ過、濃縮した。これをシリカゲルクロマトグラフィー(ヘキサン:ジクロロメタン=3:1~7:3)で精製し、白色の固体を得た。
収量は3.75g、収率は71%であった。
FD-MS分析の結果、分子量730に対してm/e=730であった。
[有機EL素子の製造及び評価]
実施例1
膜厚130nmのITO電極ライン付きガラス基板(ジオマティック社製)を、イソプロピルアルコール中で5分間、超音波洗浄した後、UVオゾン洗浄を30分間行なった。
洗浄後のITO電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まずITO電極ラインが形成されている側の面上に、ITO電極ラインを覆うようにして化合物(HI1)を厚さ20nmで、次いで化合物(HT1)を厚さ50nmで抵抗加熱蒸着し、順次薄膜を成膜した。成膜レートは1Å/sとした。これらの薄膜は、それぞれ正孔注入層及び正孔輸送層として機能する。
次に、正孔輸送層上に、化合物(149)を抵抗加熱蒸着して膜厚10nmの薄膜(第一有機薄膜層)を成膜した。
次に、第一有機薄膜層上に、化合物(H1)と化合物(BD1)を同時に抵抗加熱蒸着して膜厚40nmの薄膜(第二有機薄膜層)を成膜した。このとき、化合物(BD1)を、化合物(H1)と化合物(BD1)の総質量に対し質量比で20%になるように蒸着した。成膜レートはそれぞれ1.2Å/s、0.3Å/sとした。この薄膜は、燐光発光層として機能する。
次に、この燐光発光層上に、化合物(HB1)を抵抗加熱蒸着して膜厚5nmの薄膜を成膜した。成膜レートは1.2Å/sとした。この薄膜は障壁層として機能する。
次に、この障壁層上に、化合物(ET1)を抵抗加熱蒸着して膜厚25nmの薄膜を成膜した。成膜レートは1Å/sとした。この膜は電子注入層として機能する。
次に、この電子注入層上に膜厚1.0nmのLiFを成膜レート0.1Å/sで蒸着した。
次に、このLiF膜上に金属アルミニウムを成膜レート8.0Å/sにて蒸着し、膜厚80nmの金属陰極を形成して有機EL素子を製造した。
実施例1
膜厚130nmのITO電極ライン付きガラス基板(ジオマティック社製)を、イソプロピルアルコール中で5分間、超音波洗浄した後、UVオゾン洗浄を30分間行なった。
洗浄後のITO電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まずITO電極ラインが形成されている側の面上に、ITO電極ラインを覆うようにして化合物(HI1)を厚さ20nmで、次いで化合物(HT1)を厚さ50nmで抵抗加熱蒸着し、順次薄膜を成膜した。成膜レートは1Å/sとした。これらの薄膜は、それぞれ正孔注入層及び正孔輸送層として機能する。
次に、正孔輸送層上に、化合物(149)を抵抗加熱蒸着して膜厚10nmの薄膜(第一有機薄膜層)を成膜した。
次に、第一有機薄膜層上に、化合物(H1)と化合物(BD1)を同時に抵抗加熱蒸着して膜厚40nmの薄膜(第二有機薄膜層)を成膜した。このとき、化合物(BD1)を、化合物(H1)と化合物(BD1)の総質量に対し質量比で20%になるように蒸着した。成膜レートはそれぞれ1.2Å/s、0.3Å/sとした。この薄膜は、燐光発光層として機能する。
次に、この燐光発光層上に、化合物(HB1)を抵抗加熱蒸着して膜厚5nmの薄膜を成膜した。成膜レートは1.2Å/sとした。この薄膜は障壁層として機能する。
次に、この障壁層上に、化合物(ET1)を抵抗加熱蒸着して膜厚25nmの薄膜を成膜した。成膜レートは1Å/sとした。この膜は電子注入層として機能する。
次に、この電子注入層上に膜厚1.0nmのLiFを成膜レート0.1Å/sで蒸着した。
次に、このLiF膜上に金属アルミニウムを成膜レート8.0Å/sにて蒸着し、膜厚80nmの金属陰極を形成して有機EL素子を製造した。
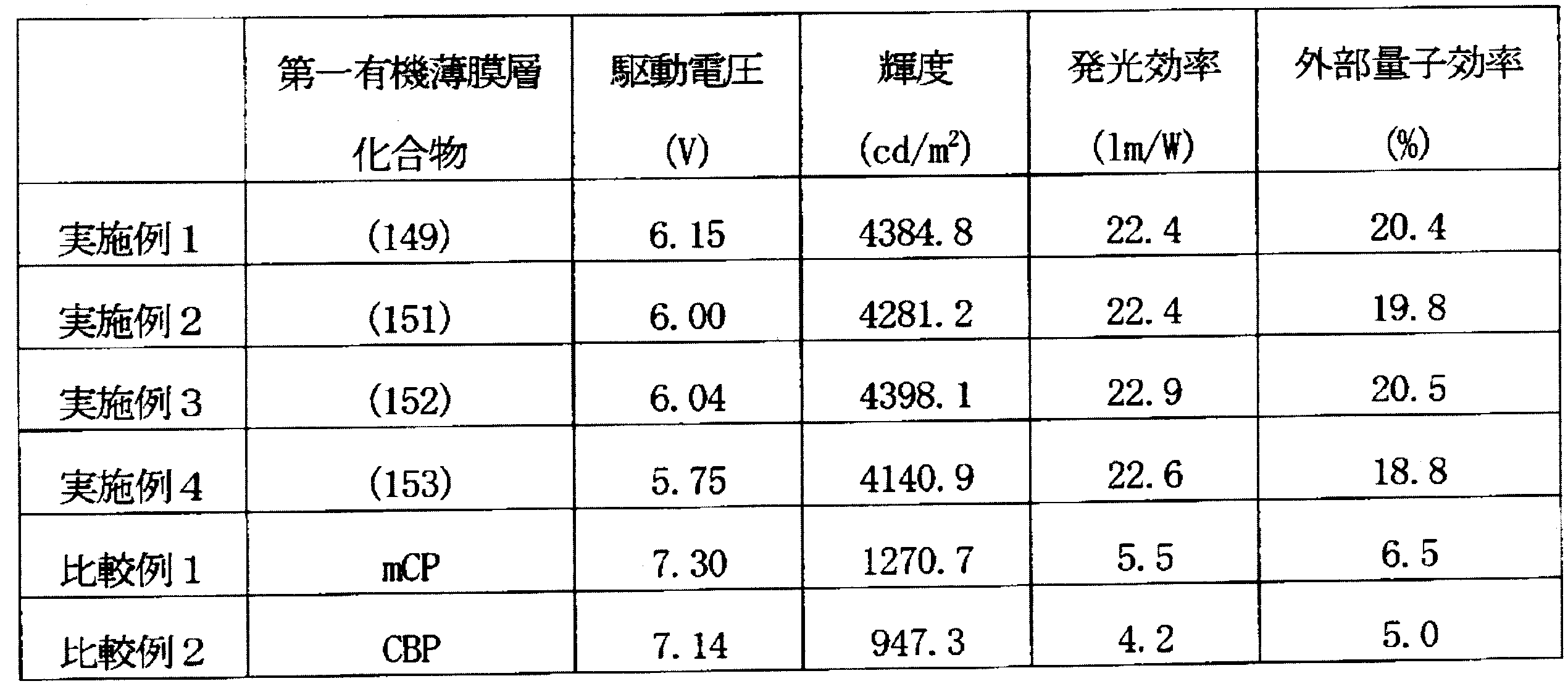
得られた有機EL素子の外部量子効率を以下の方法で評価した。結果を表1に示す。
また、第一有機薄膜層で使用した有機化合物の配向パラメータS及び三重項エネルギー(EgT)、並びに、発光材料の発光極大波長を以下の方法で評価した。結果を表2に示す。
(1)外部量子効率(%)
23℃、乾燥窒素ガス雰囲気下で、電流密度が10mA/cm2のときの外部量子効率(EQE)を輝度計(ミノルタ社製分光輝度放射計CS-1000)を用いて測定した。
また、第一有機薄膜層で使用した有機化合物の配向パラメータS及び三重項エネルギー(EgT)、並びに、発光材料の発光極大波長を以下の方法で評価した。結果を表2に示す。
(1)外部量子効率(%)
23℃、乾燥窒素ガス雰囲気下で、電流密度が10mA/cm2のときの外部量子効率(EQE)を輝度計(ミノルタ社製分光輝度放射計CS-1000)を用いて測定した。
(2)配向パラメータS
中性洗剤、純水、アセトン、イソプロピルアルコールで超音波洗浄後、イソプロピルアルコールによる沸騰洗浄したシリコン基板を真空蒸着装置に設置し、5×10-5Paになるまで、真空ポンプにて排気した。測定化合物を蒸着速度0.1nm/秒で100nm蒸着し、測定用の薄膜を形成した。作製した薄膜について、多入射角分光エリプソメータ(J.A.Woollam社製のM-2000D)を用い、入射角を5°毎に45°~80°の範囲、波長は200~1000nmの範囲でエリプソメトリパラメータを測定した。得られたデータをJ.A.Woollam社製の解析ソフトWVASE32で解析し、配向パラメータSを算出した。
中性洗剤、純水、アセトン、イソプロピルアルコールで超音波洗浄後、イソプロピルアルコールによる沸騰洗浄したシリコン基板を真空蒸着装置に設置し、5×10-5Paになるまで、真空ポンプにて排気した。測定化合物を蒸着速度0.1nm/秒で100nm蒸着し、測定用の薄膜を形成した。作製した薄膜について、多入射角分光エリプソメータ(J.A.Woollam社製のM-2000D)を用い、入射角を5°毎に45°~80°の範囲、波長は200~1000nmの範囲でエリプソメトリパラメータを測定した。得られたデータをJ.A.Woollam社製の解析ソフトWVASE32で解析し、配向パラメータSを算出した。
(3)三重項エネルギー(EgT)
市販の装置F-4500(日立社製)を用いて測定した。EgTの換算式は以下のとおりである。
換算式 EgT(eV)=1239.85/λph
「λph」(単位:nm)とは、縦軸に燐光強度、横軸に波長をとって、燐光スペクトルを表したときに、燐光スペクトルの短波長側の立ち上がりに対して接線を引き、その接線と横軸の交点の波長値を意味する。
各化合物を溶媒に溶解し(試料10μmol/リットル、EPA(ジエチルエーテル:イソペンタン:エタノール=5:5:5(容積比)、各溶媒は分光用グレード)、燐光測定用試料とした。石英セルへ入れた燐光測定用試料を77(K)に冷却し、励起光を燐光測定用試料に照射し、波長を変えながら燐光強度を測定した。燐光スペクトルは、縦軸を燐光強度、横軸を波長とした。
この燐光スペクトルの短波長側の立ち上がりに対して接線を引き、その接線と横軸との交点の波長値λph(nm)を求めた。
燐光スペクトルの短波長側の立ち上がりに対する接線は以下のように引く。燐光スペクトルの短波長側から、スペクトルの極大値のうち、最も短波長側の極大値までスペクトル曲線上を移動する際に、長波長側に向けて曲線上の各点における接線を考える。この接線は、曲線が立ち上がるにつれ(つまり縦軸が増加するにつれ)傾きが増加する。この傾きの値が極大値をとる点において引いた接線を、当該燐光スペクトルの短波長側の立ち上がりに対する接線とする。
尚、スペクトルの最大ピーク強度の10%以下のピーク強度をもつ極大点は、上述の最も短波長側の極大値には含めず、最も短波長側の極大値に最も近い、傾きの値が極大値をとる点において引いた接線を当該燐光スペクトルの短波長側の立ち上がりに対する接線とする。
市販の装置F-4500(日立社製)を用いて測定した。EgTの換算式は以下のとおりである。
換算式 EgT(eV)=1239.85/λph
「λph」(単位:nm)とは、縦軸に燐光強度、横軸に波長をとって、燐光スペクトルを表したときに、燐光スペクトルの短波長側の立ち上がりに対して接線を引き、その接線と横軸の交点の波長値を意味する。
各化合物を溶媒に溶解し(試料10μmol/リットル、EPA(ジエチルエーテル:イソペンタン:エタノール=5:5:5(容積比)、各溶媒は分光用グレード)、燐光測定用試料とした。石英セルへ入れた燐光測定用試料を77(K)に冷却し、励起光を燐光測定用試料に照射し、波長を変えながら燐光強度を測定した。燐光スペクトルは、縦軸を燐光強度、横軸を波長とした。
この燐光スペクトルの短波長側の立ち上がりに対して接線を引き、その接線と横軸との交点の波長値λph(nm)を求めた。
燐光スペクトルの短波長側の立ち上がりに対する接線は以下のように引く。燐光スペクトルの短波長側から、スペクトルの極大値のうち、最も短波長側の極大値までスペクトル曲線上を移動する際に、長波長側に向けて曲線上の各点における接線を考える。この接線は、曲線が立ち上がるにつれ(つまり縦軸が増加するにつれ)傾きが増加する。この傾きの値が極大値をとる点において引いた接線を、当該燐光スペクトルの短波長側の立ち上がりに対する接線とする。
尚、スペクトルの最大ピーク強度の10%以下のピーク強度をもつ極大点は、上述の最も短波長側の極大値には含めず、最も短波長側の極大値に最も近い、傾きの値が極大値をとる点において引いた接線を当該燐光スペクトルの短波長側の立ち上がりに対する接線とする。
(4)発光極大波長
測定化合物を、溶媒に溶解(試料5.0[μmol/リットル]、ジクロロメタン、溶媒は分光用グレード)し、発光スペクトル測定用試料とした。石英セルへ入れた発光スペクトル用試料に室温(300[K])で励起光:350nmを照射し、発光強度を測定した。
発光スペクトルは、縦軸を発光強度、横軸を波長とした。
発光スペクトルの測定には、(株)日立ハイテクノロジー製のF-4500形分光蛍光光度計を用い、蛍光モードにて測定をおこなった。
得られた発光スペクトルから発光強度が最大となる波長を発光極大波長と定義した。
発光材料である化合物BD1の発光極大波長は、471nmであった。
測定化合物を、溶媒に溶解(試料5.0[μmol/リットル]、ジクロロメタン、溶媒は分光用グレード)し、発光スペクトル測定用試料とした。石英セルへ入れた発光スペクトル用試料に室温(300[K])で励起光:350nmを照射し、発光強度を測定した。
発光スペクトルは、縦軸を発光強度、横軸を波長とした。
発光スペクトルの測定には、(株)日立ハイテクノロジー製のF-4500形分光蛍光光度計を用い、蛍光モードにて測定をおこなった。
得られた発光スペクトルから発光強度が最大となる波長を発光極大波長と定義した。
発光材料である化合物BD1の発光極大波長は、471nmであった。
実施例2~4、比較例1、2
第一有機薄膜層に表1に記載の化合物を使用した以外は、実施例1と同様にして有機EL素子を作製し、評価した。結果を表1に示す。また、各例で使用した化合物を以下に示す。
第一有機薄膜層に表1に記載の化合物を使用した以外は、実施例1と同様にして有機EL素子を作製し、評価した。結果を表1に示す。また、各例で使用した化合物を以下に示す。
図2に、実施例及び比較例で作製した有機EL素子の電流密度と発光効率(L/J)の関係を示す。尚、横軸の「1.E±XX」は「1×10±XX」を意味する。例えば、「1.E+01」は「1×101」である。
表1が示すように、実施例の本発明の化合物を発光層に用いた有機EL素子は、比較例の素子に比べて、輝度が高く、外部発光効率が改善していることが分かる。また、図2より、本発明の有機EL素子は、電流密度が高い領域においても、高い発光効率を維持していることが確認できる。
表1が示すように、実施例の本発明の化合物を発光層に用いた有機EL素子は、比較例の素子に比べて、輝度が高く、外部発光効率が改善していることが分かる。また、図2より、本発明の有機EL素子は、電流密度が高い領域においても、高い発光効率を維持していることが確認できる。
2.化合物の特性の測定方法は下記の通りである。
(1)三重項エネルギー(EgT)
実施例1において説明したとおりである。
(1)三重項エネルギー(EgT)
実施例1において説明したとおりである。
(2)イオン化ポテンシャル
真空蒸着法又は塗布法により、ITO基板上に測定化合物の薄膜を形成し、市販の装置大気中光電子分光装置AC-3(理研計器社製)を用いて測定した。
真空蒸着法又は塗布法により、ITO基板上に測定化合物の薄膜を形成し、市販の装置大気中光電子分光装置AC-3(理研計器社製)を用いて測定した。
3.有機EL素子の評価方法は下記の通りである。
(1)外部量子効率(%)
23℃、乾燥窒素ガス雰囲気下で、輝度1000cd/m2時の外部量子効率を輝度計(ミノルタ社製分光輝度放射計CS-1000)を用いて測定した。
(1)外部量子効率(%)
23℃、乾燥窒素ガス雰囲気下で、輝度1000cd/m2時の外部量子効率を輝度計(ミノルタ社製分光輝度放射計CS-1000)を用いて測定した。
(2)電圧(V)
23℃、乾燥窒素ガス雰囲気下で、KEITHLY 236 SOURCE MEASURE UNITを用いて、電気配線された素子に電圧を印加して発光させ、素子以外の配線抵抗にかかる電圧を差し引いて素子印加電圧を測定した。
電圧の印加・測定と同時に輝度計(ミノルタ社製分光輝度放射計CS-1000)を用いて輝度測定も行い、これらの測定結果から素子輝度が1000cd/m2時の電圧を読み取った。
23℃、乾燥窒素ガス雰囲気下で、KEITHLY 236 SOURCE MEASURE UNITを用いて、電気配線された素子に電圧を印加して発光させ、素子以外の配線抵抗にかかる電圧を差し引いて素子印加電圧を測定した。
電圧の印加・測定と同時に輝度計(ミノルタ社製分光輝度放射計CS-1000)を用いて輝度測定も行い、これらの測定結果から素子輝度が1000cd/m2時の電圧を読み取った。
実施例5
膜厚130nmのITO電極ライン付きガラス基板(ジオマティック社製)を、イソプロピルアルコール中で5分間、超音波洗浄した後、UVオゾン洗浄を30分間行なった。
洗浄後のITO電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まずITO電極ラインが形成されている側の面上に、ITO電極ラインを覆うようにして化合物(HI1)を厚さ20nmで、次いで化合物(HT1)を厚さ50nmで抵抗加熱蒸着し、順次薄膜を成膜した。成膜レートは1Å/sとした。これらの薄膜は、それぞれ正孔注入層及び正孔輸送層として機能する。
正孔注入・輸送層上に、化合物(1)を厚さ10nmで抵抗加熱蒸着し、順次薄膜を成膜した。この薄膜は、電子阻止層として機能する。
この電子阻止層上に、化合物(H1)と化合物(BD1)を同時に抵抗加熱蒸着して膜厚50nmの薄膜を成膜した。このとき、化合物(BD1)を、化合物(H1)と化合物(BD1)の総質量に対し質量比で20%になるように蒸着した。成膜レートはそれぞれ1.2Å/s、0.3Å/sとした。この薄膜は、燐光発光層として機能する。
膜厚130nmのITO電極ライン付きガラス基板(ジオマティック社製)を、イソプロピルアルコール中で5分間、超音波洗浄した後、UVオゾン洗浄を30分間行なった。
洗浄後のITO電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まずITO電極ラインが形成されている側の面上に、ITO電極ラインを覆うようにして化合物(HI1)を厚さ20nmで、次いで化合物(HT1)を厚さ50nmで抵抗加熱蒸着し、順次薄膜を成膜した。成膜レートは1Å/sとした。これらの薄膜は、それぞれ正孔注入層及び正孔輸送層として機能する。
正孔注入・輸送層上に、化合物(1)を厚さ10nmで抵抗加熱蒸着し、順次薄膜を成膜した。この薄膜は、電子阻止層として機能する。
この電子阻止層上に、化合物(H1)と化合物(BD1)を同時に抵抗加熱蒸着して膜厚50nmの薄膜を成膜した。このとき、化合物(BD1)を、化合物(H1)と化合物(BD1)の総質量に対し質量比で20%になるように蒸着した。成膜レートはそれぞれ1.2Å/s、0.3Å/sとした。この薄膜は、燐光発光層として機能する。
次に、燐光発光層上に、化合物(H1)を抵抗加熱蒸着して膜厚10nmの薄膜を成膜した。成膜レートは1Å/sとした。この薄膜は正孔阻止層として機能する。
この正孔阻止層上に、化合物(ET1)を抵抗加熱蒸着して膜厚10nmの薄膜を成膜した。成膜レートは1Å/sとした。この膜は電子注入層として機能する。
さらに、この電子注入層上に膜厚1.0nmのLiFを成膜レート0.1Å/sで蒸着した。
次に、このLiF膜上に金属アルミニウムを成膜レート8.0Å/sにて蒸着し、膜厚80nmの金属陰極を形成して有機EL素子を製造した。
この正孔阻止層上に、化合物(ET1)を抵抗加熱蒸着して膜厚10nmの薄膜を成膜した。成膜レートは1Å/sとした。この膜は電子注入層として機能する。
さらに、この電子注入層上に膜厚1.0nmのLiFを成膜レート0.1Å/sで蒸着した。
次に、このLiF膜上に金属アルミニウムを成膜レート8.0Å/sにて蒸着し、膜厚80nmの金属陰極を形成して有機EL素子を製造した。
実施例6~12及び比較例3,4
化合物(1)の代わりに表1に記載の化合物を電子阻止層材料として用いた以外は実施例5と同様にして有機EL素子を作製し、評価した。尚、比較例4では電子阻止層を作製しなかった以外は実施例5と同様にして有機EL素子を作製した。使用した化合物の三重項エネルギー及びイオン化ポテンシャルを表3に、素子の評価結果を表4に示す。
化合物(1)の代わりに表1に記載の化合物を電子阻止層材料として用いた以外は実施例5と同様にして有機EL素子を作製し、評価した。尚、比較例4では電子阻止層を作製しなかった以外は実施例5と同様にして有機EL素子を作製した。使用した化合物の三重項エネルギー及びイオン化ポテンシャルを表3に、素子の評価結果を表4に示す。
表4が示すように、本発明の化合物を電子阻止層に用いた実施例の有機EL素子は、比較例5の素子に比べて、発光効率が改善していることが分かる。
実施例13~24、比較例5
第一有機薄膜層に表5に記載の化合物を使用した以外は、実施例1と同様にして有機EL素子を作製し、評価した。結果を表5に示す。また、各例で使用した化合物を以下に示す。
第一有機薄膜層に表5に記載の化合物を使用した以外は、実施例1と同様にして有機EL素子を作製し、評価した。結果を表5に示す。また、各例で使用した化合物を以下に示す。
上記に本発明の実施形態及び/又は実施例を幾つか詳細に説明したが、当業者は、本発明の新規な教示及び効果から実質的に離れることなく、これら例示である実施形態及び/又は実施例に多くの変更を加えることが容易である。従って、これらの多くの変更は本発明の範囲に含まれる。
本願のパリ優先の基礎となる日本出願明細書の内容を全てここに援用する。
本願のパリ優先の基礎となる日本出願明細書の内容を全てここに援用する。
Claims (17)
- 陽極と陰極の間に、第一有機薄膜層と第二有機薄膜層を互いに隣接して含み、
前記第一有機薄膜層は、配向パラメータSが-0.2~-0.5である有機化合物を含み、
前記第二有機薄膜層は、発光極大波長が550nm未満の発光材料を含む、
有機エレクトロルミネッセンス素子。 - 前記有機化合物は、6環以上の縮合環構造を有する、請求項1に記載の有機エレクトロルミネッセンス素子。
- 前記6環以上の縮合環構造が下記式(1)で表される構造を含む請求項2に記載の有機エレクトロルミネッセンス素子。
環Bの構成元素であるX1及びX2の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。
環Dの構成元素であるX3及びX4の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。
環Fの構成元素であるX5及びX6の少なくとも一方は、窒素原子、酸素原子、硫黄原子及び電子状態がSp3の炭素原子から選択される原子である。) - 前記式(1)の環B、環D及び環Fがすべて5員環であり、かつ環A、環C及び環Eがすべて6員環である、請求項3に記載の有機エレクトロルミネッセンス素子。
- 前記6環以上の縮合環構造が、下記式(2)で表される構造である、請求項2~4のいずれかに記載の有機エレクトロルミネッセンス素子。
X1~X3は、それぞれ独立に、>NR1、>CR2R3、酸素原子又は硫黄原子であり、
Raは、水素原子、置換もしくは無置換の環形成炭素数6~18の芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の芳香族複素環基、置換もしくは無置換の炭素数1~12のアルキル基、シアノ基、又は炭素数1~12のハロアルキル基であり、Raが複数ある場合、Raはそれぞれ同一でも異なっていてもよく、
R1~R3は、それぞれ独立に、置換もしくは無置換の環形成炭素数6~18の芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の芳香族複素環基、又は置換もしくは無置換の炭素数1~12のアルキル基であり、R1~R3がそれぞれ複数ある場合、各R1、R2、及び各R3はそれぞれ同一でも異なっていてもよい。) - 前記有機化合物が、下記式(3)で表される化合物である、請求項1に記載の有機エレクトロルミネッセンス素子。
L1及びL2は、それぞれ独立に、単結合、置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基、又は置換もしくは無置換の環形成原子数3~30の芳香族複素環基であり、
G1~G4及びG13~G16は、それぞれ独立に、N、又は、>CRb1であり、
G5~G8の1つはG9~G12の1つと結合する単結合であり、他のG5~G8は、それぞれ独立に、N、又は、>CRb1であり、
G9~G12の1つはG5~G8の1つと結合する単結合であり、他のG9~G12は、それぞれ独立に、N、又は、>CRb1であり、
Rb1は、それぞれ独立に、水素原子、置換もしくは無置換の炭素数1~30のアルキル基、置換もしくは無置換の環形成炭素数3~30のシクロアルキル基、置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基、置換もしくは無置換の環形成原子数3~30の芳香族複素環基、-Si(Rc)3、又は-ORcである。
Rcは、水素原子、置換もしくは無置換の炭素数1~30のアルキル基、又は置換もしくは無置換の環形成炭素数6~30の芳香族炭化水素環基である。
複数のCRb1が存在する場合、複数のRb1は、それぞれ同一又は異なっていてもよい。
複数のNRb1が存在する場合、複数のRb1は、それぞれ同一又は異なっていてもよい。
複数のRcが存在する場合、複数のRcは、それぞれ同一又は異なっていてもよい。) - 前記式(2)の構造を有する有機化合物が、前記式(2)において、
Y1~Y12は、それぞれ独立に、N、又は、>CRaであり、
X1~X3は、それぞれ独立に、>NR1、>CR2R3、酸素原子又は硫黄原子であり、
Raは、水素原子、置換もしくは無置換の環形成炭素数6~18の非縮合芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の複素環基、置換もしくは無置換の炭素数1~12のアルキル基、シアノ基、又は炭素数1~12のハロアルキル基であり、Raが複数ある場合、Raはそれぞれ同一でも異なっていてもよく、
R1~R3は、それぞれ独立に、置換もしくは無置換の環形成炭素数6~18の非縮合芳香族炭化水素基、置換もしくは無置換の環形成原子数5~14の複素環基、又は置換もしくは無置換の炭素数1~12のアルキル基であり、R1~R3がそれぞれ複数ある場合、各R1、R2、及び各R3はそれぞれ同一でも異なっていてもよい、
有機化合物である、請求項8に記載の有機エレクトロルミネッセンス素子。 - 前記式(2)のX1及びX3がそれぞれ独立に>NR1であり、
X2が酸素原子又は硫黄原子である、請求項5、8又は9のいずれかに記載の有機エレクトロルミネッセンス素子。 - 前記発光材料が燐光発光性材料である、請求項1~10のいずれかに記載の有機エレクトロルミネッセンス素子。
- 前記燐光発光性材料がIr,Pt、Os、Cu及びAuのいずれかの原子を含む錯体である請求項11に記載の有機エレクトロルミネッセンス素子。
- 前記発光材料が蛍光発光性材料を含む、請求項1~12のいずれかに記載の有機エレクトロルミネッセンス素子。
- 前記発光材料の発光極大波長が480nm未満である、請求項1~13のいずれかに記載の有機エレクトロルミネッセンス素子。
- 前記有機化合物の三重項エネルギーが2.8eV以上である、請求項1~14のいずれかに記載の有機エレクトロルミネッセンス素子。
- 前記陽極、前記第一有機薄膜層、前記第二有機薄膜層及び前記陰極を、この順に積層して含む、請求項1~15のいずれかに記載の有機エレクトロルミネッセンス素子。
- 請求項1~16のいずれかに記載の有機エレクトロルミネッセンス素子を搭載した電子機器。
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012-225916 | 2012-10-11 | ||
| JP2012225916 | 2012-10-11 | ||
| JP2013004809 | 2013-01-15 | ||
| JP2013-004809 | 2013-01-15 | ||
| JP2013-145382 | 2013-07-11 | ||
| JP2013145382 | 2013-07-11 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014057685A1 true WO2014057685A1 (ja) | 2014-04-17 |
Family
ID=50477167
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2013/006063 Ceased WO2014057685A1 (ja) | 2012-10-11 | 2013-10-10 | 有機エレクトロルミネッセンス素子 |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2014057685A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014148047A1 (ja) * | 2013-03-22 | 2014-09-25 | 出光興産株式会社 | ヘテロ縮合環を有するアミン化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP3258512A4 (en) * | 2015-02-09 | 2018-01-17 | Fujifilm Corporation | Organic semiconductor element and method for manufacturing same, composition for forming organic semiconductor film, and method for manufacturing organic semiconductor film |
| US10249826B2 (en) * | 2014-04-16 | 2019-04-02 | Idemitsu Kosan Co., Ltd. | Compound, organic electroluminescent element and electronic device |
| KR20200122854A (ko) * | 2019-04-19 | 2020-10-28 | (주)알로스 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2022264857A1 (ja) * | 2021-06-15 | 2022-12-22 | 株式会社Kyulux | 有機発光素子およびその製造方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007039406A (ja) * | 2005-08-05 | 2007-02-15 | Idemitsu Kosan Co Ltd | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2009148015A1 (ja) * | 2008-06-05 | 2009-12-10 | 出光興産株式会社 | ハロゲン化合物、多環系化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2011198900A (ja) * | 2010-03-18 | 2011-10-06 | Nippon Steel Chem Co Ltd | 有機電界発光素子 |
| WO2012089294A1 (de) * | 2010-12-28 | 2012-07-05 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012108389A1 (ja) * | 2011-02-07 | 2012-08-16 | 出光興産株式会社 | ビスカルバゾール誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2012128298A1 (ja) * | 2011-03-24 | 2012-09-27 | 出光興産株式会社 | ビスカルバゾール誘導体およびこれを用いた有機エレクトロルミネッセンス素子 |
-
2013
- 2013-10-10 WO PCT/JP2013/006063 patent/WO2014057685A1/ja not_active Ceased
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007039406A (ja) * | 2005-08-05 | 2007-02-15 | Idemitsu Kosan Co Ltd | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2009148015A1 (ja) * | 2008-06-05 | 2009-12-10 | 出光興産株式会社 | ハロゲン化合物、多環系化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2011198900A (ja) * | 2010-03-18 | 2011-10-06 | Nippon Steel Chem Co Ltd | 有機電界発光素子 |
| WO2012089294A1 (de) * | 2010-12-28 | 2012-07-05 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012108389A1 (ja) * | 2011-02-07 | 2012-08-16 | 出光興産株式会社 | ビスカルバゾール誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2012128298A1 (ja) * | 2011-03-24 | 2012-09-27 | 出光興産株式会社 | ビスカルバゾール誘導体およびこれを用いた有機エレクトロルミネッセンス素子 |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014148047A1 (ja) * | 2013-03-22 | 2014-09-25 | 出光興産株式会社 | ヘテロ縮合環を有するアミン化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| US9842996B2 (en) | 2013-03-22 | 2017-12-12 | Idemitsu Kosan Co., Ltd. | Amine compound having hetero-fused ring and organic electroluminescent element using amine compound |
| US10249826B2 (en) * | 2014-04-16 | 2019-04-02 | Idemitsu Kosan Co., Ltd. | Compound, organic electroluminescent element and electronic device |
| EP3258512A4 (en) * | 2015-02-09 | 2018-01-17 | Fujifilm Corporation | Organic semiconductor element and method for manufacturing same, composition for forming organic semiconductor film, and method for manufacturing organic semiconductor film |
| US10651400B2 (en) | 2015-02-09 | 2020-05-12 | Fujifilm Corporation | Organic semiconductor element, manufacturing method thereof, composition for forming organic semiconductor film, and method of manufacturing organic semiconductor film |
| KR20200122854A (ko) * | 2019-04-19 | 2020-10-28 | (주)알로스 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102173478B1 (ko) | 2019-04-19 | 2020-11-03 | (주)알로스 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2022264857A1 (ja) * | 2021-06-15 | 2022-12-22 | 株式会社Kyulux | 有機発光素子およびその製造方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7226718B2 (ja) | 有機発光素子、組成物および膜 | |
| CN110233206B (zh) | 有机电致发光元件、以及电子设备 | |
| JP6088995B2 (ja) | 有機エレクトロルミネッセンス素子および電子機器 | |
| CN108026106B (zh) | 用于有机电致发光元件的化合物、有机电致发光元件和电子设备 | |
| JP6196554B2 (ja) | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 | |
| WO2018186404A1 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| EP3422431B1 (en) | Organic electroluminescent element and electronic device | |
| JP6378106B2 (ja) | 化合物、有機エレクトロルミネッセンス素子および電子機器 | |
| CN104718210B (zh) | 梯形化合物以及使用其的有机电致发光元件 | |
| JP6374329B2 (ja) | 有機エレクトロルミネッセンス素子、有機エレクトロルミネッセンス素子用材料、および電子機器 | |
| JP7109409B2 (ja) | 有機金属化合物とそれを含む有機発光素子及び診断用組成物 | |
| KR20190132646A (ko) | 유기 전기발광 소자 및 전자 기기 | |
| KR20140056215A (ko) | 질소 함유 방향족 복소환 유도체 및 그것을 이용한 유기 전기발광 소자 | |
| KR102856013B1 (ko) | 유기 일렉트로루미네센스 소자 및 전자 기기 | |
| TW201343639A (zh) | 有機電激發光元件用材料及使用其之元件 | |
| JP2025061694A (ja) | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子及び電子機器 | |
| KR20200132969A (ko) | 유기 일렉트로루미네센스 소자 및 전자 기기 | |
| WO2018123924A1 (ja) | 組成物、有機エレクトロルミネッセンス素子用材料、組成物膜、有機エレクトロルミネッセンス素子、及び電子機器 | |
| JP2013108015A (ja) | 有機エレクトロルミネッセンス素子用材料 | |
| JP2014094935A (ja) | 化合物、及びそれを用いた有機エレクトロルミネッセンス素子 | |
| WO2020085446A1 (ja) | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、および電子機器 | |
| JP6145158B2 (ja) | ヘテロ縮合環を有するアミン化合物及びそれを用いた有機エレクトロルミネッセンス素子 | |
| WO2014057685A1 (ja) | 有機エレクトロルミネッセンス素子 | |
| JP2020174072A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2015078169A (ja) | 新規な化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13845542 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 13845542 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: JP |