WO2003043983A1 - Piperazine derivatives destabilising androgen receptors - Google Patents
Piperazine derivatives destabilising androgen receptors Download PDFInfo
- Publication number
- WO2003043983A1 WO2003043983A1 PCT/EP2002/012182 EP0212182W WO03043983A1 WO 2003043983 A1 WO2003043983 A1 WO 2003043983A1 EP 0212182 W EP0212182 W EP 0212182W WO 03043983 A1 WO03043983 A1 WO 03043983A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- trifluoromethyl
- piperazin
- dihydro
- methyl
- benzonitrile
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 BC(C)(C(*)C=C1)C=C1N Chemical compound BC(C)(C(*)C=C1)C=C1N 0.000 description 7
- KHOCBASWEGDFNI-HWKANZROSA-N CC(C)(C#N)NC/C=C/O Chemical compound CC(C)(C#N)NC/C=C/O KHOCBASWEGDFNI-HWKANZROSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/44—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having three double bonds between ring members or between ring members and non-ring members
- C07D207/444—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having three double bonds between ring members or between ring members and non-ring members having two doubly-bound oxygen atoms directly attached in positions 2 and 5
- C07D207/448—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having three double bonds between ring members or between ring members and non-ring members having two doubly-bound oxygen atoms directly attached in positions 2 and 5 with only hydrogen atoms or radicals containing only hydrogen and carbon atoms directly attached to other ring carbon atoms, e.g. maleimide
- C07D207/452—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having three double bonds between ring members or between ring members and non-ring members having two doubly-bound oxygen atoms directly attached in positions 2 and 5 with only hydrogen atoms or radicals containing only hydrogen and carbon atoms directly attached to other ring carbon atoms, e.g. maleimide with hydrocarbon radicals, substituted by hetero atoms, directly attached to the ring nitrogen atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/66—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D233/86—Oxygen and sulfur atoms, e.g. thiohydantoin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
Definitions
- the present invention relates to substituted piperazine derivatives which destabilize the androgen receptor (AR), and to processes for preparing these piperazine derivatives, their intermediates and pharmaceutical preparations containing the piperazine derivatives according to the invention and their use for the production of medicaments.
- AR androgen receptor
- prostate cancer is the second leading cause of cancer death in men after lung carcinoma.
- men over the age of 55 4% of deaths are due to prostate cancer and it is estimated that the proportion increases to 80% of deaths in men over 80 years of age. While the mortality rate is still relatively low, it is increasing by about 14% annually.
- the number of men diagnosed with a prostate tumor has risen by 30% in recent years, but this is due less to an increasing number of new cases, but rather to the fact that the general population is getting older, that the diagnostic procedures are improving and that systematic screening programs have been introduced (EJ Small, DM Reese, Curr. Op. Oncol. 2000, 12, 265-272).
- the prostate tumor grows androgen-dependent in early stages. As long as the tumor is localized to the prostate, it can be surgically removed or treated by radiation therapy, with associated risks. In cases where the tumor is no longer localized and has already metastasized, the tumor is palliatively treated by reducing testosterone levels in the blood. This is done either surgically by castration or medication by treatment with antiandrogens (bicalutamide, cyproterone acetate, flutamide), LHRH agonists (buserelin, Zoladex), LHRH antagonists (cetrorelix) or 5 ⁇ reductase inhibitors (finasteride). Since surgical castration does not affect adrenal androgen synthesis, combined surgical and drug treatment is frequently used.
- the androgen receptor plays an important role in the development and growth of the prostate tumor not only in the early hormone-dependent, but also in late hormone-independent stages of tumor progression.
- the androgen receptor belongs to the family of steroid hormone receptors, which act as transcription factors.
- the androgen receptor binds androgens, stabilizing it and protecting it from rapid proteolytic degradation. After hormone binding, it is transported to the nucleus, where it activates certain genes by binding to so-called androgen-responsive DNA elements located in promoter regions (D.J. Lamb et al., Vitam. Horm., 2001, 62, 199-230).
- Mutant receptors may either have a higher affinity for androgens, become constitutively active, alter their ligand specificity, so as to be activated by other steroid hormones or even antiandrogens, be activated via interactions with molecules from other growth promoting signal transduction pathways, alter the interaction with cofactors, or activate the target genes (JP Elo, T. Visakorpi, Ann. Med. 2001, 33, 130-41).
- Nonsteroidal antiandrogens are described in US Pat. No. 5,411,981 (phenylimidazolidine derivatives), WO97 / 00071 (specifically substituted phenyldimethylhydantoins and their imino or thione derivatives) in WO00 / 37430 (phenylalanines, phenylhydantoins and phenylureas), WO01 / 58855 (aminopropanilides) and EP1122242 (substituted Cyanphenylpiperazine) described.
- the object of the present invention is to provide compounds with antiandrogenic action which destabilize the androgen receptor, inhibit prostate tumor growth, and at the same time have a high, possibly oral bioavailability.
- nonsteroidal antiandrogens have advantages over the steroidal compounds and are therefore to be preferred. Thus, a more selective action can be achieved with non-steroidal compounds with less adverse side effects.
- the known nonsteroids lack bicalutamide and flutamide, e.g. the progestagenic activity and, in addition, their use leads to an increase in serum testosterone levels, which could clinically lead to maintenance of potency.
- the present invention relates to compounds of general formula I, wherein
- V is a substituted aromatic radical of the general formula II
- A is an acetyl group, an acetylamino group, a cyano group, a nitro group, a trifluoromethyl group or a halogen (fluorine, chlorine),
- B is a hydrogen atom, a halogen (fluorine, chlorine) or a trifluoromethyl group, or
- a and B together represent a cyclic group of the formula III or IV attached to the aromatic ring, where E is a methylene group or an oxygen atom,
- w is a heterocycle of the formula V
- T can represent carbon or nitrogen
- T when T is nitrogen, there should be a single bond between Q. and T and Q is a group -C (CH 3 ) 2 - and U is sulfur and n is one of the integer values 2, 3, 4, 5, 6, 7, 8 accept, i and j are independently of one another the values 1 and 2, where i + j can assume the values 2 or 3,
- R and R ' may independently be a hydrogen atom or a methyl group
- Y is a bond between the heterocyclic nitrogen and Z, for a
- Z and Z 'independently of one another are an unbranched C 1 -C 5 -alkyl group or branched C 3 -C 8 -alkyl group, a C 3 -C 6 -cycloalkyl group optionally substituted by a phenyl radical, a (C 3 -C 6 -cycloalkyl) -C 1 -C 4 -alkylene group, a branched or unbranched C 2 -C 5 -alkenyl group, a branched or unbranched C 2 -C 5 -alkenyl group, a C 3 -C 5 -alkynyl group, a C 1 -C -alkoxy group , Cyano, phenylsulfanyl or hydroxy-d
- C 1 -C 2 alkylene group a (2-methoxyethoxy) methyl group, a [2- (2-methoxyethoxy) ethoxy] methyl group, a 2- (2-methoxyethoxy) ethyl group, a 2- [2- (2-methoxyethoxy) ethoxy] ethyl group, a C 1 -C 4 -alkoxy-C 1 -C 4 -alkylene group, a C 1 -C 4 -alkoxyalkoxycarbonyl group, an adamantyl group, a trichloroacetyl group, an unsubstituted or with up to three branched or unbranched C 1 -C 4 -alkyl, C 2 - C 6 alkenyl, C 3 -C 6 - cycloalkyl, C 3 -C 6 cycloalkyloxy, phenyl, cyano, halogen, methoxy, ethoxy
- the compounds of the invention are characterized in that they each contain a Diazacycloalkankern whose nitrogen atoms are each substituted.
- unbranched -C-C 8 alkyl groups for the radicals Z and __ 'and may for example be a methyl, ethyl, n-propyl, n-butyl, n-pentyl, n-hexyl, n Heptyl, n-octyl; in the branched C 3 -C 8 alkyl groups to a ' so-propyl, iso-butyl, sec-butyl, ferf-butyl, / so-pentyl, neo-pentyl, 2-methylpentyl, 2 , 2-dimethylbutyl, 2,3-dimethylbutyl, 2-methylhexyl, 2,2-dimethylpentyl, 2,2,3-trimethylbutyl, 2,3,3-trimethylbutyl.
- the optionally substituted with a phenyl radical C 3 -C 6 -cycloalkyl groups for the radicals Z and Z may be consistently to a cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, or phenylcyclopropyl, Phenylcyclobutyl-, Phenylcyclo- pentyl, phenylcyclohexyl group act.
- the (C 3 -C 6 -cycloalkyl) -CC-C-alkylene groups for the radicals Z and 11 may be, for example, a cyclopropylmethyl, cyclobutylmethyl, cyclopentylmethyl, cyclohexylmethyl, cyclopropylethyl, cyclobutylethyl, cyclopentylethyl, cyclohexyl - ethyl, cyclopropylpropyl, cyclobutylpropyl, cyclopentylpropyl, cyclohexylpropyl, cyclopropylbutyl, cyclobutylbutyl, cyclopentylbutyl or cyclohexylbutyl act.
- the branched or unbranched C 2 -C 5 -alkenyl groups for the radicals Z and Z ' may, for example, be a vinyl, allyl, homoallyl, ( ⁇ ) -but-2-enyl, (Z) -butyne -2-enyl, (E) -but-1-enyl, (Z) -but-1-enyl, pent-4-enyl, (E) -pent-3-enyl, (Z) - Pent-3-enyl, (E) -pent-2-enyl, (Z) -pent-2-enyl, ()) -pent-1-enyl, (Z) -pent-1-enyl, , 2-methylvinyl, 3-methylbut-3-enyl, 2-methylbut-3-enyl, (2'-methylbut-2-enyl, (Z) -2-methylbut-2-enyl-, 3-methylbut-2-enyl group act.
- the C 3 -C 5 -alkynyl groups for the radicals Z and Z ' may be, for example, a prop-1-ynyl, prop-2-ynyl, but-1-ynyl, but-2-ynyl, But-3-ynyl, pent-1-ynyl, pent-2-ynyl, pent-3-ynyl, pent-4-ynyl, 1-methylprop-2-ynyl, 1-methylbut-3 inyl, 1-ethylprop-2-inyl group.
- the C 1 -C 4 -alkoxy groups for the radicals Z and Z ' may be, for example, a methoxy, ethoxy, n-propoxy, / so-propoxy, n-butoxy, sec-butoxy-, / ' so-butoxy, ferf-butoxy act.
- the C 1 -C 4 -alkylene groups within the radicals Z and Z ' may be, for example, a methylene (-CH 2 -), ethylidene [-CH (CH 3 ) -], ethylene (-CH 2 CH 2 -) ), 1,3-propylene- (-CH 2 CH 2 CH 2 -), 1, 2-propylene- [-CH 2 CH (CH 3 ) -], 1, 4-butylene-, (-CH 2 CH 2 CH 2 CH 2 -), 1, 3-butylene- [-CH 2 CH 2 CH (CH 3 ) -], 1,2-butylene- [-CH 2 CH (CH 2 CH 3 ) -], 2-methyl -1, 2-propylene- [-CH 2 C (CH 3 ) 2 -], 2-methyl-1,3-propylene group [-CH 2 CH (CH 3 ) CH 2 -].
- the hydroxy-dC 4 -alkylene groups for the radicals Z and Z ' may be a hydroxymethyl (HOCH 2 -), 2-hydroxyethyl- (HOCH 2 CH 2 -), 1-hydroxyethyl- [CH 3 CH (OH ) -], 3-hydroxypropyl (HOCH 2 CH 2 CH 2 -), 2-hydroxypropyl
- the C 1 -C 4 -alkoxycarbonyl-dC-alkylene groups for the radicals Z and Z ' are, for example, a combination of the C 1 -C 4 -alkoxycarbonyl and the C 1 -C 4 -alkylene functions.
- a C 1 -C 4 -alkoxycarbonyl group includes methoxycarbonyl- [MeOC (O) -], ethoxycarbonyl [EtOC (O) -), n-propoxycarbonyl- [CH 3 CH 2 CH 2 OC (O) -], isopropoxycarbonyl- [(CH 3 ) 2 CHOC (O) -], n-butoxycarbonyl- [CH 3 CH 2 CH 2 CH 2 OC (O) -], isobutoxycarbonyl- [(CH 3 ) 2 CHCH 2 OC (O) - ], sec-butoxycarbonyl- [CH 3 CH 2 (CH 3 ) CHOC (O) -], ferf -butoxycarbonyl [(CH 3 ) 3 COC (O) -].
- a C 1 -C 4 -alkylene group is understood to mean the C 1 -C 4 -alkylene groups mentioned above.
- C 4 alkylene groups give the following radicals: (methoxycarbonyl) methyl- [CH 3 OC (O) CH 2 -] (Ethoxycarbonyl) methyl- [CH 3 CH 2 OC (O) CH 2 -], (ry-propoxycarbonyl) methyl- [CH 3 CH 2 CH 2 OC (O) CH 2 -], (/ ' so-propoxycarbonyl) methyl - [(CH 3 ) 2 CHOC (O) CH 2 -], (n-butoxycarbonyl) methyl- [CH 3 CH 2 CH 2 CH 2 OC (O) CH 2 -], (/ so-butoxycarbonyl) methyl- [ (CH 3 ) 2 CHCH 2 OC (O) CH 2 -], (sec-butoxycarbonyl) methyl- [CH 3 CH 2 (CH 3 ) CH
- the aryl groups for radicals Z and 11 may be a phenyl, naphthalene-1-yl, naphthalen-2-yl, [1, 1'-biphenyl] -2-yl-, [1, 1 ' Biphenyl] -3-yl or a [1, 1'-biphenyl] -4-yl group.
- heteroaryl groups for the radicals Z and Z ' can be a pyridinyl, pyrimidinyl, quinolinyl, isoquinolinyl, benzofuranyl, benzothienyl, 1,3-benzodioxolyl, 2.1 linked via one of the substitutable sites, 3-benzothiadiazolyl, indolyl,
- the heterocyclyl groups for the radicals Z and 11 may be a piperidinyl, morpholinyl, thiomorpholinyl, piperazinyl, tetrahydrofuranyl, tetrahydrothienyl, imidazolidinyl or pyrrolidinyl group linked via one of the substitutable sites.
- aryl, heteroaryl, heterocyclyl also in each case within the aryl-dC 4 -alkylene, heteroaryl-C 4 -alkylene, aryloxy-Ci-d-alkylene, heteroaryl-oxy-C-C alkyl, aryl-C 1 -C 4 -alkyleneoxy-d-alkylene units for the radical Z may be, inter alia, unbranched or branched C 1 -C 4 -alkyl groups (methyl, ethyl, n-propyl, iso-propyl, n-butyl); Butyl, sec-butyl, so-butyl and te-butyl) and / or C 2 -C 6 -alkenyl groups (vinyl, allyl, homoallyl, (E) -but-2-enyl-, ( Z) but-2-enyl, pent-4-enyl, (E) -pent-3-
- Halogen fluorine, chlorine, bromine, iodine
- the aryl-C ⁇ d-alkylene groups for the radicals Z and Z ' may be a combination of the previously defined aryl and C 1 -C 4 -alkyl groups, for example: a phenylmethyl, 1-phenylethyl, 2-phenylethyl -, 1-methyl-1-phenylethyl, 3-phenylpropyl-4-phenylbutyl, (naphthalen-1-yl) methyl, 1- (naphthalen-1-yl) ethyl, 2- (naphthalen-1-yl ) - ethyl, (naphthalen-2-yl) methyl, 1- (naphthalen-2-yl) ethyl, 2- (naphthalen-2-yl) ethyl, ([1,1'-biphenyl] -2 -yl) methyl, ([1,1'-biphenyl] -3-yl) methyl or a ([1,1'-
- the heteroaryl-C 1 -C 4 -alkylene groups for the radicals Z and 11 may be a combination of the previously defined heteroaryl and C 1 -C 4 -alkylene groups, for example a (pyridin-2-yl) methyl- , (Pyridin-3-yl) methyl, (pyridin-4-yl) methyl, (furan-2-yl) methyl, (furan-3-yl) methyl, (thien-2-yl) methyl , (Thien-3-yl) methyl, 2- (thien-2-yl) ethyl or a 2- (thien-3-yl) ethyl group.
- the aryloxy-dC-alkylene groups for the radicals Z and Z ' may be a combined linkage of the previously defined aryl and C 1 -C 4 -alkylene groups via an ether function (-O-), for example: a phenoxymethyl-, 1-phenoxyethyl, 2-phenoxyethyl, 1-methyl-1-phenoxyethyl, 3-phenoxypropyl, 4-phenoxybutyl, [(naphthalen-1-yl) oxy] methyl, 1 - [(naphthalene-1 yl) oxy] ethyl, 2 - [(naphthalen-1-yl) oxy] ethyl, [(naphthalen-2-yl) oxy] methyl, 1 - [(naphthalen-2-yl) oxy] ethyl , 2 - [(naphthalen-2-yl) -oxyethyl, [([1, 1'-biphenyl] -2-
- the heteroaryloxy-dC 4 -alkylene groups for the radicals Z and Z ' may be a combined linkage of the previously defined heteroaryl and dC 4 -alkylene groups via an ether function (-O-), for example: a [( Pyridin-2-yl) oxy] methyl, [(pyridin-3-yl) oxy] methyl or a [(pyridin-4-yl) oxy] methyl group.
- the aryl-C 1 -C -alkyleneoxy-C 1 -C 4 -alkylene groups for the radicals Z and 11 may be a sequentially combined linkage of the previously defined aryl and C 1 -C 4 -alkylene groups via an ether function (-O-) to the alkylene group, for example: a (phenylmethoxy) methyl or a 2- (phenylmethoxy) ethyl group.
- Preferred according to the present invention are those compounds of general formula I. in which:
- B is a trifluoromethyl group
- R and R ' represent a hydrogen atom, Y for a carbonyl group -C (O) -, for a sulfonyl group -S (O) 2 -, for a
- Iminocarbonyl group -C (O) N (Z ') - for an iminosulfonyl group -S (O) 2 N (Z') -, for an imino (thioxomethyl) group -C (S) N (Z ') -, for a Oxycarbonylimino (thioxomethyl) group -C (S) N (Z ') C (O) O-, for an oxycarbonyl group -C (O) O-, for a sulfanylcarbonyl group ⁇ C (O) S-, and
- Z and II independently of one another represent an unbranched C 1 -C 4 -alkyl group or branched C 3 -C -alkyl group, an optionally substituted C 3 -C 6 -cycloalkyl group substituted by a phenyl radical, or a (C 3 -C 6 -cycloalkyl) -d -
- C alkylene group a branched or unbranched C 2 -C 3 alkenyl group a dC 4 alkoxy, cyano, phenylsulfanyl or hydroxy-dd-alkylene group, a (2-methoxyethoxy) methyl group, a [2- (2 -Methoxyethoxy) - ethoxymethyl, a 2- (2-methoxyethoxy) ethyl group, a 2- [2- (2-methoxyethoxy) ethoxy] ethyl group, a -C-C 4 alkoxy-dC 4 -alkylene, a dC alkoxycarbonyl -C C 4 alkylene group, an unsubstituted or with up to three branched or unbranched dC alkyl, C 2 -C alkenyl, C 3 -C 6 cycloalkyl, C 3 -C 6 cycloalkyloxy, phenyl, Cyan
- Z ' is, in addition to the abovementioned definitions, a hydrogen atom.
- inorganic acids inter alia hydrochloric, hydrobromic, sulfuric and phosphoric acid, nitric acid, as carboxylic acids, inter alia, acetic acid, propionic acid, hexanoic acid , Octanoic, decanoic, oleic, stearic, maleic, fumaric, succinic, benzoic, ascorbic, oxalic, salicylic, tartaric, citric, lactic, glycolic, malic, mandelic, cinnamic, glutamic, aspartic, sulfonic acids, including methanesulfonic, ethanesulfonic Benzenesulfonic acid and naphthalenesulfonic into consideration.
- the compounds of the invention were tested in various models.
- the compounds of general formula I according to the invention are distinguished by the fact that they are antiandrogenic compounds which destabilize the androgen receptor, inhibit prostate tumor growth, and at the same time have a high, possibly oral bioavailability.
- the in vitro tests for the influences on the activity of the androgen receptor were carried out as follows:
- CPA cyproterone acetate, 17- (acetyloxy) -6-chloro-1 ⁇ , 2 ⁇ -dihydro-3'H-cyclopropa [1, 2] pregna-1, 4,6-triene-3,20-dione
- Model 1 DeStabilization of AR in LNCaP cells by test substances
- the cells are washed with PBS, detached with PBS / 20 mM EDTA, washed again with PBS-Ca 2+ / Mg 2+ and then frozen for at least 2 hours as cell pellet at -80 ° C. Thereafter, the cell pellet is dissolved in 200 ⁇ l of lysis buffer (50 mM Tris / HCl pH 7.5, 150 mM NaCl, 1.5 mM MgCl 2 , 0.2% SDS, 10% glycerol, 1 mM DTT, 0.01 ⁇ Complete).
- EDTA protease inhibitors (Roche, Mannheim)) and treated with 10 U benzonase (Merck, Darmstadt) for 10 minutes at 4 ° C.
- insoluble material is pelleted and 25 ⁇ g of the cell extract are separated in a 4-12% SDS-polyacrylamide gel (Invitrogen). Subsequently, the proteins are transferred to nitrocellulose (HyBondECL, Amersham) and incubated with monoclonal antibodies to the androgen receptor (AR441, Santa Cruz Biotechnologies, 1: 400 dilution) and actin (ICN, 1: 5000-1: 20000 dilution).
- monoclonal antibodies to the androgen receptor AR441, Santa Cruz Biotechnologies, 1: 400 dilution
- actin ICN, 1: 5000-1: 20000 dilution
- Table 1 shows the effect of selected test substances at concentrations of 10 and 1 ⁇ M on the content of androgen receptor protein in the human prostate cell line LNCaP.
- Treatment of the cells with the test substances listed results in a reduction in the AR content to a fifth of the control at a treatment concentration of 10 ⁇ M (22% in Example 248: 4- [2,5-dihydro-3- [6- [4 - (2-methoxybenzoyl) piperazin-1-yl] hexyl] -4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile).
- the comparative substance bicalutamide does not affect the AR content, while the synthetic androgen R1881 stabilizes the AR protein.
- the latter is known from the literature (J.A. Kemppainen et al, J. Biol. Chem. 1992, 267, 968-974).
- Example 248 4- [2,5-Dihydro-3- [6- [4- (2-methoxybenzoyl) piperazin-1-yl] hexyl] -4-methyl-2,5-dioxo-1H-pyrrole-1 yl] -2- (trifluoromethyl) benzonitrile and
- Example 629 4- [3- [5- [4- (ethylsulfonyl) piperazin-1-yl] pentyl] -4,4-dimethyl-5-oxo-2- thioxoimidazolidin-1-yl] -2- (trifluoromethyl) benzonitrile reduce the AR content even at a concentration of 1 ⁇ M to a value up to half of the control. By lowering the AR content, which probably takes place by a destabilization of the AR protein, the inhibitory effect of the anti-hormones on cell proliferation is to be enhanced.
- 6000 LNCaP cells / well are seeded in a microtiter plate (96-well) in 50 ⁇ l RPMI1640 medium with 5% CCS and cultured as in model 1. After 24 hours, the cells receive 50 ⁇ l of doubly concentrated test substance diluted in culture medium. The solvent concentration is 0.5% DMSO. After 4 days, the cells receive another 100 .mu.l single-concentrated, diluted in culture medium test substance. After 7 to 8 days, the proliferation rate of the cells is determined by crystal violet assay (Gillies et al., Anal. Biochem., 1986, 159, 109-113).
- the substance treatment is carried out in the presence of 0.1 nM R1881 (1: 1000 dilution from ethanolic solution). Control cells receive only 0.5% DMSO. For agonism, the cells are treated only with test substance (without R1881).
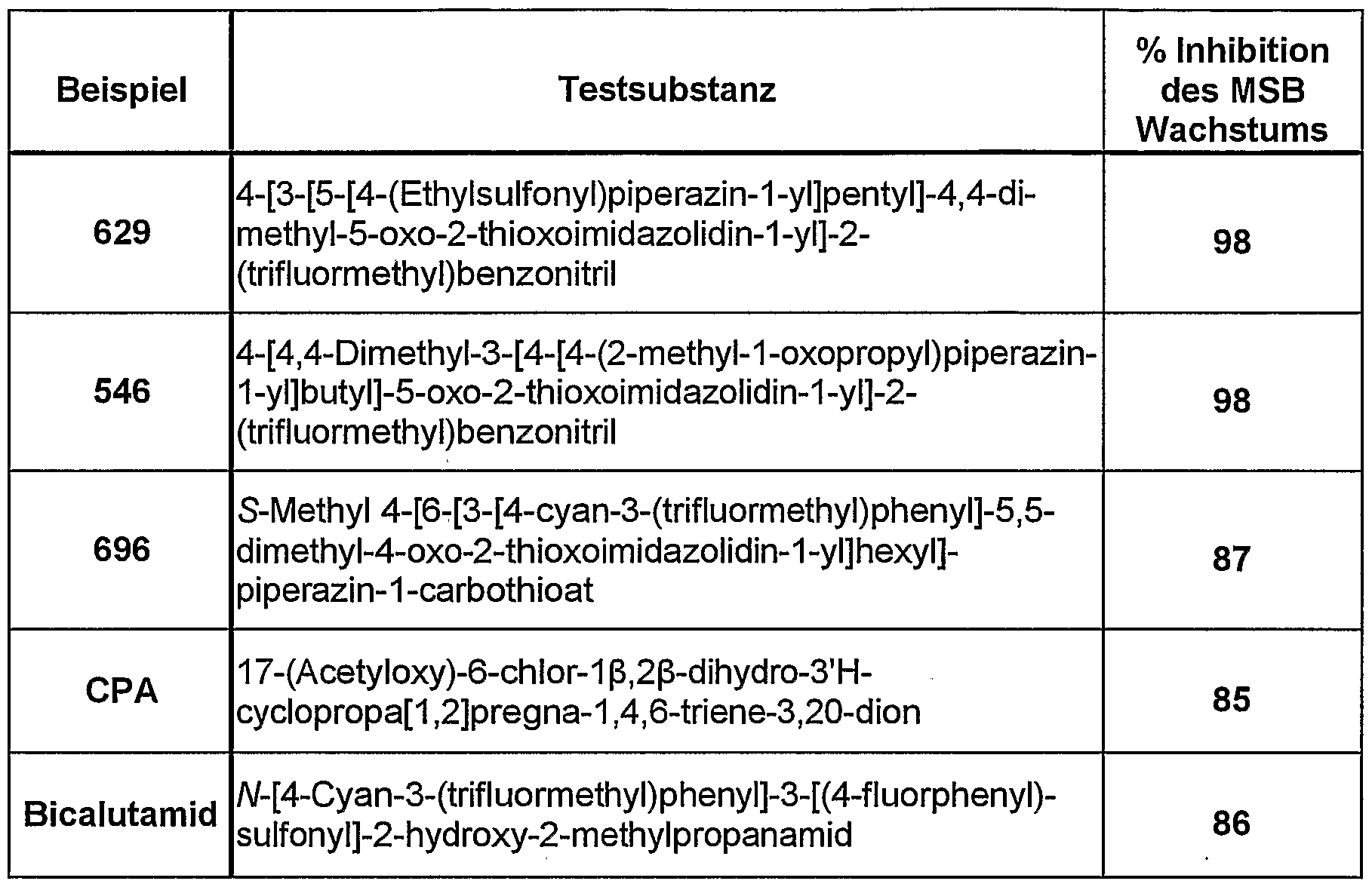
- Table 2 shows the inhibitory effect of test substances on the proliferation of the human androgen-dependent prostate cell line LNCaP.
- the inhibition of cell proliferation is an important prerequisite for the therapeutic use of the substances in the treatment of prostate cancer.
- Seven selected AR destabilizing test compounds of the present invention inhibit cell proliferation in the presence of 0.1 nM of the synthetic androgen R1881 with a similar to significantly lower IC50 than the approved nonsteroidal antiandrogen bicalutamide. At a substance concentration of 1 ⁇ M, proliferation is reduced by at least 80% compared to cell growth in the presence of 0.1 nM R1881.
- Example 696 S-Methyl 4- [6- [3- [4-cyano-3- (trifluoromethyl) phenyl] -5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1-yl] hexyl] piperazine-1 carbothioate and
- Example 653 4- [4,4-dimethyl-3- [6- [4- (2-methyl-1-oxopropyl) piperazin-1-yl] hexyl] -5-oxo-2-thioxoimidazolidine-1 -yl] -2- (trifluoromethyl) benzonitrile completely blocks growth at this concentration, whereas bicalutamide only achieves an inhibition of 85% under these conditions. Up to a tested concentration of 10 ⁇ M, no proliferation-stimulating effect was observed in any of the seven test substances. Tab. 2. Inhibition of the proliferation of LNCaP cells by test substances.
- Model 3 Inhibition of the proliferation of other non-prostate cell lines
- MaTu human mammary carcinoma cell line
- MaTu / Adr Adriamycin-resistant MaTu cell line
- HaCaT human fibroblast cell line
- A-431 human epidermis cell line.
- Table 3 shows the effect of selective test substances on the proliferation of non-prostate-derived human cells.
- the substances were tested at a concentration of 10 ⁇ M and the data correspond to the percentage of cell growth of the solvent control. It turns out that the test substances had no, in some cases low, inhibitory effect on the four different cell lines.
- the reference substance bicalutamide showed a slight inhibition in all cell lines except MaTu under the given experimental conditions. These results indicate that the antiproliferative effect of the test substances is androgen receptor-dependent, and that no secondary cytotoxic effects occur even at high concentrations of micromolar substances.
- Table 4 Effect of selective test substances on the proliferation of non-prostate cells at a concentration of 10 ⁇ M.
- Model 4 Antiandrogenic effect of selective test substances on the growth of accessory sex glands of the mouse
- the function and size of the accessory sexual glands are dependent on androgens. In castrated animals, androgen application induces growth of these organs. Concomitant treatment with antiandrogens inhibits this growth dose-dependently.
- the mice were castrated. On the same day, the treatment with testosterone propionate (0.03 mg / mouse) and the test substances (twice daily 30 mg / kg s.c. in benzyl benzoate castor oil (10:90) was formulated). The treatment took place over 7 days and at the end of the trial the weights of seminal vesicle and prostate were determined. The percentage inhibition of seminal vesicle growth was calculated with respect to the control groups (with and without testosterone). Cyproterone acetate (30 mg / kg s.c.) was used as reference substance.
- Example 629 4- [3- [5- [4- (ethylsulfonyl) -piperazin-1-yl] pentyl] -4,4-dimethyl-5-oxo-2-thioxoimidazolidin-1-yl] -2- (trifluoromethyl) benzonitrile; and
- Example 546 4- [4,4-dimethyl-3- [4- [4- (2-methyl-1-oxopropyl) -piperacin-1-yl] -butyl] -5 oxo-2-thioxoimidazolidin-1-yl] -2- (trifluoromethyl) benzonitrile resulted in almost 100% inhibition of seminal vesicle growth, whereas treatment with the reference substance cyproterone acetate resulted in only 85% inhibition. The inhibition values for bicalutamide, determined in previous experiments, were only 86%.
- Model 5 Antiandrogenic effect of a selective test substance on the growth of human prostate carcinoma xenografts in vivo
- Example 117 4- [2,5-dihydro-3-methyl-4- [4- [4- (methylsulfonyl) piperazin-1-yl] butyl] -2,5-dioxo -1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile was assayed for tumor growth in vivo by mouse xenograft models in which the compounds of the invention were administered continuously subcutaneously.
- the CWR22 Tumor Model [MA Wainstein, F. He, D. Robinson, HJ Kung, S. Schwartz, JM Giaconia, N.L Edgehouse, TP Pretlow, DR Bodner, ED Kursh, Cancer Res. 1994, 1; 54 (23), 6049-52] is a hormone-dependent human prostate carcinoma model.
- the tumor model was established and propagated on immune-deficient nude mice by serial passaging of prostate cancer tissue taken during surgery.
- the androgen-dependent LNCaP prostate cancer model was also established by a patient tumor, a tumor model that grows both in cell culture and as a xenograft immunodeficient mice (Culig, Hoffmann Bt, J. Cancer, 1999, 242-251).
- Diagram 1 Growth inhibition of LNCaP prostate cancer by substance B. Treatment was performed 2 x daily s.c. with 30 mg / kg.
- the treatment with the substance of the invention leads to a significant growth inhibition of the prostate tumors.
- this growth inhibition is comparable to the effects of castration.
- Diagram 2 Growth inhibition of CWR22 prostate carcinoma by substance B. The treatment was carried out twice a day s.c. with 30 mg / kg.
- the effect of a compound of the invention on tumor growth in vivo was examined by means of a mouse xenograft model in which the compound of the invention was administered subcutaneously twice daily for the entire treatment period. Compared to the untreated control animals resulted in an inhibition of tumor growth. Retardation of tumor growth was found to be significant in castrated mice. The treatment was well tolerated.
- the present invention shows that the compound of the present invention causes inhibition of prostate tumor growth superior to that of bicalutamide. dosage
- the daily doses range from 5 ⁇ g to 50 mg of the compound of the invention per kg of body weight.
- a recommended daily dose is in the range of 10 ⁇ g to 30 mg per kg body weight.
- Suitable dosages for the compounds according to the invention are from 0.005 to 50 mg per day per kg of body weight, depending on the age and constitution of the patient, wherein the necessary daily dose can be administered by single or multiple delivery.
- the formulation of the pharmaceutical compositions based on the novel compounds is carried out in a manner known per se by mixing the active ingredient with the excipients which are commonly used in galenicals, fillers, disintegrants, binders, humectants, lubricants, absorbents, diluents, flavoring agents, colorants processed and converted into the desired application form. It is made to Remington's Pharmaceutical Science, 15 tn ed. Mack Publishing Company, pointing East Pennsylvania (1980).
- the new compounds can be used in the form of suppositories, capsules, solutions (eg in the form of enemas) and ointments for both systemic and local therapy.
- formulations in gels, ointments, greases, creams, pastes, powders, milk and tinctures are possible.
- the dosage of the compounds of the general formula I should be 0.01% -20% in these preparations in order to achieve a sufficient pharmacological effect.
- the topical application can also take place by means of a transdermal system, for example a plaster.
- the invention likewise encompasses the compounds of general formula I according to the invention as therapeutic active ingredient.
- the invention compounds of the general formula I according to the invention as therapeutic agents together with pharmaceutically acceptable and acceptable excipients and carriers.
- the invention also encompasses a pharmaceutical composition containing one of the pharmaceutically active compounds of the invention or mixtures thereof and a pharmaceutically acceptable salt or excipients and excipients.
- compositions containing at least one compound of the general formula I, optionally together with pharmaceutically acceptable excipients and / or carriers.
- compositions and pharmaceutical compositions may be for oral, rectal, subcutaneous, transdermal, percutaneous, intravenous or intramuscular administration.
- customary carriers and / or diluents they contain at least one compound of the general formula I.
- the pharmaceuticals of the invention are prepared in a known manner with the usual solid or liquid carriers or diluents and the commonly used pharmaceutical excipients according to the desired mode of administration with a suitable dosage ,
- the preferred formulations consist of a dosage form which is suitable for oral administration.
- dosage forms are, for example, tablets, coated tablets, dragees, capsules, pills, powders, solutions or suspensions or depot forms.
- the pharmaceutical compositions containing at least one of the compounds of the invention are preferably administered orally. There are also parenteral preparations such as injection solutions into consideration. Further examples of preparations which may be mentioned are suppositories.
- Corresponding tablets can be prepared, for example, by mixing the active compound with known auxiliaries, for example inert diluents such as dextrose, sugar, sorbitol, mannitol, polyvinylpyrrolidone, disintegrants such as corn starch or alginic acid, binders such as starch or gelatin, lubricants such as magnesium stearate or talc and / or Achieving a depot effect such as carboxyl polymethylene, Carboxylmethylcellulose, cellulose acetate phthalate or polyvinyl acetate.
- the tablets can also consist of several layers.
- Coated tablets can accordingly be produced by coating cores produced analogously to the tablets with agents customarily used in tablet coatings, for example polyvinylpyrrolidone or shellac, gum arabic, talc, titanium oxide or sugar.
- the dragee wrapper can also consist of several layers, wherein the auxiliaries mentioned above in the case of the tablets can be used.
- Solutions or suspensions with the compounds of general formula I according to the invention may additionally taste-improving agents such as saccharin, cyclamate or sugar and z.
- B. flavorings such as vanillin or orange extract. They may also contain suspending aids such as sodium carboxymethylcellulose or preservatives such as p-hydroxybenzoates.
- the capsules containing the compounds of the general formula I can be prepared, for example, by mixing the compound (s) of the general formula I with an inert carrier such as lactose or sorbitol and encapsulating it in gelatine capsules.
- an inert carrier such as lactose or sorbitol
- Suitable suppositories can be prepared, for example, by mixing with suitable carriers such as neutral fats or polyethylene glycol or derivatives thereof.
- the compounds according to the invention can be administered combined with one or more of the following active substances for the treatment of prostate carcinomas:
- GnRH Gonadrotrophormone
- Estrogens It is also possible in the treatment of prostate carcinoma with the compounds according to the invention, the application of which with a method known per se of to combine niche radiology. (Laverdiere J. et al., 1997, Intl. J. of Rad. One, Biol. Phys., 37, 247-252; Bolla M. et al., 1997, New Engl. J. Med., 337, 95 -300.)
- the compounds of general formula I according to the invention for the therapy and prophylaxis of other disease states not mentioned above can be used.
- the compounds of the general formula I according to the invention can be prepared as described below.
- the present invention also relates to the intermediates of general formula VII
- V is a substituted aromatic radical of the general formula II
- A is an acetyl group, an acetylamino group, a cyano group, a nitro group, a trifluoromethyl group or a halogen (fluorine, chlorine),
- B is a hydrogen atom, a halogen (fluorine, chlorine) or a
- Trifluoromethyl group or A and B together represent a cyclic group of the formula III or IV attached to the aromatic ring, where E is a methylene group or an oxygen atom,
- W is a heterocycle of the formula V
- n can assume one of the integer values 1, 2, 3, 4, 5, 6, 7, 8,
- i and j are independently of one another the values 1 and 2, where i + j can assume the values 2 or 3,
- R and R ' may independently be a hydrogen atom or a methyl group
- W is a heterocycle of the formula V
- T is nitrogen, and there is a single bond between Q and T, and Q is a group -C (CH 3 ) 2 - and U is sulfur,
- n can assume one of the integer values 4, 5, 6, 7, 8,
- i and j are independently of one another the values 1 and 2, where i + j can assume the values 2 or 3,
- R and R ' independently represent a hydrogen atom or a
- Reagents (d) NaI, ethyl methyl ketone; (e) THF; (f) trifluoroacetic acid, CH 2 Cl 2 ; (g) NEt 3 , THF; (o) CSCI 2 , H 2 O; (p) NEfe, THF; (q) 4M HCl; (r) RSO 2 Cl, NEt ,, CH 2 Cl 2 .
- Reagents (f) trifluoroacetic acid, CH 2 Cl 2 ; (g) Nths, THF; (o) CSCI 2 , H 2 O; (p) nts, THF; (q) 4M HCI. production method
- the mixture was cooled to -60 ° C. with stirring, 410 ml of saturated ammonium chloride solution (adjusted to pH 8 with concentrated ammonia solution), warmed to room temperature and stirred at room temperature for 45 minutes.
- This mixture was extracted four times with ethyl acetate, the combined organic phases with saturated ammonium chloride solution (adjusted to pH 8 with concentrated ammonia solution) until the organic phase was light blue and then washed with water until the organic phase was colorless.
- reaction mixture was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After concentration of the organic phase was chromatographed on silica gel with methanol / dichloromethane to give 7 mg of the title compound as a yellowish oil.
- reaction mixture was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After concentration of the organic phase was chromatographed on silica gel with methanol / dichloromethane to obtain 6 mg of the title compound as a white solid
- reaction mixture was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After concentration of the organic phase was chromatographed on silica gel with methanol / dichloromethane to give 3 mg of the title compound as a yellowish oil.
- a solution of 720 mg of the compound prepared under 7c in 15 ml of THF was added under a nitrogen atmosphere at -78 ° C with 5.9 ml of a 0.5 molar solution of 9-borabicyclo (3.3.1) nonane.
- the solution was slowly warmed to room temperature and stirred overnight at room temperature.
- the vigorously stirred solution was mixed at 0 ° C with 3.1 ml of 10 percent sodium hydroxide solution and with 2.7 ml of 33 percent hydrogen peroxide solution and stirred for 12 hours at room temperature.
- water (20 ml) was added and the mixture was extracted three times with ethyl acetate.
- the title compound was prepared analogously to the reaction described under 1e. Starting from 550 mg of the compound prepared under 7e, 372 mg of the title compound were obtained.
- the title compound was prepared analogously to the reaction described under 1e. Starting from 1.95 g of the compound prepared under 9c, 1.01 g of the title compound were obtained.
- the title compound was prepared analogously to the reaction described under 7h. Starting from 25 mg of the compound prepared under 9f, 20 mg of the title compound were obtained.
- the crude isothiocyanate thus obtained was combined with the cyanoamine produced by stirring 420 ⁇ l of 5-aminopentan-1-ol for 4 hours at room temperature and heated to boiling point with 4.7 ml of triethylamine in 100 ml of tetrahydrofuran for 30 minutes. Concentration in vacuo gave the title compound as a crude product, which was immediately reacted further.
- the crude isothiocyanate thus obtained was produced and filtered with room temperature stirring of 743 ⁇ l of acetone cyanohydrin with 930 mg of 1, 1-dimethylethyl 4- (2-aminoethyl) piperazine-1-carboxylate and 406 mg of 3X molecular sieve in 20 ml of tetrahydrofuran at room temperature Cyanamine combined and heated with 0.57 ml of triethylamine in 40 ml of tetrahydrofuran for one hour to boiling. Concentration in vacuo gave the title compound as a crude product, which was immediately reacted further.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
Androgenrezeptor destabilisierende Piperazinderivate Androgen receptor destabilizing piperazine derivatives
Die vorliegende Erfindung betrifft substituierte Piperazinderivate, die den Androgenrezeptor (AR) destabilisieren, und Verfahren zur Herstellung dieser Piperazin- derivate, deren Zwischenprodukte sowie pharmazeutische Präparate enthaltend die erfindungsgemäßen Piperazinderivate und deren Verwendung zur Herstellung von Arzneimitteln.The present invention relates to substituted piperazine derivatives which destabilize the androgen receptor (AR), and to processes for preparing these piperazine derivatives, their intermediates and pharmaceutical preparations containing the piperazine derivatives according to the invention and their use for the production of medicaments.
In den Industrieländern ist das Prostatakarzinom hinter dem Lungenkarzinom die zweite Hauptursache für den Tod durch Krebs bei Männern. Bei Männern über 55 Jahre sind 4% der Todesfälle auf eine Prostatatumorerkrankung zurückzuführen und es wird vermutet, dass der Anteil bei Männern über 80 auf bis zu 80% der Todesfälle ansteigt. Die Sterberate ist zwar immer noch relativ niedrig, sie steigt jedoch jährlich um etwa 14%. Die Anzahl der Männer, bei denen ein Prostatatumor diagnostiziert wurde, ist in den letzten Jahren um 30% gestiegen, was allerdings weniger auf eine steigende Anzahl von Neuerkrankungen, sondern vielmehr darauf zurückzuführen ist, dass die Bevölkerung generell älter wird, dass die Diagnoseverfahren sich verbessert haben und dass systematische Screeningprogramme eingeführt wurden (E. J. Small, D. M. Reese, Curr. Opi. Oncol. 2000, 12, 265-272).In industrialized countries, prostate cancer is the second leading cause of cancer death in men after lung carcinoma. In men over the age of 55, 4% of deaths are due to prostate cancer and it is estimated that the proportion increases to 80% of deaths in men over 80 years of age. While the mortality rate is still relatively low, it is increasing by about 14% annually. The number of men diagnosed with a prostate tumor has risen by 30% in recent years, but this is due less to an increasing number of new cases, but rather to the fact that the general population is getting older, that the diagnostic procedures are improving and that systematic screening programs have been introduced (EJ Small, DM Reese, Curr. Op. Oncol. 2000, 12, 265-272).
Der Prostatatumor wächst in frühen Stadien androgenabhängig. Solange der Tumor lokal auf die Prostata begrenzt ist, kann er durch einen chirurgischen Eingriff entfernt oder durch Strahlentherapie behandelt werden, wobei diese Methoden mit entsprechenden Risiken verbunden sind. In den Fällen, in denen der Tumor nicht mehr lokal begrenzt ist und schon Metastasen gebildet hat, wird der Tumor palliativ durch Reduktion der Testosteronspiegel im Blut behandelt. Dies erfolgt entweder chirurgisch durch Kastration oder medikamentös durch Behandlung mit Antiandrogenen (Bicalutamid, Cyproteronacetat, Flutamid), LHRH-Agonisten (Buserelin, Zoladex), LHRH-Antagonis- ten (Cetrorelix) oder 5α-Reduktasehemmern (Finasterid). Da bei einer chirurgischen Kastration die adrenale Androgensynthese unbeeinflusst bleibt, wird in jüngerer Zeit häufig eine kombinierte chirurgische und medikamentöse Behandlung durchgeführt. Diese Behandlung hat aber nur vorübergehenden Erfolg, da es in der Regel nach spätestens zwei Jahren zum erneuten Wachstum des Tumors kommt, das in den meisten Fällen dann hormonunabhängig ist (L. J. Denis, K. Griffith, Semin. in Surg. One. 2000, 18, 52-74). Gegen diese fortgeschrittenen Stadien gibt es bis heute trotz intensiver For- schung in den letzten 50 Jahren keine wirksame Behandlung. Die 5-Jahres Überlebensrate liegt bei diesen Patienten unter 15%.The prostate tumor grows androgen-dependent in early stages. As long as the tumor is localized to the prostate, it can be surgically removed or treated by radiation therapy, with associated risks. In cases where the tumor is no longer localized and has already metastasized, the tumor is palliatively treated by reducing testosterone levels in the blood. This is done either surgically by castration or medication by treatment with antiandrogens (bicalutamide, cyproterone acetate, flutamide), LHRH agonists (buserelin, Zoladex), LHRH antagonists (cetrorelix) or 5α reductase inhibitors (finasteride). Since surgical castration does not affect adrenal androgen synthesis, combined surgical and drug treatment is frequently used. However, this treatment has only temporary success, as it usually comes after two years at the latest to the growth of the tumor, which is then hormone independent in most cases (LJ Denis, K. Griffith, Semin., Surg., One, 2000, 18 , 52-74). Despite these advanced stages, there are still no effective treatment in the past 50 years. The 5-year survival rate for these patients is below 15%.
Es gibt verschiedene Hinweise, die zeigen, dass der Androgenrezeptor bei der Entwick- lung und dem Wachstum des Prostatatumors nicht nur in den frühen hormon-abhängi- gen, sondern auch in späten hormonunabhängigen Stadien der Tumorprogression, eine wichtige Rolle spielt.There are several indications that the androgen receptor plays an important role in the development and growth of the prostate tumor not only in the early hormone-dependent, but also in late hormone-independent stages of tumor progression.
Der Androgenrezeptor gehört zur Familie der Steroidhormonrezeptoren, die als Trans- kriptionsfaktoren wirken. Der Androgenrezeptor bindet Androgene, wodurch er stabilisiert und vor einem schnellen proteolytischen Abbau geschützt wird. Nach Hormonbindung wird er in den Kern transportiert, wo er durch Bindung an sogenannte androgen- responsive DNA-Elemente, die in Promoterregionen liegen, bestimmte Gene aktiviert (D. J. Lamb et. al. Vitam. Horm. 2001, 62, 199-230).The androgen receptor belongs to the family of steroid hormone receptors, which act as transcription factors. The androgen receptor binds androgens, stabilizing it and protecting it from rapid proteolytic degradation. After hormone binding, it is transported to the nucleus, where it activates certain genes by binding to so-called androgen-responsive DNA elements located in promoter regions (D.J. Lamb et al., Vitam. Horm., 2001, 62, 199-230).
Untersuchungen an Prostatatumoren zeigen, dass in 30% der fortgeschrittenen Tumore eine Amplifikation des Androgenrezeptorgenlocus detektiert wurde. In anderen Fällen wurde eine Reihe von Mutationen im Androgenrezeptorgen gefunden, die in verschiedenen Domänen des Androgenrezeptormoleküls lokalisiert sind und zu veränderten Rezeptoreigenschaften führen. Mutierte Rezeptoren können entweder eine höhere Affinität für Androgene besitzen, konstitutiv aktiv werden, ihre Ligandenspezifität ändern, sodass sie von anderen Steroidhormonen oder sogar Antiandrogenen aktiviert werden, über Wechselwirkungen mit Molekülen aus anderen wachstumsfördernden Signalübertragungswegen aktiviert werden, die Interaktion mit Cofaktoren ändern, oder an- dere Zielgene aktivieren (J. P. Elo, T. Visakorpi, Ann. Med. 2001 , 33, 130-41).Studies on prostate tumors show that amplification of the androgen receptor gene locus was detected in 30% of advanced tumors. In other cases, a number of androgen receptor gene mutations have been found that are located in different domains of the androgen receptor molecule and lead to altered receptor properties. Mutant receptors may either have a higher affinity for androgens, become constitutively active, alter their ligand specificity, so as to be activated by other steroid hormones or even antiandrogens, be activated via interactions with molecules from other growth promoting signal transduction pathways, alter the interaction with cofactors, or activate the target genes (JP Elo, T. Visakorpi, Ann. Med. 2001, 33, 130-41).
Die Identifizierung von Antiandrogenen, die nicht nur den natürlichen Androgenrezeptor, sondern auch dessen mutierte Formen hemmen und zusätzlich das Rezeptormolekül so verändern, dass es destabilisiert wird, wäre vermutlich sehr hilfreich, um Prostatatumoren in verschiedenen Stadien zu behandeln. Solche Verbindungen könnten ein Wiederauftreten des Tumorwachstums verhindern oder zumindest den Zeitraum bis dahin deutlich verlängern. Im Falle des Östrogenrezeptors konnten Liganden identifiziert werden, die den Rezeptor destabilisieren und zu einer Verringerung des Rezeptorgehaltes in vitro und in vivo führen (S. Dauvois et. al. Proc. Natl. Acad. Sei. USA 1992, 89, 4037-41; R. A. McClelland et. al. Eur. J. Cancer 1996, 32A, 413-6). Nichtsteroidale Antiandrogene werden in US 5,411,981 (Phenylimidazolidinderivate), in WO97/00071 (spezifisch substituierte Phenyldimethylhydantoine sowie deren Imino- bzw. Thionderivate) in WO00/37430 (Phenylalanine, Phenylhydantoine sowie Phenyl- harnstoffe), in WO01/58855 (Aminopropanilide) und in EP1122242 (substituierte Cyanphenylpiperazine) beschrieben.The identification of antiandrogens, which inhibit not only the natural androgen receptor but also its mutated forms, and in addition alter the receptor molecule to destabilize it, would probably be very helpful in treating prostate tumors at various stages. Such compounds could prevent the recurrence of tumor growth, or at least significantly prolong the period until then. In the case of the estrogen receptor, it has been possible to identify ligands which destabilize the receptor and lead to a reduction in the receptor content in vitro and in vivo (S. Dauvois et al., Proc. Natl. Acad. See, USA 1992, 89, 4037-41; RA McClelland et al, Eur. J. Cancer 1996, 32A, 413-6). Nonsteroidal antiandrogens are described in US Pat. No. 5,411,981 (phenylimidazolidine derivatives), WO97 / 00071 (specifically substituted phenyldimethylhydantoins and their imino or thione derivatives) in WO00 / 37430 (phenylalanines, phenylhydantoins and phenylureas), WO01 / 58855 (aminopropanilides) and EP1122242 (substituted Cyanphenylpiperazine) described.
Die Aufgabe der vorliegenden Erfindung besteht darin, Verbindungen mit antiandroge- ner Wirkung zur Verfügung zu stellen, die den Androgenrezeptor destabilisieren, das Prostatatumorwachstum hemmen, und gleichzeitig eine hohe, ggf. orale Bioverfügbarkeit aufweisen.The object of the present invention is to provide compounds with antiandrogenic action which destabilize the androgen receptor, inhibit prostate tumor growth, and at the same time have a high, possibly oral bioavailability.
Untersuchungen mit nichtsteroidalen Antiandrogenen haben gezeigt, dass sie gegenüber den steroidalen Verbindungen Vorteile aufweisen und daher zu bevorzugen sind. So kann mit nichtsteroidalen Verbindungen eine selektivere Wirkung mit geringeren adversen Nebenwirkungen erzielt werden. Im Gegensatz zu den steroidalen Antiandrogenen fehlt den bekannten Nichtsteroiden Bicalutamid und Flutamid z.B. die progestagene Aktivität und außerdem führt deren Verwendung zu einer Erhöhung der Testosteronspiegel im Serum, das klinisch zu einer Erhaltung der Potenz führen könnte.Studies with nonsteroidal antiandrogens have shown that they have advantages over the steroidal compounds and are therefore to be preferred. Thus, a more selective action can be achieved with non-steroidal compounds with less adverse side effects. In contrast to the steroidal antiandrogens, the known nonsteroids lack bicalutamide and flutamide, e.g. the progestagenic activity and, in addition, their use leads to an increase in serum testosterone levels, which could clinically lead to maintenance of potency.
Diese Aufgabe wird erfindungsgemäß durch die neuen Verbindungen der allgemeinen Formel I gelöst:This object is achieved by the novel compounds of general formula I:
Die vorliegende Erfindung betrifft Verbindungen der allgemeinen Formel I, wobeiThe present invention relates to compounds of general formula I, wherein
V für einen substituierten aromatischen Rest der allgemeinen Formel II steht,V is a substituted aromatic radical of the general formula II,
worin A für eine Acetylgruppe, eine Acetylaminogruppe, eine Cyangruppe, eine Nitro- gruppe, eine Trifluormethylgruppe oder ein Halogen (Fluor, Chlor), wherein A is an acetyl group, an acetylamino group, a cyano group, a nitro group, a trifluoromethyl group or a halogen (fluorine, chlorine),
B für ein Wasserstoff atom, ein Halogen (Fluor, Chlor) oder eine Trifluormethyl- gruppe, oderB is a hydrogen atom, a halogen (fluorine, chlorine) or a trifluoromethyl group, or
A und B zusammen für eine an den aromatischen Ring gebundene cyclische Gruppe der Formel III oder IV, wobei E für eine Methylengruppe oder ein Sauerstoffatom steht,A and B together represent a cyclic group of the formula III or IV attached to the aromatic ring, where E is a methylene group or an oxygen atom,
w für einen Heterocyclus der Formel V,w is a heterocycle of the formula V,
v. worin v. wherein
T Kohlenstoff oder Stickstoff darstellen kann,T can represent carbon or nitrogen,
wenn T für Kohlenstoff steht, soll zwischen Q und T eine Doppelbindung vorliegen und Q eine Gruppe =C(CH3)- und U Sauerstoff bedeuten und n einen der ganzzahligen Werte 1 , 2, 3, 4, 5, 6, 7, 8 annehmen, oderwhen T is carbon, there should be a double bond between Q and T and Q is a group = C (CH 3 ) - and U is oxygen and n is one of the integer values 1, 2, 3, 4, 5, 6, 7, 8 accept, or
wenn T für Stickstoff steht, soll zwischen Q.und T eine Einfachbindung vorliegen und Q eine Gruppe -C(CH3)2- und U Schwefel bedeuten und n einen der ganzzahligen Werte 2, 3, 4, 5, 6, 7, 8 annehmen, i und j unabhängig voneinander für die Werte 1 und 2 stehen, wobei i + j die Werte 2 oder 3 annehmen kann,when T is nitrogen, there should be a single bond between Q. and T and Q is a group -C (CH 3 ) 2 - and U is sulfur and n is one of the integer values 2, 3, 4, 5, 6, 7, 8 accept, i and j are independently of one another the values 1 and 2, where i + j can assume the values 2 or 3,
R und R' unabhängig voneinander ein Wasserstoffatom oder eine Methylgruppe sein können,R and R 'may independently be a hydrogen atom or a methyl group,
Y für eine Bindung zwischen dem heterocyclischen Stickstoff und Z, für eineY is a bond between the heterocyclic nitrogen and Z, for a
Carbonylgruppe -C(O)-, für eine Sulfonylgruppe -S(O)2-, für eine Iminocarbonylgruppe -C(O)N(Z')-> für eine Iminosulfonylgruppe -S(O)2 Carbonyl group -C (O) -, for a sulfonyl group -S (O) 2 -, for an iminocarbonyl group -C (O) N (Z ') - > for an iminosulfonyl group -S (O) 2
N(Z')-, für eine lmino(thioxomethyl)gruppe -C(S)N(Z')-, für eine Oxycarbonylimino(thioxomethyl)gruppe -C(S)N(Z')C(O)O-, für eine Oxycarbonylgruppe -C(O)O-, für eine Sulfanylcarbonylgruppe -C(O)S-, undN (Z ') -, for an imino (thioxomethyl) group -C (S) N (Z') -, for an oxycarbonylimino (thioxomethyl) group -C (S) N (Z ') C (O) O-, for an oxycarbonyl group -C (O) O-, for a sulfanylcarbonyl group -C (O) S-, and
Z und Z' unabhängig voneinander für eine unverzweigte d-Cs-Alkylgruppe oder verzweigte C3-C8-Alkylgruppe, eine gegebenenfalls mit einem Phenyl-Rest substituierte C3-C6-Cycloalkylgruppe, eine (C3-C6-Cycloalkyl)-Cι-C4- alkylengruppe, eine verzweigte oder unverzweigte C2-C5-Alkenylgruppe, eine verzweigte oder unverzweigte C2-C5-Alkenylgruppe, eine C3-C5- Alkinylgruppe, eine C-ι-C -Alkoxy-, Cyan-, Phenylsulfanyl- oder Hydroxy-d-Z and Z 'independently of one another are an unbranched C 1 -C 5 -alkyl group or branched C 3 -C 8 -alkyl group, a C 3 -C 6 -cycloalkyl group optionally substituted by a phenyl radical, a (C 3 -C 6 -cycloalkyl) -C 1 -C 4 -alkylene group, a branched or unbranched C 2 -C 5 -alkenyl group, a branched or unbranched C 2 -C 5 -alkenyl group, a C 3 -C 5 -alkynyl group, a C 1 -C -alkoxy group , Cyano, phenylsulfanyl or hydroxy-d
C -alkylengruppe, eine (2-Methoxyethoxy)methylgruppe, eine [2-(2- Methoxyethoxy)ethoxy]methylgruppe, eine 2-(2-Methoxyethoxy)ethylgruppe, eine 2-[2-(2-Methoxyethoxy)ethoxy]ethylgruppe, eine Cι-C -Alkoxy-Cι-C - alkylengruppe, eine d-C Ikoxycarbonyl-Ci-C^alkylengruppe, eine Adamantylgruppe, eine Trichloracetylgruppe, eine unsubstituierte oder mit bis zu drei verzweigten oder unverzweigten Cι-C4-Alkyl-, C2-C6-Alkenyl-, C3-C6- Cycloalkyl-, C3-C6-Cycloalkyloxy-, Phenyl-, Cyan-, Halogen-, Methoxy-, Ethoxy-, Phenoxy-, Benzyloxy-, Methylsulfanyl-, Ethylsulfanyl-, Benzylsulfanyl-, Phenylsulfanyl-, Dimethylamino-, Acetylamino-, Trifluormethyl-, Trifluormethoxy-, Trifluormethylsulfanyl-, Acetyl-, (1-C 1 -C 2 alkylene group, a (2-methoxyethoxy) methyl group, a [2- (2-methoxyethoxy) ethoxy] methyl group, a 2- (2-methoxyethoxy) ethyl group, a 2- [2- (2-methoxyethoxy) ethoxy] ethyl group, a C 1 -C 4 -alkoxy-C 1 -C 4 -alkylene group, a C 1 -C 4 -alkoxyalkoxycarbonyl group, an adamantyl group, a trichloroacetyl group, an unsubstituted or with up to three branched or unbranched C 1 -C 4 -alkyl, C 2 - C 6 alkenyl, C 3 -C 6 - cycloalkyl, C 3 -C 6 cycloalkyloxy, phenyl, cyano, halogen, methoxy, ethoxy, phenoxy, benzyloxy, methylsulfanyl, Ethylsulfanyl- , Benzylsulfanyl, phenylsulfanyl, dimethylamino, acetylamino, trifluoromethyl, trifluoromethoxy, trifluoromethylsulfanyl, acetyl, (1)
Iminoethyl)- oder Nitro-Gruppen substituierte Aryl-, Heteroaryl-, Heterocyclyl-, Aryloxy-Cι-C4-alkylen-, Heteroaryloxy-Cι-C -alkylen-, Aryl-Cι-C -alkylenoxy-Cι-C4-alkylen-Gruppe oder einen Rest der Formel CpFqHr mit p = 1, 2, 3, 4, q>1 und q+r = 2p+1 stehen, und Z' zusätzlich zu den vorgenannten Definitionen für ein Wasserstoffatom steht.Iminoethyl) - or nitro groups substituted aryl, heteroaryl, heterocyclyl, Aryloxy-C 1 -C 4 -alkylene, heteroaryloxy-C 1 -C 4 -alkylene, aryl-C 1 -C 4 -alkyleneoxy-C 1 -C 4 -alkylene group or a radical of the formula C p F q H r where p = 1 , 2, 3, 4, q> 1 and q + r = 2p + 1, and Z 'is, in addition to the abovementioned definitions, a hydrogen atom.
Die erfindungsgemäßen Verbindungen zeichnen sich dadurch aus, dass sie jeweils einen Diazacycloalkankern enthalten, dessen Stickstoffatome jeweils substituiert vorliegen.The compounds of the invention are characterized in that they each contain a Diazacycloalkankern whose nitrogen atoms are each substituted.
Bei den unverzweigten Cι-C8-Alkylgruppen für die Reste Z und __' und kann es sich beispielsweise um eine Methyl-, Ethyl-, n-Propyl-, n-Butyl-, n-Pentyl-, n-Hexyl-, n- Heptyl-, n-Octyl-; bei den verzweigten C3-C8-Alkylgruppen um eine /'so-Propyl-, iso- Butyl-, sec-Butyl, ferf-Butyl-, /so-Pentyl-, neo-Pentyl-, 2-Methylpentyl-, 2,2-Dimethyl- butyl-, 2,3-Dimethylbutyl-, 2-Methylhexyl-, 2,2-Dimethylpentyl-, 2,2,3-Trimethylbutyl-, 2,3,3-Trimethylbutylgruppe handeln.In the unbranched -C-C 8 alkyl groups for the radicals Z and __ 'and may for example be a methyl, ethyl, n-propyl, n-butyl, n-pentyl, n-hexyl, n Heptyl, n-octyl; in the branched C 3 -C 8 alkyl groups to a ' so-propyl, iso-butyl, sec-butyl, ferf-butyl, / so-pentyl, neo-pentyl, 2-methylpentyl, 2 , 2-dimethylbutyl, 2,3-dimethylbutyl, 2-methylhexyl, 2,2-dimethylpentyl, 2,2,3-trimethylbutyl, 2,3,3-trimethylbutyl.
Bei den gegebenenfalls mit einem Phenyl-Rest substituierten C3-C6-Cycloalkylgruppen für die Reste Z und Z kann es sich durchweg um eine Cyclopropyl-, Cyclobutyl-, Cyclopentyl-, Cyclohexyl-, bzw. Phenylcyclopropyl-, Phenylcyclobutyl-, Phenylcyclo- pentyl-, Phenylcyclohexylgruppe handeln.The optionally substituted with a phenyl radical C 3 -C 6 -cycloalkyl groups for the radicals Z and Z may be consistently to a cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, or phenylcyclopropyl, Phenylcyclobutyl-, Phenylcyclo- pentyl, phenylcyclohexyl group act.
Bei den (C3-C6-Cycloalkyl)-Cι-C -alkylengruppen für die Reste Z und 11 kann es sich beispielsweise um eine Cyclopropylmethyl-, Cyclobutylmethyl-, Cyclopentylmethyl-, Cyclohexylmethyl, Cyclopropylethyl-, Cyclobutylethyl-, Cyclopentylethyl-, Cyclohexyl- ethyl-, Cyclopropylpropyl-, Cyclobutylpropyl-, Cyclopentylpropyl-, Cyclohexylpropyl-, Cyclopropylbutyl-, Cyclobutylbutyl, Cyclopentylbutyl- bzw. Cyclohexylbutylgruppe handeln.The (C 3 -C 6 -cycloalkyl) -CC-C-alkylene groups for the radicals Z and 11 may be, for example, a cyclopropylmethyl, cyclobutylmethyl, cyclopentylmethyl, cyclohexylmethyl, cyclopropylethyl, cyclobutylethyl, cyclopentylethyl, cyclohexyl - ethyl, cyclopropylpropyl, cyclobutylpropyl, cyclopentylpropyl, cyclohexylpropyl, cyclopropylbutyl, cyclobutylbutyl, cyclopentylbutyl or cyclohexylbutyl act.
Bei den verzweigten oder unverzweigten C2-C5-Alkenylgruppen für die Reste Z und Z' kann es sich beispielsweise um eine Vinyl-, Allyl-, Homoallyl-, (£)-But-2-enyl-, (Z)-But-2- enyl-, (E)-But-1-enyl-, (Z)-But-1-enyl-, Pent-4-enyl-, (E)-Pent-3-enyl-, (Z)-Pent-3-enyl-, (E)-Pent-2-enyl-, (Z)-Pent-2-enyl-, (£)-Pent-1-enyl-, (Z)-Pent-1-enyl-, 2-Methylvinyl-, 3- Methylbut-3-enyl-, 2-Methylbut-3-enyl-, (£)-2-Methylbut-2-enyl-, (Z)-2-Methylbut-2-enyl-, 3-Methylbut-2-enyl-Gruppe handeln. Bei den C3-C5-Alkinylgruppen für die Reste Z und Z' kann es sich beispielsweise um eine Prop-1-inyl-, Prop-2-inyl-, But-1-inyl-, But-2-inyl-, But-3-inyl-, Pent-1-inyl-, Pent-2- inyl-, Pent-3-inyl-, Pent-4-inyl-, 1-Methylprop-2-inyl-, 1-Methylbut-3-inyl-, 1-Ethylprop-2- inyl-Gruppe handeln.The branched or unbranched C 2 -C 5 -alkenyl groups for the radicals Z and Z 'may, for example, be a vinyl, allyl, homoallyl, (ε) -but-2-enyl, (Z) -butyne -2-enyl, (E) -but-1-enyl, (Z) -but-1-enyl, pent-4-enyl, (E) -pent-3-enyl, (Z) - Pent-3-enyl, (E) -pent-2-enyl, (Z) -pent-2-enyl, ()) -pent-1-enyl, (Z) -pent-1-enyl, , 2-methylvinyl, 3-methylbut-3-enyl, 2-methylbut-3-enyl, (2'-methylbut-2-enyl, (Z) -2-methylbut-2-enyl-, 3-methylbut-2-enyl group act. The C 3 -C 5 -alkynyl groups for the radicals Z and Z 'may be, for example, a prop-1-ynyl, prop-2-ynyl, but-1-ynyl, but-2-ynyl, But-3-ynyl, pent-1-ynyl, pent-2-ynyl, pent-3-ynyl, pent-4-ynyl, 1-methylprop-2-ynyl, 1-methylbut-3 inyl, 1-ethylprop-2-inyl group.
Bei den Cι-C4-Alkoxygruppen für die Reste Z und Z' kann es sich beispielsweise um eine Methoxy-, Ethoxy-, n-Propoxy-, /so-Propoxy-, n-Butoxy-, sec-Butoxy-, /'so-Butoxy-, ferf-Butoxygruppe handeln.The C 1 -C 4 -alkoxy groups for the radicals Z and Z 'may be, for example, a methoxy, ethoxy, n-propoxy, / so-propoxy, n-butoxy, sec-butoxy-, / ' so-butoxy, ferf-butoxy act.
Bei den Cι-C -Alkylengruppen innerhalb der Reste Z und Z' kann es sich beispielsweise um eine Methylen- (-CH2-), Ethyliden- [-CH(CH3)-], Ethylen- (-CH2CH2-), 1,3- Propylen- (-CH2CH2CH2-), 1 ,2-Propylen- [-CH2CH(CH3)-], 1 ,4-Butylen-, (-CH2CH2CH2CH2-), 1 ,3-Butylen- [-CH2CH2CH(CH3)-], 1,2-Butylen- [-CH2CH(CH2CH3)-], 2-Methyl-1 ,2-propylen- [-CH2C(CH3)2-], 2-Methyl-1 ,3-propylen-Gruppe [-CH2CH(CH3)CH2-] handeln.The C 1 -C 4 -alkylene groups within the radicals Z and Z 'may be, for example, a methylene (-CH 2 -), ethylidene [-CH (CH 3 ) -], ethylene (-CH 2 CH 2 -) ), 1,3-propylene- (-CH 2 CH 2 CH 2 -), 1, 2-propylene- [-CH 2 CH (CH 3 ) -], 1, 4-butylene-, (-CH 2 CH 2 CH 2 CH 2 -), 1, 3-butylene- [-CH 2 CH 2 CH (CH 3 ) -], 1,2-butylene- [-CH 2 CH (CH 2 CH 3 ) -], 2-methyl -1, 2-propylene- [-CH 2 C (CH 3 ) 2 -], 2-methyl-1,3-propylene group [-CH 2 CH (CH 3 ) CH 2 -].
Bei den Hydroxy-d-C4-alkylengruppen für die Reste Z und Z' kann es sich um eine Hydroxymethyl- (HOCH2-), 2-Hydroxyethyl- (HOCH2CH2-), 1-Hydroxyethyl- [CH3CH(OH)-], 3-Hydroxypropyl- (HOCH2CH2CH2-), 2-Hydroxypropyl-The hydroxy-dC 4 -alkylene groups for the radicals Z and Z 'may be a hydroxymethyl (HOCH 2 -), 2-hydroxyethyl- (HOCH 2 CH 2 -), 1-hydroxyethyl- [CH 3 CH (OH ) -], 3-hydroxypropyl (HOCH 2 CH 2 CH 2 -), 2-hydroxypropyl
[CH3CH(OH)CH2CH2-], 1-Hydroxypropyl- [CH3CH2CH(OH)-], 4-Hydroxybutyl-, (HOCH2CH2CH2CH2-), 3-Hydroxybutyl- [CH3CH(OH)CH2CH2-], 2-Hydroxybutyl- [CH3CH2CH(OH)CH2-], 1-Hydroxybutyl- [CH3CH2CH2CH(OH)-]t 1-Hydroxy-1- methylethyl- [(CH3)2C(OH)-], 1-Hydroxy-1-methylpropyl-Gruppe [CH3CH2C(CH3)(OH)-] handeln.[CH 3 CH (OH) CH 2 CH 2 -], 1-hydroxypropyl- [CH 3 CH 2 CH (OH) -], 4-hydroxybutyl, (HOCH 2 CH 2 CH 2 CH 2 -), 3-hydroxybutyl - [CH 3 CH (OH) CH 2 CH 2 -], 2-hydroxybutyl- [CH 3 CH 2 CH (OH) CH 2 -], 1-hydroxybutyl- [CH 3 CH 2 CH 2 CH (OH) -] t is 1-hydroxy-1-methylethyl- [(CH 3 ) 2 C (OH) -], 1-hydroxy-1-methylpropyl [CH 3 CH 2 C (CH 3 ) (OH) -].
Bei den Cι-C4-Alkoxycarbonyl-d-C -alkylengruppen für die Reste Z und Z' handelt es sich beispielsweise um eine Kombination der Cι-C4-Alkoxycarbonyl- und der Cι-C - Alkylenfunktionen. Unter einer Cι-C4-Alkoxycarbonylgruppe werden Methoxycarbonyl- [MeOC(O)-], Ethoxycarbonyl [EtOC(O)-), n-Propoxycarbonyl- [CH3CH2CH2OC(O)-], iso- Propoxycarbonyl- [(CH3)2CHOC(O)-], n-Butoxycarbonyl- [CH3CH2CH2CH2OC(O)-], iso- Butoxycarbonyl- [(CH3)2CHCH2OC(O)-], sec-Butoxycarbonyl- [CH3CH2(CH3)CHOC(O)-], ferf-Butoxycarbonyl [ (CH3)3COC(O)-] verstanden. Unter einer Cι-C4-Alkylengruppe werden die weiter oben genannten Cι-C4-Alkylengruppen verstanden. Beispielsweise können sich aus der Kombination dieser Funktionen zu den C4-alkylengruppen folgende Reste ergeben: (Methoxycarbonyl)methyl- [CH3OC(O)CH2-] (Ethoxycarbonyl)methyl- [CH3CH2OC(O)CH2-], (ry-Propoxycarbonyl)methyl- [CH3CH2CH2OC(O)CH2-], (/'so-Propoxycarbonyl)methyl- [(CH3)2CHOC(O)CH2-], (n-Butoxycarbonyl)methyl- [CH3CH2CH2CH2OC(O)CH2-], (/so-Butoxycarbonyl)methyl- [(CH3)2CHCH2OC(O)CH2-], (sec-Butoxycarbonyl)methyl- [CH3CH2(CH3)CHOC(O)CH2-], (ferf-Butoxycarbonyl)methyl- [(CH3)3COC(0)CH2-],The C 1 -C 4 -alkoxycarbonyl-dC-alkylene groups for the radicals Z and Z 'are, for example, a combination of the C 1 -C 4 -alkoxycarbonyl and the C 1 -C 4 -alkylene functions. A C 1 -C 4 -alkoxycarbonyl group includes methoxycarbonyl- [MeOC (O) -], ethoxycarbonyl [EtOC (O) -), n-propoxycarbonyl- [CH 3 CH 2 CH 2 OC (O) -], isopropoxycarbonyl- [(CH 3 ) 2 CHOC (O) -], n-butoxycarbonyl- [CH 3 CH 2 CH 2 CH 2 OC (O) -], isobutoxycarbonyl- [(CH 3 ) 2 CHCH 2 OC (O) - ], sec-butoxycarbonyl- [CH 3 CH 2 (CH 3 ) CHOC (O) -], ferf -butoxycarbonyl [(CH 3 ) 3 COC (O) -]. A C 1 -C 4 -alkylene group is understood to mean the C 1 -C 4 -alkylene groups mentioned above. For example, from the combination of these functions to the C 4 alkylene groups give the following radicals: (methoxycarbonyl) methyl- [CH 3 OC (O) CH 2 -] (Ethoxycarbonyl) methyl- [CH 3 CH 2 OC (O) CH 2 -], (ry-propoxycarbonyl) methyl- [CH 3 CH 2 CH 2 OC (O) CH 2 -], (/ ' so-propoxycarbonyl) methyl - [(CH 3 ) 2 CHOC (O) CH 2 -], (n-butoxycarbonyl) methyl- [CH 3 CH 2 CH 2 CH 2 OC (O) CH 2 -], (/ so-butoxycarbonyl) methyl- [ (CH 3 ) 2 CHCH 2 OC (O) CH 2 -], (sec-butoxycarbonyl) methyl- [CH 3 CH 2 (CH 3 ) CHOC (O) CH 2 -], (ferf-butoxycarbonyl) methyl- [( CH 3 ) 3 COC (0) CH 2 -],
2-(Methoxycarbonyl)ethyl- [CH3OC(O)CH2CH2-], 2-(Ethoxycarbonyl)ethyl- [CH3CH2OC(O)CH2CH2-], 2-(n-Propoxycarbonyl)ethyl- [CH3CH2CH2OC(O)CH2CH2-], 2-(/so-Propoxycarbonyl)ethyl- [(CH3)2CHOC(O)CH2CH2-], 2-(n-Butoxycarbonyl)ethyl- [CH3CH2CH2CH2OC(O)CH2CH2-], 2-(/so-Butoxycarbonyl)ethyl- [(CH3)2CHCH2OC(O)CH2CH2-], 2-(sec-Butoxycarbonyl)- ethyl- [CH3CH2(CH3)CHOC(O)CH2CH2-], 2-(tetf-Butoxycarbonyl)ethyl- [(CH3)3COC(O)CH2CH2-].2- (methoxycarbonyl) ethyl- [CH 3 OC (O) CH 2 CH 2 -], 2- (ethoxycarbonyl) ethyl- [CH 3 CH 2 OC (O) CH 2 CH 2 -], 2- (n-propoxycarbonyl ) ethyl- [CH 3 CH 2 CH 2 OC (O) CH 2 CH 2 -], 2 - (/ so-propoxycarbonyl) ethyl- [(CH 3 ) 2 CHOC (O) CH 2 CH 2 -], 2- (n-Butoxycarbonyl) ethyl- [CH 3 CH 2 CH 2 CH 2 OC (O) CH 2 CH 2 -], 2 - (/ so -butoxycarbonyl) ethyl- [(CH 3 ) 2 CHCH 2 OC (O) CH 2 CH 2 -], 2- (sec-butoxycarbonyl) ethyl [CH 3 CH 2 (CH 3 ) CHOC (O) CH 2 CH 2 -], 2- (tetrabutoxycarbonyl) ethyl [(CH 3 ) 3 COC (O) CH 2 CH 2 -].
Bei den Arylgruppen für die Reste Z und 11 kann es sich um eine Phenyl-, Naphthalin-1- yl-, Naphthalin-2-yl-, [1 , 1 '-Biphenyl]-2-yl-, [1 , 1 '-Biphenyl]-3-yl- oder eine [1 , 1 '-Biphenyl]- 4-yl-Gruppe handeln.The aryl groups for radicals Z and 11 may be a phenyl, naphthalene-1-yl, naphthalen-2-yl, [1, 1'-biphenyl] -2-yl-, [1, 1 ' Biphenyl] -3-yl or a [1, 1'-biphenyl] -4-yl group.
Bei den Heteroarylgruppen für die Reste Z und Z' kann es sich um eine über eine der substituierbaren Stellen verknüpfte Pyridinyl-, Pyrimidinyl-, Chinolinyl-, Isochinolinyl-, Benzofuranyl-, Benzothienyl-, 1 ,3-Benzodioxolyl-, 2,1 ,3-Benzothiadiazolyl-, Indolyl-,The heteroaryl groups for the radicals Z and Z 'can be a pyridinyl, pyrimidinyl, quinolinyl, isoquinolinyl, benzofuranyl, benzothienyl, 1,3-benzodioxolyl, 2.1 linked via one of the substitutable sites, 3-benzothiadiazolyl, indolyl,
Furanyl-, Thienyl-, Oxazolyl-, Isoxazolyl-, Thiazolyl-, Pyrrolyl-, Pyrazolyl- oder eineFuranyl, thienyl, oxazolyl, isoxazolyl, thiazolyl, pyrrolyl, pyrazolyl or a
Imidazolyl-Gruppe handeln.Imidazolyl group act.
Bei den Heterocyclylgruppen für die Reste Z und 11 kann es sich um eine über eine der substituierbaren Stellen verknüpfte Piperidinyl-, Morpholinyl-, Thiomorpholinyl-, Pipera- zinyl-, Tetrahydrofuranyl-, Tetrahydrothienyl-, Imidazolidinyl- oder eine Pyrrolidinyl- gruppe handeln.The heterocyclyl groups for the radicals Z and 11 may be a piperidinyl, morpholinyl, thiomorpholinyl, piperazinyl, tetrahydrofuranyl, tetrahydrothienyl, imidazolidinyl or pyrrolidinyl group linked via one of the substitutable sites.
Bei den Substituenten der Aryl-, Heteroaryl-, Heterocyclylreste, auch jeweils innerhalb der Aryl-d-C4-alkylen-, Heteroaryl-Cι-C4-alkylen-, Aryloxy-Ci-d-alkylen-, Heteroaryl- oxy-Cι-C -alkylen-, Aryl-C-r-C^alkylenoxy-d-d-alkylen-Einheiten für den Rest Z kann es sich u.a. um unverzweigte oder verzweigte d-C4-Alkylgruppen (Methyl-, Ethyl-, n-Propyl-, iso- Propyl-, n-Butyl-, sec-Butyl-, so-Butyl- sowie te -Butyl-) und/oder C2-C6-Alkenylgruppen (Vinyl-, Allyl-, Homoallyl-, (E)-But-2-enyl-, (Z)-But-2-enyl-, Pent-4-enyl-, (E)-Pent-3-enyl-, (Z)-Pent-3-enyl-, (£)-Pent-2-enyl-, (Z)-Pent-2-enyl-,In the substituents of the aryl, heteroaryl, heterocyclyl, also in each case within the aryl-dC 4 -alkylene, heteroaryl-C 4 -alkylene, aryloxy-Ci-d-alkylene, heteroaryl-oxy-C-C alkyl, aryl-C 1 -C 4 -alkyleneoxy-d-alkylene units for the radical Z may be, inter alia, unbranched or branched C 1 -C 4 -alkyl groups (methyl, ethyl, n-propyl, iso-propyl, n-butyl); Butyl, sec-butyl, so-butyl and te-butyl) and / or C 2 -C 6 -alkenyl groups (vinyl, allyl, homoallyl, (E) -but-2-enyl-, ( Z) but-2-enyl, pent-4-enyl, (E) -pent-3-enyl, (Z) -pent-3-enyl, ()) -pent-2-enyl, (Z) -pent-2-enyl,
2-Methylvinyl-, 3-Methylbut-3-enyl-, 2-Methylbut-3-enyl-, (£)-2-Methylbut-2-enyl-, (Z)-2-Methylbut-2-enyl-, 2-Ethylprop-2-enyl-, Heχ-5-enyl-, (E)-Hex-4-enyl-, (Z)- Hex-4-enyl-, (£)-Hex-3-enyl-, (Z)-Hex-3-enyl-, (£)-Hex-2-enyl-, (Z)-Hex-2-enyl-, 1- Methylpent-4-enyl-, (E)-1-Methylpent-3-enyl-, (Z)-1-Methylpent-3-enyl-, 1- Ethylbut-3-enyl-, (£)-1-Methylpent-2-enyl-, (Z)-1-Methylpent-2-enyl-) und/oder C3-C6-Cycloalkylgruppen (Cyclopropyl-, Cyclobutyl-, Cyclopentyl-, Cyclohexyl-) und/oder2-methylvinyl, 3-methylbut-3-enyl, 2-methylbut-3-enyl, (2'-methylbut-2-enyl, (Z) -2-methylbut-2-enyl, 2-ethylprop-2-enyl, heχ-5-enyl, (E) -hex-4-enyl, (Z) -hex-4-enyl- , (£) -hex-3-enyl, (Z) -hex-3-enyl, (£) -hex-2-enyl, (Z) -hex-2-enyl, 1-methylpent-4 -enyl, (E) -1-methylpent-3-enyl, (Z) -1-methylpent-3-enyl, 1-ethylbut-3-enyl, (1) -1-methylpent-2-enyl -, (Z) -1-methylpent-2-enyl-) and / or C 3 -C 6 -cycloalkyl groups (cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl) and / or
Halogen (Fluor-, Chlor-, Brom-, lod-) handeln.Halogen (fluorine, chlorine, bromine, iodine) act.
Bei den Aryl-C^d-alkylen-Gruppen für die Reste Z und Z' kann es sich um eine Kombination der zuvor definierten Aryl- und Cι-C -Alkylgruppen, beispielsweise: eine Phenylmethyl-, 1-Phenylethyl-, 2-Phenylethyl-, 1-Methyl-1-phenylethyl-, 3-PhenylpropyI- 4-Phenylbutyl-, (Naphthalin-l-yl)methyl-, 1-(Naphthalin-1-yl)ethyl-, 2-(Naphthalin-1-yl)- ethyl-, (Naphthalin-2-yl)methyl-, 1-(Naphthalin-2-yl)ethyl-, 2-(Naphthalin-2-yl)ethyl-, ([1,1'-Biphenyl]-2-yl)methyl-, ([1,1'-Biphenyl]-3-yl)methyl- oder eine ([1,1'-Biphenyi]-4- yl)methylgruppe handeln.The aryl-C ^ d-alkylene groups for the radicals Z and Z 'may be a combination of the previously defined aryl and C 1 -C 4 -alkyl groups, for example: a phenylmethyl, 1-phenylethyl, 2-phenylethyl -, 1-methyl-1-phenylethyl, 3-phenylpropyl-4-phenylbutyl, (naphthalen-1-yl) methyl, 1- (naphthalen-1-yl) ethyl, 2- (naphthalen-1-yl ) - ethyl, (naphthalen-2-yl) methyl, 1- (naphthalen-2-yl) ethyl, 2- (naphthalen-2-yl) ethyl, ([1,1'-biphenyl] -2 -yl) methyl, ([1,1'-biphenyl] -3-yl) methyl or a ([1,1'-biphenyi] -4-yl) methyl group.
Bei den Heteroaryl-Cι-C4-alkylen-Gruppen für die Reste Z und 11 kann es sich um eine Kombination der zuvor definierten Heteroaryl- und Cι-C4-Alkylengruppen, beispiels- weise eine (Pyridin-2-yl)methyl-, (Pyridin-3-yl)methyl-, (Pyridin-4-yl)methyl-, (Furan-2- yl)methyl-, (Furan-3-yI)methyl-, (Thien-2-yl)methyl-, (Thien-3-yl)methyl-, 2-(Thien-2- yl)ethyl- oder eine 2-(Thien-3-yl)ethylgruppe handeln.The heteroaryl-C 1 -C 4 -alkylene groups for the radicals Z and 11 may be a combination of the previously defined heteroaryl and C 1 -C 4 -alkylene groups, for example a (pyridin-2-yl) methyl- , (Pyridin-3-yl) methyl, (pyridin-4-yl) methyl, (furan-2-yl) methyl, (furan-3-yl) methyl, (thien-2-yl) methyl , (Thien-3-yl) methyl, 2- (thien-2-yl) ethyl or a 2- (thien-3-yl) ethyl group.
Bei den Aryloxy-d-C -alkylen-Gruppen für die Reste Z und Z' kann es sich um eine kombinierte Verknüpfung der zuvor definierten Aryl- und Cι-C4-Alkylengruppen über eine Etherfunktion (-O-), beispielsweise: eine Phenoxymethyl-, 1-Phenoxyethyl-, 2-Phenoxyethyl-, 1-Methyl-1-phenoxyethyl-, 3-Phenoxypropyl-, 4-Phenoxybutyl-, [(Naphthalin-1-yl)oxy]methyl-, 1-[(Naphthalin-1-yl)oxy]ethyl-, 2-[(Naphthalin-1-yl)oxy]- ethyl-, [(Naphthalin-2-yl)oxy]methyl-, 1-[(Naphthalin-2-yl)oxy]ethyl-, 2-[(Naphthalin-2-yl)- oxyjethyl-, [([1 ,1 '-Biphenyl]-2-yl)oxy]methyl-, [([1 ,1 '-Biphenyl]-3-yl)oxy]methyl- oder eine [([1 ,1 '-Biphenyl]-4-yl)oxy]methyl-Gruppe handeln.The aryloxy-dC-alkylene groups for the radicals Z and Z 'may be a combined linkage of the previously defined aryl and C 1 -C 4 -alkylene groups via an ether function (-O-), for example: a phenoxymethyl-, 1-phenoxyethyl, 2-phenoxyethyl, 1-methyl-1-phenoxyethyl, 3-phenoxypropyl, 4-phenoxybutyl, [(naphthalen-1-yl) oxy] methyl, 1 - [(naphthalene-1 yl) oxy] ethyl, 2 - [(naphthalen-1-yl) oxy] ethyl, [(naphthalen-2-yl) oxy] methyl, 1 - [(naphthalen-2-yl) oxy] ethyl , 2 - [(naphthalen-2-yl) -oxyethyl, [([1, 1'-biphenyl] -2-yl) oxy] methyl, [([1, 1'-biphenyl] -3-yl) oxy] methyl or a [([1, 1 'biphenyl] -4-yl) oxy] methyl group.
Bei den Heteroaryloxy-d-C4-alkylen-Gruppen für die Reste Z und Z' kann es sich um eine kombinierte Verknüpfung der zuvor definierten Heteroaryl- und d-C4-Alkylen- gruppen über eine Etherfunktion (-O-), beispielsweise: eine [(Pyridin-2-yl)oxy]methyl-, [(Pyridin-3-yl)oxy]methyl- oder eine [(Pyridin-4-yl)oxy]methyl-Gruppe handeln. Bei den Aryl-Cι-C -alkylenoxy-Cι-C -alkylen-Gruppen für die Reste Z und 11 kann es sich um eine sequentiell kombinierte Verknüpfung der zuvor definierten Aryl- und Cι-C -Alkylengruppen über eine Etherfunktion (-O-) zu der Alkylengruppe, beispiels- weise: eine (Phenylmethoxy)methyl- oder eine 2-(Phenylmethoxy)ethyl-Gruppe handeln.The heteroaryloxy-dC 4 -alkylene groups for the radicals Z and Z 'may be a combined linkage of the previously defined heteroaryl and dC 4 -alkylene groups via an ether function (-O-), for example: a [( Pyridin-2-yl) oxy] methyl, [(pyridin-3-yl) oxy] methyl or a [(pyridin-4-yl) oxy] methyl group. The aryl-C 1 -C -alkyleneoxy-C 1 -C 4 -alkylene groups for the radicals Z and 11 may be a sequentially combined linkage of the previously defined aryl and C 1 -C 4 -alkylene groups via an ether function (-O-) to the alkylene group, for example: a (phenylmethoxy) methyl or a 2- (phenylmethoxy) ethyl group.
Bei dem Rest der Formel CpFqHr mit p = 1, 2, 3, 4, q > 1 und q + r = 2p + 1 für den Rest Z kann es sich um eine Trifluormethyl-, Pentafluorethyl-, Perfluorpropyl-, Perfluorbutyl- oder eine 2,2,2-Trif luorethyl-Gruppe handeln.The radical of the formula C p F q H r with p = 1, 2, 3, 4, q> 1 and q + r = 2p + 1 for the radical Z may be a trifluoromethyl, pentafluoroethyl, perfluoropropyl , Perfluorobutyl or a 2,2,2-Trif luorethyl group act.
Bevorzugt gemäß vorliegender Erfindung sind solche Verbindungen der allgemeinen Formel I., in denen:Preferred according to the present invention are those compounds of general formula I. in which:
A für eine Cyangruppe,A for a cyano group,
B für eine Trifluormethylgruppe, oderB is a trifluoromethyl group, or
AB zusammen für eine an den aromatischen Ring gebundene cyclische Gruppe der Formel lila,AB together for a cyclic group of the formula III attached to the aromatic ring,
lila purple
für einen der ganzzahligen Werte 1 (nur für den Fall, dass T Kohlenstoff darstellt), 2, 3, 4, 5, 6, 7 oder 8,for one of the integer values 1 (just in case T represents carbon), 2, 3, 4, 5, 6, 7 or 8,
i und j für den Wert 1 ,i and j for the value 1,
R und R' für ein Wasserstoffatom, Y für eine Carbonylgruppe -C(O)-, für eine Sulfonylgruppe -S(O)2-, für eineR and R 'represent a hydrogen atom, Y for a carbonyl group -C (O) -, for a sulfonyl group -S (O) 2 -, for a
Iminocarbonylgruppe -C(O)N(Z')-, für eine Iminosulfonylgruppe -S(0)2 N(Z')-, für eine lmino(thioxomethyl)gruppe -C(S)N(Z')-, für eine Oxy- carbonylimino(thioxomethyl)gruppe -C(S)N(Z')C(O)O-, für eine Oxycarbonyl- gruppe -C(O)O-, für eine Sulfanylcarbonylgruppe ~C(O)S-, undIminocarbonyl group -C (O) N (Z ') -, for an iminosulfonyl group -S (O) 2 N (Z') -, for an imino (thioxomethyl) group -C (S) N (Z ') -, for a Oxycarbonylimino (thioxomethyl) group -C (S) N (Z ') C (O) O-, for an oxycarbonyl group -C (O) O-, for a sulfanylcarbonyl group ~C (O) S-, and
Z und 11 unabhängig voneinander für eine unverzweigte Cι~C -Alkylgruppe oder verzweigte C3-C -Alkylgruppe, eine gegebenenfalls für eine mit einem Phenylrest substituierte C3-C6-Cycloalkylgruppe, eine (C3-C6-Cycloalkyl)-d-Z and II independently of one another represent an unbranched C 1 -C 4 -alkyl group or branched C 3 -C -alkyl group, an optionally substituted C 3 -C 6 -cycloalkyl group substituted by a phenyl radical, or a (C 3 -C 6 -cycloalkyl) -d -
C -alkylengruppe, eine verzweigte oder unverzweigte C2-C3-Alkenylgruppe eine d-C4-Alkoxy-, Cyan-, Phenylsulfanyl- oder Hydroxy-d-d-alkylen- gruppe, eine (2-Methoxyethoxy)methylgruppe, eine [2-(2-Methoxyethoxy)- ethoxyjmethylgruppe, eine 2-(2-Methoxyethoxy)ethylgruppe, eine 2-[2-(2- Methoxyethoxy)ethoxy]ethylgruppe, eine Cι-C4-Alkoxy-d-C4-alkylengruppe, eine d-C -Alkoxycarbonyl-Cι-C4-alkylengruppe, eine unsubstituierte oder mit bis zu drei verzweigten oder unverzweigten d-C -Alkyl-, C2-C -Alkenyl-, C3-C6-Cycloalkyl-, C3-C6-Cycloalkyloxy-, Phenyl-, Cyan-, Halogen-, Methoxy, Ethoxy-, Phenoxy-, Benzyloxy-, Methylsulfanyl-, Ethylsulfanyl-, Benzyl- sulfanyl-, Phenylsulfanyl-, Dimethylamino-, Acetylamino-, Trifluormethyl-,C alkylene group, a branched or unbranched C 2 -C 3 alkenyl group a dC 4 alkoxy, cyano, phenylsulfanyl or hydroxy-dd-alkylene group, a (2-methoxyethoxy) methyl group, a [2- (2 -Methoxyethoxy) - ethoxymethyl, a 2- (2-methoxyethoxy) ethyl group, a 2- [2- (2-methoxyethoxy) ethoxy] ethyl group, a -C-C 4 alkoxy-dC 4 -alkylene, a dC alkoxycarbonyl -C C 4 alkylene group, an unsubstituted or with up to three branched or unbranched dC alkyl, C 2 -C alkenyl, C 3 -C 6 cycloalkyl, C 3 -C 6 cycloalkyloxy, phenyl, Cyano, halogen, methoxy, ethoxy, phenoxy, benzyloxy, methylsulfanyl, ethylsulfanyl, benzylsulfanyl, phenylsulfanyl, dimethylamino, acetylamino, trifluoromethyl,
Trifluormethoxy-, Trifluormethylsulfanyl- oder Acetyl-Gruppen substituierte Aryl-, Heteroaryl-, Heterocyclyl-, Aryl-Cι-C -alkylen-, Heteroaryl-Cι-C4- alkylen-, Aryloxy-d-C -alkylen-, Heteroaryloxy-d-C -alkylen-, Aryl-d-C4- alkylenoxy-d-C -alkylen-Gruppe oder einen Rest der Formel CpFqHr mit p = 1, 2, 3, 4, q > 1 und q + r = 2p + 1 stehen, undTrifluoromethoxy, trifluoromethylsulfanyl or acetyl groups substituted aryl, heteroaryl, heterocyclyl, aryl-C-C-alkylene, heteroaryl-C 4 -alkylene, aryloxy-dC-alkylene, heteroaryloxy-dC-alkylene -, aryl-dC 4 - alkylenoxy-dC-alkylene group or a radical of the formula C p F q H r with p = 1, 2, 3, 4, q> 1 and q + r = 2p + 1, and
Z' zusätzlich zu den vorgenannten Definitionen für ein Wasserstoffatom steht. Für die Bildung von pharmazeutisch verträglichen Salzen der erfindungsgemäßen Verbindungen der allgemeinen Formel I. kommen, nach den dem Fachmann bekannten Methoden, als anorganische Säuren unter anderem Chlorwasserstoffsäure, Brom- wasserstoffsäure, Schwefelsäure und Phosphorsäure, Salpetersäure, als Carbonsäuren unter anderem Essigsäure, Propionsäure, Hexansäure, Octansäure, Decansäure, Oleinsäure, Stearinsäure, Maleinsäure, Fumarsäure, Bernsteinsäure, Benzoesäure, Ascorbinsäure, Oxalsäure, Salicylsäure, Weinsäure, Zitronensäure, Milchsäure, Glykolsäure Äpfelsäure, Mandelsäure, Zimtsäure, Glutaminsäure, Asparaginsäure, als Sulfonsäuren unter anderem Methansulfonsäure, Ethansulfonsäure, Toluolsulfonsäure, Benzolsulfonsäure sowie Naphthalinsulfonsäure in Betracht.Z 'is, in addition to the abovementioned definitions, a hydrogen atom. For the formation of pharmaceutically acceptable salts of the compounds of the general formula I. come, according to the methods known in the art, as inorganic acids, inter alia hydrochloric, hydrobromic, sulfuric and phosphoric acid, nitric acid, as carboxylic acids, inter alia, acetic acid, propionic acid, hexanoic acid , Octanoic, decanoic, oleic, stearic, maleic, fumaric, succinic, benzoic, ascorbic, oxalic, salicylic, tartaric, citric, lactic, glycolic, malic, mandelic, cinnamic, glutamic, aspartic, sulfonic acids, including methanesulfonic, ethanesulfonic Benzenesulfonic acid and naphthalenesulfonic into consideration.
Die nachstehend genannten erfindungsgemäßen Verbindungen der Beispiele 1 bis 745 sind besonders bevorzugt. The compounds according to the invention of Examples 1 to 745 mentioned below are particularly preferred.
Pharmakologische UntersuchungenPharmacological investigations
Die erfindungsgemäßen Verbindungen wurden in verschiedenen Modellen getestet. Die erfindungsgemäßen Verbindungen der allgemeinen Formel I zeichnen sich dadurch aus, dass es sich dabei um Verbindungen mit antiandrogener Wirkung handelt, die den Androgenrezeptor destabilisieren, das Prostatatumorwachstum hemmen, und gleichzeitig eine hohe, ggf. orale Bioverfügbarkeit aufweisen. Die in vitro Tests zu den Einflüssen auf die Aktivitäten des Androgenrezeptors wurden folgendermaßen durchgeführt:The compounds of the invention were tested in various models. The compounds of general formula I according to the invention are distinguished by the fact that they are antiandrogenic compounds which destabilize the androgen receptor, inhibit prostate tumor growth, and at the same time have a high, possibly oral bioavailability. The in vitro tests for the influences on the activity of the androgen receptor were carried out as follows:
In den hier aufgeführten Schemata wurden die folgenden Abkürzungen benutzt:The following abbreviations have been used in the schemes listed here:
Bicalutamid: Λ/-[4-Cyan-3-(trifluormethyl)phenyl]-3-[(4-fluorphenyl)sulfonyl]-2- hydroxy-2-methylpropanamid R1881: Methyltrienolon, 17ß-Hydroxy-17α-methylestra-4,9,11-trien-3-onBicalutamide: Λ / - [4-cyano-3- (trifluoromethyl) phenyl] -3 - [(4-fluorophenyl) sulfonyl] -2-hydroxy-2-methylpropanamide R1881: methyltrienolone, 17β-hydroxy-17α-methylestra-4, 9,11-triene-3-one
CPA: Cyproteronacetat, 17-(Acetyloxy)-6-chlor-1 ß,2ß-dihydro-3'H- cyclopropa[1 ,2]pregna-1 ,4,6-triene-3,20-dionCPA: cyproterone acetate, 17- (acetyloxy) -6-chloro-1β, 2β-dihydro-3'H-cyclopropa [1, 2] pregna-1, 4,6-triene-3,20-dione
Verbindung B: 4-[2,5-Dihydro-3-methyl-4-[4-[4-(methylsulfonyl)piperazin-1-yl]butyl]- 2,5-dioxo-1H-pyrrol-1-yl]-2-(trifluormethyl)benzonitril (Beispiel 117) Compound B: 4- [2,5-dihydro-3-methyl-4- [4- [4- (methylsulfonyl) piperazin-1-yl] butyl] -2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile (Example 117)
Modell 1 : DeStabilisierung des AR in LNCaP-Zellen durch TestsubstanzenModel 1: DeStabilization of AR in LNCaP cells by test substances
In einer 25 cm2 Zellkulturflasche werden 2*106 LNCaP-Zellen in 6 ml RPMI 1640 ohne Phenolrot mit 4 mM Glutamin und 5% Aktivkohle-behandeltem Serum (CCS) ausgesät und über Nacht bei 37°C, 5% CO2 in feuchter Atmosphäre kultiviert. Am nächsten Tag werden die Zellen mit der Testsubstanz bei einer Konzentration von 10 bzw. 1 μM behandelt, wobei die Endkonzentration des Lösungsmittels 0,5% DMSO beträgt. Als Kontrolle werden Zellen nur mit 0,5% DMSO behandelt. Nach einer Inkubationszeit von 24 Stunden erfolgt ein Mediumwechsel mit erneuter Substanzzugabe und weiteren 24 Stunden Inkubation. Nach 48 Stunden werden die Zellen mit PBS gewaschen, mit PBS/20mM EDTA abgelöst, nochmals mit PBS-Ca2+/Mg2+ gewaschen und anschließend für mindestens 2 Stunden als Zellpellet bei -80°C eingefroren. Danach wird das Zellpellet in 200 μl Lysepuffer (50 mM Tris/HCI pH 7,5; 150 mM NaCI, 1,5 mM MgCI2, 0,2% SDS, 10% Glycerin, 1 mM DTT, 0,01 x Complete-EDTA Proteaseinhibitoren (Röche, Mannheim)) resuspendiert und mit 10U Benzonase (Merck, Darmstadt) für 10 Minuten bei 4°C behandelt. Nach Zugabe von 5 mM EDTA wird unlösliches Material pelletiert und 25 μg des Zeliextraktes in einem 4-12% SDS-Polyacrylamidgel (Invitrogen) aufgetrennt. Anschließend werden die Proteine auf Nitrozellulose (HyBondECL, Amersham) transferiert und mit monoklonalen Antiköφern gegen den Androgenrezeptor (AR441 ; Santa Cruz Biotechnologies; 1 : 400 Verdünnung) und Aktin (lCN, 1:5000 - 1 : 20000 Verdünnung) inkubiert. Nach Inkubation mit dem Sekundärantikörper (anti mouse IgG-HRP, Amersham oder -AP, Invitrogen,) wird der Westemblot mittels Chemilumineszenz (ECL, Amersham; Western Breeze, Invitrogen) entwickelt und die Lichtsignale werden mit einem Chemilmager™ (Kodak) quantifiziert. Die Menge des Androgenrezeptors wird im Verhältnis zu Aktin als Prozent der DMSO- Kontrolle berechnet. In a 25 cm 2 cell culture flask, 2 × 10 6 LNCaP cells are seeded in 6 ml RPMI 1640 without phenol red with 4 mM glutamine and 5% charcoal-treated serum (CCS) and wet overnight at 37 ° C., 5% CO 2 Atmosphere cultivated. The next day, the cells are treated with the test substance at a concentration of 10 or 1 μM, the final concentration of the solvent being 0.5% DMSO. As a control, cells are treated with only 0.5% DMSO. After an incubation period of 24 hours, the medium is changed with renewed addition of the substance and a further 24 hours incubation. After 48 hours, the cells are washed with PBS, detached with PBS / 20 mM EDTA, washed again with PBS-Ca 2+ / Mg 2+ and then frozen for at least 2 hours as cell pellet at -80 ° C. Thereafter, the cell pellet is dissolved in 200 μl of lysis buffer (50 mM Tris / HCl pH 7.5, 150 mM NaCl, 1.5 mM MgCl 2 , 0.2% SDS, 10% glycerol, 1 mM DTT, 0.01 × Complete). EDTA protease inhibitors (Roche, Mannheim)) and treated with 10 U benzonase (Merck, Darmstadt) for 10 minutes at 4 ° C. After addition of 5 mM EDTA, insoluble material is pelleted and 25 μg of the cell extract are separated in a 4-12% SDS-polyacrylamide gel (Invitrogen). Subsequently, the proteins are transferred to nitrocellulose (HyBondECL, Amersham) and incubated with monoclonal antibodies to the androgen receptor (AR441, Santa Cruz Biotechnologies, 1: 400 dilution) and actin (ICN, 1: 5000-1: 20000 dilution). After incubation with the secondary antibody (anti mouse IgG-HRP, Amersham or -AP, Invitrogen,) the Western blot is developed by chemiluminescence (ECL, Amersham, Western Breeze, Invitrogen) and the light signals are quantitated with a Chemilmager ™ (Kodak). The amount of androgen receptor is calculated relative to actin as a percentage of the DMSO control.
Tabelle 1 zeigt die Wirkung ausgewählter Testsubstanzen bei Konzentrationen von 10 bzw. 1 μM auf den Gehalt an Androgenrezeptorprotein in der humanen Prostatazelllinie LNCaP. Die Angaben entsprechen dem prozentualen Anteil des AR-Gehaltes von Zel- len, die nur mit dem Lösungsmittel DMSO behandelt wurden (=Kontrolle). Die Behandlung der Zellen mit den aufgeführten Testsubstanzen führt bei einer Behandlungskonzentration von 10μM zu einer Erniedrigung des AR-Gehaltes bis zu einem Fünftel der Kontrolle (22% bei Beispiel 248: 4-[2,5-Dihydro-3-[6-[4-(2-methoxybenzoyl)piperazin-1- yl]hexyl]-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2-(trifluormethyl)benzonitril). Die Vergleichs- Substanz Bicalutamid beeinflusst den AR-Gehalt nicht, während das synthetische Androgen R1881 das AR-Protein stabilisiert. Letzteres ist aus der Literatur bekannt (J. A. Kemppainen et. al. J. Biol. Chem. 1992, 267, 968-974).Table 1 shows the effect of selected test substances at concentrations of 10 and 1 μM on the content of androgen receptor protein in the human prostate cell line LNCaP. The data correspond to the percentage of the AR content of cells which were treated only with the solvent DMSO (= control). Treatment of the cells with the test substances listed results in a reduction in the AR content to a fifth of the control at a treatment concentration of 10 μM (22% in Example 248: 4- [2,5-dihydro-3- [6- [4 - (2-methoxybenzoyl) piperazin-1-yl] hexyl] -4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile). The comparative substance bicalutamide does not affect the AR content, while the synthetic androgen R1881 stabilizes the AR protein. The latter is known from the literature (J.A. Kemppainen et al, J. Biol. Chem. 1992, 267, 968-974).
Beispiel 248: 4-[2,5-Dihydro-3-[6-[4-(2-methoxybenzoyl)piperazin-1-yl]hexyl]-4-methyl- 2,5-dioxo-1H-pyrrol-1-yl]-2-(trifluormethyl)benzonitril und Beispiel 629: 4-[3-[5-[4-(Ethyl- sulfonyl)piperazin-1-yl]pentyl]-4,4-dimethyl-5-oxo-2-thioxoimidazolidin-1-yl]-2-(trifluor- methyl)benzonitril reduzieren den AR-Gehalt auch bei einer Konzentration von 1 μM auf einen Wert bis zur Hälfte der Kontrolle. Durch die Erniedrigung des AR-Gehaltes, die vermutlich durch eine Destabilisierung des AR-Proteins erfolgt, soll die inhibitorische Wirkung der Antihormone auf die Zellproliferation noch verstärkt werden. Example 248: 4- [2,5-Dihydro-3- [6- [4- (2-methoxybenzoyl) piperazin-1-yl] hexyl] -4-methyl-2,5-dioxo-1H-pyrrole-1 yl] -2- (trifluoromethyl) benzonitrile and Example 629: 4- [3- [5- [4- (ethylsulfonyl) piperazin-1-yl] pentyl] -4,4-dimethyl-5-oxo-2- thioxoimidazolidin-1-yl] -2- (trifluoromethyl) benzonitrile reduce the AR content even at a concentration of 1 μM to a value up to half of the control. By lowering the AR content, which probably takes place by a destabilization of the AR protein, the inhibitory effect of the anti-hormones on cell proliferation is to be enhanced.
Tab. 1. AR-Gehalt (%) in LNCaP-Zellen nach Behandlung mit ausgewählten TestsubstanzenTab. 1. AR content (%) in LNCaP cells after treatment with selected test substances
Modell 2: Inhibition der Proliferation von LNCaP-Zellen Model 2: Inhibition of proliferation of LNCaP cells
Für den Proliferationsassay werden 6000 LNCaP-Zellen/well in einer Microtiterplatte (96-well) in 50 μl RPMI1640-Medium mit 5% CCS ausgesät und wie in Modell 1 kulti- viert. Nach 24 Stunden erhalten die Zellen 50 μl zweifach konzentrierte in Kulturmedium verdünnte Testsubstanz. Die Lösungsmittelkonzentration beträgt 0,5% DMSO. Nach 4 Tagen erhalten die Zellen weitere 100 μl einfach-konzentrierte, in Kulturmedium verdünnte Testsubstanz. Nach 7 - 8 Tagen wird die Proliferationsrate der Zellen mittels Kristallviolettassay bestimmt (Gillies et al. Anal. Biochem. 1986, 159, 109-113). Für die Bestimmung des Antagonismus wird die Substanzbehandlung in Gegenwart von 0,1 nM R1881 durchgeführt (1 : 1000 Verdünnung aus ethanolischer Lösung). Kontrollzellen erhalten nur 0,5% DMSO. Für den Agonismus werden die Zellen nur mit Testsubstanz (ohne R1881) behandelt.For the proliferation assay, 6000 LNCaP cells / well are seeded in a microtiter plate (96-well) in 50 μl RPMI1640 medium with 5% CCS and cultured as in model 1. After 24 hours, the cells receive 50 μl of doubly concentrated test substance diluted in culture medium. The solvent concentration is 0.5% DMSO. After 4 days, the cells receive another 100 .mu.l single-concentrated, diluted in culture medium test substance. After 7 to 8 days, the proliferation rate of the cells is determined by crystal violet assay (Gillies et al., Anal. Biochem., 1986, 159, 109-113). For the determination of antagonism, the substance treatment is carried out in the presence of 0.1 nM R1881 (1: 1000 dilution from ethanolic solution). Control cells receive only 0.5% DMSO. For agonism, the cells are treated only with test substance (without R1881).
Tabelle 2 zeigt die inhibitorische Wirkung von Testsubstanzen auf die Proliferation der humanen androgenabhängigen Prostatazelllinie LNCaP. Die Inhibition der Zellprolife- ration ist eine wichtige Vorraussetzung für den therapeutischen Einsatz der Substanzen bei der Behandlung des Prostatakarzinoms. Sieben ausgewählte erfindungsgemäße AR-destabilisierende Testsubstanzen inhibieren die Zeilproliferation in Gegenwart von 0,1 nM des synthetischen Androgens R1881 mit einer ähnlichen bis deutlich niedrigeren IC50, wie das zugelassene nichtsteroidale Antiandrogen Bicalutamid. Bei einer Substanzkonzentration von 1 μM ist die Proliferation verglichen mit dem Zellwachstum in Gegenwart von 0,1 nM R1881 um mindestens 80% reduziert. Beispiel 696: S-Methyl 4- [6-[3-[4-cyan-3-(trifluormethyl)phenyl]-5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1- yl]hexyl]piperazin-1-carbothioat und Beispiel 653: 4-[4,4-Dimethyl-3-[6-[4-(2-methyl-1- oxopropyl)piperazin-1-yl]hexyl]-5-oxo-2-thioxoimidazolidin-1-yl]-2-(trifluormethyl)benzo- nitril blockieren das Wachstum bei dieser Konzentration vollständig, während Bicalutamid unter diesen Bedingungen nur eine Inhibition von 85% erreicht. Bis zu einer getesteten Konzentration von 10 μM wurde bei keiner der sieben Testsubstanzen eine proliferationsstimulierende Wirkung beobachtet. Tab. 2. Inhibition der Proliferation von LNCaP-Zellen durch Testsubstanzen.Table 2 shows the inhibitory effect of test substances on the proliferation of the human androgen-dependent prostate cell line LNCaP. The inhibition of cell proliferation is an important prerequisite for the therapeutic use of the substances in the treatment of prostate cancer. Seven selected AR destabilizing test compounds of the present invention inhibit cell proliferation in the presence of 0.1 nM of the synthetic androgen R1881 with a similar to significantly lower IC50 than the approved nonsteroidal antiandrogen bicalutamide. At a substance concentration of 1 μM, proliferation is reduced by at least 80% compared to cell growth in the presence of 0.1 nM R1881. Example 696: S-Methyl 4- [6- [3- [4-cyano-3- (trifluoromethyl) phenyl] -5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1-yl] hexyl] piperazine-1 carbothioate and Example 653: 4- [4,4-dimethyl-3- [6- [4- (2-methyl-1-oxopropyl) piperazin-1-yl] hexyl] -5-oxo-2-thioxoimidazolidine-1 -yl] -2- (trifluoromethyl) benzonitrile completely blocks growth at this concentration, whereas bicalutamide only achieves an inhibition of 85% under these conditions. Up to a tested concentration of 10 μM, no proliferation-stimulating effect was observed in any of the seven test substances. Tab. 2. Inhibition of the proliferation of LNCaP cells by test substances.
Tab. 3. (Fortsetzung) Inhibition der Proliferation von LNCaP-Zellen durch Testsubstanzen. Tab. 3. (continued) Inhibition of the proliferation of LNCaP cells by test substances.
Modell 3: Inhibition der Proliferation anderer Zellenlinien, die nicht aus der Prostata stammenModel 3: Inhibition of the proliferation of other non-prostate cell lines
Zur Untersuchung der wachstumsinhibierenden Wirkung von Testsubstanzen in Zellen, die nicht prostatischen Ursprungs sind, wurden MaTu-, MaTu/Adr-, HaCaT- und A431- Zellen mit Testsubstanzen behandelt, wobei MaTu: humane MammakarzinomzelllinieTo study the growth-inhibiting effect of test substances in non-prostatic cells, MaTu, MaTu / Adr, HaCaT and A431 cells were treated with test substances, with MaTu: human mammary carcinoma cell line
MaTu/Adr: Adriamycin-resistente MaTu-Zelllinie HaCaT: humane FibroblastenzellinieMaTu / Adr: Adriamycin-resistant MaTu cell line HaCaT: human fibroblast cell line
A-431: humane Epidermiszellline bedeutet.A-431: human epidermis cell line.
Je nach Zelllinie wurden 1000-4000 Zellen/well in RPMI 1640- (A431; MaTu und MaTu/Adr) oder DMEM/HAM'SF12-Medium (HaCaT) ohne Phenolrot mit 2 mM L- Glutamin und 10% CCS ausgesät und nach 24 Stunden Inkubation mit verschiedenen Konzentrationen in Kulturmedium verdünnten Testsubstanzen behandelt. Nach 3- tägiger Behandlungsdauer wurde die Anzahl der Zellen mittels Kristallviolettassay, wie in Modell 2, bestimmt. Die Lösungsmittelkontrolle enthielt 0,1% Ethanol.Depending on the cell line, 1000-4000 cells / well were seeded in RPMI 1640 (A431, MaTu and MaTu / Adr) or DMEM / HAM'SF12 medium (HaCaT) without phenol red with 2 mM L-glutamine and 10% CCS and after 24 Hours incubation with various concentrations in culture medium diluted test substances. After 3 days of treatment, the number of cells was determined by crystal violet assay as in Model 2. The solvent control contained 0.1% ethanol.
Tabelle 3 zeigt die Auswirkung selektiver Testsubstanzen auf die Proliferation von humanen Zellen, die nicht von der Prostata abstammen. Die Substanzen wurden bei einer Konzentration von 10 μM getestet und die Angaben entsprechen dem prozentualen Anteil des Zellwachstums der Lösungsmittelkontrolle. Es zeigt sich, dass die Testsubstanzen keine, in Einzelfällen geringe inhibitorische Wirkung auf die vier verschiedenen Zellinien hatten. Die Vergleichssubstanz Bicalutamid zeigte unter den gegebenen Versuchsbedingungen eine geringfügige Inhibition in allen Zelllinien außer MaTu. Dieses Ergebnisse weisen darauf hin, dass die antiproliferative Wirkung der Testsubstanzen androgenrezeptorabhängig ist, und dass auch bei hohen Substanzkonzentrationen im mikromolaren Bereich keine sekundären zytotoxischen Wirkungen auftreten. Tab.4. Wirkung selektiver Testsubstanzen auf die Proliferation von Nicht- Prostatazellen bei einer Konzentration von 10 μM.Table 3 shows the effect of selective test substances on the proliferation of non-prostate-derived human cells. The substances were tested at a concentration of 10 μM and the data correspond to the percentage of cell growth of the solvent control. It turns out that the test substances had no, in some cases low, inhibitory effect on the four different cell lines. The reference substance bicalutamide showed a slight inhibition in all cell lines except MaTu under the given experimental conditions. These results indicate that the antiproliferative effect of the test substances is androgen receptor-dependent, and that no secondary cytotoxic effects occur even at high concentrations of micromolar substances. Table 4. Effect of selective test substances on the proliferation of non-prostate cells at a concentration of 10 μM.
Modell 4: Antiandrogene Wirkung selektiver Testsubstanzen auf das Wachstum der akzessorischen Geschlechtsdrüsen der MausModel 4: Antiandrogenic effect of selective test substances on the growth of accessory sex glands of the mouse
Die Funktion und die Größe der akzessorischen Geschlechtsdrüsen (Prostata und Samenblase) sind abhängig von Androgenen. Bei kastrierten Tieren wird durch Andro- genapplikation ein Wachstum dieser Organe induziert. Die gleichzeitige Behandlung mit Antiandrogenen hemmt dieses Wachstum dosisabhängig. Für die Prüfung der Testsubstanzen wurden die Mäuse kastriert. Am gleichen Tag wurde die Behandlung mit Testosteronpropionat (0.03 mg/Maus) und den Testsubstanzen (2 x täglich 30 mg/kg s.c. in Benzylbenzoat-Rizinusöl (10:90) formuliert). Die Behandlung erfolgte über 7 Tage und zum Versuchsabschluss wurden die Gewichte von Samenblase und Prostata bestimmt. Die prozentuale Hemmung des Samenblasenwachstums wurde in Bezug auf die Kontrollgruppen (mit und ohne Testosteron) berechnet. Als Referenzsubstanz wurde Cyproteronacetat (30 mg/kg s.c.) eingesetzt.The function and size of the accessory sexual glands (prostate and seminal vesicle) are dependent on androgens. In castrated animals, androgen application induces growth of these organs. Concomitant treatment with antiandrogens inhibits this growth dose-dependently. For testing the test substances, the mice were castrated. On the same day, the treatment with testosterone propionate (0.03 mg / mouse) and the test substances (twice daily 30 mg / kg s.c. in benzyl benzoate castor oil (10:90) was formulated). The treatment took place over 7 days and at the end of the trial the weights of seminal vesicle and prostate were determined. The percentage inhibition of seminal vesicle growth was calculated with respect to the control groups (with and without testosterone). Cyproterone acetate (30 mg / kg s.c.) was used as reference substance.
Die Ergebnisse sind in der Tabelle 4 dargestellt.The results are shown in Table 4.
Die Behandlung mit den Testsubstanzen Beispiel 629: 4-[3-[5-[4-(Ethylsulfonyl)- piperazin-1-yl]pentyl]-4,4-dimethyl-5-oxo-2-thioxoimidazolidin-1-yI]-2-(trifluormethyl)- benzonitril und Beispiel 546: 4-[4,4-Dimethyl-3-[4-[4-(2-methyl-1-oxopropyl)pipera∑in-1- yl]butyl]-5-oxo-2-thioxoimidazolidin-1-yl]-2-(trifluormethyl)benzonitril führte zu einer fast 100% Hemmung des Wachstums der Samenblase, während die Behandlung mit der Referenzsubstanz Cyproteronacetat nur zu einer Hemmung von 85% führte. Auch die Hemmwerte für Bicalutamid, ermittelt in vorangegangenen Versuchen, lagen nur bei 86%. Treatment with the test substances Example 629: 4- [3- [5- [4- (ethylsulfonyl) -piperazin-1-yl] pentyl] -4,4-dimethyl-5-oxo-2-thioxoimidazolidin-1-yl] -2- (trifluoromethyl) benzonitrile; and Example 546: 4- [4,4-dimethyl-3- [4- [4- (2-methyl-1-oxopropyl) -piperacin-1-yl] -butyl] -5 oxo-2-thioxoimidazolidin-1-yl] -2- (trifluoromethyl) benzonitrile resulted in almost 100% inhibition of seminal vesicle growth, whereas treatment with the reference substance cyproterone acetate resulted in only 85% inhibition. The inhibition values for bicalutamide, determined in previous experiments, were only 86%.
Tab. 4. Wirkung selektiver Testsubstanzen auf das Testosteron stimulierte Wachstum der Samenblase bei einer Dosierung von 2 x 30 mg/kg.Tab. 4. Effect of selective test substances on the testosterone stimulated growth of the seminal vesicle at a dosage of 2 x 30 mg / kg.
Modell 5: Antiandrogene Wirkung einer selektiven Testsubstanz auf das Wachstum von humanen Prostatakarzinomxenografts in vivoModel 5: Antiandrogenic effect of a selective test substance on the growth of human prostate carcinoma xenografts in vivo
In der vorliegenden Erfindung wurde die Wirkung des erfindungsgemäßen Beispiel 117: 4-[2,5-Dihydro-3-methyi-4-[4-[4-(methylsulfonyl)piperazin-1-yl]butyl]-2,5-dioxo-1H- pyrroI-1-yl]-2-(trifluormethyl)benzonitril auf das Tumorwachstum in vivo mittels Maus- Xenograft-Modellen untersucht, bei denen die erfindungsgemäße Verbindung kontinuierlich subkutan verabreicht wurden.In the present invention, the effect of Inventive Example 117 was: 4- [2,5-dihydro-3-methyl-4- [4- [4- (methylsulfonyl) piperazin-1-yl] butyl] -2,5-dioxo -1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile was assayed for tumor growth in vivo by mouse xenograft models in which the compounds of the invention were administered continuously subcutaneously.
Das CWR22 Tumormodell [M. A. Wainstein, F. He, D. Robinson, H. J. Kung, S. Schwartz, J. M. Giaconia, N. L Edgehouse, T. P. Pretlow, D. R. Bodner, E. D. Kursh, Cancer Res. 1994, 1 ; 54(23), 6049-52] ist ein hormonabhängiges humanes Prostatakarzinommodell. Das Tumormodell wurde durch „serial passaging" von Prostatakarzinomgewebe, das während einer OP entnommen wurde, auf immun- defizienten Nacktmäusen etabliert und weiter propagiert. Das androgenabhängige LNCaP Prostatakarzinommodell wurde ebenfalls von einem Patiententumor etabliert. Dieses Tumormodell wächst sowohl in Zellkultur als auch als Xenotransplantat auf immundefizienten Mäusen (Culig, Hoffmann B t. J. Cancer, 1999, 242-251). Für Therapieversuche wurden 6 Wochen alte männliche Nacktmäuse, (NMRI-Maus, M&B, Bomholdtgard, Denmark) mit Testosteron-Pellets (12,5 mg, 90 Tage Freisetzung; IRA, Sarasota, FL) supplementiert. Den Tieren wurden entweder LNCaP Zellen (1.5 x 106 Zellen ) oder kleine CWR22 Tumorfragmente (2 x 2 mm) subkutan in die linke Flanke implantiert . Nachdem die Tumoren eine Größe von 20-25 mm2 erreicht hatten, wurde die Behandlung mit der Erfindungssubstanz begonnen. [M. A. Wainstein, F. He, D. Robinson, H. J. Kung, S. Schwartz, J. M. Giaconia, N. L. Edgehouse, T. P. Pretlow, D. R. Bodner, E. D. Kursh, Cancer Res. 1994, 1; 54(23), 6049-52]. Die Ergebnisse sind in den Diagrammen 1 und 2 dargestellt.The CWR22 Tumor Model [MA Wainstein, F. He, D. Robinson, HJ Kung, S. Schwartz, JM Giaconia, N.L Edgehouse, TP Pretlow, DR Bodner, ED Kursh, Cancer Res. 1994, 1; 54 (23), 6049-52] is a hormone-dependent human prostate carcinoma model. The tumor model was established and propagated on immune-deficient nude mice by serial passaging of prostate cancer tissue taken during surgery.The androgen-dependent LNCaP prostate cancer model was also established by a patient tumor, a tumor model that grows both in cell culture and as a xenograft immunodeficient mice (Culig, Hoffmann Bt, J. Cancer, 1999, 242-251). For therapeutic trials, 6-week-old male nude mice (NMRI mouse, M & B, Bomholdtgard, Denmark) were supplemented with testosterone pellets (12.5 mg, 90-day release; IRA, Sarasota, FL). The animals were implanted with either LNCaP cells (1.5 x 10 6 cells) or small CWR22 tumor fragments (2 x 2 mm) subcutaneously in the left flank. After the tumors reached a size of 20-25 mm 2 , the treatment with the invention substance was started. [MA Wainstein, F. He, D. Robinson, HJ Kung, S. Schwartz, JM Giaconia, NL Edgehouse, TP Pretlow, DR Bodner, ED Kursh, Cancer Res. 1994, 1; 54 (23), 6049-52]. The results are shown in Diagrams 1 and 2.
Diagramm 1. Wachstumshemmung von LNCaP Prostatakarzinomen durch Substanz B. Die Behandlung erfolgte 2 x täglich s.c. mit 30 mg/kg.Diagram 1. Growth inhibition of LNCaP prostate cancer by substance B. Treatment was performed 2 x daily s.c. with 30 mg / kg.
Während in den unbehandelten Kontrolltieren der Tumor schnell wächst führt die Behandlung mit der Erfindungssubstanz zu einer deutlichen Wachstumshemmung der Prostatatumoren. Sowohl im CWR22-, als auch im LNCaP-Tumor ist diese Wachstumshemmung vergleichbar mit den Effekten der Kastration. While the tumor grows rapidly in the untreated control animals, the treatment with the substance of the invention leads to a significant growth inhibition of the prostate tumors. In both the CWR22 and LNCaP tumors, this growth inhibition is comparable to the effects of castration.
Diagramm 2: Wachstumshemmung von CWR22 Prostatakarzinomen durch Substanz B. Die Behandlung erfolgte 2 x täglich s.c. mit 30 mg/kg.Diagram 2: Growth inhibition of CWR22 prostate carcinoma by substance B. The treatment was carried out twice a day s.c. with 30 mg / kg.
In beiden Modellen ist die Hemmung des Tumorwachstums der Behandlung mit dem Antiandrogen Bicalutamid überlegen. Die Ergebnisse der Versuche in den Prostatakarzinom-Modellen zeigen eine Hemmung des Tumorwachstums durch die erfindungsgemäße Verbindung.In both models, inhibition of tumor growth is superior to treatment with antiandrogen bicalutamide. The results of the experiments in the prostate carcinoma models show an inhibition of tumor growth by the compound according to the invention.
In der vorliegenden Erfindung wurde die Wirkung von einer erfindungsgemäßen Verbindung auf das Tumorwachstum in vivo mittels eines Maus-Xenograft-Modells untersucht, bei dem die erfindungsgemäße Verbindung 2 x täglich über den gesamten Behandlungszeitraum subkutan verabreicht wurde. Im Vergleich zu den unbehandelten Kontrolltieren resultierte eine Hemmung des Tumorwachstums. Retardation des Tumor- Wachstums zeigte sich als signifikant in kastrierten Mäusen. Die Behandlung wurde gut vertragen.In the present invention, the effect of a compound of the invention on tumor growth in vivo was examined by means of a mouse xenograft model in which the compound of the invention was administered subcutaneously twice daily for the entire treatment period. Compared to the untreated control animals resulted in an inhibition of tumor growth. Retardation of tumor growth was found to be significant in castrated mice. The treatment was well tolerated.
Die vorliegende Erfindung zeigt, dass die erfindungsgemäße Verbindung eine Inhibition des Prostatatumorwachstums verursacht, die der von Bicalutamid überlegen ist. DosierungThe present invention shows that the compound of the present invention causes inhibition of prostate tumor growth superior to that of bicalutamide. dosage
Im allgemeinen sind zufriedenstellende Resultate zu erwarten, wenn die täglichen Dosen einen Bereich von 5 μg bis 50 mg der erfindungsgemäßen Verbindung pro kg Körpergewicht umfassen. Bei größeren Säugetieren, beispielsweise dem Menschen, liegt eine empfohlene tägliche Dosis im Bereich von 10 μg bis 30 mg pro kg Körpergewicht. Geeignete Dosierungen für die erfindungsgemäßen Verbindungen betragen von 0,005 bis 50 mg pro Tag pro kg Körpergewicht, je nach Alter und Konstitution des Patienten, wobei die notwendige Tagesdosis durch Einmal- oder Mehrfachabgabe appliziert werden kann.In general, satisfactory results are expected when the daily doses range from 5 μg to 50 mg of the compound of the invention per kg of body weight. For larger mammals, such as humans, a recommended daily dose is in the range of 10 μg to 30 mg per kg body weight. Suitable dosages for the compounds according to the invention are from 0.005 to 50 mg per day per kg of body weight, depending on the age and constitution of the patient, wherein the necessary daily dose can be administered by single or multiple delivery.
Die Formulierung der pharmazeutischen Präparate auf Basis der neuen Verbindungen erfolgt in an sich bekannter Weise, indem man den Wirkstoff mit den in der Galenik ge- bräuchlichen Trägersubstanzen, Füllstoffen, Zerfallsbeeinflussem, Bindemitteln, Feuchthaltemitteln, Gleitmitteln, Absorptionsmitteln, Verdünnungsmitteln, Geschmacks- korrigentien, Färbemitteln usw. verarbeitet und in die gewünschte Applikationsform überführt. Dabei ist auf Remington's Pharmaceutical Science, 15tn ed. Mack Publishing Company, East Pennsylvania (1980) hinzuweisen.The formulation of the pharmaceutical compositions based on the novel compounds is carried out in a manner known per se by mixing the active ingredient with the excipients which are commonly used in galenicals, fillers, disintegrants, binders, humectants, lubricants, absorbents, diluents, flavoring agents, colorants processed and converted into the desired application form. It is made to Remington's Pharmaceutical Science, 15 tn ed. Mack Publishing Company, pointing East Pennsylvania (1980).
Für die orale Applikation kommen insbesondere Tabletten, Dragees, Kapseln, Pillen, Pulver, Granulate, Pastillen, Suspensionen, Emulsionen oder Lösungen in Frage. Für die parenterale Applikation sind Injektions- und Infusionszubereitungen möglich. Für die intraartikuläre Injektion können entsprechend zubereitete Kristallsuspensionen ver- wendet werden. Für die intramuskuläre Injektion können wässrige und ölige Injektionslösungen oder Suspensionen und entsprechende Depotpräparationen Verwendung finden. Für die rektale Applikation können die neuen Verbindungen in Form von Supposito- rien, Kapseln, Lösungen (z.B. in Form von Klysmen) und Salben sowohl zur systemischen als auch zur lokalen Therapie verwendet werden. Für die topische Auftragung sind Formulierungen in Gelen, Salben, Fettsalben, Cremes, Pasten, Puder, Milch und Tinkturen möglich. Die Dosierung der Verbindungen der allgemeinen Formel I sollte in diesen Zubereitungen 0,01% - 20% betragen um eine ausreichende pharmakologische Wirkung zu erzielen. Die topische Anwendung kann auch mittels eines transdermalen Systems beispielsweise eines Pflasters erfolgen. Die Erfindung umfasst ebenfalls die erfindungsgemäßen Verbindungen der allgemeinen Formel I als therapeutischen Wirkstoff. Weiterhin gehören zur Erfindung die erfindungsgemäßen Verbindungen der allgemeinen Formel I als therapeutische Wirkstoffe zusammen mit pharmazeutisch verträglichen und annehmbaren Hilfsstoffen und Trägerstoffen. Ebenfalls umfasst die Erfindung eine pharmazeutische Zusammensetzung, die eine der pharmazeutisch aktiven, erfindungsgemäßen Verbindungen oder deren Gemisch und ein pharmazeutisch verträgliches Salz oder pharmazeutisch verträgliche Hilfsstoffe und Trägerstoffe enthält.For oral administration in particular tablets, dragees, capsules, pills, powders, granules, lozenges, suspensions, emulsions or solutions in question. For parenteral administration, injection and infusion preparations are possible. For intraarticular injection, appropriately prepared crystal suspensions may be used. For intramuscular injection, aqueous and oily injection solutions or suspensions and corresponding depot preparations can be used. For rectal administration, the new compounds can be used in the form of suppositories, capsules, solutions (eg in the form of enemas) and ointments for both systemic and local therapy. For topical application, formulations in gels, ointments, greases, creams, pastes, powders, milk and tinctures are possible. The dosage of the compounds of the general formula I should be 0.01% -20% in these preparations in order to achieve a sufficient pharmacological effect. The topical application can also take place by means of a transdermal system, for example a plaster. The invention likewise encompasses the compounds of general formula I according to the invention as therapeutic active ingredient. Furthermore, the invention compounds of the general formula I according to the invention as therapeutic agents together with pharmaceutically acceptable and acceptable excipients and carriers. The invention also encompasses a pharmaceutical composition containing one of the pharmaceutically active compounds of the invention or mixtures thereof and a pharmaceutically acceptable salt or excipients and excipients.
Gegenstand der vorliegenden Erfindung sind deshalb auch pharmazeutische Zusammensetzungen, die mindestens eine Verbindung der allgemeinen Formel I enthalten, gegebenenfalls zusammen mit pharmazeutisch verträglichen Hilfs- und/oder Trägerstoffen.The present invention therefore also pharmaceutical compositions containing at least one compound of the general formula I, optionally together with pharmaceutically acceptable excipients and / or carriers.
Diese pharmazeutischen Zusammensetzungen und Arzneimittel können zur oralen, rektalen, subkutanen, transdermalen, perkutanen, intravenösen oder intramuskulären Applikation vorgesehen sein. Sie enthalten neben üblichen Träger- und/oder Verdünnungsmitteln mindestens eine Verbindung der allgemeinen Formel I. Die Arzneimittel der Erfindung werden mit den üblichen festen oder flüssigen Trägerstoffen oder Verdünnungsmitteln und den üblicherweise verwendeten pharmazeutischtechnischen Hilfsstoffen entsprechend der gewünschten Applikationsart mit einer geeigneten Dosierung in bekannter Weise hergestellt. Die bevorzugten Zubereitungen bestehen aus einer Darreichungsform, die zur oralen Applikation geeignet ist. Solche Darreichungsformen sind beispielsweise Tabletten, Filmtabletten, Dragees, Kapseln, Pillen, Pulver, Lösungen oder Suspensionen oder auch Depotformen. Die pharmazeutischen Zusammensetzungen, die mindestens eine der erfindungsgemäßen Verbindungen enthalten, werden bevorzugt oral appliziert. Es kommen auch parenterale Zubereitungen wie Injektionslösungen in Betracht. Weiterhin seien als Zubereitungen beispielsweise auch Suppositorien genannt.These pharmaceutical compositions and pharmaceutical compositions may be for oral, rectal, subcutaneous, transdermal, percutaneous, intravenous or intramuscular administration. In addition to customary carriers and / or diluents they contain at least one compound of the general formula I. The pharmaceuticals of the invention are prepared in a known manner with the usual solid or liquid carriers or diluents and the commonly used pharmaceutical excipients according to the desired mode of administration with a suitable dosage , The preferred formulations consist of a dosage form which is suitable for oral administration. Such dosage forms are, for example, tablets, coated tablets, dragees, capsules, pills, powders, solutions or suspensions or depot forms. The pharmaceutical compositions containing at least one of the compounds of the invention are preferably administered orally. There are also parenteral preparations such as injection solutions into consideration. Further examples of preparations which may be mentioned are suppositories.
Entsprechende Tabletten können beispielsweise durch Mischen des Wirkstoffs mit bekannten Hilfsstoffen, beispielsweise inerten Verdünnungsmitteln wie Dextrose, Zucker, Sorbit, Mannit, Polyvinylpyrrolidon, Sprengmitteln wie Maisstärke oder Algin- säure, Bindemitteln wie Stärke oder Gelatine, Gleitmitteln wie Magnesiumstearat oder Talk und/oder Mitteln zur Erzielung eines Depoteffektes wie Carboxylpolymethylen, Carboxylmethylcellulose, Celluloseacetatphthalat oder Polyvinylacetat, erhalten werden. Die Tabletten können auch aus mehreren Schichten bestehen. Entsprechend können Dragees durch Überziehen von analog den Tabletten hergestellten Kernen mit üblicherweise in Drageeüberzügen verwendeten Mitteln, beispiels- weise Polyvinylpyrrolidon oder Schellack, Gummiarabicum, Talk, Titanoxid oder Zucker, hergestellt werden. Dabei kann auch die Drageehülle aus mehreren Schichten bestehen, wobei die oben bei den Tabletten erwähnten Hilfsstoffe verwendet werden können.Corresponding tablets can be prepared, for example, by mixing the active compound with known auxiliaries, for example inert diluents such as dextrose, sugar, sorbitol, mannitol, polyvinylpyrrolidone, disintegrants such as corn starch or alginic acid, binders such as starch or gelatin, lubricants such as magnesium stearate or talc and / or Achieving a depot effect such as carboxyl polymethylene, Carboxylmethylcellulose, cellulose acetate phthalate or polyvinyl acetate. The tablets can also consist of several layers. Coated tablets can accordingly be produced by coating cores produced analogously to the tablets with agents customarily used in tablet coatings, for example polyvinylpyrrolidone or shellac, gum arabic, talc, titanium oxide or sugar. In this case, the dragee wrapper can also consist of several layers, wherein the auxiliaries mentioned above in the case of the tablets can be used.
Lösungen oder Suspensionen mit den erfindungsgemäßen Verbindungen der allgemeinen Formel I können zusätzlich geschmacksverbessernde Mittel wie Saccharin, Cyclamat oder Zucker sowie z. B. Aromastoffe wie Vanillin oder Orangenextrakt enthalten. Sie können außerdem Suspendierhilfsstoffe wie Natriumcarboxymethylcellulose oder Konservierungsstoffe wie p-Hydroxybenzoate enthalten.Solutions or suspensions with the compounds of general formula I according to the invention may additionally taste-improving agents such as saccharin, cyclamate or sugar and z. B. flavorings such as vanillin or orange extract. They may also contain suspending aids such as sodium carboxymethylcellulose or preservatives such as p-hydroxybenzoates.
Die Verbindungen der allgemeinen Formel I enthaltenden Kapseln können beispielsweise hergestellt werden, indem man die Verbindung(en) der allgemeinen Formel I mit einem inerten Träger wie Milchzucker oder Sorbit mischt und in Gelatinekapseln einkapselt.The capsules containing the compounds of the general formula I can be prepared, for example, by mixing the compound (s) of the general formula I with an inert carrier such as lactose or sorbitol and encapsulating it in gelatine capsules.
Geeignete Suppositorien lassen sich beispielsweise durch Vermischen mit dafür vorgesehenen Trägermitteln wie Neutralfetten oder Polyethylenglykol bzw. deren Derivaten herstellen.Suitable suppositories can be prepared, for example, by mixing with suitable carriers such as neutral fats or polyethylene glycol or derivatives thereof.
Die erfindungsgemäßen Verbindungen können zur Therapie von Prostatakarzinomen mit einem oder mehreren der folgenden Wirkstoffen kombiniert verabreicht werden:The compounds according to the invention can be administered combined with one or more of the following active substances for the treatment of prostate carcinomas:
1) Gonadrotrophormon (GnRH) Agonisten1) Gonadrotrophormone (GnRH) agonists
2) 5α-Reduktase Hemmer wie Finasterid2) 5α-reductase inhibitors such as finasteride
3) Zytostatika3) cytostatics
4) VEGF-Kinase-Inhibitoren 5) Antigestagene4) VEGF kinase inhibitors 5) Antigestagens
6) Antiestrogene6) Antiestrogens
7) Antisense Oligonukleotide7) antisense oligonucleotides
8) EGF-Antikörper8) EGF antibodies
9) Estrogene Es ist auch möglich, bei der Behandlung des Prostatakarzinoms mit den erfindungsgemäßen Verbindungen, deren Anwendung mit einer an sich bekannten Methode der kli- nischen Radiologie zu kombinieren. (Laverdiere J. et al., 1997, Intl. J. of Rad. One. Biol. Phys., 37, 247-252; Bolla M. et al., 1997, New Engl. J. Med., 337, 95-300.) Darüber hinaus können die erfindungsgemäßen Verbindungen der allgemeinen Formel I zur Therapie und Prophylaxe weiterer oben nicht genannter Krankheits- zustände eingesetzt werden.9) Estrogens It is also possible in the treatment of prostate carcinoma with the compounds according to the invention, the application of which with a method known per se of to combine niche radiology. (Laverdiere J. et al., 1997, Intl. J. of Rad. One, Biol. Phys., 37, 247-252; Bolla M. et al., 1997, New Engl. J. Med., 337, 95 -300.) In addition, the compounds of general formula I according to the invention for the therapy and prophylaxis of other disease states not mentioned above can be used.
Die erfindungsgemäßen Verbindungen der allgemeinen Formel I lassen sich wie nachstehend beschrieben herstellen. Die vorliegende Erfindung betrifft auch die Zwischenprodukte der allgemeinen Formel VIIThe compounds of the general formula I according to the invention can be prepared as described below. The present invention also relates to the intermediates of general formula VII
V-W-(CH2)n— I VIIVW- (CH 2 ) n - I VII
sowie der allgemeinen Formel VIIIand the general formula VIII
worinwherein
V für einen substituierten aromatischen Rest der allgemeinen Formel II steht,V is a substituted aromatic radical of the general formula II,
worin wherein
A für eine Acetylgruppe, eine Acetylaminogruppe, eine Cyangruppe, eine Nitrogruppe, eine Trifluormethylgruppe oder ein Halogen (Fluor, Chlor),A is an acetyl group, an acetylamino group, a cyano group, a nitro group, a trifluoromethyl group or a halogen (fluorine, chlorine),
B für ein Wasserstoff atom, ein Halogen (Fluor, Chlor) oder eineB is a hydrogen atom, a halogen (fluorine, chlorine) or a
Trifluormethylgruppe, oder A und B zusammen für eine an den aromatischen Ring gebundene cyclische Gruppe der Formel III oder IV, wobei E für eine Methylengruppe oder ein Sauerstoffatom steht,Trifluoromethyl group, or A and B together represent a cyclic group of the formula III or IV attached to the aromatic ring, where E is a methylene group or an oxygen atom,
W für einen Heterocyclus der Formel V,W is a heterocycle of the formula V,
V worinIn which
T T für Kohlenstoff steht, und zwischen Q und T eine Doppelbindung vorliegt, sowie Q eine Gruppe =C(CH3)~ und U Sauerstoff bedeuten,TT is carbon, and between Q and T is a double bond, and Q is a group = C (CH 3 ) ~ and U is oxygen,
n einen der ganzzahligen Werte 1, 2, 3, 4, 5, 6, 7, 8 annehmen kann,n can assume one of the integer values 1, 2, 3, 4, 5, 6, 7, 8,
i und j unabhängig voneinander für die Werte 1 und 2 stehen, wobei i + j die Werte 2 oder 3 annehmen kann,i and j are independently of one another the values 1 and 2, where i + j can assume the values 2 or 3,
R und R' unabhängig voneinander ein Wasserstoffatom oder eine Methylgruppe sein können,R and R 'may independently be a hydrogen atom or a methyl group,
sowie die Zwischenprodukte der allgemeinen Formel VII und der allgemeinen Formel VIII, worin A und B zusammen für eine an den aromatischen Ring gebundene cyclische Gruppe der Formel IM oder IV, wobei E für eine Methylengruppe oder ein Sauerstoffatom steht,as well as the intermediates of general formula VII and general formula VIII, wherein A and B together represent a cyclic group of the formula IM or IV attached to the aromatic ring, where E is a methylene group or an oxygen atom,
W für einen Heterocyclus der Formel V,W is a heterocycle of the formula V,
V worinIn which
T für Stickstoff steht, und zwischen Q und T eine Einfachbindung vorliegt, sowie Q eine Gruppe -C(CH3)2- und U Schwefel bedeuten,T is nitrogen, and there is a single bond between Q and T, and Q is a group -C (CH 3 ) 2 - and U is sulfur,
n einen der ganzzahligen Werte 4, 5, 6, 7, 8 annehmen kann,n can assume one of the integer values 4, 5, 6, 7, 8,
i und j unabhängig voneinander für die Werte 1 und 2 stehen, wobei i + j die Werte 2 oder 3 annehmen kann,i and j are independently of one another the values 1 and 2, where i + j can assume the values 2 or 3,
R und R' unabhängig voneinander ein Wasserstoffatom oder eineR and R 'independently represent a hydrogen atom or a
Methylgruppe sein können.Be methyl group.
Die vorliegende Erfindung wird anhand der nachfolgenden Beispiele näher erläutert, ohne sie darauf einzuschränken. SyntheseschemataThe present invention will be further illustrated by the following examples without being limited thereto. synthetic schemes
Nach folgendem Schema können Maleimid-Derivate der Kettenlängen n = 4 bis 8 hergestellt werden:Maleimide derivatives of chain lengths n = 4 to 8 can be prepared according to the following scheme:
Villa Reagenzien: (a) BrMg(CH2)nCI, CuBr-Me2S, THF, dann Mel, HMPT, THF; (b) LiOH, H2O, THF, dann HCI, Extraktion; (c) Anilinderivat, EtOH, MS 4Ä; (d) NaI, Ethylmethyl- keton; (e) THF; (f) Trifluoressigsäure, CH2CI2; (g) NEt3, THF. Nach folgendem Schema können Maleimid-Derivate der Kettenlängen n = 1 bis 8 hergestellt werden:Villa Reagents: (a) BrMg (CH 2 ) n CI, CuBr-Me 2 S, THF, then Mel, HMPT, THF; (b) LiOH, H 2 O, THF, then HCl, extraction; (c) aniline derivative, EtOH, MS 4E; (d) NaI, ethyl methyl ketone; (e) THF; (f) trifluoroacetic acid, CH 2 Cl 2 ; (g) NEt 3 , THF. Maleimide derivatives of chain lengths n = 1 to 8 can be prepared according to the following scheme:
Reagenzien: (b) LiOH, H2O, THF, dann HCI, Extraktion; (c) Anilinderivat, EtOH, MS 4Ä;; (e) THF; (f) Trifluoressigsäure, CH2CI2; (g) NEta, THF; (h) BrMg(CH2)mCH=CH2, CuBr-Me2S, THF, dann Mel, HMPT, THF; (i) BrMg(CH2)nOPG, CuBr-Me2S, THF, dann Mel, HMPT, THF; (PG = Schutzgruppe); (j) Entschützung; (k) 9-BBN, dann NaOH, H2O2; (I) OsO4; (m) NalO ; (n) Na(OAc)3BH; (s) Imidazol, lod, Triphenylphosphin. Nach folgendem Schema können Thiohydantoin-Derivate der Kettenlängen n = 4 bis 8 hergestellt werden:Reagents: (b) LiOH, H 2 O, THF, then HCl, extraction; (c) aniline derivative, EtOH, MS 4E ;; (e) THF; (f) trifluoroacetic acid, CH 2 Cl 2 ; (g) NEta, THF; (h) BrMg (CH 2 ) m CH = CH 2 , CuBr-Me 2 S, THF, then Mel, HMPT, THF; (i) BrMg (CH 2 ) n OPG, CuBr-Me 2 S, THF, then Mel, HMPT, THF; (PG = protecting group); (j) deprotection; (k) 9-BBN, then NaOH, H 2 O 2 ; (I) OsO 4 ; (m) NalO; (n) Na (OAc) 3 BH; (s) imidazole, iodine, triphenylphosphine. Thiohydantoin derivatives of chain lengths n = 4 to 8 can be prepared according to the following scheme:
p, q p, q
r, dr, d
Reagenzien: (d) NaI, Ethylmethylketon; (e) THF; (f) Trifluoressigsäure, CH2CI2; (g) NEt3, THF; (o) CSCI2, H2O; (p) NEfe, THF; (q) 4M HCI; (r) RSO2CI, NEt,, CH2CI2. Nach folgendem Schema können Thiohydantoin-Derivate der Kettenlängen n = 2 bis 8 hergestellt werden:Reagents: (d) NaI, ethyl methyl ketone; (e) THF; (f) trifluoroacetic acid, CH 2 Cl 2 ; (g) NEt 3 , THF; (o) CSCI 2 , H 2 O; (p) NEfe, THF; (q) 4M HCl; (r) RSO 2 Cl, NEt ,, CH 2 Cl 2 . Thiohydantoin derivatives of chain lengths n = 2 to 8 can be prepared according to the following scheme:
p, q p, q
y-v R' Vlllby-v R 'VIIIb
Z— N=0 Z— N=S Z— COCI z— so2cιZ- N = 0 Z- N = SZ- COCI z- so 2 cι
ZO— COCI ZS— COCI ZZ'N-COCI ZZ'N— S02CI Z(CO)— N=SZO-COCI ZSCOCI ZZ'N-COCI ZZ'N- S0 2 CI Z (CO) - N = S
Reagenzien: (f) Trifluoressigsäure, CH2CI2; (g) NEts, THF; (o) CSCI2, H2O; (p) NEts, THF; (q) 4M HCI. HerstellungsverfahrenReagents: (f) trifluoroacetic acid, CH 2 Cl 2 ; (g) Nths, THF; (o) CSCI 2 , H 2 O; (p) nts, THF; (q) 4M HCI. production method
Beispiel 1example 1
1,1-Dimethylethyl 4-r5-ri-r4-cvan-3-(trifluormethyl)phenyll-2.5-dihydro-4-methyl-2,5- dioxo-1H-pyrrol-3-yl1pentvnpiperazin-1-carboxylat1,1-Dimethylethyl 4-r5-ri-r4-van-3- (trifluoromethyl) -phenyl-2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-3-yl-1-pentapnazine-1-carboxylate
1 a) Dimethyl (Z)-2-(5-chlorpentyl)-3-methyl-2-butendicarboxylat1 a) Dimethyl (Z) -2- (5-chloropentyl) -3-methyl-2-butenedicarboxylate
Zur Herstellung eines Grignardreagenzes wurden unter Stickstoffatmosphäre 4,1 g Magnesiumspäne in 22 ml Tetrahydrofuran vorgelegt, mit 31,3 g 1-Brom-5-chlorpentan in 200 ml Tetrahydrofuran versetzt und 1 Stunde bei Raumtemperatur gerührt. Diese Mischung wurde dann unter Stickstoffatmosphäre und Rühren bei -35 bis -40 °C zu einer Suspension von 34,7 g Kupfer(l)-bromid-Dimethylsulfidkomplex in 700 ml Tetrahydrofuran getropft und weitere 2 Stunden bei -40 °C gerührt. Anschließend wurde auf -65 bis -70 °C abgekühlt und bei dieser Temperatur unter Rühren eine Lösung von 20 g Dimethyl acetylendicarboxylat und 48 ml Hexamethylphosphorsäuretriamid in 290 ml Tetrahydrofuran zugetropft, nach 5 Minuten eine Lösung von 95 ml Hexamethylphosphorsäuretriamid in 95 ml Tetrahydrofuran bei -65 bis -70 °C zugegeben, weitere 5 Minuten bei dieser Temperatur gerührt, 100 g lodmethan in 280 ml Tetrahydrofuran zugetropft und diese Mischung über Nacht auf Raumtemperatur erwärmt. Zur Aufarbeitung wurde unter Rühren auf -60 °C abgekühlt, 410 ml gesättigte Ammoniumchloridlösung (mit konzentrierter Ammoniak-Lösung auf pH 8 eingestellt) zugetropft, auf Raumtemperatur erwärmt und 45 Minuten bei Raumtemperatur gerührt. Diese Mischung wurde viermal mit Ethylacetat extrahiert, die vereinigten organischen Phasen mit gesättigter Ammoniumchloridlösung (mit konzentrierter Ammoniaklösung auf pH 8 eingestellt) gewaschen bis die organische Phase hellblau und mit dann mit Wasser gewaschen bis die organische Phase farblos war. Nach Waschen mit gesättigter Natrium- chloridlösung, Trocknen über Natriumsulfat und Einengen wurde mit Ethylacetat/Hexan an Kieselgel chromatographiert und so 10,0 g der Titelverbindung neben 7,2 g Dimethyl (£)-2-(5-chlorpentyl)-3-methyl-2-butendicarboxylat jeweils als gelbliches Öl erhalten.To prepare a Grignard reagent, 4.1 g of magnesium turnings in 22 ml of tetrahydrofuran were placed under nitrogen atmosphere, treated with 31.3 g of 1-bromo-5-chloropentane in 200 ml of tetrahydrofuran and stirred for 1 hour at room temperature. This mixture was then added dropwise under nitrogen atmosphere and stirring at -35 to -40 ° C to a suspension of 34.7 g of copper (I) bromide-dimethyl sulfide complex in 700 ml of tetrahydrofuran and stirred at -40 ° C for a further 2 hours. It was then cooled to -65 to -70 ° C and added dropwise at this temperature with stirring, a solution of dimethylacetylenedicarboxylate 20 g and 48 ml of hexamethylphosphoric triamide in 290 ml of tetrahydrofuran, after 5 minutes, a solution of 95 ml of hexamethylphosphoric triamide in 95 ml of tetrahydrofuran at -65 added to -70 ° C, stirred for a further 5 minutes at this temperature, added dropwise 100 g of iodomethane in 280 ml of tetrahydrofuran and this mixture was warmed to room temperature overnight. For work-up, the mixture was cooled to -60 ° C. with stirring, 410 ml of saturated ammonium chloride solution (adjusted to pH 8 with concentrated ammonia solution), warmed to room temperature and stirred at room temperature for 45 minutes. This mixture was extracted four times with ethyl acetate, the combined organic phases with saturated ammonium chloride solution (adjusted to pH 8 with concentrated ammonia solution) until the organic phase was light blue and then washed with water until the organic phase was colorless. After washing with saturated sodium chloride solution, drying over sodium sulfate and concentration, the residue was chromatographed on silica gel with ethyl acetate / hexane to give 10.0 g of the title compound in addition to 7.2 g of dimethyl (ε) -2- (5-chloropentyl) -3-methyl -2-butenedicarboxylate each obtained as a yellowish oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 3,76 s (3H, OCH3); 3,75 s (3H, OCH3); 3,53 t (J=6,5 Hz, 2H, CH2CI); 2,35 tbr (J=7 Hz, 2H, CH2Olefin); 1 ,95 s (3H, CH3); 1,78 m (2H, CH2); 1,47 m (4H, CH2). 1 b) 3-(5-Chlorpentyl)-4-methyl-2,5-furandion 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 3.76 s (3H, OCH 3 ); 3.75 s (3H, OCH 3 ); 3.53 t (J = 6.5 Hz, 2H, CH 2 Cl); 2.35 tbr (J = 7 Hz, 2H, CH 2 olefin); 1, 95 s (3H, CH3); 1.78 m (2H, CH 2 ); 1.47 m (4H, CH 2 ). 1 b) 3- (5-chloropentyl) -4-methyl-2,5-furandione
Zu einer unter einer Stickstoffatmosphäre gerührten Lösung von 7,16 g (Z)-Dimethyl 2- (5-chlorpentyl)-3-methyl-2-butendicarboxylat wurden 86 ml Wasser sowie 164 ml einer Lösung von Lithiumhydroxid in Wasser (1 mol/l) gegeben und 2 d bei Raumtemperatur gerührt. Zur Aufarbeitung wurde eingeengt, der Rückstand in 290 ml Wasser gelöst, unter Eisbadkühlung mit Salzsäure (2 mol/l) auf pH 2 eingestellt und dreimal mit Diethylether extrahiert. Die vereinigten organischen Phasen wurden mit gesättigter Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, eingeengt und so die Titelverbindung als gelbliches Öl erhalten.To a stirred under a nitrogen atmosphere solution of 7.16 g of (Z) -dimethyl 2- (5-chloropentyl) -3-methyl-2-butenedicarboxylate 86 ml of water and 164 ml of a solution of lithium hydroxide in water (1 mol / l ) and stirred for 2 d at room temperature. For working up, the mixture was concentrated, the residue dissolved in 290 ml of water, adjusted with ice-bath cooling with hydrochloric acid (2 mol / l) to pH 2 and extracted three times with diethyl ether. The combined organic phases were washed with saturated sodium chloride solution, dried over sodium sulfate, concentrated and the title compound was obtained as a yellowish oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 3,54 t (J=6,5 Hz, 2H, CH2CI); 2,48 tbr (J=7,5 Hz, 2H, CH2Olefin); 2,08 sbr (3H, CH3); 1,81 m (2H, CH2); 1,63 m (2H, CH2); 1,51 m (2H, CH2). 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 3.54 t (J = 6.5 Hz, 2H, CH 2 Cl); 2.48 tbr (J = 7.5 Hz, 2H, CH 2 olefin); 2.08 sbr (3H, CH 3); 1.81 m (2H, CH 2 ); 1.63 m (2H, CH 2 ); 1.51 m (2H, CH 2 ).
1c) 4-[3-(5-Chlorpentyl)-2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril1c) 4- [3- (5-Chloropentyl) -2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Eine Mischung von 9,46 g 3-(5-Chlorpentyl)-4-methyl-2,5-furandion und 8,13 g 4- Amino-2-(trifluormethyl)benzonitril in 22 ml Ethanol wurde unter einer Stickstoffatmosphäre mit 2,5 g aktiviertem Molsieb (0,3 nm) versetzt und 2 d bei 90 °C gerührt. Zur Aufarbeitung wurde das Molsieb nach dem Abkühlen abfiltriert, mit Ethanol gewaschen und die vereinigten Ethanol-Lösungen eingeengt. Der Rückstand wurde in Ethylacetat aufgenommen und mit Wasser sowie gesättigter Natriumchloridlösung gewaschen. Nach Trocknen über Natriumsulfat und Einengen wurde mit Ethylacetat/Hexan/Toluol an Kieselgel chromatographiert und so 11 ,69 g der Titelverbindung als weißer Feststoff erhalten.A mixture of 9.46 g of 3- (5-chloropentyl) -4-methyl-2,5-furandione and 8.13 g of 4-amino-2- (trifluoromethyl) benzonitrile in 22 ml of ethanol was added under a nitrogen atmosphere with 2, 5 g of activated molecular sieve (0.3 nm) and stirred at 90 ° C for 2 d. For workup, the molecular sieve was filtered off after cooling, washed with ethanol and concentrated the combined ethanol solutions. The residue was taken up in ethyl acetate and washed with water and saturated sodium chloride solution. After drying over sodium sulfate and concentration, it was chromatographed on silica gel with ethyl acetate / hexane / toluene to give 11.69 g of the title compound as a white solid.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,06 sbr (1H, aryl); 7,91 s (2H, aryl); 3,56 t (J=7 Hz, 2H, CH2CI); 2,53 t (J=7,5 Hz, 2H, CH2Olefin); 2,11 s (3H, CH3); 1 ,83 m (2H, CH2); 1 ,69-1,50 m (4H, CH2). 1d) 4-[2,5-Dihydro-3-(5-iodpentyl)-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.06 sbr (1H, aryl); 7.91 s (2H, aryl); 3.56 t (J = 7 Hz, 2H, CH 2 Cl); 2.53 t (J = 7.5 Hz, 2H, CH 2 olefin); 2.11 s (3H, CH3); 1.83 m (2H, CH 2 ); 1, 69-1.50 m (4H, CH 2 ). 1d) 4- [2,5-Dihydro-3- (5-iodopentyl) -4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Eine Mischung von 11,68 g 4-[3-(5-Chlorpentyl)-2,5-dihydro-4-methyl-2,5-dioxo-1H- pyrrol-1-yl]-2-(trifluormethyl)benzonitril und 18,2 g Natriumiodid in 180 ml Ethylmethylketon wurde unter einer Stickstoffatmosphäre 19 Stunden bei 80 °C gerührt. Nach dem Abkühlen wurde mit Ethylacetat verdünnt und mit Wasser sowie gesättigter Natrium- chloridlösung gewaschen. Nach Trocknen über Natriumsulfat und Einengen wurde so 11 ,26 g der Titelverbindung als weißer Feststoff erhalten.A mixture of 11.68 g of 4- [3- (5-chloropentyl) -2,5-dihydro-4-methyl-2,5-dioxo-1 H -pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile and 18.2 g of sodium iodide in 180 ml of ethyl methyl ketone was stirred under a nitrogen atmosphere at 80 ° C for 19 hours. After cooling, it was diluted with ethyl acetate and washed with water and saturated sodium chloride solution. After drying over sodium sulfate and concentration, 11.26 g of the title compound were obtained as a white solid.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,06 sbr (1 H, aryl); 7,91 s (2H, aryl); 3,20 t (J=7 Hz, 2H, CH2I); 2,52 t (J=7,5 Hz, 2H, CH2Olefin); 2,11 s (3H, CH3); 1,86 m (2H, CH2); 1,63 m (2H, CH2); 1,50 m (2H, CH2). 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.06 sbr (1 H, aryl); 7.91 s (2H, aryl); 3.20 t (J = 7 Hz, 2H, CH 2 I); 2.52 t (J = 7.5 Hz, 2H, CH 2 olefin); 2.11 s (3H, CH3); 1.86 m (2H, CH 2 ); 1.63 m (2H, CH 2 ); 1.50 m (2H, CH 2 ).
1e) 1,1-Dimethylethyl 4-[5-[1-[4-cyan-3-(trifluormethyl)phenyl]-2,5-dihydro-4-methyl- 2,5-dioxo-1H-pyrrol-3-yl]pentyl]piperazin-1-carboxylat1e) 1,1-dimethylethyl 4- [5- [1- [4-cyano-3- (trifluoromethyl) phenyl] -2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrole-3 yl] pentyl] piperazine-1-carboxylate
Zu einer Lösung von 2,0 g 4-[2,5-Dihydro-3-(5-iodpentyl)-4-methyl-2,5-dioxo-1/V-pyrrol- 1-yl]-2-(trifluormethyl)benzonitril in 53 ml Tetrahydrofuran wurde unter einer Stickstoffatmosphäre 1,56 g 1,1-Dimethylethyl piperazin-1-carboxylat gegeben und diese Mischung 7 d bei Raumtemperatur gerührt. Zur Aufarbeitung wurde mit Ethylacetat ver- dünnt und mit halbgesättigter Natriumhydrogencarbonatlösung gewaschen. Nach Trocknen über Natriumsulfat und Einengen wurde mit Methanol/Dichlormethan an Kieselgel chromatographiert und so 2,2 g der Titelverbindung als gelbliches Öl erhalten.To a solution of 2.0 g of 4- [2,5-dihydro-3- (5-iodopentyl) -4-methyl-2,5-dioxo-1 / V-pyrrol-1-yl] -2- (trifluoromethyl ) Benzonitrile in 53 ml of tetrahydrofuran was added under a nitrogen atmosphere 1.56 g of 1,1-dimethylethyl piperazine-1-carboxylate and this mixture was stirred for 7 d at room temperature. For work-up, it was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After drying over sodium sulfate and concentration was chromatographed on silica gel with methanol / dichloromethane to obtain 2.2 g of the title compound as a yellowish oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,06 sbr (1H, aryl); 7,90 m (2H, aryl); 3,43 m (4H, Piperazin); 2,50 tbr (J=7,5 Hz, 2H, CH2Olefin); 2,40-2,31 m (4H, Piperazin); 2,40-2,31 m (2H, CH2Piperazin); 2,09 s (3H, CH3); 1,66-1,36 m (6H, CH2); 1,45 s (9H, CH3). Beispiel 2 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.06 sbr (1H, aryl); 7.90 m (2H, aryl); 3.43 m (4H, piperazine); 2.50 tbr (J = 7.5 Hz, 2H, CH 2 olefin); 2.40-2.31 m (4H, piperazine); 2.40-2.31 m (2H, CH 2 piperazine); 2.09 s (3H, CH3); 1.66-1.36 m (6H, CH 2 ); 1.45 s (9H, CH 3). Example 2
4-r2,5-Dihydro-3-methyl-2.5-dioxo-4-[5-(piperazin-1-yl')pentvn-1 -/-pyrrol-1-yl1-2- (trifluormethvDbenzonitril4-r2,5-dihydro-3-methyl-2,5-dioxo-4- [5- (piperazin-1-yl ' ) pentyn-1 - / - pyrrol-1-yl1-2- (trifluoromethylbenzonitrile
Zu einer Lösung von 4,5 g 1,1-DimethylethyI 4-[5-[1-[4-cyan-3-(trifluormethyl)phenyl]- 2,5-dihydro-4-methyl-2,5-dioxo-1ry-pyrrol-3-yl]pentyl]piperazin-1-carboxylat in 120 ml Dichlormethan wurden unter einer Stickstoffatmosphäre und Eisbadkühlung 60 ml Trifluoressigsäure zugetropft und 1 Stunde bei Raumtemperatur gerührt. Zur Aufarbeitung wurde die Reaktionslösung mit 250 ml Toluol verdünnt und die Mischung eingeengt. Der Rückstand wurde in Ethylacetat aufgenommen und mit gesättigter Natriumhydrogencarbonatlösung gewaschen. Nach Trocknen über Natriumsulfat und Einengen wurde mit Methanol/Dichlormethan an Kieselgel chromatographiert und so 3,5 g der Titelverbindung als weißer Feststoff erhalten.To a solution of 4.5 g of 1,1-dimethylethyl 4- [5- [1- [4-cyano-3- (trifluoromethyl) phenyl] -2,5-dihydro-4-methyl-2,5-dioxo 1yr-pyrrol-3-yl] pentyl] -piperazine-1-carboxylate in 120 ml of dichloromethane was added dropwise under a nitrogen atmosphere and ice bath cooling 60 ml of trifluoroacetic acid and stirred for 1 hour at room temperature. For workup, the reaction solution was diluted with 250 ml of toluene and the mixture was concentrated. The residue was taken up in ethyl acetate and washed with saturated sodium bicarbonate solution. After drying over sodium sulfate and concentration was chromatographed on silica gel with methanol / dichloromethane to obtain 3.5 g of the title compound as a white solid.
1H-NMR (300 MHz, CD3OD): δ [ppm] = 8,13 dbr (J=2 Hz, 1 H, aryl); 8,08 dbr (J=8,5 Hz, 1 H, aryl); 8,01 dd (J=8,5 Hz + 2 Hz, 1 H, aryl); 3,18 m (4H, Piperazin); 2,69 m (4H, Piperazin); 2,53 tbr (J=7,5 Hz, 2H, CH2Olefin); 2,47 tbr (J=7,5 Hz, 2H, CH2Piperazin); 2,07 s (3H, CH3); 1 ,69-1,53 m (4H, CH2); 1 ,44 m (2H, CH2). 1 H NMR (300 MHz, CD 3 OD): δ [ppm] = 8.13 dbr (J = 2 Hz, 1 H, aryl); 8.08 dbr (J = 8.5 Hz, 1H, aryl); 8.01 dd (J = 8.5 Hz + 2 Hz, 1H, aryl); 3.18 m (4H, piperazine); 2.69 m (4H, piperazine); 2.53 tbr (J = 7.5 Hz, 2H, CH 2 olefin); 2.47 tbr (J = 7.5 Hz, 2H, CH 2 piperazine); 2.07s (3H, CH 3 ); 1, 69-1.53 m (4H, CH 2 ); 1.44m (2H, CH 2 ).
Beispiel 3Example 3
4-r2.5-Dihvdro-3-methyl-4-r5-[4-f2-(methylsulfanvnphenvnpiperazin-1-vnpentyll-2.5- dioxo-1H-pyrrol-1-yll-2-(trifluormethyDbenzonitril4-r2,5-Dihydro-3-methyl-4-r5- [4-f2- (methylsulfanphenphenylpiperazine-1-pentnyl-2,5-dioxo-1H-pyrrol-1-yl-2- (trifluoromethyldbenzonitrile
Zu einer Lösung von 10 mg 4-[2,5-Dihydro-3-(5-iodpentyl)-4-methyl-2,5-dioxo-1 -/- pyrrol-1-yl]-2-(trifluormethyl)benzonitril in 0,4 ml Tetrahydrofuran wurden 9 mg 1-(2- Thiomethylphenyl)piperazin in 0,5 ml Tetrahydrofuran gegeben und die Mischung 2 d bei Raumtemperatur gerührt. Zur Aufarbeitung wurde die Reaktionsmischung mit Ethylacetat verdünnt und mit halbgesättigter Natriumhydrogencarbonatlösung gewaschen. Nach Einengen der organischen Phase wurde mit Methanol/Dichlormethan an Kieselgel chromatographiert und so 6 mg der Titelverbindung als gelbliches Öl erhalten.To a solution of 10 mg of 4- [2,5-dihydro-3- (5-iodopentyl) -4-methyl-2,5-dioxo-1 - / - pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile in 0.4 ml of tetrahydrofuran was added 9 mg of 1- (2-thiomethylphenyl) piperazine in 0.5 ml of tetrahydrofuran and the mixture was stirred for 2 d at room temperature. For work-up, the reaction mixture was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After concentration of the organic phase was chromatographed on silica gel with methanol / dichloromethane to obtain 6 mg of the title compound as a yellowish oil.
ESI-MS: 557. Beispiel 4ESI MS: 557. Example 4
4-r3-r5-r4-(4-Cvanbenzoyl)piperazin-1-yllpentvn-215-dihydro-4-methyl-2,5-dioxo-1/-/- pyrrol-1-yll-2-(trifluormethyl)benzonitril4-r3-r5-r4- (4-vanbenzoyl) -piperazin-1-yl-pentene-2 1 5-dihydro-4-methyl-2,5-dioxo-1 / - / - pyrrol-1-yl-2- (trifluoromethyl benzonitrile)
Zu einer Lösung von 9 mg 4-[2,5-Dihydro-3-methyl-2,5-dioxo-4-[5-(piperazin-1-yl)- pentyl]-1 -/-pyrrol-1-yl]-2-(trifluormethyI)benzonitril in 0,4 ml Tetrahydrofuran wurden 0,2 ml einer Lösung von Triethylamin in Tetrahydrofuran (1,5 mol/l) und 7 mg 4-Cyan- benzoylchlorid in 0,4 ml Tetrahydrofuran gegeben und die Mischung 8 Stunden bei Raumtemperatur gerührt. Zur Aufarbeitung wurde die Reaktionsmischung mit Ethyl- acetat verdünnt und mit halbgesättigter Natriumhydrogencarbonatlösung gewaschen. Nach Einengen der organischen Phase wurde mit Methanol/Dichlormethan an Kieselgel chromatographiert und so 7 mg der Titelverbindung als gelbliches Öl erhalten.To a solution of 9 mg of 4- [2,5-dihydro-3-methyl-2,5-dioxo-4- [5- (piperazin-1-yl) -pentyl] -1- / -pyrrol-1-yl ] -2- (trifluoromethyl) benzonitrile in 0.4 ml of tetrahydrofuran, 0.2 ml of a solution of triethylamine in tetrahydrofuran (1.5 mol / l) and 7 mg of 4-cyanobenzoyl chloride in 0.4 ml of tetrahydrofuran were added and the Mixture stirred for 8 hours at room temperature. For workup, the reaction mixture was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After concentration of the organic phase was chromatographed on silica gel with methanol / dichloromethane to give 7 mg of the title compound as a yellowish oil.
ESI-MS: 564.ESI MS: 564.
Beispiel δExample δ
4-[3-r5-r4-[(3-Fluorphenyl)sulfonyl1piperazin-1-vnpentyl1-2,5-dihvdro-4-methyl-2,5-dioxo- 1 y-pyrrol-1 -yl]-2-(trif luormethyl)benzonitril4- [3-r5-r4 - [(3-Fluorophenyl) sulfonyl-1-piperazine-1-pentyl-2,5-dihydro-4-methyl-2,5-dioxo-1-yl-pyrrol-1-yl] -2- ( trifluoromethyl) benzonitrile
Zu einer Lösung von 9 mg 4-[2,5-Dihydro-3-methyl-2,5-dioxo-4-[5-(piperazin-1- yl)pentyl]-1H-pyrrol-1-yl]-2-(trifluormethyl)benzonitril in 0,4 ml Tetrahydrofuran wurden 0,2 ml einer Lösung von Triethylamin in Tetrahydrofuran (1,5 mol/l) und 8 mg 3-Fluor- phenylsulfonylchlorid in 0,4 ml Tetrahydrofuran gegeben und die Mischung 8 Stunden bei Raumtemperatur gerührt. Zur Aufarbeitung wurde die Reaktionsmischung mit Ethylacetat verdünnt und mit halbgesättigter Natriumhydrogencarbonatlösung gewaschen. Nach Einengen der organischen Phase wurde mit Methanol/Dichlormethan an Kieselgel chromatographiert und so 6 mg der Titelverbindung als weißer Feststoff erhaltenTo a solution of 9 mg of 4- [2,5-dihydro-3-methyl-2,5-dioxo-4- [5- (piperazin-1-yl) pentyl] -1H-pyrrol-1-yl] -2 - (Trifluoromethyl) benzonitrile in 0.4 ml of tetrahydrofuran was added 0.2 ml of a solution of triethylamine in tetrahydrofuran (1.5 mol / l) and 8 mg of 3-fluoro-phenylsulfonyl chloride in 0.4 ml of tetrahydrofuran and the mixture 8 hours stirred at room temperature. For work-up, the reaction mixture was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After concentration of the organic phase was chromatographed on silica gel with methanol / dichloromethane to obtain 6 mg of the title compound as a white solid
ESI-MS: 593. Beispiel 6ESI MS: 593. Example 6
4-r5-[1-r4-Cyan-3-(trifluormethyl)phenyl1-2.5-dihvdro-4-methyl-2,5-dioxo-1H-pyrrol-3- yllpentyl1-Λ/-f4-(dimethylamino)phenvnpiperazin-1-carboxamid4-r5- [1-r4-cyano-3- (trifluoromethyl) phenyl] -2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-3-yl-pentyl-1-f4- (dimethylamino) -pheniphenyl-piperazine 1-carboxamide
Zu einer Lösung von 9 mg 4-[2,5-Dihydro-3-methyl-2,5-dioxo-4-[5-(piperazin-1- yl)pentyl]-1H-pyrrol-1-yl]-2-(trifluormethyl)benzonitril in 0,4 ml Tetrahydrofuran wurden 0,2 ml einer Lösung von Triethylamin in Tetrahydrofuran (1 ,5 mol/l) und 7 mg 4- (Dimethylamino)phenylisocyanat in 0,4 ml Tetrahydrofuran gegeben und die Mischung 8 Stunden bei Raumtemperatur gerührt. Zur Aufarbeitung wurde die Reakti- onsmischung mit Ethylacetat verdünnt und mit halbgesättigter Natriumhydrogencarbonatlösung gewaschen. Nach Einengen der organischen Phase wurde mit Methanol/Dichlormethan an Kieselgel chromatographiert und so 3 mg der Titelverbindung als gelbliches Öl erhalten.To a solution of 9 mg of 4- [2,5-dihydro-3-methyl-2,5-dioxo-4- [5- (piperazin-1-yl) pentyl] -1H-pyrrol-1-yl] -2 - (Trifluoromethyl) benzonitrile in 0.4 ml of tetrahydrofuran were added 0.2 ml of a solution of triethylamine in tetrahydrofuran (1, 5 mol / l) and 7 mg of 4- (dimethylamino) phenyl isocyanate in 0.4 ml of tetrahydrofuran and the mixture 8 Stirred hours at room temperature. For work-up, the reaction mixture was diluted with ethyl acetate and washed with half-saturated sodium bicarbonate solution. After concentration of the organic phase was chromatographed on silica gel with methanol / dichloromethane to give 3 mg of the title compound as a yellowish oil.
ESI-MS: 597.ESI MS: 597.
Beispiel 7Example 7
4-f215-Dihvdro-3-methyl-4-r3-[4-(1-methylethylsulfonyl)piperazin-1-yllpropyl1-215-dioxo- 1r/-PVrrol-1-yl1-2-(trifluormethyl)benzonitril4-f2 1 5-Dihydro-3-methyl-4-R3- [4- (1-methylethylsulfonyl) piperazine-1-yllpropyl1-2 1 5-dioxo- 1r / -PVrrol-1-yl1-2- (trifluoromethyl) benzonitrile
7a) Dimethyl (Z)-2-methyl-3-(prop-2-enyl)-2-butendicarboxylat7a) Dimethyl (Z) -2-methyl-3- (prop-2-enyl) -2-butenedicarboxylate
Eine Lösung von Allylmagnesiumchlorid in Tetrahydrofuran (8,5 ml, c=2,0 M) wurde unter Stickstoffatmosphäre und Rühren bei -35 bis -40 °C zu einer Suspension von 3,47 g Kupfer(l)-bromid-Dimethylsulfidkomplex in 70 ml Tetrahydrofuran getropft und 2 Stunden bei -40 °C gerührt. Anschließend wurde auf -70 °C abgekühlt und bei dieser Temperatur unter Rühren eine Lösung von 2,0 g Dimethyl acetylendicarboxylat und 4,8 ml Hexamethylphosphorsäuretriamid in 29 ml Tetrahydrofuran zugetropft. Nach 5 Minuten wurde eine Lösung von 9,5 ml Hexamethylphosphorsäuretriamid in 9,5 ml Tetrahydrofuran bei -70 °C zugegeben. Es wurde 5 Minuten bei dieser Temperatur gerührt, dann wurden 4,2 ml lodmethan in 28 ml Tetrahydrofuran zugetropft und diese Mischung über Nacht auf Raumtemperatur erwärmt. Zur Aufarbeitung wurde unter Rüh- ren auf -60 °C abgekühlt, es wurden 200 ml gesättigte Ammoniumchloridlösung (mit konzentrierter Ammoniak-Lösung auf pH 8 eingestellt) zugetropft, auf Raumtemperatur erwärmt und 45 Minuten bei Raumtemperatur gerührt. Diese Mischung wurde viermal mit Ethylacetat extrahiert, die vereinigten organischen Phasen wurden mit gesättigter Ammoniumchloridlösung (mit konzentrierter Ammoniaklösung auf pH 8 eingestellt) gewaschen bis die organische Phase hellblau war und mit dann mit Wasser gewaschen bis die organische Phase farblos war. Nach Waschen mit gesättigter Natriumchloridlö- sung, Trocknen über Natriumsulfat und Einengen wurde mit Ethylacetat/Hexan an Kieselgel chromatographiert und so 980 mg der Titelverbindung neben 950 mg Dimethyl (£)-2-methyl-3-(prop-2-enyl)-2-butendicarboxylat jeweils als gelbliches Öl erhalten.A solution of allylmagnesium chloride in tetrahydrofuran (8.5 mL, c = 2.0 M) was added under nitrogen atmosphere and stirring at -35 to -40 ° C to a suspension of 3.47 g of copper (I) bromide-dimethylsulfide complex in 70 Added dropwise tetrahydrofuran and stirred at -40 ° C for 2 hours. It was then cooled to -70 ° C and added dropwise at this temperature with stirring, a solution of 2.0 g of dimethyl acetylenedicarboxylate and 4.8 ml of hexamethylphosphoric triamide in 29 ml of tetrahydrofuran. After 5 minutes, a solution of 9.5 ml of hexamethylphosphoric triamide in 9.5 ml of tetrahydrofuran was added at -70 ° C. It was stirred for 5 minutes at this temperature, then 4.2 ml of iodomethane in 28 ml of tetrahydrofuran were added dropwise and this mixture was warmed to room temperature overnight. For workup, the mixture was cooled to -60 ° C. with stirring, 200 ml of saturated ammonium chloride solution (adjusted to pH 8 with concentrated ammonia solution) were added dropwise to room temperature heated and stirred for 45 minutes at room temperature. This mixture was extracted four times with ethyl acetate, the combined organic phases were washed with saturated ammonium chloride solution (adjusted to pH 8 with concentrated ammonia solution) until the organic phase was light blue and then washed with water until the organic phase was colorless. After washing with saturated sodium chloride solution, drying over sodium sulfate and concentration, the mixture was chromatographed on silica gel with ethyl acetate / hexane to give 980 mg of the title compound in addition to 950 mg of dimethyl (ε) -2-methyl-3- (prop-2-enyl) -2 butene dicarboxylate each obtained as a yellowish oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 5,8 m (1H); 5,1 m (2H); 3,77 s (3H); 3,75 s (3H); 3,10 d (J=6,58 Hz, 2H); 1,96 s (3H). 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 5.8 m (1H); 5.1 m (2H); 3.77s (3H); 3.75s (3H); 3.10 d (J = 6.58 Hz, 2H); 1.96 s (3H).
ESI-MS: 198ESI-MS: 198
7b) 3-Methyl-4-(prop-2-enyl)-2,5-furandion7b) 3-methyl-4- (prop-2-enyl) -2,5-furandione
Zu einer unter einer Stickstoffatmosphäre gerührten Lösung von 980 mg der unter 7a hergestellten Verbindung in 10 ml Tetrahydrofuran wurden 10 ml Wasser sowie 16 ml einer Lösung von Lithiumhydroxid in Wasser (1 mol/l) gegeben und 2 Tage bei Raumtemperatur gerührt. Zur Aufarbeitung wurde eingeengt, der Rückstand in 30 ml Wasser gelöst, unter Eisbadkühlung mit Salzsäure (2 mol/l) auf pH 2 eingestellt und dreimal mit Diethylether extrahiert. Die vereinigten organischen Phasen wurden mit gesättigter Nat- riumchloridlösung gewaschen, über Natriumsulfat getrocknet, eingeengt und so 750 mg der Titelverbindung als gelbliches Öl erhalten.To a stirred under a nitrogen atmosphere solution of 980 mg of the compound prepared under 7a in 10 ml of tetrahydrofuran were added 10 ml of water and 16 ml of a solution of lithium hydroxide in water (1 mol / l) and stirred for 2 days at room temperature. For working up, the mixture was concentrated, the residue dissolved in 30 ml of water, adjusted with ice-bath cooling with hydrochloric acid (2 mol / l) to pH 2 and extracted three times with diethyl ether. The combined organic phases were washed with saturated sodium chloride solution, dried over sodium sulfate, concentrated and 750 mg of the title compound were obtained as a yellowish oil.
ESI-MS: 152ESI MS: 152
7c) 4-[2,5-Dihydro-3-methyl-2,5-dioxo-4-(prop-2-enyl)-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril7c) 4- [2,5-dihydro-3-methyl-2,5-dioxo-4- (prop-2-enyl) -1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Eine Mischung von 750 mg der unter 7b hergestellten Verbindung und 920 mg 4- Amino-2-(trifluormethyl)benzonitril in 10 ml Ethanol wurde unter einer Stickstoffatmosphäre mit 0,5 g aktiviertem Molsieb (0,3 nm) versetzt und 2 Tage bei 90 °C gerührt. Zur Aufarbeitung wurde das Molsieb nach dem Abkühlen abfiltriert, mit Ethanol gewa- sehen und die vereinigten Ethanol-Lösungen eingeengt. Der Rückstand wurde in Ethylacetat aufgenommen und mit Wasser sowie gesättigter Natriumchloridlösung gewaschen. Nach Trocknen über Natriumsulfat und Einengen wurde mit Ethylacetat/Hexan an Kieselgel chromatographiert und so 731 mg der Titelverbindung als farbloses Öl erhalten.A mixture of 750 mg of the compound prepared under 7b and 920 mg of 4-amino-2- (trifluoromethyl) benzonitrile in 10 ml of ethanol was added under a nitrogen atmosphere with 0.5 g of activated molecular sieve (0.3 nm) and 90 days for 2 days ° C stirred. For workup, the molecular sieve was filtered off after cooling, washed with ethanol gewa see and concentrated the combined ethanol solutions. The residue was taken up in ethyl acetate and washed with water and saturated sodium chloride solution. After drying over sodium sulfate and concentration, it was combined with ethyl acetate / hexane chromatographed on silica gel to give 731 mg of the title compound as a colorless oil.
ESI-MS: 320ESI-MS: 320
7d) 4-[2,5-Dihydro-3-(3-hydroxypropyl)-4-methyl-2,5-dioxo-1 H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril7d) 4- [2,5-Dihydro-3- (3-hydroxypropyl) -4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Eine Lösung von 720 mg der unter 7c hergestellten Verbindung in 15 ml THF wurde unter einer Stickstoffatmosphäre bei -78 °C mit 5,9 ml einer 0,5 molaren Lösung von 9- Borabicyclo(3.3.1)nonan versetzt. Die Lösung wurde langsam auf Raumtemperatur erwärmt und über Nacht bei Raumtemperatur gerührt. Die heftig gerührte Lösung wurde bei 0 °C mit 3,1 ml 10 prozentiger Natriumhydroxidlösung und mit 2,7 ml 33 prozentiger Wasserstoffperoxid-Lösung versetzt und 12 Stunden bei Raumtemperatur gerührt. Zur Aufarbeitung wurde mit Wasser (20 ml) versetzt und dreimal mit Ethylacetat extrahiert. Die vereinigten organischen Phasen wurden mit gesättigter Natriumchloridlösung ge- waschen, über Natriumsulfat getrocknet, eingeengt, mit Ethylacetat/Hexan an Kieselgel chromatographiert und so 623 mg der Titelverbindung als gelbliches Öl erhalten.A solution of 720 mg of the compound prepared under 7c in 15 ml of THF was added under a nitrogen atmosphere at -78 ° C with 5.9 ml of a 0.5 molar solution of 9-borabicyclo (3.3.1) nonane. The solution was slowly warmed to room temperature and stirred overnight at room temperature. The vigorously stirred solution was mixed at 0 ° C with 3.1 ml of 10 percent sodium hydroxide solution and with 2.7 ml of 33 percent hydrogen peroxide solution and stirred for 12 hours at room temperature. For workup, water (20 ml) was added and the mixture was extracted three times with ethyl acetate. The combined organic phases were washed with saturated sodium chloride solution, dried over sodium sulfate, concentrated by evaporation, chromatographed on silica gel with ethyl acetate / hexane to give 623 mg of the title compound as a yellowish oil.
ESI-MS: 338ESI MS: 338
7e) 4-[2,5-Dihydro-3-(3-iodpropyl)-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril7e) 4- [2,5-dihydro-3- (3-iodopropyl) -4-methyl-2,5-dioxo-1 H -pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Eine Lösung von 610 mg der unter 7d hergestellten Verbindung, von 565 mg Triphe- nylphosphin und von 183 mg 1H-lmidazol in 50 ml THF wurde unter einer Stickstoffatmosphäre mit 545 mg lod versetzt. Die Lösung über Nacht bei Raumtemperatur gerührt und anschließend mit 20 ml Wasser und 10 ml 20 prozentiger Natriumthiosulfat-Lösung versetzt und dreimal mit Ethylacetat extrahiert. Die vereinigten organischen Phasen wurden mit gesättigter Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, eingeengt, mit Ethylacetat/Hexan an Kieselgel chromatographiert und so 572 mg der Titelverbindung als gelbliches Öl erhalten.A solution of 610 mg of the compound prepared under 7d, 565 mg of triphenylphosphine and 183 mg of 1H-imidazole in 50 ml of THF was admixed with 545 mg of iodine under a nitrogen atmosphere. The solution was stirred overnight at room temperature and then treated with 20 ml of water and 10 ml of 20 percent sodium thiosulfate solution and extracted three times with ethyl acetate. The combined organic phases were washed with saturated sodium chloride solution, dried over sodium sulfate, concentrated by evaporation, chromatographed on silica gel with ethyl acetate / hexane to give 572 mg of the title compound as a yellowish oil.
ESI-MS: 448 7f) 1 ,1-Dimethylethyl 4-[3-[1-[4-cyan-3-(trifluormethyl)phenyl]-2,5-dihydro-4-methyl- 2,5-dioxo-1H-pyrrol-3-yl]propyl]piperazin-1-carboxylatESI MS: 448 7f) 1, 1-Dimethylethyl 4- [3- [1- [4-cyano-3- (trifluoromethyl) phenyl] -2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrole-3 yl] propyl] piperazine-1-carboxylate
Die Herstellung der Titelverbindung erfolgte analog zu der unter 1e beschriebenen Umsetzung. Ausgehend von 550 mg der unter 7e hergestellten Verbindung wurden 372 mg der Titelverbindung erhalten.The title compound was prepared analogously to the reaction described under 1e. Starting from 550 mg of the compound prepared under 7e, 372 mg of the title compound were obtained.
ESI-MS: 506ESI-MS: 506
7g) 4-[2,5-Dihydro-3-methyl-2,5-dioxo-4-[3-(piperazin-1-yl)propyl]-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril7g) 4- [2,5-dihydro-3-methyl-2,5-dioxo-4- [3- (piperazin-1-yl) -propyl] -1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
350 mg der unter 7f hergestellten Verbindung wurden mit 3 ml Trifluoressigsäure in 10 ml Dichlormethan 6 Stunden bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde im Vakuum eingeengt und mehrfach mit Toluol im Vakuum eingeengt, in Methanol aufgenommen, mit Anionenaustauscher (Bio-Rad AG 1-X8, OH-Form) auf einen pH-Wert von 8 bis 9 gestellt, filtriert und im Vakuum eingeengt. Man erhielt 227 mg der Titelverbindung als Rohprodukt, das in dieser Form weiter umgesetzt wurde.350 mg of the compound prepared under 7f were stirred with 3 ml of trifluoroacetic acid in 10 ml of dichloromethane for 6 hours at room temperature. The reaction mixture was concentrated in vacuo and concentrated several times with toluene in vacuo, taken up in methanol, adjusted to a pH of 8 to 9 with anion exchanger (Bio-Rad AG 1-X8, OH form), filtered and concentrated in vacuo. This gave 227 mg of the title compound as a crude product, which was reacted further in this form.
ESI-MS: 406ESI MS: 406
7h) 4-[2,5-Dihydro-3-methyl-4-[3-[4-(1-methylethylsulfonyl)piperazin-1-yl]propyl]-2,5- dioxo-1 H-pyrrol-l -yl]-2-(trif luormethyl)benzonitril7h) 4- [2,5-dihydro-3-methyl-4- [3- [4- (1-methylethylsulfonyl) piperazin-1-yl] propyl] -2,5-dioxo-1H-pyrrole-1 L yl] -2- (trifluoromethyl) benzonitrile
25 mg der unter 7g hergestellten Verbindung wurden mit 11 μl 1-Methylethylsulfo- nylchlorid und 25 μl Triethylamin in 2 ml Tetrahydrofuran 16 Stunden bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergab 23 mg der Titelverbindung als farbloses Öl.25 mg of the compound prepared under 7 g were stirred with 11 .mu.l of 1-methylethylsulfonyl chloride and 25 .mu.l of triethylamine in 2 ml of tetrahydrofuran for 16 hours at room temperature. The reaction mixture was concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gave 23 mg of the title compound as a colorless oil.
ESI-MS: 512 Beispiel 8ESI-MS: 512 Example 8
4-[2,5-Dihvdro-3-methyl-4-f[4-(1-methylethylsulfonyl)piperazin-1-vnmethyl1-2,5-dioxo- 1H-pyrrol-1-yll-2-(trifluormethyl)benzonitril4- [2,5-Dihydro-3-methyl-4-f [4- (1-methylethylsulfonyl) -piperazine-1-methyl-1,2,5-dioxo-1H-pyrrol-1-yl-2- (trifluoromethyl) -benzonitrile
8a) Dimethyl (Z)-2-ethenyl-3-methyl-2-butendicarboxylat8a) Dimethyl (Z) -2-ethenyl-3-methyl-2-butenedicarboxylate
Die Umsetzung von Vinylmagnesiumchlorid mit 5 g Dimethyl acetylendicarboxylat analog der unter 7a beschriebenen Vorschrift ergab 1 ,8 g der Titelverbindung als gelbliches Öl.The reaction of vinylmagnesium chloride with 5 g of dimethyl acetylenedicarboxylate analogously to the procedure described under 7a gave 1. 8 g of the title compound as a yellowish oil.
ESI-MS: 184ESI MS: 184
8b) 4-[3-Ethenyl-2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril8b) 4- [3-Ethenyl-2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Die Umsetzung von 1,8 g der unter 8a hergestellten Verbindung analog der unter 7b und 7c beschriebenen Vorschriften ergab 1,1 g der Titelverbindung als farbloses Öl.Reaction of 1.8 g of the compound prepared under 8a analogously to the instructions described under 7b and 7c gave 1.1 g of the title compound as a colorless oil.
ESI-MS: 306ESI-MS: 306
8c) 4-[3-(1 ,2-Dihydroxyethyl)-2,5-dihydro-4-methyl-2,5-dioxo-1 W-pyrrol-1 -yl]-2- (trifluormethyl)benzonitril8c) 4- [3- (1,2-Dihydroxyethyl) -2,5-dihydro-4-methyl-2,5-dioxo-1 W -pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Eine Lösung von 1,1 g der unter 8b hergestellten Verbindung in 50 ml Aceton wurde bei Raumtemperatur mit einer Lösung von 640 mg Λ/-Methylmorpholin-Λ/-oxid in 10 ml Wasser und 0,9 ml einer 10 prozentigen Lösung von Osmiumtetraoxid versetzt. Es wurde 30 Stunden bei Raumtemperatur gerührt, anschließend mit gesättigter Natri- umthiosulfatlösung versetzt und dreimal mit Ethylacetat extrahiert. Die vereinigten organischen Phasen wurden mit gesättigter Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, eingeengt, mit Dichlormethan/Methanol an Kieselgel chromatographiert und so 770 mg der Titelverbindung als farbloses Öl erhalten.A solution of 1.1 g of the compound prepared under 8b in 50 ml of acetone was added at room temperature with a solution of 640 mg / methylmorpholine-Λ / oxide in 10 ml of water and 0.9 ml of a 10 percent solution of osmium tetraoxide , The mixture was stirred at room temperature for 30 hours, then combined with saturated sodium thiosulfate solution and extracted three times with ethyl acetate. The combined organic phases were washed with saturated sodium chloride solution, dried over sodium sulfate, concentrated, chromatographed on silica gel with dichloromethane / methanol to give 770 mg of the title compound as a colorless oil.
ESI-MS: 340 8d) 4-[3-Formyl-2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitrilESI-MS: 340 8d) 4- [3-Formyl-2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Eine Lösung von 750 mg der unter 8c hergestellten Verbindung in 50 ml Dichlormethan wurde bei Raumtemperatur nacheinander mit 619 mg Natriumperiodat und mit 5 ml einer 10 prozentigen wässrigen Lösung von Natriumhydrogencarbonat versetzt. Es wurde 5 Stunden bei Raumtemperatur gerührt, anschließend mit Natriumsulfat versetzt und mit 50 ml Dichlormethan verdünnt. Die Mischung wurde filtriert und eingeengt. Man erhielt 705 mg der Titelverbindung als Rohprodukt, das in dieser Form weiter umgesetzt wurde.A solution of 750 mg of the compound prepared under 8c in 50 ml of dichloromethane was added successively at room temperature with 619 mg of sodium periodate and with 5 ml of a 10 percent aqueous solution of sodium bicarbonate. It was stirred for 5 hours at room temperature, then treated with sodium sulfate and diluted with 50 ml of dichloromethane. The mixture was filtered and concentrated. 705 mg of the title compound were obtained as crude product, which was reacted further in this form.
ESI-MS: 308ESI-MS: 308
8e) 4-[2,5-Dihydro-3-methyl-4-[[4-(1-methylethylsulfonyl)piperazin-1-yl]methyl]-2,5- dioxo-1r -pyrrol-1-yl]-2-(trifluormethyl)benzonitril8e) 4- [2,5-dihydro-3-methyl-4 - [[4- (1-methylethylsulfonyl) piperazin-1-yl] methyl] -2,5-dioxo-1r-pyrrol-1-yl] - 2- (trifluoromethyl) benzonitrile
25 mg der unter 8d hergestellten Verbindung in 1 ml 1 ,2-Dichlorethan wurden mit 19 mg 1-(1-Methylethylsulfonyl)piperazin versetzt und 15 Minuten bei Raumtemperatur gerührt. Es wurden portionsweise 25 mg Natriumtrisacetoxyborhydrid zugegeben und 2 Stunden bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde mit 10 ml Natriumhydrogencarbonatlösung versetzt, 15 Minuten bei Raumtemperatur gerührt und dreimal mit Ethylacetat extrahiert. Die vereinigten organischen Phasen wurden mit gesättigter Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, eingeengt und mit Dichlormethan/Methanol an Kieselgel chromatographiert. Es wurden 17 mg der Titelverbindung als farbloses Öl erhalten.25 mg of the compound prepared under 8d in 1 ml of 1, 2-dichloroethane were added 19 mg of 1- (1-methylethylsulfonyl) piperazine and stirred for 15 minutes at room temperature. 25 mg of sodium trisacetoxyborohydride were added in portions and the mixture was stirred at room temperature for 2 hours. The reaction mixture was added with 10 ml of sodium bicarbonate solution, stirred for 15 minutes at room temperature and extracted three times with ethyl acetate. The combined organic phases were washed with saturated sodium chloride solution, dried over sodium sulfate, concentrated and chromatographed on silica gel using dichloromethane / methanol. There were obtained 17 mg of the title compound as a colorless oil.
ESI-MS: 484 Beispiel 9ESI-MS: 484 Example 9
4-r2.5-Dihvdro-3-methyl-4-r7-r4-(1-methylethylsulfonyl)piperazin-1-yllheptyll-2.5-dioxo- 1 H-pyrrol-l -yl]-2-(trifluormethyl)benzonitril4-r2,5-Dihydro-3-methyl-4-r7-r4- (1-methylethylsulfonyl) -piperazin-1-yl-heptyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) -benzonitrile
9a) Dimethyl (Z)-2-[7-[(4-methoxyphenyl)methoxy]heptyl]-3-methyl-2-butendicarboxylat9a) Dimethyl (Z) -2- [7 - [(4-methoxyphenyl) methoxy] heptyl] -3-methyl-2-butenedicarboxylate
Die Umsetzung von 12,4 g 1-[[(7-Chlorheptyl)oxy]methyl]-4-methoxybenzol mit 5,0 g Dimethyl acetylendicarboxylat analog der unter 1a beschriebenen Vorschrift ergab 4,18 g der Titelverbindung als gelbliches Öl.The reaction of 12.4 g of 1 - [[(7-chloroheptyl) oxy] methyl] -4-methoxybenzene with 5.0 g of dimethyl acetylenedicarboxylate analogously to the procedure described under 1a gave 4.18 g of the title compound as a yellowish oil.
ESI-MS: 378ESI MS: 378
9b) 4-[2,5-Dihydro-3-[7-[(4-methoxyphenyl)methoxy]heptyl]-4-methyl-2,5-dioxo-1r/- pyrrol-1-yl]-2-(trifluormethyl)benzonitril9b) 4- [2,5-dihydro-3- [7 - [(4-methoxyphenyl) methoxy] heptyl] -4-methyl-2,5-dioxo-1r / -pyrrol-1-yl] -2- ( trifluoromethyl) benzonitrile
Die Umsetzung von 4,10 g der unter 9a hergestellten Verbindung analog der unter 7b und 7c beschriebenen Vorschriften ergab 3,35 g der Titelverbindung als farbloses Öl.The reaction of 4.10 g of the compound prepared under 9a analogously to the instructions described under 7b and 7c gave 3.35 g of the title compound as a colorless oil.
ESI-MS: 514ESI MS: 514
9c) 4-[2,5-Dihydro-3-(7-hydroxyheptyl)-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril9c) 4- [2,5-dihydro-3- (7-hydroxyheptyl) -4-methyl-2,5-dioxo-1 H -pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
3,30 g der unter 9b hergestellten Verbindung in 100 ml Dichlormethan wurden mit 10 ml Wasser und 1,90 g 4,5-Dichlor-3,6-dioxocyclohexa-1,4-dien-1,2-dicarbonitril versetzt und 5 Stunden bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde mit 20 ml Natriumhydrogencarbonatlösung versetzt und dreimal mit Dichlormethan extrahiert. Die vereinigten organischen Phasen wurden mit gesättigter Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, eingeengt und mit Dichlormethan/Methanol an Kieselgel chromatographiert. Es wurden 2,05 g der Titelverbindung als farbloses Öl erhalten.3.30 g of the compound prepared under 9b in 100 ml of dichloromethane were mixed with 10 ml of water and 1.90 g of 4,5-dichloro-3,6-dioxocyclohexa-1,4-diene-1,2-dicarbonitrile and 5 hours stirred at room temperature. The reaction mixture was treated with 20 ml of sodium bicarbonate solution and extracted three times with dichloromethane. The combined organic phases were washed with saturated sodium chloride solution, dried over sodium sulfate, concentrated and chromatographed on silica gel using dichloromethane / methanol. There was obtained 2.05 g of the title compound as a colorless oil.
ESI-MS: 394 9d) 4-[3-(7-lodheptyl)-2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl]-2- (trifluormethyl)benzonitrilESI MS: 394 9d) 4- [3- (7-iodoheptyl) -2,5-dihydro-4-methyl-2,5-dioxo-1H-pyrrol-1-yl] -2- (trifluoromethyl) benzonitrile
Die Umsetzung von 2,0 g der unter 9c hergestellten Verbindung analog der unter 7e beschriebenen Vorschrift ergab 1 ,99 g der Titelverbindung als farbloses Öl.The reaction of 2.0 g of the compound prepared under 9c analogously to the procedure described under 7e gave 1.99 g of the title compound as a colorless oil.
ESI-MS: 504ESI-MS: 504
9e) 1 ,1-Dimethylethyl 4-[7-[1-[4-cyan-3-(trifluormethyl)phenyl]-2,5-dihydro-4-methyl-2,5- dioxo-1 r -pyrrol-3-yl]heptyl]piperazin-1 -carboxylat9e) 1, 1-Dimethylethyl 4- [7- [1- [4-cyano-3- (trifluoromethyl) phenyl] -2,5-dihydro-4-methyl-2,5-dioxo-1 r -pyrrol-3 -yl] heptyl] piperazine-1-carboxylate
Die Herstellung der Titelverbindung erfolgte analog zu der unter 1e beschriebenen Umsetzung. Ausgehend von 1,95 g der unter 9c hergestellten Verbindung wurden 1,01 g der Titelverbindung erhalten.The title compound was prepared analogously to the reaction described under 1e. Starting from 1.95 g of the compound prepared under 9c, 1.01 g of the title compound were obtained.
ESI-MS: 562ESI MS: 562
9f) 4-[2,5-Dihydro-3-methyl-2,5-dioxo-4-[7-(piperazin-1-yl)heptyl]-1 H-pyrrol-1-yl]-2- (trifluormethyl)benzonitril9f) 4- [2,5-dihydro-3-methyl-2,5-dioxo-4- [7- (piperazin-1-yl) heptyl] -1 H -pyrrol-1-yl] -2- (trifluoromethyl benzonitrile)
Die Herstellung der Titelverbindung erfolgte analog zu der unter 7g beschriebenen Umsetzung. Ausgehend von 1,0 g der unter 9e hergestellten Verbindung wurden 707 mg der Titelverbindung erhalten.The preparation of the title compound was carried out analogously to the reaction described under 7g. Starting from 1.0 g of the compound prepared under 9e, 707 mg of the title compound were obtained.
ESI-MS: 462ESI MS: 462
9g) 4-[2,5-Dihydro-3-methyl-4-[7-[4-(1-methylethylsulfonyl)piperazin-1-yl]heptyl]-2,5- dioxo-1H-pyrrol-1-yl]-2-(trifluormethyl)benzonitril9g) 4- [2,5-dihydro-3-methyl-4- [7- [4- (1-methylethylsulfonyl) piperazin-1-yl] heptyl] -2,5-dioxo-1H-pyrrol-1-yl ] -2- (trifluoromethyl) benzonitrile
Die Herstellung der Titelverbindung erfolgte analog zu der unter 7h beschriebenen Um- setzung. Ausgehend von 25 mg der unter 9f hergestellten Verbindung wurden 20 mg der Titelverbindung erhalten.The title compound was prepared analogously to the reaction described under 7h. Starting from 25 mg of the compound prepared under 9f, 20 mg of the title compound were obtained.
ESI-MS: 568 Beispiel 10ESI-MS: 568 Example 10
1 ,1-Dimethylethyl 4-[5-f3-(1 ,3-dihvdro-1-oxoisobenzofuran-5-ylV5,5-dimethyl-4-oxo-2- thioxoimidazolidin-1-vnpentvnpiperazin-1-carboxylat1, 1-Dimethylethyl 4- [5-f3- (1,3-dihydro-1-oxoisobenzofuran-5-yl-V, 5,5-dimethyl-4-oxo-2-thioxoimidazolidine-1-pentanediperpiperazine-1-carboxylate
10a) 5-[3-(5-Hydroxypentyl)-5-imino-4,4-dimethyl-2-thioxoimidazolidin-1- yl]isobenzofuran-1 (3/ )-on10a) 5- [3- (5-Hydroxypentyl) -5-imino-4,4-dimethyl-2-thioxoimidazolidin-1-yl] isobenzofuran-1 (3 /) -one
Unter Stickstoffatmosphäre wurden 5 g 5-Aminoisobenzofuran-1(3/-/)-on, dessen Herstellung in R. N. Warrener, L. Liu, R. A. Russell, Tetrahedron 1998, 54, 7485-7496 beschrieben ist, mit 2,8 ml Thiophosgen in 70 ml Wasser eine Stunde bei Raum- temperatur gerührt. Das Reaktionsgemisch wurde filtriert. Der Rückstand wurde mit Wasser gewaschen und anschließend 30 Minuten bei 60°C im Vakuum getrocknet. Das so erhaltene rohe Isothiocyanat wurde mit dem durch vierstündiges Rühren von 520 μl Acetoncyanhydrin mit 617 μl 5-Aminopentan-1-ol bei Raumtemperatur erzeugten Cyan- amin vereinigt und mit 4,7 ml Triethylamin in 100 ml Tetrahydrofuran 30 Minuten zum Sieden erhitzt. Nach Einengen im Vakuum erhielt man die Titelverbindung als Rohprodukt, das sofort weiter umgesetzt wurde.Under a nitrogen atmosphere, 5 g of 5-aminoisobenzofuran-1 (3 / - /) - one, the preparation of which is described in RN Warrener, L. Liu, RA Russell, Tetrahedron 1998, 54, 7485-7496, with 2.8 ml of thiophosgene in 70 ml of water for one hour at room temperature. The reaction mixture was filtered. The residue was washed with water and then dried at 60 ° C for 30 minutes in vacuo. The crude isothiocyanate thus obtained was combined with the cyanoamine produced by stirring 420 μl of 5-aminopentan-1-ol for 4 hours at room temperature and heated to boiling point with 4.7 ml of triethylamine in 100 ml of tetrahydrofuran for 30 minutes. Concentration in vacuo gave the title compound as a crude product, which was immediately reacted further.
10b) 3-(1,3-Dihydro-1-oxoisobenzofuran-5-yl)-1-(5-hydroxypentyl)-5,5-dimethyl-2- thioxoimidazolidin-4-on10b) 3- (1,3-Dihydro-1-oxoisobenzofuran-5-yl) -1- (5-hydroxypentyl) -5,5-dimethyl-2-thioxoimidazolidin-4-one
Das unter 10a hergestellte Rohprodukt wurde mit 17 ml 4 molarer wässriger Salzsäure in 150 ml Methanol über Nacht bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde dann auf gesättigte wässrige Natriumhydrogencarbonatlösung gegossen und mit Ethylacetat extrahiert. Die organische Phase wurde mit gesättigter wässriger Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 4,0 g der Titelverbindung als farblosen Schaum.The crude product prepared under 10a was stirred with 17 ml of 4 molar aqueous hydrochloric acid in 150 ml of methanol overnight at room temperature. The reaction mixture was then poured onto saturated aqueous sodium bicarbonate solution and extracted with ethyl acetate. The organic phase was washed with saturated aqueous sodium chloride solution, dried over sodium sulfate, filtered and concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 4.0 g of the title compound as a colorless foam.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,03 d (J=8 Hz, 1 H, aryl); 7,53 ddbr (J=8 Hz + 1 Hz, 1 H, aryl); 7,52 d (J=1 Hz, 1 H, aryl); 5,37 s (1 H, CH2O); 3,71 m (2H, CH2OH); 3,69 m (2H, CH2N); 1,89 m (2H, CH2); 1,66 m (2H, CH2); 1,58 s (6H, CH3); 1,49 m (2H, CH2). 10c) 3-(1,3-Dihydro-1-oxoisobenzofuran-5-yl)-5,5-dimethyl-1-[5-[[(4-methylphenyl)- sulfonyl]oxy]pentyl]-2-thioxoimidazolidin-4-on 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.03 d (J = 8 Hz, 1 H, aryl); 7.53 ddbr (J = 8 Hz + 1 Hz, 1H, aryl); 7.52 d (J = 1 Hz, 1H, aryl); 5.37 s (1H, CH 2 O); 3.71 m (2H, CH 2 OH); 3.69 m (2H, CH 2 N); 1.89 m (2H, CH 2 ); 1.66 m (2H, CH 2 ); 1.58 s (6H, CH 3); 1.49 m (2H, CH 2 ). 10c) 3- (1,3-dihydro-1-oxoisobenzofuran-5-yl) -5,5-dimethyl-1- [5 - [[(4-methylphenyl) sulfonyl] oxy] pentyl] -2-thioxoimidazolidine 4-one
3,9 g der unter 10b hergestellten Verbindung wurden mit 12,3 g p-Toluolsulfonsäure- chlorid und 15 ml Triethylamin in 100 ml Dichlormethan eine Stunde bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde in gesättigte wässrige Natriumhydrogencarbonatlösung gegossen und mit Dichlormethan extrahiert. Die organische Phase wurde mit gesättigter wässriger Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und im Vakuum eingeengt. Säulenchromatographie an Kiesel- gel mit einem Gemisch aus Hexan/Ethylacetat ergibt 5,15 g der Titelverbindung als farblosen Schaum.3.9 g of the compound prepared under 10b were stirred with 12.3 g of p-toluenesulfonic acid chloride and 15 ml of triethylamine in 100 ml of dichloromethane for one hour at room temperature. The reaction mixture was poured into saturated aqueous sodium bicarbonate solution and extracted with dichloromethane. The organic phase was washed with saturated aqueous sodium chloride solution, dried over sodium sulfate, filtered and concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 5.15 g of the title compound as a colorless foam.
Fp 164,9°C (Methanol)Mp 164.9 ° C (methanol)
1 H-NMR (300 MHz, CDCI3): δ [ppm] = 8,04 d (J=8 Hz, 1 H, aryl); 7,81 d (J=9 Hz, 2H, tolyl); 7,54 dbr (J=8 Hz, 1H, aryl); 7,53 sbr (1H, aryl); 7,37 d (J=9 Hz, 2H, tolyl); 5,38 s (1 H, CH2O); 4,08 t (J=6 Hz, 2H, CH2OTs); 3,68 m (2H, CH2N); 1,86 m (2H, CH2); 1 ,76 m (2H, CH2); 1,58 s (6H, CH3); 1,49 m (2H, CH2).1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.04 d (J = 8 Hz, 1 H, aryl); 7.81 d (J = 9 Hz, 2H, tolyl); 7.54 dbr (J = 8 Hz, 1H, aryl); 7.53 sbr (1H, aryl); 7.37 d (J = 9 Hz, 2H, tolyl); 5.38 s (1H, CH 2 O); 4.08 t (J = 6 Hz, 2H, CH 2 OTs); 3.68 m (2H, CH 2 N); 1.86 m (2H, CH 2 ); 1.76m (2H, CH 2 ); 1.58 s (6H, CH 3); 1.49 m (2H, CH 2 ).
10d) 3-(1,3-Dihydro-1-oxoisobenzofuran-5-yl)-5,5-dimethyl-1-(5-iodpentyl)-2-thioxo- imidazolidin-4-on10d) 3- (1,3-Dihydro-1-oxoisobenzofuran-5-yl) -5,5-dimethyl-1- (5-iodopentyl) -2-thioxo-imidazolidin-4-one
5,15 g der unter 10c hergestellten Verbindung wurden mit 3 g Natriumiodid in 100 ml Aceton eine Stunde zum Sieden erhitzt. Das Reaktionsgemisch wurde bei Raumtemperatur filtriert und im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 4,16 g der Titelverbindung als gelblichen Schaum.5.15 g of the compound prepared under 10c were heated to boiling with 3 g of sodium iodide in 100 ml of acetone for one hour. The reaction mixture was filtered at room temperature and concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 4.16 g of the title compound as a yellowish foam.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,03 d (J=8 Hz, 1 H, aryl); 7,53 ddbr (J=8 Hz + 2 Hz, 1 H, aryl); 7,52 sbr (1 H, aryl); 5,37 s (1 H, CH2O); 3,70 m (2H, CH2N); 3,23 t (J=7 Hz, 2H, CH2I); 1 ,89 m (4H, CH2); 1,59 s (6H, CH3); 1,53 m (2H, CH2). 10e) 1 ,1-Dimethylethyl 4-[5-[3-(1 ,3-dihydro-1-oxoisobenzofuran-5-yl)-5,5-dimethyl-4- oxo-2-thioxoimidazolidin-1-yl]pentyl]piperazin-1-carboxylat 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.03 d (J = 8 Hz, 1 H, aryl); 7.53 ddbr (J = 8 Hz + 2 Hz, 1H, aryl); 7.52 sbr (1H, aryl); 5.37 s (1H, CH 2 O); 3.70 m (2H, CH 2 N); 3.23 t (J = 7 Hz, 2H, CH 2 I); 1.89 m (4H, CH 2 ); 1.59 s (6H, CH 3); 1.53 m (2H, CH 2 ). 10e) 1, 1-Dimethylethyl 4- [5- [3- (1,3-dihydro-1-oxoisobenzofuran-5-yl) -5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1-yl] pentyl ] piperazine-1-carboxylate
1 g der unter 10d hergestellten Verbindung wurden mit 790 mg 1,1-Dimethylethyl piperazin-1-carboxylat und 591 μl Triethylamin drei Tage bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 903 mg der Titelverbindung als gelblichen Schaum.1 g of the compound prepared under 10d were stirred for 3 days at room temperature with 790 mg of 1,1-dimethylethyl piperazine-1-carboxylate and 591 μl of triethylamine. The reaction mixture was concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 903 mg of the title compound as a yellowish foam.
H-NMR (300 MHz, CDCI3): δ [ppm] = 8,04 d (J=8 Hz, 1 H, aryl); 7,54 dbr (J=8 Hz, 1H, aryl); 7,52 sbr (1H, aryl); 5,37 s (1H, CH2O); 3,69 m (2H, CH2N); 3,44 m (4H, Piperazin); 2,38 m (4H, Piperazin); 2,36 m (2H, CH2Piperazin); 1,86 m (2H, CH2); 1,58 s (6H, CH3); 1,57 m (2H, CH2); 1,46 s (9H, fBu); 1,42 m (2H, CH2).H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.04 d (J = 8 Hz, 1 H, aryl); 7.54 dbr (J = 8 Hz, 1H, aryl); 7.52 sbr (1H, aryl); 5.37s (1H, CH 2 O); 3.69 m (2H, CH 2 N); 3.44 m (4H, piperazine); 2.38 m (4H, piperazine); 2.36 m (2H, CH 2 piperazine); 1.86 m (2H, CH 2 ); 1.58 s (6H, CH 3); 1.57 m (2H, CH 2 ); 1.46 s (9H, f Bu); 1.42 m (2H, CH 2 ).
Beispiel 11Example 11
3-(1,3-Dihvdro-1-oxoisobenzofuran-5-yl)-1-[5-(piperazin-1-yl)pentyl1-5,5-dimethyl-2- thioxoimidazolidin-4-on3- (1,3-Dihydro-1-oxoisobenzofuran-5-yl) -1- [5- (piperazin-1-yl) -pentyl-1,5-dimethyl-2-thioxoimidazolidin-4-one
450 mg der unter 10e hergestellten Verbindung wurden mit 653 μl Trifluoressigsäure in 8,5 ml Dichlormethan 24 Stunden bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde im Vakuum eingeengt und mehrfach mit Toluol im Vakuum eingeengt, in Metha- noi aufgenommen, mit Anionenaustauscher (Bio-Rad AG 1-X8, OH-Form) auf einen pH-Wert von 8 bis 9 gestellt, filtriert und im Vakuum eingeengt. Man erhielt 313 mg der Titelverbindung als Rohprodukt, das in dieser Form weiter umgesetzt wurde.450 mg of the compound prepared under 10e were stirred with 653 μl of trifluoroacetic acid in 8.5 ml of dichloromethane for 24 hours at room temperature. The reaction mixture was concentrated in vacuo and concentrated several times with toluene in vacuo, taken up in methanol, adjusted to a pH of 8 to 9 with anion exchanger (Bio-Rad AG 1-X8, OH form), filtered and concentrated in vacuo concentrated. This gave 313 mg of the title compound as a crude product, which was reacted further in this form.
1H-NMR (300 MHz, CD3OD): δ [ppm] = 7,96 d (J=8 Hz, 1H, aryl); 7,57 dbr (J=8 Hz, 1 H, aryl); 7,65 sbr (1H, aryl); 5,43 s (1H, CH2O); 3,75 m (2H, CH2N); 2,87 m (4H, Piperazin); 2,48 m (4H, Piperazin); 2,39 m (2H, CH2Piperazin); 1,88 m (2H, CH2); 1 ,61 m (2H, CH2); 1 ,58 s (6H, CH3); 1,42 m (2H, CH2). Beispiel 12 1 H-NMR (300 MHz, CD 3 OD): δ [ppm] = 7.96 d (J = 8 Hz, 1H, aryl); 7.57 dbr (J = 8 Hz, 1H, aryl); 7.65 sbr (1H, aryl); 5.43 s (1H, CH 2 O); 3.75 m (2H, CH 2 N); 2.87m (4H, piperazine); 2.48 m (4H, piperazine); 2.39 m (2H, CH 2 piperazine); 1.88 m (2H, CH 2 ); 1.61m (2H, CH 2 ); 1, 58 s (6H, CH 3); 1.42 m (2H, CH 2 ). Example 12
4-r5-[3-(1 ,3-Dihydro-1-oxoisobenzofuran-5-yl)-5.5-dimethyl-4-oxo-2-thioxoimidazolidin- 1-yllpentvn-Λ/-ethylpiperazin-1-carbothioamid4-r5- [3- (1,3-dihydro-1-oxoisobenzofuran-5-yl) -5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1-yl-pentene-Λ / -ethyl-piperazine-1-carbothioamide
20 mg der unter 11 hergestellten Verbindung wurden mit 7,7 ml Isothiocyanatoethan und 12,4 μl Triethylamin in 3 ml Tetrahydrofuran 6 Stunden auf 80° C erhitzt. Das Reaktionsgemisch wurde im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 11 mg der Titelverbindung als farbloses Öl.20 mg of the compound prepared under 11 were heated to 80 ° C. with 7.7 ml of isothiocyanatoethane and 12.4 μl of triethylamine in 3 ml of tetrahydrofuran for 6 hours. The reaction mixture was concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 11 mg of the title compound as a colorless oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,02 d (J=8 Hz, 1H, aryl); 7,53 dbr (J=8 Hz, 1 H, aryl); 7,51 sbr (1 H, aryl); 5,47 tbr (J=5 Hz, 1H, NH); 5,37 s (1 H, CH2O); 3,81 m (4H, Piperazin); 3,70 qd (J=7 Hz + 5 Hz, 2H, CH2N); 3,67 m (2H, CH2N); 2,47 m (4H, Piperazin); 2,38 m (2H, CH2Piperazin); 1,86 m (2H, CH2); 1,57 s (6H, CH3); 1,57 m (2H, CH2); 1 ,41 m (2H, CH2); 1 ,24 t (J=7 Hz, 3H, CH3). 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.02 d (J = 8 Hz, 1H, aryl); 7.53 dbr (J = 8 Hz, 1H, aryl); 7.51 sbr (1H, aryl); 5.47 tbr (J = 5 Hz, 1H, NH); 5.37 s (1H, CH 2 O); 3.81m (4H, piperazine); 3.70 qd (J = 7 Hz + 5 Hz, 2H, CH 2 N); 3.67 m (2H, CH 2 N); 2.47 m (4H, piperazine); 2.38 m (2H, CH 2 piperazine); 1.86 m (2H, CH 2 ); 1.57 s (6H, CH 3); 1.57 m (2H, CH 2 ); 1.41m (2H, CH 2 ); 1, 24 t (J = 7 Hz, 3H, CH 3 ).
Beispiel 13Example 13
S-Methyl 4-[5-r3-(1 ,3-dihvdro-1-oxoisobenzofuran-5-yl)-5,5-dimethyl-4-oxo-2- thioxoimidazolidin-1 -yllpentyllpiperazin-l -carbothioatS-Methyl 4- [5-r3- (1,3-dihydro-1-oxoisobenzofuran-5-yl) -5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1-yl-pentylpiperazine-1-carbothioate
15,5 mg der unter 11 hergestellten Verbindung wurden mit 6,2 ml S-Methyl chlorthio- formiat und 10 μl Triethylamin in 1 ml Tetrahydrofuran 4 Stunden unter Rückfluss erhitzt. Das Reaktionsgemisch wurde im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 8 mg der Titelverbindung als farbloses Öl.15.5 mg of the compound prepared under 11 were refluxed for 4 hours with 6.2 ml of S-methyl chloroformate and 10 μl of triethylamine in 1 ml of tetrahydrofuran. The reaction mixture was concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 8 mg of the title compound as a colorless oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,03 d (J=8 Hz, 1H, aryl); 7,53 dbr (J=8 Hz, 1H, aryl); 7,52 sbr (1 H, aryl); 5,37 s (1 H, CH2O); 3,69 m (2H, CH2N); 3,56 m (4H, Piperazin); 2,43 m (4H, Piperazin); 2,38 (2H, CH2Piperazin); 2,33 s (3H, CH3); 1,86 m (2H, CH2); 1 ,57 s (6H, CH3); 1 ,56 m (2H, CH2); 1,42 m (2H, CH2). Beispiel 14 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.03 d (J = 8 Hz, 1H, aryl); 7.53 dbr (J = 8 Hz, 1H, aryl); 7.52 sbr (1H, aryl); 5.37 s (1H, CH 2 O); 3.69 m (2H, CH 2 N); 3.56 m (4H, piperazine); 2.43 m (4H, piperazine); 2.38 (2H, CH 2 piperazine); 2.33s (3H, CH 3 ); 1.86 m (2H, CH 2 ); 1, 57 s (6H, CH 3); 1.56 m (2H, CH 2 ); 1.42 m (2H, CH 2 ). Example 14
4-r5-r3-(1,3-Dihvdro-1-oxoisobenzofuran-5-vπ-5.5-dimethyl-4-oxo-2-thioxoimidazolidin- 1-vnpentyπ-Λ/,Λ/-diethylpiperazin-1-carboxamid4-r5-r3- (1,3-Dihydro-1-oxoisobenzofuran-5-vi-5,5-dimethyl-4-oxo-2-thioxoimidazolidine-1-pentyno-Λ /, Λ / -diethyl-piperazine-1-carboxamide
15,5 mg der unter 11 hergestellten Verbindung wurden mit 9,8 ml Diethylcarbamidoyl- chlorid und 10 μl Triethylamin in 1 ml Tetrahydrofuran 4 Stunden unter Rückfluss erhitzt. Das Reaktionsgemisch wurde im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 6 mg der Titelverbindung als farbloses Öl.15.5 mg of the compound prepared under 11 were refluxed with 9.8 ml of diethylcarbamidoyl chloride and 10 μl of triethylamine in 1 ml of tetrahydrofuran for 4 hours. The reaction mixture was concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 6 mg of the title compound as a colorless oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 8,03 d (J=8 Hz, 1H, aryl); 7,53 dbr (J=8 Hz, 1 H, aryl); 7,52 sbr (1H, aryl); 5,37 s (1H, CH20); 3,69 m (2H, CH2N); 3,23 m (4H, Piperazin); 3,19 q (J=7 Hz, 4H, CH2N); 2,43 m (4H, Piperazin); 2,37 m (2H, CH2Piperazin); 1,86 m (2H, CH2); 1,59 m (2H, CH2); 1,58 s (6H, CH3); 1,41 m (2H, CH2); 1,11 t (J=7 Hz, 6H, CH3). 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 8.03 d (J = 8 Hz, 1H, aryl); 7.53 dbr (J = 8 Hz, 1H, aryl); 7.52 sbr (1H, aryl); 5.37 s (1H, CH 2 O); 3.69 m (2H, CH 2 N); 3.23 m (4H, piperazine); 3.19 q (J = 7 Hz, 4H, CH 2 N); 2.43 m (4H, piperazine); 2.37 m (2H, CH 2 piperazine); 1.86 m (2H, CH 2 ); 1.59 m (2H, CH 2 ); 1.58 s (6H, CH 3); 1.41 m (2H, CH 2 ); 1.11 t (J = 7 Hz, 6H, CH 3 ).
Beispiel 15Example 15
4-|'3-[2-f4-(2-Methoxybenzoyl)piperazin-1-vnethyl1-4,4-dimethyl-5-oxo-2- thioxoimidazolidin-1-vn-2-(trifluormethyl)benzonitril4 | ' 3- [2-f4- (2-Methoxybenzoyl) piperazine-1-dimethyl-4,4-dimethyl-5-oxo-2-thioxoimidazolidin-1-vn-2- (trifluoromethyl) benzonitrile
15a) 1 ,1-Dimethylethyl 4-[2-[3-[4-cyan-3-(trifluormethyl)phenyl]-4-imino-5,5-dimethyl-2- thioxoimidazolidin-1-yl]ethyl]piperazin-1-carboxylat15a) 1,1-dimethylethyl 4- [2- [3- [4-cyano-3- (trifluoromethyl) phenyl] -4-imino-5,5-dimethyl-2-thioxoimidazolidin-1-yl] ethyl] piperazine 1-carboxylate
Unter Stickstoffatmosphäre wurden 687 g 4-Amino-2-(trifluormethyl)benzonitril mit 311 μl Thiophosgen in 4 ml Λ/,Λ/-Dimethylformamid eine Stunde bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde mit Ethylacetat verdünnt, mit Wasser gewaschen und anschließend im Vakuum eingeengt. Das so erhaltene rohe Isothiocyanat wurde mit dem durch zweistündiges Rühren von 743 μl Acetoncyanhydrin mit 930 mg 1 ,1- Dimethylethyl 4-(2-aminoethyl)piperazin-1-carboxylat und 406 mg Molsieb 3 Ä in 20 ml Tetrahydrofuran bei Raumtemperatur erzeugten und filtrierten Cyanamin vereinigt und mit 0,57 ml Triethylamin in 40 ml Tetrahydrofuran eine Stunde zum Sieden erhitzt. Nach Einengen im Vakuum erhielt man die Titelverbindung als Rohprodukt, das sofort weiter umgesetzt wurde. 15b) 1,1-Dimethylethyl 4-[2-[3-[4-cyan-3-(trifluormethyl)phenyl]-5,5-dimethyl-4-oxo-2- thioxoimidazolidin-1-yl]ethyl]piperazin-1-carboxylatUnder a nitrogen atmosphere, 687 g of 4-amino-2- (trifluoromethyl) benzonitrile were stirred with 311 .mu.l of thiophosgene in 4 ml of Λ /, Λ / -dimethylformamide for one hour at room temperature. The reaction mixture was diluted with ethyl acetate, washed with water and then concentrated in vacuo. The crude isothiocyanate thus obtained was produced and filtered with room temperature stirring of 743 μl of acetone cyanohydrin with 930 mg of 1, 1-dimethylethyl 4- (2-aminoethyl) piperazine-1-carboxylate and 406 mg of 3X molecular sieve in 20 ml of tetrahydrofuran at room temperature Cyanamine combined and heated with 0.57 ml of triethylamine in 40 ml of tetrahydrofuran for one hour to boiling. Concentration in vacuo gave the title compound as a crude product, which was immediately reacted further. 15b) 1,1-dimethylethyl 4- [2- [3- [4-cyano-3- (trifluoromethyl) phenyl] -5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1-yl] ethyl] piperazine 1-carboxylate
Das unter 15a hergestellte Rohprodukt wurde mit 3,7 ml 4 molarer wässriger Salzsäure in 40 ml Methanol über Nacht bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde dann auf gesättigte wässrige Natriumhydrogencarbonatlösung gegossen und mit Ethylacetat extrahiert. Die organische Phase wurde mit gesättigter wässriger Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 553 mg der Titelverbindung als farblosen Schaum.The crude product prepared under 15a was stirred with 3.7 ml of 4 molar aqueous hydrochloric acid in 40 ml of methanol overnight at room temperature. The reaction mixture was then poured onto saturated aqueous sodium bicarbonate solution and extracted with ethyl acetate. The organic phase was washed with saturated aqueous sodium chloride solution, dried over sodium sulfate, filtered and concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 553 mg of the title compound as a colorless foam.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 7,95 d (J=8 Hz, 1H, aryl); 7,88 d (J=2 Hz, 1H, aryl); 7,77 ddbr (J=8 Hz + 2 Hz, 1H, aryl); 3,85 m (2H, CH2N); 3,44 m (4H, Piperazin); 2,78 m (2H, CH2N); 2,52 m (4H, Piperazin); 1,59 s (6H, CH3); 1,46 m (9H, fBu). 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 7.95 d (J = 8 Hz, 1H, aryl); 7.88 d (J = 2 Hz, 1H, aryl); 7.77 ddbr (J = 8 Hz + 2 Hz, 1H, aryl); 3.85 m (2H, CH 2 N); 3.44 m (4H, piperazine); 2.78 m (2H, CH 2 N); 2.52 m (4H, piperazine); 1.59 s (6H, CH 3); 1.46 m (9H, f Bu).
15c) 4-[4,4-Dimethyl-5-oxo-3-[2-(piperazin-1-yl)ethyl]-2-thioxoimidazolidin-1-yl]-2- (trifluormethyl)benzonitril15c) 4- [4,4-dimethyl-5-oxo-3- [2- (piperazin-1-yl) ethyl] -2-thioxoimidazolidin-1-yl] -2- (trifluoromethyl) benzonitrile
553 mg der unter 15b hergestellten Verbindung wurden mit 809 μl Trifluoressigsäure in 10 ml Dichlormethan 24 Stunden bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde im Vakuum eingeengt und mehrfach mit Toluol im Vakuum eingeengt, in Metha- noi aufgenommen, mit Anionenaustauscher (Bio-Rad AG 1-X8, OH-Form) auf einen pH-Wert von 8 bis 9 gestellt, filtriert und im Vakuum eingeengt. Man erhielt 426 mg der Titelverbindung als Rohprodukt, das in dieser Form weiter umgesetzt wurde.553 mg of the compound prepared under 15b were stirred with 809 μl trifluoroacetic acid in 10 ml dichloromethane for 24 hours at room temperature. The reaction mixture was concentrated in vacuo and concentrated several times with toluene in vacuo, taken up in methanol, adjusted to a pH of 8 to 9 with anion exchanger (Bio-Rad AG 1-X8, OH form), filtered and concentrated in vacuo concentrated. This gave 426 mg of the title compound as a crude product, which was reacted further in this form.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 7,95 d (J=8 Hz, 1H, aryl); 7,89 d (J=2 Hz, 1H, aryl); 7,77 ddbr (J=8 Hz + 2 Hz, 1H, aryl); 3,85 m (2H, CH2N); 2,91 m (4H, Piperazin); 2,76 m (2H, CH2N); 2,55 m (4H, Piperazin); 1,59 s (6H, CH3). 15d) 4-[3-[2-[4-(2-Methoxybenzoyl)piperazin-1 -yl]ethyl]-4,4-dimethyl-5-oxo-2- thioxoimidazolidin-1-yl]-2-(trifluormethyl)benzonitril 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 7.95 d (J = 8 Hz, 1H, aryl); 7.89d (J = 2Hz, 1H, aryl); 7.77 ddbr (J = 8 Hz + 2 Hz, 1H, aryl); 3.85 m (2H, CH 2 N); 2.91m (4H, piperazine); 2.76 m (2H, CH 2 N); 2.55 m (4H, piperazine); 1.59 s (6H, CH 3). 15d) 4- [3- [2- [4- (2-methoxybenzoyl) piperazine-1-yl] ethyl] -4,4-dimethyl-5-oxo-2-thioxoimidazolidin-1-yl] -2- (trifluoromethyl benzonitrile)
20 mg der unter 15c hergestellten Verbindung wurden mit 14 ml 2-Methoxybenzoyl- chlorid und 13,1 μl Triethylamin in 1 ml Tetrahydrofuran 4 Stunden unter Rückfluss erhitzt. Das Reaktionsgemisch wurde im Vakuum eingeengt. Säulenchromatographie an Kieselgel mit einem Gemisch aus Hexan/Ethylacetat ergibt 16 mg der Titelverbindung als farbloses Öl.20 mg of the compound prepared under 15c were refluxed with 14 ml of 2-methoxybenzoyl chloride and 13.1 μl of triethylamine in 1 ml of tetrahydrofuran for 4 hours. The reaction mixture was concentrated in vacuo. Column chromatography on silica gel with a mixture of hexane / ethyl acetate gives 16 mg of the title compound as a colorless oil.
1H-NMR (300 MHz, CDCI3): δ [ppm] = 7,95 d (J=8 Hz, 1H, aryl); 7,88 d (J=2 Hz, 1 H, aryl); 7,76 ddbr (J=8 Hz + 2 Hz, 1 H, aryl); 7,35 ddd (J=8 Hz + 7 Hz + 2 Hz, 1 H, aryl); 7,23 dd (J=7 Hz + 2 Hz, 1H, aryl); 6,99 dd (J=7 Hz + 7 Hz, 1 H, aryl); 6,91 dbr (J=8 Hz, 1 H, aryl); 3,85 m (2H, CH2N); 3,84 m (1H, Piperazin); 3,83 s (3H, OCH3); 3,81 m (1 H, Piperazin); 3,28 m (2H, Piperazin); 2,80 m (2H, CH2N); 2,67 m (1 H, Piperazin); 2,60 m (1H, Piperazin); 2,55 m (1 H, Piperazin); 2,47 m (1H, Piperazin); 1,59 s (6H, CH3). 1 H-NMR (300 MHz, CDCl 3 ): δ [ppm] = 7.95 d (J = 8 Hz, 1H, aryl); 7.88 d (J = 2 Hz, 1H, aryl); 7.76 ddbr (J = 8 Hz + 2 Hz, 1H, aryl); 7.35 ddd (J = 8 Hz + 7 Hz + 2 Hz, 1H, aryl); 7.23 dd (J = 7 Hz + 2 Hz, 1H, aryl); 6.99 dd (J = 7 Hz + 7 Hz, 1H, aryl); 6.91 dbr (J = 8 Hz, 1H, aryl); 3.85 m (2H, CH 2 N); 3.84m (1H, piperazine); 3.83 s (3H, OCH 3 ); 3.81m (1H, piperazine); 3.28m (2H, piperazine); 2.80 m (2H, CH 2 N); 2.67 m (1H, piperazine); 2.60 m (1H, piperazine); 2.55 m (1H, piperazine); 2.47 m (1H, piperazine); 1.59 s (6H, CH 3).
Die folgenden erfindungsgemäßen Verbindungen wurden analog zu den vorbeschriebenen hergestellt.The following compounds of the invention were prepared analogously to those described above.
Tab. 5. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 1Tab. 5. Compounds of the general formula I according to the invention, in which V = trifluoromethylbenzonitrile, W = maleimide, n = 1
Tab. 6. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 2Tab. 6. Compounds of the general formula I according to the invention, in which V = trifluoromethylbenzonitrile, W = maleimide, n = 2
Tab. 7. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 3Tab. 7. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = maleimide, n = 3
Tab. 8. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 4 Tab. 8. Compounds of the general formula I according to the invention, in which V = trifluoromethylbenzonitrile, W = maleimide, n = 4
Tab. 9. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 5Tab. 9. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = maleimide, n = 5
Tab. 10. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 6Tab. 10. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = maleimide, n = 6
Tab. 11. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 7Tab. 11. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = maleimide, n = 7
Tab. 12. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Maleimid, n = 8Tab. 12. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = maleimide, n = 8
Tab. 13. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylphenylacetamid, W = Maleimid, n = 6Tab. 13. Compounds of the general formula I according to the invention in which V = trifluoromethylphenylacetamide, W = maleimide, n = 6
Tab. 14. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Nitrotrifluormethylbenzol, W = Maleimid, n = 6 Tab. 14. Compounds of the general formula I according to the invention in which V = nitrotrifluoromethylbenzene, W = maleimide, n = 6
Tab. 15. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Bistrifluormethylbenzol, W = Maleimid, n = 6Tab. 15. Compounds of the general formula I according to the invention, in which V = bistrifluoromethylbenzene, W = maleimide, n = 6
Tab. 16. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Fluortrifluormethylbenzol, W = Maleimid, n = 6Tab. 16. Compounds of the general formula I according to the invention in which V = fluorotrifluoromethylbenzene, W = maleimide, n = 6
Tab. 17. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Maleimid, n = 4Tab. 17. Compounds of the general formula I according to the invention, in which V = isobenzofuranone, W = maleimide, n = 4
Tab. 18. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Maleimid, ^ = 5 ' Tab. 18. Compounds of the general formula I according to the invention in which V = isobenzofuranone, W = maleimide, ^ = 5 '
Tab. 19. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Maleimid, n = 6 Tab. 19. Compounds of the general formula I according to the invention, in which V = isobenzofuranone, W = maleimide, n = 6
Tab. 20. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V - Methylbenzoxazinon, W = Maleimid, n = 6Table 20. Compounds of the general formula I according to the invention in which V is methylbenzoxazinone, W is maleimide, n is 6
Tab. 21. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Indanon, W = Maleimid, n = 6Tab. 21. Compounds of the general formula I according to the invention in which V = indanone, W = maleimide, n = 6
Tab. 22. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Thiohydantoin, n = 2Tab. 22. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = thiohydantoin, n = 2
Tab. 23. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Thiohydantoin, n = 3 Tab. 23. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = thiohydantoin, n = 3
Tab. 24. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Thiohydantoin, n = 4Tab. 24. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = thiohydantoin, n = 4
Tab. 25. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Thiohydantoin, n = 5 Tab. 25. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = thiohydantoin, n = 5
Tab. 26. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Thiohydantoin, n = 6Tab. 26. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = thiohydantoin, n = 6
Tab. 27. Erfindungsgemäße Verbindungen der allgemeinen Formel worin V = Trifluormethylbenzonitril, W = Thiohydantoin, n = 7Tab. 27. Compounds of the general formula according to the invention wherein V = trifluoromethylbenzonitrile, W = thiohydantoin, n = 7
Tab. 28. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Trifluormethylbenzonitril, W = Thiohydantoin, n = 8Tab. 28. Compounds of the general formula I according to the invention in which V = trifluoromethylbenzonitrile, W = thiohydantoin, n = 8
Tab. 29. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Thiohydantoin, n = 3Tab. 29. Compounds of the general formula I according to the invention in which V = isobenzofuranone, W = thiohydantoin, n = 3
Tab. 30. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Thiohydantoin, n = 4Table 30. Compounds of the general formula I according to the invention in which V = isobenzofuranone, W = thiohydantoin, n = 4
Tab. 31. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Thiohydantoin, n = 5 Tab. 31. Compounds of the general formula I according to the invention in which V = isobenzofuranone, W = thiohydantoin, n = 5
Tab. 32. Erfindungsgemäße Verbindungen der allgemeinen Formel worin V = Isobenzofuranon, W = Thiohydantoin, n = 6Table 32. Compounds of the general formula of the invention wherein V = isobenzofuranone, W = thiohydantoin, n = 6
Tab. 33. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Thiohydantoin, n = 7 Table 33. Compounds of the general formula I according to the invention in which V = isobenzofuranone, W = thiohydantoin, n = 7
Tab. 34. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Isobenzofuranon, W = Thiohydantoin, n = 8 Tab. 34. Compounds of the general formula I according to the invention in which V = isobenzofuranone, W = thiohydantoin, n = 8
Tab. 35. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Methylbenzoxazinon, W = Thiohydantoin, n = 5Tab. 35. Compounds of the general formula I according to the invention in which V = methylbenzoxazinone, W = thiohydantoin, n = 5
Tab. 36. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Methylbenzoxazinon, W = Thiohydantoin, n = 6Tab. 36. Compounds of the general formula I according to the invention in which V = methylbenzoxazinone, W = thiohydantoin, n = 6
Tab.37. Erfindungsgemäße Verbindungen der allgemeinen Formel I, worin V = Indanon, W = Thiohydantoin, n = 6Tab.37. Compounds of the general formula I according to the invention in which V = indanone, W = thiohydantoin, n = 6
Claims
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2002360932A AU2002360932A1 (en) | 2001-11-23 | 2002-10-31 | Piperazine derivatives destabilising androgen receptors |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10159035.0 | 2001-11-23 | ||
| DE2001159035 DE10159035A1 (en) | 2001-11-23 | 2001-11-23 | New N-(maleimidyl- or thiohydantoinyl-alkyl)-piperazine derivatives, are androgen receptor destabilizers and/or inhibitors useful e.g. for treating prostate carcinoma or hyperplasia |
| DE2002138742 DE10238742A1 (en) | 2002-08-19 | 2002-08-19 | New N-(maleimidyl- or thiohydantoinyl-alkyl)-piperazine derivatives, are androgen receptor destabilizers and/or inhibitors useful e.g. for treating prostate carcinoma or hyperplasia |
| DE10238742.7 | 2002-08-19 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2003043983A1 true WO2003043983A1 (en) | 2003-05-30 |
Family
ID=26010698
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2002/012182 Ceased WO2003043983A1 (en) | 2001-11-23 | 2002-10-31 | Piperazine derivatives destabilising androgen receptors |
Country Status (5)
| Country | Link |
|---|---|
| AU (1) | AU2002360932A1 (en) |
| PE (1) | PE20030708A1 (en) |
| TW (1) | TW200301117A (en) |
| UY (1) | UY27544A1 (en) |
| WO (1) | WO2003043983A1 (en) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003086398A1 (en) * | 2002-04-05 | 2003-10-23 | Abbott Laboratories | Aminocarbonyl substituted pyridines, pyridazines, pyrimidines, pyrazines and triazines having antiangiogenic activity |
| FR2847160A1 (en) * | 2002-11-20 | 2004-05-21 | Oreal | HAIR COMPOSITION CONTAINING A PYRASOL-CARBOXAMIDE COMPOUND, ITS USE FOR STIMULATING HAIR GROWTH AND / OR BRAKING FALLING |
| WO2004047776A1 (en) * | 2002-11-20 | 2004-06-10 | L'oreal | Composition for hair care or eyelashes containing a pyrazol-carboxamide, its use for stimulating hair and eyelash growth and/or for preventing loss thereof |
| EP1798227A4 (en) * | 2004-09-09 | 2009-09-09 | Res Found Itsuu Lab | Serotonin 5-ht3 receptor agonist |
| US7592466B2 (en) | 2003-10-09 | 2009-09-22 | Abbott Laboratories | Ureas having antiangiogenic activity |
| EP1722781A4 (en) * | 2004-02-22 | 2010-07-21 | Us Gov Health & Human Serv | ANTITUMOR PHOSPHATASE INHIBITORS BASED ON MALEIIMIDE |
| CN102464631A (en) * | 2010-11-08 | 2012-05-23 | 中国科学院上海药物研究所 | Piperazine substituted 1,3-disubstitued urea compounds and piperazine substituted amide compounds, preparation method, and use thereof |
| WO2013102249A1 (en) * | 2012-01-05 | 2013-07-11 | Universidade Federal Do Rio De Janeiro-Ufrj | N-phenylpiperazine derivatives that are antagonists of α1a, α1d adrenoceptors and 5-ht1a receptors for the treatment of benign prostate hyperplasia, pharmaceutical compositions containing the same |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI813106B (en) * | 2020-12-30 | 2023-08-21 | 財團法人工業技術研究院 | Androgen receptor binding molecule and use thereof |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0580459A1 (en) * | 1992-07-08 | 1994-01-26 | Roussel Uclaf | Substituted Phenylimidazolidins, process for their preparation, their use as medicaments and their pharmaceutical compositions containing them |
| WO1997000071A1 (en) * | 1995-06-16 | 1997-01-03 | Biophysica Foundation | Androgenic directed compositions |
| US5859014A (en) * | 1995-06-09 | 1999-01-12 | Syntex (U.S.A.) Inc. | Pyrimidinedione, pyrimidinetrione, triazinedione and tetrahydroquinazolinedione derivatives as α1 -adrenergic receptor antagonists |
| EP1122242A1 (en) * | 1998-09-22 | 2001-08-08 | Yamanouchi Pharmaceutical Co. Ltd. | Cyanophenyl derivatives |
-
2002
- 2002-10-31 WO PCT/EP2002/012182 patent/WO2003043983A1/en not_active Ceased
- 2002-10-31 AU AU2002360932A patent/AU2002360932A1/en not_active Abandoned
- 2002-11-21 UY UY27544A patent/UY27544A1/en not_active Application Discontinuation
- 2002-11-22 PE PE2002001124A patent/PE20030708A1/en not_active Application Discontinuation
- 2002-11-22 TW TW091134064A patent/TW200301117A/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0580459A1 (en) * | 1992-07-08 | 1994-01-26 | Roussel Uclaf | Substituted Phenylimidazolidins, process for their preparation, their use as medicaments and their pharmaceutical compositions containing them |
| US5859014A (en) * | 1995-06-09 | 1999-01-12 | Syntex (U.S.A.) Inc. | Pyrimidinedione, pyrimidinetrione, triazinedione and tetrahydroquinazolinedione derivatives as α1 -adrenergic receptor antagonists |
| WO1997000071A1 (en) * | 1995-06-16 | 1997-01-03 | Biophysica Foundation | Androgenic directed compositions |
| EP1122242A1 (en) * | 1998-09-22 | 2001-08-08 | Yamanouchi Pharmaceutical Co. Ltd. | Cyanophenyl derivatives |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003086398A1 (en) * | 2002-04-05 | 2003-10-23 | Abbott Laboratories | Aminocarbonyl substituted pyridines, pyridazines, pyrimidines, pyrazines and triazines having antiangiogenic activity |
| FR2847160A1 (en) * | 2002-11-20 | 2004-05-21 | Oreal | HAIR COMPOSITION CONTAINING A PYRASOL-CARBOXAMIDE COMPOUND, ITS USE FOR STIMULATING HAIR GROWTH AND / OR BRAKING FALLING |
| WO2004047776A1 (en) * | 2002-11-20 | 2004-06-10 | L'oreal | Composition for hair care or eyelashes containing a pyrazol-carboxamide, its use for stimulating hair and eyelash growth and/or for preventing loss thereof |
| US7592466B2 (en) | 2003-10-09 | 2009-09-22 | Abbott Laboratories | Ureas having antiangiogenic activity |
| EP1722781A4 (en) * | 2004-02-22 | 2010-07-21 | Us Gov Health & Human Serv | ANTITUMOR PHOSPHATASE INHIBITORS BASED ON MALEIIMIDE |
| EP1798227A4 (en) * | 2004-09-09 | 2009-09-09 | Res Found Itsuu Lab | Serotonin 5-ht3 receptor agonist |
| CN102464631A (en) * | 2010-11-08 | 2012-05-23 | 中国科学院上海药物研究所 | Piperazine substituted 1,3-disubstitued urea compounds and piperazine substituted amide compounds, preparation method, and use thereof |
| CN102464631B (en) * | 2010-11-08 | 2016-08-10 | 中国科学院上海药物研究所 | Piperazine substituted 1,3-2-substituted carbamide compounds and the substituted amides compound of piperazine and its production and use |
| WO2013102249A1 (en) * | 2012-01-05 | 2013-07-11 | Universidade Federal Do Rio De Janeiro-Ufrj | N-phenylpiperazine derivatives that are antagonists of α1a, α1d adrenoceptors and 5-ht1a receptors for the treatment of benign prostate hyperplasia, pharmaceutical compositions containing the same |
Also Published As
| Publication number | Publication date |
|---|---|
| UY27544A1 (en) | 2003-06-30 |
| TW200301117A (en) | 2003-07-01 |
| AU2002360932A1 (en) | 2003-06-10 |
| PE20030708A1 (en) | 2003-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6861432B2 (en) | Piperazine derivatives that destabilize androgen receptors | |
| DE60001190T2 (en) | Aminotriazole compounds, processes for their preparation and pharmaceutical compositions containing them | |
| DE3875073T2 (en) | 3- (4 (1-SUBSTITUTED-4-PIPERAZINYL) BUTYL) -4-THIAZOLIDINONE, METHOD FOR THE PRODUCTION THEREOF AND THEIR USE AS A MEDICINAL PRODUCT. | |
| DE2836073A1 (en) | NEW NITROIMIDAZOLES AND METHOD FOR MANUFACTURING THEREOF | |
| DE10322108B4 (en) | Antiandrogenic pyrrolidines with antitumor activity | |
| DE602005005456T2 (en) | NEW AZABIC DERIVATIVES, METHOD OF MANUFACTURING THE SAME AND PHARMACEUTICAL COMPOSITIONS CONTAINING THEM | |
| DE2638184A1 (en) | SUBSTITUTED PHENYL-PIPERAZINE-N-OXIDES, PROCESS FOR THEIR MANUFACTURING AND MEDICINAL PRODUCTS CONTAINING THEM | |
| EP1124809B1 (en) | Benzoylpyridazines | |
| WO2003043983A1 (en) | Piperazine derivatives destabilising androgen receptors | |
| DE60222286T2 (en) | PROCESS FOR INCREASING THE TESTOSTERONE MIRROR | |
| DE60010126T2 (en) | BRANCHED SUBSTITUTED AMINO DERIVATIVES OF 3-AMINO-1-PHENYL-1H (1,2,4) TRIAZOL, PROCESS FOR THE PREPARATION THEREOF AND PHARMACEUTICAL COMPOSITIONS CONTAINING THE SAME | |
| DD202433A5 (en) | PROCESS FOR THE PREPARATION OF AMIDOBENZAMIDES | |
| EP0445073A1 (en) | Benzofurans | |
| EP1903037A1 (en) | 1-(hetero)aryl-3-[heteroaryl-piperidin-4yl]-thiourea derivatives as modulators of EP2 receptors | |
| DE3618724C2 (en) | N- [3- (Nitro) -quinol-4-yl] carboxamidinamides, process for their preparation and medicaments containing these compounds | |
| EP0298921B1 (en) | 1,2-benzisoxazoles and 1,2-benzisothiazoles | |
| WO1992010482A1 (en) | Pharmaceutical compositions containing functionalized vinylazoles, use of these vinylazoles for producing medicaments, these vinylazoles themselves and process for producing the same | |
| EP0346683A1 (en) | Pyrrole derivatives, their preparation and their use | |
| DE10238742A1 (en) | New N-(maleimidyl- or thiohydantoinyl-alkyl)-piperazine derivatives, are androgen receptor destabilizers and/or inhibitors useful e.g. for treating prostate carcinoma or hyperplasia | |
| DE10159035A1 (en) | New N-(maleimidyl- or thiohydantoinyl-alkyl)-piperazine derivatives, are androgen receptor destabilizers and/or inhibitors useful e.g. for treating prostate carcinoma or hyperplasia | |
| DE4120107A1 (en) | BICYCLICALLY SUBSTITUTED VINYLIMIDAZOLES, TRIAZOLES AND TETRAZOLES | |
| DE102009049662A1 (en) | 2,5-disubstituted 2H-indazoles as EP2 receptor antagonists | |
| DD234005A5 (en) | PROCESS FOR THE PREPARATION OF NEW 1,2,4-TRIAZACYCLOALKADIEN DERIVATIVES | |
| DE112012005325T5 (en) | Nitrofurfuryl-substituted phenyl-linked piperidino-oxadiazoline conjugates as tuberculosis agents and process for their preparation | |
| EP0287988A2 (en) | Pyrrole aldehydes, their preparation and use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AE AG AL AM AT AU AZ BA BB BG BR BY BZ CA CH CN CO CR CU CZ DK DM DZ EC EE ES FI GB GD GE GH GM HR HU ID IL IN IS JP KE KG KP KR KZ LC LK LR LS LT LU LV MA MD MG MK MN MW MX MZ NO NZ OM PH PL PT RO RU SD SE SG SI SK SL TJ TM TN TR TT TZ UA UG UZ VC VN YU ZA ZM ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): GH GM KE LS MW MZ SD SL SZ TZ UG ZM ZW AM AZ BY KG KZ MD RU TJ TM AT BE BG CH CY CZ DE DK EE ES FI FR GB GR IE IT LU MC NL PT SE SK TR BF BJ CF CG CI CM GA GN GQ GW ML MR NE SN TD TG |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| 122 | Ep: pct application non-entry in european phase | ||
| NENP | Non-entry into the national phase |
Ref country code: JP |
|
| WWW | Wipo information: withdrawn in national office |
Country of ref document: JP |