WO2003000697A1 - Furoisoquinoline derivative, process for producing the same, and use - Google Patents
Furoisoquinoline derivative, process for producing the same, and use Download PDFInfo
- Publication number
- WO2003000697A1 WO2003000697A1 PCT/JP2002/006158 JP0206158W WO03000697A1 WO 2003000697 A1 WO2003000697 A1 WO 2003000697A1 JP 0206158 W JP0206158 W JP 0206158W WO 03000697 A1 WO03000697 A1 WO 03000697A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- alkyl
- substituent
- atom
- ruponiru
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Definitions
- the present invention has a phosphodiesterase (PDE) IV inhibitory effect, and has an inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, Alzheimer's dementia, memory impairment, diabetes, arteriosclerosis
- PDE phosphodiesterase
- the present invention relates to novel freusoquinoline derivatives useful as preventive and therapeutic agents, their production methods and uses. Background art
- cAMP cyclic guanosine-3 ', 5'-phosphate
- the PDE has identified 11 isozymes, [Proceedings of the National Academy of Sciences of the National Academy of Sciences of the United States. 97, p. 3702 (2000).], in various cells such as the central, circulatory, respiratory, digestive, genital, blood cells, and tracheal smooth muscle. Regulates intracellular cAMP and cGMP levels and regulates cell functions. It is known that inflammatory cells such as eosinophils, neutrophils, monocytes, T-lymphocytes, and macrophages mainly contain PDE IV, one of the isozymes of PDE. Perimental allergy (Clinical and Experimental Allergy), 22, 337 (1992).].
- bronchodilators e.g., beta-adrenergic receptor agonists
- anti-inflammatory drugs e.g., corticosteroids
- xanthine derivatives having both bronchodilator and anti-inflammatory effects
- theophylline has been widely used as a therapeutic agent for asthma since ancient times. It has been shown that theophylline's bronchodilator activity is based on PDE inhibitory activity, and has recently attracted attention. However, theophylline is a non-selective PDE inhibitor, and cardiovascular side effects are often observed and require strict control of blood levels. Therefore, there is a demand for a therapeutic drug for inflammatory diseases such as asthma that selectively inhibits only PDE IV and does not act on other PDE isozymes.
- PDE IV selective inhibitors may be effective therapeutic agents for inflammatory diseases such as asthma [Pulmonary Pharmacology, 7, 1 (1994) ⁇ ].
- inflammatory diseases such as asthma [Pulmonary Pharmacology, 7, 1 (1994) ⁇ ].
- PDE IV selective inhibitory action As a compound having a PDE IV selective inhibitory action,
- W001 / 70746 includes, as a compound having a PDE IV selective inhibitory action, The compound which has the partial structure represented by these is disclosed.
- W002 / 04455 includes a formula as a therapeutic agent for neurological and psychiatric deficiencies based on the reuptake inhibitory effect of the norepinephrine transporter protein.
- R 1 is - 6 have alkyl, C 2 _ 6 alkenyl, C 2 _ 6 alkynyl, C 3 6 consequent opening alkyl, a C 4 _ 7 cycloalkylalkyl or base Njiru (These particular substituent May be)
- R 2 is a hydrogen atom, alkyl, C 26 alkenyl, C 2 _ 6 alkynyl, C. 6 A cycloalkyl, C 4 7 cycloalkylalkyl or C ⁇ 6 eight-necked alkyl,
- R 3 is a hydrogen atom, a halogen atom, alkyl, haloalkyl or C 3 _ 6 cycloalkyl (said C i 6 alkyl, (6 haloalkyl, C 3 6 cycloalkyl may have a specific substituent),
- R 4 , R 5 and R 6 each independently represent a hydrogen atom, a halogen atom, nitro, etc., and R 7 represents a hydrogen atom, a halogen atom, etc.
- the present invention provides a novel heterocyclic compound having a selective inhibitory effect on PDE IV, a bronchodilator effect and an anti-inflammatory effect by increasing the intracellular cAMP concentration, and further having excellent safety and other aspects.
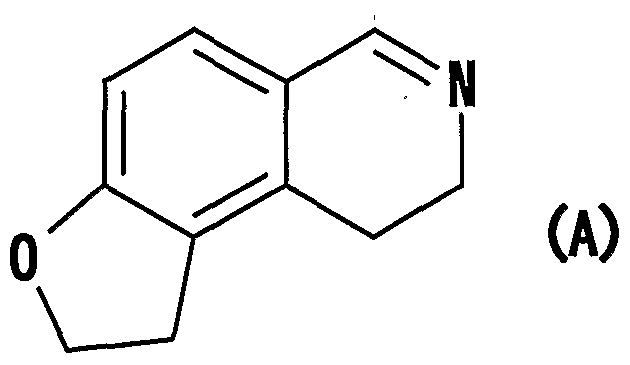
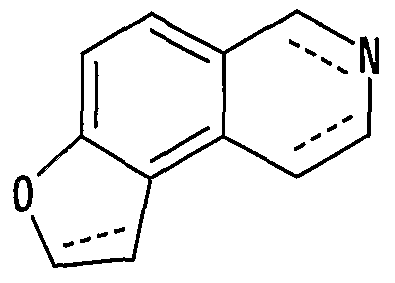
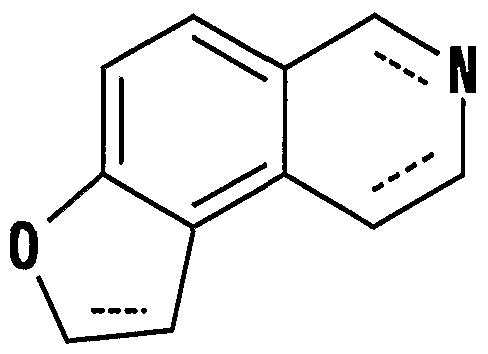
- a novel furoisoquinoline compound having a partial structure represented by the following formula (hereinafter abbreviated as compound (I) )
- compound (I) A novel furoisoquinoline compound having a partial structure represented by the following formula (hereinafter abbreviated as compound (I) )
- compound (I) A novel furoisoquinoline compound having a partial structure represented by the following formula (hereinafter abbreviated as compound (I) )
- compound (I) A novel furoisoquinoline compound having a partial structure represented by the following formula (hereinafter abbreviated as compound (I) )
- it has a great chemical structural characteristic when a substituent is introduced at the 1st, 2nd, 4th, 5th, 6th, 7th, 8th, 9th, etc. positions of the furoisoquinoline skeleton .
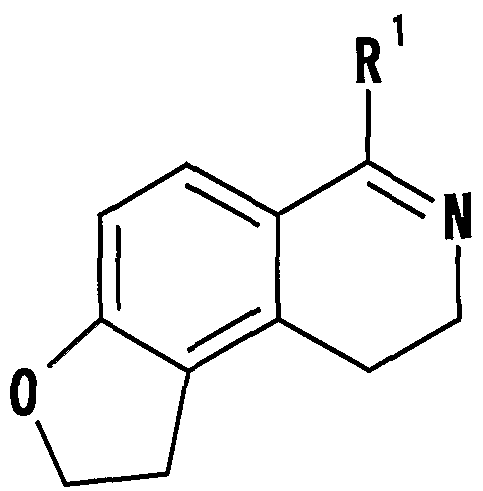
- R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent
- R 2 and R 3 each represent a hydrogen atom or a substituent.
- R 2 and R 3 may have a substituent together with adjacent carbon atoms to form a 3- to 8-membered ring.
- R 4 and R 5 each represent a hydrogen atom or a hydrocarbon group which may have a substituent
- R 6 and R 7 each represent a hydrogen atom or a hydrocarbon group which may have a substituent
- 13 ⁇ 4 6 and 1 ⁇ 7 may form a 8-membered ring to 3 which may have a substituent together with the adjacent carbon atoms
- R 8 is (1) a hydrogen atom, Yure (2) substituent hydrocarbon group which may be substituted, (3) Ashiru group, (4) an optionally substituted heterocyclic group, (5) halogen atom, (6) -OR 10
- R 1Q is a hydrogen atom Substituent has optionally may hydrocarbon group, was Ashiru group or indicates a heterocyclic group which may have a substituent
- (7) -SR 11 R 11 is a hydrogen atom, a substituent A hydrocarbon group, an acyl group or an optionally substituted heterocyclic group
- (8) -S (0) R 12 where R 12 has a substituent A
- R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent] or a salt thereof.
- R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent
- R 2 and R 3 each represent a hydrogen atom or a substituent.
- R 2 and R 3 may form a 3- to 8-membered ring which may have a substituent together with an adjacent carbon atom
- R 6 and R 7 each represent a hydrogen atom or an optionally substituted hydrocarbon group
- R 6 And R 7 may form a 3- to 8-membered ring which may have a substituent together with an adjacent carbon atom
- R 8 is (1) a hydrogen atom, or (2) A good hydrocarbon group, (3) an acyl group, (4) an optionally substituted heterocyclic group, (5) a halogen atom, (6) -OR 10 (R 1Q is a hydrogen
- R 1 represents any of the following (i) or (ii): (i) (1) halogen atom, (2) alkylenedioxy group, (3) nitro group,
- R 2 and R 3 each represent one of the following (i) to (iii):
- (iii) said may have 1 to 5 substituents selected from the substituent group A, E mill, force Rupokishi force Rubamoiru, alkyl Ichiriki Ruponiru, C 3 - 6 cycloalkyl Alkyl - carbonyl, C 6 alkoxy Ichiriki Ruponiru, c 6 _ 14 ⁇ Li one Rukarubo alkenyl, C 7 _ 16 Ararukiru Ichiriki Ruponiru, C 6 _ 14 Ariruokishi Ichiriki Ruponiru, C
- Ichiriki 7 _ 16 Ararukiruokishi Ruponiru nitrogen atom in addition to carbon atom, a sulfur atom and 1 to containing heteroatoms three of the 5 or 6-membered heterocyclic force Ruponiru selected from oxygen atom, mono- C - 6 alkyl Ichiriki Rubamoiru, di - 6 alkyl - power resolver moil, c 6 - 14 Ariru Ichiriki Rubamoiru, nitrogen atom in addition to carbon atoms, 5 or containing 1 to heteroatoms three of the selected sulfur atom Contact and oxygen atom 6 membered double ring force Rubamoiru, C _ 6 alkyl one Chiokaruponiru, C 3 _ 6 cycloalkyl over Ji Okaruboniru, C 6 alkoxy - Chio force Ruponiru, C 6 _ 14 ⁇ Li one Ruchiokarupo alkenyl, c 7 _ 16 Ararukiru one Chiokaruponir
- R 2 and R 3 together with the adjacent carbon atom, alkyl, C 6 _ 14 7 reel, C 7 - 16 Ararukiru, Amino, mono- Arukiruamino, mono- C 6 - 14 Arirua amino, di- (: Preparative 6 Arukiruamino, di one C 6 — 14 arylamino and a C 3 _ 8 cycloalkane optionally having 1 to 3 substituents selected from a 4- to 10-membered aromatic heterocyclic group or a 3- to 8-membered heterocyclic group Often ;
- R 4 and R 5 may have, respectively (i) a hydrogen atom or (ii) the substituent, 1 to selected Ru substituents from group A 5 each - 6 alkyl group, C 2 _ 6 Al Kenyir group, c 2 - 6 alkynyl group, c 3 _ 6 cycloalkyl group, c 3 - 6 Shikuroaruke two Le group, c 6 _ 14 Ariru group or c 7 - 16 Ararukiru group;
- R 6 and R 7 are each (i) a hydrogen atom or (ii) an alkyl group, a C 2 _ 6 alkenyl group which may have 1 to 5 substituents each selected from the aforementioned substituent group A, C 2 _ 6 alkynyl, C 3 - 6 cycloalkyl group, C 3 _ 6 Shikuroaruke two Le group, C 6 - 14 Ariru radical or C 7 - 16 show the Ararukiru group,
- R 6 and R 7 together with the adjacent carbon atom, alkyl, C 6 one 14 Ariru, C 7 _ 1 6 Ararukiru, Amino, mono- - 6 Arukiruamino, mono- C 6 _ 14 Arirua amino, di- (6 Arukiruamino, di C 6 - 14 to Ariruamino and 3 good C 3 no one 8 cycloalkane or 3 have respectively, 1 to substituents selected from 4- to 10-membered aromatic heterocyclic group may form a 8-membered heterocyclic ring;
- R 8 represents one of the following (i) to (X):
- the substituents selected from substituent group A may have 1 to have five, Ho mill, carboxy, force Rubamoiru, CI- 6 alkyl one carbonyl, C 3 one 6 cycloalkyl - Power Ruponiru, C ⁇ _ 6 alkoxy Ichiriki Ruponiru, C 6 _ 14 Ariru Ichiriki Lupo El, C 7 _ 16 Ararukiru Ichiriki Ruponiru, C 6 - 14 Ariruokishi Ichiriki Ruponiru, C 7 _ 16 Ararukiruokishi Ichiriki Ruponiru, in addition to carbon atoms nitrogen atom, sulfur atom and 1 to containing heteroatoms three of the 5 or 6-membered heterocyclic force Ruponiru selected from oxygen atom, mono-one C DOO 6 alkyl - force Rubamoiru, di - alkyl Ichiriki resolver moil, C 6 - 14 Ariru Ichiriki Rubamoiru, nitrogen atom,
- R 1Q is (i ′) a hydrogen atom, and (ii ′) a C i-6 alkyl group which may have 1 to 5 substituents each selected from the aforementioned substituent group A.
- R 12 is (i,) a Ci- 6 alkyl group optionally having 1 to 5 substituents selected from the aforementioned substituent group A, C 2 - 6 alkenyl, C 2 one 6 alkynyl group, C 3 _ 6 cycloalkyl group, C 3 - 6 cycloalkenyl group, C 6 - 14 ⁇ aryl group or C 7 - 16 Ararukiru group or (ii ') the substituent Group A 5- to 14-membered heterocyclic ring containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may have 1 to 5 substituents selected from group A ),
- R 13 is (i,) an alkyl group optionally having 1 to 5 substituents selected from the above-mentioned substituent group A, C 2 _ 6 alkenyl group, C 2 _ 6 alkynyl, C 3 _ 6 cycloalkyl group, C 3 - 6 cycloalkenyl group, (6 - 14 ⁇ aryl group or ⁇ 7 _ 16 Ararukiru group or (ii,) the substituent group A A 5- to 14-membered heterocyclic ring containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may have 1 to 5 substituents selected from) ,
- R 14 and R 15 are each a ( ⁇ ′) hydrogen atom, (ii,) the above substitution , 1 to substituents selected from group A five may have respective C ⁇ 6 Al kill groups, C 2 - 6 alkenyl groups, C 2 - 6 alkynyl groups, C 3 _ 6 cycloalkyl groups, C 3 - 6 cycloalkenyl group, (6 _ 14 Ariru group or C 7 _ 16 Ararukiru group, (iii 5) said may have 1 to 5 substituents selected from the substituent group a, formyl, Karupamoiru , alkyl Ichiriki Ruponiru, C 3 - 6 cycloalkyl - force Ruponiru, alkoxy Ichiriki Ruponiru, C 6 - 14 Ariru Ichiriki Ruponiru, C 7 - 16 Araruki Lou force Ruponiru, C 6 _ 14 ⁇ Li one Ruok
- R 9 is (i) a hydrogen atom, (ii) a cyano group,
- 1 to substituents selected from the substituent group A may have five, respectively - 6 alkyl group, C 2 _ 6 alkenyl, C 2 - 6 alkynyl group, C 3 - 6 Shikuroa alkyl group, C 3 _ 6 cycloalkenyl group, C 6 _ 14 Ariru group or C 7 - 16 Araruki group,
- the substituents selected from substituent group A may have 1-5 amino acids, formyl, carboxy, force Rubamoiru, ⁇ - 6 alkyl - carbonyl, C 3 _ 6 Shikuroa Ruki Lou carbonyl, C _ 6 alkoxy - force Ruponiru, C 6 _ 14 ⁇ Li one Roux force Lupo two Le, C 7 _ 6 Ararukiru Ichiriki Ruponiru, C 6 - 14 ⁇ Li one Ruokishi - force Ruponiru, C 7 - 16 Ararukiruokishi Ichiriki Ruponiru, nitrogen atom in addition to carbon atoms, to 1 selected from sulfur atom and oxygen radicals three of the 5 or 6-membered heterocyclic ring force containing heteroatoms Ruponiru, mono one C Bok 6 alkyl - force Rubamoiru, di - CI- 6- alkyl-carbamoyl, 4- aryl-lubamoyl, 5-
- 1 to substituents selected from the substituent group A may have five each C Bok 6 alkyl group, C 2 _ 6 alkenyl, C 2 _ 6 alkynyl, C 3 _ 6 cycloalkyl Le group , C 3 - 6 cycloalkenyl group, C 6 _ 14 ⁇ Li Ichiru group or C 7 _ 16 Ararukiru group or,
- said substituent selected from the substituent group A may have 1-5 amino acids, formyl, force Rubamoiru, C WINCH 6 alkyl one carbonyl, C 3 - 6 cycloalkyl Ichiriki Ruponiru, c i_ 6 alkoxy one power Ruponiru, c 6 _ 14 ⁇ Li one Roux carbonyl, c 7 _ 16 Araruki Lou force Ruponiru, c 6 - 14 Ariruokishi - force Ruponiru, c 7 - 16 Ararukiruokishi Ichiriki Ruponiru, nitrogen atom in addition to carbon atom, sulfur atom and 5- or 6-membered heterocyclic carbonyl containing 1 to 3 heteroatoms selected from oxygen atoms, mono-C 6 alkyl mono-rubamoyl, di-C r — 6 alkyl mono-rubamoyl, C 6 — 14 aryl mono-rubamoyl , nitrogen atom in addition to carbon
- X is 1a methylene group which may have a substituent selected from the above-mentioned substituent group A or 2a carpenyl group;
- R 2 and R 3 are each ( ⁇ _ 6 alkyl group [3]
- R 4 and R 5 are the represents a hydrogen atom, respectively [3]
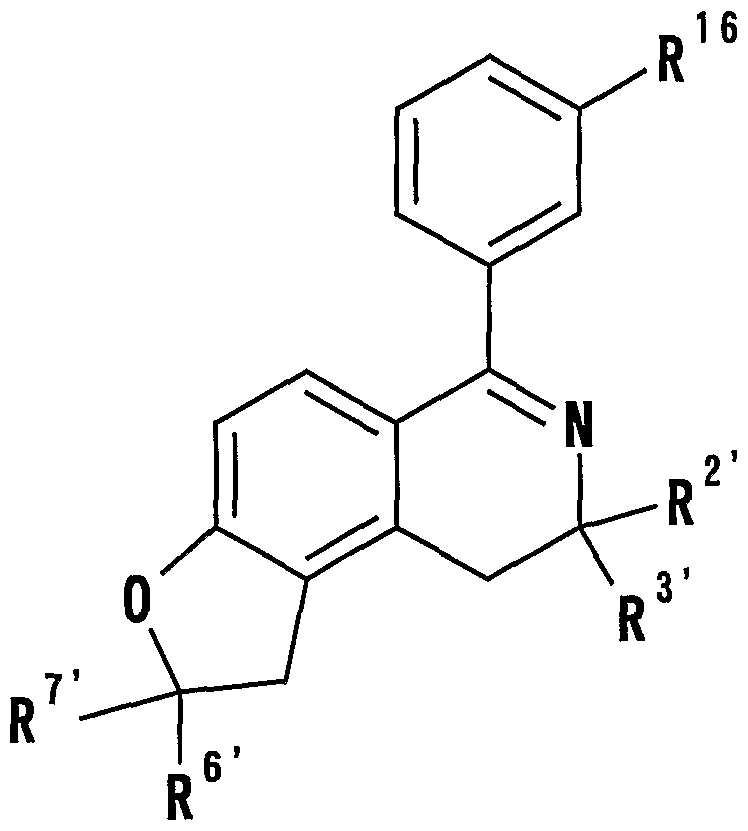
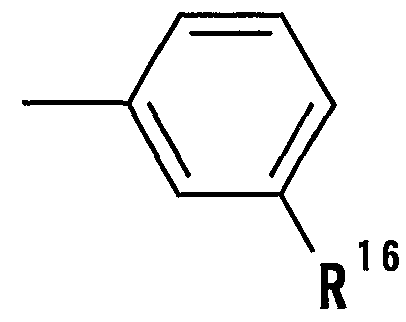
- R 1 is the formula
- R 16 is a hydrogen atom, which may have a substituent C 6 - 14 Ariru group, an optionally substituted amino group, heterocyclic group which may have a substituent R 2 and R 3 each represent an alkyl group; R 4 and R 5 each represent a hydrogen atom; R 6 and R 7 each represent a Ci- 6 alkyl group; and R 8 represents a halogen atom.
- a hydrogen atom or a monovalent R 1Q (R 1Q represents a hydrogen atom, which may have a substituent—a 6-alkyl group or an acyl group), R 9 represents a hydrogen atom, and n represents 0; 3] The compound as described;
- R 1 () is (1) a hydrogen atom, (2) a C— 6 alkyl group optionally substituted with pyridyl, or (3) a Ct- 6 alkylsulfonyl substituted with a halogen atom
- R 16 is selected from (1) hydrogen atom, (2) phenyl substituted by acetylamino, (S Ci- 6 alkylsulfonyl group, (ii) pyridyl carpoel or (iii) sulfamoyl-Ci-e alkyl group
- the compound of the above-mentioned [10] which represents an amino which may be mono- or di-substituted by a substituent, (4) a pyridyl or (5) a halogen atom;
- R 17 represents a vinyl group or an aryl group which may have a substituent] or a compound having a partial structure represented by the formula:
- R 1 has the same meaning as described in the above [2]] or a salt thereof.
- R 1 is as defined above; or a method for producing a compound having a partial structure represented by the formula:
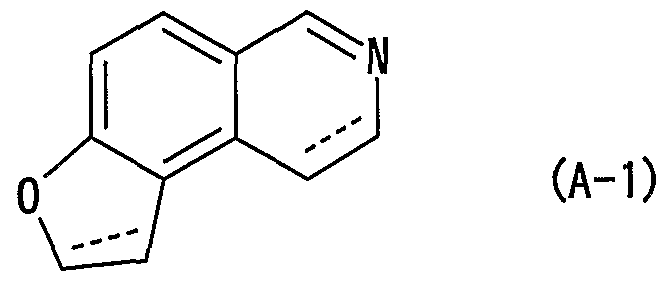
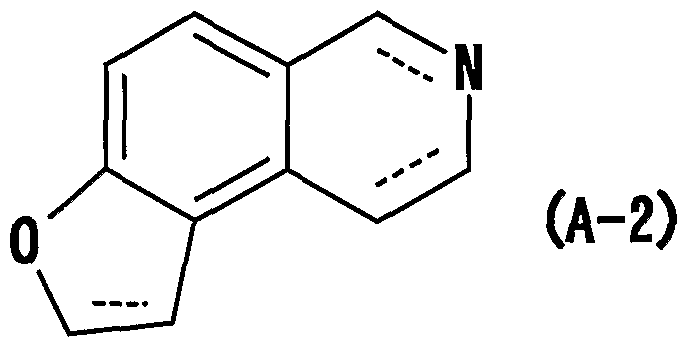
- ninini represents a single bond or a double bond
- compound (A-1) ninini represents a single bond or a double bond
- R 16' is hydrogen atom, which may have a substituent ⁇ 6 _ 14 Ariru group, a substituted An amino group which may have a group, a heterocyclic group which may have a substituent or a halogen atom], or a salt thereof.
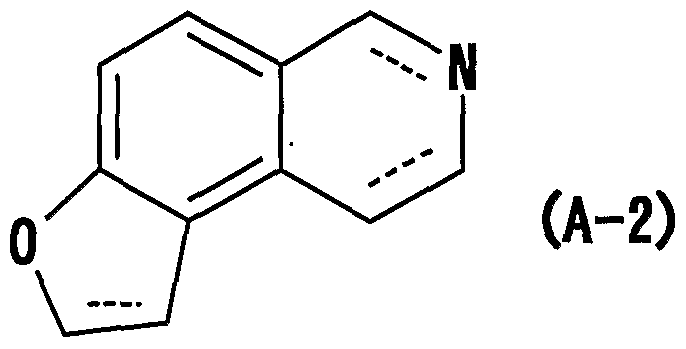
- JI represents a single bond or a double bond
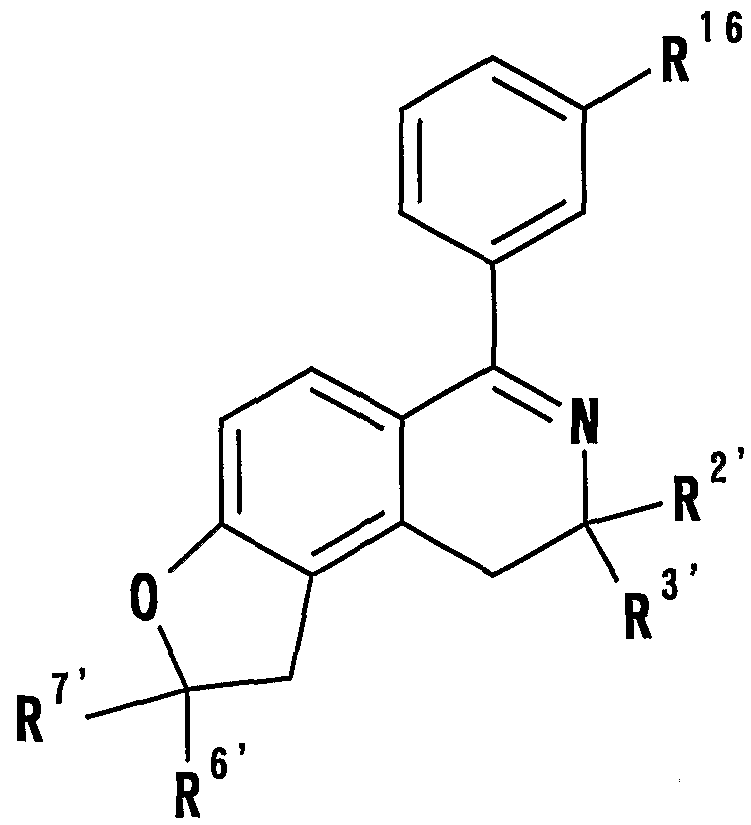
- a compound having a partial structure represented by Prophylactic / therapeutic agents for autoimmune diseases depression, Alzheimer's dementia, memory impairment, diabetes or arteriosclerosis;
- R 2 ', R 3 ,, R 6' and R 7 ' is a C ⁇ 6 alkyl groups, respectively, R 16, are hydrogen atoms, which may have a substituent C 6 _ 14 Ariru group Represents an amino group which may have a substituent, a heterocyclic group which may have a substituent or a halogen atom), or an effective amount of a salt thereof.
- ninii represents a single bond or a double bond
- R 2 , R 3 , R 6 , and R 7 ′ are each —6 alkyl groups
- R 16 is a hydrogen atom, and a C 6 14 aryl group which may have a substituent.
- ⁇ represents a single bond or a double bond
- ⁇ Z represents a single bond or a double bond
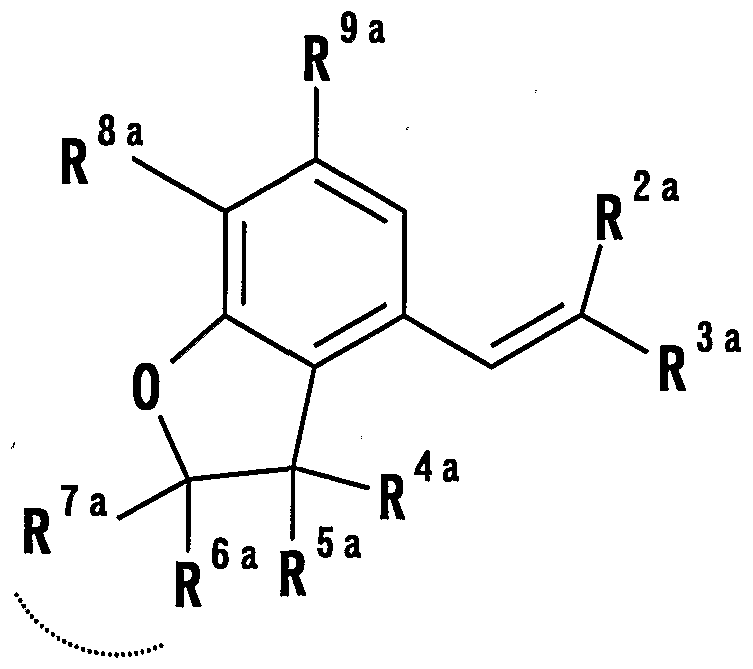
- R 2a and an R 3a are each an aliphatic substituted hydrocarbon group
- R 4a and R 5 a may hydrocarbons which also each have a hydrogen atom or a substituent group
- R 6 a and R 7a each represents a hydrogen atom or an optionally substituted carbon hydrocarbon radical
- R 6a and R 7a are optionally substituted with adjacent carbon atoms
- R 8a may form a (1) hydrogen atom, (2) a hydrocarbon group which may have a substituent, (3) an acyl group, or (4) a substituent.
- (6) -OR 10a (R 1Ga represents a hydrogen atom, an optionally substituted hydrocarbon group, an acyl group or a substituent.
- R lla is hydrogen atom, which may have a substituent charcoal hydrocarbon group, a Ashiru group or substituent
- R 9a represents a hydrogen atom, a hydrocarbon group which may have a substituent, an acyl group or a hydroxyl group which may have a substituent
- ring A, ring B and ring C may each have a substituent. Or a salt thereof;
- the substituents on ring A, ring B and ring C are (1) a hydrocarbon group which may have a substituent, (2) a heterocyclic group which may have a substituent, 3) an amino group which may have a substituent, (4) an acyl group, (5) a hydroxyl group which may have a substituent, (6) a sulfenyl group which may have a substituent, (7) halogen atom, (8) lower alkylene dioxy group, (9) nitro group, (10) cyano group, (11) imino group which may have a substituent, (12) oxo group, (13) A ureido group which may have a substituent, (14) an azide group, (15) an amidino group which may have a substituent, (16) a guanidino group which may have a substituent, ( 17) The compound according to the above [29], wherein the compound is 1-5 substituents selected from the group consisting of a hydrazino group which may have
- Compound (A-1) has the formula (-1)
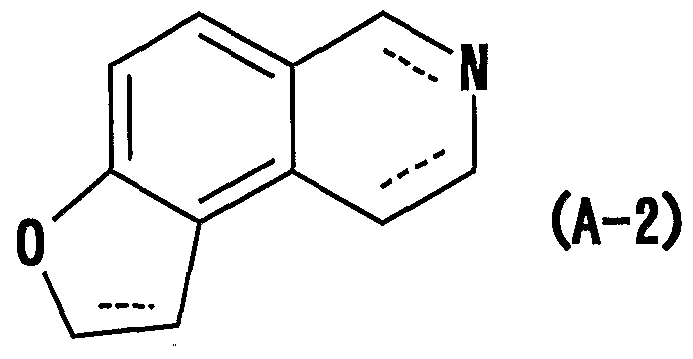
- the compound (A), (.1), ( ⁇ ), ( ⁇ -1), (1-1), (I, 1-1), (A-2) or a salt thereof has an asymmetric carbon in the structure.
- both optically active forms and racemic forms are included in the scope of the present invention, and the compounds (A), (I), ( ⁇ ), (A-1), (1-1), (1 , ⁇ 1), (A-2) or salts thereof may be either hydrates or anhydrides.
- the compounds of the present invention have the formula
- It is 1000 or less, preferably about 900 or less, more preferably about 800 or less, and particularly preferably about 700 or less.
- ring A, ring B and ring C have a substitutable number of substituents at substitutable positions. You may have.
- halogen atoms eg, fluorine, chlorine, bromine, iodine
- lower alkylenedioxy O carboxymethyl group e.g., Mechirenjiokishi, etc. ⁇ 3 alkylenedioxy O alkoxy groups such Echirenjiokishi
- Examples of the “optionally substituted hydrocarbon group” used as a substituent on the ring A, ring B and ring C include, for example, an alkyl group, an alkenyl group, an alkynyl group, and a cycloalkyl group.
- a chain or cyclic hydrocarbon group such as a cycloalkenyl group, an aryl group or an aralkyl group is used.
- a linear (branched or branched) or cyclic hydrocarbon group having 1 to 16 carbon atoms is used.
- an alkyl group [preferably a lower alkyl group (eg, methyl, ethyl, propyl) Le, isopropyl, butyl, isobutyl, sec- butyl, ter t-butyl, pentyl, (such as ⁇ -6 alkyl group) such as cyclohexyl,
- alkenyl group preferably a lower alkenyl group (for example, C 2 _ such as vinyl, aryl, isopropenyl, 2-butenyl, 2-methyl-2-propenyl, 4-pentenyl, 5-hexenyl and the like); 6 alkenyl groups)]
- C 2 _ such as vinyl, aryl, isopropenyl, 2-butenyl, 2-methyl-2-propenyl, 4-pentenyl, 5-hexenyl and the like
- 6 alkenyl groups preferably a lower alkenyl group (for example, C 2 _ such as vinyl, aryl, isopropenyl, 2-butenyl, 2-methyl-2-propenyl, 4-pentenyl, 5-hexenyl and the like); 6 alkenyl groups)]
- alkynyl groups [preferably, lower alkynyl group (e.g., propargyl, E Ji sulfonyl, 2-Bucheru, C 2 such hexynyl to 2 - such as 6 alkynyl group)]
- lower alkynyl group e.g., propargyl, E Ji sulfonyl, 2-Bucheru, C 2 such hexynyl to 2 - such as 6 alkynyl group
- cycloalkyl groups [preferably, a lower cycloalkyl group (e.g., Shikuropuro pills, cyclobutyl, cyclopentyl, c 3 _ 6 cycloalkyl Le group such as cyclohexyl), may be condensed with a benzene ring,
- a lower cycloalkyl group e.g., Shikuropuro pills, cyclobutyl, cyclopentyl, c 3 _ 6 cycloalkyl Le group such as cyclohexyl
- a cycloalkenyl group [preferably, a lower cycloalkenyl group (for example, 1 over sheet Kuropuro Bae cycloalkenyl, 1 Shikurobuarticulu, -1-cyclopentenyl, C 3 _ 6 cycloalkenyl group such as xenon alkenyl to 1 Shikuro) benzene May be condensed with a ring].
- a cycloalkenyl group preferably, a lower cycloalkenyl group (for example, 1 over sheet Kuropuro Bae cycloalkenyl, 1 Shikurobuarticulu, -1-cyclopentenyl, C 3 _ 6 cycloalkenyl group such as xenon alkenyl to 1 Shikuro) benzene May be condensed with a ring].
- Aromatic hydrocarbon group preferably, a lower cycloalkenyl group (for example, 1 over sheet Kuropuro Bae cycloalkeny
- Ariru group e.g., phenyl, 1 one-naphthyl, 2-Nafuchirire, 1 one anthryl, 2-anthryl, 9 one anthryl, 1 one Fuenantoriru, 2 Fuenantoriru, three to Fuenantoriru, C 6, such as 4 _ Fuenantoriru or 9 one Fuenantoriru such as _ 1 4 Ariru group, preferably a phenyl group
- Lower aralkyl groups e.g., benzyl, phenethyl, diphenylmethyl, 1-naphthylmethyl, 2-naphthylmethyl, 2-phenyl, 2,2-diphenylethyl, 1-phenylpropyl, 2-phenylpropyl, 3 - phenylpropyl, 4 one Hue Nirupuchiru, etc.
- Flip 7 _ 1 6 Ararukiru groups such as 5-phenylene Rupenchiru, preferably benzyl group).
- substituent of these hydrocarbon groups include (1) a halogen atom (for example, fluorine, chlorine, bromine, and iodine), and (2) a lower alkylenedioxy group (for example, methylenedioxy, ethylenedioxy and the like). (3) nitro group, (4) cyano group, (5) lower alkyl group which may be halogenated, (6) Lower alkenyl group which may be halogenated, (7) lower alkynyl group which may be halogenated, (8) lower cycloalkyl group (for example, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, etc.
- a halogen atom for example, fluorine, chlorine, bromine, and iodine
- a lower alkylenedioxy group for example, methylenedioxy, ethylenedioxy and the like.
- C such as 3 _ 6 cycloalkyl group
- C 6 - 1 4 ⁇ Li Ichiru group e.g., phenyl, 2 - naphthyl
- 10 optionally halogenated substituted lower alkoxy group
- 11 Lower alkylthio group which may be halogenated
- mono-lower alkylamino group e.g., monoamino such as methylamino, ethylamino, propylamino, isopropylamino, butylamino, etc.
- C such as E _ 6 Arukiruamino group
- mono- C 6 one 1 4 Ariruamino group eg, Fueniruamino, 2 - etc.
- G C 6 - 1 4 Ariruamino group eg, Jifueeruamino, di (2-naphthyl) Amino etc.
- Ashiru group eg, Jifueeruamino, di (2-naphthyl) Amino etc.
- (21) 4- to 14-membered heterocyclic group (preferably 4- to 10-membered, more preferably 4- or 7-membered heterocyclic group, particularly preferably 5- or 6-membered heterocyclic group) (eg, 4-pyridyl, 2 1-Cenyl, 2-furyl, 2-thiazolyl, 3-indolyl, morpholino, 1-piperazinyl, piperidino, 1-pyrrolidinyl, 2-isoindolyl, etc., other than carbon, nitrogen, sulfur, oxygen, etc.
- 4-pyridyl 2 1-Cenyl, 2-furyl, 2-thiazolyl, 3-indolyl, morpholino, 1-piperazinyl, piperidino, 1-pyrrolidinyl, 2-isoindolyl, etc., other than carbon, nitrogen, sulfur, oxygen, etc.
- a lower alkyl group optionally having 1 to 3 halogen atoms eg, fluorine, chlorine, bromine, iodine
- alkyl group e.g., methyl, Echiru, propyl, isopropyl, butyl, isobutyl, sec - heptyl, tert- butyl, pentyl, etc.
- ( ⁇ _ 6 alkyl groups such as hexyl) and the like are used, as a specific example, Methyl, chloromethyl, difluoromethyl, trichloromethyl, trifluoromethyl, ether, 2-bromoethyl, 2,2,2-trifluoroethyl, propyl, 3,3,3-trifluorotrifluoropropyl, isopropyl, butyl, 4 , 4,4-Trifluorobutyl, isobutyl, sec-butyl, tert-butyl, pentyl, isopentyl, neope Chill, 5, 5, 5-triflate Ruo b hexyl pentyl to,, 6, 6, etc. hexyl and the like to 6 Torifuruo port.
- the “lower alkenyl group optionally octogenated” in the substituent group A may have, for example, 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) lower alkenyl groups (e.g., vinyl, Ariru, isoproterenol base alkenyl, 2-butenyl, 2-methyl-2 _ propenyl, 4 one-pentenyl, 5 one hexenyl such which C 2 - 6 alkenyl group) and the like.
- halogen atoms eg, fluorine, chlorine, bromine, iodine
- lower alkenyl groups e.g., vinyl, Ariru, isoproterenol base alkenyl, 2-butenyl, 2-methyl-2 _ propenyl, 4 one-pentenyl, 5 one hexenyl such which C 2 - 6 alkenyl group
- the “lower alkynyl group optionally octogenated” in the substituent group A may have, for example, 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) a lower alkynyl group (e.g., propargyl, Echiniru, 2-Petit El and C 2 _ 6 alkynyl group such as hexynyl to 2) and the like.
- halogen atoms eg, fluorine, chlorine, bromine, iodine
- a lower alkynyl group e.g., propargyl, Echiniru, 2-Petit El and C 2 _ 6 alkynyl group such as hexynyl to 2
- Examples of the “optionally halogenated lower alkoxy group” in the above-mentioned substituent group A include, for example, lower optionally having 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) an alkoxy group (e.g., methoxy, ethoxy, Purobokishi, iso-propoxy, butoxy, isobutoxy, sec- butoxy, tert- butoxy, pentyl Ruokishi, isopentyl Ruo alkoxy, neopentyl Ruo alkoxy, to a C ⁇ _ 6 alkoxy group such as Kishiruokishi
- Specific examples include methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, sec-butoxy, tert-butoxy, trichloromethoxy, 3,3,3-trifluoropropoxy, 4,4, 4 Trifluorobutoxy, 5, 5, 5—Trifluoropentyloxy, 6,
- halogenated lower alkylthio group in the above-mentioned Substituent group A, for example, may have 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) ( ⁇ - 6 alkylthio group (e.g., methylthio, Echiruchio, pro Piruchio, isopropylthio, Puchiruchio, isobutylthio, sec- butylthio, ter t one Puchiruchio, pentylthio, cyclohexylthio C WINCH 6 alkylthio group such as to) and the like are used, specifically Examples thereof include methylthio, difluoromethylthio, trifluoromethylthio, ethylthio, propylthio, isopropylthio, butylthio, 4,4,4-trifluorobutylthio, pentylthio, hexylthio
- C 3 _ 6 cycloalkyl - Karuponiru e.g., cyclopentyl Luca Lupo, cycloalkenyl, cycloheteroalkyl, etc. keys Shirukaruponiru
- C ⁇ - 6 alkoxy Ichiriki Ruponiru e.g., methoxy Cal Poni le, X Tokishikaruponiru, Isopuropokishi force Ruponiru, t er t-butoxycarbonyl etc.
- C 6 _ 1 4 Ariru - Karuponiru eg, Benzoiru and 2 one naphthoyl
- C 7 _ 1 6 Ararukiru Ichiriki Ruponiru eg, phenylene Ruasechiru, 3-phenylpropyl propionyl, etc.
- C 6 _ 1 4 Aryloxy-one-strand eg, phenoxy-th, 2-nap
- Jechirukarubamo I le C 6 - 1 4 ⁇ Li one Roux force Rubamoiru (e.g., Hue carbamoylmethyl, 2-naphthylcarbamoyl etc.), 5- or 6-membered heterocyclic ring force Rubamoiru (eg, 1 one Pyrrolidinylcarbamoyl, 4-piberidylcarbamoyl, 1-piperazinylcarbamoy Selected from nitrogen atoms, sulfur atoms, oxygen atoms, etc., in addition to carbon atoms such as 1, 2-morpholinylcarbamoyl, 4-pyridylcarbamoyl, 3-chlorocarbamoyl, 2-furyl-rubamoyl, 2-thiazolylcarbamoyl, etc.
- Roux force Rubamoiru e.g., Hue carbamoylmethyl, 2-naphthylcarbamoyl etc.
- Chiokarubamoiru eg, phenylene Lucio force Rubamoiru, 2- 5- or 6-membered heterocyclic thiocarbamoyl (e.g., 2-pyrrolidinylthio-potassium, 2-piperidylthio-potassium, 2-piperazinyl-thio-potsubamoyl, 2-morpholinyl-thio-potsubamoyl, 4-pyridylthio-potassium) Containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon atoms such as 3-chlorothiocarbamoyl, 2-furylthiocarbamoyl, 2-thiazolylthiocarbamoyl, etc.
- 2-pyrrolidinylthio-potassium e.g., 2-piperidylthio-potassium, 2-piperazinyl-thio-potsubamoyl, 2-morpholinyl-thio-potsubam
- C 6 — 14 arylsulfamoyl eg, phenylsulfamoyl
- 0 _ 6 alkylsulfonyl (eg, methylsulfonyl, ethylsulfonyl, etc.)
- C 6 _ 14 arylsulfonyl eg, phenyl
- sulfonyl such as 2 one-naphthylsulfonyl
- G 6 alkylsulfinyl e.g., methylsulfinyl, etc.
- E chill sulfide El C 6 - 14 ⁇ reel sulfinyl (e.g., Hue Nils sulfinyl, such as 2 one Nafuchirusurufu Iniru), sulfino, sulfo, C ⁇ _ 6 alkoxysulfinyl sulfinyl (e.g., methoxide Shisurufiniru, e Toki cis sulfinyl), Ji 6 _ 14 ⁇ reel O carboxymethyl sulfinyl (e.g., full enoki cis sulfinyl), Ci-e alkoxy sulfonyl (e.g., main Bok Kishisu Ruhoniru , E butoxy-benzenesulfonyl) and C 6 - 14 ⁇ reel O carboxymethyl sulfonyl (e.g., Fueno Shisuruhoniru) and the like
- Substituent Group A for example, Horumiruamino, C ⁇ 6 alkyl Ichiriki Rupokisamido (eg, Asetoamido and propionamide), C 6 - 14 Ariru Ichiriki Rupokisamido (e.g., benzamide, 2- naphthyl Cal poke Sami Donado), alkoxy Ichiriki Rupokisamido (e.g., methoxy carboxamide, X Toki deer Lupo alkylcarboxamide, isopropoxycarbonyl carboxamide, such as tert- Butokishikarupoki Samido), C 6 alkylsulfonyl ⁇ amino (e.g., methylsulfonyl ⁇ Mino, E such as chill sulfonyl ⁇ Mino), bis (( ⁇ - 6 alkylsulfonyl) amino (e.g., bis (methylsulf) amino (e.g., bis (methylsulf
- Ruo carboxymethyl C 6 one 1 4 ⁇ Li one Luca Lupo sulfonyl O carboxymethyl (e.g., Benzoyloxy, 2-naphthoyloxy, etc.), alkoxy monopropyloxy (e.g., methoxycarboxy, ethoxypropyloxy, isopropoxyoxy, tert-butoxycarboxy), mono-Ci- 6 alkyl monorubamoyloxy (e.g.
- 6 alkyl Ichiriki Ruponiruokishi, - 6 C 2 _ 7 Ashiruokishi groups such as alkoxy Ichiriki Ruponiruokishi are preferred.
- Examples of the group formed by bonding two or three members selected from the groups (1) to (32) include, for example,
- R 18 and R 19 each represent (i) a 5- or 6-membered heterocyclic ring (eg, a 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom, etc., in addition to a carbon atom) Or 6-membered heterocycle) monoalkyl, (iDCi-ealkoxy mono-propionyl-alkyl), (iii) dialkyl 6- alkylamino-methylene-sulfamoyl-alkyl, (iv) di-rubmoyl-C 6- alkyl, (V) sulfamoyl - 6 alkyl le, (vi) C 6 alkyl chromatography alkylsulfonyl, (VIOC -e alkoxy - carbonyl, (viii) di - C i_ 6 alkoxy Ichiriki Lupo two Lou C 2 _ 6 alkenyl, (ix) 5 or 6-member
- R 2Q and R 21 each represent (i) a 5- or 6-membered heterocyclic ring (eg, 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as pyridyl and imidazolyl) 5 or 6 membered heterocyclic ring containing) -C ⁇ e alkyl, (ii) Karupoki sheet - - 6 alkyl, (iii) C Les 6 alkoxy - force Lupo two Lou C 6 alkyl, (iv) di - C e _ 6- Alkylamino—C 6- Alkyl, (V) Alkyl C 6 Alkyl, (vi) Alkyl Rubamoyl—— 6 Alkyl, (vii) 5- or 6-membered Heterocycle
- the 4- to 10-membered heterocyclic group may have one or two substituents selected from a halogen atom, alkyl, oxo, etc.], (xiii) C 6 — 14 arylene 6 alkyl, etc.],
- halogenated C ⁇ - 6 alkyl Cal poke Sami de e.g., 2-Kuroroaseta bromide, 2, 2-dichloro-acetamide, 2, 2, 2-trichloro acetamide, etc.
- the ⁇ optionally substituted heterocyclic group '' used as a substituent on the ring A, ring B and ring C includes, for example, nitrogen, sulfur, oxygen and the like in addition to carbon.
- a 4- to 14-membered heterocyclic group containing 1 to 4 (preferably 1 to 3) heteroatoms to be selected and the like are used. Specifically, (a) a 4- to 14-membered aromatic heterocyclic group,
- the 4- to 14-membered aromatic heterocyclic group includes, for example, 1 to 4 (preferably 1 to 3) heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom and the like in addition to a carbon atom. Or a 14-membered aromatic heterocyclic group or the like. Specific examples thereof include thiophene, furan, indolizine, pyrrole, imidazole, triazole, thiazole, thixazole, pyrazole, pyridine, and N-dioxide.
- pyridine, thiophene, furan and the like are preferably used.
- Examples of the 4- to 14-membered aliphatic heterocyclic group include 1 to 4 (preferably 1 to 3) heteroatoms selected from nitrogen, sulfur, and oxygen atoms in addition to carbon atoms.
- a 4-membered aliphatic heterocyclic group or the like is used, and specific examples include pyrrolidine, piperidine, piperazine, morpholine, thiomorpholine, 1,2-dihydropyridine, imidazolidine and the like.
- the bicyclic or tricyclic fused ring group of a 4- to 14-membered heterocyclic ring and a benzene ring may include, in addition to carbon atoms, 1 to 4 heteroatoms selected from nitrogen, sulfur and oxygen (preferably (1 to 3) and a bicyclic or tricyclic fused ring group of a benzene ring and a heterocyclic ring, such as benzo [b] thiophene, benzofuran, 1H-benzimidazole, and benzzo Xazole, benzothiazole, 1,2-benzisothiazole, naphtho [2,3-b] thiophene, thianthrene, xanthene, phenoxatiin, indole, isoindole, 1H-indazole, isoquinoline, quinoline, phthalazine, quinoxaline, Quinazoline, cinnoline, carbazole,) 3-caprolactin, phenanthridine
- substituent of these heterocyclic groups 1 to 5, preferably 1 to 3 selected from the above-mentioned substituent group A are used.
- the “optionally substituted amino group” used as a substituent on the A ring, the B ring and the C ring includes the “optionally substituted hydrocarbon group” and the “optionally substituted hydrocarbon group”.
- an amino group which may have one or two substituent (s) selected from the above.
- acyl group used as a substituent of the ring A, ring B and ring C, those similar to the “acyl group” in the aforementioned substituent group A can be used.
- This “acyl group” may further have 1 to 5, preferably 1 to 3 substituents selected from substituent group A.
- R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent].
- R 1 represents (1) a hydrogen atom, (2) a hydrocarbon group optionally having a substituent, or (3) a heterocyclic group optionally having a substituent.
- R 1 (1) an aromatic hydrocarbon group optionally having a substituent, (2) a heterocyclic group optionally having a substituent, (3) an optionally substituted substituent A good aliphatic cyclic hydrocarbon group, (4) Formula 1: L—R la wherein L is methylene or carbonyl, R la is a hydrogen atom, an aromatic group which may have a substituent, a substituent A hydroxyl group optionally having a substituent or an amino group optionally having a substituent].
- the “aromatic hydrocarbon group optionally having substituent (s)” and the “heterocyclic group optionally having substituent (s)” are represented by the formula:
- R lb represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent
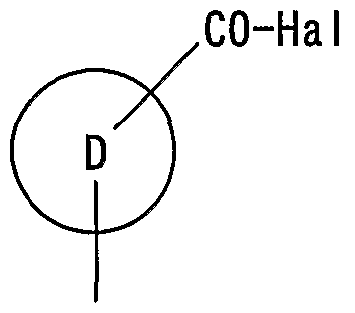
- the ring D is an aromatic which may have a substituent.
- Group E is a bond, methylene, oxygen atom, acid Optionally substituted sulfur atom, optionally substituted nitrogen atom or formula —CS—O—, one CO—O—, one S—CO—, one (CH 2 ) k —CO—, one NR lc - CO - (CH 2 ) m -, -NR lc -S0 2 - (CH 2) m -, one S_ ⁇ 2 - NR lc - (CH 2 ) m -, one ⁇ - CS-NR lc - (CH 2 ) m- , one NR lc — CO-NR lc — (CH 2 ) m —, — NR lc _C ⁇ one CH 2 — (
- Ha 1 represents a halogen atom
- ring D has the same meaning as described above].
- R 1 "aromatic hydrocarbon group", for example, etc.
- C 6 -C 14 membered monocyclic or condensed polycyclic aromatic hydrocarbon group (C 6 _ 14 Ariru group) Is used.
- the C 6 _ 14 Ariru group e.g., phenyl, 1 one-naphthyl, 2-naphthyl, 1 one anthryl, 2 one anthryl, 9 _ anthryl, 1 one Fouesnant tolyl, 2 _ Fuenantoriru, 3 Fuenantoriru, 4 one Fuenantoriru, 9-phenanthryl and the like are used, and among them, phenyl, 1-naphthyl, 2-naphthyl and the like are preferable, and phenyl and the like are particularly preferable.
- substituent for the “aromatic hydrocarbon group” 1 to 5, preferably 1 to 3 selected from the above-mentioned substituent group A is used.
- substituents (1) a halogen atom,
- the ( ⁇ -6 alkyl group is a halogen atom, cyano, carbamoyl, 6- alkaryl pamoyl, C i _ 6 alkyl monopropylamine, alkoxy-carbonyl- 6 alkyl monorubumoyl, 5- or 6-membered heterocycle (Eg, 1 to 3 carbon atoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon such as pyridyl 5 or 6 membered heterocyclic ring) -C x _ 6 alkyl Ichiriki Rubamoiru containing hetero atoms,
- Horumiruamino may have a halogen atom or carboxy alkyl - carbonyl amino (eg, Asechiruamino, propionyl Rua Mino, triflumizole Ruo b acetylide relay amino, Bibaroiruamino), c 6 one 14 Ariru Ichiriki Ruponiruamino (eg, Benzoiruami Bruno), ( ⁇ _ 6 alkoxy - power Ruponiruamino (e.g., methoxy Karuponiruamino), ureido, mono- or di- (: e alkylureido, 6 alkylsulfonyl amino (e.g., methylsulfony
- Ci- 6 alkoxy group which may have a —6 alkoxy-C 6 _ 14 aryl (eg, methoxy, trifluoromethoxy, isopropoxy, 2- (4-methoxy Phenyl) ethoxy)),
- C- 6 alkylthio group which may have carbamoyl (eg, methylthio, carbamoylmethylthio),
- alkylsulfinyl group which may have a carpamoyl (eg, methylsulfinyl, carbamoylmethylsulfinyl),
- the heterocyclic group is old Kiso, Karubokishi alkyl, alkyl Ichiriki Honoré Boniruokishi - C i _ 6 alkyl, (6 alkyl, C i-6 alkoxy - Karuponiru - alkyl, C x _ 6 alkoxy Ichiriki Ruponiru force Rubamoiru - C - 6 alkyl Le, C x _ 6 alkyl - may have a force Rubamoiru C i _ 6 substituents selected from an alkyl, (13) a carboxy group,
- alkyl-sulfonyl group eg, methylsulfonyl, etc.
- the sulfamoyl group, (_ 6 alkyl, force Rubamoiru C Bok 6 alkyl, C, ⁇ - 6 alkoxy Ichiriki Ruponiru - d_ 6 alkyl, 5 to may have Okiso group 7-membered Hajime Tamaki ( Example: 5- to 7-membered heterocyclic group containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc.
- R a and R b each represent (i) a hydrogen atom, (iO ⁇ -e alkyl, (iii) a 5- or 6-membered heterocyclic ring (eg, a nitrogen atom, a sulfur atom, an oxygen atom, etc.
- 5- or 6-membered heterocyclic ring in addition to carbon such as pyrrolidinyl, pyridyl, etc.
- One-strand ruponyl (xxii i) 5- or 6-membered heterocyclic ring (eg, one or three selected from nitrogen, sulfur, oxygen, etc.
- a heteroatom 5 or 6 membered heterocyclic ring) i ( ⁇ _ 6 alkyl Ichiriki Lupo two Le has, fcdv) C 6 - 14 Ariru one Okishi Ichiriki Ruponiru, (XXV) force Rupokishi - C - 6 ⁇ alkyl, (xxvi) force Rubamoiru , (xxvii) optionally halogenated good alkylcarbamoyl, (xxviii) C ⁇ alkyl one carbonyl ⁇ Mino but it may also have a C 6 _ 14 ⁇ Lee carbamoyl, (xxix) 5 or 6-membered heterocyclic ring ( examples, nitrogen atom in addition to a pyridyl that any carbon atom, a sulfur atom, 1 selected from oxygen atom, etc.
- Rc and R d are each (i) hydrogen atom, (i C ⁇ - 6 alkyl, (iii) 5 or 6-membered heterocyclic ring (e.g., pyridyl, nitrogen atom in addition to carbon atoms, such as imidazolyl, sulfur atom, an oxygen atom 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from the group consisting of: 1 Ci- 6 alkyl, (iv) carboxy-alkyl, WCi- 6 alkoxy-carbocarbonyl C 6 alkyl, (vi) G C ⁇ 6 alkylamino one C Bok 6 alkyl, (vii) force Rubamoiru 6 alkyl, (viii) C 6 alkyl force Rubamoiru - C E _ 6 alkyl, (ix) 5 or 6-membered heterocyclic ring (e.g., carbon, such as pyridyl A 5- or 6-membered heterocyclic ring containing
- heterocyclic group represented as a preferable group of R 1
- examples of the “heterocyclic group” represented as a preferable group of R 1 include pyridyl, phenyl, furyl, imidazolyl, thiazolyl, quinolyl, 1,2-dihydropyridyl, dihydrobenzofuranyl, benzodioxolyl, and benzothiazolyl.
- Piperidyl, piperazinyl and the like are preferable, and pyridyl, 1,2-dihydropyridyl and the like are particularly preferable.
- Ci- 6 alkyl group eg, methyl, ethyl, etc.
- alkyl, force Rupokishi, 6 alkoxy, alkoxy - has Karupamoiru, a Okiso - force Lupo two Le, mono one C ⁇ - 6 Arukiruamino, di - 6 Arukiruamino force Rubamoiru, alkyl which may have hydroxy
- a 4- to 10-membered heterocyclic group e.g., containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyridyl and quinolyl
- 10-membered heterocyclic group 4- to 10-membered heterocyclic ring (eg, containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc.
- the C 7 _ 1 6 Ararukiru is carboxy, alkoxy one carbonyl, force Luba moil, hydroxy may have - 6 alkyl Ichiriki Rubamoiru, 4 to 1 0-membered heterocyclic ring (e.g., carbon atoms, such as pyridyl A 4- to 10-membered heterocyclic ring containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc.) — Which may have a substituent selected from rubamoyl, etc.] ,
- 4- to 10-membered heterocyclic group eg, charcoal such as pyridyl, quinolyl, isoquinolyl, etc.
- heterocyclic group in which R 1 has an oxoxide group for example, N-aminopyridyl pyridyl and the like are preferable.
- Aliphatic cyclic hydrocarbon group represented as preferable groups for R 1, for example, cyclopropyl, cyclobutyl, cyclopentyl, C 3 _ 6 shea click port alkyl groups such as cyclohexyl may be used, in particular cyclopentyl, Cyclohexyl is preferred.
- This “aliphatic cyclic hydrocarbon group” may have the same substituent as the substituent that the hydrocarbon group represented by R 1 may have.
- Examples of the preferred group for R 1 include an “optionally substituted aromatic hydrocarbon group” and an “optionally substituted heterocyclic group”.
- the “optionally substituted hydrocarbon group” represented by R lb may be the same as the “optionally substituted optionally substituted hydrocarbon group” exemplified as the substituent for the ring A. Is used. Above all,
- Ci- 6 alkyl group (methyl, isopropyl, tert-butyl, etc.)
- This alkyl group is a halogen atom, cyano, hydroxy, C- 6 alkoxy Sheet - Power Ruponiru, di - C ⁇ e Arukiruamino may be halogenated - 6 alkyl - force Lupo two Ruamino force Rupokishi force Rubamoiru, C ⁇ -e alkyl Ichiriki 'Rubamoiru, C 6 alkyl one Karuboniruo Xy, alkoxy-carbonyl-alkyl-alkanoyl, 5- or 6-membered heterocyclic ring (eg, 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc.
- Yl, 5- or 6-membered heterocycle eg, 5- or 6-membered heterocycle containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc.
- the C 6 _ 14 Ariru groups, - 6 alkoxy (e.g., methoxy) Amino, carboxy may be halogenated d-6 alkyl Ichiriki Ruponiruamino (eg, ⁇ Se Chiruamino, triflumizole Ruo b acetyl ⁇ Mino ), C ⁇ -e alkoxy - Karuponiruami Bruno (e.g., methoxy Cal Poni Rua Mino), Horumiruamino, ureido, 6 alkynyl Le sulfonyl ⁇ amino (e.g., methylsulfonyl ⁇ Mino), (CI- 6 alkyl) (d - 6 alkyl Sulfonyl) amino (eg, methyl (methylsulfonyl) amino, etc.), C 6 alkoxy-potassium C 6 alkylamino (eg, 2-ethoxycarbo 2-ru-propy
- a C 2 _ 6 alkenyl group is preferred.
- heterocyclic group optionally having substituent (s) represented by R lb
- those similar to the “heterocyclic group optionally having substituent (s)” exemplified as the substituent for ring A are used. It is possible. Among them, halogen atom, C 6 alkyl, carboxyl-C ⁇ -e alkyl, C 6 alkoxy mono-potential C 6- alkyl, C 6 alkoxy mono-proponyl, dipotamoyl, oxo, 4- to 10-member complex A ring group (eg, a 4- to 10-membered heterocyclic group containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc.
- substituents E.g., azetinyl, piperidinyl, piperidyl, isothiazolidinyl, thiadiazolidinyl, hexahydrroazepier, frill, chenyl, pyridyl, quino
- the aromatic hydrocarbon ring represented by D ring e.g., C 6 -C to 1 4-membered monocyclic or condensed polycyclic aromatic hydrocarbon ring (C 6 1 4 Ariru ring), and the like Ru is used.
- C 6 14 aryl ring for example, a benzene ring, a naphthalene ring, an anthryl ring, a phenanthryl ring and the like are used, and among them, a benzene ring, a naphthylene ring and the like are preferable, and a benzene ring is particularly preferable. .
- aromatic hydrocarbon rings may have 1 to 5, preferably 1 to 3, substituents selected from the aforementioned substituent group A.
- heterocycle represented by the ring D examples include a 5- to 14-membered heterocyclic ring having 1 to 4 (preferably 1 to 3) heteroatoms selected from nitrogen, sulfur, oxygen and the like in addition to carbon atoms. Heterocycles and the like are used. Specific examples include (a) a 5- to 14-membered aromatic heterocycle, (b) a 5- to 14-membered aliphatic heterocycle, and (c) a 5- to 14-membered heterocycle. A bicyclic or tricyclic fused ring with a zen ring is used.
- Examples of the 5- to 14-membered aromatic heterocycle include a nitrogen atom and a sulfur atom in addition to a carbon atom.
- a 5- to 14-membered aromatic heterocycle containing 1 to 4 (preferably 1 to 3) heteroatoms selected from a yellow atom, an oxygen atom and the like is used, and specifically, thiophene, furan, indolizine and the like are used.
- pyridine Pyrrole, imidazole, triazole, thiazole, oxazole, pyrazole, pyridine, N-oxidized pyridine, pyrazine, pyrimidine, pyridazine, purine, 4H-quinolizine, naphthyridine, isothiazole, isoxazole, furazan, etc. .
- pyridine, thiophene, furan and the like are preferably used.
- the 5- to 14-membered aliphatic heterocycle includes 1 to 4 (preferably 1 to 3) heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom and the like in addition to a carbon atom.
- a membered aliphatic heterocycle or the like is used, and specific examples include pyrrolidine, piperidine, piperazine, morpholine, thiomorpholine, 1,2-dihydropyridine, imidazolidine and the like.
- bi- or tricyclic fused ring of the 5- to 14-membered heterocyclic ring and a benzene ring one to four heteroatoms (preferably one to four) selected from nitrogen, sulfur and oxygen other than carbon atoms And 3 or more condensed rings of a benzene ring with a heterocyclic ring containing benzene [b] thiophene, benzofuran, 1H-benzimidazole, benzoxazole, benzo Thiazole, 1,2-benzisothiazol, naphtho [2,3-b] thiophene, thianthrene, xanthene, phenoxatiin, indole, isoindole, 1H-indazole, isoquinoline, quinoline, phthalazine, quinoxaline, quinazoline, Cinnoline, carbazole, 3-ketoporin, phenanthridine, acridine, phenazine, phenothia
- pyridine, thiophene, furan, imidazole, thiazole, quinoline, N-hydroxylated pyridine, 1,2-dihydropyridine, dihydrobenzofuran, benzodioxole, Benzothiazole, piperidine, piperazine and the like are preferable, and pyridine, 1,2-dihydropyridine and the like are particularly preferable.
- heterocycles may have 1 to 5, preferably 1 to 3, substituents selected from the aforementioned substituent group A.
- substituents selected from the aforementioned substituent group A As the “optionally oxidized sulfur atom” represented by E, S, SO, and SO 2 are used.
- Examples of the optionally substituted nitrogen atom represented by E include (i) a hydrogen atom, (ii) an optionally substituted hydrocarbon group, and (iii) an acyl group. A nitrogen atom which may be present is used.
- hydrocarbon group optionally having substituent (s) those similar to the “hydrocarbon group optionally having substituent (s)” exemplified as the substituent for ring A can be used.
- acyl group those similar to the “acyl group” exemplified as the substituent for the ring A are used, and this acyl group further has 1 to 5, preferably 1 to 5, substituents selected from the substituent group A. May have one to three.
- alkyl group represented by R examples include methyl, ethyl, propyl, isopropyl, butyl, isobutyl, sec-butyl, tert-butyl - butyl, etc.
- C WINCH 6 alkyl groups such as pentyl, carboxymethyl Le is used.
- the alkyl group represented by R le may have 1 to 5, preferably 1 to 3 substituents selected from the aforementioned substituent group A.
- acyl group represented by R lc those similar to the ⁇ acyl group '' exemplified as the substituent for the ring A are used, and the acyl group further has 1 to 5 substituents selected from the substituent group A. Preferably, it may have one to three.
- k represents 0 or 1, particularly preferably 0.
- n represents an integer of 0 to 3, and among them, 0 or 1 is preferable.
- ⁇ 6 alkyl group e.g., methyl
- R m is hydrogen or ⁇ - group 6 alkyl group (e.g., methylation) and represented by m6 is 0 or 1]
- Examples of the preferred group for R 1 include an “optionally substituted aromatic hydrocarbon group” and an “optionally substituted heterocyclic group”.
- halogen atom represented by H a1 a fluorine atom, a chlorine atom, a bromine atom, an iodine atom and the like are used, and among them, a chlorine atom is preferable.
- L is preferably methylene or heptonyl.
- R 1 a The aromatic group represented by R 1 a, for example,
- 1Monocyclic or condensed polycyclic aromatic hydrocarbons more specifically phenyl, 1-naphthyl, 2-naphthyl, 1-anthryl, 2-anthryl, 9-anthryl, 1.1-phenanthryl, 2- 1 4 Ariru group (preferably, phenyl, 1 - - naphthyl or 2-naphthyl, particularly preferably phenyl)
- one or more heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom and the like in addition to a carbon atom may be used.
- monocyclic heterocyclic group preferably 5 to 8 members
- a fused aromatic heterocyclic group thereof more specifically, thiophene, benzo [b] thiophene, benzofuran, 1 H-benzimidazole, benzoxazole, benzothiazole, 1,2-benzisothiazole, naphth C2,3-b] thiophene, thianthrene, furan, indolizine, xanthene, phenoxatiin, pyrrole, Imidazole, triazole, thiazole, oxazole, pyrazole, pyridine, pyrazine, pyrimidine, pyridazine, indole, isoindole 1 H one-in
- R 1 The aromatic group which may have a substituent represented by a, alkyl, 1 to 5 optionally having C 4 Ariru group (e.g., phenyl) substituents such as alkoxy and preferable.
- a substituent represented by a, alkyl, 1 to 5 optionally having C 4 Ariru group (e.g., phenyl) substituents such as alkoxy and preferable.
- R la As the “optionally substituted hydroxyl group” represented by R la , those similar to the aforementioned “optionally substituted hydroxyl group” exemplified as the substituent of the ring A described above are used. Among them, a hydroxyl group which may have a C 6 alkyl group (eg, methyl) is preferable.
- Examples of the “amino group optionally having substituent (s)” represented by R la include, for example, an alkyl group optionally having a substituent, an aryl group optionally having a substituent, and the like. And an amino group which may have 2 or more, particularly preferably a 4- to 10-membered heterocyclic group (1 to 3 hetero atoms selected from nitrogen atom, oxygen atom, sulfur atom and the like in addition to carbon atom) May be substituted with a 4- to 10-membered heterocyclic group having an atom, eg, pyridyl) — 6-alkyl-amino group, 2 C 6 4 aryl-amino group, 3 4- to 10-membered heterocyclic ring (nitrogen other than carbon atom)
- a 4- to 10-membered heterocyclic ring having 1 to 3 heteroatoms selected from an atom, an oxygen atom, a sulfur atom and the like, eg, pyridyl) -amino group is preferred.
- R 16 is a hydrogen atom, which may have a substituent C 6 _ 14 ⁇ Li Ichiru group, an optionally substituted amino group, which may have a substituent A heterocyclic group or a halogen atom].
- R 16 is a substituent selected from (1) a hydrogen atom, (2) phenyl substituted with an acetylamino group, (3) (i) an alkylsulfonyl group, (ii) pyridylcarbonyl or (iii) a sulfamoyl-alkyl group.
- Preferred are mono- or di-substituted amino, (4) pyridyl or (5) halogen atom (fluorine atom, chlorine atom, bromine atom, iodine atom).
- the ⁇ optionally substituted hydrocarbon group '' represented by R 2 and R 3 is the same as the ⁇ optionally substituted hydrocarbon group '' exemplified as the substituent of ring A Is used.
- 10-membered heterocyclic group which may have a substituent (for example, which may have an oxo group, other than carbon atom, is selected from nitrogen atom, oxygen atom, sulfur atom, etc.
- 4- to 10-membered heterocyclic group having one heteroatom eg, phthalimide, imidazolyl, piperidyl, pyrrolidinyl)
- a hydrocarbon group which may be substituted by, for example, is used.
- 1 halogen atom especially, bromine atom
- 2 hydroxy especially, 3 _ 6 alkyl Le - Karuponiruokishi (eg, Asetokishi)
- 4 Amino, 5 4 which may have a Okiso group to 1 0-membered heterocyclic group (Substituted with a 4- to 10-membered heterocyclic group having 1 to 3 hetero atoms selected from nitrogen, oxygen, sulfur, etc. in addition to carbon (eg, phthalimide, imidazolyl, piperidyl, pyrrolidinyl)) etc.
- C 6 alkyl group is preferable be news halogen atom (especially, bromine atom) may be halogenated and the like - 6 alkyl group (e.g., methyl, etc. Echiru) and the like are preferable, especially methyl Groups are preferred.
- R 2 and R 3 Represented by R 2 and R 3 as “Ashiru group", those similar to the Ru is exemplified as the substituents for ring A “Ashiru group” is used, inter alia - 6 alkoxy - Karuponiru groups are preferred, especially methoxycarbonyl Groups are preferred.
- the 3- to 8-membered homocyclic R 2 and R 3 form together with the adjacent carbon atom, 3- to consist carbon atom used cyclic hydrocarbons to 8-membered, particularly, C 3 _ 8 consequent Roarukan (e.g., cyclobutane, cyclopentane, cyclohexane, heptane cyclohexane, cyclooctane), C 3 _ 8 Shikuroarugen (e.g., cyclobutene, consequent opening pentene, cyclohexene, cycloheptene, Shikurookuten) etc. is Ru mentioned. Of these C 3 8 cycloalkane is preferred, cyclopentane, 5 or 6-membered homocyclic ring such as key San cyclohexane (especially, cyclohexane) are preferred.
- C 3 _ 8 consequent Roarukan e.g., cyclobutane, cyclopentane,
- the 3- to 8-membered heterocyclic ring formed by R 2 and R 3 together with adjacent carbon atoms includes, in addition to a carbon atom, one or two hetero atoms selected from a nitrogen atom, a sulfur atom and an oxygen atom.
- a 5- to 8-membered aliphatic heterocycle (preferably a 5- or 6-membered aliphatic heterocycle) containing at least one (for example, 1 to 4, preferably 1 to 3) is used.
- piperidine, piperazine, morpholine, thiomorphol 5 to 8 members preferably 5 or 6) containing 1 to 3 heteroatoms selected from nitrogen, oxygen and sulfur atoms, in addition to carbon and nitrogen atoms, such as a nitrogen atom, a pyrrolidine and an imidazolidine ring. Member
- a nitrogen atom such as a nitrogen atom, a pyrrolidine and an imidazolidine ring. Member
- the 3- to 8-membered allo-heterocyclic or heterocyclic ring formed by R 2 and R 3 together with the adjacent carbon atom has the same substituent as the above-mentioned substituent which the heterocyclic ring represented by R 1 may have. It may have 1 to 5, preferably 1 to 3.
- Substituents include: — 6-alkyl, C 6 — 14 aryl, C 7 — 16 aralkyl, amino, mono— — 6-alkylamino, mono-C 6 — 14 arylamino, di- 6 alkylamino, di— C 6 — 14 arylamino
- a 4- to 10-membered heterocyclic group eg, a 4- to 10-membered (preferably 5- or 6-membered) containing 1 to 3 heteroatoms selected from nitrogen, oxygen and sulfur atoms in addition to carbon atoms) 1 to 3 members selected from heterocycles
- a 4- to 10-membered heterocyclic group eg, a 4- to 10-membered (preferably 5- or 6-membered) containing 1 to 3 heteroatoms selected from nitrogen, oxygen and sulfur atoms in addition to carbon atoms) 1 to 3 members selected from heterocycles
- R 2 and R 3 respectively a halogen atom, respectively a halogen atom, and a 6- alkoxy-carbonyl group is preferred, and a methyl group and a methoxycarbonyl group are particularly preferred.
- C 3 8 cycloalkane together with the carbon atoms to which R 2 and R 3 are adjacent preferably cyclopentane, 5 or 6-membered homocyclic ring such as cyclohexane (in particular, key San cyclohexylene) may form a preferable.
- ⁇ optionally substituted hydrocarbon group '' represented by R 4 and R 5
- the same as the ⁇ optionally substituted hydrocarbon group '' exemplified as the substituent of ring A Things are used.
- (1) halogen atom, (2) halogenated alkyl, (3) optionally halogenated — 6 alkoxy, (4) halogenated alkylthio, (5 ) May have 1 to 5 substituents selected from hydroxy, (6) amino, (7) monoalkylamino, (8) dialkylamino, etc. — 6 alkyl group, C 26 alkenyl group or C preferably 2 _ 6 alkynyl group, particularly an alkyl group (e.g., methyl, etc. Echiru) are preferred.
- R 4 and R 5 for example, a hydrogen atom, an alkyl group (eg, methyl, ethyl) and the like are preferable, and a hydrogen atom is particularly preferable.
- a hydrogen atom is particularly preferable.
- the ⁇ optionally substituted hydrocarbon group '' represented by R 6 and R 7 the same as the ⁇ optionally substituted hydrocarbon group '' exemplified as the substituent of the ring A Of these, a (-6) alkyl group (eg, methyl, ethyl, etc.) is preferred, and a methyl group is particularly preferred.
- the above-mentioned “replacement formed by R 2 and R 3 together with adjacent carbon atoms” have a substituent like are used and may also be 3 to 8-membered ring ", among them is preferably 8-membered homocyclic to 3 which may have a substituent, of these C 3 _ 8 Preferred are cycloalkanes (eg, cyclobutane, cyclopentane, cyclohexane, cycloheptane, cyclooctane), and particularly preferred are 5- or 6-membered homocyclic rings (particularly, cyclopentane) such as cyclopentane and cyclohexane.
- cycloalkanes eg, cyclobutane, cyclopentane, cyclohexane, cycloheptane, cyclooctane
- 5- or 6-membered homocyclic rings particularly, cyclopentane
- C 2 - 6 alkenyl group e.g., Ariru, such as 2-methyl-2-propenyl
- C 2 _ 6 alkynyl group e.g., propargyl, etc.
- C 3 _ 6 cycloalkyl group
- substituent of the hydrocarbon group examples include (1) a halogen atom (for example, fluorine, chlorine, bromine, and iodine), (2) a hydroxy group, (3) an amino group, (4) lipoxy, and (5) rubamoyl.
- a halogen atom for example, fluorine, chlorine, bromine, and iodine
- a hydroxy group for example, an amino group, (4) lipoxy, and (5) rubamoyl.
- C- 6 alkoxy monopropionyl eg, methoxycarbonyl, X toxiccarbonyl, etc.
- Monono C i _ 6 alkyl monopotassium rubamoyl eg, methylcarbamoyl, ethylcarbamoyl, etc.
- G-alkyl-carbamoyl eg, dimethylcarbamoyl, getylcarbamoyl, etc.
- one to three carbon atoms which may have an oxo atom, other than nitrogen atom, sulfur atom, oxygen atom, etc.
- Hetero atom-containing 4- to 10-membered heterocyclic groups eg, pyridyl, 2-isoindolyl, etc.
- C 6 monoaryl groups eg, phenyl, etc.
- acyl group '' represented by R 8 those similar to the ⁇ acyl group '' exemplified as the substituent for the ring A are used, and this acyl group further has a substituent selected from the group of substituents A to 1 to 5 , Preferably one to three.
- the heterocyclic group represented by R 8 is a 4- to 10-membered aromatic heterocyclic group containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms.
- ring groups eg, tetrazolyl, etc.
- the substituent of the heterocyclic group, C 6 - 1 4 Ariru group (e.g., phenyl etc.) and the like are preferable.
- the halogen atom represented by R 8 fluorine atom, chlorine atom, bromine atom, iodine atom are used, inter alia as chlorine atom is preferable. ,
- Examples of the hydrocarbon group represented by R 1 G include (OC ⁇ -e alkyl group (eg, methyl, ethyl, isopropyl, butyl, etc.) [the 6- alkyl group is (1) halogen atom, (2) hydroxy Group, (3) amino group, (4) diluvamoyl, (5) diluvamoyl, (6) alkoxy-diluponyl, (7) monol-alkyl diluvamoyl, (8) Di--6 alkyl monorubumoyl, (9) containing from 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon which may have oxo, 10-membered aromatic Hajime Tamaki (e.g., pyridyl, 2-isoindolyl, etc.) which may have a substituent selected from such], (ii) C 2 _ 6 alkenyl group (e.g., ⁇ Lil, 2-methyl 2-propeny
- the “acyl group” represented by R 1Q includes, for example, formyl, sorbamoyl, —6 alkyl monopropionyl (eg, acetyl, propionyl, etc.), c 3 _ 6 Cycloalkyl-carbonyl (eg, cyclopentylcarbonyl, cyclohexylcarbonyl, etc.), C 6 alkoxy mono-proponyl (eg, methoxy-proponyl, ethoxycarbonyl, isopropoxy-proponyl, tert-butoxycarbonyl, etc.), C 6 _ 14 Ariru - carbonyl (e.g., Benzoiru, 2 Nafutoi Le etc.), C 7 _ 16 Ararukiru - Karuponiru (eg, phenylene Ruasechiru, 3-phenylene Rupuropioniru), C 6 ⁇ 4 ⁇ Li one
- E Ji carbamoyl di -C - 6 alkyl Ichiriki Rubamoiru (e.g., dimethyl carbamoyl, such as GETS Ji carbamoyl), C 6 - 14 ⁇ Li one Roux force Rubamoiru (eg, full E carbamoylmethyl Such as 2 _ naphthylcarbamoyl), 5- or 6-membered heterocyclic Cal Bamoiru (e.g., 1-pyrrolidinylmethyl carbamoyl, 4 one piperidylcarbamoyl, 1 —Selected from nitrogen, sulfur, oxygen, etc.
- cyclohexyl Chiokaruponiru alkoxy - Chiokaruponiru (e.g., methoxide ⁇ Chioka Ruponiru, Etokishichi Sairyoku Ruponiru, propoxycarbonyl Chio carbonyl, etc.
- E chill sulfamoyl E chill sulfamoyl
- G ⁇ _ 6 alkyl - sulfamoyl (e.g., dimethylsulfamoyl, etc. Jechirusu Rufamoiru)
- C 6 ⁇ 4 Ariru - sulfamoyl e.g., such as Fuenirusurufa Moyle
- ⁇ _ 6 alkylsulfonyl e.g., methylsulfonyl, etc.
- Echirusuruho sulfonyl C 6 - 14 ⁇ reel sulfonyl ( examples, phenylalanine sulfonyl, such as 2-naphthyl Rusuruhoniru), ( ⁇ 6 alkylsulfinyl (e.g., methylsulfinyl, etc.
- C 6 _ 14 ⁇ reel sulfinyl e.g., Hue Nils sulfinyl, 2- Nafuchirusuru Fiel, etc.
- sulfino e.g., sulfo
- alkoxys Rufiniru e.g., methoxysulfinyl, E Toki cis sulfinyl
- c 6 - 14 ⁇ reel O carboxymethyl sulfinyl e.g., full enoki cis Luffy El
- Arukokishisu Ruhoniru e.g., methoxysulfonyl, E butoxy-benzenesulfonyl
- c 6 _ 14 Ari Ruo Xylsulfonyl e.g, phenoxysulfonyl
- this acyl group may further have 1 to 5, preferably 1 to 3, substituents selected from the substituent group A.
- ⁇ 6 alkoxy carbonyl group eg, methoxycarbonyl, ethoxycarbonyl, etc.
- V monomer
- Other di primary alkyl one Chiokarubamoiru group e.g., methylthio Scarpa moil, such as di-methylthio force Rubamoiru
- halogenated may CI_ 6 alkyl one sulfonyl group (e.g., methyl sulfonyl), etc. are preferable.
- examples of the heterocyclic group represented by R 1Q include a 4- to 10-membered aromatic heterocyclic group containing 1 to 4 hetero atoms selected from nitrogen, sulfur, and oxygen atoms in addition to carbon atoms. (eg, such as tetrazolyl) [this double ring group C 6 - 14 Ariru (e.g., phenyl) which may have a. ] Is preferred.
- SR 11 may be a ⁇ carbonized optionally having substituent (s) '' represented by R 11 As the “hydrogen group”, those similar to the “optionally substituted carbon hydride group” exemplified as the substituent for the ring A are used.
- the hydrocarbon group represented by R 11, are preferred, such as ( ⁇ _ 6 alkyl group (e.g., methyl, etc. Echiru).
- acyl group represented by R 11 in the formula—31 11 of the formula—31 11 represented by the scale 8 the same “acyl group” represented by R 1Q can be used. It may have 1 to 5, preferably 1 to 3, substituents selected therefrom.
- the “acyl group” represented by R 11 is preferably a monol or dialkyl-carbamoyl group (eg, methylcarbamoyl, dimethylcarbamoyl, etc.).
- the “optionally substituted hydrocarbon group” represented by R 12 includes the “substituent having a substituent” exemplified as the substituent for ring A.
- the same hydrocarbon groups as those described above may be used.
- the hydrocarbon group represented by R 12, ⁇ alkyl group (e.g., methyl, etc. Echiru) is preferable.
- hydrocarbon group represented by R 13 (: Preparative 6 alkyl group (e.g., methyl, etc. Echiru) is preferably such.
- Examples of the hydrocarbon group represented by R 14 and R 15 include a C 6 alkyl group (eg, methyl, ethyl, etc.) [This alkyl group may have an alkoxyl monopropyl. And the like are preferred.
- acyl group represented by R 14 and R 15 of the formula 1 NR 14 R 15 represented by R 8
- R 1Q can be used.
- substituents selected from substituent group A.
- formyl, c ⁇ 6 alkyl-caprolponyl group eg, acetyl, propionyl, etc.
- alkoxy-carbonyl group eg, methoxycarbonyl, ethoxycarponyl, etc.
- caprolvamoyl group mono- or dialkyl Carbamoyl groups (eg, methylcarbamoyl, dimethylcarbamoyl, etc.)
- C ⁇ - 6 alkyl chromatography sulfonyl group e.g., methyl sulfonyl, etc. are preferable.
- Examples of the ⁇ heterocyclic group optionally having substituent (s) '' represented by R 14 and R 15 in the formula 1 NR 14 R 15 represented by R 8 include ⁇ substituents exemplified as substituents on ring A. The same ones as those described for the "heterocyclic group which may be possessed" are used.
- R 14 is a hydrogen atom, (2) a 6- alkyl group (eg, methyl, ethyl, etc.) [This alkyl group has 6 alkoxy-carbonyl Is also good.
- R 15 is 1 a hydrogen atom , 2 (: preparative 6 alkyl (e.g., methyl, Echiru, propyl Le, isopropyl, etc.), 3 C 6 - 14 Ariru (e.g., phenyl, 2-naphthyl, etc.) or 4 C 7 - 16 Ararukiru (e.g., benzyl, phenethyl
- R 14 is preferably a hydrogen atom, or an alkyl group (eg, methyl, ethyl, etc.) [this alkyl group May have alkoxy-carbonyl No.
- R 8 represents a hydrogen atom or a formula —OR 1Q (R 1Q represents a hydrogen atom, a hydrocarbon group which may have a substituent, an acyl group or a heterocyclic group which may have a substituent) Is preferred.
- R 8 a hydrogen atom, a hydroxyl group (where R 1Q is a hydrogen atom), an optionally substituted Ci-e alkoxy (R 1G may have a substituted C Preferred are i- 6 alkyl) or acyloxy (where R 10 is acyl).
- substituent for the hydrocarbon group examples include an ⁇ halogen atom (for example, fluorine, chlorine, bromine, and iodine), (2) a cyano group, (3) a lower alkoxy group (eg, methoxy, ethoxy), and (4) hydroxy.
- acyl group represented by R 9
- those similar to the “acyl group” exemplified as the substituent for the ring A can be used. Specifically, (1) formyl, (2) 0 ⁇ 6 alkyl- power Lupo sulfonyl group (e.g., Asechiru, propionyl and the like), (3) C 6 _ 14 Ariru - power Ruponiru group (eg, a Benzoiru), (4) C 7 - 16 Ararukiru - carbonyl group (e.g., Fuenirua cetyl etc.) , (5) C ⁇ 6 alkoxy Ichiriki Ruponiru group (e.g., methoxy Cal Poni Le, an ethoxy Cal Poni le), (6) force Rubamoiru group, (7) mono - or di C ⁇ - 6 Al kill Ichiriki Rubamoiru group (e.g., methylcarbamoyl, etc.
- dimethylcarbamoyl dimethylcarbamoyl
- mono- or di-primary alkyl one Chiokarubamoiru group eg, Mechiruchiokaru Bamoiru, dimethylthiocarbamoyl Kalpa moil etc.
- C _ 6 alkyl one sulfonyl group e.g. And methylsulfonyl
- C 1 _ 6 alkyl one sulfinyl group e.g., a methylcarbamoyl Rusurufiniru
- R 9 As the "optionally substituted hydroxy group" represented by R 9, for example, the formula - OR 9 '(R 9' may be a hydrogen atom, an optionally substituted hydrocarbon group or Ashiru group The group represented by is used.
- optionally substituted hydrocarbon group represented by R 9 those similar to the “optionally substituted hydrocarbon group” exemplified as the substituent for the ring A can be mentioned. Used, and among them, alkyl and the like are preferable.
- acyl group represented by R 9 those similar to the “acyl group” represented by R 1Q can be used, and among them, Ci- 6 alkyl-pyruonyl and the like are preferable.
- R 9 is preferably a hydrogen atom, a cyano group, an alkyl group optionally substituted with cyano, formyl, and the like, and particularly preferably a hydrogen atom.
- X represents (1) a methylene group which may have a substituent or (2) a carbonyl group.
- substituent of the methylene group a group selected from the above-mentioned substituent group A is used, and among them, one or two alkyl groups (eg, methyl, ethyl, etc.) and a hydroxyl group are preferable.
- the X (1) one or two ( ⁇ _ 6 alkyl group (e.g., methyl, good methylene group or (2) a carbonyl group which may have a like) or a hydroxyl group Echiru preferable, 1 or A methylene group which may have two methyl groups is preferred, and a methylene group is particularly preferred.
- ⁇ _ 6 alkyl group e.g., methyl, good methylene group or (2) a carbonyl group which may have a like
- a hydroxyl group Echiru preferable 1 or
- a methylene group which may have two methyl groups is preferred, and a methylene group is particularly preferred.
- n 0 or 1, and particularly preferably 0.
- R 1 is the formula
- R 2 and R 3 each represent a hydrocarbon group which may have a substituent
- R 4 and R 5 represent A hydrogen atom
- R 6 and R 7 each represent a hydrocarbon group which may have a substituent
- R 8 represents a hydrogen atom or a formula OR 1Q (R 1Q represents a hydrogen atom or a substituent A hydrocarbon group, an acyl group or a heterocyclic group which may have a substituent)
- R 9 is a hydrogen atom
- X is methylene
- n is 0 ( ⁇ ) Or its salt.
- R 1 is the formula
- R 16 is a hydrogen atom, which may have a substituent C 6 _ 14 Ariru group, an optionally substituted amino group, optionally substituted heterocyclic group Or a halogen atom), R 2 and R 3 each may have an alkyl group, R 4 and R 5 may represent a hydrogen atom, and R 6 and R 7 may represent a hydrogen atom.
- R 8 represents a hydrogen atom or a group represented by the formula OR 1 Q (R 1 ° represents a hydrogen atom, a hydrocarbon group optionally having a substituent, an acyl group or A compound ( ⁇ ) or a salt thereof, wherein R 9 represents a hydrogen atom, X represents methylene, and n is 0.
- R 1 is the formula
- R 16 represents (1) a hydrogen atom, (2) phenyl substituted with an acetylamino group, (3) (i) C i_ 6 alkylsulfonyl group, (ii) pyridylcarponyl or (iii) sulfamoyl ⁇ _ 6 represents an amino, which may be mono- or di-substituted by a substituent selected from an alkyl group, (4) pyridyl or (5) a halogen atom], wherein R 2 and R 3 are each Ce alkyl R 4 and R 5 are hydrogen atoms; R 6 and R 7 are each 6 alkyl groups; R 8 is a hydrogen atom or a formula —OR 1 Q (R 1Q is (1) hydrogen atom, (2 ) Represents an alkyl group optionally substituted with pyridyl or (3) alkylsulfonyl substituted with a halogen atom), R 9 represents a hydrogen atom, represents methylene
- ring A, ring B and ring C may each have the same substituent as described above], and the like.
- R 2 ,, R 3 ', R 6' and R 7, each represents an alkyl group
- R 16 are hydrogen atoms, which may have a substituent C 6 14 Ariru group, a substituent Which may have an amino group, a heterocyclic group which may have a substituent or a halogen atom].
- the compound (A-1), (1-1) or ( ⁇ ′-1) of the present invention specifically, the compounds produced in Examples 1 to 16 and the like are used.
- Compound (la) is a compound included in compound (I).
- the compounds (I) and ( ⁇ ) of the present invention can be obtained, for example, by the method represented by the following reaction formulas 1 and 2, or a method analogous thereto.
- Compounds (A), (A-1), (1-1) and (II-1) can also be produced according to the following production method.
- the compounds ( ⁇ ) to (VI) and ( ⁇ ') to ( ⁇ ) in the reaction formula include those in the form of a salt.
- Examples of the salt include the same as the salt of the compound (I) or ( ⁇ ). And the like.
- Alcohols such as methanol, ethanol, 1-propanol, 2-propanol, tert-butyl alcohol, etc.
- Ethers such as getyl ether, diisopropyl ether, diphenyl ether, tetrahydrofuran, 1,4-dioxane, 1,2 —Dimethoxyethane, etc.
- Hydrocarbons such as benzene, toluene, cyclohexane and hexane, and amides such as N, N-dimethylformamide, N, N—dimethylacetamide, hexamethylphosphoric triamide
- Halogenated hydrocarbons such as dichloromethane, chloroform, carbon tetrachloride, and 1,2-dichloroethane; nitriles such as acetonitrile and propionitrile; ketones such as acetone and ethyl methyl ketone
- Organic acids such as formic acid, acetic acid, Acid, Torifuruoro acetic acid, methanesulfonic acid, aromatic Amin compounds show pyridine, 2, 6-lutidine, quinoline, etc., and etc. dimethylsulfoxide as sulfoxides.
- the bases used in the following reactions and represented by a generic name include sodium hydroxide, potassium hydroxide, lithium hydroxide and barium hydroxide as inorganic bases, sodium carbonate as basic salts, and the like. Potassium carbonate, cesium carbonate, sodium hydrogen carbonate, sodium acetate, ammonium acetate, etc. Pyridine, lutidine, etc.
- Sodium hydride, alkali metal hydrides such as amine, cyclohexyl dimethylamine, 4-dimethylaminopyridine, N, N-dimethylaniline, N-methylpiperidine, N-methylpyrrolidine, N-methylmorpholine Metals such as potassium Alkoxides such as sodium amide, lithium diisopropylamide, and lithium hexamethyldisilazide; alkyl metals such as butyllithium and tert-butyllithium; aryl metals such as phenyllithium; and metal alkoxides such as sodium methoxide and sodium ethoxide.
- the product can be used in the next reaction as a reaction solution or as a crude product, but it can also be isolated from the reaction mixture according to a conventional method, and can be separated by a usual separation method (eg, recrystallization, distillation, chromatography, etc.). Can be easily purified.
- Compound (la) wherein the C ′ ring may have a substituent other than RR 2 and R 3 is produced by the process shown in Reaction Scheme 1.
- Compound (III) is produced by converting compound (II) into an organometallic compound using magnesium or a base, and reacting the compound with a formylating agent.
- base examples include alkyl metals, aryl metals and the like.
- the amount of the base to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound (II).
- the "formylating agent” examples include N, N-dimethylformamide, 1-formylpiperidine, 4-formylmorpholine, N-methylformanilide and the like.
- the amount of the formylide used is about 1 to about 10 mol, preferably about 1 to about 5 mol, per 1 mol of compound (II).
- This reaction is advantageously performed using a solvent inert to the reaction.
- the solvent is not particularly limited as long as the reaction proceeds, but is preferably, for example, a solvent such as ethers or hydrocarbons, or a mixed solvent thereof.
- the reaction time is generally about 10 minutes to about 48 hours, preferably about 30 minutes to about 24 hours.
- the reaction temperature is usually about ⁇ 100 to about 150 ° C., preferably about 180 to about 100 ° C.
- hydrocarbon group include chain or cyclic hydrocarbon group (e.g., _ 6 ⁇ alkyl (e.g., methyl, Echiru, propyl, isopropyl, butyl, Isopuchiru, sec - heptyl, ter t-heptyl, pentyl , the like hexyl), C 3 _ 6 cycloalkyl (eg example, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexylene hexyl, etc.), C 6 - 1 4 Ariru (e.g., phenyl, 1 one-naphthyl, 2-naphthyl, Bifue two Lilly, 2-anthryl, etc.).
- alkyl e.g., methyl, Echiru, propyl, isopropyl, butyl, Isopuchiru, sec - heptyl, ter t
- the amount of compound (IV) to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound (III).
- base examples include inorganic bases, basic salts, aromatic amines, tertiary amines, alkali metal hydrides, alkyl metals, aryl metals, metal amides, metal alkoxides and the like. Is mentioned.
- the amount of base used is the same as that of compound (III) About 1 to about 5 moles, preferably about 1 to about 2 moles, based on
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds, but examples thereof include solvents such as alcohols, ethers, hydrocarbons, amides, halogenated hydrocarbons, nitriles, sulfoxides, and water. Are preferred.
- the reaction time is usually about 30 minutes to about 48 hours, preferably about 1 hour to about 24 hours.
- the reaction temperature is usually about 100 to about 200 ° C, preferably about 180 to about 150 ° C.
- Compound (la) is produced by reacting compound (V) with compound (VI) in the presence of an acid.
- the amount of compound (VI) to be used is about 0.5 to about 5 mol, preferably about 0.5 to about 2 mol, per 1 mol of compound (V).
- Examples of the “acid” include mineral acids such as sulfuric acid, hydrogen chloride, hydrogen bromide, hydrogen iodide, and perchloric acid; boron trifluoride dimethyl ether complex; Lewis acids such as zinc chloride and aluminum chloride; .
- the amount of the acid to be used is about 1 to about 5 mol, preferably about 1 to about 3 mol, per 1 mol of compound (V).
- This reaction is advantageously performed using a solvent inert to the reaction.
- the solvent is not particularly limited as long as the reaction proceeds, but is preferably, for example, a hydrocarbon, an organic acid, a halogenated hydrocarbon, or a mixture thereof.
- the reaction time is generally about 10 minutes to about 48 hours, preferably about 15 minutes to about 24 hours.
- the reaction temperature is usually about 120 to about 150 ° C, preferably about 0 to about 10 ° C.
- the compound ( ⁇ ′) is a compound ( ⁇ ) and a compound ( ⁇ ) wherein R 23 and R 24 are a hydrocarbon group which may form a part of R 7 and may have a substituent. those similar to R 7 can be exemplified, W is is prepared by reacting in the presence of a base as desired and represents a leaving group].
- Examples of the “leaving group” include hydroxy, halogen atom (eg, fluorine, chlorine, bromine, iodine, etc.), and optionally halogenated Ci-s alkylsulfonyloxy (eg, methanesulfonyloxy, E evening down sulfonyl O carboxymethyl, trichloro methane sulfonyl O carboxymethyl, etc.), one C 6 which may have a substituent 1 () Arirusuruhoni Ruokishi the like. ".
- ⁇ Li one Rusuruhoni Ruokishi as, for example (6 alkyl (e.g., methyl, Echiru etc.), selected from (6 ⁇ alkoxy (e.g., methoxy, ethoxy, etc.) and nitro C 6 _ 1Q 7 reelsulfonyloxy (e.g., phenylsulfonyloxy, naphthylsulfonyloxy, etc.) which may have 1 to 3 substituents, and specific examples thereof include benzenesulfonyl Xy, m-nitrobenzenesulfonyloxy, p-toluenesulfonyloxy and the like.
- 6 alkyl e.g., methyl, Echiru etc.
- 6 ⁇ alkoxy e.g., methoxy, ethoxy, etc.
- nitro C 6 _ 1Q 7 reelsulfonyloxy e.g., phenylsul
- the amount of compound (VIII ′) to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound (VII ′).
- base examples include inorganic bases, basic salts, aromatic amines, tertiary amines, metal hydrides, metal amides, metal alkoxides and the like.
- the amount of the base to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound ( ⁇ ).
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds, and examples thereof include solvents such as alcohols, ethers, hydrocarbons, amides, halogenated hydrocarbons, nitriles, ketones, and sulfoxides. Alternatively, a mixed solvent thereof is preferable.
- the reaction time is usually about 15 minutes to about 48 hours, preferably about 30 minutes to about 24 hours.
- the reaction temperature is generally about 120 to about 150 ° C, preferably about 0 to about 100 ° C.
- the compound ( ⁇ ⁇ ) and the compound ( ⁇ ⁇ ⁇ ) in which W is ⁇ ⁇ are reacted with an azodicarboxylate (eg, getyl azodicarboxylate, etc.) and a phosphine (Eg, triphenylphosphine, tributylphosphine, etc.).
- an azodicarboxylate eg, getyl azodicarboxylate, etc.
- a phosphine eg, triphenylphosphine, tributylphosphine, etc.
- the amount of the compound in which W is ⁇ in the compound ( ⁇ ⁇ ′) is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of the compound ( ⁇ ⁇ ).
- the amount of the “azodicarboxylates” and “phosphines” to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of the compound ( ⁇ )).
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds, but examples thereof include solvents such as ethers, hydrocarbons, amides, halogenated carbons, nitriles, ketones, and sulfoxides. Preferred are mixed solvents thereof.
- the reaction time is generally about 5 minutes to about 48 hours, preferably about 10 minutes to about 24 hours.
- the reaction temperature is usually about 120 to about 200, preferably about 0 to about 100.
- Compound ( ⁇ ′) is produced by subjecting compound ( ⁇ ′) to Claisen rearrangement.
- This reaction is advantageously performed without a solvent or using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds.
- alcohols, hydrocarbons, organic acids, ethers, and anilines eg, ⁇ , ⁇ -dimethyl aniline, ⁇ , ⁇ — Phenethylaniline, etc.
- phenols eg, 2,6-dimethylphenol
- halogenated hydrocarbons or a mixed solvent thereof.
- This reaction may be performed using an acid catalyst, if desired.
- the acid catalyst Lewis acids such as aluminum chloride and boron bromide are used.
- the amount of the acid catalyst to be used is, for example, in the case of a Lewis acid, usually about 0.1 to about 20 mol, preferably about 0.1 to about 5 mol, per 1 mol of compound (IX ').
- the reaction time is usually about 30 minutes to about 24 hours, preferably about 1 to about 8 hours.
- the reaction temperature is usually about -70 to About 30 Ot: preferably about 150 to about 250 ° C.
- Compound ( ⁇ ) can be produced by cyclizing compound ( ⁇ ') in the presence of a protonic acid, a Lewis acid or iodine.
- protic acids include mineral acids such as hydrochloric acid, hydrobromic acid, and sulfuric acid, and sulfonic acids such as methanesulfonic acid, trifluoromethanesulfonic acid, and fluorosulfonic acid.
- Lewis acids include aluminum chloride, aluminum bromide, and the like. Titanium chloride ( ⁇ ), tin chloride ⁇ ), zinc chloride, boron trichloride, boron tribromide, boron trifluoride and the like are used.
- a protonic acid or a Lewis acid is used alone, but both may be combined as desired.
- protonic acid it is used in an amount of about 1 to about 200 mol, preferably about 1 to about 100 mol, per 1 mol of the compound ⁇ ').
- a Lewis acid it is used in an amount of about 1 to about 5 mol, preferably about 1 to about 3 mol, per 1 mol of compound ( ⁇ ′).
- iodine it is used in an amount of about 0.05 to about 1 mol, preferably about 0.1 to about 0.5 mol, per 1 mol of the compound ( ⁇ ′).
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent inert there is no particular limitation as long as the reaction proceeds as such a solvent, but examples thereof include ethers, hydrocarbons, alcohols, amides, halogenated hydrocarbons, nitriles, ketones, and sulfoxides. Or a mixed solvent thereof is preferred.
- the reaction temperature is usually about -20 to about 150, preferably about 0 to about 120 ° C.
- the reaction time is usually about 5 minutes to about 24 hours, preferably about 10 minutes to about 5 hours.
- Compound (II) is produced from compound (II) in the same manner as when producing compound (III) from compound (II).
- Compound ( ⁇ ') can be prepared in the same manner as in the production of compound (V) from compound (III) and compound (IV); compound ⁇ ) and compound (IV) wherein R 22 and hal are as defined above. Show the same significance].
- Compound ( ⁇ ) is produced from compound ⁇ ′) and compound (VI) in the same manner as in the production of compound (la) from compound (V) and compound (VI).
- a compound in which X is methylene in compound (r) can be produced.
- the compound thus obtained is optionally subjected to a functional group conversion based on a reaction known per se, whereby X is a substituted methylene and a carbonyl compound.
- X is a substituted methylene and a carbonyl compound.
- a protecting group generally used in peptide chemistry or the like may be introduced into these groups.
- the target compound can be obtained by removing the protecting group as necessary.
- the protecting group of Amino for example, formyl or each alkyl Ichiriki be substituted Ruponiru (e.g., Asechiru, propionyl, etc.), benzo I Le, C WINCH 6 alkoxy - carbonyl (e.g., methoxy Cal Poni Le, Etokishika Ruponiru etc.), phenylalanine O carboxymethyl Cal Poni le, c 7 _ 1 6 Ararukiruokishi Ichiriki Lupo two Le (e.g., benzyl O carboxymethyl cull Poni Le etc.), trityl, phthaloyl and the like Ru is used.
- Ruponiru e.g., Asechiru, propionyl, etc.
- benzo I Le C WINCH 6 alkoxy - carbonyl (e.g., methoxy Cal Poni Le, Etokishika Ruponiru etc.), phenylalanine O carboxymethyl Cal Poni le,
- halogen atom for example, fluorine, chlorine, bromine, iodine, etc.
- 6- alkyl monopropanol for example, acetyl, propionyl, parryl, etc.
- nitro and the like are used. Is about one to three.
- Examples of the protecting group for alkoxy include alkyl which may have a substituent (eg, methyl, ethyl, propyl, isopropyl, butyl, tert-butyl, etc.), phenyl, trityl, silyl, etc. .
- alkyl which may have a substituent (eg, methyl, ethyl, propyl, isopropyl, butyl, tert-butyl, etc.), phenyl, trityl, silyl, etc.
- substituents include halogen atom (e.g., fluorine, chlorine, bromine, iodine), formyl, ( ⁇ _ 6 Al kills one force Ruponiru (e.g., Asechiru, propionyl, butylcarbonyl, etc.), Two Toro, C - 6 alkyl (e.g., methyl, Echiru, ter t-butyl, etc.), C 6 - 1 4 ⁇ Li - Le (e.g., phenyl, naphthyl and the like) and the like are used, and the number of substituents is 3 or so from 1 .
- halogen atom e.g., fluorine, chlorine, bromine, iodine
- formyl e.g., ⁇ _ 6 Al kills one force Ruponiru (e.g., Asechiru, propionyl, butylcarbonyl, etc.), Two Toro, C - 6 alkyl
- hydroxy-protecting group examples include formyl, or each of which may have a substituent — 6-alkyl (eg, methyl, ethyl, propyl, isopropyl, butyl, tert-butyl, etc.), phenyl, ⁇ 7 _ 1 6 Ararukiru (e.g., benzyl, etc.), single 6 alkyl Ichiriki Ruponiru (e.g., Asechiru, propionyl, etc.), Fueniruo Kishikaruponiru, C 7 - 1 6 Ararukiruokishi Ichiriki Ruponiru (e.g., Benjiruoki aryloxycarbonyl, etc.), tetrahydronaphthalene Villa alkenyl, Tetrahydrofurel, silyl, etc.
- substituent — 6-alkyl eg, methyl, ethyl, propyl, isopropyl, butyl
- substituents include a halogen atom (eg, fluorine, chlorine, bromine, iodine, etc.), 6- alkyl (eg, methyl, ethyl, tert-butyl, etc.), C 7 - 1 6 Ararukiru (e.g., benzyl etc.), C 6 _ 1 4 7 reel (e.g., phenyl, naphthyl, etc.), nitro and the like are used, and the number of the substituents is about four from 1.
- halogen atom eg, fluorine, chlorine, bromine, iodine, etc.
- 6- alkyl eg, methyl, ethyl, tert-butyl, etc.
- C 7 - 1 6 Ararukiru e.g., benzyl etc.
- C 6 _ 1 4 7 reel e.g., phenyl, naphthyl, etc.
- nitro and the like are used
- a method for removing the protecting group a method known per se or a method analogous thereto is used. Examples thereof include an acid, a base, ultraviolet light, hydrazine, phenylhydrazine, sodium N-methyldithiocarbamate, and tetrabutylammonium fluoride. , A method of treating with palladium (II) acetate or the like, or a reduction reaction is used.
- a deprotection reaction an acylation reaction, an alkylation reaction, a hydrogenation reaction, an oxidation reaction, a reduction reaction, a carbon chain extension reaction, and a substituent exchange reaction may be used alone or in combination of two or more.
- compounds (A), (I), (1 ′), (A-1), (1-1) or ( ⁇ ′-1) can be synthesized.
- the methods described in New Experimental Chemistry Lectures 14, 15 and 1977 are adopted.
- the compound (A;), (1), ( ⁇ ), ( ⁇ -1), (I-1) or (-1) thus obtained can be obtained by known means such as phase transfer, concentration, solvent extraction, fractionation, It can be isolated and purified from the reaction solution by crystallization, recrystallization, chromatography and the like.
- Compound (A), (I), (), (A-1), (1-1) or ( ⁇ -1) is a conjugated isomer (configuration isomer), diastereomer, conformer, etc. If present, each can be isolated by the above-mentioned separation and purification means, if desired. Further, when the compound (A), (I), ( ⁇ ), (A-1), (1-1) or ( ⁇ -1) is a racemate, the S-isomer and the S-isomer are obtained by ordinary optical resolution means. Can be separated into R-forms.
- Compounds (A), (I), (), (A-1), (1-1) or (I, -1) may be hydrates or non-hydrates.
- Compound (A), (1), ( ⁇ ), (A- 1), (I - 1) or (I, - 1) is (For example, 3 H, 14 35 S) isotopes are labeled with like You may.
- R 2a and R 3a each may be an aliphatic hydrocarbon group which may have a substituent
- R 4a and R 5a may each have a hydrogen atom or a substituent
- the hydrocarbon group, R 6 a and R 7 a are each a hydrogen atom or an optionally substituted carbon hydrocarbon group, the substituent together with the carbon atoms R 6 a and R 7 a is adjacent May form a 3- to 8-membered ring
- R 8a is (1) a hydrogen atom, (2) a hydrocarbon group which may have a substituent, (3) an acyl group, (4) a heterocyclic group which may have a substituent, (5) a halogen atom, (6) -OR 10a
- R 1Qa represents a hydrogen atom, a hydrocarbon group which may have a substituent
- —SR lla R lla is a hydrogen atom, a hydrocarbon group which may have a substituent, an acyl group or a heterocyclic
- R 12a R 12a is have may have a substituent hydrocarbon group or a substituted group (9) — S (O) 2 R 13a (where R 13a is a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent) the illustrated) or (10) _NR 14a R 15a ( R 14 a and R 15 a are each a hydrogen atom, may be an optionally substituted hydrocarbon group, which may have a Ashiru group or substituent heterocyclic R 9a represents a hydrogen atom, a hydrocarbon group optionally having substituent (s), an acyl group or a hydroxyl group optionally having substituent (s), or a salt thereof. Is a novel compound.
- Alkyl group [preferably, a lower alkyl group (e.g., methyl, Echiru, propyl, isopropyl, butyl, isobutyl, sec- butyl, tert- butyl, pentyl, etc. ( ⁇ _ 6 alkyl groups such as hexyl)],
- a lower alkyl group e.g., methyl, Echiru, propyl, isopropyl, butyl, isobutyl, sec- butyl, tert- butyl, pentyl, etc. ( ⁇ _ 6 alkyl groups such as hexyl)
- Cycloalkyl groups [preferably, a lower cycloalkyl group (e.g., Shikuropuropi Le, cyclobutyl, cyclopentyl, C 3 _ 6 cycloalkyl group such as cyclohexyl), may be condensed with a benzene ring,
- a lower cycloalkyl group e.g., Shikuropuropi Le, cyclobutyl, cyclopentyl, C 3 _ 6 cycloalkyl group such as cyclohexyl
- substituent of these "aliphatic hydrocarbon group” for example, (1) a halogen atom, (2) 0, _ 3 alkylene O alkoxy group, (3) a nitro group, be (4) a halogenated good C ⁇ - 6 alkyl group, (5) C 3 _ 6 cycloalkyl group, (6) C 6 - 14 Ariru group, (7) optionally halogenated alkoxy group, optionally be (8) halogenated also alkylthio group, (9) hydroxy group, (10) amino group, (11) mono - 6 alkylamino group, (12) mono- C 6 _ 14 Ariruamino group, (13) G ⁇ - 6 alkylamino group, (14) G C 6 - 14 ⁇ Li one Ruamino group, (15) formyl, carboxy, force Rubamoiru, alkyl one carbonyl, C 3 - 6 cycloalkyl one carbonyl, c I 6 alkoxy one carbonyl, C 6 _
- substituent group B A group selected from the group consisting of groups formed by bonding three groups (hereinafter, abbreviated as substituent group B) is used. Specific examples of these substituents include the same as those exemplified in the above-mentioned substituent group A.
- R 6 a and R 7 a it is may be formed together with the adjacent carbon atoms as "no 3 may have a substituent to 8-membered ring" formed together with the carbon atom to which R 6 and R 7 adjacent And the same as the “3- to 8-membered ring optionally having substituent (s)” may be used.
- R 8a represents a “hydrocarbon group which may have a substituent”, an “acyl group”, a “heterocyclic group which may have a substituent”, a “halogen atom”, or a compound represented by the formula R 1 () a , “Formula — SR lla ”, “Formula —S (O) R 12a J”, “Formula —S (O) 2 R 13a ” or “Formula — N 1 a R 15a j, "optionally substituted hydrocarbon group” represented by 8 "Ashiru group", "substituted heterocyclic group which may have a", “halogen atom", “formula - OR 10"
- the same formulas as those of “Formula—SR 11 ,“ Formula—S (O) R 12 ”,“ Formula 1 S (0) 2 R 13 ”or“ Formula 1 NR 14 R 15 ” are used.
- Examples of the “optionally substituted hydrocarbon group”, “acyl group” and “optionally substituted hydroxyl group” represented by R 9a include “substituents” represented by R 9 The same groups as those described for the "hydrocarbon group optionally having", the "acyl group” and the “hydroxyl group optionally having a substituent" are used.
- R 2 a and R 3 a are each 1 halogen atoms, 2 Ji 6 alkyl, - 6 Al kill one Karuboeru, substituted by C i _ 6 alkylsulfonyl and C 7 _ 16 substituents
- Ru is selected from Ararukiru hydroxy which may, 3 1 or 2 CI- 6 alkyl, Ji E - 6 alkyl Ichiriki Ruponiru and C e- i 4 Ariru Ichiriki optionally substituted amino group with a substituent selected from Ruponiru, 4 A 4- to 10-membered heterocyclic group having 1 to 3 heteroatoms selected from a nitrogen atom, an oxygen atom and a sulfur atom in addition to a carbon atom, a thio group optionally substituted with ⁇ ⁇ ⁇ alkyl, 6 — 6 A C 6 alkyl group optionally substituted with an alkylsulfinyl group or a ⁇ C alkyl-sulfonyl group,
- R 8a is 1 (: 6 alkyl group, 2 Nono androgenic atoms, 3 Shiki ⁇ _R 10a
- R 10a is, (i) a hydrogen atom, (ii) ( ⁇ -6 alkyl [the alkyl group (1) halogen atom, (2) hydroxy group, (3) amino group, (4) force Rupokishi, (5) force Rubamoiru, (6) ( ⁇ - 6 alkoxy - power Ruponiru, (7) mono - alkyl Ichiriki Rubamoiru, (8 ) Di-C- 6- alkyl-rubamoyl, (9) containing from 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may have oxo.
- R 9 a is (i) a hydrogen atom, (ii) a C 6 alkyl group [this — 6 alkyl group is (1) a halogen atom, (2) 6 alkoxy group, (3) hydroxy group,) amino group, (5 ) Mono C 1-6 alkylamino group, (6) di-alkylamino group, (7) A 4- to 10-membered heterocyclic group containing 1 to 3 hetero atoms selected from a nitrogen atom, a sulfur atom and an oxygen atom in addition to a carbon atom; (8) C 6 _ 1 4 Arylthio, (9) Ureido, (10) Power Lupoxyl, (11) Power Lubamoyl, (12) (: 6 Alkoxy One Power Luponil, (13) Mono-( ⁇ _ 6 alkyl-Power Lubamoyl, (14) Formylamino and (15) it may have a substituent selected from alkyl-carboxamides] or (iii) a compound showing a formyl group (B)
- the prodrugs of the compounds (I), (1 '), (1-1) and (-1) are prepared by reacting the compounds (I), ( ⁇ ), (1) (1) or (1'-1), that is, compounds (I), ( ⁇ ), (1-1) or (1, -1) which are enzymatically oxidized, reduced, hydrolyzed, etc. ), Or a compound that undergoes hydrolysis by gastric acid or the like to change to a compound (I), ( ⁇ ), (1-1) or ( ⁇ -l).
- a prodrug of the compound (I), (1,), (1-1) or (1′_1) a prodrug of the compound (I), (I ⁇ , (1-1) or (1′-1)
- the group is acylated, alkylated or phosphorylated (for example, the amino group of compound (I), (I ⁇ , (1-1) or (1′-1) is eicosanoylated, araellated, pentylized) Minocarbonylation, (5-methyl_2-oxo-1,3-dioxolen-4-yl) methoxycarbonylation, tetrahydrofuranylation, pyrrolidinomethylation, pivaloyloxymethylation, tert- Compounds in which the hydroxyl group of the compound (I), ( ⁇ ), (1-1) or (1′-1) is acylated, alkylated, phosphorylated, or borated (for example, The hydroxyl group of compound (I), ( ⁇ ), (1-1) or (1'
- prodrugs of compounds (I), (), (1-1) or (1'-1) are disclosed in Hirokawa Shoten, 1990, “Development of Pharmaceuticals,” Volume 7, Molecular Design, 163-1. It may be changed to the compound (I), ( ⁇ ), (1-1) or ( ⁇ '-1) under physiological conditions as described in 98.
- Examples of the salt of the compound (A), (1), ( ⁇ ), (A-1), (1-1), ( ⁇ -1) or (B) include, for example, pharmacologically acceptable salts and the like. Used. Examples include salts with inorganic bases, ammonium salts, salts with organic bases, salts with inorganic acids, salts with organic acids, salts with basic or acidic amino acids, and the like. Preferred examples of the salt with an inorganic base include an alkali metal salt such as a sodium salt and a potassium salt, an alkaline earth metal salt such as a calcium salt and a magnesium salt, and an aluminum salt.
- Preferred examples of the salt with an organic base include, for example, trimethylamine, triethylamine, pyridine, picoline, 2,6-lutidine, ethanolamine, diethanolamine, triethanolamine, cyclohexylamine, dicyclohexylamine. , N, N 'salts with dibenzyldiethylenediamine and the like.
- Preferable examples of the salt with an inorganic acid include, for example, salts with hydrochloric acid, hydrobromic acid, nitric acid, sulfuric acid, phosphoric acid, and the like.
- Preferred examples of salts with organic acids include, for example, formic acid, acetic acid, trifluoroacetic acid, phthalic acid, fumaric acid, oxalic acid, tartaric acid, maleic acid, citric acid, succinic acid, malic acid, methanesulfonic acid, benzenesulfone And salts with an acid, p-toluenesulfonic acid and the like.
- Preferred examples of the salt with a basic amino acid include, for example, salts with arginine, lysine, ordinine, and the like.
- Preferred examples of the salt with an acidic amino acid include, for example, aspartic acid, glutamic acid, and the like. Salts.
- salts are preferable.
- examples thereof include compounds having a basic functional group in compound (I) or (III), for example, hydrochloric acid, hydrobromic acid, nitric acid, sulfuric acid, phosphoric acid Salts with inorganic acids such as acetic acid, fumaric acid, fumaric acid, oxalic acid, tartaric acid, maleic acid, citric acid, succinic acid, methanesulfonic acid, p-toluenesulfonic acid, etc.
- examples thereof include alkali metal salts such as sodium salts and potassium salts, and alkaline earth metals such as calcium salts and magnesium salts. Genus salts, ammonium salts and the like.
- ninii represents a single bond or a double bond
- a salt thereof has a PDE inhibitory activity, particularly a PDE IV inhibitory activity, and is caused by PDE. It can be used as an agent for preventing and treating diseases.
- the salt of the compound (A-2) include the salt of the above compound (A), (1), (I,), (A-1), (1-1), (-1) or (B). Similar ones can be mentioned.
- the compounds (A), (1), (1,), (A-1), (1-1), ( ⁇ -1) of the present invention included in the above compound (A-2) or a salt thereof Or a salt thereof (including prodrugs of compounds (I), (1-1), ( ⁇ ), and ( ⁇ -l)) (hereinafter abbreviated as compound of the present invention) is excellent: PDE inhibitory action
- PDE IV inhibitory activity is low in toxicity, and is safe, so it can be used in mammals (eg, humans, mice, dogs, rats, mice, etc.) for inflammatory diseases, autoimmune diseases, Diabetes, arteriosclerosis, graft-versus-host disease, multiple sclerosis, sepsis, psoriasis, osteoporosis, depression, central dysfunction after cerebral vascular obstruction, cerebrovascular dementia, Alzheimer's dementia, memory impairment, obesity, Heart failure, pulmonary fibrosis, allergic disease, angina, myocardial infarction, hypertension, pulmonary hypertension, Disease, brain function disorders, immunodefici
- inflammatory disease asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, diabetes, arteriosclerosis, graft-versus-host disease, multiple sclerosis, sepsis, psoriasis, osteoporosis, depression, cerebral vascular obstruction Later central dysfunction, cerebral vascular dementia, dementia of aruhaima type 1, memory impairment, obesity, heart failure, pulmonary fibrosis, allergic diseases (eg, atopic dermatitis, allergic rhinitis, juniper measles) ) Can be used as prophylactic or therapeutic agents, and PDE IV inhibitors.
- the route of administration may be oral or parenteral.
- dosage forms include, for example, tablets (including sugar-coated tablets and film-coated tablets), Pills, capsules (including microcapsules), granules, fine granules, powders, tablets, emulsions, suspensions, injections, inhalants, ointments, eye drops, aerosols, eye ointments, plasters Suppositories, troches, cataplasms, liniments and the like are used.
- These preparations are prepared according to a conventional method (for example, a method described in the Japanese Pharmacopoeia).
- the content of the compound of the present invention varies depending on the form of the preparation, but is usually from 0.01 to 100% by weight, preferably from 0.1 to 50% by weight, based on the whole preparation. % By weight, more preferably about 0.5 to 20% by weight.
- the drug was used as is, and excipients, binders, disintegrants, or other appropriate additives were added, and the mixture was uniformly mixed to obtain granules by an appropriate method.
- a lubricant is added and compression molding is performed, or the medicine is directly mixed or directly mixed with excipients, binders, disintegrants or other suitable additives.
- the granules can be produced by compression-molding the granules prepared beforehand as they are, or after adding an appropriate additive thereto and mixing them uniformly.
- the present agent can contain a coloring agent, a flavoring agent, and the like as needed.
- the agent can be coated with an appropriate coating agent.
- a certain amount of a drug is dissolved, suspended or emulsified in water for injection, physiological saline, Ringer's solution, etc. in the case of an aqueous solvent, or vegetable oil in the case of a non-aqueous solvent, to make a certain amount.
- a predetermined amount of the drug can be taken and sealed in a container for injection.
- the pharmaceutical carrier for oral use for example, substances commonly used in the pharmaceutical field such as starch, mannitol, crystalline cellulose, sodium propyloxymethylcellulose and the like are used.
- the carrier for injection for example, distilled water, physiological saline, glucose solution, infusion agent and the like are used.
- additives generally used in pharmaceutical preparations can be appropriately added.
- the dosage of these preparations varies depending on age, body weight, symptoms, route of administration, number of administrations, etc. For example, for adult asthma patients, it is converted into the active ingredient (compound of the present invention) per day. Usually 0.1 to 100 mg / kg, preferably 0.1 to 5.0 mg / kg, more preferably 0.5 to 10 mg / kg, divided orally once or twice daily It should be administered.
- the compound of the present invention exhibits excellent PDE IV inhibitory activity even when used as a single agent, it is also used in combination with other pharmaceutical ingredients other than the compound of the present invention (hereinafter abbreviated as concomitant drug) (multiple drug combination) You can also.
- concomitant drugs include anti-asthmatic agents (eg, flutidinzone propionate, beclomethasone propionate, theophylline, propoterol, ketotifen, azelastine, seratrodast, etc.), antiallergic agents (eg, fexofenadine, etc.) , Epinastine, ebastine, etc.), anticholinergic agents (eg, ipratropium bromide, fructophorium pium bromide, oxotropium bromide, etc.), anti-inflammatory agents (eg, diclofenac sodium, ibuprofen, indomethacin, loxoprofen sodium, etc.), Antibacterial agents (eg, cefixime, cefdinir, ofloxacin, tosfloxacin tosylate, lepofloxacin, etc.), antifungal agents (eg, fluconazole, itraconazole, etc.), antidia
- the timing of administration of the compound of the present invention and the concomitant drug is not limited, and the compound of the present invention and the concomitant drug may be simultaneously administered to a subject to be administered. It may be administered at a time interval.
- the dose of the concomitant drug may be in accordance with the dose clinically used, and can be appropriately selected depending on the administration subject, administration route, disease, combination, and the like.
- the administration form of the compound of the present invention and the concomitant drug is not particularly limited as long as the compound of the present invention and the concomitant drug are combined at the time of administration.
- Such administration forms include, for example, (1) administration of a single preparation obtained by simultaneously preparing a compound of the present invention and a concomitant drug, and (2) separate administration of the compound of the present invention and the concomitant drug. Simultaneous administration of the two preparations obtained as a formulation by the same administration route, (3) the time difference between the same administration route of the two preparations obtained by separately preparing the compound of the present invention and the concomitant drug.
- the concomitant drug of the present invention has low toxicity.
- the compound of the present invention or (and) the above concomitant drug is mixed with a pharmacologically acceptable carrier according to a method known per se to obtain a pharmaceutical composition such as a tablet.
- Injectables can be administered intravenously, intramuscularly, subcutaneously, in organs, intranasally, intradermally, instilled, in the brain, rectum, intravaginally and intraperitoneally, inside tumors, near tumors, or directly into lesions It can be administered.
- the same carriers as those used in the aforementioned pharmaceutical composition of the present invention can be used.
- the compounding ratio of the compound of the present invention and the concomitant drug in the concomitant drug of the present invention can be appropriately selected depending on the administration subject, administration route, disease and the like.
- the content of the compound of the present invention in the combination preparation of the present invention varies depending on the form of the preparation, but is usually about 0.01 to 100% by weight, preferably about 0. It is about 1 to about 50% by weight, more preferably about 0.5 to about 20% by weight.
- the content of the concomitant drug in the concomitant drug of the present invention varies depending on the form of the preparation, but is usually about 0.01 to 100% by weight, preferably about 0.1 to about 50% by weight, based on the whole preparation. %, More preferably about 0.5 to about 20% by weight.
- the content of additives such as carriers in the concomitant drug of the present invention varies depending on the form of the preparation, but is usually about 1 to about 99.99% by weight, preferably about 10 to 10% by weight, based on the whole preparation. It is about 90% by weight.
- the same content may be used when the compound of the present invention and the concomitant drug are separately formulated.
- preparations can be produced by a method known per se that is generally used in the preparation process.
- the compound of the present invention or the concomitant drug may be a dispersant (eg, Tween 80 (manufactured by Atlas Powder Co., USA), HC060 (manufactured by Nikko Chemicals), polyethylene) Glycol, carboxymethylcellulose, sodium alginate, hydroxypropylmethylcellulose, dextrin, etc., stabilizers (eg, ascorbic acid, sodium pyrosulfite, etc.), surfactants (eg, polysorbate 80, macrogol, etc.), possible Solvents (eg, glycerin, ethanol, etc.), buffers (eg, phosphoric acid and its alkali metal salts, citrate and its alkali metal salts, etc.), tonicity agents (eg, sodium chloride, potassium chloride, mannitol) Sorbitol, glucose, etc.), pH regulators (eg, hydrochloric acid, sodium hydroxide, etc.), preservatives (eg, ethoxych
- the compound of the present invention or the concomitant drug is used in accordance with a method known per se, for example, excipients (eg, lactose, sucrose, starch, etc.), disintegrants (eg, starch, calcium carbonate, etc.) , A binder (eg, starch, gum arabic, carboxymethylcellulose, polyvinylpyrrolidone, hydroxypropylcellulose, etc.) or a lubricant (eg, talc, magnesium stearate, polyethylene glycol 600, etc.)
- excipients eg, lactose, sucrose, starch, etc.
- disintegrants eg, starch, calcium carbonate, etc.
- a binder eg, starch, gum arabic, carboxymethylcellulose, polyvinylpyrrolidone, hydroxypropylcellulose, etc.
- a lubricant eg, talc, magnesium stearate, polyethylene glycol 600, etc.
- the coating agent examples include hydroxypropylmethylcellulose, ethylcellulose, hydroxymethylcellulose, hydroxypropylcellulose, polyoxyethylene glycol, tween 80, pull mouth nick F68, cellulose acetate phthalate, and hydroxypropylmethyl cellulose.
- tyl cellulose phthalate, hydroxymethyl cellulose acetate succinate, Eudragit (manufactured by Rohm, Germany, copolymerization of methacrylic acid / acrylic acid), and pigments (eg, bengara, titanium dioxide, etc.) are used.
- the preparation for oral administration may be either a quick release preparation or a sustained release preparation.
- a compound of the present invention or a concomitant drug may be prepared according to a method known per se.
- the product can be an oily or aqueous solid, semi-solid or liquid suppository.
- the oily base used in the composition include glycerides of higher fatty acids (eg, cocoa butter, witepsols (manufactured by Dynamite Nobel, Germany), etc.), intermediate fatty acids [eg, migliols (manufactured by Dynamite Nobel And vegetable oils (eg, sesame oil, soybean oil, cottonseed oil, etc.).
- the aqueous base include polyethylene glycols and propylene glycol
- examples of the aqueous gel base include natural gums, cellulose derivatives, bier polymers, and acrylic acid polymers.
- sustained-release preparation examples include sustained-release micro force capsules.
- a method known per se can be used to prepare a sustained release microcapsule.
- the compound of the present invention is preferably formed into a preparation for oral administration such as a solid preparation (eg, powder, granules, tablets, capsules) or a preparation for rectal administration such as a suppository.
- a preparation for oral administration such as a solid preparation (eg, powder, granules, tablets, capsules) or a preparation for rectal administration such as a suppository.
- preparations for oral administration are preferred.
- the concomitant drug can be in the above-mentioned dosage form depending on the type of the drug.
- An injection prepared by dissolving the compound of the present invention or the concomitant drug in water is preferable.
- the injection may contain benzoate and / or salicylate.
- the injection can be obtained by dissolving the compound of the present invention or the concomitant drug and, if desired, both benzoate or Z and salicylate in water.
- Examples of the salts of benzoic acid and salicylic acid include alkali metal salts such as sodium and potassium, alkaline earth metal salts such as calcium and magnesium, ammonium salts, medalmine salts, and organic acid salts such as trometamol. .
- the concentration of the compound of the present invention or the concomitant drug in the injection is about 0.5 to about 50 w / v%, preferably about 3 to about 20 wZV%.
- Also benzoate or and salic The concentration of the luate is preferably from about 0.5 to about 50 w / v%, preferably from about 3 to about 20 wZ v%.
- this agent contains additives commonly used for injections, such as stabilizers (ascorbic acid, sodium pyrosulfite, etc.), surfactants (polysorbate 80, macrogol, etc.), and solvents.
- stabilizers ascorbic acid, sodium pyrosulfite, etc.
- surfactants polysorbate 80, macrogol, etc.
- solvents such as buffers (phosphoric acid and its alkali metal salts, citric acid and its alkali metal salts, etc.), tonicity agents (sodium chloride, potassium chloride, etc.), dispersants (hydroxypropyl methylcellulose, dextrin, etc.) ), PH regulators (hydrochloric acid, sodium hydroxide, etc.), preservatives (ethyl ethyl parabenzoate, benzoic acid, etc.), solubilizers (concentrated glycerin, meglumine, etc.), solubilizers (propylene glycol, sucrose, etc.) And soothing
- the pH of the injection can be adjusted to 2 to 12, preferably 2.5 to 8.0 by adding a pH regulator.
- An injection is obtained by dissolving both the compound of the present invention or the concomitant drug and, if desired, a benzoate and / or a salicylate, and if necessary, the above-mentioned additives in water. These dissolutions may be performed in any order, and can be appropriately performed in the same manner as in the conventional method for producing an injection.
- the aqueous solution for injection is preferably heated, and can be used as an injection by performing, for example, filtration sterilization or high-pressure heat sterilization in the same manner as an ordinary injection.
- the aqueous solution for injection is preferably subjected to high-pressure heat sterilization at 100 ° C. to 121 ° C. for 5 minutes to 30 minutes.
- a formulation having antimicrobial properties of the solution may be used so that it can be used as a multiple-dose formulation.
- a sustained-release preparation comprising a core comprising the compound of the present invention or the concomitant drug optionally coated with a film-forming agent such as a water-insoluble substance-swellable polymer is preferred.
- a once-daily sustained release preparation for oral administration is preferred.
- water-insoluble substance used in the coating agent examples include ethyl cellulose and butyl cellulose.
- Cellulose ethers such as cellulose, cellulose esters such as cellulose acetate and cellulose propionate, polyvinyl esters such as polybier acetate and polypinyl butyrate, acrylic acid Z methacrylic acid copolymer, methyl methacrylate copolymer, X toki Shetyl methacrylate / cinnamethyl methacrylate Z-aminoalkyl methacrylate copolymer, polyacrylic acid, polymethacrylic acid, methacrylic acid alkylamide copolymer, poly (methyl methacrylate), poly methacrylate, polymethacrylamide, Aminoalkyl methacrylate copolymer, poly (methacrylic anhydride), glycidyl methacrylate copolymer, especially Eudragit RS-100, RL-100, RS-3OD, RL-3OD
- hardened oils such as hardened castor oil (eg, Secondary wax (Freund Corporation)), carnauba wax, fatty acids glycerin ester, waxes such as paraffin, polyglycerin fatty acid esters, and the like.
- swellable polymer a polymer having an acidic dissociating group and exhibiting pH-dependent swelling is preferable.Swelling is less in an acidic region such as in the stomach and swelling in a neutral region such as the small intestine and the large intestine. Polymers having an acidic dissociating group that grows are preferred.
- Examples of the polymer having such an acidic dissociating group and exhibiting pH-dependent swelling include, for example, carbomer 934P, 940, 941, 944, 980, 1342, and the like, such as polycarbophil 1 , Calcium polycarbophil (all of which are manufactured by BF Goodrich), and Hibis Pico 103, 104, 105, 304 (all of which are manufactured by Wako Pure Chemical Industries, Ltd.). Coalescence.
- the coating agent used in the sustained-release preparation may further contain a hydrophilic substance.
- hydrophilic substance examples include polysaccharides which may have a sulfate group, such as pullulan, dextrin, alkali metal alginate, hydroxypropylcellulose, hydroxypropylmethylcellulose, carboxymethylcellulose-snadium, and the like.
- the content of the water-insoluble substance in the coating agent of the sustained-release preparation is about 30 to about 90% (w / w), preferably about 35 to about 80% (w / w), more preferably about 4 0 to 75% (w / w), swellable polymer content of about 3 to about 30% (w / w), preferably about 3 to about 15% (w / w) .
- the coating may further comprise a hydrophilic substance, in which case the content of the hydrophilic substance in the coating is not more than about 50% (w / w), preferably about 5 to about 40% (w / w), more preferably from about 5 to about 35% (w / w).
- the above-mentioned% (w / w) refers to% by weight based on the coating composition obtained by removing the solvent (eg, water, lower alcohol such as methanol, ethanol, etc.) from the coating composition liquid.
- the sustained-release preparation is prepared by preparing a nucleus containing a drug as exemplified below, and then dissolving the obtained nucleus by heating or dissolving or dispersing a water-insoluble substance or a swellable polymer in a solvent. It is manufactured by coating with
- the form of the nucleus containing the drug to be coated with the coating agent (hereinafter sometimes simply referred to as the nucleus) is not particularly limited, but is preferably formed into particles such as granules or fine granules.
- the average particle size is preferably from about 150 to about 2,000 um, more preferably from about 500 to about 1,400 x m.
- the nucleus can be prepared by a usual production method.
- a drug is mixed with an appropriate excipient, binder, disintegrant, lubricant, stabilizer, and the like, and the mixture is prepared by wet extrusion granulation, fluidized bed granulation, or the like.
- the drug content of the core is about 0.5 to about 95% (w / w), preferably about 5 to about 80% (w / w), and more preferably about 30 to about 70% (w / w). w).
- excipients contained in the core include sugars such as sucrose, lactose, mannitol, glucose, starch, crystalline cellulose, calcium phosphate, corn starch and the like. Among them, crystalline cellulose and corn starch are preferred.
- binder examples include polyvinyl alcohol, hydroxypropylcellulose, polyethylene glycol, polyvinylpyrrolidone, pull nick F68, and Arabic Rubber, gelatin, starch and the like are used.
- Disintegrants include, for example, carboxymethylcellulose calcium (ECG505), croscarmethylene monosodium sodium (Ac-Di-Sol), cross-linked polyvinylpyrrolidone (crospovidone), low-substituted hydroxypropylcellulose (L-HPC) Are used. Among them, hydroxypropylcellulose, polyvinylpyrrolidone and low-substituted hydroxypropylcellulose are preferred.
- talc and magnesium stearate are used as a lubricant and an anti-agglomeration agent, and polyethylene glycol and the like are used as a lubricant.
- Acids such as tartaric acid, citric acid, succinic acid, fumaric acid and maleic acid are used as stabilizers.
- the nucleus may be formed by spraying a binder dissolved in a suitable solvent such as water, lower alcohol (eg, methanol, ethanol, etc.) onto the inert carrier particles serving as the center of the nucleus, in addition to the above-mentioned production method.
- a suitable solvent such as water, lower alcohol (eg, methanol, ethanol, etc.)
- It can be prepared by the tumbling granulation method, pan coating method, fluidized bed coating method or melt granulation method, in which a small amount of a drug or a mixture of an excipient and a lubricant is added. it can.
- the inert carrier particles for example, those made of sucrose, lactose, starch, crystalline cellulose, and waxes can be used, and the average particle size is about 100 111, or about 1,500 m. Is preferred.
- the surface of the nucleus may be coated with a protective agent.
- a protective agent for example, the above-mentioned hydrophilic substances, water-insoluble substances and the like are used.
- a polysaccharide having a polyethylene glycol-hydroxyalkyl group or a carboxyalkyl group is preferably used, and hydroxypropylmethyl cellulose and hydroxypropylcellulose are more preferably used.
- the protective agent may contain, as a stabilizer, an acid such as tartaric acid, citric acid, succinic acid, fumaric acid, and maleic acid, and a lubricant such as talc.
- its coating amount is about 1 to about 15% (w / w), preferably about 1 to about 10% (w / w), more preferably about 2 to about 8% based on the core. (w / w).
- the protective agent can be coated by a usual coating method.
- the protective agent can be coated by spray-coating the nucleus by, for example, a fluidized-bed coating method or a pan coating method. .
- a sustained-release preparation is produced by heating and dissolving a hydrophilic substance or coating with a coating agent solution in which a hydrophilic substance is dissolved or dispersed in a solvent.
- Examples of the method of coating the core with a coating agent solution include a spray coating method.
- composition ratio of the water-insoluble substance, the swellable polymer or the hydrophilic substance in the coating solution is appropriately selected so that the content of each component in the coating becomes the above-mentioned content.
- the coating amount of the coating agent is about 1 to about 90% (w / w), preferably about 5 to about 50% (w / w), based on the core (not including the protective agent). Preferably it is about 5 to 35% (w / w).
- the solvent for the coating agent solution water or an organic solvent can be used alone or in a mixture of both.
- the mixing ratio of water and organic solvent (water / organic solvent: weight ratio) when using the mixed solution can be changed in the range of 1 to 100%, and is preferably 1 to about 30%.
- the organic solvent is not particularly limited as long as it dissolves a water-insoluble substance. Examples thereof include lower alcohols such as methanol, ethanol, 2-propanol and 1-butanol, lower alkynones such as acetone, acetonitrile, and the like. Chloroform, dichloromethane and the like are used. Of these, lower alcohols are preferred, and ethanol and 2-propanol are particularly preferred.
- Water and a mixture of water and an organic solvent are preferably used as a solvent for the coating agent.
- an acid such as tartaric acid, citric acid, succinic acid, fumaric acid, or maleic acid may be added to the coating agent solution for stabilization.
- the operation for coating by spray coating can be performed by a usual coating method.
- the coating agent solution is spray-coated on the nucleus by, for example, a fluidized bed coating method or anadoo coating method. It can be implemented at At this time, if necessary, talc, titanium oxide, magnesium stearate, calcium stearate, light gay anhydride, etc. are used as lubricants, and glycerin fatty acid ester, hydrogenated castor oil, triethyl quenate, cetyl alcohol, stearyl alcohol are used. May be added as a plasticizer.
- an antistatic agent such as talc may be mixed as necessary.
- Immediate release preparations can be liquid (solutions, suspensions, emulsions, etc.) or solid (particles, Pills, tablets, etc.).
- Parenteral preparations such as oral preparations and injections are used, but oral preparations are preferred.
- Immediate release preparations may generally contain, in addition to the drug as an active ingredient, carriers, additives and excipients (hereinafter sometimes abbreviated as excipients) commonly used in the pharmaceutical field.
- excipients commonly used in the pharmaceutical field.
- the formulation excipient used is not particularly limited as long as it is a commonly used excipient.
- excipients for oral solid preparations include lactose, starch, corn starch, crystalline cellulose (such as Avicel PH101, manufactured by Asahi Kasei Corporation), powdered sugar, granulated sugar, mannitol, light caffeic anhydride, magnesium carbonate, carbonate Calcium, L-cysteine and the like, preferably corn starch and mannitol.
- excipients can be used alone or in combination of two or more.
- the content of the excipient is, for example, about 4.5 to about 99.4 w / w%, preferably about 20 to about 98.5 w / w%, more preferably about 30 to It is about 97w / w%.
- the content of the drug in the immediate release preparation can be appropriately selected from the range of about 0.5 to about 95%, preferably about 1 to about 60%, based on the total amount of the immediate release preparation.
- the immediate release preparation When the immediate release preparation is an oral solid preparation, it usually contains a disintegrant in addition to the above components.
- disintegrants include carboxymethylcellulose calcium (manufactured by Gotoku Pharmaceutical Co., ECG-505), croscarmellose sodium (eg, Asahi Kasei Co., Ltd., AXIDISOL), crospovidone (eg, BASF Corporation, Kolydone CL) , Low-substituted hydroxypropylcells (Shin-Etsu Chemical Co., Ltd.), carboxymethyl starch (Matsuya Chemical Co., Ltd.), carboxymethyl starch sodium (Kimura Sangyo, X Kisprotab), part Pregelatinized starch (PCS, manufactured by Asahi Kasei Corporation) is used.
- PCS Pregelatinized starch
- Granules are formed by, for example, contacting with water to absorb water, swell, or create a channel between the active ingredient constituting the core and the excipient. Can be used. These disintegrants can be used alone or in combination of two or more. The blending amount of the disintegrant is appropriately selected depending on the kind and blending amount of the drug to be used, the design of the release preparation, and the like. Is from about 0.5 to about 15 w / w%.
- the immediate-release preparation is an oral solid preparation, or if it is an oral solid preparation, it is added to the above composition.
- the solid preparation may further contain an additive for placement.
- additives include binders (for example, sucrose, gelatin, gum arabic, methylcellulose, hydroxypropylcellulose, hydroxypropylmethylcellulose, carboxymethylcellulose, polyvinylpyrrolidone, pullulan, dextrin, etc.) Sourcing agents (eg, polyethylene glycol, magnesium stearate, talc, light gay anhydride (eg, AEROSIL (Nippon AEROSIL)), surfactants (eg, anionic surfactants such as sodium alkyl sulfate, polyoxyethylene fatty acid esters) And non-ionic surfactants such as polyoxyethylene sorbitan fatty acid ester, polyoxyethylene castor oil derivative, etc.), coloring agents (for example, tar pigments, caramel, bengara, acid) Titanium,
- binders for example
- hydroxypropyl cellulose polyethylene glycol, polyvinyl pyrrolidone and the like are preferably used.
- the immediate-release preparation can be prepared by mixing the above-mentioned components, kneading and molding as necessary, based on a usual preparation production technique.
- the mixing is performed by a generally used method such as mixing and kneading.
- a rapid-release preparation is formed into particles, a vertical granulator, a universal kneading machine (Hata Tekko And fluidized-bed granulator FD-5S (manufactured by Palek Co., Ltd.), followed by granulation by wet extrusion granulation, fluidized bed granulation, or the like.
- the immediate-release preparation and the sustained-release preparation thus obtained can be administered as they are, or separately, separately and in combination with excipients, etc., according to a conventional method, and then administered simultaneously or in combination at an arbitrary administration interval.
- both preparations may be formulated as a single orally administered preparation (eg, granules, fine granules, tablets, capsules, etc.) as they are or as appropriate, together with excipients.
- Both preparations may be made into granules or fine granules and filled in the same capsule or the like to prepare a preparation for oral administration.
- Sublingual tablet, puccal or oral fast disintegrating agent and its preparation The sublingual tablet, the puccal preparation, and the quick disintegrating agent in the oral cavity may be a solid preparation such as a tablet or an oral mucosa patch (film).
- a preparation containing the compound of the present invention or the concomitant drug and an excipient is preferable.
- auxiliary agents such as a lubricant, a tonicity agent, a hydrophilic carrier, a water-dispersible polymer, and a stabilizer may be contained. Further, it may contain a / 3-cyclodextrin or
- 3-cyclodextrin derivative eg, hydroxypropyl-13-cyclodextrin
- excipients examples include lactose, sucrose, D-mannitol, starch, crystalline cellulose, light caffeic anhydride and the like.
- examples of the lubricant include magnesium stearate, calcium stearate, talc, colloidal silica, and the like, and magnesium stearate-colloidal silica is particularly preferable.
- examples of the tonicity agent include sodium chloride, glucose, fructose, mannitol, sorbitol, lactose, saccharose, glycerin, urea and the like, with mannitol being particularly preferred.
- hydrophilic carrier examples include swellable hydrophilic carriers such as crystalline cellulose, ethyl cellulose, cross-linkable polybierpyrrolidone, light caffeic anhydride, citric acid, dicalcium phosphate, and calcium carbonate. Microcrystal cell openings) are preferred.
- Water-dispersible polymers include gums (eg, tragacanth, acacia, guar gum), alginates (eg, sodium alginate), cellulose derivatives (eg, methylcellulose, carboxymethylcellulose, hydroxymethylcellulose, hydroxypropylcellulose) , Hydroxypropyl methylcellulose), gelatin, water-soluble starch, polyacrylic acid (eg, carpomer), polymethacrylic acid, polyvinyl alcohol, polyethylene glycol, polyvinylpyrrolidone, polycarpyl, ascorbic acid palmitate, and the like. Propyl methylcellulose, polyacrylic acid, alginate, gelatin, carboxymethyl cellulose, polypierpyrrolidone, polyethylene Glycol is preferred.
- gums eg, tragacanth, acacia, guar gum
- alginates eg, sodium alginate
- cellulose derivatives eg, methylcellulose, carboxymethylcellulose, hydroxymethylcellulose, hydroxypropyl
- hydroxypropyl methylcellulose is preferable.
- the stabilizer include cystine, thiosorbitol, tartaric acid, cunic acid, sodium carbonate, ascorbic acid, glycine, sodium sulfite, and the like. Good.
- the sublingual disintegrant, buccal or intraoral quick disintegrating agent can be produced by mixing the compound of the present invention or the concomitant drug with an excipient by a method known per se. Further, if necessary, the above-mentioned auxiliary agents such as a lubricant, an isotonic agent, a hydrophilic carrier, a water-dispersible polymer, a stabilizer, a coloring agent, a sweetening agent and a preservative may be mixed. By mixing the above components at the same time or with a time difference, and then press-molding, sublingual tablets, buccal tablets or intraorally rapidly disintegrating tablets can be obtained. In order to obtain an appropriate hardness, it may be manufactured by humidifying and moisturizing with a solvent such as water or alcohol before and after the tableting process, if necessary, molding, and then drying.
- a solvent such as water or alcohol
- the compound of the present invention or the concomitant drug When molded into a mucosa-adhered tablet (film), the compound of the present invention or the concomitant drug, the above-mentioned water-dispersible polymer (preferably hydroxypropylcellulose, hydroxypropylmethylcellulose), an excipient, etc. Dissolve in a solvent and cast the resulting solution into a film. Further, additives such as a plasticizer, a stabilizer, an antioxidant, a preservative, a coloring agent, a buffer, and a sweetener may be added.
- Glycols such as polyethylene glycol and propylene glycol can be included to impart appropriate properties to the film, and bioadhesive polymers (eg, Polycarbophil, Carbofil, etc.) can be used to enhance the adhesion of the film to the oral mucosal lining. Paul) may be contained. Casting involves pouring the solution onto the non-adhesive surface, spreading it to a uniform thickness (preferably about 100 to 100 microns) with an application tool such as a doctor blade, and then drying the solution. This is achieved by forming a film. The film thus formed may be dried at room temperature or under heating, and cut into a desired surface area.
- bioadhesive polymers eg, Polycarbophil, Carbofil, etc.
- Paul may be contained. Casting involves pouring the solution onto the non-adhesive surface, spreading it to a uniform thickness (preferably about 100 to 100 microns) with an application tool such as a doctor blade, and then drying the solution. This is achieved
- a preferred rapid intraoral disintegrant is a solid rapid diffusion administration comprising a network of the compound of the present invention or the concomitant drug and a water-soluble or water-diffusible carrier inactive with the compound of the present invention or the concomitant drug.
- Agents. The network can be obtained by sublimating the solvent from the solid composition composed of a solution of the compound of the present invention or the concomitant drug in a suitable solvent. .
- composition of the oral disintegrating agent preferably contains a matrix-forming agent and a secondary component in addition to the compound of the present invention or the concomitant drug.
- the matrix forming agent examples include gelatins, dextrins, soybeans, and wheat. And animal or plant proteins such as psyl 1 ium seed protein; gums such as gum arabic, guar gum, agar and xanthan; polysaccharides; alginic acids; carboxymethylcellulose; Dextrans; pectins; synthetic polymers such as polyvinylpyrrolidone; and substances derived from gelatin-gum arabic complex.
- animal or plant proteins such as psyl 1 ium seed protein; gums such as gum arabic, guar gum, agar and xanthan; polysaccharides; alginic acids; carboxymethylcellulose; Dextrans; pectins; synthetic polymers such as polyvinylpyrrolidone; and substances derived from gelatin-gum arabic complex.
- saccharides such as mannitol, dextrose, lactose, galactose and trehalose; cyclic saccharides such as cyclodextrin; inorganic salts such as sodium phosphate, sodium chloride and aluminum silicate; glycine, L-alanine, L-aspartic acid, Includes amino acids with 2 to 12 carbon atoms such as L-glutamic acid, L-hydroxyproline, L-isoleucine, L-leucine, and L-phenylalanine. '
- One or more matrix-forming agents can be introduced into a solution or suspension before solidification.
- a matrix forming agent may be present in addition to the surfactant, or may be present without the surfactant.
- the matrix former in addition to forming its matrix, can help maintain the compound or compound of the invention or the concomitant drug in a dispersed state in the solution or suspension.
- Suitable colorants include red, black and yellow iron oxides and FD & C dyes such as FD & C Blue No. 2 and FD & C Red 40 from Ellis' Anderbergerd.
- Suitable flavors include mint, raspberry, licorice, orange, lemon, grapefruit, caramel, vanilla, cherry and grape flavor and combinations thereof.
- Suitable pH regulators include citric acid, tartaric acid, phosphoric acid, hydrochloric acid and maleic acid.
- Suitable sweeteners include aspartame, acesulfame K and thaumatin.
- Suitable taste masking agents include sodium bicarbonate, ion exchange resins, cyclodextrin inclusion compounds, adsorbate materials, and microencapsulated apomorphine.
- Formulations usually contain about 0.1 to about 50% by weight, preferably about 0.1 to about 30% by weight of book. Comprising between about 1 minute and about 60 minutes, preferably between about 1 minute and about 15 minutes, more preferably between about 2 minutes and about 5 minutes (in water) comprising the compound of the invention or the concomitant drug.
- Formulations capable of dissolving 90% or more of the compound of the present invention or the concomitant drug (the above-mentioned sublingual tablets, puccal, etc.), and preferably within about 1 to about 60 seconds after being placed in the oral cavity Is preferably a fast disintegrating agent in the oral cavity that disintegrates within about 1 to about 30 seconds, more preferably within about 1 to about 10 seconds.
- the content of the above-mentioned excipient in the whole preparation is about 10 to about 99% by weight, preferably about 30 to about 90% by weight.
- the content of the 3-cyclodextrin or) 3-cyclodextrin derivative in the whole preparation is 0 to about 30% by weight.
- the content of the lubricant in the whole preparation is about 0.01 to about 10% by weight, preferably about 1 to about 5% by weight.
- the content of the tonicity agent in the whole preparation is about 0.1 to about 90% by weight, preferably about 10 to about 70% by weight.
- the content of the hydrophilic carrier in the whole preparation is about 0.1 to about 50% by weight, preferably about 10 to about 30% by weight.
- the content of the water-dispersible lima in the whole preparation is about 0.1 to about 30% by weight, preferably about 10 to about 25% by weight.
- the content of the stabilizer relative to the whole preparation is about 0.1 to about 10% by weight, preferably about 1 to about 5% by weight.
- the above preparations may further contain additives such as coloring agents, sweetening agents, preservatives and the like, if necessary.
- the dose of the concomitant drug of the present invention varies depending on the type, age, body weight, symptom, dosage form, administration method, administration period, and the like of the compound of the present invention. Usually, about 0.01 to about 1000 mgZkg, preferably about 0.01 to about 100 mgZkg per day, as the compound of the present invention and the concomitant drug, is more preferable. 1 to about 10 Omg Zkg, especially about 0.1 to about 5 OmgZkg, especially about 1.5 to about 30 mgZkg, is administered intravenously once or several times a day. You. Of course, as described above, since the dose varies under various conditions, a dose smaller than the above dose may be sufficient, or it may be necessary to administer beyond the range.
- the concomitant drug can be used in any amount as long as side effects are not a problem.
- the daily dosage of the concomitant drug varies depending on the severity of symptoms, age, gender, body weight, sensitivity difference, administration timing, interval, characteristics of pharmaceutical preparation, preparation, type, type of active ingredient, etc.
- the amount of the drug is usually The dose is about 0.001 to 2000 mg, preferably about 0.01 to 500 mg, more preferably about 0.1 to 10 Omg per kg body weight of the mammal, and is usually administered in 1 to 4 times a day.
- the concomitant drug may be administered at the same time, but after administering the concomitant drug first, the compound of the present invention may be administered, or the compound of the present invention may be administered first. Thereafter, the concomitant drug may be administered.
- the time difference depends on the active ingredient to be administered, dosage form, and administration method.For example, when the concomitant drug is administered first, within 1 minute to 3 days after administration of the concomitant drug, preferably Examples include a method of administering the compound of the present invention within 10 minutes to 1 day, more preferably within 15 minutes to 1 hour.
- the concomitant drug is administered within 1 minute to 1 day, preferably within 10 minutes to 6 hours, more preferably within 15 minutes to 1 hour after administering the compound of the present invention.
- Method. BEST MODE FOR CARRYING OUT THE INVENTION
- the transformant Escherichia coli BL21ZPPDE4D3 obtained in Test Example 1 described below was deposited with the National Institute of Advanced Industrial Science and Technology (NI BH) on March 8, 2000 under the deposit number FERM BP. -Deposited with the Fermentation Research Institute (IFO) under the accession number IF 216 383 from February 24, 2000 as 7075.
- NI BH National Institute of Advanced Industrial Science and Technology
- IFO Fermentation Research Institute
- sequence numbers in the sequence listing in the present specification indicate the following sequences.
- Example 3 shows the amino acid sequence encoded by the nucleotide sequence of cDNA carried by Escherichia coli BL21 / pPDE4D3 obtained in Test Example 1.
- reaction mixture was poured into a saturated aqueous solution of ammonium chloride and extracted twice with ethyl acetate.
- the combined organic layer was washed with water and a saturated aqueous solution of sodium chloride, dried over magnesium sulfate, filtered, and concentrated under reduced pressure.
- Hexane / ethyl acetate (4: 1) mixture was added to the residue, the insolubles were filtered and concentrated under reduced pressure.
- the residue was subjected to silica gel column chromatography (hexane / ethyl acetate 100: 1 followed by 10: 1) to give the title compound (11.0 g, yield 94). .
- the reaction mixture was ice-cooled, water was added, neutralized with concentrated aqueous ammonia, and extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure. The residue was suspended in ethanol (30 mL), a 2 M aqueous sodium hydroxide solution (30 mL, 60 mmol) was added, and the mixture was heated under reflux for 1 hour. The insolubles were filtered, and the filtrate was concentrated under reduced pressure. The residue was dissolved in ethyl acetate, washed twice with water, and concentrated under reduced pressure.
- Orchid ol was added, and the mixture was stirred at room temperature for 10 minutes and at 80 for 4 hours.
- the reaction mixture was poured into a saturated aqueous solution of ammonium chloride and extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure.
- 6- (3-bromophenyl) -1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylfuro [3,2-f] isoquinoline (207 mg, 0.500 mmol), 4 ' -(4,4,5,5-tetramethyl-1, 3,2-dioxaborolan-2-yl) acetanilide (144mg, 0.551 bandol ol), sodium carbonate Thorium (133 mg, 1.25 bandol) and tetrakis (triphenylphosphine) palladium (0) (12 mg, 0.010 mmol) in 1,2-dimethoxyethane (1.5 mL), ethanol (0.8 mL) and water (0.8 mL) mL) suspension was stirred at 85 under a nitrogen atmosphere for 16 hours.
- Trifluoromethanesulfonic acid 6- [4 '-(acetylamino) [1, ⁇ -biphenyl] -3-yl] -1,2,8,9-tetrahydrido-2,2,8,8-tetramethylfur [ 3, 2-f] isoquinoline-4-yl ester
- Trifluoromethanesulfonic acid 6- [4 '-(acetylamino) [1,1'-biphenyl] -3-yl] -1,2,8,9-tetrahydro-2,2,8,8-tetramethylphenyl Mouth [3,2-f] isoquinoline-4-yl ester (470 mg, 0.801 virgin ol), triethylamine (0.34 mL, 2.4 mmol), palladium (II) acetate (4.5 m.
- Omg and corn starch 35.0 fflg was granulated through a 1-mesh mesh sieve using 0.03 ml of 10% gelatin aqueous solution (3.0 mg as gelatin). Thereafter, it was dried at 40 ° C. and sieved again.
- the granules thus obtained were mixed with 2.0 mg of magnesium stearate and compressed.
- the obtained central tablets were coated with a sugar coating using an aqueous suspension of sucrose, titanium dioxide, talc and gum arabic.
- the coated tablets were glazed with beeswax to obtain coated tablets.
- Example 2 5.0 mg of the compound obtained in Example 1 and 20.0 mg of common salt were dissolved in distilled water, and water was added to make a total volume of 2.0 ml. Filter the solution into 2 ml ampules under aseptic conditions Filled. The ampoule was sterilized and sealed to obtain a solution for injection.
- a water-absorbing ointment having the above composition (100 g) was previously heated to 70 ° C, and a solution prepared by heating 1 g of the compound obtained in Example 1 in 20 ml of methanol was added to the solution. Was. The mixture was heated and mixed at the same temperature for 10 minutes to remove residual methanol, and cooled to room temperature to obtain a water-absorbing ointment.
- PCR was performed using MiniCycler TM (MJRESERCH) using Taq (Takara Shuzo) (reaction conditions: 0.5 min at 94 ° C, 0.5 min at 55T, 4 min at 72 ° C). 30 cycles).
- the PCR product was subjected to agarose gel electrophoresis, and a DNA fragment of about 2.4 kb was recovered. After blunting the fragment with Pfu DNA polymerase (STRATAGENE), Zero Blunt PCR Cloning
- the PDE 4D3 gene was cloned using Kit (Invitrogen).
- the plasmid obtained in the above (1) was digested with restriction enzyme EcoRI (Takara Shuzo), and then subjected to agarose gel electrophoresis to recover a DNA fragment of about 2.4 kb.
- the PNA fragment was digested with restriction enzyme EcoRI (Takara Shuzo) and ligated with pAPEX4T-3 (Pharmacia) treated with BAP (Takara Shuzo).
- the obtained cDNA fragment has the nucleotide sequence represented by SEQ ID NO: 3, and encodes the amino acid sequence represented by SEQ ID NO: 4 at the 74th to 2092th positions of the nucleotide sequence. I understood that it was.
- This cDNA fragment was transformed into Escherichia coli BL21 (Funakoshi) using a ligase solution to obtain Escherichia coli BL21ZPPDE4D3 expressing the PDE4D3 gene.
- the airway constriction response was measured by a modification of the Konzett-Rossler method.
- Hartley male guinea pigs weighing 400-500 g were intravenously administered with 1.0 ml of anti-OA serum diluted 8 to 16 times under ether anesthesia, and used for experiments 16 to 24 hours later.
- Anesthetize with urethane (1.2 g / kg, ip) (manufactured by Aldrich), inject tracheal force in the trachea, and in order to stop spontaneous breathing, garamine trietiodide (lmg / kg, iv) ( (Sigma).
- Example compound ling / kg was dissolved in 25% dimethylacetamide, 25% polyethylene glycol 400, and 50% physiological saline, and administered intravenously 5 minutes before antigen induction.
- the inhibition rate was calculated by comparing with the control group (intravenous administration of a mixture of 25% dimethylacetamide, 25% polyethylene glycol 400, and 50% saline).
- Table 3 shows the inhibition rates of the compounds of the present invention.
- the furoisoquinoline derivative of the present invention has an excellent PDE IV inhibitory action, and is used for inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, Alzheimer's disease, memory It is useful as a prophylactic and therapeutic agent for disorders, diabetes, arteriosclerosis, etc.
Landscapes
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Diabetes (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Pulmonology (AREA)
- Biomedical Technology (AREA)
- Pain & Pain Management (AREA)
- Psychiatry (AREA)
- Emergency Medicine (AREA)
- Heart & Thoracic Surgery (AREA)
- Immunology (AREA)
- Cardiology (AREA)
- Vascular Medicine (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Endocrinology (AREA)
- Rheumatology (AREA)
- Hospice & Palliative Care (AREA)
- Obesity (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
明細書 Specification
リン誘導体、 その製造法および用途 技術分野 Phosphorus derivatives, their production methods and applications
本発明は、 ホスホジエステラーゼ (PDE) IV阻害作用を有し、炎症性疾患、 喘息、 慢性閉塞性肺疾患、慢性関節リウマチ、 自己免疫疾患、 うつ病、 アルツハイマー型 痴呆症、 記憶障害、 糖尿病、 動脈硬化などの予防 ·治療剤として有用な新規フロイ ソキノリン誘導体、その製造法および用途に関する。 背景技術 The present invention has a phosphodiesterase (PDE) IV inhibitory effect, and has an inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, Alzheimer's dementia, memory impairment, diabetes, arteriosclerosis The present invention relates to novel freusoquinoline derivatives useful as preventive and therapeutic agents, their production methods and uses. Background art
今日、多くのホルモンや神経伝達物質は細胞内のセカンドメッセンジャーである シン- 3',5' -—リン酸 (cAMP) の細胞内濃度の上昇あるいは低 下させることにより、それらの細胞機能を調節している。この cAMP の細胞内濃度 は合成酵素および分解酵素により制御されている。すなわち cAMP はアデ二ルシク ラ一ゼにより産生され、 PDE により分解される。この分解酵素はサイクリックグァ ノシン - 3',5' -—リン酸 (cGMP) の分解をも制御している。 Today, many hormones and neurotransmitters regulate their cellular functions by increasing or decreasing the intracellular concentration of the intracellular second messenger syn-3 ', 5'-phosphate (cAMP). are doing. The intracellular concentration of cAMP is controlled by synthases and degradative enzymes. That is, cAMP is produced by adenyl cyclase and degraded by PDE. This degrading enzyme also controls the degradation of cyclic guanosine-3 ', 5'-phosphate (cGMP).
これまでに PDE は、 1 1種のアイソザィムの存在が明らかにされており [プロ シ一ディングス ォブ ザ ナショナル アカデミー ォブ サイェンシィズ ォブ ザ ユナイテッド ステイツ ォブ アメリカ(Proceedings of the Nat i onal Academy of Sc i ences of the Uni ted States of Amer i ca) > 97巻、 3702 頁 (2000) . ]、中枢、循環器、呼吸器、消化器、生殖器、血球、気管平滑筋などの各種の細 胞においてそれらが細胞内 cAMP、 cGMP の濃度を調節し、細胞機能を制御している。 そして好酸球、好中球、 単球、 T一リンパ球、 マクロファージなどの炎症細胞には PDEの 1つのアイソザィムである PDE IVが主に存在することが知られている [ク リニカル アンド ェクスペリメンタル アレルギー(Cl ini cal and Exper imental Al lergy) , 22巻, 337頁 (1992) . ]。 To date, the PDE has identified 11 isozymes, [Proceedings of the National Academy of Sciences of the National Academy of Sciences of the United States. 97, p. 3702 (2000).], in various cells such as the central, circulatory, respiratory, digestive, genital, blood cells, and tracheal smooth muscle. Regulates intracellular cAMP and cGMP levels and regulates cell functions. It is known that inflammatory cells such as eosinophils, neutrophils, monocytes, T-lymphocytes, and macrophages mainly contain PDE IV, one of the isozymes of PDE. Perimental allergy (Clinical and Experimental Allergy), 22, 337 (1992).].
喘息の治療薬として主に 3種類に大別される薬物が用いられている。すなわち、 気管支拡張薬 (例えば、 β -ァドレナリン受容体作動薬)、抗炎症薬 (例えば、コルチコ ステロイド)、および気管支拡張作用と抗炎症作用を併有するキサンチン誘導体 (例 えば、テオフィリン)の 3種類である。なかでもテオフィリンは古くから喘息の治療 薬として広く用いられている。そして、 テオフィリンの気管支拡張作用が PDE阻害 作用に基づくことが明らかになり、最近注目を集めている。しかしながら、テオフィ リンは非選択的 PDE 阻害剤であり、心血管系への副作用がしばしば観察され血中 濃度を厳格にコントロールする必要がある。したがって喘息等の炎症性疾患の治療 薬には PDE IV のみを選択的に阻害して、 PDE のその他のアイソザィムには作用し ない薬物が望まれている。 As a treatment for asthma, three main types of drugs are used. That is, bronchodilators (e.g., beta-adrenergic receptor agonists), anti-inflammatory drugs (e.g., corticosteroids), and xanthine derivatives having both bronchodilator and anti-inflammatory effects (e.g., For example, theophylline). In particular, theophylline has been widely used as a therapeutic agent for asthma since ancient times. It has been shown that theophylline's bronchodilator activity is based on PDE inhibitory activity, and has recently attracted attention. However, theophylline is a non-selective PDE inhibitor, and cardiovascular side effects are often observed and require strict control of blood levels. Therefore, there is a demand for a therapeutic drug for inflammatory diseases such as asthma that selectively inhibits only PDE IV and does not act on other PDE isozymes.
PDE IV選択的阻害剤が有効な喘息等の炎症性疾患の治療薬となり得る可能性を 示した研究結果が報告されている [プルモナリー ファーマコロジー (Pulmonary Pharmaco logy) , 7巻, 1頁 (1994) · ]。 PDE IV選択的阻害作用を有する化合物と して、 式 Studies have shown that PDE IV selective inhibitors may be effective therapeutic agents for inflammatory diseases such as asthma [Pulmonary Pharmacology, 7, 1 (1994) ·]. As a compound having a PDE IV selective inhibitory action,
で示されるロリプラム(特開昭 5 0 - 1 5 7 3 6 0号公報)や式 Rolipram (JP-A 50-157 7 360) and formulas represented by
で示される S B 2 0 7 4 9 9 [ザ ジャーナル ォブ ファ一マコロジ一 アン ド ェクスペリメンタ レ セラピューティック (The Journal o f Pharmacology and Exper imental Therapeut i cs) , 287卷, 988頁(1998) ·, ジャーナル ォブ メディ シナル ケミストリ一 (Journal of Medic inal Chemi s try) , 41卷, 821頁(1998) . ] が知られている。 しかしながら、現在までに臨床上適用されるまでには至っていな レ^ SB 2 0 7 4 9 9 [The Journal of Pharmacology and Experimental Therapeutics], 287, 988 (1998) ·, Journal Journal of Medicinal Chemistry, vol. 41, p. 821 (1998).] Is known. However, it has not been applied clinically to date.
また、 W001/70746には、 PDE IV選択的阻害作用を有する化合物として、 式 で表される部分構造を有する化合物が開示されている。 In addition, W001 / 70746 includes, as a compound having a PDE IV selective inhibitory action, The compound which has the partial structure represented by these is disclosed.
一方、 ブレタン デ ラ ソサイエテ キミク デ フランス(Bulletin De La Societe Chimique De France) 4201 (1972) には、 式 On the other hand, Bulletin De La Societe Chimique De France 4201 (1972)
〔——は単結合または二重結合を示す〕 で表される化合物の合成法が開示されて いる。 [— Represents a single bond or a double bond].
また、 W002/04455 には、 ノルェピネフリントランスポーター蛋白質の再取り込 み阻害作用に基づいた神経 ·心神欠陥症の治療剤として式 In addition, W002 / 04455 includes a formula as a therapeutic agent for neurological and psychiatric deficiencies based on the reuptake inhibitory effect of the norepinephrine transporter protein.
〔式中、 R1は — 6アルキル、 C2_6アルケニル、 C2_6アルキニル、 C3 6シク 口アルキル、 C4_7シクロアルキルアルキルまたはべンジル (これらは特定の置換 基を有していてもよい) 、 Wherein, R 1 is - 6 have alkyl, C 2 _ 6 alkenyl, C 2 _ 6 alkynyl, C 3 6 consequent opening alkyl, a C 4 _ 7 cycloalkylalkyl or base Njiru (These particular substituent May be)
R 2は水素原子、 アルキル、 C 2 6アルケニル、 C2_6アルキニル、 C。 6シ クロアルキル、 C 4 7シクロアルキルアルキルまたは C^ 6八口アルキル、 R 2 is a hydrogen atom, alkyl, C 26 alkenyl, C 2 _ 6 alkynyl, C. 6 A cycloalkyl, C 4 7 cycloalkylalkyl or C ^ 6 eight-necked alkyl,
R 3は水素原子、 ハロゲン原子、 アルキル、 ハロアルキルまたは C 3_6 シクロアルキル (該 C i 6アルキル、 (: 6ハロアルキル、 C 3 6シクロアルキル は特定の置換基を有していてもよい) 、 R 3 is a hydrogen atom, a halogen atom, alkyl, haloalkyl or C 3 _ 6 cycloalkyl (said C i 6 alkyl, (6 haloalkyl, C 3 6 cycloalkyl may have a specific substituent),
R 4、 R 5および R 6はそれぞれ独立して水素原子、 ハロゲン原子、 ニトロ等を、 R 7は水素原子、 ハロゲン原子等を示す〕 R 4 , R 5 and R 6 each independently represent a hydrogen atom, a halogen atom, nitro, etc., and R 7 represents a hydrogen atom, a halogen atom, etc.)
で表される化合物が開示されている。 Are disclosed.
強い選択的 PDE IV阻害剤は炎症を伴う広範囲な疾患に対して充分な予防あるい は治療効果が期待できる。 本発明は PDE IV選択的阻害作用を有し、細胞内の cAMP 濃度を上昇させることにより、気管支拡張作用および抗炎症作用を示し、さらに安 全性面などの点で優れた新規複素環化合物を提供することにある。 発明の開示 Strong selective PDE IV inhibitors can be expected to be fully effective in preventing or treating a wide range of diseases involving inflammation. The present invention provides a novel heterocyclic compound having a selective inhibitory effect on PDE IV, a bronchodilator effect and an anti-inflammatory effect by increasing the intracellular cAMP concentration, and further having excellent safety and other aspects. To provide. Disclosure of the invention
本発明者らは、種々鋭意研究を行った結果、 式 The present inventors have conducted various studies and found that the formula
〔式中、 A環、 B環および C環はそれぞれ置換基を有していてもよい〕で表わされ る部分構造を有する新規なフロイソキノリン化合物 (以下、 化合物(I ) と略記す る場合がある) 、 特に、 フロイソキノリン骨格の 1位、 2位、 4位、 5位、 6位、 7位、 8位、 9位などに置換基を導入したところに化学構造上の大きな特徴を持つ、 式 [Wherein, ring A, ring B and ring C may each have a substituent.] A novel furoisoquinoline compound having a partial structure represented by the following formula (hereinafter abbreviated as compound (I) ) In particular, it has a great chemical structural characteristic when a substituent is introduced at the 1st, 2nd, 4th, 5th, 6th, 7th, 8th, 9th, etc. positions of the furoisoquinoline skeleton , Expression
〔式中、 R1は水素原子、 置換基を有していてもよい炭化水素基または置換基を有 していてもよい複素環基を、 R 2および R 3はそれぞれ水素原子、 置換基を有して いてもよい炭ィ匕水素基またはァシル基を示し、 R 2と R 3は隣接する炭素原子と共 に置換基を有していてもよい 3ないし 8員環を形成してもよく、 R4および R5は それぞれ水素原子または置換基を有していてもよい炭化水素基を、 R6および R7 はそれぞれ水素原子または置換基を有していてもよい炭化水素基を示し、 1¾6と1^ 7は隣接する炭素原子と共に置換基を有していてもよい 3ないし 8員環を形成して もよく、 R8は(1)水素原子、 (2)置換基を有レていてもよい炭化水素基、 (3) ァシル基、 (4)置換基を有していてもよい複素環基、 (5)ハロゲン原子、 (6) -OR10 (R1Qは水素原子、 置換基を有していてもよい炭化水素基、 ァシル基ま たは置換基を有していてもよい複素環基を示す) 、 (7) -SR11 (R11は水素 原子、置換基を有していてもよい炭化水素基、 ァシル基または置換基を有していて もよい複素環基を示す) 、 (8) -S (0) R12 (R12は置換基を有していても よい炭化水素基または置換基を有していてもよい複素環基を示す)、 (9)一 S(O) 2R13 (R 13は置換基を有していてもよい炭化水素基または置換基を有していても よい複素環基を示す) または (10) — NR14R15 (R14および R15はそれぞれ 水素原子、置換基を有していてもよい炭化水素基、 ァシル基または置換基を有して いてもよい複素環基を示す) を、 R9は水素原子、 シァノ基、 置換基を有していて もよい炭化水素基、ァシル基または置換基を有していてもよい水酸基を、 Xは置換 基を有していてもよいメチレン基または力ルポニル基を、 nは 0または 1を示す〕 で表される新規なフロイソキノリン化合物 (以下、 化合物 ( ) と略記する場合 がある)もしくはその塩またはそのプロドラッグあるいはそれらの水和物を初めて 合成することに成功し、 これらの化合物がその特異な化学構造に基づいて、予想外 にも優れた PDE阻害作用、 特に PDE IV阻害作用を有し、炎症性疾患、 喘息、 慢性 閉塞性肺疾患、 慢性関節リウマチ、 自己免疫疾患、 うつ病、 アルツハイマー型痴呆 症、 記憶障害、 糖尿病、 動脈硬化などの予防、 治療剤等の医薬として用いられるこ とを見出した。 本発明者らは、 これらの知見に基づき、 さらに検討を重ねた結果、 本発明を完成するに至った。 [In the formula, R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent, and R 2 and R 3 each represent a hydrogen atom or a substituent. R 2 and R 3 may have a substituent together with adjacent carbon atoms to form a 3- to 8-membered ring. R 4 and R 5 each represent a hydrogen atom or a hydrocarbon group which may have a substituent; R 6 and R 7 each represent a hydrogen atom or a hydrocarbon group which may have a substituent; 1¾ 6 and 1 ^ 7 may form a 8-membered ring to 3 which may have a substituent together with the adjacent carbon atoms, R 8 is (1) a hydrogen atom, Yure (2) substituent hydrocarbon group which may be substituted, (3) Ashiru group, (4) an optionally substituted heterocyclic group, (5) halogen atom, (6) -OR 10 (R 1Q is a hydrogen atom Substituent has optionally may hydrocarbon group, was Ashiru group or indicates a heterocyclic group which may have a substituent), (7) -SR 11 ( R 11 is a hydrogen atom, a substituent A hydrocarbon group, an acyl group or an optionally substituted heterocyclic group), (8) -S (0) R 12 (where R 12 has a substituent A hydrocarbon group or a heterocyclic group which may have a substituent), (9) one S (O) 2 R 13 (R 13 is a hydrocarbon group which may have a substituent or (Shows an optionally substituted heterocyclic group) or (10) — NR 14 R 15 (R 14 and R 15 are each a hydrogen atom, an optionally substituted hydrocarbon group, an acyl group Or R 9 represents a hydrogen atom, a cyano group, a hydrocarbon group optionally having a substituent, an acyl group or a substituent. Moyo A hydroxyl group, X represents a methylene group or an oleponyl group which may have a substituent, and n represents 0 or 1.] A novel furisoquinoline compound represented by the following formula (hereinafter sometimes referred to as compound (): A) or its salt or its prodrug or its hydrate for the first time Synthesized successfully, these compounds have unexpectedly excellent PDE inhibitory activity, especially PDE IV inhibitory activity, based on their unique chemical structure, and have inflammatory disease, asthma, chronic obstructive pulmonary disease It has been found that it can be used as a drug for the prevention and treatment of rheumatoid arthritis, autoimmune diseases, depression, Alzheimer's dementia, memory impairment, diabetes, arteriosclerosis and the like. The present inventors have further studied based on these findings, and as a result, completed the present invention.
すなわち、 本発明は、 That is, the present invention
〔1〕 式 〔1 set
で表される部分構造を有する化合物 (以下、 化合物 (A) と略記する場合がある) またはその塩; A compound having a partial structure represented by (hereinafter sometimes abbreviated as compound (A)) or a salt thereof;
〔2〕 式 (2) Expression
〔式中、 R 1は水素原子、 置換基を有していてもよい炭化水素基または置換基を有 していてもよい複素環基を示す〕 で表される部分構造を有する化合物またはその 塩; [Wherein, R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent] or a salt thereof. ;
〔3〕 式 ( ) (3) Expression ()
〔式中、 R1は水素原子、 置換基を有していてもよい炭化水素基または置換基を有 していてもよい複素環基を、 R2および R3はそれぞれ水素原子、 置換基を有して いてもよい炭化水素基またはァシル基を示し、 R 2と R 3は隣接する炭素原子と共 に置換基を有していてもよい 3ないし 8員環を形成してもよく、 R4および R5は それぞれ水素原子または置換基を有していてもよい炭化水素基を、 R6および R7 はそれぞれ水素原子または置換基を有していてもよい炭化水素基を示し、 R6と R 7は隣接する炭素原子と共に置換基を有していてもよい 3ないし 8員環を形成して もよく、 R8は(1)水素原子、 (2)置換基を有していてもよい炭化水素基、 (3) ァシル基、 (4)置換基を有していてもよい複素環基、 (5)ハロゲン原子、 (6) -OR10 (R1Qは水素原子、 置換基を有していてもよい炭化水素基、 ァシル基ま たは置換基を有していてもよい複素環基を示す) 、 (7) -SR11 (R11は水素 原子、置換基を有していてもよい炭化水素基、 ァシル基または置換基を有していて もよい複素環基を示す) 、 (8) — S (O) R12 (R 12は置換基を有していても よい炭化水素基または置換基を有していてもよい複素環基を示す)、 O)-S(O) 2R13 (R13は置換基を有していてもよい炭ィヒ水素基または置換基を有していても よい複素環基を示す) または (10) — NR14R15 (R 14および R 15はそれぞれ 水素原子、置換基を有していてもよい炭化水素基、 ァシル基または置換基を有して いてもよい複素環基を示す) を、 R9は水素原子、 シァノ基、 置換基を有していて もよい炭化水素基、 ァシル基または置換基を有していてもよい水酸基を、 Xは置換 基を有していてもよいメチレン基または力ルポニル基を、 nは 0または 1を示す〕 で表される化合物またはその塩; [In the formula, R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent, and R 2 and R 3 each represent a hydrogen atom or a substituent. Represents a hydrocarbon group or an acyl group which may be possessed; R 2 and R 3 may form a 3- to 8-membered ring which may have a substituent together with an adjacent carbon atom; 4 and R 5 hydrocarbon group which may have a each represent a hydrogen atom or a substituent, R 6 and R 7 each represent a hydrogen atom or an optionally substituted hydrocarbon group, R 6 And R 7 may form a 3- to 8-membered ring which may have a substituent together with an adjacent carbon atom, and R 8 is (1) a hydrogen atom, or (2) A good hydrocarbon group, (3) an acyl group, (4) an optionally substituted heterocyclic group, (5) a halogen atom, (6) -OR 10 (R 1Q is a hydrogen atom, A hydrocarbon group which may have a substituent, an acyl group or a heterocyclic group which may have a substituent), (7) -SR 11 (R 11 is a hydrogen atom or a substituent A hydrocarbon group, an acyl group, or an optionally substituted heterocyclic group), (8) — S (O) R 12 (where R 12 has a substituent A hydrocarbon group or a heterocyclic group optionally having substituent (s)), O) -S (O) 2 R 13 (R 13 is a hydrocarbon group optionally having substituent (s)) Or a heterocyclic group which may have a substituent) or (10) — NR 14 R 15 (R 14 and R 15 are each a hydrogen atom, a hydrocarbon group which may have a substituent, R 9 represents a hydrogen atom, a cyano group, a hydrocarbon group which may have a substituent, an acyl group or a substituent. May A hydroxyl group, X represents a methylene group or a carbonyl group which may have a substituent, and n represents 0 or 1.] or a salt thereof;
〔4〕 R1が以下の (i) または (ii) のいずれかを示す: ( i) (1) ハロゲン原子、 (2) アルキレンジォキシ基、 (3) ニトロ基、[4] R 1 represents any of the following (i) or (ii): (i) (1) halogen atom, (2) alkylenedioxy group, (3) nitro group,
(4) シァノ基、 (5) ハロゲン化されていてもよい — 6アルキル基、 (6) ハロ ゲン化されていてもよい C2_6アルケニル基、 (7) ハロゲン化されていてもよい C2_6アルキニル基、 (8) C3_6シクロアルキル基、 (9) C6— 14ァリール基、 (10) ハロゲン化されていてもよい C^— 6アルコキシ基、 (11) ハロゲン化されていても よい アルキルチオ基、 (12) ヒドロキシ基、 (13) アミノ基、 (14) モノ—(4) cyano group, (5) optionally halogenated — 6 alkyl group, (6) optionally halogenated C 2 _ 6 alkenyl group, (7) optionally halogenated C 2 _ 6 alkynyl group, (8) C 3 _ 6 cycloalkyl group, (9) C 6 - 14 Ariru group, (10) optionally halogenated C ^ - 6 alkoxy group, a (11) halogenated Alkylthio group, (12) hydroxy group, (13) amino group, (14) mono-
6アルキルアミノ基、 (15) モノー C6— 14ァリールアミノ基、 (16) 6- alkylamino group, (15) MONO C 6 — 14 arylamino group, (16)
_6アルキルアミノ基、 (17) ジ— C6— 14ァリールアミノ基、 (18) ホルミル、 力 ルポキシ、 力ルバモイル、 アルキル一力ルポニル、 C3— 6シクロアルキル一 力ルポニル、 アルコキシ—力ルポニル、 C 6^ 4ァリール一力ルポニル、 c7 ― 16ァラルキル一力ルポニル、 c6_14ァリールォキシ一力ルポニル、 c7_16ァラ ルキルォキシ—力ルポニル、炭素原子以外に窒素原子、硫黄原子および酸素原子か ら選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環カルボニル、 モノ _C アルキル一力ルバモイル、 ジーじ アルキル一力ルバモイル、 C6_ 14ァリール一力ルバモイル、 炭素原子以外に窒素原子、 硫黄原子および酸素原子 から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環カルバモ ィル、 C — 6アルキル—チォカルボニル、 C 3— 6シクロアルキル一チォカルポニル、_ 6 alkylamino group, (17) di - C 6 - 14 Ariruamino group, (18) formyl, force Rupokishi force Rubamoiru, alkyl Ichiriki Ruponiru, C 3 - 6 cycloalkyl Ichiriki Ruponiru, alkoxy - force Ruponiru, C 6 ^ 4 Ariru Ichiriki Ruponiru, c 7 - 16 Ararukiru Ichiriki Ruponiru, c 6 _ 14 Ariruokishi Ichiriki Ruponiru, c 7 _ 16 § La Rukiruokishi - force Ruponiru, nitrogen atom in addition to carbon atoms, or a sulfur atom and an oxygen atom et 1 to 5 or 6-membered heterocyclic carbonyl containing heteroatoms three of the selected, mono _C alkyl Ichiriki Rubamoiru, di Ji alkyl Ichiriki Rubamoiru, C 6 _ 14 Ariru Ichiriki Rubamoiru, nitrogen in addition to carbon atoms 5- or 6-membered heterocyclic carbamoyl containing 1 to 3 heteroatoms selected from atoms, sulfur atoms and oxygen atoms, C- 6 alkyl-thiocal Boniru, C 3 - 6 cycloalkyl one Chiokaruponiru,
C ^6アルコキシ一チォカルポニル、 C6_14ァリール—チォカルポニル、 C7_16 ァラルキル一チォカルポニル、 C6— 14ァリールォキシ—チォ力ルポニル、 C7_16 ァラルキルォキシ一チォカルポニル、炭素原子以外に窒素原子、硫黄原子および酸 素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チ 才力ルポニル、 チォカルバモイル、 モノー (^_6アルキル一チォカルバモイル、 ジ 一 Ci— 6アルキル一チォカルバモイル、 C6_14ァリールーチォカルパモイル、炭素 原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテロ 原子を含有する 5または 6員複素環チォカルバモイル、スルファモイル、モノ— C 丄-6アルキルスルファモイル、 ジ— — 6アルキルスルファモイル、 C6一 14ァリ一 ルスルファモイル、 アルキルスルホニル、 C6— 14ァリールスルホニル、 C, _6アルキルスルフィニル、 C6_14ァリールスルフィエル、 スルフィノ、 スルホ、 C — 6アルコキシスルフィニル、 C6_14ァリ一ルォキシスルフィニル、 Cト 6アル コキシスルホニルおよび〇6_14ァリールォキシスルホニルから選ばれるァシル基、 (19)ホルミルァミノ、 アルキル一力ルポキサミド、 C6— 14ァリール—カル ポキサミド、 (^-6アルコキシ一力ルポキサミド、 Ci— 6アルキルスルホニルアミ ノおよび C 6— i 4ァリ一ルスルホニルァミノから選ばれるァシルァミノ基、 (20) (: 6アルキル—力ルポニルォキシ、 C6— 14ァリール一力ルポニルォキシ、 (:ト .6 ア^/コキシ一力ルポニルォキシ、 モノー c i _ 6アルキル—力ルバモイルォキシ、 ジ 一 C 6アルキル一力ルバモイルォキシ、 C 6— 1 4ァリ一ルー力ルバモイルォキシぉ よびニコチノィルォキシから選ばれるァシルォキシ基、 (21)炭素原子以外に窒素 原子、硫黄原子および酸素原子から選ばれる 1ないし 4個のへテロ原子を含有する 4ないし 14員複素環基、 (22) ホスホノ基、 (23) C 644ァリールォキシ基、 (24) ジ— Ci— 6アルコキシ一ホスホリル基、 (25) C6— 14ァリ一ルチオ基、 (26) ヒドラジノ基、 (27) イミノ基、 (28) ォキソ基、 (29) ウレイド基、 (30) Cx_ 6アルキル一ウレイド基、 (31) ジー( 6アルキルーゥレイド基、 (32) ォキシ ド基および (33) 前記 (1) 〜 (32) の基から選ばれる 2ないし 3個が結合してで きる基などからなる群(以下、 置換基 A群と略記する) から選ばれる置換基を 1な いし 5個それぞれ有していてもよい C _ 6アルキル基、 C 2— 6アルケニル基、 C2一 6アルキニル基、 C3_ 6シクロアルキル基、 C 3— 6シクロアルケニル基、 C6_14T リール基または C7_16ァラルキル基、 C ^ 6 alkoxy one Chiokaruponiru, C 6 _ 14 Ariru - Chiokaruponiru, C 7 _ 16 Ararukiru one Chiokaruponiru, C 6 - 14 Ariruokishi - Chio force Ruponiru, C 7 _ 16 Ararukiruokishi one Chiokaruponiru, nitrogen atom in addition to carbon atom, a sulfur atom and to 1 selected from oxygen radicals containing heteroatoms three of the 5 or 6-membered heterocyclic Ji Sairyoku Ruponiru, Chiokarubamoiru, mono- (^ _ 6 alkyl one Chiokarubamoiru, di one CI- 6 alkyl one Chio carbamoyl, C 6 _ 14 § reel over Chio Scarpa moil, nitrogen atom in addition to carbon atom, a sulfur atom and 1 to containing heteroatoms three of the 5 or 6-membered heterocyclic ring Chiokarubamoiru selected from oxygen atom, sulfamoyl, mono - C丄-6 alkylsulfamoyl, di - - 6 alkylsulfamoyl, C 6 one 14 § Li one Rusurufamo Le, alkylsulfonyl, C 6 - 14 § reel sulfonyl, C, _ 6 alkylsulfinyl, C 6 _ 14 § reel sulfide El, sulfino, sulfo, C - 6 alkoxysulfinyl sulfinyl, C 6 _ 14 § Li one Ruo carboxymethyl sulfinyl, C to 6 Al Kokishisuruhoniru and 〇 6 _ 14 Ashiru group selected from § reel O carboxymethyl sulfonyl, (19) Horumiruamino, alkyl Ichiriki Rupokisamido, C 6 - 14 Ariru - Cal Pokisamido, (^ -6 alkoxy Ichiriki Rupokisamido, CI- 6 alkylsulfonyl amino, and C 6 - i 4 § Li one Le sulfonyl Ashiruamino group selected from § amino, (20) (:. 6 alkyl - force Ruponiruokishi, C 6 - 14 Ariru Ichiriki Ruponiruokishi, (: City 6 a ^ / Kokishi Ichiriki Ruponiruokishi, mono- ci _ 6 alkyl - force Rubamoiruokishi, di one C 6 alkyl Ichiriki Rubamoiruokishi, C 6 - 1 4 § Li one Roux force Rubamoiruokishi per cent and Ashiruokishi group selected from nicotinyl Noi Ruo alkoxy, (21) 4 to 14 containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms Membered heterocyclic group, (22) phosphono group, (23) C 64 4 Ariruokishi group, (24) di - CI- 6 alkoxy one phosphoryl group, (25) C 6 - 14 § Li one thio group, (26) hydrazino group, (27) imino group, (28) Okiso group, (29) an ureido group, (30) C x _ 6 alkyl one ureido group, (31) G (6 alkyl chromatography © raid group, (32) Okishi de group And (33) a group selected from the group consisting of two or three groups selected from the groups (1) to (32) and the like (hereinafter, abbreviated as substituent group A); Do stone five good C _ 6 alkyl group which may have, respectively, C 2 - 6 alkenyl, C 2 one 6 alkynyl group, C 3 _ 6 cycloalkyl group, C 3 - 6 cycloalkenyl group, C 6 _ 14 T reel base or the C 7 _ 16 Ararukiru group,
(ii)前記置換基 A群から選ばれる置換 を 1ないし 5個有していてもよい炭素原 子以外に窒素原子、硫黄原子および酸素原子から選ばれるヘテロ原子を 1ないし 4 個含む 5ないし 14員複素環基; (ii) 5 to 14 containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to the carbon atom which may have 1 to 5 substituents selected from the substituent group A. Membered heterocyclic group;
R 2および R 3がそれぞれ以下の (i) 〜 (iii) のいずれかを示す: R 2 and R 3 each represent one of the following (i) to (iii):
(i) 水素原子、 (i) a hydrogen atom,
(ii)前記置換基 A群から選ばれる置換基を 1ないし 5個それぞれ有していてもよ い アルキル基、 C2— 6アルケニル基、 C2_6アルキニル基、 C3— 6シクロアル キル基、 C3_6シクロアルケニル基、 C6— 14ァリール基または C7_16ァラルキル (ii) the 1 a substituent selected from the substituent group A to 5 but it may also have each an alkyl group, C 2 - 6 alkenyl group, C 2 _ 6 alkynyl, C 3 - 6 a cycloalkyl group , C 3 _ 6 cycloalkenyl group, C 6 - 14 Ariru group or C 7 _ 16 Ararukiru
(iii) 前記置換基 A群から選ばれる置換基を 1ないし 5個有していてもよい、 ホ ルミル、 力ルポキシ、 力ルバモイル、 アルキル一力ルポニル、 C3— 6シクロ アルキル—カルボニル、 C 6アルコキシ一力ルポニル、 c6_14ァリ一ルーカルボ ニル、 C7_16ァラルキル一力ルポニル、 C6_14ァリールォキシ一力ルポニル、 C(iii) said may have 1 to 5 substituents selected from the substituent group A, E mill, force Rupokishi force Rubamoiru, alkyl Ichiriki Ruponiru, C 3 - 6 cycloalkyl Alkyl - carbonyl, C 6 alkoxy Ichiriki Ruponiru, c 6 _ 14 § Li one Rukarubo alkenyl, C 7 _ 16 Ararukiru Ichiriki Ruponiru, C 6 _ 14 Ariruokishi Ichiriki Ruponiru, C
7_16ァラルキルォキシ一力ルポニル、 炭素原子以外に窒素原子、 硫黄原子および 酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環 力ルポニル、 モノー C — 6アルキル一力ルバモイル、 ジー — 6アルキル—力ルバ モイル、 c6— 14ァリール一力ルバモイル、 炭素原子以外に窒素原子、 硫黄原子お よび酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複 素環力ルバモイル、 C _6アルキル一チォカルポニル、 C3_6シクロアルキルーチ ォカルボニル、 C 6アルコキシ—チォ力ルポニル、 C6_14ァリ一ルーチォカルポ ニル、 c7_16ァラルキル一チォカルポニル、 c6_14ァリールォキシ一チォカルポ エル、 c7— 16ァラルキルォキシーチォカルボニル、 炭素原子以外に窒素原子、 硫 黄原子および酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5また は 6員複素環チォカルポニル、 チォカルバモイル、 モノー C _ 6アルキル一チォカ ルバモイル、ジー(^_6アルキル一チォカルバモイル、 C6— 14ァリ一ルーチォカル バモイル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ない し 3個のへテロ原子を含有する 5または 6員複素環チォカルパモイル、スルファモ ィル、モノー C i— eアルキルスルファモイル、ジー C アルキルスルファモイル、 C6一 14ァリールスルファモイル、 6アルキルスルホニル、 C6— 14ァリールス ルホニル、 Ci-eアルキルスルフィニル、 C 6— 14ァリ一ルスルフィニル、 スルフィ ノ、スルホ、 C i_6アルコキシスルフィエル、 C 6_14ァリ一ルォキシスルフィニル、 C ^6アルコキシスルホニルおよび C 6 4ァリールォキシスルホエルから選ばれ るァシル基; Ichiriki 7 _ 16 Ararukiruokishi Ruponiru, nitrogen atom in addition to carbon atom, a sulfur atom and 1 to containing heteroatoms three of the 5 or 6-membered heterocyclic force Ruponiru selected from oxygen atom, mono- C - 6 alkyl Ichiriki Rubamoiru, di - 6 alkyl - power resolver moil, c 6 - 14 Ariru Ichiriki Rubamoiru, nitrogen atom in addition to carbon atoms, 5 or containing 1 to heteroatoms three of the selected sulfur atom Contact and oxygen atom 6 membered double ring force Rubamoiru, C _ 6 alkyl one Chiokaruponiru, C 3 _ 6 cycloalkyl over Ji Okaruboniru, C 6 alkoxy - Chio force Ruponiru, C 6 _ 14 § Li one Ruchiokarupo alkenyl, c 7 _ 16 Ararukiru one Chiokaruponiru, c 6 _ 14 Ariruokishi one Chiokarupo el, c 7 - 16 § Lal kill O Kishi Chio carbonyl, nitrogen atom in addition to carbon atoms, sulfur atoms and 5 or 6 membered heterocyclic ring Chiokaruponiru containing hetero atoms to 1 selected from atom 3 of the, Chiokarubamoiru, mono- C _ 6 alkyl one Chioka Rubamoiru, di- (^ _ 6 alkyl one Chiokarubamoiru, C 6 - 14- Rutical Bamoyl, 5- or 6-membered heterocyclic thiocarpamoyl containing 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms, sulfamoyl, mono-C i— e alkylsulfamoyl, di-C alkylsulfamoyl, C 6 one 14 § reel sulfamoyl, 6 alkylsulfonyl, C 6 - 14 Arirusu Ruhoniru, Ci-e alkylsulfinyl, C 6 - 14 § Li one Rusurufiniru, Surufi Bruno, sulfo, C i_ 6 alkoxysulfinyl sulfide El, C 6 _ 14 § Li one Ruo alkoxy sulfinyl, C ^ 6 alkoxysulfonyl And C 6 4 Ashiru group § reel O carboxymethyl Ru selected from sulfo El;
R 2と R 3は隣接する炭素原子と共に、 アルキル、 C6_147リール、 C7— 16ァラルキル、 ァミノ、 モノー アルキルァミノ、 モノー C6— 14ァリールァ ミノ、ジー(:ト 6アルキルァミノ、 ジ一 C6— 14ァリールァミノおよび 4ないし 10 員芳香族複素環基から選ばれる置換基を 1ないし 3個それぞれ有していてもよい C 3_ 8シクロアルカンまたは 3ないし 8員複素環を形成しても'よく ; R 2 and R 3 together with the adjacent carbon atom, alkyl, C 6 _ 14 7 reel, C 7 - 16 Ararukiru, Amino, mono- Arukiruamino, mono- C 6 - 14 Arirua amino, di- (: Preparative 6 Arukiruamino, di one C 6 — 14 arylamino and a C 3 _ 8 cycloalkane optionally having 1 to 3 substituents selected from a 4- to 10-membered aromatic heterocyclic group or a 3- to 8-membered heterocyclic group Often ;
R 4および R 5がそれぞれ (i) 水素原子または (ii) 前記置換基 A群から選ばれ る置換基を 1ないし 5個それぞれ有していてもよい — 6アルキル基、 C2_6アル ケニル基、 c2— 6アルキニル基、 c3_6シクロアルキル基、 c3— 6シクロアルケ二 ル基、 c6_14ァリール基または c7— 16ァラルキル基を; R 4 and R 5 may have, respectively (i) a hydrogen atom or (ii) the substituent, 1 to selected Ru substituents from group A 5 each - 6 alkyl group, C 2 _ 6 Al Kenyir group, c 2 - 6 alkynyl group, c 3 _ 6 cycloalkyl group, c 3 - 6 Shikuroaruke two Le group, c 6 _ 14 Ariru group or c 7 - 16 Ararukiru group;
R 6および R 7がそれぞれ (i) 水素原子または (ii) 前記置換基 A群から選ばれ る置換基を 1ないし 5個それぞれ有していてもよい アルキル基、 C2_6アル ケニル基、 C2_6アルキニル基、 C3-6シクロアルキル基、 C3_6シクロアルケ二 ル基、 C6— 14ァリール基または C7— 16ァラルキル基を示し、 R 6 and R 7 are each (i) a hydrogen atom or (ii) an alkyl group, a C 2 _ 6 alkenyl group which may have 1 to 5 substituents each selected from the aforementioned substituent group A, C 2 _ 6 alkynyl, C 3 - 6 cycloalkyl group, C 3 _ 6 Shikuroaruke two Le group, C 6 - 14 Ariru radical or C 7 - 16 show the Ararukiru group,
R 6と R 7は隣接する炭素原子と共に、 アルキル、 C6一 14ァリール、 C7_ 1 6ァラルキル、 ァミノ、 モノー — 6アルキルァミノ、 モノー C6_14ァリールァ ミノ、ジー( 6アルキルァミノ、ジー C6— 14ァリールァミノおよび 4ないし 10 員芳香族複素環基から選ばれる置換基を 1ないし 3個それぞれ有していてもよい C 3一 8シクロアルカンまたは 3ないし 8員複素環を形成してもよく ; R 6 and R 7 together with the adjacent carbon atom, alkyl, C 6 one 14 Ariru, C 7 _ 1 6 Ararukiru, Amino, mono- - 6 Arukiruamino, mono- C 6 _ 14 Arirua amino, di- (6 Arukiruamino, di C 6 - 14 to Ariruamino and 3 good C 3 no one 8 cycloalkane or 3 have respectively, 1 to substituents selected from 4- to 10-membered aromatic heterocyclic group may form a 8-membered heterocyclic ring;
R8が以下の (i) 〜 (X) のいずれかを示す: R 8 represents one of the following (i) to (X):
(i) 水素原子、 (i) a hydrogen atom,
(ii)前記置換基 A群から選ばれる置換基を 1ないし 5個それぞれ有していてもよ い — 6アルキル基、 C 2一 6アルケニル基、 C2— 6アルキニル基、 C3_6シクロアル キル基、 C3_6シクロアルケニル基、 C6— 14ァリール基または C7— 16ァラルキル (ii) but it may also have the, 1 to substituents selected from the substituent group A 5 each - 6 alkyl group, C 2 one 6 alkenyl, C 2 - 6 alkynyl group, C 3 _ 6 cycloalk kill group, C 3 _ 6 cycloalkenyl group, C 6 - 14 Ariru radical or C 7 - 16 Ararukiru
(iii) 前記置換基 A群から選ばれる置換基を 1ないし 5個有していてもよい、 ホ ルミル、 カルボキシ、 力ルバモイル、 Ci— 6アルキル一カルボニル、 C3一 6シクロ アルキル—力ルポニル、 C丄_6アルコキシ一力ルポニル、 C6_14ァリール一力ルポ エル、 C7_16ァラルキル一力ルポニル、 C6— 14ァリールォキシ一力ルポニル、 C 7_16ァラルキルォキシ一力ルポニル、 炭素原子以外に窒素原子、 硫黄原子および 酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環 力ルポニル、 モノ一 Cト 6アルキル—力ルバモイル、 ジ— アルキル一力ルバ モイル、 C6— 14ァリール一力ルバモイル、 炭素原子以外に窒素原子、 硫黄原子お よび酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複 素環力ルバモイル、 C丄 _ 6アルキル一チォカルポニル、 C3_6シクロアルキル—チ 才力ルポニル、 C^— 6アルコキシ—チォカルボニル、 C6_14ァリール一チォカルポ エル、 C7_16ァラルキル—チォカルボニル、 C6— 14ァリールォキシーチォカルボ ニル、 C7一 16ァラルキルォキシ—チォ力ルポニル、 炭素原子以外に窒素原子、 硫 黄原子および酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5また は 6員複素環チォカルポニル、 チォカルバモイル、 モノー アルキル一チォカ ルバモイル、ジー アルキル一チォカルバモイル、 C6— 14ァリールーチォカル バモイル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ない し 3個のへテロ原子を含有する 5または 6員複素環チォカルバモイル、スルファモ ィル、モノー C i— 6アルキルスルファモイル、ジー 6アルキルスルファモイル、 C6_14ァリ一ルスルファモイル、 アルキルスルホニル、 C6一 14ァリールス ルホニル、 Ci_6アルキルスルフィエル、 C6_14ァリールスルフィニル、 スルフィ ノ、スルホ、(^_6アルコキシスルフィニル、 c6— 14ァリ一ルォキシスルフィエル、(iii) the substituents selected from substituent group A may have 1 to have five, Ho mill, carboxy, force Rubamoiru, CI- 6 alkyl one carbonyl, C 3 one 6 cycloalkyl - Power Ruponiru, C丄_ 6 alkoxy Ichiriki Ruponiru, C 6 _ 14 Ariru Ichiriki Lupo El, C 7 _ 16 Ararukiru Ichiriki Ruponiru, C 6 - 14 Ariruokishi Ichiriki Ruponiru, C 7 _ 16 Ararukiruokishi Ichiriki Ruponiru, in addition to carbon atoms nitrogen atom, sulfur atom and 1 to containing heteroatoms three of the 5 or 6-membered heterocyclic force Ruponiru selected from oxygen atom, mono-one C DOO 6 alkyl - force Rubamoiru, di - alkyl Ichiriki resolver moil, C 6 - 14 Ariru Ichiriki Rubamoiru, nitrogen atom, to 1 selected from nitrogen atom Contact and oxygen atoms containing hetero atoms 3 of the 5 or 6 membered double ring force Rubamoiru in addition to carbon atoms C丄_ 6 alkyl one Chiokaruponiru, C 3 _ 6 cycloalkyl - Chi Sairyoku Ruponiru, C ^ - 6 alkoxy - Chio carbonyl, C 6 _ 14 Ariru one Chiokarupo El, C 7 _ 16 Ararukiru - Chio carbonyl, C 6 - 14 Aryloxy-Carbo Alkenyl, C 7 one 16 Ararukiruokishi - Chio force Ruponiru, 5 or 6 membered heterocyclic ring Chiokaruponiru containing 1 to heteroatoms three of the selected from a nitrogen atom, sulfur atom and oxygen atom in addition to carbon atoms, Chiokarubamoiru , mono- alkyl one Chioka Rubamoiru, di-alkyl one Chiokarubamoiru, C 6 - 14 § reel over Chio local Bamoiru, nitrogen atom in addition to carbon atoms, a sulfur atom and 1 to heteroatoms three of the selected oxygen atom 5 or 6 membered heterocyclic ring Chiokarubamoiru, Surufamo I Le, mono- C i-6 alkylsulfamoyl, di-6 alkylsulfamoyl, C 6 _ 14 § Li one Rusurufamoiru, alkylsulfonyl, C 6 one 14 Arirusu Ruhoniru, CI_ 6 alkyl sulfide El, C 6 _ 14 § reel sulfinyl, Surufi Roh, sulfo, (^ _ 6 Arco Shisurufiniru, c 6 - 14 § Li one Ruo carboxymethyl sulfide El,
Ci— eアルコキシスルホニルおよび C6— 14ァリ一ルォキシスルホエルから選ばれ るァシル基、 Ci- e alkoxysulfonyl and C 6 - 14 § Li one Ruo carboxymethyl sulfonyl El from selected Ru Ashiru group,
(iv)前記置換基 A群から選ばれる置換基を 1ないし 5個有していてもよい炭素原 子以外に窒素原子、硫黄原子および酸素原子から選ばれるヘテロ原子を 1ないし 4 個含む 5ないし 14員複素環、 (iv) In addition to the carbon atom which may have 1 to 5 substituents selected from the aforementioned substituent group A, including 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms, 5 to 5 14-membered heterocycle,
(v) ハロゲン原子、 (v) a halogen atom,
(vi) -OR10 (R1Qは、 (i') 水素原子、 (ii') 前記置換基 A群から選ばれる 置換基を 1ないし 5個それぞれ有していてもよい C i— 6アルキル基、 C 2_6アルケ ニル基、 C2_6アルキニル基、 C 3— 6シクロアルキル基、 C 3— 6シクロアルケニル 基、 (:6„14ァリール基または C7_16ァラルキル基、 (iii') 前記置換基 A群から 選ばれる置換基を 1ないし 5個有していてもよい、 ホルミル、 力ルバモイル、 ェ _6アルキル一力ルポニル、 C3— 6シクロアルキル—力ルポニル、 — 6アルコキシ —カルボニル、 C6— 14ァリール—力ルポニル、 C7— 16ァラルキル—力ルポニル、 C6_14ァリ一ルォキシーカルボニル、 C7_16ァラルキルォキシ一力ルポニル、 炭 素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテ 口原子を含有する 5または 6員複素環力ルポニル、 モノー Cト6アルキル—力ルバ モイル、 ジー — 6アルキル一力ルバモイル、 C6_14ァリール—力ルバモイル、炭 素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテ 口原子を含有する 5または 6員複素環力ルバモイル、 アルキル一チォカルポ ニル、 C3_6シクロアルキル一チォカルポニル、 アルコキシーチォカルボ二 ル、 C6_14ァリール—チォカルボニル、 C7一 16ァラルキル—チォカルボニル、 C(vi) -OR 10 (R 1Q is (i ′) a hydrogen atom, and (ii ′) a C i-6 alkyl group which may have 1 to 5 substituents each selected from the aforementioned substituent group A. , C 2 _ 6 alkenyl group, C 2 _ 6 alkynyl, C 3 - 6 cycloalkyl group, C 3 - 6 cycloalkenyl group, (6 "14 Ariru group or C 7 _ 16 Ararukiru group, (iii ' ) wherein, 1 to substituents selected from the substituent group a may have five, formyl, force Rubamoiru, E _ 6 alkyl Ichiriki Ruponiru, C 3 - 6 cycloalkyl - power Ruponiru, - 6 alkoxy - carbonyl, C 6 - 14 Ariru - force Ruponiru, C 7 - 16 Ararukiru - force Ruponiru, C 6 _ 14 § Li one Ruo Kishi carbonyl, C 7 _ 16 Ararukiruokishi Ichiriki Ruponiru, nitrogen atom besides carbon atom, a sulfur atom Contains 1 to 3 hetero atoms selected from That 5 or 6 membered heterocyclic force Ruponiru, mono- C bets 6 alkyl - Power resolver moil, di - 6 alkyl Ichiriki Rubamoiru, C 6 _ 14 Ariru - force Rubamoiru, nitrogen atom besides carbon atom, sulfur atom and oxygen atom 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from: rubamoyl, alkyl monocarbo Alkenyl, C 3 _ 6 cycloalkyl one Chiokaruponiru, alkoxycarbonyl Kishi Chio carbonylation Le, C 6 _ 14 Ariru - Chio carbonyl, C 7 one 16 Ararukiru - Chio carbonyl, C
6_14ァリールォキシ一チォカルポニル、 C 7— 16ァラルキルォキシ一チォカルポ二 ル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個 のへテロ原子を含有する 5または 6員複素環チォカルボニル、 チォカルバモイル、 モノー C卜 6アルキル一チォカルバモイル、 ジー C — 6アルキル一チォカルバモイ ル、 c6_14ァリ一ルーチォカルバモイル、 炭素原子以外に窒素原子、 硫黄原子お よび酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複 素環チォカルバモイル、 スルファモイル、 モノー C i一 6アルキルスルファモイル、 ジー C _ 6アルキルスルファモイル、 C6— 14ァリ一ルスルファモイル、 C 6アル キルスルホニル、 C 6— 14ァリ一ルスルホニル、 6アルキルスルフィエル、 C6 6 _ 14 Ariruokishi one Chiokaruponiru, C 7 - 16 Ararukiruokishi one Chiokarupo two Le, nitrogen atom, sulfur atom and to 1 selected from an oxygen atom containing heteroatoms three of the 5 or 6-membered heterocyclic ring Chio in addition to carbon atoms selected 6 alkyl one Chiokarubamoi le, c 6 _ 14 § Li one Roux Chio carbamoyl, nitrogen atom in addition to carbon atoms, a sulfur atom Contact and oxygen atom - carbonyl, Chiokarubamoiru, mono- C WINCH 6 alkyl one Chiokarubamoiru, di C 1 to 3 containing heteroatoms of 5 or 6 membered double ring Chiokarubamoiru, sulfamoyl, mono- C i one 6 alkylsulfamoyl, di C _ 6 alkylsulfamoyl, C 6 - 14 § Li one Rusurufamoiru , C 6 Al alkylsulfonyl, C 6 - 14 § Li one Rusuruhoniru, 6 alkylsulfide El, C 6
-14ァリールスルフィエル、 C — 6アルコキシスルフィエル、 C6_14ァリ一ルォキ シスルフィエル、 アルコキシスルホニルおよび C6— 14ァリ一ルォキシスルホ エルから選ばれるァシル基または (iv') 前記置換基 A群から選ばれる置換基を 1 ないし 5個有していてもよい炭素原子以外に窒素原子、硫黄原子および酸素原子か ら選ばれるヘテロ原子を 1ないし 4個含む 5ないし 14員複素環を示す) 、 (vii) -SR11 (R11は、 (i,) 水素原子、 (iiゥ 前記置換基 A群から選ばれる 置換基を 1ないし 5個それぞれ有していてもよいじ 6アルキル基、 C2_6アルケ ニル基、 C2_6アルキニル基、 C 3— 6シクロアルキル基、 C3— 6シクロアルケニル 基、 C6— 14ァリール基または C7_16ァラルキル基、 (iii') 前記置換基 A群から 選ばれる置換基を 1ないし 5個有していてもよい、 ホルミル、 力ルバモイル、 d-14 § reel sulfide El, C - 6 alkoxysulfinyl Luffy El, C 6 _ 14 § Li one Ruoki Shisurufieru, Alkoxysulfonyl and C 6 - 14 Ashiru group or (iv ') the substituent A 1 without a substituent selected from the group to five has optionally a nitrogen atom in addition also be carbon atoms selected from § Li one Ruokishisuruho El, A 5- to 14-membered heterocyclic ring containing 1 to 4 hetero atoms selected from a sulfur atom and an oxygen atom), (vii) -SR 11 (R 11 is a (i,) hydrogen atom, (ii 1 to 5 Ji may have respectively 6 alkyl group a substituent selected from group a, C 2 _ 6 alkenyl group, C 2 _ 6 alkynyl, C 3 - 6 cycloalkyl group, C 3 - 6 cycloalkenyl group, C 6 - 14 Ariru group or C 7 _ 16 Ararukiru group, which may have five to 1 substituent selected from (iii ') the substituent group a, formyl, force Rubamoiru , D
—6アルキル—カルボニル、 C 3— 6シクロアルキル一力ルポニル、 一 6アルコキシ 一力ルポニル、 C6— 14ァリール一力ルポニル、 C7_16ァラルキル一カルボニル、 C6_14ァリールォキシ—力ルポ: ίル、 C7— 16ァラルキルォキシ一力ルポニル、 炭 素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテ 口原子を含有する 5'または 6員複素環力ルポニル、 モノー C i_6アルキル一力ルバ モイル、 ジ _ C _ 6アルキル一力ルバモイル、 C6_14ァリール—カルパモイル、 炭 素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテ 口原子を含有する 5または 6員複素環力ルバモイル、 アルキル一チォカルポ ニル、 C3— 6シクロアルキルーチォカルボニル、 (^ アルコキシ一チォカルポ二 ル、 C 6— 14ァリール一チォカルポニル、 C7_16ァラルキル—チォカルポニル、 C- 6 alkyl - carbonyl, C 3 - 6 cycloalkyl Ichiriki Ruponiru one 6 alkoxy Ichiriki Ruponiru, C 6 - 14 Ariru Ichiriki Ruponiru, C 7 _ 16 Ararukiru one carbonyl, C 6 _ 14 Ariruokishi - Power Lupo: I Le, C 7 - 16 Ararukiruokishi Ichiriki Ruponiru, nitrogen atom besides carbon atom, a sulfur atom and to 1 selected from an oxygen atom containing terrorist atom 3 of the 5 'or 6-membered heterocyclic ring force Ruponiru, mono- C i_ 6 alkyl Ichiriki resolver moil, di _ C _ 6 alkyl Ichiriki Rubamoiru, C 6 _ 14 Ariru - Karupamoiru, nitrogen atom in addition to carbon atom, to 1 selected from sulfur atom and an oxygen atom Te to three of 5- or 6-membered heterocyclic moieties containing an orbital atom Lubamoyl, alkyl monocarbo Alkylsulfonyl, C 3 - 6 cycloalkyl over Chio carbonyl, (^ alkoxy one Chiokarupo two Le, C 6 - 14 Ariru one Chiokaruponiru, C 7 _ 16 Ararukiru - Chiokaruponiru, C
6^ 4ァリ一ルォキシーチ才力ルポニル、 C 7^ 6ァラルキルォキシ—チォ力ルポ二 ル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個 のへテロ原子を含有する 5または 6員複素環チォカルポニル、 チォカルバモイル、 モノー C i _ 6アルキル一チォカルバモイル、 ジー C i _ 6アルキル一チォカルバモイ ル、 C6_14ァリ一ルーチォカルバモイル、 炭素原子以外に窒素原子、 硫黄原子お よび酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複 素環チォカルバモイル、 スルファモイル、 モノー C i— 6アルキルスルファモイル、 ジー — 6アルキルスルファモイル、 C6_14ァリールスルファモイル、 C — 6アル キルスルホニル、 C6_14ァリ一ルスルホニル、 (^_6アルキルスルフィエル、 C6 6 ^ 4 aralkyloxyl talc, C7 ^ 6 aralkyloxyl oxyl, containing 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen in addition to carbon 5 or 6-membered heterocyclic ring Chiokaruponiru, Chiokarubamoiru, mono- C i _ 6 alkyl one Chiokarubamoiru, di C i _ 6 alkyl one Chiokarubamoi Le, C 6 _ 14 § Li one Roux Chio carbamoyl, nitrogen atom in addition to carbon atom, a sulfur atom 1 to 3 containing heteroatoms of 5 or 6 membered double ring Chiokarubamoiru selected from Contact and oxygen atoms, sulfamoyl, mono- C i-6 alkylsulfamoyl, di - 6 alkylsulfamoyl, C 6 _ 14 § reel sulfamoyl, C - 6 Al alkylsulfonyl, C 6 _ 14 § Li one Rusuruhoniru, (^ _ 6 alkyl sulfide El, C 6
-14ァリールスルフィニル、 アルコキシスルフィエル、 C6一 14ァリールォキ シスルフィニル、 アルコキシスルホニルおよび C 6^ 4ァリールォキシスルホ ニルから選ばれるァシル基または (ίν') 前記置換基 Α群から選ばれる置換基を 1 ないし 5個有していてもよい炭素原子以外に窒素原子、硫黄原子および酸素原子か ら選ばれるヘテロ原子を 1ないし 4個含む 5ないし 14員複素環を示す) 、 -14 § reel sulfinyl substitutions, alkoxysulfinyl sulfide El, C 6 one 14 Ariruoki Shisurufiniru, selected from alkoxysulfonyl and C 6 ^ 4 § reel O alkoxy or Ashiru selected from sulfonyl group (ίν ') the substituent Α group A 5- to 14-membered heterocyclic ring containing 1 to 4 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may have 1 to 5 groups),
(viii) -S (〇) R12 (R12は、 (i,) 前記置換基 A群から選ばれる置換基を 1な いし 5個それぞれ有していてもよい Ci— 6アルキル基、 C2— 6アルケニル基、 C2一 6アルキニル基、 C3_ 6シクロアルキル基、 C 3— 6シクロアルケニル基、 C6—— 14ァ リール基または C7— 16ァラルキル基または (ii') 前記置換基 A群から選ばれる置 換基を 1ないし 5個有していてもよい炭素原子以外に窒素原子、硫黄原子および酸 素原子から選ばれるヘテロ原子を 1ないし 4個含む 5ないし 14員複素環を示す)、(viii) -S (〇) R 12 (R 12 is (i,) a Ci- 6 alkyl group optionally having 1 to 5 substituents selected from the aforementioned substituent group A, C 2 - 6 alkenyl, C 2 one 6 alkynyl group, C 3 _ 6 cycloalkyl group, C 3 - 6 cycloalkenyl group, C 6 - 14 § aryl group or C 7 - 16 Ararukiru group or (ii ') the substituent Group A 5- to 14-membered heterocyclic ring containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may have 1 to 5 substituents selected from group A ),
(ix) -S (〇) 2R13 (R13は、 (i,) 前記置換基 A群から選ばれる置換基を 1な いし 5個それぞれ有していてもよい アルキル基、 C2_6アルケニル基、 C2_ 6アルキニル基、 C3_ 6シクロアルキル基、 C 3— 6シクロアルケニル基、 ( 6—14ァ リール基または〇7_16ァラルキル基または (ii,) 前記置換基 A群から選ばれる置 換基を 1ないし 5個有していてもよい炭素原子以外に窒素原子、硫黄原子および酸 素原子から選ばれるヘテロ原子を 1ないし 4個含む 5ないし 14員複素環を示す)、(ix) -S (〇) 2 R 13 (R 13 is (i,) an alkyl group optionally having 1 to 5 substituents selected from the above-mentioned substituent group A, C 2 _ 6 alkenyl group, C 2 _ 6 alkynyl, C 3 _ 6 cycloalkyl group, C 3 - 6 cycloalkenyl group, (6 - 14 § aryl group or 〇 7 _ 16 Ararukiru group or (ii,) the substituent group A A 5- to 14-membered heterocyclic ring containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may have 1 to 5 substituents selected from) ,
(X) — NR14R15 (R 14および R 15はそれぞれ (ί') 水素原子、 (ii,) 前記置換 基 A群から選ばれる置換基を 1ないし 5個それぞれ有していてもよい C ^6アル キル基、 C2— 6アルケニル基、 C2— 6アルキニル基、 C3_6シクロアルキル基、 C3 -6シクロアルケニル基、 ( 6_14ァリール基または C7_16ァラルキル基、 (iii5) 前記置換基 A群から選ばれる置換基を 1ないし 5個有していてもよい、 ホルミル、 カルパモイル、 アルキル一力ルポニル、 C3— 6シクロアルキル—力ルポニル、 アルコキシ一力ルポニル、 C6— 14ァリール一力ルポニル、 C7— 16ァラルキ ルー力ルポニル、 C6_14ァリ一ルォキシ—力ルポニル、 C7_16ァラルキルォキシ 一カルボニル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1 ないし 3個のへテロ原子を含有する .5または 6員複素環力ルポニル、 モノ— C アルキル一力ルバモイル、ジ アルキル一力ルバモイル、 C6— 14ァリール一 力ルバモイル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1 ないし 3個のへテロ原子を含有する 5または 6員複素環力ルバモイル、 (^_6アル キル一チォカルポニル、 C 3— 6シクロアルキル一チォカルポニル、 。ト6アルコキ シーチォカルボニル、 C6_14ァリ一ルーチォカルポニル、 C7— 16ァラルキルーチ 才力ルポニル、 C 6— 14ァリールォキシ—チォカルボニル、 C7_16ァラルキルォキ シ-チ才力ルポニル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ば れる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカルボニル、チ 才力ルバモイル、 モノー C i _ 6アルキル一チォカルバモイル、 ジ一 C 6アルキル —チォ力ルバモイル、 C6_14ァリ一ルーチォカルバモイル、 炭素原子以外に窒素 原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカルバモイル、 スルファモイル、 モノー — 6アルキルス ルファモイル、ジ _ C — 6アルキルスルファモイル、 C6_14ァリールスルファモイ ル、 C卜 6アルキルスルホニル、 C6— 14ァリールスルホニル、 アルキルスル フィエル、 C6_14ァリ一ルスルフィニル、 C 一 6アルコキシスルフィニル、 C6—ェ(X) — NR 14 R 15 (R 14 and R 15 are each a (ί ′) hydrogen atom, (ii,) the above substitution , 1 to substituents selected from group A five may have respective C ^ 6 Al kill groups, C 2 - 6 alkenyl groups, C 2 - 6 alkynyl groups, C 3 _ 6 cycloalkyl groups, C 3 - 6 cycloalkenyl group, (6 _ 14 Ariru group or C 7 _ 16 Ararukiru group, (iii 5) said may have 1 to 5 substituents selected from the substituent group a, formyl, Karupamoiru , alkyl Ichiriki Ruponiru, C 3 - 6 cycloalkyl - force Ruponiru, alkoxy Ichiriki Ruponiru, C 6 - 14 Ariru Ichiriki Ruponiru, C 7 - 16 Araruki Lou force Ruponiru, C 6 _ 14 § Li one Ruokishi - power Ruponiru , C 7 _ 16 aralkyloxycarbonyl, containing 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms. 5- or 6-membered heterocyclic carbonyl, mono-C alkyl. Force rubamo Le, di alkyl Ichiriki Rubamoiru, C 6 - 14 Ariru Ichiriki Rubamoiru, nitrogen atom in addition to carbon atom, a sulfur atom and 1 to 5 or 6-membered heterocyclic ring force containing heteroatoms three of the selected oxygen atom Rubamoiru, (^ _ 6 Al kill one Chiokaruponiru, C 3 -. 6 cycloalkyl one Chiokaruponiru, DOO 6 alkoxy Sea Chio carbonyl, C 6 _ 14 § Li one Roux Chio local Poni Le, C 7 - 16 Ararukiruchi Sairyoku Ruponiru, C 6 - 14 Ariruokishi - Chio carbonyl, C 7 _ 16 Ararukiruoki sheet - Chi Sairyoku Ruponiru, nitrogen atom in addition to carbon atoms, 5 or 6 membered heterocyclic containing 1 to heteroatoms three of the selected sulfur atom and an oxygen atom ring Chio carbonyl, Ji Sairyoku Rubamoiru, mono- C i _ 6 alkyl one Chiokarubamoiru, di one C 6 alkyl - Chio force Rubamoiru, C 6 _ 14 § Li Luciocarbamoyl, 5- or 6-membered heterocyclic thiocarbamoyl containing 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms, thiocarbamoyl, sulfamoyl, mono--6 alkylsulfamoyl, di _C - 6 alkylsulfamoyl, C 6 _ 14 § reel sulfamoyl Le, C WINCH 6 alkylsulfonyl, C 6 - 14 § reel sulfonyl, alkylsulfinyl Fier, C 6 _ 14 § Li one Rusurufiniru, C one 6 alkoxysulfinyl sulfinyl , C 6 —e
4ァリ—ルォキシスルフィニル、 Cト 6アルコキシスルホニルおよび C 6— 14ァリー ルォキシスルホニルから選ばれるァシル基または (ίν') 前記置換基 Α群から選ば れる置換基を 1ないし 5個有していてもよい炭素原子以外に窒素原子、硫黄原子お よび酸素原子から選ばれるヘテロ原子を 1ないし 4個含む 5ないし 14員複素環 を示す) R9が (i) 水素原子、 (ii) シァノ基、 4 § Li - Ruo alkoxy sulfinyl, C DOO 6 alkoxysulfonyl and C 6 - 14 Ari Ruo carboxymethyl sulfo Ashiru selected from sulfonyl group or (ίν ') wherein have 1 to 5 substituents selected from substituent group Α group A 5- to 14-membered heterocyclic ring containing 1 to 4 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may be present) R 9 is (i) a hydrogen atom, (ii) a cyano group,
(iii) 前記置換基 A群から選ばれる置換基を 1ないし 5個それぞれ有していても よい — 6アルキル基、 C2_6アルケニル基、 C2— 6アルキニル基、 C3— 6シクロア ルキル基、 C3_6シクロアルケニル基、 C6_14ァリール基または C7— 16ァラルキ ル基、 (iii) said, 1 to substituents selected from the substituent group A may have five, respectively - 6 alkyl group, C 2 _ 6 alkenyl, C 2 - 6 alkynyl group, C 3 - 6 Shikuroa alkyl group, C 3 _ 6 cycloalkenyl group, C 6 _ 14 Ariru group or C 7 - 16 Araruki group,
(iv)前記置換基 A群から選ばれる置換基を 1ないし 5個有していてもよい、ホル ミル、 カルボキシ、 力ルバモイル、 ^— 6アルキル—カルボニル、 C3_6シクロア ルキルーカルボニル、 C _6アルコキシ—力ルポニル、 C6_14ァリ一ルー力ルポ二 ル、 C 7 _ 6ァラルキル一力ルポニル、 C6— 14ァリ一ルォキシ—力ルポニル、 C7— 16ァラルキルォキシ一力ルポニル、 炭素原子以外に窒素原子、 硫黄原子および酸 素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環力 ルポニル、 モノ一 C卜 6アルキル—力ルバモイル、 ジ— Ci— 6アルキル—カルバモ ィル、 4ァリール一力ルバモイル、 炭素原子以外に窒素原子、 硫黄原子およ び酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素 環力ルバモイル、 C卜 6アルキル—チォカルポニル、 C 3— 6シクロアルキル—チォ 力ルポニル、 — 6アルコキシ—チォ力ルポニル、 C6_14ァリ一ルーチォカルポ二 ル、 C7— 16ァラルキル—チォカルポニル、 C 6— 14ァリールォキシ—チォ力ルポ二 ル、 C 7— 16ァラルキルォキシーチォカルボニル、 炭素原子以外に窒素原子、 硫黄 原子および酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカルボニル、 チォカルバモイル、 モノー C ^6アルキル一チォカル バモイル、ジ一 6アルキル一チォカルバモイル、 C 4ァリール一チォカルバ モイル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカルバモイル、スルファモイ ル、 モノー Cェ _ 6アルキルスルファモイル、 ジー — 6アルキルスルファモイル、 C6— 14ァリールスルファモイル、 アルキルスルホニル、 C6一 1 4ァリールス ルホニル、 アルキルスルフィエル、 < 6_14ァリールスルフィニル、 スルフィ ノ、スルホ、 C 6アルコキシスルフィニル、 C 6— 14ァリ一ルォキシスルフィニル、 d— 6アルコキシスルホニルぉよび C6一 14ァリ一ルォキシスルホニルから選ばれ るァシル基、 または (v) 式一 OR 9' (iv) the substituents selected from substituent group A may have 1-5 amino acids, formyl, carboxy, force Rubamoiru, ^ - 6 alkyl - carbonyl, C 3 _ 6 Shikuroa Ruki Lou carbonyl, C _ 6 alkoxy - force Ruponiru, C 6 _ 14 § Li one Roux force Lupo two Le, C 7 _ 6 Ararukiru Ichiriki Ruponiru, C 6 - 14 § Li one Ruokishi - force Ruponiru, C 7 - 16 Ararukiruokishi Ichiriki Ruponiru, nitrogen atom in addition to carbon atoms, to 1 selected from sulfur atom and oxygen radicals three of the 5 or 6-membered heterocyclic ring force containing heteroatoms Ruponiru, mono one C Bok 6 alkyl - force Rubamoiru, di - CI- 6- alkyl-carbamoyl, 4- aryl-lubamoyl, 5- or 6-membered heterocyclic lubamoyl containing 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms, C 6 Alkyl - Chiokaruponiru, C 3 - 6 cycloalkyl - Chio force Ruponiru, - 6 alkoxy - Chio force Ruponiru, C 6 _ 14 § Li one Ruchiokarupo two Le, C 7 - 16 Ararukiru - Chiokaruponiru, C 6 - 14 Ariruokishi - Chio force Lupo two Le, C 7 - 16 § Lal kill O Kishi Chio carbonyl, nitrogen atom in addition to carbon atom, a sulfur atom and 1 to 5 or 6-membered heterocyclic ring Chio carbonyl containing heteroatoms three of the selected oxygen atom , terrorism Chiokarubamoiru, mono- C ^ 6 alkyl one Chiokaru Bamoiru, di one 6 alkyl one Chiokarubamoiru, C 4 Ariru one Chiokaruba moil, nitrogen atom in addition to carbon atoms, to 1 selected from sulfur and oxygen atoms to three of containing an atom 5 or 6-membered heterocyclic ring Chiokarubamoiru, Surufamoi Le, mono- C E _ 6 alkylsulfamoyl Famo Le, di - 6 alkylsulfamoyl, C 6 - 14 § reel sulfamoyl, alkylsulfonyl, C 6 one 1 4 Arirusu Ruhoniru, alkylsulfide El, <6 _ 14 § reel sulfinyl, Surufi Bruno, sulfo, C 6 alkoxy sulfinyl, C 6 - 14 § Li one Ruo alkoxy sulfinyl, d-6 alkoxy sulfonyl Oyobi C 6 one 14 § Li one Ruo carboxymethyl sulfonyl from Ru selected Ashiru group or, (v) Formula 1 OR 9 '
(R9'は①水素原子、 (R 9 'is a ① hydrogen atom,
②前記置換基 A群から選ばれる置換基を 1ないし 5個それぞれ有していてもよい C卜 6アルキル基、 C2_6アルケニル基、 C2_6アルキニル基、 C3_6シクロアルキ ル基、 C3— 6シクロアルケニル基、 C6_14ァリ一ル基または C7_16ァラルキル基、 または ② said, 1 to substituents selected from the substituent group A may have five each C Bok 6 alkyl group, C 2 _ 6 alkenyl, C 2 _ 6 alkynyl, C 3 _ 6 cycloalkyl Le group , C 3 - 6 cycloalkenyl group, C 6 _ 14 § Li Ichiru group or C 7 _ 16 Ararukiru group or,
③前記置換基 A群から選ばれる置換基を 1ないし 5個有していてもよい、ホルミル、 力ルバモイル、 C卜 6アルキル一カルボニル、 C3— 6シクロアルキル一力ルポニル、 c i_6アルコキシ一力ルポニル、 c6_14ァリ一ルーカルボニル、 c7_16ァラルキ ルー力ルポニル、 c6— 14ァリールォキシ—力ルポニル、 c7— 16ァラルキルォキシ 一力ルポニル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1 ないし 3個のへテロ原子を含有する 5または 6員複素環カルボニル、 モノー C 6 アルキル一力ルバモイル、ジ _Cr— 6アルキル一力ルバモイル、 C6— 14ァリール一 力ルバモイル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1 ないし 3個のへテロ原子を含有する 5または 6員複素環力ルバモイル、 6アル キルーチォカルボニル、 C 3_6シクロアルキルーチォカルボニル、 6アルコキ シーチ才力ルポニル、 c6— 14ァリール—チォカルボニル、 c7_16ァラルキル—チ 才力ルポニル、 〇6,14ァリールォキシ—チォ力ルポ二ル、 c7— 16ァラルキルォキ シーチォカルボニル、炭素原子以外に窒素原子、硫黄原子および酸素原子から選ば れる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカルポニル、チ 才力ルバモイル、 モノー — 6アルキルーチォカルパモイル、 ジ _Ci— 6アルキル 一チォカルバモイル、 c6_14ァリール一チォカルバモイル、 炭素原子以外に窒素 原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカルバモイル、 スルファモイル、 モノ— ^— 6アルキルス ルファモイル、ジー アルキルスルファモイル、 C6— 14ァリールスルファモイ ル、 (^_6アルキルスルホニル、 C 6 4ァリールスルホニル、 — 6アルキルスル フィニル、 C6_14ァリ一ルスルフィニル、 — 6アルコキシスルフィニル、 CQ_1 ③ said substituent selected from the substituent group A may have 1-5 amino acids, formyl, force Rubamoiru, C WINCH 6 alkyl one carbonyl, C 3 - 6 cycloalkyl Ichiriki Ruponiru, c i_ 6 alkoxy one power Ruponiru, c 6 _ 14 § Li one Roux carbonyl, c 7 _ 16 Araruki Lou force Ruponiru, c 6 - 14 Ariruokishi - force Ruponiru, c 7 - 16 Ararukiruokishi Ichiriki Ruponiru, nitrogen atom in addition to carbon atom, sulfur atom and 5- or 6-membered heterocyclic carbonyl containing 1 to 3 heteroatoms selected from oxygen atoms, mono-C 6 alkyl mono-rubamoyl, di-C r — 6 alkyl mono-rubamoyl, C 6 — 14 aryl mono-rubamoyl , nitrogen atom in addition to carbon atom, a sulfur atom and 1 to containing heteroatoms three of the 5 or 6-membered heterocyclic force Rubamoiru selected from oxygen atom, 6 Al Kiruchio Carbonyl, C 3 _ 6 cycloalkyl over Chio carbonyl, 6 alkoxy Sich Sairyoku Ruponiru, c 6 - 14 Ariru - Chio carbonyl, c 7 _ 16 Ararukiru - Chi Sairyoku Ruponiru, 〇 6, 14 Ariruokishi - Chio force Lupo sulfonyl , c 7 - 16 Ararukiruoki Sea Chio carbonyl, nitrogen atom in addition to carbon atoms, 1 selected from sulfur atom and an oxygen atom to 3 for containing heteroatoms 5 or 6-membered heterocyclic ring Chiokaruponiru, Ji Sairyoku Rubamoiru, mono- - 6 alkyl chromatography Chio Scarpa moil, di _Ci- 6 alkyl one Chiokarubamoiru, c 6 _ 14 Ariru one Chiokarubamoiru, nitrogen atom in addition to carbon atoms, 1 to heteroatoms three of the selected sulfur atom and an oxygen atom Contains 5- or 6-membered heterocyclic thiocarbamoyl, sulfamoyl, mono-^- 6 alkylsulfamoyl, di Alkylsulfamoyl, C 6 - 14 § reel sulfamoyl Le, (^ _ 6 alkylsulphonyl, C 6 4 § reel sulfonyl, - 6 alkylsulfinyl Finiru, C 6 _ 14 § Li one Rusurufiniru, - 6 alkoxysulfinyl sulfinyl, C Q _ 1
4ァリ一ルォキシスルフィニル、 C — 6アルコキシスルホニルおよび C6_14ァリ一 ルォキシスルホニルから選ばれるァシル基を示す) で表される基を; Xが①前記置換基 A群から選ばれる置換基を有していてもよいメチレン基また は②カルポ二ル基を; 4 § Li one Ruo alkoxy sulfinyl, C - 6 alkoxysulfonyl and C 6 _ 14 group represented by Ashiru a group) selected from § Li one Ruo carboxymethyl sulfonyl; X is ①a methylene group which may have a substituent selected from the above-mentioned substituent group A or ②a carpenyl group;
nが 0または 1を示す前記 〔3〕 記載の化合物; The compound according to the above [3], wherein n represents 0 or 1;
〔5〕 R2および R3がそれぞれ (^_6アルキル基を示す前記 〔3〕 記載の化合物; 〔6〕 R 4および R 5がそれぞれ水素原子を示す前記 〔3〕 記載の化合物; [5] The indicating the R 2 and R 3 are each (^ _ 6 alkyl group [3] The compound according; [6] R 4 and R 5 are the represents a hydrogen atom, respectively [3] The compound according;
'〔7〕 R6および R7がそれぞれ アルキル基を示す前記 〔3〕 記載の化合物; 〔8〕 R 9が水素原子を示す前記 〔3〕 記載の化合物; '[7] The compound according to the above [3], wherein R 6 and R 7 each represent an alkyl group; [8] the compound according to the above [3], wherein R 9 represents a hydrogen atom;
〔9〕 nが 0を示す前記 〔3〕 記載の化合物; [9] the compound of the above-mentioned [3], wherein n represents 0;
〔10〕 R1が式 [10] R 1 is the formula
〔式中、 R16は水素原子、 置換基を有していてもよい C6— 14ァリール基、 置換基 を有していてもよいアミノ基、置換基を有していてもよい複素環基またはハロゲン 原子を示す〕 を、 R2および R3がそれぞれ アルキル基を、 R4および R5がそ れぞれ水素原子を、 R 6および R7がそれぞれ Ci— 6アルキル基を、 R8が水素原子 または一〇R1Q (R1Qは、水素原子、置換基を有していてもよい — 6アルキル基 またはァシル基を示す) を、 R9が水素原子を、 nが 0を示す前記 〔3〕 記載の化 合物; Wherein, R 16 is a hydrogen atom, which may have a substituent C 6 - 14 Ariru group, an optionally substituted amino group, heterocyclic group which may have a substituent R 2 and R 3 each represent an alkyl group; R 4 and R 5 each represent a hydrogen atom; R 6 and R 7 each represent a Ci- 6 alkyl group; and R 8 represents a halogen atom. A hydrogen atom or a monovalent R 1Q (R 1Q represents a hydrogen atom, which may have a substituent—a 6-alkyl group or an acyl group), R 9 represents a hydrogen atom, and n represents 0; 3] The compound as described;
〔11〕 R1(}が、 (1)水素原子、 (2)ピリジルで置換されていてもよい C — 6アルキ ル基または(3)ハロゲン原子で置換された C t一 6アルキルスルホニルを、 R 16が、 (1)水素原子、 (2)ァセチルァミノ基で置換されたフエニル、 (S Ci— 6アルキル スルホニル基、 (ii)ピリジルカルポエルまたは(iii)スルファモイルー Ci-eアル キル基から選ばれる置換基でモノまたはジ置換されていてもよいァミノ、 (4)ピリ ジルまたは (5)ハロゲン原子を示す前記 〔10〕 記載の化合物; [11] R 1 () is (1) a hydrogen atom, (2) a C— 6 alkyl group optionally substituted with pyridyl, or (3) a Ct- 6 alkylsulfonyl substituted with a halogen atom, R 16 is selected from (1) hydrogen atom, (2) phenyl substituted by acetylamino, (S Ci- 6 alkylsulfonyl group, (ii) pyridyl carpoel or (iii) sulfamoyl-Ci-e alkyl group The compound of the above-mentioned [10], which represents an amino which may be mono- or di-substituted by a substituent, (4) a pyridyl or (5) a halogen atom;
〔12〕 前記 〔3〕 記載の化合物のプロドラッグ; [12] A prodrug of the compound according to [3];
〔13〕 式 (13) Expression
〔式中、 R17は置換基を有していてもよいビニル基またはァリル基を示す〕 で表 される部分構造を有する化合物またはその塩と式 [Wherein, R 17 represents a vinyl group or an aryl group which may have a substituent] or a compound having a partial structure represented by the formula:
R1 - CN R 1 -CN
〔式中、 R1は前記 〔2〕 記載と同意義を示す〕 で表される化合物またはその塩と を反応させることを特徴とする式 [Wherein R 1 has the same meaning as described in the above [2]] or a salt thereof.
〔式中、 R1は前記と同意義を示す〕 で表される部分構造を有する化合物またはそ の塩の製造法; Wherein R 1 is as defined above; or a method for producing a compound having a partial structure represented by the formula:
〔14〕 式 (14) Expression
〔式中、 各記号は前記 〔3〕 記載と同意義を示す〕 で表される化合物またはその塩 と式 R1— CN [Wherein each symbol is as defined in the above [3]] or a salt thereof and a compound represented by the formula R 1 — CN
〔式中、 R1は前記 〔3〕 記載と同意義を示す〕 で表される化合物またはその塩と を反応させることを特徴とする前記 〔3〕 記載の化合物の製造法; 〔15〕 式 [Wherein, R 1 has the same meaning as described in the above [3].] Or a salt thereof, the method for producing the compound according to the above [3]; (15) Expression
〔式中、 ニニ二は、 単結合または二重結合を示す〕 で表される部分構造を有する化 合物 (以下、 化合物 (A— 1) と略記する場合がある) またはその塩を含有してな る医薬組成物; [Wherein, ninini represents a single bond or a double bond] (hereinafter sometimes abbreviated as compound (A-1)) or a salt thereof. A pharmaceutical composition;
〔16〕 式 (16) Expression
〔式中、 R2,、 R3,、 R6'および R7,はそれぞれ 6アルキル基を、 R16'は水素 原子、 置換基を有していてもよい〇6_14ァリール基、 置換基を有していてもよい アミノ基、置換基を有していてもよい複素環基またはハロゲン原子を示す〕で表さ れる部分構造を有する化合物またはその塩を含有してなる医薬組成物; Wherein, R 2 ,, R 3 ,, R 6 ' and R 7, respectively, a 6 alkyl group, R 16' is hydrogen atom, which may have a substituent 〇 6 _ 14 Ariru group, a substituted An amino group which may have a group, a heterocyclic group which may have a substituent or a halogen atom], or a salt thereof.
〔17〕 前記〔3〕記載の化合物またはその塩あるいはそのプロドラッグを含有し てなる医薬組成物; [17] a pharmaceutical composition comprising the compound of the above-mentioned [3], a salt thereof, or a prodrug thereof;
〔18〕 式 (18) Expression
(A-2)(A-2)
〔式中、 は、 単結合または二重結合を示す〕 で表される部分構造を有する化 合物 (以下、 化合物 (A— 2 ) と略記する塲合がある) またはその塩を含有してな るホスホジエステラーゼ IV阻害剤; [In the formula, represents a single bond or a double bond] (hereinafter, there is a compound abbreviated as compound (A-2)) or a salt thereof. Phosphodiesterase IV inhibitors;
〔1 9〕 式 (19) Expression
〔式中、 JI は、 単結合または二重結合を示す〕 で表される部分構造を有する化 合物またはその塩を含有してなる炎症性疾患、 喘息、 慢性閉塞性肺疾患、 慢性関節 リウマチ、 自己免疫疾患、 うつ病、 アルツハイマー型痴呆症、 記憶障害、 糖尿病ま たは動脈硬化の予防 ·治療剤; [Wherein, JI represents a single bond or a double bond] .Inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis containing a compound having a partial structure represented by Prophylactic / therapeutic agents for autoimmune diseases, depression, Alzheimer's dementia, memory impairment, diabetes or arteriosclerosis;
〔2 0〕 ホスホジエステラーゼ IV阻害剤である前記 〔1 5〕 ないし 〔1 7〕 記載 の医薬組成物; [20] the pharmaceutical composition of the above-mentioned [15] to [17], which is a phosphodiesterase IV inhibitor;
〔2 1〕炎症性疾患、喘息、慢性閉塞性肺疾患、慢性関節リウマチ、 自己免疫疾患、 うつ病、 アルツハイマー型痴呆症、 記憶障害、 糖尿病または動脈硬化の予防,治療 剤である前記 〔1 5〕 ないし 〔1 7〕 記載の医薬組成物; [21] The above-mentioned [15] which is an agent for preventing or treating inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, Alzheimer's dementia, memory disorder, diabetes or arteriosclerosis. Or the pharmaceutical composition of [17];
〔2 2〕 哺乳動物に対して式 [22] Formula for mammals
〔式中、 は、 単結合または二重結合を示す〕 で表される部分構造を有する化 合物またはその塩の有効量を投与することを特徴とするホスホジエステラーゼ IV 阻害方法; [Wherein represents a single bond or a double bond] a method for inhibiting phosphodiesterase IV, which comprises administering an effective amount of a compound having a partial structure represented by the following formula or a salt thereof:
〔2 3〕 哺乳動物に対して式 ' [23] Formula for mammals '
〔式中、 R2'、 R3,、 R6'および R7'はそれぞれ C ^6アルキル基を、 R16,は水素 原子、 置換基を有していてもよい C6_14ァリール基、 置換基を有していてもよい アミノ基、置換基を有していてもよい複素環基またはハ'ロゲン原子を示す〕で表さ れる部分構造を有する化合物またはその塩の有効量を投与することを特徴とする ホスホジエステラーゼ IV阻害方法; Wherein, R 2 ', R 3 ,, R 6' and R 7 'is a C ^ 6 alkyl groups, respectively, R 16, are hydrogen atoms, which may have a substituent C 6 _ 14 Ariru group Represents an amino group which may have a substituent, a heterocyclic group which may have a substituent or a halogen atom), or an effective amount of a salt thereof. A method for inhibiting phosphodiesterase IV;
〔24〕 哺乳動物に対して式 [24] Formula for mammals
〔式中、 ニニ二は、 単結合または二重結合を示す〕 で表される部分構造を有する化 合物またはその塩の有効量を投与することを特徴とする炎症性疾患、喘息、慢性閉 塞性肺疾患、慢性関節リウマチ、自己免疫疾患、うつ病、アルッ八イマ一型痴呆症、 記憶障害、 糖尿病または動脈硬化の予防 ·治療方法; (Wherein, ninii represents a single bond or a double bond), characterized by administering an effective amount of a compound having a partial structure represented by Prevention and treatment of obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, dementia of aruhaimai type, memory impairment, diabetes or arteriosclerosis;
〔25〕 哺乳動物に対して式 [25] Formula for mammals
〔式中、 R 2,、 R 3,、 R 6,および R 7'はそれぞれ — 6アルキル基を、 R 1 6,は水素 原子、 置換基を有していてもよい C 6 1 4ァリ一ル基、 置換基を有していてもよい アミノ基、置換基を有していてもよい複素環基またはハロゲン原子を示す〕で表さ れる部分構造を有する化合物またはその塩の有効量を投与することを特徴とする 炎症性疾患、喘息、慢性閉塞性肺疾患、慢性関節リウマチ、自己免疫疾患、うつ病、 アルツハイマー型痴呆症、 記憶障害、 糖尿病または動脈硬化の予防■治療方法;[Wherein R 2 , R 3 , R 6 , and R 7 ′ are each —6 alkyl groups, R 16 is a hydrogen atom, and a C 6 14 aryl group which may have a substituent. An aryl group, an amino group which may have a substituent, a heterocyclic group which may have a substituent or a halogen atom) or a salt thereof. Administering inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, Alzheimer's dementia, memory impairment, diabetes or arteriosclerosis;
〔2 6〕 ホスホジエステラーゼ IV阻害剤を製造するための式 [26] Formula for producing phosphodiesterase IV inhibitor
〔式中、 ^ は、 単結合または二重結合を示す〕 で表される部分構造を有する化 合物またはその塩の使用; [In the formula, ^ represents a single bond or a double bond] Use of a compound having a partial structure represented by the following formula or a salt thereof;
〔2 7〕炎症性疾患、喘息、慢性閉塞性肺疾患、慢性関節リウマチ、自己免疫疾患、 うつ病、 アルツハイマー型痴呆症、 記憶障害、 糖尿病または動脈硬化の予防 '治療 剤を製造するための式 (27) Formula for producing a therapeutic agent for preventing inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, Alzheimer's dementia, memory disorder, diabetes or arteriosclerosis
(A-2)(A-2)
〔式中、 ^ Zは、 単結合または二重結合を示す〕 で表される部分構造を有する化 合物またはその塩の使用; [In the formula, ^ Z represents a single bond or a double bond] Use of a compound having a partial structure represented by the following formula or a salt thereof;
〔28〕 [28]
〔式中、 R2aおよび R3aはそれぞれ置換基を有していてもよい脂肪族炭化水素基 を、 R4aおよび R 5 aはそれぞれ水素原子または置換基を有していてもよい炭化水 素基を、 R6 aおよび R7aはそれぞれ水素原子または置換基を有していてもよい炭 化水素基を示し、 R6aと R7aは隣接する炭素原子と共に置換基を有していてもよ い 3ないし 8員環を形成してもよく、 R8aは (1) 水素原子、 (2) 置換基を有 していてもよい炭化水素基、 (3) ァシル基、 (4) 置換基を有していてもよい複 素環基、 (5) ハロゲン原子、 (6) -OR10a (R1Gaは、 水素原子、 置換基を 有していてもよい炭化水素基、ァシル基または置換基を有していてもよい複素環基 を示す) 、 (7) — SRlla (Rllaは、 水素原子、 置換基を有していてもよい炭 化水素基、 ァシル基または置換基を有していてもよい複素環基を示す) 、 (8) — S (O) R12a (R12aは、 置換基を有していてもよい炭化水素基または置換基を 有していてもよい複素環基を示す) 、 (9) 一 S (O) 2R13a (R13aは、 置換基 を有していてもよい炭ィ匕水素基または置換基を有していてもよい複素環基を示す) または(10) — NR14aR15a (R14aおよび R15aはそれぞれ水素原子、 置換基 を有していてもよい炭化水素基、ァシル基または置換基を有していてもよい複素環 基を示す) を、 ; R9aは水素原子、 置換基を有していてもよい炭化水素基、 ァシル 基または置換基を有していてもよい水酸基を示す〕 で表される化合物またはその 塩;などに関する。 · [Wherein, R 2a and an R 3a are each an aliphatic substituted hydrocarbon group, R 4a and R 5 a may hydrocarbons which also each have a hydrogen atom or a substituent group, R 6 a and R 7a each represents a hydrogen atom or an optionally substituted carbon hydrocarbon radical, R 6a and R 7a are optionally substituted with adjacent carbon atoms R 8a may form a (1) hydrogen atom, (2) a hydrocarbon group which may have a substituent, (3) an acyl group, or (4) a substituent. (5) a halogen atom, (6) -OR 10a (R 1Ga represents a hydrogen atom, an optionally substituted hydrocarbon group, an acyl group or a substituent. shows also heterocyclic group optionally having), (7) - SR lla (R lla is hydrogen atom, which may have a substituent charcoal hydrocarbon group, a Ashiru group or substituent ) Shows a heterocyclic group which may have (8) - S (O) R 12a (R 12a is may have may have a substituent hydrocarbon group or an optionally substituted heterocyclic Represents a cyclic group), (9) one S (O) 2 R 13a (R 13a represents a hydrogen atom which may have a substituent or a heterocyclic group which may have a substituent; Or (10) — NR 14a R 15a (R 14a and R 15a are each a hydrogen atom, a hydrocarbon group which may have a substituent, an acyl group or a heterocyclic group which may have a substituent.) R 9a represents a hydrogen atom, a hydrocarbon group which may have a substituent, an acyl group or a hydroxyl group which may have a substituent] or a salt thereof; And so on. ·
さらに、 本発明は、 〔2 9〕 式 Further, the present invention provides (29) Expression
〔式中、 A環、 B環および C環はそれぞれ置換基を有していてもよい。 〕 で表わさ れる化合物またはその塩; [In the formula, ring A, ring B and ring C may each have a substituent. Or a salt thereof;
〔3 0〕 A環、 B環および C環の置換基が、 (1) 置換基を有していてもよい炭化 水素基、 (2) 置換基を有していてもよい複素環基、 (3)置換基を有していてもよ ぃァミノ基、 (4) ァシル基、 (5) 置換基を有していてもよい水酸基、 (6) 置換 基を有していてもよいスルフエニル基、 (7)ハロゲン原子、 (8) 低級アルキレン ジォキシ基、 (9) ニトロ基、 (10) シァノ基、 (11) 置換基を有していてもよい イミノ基、 (12) ォキソ基、 (13) 置換基を有していてもよいウレイド基、 (14) アジド基、 (15) 置換基を有していてもよいアミジノ基、 (16) 置換基を有してい てもよぃグァニジノ基、 (17)置換基を有していてもよいヒドラジノ基および(18) ォキシド基から成る群から選ばれる 1ないし 5個の置換基である前記〔2 9〕記載 の化合物; (30) The substituents on ring A, ring B and ring C are (1) a hydrocarbon group which may have a substituent, (2) a heterocyclic group which may have a substituent, 3) an amino group which may have a substituent, (4) an acyl group, (5) a hydroxyl group which may have a substituent, (6) a sulfenyl group which may have a substituent, (7) halogen atom, (8) lower alkylene dioxy group, (9) nitro group, (10) cyano group, (11) imino group which may have a substituent, (12) oxo group, (13) A ureido group which may have a substituent, (14) an azide group, (15) an amidino group which may have a substituent, (16) a guanidino group which may have a substituent, ( 17) The compound according to the above [29], wherein the compound is 1-5 substituents selected from the group consisting of a hydrazino group which may have a substituent and (18) an oxoxide group;
〔3 1〕 置換基が置換基 A群から選ばれる基である前記 〔2 9〕 記載の化合物; 〔3 23 化合物 (A— 1 ) が、 式 [31] the compound of the above-mentioned [29], wherein the substituent is a group selected from substituent group A; [323 compound (A-1) is a compound of the formula:
〔式中、 - - -は単結合または二重結合を、 A環、 B環および C環はそれぞれ置換 基を有していてもよい。 〕 で表される化合物 (以下、 化合物 (1— 1 ) と略記する 場合がある) である前記 〔1 5〕 記載の医薬組成物; [In the formula,---may have a single bond or a double bond, and ring A, ring B and ring C may each have a substituent. (Hereinafter may be abbreviated as compound (1-1)), wherein the pharmaceutical composition according to the above [15],
〔3 3〕 化合物 (A— 1 ) が、 式 ( - 1)[33] Compound (A-1) has the formula (-1)
〔式中、 記号は前記 〔3〕 記載と同意義を示す〕 で表される化合物 (以下、 化合物 ( - 1) と略記する場合がある) である前記 〔15〕 記載の医薬組成物を提供 する。 [Wherein the symbols have the same meanings as described in the above [3]] (hereinafter sometimes abbreviated as compound (-1)). I do.
さらに、 化合物 (A) 、 (.1)、 (Γ) 、 (Α— 1) 、 (1— 1)、 (I,一 1) 、 (A-2) またはその塩が構造中に不斉炭素を含有する場合、光学活性体およびラ セミ体の何れも本発明の範囲に含まれ、 化合物 (A) 、 (I) 、 (Γ) 、 (A- 1) 、 (1 - 1) , (1,ー 1) 、 (A— 2) またはその塩は水和物、 無水物のど ちらであってもよい。 Further, the compound (A), (.1), (Γ), (Α-1), (1-1), (I, 1-1), (A-2) or a salt thereof has an asymmetric carbon in the structure. When included, both optically active forms and racemic forms are included in the scope of the present invention, and the compounds (A), (I), (Γ), (A-1), (1-1), (1 , ー 1), (A-2) or salts thereof may be either hydrates or anhydrides.
本発明の化合物は、 式 The compounds of the present invention have the formula
で表される部分構造を有し、 具体的には、 式 Having a partial structure represented by the formula:
〔式中、 各記号は前記と同意義を示す〕 で表される。 本発明の化合物の分子量は約 Wherein each symbol is as defined above. The molecular weight of the compounds of the invention is about
1000以下、好ましくは約 900以下、 より好ましくは約 800以下、 特に好ま しくは約 700以下である。 It is 1000 or less, preferably about 900 or less, more preferably about 800 or less, and particularly preferably about 700 or less.
上記式中、 A環、 B環および C環は、 置換可能な位置に置換可能な数の置換基を 有していてもよい。 In the above formula, ring A, ring B and ring C have a substitutable number of substituents at substitutable positions. You may have.
A環、 B環および C環の置換基としては、 それぞれ The substituents on the ring A, ring B and ring C are respectively
(1) 置換基を有していてもよい炭化水素基、 (1) a hydrocarbon group which may have a substituent,
(2) 置換基を有していてもよい複素環基、 (2) a heterocyclic group which may have a substituent,
(3) 置換基を有していてもよいアミノ基、 (3) an amino group which may have a substituent,
(4) ァシル基、 (4) an acyl group,
(5) 置換基を有していてもよい水酸基、 (5) a hydroxyl group which may have a substituent,
(6) 置換基を有していてもよいスルフエニル基、 (6) a sulfenyl group which may have a substituent,
(7) ハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ素) 、 (7) halogen atoms (eg, fluorine, chlorine, bromine, iodine),
(8) 低級アルキレンジォキシ基 (例えば、 メチレンジォキシ、 エチレンジォキシ などの〇 3アルキレンジォキシ基など) 、 (8) lower alkylenedioxy O carboxymethyl group (e.g., Mechirenjiokishi, etc. 〇 3 alkylenedioxy O alkoxy groups such Echirenjiokishi)
(9) 二卜口基、 (9) Motoki Nitoguchi,
(10) シァノ基、 (10) a cyano group,
(11) 置換基を有していてもよいイミノ基、 (11) an imino group which may have a substituent,
(12) ォキソ基、 (12) an oxo group,
(13) 置換基を有していてもよいウレイド基、 (13) an ureido group which may have a substituent,
(14) アジド基、 (14) an azide group,
(15) 置換基を有していてもよいアミジノ基、 (15) an amidino group which may have a substituent,
(16) 置換基を有していてもよいグァニジノ基、 (16) a guanidino group which may have a substituent,
(17) 置換基を有していてもよいヒドラジノ基、 (17) a hydrazino group which may have a substituent,
(18) ォキシド基などが用いられる。 (18) An oxide group or the like is used.
A環、 B環および C環の置換基として用いられる 「置換基を有していてもよい炭 化水素基」 の炭化水素基としては、 例えば、 アルキル基、 アルケニル基、 アルキニ ル基、 シクロアルキル基、 シクロアルケニル基、 ァリール基、 ァラルキル基などの 鎖状または環状炭化水素基が用いられ、なかでも炭素数 1ないし 1 6個の鎖状(直 鎖状あるいは分枝状) または環状炭化水素基(例、 芳香族炭化水素基、 脂肪族環状 炭化水素基) などが好ましい。 具体的には、 以下のものが用いられる。 Examples of the “optionally substituted hydrocarbon group” used as a substituent on the ring A, ring B and ring C include, for example, an alkyl group, an alkenyl group, an alkynyl group, and a cycloalkyl group. A chain or cyclic hydrocarbon group such as a cycloalkenyl group, an aryl group or an aralkyl group is used. Among them, a linear (branched or branched) or cyclic hydrocarbon group having 1 to 16 carbon atoms is used. (Eg, aromatic hydrocarbon group, aliphatic cyclic hydrocarbon group) and the like. Specifically, the following are used.
( 1 ) 鎖状炭化水素基: (1) Chain hydrocarbon group:
a ) アルキル基 [好ましくは、 低級アルキル基 (例えば、 メチル、 ェチル、 プロピ ル、イソプロピル、ブチル、イソブチル、 sec—ブチル、 ter t—ブチル、ペンチル、 へキシルなどの (^ー6アルキル基など) ] 、 a) an alkyl group [preferably a lower alkyl group (eg, methyl, ethyl, propyl) Le, isopropyl, butyl, isobutyl, sec- butyl, ter t-butyl, pentyl, (such as ^ -6 alkyl group) such as cyclohexyl,
b ) アルケニル基 [好ましくは、 低級アルケニル基 (例えば、 ビニル、 ァリル、 ィ ソプロべニル、 2—ブテニル、 2—メチル— 2—プロぺニル、 4一ペンテニル、 5 一へキセニルなどの C 2_6アルケニル基など) ] 、 b) an alkenyl group [preferably a lower alkenyl group (for example, C 2 _ such as vinyl, aryl, isopropenyl, 2-butenyl, 2-methyl-2-propenyl, 4-pentenyl, 5-hexenyl and the like); 6 alkenyl groups)],
c ) アルキニル基 [好ましくは、 低級アルキニル基 (例えば、 プロパルギル、 ェチ ニル、 2—ブチェル、 2—へキシニルなどの C 2— 6アルキニル基など) ] c) alkynyl groups [preferably, lower alkynyl group (e.g., propargyl, E Ji sulfonyl, 2-Bucheru, C 2 such hexynyl to 2 - such as 6 alkynyl group)]
( 2 ) 脂肪族環状炭化水素基: (2) Aliphatic cyclic hydrocarbon group:
a ) シクロアルキル基 [好ましくは、 低級シクロアルキル基 (例えば、 シクロプロ ピル、 シクロブチル、 シクロペンチル、 シクロへキシルなどの c 3_6シクロアルキ ル基) であり、 ベンゼン環と縮合していてもよい] 、 a) cycloalkyl groups [preferably, a lower cycloalkyl group (e.g., Shikuropuro pills, cyclobutyl, cyclopentyl, c 3 _ 6 cycloalkyl Le group such as cyclohexyl), may be condensed with a benzene ring,
b ) シクロアルケニル基 [好ましくは、 低級シクロアルケニル基(例えば、 1ーシ クロプロぺニル、 1ーシクロブテニル、 1ーシクロペンテニル、 1ーシクロへキセ ニルなどの C 3_6シクロアルケニル基)であり、ベンゼン環と縮合していてもよい] ( 3 ) 芳香族炭化水素基: b) a cycloalkenyl group [preferably, a lower cycloalkenyl group (for example, 1 over sheet Kuropuro Bae cycloalkenyl, 1 Shikurobuteniru, -1-cyclopentenyl, C 3 _ 6 cycloalkenyl group such as xenon alkenyl to 1 Shikuro) benzene May be condensed with a ring]. (3) Aromatic hydrocarbon group:
ァリール基(例えば、フエニル、 1一ナフチル、 2—ナフチリレ、 1一アントリル、 2—アントリル、 9一アントリル、 1一フエナントリル、 2—フエナントリル、 3 一フエナントリル、 4 _フエナントリルまたは 9一フエナントリルなどの C 6_ 1 4 ァリール基など、 好ましくはフエニル基) Ariru group (e.g., phenyl, 1 one-naphthyl, 2-Nafuchirire, 1 one anthryl, 2-anthryl, 9 one anthryl, 1 one Fuenantoriru, 2 Fuenantoriru, three to Fuenantoriru, C 6, such as 4 _ Fuenantoriru or 9 one Fuenantoriru such as _ 1 4 Ariru group, preferably a phenyl group)
( 4 ) ァラルキル基: (4) Aralkyl group:
低級ァラルキル基 (例えば、 ベンジル、 フエネチル、 ジフエ二ルメチル、 1ーナ フチルメチル、 2一ナフチルメチル、 2—フエネチル、 2 , 2ージフエニルェチル、 1一フエニルプロピル、 2—フエニルプロピル、 3—フエニルプロピル、 4一フエ ニルプチル、 5—フエ二ルペンチルなどのじ7_ 1 6ァラルキル基など、 好ましくは ベンジル基) 。 Lower aralkyl groups (e.g., benzyl, phenethyl, diphenylmethyl, 1-naphthylmethyl, 2-naphthylmethyl, 2-phenyl, 2,2-diphenylethyl, 1-phenylpropyl, 2-phenylpropyl, 3 - phenylpropyl, 4 one Hue Nirupuchiru, etc. Flip 7 _ 1 6 Ararukiru groups such as 5-phenylene Rupenchiru, preferably benzyl group).
これら炭化水素基の置換基としては、 例えば、 (1) ハロゲン原子 (例えば、 フ ッ素、 塩素、 臭素、 ヨウ素) 、 (2) 低級アルキレンジォキシ基 (例えば、 メチレ ンジォキシ、 エチレンジォキシなどの。 アルキレンジォキシ基など) 、 (3) ニトロ基、 (4)シァノ基、 (5)ハロゲン化されていてもよい低級アルキル基、 (6) Λロゲン化されていてもよい低級アルケニル基、 (7) ハロゲン化されていてもよ い低級アルキニル基、 (8) 低級シクロアルキル基 (例えば、 シクロプロピル、 シ クロブチル、シクロペンチル、シクロへキシルなどの C 3 _ 6シクロアルキル基など)、 (9) C 6— 1 4ァリ一ル基 (例、 フエニル、 2 —ナフチルなど) 、 (10) ハロゲン化 されていてもよい低級アルコキシ基、 (11)ハロゲン化されていてもよい低級アル キルチオ基、 (12) ヒドロキシ基、 (13) アミノ基、 (14) モノー低級アルキルァ ミノ基 (例、メチルァミノ、ェチルァミノ、プロピルアミノ、イソプロピルアミノ、 プチルァミノなどのモノー Cェ _ 6アルキルァミノ基など) 、 (15) モノー C 6一 1 4 ァリールアミノ基 (例、 フエニルァミノ、 2 —ナフチルァミノなど) 、 (16) ジ一 低級アルキルアミノ基(例、ジメチルァミノ、ジェチルァミノ、ジプロピルァミノ、 ジブチルァミノ、 ェチルメチルァミノなどのジー c i— 6アルキルァミノ基など) 、Examples of the substituent of these hydrocarbon groups include (1) a halogen atom (for example, fluorine, chlorine, bromine, and iodine), and (2) a lower alkylenedioxy group (for example, methylenedioxy, ethylenedioxy and the like). (3) nitro group, (4) cyano group, (5) lower alkyl group which may be halogenated, (6) Lower alkenyl group which may be halogenated, (7) lower alkynyl group which may be halogenated, (8) lower cycloalkyl group (for example, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, etc. C, such as 3 _ 6 cycloalkyl group), (9) C 6 - 1 4 § Li Ichiru group (e.g., phenyl, 2 - naphthyl), (10) optionally halogenated substituted lower alkoxy group, (11 ) Lower alkylthio group which may be halogenated, (12) hydroxy group, (13) amino group, (14) mono-lower alkylamino group (e.g., monoamino such as methylamino, ethylamino, propylamino, isopropylamino, butylamino, etc.) C, such as E _ 6 Arukiruamino group), (15) mono- C 6 one 1 4 Ariruamino group (eg, Fueniruamino, 2 - etc. Nafuchiruamino), (16) di-one lower A Kiruamino group (eg, Jimechiruamino, Jechiruamino, Jipuropiruamino, Jibuchiruamino, such as di-ci- 6 Arukiruamino groups such as E chill methyl § Mino),
(17) ジー C 6— 1 4ァリールアミノ基 (例、 ジフエエルァミノ、 ジ (2—ナフチル) ァミノなど) 、 (18) ァシル基、 (19) ァシルァミノ基、 (20) ァシルォキシ基、(17) G C 6 - 1 4 Ariruamino group (eg, Jifueeruamino, di (2-naphthyl) Amino etc.), (18) Ashiru group, (19) Ashiruamino group, (20) Ashiruokishi group,
(21) 4ないし 1 4員複素環基(好ましくは 4ないし 1 0員、 より好ましくは 4な いし 7員複素環、 特に好ましくは 5または 6員複素環基) (例、 4 _ピリジル、 2 一チェニル、 2 _フリル、 2 一チアゾリル、 3 一インドリル、 モルホリノ、 1ーピ ペラジニル、 ピペリジノ、 1—ピロリジニル、 2—イソインドリルなどの炭素原子 以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 4個のへテロ原子を 含有する 4ないし 1 4員、好ましくは 4ないし 7員、 より好ましくは 5または 6員 複素環基など) 、 (22) ホスホノ基、 (23) C 6— ァリールォキシ基 (例、 フェ ノキシ)、 (24) ジじュ アルコキシ一ホスホリル基 (例、ジメトキシホスホリル、 ジエトキシホスホリル) 、 (25) C 6— 1 4ァリールチオ基 (例、 フエ二ルチオ) 、 (26)ヒドラジノ基、 (27) イミノ基、 (28) ォキソ基 (ただし、 ォキソ基が炭化水 素基と結合してァシル基を作る場合を除く。 ) 、 (29) ウレイド基、 (30) C^— 6 ' アルキル—ウレイド基 (例、 メチルウレイド、 ェチルゥレイドなど) 、 (31) ジー 6アルキル—ゥレイド基 (例、 ジメチルウレイド、 ジェチルウレイドなど) 、 (32) ォキシド基、 (33) 前記 (1) 〜 (32) の基から選ばれる 2ないし 3個が結 合してできる基などからなる群(置換基 A群)から選ばれる 1ないし 5個、好まし くは 1ないし 3個が用いられる。 前記置換基 A群中の 「ハロゲン化されていてもよい低級アルキル基」 としては、 例えば、 1ないし 3個のハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ素) を 有していてもよい低級アルキル基 (例えば、 メチル、 ェチル、 プロピル、 イソプロ ピル、 ブチル、 イソブチル、 sec -プチル、 tert—ブチル、 ペンチル、 へキシルなど の (^ _ 6アルキル基など) などが用いられ、 具体例としては、 メチル、 クロロメチ ル、 ジフルォロメチル、 トリクロロメチル、 トリフルォロメチル、 ェテル、 2—ブ ロモェチル、 2 , 2 , 2—トリフルォロェチル、 プロピル、 3, 3 , 3—卜リフル ォロプロピル、 イソプロピル、 プチル、 4 , 4, 4一トリフルォロブチル、 イソブ チル、 sec—ブチル、 tert—ブチル、 ペンチル、 イソペンチル、 ネオペンチル、 5 , 5, 5—トリフルォロペンチル、 へキシル、 6 , 6, 6—トリフルォ口へキシルな どが挙げられる。 (21) 4- to 14-membered heterocyclic group (preferably 4- to 10-membered, more preferably 4- or 7-membered heterocyclic group, particularly preferably 5- or 6-membered heterocyclic group) (eg, 4-pyridyl, 2 1-Cenyl, 2-furyl, 2-thiazolyl, 3-indolyl, morpholino, 1-piperazinyl, piperidino, 1-pyrrolidinyl, 2-isoindolyl, etc., other than carbon, nitrogen, sulfur, oxygen, etc. 1 A 4- to 14-membered, preferably 4- to 7-membered, more preferably a 5- or 6-membered heterocyclic group containing from 4 to 4 heteroatoms), (22) a phosphono group, (23) a C 6 -aryloxy group (eg, Fe phenoxy), (24) Jiju alkoxy one phosphoryl group (e.g., dimethoxyphosphoryl, diethoxyphosphoryl), (25) C 6 - 1 4 Ariruchio group (e.g., phenylene thio), (26) hydrazino Base (. Except when making However, Ashiru group Okiso group bonded to a hydrocarbon group) (27) imino group, (28) Okiso group, (29) an ureido group, (30) C ^ - 6 ' alkyl —Ureido group (eg, methyl ureide, ethyl pereide, etc.), (31) di6-alkyl-pereide group (eg, dimethyl ureide, getyl ureide, etc.), (32) oxide group, (33) above (1) to (32) One to five, and preferably one to three, selected from the group consisting of a group formed by combining two to three groups selected from groups (substituent group A) is used. As the “optionally halogenated lower alkyl group” in the above-mentioned substituent group A, for example, a lower alkyl group optionally having 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) alkyl group (e.g., methyl, Echiru, propyl, isopropyl, butyl, isobutyl, sec - heptyl, tert- butyl, pentyl, etc. (^ _ 6 alkyl groups such as hexyl) and the like are used, as a specific example, Methyl, chloromethyl, difluoromethyl, trichloromethyl, trifluoromethyl, ether, 2-bromoethyl, 2,2,2-trifluoroethyl, propyl, 3,3,3-trifluorotrifluoropropyl, isopropyl, butyl, 4 , 4,4-Trifluorobutyl, isobutyl, sec-butyl, tert-butyl, pentyl, isopentyl, neope Chill, 5, 5, 5-triflate Ruo b hexyl pentyl to,, 6, 6, etc. hexyl and the like to 6 Torifuruo port.
前記置換基 A群中の「八ロゲン化されていてもよい低級アルケニル基」としては、 例えば、 1ないし 3個のハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ素) を 有していてもよい低級アルケニル基 (例えば、 ビニル、 ァリル、 イソプロべニル、 2—ブテニル、 2—メチルー 2 _プロぺニル、 4一ペンテニル、 5一へキセニルな どの C 2— 6アルケニル基) などが用いられる。 The “lower alkenyl group optionally octogenated” in the substituent group A may have, for example, 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) lower alkenyl groups (e.g., vinyl, Ariru, isoproterenol base alkenyl, 2-butenyl, 2-methyl-2 _ propenyl, 4 one-pentenyl, 5 one hexenyl such which C 2 - 6 alkenyl group) and the like.
前記置換基 A群中の「八ロゲン化されていてもよい低級アルキニル基」としては、 例えば、 1ないし 3個のハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ素) を 有していてもよい低級アルキニル基 (例えば、 プロパルギル、 ェチニル、 2—プチ エル、 2—へキシニルなどの C 2_ 6アルキニル基など) などが用いられる。 The “lower alkynyl group optionally octogenated” in the substituent group A may have, for example, 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) a lower alkynyl group (e.g., propargyl, Echiniru, 2-Petit El and C 2 _ 6 alkynyl group such as hexynyl to 2) and the like.
前記置換基 A群中の「ハロゲン化されていてもよい低級アルコキシ基」としては、 例えば、 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素) を有し ていてもよい低級アルコキシ基 (例えば、 メトキシ、 エトキシ、 プロボキシ、 イソ プロポキシ、 ブトキシ、 イソブトキシ、 sec—ブトキシ、 tert—ブトキシ、 ペンチ ルォキシ、 イソペンチルォキシ、 ネオペンチルォキシ、 へキシルォキシなどの C丄 _ 6アルコキシ基など) などが用いられ、 具体例としては、 メトキシ、 エトキシ、 プロポキシ、 イソプロポキシ、 ブトキシ、 イソブトキシ、 sec—ブトキシ、 tert— ブトキシ、 トリクロロメトキシ、 3, 3 , 3—トリフルォロプロポキシ、 4 , 4 , 4一トリフルォロブトキシ、 5 , 5 , 5—トリフルォロペンチルォキシ、 6, 6, 6—トリフルォ口へキシルォキシなどが用いられる。 Examples of the “optionally halogenated lower alkoxy group” in the above-mentioned substituent group A include, for example, lower optionally having 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) an alkoxy group (e.g., methoxy, ethoxy, Purobokishi, iso-propoxy, butoxy, isobutoxy, sec- butoxy, tert- butoxy, pentyl Ruokishi, isopentyl Ruo alkoxy, neopentyl Ruo alkoxy, to a C丄_ 6 alkoxy group such as Kishiruokishi Specific examples include methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, sec-butoxy, tert-butoxy, trichloromethoxy, 3,3,3-trifluoropropoxy, 4,4, 4 Trifluorobutoxy, 5, 5, 5—Trifluoropentyloxy, 6, 6 6-Trifluohexyloxy is used.
前記置換基 A群中の「ハロゲン化されていてもよい低級アルキルチオ基」 として は、 例えば、 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素) を 有していてもよい (^ - 6アルキルチオ基 (例えば、 メチルチオ、 ェチルチオ、 プロ ピルチオ、イソプロピルチオ、プチルチオ、イソブチルチオ、 sec-ブチルチオ、 ter t 一プチルチオ、 ペンチルチオ、 へキシルチオなどの C卜 6アルキルチオ基) などが 用いられ、 具体例としては、 メチルチオ、 ジフルォロメチルチオ、 トリフルォロメ チルチオ、 ェチルチオ、 プロピルチオ、 イソプロピルチオ、 プチルチオ、 4 , 4 , 4一トリフルォロブチルチオ、 ペンチルチオ、 へキシルチオなどが挙げられる。 前記置換基 A群中の 「ァシル基」 としては、 例えば、 ホルミル、 力ルポキシ、 力 ルバモイル、 (3 ^ 6アルキル—カルポニル (例、 ァセチル、 プロピオニルなど) 、As the “optionally halogenated lower alkylthio group” in the above-mentioned Substituent group A, for example, may have 1 to 3 halogen atoms (eg, fluorine, chlorine, bromine, iodine) ( ^ - 6 alkylthio group (e.g., methylthio, Echiruchio, pro Piruchio, isopropylthio, Puchiruchio, isobutylthio, sec- butylthio, ter t one Puchiruchio, pentylthio, cyclohexylthio C WINCH 6 alkylthio group such as to) and the like are used, specifically Examples thereof include methylthio, difluoromethylthio, trifluoromethylthio, ethylthio, propylthio, isopropylthio, butylthio, 4,4,4-trifluorobutylthio, pentylthio, hexylthio and the like. Examples of the "acyl group" include formyl, Alkoxy, force Rubamoiru, (3 ^ 6 alkyl - Karuponiru (eg, Asechiru, propionyl, etc.),
C 3_6シクロアルキル—カルポニル (例、 シクロペンチルカルポニル、 シクロへキ シルカルポニルなど)、 C丄— 6アルコキシ一力ルポニル (例、メトキシカルポニル、 Xトキシカルポニル、ィソプロポキシ力ルポニル、 t er t—ブトキシカルボニルなど)、 C 6 _ 1 4ァリール—カルポニル (例、 ベンゾィル、 2一ナフトイルなど) 、 C 7 _ 1 6 ァラルキル一力ルポニル(例、フエ二ルァセチル、 3—フエニルプロピオニルなど)、 C 6 _ 1 4ァリールォキシ一力ルポニル (例、 フエノキシ力ルポニル、 2—ナフチル ォキシカルポニルなど) 、 C 7 ^ 6ァラルキルォキシ一力ルポニル (例、 ベンジル ォキシカルボニル、 2—ナフチルメチルォキシカルポニルなど) 、 5または 6員複 素環カルボニル (例、 1一ピロリジニルカルポニル、 4ーピペリジルカルボニル、 1 -ピペラジニルカルポニル、 2—モルホリニルカルポニル、 4—ピリジルカルポ ニル、 3一チェ二ルカルポニル、 2—フリルカルボニル、 2一チアゾリルカルポ二 ルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3 個のへテロ原子を含有する 5または 6員複素環カルポニルなど) 、 モノー 6ァ ルキル一力ルバモイル (例、 メチルカルバモイル、 ェチルカルバモイルなど) 、 ジ 一 C 6アルキル一力ルバモイル (例、 ジメチルカルバモイル、 ジェチルカルバモ ィルなど) 、 C 6— 1 4ァリ一ルー力ルバモイル (例、 フエ二ルカルバモイル、 2— ナフチルカルバモイルなど) 、 5または 6員複素環力ルバモイル (例、 1一ピロリ ジニルカルバモイル、 4ーピベリジルカルバモイル、 1ーピペラジニルカルバモイ ル、 2一モルホリニルカルバモイル、 4一ピリジルカルバモイル、 3一チェ二ルカ ルバモイル、 2—フリル力ルバモイル、 2—チアゾリルカルバモイルなどの炭素原 子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子 を含有する 5または 6員複素環力ルバモイルなど) 、 (^_6アルキルーチォカルボ ニル (例、 メチルチオカルポニルなど) 、 じ3_6シクロアルキルーチォカルポニル (例、 シク口ペンチルチオ力ルポニル、 シクロへキシルチオカルポニルなど) 、 C ト6アルコキシーチォカルポニル (例、 メトキシチォ力ルポニル、 エトキシチ才力 ルポニル、 プロポキシチォ力ルポニル、 ブトキシチォカルボニルなど) 、 c 6_14 ァリール—チォカルポニル (例、 フエ二ルチオカルボニル、 2一ナフチルチオカル ポニルなど) 、 c 7_1 6ァラルキルーチォカルボニル (例、 ベンジルチオ力ルポ二 ル、 フエネチルチオカルボエルなど) 、 C 6— 1 4ァリールォキシーチォカルボニルC 3 _ 6 cycloalkyl - Karuponiru (e.g., cyclopentyl Luca Lupo, cycloalkenyl, cycloheteroalkyl, etc. keys Shirukaruponiru), C丄- 6 alkoxy Ichiriki Ruponiru (e.g., methoxy Cal Poni le, X Tokishikaruponiru, Isopuropokishi force Ruponiru, t er t-butoxycarbonyl etc.), C 6 _ 1 4 Ariru - Karuponiru (eg, Benzoiru and 2 one naphthoyl), C 7 _ 1 6 Ararukiru Ichiriki Ruponiru (eg, phenylene Ruasechiru, 3-phenylpropyl propionyl, etc.), C 6 _ 1 4 Aryloxy-one-strand (eg, phenoxy-th, 2-naphthyl-thoxyl-ponyl), C 7 ^ 6 Arar-l-oxy-strand-thruponyl (eg, benzyloxy-carbonyl, 2-naphthylmethyloxy-thyl), 5- or 6-membered Ring carbonyl (e.g., 1-pyrrolidinylcarbonyl, 4-piperidylcarbonyl, 1 -From carbon atoms such as piperazinylcarbonyl, 2-morpholinylcarbonyl, 4-pyridylcarbonyl, 3-phenylcarbonyl, 2-furylcarbonyl, 2-thiazolylcarbonyl, nitrogen, sulfur, oxygen, etc. chosen such 1 to 3 for 5 or 6-membered heterocyclic ring Karuponiru containing heteroatoms are) mono- 6 § alkyl Ichiriki Rubamoiru (e.g., methylcarbamoyl, etc. E Ji carbamoyl), di one C 6 alkyl Ichiriki Rubamoiru (eg, dimethylcarbamoyl, etc. Jechirukarubamo I le), C 6 - 1 4 § Li one Roux force Rubamoiru (e.g., Hue carbamoylmethyl, 2-naphthylcarbamoyl etc.), 5- or 6-membered heterocyclic ring force Rubamoiru (eg, 1 one Pyrrolidinylcarbamoyl, 4-piberidylcarbamoyl, 1-piperazinylcarbamoy Selected from nitrogen atoms, sulfur atoms, oxygen atoms, etc., in addition to carbon atoms such as 1, 2-morpholinylcarbamoyl, 4-pyridylcarbamoyl, 3-chlorocarbamoyl, 2-furyl-rubamoyl, 2-thiazolylcarbamoyl, etc. is a 5- or 6-membered heterocyclic force Rubamoiru containing 1 to heteroatoms 3 of the) (^ _ 6 alkyl chromatography Chio carboxymethyl sulfonyl (e.g., methyl thio Cal Poni Le), Ji 3 _ 6 cycloalkyl over Chio local Poni Le ( E.g., pentyl thiol carbonyl, cyclohexyl thiocarbonyl, etc., C 6 alkoxy-thio carbonyl (e.g., methoxy thiol, ethoxy luponyl, propoxy thiol, butoxy carbonyl, etc.), c 6 _ 14 Aryl-thiocarbonyl (eg, phenylthiocarbonyl, 21-naphthylthiocarbonyl Etc.), c 7 _ 1 6 § Lal kills over Chio carbonyl (e.g., benzylthio force Lupo two Le, Hue phenethyl Lucio carbonitrile El, etc.), C 6 - 1 4 § reel O Kishi Chio carbonyl
(例、 フエノキシチォカルポニル、 2一ナフチルォキシチ才力ルポニルなど) 、 C 7 _ 1 6ァラルキルォキシ—チォカルボニル (例、 ベンジルォキシチ才力ルポニル、 2—ナフチルメチルォキシチ才力ルポニルなど)、 5または 6員複素環チォカルボ ニル (例、 1 _ピロリジニルチオ力ルポニル、 4―ピペリジルチオ力ルポニル、 1 一ピペラジニルチオ力ルポニル、 2—モルホリニルチオ力ルポニル、 4—ピリジル チォカルボニル、 3一チェ二ルチオ力ルポニル、 2—フリルチォカルポニル、 2— チアゾリルチオカルボニルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等 から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカル ポニルなど)、チォカルバモイル、モノ— アルキル一チォカルバモイル (例、 メチルチオ力ルバモイル、 ェチルチオ力ルバモイルなど) 、 ジ—C eアルキル一 チォカルバモイル (例えば、 ジメチルチオ力ルバモイル、 ジェチルチオ力ルバモイ ルなど)、 C 6— 1 4ァリール一チォカルバモイル (例、 フエ二ルチオ力ルバモイル、 2—ナフチルチオ力ルバモイルなど)、 5または 6員複素環チォカルバモイル (例、 2—ピロリジニルチオ力ルバモイル、 4ーピペリジルチオ力ルバモイル、 2—ピぺ ラジニルチオ力ルバモイル、 2一モルホリニルチオ力ルバモイル、 4一ピリジルチ 才力ルバモイル、 3一チェ二ルチオ力ルバモイル、 2—フリルチォカルバモイル、 2—チアゾリルチオ力ルバモイルなどの炭素原子以外に窒素原子、硫黄原子、酸素 原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チ 才力ルバモイルなど) 、 スルファモイル、 モノー C i— 6アルキルースルファモイル (例、 メチルスルファモイル、 ェチルスルファモイルなど) 、 ジー ^— 6アルキル ースルファモイル (例、ジメチルスルファモイル、ジェチルスルファモイルなど)、(Eg, phenoxyethanol Chio Cal Poni le, etc. 2 one Nafuchiruokishichi Sairyoku Ruponiru), C 7 _ 1 6 Ararukiruokishi - Chio carbonyl (e.g., Benjiruokishichi Sairyoku Ruponiru, 2-naphthylmethyl O carboxymethyl like Chi Sairyoku Ruponiru), 5 or 6-membered heterocyclic thiocarbonyl (e.g., 1-pyrrolidinyl thiol propyl, 4-piperidyl thiol, 1-piperazinyl thiol, 2-morpholinyl thiol, 4-pyridyl thiol, 3-pyridyl thiol, 3 5- or 6-membered heterocyclic thiocarbonyl containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as 2-furylthiocarbonyl and 2-thiazolylthiocarbonyl ), Thiocarbamoyl, mono-alkyl-thiocarbamoyl (eg, methyl thiocarbayl) Yl, etc. Echiruchio force Rubamoiru), di -C e alkyl one Chiokarubamoiru (e.g., dimethylthio force Rubamoiru, etc. Jechiruchio force Rubamoi Le), C 6 - 1 4 Ariru one Chiokarubamoiru (eg, phenylene Lucio force Rubamoiru, 2- 5- or 6-membered heterocyclic thiocarbamoyl (e.g., 2-pyrrolidinylthio-potassium, 2-piperidylthio-potassium, 2-piperazinyl-thio-potsubamoyl, 2-morpholinyl-thio-potsubamoyl, 4-pyridylthio-potassium) Containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon atoms such as 3-chlorothiocarbamoyl, 2-furylthiocarbamoyl, 2-thiazolylthiocarbamoyl, etc. 5 Or 6-membered heterocyclic ring Sairyoku etc. Rubamoiru), sulfamoyl, mono- C i-6 alkyl loose sulfamoyl (e.g., methylsulfamoyl, etc. E chill sulfamoyl), G ^ - 6 alkyl Surufamoiru (e.g., dimethylsulfamoyl, Jefferies chill sulfamoyl Such),
C6— 14ァリ一ルースルファモイル (例、 フェニルスルファモイルなど) 、 0:_6 アルキルスルホニル (例、 メチルスルホニル、 ェチルスルホニルなど) 、 C6_14 ァリールスルホニル (例、 フエニルスルホニル、 2一ナフチルスルホニルなど) 、 ( ト6アルキルスルフィニル (例、メチルスルフィニル、ェチルスルフィエルなど)、 C6— 14ァリールスルフィニル (例、 フエニルスルフィニル、 2一ナフチルスルフ ィニルなど) 、 スルフィノ、 スルホ、 C丄_6アルコキシスルフィニル (例、 メトキ シスルフィニル、 ェトキシスルフィニル) 、 じ6_14ァリールォキシスルフィニル (例、 フエノキシスルフィニル) 、 Ci-eアルコキシスルホニル (例、 メ卜キシス ルホニル、 ェトキシスルホニル) および C 6— 14ァリールォキシスルホニル (例、 フエノキシスルホニル) などが用いられる。 なかでも、 ホルミル、 力ルポキシ、 C i_6アルキル—力ルポニル、 C i_6アルコキシ一力ルポニル、 力ルバモイル、 モノ 一 C i _ 6アルキル力ルバモイル、 スルファモイル、 モノー。エ アルキル—スルフ ァモイルなどの ァシル基が好ましい。 C 6 — 14 arylsulfamoyl (eg, phenylsulfamoyl), 0 : _ 6 alkylsulfonyl (eg, methylsulfonyl, ethylsulfonyl, etc.), C 6 _ 14 arylsulfonyl (eg, phenyl) sulfonyl, such as 2 one-naphthylsulfonyl), (G 6 alkylsulfinyl (e.g., methylsulfinyl, etc. E chill sulfide El), C 6 - 14 § reel sulfinyl (e.g., Hue Nils sulfinyl, such as 2 one Nafuchirusurufu Iniru), sulfino, sulfo, C丄_ 6 alkoxysulfinyl sulfinyl (e.g., methoxide Shisurufiniru, e Toki cis sulfinyl), Ji 6 _ 14 § reel O carboxymethyl sulfinyl (e.g., full enoki cis sulfinyl), Ci-e alkoxy sulfonyl (e.g., main Bok Kishisu Ruhoniru , E butoxy-benzenesulfonyl) and C 6 - 14 § reel O carboxymethyl sulfonyl (e.g., Fueno Shisuruhoniru) and the like Among them, formyl, force Rupokishi, C i_ 6 alkyl -.. Force Ruponiru, C i_ 6 alkoxy Ichiriki Ruponiru force Rubamoiru, mono one C i _ 6 alkyl force Rubamoiru, sulfamoyl, mono- et An acyl group such as alkyl-sulfamoyl is preferred.
前記置換基 A群中の 「ァシルァミノ基」 としては、 例えば、 ホルミルァミノ、 C ^ 6アルキル一力ルポキサミド (例、 ァセトアミド、 プロピオンアミドなど) 、 C 6— 14ァリール一力ルポキサミド (例、 ベンズアミド、 2—ナフチルカルポキサミ ドなど) 、 アルコキシ一力ルポキサミド (例、 メトキシカルボキサミド、 X トキシカルポキサミド、 イソプロポキシカルボキサミド、 tert—ブトキシカルポキ サミドなど) 、 C 6アルキルスルホニルァミノ (例、 メチルスルホニルァミノ、 ェチルスルホニルァミノなど) 、 ビス ((^— 6アルキルスルホニル) ァミノ (例、 ビス (メチルスルホニル) ァミノ、 ビス (エヂルスルホニル) アミノなど) 、 C6 —14ァリ一ルスルホニルァミノ (例、 フエニルスルホニルァミノ、 2—ナフチルス ルホニルァミノなど) などが用いられる。 なかでも、 ホルミルァミノ、 。ト 6アル キル—カルポキサミド、 (^_6アルコキシ一力ルポキサミド、 (^― 6アルキルスル ホニルァミノ、 ビス アルキルスルホニル) ァミノなどのじ ?ァシルアミ ノ基が好ましい。 前記置換基 A群中の 「ァシルォキシ基」 としては、 例えば、 C^— 6アルキル一力 ルポニルォキシ (例、 ァセチルォキシ、 プロピオニルォキシなど) 、 C 6一 1 4ァリ 一ルーカルポニルォキシ (例、 ベンゾィルォキシ、 2—ナフトイルォキシなど) 、 アルコキシ一力ルポ二ルォキシ (例、 メトキシカルポニルォキシ、 エトキシ 力ルポニルォキシ、イソプロポキシ力ルポニルォキシ、 ter t—ブトキシカルポニル ォキシなど) 、 モノー C i _ 6アルキル一力ルバモイルォキシ (例、 メチルカルバモ ィルォキシ、 ェチルカルバモイルォキシなど) 、 ジ一 アルキル一力ルバモイ ルォキシ (例、ジメチルカルバモイルォキシ、ジェチルカルバモイルォキシなど)、 C 6— 1 4ァリール一力ルバモイルォキシ (例、 フエ二ルカルバモイルォキシ、 2一 ナフチルカルバモイルォキシなど) 、 ニコチノィルォキシなどが用いられる。 なか でも、 ( 6アルキル一力ルポニルォキシ、 — 6アルコキシ一力ルポニルォキシ などの C 2 _ 7ァシルォキシ基が好ましい。 Said the "Ashiruamino group" in Substituent Group A, for example, Horumiruamino, C ^ 6 alkyl Ichiriki Rupokisamido (eg, Asetoamido and propionamide), C 6 - 14 Ariru Ichiriki Rupokisamido (e.g., benzamide, 2- naphthyl Cal poke Sami Donado), alkoxy Ichiriki Rupokisamido (e.g., methoxy carboxamide, X Toki deer Lupo alkylcarboxamide, isopropoxycarbonyl carboxamide, such as tert- Butokishikarupoki Samido), C 6 alkylsulfonyl § amino (e.g., methylsulfonyl § Mino, E such as chill sulfonyl § Mino), bis ((^ - 6 alkylsulfonyl) amino (e.g., bis (methylsulfonyl) amino, bis (Edjirusuruhoniru) amino etc.), C 6 - 14 § Li one Le sulfonyl § Mino (eg , Phenylsulfonylamino, 2-naphthylsulfonylamino Etc.) and the like Of these, Horumiruamino, DOO 6 Al kill -.. Karupokisamido, (^ _ 6 alkoxy Ichiriki Rupokisamido, (^ - 6 alkylsulfanyl Honiruamino, bis alkylsulfonyl) of Flip Ashiruami amino group such as Amino? preferable. Examples of the "Ashiruokishi group" in Substituent Group A, for example, C ^ - 6 alkyl Ichiriki Ruponiruokishi (eg, Asechiruokishi propionyloxy, etc. Ruo carboxymethyl), C 6 one 1 4 § Li one Luca Lupo sulfonyl O carboxymethyl (e.g., Benzoyloxy, 2-naphthoyloxy, etc.), alkoxy monopropyloxy (e.g., methoxycarboxy, ethoxypropyloxy, isopropoxyoxy, tert-butoxycarboxy), mono-Ci- 6 alkyl monorubamoyloxy (e.g. examples, Mechirukarubamo Iruokishi, E Ji carbamoyl O carboxymethyl, etc.), di-primary alkyl Ichiriki Rubamoi Ruokishi (eg, dimethylcarbamoyl O carboxymethyl, Jefferies Chi carbamoyl O carboxymethyl, etc.), C 6 - 1 4 Ariru Ichiriki Rubamoiruokishi (eg, phenylene Rucarbamoyloxy, 21-Nakhchi Such as carbamoyl O carboxymethyl), such as nicotinyl Noi Ruo alkoxy is used. Among, (6 alkyl Ichiriki Ruponiruokishi, - 6 C 2 _ 7 Ashiruokishi groups such as alkoxy Ichiriki Ruponiruokishi are preferred.
前記置換基 A群において、 前記 (1) 〜 (32) の基から選ばれる 2ないし 3個が 結合してできる基としては、 例えば、 In the above-mentioned Substituent group A, examples of the group formed by bonding two or three members selected from the groups (1) to (32) include, for example,
(33a)置換 (^_6アルキル基 [この アルキル基は、 シァノ、 力ルバモイル、 C(33a) substituted (^ _ 6 alkyl group [this alkyl group, Shiano force Rubamoiru, C
^ 6アルキル一力ルバモイル、 C i _ 6アルキル一力ルポニルォキシ、 。ト6アルコ キシ一力ルポ二ルー アルキル一力ルバモイル、 5または 6員複素環 (例、 ピ リジルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ない し 3個のへテロ原子を含有する 5または 6員複素環) 一じ 6アルキル—カルバモ ィル、 C! _ 6アルキルスルホニルァミノ、 C i— 6アルコキシ—力ルポニル、 カルボ キシなどから選ばれる置換基を有する] 、 ^ 6 Alkyl Lubamoyl, C i _ 6 Alkyl Lponyloxy,. Preparative 6 alkoxy Ichiriki Lupo two Lou alkyl Ichiriki Rubamoiru, 5 or 6-membered heterocyclic ring (e.g., nitrogen atom in addition to carbon atoms, such as pin lysyl, sulfur atom, to 1 selected from oxygen atom, such as 3 to the 5- or 6-membered heterocycle containing terror atom) 1-6 alkyl-carbamoyl, C! _ 6 having a substituent selected from alkylsulfonylamino, Ci- 6 alkoxy-carbonyl, carboxy and the like],
(33b) 置換 C 6— 1 4ァリール基 [この C 6一 1 4ァリール基は、 ァミノ、 ハロゲン化 されていてもよい C — 6アルキル—力ルポニルァミノ、 ウレイド、 6アルキル スルホニルァミノ、 ( C ^ eアルキル) ( C i— 6アルキルスルホニル) ァミノ、 —6アルコキシ一力ルポニル— アルキルァミノなどから選ばれる置換基を有 する] 、 (33b) substituted C 6 - 1 4 Ariru group [this C 6 one 1 4 Ariru groups, Amino, optionally halogenated C - 6 alkyl - force Ruponiruamino, ureido, alkyl Suruhoniruamino, (C ^ e alkyl) (C i-6 alkylsulfonyl) Amino, - 6 alkoxy Ichiriki Ruponiru - to have a substituent selected from such Arukiruamino,
(33c) ( 6アルコキシ _ C 6— 1 4ァリール— 6アルコキシ基、 (33c) ( 6 alkoxy _ C 6 — 14 aryl — 6 alkoxy group,
(33d) 置換基を有する炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から選ば れる 1ないし 4個のへテロ原子を含有する 5ないし 1 4員複素環基 [この複素環基 は、 ォキソ、 力ルポキシー アルキル、 (^-6アルキル一力ルポニルォキシ— C 6アルキル、 C 6アルキル、 C アルコキシ—力ルポ二ルー C 6アルキル、 Cト6アルキル一力ルバモイルー C t_6アルキルなどから選ばれる置換基を有す る] 、 (33d) a 5- to 14-membered heterocyclic group containing 1 to 4 hetero atoms selected from nitrogen, sulfur, oxygen and the like in addition to the carbon atom having a substituent [this heterocyclic group Is Okiso force Rupokishi alkyl, (^ -6 alkyl Ichiriki Ruponiruokishi - C 6 alkyl, C 6 alkyl, C alkoxy - force Lupo two Lou C 6 alkyl, such as C DOO 6 alkyl Ichiriki Rubamoiru C t _ 6 alkyl Selected substituents],
(33e)式— NR18R19で表わされる基 Formula (33e) — a group represented by NR 18 R 19
[R18および R19はそれぞれ(i) 5または 6員複素環 (例、 炭素原子以外に窒素原 子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5ま たは 6員複素環) 一 アルキル、 (iDCi— eアルコキシ一力ルポニル— アルキル、 (iii)ジーじ 6アルキルアミノーメチレンースルファモイルー アルキル、 (iv)力ルバモイルー C卜6アルキル、 (V)スルファモイル— 6アルキ ル、 (vi) C 6アルキルースルホニル、 (viOC -eアルコキシ—カルボニル、 (viii) ジ— C i_6アルコキシ一力ルポ二ルー C 2_6アルケニル、 (ix) 5または 6員複素環 基 (例、 炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から選ばれる 1ないし 3 個のへテロ原子を含有する 5または 6員複素環基) [この 5または 6員複素環基は、 ァミノ、 Ci— 6アルキル—カルボキサミド、 Ci— 6アルキル—スルホニルァミノな どから選ばれる置換基を有していてもよい]、 (X)ハロゲン化されていてもよい[R 18 and R 19 each represent (i) a 5- or 6-membered heterocyclic ring (eg, a 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom, etc., in addition to a carbon atom) Or 6-membered heterocycle) monoalkyl, (iDCi-ealkoxy mono-propionyl-alkyl), (iii) dialkyl 6- alkylamino-methylene-sulfamoyl-alkyl, (iv) di-rubmoyl-C 6- alkyl, (V) sulfamoyl - 6 alkyl le, (vi) C 6 alkyl chromatography alkylsulfonyl, (VIOC -e alkoxy - carbonyl, (viii) di - C i_ 6 alkoxy Ichiriki Lupo two Lou C 2 _ 6 alkenyl, (ix) 5 or 6-membered Heterocyclic group (e.g., a 5- or 6-membered heterocyclic group containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms) [This 5- or 6-membered heterocyclic group Is, amino, Ci- 6 alkyl-carboxamide, Ci- 6 alkyl-sulfonylamino, etc.), and (X) may be halogenated
_ 6アルキル—力ルポニル、 6アルキルチオ一 C — 6アルキル一力ルポニル、_ 6 alkyl-potassium, 6- alkylthio-C-- 6- alkyl-luponyl,
(xii)Cい 6アルキルスルフィニルー C卜6アルキル一力ルポニル、 (xiiOC^eT ルキルスルホニルー C 6アルキル一力ルポニル、(xiv)ァミノ一 C 6アルキル一 力ルポニル、 (XV)ハロゲン化されていてもよい アルキル一力ルポ二ルーアミ ノ― C 6アルキル一力ルポニル、 (xvi) C 6_14ァリ一ルーカルボニル、 (xvii)力 ルポキシー C6一 14ァリ一ルー力ルポニル、 (xvi ii) — 6アルキルでエステル化さ れていてもよいホスホノ—(^ アルキル一 C 6— 14ァリール—力ルポニル、 ( ix) アルコキシ一力ルポニルを有していてもよい 5または 6員複素環 (例、 炭素 原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原 子を含有する 5または 6員複素環) 一力ルポニル、 (XX) 5または 6員複素環 (例、 炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテ 口原子を含有する 5または 6員複素環) —C^eアルキル一力ルポニル、 (xxi)C6 _14ァリール一ォキシ一力ルポニル、 (xxii)力ルポキシー — 6アルキル、 (xxiii) 力ルバモイルなどを示す] 、 (xii) C Medicine 6 alkylsulfinyl Lou C Bok 6 alkyl Ichiriki Ruponiru, (xiiOC ^ eT Le kills sulfonyl over C 6 alkyl Ichiriki Ruponiru, (xiv) Amino one C 6 alkyl Ichiriki Ruponiru, are (XV) halide alkyl Ichiriki be Lupo two Ruami Bruno - C 6 alkyl Ichiriki Ruponiru, (xvi) C 6 _ 14 § Li one Roux carbonyl, (xvii) force Rupokishi C 6 one 14 § Li one Roux force Ruponiru, (xvi ii ) - 6 alkyl which may optionally be esterified with a phosphono - (^ alkyl one C 6 - 14 Ariru - power Ruponiru, (ix) alkoxy Ichiriki may 5 or 6 membered heterocyclic ring which may have a Ruponiru (eg , A 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to a carbon atom. For example, besides carbon atom, nitrogen atom, sulfur atom, oxygen atom 1 to 3 5 or 6-membered heterocyclic ring containing terrorist atom to the) -C ^ e alkyl Ichiriki Ruponiru, (xxi) C 6 _ 14 Ariru one Okishi Ichiriki Ruponiru selected from such, (xxii) Power Rupoxy — 6-alkyl, (xxiii) Indicates the power of Lubamoyle, etc.],
(33f)式— C〇_Ha 1 (Ha 1はハロゲン原子を示す) で表される基、 A group represented by the formula (33f) —C〇_Ha 1 (Ha 1 represents a halogen atom),
(33g)置換スルファモイル基 [このスルファモイル基は、 力ルバモイルー ァ ルキル、 5または 6員複素環—(^_6アルキルなどから選ばれる置換基を有する]、 (33h)式—C (=0) NR20R21で表わされる基 (33 g) substituted sulfamoyl group [this sulfamoyl group may force Rubamoiru § alkyl, 5 or 6-membered heterocycle - (with a substituent selected from such ^ _ 6 alkyl], (33h) formula -C (= 0) NR Group represented by 20 R 21
[R2Qおよび R21はそれぞれ(i) 5または 6員複素環 (例、 ピリジル、 イミダゾリ ルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3 個のへテロ原子を含有する 5または 6員複素環) —C^eアルキル、 (ii)カルポキ シ— — 6アルキル、 (i i i) Cレ6アルコキシ—力ルポ二ルー C 6アルキル、 (iv) ジ— Cェ _ 6アルキルァミノ— C卜 6アルキル、 (V)力ルバモイルー C 6アルキル、 (vi) アルキル力ルバモイル— — 6アルキル、 (vii) 5または 6員複素環[R 2Q and R 21 each represent (i) a 5- or 6-membered heterocyclic ring (eg, 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as pyridyl and imidazolyl) 5 or 6 membered heterocyclic ring containing) -C ^ e alkyl, (ii) Karupoki sheet - - 6 alkyl, (iii) C Les 6 alkoxy - force Lupo two Lou C 6 alkyl, (iv) di - C e _ 6- Alkylamino—C 6- Alkyl, (V) Alkyl C 6 Alkyl, (vi) Alkyl Rubamoyl—— 6 Alkyl, (vii) 5- or 6-membered Heterocycle
(例、 ピリジルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれ る 1ないし 3個のへテロ原子を含有する 5または 6員複素環) — アルキル力 ルバモイルー(^_6アルキル、 (viii) 5または 6員複素環 (例、 ピリジルなどの 炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテ 口原子を含有す §5または 6員複素環) 一アミノー アルキル、 (ix) スルフ ァモイルー C6_14ァリ一ルー 6アルキル、 (X) アルコキシを有してい てもよい C6— 14ァリール、 (xi) C i— 6アルキルでエステル化されていてもよいホ スホノ— C^eアルキル—C6_14ァリール、 (xii) 4ないし 10員複素環基(例、 炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテ 口原子を含有する 4ないし 10員複素環) [この 4ないし 10員複素環基は、ハロ ゲン原子、 アルキル、 ォキソなどから選ばれる置換基を 1ないし 2個有して いてもよい] 、 (xiii) C6— 14ァリ一ルー力ルバモイルー C卜 6アルキルなどを示 す。 ] 、 (Eg, nitrogen atom in addition to carbon atoms, such as pyridyl, sulfur atom, 5 or 6-membered heterocyclic ring containing hetero atoms to 1 Ru selected from oxygen atom, such as 3 to the) - alkyl force Rubamoiru (^ _ 6 alkyl , (Viii) 5- or 6-membered heterocyclic ring (eg, containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyridyl, etc. ring) Single-amino alkyl, (ix) Sulf Amoiru C 6 _ 14 § Li one Roux 6 alkyl, (X) which may have an alkoxy C 6 - 14 Ariru, esterified with (xi) C i-6 alkyl which may be e Suhono - C ^ e alkyl -C 6 _ 14 Ariru, (xii) 4 to 10-membered Hajime Tamaki (e.g., nitrogen atom in addition to carbon atom, a sulfur atom, to 1 selected from oxygen atom, etc. 4- to 10-membered heterocycle containing three heteroatoms) [this The 4- to 10-membered heterocyclic group may have one or two substituents selected from a halogen atom, alkyl, oxo, etc.], (xiii) C 6 — 14 arylene 6 alkyl, etc.],
(33i)ハロゲン化された C^— 6アルキルカルポキサミド (例、 2—クロロアセトァ ミド、 2, 2—ジクロロアセトアミド、 2, 2, 2—トリクロロアセトアミドなど) などが用いられる。 (33i) halogenated C ^ - 6 alkyl Cal poke Sami de (e.g., 2-Kuroroaseta bromide, 2, 2-dichloro-acetamide, 2, 2, 2-trichloro acetamide, etc.) and the like.
A環、 B環および C環の置換基として用いられる「置換基を有していてもよい複 素環基」 としては、 例えば、 炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から 選ばれるヘテロ原子を 1ないし 4個含む(好ましくは 1ないし 3個) 4ないし 1 4 員複素環基などが用いられ、 具体的には、 (a) 4ないし 1 4員芳香族複素環基、The `` optionally substituted heterocyclic group '' used as a substituent on the ring A, ring B and ring C includes, for example, nitrogen, sulfur, oxygen and the like in addition to carbon. A 4- to 14-membered heterocyclic group containing 1 to 4 (preferably 1 to 3) heteroatoms to be selected and the like are used. Specifically, (a) a 4- to 14-membered aromatic heterocyclic group,
(b) 4ないし 1 4員脂肪族複素環基、 (c) 4ないし 1 4員複素環とベンゼン環と の 2または 3環性縮合環基などが用いられる。 (b) 4- to 14-membered aliphatic heterocyclic group, (c) 2- or 3-cyclic fused ring group of 4- to 14-membered heterocyclic ring and benzene ring, etc. are used.
該 4ないし 1 4員芳香族複素環基としては、 例えば、 炭素原子以外に窒素原子、 硫黄原子、酸素原子等から選ばれるヘテロ原子を 1ないし 4個含む(好ましくは 1 ないし 3個) .4ないし 1 4員芳香族複素環基などが用いられ、 具体的には、 チオフ ェン、 フラン、 インドリジン、 ピロール、 イミダゾール、 トリァゾ一ル、 チアゾー ル、 才キサゾール、 ピラゾール、 ピリジン、 N—才キシド化ピリジン、 ピラジン、 ピリミジン、 ピリダジン、 プリン、 4 H—キノリジン、 ナフチリジン、 イソチアゾ ール、 イソォキサゾ一ル、 フラザンなどが挙げられる。 なかでも、 ピリジン、 チォ フェン、 フランなどが好ましく用いられる。 The 4- to 14-membered aromatic heterocyclic group includes, for example, 1 to 4 (preferably 1 to 3) heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom and the like in addition to a carbon atom. Or a 14-membered aromatic heterocyclic group or the like. Specific examples thereof include thiophene, furan, indolizine, pyrrole, imidazole, triazole, thiazole, thixazole, pyrazole, pyridine, and N-dioxide. Pyridine, pyrazine, pyrimidine, pyridazine, purine, 4H-quinolidine, naphthyridine, isothiazole, isoxazole, and furazane. Among them, pyridine, thiophene, furan and the like are preferably used.
該 4ないし 1 4員脂肪族複素環基としては、炭素原子以外に窒素原子、硫黄原子、 酸素原子等から選ばれるヘテロ原子を 1ないし 4個(好ましくは 1ないし 3個) を 含む 4ないし 1 4員脂肪族複素環基などが用いられ、 具体的には、 ピロリジン、 ピ ペリジン、 ピぺラジン、モルホリン、チオモルホリン、 1 , 2—ジヒドロピリジン、 ィミダゾリジンなどが挙げられる。 Examples of the 4- to 14-membered aliphatic heterocyclic group include 1 to 4 (preferably 1 to 3) heteroatoms selected from nitrogen, sulfur, and oxygen atoms in addition to carbon atoms. A 4-membered aliphatic heterocyclic group or the like is used, and specific examples include pyrrolidine, piperidine, piperazine, morpholine, thiomorpholine, 1,2-dihydropyridine, imidazolidine and the like.
該 4ないし 1 4員複素環とベンゼン環との 2または 3環性縮合環基としては、炭 素原子以外に窒素原子、硫黄原子、酸素原子から選ばれるヘテロ原子を 1ないし 4 個(好ましくは 1ないし 3個) を含む複素環とベンゼン環との 2または 3環性縮合 環基などが用いられ、 具体的には、 ベンゾ 〔b〕 チォフェン、 ベンゾフラン、 1 H 一べンズイミダゾ一ル、 ベンズォキサゾール、 ベンゾチアゾール、 1, 2 -べンズ イソチアゾール、 ナフト 〔2 , 3— b〕 チォフェン、 チアントレン、 キサンテン、 フエノキサチイン、 インドール、 イソインドール、 1 H—インダゾール、 イソキノ リン、 キノリン、 フタラジン、 キノキサリン、 キナゾリン、 シンノリン、 カルバゾ ール、 )3—力ルポリン、 フエナントリジン、 ァクリジン、 フエナジン、 フエノチア ジン、 フエノキサジン、 イソクロマン、 ジヒドロべンゾフランなどが挙げられる。 これら複素環基の置換基としては、 前記置換基 A群から選ばれる 1ないし 5個、 好ましくは 1ないし 3個が用いられる。 A環、 B環および C環の置換基として用いられる「置換基を有していてもよいァ ミノ基」 としては、 上記 「置換基を有していてもよい炭化水素基」 、 上記 「置換基 を有していてもよい複素環基」 、 置換基 A群中の 「ァシル基」 (この 「ァシル基」 は、 さらに置換基 A群から選ばれる 1ないし 5個、好ましくは 1ないし 3個の置換 基を有していてもよい)などから選ばれる置換基を 1ないし 2個有していてもよい アミノ基などが用いられる。 The bicyclic or tricyclic fused ring group of a 4- to 14-membered heterocyclic ring and a benzene ring may include, in addition to carbon atoms, 1 to 4 heteroatoms selected from nitrogen, sulfur and oxygen (preferably (1 to 3) and a bicyclic or tricyclic fused ring group of a benzene ring and a heterocyclic ring, such as benzo [b] thiophene, benzofuran, 1H-benzimidazole, and benzzo Xazole, benzothiazole, 1,2-benzisothiazole, naphtho [2,3-b] thiophene, thianthrene, xanthene, phenoxatiin, indole, isoindole, 1H-indazole, isoquinoline, quinoline, phthalazine, quinoxaline, Quinazoline, cinnoline, carbazole,) 3-caprolactin, phenanthridine, acridine, phenazine, hue Chia Jin, Fuenokisajin, isochroman, such as dihydro base Nzofuran and the like. As the substituent of these heterocyclic groups, 1 to 5, preferably 1 to 3 selected from the above-mentioned substituent group A are used. The “optionally substituted amino group” used as a substituent on the A ring, the B ring and the C ring includes the “optionally substituted hydrocarbon group” and the “optionally substituted hydrocarbon group”. A heterocyclic group which may have a group '', an `` acyl group '' in the substituent group A (the `` acyl group '' is 1 to 5, preferably 1 to 3, further selected from the substituent group A) And an amino group which may have one or two substituent (s) selected from the above.
A環、 B環および C環の置換基として用いられる 「ァシル基」 としては、 前記し た置換基 A群中の 「ァシル基」 と同様のものが用いられる。 この 「ァシル基」 は、 さらに置換基 A群から選ばれる 1ないし 5個、好ましくは 1ないし 3個の置換基を 有していてもよい。 As the “acyl group” used as a substituent of the ring A, ring B and ring C, those similar to the “acyl group” in the aforementioned substituent group A can be used. This “acyl group” may further have 1 to 5, preferably 1 to 3 substituents selected from substituent group A.
A環、 B環および C環の置換基として用いられる「置換基を有していてもよい水 酸基」 、 「置換基を有していてもよいスルフエニル基」 、 「置換基を有していても よいイミノ基」 、 「置換基を有していてもよいウレイド基」 、 「置換基を有してい てもよいアミジノ基」 、 「置換基を有していてもよいグァニジノ基」 および「置換 基を有していてもよいヒドラジノ基」 の置換基としては、 上記「置換基を有してい てもよい炭化水素基」 、 上記 「置換基を有していてもよい複素環基」 、 置換基 A群 中の 「ァシル基」 (この 「ァシル基」 は、 さらに置換基 A群から選ばれる 1ないし 5個、 好ましくは 1ないし 3個の置換基を有していてもよい) などが用いられる。 `` Hydroxy group optionally having substituent (s) '', `` Sulfenyl group optionally having substituent (s) '', and `` Having substituent (s) '' used as substituents of ring A, ring B and ring C An optionally substituted imino group ", an" optionally substituted ureido group ", an" optionally substituted amidino group ", a" optionally substituted guanidino group "and" Examples of the substituent of the “hydrazino group optionally having a substituent” include the above “hydrocarbon group optionally having a substituent”, the above “heterocyclic group optionally having a substituent”, The “acyl group” in the substituent group A (this “acyl group” may further have 1 to 5, preferably 1 to 3 substituents selected from the substituent group A) and the like Used.
A環、 B環および C環がそれぞれ置換基を有する化合物としては、 例えば、 式 Examples of the compound in which ring A, ring B and ring C each have a substituent include, for example,
〔式中、 R 1は水素原子、 置換基を有していてもよい炭化水素基または置換基を有 していてもよい複素環基を示す〕で表される部分構造を有する化合物、 より具体的 には、 式 [Wherein, R 1 represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent]. Typically, the expression
〔式中、 各記号は前記と同意義を示す〕 で表される化合物などが用いられる。 [Wherein each symbol has the same meaning as described above], and the like.
上記式中、 R1は (1) 水素原子、 (2) 置換基を有していてもよい炭化水素基 または (3) 置換基を有していてもよい複素環基を示す。 In the above formula, R 1 represents (1) a hydrogen atom, (2) a hydrocarbon group optionally having a substituent, or (3) a heterocyclic group optionally having a substituent.
R1で示される 「置換基を有していてもよい炭化水素基」 としては、 Α環の置換 基として例示した「置換基を有していてもよい炭化水素基」 と同様のものが用いら れる。 As the “optionally substituted hydrocarbon group” for R 1 , those similar to the “optionally substituted hydrocarbon group” exemplified as the substituent for the ring can be used. It is required.
R1で示される 「置換基を有していてもよい複素環基」 としては、 A環の置換基 として例示した「置換基を有していてもよい複素環基」と同様のものが用いられる。 As the `` heterocyclic group optionally having substituent (s) '' for R 1 , the same as the `` heterocyclic group optionally having substituent (s) '' exemplified as the substituent for the ring A is used. Can be
R1としては、 (1) 置換基を有していてもよい芳香族炭化水素基、 (2) 置換 基を有していてもよい複素環基、 (3)置換基を有していてもよい脂肪族環状炭化 水素基、 (4) 式一: L— Rl a 〔式中、 Lはメチレンまたはカルポニルを、 Rl aは 水素原子、置換基を有していてもよい芳香族基、置換基を有していてもよい水酸基 または置換基を有していてもよいアミノ基を示す〕で表わされる基などが好ましい。 また、 この 「置換基を有していてもよい芳香族炭化水素基」 および「置換基を有 していてもよい複素環基」 としては、 式 As R 1 , (1) an aromatic hydrocarbon group optionally having a substituent, (2) a heterocyclic group optionally having a substituent, (3) an optionally substituted substituent A good aliphatic cyclic hydrocarbon group, (4) Formula 1: L—R la wherein L is methylene or carbonyl, R la is a hydrogen atom, an aromatic group which may have a substituent, a substituent A hydroxyl group optionally having a substituent or an amino group optionally having a substituent]. The “aromatic hydrocarbon group optionally having substituent (s)” and the “heterocyclic group optionally having substituent (s)” are represented by the formula:
〔式中、 Rlbは水素原子、 置換基を有していてもよい炭化水素基または置換基を 有していてもよい複素環基を、 D環は置換基を有していてもよい芳香族炭化水素環 または置換基を有していてもよい複素環を、 Eは結合手、 メチレン、酸素原子、 酸 化されていてもよい硫黄原子、置換基を有していてもよい窒素原子または式— CS — O—、 一 CO— O—、 一 S— CO—、 一 (CH2) k— CO—、 一 NRlc— CO - (CH2) m -、 -NRlc-S02- (CH2) m -、 一 S〇2— NRlc - (CH2) m―、 一〇— CS—NRlc— (CH2) m -、 一 NRlc— CO - NRlc— (CH2) m—、 — NRlc_C〇一 CH2— (CH2) m-NRlc- 〔式中、 Rlcは水素原子、 置換基を有していてもよいアルキル基またはァシル基を、 kは 0または 1を、 mは 0ないし 3の整数を示す〕 で表される基、 式 [Wherein, R lb represents a hydrogen atom, a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent, and the ring D is an aromatic which may have a substituent. Group E is a bond, methylene, oxygen atom, acid Optionally substituted sulfur atom, optionally substituted nitrogen atom or formula —CS—O—, one CO—O—, one S—CO—, one (CH 2 ) k —CO—, one NR lc - CO - (CH 2 ) m -, -NR lc -S0 2 - (CH 2) m -, one S_〇 2 - NR lc - (CH 2 ) m -, one 〇- CS-NR lc - (CH 2 ) m- , one NR lc — CO-NR lc — (CH 2 ) m —, — NR lc _C〇 one CH 2 — (CH 2 ) m -NR lc-where R lc is a hydrogen atom An alkyl group or an acyl group which may have a substituent, k represents 0 or 1, and m represents an integer of 0 to 3.)
〔式中、 Ha 1はハロゲン原子を、 D環は前記と同意義を示す〕 で表される基など が好ましく用いられる。 [Wherein, Ha 1 represents a halogen atom, and ring D has the same meaning as described above].
R1の好ましい基である 「芳香族炭化水素基」 としては、 例えば、 炭素数 6ない し 14員の単環式あるいは縮合多環式芳香族炭化水素基 (C6_14ァリール基) な どが用いられる。 C6_14ァリール基としては、例えば、 フエニル、 1一ナフチル、 2—ナフチル、 1一アントリル、 2一アントリル、 9 _アントリル、 1一フエナン トリル、 2 _フエナントリル、 3—フエナントリル、 4一フエナントリル、 9—フ ェナントリルなどが用いられ、 なかでも、 フエニル、 1一ナフチル、 2一ナフチル などが好ましく、 特にフエニルなどが好適である。 The preferred groups for R 1 "aromatic hydrocarbon group", for example, etc. C 6 -C 14 membered monocyclic or condensed polycyclic aromatic hydrocarbon group (C 6 _ 14 Ariru group) Is used. The C 6 _ 14 Ariru group, e.g., phenyl, 1 one-naphthyl, 2-naphthyl, 1 one anthryl, 2 one anthryl, 9 _ anthryl, 1 one Fouesnant tolyl, 2 _ Fuenantoriru, 3 Fuenantoriru, 4 one Fuenantoriru, 9-phenanthryl and the like are used, and among them, phenyl, 1-naphthyl, 2-naphthyl and the like are preferable, and phenyl and the like are particularly preferable.
この「芳香族炭化水素基」 の置換基としては、 前記した置換基 A群から選ばれる 1ないし 5個、 好ましくは 1ないし 3個が用いられる。 これら置換基の中でも、 (1) ハロゲン原子、 As the substituent for the “aromatic hydrocarbon group”, 1 to 5, preferably 1 to 3 selected from the above-mentioned substituent group A is used. Among these substituents, (1) a halogen atom,
(2) ニトロ基、 (2) nitro group,
(3) 6アルキル基 (メチル、 イソプロピル、 tert—ブチルなど) (3) 6 alkyl groups (methyl, isopropyl, tert-butyl, etc.)
[この (^— 6アルキル基は、 ハロゲン原子、 シァノ、 力ルバモイル、 6アルキ ルーカルパモイル、 C i _ 6アルキル一力ルポ二ルォキシ、 アルコキシ—カル ボニルー — 6アルキル一力ルバモイル、 5または 6員複素環 (例、 ピリジルなど の炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへ テロ原子を含有する 5または 6員複素環) -Cx_6アルキル一力ルバモイル、[The (^ -6 alkyl group is a halogen atom, cyano, carbamoyl, 6- alkaryl pamoyl, C i _ 6 alkyl monopropylamine, alkoxy-carbonyl- 6 alkyl monorubumoyl, 5- or 6-membered heterocycle (Eg, 1 to 3 carbon atoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon such as pyridyl 5 or 6 membered heterocyclic ring) -C x _ 6 alkyl Ichiriki Rubamoiru containing hetero atoms,
—6アルキルスルホニルァミノ、 C ^6アルコキシ—力ルポニル、 カルポキシなどか ら選ばれる置換基を有していてもよい] 、 — Which may have a substituent selected from 6- alkylsulfonylamino, C ^ 6- alkoxy-carbonyl, carboxy, etc.],
(4) C3— 6シクロアルキル基 (例、 シクロへキシル) 、 (4) C 3 - 6 cycloalkyl group (e.g., cyclohexyl),
(5) C6— 14ァリ一ル基 (例、 フエニル) (5) C 6 - 14 § Li Ichiru group (e.g., phenyl)
[この C6— 14ァリール基は、ァミノ、力ルポキシ、 C — 6アルコキシ—力ルポニル、 カルパモイル、 モノ—またはジー C i _ 6アルキル力ルバモイル、 ホルミルァミノ、 ハロゲン原子またはカルボキシを有していてもよい アルキル—カルボニル ァミノ (例、ァセチルァミノ、プロピオニルァミノ、 トリフルォロアセチリレアミノ、 ビバロイルァミノ) 、 c6一 14ァリール一力ルポニルァミノ (例、 ベンゾィルアミ ノ) 、 (^_6アルコキシ—力ルポニルァミノ (例、 メトキシカルポニルァミノ) 、 ウレイド、 モノーまたはジー(: ェ アルキルウレイド、 6アルキルスルホニル ァミノ (例、 メチルスルホニルァミノ) 、 (C^eアルキル) (C 6アルキルス ルホニル) ァミノ (例、 メチル (メチルスルホニル) ァミノなど) 、 アル キル) (C ^6アルキル一力ルポニル) ァミノ (例、 メチル (ァセチル) ァミノな ど) 、 (: 6アルコキシ一力ルポニル—Ci— 6アルキルアミノ (例、 2—エ トキシ 力ルポ二ルー 2—プロピルァミノなど) 、 C7— 15ァラルキルォキシ—カルポニル ァミノ (例、 ベンジルォキシカルポニルァミノ) 、 C卜 6アルキル一力ルポニルァ ミノ— C , _ 6アルキル一力ルポニルァミノ (例、ァセチルァミノァセチルァミノ)、 ^— 6アルキルチオ一 6アルキル一力ルポニルァミノ (例、 メチルチオァセチ ルァミノ) 、 アルキルースルフィエル—Ci— 6アルキル一カルボニルァミノ[The C 6 - 14 Ariru groups, Amino, force Rupokishi, C - 6 alkoxy - force Ruponiru, Karupamoiru, mono - or di C i _ 6 alkyl force Rubamoiru, Horumiruamino may have a halogen atom or carboxy alkyl - carbonyl amino (eg, Asechiruamino, propionyl Rua Mino, triflumizole Ruo b acetylide relay amino, Bibaroiruamino), c 6 one 14 Ariru Ichiriki Ruponiruamino (eg, Benzoiruami Bruno), (^ _ 6 alkoxy - power Ruponiruamino (e.g., methoxy Karuponiruamino), ureido, mono- or di- (: e alkylureido, 6 alkylsulfonyl amino (e.g., methylsulfonyl § Mino), (C ^ e alkyl) (C 6 Arukirusu Ruhoniru) amino (e.g., methyl (methylsulfonyl) Amino, etc.), alkyl) (C ^ 6 alkyl Power Ruponiru) Amino etc. (e.g., methyl (Asechiru) Amino), (6 alkoxy Ichiriki Ruponiru -Ci- 6 alkylamino (e.g., 2-d butoxy force Lupo two Lu 2 Puropiruamino), C 7 - 15 Ararukiruokishi - Karuponiru amino (e.g., benzyl O carboxymethyl Cal Poni Rua amino), C WINCH 6 alkyl Ichiriki Ruponirua amino - C, _ 6 alkyl Ichiriki Ruponiruamino (eg, § cetyl § amino § cetyl § amino) ^ - 6 alkylthio one 6- alkyl-l-ponylamino (eg, methylthioacetylamino), alkyl-sulfiel-Ci- 6- alkyl-1-carbonylamino
(例、 メチルスルフィ二ルァセチルァミノ ) 、 Cュ _6アルキルースルホニルー C! 一 6アルキル—カルボニルアミノ (例、 メチルスルホニルァセチルァミノ) 、 C6一 14ァリールォキシ—力ルポニルァミノ (例、 フエノキシ力ルポニルァミノ) 、 ヒ ドロキシー Cェ _ 6アルキル―力ルバモイル (例、 ヒドロキシメチルカルバモイル、 ヒドロキシエヂルカルバモイル)などから選ばれる置換基を有していてもよく、特 にァミノ、 力ルポキシ、 アルコキシ一力ルポニル、 力ルバモイル、 モノーま たはジー(^_6アルキル力ルバモイル、 ホルミルァミノ、 八ロゲン原子またはカル ポキシを有していてもよい Ci_6アルキル一力ルポニルァミノ (例、 ァセチルアミ ノ、 プロピオニルァミノ、 トリフルォロアセチルァミノ、 ピバロィルァミノ) 、 C(Eg, Mechirusurufi two Ruasechiruamino), C Interview _ 6 alkyl chromatography alkylsulfonyl over C! One 6 alkyl - carbonylamino (e.g., methylsulfonyl § cetyl § Mino), C 6 one 14 Ariruokishi - Power Ruponiruamino (e.g., phenoxy force Ruponiruamino), human Dorokishi C E _ 6 alkyl - Power Rubamoiru (e.g., hydroxy methylcarbamoyl, hydroxy Edji carbamoyl) may have a substituent selected from such as Amino especially, the force Rupokishi, alkoxy Ichiriki Ruponiru force Rubamoiru, mono- or is G (^ _ 6 alkyl force Rubamoiru, Horumiruamino, eight androgenic Optionally having an atom or a carboxy group, Ci_ 6 alkyl monophenylamine (eg, acetylamino , Propionylamino, trifluoroacetylamino, pivaloylamino), C
^ 6アルコキシ一力ルポニルァミノ(例、メトキシカルポニルァミノ)、ウレイド、 C i _ 6アルキルスルホニルァミノ (例、 メチルスルホニルァミノ) 、 アル キル) ((^— 6アルキルスルホニル) ァミノ (例、 メチル (メチルスルホニル) ァ ミノなど) 、 (C 6アルキル) アルキル—力ルポニル) ァミノ (例、 メ チル (ァセチル) ァミノなど) 、 アルコキシ一力ルポ二ルー アルキル ァミノ (例、 2—エトキシカルボニル一 2—プロピルァミノなど) 、 C 7— 1 5ァラ ルキルォキシ一力ルポニルァミノ (例、 ベンジルォキシカルポニルァミノ) などか ら選ばれる置換基を有していてもよい] 、 ^ 6 alkoxy Ichiriki Ruponiruamino (e.g., methoxy Cal Poni Rua Mino), ureido, C i _ 6 alkylsulphonyl § amino (e.g., methylsulfonyl § Mino), Al kill) ((^ - 6 alkylsulfonyl) Amino (e.g., methyl (Methylsulfonyl) amino, etc.), (C 6 alkyl) alkyl-aminopropyl, amino (eg, methyl (acetyl) amino, etc.), alkoxy monoalkylamine (eg, 2-ethoxycarbonyl-12-) Puropiruamino etc.), C 7 - 1 5 § La Rukiruokishi Ichiriki Ruponiruamino (e.g., may have a benzyl O carboxymethyl Cal Poni Rua mino) such as pressurized al substituents selected,
(6) ハロゲン原子または — 6アルコキシ一 C 6 _ 1 4ァリ一ルを有していてもよい C i— 6アルコキシ基 (例、 メトキシ、 トリフルォロメトキシ、 イソプロボキシ、 2 - ( 4ーメトキシフエニル) エトキシなど) 、 (6) A halogen atom or a Ci- 6 alkoxy group which may have a —6 alkoxy-C 6 _ 14 aryl (eg, methoxy, trifluoromethoxy, isopropoxy, 2- (4-methoxy Phenyl) ethoxy)),
(7) C 6一 1 4ァリールォキシ基 (例、 フエノキシ) 、 (7) C 6 one 1 4 Ariruokishi group (e.g., phenoxy),
(8) 力ルバモイルを有していてもよい C — 6アルキルチオ基 (例、 メチルチオ、 力ルバモイルメチルチオ) 、 (8) C- 6 alkylthio group which may have carbamoyl (eg, methylthio, carbamoylmethylthio),
(9) カルパモイルを有していてもよい アルキルスルフィニル基 (例、 メチ ルスルフィニル、 力ルバモイルメチルスルフィニル) 、 (9) an alkylsulfinyl group which may have a carpamoyl (eg, methylsulfinyl, carbamoylmethylsulfinyl),
(10) C 6— 1 4ァリ一ルチオ基 (例、 フエ二ルチオ) 、 (10) C 6 - 1 4 § Li one thio group (e.g., phenylene thio)
(11) ヒドロキシ基、 (11) a hydroxy group,
(12) 炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 4個 のへテロ原子を含有する 4ないし 1 4員複素環基(例、ピロリジ.二ル、ピペリジル、 イソインドリル、 フリル、 チェニル、 ピリジル、 キノリル、 ベンゾフラエル、 ピリ ミジニル、 テトラゾリル、 イミダゾリジニル、 イソチアゾリジニル、 チアジアゾリ ジニル、 ァゼチニルなど) (12) 4- to 14-membered heterocyclic group containing 1 to 4 heteroatoms selected from nitrogen, sulfur, oxygen and the like in addition to carbon atoms (eg, pyrrolidinyl, piperidyl, isoindolyl, (Furyl, chenyl, pyridyl, quinolyl, benzofurale, pyrimidinyl, tetrazolyl, imidazolidinyl, isothiazolidinyl, thiadiazolidinyl, azethinyl, etc.)
[この複素環基は、 才キソ、 カルボキシー アルキル、 アルキル一力ノレ ボニルォキシ— C i _ 6アルキル、 (: 6アルキル、 C i— 6アルコキシ—カルポニル — アルキル、 C x _ 6アルコキシ一力ルポニル、 力ルバモイル— C — 6アルキ ル、 C x _ 6アルキル—力ルバモイルー C i _ 6アルキルなどから選ばれる置換基を有 していてもよい] 、 (13)カルポキシ基、 [The heterocyclic group is old Kiso, Karubokishi alkyl, alkyl Ichiriki Honoré Boniruokishi - C i _ 6 alkyl, (6 alkyl, C i-6 alkoxy - Karuponiru - alkyl, C x _ 6 alkoxy Ichiriki Ruponiru force Rubamoiru - C - 6 alkyl Le, C x _ 6 alkyl - may have a force Rubamoiru C i _ 6 substituents selected from an alkyl, (13) a carboxy group,
(14)式— CO— Ha 1 (Ha 1はハロゲン原子を示す) で表される基(例、 クロ口 ホルミル) 、 A group represented by the formula (14) —CO—Ha 1 (where Ha 1 represents a halogen atom) (eg, formyl chloromethyl),
(15) — 6アルキル一力ルポニル基 (例、 ァセチルなど) 、 (15) — 6-alkyl monopropanol group (eg, acetyl, etc.),
(16) アルキルースルホニル基 (例、 メチルスルホニルなど) 、 (16) alkyl-sulfonyl group (eg, methylsulfonyl, etc.),
(17) C ^6アルコキシ一カルボニル基 (例、 メトキシカルボニルなど) 、 (17) C ^ 6 alkoxy monocarbonyl group (eg, methoxycarbonyl etc.),
(18)スルファモイル基 (18) Sulfamoyl group
[このスルファモイル基は、 (^_6アルキル、 力ルバモイルー C卜 6アルキル、 C, —6アルコキシ一力ルポニル— d_6アルキル、ォキソ基を有していてもよい 5ない し 7員複素環基 (例、 ピリジル、 ピロリジニル、 へキサヒドロアゼピエルなどの炭 素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ 原子を含有する 5ないし 7員複素環基) — ^― 6アルキル、 (^_6アルキル—カル ポニルァミノ— ( 6_14ァリールなどから選ばれる置換基を 1または 2個有してい てもよい] 、 [The sulfamoyl group, (_ 6 alkyl, force Rubamoiru C Bok 6 alkyl, C, ^ - 6 alkoxy Ichiriki Ruponiru - d_ 6 alkyl, 5 to may have Okiso group 7-membered Hajime Tamaki ( Example: 5- to 7-membered heterocyclic group containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyridyl, pyrrolidinyl, hexahydroazepier) — ^ - 6 alkyl, (^ _ 6 alkyl - which may have 1 or 2 substituents selected from such (6 _ 14 Ariru], - Cal Poniruamino
(19)式一 される基 (19) Formula 1 Group
[Raおよび Rbはそれぞれ(i)水素原子、 (iO ^-eアルキル、 (iii) 5または 6員 複素環(例、 ピリジルなどの炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から 選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環) — レ6アル キル、 (iv) 6アルコキシ—力ルポニル— 6アルキル、 (V)ジ— アルキ ルァミノーメチレンースルファモイルー — 6アルキル、 (vi)力ルバモイルー — 6アルキル、 (vii)スルファモイルー 6アルキル、 (viii) Ci— 6アルキルース ルホニル、 (ix) — 6アルコキシ一力ルポニル、 (X)ジ— アルコキシ一力ルポ ニル— C2一 6アルケニソレ、(xi)C6— 14ァリール、 (xii) 5または 6員複素環基(例、 ピリジルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1な いし 3個のへテロ原子を含有する 5または 6員複素環基) [この 5または 6員複素 環基は、 ァミノ、 アルキル—カルポキサミド、 6アルキル—スルホニル ァミノなどから選ばれる置換基を有していてもよい]、 (xiii)ハロゲン化されてい てもよい アルキル—力ルポニル、 (xiv)^— 6アルキルチオ一 アルキル 一力ルポニル、 (XV) Cト 6アルキルスルフィニルー C 6アルキル一力ルポニル、 (xvi) C 6アルキルスルホ二ルー C ^6アルキル一力ルポニル、 (xv i i)アミノー C !― 6アルキル—カルボニル、(xvi i i)ハロゲン化されていてもよい C i— 6アルキル— 力ルポ二ルーァミノ— ^ アルキル一力ルポニル、 (xix)C6_14ァリール—カル ポニル、 (XX)力ルポキシ—じ6-14ァリール一力ルポニル、 (xxi) 6アルキルで エステル化されていてもよいホスホノ— Ci_6アルキル一 C6_14ァリール一カル ポニル、 (xxii)ハロゲン原子、 ォキソまたは アルコキシ—力ルポニルを有し ていてもよい 5または 6員複素環(例、 ピロリジニル、 ピリジルなどの炭素原子以 外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含 有する 5または 6員複素環) 一力ルポニル、 (xxii i) 5または 6員複素環 (例、 ピ リジルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ない し 3個のへテロ原子を含有する 5または 6員複素環) 一 (^_6アルキル一力ルポ二 ル、 fcdv)C6— 14ァリール一ォキシ一力ルポニル、 (XXV) 力ルポキシ— C — 6ァ ルキル、 (xxvi)力ルバモイル、 (xxvii)ハロゲン化されていてもよい アルキ ルカルバモイル、 (xxviii) C丄 アルキル一カルボニルァミノを有していてもよ い C6_14ァリールカルバモイル、 (xxix) 5または 6員複素環 (例、 ピリジルな どの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個の ヘテロ原子を含有する 5または 6員複素環) 一力ルバモイル、 (XXX) C2_6アル ケニルー力ルポニル、 (XXX i)ォキソ基を有していてもよい 5または 6員複素環(例、 ピロリジニルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環) —ァミノ— Cト 6アル キル—力ルポニル、 (xxxii) (ォキソ基を有していてもよい 5または 6員複素環 (例、 ピロリジニルなどの炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から選 ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環) ) — 6アル キル) アミノー( 6アルキル—力ルポニル、 (xxxiii) (ォキソ基を有していて もよい 5または 6員複素環(例、 ピロリジニルなどの炭素原子以外に窒素原子、 硫 黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6 員複素環)) (C 6アルキル力ルポニル)アミノー Ci-sアルキル—カルボニル、[R a and R b each represent (i) a hydrogen atom, (iO ^ -e alkyl, (iii) a 5- or 6-membered heterocyclic ring (eg, a nitrogen atom, a sulfur atom, an oxygen atom, etc. selected 1 to 5 or 6-membered heterocyclic ring containing hetero atoms 3 of the being) - Les 6 Al kill, (iv) 6 alkoxy - power Ruponiru - 6 alkyl, (V) di - alkyl Rua plasminogen methylene chromatography sul Famo Ilu — 6- alkyl, (vi) Rubimoyl — 6- alkyl, (vii) Sulfamoyl- 6- alkyl, (viii) Ci- 6- alkylsulfonyl, (ix) — 6-alkoxy-low-proponyl, (X) Di-alkoxy-low-power-ponyl - C 2 one 6 Arukenisore, (xi) C 6 - 14 Ariru, a 1 to be chosen (xii) 5 or 6-membered Hajime Tamaki (e.g., nitrogen atom in addition to carbon atoms, such as pyridyl, sulfur atom, oxygen atom, etc. Chair 5 containing 5 heteroatoms 6-membered heterocyclic group) [this 5- or 6-membered heterocyclic group, Amino, alkyl - Karupokisamido, 6 alkyl - which may have a substituent group selected from a sulfonyl Amino] is (xiii) halide Tei be alkyl - power Ruponiru, (xiv) ^ - 6 alkylthio primary alkyl Ichiriki Ruponiru, (XV) C preparative 6 alkylsulfinyl Lou C 6 alkyl Ichiriki Ruponiru, (xvi) C 6 alkylsulfonyl C ^ 6 alkyl one-strand, (xv ii) amino-C! ― 6 alkyl-carbonyl, (xvi ii) optionally halogenated C i- 6 alkyl-potassium ruamino- ^ alkyl mono-potassium, (xix) C 6 _ 14 aryl-carbonyl, (XX) Rupokishi - Ji 6-14 Ariru Ichiriki Ruponiru, (xxi) 6 alkyl which may optionally be esterified phosphono - CI_ 6 alkyl one C 6 _ 14 Ariru one local Poniru, (xxii) a halogen atom, Okiso or alkoxy - power 5- or 6-membered heterocyclic ring optionally having luponyl (eg, containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyrrolidinyl, pyridyl, etc.) 5- or 6-membered heterocyclic ring One-strand ruponyl, (xxii i) 5- or 6-membered heterocyclic ring (eg, one or three selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyridyl) A heteroatom 5 or 6 membered heterocyclic ring) i (^ _ 6 alkyl Ichiriki Lupo two Le has, fcdv) C 6 - 14 Ariru one Okishi Ichiriki Ruponiru, (XXV) force Rupokishi - C - 6 § alkyl, (xxvi) force Rubamoiru , (xxvii) optionally halogenated good alkylcarbamoyl, (xxviii) C丄alkyl one carbonyl § Mino but it may also have a C 6 _ 14 § Lee carbamoyl, (xxix) 5 or 6-membered heterocyclic ring ( examples, nitrogen atom in addition to a pyridyl that any carbon atom, a sulfur atom, 1 selected from oxygen atom, etc. to three 5 or 6-membered heterocyclic ring containing a heteroatom) Ichiriki Rubamoiru, (XXX) C 2 _ 6 Al Kenyl-Ruponyl, (XXXi) 5- or 6-membered heterocyclic ring optionally having an oxo group (eg, 1 to 3 members selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyrrolidinyl) 5 or 6 members containing hetero atoms Elementary ring) —amino—C 6 alkyl—caprolponyl, (xxxii) (5- or 6-membered heterocyclic ring optionally having an oxo group (eg, a nitrogen atom, a sulfur atom, 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from oxygen atoms, etc.)) — 6 alkyl) amino- ( 6- alkyl-carbonyl), (xxxiii) (even if it has an oxo group Good 5- or 6-membered heterocycle (eg, a 5- or 6-membered heterocycle containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as pyrrolidinyl)) C 6 alkyl force ruponyl) amino-Cis-alkyl-carbonyl,
(xxx iv) Ci_6アルキルチオ一 6アルキルカルボニル(硫黄原子は酸化されて いてもよい) 、 (XXXV) 八ロゲン化されていてもよい アルキルスルホニル、 (xxxvi)スルファモイル、 (XXXV i i) Ca_ 6アルキルスルファモイルなどを示す]、 (20)式一 C (=0) NRcRdで表わされる基 (xxx iv) CI_ 6 alkylthio one 6 alkylcarbonyl (sulfur atom may be oxidized), (XXXV) eight halogenated which may be alkylsulfonyl, (xxxvi) sulfamoyl, (XXXV ii) C a _ 6 alkylsulfamoyl, etc.], (20) a group represented by the formula C (= 0) NR c R d
[Rcおよび Rdはそれぞれ(i)水素原子、 (i C^— 6アルキル、 (iii) 5または 6員 複素環 (例、 ピリジル、 イミダゾリルなどの炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素 環) 一 Ci— 6アルキル、 (iv)カルボキシー アルキル、 WCi— 6アルコキシ— カルボ二ルー C 6アルキル、 (vi)ジー C ^6アルキルアミノ一 C卜 6アルキル、 (vii)力ルバモイルー 6アルキル、 (viii) C 6アルキル力ルバモイル— Cェ _6アルキル、 (ix) 5または 6員複素環 (例、 ピリジルなどの炭素原子以外に窒 素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環) 一 C — 6アルキル力ルバモイルー C — 6アルキル、 (X) 5ま たは 6員複素環(例、 ピリジルなどの炭素原子以外に窒素原子、 硫黄原子、 酸素原 子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環)—ァ ミノ— C — 6アルキル、 (xi)スルファモイルー C6— 14ァリール—(: 6アルキル、 (xii) — 6アルコキシを有していてもよい C6— 14ァリール、 (xiii) C^— 6ァ ルキルでエステル化されていてもよいホスホノー C i _ 6アルキル— C 6 _ J 4ァリー ル、 (xiv) 4ないし 10員複素環基 (例、 ァゼチェル、 ピロリジニル、 ピベリジ レ、 へキサヒドロアゼピエル、 ピリジル、 ピリミジェル、 ピラジニル、 ピリダジニ ル、 1ーァザビシクロ [2. 2. 2] ォクト—3—ィルなどの炭素原子以外に窒素 原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 4 ないし 10員複素環) [この 4ないし 10員複素環基は、 ハロゲン原子、 ^— 6ァ ルキル、 ォキソなどから選ばれる置換基を 1ないし 2個有していてもよい] 、 (XV) 。6-14ァリール—力ルバモイルー — 6アルキル、 (xvi) ヒドロキシー C^— 6ァ ルキル、 (xvii) ォキソ基を有していてもよい 5または 6員複素環(例、 ピロリニ ジル、 ピリジルなどの炭素原子以外に窒素原子、 硫黄原子、酸素原子等から選ばれ る 1ないし 3個のへテロ原子を含有する 5または 6員複素環)一力ルバモイルー C —6アルキルなどを示す。 Rcとしては水素原子が好ましい。 ] 、 [Rc and R d are each (i) hydrogen atom, (i C ^ - 6 alkyl, (iii) 5 or 6-membered heterocyclic ring (e.g., pyridyl, nitrogen atom in addition to carbon atoms, such as imidazolyl, sulfur atom, an oxygen atom 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from the group consisting of: 1 Ci- 6 alkyl, (iv) carboxy-alkyl, WCi- 6 alkoxy-carbocarbonyl C 6 alkyl, (vi) G C ^ 6 alkylamino one C Bok 6 alkyl, (vii) force Rubamoiru 6 alkyl, (viii) C 6 alkyl force Rubamoiru - C E _ 6 alkyl, (ix) 5 or 6-membered heterocyclic ring (e.g., carbon, such as pyridyl A 5- or 6-membered heterocyclic ring containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to the atom) 1 C— 6 alkyl rubamoyl-C— 6 alkyl, (X) 5 Or 6-membered heterocycle (eg, charcoal such as pyridyl) Nitrogen atom besides atom, a sulfur atom, 5 or 6-membered heterocyclic ring containing hetero atoms to 1 selected from SansoHara child like to three of) - § amino - C - 6 alkyl, (xi) Surufamoiru C 6 — 14 aryl — (: 6 alkyl, (xii) — 6 alkoxy optionally having C 6 — 14 aryl, (xiii) C ^ — 6 phosphono optionally esterified with alkyl C i _ 6 Alkyl-C 6 _ J 4 aryl, (xiv) 4- to 10-membered heterocyclic group (e.g., azechel, pyrrolidinyl, piberidile, hexahydroazepier, pyridyl, pyrimigel, pyrazinyl, pyridazinyl, 1-azabicyclo [2. 2.2] 4- to 10-membered heterocycle containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as oct-3-yl The 10-membered heterocyclic group is halo Emissions atom, ^ - 6 § alkyl may have two, 1 to substituents selected from such Okiso], (XV) 6 -. 14 Ariru - Power Rubamoiru - 6 alkyl, (xvi) hydroxy-C ^ — 6- alkyl, (xvii) 5- or 6-membered heterocyclic ring which may have an oxo group (eg, selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyrrolidinyl, pyridyl, etc. 1 to 3 of 5 or 6 membered heterocyclic ring) Ichiriki containing heteroatoms Rubamoiru C - 6 alkyl shows the like. Rc is preferably a hydrogen atom. ],
(22)モノーまたはジー C 6アルキル力ルバモイルチオ基 (例、 ジメチルカルバモ ィルチオ) 、 (22) Mono- or di-C 6 alkyl rubamoylthio group (eg, dimethylcarbamo Iruchio),
(23)モノーまたはジー C^ -eアルキルチオ力ルバモイルォキシ基 (例、 ジメチルチ 才力ルバモイルォキシ) などが好ましい。 (23) Mono- or di-C ^ -ealkylthiolrubamoyloxy groups (eg, dimethylthiolrubamoyloxy) and the like are preferable.
R 1の好ましい基として示される 「複素環基」 としては、 ピリジル、 チェニル、 フリル、 イミダゾリル、 チアゾリル、 キノ.リル、 1, 2—ジヒドロピリジル、 ジヒ ドロベンゾフラニル、 ベンゾジォキソリル、 ベンゾチアゾリル、 ピペリジル、 ピぺ ラジニルなどが好ましく、 特にピリジル、 1, 2—ジヒドロピリジルなどが好適で ある。 Examples of the “heterocyclic group” represented as a preferable group of R 1 include pyridyl, phenyl, furyl, imidazolyl, thiazolyl, quinolyl, 1,2-dihydropyridyl, dihydrobenzofuranyl, benzodioxolyl, and benzothiazolyl. , Piperidyl, piperazinyl and the like are preferable, and pyridyl, 1,2-dihydropyridyl and the like are particularly preferable.
この 「複素環基」 の置換基としては、 As the substituent of the “heterocyclic group”,
(1) ハロゲン原子、 (1) a halogen atom,
(2) C i— 6アルキル基 (例、 メチル、 ェチルなど) (2) Ci- 6 alkyl group (eg, methyl, ethyl, etc.)
[このアルキルは、 力ルポキシ、 6アルコキシ、 アルコキシ—力ルポ二 ル、モノ一 C^— 6アルキルーァミノ、ジー — 6アルキルーァミノ、力ルバモイル、 ヒドロキシを有していてもよい アルキル—カルパモイル、 ォキソを有してい てもよい 4ないし 1 0員複素環基(例、 ピリジル、 キノリルなどの炭素原子以外に 窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有す る 4ないし 1 0員複素環基) 、 4ないし 1 0員複素環 (例、 ピリジル、 キノリルな どの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個の ヘテロ原子を含有する 4ないし 1 0員複素環) —力ルバモイル、力ルバモイルー C ト6アルキル一力ルバモイルなどから選ばれる置換基を有していてもよい][Wherein alkyl, force Rupokishi, 6 alkoxy, alkoxy - has Karupamoiru, a Okiso - force Lupo two Le, mono one C ^ - 6 Arukiruamino, di - 6 Arukiruamino force Rubamoiru, alkyl which may have hydroxy A 4- to 10-membered heterocyclic group (e.g., containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyridyl and quinolyl) 10-membered heterocyclic group), 4- to 10-membered heterocyclic ring (eg, containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as pyridyl and quinolyl) Or a 10-membered heterocyclic ring) —which may have a substituent selected from rubamoyl, rubamoyl-C 6 -alkyl monobutylammonium, etc.]
(3) (: 6アルコキシ基 (例、 メトキシ) 、 (3) (: 6 alkoxy groups (eg, methoxy),
(4) C 6— 1 4ァリール基 (例、 フエニル) 、 -(4) C 6 - 1 4 Ariru group (e.g., phenyl), -
(5) C 7— 1 6ァラルキル基 (例、 ベンジル) (5) C 7 — 16 aralkyl group (eg, benzyl)
[この C 7_ 1 6ァラルキルは、カルボキシ、 アルコキシ一カルボニル、 力ルバ モイル、 ヒドロキシを有していてもよい — 6アルキル一力ルバモイル、 4ないし 1 0員複素環 (例、 ピリジルなどの炭素原子以外に窒素原子、 硫黄原子、 酸素原子 等から選ばれる 1ないし 3個のへテロ原子を含有する 4ないし 1 0員複素環)—力 ルバモイルなどから選ばれる置換基を有していてもよい] 、 [The C 7 _ 1 6 Ararukiru is carboxy, alkoxy one carbonyl, force Luba moil, hydroxy may have - 6 alkyl Ichiriki Rubamoiru, 4 to 1 0-membered heterocyclic ring (e.g., carbon atoms, such as pyridyl A 4- to 10-membered heterocyclic ring containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc.) — Which may have a substituent selected from rubamoyl, etc.] ,
(6) 4ないし 1 0員複素環基 (例、 ピリジル、 キノリル、 イソキノリルなどの炭 素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ 原子を含有する 4ないし 1 0員複素環基) (6) 4- to 10-membered heterocyclic group (eg, charcoal such as pyridyl, quinolyl, isoquinolyl, etc.) 4- to 10-membered heterocyclic group containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc., in addition to elemental atoms)
[この 4ないし 1 0員複素環基は、 アルキル、 C^— 6アルコキシ—カルボ二 ル、 力ルバモイル、 ォキソ、 4ないし 1 0員複素環基 (例、 ピリジルなどの炭素原 子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子 を含有する 4ないし 1 0員複素環基) などから選ばれる置換基を有していてもよ い] 、 [This 4 to 1 0-membered heterocyclic group, alkyl, C ^ - 6 alkoxy - carbonylation Le force Rubamoiru, Okiso, 4 to 1 0-membered Hajime Tamaki (e.g., nitrogen atom besides carbon atom, such as pyridyl , A sulfur atom, a 4- to 10-membered heterocyclic group containing 1 to 3 hetero atoms selected from oxygen atoms, etc.), and the like.)
(7) ォキソ基、 (7) an oxo group,
(8) ォキシド基などから選ばれる 1ないし 5個、 好ましくは 1ないし 3個の置換 基が好ましい。 (8) One to five, preferably one to three substituents selected from an oxoxide group and the like are preferable.
R 1がォキシド基を有する複素環基としては、 例えば、 N—才キシド化ピリジル などが好ましい。 As the heterocyclic group in which R 1 has an oxoxide group, for example, N-aminopyridyl pyridyl and the like are preferable.
R 1の好ましい基として示される 「脂肪族環状炭化水素基」 としては、 例えば、 シクロプロピル、 シクロブチル、 シクロペンチル、 シクロへキシルなどの C 3_6シ ク口アルキル基などが用いられ、特にシクロペンチル、シク口へキシルが好ましい。 この 「脂肪族環状炭化水素基」 は前記した R 1で示される炭化水素基が有してい てもよい置換基と同様の置換基を有していてもよい。 "Aliphatic cyclic hydrocarbon group" represented as preferable groups for R 1, for example, cyclopropyl, cyclobutyl, cyclopentyl, C 3 _ 6 shea click port alkyl groups such as cyclohexyl may be used, in particular cyclopentyl, Cyclohexyl is preferred. This “aliphatic cyclic hydrocarbon group” may have the same substituent as the substituent that the hydrocarbon group represented by R 1 may have.
R 1の好ましい基として例示される 「置換基を有していてもよい芳香族炭化水素 基」 および 「置換基を有していてもよい複素環基」 としては、 式 Examples of the preferred group for R 1 include an “optionally substituted aromatic hydrocarbon group” and an “optionally substituted heterocyclic group”.
〔各記号は前記と同意義を示す〕 で表わされる基が好ましく用いられる。 [The symbols have the same meanings as described above] are preferably used.
R l bで示される 「置換基を有していてもよい炭化水素基」 としては、 A環の置 換基として例示した「置換基を有していてもよい炭ィ匕水素基」 と同様のものが用い られる。 なかでも、 The “optionally substituted hydrocarbon group” represented by R lb may be the same as the “optionally substituted optionally substituted hydrocarbon group” exemplified as the substituent for the ring A. Is used. Above all,
(1) C i— 6アルキル基 (メチル、 イソプロピル、 t er t—ブチルなど) (1) Ci- 6 alkyl group (methyl, isopropyl, tert-butyl, etc.)
[この アルキル基は、 ハロゲン原子、 シァノ、 ヒドロキシ、 C — 6アルコキ シ—力ルポニル、 ジ— C^eアルキルァミノ、 ハロゲン化されていてもよい — 6 アルキル—力ルポ二ルーアミノ、 力ルポキシ、 力ルバモイル、 C^-eアルキル一力 'ルバモイル、 C 6アルキル一カルボニルォキシ、 アルコキシ一カルポニル — アルキル—力ルバモイル、 5または 6員複素環 (例、 ピリジル、 イミダゾ リルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環) 一 C ^6アルキル一力ルバモイ ル、 アルキルチオ、 C 6アルキルスルフィエル、 — 6アルキルスルホ二 ルァミノ、 5または 6員複素環 (例、 ピリジルなどの炭素原子以外に窒素原子、 硫 黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6 員複素環) —C^eアルキル力ルバモイル、 5または 6員複素環 (例、 ピリジルな どの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個の ヘテロ原子を含有する 5または 6員複素環) —ァミノ、 スルファモイルー C6— 14 ァリール、 カルポキシ _C6_14ァリール、 — 6アルコキシ—カルポニル _C6— 4ァリール、 力ルバモイルー C6_14ァリール、 ヒドロキシを有していてもよい _6アルキル一力ルバモイル— C6_14ァリール、 4ないし 10員複素環 (例、 ピリ ジルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 4ないし 10員複素環) 一力ルバモイルー C6_14ァ リールなどから選ばれる置換基を有していてもよい] 、 [This alkyl group is a halogen atom, cyano, hydroxy, C- 6 alkoxy Sheet - Power Ruponiru, di - C ^ e Arukiruamino may be halogenated - 6 alkyl - force Lupo two Ruamino force Rupokishi force Rubamoiru, C ^ -e alkyl Ichiriki 'Rubamoiru, C 6 alkyl one Karuboniruo Xy, alkoxy-carbonyl-alkyl-alkanoyl, 5- or 6-membered heterocyclic ring (eg, 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyridyl, imidazolyl, etc.) A 5- or 6-membered heterocyclic ring containing) 1-C ^ 6- alkyl mono-rubbamoyl, alkylthio, C 6- alkylsulfiel, — 6-alkylsulfonylamino, 5- or 6-membered heterocyclic ring (eg other than carbon atoms such as pyridyl) A 5- or 6-membered heterocycle containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc.) Yl, 5- or 6-membered heterocycle (eg, 5- or 6-membered heterocycle containing 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as pyridyl) —amino Sulfamoyl C 6 — 14 aryls, carboxy _C 6 _ 14 aryls, — 6 alkoxy-carbonyl _C 6 — 4 aryls, power rubamoyl C 6 _ 14 aryles, optionally with hydroxy _ 6 alkyl mono-functional rubamoyl — C 6 _ 14 aryl, 4- to 10-membered heterocyclic ring (eg, 4- to 10-membered heterocyclic ring containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon such as pyridyl) ) may have a substituent selected from such as single force Rubamoiru C 6 _ 14 § reel,
(2) C3— 6シクロアルキル基 (例、 シクロへキシル) 、 (2) C 3 - 6 cycloalkyl group (e.g., cyclohexyl),
(3) C6— 14ァリール基 (例、 フエニル) (3) C 6 - 14 Ariru group (e.g., phenyl)
[この C6_14ァリール基は、 — 6アルコキシ (例、 メトキシ) ァミノ、 カルボ キシ、 ハロゲン化されていてもよい d— 6アルキル一力ルポニルァミノ (例、 ァセ チルァミノ、 トリフルォロアセチルァミノ) 、 C^-eアルコキシ—カルポニルアミ ノ (例、 メトキシカルポニルァミノ) 、 ホルミルァミノ、 ウレイド、 6アルキ ルスルホニルァミノ (例、 メチルスルホニルァミノ) 、 (Ci— 6アルキル) (d —6アルキルスルホニル) ァミノ (例、 メチル (メチルスルホニル) ァミノなど) 、 C 6アルコキシ—力ルポ二ルー C 6アルキルアミノ (例、 2—エトキシカルポ 二ルー 2—プロピルァミノなど) 、 C i一 6アルキルでエステル化されていてもよい ホスホノー〇,_6アルキル、モノ—またはジ— アルキル一力ルバモイル、 C7 _ 1 6ァラルキルォキシ一力ルポニルァミノ (例、ベンジルォキシカルポニルァミノ) などから選ばれる置換基を有していてもよい] または [The C 6 _ 14 Ariru groups, - 6 alkoxy (e.g., methoxy) Amino, carboxy, may be halogenated d-6 alkyl Ichiriki Ruponiruamino (eg, § Se Chiruamino, triflumizole Ruo b acetyl § Mino ), C ^ -e alkoxy - Karuponiruami Bruno (e.g., methoxy Cal Poni Rua Mino), Horumiruamino, ureido, 6 alkynyl Le sulfonyl § amino (e.g., methylsulfonyl § Mino), (CI- 6 alkyl) (d - 6 alkyl Sulfonyl) amino (eg, methyl (methylsulfonyl) amino, etc.), C 6 alkoxy-potassium C 6 alkylamino (eg, 2-ethoxycarbo 2-ru-propylamino, etc.), esterified with Ci 6 alkyl is optionally Hosuhono 〇, _ 6 alkyl, mono- - or di - alkyl Ichiriki Rubamoiru, C 7 _ 1 6 Ararukiruokishi Ichiriki Ruponiruamino (e.g., benzyl O carboxymethyl Cal Poni Rua mino) may have a substituent group selected from, etc.] or the
(4) C 2_6アルケニル基などが好ましい。 (4) A C 2 _ 6 alkenyl group is preferred.
R l bで示される 「置換基を有していてもよい複素環基」 としては、 A環の置換 基として例示した「置換基を有していてもよい複素環基」 と同様のものが用いられ る。 なかでも、 ハロゲン原子、 C 6アルキル、 カルボキシルー C^ -eアルキル、 C i 6アルコキシ一力ルポ二ルー Cト 6アルキル、 C 6アルコキシ一力ルポニル、 力ルバモイル、 ォキソ、 4ないし 1 0員複素環基 (例、 ピリジルなどの炭素原子以 外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含 有する 4ないし 1 0員複素環基)などから選ばれる 1ないし 2個の置換基で置換さ れていてもよい、 炭素原子以外に窒素原子、 硫黄原子、酸素原子等から選ばれる 1 ないし 4個のへテロ原子を含有する 5ないし 1 4員複素環基(例、 ァゼチニル、 ピ 口リジニル、 ピぺリジル、 ィソチアゾリジニル、 チアジアゾリジニル、 へキサヒド ロアゼピエル、 フリル、 チェニル、 ピリジル、 キノリル、 イソキノリル、 ベンゾフ ラエル、 ピリミジニル、 テトラゾリル、 イミダゾリジニル、 ピラジニル、 ピリダジ ニルなど) などが好ましい。 As the “heterocyclic group optionally having substituent (s)” represented by R lb , those similar to the “heterocyclic group optionally having substituent (s)” exemplified as the substituent for ring A are used. It is possible. Among them, halogen atom, C 6 alkyl, carboxyl-C ^ -e alkyl, C 6 alkoxy mono-potential C 6- alkyl, C 6 alkoxy mono-proponyl, dipotamoyl, oxo, 4- to 10-member complex A ring group (eg, a 4- to 10-membered heterocyclic group containing 1 to 3 hetero atoms selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as pyridyl) 1 A 5- to 14-membered heterocyclic group containing 1 to 4 hetero atoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon, which may be substituted with 1 to 2 substituents (E.g., azetinyl, piperidinyl, piperidyl, isothiazolidinyl, thiadiazolidinyl, hexahydrroazepier, frill, chenyl, pyridyl, quinolyl, isoquinolyl, benzofurel Pyrimidinyl, tetrazolyl, imidazolidinyl, pyrazinyl, etc. Piridaji yl) and the like are preferable.
D環で示される芳香族炭化水素環としては、例えば、炭素数 6ないし 1 4員の単 環式あるいは縮合多環式芳香族炭化水素環 (C 6 1 4ァリール環) などが用いられ る。 C 6 1 4ァリール環としては、 例えば、 ベンゼン環、 ナフタレン環、 アントリ ル環、 フエナントリル環などが用いられ、 なかでも、 ベンゼン環、 ナフ夕レン環な どが好ましく、 特にベンゼン環が好適である。 The aromatic hydrocarbon ring represented by D ring, e.g., C 6 -C to 1 4-membered monocyclic or condensed polycyclic aromatic hydrocarbon ring (C 6 1 4 Ariru ring), and the like Ru is used. As the C 6 14 aryl ring, for example, a benzene ring, a naphthalene ring, an anthryl ring, a phenanthryl ring and the like are used, and among them, a benzene ring, a naphthylene ring and the like are preferable, and a benzene ring is particularly preferable. .
これら芳香族炭化水素環は、前記した置換基 A群から選ばれる置換基を 1ないし 5個、 好ましくは 1ないし 3個有していてもよい。 These aromatic hydrocarbon rings may have 1 to 5, preferably 1 to 3, substituents selected from the aforementioned substituent group A.
D環で示される複素環としては、 例えば、 炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から選ばれるヘテロ原子を 1ないし 4個(好ましくは 1ないし 3個)含 む 5ないし 1 4員複素環などが用いられ、 具体的には、 (a) 5ないし 1 4員芳香 族複素環、 (b) 5ないし 1 4員脂肪族複素環、 (c) 5ないし 1 4員複素環とベン ゼン環との 2または 3環性縮合環などが用いられる。 Examples of the heterocycle represented by the ring D include a 5- to 14-membered heterocyclic ring having 1 to 4 (preferably 1 to 3) heteroatoms selected from nitrogen, sulfur, oxygen and the like in addition to carbon atoms. Heterocycles and the like are used. Specific examples include (a) a 5- to 14-membered aromatic heterocycle, (b) a 5- to 14-membered aliphatic heterocycle, and (c) a 5- to 14-membered heterocycle. A bicyclic or tricyclic fused ring with a zen ring is used.
該 5ないし 1 4員芳香族複素環としては、 例えば、 炭素原子以外に窒素原子、 硫 黄原子、酸素原子等から選ばれるヘテロ原子を 1ないし 4個(好ましくは 1ないし 3個)含む 5ないし 1 4員芳香族複素環などが用いられ、具体的には、チォフェン、 フラン、 インドリジン、 ピロール、 イミダゾール、 トリァゾール、 チアゾール、 ォ キサゾール、 ピラゾール、 ピリジン、 N—ォキシド化ピリジン、 ピラジン、 ピリミ ジン、 ピリダジン、 プリン、 4 H—キノリジン、 ナフチリジン、 イソチアゾール、 イソォキサゾ一ル、フラザンなどが挙げられる。なかでも、ピリジン、チォフェン、 フランなどが好ましく用いられる。 Examples of the 5- to 14-membered aromatic heterocycle include a nitrogen atom and a sulfur atom in addition to a carbon atom. A 5- to 14-membered aromatic heterocycle containing 1 to 4 (preferably 1 to 3) heteroatoms selected from a yellow atom, an oxygen atom and the like is used, and specifically, thiophene, furan, indolizine and the like are used. , Pyrrole, imidazole, triazole, thiazole, oxazole, pyrazole, pyridine, N-oxidized pyridine, pyrazine, pyrimidine, pyridazine, purine, 4H-quinolizine, naphthyridine, isothiazole, isoxazole, furazan, etc. . Among them, pyridine, thiophene, furan and the like are preferably used.
該 5ないし 1 4員脂肪族複素環としては、 炭素原子以外に窒素原子、 硫黄原子、 酸素原子等から選ばれるヘテロ原子を 1ないし 4個(好ましくは 1ないし 3個) を 含む 5ないし 1 4員脂肪族複素環などが用いられ、 具体的には、 ピロリジン、 ピぺ リジン、 ピぺラジン、 モルホリン、 チオモルホリン、 1 , 2—ジヒドロピリジン、 ィミダゾリジンなどが挙げられる。 The 5- to 14-membered aliphatic heterocycle includes 1 to 4 (preferably 1 to 3) heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom and the like in addition to a carbon atom. A membered aliphatic heterocycle or the like is used, and specific examples include pyrrolidine, piperidine, piperazine, morpholine, thiomorpholine, 1,2-dihydropyridine, imidazolidine and the like.
該 5ないし 1 4員複素環とベンゼン環との 2または 3環性縮合環としては、炭素 原子以外に窒素原子、硫黄原子、酸素原子から選ばれるヘテロ原子を 1ないし 4個 (好ましくは 1ないし 3個)を含む複素環とベンゼン環との 2または 3環性縮合環 などが用いられ、 具体的には、 ベンゾ 〔b〕 チォフェン、 ベンゾフラン、 1 H—べ ンズイミダゾール、 ベンズォキサゾール、 ベンゾチアゾール、 1 , 2一べンズイソ チアゾ一ル、 ナフト 〔2, 3— b〕 チォフェン、 チアントレン、 キサンテン、 フエ ノキサチイン、インドール、イソインド一ル、 1 H—ィンダゾール、イソキノリン、 キノリン、 フタラジン、 キノキサリン、 キナゾリン、 シンノリン、 カルバゾール、 3—力ルポリン、 フエナントリジン、 ァクリジン、 フエナジン、 フエノチアジン、 フエノキサジン、 イソクロマン、 ジヒドロべンゾフランなどが挙げられる。 As the bi- or tricyclic fused ring of the 5- to 14-membered heterocyclic ring and a benzene ring, one to four heteroatoms (preferably one to four) selected from nitrogen, sulfur and oxygen other than carbon atoms And 3 or more condensed rings of a benzene ring with a heterocyclic ring containing benzene [b] thiophene, benzofuran, 1H-benzimidazole, benzoxazole, benzo Thiazole, 1,2-benzisothiazol, naphtho [2,3-b] thiophene, thianthrene, xanthene, phenoxatiin, indole, isoindole, 1H-indazole, isoquinoline, quinoline, phthalazine, quinoxaline, quinazoline, Cinnoline, carbazole, 3-ketoporin, phenanthridine, acridine, phenazine, phenothiazine Fuenokisajin, isochroman, such as dihydro base Nzofuran and the like.
■ なかでも D環で示される複素環としては、 ピリジン、 チォフェン、 フラン、 イミ ダゾール、 チアゾール、 キノリン、 N—才キシド化ピリジン、 1 , 2—ジヒドロピ リジン、 ジヒドロべンゾフラン、 ベンゾジォキソール、 ベンゾチアゾール、 ピペリ ジン、 ピぺラジンなどが好ましく、 特にピリジン、 1, 2—ジヒドロピリジンなど が好適である。 ■ Among the heterocycles represented by the D ring, pyridine, thiophene, furan, imidazole, thiazole, quinoline, N-hydroxylated pyridine, 1,2-dihydropyridine, dihydrobenzofuran, benzodioxole, Benzothiazole, piperidine, piperazine and the like are preferable, and pyridine, 1,2-dihydropyridine and the like are particularly preferable.
これら複素環は、前記した置換基 A群から選ばれる置換基を 1ないし 5個、好ま しくは 1ないし 3個有していてもよい。 Eで示される 「酸化されていてもよい硫黄原子」 としては、 S、 SO、 S02が 用いられる。 These heterocycles may have 1 to 5, preferably 1 to 3, substituents selected from the aforementioned substituent group A. As the “optionally oxidized sulfur atom” represented by E, S, SO, and SO 2 are used.
Eで示される置換基を有していてもよい窒素原子としては、 例えば、 (i) 水素 原子、 (ii) 置換基を有していてもよい炭化水素基、 (iii) ァシル基などを 1個 有していてもよい窒素原子などが用いられる。 Examples of the optionally substituted nitrogen atom represented by E include (i) a hydrogen atom, (ii) an optionally substituted hydrocarbon group, and (iii) an acyl group. A nitrogen atom which may be present is used.
該「置換基を有していてもよい炭化水素基」 としては、 A環の置換基として例示 した 「置換基を有していてもよい炭化水素基」 と同様のものが用いられる。 As the “hydrocarbon group optionally having substituent (s)”, those similar to the “hydrocarbon group optionally having substituent (s)” exemplified as the substituent for ring A can be used.
該「ァシル基」 としては、 A環の置換基として例示した 「ァシル基」 と同様のも のが用いられ、このァシル基はさらに置換基 A群から選ばれる置換基を 1ないし 5 個、 好ましくは 1ないし 3個有していてもよい。 As the “acyl group”, those similar to the “acyl group” exemplified as the substituent for the ring A are used, and this acyl group further has 1 to 5, preferably 1 to 5, substituents selected from the substituent group A. May have one to three.
Eで示される式一 C S—〇一、 一 CO— 0—、 一 S— CO—、 - (CH2) k— CO -、 -NRlc-CO- (CH2) m -、 _NRlc_S〇2― (CH2) m -、 - S〇2 - NRlc— (CH2) m―、 -O-CS-NR10- (CH2) m―、 — NRlc 一 C〇— NRlc— (CH2) m―、 一 NRlc— CO— CH2— (CH2) m— NRlc 一 〔式中、 は水素原子、 置換基を有していてもよいアルキル基またはァシル 基を、 kは 0または 1を、 mは 0ないし 3の整数を示す〕で表わされる基において、 R で示されるアルキル基としては、 例えば、 メチル、 ェチル、 プロピル、 イソ プロピル、 ブチル、 イソブチル、 sec—ブチル、 tert—ブチル、 ペンチル、 へキシ ルなどの C卜 6アルキル基などが用いられる。 Formula expressed by E CS—〇 one, one CO— 0—, one S—CO—,-(CH 2 ) k — CO-, -NR lc -CO- (CH 2 ) m- , _NR lc _S〇 2 ― (CH 2 ) m -,-S〇 2 -NR lc — (CH 2 ) m ―, -O-CS-NR 10- (CH 2 ) m ―, — NR lc- C〇— NR lc — ( CH 2 ) m —, NR lc —CO—CH 2 — (CH 2 ) m — NR lc [wherein, is a hydrogen atom, an alkyl group or an acyl group which may have a substituent, and k is And m represents an integer of 0 to 3]. Examples of the alkyl group represented by R include methyl, ethyl, propyl, isopropyl, butyl, isobutyl, sec-butyl, tert-butyl - butyl, etc. C WINCH 6 alkyl groups such as pentyl, carboxymethyl Le is used.
Rleで示されるアルキル基は、 前記した置換基 A群から選ばれる置換基を 1な いし 5個、 好ましくは 1ないし 3個有していてもよい。 The alkyl group represented by R le may have 1 to 5, preferably 1 to 3 substituents selected from the aforementioned substituent group A.
Rlcで示されるァシル基としては、 A環の置換基として例示した 「ァシル基」 と同様のものが用いられ、このァシル基はさらに置換基 A群から選ばれる置換基を 1ないし 5個、 好ましくは 1ないし 3個有していてもよい。 As the acyl group represented by R lc , those similar to the `` acyl group '' exemplified as the substituent for the ring A are used, and the acyl group further has 1 to 5 substituents selected from the substituent group A. Preferably, it may have one to three.
kは 0または 1を示し、 特に 0が好ましい。 k represents 0 or 1, particularly preferably 0.
mは 0ないし 3の整数を示し、 なかでも 0または 1が好ましい。 m represents an integer of 0 to 3, and among them, 0 or 1 is preferable.
上記した中でも、 Eとしては、 Among the above, as E
(i)結合手、 (ii)メチレン、 (iii) 〇、 (iv)S、 (v) SO、 (vi)S〇2、 (vii)- NH—、 (viii)-N (C — 6アルキル) 一 (例、 一 N (メチル) 一など) 、 (ix)— N アルキル—力ルポニル) 一 (例、 一 N (ァセチル) 一など) 、 (X) N(i) bond, (ii) methylene, (iii) 〇, (iv) S, (v) SO, (vi) S〇 2 , (vii) -NH—, (viii) -N (C— 6 alkyl ) One (eg, one N (methyl) one etc.), (ix) — N alkyl-capillonyl) (eg, one N (acetyl) one), (X) N
— 6アルコキシ一力ルポニル) 一 (例、 — N (エトキシカルポニル) 一など)、 (xi)-N アルキルースルホニル) - (例、 一 N (メチルスルホニル) 一な ど) 、 (xii)— C〇一 O—、 (xiii)— S— C〇一、 — 6 alkoxy monopropionyl) (eg, — N (ethoxycarbonyl), etc.), (xi) -N alkyl-sulfonyl)-(eg, 1 N (methylsulfonyl), etc.), (xii) — C 〇 一 O—, (xiii) — S— C〇-1,
(xiv) - (CH2) k—CO— 〔式中、 kは 0または 1を示す〕 で表される基、a group represented by (xiv)-(CH 2 ) k —CO—, wherein k represents 0 or 1;
(xv) -NRf-C0- (CH2) ml— 〔式中、 Rfは水素原子または C^— 6アルコキ シ一力ルポニル(例、 メトキシカルボニル) または炭素原子以外に窒素原子、 酸素 原子、硫黄原子等から選ばれる 1ないし 3個のへテロ原子を含有する複素環基 (例、 ピリジル) で置換されていてもよい アルキル基を、 mlは 0ないし 3の整数 を示す〕 で表される基、 (xv) -NR f -C0- (CH 2) ml - [wherein, R f is a hydrogen atom or a C ^ - 6 an alkoxy Ichiriki Ruponiru (e.g., methoxycarbonyl) or a nitrogen atom in addition to carbon atom, an oxygen atom , An alkyl group which may be substituted with a heterocyclic group containing 1 to 3 hetero atoms (e.g., pyridyl) selected from a sulfur atom, etc., and ml represents an integer of 0 to 3.) Group,
(xvi) -NRg-S02- (CH2) m2— 〔式中、 Rgは水素原子または 6アルキ ルースルホニル基 (例、 メチルスルホニル) を、 m 2は 0を示す〕 で表される基、 (xvi0-SO2-NRh- (CH2) m「 〔式中、 Rhは水素原子または C ^6アルキ ル基 (例、 メチル) を、 m3は 0または 1を示す〕 で表される基 (xvi) -NR g -S0 2 - (CH 2) m2 - wherein, R g represents a hydrogen atom or a 6 alkyl Rusuruhoniru group (e.g., methylsulfonyl) and, m 2 represents 0] is represented by Group, (xvi0-SO 2 -NR h- (CH 2 ) m [where R h represents a hydrogen atom or a C ^ 6 alkyl group (eg, methyl), and m3 represents 0 or 1]. Group
(xviiD-O-CS-NR1- (CH2) m4— 〔式中、 R 1は水素原子または C アルキル基 (例、 メチル) を、 m4は 0または 1を示す〕 で表される基、 (xviiD-O-CS-NR 1- (CH 2 ) m4 — wherein R 1 represents a hydrogen atom or a C alkyl group (eg, methyl), and m4 represents 0 or 1),
(xix)-NR j-CO-NRk- (CH2) m5- 〔式中、 R jは水素原子または C 6 アルキル基 (例、 メチル) を、 R kは水素原子または 6アルキル基 (例、 メチ ル) を、 m5は 0または 1を示す〕 で表される基、 (xix) -NR j -CO-NR k- (CH 2 ) m5- (wherein, R j is a hydrogen atom or a C 6 alkyl group (e.g., methyl); R k is a hydrogen atom or a 6 alkyl group (e.g., , Methyl), and m5 represents 0 or 1.]
(xx)-NRL-CO-CH2 (CH2) mS— 'NRm— 〔式中、 RLは水素原子または C(xx) -NR L -CO-CH 2 (CH 2 ) mS — 'NR m — (where R L is a hydrogen atom or C
^6アルキル基 (例、 メチル) を、 Rmは水素原子または ^— 6アルキル基 (例、 メ チル) を、 m6は 0または 1を示す〕 で表される基、 ^ 6 alkyl group (e.g., methyl), and R m is hydrogen or ^ - group 6 alkyl group (e.g., methylation) and represented by m6 is 0 or 1],
などが好ましい。 Are preferred.
R1の好ましい基として例示される 「置換基を有していてもよい芳香族炭化水素 基」 および 「置換基を有していてもよい複素環基」 としては、 式 Examples of the preferred group for R 1 include an “optionally substituted aromatic hydrocarbon group” and an “optionally substituted heterocyclic group”.
CO-Hal 〔各記号は前記と同意義を示す〕 で表わきれる基も好ましく用いられる。 CO-Hal [Each symbol has the same meaning as described above] is also preferably used.
H a 1で示されるハロゲン原子としては、 フッ素原子、 塩素原子、 臭素原子、 ョ ゥ素原子などが用いられ、 なかでも塩素原子が好ましい。 As the halogen atom represented by H a1, a fluorine atom, a chlorine atom, a bromine atom, an iodine atom and the like are used, and among them, a chlorine atom is preferable.
D環としては、 前記と同様のものが用いられる。 As the D ring, those similar to the above can be used.
R 1の好ましい基として例示される式一 L— R l a 〔式中、 各記号は前記と同意義 を示す〕 で表わされる基において、 Lとしては、 メチレンまたは力ルポニルが好ま しい。 In the group represented by the formula L-R la exemplified as a preferable group of R 1 , wherein each symbol has the same meaning as described above, L is preferably methylene or heptonyl.
R 1 aで示される芳香族基としては、 例えば、 The aromatic group represented by R 1 a, for example,
①単環式あるいは縮合多環式芳香族炭化水素塞、 より具体的にはフエニル、 1—ナ フチル、 2—ナフチル、 1一アントリル、 2—アントリル、 9一アントリル、 1.一 フエナントリル、 2—フエナン卜リル、 3—フエナントリル、 4 _フエナントリル または 9 _フエナントリルなどの C 6— 1 4ァリール基 (好ましくは、 フエニル、 1 —ナフチルまたは 2—ナフチルなど、特に好ましくはフエニル)などの 6ないし 1 4員の単環式あるいは縮合多環式芳香族炭化水素基、 ①Monocyclic or condensed polycyclic aromatic hydrocarbons, more specifically phenyl, 1-naphthyl, 2-naphthyl, 1-anthryl, 2-anthryl, 9-anthryl, 1.1-phenanthryl, 2- 1 4 Ariru group (preferably, phenyl, 1 - - naphthyl or 2-naphthyl, particularly preferably phenyl) Fouesnant Bok Lil, 3 Fuenantoriru, C 6, such as 4 _ Fuenantoriru or 9 _ Fuenantoriru 6 to such 1 4 Membered monocyclic or fused polycyclic aromatic hydrocarbon group,
②炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1種または 2種の ヘテロ原子を 1個以上 (例えば、 1ないし 4個、 好ましくは 1ないし 3個) を含む 4ないし 1 4員芳香族複素環基などが用いられる。 ② Including one or more (for example, 1 to 4, preferably 1 to 3) one or more heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon atoms 4 to 14 A membered aromatic heterocyclic group or the like is used.
この 4ないし 1 4員芳香族複素環基としては、炭素原子以外に窒素原子、硫黄原 子、酸素原子等から選ばれる 1種または 2種のへテロ原子を 1個以上(例えば、 1 ないし 4個、好ましくは 1ないし 3個) を含む単環複素環基(好ましくは 5ないし 8員) またはその縮合芳香族複素環基、 より具体的には、チォフェン、ベンゾ〔b〕 チォフェン、 ベンゾフラン、 1 H—べンズイミダゾール、 ベンズォキサゾール、 ベ ンゾチアゾール、 1, 2一べンズイソチアゾ一ル、 ナフ卜 C 2 , 3— b〕 チォフエ ン、 チアントレン、 フラン、 インドリジン、 キサンテン、 フエノキサチイン、 ピロ ール、 イミダゾール、 トリアゾール、 チアゾ一ル、 ォキサゾール、 ピラゾール、 ピ リジン、 ピラジン、 ピリミジン、 ピリダジン、 インドール、 イソインドール、 1 H 一インダゾール、 プリン、 4 H—キノリジン、 イソキノリン、 キノリン、 フタラジ ン、 ナフチリジン、 キノキサリン、 キナゾリン、 シンノリン、 カルバゾール、 β— カルボリン、 フエナントリジン、 ァクリジン、 フエナジン、 イソチアゾール、 フエ ノチアジン、 イソォキサゾール、 フラザン、 フエノキサジン、 イソクロマンなどの 芳香族複素環 (好ましくは、 ピリジン、 チォフェンまたはフランなど、 より好まし くはピリジン) またはこれらの環 (好ましくは、 単環複素環) が 1個あるいは複数 個 (好ましくは 1または 2個、 さらに好ましくは 1個) と芳香環 (例えば、 上記し た芳香族炭化水素基など、好ましくはベンゼン環)との縮合環基などが用いられる。 該芳香族基の置換基としては、 前記した置換基 A群から選ばれる 1ないし 5個、 好ましくは 1ないし 3個の置換基が用いられる。 As the 4- to 14-membered aromatic heterocyclic group, one or more heteroatoms selected from a nitrogen atom, a sulfur atom, an oxygen atom and the like in addition to a carbon atom may be used. (Preferably 1 to 3) monocyclic heterocyclic group (preferably 5 to 8 members) or a fused aromatic heterocyclic group thereof, more specifically, thiophene, benzo [b] thiophene, benzofuran, 1 H-benzimidazole, benzoxazole, benzothiazole, 1,2-benzisothiazole, naphth C2,3-b] thiophene, thianthrene, furan, indolizine, xanthene, phenoxatiin, pyrrole, Imidazole, triazole, thiazole, oxazole, pyrazole, pyridine, pyrazine, pyrimidine, pyridazine, indole, isoindole 1 H one-indazole, purine, 4 H- quinolizine, isoquinoline, quinoline, Futaraji down, naphthyridine, quinoxaline, quinazoline, cinnoline, carbazole, beta-carboline, Hue phenanthridine, Akurijin, Fuenajin, isothiazole, Hue One or more aromatic heterocycles (preferably pyridine, thiophene or furan, more preferably pyridine) or one of these rings (preferably monocyclic heterocycles) such as nothiazine, isooxazole, furazane, phenoxazine, and isochroman; A condensed ring group of a plurality (preferably 1 or 2, more preferably 1) and an aromatic ring (for example, the above-mentioned aromatic hydrocarbon group, preferably a benzene ring) is used. As the substituent of the aromatic group, 1 to 5, preferably 1 to 3 substituents selected from the aforementioned substituent group A are used.
R 1 aで示される置換基を有していてもよい芳香族基としては、 アルキル、 アルコキシなどの置換基を 1ないし 5個有していてもよい C 4ァリール 基 (例、 フエニル) などが好ましい。 R 1 The aromatic group which may have a substituent represented by a, alkyl, 1 to 5 optionally having C 4 Ariru group (e.g., phenyl) substituents such as alkoxy and preferable.
R l aで示される 「置換基を有していてもよい水酸基」 としては、 前記,した A環 の置換基として例示される「置換基を有していてもよい水酸基」 と同様のものが用 いられ、 なかでも C 6アルキル基 (例、 メチル) を有していてもよい水酸基が好 ましい。 As the “optionally substituted hydroxyl group” represented by R la , those similar to the aforementioned “optionally substituted hydroxyl group” exemplified as the substituent of the ring A described above are used. Among them, a hydroxyl group which may have a C 6 alkyl group (eg, methyl) is preferable.
R l aで示される 「置換基を有していてもよいアミノ基」 としては、 A環の置換 基として例示した「置換基を有していてもよいアミノ基」 と同様のものが用いられ る。 As the “optionally substituted amino group” represented by R la , those similar to the “optionally substituted amino group” exemplified as the substituent for the ring A can be used. .
R l aで示される 「置換基を有していてもよいアミノ基」 としては、 例えば、 置 換基を有していてもよいアルキル基や置換基を有していてもよいァリール基など を 1ないし 2個有していてもよいアミノ基が好ましく、特に、① 4ないし 1 0員複 素環基(炭素原子以外に窒素原子、酸素原子、 硫黄原子などから選ばれる 1ないし 3個のへテロ原子を有する 4ないし 1 0員複素環基、例、 ピリジル) で置換されて いてもよい — 6アルキルーァミノ基、② C 6 1 4ァリールーァミノ基、③ 4ないし 1 0員複素環(炭素原子以外に窒素原子、酸素原子、硫黄原子などから選ばれる 1 ないし 3個のへテロ原子を有する 4ないし 1 0員複素環、 例、 ピリジル) —ァミノ 基などが好ましい。 Examples of the “amino group optionally having substituent (s)” represented by R la include, for example, an alkyl group optionally having a substituent, an aryl group optionally having a substituent, and the like. And an amino group which may have 2 or more, particularly preferably a 4- to 10-membered heterocyclic group (1 to 3 hetero atoms selected from nitrogen atom, oxygen atom, sulfur atom and the like in addition to carbon atom) May be substituted with a 4- to 10-membered heterocyclic group having an atom, eg, pyridyl) — 6-alkyl-amino group, ② C 6 4 aryl-amino group, ③ 4- to 10-membered heterocyclic ring (nitrogen other than carbon atom) A 4- to 10-membered heterocyclic ring having 1 to 3 heteroatoms selected from an atom, an oxygen atom, a sulfur atom and the like, eg, pyridyl) -amino group is preferred.
これらの中でも、 R 1としては、 式 Among these, as R 1 , the formula
〔式中、 R16は水素原子、 置換基を有していてもよい C6_14ァリ一ル基、 置換基 を有していてもよいアミノ基、置換基を有していてもよい複素環基またはハロゲン 原子を示す〕で表される基であるものが好ましい。特に R16が、 (1)水素原子、 (2) ァセチルァミノ基で置換されたフエニル、 (3) (i) アルキルスルホニル基、 (ii)ピリジルカルポニルまたは(iii)スルファモイルー アルキル基から選ば れる置換基でモノまたはジ置換されていてもよいァミノ、 (4)ピリジルまたは(5) ハロゲン原子 (フッ素原子、 塩素原子、 臭素原子、 ヨウ素原子) などであるものが 好ましい。 Wherein, R 16 is a hydrogen atom, which may have a substituent C 6 _ 14 § Li Ichiru group, an optionally substituted amino group, which may have a substituent A heterocyclic group or a halogen atom]. In particular, R 16 is a substituent selected from (1) a hydrogen atom, (2) phenyl substituted with an acetylamino group, (3) (i) an alkylsulfonyl group, (ii) pyridylcarbonyl or (iii) a sulfamoyl-alkyl group. Preferred are mono- or di-substituted amino, (4) pyridyl or (5) halogen atom (fluorine atom, chlorine atom, bromine atom, iodine atom).
R2および R3で示される 「置換基を有していてもよい炭化水素基」 としては、 A環の置換基として例示される「置換基を有していてもよい炭化水素基」 と同様の ものが用いられる。 The `` optionally substituted hydrocarbon group '' represented by R 2 and R 3 is the same as the `` optionally substituted hydrocarbon group '' exemplified as the substituent of ring A Is used.
この 「置換基を有していてもよい炭化水素基」 としては、 例えば、 As the “optionally substituted hydrocarbon group”, for example,
①ハロゲン原子、 ① halogen atom,
②置換基を有していてもよい水酸基 (例えば、 ^— 6アルキル、 アルキル— 力ルポニル、 アルキルスルホニル、 C 6ァラルキルなどで置換されていて もよい水酸基など) 、 ② hydroxyl group which may have a substituent (e.g., ^ - 6 alkyl, - force Ruponiru, alkylsulfonyl, C 6 Ararukiru such like hydroxy group which may be substituted),
③置換基を有していてもよいアミノ基 (例えば、 1または 2個の Ci— 6アルキル、 C^gアルキル—力ルポニル、 C 6 _ i 4ァリ一ルー力ルポニルなどで置換されていて もよぃァミノ基) 、 ③ substituent amino group which may have a (e.g., one or two CI- 6 alkyl, C ^ g alkyl - force Ruponiru, etc. In substituted C 6 _ i 4 § Li one Lou force Ruponiru Molypamino group),
④置換基を有していてもよい 4ないし 10員複素環基(例えば、ォキソ基を有して いてもよい、 炭素原子以外に窒素原子、 酸素原子、 硫黄原子などから選ばれる 1な いし 3個のへテロ原子を有する 4ないし 10員複素環基(例、 フタルイミド、 イミ ダゾリル、 ピペリジル、 ピロリジニル) ) 、 44- to 10-membered heterocyclic group which may have a substituent (for example, which may have an oxo group, other than carbon atom, is selected from nitrogen atom, oxygen atom, sulfur atom, etc. 4- to 10-membered heterocyclic group having one heteroatom (eg, phthalimide, imidazolyl, piperidyl, pyrrolidinyl)),
⑤置換基を有していてもよいチォ基 (例えば、 (^_6アルキルなどで置換されてい てもよぃチォ基) 、 ⑥ C i- eアルキルースルフィニル基、 ⑤ which may have a substituent Chio group (e.g., (^ _ 6 alkyl such Yoi Chio group optionally substituted with) ⑥C i-e alkyl-sulfinyl group,
⑦ C 6アルキル―スルホニル基、 ⑦ C 6 alkyl-sulfonyl group,
などで置換されていてもよい炭化水素基(特に、 アルキル基)が用いられる。 なかでも、 ①ハロゲン原子 (特に、 臭素原子) 、 ②ヒドロキシ、 ③ _6アルキ ル—カルポニルォキシ (例、 ァセトキシ) 、 ④ァミノ、 ⑤ォキソ基を有していても よい 4ないし 1 0員複素環基(炭素原子以外に窒素原子、酸素原子、硫黄原子など から選ばれる 1ないし 3個のへテロ原子を有する 4ないし 1 0員複素環基(例、 フ タルイミド、 イミダゾリル、 ピペリジル、 ピロリジニル) などで置換されていても よい C 6アルキル基などが好ましく、 さらにはハロゲン原子 (特に、 臭素原子) などでハロゲン化されていてもよい — 6アルキル基 (例、 メチル、 ェチルなど) などが好ましく、 特にメチル基が好適である。 A hydrocarbon group (particularly, an alkyl group) which may be substituted by, for example, is used. Among them, ① halogen atom (especially, bromine atom), ② hydroxy, ③ _ 6 alkyl Le - Karuponiruokishi (eg, Asetokishi), ④ Amino, ⑤ 4 which may have a Okiso group to 1 0-membered heterocyclic group (Substituted with a 4- to 10-membered heterocyclic group having 1 to 3 hetero atoms selected from nitrogen, oxygen, sulfur, etc. in addition to carbon (eg, phthalimide, imidazolyl, piperidyl, pyrrolidinyl)) etc. good C 6 alkyl group is preferable be news halogen atom (especially, bromine atom) may be halogenated and the like - 6 alkyl group (e.g., methyl, etc. Echiru) and the like are preferable, especially methyl Groups are preferred.
R 2および R 3で示される 「ァシル基」 としては、 A環の置換基として例示され る 「ァシル基」 と同様のものが用いられ、 なかでも — 6アルコキシ—カルポニル 基が好ましく、 特にメトキシカルボニル基が好適である。 Represented by R 2 and R 3 as "Ashiru group", those similar to the Ru is exemplified as the substituents for ring A "Ashiru group" is used, inter alia - 6 alkoxy - Karuponiru groups are preferred, especially methoxycarbonyl Groups are preferred.
R 2と R 3が隣接する炭素原子と共に形成する 3ないし 8員環としては、 例えば、 3ないし 8員同素環または複素環が用いられる。 As the 3- to 8-membered ring formed by R 2 and R 3 together with adjacent carbon atoms, for example, a 3- to 8-membered homocyclic or heterocyclic ring is used.
R 2と R 3が隣接する炭素原子と共に形成する 3ないし 8員同素環としては、 炭 素原子からなる 3ないし 8員の環状炭化水素が用いられ、 具体的には、 C 3_ 8シク ロアルカン (例えば、 シクロブタン、 シクロペンタン、 シクロへキサン、 シクロへ プタン、 シクロオクタン) 、 C 3 _ 8シクロアルゲン (例えば、 シクロブテン、 シク 口ペンテン、 シクロへキセン、 シクロヘプテン、 シクロォクテン) などが挙げられ る。 なかでも C 3 8シクロアルカンが好ましく、 特にシクロペンタン、 シクロへキ サンなどの 5または 6員の同素環 (特に、 シクロへキサン) が好ましい。 The 3- to 8-membered homocyclic R 2 and R 3 form together with the adjacent carbon atom, 3- to consist carbon atom used cyclic hydrocarbons to 8-membered, particularly, C 3 _ 8 consequent Roarukan (e.g., cyclobutane, cyclopentane, cyclohexane, heptane cyclohexane, cyclooctane), C 3 _ 8 Shikuroarugen (e.g., cyclobutene, consequent opening pentene, cyclohexene, cycloheptene, Shikurookuten) etc. is Ru mentioned. Of these C 3 8 cycloalkane is preferred, cyclopentane, 5 or 6-membered homocyclic ring such as key San cyclohexane (especially, cyclohexane) are preferred.
R 2と R 3が隣接する炭素原子と共に形成する 3ないし 8員複素環としては、 炭 素原子以外に窒素原子、硫黄原子および酸素原子から選ばれた 1種または 2種のへ テロ原子を 1個以上(例えば、 1個ないし 4個、 好ましくは 1個ないし 3個)含む 5ないし 8員の脂肪族複素環(好ましくは 5または 6員の脂肪族複素環)などが用 いられる。 The 3- to 8-membered heterocyclic ring formed by R 2 and R 3 together with adjacent carbon atoms includes, in addition to a carbon atom, one or two hetero atoms selected from a nitrogen atom, a sulfur atom and an oxygen atom. A 5- to 8-membered aliphatic heterocycle (preferably a 5- or 6-membered aliphatic heterocycle) containing at least one (for example, 1 to 4, preferably 1 to 3) is used.
より具体的には、 例えば、 ピぺリジン、 ピぺラジン、 モルホリン、 チオモルホリ ン、 ピロリジン、 イミダゾリジン環などの炭素原子および窒素原子以外に、 窒素原 子、酸素原子および硫黄原子から選ばれたヘテロ原子を 1個ないし 3個含む 5ない し 8員 (好ましくは 5または 6員) の脂肪族複素環などが用いられる。 More specifically, for example, piperidine, piperazine, morpholine, thiomorphol 5 to 8 members (preferably 5 or 6) containing 1 to 3 heteroatoms selected from nitrogen, oxygen and sulfur atoms, in addition to carbon and nitrogen atoms, such as a nitrogen atom, a pyrrolidine and an imidazolidine ring. Member) is used.
これらの R2と R3が隣接する炭素原子と共に形成する 3ないし 8員同素または 複素環は、 前記した R1で示される複素環が有していてもよい置換基と同様の置換 基を 1ないし 5個、 好ましくは 1ないし 3個有していてもよい。 置換基としては、 — 6アルキル、 C6_14ァリール、 C7_16ァラルキル、 ァミノ、 モノ— — 6ァ ルキルァミノ、モノー C6_14ァリールァミノ、 ジ—じ 6アルキルァミノ、 ジ— C 6_14ァリールァミノ、 4ないし 10員複素環基(例、炭素原子以外に、窒素原子、 酸素原子および硫黄原子から選ばれたヘテロ原子を 1個ないし 3個含む 4ないし 10員 (好ましくは 5または 6員) の複素環) などから選ばれる 1ないし 3個が好 ましい。 The 3- to 8-membered allo-heterocyclic or heterocyclic ring formed by R 2 and R 3 together with the adjacent carbon atom has the same substituent as the above-mentioned substituent which the heterocyclic ring represented by R 1 may have. It may have 1 to 5, preferably 1 to 3. Substituents include: — 6-alkyl, C 6 — 14 aryl, C 7 — 16 aralkyl, amino, mono— — 6-alkylamino, mono-C 6 — 14 arylamino, di- 6 alkylamino, di— C 6 — 14 arylamino A 4- to 10-membered heterocyclic group (eg, a 4- to 10-membered (preferably 5- or 6-membered) containing 1 to 3 heteroatoms selected from nitrogen, oxygen and sulfur atoms in addition to carbon atoms) 1 to 3 members selected from heterocycles) are preferred.
上記した中でも、 R2および R3としては、 それぞれハロゲン原子などで置換さ れていてもよい C _ 6アルキル基、 。ト 6アルコキシ—カルボニル基が好ましく、 特にメチル基、 メトキシカルボニル基が好適である。 The Among that, as the R 2 and R 3, etc. In the optionally substituted C _ 6 alkyl groups, respectively a halogen atom,. A 6- alkoxy-carbonyl group is preferred, and a methyl group and a methoxycarbonyl group are particularly preferred.
さらに、 R2と R3が隣接する炭素原子と共に C3 8シクロアルカン、好ましくは シクロペンタン、 シクロへキサンなどの 5または 6員の同素環(特に、 シクロへキ サン) を形成する場合も好ましい。 Furthermore, C 3 8 cycloalkane together with the carbon atoms to which R 2 and R 3 are adjacent, preferably cyclopentane, 5 or 6-membered homocyclic ring such as cyclohexane (in particular, key San cyclohexylene) may form a preferable.
R4および R5で示される 「置換基を有していてもよい炭化水素基」 としては、 A環の置換基として例示した「置換基を有していてもよい炭化水素基」 と同様のも のが用いられる。 なかでも (1) ハロゲン原子、 (2) ハロゲン.化されていてもよい アルキル、 (3) ハロゲン化されていてもよい — 6アルコキシ、 (4) ハロ ゲン化されていてもよい アルキルチオ、 (5) ヒドロキシ、 (6)ァミノ、 (7) モノー アルキルァミノ、 (8)ジー アルキルァミノなどから選ばれる置 換基を 1ないし 5個有していてもよい — 6アルキル基、 C2 6アルケニル基また は C2_6アルキニル基が好ましく、 特に アルキル基 (例、 メチル、 ェチルな ど) が好ましい。 As the `` optionally substituted hydrocarbon group '' represented by R 4 and R 5 , the same as the `` optionally substituted hydrocarbon group '' exemplified as the substituent of ring A Things are used. Among them, (1) halogen atom, (2) halogenated alkyl, (3) optionally halogenated — 6 alkoxy, (4) halogenated alkylthio, (5 ) May have 1 to 5 substituents selected from hydroxy, (6) amino, (7) monoalkylamino, (8) dialkylamino, etc. — 6 alkyl group, C 26 alkenyl group or C preferably 2 _ 6 alkynyl group, particularly an alkyl group (e.g., methyl, etc. Echiru) are preferred.
R4および R5としては、 例えば、 水素原子、 アルキル基 (例、 メチル、 ェ チル) などが好ましく、 特に水素原子が好ましい。 R 6および R 7で示される 「置換基を有していてもよい炭化水素基」 としては、 A環の置換基として例示した「置換基を有していてもよい炭化水素基」 と同様のも のが用いられ、 なかでも(^ - 6アルキル基 (例、 メチル、 ェチルなど) などが好ま しく、 特にメチル基が好適である。 As R 4 and R 5 , for example, a hydrogen atom, an alkyl group (eg, methyl, ethyl) and the like are preferable, and a hydrogen atom is particularly preferable. As the `` optionally substituted hydrocarbon group '' represented by R 6 and R 7 , the same as the `` optionally substituted hydrocarbon group '' exemplified as the substituent of the ring A Of these, a (-6) alkyl group (eg, methyl, ethyl, etc.) is preferred, and a methyl group is particularly preferred.
R 6と R 7が隣接する炭素原子と共に形成する 「置換基を有していてもよい 3な いし 8員環」 としては、前記した R 2と R 3が隣接する炭素原子と共に形成する 「置 換基を有していてもよい 3ないし 8員環」 と同様のものが用いられ、なかでも置換 基を有していてもよい 3ないし 8員同素環が好ましく、なかでも C 3 _ 8シクロアル カン (例えば、シクロブタン、シクロペンタン、シクロへキサン、シクロヘプタン、 シクロオクタン) が好ましく、特にシクロペンタン、 シクロへキサンなどの 5また は 6員の同素環 (特に、 シクロペンタン) が好ましい。 As the “optionally substituted 3- or 8-membered ring” formed by R 6 and R 7 together with adjacent carbon atoms, the above-mentioned “replacement formed by R 2 and R 3 together with adjacent carbon atoms” have a substituent like are used and may also be 3 to 8-membered ring ", among them is preferably 8-membered homocyclic to 3 which may have a substituent, of these C 3 _ 8 Preferred are cycloalkanes (eg, cyclobutane, cyclopentane, cyclohexane, cycloheptane, cyclooctane), and particularly preferred are 5- or 6-membered homocyclic rings (particularly, cyclopentane) such as cyclopentane and cyclohexane.
R 8で示される 「置換基を有していてもよい炭化水素基」 としては、 A環の置換 基として例示した「置換基を有していてもよい炭化水素基」 と同様のものが用いら れる。 As the “optionally substituted hydrocarbon group” for R 8 , those similar to the “optionally substituted hydrocarbon group” exemplified as the substituent for the ring A can be used. It is required.
R 8で示される炭化水素基としては、 アルキル基 (例、 メチル、 ェチルな ど) 、 C 2— 6アルケニル基 (例、 ァリル、 2—メチルー 2—プロぺニルなど) 、 C 2 _ 6アルキニル基 (例、 プロパルギルなど) 、 C 3_ 6シクロアルキル基 (例、 シク 口ペンチルなど)、 C 7— 1 6ァラルキル基 (例、 ベンジル、 3 _フエニルプロピル、 5—フエ二ルペンチルなど) などが好ましく、 特に (^ _ 6アルキル基 (特に、 メチ ル) が好適である。 The hydrocarbon group represented by R 8, an alkyl group (e.g., methyl, etc. Echiru), C 2 - 6 alkenyl group (e.g., Ariru, such as 2-methyl-2-propenyl), C 2 _ 6 alkynyl group (e.g., propargyl, etc.), C 3 _ 6 cycloalkyl group (e.g., consequent opening pentyl, etc.), C 7 - 1 6 Ararukiru group (e.g., benzyl, 3 _ phenylpropyl, 5 etc. phenylene Rupenchiru) etc. it is preferred, (^ _ 6 alkyl group (particularly, methylation) are suitable.
該炭化水素基の置換基としては、 (1) ハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ素) 、 (2) ヒドロキシ基、 (3) アミノ基、 (4) 力ルポキシ、 (5) 力 ルバモイル、 (6) C — 6アルコキシ一力ルポニル (例、 メトキシカルポニル、 X トキシカルポニルなど) 、 (7) モノー C i _ 6アルキル一力ルバモイル (例、 メチ ルカルバモイル、 ェチルカルバモイルなど) 、 (8) ジー アルキル—力ルバ モイル (例、 ジメチルカルバモイル、 ジェチルカルバモイルなど) 、 (9) ォキソ を有していてもよい炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 4ないし 1 0員複素環基(例、 ピリジル、 2 一イソインドリルなど) 、 (10) C 6一 ァリール基 (例、 フエニルなど) などが 好ましい。 Examples of the substituent of the hydrocarbon group include (1) a halogen atom (for example, fluorine, chlorine, bromine, and iodine), (2) a hydroxy group, (3) an amino group, (4) lipoxy, and (5) rubamoyl. , (6) C- 6 alkoxy monopropionyl (eg, methoxycarbonyl, X toxiccarbonyl, etc.), (7) Monono C i _ 6 alkyl monopotassium rubamoyl (eg, methylcarbamoyl, ethylcarbamoyl, etc.), (8) G-alkyl-carbamoyl (eg, dimethylcarbamoyl, getylcarbamoyl, etc.), (9) one to three carbon atoms which may have an oxo atom, other than nitrogen atom, sulfur atom, oxygen atom, etc. Hetero atom-containing 4- to 10-membered heterocyclic groups (eg, pyridyl, 2-isoindolyl, etc.), (10) C 6 monoaryl groups (eg, phenyl, etc.), etc. preferable.
R 8で示される 「ァシル基」 としては、 A環の置換基として例示した 「ァシル基」 と同様のものが用いられ、このァシル基はさらに置換基 A群から選ばれる置換基を 1ないし 5個、 好ましくは 1ないし 3個有していてもよい。 なかでも、 (1)ホルミ ル、 (2) C 6アルキル—力ルポニル基 (例、 ァセチル、 プロピオニルなど) 、 (3) < 6 _ 1 4ァリール一力ルポニル基 (例、 ベンゾィルなど) 、 (4) C 7— 1 6ァラルキル 一力ルポニル基 (例、 フエニルァセチルなど) 、 (5) (:ぃ 6アルコキシ一力ルポ二 ル基 (例、 メトキシカルボニル、エトキシカルポニルなど)、 (6)力ルバモイル基、 (7)モノーまたはジ— C i _ 6アルキル -力ルバモイル基 (例、メチルカルバモイル、 ジメチルカルバモイルなど) 、 (8)モノーまたはジー C 卜6アルキル一チォカルバ モイル基 (例、 メチルチオ力ルバモイル、 ジメチルチオ力ルバモイルなど) 、 (9) (^— 6アルキル—スルホニル基 (例、 メチルスルホニルなど) または(lCD C i— 6ァ ルキル—スルフィニル基 (例、 メチルスルフィエルなど) などが好ましい。 As the `` acyl group '' represented by R 8 , those similar to the `` acyl group '' exemplified as the substituent for the ring A are used, and this acyl group further has a substituent selected from the group of substituents A to 1 to 5 , Preferably one to three. Of these, (1) formyl, (2) C 6 alkyl - Power Ruponiru group (eg, Asechiru, propionyl and the like), (3) <6 _ 1 4 Ariru Ichiriki Ruponiru group (eg, a Benzoiru), (4 ) C 7 — 16 aralkyl monofunctional ruponyl group (eg, phenylacetyl), (5) (:) 6 alkoxy monofunctional group (eg, methoxycarbonyl, ethoxycarponyl, etc.), (6) functional rubamoyl group, (7) mono- or di - C i _ 6 alkyl - power Rubamoiru group (e.g., methylcarbamoyl, dimethylcarbamoyl, etc.), (8) mono- or di-C Bok 6 alkyl one Chiokaruba carbamoyl group (e.g., methylthio force Rubamoiru, dimethylthio force Rubamoiru etc.), (9) (^ - 6 alkyl - sulfonyl group (e.g., methylsulfonyl, etc.) or (lCD C i-6 § alkyl - sulfinyl group (e.g., methyl sulfide El) and preferably .
R 8で示される 「置換基を有していてもよい複素環基」 としては、 A環の置換基 として例示した「置換基を有していてもよい複素環基」と同様のものが用いられる。 なかでも、 R 8で示される複素環基としては、 炭素原子以外に窒素原子、 硫黄原 子、酸素原子等から選ばれる 1ないし 4個のへテロ原子を含有する 4ないし 1 0員 芳香族複素環基 (例、 テトラゾリルなど) などが好ましい。 ' As the `` heterocyclic group optionally having substituent (s) '' for R 8 , those similar to the `` heterocyclic group optionally having substituent (s) '' exemplified as the substituent for the ring A are used. Can be Among them, the heterocyclic group represented by R 8 is a 4- to 10-membered aromatic heterocyclic group containing 1 to 4 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms. Preferred are ring groups (eg, tetrazolyl, etc.). '
該複素環基の置換基としては、 C 6— 1 4ァリール基 (例、 フエニルなど) などが 好ましい。 The substituent of the heterocyclic group, C 6 - 1 4 Ariru group (e.g., phenyl etc.) and the like are preferable.
R 8で示されるハロゲン原子としては、 フッ素原子、 塩素原子、 臭素原子、 ヨウ 素原子が用いられ、 なかでも塩素原子などが好ましい。 ,The halogen atom represented by R 8, fluorine atom, chlorine atom, bromine atom, iodine atom are used, inter alia as chlorine atom is preferable. ,
R 8で示される式一 O R 1 Qの、 : 1 Gで示される 「置換基を有していてもよい炭化 水素基」 としては、 A環の置換基として例示した 「置換基を有していてもよい炭化 水素基」 と同様のものが用いられる。 Of formula one OR 1 Q represented by R 8,: 1 as "optionally substituted hydrocarbon group" represented by G, have a "substituent exemplified as the substituent of ring A The same hydrocarbon groups as those described above may be used.
R 1 Gで示される炭化水素基としては、 (O C^— eアルキル基 (例、 メチル、 ェチ ル、 イソプロピル、 ブチルなど) [この — 6アルキル基は (1) ハロゲン原子、 (2) ヒドロキシ基、 (3) アミノ基、 (4) 力ルポキシ、 (5) 力ルバモイル、 (6) アルコキシ—力ルポニル、 (7) モノー アルキル一力ルバモイル、 (8) ジ一 — 6アルキル一力ルバモイル、 (9) ォキソを有していてもよい炭素原子以 外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含 有する 4ないし 10員芳香族複素環基 (例、 ピリジル、 2—イソインドリルなど) などから選ばれる置換基を有していてもよい] 、 (ii)C2_6アルケニル基 (例、 ァ リル、 2—メチルー 2—プロぺニルなど) [この C2_6アルケニル基は C6— 14ァリ ール (例、 フエニル) を有していてもよい] 、 (iii)C2_6アルキニル基 (例、 プ 口パルギルなど) 、 (iv)C3_6シクロアルキル基 (例、 シクロペンチルなど) 、 (v) C7_16ァラルキル基 (例、 ベンジル、 3—フエニルプロピル、 5—フエ二ルペン チルなど) などが好適である。 Examples of the hydrocarbon group represented by R 1 G include (OC ^ -e alkyl group (eg, methyl, ethyl, isopropyl, butyl, etc.) [the 6- alkyl group is (1) halogen atom, (2) hydroxy Group, (3) amino group, (4) diluvamoyl, (5) diluvamoyl, (6) alkoxy-diluponyl, (7) monol-alkyl diluvamoyl, (8) Di--6 alkyl monorubumoyl, (9) containing from 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon which may have oxo, 10-membered aromatic Hajime Tamaki (e.g., pyridyl, 2-isoindolyl, etc.) which may have a substituent selected from such], (ii) C 2 _ 6 alkenyl group (e.g., § Lil, 2-methyl 2-propenyl, etc.) [this C 2 _ 6 alkenyl group C 6 - 14 § Li Lumpur (eg, which may have a phenyl)], (iii) C 2 _ 6 alkynyl group (e.g., such flop port Parugiru), (iv) C 3 _ 6 cycloalkyl group (e.g., cyclopentyl, etc.), (v) C 7 _ 16 Ararukiru group (e.g., benzyl, 3-phenylpropyl, 5-phenylene point pen chill etc. Are preferred.
R8で示される式— OR1Qの、 R1Qで示される 「ァシル基」 としては、 例えば、 ホルミル、 力ルバモイル、 — 6アルキル一力ルポニル (例、 ァセチル、 プロピオ ニルなど)、 c 3_6シクロアルキル—カルポニル (例、シクロペンチルカルポニル、 シク口へキシルカルポニルなど) 、 C 6アルコキシ一力ルポニル (例、 メトキシ 力ルポニル、 エトキシカルポニル、 イソプロポキシ力ルポニル、 tert—ブトキシカ ルポニルなど) 、 C6_14ァリール—カルボニル (例、 ベンゾィル、 2—ナフトイ ルなど) 、 C7_16ァラルキル—カルポニル (例、 フエ二ルァセチル、 3—フエ二 ルプロピオニルなど) 、 C 6^ 4ァリ一ルォキシ一力ルポニル (例、 フエノキシ力 ルポニル、 2一ナフチルォキシカルポニルなど) 、 C7_16ァラルキルォキシ—力 ルポニル (例、 ベンジルォキシカルポニル、 2—ナフチルメチルォキシカルポニル など) 、 5または 6員複素環カルポニル (例、 1—ピロリジニルカルポニル、 4一 ピベリジルカルポニル、 1 -ピペラジニルカルポニル、 2—モルホリニルカルポ二 ル、 4 _ピリジルカルポニル、 3—チェ二ルカルポニル、 2 _フリル力ルポニル、 2一チアゾリルカルポニルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等 から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環力ルポ二 ルなど) 、 モノ— Cェ _ 6アルキル一力ルバモイル (例、 メチルカルバモイル、 ェチ ルカルバモイルなど) 、 ジ—C — 6アルキル一力ルバモイル (例、 ジメチルカルバ モイル、 ジェチルカルバモイルなど) 、 C6— 14ァリ一ルー力ルバモイル (例、 フ ェニルカルバモイル、 2 _ナフチルカルバモイルなど) 、 5または 6員複素環カル バモイル(例、 1—ピロリジニルカルバモイル、 4一ピペリジルカルバモイル、 1 —ピペラジニルカルバモイル、 2一モルホリニルカルバモイル、 4—ピリジルカル パモイル、 3—チェ二ルカルバモイル、 2—フリルカルパモイル、 2—チアゾリル カルパモイルなどの炭素原子以外に窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環力ルバモイルなど)、 C ^ 6アルキルーチォカルポニル (例、 メチルチオカルポニルなど) 、 C 3— 6シクロ アルキルーチォカルポニル(例、 シクロペンチルチオ力ルポニル、 シクロへキシル チォカルポニルなど) 、 アルコキシ—チォカルポニル (例、 メトキ^チォカ ルポニル、 エトキシチ才力ルポニル、 プロポキシチォカルボニル、 ブトキシチォカ ルポニルなど) 、 C 6— 1 4ァリールーチォカルボニル (例、 フエ二ルチオカルボ二 ル、 2—ナフチルチオカルポニルなど)、 C 6ァラルキルーチォカルポニル(例、 ベンジル^^ォ力ルポニル、 フエネチルチオカルポニルなど) 、 C 6_ 1 4ァリールォ キシ—チォカルボニル (例、 フエノキシチォカルポニル、 2—ナフチルォキシチォ カルボニルなど) 、 C 7— 1 6ァラルキルォキシーチォカルボニル (例、 ベンジルォ キシチォカルボニル、 2—ナフチルメチルォキシチォカルポニルなど) 、 5または 6員複素環チォカルポニル(例、 1一ピロリジニルチオカルボニル、 4一ピペリジ ルチオ力ルポニル、 1ーピペラジニルチオ力ルポニル、 2—モルホリニルチオカル ポニル、 4—ピリジルチオ力ルポニル、 3—チェ二ルチオカルボニル、 2—フリル チォカルポニル、 2—チアゾリルチオカルポニルなどの炭素原子以外に窒素原子、 硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チォカルポニルなど) 、 チォカルバモイル、 モノー — 6アルキル—チ 才力ルバモイル (例、 メチルチオ力ルバモイル、 ェチルチオ力ルバモイルなど) 、 ジー 卜6アルキル一チォカルバモイル (例えば、 ジメチルチオ力ルバモイル、 ジ ェチルチオ力ルバモイルなど) 、 C 4ァリール—チォカルバモイル (例、 フエ 二ルチオ力ルバモイル、 2—ナフチルチオ力ルバモイルなど) 、 5または 6員複素 環チォカルバモイル(例、 2—ピロリジニルチオ力ルバモイル、 4ーピペリジルチ 才力ルバモイル、 2—ピペラジニルチオ力ルバモイル、 2—モルホリニルチオカル バモイル、 4一ピリジルチオ力ルバモイル、 3一チェ二ルチオ力ルバモイル、 2― フリルチォカルバモイル、 2一チアゾリルチオ力ルバモイルなどの炭素原子以外に 窒素原子、硫黄原子、酸素原子等から選ばれる 1ないし 3個のへテロ原子を含有す る 5または 6員複素環チォカルバモイルなど、 スルファモイル、 モノ— C 3_ _ 6アル キルースルファモイル (例、メチルスルファモイル、ェチルスルファモイルなど)、 ジー(^_6アルキル—スルファモイル (例、 ジメチルスルファモイル、 ジェチルス ルファモイルなど) 、 C 6^ 4ァリール—スルファモイル (例、 フエニルスルファ モイルなど) 、 (^_6アルキルスルホニル (例、 メチルスルホニル、 ェチルスルホ ニルなど) 、 C6— 14ァリールスルホニル (例、 フエニルスルホニル、 2—ナフチ ルスルホニルなど) 、 ( ^6アルキルスルフィニル (例、 メチルスルフィニル、 ェ チルスルフィニルなど) 、 C6_14ァリールスルフィニル (例、 フエニルスルフィ ニル、 2—ナフチルスルフィエルなど) 、 スルフィノ、 スルホ、 アルコキシ スルフィニル (例、 メトキシスルフィニル、 ェトキシスルフィニル) 、 c6— 14ァ リールォキシスルフィニル (例、 フエノキシスルフィエル) 、 アルコキシス ルホニル (例、 メトキシスルホニル、 ェトキシスルホニル) および c6_14ァリー ルォキシスルホニル (例、 フエノキシスルホニル) が用いられ、 このァシル基はさ らに置換基 A群から選ばれる置換基を 1ないし 5個、好ましくは 1ないし 3個有し ていてもよい。なかでも、 (i) C i— 6アルキル一力ルポニル基 (例、ァセチルなど)、 (ii) C6_14ァリ一ルー力ルポニル基 (例、 ベンゾィルなど) 、 (iii)C7— 16ァラ ルキル一力ルポニル基 (例、 フエニルァセチルなど) 、 (iv)!^^ 6アルコキシ一力 ルポニル基 (例、 メトキシカルポニル、 エトキシカルポニルなど) 、 (V)モノーま たはジ一 アルキル一チォカルバモイル基 (例、 メチルチオカルパモイル、 ジ メチルチオ力ルバモイルなど) 、 (vi)ハロゲン化されていてもよい Ci_6アルキル 一スルホニル基 (例、 メチルスルホニルなど) などが好ましい。 The formula represented by R 8 — OR 1Q , the “acyl group” represented by R 1Q includes, for example, formyl, sorbamoyl, —6 alkyl monopropionyl (eg, acetyl, propionyl, etc.), c 3 _ 6 Cycloalkyl-carbonyl (eg, cyclopentylcarbonyl, cyclohexylcarbonyl, etc.), C 6 alkoxy mono-proponyl (eg, methoxy-proponyl, ethoxycarbonyl, isopropoxy-proponyl, tert-butoxycarbonyl, etc.), C 6 _ 14 Ariru - carbonyl (e.g., Benzoiru, 2 Nafutoi Le etc.), C 7 _ 16 Ararukiru - Karuponiru (eg, phenylene Ruasechiru, 3-phenylene Rupuropioniru), C 6 ^ 4 § Li one Ruokishi Ichiriki Ruponiru ( examples, phenoxy force Ruponiru, 2 one naphthyl O carboxymethyl like Cal Poni Le), C 7 _ 16 Ararukiruokishi - power Ruponiru (eg Benzyloxycarbonyl, 2-naphthylmethyloxycarbonyl, etc., 5- or 6-membered heterocyclic carbonyl (eg, 1-pyrrolidinylcarbonyl, 4-piberidylcarbonyl, 1-piperazinylcarbonyl, 2-morpholini) 1 to 3 selected from nitrogen, sulfur, oxygen, etc., in addition to carbon atoms such as nilcarponyl, 4-pyridylcarbonyl, 3-cerylcarbonyl, 2-furylcapillon, and 2- thiazolylcarbonyl a 5- or 6-membered heterocyclic force Lupo two Le containing hetero atoms) to the mono - C E _ 6 alkyl Ichiriki Rubamoiru (e.g., methylcarbamoyl, etc. E Ji carbamoyl), di -C - 6 alkyl Ichiriki Rubamoiru (e.g., dimethyl carbamoyl, such as GETS Ji carbamoyl), C 6 - 14 § Li one Roux force Rubamoiru (eg, full E carbamoylmethyl Such as 2 _ naphthylcarbamoyl), 5- or 6-membered heterocyclic Cal Bamoiru (e.g., 1-pyrrolidinylmethyl carbamoyl, 4 one piperidylcarbamoyl, 1 —Selected from nitrogen, sulfur, oxygen, etc. in addition to carbon atoms such as piperazinylcarbamoyl, 21-morpholinylcarbamoyl, 4-pyridylcarbamoyl, 3-cerylcarbamoyl, 2-furylcarbamoyl, 2-thiazolylcarbamoyl, etc. is a 5- or 6-membered heterocyclic force Rubamoiru containing 1 to 3 heteroatom), C ^ 6 alkyl chromatography Chio local Poni Le (e.g., methyl thio Cal Poni Le), C 3 - 6 cycloalkyl over Chio local Poni Le (e.g., cyclopentylthio force Ruponiru, cyclohexane, etc. cyclohexyl Chiokaruponiru) alkoxy - Chiokaruponiru (e.g., methoxide ^ Chioka Ruponiru, Etokishichi Sairyoku Ruponiru, propoxycarbonyl Chio carbonyl, etc. Butokishichioka Ruponiru), C 6 - 1 4 § reel over Chio carbonyl (e.g., Hue Nilthiocarbonyl, 2 Na like border Lucio Cal Poni Le), C 6 § Lal kills over Chio local Poni Le (e.g., benzyl ^^ O force Ruponiru and Hue phenethyl Lucio Cal Poni Le), C 6 _ 1 4 Ariruo carboxymethyl - Chio carbonyl (e.g., phenoxyethanol Chio Cal Poni Le, and 2-naphthyl O carboxymethyl Chio carbonyl), C 7 - 1 6 § Lal kill O Kishi Chio carbonyl (e.g., Benjiruo carboxymethyl Chio carbonyl, 2-naphthylmethyl O carboxymethyl Chio Cal Poni Le etc.), 5- or 6-membered heterocyclic ring Chiokaruponiru (eg , 1-pyrrolidinylthiocarbonyl, 4-piperidylthiothiol-ponyl, 1-piperazinylthiothiol-ponyl, 2-morpholinylthiocarbonyl, 4-pyridylthio-thiol-ponyl, 3-cherylthiocarbonyl, 2-furyl-thiocarbonyl, In addition to carbon atoms such as 2-thiazolylthiocarbonyl, nitrogen, sulfur and acid 5- or 6-membered heterocyclic thiocarbonyl containing 1 to 3 heteroatoms selected from elementary atoms, etc.), thiocarbamoyl, mono--6alkyl-thi-substituted rubamoyl (eg, methylthiolrubamoyl, ethylthiolrubamoyl, etc.) ), di-Bok 6 alkyl one Chiokarubamoiru (e.g., dimethylthio force Rubamoiru, such as di Echiruchio force Rubamoiru), C 4 Ariru - Chiokarubamoiru (eg, phenylene Lucio force Rubamoiru, such as 2-naphthylthio force Rubamoiru), 5 or 6-membered Heterocyclic thiocarbamoyl (eg, 2-pyrrolidinylthiolrubamoyl, 4-piperidylti talent rubamoyl, 2-piperazinylthiolrubamoyl, 2-morpholinylthiocarbamoyl, 4-pyridylthiolrubamoyl, 3-1-chelylthiolrubamoyl, 2-Ruffle Chacarbamoy Contains 1 to 3 heteroatoms selected from nitrogen, sulfur, oxygen, etc., in addition to carbon atoms such as That a 5- or 6-membered heterocyclic Chiokarubamoiru, sulfamoyl, mono - C 3_ _ 6 Al key loose sulfamoyl (e.g., methylsulfamoyl, etc. E chill sulfamoyl), G (^ _ 6 alkyl - sulfamoyl (e.g., dimethylsulfamoyl, etc. Jechirusu Rufamoiru), C 6 ^ 4 Ariru - sulfamoyl (e.g., such as Fuenirusurufa Moyle) (^ _ 6 alkylsulfonyl (e.g., methylsulfonyl, etc. Echirusuruho sulfonyl), C 6 - 14 § reel sulfonyl ( examples, phenylalanine sulfonyl, such as 2-naphthyl Rusuruhoniru), (^ 6 alkylsulfinyl (e.g., methylsulfinyl, etc. E Chirusurufiniru), C 6 _ 14 § reel sulfinyl (e.g., Hue Nils sulfinyl, 2- Nafuchirusuru Fiel, etc.), sulfino, sulfo, alkoxys Rufiniru (e.g., methoxysulfinyl, E Toki cis sulfinyl), c 6 - 14 § reel O carboxymethyl sulfinyl (e.g., full enoki cis Luffy El), Arukokishisu Ruhoniru (e.g., methoxysulfonyl, E butoxy-benzenesulfonyl) and c 6 _ 14 Ari Ruo Xylsulfonyl (eg, phenoxysulfonyl) is used, and this acyl group may further have 1 to 5, preferably 1 to 3, substituents selected from the substituent group A. But, (i) C i-6 alkyl Ichiriki Ruponiru group (eg, a Asechiru), (ii) C 6 _ 14 § Li one Roux force Ruponiru group (eg, a Benzoiru), (iii) C 7 - 16 § (1) alkenyl carbonyl group (eg, phenyl acetyl), (iv)! ^^ 6 alkoxy carbonyl group (eg, methoxycarbonyl, ethoxycarbonyl, etc.), (V) monomer Other di primary alkyl one Chiokarubamoiru group (e.g., methylthio Scarpa moil, such as di-methylthio force Rubamoiru), (vi) halogenated may CI_ 6 alkyl one sulfonyl group (e.g., methyl sulfonyl), etc. are preferable.
R8で示される式一 OR1Gの、 R1Qで示される 「置換基を有していてもよい複素 環基」 としては、 A環の置換基として例示した「置換基を有していてもよい複素環 基」 と同様のものが用いられる。 As the `` heterocyclic group optionally having substituent (s) '' represented by R 1Q of the formula 1 OR 1G represented by R 8 , the `` optionally substituted heterocyclic group '' exemplified as the substituent on ring A The same as "good heterocyclic group" are used.
なかでも、 R1Qで示される複素環基としては、 炭素原子以外に窒素原子、 硫黄 原子、酸素原子等から選ばれる 1ないし 4個のへテロ原子を含有する 4ないし 10 員芳香族複素環基(例、テトラゾリルなど) [この複 環基は C6— 14ァリール (例、 フエニル) を有していてもよい。 ] などが好ましい。 Among them, examples of the heterocyclic group represented by R 1Q include a 4- to 10-membered aromatic heterocyclic group containing 1 to 4 hetero atoms selected from nitrogen, sulfur, and oxygen atoms in addition to carbon atoms. (eg, such as tetrazolyl) [this double ring group C 6 - 14 Ariru (e.g., phenyl) which may have a. ] Is preferred.
R8で示される式一 SR11の、 R11で示される 「置換基を有していてもよい炭化 水素基」 としては、 A環の置換基として例示した 「置換基を有していてもよい炭ィ匕 水素基」 と同様のものが用いられる。 In the formula (1) represented by R 8 , SR 11 may be a `` carbonized optionally having substituent (s) '' represented by R 11 As the “hydrogen group”, those similar to the “optionally substituted carbon hydride group” exemplified as the substituent for the ring A are used.
R 11で示される炭化水素基としては、 (^_6アルキル基 (例、 メチル、 ェチルな ど) などが好適である。 The hydrocarbon group represented by R 11, are preferred, such as (^ _ 6 alkyl group (e.g., methyl, etc. Echiru).
尺8で示される式—31 11の、 R 11で示される 「ァシル基」 としては、 R1Qで示 される 「ァシル基」 と同様のものが用いられ、 このァシル基はさらに置換基 A群か ら選ばれる置換基を 1ないし 5個、 好ましくは 1ないし 3個有していてもよい。 As the “acyl group” represented by R 11 in the formula—31 11 of the formula—31 11 represented by the scale 8 , the same “acyl group” represented by R 1Q can be used. It may have 1 to 5, preferably 1 to 3, substituents selected therefrom.
R 11で示される 「ァシル基」 としては、 モノーまたはジー アルキル一カル パモイル基 (例、 メチルカルバモイル、 ジメチルカルバモイルなど) などが好適で ある。 The “acyl group” represented by R 11 is preferably a monol or dialkyl-carbamoyl group (eg, methylcarbamoyl, dimethylcarbamoyl, etc.).
R8で示される式—SR11の、 R11で示される 「置換基を有していてもよい複素 環基」 としては、 A環の置換基として例示した 「置換基を有していてもよい複素環 基」 と同様のものが用いられる。 Of formula -SR 11 represented by R 8, as the "optionally heterocyclic group which may have a substituent" represented by R 11, exemplified as the substituent of the ring A 'may have a substituent The same as "good heterocyclic group" are used.
R8で示される式 _S (O) R12の、 R12で示される 「置換基を有していてもよ い炭化水素基」 としては、 A環の置換基として例示した「置換基を有していてもよ い炭化水素基」 と同様のものが用いられる。 In the formula _S (O) R 12 represented by R 8 , the “optionally substituted hydrocarbon group” represented by R 12 includes the “substituent having a substituent” exemplified as the substituent for ring A. The same hydrocarbon groups as those described above may be used.
R 12で示される炭化水素基としては、 ^アルキル基 (例、 メチル、 ェチルな ど) などが好適である。 The hydrocarbon group represented by R 12, ^ alkyl group (e.g., methyl, etc. Echiru) is preferable.
R8で示される式— S (〇) R12の、 R12で示される 「置換基を有していてもよ い複素環基」 としては、 A環の置換基として例示した「置換基を有していてもよい 複素環基」 と同様のものが用いられる。 Formula represented by R 8 - the S (〇) R 12, as the "but it may also be substituted heterocyclic group" represented by R 12, the illustrated "substituent as the substituent of ring A The same as the "heterocyclic group which may be possessed" is used.
R8で示される式—S (〇) 2R13の、 R13で示される 「置換基を有していても よい炭化水素基」 としては、 A環の置換基とし 例示した「置換基を有していても よい炭化水素基」 と同様のものが用いられる。 Of formula -S (〇) 2 R 13 represented by R 8, as the "optionally substituted hydrocarbon group" represented by R 13, the illustrated "substituent as the substituent of ring A The same as the "hydrocarbon group which may be possessed" is used.
R 13で示される炭化水素基としては、 (:ト 6アルキル基 (例、 メチル、 ェチルな ど) などが好適である。 As the hydrocarbon group represented by R 13, (: Preparative 6 alkyl group (e.g., methyl, etc. Echiru) is preferably such.
R8で示される式一 S (O) 2R13の、 R13で示される 「置換基を有していても よい複素環基」 としては、 A環の置換基として例示した「置換基を有していても い複素環基」 と同様のものが用いられる。 R8で示される式一 NR14R15の、 R14および R15で示される 「置換基を有し ていてもよい炭化水素基」 としては、 A環の置換基として例示した「置換基を有し ていてもよい炭化水素基」 と同様のものが用いられる。 As the `` heterocyclic group optionally having substituent (s) '' for R 13 of the formula (1) S (O) 2 R 13 represented by R 8 , the `` substituents '' exemplified as the substituents for ring A The same as those described for the "heterocyclic group which may be possessed" are used. As the `` optionally substituted hydrocarbon group '' represented by R 14 and R 15 of the formula 1 NR 14 R 15 represented by R 8 , the `` substituents '' exemplified as the substituents for ring A The same as the "hydrocarbon group which may be possessed" is used.
R 14および R 15で示される炭化水素基としては、 Cト6アルキル基 (例、メチル、 ェチルなど) [この アルキル基は アルコキシ一力ルポニルを有してい てもよい。 ] などが好適である。 Examples of the hydrocarbon group represented by R 14 and R 15 include a C 6 alkyl group (eg, methyl, ethyl, etc.) [This alkyl group may have an alkoxyl monopropyl. And the like are preferred.
R8で示される式一 NR14R15の、 R14および R15で示される 「ァシル基」 と しては、 R1Qで示される 「ァシル基」 と同様のものが用いられ、 このァシル基は さらに置換基 A群から選ばれる置換基を 1ないし 5個、好ましくは 1ないし 3個有 していてもよい。 なかでも、 ホルミル、 c ^6アルキル—力ルポニル基 (例、 ァセ チル、 プロピオニルなど) アルコキシ—カルボニル基 (例、 メトキシカル ポニル、 エトキシカルポニルなど) 、 力ルバモイル基、 モノ—またはジ— ァ ルキル一力ルバモイル基 (例、メチルカルバモイル、ジメチルカルバモイルなど)、As the “acyl group” represented by R 14 and R 15 of the formula 1 NR 14 R 15 represented by R 8 , the same as the “acyl group” represented by R 1Q can be used. May further have 1 to 5, preferably 1 to 3, substituents selected from substituent group A. Among them, formyl, c ^ 6 alkyl-caprolponyl group (eg, acetyl, propionyl, etc.) alkoxy-carbonyl group (eg, methoxycarbonyl, ethoxycarponyl, etc.), caprolvamoyl group, mono- or dialkyl Carbamoyl groups (eg, methylcarbamoyl, dimethylcarbamoyl, etc.),
C^— 6アルキルースルホニル基 (例、 メチルスルホニルなど) などが好ましい。 C ^ - 6 alkyl chromatography sulfonyl group (e.g., methyl sulfonyl), etc. are preferable.
R8で示される式一 NR14R15の、 R14および R15で示される 「置換基を有し ていてもよい複素環基」 としては、 A環の置換基として例示した 「置換基を有して いてもよい複素環基」 と同様のものが用いられる。 Examples of the `` heterocyclic group optionally having substituent (s) '' represented by R 14 and R 15 in the formula 1 NR 14 R 15 represented by R 8 include `` substituents exemplified as substituents on ring A. The same ones as those described for the "heterocyclic group which may be possessed" are used.
R8で示される式—NR14R15としては、 R14が①水素原子、 ②じト 6アルキル 基 (例、 メチル、 ェチルなど) [この アルキル基は 6アルコキシ—カル ボニルを有していてもよい。] ③ホルミル、④ C i— 6アルキル—力ルポニル基 (例、 ァセチル、 プロピオニルなど) 、 (Dc 6アルコキシ一力ルポニル基 (例、 メトキ シカルポニル、 エトキシカルボニルなど) 、 ⑥カルバモイル基、 ⑦モノーまたはジ 一 c^— 6アルキル一力ルバモイル基 (例、 メチルカルバモイル、 ジメチルカルバモ ィルなど) または⑧ (^_6アルキルースルホニル基 (例、 メチルスルホニルなど) などであり、 R 15が①水素原子、 ② (:ト 6アルキル (例、 メチル、 ェチル、 プロピ ル、 イソプロピルなど) 、 ③ C6— 14ァリール (例、 フエニル、 2—ナフチルなど) または④ C7— 16ァラルキル (例、 ベンジル、 フエネチルなど) などであるものが 好ましい。 なかでも R 14が①水素原子、 ② アルキル基 (例、 メチル、 ェチル など) [この アルキル基は アルコキシ—力ルポニルを有していてもよ い。 ] 、 ③ホルミル、 @C1→アルキル一力ルポニル基 (例、 ァセチル、 プロピオ ニルなど) 、 ⑤じ 6アルコキシ—カルボニル基 (例、 メトキシカルポニル、 エト キシカルボニルなど) 、 ⑥カルバモイル基、 ⑦モノ—またはジ— — 6アルキル一 力ルバモイル基 (例、 メチルカルバモイル、 ジメチルカルバモイルなど) または⑧ アルキル—スルホニル基 (例、 メチルスルホニルなど) であり、 R 15が水素 原子またはメチルなどであるものが好ましい。 In the formula —NR 14 R 15 represented by R 8 , R 14 is a hydrogen atom, (2) a 6- alkyl group (eg, methyl, ethyl, etc.) [This alkyl group has 6 alkoxy-carbonyl Is also good. ] ③ formyl, ④ C i- 6 alkyl-propionyl group (eg, acetyl, propionyl, etc.), (Dc 6 alkoxy mono-propionyl group (eg, methoxycarbonyl, ethoxycarbonyl, etc.), ⑥ carbamoyl group, ⑦ mono- or di- one c ^ - 6 alkyl Ichiriki Rubamoiru group (e.g., methylcarbamoyl, dimethylcarbamyl model etc. I le) or ⑧ (^ _ 6 alkyl chromatography sulfonyl group (e.g., methyl sulfonyl) and the like, R 15 is ① a hydrogen atom , ② (: preparative 6 alkyl (e.g., methyl, Echiru, propyl Le, isopropyl, etc.), ③ C 6 - 14 Ariru (e.g., phenyl, 2-naphthyl, etc.) or ④ C 7 - 16 Ararukiru (e.g., benzyl, phenethyl In particular, R 14 is preferably a hydrogen atom, or an alkyl group (eg, methyl, ethyl, etc.) [this alkyl group May have alkoxy-carbonyl No. ], ③ formyl, @C 1 → alkyl Ichiriki Ruponiru group (eg, Asechiru, etc. propionitrile sulfonyl), ⑤ Ji 6 alkoxy - carbonyl group (e.g., methoxy Cal Poni Le, like ethoxy alkoxycarbonyl), ⑥ a carbamoyl group, ⑦ mono - or di - - 6 alkyl Ichiriki Rubamoiru group (e.g., methylcarbamoyl, etc. dimethylcarbamoyl) or ⑧ alkyl - or a sulfonyl group (e.g., methyl sulfonyl), which R 15 is a hydrogen atom or the like or methyl are preferred.
R8としては、 水素原子または式— OR1Q (R1Qは水素原子、 置換基を有してい てもよい炭化水素基、 ァシル基または置換基を有していてもよい複素環基を示す) が好ましい。 なかでも、 R8としては、 水素原子、 水酸基 (R1Qが水素原子である もの) 、 置換基を有していてもよい Ci-eアルコキシ (R1Gが置換基を有していて もよい C i— 6アルキルであるもの)またはァシルォキシ (R10がァシルであるもの) が好ましい。 特に、 水素原子、 水酸基 (R1Qが水素原子であるもの) 、 ピリジル で置換されていてもよい アルコキシ(R 10がピリジルで置換されていてもよ い C i _ 6アルキルであるもの) またはハ口ゲン原子で置換された C _ 6アルキルス ルホニルォキシ(R1Qがハロゲン原子で置換された アルキルスルホニルであ るもの) が好ましい。 R 8 represents a hydrogen atom or a formula —OR 1Q (R 1Q represents a hydrogen atom, a hydrocarbon group which may have a substituent, an acyl group or a heterocyclic group which may have a substituent) Is preferred. Among them, as R 8 , a hydrogen atom, a hydroxyl group (where R 1Q is a hydrogen atom), an optionally substituted Ci-e alkoxy (R 1G may have a substituted C Preferred are i- 6 alkyl) or acyloxy (where R 10 is acyl). In particular, a hydrogen atom, a hydroxyl group (where R 1Q is a hydrogen atom), an alkoxy optionally substituted with pyridyl (where R 10 is C i _ 6 alkyl optionally substituted with pyridyl) or ha C _ 6 Arukirusu Ruhoniruokishi substituted mouth Gen atoms (R 1Q alkylsulfonyl der shall substituted with halogen atom) is preferable.
R 9で示される 「置換基を有していてもよい炭化水素基」 としては、 A環の置換 基として例示した「置換基を有していてもよい炭化水素基」 と同様のものが用いら れる。 As the “optionally substituted hydrocarbon group” for R 9 , those similar to the “optionally substituted hydrocarbon group” exemplified as the substituent for the ring A can be used. It is required.
R 9で示される炭化水素基としては、 6アルキル基 (例、 メチル、 ェチル、 プロピル、 イソプロピルなど) 、 C 2— 6アルケニル基 (例、 2—メチルー 2—プロ ぺニルなど) が好ましく、 特にメチル、 イソプロピルなどの (^_3アルキル基が好 ましい。 The hydrocarbon group represented by R 9, 6 alkyl group (e.g., methyl, Echiru, propyl, isopropyl, etc.), C 2 - 6 alkenyl group (e.g., 2-methyl-2-pro Bae sulfonyl) are preferred, methyl, (^ _ 3 alkyl groups such as isopropyl good preferable.
該炭化水素基の置換基としては、 ωハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ素) 、 (2) シァノ基、 (3) 低級アルコキシ基 (例、 メトキシ、 ェトキ シ)、 (4) ヒドロキシ基、 (5)アミノ基、 (6)モノ—低級アルキルアミノ基(例、 メチルァミノ、 ェチルァミノなどのモノ— アルキルアミノ基など) 、 (7) ジー低級アルキルアミノ基 (例、 ジメチルァミノ、 ジェチルァミノなどのジ— C t __6アルキルアミノ基など) 、 (8) ォキソを有していてもよい炭素原子以外に、 窒 素原子、酸素原子および硫黄原子から選ばれたヘテロ原子を 1個ないし 3個含む 4 ないし 10員複素環 (例、 ピペリジノ、 2—イソインドリルなど) 、 (9) C6_14 ァリールチオ(例、フエ二ルチオなど)、 (10)ウレイド、 (11)力ルポキシ、 (12) 力ルバモイル、 (13) アルコキシ一力ルポニル (例、 メトキシカルボニル、 エトキシカルポニルなど) 、 (14) モノ— C アルキル一力ルバモイル (例、 メ チルカルバモイル、 ェチルカルバモイルなど) 、 (15) ホルミルァミノ、 (16) C 丄—6アルキル一力ルポキサミド (例、 ァセトアミド、 プロピオンアミドなど) など が好ましい。 Examples of the substituent for the hydrocarbon group include an ω halogen atom (for example, fluorine, chlorine, bromine, and iodine), (2) a cyano group, (3) a lower alkoxy group (eg, methoxy, ethoxy), and (4) hydroxy. Group, (5) amino group, (6) mono-lower alkylamino group (eg, mono-alkylamino group such as methylamino, ethylamino, etc.), (7) G-lower alkylamino group (eg, dimethylamino, dimethylamino, etc.) — C t __ 6 alkylamino group), (8) In addition to the carbon atom which may have oxo, Atom, one oxygen atom and hetero atom selected from sulfur atom to 4 not containing 3 to 10-membered heterocyclic ring (e.g., piperidino, 2-isoindolyl), (9) C 6 _ 14 Ariruchio (e.g., Hue (10) ureido, (11) lipoxy, (12) rubamoyl, (13) alkoxy monopropyl (eg, methoxycarbonyl, ethoxycarbonyl, etc.), (14) mono-C alkyl monorubamoyl (Eg, methyl carbamoyl, ethyl carbamoyl, etc.), (15) formylamino, (16) C ア ル キ ル -6 alkyl monol lipoxamide (eg, acetoamide, propionamide, etc.) are preferred.
R9で示される 「ァシル基」 としては、 A環の置換基として例示した「ァシル基」 と同様のものが用いられ、 具体的には、 (1)ホルミル、 (2)0^6アルキル—力ルポ ニル基 (例、 ァセチル、 プロピオニルなど) 、 (3)C6_14ァリール—力ルポニル基 (例、 ベンゾィルなど) 、 (4)C7— 16ァラルキル—カルボニル基 (例、 フエニルァ セチルなど) 、 (5) C ^6アルコキシ一力ルポニル基 (例、 メトキシカルポニル、 エトキシカルポニルなど) 、 (6)力ルバモイル基、 (7)モノ—またはジー C^— 6アル キル一力ルバモイル基 (例、 メチルカルバモイル、 ジメチルカルバモイルなど) 、 (8)モノーまたはジ一 アルキル一チォカルバモイル基 (例、 メチルチオカル バモイル、 ジメチルチオカルパモイルなど) 、 (9) C _ 6アルキル一スルホニル基 (例、 メチルスルホニルなど) 、 (10)C1_6アルキル一スルフィニル基 (例、 メチ ルスルフィニルなど) などが用いられ、 なかでもホルミルが好ましい。 As the “acyl group” represented by R 9 , those similar to the “acyl group” exemplified as the substituent for the ring A can be used. Specifically, (1) formyl, (2) 0 ^ 6 alkyl- power Lupo sulfonyl group (e.g., Asechiru, propionyl and the like), (3) C 6 _ 14 Ariru - power Ruponiru group (eg, a Benzoiru), (4) C 7 - 16 Ararukiru - carbonyl group (e.g., Fuenirua cetyl etc.) , (5) C ^ 6 alkoxy Ichiriki Ruponiru group (e.g., methoxy Cal Poni Le, an ethoxy Cal Poni le), (6) force Rubamoiru group, (7) mono - or di C ^ - 6 Al kill Ichiriki Rubamoiru group (e.g., methylcarbamoyl, etc. dimethylcarbamoyl), (8) mono- or di-primary alkyl one Chiokarubamoiru group (eg, Mechiruchiokaru Bamoiru, dimethylthiocarbamoyl Kalpa moil etc.), (9) C _ 6 alkyl one sulfonyl group (e.g. And methylsulfonyl), (10) C 1 _ 6 alkyl one sulfinyl group (e.g., a methylcarbamoyl Rusurufiniru) and may be used, inter alia formyl is preferred.
R9で示される 「置換基を有していてもよい水酸基」 としては、 例えば、 式— O R9' (R9'は水素原子、 置換基を有していてもよい炭化水素基またはァシル基を示 す) で表される基などが用いられる。 As the "optionally substituted hydroxy group" represented by R 9, for example, the formula - OR 9 '(R 9' may be a hydrogen atom, an optionally substituted hydrocarbon group or Ashiru group The group represented by is used.
R 9,で示される置換基を有していてもよい炭化水素基としては、 A環の置換基と して例示した 「置換基を有していてもよい炭化水素基」 と同様のものが用いられ、 なかでも アルキルなどが好ましい。 As the optionally substituted hydrocarbon group represented by R 9 , those similar to the “optionally substituted hydrocarbon group” exemplified as the substituent for the ring A can be mentioned. Used, and among them, alkyl and the like are preferable.
R9,で示されるァシル基としては、 R1Qで示される 「ァシル基」 と同様のものが 用いられ、 なかでも C i— 6アルキル—力ルポニルなどが好ましい。 As the acyl group represented by R 9 , those similar to the “acyl group” represented by R 1Q can be used, and among them, Ci- 6 alkyl-pyruonyl and the like are preferable.
R9としては、 特に水素原子、 シァノ基、 シァノで置換されていてもよい アルキル基、 ホルミルなどが好ましく、 特に水素原子が好ましい。 Xは(1) 置換基を有していてもよいメチレン基または (2) 力ルポ二ル基を示 す。 ' R 9 is preferably a hydrogen atom, a cyano group, an alkyl group optionally substituted with cyano, formyl, and the like, and particularly preferably a hydrogen atom. X represents (1) a methylene group which may have a substituent or (2) a carbonyl group. '
メチレン基の置換基としては、 上記置換基 A群から選ばれる基な が用いられ、 なかでも 1または 2個の アルキル基 (例、 メチル、 ェチルなど) 、 水酸基な どが好ましい。 As the substituent of the methylene group, a group selected from the above-mentioned substituent group A is used, and among them, one or two alkyl groups (eg, methyl, ethyl, etc.) and a hydroxyl group are preferable.
Xとしては、 (1) 1または 2個の (^_6アルキル基(例、 メチル、ェチルなど) または水酸基を有していてもよいメチレン基または(2)カルボニル基が好ましく、 なかでも 1または 2個のメチルを有していてもよいメチレン基が好ましぐ特にメ チレン基が好ましい。 The X, (1) one or two (^ _ 6 alkyl group (e.g., methyl, good methylene group or (2) a carbonyl group which may have a like) or a hydroxyl group Echiru preferable, 1 or A methylene group which may have two methyl groups is preferred, and a methylene group is particularly preferred.
nは 0または 1を示し、 なかでも 0が好ましい。 n represents 0 or 1, and particularly preferably 0.
本発明の化合物としては、 次のようなものが好ましい。 As the compound of the present invention, the following are preferable.
〔化合物 ( ) — I〕 [Compound ()-I]
R1が式 R 1 is the formula
〔式中、 各記号は前記と同意義を示す〕 で表される基または式 Wherein each symbol is as defined above, or a group represented by the formula:
〔式中、 各記号は前記と同意義を示す〕 で表される基を、 R2および R3がそれぞ れ置換基を有していてもよい炭化水素基を、 R4および R 5が水素原子を、 R6およ び R 7がそれぞれ置換基を有していてもよい炭化水素基を、 R 8が水素原子または 式一 OR1Q (R1Qは、 水素原子、 置換基を有していてもよい炭化水素基、 ァシル 基または置換基を有していてもよい複素環基を示す) を、 R9が水素原子を、 Xが メチレンを示し、 nが 0である化合物 (Γ) またはその塩。 Wherein each symbol is as defined above, R 2 and R 3 each represent a hydrocarbon group which may have a substituent, and R 4 and R 5 represent A hydrogen atom, R 6 and R 7 each represent a hydrocarbon group which may have a substituent, and R 8 represents a hydrogen atom or a formula OR 1Q (R 1Q represents a hydrogen atom or a substituent A hydrocarbon group, an acyl group or a heterocyclic group which may have a substituent), R 9 is a hydrogen atom, X is methylene, and n is 0 (化合物) Or its salt.
〔化合物 (Γ) 一 II〕 R1が式 [Compound (II) II] R 1 is the formula
〔式中、 R16は水素原子、 置換基を有していてもよい C6_14ァリール基、 置換基 を有していてもよいアミノ基、置換基を有していてもよい複素環基またはハロゲン 原子を示す〕 で表される基を、 R2および R3がそれぞれ置換基を有していてもよ い アルキル基を、 R4および R5が水素原子を、 R 6および R 7がそれぞれ置換 基を有していてもよい アルキル基を、 R8が水素原子または式一 OR1 Q (R1 °は、 水素原子、 置換基を有していてもよい炭化水素基、 ァシル基または複素環基 を示す) を、 R 9が水素原子を、 Xがメチレンを示し、 nが 0である化合物 (Γ) またはその塩。 Wherein, R 16 is a hydrogen atom, which may have a substituent C 6 _ 14 Ariru group, an optionally substituted amino group, optionally substituted heterocyclic group Or a halogen atom), R 2 and R 3 each may have an alkyl group, R 4 and R 5 may represent a hydrogen atom, and R 6 and R 7 may represent a hydrogen atom. R 8 represents a hydrogen atom or a group represented by the formula OR 1 Q (R 1 ° represents a hydrogen atom, a hydrocarbon group optionally having a substituent, an acyl group or A compound (Γ) or a salt thereof, wherein R 9 represents a hydrogen atom, X represents methylene, and n is 0.
〔化合物 (Γ) -III] [Compound (Γ) -III]
R1が式 R 1 is the formula
〔式中、 R16は (1)水素原子、 (2)ァセチルァミノ基で置換されたフエニル、 (3)(i) C i_6アルキルスルホニル基、 (ii)ピリジルカルポニルまたは(iii)スルファモイ ルー ^_6アルキル基から選ばれる置換基でモノまたはジ置換されていてもよい ァミノ、 (4)ピリジルまたは(5)ハロゲン原子を示す〕 で表される基を、 R2および R3がそれぞれ C eアルキル基を、 R 4および R 5が水素原子を、 R 6および R 7が それぞれ 6アルキル基を、 R 8が水素原子または式—OR1 Q (R1Qは、 (1)水 素原子、 (2)ピリジルで置換されていてもよい アルキル基または (3)ハロゲン 原子で置換された アルキルスルホニルを示す) を、 R9が水素原子を、 が メチレンを示し、 nが 0である化合物 (Γ) [Wherein, R 16 represents (1) a hydrogen atom, (2) phenyl substituted with an acetylamino group, (3) (i) C i_ 6 alkylsulfonyl group, (ii) pyridylcarponyl or (iii) sulfamoyl ^ _ 6 represents an amino, which may be mono- or di-substituted by a substituent selected from an alkyl group, (4) pyridyl or (5) a halogen atom], wherein R 2 and R 3 are each Ce alkyl R 4 and R 5 are hydrogen atoms; R 6 and R 7 are each 6 alkyl groups; R 8 is a hydrogen atom or a formula —OR 1 Q (R 1Q is (1) hydrogen atom, (2 ) Represents an alkyl group optionally substituted with pyridyl or (3) alkylsulfonyl substituted with a halogen atom), R 9 represents a hydrogen atom, represents methylene, and n represents 0.
〔化合物 ( ) -IV] 実施例 1〜 1 6で製造された化合物またはその塩。 [Compound () -IV] Compounds produced in Examples 1-16 or salts thereof.
本発明の医薬組成物に用いられる式 Formula used in the pharmaceutical composition of the present invention
〔式中、 ——は単結合または二重結合を示す〕 で表される部分構造を有する化合 物としては、 具体的には、 式 [In the formula,-represents a single bond or a double bond] Specifically, the compound having a partial structure represented by the formula:
〔式中、 A環、 B環および C環はそれぞれ前記と同様の置換基を有していてもよい〕 で表される化合物などが用いられ、 より具体的には、 式 [Wherein, ring A, ring B and ring C may each have the same substituent as described above], and the like.
( - 1)(-1)
〔式中、 記号は前記と同意義を示す〕 で表される化合物などが用いられる。 [Wherein the symbols have the same meanings as described above], and the like.
また、 なかでも式 ' In addition, the expression '
〔式中、 R2,、 R3'、 R6'および R7,はそれぞれ アルキル基を、 R16,は水素 原子、 置換基を有していてもよい C6 14ァリール基、 置換基を有していてもよい アミノ基、置換基を有していてもよい複素環基またはハロゲン原子を示す〕で表さ れる部分構造を有する化合物などが好ましい。 Wherein, R 2 ,, R 3 ', R 6' and R 7, each represents an alkyl group, R 16, are hydrogen atoms, which may have a substituent C 6 14 Ariru group, a substituent Which may have an amino group, a heterocyclic group which may have a substituent or a halogen atom].
本発明の化合物 (A-1) 、 (1-1) または (Ι'- 1) としては、 具体的には、 実施例 1〜16で製造された化合物などが用いられる。 As the compound (A-1), (1-1) or (Ι′-1) of the present invention, specifically, the compounds produced in Examples 1 to 16 and the like are used.
本発明の化合物 (I) および (Γ) の释造法について以下に述べる。 なお、 化合 物 (la) は化合物 (I) に含まれる化合物である。 The method for producing the compounds (I) and (II) of the present invention will be described below. Compound (la) is a compound included in compound (I).
本発明の化合物 (I) および (Γ) は、 例えば以下の反応式 1および 2で示され る方法またはこれに準じた方法等により得られる。 The compounds (I) and (Γ) of the present invention can be obtained, for example, by the method represented by the following reaction formulas 1 and 2, or a method analogous thereto.
なお、 化合物 (A) 、 (A— 1) 、 (1 - 1) , (Γ— 1) も下記の製造法に準 じて製造することができる。 Compounds (A), (A-1), (1-1) and (II-1) can also be produced according to the following production method.
以下の反応式の略図中の化合物の各記号は特に記載のないかぎり前記と同意義 を示す。 反応式中の化合物 (Π) 〜 (VI) および (νπ') 〜 (ΧΙΙΓ) は塩を形成 している場合も含み、 該塩としては、 例えば化合物 (I) または (Γ) の塩と同様 のもの等が挙げられる。 Each symbol of the compounds in the following schemes has the same meaning as described above unless otherwise specified. The compounds (Π) to (VI) and (νπ ') to (ΧΙΙΓ) in the reaction formula include those in the form of a salt. Examples of the salt include the same as the salt of the compound (I) or (Γ). And the like.
化合物 (II) 、 (III) 、 (IV) 、 (VI) 、 (VII' ) 、 (VIII') 、 (XI' ) およ び(ΧΙΓ) は市販されているものを容易に入手でき、 また、 自体公知の方法または これらに準じた方法に従つて製造することもできる。 Compounds (II), (III), (IV), (VI), (VII '), (VIII'), (XI ') and (II) are readily available commercially, and It can also be produced according to a method known per se or a method analogous thereto.
以下の反応で用いられる、総称で示される溶媒としては、特に記載がないかぎり、 アルコール類としてメタノール、 エタノール、 1 一プロパノール、 2—プロパノー ル、 ter t-ブチルアルコールなど、 エーテル類としてジェチルエーテル、 ジイソプ 口ピルエーテル、ジフエニルエーテル、テトラヒドロフラン、 1, 4—ジォキサン、 1, 2—ジメトキシェタンなど、 炭化水素類としてベンゼン、 トルエン、 シクロへ キサン、 へキサンなど、 アミド類として N, N—ジメチルホルムアミド、 N, N— ジメチルァセトアミド、へキサメチルホスホリックトリアミドなど、ハロゲン化炭 化水素類としてジクロロメタン、 クロ口ホ^/ム、 四塩化炭素、 1, 2—ジクロロェ タンなど、 二トリル類としてァセトニトリル、 プロピオ二トリルなど、 ケトン類と してアセトン、 ェチルメチルケトンなど、 有機酸類としてギ酸、酢酸、 プロピオン 酸、 トリフルォロ酢酸、メタンスルホン酸など、芳香族ァミン類として、ピリジン、 2 , 6—ルチジン、 キノリンなど、 スルホキシド類としてジメチルスルホキシドな どを示す。 As the solvent used in the following reactions and represented by a generic name, unless otherwise specified, Alcohols such as methanol, ethanol, 1-propanol, 2-propanol, tert-butyl alcohol, etc. Ethers such as getyl ether, diisopropyl ether, diphenyl ether, tetrahydrofuran, 1,4-dioxane, 1,2 —Dimethoxyethane, etc. Hydrocarbons such as benzene, toluene, cyclohexane and hexane, and amides such as N, N-dimethylformamide, N, N—dimethylacetamide, hexamethylphosphoric triamide Halogenated hydrocarbons such as dichloromethane, chloroform, carbon tetrachloride, and 1,2-dichloroethane; nitriles such as acetonitrile and propionitrile; ketones such as acetone and ethyl methyl ketone Organic acids such as formic acid, acetic acid, Acid, Torifuruoro acetic acid, methanesulfonic acid, aromatic Amin compounds show pyridine, 2, 6-lutidine, quinoline, etc., and etc. dimethylsulfoxide as sulfoxides.
以下の反応で用いられる、総称で示される塩基としては、特に記載がないかぎり、 無機塩基類として水酸化ナトリウム、 水酸化カリウム、水酸化リチウム、 水酸化バ リウムなど、 塩基性塩類として炭酸ナトリウム、 炭酸カリウム、 炭酸セシウム、 炭 酸水素ナトリウム、 酢酸ナトリウム、 酢酸アンモニゥムなど、 芳香族ァミン類とし てピリジン、 ルチジンなど、 第 3級ァミン類としてトリェチルァミン、 トリプロピ ルァミン、 トリプチルァミン、 N—ェチルジィソプロピルァミン、 シクロへキシル ジメチルァミン、 4ージメチルァミノピリジン、 N, N—ジメチルァニリン、 N— メチルピペリジン、 N—メチルピロリジン、 N—メチルモルホリンなど、 アルカリ 金属水素化物類として水素化ナトリウム、水素化カリウムなど、金属アミド類とし てナトリウムアミド、 リチウムジイソプロピルアミド、 リチウムへキサメチルジシ ラジドなど、 アルキル金属類としてブチルリチウム、 tert-ブチルリチウムなど、 ァリール金属類としてフエ二ルリチウムなど、金属アルコキシド類としてナトリウ ムメトキシド、 ナトリウムエトキシド、 ナトリウム tert-ブトキシド、 カリウム t er t -ブトキシドなどを示す。 Unless otherwise specified, the bases used in the following reactions and represented by a generic name include sodium hydroxide, potassium hydroxide, lithium hydroxide and barium hydroxide as inorganic bases, sodium carbonate as basic salts, and the like. Potassium carbonate, cesium carbonate, sodium hydrogen carbonate, sodium acetate, ammonium acetate, etc. Pyridine, lutidine, etc. as aromatic amines, Triethylamine, trippropylamine, triptylamine, N-ethyldiisopropylamine as tertiary amines Sodium hydride, alkali metal hydrides such as amine, cyclohexyl dimethylamine, 4-dimethylaminopyridine, N, N-dimethylaniline, N-methylpiperidine, N-methylpyrrolidine, N-methylmorpholine Metals such as potassium Alkoxides such as sodium amide, lithium diisopropylamide, and lithium hexamethyldisilazide; alkyl metals such as butyllithium and tert-butyllithium; aryl metals such as phenyllithium; and metal alkoxides such as sodium methoxide and sodium ethoxide. Sodium tert-butoxide, potassium tert-butoxide and the like.
生成物は反応液のまま、 あるいは粗製物として次反応に用いることもできるが、 常法に従って反応混合物から単離することもでき、 通常の分離手段 (例、 再結晶、 蒸留、 クロマトグラフィー等) により容易に精製することもできる。 化合物 (la) 〔式中、 C'環は R R2および R3以外に置換基を有していても よい〕 は反応式 1に示した工程によって製造される。 The product can be used in the next reaction as a reaction solution or as a crude product, but it can also be isolated from the reaction mixture according to a conventional method, and can be separated by a usual separation method (eg, recrystallization, distillation, chromatography, etc.). Can be easily purified. Compound (la) wherein the C ′ ring may have a substituent other than RR 2 and R 3 is produced by the process shown in Reaction Scheme 1.
Rj¾、式 1 Rj¾, Equation 1
(II) (II)
R R
、P+(R 3(hal)- (IV) , P + (R 3 (hal)-(IV)
(V) (V)
化合物 (I I I) は化合物 (I I) をマグネシウムあるいは塩基を用いて有機金属化 合物に変換し、 ホルミル化剤と反応させることにより製造される。 Compound (III) is produced by converting compound (II) into an organometallic compound using magnesium or a base, and reacting the compound with a formylating agent.
該「塩基」 としては、 アルキル金属類、 ァリール金属類などが挙げられる。塩基 の使用量は、 化合物 (Π) 1モルに対し約 1ないし約 5モル、 好ましくは約 1ない し約 2モルである。 Examples of the “base” include alkyl metals, aryl metals and the like. The amount of the base to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound (II).
該「ホルミル化剤」 としては、 N, N—ジメチルホルムアミド、 1—ホルミルピ ペリジン、 4 _ホルミルモルホリン、 N—メチルホルムァニリドなどが挙げられる。 ホルミルィ匕剤の使用量は、 化合物(I I) 1モルに対し約 1ないし約 1 0モル、 好ま しくは約 1ないし約 5モルである。 Examples of the "formylating agent" include N, N-dimethylformamide, 1-formylpiperidine, 4-formylmorpholine, N-methylformanilide and the like. The amount of the formylide used is about 1 to about 10 mol, preferably about 1 to about 5 mol, per 1 mol of compound (II).
本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒とし ては反応が進行する限り特に限定されないが、例えばエーテル類、炭化水素類など の溶媒またはこれらの混合溶媒などが好ましい。 This reaction is advantageously performed using a solvent inert to the reaction. The solvent is not particularly limited as long as the reaction proceeds, but is preferably, for example, a solvent such as ethers or hydrocarbons, or a mixed solvent thereof.
反応時間は通常約 1 0分ないし約 4 8時間、好ましくは約 3 0分ないし約 2 4時 間である。反応温度は通常約— 1 0 0ないし約 1 5 0 °C、好ましくは約一 8 0ない し約 1 0 0 °Cである。 The reaction time is generally about 10 minutes to about 48 hours, preferably about 30 minutes to about 24 hours. The reaction temperature is usually about −100 to about 150 ° C., preferably about 180 to about 100 ° C.
化合物 (V) は、 化合物 (I I I) と化合物 (IV) 〔式中、 R 2 2は炭化水素基、 hal はハロゲンを示す〕とを所望により塩基の存在下で反応させることにより製造され る。 Compound (V), the compound (III) with the compound (IV) wherein, R 2 2 is a hydrocarbon group, hal is a halogen] Ru is prepared by reacting in the presence of a base optionally a.
該 「炭化水素基」 としては、 例えば、 鎖状または環状炭化水素基 (例、 _6ァ ルキル (例えば、 メチル、ェチル、 プロピル、イソプロピル、 ブチル、イソプチル、 sec -プチル、 ter t-プチル、 ペンチル、 へキシルなど) 、 C 3_ 6シクロアルキル(例 えば、 シクロプロピル、 シクロブチル、 シクロペンチル、 シクロへキシルなど) 、 C 6— 1 4ァリール (例えば、 フエニル、 1 一ナフチル、 2—ナフチル、 ビフエ二リ ル、 2—アンスリルなど) など) などが挙げられる。 As the "hydrocarbon group" include chain or cyclic hydrocarbon group (e.g., _ 6 § alkyl (e.g., methyl, Echiru, propyl, isopropyl, butyl, Isopuchiru, sec - heptyl, ter t-heptyl, pentyl , the like hexyl), C 3 _ 6 cycloalkyl (eg example, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexylene hexyl, etc.), C 6 - 1 4 Ariru (e.g., phenyl, 1 one-naphthyl, 2-naphthyl, Bifue two Lilly, 2-anthryl, etc.).
化合物 (IV) の使用量は、 化合物 (I I I) 1モルに対し約 1ないし約 5モル、 好 ましくは約 1ないし約 2モルである。 The amount of compound (IV) to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound (III).
該 「塩基」 としては、 例えば無機塩基類、 塩基性塩類、 芳香族ァミン類、 第 3級 アミン類、 アルカリ金属水素化物類、 アルキル金属類、 ァリール金属類、 金属アミ ド類、 金属アルコキシド類等が挙げられる。 塩基の使用量は、 化合物 (I I I) 1モ ルに対し約 1ないし約 5モル、 好ましくは約 1ないし約 2モルである。 Examples of the "base" include inorganic bases, basic salts, aromatic amines, tertiary amines, alkali metal hydrides, alkyl metals, aryl metals, metal amides, metal alkoxides and the like. Is mentioned. The amount of base used is the same as that of compound (III) About 1 to about 5 moles, preferably about 1 to about 2 moles, based on
本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒とし ては反応が進行する限り特に限定されないが、 例えばアルコール類、 エーテル類、 炭化水素類、 アミド類、 ハロゲン化炭化水素類、 二トリル類、 スルホキシド類、 水 などの溶媒またはこれらの混合溶媒などが好ましい。 This reaction is advantageously performed using a solvent inert to the reaction. Such a solvent is not particularly limited as long as the reaction proceeds, but examples thereof include solvents such as alcohols, ethers, hydrocarbons, amides, halogenated hydrocarbons, nitriles, sulfoxides, and water. Are preferred.
反応時間は通常約 3 0分ないし約 4 8時間、好ましくは約 1時間ないし約 2 4時 間である。反応温度は通常約一 1 0 0ないし約 2 0 0 °C、好ましくは約一 8 0ない し約 1 5 0 °Cである。 The reaction time is usually about 30 minutes to about 48 hours, preferably about 1 hour to about 24 hours. The reaction temperature is usually about 100 to about 200 ° C, preferably about 180 to about 150 ° C.
化合物 (la) は、 化合物 (V) と化合物 (VI) とを酸存在下反応させることによ り製造される。 Compound (la) is produced by reacting compound (V) with compound (VI) in the presence of an acid.
化合物 (VI) の使用量は、 化合物 (V) 1モルに対し約 0 . 5ないし約 5モル、 好ましくは約 0 . 5ないし約 2モルである。 The amount of compound (VI) to be used is about 0.5 to about 5 mol, preferably about 0.5 to about 2 mol, per 1 mol of compound (V).
該「酸」 としては、硫酸、塩化水素、臭化水素、 ヨウ化水素、過塩素酸等の鉱酸、 三フッ化ホウ素ジェチルエーテル錯体、塩化亜鉛、塩化アルミニウム等のルイス酸 等が用いられる。 酸の使用量は化合物 (V) 1モルに対し約 1ないし約 5モル、 好 ましくは約 1ないし約 3モルである。 Examples of the "acid" include mineral acids such as sulfuric acid, hydrogen chloride, hydrogen bromide, hydrogen iodide, and perchloric acid; boron trifluoride dimethyl ether complex; Lewis acids such as zinc chloride and aluminum chloride; . The amount of the acid to be used is about 1 to about 5 mol, preferably about 1 to about 3 mol, per 1 mol of compound (V).
本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒とし ては反応が進行する限り特に限定されないが、例えば炭化水素類、 有機酸類、ハロ ゲン化炭化水素類またはこれらの混合物等が好ましい。 ' 反応時間は通常約 1 0分ないし約 4 8時間、好ましくは約 1 5分ないし約 2 4時 間である。反応温度は通常約一 2 0ないし約 1 5 0 °C、好ましくは約 0ないし約 1 0 o °cである。 This reaction is advantageously performed using a solvent inert to the reaction. The solvent is not particularly limited as long as the reaction proceeds, but is preferably, for example, a hydrocarbon, an organic acid, a halogenated hydrocarbon, or a mixture thereof. The reaction time is generally about 10 minutes to about 48 hours, preferably about 15 minutes to about 24 hours. The reaction temperature is usually about 120 to about 150 ° C, preferably about 0 to about 10 ° C.
化合物 (Γ ) は反応式 2に示した工程によって製造される。 反応式 2 Compound (Γ) is produced by the process shown in Reaction Scheme 2. Reaction formula 2
(Ι') (X = CH2, n = o) 化合物 (ΙΧ') は、 化合物 (νΐΓ) と化合物 (νΐΐΓ) 〔式中、 R23および R24 は、 R7の一部を形成する、 置換基を有していてもよい炭化水素基で、 R7と同様 のものが挙げられ、 Wは脱離基を示す〕 とを所望により塩基の存在下で反応させる ことにより製造される。 (Ι ') (X = CH 2 , n = o) The compound (ΙΧ ′) is a compound (νΐΓ) and a compound (νΐΐΓ) wherein R 23 and R 24 are a hydrocarbon group which may form a part of R 7 and may have a substituent. those similar to R 7 can be exemplified, W is is prepared by reacting in the presence of a base as desired and represents a leaving group].
該「脱離基」 としては、 例えばヒドロキシ、 ハロゲン原子 (例えば、 フッ素、 塩 素、 臭素、 ヨウ素等) 、 ハロゲン化されていてもよい Ci-sアルキルスルホニルォ キシ (例えば、 メタンスルホニルォキシ、 ェ夕ンスルホニルォキシ、 トリクロロメ タンスルホニルォキシ等) 、 置換基を有していてもよい C6一 1()ァリールスルホニ ルォキシ等が挙げられる。 「置換基を有していてもよい 。ァリ一ルスルホニ ルォキシ」 としては、 例えば (: 6アルキル (例、 メチル、 ェチル等) 、 ( 6ァ ルコキシ (例、 メトキシ、 エトキシ等) およびニトロから選ばれる置換基を 1ない し 3個有していてもよい C6_1Q7リールスルホニルォキシ (例、 フエニルスルホ ニルォキシ、 ナフチルスルホニルォキシ等) 等が挙げられ、 具体例としては、 ベン ゼンスルホニルォキシ、 m—二トロベンゼンスルホニルォキシ、 p—トルエンスル ホニルォキシ等が挙げられる。 Examples of the “leaving group” include hydroxy, halogen atom (eg, fluorine, chlorine, bromine, iodine, etc.), and optionally halogenated Ci-s alkylsulfonyloxy (eg, methanesulfonyloxy, E evening down sulfonyl O carboxymethyl, trichloro methane sulfonyl O carboxymethyl, etc.), one C 6 which may have a substituent 1 () Arirusuruhoni Ruokishi the like. ". Which may have a substituent § Li one Rusuruhoni Ruokishi" as, for example (6 alkyl (e.g., methyl, Echiru etc.), selected from (6 § alkoxy (e.g., methoxy, ethoxy, etc.) and nitro C 6 _ 1Q 7 reelsulfonyloxy (e.g., phenylsulfonyloxy, naphthylsulfonyloxy, etc.) which may have 1 to 3 substituents, and specific examples thereof include benzenesulfonyl Xy, m-nitrobenzenesulfonyloxy, p-toluenesulfonyloxy and the like.
化合物 (VIII') の使用量は、化合物 (VII') 1モルに対し約 1ないし約 5モル、 好ましくは約 1ないし約 2モルである。 The amount of compound (VIII ′) to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound (VII ′).
該「塩基」 としては、 例えば無機塩基類、 塩基性塩類、 芳香族ァミン類、 第 3級 アミン類、 金属水素化物類、 金属アミド類、 金属アルコキシド類等が挙げられる。 塩基の使用量は、 化合物 (νΐΓ) 1モルに対し約 1ないし約 5モル、 好ましくは約 1ないし約 2モルである。 Examples of the “base” include inorganic bases, basic salts, aromatic amines, tertiary amines, metal hydrides, metal amides, metal alkoxides and the like. The amount of the base to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of compound (νΐΓ).
本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒とし ては反応が進行する限り特に限定されないが、 例えばアルコール類、 エーテル類、 炭化水素類、 アミド類、 ハロゲン化炭化水素類、 二トリル類、 ケトン類、 スルホキ シド類等の溶媒またはこれらの混合溶媒等が好ましい。 This reaction is advantageously performed using a solvent inert to the reaction. Such a solvent is not particularly limited as long as the reaction proceeds, and examples thereof include solvents such as alcohols, ethers, hydrocarbons, amides, halogenated hydrocarbons, nitriles, ketones, and sulfoxides. Alternatively, a mixed solvent thereof is preferable.
反応時間は通常約 15分ないし約 48時間、好ましくは約 30分ないし約 24時 間である。反応温度は通常約一 20ないし約 150°C、好ましくは約 0ないし約 1 00°Cである。 The reaction time is usually about 15 minutes to about 48 hours, preferably about 30 minutes to about 24 hours. The reaction temperature is generally about 120 to about 150 ° C, preferably about 0 to about 100 ° C.
前記反応に代え、 光延反応 (シンセシス (Synthesis) 、 1981年、 1〜27 頁) を用いることもできる。 Instead of the above reaction, Mitsunobu reaction (Synthesis, 1981, 1-27) Page) can also be used.
該反応は、 化合物 (νΐ Γ ) と化合物 (νΐ ΐ Γ ) 中、 Wが Ο Ηである化合物とを、 ァゾジカルボキシラート類(例、 ジェチルァゾジカルボキシラート等)およびホス フィン類(例、 トリフエニルホスフィン、 トリブチルホスフィン等) の存在下反応 させる。 In the reaction, the compound (νΐ Γ) and the compound (νΐ ΐ Γ) in which W is Ο を are reacted with an azodicarboxylate (eg, getyl azodicarboxylate, etc.) and a phosphine (Eg, triphenylphosphine, tributylphosphine, etc.).
化合物 (νΐ Π' ) 中、 Wが ΟΗである化合物の使用量は、 化合物 (νΐ Γ ) 1モル に対し、 約 1ないし約 5モル、 好ましくは約 1ないし約 2モルである。 The amount of the compound in which W is 中 in the compound (νΐ Π ′) is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of the compound (νΐ Π).
該「ァゾジカルボキシラート類」 および「ホスフィン類」 の使用量は、 それぞれ 化合物 (νΐ Γ ) 1モルに対し、 約 1ないし約 5モル、 好ましくは約 1ないし約 2モ ルである。 The amount of the “azodicarboxylates” and “phosphines” to be used is about 1 to about 5 mol, preferably about 1 to about 2 mol, per 1 mol of the compound (νΐ)).
本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒とし ては反応が進行する限り特に限定されないが、 例えばエーテル類、 炭化水素類、 ァ ミド類、 ハロゲン化炭ィ匕水素類、 二トリル類、 ケトン類、 スルホキシド類等の溶媒 またはそれらの混合溶媒等が好ましい。 This reaction is advantageously performed using a solvent inert to the reaction. Such a solvent is not particularly limited as long as the reaction proceeds, but examples thereof include solvents such as ethers, hydrocarbons, amides, halogenated carbons, nitriles, ketones, and sulfoxides. Preferred are mixed solvents thereof.
反応時間は通常約 5分ないし約 4 8時間、好ましくは約 1 0分ないし約 2 4時間 である。反応温度は通常約一 2 0ないし約 2 0 O 、好ましくは約 0ないし約 1 0 0 である。 The reaction time is generally about 5 minutes to about 48 hours, preferably about 10 minutes to about 24 hours. The reaction temperature is usually about 120 to about 200, preferably about 0 to about 100.
化合物(Χ' )は、化合物(ΙΧ' ) をクライゼン転位させることにより製造される。 本反応は、 無溶媒で行うか、'反応に不活性な溶媒を用いて行うのが有利である。 このような溶媒としては、反応が進行する限り特に限定されないが、例えばアルコ ール類、 炭化水素類、 有機酸類、 ェ一テル類、 ァニリン類 (例、 Ν, Ν—ジメチル ァニリン、 Ν, Ν—ジェチルァニリンなど) 、 フエノール類 (例、 2 , 6—ジメチ ルフエノールなど)、ハロゲン化炭化水素類またはこれらの混合溶媒などが用いら れる。 Compound (Χ ′) is produced by subjecting compound (ΙΧ ′) to Claisen rearrangement. This reaction is advantageously performed without a solvent or using a solvent inert to the reaction. Such a solvent is not particularly limited as long as the reaction proceeds. For example, alcohols, hydrocarbons, organic acids, ethers, and anilines (eg, Ν, Ν-dimethyl aniline, Ν, Ν — Phenethylaniline, etc.), phenols (eg, 2,6-dimethylphenol), halogenated hydrocarbons, or a mixed solvent thereof.
また、所望により酸触媒を用いて本反応を行ってもよい。酸触媒としては、塩化 アルミニウム、ミ臭化ホウ素等のルイス酸類などが用いられる。酸触媒の使用量は、 例えばルイス酸の場合、 通常化合物 (IX' ) 1モルに対し約 0 . 1ないし約 2 0モ ル、 好ましくは約 0 . 1ないし約 5モルである。 反応時間は通常約 3 0分ないし約 2 4時間、好ましくは約 1ないし約 8時間である。反応温度は通常約— 7 0ないし 約 30 Ot:、 好ましくは約 150ないし約 250°Cである。 This reaction may be performed using an acid catalyst, if desired. As the acid catalyst, Lewis acids such as aluminum chloride and boron bromide are used. The amount of the acid catalyst to be used is, for example, in the case of a Lewis acid, usually about 0.1 to about 20 mol, preferably about 0.1 to about 5 mol, per 1 mol of compound (IX '). The reaction time is usually about 30 minutes to about 24 hours, preferably about 1 to about 8 hours. The reaction temperature is usually about -70 to About 30 Ot: preferably about 150 to about 250 ° C.
化合物 (ΧΓ) は化合物 (Χ') をプロトン酸、 ルイス酸またはヨウ素存在下、 閉 環することにより製造することができる。 プロトン酸としては、 例えば塩酸、臭化 水素酸、硫酸等の鉱酸類やメタンスルホン酸、 トリフルォロメ夕ンスルホン酸、 フ ルォロスルホン酸等のスルホン酸類が、ルイス酸類としては例えば塩化アルミニゥ ム、臭化アルミニウム、塩化チタン(ιν)、塩化すず αν)、塩化亜鉛、三塩化ホウ素、 三臭化ホウ素、三フッ化ホウ素等が用いられる。通常、 プロトン酸あるいはルイス 酸はそれぞれ単独で用いられるが、所望により両者を組み合わせてもよい。プロト ン酸を用いる場合は、 化合物 α') 1モルに対し約 1ないし約 200モル、 好まし くは約 1ないし約 100モル用いる。 ルイス酸を用いる場合は、 化合物 (Χ') 1モ ルに対し約 1ないし約 5モル、好ましくは約 1ないし約 3モル用いる。 ヨウ素を用 いる場合は化合物 (Χ' ) 1モルに対し約 0. 05ないし約 1モル、好ましくは約 0. 1ないし約 0. 5モル用いる。 Compound (ΧΓ) can be produced by cyclizing compound (Χ ') in the presence of a protonic acid, a Lewis acid or iodine. Examples of protic acids include mineral acids such as hydrochloric acid, hydrobromic acid, and sulfuric acid, and sulfonic acids such as methanesulfonic acid, trifluoromethanesulfonic acid, and fluorosulfonic acid. Examples of Lewis acids include aluminum chloride, aluminum bromide, and the like. Titanium chloride (ιν), tin chloride αν), zinc chloride, boron trichloride, boron tribromide, boron trifluoride and the like are used. Usually, a protonic acid or a Lewis acid is used alone, but both may be combined as desired. When using protonic acid, it is used in an amount of about 1 to about 200 mol, preferably about 1 to about 100 mol, per 1 mol of the compound α '). When a Lewis acid is used, it is used in an amount of about 1 to about 5 mol, preferably about 1 to about 3 mol, per 1 mol of compound (Χ ′). When iodine is used, it is used in an amount of about 0.05 to about 1 mol, preferably about 0.1 to about 0.5 mol, per 1 mol of the compound (Χ ′).
本反応は反応に不活性な溶媒を用いて行なうのが有利である。このような溶媒と して反応が進行する限り特に限定されないが、例えばェ一テル類、炭化水素類、 ァ ルコール類、 アミド類、 ハロゲン化炭化水素類、 二トリル類、 ケトン類、 スルホキ シド類等の溶媒またはこれらの混合溶媒等が好ましい。反応温度は通常約— 20な いし約 150で、好ましくは約 0ないし約 120°Cである。反応時間は通常約 5分 ないし約 24時間、 好ましくは約 10分ないし約 5時間である。 This reaction is advantageously performed using a solvent inert to the reaction. There is no particular limitation as long as the reaction proceeds as such a solvent, but examples thereof include ethers, hydrocarbons, alcohols, amides, halogenated hydrocarbons, nitriles, ketones, and sulfoxides. Or a mixed solvent thereof is preferred. The reaction temperature is usually about -20 to about 150, preferably about 0 to about 120 ° C. The reaction time is usually about 5 minutes to about 24 hours, preferably about 10 minutes to about 5 hours.
化合物 (ΧΙΓ) は、 化合物 (II) から化合物 (III) を製造するときと同様にし て、 化合物 (ΧΓ) から製造される。 Compound (II) is produced from compound (II) in the same manner as when producing compound (III) from compound (II).
化合物 ( ΙΙΙ') は、 化合物 (III) と化合物 (IV) から化合物 (V) を製造する ときと同様にして、 化合物 αΐΓ) と化合物 (IV) 〔式中、 R22および hal は上 記と同意義を示す〕 力、ら製造される。 Compound (ΙΙΙ ') can be prepared in the same manner as in the production of compound (V) from compound (III) and compound (IV); compound αΐΓ) and compound (IV) wherein R 22 and hal are as defined above. Show the same significance].
化合物 (Γ) は、 化合物 (V) と化合物 (VI) から化合物 (la) を製造するとき と同様にして、 化合物 απι') と化合物 (VI) から製造される。 Compound (Γ) is produced from compound απι ′) and compound (VI) in the same manner as in the production of compound (la) from compound (V) and compound (VI).
上記反応により、 化合物(r)において Xがメチレンである化合物を製造するこ とができる。また、 このようにして得られた化合物を所望により自体公知の反応に 基づき官能基変換を行うことにより、 Xが置換基を有するメチレンおよび力ルポ二 ルである化合物に変換することができる。 By the above reaction, a compound in which X is methylene in compound (r) can be produced. The compound thus obtained is optionally subjected to a functional group conversion based on a reaction known per se, whereby X is a substituted methylene and a carbonyl compound. Can be converted to a compound that is
上記各反応において、原料化合物が置換基としてァミノ、 カルボキシ、 ヒドロキ シを有する場合、これらの基にペプチド化学等で一般的に用いられるような保護基 が導入されたものであってもよく、反応後に必要に応じて保護基を除去することに より目的化合物を得ることができる。 In each of the above reactions, when the starting compound has an amino, carboxy, or hydroxy substituent, a protecting group generally used in peptide chemistry or the like may be introduced into these groups. The target compound can be obtained by removing the protecting group as necessary.
ァミノの保護基としては、例えばホルミルまたはそれぞれ置換基を有していても よい アルキル一力ルポニル (例えば、 ァセチル、 プロピオニル等) 、 ベンゾ ィル、 C卜6アルコキシ—カルボニル (例えば、 メトキシカルポニル、 エトキシカ ルポニル等) 、 フエニルォキシカルポニル、 c 7 _ 1 6ァラルキルォキシ一力ルポ二 ル (例えば、 ベンジルォキシカルポニル等) 、 トリチル、 フタロイル等が用いられ る。 これらの置換基としては、 ハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ 素等) 、 6アルキル一力ルポニル (例えば、 ァセチル、 プロピオニル、 パレリ ル等) 、 ニトロ等が用いられ、 置換基の数は 1ないし 3個程度である。 The protecting group of Amino, for example, formyl or each alkyl Ichiriki be substituted Ruponiru (e.g., Asechiru, propionyl, etc.), benzo I Le, C WINCH 6 alkoxy - carbonyl (e.g., methoxy Cal Poni Le, Etokishika Ruponiru etc.), phenylalanine O carboxymethyl Cal Poni le, c 7 _ 1 6 Ararukiruokishi Ichiriki Lupo two Le (e.g., benzyl O carboxymethyl cull Poni Le etc.), trityl, phthaloyl and the like Ru is used. As these substituents, a halogen atom (for example, fluorine, chlorine, bromine, iodine, etc.), a 6- alkyl monopropanol (for example, acetyl, propionyl, parryl, etc.), nitro and the like are used. Is about one to three.
力ルポキシの保護基としては、 例えばそれぞれ置換基を有していてもよい アルキル (例えば、 メチル、 ェチル、 プロピル、 イソプロピル、 ブチル、 ter t-ブ チル等)、フエニル、 トリチル、シリル等が用いられる。これらの置換基としては、 ハロゲン原子 (例えば、 フッ素、 塩素、 臭素、 ヨウ素等) 、 ホルミル、 (^_6アル キル一力ルポニル (例えば、 ァセチル、 プロピオニル、 ブチルカルボニル等) 、 二 トロ、 C — 6アルキル (例えば、 メチル、 ェチル、 ter t-ブチル等) 、 C 6— 1 4ァリ —ル (例えば、 フエニル、 ナフチル等) 等が用いられ、 置換基の数は 1ないし 3個 程度である。 Examples of the protecting group for alkoxy include alkyl which may have a substituent (eg, methyl, ethyl, propyl, isopropyl, butyl, tert-butyl, etc.), phenyl, trityl, silyl, etc. . Examples of these substituents include halogen atom (e.g., fluorine, chlorine, bromine, iodine), formyl, (^ _ 6 Al kills one force Ruponiru (e.g., Asechiru, propionyl, butylcarbonyl, etc.), Two Toro, C - 6 alkyl (e.g., methyl, Echiru, ter t-butyl, etc.), C 6 - 1 4 § Li - Le (e.g., phenyl, naphthyl and the like) and the like are used, and the number of substituents is 3 or so from 1 .
ヒドロキシの保護基としては、例えばホルミル、 またはそれぞれ置換基を有して いてもよい — 6アルキル (例えば、 メチル、 ェチル、 プロピル、 イソプロピル、 プチル、 ter t-ブチル等)、 フエニル、 〇7 _ 1 6ァラルキル (例えば、 ベンジル等)、 一 6アルキル一力ルポニル (例えば、 ァセチル、 プロピオニル等) 、 フエニルォ キシカルポニル、 C 7— 1 6ァラルキルォキシ一力ルポニル (例えば、 ベンジルォキ シカルボニル等) 、 テトラヒドロビラニル、 テトラヒドロフラエル、 シリル等が用 いられる。 これらの置換基としては、ハロゲン原子(例えば、 フッ素、塩素、臭素、 ヨウ素等) 、 6アルキル (例えば、 メチル、 ェチル、 tert—ブチル等) 、 C 7 ― 1 6ァラルキル (例えば、 ベンジル等) 、 C 6_ 1 47リール (例えば、 フエニル、 ナ フチル等) 、 ニトロ等が用いられ、 置換基の数は 1ないし 4個程度である。 Examples of the hydroxy-protecting group include formyl, or each of which may have a substituent — 6-alkyl (eg, methyl, ethyl, propyl, isopropyl, butyl, tert-butyl, etc.), phenyl, 〇 7 _ 1 6 Ararukiru (e.g., benzyl, etc.), single 6 alkyl Ichiriki Ruponiru (e.g., Asechiru, propionyl, etc.), Fueniruo Kishikaruponiru, C 7 - 1 6 Ararukiruokishi Ichiriki Ruponiru (e.g., Benjiruoki aryloxycarbonyl, etc.), tetrahydronaphthalene Villa alkenyl, Tetrahydrofurel, silyl, etc. are used. These substituents include a halogen atom (eg, fluorine, chlorine, bromine, iodine, etc.), 6- alkyl (eg, methyl, ethyl, tert-butyl, etc.), C 7 - 1 6 Ararukiru (e.g., benzyl etc.), C 6 _ 1 4 7 reel (e.g., phenyl, naphthyl, etc.), nitro and the like are used, and the number of the substituents is about four from 1.
また、保護基の除去方法としては、 自体公知またはそれに準じる方法が用いられ るが、 例えば酸、 塩基、 紫外光、 ヒドラジン、 フエニルヒドラジン、 N—メチルジ チォカルバミン酸ナトリウム、テトラプチルアンモニゥムフルオリド、酢酸パラジ ゥム(I I)等で処理する方法または還元反応が用いられる。 As a method for removing the protecting group, a method known per se or a method analogous thereto is used. Examples thereof include an acid, a base, ultraviolet light, hydrazine, phenylhydrazine, sodium N-methyldithiocarbamate, and tetrabutylammonium fluoride. , A method of treating with palladium (II) acetate or the like, or a reduction reaction is used.
いずれの場合にも、 さらに所望により、 脱保護反応、 ァシル化反応、 アルキル化 反応、水素添加反応、酸化反応、還元反応、炭素鎖延長反応、置換基交換反応を各々、 単独あるいはその二つ以上を組み合わせて行うことにより化合物 (A) 、 (I) 、 (1' ) 、 (A-1) 、 (1-1) または (Ι'- 1) を合成することができる。 これらの反応 は、 例えば、 新実験化学講座 1 4、 1 5巻、 1 9 7 7年 (丸善出版) 等に記載の方 法が採用される。 In any case, if desired, a deprotection reaction, an acylation reaction, an alkylation reaction, a hydrogenation reaction, an oxidation reaction, a reduction reaction, a carbon chain extension reaction, and a substituent exchange reaction may be used alone or in combination of two or more. By carrying out in combination, compounds (A), (I), (1 ′), (A-1), (1-1) or (Ι′-1) can be synthesized. For these reactions, for example, the methods described in New Experimental Chemistry Lectures 14, 15 and 1977 (Maruzen Publishing) are adopted.
上記反応により、 目的物が遊離の状態で得られる場合には、常法に従って塩に変 換してもよく、 また塩として得られる場合には、常法に従って遊離体または他の塩 に変換することもできる。かくして得られる化合物(A;)、 (1)、 (Γ )、 (Α-1) , (I - 1) または ( - 1) は、 公知の手段例えば転溶、 濃縮、 溶媒抽出、 分溜、 結晶 化、再結晶、 クロマトグラフィー等により反応溶液から単離、精製することができ る。 When the desired product is obtained in a free state by the above reaction, it may be converted to a salt according to a conventional method, and when obtained as a salt, converted to a free form or another salt according to a conventional method. You can also. The compound (A;), (1), (Γ), (Α-1), (I-1) or (-1) thus obtained can be obtained by known means such as phase transfer, concentration, solvent extraction, fractionation, It can be isolated and purified from the reaction solution by crystallization, recrystallization, chromatography and the like.
化合物 (A) 、 (I) 、 ( ) 、 (A-1) 、 (1-1) または (Γ- 1) が、 コンフィ ギユレ一ショナル アイソマ一 (配置異性体) 、 ジァステレオマー、 コンフォーマ 一等として存在する場合には、所望により、 前記の分離、精製手段によりそれぞれ を単離することができる。 また、 化合物 (A) 、 (I) 、 (Γ ) 、 (A-1) 、 (1-1) または (Γ- 1) がラセミ体である場合には、 通常の光学分割手段により S体および R体に分離することができる。 Compound (A), (I), (), (A-1), (1-1) or (Γ-1) is a conjugated isomer (configuration isomer), diastereomer, conformer, etc. If present, each can be isolated by the above-mentioned separation and purification means, if desired. Further, when the compound (A), (I), (Γ), (A-1), (1-1) or (Γ-1) is a racemate, the S-isomer and the S-isomer are obtained by ordinary optical resolution means. Can be separated into R-forms.
化合物 (A) 、 (I) 、 (Γ ) 、 (A-1) 、 (1-1) または (1,-1) に立体異性体 が存在する塲合には、この異性体が単独の場合およびそれらの混合物の場合も本発 明に含まれる。 If the compound (A), (I), (Γ), (A-1), (1-1) or (1, -1) has a stereoisomer, And mixtures thereof are also included in the present invention.
また、 化合物 (A) 、 (I) 、 (Γ ) 、 (A- 1) 、 (1-1) または (I,- 1) は、 水 和物または非水和物であってもよい。 化合物 (A) 、 (1) 、 (Γ) 、 (A- 1) 、 (I - 1) または (I,- 1) は同位元素 (例 えば、 3H、 14 35 S) 等で標識されていてもよい。 Compounds (A), (I), (), (A-1), (1-1) or (I, -1) may be hydrates or non-hydrates. Compound (A), (1), (Γ), (A- 1), (I - 1) or (I, - 1) is (For example, 3 H, 14 35 S) isotopes are labeled with like You may.
なお、 本発明の化合物 (A) 、 (I) 、 (Γ) 、 (A-1) 、 (1-1) または (1, - 1) の製造に用いられる式 The compound used in the production of the compounds (A), (I), (Γ), (A-1), (1-1) or (1, -1) of the present invention
〔式中、 R2 aおよび R 3 aはそれぞれ置換基を有していてもよい脂肪族炭化水素基 を、 R4 aおよび R 5 aはそれぞれ水素原子または置換基を有していてもよい炭化水 素基を、 R 6 aおよび R 7 aはそれぞれ水素原子または置換基を有していてもよい炭 化水素基を示し、 R 6 aと R 7 aは隣接する炭素原子と共に置換基を有していてもよ い 3ないし 8員環を形成してもよく、 R8aは (1) 水素原子、 (2) 置換基を有 していてもよい炭化水素基、 (3) ァシル基、 (4) 置換基を有していてもよい複 素環基、 (5) ハロゲン原子、 (6) -OR10a (R1Qaは、 水素原子、 置換基を 有していてもよい炭化水素基、ァシル基または置換基を有していてもよい複素環基 を示す) 、 (7) — SRlla (Rllaは、 水素原子、 置換基を有していてもよい炭 化水素基、 ァシル基または置換基を有していてもよい複素環基を示す) 、 (8) ― S .(〇) R12a (R12aは、 置換基を有していてもよい炭化水素基または置換基を 有していてもよい複素環基を示す) 、 (9) — S (O) 2R13a (R13aは、置換基 を有していてもよい炭化水素基または置換基を有していてもよい複素環基を示す) または(10) _NR14aR15a (R 14 aおよび R 15 aはそれぞれ水素原子、 置換基 を有していてもよい炭化水素基、ァシル基または置換基を有していてもよい複素環 基を示す) を、 R9aは水素原子、 置換基を有していてもよい炭化水素基、 ァシル 基または置換基を有していてもよい水酸基を示す〕で表される化合物またはその塩 は新規化合物である。 R2aおよび R "で示される 「置換基を有していてもよい脂肪族炭化水素基」 の 「脂肪族炭化水素基」 としては、 例えば、 アルキル基、 アルケニル基、 アルキニル 基、シクロアルキル基などの鎖状炭化水素または脂肪族環状炭化水素基が用いられ、 なかでも炭素数 1ないし 16個の鎖状(直鎖状あるいは分枝状) または脂肪族環状 炭化水素基などが好ましい。 具体的には、 以下のものが用いられる。 (In the formula, R 2a and R 3a each may be an aliphatic hydrocarbon group which may have a substituent, and R 4a and R 5a may each have a hydrogen atom or a substituent. the hydrocarbon group, R 6 a and R 7 a are each a hydrogen atom or an optionally substituted carbon hydrocarbon group, the substituent together with the carbon atoms R 6 a and R 7 a is adjacent May form a 3- to 8-membered ring, and R 8a is (1) a hydrogen atom, (2) a hydrocarbon group which may have a substituent, (3) an acyl group, (4) a heterocyclic group which may have a substituent, (5) a halogen atom, (6) -OR 10a (R 1Qa represents a hydrogen atom, a hydrocarbon group which may have a substituent, (7) —SR lla (R lla is a hydrogen atom, a hydrocarbon group which may have a substituent, an acyl group or a heterocyclic group which may have a substituent.) Replace The showing a heterocyclic group which may have), (8) -. S ( 〇) R 12a (R 12a is have may have a substituent hydrocarbon group or a substituted group (9) — S (O) 2 R 13a (where R 13a is a hydrocarbon group which may have a substituent or a heterocyclic group which may have a substituent) the illustrated) or (10) _NR 14a R 15a ( R 14 a and R 15 a are each a hydrogen atom, may be an optionally substituted hydrocarbon group, which may have a Ashiru group or substituent heterocyclic R 9a represents a hydrogen atom, a hydrocarbon group optionally having substituent (s), an acyl group or a hydroxyl group optionally having substituent (s), or a salt thereof. Is a novel compound. Examples of the “aliphatic hydrocarbon group” of the “optionally substituted aliphatic hydrocarbon group” for R 2a and R ”include, for example, an alkyl group, an alkenyl group, an alkynyl group, a cycloalkyl group, and the like. And a chain (linear or branched) or aliphatic cyclic hydrocarbon group having 1 to 16 carbon atoms is preferable. Specifically, the following are used.
( 1 ) 鎖状炭化水素基: (1) Chain hydrocarbon group:
アルキル基 [好ましくは、低級アルキル基(例えば、メチル、ェチル、 プロピル、 イソプロピル、 ブチル、 イソブチル、 sec—ブチル、 tert—ブチル、 ペンチル、 へ キシルなどの (^_6アルキル基など) ] 、 Alkyl group [preferably, a lower alkyl group (e.g., methyl, Echiru, propyl, isopropyl, butyl, isobutyl, sec- butyl, tert- butyl, pentyl, etc. (^ _ 6 alkyl groups such as hexyl)],
(2) 脂肪族環状炭化水素基: ' (2) Aliphatic cyclic hydrocarbon group: ''
シクロアルキル基 [好ましくは、 低級シクロアルキル基(例えば、 シクロプロピ ル、 シクロブチル、 シクロペンチル、 シクロへキシルなどの C3_6シクロアルキル 基) であり、 ベンゼン環と縮合していてもよい] 、 Cycloalkyl groups [preferably, a lower cycloalkyl group (e.g., Shikuropuropi Le, cyclobutyl, cyclopentyl, C 3 _ 6 cycloalkyl group such as cyclohexyl), may be condensed with a benzene ring,
これら 「脂肪族炭化水素基」 の置換基としては、 例えば、 (1) ハロゲン原子、 (2) 0,_3アルキレンジォキシ基、 (3) ニトロ基、 (4) ハロゲン化されていて もよい C^— 6アルキル基、 (5) C3_6シクロアルキル基、 (6) C6— 14ァリール基、 (7) ハロゲン化されていてもよい アルコキシ基、 (8) ハロゲン化されてい てもよい アルキルチオ基、 (9) ヒドロキシ基、 (10) アミノ基、 (11) モ ノ— 6アルキルアミノ基、 (12) モノー C6_14ァリールアミノ基、 (13) ジー ^— 6アルキルアミノ基、 (14) ジー C6— 14ァリ一ルァミノ基、 (15) ホルミル、 カルボキシ、 力ルバモイル、 アルキル一カルボニル、 C 3— 6シクロアルキル 一カルボニル、 cぃ6アルコキシ一カルボニル、 C6_14ァリ一ルー力ルポニル、 C 7— 16ァラルキル—カルボニル、 C6_147リールォキシ—力ルポニル、 C7一 1βァラ ルキルォキシ一力ルポニル、炭素原子以外に窒素原子、硫黄原子および酸素原子か ら選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環力ルポニル、 モノー 6アルキル一力ルバモイル、 ジー アルキル一力ルバモイル、 C6—Examples of the substituent of these "aliphatic hydrocarbon group", for example, (1) a halogen atom, (2) 0, _ 3 alkylene O alkoxy group, (3) a nitro group, be (4) a halogenated good C ^ - 6 alkyl group, (5) C 3 _ 6 cycloalkyl group, (6) C 6 - 14 Ariru group, (7) optionally halogenated alkoxy group, optionally be (8) halogenated also alkylthio group, (9) hydroxy group, (10) amino group, (11) mono - 6 alkylamino group, (12) mono- C 6 _ 14 Ariruamino group, (13) G ^ - 6 alkylamino group, (14) G C 6 - 14 § Li one Ruamino group, (15) formyl, carboxy, force Rubamoiru, alkyl one carbonyl, C 3 - 6 cycloalkyl one carbonyl, c I 6 alkoxy one carbonyl, C 6 _ 14 § Li one Lou force Ruponiru, C 7 - 16 Ararukiru - carbonyl, C 6 _ 14 7 reel Carboxymethyl - Power Ruponiru, C 7 one 1β § la Rukiruokishi Ichiriki Ruponiru, nitrogen atom in addition to carbon atom, a sulfur atom and an oxygen atom or al 1 to 5 or 6-membered heterocyclic ring force containing heteroatoms three of the selected Luponyl, Monobut 6 alkyl Lubamoyl, G alkyl 1 Lubamoyl, C 6 —
14ァリール一力ルバモイル、 炭素原子以外に窒素原子、 硫黄原子および酸素原子 から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環カルバモ ィル、。ェ アルキルーチォカルボニル、 C3— 6シクロアルキル—チォカルポニル、 アルコキシ—チォ力ルポニル、 (:6_14ァリール一チォカルポニル、 C7— 16 ァラルキル一チォカルポニル、 c6_14ァリールォキシ—チォ力ルポニル、 c7_16 ァラルキルォキシ一チォカルポニル、炭素原子以外に窒素原子、硫黄原子および酸 素原子から選ばれる 1ないし 3個のへテロ原子を含有する 5または 6員複素環チ 才力ルポニル、 チォカルバモイル、 モノー アルキル一チォカルバモイル、 ジ —Cエ アルキル一チォカルバモイル、 C6_14ァリール—チォカルバモイル、炭素 原子以外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテロ 原子を含有する 5または 6員複素環チォカルバモイル、 モノー 6アルキルスル ファモイル、ジ— C i— 6アルキルスルファモイル、 C6_14ァリ一ルスルファモイル、 アルキルスルホニル、 C6— 14ァリールスルホニル、 C — 6アルキルスルフィ ニル、 C6— 14ァリールスルフィエル、 スルフィノ、 スルホ、 — 6アルコキシスル フィエル、 C6— 14ァリールォキシスルフィニル、 アルコキシスルホニルおよ び C6一 14ァリールォキシスルホニルから選ばれるァシル基、 (16) ホルミルアミ ノ、 C^— 6アルキル—カルボキサミド、 C6— 14ァリ一ルーカルポキサミド、 Cx_6 アルコキシ—力ルポキサミド、 6アルキルスルホニルァミノおよび C6_14ァリ 一ルスルホニルァミノから選ばれるァシルァミノ基、 (17) 6アルキル一カル ポニルォキシ、 C6_14ァリール—力ルポニルォキシ、 ( 6アルコキシ一力ルポ二 ルォキシ、 モノー アルキル一力ルバモイルォキシ、 ジー 6アルキル一力 ルバモイルォキシ、 C6_14ァリール一力ルバモイルォキシおよびニコチノィルォ キシから選ばれるァシルォキシ基、 (18)炭素原子以外に窒素原子、 硫黄原子およ び酸素原子から選ばれる 1ないし 3個のへテロ原子を含有する 4ないし 14員複 素環基、 (19) ホスホノ基、 (20) C6— 14ァリールォキシ基、 (21) ジー アルコキシ一ホスホリル基、 (22) C6_14ァリールチオ基、 (23)ヒドラジノ基、 (24) ィミノ基、. (25) ォキソ基、 (26) ウレイド基、 (27) アルキルーゥ レイド基、 (28) ジ— アルキル—ウレイド基、 (29) ォキシドおよび (30) 前記 (1) 〜 (29) の基から選ばれる 2ないし 3個が結合してできる基などからな る群 (以下、 置換基 B群と略記する) から選ばれる基が用いられる。 これら置換基 の具体例としては、 前記の置換基 A群で例示したものと同様のものが挙げられる。 14 aryl carbamoyl, a 5- or 6-membered heterocyclic carbamoyl containing 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms. E alkyl chromatography Chio carbonyl, C 3 - 6 cycloalkyl - Chiokaruponiru, Alkoxy - Chio force Ruponiru, (: 6 _ 14 Ariru one Chiokaruponiru, C 7 - 16 Ararukiru one Chiokaruponiru, c 6 _ 14 Ariruokishi - Chio force Ruponiru, c 7 _ 16 Ararukiruokishi one Chiokaruponiru, nitrogen atom in addition to carbon atom, a sulfur atom 5- or 6-membered heterocyclic thiophene containing 1 to 3 heteroatoms selected from and oxygen atoms, thiocarbamoyl, mono-alkyl-thiocarbamoyl, di-C-alkyl-thiocarbamoyl, C 6 _ 14- aryl-thiocarbamoyl, 5- or 6-membered heterocyclic thiocarbamoyl containing 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen in addition to carbon, mono- 6- alkylsulfamoyl, di-C i-6 alkylsulfamoyl, C 6 _ 14 § Li one Rusurufamoiru, alkyl sulfonyl , C 6 - 14 § reel sulfonyl, C - 6 alkylsulfide alkylsulfonyl, C 6 - 14 § reel sulfide El, sulfino, sulfo, - 6 Arukokishisuru Fier, C 6 - 14 § reel O carboxymethyl sulfinyl, alkoxysulfonyl Oyo fine C 6 one 14 Ashiru group selected from § reel O carboxymethyl sulfonyl, (16) Horumiruami Bruno, C ^ - 6 alkyl - carboxamide, C 6 - 14 § Li one Luca Lupo alkylcarboxamide, C x _ 6 alkoxy - power Rupokisamido , 6 alkylsulfonyl § amino and C 6 _ 14 Ashiruamino group selected from § Li one Le sulfonyl § amino, (17) 6 alkyl one local Poniruokishi, C 6 _ 14 Ariru - power Ruponiruokishi, (6 alkoxy Ichiriki Lupo two Ruokishi , mono- alkyl Ichiriki Rubamoiruokishi, Gee 6 alkyl Ichiriki Rubamoiruokishi, C 6 _ 14 Ariru Ichiriki Rubamoiru An acyloxy group selected from xy and nicotinyloxy; (18) a 4- to 14-membered cyclic group containing 1 to 3 hetero atoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms; (19) phosphono group, (20) C 6 -. 14 Ariruokishi group, (21) G alkoxy one phosphoryl group, (22) C 6 _ 14 Ariruchio group, (23) a hydrazino group, (24) Imino group, (25 Oxo groups, (26) ureido groups, (27) alkyl-perido groups, (28) dialkyl-ureido groups, (29) oxides and (30) 2 to 2 groups selected from the above (1) to (29) A group selected from the group consisting of groups formed by bonding three groups (hereinafter, abbreviated as substituent group B) is used. Specific examples of these substituents include the same as those exemplified in the above-mentioned substituent group A.
R4aおよび R5aで示される「置換基を有していてもよい炭化水素基」としては、 R4および R5で示される 「置換基を有していてもよい炭化水素基」 と同様のもの が用いられる。 As the `` hydrocarbon group which may have a substituent '' represented by R 4a and R 5a , The same ones as the “optionally substituted hydrocarbon group” represented by R 4 and R 5 are used.
R6aおよび R7aで示される「置換基を有していてもよい炭化水素基 jとしては、 R6および R7で示される 「置換基を有していてもよい炭化水素基」 と同様のもの が用いられる。 As the `` optionally substituted hydrocarbon group j '' represented by R 6a and R 7a , the same as the `` optionally substituted hydrocarbon group '' represented by R 6 and R 7 Is used.
R 6 aと R 7 aが隣接する炭素原子と共に形成してもよい 「置換基を有していても よい 3ないし 8員環」 としては、 R6と R7が隣接する炭素原子と共に形成しても よい 「置換基を有していてもよい 3ないし 8員環」 と同様のものが用いられる。 R 6 a and R 7 a it is may be formed together with the adjacent carbon atoms as "no 3 may have a substituent to 8-membered ring" formed together with the carbon atom to which R 6 and R 7 adjacent And the same as the “3- to 8-membered ring optionally having substituent (s)” may be used.
R8aで示される 「置換基を有していてもよい炭化水素基」 、 「ァシル基」 、 「置 換基を有していてもよい複素環基」 、 「ハロゲン原子」 、 「式一〇R1()a」 、 「式 — SRlla」 、 「式—S (O) R12aJ 、 「式—S (O) 2R13a」 または 「式— N 1 aR15ajとしては、 R8で示される「置換基を有していてもよい炭化水素基」、 「ァシル基」 、 「置換基を有していてもよい複素環基」 、 「ハロゲン原子」 、 「式 — OR10」 、 「式— SR11 、 「式—S (O) R12」 、 「式一 S (0) 2R13」 または 「式一 NR14R15」 と同様のものが用いられる。 R 8a represents a “hydrocarbon group which may have a substituent”, an “acyl group”, a “heterocyclic group which may have a substituent”, a “halogen atom”, or a compound represented by the formula R 1 () a , “Formula — SR lla ”, “Formula —S (O) R 12a J”, “Formula —S (O) 2 R 13a ” or “Formula — N 1 a R 15a j, "optionally substituted hydrocarbon group" represented by 8 "Ashiru group", "substituted heterocyclic group which may have a", "halogen atom", "formula - OR 10" The same formulas as those of “Formula—SR 11 ,“ Formula—S (O) R 12 ”,“ Formula 1 S (0) 2 R 13 ”or“ Formula 1 NR 14 R 15 ”are used.
R9aで示される 「置換基を有していてもよい炭化水素基」 、 「ァシル基」 およ び 「置換基を有していてもよい水酸基」 としては、 R9で示される 「置換基を有し ていてもよい炭化水素基」 、 「ァシル基」 および「置換基を有していてもよい水酸 基」 と同様のものが用いられる。 Examples of the “optionally substituted hydrocarbon group”, “acyl group” and “optionally substituted hydroxyl group” represented by R 9a include “substituents” represented by R 9 The same groups as those described for the "hydrocarbon group optionally having", the "acyl group" and the "hydroxyl group optionally having a substituent" are used.
化合物 (B) としては、 次の化合物などが好ましい。 As the compound (B), the following compounds are preferred.
(1) R 2 aおよび R 3 aがそれぞれ①ハロゲン原子、 ②じ 6アルキル、 — 6アル キル一カルボエル、 C i _ 6アルキルスルホニルおよび C 7_16ァラルキルから選ばれ る置換基で置換されていてもよい水酸基、 ③ 1または 2個の Ci— 6アルキル、 じェ —6アルキル一力ルポニルおよび C e— i 4ァリール一力ルポニルから選ばれる置換基 で置換されていてもよいアミノ基、④炭素原子以外に窒素原子、酸素原子および硫 黄原子などから選ばれる 1ないし 3個のへテロ原子を有する 4ないし 10員複素 環基、 ⑤ アルキルで置換されていてもよいチォ基、 ⑥ — 6アルキル一スル フィニル基または⑦ C アルキル—スルホニル基で置換されていてもよい C 6 アルキル基を示し、 R4a、 R5a、 R6aおよび R7aがそれぞれ水素原子または アルキル基を示 し、 (1) R 2 a and R 3 a are each ① halogen atoms, ② Ji 6 alkyl, - 6 Al kill one Karuboeru, substituted by C i _ 6 alkylsulfonyl and C 7 _ 16 substituents Ru is selected from Ararukiru hydroxy which may, ③ 1 or 2 CI- 6 alkyl, Ji E - 6 alkyl Ichiriki Ruponiru and C e- i 4 Ariru Ichiriki optionally substituted amino group with a substituent selected from Ruponiru, ④ A 4- to 10-membered heterocyclic group having 1 to 3 heteroatoms selected from a nitrogen atom, an oxygen atom and a sulfur atom in addition to a carbon atom, a thio group optionally substituted with ア ル キ ル alkyl, ⑥ — 6 A C 6 alkyl group optionally substituted with an alkylsulfinyl group or a で C alkyl-sulfonyl group, R 4a , R 5a , R 6a and R 7a are each a hydrogen atom or Represents an alkyl group,
R8aが① (: 6アルキル基、 ②ノヽロゲン原子、 ③式ー〇R10a (R10aは、 (i) 水素原子、 (ii) (^-6アルキル基 [この アルキル基は (1) ハロゲン原子、 (2) ヒドロキシ基、 (3) アミノ基、 (4) 力ルポキシ、 (5) 力ルバモイル、 (6) ( 丄— 6アルコキシ—力ルポニル、 (7) モノ— アルキル一力ルバモイル、 (8) ジー C — 6アルキル—力ルバモイル、 (9) ォキソを有していてもよい炭素原子以 外に窒素原子、硫黄原子および酸素原子から選ばれる 1ないし 3個のへテロ原子を 含有する 4ないし 10員複素環基から選ばれる置換基を有していてもよい]、(i i i) C3— 6シクロアルキル基、 (iv)C7— 16ァラルキル基、 (V) アルキル—カルボ ニル基、 (vi)C6— 14ァリール一力ルポニル基、 (viOC^-eアルコキシ—力ルポ二 ル基、 (viii)モノーまたはジ— C^-eアルキル—チォカルバモイル基、 (ix)ハロゲ ン化されていてもよい — 6アルキルースルホニル基または (X)炭素原子以外に窒 素原子、硫黄原子および酸素原子から選ばれる 1ないし 4個のへテロ原子を含有す る 4ないし 10員複素環基 [この複素環基は < 6_14ァリールを有していてもよい] を示す) 、 ④式ー SRlla (Rllaは、 (i) 水素原子、 (10(^— 6アルキル基また は(iii)モノ—またはジ—C^eアルキル一力ルバモイル基を示す)、⑤式— S (O) R12a (R12aは、 (OCi— 6アルキル基または(ii)モノーまたはジ一 -6アルキ ルー力ルバモイル基を示す) 、 ⑥式ー S (O) 2R13a (: R13aは、 (i)*^— 6アル キル基または(ii)モノーまたはジ一C^eアルキル一力ルパモイル基を示す) また は⑦式ー NR14aR15a (R14aは、 (i) 水素原子、 (i C — eアルキル基 [この C i_6アルキル基は Cェ—6アルコキシ一力ルポニルを有していてもよい] 、 (iii) ホルミル、 (1 )0^6アルキル一力ルポニル基、 WCi— 6アルコキシ—カルボニル 基、 (vi)力ルバモイル基、 (vii)モノ—またはジー(^— 6アルキル一力ルバモイル 基または (vii C^ 6アルキルースルホニル基を、 R15aは、 水素原子またはメチ レを示す) を示し、 R 8a is ① (: 6 alkyl group, ② Nono androgenic atoms, ③ Shiki 〇_R 10a (R 10a is, (i) a hydrogen atom, (ii) (^ -6 alkyl [the alkyl group (1) halogen atom, (2) hydroxy group, (3) amino group, (4) force Rupokishi, (5) force Rubamoiru, (6) (丄- 6 alkoxy - power Ruponiru, (7) mono - alkyl Ichiriki Rubamoiru, (8 ) Di-C- 6- alkyl-rubamoyl, (9) containing from 1 to 3 heteroatoms selected from nitrogen, sulfur and oxygen atoms in addition to carbon atoms which may have oxo. a substituent selected from the 10-membered heterocyclic group which may have], (iii) C 3 - 6 cycloalkyl group, (iv) C 7 - 16 Ararukiru group, (V) Alkyl - carboxymethyl sulfonyl group, (vi) C 6 - 14 Ariru Ichiriki Ruponiru group, (VIOC ^ -e alkoxy - force Lupo two Le group, (viii) mono- or di - C ^ -e alkyl - Chiokarubamoiru group, ( ix) May be halogenated — 4 to 4 containing, in addition to the 6 alkyl-sulfonyl group or (X) carbon atom, 1 to 4 heteroatoms selected from nitrogen, sulfur and oxygen 10-membered Hajime Tamaki [this heterocyclic group may have a <6 _ 14 Ariru] shows a), ④ Shiki SR lla (R lla is, (i) a hydrogen atom, (10 (^ - 6 An alkyl group or (iii) a mono- or di-C ^ e alkyl monorubamoyl group), a formula — S (O) R 12a (R 12a is an (OCi- 6 alkyl group or (ii) a mono- or di one -6 showing the alkylene Lou force Rubamoiru group), ⑥ Shiki S (O) 2 R 13a ( : R 13a is, (i) * ^ - 6 Al kill group or (ii) Mo Over or di illustrating an C ^ e alkyl Ichiriki Rupamoiru group) or ⑦ Shiki NR 14a R 15a (R 14a is, (i) a hydrogen atom, (i C - e alkyl group [this C i_ 6 alkyl group (Iii) formyl, (1) 0 ^ 6 alkyl monopropyl, WCi- 6 alkoxy-carbonyl, (vi) dirubamoyl, vii) mono- or di-(^-6 alkyl monorubumoyl group or (vii C ^ 6 alkyl-sulfonyl group, R 15a represents a hydrogen atom or methyl),
R 9 aが(i)水素原子、 (ii) C 6アルキル基 [この — 6アルキル基は、 (1) ハロゲン原子、 (2) 6アルコキシ基、 (3) ヒドロキシ基、 ) アミノ基、 (5) モノー C1-6アルキルアミノ基、 (6) ジ— アルキルアミノ基、 (7) ォ キソを有していてもょ ゝ炭素原子以外に窒素原子、硫黄原子および酸素原子から選 ばれる 1ないし 3個のへテロ原子を含有する 4ないし 1 0員複素環基、 (8) C 6_ 1 4ァリールチオ、 (9) ウレイド、 (10) 力ルポキシ、 (11) 力ルバモイル、 (12) (: 6アルコキシ一力ルポニル、 (13)モノー(^_6アルキル—力ルバモイル、 (14) ホルミルァミノおよび(15) アルキル一カルボキサミドから選ばれる置換基 を有していてもよい] または (i i i) ホルミル基を示す化合物 (B ) R 9 a is (i) a hydrogen atom, (ii) a C 6 alkyl group [this — 6 alkyl group is (1) a halogen atom, (2) 6 alkoxy group, (3) hydroxy group,) amino group, (5 ) Mono C 1-6 alkylamino group, (6) di-alkylamino group, (7) A 4- to 10-membered heterocyclic group containing 1 to 3 hetero atoms selected from a nitrogen atom, a sulfur atom and an oxygen atom in addition to a carbon atom; (8) C 6 _ 1 4 Arylthio, (9) Ureido, (10) Power Lupoxyl, (11) Power Lubamoyl, (12) (: 6 Alkoxy One Power Luponil, (13) Mono-(^ _ 6 alkyl-Power Lubamoyl, (14) Formylamino and (15) it may have a substituent selected from alkyl-carboxamides] or (iii) a compound showing a formyl group (B)
( 2 ) 参考例 4で製造される化合物 (B) 。 (2) Compound (B) produced in Reference Example 4.
化合物 (I) 、 (1') 、 (1-1) または( -1)のプロドラッグは、 生体内における 生理条件下で酵素や胃酸等による反応により化合物 (I) 、 (Γ) 、 (1-1) または (1'- 1)に変換する化合物、 すなわち酵素的に酸化、 還元、 加水分解等を受けて化合 物 (I) 、 (Γ) 、 (1-1) または(1,- 1)に変化する化合物、 胃酸等により加水分解 等を受けて化合物 (I) 、 (Γ) 、 (1-1) または(Γ-l)に変化する化合物をいう。 化合物 (I) 、 (1,) 、 (1-1) または(1'_1)のプロドラッグとしては、化合物 (I) 、 (Iゥ 、 (1-1) または(1'- 1)のァミノ基がァシル化、 アルキル化、 りん酸化された 化合物 (例えば、 化合物 (I) 、 (Iゥ 、 (1-1) または(1'-1)のァミノ基がエイコ サノィル化、 ァラエル化、 ペンチルァミノカルボ二ル化、 (5—メチル _ 2—ォキ ソー 1 , 3—ジォキソレン— 4—ィル) メトキシカルポニル化、 テトラヒドロフラ ニル化、 ピロリジノメチル化、 ピバロィルォキシメチル化、 tert—ブチル化された 化合物等) ;化合物 (I) 、 (Γ) 、 (1-1) または(1'- 1)の水酸基がァシル化、 ァ ルキル化、 りん酸化、 ホウ酸化された化合物(例えば、化合物(I) 、 (Γ) 、 (1-1) または(1'-1)の水酸基がァセチル化、 パルミ卜ィル化、 プロパノィル化、 ピバロイ ル化、 スクシ二ル化、 フマリル化、 ァラニル化、 ジメチルアミノメチルカルポニル 化された化合物等) ;化合物 (I) 、 (Γ) 、 (1-1) または(P-1)のカルボキシ基 がエステル化、 アミド化された化合物 (例えば、 化合物 (I) 、 (Γ) 、 (1-1) ま たは(Γ-1)のカルボキシ基がェチルエステル化、 フエニルエステル化、 カルポキシ メチルエステル化、 ジメチルァミノメチルエステル化、 ピバロィルォキシメチルェ ステル化、 エトキシカルポニルォキシェチルエステル化、 フタリジルエステル化、 ( 5—メチルー 2一ォキソ一 1, 3一ジォキソレン一 4一ィル)メチルエステル化、 シクロへキシルォキシカルポニルェチルエステル化、メチルアミド化された化合物 等)等が挙げられる。これらの化合物は自体公知の方法によって化合物(1)、 (1,)、 (1-1) または (Γ-1)から製造することができる。 The prodrugs of the compounds (I), (1 '), (1-1) and (-1) are prepared by reacting the compounds (I), (Γ), (1) (1) or (1'-1), that is, compounds (I), (Γ), (1-1) or (1, -1) which are enzymatically oxidized, reduced, hydrolyzed, etc. ), Or a compound that undergoes hydrolysis by gastric acid or the like to change to a compound (I), (Γ), (1-1) or (Γ-l). As a prodrug of the compound (I), (1,), (1-1) or (1′_1), a prodrug of the compound (I), (I ゥ, (1-1) or (1′-1) Compounds in which the group is acylated, alkylated or phosphorylated (for example, the amino group of compound (I), (I ゥ, (1-1) or (1′-1) is eicosanoylated, araellated, pentylized) Minocarbonylation, (5-methyl_2-oxo-1,3-dioxolen-4-yl) methoxycarbonylation, tetrahydrofuranylation, pyrrolidinomethylation, pivaloyloxymethylation, tert- Compounds in which the hydroxyl group of the compound (I), (Γ), (1-1) or (1′-1) is acylated, alkylated, phosphorylated, or borated (for example, The hydroxyl group of compound (I), (Γ), (1-1) or (1'-1) is acetylated, palmitoylated, propanoylated, or pivaloylic. , Succinylation, fumarylation, alanylation, dimethylaminomethylcarbonylation, etc.); the carboxy group of compound (I), ()), (1-1) or (P-1) is esterified, Amidated compounds (for example, when the carboxy group of compound (I), (), (1-1) or (Γ-1) is esterified, phenylesterified, carboxymethylesterified, dimethylamino Methyl esterification, pivalyloxymethyl esterification, ethoxycarponyloxyshethyl esterification, phthalidyl esterification, (5-methyl-2-oxo1-1,3-dioxolen-1-41) methyl esterification , Cyclohexyloxycarponylethyl esterified, methylamidated compounds Etc.). These compounds can be produced from compound (1), (1,), (1-1) or (Γ-1) by a method known per se.
また、 化合物 (I) 、 (Γ) 、 (1-1) または(1'- 1)のプロドラッグは、 広川書店 1 9 9 0年刊「医薬品の開発」第 7巻分子設計 1 6 3〜1 9 8貢に記載されている ような生理的条件で化合物 (I) 、 (Γ) 、 (1-1) または (Ι'- 1)に変化するもので あってもよい。 In addition, prodrugs of compounds (I), (), (1-1) or (1'-1) are disclosed in Hirokawa Shoten, 1990, “Development of Pharmaceuticals,” Volume 7, Molecular Design, 163-1. It may be changed to the compound (I), (Γ), (1-1) or (Ι'-1) under physiological conditions as described in 98.
化合物 (A) 、 (1 ) 、 (Γ) 、 (A— 1 ) 、 (1— 1 ) 、 (Γ—1 ) または (B) の塩としては、 例えば薬理学的に許容される塩等が用いられる。例えば、 無 機塩基との塩、 アンモニゥム塩、 有機塩基との塩、 無機酸との塩、 有機酸との塩、 塩基性または酸性ァミノ酸との塩等が挙げられる。無機塩基との塩の好適な例とし ては、 例えばナトリウム塩、 カリウム塩等のアルカリ金属塩、 カルシウム塩、 マグ ネシゥム塩等のアルカリ土類金属塩、 またはアルミニウム塩等が挙げられる。有機 塩基との塩の好適な例としては、例えばトリメチルァミン、 トリェチルァミン、 ピ リジン、 ピコリン、 2, 6—ルチジン、 エタノールァミン、 ジエタノールァミン、 トリエタノールァミン、 シクロへキシルァミン、ジシクロへキシルァミン、 N, N ' 一ジべンジルェチレンジァミン等との塩が挙げられる。無機酸との塩の好適な例と しては、 例えば塩酸、 臭化水素酸、 硝酸、 硫酸、 リン酸等との塩が挙げられる。 有 機酸との塩の好適な例としては、例えばギ酸、酢酸、 トリフルォロ酢酸、フタル酸、 フマル酸、 シユウ酸、 酒石酸、 マレイン酸、 クェン酸、 コハク酸、 リンゴ酸、 メタ ンスルホン酸、ベンゼンスルホン酸、 p—トルエンスルホン酸等との塩が挙げられ る。塩基性アミノ酸との塩の好適な例としては、 例えばアルギニン、 リジン、 オル 二チン等との塩が挙げられ、酸性アミノ酸との塩の好適な例としては、例えばァス パラギン酸、 グルタミン酸等との塩が挙げられる。 Examples of the salt of the compound (A), (1), (Γ), (A-1), (1-1), (Γ-1) or (B) include, for example, pharmacologically acceptable salts and the like. Used. Examples include salts with inorganic bases, ammonium salts, salts with organic bases, salts with inorganic acids, salts with organic acids, salts with basic or acidic amino acids, and the like. Preferred examples of the salt with an inorganic base include an alkali metal salt such as a sodium salt and a potassium salt, an alkaline earth metal salt such as a calcium salt and a magnesium salt, and an aluminum salt. Preferred examples of the salt with an organic base include, for example, trimethylamine, triethylamine, pyridine, picoline, 2,6-lutidine, ethanolamine, diethanolamine, triethanolamine, cyclohexylamine, dicyclohexylamine. , N, N 'salts with dibenzyldiethylenediamine and the like. Preferable examples of the salt with an inorganic acid include, for example, salts with hydrochloric acid, hydrobromic acid, nitric acid, sulfuric acid, phosphoric acid, and the like. Preferred examples of salts with organic acids include, for example, formic acid, acetic acid, trifluoroacetic acid, phthalic acid, fumaric acid, oxalic acid, tartaric acid, maleic acid, citric acid, succinic acid, malic acid, methanesulfonic acid, benzenesulfone And salts with an acid, p-toluenesulfonic acid and the like. Preferred examples of the salt with a basic amino acid include, for example, salts with arginine, lysine, ordinine, and the like. Preferred examples of the salt with an acidic amino acid include, for example, aspartic acid, glutamic acid, and the like. Salts.
中でも薬学的に許容可能な塩が好ましく、 その例としては、 化合物 (I) または (Γ )内に塩基性官能基を有する場合には、例えば塩酸、臭化水素酸、硝酸、硫酸、 リン酸等無機酸との塩、 例えば酢酸、 フ夕ル酸、 フマル酸、 シユウ酸、 酒石酸、 マ レイン酸、 クェン酸、 コハク酸、 メタンスルホン酸、 p—トルエンスルホン酸等の 有機酸との塩が挙げられ、酸性官能基を有する場合には、 例えばナトリウム塩、 力 リウム塩等のアルカリ金属塩、カルシウム塩、マグネシウム塩等のアルカリ土類金 属塩、 アンモニゥム塩等が挙げられる。 Among them, pharmaceutically acceptable salts are preferable. Examples thereof include compounds having a basic functional group in compound (I) or (III), for example, hydrochloric acid, hydrobromic acid, nitric acid, sulfuric acid, phosphoric acid Salts with inorganic acids such as acetic acid, fumaric acid, fumaric acid, oxalic acid, tartaric acid, maleic acid, citric acid, succinic acid, methanesulfonic acid, p-toluenesulfonic acid, etc. In the case of having an acidic functional group, examples thereof include alkali metal salts such as sodium salts and potassium salts, and alkaline earth metals such as calcium salts and magnesium salts. Genus salts, ammonium salts and the like.
式 Expression
〔式中、 ニニ二 は単結合または二重結合を示す〕 で表される部分構造を有する化 合物またはその塩は PDE阻害作用、 特に PDE IV阻害作用を有しており、 PDEに起 因する疾患の予防 ·治療剤として用いることが可能である。化合物(A— 2 ) の塩 としては、上記の化合物(A)、 (1 )、 (I, )、 (A— 1 )、 (1— 1 )、 ( — 1 ) または (B ) の塩と同様のものが挙げられる。 [Wherein, ninii represents a single bond or a double bond] or a salt thereof has a PDE inhibitory activity, particularly a PDE IV inhibitory activity, and is caused by PDE. It can be used as an agent for preventing and treating diseases. Examples of the salt of the compound (A-2) include the salt of the above compound (A), (1), (I,), (A-1), (1-1), (-1) or (B). Similar ones can be mentioned.
なかでも上記化合物(A— 2 )またはその塩に包含される本発明の化合物(A)、 ( 1 )、 (1,)、 (A— 1 )、 (1— 1 )、 (Γ— 1 ) またはその塩(化合物(I )、 ( 1— 1 ) 、 (Γ) 、 (Γ— l ) のプロドラッグを含む) (以下、 本発明の化合 物と略記する) は、 優れた: PDE阻害作用、 特に PDE IV阻害作用を有しており、 か つ毒性が低く、安全であるので、哺乳動物(例えば、 ヒト, マウス, ィヌ, ラット, ゥシなど) における炎症性疾患、 自己免疫疾患、 糖尿病、 動脈硬化、 移植片対宿主 疾患、 多発性硬化症、 敗血症、 乾癬、 骨粗鬆症、 うつ病、 脳血管閉塞後の中枢機能 低下症、 脳血管痴呆症、 アルツハイマー型痴呆症、 記憶障害、 肥満、 心不全、 肺繊 維症、 アレルギー性疾患、 狭心症、 心筋梗塞、 高血圧症、 肺高血圧症、 腎疾患、 脳 機能疾患、 免疫不全、 眼科疾患、 男性または女性の性機能障害等の予防 ·治療剤、 PDE阻害剤として用いることができる。 とりわけ、 炎症性疾患、 喘息、 慢性閉塞性 肺疾患、慢性関節リゥマチ、 自己免疫疾患、糖尿病、動脈硬化、移植片対宿主疾患、 多発性硬化症、敗血症、乾癬、骨粗鬆症、 うつ病、脳血管閉塞後の中枢機能低下症、 脳血管痴呆症、 アルッ八イマ一型痴呆症、 記憶障害、 肥満、 心不全、 肺繊維症、 ァ レルギ一性疾患 (例えば、 アトピー性皮膚炎、 アレルギー性鼻炎、 蓴麻疹) などの 予防'治療剤、 PDE IV阻害剤として用いることができる。 投与経路は経口、 非経 口のいずれでもよい。 In particular, the compounds (A), (1), (1,), (A-1), (1-1), (Γ-1) of the present invention included in the above compound (A-2) or a salt thereof Or a salt thereof (including prodrugs of compounds (I), (1-1), (Γ), and (Γ-l)) (hereinafter abbreviated as compound of the present invention) is excellent: PDE inhibitory action In particular, it has PDE IV inhibitory activity, is low in toxicity, and is safe, so it can be used in mammals (eg, humans, mice, dogs, rats, mice, etc.) for inflammatory diseases, autoimmune diseases, Diabetes, arteriosclerosis, graft-versus-host disease, multiple sclerosis, sepsis, psoriasis, osteoporosis, depression, central dysfunction after cerebral vascular obstruction, cerebrovascular dementia, Alzheimer's dementia, memory impairment, obesity, Heart failure, pulmonary fibrosis, allergic disease, angina, myocardial infarction, hypertension, pulmonary hypertension, Disease, brain function disorders, immunodeficiency, prophylactic or therapeutic agent such as sexual dysfunction ophthalmic diseases, male or female, can be used as a PDE inhibitor. Above all, inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, diabetes, arteriosclerosis, graft-versus-host disease, multiple sclerosis, sepsis, psoriasis, osteoporosis, depression, cerebral vascular obstruction Later central dysfunction, cerebral vascular dementia, dementia of aruhaima type 1, memory impairment, obesity, heart failure, pulmonary fibrosis, allergic diseases (eg, atopic dermatitis, allergic rhinitis, juniper measles) ) Can be used as prophylactic or therapeutic agents, and PDE IV inhibitors. The route of administration may be oral or parenteral.
剤形の具体例としては、例えば、錠剤 (糖衣錠、フィルムコ一ティング錠を含む)、 丸剤、 カプセル剤 (マイクロカプセルを含む) 、 顆粒剤、 細粒剤、 散剤、 剤、 乳剤、 懸濁剤、 注射剤、 吸入剤、 軟膏、 点眼剤、 エアゾール剤、 眼軟膏剤、 硬 膏剤、 座剤、 トロ一チ剤、 パップ剤、 リニメント剤などが用いられる。 これらの製 剤は常法 (例えば、 日本薬局方記載の方法など) に従って調製される。 Specific examples of dosage forms include, for example, tablets (including sugar-coated tablets and film-coated tablets), Pills, capsules (including microcapsules), granules, fine granules, powders, tablets, emulsions, suspensions, injections, inhalants, ointments, eye drops, aerosols, eye ointments, plasters Suppositories, troches, cataplasms, liniments and the like are used. These preparations are prepared according to a conventional method (for example, a method described in the Japanese Pharmacopoeia).
本発明の製剤において、本発明の化合物の含有量は、製剤の形態によって相違す るが、 通常製剤全体に対して 0 . 0 1ないし 1 0 0重量%、 好ましくは 0 . 1ない し 5 0重量%、 さらに好ましくは 0 . 5ないし 2 0重量%程度である。 In the preparation of the present invention, the content of the compound of the present invention varies depending on the form of the preparation, but is usually from 0.01 to 100% by weight, preferably from 0.1 to 50% by weight, based on the whole preparation. % By weight, more preferably about 0.5 to 20% by weight.
具体的には、 錠剤の製造法は、 医薬品をそのまま、 賦形剤、 結合剤、 崩壊剤もし くはそのほかの適当な添加剤を加えて均等に混和したものを、適当な方法で顆粒と した後、 滑沢剤などを加え、 圧縮成型するかまたは、 医薬品をそのまま、 または賦 形剤、結合剤、崩壊剤もしくはそのほかの適当な添加剤を加えて均等に混和したも のを、 直接圧縮成型して製するか、 またはあらかじめ製した顆粒にそのまま、 もし くは適当な添加剤を加えて均等に混合した後、圧縮成型しても製造することもでき る。 また、 本剤は、 必要に応じて着色剤、 矯味剤などを加えることができる。 さら に、 本剤は、 適当なコーティング剤で剤皮を施すこともできる。 Specifically, in the tablet manufacturing method, the drug was used as is, and excipients, binders, disintegrants, or other appropriate additives were added, and the mixture was uniformly mixed to obtain granules by an appropriate method. After that, a lubricant is added and compression molding is performed, or the medicine is directly mixed or directly mixed with excipients, binders, disintegrants or other suitable additives. Alternatively, the granules can be produced by compression-molding the granules prepared beforehand as they are, or after adding an appropriate additive thereto and mixing them uniformly. In addition, the present agent can contain a coloring agent, a flavoring agent, and the like as needed. In addition, the agent can be coated with an appropriate coating agent.
注射剤の製造法は、医薬品の一定量を、水性溶剤の場合は注射用水、生理食塩水、 リンゲル液など、非水性溶剤の場合は通常植物油などに溶解、懸濁もしくは乳化し て一定量とするか、または医薬品の一定量をとり注射用の容器に密封して製するこ とができる。 In the method of manufacturing an injection, a certain amount of a drug is dissolved, suspended or emulsified in water for injection, physiological saline, Ringer's solution, etc. in the case of an aqueous solvent, or vegetable oil in the case of a non-aqueous solvent, to make a certain amount. Alternatively, a predetermined amount of the drug can be taken and sealed in a container for injection.
経口用製剤担体としては、 例えば、 デンプン、 マンニット、 結晶セルロース、 力 ルポキシメチルセルロースナトリウムなどの製剤分野において常用されている物 質が用いられる。 注射用担体としては、 例えば、 蒸留水、 生理食塩水、 グルコース 溶液、 輸液剤などが用いられる。 その他、 製剤一般に用いられる添加剤を適宜添加 することもできる。 As the pharmaceutical carrier for oral use, for example, substances commonly used in the pharmaceutical field such as starch, mannitol, crystalline cellulose, sodium propyloxymethylcellulose and the like are used. As the carrier for injection, for example, distilled water, physiological saline, glucose solution, infusion agent and the like are used. In addition, additives generally used in pharmaceutical preparations can be appropriately added.
これらの製剤の投与量は、 年令, 体重, 症状, 投与経路, 投与回数などにより異 なるが、例えば、成人の喘息患者に対して、 1日当たり有効成分(本発明の化合物) に換算して通常 0 . 0 1ないし 1 0 0 mg/kg、好ましくは 0 . 1ないし 5. 0 mg/kg、 より好ましくは 0 . 5ないし 1 0 mg/kgを 1日 1または 2回に分割して経口投与 するのがよい。 本発明の化合物は単剤として使用しても優れた PDE IV阻害作用を示すが、 さら に本発明の化合物以外の他の医薬成分 (以下、 併用薬物と略記する) と併用 (多剤 併用) することもできる。 The dosage of these preparations varies depending on age, body weight, symptoms, route of administration, number of administrations, etc. For example, for adult asthma patients, it is converted into the active ingredient (compound of the present invention) per day. Usually 0.1 to 100 mg / kg, preferably 0.1 to 5.0 mg / kg, more preferably 0.5 to 10 mg / kg, divided orally once or twice daily It should be administered. Although the compound of the present invention exhibits excellent PDE IV inhibitory activity even when used as a single agent, it is also used in combination with other pharmaceutical ingredients other than the compound of the present invention (hereinafter abbreviated as concomitant drug) (multiple drug combination) You can also.
このような併用薬物としては、 例えば抗喘息剤(例えば、 プロピオン酸フルチ力 ゾン、 プロピオン酸べクロメタゾン、 テオフィリン 、 プロ力テロール、 ケトチフ ェン、 ァゼラスチン、 セラトロダストなど) 、 抗アレルギー剤 (例えば、 フエキソ フエナジン、 ェピナスチン、 ェバスチンなど) 、 抗コリン剤 (例えば、 臭化ィプラ トロピウム、 臭化フルト口ピウム、 臭化ォキシトロピウムなど) 、 抗炎症剤 (例え ば、 ジクロフェナクナトリウム、 イブプロフェン、 インドメタシン、 ロキソプロフ エンナトリウムなど) 、 抗菌剤 (例えば、 セフィキシム、 セフジニル、 オフロキサ シン、 トシル酸トスフロキサシン、 レポフロキサシンなど) 、 抗真菌剤 (例えば、 フルコナゾール、 イトラコナゾールなど) 、 抗糖尿病用剤 (例えば、 ピオダリ夕ゾ ン、 ナテグリニド、 ポグリポース、 ァカルポースなど) などが挙げられる。 Examples of such concomitant drugs include anti-asthmatic agents (eg, flutidinzone propionate, beclomethasone propionate, theophylline, propoterol, ketotifen, azelastine, seratrodast, etc.), antiallergic agents (eg, fexofenadine, etc.) , Epinastine, ebastine, etc.), anticholinergic agents (eg, ipratropium bromide, fructophorium pium bromide, oxotropium bromide, etc.), anti-inflammatory agents (eg, diclofenac sodium, ibuprofen, indomethacin, loxoprofen sodium, etc.), Antibacterial agents (eg, cefixime, cefdinir, ofloxacin, tosfloxacin tosylate, lepofloxacin, etc.), antifungal agents (eg, fluconazole, itraconazole, etc.), antidiabetic Use agents (e.g., Piodari Yuzo down, nateglinide, Poguriposu, etc. Akaruposu) and the like.
本発明の化合物と併用薬物との併用に際しては、本発明の化合物と併用薬物の投 与時期は限定されず、本発明の化合物と併用薬物とを、 投与対象に対し、 同時に投 与してもよいし、 時間差をおいて投与してもよい。併用薬物の投与量は、 臨床上用 いられている投与量に準ずればよく、 投与対象、 投与ルート、 疾患、 組み合わせ等 により適宜選択することができる。 When the compound of the present invention and a concomitant drug are used in combination, the timing of administration of the compound of the present invention and the concomitant drug is not limited, and the compound of the present invention and the concomitant drug may be simultaneously administered to a subject to be administered. It may be administered at a time interval. The dose of the concomitant drug may be in accordance with the dose clinically used, and can be appropriately selected depending on the administration subject, administration route, disease, combination, and the like.
本発明の化合物と併用薬物の投与形態は、 特に限定されず、投与時に、 本発明の 化合物と併用薬物とが組み合わされていればよい。 このような投与形態としては、 例えば、 (1 )本発明の化合物と併用薬物とを同時に製剤化して得られる単一の製 剤の投与、 (2 )本発明の化合物と併用薬物とを別々に製剤化して得られる 2種の 製剤の同一投与経路での同時投与、 (3 )本発明の化合物と併用薬物とを別々に製 剤化して得られる 2種の製剤の同一投与経路での時間差をおいての投与、 (4 )本 発明の化合物と併用薬物とを別々に製剤化して得られる 2種の製剤の異なる投与 経路での同時投与、 (5 )本発明の化合物と併用薬物とを別々に製剤化して得られ る 2種の製剤の異なる投与経路での時間差をおいての投与(例えば、本発明の化合 物→併用薬物の順序での投与、 あるいは逆の順序での投与) などが挙げられる。以 下、 これらの投与形態をまとめて、 本発明の併用剤と略記する。 本発明の併用剤は、 毒性が低く、 例えば、 本発明の化合物または (および) 上記 併用薬物を自体公知の方法に従って、薬理学的に許容される担体と混合して医薬組 成物、 例えば錠剤 (糖衣錠、 フィルムコーティング錠を含む) 、 散剤、 顆粒剤、 力 プセル剤 (ソフトカプセルを含む) 、 液剤、 注射剤、 坐剤、 徐放剤等として、 経口 的又は非経口的 (例、 局所、 直腸、 静脈投与等) に安全に投与することができる。 注射剤は、 静脈内、 筋肉内、 皮下、 臓器内、 鼻腔内、 皮内、 点眼、 脳内、 直腸内、 膣内および腹腔内、腫瘍内部、腫瘍の近位などへの投与あるいは直接病巣に投与す ることができる。 The administration form of the compound of the present invention and the concomitant drug is not particularly limited as long as the compound of the present invention and the concomitant drug are combined at the time of administration. Such administration forms include, for example, (1) administration of a single preparation obtained by simultaneously preparing a compound of the present invention and a concomitant drug, and (2) separate administration of the compound of the present invention and the concomitant drug. Simultaneous administration of the two preparations obtained as a formulation by the same administration route, (3) the time difference between the same administration route of the two preparations obtained by separately preparing the compound of the present invention and the concomitant drug. (4) Simultaneous administration of two types of preparations obtained by separately formulating the compound of the present invention and the concomitant drug by different administration routes, (5) Separating the compound of the present invention and the concomitant drug (Eg, administration of the compound of the present invention → concomitant drug, or administration in the reverse order) of two types of preparations obtained by different preparation routes at different times. No. Hereinafter, these administration forms are collectively abbreviated as the concomitant drug of the present invention. The concomitant drug of the present invention has low toxicity. For example, the compound of the present invention or (and) the above concomitant drug is mixed with a pharmacologically acceptable carrier according to a method known per se to obtain a pharmaceutical composition such as a tablet. (Including sugar-coated tablets, film-coated tablets), powders, granules, capsules (including soft capsules), liquids, injections, suppositories, sustained-release preparations, etc., orally or parenterally (eg, topical, rectal) , Intravenous administration, etc.). Injectables can be administered intravenously, intramuscularly, subcutaneously, in organs, intranasally, intradermally, instilled, in the brain, rectum, intravaginally and intraperitoneally, inside tumors, near tumors, or directly into lesions It can be administered.
本発明の併用剤の製造に用いられてもよい薬理学的に許容される担体としては、 前記した本発明の医薬組成物に使用されるものと同様のものを使用することがで さる。 As the pharmacologically acceptable carrier that may be used in the production of the concomitant drug of the present invention, the same carriers as those used in the aforementioned pharmaceutical composition of the present invention can be used.
本発明の併用剤における本発明の化合物と併用薬物との配合比は、投与対象、投 与ルート、 疾患等により適宜選択することができる。 The compounding ratio of the compound of the present invention and the concomitant drug in the concomitant drug of the present invention can be appropriately selected depending on the administration subject, administration route, disease and the like.
例えば、本発明の併用剤における本発明の化合物の含有量は、製剤の形態によつ て相違するが、通常製剤全体に対して約 0 . 0 1ないし 1 0 0重量%、好ましくは 約 0 . 1ないし約 5 0重量%、 さらに好ましくは約 0 . 5ないし約 2 0重量%程度 である。 For example, the content of the compound of the present invention in the combination preparation of the present invention varies depending on the form of the preparation, but is usually about 0.01 to 100% by weight, preferably about 0. It is about 1 to about 50% by weight, more preferably about 0.5 to about 20% by weight.
本発明の併用剤における併用薬物の含有量は、 製剤の形態によって相違するが、 通常製剤全体に対して約 0 . 0 1ないし 1 0 0重量%、 好ましくは約 0 . 1ないし 約 5 0重量%、 さらに好ましくは約 0 . 5ないし約 2 0重量%程度である。 The content of the concomitant drug in the concomitant drug of the present invention varies depending on the form of the preparation, but is usually about 0.01 to 100% by weight, preferably about 0.1 to about 50% by weight, based on the whole preparation. %, More preferably about 0.5 to about 20% by weight.
本発明の併用剤における担体等の添加剤の含有量は、製剤の形態によって相違す るが、通常製剤全体に対して約 1ないし約 9 9 . 9 9重量%、好ましくは約 1 0な いし約 9 0重量%程度である。 The content of additives such as carriers in the concomitant drug of the present invention varies depending on the form of the preparation, but is usually about 1 to about 99.99% by weight, preferably about 10 to 10% by weight, based on the whole preparation. It is about 90% by weight.
また、本発明の化合物および併用薬物をそれぞれ別々に製剤化する場合も同様の 含有量でよい。 The same content may be used when the compound of the present invention and the concomitant drug are separately formulated.
これらの製剤は、製剤工程において通常一般に用いられる自体公知の方法により 製造することができる。 These preparations can be produced by a method known per se that is generally used in the preparation process.
例えば、 本発明の化合物または併用薬物は、 分散剤 (例、 ツイ一ン (Tween) 8 0 (アトラスパウダ一社製、 米国) 、 HC0 60 (日光ケミカルズ製) .、 ポリエチレン グリコール、 カルポキシメチルセルロース、 アルギン酸ナトリウム、 ヒドロキシプ 口ピルメチルセルロース、 デキストリンなど) 、 安定化剤 (例、 ァスコルビン酸、 ピロ亜硫酸ナトリウム等) 、 界面活性剤 (例、 ポリソルベート 8 0、 マクロゴール 等) 、 可溶剤 (例、 グリセリン、 エタノール等) 、 緩衝剤 (例、 リン酸及びそのァ ルカリ金属塩、 クェン酸及びそのアルカリ金属塩等) 、 等張化剤 (例、 塩化ナトリ ゥム、塩化カリウム、マンニトール、ソルビトール、ブドウ糖等)、 p H調節剤(例、 • 塩酸、水酸化ナトリウム等)、保存剤(例、パラォキシ安息香酸ェチル、安息香酸、 メチルパラベン、 プロピルパラベン、 ベンジルアルコール等) 、 溶解剤 (例、 濃グ リセリン、 メダルミン等) 、 溶解補助剤 (例、 プロピ ングリコール、 白糖等) 、 無痛化剤 (例、 ブドウ糖、 ベンジルアルコール等) などと共に水性注射剤に、 ある いはオリーブ油、 ゴマ油、 綿実油、 コ一ン油などの植物油、 プロピレングリコール などの溶解補助剤に溶解、懸濁あるいは乳化して油性注射剤に成形し、注射剤とす ることができる。 For example, the compound of the present invention or the concomitant drug may be a dispersant (eg, Tween 80 (manufactured by Atlas Powder Co., USA), HC060 (manufactured by Nikko Chemicals), polyethylene) Glycol, carboxymethylcellulose, sodium alginate, hydroxypropylmethylcellulose, dextrin, etc., stabilizers (eg, ascorbic acid, sodium pyrosulfite, etc.), surfactants (eg, polysorbate 80, macrogol, etc.), possible Solvents (eg, glycerin, ethanol, etc.), buffers (eg, phosphoric acid and its alkali metal salts, citrate and its alkali metal salts, etc.), tonicity agents (eg, sodium chloride, potassium chloride, mannitol) Sorbitol, glucose, etc.), pH regulators (eg, hydrochloric acid, sodium hydroxide, etc.), preservatives (eg, ethyl parabenzoyl benzoate, benzoic acid, methyl paraben, propyl paraben, benzyl alcohol, etc.), dissolving agents (eg, , Concentrated glycerin, medalmin, etc.), dissolution aid ( , Propylene glycol, sucrose, etc.) and soothing agents (eg, glucose, benzyl alcohol, etc.) in aqueous injections or dissolving olive oil, sesame oil, cottonseed oil, vegetable oils such as corn oil, propylene glycol, etc. It can be dissolved, suspended or emulsified in an auxiliary agent and formed into an oil-based injection to give an injection.
経口投与用製剤とするには、 自体公知の方法に従い、本発明の化合物または併用 薬物を例えば、賦形剤(例、乳糖、 白糖、 デンプンなど) 、崩壊剤(例、デンプン、 炭酸カルシウムなど) 、 結合剤 (例、 デンプン、 アラビアゴム、 カルポキシメチル セルロース、 ポリビニルピロリドン、 ヒドロキシプロピルセルロースなど)又は滑 沢剤 (例、 タルク、 ステアリン酸マグネシウム、 ポリエチレングリコール 6 0 0 0など) などを添加して圧縮成形し、 次いで必要により、 味のマスキング、 腸溶性 あるいは持続性の目的のため自体公知の方法でコーティングすることにより経口 投与製剤とすることができる。そのコーティング剤としては、 例えば、 ヒドロキシ プロピルメチルセルロース、 ェチルセルロース、 ヒドロキシメチルセルロース、 ヒ ドロキシプロピルセルロース、 ポリオキシエチレングリコ一ル、 ツイーン 8 0、 プル口ニック F 6 8、セルロースアセテートフタレート、 ヒドロキシプロピルメ チルセルロースフタレート、ヒドロキシメチルセル口ースアセテートサクシネート、 オイドラギット (ローム社製、 ドイツ、 メタアクリル酸 ·アクリル酸共重合) およ び色素 (例、 ベンガラ、 二酸化チタン等) などが用いられる。 経口投与用製剤は速 放性製剤、 徐放性製剤のいずれであってもよい。 In order to prepare a preparation for oral administration, the compound of the present invention or the concomitant drug is used in accordance with a method known per se, for example, excipients (eg, lactose, sucrose, starch, etc.), disintegrants (eg, starch, calcium carbonate, etc.) , A binder (eg, starch, gum arabic, carboxymethylcellulose, polyvinylpyrrolidone, hydroxypropylcellulose, etc.) or a lubricant (eg, talc, magnesium stearate, polyethylene glycol 600, etc.) By compression molding and, if necessary, coating with a method known per se for taste masking, enteric coating or long-lasting purposes, a preparation for oral administration can be obtained. Examples of the coating agent include hydroxypropylmethylcellulose, ethylcellulose, hydroxymethylcellulose, hydroxypropylcellulose, polyoxyethylene glycol, tween 80, pull mouth nick F68, cellulose acetate phthalate, and hydroxypropylmethyl cellulose. For example, tyl cellulose phthalate, hydroxymethyl cellulose acetate succinate, Eudragit (manufactured by Rohm, Germany, copolymerization of methacrylic acid / acrylic acid), and pigments (eg, bengara, titanium dioxide, etc.) are used. The preparation for oral administration may be either a quick release preparation or a sustained release preparation.
例えば、坐剤とするには、 自体公知の方法に従い、 本発明の化合物または併用薬 物を油性又は水性の固状、半固状あるいは液状の坐剤とすることができる。上記組 成物に用いる油性基剤としては、例えば、高級脂肪酸のグリセリド〔例、カカオ脂、 ウイテプゾル類 (ダイナマイトノーベル社製、 ドイツ) など〕 、 中級脂肪酸 〔例、 ミグリオ一ル類(ダイナマイトノーベル社,製、 ドイツ)など〕、あるいは植物油(例、 ゴマ油、 大豆油、 綿実油など) などが挙げられる。 また、 水性基剤としては、 例え ばポリエチレングリコール類、 プロピレングリコール、 水性ゲル基剤としては、 例 えば天然ガム類、 セルロース誘導体、 ビエル重合体、 アクリル酸重合体などが挙げ られる。 For example, to prepare a suppository, a compound of the present invention or a concomitant drug may be prepared according to a method known per se. The product can be an oily or aqueous solid, semi-solid or liquid suppository. Examples of the oily base used in the composition include glycerides of higher fatty acids (eg, cocoa butter, witepsols (manufactured by Dynamite Nobel, Germany), etc.), intermediate fatty acids [eg, migliols (manufactured by Dynamite Nobel And vegetable oils (eg, sesame oil, soybean oil, cottonseed oil, etc.). Examples of the aqueous base include polyethylene glycols and propylene glycol, and examples of the aqueous gel base include natural gums, cellulose derivatives, bier polymers, and acrylic acid polymers.
上記徐放性製剤としては、 徐放性マイクロ力プセル剤などが挙げられる。 Examples of the sustained-release preparation include sustained-release micro force capsules.
徐放型マイクロカプセルとするには、 自体公知の方法を採用できるが、 例えば、 下記 〔2〕 に示す徐放性製剤に成型して投与するのが好ましい。 A method known per se can be used to prepare a sustained release microcapsule. For example, it is preferable to administer the composition into a sustained release preparation shown in the following [2].
本発明の化合物は、 固形製剤 (例、 散剤、 顆粒剤、 錠剤、 カプセル剤) などの経 口投与用製剤に成型するか、 坐剤などの直腸投与用製剤に成型するのが好ましい。 特に経口投与用製剤が好ましい。 The compound of the present invention is preferably formed into a preparation for oral administration such as a solid preparation (eg, powder, granules, tablets, capsules) or a preparation for rectal administration such as a suppository. In particular, preparations for oral administration are preferred.
併用薬物は、 薬物の種類に応じて上記した剤形とすることができる。 The concomitant drug can be in the above-mentioned dosage form depending on the type of the drug.
以下に、 〔1〕 本発明の化合物または併用薬物の注射剤およびその調製、 〔2〕 本発明の化合物または併用薬物の徐放性製剤又は速放性製剤およびその調製、 In the following, (1) an injection of the compound of the present invention or the concomitant drug and its preparation, (2) a sustained-release preparation or immediate-release preparation of the compound or the concomitant drug of the present invention and its preparation,
〔3〕本発明の化合物または併用薬物の舌下錠、バッカル又は口腔内速崩壊剤およ びその調製について具体的に示す。 [3] Specific examples of the sublingual tablet, buccal or buccal disintegrant of the compound of the present invention or the concomitant drug and its preparation are shown below.
〔1〕 注射剤およびその調製 [1] Injection and its preparation
本発明の化合物または併用薬物を水に溶解してなる注射剤が好ましい。該注射剤 には安息香酸塩又は/およぴサリチル酸塩を含有させてもよい。 An injection prepared by dissolving the compound of the present invention or the concomitant drug in water is preferable. The injection may contain benzoate and / or salicylate.
該注射剤は、本発明の化合物または併用薬物と所望により安息香酸塩又は Zおよ びサリチル酸塩の双方を水に溶解することにより得られる。 The injection can be obtained by dissolving the compound of the present invention or the concomitant drug and, if desired, both benzoate or Z and salicylate in water.
上記安息香酸、 サリチル酸の塩としては、 例えばナトリウム, カリウムなどのァ ルカリ金属塩、 カルシウム, マグネシウムなどのアルカリ土類金属塩、 アンモニゥ ム塩、 メダルミン塩、 その他トロメタモールなどの有機酸塩などが挙げられる。 注射剤中の本発明の化合物または併用薬物の濃度は約 0 . 5〜約 5 0 w/v %、 好ましくは約 3〜約 2 0 wZ V %程度である。また安息香酸塩又は およびサリチ ル酸塩の濃度は約 0 . 5〜約 5 0 w/ v %、 好ましくは約 3〜約 2 0 wZ v %が好 ましい。 Examples of the salts of benzoic acid and salicylic acid include alkali metal salts such as sodium and potassium, alkaline earth metal salts such as calcium and magnesium, ammonium salts, medalmine salts, and organic acid salts such as trometamol. . The concentration of the compound of the present invention or the concomitant drug in the injection is about 0.5 to about 50 w / v%, preferably about 3 to about 20 wZV%. Also benzoate or and salic The concentration of the luate is preferably from about 0.5 to about 50 w / v%, preferably from about 3 to about 20 wZ v%.
また、 本剤には一般に注射剤に使用される添加剤、例えば安定化剤(ァスコルビ ン酸、 ピロ亜硫酸ナトリウム等) 、 界面活性剤 (ポリソルべ一ト 8 0、 マクロゴ一 ル等) 、 可溶剤 (グリセリン、 エタノール等) 、 緩衝剤 (リン酸及びそのアルカリ 金属塩、 クェン酸及びそのアルカリ金属塩等) 、 等張化剤 (塩化ナトリウム、 塩化 カリウム等)、分散剤(ヒドロキシプロピルメチルセルロース、デキストリン等)、 p H調節剤 (塩酸、 水酸化ナトリウム等) 、 保存剤 (パラォキシ安息香酸ェチル、 安息香酸等) 、 溶解剤 (濃グリセリン、 メグルミン等) 、 溶解補助剤 (プロピレン グリコ一ル、 白糖等) 、 無痛化剤 (ブドウ糖、 ベンジルアルコール等) などを適宜 配合することができる。これらの添加剤は一般に注射剤に通常用いられる割合で配 合される。 In addition, this agent contains additives commonly used for injections, such as stabilizers (ascorbic acid, sodium pyrosulfite, etc.), surfactants (polysorbate 80, macrogol, etc.), and solvents. (Glycerin, ethanol, etc.), buffers (phosphoric acid and its alkali metal salts, citric acid and its alkali metal salts, etc.), tonicity agents (sodium chloride, potassium chloride, etc.), dispersants (hydroxypropyl methylcellulose, dextrin, etc.) ), PH regulators (hydrochloric acid, sodium hydroxide, etc.), preservatives (ethyl ethyl parabenzoate, benzoic acid, etc.), solubilizers (concentrated glycerin, meglumine, etc.), solubilizers (propylene glycol, sucrose, etc.) And soothing agents (glucose, benzyl alcohol, etc.) and the like can be appropriately compounded. These additives are generally mixed in a ratio usually used for an injection.
注射剤の p Hは、 p H調節剤の添加により 2〜 1 2好ましくは 2 . 5〜 8 . 0に調 整することができる。 The pH of the injection can be adjusted to 2 to 12, preferably 2.5 to 8.0 by adding a pH regulator.
注射剤は本発明の化合物または併用薬物と所望により安息香酸塩又は/および サリチル酸塩の双方を、また必要により上記添加剤を水に溶解することにより得ら れる。 これらの溶解はどのような順序で行ってもよく、従来の注射剤の製法と同様 に適宜行うことができる。 An injection is obtained by dissolving both the compound of the present invention or the concomitant drug and, if desired, a benzoate and / or a salicylate, and if necessary, the above-mentioned additives in water. These dissolutions may be performed in any order, and can be appropriately performed in the same manner as in the conventional method for producing an injection.
注射用水溶液は加温するのがよく、また通常の注射剤と同様にたとえば濾過滅菌, 高圧加熱滅菌などを行うことにより注射剤として供することができる。 The aqueous solution for injection is preferably heated, and can be used as an injection by performing, for example, filtration sterilization or high-pressure heat sterilization in the same manner as an ordinary injection.
注射用水溶液は、例えば 1 0 0 °C〜 1 2 1 °Cの条件で 5分〜 3 0分高圧加熱滅菌 するのがよい。 The aqueous solution for injection is preferably subjected to high-pressure heat sterilization at 100 ° C. to 121 ° C. for 5 minutes to 30 minutes.
さらに多回分割投与製剤として使用できるように、溶液の抗菌性を付与した製剤 としてもよい。 Further, a formulation having antimicrobial properties of the solution may be used so that it can be used as a multiple-dose formulation.
〔2〕 徐放性製剤又は速放性製剤およびその調製 [2] Sustained-release preparation or immediate-release preparation and its preparation
本発明の化合物または併用薬物を含んでなる核を所望により水不溶性物質ゃ膨 潤性ポリマーなどの被膜剤で被覆してなる徐放性製剤が好ましい。例えば、 1日 1 回投与型の経口投与用徐放性製剤が好ましい。 A sustained-release preparation comprising a core comprising the compound of the present invention or the concomitant drug optionally coated with a film-forming agent such as a water-insoluble substance-swellable polymer is preferred. For example, a once-daily sustained release preparation for oral administration is preferred.
被膜剤に用いられる水不溶性物質としては、例えばェチルセルロース、 プチルセ ルロースなどのセルロースエーテル類、セルロースアセテート、セルロースプロピ ォネートなどのセルロースエステル類、ポリビエルアセテート、ポリピニルブチレ ートなどのポリビニルエステル類、 アクリル酸 Zメタクリル酸共重合体、 メチルメ タクリレー卜共重合体、 Xトキシェチルメタクリレ一ト /シンナモェチルメタクリ レート Zアミノアルキルメタクリレート共重合体、ポリアクリル酸、ポリメタクリ ル酸、 メタクリル酸アルキルアミド共重合体、 ポリ (メタクリル酸メチル) 、 ポリ メタクリレート、ポリメタクリルアミド、アミノアルキルメタクリレー卜共重合体、 ポリ (メタクリル酸アンヒドリド) 、 グリシジルメタクリレート共重合体、 とりわ けオイドラギット RS— 100, RL- 100, RS- 3 OD, RL- 3 OD, R L-PO, RS— PO (アクリル酸ェチル ·メタクリル酸メチル ·メタクリル酸塩 化トリメチル ·アンモニゥムェチル共重合体) 、 オイドラギット NE—30D (メ タクリル酸メチル 'ァクリル酸ェチル共重合体)などのオイドラギット類(ローム · ファーマ社) などのアクリル酸系ポリマー、 硬化ヒマシ油 (例、 ラブリーワックス (フロイント産業) など) などの硬化油、 カルナバワックス、 脂肪酸グリセリンェ ステル、パラフィンなどのワックス類、ポリグリセリン脂肪酸エステル等が挙げら れる。 Examples of the water-insoluble substance used in the coating agent include ethyl cellulose and butyl cellulose. Cellulose ethers such as cellulose, cellulose esters such as cellulose acetate and cellulose propionate, polyvinyl esters such as polybier acetate and polypinyl butyrate, acrylic acid Z methacrylic acid copolymer, methyl methacrylate copolymer, X toki Shetyl methacrylate / cinnamethyl methacrylate Z-aminoalkyl methacrylate copolymer, polyacrylic acid, polymethacrylic acid, methacrylic acid alkylamide copolymer, poly (methyl methacrylate), poly methacrylate, polymethacrylamide, Aminoalkyl methacrylate copolymer, poly (methacrylic anhydride), glycidyl methacrylate copolymer, especially Eudragit RS-100, RL-100, RS-3OD, RL-3OD, RL-PO, RS — PO (Acri Eudragits (Rohm Pharma Co., Ltd.) such as ethyl acrylate, methyl methacrylate, trimethyl methacrylate, and ammonium methacrylate copolymer, and Eudragit NE-30D (methyl methacrylate and ethyl acrylate acrylate). And hardened oils such as hardened castor oil (eg, Lovely wax (Freund Corporation)), carnauba wax, fatty acids glycerin ester, waxes such as paraffin, polyglycerin fatty acid esters, and the like.
膨潤性ポリマーとしては、 酸性の解離基を有し、 p H依存性の膨潤を示すポリ マーが好ましく、 胃内のような酸性領域では膨潤が少なく、小腸や大腸などの中性 領域で膨潤が大きくなる酸性の解離基を有するポリマーが好ましい。 As the swellable polymer, a polymer having an acidic dissociating group and exhibiting pH-dependent swelling is preferable.Swelling is less in an acidic region such as in the stomach and swelling in a neutral region such as the small intestine and the large intestine. Polymers having an acidic dissociating group that grows are preferred.
このような酸性の解離基を有し p H依存性の膨潤を示すポリマーとしては、 例 えば力一ポマー (carbomer) 934P、 940、 941、 974P、 980、 13 42等、ポリカーボフィル(polycarbophi 1)、カルシウムポリカーボフィル(calcium polycarbophil) (前記はいずれも B Fグッドリッチ社製) 、 ハイビスヮコ一 10 3、 104、 105、 304 (いずれも和光純薬 (株). 製) などの架橋型ポリアク リル酸重合体が挙げられる。 Examples of the polymer having such an acidic dissociating group and exhibiting pH-dependent swelling include, for example, carbomer 934P, 940, 941, 944, 980, 1342, and the like, such as polycarbophil 1 , Calcium polycarbophil (all of which are manufactured by BF Goodrich), and Hibis Pico 103, 104, 105, 304 (all of which are manufactured by Wako Pure Chemical Industries, Ltd.). Coalescence.
徐放性製剤に用いられる被膜剤は親水性物質をさらに含んでいてもよい。 The coating agent used in the sustained-release preparation may further contain a hydrophilic substance.
該親水性物質としては、例えばプルラン、 デキストリン、 アルギン酸アルカリ金 属塩などの硫酸基を有していてもよい多糖類、 ヒドロキシプロピルセルロース、 ヒ ドロキシプロピルメチルセルロース、カルポキシメチルセル口一スナトリゥムなど のヒドロキシアルキル基又はカルポキシアルキル基を有する多糖類、メチルセル口 ース、 ポリビエルピロリドン、 ポリビニルアルコール、 ポリエチレングリコールな どが挙げられる。 Examples of the hydrophilic substance include polysaccharides which may have a sulfate group, such as pullulan, dextrin, alkali metal alginate, hydroxypropylcellulose, hydroxypropylmethylcellulose, carboxymethylcellulose-snadium, and the like. Polysaccharides having a hydroxyalkyl group or a carboxyalkyl group, methylcellulose, polyvinylpyrrolidone, polyvinyl alcohol, polyethylene glycol and the like.
徐放性製剤の被膜剤における水不溶性物質の含有率は約 3 0ないし約 9 0 % (w/w) 、 好ましくは約 3 5ないし約 8 0 % (w/w) 、 さらに好ましくは約 4 0ない し 7 5 % (w/w) 、 膨潤性ポリマーの含有率は約 3ないし約 3 0 % (w/w) 、 好まし くは約 3ないし約 1 5 % (w/w)である。 被膜剤は親水性物質をさらに含んでいても よく、 その場合被膜剤における親水性物質の含有率は約 5 0 % (w/w)以下、 好まし くは約 5〜約 4 0 % (w/w) 、 さらに好ましくは約 5〜約 3 5 % (w/w) である。こ こで上記% (w/w) は被膜剤液から溶媒 (例、 水、 メタノール、 エタノール等の低 級アルコール等) を除いた被膜剤組成物に対する重量%を示す。 The content of the water-insoluble substance in the coating agent of the sustained-release preparation is about 30 to about 90% (w / w), preferably about 35 to about 80% (w / w), more preferably about 4 0 to 75% (w / w), swellable polymer content of about 3 to about 30% (w / w), preferably about 3 to about 15% (w / w) . The coating may further comprise a hydrophilic substance, in which case the content of the hydrophilic substance in the coating is not more than about 50% (w / w), preferably about 5 to about 40% (w / w), more preferably from about 5 to about 35% (w / w). Here, the above-mentioned% (w / w) refers to% by weight based on the coating composition obtained by removing the solvent (eg, water, lower alcohol such as methanol, ethanol, etc.) from the coating composition liquid.
徐放性製剤は、以下に例示するように薬物を含む核を調製し、次いで得られた核 を、水不溶性物質や膨潤性ポリマーなどを加熱溶解あるいは溶媒に溶解又は分散さ せた被膜剤液で被覆することにより製造される。 The sustained-release preparation is prepared by preparing a nucleus containing a drug as exemplified below, and then dissolving the obtained nucleus by heating or dissolving or dispersing a water-insoluble substance or a swellable polymer in a solvent. It is manufactured by coating with
I . 薬剤を含む核の調製 I. Preparation of nuclei containing drugs
被膜剤で被覆される薬物を含む核(以下、単に核と称することがある) の形態は 特に制限されないが、 好ましくは顆粒あるいは細粒などの粒子状に形成される。 核が顆粒又は細粒の場合、 その平均粒子径は、 好ましくは約 1 5 0ないし約 2 , 0 0 0 u m, さらに好ましくは約 5 0 0ないし約 1, 4 0 0 x mである。 The form of the nucleus containing the drug to be coated with the coating agent (hereinafter sometimes simply referred to as the nucleus) is not particularly limited, but is preferably formed into particles such as granules or fine granules. When the core is granules or fine granules, the average particle size is preferably from about 150 to about 2,000 um, more preferably from about 500 to about 1,400 x m.
核の調製は通常の製造方法で実施することができる。例えば、薬物に適当な賦形 剤、 結合剤、 崩壊剤、 滑沢剤、 安定化剤等を混合し、 湿式押し出し造粒法、 流動層 造粒法などにより調製する。 ' The nucleus can be prepared by a usual production method. For example, a drug is mixed with an appropriate excipient, binder, disintegrant, lubricant, stabilizer, and the like, and the mixture is prepared by wet extrusion granulation, fluidized bed granulation, or the like. '
核の薬物含量は、約 0 . 5ないし約 9 5 % (w/w)、好ましくは約 5ないし約 8 0 % (w/w) 、 さらに好ましくは約 3 0ないし約 7 0 % (w/w) である。 The drug content of the core is about 0.5 to about 95% (w / w), preferably about 5 to about 80% (w / w), and more preferably about 30 to about 70% (w / w). w).
核に含まれる賦形剤としては、 例えば白糖、 乳糖、 マンニト一ル、 グルコースな どの糖類、澱粉、 結晶セルロース、 リン酸カルシウム、 コーンスターチなどが用い られる。 中でも、 結晶セルロース、 コーンスターチが好ましい。 Examples of excipients contained in the core include sugars such as sucrose, lactose, mannitol, glucose, starch, crystalline cellulose, calcium phosphate, corn starch and the like. Among them, crystalline cellulose and corn starch are preferred.
結合剤としては、例えばポリビエルアルコール、ヒドロキシプロピルセルロース、 ポリエチレングリコール、 ポリビニルピロリドン、 プル口ニック F 6 8、 アラビア ゴム、 ゼラチン、 澱粉などが用いられる。崩壊剤としては、 例えばカルポキシメチ ルセルロースカルシウム(ECG505)、 クロスカルメ口一スナトリゥム(Ac-Di- Sol)、 架橋型ポリビニルピロリドン (クロスポビドン) 、 低置換度ヒドロキシプロピルセ ルロ一ス (L- HPC) などが用いられる。 中でも、 ヒドロキシプロピルセルロース、 ポリビニルピロリドン、低置換度ヒドロキシプロピルセルロースが好ましい。滑沢 剤、 凝集防止剤としては例えばタルク、 ステアリン酸マグネシウム、 また潤滑剤と してポリエチレングリコールなどが用いられる。安定化剤としては酒石酸、 クェン 酸、 コハク酸、 フマル酸、 マレイン酸などの酸が用いられる。 Examples of the binder include polyvinyl alcohol, hydroxypropylcellulose, polyethylene glycol, polyvinylpyrrolidone, pull nick F68, and Arabic Rubber, gelatin, starch and the like are used. Disintegrants include, for example, carboxymethylcellulose calcium (ECG505), croscarmethylene monosodium sodium (Ac-Di-Sol), cross-linked polyvinylpyrrolidone (crospovidone), low-substituted hydroxypropylcellulose (L-HPC) Are used. Among them, hydroxypropylcellulose, polyvinylpyrrolidone and low-substituted hydroxypropylcellulose are preferred. For example, talc and magnesium stearate are used as a lubricant and an anti-agglomeration agent, and polyethylene glycol and the like are used as a lubricant. Acids such as tartaric acid, citric acid, succinic acid, fumaric acid and maleic acid are used as stabilizers.
核は上記製造法以外にも、例えば核の中心となる不活性担体粒子上に水、低級ァ ルコール(例、 メタノ一ル、 エタノールなど) 等の適当な溶媒に溶解した結合剤を スプレーしながら、薬物あるいはこれと賦形剤、滑沢剤などとの混合物を少量づっ 添加して行なう転動造粒法、パンコーティング法、流動層コ一ティング法や溶融造 粒法によって ¾調製することができる。不活性担体粒子としては、例えば白糖、 乳 糖、 澱粉、 結晶セルロース、 ワックス類で製造されたものが使用でき、 その平均粒 子径は約 1 0 0 111なぃし約1 , 5 0 0 mであるものが好ましい。 The nucleus may be formed by spraying a binder dissolved in a suitable solvent such as water, lower alcohol (eg, methanol, ethanol, etc.) onto the inert carrier particles serving as the center of the nucleus, in addition to the above-mentioned production method. It can be prepared by the tumbling granulation method, pan coating method, fluidized bed coating method or melt granulation method, in which a small amount of a drug or a mixture of an excipient and a lubricant is added. it can. As the inert carrier particles, for example, those made of sucrose, lactose, starch, crystalline cellulose, and waxes can be used, and the average particle size is about 100 111, or about 1,500 m. Is preferred.
核に含まれる薬物と被膜剤とを分離するために、防護剤で核の表面を被覆しても よい。 防護剤としては、 例えば前記親水性物質や、 水不溶性物質等が用いられる。 防護剤は、好ましくはポリエチレングリコールゃヒドロキシアルキル基又はカルボ キシアルキル基を有する多糖類、より好ましくはヒドロキシプロピルメチルセル口 ース、 ヒドロキシプロピルセルロースが用いられる。該防護剤には安定化剤として 酒石酸、 クェン酸、 コハク酸、 フマル酸、 マレイン酸等の酸や、 タルクなどの滑沢 剤を含んでいてもよい。防護剤を用いる場合、その被覆量は核に対して約 1ないし 約 1 5 % ( /w) 、 好ましくは約 1ないし約 1 0 % (w/w) 、 さらに好ましくは約 2 ないし約 8 % (w/w) である。 To separate the drug contained in the nucleus from the coating agent, the surface of the nucleus may be coated with a protective agent. As the protective agent, for example, the above-mentioned hydrophilic substances, water-insoluble substances and the like are used. As the protective agent, a polysaccharide having a polyethylene glycol-hydroxyalkyl group or a carboxyalkyl group is preferably used, and hydroxypropylmethyl cellulose and hydroxypropylcellulose are more preferably used. The protective agent may contain, as a stabilizer, an acid such as tartaric acid, citric acid, succinic acid, fumaric acid, and maleic acid, and a lubricant such as talc. When a protective agent is used, its coating amount is about 1 to about 15% (w / w), preferably about 1 to about 10% (w / w), more preferably about 2 to about 8% based on the core. (w / w).
防護剤は通常のコ一ティング法により被覆することができ、具体的には、防護剤 を例えば流動層コ一ティング法、パンコーティング法等により核にスプレーコーテ ィングすることで被覆することができる。 The protective agent can be coated by a usual coating method.Specifically, the protective agent can be coated by spray-coating the nucleus by, for example, a fluidized-bed coating method or a pan coating method. .
I I. 核の被膜剤による被覆 I I. Coating of core with coating agent
前記 Iで得られた核を、 前記水不溶性物質及び p H依存性の膨潤性ポリマー、 および親水性物質を加熱溶解あるいは溶媒に溶解又は分散させた被膜剤液により 被覆することにより徐放性製剤が製造される。 The nuclei obtained in I above, the water-insoluble substance and a pH-dependent swellable polymer, In addition, a sustained-release preparation is produced by heating and dissolving a hydrophilic substance or coating with a coating agent solution in which a hydrophilic substance is dissolved or dispersed in a solvent.
核の被膜剤液による被覆方法として、例えば噴霧コーティングする方法などが挙 げられる。 Examples of the method of coating the core with a coating agent solution include a spray coating method.
被膜剤液中の水不溶性物質、膨潤性ポリマー又は親水性物質の組成比は、被膜中 の各成分の含有率がそれぞれ前記含有率となるように適宜選ばれる。 The composition ratio of the water-insoluble substance, the swellable polymer or the hydrophilic substance in the coating solution is appropriately selected so that the content of each component in the coating becomes the above-mentioned content.
被膜剤の被覆量は、核(防護剤の被覆量を含まない)に対して約 1ないし約 9 0 % (w/w) 、 好ましくは約 5ないし約 5 0 % (w/w) 、 さらに好ましくは約 5ないし 3 5 % (w/w) である。 The coating amount of the coating agent is about 1 to about 90% (w / w), preferably about 5 to about 50% (w / w), based on the core (not including the protective agent). Preferably it is about 5 to 35% (w / w).
被膜剤液の溶媒としては水又は有機溶媒を単独であるいは両者の混液を用いる ことができる。混液を用いる際の水と有機溶媒との混合比(水/有機溶媒:重量比) は、 1ないし 1 0 0 %の範囲で変化させることができ、 好ましくは 1ないし約 3 0 %である。該有機溶媒としては、水不溶性物質を溶解するものであれば特に限定 されないが、 例えばメタノール、 エタノール、 2—プロパノール、 1ーブ夕ノール 等の低級アルコール、 ァセトンなどの低級アル力ノン、 ァセトニトリル、 クロロホ ルム、 ジクロロメタンなどが用いられる。 このうち低級アルコールが好ましく、 ェ タノール、 2—プロパノールが特に好ましい。水及び水と有機溶媒との混液が被膜 剤の溶媒として好ましく用いられる。 この時、必要であれば被膜剤液中に被膜剤液 安定化のために酒石酸、 クェン酸、 コハク酸、 フマル酸、 マレイン酸などの酸を加 えてもよい。 As the solvent for the coating agent solution, water or an organic solvent can be used alone or in a mixture of both. The mixing ratio of water and organic solvent (water / organic solvent: weight ratio) when using the mixed solution can be changed in the range of 1 to 100%, and is preferably 1 to about 30%. The organic solvent is not particularly limited as long as it dissolves a water-insoluble substance. Examples thereof include lower alcohols such as methanol, ethanol, 2-propanol and 1-butanol, lower alkynones such as acetone, acetonitrile, and the like. Chloroform, dichloromethane and the like are used. Of these, lower alcohols are preferred, and ethanol and 2-propanol are particularly preferred. Water and a mixture of water and an organic solvent are preferably used as a solvent for the coating agent. At this time, if necessary, an acid such as tartaric acid, citric acid, succinic acid, fumaric acid, or maleic acid may be added to the coating agent solution for stabilization.
噴霧コーティングにより被覆する場合の操作は通常のコ一ティング法により実 施することができ、具体的には、被膜剤液を例えば流動層コーティング法、 バンコ 一ティング法等により核にスプレーコーティングすることで実施することがでさ る。 この時必要であれば、 タルク、 酸化チタン、 ステアリン酸マグネシウム、 ステ ァリン酸カルシウム、軽質無水ゲイ酸などを滑沢剤として、 グリセリン脂肪酸エス テル、 硬化ヒマシ油、 クェン酸トリエチル、 セチルアルコール、 ステアリルアルコ ールなどを可塑剤として添加してもよい。 The operation for coating by spray coating can be performed by a usual coating method.Specifically, the coating agent solution is spray-coated on the nucleus by, for example, a fluidized bed coating method or a banco coating method. It can be implemented at At this time, if necessary, talc, titanium oxide, magnesium stearate, calcium stearate, light gay anhydride, etc. are used as lubricants, and glycerin fatty acid ester, hydrogenated castor oil, triethyl quenate, cetyl alcohol, stearyl alcohol are used. May be added as a plasticizer.
被膜剤による被膜後、 必要に応じてタルクなどの帯電防止剤を混合してもよい。 速放性製剤は、 液状 (溶液、 懸濁液、 乳化物など)であっても固形状 (粒子状、 丸剤、 錠剤など) であってもよい。 経口投与剤、 注射剤など非経口投与剤が用いら れるが、 経口投与剤が好ましい。 After coating with a coating agent, an antistatic agent such as talc may be mixed as necessary. Immediate release preparations can be liquid (solutions, suspensions, emulsions, etc.) or solid (particles, Pills, tablets, etc.). Parenteral preparations such as oral preparations and injections are used, but oral preparations are preferred.
速放性製剤は、通常、活性成分である薬物に加えて、製剤分野で慣用される担体、 添加剤や賦形剤 (以下、 賦形剤と略称することがある) を含んでいてもよい。用い られる製剤賦形剤は、製剤賦形剤として常用される賦形剤であれば特に限定されな い。 例えば経口固形製剤用の賦形剤としては、 乳糖、 デンプン、 コーンスターチ、 結晶セルロース (旭化成 (株) 製、 アビセル PH 101など) 、 粉糖、 グラニュー 糖、 マンニトール、 軽質無水ケィ酸、 炭酸マグネシウム、 炭酸カルシウム、 L—シ スティンなどが挙げられ、好ましくはコーンスターチおよびマンニトールなどが挙 げられる。 これらの賦形剤は一種又は二種以上を組み合わせて使用できる。賦形剤 の含有量は速放性製剤全量に対して、 例えば約 4. 5〜約 99. 4w/w%、 好ま しくは約 20〜約 98. 5w/w%、 さらに好ましくは約 30〜約 97w/w%であ る。 Immediate release preparations may generally contain, in addition to the drug as an active ingredient, carriers, additives and excipients (hereinafter sometimes abbreviated as excipients) commonly used in the pharmaceutical field. . The formulation excipient used is not particularly limited as long as it is a commonly used excipient. For example, excipients for oral solid preparations include lactose, starch, corn starch, crystalline cellulose (such as Avicel PH101, manufactured by Asahi Kasei Corporation), powdered sugar, granulated sugar, mannitol, light caffeic anhydride, magnesium carbonate, carbonate Calcium, L-cysteine and the like, preferably corn starch and mannitol. These excipients can be used alone or in combination of two or more. The content of the excipient is, for example, about 4.5 to about 99.4 w / w%, preferably about 20 to about 98.5 w / w%, more preferably about 30 to It is about 97w / w%.
速放性製剤における薬物の含量は、速放性製剤全量に対して、約 0.5〜約 95%、 好ましくは約 1〜約 60%の範囲から適宜選択することができる。 The content of the drug in the immediate release preparation can be appropriately selected from the range of about 0.5 to about 95%, preferably about 1 to about 60%, based on the total amount of the immediate release preparation.
速放性製剤が経口固形製剤の場合、 通常上記成分に加えて、 崩壊剤を含有する。 このような崩壊剤としては、例えばカルボキシメチルセルロースカルシウム(五徳 薬品製、 ECG— 505) 、 クロスカルメロースナトリウム (例えば、旭化成(株) 製、 ァクジゾル) 、 クロスポビドン (例えば、 BASF社製、 コリドン CL) 、 低 置換度ヒドロキシプロピルセル口一ス (信越化学 (株) ) 、 カルポキシメチルス夕 ーチ (松谷化学 (株) ) 、 カルポキシメチルスターチナトリゥム (木村産業製、 X キスプロタブ)、 部分 α化デンプン (旭化成 (株) 製、 PCS) などが用いられ、 例えば水と接触して吸水、膨潤、 あるいは核を構成している有効成分と賦形剤との 間にチャネルを作るなどにより顆粒を崩壊させるものを用いることができる。これ らの崩壊剤は、 一種又は二種以上を組み合わせて使用できる。 崩壊剤の配合量は、 用いる薬物の種類や配合量、放出性の製剤設計などにより適宜選択されるが、速放 性製剤全量に対して、 例えば約 0. 05〜約 30w/w%、 好ましくは約 0. 5〜 約 15w/w%である。 When the immediate release preparation is an oral solid preparation, it usually contains a disintegrant in addition to the above components. Examples of such disintegrants include carboxymethylcellulose calcium (manufactured by Gotoku Pharmaceutical Co., ECG-505), croscarmellose sodium (eg, Asahi Kasei Co., Ltd., AXIDISOL), crospovidone (eg, BASF Corporation, Kolydone CL) , Low-substituted hydroxypropylcells (Shin-Etsu Chemical Co., Ltd.), carboxymethyl starch (Matsuya Chemical Co., Ltd.), carboxymethyl starch sodium (Kimura Sangyo, X Kisprotab), part Pregelatinized starch (PCS, manufactured by Asahi Kasei Corporation) is used. Granules are formed by, for example, contacting with water to absorb water, swell, or create a channel between the active ingredient constituting the core and the excipient. Can be used. These disintegrants can be used alone or in combination of two or more. The blending amount of the disintegrant is appropriately selected depending on the kind and blending amount of the drug to be used, the design of the release preparation, and the like. Is from about 0.5 to about 15 w / w%.
速放性製剤が経口固形製剤である場合、経口固形製剤の場合には上記の組成に加 えて、所望により固形製剤において'置用の添加剤をさらに含んでいてもよい。 この ような添加剤としては、 例えば結合剤 (例えば、 ショ糖、 ゼラチン、 アラビアゴム 末、 メチルセルロース、 ヒドロキシプロピルセルロース、 ヒドロキシプロピルメチ ルセルロース、 カルポキシメチルセルロース、 ポリビュルピロリドン、 プルラン、 デキストリンなど)、 滑沢剤 (例えば、 ポリエチレングリコール、 ステアリン酸マ グネシゥム、 タルク、軽質無水ゲイ酸(例えば、 ァエロジル(日本ァエロジル))、 界面活性剤 (例えば、 アルキル硫酸ナトリウムなどのァニオン系界面活性剤、 ポリ ォキシエチレン脂肪酸エステルおよびポリオキシエチレンソルビタン脂肪酸エス テル、 ポリオキシエチレンヒマシ油誘導体等の非イオン系界面活性剤など)、 着色 剤(例えば、 タール系色素、 カラメル、 ベンガラ、酸化チタン、 リボフラビン類)、 必要ならば、 矯味剤 (例えば、 甘味剤、 香料など)、 吸着剤、 防腐剤、 湿潤剤、 帯 電防止剤などが用いられる。 また、 安定化剤として酒石酸、 クェン酸、 コハク酸、 フマル酸などの有機酸を加えてもよい。 If the immediate-release preparation is an oral solid preparation, or if it is an oral solid preparation, it is added to the above composition. Alternatively, if necessary, the solid preparation may further contain an additive for placement. Examples of such additives include binders (for example, sucrose, gelatin, gum arabic, methylcellulose, hydroxypropylcellulose, hydroxypropylmethylcellulose, carboxymethylcellulose, polyvinylpyrrolidone, pullulan, dextrin, etc.) Sourcing agents (eg, polyethylene glycol, magnesium stearate, talc, light gay anhydride (eg, AEROSIL (Nippon AEROSIL)), surfactants (eg, anionic surfactants such as sodium alkyl sulfate, polyoxyethylene fatty acid esters) And non-ionic surfactants such as polyoxyethylene sorbitan fatty acid ester, polyoxyethylene castor oil derivative, etc.), coloring agents (for example, tar pigments, caramel, bengara, acid) Titanium, riboflavins), if necessary, flavoring agents (eg, sweeteners, flavors, etc.), adsorbents, preservatives, wetting agents, antistatic agents, etc. Tartaric acid, citrate as a stabilizer Organic acids such as succinic acid and fumaric acid may be added.
上記結合剤としては、 ヒドロキシプロピルセルロース、ポリエチレングリコール およびポリビニルピロリドンなどが好ましく用いられる。 As the above-mentioned binder, hydroxypropyl cellulose, polyethylene glycol, polyvinyl pyrrolidone and the like are preferably used.
速放性製剤は、通常の製剤の製造技術に基づき、 前記各成分を混合し、 必要によ り、 さらに練合し、 成型することにより調製することができる。 上記混合は、 一般 に用いられる方法、 例えば、 混合、 練合などにより行われる。 具体的には、 例えば 速放性製剤を粒子状に形成する場合、前記徐放性製剤の核の調製法と同様の手法に より、 バーチカルグラ二ユレ一タ一、 万能練合機 (畑鉄工所製)、 流動層造粒機 F D - 5 S (パゥレック社製) 等を用いて混合しその後、 湿式押し出し造粒法、 流動 層造粒法などにより造粒することにより調製することができる。 The immediate-release preparation can be prepared by mixing the above-mentioned components, kneading and molding as necessary, based on a usual preparation production technique. The mixing is performed by a generally used method such as mixing and kneading. Specifically, for example, when a rapid-release preparation is formed into particles, a vertical granulator, a universal kneading machine (Hata Tekko And fluidized-bed granulator FD-5S (manufactured by Palek Co., Ltd.), followed by granulation by wet extrusion granulation, fluidized bed granulation, or the like.
このようにして得られた速放性製剤と徐放性製剤とは、 そのままあるいは適宜、 製剤賦形剤等と共に常法により別々に製剤化後、同時あるいは任意の投与間隔を挟 んで組み合わせて投与する製剤としてもよく、 また両者をそのままあるいは適宜、 製剤賦形剤等と共に一つの経口投与製剤(例、顆粒剤、細粒剤、錠剤、カプセル等) に製剤化してもよい。両製剤を顆粒あるいは細粒に製して、 同一のカプセル等に充 填して経口投与用製剤としてもよい。 The immediate-release preparation and the sustained-release preparation thus obtained can be administered as they are, or separately, separately and in combination with excipients, etc., according to a conventional method, and then administered simultaneously or in combination at an arbitrary administration interval. Alternatively, both preparations may be formulated as a single orally administered preparation (eg, granules, fine granules, tablets, capsules, etc.) as they are or as appropriate, together with excipients. Both preparations may be made into granules or fine granules and filled in the same capsule or the like to prepare a preparation for oral administration.
〔3〕 舌下錠、 パッカル又は口腔内速崩壊剤およびその調製 舌下錠、パッカル製剤、口腔内速崩壊剤は錠剤などの固形製剤であってもよいし、 口腔粘膜貼付錠 (フィルム) であってもよい。 [3] Sublingual tablet, puccal or oral fast disintegrating agent and its preparation The sublingual tablet, the puccal preparation, and the quick disintegrating agent in the oral cavity may be a solid preparation such as a tablet or an oral mucosa patch (film).
舌下錠、バッカル又は口腔内速崩壊剤としては、本発明の化合物または併用薬物 と賦形剤とを含有する製剤が好ましい。 また、 滑沢剤、 等張化剤、 親水性担体、 水 分散性ポリマー、 安定化剤などの補助剤を含有していてもよい。 また、 吸収を容易 にし、生体内利用率を高めるために /3—シクロデキストリン又は |3—シクロデキス トリン誘導体(例、 ヒドロキシプロピル一 3—シクロデキストリンなど) などを含 有していてもよい。 As the sublingual tablet, buccal or intraoral quick disintegrating agent, a preparation containing the compound of the present invention or the concomitant drug and an excipient is preferable. In addition, auxiliary agents such as a lubricant, a tonicity agent, a hydrophilic carrier, a water-dispersible polymer, and a stabilizer may be contained. Further, it may contain a / 3-cyclodextrin or | 3-cyclodextrin derivative (eg, hydroxypropyl-13-cyclodextrin) for facilitating absorption and increasing bioavailability.
上記賦形剤としては、 乳糖、 白糖、 D—マンニトール、 デンプン、 結晶セルロー ス、軽質無水ケィ酸などが挙げられる。滑沢剤としてはステアリン酸マグネシウム、 ステアリン酸カルシウム、 タルク、 コロイドシリカなどが挙げられ、 特に、 ステア リン酸マグネシウムゃコロイドシリ力が好ましい。等張化剤としては塩化ナトリウ ム、 グルコース、 フルクトース、 マンニトール、 ソルビ! ^一ル、 ラクト一ス、 サッ 力ロース、 グリセリン、 尿素などが挙げられ、 特にマンニトールが好ましい。 親水 性担体としては結晶セルロース、ェチルセルロース、架橋性ポリビエルピロリドン、 軽質無水ケィ酸、 ケィ酸、 リン酸二カルシウム、 炭酸カルシウムなどの膨潤性親水 性担体が挙げられ、特に結晶セルロース(例、微結晶セル口一スなど)が好ましい。 水分散性ポリマーとしてはガム (例、 トラガカントガム、 アカシアガム、 グァ一ガ ム) 、 アルギン酸塩 (例、 アルギン酸ナトリウム) 、 セルロース誘導体 (例、 メチ ルセルロース、 カルポキシメチルセルロース、 ヒドロキシメチルセルロース、 ヒド ロキシプロピルセルロース、 ヒドロキシプロピルメチルセルロース) 、 ゼラチン、 水溶性デンプン、 ポリアクリル酸 (例、 カーポマー) 、 ポリメタクリル酸、 ポリビ ニルアルコール、 ポリエチレングリコール、 ポリビニルピロリドン、 ポリカーポフ ィル、 ァスコルビン酸パルミチン酸エステルなどが挙げられ、 ヒドロキシプロピル メチルセルロース、 ポリアクリル酸、 アルギン酸塩、 ゼラチン、 カルポキシメチル セ^)レロース、 ポリピエルピロリドン、 ポリエチレングリコールなどが好ましい。 特 にヒドロキシプロピルメチルセルロースが好ましい。安定化剤としては、 システィ ン、 チォソルビトール、 酒石酸、 クェン酸、 炭酸ナトリウム、 ァスコルビン酸、 グ リシン、亜硫酸ナトリウムなどが挙げられ、 特に、 クェン酸ゃァスコルビン酸が好 ましい。 Examples of the above-mentioned excipients include lactose, sucrose, D-mannitol, starch, crystalline cellulose, light caffeic anhydride and the like. Examples of the lubricant include magnesium stearate, calcium stearate, talc, colloidal silica, and the like, and magnesium stearate-colloidal silica is particularly preferable. Examples of the tonicity agent include sodium chloride, glucose, fructose, mannitol, sorbitol, lactose, saccharose, glycerin, urea and the like, with mannitol being particularly preferred. Examples of the hydrophilic carrier include swellable hydrophilic carriers such as crystalline cellulose, ethyl cellulose, cross-linkable polybierpyrrolidone, light caffeic anhydride, citric acid, dicalcium phosphate, and calcium carbonate. Microcrystal cell openings) are preferred. Water-dispersible polymers include gums (eg, tragacanth, acacia, guar gum), alginates (eg, sodium alginate), cellulose derivatives (eg, methylcellulose, carboxymethylcellulose, hydroxymethylcellulose, hydroxypropylcellulose) , Hydroxypropyl methylcellulose), gelatin, water-soluble starch, polyacrylic acid (eg, carpomer), polymethacrylic acid, polyvinyl alcohol, polyethylene glycol, polyvinylpyrrolidone, polycarpyl, ascorbic acid palmitate, and the like. Propyl methylcellulose, polyacrylic acid, alginate, gelatin, carboxymethyl cellulose, polypierpyrrolidone, polyethylene Glycol is preferred. Particularly, hydroxypropyl methylcellulose is preferable. Examples of the stabilizer include cystine, thiosorbitol, tartaric acid, cunic acid, sodium carbonate, ascorbic acid, glycine, sodium sulfite, and the like. Good.
舌下綻、バッカル又は口腔内速崩壊剤は、本発明の化合物または併用薬物と賦形 剤とを自体公知の方法により混合することにより製造することができる。 さらに、 所望により上記した滑沢剤、等張化剤、親水性担体、水分散性ポリマー、安定化剤、 着色剤、 甘味剤、 防腐剤などの補助剤を混合してもよい。上記成分を同時に若しく は時間差をおいて混合した後、加圧打錠成形することにより舌下錠、バッカル錠又 は口腔内速崩壊錠が得られる。適度な硬度を得るため、打錠成形の過程の前後にお いて必要に応じ水やアルコールなどの溶媒を用いて加湿 *湿潤させ、 成形後、 乾燥 させて製造してもよい。 The sublingual disintegrant, buccal or intraoral quick disintegrating agent can be produced by mixing the compound of the present invention or the concomitant drug with an excipient by a method known per se. Further, if necessary, the above-mentioned auxiliary agents such as a lubricant, an isotonic agent, a hydrophilic carrier, a water-dispersible polymer, a stabilizer, a coloring agent, a sweetening agent and a preservative may be mixed. By mixing the above components at the same time or with a time difference, and then press-molding, sublingual tablets, buccal tablets or intraorally rapidly disintegrating tablets can be obtained. In order to obtain an appropriate hardness, it may be manufactured by humidifying and moisturizing with a solvent such as water or alcohol before and after the tableting process, if necessary, molding, and then drying.
粘膜貼付錠(フィルム) に成型する場合は、 本発明の化合物または併用薬物およ び上記した水分散性ポリマー (好ましくは、 ヒドロキシプロピルセルロース、 ヒド ロキシプロピルメチルセルロース) 、賦形剤などを水などの溶媒に溶解させ、 得ら れる溶液を流延させて(cas t)フィルムとする。 さらに、 可塑剤、 安定剤、 酸化防止 剤、 保存剤、 着色剤、 緩衝剤、 甘味剤などの添加物を加えてもよい。 フィルムに適 度の弹性を与えるためポリエチレングリコ一ルゃプロピレングリコールなどのグ リコール類を含有させたり、口腔の粘膜ライニングへのフィルムの接着を高めるた め生物接着性ポリマー (例、 ポリカーボフィル、 カーボポール) を含有させてもよ い。流延は、 非接着性表面に溶液を注ぎ、 ドクターブレードなどの塗布用具で均一' な厚さ (好ましくは 1 0〜1 0 0 0ミクロン程度) にそれを広げ、 次いで溶液を乾 燥してフィルムを形成することにより達成される。このように形成されたフィルム は室温若しくは加温下乾燥させ、 所望の表面積に切断すればよい。 When molded into a mucosa-adhered tablet (film), the compound of the present invention or the concomitant drug, the above-mentioned water-dispersible polymer (preferably hydroxypropylcellulose, hydroxypropylmethylcellulose), an excipient, etc. Dissolve in a solvent and cast the resulting solution into a film. Further, additives such as a plasticizer, a stabilizer, an antioxidant, a preservative, a coloring agent, a buffer, and a sweetener may be added. Glycols such as polyethylene glycol and propylene glycol can be included to impart appropriate properties to the film, and bioadhesive polymers (eg, Polycarbophil, Carbofil, etc.) can be used to enhance the adhesion of the film to the oral mucosal lining. Paul) may be contained. Casting involves pouring the solution onto the non-adhesive surface, spreading it to a uniform thickness (preferably about 100 to 100 microns) with an application tool such as a doctor blade, and then drying the solution. This is achieved by forming a film. The film thus formed may be dried at room temperature or under heating, and cut into a desired surface area.
好ましい口腔内速崩壊剤としては、本発明の化合物または併用薬物と、本発明の 化合物または併用薬物とは不活性である水溶性若しくは水拡散性キヤリヤーとの 網状体からなる固体状の急速拡散投与剤が挙げられる。該網状体は、本発明の化合 物または併用薬物を適当な溶媒に溶解した溶液とから構成されている固体状の該 組成物から溶媒を昇華することによって得られる。 . A preferred rapid intraoral disintegrant is a solid rapid diffusion administration comprising a network of the compound of the present invention or the concomitant drug and a water-soluble or water-diffusible carrier inactive with the compound of the present invention or the concomitant drug. Agents. The network can be obtained by sublimating the solvent from the solid composition composed of a solution of the compound of the present invention or the concomitant drug in a suitable solvent. .
該口腔内速崩壊剤の組成物中には、本発明の化合物または併用薬物に加えて、マ トリックス形成剤と二次成分とを含んでいるのが好ましい。 The composition of the oral disintegrating agent preferably contains a matrix-forming agent and a secondary component in addition to the compound of the present invention or the concomitant drug.
該マトリックス形成剤としてはゼラチン類、デキストリン類ならびに大豆、小麦 ならびにォォバコ(psyl 1 ium)種子夕ンパクなどの動物性夕ンパク類若しくは植物 性タンパク類;アラビアゴム、 ガーガム、寒天ならびにキサンタンなどのゴム質物 質;多糖類;アルギン酸類;カルポキシメチルセルロース類;力ラゲナン類;デキ ストラン類;ぺクチン類;ポリビニルピロリドンなどの合成ポリマー類;ゼラチン —アラビアゴムコンプレックスなどから誘導される物質が含まれる。さらに、マン 二トール、 デキストロース、 ラクトース、 ガラクトースならびにトレハロースなど の糖類;シクロデキストリンなどの環状糖類;リン酸ナトリゥム、塩化ナトリゥム ならびにケィ酸アルミニウムなどの無機塩類;グリシン、 L—ァラニン、 Lーァス パラギン酸、 L—グルタミン酸、 L—ヒドロシキプロリン、 L—イソロイシン、 L —ロイシンならびに L—フエ二ルァラニンなどの炭素原子数が 2から 1 2までの アミノ酸などが含まれる。 ' Examples of the matrix forming agent include gelatins, dextrins, soybeans, and wheat. And animal or plant proteins such as psyl 1 ium seed protein; gums such as gum arabic, guar gum, agar and xanthan; polysaccharides; alginic acids; carboxymethylcellulose; Dextrans; pectins; synthetic polymers such as polyvinylpyrrolidone; and substances derived from gelatin-gum arabic complex. Furthermore, saccharides such as mannitol, dextrose, lactose, galactose and trehalose; cyclic saccharides such as cyclodextrin; inorganic salts such as sodium phosphate, sodium chloride and aluminum silicate; glycine, L-alanine, L-aspartic acid, Includes amino acids with 2 to 12 carbon atoms such as L-glutamic acid, L-hydroxyproline, L-isoleucine, L-leucine, and L-phenylalanine. '
マトリックス形成剤は、 その 1.種若しくはそれ以上を、 固形化の前に、溶液又は 懸濁液中に導入することができる。かかるマ卜リックス形成剤は、界面活性剤に加 えて存在していてもよく、 また界面活性剤が排除されて存在していてもよい。マト リックス形成剤はそのマトリックスを形成することに加えて、本発明の化合物また は併用薬物の拡散状態をその溶液又は懸濁液中に維持する助けをすることができ る。 One or more matrix-forming agents can be introduced into a solution or suspension before solidification. Such a matrix forming agent may be present in addition to the surfactant, or may be present without the surfactant. The matrix former, in addition to forming its matrix, can help maintain the compound or compound of the invention or the concomitant drug in a dispersed state in the solution or suspension.
保存剤、 酸化防止剤、 界面活性剤、 増粘剤、 着色剤、 P H調整剤、 香味料、 甘味 料若しくは食味マスキング剤などの二次成分を組成物中に含有していてよい。適当 な着色剤としては、赤色、黒色ならびに黄色酸化鉄類およびエリス'アンド'ェベラ —ルド社の F D & Cブルー 2号ならびに F D & Cレッド 4 0号などの F D & C染 料が挙げられる。 適当な香味料には、 ミント、 ラスべリー、 甘草、 オレンジ、 レモ ン、 グレープフルーツ、 カラメル、 バニラ、 チェリーならびにグレープフレーバー およびその組合せたものが含まれる。 適当な P H調整剤は、 クェン酸、 酒石酸、 リ ン酸、 塩酸およびマレイン酸が含まれる。 適当な甘味料としてはアスパルテーム、 アセスルフエ一ム Kならびにタウマチンなどが含まれる。適当な食味マスキング剤 としては、 重炭酸ナトリウム、 イオン交換樹脂、 シクロデキストリン包接化合物、 吸着質物質ならびにマイクロカプセル化アポモルフィンが含まれる。 Secondary components such as preservatives, antioxidants, surfactants, thickeners, coloring agents, pH adjusters, flavors, sweeteners or taste masking agents may be included in the composition. Suitable colorants include red, black and yellow iron oxides and FD & C dyes such as FD & C Blue No. 2 and FD & C Red 40 from Ellis' Anderbergerd. Suitable flavors include mint, raspberry, licorice, orange, lemon, grapefruit, caramel, vanilla, cherry and grape flavor and combinations thereof. Suitable pH regulators include citric acid, tartaric acid, phosphoric acid, hydrochloric acid and maleic acid. Suitable sweeteners include aspartame, acesulfame K and thaumatin. Suitable taste masking agents include sodium bicarbonate, ion exchange resins, cyclodextrin inclusion compounds, adsorbate materials, and microencapsulated apomorphine.
製剤には通常約 0 . 1〜約 5 0重量%、 好ましくは約 0 . 1〜約 3 0重量%の本 発明の化合物または併用薬物を含み、約 1分〜約 6 0分の間、好ましくは約 1分〜 約 1 5分の間、 より好ましくは約 2分〜約 5分の間に (水に)本発明の化合物また は併用薬物の 9 0 %以上を溶解させることが可能な製剤 (上記、 舌下錠、 パッカル など)や、 口腔内に入れられて約 1ないし約 6 0秒以内に、好ましくは約 1ないし 約 3 0秒以内に、さらに好ましくは約 1ないし約 1 0秒以内に崩壊する口腔内速崩 壊剤が好ましい。 Formulations usually contain about 0.1 to about 50% by weight, preferably about 0.1 to about 30% by weight of book. Comprising between about 1 minute and about 60 minutes, preferably between about 1 minute and about 15 minutes, more preferably between about 2 minutes and about 5 minutes (in water) comprising the compound of the invention or the concomitant drug. Formulations capable of dissolving 90% or more of the compound of the present invention or the concomitant drug (the above-mentioned sublingual tablets, puccal, etc.), and preferably within about 1 to about 60 seconds after being placed in the oral cavity Is preferably a fast disintegrating agent in the oral cavity that disintegrates within about 1 to about 30 seconds, more preferably within about 1 to about 10 seconds.
上記賦形剤の製剤全体に対する含有量は、約 1 0〜約 9 9重量%、好ましくは約 3 0〜約 9 0重量%である。 ]3—シクロデキストリン又は )3—シクロデキストリン 誘導体の製剤全体に対する含有量は 0〜約 3 0重量%である。滑沢剤の製剤全体に 対する含有量は、約 0 . 0 1〜約 1 0重量%、好ましくは約 1〜約 5重量%である。 等張化剤の製剤全体に対する含有量は、 約 0 . 1〜約 9 0重量%、 好ましくは、 約 1 0〜約 7 0重量%である。親水性担体の製剤全体に対する含有量は約 0 . 1〜約 5 0重量%、好ましくは約 1 0〜約 3 0重量%である。水分散性 リマ一の製剤全 体に対する含有量は、 約 0 . 1〜約 3 0重量%、好ましくは約 1 0〜約 2 5重量% である。安定化剤の製剤全体に対する含有量は約 0 . 1〜約 1 0重量%、好ましく は約 1〜約 5重量%である。上記製剤はさらに、 着色剤、 甘味剤、 防腐剤などの添 加剤を必要に応じ含有していてもよい。 The content of the above-mentioned excipient in the whole preparation is about 10 to about 99% by weight, preferably about 30 to about 90% by weight. ] The content of the 3-cyclodextrin or) 3-cyclodextrin derivative in the whole preparation is 0 to about 30% by weight. The content of the lubricant in the whole preparation is about 0.01 to about 10% by weight, preferably about 1 to about 5% by weight. The content of the tonicity agent in the whole preparation is about 0.1 to about 90% by weight, preferably about 10 to about 70% by weight. The content of the hydrophilic carrier in the whole preparation is about 0.1 to about 50% by weight, preferably about 10 to about 30% by weight. The content of the water-dispersible lima in the whole preparation is about 0.1 to about 30% by weight, preferably about 10 to about 25% by weight. The content of the stabilizer relative to the whole preparation is about 0.1 to about 10% by weight, preferably about 1 to about 5% by weight. The above preparations may further contain additives such as coloring agents, sweetening agents, preservatives and the like, if necessary.
本発明の併用剤の投与量は、 本発明の化合物の種類、 年齢、 体重、 症状、 剤形、 投与方法、 投与期間などにより異なるが、 例えば、 乳癌の患者 (成人、体重約 6 0 k g ) 一人あたり、 通常、 本発明の化合物および併用薬物として、 それぞれ 1日約 0 . 0 1〜約 1 0 0 0 mgZkg、 好ましくは約 0 . 0 1〜約 1 0 0 mgZkg より好ま し <は約 0 . 1〜約 1 0 O m g Z k g、 とりわけ約 0 . 1〜約 5 O m g Z k gを、 なかでも約 1 . 5〜約 3 0 mgZkgを 1日 1回から数回に分けて静脈投与される。 もちろん、前記したように投与量は種々の条件で変動するので、前記投与量より少 ない量で十分な場合もあり、 また範囲を超えて投与する必要のある場合もある。 併用薬物は、副作用が問題とならない範囲でどのような量を設定することも可能 である。 併用薬物としての一日投与量は、 症状の程度、 投与対象の年齢、 性別、 体 重、 感受性差、 投与の時期、 間隔、 医薬製剤の性質、 調剤、 種類、 有効成分の種類 などによって異なり、 特に限定されないが、薬物の量として通常、 たとえば経口投 与で哺乳動物 1 kg体重あたり約 0.001〜2000mg、好ましくは約 0.01 〜500mg、 さらに好ましくは、 約 0.1〜10 Omg程度であり、 これを通常 1日 1〜4回に分けて投与する。 The dose of the concomitant drug of the present invention varies depending on the type, age, body weight, symptom, dosage form, administration method, administration period, and the like of the compound of the present invention. Usually, about 0.01 to about 1000 mgZkg, preferably about 0.01 to about 100 mgZkg per day, as the compound of the present invention and the concomitant drug, is more preferable. 1 to about 10 Omg Zkg, especially about 0.1 to about 5 OmgZkg, especially about 1.5 to about 30 mgZkg, is administered intravenously once or several times a day. You. Of course, as described above, since the dose varies under various conditions, a dose smaller than the above dose may be sufficient, or it may be necessary to administer beyond the range. The concomitant drug can be used in any amount as long as side effects are not a problem. The daily dosage of the concomitant drug varies depending on the severity of symptoms, age, gender, body weight, sensitivity difference, administration timing, interval, characteristics of pharmaceutical preparation, preparation, type, type of active ingredient, etc. Although not particularly limited, the amount of the drug is usually The dose is about 0.001 to 2000 mg, preferably about 0.01 to 500 mg, more preferably about 0.1 to 10 Omg per kg body weight of the mammal, and is usually administered in 1 to 4 times a day.
本発明の併用剤を投与するに際しては、 同時期に投与してもよいが、併用薬物を 先に投与した後、本発明の化合物を投与してもよいし、本発明の化合物を先に投与 し、 その後で併用薬物を投与してもよい。 時間差をおいて投与する場合、 時間差は 投与する有効成分、 剤形、 投与方法により異なるが、 例えば、 併用薬物を先に投与 する場合、 併用薬物を投与した後 1分〜 3日以内、 好ましくは 10分〜 1日以内、 より好ましくは 15分〜 1時間以内に本発明の化合物を投与する方法が挙げられ る。本発明の化合物を先に投与する場合、本発明の化合物を投与した後、 1分〜 1 日以内、好ましくは 10分〜 6時間以内、 より好ましくは 15分から 1時間以内に 併用薬物を投与する方法が挙げられる。 発明を実施するための最良の形態 When administering the concomitant drug of the present invention, the concomitant drug may be administered at the same time, but after administering the concomitant drug first, the compound of the present invention may be administered, or the compound of the present invention may be administered first. Thereafter, the concomitant drug may be administered. When administered at different times, the time difference depends on the active ingredient to be administered, dosage form, and administration method.For example, when the concomitant drug is administered first, within 1 minute to 3 days after administration of the concomitant drug, preferably Examples include a method of administering the compound of the present invention within 10 minutes to 1 day, more preferably within 15 minutes to 1 hour. When the compound of the present invention is administered first, the concomitant drug is administered within 1 minute to 1 day, preferably within 10 minutes to 6 hours, more preferably within 15 minutes to 1 hour after administering the compound of the present invention. Method. BEST MODE FOR CARRYING OUT THE INVENTION
本発明は、 更に以下の参考例、 実施例、 製剤例及び試験例によって詳しく説明さ れるが、 これらの例は単なる実施であって、 本発明を限定するものではなく、 また 本発明の範囲を逸脱しない範囲で変化させてもよい。 The present invention will be further described in detail with reference to the following Reference Examples, Examples, Formulation Examples and Test Examples, which are merely examples and do not limit the present invention. It may be changed without departing from the scope.
以下の参考例、 実施例中の 「室温」 は通常約 10 °Cないし約 35 でを示す。 % は、 '収率は mol/mol%を、 その他は重量%を示す。 また塩基性シリカゲルは、 富士 シリシァ化学株式会社製 NH— DM1020を用いた。プロトン NMRスぺクト ルで、 0Hや NHプロトン等ブロードで確認できないものについてはデータに記載 していない。 "Room temperature" in the following Reference Examples and Examples usually indicates about 10 ° C to about 35 ° C. % Means' mol / mol% yield, and the others indicate% by weight. As the basic silica gel, NH-DM1020 manufactured by Fuji Silicon Chemical Co., Ltd. was used. In the proton NMR spectrum, those which cannot be confirmed by broad, such as 0H and NH protons, are not described in the data.
その他の本文中で用いられている略号は下記の意味を示す。 Abbreviations used in other texts have the following meanings.
s 卜 (singlet) s u (singlet)
d ダブレツト (doublet) d doublet
t 卜リプレツト (triplet) t Triplet (triplet)
q クアルテツ卜 (quartet) q quartet
m マルチプレツト (multiple!) m multiple (multiple!)
br ブロード (broad) J : カップリング定数 (coupling constant) br broad J: Coupling constant
Hz : ヘルツ (Hertz) Hz: Hertz
CDC13 : 重クロ口ホルム CDC1 3 : Double-mouthed holm
DMS0- d6 : 重ジメチルスルホキシド DMS0- d 6 : heavy dimethyl sulfoxide
Ή NMR : プロトン核磁気共鳴 Ή NMR: proton nuclear magnetic resonance
後述の試験例 1で得られた形質転換体ェシエリヒア コリ (Escherichia coli) BL21ZPPDE4D3は、平成 12年 3月 8日から通商産業省工業技術院生命 工学工業技術研究所(N I BH) に寄託番号 FERM BP- 7075として、 平 成 12年 2月 24日から財団法人 ·発酵研究所(I FO) に寄託番号 I F〇 16 383として寄託されている。 The transformant Escherichia coli BL21ZPPDE4D3 obtained in Test Example 1 described below was deposited with the National Institute of Advanced Industrial Science and Technology (NI BH) on March 8, 2000 under the deposit number FERM BP. -Deposited with the Fermentation Research Institute (IFO) under the accession number IF 216 383 from February 24, 2000 as 7075.
なお、大腸菌を用いての遺伝子操作法は、モレキユラ一 ·クロ一ニング (Molecular cloning) に記載されている方法に従った。 In addition, the gene manipulation method using Escherichia coli followed the method described in Molecular cloning.
本明細書の配列表の配列番号は、 以下の配列を示す。 The sequence numbers in the sequence listing in the present specification indicate the following sequences.
〔配列番号: 1〕 [SEQ ID NO: 1]
試験例 1において使用したプライマ一の塩基配列を示す。 1 shows the nucleotide sequence of a primer used in Test Example 1.
〔配列番号: 2〕 [SEQ ID NO: 2]
試験例 1において使用したプライマ一の塩基配列を示す。 1 shows the nucleotide sequence of a primer used in Test Example 1.
〔配列番号: 3〕 [SEQ ID NO: 3]
試験例 1で得られた大腸菌 (Escherichia coli) B L 21 Zp P D E 4 D 3が保 持する c D N Aの塩基配列を示す。 1 shows the nucleotide sequence of cDNA carried by Escherichia coli BL21ZpPDE4D3 obtained in Test Example 1.
〔配列番号: 4〕 [SEQ ID NO: 4]
試験例 1で得られた大腸菌 (Escherichia coli) B L 21 /p P D E 4 D 3が保 持する c D N Aの塩基配列にコードされるアミノ酸配列を示す。 実施例 安息香酸 5-ブロモ -2-メトキシフエニルエステル 3 shows the amino acid sequence encoded by the nucleotide sequence of cDNA carried by Escherichia coli BL21 / pPDE4D3 obtained in Test Example 1. Example benzoic acid 5-bromo-2-methoxyphenyl ester
グアヤコール (125 g、 1.01 mol) のピリジン (300 mL) 溶液を氷冷し、 窒素雰 囲気下べンゾイルクロリド (149 g、 1.06 mol) を 30分間かけて滴下、 同温で 30 分間攙拌した。反応混合物に水を加え、酢酸ェチルで 2回抽出した。合わせた有機 層を水、 2M塩酸 (2回)、 および水で洗浄、 濃縮して安息香酸 2-メトキシフエ二 ルエステル (234 g) を固体として得た。 A solution of guaiacol (125 g, 1.01 mol) in pyridine (300 mL) was cooled on ice, and benzoyl chloride (149 g, 1.06 mol) was added dropwise over 30 minutes in a nitrogen atmosphere. Stirred for minutes. Water was added to the reaction mixture, which was extracted twice with ethyl acetate. The combined organic layers were washed with water, 2M hydrochloric acid (twice), and water, and concentrated to give benzoic acid 2-methoxyphenyl ester (234 g) as a solid.
この 229 g を酢酸 (700 mL) に溶解し、 15 °Cで臭素 (176 g、 1.10 mol) の酢 酸 (100 mL) 溶液を 1.5 時間かけて滴下、 室温で 15.5 時間攪拌した。 得られた 混合物に臭素 (24 g、 0.15 mol) の酢酸 (10 mL) 溶液を 10 分かけて滴下し、 室 温で 8 時間攪拌した。 反応混合物を減圧濃縮し、 酢酸ェチルと飽和炭酸水素ナト リウム水溶液を加え、有機層を分離、 水層を酢酸ェチルで抽出した。合わせた有機 層を水洗、 減圧濃縮して表題化合物 (267 g、 収率 89%) を得た。 229 g of this was dissolved in acetic acid (700 mL), and a solution of bromine (176 g, 1.10 mol) in acetic acid (100 mL) was added dropwise at 15 ° C over 1.5 hours, followed by stirring at room temperature for 15.5 hours. To the resulting mixture, a solution of bromine (24 g, 0.15 mol) in acetic acid (10 mL) was added dropwise over 10 minutes, and the mixture was stirred at room temperature for 8 hours. The reaction mixture was concentrated under reduced pressure, ethyl acetate and a saturated aqueous solution of sodium hydrogen carbonate were added, the organic layer was separated, and the aqueous layer was extracted with ethyl acetate. The combined organic layer was washed with water and concentrated under reduced pressure to obtain the title compound (267 g, yield 89%).
融点 74-78 °C。 74-78 ° C.
¾ NMR (CDC13) 53.80 (3H, s), 6.89 (1H, d, J = 8.6 Hz), 7.32 (1H, d, J = 2.5 Hz), 7.36 (1H, dd, J = 8.6, 2.5 Hz), 7.46-7.56 (2H, m), 7.59-7.70 (1H, m), 8.16-8.24 (2H, m)。 ¾ NMR (CDC1 3) 53.80 ( 3H, s), 6.89 (1H, d, J = 8.6 Hz), 7.32 (1H, d, J = 2.5 Hz), 7.36 (1H, dd, J = 8.6, 2.5 Hz) , 7.46-7.56 (2H, m), 7.59-7.70 (1H, m), 8.16-8.24 (2H, m).
参考例 2 Reference example 2
5_ブロモ -2 -メトキシフエノール 5_bromo-2-methoxyphenol
安息香酸 5 -ブロモ -2-メトキシフエ二ルエステル (261 g、 0.850 mol) のテトラ ヒドロフラン (100 mL) /メタノール (100 mL) 懸濁液に 5 M水酸化ナトリウム水 溶液 (350 mL、 1.75 mol) を加え、 室温で 1 時間攪拌した。 反応混合物を 2 M塩 酸 (500 mL、 1.00 mol) で酸性にし、 炭酸水素ナトリウム (10 g、 0.12 mol) を加 えて中和した。得られた混合物を酢酸ェチル /へキサン (1:1)混合液で 2回抽出し た。合わせた有機層を水洗、 減圧濃縮した。残渣をへキサンから再結晶して表題化 合物 (148 g、 収率 86%) を得た。 To a suspension of benzoic acid 5-bromo-2-methoxyphenyl ester (261 g, 0.850 mol) in tetrahydrofuran (100 mL) / methanol (100 mL) was added a 5 M aqueous sodium hydroxide solution (350 mL, 1.75 mol). The mixture was stirred at room temperature for 1 hour. The reaction mixture was acidified with 2 M hydrochloric acid (500 mL, 1.00 mol) and neutralized by adding sodium hydrogen carbonate (10 g, 0.12 mol). The resulting mixture was extracted twice with a mixture of ethyl acetate / hexane (1: 1). The combined organic layers were washed with water and concentrated under reduced pressure. The residue was recrystallized from hexane to give the title compound (148 g, yield 86%).
融点 66-67 。 Melting point 66-67.
Ή NMR (CDC13) 53.88 (3H, s), 5.65 (1H, br s), 6.71 (1H, d, J = 8.5 Hz) , 6.97 (1H, dd, J = 8.5, 2.5 Hz), 7.07 (1H, d, J = 2.5 Hz)。 Ή NMR (CDC1 3) 53.88 ( 3H, s), 5.65 (1H, br s), 6.71 (1H, d, J = 8.5 Hz), 6.97 (1H, dd, J = 8.5, 2.5 Hz), 7.07 (1H , d, J = 2.5 Hz).
参考例 3 Reference example 3
2,3-ジヒドロ- 7-メトキシ -2, 2-ジメチル -4-ベンゾフランカルボキサルデヒド 2,3-dihydro-7-methoxy-2,2-dimethyl-4-benzofurancarboxaldehyde
5_ブロモ -2-メトキシフエノ一ル (102 g、 0.502 mol) の N,N-ジメチルホルムァ ミド (400 mL) 溶液に 3-クロ口- 2-メチル -1-プロペン (55 mL, 0.56 mol) および 炭酸カリウム (83.3 g, 0.603 mol) を加え、 窒素雰囲気下 75 で 2.5 時間攪 拌した。 反応混合物に水を加え、 へキサン/酢酸ェチル (1:1)混合液で 2.回抽出し た。 合わせた有機層を水で 2回洗浄、 活性炭処理、 ろ過、 減圧濃縮して 4-ブロモ -卜メトキシ- 2- [(2-メチル -2 -プロべ二ル)ォキシ]ベンゼン (130 g) を油状物とし て得た。 To a solution of 5_bromo-2-methoxyphenol (102 g, 0.502 mol) in N, N-dimethylformamide (400 mL) was added 3-chloro-2-methyl-1-propene (55 mL, 0.56 mol) and Potassium carbonate (83.3 g, 0.603 mol) was added, and the mixture was stirred at 75 under a nitrogen atmosphere for 2.5 hours. Water was added to the reaction mixture, and the mixture was extracted twice with a hexane / ethyl acetate (1: 1) mixed solution. The combined organic layers were washed twice with water, treated with activated carbon, filtered, and concentrated under reduced pressure to give 4-bromo-trimethoxy-2-[(2-methyl-2-propyl) oxy] benzene (130 g). Obtained as an oil.
これを N,N_ジェチルァニリン (100 mL) に溶解し、 窒素雰囲気下 200 で 5.5 時間攪拌した。反応混合物をジイソプロピルエーテルに溶解し、 1 M塩酸 (2回)お よび水で洗浄、活性炭処理、 ろ過、減圧濃縮して 3 -ブロモ -6-メトキシ -2- (2-メチ ル -2-プロぺニル)フエノール (129 g) を油状物として得た。 This was dissolved in N, N_ cetiraniline (100 mL) and stirred at 200 for 5.5 hours under a nitrogen atmosphere. The reaction mixture was dissolved in diisopropyl ether, washed with 1 M hydrochloric acid (twice) and water, treated with activated carbon, filtered, and concentrated under reduced pressure to give 3-bromo-6-methoxy-2- (2-methyl-2-prop. (Pinyl) phenol (129 g) was obtained as an oil.
これをエタノール (200 mL) に溶解し、 濃塩酸 (50 mL)のエタノール (50mL)溶 液を加え、 2.5時間加熱還流した。 反応混合物を減圧濃縮し、 へキサンを加え、 水 層を分離した。 有機層を水、 1 M水酸化ナトリウム水溶液 (3回)、 水で洗浄、 活 性炭処理、 ろ過、減圧濃縮して 4-ブロモ -2, 3-ジヒドロ- 7-メトキシ- 2, 2 -ジメチレ ベンゾフラン (113 g) を油状物として得た。 This was dissolved in ethanol (200 mL), a solution of concentrated hydrochloric acid (50 mL) in ethanol (50 mL) was added, and the mixture was heated under reflux for 2.5 hours. The reaction mixture was concentrated under reduced pressure, hexane was added, and the aqueous layer was separated. The organic layer is washed with water, 1 M aqueous sodium hydroxide solution (3 times), water, treated with activated carbon, filtered, and concentrated under reduced pressure to give 4-bromo-2,3-dihydro-7-methoxy-2,2-dimethylene. Benzofuran (113 g) was obtained as an oil.
この 1.37 gをテトラヒドロフラン (15 mL) に溶解し、 窒素雰囲気下 -78でに 冷却、 1.6 M n_ブチルリチウム/へキサン溶液 (4.0 mL, 6.4 mmol) を滴下し、 同 温で 10 分間攪拌した。 得られた混合物に Ν,Ν -ジメチルホルムアミド (1.2 mL、 15 mmol) を滴下し、 -78 で 30分間、 室温で 30分間攪拌した。 反応混合物を 飽和塩化アンモニゥム水溶液に注ぎ、酢酸ェチルで 2回抽出した。合わせた有機層 を水および飽和塩化ナトリウム水溶液で洗浄、 硫酸マグネシウム上で乾燥、 ろ過、 減圧濃縮した。 残渣をシリカゲルカラムクロマトグラフィー (へキサン/酢酸ェチ ル 20:1) に供し、 酢酸エヂルーへキサンから再結晶して表題化合物 (741 mg、 収 率 59%) を得た。 This 1.37 g was dissolved in tetrahydrofuran (15 mL), cooled to -78 in a nitrogen atmosphere, 1.6 M n_butyllithium / hexane solution (4.0 mL, 6.4 mmol) was added dropwise, and the mixture was stirred at the same temperature for 10 minutes. . Ν, Ν-Dimethylformamide (1.2 mL, 15 mmol) was added dropwise to the obtained mixture, and the mixture was stirred at -78 for 30 minutes and at room temperature for 30 minutes. The reaction mixture was poured into a saturated aqueous solution of ammonium chloride and extracted twice with ethyl acetate. The combined organic layer was washed with water and a saturated aqueous solution of sodium chloride, dried over magnesium sulfate, filtered, and concentrated under reduced pressure. The residue was subjected to a silica gel column chromatography (hexane / ethyl acetate 20: 1), and recrystallized from ethyl acetate to give the title compound (741 mg, yield 59%).
融点 89-90 °C。 89-90 ° C.
¾ NMR (CDC13) 51.54 (6H, s), 3.39 (2H, s), 3.96 (3H, s), 6.88 (1H, d, J = 8.4 Hz), 7.31 (1H, d, J = 8.4 Hz), 9.90 (1H, s)D ¾ NMR (CDC1 3) 51.54 ( 6H, s), 3.39 (2H, s), 3.96 (3H, s), 6.88 (1H, d, J = 8.4 Hz), 7.31 (1H, d, J = 8.4 Hz) , 9.90 (1H, s) D
参考例 4 Reference example 4
2,3-ジヒドロ- 7-メトキシ- 2, 2 -ジメチル- 4_(2-メチル -1-プロぺニル)ベンゾフラ ン 2, 3-ジヒドロ- 7-メトキシ- 2,2-ジメチル- 4_ベンゾフランカルポキサルデヒド (10.4 g、 50.4 imol) およびイソプロピルトリフエニルホスホニゥムョ一ジド (23.8 g、 55.1 mmol) のテトラヒドロフラン (100 mL) 懸濁液に水素化ナトリウム (66% 油分散物) (1.99 g、 55 腿 ol) を加え、 1 時間加熱還流した。 反応混合物を 飽和塩化アンモニゥム水溶液に注ぎ、酢酸ェチルで 2回抽出した。合わせた有機層 を水および飽和塩化ナトリウム水溶液で洗浄、 硫酸マグネシウム上で乾燥、 ろ過、 減圧濃縮した。 残渣にへキサン/酢酸ェチル (4:1) 混合物を加え、 不溶物をろ過、 減圧濃縮した。 残渣をシリカゲルカラムクロマトグラフィー (へキサン/酢酸ェチ ル 100:1 の後 10:1) に供し、 表題化合物 (11.0 g、 収率 94 ) を得た。. 2,3-dihydro-7-methoxy-2,2-dimethyl-4_ (2-methyl-1-propenyl) benzofuran 2,3-dihydro-7-methoxy-2,2-dimethyl-4_benzofurancarboxaldehyde (10.4 g, 50.4 imol) and isopropyltriphenylphosphonidumodizide (23.8 g, 55.1 mmol) in tetrahydrofuran (100 mL ) Sodium hydride (66% oil dispersion) (1.99 g, 55 t ol) was added to the suspension, and the mixture was refluxed for 1 hour. The reaction mixture was poured into a saturated aqueous solution of ammonium chloride and extracted twice with ethyl acetate. The combined organic layer was washed with water and a saturated aqueous solution of sodium chloride, dried over magnesium sulfate, filtered, and concentrated under reduced pressure. Hexane / ethyl acetate (4: 1) mixture was added to the residue, the insolubles were filtered and concentrated under reduced pressure. The residue was subjected to silica gel column chromatography (hexane / ethyl acetate 100: 1 followed by 10: 1) to give the title compound (11.0 g, yield 94). .
油状物。 Oil.
Ή NMR (CDC13) 51.51 (6H, s), 1.81 (3H, d, J = 1.1 Hz), 1.87 (3H, d, J = 1.1 Hz), 2.94 (2H, s), 3.86 (3H, s), 6.03 (1H, s), 6.70 (2H, s)D Ή NMR (CDC1 3) 51.51 ( 6H, s), 1.81 (3H, d, J = 1.1 Hz), 1.87 (3H, d, J = 1.1 Hz), 2.94 (2H, s), 3.86 (3H, s) , 6.03 (1H, s), 6.70 (2H, s) D
実施例 1 Example 1
1,2, 8, 9 -テトラヒドロ- 4-メトキシ- 2, 2, 8, 8-テトラメチル -6-フエ二ルフロ 〔3,2-f]イソキノリン 1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethyl-6-phenylfuro [3,2-f] isoquinoline
2, 3-ジヒドロ- 7 -メトキシ- 2, 2-ジメチル- 4- (2 -メチル- 1-プロぺニル)ベンゾフ ラン (2.09 g、 9.00匪01)およびべンゾニトリル (1.21 g、 11.7 mmol) の酢酸 (3 mL) 溶液に 10 で濃硫酸 (1.2 mL) を滴下し、 同温で 30分間攪拌した。 反応混 合物を氷水に注ぎ、 ジイソプロピルエーテルで洗浄した。 水層を 5 M水酸化ナト リウム水溶液で塩基性にし、 テトラヒドロフラン/ジイソプロピルエーテル (1:1) 混合液で 2回抽出した。合わせた有機層を飽和塩化ナトリゥム水溶液で洗浄、硫酸 ナトリウム上で乾燥、 ろ過、 減圧濃縮した。残渣を酢酸ェチル—ジイソプロピルェ 一テルから再結晶して表題化合物 (1.37 g、 収率 45» を得た。 Of 2,3-dihydro-7-methoxy-2,2-dimethyl-4- (2-methyl-1-propenyl) benzofuran (2.09 g, 9.00 maraudal 01) and benzonitrile (1.21 g, 11.7 mmol) Concentrated sulfuric acid (1.2 mL) was added dropwise to the acetic acid (3 mL) solution at 10 and stirred at the same temperature for 30 minutes. The reaction mixture was poured into ice water and washed with diisopropyl ether. The aqueous layer was made basic with a 5 M aqueous sodium hydroxide solution, and extracted twice with a mixed solution of tetrahydrofuran / diisopropyl ether (1: 1). The combined organic layer was washed with a saturated aqueous sodium chloride solution, dried over sodium sulfate, filtered, and concentrated under reduced pressure. The residue was recrystallized from ethyl acetate-diisopropyl ether to give the title compound (1.37 g, yield 45 »).
融点 128-129 °C。 128-129 ° C.
Ή NMR (CDC13) (51.28 (6H, s), 1.57 (6H, s), 2.59 (2H, s), 3.01 (2H, s), 3.69 (3H, s), 6.62 (1H, s), 7.36-7.45 (3H, m), 7.49-7.60 (2H, m)。 Ή NMR (CDC1 3) (51.28 (6H, s), 1.57 (6H, s), 2.59 (2H, s), 3.01 (2H, s), 3.69 (3H, s), 6.62 (1H, s), 7.36 -7.45 (3H, m), 7.49-7.60 (2H, m).
実施例 2 Example 2
1,2,8, 9 -テ卜ラヒドロ- 2, 2, 8, 8 -テトラメチル -6 -フエ二ルフロ [3, 2-f]イソキノリ ン -4-オール 1,2,8, 9-テトラヒドロ- 4-メトキシ- 2, 2, 8, 8 -テトラメチル -6 -フエ二ルフロ [3, 2 - f]イソキノリン (3.70g、 11.0 mmol) の 48%臭化水素酸 (25 mL)溶液を 13 時間加熱還流した。 冷後、 反応混合物を濃アンモニア水で中和し、酢酸ェチルで 2 回抽出した。合わせた有機層を飽和塩化ナトリゥム水溶液で洗浄、硫酸ナトリゥム 上で乾燥、ろ過、減圧濃縮した。析出した結晶をジイソプロピルエーテルで洗浄し、 エタノール—酢酸ェチルから再結晶して表題化合物 (2.17 g、 収率 61%) を得た。 軟化点 187 °C。 1,2,8,9-tetrahydro-2,2,8,8-tetramethyl-6-phenylfuro [3,2-f] isoquinolin-4-ol 48% bromination of 1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethyl-6-phenylfuro [3,2-f] isoquinoline (3.70 g, 11.0 mmol) The solution of hydrogen acid (25 mL) was heated under reflux for 13 hours. After cooling, the reaction mixture was neutralized with concentrated aqueous ammonia and extracted twice with ethyl acetate. The combined organic layer was washed with a saturated aqueous sodium chloride solution, dried over sodium sulfate, filtered, and concentrated under reduced pressure. The precipitated crystals were washed with diisopropyl ether and recrystallized from ethanol-ethyl acetate to give the title compound (2.17 g, yield 61%). Softening point 187 ° C.
¾ NMR (CDC13) 51.25 (6H, s), 1.54 (6H, s), 2.53 (2H, s), 3.00 (2H, s), 6.56 (1H, s), 7.30-7.33 (3H, m), 7.43-7.50 (2H, m)。 ¾ NMR (CDC1 3) 51.25 ( 6H, s), 1.54 (6H, s), 2.53 (2H, s), 3.00 (2H, s), 6.56 (1H, s), 7.30-7.33 (3H, m), 7.43-7.50 (2H, m).
実施例 3 Example 3
4 -エトキシ -1, 2, 8, 9-テ卜ラヒドロ _2, 2, 8, 8-テトラメチル -6-フエ二ルフロ [3, 2-f]イソキノリン 4-Ethoxy-1,2,8,9-tetrahydro_2,2,8,8-tetramethyl-6-phenylfuro [3,2-f] isoquinoline
1, 2, 8, 9-テトラヒド口- 2, 2, 8, 8-テトラメチル- 6 -フエニルフ口 [3, 2-f]イソキノ リン- 4 -オール (638 mg、 1.99腿 ol) の N, N -ジメチルホルムアミド (6 mL) 溶液 にョ一ドエタン (0.19mL、 2.4腿 ol)および水素化ナトリウム (66%油分散物) (87 mg、 2.4 mmol) を加え、 室温で 1 時間攪拌した。 反応混合物に氷水を加え、 酢酸 ェチルで 2回抽出した。合わせた有機層を水および飽和塩ィ匕ナトリゥム水溶液で洗 浄、 硫酸マグネシウム上で乾燥、 ろ過、 減圧濃縮した。 残渣を塩基性シリカゲル力 ラムクロマトグラフィー (へキサン/酢酸ェチル 20:1の後 10:1) に供し、 へキサ ンから結晶化させて表題化合物 (465 mg、 収率 67 ) を得た。 1,2,8,9-Tetrahydrido-2,2,8,8-tetramethyl-6-phenylphenol [3,2-f] isoquinolin-4-ol (638 mg, 1.99 t) To a solution of N-dimethylformamide (6 mL) were added iodoethane (0.19 mL, 2.4 mol) and sodium hydride (66% oil dispersion) (87 mg, 2.4 mmol), and the mixture was stirred at room temperature for 1 hour. Ice water was added to the reaction mixture, and the mixture was extracted twice with ethyl acetate. The combined organic layer was washed with water and a saturated aqueous sodium chloride solution, dried over magnesium sulfate, filtered, and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 20: 1 followed by 10: 1), and crystallized from hexane to give the title compound (465 mg, yield 67).
融点 120-122 °C。 120-122 ° C.
Ή NMR (CDCI3) δΐ.29 (6H, s), 1.32 (3Η, t, J = 7.0 Hz), 1.57 (6H, s), 2.60 (2H, s), 3.00 (2H, s), 3.93 (2H, q, J = 7.0 Hz), 6.63 (1H, s), 7.39-7.42 (3H, m), 7.52-7.57 (2H, m)。 Ή NMR (CDCI3) δΐ.29 (6H, s), 1.32 (3Η, t, J = 7.0 Hz), 1.57 (6H, s), 2.60 (2H, s), 3.00 (2H, s), 3.93 (2H , q, J = 7.0 Hz), 6.63 (1H, s), 7.39-7.42 (3H, m), 7.52-7.57 (2H, m).
実施例 4 Example 4
3-(l, 2, 8, 9-テトラヒド口 _4 -メトキシ- 2, 2, 8, 8-テトラメチルフロ [3, 2-f]イソキ ノリン 6-ィル)ベンゼンァミン 3- (l, 2,8,9-tetrahydrido _4-methoxy-2,2,8,8-tetramethylfuro [3,2-f] isoquinoline 6-yl) benzenamine
N- (3-シァノフエニル) -2, 2, 2-トリフルォロアセトアミド (5.89 g, 27.5 mmol) のトルエン (25 mL) および酢酸 (12 mL) 懸濁液を氷冷し、 濃硫酸 (3.0 mL), 次 いで 2, 3-ジヒドロ- 7 -メトキシ- 2, 2-ジメチル- 4- (2-メチル -1-プロぺニル)ベンゾ フラン (5.81 , 25.0 mmol) のトルエン (25 mL) 溶液を滴下、 80 で 1 時間攪 拌した。 得られた混合物に同温でエタノール (20mL) を滴下し、 1時間攪拌した。 反応混合物を氷冷し、 水を加え、 濃アンモニア水で中和、酢酸ェチルで 2回抽出し た。合わせた有機層を水で 2回洗浄、減圧濃縮した。残渣をエタノール (30mL)に 懸濁し、 2 M水酸化ナトリウム水溶液 (30 mL、 60 mmol) を加え、 1 時間加熱還流 した。不溶物をろ過し、 ろ液を減圧濃縮した。残渣を酢酸ェチルに溶解し、 水で 2 回洗浄、減圧濃縮した。残渣を塩基性シリカゲルカラムクロマトグラフィー (へキ サン/酢酸ェチル 3:1の後 1:1) に供し、 酢酸ェチルーへキサンから結晶化させて 表題化合物 (4.47 g、 収率 51 ) を得た。 A suspension of N- (3-cyanophenyl) -2,2,2-trifluoroacetamide (5.89 g, 27.5 mmol) in toluene (25 mL) and acetic acid (12 mL) was cooled on ice and concentrated sulfuric acid (3.0 mL). ), Next A solution of 2,3-dihydro-7-methoxy-2,2-dimethyl-4- (2-methyl-1-propenyl) benzofuran (5.81, 25.0 mmol) in toluene (25 mL) was added dropwise. Stirred for 1 hour. Ethanol (20 mL) was added dropwise to the resulting mixture at the same temperature, and the mixture was stirred for 1 hour. The reaction mixture was ice-cooled, water was added, neutralized with concentrated aqueous ammonia, and extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure. The residue was suspended in ethanol (30 mL), a 2 M aqueous sodium hydroxide solution (30 mL, 60 mmol) was added, and the mixture was heated under reflux for 1 hour. The insolubles were filtered, and the filtrate was concentrated under reduced pressure. The residue was dissolved in ethyl acetate, washed twice with water, and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 3: 1 followed by 1: 1), and crystallized from ethyl acetate-hexane to give the title compound (4.47 g, yield 51).
融点 163-165 Va Melting point 163-165 V a
Ή NMR (CDC13) δ 1.26 (6H, s), 1.56 (6H, s), 2.58 (2H, s), 3.00 (2H, s), 3.20-4.00 (2H, br), 3.71 (3H, s), 6.68-6.76 (1H, m), 6.69 (1H, s), 6.84-6.92 (2H, m), 7.17 (1H, t, J = 7.7 Hz)。 Ή NMR (CDC1 3) δ 1.26 (6H, s), 1.56 (6H, s), 2.58 (2H, s), 3.00 (2H, s), 3.20-4.00 (2H, br), 3.71 (3H, s) , 6.68-6.76 (1H, m), 6.69 (1H, s), 6.84-6.92 (2H, m), 7.17 (1H, t, J = 7.7 Hz).
実施例 5 Example 5
N- [3- (1, 2, 8, 9-テトラヒドロ- 4 -メトキシ -2, 2, 8, 8 -テトラメチルフ口 [3, 2-f]ィソ キノリン- 6-イリレ)フエニル] -4-ピリジンカルボキサミド N- [3- (1,2,8,9-Tetrahydro-4-methoxy-2,2,8,8-tetramethylfuran [3,2-f] isoquinoline-6-ylyl) phenyl] -4- Pyridinecarboxamide
.3 -(1,2,8,9-テトラヒドロ- 4 -メトキシ -2, 2, 8, 8 -テトラメチルフ口 [3, 2-f]イソ キノリン- 6 -ィル)ベンゼンァミン (701 mg, 2.00 mmol) および 4-ジメチルァミノ ピリジン (611 mg, 5.00 mmol) の N, N-ジメチルホルムアミド (10 mL) 溶液にィ ソニコチノイルクロリド塩酸塩 (712 mg, 4.00匪 ol) を加え、 室温で 20 分間攪 拌した。反応混合物に水および飽和炭酸水素ナトリウム水溶液を加え、酢酸ェチル で 2回抽出した。合わせた有機層を水で 2回洗浄、 減圧濃縮した。残渣をエタノー ルージェチルエーテルから再結晶して表題化合物 (800 mg、 収率 88» を得た。 融点 247-249 °C。 .3- (1,2,8,9-Tetrahydro-4-methoxy-2,2,8,8-tetramethylph [3,2-f] isoquinolin-6-yl) benzenamine (701 mg, 2.00 mmol ) And 4-dimethylaminopyridine (611 mg, 5.00 mmol) in N, N-dimethylformamide (10 mL) were added with isonicotinoyl chloride hydrochloride (712 mg, 4.00 methylol) and stirred at room temperature for 20 minutes. did. Water and a saturated aqueous solution of sodium hydrogen carbonate were added to the reaction mixture, and the mixture was extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure. The residue was recrystallized from ethanol lugetyl ether to give the title compound (800 mg, yield 88 »; melting point 247-249 ° C.
¾ NMR (CDCI3) 51.21 (6H, s), 1.57 (6H, s), 2.51 (2H, s), 3.00 (2H, s), 3.73 (3H, s), 6.68 (1H, s), 7.25-7.33 (1H, m), 7.42 (1H, i, J = 7.9 Hz), 7.66 (2H, d, J = 6.2 Hz), 7.74 (1H, t, J = 1.7 Hz), 7.90-7.98 (1H, m), 8.73 (1H, br s), 8.76 (2H, d, J = 6.2 Hz 実施例 6 ¾ NMR (CDCI3) 51.21 (6H, s), 1.57 (6H, s), 2.51 (2H, s), 3.00 (2H, s), 3.73 (3H, s), 6.68 (1H, s), 7.25-7.33 (1H, m), 7.42 (1H, i, J = 7.9 Hz), 7.66 (2H, d, J = 6.2 Hz), 7.74 (1H, t, J = 1.7 Hz), 7.90-7.98 (1H, m) , 8.73 (1H, br s), 8.76 (2H, d, J = 6.2 Hz Example 6
N - [3- (1 , 2, 8, 9-テトラヒドロ- 4 -メトキシ -2, 2, 8, 8-テトラメチルフ口 [3, 2-f]ィソ キノリン- 6-ィル)フエニル]メタンスルホンアミド N- [3- (1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylphenyl [3,2-f] isoquinolin-6-yl) phenyl] methanesulfone Amide
3- (1 , 2, 8, 9 -テトラヒドロ- 4 -メトキシ- 2, 2, 8, 8-テトラメチルフ口 [3, 2-f]ィソ キノリン -6-ィル)ベンゼンァミン (2.11 g, 6.02腿 ol) のピリジン (15虬) 溶液 に、 氷冷下メタンスルホニルクロリド (0.51 mL, 6.6匪01) を滴下し、 同温で 20 分間攪拌した。反応混合物に水および飽和炭酸水素ナトリウム水溶液を加え、酢酸 ェチルで 2回抽出した。合わせた有機層を水で 2回洗浄、減圧濃縮した。残渣をト ルェンに溶解し、減圧濃縮した後、酢酸ェチルージェチルエーテルから結晶化させ て表題化合物 (2.28 g、 収率 88%) を得た。 3- (1,2,8,9-Tetrahydro-4-methoxy-2,2,8,8-tetramethylph [3,2-f] isoquinolin-6-yl) benzenamine (2.11 g, 6.02 thighs) To a solution of ol) in pyridine (15 虬), methanesulfonyl chloride (0.51 mL, 6.6 band01) was added dropwise under ice cooling, and the mixture was stirred at the same temperature for 20 minutes. Water and a saturated aqueous sodium hydrogen carbonate solution were added to the reaction mixture, and the mixture was extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure. The residue was dissolved in toluene, concentrated under reduced pressure, and crystallized from ethyl acetate-ethyl ether to give the title compound (2.28 g, yield 88%).
融点 211-215 。C。 Melting point 211-215. C.
¾ NMR (CDC13) δΐ.34 (6H, s), 1.58 (6Η, s), 2.60-2.81 (5H, m), 3.02 (2H, s), 3.73 (3H, s), 6.66 (1H, s), 7.21-7.44 (3H, m), 7.53 (1H, br s)0 ¾ NMR (CDC1 3) δΐ.34 ( 6H, s), 1.58 (6Η, s), 2.60-2.81 (5H, m), 3.02 (2H, s), 3.73 (3H, s), 6.66 (1H, s ), 7.21-7.44 (3H, m), 7.53 (1H, br s) 0
実施例 7 · Example 7
3 - [(メチルスルホニル) [3-(1,2,8, 9-テトラヒドロ- 4 -メトキシ- 2, 2, 8, 8 -テ卜ラメ チルフ口 [3, 2-f]イソキノリン- 6-ィル)フエニル]ァミノ]プロパンスルホンァミド 3-クロ口-卜プロパンスルホンアミド (788 mg, 5.00 mmol) のトルエン (10 mL) 懸濁液に Ν,Ν-ジメチルホルムアミドジメチルァセタール (0.73 mL, 5.5匪01) を 加え、 60 で 30分間攪拌した。 反応混合物を減圧濃縮して 3-クロ口- N- [(ジメ チルァミノ)メチレン] -1-プロパンスルホンアミドを含む混合物 (1.15 g) を得た。 この混合物 600 mg、 N - [3_(1, 2, 8, 9-テトラヒドロ- 4-メトキシ- 2, 2, 8, 8-テトラ メチルフロ [3, 2- f]イソキノリン- 6-ィル)フエニル]メタンスルホンアミド (806 mg, 1.88 mmol) およびヨウ化ナトリウム (282 mg, 1.88 mmol) の Ν,Ν-ジメチル ホルムアミド (4 niL) 懸濁液に水素化ナトリウム (66 油分散物) (89 mg, 2.4 蘭 ol) を加え、 室温で 10分間、 80 で 4時間攪拌した。 反応混合物を飽和塩化 アンモニゥム水溶液に注ぎ、酢酸ェチルで 2回抽出した。合わせた有機層を水で 2 回洗浄、減圧濃縮した。残渣を塩基性シリカゲルカラムクロマトグラフィー (へキ サン/酢酸ェチル 1:1 の後酢酸ェチル) に供し、 N- [(ジメチルァミノ)メチレ ン] - 3- [(メテルスルホニル) [3- (1,2, 8, 9-テトラヒドロ- 4-メ卜キシ- 2, 2,8, 8-テト ラメチルフ口 [3, 2-f]イソキノリン -6 -ィル)フエニル]ァミノ]プロパンスルホンァ ミド (1.05 g) を非晶質として得た。 3-[(Methylsulfonyl) [3- (1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethyl] [3,2-f] isoquinoline-6- L) Phenyl] amino] propanesulfonamide To a suspension of 3-chloro-propanesulfonamide (788 mg, 5.00 mmol) in toluene (10 mL) was added Ν, Ν-dimethylformamide dimethyl acetal (0.73 mL, 5.5 Bandit 01) was added and stirred at 60 for 30 minutes. The reaction mixture was concentrated under reduced pressure to obtain a mixture (1.15 g) containing 3-chloro-N-[(dimethylamino) methylene] -1-propanesulfonamide. 600 mg of this mixture, N- [3_ (1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylfuro [3,2-f] isoquinolin-6-yl) phenyl] To a suspension of methanesulfonamide (806 mg, 1.88 mmol) and sodium iodide (282 mg, 1.88 mmol) in Ν, Ν-dimethylformamide (4 niL) was added sodium hydride (66 oil dispersion) (89 mg, 2.4 mg). Orchid ol) was added, and the mixture was stirred at room temperature for 10 minutes and at 80 for 4 hours. The reaction mixture was poured into a saturated aqueous solution of ammonium chloride and extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 1: 1 followed by ethyl acetate) to give N-[(dimethylamino) methylene] -3-[(methylsulfonyl) [3- (1,2 , 8, 9-Tetrahydro-4-methoxy-2,2,8,8-tetra [3,2-f] isoquinoline-6-yl) phenyl] amino] propanesulfonamide (1.05 g) was obtained as amorphous.
これを 2 M塩酸に溶解し、 40分間加熱還流した。 反応混合物を飽和炭酸水素ナ トリウム水溶液で中和、酢酸ェチルで 2回抽出した。合わせた有機層を水および飽 和塩化ナトリウム水溶液で洗浄、 硫酸ナトリウム上で乾燥、 ろ過、 減圧濃縮した。 残渣を酢酸ェチルーへキサンから結晶化させて表題化合物 (820 mg、 収率 79%) を 得た。 This was dissolved in 2 M hydrochloric acid and heated under reflux for 40 minutes. The reaction mixture was neutralized with a saturated aqueous sodium hydrogen carbonate solution and extracted twice with ethyl acetate. The combined organic layer was washed with water and a saturated aqueous solution of sodium chloride, dried over sodium sulfate, filtered, and concentrated under reduced pressure. The residue was crystallized from ethyl acetate-hexane to give the title compound (820 mg, yield 79%).
融点 165-167 °C。 Mp 165-167 ° C.
¾ NMR (CDC13) δΐ.29 (6Η, s), 1.57 (6H, s), 1.89-2.05 (2H, m), 2.59 (2H, s), 2.96 (3H, s), 3.01 (2H, s), 3.21 (2H, t, J = 7.3 Hz), 3.73 (3H, s), 3.91 (2H, t, J = 6.6 Hz), 5.38 (2H, br s), 6.62 (1H, s), 7.39-7.56 (3H, m), 7.57-7.61 (1H, m)。 ¾ NMR (CDC1 3) δΐ.29 ( 6Η, s), 1.57 (6H, s), 1.89-2.05 (2H, m), 2.59 (2H, s), 2.96 (3H, s), 3.01 (2H, s ), 3.21 (2H, t, J = 7.3 Hz), 3.73 (3H, s), 3.91 (2H, t, J = 6.6 Hz), 5.38 (2H, br s), 6.62 (1H, s), 7.39- 7.56 (3H, m), 7.57-7.61 (1H, m).
実施例 8 Example 8
6 -(3-ブロモフエニル) -1,2, 8, 9-テトラヒドロ- 4-メトキシ -2, 2, 8, 8-テトラメチル フロ [3, 2-f]イソキノリン 6- (3-bromophenyl) -1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylfuro [3,2-f] isoquinoline
3一ブロモベンゾニトリル (4.47 g、 24.6籠 ol) および 2, 3-ジヒドロ- 7-メトキ シ- 2, 2 -ジメチル _4-(2_メチル -卜プロぺニル)ベンゾフラン (5.70 g、 24.5匪 ol) のトルエン (20mL)溶液を 85 °Cに加熱し、 濃硫酸 (3.0 mL、 56讓 ol)の酢酸 (10 mL) 溶液を滴下、 同温で 1 時間攪拌した。 反応混合物に水を加え、 ジイソプロピ ルエーテルで洗浄した。 有機層を 2 M塩酸で抽出した。 合わせた水層を氷冷し、 濃アンモニア水で中和、酢酸ェチルで 2回抽出した。合わせた有機層を水で 2回洗 浄、減圧濃縮した。残渣を塩基性シリカゲルカラムクロマトグラフィー (へキサン /酢酸ェチル 10:1) に供し、 へキサンから結 化させて表題化合物 (2.88g、 収率 28¾) を得た。 3 one-bromobenzonitrile (4 47 g, 24.6 cage ol.) And 2, 3-dihydro - 7-methoxyethanol - 2, 2 - dimethyl _4- (2_ methyl - Bok propenyl) benzofuran (5.70 g, 24.5 A toluene solution (20 mL) of dandelion (ol) was heated to 85 ° C, a solution of concentrated sulfuric acid (3.0 mL, 56 mL) in acetic acid (10 mL) was added dropwise, and stirred at the same temperature for 1 hour. Water was added to the reaction mixture, which was washed with diisopropyl ether. The organic layer was extracted with 2M hydrochloric acid. The combined aqueous layer was ice-cooled, neutralized with concentrated aqueous ammonia, and extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 10: 1), and condensed from hexane to obtain the title compound (2.88 g, yield 28¾).
融点 128-130 °C。 128-130 ° C.
'HNMR (CDC <51.27 (6H, s), 1.57 (6H, s), 2.58 (2H, s), 3.01 (2H, s), 3.71 (3H, s), 6.56 (1H, s), 7.27 (1H, t, J = 7.8 Hz), 7.46 (1H, dt, J = 7.8, 1.3 Hz), 7.54 (1H, ddd, J - 7.8, 2.0, LI Hz), 7.72 (1H, t, J = 1.7 Hz) 0. 実施例 9 1, 2, 8, 9 -テトラヒドロ- 4-メトキシ- 2, 2, 8, 8 -テトラメチル -6- [3- (4 -ピリジニル) フエニル]フ口 [3, 2-f ]イソキノリン 'HNMR (CDC <51.27 (6H, s), 1.57 (6H, s), 2.58 (2H, s), 3.01 (2H, s), 3.71 (3H, s), 6.56 (1H, s), 7.27 (1H , t, J = 7.8 Hz), 7.46 (1H, dt, J = 7.8, 1.3 Hz), 7.54 (1H, ddd, J-7.8, 2.0, LI Hz), 7.72 (1H, t, J = 1.7 Hz) 0. Example 9 1,2,8,9-Tetrahydro-4-methoxy-2,2,8,8-tetramethyl-6- [3- (4-pyridinyl) phenyl] aceto [3,2-f] isoquinoline
6 -(3 -ブロモフエニル)-1, 2, 8, 9-テトラヒドロ- 4 -メトキシ- 2, 2, 8, 8-テトラメチ ルフロ [3,2- イソキノリン (3.34 g、 8.06匪01) および 4-ピリジニルポロン酸 (1.49 g、 12.1 mmol) の N, N-ジメチルホルムアミド (20 mL) 懸濁液に炭酸ナトリ ゥム (1.41 g、 13.3 mmol) の水 (10 mL) 溶液およびテトラキス(トリフエニルホ スフイン)パラジウム(0) (466 mg, 0.403匪 ol) を加え、 窒素雰囲気下、 120 で 6時間攪拌した。 反応混合物に水を加え、 酢酸ェチルで 2回抽出レた。 合わせた有 機層を水で 2回洗浄、 ろ過、減圧濃縮した。残渣を塩基性シリカゲルカラムクロマ トグラフィー (へキサン/酢酸ェチル 10:1 の後 2:1) に供し、 酢酸ェチルーへキ サンから結晶化させて表題化合物 (1.95 g、 収率 59%) を得た。 6- (3-Bromophenyl) -1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylfuro [3,2-isoquinoline (3.34 g, 8.06 bandages01) and 4-pyridinylporone A suspension of acid (1.49 g, 12.1 mmol) in N, N-dimethylformamide (20 mL) was added to a solution of sodium carbonate (1.41 g, 13.3 mmol) in water (10 mL) and tetrakis (triphenylphosphine) palladium (0. ) (466 mg, 0.403 bandol) was added, and the mixture was stirred at 120 under a nitrogen atmosphere for 6 hours. Water was added to the reaction mixture, and the mixture was extracted twice with ethyl acetate. The combined organic layers were washed twice with water, filtered, and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 10: 1 followed by 2: 1) and crystallized from ethyl acetate-hexane to give the title compound (1.95 g, yield 59%). Was.
融点 125-127 °Co Melting point 125-127 ° Co
Ή NMR (CDC ) 51.30 (6H, s), 1.58 (6H, s), 2.62 (2H, s), 3.03 (2H, s), 3.69 (3H, s), 6.62 (1H, s), 7.48-7.57 (1H, m), 7.55 (2H, d, J = 6.2 Hz), 7.61 (1H, dt, J = 7.6, 1.7 Hz), 7.69 (1H, dt, J = 7. , 1.7 Hz), 7.83 (1H, t, J = 1.7 Hz), 8.66 (2H, d, J = 6.2 Hz)。 Ή NMR (CDC) 51.30 (6H, s), 1.58 (6H, s), 2.62 (2H, s), 3.03 (2H, s), 3.69 (3H, s), 6.62 (1H, s), 7.48-7.57 (1H, m), 7.55 (2H, d, J = 6.2 Hz), 7.61 (1H, dt, J = 7.6, 1.7 Hz), 7.69 (1H, dt, J = 7., 1.7 Hz), 7.83 (1H , t, J = 1.7 Hz), 8.66 (2H, d, J = 6.2 Hz).
実施例 10 Example 10
1, 2, 8,9-テトラヒドロ- 2,2,8,8-テトラメチル- 6 - [3- (4-ピリジニル)フェニル]フ 口 [3,2_f]イソキノリン- 4 オール 1,2,8,9-Tetrahydro-2,2,8,8-tetramethyl-6- [3- (4-pyridinyl) phenyl] fluoro [3,2_f] isoquinoline-4ol
1, 2, 8, 9-テトラヒドロ- 4-メトキシ- 2, 2, 8, 8 -テトラメチル- 6_ [3- (4-ピリジニ ル)フエニル]フロ [3, 2 - f]イソキノリン (1.11 g、 2.69腿 ol) に 48 臭化水素酸 (13 mL) を加え、 105 でで 17 時間攪拌した。 反応混合物を氷冷し、 濃アンモニ ァ水で中和、酢酸ェチルーテトラヒドロフラン混合液で 2回抽出した。合わせた有 機層を飽和塩化ナトリウム水溶液で洗浄、 硫酸ナトリウム上で乾燥、 活性炭処理、 ろ過、減圧濃縮した。残渣をエタノールージェチルエーテルから再結晶して表題化 合物 (766 mg、 収率 71%) を得た。 1,2,8,9-Tetrahydro-4-methoxy-2,2,8,8-tetramethyl-6_ [3- (4-pyridinyl) phenyl] furo [3,2-f] isoquinoline (1.11 g, 2.69 t) was added 48 hydrobromic acid (13 mL), and the mixture was stirred at 105 for 17 hours. The reaction mixture was ice-cooled, neutralized with concentrated aqueous ammonia, and extracted twice with a mixed solution of ethyl acetate and tetrahydrofuran. The combined organic layers were washed with a saturated aqueous solution of sodium chloride, dried over sodium sulfate, treated with activated carbon, filtered, and concentrated under reduced pressure. The residue was recrystallized from ethanol-ethyl ether to give the title compound (766 mg, yield 71%).
融点 221-223 。C。 Melting point 221-223. C.
¾ NMR (CDC13) (51.29 (6H, s), 1.56 (6H, s), 2.59 (2H, s), 3.02 (2H, s), 6.60 (1H, s), 7.35 (2H, d, J = 6.2 Hz), 7.45-7.54 (1H, m), 7.57-7.68 (3H, m), 8.44 (2H, d, J = 6.2 Hz ¾ NMR (CDC1 3) (51.29 (6H, s), 1.56 (6H, s), 2.59 (2H, s), 3.02 (2H, s), 6.60 (1H, s), 7.35 (2H, d, J = 6.2 Hz), 7.45-7.54 (1H, m), 7.57-7.68 (3H, m), 8.44 (2H, d, J = 6.2 Hz
実施例 11 Example 11
1,2, 8, 9-テトラヒドロ- 2, 2, 8, 8 -テトラメチル -4- [2 -(2-ピリジニル)ェトキ シ] - 6- [3 - (4-ピリジニル)フェニル]フロ [3, 2-f]イソキノリン 1,2,8,9-Tetrahydro-2,2,8,8-tetramethyl-4- [2- (2-pyridinyl) ethoxy] -6- [3- (4-pyridinyl) phenyl] furo [3 , 2-f] isoquinoline
1, 2, 8, 9-テトラヒドロ- 2, 2, 8, 8-テトラメチル - 6_[3- (4 -ピリジニル)フエニル] フロ [3, 2-f]イソキノリン- 4 -オール (598 mg、 1.50 mmol)、 2- (2-ヒドロキシェチ ル)ピリジン (277 mg、 2.25 mmol) およびトリフエニルホスフィン (787 mg、 3.00 mmol) のテトラヒドロフラン (6mL)溶液に氷冷下、 ァゾジカルボン酸ジイソプロ ピル (0.59 mL、 3.0 mmol) を滴下、 室温で 30分間、 60 で 1 時間攪拌した。 得られた混合物に 2- (2-ヒドロキシェチル)ピリジン (0.17 mL、 1,5腿 ol)、 トリ フエニルホスフィン (394 mg、 1.50 mmol) およびァゾジ力ルポン酸ジイソプロピ ル (0.30 mL、 1.5删 ol) を追加し、 60でで 1.5 時間攪拌した。 反応混合物を氷 冷し、 1M塩酸で酸性にし、 酢酸ェチルで 2回洗浄した。 水層を濃アンモニア水で 中和、 酢酸ェチルで 2回抽出した。 合わせた有機層を 1 M水酸化ナトリウム水溶 液 (2回)および水で洗浄、 減圧濃縮した。 残渣を塩基性シリカゲルカラムクロマ トグラフィ一 (へキサン/酢酸ェチル 10:1、 5:1、 3:1 の後 1:1) に供し、 ジェチ ルエーテル一へキサンから再結晶して表題化合物 (348 mg、 収率 46» を得た。 融点 110- 113 1,2,8,9-Tetrahydro-2,2,8,8-tetramethyl-6_ [3- (4-pyridinyl) phenyl] furo [3,2-f] isoquinolin-4-ol (598 mg, 1.50 mmol), 2- (2-hydroxyethyl) pyridine (277 mg, 2.25 mmol) and triphenylphosphine (787 mg, 3.00 mmol) in tetrahydrofuran (6 mL) under ice-cooling with diisopropyl azodicarboxylate (0.59 mL, 3.09 mmol). mmol), and the mixture was stirred at room temperature for 30 minutes and at 60 for 1 hour. The resulting mixture was added to 2- (2-hydroxyethyl) pyridine (0.17 mL, 1.5 liters), triphenylphosphine (394 mg, 1.50 mmol) and diisopropyl azodiphenol (0.30 mL, 1.5 mL). ol) and stirred at 60 for 1.5 hours. The reaction mixture was cooled on ice, acidified with 1M hydrochloric acid, and washed twice with ethyl acetate. The aqueous layer was neutralized with concentrated aqueous ammonia and extracted twice with ethyl acetate. The combined organic layer was washed with 1 M aqueous sodium hydroxide solution (twice) and water, and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 10: 1, 5: 1, 3: 1 followed by 1: 1), and recrystallized from ethyl ether-hexane to give the title compound (348 mg). The yield was 46. The melting point was 110-113.
¾ NMR (CDC13) 51.29 (6H, s), 1.56 (6H, s), 2.60 (2H, s), 3.00 (2H, s), 3.17 (2H, t, J = 7.0 Hz), 4.28 (2H, t, J = 7.0 Hz), 6.66 (1H, s), 7.06 (1H, ddd, J = 7.6, 4.9, 1.2 Hz), 7.11-7.17 (1H, m), 7.45-7.61 (5H, m), 7.67 (1H, dt, J = 7.0, 1.9 Hz), 7.78-7.81 (1H, m), 8.45 (1H, ddd, J = 5.0, 1.9, 0.9 Hz), 8.63 (2H, d, J = 6.2 Hz)0 ¾ NMR (CDC1 3) 51.29 ( 6H, s), 1.56 (6H, s), 2.60 (2H, s), 3.00 (2H, s), 3.17 (2H, t, J = 7.0 Hz), 4.28 (2H, t, J = 7.0 Hz), 6.66 (1H, s), 7.06 (1H, ddd, J = 7.6, 4.9, 1.2 Hz), 7.11-7.17 (1H, m), 7.45-7.61 (5H, m), 7.67 (1H, dt, J = 7.0, 1.9 Hz), 7.78-7.81 (1H, m), 8.45 (1H, ddd, J = 5.0, 1.9, 0.9 Hz), 8.63 (2H, d, J = 6.2 Hz) 0
実施例 12 Example 12
N- [3'- (1,2,8,9 -テトラヒドロ- 4-メトキシ- 2, 2, 8, 8 -テトラメチルフ口 [3, 2 - f]ィ ソキノリン - 6-ィル) [1,1' -ビフエニル] -4-ィル]ァセトアミド N- [3 '-(1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylfuran [3,2-f] isoquinoline-6-yl) [1,1 '-Biphenyl] -4-yl] acetoamide
6 -(3-ブロモフエニル) -1, 2, 8, 9-テトラヒドロ- 4-メトキシ- 2, 2, 8, 8-テトラメチ ルフロ [3, 2- f]イソキノリン (207 mg、 0.500 mmol), 4' -(4, 4, 5, 5-テトラメチル - 1,3, 2-ジォキサボロラン -2-ィル)ァセトァニリド (144mg、 0.551匪 ol)、 炭酸ナ トリウム (133 mg、 1.25匪 ol) およびテトラキス(トリフエニルホスフィン)パラ ジゥム(0) (12 mg、 0.010 mmol) の 1,2-ジメトキシェタン (1.5 mL)、 エタノール (0.8 mL) および水 (0.8 mL)懸濁液を、 窒素雰囲気下 85 で 16時間攪拌した。 反応混合物に水を加え、酢酸ェチルで 2回抽出した。合わせた有機層を水および飽 和塩化ナトリゥム水溶液で洗浄、硫酸ナトリゥムー塩基性シリ力ゲルを通して乾燥 (酢酸ェチルで溶出)、減圧濃縮した。残渣を酢酸ェチルーへキサンから結晶化させ て表題化合物 (218 rag, 収率 93%) を得た。 6- (3-bromophenyl) -1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylfuro [3,2-f] isoquinoline (207 mg, 0.500 mmol), 4 ' -(4,4,5,5-tetramethyl-1, 3,2-dioxaborolan-2-yl) acetanilide (144mg, 0.551 bandol ol), sodium carbonate Thorium (133 mg, 1.25 bandol) and tetrakis (triphenylphosphine) palladium (0) (12 mg, 0.010 mmol) in 1,2-dimethoxyethane (1.5 mL), ethanol (0.8 mL) and water (0.8 mL) mL) suspension was stirred at 85 under a nitrogen atmosphere for 16 hours. Water was added to the reaction mixture, which was extracted twice with ethyl acetate. The combined organic layers were washed with water and saturated aqueous sodium chloride solution, dried over sodium sulfate basic silica gel (eluted with ethyl acetate) and concentrated under reduced pressure. The residue was crystallized from ethyl acetate-hexane to give the title compound (218 rag, yield 93%).
融点 231-234 °Co Melting point 231-234 ° Co
¾ NMR (CDC13) 1.31 (6H, s), 1.58 (6H, s), 2.13 (3H, s), 2.63 (2H, s), 3.03 (2H, s), 3.69 (3H, s), 6.67 (1H, s), 7.40-7.61 (7H, m), 7.68-7.76 (2H, m)。 実施例 13 ¾ NMR (CDC1 3) 1.31 ( 6H, s), 1.58 (6H, s), 2.13 (3H, s), 2.63 (2H, s), 3.03 (2H, s), 3.69 (3H, s), 6.67 ( 1H, s), 7.40-7.61 (7H, m), 7.68-7.76 (2H, m). Example 13
6- (3 -ブロモフエ二ル)- 1, 2, 8, 9 -テトラヒドロ- 2, 2, 8, 8 -テトラメチルフロ [3, 2-f] イソキノリン- 4-オール 6- (3-Bromophenyl) -1,2,8,9-tetrahydro-2,2,8,8-tetramethylfuro [3,2-f] isoquinolin-4-ol
6- (3-ブロモフエ二ル)- 1, 2, 8, 9-テトラヒドロ- 4-メトキシ- 2, 2, 8, 8-テトラメチ ルフロ [3, 2-f]イソキノリン (2.08 g、 5.02 mmol) に 48%臭化水素酸 (30 mL) を 加え、 105 °Cで 14.5時間攪拌した。反応混合物を氷冷し、濃アンモニア水で中和、 クロロホルムで 2回抽出した。合わせた有機層を飽和塩化ナトリゥム水溶液で洗浄、 硫酸ナトリウム上で乾燥、 ろ過、 減圧濃縮した。残渣をエタノールから再結晶して 表題化合物 (1.09 g、 収率 54¾) を得た。 To 6- (3-bromophenyl) -1,2,8,9-tetrahydro-4-methoxy-2,2,8,8-tetramethylfuro [3,2-f] isoquinoline (2.08 g, 5.02 mmol) 48% Hydrobromic acid (30 mL) was added, and the mixture was stirred at 105 ° C for 14.5 hours. The reaction mixture was ice-cooled, neutralized with concentrated aqueous ammonia, and extracted twice with chloroform. The combined organic layer was washed with a saturated aqueous sodium chloride solution, dried over sodium sulfate, filtered, and concentrated under reduced pressure. The residue was recrystallized from ethanol to give the title compound (1.09 g, yield 54¾).
融点 236-239 °C。 236-239 ° C.
¾ NMR (CDCI3) δ 1.24 (6Η, s), 1.54 (6H, s), 2.54 (2H, s), 3.00 (2H, s), ¾ NMR (CDCI3) δ 1.24 (6Η, s), 1.54 (6H, s), 2.54 (2H, s), 3.00 (2H, s),
5.60-5.80 (1H, br), 6.50 (1H, s), 7.19 (1H, t, J = 7.8 Hz), 7.33-7.38 (1H, m), 7.43-7.48 (1H, m), 7.61 (1H, t, J = 1.7 Hz)0 5.60-5.80 (1H, br), 6.50 (1H, s), 7.19 (1H, t, J = 7.8 Hz), 7.33-7.38 (1H, m), 7.43-7.48 (1H, m), 7.61 (1H, t, J = 1.7 Hz) 0
実施例 1 Example 1
N - [3'-(1,2,8,9-テトラヒドロ- 4—ヒドロキシ -2, 2, 8, 8-テトラメチルフ口 [3, 2 - Π イソキノリン- 6-ィル) [1, Γ-ビフエ二ル]- 4-ィル]ァセトアミド N- [3 '-(1,2,8,9-tetrahydro-4-hydroxy-2,2,8,8-tetramethylfuran [3,2- -isoquinolin-6-yl] [1, Γ-bihue Nil] -4-yl] acetamide
6 -(3-ブロモフエニル) - 1, 2, 8, 9 -テトラヒドロ- 2, 2, 8, 8-テトラメチルフ口 [3, 2 - ί]イソキノリン -4-オール (1.00 g、 2.50 mmol), 4' -(4, 4, 5, 5-テトラメチル - 1,3, 2 -ジォキサボロラン- 2 -ィル)ァセトァニリド (718 mg、 2.75 mmol), 炭酸ナ トリウム (662 mg、 6.25腿 ol) およびテトラキス(トリフエニルホスフィン)パラ ジゥム(0) (58mg、 0.050 mmol)の 1,2 -ジメトキシェタン (12mL)、 エタノール (6 mL) および水 (6 mL) 懸濁液を、 窒素雰囲気下 85 で 21 時間攪拌した。 反応混 合物に水を加え、酢酸ェチルで 2回抽出した。合わせた有機層を水および飽和塩化 ナトリゥム水溶液で洗浄、硫酸ナトリゥム—塩基性シリカゲルを通して乾燥 (酢酸 ェチルで溶出)、 減圧濃縮した。 残渣を酢酸ェチルから結晶化させて表題化合物 (1.12 g、 収率 99%) を得た。 6- (3-Bromophenyl) -1,2,8,9-tetrahydro-2,2,8,8-tetramethylfuran [3,2--] isoquinolin-4-ol (1.00 g, 2.50 mmol), 4 ' -(4,4,5,5-Tetramethyl-1,3,2-dioxaborolan-2-yl) acetoanilide (718 mg, 2.75 mmol), sodium carbonate Thorium (662 mg, 6.25 mol) and tetrakis (triphenylphosphine) palladium (0) (58 mg, 0.050 mmol) in 1,2-dimethoxyethane (12 mL), ethanol (6 mL) and water (6 mL) The suspension was stirred at 85 under a nitrogen atmosphere for 21 hours. Water was added to the reaction mixture, and extracted twice with ethyl acetate. The combined organic layer was washed with water and a saturated aqueous solution of sodium chloride, dried over sodium sulfate-basic silica gel (eluted with ethyl acetate), and concentrated under reduced pressure. The residue was crystallized from ethyl acetate to give the title compound (1.12 g, yield 99%).
融点 272-275 。 Mp 272-275.
¾NMR (DMSO- d6) dl.17 (6Η, s), 1.46 (6H, s), 2.06 (3H, s), 2.52 (2H, s), 2.99 (2H, s), 6.58 (1H, s), 7.37-7.44 (1H, m), 7.51 (1H, t, J = 7.7 Hz), 7.59-7.72 (6H, m), 9.03 (1H, s), 10.04 (1H, s)。 ¾NMR (DMSO-d 6 ) dl.17 (6Η, s), 1.46 (6H, s), 2.06 (3H, s), 2.52 (2H, s), 2.99 (2H, s), 6.58 (1H, s) , 7.37-7.44 (1H, m), 7.51 (1H, t, J = 7.7 Hz), 7.59-7.72 (6H, m), 9.03 (1H, s), 10.04 (1H, s).
実施例 15 Example 15
トリフルォロメタンスルホン酸 6- [4' - (ァセチルァミノ) [1, Γ -ビフエニル] -3 -ィ ル]- 1, 2, 8, 9-テトラヒド口- 2, 2, 8, 8 -テトラメチルフ口 [3, 2-f]イソキノリン- 4 -ィ ルエステル Trifluoromethanesulfonic acid 6- [4 '-(acetylamino) [1, Γ-biphenyl] -3-yl] -1,2,8,9-tetrahydrido-2,2,8,8-tetramethylfur [ 3, 2-f] isoquinoline-4-yl ester
N - [3' -(1, 2, 8, 9-テトラヒドロ- 4-ヒドロキシ _2, 2, 8, 8-テトラメチルフロ [3, 2- f]イソキノリン- 6-ィル) [1,1'-ピフエ二ル] -4-ィル]ァセトアミド (546 mg、 1.20 mmol) のピリジン (6 mL) 溶液に氷冷下トリフルォロメタンスルホン酸無水 物 (0.51 mL、 3.0腿 ol) を滴下し、 同温で 15 分間攪拌した。 反応混合物に水お よび飽和炭酸水素ナトリゥム水溶液を加え、酢酸ェチルで 2回抽出した。合わせた 有機層を水で 2回洗浄、減圧濃縮した。残渣を塩基性シリカゲルカラムクロマトグ ラフィー (へキサン/酢酸ェチル 5:1、 2:1 の後 1:1) に供し、 酢酸ェチルーへキ サンから結晶化させて表題化合物 (595 mg、 収率 85» を得た。 N- [3 '-(1,2,8,9-tetrahydro-4-hydroxy_2,2,8,8-tetramethylfuro [3,2-f] isoquinolin-6-yl) [1,1' To a solution of [-pifenyl] -4-yl] acetoamide (546 mg, 1.20 mmol) in pyridine (6 mL) was added dropwise trifluoromethanesulfonic anhydride (0.51 mL, 3.0 tmol) under ice-cooling. The mixture was stirred at warm for 15 minutes. Water and a saturated aqueous solution of sodium hydrogen carbonate were added to the reaction mixture, and the mixture was extracted twice with ethyl acetate. The combined organic layer was washed twice with water and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 5: 1, 2: 1 followed by 1: 1) and crystallized from ethyl acetate-hexane to give the title compound (595 mg, yield 85 » I got
融点 233-235 。C。 233-235. C.
¾ NMR (CDC13) (51.31 (6H, s), 1.58 (6H, s), 2.18 (3H, s), 2.65 (2H, s), 3.07 (2H, s), 7.02 (1H, s), 7.32 (1H, br s), 7.34-7.51 (2H, m), 7.57 (4H, s), 7.60-7.65 (1H, m), 7.69-7.71 (1H, m)。 ¾ NMR (CDC1 3) (51.31 (6H, s), 1.58 (6H, s), 2.18 (3H, s), 2.65 (2H, s), 3.07 (2H, s), 7.02 (1H, s), 7.32 (1H, br s), 7.34-7.51 (2H, m), 7.57 (4H, s), 7.60-7.65 (1H, m), 7.69-7.71 (1H, m).
実施例 16 Example 16
N-[3'-(l, 2, 8, 9 -テトラヒドロ- 2, 2, 8, 8-テトラメチルフ口 [3, 2-f]ィソキノリン - 6 -ィル) [1,Γ-ビフエニル]一 4 -ィル]ァセトアミド N- [3 '-(l, 2,8,9-tetrahydro-2,2,8,8-tetramethylfuro [3,2-f] isoquinoline -6-yl) [1, Γ-biphenyl] -1-4-yl] acetamide
トリフルォロメタンスルホン酸 6-[4'- (ァセチルァミノ) [1,1'-ビフエ二ル] - 3 - ィル] - 1, 2, 8, 9-テトラヒドロ- 2, 2, 8, 8-テトラメチルフ口 [3, 2-f]イソキノリン- 4 - ィルエステル (470 mg、 ,0.801 醒 ol)、 トリェチルァミン (0.34 mL、 2.4 mmol)、 酢酸パラジウム (II) (4.5 m . 0.020 mmol)およびトリフエニルホスフィン (10.5 mg、 0.0400 讓 ol) の N,N-ジメチルホルムアミド (1.5 mL) 溶液にギ酸 (60 βί、 1.6腿 ol) を加え、 窒素雰囲気下 70 °Cで 4.5 時間攪拌した。 反応混合物に水お よび飽和炭酸水素ナトリウム水溶液を加え、酢酸ェチルで 2回抽出した。合わせた 有機層を水および飽和塩化ナトリゥム水溶液で洗浄、硫酸ナトリゥムー塩基性シリ 力ゲルを通して乾燥 (酢酸ェチルで溶出)、 減圧濃縮した。 残渣を塩基性シリカゲ ルカラムクロマトグラフィー (へキサン/酢酸ェチル 1:1の後 1:2) に供し、 酢酸 ェチルーへキサンから結晶化させて表題化合物 (340 mg、 収率 97%) を得た。 融点 140-152 °C。 Trifluoromethanesulfonic acid 6- [4 '-(acetylamino) [1,1'-biphenyl] -3-yl] -1,2,8,9-tetrahydro-2,2,8,8-tetramethylphenyl Mouth [3,2-f] isoquinoline-4-yl ester (470 mg, 0.801 virgin ol), triethylamine (0.34 mL, 2.4 mmol), palladium (II) acetate (4.5 m. 0.020 mmol) and triphenylphosphine (10.5 mg, 0.0400 mL) of N, N-dimethylformamide (1.5 mL) was added with formic acid (60 βί, 1.6 t ol), and the mixture was stirred at 70 ° C for 4.5 hours under a nitrogen atmosphere. Water and a saturated aqueous solution of sodium hydrogen carbonate were added to the reaction mixture, and the mixture was extracted twice with ethyl acetate. The combined organic layer was washed with water and a saturated aqueous sodium chloride solution, dried over sodium sulfate basic silica gel (eluted with ethyl acetate), and concentrated under reduced pressure. The residue was subjected to basic silica gel column chromatography (hexane / ethyl acetate 1: 1 followed by 1: 2), and crystallized from ethyl acetate-hexane to give the title compound (340 mg, yield 97%). . 140-152 ° C.
Ή NMR (CDC13) δ 1.31 (6Η, s), 1.53 (6H, s), 2.17 (3H, s), 2.67 (2H, s), 2.99 (2H, s), 6.53 (1H, d, J = 8.1 Hz), 7.04 (1H, d, J = 8.1 Hz), 7.40-7.49 (3H, m), 7.54 (4H, s), 7.55-7.62 (1H, m), 7.66-7.69 (1H, m)。 Ή NMR (CDC1 3) δ 1.31 (6Η, s), 1.53 (6H, s), 2.17 (3H, s), 2.67 (2H, s), 2.99 (2H, s), 6.53 (1H, d, J = 8.1 Hz), 7.04 (1H, d, J = 8.1 Hz), 7.40-7.49 (3H, m), 7.54 (4H, s), 7.55-7.62 (1H, m), 7.66-7.69 (1H, m).
上記の実施例で製造された化合物を以下の表 1に示す。 The compounds prepared in the above examples are shown in Table 1 below.
(0 ίιίί3?¾ (0 ίιίί3? ¾
〔I拏〕[Ihara]
6ΤΙ 6ΤΙ
8ST90/Z0df/X3d .69000/CO OAV 製剤例 1 8ST90 / Z0df / X3d .69000 / CO OAV Formulation Example 1
(1)実施例 1の化合物 l O. O mg (1) Compound of Example 1 l O.O mg
(2)乳糖 60.0 mg (2) Lactose 60.0 mg
(3)コーンスターチ 35.0 mg (3) Corn starch 35.0 mg
(4)ゼラチン 3.0 mg (4) Gelatin 3.0 mg
(5)ステアリン酸マグネシウム 2.0 mg (5) Magnesium stearate 2.0 mg
実施例 1で得られた化合物 10. Omgと乳糖 60. Omgおよびコーンスターチ 3 5.0 fflgの混合物を 10%ゼラチン水溶液 0, 03 ml (ゼラチンとして 3.0 mg) を用い、 1腿メッシュの篩を通して顆粒化した後、 40°Cで乾燥し再び篩過した。 かくして得られた顆粒をステアリン酸マグネシウム 2.0 mgと混合し、 圧縮した。 得られた中心錠を、蔗糖, 二酸化チタン, タルクおよびアラビアゴムの水懸液によ る糖衣でコ一ティングした。コ一ティングが施された錠剤をミツロウで艷出してコ —ト錠を得た。 A mixture of the compound obtained in Example 1 10. Omg, lactose 60. Omg and corn starch 35.0 fflg was granulated through a 1-mesh mesh sieve using 0.03 ml of 10% gelatin aqueous solution (3.0 mg as gelatin). Thereafter, it was dried at 40 ° C. and sieved again. The granules thus obtained were mixed with 2.0 mg of magnesium stearate and compressed. The obtained central tablets were coated with a sugar coating using an aqueous suspension of sucrose, titanium dioxide, talc and gum arabic. The coated tablets were glazed with beeswax to obtain coated tablets.
製剤例 2 Formulation Example 2
(1)実施例 1の化合物 10.0 mg (1) Compound of Example 1 10.0 mg
(2)乳糖 70. O mg (2) Lactose 70.O mg
(3)コ一ンスターチ 50. O mg (3) Corn starch 50.O mg
(4)可溶性デンプン 7.0 mg (4) Soluble starch 7.0 mg
(5)ステアリン酸マグネシウム 3.0 mg (5) Magnesium stearate 3.0 mg
実施例 1で得られた化合物 10.0 mgとステアリン酸マグネシウム 3.0 mgを可 溶性デンプンの水溶液 0.07 ml (可溶性デンプンとして 7.0 mg) で顆粒化した 後、 乾燥し、 乳糖 70.0 mgおよびコーンスターチ 50.0 mgと混合した。混合物 を圧縮して錠剤を得た。 10.0 mg of the compound obtained in Example 1 and 3.0 mg of magnesium stearate were granulated with 0.07 ml of an aqueous solution of soluble starch (7.0 mg as soluble starch), dried, and mixed with 70.0 mg of lactose and 50.0 mg of corn starch. . The mixture was compressed to give tablets.
製剤例 3 Formulation Example 3
(1)実施例 1の化合物 5. O mg (1) Compound of Example 1 5.O mg
(2)食塩 20. O mg (2) Salt 20.O mg
(3)蒸留水 全量 2 mlとする (3) Total volume of distilled water is 2 ml
実施例 1で得られた化合物 5.0 mgおよび食塩 20.0 mgを蒸留水に溶解させ、 水を加えて全量 2.0 mlとした。 溶液をろ過し、 無菌条件下に 2 mlのアンプルに 充填した。 アンプルを滅菌した後、 密封し注射用溶液を得た。 5.0 mg of the compound obtained in Example 1 and 20.0 mg of common salt were dissolved in distilled water, and water was added to make a total volume of 2.0 ml. Filter the solution into 2 ml ampules under aseptic conditions Filled. The ampoule was sterilized and sealed to obtain a solution for injection.
製剤例 4 Formulation Example 4
流動層造粒乾燥機 (FD-5 S, (株)パゥレック) 中で、 実施例 1で得られた化合物 1500 g、 乳糖 2025 gおよびトウモロコシデンプン 556. 5 gを均一に 混合後、機内でヒドロキシプロピルセルロース 126 g を溶解した水溶液を噴霧 して造粒し、 ついで流動層造粒乾燥機中で乾燥した。得られた造粒物を、 パワーミ ルを用いて 直径 1. 5mm のパンチングスクリーンで解碎して整粒末とした。 こ の整粒末 3927 gをとり、 これにクロスカルメロースナトリウム 210 g と ステアリン酸マグネシウム 63 gを加え、 タンブラ一混合機で混合して打錠用顆 粒とする。 この顆粒を打錠機で直径 6. 5mm の枠を用いて重量 300 mgで打 錠し裸錠とした。得られた裸錠はドリアコ一ターコーティング機中でヒド口キシプ 口ピルメチルセルロース 2910 (TC- 5) とマクロゴール 6000を溶解、酸 化チタン、 三二酸化鉄を分散した液を噴霧し、 1錠当たり l O Omg を含有す る下記処方のフィルム錠、 約 13500錠を得た。 After uniformly mixing 1500 g of the compound obtained in Example 1, lactose 2025 g and 556.5 g of corn starch in a fluidized bed granulating drier (FD-5S, Parec Co., Ltd.), An aqueous solution in which 126 g of propylcellulose was dissolved was sprayed and granulated, and then dried in a fluidized bed granulating dryer. The obtained granules were pulverized using a power mill with a punching screen having a diameter of 1.5 mm to give sized powder. Take 3927 g of the sized powder, add 210 g of croscarmellose sodium and 63 g of magnesium stearate, and mix with a tumbler mixer to obtain granules for tableting. The granules were tableted with a tableting machine at a weight of 300 mg using a frame with a diameter of 6.5 mm to give naked tablets. The obtained uncoated tablets were prepared by dissolving hydr-methyl oxymethyl-pyrumethylcellulose 2910 (TC-5) and macrogol 6000 in a doria coater and spraying a liquid containing titanium oxide and iron sesquioxide dispersed therein. About 13500 film tablets containing lO Omg and having the following formulation were obtained.
錠剤処方: Tablet prescription:
組 成 配合垦 (mgj Composition Formula II (mgj
(1)実施例 1の化合物 100. 0 (1) Compound of Example 1 100.0
(2)乳糖 135. 0 (2) Lactose 135.0
(3)トウモロコシデンプン 37. 1 (3) Corn starch 37.1
(4)クロスカルメロースナトリゥム 15. 0 (4) Croscarmellose sodium 15.0
(5)ヒドロキシプロピルセルロース 8. 4 (5) Hydroxypropyl cellulose 8.4
(6)ステアリン酸マグネシウム 4. 5 (6) Magnesium stearate 4.5
合計 (裸錠) 300. 0 Total (naked tablets) 300. 0
フィルム錠処方: Film tablet formula:
(1)裸錠 300. 0 (1) Nude tablets 300.0
(フィルム成分) (Film components)
(2)ヒドロキシプロピルメチルセルロース 29 0 7 485 (2) Hydroxypropyl methylcellulose 29 0 7 485
(3)マクロゴ一ル 6000 5 (3) Macrogol 6000 5
(4)酸化チタン 0 (5)三二酸化鉄 0. 015 (4) Titanium oxide 0 (5) Iron sesquioxide 0.015
合計 310. 0 Total 310.0
製剤例 5 Formulation Example 5
製剤例 4に記載の方法に準じて実施例 1で得られた化合物を 1錠当たり、 25m g 含有する下記処方のフィルム錠約 13500錠を得た。 According to the method described in Formulation Example 4, about 13,500 film tablets of the following formulation containing 25 mg per compound of the compound obtained in Example 1 were obtained.
錠剤処方: Tablet prescription:
組 成 配合垦 (m ) Composition Formula (m)
(1)実施例 1の化合物 25. 0 (1) Compound of Example 1 25.0
(2)乳糖 210. 0 (2) Lactose 210.0
(3)トウモロコシデンプン 37. 1 (3) Corn starch 37.1
(4)クロスカルメロースナトリゥム 15. 0 (4) Croscarmellose sodium 15.0
(5)ヒドロキシプロピルセルロース 8. 4 (5) Hydroxypropyl cellulose 8.4
(6)ステアリン酸マグネシウム 4. 5 (6) Magnesium stearate 4.5
合計 (裸錠) 300. 0 Total (naked tablets) 300. 0
フィルム錠処方: Film tablet formula:
(1)裸錠 300. 0 (1) Nude tablets 300.0
(フィルム成分) (Film component)
(2)ヒドロキシプロピルメチルセルロース 2910 7. 485 (2) Hydroxypropyl methylcellulose 2910 7.485
(3)マクロゴール 6000 1. 5 (3) Macro goal 6000 1.5
(4)酸化チタン 1. 0 (4) Titanium oxide 1.0
(5)三二酸化鉄 0. 01 5 (5) Iron sesquioxide 0.015
合計 310. 0 Total 310.0
製剤例 6 Formulation Example 6
製剤例 4に記載の方法に準じて実施例 1で得られた化合物を 1錠当たり、 5 m g 含有する下記処方のフィルム錠約 13500錠を得た。 According to the method described in Formulation Example 4, about 13500 film tablets of the following formulation containing 5 mg of the compound obtained in Example 1 per tablet were obtained.
錠剤処方: Tablet prescription:
組 成 配合量 (mg) Composition Amount (mg)
(1)実施例 1の化合物 5. 0 (1) Compound of Example 1 5.0
(2)乳糖 230. 0 (3)トウモロコシデンプン 37. 1 (2) Lactose 230.0 (3) Corn starch 37.1
(4)クロスカルメロースナトリウム 15. 0 (4) Croscarmellose sodium 15.0
(5)ヒドロキシプロピルセルロース 8. 4 (5) Hydroxypropyl cellulose 8.4
(6)ステアリン酸マグネシウム 4. 5 (6) Magnesium stearate 4.5
合計 (裸錠) 300. 0 Total (naked tablets) 300. 0
フィルム錠処方: Film tablet formula:
(1)裸錠 300. 0 (1) Nude tablets 300.0
(フィルム成分) (Film components)
(2)ヒドロキシプロピルメチルセル口一ス 2910 7. 485 (2) Hydroxypropyl methyl cell mouth 2910 7.485
(3)マクロゴール 6000 1. 5 (3) Macro goal 6000 1.5
(4)酸化チタン 1. 0 (4) Titanium oxide 1.0
(5)三二酸化鉄 0. 015 (5) Iron sesquioxide 0.015
合計 310. 0 Total 310.0
製剤例 7 Formulation Example 7
製剤例 4に記載の方法に準じて実施例 1で得られた化合物を 1錠当たり、 1 m g 含有する下記処方のフィルム錠約 13500錠を得た。 According to the method described in Formulation Example 4, about 13500 film tablets of the following formulation containing 1 mg of the compound obtained in Example 1 per tablet were obtained.
錠剤処方: Tablet prescription:
組 成 配合量 (mg) Composition Amount (mg)
(1)実施例 1の化合物 1. 0 (1) Compound of Example 1 1.0
(2)乳糖 234. 0 (2) Lactose 234.0
(3)トウモロコシデンプン 37. 1 (3) Corn starch 37.1
(4)クロスカルメロースナトリゥム 15. 0 (4) Croscarmellose sodium 15.0
(5)ヒドロキシプロピルセルロース 8. 4 (5) Hydroxypropyl cellulose 8.4
(6)ステアリン酸マグネシゥム 4. 5 (6) Magnesium stearate 4.5
合計 (裸錠) 300. 0 Total (naked tablets) 300. 0
フィルム錠処方: Film tablet formula:
(1)裸錠 300. 0 (1) Nude tablets 300.0
(フィルム成分) (Film components)
(2)ヒドロキシプロピルメチルセルロース 2910 7. 485 (3)マクロゴール 6000 1. 5 (2) Hydroxypropyl methylcellulose 2910 7.485 (3) Macro goal 6000 1.5
(4)酸化チタン 1. 0 (4) Titanium oxide 1.0
(5)三二酸化鉄 0. 01 5 (5) Iron sesquioxide 0.015
合計 310. 0 Total 310.0
製剤例 8 Formulation Example 8
白色ヮセリン 40 g White ginseng 40 g
セタノール 10 g Cetanol 10 g
サラシミツロウ 5 g 5 g of beeswax
セスキォレイン酸ソルビタン 5 g Sorbitan sesquioleate 5 g
ラウ口モク口ゴールド 0 . 5 g Mouth Mouth Gold 0.5 g
パラォキシ安息香酸メチル 0. 1 g Methyl paraoxybenzoate 0.1 g
パラォキシ安息香酸プロピル 0 1 Propyl paraoxybenzoate 0 1
精製水 purified water
上記組成からなる局方吸水軟膏(100 g) を予め 70°Cに加熱して、 その溶液 中に実施例 1で得られた化合物 1 gをメタノール 20m lに加熱して溶解した溶 液を加えた。 同温度で 10分間加熱混合し、 残存するメタノールを除き、 室温まで 冷却して吸水軟膏を得た。 A water-absorbing ointment having the above composition (100 g) was previously heated to 70 ° C, and a solution prepared by heating 1 g of the compound obtained in Example 1 in 20 ml of methanol was added to the solution. Was. The mixture was heated and mixed at the same temperature for 10 minutes to remove residual methanol, and cooled to room temperature to obtain a water-absorbing ointment.
試験例 1 PDE IV阻害作用の測定 Test Example 1 Measurement of PDE IV inhibitory action
(1) ヒト脳由来 PDE 4D3をコードする遺伝子のクロ一ニング (1) Cloning of the gene encoding PDE 4D3 from human brain
ヒト脳 c DNAライブラリ一から P CR法で PDE 4D3をコードする遺伝子のク ローニングを行った。 1 ngの脳 QUICK-Clone TM c DNA (Clontech社) を錶型 とし、 emozらが報告 (FEBS Letters 384, 97-102 (1996) ) している PDE 4D3遺 伝 子 塩 基 配 列 を 参 考 に 作 製 し た プ ラ イ マ ー セ ッ ト : 5,_ccacgatagctgctcaaacaagag-3, (配列番号: 1)と 5'-atagaaaccccaagtccaataaac-3' (配列番号: 2) を各 20 pmolずつ添加し、 TaKaRa EX T aq (宝酒造) を使用 して、 PCR反応を MiniCycler™ (MJRESERCH社) にて行った (反応条件: 94°C で 0. 5分間、 55Tで 0. 5分間、 72°Cで 4分間を 30サイクル) 。 その PC R産物をァガロースゲル電気泳動し、 約 2. 4 kbの DNA断片を回収した。 その 断片を Pfu DNAポリメラーゼ(STRATAGENE社)で平滑化後、 Zero Blunt PCR Cloning Kit (Invitrogen社) を用いて、 PDE 4D3遺伝子をクローニングした。 From the human brain cDNA library, the gene encoding PDE 4D3 was cloned by the PCR method. Type 1 ng of brain QUICK-Clone ™ cDNA (Clontech) and refer to the PDE 4D3 gene base sequence reported by emoz et al. (FEBS Letters 384, 97-102 (1996)). To the primer set, 5, _ccacgatagctgctcaaacaagag-3, (SEQ ID NO: 1) and 5'-atagaaaccccaagtccaataaac-3 '(SEQ ID NO: 2) were added to each of the prepared primer sets. PCR was performed using MiniCycler ™ (MJRESERCH) using Taq (Takara Shuzo) (reaction conditions: 0.5 min at 94 ° C, 0.5 min at 55T, 4 min at 72 ° C). 30 cycles). The PCR product was subjected to agarose gel electrophoresis, and a DNA fragment of about 2.4 kb was recovered. After blunting the fragment with Pfu DNA polymerase (STRATAGENE), Zero Blunt PCR Cloning The PDE 4D3 gene was cloned using Kit (Invitrogen).
(2) 大腸菌発現ベクターの構築 (2) Construction of E. coli expression vector
上記(1)で得られたプラスミドを制限酵素 Ec oR I (宝酒造)で消化した後、 ァガロースゲル電気泳動して約 2. 4 kbの DNA断片を回収した。 その PNA断 片を制限酵素 Ec oR I (宝酒造) で消化後、 BAP (宝酒造) 処理した pGEX 4T-3 (フアルマシア社) とライゲーシヨンした。 得られた cDNA断片は、 配 列番号: 3で表わされる塩基配列を有しており、その塩基配列の第 74番目〜第 2 092番目に配列番号: 4で表わされる表わされるアミノ酸配列がコードされてい ることが分かった。この cDNA断片をライゲ一シヨン液を用いて大腸菌 BL 21 (フナコシ社)に形質転換し、 PDE4D3遺伝子を発現する大腸菌(Escherichia col i) BL 21ZPPDE4D3を取得した。 The plasmid obtained in the above (1) was digested with restriction enzyme EcoRI (Takara Shuzo), and then subjected to agarose gel electrophoresis to recover a DNA fragment of about 2.4 kb. The PNA fragment was digested with restriction enzyme EcoRI (Takara Shuzo) and ligated with pAPEX4T-3 (Pharmacia) treated with BAP (Takara Shuzo). The obtained cDNA fragment has the nucleotide sequence represented by SEQ ID NO: 3, and encodes the amino acid sequence represented by SEQ ID NO: 4 at the 74th to 2092th positions of the nucleotide sequence. I understood that it was. This cDNA fragment was transformed into Escherichia coli BL21 (Funakoshi) using a ligase solution to obtain Escherichia coli BL21ZPPDE4D3 expressing the PDE4D3 gene.
(3) 組換え型ヒト脳由来 PDE 4D3の大腸菌での発現と精製 (3) Expression and purification of recombinant human brain-derived PDE 4D3 in Escherichia coli
上記(2) で得られた大腸菌 BL 21/pPDE4D 3を用いて、 組換え型ヒト 脳由来 PDE 4D3を取得した。大腸菌での発現および精製は G ST Gene Fu s i on S y s t em (フアルマシア社) 添付のプロトコールに準じて行った。 そ の結果、 目的の約 76 k D aの組換え型ヒト脳由来 PDE 4D3を 1 Lの大腸菌培養液 から 34m g取得できた。 Using the Escherichia coli BL21 / pPDE4D3 obtained in (2) above, a recombinant human brain-derived PDE4D3 was obtained. Expression and purification in Escherichia coli were performed according to the protocol attached to GST Gene Fusion System (Pharmacia). As a result, 34 mg of the desired recombinant human brain-derived PDE 4D3 of about 76 kDa was obtained from 1 L of E. coli culture.
(4) PDE IV阻害作用の測定 (4) Measurement of PDE IV inhibitory action
96穴プレート (OPT Iプレート、 パッカード社) に緩衝液〔0. 5Μ T r i s— HC 1 (pH7. 5) 、 83mM MgC l 2、 17mM EGTA〕 10 1、 上記 (1) で得られた組換え型ヒト脳由来 PDE 4D3 (0. 0034mgZm 1 ) 10 し 超純水 65 1、 阻害剤サンプル 5 1、 [3H] c AMP 10 1を添加し、 30 にて 30分間反応した。 反応終了後、 SPA be ad s溶液 C 1 Smg/m 1 Yttrium silicate beads, 18mMZnS〇4〕 50 1を添カロ し、 約 20分間、 室温で放置した後、 シンチレ一ションカウンター (To p c o u n t、 パッカード社) を用いて測定した。 無添加の場合の放射活性 (1020 c p m) に対し、 組換え型ヒト脳由来 PDE4D3を添加した場合は、 28245 c pmの 放射活性を示した。 この反応に各種濃度の PDE IV の阻害剤であるロリプラム (BIOMOL Research Laboratories, Inc. )を添加することにより PDE活性は阻害され、 ロリプラムは約 100 nMでこの酵素反応を 50%阻害した。本アツセィ系を用いて、 本発明の化合物の組換え型ヒト脳由来 PDE阻害活性 (I C5()値) を測定した。 そ の結果を表 2に示す。 〔表 2〕 試験例 2 モルモットにおける抗原誘発気道狭窄抑制作用 96 well plates (OPT I plate, Packard) buffer [0. 5Μ T ris- HC 1 (pH7 . 5), 83mM MgC l 2, 17mM EGTA ] 10 1, recombinant obtained above (1) Human brain-derived PDE 4D3 (0.0034 mg Zm 1) 10, ultrapure water 65 1, inhibitor sample 51, [ 3 H] c AMP 101 were added, and reacted at 30 for 30 minutes. After completion of the reaction, SPA BE ad s solution C 1 Smg / m 1 Yttrium silicate beads, 18MMZnS_〇 4] 50 1 was added Caro, about 20 minutes, allowed to stand at room temperature, scintillation one Deployment counter (the To PCOUNT, Packard ) Was measured. In contrast to the radioactivity without addition (1020 cpm), the addition of recombinant human brain-derived PDE4D3 showed a radioactivity of 28245 cpm. PDE activity was inhibited by adding rolipram (BIOMOL Research Laboratories, Inc.), which is an inhibitor of PDE IV at various concentrations, to this reaction. Rolipram inhibited this enzyme reaction by 50% at about 100 nM. Using this Assay system, the PDE inhibitory activity (IC5 () value) of the compound of the present invention derived from recombinant human brain was measured. The results are shown in Table 2. (Table 2) Test Example 2 Antigen-induced airway constriction in guinea pigs
(1) ゥサギ抗卵白アルブミン (〇A) 血清の作製 (1) Preparation of Egret anti-ovalbumin (〇A) serum
白色ゥサギ (体重約 3 kg;ニュージーランドホワイト:北山ラベス) に 10%〇 A (Grade III、 シグマ社製) 溶液 0.5 mlとフロイト コンプリート アジュバント (和光純薬社製) 0.5 mlとの乳濁液 1.0 mlを筋肉内投与することにより免疫した。 この操作を 1週間ごとに 1回、計 4回繰り返した。最終免疫から 1週間後に全採血 した。採取した血液は室温にて 1時間以上静置した後、冷蔵室にてさらに一昼夜静 置した。 翌日、 血清部分を分取し、 遠心分離した後 (3000 rpm,10 min) 、 その上 清を抗血清として一 20°Cに保存した。 1.0 ml of an emulsion of white ゥ egret (body weight: about 3 kg; New Zealand White: Kitayama Labes) in 10% 〇 A (Grade III, Sigma) solution 0.5 ml and Freud Complete Adjuvant (Wako Pure Chemical) 0.5 ml Was immunized by intramuscular administration. This operation was repeated once a week, for a total of four times. One week after the final immunization, whole blood was collected. The collected blood was allowed to stand at room temperature for at least 1 hour, and then left to stand in a refrigerator overnight. The next day, the serum portion was separated, centrifuged (3000 rpm, 10 min), and the supernatant was stored at 120 ° C as an antiserum.
(2) 抗原誘発による気道狭窄反応 (2) Antigen-induced airway constriction response
気道狭窄反応は Konzett-Rossler法の変法にて測定した。体重 400〜500gのハー トレー系雄性モルモット(日本エスエルシ—、 静岡)をエーテル麻酔下にて、 8〜16 倍希釈した抗 OA血清 1.0 mlを静脈内投与し、 16〜24 時間後に実験に使用した。 ウレタン (1.2 g/kg,i.p.) (アルドリッチ社製) にて麻酔し、 気管に気管力ニュー レを揷管し、自発呼吸を止めるために、ガラミントリェチオダイド (lmg/kg,i.v.) (シグマ社製) を投与した。 動物は人工呼吸装置 (Harvard model 683) にて呼吸回 数 70回/分、 一回換気量 2〜3 mlならびに初期負荷圧 10 cmH20にて人工換気し、 気管力ニューレの側枝より気管内圧を、差圧トランスデューサーを介して測定した。 マレイン酸メピラミン (l.O mg/kg) (シグマ社製) およびプロブラノロ一ル (1.0 mg/kg) (シグマ社製) をガラミントリェチオダイド投与 2分後に静脈内投与し、 さ らに 2分後に OA抗原 (1.0 mg/kg) を静脈内投与し、 気道狭窄反応を惹起した。 実施例化合物 ling/kgを 25 %ジメチルァセトアミド、 25 %ポリエチレングリコー ル 400, 50%生理食塩液に溶解し、 抗原誘発の 5分前に静脈内投与した。 抑制率は コントロール群 (25 %ジメチルァセトアミド、 25%ポリエチレングリコール 400, 50%生理食塩液の混合液を静脈内投与) との比較により%抑制率を算出した。本発 明の化合物の抑制率を 〔表 3〕 に示した。 The airway constriction response was measured by a modification of the Konzett-Rossler method. Hartley male guinea pigs weighing 400-500 g (Nippon S.L.C., Shizuoka) were intravenously administered with 1.0 ml of anti-OA serum diluted 8 to 16 times under ether anesthesia, and used for experiments 16 to 24 hours later. . Anesthetize with urethane (1.2 g / kg, ip) (manufactured by Aldrich), inject tracheal force in the trachea, and in order to stop spontaneous breathing, garamine trietiodide (lmg / kg, iv) ( (Sigma). Animals breathe times several 70 times with an artificial respirator (Harvard model 683) / min, ventilator at a tidal volume 2 to 3 ml and the initial load pressure 10 cm H 2 0, tracheal pressure from the side branch of the tracheal force Nyure Was measured via a differential pressure transducer. Mepyramine maleate (lO mg / kg) (Sigma) and propranolol (1.0 mg / kg) (Sigma) were administered intravenously two minutes after the administration of gallamine trietiodide, and two minutes later. OA antigen (1.0 mg / kg) was administered intravenously to induce airway stenosis. Example compound ling / kg was dissolved in 25% dimethylacetamide, 25% polyethylene glycol 400, and 50% physiological saline, and administered intravenously 5 minutes before antigen induction. The inhibition rate was calculated by comparing with the control group (intravenous administration of a mixture of 25% dimethylacetamide, 25% polyethylene glycol 400, and 50% saline). Table 3 shows the inhibition rates of the compounds of the present invention.
〔表 3〕 産業上の利用可能性 (Table 3) Industrial applicability
本発明のフロイソキノリン誘導体は、 優れた PDE IV阻害作用を有しており、 炎 症性疾患、 喘息、 慢性閉塞性肺疾患、 慢性関節リウマチ、 自己免疫疾患、 うつ病、 アルツハイマー型痴呆症、 記憶障害、 糖尿病、 動脈硬化などの予防 ·治療剤として 有用である。 The furoisoquinoline derivative of the present invention has an excellent PDE IV inhibitory action, and is used for inflammatory disease, asthma, chronic obstructive pulmonary disease, rheumatoid arthritis, autoimmune disease, depression, Alzheimer's disease, memory It is useful as a prophylactic and therapeutic agent for disorders, diabetes, arteriosclerosis, etc.
Claims
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001190338 | 2001-06-22 | ||
| JP2001-190338 | 2001-06-22 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2003000697A1 true WO2003000697A1 (en) | 2003-01-03 |
Family
ID=19029122
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2002/006158 Ceased WO2003000697A1 (en) | 2001-06-22 | 2002-06-20 | Furoisoquinoline derivative, process for producing the same, and use |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2003000697A1 (en) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9120788B2 (en) | 2013-02-19 | 2015-09-01 | Pfizer Inc. | Azabenzimidazole compounds |
| US9399094B2 (en) | 2006-06-06 | 2016-07-26 | Novo Nordisk A/S | Assembly comprising skin-mountable device and packaging therefore |
| US9598421B2 (en) | 2014-08-06 | 2017-03-21 | Pfizer Inc. | Imidazopyridazine compounds |
| US10131669B2 (en) | 2014-07-24 | 2018-11-20 | Pfizer Inc. | Pyrazolopyrimidine compounds |
| CN113717185A (en) * | 2021-08-19 | 2021-11-30 | 云南省烟草农业科学研究院 | Quinoline alkaloid compound with antibacterial activity in cigar rhizome and preparation method and application thereof |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07267961A (en) * | 1994-03-30 | 1995-10-17 | Taisho Pharmaceut Co Ltd | Benzofuro [3,2-d pyrimidin-4-one derivative |
| WO1996036624A1 (en) * | 1995-05-19 | 1996-11-21 | Kyowa Hakko Kogyo Co., Ltd. | Oxygen-containing heterocyclic compounds |
| WO1999033460A1 (en) * | 1997-12-24 | 1999-07-08 | Bristol-Myers Squibb Company | Acyl guanidine sodium/proton exchange inhibitors and method |
| WO2001070746A1 (en) * | 2000-03-23 | 2001-09-27 | Takeda Chemical Industries, Ltd. | Furoisoquinoline derivatives, process for producing the same and use thereof |
| WO2002004455A2 (en) * | 2000-07-11 | 2002-01-17 | Albany Molecular Research, Inc | 4-phenyl substituted tetrahydroisoquinolines and therapeutic use thereof |
-
2002
- 2002-06-20 WO PCT/JP2002/006158 patent/WO2003000697A1/en not_active Ceased
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07267961A (en) * | 1994-03-30 | 1995-10-17 | Taisho Pharmaceut Co Ltd | Benzofuro [3,2-d pyrimidin-4-one derivative |
| WO1996036624A1 (en) * | 1995-05-19 | 1996-11-21 | Kyowa Hakko Kogyo Co., Ltd. | Oxygen-containing heterocyclic compounds |
| WO1999033460A1 (en) * | 1997-12-24 | 1999-07-08 | Bristol-Myers Squibb Company | Acyl guanidine sodium/proton exchange inhibitors and method |
| WO2001070746A1 (en) * | 2000-03-23 | 2001-09-27 | Takeda Chemical Industries, Ltd. | Furoisoquinoline derivatives, process for producing the same and use thereof |
| WO2002004455A2 (en) * | 2000-07-11 | 2002-01-17 | Albany Molecular Research, Inc | 4-phenyl substituted tetrahydroisoquinolines and therapeutic use thereof |
Non-Patent Citations (3)
| Title |
|---|
| BULLETIN SOCIETY CHIM. FR., vol. 11, 1972, pages 4201 - 4208 * |
| CHEMICAL ABSTRACTS, vol. 78, 1973, Columbus, Ohio, US; abstract no. 71948M, RENE ROYER ET AL.: "Benzofurans. L. Access to furoisoquinolines" page 457-458; XP002957192 * |
| SHIOTANI SHUNSAKU: "Furopyridines. IV. Unexpected dimerization of 5-methyl-4,5,6,7-tetrahydrofuro(3,2-c)- and 6-methyl-4,5,6,7-tetrahydrofuro(2,3-c)pyridine by acidic hydrolysis", J. HETEROCYCL. CHEMICAL, vol. 23, no. 1, 1986, pages 233 - 240, XP002957193 * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9399094B2 (en) | 2006-06-06 | 2016-07-26 | Novo Nordisk A/S | Assembly comprising skin-mountable device and packaging therefore |
| US9120788B2 (en) | 2013-02-19 | 2015-09-01 | Pfizer Inc. | Azabenzimidazole compounds |
| US9815832B2 (en) | 2013-02-19 | 2017-11-14 | Pfizer Inc. | Azabenzimidazole compounds |
| US10131669B2 (en) | 2014-07-24 | 2018-11-20 | Pfizer Inc. | Pyrazolopyrimidine compounds |
| US9598421B2 (en) | 2014-08-06 | 2017-03-21 | Pfizer Inc. | Imidazopyridazine compounds |
| US10077269B2 (en) | 2014-08-06 | 2018-09-18 | Pfizer Inc. | Imidazopyridazine compounds |
| US10669279B2 (en) | 2014-08-06 | 2020-06-02 | Pfizer Inc. | Imidazopyridazine compounds |
| CN113717185A (en) * | 2021-08-19 | 2021-11-30 | 云南省烟草农业科学研究院 | Quinoline alkaloid compound with antibacterial activity in cigar rhizome and preparation method and application thereof |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60125026T2 (en) | FLUOROISOCHINOLINE DERIVATIVES, METHOD FOR THEIR PREPARATION AND THEIR USE | |
| EP2380881B1 (en) | Novel bicyclic heterocyclic compound | |
| TWI296625B (en) | Novel cyclic amide derivatives | |
| US10676438B2 (en) | KCNQ2-5 channel activator | |
| TW201307284A (en) | FAAH inhibitors | |
| TW401299B (en) | Use of 5-substituted pyridine-and hexahydroquinoline-3-carboxylic acid derivatives for the treatment of disorders of the central nervous system, novel active compounds, a process for their preparation and their use | |
| HUP0104204A2 (en) | Pyrazolopyridine derivatives as cox-2 inhibitors, process for their preparation and pharmaceutical compositions thereof | |
| CA3157798A1 (en) | 6-membered heteroarylaminosulfonamides for treating diseases and conditions mediated by deficient cftr activity | |
| ZA200603181B (en) | 3-(4-aminophenyl) thienopyrimid-4-one derivatives as MCH R1 antagonists for the treatment of obesity, diabetes, depression and anxiety | |
| CN102869647A (en) | Sulfone compounds as 5-HT6 receptor ligands | |
| WO2003000697A1 (en) | Furoisoquinoline derivative, process for producing the same, and use | |
| ES2866324T3 (en) | Derivatives of 1- (1-hydroxy-2,3-dihydro-1H-inden5-yl) -urea and similar compounds as activators of the KCNQ2-5 channel for the treatment of dysuria | |
| KR20050063747A (en) | 1-substituted-1,2,3-triazole derivatives, their intermediates, and method for production thereof | |
| WO2004011470A1 (en) | Furoisoquinoline derivative and use thereof | |
| JP2003171381A (en) | Entry inhibitory agent | |
| TW200900408A (en) | Fused pyridine derivative | |
| TW200836726A (en) | Pyrrolopyridine-2-carboxamide derivatives, preparation thereof and therapeutic use thereof | |
| WO2001014385A1 (en) | Dihydrobenzofuran derivatives, process for the preparation thereof and agents | |
| US20250255848A1 (en) | Substituted 6,7-dihydro-5h-benzo[7]annulene derivatives, processes for their preparation and therapeutic uses thereof | |
| JP2003073380A (en) | Furoisoquinoline derivative, method for producing the same and use | |
| JP2004067690A (en) | Furoisoquinoline inducer and its application | |
| TW202513551A (en) | Inhibitors of trek (twik related k+ channels) channel function | |
| TW202410897A (en) | Biaryl ether urea compounds | |
| JPH0517441A (en) | Spiroisoindorin compound, preparation thereof, drug containing it for curing neurosis and intermediate for preparation | |
| JPH09118660A (en) | Aromatic hydroxamic acid derivative, production and agent |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AE AG AL AM AT AU AZ BA BB BG BR BY BZ CA CH CN CO CR CU CZ DE DK DM DZ EC EE ES FI GB GD GE GH GM HR HU ID IL IN IS JP KE KG KR KZ LC LK LR LS LT LU LV MA MD MG MK MN MW MX MZ NO NZ OM PH PL PT RO RU SD SE SG SI SK SL TJ TM TN TR TT TZ UA UG US UZ VN YU ZA ZM ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): GH GM KE LS MW MZ SD SL SZ TZ UG ZM ZW AM AZ BY KG KZ MD RU TJ TM AT BE CH CY DE DK ES FI FR GB GR IE IT LU MC NL PT SE TR BF BJ CF CG CI CM GA GN GQ GW ML MR NE SN TD TG |
|
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| REG | Reference to national code |
Ref country code: DE Ref legal event code: 8642 |
|
| 122 | Ep: pct application non-entry in european phase | ||
| NENP | Non-entry into the national phase |
Ref country code: JP |