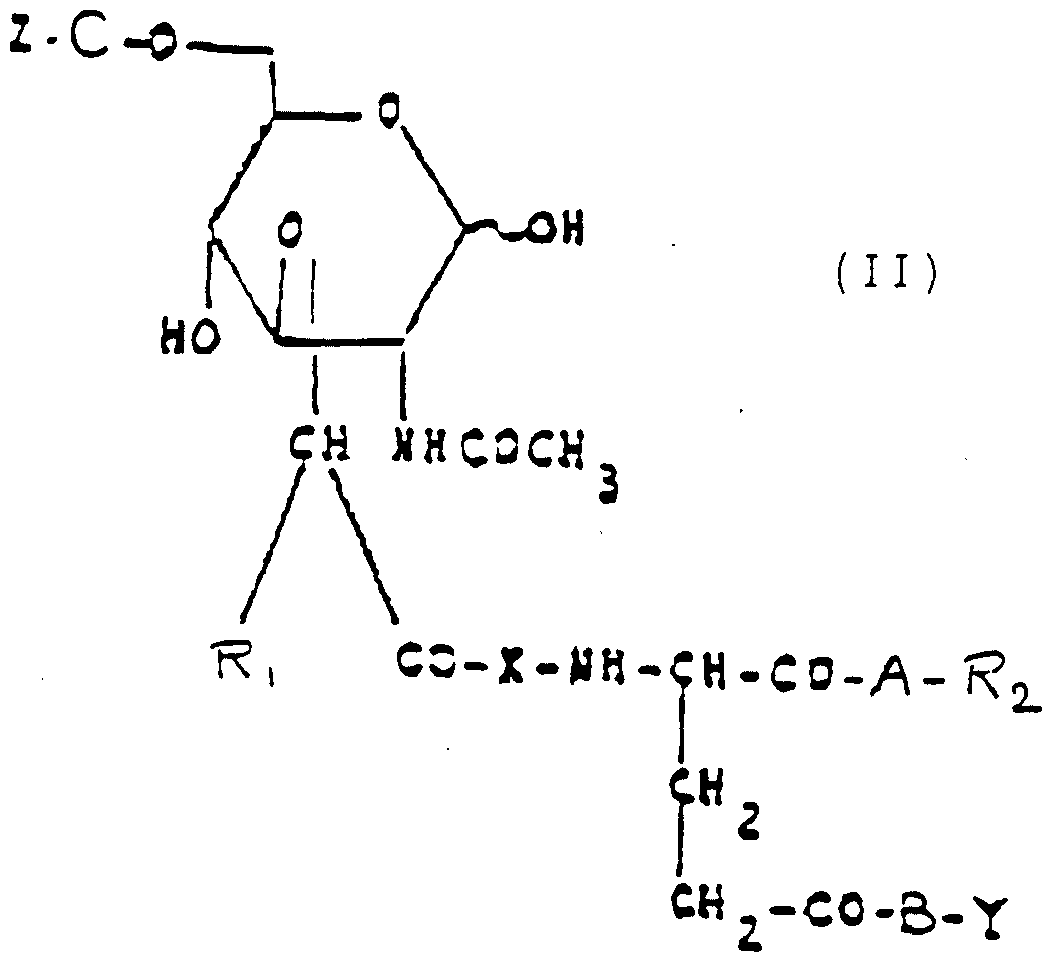WO1993025236A1 - Humoral immunity and cell mediation adjuvant composition inducing no response to auto-antigenic determinants - Google Patents
Humoral immunity and cell mediation adjuvant composition inducing no response to auto-antigenic determinants Download PDFInfo
- Publication number
- WO1993025236A1 WO1993025236A1 PCT/FR1993/000569 FR9300569W WO9325236A1 WO 1993025236 A1 WO1993025236 A1 WO 1993025236A1 FR 9300569 W FR9300569 W FR 9300569W WO 9325236 A1 WO9325236 A1 WO 9325236A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- antigen
- carbon atoms
- composition according
- response
- adjuvant
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/39—Medicinal preparations containing antigens or antibodies characterised by the immunostimulating additives, e.g. chemical adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/5555—Muramyl dipeptides
Definitions
- ACF Freund's Complete Adjuvant
- MDP N-acetyl-muramyl-L-alanyl-D-isoglutamine
- MurNac- L-Ala-D-isoGln also known as "Muramyl-dipeptide” or "MDP”.
- MDP N-acetyl-muramyl-L-alanyl-D-isoglutamine
- MurNac- L-Ala-D-isoGln also known as "Muramyl-dipeptide” or "MDP”.
- MDP N-acetyl-muramyl-L-alanyl-D-isoglutamine
- the invention therefore relates more particularly to a pharmaceutical composition using MDP-DD-GDP for its application as an adjuvant capable of inducing a selective response vis-à-vis antigens foreign to the organism of the host (heteroantigens) in the absence of any induction of autoimmune disease linked to a response to autoantigenic determinants.
- this action may manifest itself during administration in the form of a single-phase aqueous solution, it is preferable to use it in the form of a two-phase, injectable dispersion, based on an aqueous solution. and a pharmaceutically acceptable hydrophobic component. This constituent is often lipid in nature.
- the pharmaceutically acceptable hydrophobic constituent intervening or having to intervene in the constitution of the above-mentioned two-phase dispersion is chosen in such a way that its presence within the dispersion containing the MDP-DD-GDP induces a reinforcement of the humoral response or of the cell-mediated response, or preferably both, in the recipient host vis-à-vis the vaccinating antigen administered to the host in the presence of MDP-DD-GDP.
- This hydrophobic constituent will most often consist of a mineral oil, for example paraffin oil, or vegetable oil.
- Water-in-vegetable oil emulsions which can be used for the constitution of adjuvant compositions are described, for example in French patent n ° 7504003.
- the hydrophobic compound can also be the basis of lipids capable of forming liposomes. Reference is again made to European patent No. 0165123 already identified above, with regard to the constitution of such liposomes. It can also be formed from a hydrophobic detergent.
- the hydrophobic compound can also be based on polyoxylene-polyoxypropylene polymers, such as those known under the trademark PLURONIC and / or polyoxyethylene esters of sorbitan, in particular those marketed under the trademark TWEEN 20.
- the hydrophobic compound can also be formed by microspheres, having sizes normally less than 7 microns.
- the invention is of particular interest when it is applied to the induction of a vaccinating and more generally immunogenic response with regard to an antigen which is not devoid of antigenic determinants characteristic of the self or capable of crossing immunologically with these antigenic determinants.
- antigen which is not devoid of antigenic determinants characteristic of the self or capable of crossing immunologically with these antigenic determinants.
- These can either belong to the vaccinating antigen, or be associated with it under conditions which prevent a complete prior purification of the vaccinating antigen. As we have seen, this situation can arise each time that the vaccinating antigen has been produced, for example in human or animal cells (for example inactivated viruses or fractions of virus cultivated in these cells).
- the invention finds a particularly advantageous application in the constitution - or for the production - of vaccinating pharmaceutical compositions containing an inactivated HIV virus, or an anti-tumor antigen or also certain parasitic antigens capable of giving rise to cross-reactions with certain host structures.
- the invention finds an advantageous application in combination with any virus or fraction of virus obtained by culture in human or mammalian cells, or also with any antigen whose conditions of production introduce a risk of contamination by structural elements. belonging to human or mammalian cells, in particular cells of the white line.
- the pharmaceutical composition as it has just been defined can be prepared extemporaneously. Furthermore, if the antigen is often administered at the same time as the other constituents of the pharmaceutical composition, the invention cannot be limited to this specific case.
- the administration of MDP-DD-GDP in the form of a two-phase dispersion on the one hand, and that of the vaccinating antigen on the other hand, can also be done in a non-simultaneous manner, the only condition being that the time intervals which flow between these separate administrations are such that the munological adjuvant effect of the preparation containing MDP-DD-GDP against the vaccinating antigen can be manifested.
- composition covers both compositions formed from the various named constituents and found in a premixing stage, that all of these different constituents taken in isolation but combined at the time (s) of their respective administration (s) to patients (humans or animals) under conditions allowing obtaining the above-mentioned results.
- the relative proportions in the emulsion of the aqueous solution and of the hydrophobic component are chosen such that an emulsion which is sufficiently stable, in particular at the time of administration, is capable of being formed between the aqueous solution and the hydrophobic component.
- the hydrophobic constituent consists of a mineral oil
- the proportion of the latter will preferably be from 50% to 90% (volume / volume) relative to the entire mixture.
- the basic protein of myelin is an auto ⁇ antigen known for its capacity to induce an immunological reaction vis-à-vis the myelin present in the spinal cord and the brain.
- the animals are Hartley male guinea pigs. They receive in the pads of the hind legs, 50 ⁇ g of protein basic.
- the negative controls receive the antigen in an emulsion of Freund's Incomplete Adjuvant (oil only) and the positive controls in an emulsion of Complete Adjuvant (oil + mycobacteria).
- the experimental batches receive the incomplete adjuvant added with 50 ⁇ g MDP-GDP (Mur-Nac-L-Ala-D-isoGln- GDP) or MDP-Thr-GDP (Mur-Nac-L-Thr-D-isoGln- GDP) or MDP-DD-GDP.
- the animals are weighed weekly, clinical signs appear after 10 days and the animals die between the 12th and 19th days. After 3 weeks, cuti-reactions are practiced on healthy animals and on animals that have survived the disease. Blood is also taken by cardiac puncture to test for antibodies by ELISA.
- Table 1 gives indications on the number of animals of each group which was affected by clinical signs characteristic of allergic encephalomyelitis: weight loss, paralysis of the hind legs then generalized, incontinence. the number of dead animals per group, the anti-myelin basic protein antibody titers, and the presence of a positive cuti-reaction (when tested) in the survivors. NT stands for "untested”.
- mice 25 g female Swiss mice receive physiological water via the venous route, either alone (negative control) or containing lipophilic derivatives of MDP at a dose of 300 ⁇ g. Two hours later they still receive 25 ⁇ g of endotoxin (lipopolysaccharide from S. Enderitidis) by vein. It is seen from Table 3 that MDP-GDP sensitized mice to the administration of endotoxin unlike MDP-DD-GDP and MDP-Thr-GDP.
- the lipophilic derivatives were tested (according to the method described in the European Pharmacopoeia) for their pyrogenic activity and the MDP-DD-GDP was found to be 10 times less pyrogenic than the MDP-GDP.
- MDP-DD-GDP can be replaced by analogous structures in which the first amino acid of the peptide chain has a D configuration (in other words a muramyl peptide type DD, preferably a product of this type having a chain lipophilic).
- muramyl-peptides of type DD capable of being used in the pharmaceutical compositions according to the invention, mention will be made of those which would not induce autoimmune manifestations in the above-mentioned experimental protocols and which would correspond to the following general formula :
- R 1 is H or CH3.
- R 2 is a hydrogen atom, an NH2 group, or a group W consisting of a hydrocarbon chain comprising from 1 to 4 carbon atoms.
- X is an aminoacyl residue of configuration D comprising: alanyl, valyl, isoleucyl, leucyl, seryl, threonyl, prolyl, methionyl.
- Y has the same meaning as R 2 or is a hydrocarbon chain of linear or branched structure comprising from 4 to 90 carbon atoms, or also a group -CH 2 -CHO (R 3 ) -CH20 (R 4 ), with R 3 and R ⁇ being hydrocarbon chains, identical or different, comprising from 8 to 20 carbon atoms.
- A, B and C are, with regard to each of them, independently of each other, either a direct bond, or an oxygen atom, or a structure -NH-CHCR ⁇ -CO-, corresponding to all aminoacyl of configuration L, with R5 being an aminoacyl residue characteristic of one of the 20 natural amino acids.
- Z is a hydrogen atom or else is a hydrocarbon acyl group of linear or branched structure comprising from 1 to 90 carbon atoms, or else a CO-CHO- (R 3 ) -CH 2 0 (R 4 ) group, with R 3 and R 4 being hydrocarbon chains, identical or different, comprising from 8 to 20 carbon atoms.
- the invention relates to a process for the preparation of a pharmaceutical composition capable of preventing the induction of an autoimmune disease linked to a response towards autoantigenic determinants, when this composition contains a principle active capable of exerting a selective adjuvant action of the immunity implementing a humoral response or a response mediated by cell, preferably both at the same time, against determined antigens, characterized in that the adjuvant principle of this pharmaceutical composition consists of a muramyl-peptide of formula I or II.
- the invention therefore also relates to compositions of the genus in question, containing an adjuvant active principle which is not free from auto-antigenic determinants, associated with a muramyl-peptide of formula I or of general formula II.
- the MDP-DD-GDP or the compounds of general formula II appear adjuvant-active vis-à-vis hetero-antigens and adjuvant-inactive (or passive) vis-à-vis auto ⁇ antigens.
- the pharmaceutical composition which is the subject of the patent makes it possible not only to obtain an immune response directed only against antigens distinct from the self but to prevent the triggering of an autoimmune disease linked to the autoantigenic determinants (or elements of the self) possibly present in the vaccinating pharmaceutical composition.
- composition according to the invention is meant both a composition containing simultaneously or in a mixture the heterogeneous against which protection is sought, if necessary not devoid of auto-antigens, on the one hand, and the compound of formula I or of general formula II, on the other hand, that any form of association intended to allow the administrations of the two principles at distinct times, the time interval separating these distinct moments being however sufficiently short so that these two principles are still able to interact with each other in vivo as described.
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Mycology (AREA)
- General Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
Description
COMPOSITION ADJUVANTE DE L'IMMUNITE HUMORALE ET A MEDIATION CELLULAIRE N'INDUISANT PAS DE REPONSE VIS¬ A-VIS DE DETERMINANTS AUTO-ANTIGENIQUESADJUVANT COMPOSITION OF HUMOR AND CELL MEDIATION IMMUNITY WITHOUT RESULTING IN RESPECT OF SELF-ANTIGENIC DETERMINANTS
L'adjuvant Complet de Freund (ACF) est le plus fort immuno-adj vant connu capable d'augmenter les réponses immunitaires spécifiques humorales et à médiation cellulaire vis-à-vis d'un antigène. Il se compose de mycobactéries administrées dans une émulsion eau dans l'huile minérale, l'emploi de cet adjuvant en clinique humaine ou vétérinaire est exclu, car il induit des réactions secondaires importantes, notamment induction de polyarthrites et sensibilisation à la tuberculine. Il est déjà connu que l'on peut reproduire les effets adjuvants sans les effets secondaires des mycobactéries en les remplaçant par une petite molécule de 500 daltons, la N-acétyl- muramyl-L-alanyl-D-isoglutamine, souvent abréviée comme MurNac-L-Ala-D-isoGln, encore dénommée "Muramyl-dipeptide" ou "MDP". Cette molécule consiste en un élément de structure de la paroi mycobactérienne. De nombreux analogues du MDP présentent aussi des activités adjuvantes comme le MDP, ils peuvent être produits par synthèse chimique. Ces analogues, souvent dénommés "Muramyl-peptides" sont en général dérivés du MDP par l'une ou plusieurs des modifications suivantes :Freund's Complete Adjuvant (ACF) is the strongest known immuno-adjuvant capable of increasing specific humoral and cell-mediated immune responses to an antigen. It is composed of mycobacteria administered in a water in mineral oil emulsion, the use of this adjuvant in human or veterinary clinic is excluded, because it induces significant side reactions, in particular induction of polyarthritis and sensitization to tuberculin. It is already known that we can reproduce the adjuvant effects without the side effects of mycobacteria by replacing them with a small molecule of 500 daltons, N-acetyl-muramyl-L-alanyl-D-isoglutamine, often abbreviated as MurNac- L-Ala-D-isoGln, also known as "Muramyl-dipeptide" or "MDP". This molecule consists of a structural element of the mycobacterial wall. Many analogs of MDP also exhibit adjuvant activities like MDP, they can be produced by chemical synthesis. These analogues, often called "Muramyl-peptides" are generally derived from MDP by one or more of the following modifications:
- remplacement du résidu du L-alanyle de la chaîne peptidique par un autre résidu L-aminoacyle ou par le résidu glycyle, substitutions sur l'un au moins des groupes carboxyle du résidu D-glutamyle, substitutions sur les positions 1, 4 et 6 du groupe muramyle. Ces substitutions s'accompagnent parfois d'une modulation des propriétés adjuvantes du MDP. Par exemple les dérivés lipophiles du Muramyl peptide sont souvent de plus forts adjuvants que les dérivés hydrophiles.- replacement of the L-alanyl residue of the peptide chain by another L-aminoacyl residue or by the glycyl residue, substitutions on at least one of the carboxyl groups of the D-glutamyl residue, substitutions at positions 1, 4 and 6 of the muramyl group. These substitutions are sometimes accompanied by modulation of the adjuvant properties of MDP. For example, the lipophilic derivatives of the Muramyl peptide are often stronger adjuvants than the hydrophilic derivatives.
D'autres types de modifications de la molécule de MDP peuvent cependant altérer le spectre de ses propriétés biologiques de façon plus considérable. Par exemple —et à la notable exception de la N-acétyl- muramyl-L-( éthyl)alanyl-D-isoglutamine— des substi¬ tutions du résidu L-alanyle de la chaîne peptidique s'accompagnent le plus souvent de la perte des propriétés adjuvantes du muramyl peptide modifié correspondant. Le remplacement dans le MDP du résidu L-alanyle par un résidu D-alanyle, pour obtenir le "MDP-DD", entraîne même 1'apparition de propriétés contraires. Cette molécule est alors douée de propriétés anti-adjuvantes ou immuno-suppressives.Other types of modifications to the MDP molecule can, however, alter the spectrum of its biological properties to a greater extent. For example — and with the notable exception of N-acetyl-muramyl-L- (ethyl) alanyl-D-isoglutamine— substitutions of the L-alanyl residue of the peptide chain are most often accompanied by the loss of adjuvant properties of the corresponding modified muramyl peptide. The replacement in MDP of the L-alanyl residue by a D-alanyl residue to obtain "MDP-DD" even results in the appearance of contrary properties. This molecule is then endowed with anti-adjuvant or immuno-suppressive properties.
Mais pour en revenir aux muramyl peptides doués de propriétés adjuvantes, il est également connu que leur administration avec un antigène dans une émulsion eau dans l'huile minérale permet l'obtention de très fortes réponses spécifiques humorales et à médiation cellulaire. Cette activité est spécialement recherchée dans le cas de certains vaccins prophylactiques ou thérapeutiques destinés à lutter contre des maladies spécialement graves. Parmi ces maladies, on peut citer des maladies virales comme le SIDA, et différents types de cancers dont on sait déterminer les antigènes spécifiques de la tumeur. Dans tous les cas cités, il est nécessaire d'induire de hauts niveaux de réponse humorale et aussi à médiation cellulaire. Ces niveaux de réponses pourraient être obtenus en utilisant de l'Adjuvant Complet de Freund ou plutôt des dérivés lipophiles du MDP, en émulsion eau dans l'huile afin d'éviter les effets secondaires dûs à l'adjuvant complet de Freund. Mais ici s'ajoute un risque qui est lié à la composition des préparations vaccinantes. En effet, celles-ci peuvent contenir des auto-antigènes, c'est-à-dire des structures susceptibles de provoquer une maladie auto-immune. C'est ainsi que : a) le virus du SIDA utilisé dans certains vaccins a été cultivé sur des cellules humaines ou des lignées cellulaires dérivées de cellules humaines. Même après purification il y a un risque potentiel de présence d'auto-antigènes dans la préparation vaccinale. ) certains "vaccins anti-cancer", qui font déjà l'objet d'essais cliniques, contiennent des structures comportant à la fois des déterminants antigéniques spécifiques de la tumeur et des déterminants antigéniques du tissu naturel de l'hôte.But to return to muramyl peptides endowed with adjuvant properties, it is also known that their administration with an antigen in a water-in-mineral oil emulsion makes it possible to obtain very strong specific humoral and cell-mediated responses. This activity is especially sought after in the case of certain prophylactic or therapeutic vaccines intended to fight against especially serious diseases. Among these diseases, mention may be made of viral diseases such as AIDS, and various types of cancer, the specific antigens of which can be determined for the tumor. In all the cases cited, it is necessary to induce high levels of humoral and also cell-mediated response. These response levels could be obtained by using Freund's Complete Adjuvant or rather lipophilic derivatives of MDP, in water-in-oil emulsion in order to avoid the side effects due to the adjuvant. complete by Freund. But here is added a risk which is linked to the composition of the vaccine preparations. Indeed, these can contain auto-antigens, that is to say structures capable of causing an autoimmune disease. Thus: a) the AIDS virus used in certain vaccines has been cultured on human cells or cell lines derived from human cells. Even after purification there is a potential risk of the presence of autoantigens in the vaccine preparation. ) certain "cancer vaccines", which are already the subject of clinical trials, contain structures comprising both tumor-specific antigenic determinants and antigenic determinants of the host's natural tissue.
Or c'est dans le cas de ces pathologies particulièrement graves que le clinicien voudrait être à même d'induire chez l'hôte de fortes réponses humorales et à médiation cellulaire, mais à 1*encontre des seuls déterminants antigéniques spécifiques des agents pathogènes qui en sont la cause (cas du SIDA) ou des déterminants antigéniques tumoraux. De telles réponses sont spécialement recherchées dans le cas de certains vaccins prophylactiques ou thérapeutiques destinés à lutter contre des maladies spécialement graves, parmi lesquelles des maladies virales comme le SIDA, et différents types de cancers, lorsque l'on sait identifier les antigènes spécifiques de la tumeur. Mais dans ces exemples on voit que si l'on induit une très forte réponse immunitaire vis-à-vis des structures susceptibles d'évoquer une réponse protectrice, on risque d'induire également une réaction auto-immune liée à une réaction vis-à-vis des structures de l'hôte présentes dans la composition administrée contenant le vaccin. C'est ce que l'on observe effectivement dans des modèles expérimentaux où des auto-antigènes sont administrés avec un adjuvant de type "Adjuvant Complet de Freund", ou un adjuvant incomplet de Freund (AIF) contenant du MurNac-L-Ala-D-isoGln 1,2-dipalmitoyl-sn-glycérol ou "MDP-GDP".However, it is in the case of these particularly serious pathologies that the clinician would like to be able to induce strong humoral and cell-mediated responses in the host, but against the only specific antigenic determinants of pathogens are the cause (case of AIDS) or tumor antigenic determinants. Such responses are specially sought in the case of certain prophylactic or therapeutic vaccines intended to combat especially serious diseases, including viral diseases such as AIDS, and different types of cancer, when it is possible to identify the specific antigens of the tumor. But in these examples we see that if we induce a very strong immune response vis-à-vis structures capable of evoking a protective response, we risk also inducing an autoimmune reaction linked to a reaction towards -vis host structures present in the administered composition containing the vaccine. This is what we actually observe in experimental models where autoantigens are administered with an adjuvant of the "Freund Complete Adjuvant" type, or an incomplete Freund adjuvant (AIF) containing MurNac-L-Ala-D-isoGln 1,2-dipalmitoyl-sn-glycerol or " MDP-GDP ".
C'est pourquoi il est tout à fait inattendu qu'une molécule de la famille des Muramyl-peptides lipophiles se soit révélée douée de propriétés uniques. En effet le N-acétyl-muramyl-D-alanyl- D-(7-[Sn dipalmytoyl]glycérόl) isoglutamine (Mur- Nac-D-Ala-DIsoGln 1,2-dipalmrtoyl-sn-glycérol ou MDP- DD-GDP) est aussi fortement adjuvant que les autres Muramyl-peptides lipophiles, en particulier lorsqu'il est administré sous forme de dispersion eau dans l'huile et quand son action s'exerce vis-à-vis de déterminants antigéniques étrangers à l'hôte. En revanche, même lorsqu'il est administré dans une émulsion eau-dans-l'huile, il n'induit pas de maladie auto-immune liée à une réponse vis-à-vis de déterminants auto-antigéniques.This is why it is quite unexpected that a molecule of the family of lipophilic Muramyl-peptides has been shown to have unique properties. Indeed N-acetyl-muramyl-D-alanyl- D- (7- [Sn dipalmytoyl] glycérόl) isoglutamine (Mur- Nac-D-Ala-DIsoGln 1,2-dipalmrtoyl-sn-glycerol or MDP- DD-GDP ) is as strongly adjuvant as the other lipophilic Muramyl-peptides, in particular when it is administered in the form of a water-in-oil dispersion and when its action is exerted against antigenic determinants foreign to the host. On the other hand, even when administered in a water-in-oil emulsion, it does not induce autoimmune disease linked to a response towards autoantigenic determinants.
Le MDP-DD-GDP, de formule :MDP-DD-GDP, of formula:
est une molécule en soi connue. Il est fait plus spécifiquement référence au brevet européen n°85.400921.4/0165123 dans lequel est décrit un procédé pour sa préparation. Ce brevet était plus particulièrement relatif à une classe de molécules, parmi lesquelles le MDP-DD-GDP, choisies en raison de leur action d'activation des macrophages. is a molecule known per se. More specifically, reference is made to European Patent No. 85.400921.4 / 0165123 in which a process for its preparation is described. This patent related more particularly to a class of molecules, among which MDP-DD-GDP, chosen because of their macrophage activation action.
L'invention concerne donc plus particulièrement une composition pharmaceutique mettant en oeuvre le MDP-DD-GDP pour son application en tant qu'adjuvant susceptible d'induire une réponse sélective vis-à-vis d'antigènes étrangers à l'organisme de l'hôte (hétéro-antigènes) en l'absence de toute induction de maladie auto-immune liée à une réponse vis-à-vis de déterminants auto-antigéniques. Bien que cette action puisse se manifester à l'occasion d'une administration sous forme d'une solution aqueuse monophasée, il est préférable de le mettre en oeuvre sous la forme d'une dispersion biphasée, injectable, à base d'une solution aqueuse et d'un constituant hydrophobe pharmaceutiquement acceptable. Ce constituant est souvent de nature lipidique. Mais plus généralement le constituant hydrophobe pharmaceutiquement acceptable intervenant ou devant intervenir dans la constitution de la dispersion biphasée susdite est choisi de telle façon que sa présence au sein de la dispersion contenant le MDP-DD-GDP induise un renforcement de la réponse humorale ou de la réponse à médiation cellulaire, ou de préférence des deux à la fois, chez l'hôte receveur vis-à-vis de l'antigène vaccinant administré à l'hôte en présence du MDP-DD-GDP.The invention therefore relates more particularly to a pharmaceutical composition using MDP-DD-GDP for its application as an adjuvant capable of inducing a selective response vis-à-vis antigens foreign to the organism of the host (heteroantigens) in the absence of any induction of autoimmune disease linked to a response to autoantigenic determinants. Although this action may manifest itself during administration in the form of a single-phase aqueous solution, it is preferable to use it in the form of a two-phase, injectable dispersion, based on an aqueous solution. and a pharmaceutically acceptable hydrophobic component. This constituent is often lipid in nature. But more generally the pharmaceutically acceptable hydrophobic constituent intervening or having to intervene in the constitution of the above-mentioned two-phase dispersion is chosen in such a way that its presence within the dispersion containing the MDP-DD-GDP induces a reinforcement of the humoral response or of the cell-mediated response, or preferably both, in the recipient host vis-à-vis the vaccinating antigen administered to the host in the presence of MDP-DD-GDP.
Ce constituant hydrophobe consistera le plus souvent en une huile minérale, par exemple huile de paraffine, ou végétale. Des émulsions eau dans l'huile végétale utilisables pour la constitution de compositions adjuvantes sont décrites, par exemple dans le brevet français n°7504003. Le composé hydrophobe peut aussi être à la base de lipides susceptibles de former des liposomes. Référence est de nouveau faite au brevet européen n°0165123 déjà identifié plus haut, pour ce qui concerne la constitution de tels liposomes. Il peut encore être formé d'un détergent hydrophobe. Le composé hydrophobe peut aussi être à base de polymères polyoxylène- polyoxypropylène, tels que ceux connus sous la marque PLURONIC et/ou d'esters polyoxyéthyléniques du sorbitane, notamment de ceux commercialisés sous la marque TWEEN 20. Le composé hydrophobe peut également être formé par des microsphères, ayant des tailles normalement inférieures à 7 microns.This hydrophobic constituent will most often consist of a mineral oil, for example paraffin oil, or vegetable oil. Water-in-vegetable oil emulsions which can be used for the constitution of adjuvant compositions are described, for example in French patent n ° 7504003. The hydrophobic compound can also be the basis of lipids capable of forming liposomes. Reference is again made to European patent No. 0165123 already identified above, with regard to the constitution of such liposomes. It can also be formed from a hydrophobic detergent. The hydrophobic compound can also be based on polyoxylene-polyoxypropylene polymers, such as those known under the trademark PLURONIC and / or polyoxyethylene esters of sorbitan, in particular those marketed under the trademark TWEEN 20. The hydrophobic compound can also be formed by microspheres, having sizes normally less than 7 microns.
L'invention présente un intérêt tout particulier, lorsqu'elle est appliquée à l'induction d'une réponse vaccinante et plus généralement immunogène à l'égard d'un antigène non dépourvu de déterminants antigéniques caractéristiques du soi ou susceptibles de croiser immunologiquement avec ces déterminants antigéniques. Ceux-ci peuvent soit appartenir à l'antigène vaccinant, soit être associés à lui dans des conditions faisant obstacle à une purification complète préalable de l'antigène vaccinant. On l'a vu, cette situation, peut se présenter chaque fois que l'antigène vaccinant a été produit, par exemple dans des cellules humaines ou animales (par exemple virus inactivés ou fractions de virus cultivés dans ces cellules) .The invention is of particular interest when it is applied to the induction of a vaccinating and more generally immunogenic response with regard to an antigen which is not devoid of antigenic determinants characteristic of the self or capable of crossing immunologically with these antigenic determinants. These can either belong to the vaccinating antigen, or be associated with it under conditions which prevent a complete prior purification of the vaccinating antigen. As we have seen, this situation can arise each time that the vaccinating antigen has been produced, for example in human or animal cells (for example inactivated viruses or fractions of virus cultivated in these cells).
L'invention trouve une application particulièrement intéressante dans la constitution -ou pour la production- de compositions pharmaceutiques vaccinantes contenant un virus HIV inactivé, ou un antigène anti-tumoral ou encore certains antigènes parasitaires susceptibles de donner lieu à des réactions croisées avec certaines structures de l'hôte.The invention finds a particularly advantageous application in the constitution - or for the production - of vaccinating pharmaceutical compositions containing an inactivated HIV virus, or an anti-tumor antigen or also certain parasitic antigens capable of giving rise to cross-reactions with certain host structures.
Il va de soi que chaque fois qu'une préparation de l'antigène vaccinant implique un risque de présence de déterminant auto-antigénique ou croisant avec les déterminants du soi à l'issue de cette préparation, il convient de le considérer comme "principe vaccinant non totalement dépourvu de constituants auto- antigéniques".It goes without saying that whenever a preparation of the vaccinating antigen involves a risk of the presence of an auto-antigenic determinant or crossing with the determinants of the self at the end of this preparation, it should be considered as "vaccinating principle not completely devoid of auto-antigenic constituents ".
En particulier 1'invention trouve une application avantageuse en combinaison avec tout virus ou fraction de virus obtenu par culture dans des cellules humaines ou de mammifères, ou encore avec tout antigène dont les conditions d'obtention introduisent un risque de contamination par des éléments de structure appartenant à des cellules humaines ou de mammifères en particulier des cellules de la lignée blanche.In particular, the invention finds an advantageous application in combination with any virus or fraction of virus obtained by culture in human or mammalian cells, or also with any antigen whose conditions of production introduce a risk of contamination by structural elements. belonging to human or mammalian cells, in particular cells of the white line.
Il est entendu que la composition pharmaceutique telle qu'elle est vient d'être définie peut être préparée de façon extemporanée. Par ailleurs, si 1'antigène est souvent administré en même temps que les autres constituants de la composition pharmaceutique, l'invention ne saurait être limitée à ce cas de figure précis. L'administration du MDP-DD- GDP sous forme de dispersion biphasée d'une part, et celle de l'antigène vaccinant, d'autre part, peuvent également être faites de façon non simultanée, la seule condition étant que les intervalles de temps qui s'écoulent entre ces administrations distinctes soient tels que l'effet d'adjuvant i munologique de la préparation contenant le MDP-DD-GDP à 1'égard de l'antigène vaccinant puisse se manifester.It is understood that the pharmaceutical composition as it has just been defined can be prepared extemporaneously. Furthermore, if the antigen is often administered at the same time as the other constituents of the pharmaceutical composition, the invention cannot be limited to this specific case. The administration of MDP-DD-GDP in the form of a two-phase dispersion on the one hand, and that of the vaccinating antigen on the other hand, can also be done in a non-simultaneous manner, the only condition being that the time intervals which flow between these separate administrations are such that the munological adjuvant effect of the preparation containing MDP-DD-GDP against the vaccinating antigen can be manifested.
En d'autres termes l'expression "composition pharmaceutique" telle qu'elle est utilisée ci-dessus, couvre aussi bien des compositions formées à partir des divers constituants nommés et se trouvant dans un stade de prémélange, que l'ensemble de ces différents constituants pris isolément mais réunis au(x) moment(s) de leur(s) administrations(s) respective(s) aux patients (humains ou animaux) dans des conditions permettant l'obtention des résultats sus-indiqués.In other words, the term "pharmaceutical composition" as used above covers both compositions formed from the various named constituents and found in a premixing stage, that all of these different constituents taken in isolation but combined at the time (s) of their respective administration (s) to patients (humans or animals) under conditions allowing obtaining the above-mentioned results.
Les proportions relatives dans l'émulsion de la solution aqueuse et du constituant hydrophobe sont choisies de façon telle qu'une émulsion suffisamment stable, notamment au moment de l'administration, soit susceptible d'être formée entre la solution aqueuse et le constituant hydrophobe. En particulier, lorsque le constituant hydrophobe est constitué par une huile minérale, la proportion de cette dernière sera de préférence de 50 % à 90 % (volume/volume) par rapport à la totalité du mélange.The relative proportions in the emulsion of the aqueous solution and of the hydrophobic component are chosen such that an emulsion which is sufficiently stable, in particular at the time of administration, is capable of being formed between the aqueous solution and the hydrophobic component. In particular, when the hydrophobic constituent consists of a mineral oil, the proportion of the latter will preferably be from 50% to 90% (volume / volume) relative to the entire mixture.
Il va de soi que ces intervalles ne sont indiqués qu'à titre d'exemples. Ils n'ont aucun caractère limitatif.It goes without saying that these intervals are given only as examples. They are in no way limiting.
L'invention sera encore davantage illustrée par les exemples qui suivent. Comme on pourra le constater, les tests mis en oeuvre sont d'une très grande sévérité, puisque le animaux recevant la préparation capable d'induire une auto-immunisation sont frappés de paralysie et meurent.The invention will be further illustrated by the following examples. As we can see, the tests used are very severe, since the animals receiving the preparation capable of inducing autoimmunization are paralyzed and die.
Exemple 1:Example 1:
Absence d'induction d'une maladie auto-immune (1'encéphalomyélite allergique) chez le cobaye après administration de la protéine basique de myéline avec du MDP-DD-GDP en émulsion eau dans l'huile.Absence of induction of an autoimmune disease (allergic encephalomyelitis) in guinea pigs after administration of the basic myelin protein with MDP-DD-GDP in water-in-oil emulsion.
La protéine basique de myéline est un auto¬ antigène connu pour sa capacité à induire une réaction immunologique vis-à-vis de la myéline présente dans la moelle épinière et le cerveau. Les animaux sont des cobayes mâles Hartley. Ils reçoivent dans les coussinets des pattes arrières, 50 μg de protéine basique. Les témoins négatifs reçoivent l'antigène dans une émulsion d'Adjuvant Incomplet de Freund (huile seule) et les témoins positifs dans une émulsion d'Adjuvant Complet (huile + mycobactéries) . Les lots expérimentaux reçoivent l'adjuvant incomplet additionné de 50 μg MDP-GDP (Mur-Nac-L-Ala-D-isoGln- GDP) ou de MDP-Thr-GDP (Mur-Nac-L-Thr-D-isoGln-GDP) ou de MDP-DD-GDP.The basic protein of myelin is an auto¬ antigen known for its capacity to induce an immunological reaction vis-à-vis the myelin present in the spinal cord and the brain. The animals are Hartley male guinea pigs. They receive in the pads of the hind legs, 50 μg of protein basic. The negative controls receive the antigen in an emulsion of Freund's Incomplete Adjuvant (oil only) and the positive controls in an emulsion of Complete Adjuvant (oil + mycobacteria). The experimental batches receive the incomplete adjuvant added with 50 μg MDP-GDP (Mur-Nac-L-Ala-D-isoGln- GDP) or MDP-Thr-GDP (Mur-Nac-L-Thr-D-isoGln- GDP) or MDP-DD-GDP.
Les animaux sont pesés toutes les semaines, les signes cliniques apparaissent après 10 jours et les animaux meurent entre le 12ème et 19ème jours. Après 3 semaines, on pratique des cuti-réactions sur les animaux sains et sur les animaux qui ont réchappé à la maladie. On prélève également du sang par ponction cardiaque afin de doser les anticorps par ELISA.The animals are weighed weekly, clinical signs appear after 10 days and the animals die between the 12th and 19th days. After 3 weeks, cuti-reactions are practiced on healthy animals and on animals that have survived the disease. Blood is also taken by cardiac puncture to test for antibodies by ELISA.
Le tableau 1 fournit des indications sur le nombre d'animaux de chaque groupe qui s'est trouvé affecté des signes cliniques caractéristiques de 1'encéphalomyélite allergique : perte de poids, paralysie des pattes arrières puis généralisée, incontinence. le nombre d'animaux morts par groupe, les titres en anticorps anti-protéine basique de myéline, enfin, la présence de cuti-réaction positive (lorsqu'elle a été testée) chez les survivants. NT signifie "non-testé".Table 1 gives indications on the number of animals of each group which was affected by clinical signs characteristic of allergic encephalomyelitis: weight loss, paralysis of the hind legs then generalized, incontinence. the number of dead animals per group, the anti-myelin basic protein antibody titers, and the presence of a positive cuti-reaction (when tested) in the survivors. NT stands for "untested".
On voit sur le tableau 1, que seuls le lot témoin négatif et le lot ayant reçu comme adjuvant le MDP- DD-GDP échappent à la maladie. Néanmoins, les animaux ayant reçu le MDP-DD-GDP ont synthétisé des anticorps et ont eu des réactions cutanées positives, quand on a pratiqué une cuti-réaction avec la protéine basique. It can be seen from table 1 that only the negative control batch and the batch which received MDP-DD-GDP as an adjuvant are immune to the disease. However, the animals which received MDP-DD-GDP synthesized antibodies and had positive skin reactions, when a cuti-reaction was carried out with the basic protein.
Sur le tableau 2 , on voit l ' évolution du poids . La moyenne des poids est donnée pour chaque lot.On table 2, we see the evolution of the weight. The average of the weights is given for each batch.
TABLEAU 2TABLE 2
Semaine Semaine Semaine SemaineWeek Week Week Week
Immunisation 1 2 3 4Immunization 1 2 3 4
Protéine basique + AIF 510 537 620 695Basic protein + AIF 510 537 620 695
Protéine basique + ACF 500 560 425 450Basic protein + ACF 500 560 425 450
Protéine basique + AIF + MDP-GDP 480 550 546 480Basic protein + AIF + MDP-GDP 480 550 546 480
Protéine basique + AIF + MDP-L-Thr-GDP 480 549 466*Basic protein + AIF + MDP-L-Thr-GDP 480 549 466 *
Protéine basique + AIF + MDP-DD-GDP 490 568 638 685Basic protein + AIF + MDP-DD-GDP 490 568 638 685
: 2 survivants : 3 survivants On constate à l'examen de ce tableau que l'injection de la protéine basique ne s'accompagne pas d'une perte de poids, bien au contraire, des animaux traités, lorsque ceux-ci n'ont reçu en sus de la protéine basique, que l'AIF, ou à la fois l'AIF et le MDP-DD-GDP, alors que l'on enregistre une perte de poids (dans la mesure où d'ailleurs les animaux survivent) chez ceux des animaux qui ont reçu en sus de la protéine basique, soit de l'ACF, soit de l'AIF et du MDP-GDP, soit encore de l'AIF et du MDP-Thr-GDP.: 2 survivors: 3 survivors It can be seen from the examination of this table that the injection of the basic protein is not accompanied by a loss of weight, on the contrary, of the animals treated, when these have not received in addition to the protein basic, that the AIF, or both the AIF and the MDP-DD-GDP, while there is a loss of weight (insofar as the animals survive) in those of animals which have received in addition to the basic protein, either from ACF, or from AIF and MDP-GDP, or again from AIF and MDP-Thr-GDP.
Exemple 2;Example 2;
Absence de synergie toxique entre le MDP-DD-GDP et les endotoxines;Absence of toxic synergy between MDP-DD-GDP and endotoxins;
Des souris Swiss femelles de 25 g reçoivent par la voie veineuse de l'eau physiologique, soit seule (témoin négatif) , soit contenant des dérivés lipophiles du MDP à la dose de 300 μg. Deux heures plus tard elles reçoivent toujours par voie veineuse 25 μg d'endotoxine (lipopolysaccharide de S. Enderitidis) . On voit sur le tableau 3 que le MDP-GDP a sensibilisé les souris à l'administration d'endotoxine contrairement au MDP-DD-GDP et au MDP- Thr-GDP.25 g female Swiss mice receive physiological water via the venous route, either alone (negative control) or containing lipophilic derivatives of MDP at a dose of 300 μg. Two hours later they still receive 25 μg of endotoxin (lipopolysaccharide from S. Enderitidis) by vein. It is seen from Table 3 that MDP-GDP sensitized mice to the administration of endotoxin unlike MDP-DD-GDP and MDP-Thr-GDP.
Exemple 3: Example 3:
Les dérivés lipophiles ont été testés (selon la méthode décrite dans la Pharmacopie Européenne) pour leur activité pyrogène et le MDP-DD-GDP s'est révélé 10 fois moins pyrogène que le MDP-GDP.The lipophilic derivatives were tested (according to the method described in the European Pharmacopoeia) for their pyrogenic activity and the MDP-DD-GDP was found to be 10 times less pyrogenic than the MDP-GDP.
Il va de soi que le MDP-DD-GDP peut être remplacé par des structures analogues dans lesquelles le premier acide aminé de chaîne peptidique a une configuration D (autrement dit un muramyl peptide type DD, de préférence un produit de ce type possédant une chaîne lipophile) . Ainsi font partie de l'invention toutes les compositions pharmaceutiques qui ont été définies ci-dessus, mais dans lesquelles le MDP-DD-GDP serait remplacé par un autre muramyl-peptide adjuvant de type DD, dès lors que dans des protocoles expérimentaux faisant l'objet des tests qui ont été illustrés dans les exemples 1 et 2, cet autre muramyl-peptide induirait des résultats semblables à ceux obtenus avec le MDP-DD-GDP chez les animaux d'essais, à savoir absence d'induction d'une encéphalomyélite allergique chez le cobaye après administration de la protéine basique de myéline et de cet autre muramyl-peptide de type DD, et absence de synergie toxique chez le cobaye entre ce dernier produit et des endotoxines bactériennes, notamment de S. enteritidiε.It goes without saying that MDP-DD-GDP can be replaced by analogous structures in which the first amino acid of the peptide chain has a D configuration (in other words a muramyl peptide type DD, preferably a product of this type having a chain lipophilic). Thus form part of the invention all the pharmaceutical compositions which have been defined above, but in which the MDP-DD-GDP would be replaced by another adjuvant muramyl-peptide of the DD type, since in experimental protocols making the object of the tests which have been illustrated in examples 1 and 2, this other muramyl-peptide would induce results similar to those obtained with MDP-DD-GDP in test animals, namely absence of induction of a allergic encephalomyelitis in guinea pigs after administration of the basic protein myelin and this other muramyl-peptide type DD, and absence of toxic synergy in guinea pigs between this latter product and bacterial endotoxins, in particular of S. enteritidiε.
Parmi les muramyl-peptides de type DD susceptibles d'être utilisés dans les compositions pharmaceutiques selon l'invention, on mentionnera ceux qui n'induiraient pas des manifestations auto-immunes dans les protocoles expérimentaux sus-indiqués et qui répondraient à la formule générale suivante : Among the muramyl-peptides of type DD capable of being used in the pharmaceutical compositions according to the invention, mention will be made of those which would not induce autoimmune manifestations in the above-mentioned experimental protocols and which would correspond to the following general formula :
dans laquelle les substituants R1# R2, X, Y et B ont les significations suivantes : in which the substituents R 1 # R 2 , X, Y and B have the following meanings:
R1 : est H ou CH3.R 1 : is H or CH3.
R2 : est un atome d'hydrogène, un groupe NH2, ou un groupe W constitué d'une chaîne hydrocarbonée comprenant de 1 à 4 atomes de carbone.R 2 : is a hydrogen atom, an NH2 group, or a group W consisting of a hydrocarbon chain comprising from 1 to 4 carbon atoms.
X : est un résidu aminoacyle de configuration D comprenant : alanyle, valyle, isoleucyle, leucyle, séryle, thréonyle, prolyle, méthionyle.X: is an aminoacyl residue of configuration D comprising: alanyl, valyl, isoleucyl, leucyl, seryl, threonyl, prolyl, methionyl.
Y : a la même signification que R2 ou bien est une chaîne hydrocarbonée de structure linéaire ou ramifiée comprenant de 4 à 90 atomes de carbone, ou encore un groupe -CH2-CHO(R3)-CH20(R4) , avec R3 et R^ étant des chaînes hydrocarbonées, identiques ou différentes, comprenant de 8 à 20 atomes de carbone.Y: has the same meaning as R 2 or is a hydrocarbon chain of linear or branched structure comprising from 4 to 90 carbon atoms, or also a group -CH 2 -CHO (R 3 ) -CH20 (R 4 ), with R 3 and R ^ being hydrocarbon chains, identical or different, comprising from 8 to 20 carbon atoms.
A, B et C : sont, en ce qui concerne chacun d'eux, indépendamment les uns des autres, soit une liaison directe, soit un atome d'oxygène, soit une structure -NH-CHCR^-CO-, correspondant à tout aminoacyle de configuration L, avec R5 étant un résidu aminoacyle caractéristique de l'un des 20 acides aminés naturels. Z : est un atome d'hydrogène ou bien est un groupe acyle hydrocarboné de structure linéaire ou ramifiée comprenant de 1 à 90 atomes de carbone, ou encore un groupe CO-CHO-(R3)-CH20(R4) , avec R3 et R4 étant des chaînes hydrocarbonées, identiques ou différentes, comprenant de 8 à 20 atomes de carbone.A, B and C: are, with regard to each of them, independently of each other, either a direct bond, or an oxygen atom, or a structure -NH-CHCR ^ -CO-, corresponding to all aminoacyl of configuration L, with R5 being an aminoacyl residue characteristic of one of the 20 natural amino acids. Z: is a hydrogen atom or else is a hydrocarbon acyl group of linear or branched structure comprising from 1 to 90 carbon atoms, or else a CO-CHO- (R 3 ) -CH 2 0 (R 4 ) group, with R 3 and R 4 being hydrocarbon chains, identical or different, comprising from 8 to 20 carbon atoms.
A titre d'exemples de composés susceptibles d'être utilisés de façon avantageuse on mentionnera : le MurNac-D-Thr-D-IsoGln l,2-dipalmitoyl-sn- glycérolAs examples of compounds which can be used advantageously, mention will be made of: MurNac-D-Thr-D-IsoGln 1,2-dipalmitoyl-sn-glycerol
Pour des modes de préparation de ces produits, on se référera par exemple, soit au brevet européen n"0165123, soit au brevet européen n"0004512.For methods of preparing these products, reference may be made, for example, to European patent No. 0165123 or to European patent No. 0004512.
En variante, l'invention concerne un procédé de préparation d'une composition pharmaceutique capable de prévenir l'induction d'une maladie auto-immune liée à une réponse vis-à-vis de déterminants auto- antigéniques, lorsque cette composition contient un principe actif capable d'exercer une action adjuvante sélective de 1'immunité mettant en oeuvre une réponse humorale ou une réponse à médiation cellulaire, de préférence les deux à la fois, à l'encontre d'antigènes déterminés, caractérisé en ce que le principe adjuvant de cette composition pharmaceutique est constitué par un muramyl-peptide de formule I ou II.As a variant, the invention relates to a process for the preparation of a pharmaceutical composition capable of preventing the induction of an autoimmune disease linked to a response towards autoantigenic determinants, when this composition contains a principle active capable of exerting a selective adjuvant action of the immunity implementing a humoral response or a response mediated by cell, preferably both at the same time, against determined antigens, characterized in that the adjuvant principle of this pharmaceutical composition consists of a muramyl-peptide of formula I or II.
L'invention concerne donc aussi des compositions du genre en question, contenant un principe actif adjuvant qui n'est pas exempte de déterminants auto- antigéniques, associé à un muramyl-peptide de formule I ou de formule générale II.The invention therefore also relates to compositions of the genus in question, containing an adjuvant active principle which is not free from auto-antigenic determinants, associated with a muramyl-peptide of formula I or of general formula II.
Sous l'influence de ces adjuvants particuliers, il n'y a pas induction d'une réponse auto-immune même si la préparation vaccinante contient des auto- antigènes. En d'autres termes le MDP-DD-GDP ou les composés de formule générale II apparaissent adjuvant-actifs vis-à-vis des hétéro-antigènes et adjuvants-inactifs (ou passifs) vis-à-vis des auto¬ antigènes.Under the influence of these particular adjuvants, there is no induction of an autoimmune response even if the vaccine preparation contains autoantigens. In other words the MDP-DD-GDP or the compounds of general formula II appear adjuvant-active vis-à-vis hetero-antigens and adjuvant-inactive (or passive) vis-à-vis auto¬ antigens.
Donc la composition pharmaceutique faisant l'objet du brevet permet non seulement d'obtenir une réponse immunitaire dirigée uniquement contre des antigènes distincts du self mais de prévenir le déclenchement d'une maladie auto-immunitaire liée aux déterminants auto-antigéniques (ou des éléments du self) éventuellement présents dans la composition pharmaceutique vaccinante.Therefore the pharmaceutical composition which is the subject of the patent makes it possible not only to obtain an immune response directed only against antigens distinct from the self but to prevent the triggering of an autoimmune disease linked to the autoantigenic determinants (or elements of the self) possibly present in the vaccinating pharmaceutical composition.
Par "composition selon l'invention", il faut entendre aussi bien une composition contenant simultanément ou en mélange l'hétérogène contre lequel une protection est recherchée, le cas échéant non dépourvu d'auto-antigènes, d'une part, et le composé de formule I ou de formule générale II, d'autre part, que toute forme d'association destinés à permettre les administrations des deux principes à des moments distincts, l'intervalle de temps séparant ces moments distincts étant cependant suffisamment court pour que ces deux principes soient encore à même d'interagir mutuellement in vivo comme cela a été décrit. By "composition according to the invention" is meant both a composition containing simultaneously or in a mixture the heterogeneous against which protection is sought, if necessary not devoid of auto-antigens, on the one hand, and the compound of formula I or of general formula II, on the other hand, that any form of association intended to allow the administrations of the two principles at distinct times, the time interval separating these distinct moments being however sufficiently short so that these two principles are still able to interact with each other in vivo as described.
Claims
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU43318/93A AU4331893A (en) | 1992-06-12 | 1993-06-14 | Humoral immunity and cell mediation adjuvant composition inducing no response to auto-antigenic determinants |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR92/07125 | 1992-06-12 | ||
| FR9207125A FR2692149B1 (en) | 1992-06-12 | 1992-06-12 | ADJUVANT COMPOSITION OF HUMOR AND CELL-MEDIATED IMMUNITY WITHOUT RESPONSE TO SELF-ANTIGENIC DETERMINANTS. |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO1993025236A1 true WO1993025236A1 (en) | 1993-12-23 |
Family
ID=9430680
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/FR1993/000569 Ceased WO1993025236A1 (en) | 1992-06-12 | 1993-06-14 | Humoral immunity and cell mediation adjuvant composition inducing no response to auto-antigenic determinants |
Country Status (4)
| Country | Link |
|---|---|
| AU (1) | AU4331893A (en) |
| CA (1) | CA2137571A1 (en) |
| FR (1) | FR2692149B1 (en) |
| WO (1) | WO1993025236A1 (en) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2603321A1 (en) * | 1975-02-07 | 1976-08-19 | Anvar | EMULSION BASED ON A METABOLIZABLE VEGETABLE OIL AND WATER |
| EP0013651A1 (en) * | 1979-01-12 | 1980-07-23 | ANVAR Agence Nationale de Valorisation de la Recherche | Muramyl peptides fixed on peptide polymers and medicaments containing them |
| FR2533827A1 (en) * | 1982-09-30 | 1984-04-06 | Anvar | Composition possessing immunoregulatory properties, in particular of non-specific immunological adjuvants, based on muramyl peptide and an aluminium derivative |
| EP0165123A2 (en) * | 1984-05-11 | 1985-12-18 | ANVAR Agence Nationale de Valorisation de la Recherche | Lipophile derivatives of muramyl peptides having macrophage-activating properties, compositions containing them and processes for obtaining them |
| WO1992000081A1 (en) * | 1990-06-29 | 1992-01-09 | Chiron Corporation | Vaccine compositions containing liposomes |
| WO1992001475A1 (en) * | 1990-07-18 | 1992-02-06 | Vacsyn France, S.A. | Compositions based on active principles of hydrophobic medicaments solubilizable in an aqueous solvent |
-
1992
- 1992-06-12 FR FR9207125A patent/FR2692149B1/en not_active Expired - Fee Related
-
1993
- 1993-06-14 CA CA 2137571 patent/CA2137571A1/en not_active Abandoned
- 1993-06-14 AU AU43318/93A patent/AU4331893A/en not_active Abandoned
- 1993-06-14 WO PCT/FR1993/000569 patent/WO1993025236A1/en not_active Ceased
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2603321A1 (en) * | 1975-02-07 | 1976-08-19 | Anvar | EMULSION BASED ON A METABOLIZABLE VEGETABLE OIL AND WATER |
| EP0013651A1 (en) * | 1979-01-12 | 1980-07-23 | ANVAR Agence Nationale de Valorisation de la Recherche | Muramyl peptides fixed on peptide polymers and medicaments containing them |
| FR2533827A1 (en) * | 1982-09-30 | 1984-04-06 | Anvar | Composition possessing immunoregulatory properties, in particular of non-specific immunological adjuvants, based on muramyl peptide and an aluminium derivative |
| EP0165123A2 (en) * | 1984-05-11 | 1985-12-18 | ANVAR Agence Nationale de Valorisation de la Recherche | Lipophile derivatives of muramyl peptides having macrophage-activating properties, compositions containing them and processes for obtaining them |
| WO1992000081A1 (en) * | 1990-06-29 | 1992-01-09 | Chiron Corporation | Vaccine compositions containing liposomes |
| WO1992001475A1 (en) * | 1990-07-18 | 1992-02-06 | Vacsyn France, S.A. | Compositions based on active principles of hydrophobic medicaments solubilizable in an aqueous solvent |
Non-Patent Citations (1)
| Title |
|---|
| FILE SERVER STN KARLSRUHE,FILE BIOSIS ABSTRACT NO.85:355260 * |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2692149B1 (en) | 1995-06-09 |
| FR2692149A1 (en) | 1993-12-17 |
| CA2137571A1 (en) | 1993-12-23 |
| AU4331893A (en) | 1994-01-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| FR2598622A1 (en) | IMMUNOLOGICAL ADJUVANTS FOR POLYSACCHARIDE VACCINES | |
| RU2129439C1 (en) | Antigenic composition for inducing cytotoxic t-lymphocytes response, method of induction and method of patients treatment | |
| JP2648305B2 (en) | Polysaccharide vaccine | |
| JP2690620B2 (en) | Improvements in or related to vaccines | |
| EP1326636B1 (en) | Vaccine composition | |
| FR2726764A1 (en) | ADDITIVE FOR VACCINE COMPOSITION | |
| JP2002513773A (en) | Adjuvant composition and use thereof | |
| JP2003502388A5 (en) | ||
| EP1121148A2 (en) | Immunostimulant emulsion | |
| JP2002537353A (en) | Enhancement of Neisseria antigen bactericidal activity using oligonucleotide containing CG motif | |
| WO2005060966A1 (en) | Immunostimulant composition comprising at least one toll-like receptor 7 or toll-like receptor 8 agonist and a toll-like receptor 4 agonist | |
| JP2746272B2 (en) | Vaccine adjuvant | |
| US6890540B1 (en) | Vaccine formulation | |
| JPH05507498A (en) | Improved adjuvants and vaccines | |
| EP0015810A1 (en) | N-Acetyl-L-(N-methyl-alanil)-D-isoglutamine and compositions containing it for use as regulator of the immune reactions | |
| EP1696954B1 (en) | Vaccine composition admixed with an alkylphosphatidylcholine | |
| US6936260B1 (en) | Vaccine composition | |
| EP0391962A1 (en) | Compositions possessing immunostimulating properties and their applications in human and veterinary medecine | |
| EP0165123A2 (en) | Lipophile derivatives of muramyl peptides having macrophage-activating properties, compositions containing them and processes for obtaining them | |
| CA2235110C (en) | Pharmaceutical compositions containing steroid derivatives involved in triggering an immune response | |
| WO1993025236A1 (en) | Humoral immunity and cell mediation adjuvant composition inducing no response to auto-antigenic determinants | |
| FR2692148A1 (en) | Use of lipophilic muramyl peptide MDP:DD:GPD - in vaccines against HIV and tumours | |
| CA2406949A1 (en) | Use of particulate vectors in immunomodulation | |
| RU2311926C2 (en) | Antigen carrier and adjuvant | |
| WO1999016468A1 (en) | Antigen vectors in the form of multilamellar vesicles |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AT AU BB BG BR CA CH CZ DE DK ES FI GB HU JP KP KR LK LU MG MN MW NL NO NZ PL PT RO RU SD SE SK UA US VN |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): AT BE CH DE DK ES FR GB GR IE IT LU MC NL PT SE BF BJ CF CG CI CM GA GN ML MR NE SN TD TG |
|
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2137571 Country of ref document: CA |
|
| ENP | Entry into the national phase |
Ref document number: 1995 351380 Country of ref document: US Date of ref document: 19950210 Kind code of ref document: A |
|
| REG | Reference to national code |
Ref country code: DE Ref legal event code: 8642 |
|
| 122 | Ep: pct application non-entry in european phase | ||
| ENP | Entry into the national phase |
Ref document number: 1997 791471 Country of ref document: US Date of ref document: 19970127 Kind code of ref document: A |