TWI801561B - 化合物及其用於緩解絕經相關症狀的用途 - Google Patents
化合物及其用於緩解絕經相關症狀的用途 Download PDFInfo
- Publication number
- TWI801561B TWI801561B TW108113543A TW108113543A TWI801561B TW I801561 B TWI801561 B TW I801561B TW 108113543 A TW108113543 A TW 108113543A TW 108113543 A TW108113543 A TW 108113543A TW I801561 B TWI801561 B TW I801561B
- Authority
- TW
- Taiwan
- Prior art keywords
- progesterone
- estetrol
- component
- vms
- daily
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/565—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
- A61K31/585—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin containing lactone rings, e.g. oxandrolone, bufalin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/12—Drugs for genital or sexual disorders; Contraceptives for climacteric disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/24—Drugs for disorders of the endocrine system of the sex hormones
- A61P5/30—Oestrogens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Endocrinology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Reproductive Health (AREA)
- Diabetes (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines Containing Plant Substances (AREA)
Abstract
本發明係涉及用於緩解絕經相關症狀的激素替代療法,且涉及相關的化合物與相關的包裝單元,其係基於以特定每日劑量向雌性哺乳動物施予雌四醇成分,且選擇性地與黃體酮類成分併用。相較於目前能用於緩解絕經相關症狀的方法,所述療法具有統計學上顯著的功效,且同時具有有利的副作用特徵。
Description
本發明係涉及用於減緩絕經相關(menopause-associated)症狀的激素替代療法(hormone replacement therapy),且涉及相關的化合物與相關的包裝單元,其係基於以特定每日劑量(daily doses)向雌性哺乳動物施予雌四醇(estetrol)成分,且選擇性地與黃體酮類(progestogenic)成分併用。
如本文進一步描述的,相較於目前能用於緩解絕經相關症狀的方法,所述療法展現統計學上顯著的功效,且同時具有有利的副作用特徵(profile for side effects)。
激素替代療法(hormone replacement therapy,HRT)被用於描述未平衡的(unopposed)雌激素(oestrogen)用途(對於接受子宮切除術(hysterectomy)的女性)或組合雌激素-黃體酮類治療(對於仍有子宮的女性)。HRT的目標是緩解絕經症狀,更重要地是緩解例如熱潮紅(hot flushes)的血管舒縮症狀(vasomotor symptoms,VMS)。與絕經前期(perimenopause)及絕經相關的與雌激素治療相關的其他疾病及症狀包含骨質疏鬆症(osteoporosis)、陰道萎縮(vaginal atrophy)及睡眠障礙(當與熱潮紅相關時)。
VMS最常發生在絕經過渡期(menopausal transition)之後期及絕經後期(post-menopause)之早期。VMS是最重要的絕經困擾。據估計,超過50歲的女性中約有75%受到熱潮紅困擾(Utian et al.,2005,"Comparative controlled trial of a novel oral estrogen therapy,estradiol acetate,for relief of menopause symptoms" Menopause 12(6):708-715)。雖然大約10%的人受到超過10年的困擾,大多數人經歷了約兩年的熱潮紅(Rodstrom et al.,2002,"A longitudinal study of the treatment of hot flushes:the population study of women in Gothenburg during a quarter of a century" Menopause 9(3):156-161)。VMS可導致身體及心理社會障礙,從而降低生活品質,並且是為什麼女性可能尋求絕經的醫療護理的主要原因之一(Santoro,2008,"Symptoms of menopause:hot flushes" Clin Obstet Gynecol 51(3):539-548)。
陰道及尿道的上皮組織(epithelial linings)對雌激素非常敏感,且雌激素缺乏會導致兩者之上皮細胞變薄。此導致外陰陰道萎縮(vulvovaginal atrophy,VVA)及尿路疾病,引起陰道乾燥(vaginal dryness)、瘙癢(itching)、性交困難(dyspareunia)、排尿困難(dysuria)、頻尿(urinary frequency)及復發性尿路感染風險增加的症狀。2014年初,國際女性性健康研究協會(International Society for the Study of Women’s Sexual Health,SSWSH)及北美絕經協會(North American Menopause Society,NAMS)批准新的用語「絕經泌尿生殖綜合徵(genitourinary syndrome of menopause,GSM)」以取代VVA用語。使用此種新用語的理由是VVA用語過於嚴格,而GSM則是一個更全面的用語,其包含症狀性VVA以及與低雌激素等級(levels)相關的下尿路症狀(Portman et al.,2014,"Genitourinary syndrome of menopause:new terminology for vulvovaginal atrophy from the International Society for the Study of Women's Sexual Health and the North American Menopause
Society" Menopause 21(10):1063-1068)。請注意的是,FDA及EMA發布的工業指南尚未採用GSM用語,因此本文將使用VVA用語。
雌激素療法仍然是緩解絕經症狀的黃金標準,特別是VMS。所有給藥(administration)途徑似乎對症狀緩解同樣有效,但它們的代謝作用不同。雌激素應被連續給藥;在日曆月的第1天至第25天施用雌激素的過去的治療方案(regimen)被認為是過時的。女性將通常會在休息期間(days off)得到VMS,且每個月停止幾天沒有任何已知的優勢。
目前的HRT,具有完整子宮的所有女性除了雌激素外還需要黃體酮(progestin)來預防子宮內膜增生(endometrial hyperplasia)-以及隨後的癌症(subsequent carcinoma)-其發生在短短6個月的雌激素治療後。黃體酮可連續或依次給藥(例如,每月10至14天、或者每3個月14天)。
雌激素療法是在美國及歐洲用於絕經期的VMS的最持久有效的治療方法。遵循基本女性健康倡議出版物中報告的安全問題(Anderson et al.,2004,"Effects of conjugated equine estrogen in postmenopausal women with hysterectomy:the Women's Health Initiative randomized controlled trial" JAMA 291(14):1701-1712)以及對於持續的受試者治療要求,臨床醫生面臨的一個挑戰是確定用於緩解絕經症狀的雌激素的最小有效劑量(Simon et al.,2007,"絕經hormone therapy for vasomotor symptoms:balancing the risks and benefits with ultra-low doses of estrogen" Expert Opin Investig Drugs 16(12):2005-2020)。此外,開發比目前使用的更安全的雌激素是一項挑戰。
在2016年出版物中,Coelingh Bennink等人;("Clinical effects of the fetal estrogen estetrol in a multiple-rising-dose study in postmenopausal women",
Maturitas,2016 Sep;91:93-100)報告了一項在49位絕經後期的女性的部分隨機、開放標籤(open-label)、多劑量增加(multiple-rising-dose)的研究,所述女性每天接受2mg雌四醇、或2mg戊酸雌二醇(estradiol-valerate)持續28天(研究的隨機部分),然後每天10、20及40mg的雌四醇的劑量逐步增加(研究的非隨機部分)。作者比較戊酸雌二醇(2mg)跟僅兩種劑量的雌四醇(2及10mg)的對於篩選每週>35次熱潮紅的受試者的熱潮紅的緩解效果(請注意表1)。作者報告的是,在每天劑量為2mg雌四醇,於熱潮紅及出汗的平均次數減少,同時在2mg雌四醇組別中發現子宮內膜厚度穩定,但在10mg雌四醇組別中增加(摘要)。
從這項研究中,由於作者沒有測量20mg及40mg雌四醇組別中的VMS,因此通常知識者顯而易見的是,作者認為只有較低劑量(2mg及10mg)適合於管理VMS。此外,本領域通常知識者了解的是,每日劑量為2mg雌四醇與每日劑量為10mg雌四醇在減少每天的熱潮紅次數上一樣有效(參見例如Coelingh Bennink et al.,Maturitas,2016中的第3圖)。此外,所述出版物教導通常知識者的是,每日劑量2mg不改變子宮內膜厚度,而每日劑量10mg對子宮內膜厚度具有重要影響(參見例如Coelingh Bennink et al.,2016中的第2圖)。因此,通常知識者得出結論為,用於治療VMS的最小有效劑量的雌四醇是每天2mg。
在這種背景下,本發明人現已驚奇地發現,用於減輕絕經前期及絕經後期的女性的VMS的雌四醇的最小有效劑量(Minimal Effective Dose)為約每日15mg。
最小有效劑量的判定(determination)實際上牽涉到許多參數,所述參數不僅考慮了每天的VMS平均次數(如同Coelingh Bennink et al in Maturitas,2016中所做),而且也考慮VMS的嚴重程度,亦還有每週的加權分數,其如本文進一步定義的。
因此,就功效而言,其令人驚訝地發現,需要15mg的每日劑量才能對VMS產生明確的效果。
此外,本發明人觀察到的是治療的幾種副作用,例如反映在治療引起的不良事件(treatment-emergent adverse events,TEAE)的數量、或者在每個組別中離開研究的患者數量、或者在每個組別中必須進行的活檢(biopsies)的數量中的例子,在每天約10mg處趨向達到平台期,且當劑量進一步增加時不會惡化。令人驚訝地,此些參數中的部分實際上從每天10mg至每天15mg時降低,因此表明當劑量高於每天10mg時,不良事件可更被忍受。
基於此令人驚訝的發現、以及當施用20mg每日劑量時進行的測量,本發明人因此得出了意想不到的結論,所述結論為用於緩解在絕經後期的女性的VMS的雌四醇的最佳每日劑量為15mg至25mg。如實例中所示,此劑量範圍確實允許觀察到對VMS的統計學顯著效果,同時維持治療副作用在可接受的目標內。
在以下編號段落1至14中,描述本發明的實施例。
1.一種用於緩解絕經相關症狀的組合物,其中所述組合物包含雌四醇(estetrol)成分,且其中所述組合物以相當於從約15mg至約25mg的雌四醇的每日劑量被施予。
2.一種用於緩解血管舒縮症狀的組合物,所述血管舒縮症狀選自熱潮紅、出汗發作(sweating attacks)、夜間盜汗(night sweats)、畏寒(chills)、多汗
(increased perspiration)、心悸(palpitations)及其組合,其中所述組合物包含雌四醇成分,且其中所述組合物以相當於從約15mg至約25mg的雌四醇的每日劑量被施予。
3.一種用於減輕絕經過渡期的情緒方面(emotional aspects)的組合物,所述情緒方面選自憂鬱(depression)、易怒(irritability)、情緒變化(mood changes)、失眠(insomnia)、睡眠障礙(sleep disturbance)、焦慮(anxiety)、神經緊張(nervous tension)及其組合,其中所述組合物包含雌四醇成分,且其中所述組合物以相當於從約15mg至約25mg的雌四醇的每日劑量被施予。
4.一種用於減輕絕經過渡期的生理方面(physiological aspects)的組合物,所述生理方面選自關節疼痛(joint pain)、骨密度降低(loss of bone density)、尿路感染(urinary tract infections)、尿失禁(urinary incontinence)、陰道乾燥(dryness of the vagina)、子宮脫垂(uterine prolapse)、皮膚質地改變(changes in skin texture)、體重增加(weight gain)、性交困難(dyspareunia)、心血管疾病(cardiovascular diseases)、糖尿病(diabetes)及其組合,其中所述組合物包含雌四醇成分,且其中所述組合物以相當於從約15mg至約25mg的雌四醇的每日劑量被施予。
5.一種用於降低VMS頻率、VMS嚴重程度(severity)、熱潮紅每週加權分數(weekly weighted score)、陰道乾燥、性交困難及其組合、或者用於根據MRS及/或MENQOL調查表改善生活品質的組合物,其中所述組合物包含雌四醇成分,且其中所述組合物以相當於從約15mg至約25mg的雌四醇的每日劑量被施予。
6.用於根據以上段落1-5中任一段的組合物,其中所述組合物每天施予維持至少1週、至少2週、至少4週、至少6週、至少12週。
7.用於段落1-6中任一段的組合物,其中包含黃體酮類成分(progestogenic)的第二組合物被額外地使用。
8.用於段落7的組合物,其中所述黃體酮類成分選自屈螺酮(drospirenone)、黃體酮(progesterone)及地屈黃體酮(dydrogesterone)。
9.用於段落7的組合物,其中黃體酮以從50mg至200mg的每日給藥劑量被施予。
10.用於段落1-6中任一段的組合物,其中包含巴多昔芬(bazedoxifene)的第二組合物被額外地使用。
11.用於根據段落7-10中任一段的組合物,其中包含黃體酮類成分或巴多昔芬的所述第二組合物與包含雌四醇成分的組合物相同。
12.用於根據段落1-11中任一段的組合物,其中雌四醇成分係為雌四醇,較佳地為雌四醇單水合物(estetrol monohydrate)。
13.用於根據前述段落中任一段的組合物,其中組合物係被配製為口服劑量單位(oral dosage unit)。
14.用於根據段落13的組合物,其中口服劑量單位係被配製為對應於每日劑量單位(daily dosage unit)。
在以下編號段落15至28中,描述了本發明的其他實施例。
15一種減輕絕經相關症狀的方法,其包含施予含有相當於從約15mg至約25mg的雌四醇的每日劑量的雌四醇成分的組合物。
16.一種緩解血管舒縮症狀的方法,所述血管舒縮症狀選自熱潮紅、出汗發作、夜間盜汗、畏寒、多汗、心悸及其組合,其中所述方法包含施予含有相當於從約15mg至約25mg的雌四醇的每日劑量的雌四醇成分的組合物。
17.一種減輕絕經過渡期的情緒方面的方法,所述情緒方面選自憂鬱、易怒、情緒變化、失眠、睡眠障礙、焦慮、神經緊張及其組合,其中所述方法包含施予含有相當於從約15mg至約25mg的雌四醇的每日劑量的雌四醇成分的組合物。
18.一種減輕絕經過渡期的生理方面的方法,所述生理方面選自關節疼痛、骨密度降低、尿路感染、尿失禁、陰道乾燥、子宮脫垂、皮膚質地改變、體重增加、性交困難、心血管疾病、糖尿病及其組合,其中所述方法包含施予含有相當於從約15mg至約25mg的雌四醇的每日劑量的雌四醇成分的組合物。
19.一種降低VMS頻率、VMS嚴重程度、熱潮紅每週加權分數、陰道乾燥、性交困難及其組合、或者根據MRS及/或MENQOL調查表改善生活品質的方法,其包含施予含有相當於從約15mg至約25mg的雌四醇的每日劑量的雌四醇成分的組合物。
20.根據以上段落15-19中任一段的方法,其中所述組合物每天施予維持至少1週、至少2週、至少4週、至少6週、至少12週。
21.根據段落15-20中任一段的方法,其中包含黃體酮類成分的第二組合物被額外地使用。
22.根據段落21的方法,其中所述黃體酮類成分選自屈螺酮、黃體酮及地屈黃體酮。
23.根據段落22的方法,其中黃體酮以從50mg至200mg的每日給藥劑量被施予。
24.根據段落15-20中任一段的方法,其中包含巴多昔芬的第二組合物被額外地使用。
25.根據段落21-24中任一段的方法,其中包含黃體酮類成分或巴多昔芬的所述第二組合物與包含雌四醇成分的組合物相同。
26.根據段落15-25中任一段的方法,其中雌四醇成分係為雌四醇,較佳地為雌四醇單水合物。
27.根據前述段落中任一段的方法,其中組合物係被配製為口服劑量單位。
28.根據段落27的方法,其中口服劑量單位係被配製為對應於每日劑量單位。
在以下編號段落29至42中,描述了本發明的其他實施例。
29.有效含量的雌四醇成分在製備用於緩解絕經相關症狀的組合物中的用途,其中雌四醇成分以相當於從約15mg至約25mg的雌四醇的每日劑量被使用。
30.有效含量的雌四醇成分在製備用於緩解血管舒縮症狀的組合物中的用途,所述血管舒縮症狀選自熱潮紅、出汗發作、夜間盜汗、畏寒、多汗、心悸及其組合,其中雌四醇成分以相當於從約15mg至約25mg的雌四醇的每日劑量被使用。
31.有效含量的雌四醇成分在製備用於減輕絕經過渡期的情緒方面的組合物中的用途,所述情緒方面選自憂鬱、易怒、情緒變化、失眠、睡眠障礙、焦慮、神經緊張及其組合,其中雌四醇成分以相當於從約15mg至約25mg的雌四醇的每日劑量被使用。
32.有效含量的雌四醇成分在製備用於減輕絕經過渡期的生理方面的組合物中的用途,所生理方面選自關節疼痛、骨密度降低、尿路感染、尿失禁、陰道乾燥、子宮脫垂、皮膚質地改變、體重增加、性交困難、心血管疾病、糖尿病及其組合,其中雌四醇成分以相當於從約15mg至約25mg的雌四醇的每日劑量被使用。
33.有效含量的雌四醇成分在製備組合物中的用途,所述組合物用於降低VMS頻率、VMS嚴重程度、熱潮紅每週加權分數、陰道乾燥、性交困難
及其組合、或者用於根據MRS及/或MENQOL調查表改善生活品質,其中雌四醇成分以相當於從約15mg至約25mg的雌四醇的每日劑量被使用。
34.根據以上段落29-33中任一段的用途,其中所述組合物每天施予維持至少1週、至少2週、至少4週、至少6週、至少12週。
35.根據段落29-34中任一段的用途,其中包含黃體酮類成分的第二組合物被額外地使用。
36.根據段落35的用途,其中所述黃體酮類成分選自屈螺酮、黃體酮及地屈黃體酮。
37.根據段落35的用途,其中黃體酮以從50mg至200mg的每日給藥劑量被施予。
38.根據段落29-34中任一段的用途,其中包含巴多昔芬的第二組合物被額外地使用。
39.根據段落35-38中任一段的用途,其中包含黃體酮類成分或巴多昔芬的所述第二組合物與包含雌四醇成分的組合物相同。
40.根據段落29-39中任一段的用途,其中雌四醇成分係為雌四醇,較佳地為雌四醇單水合物。
41.根據前述段落中任一項的用途,其中組合物係被配製為口服劑量單位。
42.根據段落41的用途,其中口服劑量單位係被配製為對應於每日劑量單位。
在以下編號的段落43至50中,描述了本發明的其他實施例。
43.包裝單元,包含至少14個,較佳地為至少21個,甚至更佳地為至少28個容器的包裝單元,所述容器係用於保存(holding)經單獨包裝(separately packaged)且能單獨地移除的(individually removable)每日固
體口服劑型,其中容器的每一個包含含有從約15mg至約25mg的雌四醇的至少一固體劑型。
44.根據段落43的包裝單元,其中包裝單元額外地包含至少10個,較佳地為12個,更佳地為14個額外容器,所述額外容器係用於保存經單獨包裝且能單獨移除的每日,較佳地為固體,口服劑型,其中額外容器的每一個包含至少一,較佳地為固體,含有黃體酮類成分的劑型。
45.根據段落43的包裝單元,其中當這兩種固體劑型必須於同一天施予,用於保存包含黃體酮類成分的劑型的額外容器的每一個單獨可視地佈置在用於保存包含雌四醇的固體劑型的容器旁邊。
46.根據段落44或45的包裝單元,其中所述黃體酮類成分選自屈螺酮、黃體酮及地屈黃體酮。
47.根據段落46的包裝單元,其中所述黃體酮類成分係為黃體酮,且其中額外容器的每一個包含含有約200mg黃體酮的至少一劑型。
48.根據段落43所述的包裝單元,其中所述包裝單元額外包含相同數量的額外容器,所述額外容器用於保存經單獨包裝且能單獨移除的每日,較佳地為固體,口服劑型,其中所述額外容器的每一個包含至少一,較佳地為固體,包含黃體酮類成分的劑型,其中所述黃體酮類成分較佳地選自屈螺酮、黃體酮與地屈黃體酮,其中所述黃體酮類成分甚至更佳地為黃體酮,且其中所述額外容器包含含有約100mg的黃體酮的至少一固體劑型。
49.根據段落43的包裝單元,其中至少10個,較佳地為12個,更佳地為14個固體劑型額外包含黃體酮類成分。
50.根據段落43的包裝單元,其中固體劑型的每一個額外包含黃體酮類成分。
本領域通常知識者將理解的是,編號段落44至50中描述的實施例可等同地呈現為組件式套組(kit-of-parts),其含有第一包裝單元,例如含有包含雌四醇成分的劑量單位的泡鼓包裝(blister pack)、以及不同的第二包裝單元,例如含有包含黃體酮類成分的劑量單位不同的第二種泡鼓包裝。
本領域通常知識者還將知道的是,在本發明的範圍內,包裝單元的每一個,例如泡鼓包裝,可被編號或以其他方式標記。
在本發明的範圍內,包裝單元的每一個可以是具有紙板(cardboard)、紙板(paperboard),鋁箔塑膠背襯(foil plastic backing)且封裝在合適的蓋子中的經密封的泡鼓包裝。
在本發明的特定實施例中,包裝單元包含28個容器或28個容器的倍數,例如28個容器的2到12倍。
定義(Definitions)
在本文件中使用的用語「雌四醇成分(estetrol component)」,包含選自由雌四醇;雌四醇的酯類(esters of estetrol),其中至少一個羥基(hydroxyl groups)的氫原子被具有1-25個碳原子的烴羧酸(hydrocarbon carboxylic)、磺酸(sulfonic acid)或胺磺酸(sulfamic acid)的醯基(acyl radical)取代;及其組合所組成的群組中的物質。甚至更佳地,雌四醇成分是雌四醇(包含雌四醇水合物(hydrates))。最佳地,在劑量單位中包含的雌四醇成分是雌四醇單水合物。
本文所用的用語「雌四醇(estetrol)」是指1,3,5(10)-雌三烯-3,15α、16α、17β-四醇、或15α-羥基三醇(1,3,5(10)-estratrien-3,15alpha,16alpha,17beta-tetrol or 15alpha-hydroxyestriol)以及雌四醇的水合物,例如,雌四醇單水合物。
用語「黃體酮類成分(progestogenic component)」被定義為能夠在體內引發黃體酮類反應(progestogenic response)的物質、或能夠在體內釋放這種物質的前驅物。通常黃體酮類成分能夠結合至黃體酮受體(progestogen receptor)。
在本發明的上下文中,其他化合物可以與對具有子宮的女性施予的雌四醇成分一起使用。選擇性雌激素受體調節劑(Selective Estrogen Receptor Modulators,SERM)定義這樣的化合物的類別,其被認為是本發明方法中的雌四醇成分的有用補充物(complements)。用於本發明上下文的較佳SERM是巴多昔芬。
在本文進一步描述的方法及組合物中,必須理解的是,當提及「黃體酮類成分」時,這種參考包含SERM,特別是巴多昔芬。
如本文所用,「約(about)」指的是諸如參數、含量、時間長度(temporal duration)、及其類似物的可測量值,意味著包含+/-10%或更小的變化,更佳地為+/-5%或更小,甚至更佳地為+/-1%或更少,且從特定數值開始,到目前為止,這些變化適合於在所揭露的發明中進行。然而,其應該理解的是,修飾語「約」所指的數值本身也是具體公開的數值。
用語「有效量(effective amount)」是指獲得生理效應(physiological effect)所必需的含量。可藉由一劑(one dose)或重複劑量(repeated doses)實現生理效應。
本文所用的用語「絕經前期(perimenopause)」(也在「絕經前期女性(perimenopausal women)」及「絕經前期受試者(perimenopausal subject)」及其
類似者的背景下)是指在絕經前約三至四年開始且在末次月經(final menstrual period)後一年結束的生命期(period of life)。絕經前期的特徵是持續不規則的月經週期(menstrual cycles)、激素等級(hormonal levels)的極端波動、頻繁的無排卵(anovulation)及VMS的出現(參考:Harlow et al.,Menopause,Vol.19,No.4,2012,“Executive summary of the Stages of Reproductive Aging Workshop+10:addressing the unfinished agenda of staging reproductive aging”,特別參見其中的第2圖)。在這個過渡期間,臨床護理的重點發生了變化。雖然女性在絕經前期期間內仍需要有效的避孕措施(contraception),但還需要解決包含骨礦物質密度下降、月經週期變化及血管舒縮不穩定等問題。相當數量的女性也經歷憂鬱症狀,例如情緒波動、易怒及注意力不集中(Bosworth et al.,Psychosom Med.,2001,Jul-Aug;63(4):603-8,“Depressive symptoms,menopausal status,and climacteric symptoms in women at midlife”)。
本文所用的用語「絕經後(postmenopause)」(也在「絕經後女性(postmenopausal women)」及「絕經後受試者(postmenopausal subject)」及其類似者的背景下)首先涵蓋自發性絕經後女性,即在經歷了12個月的閉經(amenorrhea)而沒有任何其他明顯的病理或生理原因的情況下,經歷經期永久停止的自然絕經的女性。在正常女性中,其發生的年齡中位數是51.4年,並且其完整地反映、或者接近完全反映卵巢濾泡(ovarian follicular)耗盡,且導致低雌性素血症(hypoestrogenemia)(雌二醇(estradiol)等級通常低於20pg/mL)及高促卵泡激素(follicle-stimulating hormone)(FSH等級>40IU/L)濃度。用語「絕經後」還包含由於卵巢早衰(premature ovarian failure)、手術(例如卵巢切除術(ovariectomy))、癌症的化學療法或放射療法、以及某些疾病(例如,感染或甲狀腺機能低下症(hypothyroidism))導致的絕經。
本文使用的用語「VMS」(或者以其非縮寫形式,「血管舒縮症狀(vasomotor symptoms)」)對應於絕經期特有的熱調節紊亂。VMS包含熱潮紅(有時拼寫為「熱潮紅(hot flushes)」);出汗發作,例如:夜間盜汗、畏寒及多汗;以及心悸。VMS伴隨出汗及潮紅的大量熱量,主要在頭部、頸部、胸部及上背周圍經歷。如下面進一步定義的,VMS分為輕度、中度及重度類別。
如本文所用,用語「絕經相關症狀(menopause-associated symptoms)」用於描述如上定義的VMS,但還包含絕經過渡期的情緒方面(包含但不限於憂鬱、易怒、情緒變化、失眠、睡眠障礙、焦慮及神經緊張)及絕經過渡期的生理方面(包含但不限於關節疼痛、骨密度降低、尿路感染、尿失禁、陰道乾燥、子宮脫垂、皮膚質地改變、體重增加、性交困難、心血管疾病及糖尿病)。
如本文所用,用語「生活品質(Quality of Life)」(及其縮寫「QoL」)是指可以例如藉由使用問卷來評估的參數,例如,藉由示例性的方式而非限制性的方式,「絕經評級量表(Menopause Rating Scale)」問卷(Heinemann et al.,2003,“International versions of the Menopause Rating Scale(MRS)" Health Qual Life Outcomes 1:28;Heinemann et al.,2004,"The Menopause Rating Scale(MRS)scale:A methodological review".Health Qual Life Outcomes 2:45;Heinemann et al.,2004,"The Menopause Rating Scale(MRS)as outcome measure for hormone treatment?A validation study".Health Qual Life Outcomes 2:67;如下述實例1之C部分中進一步詳述。)或者MENQOL問卷(The Menopause-specific Quality of Life(MENQOL)questionnaire,Hilditch et al.;Maturitas 1996;A menopause-specific quality of life questionnaire:development and psychometric properties;24(3);p.161-175)。
如本文所用,「BMI」(或「身體質量指數(Body Mass Index)」以其非縮寫形式是指與受試者的體重及身高相關的指數,其藉由將受試者的體重(公斤)除以受試者的身高(公尺)的平方來計算。BMI為27.3或更高將女性受試者分類為「超重(overweight)」,而BMI為30或更高的BMI將受試者分類為「肥胖(obese)」。
最小有效劑量的判斷(Determination of the Minimum Effective Dose)
為了判斷最小有效劑量(Minimum Effective Dose,MED),第一,選擇標準要求患者在隨機化(randomization)之前的一週內呈現至少7個中度至重度VMS/天、或至少50個中度至重度VMS/週。第二,安慰劑(placebo)組以雙盲方式(double-blind)被包含在內。第三,總患者數量使得可以在研究的個別目標(arms)之間獲得統計學顯著性。第四,考慮了中度至重度VMS的每週頻率從基線的絕對變化。基於從基線到中度至重度VMS的每週頻率的未轉化(untransformed)變化,進行協方差分析(analysis of covariance,ANCOVA)。最後,評估了從基線的嚴重程度變化。為此,藉由受試者記錄VMS的嚴重程度分數系統如下:輕度的分數(1),沒有出汗的感覺;中度的分數(2),有出汗的熱的感覺/受試者能夠繼續活動;以及重度的分數(3),有出汗的熱的感覺/導致活動停止。
此外,嚴重程度分數為零被歸因於在給定的一週內經歷了100%VMS緩解的患者。
根據這些分數記錄,藉由僅考慮中度及嚴重VMS來計算在基線處的嚴重程度,使得在基線週(baseline week)的7天期間內中等VMS的總數乘以2,
並且被加到在基線週的7天期間內重度VMS的總數中乘以3。然後將總體除以在基線週期間之中度及重度VMS的總數。
對於這些週中的每一個,第4週及第12週的嚴重程度使用以下公式計算:在7天內的輕度VMS的數量乘以1;在7天內的中度VMS的數量乘以2;在7天內的重度VMS的數量乘以3。
且在將此總數除以在一週的7天期間輕度、中度及重度VMS的總數之前,將3個得到的數字加在一起。
在下面A部分的(b)「VMS嚴重程度」,此方法被用於產生進一步包含在實例1的數據。
在替代實施例中,VMS嚴重程度評估如下:基線處的嚴重程度也藉由僅考慮中等及嚴重VMS來計算,使得在基線週的7天期間之中度VMS的總數乘以2,並且被加到在基線週的7天期間內重度VMS的總數中乘以3。然後將總體除以在基線週期間之中度及重度VMS的總數。
然而,對於這些週中的每一個,第4週及第12週的嚴重程度使用以下公式計算:在7天內的中度VMS的數量乘以2;在7天內的重度VMS的數量乘以3。
且在將此總數除以在一週的7天期間中度及重度VMS的總數之前,將2個得到的數字加在一起。
在另一實施例中,嚴重程度分數可以根據Archer等人,2014年(A randomized,double-blind,placebo-controlled study of the lowest effective dose of drospirenone with 17A-estradiol for moderate to severe vasomotor symptoms in
postmenopausal women;Menopause,2014;21(3);p.227-235)中描述的方法計算。根據此方法,在7天期間的每一天使用以下公式計算每日嚴重程度分數:在1天內的中度VMS的數量乘以2;在1天內的重度VMS的數量乘以3;將2個得到的數字加在一起;加法結果又除以同一天期間的VMS總數(中度及重度)。
連續7天應用相同的公式,將7個得到的數字加在一起並除以7,以計算中度到重度VMS的「每週平均每日嚴重程度(weekly mean daily severity)」分數。
此外,本文所使用的用語「熱潮紅每週加權分數(Hot Flush Weekly Weighted Score)」對應於考慮頻率及嚴重程度的分數,其藉由使用嚴重程度分數(如上計算)計算:在7天期間[(1x輕度VMS的數量)+(7x中度VMS的數量)+(3x重度VMS的數量)]([(1xNo.of mild VMS)+(2x No.of moderate VMS)+(3xNo.of severe VMS)])。
這種加權分數例如由Notelovitz等人使用(“Initial 17β-Estradiol Dose for Treating Vasomotor Symptoms”;Obstetrics and Gynaecology,Vol.95(5),May 2000,p.726-731)。
在下面的A部分的(c)「熱潮紅每週加權分數」,此方法被用於產生進一步包含在實例1的數據。
在替代實施例中,上述方法的任何組合可被採用來評估VMS的每週嚴重程度及/或頻率。
激素替代療法(Hormone replacement therapy)
本療法通常在至少10天,較佳為至少20天的期間內連續施予雌四醇成分。
雌四醇成分以約15mg至約25mg的每日劑量施予。
在一個具體實施例中,雌四醇成分以約15mg至小於20mg的每日劑量施予。
在另一具體實施例中,雌四醇成分以大於20mg至約25mg的每日劑量施予。
在一個實施例中,本療法施用於非子宮切除的患者。在一個具體實施例中,本療法包含每日施予約20mg的雌四醇成分,較佳地為向非子宮切除的患者施予。
在將本療法施予於經歷子宮切除術的患者的情況下,較佳地為將雌四醇成分作為唯一(sole)的活性成分施予。
當將本療法施用於非子宮切除的患者時,雌四醇成分可作為唯一的活性成分施予、或者可與任選的(optional)黃體酮類成分一起施予。任選的黃體酮類成分可被連續施予(即,每天除了雌四醇成分之外施予)或依次施予(其中,依次地表示在例如每月10至14天、或每3個月14天期間施予黃體酮類成分)。
本文所用的用語「連續的(continuous)」/「連續地(continuously)」是指成分以相對規則的間隔施予,而沒有(治療上地)顯著中斷。自然地,可能發生不會影響本方法的整體有效性的微小中斷,並且實際上這些過失被包含在本發明中。在一較佳實施例中,更具算術性地,如果介於2次隨後施予(subsequent administrations)之間的最長間隔不大於平均間隔的3.5倍,則施予方案被認為是連續的。甚至更佳地,最長間隔不大於平均間隔的2.5倍,最佳地不大於1.5倍。
在一個實施例中,任選的黃體酮類成分藉由非口服途徑施予,例如使用子宮內裝置(Intra Uterine Device,IUD)。在一個實施例中,IUD遞送黃體酮類成分左炔諾黃體酮(levonorgestrel)。在一個這樣的實施例中,IUD是Mirena®IUD或Levosert®IUD。
在一個實施例中,本發明的療法採用口服(oral)、舌下(sublingual)、口頰(buccal)或唇下(sublabial)施予雌四醇成分。後3種施予模式提供了雌四醇成分不必經過消化系統,並且避免了首渡肝臟暴露(first-pass liver exposure)的優點。此外,這些施予模式提供快速的起始作用時間(onset of action)。
本文所用的用語「舌下(sublingual)」是指施予的藥理(pharmacological)途徑,其中雌四醇成分透過舌下組織擴散到血液中。
本文所用的用語「口頰(buccal)」是指施予的藥理途徑,其中雌四醇成分透過頰側邊緣(buccal vestibule)的組織擴散到血液中,所述區域在介於臉頰內(lining of cheek)(頰黏膜(buccal mucosa))與牙齒/牙齦之間的口腔內區域。
如本文所用的用語「唇下(sublabial)」是指施予的藥理途徑,其中雌四醇成分被放置於唇部及牙齦之間的藥理學給藥途徑。
在本方法中,雌四醇及黃體酮類成分可以分開的劑量單位施予。然而,其係為可能且實際上非常方便的是,將這兩種成分組合成單一劑量單位。
在根據本發明的方法中,黃體酮類及雌四醇成分的組合適當地在至少10天的期間內連續施予。
本發明可被適當地簡化為以本領域通常知識者習知的各種施予方法的形式實施。在這些方法中,有使用含有具有恆定量的雌四醇成分及任選的黃體酮類成分的劑量單位之單相製劑(monophasic preparations)的方法。
在選擇黃體酮類成分的依序施予的本發明實施例中,其係為可能且實際上非常方便的是,在施予兩種成分的日子,組合成分為單一劑量單位。
在本發明的一個實施例中,將激素替代療法施予於絕經前期的受試者。在此實施例中,受試者將受益於透過施用本發明的組合物來減輕VMS,同時受益於避孕效果。在特定的絕經前期的群體中,確實經常需要避孕,且由
於VMS在此生命期間發生,因此本發明的治療將在單一且簡單的治療中獨特地解決這兩個需求。
在本發明的另一個實施例中,將激素替代療法施予於絕經後期的受試者。
在本發明的一個具體實施例中,激素替代療法係被有益地施予,以產生對於受試者的吸煙狀況不會影響本發明的治療之優點。其被知道的是,吸煙顯著降低血清雌激素濃度,例如在Bjarnason等人(Bjarnason et al.;Climacteric 2012;Acute and long-term estradiol kinetics in smoking postmenopausal women;15:5;p.449-454)的臨床研究分析中報導的是,在雌激素組中,吸煙導致在所有隨機化時間點的血清雌酮(estrone)及血清雌二醇之兩者的等級顯著降低,而在安慰劑組上,吸煙者及非吸煙者之間沒有差異。Bjarnason等人總結的是:在絕經後女性接受雌激素治療的情況下,吸煙會降低在最低濃度(trough)及2小時後之兩者的血清雌激素,吸煙對雌激素濃度的影響在每天吸煙十支(ten)或更少的女性中充分表現,以及吸煙的影響對於雌激素療法的代謝是恆定的,且對標準吸煙強度(standard smoking intensities)沒有劑量反應(dose-response)。
在此具體實施例中,基於令人驚訝的發現,即本發明的療法不受受試者吸煙狀況的影響,激素替代療法較佳地施予於每天吸菸5支或更多支的患者群體、於每天吸菸10支或更多支的患者群體、或者於每天吸菸15支或更多支的患者群體。
在本發明的另一個具體實施例中,激素替代療法被有益地施予,以產生對於受試者的BMI不會影響本發明的治療之優點。確實令人驚訝地發現的是,與習知技術的激素替代療法相反,本發明的療法的功效不受受試者的BMI值的影響。在此具體實施例中,本發明的激素療法較佳地施予於BMI為25或更高、28或更高、30或更高、33或更高、35或更高、37或更高、或40或更高的受
試者。在此具體實施例中,本發明的激素療法較佳地施予於超重受試者、或者於肥胖受試者。
本發明的激素替代療法被發現為特別有益於減輕絕經相關症狀,同時對肝臟(hepatic)、止血(haemostatic)、內分泌及代謝參數的大部分具有極其有限的影響。事實上,習知技術的HRT治療對這些參數具有負面影響。令人驚訝且非常有益的是,相比之下,本發明的治療被發現不修改或僅僅是最低限度地修改大多數參數。
成分(Compositions)
本發明的雌四醇成分包含選自由雌四醇;雌四醇的酯類,其中至少一個羥基的氫原子被具有1-25個碳原子的烴羧酸、磺酸或胺磺酸的醯基取代;及其組合所組成的群組中的物質。更佳地,雌四醇成分是雌四醇(包含雌四醇水合物)。更佳地,在劑量單位中包含的雌四醇成分是雌四醇單水合物。
本發明的雌四醇成分以相當於從約15mg至約25mg的雌四醇單水合物的每日劑量被使用。換句話說,當雌四醇成分本身不是雌四醇單水合物時,調節雌四醇成分的每日劑量,以產生相當於約15mg至約25mg的雌四醇單水合物的每日劑量的治療效果。
在本發明特別佳的實施例中,根據本發明的藥物組合物被設計來用於每日施予,即其代表每日劑量單位。
在口服給藥的情況下,根據本發明的口服劑量單位較佳地為固體或半固體劑型(solid or semi-solid dosage form),例如片劑(tablets)、膠囊(capsules)、扁囊劑(cachets)、丸劑(pellets)、丸劑(pills)、粉劑及顆粒劑(granules)。用語「固體或半固體劑型」還包含含有液體,例如油的膠囊,其中本發明的雌四醇成分及/或任選的黃體酮類成分溶解或分散於其中。片劑及等效的固體及半
固體劑型可適當地含有諸如結合劑(例如,羥丙基甲基纖維素(hydroxypropylmethyl cellulose)、聚乙烯基吡咯啶酮(polyvinyl pyrrolidone)、其他纖維素材料及澱粉);稀釋劑(例如,乳糖及其他糖、澱粉、磷酸二鈣(dicalcium phosphate)及纖維素材料);崩解劑(例如,澱粉聚合物及纖維素材料);以及潤滑劑(例如,硬脂酸鹽(stearates)及滑石(talc))。這些片劑及等效的固體劑型可以藉由濕式造粒,例如使用水溶液或有機溶液製備,也可以藉由直接壓製來製備。
在舌下、口頰或唇下施予的情況下,根據本發明的藥物組合物較佳地為口頰分散劑量單位(orodispersible dosage unit)。
本文所使用的用語「口頰分散劑量單位」是指劑量單位,其被設計,當它與唾液接觸並將雌四醇成分散到唾液中時,其在口腔中快速崩解,因此其可透過口腔的黏膜組織(mucosal lining)吸收。
當劑量單位是口頰分散劑量單位時,可以使用根據Ph.Eur.2.9.1(“Disintegration of tablets and capsules”)及USP<701>(“Disintegration”)的崩散測試,例如,使用水作為崩解介質,可適當地判斷從劑量單位釋放雌四醇成分的速率。當進行上述崩解測試時,本發明的口頰分散固體劑量單位通常在小於5分鐘內,更佳地在小於2分鐘內,又更佳地小於1.5分鐘內,又更佳地小於1分鐘內,又更佳地小於45秒內,且最佳地小於30秒內崩解。
當患者仍有子宮時,除了雌四醇成分外,還可以施予任選的黃體酮類成分。
根據本發明,可被適當地使用的黃體酮類成分的實例包含:左炔諾黃體酮、諾孕酯(norgestimate)、炔諾酮(norethisterone)、地屈黃體酮、屈螺酮、3-β-羥基去氧孕烯(3-beta-hydroxydesogestrel)、3-酮去氧孕烯(3-ketodesogestrel)、17-去乙醯基諾孕酯(17-deacetylnorgestimate)、19-去甲孕酮(19-norprogesterone)、乙醯氧基孕烯諾龍(acetoxypregnenolone)、烯丙雌醇(allylestrenol)、阿那孕酮
(amgestone)、氯地孕酮(chlormadinone)、環丙孕酮(cyproterone)、地美孕酮(demegestone)、去氧孕烯(desogestre)、地諾孕素(dienogest)、二氫孕酮(dihydrogesterone)、地美炔酮(dimethisterone)、炔孕酮(ethisterone)、二乙酸炔諾醇(ethynodiol diacetate)、乙酸氟孕酮(fluorogestone acetate)、孕三烯酮(gastrinone)、孕二烯酮(gestodene)、孕三烯酮(gestrinone)、羥基甲基孕酮(hydroxymethylprogesterone)、羥基孕酮(hydroxyprogesterone)、利奈孕醇(lynestrenol)、美屈孕酮(mecirogestone)、甲羥孕酮(medroxyprogesterone)、甲地孕酮(megestrol)、美侖孕酮(mele,gestrol)、諾美孕酮(nomegestrol)、去甲基脫氫羥孕酮(norethindrone)、異炔諾酮(norethynodrel)、炔諾孕酮(norgestrel)(包含d-炔諾孕酮(d-norgestrel)及d1-炔諾孕酮(dl-norgestrel))、諾孕烯酮(norgestrienone)、甲諾酮(normethisterone)、孕酮(progesterone)、奎孕醇(quingestanol)、(17α)-17-羥基-11-伸甲基-19-去甲孕甾(norpregna)-4((17alpha)-17-hydroxy-11-methylene-19-norpregna-4)、15-二烯-20-炔-3-酮(15-dien-20-yn-3-one)、替勃龍(tibolone)、曲美孕酮(trimegestone)、醋苯阿爾孕酮(algestone-acetophenide)、乙酸烯諾孕酮(nestorone)、普美孕酮(promegestone)、17-羥基孕酮酯(17-hydroxyprogesterone esters)、19-去甲-17-羥基孕酮(19-nor-17hydroxyprogesterone)、17α-乙炔基-睪酮(17alpha-ethynyltestosterone)、17α-乙炔基-19-去甲-睪酮(17alpha-ethynil-19-nortestosterone)、d-17β-乙醯氧基-13β-乙基-17α-乙炔基-甾-4-烯-3-酮肟(d-17beta-acetoxy-13beta-ethyl-17alpha-ethynylgon-4-en-3-one oxime)、6β-7β-15β-16β-二伸甲基-3-氧代-17-孕-4,9(11)-二烯-21(6beta,7beta;15beta,16beta-dimethylene-3-oxo-17-pregna-4,9(11)-diene-21)、17β-內酯(17beta-carbolactone)或他那羅特(tanaproget)及此些化合物的前驅物,其中,當被用於本發明方法時,所述前驅物能夠在體內釋放這些黃體酮(progestogens)。
較佳地,本方法中使用的黃體酮類成分選自由黃體酮、屈螺酮、地屈黃體酮、此些黃體酮的前驅物及其混合物。
在一個實施例中,本發明提供了包含雌四醇成分及黃體酮的組合組合物(combination composition)。
在一個實施例中,本發明提供了包含雌四醇成分及屈螺酮的組合組合物。
在一個實施例中,本發明提供包含雌四醇成分及地屈黃體酮的組合組合物。
當本發明的黃體酮類成分是屈螺酮時,較佳地以從0.5mg至10mg,甚至更佳地以從1mg至4mg的每日劑量使用。
當本發明的黃體酮類成分是地屈黃體酮時,較佳地以從約5mg至約10mg的每日劑量使用,更佳地以約5mg的每日劑量使用。
當本發明的黃體酮類成分是黃體酮時,較佳地以從50mg至200mg的每日劑量使用。在一個實施例中,當其被連續使用時,黃體酮以50mg至100mg的每日劑量使用。在另一個實施例中,當其被依次使用時,黃體酮以100mg至200mg的每日劑量使用,例如當其在每月施用約14天的期間施予時。
當使用不同的黃體酮類成分時,調整每日劑量以產生與50mg至200mg的黃體酮劑量相同的藥理作用。
在本發明的較佳實施例中,組合物將雌四醇成分及任選的黃體酮類成分組合成單一劑量單位,較佳地為每日劑量單位。在本發明更佳實施例中,所述經組合的每日劑量單位是口服的經組合的每日劑量單位。
在一個實施例中,本發明提供口服的經組合的每日劑量單位,其包含雌四醇成分及黃體酮。
在一個實施例中,本發明提供口服的經組合的每日劑量單位,其包含雌四醇成分及屈螺酮。
在一個實施例中,本發明提供口服的經組合的每日劑量單位,其包含雌四醇成分及地屈黃體酮。
在本發明的較佳實施例中,提供口服的經組合的每日劑量單位,其組合約20mg的每日劑量的雌四醇與約100mg的每日劑量的黃體酮。
在本發明的另一實施例中,雌四醇成分被施予至仍然具有子宮的患者,且一併施予選擇性雌激素受體調節劑(SERM),特別是與巴多昔芬一併使用。巴多昔芬較佳以約10mg至50mg的每日劑量施予。更佳地,巴多昔芬以約20mg的每日劑量施予。
在一個實施例中,本發明提供包含雌四醇成分及巴多昔芬的組合療法。
在一個實施例中,本發明提供口服的經組合的每日劑量單位,其包含雌四醇成分及巴多昔芬。
參考多個例示性實施例,本發明被如上描述。一些部份或元件的修改及替代實施方式為可能的,且被包含在所附申請專利範圍中定義的保護範圍內。
實例
實施例1-選擇每日口服劑量的雌四醇(E4)用於治療絕經後女性血管舒縮症狀的劑量研究
研究登記及持續時間:
登記時間為約18個月。在個體受試者中,參與時間(participation)長達27週:預篩檢(washout)及沖洗(washout)後長達6週;篩檢及試用階段(run-in
period)最長達4週,E4/安慰劑治療最長達91天(13週),然後是2週(14天)的黃體酮治療,且僅在非經子宮切除的(non-hysterectomised)受試者中完成黃體酮治療後1週的隨訪(Follow up visit)。
主要功效目標:
藉由評估中度至重度血管舒縮症狀(VMS)的頻率及嚴重程度的變化來定義E4的口服劑量的最小有效劑量(MED)。
方法學:
這是一項前瞻性、多中心、隨機、安慰劑對照、雙盲、找尋劑量的研究。
受試者群體:
符合條件的受試者是經子宮切除的及非經子宮切除的40至65歲的絕經後女性,包含表現每天至少7次中度至重度熱潮紅、或每週至少50次中度至重度熱潮紅。
診斷及入選標準:
受試者在隨機化訪視時符合以下所有入選標準。在篩檢期間評估這些標準:
1、年齡在40至65歲之間的女性,包含在進行隨機化前一週中表現每天至少7次中度至重度熱潮紅、或每週至少50次中度至重度熱潮紅。
2、身體質量指數(BMI)介於18.0及35.0kg/m2(含)之間。
3、被定義為高促卵泡激素(FSH)>40IU/L)等級之絕經後狀態,且:-閉經(amenorrhoea)至少連續12個月;或-閉經至少6個月,且雌二醇(E2)<20pg/mL;或
-無論是否進行子宮切除術,至少需要在雙側卵巢切除術(bilateral oophorectomy)之術後6週提供病理報告的複本、或從受試者醫師的抬頭信件,以證明兩個卵巢均被切除。
5、陰性妊娠試驗。
6、根據醫學、外科及婦科病史;體格檢查;婦科檢查;臨床實驗室及生命體徵,在首席研究員(Principal Investigator,PI)的判斷下,身體及心理健康狀況良好。
7、在進入研究之前,受試者已提供經簽署並已註明日期的書面知情同意書。
8、受試者能夠理解並遵守協議要求、指令及協議規定的限制。
排除標準:
如果在隨機化訪視中存在以下排除標準中的一個,則排除潛在的研究受試者。在篩檢期間評估了這些標準:
1、對於非經子宮切除的女性:子宮疾病或醫療狀況,其包含:a、藉由TVUS判斷雙層子宮內膜厚度>5mm;b、子宮肌瘤的存在使TVUS無法評估子宮內膜;c、子宮癌的病史或存在;d、存在子宮內膜增生;e、存在子宮內膜息肉且伴隨增生或惡性上皮。
2、在過去12個月的未經診斷之陰道出血。
3、任何惡性腫瘤(history of malignancy)史,除了基底細胞(如果在前2年內排除)或鱗狀細胞(如果在前一年內排除)皮膚癌。在乳房檢查中的任何臨
床重要發現及/或乳房攝影檢查(mammography)中懷疑乳腺惡性腫瘤,都需要額外的臨床試驗以排除乳腺癌(但是,藉由超音波確認的簡單囊腫被允許)。注意:除非受試者有過去9個月內進行的乳房攝影檢查的書面文件,否則需要進行乳房攝影檢查的篩選。
4、在非子宮切除受試者的子宮頸抹片異常(Abnormal cervical Pap smear)(過去18個月內的測試的書面文件或篩選檢查中的測試),子宮頸發育不良的證據大於低度鱗狀上皮內病變(low grade squamous intraepithelial lesion,LSIL)。錄取診斷為具有不確定意義的非典型鱗狀細胞(ASCUS)的女性。
5、收縮壓(BP)在90至140mmHg範圍之外,舒張壓在60至90mmHg之外,及/或心率在40至100bpm範圍之外。如果他們符合入選/排除標準,則錄取具有控制穩定的抗高血壓方案的患有輕度至中度高血壓的受試者。
6、篩選12導程心電圖(12-lead ECG)上判斷任何臨床顯著異常。
7、靜脈或動脈血栓栓塞性疾病(例如,深靜脈血栓形成(deep vein thrombosis)、肺栓塞(pulmonary embolism)、中風(stroke)、心肌梗塞(myocardial infarction)、心絞痛(angina pectoris)等)的歷史,已知凝血病史或凝血因子異常。
8、藉由葡萄糖超出正常範圍且糖化血紅蛋白超過7%的實驗值進行評估,在過去6個月中血糖控制不佳的糖尿病。
9、血脂異常脂蛋白血症(Dyslipoproteinaemia)使受試者易患動脈粥樣硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)。如果使用ASCVD風險評估(ACC/AHA心血管風險評估指南(Cardiovascular risk assessment guideline),2013)計算,受試者具有10年ASCVD評分5%,則她不能包含於此試驗。在所有情況下,LDL膽固醇等級190mg/dL或三酸甘油脂血漿等級>400mg/dL是被排除的。
如果受試者正在接受降脂(lipid-lowering)治療,則在篩選前她的治療必須保持穩定劑量至少1個月,並且必須使用相同的資格標準。
10、抽菸>10支(cigarettes)/天、或使用用於電子煙之含尼古丁的液體>1mL/天。
11、除非進行了膽囊切除術,膽囊疾病的存在或病史。
12、系統性紅斑狼瘡(Systemic lupus erythematosus)。
13、多發性硬化症(Multiple sclerosis)。
14、急性或慢性肝病。
15、急性或慢性腎功能損害,包含重度的腎功能損害。
16、不受控制的甲狀腺疾病。
17、受試者在2年內有嚴重憂鬱症或創傷後壓力疾患(PTSD)的病史、或者在任何時間有其他嚴重精神疾病史(例如,精神分裂症(schizophrenia)、躁鬱症(bipolar disorder)等)。
18、使用含有雌激素或黃體酮的藥物。如果使用以下情況,在試用階段之前需要沖洗期:a、陰道激素產品(環(rings)、乳霜、凝膠):沖洗至少4週;b、經皮(Transdermal)雌激素或雌激素/黃體酮:沖洗至少4週;c、口服雌激素及/或黃體酮:沖洗至少4週;d、子宮內黃體酮治療:沖洗至少4週;除非治療在超過3個月前停止,否則黃體酮植入物或雌激素單獨注射藥物治療的當前使用者不被允許參與。除非治療在超過6個月前停止,否則不允許使用雌激素丸劑治療、或黃體酮注射藥物治療的使用者參與。
19、使用非激素治療來減少熱潮紅。在使用非激素處方及非處方(over-the-counter,OTC)治療熱潮紅(像是:抗憂鬱藥帕羅西汀(paroxetine)、依他
普崙(escitalopram)、文拉法辛(venlafaxine)及可樂定(clonidine)、或植物雌激素,黑升麻(black cohosh)等)的情況下,在試用階段之前需要1週的沖洗期。如果這些治療中的一種同時與含有雌激素或黃體酮的藥物一起服用,則可以組合沖洗期並且不必依序。
20、在試用階段之前28天內使用可能影響VMS終點結果的藥物。此包含(但不限於):SSRIs[選擇性5-羥色胺再攝取抑制劑(selective serotonin reuptake inhibitors)]、SNRIs[5-羥色胺及去甲腎上腺素再攝取抑製劑(serotonin and norepinephrine reuptake inhibitors)]、多巴胺能(dopaminergic)或抗多巴胺能(antidopaminergic)藥物或加巴噴丁(gabapentin)。
21、研究產品或此類藥物過敏的歷史或存在、或在研究者認為禁止受試者參與的選項內的藥物或其他過敏史。
22、對研究產品的任何成分的過敏或不耐受的歷史或存在。
23、由調查員判斷在12個月內酒精或藥物濫用或依賴的歷史,即受試者消耗過量酒精、濫用藥物、或者具有可能影響受試者遵守研究者認為的研究要求的能力的條件。
24、贊助商或受託研究機構(Contract Research Organization,CRO)員工、或調查員部門的人員以及與本研究相關的親屬。
25、具有紫質症(porphyria)的受試者、及具有臨床上顯著的系統性疾病、不穩定的醫學疾病、危及生命的疾病或當前惡性腫瘤的已知或懷疑病史的受試者,或研究人員認為目前可能對受試者造成風險的惡性腫瘤。
26、在1個月(30天)內參與另一項研究藥物臨床研究、或在最近3個月(90天)內接受過研究藥物。
27、由調查員判斷因任何原因而不適合。
受試者數量:
意向分析原則(Intention-To-Treat Principle)
此原則宣稱,藉由基於受試者的治療(即,經計劃的治療方案)的意向,而不是給出的實際治療進行評估,可以最好地評估治療政策的效果。其結果是,無論他們是否遵守經計劃的治療方案,分配給治療組別的受試者應作為該組的成員進行隨訪、評估與分析。
此外,意向分析原則暗示著主要分析應包含所有隨機受試者。
保持分析中的初始隨機化對於預防偏倚(bias)及為統計檢驗提供可靠性基礎(secure foundation)非常重要。在許多臨床試驗中,完整分析集的使用提供了保守策略。在許多情況下,其還可能提供治療效果的估計值,所述估計值更可能反映在隨後的實施中觀察到的效果。
在本研究中,意向分析組別包含總共257名患者。
將受試者以1:1:1:1:1的比例隨機分配到5個治療目標中的一個。隨機化按中心分層。
研究訪問:
測試產品及參考治療、劑量及給藥模式
所有治療(雌四醇,下文稱E4,[2.5mg、5mg、10mg、15mg]膠囊)每天一次(QD)口服(per os)給藥至少連續12週,直到執行最後的生物學評估(最大值為第91天)為止。
安慰劑,1個膠囊口服QD至少連續12週,直到執行最後的生物學評估(最大值為第90天)為止。
如果在試驗過程中,由非子宮切除的女性報告在TVUS檢測到雙層子宮內膜厚度15mm、及/或異常子宮出血(婦科醫生根據雌激素治療判斷),她接受子宮內膜活檢,且除了E4/安慰劑治療外,用黃體酮(10mg地屈黃體酮)QD依序進行治療(即,14天黃體酮治療期,然後是暫停14天黃體酮治療)直至第11週結束。如果子宮內膜活檢顯示子宮內膜增生,則立即停止受試者參與,並根據當地指南進行增生治療。如果在第一次正常子宮內膜活檢後再次發生異常子宮出血,則進行徹底的婦科檢查及TVUS。如果在婦科醫生的判斷中為需要,則進行第二次子宮內膜活檢。
在E4/安慰劑治療期後,所有非子宮切除的受試者(包含之前接受過黃體酮的受試者)接受使用10mg地屈黃體酮QD之黃體酮治療14天。
結果
A、5個治療組中每一個的血管舒張能力(vasomotors)參數
a、VMS頻率
i、在中度至重度VMS的每週頻率的絕對變化(從基線的平均變化)
a)每個小組每週一次
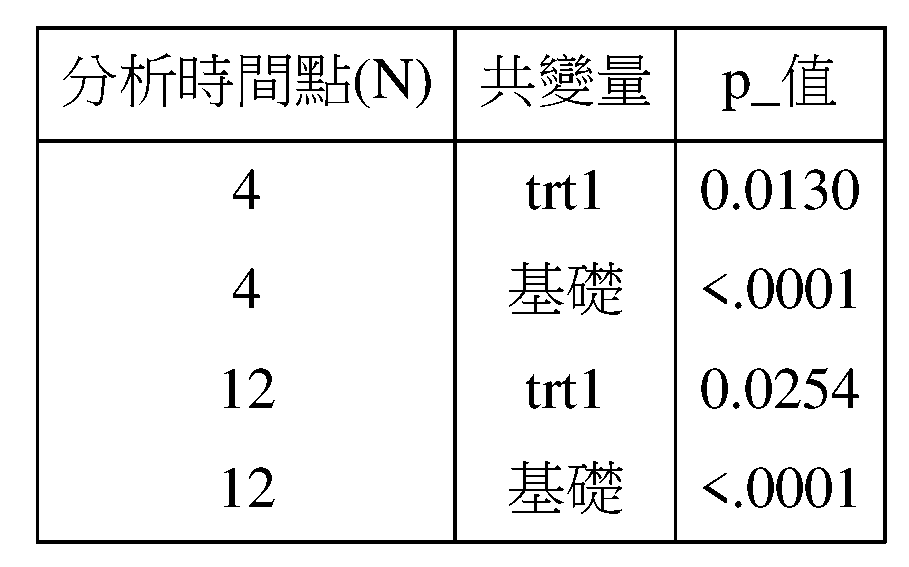
為了分析本研究中記錄的數據,使用ANCOVA(協方差分析)比較治療組別對於第4週及第12週從基線的中度至重度VMS每週頻率的變化。ANCOVA模型包含治療(「trt1」)及研究中心(study centre)(「SITEPOOL」)作為固定效應及基線(「基礎(base)」)作為共變量(covariate)。
b)共變量顯著性(significance)
下表顯示了所有治療組別的比較。
經審查,認為研究中心的影響不是很重要,且第二次ANCOVA在沒有考慮研究中心的情況下進行。
沒有位置效應(Site Effect)
c)下表顯示了按週及治療從基線的平均變化:
沒有位置效應
藉由提出最小平方(Least Square)調整的平均值(LS調整平均值:此組意味著控制共變量之後;也稱為邊緣平均值(marginal means)或經估計的邊緣平均值(estimated marginal means))及相應治療效果的95%信賴區間(confidence
intervals)來支持所有統計檢驗。這些LS調整平均值及信賴區間係基於用於分析的統計模型。
信賴區間暗示著如果在多個場合對相同群體進行抽樣,且在每個場合都進行區間估計,得到的區間將在大約95%的情況下包含真實的群體參數。
d)下表顯示了按週及治療與安慰劑的差異
沒有位置效應
從此表中可以看出的是,15mg每日劑量在4週時(在第一次統計分析中p值為0.10653,且在沒有合併位點(pooled site)的分析中為0.06834)及12週(在第一次統計分析中p值為0.10838,且在沒有合併位點的分析中為0.07057)與安慰劑產生幾乎統計學上顯著的差異。
ii、中度至重度VMS每週頻率的相對變化(從基線起的%)
a)每個小組每週一次
從此表中可以看出的是,與基線相比,15mg每日劑量導致中度至重度VMS頻率降低超過80%。
b)共變量顯著性
下表顯示了所有治療組別的比較。
沒有位置效應
c)下表顯示了按週及治療從基線的平均相對變化(%)
沒有位置效應
d)下表顯示了按週及治療與安慰劑的差異
從此表中可以看出的是,15mg每日劑量在12週時與安慰劑產生統計學顯著差異(p值為0.03771),並且在4週時與安慰劑幾乎具有統計學顯著性差異(p值為0.05622)。
藉由與10mg劑量獲得的經提升的p值相較,觀察到的是,15mg劑量獲得的低p值尤其引人注目。
沒有位置效應
從此表中可以看出的是,在不考慮位置效應的統計分析中,15mg每日劑量在4週(p=0.03206)及12週(p=0.02210)與安慰劑產生統計學顯著差異。
藉由與10mg劑量獲得的經提升的p值相較,觀察到的是,15mg劑量獲得的低p值尤其引人注目。
iii、中度至重度VMS每週頻率的反應者(responders)組的頻率變化
亦藉由根據他們的反應程度對患者進行分組來研究VMS頻率。
準備顯示50%或更高的反應(從基線的相對變化)的第一組患者。根據此分析,在第12週,15mg每日劑量組包含91.8%的反應者,而安慰劑組包含65.5%的反應者。這兩組之間的p值差異低於0.01,而10mg每日劑量組及安慰劑組之間的差異無統計學意義(p值>0.1)。
準備顯示75%或更高反應的第二組患者。根據此分析,在第12週,15mg每日劑量組包含77.6%的反應者,而安慰劑組包含43.6%的反應者。這兩組之間的p值低差異於0.001,而10mg每日劑量組及安慰劑組之間的差異無統計學意義(p值>0.05)。
b、VMS嚴重程度
i、在中度至重度VMS的每週嚴重程度的絕對變化(從基線的平均變化)
a)每個小組每週一次
為了更好地分析本研究中記錄的數據,使用ANCOVA(協方差分析),從每個活性(active)治療與安慰劑,在第4週及第12週,從輕度、中度及重度VMS的基線到中度至重度的嚴重程度的改變,來比較治療組別。對於在第4週及/或第12週經歷100%VMS緩解的女性,歸於零值。ANCOVA模型包含作為固定效應的治療(「trt1」)及作為共變量的基線(「基礎」)。
b)共變量顯著性
下表顯示了所有治療組別的比較。
c)下表顯示了按週及治療從基線的平均變化:
d)下表顯示了按週及治療與安慰劑的差異
從此表中可以看出的是,15mg每日劑量在第4週(p值為0.0486)及第12週(p值為0.0489)時與安慰劑產生統計學顯著差異。因此,與安慰劑相較,15mg劑量在第4週及第12週顯著改善VMS的嚴重程度。
對於嚴重程度參數,10mg和15mg劑量之間的差異也令人印象深刻:此首先反映在以上部分c)中的表格內的從基線的平均變化中,例如在12週
時,10mg的LS調整平均值為-0.69(與從安慰劑組可知為-0.66相比),而15mg每日劑量組為-1.04。其反映出的明顯差異是,當從每天10mg轉換為每天15mg時,在第4週的p值提高接近8倍,且當從每天10mg轉換為每天15mg時,在第12週的p值提高20倍以上。
ii、中度至重度VMS的每週嚴重程度的相對變化(從基線起的%)
a)每個小組每週一次
從此表中可以看出的是,與基線相比,15mg每日劑量導致中度至重度VMS嚴重程度降低超過40%。
b)共變量顯著性
下表顯示了所有治療組別的比較。
c)下表顯示了按週及治療從基線的平均相對變化
d)下表顯示了按週及治療與安慰劑的差異
從此表中可以看出的是,15mg每日劑量在12週(p值為0.0568)時與安慰劑產生幾乎統計學上顯著的差異。與安慰劑相較,15mg的每日劑量改善在第4週及第12週的VMS嚴重程度,而10mg的每日劑量在這裡再次難與安慰劑進行區分,特別是在第12週。
c、熱潮紅每週加權分數
i、每週加權分數的絕對變化(從基線的平均變化)
a)每個小組每週一次
b)共變量顯著性
下表顯示了所有治療組別的比較。
c)下表顯示了按週及治療從基線的平均變化:
d)下表顯示了按週及治療與安慰劑的差異
每週加權分數的相對變化(從基線起的%)
a)每個小組每週一次。
b)共變量顯著性
下表顯示了所有治療組別的比較。
c)下表顯示了按週及治療從基線的平均相對變化。
d)下表顯示了按週及治療與安慰劑的差異。
從此表中可以看出的是,15mg每日劑量在第4週(p值為0.0267)及第12週(p值為0.0276)時與安慰劑產生統計學顯著差異。
藉由與10mg劑量獲得的經提升的p值相較,觀察到的是,15mg劑量獲得的低p值尤其引人注目。
B.與安慰劑及無效(inefficient)劑量(2.5mg及5mg)組一同比較,10mg及15mg組的血管舒縮參數
基於上文A部分中觀察到的結果,顯而易見的是,經測試的兩個最低劑量(每天2.5mg及每天5mg)未顯示功效。由此製備了對結果的進一步分析,其中來自這兩個劑量的數據與安慰劑劑量被進行分組,並與10mg及15mg劑量進行比較。
1、中度至重度VMS每週頻率的相對變化(從基線起的%)
a)每個小組每週一次
b)共變量顯著性
c)與安慰劑成對(pairwise)比較(包含無效劑量2.5mg及5mg)
d)與安慰劑的差異(包含無效劑量2.5mg及5mg)
如上文A)部分已經提到的,藉由與從10mg每日劑量獲得的經提升的p值相較,觀察到15mg每日劑量獲得的低p值是特別引人注目的,證明用15mg每日劑量獲得的獨特的緩解。
2、熱潮紅每週加權分數的相對變化(從基線起的%):
a)每個小組每週一次。
b)共變量顯著性。
c)與安慰劑成對比較(包含無效劑量2.5mg及5mg)
d)與安慰劑的差異(包含無效劑量2.5mg及5mg)。
如上文A)部分已經提到的,可以看出的是,15mg每日劑量在第4週(p值為0.00178)及第12週(p值為0.00097)時與安慰劑產生統計學顯著差異。
同樣,藉由與10mg劑量獲得的經提升的p值相較,觀察到的是,15mg劑量獲得的低p值尤其引人注目。
C.絕經評定量表
絕經評定量表(MRS)是一種與健康相關的生活品質量表,可藉由評估症狀特徵來衡量年齡/絕經相關投訴(age-/menopause-related complaints)的嚴重程度(Heinemann et al.,2003,“International versions of the Menopause Rating Scale(MRS)" Health Qual Life Outcomes 1:28;Heinemann et al.,2004,"The Menopause Rating Scale(MRS)scale:A methodological review".Health Qual Life Outcomes 2:45;Heinemann et al.,2004,"The Menopause Rating Scale(MRS)as outcome measure for hormone treatment?A validation study".Health Qual Life Outcomes 2:67)。
隨著11個項目中的每個項目中主觀感知的投訴的嚴重程度增加,評分逐漸增加(嚴重程度在每個項目中以0到4點表示)。藉由檢查在問卷中每個項目的這5個可能的「嚴重程度」欄框,被訪者提供了她的個人感知。總MRS評分介於0(無症狀(asymptomatic))至44(最高投訴程度(highest degree of complaints))之間。取決於分配給各個症狀維度(dimension)的投訴數量,最小/最
大分數在三個維度之間變化(Heinemann et al.,2003,Health Qual Life Outcomes 1:28):1.心理症狀:0到16分得分(4個症狀:憂鬱(depressed)、煩躁(irritable)、焦慮(anxious)、精疲力竭(exhausted));2.軀體營養(somato-vegetative)症狀:0至16分(4個症狀:出汗/潮紅(sweating/flush)、心臟類投訴(cardiac complaints)、睡眠障礙、關節及肌肉類投訴(joint & muscle complaints));3.泌尿生殖系統症狀:0至12分(3個症狀:性功能障礙(sexual problems)、泌尿類投訴(urinary complaints)、陰道乾澀)。
總MRS分數
絕經評定量表(MRS)指出具有對15mg劑量的影響最大之生活品質的總體改善。在此劑量下,藉由與p值為0.0113之第4週的安慰劑及接近統計學顯著的效果之p值為0.0694之第12週相較,觀察到的是統計學上顯著的效果。
D.泌尿生殖系統症狀(Genito-urinary symptoms,GSM)
記錄以下GSM症狀(VVA受試者自我評估)從基線到第12週的變化:
與第12週的安慰劑相比,*p<0.05。
*與第12週的安慰劑相比,*p<0.05;與第12週時的安慰劑相比,**p<0.001。
#有些患者沒有性活動
VVA症狀的演變指向對15mg每日劑量具有最強效果之總體改善。對於與性活動有關的陰道疼痛,5、10與15mg每日劑量與安慰劑有顯著差異,其p值分別為0.0246、0.0004與0.0006。然而,通常被認為是最令人煩惱的症狀的陰道乾燥僅藉由p值為0.0291之15mg每日劑量顯著改善。
E.與治療副作用(treatment side effects)有關的測量
1、活檢患者數量
2、不良事件(Adverse Events,AEs)
從上表中可以看出,15mg組中的患者比10mg組中的患者呈現更少的TEAE。在10mg組中患有AE的患者中,平均每位患者為3.2AE。相較而言,15mg組中,患有AE的患者平均為2.6AE。全球性地,這些數據表明的是,15mg每日劑量可顯著緩解VMS,而不會為患者產生額外的AE。此外,每天15mg的組別的活組織檢查需求比每天10mg的組別更少。
這藉由以下統計分析得到證實。對患者及治療組使用具有隨機效應的泊松回歸模型(poisson regression model)作為共變量,來模擬不同治療組別中TEAE的數量,其可以顯示的是,治療組別之間沒有統計學差異(p值為0.099)。其次,使用卡方檢驗(chi-square test)來評估在每個治療組別中經報告TEAE的患者的盛行率(prevalence)是否相似。治療組別之間未發現統計學差異(p值為0.575)。
3、離開研究的患者
F.以15mg及20mg每日劑量進行的測量
為了更好地評估每日劑量增加超過15mg之每日最小有效劑量的可能性,在研究中遵循許多參數,其中以每天20mg之經增加的劑量給予雌四醇。
1、三酸甘油脂等級(mmol/L)
*20mg劑量治療結束28天後及15mg劑量治療結束12週後治療結束。
2、葡萄糖等級(mmol/L)
*20mg劑量治療結束28天後及15mg劑量治療結束12週後治療結束。
3、膽固醇等級(mmol/L)
*20mg劑量治療結束28天後及15mg劑量治療結束12週後治療結束。
4、高密度脂蛋白膽固醇(HDL-cholesterol)等級(mmol/L)
*20mg劑量治療結束28天後及15mg劑量治療結束12週後治療結束。
5、低密度脂蛋白膽固醇(LDL-cholesterol)等級(mmol/L)
*20mg劑量治療結束28天後及15mg劑量治療結束12週後治療結束。
從上述5個表中可以觀察到的是,當使用20mg每日劑量取代15mg每日劑量時,這些脂質參數及葡萄糖等級沒有表現出顯著地不同。
6、骨膠原蛋白碳末端肽鏈(C-terminal telopeptide,CTX-1)(ng/L)
*20mg劑量治療結束28天後及15mg劑量治療結束12週後治療結束。
CTX-1是骨吸收(bone resorption)的特異性標誌物。
在上表中,可以看出15mg每日劑量導致骨吸收的小幅下降,且此效果在以20mg每日劑量治療28天後已經更明顯。
G.以15mg及30mg每日劑量進行的測量
根據隨機化代碼,對健康女性(介於15至50歲之間)施予以下治療。
安慰劑(n=16);15mg組:依序單次口服15mg雌四醇/3mg屈螺酮(a single oral dose of 15mg Estetrol/3mg Drospirenone followed)(n=10),14天沖洗後,多次口服15mg雌四醇/每日一次3mg屈螺酮(by multiple oral doses of 15mg Estetrol/3mg Drospirenone once daily for 14days)(n=10),持續14天;30mg組:依序單次口服30mg雌四醇/6mg屈螺酮(a single oral dose of 30mg Estetrol/6mg Drospirenone,followed,)(n=10),14天沖洗後,多次口服30mg雌四醇/每日一次6mg屈螺酮(by multiple oral doses of 30mg Estetrol/6mg Drospirenone once daily for 14days)(n=10),持續14天。
從第一次入院到隨訪完成(在第一天治療後37至42天之間)記錄不良事件。
%=報告一或多個AE的受試者人數佔相應治療組的受試者總數的百分比
總體而言,單一劑量施予及14天每日一次口服施予雌四醇/屈螺酮的劑量範圍為15mg雌四醇/3mg屈螺酮至30mg雌四醇/15mg屈螺酮,對於健康女性受試者來說是安全且耐受性良好的研究。隨著單次及多次雌四醇/屈螺酮劑量的增加(劑量加倍),觀察到TEAE或TEAE數量的受試者百分比沒有增加。
因此,有必要設想一種用於緩解絕經相關的症狀之激素替代療法,其使用介於最小有效劑量之15mg及20mg或藉由以上數據的擴展之甚至25mg之間的雌四醇每日劑量,將允許獲得更好的利益-風險概況(benefit-to-risk profile)。將雌四醇劑量增加到15mg的每日最小有效劑量確實可以在VMS緩解及骨吸收等參數上提供上述更好的功效,同時保持出色的安全性(包含但不限於,不良事件,如上文E)2及G)部分所示)、及如上文F)1)至5)部分所示之特定的脂質參數與葡萄糖等級。當患者開始激素替代療法時,增加雌四醇至超過15mg的每日最小有效劑量也可以更快地緩解症狀。
Claims (12)
- 一種雌四醇(estetrol)成分用於製備緩解絕經相關血管舒縮症狀(VMS)之藥物的用途,其中該藥物係配製為每日口服劑量單位,並包含約20mg的雌四醇單水合物(estetrol monohydrate)。
- 如請求項1所述的用途,其中包含一黃體酮類(progestogenic)成分的一第二組合物被額外地使用。
- 如請求項2所述的用途,其中該黃體酮類成分選自屈螺酮(drospirenone)、黃體酮(progesterone)與地屈黃體酮(dydrogesterone)。
- 如請求項3所述的用途,其中黃體酮以從50mg至200mg的每日給藥劑量被施予。
- 如請求項1所述的用途,其中包含巴多昔芬(bazedoxifene)的一第二組合物被額外地使用。
- 如請求項2至5中的任一項所述的用途,其中包含該黃體酮類成分或巴多昔芬的該第二組合物與包含該雌四醇成分的組合物相同。
- 一種用於緩解絕經相關血管舒縮症狀(VMS)之包裝單元的用途,其包含至少21個,較佳地為至少28個容器,該容器係用於保存經單獨包裝且能單獨地移除的每日固體口服劑型,其中該容器的每一個包含含有約20mg的雌四醇單水合物(estetrol monohydrate)。
- 如請求項7所述的包裝單元的用途,其中該包裝單元額外地包含至少10個,較佳地為12個,更佳地為14個額外容器,該 額外容器係用於保存經單獨包裝且能單獨移除的每日,較佳地為固體,口服劑型,其中該額外容器的每一個包含至少一,較佳地為固體,含有一黃體酮類成分的劑型。
- 如請求項8所述的包裝單元的用途,其中該黃體酮類成分選自屈螺酮、黃體酮與地屈黃體酮。
- 如請求項9所述的包裝單元的用途,其中該黃體酮類成分係為黃體酮,且其中該額外容器的每一個包含含有約200mg的黃體酮的至少一劑型。
- 如請求項7所述的包裝單元的用途,其中該包裝單元額外包含相同數量的額外容器,該額外容器用於保存經單獨包裝且能單獨移除的每日固體口服劑型,其中該額外容器中的每一個包含含有一黃體酮類成分的至少一固體劑型,其中該黃體酮類成分較佳地選自屈螺酮、黃體酮與地屈黃體酮,其中該黃體酮類成分甚至更佳地為黃體酮,且其中該額外容器包含含有約100mg的黃體酮的至少一固體劑型。
- 如請求項7所述的包裝單元的用途,其中該固體劑型的每一個額外地包含一黃體酮類成分。
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18168336 | 2018-04-19 | ||
| EP18168336.8 | 2018-04-19 | ||
| EP18174982 | 2018-05-30 | ||
| EP18174982.1 | 2018-05-30 | ||
| EP19150423.2 | 2019-01-04 | ||
| EP19150423 | 2019-01-04 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| TW202017573A TW202017573A (zh) | 2020-05-16 |
| TWI801561B true TWI801561B (zh) | 2023-05-11 |
Family
ID=66440000
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW108113543A TWI801561B (zh) | 2018-04-19 | 2019-04-18 | 化合物及其用於緩解絕經相關症狀的用途 |
Country Status (29)
| Country | Link |
|---|---|
| US (5) | US11452733B2 (zh) |
| EP (4) | EP4154893A1 (zh) |
| JP (3) | JP7308925B2 (zh) |
| KR (2) | KR102748805B1 (zh) |
| CN (3) | CN115645415A (zh) |
| AU (2) | AU2019254680B2 (zh) |
| BR (1) | BR112020021211A2 (zh) |
| CA (1) | CA3097278C (zh) |
| CL (1) | CL2020002710A1 (zh) |
| CO (1) | CO2020012603A2 (zh) |
| CR (1) | CR20200485A (zh) |
| CU (1) | CU20200073A7 (zh) |
| EC (1) | ECSP20066226A (zh) |
| GE (2) | GEP20227395B (zh) |
| IL (1) | IL278156B2 (zh) |
| JO (1) | JOP20200261A1 (zh) |
| MA (1) | MA52291A (zh) |
| MX (4) | MX2020011015A (zh) |
| MY (1) | MY208399A (zh) |
| NI (1) | NI202000070A (zh) |
| NZ (1) | NZ768714A (zh) |
| PE (1) | PE20211239A1 (zh) |
| PH (1) | PH12020551696A1 (zh) |
| SG (1) | SG11202009726SA (zh) |
| TW (1) | TWI801561B (zh) |
| UA (1) | UA127898C2 (zh) |
| UY (1) | UY38187A (zh) |
| WO (1) | WO2019202141A1 (zh) |
| ZA (1) | ZA202006406B (zh) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20160367567A1 (en) | 2015-06-18 | 2016-12-22 | Mithra Pharmaceuticals S.A. | Orodispersible dosage unit containing an estetrol component |
| PL3310333T3 (pl) | 2015-06-18 | 2020-07-13 | Estetra Sprl | Ulegająca rozpadowi w jamie ustnej jednostka dawkowana zawierająca składnik estetrolowy |
| CA3178291A1 (en) | 2016-08-05 | 2018-04-12 | Estetra Srl | Method for the management of dysmenorrhea and menstrual pain |
| JOP20200260A1 (ar) * | 2018-04-19 | 2019-10-19 | Estetra Sprl | مركبات واستخداماتها للتخفيف من الأعراض المصاحبة لانقطاع الطمث |
| TWI801561B (zh) * | 2018-04-19 | 2023-05-11 | 比利時商依思特拉私人有限責任公司 | 化合物及其用於緩解絕經相關症狀的用途 |
| TWI893101B (zh) | 2020-04-16 | 2025-08-11 | 比利時商埃斯特拉有限責任公司 | 具有降低之副作用之避孕組成物 |
| MX2024006490A (es) * | 2021-11-29 | 2024-06-05 | Estetra Srl | Composiciones para prevenir o tratar el envejecimiento de la piel. |
| US12233074B2 (en) | 2022-02-10 | 2025-02-25 | Estetra Srl | Contraceptive methods with improved pearl index |
| WO2023174947A1 (en) * | 2022-03-14 | 2023-09-21 | Estetra Srl | Estetrol for use in re-endothelialization |
| WO2024133210A1 (en) * | 2022-12-20 | 2024-06-27 | Estetra Srl | Use of estetrol in hepatically impaired patients |
| WO2025061912A1 (en) * | 2023-09-21 | 2025-03-27 | Estetra Srl | Estetrol for use in the treatment of female sexual arousal disorder |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002508330A (ja) * | 1997-12-16 | 2002-03-19 | アベンテイス・フアルマ・ソシエテ・アノニム | ダルホプリスチンおよびキヌプリスチンに基づく医薬組成物ならびに調製 |
| US20050106240A1 (en) * | 2003-10-15 | 2005-05-19 | Fuji Chemical Industry Co., Ltd. | Composition for rapid disintegrating tablet in oral cavity |
| CN102058604A (zh) * | 2009-11-17 | 2011-05-18 | 北京万全阳光医学技术有限公司 | 一种含有地诺孕素和戊酸雌二醇的药物组合物及其制备方法 |
| US20110250274A1 (en) * | 2008-09-19 | 2011-10-13 | Shaked Ze Ev | Estriol formulations |
| EP3106148A1 (en) * | 2015-06-18 | 2016-12-21 | Mithra Pharmaceuticals S.A. | Orodispersible dosage unit containing an estetrol component |
Family Cites Families (132)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3138588A (en) | 1962-08-24 | 1964-06-23 | American Home Prod | 17-ketals of estrone and derivatives thereof |
| US3433785A (en) | 1966-07-11 | 1969-03-18 | Sterling Drug Inc | 15,16-disubstituted aromatic steroids,intermediates and processes |
| US4826831A (en) | 1983-08-05 | 1989-05-02 | Pre Jay Holdings Limited | Method of hormonal treatment for menopausal or post-menopausal disorders involving continuous administration of progestogens and estrogens |
| CA1306950C (en) | 1987-04-10 | 1992-09-01 | Alec D. Keith | Buccal administration of estrogens |
| US5073374A (en) | 1988-11-30 | 1991-12-17 | Schering Corporation | Fast dissolving buccal tablet |
| BE1003647A5 (fr) | 1989-02-28 | 1992-05-12 | Syntex Inc | Composition pharmaceutique de nicardipine pour administration parenterale. |
| JPH03237557A (ja) | 1990-02-14 | 1991-10-23 | Oki Electric Ind Co Ltd | ニューラルネットワークシミュレータ及び計算機システム |
| US5340586A (en) | 1991-04-12 | 1994-08-23 | University Of Southern California | Methods and formulations for use in treating oophorectomized women |
| US5340585A (en) | 1991-04-12 | 1994-08-23 | University Of Southern California | Method and formulations for use in treating benign gynecological disorders |
| US5468736A (en) | 1993-02-25 | 1995-11-21 | The Medical College Of Hampton Road | Hormone replacement therapy |
| US5895783A (en) | 1993-07-16 | 1999-04-20 | Schering Aktiengesellschaft | Treatment of preeclampsia and preterm labor with combination of progestational agent and a nitric oxide synthase substrate and/or donor |
| JPH07101977A (ja) | 1993-10-05 | 1995-04-18 | Kureha Chem Ind Co Ltd | ホルモン作用を軽減した新規なエストラジオール誘導体及びその増殖因子阻害剤 |
| DE4344405C2 (de) | 1993-12-24 | 1995-12-07 | Marika Dr Med Ehrlich | Ovulationshemmendes Mittel und Verfahren zur hormonalen Kontrazeption |
| AU2103495A (en) | 1994-08-04 | 1996-03-04 | Biex, Inc. | Method for prediction of premature delivery using estetrol (e4) as an indicator |
| WO1997004752A1 (en) | 1995-07-26 | 1997-02-13 | Duramed Pharmaceuticals, Inc. | Pharmaceutical compositions of conjugated estrogens and methods for their use |
| AU1931999A (en) | 1997-12-19 | 1999-07-12 | Smithkline Beecham Corporation | Process for manufacturing bite-dispersion tablets |
| US7815937B2 (en) | 1998-10-27 | 2010-10-19 | Biovail Laboratories International Srl | Quick dissolve compositions and tablets based thereon |
| US6117446A (en) | 1999-01-26 | 2000-09-12 | Place; Virgil A. | Drug dosage unit for buccal administration of steroidal active agents |
| US6180682B1 (en) | 1999-01-26 | 2001-01-30 | Virgil A. Place | Buccal drug delivery system for use in male contraception |
| TW548277B (en) | 1999-07-16 | 2003-08-21 | Akzo Nobel Nv | Orally active androgens |
| AU778017B2 (en) | 1999-12-02 | 2004-11-11 | N.V. Organon | 14,15-beta-methylene substituted androgens |
| NZ520630A (en) | 2000-01-18 | 2004-09-24 | Schering Ag | Drospirenone for hormone replacement therapy |
| US20020132801A1 (en) | 2001-01-11 | 2002-09-19 | Schering Aktiengesellschaft | Drospirenone for hormone replacement therapy |
| FR2809619B1 (fr) | 2000-06-06 | 2004-09-24 | Pharmatop | Nouvelles formulations aqueuses de principes actifs sensibles a l'oxydation et leur procede d'obtention |
| EP1216713A1 (en) | 2000-12-20 | 2002-06-26 | Schering Aktiengesellschaft | Compositions of estrogen-cyclodextrin complexes |
| WO2002094276A1 (en) | 2001-05-18 | 2002-11-28 | Pantarhei Bioscience B.V. | Pharmaceutical composition for use in hormone replacement therapy |
| EP1260225A1 (en) | 2001-05-18 | 2002-11-27 | Pantarhei Bioscience B.V. | A pharmaceutical composition for use in hormone replacement therapy |
| TR200400183T4 (tr) | 2001-05-23 | 2004-02-23 | Pantarhei Bioscience B.V. | Hormonal kontrasepsiyon için vasıta ve metot |
| ES2296943T3 (es) | 2001-05-23 | 2008-05-01 | Pantarhei Bioscience B.V. | Sistema de administracion de un medicamento estrogeno tetrahidroxilado destinado a la contracepcion hormonal. |
| EP1390041B1 (en) | 2001-05-23 | 2009-11-25 | Pantarhei Bioscience B.V. | Drug delivery system comprising a tetrahydroxylated estrogen for use in hormonal contraception |
| CA2448271A1 (en) | 2001-05-23 | 2002-11-28 | Panterhei Bioscience B.V. | Means and method for hormonal contraception |
| US20020193356A1 (en) | 2001-05-23 | 2002-12-19 | Van Beek Agatha Antonia Magdalena | Means and method for hormonal contraception |
| WO2002094277A1 (en) | 2001-05-23 | 2002-11-28 | Pantarhei Bioscience B.V. | Means and method for hormonal contraception |
| WO2003018026A1 (en) * | 2001-08-31 | 2003-03-06 | Pantarhei Bioscience B.V. | Use of estrogenic compounds in combination with progestogenic compounds in hormone-replacement therapy |
| ES2278925T3 (es) * | 2001-11-15 | 2007-08-16 | Pantarhei Bioscience B.V. | Uso de compuestos estrogenicos en combinacion con compuestos progestogenicos en terapias de sustitucion hormonal. |
| US6723348B2 (en) | 2001-11-16 | 2004-04-20 | Ethypharm | Orodispersible tablets containing fexofenadine |
| HU227198B1 (en) | 2001-11-27 | 2010-10-28 | Richter Gedeon Nyrt | Pharmaceutical composition for emergency contraception containing levonorgestrel |
| EP1478373B1 (en) | 2002-02-21 | 2006-10-04 | Schering Aktiengesellschaft | Pharmaceutical compositions comprising one or more steroids one or more tetrahydrofolate components and vitamin b12 |
| US20050147670A1 (en) | 2002-05-29 | 2005-07-07 | Impax Laboratories Inc. | Oral disintegrating dosage forms |
| WO2003103685A1 (en) | 2002-06-11 | 2003-12-18 | Pantarhei Bioscience B.V. | A method of treating human skin and a skin care composition for use in such a method |
| SI1511496T1 (sl) | 2002-06-11 | 2007-04-30 | Pantarhei Bioscience Bv | Metoda zdravljenja ali prevencije imunsko mediiranih motenj in farmacevtska formulacija za njeno uporabo |
| CA2492287C (en) | 2002-07-12 | 2011-12-13 | Pantarhei Bioscience B.V. | Pharmaceutical composition comprising estetrol derivatives for use in cancer therapy |
| WO2004019954A1 (en) | 2002-08-28 | 2004-03-11 | Robert Casper | Estrogen replacement regimen |
| SI1556058T1 (sl) | 2002-10-23 | 2008-02-29 | Pantarhei Bioscience Bv | Farmacevtski sestavki, ki obsegajo estetrolne derivate, za uporabo pri zdravljenju raka |
| ATE454155T1 (de) | 2002-11-05 | 2010-01-15 | Bayer Schering Pharma Ag | Verwendung von drospirenon zur behandlung von hypertension |
| CA2505190C (en) | 2002-11-08 | 2012-07-10 | Pantarhei Bioscience B.V. | Synthesis of estetrol via estrone derived steroids |
| JP2006525306A (ja) | 2003-04-30 | 2006-11-09 | デビオファーム ソシエテ アノニム | ゴナドトロピン・ホルモン放出ホルモンを使用する方法及び組成物 |
| CN100431545C (zh) | 2003-05-22 | 2008-11-12 | 潘塔希生物科学股份有限公司 | 雌激素成分在制备用于治疗及预防肌与骨疼痛中的组合物中的应用 |
| EP1673071A1 (en) | 2003-09-29 | 2006-06-28 | Novo Nordisk Femcare AG | Improved stability of progestogen formulations |
| AU2004275469B2 (en) | 2003-09-29 | 2010-07-15 | Novo Nordisk Health Care Ag | HRT formulations |
| EP1535618A1 (en) | 2003-11-26 | 2005-06-01 | Schering Aktiengesellschaft | Pharmaceutical preparation for continuous hormonal treatment over a period of longer than 21-28 days comprising two estrogen and/or progestin compositions |
| US20050113350A1 (en) | 2003-11-26 | 2005-05-26 | Bernd Duesterberg | Extended use combination comprising estrogens and progestins |
| MY151322A (en) | 2004-04-30 | 2014-05-15 | Bayer Ip Gmbh | Management of breakthrough bleeding in extended hormonal contraceptive regimens |
| GB0410616D0 (en) | 2004-05-13 | 2004-06-16 | Unilever Plc | Antiperspirant or deodorant compositions |
| SI1755562T1 (sl) | 2004-05-28 | 2014-02-28 | Richter Gedeon Nyrt. | Kontracepcijsko sredstvo, ki vsebuje folno kislino |
| DE102004026670A1 (de) | 2004-05-28 | 2005-12-15 | Grünenthal GmbH | Hormonales Kontrazeptivum enthaltend eine Kombination aus Ethinylestradiol und Chlormadinonacetat |
| DE602005013232D1 (de) | 2004-07-01 | 2009-04-23 | Lek Pharmaceuticals | Schnell zerfallende im mund dispergierbare zusammensetzung mit nicht-filamentösen mitverarbeiteten polyol-teilchen und verkieselter mikrokristalliner cellulose |
| UA89964C2 (ru) | 2004-09-08 | 2010-03-25 | Н.В. Органон | 15β-ЗАМЕЩЕННЫЕ СТЕРОИДЫ, КОТОРЫЕ ИМЕЮТ СЕЛЕКТИВНУЮ ЭСТРОГЕННУЮ АКТИВНОСТЬ |
| CN103479582A (zh) | 2005-02-03 | 2014-01-01 | 武田奈科明有限公司 | 制备含钙组合物的快速湿聚结方法 |
| IS7724A (is) | 2005-03-02 | 2006-09-03 | Actavis Group | Samsetning á töflum með hraða sundrun sem innihalda þungt magnesíum karbónat |
| UY29527A1 (es) | 2005-05-13 | 2006-12-29 | Schering Ag | Composicinn farmaccutica que contienen gestrgenos y/o estrngenos y 5-metil - (6s) - tetrhidrofolato. |
| AU2006251154B2 (en) | 2005-05-26 | 2012-06-28 | Solvay Pharmaceuticals Gmbh | 17beta-HSD1 and STS inhibitors |
| BRPI0612586A2 (pt) | 2005-06-29 | 2010-11-23 | Wyeth Corp | formulações de estrogênios conjugados e bazedoxifeno |
| US20070048369A1 (en) | 2005-08-26 | 2007-03-01 | National Starch And Chemical Investment Holding Corporation | Mucosal delivery tablet |
| EP1971344B1 (en) | 2006-01-09 | 2010-09-22 | Pantarhei Bioscience B.V. | A method of treating an acute vascular disorder |
| ATE481973T1 (de) | 2006-01-09 | 2010-10-15 | Pantarhei Bioscience Bv | Verfahren zur behandlung einer akuten gefässerkrankung |
| EP1993531B1 (en) | 2006-03-02 | 2015-10-14 | Warner Chilcott Company, LLC | Extended cycle multiphasic oral contraceptive method |
| US20080113953A1 (en) | 2006-06-08 | 2008-05-15 | Warner Chilcott Company, Inc. | Methods to administer solid dosage forms of ethinyl estradiol and prodrugs thereof with improved bioavailability |
| CA2649361C (en) | 2006-06-08 | 2014-09-30 | Warner Chilcott Company, Inc. | Methods to administer solid dosage forms of ethinyl estradiol and prodrugs thereof with improved bioavailability |
| US20070286819A1 (en) | 2006-06-08 | 2007-12-13 | Warner Chilcott Company, Inc. | Methods to administer ethinyl estradiol and prodrugs thereof with improved bioavailability |
| JP2009542588A (ja) | 2006-07-06 | 2009-12-03 | バイエル・シエーリング・ファーマ アクチエンゲゼルシャフト | 避妊及び先天的異常の危険性の予防のための医薬製剤 |
| CN101489563A (zh) | 2006-07-06 | 2009-07-22 | 拜耳先灵医药股份有限公司 | 用于避孕和预防先天性畸形风险的药物制剂 |
| BRPI0719675A2 (pt) | 2006-11-29 | 2013-12-24 | Wyeth Corp | Comprimido com bicamada de estrogênio/serm e estrogênio/progestina |
| BRPI0719486A2 (pt) | 2006-12-20 | 2014-02-18 | Duramed Pharmaceuticals Inc | "forma farmacêutica sólida oral desitegrante, não-efervescente, métodos para tratar uma mulher que necessite de um contraceptivo de emergência, pacote terapêutico para tratar uma mulher que necessite de contracepção de emergência e processo para a preparação de uma forma sólida de dosagem farmacêutica oral desintegrante, não-efervescente" |
| DE602008001783D1 (de) | 2007-01-08 | 2010-08-26 | Pantarhei Bioscience Bv | Verfahren zur behandlung oder prävention von unfruchtbarkeit bei weiblichen säugern und pharmazeutisches kit zur anwendung dieses verfahrens |
| WO2008089087A2 (en) | 2007-01-12 | 2008-07-24 | Wyeth | Tablet-in-tablet compositions |
| EP1972618A1 (en) | 2007-03-20 | 2008-09-24 | Nabriva Therapeutics AG | Pleuromutilin derivatives for the treatment of diseases mediated by microbes |
| EP2155205B1 (en) | 2007-06-21 | 2011-12-21 | Pantarhei Bioscience B.V. | Treatment of meconium aspiration syndrome with estrogens |
| WO2009011576A1 (en) | 2007-07-19 | 2009-01-22 | Pantarhei Bioscience B.V. | Treatment or prevention of hypertensive disorders of pregnancy or fetal growth retardation |
| FR2920311B1 (fr) | 2007-08-31 | 2010-06-18 | Galenix Innovations | Composition solide, orodispersible et/ou dispersible, sans excipient a effet notoire et son procede de preparation |
| JP5399749B2 (ja) | 2008-03-27 | 2014-01-29 | 沢井製薬株式会社 | プロトンポンプ阻害剤を含有する被覆微粒子 |
| PT2262486E (pt) | 2008-08-01 | 2013-03-27 | Tovarna Zdravil D D Novo Mesto Krka | Composição de quetiapina |
| CN101780073B (zh) | 2009-01-21 | 2013-07-03 | 重庆圣华曦药业股份有限公司 | 非布司他分散片药物及其制备方法 |
| EP3031451B1 (en) | 2009-01-26 | 2018-03-07 | Shin-Etsu Chemical Co., Ltd | Wet granulation tableting method using aqueous dispersion of low-substituted hydroxypropyl cellulose |
| DE102009007771B4 (de) | 2009-02-05 | 2012-02-16 | Bayer Schering Pharma Aktiengesellschaft | Bukkales Applikationssystem, 17α-Estradiol enthaltend |
| US20120077888A1 (en) | 2009-03-26 | 2012-03-29 | Royal College Of Surgeons In Ireland | Orodispersible tablets |
| ITMI20091109A1 (it) * | 2009-06-23 | 2010-12-24 | Wyeth Corp | Forma polimorfa d di bazedoxifene acetato e metodi per la sua preparazione |
| EP3178476A1 (de) | 2009-06-23 | 2017-06-14 | Bayer Intellectual Property GmbH | Pharmazeutische zusammensetzung und behandlungsverfahren zur notfallempfängnisverhütung |
| US8901185B2 (en) | 2010-04-12 | 2014-12-02 | Universite Claude Bernard Lyon I | Hybrid organic-inorganic material constituted by a silica network having photochromic agents and optical power limiting agents as a doping agent in the material |
| CN102985070A (zh) | 2010-04-15 | 2013-03-20 | 拜耳知识产权有限责任公司 | 用于hrt的极低剂量的固体口服剂型 |
| EP2399904A1 (en) | 2010-05-26 | 2011-12-28 | Nabriva Therapeutics AG | Process for the preparation of pleuromutilins |
| US10849857B2 (en) | 2010-07-28 | 2020-12-01 | Laboratorios Leon Farma Sa | Pharmaceutical compositions comprising active drugs, contraceptive kits comprising active drugs, and methods of administering the same |
| AR081670A1 (es) | 2010-06-29 | 2012-10-10 | Leon Farma Sa Lab | Composicion farmaceutica que comprende drospirenona y kit anticonceptivo |
| US9603860B2 (en) | 2010-07-28 | 2017-03-28 | Laboratorios Leon Farma Sa | Pharmaceutical compositions comprising active drugs, contraceptive kits comprising active drugs, and methods of administering the same |
| WO2012055840A1 (en) | 2010-10-28 | 2012-05-03 | Bayer Pharma Aktiengesellschaft | Composition and preparation for treatment of dysmenorrhea and menstrual pain and use of a hormonal agent and a zinc salt for treatment of menstrual disorders |
| EP2646003B1 (en) | 2010-12-02 | 2020-06-03 | Adare Pharmaceuticals, Inc. | Rapidly dispersing granules, orally disintegrating tablets and methods |
| JP2012240917A (ja) | 2011-05-16 | 2012-12-10 | Zensei Yakuhin Kogyo Kk | 製剤化用微粒子とそれを含む製剤 |
| CN107266514A (zh) | 2011-06-01 | 2017-10-20 | 埃斯特拉私人有限责任公司 | 用于产生雌四醇中间体的方法 |
| CL2013003435A1 (es) | 2011-06-01 | 2014-08-01 | Estetra Sprl | Proceso de preparacion de intermediarios de estetrol utilizando catalizadores de paladio y grupos protectores acilantes o sililantes; y uso de dicho proceso para preparar estetrol. |
| BR112013030833B1 (pt) | 2011-06-01 | 2019-09-03 | Estetra S A | processo para a preparação de um composto de fórmula (i) e processo para a preparação de estetrol |
| EP2383279A1 (en) | 2011-07-19 | 2011-11-02 | Pantarhei Bioscience B.V. | Process for the preparation of estetrol |
| ES2545337T3 (es) | 2011-07-19 | 2015-09-10 | Pantarhei Bioscience B.V. | Comprimido que contiene dehidroepiandrosterona (DHEA) |
| HUE033590T2 (hu) | 2011-08-11 | 2017-12-28 | Estetra Sprl | Esztetrol alkalmazása sürgõsségi fogamzásgátlóként |
| CA2848785A1 (en) | 2011-09-16 | 2013-03-21 | Ferring B.V. | A fast dissolving pharmaceutical composition |
| PT2764008T (pt) | 2011-10-07 | 2016-11-10 | Estetra Sprl | Processo para a produção de estetrol |
| EP2790688B1 (en) | 2011-12-13 | 2019-11-20 | Arstat, Inc. | A multiphasic contraceptive regimen for an oral formulation of progestin and estrogen |
| EP2653163A1 (en) | 2012-04-19 | 2013-10-23 | Université de Liège | Estrogenic components for use in the treatment of neurological disorders |
| US9808470B2 (en) | 2012-04-19 | 2017-11-07 | Universite De Liege | Estrogenic components for use in the treatment of neurological disorders |
| US9238265B2 (en) | 2012-09-27 | 2016-01-19 | General Electric Company | Backstrike protection during machining of cooling features |
| WO2014159377A1 (en) | 2013-03-14 | 2014-10-02 | Teva Women's Health, Inc. | Compositions containing tanaproget and natural estrogens |
| JP6126456B2 (ja) | 2013-05-17 | 2017-05-10 | 東和薬品株式会社 | 打錠用顆粒とその製造方法、その打錠用顆粒を用いた口腔内崩壊錠 |
| US20140341326A1 (en) | 2013-05-20 | 2014-11-20 | Qualcomm Incorporated | Channel estimation with discontinuous pilot signals |
| EP2999474A4 (en) | 2013-05-21 | 2016-12-28 | Predictive Therapeutics Llc | THERAPEUTIC AND METHOD FOR USE |
| WO2015040051A1 (en) | 2013-09-18 | 2015-03-26 | Crystal Pharma, S.A.U. | Process for the preparation of estetrol |
| US12274276B2 (en) | 2013-10-03 | 2025-04-15 | Altria Client Services Llc | Dissolvable-chewable tablet |
| MA39105B1 (fr) | 2013-12-12 | 2018-05-31 | Donesta Bioscience B V | Unité de dosage solide se désintégrant par voie orale contenant un constituant estétrol |
| US10571371B2 (en) | 2014-08-07 | 2020-02-25 | Wake Forest University Health Sciences | Compositions and methods for clearing a biological sample |
| US9962395B2 (en) | 2014-09-29 | 2018-05-08 | The Regents Of The University Of California | Compositions and methods for maintaining cognitive function |
| BR112017024783A2 (pt) | 2015-05-18 | 2018-08-07 | Agile Therapeutics Inc | composições contraceptivas e métodos para eficácia melhorada e modulação dos efeitos colaterais |
| EP3310346B1 (en) | 2015-06-18 | 2021-03-24 | Estetra SPRL | Orodispersible tablet containing estetrol |
| PL3310333T3 (pl) | 2015-06-18 | 2020-07-13 | Estetra Sprl | Ulegająca rozpadowi w jamie ustnej jednostka dawkowana zawierająca składnik estetrolowy |
| WO2016203009A1 (en) | 2015-06-18 | 2016-12-22 | Mithra Pharmaceuticals S.A. | Orodispersible tablet containing estetrol |
| JP6827962B2 (ja) | 2015-06-23 | 2021-02-10 | ラボラトリオス レオン ファーマ エスエー | 過剰体重に影響される女性患者のためのドロスピレノン系避妊薬 |
| EP3272333A1 (en) | 2016-07-22 | 2018-01-24 | Chemo Research, S.L. | Vaginal composition comprising a combination of estrogen and vitamin d |
| US20200046729A1 (en) | 2016-08-05 | 2020-02-13 | Estetra Sprl | Methods using combined oral contraceptive compositions with reduced cardiovascular effects |
| CA3178291A1 (en) | 2016-08-05 | 2018-04-12 | Estetra Srl | Method for the management of dysmenorrhea and menstrual pain |
| JP2018533542A (ja) | 2016-10-28 | 2018-11-15 | エステトラ ソシエテ プリーヴ ア レスポンサビリテ リミテ | 月経困難症および月経痛の管理のための方法 |
| JP2021513507A (ja) | 2018-02-07 | 2021-05-27 | エステトラ ソシエテ プリーヴ ア レスポンサビリテ リミテ | 心臓血管系への影響を低減した避妊薬組成物 |
| JOP20200260A1 (ar) | 2018-04-19 | 2019-10-19 | Estetra Sprl | مركبات واستخداماتها للتخفيف من الأعراض المصاحبة لانقطاع الطمث |
| TWI801561B (zh) | 2018-04-19 | 2023-05-11 | 比利時商依思特拉私人有限責任公司 | 化合物及其用於緩解絕經相關症狀的用途 |
| US10929286B2 (en) | 2018-06-29 | 2021-02-23 | Seagate Technology Llc | Arbitrated management of a shared non-volatile memory resource |
| TWI893101B (zh) | 2020-04-16 | 2025-08-11 | 比利時商埃斯特拉有限責任公司 | 具有降低之副作用之避孕組成物 |
-
2019
- 2019-04-18 TW TW108113543A patent/TWI801561B/zh active
- 2019-04-19 CN CN202211280507.8A patent/CN115645415A/zh active Pending
- 2019-04-19 MY MYPI2020005405A patent/MY208399A/en unknown
- 2019-04-19 PE PE2020001623A patent/PE20211239A1/es unknown
- 2019-04-19 KR KR1020207031282A patent/KR102748805B1/ko active Active
- 2019-04-19 KR KR1020227038135A patent/KR20220153664A/ko active Pending
- 2019-04-19 MX MX2020011015A patent/MX2020011015A/es unknown
- 2019-04-19 CR CR20200485A patent/CR20200485A/es unknown
- 2019-04-19 CA CA3097278A patent/CA3097278C/en active Active
- 2019-04-19 BR BR112020021211-3A patent/BR112020021211A2/pt unknown
- 2019-04-19 CN CN202411405055.0A patent/CN119424448A/zh active Pending
- 2019-04-19 GE GEAP201915472A patent/GEP20227395B/en unknown
- 2019-04-19 JO JOP/2020/0261A patent/JOP20200261A1/ar unknown
- 2019-04-19 MA MA052291A patent/MA52291A/fr unknown
- 2019-04-19 GE GEAP202215472A patent/GEAP202215472A/en unknown
- 2019-04-19 JP JP2021506061A patent/JP7308925B2/ja active Active
- 2019-04-19 AU AU2019254680A patent/AU2019254680B2/en active Active
- 2019-04-19 UA UAA202006879A patent/UA127898C2/uk unknown
- 2019-04-19 EP EP22202069.5A patent/EP4154893A1/en active Pending
- 2019-04-19 SG SG11202009726SA patent/SG11202009726SA/en unknown
- 2019-04-19 CU CU2020000073A patent/CU20200073A7/es unknown
- 2019-04-19 EP EP22202086.9A patent/EP4159218A1/en active Pending
- 2019-04-19 WO PCT/EP2019/060220 patent/WO2019202141A1/en not_active Ceased
- 2019-04-19 NZ NZ768714A patent/NZ768714A/en unknown
- 2019-04-19 IL IL278156A patent/IL278156B2/en unknown
- 2019-04-19 EP EP19722528.7A patent/EP3781170A1/en active Pending
- 2019-04-19 CN CN201980026758.3A patent/CN112020360B/zh active Active
- 2019-04-19 EP EP22210160.2A patent/EP4166143A1/en active Pending
- 2019-04-19 US US17/048,538 patent/US11452733B2/en active Active
- 2019-04-23 UY UY0001038187A patent/UY38187A/es not_active Application Discontinuation
-
2020
- 2020-10-09 CO CONC2020/0012603A patent/CO2020012603A2/es unknown
- 2020-10-14 PH PH12020551696A patent/PH12020551696A1/en unknown
- 2020-10-15 ZA ZA2020/06406A patent/ZA202006406B/en unknown
- 2020-10-16 MX MX2023004814A patent/MX2023004814A/es unknown
- 2020-10-16 MX MX2022013733A patent/MX2022013733A/es unknown
- 2020-10-16 NI NI202000070A patent/NI202000070A/es unknown
- 2020-10-16 MX MX2023004813A patent/MX2023004813A/es unknown
- 2020-10-19 EC ECSENADI202066226A patent/ECSP20066226A/es unknown
- 2020-10-19 CL CL2020002710A patent/CL2020002710A1/es unknown
-
2022
- 2022-08-23 US US17/893,999 patent/US12390478B2/en active Active
- 2022-10-11 US US17/963,712 patent/US11666585B2/en active Active
- 2022-10-24 US US17/972,403 patent/US12458651B2/en active Active
- 2022-10-26 AU AU2022259753A patent/AU2022259753B2/en active Active
-
2023
- 2023-06-30 JP JP2023108014A patent/JP2023123762A/ja active Pending
- 2023-06-30 JP JP2023108013A patent/JP2023123761A/ja active Pending
-
2025
- 2025-10-10 US US19/355,373 patent/US20260034147A1/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002508330A (ja) * | 1997-12-16 | 2002-03-19 | アベンテイス・フアルマ・ソシエテ・アノニム | ダルホプリスチンおよびキヌプリスチンに基づく医薬組成物ならびに調製 |
| US20050106240A1 (en) * | 2003-10-15 | 2005-05-19 | Fuji Chemical Industry Co., Ltd. | Composition for rapid disintegrating tablet in oral cavity |
| US20110250274A1 (en) * | 2008-09-19 | 2011-10-13 | Shaked Ze Ev | Estriol formulations |
| CN102058604A (zh) * | 2009-11-17 | 2011-05-18 | 北京万全阳光医学技术有限公司 | 一种含有地诺孕素和戊酸雌二醇的药物组合物及其制备方法 |
| EP3106148A1 (en) * | 2015-06-18 | 2016-12-21 | Mithra Pharmaceuticals S.A. | Orodispersible dosage unit containing an estetrol component |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI801561B (zh) | 化合物及其用於緩解絕經相關症狀的用途 | |
| TWI805742B (zh) | 化合物及其用於緩解停經相關症狀的用途 | |
| HK40082367A (zh) | 雌四醇及其用於缓解更年期相关症状的用途 | |
| HK40090929A (zh) | 一水合雌四醇及其用於缓解更年期相关症状的用途 | |
| EA046158B1 (ru) | Соединения и пути их применения для облегчения симптомов, связанных с менопаузой | |
| EA049012B1 (ru) | Соединения и пути их применения для облегчения симптомов, связанных с менопаузой | |
| EA047221B1 (ru) | Соединения и пути их применения для облегчения симптомов, связанных с менопаузой | |
| HK40091287A (zh) | 雌四醇及其用於缓解更年期相关症状的用途 | |
| HK40036678B (zh) | 化合物以及它们在缓解绝经相关症状中的用途 | |
| HK40036678A (zh) | 化合物以及它们在缓解绝经相关症状中的用途 |