TW202227042A - 雙重鎮痛/消炎組合物、組合及其使用方法 - Google Patents
雙重鎮痛/消炎組合物、組合及其使用方法 Download PDFInfo
- Publication number
- TW202227042A TW202227042A TW110130884A TW110130884A TW202227042A TW 202227042 A TW202227042 A TW 202227042A TW 110130884 A TW110130884 A TW 110130884A TW 110130884 A TW110130884 A TW 110130884A TW 202227042 A TW202227042 A TW 202227042A
- Authority
- TW
- Taiwan
- Prior art keywords
- composition
- cb2ra
- pain
- compound
- formula
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/075—Ethers or acetals
- A61K31/085—Ethers or acetals having an ether linkage to aromatic ring nuclear carbon
- A61K31/09—Ethers or acetals having an ether linkage to aromatic ring nuclear carbon having two or more such linkages
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/63—Compounds containing para-N-benzenesulfonyl-N-groups, e.g. sulfanilamide, p-nitrobenzenesulfonyl hydrazide
- A61K31/635—Compounds containing para-N-benzenesulfonyl-N-groups, e.g. sulfanilamide, p-nitrobenzenesulfonyl hydrazide having a heterocyclic ring, e.g. sulfadiazine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/186—Quaternary ammonium compounds, e.g. benzalkonium chloride or cetrimide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/34—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyesters, polyamino acids, polysiloxanes, polyphosphazines, copolymers of polyalkylene glycol or poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
- A61K9/1075—Microemulsions or submicron emulsions; Preconcentrates or solids thereof; Micelles, e.g. made of phospholipids or block copolymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4808—Preparations in capsules, e.g. of gelatin, of chocolate characterised by the form of the capsule or the structure of the filling; Capsules containing small tablets; Capsules with outer layer for immediate drug release
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/485—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4866—Organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C43/00—Ethers; Compounds having groups, groups or groups
- C07C43/02—Ethers
- C07C43/20—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring
- C07C43/23—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring containing hydroxy or O-metal groups
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Inorganic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Dispersion Chemistry (AREA)
- Dermatology (AREA)
- Biochemistry (AREA)
- Ophthalmology & Optometry (AREA)
- Zoology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本發明部分地提供用於在個體中促效大麻素2型(CB
2)受體活性之醫藥組合物、醫療套組以及製造使用此類組合物之方法。
當個體受傷時,例如經由事故或手術造成的身體創傷,啟動各種反應機制以保護個體免受進一步傷害且啟動癒合過程。舉例而言,在傷害發生後立即活化快速作用的周邊神經纖維(「痛覺受器(nociceptor)」),以觸發肌肉回彈及刺痛感覺的增強,從而降低進一步受傷的風險(Basbaum等人, (2009) 《細胞》(Cell), 139(2): 267-84)。損傷亦觸發局部炎症。
炎症為哺乳動物對損傷的一線反應,且主要由先天性免疫系統之白血球介導(Janeway等人, (2001) 《免疫生物學:健康與疾病之免疫系統》(Immunobiology: The Immune System in Health and Disease).第5版.紐約(New York): Garland Science)。此等細胞在被受損組織活化時會迅速轉化,以數種方式放大初始的急性反應(Krystel-Whittemore等人, (2016) 《免疫學前沿》(Front.Immunol.), 6: 620;Zhang等人, (2007) 《國際麻醉學臨床》(International Anesthesiology Clinic), 45(2): 27-37);Vance等人, (2009) 《細胞宿主及微生物》(Cell Host & Microbe), 6(1): 10-21)。舉例而言,誘導型環氧合酶2(COX-2)之表現上調,引起諸如前列腺素E2(PGE2)及凝血脂素之類前列腺素(prostanoid)的快速增加(Cadieux等人, (2005) 《細胞科學雜誌》(J. Cell Science), 118(Pt 7): 1437-47)。此等早期分子增加由局部痛覺受器誘導之疼痛感覺(Zeilhofer等人, (2007) 《生化藥理學》(Biochemical Pharmacol.), 73: 165-174)、活化遠端痛覺受器(Funk (2001) 《科學》(Science), 294(5548): 1871-5;Reinold等人 (2005) 《臨床研究雜誌》(J. Clin. Invest.), 115: 673-679;Lehnardt等人 (2003) 《美國國家科學院院刊》(Proc. Natl. Acad. Sci. USA), 100: 8514-8519)且促進動脈擴張及組織通透性增強(Ricciotti等人, (2011) 《動脈硬化、血栓形成及血管生物學》(Arterioscler. Thromb. Vasc. Biol.), 31(5): 986-1000)。此等後者效應有助於免疫細胞進入該區域且增加局部血流量,從而產生典型的炎症跡象,諸如目視發紅、腫脹及體溫升高。類前列腺素亦加強其他免疫介質(諸如趨化介素)之作用。
趨化介素為誘導循環免疫細胞遷移至發炎區域的化學引誘物(Krystel-Whittemore (2016) 同上;Zhang等人, (2007) 同上;Vance (2009) 同上)。由於在循環中的數量較多,嗜中性白血球通常為首先募集至損傷部位的細胞,且其連同巨噬細胞以及T及B淋巴球之存在增加放大免疫反應,提高疼痛感覺且增加腫脹。此等效應一起進一步減輕對該部位的額外傷害。
新的免疫細胞積聚在炎症部位亦增加局部細胞介素濃度,尤其IL-1β及TNF∝之濃度,它們協同作用以進一步加強血管擴張及組織通透性,且上調黏附分子以保留新到達的免疫細胞。
隨著炎症的加劇,細胞介素亦增加疼痛反應及疼痛感覺。舉例而言,IL-1β已經證明為周邊組織中之強效機械及熱痛覺過敏劑(Ferreira SH等人, (1988) 《自然》(Nature), 334: 698-700;Zelenka等人, (2005) 《疼痛》(Pain), 116(3): 257-263.),而相反,TNF∝引起中樞CNS介導之痛覺過敏(Hess等人, (2011) 《美國國家科學院院刊》, 108(9): 3731-6)。緩激肽,另一種早期細胞介素,產生類似的疼痛感覺,與其他細胞介素共同導致急性疼痛。
急性疼痛為暫時的且通常在癒合過程中減輕。然而,除了介導炎症外,活化的免疫細胞亦釋放一系列有毒分子來消滅感染受傷組織的病原體。此等包括活性含氧物(諸如超氧陰離子、過氧化氫、羥基自由基及次氯酸)(Teng等人, (2017) 《免疫學研究雜誌》(J. Immunol Res.), 2017: 9671604)及破壞性酶,諸如膠原酶及髓過氧化酶,其均與宿主組織接觸(Brinkmann等人, (2004) 《科學》, 303(5663): 1532-1535;Wang (2018) 《細胞組織研究》(Cell Tissue Res.), 371(3): 531-539)。
若感染源未經消除,損傷未癒合,或免疫細胞活化之原因繼續存在(如發生在自體免疫性疾病中),則宿主組織可能會經歷持續反應帶來的顯著損害。在此等情況下,急性炎症可能轉變為慢性炎症,且可能對局部及遠端組織造成長期損害(Garn等人, (2016) 《過敏及臨床免疫學雜誌》(J. Allergy and Clin.Immunol.), 138(1): 47-56)。急性疼痛亦將轉變為慢性疼痛,其經由神經重塑變得難以治療(Voscopoulos等人, (2010) 《英國麻醉學雜誌》(Br. J. Anaesth), 105(S1): 69-85)。
因此,雖然急性炎症及由此產生的疼痛為有益(但不適)的反應以使宿主損傷降至最低且促進癒合,但慢性炎症為一種疾病狀態,造成宿主組織損傷及長期疼痛。雖然以前被認為是一種孤立的病況,但現在愈來愈多的證據表明,慢性炎症為一系列使人衰弱之疾病的基礎,包括某些心血管疾病、眼睛疾病、多發性硬化症及癌症。
因此,早期及有效地控制炎症對於控制急性疼痛、避免慢性疼痛及防止復發性組織損傷非常重要。
很明顯,某些具有抑制炎症能力之藥劑亦可藉由抑制痛覺受器敏化及細胞介素釋放而直接起到鎮痛作用,且經由抑制腫脹之異常疼痛作用間接起到鎮痛作用。非類固醇消炎藥(NSAID)及皮質類固醇(類固醇)為兩種如此類別之消炎劑。
許多NSAID藥品可用作鎮痛劑,包括例如酮咯酸(Toradol
®;羅氏(Roche))、雙氯芬酸(Voltaren
®;諾華(Novartis))及布洛芬(Nurofen
®;Reckitt Benckiser)。作為一種類別,此等藥物結合且抑制在全身發現之組成型COX-1酶及誘導型COX-2酶,從而減少上文提及之類前列腺素的產生。NSAID全身用於急性病況,諸如術後軀體疼痛;及慢性病痛,諸如骨關節炎及類風濕性關節炎。許多NSAID亦經批准用於局部使用,例如用於眼睛,以治療與急性病況相關之疼痛,諸如白內障摘除術(Hoffman等人, (2016) 《白內障與屈光外科學雜誌》(J. Cataract Refract. Surg.), 42(9): 1368-1379)、屈光性角膜切除術(PRK)(Razmju等人, (2012) 《國際預防醫學雜誌》(INT. J. PREV. MED.), 3(增刊1): S199-S206))、角膜交聯(CXL)(Sameen等人, (2017) 《巴基斯坦醫學雜誌》(Pak. J. Med. Sci.), 33(5): 1101-1105)引起之術後疼痛及諸如乾眼症候群之慢性病況(Colligris等人, (2014) 《沙特眼科雜誌》(Saudi J. Ophthalmol.) 28(1): 19-30)。
雖然通常有效,但NSAIDS之廣泛特異性,特別是其對組成型COX-1之抑制,可能會產生嚴重的副作用,且作為一種類別,其顯示心血管毒性(包括心臟病發作及中風)及出血風險的警告。由於此等危險,某些NSAID,例如Toradol
®及Voltaren
®對於許多個體(尤其老年個體)及對於治療可能發生出血之適應症,包括在心臟手術期間為禁忌的。採用NSAID治療局部疼痛及炎症亦可能存在問題,因為作為一種類別,其與傷口癒合延遲有關,從而增加疼痛持續時間及感染風險(Iwamoto等人, (2017) 《自然科學報告》(Nature Scientific Reports), 7: 13267)。在眼睛中使用NSAID亦與角膜融解相關,此為一種嚴重病況,其中角膜上皮及下層基質喪失,導致穿孔及失明(Flach (2001) 《美國眼科學會學報》(Trans. Am. Ophthalmol. Soc.), 99: 205-212)。
COX-2抑制劑為傳統NSAID之一個子集,主要抑制在炎症部位產生之可誘導形式之COX-2,且降低該部位之類前列腺素水準。因此,COX-2藥物可避免傳統NSAID所發現之COX-1抑制的全身性副作用。此方面之證據來自一項歐洲研究(Arfè等人, (2016) 《英國醫學雜誌》(Brit. Med. J.), 354: i4857),其中因鎮痛作用而服用的非特異性NSAID藥物,包括酮咯酸、萘普生及布洛芬,增加此等患者之心臟衰竭風險,而給予同一群體之COX-2特異性抑制劑不會造成此類風險。除了在全身使用期間之益處外,COX-2抑制劑在局部遞送時亦顯示出優於COX-1抑制劑之優勢。舉例而言,塞來昔布(Celebrex
®;輝瑞(Pfizer))為COX-2之強效抑制劑,當直接投與眼睛時,已經證明減輕導致失明之兩個主要原因,亦即年齡相關性黃斑變性及糖尿病性視網膜病變之衰弱作用(Kompella等人, (2010) 《關於藥物遞送之專家意見》(Expert Opin. Drug Deliv.), 7(5): 631-645)。COX-1抑制無法實現此等益處。然而,儘管有此等優勢,但COX-2藥物作為一種類別顯示嚴重副作用的警告,包括心血管及胃腸道毒性(參見例如CELEBREX
®處方資訊要點2018年6月修訂版(Highlights of Prescribing information for CELEBREX
®June 2018 revision),可在www at accessdata.fda.gov/drugsatfda_docs/label/2018/ 020998s050lbl.pdf獲得)。
皮質類固醇(類固醇)為模擬腎上腺產生之激素的廣譜消炎藥。類固醇之價值在於其對廣泛適應症之普遍適用性及進入多種細胞類型之能力(Oren等人, (2004) 《生物物理雜誌》(Biophys. J.)87(2): 768-79)。進入細胞後,類固醇迅速與細胞質中之糖皮質激素受體(GR)結合,從而啟動兩種互補的消炎路徑;在低濃度下,類固醇經由基因共活化因子諸如NF-κB間接起作用,以抑制促炎性細胞介素、趨化介素及黏附分子之產生(Hua (2013) 《藥理學前沿》(Front Pharmacol.), 4: 127);在較高濃度下,類固醇亦直接與DNA相互作用,以誘導消炎分子諸如脂皮質素1(lipocortin 1)、IκB-α及IL-10之產生(Dostert等人, (2004) 《當今藥物設計》(Curr. Pharm. Des.), 10: 2807-2816;Couper等人, (2008) 《免疫學雜誌》(J. Immunol.), 180(9): 5771-5777)。此等分子之產生有助於抑制任何進行中的發炎過程。
由於此等深入的免疫調節作用,類固醇為當今世界上最廣泛的處方藥之一,且其使用持續增加(參見例如Dennison等人, (1998) 《英國醫學雜誌》(B.M.J.), 316(7134): 789-90)。然而,類固醇之鎮痛作用為有限的。舉例而言,在對研究皮質類固醇介導之術後鎮痛之14項對照試驗的綜合分析中,皮質類固醇在經口給予時僅非常輕微地減輕疼痛,且在局部給予時無益處(Mohammad等人, (2017) 《系統綜述》(SYSTEMATIC REV.), 6(1): 92)。眼科手術後疼痛控制之證據亦有限,儘管其廣泛使用。
類固醇之無處不在的細胞攝取及其多效活性有利於獲得廣泛的療效。然而,缺乏特異性可導致廣泛分脫靶結合,且由此產生的與類固醇使用相關之副作用(例如高血壓、體重增加、糖尿病、白內障、青光眼、靜脈血栓栓塞及骨折)可能為廣泛且嚴重的。
NSAID、COX-2及類固醇藥物為治療炎症提供廣泛而顯著的益處,同時NSAID及COX-2藥物具有控制急性疼痛之能力,而類固醇則沒有觀察到。然而,儘管有此優勢,NSAID及COX-2藥物之鎮痛作用亦受限,因為兩者均顯示出飽和或天花板效應,之後更高的投與劑量不會產生更大的鎮痛效果,但副作用繼續上升(Motov等人, (2017) 《急診醫學年鑒》(Ann. Emerg. Med.), 70(2): 177-184)。因此,對於彼等重度或極度疼痛者,其價值會降低。此限制無法藉由組合NSAID及/或COX-2藥物來克服,因為其共同的作用機制僅導致累積的副作用,而不會增加疼痛緩解。因此,醫師一般不單獨依靠NSAID及COX-2藥物來治療彼等極度疼痛者。
同樣,皮質類固醇藥物均具有共同的作用機制,因此其亦無法組合以獲得更大的效果,因為可能會產生嚴重及持久的副作用。其缺乏鎮痛作用亦決定類固醇與NSAID或COX-2藥物之組合不太可能對疼痛不受控制的患者有益,尤其在急性期,類固醇之延遲起效時間為一個問題(Williams (2018) 《皮質類固醇的臨床藥理學·呼吸護理》(Clin. Pharmacol. Corticosteroids Resp. Care), 63(6): 655-670;Becker (2013) 《麻醉進展》(Anesthesia Progress), 60(1): 25-31)。
在全球每年進行的估計3億多例外科手術中(Weiser等人, (2016) 《世界衛生組織簡報》(Bull. World Health Org.), 94(3): 201-209),90%引起中度至極度疼痛,其中12%的極度疼痛類別不受類固醇NSAID或COX-2藥物充分控制(Gan等人, (2014) 《當前醫學研究與意見》(Curr. Med. Res. Opin.), 30(1): 149-60);Gan (2017) 《疼痛研究雜誌》(J. Pain Res.) 10: 2287-2298)。對此等患者所經歷之疼痛治療不足可導致生活品質下降,且若繼續不當的管理,則慢性疼痛及炎症可能會隨之而來(Kehlet等人, (2001) 《英國麻醉學雜誌》(Br. J. Anaesth.)87(1): 62-72)。
類鴉片鎮痛劑通常用於管理類固醇NSAID及COX-2藥物治療不足之患者的疼痛,儘管存在已知危險,但其仍為許多醫師之主力(Zhao等人, (2019) 《疼痛研究與管理》(Pain Res. Manage.), 2019: 7490801;Lail等人, (2014) 《加拿大醫院藥學雜誌》(Can. J. Hosp. Pharm.), 67(5): 337-42;Garimella (2013) 《結腸直腸外科臨床》(Clinics Colon Rectal Surg.), 26(3): 191-196)。據估計,在全世界範圍內,80%的所有手術患者接受類鴉片鎮痛劑作為緩解疼痛之基本藥劑(Zhao (2019)同上;Wunsch等人, (2016)《美國醫學會雜誌》(JAMA) 315(15): 1654-1657)。
在全球每年進行的3億例手術中,有7000萬例在美國進行,其中約700萬例為眼科手術。經歷眼科手術之患者通常接受NSAID鎮痛劑及類固醇,且約100萬患者被開具類鴉片。儘管進行此等治療,但咸信眼科手術之疼痛仍未得到充分治療(Galor等人, (2015) 《眼睛》(Eye), 29: 301-312;Pereira等人, (2017) 《疼痛醫師》(Pain Physician), 20: 429-436),增加急性手術疼痛發展為慢性病況的風險,包括乾眼症候群,尤其在需要類鴉片治療之情況下。乾眼症候群為一種慢性病況,需要更強大但往往無效的免疫抑制藥物(Trattler等人, (2017) 《臨床眼科雜誌》(Clin.Ophthalmol.), 11: 1423-1430;Shtein (2011) 《眼科專家綜述》(Expert Review Ophthalmol.), 6(5): 575-582;Schwatrtz (2018) 《美國醫學會雜誌·內科學》(JAMA Intern.Med.), 178(2): 181-182)。現今,估計約有5%的美國人口發生乾眼症(或約1650萬人),且患病率逐年增加(Dana等人, (2019) 《美國眼科雜誌》(Am. J. Ophthalmol.) 202: 47-54)。
預期為了避免手術疼痛治療不足,同時亦最大限度地減少對當今使用的類鴉片或其他鎮痛藥物的依賴,需要具有同等或更大療效的更安全的鎮痛替代品,以避免當今療法的副作用。此類替代品可用作單一療法或用作多模態方案之一部分,其與現有療法一起發揮相加或協同作用(Ong等人, (2007) 《臨床醫藥研究》(Clin.Med. Res.), 5(1):19-34)。然而,需要具有不同於目前可用之作用機制的藥物來實現此點。因此,儘管迄今為止在疼痛管理,尤其術後疼痛管理方面做出努力,但仍需要解決與市售鎮痛劑相關之缺陷的新藥物。
本發明提供藥物組合物、醫藥組合物、調配物、醫療套組以及製造及使用此類組合物之方法。本文所揭示之組合物表現出與NSAID、COX-2、類鴉片及類固醇藥物不同的作用模式,例如藉由促效內源性大麻素受體活性,且尤其CB
2內源性大麻素受體活性,具有減輕個體之疼痛及炎症的雙重作用。大麻素2型(CB
2)受體為大麻素受體家族之G蛋白偶合受體,其在人類中由CNR2基因編碼。
本文所述之組合物顯示出雙重鎮痛及消炎活性,且代表一類新的鎮痛及/或消炎藥物。此外,由於其獨特的作用模式,本文所揭示之組合物可與藉由不同作用模式起作用之藥物組合,以獲得更大的總治療效果。該等組合物亦可增強經由不同作用模式起作用之其他藥物的功效(協同活性)。因此,本文所述之組合物能夠與環氧合酶抑制劑藥物協同作用以減輕疼痛炎症。換言之,本文所述之組合物具有以下能力:(a)減少實現個體經歷之疼痛或炎症之給定減少所需的環氧合酶抑制劑藥物的量(COX減量)或(ii)增加接受環氧合酶抑制劑之個體經歷之疼痛及炎症減少程度,以達到環氧合酶抑制劑單獨或與其他經由相同作用模式起作用之藥物組合所無法實現的程度(COX增強)。
在第一態樣中,本發明提供一種組合物,包括用於促效個體之CB
2受體活性的組合物。該組合物包含以下之組合:
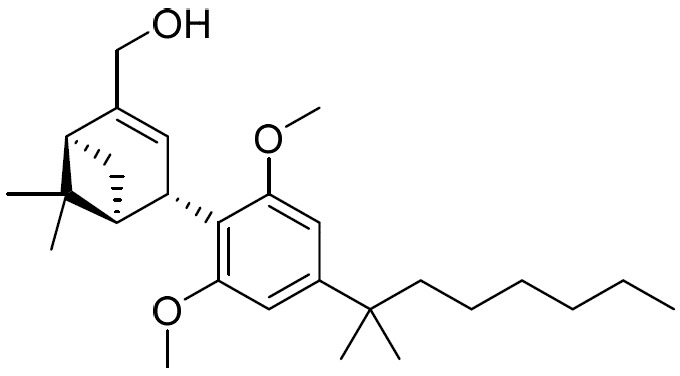
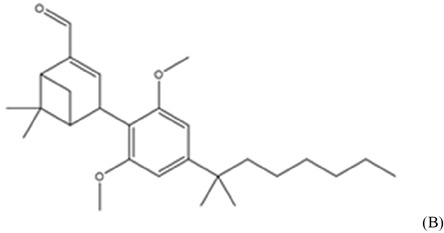
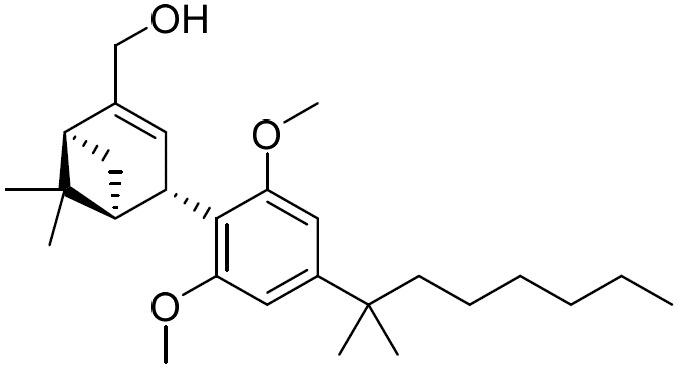
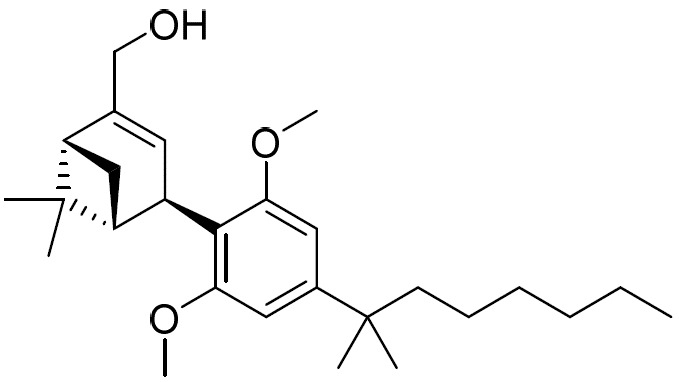
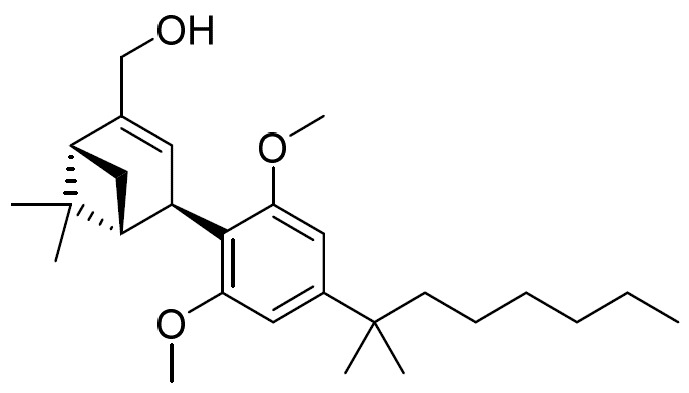
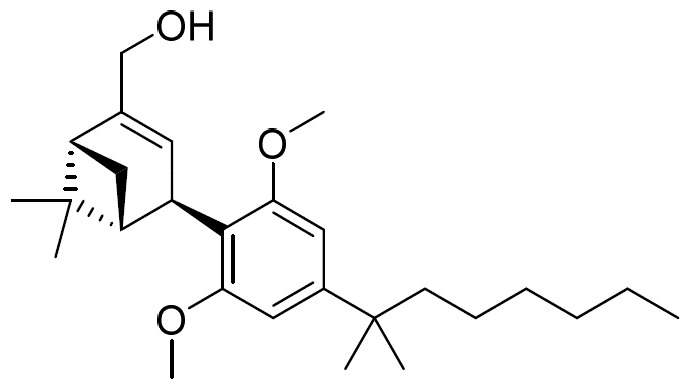
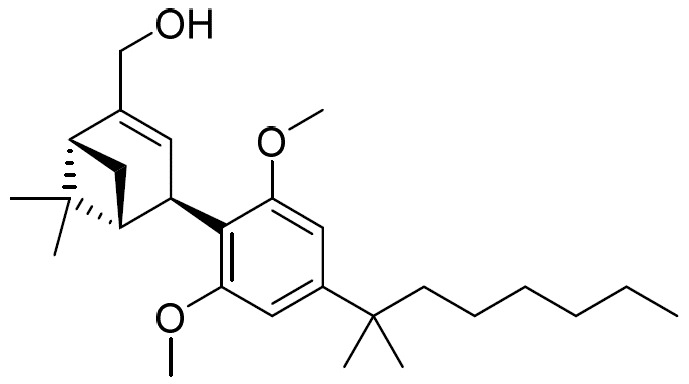
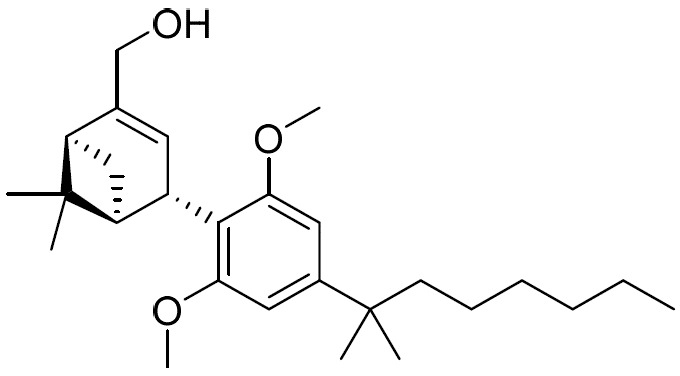
(a)式I之第一化合物:
(E1)或其醫藥學上可接受之鹽;
及
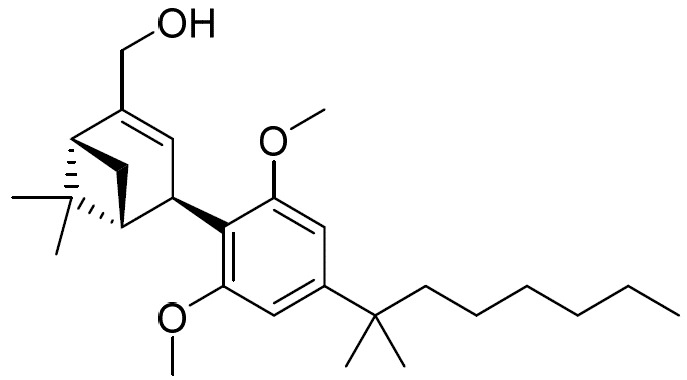
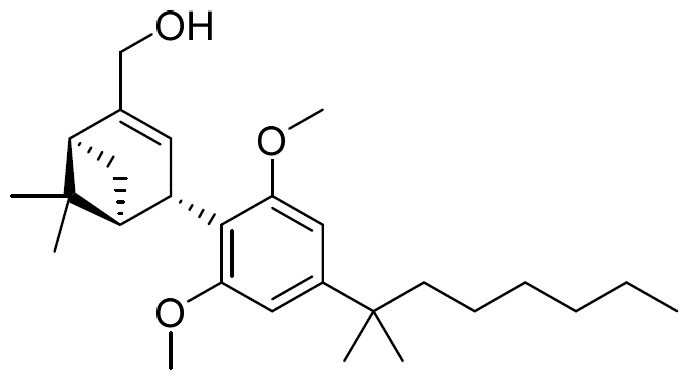
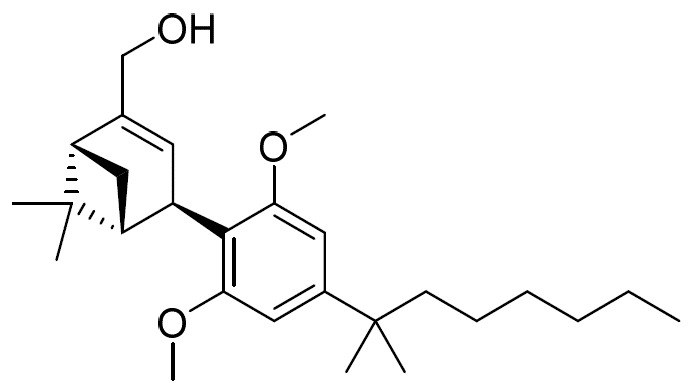
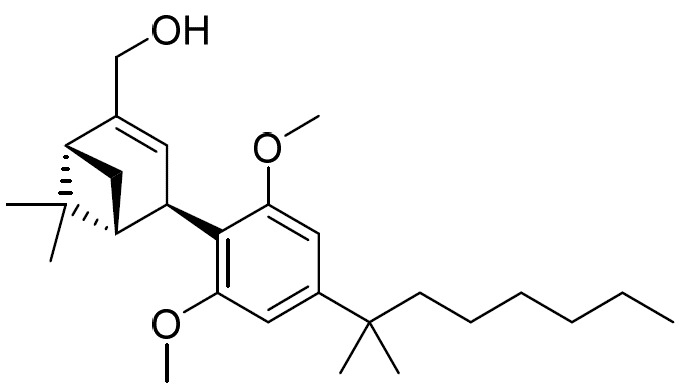
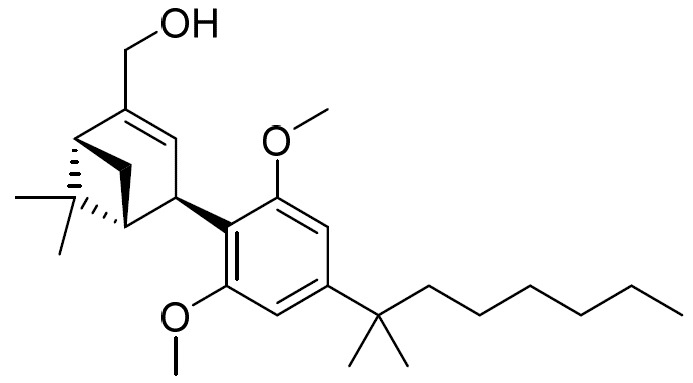
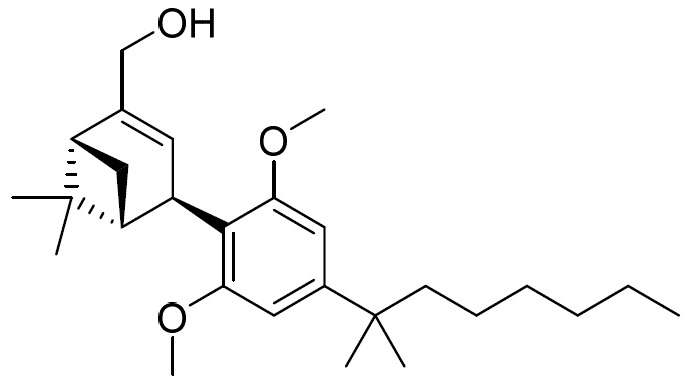
(b)式II之第二化合物:
(E2)或其醫藥學上可接受之鹽;
其中該組合物包括式I化合物及式II化合物(其組合在一起稱為「CB
2受體促效劑組合物」或「CB2RA組合物」),其重量比為99.85:0.15至93.5:6.5。醫藥組成物亦包含醫藥學上可接受之賦形劑。在本發明之CB2RA組合物中,式I化合物與式II化合物之重量比可為99.8:0.2至98.2:1.8;98.8:1.2至98.4:1.6;及99.3:0.7至98.7:1.3。在本發明之CB2RA組合物中,式I化合物與式II化合物之重量比可為約99:1或99:1。
預期包含CB2RA組合物之醫藥組合物可包含一或多種醫藥學上可接受之賦形劑,以促進CB2RA組合物在醫藥組合物中之溶解及/或遞送。例示性賦形劑包括溶解CB2RA組合物之藥劑,包括例如一或多種聚合物(例如兩性聚合物,包括非離子聚合物、泊洛沙姆、二嵌段及三嵌段聚合物、接枝聚合物及星形聚合物)、鹽、緩衝劑(例如,碳酸氫鹽緩衝劑、檸檬酸鹽緩衝劑、磷酸鹽緩衝劑、溴甲烷緩衝劑、乳酸鹽緩衝劑及乙酸鹽緩衝劑)或其組合。可用於本文所述之醫藥組合物中之其他賦形劑包括例如複合糖(例如,右旋糖、環糊精、果糖、葡萄糖、海藻糖及甘露糖醇)、油及蠟(例如,礦物油、棉籽油及大豆油)、穩定劑(例如,甘胺酸、組胺酸或卵磷脂)、黏度增強劑(例如,海藻酸鹽、卡波姆、殼聚醣、黃原膠、玻尿酸及纖維素衍生物)、穩定劑(例如,抗壞血酸、半胱胺酸、麩胺酸及α生育酚)及防腐劑(例如,苯紮氯銨、苯甲醇及苯甲酸鈉)。
預期本文所述之CB2RA組合物可以多種形式提供用於儲存、遞送或使用,包括乾粉、用於復原之凍乾餅、注射劑、輸注劑、噴霧劑、凝膠、乳膏、軟膏、珠粒、丸粒、粒子、微米粒子、奈米粒子、微胞、脂質體、奈米材料、壓縮奈米材料、壓縮粒子、壓縮粉末、膠囊、錠劑、栓劑、子宮托或其類似物。
視預期用途而定,CB2RA組合物可調配成立即釋放或修飾釋放形式,例如其中修飾釋放特徵包括CB2RA組合物之加速釋放、延遲釋放、延長釋放、單相釋放、雙相釋放或多相釋放。
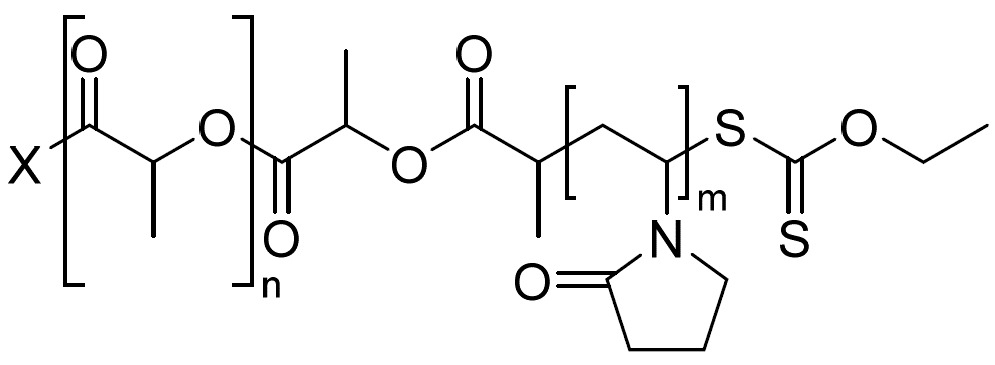
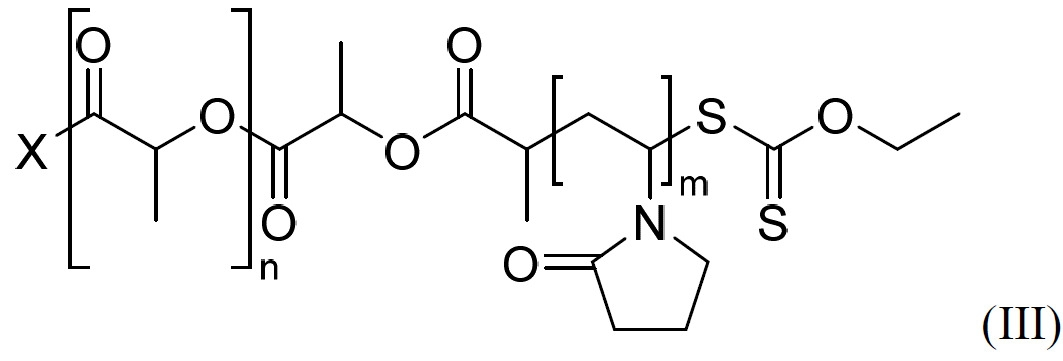
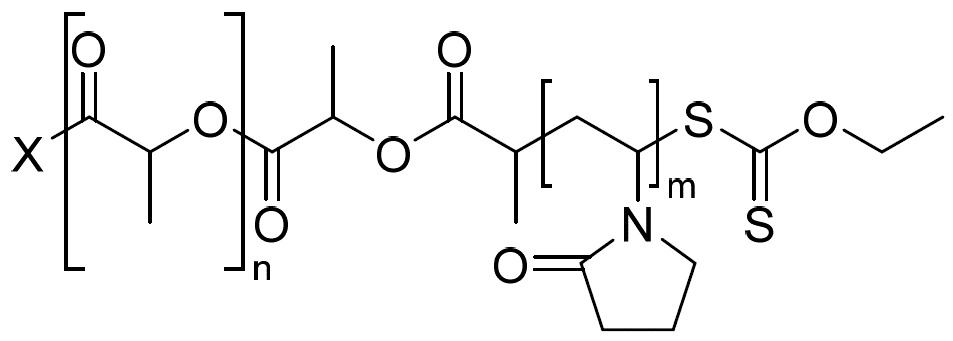
視情況而定,CB2RA組合物可調配成例如微胞、奈米粒子、微米粒子、粉末或分散液用於遞送。調配物視情況包括有助於形成此類微胞、奈米粒子、微米粒子、粉末或分散液之聚合物或一系列聚合物。在一實施例中,聚合物可為嵌段共聚物,諸如聚乙烯吡咯啶酮-聚乳酸(PVP-PLA)共聚物。例示性PVP-PLA共聚物具有式III之結構:
(III),其中X、n及m定義如下。
預期包含CB2RA組合物之調配物(例如醫藥組合物)可包括緩衝劑,例如磷酸鹽緩衝劑。此外,預期包含CB2RA組合物之醫藥組合物亦可包括鹽,以提供適合於遞送至個體之溶液。例示性鹽包括例如鈉鹽、鉀鹽或其組合。
在某些實施例中,含有CB2RA組合物之調配物可呈微胞製劑形式,其可呈液體形式或可呈固體形式(例如壓縮粉末、凍乾粉末或噴霧乾燥粉末)。固體形式可隨後在投與個體之前再水合。
在某些實施例中,醫藥組合物可包括約0.25%(w/w)至約60%(w/w)、約0.5%(w/w)至約40%(w/w)、約0.75%(w/w)至約30%(w/w)或約1%(w/w)至約20%(w)的CB2RA組合物。另外,醫藥組合物可包括約5%(w/w)至約95%(w/w)或30重量%至約90重量%或約60重量%至約85重量%或約70重量%至約80重量%的聚合物。此外,醫藥組合物可包括約1重量%至約20重量%之緩衝劑。視預期遞送模式及用途而定,醫藥組合物亦可進一步包括防腐劑、複合糖、張力劑、冷凍保護劑、增積劑、溶劑或媒劑、脂質及脂肪酸。預期所選實際醫藥組合物將取決於多種因素,包括但不限於待治療個體之年齡及性別、待治療適應症及適應症之嚴重程度、所需釋放動力學及所需遞送模式。
在某些實施例中,固體劑型,例如在遞送及儲存後,可按原樣直接投與個體,或在使用前在溶劑中溶解或再水合以產生微胞溶液。溶劑可為例如醇、水(例如注射用水)、抑菌水、右旋糖溶液(例如5%右旋糖溶液)、林格氏溶液、林格氏乳酸鹽溶液或鹽水。
當呈液體、凝膠、軟膏或其他半固體形式時,本文所述之醫藥組合物的pH值可為約5至約9、約6至約8或約6.5至約7.5。預期組合物之微胞溶液可包括粒度(Z.av)在12-50 nm、15-45 nm或20-40 nm之間及/或多分散性指數(PDi)為約0.05至約0.5的粒子。粒子可帶電或不帶電。
當呈液體、凝膠、軟膏或其他半固體形式時,本文所述之醫藥組合物的黏度可在約0.2 mPas至約80,000 mPas、約0.5 mPas至約70,000 mPas、約1 mPas至約60,000 mPas、約10 mPas至約50,000 mPas、約50 mPas至約50,000 mPas、約100 mPas至約50,000 mPas的範圍內。
視情況而定,預期CB2RA組合物可進一步包含第三化合物、第四化合物、第五化合物、第六化合物及第七化合物,其相對於各第三、第四、第五、第六及第七化合物之量在組合物之0.015%與1.5%(wt/wt)之間。
本文亦提供一種治療有需要個體之炎症及/或疼痛的方法,其中該方法包括向該個體投與治療有效量之CB2RA組合物或含有CB2RA組合物之醫藥組合物。炎症或疼痛可為慢性或急性的。炎症或疼痛可為軀體炎症或軀體疼痛,其可為術後軀體炎症或術後軀體疼痛。炎症或疼痛可為眼部炎症或眼部疼痛,其可為術後眼部炎症或術後眼部疼痛。炎症或疼痛可能與眼部疾病或創傷有關,包括角膜創傷(例如,角膜手術或損傷)。炎症或疼痛可為內臟炎症或內臟疼痛,其可為術後內臟炎症或術後內臟疼痛。炎症或疼痛可為神經性炎症或神經性疼痛,其可為術後神經性炎症或術後神經性疼痛。
該方法可進一步包含向個體投與治療有效量之非類固醇消炎藥(NSAID)及/或類固醇。NSAID可為例如阿司匹林(aspirin)、萘普生(naproxen)、雙氯芬酸(diclofenac)、美洛昔康(meloxicam)、布洛芬(ibuprofen)、酮洛芬(ketoprofen)、托美丁(tolmetin)、吲哚美辛(indomethacin)、舒林酸(sulindac)、吡羅昔康(piroxicam)、甲芬那酸(mefenamic acid)、依託度酸(etodolac)、氟比洛芬(flurbiprofen)、奈帕芬胺(nepafenac)、乙醯胺酚(acetaminophen)、溴芬酸(bromofenac)、酮咯酸(ketorolac)、塞來昔布(celecoxib)、依他昔布(etoricoxib)、羅美昔布(lumiroacoxib)、羅非昔布(rofecoxib)、伐地考昔(valdecoxib)、帕瑞考昔(parecoxib)、阿西美辛(acemethacin)、右布洛芬(dexibuprofen)、尼美舒利(nimesulide)、萘丁美酮(nabumetone)、噻洛芬酸(tiaprofenic acid)、氯諾昔康(lornoxicam)、替諾昔康(tenoxicam)、醋氯芬酸(aceclofenac)、丙谷美辛(proglumethacin)、右酮洛芬(dexketoprofen)或奧沙普
(oxaprozin)。類固醇可為例如皮質類固醇,包括糖皮質類固醇。皮質類固醇或糖皮質類固醇可為丙酸倍氯松(clobetasol propionate)、丙酸鹵倍他索(halobetasol propionate)、氟西奈德(fluocinonide)、二乙酸二氟拉松(diflorasone diacetate)、去羥米松(desoximetasone)、特戊酸氯可托龍(clocortolone pivalate)、糠酸莫米松(mometasone furoate)、曲安奈德(triamcinolone acetonide)、戊酸倍他米松(betamethasone valerate)、丙酸氟替卡松(fluticasone propionate)、潑尼卡酯(prednicarvate)、丙丁酸氫化可的松(hydrocortisone probutate)、曲安奈德氟西奈德(triamcinolone acetonide fluocinolone acetonide)、地塞米松氯替潑諾依碳酸氯替潑諾(dexamethasone loteprednolloteprednol etabonate)、二丙酸阿氯米松(alclometasone)、地奈德(desonide)或氫化可的松(hydrocortisone)。
NSAID及/或類固醇可在CB2RA組合物投與之前、同時或之後向個體投與。CB2RA組合物之投與可與組合投與個體之NSAID及/或類固醇或其他鎮痛或消炎藥物協同起作用。
當與NSAID及/或類固醇或其他鎮痛或消炎藥物組合投與時,CB2RA組合物之投與可增強NSAID及/或類固醇及/或其他鎮痛及/或消炎藥物之作用,以達成比藉由單獨投與NSAID及/或類固醇及/或其他鎮痛及/或消炎藥物所達成更多的疼痛及炎症之減少。當與NSAID及/或類固醇及或其他鎮痛或消炎藥物組合投與時,CB2RA組合物之投與可減少達成期望的疼痛及炎症減少所需的NSAID及/或類固醇及/或其他鎮痛及/或消炎藥物之量。
在另一態樣中,本發明提供一種組合物,其包含醫藥學上有效量之CB2RA組合物及醫藥學上有效量之非類固醇消炎藥(NSAID)及/或類固醇。NSAID可為例如阿司匹林、萘普生、雙氯芬酸、美洛昔康、布洛芬、酮洛芬、托美丁、吲哚美辛、舒林酸、吡羅昔康、甲芬那酸、依託度酸、奈帕芬胺、氟比洛芬、乙醯胺酚、溴芬酸、酮咯酸、塞來昔布、依他昔布、羅美昔布、羅非昔布、伐地考昔、帕瑞考昔、阿西美辛、右布洛芬、尼美舒利、萘丁美酮、噻洛芬酸、氯諾昔康、替諾昔康、醋氯芬酸、丙谷美辛、右酮洛芬環孢素、立他司特或奧沙普
。類固醇可為例如皮質類固醇,包括糖皮質類固醇。皮質類固醇或糖皮質類固醇可為丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸氫化可的松、曲安奈德氟西奈德、地塞米松氯替潑諾依碳酸氯替潑諾、二丙酸阿氯米松、地奈德或氫化可的松。本發明之CB2RA組合物及NSAID及/或類固醇及或其他鎮痛藥物及/或其他消炎藥物可調配成單一劑型。其他鎮痛藥物可為麻醉藥物、刺激劑、類鴉片藥物、抗抑鬱藥物或抗驚厥藥物。
本申請案主張2020年8月21日申請之名稱為「雙重鎮痛/消炎組合物、組合及其使用方法(DUAL ANALGESIC/ANTI-INFLAMMATORY COMPOSITIONS, COMBINATIONS, AND METHODS OF USE THEREOF)」的美國臨時申請案第63/068,737號;2020年10月2日申請之名稱為「雙重鎮痛/消炎組合物、組合及其使用方法」的美國臨時申請案第63/087,038號;及2021年5月20日申請之名稱為「雙重鎮痛/消炎組合物、組合及其使用方法」的美國臨時申請案第63/191,107號的優先權,前述三項申請案以其各自全部引用的方式併入。
本發明部分基於發現一種新的物質組合物,亦即CB2RA組合物,其具有獨特的作用模式,不同於目前可用的消炎及/或鎮痛藥品之作用模式,亦即大麻素CB
2受體之促效作用。本文所述之組合物代表一種用於治療個體之疼痛及/或炎症的新組合物,且代表同類中第一種內源性大麻素受體介導之雙重鎮痛及消炎劑。因此,本發明提供治療組合物、治療調配物、治療劑型、醫療套組以及製造及使用此類組合物、治療劑型及醫療套組之方法。
除非另外指明,否則本發明之實踐採用有機化學、藥理學及生物化學之習知技術。此類技術在文獻中進行解釋,諸如在「綜合有機合成(Comprehensive Organic Synthesis)」(B.M. Trost及I. Fleming編, 1991-1992)中,其中之每一者以全文引用之方式併入本文中。本發明之各種態樣闡述於下文部分中;然而,一個特定部分中所述之本發明之態樣不限於任何特定部分。
I. 定義
為便於理解本發明,下文定義多個術語及片語。
如本文所用,術語「一(a/an)」意謂「一或多個」且包括複數個,除非上下文不適合。
本揭示案之化合物及組合物可含有一或多個手性中心及/或雙鍵,且因此以立體異構體形式存在,諸如幾何異構體、對映異構體或非對映異構體。當在本文中使用時,術語「立體異構體」由所有幾何異構體、對映異構體或非對映異構體組成。視圍繞立體生成碳原子之取代基的組態而定,此等化合物可由符號「R」或「S」表示。本發明涵蓋此等化合物之各種立體異構體及其混合物。立體異構體包含對映異構體及非對映異構體。對映異構體或非對映異構體之混合物在命名法中可指定為「(±)」,但熟習此項技術者應認識到結構可隱含地表示手性中心。應理解,除非另有說明,否則化學結構之圖形描述,例如通用化學結構,涵蓋指定化合物之所有立體異構形式。
本發明化合物之個別立體異構體可由市售起始材料合成製備,該等起始材料可含有或藉由處理導致含有不對稱或立體對稱中心。相反,此類起始材料可能需要新穎的合成方法以精確控制化合物中之立體異構比率。本發明化合物之個別立體異構體亦可藉由製備立體異構混合物,隨後藉由一般熟習此項技術者熟知之解析方法獲得。此等解析方法藉由在手性層析管柱上直接分離光學對映異構體之混合物來例示。立體異構混合物亦可藉由眾所周知的方法,諸如手性相氣相層析或手性相高效液相層析解析成其組分立體異構體。此外,可使用文獻中所述之超臨界流體層析(SFC)技術分離對映異構體。再者,立體異構體可藉由眾所周知的不對稱合成方法自立體異構純中間物、試劑及催化劑獲得。
幾何異構體亦可存在於本發明之化合物中。符號
表示可為如本文所描述之單鍵、雙鍵或參鍵之鍵。本發明涵蓋由碳-碳雙鍵周圍之取代基之排列或碳環周圍之取代基之排列產生的各種幾何異構體及其混合物。圍繞碳-碳雙鍵之取代基指定為「
Z」或「
E」組態,其中術語「
Z」及「
E」係根據IUPAC標準使用。除非另外規定,否則描繪雙鍵之結構涵蓋「
E」及「
Z」異構體。
圍繞碳-碳雙鍵之取代基可替代地稱為「順式」或「反式」,其中「順式」表示在雙鍵同一側之取代基,且「反式」表示在雙鍵相對側之取代基。圍繞碳環之取代基之排列指定為「順式」或「反式」。術語「順式」表示在環平面同一側之取代基,且術語「反式」表示在環平面相對側之取代基。取代基位於環平面同一側及相對側之化合物的混合物指定為「順式/反式」。
本發明亦涵蓋同位素標記之本發明化合物,其與本文中所列舉之化合物相同,不同之處在於一或多個原子經原子質量或質量數不同於自然界中通常所見之原子質量或質量數的原子置換。可併入本發明化合物中之同位素之實例包括氫、碳、氮、氧、磷、氟及氯之同位素,分別諸如
2H、
3H、
13C、
14C、
15N、
18O、
17O、
31P、
32P、
35S、
18F及
36Cl。
某些同位素標記之所揭示化合物(例如經
3H及
14C標記之彼等化合物)可用於化合物及/或受質組織分佈分析。氚化(亦即
3H)及碳-14(亦即
14C)同位素因其易於製備及可偵測性而尤其較佳。此外,用諸如氘(亦即
2H)之較重同位素取代可提供由較大代謝穩定性產生之某些治療優勢(例如活體內半衰期增加或劑量需求減少),且因此在某些情況下可為較佳的。同位素標記之本發明化合物一般可藉由按照與例如本文實例中所揭示之程序類似的程序,藉由用同位素標記之試劑取代未經同位素標記之試劑來製備。
如本文所用,術語「個體」及「患者」係指待藉由本發明之方法治療的生物體。此類生物體較佳為哺乳動物(例如鼠科、猿猴、馬科、牛科、豬科、犬科、貓科及其類似動物),且更佳為人類。
如本文所用,術語「有效量」係指足以實現有益或期望結果之化合物或組合物(例如本發明之化合物或組合物)的量。有效量可藉由一種化合物單獨或兩種或更多種化合物一起作用,以一或多次投與、施用或劑量投與,且不意欲限於特定調配物或投與途徑。如本文所用,術語「治療(treat/treating/treatment)」包括使得病況、疾病、病症及其類似物得以改善的任何作用,例如減輕、減少、調節、改善或消除,或改善其症狀。
如本文所用,術語「醫藥組合物」係指活性劑與惰性或活性載劑之組合,使得該組合物尤其適用於活體內或離體診斷或治療用途。
如本文所用,術語「醫藥學上可接受之載劑」係指任何標準醫藥學載劑,諸如磷酸鹽緩衝鹽水溶液、水、乳液(例如油/水或水/油乳液)及各種類型之潤濕劑。組合物亦可包括穩定劑及防腐劑。關於載劑、穩定劑及佐劑之實例,參見Martin, 《雷明頓醫藥科學》(Remington's Pharmaceutical Sciences), 第15版, Mack Publ. Co., Easton, PA [1975]。
如本文所用,術語「醫藥學上可接受之鹽」係指本發明化合物之任何醫藥學上可接受之鹽(例如酸或鹼),其在投與個體後能夠提供本發明化合物或其活性代謝物或殘餘物。如熟習此項技術者所知,本發明化合物之「鹽」可衍生自無機或有機酸及鹼。酸之實例包括但不限於鹽酸、氫溴酸、硫酸、硝酸、過氯酸、反丁烯二酸、順丁烯二酸、磷酸、乙醇酸、乳酸、水楊酸、丁二酸、甲苯對磺酸、酒石酸、乙酸、檸檬酸、甲磺酸、乙磺酸、甲酸、苯甲酸、丙二酸、萘-2-磺酸、苯磺酸及其類似物。其他酸,諸如草酸,儘管本身並非醫藥學上可接受的,但可用於製備可用作中間物之鹽,以獲得本發明化合物及其醫藥學上可接受之酸加成鹽。
鹼之實例包括但不限於鹼金屬(例如鈉)氫氧化物、鹼土金屬(例如鎂)氫氧化物、氨及式NW
4 +化合物,其中W為C
1-4烷基,及其類似物。
鹽之實例包括但不限於:乙酸鹽、己二酸鹽、海藻酸鹽、天冬胺酸鹽、苯甲酸鹽、苯磺酸鹽、硫酸氫鹽、丁酸鹽、檸檬酸鹽、樟腦酸鹽、樟腦磺酸鹽、環戊烷丙酸鹽、二葡糖酸鹽、十二烷基硫酸鹽、乙磺酸鹽、反丁烯二酸鹽、氟庚酸鹽、甘油磷酸鹽、半硫酸鹽、庚酸鹽、己酸鹽、鹽酸鹽、氫溴酸鹽、氫碘酸鹽、2-羥基乙磺酸鹽、乳酸鹽、順丁烯二酸鹽、甲磺酸鹽、2-萘磺酸鹽、菸鹼酸鹽、草酸鹽、雙羥萘酸鹽、果膠酸鹽、過硫酸鹽、苯基丙酸鹽、苦味酸鹽、特戊酸鹽、丙酸鹽、丁二酸鹽、酒石酸鹽、硫氰酸鹽、甲苯磺酸鹽、十一烷酸鹽及其類似物。鹽之其他實例包括與適合陽離子諸如Na
+、NH
4 +及NW
4 +(其中W為C
1-4烷基)及其類似物複合之本發明化合物之陰離子。
對於治療用途,預期本發明化合物之鹽為醫藥學上可接受的。然而,非醫藥學上可接受之酸及鹼的鹽亦可用於例如製備或純化醫藥學上可接受之化合物。
如本文所用,片語「治療有效量」意謂化合物、材料或組合物(例如包含本發明之一或多種化合物的組合物)之量,其在適用於任何醫學治療的合理益處/風險比下,有效地在動物之至少一個亞群細胞中產生某種期望的治療效果。
片語「醫藥學上可接受」在本文中用於指在合理醫學判斷範疇內,適用於與人類及動物之組織接觸而無過度毒性、刺激、過敏反應或其他問題或併發症,與合理益處/風險比相稱的彼等化合物、材料、組合物及/或劑型。
在本申請案中,當元素或組分被稱為包括在及/或選自所列舉之元素或組分的清單中時,應理解,該元素或組分可為所列舉之元素或組分中之任一者,或該元素或組分可選自由所列舉之元素或組分中之兩者或更多者組成之群。
此外,應理解,本文所述之組合物或方法之元素及/或特徵可以多種方式組合而不背離本發明之精神及範疇,無論在本文中為明確的或隱含的。舉例而言,除非上下文另外理解,否則當提及特定化合物時,該化合物可用於本發明組合物之各種實施例及/或本發明之方法中。換言之,在本申請案內,實施例之描述及描繪方式能夠使本申請案之編寫及繪製清晰簡潔,但希望且應瞭解,可在不脫離本發明教示及本發明之情況下以各種方式組合或分離實施例。舉例而言,應瞭解,本文中所描述及描繪之所有特徵可適用於本文中所描述及描繪之本發明之所有態樣。
應理解,除非自上下文及用途另外理解,否則表述「……中之至少一者」單獨地包括該表述前之列舉對象中之每一者及列舉對象中之兩者或更多者之各種組合。除非自上下文另外理解,否則與三個或更多個列舉對象相關之表述「及/或」應理解為具有相同含義。
除非另外具體陳述或自上下文中理解,否則術語「包括(include/includes/including)」、「具有(have/has/having)」、「含有(contain/contains/containing)」,包括其文法等效物之使用,通常應理解為開放式及非限制性的,例如不排除其他未列舉的元素或步驟。
除非另外具體說明,否則在數量值之前使用術語「約」時,本發明亦包括具體數量值本身。在本發明中立體異構體之比率存在差異之情況下,除非另外具體說明,否則在具體數量值之前的術語『約』亦包括具體數量值本身。
應理解,步驟次序或用於執行某些動作之次序並不重要,只要本發明保持可操作即可。此外,可同時進行兩個或更多個步驟或動作。
在本說明書中各個位置處,取代基以群組或範圍形式揭示。本說明書特別意欲包括此類群組及範圍之成員的每一個單獨的子組合。舉例而言,術語「C
1-6烷基」專門用於單獨揭示C
1、C
2、C
3、C
4、C
5、C
6、C
1-C
6、C
1-C
5、C
1-C
4、C
1-C
3、C
1-C
2、C
2-C
6、C
2‑C
5、C
2‑C
4、C
2‑C
3、C
3‑C
6、C
3‑C
5、C
3‑C
4、C
4‑C
6、C
4‑C
5及C
5‑C
6烷基。藉助於其他實例,0至40範圍內之整數專門用於單獨揭示0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39及40,且1至20範圍內之整數專門用於單獨揭示1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19及20。其他實例包括,片語「視情況經1-5個取代基取代」專門用於單獨揭示可包括0、1、2、3、4、5、0-5、0-4、0-3、0-2、0-1、1-5、1-4、1-3、1-2、2-5、2-4、2-3、3-5、3-4及4-5個取代基的化學基團。
除非主張,否則本文使用任何及所有實例或例示性語言,例如「諸如」或「包括」僅意欲更好地說明本發明,且不對本發明的範疇構成限制。本說明書中之語言不應解釋為表明任何未主張之元素對於本發明之實踐必不可少。
在整個說明書中,當組合物及套組描述為具有、包括或包含特定組分時,或當製程及方法描述為具有、包括或包含特定步驟時,預期另外存在基本上由列舉組分組成或由列舉組分組成的本發明之組合物及套組,且存在基本上由列舉之處理步驟組成或由列舉之處理步驟組成的根據本發明之製程及方法。
一般而言,除非另外規定,否則指定百分比之組合物係以重量計。此外,若變數未附定義,則以該變數之先前定義為準。
如本文所用之縮寫包括質譜(MS)、氣相層析(GC)、滯留時間(RT)、相對滯留時間(RRT)、超臨界流體層析(SFC)及高效液相層析(HPLC)。
II. 組合物及醫藥組合物
本發明部分地涉及一種新的化學組合物,其作為CB
2R促效劑,提供用於同時治療個體之疼痛及/或炎症之新作用機制。
在一個態樣中,本文提供一種組合物,例如醫藥組合物,其能夠促效個體之CB
2受體活性。該組合物包含以下之組合:
(a)式I之第一化合物:
(E1)或其醫藥學上可接受之鹽;
及
(b)式II之第二化合物:
(E2)或其醫藥學上可接受之鹽;
其中該組合物包含式I化合物及式II化合物,其重量比為99.85:0.15至93.5:6.5。醫藥組成物亦包含醫藥學上可接受之賦形劑。
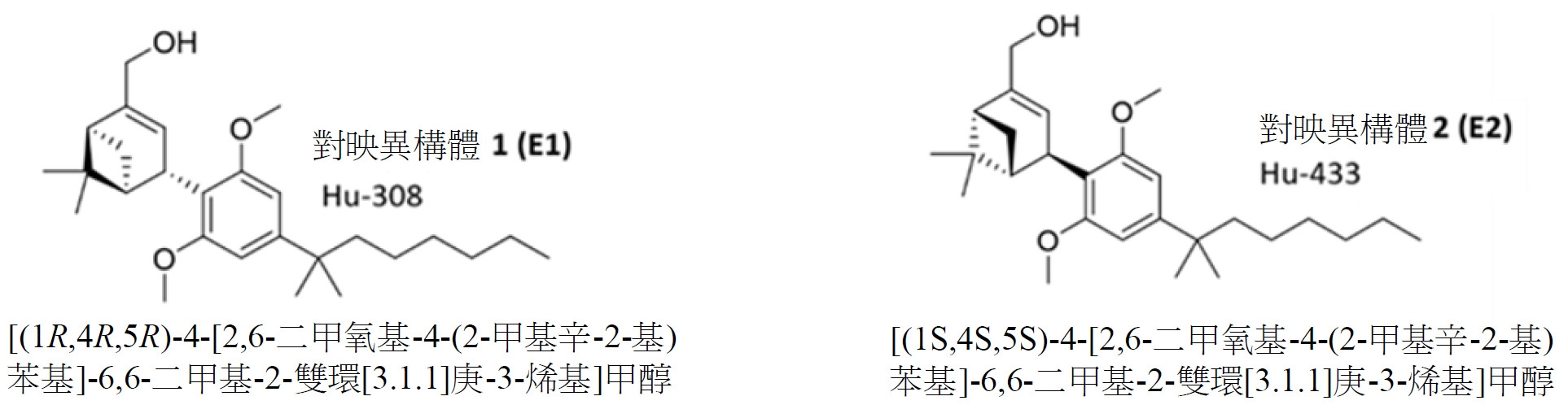
包含式I之第一化合物及式II之第二化合物的組合物在本文中稱為CB2受體促效劑組合物或CB2RA組合物。式I化合物在本文中亦稱為對映異構體1(「E1」),且係基於稱為Hu-308之CB
2受體促效劑(Soethoudt (2017) 《自然-通訊》(Nature Commun.), 8: 13958)。式II化合物在本文中亦稱為對映異構體2(「E2」),且係基於稱為Hu-433之CB
2受體促效劑(Morales等人, (2017) 《藥理學前沿》, 8: 422)。據報導,E2對映異構體之效力為E1之1,000至10,000倍,同時結合相同的受體,但對CB
2受體之親和力低於E1(Smoum等人 (2015) 《美國國家科學院院刊》, 112.28: 8774-8779)。
在描述此新化學實體時,提供包含不同比率之稱為E1及E2之第一及第二化合物的對映異構體組合物的活性概況。此等比率可根據一種對映異構體與另一種之重量比(wt/wt)或根據對映異構體過量來定義,其中對映異構體過量使用下式(E1-E2)/(E1+E2)計算。
本發明部分基於以下出人意料的發現:包含式I化合物(E1)及式II化合物(E2)之組合的CB
2受體促效劑組合物在急性疼痛及炎症之模型中顯示不同程度的鎮痛及/或消炎作用,視對映異構體E1與E2之重量比而定(參見
圖 6B及
圖 8-11)。
此外,已出乎意料地發現,儘管據報導E2在單獨投與動物時顯示出比E1高1,000至10,000倍的效力(Smoum等人 (2015) 同上),但當E1存在時,及當E2之量相對於組合物中E1之量增加時,鎮痛反應之變化並未反映所報導之1,000 -10,000倍效力增加。實際上,已發現使用E1與E2之特定比率可實現最佳活性,其中E1超過E2。換言之,本發明部分基於以下出人意料的發現:儘管據報導E2之效力高於E1,但本發明之CB2RA組合物的效力並不隨著組合物中E2之量增加而繼續增加,而是實際上,效力增加限於對映異構體混合物中E2濃度之限定範圍(
圖 12A)。雖然具有本文所述之E1與E2之重量比的本發明之CB2RA組合物提供的鎮痛及/或消炎反應大於對照投與產生的反應,但具有限定重量比範圍之組合物提供相對於其他比率增強的鎮痛反應。
因此,例如,已經由曲線擬合(參見
圖 12B)發現,當CB2RA組合物中E2之量在約0.15%至約2%之間或在約0.2%至約1.8%之間時,則CB2RA組合物之鎮痛效力(例如每毫克CB2RA組合物之鎮痛作用)增加。當E1與E2之重量比為約99:1時,CB2RA組合物之效力為E2之量在此範圍之外的CB2RA組合物的兩倍以上。此類增強之效力極大地有益於需要鎮痛之個體,因為可投與較低劑量之CB2RA組合物以達成所需程度之鎮痛。如此項技術中眾所周知的,較低劑量之藥物(諸如鎮痛劑藥物)與較少不良副作用相關。若投與更高效力的CB2RA組合物,則患者的生活品質可因此增加。
相反,由於其效力較高,E2之量在約0.15%至約2%之間或在約0.2%至約1.8%之間的CB2RA組合物可比E2之量在此範圍之外的CB2RA組合物實現每劑量更多的鎮痛作用。因此,對於給定程度的不良副作用,當投與E2之量在約0.15%至約2%之間或在約0.2%至約1.8%之間的CB2RA組合物時,可實現比E2之量在此範圍之外的CB2RA組合物可實現的更大的鎮痛緩解。此對於需要鎮痛之個體可為有益的,因為可獲得更大的緩解。
因此,E2之量在約0.15%至約2%之間或在約0.2%至約1.8%之間的CB2RA組合物實現的增加的效力可具有比E2之量在此範圍之外的CB2RA組合物更大的上限劑量。
另外,已發現本文所述之CB2RA組合物在與非CB2RA組合物例如環氧合酶抑制劑止痛劑混合時可協同地起作用,以產生比單獨使用環氧合酶抑制劑或CB2RA組合物中之任一者更有效的醫藥組合物。預期此協同作用將極大地有益於需要鎮痛及/或抗炎作用之個體,尤其在多模態情況下。預期需要鎮痛及或消炎緩解者可自共同投與具有不同但互補作用模式之醫藥劑獲得最大益處,無論單獨或以混合物形式投與。因此,相較於若單獨投與CB2RA組合物或環氧合酶抑制劑,或若藉由其混合實現純粹的相加鎮痛作用所需的投與劑量,本文所述之CB2RA組合物與環氧合酶抑制劑(例如COX抑制劑)之協同作用允許大大減少CB2RA組合物、環氧合酶抑制劑或兩種藥劑之投與劑量,以提供令人滿意的鎮痛及或消炎作用。因此,多模態協同組合可產生較少的不良副作用,從而使個體之治療效果得到改善且個體之體驗更好。相反,藉由組合或以其他方式共投與CB2RA組合物及環氧合酶抑制劑所達成之更大效力,使得如果單獨給予的任何給定劑量之CB2RA組合物或環加氧酶抑制劑能產生更大量的鎮痛及或消炎作用。因此,本發明之CB2RA組合物可與環氧合酶抑制劑協同起作用的發現允許安全地達成更高水準的鎮痛及消炎作用。
已發現一種新的對映異構體CB
2受體介導之鎮痛及/或消炎劑,亦即本文所述之CB2RA組合物,其作用模式不同於常用於分別治療疼痛及炎症之市售類鴉片受體促效劑、環加氧酶抑制劑及類固醇,可與常用NSAID鎮痛劑協同地起作用。此外,已意外地發現,CB2RA組合物中對映異構體之比率對組合物之效力具有深遠的影響,因此可界定比率範圍,其中對映異構體之組合作用使得效力增加,可將治療個體所需的CB2RA組合物之量減少一半。另外,已發現,當使用微胞技術(例如使用基於PVP-PLA之聚合物)調配且靜脈內遞送時,CB2RA組合物在急性切口疼痛模型中引起即時及長時間的鎮痛及/或消炎作用,其效力根據ED
50,大致為市售NSAIDS及COX-2抑制劑之十倍(參見例如表3)。
鑒於前述,預期組合物之式I化合物(E1)與式II化合物(E2)之重量比可為99.85:0.15至93.5:6.5、99.8:0.2至98.2:1.8、98.8:1.2至98.4:1.6及99.3:0.70至98.7:1.3。CB2RA組合物中式I化合物與式II化合物之重量比可為約99:1或99:1。
為方便起見,以E1:E2之重量比範圍列出之值及以對映異構體過量範圍列出之等效值彙總於表1中。
表 1
1EE% = (|E1-E2|)/(E1+E2) *100
| 重量比範圍(E1:E2) | 對映異構體過量範圍 1 |
| 99.85:0.15至93.5:6.5 | 99.7 - 87.0 |
| 99.8:0.2至98.22:1.8 | 99.6 - 96.4 |
| 99.3:0.7至98.7:1.3 | 98.6 - 97.4 |
| 98.8: 1.2至98.4: 1.6 | 97.6 - 96.8 |
| 99:1 | 98 |
此外,在某些實施例中,式I化合物與式II化合物之重量比為或約99:1、為或約98:2、為或約97:3、為或約96:4、為或約95:5、或為或約94:6。此等值分別對應於約98、約96、約94、約92、約90及約88之EE值。
類似地,本文所述之CB2RA組合物可具有約87%至約99.7%、約96.4%至約99.6%、約97.4%至98.6%、約88%至98%、約90%至約98%、約92%至約98%、約94%至約98%、約96%至約98%之EE,相對於式(II)化合物有利於式(I)化合物。本文所述之組合物可具有約87%、約88%、約90%、約92%、約94%、約96%或約98%之EE,相對於式(II)化合物有利於式(I)化合物。
組合物可進一步包括0.015%至1.5%或0.01%至1%之第三、第四、第五或第六化合物,其滯留時間(RT)及相對滯留時間(RRT)根據實例2之逆相HPLC分析方法產生,如表2中所指定。在表2中,含量(%)表示以相對於整個組合物之百分比組成表示之化合物的量測量,且(+)表示經鑑別之化合物相對於整個組合物之百分比組成低於指定分析方法之定量水準。
表 2
| 化合物編號 | |||||||
| 1 | 2 | 3 | 4 | CB2RA組合物 | 6 | 7 | |
| 滯留時間(RT min.) | |||||||
| 17.4 | 18.1 | 18.4 | 19.2 | 19.9 | 20.2 | 23.2 | |
| 相對滯留時間(RRT. min) | |||||||
| 0.87 | 0.91 | 0.92 | 0.96 | 1.00 | 1.02 | 1.16 | |
| 含量(%) | |||||||
| 批次1 | 0.32 | + | 0.65 | + | 98.18 | 0.13 | 0.08 |
| 批次2 | 0.54 | 0.11 | 0.29 | 0.13 | 98.01 | 0.09 | + |
表2顯示如實例9中所產生之兩批例示性材料中除CB2RA組合物以外的某些化合物之存在、其峰數、其相對於CB2RA組合物之百分比組成及其滯留時間,如
圖 2A之藉由實例2中所述之逆相HPLC方法所鑑別。CB2RA組合物(亦即含有對映異構體E1及E2)使用
圖 2引用之逆相HPLC方法的滯留時間為19.9分鐘,且(+)表示存在除CB2RA組合物以外的化合物,其百分比組成低於逆相HPLC方法之定量水準。峰值在17.4分鐘處之第一化合物以0.1%至0.6%之量存在,峰值在18.1分鐘處之第二化合物以0.01%至0.2%之量存在,峰值在18.4分鐘處之第三化合物以0.2%至0.7%之量存在,峰值在19.2分鐘處之第四化合物以0.01至0.15%之量存在,峰值在20.2分鐘處之第六化合物以0.05%至0.15%之量存在,且峰值在23.2分鐘處之第七化合物以0.01%至0.1%之量存在。
在一個實施例中,組合物包含至多14% wt/wt之雜質。在一個實施例中,組合物包含至多13% wt/wt之雜質。在一個實施例中,組合物包含至多12% wt/wt之雜質。在一個實施例中,組合物包含至多11% wt/wt之雜質。在一個實施例中,組合物包含至多10% wt/wt之雜質。在一個實施例中,組合物包含至多9% wt/wt之雜質。在一個實施例中,組合物包含至多8% wt/wt之雜質。在一個實施例中,組合物包含至多7% wt/wt之雜質。在一個實施例中,組合物包含至多6% wt/wt之雜質。在一個實施例中,組合物包含至多5% wt/wt之雜質。在一個實施例中,組合物包含至多4% wt/wt之雜質。在一個實施例中,組合物包含至多3% wt/wt之雜質。在一個實施例中,組合物包含至多2% wt/wt之雜質。在一個實施例中,組合物包含至多1% wt/wt之雜質。在一個實施例中,組合物包含至多0.5% wt/wt之雜質。在一個實施例中,組合物包含至多0.1% wt/wt之雜質。在一個實施例中,組合物包含至多0.05% wt/wt之雜質。在一個實施例中,組合物包含至多0.01% wt/wt之雜質。在一個實施例中,組合物包含至多0.005% wt/wt之雜質。在一個實施例中,組合物包含至多0.001% wt/wt之雜質。
在一些實施例中,上述量測之雜質量為在40℃下培育後的。在一些實施例中,上述量測之雜質量為在40℃下培育1個月後的。在一些實施例中,上述量測之雜質量為在40℃下培育2個月後的。在一些實施例中,上述量測之雜質量為在40℃下培育3個月後的。在一些實施例中,上述量測之雜質量為在40℃下培育6個月後的。
在一些實施例中,上述量測之雜質量為在65℃下培育後的。在一些實施例中,上述量測之雜質量為在65℃下培育24小時後的。在一些實施例中,上述量測之雜質量為在65℃下培育48小時後的。
在一些實施例中,上述量測之雜質量為在80℃下培育後的。在一些實施例中,上述量測之雜質量為在80℃下培育24小時後的。在一些實施例中,上述量測之雜質量為在80℃下培育48小時後的。
在一個實施例中,組合物進一步包含用於減少雜質形成之抗氧化劑。
在一個實施例中,抗氧化劑係選自由以下組成之群:抗壞血酸、丁基化羥基甲苯、芝麻酚、愈創木樹脂、甲硫胺酸、檸檬酸、酒石酸、磷酸、硫醇衍生物、偏亞硫酸氫鉀、抗壞血酸棕櫚酸酯、硬脂酸鈣、沒食子酸丙酯、硫代硫酸鈉、麩胱甘肽、二羥基苯甲酸、苯甲酸、尿酸鹽及尿酸、山梨酸、苯甲酸鈉、EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
在一個實施例中,抗氧化劑係選自由以下組成之群:EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
在一個實施例中,抗氧化劑包含丁基化羥基大茴香醚。
在一個實施例中,組合物基本上不含氧。
在一個實施例中,組合物不含氧。
在一個實施例中,組合物儲存在惰性氣體下。
III. 活性成分之合成
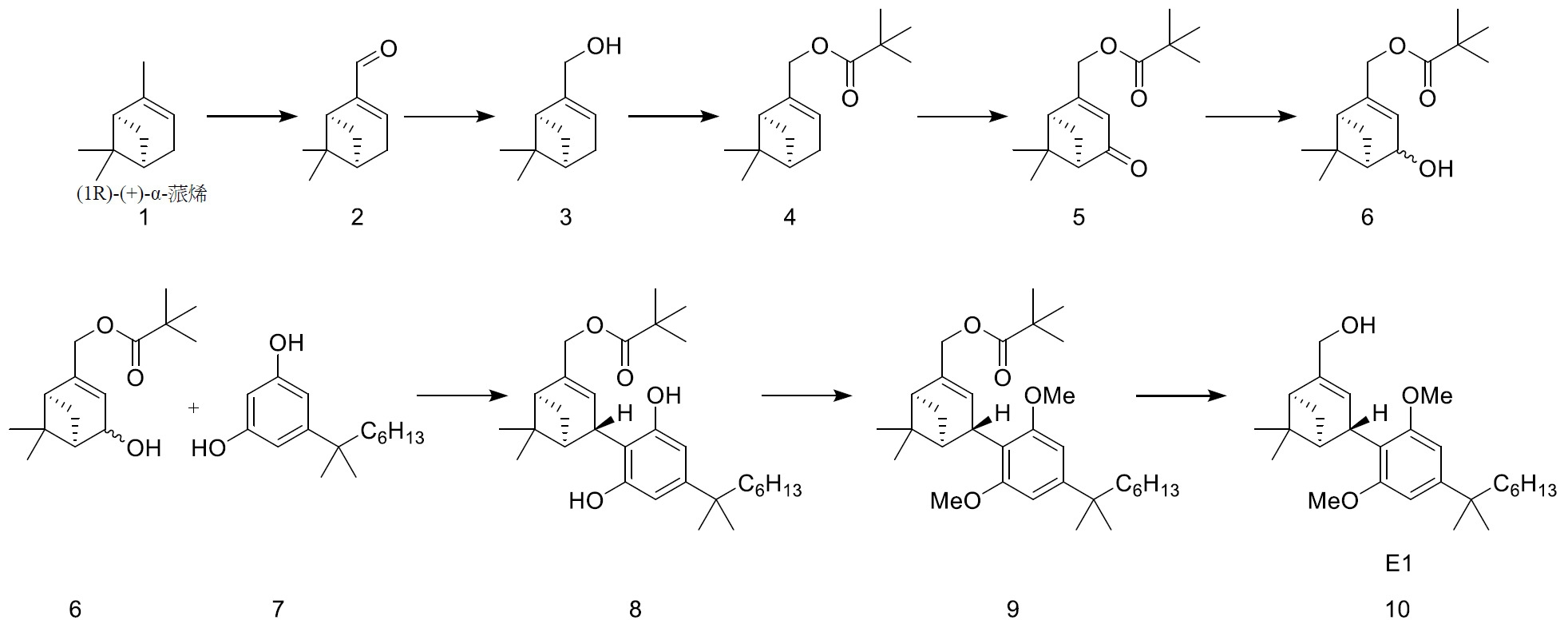
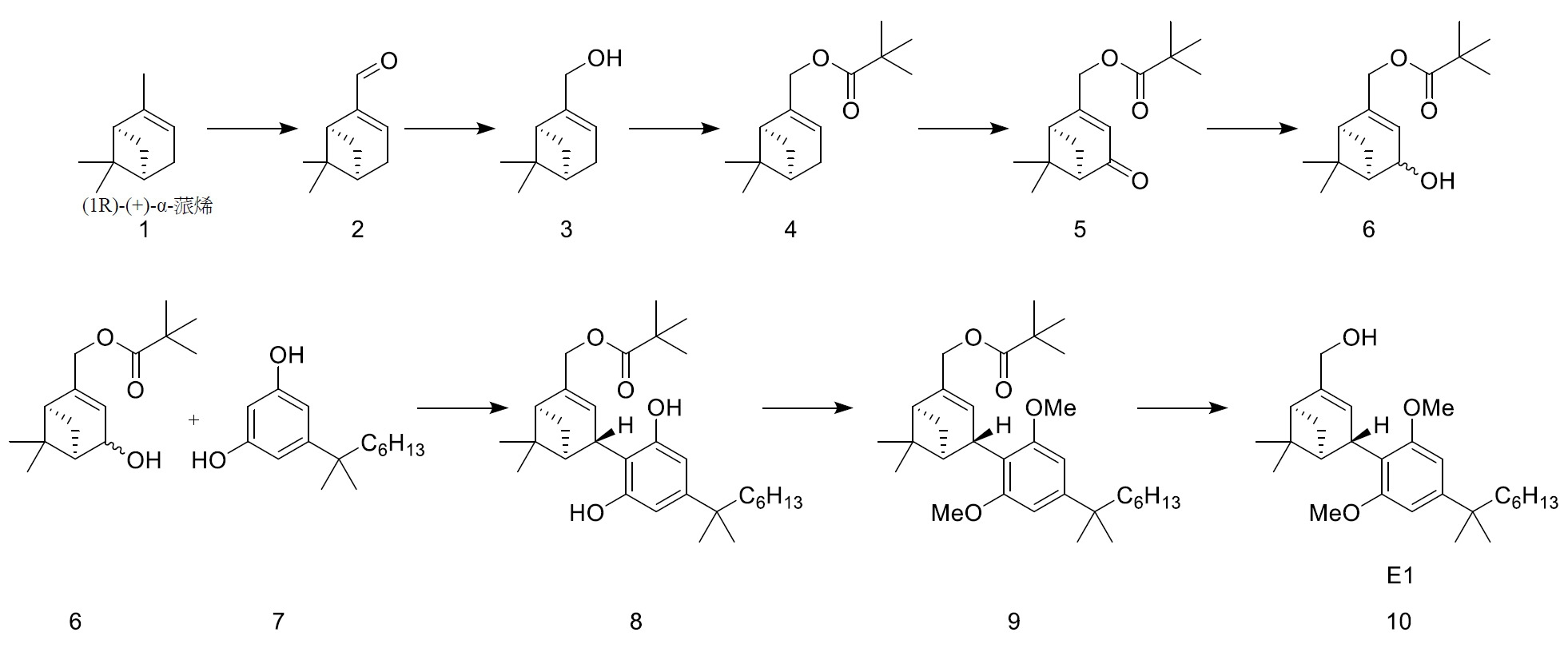
式I化合物(對映異構體E1)可以(1R)-(+)-α-蒎烯作為起始材料開始,經由一系列八個步驟合成。簡言之,(1R)-(+)-α-蒎烯之C2位置處的甲基碳可經氧化以產生桃金娘烯醛,隨後還原成(+)-桃金娘烯醇。隨後,(+)-桃金娘烯醇之醇基可用特戊醯基保護。受保護之(+)-桃金娘烯醇可在亞甲基碳(C4位置)處進一步氧化,且還原得到特戊酸4-羥基-桃金娘烯基酯。接下來,特戊酸4-羥基-桃金娘烯基酯可與5-(1,1-二甲基庚基)-間苯二酚縮合,得到(特戊酸2-[2,6-二羥基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)。在接下來的步驟中,間苯二酚部分之C2及C6位置處的醇基可經甲基化為甲氧基。在最後一步中,特戊酸酯保護基可經由還原(特戊酸2-[2,6-二甲氧基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)來移除,得到所需產物(E1,式I化合物)。可藉由所需組分之手性分離來獲得對映異構純材料。
式II化合物(對映異構體E2)可自(1R)-(-)-桃金娘烯醇以6個步驟合成。簡言之,(1R)-(-)-桃金娘烯醇之C2位置處的醇基可使用特戊醯基保護基來保護。受保護之(1R)-(-)-桃金娘烯醇可隨後在其C4位置處經氧化以產生特戊酸4-側氧基-桃金娘烯基酯,其隨後還原成特戊酸4-羥基-桃金娘烯基酯。特戊酸(1R)-(-)-4-羥基-桃金娘烯基酯可隨後與5-(1,1-二甲基庚基)-間苯二酚縮合,得到(特戊酸2-[2,6-二羥基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)。在最後兩個步驟中,C2及C6位置處之醇可經甲基化,且特戊酸酯保護基可經由還原移除,產生式II化合物(對映異構體E2)。可藉由所需組分之手性分離來獲得對映異構純材料。
式II之化合物3'亦可以(1S)-(+)-α-蒎烯作為起始材料開始以兩步合成來合成。簡言之,(1S)-(+)-α-蒎烯之C2位置處的甲基碳可經氧化以產生桃金娘烯醛,隨後還原成(+)-桃金娘烯醇。(+)-桃金娘烯醇可隨後如所述用於產生式2化合物(E2)。
E1及E2可在其各自的合成途徑結束時經由熟習此項技術者已知的方法(例如手性HPLC、SFC)進行對映異構純化。一旦獲得對映異構純材料,其可以所需量組合以實現所需E1與E2之比,例如99:1。
或者,E1及E2之起始材料或合成中間物可經對映異構純化。預期組合物之E1/E2比率可隨後藉由混合已知量的對映異構純E1及E2且藉由手性HPLC確認比率來控制。
或者,含有式I及式II之化合物的組合物可以特戊酸4-羥基-桃金娘烯基酯作為起始材料開始,經由一系列三個步驟來合成。簡言之,特戊酸(1S)-(+)4-羥基-桃金娘烯基酯與特戊酸(1R)-(-)-4-羥基-桃金娘烯基酯混合,且混合物與5-(1,1-二甲基庚基)-間苯二酚縮合以產生(特戊酸2-[2,6-二羥基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)。在下一步驟中,間苯二酚部分之C2及C6位置處的醇基經甲基化為甲氧基。在最後一步中,經由還原(特戊酸2-[2,6-二甲氧基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)移除特戊酸酯保護基,產生所需組合物。
類似地,含有式I及式II之化合物的組合物可藉由在所需製程內階段混合方案1及2之任一步驟的等效產物,且隨後經由單一反應方案完成合成之其餘合成步驟來合成。
IV. 醫藥調配物及投與
如下文所述,含有本文所述之CB2RA組合物的醫藥組合物可專門調配成以固體或液體形式投與,包括適用於以下之醫藥組合物:(1)經口投與,例如溶液或懸浮液(例如水性或非水性溶液或懸浮液)、錠劑(例如以經頰、舌下及/或全身吸收或局部吸收為目標之錠劑)、大丸劑、散劑,包括用於經肺遞送之散劑、顆粒劑、施用於舌頭之糊劑;(2)非經腸投與,藉由例如靜脈內、皮下、肌肉內或硬膜外注射,作為例如無菌溶液或懸浮液,或持續或其他修飾釋放調配物;(3)局部施用,例如作為乳膏、軟膏、粉末或控制釋放貼片、或植入物、或施用於皮膚或吸入之噴霧劑;(4)陰道內或直腸內,例如作為子宮托、乳膏或泡沫;(5)舌下;(6)經眼;(7)經皮;或(8)經鼻。在某些實施例中,醫藥組合物可經口投與有需要之個體。在其他實施例中,醫藥組合物可靜脈內或皮下或腹膜內或眼內或眼周投與有需要之個體。在某些實施例中,醫藥組合物可局部投與有需要之個體。在某些實施例中,醫藥組合物可鼻內投與有需要之個體。
無論對映異構體之對映異構體過量或重量比如何,本文所述之含有E1及E2之組合物的水溶性通常低於0.5 mg/L。因此,組合物較佳經調配以增加水性藥物濃度,尤其在欲達成靜脈內、皮下或眼部給藥的情況下。預期含有某種聚合物技術之調配物,例如基於PVP-PLA之聚合物,可用於將溶解度提高到至少5 g/L,其代表溶解度增加超過四個數量級。
應理解,醫藥組合物可視所需遞送模式而調配。然而,預期醫藥組合物用一或多種醫藥學上可接受之賦形劑調配,該等賦形劑可包括例如溶解聚合物(例如包括非離子聚合物之兩性聚合物)、緩衝劑、鹽或其組合。可用於醫藥組合物中之其他賦形劑包括複合糖(例如右旋糖、環糊精、果糖、葡萄糖、海藻糖及甘露糖醇、纖維素衍生物、澱粉及澱粉衍生物)、油及蠟(例如礦物油、棉籽油及大豆油)、穩定劑(例如甘胺酸、組胺酸或卵磷脂)、黏度增強劑(例如海藻酸鹽、卡波姆、殼聚醣、黃原膠、聚乙烯醇及玻尿酸)、穩定劑(例如抗壞血酸、半胱胺酸、麩胺酸及α生育酚)及防腐劑(例如,苯紮氯銨、苯甲醇及苯甲酸鈉)、乳化劑、著色劑、脫模劑、包衣劑、甜味劑及潤滑劑。
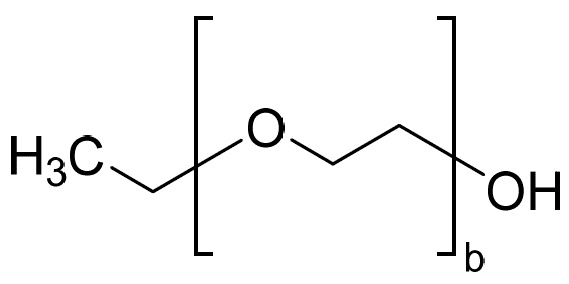
例示性增溶聚合物可為聚乙烯吡咯啶酮-聚乳酸(PVP-PLA)共聚物,如國際公開案第WO2018176158A1號中所述,其教示內容以全文引用之方式併入本文中。PVP-PLA聚合物包含式III之結構:
,
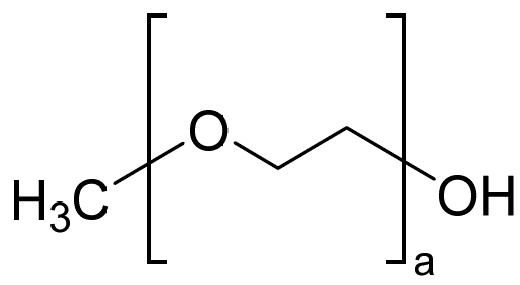
其中x為沸點大於145℃之引發劑醇,n平均為20至40,且m平均為10至40,其中嵌段共聚物之數目平均分子量(Mn)為至少3,000 Da。「引發劑醇」應理解為意謂具有羥基且能夠充當聚合之受質的物種,在此情況下為聚(D,L丙交酯)(PLA)。
其中b≥1;及其混合物。預期x可為例如二乙二醇單乙醚(DEGMEE)。在某些實施例中,嵌段共聚物之Mn小於12,000 Da、11,000 Da、10,000 Da、9,000 Da、8000 Da、7000 Da或6000 Da。在某些實施例中,嵌段共聚物之Mn小於7,000 Da。在某些實施例中,嵌段共聚物之Mn大於4,000 Da、5,000 Da或6,000 Da。
在某些實施例中,醫藥組合物可包含約5重量%至約95重量%、或30重量%至約90重量%、或約60重量%至約85重量%或約70重量%至約80重量%的嵌段共聚物。
在某些實施例中,嵌段共聚物能夠形成含有本發明組合物之微米粒子,其中該等微米粒子適合向個體投與。微米粒子奈米粒子之平均粒度可小於1000 µm、500 µm、100 µm、75 µm、50 µm、25 µm、10 µm或1 µm。微米粒子可經尺寸設定以允許皮下遞送本發明組合物,或可經尺寸設定以允許將本發明組合物遞送至眼睛,包括藉由眼內、眼周或眼上途徑。舉例而言,微米粒子之尺寸可大於250 nm(Lengyel等人, (2019) 《醫學科學》(Scientia Pharmaceutica), 87(3): 20-31)。
在某些實施例中,嵌段共聚物能夠形成含有CR2RA組合物之奈米粒子,其中該等奈米粒子適合向個體投與。奈米粒子之平均粒度可小於500 nm、400 nm、300 nm、200 nm、100 nm、75 nm、50 nm或25 nm。奈米粒子可經尺寸設定以避免或減少腎臟排泄。舉例而言,奈米粒子之平均粒度可大於12 nm。
另外,CB2RA組合物可調配於微胞中以產生微胞組合物。舉例而言,微胞可由兩性聚合物(例如PVP-PLA嵌段共聚物,其含有疏水區(PLA基團)以及親水區(PVP基團)產生。典型的微胞在水溶液中形成,聚合物之親水區與周圍溶劑接觸,將疏水區隔離在微胞核心。微胞可以溶液或乾燥形式(例如餅或粉末)存在,其可向個體投與或再水合以產生可向個體投與之溶液。舉例而言,微胞包括微胞之先前液體膠態組合物的乾燥形式,其中微胞結構之一些元素以乾燥形式保留,或其中該乾燥形式在水合時容易重新形成微胞。當乾燥時,微胞可在溶劑中再水合,例如水(例如WFI)、抑菌水、右旋糖溶液(例如5%右旋糖溶液)、林格氏溶液、林格氏乳酸鹽溶液或生理鹽水。在某些實施例中,調配物可含有防腐劑或抗微生物劑,諸如苯紮氯銨、苯甲醇、苯甲酸鈉及苯酚。
在某些實施例中,調配物(例如微胞調配物)可為基本上透明的液體,例如不含可見顆粒。在某些實施例中,溶液可具有指示溶液一般清晰度之光學透射率。光學透射率可例如大於70%、80%、90%、95%、96%、97%或98%。
預期在適當情況下,醫藥組合物可包含水凝膠,諸如熱塑性水凝膠、或交聯水凝膠、或可調水凝膠、或黏合水凝膠或可植入水凝膠(Jainyu (2016) 《自然綜述材料》(Nat. Rev. Mater.), 1(12): 1-38)。
預期在某些情況下,水凝膠可為基於澱粉之水凝膠且較佳為交聯之高直鏈澱粉水凝膠,例如,如加拿大專利第3034722號中所述。
預期水凝膠可含有聚合物,包括可交聯聚合物。
預期醫藥組合物可顯示立即釋放或修飾釋放特徵,其中修飾釋放包括加速釋放、破裂釋放、延遲釋放、延長釋放、單相、雙相、脈衝或多相釋放。
預期醫藥組合物可包含緩衝劑。例示性緩衝劑包括例如順丁烯二酸、蘋果酸、葡甲胺、甲硫胺酸、氯化鉀、氫氧化鉀、碳酸鈉、碳酸氫鈉、氯化鈉、氫氧化鈉、乳酸鈉、磷酸鈉、磷酸鉀、磷酸、硫酸、乙酸鈉、乙酸銨、乙酸、緩血酸胺(Tris)、檸檬酸鈉/檸檬酸。在一個實施例中,緩衝劑為磷酸鹽緩衝劑。在某些實施例中,緩衝劑為Tris緩衝劑。或者或另外,醫藥組合物可包括一或多種鹽,例如以產生等張溶液。例示性鹽包括例如銨鹽或鈣鹽。在某些實施例中,鹽可為鈉鹽或鉀鹽。
預期醫藥組合物可包括增積劑。例示性增積劑包括糊精右旋糖、果糖、明膠、葡萄糖、乳糖、麥芽糖、甘露糖醇、聚乙烯吡咯啶酮、蔗糖、山梨糖醇、海藻糖及棉子糖。
預期醫藥組合物可包括溶劑或媒劑。例示性溶劑及媒劑包括例如水、生理鹽水、乙醇、棉籽油、大豆油、二甲亞碸、二甲基乙醯胺、油酸乙酯、甘油、四氫呋喃聚乙二醇醚、礦物油、單乙醇胺、聚乙二醇、丙二醇及甲基吡咯啶酮。
預期醫藥組合物可包括溶解度增強劑。例示性溶解度增強劑包括油醯基聚乙二醇-6甘油酯諸如Labrafil
®M1944 CS(Gattefossé Inc.)、蓖麻油、辛酸、a-環糊精、g-環糊精、b-環糊精、依地酸二鈉、gelucire 44/14(Gattefossé Inc.)、羥丙基β-環糊精、聚乙二醇15羥基硬脂酸酯、中鏈甘油三酯、聚(L-丙交酯)、聚(DL-丙交酯)、聚(丙交酯-共-乙交酯或PLGA)、泊洛沙姆、聚氧乙烯蓖麻油衍生物、聚氧乙烯脫水山梨糖醇脂肪酸酯、聚維酮及甘油三油酸酯。
預期醫藥組合物可包括黏度控制或膠凝劑。例示性黏度控制或膠凝劑包括海藻酸、海藻酸鈉、羧甲基纖維素鈉、卡波姆、殼聚醣、玻尿酸、羥丙甲纖維素、羥丙基纖維素、聚乙烯醇、黃原膠及木葡聚糖。
預期醫藥組合物可包括抗氧化劑。例示性抗氧化劑包括抗壞血酸鹽、氬氣、亞硫酸氫鈉、丁基化羥基苯甲醚、丁基化羥基甲苯、半胱胺酸、二硫亞磺酸鈉、龍膽酸、麩胺酸、偏亞硫酸氫鈉、硫代甘油、氮、亞硫酸鈉及α-生育酚。
預期醫藥組合物可包括穩定劑。例示性穩定劑包括白蛋白、二乙醇胺、甘胺酸、組胺酸及卵磷脂。
預期醫藥組合物可包括釋放控制聚合物。例示性釋放控制聚合物包括例如聚氧化乙烯、聚乙烯吡咯啶酮-聚丙交酯共聚物、聚乙烯吡咯啶酮、普魯蘭、果膠、殼聚醣、海藻酸鈉、角叉菜膠、明膠、甲基纖維素、羧甲基纖維素鈉、交聯羧甲基纖維素鈉、交聯羥丙基纖維素、交聯澱粉、交聯高直鏈澱粉、羥丙基甲基纖維素、羧甲基澱粉、聚甲基丙烯酸酯、聚乙烯吡咯啶酮、聚乙烯醇、聚乙二醇或甲基丙烯酸鉀-二乙烯基苯共聚物及其混合物。
預期醫藥組合物可包括釋放加速劑。例示性釋放加速劑包括澱粉及交聯澱粉及乙醇酸澱粉、交聯纖維素、矽酸鈣及聚乙烯吡咯啶酮。
在某些實施例中,組合物可包含約0.25%(w/w)至約80%(w/w)、約0.5%(w/w)至約60%(w/w)、或約0.75%(w/w)至約30%或約1%(w/w)至約20%(w/w)之CB2RA組合物。在某些實施例中,組合物可包含約0.5%(w/w)至約10%(w/w)、約0.5%(w/w)至約20%(w/w)、或約0.75%(w/w)至約10%(w/w)或約1%至約5%(w/w)之CB2RA組合物。
在某些實施例中,組合物可包含約1重量%至約20重量%、約5重量%至約15重量%、約10重量%、約11重量%、約12重量%、約13重量%、約14重量%、約15重量%、約16重量%、約17重量%、約18重量%、約19重量%、約20重量%之緩衝劑。在某些實施例中,當呈液體形式時,醫藥組合物之pH值可為約4至約9、約6至約8或約6.5至約7.5。在其他實施例中,組合物之pH值可為約6、約6.5、約7、約7.5或約8。
在某些實施例中,當呈液體、凝膠、軟膏或其他半固體形式時,本文所述之醫藥組合物的黏度可在約0.2 mPas至約80,000 mPas、約0.5 mPas至約70,000 mPas、約1 mPas至約60,000 mPas、約10 mPas至約50,000 mPas、約50 mPas至約50,000 mPas、約100 mPas至約50,000 mPas的範圍內。
在某些實施例中,當呈微胞溶液形式時,本文所述之醫藥組合物可包含粒度(Z.av)為12-50 nm、20-40 nm、10-20 nm、20-40 nm、20-35 nm、20 nm-30 nm、25 nm-40 nm、25 nm-35 nm、約20 nm、約25 nm、約30 nm、約35 nm、約40 nm、約50 nm之粒子。在某些實施例中,粒子之多分散性指數(PDi)可為約0.05至約0.15、約0.1至約0.15、約0.05至約0.1、約0.05、約0.10、約0.11、約0.12、約0.13、約0.14或約0.15。
預期調配物可進一步包括潤濕劑、乳化劑、潤滑劑、著色劑、脫模劑、包衣劑、甜味劑、調味劑及防腐劑以及抗氧化劑。例示性潤濕劑包括例如苯紮氯銨、苄索氯銨、氯化十六烷基吡錠單水合物、泊洛沙姆188、泊洛沙姆407、聚乙二醇40硬脂酸酯II型、聚山梨醇酯20、聚山梨醇酯40。例示性乳化劑包括例如阿拉伯膠、卡波姆共聚物、卡波姆互聚物、膽固醇、椰子油、二乙二醇、硬脂酸酯、乙二醇硬脂酸酯、二硬脂酸甘油酯、單亞油酸甘油酯、單油酸甘油酯、單硬脂酸甘油酯、羊毛脂醇、卵磷脂單及二甘油酯、泊洛沙姆、聚氧乙烯硬脂酸酯、聚乙二醇10油基醚、聚乙二醇20鯨蠟硬脂基醚、聚乙二醇35、蓖麻油、聚乙二醇40、氫化蓖麻油、聚乙二醇40硬脂酸酯、聚乙二醇月桂基醚、聚乙二醇硬脂基醚、聚山梨醇酯20、聚山梨醇酯40、聚山梨醇酯60、聚山梨醇酯80、丙二醇單硬脂酸酯、鯨蠟硬脂基硫酸鈉、月桂基硫酸鈉、硬脂酸鈉、脫水山梨糖醇單月桂酸酯、脫水山梨糖醇單油酸酯、脫水山梨糖醇單棕櫚酸酯、脫水山梨糖醇單硬脂酸酯、脫水山梨糖醇倍半油酸酯、脫水山梨糖醇三油酸酯硬脂酸及蠟(乳化)。
例示性潤滑劑包括例如矽酸鈣、硬脂酸鈣、羥丙甲纖維素、硬脂酸鎂、礦物油、聚乙二醇、聚乙二醇硬脂酸酯、聚山梨醇酯、聚乙烯醇、膠態二氧化矽、月桂基硫酸鈉、硬脂醯反丁烯二酸鈉、脫水山梨糖醇單油酸酯、脫水山梨糖醇單棕櫚酸酯、脫水山梨糖醇單硬脂酸酯、脫水山梨糖醇倍半油酸酯、硬脂酸及滑石。例示性釋放控制劑包括例如聚氧化乙烯、聚乙烯吡咯啶酮-聚丙交酯共聚物、聚乙烯吡咯啶酮、普魯蘭、果膠、殼聚醣、海藻酸鈉、角叉菜膠、明膠、甲基纖維素、羧甲基纖維素鈉、交聯羧甲基纖維素鈉、交聯羥丙基纖維素、交聯澱粉、交聯高直鏈澱粉、羥丙基甲基纖維素、羧甲基澱粉、聚甲基丙烯酸酯、聚乙烯吡咯啶酮、聚乙烯醇、聚乙二醇或甲基丙烯酸鉀-二乙烯基苯共聚物及其混合物。例示性包衣劑包括例如乙基纖維素、明膠、羥丙基纖維素、羥丙甲纖維素、甲基纖維素、聚乙二醇、聚乙烯醇、聚乙烯吡咯啶酮、甲基丙烯酸、羥乙基甲基纖維素、乙基纖維素、聚乙酸乙烯酯鄰苯二甲酸酯、鄰苯二甲酸乙酸纖維素、鄰苯二甲酸羥丙基甲基纖維素、馬來酸酐共聚物,包括聚(甲基乙烯基醚/馬來酸酐)及羥丙基甲基纖維素。
例示性防腐劑包括例如對羥基苯甲酸甲酯、對羥基苯甲酸乙酯、對羥基苯甲酸丙酯、對羥基苯甲酸丁酯、苯甲醇、氯丁醇、苯酚、間甲酚、氯甲酚、苯甲酸、山梨酸、硫柳汞、硝酸苯汞、溴硝醇、丙二醇、苯紮氯銨及苄索氯銨。例示性抗氧化劑包括例如(1)水溶性抗氧化劑,諸如抗壞血酸、半胱胺酸鹽酸鹽、硫酸氫鈉、偏亞硫酸氫鈉、亞硫酸鈉及其類似物;(2)油溶性抗氧化劑,諸如抗壞血酸棕櫚酸酯、丁基化羥基大茴香醚(BHA)、丁基化羥基甲苯(BHT)、卵磷脂、沒食子酸丙酯、α-生育酚及其類似物;及(3)金屬螯合劑,諸如檸檬酸、乙二胺四乙酸(EDTA)、山梨糖醇、酒石酸、磷酸及其類似物。
在一個實施例中,醫藥組合物包含至多14% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多13% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多12% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多11% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多10% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多9% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多8% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多7% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多6% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多5% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多4% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多3% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多2% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多1% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多0.5% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多0.1% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多0.05% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多0.01% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多0.005% wt/wt之雜質。在一個實施例中,醫藥組合物包含至多0.001% wt/wt之雜質。
在一些實施例中,上述量測之雜質量為在40℃下培育後的。在一些實施例中,上述量測之雜質量為在40℃下培育1個月後的。在一些實施例中,上述量測之雜質量為在40℃下培育2個月後的。在一些實施例中,上述量測之雜質量為在40℃下培育3個月後的。在一些實施例中,上述量測之雜質量為在40℃下培育6個月後的。
在一些實施例中,上述量測之雜質量為在65℃下培育後的。在一些實施例中,上述量測之雜質量為在65℃下培育24小時後的。在一些實施例中,上述量測之雜質量為在65℃下培育48小時後的。
在一些實施例中,上述量測之雜質量為在80℃下培育後的。在一些實施例中,上述量測之雜質量為在80℃下培育24小時後的。在一些實施例中,上述量測之雜質量為在80℃下培育48小時後的。
在一個實施例中,醫藥組合物進一步包含用於減少雜質形成之抗氧化劑。
在一個實施例中,抗氧化劑係選自由以下組成之群:抗壞血酸、丁基化羥基甲苯、芝麻酚、愈創木樹脂、甲硫胺酸、檸檬酸、酒石酸、磷酸、硫醇衍生物、偏亞硫酸氫鉀、抗壞血酸棕櫚酸酯、硬脂酸鈣、沒食子酸丙酯、硫代硫酸鈉、麩胱甘肽、二羥基苯甲酸、苯甲酸、尿酸鹽及尿酸、山梨酸、苯甲酸鈉、EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
在一個實施例中,抗氧化劑係選自由以下組成之群:EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
在一個實施例中,抗氧化劑包含丁基化羥基大茴香醚。
在一個實施例中,醫藥組合物基本上不含氧。
在一個實施例中,醫藥組合物不含氧。
在一個實施例中,醫藥組合物儲存在惰性氣體下。
調配物可宜以單位劑型呈現且可藉由藥劑學技術中熟知之任何方法製備。可與載劑材料組合以產生單一劑型之活性成分之量將視所治療之宿主、特定投與模式而變化。可與載劑材料組合以產生單一劑型之活性成分之量一般將為產生治療效果之化合物之量。醫藥組合物可包含例如0.1 mg至1 mg、5 mg至50 mg、50 mg至500 mg或500 mg至1000 mg之活性成分。就本發明組合物呈液體形式而言,活性成分之濃度可為約0.05 mg/mL至約0.5 mg/mL、約0.1 mg/mL至約5 mg/mL、約0.5 mg/mL至約5 mg/mL、約1 mg/mL至5 mg/mL、約2 mg/mL至5 mg/mL、約0.5 mg/mL、約1 mg/mL、約2 mg/mL、約3 mg/mL、約4 mg/mL、約5 mg/mL、約10 mg/mL、約20 mg/mL或約30 mg/mL。
本揭示案表明,藉由將CB2RA組合物調配為微胞組合物,其包含具有限定分子量及嵌段與嵌段比之聚乙烯吡咯啶酮及聚丙交酯之二嵌段聚合物(PVP-PLA),CB2RA組合物之表觀水溶性可增加數千倍,每公升含量自毫克至公克,產生黏度、pH值及CB2RA組合物之濃度足以允許簡單非經腸投與哺乳動物及/或簡單局部投與哺乳動物的溶液。
在用於局部投與之液體劑型諸如乳膏、軟膏、噴霧劑或滴眼劑中,活性成分可與一或多種醫藥學上可接受之聚合物混合,諸如:(1)兩親聚合物,包括PVP-PLA;(2)增溶劑,諸如油醯基聚乙二醇-6甘油酯諸如Labrafil
®M1944 CS(Gattefossé Inc.)、a-環糊精、g-環糊精、b-環糊精、依地酸二鈉、羥丙基β-環糊精、聚乙二醇15羥基硬脂酸酯、中鏈甘油三酯、聚(L-丙交酯)、聚(DL-丙交酯)、聚(丙交酯-共-乙交酯或PLGA)、泊洛沙姆、聚氧乙烯蓖麻油衍生物、聚氧乙烯脫水山梨糖醇脂肪酸酯、聚維酮及甘油三油酸酯或其混合物;(3)緩衝劑,諸如磷酸鹽或檸檬酸鹽或碳酸氫鹽或Tris緩衝劑;(4)防腐劑或抗氧化劑,諸如抗壞血酸或半胱胺酸鹽酸鹽;(5)防腐劑,諸如苯紮氯銨或苄索氯銨;及(6)溶劑,諸如水、生理鹽水、乙醇、棉籽油、大豆油、二甲亞碸、二甲基乙醯胺、油酸乙酯、甘油、四氫呋喃聚乙二醇醚、礦物油、單乙醇胺、聚乙二醇、丙二醇及甲基吡咯啶酮,或其混合物。
在用於經口投與之本發明之固體劑型(膠囊、錠劑、丸劑、糖衣藥丸、散劑、顆粒劑、口含錠及其類似物)中,活性成分可與一或多種醫藥學上可接受之載劑諸如檸檬酸鈉或磷酸二鈣及/或以下任一者混合:(1)填充劑或釋放控制劑或增量劑,諸如澱粉、乳糖、蔗糖、葡萄糖、甘露糖醇及/或矽酸;(2)黏合劑,諸如羧甲基纖維素、海藻酸鹽、明膠、聚乙烯吡咯啶酮、蔗糖及/或阿拉伯膠;(3)保濕劑,諸如甘油;(4)崩解劑,諸如瓊脂、碳酸鈣、馬鈴薯或木薯澱粉、海藻酸、某些矽酸鹽及碳酸鈉;(5)溶液阻滯劑,諸如石蠟;(6)吸收促進劑,諸如四級銨化合物,及界面活性劑,諸如泊洛沙姆及月桂基硫酸鈉;(7)潤濕劑,諸如鯨蠟醇、單硬脂酸甘油酯及非離子界面活性劑;(8)吸收劑,諸如高嶺土及膨潤土;(9)潤滑劑,諸如滑石、硬脂酸鈣、硬脂酸鎂、固體聚乙二醇、月桂基硫酸鈉、硬脂酸鋅、硬脂酸鈉、硬脂酸及其混合物;(10)著色劑;及(11)控制釋放劑,諸如交聯聚維酮或乙基纖維素。在膠囊、錠劑及丸劑之情況下,醫藥組合物亦可包含緩衝劑。類似類型之固體組合物亦可用作使用諸如乳糖或奶糖以及高分子量聚乙二醇及其類似物之賦形劑之軟及硬殼明膠膠囊中的填充劑。
錠劑可藉由視情況與一或多種附屬成分一起壓縮或模製來製造。壓縮錠劑可使用黏合劑(例如明膠或羥丙基甲基纖維素)、潤滑劑、惰性稀釋劑、防腐劑、崩解劑(例如羥基乙酸澱粉鈉或交聯羧甲基纖維素鈉)、表面活性劑或分散劑來製備。模製錠劑可藉由在適合的機器中模製用惰性液體稀釋劑潤濕之粉末狀化合物的混合物來製造。
本發明之醫藥組合物之錠劑及其他固體劑型,諸如糖衣藥丸、膠囊、丸劑及顆粒劑,可視情況經刻痕或製備成具有包衣及殼層,諸如腸溶包衣及醫藥調配技術中熟知之其他包衣。其亦可使用例如不同比例之羥丙基甲基纖維素以提供所需釋放特徵、其他聚合物基質、脂質體及/或微米球及或奈米球或其他奈米粒子來調配以便提供其中活性成分之緩慢或控制釋放。其可調配用於快速釋放。其可藉由例如經由細菌截留過濾器過濾、或照射、或高壓滅菌、或藉由併入滅菌劑來滅菌,呈臨用前可溶解於無菌水或一些其他無菌可注射介質中之無菌固體組合物形式。此等組合物亦可視情況含有遮光劑且可為視情況以延遲方式僅僅或優先在胃腸道之某一部分中釋放活性成分之組合物。可使用之包埋組合物之實例包括聚合物質及蠟。適當時,活性成分亦可與上述賦形劑中之一或多者呈微囊封形式。
本發明化合物之用於局部或經皮投與的劑型包括軟膏、糊劑、乳膏、洗劑、凝膠、溶液、散劑、噴霧劑、貼片及吸入劑。活性化合物可在無菌條件下與醫藥學上可接受之載劑及可能需要之任何防腐劑、緩衝劑或推進劑混合。
除活性成分之外,軟膏、糊劑、乳膏及凝膠亦可含有賦形劑,諸如動物及植物脂肪、油、蠟、石蠟、澱粉、黃蓍、纖維素衍生物、聚乙二醇、聚矽氧、膨潤土、矽酸、滑石及氧化鋅或其混合物。
除本發明之活性成分以外,散劑及噴霧劑可含有賦形劑,諸如乳糖、滑石、矽酸、氫氧化鋁、矽酸鈣及聚醯胺粉末或此等物質之混合物。噴霧劑可另外含有習用推進劑,諸如氯氟烴及未經取代之揮發性烴,諸如丁烷及丙烷。
經皮貼片具有提供將CB2RA組合物受控遞送至個體之優點。此類劑型可藉由將活性成分溶解或分散於適當介質中來製備。亦可使用吸收增強劑來增加化合物穿過皮膚之通量。此類通量之速率可藉由提供速率控制膜或使化合物分散於聚合物基質或凝膠中來控制。
可注射儲槽形式可藉由在諸如聚丙交酯-聚乙交酯之可生物降解聚合物中形成主題化合物之微膠囊基質來製備。視藥物與聚合物之比率及所用特定聚合物之性質而定,可控制藥物釋放速率。其他可生物降解聚合物之實例包括聚(原酸酯)聚(酸酐)及複合碳水化合物。可藉由將藥物包覆於與身體組織相容之脂質體或微乳液中來製備儲槽式可注射調配物。
本發明化合物之可植入儲槽形式可呈手術網、基於聚矽氧之植入物、基於聚乙烯之植入物、基於鈦之植入物、聚胺基甲酸酯發泡體植入物、聚乳酸植入物、3D列印生物材料及其類似物形式。可植入儲槽形式亦可呈水凝膠形式,無論是固體或液體或半固體水凝膠,包括生物聚合物及合成聚合物水凝膠、熱塑性水凝膠、熱塑性凝膠、交聯或可交聯水凝膠(包括含膠原蛋白之水凝膠或含膠原蛋白衍生肽之水凝膠)。水凝膠及其他可植入裝置可包含乙烯乙酸乙烯酯及丙烯酸酯。植入物可包括可生物降解的植入物及不可生物降解的植入物。
CB2RA組合物之實際劑量水準可變化,以便獲得有效達成特定患者、組合物及投與模式之所需治療反應而對個體無毒的活性成分之量。所選劑量水準將視多種因素而定,包括所採用之本發明之特定化合物或其酯、鹽或醯胺之活性;投與途徑;投與時間;所採用之特定化合物之排泄或代謝速率;吸收速率及程度;治療持續時間;與所採用之特定化合物組合使用之其他藥物、化合物及/或材料;所治療患者之年齡、性別、體重、病況、一般健康狀況及先前病史;以及醫學技術中熟知之類似因素。
在一些實施例中,具有此項技術普通技能之醫師或獸醫可容易地確定及開具所需CB2RA組合物之有效量。舉例而言,醫師或獸醫可以低於為達成所需治療效果所需之水準的醫藥組合物中所用之本發明化合物的劑量開始,且逐漸增加劑量直至達成所需效果。
一般而言,CB2RA組合物之適合劑量將為作為有效產生治療效果之最低劑量的組合物之量。此類有效劑量將一般視上述因素而定。較佳地,本發明化合物以約0.01 mg/kg至約200 mg/kg、更佳以約0.1 mg/kg至約100 mg/kg、甚至更佳以約0.5 mg/kg至約50 mg/kg投與。當本文所述之組合物與另一藥劑(例如,作為敏化劑,或作為固定劑量組合,或作為佐劑)共投與時,有效量可低於單獨使用該藥劑時之有效量。
必要時,活性化合物之有效劑量可每日以兩次、三次、四次、五次、六次或更多次亞劑量在全天以適當的間隔分開投與,視情況以單位劑型投與。在某些情形下,給藥較佳涉及經由經口投與每天投與一次。必要時,活性化合物之有效劑量可以單次投與劑量每週遞送或以單次投與劑量每兩週遞送。必要時,活性化合物之有效劑量可以單次投與劑量每月遞送。必要時,活性化合物之有效劑量可以單次投與劑量以大於每月一次之時間間隔遞送。
在某些實施例中,醫藥組合物在投與4、3、2、1或0.5小時內提供活性成分之醫藥學上有效之血漿水準。術語「醫藥學上有效之血漿水準」應理解為意謂當在血漿中時足以達成所需治療功效之活性成分的量。此水準可視例如疾病、病症及/或疾病或病症之症狀;疾病、病症及/或疾病或病症之症狀之嚴重程度;待治療個體之年齡、體重及/或健康狀況而變化。
在某些實施例中,醫藥組合物在投與20、15、10、9、8、7、6、5、4、3或2分鐘內提供活性成分之醫藥學上有效之血漿水準。在某些實施例中,活性成分之醫藥學上有效之血漿水準維持至少2、3、4、5、6、7、8、9、10、11、13或24小時。在某些實施例中,活性成分之醫藥學上有效之血漿水準維持至少2、3、4、5、6或7天。在某些實施例中,活性成分之醫藥學上有效之血漿水準維持至少2、3、4或5週。在某些實施例中,活性成分之醫藥學上有效之血漿水準維持至少2、3、4、5、6、7、8、9、10、11或12個月。
例示性醫藥組合物闡述於實例10-24中。
實例10提供CB2RA組合物與PCP-PLA及海藻糖之例示性凍乾餅,其可用於例如錠劑或膠囊中或復原用於注射或局部投與。實例11提供實例10之組合物的例示性噴霧乾燥組合物,其可用於例如錠劑或膠囊、吸入性粉末中。實例12提供CB2RA組合物與環糊精之例示性凍乾餅,其可用於例如錠劑或膠囊中或復原用於注射或局部投與。實例13-14提供用於局部施用之例示性水性調配物,例如用於局部施用於眼睛。實例15提供用於局部施用之例示性凝膠調配物,例如局部施用於眼睛。實例16提供用於局部施用之例示性軟膏,例如局部施用於眼睛。實例17及18提供例示性口服控制釋放劑型。實例19及20提供例示性口服立即釋放調配物。實例21提供例示性口服立即及延遲釋放調配物。實例22及23提供用於併入膠囊中之例示性粉末。實例24提供呈口服立即釋放劑型之含有CB2RA組合物及塞來昔布之組合的例示性組合產品。預期其他劑型可視CB2RA組合物之預期遞送模式、劑量及用途而產生。
V. 組合產品
應理解,本文所述之醫藥組合物可單獨或與醫藥學上有效或亞醫藥學上有效量之非類固醇消炎藥(NSAID)及/或類固醇一起投與。預期額外藥劑可(i)例如經由在本發明組合物之前、同時或之後向個體投與之獨立劑型分開投與,或(ii)以與本發明組合物組合投與額外藥劑之整體劑型投與。
已發現,本文所述之CB2RA組合物之E1與E2的重量比或對映異構體過量程度控制該化合物或組合物表現出的鎮痛及/或消炎作用的水準。另外,已發現E1與E2之重量比存在確定範圍,其中其組合提供有益、更強力或更有效的鎮痛及/或消炎作用。已確定E1與E2之例示性重量比範圍為約99:1或99:1。
由於本文所述之CB2RA組合物具有與常用鎮痛劑、麻醉劑及消炎劑不同的作用模式,例如類鴉片麻醉鎮痛劑(例如羥考酮及其鹽)、加巴噴丁及GABA受體介導之藥劑(例如普瑞巴林及其鹽或丙泊酚)、三環藥劑(例如阿米替林及其鹽)、環氧合酶抑制劑(例如酮咯酸及其鹽或塞來昔布)及離子通道阻斷劑(例如布比卡因),CB2RA組合物可用作個體之多模態治療方案之一部分。
亦已證明(參見實例8),NSAID環氧合酶(COX)酶抑制劑之『上限劑量』鎮痛作用可藉由與本文所述之CB2RA組合物共同投與來避免。不希望受理論所束縛,似乎CB
2受體促效作用及COX酶抑制作用的不同但潛在互補的作用機制可組合,以產生鎮痛活性之新穎且臨床上有意義的協同增強。舉例而言,當本文所述之CB2RA組合物以受控且有效的E1及E2比率與COX酶抑制劑塞來昔布組合時,會產生協同作用,從而使達成有意義的鎮痛及/或抗炎作用所需的各藥劑之量大大減少,其程度大於各藥劑之作用在本質上純粹為相加之情況下發生的程度。舉例而言,此作用特別有用,因為本發明組合物可(i)單獨作為一種新的鎮痛劑使用,其具有新穎作用機制,有利於類鴉片減量或消除或COX酶抑制劑減量或消除,(ii)作為多模態治療方案之一部分使用,以增強COX酶抑制劑之作用,從而使每次投與之鎮痛劑總量獲得更大的鎮痛作用,及(iii)作為固定劑量組合藥物單獨使用,或與其他消炎及/或鎮痛藥物組合使用,以達成所需治療效果,同時使有害的不良副作用的發生減至最少。
已首次證明CB
2R受體促效劑若與抑制環氧合酶之藥物共同投與,可與彼等藥物協同作用,以產生優於各藥物單獨使用之效力的藥物組合,達到與類鴉片鎮痛劑所達成之鎮痛水準相當的水準。
在某些實施例中,本發明提供一種醫藥組合物,其包含本文所述之CB2RA組合物及醫藥學上有效量之非類固醇消炎藥(NSAID)。CB2RA組合物及NSAID可調配成單一劑型。
在某些實施例中,本發明提供一種醫藥組合物,其包含本文所述之CB2RA組合物及醫藥學上有效量之非類固醇消炎藥(NSAID)及/或類固醇。CB2RA組合物及NSAID及/或類固醇可調配成單一劑型。
在一個態樣中,本發明提供一種醫藥組合物,其包含本文所述之CB2RA組合物及醫藥學上有效量之非類固醇消炎藥(NSAID)及/或類固醇及/或神經阻斷劑。CB2RA組合物及NSAID及/或類固醇及/或神經阻斷劑可調配成單一劑型。
在某些實施例中,本發明提供一種醫藥組合物,其包含本文所述之CB2RA組合物及醫藥學上有效量之非類固醇消炎藥(NSAID)及/或類固醇及/或神經阻斷劑及/或免疫調節劑。CB2RA組合物及NSAID及/或類固醇及/或神經阻斷劑及/或免疫調節劑可調配成單一劑型。
NSAID可為例如溴芬酸阿司匹林、萘普生、溴芬酸、雙氯芬酸、美洛昔康、布洛芬、酮洛芬、托美丁、吲哚美辛、舒林酸、吡羅昔康、甲芬那酸、依託度酸、奈帕芬胺、氟比洛芬、乙醯胺酚、溴芬酸、酮咯酸、塞來昔布、依他昔布、羅美昔布、羅非昔布、伐地考昔、帕瑞考昔、阿西美辛、右布洛芬、尼美舒利、萘丁美酮、噻洛芬酸、氯諾昔康、替諾昔康、醋氯芬酸、丙谷美辛、右酮洛芬或奧沙普
。在一個實施例中,NSAID為塞來昔布。
類固醇可為皮質類固醇且可為例如皮質類固醇,包括糖皮質類固醇。皮質類固醇或糖皮質類固醇可為丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸氫化可的松、曲安奈德氟西奈德、地塞米松氯替潑諾依碳酸氯替潑諾、二丙酸阿氯米松、地奈德或氫化可的松。皮質類固醇可為例如地塞米松或氯替潑諾。
神經阻斷劑可為普魯卡因、苯佐卡因、氯普魯卡因、可卡因、環甲卡因、二甲卡因、哌羅卡因、丙氧卡因、普魯卡因、丙美卡因、四卡因阿美索卡因、利多卡因、阿替卡因、布比卡因、辛可卡因、依替卡因、左布比卡因、利多卡因、甲哌卡因、丙胺卡因、羅比卡因、三甲卡因左布比卡因、丙胺卡因、四卡因、龍托卡因、塞普卡因、羅比卡因、布比卡因或甲哌卡因,其可視情況包括或與佐劑一起投與,諸如碳酸氫鈉、咪達唑侖、鎂、氯胺酮、右美托咪啶、維拉帕米及可樂定。
免疫調節劑可為環孢菌素、利非格司特、硫唑嘌呤、黴酚酸酯、甲胺喋呤、來氟米特他克莫司、西羅莫司、環磷醯胺、苯丁酸氮芥或腫瘤壞死因子抑制劑。
在一個態樣中,提供一種用於促效個體之CB2受體活性之醫藥組合物,該組合物包含以下之組合:
(a)式I之第一化合物:
(b)式II之第二化合物:
在一個態樣中,提供一種用於促效個體之CB2受體活性之醫藥組合物,該組合物包含以下之組合:
(a)式I之第一化合物:
(b)式II之第二化合物:
其中該組合物包含重量比為99.85:0.15至93.5:6.5之式I化合物及式II化合物,以及醫藥學上可接受之賦形劑。
在一個實施例中,式I化合物與式II化合物之重量比為99.8:0.2至98.2:1.8。
在一個實施例中,式I化合物與式II化合物之重量比為98.8:1.2至98.4:1.6。
在一個實施例中,式I化合物與式II化合物之重量比為99.3:0.7至98.7:1.3。
在一個實施例中,式I化合物與式II化合物之重量比為約99:1。
在一個實施例中,醫藥學上可接受之賦形劑包含聚合物、增溶劑、緩衝劑、鹽、防腐劑或其組合。
在一個實施例中,聚合物為聚乙烯吡咯啶酮-聚乳酸(PVP-PLA)共聚物。
在一個實施例中,PVP-PLA共聚物具有式III之結構:
在一個實施例中,緩衝劑為磷酸鹽緩衝劑。
在一個實施例中,鹽為鈉鹽或鉀鹽。
在一個實施例中,組合物呈微胞製劑形式。
在一個實施例中,微胞製劑呈液體形式。
在一個實施例中,微胞製劑脫水成固體形式(例如凍乾或噴霧乾燥的固體)。
在一個實施例中,組合物包含約0.25%(w/w)至約60%(w/w)、約0.5%(w/w)至約40%(w/w)、或約0.75%(w/w)至約30%或約1%(w/w)至約20%(w/w)之第一及第二化合物之組合。
在一個實施例中,組合物包含約5重量%至約99.5重量%、或約5重量%至95重量%、或30重量%至約90重量%、或約60重量%至約85重量%或約70重量%至約80重量%之聚合物。
在一個實施例中,組合物包含約1重量%至約20重量%之緩衝劑。
在一個實施例中,組合物進一步包含乳化劑、抗氧化劑、控制釋放劑、潤滑劑或調味劑。
在一個實施例中,固體形式已在溶劑中再水合以產生微胞溶液。
在一個實施例中,溶劑為水(例如WFI)、醇、右旋糖溶液(例如5%右旋糖溶液)或生理鹽水。
在一個實施例中,第一及第二化合物之組合濃度為約0.1 mg/mL至約50 mg/mL。
在一個實施例中,第一及第二化合物之組合濃度為約0.5 mg/mL至約15 mg/mL。
在一個實施例中,組合物之pH值為約5至約9、約6至約8或約6.5至約7.5及/或黏度在約0.2 mPas至約80,000 mPas範圍內。
在一個實施例中,微胞溶液包含粒度(Z.av)為5 nm-100 nm、10-50 nm、12050nm、15-45 nm或20-40 nm之粒子。
在一個實施例中,粒子之多分散性指數(PDi)為約0.05至約0.15。
在一個實施例中,粒子之多分散性指數(PDi)為約0.05至約0.2。
在一個實施例中,組合物進一步包含0.015%至1.5%之第三或第四化合物。
在一個實施例中,組合物進一步包含0.01%至30%之第三或第四化合物。
在一個態樣中,提供一種醫藥組合物,其包含如本文所定義之醫藥組合物及醫藥學上有效量之非類固醇消炎藥(NSAID)及/或類固醇。
在一個實施例中,NSAID為溴芬酸、奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、酮咯酸或塞來昔布。在一個實施例中,NSAID為塞來昔布。
在一個實施例中,類固醇為皮質類固醇。
在一個實施例中,皮質類固醇為地塞米松氯替潑諾、依碳氯替潑諾、丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸酯、曲安奈德氟西奈德、地塞米松氯替潑諾依碳酸氯替潑諾、二丙酸阿氯米松、地奈德或氫化可的松。
在一個實施例中,第一及第二化合物及NSAID及/或類固醇調配成單一劑型。
VI. 使用方法及用途
本文所述之CB2RA組合物能夠促效個體之CB2大麻素受體活性且可藉由提供鎮痛及/或消炎特性提供有益治療效果。因此,本文所述之組合物(包括醫藥組合物)可用於治療有需要之個體之疼痛及/或炎症。
在某些實施例中,疼痛及/或炎症可為慢性或急性疼痛及/或炎症。在某些實施例中,疼痛及/或炎症與自體免疫性病症相關,包括糖尿病、多發性硬化症、牛皮癬、全身性紅斑狼瘡、發炎性腸病、艾迪森氏病(Addison's disease)、葛瑞夫茲氏病(Graves' disease)、橋本氏甲狀腺炎(Hashimoto's thyroiditis)、重症肌無力、自體免疫血管炎、惡性貧血、乳糜瀉及其類似病症,或與輻射(如治療某些癌症時發生)、或感染、或暴露於刺激物相關、或來自心臟病、或哮喘、或阿茲海默氏病(Alzheimer's disease)或其他神經病症。所揭示之本發明可用於治療此等病症。
所揭示之組合物亦可用於治療關節及結締組織之發炎性疾病,諸如結締組織之血管疾病、扭傷及骨折,及具有發炎性症狀之肌肉骨胳疾病,諸如急性風濕熱、風濕性多肌痛、反應性關節炎、類風濕性關節炎、椎關節炎以及骨關節炎,及其他起源之結締組織炎症及所有起源之膠原病,諸如全身性紅斑狼瘡、硬皮病、多發性肌炎、皮肌炎、休格連症候群(Sjogren syndrome)、斯蒂爾病(Still's disease)或費爾蒂症候群(Felty syndrome);以及血管疾病,諸如結節性動脈炎、結節性多關節炎、結節性動脈周圍炎、顳動脈炎、韋格納氏肉芽腫病(Wegner's granulomatosis)、巨細胞動脈炎、動脈硬化及結節性紅斑。
在某些實施例中,疼痛由創傷(無論例如來自個人損傷抑或來自手術程序)、癌症或其他潛在急性或慢性醫學病況、灼傷、燙傷、或暴露於化學物質或頭痛或偏頭痛引起。
本文所述之組合物可適用於治療急性疼痛,諸如牙痛、術前及術後疼痛、創傷性疼痛、肌肉疼痛、燒傷、曬傷、三叉神經痛引起之疼痛、絞痛引起之疼痛以及胃腸道或子宮痙攣;扭傷、內臟疼痛,例如慢性骨盆疼痛、婦科疼痛、月經前及月經期間的疼痛、胰腺炎、胃潰瘍、間質性膀胱炎、腎絞痛、膽囊炎、前列腺炎、心絞痛引起之疼痛、腸激躁、非潰瘍性消化不良及胃炎、前列腺炎、非心源性胸痛引起之疼痛以及心肌缺血及心肌梗塞引起之疼痛。
本文所述之方法可進一步包含向該個體投與治療有效量之NSAID及/或類固醇。在某些實施例中,NSAID可為溴芬酸阿司匹林、萘普生、溴芬酸、雙氯芬酸、美洛昔康、布洛芬、酮洛芬、托美丁、吲哚美辛、舒林酸、吡羅昔康、甲芬那酸、依託度酸、奈帕芬胺、氟比洛芬、乙醯胺酚、溴芬酸、酮咯酸、塞來昔布、依他昔布、羅美昔布、羅非昔布、伐地考昔、帕瑞考昔、阿西美辛、右布洛芬、尼美舒利、萘丁美酮、噻洛芬酸、氯諾昔康、替諾昔康、醋氯芬酸、丙谷美辛、右酮洛芬或奧沙普
。在一個實施例中,NSAID為塞來昔布。在其他實施例中,類固醇可為皮質類固醇,例如皮質類固醇,包括糖皮質類固醇。皮質類固醇或糖皮質類固醇可為丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸氫化可的松、曲安奈德氟西奈德、地塞米松氯替潑諾依碳酸氯替潑諾、二丙酸阿氯米松或地奈德。NSAID及/或類固醇可在投與第一及第二化合物之前、同時或之後向個體投與。在某些實施例中,當與NSAID及/或類固醇組合投與時,本文所述之組合物的投與協同減少個體之炎症及/或疼痛。
在某些實施例中,炎症或疼痛可為眼部炎症或眼部疼痛,例如術後炎症或術後疼痛或與眼睛創傷相關之疼痛,諸如角膜擦傷、或青光眼、或麥粒腫(或其他感染)、或圓錐角膜、或眼眶蜂窩織炎、或角膜交聯、或眼睛燒傷或化學損傷、或潰瘍、或乾眼症候群、或淚液形成不良或結膜炎,或視神經炎或鞏膜炎或葡萄膜炎或角膜炎或影響視網膜的眼底疾病。
角膜炎症可導致角膜神經性疼痛(痛覺過敏)。角膜神經性疼痛可由最初的創傷及炎症反應引起,或由持續的慢性炎症/刺激(例如乾眼症)引起。眼部神經性疼痛病症通常與角膜損傷及炎症有關,其中炎症為神經性疼痛症候群之重要促成因素。
角膜神經性疼痛通常表現為異常疼痛(對正常刺激之異常反應)及痛覺過敏(對輕度有害刺激之過度反應)。角膜疼痛狀況非常常見,因為角膜高度受感覺神經支配。因此,在一實施例中,本文所述之組合物可用於治療由非感染性病況引起之眼部炎症及神經性疼痛。在某些實施例中,眼部神經性疼痛為角膜神經性疼痛。在某些實施例中,眼部神經性疼痛由乾眼症、創傷(例如屈光手術或損傷)、角膜擦傷、角膜燒傷、角膜移植、自體免疫性疾病或過敏原引起。熟習此項技術者應瞭解,此類病況通常同時存在神經性疼痛及炎症,且用本申請案之方法治療可減少眼部炎症且因此減少眼部神經性疼痛。
角膜疼痛亦發生在眼睛手術後,其中角膜上皮完全或部分移除,如屈光性角膜切除術所發生。在某些實施例中,眼部疼痛係由角膜上皮移除隨後角膜基質交聯以矯正圓錐角膜包括進行性圓錐角膜引起。
在某些實施例中,眼病引起眼內炎症。視情況,眼病為葡萄膜炎、葡萄膜視網膜炎或增生性玻璃體視網膜病變。在某些實施例中,眼病引起眼外炎症。視情況,眼病為角膜炎症或神經病理學、上鞏膜炎或鞏膜炎。在某些實施例中,眼病引起疼痛及視力喪失,且藥劑減輕疼痛及/或減少視力喪失。
人眼包含許多半隔離的微環境,其若受傷或患病,則可能需要多種治療。眼睛之病變一般可分為發生在以下之病變:(i)前段,包括例如角膜、虹膜、睫狀體、小樑網及晶狀體以及與之接觸的房水,及(ii)後段,包括例如玻璃體液、視網膜及其種組分、脈絡膜及視神經。
影響前段之病變包括與衰老相關之屈光變化或可能需要手術干預之先天性缺陷(例如近視、遠視、老花眼及白內障、圓錐形角膜及內皮營養不良),以及例如經由感染或其他發炎原因引起之病變,諸如乾眼症、葡萄膜炎、瞼緣炎、角膜潰瘍及結膜炎。創傷,例如經由化學灼傷或異物發生,通常為前段病況。在許多情況下,未能接受充分及適當的醫療干預可能會導致視力受損或視力喪失。
影響眼睛後部後段之病變,包括影響視網膜及視神經之病變,若沒有得到充分及適當的治療,亦可導致視力受損或視力喪失。此等病變包括濕性及乾性年齡相關性黃斑變性(AMD)、糖尿病性黃斑水腫(DME)、視網膜炎、視網膜脫離及眼部缺血症候群。青光眼為一種威脅視力之病況,其中眼內壓力(眼內壓或IOP)的增加可導致眼睛後部之視神經受損,亦可視為後段疾病,儘管其原因可能為經由前段小樑網之液體排出不暢。
炎症及疼痛是前段及後段疾病之常見表現,無論是病況之原因還是結果。舉例而言,角膜手術可能涉及角膜上皮之損傷或移除,諸如為矯正屈光不正而進行的手術,包括PRK(屈光性角膜切除術)及圓錐形角膜交聯手術,其可能為極其疼痛的,因為角膜為人體中神經最密集之表面上皮之一,其敏感性為正常皮膚的600倍(Yang, A. Y.等人 (2018) 《耶魯生物學與醫學雜誌》(Yale J. Biol. Med.) 91(1): 13-21)。手術後發生之炎症亦可進展且加劇疼痛,在一些患者中,導致更多慢性發炎病況,諸如乾眼病(Shtein R.M.(2011) 《眼科專家綜述》(Expert Rev. Ophthalmol.) 6(5): 575-582),其為一種多因素的眼表病況,常常導致嚴重的不適及視覺障礙,有可能對角膜表面造成永久性損傷(Javadi MA, Feizi S.(2011) 《眼科及視覺研究雜誌》(J. Ophthalmic Vis. Res.) 6(3): 192-198)。
相反,青光眼及其引起的視神經損傷被認為是在某些情況下由於小樑網之炎症及阻塞而引起的(Ozan-Yuksel Tektas等人 (2009) 《實驗性眼研究》(Exper.Eye Res.) 88(4): 769-775)。炎症同樣被視為產生兩種形式AMD之主要因素,在最普遍之病況乾性AMD中尤為重要(Kauppinen, A.等人 (2016) 《細胞及分子生命科學》(Cell.Mol. Life Sci.) 73(9): 1765-868)。目前針對眼部疼痛及炎症之治療劑(相對於預防炎症原因之治療劑,諸如抗微生物產品)通常分為三類,包括(i)口服類鴉片藥物、非類固醇消炎藥(NSAID)及(iii)皮質類固醇。類鴉片口服藥物為鎮痛劑,雖然通常用於最嚴重的眼科疼痛,例如交聯手術或PRK後出現的疼痛,但由於擔心誤用及濫用,以及經口投與後無法有效控制眼睛局部的疼痛,因此處方的頻率愈來愈低。局部NSAID,諸如酮咯酸、溴芬酸及奈帕芬胺為常用的局部鎮痛劑,用於治療眼科疼痛及炎症,但其效力不如類鴉片可達成的。NSAID亦與許多類別相關之副作用相關,該等副作用可能會妨礙其在例如眼科手術中之短期使用,以及其在例如青光眼或乾眼症患者中之長期使用。此外,NSAIDS通常與以下情況相關:(i)延遲傷口癒合,其可能導致長時間的疼痛及炎症,以及更大的感染機率及角膜炎,以及(ii)增加出血時間,在短至14天的重複使用中,可能導致IOP升高,從而對患有青光眼之患者造成不利的結果(Kashiwagi K等人 (2003) 《英國眼科雜誌》(Br. J. Ophthalmol.) 87297-301)。皮質類固醇,諸如氯替潑諾、地塞米松及潑尼松龍廣泛用於控制眼睛之炎症,但不用於控制眼科手術後可能出現的嚴重急性疼痛,因為其在基因層面下之作用模式不允許快速起效。眼用皮質類固醇之眼部使用亦與白內障之形成及臨床上IOP之顯著升高以及隨後發生青光眼的可能性相關,該可能性同樣隨著治療時間之延長而增加。
本文提供之組合物解決未滿足的醫療需求,其包括對新的鎮痛及消炎藥物之需求,該等藥物提供早起的鎮痛,其程度大於NSAID或皮質類固醇可達到的程度,不容易被誤用及濫用,且不與出血時間增加、傷口癒合延遲及IOP眼壓增加有關。
藥物自一般循環遞送至眼睛內腔(例如口服或非經腸遞送後)受到後段之血-視網膜屏障及區段之血-房水屏障的阻礙,其共同阻止有效藥物眼內濃度的實現(Sharma, M.等人 (2019) 《微生物學方法》(Methods in Microbiol.)46: 93-114)。局部或侵入性前房內、玻璃體內或眼周注射目前為克服此等障礙之較佳途徑,但全部與各種缺點相關,包括例如(i)玻璃體內及前房內注射液體進入眼睛可能會增加眼壓且有損害及感染眼部組織之風險,(ii)眼睛周圍的眼周注射雖然至少在目標群組織的局部,但在進入內腔之前必須穿過眼睛的外層(鞏膜及脈絡膜),且此類注射僅可由受過訓練的醫師進行,以及(iii)局部遞送,雖然其可克服上述挑戰,但由於覆蓋在眼球表面之淚液的快速周轉、眨眼以移除施用之液體及角膜上皮的親水性,對親脂性藥物遞送形成有效的障礙,所以亦存在問題。
已知哺乳動物的眼睛在角膜、小樑網及前段之施累姆氏管中以及在後段的視網膜穆勒細胞、視網膜色素上皮及水準細胞及無軸突神經細胞中差異表現CB2受體。儘管已經發現本文所述之CB2R組合物在全身靜脈內遞送後之手術損傷模型中提供有效的局部鎮痛(參見實例5),但亦發現PVP-PLA CB2RA組合物局部遞送至測試個體之受傷眼睛後可達到鎮痛作用(參見實例25)。舉例而言,
圖 20顯示,當局部遞送至用硝酸銀燒灼以模擬例如圓錐形角膜、PRK或LASIK手術中之上皮損傷之嚙齒動物眼睛時,隨後在後續辣椒素攻擊後,測試個體接受局部施用量之包含CB2RA組合物(E1與E2之比率為98.8比1.2)之醫藥調配物,CB2RA組合物濃度為0.5%,所經歷的疼痛程度低於僅施用媒劑(缺乏CB2RA組合物之醫藥調配物)的動物。此外,測試個體所經歷之疼痛減輕程度與Thapa等人 (2018) 同上所述之包含濃度為1.5%之Hu-308的醫藥組合物所產生的疼痛減輕程度相當,1.5% Hu-308組合物濃度為報告的有效最低劑量。
圖 21顯示,使用PVP-PLA調配物將CB2RA組合物遞送至眼睛表面亦導致積聚於角膜下層中之白血球(嗜中性白血球)之數目減少,表明PVP-PLA調配物在表面上皮下之角膜層中達到CB2RA之水準,其明顯為消炎的,因為其減少白血球結合及積聚之程度。亦發現,以PVP-PLA調配物形式施用於眼睛之CB2RA組合物的濃度自0.5%降低至0.25%,令人驚訝地導致測試個體之鎮痛量增加。
方法
在一個態樣中,提供一種治療有需要之個體之炎症或疼痛的方法,該方法包含向該個體投與治療有效量之如本文所定義之組合物。
在一個態樣中,提供一種治療有需要之個體之炎症及疼痛的方法,該方法包含向該個體投與治療有效量之如本文所定義之組合物。
在一個實施例中,炎症或疼痛為慢性或急性的。
在一個實施例中,疼痛為急性疼痛。
在一個實施例中,炎症或疼痛為眼部炎症或眼部疼痛。
在一個實施例中,炎症或疼痛為術後炎症或術後疼痛。
在一個實施例中,炎症或疼痛與角膜創傷(例如角膜手術或損傷)相關。
在一個實施例中,眼部炎症為乾性AMD相關之視網膜炎症。
在一個態樣中,提供一種治療或預防有需要之個體之年齡相關性黃斑變性(AMD)的方法,該方法包含向該個體投與治療有效量之如本文所定義之組合物。
在一個實施例中,AMD為濕性AMD。
在一個實施例中,AMD為乾性AMD。
在一個態樣中,提供一種治療或預防有需要個體之血管生成的方法,該方法包含向該個體投與治療有效量之如本文所定義之組合物。
在一個實施例中,血管生成為眼部血管生成。
在一個實施例中,眼部血管生成為視網膜血管生成。
在一個實施例中,眼部血管生成為脈絡膜血管生成。
在一個實施例中,視網膜或脈絡膜血管生成為濕性AMD相關血管生成。
在一個實施例中,視網膜或脈絡膜血管生成為乾性AMD相關血管生成。
在一個態樣中,提供一種促進有需要之個體之傷口癒合的方法,該方法包含向該個體投與治療有效量之如本文所定義之組合物。
在一個實施例中,傷口癒合為眼部傷口癒合。
在一個實施例中,眼部傷口癒合為角膜傷口癒合。
在一個實施例中,眼部傷口癒合為術後眼部傷口癒合。
在一個態樣中,提供一種預防或治療有需要之個體之乾眼症候群的方法,該方法包含向該個體投與治療有效量之如本文所定義之組合物。
在一個態樣中,提供一種泛眼遞送以下各物之方法:
(a)式I之第一化合物:
(b)式II之第二化合物:
在一個態樣中,提供一種向有需要之個體泛眼遞送以下各物之方法:
式I之第一化合物:
(b)式II之第二化合物:
其中該組合物包含重量比為99.85:0.15至93.5:6.5之式I化合物及式II化合物,以及醫藥學上可接受之賦形劑,
其中該方法包含向該個體投與治療有效量之如本文所定義之組合物,該組合物包含E1或其醫藥學上可接受之鹽、E2或其醫藥學上可接受之鹽及PVP-PLA共聚物。
在一個實施例中,投與步驟為腹膜內投與、局部投與、經口投與、舌下投與、經頰投與、靜脈內投與、肌肉內投與、皮下投與、鞘內投與、經耳投與、經皮投與、鼻內投與、唇下投與、經肺投與、顱內投與、腦室內投與、陰道內投與、經直腸投與、皮膚投與、腸內投與、眼周投與、玻璃體內投與或結膜下投與。
在一個實施例中,組合物以儲槽調配物、立即釋放調配物或調節釋放調配物形式投與。
在一個態樣中,提供一種提高NSAID之治療功效的方法,其包含將NSAID與如本文所定義之組合物共同投與。
在一個實施例中,NSAID為溴芬酸、奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、酮咯酸或塞來昔布。在一個實施例中,NSAID為塞來昔布。
在一個實施例中,該方法進一步包含向個體投與治療有效量之非類固醇消炎藥(NSAID)及/或類固醇。
在一個實施例中,NSAID係選自奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、溴芬酸、酮咯酸或塞來昔布。在一個實施例中,NSAID為塞來昔布。
在一個實施例中,類固醇為皮質類固醇或糖皮質類固醇。
在一個實施例中,皮質類固醇為地塞米松、潑尼松、氯替潑諾、氟輕鬆、氟米龍、二氟潑尼酯、曲安西龍或利美索龍。
在一個實施例中,糖皮質類固醇為丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸酯、曲安奈德氟西奈德、地塞米松氯替潑諾依碳酸氯替潑諾、二丙酸阿氯米松、地奈德或氫化可的松。
在一個實施例中,NSAID及/或類固醇在投與第一及第二化合物之前、同時或之後向個體投與。
在一個實施例中,當與NSAID及/或類固醇組合投與時,如本文所定義之組合物的投與協同減少個體之炎症及/或疼痛。在一個實施例中,NSAID為塞來昔布。
用途/使用組合物(同上)
在一個態樣中,提供如本文所定義之組合物用於治療有需要之個體之炎症或疼痛的用途。
在一個態樣中,提供如本文所定義之組合物用於製備供治療有需要之個體之炎症或疼痛用之藥物的用途。
在一個態樣中,提供如本文所定義之組合物,其用於治療有需要之個體之炎症或疼痛。
在一個實施例中,炎症或疼痛為慢性疼痛或急性疼痛。
在一個實施例中,疼痛為急性疼痛。
在一個實施例中,炎症或疼痛為眼部炎症或眼部疼痛。
在一個實施例中,炎症或疼痛為術後炎症或術後疼痛。
在一個實施例中,炎症或疼痛與角膜創傷(例如角膜手術或損傷)相關。
在一個實施例中,眼部炎症為乾性AMD相關之視網膜炎症。
在一個態樣中,提供如本文所定義之組合物用於治療有需要之個體之年齡相關性黃斑變性(AMD)的用途。
在一個態樣中,提供如本文所定義之組合物的用途,其用於製備供治療有需要之個體之年齡相關性黃斑變性(AMD)的藥物。
在一個態樣中,提供如本文所定義之組合物,其用於治療有需要之個體之年齡相關性黃斑變性(AMD)。
在一個實施例中,AMD為濕性AMD。
在一個實施例中,AMD為乾性AMD。
在一個態樣中,提供如本文所定義之組合物用於治療或預防有需要個體之血管生成的用途。
在一個態樣中,提供如本文所定義之組合物用於製備供治療或預防有需要個體之血管生成用之藥物的用途。
在一個態樣中,提供如本文所定義之組合物,其用於治療或預防有需要個體之血管生成。
在一個實施例中,血管生成為眼部血管生成。
在一個實施例中,眼部血管生成為視網膜血管生成。
在一個實施例中,視網膜血管生成為濕性AMD相關血管生成。
在一個態樣中,提供如本文所定義之組合物用於促進有需要之個體之傷口癒合的用途。
在一個態樣中,提供如本文所定義之組合物用於製備供促進有需要之個體之傷口癒合用之藥物的用途。
在一個態樣中,提供如本文所定義之組合物,其用於促進有需要之個體的傷口癒合。
在一個實施例中,傷口癒合為眼部傷口癒合。
在一個實施例中,眼部傷口癒合為角膜傷口癒合。
在一個實施例中,眼部傷口癒合為術後眼部傷口癒合。
在一個態樣中,提供如本文所定義之組合物用於預防或治療有需要之個體之乾眼症候群的用途。
在一個態樣中,提供如本文所定義之組合物用於製備供預防或治療有需要之個體之乾眼症候群用之藥物的用途。
在一個態樣中,提供如本文所定義之組合物用於預防或治療有需要之個體之乾眼症候群的用途。
在一個態樣中,提供如本文所定義之組合物,其用於預防或治療有需要之個體之乾眼症候群。
在一個態樣中,提供如本文所定義之組合物的用途,該組合物包含E1或其醫藥學上可接受之鹽、E2或其醫藥學上可接受之鹽及PVP-PLA共聚物,用於向有需要之個體泛眼遞送:
(a)式I之第一化合物:
(b)式II之第二化合物:
其中該組合物包含重量比為99.85:0.15至93.5:6.5之式I化合物及式II化合物,以及醫藥學上可接受之賦形劑
。
在一個態樣中,提供如本文所定義之組合物的用途,該組合物包含E1或其醫藥學上可接受之鹽、E2或其醫藥學上可接受之鹽及PVP-PLA共聚物,用於製備向有需要之個體泛眼遞送以下各物之藥物:
(a)式I之第一化合物:
(b)式II之第二化合物:
其中該組合物包含重量比為99.85:0.15至93.5:6.5之式I化合物及式II化合物,以及醫藥學上可接受之賦形劑
。
在一個態樣中,提供如本文所定義之組合物,其包含E1或其醫藥學上可接受之鹽、E2或其醫藥學上可接受之鹽及PVP-PLA共聚物,用於向有需要之個體泛眼遞送:
(a)式I之第一化合物:
(b)式II之第二化合物:
其中該組合物包含重量比為99.85:0.15至93.5:6.5之式I化合物及式II化合物,以及醫藥學上可接受之賦形劑
。
在一個實施例中,組合物經調配以用於腹膜內使用、局部使用、經口使用、舌下使用、經頰使用、靜脈內使用、肌肉內使用、皮下使用、鞘內使用、經耳使用、經皮使用、鼻內使用、唇下使用、經肺使用、顱內使用、腦室內使用、陰道內使用、經直腸使用、皮膚使用、腸內使用、眼周使用、玻璃體內使用或結膜下使用。
在一個態樣中,提供如本文所定義之組合物用於提高NSAID之治療功效的用途。
在一個實施例中,NSAID為溴芬酸、奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、酮咯酸或塞來昔布。在一個實施例中,NSAID為塞來昔布。
在一個實施例中,該用途進一步包含用途治療有效量之非類固醇消炎藥(NSAID)及/或類固醇。
在一個實施例中,NSAID係選自奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、溴芬酸、酮咯酸或塞來昔布。在一個實施例中,NSAID為塞來昔布。
在一個實施例中,類固醇為皮質類固醇或糖皮質類固醇。
在一個實施例中,皮質類固醇為地塞米松、潑尼松、氯替潑諾、氟輕鬆、氟米龍、二氟潑尼酯、曲安西龍或利美索龍。
在一個實施例中,糖皮質類固醇為丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸酯、曲安奈德氟西奈德、地塞米松氯替潑諾依碳酸氯替潑諾、二丙酸阿氯米松、地奈德或氫化可的松。
在一個實施例中,NSAID及/或類固醇在投與第一及第二化合物之前、同時或之後使用。
在一個實施例中,當該用途與NSAID及/或類固醇組合時,該用途用於協同減少個體之炎症及/或疼痛。在一個實施例中,NSAID為塞來昔布。
VII. 用於醫療應用之套組及市售套件
另一個態樣,本發明提供一種用於緩解個體之疼痛及/或炎症的套組。在某些實施例中,本發明提供一種套組,其包含用於促效個體之CB
2大麻素受體活性之CB2RA組合物及用於緩解個體之疼痛及/或炎症之說明書。在某些實施例中,套組進一步包含含有CB2RA組合物之多個劑量單位中之一或多者。
在一個實施例中,套組包含如本文所述之組合物或如本文所述之醫藥組合物及如本文所述之使用說明書。在一些實施例中,存在於套組中之組合物或醫藥組合物基本上不含氧。舉例而言,組合物可儲存在惰性氣體下。組合物或醫藥組合物可不含氧。
在一個態樣中,提供一種市售套件,其包含如本文所述之組合物或如本文所述之醫藥組合物以及適合之包裝,其中該組合物基本上不含氧。舉例而言,組合物或醫藥組合物可儲存在惰性氣體下。組合物或醫藥組合物可不含氧。
以上描述描述本發明之多個態樣及實施例,包括組合物、醫療套組以及製備及使用此類組合物治療緩解個體之疼痛及/或炎症的方法。
實例
現在對本發明進行一般性描述,藉由參考以下實例將更容易理解,包括該等實例僅用於說明本發明之某些態樣及實施例的目的,且不意欲限制本發明。
實例 1.HU-308 批次中 E1 及 E2 之定量
此實例描述某些市售批次之HU-308關於在此等批次中量測之式I化合物(E1)及式II化合物(E2)之光學純度及量的表徵。
六個批次之HU-308中對映異構體E1及E2之量係藉由使用UPC2系統(Waters)與Trefoil AMY1管柱(2.5 µm,3.0×150 mm)之快速超效合相層析來測定。使用超臨界CO
2及含20 mM乙酸銨之甲醇的二元系統,在2,100 psi之背壓、1.2 mL/min之流動速率下實現梯度溶離,且應用230至300 nm之DAD偵測(Waters)。在此等實驗條件下,E1及E2對映異構體之滯留時間分別為3.53及3.69 min。
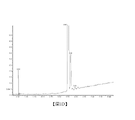
圖 1A 至 1F顯示針對不同測試批次所獲得的例示性UPC2層析圖。各種批次相對於E1及E2量之手性組成顯示於表3中。
表 3. 如藉由 UPC2/DAD 層析所量測之 Hu-308 批次中之對映異構體( E1 及 E2 )量 .
實例 2. 藉由逆相 HPLC 對 HU-308 批次之純度分析
| 批次號 | 對映異構體濃度(重量百分比) | E1之對映異構體過量(EE%) | |
| E1之量 | E2之量 | ||
| 001 | 99.4% | 0.6% | 98.8% |
| 003 | 98.8% | 1.2% | 97.6% |
| 004 | 98.4% | 1.6% | 96.8% |
| 005 | 93.6% | 6.4% | 87.2% |
| 007 | 99.3% | 0.7% | 98.6% |
| 009 | 82.4% | 17.6% | 64.8% |
此實例顯示如藉由逆相HPLC(RPC)所測定之實例1中所述之六個批次HU-308的純度。
使用配備有四元泵、管柱加熱室及二極體陣列偵測器之Agilent 1100 HPLC系統對HU-308之各批料進行分析。使用Zorbax-Eclipse XDB-C8 5 µm, 15×4.6 mm管柱(Agilent Technologies)進行分析,移動相含有水及乙腈之梯度混合物。梯度程式(時間/%乙腈)設定為0/50、20/100、30/100、40/50,且流動速率為1.0 mL/min。管柱溫度維持在30℃下且在210 nm(帶寬為4 nm)下監測層析。注射體積為10 µL。在乙腈中製備0.08 mg/mL之樣品。
在此等條件下,兩種對映異構體E1及E2之溶離時間為19.9 min。如藉由RPC所測定,在所得RPC層析圖中觀察到的其他峰及各種批次之對映異構體E1及E2的相關純度列於表4中。在某些批次中鑑別具有在18.6、19.2、20.9、21.4及21.8分鐘溶離之峰的化合物。
圖 2顯示針對HU-308之兩個例示性批次記錄的RPC跡線。
表 4. 組分之滯留時間及相關純度
* 含有對映異構體E1及E2之峰的滯留時間為19.9分鐘(以粗體顯示)。
實例 3.PVP-PLA 調配物之製備
| 批次號 | 滯留時間(min.)* | 含有E1及E2之組合物的純度% | |||||
| 18.6 | 19.2 | 19.9 | 20.9 | 21.4 | 21.8 | ||
| 001 | + | + | + | + | 98.9% | ||
| 003 | + | + | + | + | + | 98.7% | |
| 004 | + | + | + | 99.2% | |||
| 005 | + | + | + | + | 98.8% | ||
| 007 | + | + | + | + | 91.7% | ||
| 009 | + | + | + | 98.7% |
此實例描述包含E1及E2對映異構體之組合物於PVP-PLA微胞中之調配物,稱為CB2RA調配物1。
如下製備調配物。將PVP-PLA嵌段共聚物(Altus Formulation Inc.;嵌段比32:35,分子量6,300)(2.45 g)在磁力攪拌下溶解於乙醇(12.25 mL)中10分鐘。將實例1中所述之含有對映異構體E1及E2之各批次材料(50 mg)在磁力攪拌下分別溶解於玻璃小瓶中之乙醇(10 mL)中,且在室溫下直接與聚合物溶液混合。隨後再向混合物中添加一定量的乙醇(10.25 mL),隨後逐滴添加水(17.5 mL)。所得澄清溶液在室溫下保持攪拌30分鐘。
隨後移除乙醇,且使用設定在HPLC溶離份模式下之Rocket Synergy蒸發器(ThermoFisher Scientific)將PVP-PLA:E1及E2組合物濃縮至其初始重量之10%,持續150分鐘。隨後將10×PBS緩衝液(5 mL)添加至濃縮溶液中,隨後添加2.2 mL水,使得含有E1及E2之組合物的最終濃度為4 g/L。隨後使用0.2 µm過濾器過濾本體溶液且轉移至10 mL玻璃小瓶中。隨後使用VirTis Genesis 25EL凍乾器對小瓶進行凍乾。調配方法之示意圖顯示於
圖 3中,且所得凍乾餅之組成顯示於表5中。
表 5.CB2RA 調配物 1 (凍乾)之定量組成
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.7% |
| PVP-PLA共聚物 | 196.0 | 81.8% |
| 氯化鈉 | 32.0 | 13.3% |
| 磷酸氫鈉 | 5.8 | 2.4% |
| 磷酸二氫鉀 | 1.0 | 0.5% |
| 氯化鉀 | 0.8 | 0.3% |
| 總計 | 239.6 | 100% |
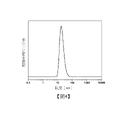
使用各種批次之材料的各種形式之CB2RA調配物1之凍乾餅具有無開裂或塌陷之精細海綿樣結構。所有小瓶材料可在注射用水(1 mL)、右旋糖溶液(1 mL)或生理鹽水(1 mL)中快速復原(在不到2分鐘內),產生澄清、無粒子溶液。復原溶液之平均pH值為6.6(+/-0.2),如使用配備有凝膠填充環氧體組合電極之pH211 pH計(Hanna Instruments)所量測。
在加工過程中形成之微胞的尺寸(Z平均值)在25℃下藉由動態光散射測定,使用Malvern Nano ZS90 Zetasizer,其90度散射光學器件配備有4mW He-Ne雷射器,在633 nm下操作,而形成之微胞群體的粒度分佈(PDI)係由最大峰高h及其標準偏差σ使用方程式PDI=(σ/h)
2計算。
圖 4提供例示性CB2RA調配物1之微胞的典型粒度分佈圖,其顯示分佈為單峰的。無論使用含有E1及E2之何種批次,此特徵均得以保留。表6彙總所產生之所有調配物的表徵資料,且表明微胞調配物之物理化學特性不取決於測試批次之E1及E2組成。所製備之CB2RA調配物1之各種批料的特徵亦似乎不受所使用之PVP-PLA嵌段共聚物批料的影響。
表 6. 所製備之 CB2RA 調配物 1 之各種批料的表徵資料
*ZAv:微胞粒度;**PDi:多分散性指數
實例 4. 術後手術疼痛之臨床前模型
| CB2RA調配物1/批料號 | 活性劑批次號 | PVP-PLA批次號 | E1之量 | E2之量 | 對映異構體過量(EE) | 粒度 | pH | |
| ZAv*(nm) | PDi** | |||||||
| A | 001 | 001 | 99.4% | 0.6% | 98.8% | 33 | 0.125 | 6.8 |
| B | 003 | 002 | 98.8% | 1.2% | 97.6% | 23 | 0.075 | 6.4 |
| C | 004 | 003 | 98.4% | 1.6% | 96.8% | 24 | 0.076 | 6.3 |
| D | 005 | 002 | 93.6% | 6.4% | 87.2% | 24 | 0.086 | 6.6 |
| E | 010 | 002 | 97.0% | 3.0% | 94.0% | 23 | 0.088 | 6.7 |
| F | 009 | 002 | 82.4% | 17.6% | 64.8% | 33 | 0.181 | 6.6 |
| 平均值 | 27 | 0.105 | 6.5 |
此實例描述術後手術疼痛之臨床前模型的產生及驗證。
確定候選藥物緩解手術疼痛之能力的臨床前研究一般依賴於發炎性或神經痛模型,而非在手術切口後立即經歷的極度疼痛。當採用切口疼痛模型時,其通常僅在手術切口後24小時評估疼痛反應(Labud等人 (2005) 《歐洲藥理學雜誌》(European J. Of Pharmacol.), 527: 172-174),此時急性疼痛已消退且急性反應之發炎組分已充分確定。通常,藥物投與亦僅藉由腹膜內途徑,其並非模擬臨床情況。
開發代表手術後立即經歷之極度疼痛的臨床前模型,且用於確定實例3中所述之CB2RA調配物1的批料是否(i)能夠緩解此類極度的術後疼痛;及(ii)若如此,則其功效與市售NSAID COX抑制劑藥物相比如何。所開發之模型係基於由Labuda等人(同上)描述之模型。然而,為了確定對急性極度疼痛之功效,疼痛評估立即開始,而非手術後24小時。所有測試物品均經由尾部靜脈以單次推注形式靜脈內投與。
購買雄性史泊格多利大白鼠(Charles River, St-Constant, Qc, Canada)且圈養於12小時光/暗循環之氣候控制室內的自動通風籠中。允許動物自由獲取食物丸粒及水,且在測試時稱重為200-225 g。
術後切口疼痛係經由後爪之1 cm足底切口誘發的。簡言之,在用異氟醚深度麻醉下,清潔後爪之足底面且使用10%聚維酮-碘溶液消毒,之後用11號刀片製造1 cm縱向切口。切口穿透足底面之皮膚及筋膜。蹠肌亦被抬高並縱向切開,肌肉起點保持完整。輕輕按壓止血後,用2條5-0耐綸之褥式縫合線縫合皮膚,且用抗細菌軟膏覆蓋傷口部位。隨後將大鼠置放於具有塑膠柵格地板(8×8 mm)之透明塑膠玻璃籠中且使其適應環境。
疼痛反應係使用von Frey機械刺激測試來評估,該測試採用von Frey細絲垂直施加於傷口附近的區域。每根von Frey細絲施加一次,自15 mN壓力(最低細絲強度)開始且繼續使用強度增加之細絲,直至施加後觀察到縮回反應(抬起受傷的爪子)。隨後將造成縮回反應之細絲的彎曲阻力(反映所施加的壓力)記錄為縮回臨限值。若在522 mN之最大細絲強度下未觀察到縮回反應,則將此值記錄為縮回臨限值。每次施用細絲後,給予動物5分鐘的無測試期,之後重複測試,將2次測試之縮回反應所需的最低力記錄為縮回臨限值(WT)。
為了在疼痛反應方面驗證模型,首先在切口前一天進行Von Frey分析以獲得基線反應,隨後在足底切口1小時後進行第二次評估。
採用市售鎮痛劑作為陽性對照,以驗證模型量測鎮痛反應的能力。所使用之鎮痛劑為NSAID酮咯酸(Toradol
®:輝瑞)及類鴉片丁丙諾啡(可用作通用藥品)。
測試物品為如實例3中所述製備之CB2RA調配物1的各種批料。陰性對照(媒劑)為生理鹽水。
在手術後一小時,使用插入尾靜脈中之25G針頭以單次15秒推注注射形式投與所有測試物品及對照,待注射之體積基於動物之個體體重進行調整。在注射後15分鐘進行第一次給藥後評定之後,接著在8小時測試期間每隔一小時進行進一步評定。
模型驗證
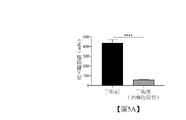
圖 5A顯示對動物在足底切口手術前後量測之縮回臨限值的比較。如圖所示,手術後縮回臨限值顯著降低,證實在受傷的後爪中誘發機械超敏反應。研究中包括六隻動物,其產生的反應範圍在約100 mN與400 mN之間,該範圍足夠寬以評定測試物品之鎮痛功效。
為了驗證此假設,手術後一小時,各別動物組(每組n=6)接受單次靜脈內注射市售且經臨床驗證之NSAID酮咯酸(Toradol
®輝瑞)。酮咯酸劑量介於5 mg/kg至30 mg/kg,且各組六隻僅接受一個劑量。作為額外的驗證,單獨的一組動物亦接受靜脈內丁丙諾啡(0.05 mg/kg)。
隨後,在測試物品注射後0.25、1、2、3、4、5、6、7及8小時,使用von Frey細絲量測各動物表現出的疼痛臨限值。隨後計算投與各劑量之酮咯酸或丁丙諾啡之縮回臨限值/時間曲線下面積(AUC
0-8 小時),結果顯示於
圖 5B。如圖所示,酮咯酸顯示明顯的劑量反應效應,隨著劑量自5 mg/kg增加至30 mg/kg,實現反應逐漸增加,且ED
50為23.1 mg/kg,如
圖 5C所示。以0.05 mg/kg之低得多的劑量投與之丁丙諾啡提供與30 mg/kg酮咯酸相似的鎮痛水平,突出類鴉片鎮痛劑之優越效力。基於此等發現,該模型用於評定靜脈內投與後測試物品之疼痛及鎮痛被認為可接受的。
實例 5.CB2RA 調配物在術後手術疼痛模型中之評估
此實例描述實例3表6中所述之CB2RA調配物1的某些批料在實例4中所述之手術疼痛模型中顯示的鎮痛功效。
在第一個實驗中,各別組的動物接受媒劑(生理鹽水)或增加劑量之CB2RA調配物1批料A(包含重量比為99.4:0.6之E1與E2)的靜脈內推注注射。用於此第一個實驗之CB2RA調配物1的劑量相對於CB2RA組合物之量在2-11 mg/kg之範圍內。
在治療投與後0.25、1、2、3、4、5、6、7、8小時再次測量縮爪臨限值,將動物反應繪製為如前給出之各劑量的縮回反應/時間曲線。如
圖 6A所示,在第一測試點(0.25小時)時,所有測試劑量均發現大於對照之縮回臨限值,所有劑量保持高於對照值持續長達5小時且11 mg/kg劑量持續長達8小時。因此,單次靜脈內劑量之鎮痛為即時的且持續長達8小時。
亦計算各投與劑量之縮回反應/時間曲線下面積(AUC
0.25-8 小時)(
圖 6),且此等值用於確定CB2RA調配物1之中位有效劑量(ED
50)值,批料A為2.9 mg/kg(參見
圖 7),該值比酮咯酸之23.1 mg/kg計算值低大致10倍(參見
圖 5C)。
EE 值對 CB2RA 調配物功效之影響
隨後使用所選批次之CB2RA調配物1重複實驗,亦即批料B(E1與E2之重量比為98.8:1.2)、批料C(E1與E2之重量比為98.4:1.6)、批料D(E1與E2之重量比為93.6:6.4)及批料F(E1與E2之重量比為82.4.6:17.6)。實驗僅以4 mg/kg及2 mg/kg之劑量進行。選擇4 mg/kg劑量,因為其為
圖 6之劑量反應曲線的中心,且因此代表最可能顯示由E1與E2比率之變化引起的鎮痛功效之任何變化的劑量。選擇2 mg/kg劑量以確定劑量之間是否維持劑量/反應關係。結果顯示於
圖 8-11中。
圖 8顯示,當組合物中E2之量自99.4:0.6增加至98.8:1.2時,觀察到明顯的鎮痛作用,其大於當活性成分之E1與E2重量比為99.4:0.6時產生的鎮痛作用(
圖 6B)。鎮痛作用亦大於相同劑量之酮咯酸或塞來昔布產生的鎮痛作用(分別參見
圖 5C及
14)。
圖 9顯示,當組合物中E2相對於E1之量進一步增加至1.6%時,在維持鎮痛作用及明確的劑量反應關係(與酮咯酸或塞來昔布相比,鎮痛劑量/劑量之程度再次提高)的同時,鎮痛作用低於E2重量百分比比率為0.6%或1.2%的組合物所達成之鎮痛作用。
圖 10及11顯示,當評定含有較大量E2之組合物(E2重量百分比分別為6.4及17.6)時,鎮痛作用進一步降低。對於此兩種組合物,2 mg/kg及4 mg/kg劑量之AUC
0.25-8 小時為相似的,且在兩種情況下均沒有可觀察到的劑量/反應關係。此可觀察到的劑量/反應關係之缺乏表明,E2之量大於6.4%的組合物不會成為有效治療劑。
所測試之各種組合物在4 mg/kg給藥水準下之AUC
0.25-8 小時的變化彙總於
圖 12A中,該圖顯示對增加E1及E2組合物中之E2量之影響的鐘形反應分佈。
圖 12B顯示使用高斯分佈擬合之
圖 12A中之資料。
所有測試之CB2RA組合物產生的鎮痛效果均高於對照水準。雖然均為鎮痛的;相對於組合物低於6.4%之E2量顯示出增強或有益的鎮痛作用,該作用與高斯分佈曲線很好地擬合,該曲線預測相對於E2在約0.19至約1.78%之E2量將顯示出相對於該範圍以外之量的此效力增強作用。另外,發現在含有E1及E2之組合物中,E2之效力增強作用在約1%之水準下最大。舉例而言,已證明,E1與E2之組成比為99:1的CB2RA組合物在測試模型中具有最大的鎮痛作用。
實例 6. 藥物動力學研究
此實例描述如藉由PVP-PLA調配物遞送之CB2RA組合物的藥物動力學。此實驗係用來自實例3之CB2RA調配物1批料A進行的。
組合物靜脈內投與後之藥物動力學係在嚙齒動物模型中以手術模型中顯示為鎮痛之劑量來確定。簡言之,在測試時稱重為200-225 g的雄性史泊格多利大白鼠(Charles River, St-Constant, Qc, Canada)圈養於12小時光/暗循環之氣候控制室內的自動通風籠中。允許動物自由獲取食物丸粒及水。
CB2RA調配物1批料A在麻醉下使用25G針頭以2、4及8 mg/kg之劑量單次緩慢推注投與至尾靜脈中。注射體積基於個體體重進行調整,以確保投與正確劑量。在調配物投與前及投與後0.083小時、0.5小時、1小時、2小時、4小時、8小時及12小時,藉由經右頸靜脈之靜脈穿刺自各動物收集血液樣品(500 µL)。五隻動物用於投與CB2RA調配物1之各劑量。藉由LC-MS/MS分析進行E1/E2組成之定量血漿量測。使用Kinetica 5.1軟體(ThermoFisher Scientific)生成藥物動力學參數。
使用Agilent HP-5ms UltraInert(30 m,0.25 mm,0.25 µm)分析型管柱,採用乙酸乙酯作為移動相,藉由GC-MS/MS來測定大鼠血漿中E1/E2隨時間推移的濃度。CB2RA組合物之母產物離子躍遷(m/z 318.0 233.0)係在以多反應監測(MRM)模式操作之三重四級質譜儀(Agilent 7000C)上進行監測。相對於CB2RA組合物,該方法限定在10至1000 ng/mL之濃度範圍內。由各種PVP-PLA:調配物產生之CB2RA組合物的時間-濃度概況彙總於表7-9及
圖 13中。藉由Kinetica軟體計算之藥物動力學參數彙總於表10中。
表 7.2 mg/kg IV 劑量後之時間濃度概況
表 8.4 mg/kg IV 劑量後之時間濃度概況
表 9.8 mg/kg IV 劑量後之時間濃度概況
表 10. 血漿中平均 PK 參數之比較
| 時間(小時) | 平均值(ng/mL) | SD | CV% |
| 0.083 | 2142.00 | 1713.73 | 80.0% |
| 0.15 | 325.60 | 236.96 | 71.5% |
| 0.5 | 200.00 | 84.16 | 42.1% |
| 1 | 169.80 | 87.27 | 51.4% |
| 2 | 152.60 | 69.08 | 45.3% |
| 4 | 143.50 | 45.63 | 31.8% |
| 8 | 62.00 | 5.66 | 9.1% |
| 12 | BLQ | 0 | 0% |
| 24 | BLQ | 0 | 0% |
| 時間(小時) | 平均值(ng/mL) | SD | CV% |
| 0.083 | 6817.50 | 4363.25 | 64.0% |
| 0.15 | 753.25 | 594.70 | 79.0% |
| 0.5 | 376.00 | 155.48 | 41.4% |
| 1 | 261.50 | 72.53 | 27.7% |
| 2 | 208.25 | 61.92 | 29.7% |
| 4 | 182.50 | 64.68 | 35.4% |
| 8 | 81.00 | 28.25 | 34.9% |
| 12 | 64.00 | 0 | 0% |
| 24 | BLQ | 0 | 0% |
| 時間(小時) | 平均值(ng/mL) | SD | CV% |
| 0.083 | 13535.60 | 6924.71 | 51.2% |
| 0.15 | 2220.60 | 1004.79 | 45.2% |
| 0.5 | 901.80 | 276.07 | 30.6% |
| 1 | 468.40 | 204.04 | 43.6% |
| 2 | 363.00 | 132.50 | 36.5% |
| 4 | 282.20 | 74.32 | 26.3% |
| 8 | 129.00 | 24.28 | 18.8% |
| 12 | 66.00 | 4.24 | 6.4% |
| 24 | BLQ | 0 | 0% |
| 參數 | 劑量 | ||
| 2 mg/kg | 4 mg/kg | 8 mg/kg | |
| t 1/2(h) | 3.55 | 3.45 | 4.87 |
| C max(ng/mL) | 2142 | 6818 | 13536 |
| C 0(ng/mL) | 3137 | 10761 | 19658 |
| AUC 0-t(ng/mL*h) | 1392 | 3452 | 7011 |
| AUC 0-inf(ng/mL*h) | 1837 | 3783 | 7781 |
| AUMC(ng/mL* /kg) | 7729 | 10567 | 26388 |
| MRT(h) | 4.25 | 3.11 | 3.91 |
| V ss(mL/kg) | 4910 | 3849 | 4784 |
| V z(mL/kg) | 5902 | 5644 | 8285 |
| CL(mL/h/kg) | 1217 | 1122 | 1070 |
如
圖 13所示,作為CB2RA調配物1遞送之組合物表現出三階段消除概況,初始分佈階段顯示濃度快速下降,隨後為平線區及消除階段。表10顯示,對於此等劑量,大鼠藥物動力學為成比例的且清除緩慢。E1/E2在大鼠體內之半衰期為大致4小時。
實例 7.PVP-PLA 塞來昔布之藥效學評估
此實例顯示PVP-PLA塞來昔布調配物(COX調配物1)之藥效學評估。
用與實例3相同的方式製備之COX調配物1進行與實例6中所進行之實驗相同的實驗。
圖 14顯示所生成之劑量反應概況,其中高於22.5 mg/mg之劑量表現出大於對照之鎮痛作用。在此模型中,藉由PVP-PLA微胞遞送之塞來昔布的ED
50計算為22.3 mg/kg(參見
圖 15),該數字與此模型中酮咯酸生成之數字(參見實例4及
圖 5C)相似。
表11提供酮咯酸塞來昔布及實例3中製備之CB2RA組合物(批次1,批料A)使用PVP-PLA作為遞送劑之ED
50值的彙總。本文所述之含有E1/E2之CB2RA組合物比測試之市售產品的效力高大致10倍。
表 11. 酮咯酸調配物、塞來昔布調配物及 CB2RA 調配物之中位有效劑量( ED
50 )
實例 8.CB2RA 組合物及 COX 酶抑制劑之組合
| 治療劑 | ED 50(mg/kg) |
| 酮咯酸(Toradol) | 23.1 |
| 塞來昔布(PVP-PLA) | 22.3 |
| CB2RA調配物1(PVP-PLA) | 2.9 |
此實例顯示當本文所述之CB2RA組合物與COX酶抑制劑組合時所達成之協同作用,該抑制劑在此實例中為塞來昔布。
進行實驗以評估CB2受體促效劑(由本文所述之CB2RA組合物表示)與COX酶抑制劑(由塞來昔布表示)之間在大鼠手術模型中消炎及鎮痛功效方面的協同潛力。
如實例4中所詳細描述進行實驗,其中待混合之CB2RA調配物1批料A及COX調配物1之劑量係基於其相對ED
25值計算(分別參見
圖 7及
15)。簡言之,藉由計算對應於總反應之25%的AUC值且藉由使用Prism軟體內插所需劑量來確定各調配物所達成之ED
25。接著按體積混合復原調配物之劑量以獲得所需固定劑量組合,此調配物混合物稱為CB2RA調配物2。計算出的COX調配物1及CB2RA調配物1批料A之ED
25值分別為11.25 mg/kg及0.85 mg/kg,表示COX抑制劑與CB2RA組合物之比率為13:1。接著將各種劑量之此兩種含藥物混合物(參見表12)靜脈內投與如實例4中所述之經手術處理之大鼠。
圖 16顯示此等組合在靜脈內投與後所達成之AUC
(0.25-8 小時 )。
表 12. 劑型
| 動物組 | 塞來昔布劑量( mg/kg ) | CB2RA 組合物劑量( mg/kg ) | 塞來昔布: CB 2RA 比率 | 動物數量 |
| 1 | 4.22 | 0.32 | 13 | 6 |
| 2 | 5.62 | 0.425 | 13 | 6 |
| 3 | 11.25 | 0.85 | 13 | 6 |
| 4 | 15 | 1.125 | 13 | 6 |
發現對於CB2RA調配物2之固定劑量組合的每個劑量,觀察到比藉由兩種藥物之鎮痛作用簡單相加所預期顯著更大的縮回臨限值(亦稱為顯著更大的鎮痛作用)。如
圖 17所示,CB2R促效劑(
圖 17)及COX酶抑制劑(
圖 18)之組合所獲得的AUC對劑量曲線顯著向左偏移。CB2RA組合物單獨及與塞來昔布組合之ED
50計算值分別自2.9 mg/kg下降至0.42 mg/kg,且單獨及與CB2RA組合物組合使用之塞來昔布之ED
50計算值分別自22.3 mg/kg下降至5.6 mg/kg。
圖 19中所示之等效線圖顯示分別針對各藥物及針對組合計算之ED
50值。連接分別針對各藥物計算之兩點的直線為理論相加線。若實驗得出的等值線(代表ED
50之x,y座標的點)顯著低於理論相加等值線,則相互作用鑑別為協同的。相反,當實驗得出的ED
50點顯著高於理論相加等值線時,兩種藥物為拮抗劑。
圖 19顯示固定劑量組合之ED
50值落在相加作用線下方,表明兩種藥物之間發生協同作用。
已出人意料地發現,藉由組合一定量的CB2RA組合物及COX酶抑制劑(例如塞來昔布)產生協同反應,使得在所評估之所有濃度下,各藥物分子之表觀效力增加,從而克服NSAID及COX-2藥物經歷之上限效應且允許以較低總藥物濃度有效給藥,由此避免劑量限制不良副作用,或為彼等極度疼痛者獲得更高水準的鎮痛而無需求助於類鴉片。
實例 9. 合成方法
組合物式I化合物(對映異構體E1)係以(1R)-(+)-α-蒎烯作為起始材料開始,經由一系列八個步驟合成。簡言之,(1R)-(+)-α-蒎烯之C2位置處的甲基碳經氧化以產生桃金娘烯醛,隨後還原成(+)-桃金娘烯醇。隨後,(+)-桃金娘烯醇之醇基用特戊醯基保護。受保護之(+)-桃金娘烯醇在亞甲基碳(C4位置)處進一步氧化,且還原得到特戊酸4-羥基-桃金娘烯基酯。接下來,特戊酸4-羥基-桃金娘烯基酯與5-(1,1-二甲基庚基)-間苯二酚縮合,得到(特戊酸2-[2,6-二羥基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)。在接下來的步驟中,間苯二酚部分之C2及C6位置處的醇基經甲基化為甲氧基。在最後一步中,特戊酸酯保護基經由還原(特戊酸2-[2,6-二甲氧基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)來移除,得到所需產物(E1,式I化合物)。
方案 2.E2 之合成
為了合成式II化合物(對映異構體E2),首先使用特戊醯基保護基保護(1R)-(-)-桃金娘烯醇之C2位置處的醇基。受保護之(1R)-(-)-桃金娘烯醇隨後在其C4位置處經氧化以產生特戊酸4-側氧基-桃金娘烯基酯,其隨後還原成特戊酸4-羥基-桃金娘烯基酯。特戊酸(1R)-(-)-4-羥基-桃金娘烯基酯隨後與5-(1,1-二甲基庚基)-間苯二酚縮合,得到(特戊酸2-[2,6-二羥基-4-(2-甲基辛-2-基)苯基]-7,7-二甲基-4-雙環[3.1.1]庚-3-烯基]酯)。在最後兩個步驟中,C2及C6位置處之醇經甲基化,且特戊酸酯保護基經由還原移除,產生式II化合物(對映異構體E2)。
E1及E2可在合成結束時經由熟習此項技術者已知的方法(例如手性HPLC、SFC)進行對映異構純化。或者,E1及E2之起始材料或合成中間物可經對映異構純化且用於合成方案中。所需CB2RA組合物之E1/E2比率可藉由混合已知量的對映異構性純E1及E2且藉由手性HPLC確認比率來控制。
產生兩個批次藉由此等方案1及2產生之例示性CB2RA組合物。一個批次係藉由單獨進行反應方案來製備,而另一個批次係藉由組合反應方案,使各方案之某些步驟在單個容器中發生來製備。如實例2中所述,藉由逆相HPLC分析來分析所得組合物,且結果彙總於表13中。在表13中,含量(%)表示以相對於整個組合物之百分比組成表示之化合物的量測量,且(+)表示經鑑別之化合物相對於整個組合物之百分比組成低於指定分析方法之定量水準。
表 13
| 化合物編號 | |||||||
| 1 | 2 | 3 | 4 | CB2RA組合物 | 6 | 7 | |
| 滯留時間(RT min.) | |||||||
| 17.4 | 18.1 | 18.4 | 19.2 | 19.9 | 20.2 | 23.2 | |
| 相對滯留時間(RRT. min) | |||||||
| 0.87 | 0.91 | 0.92 | 0.96 | 1.00 | 1.02 | 1.16 | |
| 含量(%) | |||||||
| 批次1 | 0.32 | + | 0.65 | + | 98.18 | 0.13 | 0.08 |
| 批次2 | 0.54 | 0.11 | 0.29 | 0.13 | 98.01 | 0.09 | + |
CB2RA組合物(亦即含有對映異構體E1及E2)使用實例2之逆相HPLC方法的滯留時間為19.9分鐘,且(+)表示存在除CB2RA組合物以外的化合物,其百分比組成低於逆相HPLC方法之定量水準。峰值在17.4分鐘處之第一化合物以0.1%至0.6%之量存在,峰值在18.1分鐘處之第二化合物以0.01%至0.2%之量存在,峰值在18.4分鐘處之第三化合物以0.2%至0.7%之量存在,峰值在19.2分鐘處之第四化合物以0.01至0.15%之量存在,峰值在20.2分鐘處之第六化合物以0.05%至0.15%之量存在,且峰值在23.2分鐘處之第七化合物以0.01%至0.1%之量存在。
實例 10.CB2RA 組合物之凍乾餅的製備
此實例提供CB2RA組合物與PCP-PLA及海藻糖之例示性凍乾餅,其可用於例如錠劑或膠囊中或復原用於注射或局部投與。
將PVP-PLA嵌段共聚物(2.45 g)在磁力攪拌下溶解於乙醇(12.25 mL)中10分鐘。隨後將CB2RA組合物(50 mg)在磁力攪拌下溶解於玻璃小瓶中之乙醇(10 mL)中,且在室溫下直接與聚合物溶液混合。隨後再向CB2RA組合物/聚合物溶液中添加一定量的乙醇(10.25 mL),接著逐滴添加海藻糖水溶液(100 mg/mL,17.5 mL)。所得澄清溶液在室溫下保持攪拌30分鐘。藉由離心蒸發移除乙醇且向所得混合物中添加水,使得最終CB2RA組合物濃度為4 g/L。隨後使用0.2 µm過濾器過濾本體溶液且轉移至10 mL玻璃小瓶中。隨後使用VirTis Genesis 25EL凍乾器對小瓶進行凍乾。可藉由此方法產生之例示性凍乾餅的組成顯示於表14中。
表 14
實例 11. 噴霧乾燥之 CB2RA 組合物
| 成分 | % (重量) |
| CB2RA組合物 | 1.2% |
| PVP-PLA共聚物 | 57.6% |
| 海藻糖 | 41.2% |
| 總計 | 100% |
此實例提供實例10之組合物的例示性噴霧乾燥組合物,其可用於例如錠劑或膠囊、吸入性粉末中。
PVP-PLA嵌段共聚物、CB2RA組合物及海藻糖溶液可如實例10中所述製備。藉由使用Buchi B-290噴霧乾燥器進行噴霧乾燥來移除溶劑(乙醇及水)。預期所得粉末之組成與表14中所列之組成相同。
實例 12.CB2RA 組合物 : 環糊精之凍乾餅
此實例提供CB2RA組合物與環糊精之例示性凍乾餅,其可用於例如錠劑或膠囊中或復原用於注射或局部投與。
羥丙基-β-環糊精(HPβCD,975 mg)在乙醇存在下與CB2RA組合物(25 mg)充分混合。蒸發乙醇且在劇烈攪拌下將水(10 mL)緩慢添加至混合物中。所得溶液在室溫下保持攪拌30分鐘,隨後使用0.2 µm過濾器過濾。將經過濾溶液轉移至10 mL玻璃小瓶中且凍乾。表15中給出凍乾餅之預期組成。
表 15
實例 13. 局部調配物
| 成分 | % (重量) |
| CB2RA組合物 | 2.5% |
| 羥丙基-β-環糊精 | 97.5% |
| 總計 | 100% |
此實例提供用於局部施用之例示性水性調配物,例如用於局部施用於眼睛。
將聚山梨醇酯80(900 mg)與CB2RA組合物(100 mg)混合,隨後添加甘露糖醇(5 g)。向此混合物中緩慢添加94 g含有苯紮氯銨(6 mg)之水。最後,所得溶液經由0.2 µm過濾器過濾。表16中給出所得溶液之預期組成。
表 16
實例 14. 局部調配物
| 成分 | % |
| CB2RA組合物 | 0.1% |
| 聚山梨醇酯80 | 0.9% |
| 甘露糖醇 | 5% |
| 苯紮氯銨 | 0.006% |
| 水 | 94% |
| 總計 | 100% |
此實例提供用於局部施用之例示性水性調配物,例如用於局部施用於眼睛。
將聚山梨醇酯80(900 mg)與CB2RA組合物(100 mg)混合。向此混合物中緩慢添加95.5 g含有甘露糖醇(3 g)、羥丙基甲基纖維素(500 mg)及苯紮氯銨(6 mg)之水。最後,所得溶液經由0.2 µm過濾器過濾。表17中給出所得溶液之預期組成。
表 17
實例 15. 眼用凝膠之製備
| 成分 | % |
| CB2RA組合物 | 0.1% |
| 聚山梨醇酯80 | 0.9% |
| 甘露糖醇 | 3% |
| 苯紮氯銨 | 0.006% |
| 羥丙基甲基纖維素 | 0.5% |
| 水 | 95.5% |
| 總計 | 100% |
此實例提供用於局部施用之例示性凝膠調配物,例如局部施用於眼睛。
在室溫下將100 mg CB2RA組合物與2 g PEG300混合以形成混合物。將Carbopol 934(2 g)懸浮於水(95.9 g)中。在劇烈混合下,將混合物緩慢添加至含有Carbopol之水溶液中,形成膠態凝膠樣分散液。表18中給出調配物之預期組成。
表 18
實例 16. 眼用軟膏
| 成分 | % |
| CB2RA組合物 | 0.1% |
| Carbopol 934 | 2.0% |
| PEG300 | 2.0% |
| 水 | 95.9% |
| 總計 | 100% |
此實例提供用於局部施用之例示性軟膏,例如局部施用於眼睛。
將CB2RA組合物(250 mg)懸浮於2 g礦物油中,隨後與白凡士林(97.75 g)混合。製劑之預期組成顯示於表19中。
表 19
實例 17. 口服控制釋放調配物
| 成分 | % |
| CB2RA組合物 | 0.25% |
| 礦物油 | 2.00% |
| 白凡士林 | 97.75% |
| 總計 | 100% |
此實例提供例示性口服控制釋放劑型。
生產控制釋放錠劑之例示性製程由去聚結、摻合、壓縮及錠劑美學包衣組成。
例示性調配物之預期組成顯示於表20中。
如下執行製造操作。首先將黃原膠與膠態二氧化矽摻合在一起2分鐘,經由Comil進行去聚結,隨後經由Comil對所有剩餘成分進行去聚結。隨後將混合物與Kollidon SR、CB2RA組合物、黃原膠/膠態二氧化矽及Amyloflex一起裝入V型摻合機中。進行摻合10分鐘。接下來,添加硬脂酸鎂且繼續摻合1分鐘。錠劑使用9/32吋具有圓形平斜邊之工具進行壓縮,且使用固體含量為15%之Opadry包衣分散液進行包衣。
為了改良摻合物之物理特性,藉由濕式造粒製程使用高剪切摻合機產生粒化CB2RA組合物。該製程由以下組成:製備CB2RA組合物及Amyloflex之乾燥摻合物5分鐘,藉由添加35%水進行濕式成型,捏合1分鐘,且乾燥最終產物。
表 20
實例 18. 口服控制釋放調配物
| 成分 | % |
| CB2RA組合物 | 24.6% |
| Amyloflex® | 17.8% |
| Kollidon SR | 36.4% |
| 黃原膠 | 18.2% |
| 硬脂酸鎂 | 0.5% |
| 膠態二氧化矽 | 0.5% |
| Opadry II,黃色85F92421 | 2% |
| 總計 | 100% |
此實例提供另一種例示性口服控制釋放劑型。
該製程由去聚結、摻合、壓縮及錠劑美學包衣組成。如下執行製造。首先,將Amyloflex及膠態二氧化矽摻合2分鐘,隨後經由Comil去聚結。經由Comil對所有剩餘成分進行去聚結,隨後將混合物裝入V型摻合機,添加羥丙甲纖維素及CB2RA組合物,且摻合5分鐘。接下來,添加硬脂醯反丁烯二酸鈉且繼續摻合1分鐘。使用工具囊片或圓形平斜邊壓縮錠劑,且使用固體含量為15%之Opadry包衣分散液進行包衣。例示性調配物之預期組成顯示於表21中。
表 21
實例 19. 口服立即釋放調配物
| 成分 | % |
| CB2RA組合物 | 27.3% |
| Amyloflex® | 46.0% |
| 羥丙甲纖維素(HPMC K100M) | 23.0% |
| 膠態二氧化矽 | 0.5% |
| 硬脂醯反丁烯二酸鈉 | 1.5% |
| Opadry II,白色 | 1.7% |
| 總計 | 100% |
此實例提供例示性口服立即釋放調配物。
該製程由去聚結、摻合、壓縮及錠劑美學包衣組成。如下執行製造操作。首先,將一部分MCC PH102與膠態二氧化矽摻合2分鐘,隨後去聚結。經由Comil對剩餘成分進行去聚結。隨後,將混合物與CB2RA組合物、Explotab及剩餘MCC一起裝入V型摻合機中,且摻合5分鐘。接下來添加硬脂酸鎂且摻合1分鐘。使用工具囊片或圓形平斜邊壓縮錠劑,且使用固體含量為15%之Opadry包衣分散液進行包衣。調配物之預期組成顯示於表22中。
表 22
實例 20. 口服立即釋放調配物
| 成分 | % |
| CB2RA組合物 | 40.0% |
| MCC PH102 | 51.5% |
| EXPLOTAB® - 羥基乙酸澱粉鈉 | 5.0% |
| 膠態二氧化矽 | 0.5% |
| 硬脂酸鎂 | 1.0% |
| Opadry II,白色 | 2.0% |
| 總計 | 100% |
此實例提供例示性口服立即釋放調配物。
該製程由去聚結、摻合、壓縮及錠劑美學包衣組成。將一部分MCC PH102與膠態二氧化矽摻合2分鐘,隨後去聚結。經由Comil對剩餘成分進行去聚結。隨後將混合物與CB2RA組合物、Explotab、剩餘MCC及澱粉1500一起裝入V型摻合機中。進行摻合5分鐘。添加硬脂酸鎂,繼續摻合1分鐘。使用工具囊片或圓形平斜邊壓縮錠劑,且使用固體含量為15%之Opadry包衣分散液進行包衣,且預期組成列於表23中。
表 23
實例 21. 立即及延遲釋放調配物(膠囊中之丸粒)
| 成分 | % |
| CB2RA組合物 | 35.0% |
| MCC PH102 | 48.5% |
| 澱粉1500 | 10.0% |
| EXPLOTAB® - 羥基乙酸澱粉鈉 | 3.0% |
| 膠態二氧化矽 | 0.5% |
| 硬脂酸鎂 | 1.0% |
| Opadry II,白色 | 2.0% |
此實例提供例示性口服立即及延遲釋放調配物。
製造製程由以下組成:藉由流化床包衣製程及囊封生產立即釋放(IR)丸粒及延遲釋放(DR)丸粒。
如下執行製造操作。如下生產立即釋放丸粒。藉由羥丙甲纖維素於水中分散,添加API且混合直至完全溶解來製備第一活性包衣溶液。接下來在糖球上進行活性包衣溶液之藥物分層,隨後用固體含量為15%之Opadry分散液進行美學包衣。
將一部分立即釋放丸粒用延遲釋放分散聚合物包衣,且隨後用固體含量為15%之Opadry分散液包衣。調配物之預期組成顯示於表24中。
表 24. 雙重脈衝遞送調配物
實例 22. 膠囊用粉末
| 成分 | % |
| 立即釋放丸粒 | |
| CB2RA組合物 | 3.95 |
| 糖球(30/35目—— | 36.35 |
| 羥丙甲纖維素E5 | 0.21 |
| Opadry II白色 | 1.00 |
| 延遲釋放丸粒 | |
| IR丸粒 | 41.51 |
| Eudragit L30 D 55(乾基) | 11.84 |
| 滑石 | 2.96 |
| 檸檬酸三乙酯 | 1.18 |
| Opadry II白色 | 1.00 |
| 總計 | 100% |
此實例提供用於併入膠囊中之例示性粉末。
製造製程由以下步驟組成:去聚結、摻合及使用膠囊填充單元囊封。
將CB2RA組合物與MCC PH301摻合5分鐘,隨後經由Comil去聚結。隨後,經由Comil進行硬脂酸鎂之去聚結。將硬脂酸鎂添加至V型摻合機中之API摻合物中,且繼續摻合1分鐘。使用膠囊填充單元將粉末填充至膠囊中。調配物之預期組成顯示於表25中。
表 25
實例 23. 塞來昔布 /CB2RA 組合物立即釋放錠劑 .
| 成分 | % |
| CB2RA組合物 | 10.0 |
| MCC PH301 | 89.5 |
| 硬脂酸鎂 | 0.5 |
| 總計 | 100% |
此實例提供呈口服立即釋放劑型之含有CB2RA組合物及塞來昔布之組合的例示性組合產品。
所執行之製程由去聚結、摻合及壓縮組成。首先,將一部分MCC PH102與膠態二氧化矽、塞來昔布及CB2RA組合物摻合2分鐘,隨後經由Comil對混合物進行去聚結。隨後將去聚結之摻合物裝入V型摻合機中。剩餘部分之MCC經由Comil去聚結,裝入V型摻合機中且與先前去聚結之摻合物摻合5分鐘。接下來,將硬脂酸鎂添加至V型摻合機中摻合1分鐘。最後,使用工具囊片或圓形平斜邊壓縮錠劑。調配物之預期組成顯示於表26中。
表 26
實例 24.CB2RA 調配物在角膜痛覺過敏臨床前模型中之評估
| 成分 | % |
| CB2RA組合物 | 2.0 |
| 塞來昔布 | 60.0 |
| MCC PH102 | 36.5 |
| 膠態二氧化矽 | 0.5 |
| 硬脂酸鎂 | 1.0 |
| 總計 | 100% |
角膜為眼睛前部之薄組織,其密集地受感覺神經末梢神經支配。例如,由於手術、疾病或感染導致的神經末梢損傷可發展為角膜神經性疼痛,其為一種炎症反應,涉及白血球浸潤至角膜組織中。此實例提供如下論證:鎮痛及消炎作用係由醫藥CB2RA組合物調配物在角膜痛覺過敏之鼠類模型中產生,角膜痛覺過敏為可由手術及其他對角膜之創傷性損傷引起的疼痛及炎症的代表。在兩種不同的濃度下,CB2RA組合物調配物抑制該模型誘發之疼痛及炎症的能力與如Thapa (2018)同上中所述在大豆油中調配之HU-308樣品進行比較。
四組4隻雄性BALB/c小鼠(20-30 g)用於實驗。在第一步中,如Thapa等人 (2018)同上所述,在各組中誘發角膜損傷。首先使用2-3%異氟醚麻醉小鼠。隨後使用微型塗抹刷用硝酸銀燒灼雙眼角膜之中心。刷子與角膜保持接觸2秒,產生2 mm之明顯淺表損傷,僅損傷上皮細胞層,如在某些人類角膜手術中所發生的(參見例如Mohammadpour等人 (2018) 《現代眼科雜誌》(J. CURR.OPHTHALMOL.)30(2): 110-124)。隨後用生理鹽水沖洗經燒灼之眼睛,且若動物出現應激,則施加眼部潤滑劑。
使用
圖 3中所述之一般程序製備包含CB2RA組合物(E1與E2之重量比為98.8:1.2)之醫藥調配物,其最終組成列於表27中。
表 27.CB2RA 調配物之組成
| 成分 | 毫克 / 小瓶 | 按重量計之量 / 小瓶( % ) |
| CB2RA組合物 | 5.0 | 1.9% |
| PVP-PLA共聚物 | 245.0 | 93.8% |
| 磷酸二氫二鈉 | 9.6 | 3.7% |
| 磷酸二氫鈉 | 1.49 | 0.6% |
| 總計 | 261.09 | 100% |
凍乾後,CB2RA組合物調配物之樣品用水復原至相對於CB2RA組合物之最終濃度為0.25%或0.5%。亦製備包含單獨溶解於水中之PVP-PLA的媒劑對照樣品。
隨後在燒灼後30、60及120分鐘,將兩種醫藥CB2RA組合物濃度中之一者或媒劑局部投與第1-3組動物之燒灼前眼睛(5μL/眼睛)。另一組動物(第4組)在30分鐘、35分鐘、60分鐘、65分鐘及120分鐘及125分鐘接受5μL劑量之0.5% CB2RA組合物樣品,亦即第3組動物接受之CB2RA組合物劑量的兩倍。表28彙總各組接受之劑量。
表 28. 投與劑量
| 組 | 測試藥劑 | 給藥(燒灼後分鐘) | 總投與體積 |
| 1 | 媒劑 | 30、60、120 | 15 µL |
| 2 | 0.25% CB2RA | 30、60、120 | 15 µL |
| 3 | 0.5% CB2RA | 30、60、120 | 15 µL |
| 4 | 0.5% CB2RA | 30、35、60、65、120、125 | 30 µL |
角膜燒灼後六小時,向各燒灼的眼睛局部投與1×5μL之1μM辣椒素以誘發疼痛反應。在每次施用辣椒素後,立即對每隻動物的行為(動物眨眼、斜眼及擦眼的次數)進行30秒的視訊記錄,以生成每隻動物的疼痛評分。對各處理組中之個別動物進行編碼,且對實驗資料進行盲法分析。隨後針對測試物品及接受體積標繪各組動物之平均疼痛評分,如
圖 20所示。
角膜燒灼後十二小時,收穫第3組及第1組動物之眼睛且固定於4%多聚甲醛中,隨後在30%蔗糖溶液中培育隔夜。使用低溫恆溫器切割角膜切片,在PBS中洗滌且阻斷非特異性結合2小時(含10%正常山羊血清之0.5% Triton-X/PBS),隨後與抗Ly-6G初級抗體(Abcam, Cambridge. MA)一起培育48小時。Ly-6G為主要在嗜中性白血球上表現之糖基化磷脂醯肌醇錨蛋白,且抗Ly-6G抗體允許偵測切片中之此等細胞。隨後用PBS洗滌切片且與二級抗體山羊抗大鼠Alexa Fluor® 488一起培育,以使嗜中性白血球可視化。染色的切片在PBS中洗滌且固定於載玻片上。
使用Zeiss Axiovert 200 M顯微鏡以20倍放大倍率在角膜切片中定量角膜切片中之嗜中性白血球的數目,其表明眼睛中誘發的炎症程度。分別自左右角膜周邊及角膜中心之各切片拍攝三張代表性影像。自各切片之此三張影像計數嗜中性白血球的總數,且相加以表示單個角膜切片中之嗜中性白血球總數。分析每隻眼睛之總共五個間隔120μm的切片,且對嗜中性白血球數目求平均值。
基於視訊記錄之疼痛評分顯示,媒劑處理產生之平均疼痛評分為34,而投與0.25%及0.5%之CB2RA調配物使得疼痛評分顯著降低(分別為12及18;參見
圖 20),疼痛評分之降低與CB2RA濃度成反比。當與Thapa等人 (2018)同上之投與HU-308之結果相比時,其中1.5%之CB2促效劑溶液產生之疼痛評分為17(參見
圖 20中之1.5% HU-308)。低於1.5%之Hu-308劑量未能產生鎮痛作用。使用相同模型產生之結果表明,當與在大豆油中調配之HU-308相比時,作為PVP-PLA調配物遞送之CB2RA在降低角膜痛覺過敏模型之疼痛評分方面至少有效三倍。令人驚訝的是,接受兩倍CB2RA劑量(共30 µL)之第4組動物的疼痛評分高於僅接受15 µL該組合物之動物。
用0.5% CB2RA調配物處理後角膜中之嗜中性白血球浸潤顯示於
圖 21中。與經媒劑處理之眼睛(嗜中性白血球/切片=214)相比,局部投與0.5% CB2RA調配物顯著減少嗜中性白血球數目(嗜中性白血球/切片=101)。0.5% CB2RA調配物觀察到的嗜中性白血球減少水準與HU-308溶液在三倍高濃度下觀察到的相似(資料提取自Thapa (2018) 同上),證實CB2RA調配物與HU-308調配物相比具有更大的消炎作用。此等資料共同表明,以微胞PVP-PLA調配物形式遞送之包含98.8% HU-308及1.2% HU-433之CB2RA組合物提供比HU-308單獨在大豆油中遞送時更大的鎮痛及消炎作用。
實例 25.CB2RA 調配物在角膜痛覺過敏臨床前模型中之進一步評估
參考實例25及圖20,進行額外的研究以評定CB2RA調配物在低於先前測試之濃度下的鎮痛作用,此等濃度相對於CB2RA組合物為0.075% wt/vol、0.25% wt/vol及0.125% wt/vol。表29顯示所有測試劑量(包括新劑量)之燒灼後6小時記錄的疼痛評分,而圖22以圖形方式呈現此等資料。
表 29 :局部投與 CB2RA 調配物後之疼痛評分
| 組 | 測試藥劑 | 燒灼後 6 小時 | |
| 疼痛評分 | SEM | ||
| 1 | 媒劑 | 34.5 | 3.9 |
| 2 | P2005 (0.075% TA-A001) | 20.0 | 5.8 |
| 3 | P2005 (0.125% TA-A001) | 13.4 | 5.5 |
| 4 | P2005 (0.25% TA-A001) | 12.5 | 2.2 |
| 5 | P2005 (0.5% TA-A001) | 18.1 | 3.5 |
如
圖 22所示,不同劑量之CB2RA組合物產生的疼痛評分呈現明顯的U形曲線,0.075%至0.25%之劑量產生增加的鎮痛水準,而0.5%劑量雖然顯著比媒劑更有效,但與例如0.25%劑量相比鎮痛作用較小。
此效果為出乎意料的,但說明CB2RA組合物可能具有確定治療窗。然而,由於任何劑量均未觀察到不良反應(眼睛發紅或其他刺激跡象),因此該觀察結果不能擴展至對治療指數之評論。因此,雖然據報導其他大麻素受體促效劑之治療指數較窄,但本發明之CB2RA組合物似乎並非如此;增加調配物之劑量不會影響耐受性。
此等資料使用三次樣條函數進行最佳擬合(參見
圖 23),其預測此模型中之最大有效劑量為大致0.18% wt/vol且基於媒劑(零反應)與最大有效劑量之間的值,ED50為0.06%。後一個數字顯著低於Thapa等人 (2018), 同上對於Δ8 THC(ED50;1%)或CBD(ED50;5%)產生之數字,實驗室亦生成本結果。
實例 26.COX 調配物在角膜痛覺過敏臨床前模型中之評估
參考實例25及26,進行額外的研究以比較CB2RA調配物及基於NSAID之COX調配物1在角膜痛覺過敏鼠類模型中之作用。採用的實驗方法與實例25中詳細描述之方法相同。
如下製備COX調配物1。在磁力攪拌下,將450 mg PVP-PLA嵌段共聚物溶解於1 mL注射用水中,持續大致10分鐘。隨後在攪拌下,將0.4 mL 0.1 NaOH之0.1 N水溶液添加至聚合物溶液中,使pH值達到大致7.5。接下來,將0.25 mL 100 mM磷酸鈉緩衝液pH 7.0添加至溶液中,隨後添加1.25 mL濃度為100 mg/mL之甘露糖醇水溶液。接下來,在室溫下,在磁力攪拌下,將50 mg塞來昔布溶解於玻璃小瓶中之1 mL乙醇中,且經大致1分鐘逐滴添加聚合物溶液。所得澄清溶液隨後在冰浴中冷卻,且隨後在攪拌下置於6℃之冷室中大致20分鐘。自冷室中移出樣品後,向調配物中添加1.10 mL水。接下來,將溶液在Rocket離心蒸發器中減壓濃縮至其初始重量之25%。隨後向濃縮溶液中添加3.6 mL水,得到最終CEL濃度為10 mg/mL之調配物。調配物隨後經由0.2um Nylon Target2過濾器(Thermo Scientific)過濾。將經過濾之調配物轉移至10 mL玻璃小瓶中且使用VirTis Genesis 25EL凍乾機冷凍乾燥。所得凍乾塞來昔布餅(COX調配物1)之組成顯示於表30中。
表 30 :冷凍乾燥之 COX 調配物 1 的組成
| 成分 | 毫克 / 小瓶 | %/ 小瓶 |
| 塞來昔布 | 50.0 | 7.8% |
| PVP-PLA共聚物WB-4 | 450.0 | 70.0% |
| 甘露糖醇 | 125 | 19.4% |
| 氫氧化鈉 | 1.6 | 0.2% |
| 磷酸二氫鈉 | 7.5 | 1.2% |
| 磷酸氫二鈉 | 8.9 | 1.4% |
| 總計 | 643 | 100% |
COX調配物1之凍乾餅在注射用水中復原,產生澄清、無粒子之溶液,其中塞來昔布濃度為25 mg/mL。如使用配備有凝膠填充環氧樹脂體組合電極的Accumet AP61 pH計所量測,復原餅之pH值在6.8至7.2之範圍內。在Agilent Cary UV-Vis-NIR 5000光譜儀上,在1 cm拋棄式聚苯乙烯比色管中測定光學透射率。使用空比色管作為空白,在650 nm及室溫下進行量測。復原混合物之光學透射率高於90%。復原樣品之滲透壓係用冰點降低3300微滲透計(Advanced Instruments)量測,且顯示各種測試樣品之滲透壓在420至450 mOsm/kg之間。溶液中微胞之Z平均值(平均尺寸)及其尺寸分佈係在25℃下使用配備有10mW He-Ne雷射器之Malvern Zetasizer Nano ZS在633 nm操作下藉由動態光散射來測定。Z平均值及多分散性分別在47至52 nm及0.38至0.45之間變化。
在實例25及26之角膜痛覺過敏模型中,COX調配物1減少眼部疼痛之能力係在兩種濃度下評定,此等濃度為1.5% wt/vol溶液(相對於塞來昔布)及3% wt/vol溶液(同樣相對於塞來昔布)。塞來昔布調配物所採用之較高藥物濃度反映在嚙齒動物後爪切口疼痛模型中塞來昔布與CB2RA組合物之間所見大致10倍的效力差異(實例7)。如自
圖 24可看出,雖然較高劑量之塞來昔布產生的疼痛評分低於較低劑量的疼痛評分(即潛在趨勢),但兩種劑量均未產生與關於媒劑所確定之值具有統計學差異的疼痛評分,記錄的值為1.5%劑量之40±2及3%劑量之24±3,均遠高於CB2RA組合物之值,證實實例7中報告之CB2RA組合物的鎮痛效力更大。在本研究中,向測試動物施用媒劑所顯示的疼痛評分與先前實驗的疼痛評分高度一致(平均疼痛評分為32±3),從而允許此結果的比較。
此等資料對於CB2RA組合物及調配物在治療角膜疼痛方面之潛在用途很重要,因為抑制COX-1及COX-2酶之NSAID藥物諸如塞來昔布(Gilad Rimon, Ranjinder S. Sidhu, D. Adam Lauver, Jullia Y. Lee, Narayan P. Sharma, Chong Yuan, Ryan A. Frieler, Raymond C. Trievel, Benedict R. Lucchesi, William L. Smith.《昔布類藉由與環氧合酶1之一個單體緊密結合干擾阿司匹林之作用》(Coxibs interfere with the action of aspirin by binding tightly to one monomer of cyclooxygenase-1))及酮咯酸目前代表角膜手術之『標準護理鎮痛劑』(https://www.reviewofoptometry.com/article/topical-nsaid-update)。此等資料支持將CB2RA組合物及調配物用於角膜手術,其劑量低於NSAID所能達到的劑量,從而避免NSAID副作用,諸如延遲傷口癒合及角膜變薄(Iwamoto, S., Koga, T., Ohba, M.等人 《非類固醇消炎藥藉由減少白三烯B4受體2之配體12-羥基十七碳烯酸的產生而延遲角膜傷口癒合》(Non-steroidal anti-inflammatory drug delays corneal wound healing by reducing production of 12-hydroxyheptadecatrienoic acid, a ligand for leukotriene B4 receptor 2.)Sci Rep 7, 13267 (2017). https://doi.org/10.1038/s41598-017-13122-8.)。
實例 27.CR2RA 組合物及 CB2RA 調配物在眼部炎症模型中之作用),單獨及與 COX 調配物 1 一起
眼睛之多種病理性病況與炎症相關或以炎症作為潛在病因。因此,眾所周知,慢性乾眼病涉及角膜及結膜內之炎症循環,例如(Baudouin C, Irkeç M, Messmer EM等人, 乾眼病中炎症之臨床影響:ODISSEY小組會議記錄(Clinical impact of inflammation in dry eye disease: proceedings of the ODISSEY group meeting.)《眼科學報》(Acta Ophthalmol.) 2018;96(2):111-119. doi:10.1111/aos.13436;Yamaguchi, T.(2018).乾眼症之炎症反應(Inflammatory Response in Dry Eye.)《眼科研究與視力學》(Investigative Ophthalmology & Visual Science), 59(14), DES192. doi:10.1167/iovs.17-23651)且消炎劑諸如環孢素及皮質類固醇可緩解症狀(Hessen M, Akpek EK.乾眼症:一種發炎性眼部疾病(Dry eye: an inflammatory ocular disease.)《眼科及視覺研究雜誌》(
J Ophthalmic Vis Res.) 2014;9(2):240-250)。如實例26中所述,CB2RA組合物已顯示減少角膜炎症。CB2RA調配物在整個眼睛前段遞送CB2RA組合物之能力(實例30)亦支持其在治療諸如可能致盲的葡萄膜炎之葡萄膜炎症疾病方面的價值。
類似地,視網膜炎症與許多致盲疾病相關,諸如糖尿病性視網膜病變(Chung YR, Kim YH, Ha SJ等人, 炎症在藉由光學相干斷層掃描技術對糖尿病性黃斑水腫分類中之作用(Role of Inflammation in Classification of Diabetic Macular Edema by Optical Coherence Tomography.)《糖尿病研究雜誌》(J Diabetes Res.) 2019;2019:8164250.發表於2019年12月20日. doi:10.1155/2019/8164250)及自體免疫性病況,諸如自體免疫性視網膜病變,一種導致視網膜變性的罕見疾病。年齡相關性黃斑變性(AMD)為另一種發炎性視網膜疾病。AMD為全球失明之主要病因,估計有1100萬北美人罹患該疾病。顧名思義,其發病率隨著年齡的增長而穩步上升,40歲時影響2%的人口,但到80歲時超過25%。AMD可分類為乾性AMD或濕性AMD;
乾性AMD:雖然乾性AMD的確切病因尚不十分清楚,但認為低級慢性視網膜炎症為該疾病之主要驅動因素。因此,視網膜之光感受器及視網膜色素上皮(RPE)細胞顯示出高呼吸速率,若其要有效發揮作用,則需要高局部氧氣濃度。然而,此富氧環境之結果為當與聚焦光曝露之高度氧化條件相結合時,會大量產生活性氧(RoS)。雖然短暫,但RoS對RPE細胞及鄰近的布魯赫膜(BM)中高濃度存在的蛋白質、脂質及膽固醇具有高度的破壞性,此等分子(包括促炎性7-酮膽固醇、補體因子及其他細胞碎片)之損壞及轉化形式構成該疾病的典型的玻璃膜疣沈積。
根據在黃斑中觀察到的玻璃膜疣的性質,乾性AMD患者可分類為患有早期、中期或晚期疾病。在早期至中期乾性AMD中,玻璃膜疣表現為小的(60 µm -130 µm)黃棕色沈積物。然而,隨著疾病的發展,玻璃膜疣在個別區域增長至高達1000 µm。此類較大的玻璃膜疣導致近端RPE細胞及其上方的光感受器死亡,視力逐漸受到該過程的損害。若細胞死亡之獨立區域匯合且影響到中央小窩,如在晚期乾性AMD(又名地圖狀萎縮)中所發生,則視力喪失嚴重。
自小的玻璃膜疣發展至不斷更大的玻璃膜疣係由促炎性玻璃膜疣組分引起之慢性視網膜炎症驅動,該炎症又會導致單核球/巨噬細胞及免疫系統之其他細胞(白細胞)被吸引並聚集至發炎區域。隨著白血球的積累,炎症反應加劇,增加RPE的破壞,隨後導致進一步形成玻璃膜疣且在RPE兩側形成沈積物。這『脂質屏障』進一步抑制RPE的功能及活力。目前沒有針對乾性AMD之治療方法,其為一個尚未滿足的主要需求。
CB2受體促效劑,包括本文所述之CB2RA組合物,已顯示具有免疫調節作用。舉例而言,其已證明可降低角膜痛覺過敏、葡萄膜炎及玻璃體視網膜病變模型中促炎性介質之水準,其中其亦減少介導慢性炎症及組織破壞之白血球的積聚。減弱視網膜中之免疫反應、減輕免疫細胞積聚且從而控制RPE破壞的能力對於治療乾性AMD很重要。
CB2RA組合物減少視網膜炎症之能力係藉由量測其在藍光曝露後調節活化單核球募集至小鼠視網膜下腔之能力來確定。對於此等首次原理驗證實驗,CB2RA調配物通過腹膜內注射以高達3 mg/kg/天之劑量投與動物。
簡言之,雄性C57BL/6小鼠曝露於發光二極體(LED)之藍光(425 nm),照度強度為6000 lux,持續4天,事先未進行暗適應。小鼠每天兩次藉由以相對於CB2RA組合物0.5mg/kg、1.5mg/kg及3mg/kg之劑量腹膜內(IP)注射生理鹽水、媒劑(PVP-PLA)或CB2RA調配物來處理。自曝露之第一天投與治療劑,直至藍光曝露結束。在照射期期間,每日投與眼用阿托品溶液1%(Alcon, USA)用於瞳孔擴張。在照射期結束時,小鼠維持於300 lux之常規12小時/12小時光/暗循環3天,隨後處死。
隨後收集去核的眼睛,且浸入磷酸鹽緩衝之4%多聚甲醛(PFA)溶液中1小時。隨後用含有0.1% Triton-X-100及10%胎牛血清(FBS)之磷酸鹽緩衝鹽水(PBS)對眼組織進行透化處理,接著與抗IBA-1抗體(FujiFilm Wako Pure Chemical Corp., Japan)在相同PBS緩衝液中培育隔夜。IBA-1為一種巨噬細胞特異性抗體,可偵測引起炎症反應之視網膜下活化單核球:羅丹明-鬼筆環肽(Abcam, Canada),一種聚合的肌動蛋白標記物,用作複染劑以觀察RPE細胞。30分鐘後,組織用PBS緩衝液洗滌,且隨後與螢光染料偶合之抗(抗IBA-1)抗體(Alexafluor-488, Life Technologies, USA)一起培育。此第二次培育後,組織用含0.1% Triton-X-100之PBS洗滌三次,每次5分鐘,且隨後展平用於螢光顯微鏡分析(Zeiss, Germany)。
如
圖 25中可見,雖然與經對照處理之動物相比,0.1%劑量之CB2RA組合物不會引起單核球數減少,但當投與3及6 mg/kg/天CB2RA組合物劑量時,視網膜下腔中之IBA-1陽性單核球之數目大大減少,證實CBRA組合物在視網膜中具有消炎作用。
濕性AMD:一些晚期AMD患者,除地圖狀萎縮之外,亦將經歷脈絡膜新生血管(CNV),亦即形成新的不成熟、脆弱及滲漏的脈絡膜血管,其突破BM進入視網膜。當此發生時,該疾病稱為新生血管性、滲出性或「濕性」AMD。濕性AMD比地圖狀萎縮更迅速地導致漸進性視力喪失,且10-15%之AMD患者會經歷。
濕性AMD之病因的核心為血管內皮生長因子(VEGF)。在正常情況下,VEFG濃度之低水準變化被認為經由所謂的脈絡膜毛細管層維持對RPE血液供應的穩態控制。然而,在AMD之發炎病況下,細胞介素IFN-γ、IL-1β及TNF-α之局部過度產生導致活化的白細胞、發炎的成纖維細胞及RPE細胞上調及過度產生VEGF。此類增加隨後導致新血管生長(血管生成)增加及血管滲透性(滲漏)增加。血管生成及此等新血管之滲漏的程度控制視網膜及視網膜下腔的血管滲出量,且因此控制濕性AMD發生之視力喪失的程度。過量的血管滲出物亦可能導致RPE及或視網膜脫離,從而導致失明。
藉由細胞介素特異性抗體調節促炎性細胞介素,或如更常發生的,使用抗VEGF抗體調節眼部VEGF水準,已證明可減少一些AMD患者之CNV進展,支持VEGF在濕性AMD中之核心作用及有效治療該疾病的方法。然而,此類療法僅對大致40%的眼睛有益,且往往僅持續有限的時間。需要替代治療方法。
本文所述之CB2RA組合物及CB2RA調配物已證明在局部投與後可降低眼睛中促炎性細胞介素及趨化介素之水準(參見實例25),支持CB2R促效作用減少VEGF產生之潛力,從而減少血管生成。此潛力使用離體模型來評定,該模型允許直接量測測試劑對脈絡膜/RPE複合體中脈絡膜血管萌發的抗血管生成作用。由於已證明CB2RA組合物在活體內模型中顯示出與NSAID(塞來昔布)之協同消炎作用,因此CB2RA組合物在存在及不存在微胞COX調配物1之情況下進行測試。
簡言之,脈絡膜外植體係自6週齡小鼠獲得,且根據Tahiri等人描述之方法製備。因此,首先將去核的眼睛置於含有1×漢克氏平衡鹽溶液(HBSS, VWR, Canada)的培養皿中。隨後在鋸齒緣下打開眼睛以移除晶狀體及角膜之前部結構,接著仔細移除包含鞏膜/脈絡膜/RPE複合體之神經視網膜。此等製備物在37℃、5% CO2中,在補充有微血管內皮SingleQuots套組(EGM-2MV, Lonza Bioscience, Switzerland)之內皮細胞生長基礎培養基(EBM-2)中培養3天。在第3天更換EBM-2培養基,隨後用以下任一者培育外植體;i) PBS;ii)抗VEGF抗體(20 ng/mL,R&D Systems, USA);iii) CB2RA調配物(CB2RA濃度:C1=0.1 µM,C2=1 µM,C3=5 µM及C4=10 µM);iv)塞來昔布(COX調配物1;塞來昔布濃度:C1=1 µM,C2=10 µM,C3=17.5 µM及C4 25 µM);v) CB2RA調配物及COX調配物1之混合物(CB2RA及塞來昔布濃度分別為5 µM及17.5 µM);或vi) PVP-PLA(媒劑)。各測試物品或對照使用七個外植體。使用Axiovert 200 M倒置顯微鏡(Zeiss, Germany)在測試處理前(T0)及24小時後(T24h)拍攝個別外植體的照片。使用ImageJ軟體(NIH, USA)確定照片中顯示的新血管生成的程度(T24h的總血管面積減去T0的總血管面積),新血管生成係由各對照或測試物品投與產生。
如自
圖 26A可看出,與PBS相比,CB2RA組合物、塞來昔布及基於PVP-PLA之媒劑顯示出顯著的抗血管生成作用,CB2RA及塞來昔布測試物品以劑量依賴的方式證明此點。當相對於PBS反應進行標準化時(
圖 26B),與PVP-PLA媒劑相比,較高劑量之CB2RA組合物及塞來昔布顯示出顯著差異。在此等濃度下,兩種化合物均能夠以比抗VEGF更好的功效減少血管面積。
CB2RA組合物與塞來昔布之間的協同作用已在急性切口疼痛模型中得到證實(實例8),當將其組合時,兩種藥劑之ED50大大降低,其程度大於簡單的相加。此處,兩種活性劑之組合又產生強烈的抗血管生成作用,比簡單的相加更大,即當參考圖26B時,以1 μM測試之CB2RA組合物相對於PBS之血管面積為0.27,而17.5 μM塞來昔布調配物相對於PBS之面積為0.17。因此,可預期1:1混合物相對於PBS產生的血管面積為:
(i) (0.27+0.17)/2 = 0.22
然而,CB2RA組合物與塞來昔布之1:1組合的量測值產生相對於PBS的0.04的血管面積,其比可能預期的要大約5倍,再次支持該兩種分子之間的協同作用。這作用再次大於在相同實驗中測試之抗VEGF抗體所達成之作用。因此,CB2RA、COX調配物1及CB2RA與NSAID分子之組合可為潛在的新治療劑,用於治療AMD或其他新血管生長有害的病變,包括腫瘤中出現的新血管生成。
實例 28.CB2RA 調配物對兔角膜傷口癒合之影響
再生眼表面完整性為維持眼部內穩定及長期健康之關鍵。角膜手術後用作鎮痛劑之NSAID及皮質類固醇藥物與傷口癒合率降低及眼內壓增加相關。兔眼表面研究之目的為測試CB2RA調配物在局部施用於兔眼時,是否影響角膜傷口癒合率及眼表面完整性,如Algerbrush誘導之角膜傷口模型中螢光素染色所示。此外,進行確定用CB2RA調配物給藥是否增加眼內壓。
使用十三隻體重大致2.5 kg之紐西蘭白化兔,且根據實驗動物護理及使用指南進行維持。動物在基線眼部檢查(第-1天)後分為三組(媒劑,n=5,及劑量為0.25%及0.5%之CBR2RA,n=4)。在研究的第0天,兔在用氯胺酮/甲苯噻
麻醉後雙眼滴入0.5%丙美卡因鹽酸鹽。3-5分鐘後,將5%必妥碘施用於眼睛且用無菌生理鹽水沖洗。在手術過程中使用窺鏡保持眼睛睜開。對於右眼(OD),角膜用3 mm衝頭工具輕輕劃痕,在衝頭工具劃定之區域內,用Algerbrush II鏽環移除上皮頂層。手術後,提供丁丙諾啡以減輕疼痛及不適。預期此處理不會干擾角膜傷口癒合。在研究期間,動物沒有表現出疼痛或痛苦的跡象。左眼未處理。在研究完成時(第3天),在深度麻醉下肌肉內投與35 mg/kg氯胺酮/5 mg/kg甲苯噻
後,藉由IV注射投與400 mg/kg劑量之戊巴比妥鈉對所有動物實施安樂死。
自第0天起,使用經校準之微量吸管將CB2RA調配物或媒劑(50 µL)小心地投與兔之眼表面(右眼),每天兩次。在第-1天(基線)藉由螢光素染色檢查傷口癒合,且隨後自第0天至第3天每天一次。簡言之,動物之右眼(OD)接受20 µL局部劑量之0.75%螢光素鈉(FischerSci, USA)。螢光素染色之嚴重程度係自使用Pictor Plus攝影機(Volk, USA)拍攝之影像來評定。在完成研究之後,使用ImageJ軟體(NIH, USA)分析3 mm直徑損傷區域中均染色強度之顯微照片。隨後計算CB2R調配物實現傷口癒合之速率(亦即,螢光強度恢復至術前基線值)(
圖 27A 及 27B)。
簡言之,如圖27A所示,雖然在研究之三天內,媒劑組之螢光強度仍高於基線,但使用CB2R調配物時,0.5%處理之動物在1天內且0.25%處理之動物在2天內獲得基線值。此等結果在圖27B中表示為癒合率。測試物品被認為在癒合角膜方面非常成功,癒合率顯示出劑量反應效應。
在手術前且隨後在後續每一天測試之任何其他測試之前,量測眼內壓。記錄動物之左眼(未處理)及右眼(經處理)之量測結果。在整個研究過程中,所有值均在此等動物之正常範圍內(9.5至15.75 mmHg),且經處理及未處理之眼睛的壓力沒有統計學差異,支持CB2RA調配物之施用不會升高眼內壓的結論。
綜上所述,該研究表明,與NSAID及皮質類固醇不同,CB2RA調配物與對照相比增加角膜傷口癒合率且對眼內壓沒有影響。
實例 29. CB2RA 組合物局部施用後在角膜痛覺過敏大鼠模型中之生物分佈及對炎症的控制
眼部疾病發生在整個眼睛中,因此,若諸如本文所述之CB2RA組合物的藥物可藉由作為滴眼劑簡單局部投與進入眼睛之所有區域,則將具有更大的治療益處。基於PVP-PLA之CB2RA調配物在局部施用後將CB2RA組合物遞送至眼睛之前部及後部的能力係使用基於Thapa等人(Thapa D, Cairns EA, Szczesniak AM, Toguri JT, Caldwell MD, Kelly MEM. 大麻素Δ
8THC、CBD及HU-308經由不同的受體起作用以減少角膜疼痛及炎症(The Cannabinoids Δ8THC, CBD, and HU-308 Act via Distinct Receptors to Reduce Corneal Pain and Inflammation.)《大麻及大麻素研究》(Cannabis Cannabinoid Res.) 2018年2月1日;3(1):11-20. doi: 10.1089/can.2017.0041. PMID: 29450258; PMCID: PMC5812319)開發之小鼠模型的角膜痛覺過敏大鼠模型來研究,大鼠的眼睛較大,能夠進行更精確的解剖,從而更準確地量測各種組織中之CB2RA組合物。
簡言之,藉由吸入2.5-4%異氟烷對大鼠進行深度麻醉,且隨後將含有硝酸銀(Grafco 6")之微型塗抹器在其眼睛表面施用2秒,燒灼直徑1 mm之區域。隨後用生理鹽水沖洗眼睛且施用眼部潤滑劑(Systane® Ultra)以防止乾燥。
對於給藥,大鼠經束縛且在燒灼後30分鐘、1小時及2小時,用10 µl生理鹽水、PVP-PLA聚合物或CB2RA調配物液滴進行局部給藥。所施用之CB2RA調配物中CB2RA組合物的濃度在0.075%與0.5%之間。燒灼後六小時,在每隻眼睛之表面施用5 μL的1 μM辣椒素溶液,八小時後,對動物進行安樂死且將所有眼睛剜出。
解剖每隻動物之左眼,在4%多聚甲醛中固定24小時,隨後在20%蔗糖中固定至少24小時。隨後將解剖的眼睛包埋於OCT化合物(Tissue Plus;Fisher)中,且使用Leica CM1950冷凍切片機切成12 µm厚的切片。用5%牛血清白蛋白阻斷非特異性蛋白質結合1小時,之後將角膜切片在4℃下黑暗中用1:200稀釋之抗CD45抗體(Abcam, Clone MRC OX-1)培育隔夜。隨後用PBS洗滌角膜切片,且施用具有DAPI之抗褪色固定介質(ProLong Glass Antifade Mountant with NucBlue Stain, Thermofisher)。用數位載玻片掃描器(Pannoramic MIDI II, 3DHISTECH)掃描每張載玻片具有一至四個角膜切片的全載玻片。使用QuantCenter影像分析平台(3DHISTECH)分析角膜中之白血球數;暴露於不同濃度之CB2RA組合物後角膜中白血球之平均數目顯示於
圖 28中。
如圖28所示,CB2RA組合物以劑量依賴性方式減少角膜炎症,如隨著CB2RA組合物劑量增加而積聚於組織中之白血球數目逐漸減少所反映。此等資料證實在小鼠模型中生成之資料,亦即CB2RA組合物在局部投與後在角膜組織中顯示出消炎作用。
剜出燒灼後8小時安樂死之大鼠的右眼,且隨後解剖為眼睛前部(角膜、睫狀體及房水)及眼睛後部(玻璃體、視網膜及脈絡膜)區段。隨後如下計算各區段中CB2RA組合物之濃度;
解剖的組織首先在CK14-2mL小瓶中之冷PBS緩衝液中用Precellys®打珠勻漿器研磨。研磨後,添加冷乙酸乙酯以自含水勻漿中提取CB2RA組合物,隨後將提取物渦旋混合15秒。隨後在4℃下以13,000 rpm進行離心15分鐘,且將150 µL上清液轉移至RSA小瓶中進行GC MS/MS分析。所有樣品在CB2RA組合物定量前保持在-80℃下。
樣品使用裝配有Agilent Technologies HP-5ms Ultra-Inert, 30m x 0.32 mm x 0.25µm之Agilent Technologies 7000C三重四極桿質譜儀進行分析,氦氣流速為2 mL/min且入口溫度為325℃。每次注射使用0.75 µL之樣品體積,在無分流模式下進行。烘箱溫度上升條件提供於表31中。
表 31 :烤箱溫度上升速率
| 上升 | 速率 (℃) | 值 (℃) | 保持時間 (分鐘) | 運行時間 (分鐘) |
| 最初 | - | 150 | 1 | 1 |
| 斜坡1 | 30 | 320 | 10 | 16.667 |
所使用之串聯質譜掃描段提供於表32中。所使用之輸送管溫度為280℃,溶劑延遲4分鐘。採用多反應監測(MRM)條件。
表 32 :串聯質譜掃描段
| # | 化合物 | 前體離子 | MS1解析度 | 產物離子 | MS1解析度 | 停留(ms) | 碰撞 ( eV) |
| 1 | TA-A001 | 318 | 寬 | 233 | 寬 | 100 | 25 |
| 2 | TA-A001 | 318 | 寬 | 219 | 寬 | 100 | 25 |
| 3 | TA-A001 | 318 | 寬 | 205 | 寬 | 100 | 25 |
| 4 | TA-A001 | 318 | 寬 | 191 | 寬 | 100 | 25 |
眼睛前段及後段之CB2RA組合物的量呈現於圖29及30中。
如可見,CB2RA組合物之顯著濃度在局部施用調配物後約6小時在眼睛之前部及後部測得。如所預期,當使用媒劑或生理鹽水時未量測到濃度。所量測之所有濃度反映施用在眼睛後部及眼睛前部樣品中之CB2RA組合物之不同量。
在投與藥物後6小時,亦即在可能預期自眼部組織完全清除時,CB2RA組合物之持續存在支援CB2RA調配物以劑量/反應方式提供長期炎症抑制作用的潛力。具有諸如乾眼病之病況及其他慢性角膜病況的患者可能極大地受益於此類特性。
僅在局部施用後在後段發現顯著(及類似)量之CB2RA組合物,此支援CB2RA調配物能夠使用簡單的滴眼劑而非目前所需之玻璃體內藥物投與來有效治療眼睛後部視網膜疾病,諸如年齡相關性黃斑變性(AMD)或糖尿病性視網膜病變(DR)。此類進步將極大地有益於此等致盲疾病之治療。
實例 30. 降解產物及其控制策略
TA-A001(亦稱CB2RA組合物)為一種合成的小分子,亦即包含充分表徵之CB2R促效劑Hu-308以及少但受控量之其對映異構體類似物Hu-433的新分子實體。CB2RA組合物之一般結構及組成以及其兩種對映異構體之化學名稱如下所示:
CB2RA組合物已證明在許多急性疼痛模型中具有強效消炎及鎮痛特性,當眼部燒傷後作為眼用滴注投與或切口手術後(同上)靜脈內投與時,其作為用於哺乳動物用於此等及其他治療環境中之治療劑具有極大潛在價值。TA-A001亦證明為抗血管生成的。
強制降解研究
為了有資格用於人類,CB2RA組合物必須在其功效及安全性方面進行嚴格的分析。安全性測試涉及對其分子化學及其降解產物及潛在代謝物的知識及理解。
CB2RA組合物降解之可能性及當CB2RA組合物降解時所形成之任何新物種可藉由進行強制降解研究來評定及確定。強制降解研究(FDS)涉及使活性劑諸如CB2RA組合物暴露於環境惡劣的條件;用於對CB2RA組合物進行FDS之條件顯示於表33中。
表 33 :在強制降解研究期間 TA-A001 暴露之條件 .
| 測試 | 試劑 | 測試條件 |
| 酸水解 | 鹽酸(1M) | 室溫,6小時 |
| 鹼水解 | 氫氧化鈉(1M) | 室溫,8小時 |
| 氧化 | 過氧化氫(0.5M) | 室溫,24小時 |
| 曝露於紫外線下 | 365nm紫外光 | 室溫,5天 |
在暴露於上述條件後,CB2RA組合物之樣品經受採用表34中所述之條件的逆相層析(分析方法1)。
表 34 :層析條件分析方法 1
| 系統 | Agilent 1100 HPLC |
| 管柱 | Zorbax-Eclipse XDB-C8 5µm, 15 x 4.6 mm管柱(Agilent Technologies) |
| 管柱溫度(℃) | 30 |
| 溶劑條件 | 移動相:水/乙腈 梯度(時間(分鐘)/%乙腈): 0/50、20/100、30/100、40/50 |
| 流量 | 1.0 mL/min |
| 偵測 | 210nm |
| 注射體積(µL) | 10 |
在所有陳述條件下新生成之物種的數目,以及其相對於母體CB2RA組合物峰(峰13:RRT=1)之相對滯留時間(RRT)提供於表35中。
表 35 :降解產物及相對滯留時間( RRT )對比母體 TA-A001 峰 .
* 峰之曲線下面積與未處理之母體TA-A001峰之曲線下面積的關係
| 峰數 | RRT | 百分比組成(%)* | 壓力條件 |
| 1 | 0.34 | 0.73 | 氧化 |
| 2 | 0.46 | 0.36 | 紫外線 |
| 3 | 0.48 | 0.45 | 紫外線 |
| 4 | 0.49 | 0.40 | 紫外線 |
| 5 | 0.50 | 0.30 | 氧化 |
| 6 | 0.53 | 0.86 | 紫外線 |
| 7 | 0.56 | 0.63 | 紫外線 |
| 8 | 0.58 | 0.99 | 紫外線 |
| 9 | 0.64 | 0.25 | 氧化 |
| 10 | 0.70 | 0.57 | 酸 |
| 11 | 0.83 | 0.32 | 氧化 |
| 12 | 0.96 | 2.81 | 氧化 |
| 13(母體) | 1 | NA | NA |
| 14/15 | 1.21 | 28.83/0.61 | 酸/鹼 |
TA-A001
之調配
CB2RA組合物為一種高度不溶性化合物,其水溶性小於0.5 mg/L。為了克服此障礙以遞送用於醫藥用途,CB2RA組合物可使用水溶性PVP-PLA嵌段共聚物進行調配,以增加其表觀溶解度。因此,PVP-PLA嵌段共聚物在高於其臨界微胞濃度(CMC)時,會形成直徑大致30 nm之單峰微胞。在微胞形成過程中,大部分CB2RA組合物包裹於微胞之核心(結合藥物)中,一部分化合物保留於低於其溶解度極限之水溶液中(游離藥物)。當向哺乳動物投與時,在游離藥物吸收後,自核心釋放結合藥物以維持游離藥物/結合藥物平衡。因此,PVP-PLA微胞代表用於高效遞送高濃度不溶性藥物之藥物儲槽。一種此類調配物,調配物(CB2RA組合物調配物1)描述於表35中。除其他途徑外,其可用於CB2RA組合物之局部、經眼、非經腸、經口、鼻內、經肺、經直腸或腦內遞送。如下製備調配物;
在第一步中,將PVP-PLA嵌段共聚物(0.539 g)在室溫下在磁力攪拌下溶解於無水乙醇(6.78 g)中10分鐘。隨後添加11 mg CB2RA組合物,隨後逐滴添加水(3.67 g)。所得澄清溶液在室溫下保持攪拌10分鐘。
隨後移除乙醇,且使用設定在HPLC溶離份模式下之Rocket Synergy蒸發器(ThermoFisher Scientific)將PVP-PLA:CB2RA組合物濃縮至其初始重量之10%,持續150分鐘。隨後將磷酸鹽緩衝液(600 mM,0.37 mL)添加至濃縮溶液中,隨後添加水以獲得4 g/L CB2RA組合物之最終濃度。接著藉由移液管將一毫升本體溶液轉移至10 mL玻璃小瓶中。隨後使用VirTis Genesis 25EL凍乾器對小瓶進行凍乾。所得凍乾餅之組成顯示於表35中。
表 35 : CBN2RA 組合物調配物 1 之組成
| 組分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| CB2RA組合物 | 4.0 | 1.9% |
| PVP-PLA共聚物 | 196.0 | 92.9% |
| 磷酸氫鈉 | 9.7 | 4.6% |
| 磷酸二氫鈉 | 1.4 | 0.6% |
| 總計 | 211.1 | 100% |
熟習此項技術者可設想包含PVP-PLA嵌段共聚物及CB2RA組合物之其他調配物。
CB2RA
組合物調配物之穩定性研究
當開發用於哺乳動物之治療用途的新調配物時,重要的是知道調配物中藥物物質(在此情況下為CB2RA組合物)之穩定性,以便可確定調配物之儲存期限。此等研究係在各種條件下進行,包括在室溫及高溫下,包括40℃之溫度,亦即所謂的加速條件。CB2RA組合物調配物1(表35)在加速條件下在玻璃小瓶中進行穩定性評定,CB2RA組合物之降解概況使用如本文所述之分析方法1進行監測。當研究CB2RA組合物在此等條件下之降解時,觀察到一種新的降解產物,其RRT為1.08,在紫外線、強酸、強鹼或氧化劑存在下單獨研究CB2RA組合物時未發現。與強制降解研究中觀察到的其他降解產物不同,此RRT為1.08之新化合物(此後稱為化合物B)的量隨時間推移迅速上升,超過習知地為醫藥產品設定之水準;在加速條件下儲存CB2RA組合物調配物1期間,隨時間推移形成之化合物B的量顯示於表36中。
表 36 : CB2RA 組合物調配物在加速條件下儲存超過 6 個月形成之化合物 B 的量 .
| 月 | 百分比組成(%) |
| 0 (研究前) | 0 |
| 1 | 1.1 |
| 2 | 2.3 |
| 6 | 4.7 |
因此,儘管在使用表33中所述之條件對單獨的CB2RA組合物進行強制降解研究時沒有形成化合物B,但化合物B為CB2RA組合物調配物1之主要降解產物。然後進行強制降解研究,其中將CB2RA組合物單獨暴露於僅加熱(80℃),持續24小時及48小時,以確定化合物B是否可由CB2RA組合物單獨形成;結果呈現於表6中。如可見,在此等條件下單獨加熱CB2RA組合物產生化合物B以及許多濃度較低的新降解產物,而在CB2RA組合物暴露於酸、鹼或過氧化物後,沒有看到該等產物。因此,表34及37中顯示之峰代表新的CB2RA組合物。
表 37 :高溫強制降解形成的新降解產物
| 峰數 | 24小時 | 48小時 | ||
| RRT | 百分比組成(%) | RRT | 百分比組成(%) | |
| 1 | 0.80 | 0.40 | 0.80 | 0.53 |
| 2 | 0.85 | 0.27 | 0.85 | 0.28 |
| 3 | 0.94 | 0.88 | 0.94 | 1.22 |
| 4 | 1.00 | 84.4 | 1.00 | 67.5 |
| 5 | 1.03 | 0.34 | 1.03 | 0 |
| 6 | 1.08 | 11.6 | 1.08 | 13.5 |
| 7 | 1.11 | 0.35 | 1.11 | 0.43 |
由於化合物B為CB2RA組合物之主要降解產物,因此確定其結構及形成方法很重要。因此,使用表38中所示之條件藉由半製備型逆相UV/MS層析處理經受24小時暴露於乾熱之CB2RA組合物的量。
表 38 : 用於半製備型逆相層析 ( 分析方法 2 ) 之層析條件
| 系統 | 配備3100質譜偵測器之Waters ARC半製備型HPLC |
| 管柱 | Sunfire C8, 19x100mm, 5 μm |
| 管柱溫度(℃) | 30 |
| 溶劑條件 | 移動相:水/乙腈 梯度(時間(分鐘)/%乙腈): 0/55、1/55、20/90、 |
| 流量 | 1.0 mL/min |
| 偵測 | UV: 200-400nm.MS: SIM: m/z 413 |
| 注射體積(µL) | 10 |
藉由此方法收集一定量的化合物B,隨後使用裝配有Bruker 5mm C/H低溫探針之Bruker AVANCE II 700 MHz光譜儀藉由溶液NMR(1H 1D、13C 1D、1H-1H COSY、1H-13C HSQC及1H-13C HMBC)來確定新分子之結構。在分析之前將樣品溶解於氘化氯仿中,在298K之溫度下進行該分析。藉由此方法確定之化合物B的結構示意圖如下,氧化部位被圈出:
藉由乾燥加熱CB2RA組合物形成之化合物B之前尚未描述於文獻中且代表一種新分子實體。對其結構之分析表明,其係由分子中之單羥基藉由新穎方法氧化而形成。藉由氧化形成化合物B為出人意料的,因為暴露於過氧化氫產生之強氧化性條件下未能產生此降解產物。因此,化合物B為藉由尚未揭示於文獻中之方法形成的新分子實體。使用手性層析對化合物B進行分析表明,化合物B本身為對映異構體,其對映異構體比率與形成其之CB2RA組合物的對映異構體比率相同;CB2RA組合物之兩種對映異構體以相同速率降解為化合物B。
控制
CB2RA
組合物中化合物
B
之產生
對於任何醫藥產品而言,將包括降解產物在內之雜質保持在一定限度內為重要的,因為此等雜質可能證明對暴露於醫藥產品之哺乳動物具有毒性。或者,即使當雜質促進所需活性時,控制雜質之量可為重要的。因此,在CB2RA組合物之情況下,特別需要控制雜質水準之方法及製程,最重要的是主要降解產物化合物B。然而,鑒於明顯導致化合物B形成之出人意料及未經證實的機制,最初並不清楚哪些方法會成功地控制其生產。評估多種抑制化合物B形成之不同方法:
單獨使用CB2RA組合物之研究
由於推定的形成過程為氧化,因此初始實驗試圖確定自培育條件中移除氧氣是否會改變CB2RA組合物產生之化合物B的量。此處,單獨的CB2RA組合物樣品在高溫下,在實驗室空氣存在下或在用惰性氣體(氬氣或氮氣)沖洗之小瓶中培育24小時及48小時。結果顯示於表40中。
表 40 :自培育條件移除氧氣之影響
| 培育 條件 | 組合物化合物B(%) | |
| 24小時 | 48小時 | |
| 在65℃下24小時(實驗室空氣) | 5.6 | 10.4 |
| 在65℃下24小時(惰性氣體) | 0.42 | 0.59 |
| 通過添加氮來降低化合物B的百分比 | 92.5% | 94.3% |
很明顯,雖然長時間加熱至65℃會直接自CB2RA組合物中產生化合物B,但在惰性氣體下培育,經48小時藉由在空氣中加熱形成之化合物B的水準降低90%以上。
使用CB2RA組合物調配物之研究
惰性氣體
之
影響
雖然當單獨測試組合物時,與惰性氣體一起培育抑制CB2RA組合物中化合物B的形成,但不清楚當CB2RA組合物作為包括賦形劑之CB2RA組合物調配物1之一部分培育時,是否會出現此種情況。因此,CB2RA組合物調配物1之小瓶如本文所述進行製備及乾燥,且在凍乾過程結束時,在封蓋前用氮氣回填或在封蓋前用實驗室空氣回填。隨後對兩種CB2RA組合物調配物1製劑進行表41中所述之測試程式。
表 41 :惰性氣體對 CB2RA 中化合物 B 形成之影響 組合物調配物 1.
| 培育 條件 | 組合物化合物B(%) |
| 24小時 | |
| 在65℃下24小時(實驗室空氣) | 0.53 |
| 在65℃下24小時(氮氣吹掃) | 0.07 |
| 在40℃下1個月(氮氣吹掃) | 0 |
如可見,用惰性氣體吹掃有效地抑制調配物中化合物B之產生至少一個月。
氧化抑制劑(抗氧化劑)之作用
雖然很明顯,在CB2RA組合物調配物1乾燥後移除氧氣在加速溫度下抑制化合物B至少一個月,但尚未知曉此程式是否會在更長時間內為調配物提供足夠的保護。因此評定在乾燥之前添加抗氧化劑至調配物之作用。由於發生氧化之確切機制並不明顯(即氧氣會導致化合物B的形成,而過氧化氫則不會),因此評估許多不同的抗氧化劑,如表42中所列。
表 42 :用於控制化合物 B 產生之實例抗氧化劑
| 抗氧化劑名稱 | 抑制機制 | 註釋 |
| 半胱胺酸鹽酸鹽 | 活性含氧物清除劑 | 直接移除誘發酮形成之氧自由基 |
| 維生素E(α-生育酚) | ||
| 丁基化羥基大茴香醚(BHA) | ||
| 亞硫酸氫鈉 | 游離氧反應物 | 藉由與氧氣之化學反應移除氧氣 |
| 偏亞硫酸氫鈉 | ||
| 山梨糖醇 | 金屬離子螯合劑 | 移除催化氧自由基產生之金屬離子 |
| EDTA |
所有均以醫藥調配物可接受之濃度按批准用於人類使用之非經腸及經眼產品使用之參考量使用,以與包括抗氧化劑之CB2RA組合物調配物1相同的方式製備之實例CB2RA組合物調配物提供於下表43-49中。
各種抗氧化劑對化合物B之形成的影響係藉由將其包括在以下實例調配物中來評定:
包含半胱胺酸之CB2RA組合物調配物
將PVP-PLA嵌段共聚物(0.541 g)在磁力攪拌下溶解於乙醇(6.78 g)中10分鐘。向此混合物中添加CB2RA組合物,隨後逐滴添加水(3.08 mL),且隨後添加0.58 mL的1 mg/mL半胱胺酸溶液。所得澄清溶液在室溫下保持攪拌10分鐘,且隨後與CB2RA組合物調配物1相同地處理。各小瓶之定量組成顯示於表43中。
表 43 :包含半胱胺酸之 CB2RA 組合物調配物 .
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.9% |
| PVP-PLA共聚物 | 196.0 | 92.8% |
| 磷酸氫鈉 | 9.7 | 4.6% |
| 磷酸二氫鈉 | 1.4 | 0.7% |
| 半胱胺酸鹽酸鹽 | 0.2 | 0.1% |
| 總計 | 211.3 | 100% |
包含維生素E之CB2RA組合物調配物
將PVP-PLA嵌段共聚物(0.541 g)在磁力攪拌下溶解於乙醇(6.78 g)中10分鐘。接著,向此混合物中添加CB2RA組合物,隨後逐滴添加水(3.08 mL),且隨後添加1.16 mL的10 mg/mL維生素E琥珀酸酯乙醇溶液。所得澄清溶液在室溫下保持攪拌10分鐘,且隨後與CB2RA組合物調配物1相同地處理。各小瓶之定量組成顯示於表44中。
表 44 :包含維生素 E 之 CB2RA 組合物調配物
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.9% |
| PVP-PLA共聚物 | 196.0 | 92.6% |
| 磷酸氫鈉 | 9.7 | 4.6% |
| 磷酸二氫鈉 | 1.4 | 0.7% |
| 維生素E琥珀酸酯 | 0.4 | 0.2% |
| 總計 | 211.5 | 100% |
包含BHA之CB2RA組合物調配物.
將PVP-PLA嵌段共聚物(0.541 g)在磁力攪拌下溶解於乙醇(5.86 g)中10分鐘。接下來,將1.16 mL BHA乙醇溶液(1 mg/mL)添加至混合物中。隨後添加11 mg CB2RA組合物,隨後逐滴添加水(3.67 mL)。所得澄清溶液在室溫下保持攪拌10分鐘,且隨後與CB2RA組合物調配物1相同地處理。各小瓶之定量組成顯示於表45中。
表45:包含BHA之CB2RA組合物調配物.
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.9% |
| PVP-PLA共聚物 | 196.0 | 92.6% |
| 磷酸氫鈉 | 9.7 | 4.6% |
| 磷酸二氫鈉 | 1.4 | 0.7% |
| BHA | 0.4 | 0.2% |
| 總計 | 211.5 | 100% |
包含亞硫酸氫鈉之CB2RA組合物調配物.
將PVP-PLA嵌段共聚物(0.541 g)在磁力攪拌下溶解於乙醇(6.77 g)中10分鐘。隨後添加11 mg CB2RA組合物,接著逐滴添加亞硫酸氫鈉水溶液(3.23 mg/mL,3.66 mL)。所得澄清溶液在室溫下保持攪拌10分鐘,之後與CB2RA組合物調配物1相同地處理。各小瓶之定量組成顯示於表46中。
表 46 :包含亞硫酸氫鈉之 CB2RA 組合物調配物
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.9% |
| PVP-PLA共聚物 | 196.0 | 91.0% |
| 磷酸氫鈉 | 9.7 | 4.5% |
| 磷酸二氫鈉 | 1.4 | 0.6% |
| 亞硫酸氫鈉 | 4.3 | 2.0% |
| 總計 | 215.4 | 100% |
包含偏亞硫酸氫鈉之CB2RA組合物調配物.
將PVP-PLA嵌段共聚物(0.541 g)在磁力攪拌下溶解於乙醇(6.77 g)中10分鐘。隨後添加11 mg CB2RA組合物,接著逐滴添加偏亞硫酸氫鈉水溶液(3.23 mg/mL,3.66 mL)。所得澄清溶液在室溫下保持攪拌10分鐘,之後與CB2RA組合物調配物1相同地處理。各小瓶之定量組成顯示於表47中。
表 47 :包含偏亞硫酸氫鈉之 CB2RA 組合物調配物
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.9% |
| PVP-PLA共聚物 | 196.0 | 91.0% |
| 磷酸氫鈉 | 9.7 | 4.5% |
| 磷酸二氫鈉 | 1.4 | 0.6% |
| 偏亞硫酸氫鈉 | 4.3 | 2.0% |
| 總計 | 215.4 | 100% |
包含山梨糖醇之CB2RA組合物調配物
將PVP-PLA嵌段共聚物(0.541 g)在磁力攪拌下溶解於乙醇(6.74 g)中10分鐘。隨後添加11 mg CB2RA組合物,接著逐滴添加山梨糖醇水溶液(17.7 mg/mL,3.64 mL)。所得澄清溶液在室溫下保持攪拌10分鐘,之後與CB2RA組合物調配物1相同地處理。各小瓶之定量組成顯示於表48中。
表 48. 包含山梨糖醇之 CB2RA 組合物調配物
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.7% |
| PVP-PLA共聚物 | 196.0 | 83.6% |
| 磷酸氫鈉 | 9.7 | 4.1% |
| 磷酸二氫鈉 | 1.4 | 0.6% |
| 山梨糖醇 | 23.4 | 10.0% |
| 總計 | 234.5 | 100% |
包含EDTA鈉之CB2RA組合物調配物.
將PVP-PLA嵌段共聚物(0.541 g)在磁力攪拌下溶解於乙醇(6.74 g)中10分鐘。隨後添加11 mg CB2RA組合物,接著逐滴添加EDTA水溶液(10.0 mg/mL,2.9 mL)。所得澄清溶液在室溫下保持攪拌10分鐘,之後與CB2RA組合物調配物1相同地處理。各小瓶之定量組成顯示於表49中。
表 49 :包含 EDTA 之 CB2RA 組合物調配物
| 成分 | 毫克/小瓶 | 按重量計之量/小瓶(%) |
| 含有E1及E2之組合物 | 4.0 | 1.9% |
| PVP-PLA共聚物 | 196.0 | 92.4% |
| 磷酸氫鈉 | 9.7 | 4.5% |
| 磷酸二氫鈉 | 1.4 | 0.7% |
| EDTA | 1.1 | 0.5% |
| 總計 | 211.9 | 100% |
用含有抗氧化劑之抗氧化劑進行的強制降解研究
.
隨後藉由在含有實驗室空氣或回填氮氣之65℃下加熱,對來自半胱胺酸鹽酸鹽、維生素E、丁基化羥基大茴香醚(BHA)、亞硫酸氫鈉、偏亞硫酸氫鈉、山梨糖醇及EDTA調配物中之每一者的封蓋小瓶進行FDS。此等研究之結果顯示於表50中。
表 50. 所評定之各種抗氧化劑的相對有效性
| 抗氧化劑 | 調配物內化合物B組成之增加(%) | 相對有效性(A+B)/2 | 排行 | |
| 實驗室空氣(A) | 氮氣(B) | |||
| 半胱胺酸鹽酸鹽 | 0.45 | 0.23 | 0.565 | 3 |
| 維生素E(α-生育酚) | 0.64 | 0.08 | 0.68 | 4 |
| 丁基化羥基大茴香醚 | 0.20 | 0.04 | 0.22 | 1 |
| 亞硫酸氫鈉 | 0.69 | 0.17 | 0.775 | 5 |
| 偏亞硫酸氫鈉 | 0.91 | 0.2 | 1.01 | 7 |
| 山梨糖醇 | 0.35 | 0.06 | 0.38 | 2 |
| EDTA | 0.75 | 0.12 | 0.81 | 6 |
如表50所示,雖然所評定之七種抗氧化劑中之6種在不同程度上有效阻礙化合物B之形成,但偏亞硫酸氫鈉在培養24小時後導致雜質之量增加。
總結
本文描述新的CB2RA組合物,其包含相對量不變之兩種對映異構體起始組分,該等組分在CB2RA組合物在各種條件下儲存期間形成,為CB2RA組合物降解產物。此等新物種可由於體溫或酶或其他代謝過程而在活體外及活體內形成。最重要的是,已發現一種新的、尚未描述之降解產物,其形成量大於其他降解產物之形成量,超過醫藥產品中允許之水準。詳細描述新的物種(化合物B)以及其形成機制。如所陳述,化合物B形成之化學機制(氧化)為出乎意料的,因為該分子並非由過氧化氫賦予之強氧化性條件產生。因此,鑒於CB2RA組合物對過氧化氫之抗性,化合物B之結構同等出乎意料。描述CB2RA組合物/化合物B之某些比率,其同樣可能尚未預測,但在將CB2RA組合物用於治療目的時可能為有用的。總之,最初的實驗教示遠離氧化作為化合物B生成方法,因此熟練的實驗者若獲得相同的結果,就不會預期氧化為合成途徑。僅經由CB2RA調配物之穩定性研究才確定此新的降解物。
由於化合物B為雜質,因此應控制其濃度。本文描述用於控制其生成之多種方法。鑒於化合物B產生之意外機制,此等方法無法先驗地預測成功,然而,所有方法均會抑制單個羥基氧化形成圖2之酮。基於此等發現,可使用其他可能對抑制化合物2之形成有價值的抗氧化劑以及本文測試之抗氧化劑,包括抗壞血酸、丁基化羥基甲苯、芝麻酚、愈創木樹脂、甲硫胺酸、檸檬酸、酒石酸、磷酸、硫醇衍生物、偏亞硫酸氫鉀、抗壞血酸棕櫚酸酯、硬脂酸鈣、沒食子酸丙酯、硫代硫酸鈉、麩胱甘肽、二羥基苯甲酸、苯甲酸、尿酸鹽及尿酸、山梨酸、苯甲酸鈉及其類似物及其混合物。包括氮氣及氬氣之惰性氣體亦單獨及與化學抗氧化劑一起使用。
另外值得注意的是,雖然一些抗氧化劑有效控制化合物B之產生,但其他抗氧化劑則無效,彼等成功的及彼等不成功的均不屬於任何一種特定的作用機制。因此,先驗地並不明顯哪些抗氧化劑將為有價值的,因此亦不明顯何種濃度之抗氧化劑將為有效的。在本文中,一些較佳抗氧化劑可單獨使用及相互組合使用以及與惰性氣體組合使用。如本文所述,包含少於0.1% wt/wt化合物B至大致14% wt/wt化合物B之CB2RA/化合物B組合物的範圍可能具有治療用途,及產生此等比率及控制化合物B之水準的方法在習知醫藥限制內。
參考文獻
Janeway, et al. (2001) IMMUNOBIOLOGY: THE IMMUNE SYSTEM IN HEALTH AND DISEASE.5th edition.New York: Garland Science.
Krystel-Whittemore, et al. (2016) FRONT.IMMUNOL., 6: 620.
Zhang, et al. (2007) INTERNATIONAL ANESTHESIOLOGY CLINIC, 45(2): 27.
Vance, et al. (2009) CELL HOST & MICROBE, 6(1): 10.
Cadieux, et al. (2005) J. CELL SCIENCE, 118(Pt 7): 1437.
Zeilhofer, et al. (2007) BIOCHEMICAL PHARMACOL., 73: 165.
Funk (2001) SCIENCE, 294(5548): 1871.
Reinold et al. (2005) J. CLIN.INVEST., 115: 673.
Lehnardt et al. (2003) PROC.NATL.ACAD.SCI.USA, 100: 8514.
Ricciotti, et al. (2011) ARTERIOSCLER.THROMB.VASC.BIOL., 31(5): 986.
Ferreira SH, et al. (1988) NATURE, 334: 698.
Zelenka, et al. (2005) PAIN, 116(3): 257.
Hess, et al. (2011) PROC.NATL.ACAD.SCI.USA, 108(9): 3731.
Teng, et al. (2017) J. IMMUNOL RES., 2017: 9671604.
Brinkmann, et al. (2004) SCIENCE, 303(5663): 1532.
Wang (2018) CELL TISSUE RES., 371(3): 531.
Garn, et al. (2016) J. ALLERGY AND CLIN.IMMUNOL., 138(1): 47.
Voscopoulos, et al. (2010) BR.J. ANAESTH, 105(S1): 69.
Hoffman, et al. (2016) J. CATARACT REFRACT.SURG., 42(9): 1368.
Razmju, et al. (2012) INT.J. PREV. MED., 3(Supp 1): S199.
Sameen, et al. (2017) PAK.J. MED.SCI., 33(5): 1101.
Colligris, et al. (2014) SAUDI J. OPHTHALMOL.28(1): 19.
Iwamoto, et al. (2017) NATURE SCIENTIFIC REPORTS, 7: 13267.
Flach (2001) TRANS.AM.OPHTHALMOL.SOC., 99: 205.
Arfè, et al. (2016) BRIT.MED.J., 354: i4857.
Kompella, et al. (2010) EXPERT OPIN.DRUG DELIV., 7(5): 631.
Highlights of Prescribing information for CELEBREX® June 2018 revision available at www.accessdata.fda.gov/drugsatfda_docs/label/2018/ 020998s050lbl.pdf
Oren, et al. (2004) BIOPHYS.J.87(2): 768.
Hua (2013) FRONT PHARMACOL., 4: 127.
Dostert, et al. (2004) CURR.PHARM.DES., 10: 2807.
Couper, et al. (2008) J. IMMUNOL., 180(9): 5771.
Dennison, et al. (1998) B.M.J., 316(7134): 789.
Mohammad, et al., (2017) SYSTEMATIC REV., 6(1): 92.
Motov, et al. (2017) ANN.EMERG.MED., 70(2): 177.
Williams (2018) CLIN.PHARMACOL.CORTICOSTEROIDS RESP.CARE, 63(6): 655.
Becker (2013) ANESTHESIA PROGRESS, 60(1): 25.
Weiser, et al. (2016) BULL.WORLD HEALTH ORG., 94(3): 201.
Gan, et al. (2014) CURR.MED.RES.OPIN., 30(1): 149.
Gan (2017) J. PAIN RES.10: 2287.
Kehlet, et al. (2001) BR.J. ANAESTH.87(1): 62.
Zhao, et al. (2019) PAIN RES.MANAGE., 2019: 7490801.
Lail et al. (2014) CAN.J. HOSP.PHARM., 67(5): 337.
Garimella (2013) CLINICS COLON RECTAL SURG., 26(3): 191.
Wunsch, et al. (2016) JAMA 315(15): 1654.
Galor et al. (2015) EYE, 29: 301.
Pereira et al. (2017) PAIN PHYSICIAN, 20: 429.
Trattler et al. (2017) CLIN.OPHTHALMOL., 11: 1423.
Shtein (2011) EXPERT REVIEW OPHTHALMOL., 6(5): 575.
Schwatrtz (2018) JAMA INTERN.MED., 178(2): 181.
Dana et al. (2019) AM.J. OPHTHALMOL.202: 47.
Ong et al. (2007) CLIN.MED.RES., 5(1):19.
Comprehensive Organic Chemistry.B.M. Trost & I. Fleming, eds., 1991-1992.
Martin, Remington's Pharmaceutical Sciences, 15th Ed., Mack Publ. Co., Easton, PA, 1975.
Soethoudt et al. (2017) NATURE COMMUN., 8: 13958.
Morales et al. (2017) FRONT.PHARMACOL., 8: 422.
Smoum et al. (2015) PROC.NATL.ACAD.SCI.USA, 112.28: 8774.
Patent No. WO2018176158A1.
Lengyel, et al. (2019) SCIENTIA PHARMACEUTICA, 87(3): 20.
Jainyu (2016) NAT.REV. MATER., 1(12): 1.
Canadian Patent No. 3034722.
Yang et al. (2018) YALE J. BIOL.MED., 91(1): 13.
Shtein (2011) EXPERT REV. OPHTHALMOL., 6(5): 575.
Javadi, Feizi (2011) J. OPHTHALMIC VIS.RES., 6(3): 192.
Ozan-Yuksel et al. (2009) EXPER.EYE RES., 88(4): 769.
Kauppinen,et al. (2016) CELL.MOL.LIFE SCI., 73(9): 1765.
Kashiwagi et al. (2003) BR.J. OPHTHALMOL.87297.
Sharma et al. (2019) METHODS IN MICROBIOL.46: 93.
Labuda et al. (2005) EUROPEAN J. OF PHARMACOL., 527: 172.
Rimon et al., (2010) PROC NATL ACAD SCI USAUSA, 107(1):28.
https://www.reviewofoptometry.com/article/topical-nsaid-update
Mohammadpour et al. (2018) J. CURR.OPHTHALMOL., 30(2): 110.
Iwamoto et al. (2017) SCI REP 7: 13267.
Baudouin et al. (2018).ACTA OPHTHALMOL., 96(2): 111.
Yamaguchi (2018) INVEST.OPTHALMOL.VIS.SCI., 59(14): DES192.
Hessen, Akpek (2014) J OPHTHALMIC VIS RES., 9(2): 240.
Chung et al. (2019) J DIABETES RES.2019: 8164250.
Thapa et al. (2018) CANNABIS CANNABINOID RES., 3(1): 11.
以引用之方式併入
本文所提及之專利文獻及科學文章中之每一者的全部揭示內容出於所有目的以引用之方式併入本文中。
等效物本發明可在不偏離其精神或基本特徵之情況下以其他特定形式實施。因此,前述實施例應在所有方面中視為說明性的而非限制本文所述之本發明。因此,本發明之範疇由隨附申請專利範圍而非前述說明指示,且本文意欲涵蓋申請專利範圍等效物之含義及範圍內出現的所有變化。
無
圖 1A-F顯示各種例示性CB2RA組合物之例示性快速超效合相(UPC2)層析圖,該等組合物包含E1及E2,E1相對於E2之重量比為(a) 98.4:1.6(
圖 1A 及 1B),其中圖1B為圖1A之分解視圖;(b) 8.4:6.4(
圖 1C 及 1D),其中圖1D為圖1C之分解視圖;(c) 82.4:17.6(
圖 1E 及 1F),其中圖1F為圖1E之分解視圖。各層析圖係使用裝配有Trefoil AMY1手性管柱(2.5 µm,3.0×150 mm)之Waters Acquity UPC2層析系統生成。各圖亦以插圖形式顯示層析圖之展開圖,該展開圖亦顯示各批料按其手性分離之各種其他組分。
圖 2A-B顯示各種例示性CB2RA組合物之例示性展開圖逆相HPLC層析圖,如藉由逆相HPLC所測定,純度(分析)值為98.9%(
圖 2A)或98.7%(
圖 2B)。E1及E2作為具有相同疏水性之對映異構體,藉由逆相HPLC未解析為獨立的峰。層析圖係使用配備有四元泵、管柱加熱室及裝配有Zorbax-Eclipse XDB-C8 5μm, 15×4.6 mm管柱之二極體陣列偵測器的Agilent 1100 HPLC系統生成。各展開圖顯示包含E1(峰2)及E2(峰3)之單峰以及此等CB2RA組合物根據其疏水性分離的各種其他組分。
圖 3顯示製備如嚙齒動物切口疼痛模型中所用之含有例示性CB2RA組合物之例示性PVP-PLA基調配物(CB2RA調配物1)之製程的示意圖。
圖 4顯示使用Malvern Nano ZS90 Zetasizer量測之用注射用水復原之例示性CB2RA調配物1的粒度分佈層析圖。包含重量比為98.4:1.6之E1與E2的CB2RA組合物用於生成此研究中所用之例示性CB2RA調配物1。
圖 5A顯示在急性手術疼痛模型中,測試動物在足底切開前後表現出的縮回臨限值的比較。
圖 5B顯示在投與媒劑(生理鹽水)、增加濃度之酮咯酸或單劑量丁丙諾啡後縮回臨限值/時間曲線之AUC
0.25-8 小時。PI:足底切開。
圖 5C顯示由
圖 5B中之資料生成之酮咯酸的AUC
0.25-8 小時/注射劑量、劑量/反應曲線。如
圖所示,計算出酮咯酸之ED
50值為23.1 mg/kg。
圖 6A顯示對於2 mg/kg、4 mg/kg及11 mg/kg靜脈內劑量之E1與E2重量比為99.4:0.6之例示性CB2RA調配物1生成的大鼠後爪縮回臨限值(鎮痛劑)反應/時間圖。在靜脈內投與例示性CB2RA調配物1後15分鐘進行縮回量測。亦顯示藉由靜脈內投與生理鹽水(對照)產生之縮回臨限值/時間。如藉由縮回臨限值相對於對照之增加所確定,在靜脈內投與CB2RA調配物之15分鐘內開始出現鎮痛作用,其中至少4 mg/kg及11 mg/kg組之鎮痛作用維持直至測試期結束。接受以相同方式投與之8 mg/kg CB2RA組合物之組的結果產生類似結果,但為了清楚起見自此圖中省略。
圖 6B顯示藉由分析縮回臨限值/時間圖所計算之
圖 5A之對照及2 mg/kg、4 mg/kg、8 mg/kg及11 mg/kg靜脈內劑量之例示性CB2RA調配物1的AUC
0.25-8 小時。2 mg/kg至8 mg/kg CB2RA組合物之AUC
0.25-8 小時值與投與劑量成比例增加,8 mg/kg及11 mg/kg劑量表現出類似或『平線區』反應。基於此等資料,4 mg/kg CB2RA組合物劑量,作為劑量/反應曲線之中心,經選擇以確定E1與E2重量比對後續實驗中之鎮痛反應的影響。
圖 7顯示
圖 6B之例示性CB2RA組合物之AUC
0.25-8 小時/注射劑量、劑量/反應曲線。如
圖所示,計算出此CB2RA組合物之ED
50值為3.0 mg/kg。
圖 8顯示2 mg/kg及4 mg/kg劑量之CB2RA調配物1的AUC
0.25-8 小時,其中E1與E2之重量比為98.8:1.2。在2 mg/kg與4 mg/kg劑量之CB2RA組合物之間觀察到劑量/反應效應,其中4 mg/kg劑量之AUC
0.25-8 小時大於由E1與E2之比為99.4:0.6之CB2RA組合物在此模型中生成的AUC
0.25-8 小時。2 mg/kg劑量之AUC
0.25-8 小時亦大於用E1與E2之比為99.4:0.6之CB2RA組合物生成的AUC
0.25-8 小時。
圖 9顯示2 mg/kg及4 mg/kg劑量之CB2RA調配物1的AUC
0.25-8 小時,其中E1與E2之重量比為98.4:1.6。在2 mg/kg與4 mg/kg劑量之間觀察到劑量/反應關係。儘管與對照相比仍有鎮痛作用,但4 mg/kg劑量之此CB2RA組合物的AUC
0.25-8 小時小於E1與E2之比為99.4:0.6或98.8:1.2之CB2RA組合物在此模型中生成的AUC
0.25-8 小時。2 mg/kg劑量之此CB2RA組合物的AUC
0.25-8 小時亦低於用E1與E2之比為99.4:0.6或98.8:1.2之CB2RA組合物生成的AUC
0.25-8 小時。
圖 10顯示2 mg/kg及4 mg/kg劑量之CB2RA調配物1的AUC
0.25-8 小時,其中E1與E2之重量比為93.6:6.4。此處,雖然觀察到兩個劑量與對照相比之鎮痛作用,但在2 mg/kg與4 mg/kg劑量之間沒有觀察到劑量/反應關係。4 mg/kg劑量之此CB2RA組合物的AUC
0.25-8 小時亦小於E1與E2之重量比為99.4:0.6、98.8:1.2或98.4:1.6之CB2RA組合物在此模型中生成的AUC
0.25-8 小時。2 mg/kg劑量之此CB2RA組合物的AUC
0.25-8 小時低於用E1與E2之重量比為99.4:0.6或98.8:1.2之CB2RA組合物生成的AUC
0.25-8 小時,但類似於由E1與E2之比為98.8:1.6之CB2RA組合物生成的AUC
0.25-8 小時。
圖 11顯示2 mg/kg及4 mg/kg劑量之CB2RA調配物1的AUC
0.25-8 小時,該調配物包含E1與E2之重量比為82.4:17.6之CB2RA組合物。與對照相比,兩個劑量均再次觀察到鎮痛作用,但在2 mg/kg與4 mg/kg劑量之間沒有觀察到劑量/反應關係。施用劑量下之結果與用E1與E2之重量比為93.6:6.4之CB2RA組合物生成的結果相似。
圖 12A比較
圖 7、
8、
9、
10及
11中所示之4 mg/kg靜脈內劑量之各種CB2RA組合物的AUC
0.25-8 小時,表明AUC
0.25-8 小時(或鎮痛作用)之變化隨各CB2RA組合物中E1與E2之重量比而變。雖然向動物投與之所有劑量之各CB2RA組合物,無論E1與E2之比如何,均顯示出相對於對照之鎮痛作用,但E1與E2之比為98.8:1.2之CB2RA組合物的鎮痛作用最大。
圖 12B顯示
圖 12A中資料之曲線擬合分析,突出顯示所測試之CB2RA組合物之所有組合物產生的鎮痛作用均大於對照(媒劑)及觀察到E2之鎮痛作用增強的E2比率範圍(0.19與1.78之間)。曲線擬合預測,最大程度的增強鎮痛作用發生在E1與E2之重量比為約99:1時,其中曲線下面積為其他E1與E2組合物之兩倍。
圖 13顯示在向雄性史泊格多利大鼠靜脈內投與例示性CB2RA調配物後,例示性CB2RA組合物(包含重量比為99.4:0.6之E1與E2)隨時間推移的血漿濃度。使用Agilent HP-5ms UltraInert(30 m,0.25 mm,0.25 µm)分析管柱,採用乙酸乙酯作為移動相,藉由GC-MS/MS來測定給藥後前12小時大鼠血漿中之CB2RA組合物濃度。
圖 14顯示如分析實例中所述之CB2RA調配物所進行,在後爪切口手術後1小時向大鼠投與對照及15 mg/kg、22.5 mg/kg、30 mg/kg及40 mg/kg靜脈內劑量之COX抑制劑塞來昔布之微胞PVP-PLA組合物(COX調配物1)的AUC
0.25-8 小時。15 mg/kg至30 mg/kg之AUC
0.25-8 小時值與投與劑量成比例增加,其中30 mg/kg及40 mg/kg塞來昔布劑量表現出類似的『平線區』反應。
圖 15顯示由
圖 14中呈現之資料生成的塞來昔布調配物(COX調配物1)之AUC
0.25-8 小時/注射劑量、劑量/反應曲線。計算出藉由PVP-PLA微胞遞送之塞來昔布之ED
50值為22.29 mg/kg。
圖 16顯示如實例5中所述向手術後大鼠投與對照及增加劑量之CB2RA調配物1與COX調配物1(統稱為CB2RA調配物2)之固定比率混合物的AUC
0.25-8 小時值。用於此研究之CB2RA調配物1含有E1與E2之重量比為99.4:0.6的CB2RA組合物。兩種調配物,亦即CB2RA調配物1及COX調配物1,以液體形式混合以產生CB2RA調配物2,基於自
圖 7及
15中所示之各自劑量/反應曲線計算之相對ED
25值,CB2RA組合物與塞來昔布之重量比約為1:13。CB2RA調配物2之投與劑量對於CB2RA組合物為0.32 mg/kg至1.125 mg/kg,對於塞來昔布為4.22 mg/kg至15 mg/kg。所有劑量之CB2RA調配物2均產生優於對照之鎮痛反應,且自所投與之最低至最高劑量均可見劑量反應關係。
圖 17顯示由
圖 16產生的關於CB2RA調配物2產生之CB2RA組合物之投與劑量的劑量/反應曲線(■),且與
圖 7之CB2RA調配物1產生之CB2RA組合物的劑量/反應曲線(●)進行比較。在與塞來昔布組合時,CB2RA組合物之劑量/反應曲線向左偏移,預測CB2RA組合物在作為固定劑量組合投與時之ED
50為0.42 mg/kg,而CB2RA調配物1為5.6 mg/kg。
圖 18顯示由
圖 16產生的關於CB2RA調配物2產生之塞來昔布之投與劑量的劑量/反應曲線(■),且與
圖 15之COX調配物1產生之塞來昔布的劑量/反應曲線(●)進行比較。在與CB2RA組合物組合時,塞來昔布之劑量/反應曲線向左偏移,預測塞來昔布在作為固定劑量組合投與時之ED
50為5.6 mg/kg,而COX調配物1為22.29 mg/kg。
圖 19顯示藉由CB2RA調配物1產生之CB2RA組合物的ED
50值、藉由COX調配物1產生之塞來昔布的ED
50值及以CB2RA調配物2形式產生之CB2RA調配物1及COX調配物1之混合物的ED
50值。作為CB2RA調配物1之CB2RA組合物的ED
50值(2.9 mg/kg)標記在x軸上,且藉由直線(等值線)連接至y軸上標繪之COX調配物1中塞來昔布的ED
50值(22.29 mg/kg)。若CB2RA組合物及塞來昔布之鎮痛作用僅為相加的,則連接的等值線表示藉由固定劑量組合比產生之ED
50值。若固定劑量組合之ED
50值落在等值線以上,則CB2RA組合物及塞來昔布之組合作用將為拮抗性的。當固定劑量組合之ED
50值落在等值線以下,則CB2RA組合物及塞來昔布之組合作用為協同的。換言之,對於任何給定劑量,組合作用大於單個藥物作用之和。
圖 20為條形圖,顯示當根據Thapa D.等人 (2018) 《大麻及大麻素研究》(CANNABIS CANNABINOID RES.)3:1, 11-20中所述之方案進行時,局部投與包含PVP-PLA之CB2RA組合物調配物減少BALB/c小鼠在角膜燒灼及辣椒素刺激後的角膜疼痛。將資料(作為疼痛評分)與藉由媒劑對照或在大豆油中調配之1.5%之HU-308溶液產生的資料進行比較。在辣椒素刺激後,以電子方式記錄疼痛評分量測30秒,以確定各種測試劑之鎮痛作用,且隨後進行盲審。然後將資料揭盲且作圖,如圖所示。
圖 21 (A)為條形圖,顯示在受傷後12小時用CB2RA組合物調配物之0.5% PVP-PLA調配物處理之小鼠角膜中每部分的嗜中性白血球數目與根據Thapa (2018)同上之方法觀測及產生之經媒劑處理之眼睛相比。將結果與施用在大豆油中調配之1.5%之HU-308溶液後產生的資料進行比較。
圖 21(B)顯示用媒劑處理之中央角膜橫向切片的代表圖,且
圖 21(C)顯示用0.5% CB2RA調配物處理之中央角膜橫向切片的代表圖;比例尺=50 μm。
圖 22為條形圖,顯示在根據Thapa D.等人 (2018)
2之方法進行角膜燒灼及辣椒素刺激後,局部投與CB2RA調配物減少BALB/c小鼠之角膜疼痛。方法如圖20。值代表平均值 + SEM。對於統計分析,使用具有Dunnett事後分析檢驗(與媒劑相比)之單向方差分析。**p<0.01,*p<0.05。
圖 23為使用三次樣條函數對表30之資料進行擬合的圖,用於確定TA-A001在鼠類角膜痛覺過敏模型中之ED50。
圖 24為條形圖,顯示在根據Thapa D.等人 (2018)之方法進行角膜燒灼及辣椒素刺激後,局部投與COX調配物不會減少BALB/c小鼠之角膜疼痛。在辣椒素刺激後,以電子方式記錄疼痛評分量測30秒,以確定測試劑之鎮痛作用,且隨後進行盲審。然後將資料揭盲且作圖,如圖所示。
圖 25為條形圖,藉由量化暴露於藍光且用生理鹽水、媒劑或不同濃度之CB2RA調配物處理之小鼠(n=5-8)的視網膜下腔中之IBA-1陽性細胞,顯示腹膜內施用CB2RA調配物對視網膜下腔中之IBA-1陽性細胞數量的影響。
圖 26A顯示藉由PBS、媒劑、抗VEGF、不同濃度之CB2RA組合物、塞來昔布或CB2RA組合物與塞來昔布之混合物產生之新血管生成的程度。描繪相對於PBS標準化之血管面積T24 - T0的變化(與PBS相比,*** P <0.001,n = 4-7)。
圖 26B顯示相對於PBS反應標準化之與圖26A中所示相同的結果(測試物品反應/PBS反應)。血管面積之變化呈現為PBS條件之倍數變化。顯示(與媒劑相比,** P <0.01,*** P <0.001)。
圖 27A為顯示隨時間變化標繪之媒劑、0.25及0.5%之CB2RA之高於基線的螢光強度的線圖。使用單指數衰減方程擬合資料。
圖 27B為條形圖,顯示藉由擬合媒劑、0.25及0.5% CB2RA之資料計算處的癒合速率常數。
圖 28為條形圖,顯示暴露於生理鹽水、PVP-PLA聚合物或增加濃度之CB2RA組合物(作為CB2RA調配物)之大鼠角膜中的白血球數目。白血球數目係在用硝酸銀燒灼後8小時量測。
圖 29為條形圖,顯示在用CB2RA調配物最終給藥後6小時收集之眼前勻漿中以ng/100 mg為單位的CB2RA組合物的濃度。結果以平均值±SEM表示。使用具有Tukey事後檢驗之雙向方差分析評估統計差異。* p < 0.05,** p < 0.01,*** p < 0.001。
圖 30為條形圖,顯示在用CB2RA調配物最終給藥後6小時收集之眼後勻漿中以ng/100 mg為單位的CB2RA組合物的濃度。結果以平均值±SEM表示。使用具有Tukey事後檢驗之雙向方差分析評估統計差異。* p < 0.05,** p < 0.01,*** p < 0.001。
Claims (78)
- 如請求項1之組合物,其中該組合物包含重量比為99.85:0.15至93.5:6.5之該式I化合物及該式II化合物,及醫藥學上可接受之賦形劑。
- 如請求項2之組合物,其中該式I化合物與該式II化合物之重量比為99.8:0.2至98.2:1.8。
- 如請求項2之組合物,其中該式I化合物與該式II化合物之重量比為98.8:1.2至98.4:1.6。
- 如請求項4之組合物,其中該式I化合物與該式II化合物之重量比為99.3:0.7至98.7:1.3。
- 如請求項5之組合物,其中該式I化合物與該式II化合物之重量比為約99:1。
- 如請求項1至6中任一項之組合物,其中該醫藥學上可接受之賦形劑包含聚合物、增溶劑、緩衝劑、鹽、防腐劑或其組合。
- 如請求項7之組合物,其中該聚合物為聚乙烯吡咯啶酮-聚乳酸(PVP-PLA)共聚物。
- 如請求項7至9中任一項之組合物,其中該緩衝劑為磷酸鹽緩衝劑。
- 如請求項7至8中任一項之組合物,其中該鹽為鈉鹽或鉀鹽。
- 如請求項7至11中任一項之組合物,其中該組合物呈微胞製劑形式。
- 如請求項12之組合物,其中該微胞製劑呈液體形式。
- 如請求項12之組合物,其中該微胞製劑脫水成固體形式(例如凍乾或噴霧乾燥的固體)。
- 如請求項14之組合物,其中該組合物包含約0.25%(w/w)至約60%(w/w)、約0.5%(w/w)至約40%(w/w)、或約0.75%(w/w)至約30%或約1%(w/w)至約20%(w/w)之該等第一及第二化合物之組合。
- 如請求項7至15中任一項之組合物,其中該組合物包含約5重量%至約95重量%、或30重量%至約90重量%、或約60重量%至約85重量%或約70重量%至約80重量%之該聚合物。
- 如請求項7至12或13至15中任一項之組合物,其中該組合物包含約1重量%至約20重量%之該緩衝劑。
- 如請求項7至13或15至17中任一項之組合物,其中該組合物進一步包含乳化劑、抗氧化劑、控制釋放劑、潤滑劑或調味劑。
- 如請求項13之組合物,其中該固體形式已在溶劑中再水合以產生微胞溶液。
- 如請求項19之組合物,其中該溶劑為水(例如WFI)、醇、右旋糖溶液(例如5%右旋糖溶液)或生理鹽水。
- 如請求項19或20之組合物,其中該等第一及第二化合物之組合濃度為約0.5 mg/mL至約15 mg/mL。
- 如請求項19至21中任一項之組合物,其中該組合物之pH值為約5至約9、約6至約8或約6.5至約7.5,及/或黏度在約0.2 mPas至約80,000 mPas範圍內。
- 如請求項21至22中任一項之組合物,其中該微胞溶液包含粒度(Z.av)為12-50 nm、15-45 nm或20-40 nm之粒子。
- 如請求項21至23中任一項之組合物,其中該等粒子之多分散性指數(PDi)為約0.05至約0.15。
- 如請求項1至24中任一項之組合物,其中該組合物進一步包含0.015%至1.5%之第三或第四化合物。
- 如請求項26之組合物,其包含至多13% wt/wt之該雜質,較佳至多10% wt/wt、更佳至多5% wt/wt、更佳至多2% wt/wt、更佳至多1% wt/wt、更佳至多0.1% wt/wt、更佳至多0.01% wt/wt、更佳至多0.001% wt/wt之該雜質。
- 如請求項26或27之組合物,其進一步包含用於減少該雜質形成之抗氧化劑。
- 如請求項28之組合物,其中該抗氧化劑係選自由以下組成之群:抗壞血酸、丁基化羥基甲苯、芝麻酚、愈創木樹脂、甲硫胺酸、檸檬酸、酒石酸、磷酸、硫醇衍生物、偏亞硫酸氫鉀、抗壞血酸棕櫚酸酯、硬脂酸鈣、沒食子酸丙酯、硫代硫酸鈉、麩胱甘肽、二羥基苯甲酸、苯甲酸、尿酸鹽及尿酸、山梨酸、苯甲酸鈉、EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
- 如請求項28之組合物,其中該抗氧化劑係選自由以下組成之群:EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
- 如請求項28之組合物,其中該抗氧化劑包含丁基化羥基大茴香醚。
- 如請求項1至31中任一項之組合物,其基本上不含氧。
- 一種醫藥組合物,其包含如請求項1至25中任一項之組合物及醫藥學上有效量之非類固醇消炎藥(NSAID)及/或類固醇。
- 如請求項33之醫藥組合物,其中該NSAID為溴芬酸、奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、酮咯酸或塞來昔布。
- 如請求項34之醫藥組合物,其中該NSAID為塞來昔布。
- 如請求項33至35中任一項之醫藥組合物,其中該類固醇為皮質類固醇。
- 如請求項36之醫藥組合物,其中該皮質類固醇為地塞米松氯替潑諾、依碳氯替潑諾、丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸酯、曲安奈德氟西奈德、地塞米松氯替潑諾依碳酸氯替潑諾、二丙酸阿氯米松、地奈德或氫化可的松。
- 如請求項33至37中任一項之醫藥組合物,其中該等第一及第二化合物及該NSAID及/或類固醇調配成單一劑型。
- 如請求項39之醫藥組合物,其包含至多13% wt/wt之該雜質,較佳至多10% wt/wt、更佳至多5% wt/wt、更佳至多2% wt/wt、更佳至多1% wt/wt、更佳至多0.1% wt/wt、更佳至多0.01% wt/wt、更佳至多0.001% wt/wt之該雜質。
- 如請求項39或40之醫藥組合物,其進一步包含用於減少該雜質形成之抗氧化劑。
- 如請求項41之醫藥組合物,其中該抗氧化劑係選自由以下組成之群:抗壞血酸、丁基化羥基甲苯、芝麻酚、愈創木樹脂、甲硫胺酸、檸檬酸、酒石酸、磷酸、硫醇衍生物、偏亞硫酸氫鉀、抗壞血酸棕櫚酸酯、硬脂酸鈣、沒食子酸丙酯、硫代硫酸鈉、麩胱甘肽、二羥基苯甲酸、苯甲酸、尿酸鹽及尿酸、山梨酸、苯甲酸鈉、EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
- 如請求項41之醫藥組合物,其中該抗氧化劑係選自由以下組成之群:EDTA、亞硫酸氫鈉、維生素E、半胱胺酸鹽酸鹽、山梨糖醇、丁基化羥基大茴香醚及其混合物。
- 如請求項41之醫藥組合物,其中該抗氧化劑包含丁基化羥基大茴香醚。
- 如請求項39至44中任一項之醫藥組合物,其基本上不含氧。
- 一種如請求項1至32中任一項之組合物或如請求項33至45中任一項之醫藥組合物的用途,其用於製備供治療個體之炎症或疼痛用的藥物。
- 如請求項45之用途,其中該炎症或該疼痛為慢性疼痛或急性疼痛。
- 如請求項46或47之用途,其中該疼痛為急性疼痛。
- 如請求項46至48中任一項之用途,其中該炎症或疼痛為眼部炎症或眼部疼痛。
- 如請求項46至49中任一項之用途,其中該炎症或疼痛為術後炎症或術後疼痛。
- 如請求項49或50之用途,其中該炎症或疼痛與角膜創傷(例如角膜手術或損傷)相關。
- 如請求項49之用途,其中該眼部炎症為乾性AMD相關之視網膜炎症。
- 一種如請求項1至32中任一項之組合物或如請求項33至45中任一項之醫藥組合物的用途,其用於製備供治療或預防個體之年齡相關性黃斑變性(AMD)用的藥物。
- 如請求項53之用途,其中該AMD為濕性AMD。
- 如請求項53之用途,其中該AMD為乾性AMD。
- 一種如請求項1至32中任一項之組合物或如請求項33至45中任一項之醫藥組合物的用途,其用於製備供治療或預防個體之血管生成用的藥物。
- 如請求項56之用途,其中該血管生成為眼部血管生成。
- 如請求項57之用途,其中該眼部血管生成為視網膜血管生成。
- 如請求項58之用途,其中該視網膜血管生成為濕性AMD相關之血管生成。
- 一種如請求項1至32中任一項之組合物或如請求項33至45中任一項之醫藥組合物的用途,其用於製備供促進個體之傷口癒合用的藥物。
- 如請求項60之用途,其中該傷口癒合為眼部傷口癒合。
- 如請求項61之用途,其中該眼部傷口癒合為角膜傷口癒合。
- 如請求項61之用途,其中該眼部傷口癒合為術後眼部傷口癒合。
- 一種如請求項1至32中任一項之組合物或如請求項33至45中任一項之醫藥組合物的用途,其用於製備供預防或治療個體之乾眼症候群用的藥物。
- 如請求項46至65中任一項之用途,其中該藥物經調配以用於腹膜內使用、局部使用、經口使用、舌下使用、經頰使用、靜脈內使用、肌肉內使用、皮下使用、鞘內使用、經耳使用、經皮使用、鼻內使用、唇下使用、經肺使用、顱內使用、腦室內使用、陰道內使用、經直腸使用、皮膚使用、腸內使用、眼周使用、玻璃體內使用或結膜下使用。
- 一種如請求項1至31中任一項之組合物或如請求項33至45中任一項之醫藥組合物的用途,其用於製備供提高NSAID之治療功效用的藥物。
- 如請求項67之用途,其中該NSAID為溴芬酸、奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、酮咯酸或塞來昔布。
- 如請求項68之用途,其中該NSAID為塞來昔布。
- 如請求項46至66中任一項之用途,其中該藥物與非類固醇消炎藥(NSAID)及/或類固醇一起使用。
- 如請求項70之用途,其中該NSAID係選自奈帕芬胺、阿司匹林、萘普生、雙氯芬酸、溴芬酸、美洛昔康、布洛芬、酮洛芬、吲哚美辛、吡羅昔康、依託度酸、氟比洛芬、乙醯胺酚、溴芬酸、酮咯酸或塞來昔布。
- 如請求項71之用途,其中該NSAID為塞來昔布。
- 如請求項70之用途,其中該類固醇為皮質類固醇或糖皮質類固醇。
- 如請求項73之用途,其中該皮質類固醇為地塞米松、潑尼松龍氯替潑諾、氟輕鬆、氟米龍、二氟潑尼酯、曲安西龍或利美索龍。
- 如請求項73之用途,其中該糖皮質類固醇為丙酸倍氯松、丙酸鹵倍他索、氟西奈德、二乙酸二氟拉松、去羥米松、特戊酸氯可托龍、糠酸莫米松、曲安奈德、戊酸倍他米松、丙酸氟替卡松、潑尼卡酯、丙丁酸酯、曲安奈德氟西奈德、依碳酸氯替潑諾、二丙酸阿氯米松、地奈德或氫化可的松。
- 如請求項46至75中任一項之用途,其中該NSAID及/或類固醇在該藥物之前、同時或之後使用。
- 如請求項66至76中任一項之用途,其中該藥物與該NSAID及/或類固醇組合協同地減輕炎症及/或疼痛。
- 如請求項77之用途,其中該NSAID為塞來昔布。
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063068737P | 2020-08-21 | 2020-08-21 | |
| US63/068,737 | 2020-08-21 | ||
| US202063087038P | 2020-10-02 | 2020-10-02 | |
| US63/087,038 | 2020-10-02 | ||
| US202163191107P | 2021-05-20 | 2021-05-20 | |
| US63/191,107 | 2021-05-20 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202227042A true TW202227042A (zh) | 2022-07-16 |
Family
ID=80322338
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW110130884A TW202227042A (zh) | 2020-08-21 | 2021-08-20 | 雙重鎮痛/消炎組合物、組合及其使用方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20240016762A1 (zh) |
| EP (1) | EP4199916A4 (zh) |
| CA (1) | CA3171726C (zh) |
| TW (1) | TW202227042A (zh) |
| WO (1) | WO2022036455A1 (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024256505A1 (en) * | 2023-06-15 | 2024-12-19 | F. Hoffmann-La Roche Ag | Cannabinoid receptor 2 modulators |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL132661A (en) * | 1999-10-31 | 2008-11-26 | Raphael Mechoulam | Agonists specific for peripheral cannabinoid receptors |
| WO2006111424A1 (en) * | 2005-04-22 | 2006-10-26 | Life & Brain Gmbh | Methods for identifying modulators of cb1 and cb2 cannabinoid receptors and their use in wound healing |
| WO2010041253A1 (en) * | 2008-10-06 | 2010-04-15 | Yissum Research Development Company Of The Hebrew University Of Jerusalem, Ltd. | Compositions comprising cb receptor agonists, uses thereof and methods for their preparation |
| CA2931039C (en) * | 2013-11-20 | 2022-07-12 | Mary Lynch | Compositions and methods for treatment of ocular inflammation and pain |
| EP3302464A4 (en) * | 2015-05-27 | 2019-01-23 | Mary Lynch | USE OF CANNABINOIDS FOR THE TREATMENT OF EYE IGNITIONS AND / OR PAIN |
| GB2561009B (en) * | 2017-03-31 | 2020-05-13 | Altus Formulation Inc | Non-ionic PVP-PLA block copolymers and pharmaceutical compositions derived therefrom |
-
2021
- 2021-08-19 WO PCT/CA2021/051152 patent/WO2022036455A1/en not_active Ceased
- 2021-08-19 EP EP21857090.1A patent/EP4199916A4/en active Pending
- 2021-08-19 CA CA3171726A patent/CA3171726C/en active Active
- 2021-08-19 US US18/042,145 patent/US20240016762A1/en active Pending
- 2021-08-20 TW TW110130884A patent/TW202227042A/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| US20240016762A1 (en) | 2024-01-18 |
| CA3171726A1 (en) | 2022-02-24 |
| CA3171726C (en) | 2025-05-13 |
| WO2022036455A1 (en) | 2022-02-24 |
| EP4199916A4 (en) | 2024-08-28 |
| WO2022036455A9 (en) | 2024-10-10 |
| EP4199916A1 (en) | 2023-06-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US12521448B2 (en) | Preparation of solid cyclodextrin complexes for ophthalmic active pharmaceutical ingredient delivery | |
| JP2019034947A (ja) | 眼疾患を予防または治療するための方法および組成物 | |
| AU2015257651A1 (en) | Compounds for treating ophthalmic diseases and disorders | |
| JP2008514645A (ja) | 眼疾患およびその他の疾患の局所的処置のためのcaiに基づくシステムおよび方法 | |
| CN105073112B (zh) | 睑板腺功能障碍的治疗剂 | |
| KR102578102B1 (ko) | 엔도텔린 수용체 길항제의 국소 안용 제형 | |
| CA3171726C (en) | DUAL ANALGESIC-ANTI-INFLAMMATORY COMPOSITIONS, COMBINATIONS AND RELATED METHODS OF USE | |
| JP2011144111A (ja) | 軸性近視の予防または治療剤 | |
| JP6271539B2 (ja) | バクロフェン及びアカンプロセートに基づいた黄斑変性疾患の治療法 | |
| Golmohammadi et al. | A comprehensive review of the effects of tacrolimus (FK-506) on dry eye disease (DED): Focus on inflammation | |
| HK40097477A (zh) | 用於眼用药物递送的环糊精纳米颗粒的制备 |