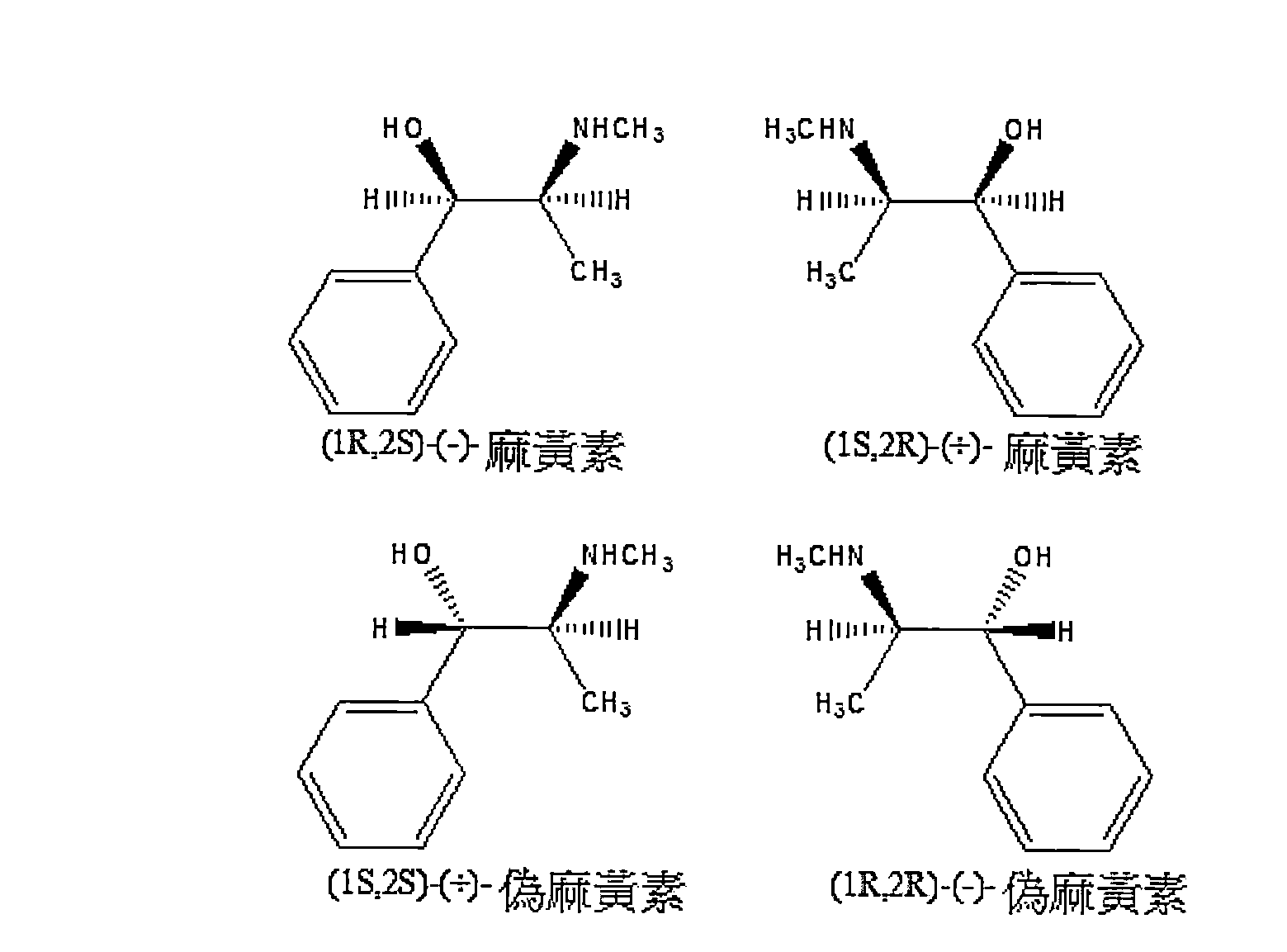
TW202002957A - 包含轉化抑制劑之麻黃素及其衍生物之抗損壞調配物 - Google Patents
包含轉化抑制劑之麻黃素及其衍生物之抗損壞調配物 Download PDFInfo
- Publication number
- TW202002957A TW202002957A TW108103594A TW108103594A TW202002957A TW 202002957 A TW202002957 A TW 202002957A TW 108103594 A TW108103594 A TW 108103594A TW 108103594 A TW108103594 A TW 108103594A TW 202002957 A TW202002957 A TW 202002957A
- Authority
- TW
- Taiwan
- Prior art keywords
- dosage form
- pharmaceutical dosage
- group
- form according
- combination
- Prior art date
Links
- KWGRBVOPPLSCSI-WPRPVWTQSA-N (-)-ephedrine Chemical compound CN[C@@H](C)[C@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-WPRPVWTQSA-N 0.000 title claims abstract description 327
- KWGRBVOPPLSCSI-UHFFFAOYSA-N d-ephedrine Natural products CNC(C)C(O)C1=CC=CC=C1 KWGRBVOPPLSCSI-UHFFFAOYSA-N 0.000 title claims abstract description 250
- 229960002179 ephedrine Drugs 0.000 title claims abstract description 160
- 238000006243 chemical reaction Methods 0.000 title claims abstract description 127
- 239000003112 inhibitor Substances 0.000 title claims abstract description 92
- 239000000203 mixture Substances 0.000 title description 58
- 238000009472 formulation Methods 0.000 title description 13
- 239000002552 dosage form Substances 0.000 claims abstract description 465
- 229960003908 pseudoephedrine Drugs 0.000 claims abstract description 86
- KWGRBVOPPLSCSI-WCBMZHEXSA-N pseudoephedrine Chemical compound CN[C@@H](C)[C@@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-WCBMZHEXSA-N 0.000 claims abstract description 86
- 150000003839 salts Chemical class 0.000 claims abstract description 81
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 claims abstract description 55
- 229960001252 methamphetamine Drugs 0.000 claims abstract description 52
- 239000000126 substance Substances 0.000 claims abstract description 43
- 230000002401 inhibitory effect Effects 0.000 claims abstract description 5
- 238000000034 method Methods 0.000 claims description 60
- -1 fatty acid esters Chemical class 0.000 claims description 53
- 239000003963 antioxidant agent Substances 0.000 claims description 42
- 235000006708 antioxidants Nutrition 0.000 claims description 42
- 230000003078 antioxidant effect Effects 0.000 claims description 34
- 239000003795 chemical substances by application Substances 0.000 claims description 29
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 claims description 28
- 239000011159 matrix material Substances 0.000 claims description 28
- 229910052783 alkali metal Inorganic materials 0.000 claims description 22
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 22
- 239000003054 catalyst Substances 0.000 claims description 20
- QGZKDVFQNNGYKY-UHFFFAOYSA-N ammonia Natural products N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 claims description 19
- 230000002860 competitive effect Effects 0.000 claims description 18
- 150000001340 alkali metals Chemical class 0.000 claims description 17
- 235000013305 food Nutrition 0.000 claims description 17
- 239000002253 acid Substances 0.000 claims description 16
- 235000010323 ascorbic acid Nutrition 0.000 claims description 16
- 239000011668 ascorbic acid Substances 0.000 claims description 16
- 239000000576 food coloring agent Substances 0.000 claims description 14
- 150000001299 aldehydes Chemical class 0.000 claims description 12
- 229960005070 ascorbic acid Drugs 0.000 claims description 12
- 239000001656 lutein Substances 0.000 claims description 12
- 235000012680 lutein Nutrition 0.000 claims description 12
- KBPHJBAIARWVSC-RGZFRNHPSA-N lutein Chemical compound C([C@H](O)CC=1C)C(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\[C@H]1C(C)=C[C@H](O)CC1(C)C KBPHJBAIARWVSC-RGZFRNHPSA-N 0.000 claims description 12
- 238000005580 one pot reaction Methods 0.000 claims description 12
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 claims description 11
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 claims description 11
- 150000002148 esters Chemical class 0.000 claims description 11
- 229910052751 metal Inorganic materials 0.000 claims description 11
- 239000002184 metal Substances 0.000 claims description 11
- 239000002516 radical scavenger Substances 0.000 claims description 11
- 235000014113 dietary fatty acids Nutrition 0.000 claims description 10
- 239000000194 fatty acid Substances 0.000 claims description 10
- 229930195729 fatty acid Natural products 0.000 claims description 10
- 238000000338 in vitro Methods 0.000 claims description 10
- 229960005375 lutein Drugs 0.000 claims description 10
- ORAKUVXRZWMARG-WZLJTJAWSA-N lutein Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2C(=CC(O)CC2(C)C)C ORAKUVXRZWMARG-WZLJTJAWSA-N 0.000 claims description 10
- KBPHJBAIARWVSC-XQIHNALSSA-N trans-lutein Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CC(O)CC1(C)C)C=CC=C(/C)C=CC2C(=CC(O)CC2(C)C)C KBPHJBAIARWVSC-XQIHNALSSA-N 0.000 claims description 10
- FJHBOVDFOQMZRV-XQIHNALSSA-N xanthophyll Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CC(O)CC1(C)C)C=CC=C(/C)C=CC2C=C(C)C(O)CC2(C)C FJHBOVDFOQMZRV-XQIHNALSSA-N 0.000 claims description 10
- 150000001450 anions Chemical class 0.000 claims description 9
- 235000019804 chlorophyll Nutrition 0.000 claims description 9
- 229930002875 chlorophyll Natural products 0.000 claims description 9
- 150000001875 compounds Chemical class 0.000 claims description 9
- MWOOGOJBHIARFG-UHFFFAOYSA-N vanillin Chemical compound COC1=CC(C=O)=CC=C1O MWOOGOJBHIARFG-UHFFFAOYSA-N 0.000 claims description 9
- FGQOOHJZONJGDT-UHFFFAOYSA-N vanillin Natural products COC1=CC(O)=CC(C=O)=C1 FGQOOHJZONJGDT-UHFFFAOYSA-N 0.000 claims description 9
- 235000012141 vanillin Nutrition 0.000 claims description 9
- VTLYFUHAOXGGBS-UHFFFAOYSA-N Fe3+ Chemical class [Fe+3] VTLYFUHAOXGGBS-UHFFFAOYSA-N 0.000 claims description 8
- 150000001323 aldoses Chemical class 0.000 claims description 8
- 230000015572 biosynthetic process Effects 0.000 claims description 8
- 150000001733 carboxylic acid esters Chemical class 0.000 claims description 8
- 235000021466 carotenoid Nutrition 0.000 claims description 8
- 150000001747 carotenoids Chemical class 0.000 claims description 8
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical class OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 claims description 8
- 150000002500 ions Chemical class 0.000 claims description 8
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 claims description 7
- 229910021529 ammonia Inorganic materials 0.000 claims description 7
- ATNHDLDRLWWWCB-AENOIHSZSA-M chlorophyll a Chemical compound C1([C@@H](C(=O)OC)C(=O)C2=C3C)=C2N2C3=CC(C(CC)=C3C)=[N+]4C3=CC3=C(C=C)C(C)=C5N3[Mg-2]42[N+]2=C1[C@@H](CCC(=O)OC\C=C(/C)CCC[C@H](C)CCC[C@H](C)CCCC(C)C)[C@H](C)C2=C5 ATNHDLDRLWWWCB-AENOIHSZSA-M 0.000 claims description 7
- 150000002989 phenols Chemical class 0.000 claims description 7
- 235000020944 retinol Nutrition 0.000 claims description 7
- 239000011607 retinol Substances 0.000 claims description 7
- 229960003471 retinol Drugs 0.000 claims description 7
- 238000006027 Birch reduction reaction Methods 0.000 claims description 6
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 claims description 6
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 6
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 claims description 6
- RRHGJUQNOFWUDK-UHFFFAOYSA-N Isoprene Chemical compound CC(=C)C=C RRHGJUQNOFWUDK-UHFFFAOYSA-N 0.000 claims description 6
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 claims description 6
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 claims description 6
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 claims description 6
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 claims description 6
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 claims description 6
- 239000012442 inert solvent Substances 0.000 claims description 6
- 150000003254 radicals Chemical class 0.000 claims description 6
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 claims description 5
- 229940123457 Free radical scavenger Drugs 0.000 claims description 5
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 claims description 5
- 150000001350 alkyl halides Chemical class 0.000 claims description 5
- 235000010208 anthocyanin Nutrition 0.000 claims description 5
- 239000004410 anthocyanin Substances 0.000 claims description 5
- 229930002877 anthocyanin Natural products 0.000 claims description 5
- 150000004636 anthocyanins Chemical class 0.000 claims description 5
- 239000000987 azo dye Substances 0.000 claims description 5
- 235000003599 food sweetener Nutrition 0.000 claims description 5
- 239000007788 liquid Substances 0.000 claims description 5
- 239000002773 nucleotide Substances 0.000 claims description 5
- 125000003729 nucleotide group Chemical group 0.000 claims description 5
- 235000019204 saccharin Nutrition 0.000 claims description 5
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 claims description 5
- 239000003765 sweetening agent Substances 0.000 claims description 5
- 150000003573 thiols Chemical class 0.000 claims description 5
- 229930003799 tocopherol Natural products 0.000 claims description 5
- 239000011732 tocopherol Substances 0.000 claims description 5
- 150000003611 tocopherol derivatives Chemical class 0.000 claims description 5
- 239000004384 Neotame Substances 0.000 claims description 4
- 150000001868 cobalt Chemical class 0.000 claims description 4
- 150000002696 manganese Chemical class 0.000 claims description 4
- 235000010434 neohesperidine DC Nutrition 0.000 claims description 4
- 235000019412 neotame Nutrition 0.000 claims description 4
- 150000002815 nickel Chemical class 0.000 claims description 4
- 230000037361 pathway Effects 0.000 claims description 4
- 230000001376 precipitating effect Effects 0.000 claims description 4
- 229930192474 thiophene Natural products 0.000 claims description 4
- PMJHHCWVYXUKFD-SNAWJCMRSA-N (E)-1,3-pentadiene Chemical group C\C=C\C=C PMJHHCWVYXUKFD-SNAWJCMRSA-N 0.000 claims description 3
- OGYGFUAIIOPWQD-UHFFFAOYSA-N 1,3-thiazolidine Chemical compound C1CSCN1 OGYGFUAIIOPWQD-UHFFFAOYSA-N 0.000 claims description 3
- SDJHPPZKZZWAKF-UHFFFAOYSA-N 2,3-dimethylbuta-1,3-diene Chemical compound CC(=C)C(C)=C SDJHPPZKZZWAKF-UHFFFAOYSA-N 0.000 claims description 3
- IMSODMZESSGVBE-UHFFFAOYSA-N 2-Oxazoline Chemical compound C1CN=CO1 IMSODMZESSGVBE-UHFFFAOYSA-N 0.000 claims description 3
- JLBJTVDPSNHSKJ-UHFFFAOYSA-N 4-Methylstyrene Chemical compound CC1=CC=C(C=C)C=C1 JLBJTVDPSNHSKJ-UHFFFAOYSA-N 0.000 claims description 3
- 229920000858 Cyclodextrin Polymers 0.000 claims description 3
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 claims description 3
- 229910000288 alkali metal carbonate Inorganic materials 0.000 claims description 3
- 150000008041 alkali metal carbonates Chemical class 0.000 claims description 3
- 229910000318 alkali metal phosphate Inorganic materials 0.000 claims description 3
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 claims description 3
- 239000008139 complexing agent Substances 0.000 claims description 3
- 239000002131 composite material Substances 0.000 claims description 3
- 238000009833 condensation Methods 0.000 claims description 3
- 230000005494 condensation Effects 0.000 claims description 3
- 150000003983 crown ethers Chemical class 0.000 claims description 3
- 239000002739 cryptand Substances 0.000 claims description 3
- CJSBUWDGPXGFGA-UHFFFAOYSA-N dimethyl-butadiene Natural products CC(C)=CC=C CJSBUWDGPXGFGA-UHFFFAOYSA-N 0.000 claims description 3
- AHAREKHAZNPPMI-UHFFFAOYSA-N hexa-1,3-diene Chemical compound CCC=CC=C AHAREKHAZNPPMI-UHFFFAOYSA-N 0.000 claims description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 3
- 150000002527 isonitriles Chemical class 0.000 claims description 3
- 125000005498 phthalate group Chemical class 0.000 claims description 3
- PMJHHCWVYXUKFD-UHFFFAOYSA-N piperylene Natural products CC=CC=C PMJHHCWVYXUKFD-UHFFFAOYSA-N 0.000 claims description 3
- 239000005076 polymer ester Substances 0.000 claims description 3
- 150000004609 retinol derivatives Chemical class 0.000 claims description 3
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical group C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 claims description 3
- 229940081974 saccharin Drugs 0.000 claims description 3
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 claims description 3
- LSNNMFCWUKXFEE-UHFFFAOYSA-L sulfite Chemical class [O-]S([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-L 0.000 claims description 3
- YTKBWWKAVMSYHE-OALUTQOASA-N (3s)-3-[3-(3-hydroxy-4-methoxyphenyl)propylamino]-4-[[(2s)-1-methoxy-1-oxo-3-phenylpropan-2-yl]amino]-4-oxobutanoic acid Chemical compound C([C@@H](C(=O)OC)NC(=O)[C@H](CC(O)=O)NCCCC=1C=C(O)C(OC)=CC=1)C1=CC=CC=C1 YTKBWWKAVMSYHE-OALUTQOASA-N 0.000 claims description 2
- NLMDJJTUQPXZFG-UHFFFAOYSA-N 1,4,10,13-tetraoxa-7,16-diazacyclooctadecane Chemical compound C1COCCOCCNCCOCCOCCN1 NLMDJJTUQPXZFG-UHFFFAOYSA-N 0.000 claims description 2
- 239000004394 Advantame Substances 0.000 claims description 2
- 238000006820 Bouveault-Blanc reduction reaction Methods 0.000 claims description 2
- 239000001329 FEMA 3811 Substances 0.000 claims description 2
- 108010093901 N-(N-(3-(3-hydroxy-4-methoxyphenyl) propyl)-alpha-aspartyl)-L-phenylalanine 1-methyl ester Proteins 0.000 claims description 2
- 235000019453 advantame Nutrition 0.000 claims description 2
- 150000001558 benzoic acid derivatives Chemical group 0.000 claims description 2
- 239000003446 ligand Substances 0.000 claims description 2
- ITVGXXMINPYUHD-CUVHLRMHSA-N neohesperidin dihydrochalcone Chemical compound C1=C(O)C(OC)=CC=C1CCC(=O)C(C(=C1)O)=C(O)C=C1O[C@H]1[C@H](O[C@H]2[C@@H]([C@H](O)[C@@H](O)[C@H](C)O2)O)[C@@H](O)[C@H](O)[C@@H](CO)O1 ITVGXXMINPYUHD-CUVHLRMHSA-N 0.000 claims description 2
- 229940089953 neohesperidin dihydrochalcone Drugs 0.000 claims description 2
- HLIAVLHNDJUHFG-HOTGVXAUSA-N neotame Chemical compound CC(C)(C)CCN[C@@H](CC(O)=O)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 HLIAVLHNDJUHFG-HOTGVXAUSA-N 0.000 claims description 2
- 108010070257 neotame Proteins 0.000 claims description 2
- 125000002640 tocopherol group Chemical class 0.000 claims description 2
- 108010011485 Aspartame Proteins 0.000 claims 1
- 125000003289 ascorbyl group Chemical class [H]O[C@@]([H])(C([H])([H])O*)[C@@]1([H])OC(=O)C(O*)=C1O* 0.000 claims 1
- 239000000605 aspartame Substances 0.000 claims 1
- 235000010357 aspartame Nutrition 0.000 claims 1
- 229960003438 aspartame Drugs 0.000 claims 1
- 235000019149 tocopherols Nutrition 0.000 claims 1
- 229920002785 Croscarmellose sodium Polymers 0.000 description 88
- 229920003086 cellulose ether Polymers 0.000 description 68
- 239000011230 binding agent Substances 0.000 description 62
- 229920006037 cross link polymer Polymers 0.000 description 62
- 239000001767 crosslinked sodium carboxy methyl cellulose Substances 0.000 description 53
- VJHCJDRQFCCTHL-UHFFFAOYSA-N acetic acid 2,3,4,5,6-pentahydroxyhexanal Chemical compound CC(O)=O.OCC(O)C(O)C(O)C(O)C=O VJHCJDRQFCCTHL-UHFFFAOYSA-N 0.000 description 52
- 229960005168 croscarmellose Drugs 0.000 description 51
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 48
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 48
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 48
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 48
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 47
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 47
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 47
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 41
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 36
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 35
- 229960001681 croscarmellose sodium Drugs 0.000 description 34
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 24
- 239000007937 lozenge Substances 0.000 description 24
- 229920000642 polymer Polymers 0.000 description 23
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 22
- 235000004835 α-tocopherol Nutrition 0.000 description 22
- 239000002076 α-tocopherol Substances 0.000 description 22
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 20
- 229940087168 alpha tocopherol Drugs 0.000 description 20
- 238000001125 extrusion Methods 0.000 description 20
- 229960000984 tocofersolan Drugs 0.000 description 20
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 18
- 238000000576 coating method Methods 0.000 description 18
- 239000011248 coating agent Substances 0.000 description 16
- 239000002245 particle Substances 0.000 description 16
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 16
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 15
- 230000003111 delayed effect Effects 0.000 description 15
- 239000007888 film coating Substances 0.000 description 15
- 238000009501 film coating Methods 0.000 description 15
- 238000004519 manufacturing process Methods 0.000 description 15
- 239000011734 sodium Substances 0.000 description 15
- 229910052708 sodium Inorganic materials 0.000 description 15
- 229920002678 cellulose Polymers 0.000 description 13
- 239000003826 tablet Substances 0.000 description 13
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 12
- 239000001913 cellulose Substances 0.000 description 12
- 235000010980 cellulose Nutrition 0.000 description 12
- 239000002831 pharmacologic agent Substances 0.000 description 12
- 239000004480 active ingredient Substances 0.000 description 11
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 11
- 239000000463 material Substances 0.000 description 11
- 239000000049 pigment Substances 0.000 description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 10
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 10
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 10
- 229930182470 glycoside Natural products 0.000 description 10
- 150000002338 glycosides Chemical class 0.000 description 10
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 10
- 239000000047 product Substances 0.000 description 10
- 230000009467 reduction Effects 0.000 description 10
- 238000006722 reduction reaction Methods 0.000 description 10
- JPIJQSOTBSSVTP-PWNYCUMCSA-N D-erythronic acid Chemical class OC[C@@H](O)[C@@H](O)C(O)=O JPIJQSOTBSSVTP-PWNYCUMCSA-N 0.000 description 9
- 239000003814 drug Substances 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- AUNGANRZJHBGPY-SCRDCRAPSA-N Riboflavin Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-SCRDCRAPSA-N 0.000 description 8
- 230000006378 damage Effects 0.000 description 8
- 235000002864 food coloring agent Nutrition 0.000 description 8
- 239000000543 intermediate Substances 0.000 description 8
- HCZKYJDFEPMADG-TXEJJXNPSA-N masoprocol Chemical compound C([C@H](C)[C@H](C)CC=1C=C(O)C(O)=CC=1)C1=CC=C(O)C(O)=C1 HCZKYJDFEPMADG-TXEJJXNPSA-N 0.000 description 8
- 238000005259 measurement Methods 0.000 description 8
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 7
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 7
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 7
- 206010028735 Nasal congestion Diseases 0.000 description 7
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 7
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 7
- 239000002775 capsule Substances 0.000 description 7
- 238000013270 controlled release Methods 0.000 description 7
- 235000010228 ethyl p-hydroxybenzoate Nutrition 0.000 description 7
- 239000004403 ethyl p-hydroxybenzoate Substances 0.000 description 7
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 7
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 7
- 239000004615 ingredient Substances 0.000 description 7
- 229910052744 lithium Inorganic materials 0.000 description 7
- 230000001953 sensory effect Effects 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Polymers OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 6
- 206010030113 Oedema Diseases 0.000 description 6
- 239000000150 Sympathomimetic Substances 0.000 description 6
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 6
- 239000001768 carboxy methyl cellulose Substances 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 239000011362 coarse particle Substances 0.000 description 6
- 208000027744 congestion Diseases 0.000 description 6
- 229920001577 copolymer Polymers 0.000 description 6
- 235000010386 dodecyl gallate Nutrition 0.000 description 6
- 238000000605 extraction Methods 0.000 description 6
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 6
- 239000004014 plasticizer Substances 0.000 description 6
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 6
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 6
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 6
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical compound [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 6
- 235000010384 tocopherol Nutrition 0.000 description 6
- 101100004280 Caenorhabditis elegans best-2 gene Proteins 0.000 description 5
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 5
- CWYNVVGOOAEACU-UHFFFAOYSA-N Fe2+ Chemical class [Fe+2] CWYNVVGOOAEACU-UHFFFAOYSA-N 0.000 description 5
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 5
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 5
- 239000004372 Polyvinyl alcohol Substances 0.000 description 5
- 239000013543 active substance Substances 0.000 description 5
- 150000001412 amines Chemical class 0.000 description 5
- 229940050390 benzoate Drugs 0.000 description 5
- 239000003638 chemical reducing agent Substances 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 208000035475 disorder Diseases 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 229960001617 ethyl hydroxybenzoate Drugs 0.000 description 5
- NUVBSKCKDOMJSU-UHFFFAOYSA-N ethylparaben Chemical compound CCOC(=O)C1=CC=C(O)C=C1 NUVBSKCKDOMJSU-UHFFFAOYSA-N 0.000 description 5
- 239000000284 extract Substances 0.000 description 5
- 150000004665 fatty acids Chemical class 0.000 description 5
- 238000000227 grinding Methods 0.000 description 5
- 238000009474 hot melt extrusion Methods 0.000 description 5
- 229920000609 methyl cellulose Polymers 0.000 description 5
- 239000001923 methylcellulose Substances 0.000 description 5
- 235000010981 methylcellulose Nutrition 0.000 description 5
- 229920002451 polyvinyl alcohol Polymers 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 238000003825 pressing Methods 0.000 description 5
- BALXUFOVQVENIU-KXNXZCPBSA-N pseudoephedrine hydrochloride Chemical compound [H+].[Cl-].CN[C@@H](C)[C@@H](O)C1=CC=CC=C1 BALXUFOVQVENIU-KXNXZCPBSA-N 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- 230000001975 sympathomimetic effect Effects 0.000 description 5
- 230000001225 therapeutic effect Effects 0.000 description 5
- 238000003856 thermoforming Methods 0.000 description 5
- DBZAKQWXICEWNW-UHFFFAOYSA-N 2-acetylpyrazine Chemical compound CC(=O)C1=CN=CC=N1 DBZAKQWXICEWNW-UHFFFAOYSA-N 0.000 description 4
- UXFSPRAGHGMRSQ-UHFFFAOYSA-N 3-isobutyl-2-methoxypyrazine Chemical compound COC1=NC=CN=C1CC(C)C UXFSPRAGHGMRSQ-UHFFFAOYSA-N 0.000 description 4
- 239000004261 Ascorbyl stearate Substances 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 239000004255 Butylated hydroxyanisole Substances 0.000 description 4
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 4
- ZAKOWWREFLAJOT-UHFFFAOYSA-N DL-alpha-tocopherylacetate Chemical compound CC(=O)OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C ZAKOWWREFLAJOT-UHFFFAOYSA-N 0.000 description 4
- RPWFJAMTCNSJKK-UHFFFAOYSA-N Dodecyl gallate Chemical compound CCCCCCCCCCCCOC(=O)C1=CC(O)=C(O)C(O)=C1 RPWFJAMTCNSJKK-UHFFFAOYSA-N 0.000 description 4
- 239000001856 Ethyl cellulose Substances 0.000 description 4
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 4
- 239000004262 Ethyl gallate Substances 0.000 description 4
- HSRJKNPTNIJEKV-UHFFFAOYSA-N Guaifenesin Chemical compound COC1=CC=CC=C1OCC(O)CO HSRJKNPTNIJEKV-UHFFFAOYSA-N 0.000 description 4
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 4
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 4
- 150000000996 L-ascorbic acids Chemical class 0.000 description 4
- UPYKUZBSLRQECL-UKMVMLAPSA-N Lycopene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1C(=C)CCCC1(C)C)C=CC=C(/C)C=CC2C(=C)CCCC2(C)C UPYKUZBSLRQECL-UKMVMLAPSA-N 0.000 description 4
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 4
- 239000002202 Polyethylene glycol Substances 0.000 description 4
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 4
- 230000009471 action Effects 0.000 description 4
- 235000012741 allura red AC Nutrition 0.000 description 4
- 239000004191 allura red AC Substances 0.000 description 4
- 125000000129 anionic group Chemical group 0.000 description 4
- 235000010385 ascorbyl palmitate Nutrition 0.000 description 4
- 235000019276 ascorbyl stearate Nutrition 0.000 description 4
- 235000012733 azorubine Nutrition 0.000 description 4
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 4
- 235000019445 benzyl alcohol Nutrition 0.000 description 4
- 235000012745 brilliant blue FCF Nutrition 0.000 description 4
- 239000004161 brilliant blue FCF Substances 0.000 description 4
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 4
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 4
- 239000006227 byproduct Substances 0.000 description 4
- 235000010237 calcium benzoate Nutrition 0.000 description 4
- 239000004301 calcium benzoate Substances 0.000 description 4
- 235000010260 calcium hydrogen sulphite Nutrition 0.000 description 4
- 235000013893 calcium inosinate Nutrition 0.000 description 4
- 239000004197 calcium inosinate Substances 0.000 description 4
- 235000010261 calcium sulphite Nutrition 0.000 description 4
- YKPUWZUDDOIDPM-SOFGYWHQSA-N capsaicin Chemical compound COC1=CC(CNC(=O)CCCC\C=C\C(C)C)=CC=C1O YKPUWZUDDOIDPM-SOFGYWHQSA-N 0.000 description 4
- 239000004202 carbamide Substances 0.000 description 4
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 4
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 4
- 235000012730 carminic acid Nutrition 0.000 description 4
- 150000001768 cations Chemical class 0.000 description 4
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 4
- FLKPEMZONWLCSK-UHFFFAOYSA-N diethyl phthalate Chemical compound CCOC(=O)C1=CC=CC=C1C(=O)OCC FLKPEMZONWLCSK-UHFFFAOYSA-N 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 4
- 235000013898 dipotassium guanylate Nutrition 0.000 description 4
- 239000004192 dipotassium guanylate Substances 0.000 description 4
- 235000013892 dipotassium inosinate Nutrition 0.000 description 4
- 239000004195 dipotassium inosinate Substances 0.000 description 4
- 235000013888 disodium 5'-ribonucleotide Nutrition 0.000 description 4
- 239000004193 disodium 5'-ribonucleotide Substances 0.000 description 4
- 235000013896 disodium guanylate Nutrition 0.000 description 4
- 239000004198 disodium guanylate Substances 0.000 description 4
- 235000013890 disodium inosinate Nutrition 0.000 description 4
- 239000004194 disodium inosinate Substances 0.000 description 4
- 239000000555 dodecyl gallate Substances 0.000 description 4
- 235000010350 erythorbic acid Nutrition 0.000 description 4
- HCZKYJDFEPMADG-UHFFFAOYSA-N erythro-nordihydroguaiaretic acid Natural products C=1C=C(O)C(O)=CC=1CC(C)C(C)CC1=CC=C(O)C(O)=C1 HCZKYJDFEPMADG-UHFFFAOYSA-N 0.000 description 4
- 229920001249 ethyl cellulose Polymers 0.000 description 4
- 235000019325 ethyl cellulose Nutrition 0.000 description 4
- 235000019277 ethyl gallate Nutrition 0.000 description 4
- VFPFQHQNJCMNBZ-UHFFFAOYSA-N ethyl gallate Chemical compound CCOC(=O)C1=CC(O)=C(O)C(O)=C1 VFPFQHQNJCMNBZ-UHFFFAOYSA-N 0.000 description 4
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 4
- FVTCRASFADXXNN-SCRDCRAPSA-N flavin mononucleotide Chemical compound OP(=O)(O)OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O FVTCRASFADXXNN-SCRDCRAPSA-N 0.000 description 4
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 4
- 229960002146 guaifenesin Drugs 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- OROGSEYTTFOCAN-UHFFFAOYSA-N hydrocodone Natural products C1C(N(CCC234)C)C2C=CC(O)C3OC2=C4C1=CC=C2OC OROGSEYTTFOCAN-UHFFFAOYSA-N 0.000 description 4
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 4
- 229940031704 hydroxypropyl methylcellulose phthalate Drugs 0.000 description 4
- 229920003132 hydroxypropyl methylcellulose phthalate Polymers 0.000 description 4
- 239000012535 impurity Substances 0.000 description 4
- 235000012738 indigotine Nutrition 0.000 description 4
- 239000004179 indigotine Substances 0.000 description 4
- 235000013902 inosinic acid Nutrition 0.000 description 4
- 239000004245 inosinic acid Substances 0.000 description 4
- 235000012661 lycopene Nutrition 0.000 description 4
- 239000001751 lycopene Substances 0.000 description 4
- OAIJSZIZWZSQBC-GYZMGTAESA-N lycopene Chemical compound CC(C)=CCC\C(C)=C\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C=C(/C)CCC=C(C)C OAIJSZIZWZSQBC-GYZMGTAESA-N 0.000 description 4
- 229960003951 masoprocol Drugs 0.000 description 4
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- PJUIMOJAAPLTRJ-UHFFFAOYSA-N monothioglycerol Chemical compound OCC(O)CS PJUIMOJAAPLTRJ-UHFFFAOYSA-N 0.000 description 4
- 239000004570 mortar (masonry) Substances 0.000 description 4
- DCUJJWWUNKIJPH-UHFFFAOYSA-N nitrapyrin Chemical compound ClC1=CC=CC(C(Cl)(Cl)Cl)=N1 DCUJJWWUNKIJPH-UHFFFAOYSA-N 0.000 description 4
- 239000003960 organic solvent Substances 0.000 description 4
- 229960005489 paracetamol Drugs 0.000 description 4
- 229920003023 plastic Polymers 0.000 description 4
- 239000004033 plastic Substances 0.000 description 4
- 229920001223 polyethylene glycol Polymers 0.000 description 4
- 235000012731 ponceau 4R Nutrition 0.000 description 4
- 239000004175 ponceau 4R Substances 0.000 description 4
- 235000019275 potassium ascorbate Nutrition 0.000 description 4
- 235000010235 potassium benzoate Nutrition 0.000 description 4
- 239000004300 potassium benzoate Substances 0.000 description 4
- 235000019252 potassium sulphite Nutrition 0.000 description 4
- 229960003415 propylparaben Drugs 0.000 description 4
- 229960003447 pseudoephedrine hydrochloride Drugs 0.000 description 4
- 235000012752 quinoline yellow Nutrition 0.000 description 4
- 239000004172 quinoline yellow Substances 0.000 description 4
- 235000019192 riboflavin Nutrition 0.000 description 4
- 239000002151 riboflavin Substances 0.000 description 4
- 235000010378 sodium ascorbate Nutrition 0.000 description 4
- PPASLZSBLFJQEF-RKJRWTFHSA-M sodium ascorbate Substances [Na+].OC[C@@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RKJRWTFHSA-M 0.000 description 4
- 235000010234 sodium benzoate Nutrition 0.000 description 4
- 239000004299 sodium benzoate Substances 0.000 description 4
- 235000010268 sodium methyl p-hydroxybenzoate Nutrition 0.000 description 4
- 235000010265 sodium sulphite Nutrition 0.000 description 4
- 238000013268 sustained release Methods 0.000 description 4
- 235000012756 tartrazine Nutrition 0.000 description 4
- 239000004149 tartrazine Substances 0.000 description 4
- 229960001295 tocopherol Drugs 0.000 description 4
- WGVKWNUPNGFDFJ-DQCZWYHMSA-N β-tocopherol Chemical compound OC1=CC(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C WGVKWNUPNGFDFJ-DQCZWYHMSA-N 0.000 description 4
- CAVQBDOACNULDN-NRCOEFLKSA-N (1s,2s)-2-(methylamino)-1-phenylpropan-1-ol;sulfuric acid Chemical compound OS(O)(=O)=O.CN[C@@H](C)[C@@H](O)C1=CC=CC=C1.CN[C@@H](C)[C@@H](O)C1=CC=CC=C1 CAVQBDOACNULDN-NRCOEFLKSA-N 0.000 description 3
- DKSZLDSPXIWGFO-BLOJGBSASA-N (4r,4ar,7s,7ar,12bs)-9-methoxy-3-methyl-2,4,4a,7,7a,13-hexahydro-1h-4,12-methanobenzofuro[3,2-e]isoquinoline-7-ol;phosphoric acid;hydrate Chemical compound O.OP(O)(O)=O.OP(O)(O)=O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC DKSZLDSPXIWGFO-BLOJGBSASA-N 0.000 description 3
- CIVCELMLGDGMKZ-UHFFFAOYSA-N 2,4-dichloro-6-methylpyridine-3-carboxylic acid Chemical compound CC1=CC(Cl)=C(C(O)=O)C(Cl)=N1 CIVCELMLGDGMKZ-UHFFFAOYSA-N 0.000 description 3
- 239000001803 2-(ethoxymethyl)pyrazine Substances 0.000 description 3
- WYUYEJNGHIOFOC-VVTVMFAVSA-N 2-[(z)-1-(4-methylphenyl)-3-pyrrolidin-1-ylprop-1-enyl]pyridine;hydrochloride Chemical compound Cl.C1=CC(C)=CC=C1C(\C=1N=CC=CC=1)=C\CN1CCCC1 WYUYEJNGHIOFOC-VVTVMFAVSA-N 0.000 description 3
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- ZKLPARSLTMPFCP-UHFFFAOYSA-N Cetirizine Chemical compound C1CN(CCOCC(=O)O)CCN1C(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-UHFFFAOYSA-N 0.000 description 3
- RRJFVPUCXDGFJB-UHFFFAOYSA-N Fexofenadine hydrochloride Chemical compound Cl.C1=CC(C(C)(C(O)=O)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 RRJFVPUCXDGFJB-UHFFFAOYSA-N 0.000 description 3
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 3
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 3
- 229910002651 NO3 Inorganic materials 0.000 description 3
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 3
- 241000206572 Rhodophyta Species 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- AQRHTGSVDQECPZ-UHFFFAOYSA-N azane;lithium Chemical compound [Li].N AQRHTGSVDQECPZ-UHFFFAOYSA-N 0.000 description 3
- 235000012677 beetroot red Nutrition 0.000 description 3
- 239000001654 beetroot red Substances 0.000 description 3
- 235000012709 brilliant black BN Nutrition 0.000 description 3
- 239000004126 brilliant black BN Substances 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 229960004415 codeine phosphate Drugs 0.000 description 3
- 229960000913 crospovidone Drugs 0.000 description 3
- 235000012754 curcumin Nutrition 0.000 description 3
- 239000004148 curcumin Substances 0.000 description 3
- 229960000525 diphenhydramine hydrochloride Drugs 0.000 description 3
- 239000007884 disintegrant Substances 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 238000013265 extended release Methods 0.000 description 3
- 229960000354 fexofenadine hydrochloride Drugs 0.000 description 3
- 230000004907 flux Effects 0.000 description 3
- 239000012458 free base Substances 0.000 description 3
- 229940074391 gallic acid Drugs 0.000 description 3
- 235000004515 gallic acid Nutrition 0.000 description 3
- 210000004051 gastric juice Anatomy 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- RQFCJASXJCIDSX-UUOKFMHZSA-N guanosine 5'-monophosphate Chemical compound C1=2NC(N)=NC(=O)C=2N=CN1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@H]1O RQFCJASXJCIDSX-UUOKFMHZSA-N 0.000 description 3
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 3
- 229940071870 hydroiodic acid Drugs 0.000 description 3
- 229960001680 ibuprofen Drugs 0.000 description 3
- 229960003088 loratadine Drugs 0.000 description 3
- JCCNYMKQOSZNPW-UHFFFAOYSA-N loratadine Chemical compound C1CN(C(=O)OCC)CCC1=C1C2=NC=CC=C2CCC2=CC(Cl)=CC=C21 JCCNYMKQOSZNPW-UHFFFAOYSA-N 0.000 description 3
- CDBRNDSHEYLDJV-FVGYRXGTSA-M naproxen sodium Chemical compound [Na+].C1=C([C@H](C)C([O-])=O)C=CC2=CC(OC)=CC=C21 CDBRNDSHEYLDJV-FVGYRXGTSA-M 0.000 description 3
- 229960003940 naproxen sodium Drugs 0.000 description 3
- 239000010695 polyglycol Substances 0.000 description 3
- 229920000151 polyglycol Polymers 0.000 description 3
- 229920002689 polyvinyl acetate Polymers 0.000 description 3
- 239000011118 polyvinyl acetate Substances 0.000 description 3
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 description 3
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 description 3
- 235000010259 potassium hydrogen sulphite Nutrition 0.000 description 3
- 229960004159 pseudoephedrine sulfate Drugs 0.000 description 3
- 125000002523 retinol group Chemical group 0.000 description 3
- 238000007086 side reaction Methods 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- 229960001593 triprolidine hydrochloride Drugs 0.000 description 3
- 235000013522 vodka Nutrition 0.000 description 3
- 239000001993 wax Substances 0.000 description 3
- AUHDWARTFSKSAC-HEIFUQTGSA-N (2S,3R,4S,5R)-3,4-dihydroxy-5-(hydroxymethyl)-2-(6-oxo-1H-purin-9-yl)oxolane-2-carboxylic acid Chemical compound [C@]1([C@H](O)[C@H](O)[C@@H](CO)O1)(N1C=NC=2C(O)=NC=NC12)C(=O)O AUHDWARTFSKSAC-HEIFUQTGSA-N 0.000 description 2
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 2
- WRRSFOZOETZUPG-FFHNEAJVSA-N (4r,4ar,7s,7ar,12bs)-9-methoxy-3-methyl-2,4,4a,7,7a,13-hexahydro-1h-4,12-methanobenzofuro[3,2-e]isoquinoline-7-ol;hydrate Chemical compound O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC WRRSFOZOETZUPG-FFHNEAJVSA-N 0.000 description 2
- KJPRLNWUNMBNBZ-QPJJXVBHSA-N (E)-cinnamaldehyde Chemical compound O=C\C=C\C1=CC=CC=C1 KJPRLNWUNMBNBZ-QPJJXVBHSA-N 0.000 description 2
- WSWCOQWTEOXDQX-MQQKCMAXSA-M (E,E)-sorbate Chemical compound C\C=C\C=C\C([O-])=O WSWCOQWTEOXDQX-MQQKCMAXSA-M 0.000 description 2
- PMGQWSIVQFOFOQ-BDUVBVHRSA-N (e)-but-2-enedioic acid;(2r)-2-[2-[1-(4-chlorophenyl)-1-phenylethoxy]ethyl]-1-methylpyrrolidine Chemical compound OC(=O)\C=C\C(O)=O.CN1CCC[C@@H]1CCOC(C)(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 PMGQWSIVQFOFOQ-BDUVBVHRSA-N 0.000 description 2
- LVGUZGTVOIAKKC-UHFFFAOYSA-N 1,1,1,2-tetrafluoroethane Chemical compound FCC(F)(F)F LVGUZGTVOIAKKC-UHFFFAOYSA-N 0.000 description 2
- XMWGTKZEDLCVIG-UHFFFAOYSA-N 1-(chloromethyl)naphthalene Chemical compound C1=CC=C2C(CCl)=CC=CC2=C1 XMWGTKZEDLCVIG-UHFFFAOYSA-N 0.000 description 2
- XQQZRZQVBFHBHL-UHFFFAOYSA-N 12-crown-4 Chemical compound C1COCCOCCOCCO1 XQQZRZQVBFHBHL-UHFFFAOYSA-N 0.000 description 2
- GZCGUPFRVQAUEE-UHFFFAOYSA-N 2,3,4,5,6-pentahydroxyhexanal Chemical compound OCC(O)C(O)C(O)C(O)C=O GZCGUPFRVQAUEE-UHFFFAOYSA-N 0.000 description 2
- PAWQVTBBRAZDMG-UHFFFAOYSA-N 2-(3-bromo-2-fluorophenyl)acetic acid Chemical compound OC(=O)CC1=CC=CC(Br)=C1F PAWQVTBBRAZDMG-UHFFFAOYSA-N 0.000 description 2
- 239000001154 2-(methoxymethyl)pyrazine Substances 0.000 description 2
- MGDMTRSONRZXOH-UHFFFAOYSA-N 2-Ethoxy-5-methylpyrazine Chemical compound CCOC1=CN=C(C)C=N1 MGDMTRSONRZXOH-UHFFFAOYSA-N 0.000 description 2
- VKJIAEQRKBQLLA-UHFFFAOYSA-N 2-Methoxy-3-methylpyrazine Chemical compound COC1=NC=CN=C1C VKJIAEQRKBQLLA-UHFFFAOYSA-N 0.000 description 2
- ILCLJQFCMRCPNM-UHFFFAOYSA-N 2-Methylpropyl 2-aminobenzoate Chemical compound CC(C)COC(=O)C1=CC=CC=C1N ILCLJQFCMRCPNM-UHFFFAOYSA-N 0.000 description 2
- SPCKHVPPRJWQRZ-UHFFFAOYSA-N 2-benzhydryloxy-n,n-dimethylethanamine;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1C(OCCN(C)C)C1=CC=CC=C1 SPCKHVPPRJWQRZ-UHFFFAOYSA-N 0.000 description 2
- XRCRJFOGPCJKPF-UHFFFAOYSA-N 2-butylbenzene-1,4-diol Chemical compound CCCCC1=CC(O)=CC=C1O XRCRJFOGPCJKPF-UHFFFAOYSA-N 0.000 description 2
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 2
- WFJIVOKAWHGMBH-UHFFFAOYSA-N 4-hexylbenzene-1,3-diol Chemical compound CCCCCCC1=CC=C(O)C=C1O WFJIVOKAWHGMBH-UHFFFAOYSA-N 0.000 description 2
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 2
- DLYPREQTTOHKSM-UHFFFAOYSA-N 7-chloro-n-[[2-[(dimethylamino)methyl]cyclopenta-1,4-dien-1-yl]methyl]quinolin-4-amine;cyclopenta-1,3-diene;iron(2+) Chemical compound [Fe+2].C1C=CC=[C-]1.C1=[C-]CC(CN(C)C)=C1CNC1=CC=NC2=CC(Cl)=CC=C12 DLYPREQTTOHKSM-UHFFFAOYSA-N 0.000 description 2
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 2
- CEZCCHQBSQPRMU-LLIZZRELSA-L Allura red AC Chemical compound [Na+].[Na+].COC1=CC(S([O-])(=O)=O)=C(C)C=C1\N=N\C1=C(O)C=CC2=CC(S([O-])(=O)=O)=CC=C12 CEZCCHQBSQPRMU-LLIZZRELSA-L 0.000 description 2
- WLDHEUZGFKACJH-ZRUFZDNISA-K Amaranth Chemical compound [Na+].[Na+].[Na+].C12=CC=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(O)=C1\N=N\C1=CC=C(S([O-])(=O)=O)C2=CC=CC=C12 WLDHEUZGFKACJH-ZRUFZDNISA-K 0.000 description 2
- LITUBCVUXPBCGA-WMZHIEFXSA-N Ascorbyl stearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](O)[C@H]1OC(=O)C(O)=C1O LITUBCVUXPBCGA-WMZHIEFXSA-N 0.000 description 2
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 description 2
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 description 2
- SGHZXLIDFTYFHQ-UHFFFAOYSA-L Brilliant Blue Chemical compound [Na+].[Na+].C=1C=C(C(=C2C=CC(C=C2)=[N+](CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=2C(=CC=CC=2)S([O-])(=O)=O)C=CC=1N(CC)CC1=CC=CC(S([O-])(=O)=O)=C1 SGHZXLIDFTYFHQ-UHFFFAOYSA-L 0.000 description 2
- RTMBGDBBDQKNNZ-UHFFFAOYSA-L C.I. Acid Blue 3 Chemical compound [Ca+2].C1=CC(N(CC)CC)=CC=C1C(C=1C(=CC(=C(O)C=1)S([O-])(=O)=O)S([O-])(=O)=O)=C1C=CC(=[N+](CC)CC)C=C1.C1=CC(N(CC)CC)=CC=C1C(C=1C(=CC(=C(O)C=1)S([O-])(=O)=O)S([O-])(=O)=O)=C1C=CC(=[N+](CC)CC)C=C1 RTMBGDBBDQKNNZ-UHFFFAOYSA-L 0.000 description 2
- 229920000623 Cellulose acetate phthalate Polymers 0.000 description 2
- 235000005940 Centaurea cyanus Nutrition 0.000 description 2
- 240000004385 Centaurea cyanus Species 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 2
- LAAPRQODJPXAHC-UHFFFAOYSA-N Coniferyl benzoate Natural products C1=C(O)C(OC)=CC(C=CCOC(=O)C=2C=CC=CC=2)=C1 LAAPRQODJPXAHC-UHFFFAOYSA-N 0.000 description 2
- 239000004212 Cryptoxanthin Substances 0.000 description 2
- AUNGANRZJHBGPY-UHFFFAOYSA-N D-Lyxoflavin Natural products OCC(O)C(O)C(O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-UHFFFAOYSA-N 0.000 description 2
- ZAKOWWREFLAJOT-CEFNRUSXSA-N D-alpha-tocopherylacetate Chemical compound CC(=O)OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C ZAKOWWREFLAJOT-CEFNRUSXSA-N 0.000 description 2
- MNQZXJOMYWMBOU-VKHMYHEASA-N D-glyceraldehyde Chemical compound OC[C@@H](O)C=O MNQZXJOMYWMBOU-VKHMYHEASA-N 0.000 description 2
- CIWBSHSKHKDKBQ-DUZGATOHSA-N D-isoascorbic acid Chemical compound OC[C@@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-DUZGATOHSA-N 0.000 description 2
- SRBFZHDQGSBBOR-IOVATXLUSA-N D-xylopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-IOVATXLUSA-N 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- ODHAQPXNQDBHSH-UHFFFAOYSA-N Dicyclohexyl disulfide Chemical compound C1CCCCC1SSC1CCCCC1 ODHAQPXNQDBHSH-UHFFFAOYSA-N 0.000 description 2
- AANLCWYVVNBGEE-IDIVVRGQSA-L Disodium inosinate Chemical compound [Na+].[Na+].O[C@@H]1[C@H](O)[C@@H](COP([O-])([O-])=O)O[C@H]1N1C(NC=NC2=O)=C2N=C1 AANLCWYVVNBGEE-IDIVVRGQSA-L 0.000 description 2
- 241000218671 Ephedra Species 0.000 description 2
- 241000208152 Geranium Species 0.000 description 2
- 108010024636 Glutathione Proteins 0.000 description 2
- GRSZFWQUAKGDAV-UHFFFAOYSA-N Inosinic acid Natural products OC1C(O)C(COP(O)(O)=O)OC1N1C(NC=NC2=O)=C2N=C1 GRSZFWQUAKGDAV-UHFFFAOYSA-N 0.000 description 2
- 229910021578 Iron(III) chloride Inorganic materials 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 2
- 239000011786 L-ascorbyl-6-palmitate Substances 0.000 description 2
- 239000004201 L-cysteine Substances 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 2
- JEVVKJMRZMXFBT-XWDZUXABSA-N Lycophyll Natural products OC/C(=C/CC/C(=C\C=C\C(=C/C=C/C(=C\C=C\C=C(/C=C/C=C(\C=C\C=C(/CC/C=C(/CO)\C)\C)/C)\C)/C)\C)/C)/C JEVVKJMRZMXFBT-XWDZUXABSA-N 0.000 description 2
- 240000000982 Malva neglecta Species 0.000 description 2
- 235000000060 Malva neglecta Nutrition 0.000 description 2
- 229910021380 Manganese Chloride Inorganic materials 0.000 description 2
- GLFNIEUTAYBVOC-UHFFFAOYSA-L Manganese chloride Chemical compound Cl[Mn]Cl GLFNIEUTAYBVOC-UHFFFAOYSA-L 0.000 description 2
- 229920000881 Modified starch Polymers 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 description 2
- JAUOIFJMECXRGI-UHFFFAOYSA-N Neoclaritin Chemical compound C=1C(Cl)=CC=C2C=1CCC1=CC=CN=C1C2=C1CCNCC1 JAUOIFJMECXRGI-UHFFFAOYSA-N 0.000 description 2
- 229910021586 Nickel(II) chloride Inorganic materials 0.000 description 2
- 241000736199 Paeonia Species 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- 229920002732 Polyanhydride Polymers 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- 229920000954 Polyglycolide Polymers 0.000 description 2
- 239000004260 Potassium ascorbate Substances 0.000 description 2
- 239000004285 Potassium sulphite Substances 0.000 description 2
- ZTHYODDOHIVTJV-UHFFFAOYSA-N Propyl gallate Chemical compound CCCOC(=O)C1=CC(O)=C(O)C(O)=C1 ZTHYODDOHIVTJV-UHFFFAOYSA-N 0.000 description 2
- 239000004228 Riboflavin-5'-Phosphate Substances 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- LSNNMFCWUKXFEE-UHFFFAOYSA-N Sulfurous acid Chemical group OS(O)=O LSNNMFCWUKXFEE-UHFFFAOYSA-N 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- XSTXAVWGXDQKEL-UHFFFAOYSA-N Trichloroethylene Chemical group ClC=C(Cl)Cl XSTXAVWGXDQKEL-UHFFFAOYSA-N 0.000 description 2
- TVLJNOHNHRBUBC-SIHAWKHTSA-J [Na+].[Na+].[Na+].[Na+].O[C@@H]1[C@@H](COP([O-])([O-])=O)O[C@H]([C@@H]1O)n1cnc2c(O)ncnc12.Nc1nc2n(cnc2c(=O)[nH]1)[C@@H]1O[C@H](COP([O-])([O-])=O)[C@@H](O)[C@H]1O Chemical compound [Na+].[Na+].[Na+].[Na+].O[C@@H]1[C@@H](COP([O-])([O-])=O)O[C@H]([C@@H]1O)n1cnc2c(O)ncnc12.Nc1nc2n(cnc2c(=O)[nH]1)[C@@H]1O[C@H](COP([O-])([O-])=O)[C@@H](O)[C@H]1O TVLJNOHNHRBUBC-SIHAWKHTSA-J 0.000 description 2
- 239000000619 acesulfame-K Substances 0.000 description 2
- 235000011054 acetic acid Nutrition 0.000 description 2
- MQRWBMAEBQOWAF-UHFFFAOYSA-N acetic acid;nickel Chemical compound [Ni].CC(O)=O.CC(O)=O MQRWBMAEBQOWAF-UHFFFAOYSA-N 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 229940072056 alginate Drugs 0.000 description 2
- 235000010443 alginic acid Nutrition 0.000 description 2
- 229920000615 alginic acid Polymers 0.000 description 2
- OENHQHLEOONYIE-UKMVMLAPSA-N all-trans beta-carotene Natural products CC=1CCCC(C)(C)C=1/C=C/C(/C)=C/C=C/C(/C)=C/C=C/C=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C OENHQHLEOONYIE-UKMVMLAPSA-N 0.000 description 2
- 150000004347 all-trans-retinol derivatives Chemical class 0.000 description 2
- 235000001014 amino acid Nutrition 0.000 description 2
- 229940024606 amino acid Drugs 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 2
- 229940072107 ascorbate Drugs 0.000 description 2
- 229960005370 atorvastatin Drugs 0.000 description 2
- 239000004176 azorubin Substances 0.000 description 2
- TVWOWDDBXAFQDG-DQRAZIAOSA-N azorubine Chemical compound C1=CC=C2C(\N=N/C3=C(C4=CC=CC=C4C(=C3)S(O)(=O)=O)O)=CC=C(S(O)(=O)=O)C2=C1 TVWOWDDBXAFQDG-DQRAZIAOSA-N 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 229960004217 benzyl alcohol Drugs 0.000 description 2
- 229940066595 beta tocopherol Drugs 0.000 description 2
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 2
- 239000001652 beta-apo-8'-carotenal Substances 0.000 description 2
- 235000013735 beta-apo-8'-carotenal Nutrition 0.000 description 2
- 235000013734 beta-carotene Nutrition 0.000 description 2
- 239000011648 beta-carotene Substances 0.000 description 2
- TUPZEYHYWIEDIH-WAIFQNFQSA-N beta-carotene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2=CCCCC2(C)C TUPZEYHYWIEDIH-WAIFQNFQSA-N 0.000 description 2
- DMASLKHVQRHNES-FKKUPVFPSA-N beta-cryptoxanthin Chemical compound C([C@H](O)CC=1C)C(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C DMASLKHVQRHNES-FKKUPVFPSA-N 0.000 description 2
- 229960002747 betacarotene Drugs 0.000 description 2
- 229940055580 brilliant blue fcf Drugs 0.000 description 2
- 239000004109 brown FK Substances 0.000 description 2
- 235000012713 brown FK Nutrition 0.000 description 2
- 239000001678 brown HT Substances 0.000 description 2
- 235000012670 brown HT Nutrition 0.000 description 2
- 229940043253 butylated hydroxyanisole Drugs 0.000 description 2
- 239000004196 calcium 5'-ribonucleotide Substances 0.000 description 2
- 235000013894 calcium 5'-ribonucleotide Nutrition 0.000 description 2
- LVGQIQHJMRUCRM-UHFFFAOYSA-L calcium bisulfite Chemical compound [Ca+2].OS([O-])=O.OS([O-])=O LVGQIQHJMRUCRM-UHFFFAOYSA-L 0.000 description 2
- 239000004244 calcium guanylate Substances 0.000 description 2
- 235000013900 calcium guanylate Nutrition 0.000 description 2
- 239000004294 calcium hydrogen sulphite Substances 0.000 description 2
- ZLHWLLPKQPKYJD-MCDZGGTQSA-L calcium inosinate Chemical compound [Ca+2].O[C@@H]1[C@H](O)[C@@H](COP([O-])([O-])=O)O[C@H]1N1C(NC=NC2=O)=C2N=C1 ZLHWLLPKQPKYJD-MCDZGGTQSA-L 0.000 description 2
- GBAOBIBJACZTNA-UHFFFAOYSA-L calcium sulfite Chemical compound [Ca+2].[O-]S([O-])=O GBAOBIBJACZTNA-UHFFFAOYSA-L 0.000 description 2
- 239000004295 calcium sulphite Substances 0.000 description 2
- BLORRZQTHNGFTI-ZZMNMWMASA-L calcium-L-ascorbate Chemical compound [Ca+2].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-] BLORRZQTHNGFTI-ZZMNMWMASA-L 0.000 description 2
- HZQXCUSDXIKLGS-UHFFFAOYSA-L calcium;dibenzoate;trihydrate Chemical compound O.O.O.[Ca+2].[O-]C(=O)C1=CC=CC=C1.[O-]C(=O)C1=CC=CC=C1 HZQXCUSDXIKLGS-UHFFFAOYSA-L 0.000 description 2
- FDSDTBUPSURDBL-DKLMTRRASA-N canthaxanthin Chemical compound CC=1C(=O)CCC(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)C(=O)CCC1(C)C FDSDTBUPSURDBL-DKLMTRRASA-N 0.000 description 2
- 235000017663 capsaicin Nutrition 0.000 description 2
- 229960002504 capsaicin Drugs 0.000 description 2
- 150000007942 carboxylates Chemical class 0.000 description 2
- 150000001735 carboxylic acids Chemical class 0.000 description 2
- 239000004106 carminic acid Substances 0.000 description 2
- 235000005473 carotenes Nutrition 0.000 description 2
- 229920002301 cellulose acetate Polymers 0.000 description 2
- 229940081734 cellulose acetate phthalate Drugs 0.000 description 2
- 229960004342 cetirizine hydrochloride Drugs 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 230000001055 chewing effect Effects 0.000 description 2
- 235000012698 chlorophylls and chlorophyllins Nutrition 0.000 description 2
- 239000001752 chlorophylls and chlorophyllins Substances 0.000 description 2
- KJPRLNWUNMBNBZ-UHFFFAOYSA-N cinnamic aldehyde Natural products O=CC=CC1=CC=CC=C1 KJPRLNWUNMBNBZ-UHFFFAOYSA-N 0.000 description 2
- 229940117916 cinnamic aldehyde Drugs 0.000 description 2
- 229960002881 clemastine Drugs 0.000 description 2
- YNNUSGIPVFPVBX-NHCUHLMSSA-N clemastine Chemical compound CN1CCC[C@@H]1CCO[C@@](C)(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 YNNUSGIPVFPVBX-NHCUHLMSSA-N 0.000 description 2
- 229960002689 clemastine fumarate Drugs 0.000 description 2
- 229940011182 cobalt acetate Drugs 0.000 description 2
- GVPFVAHMJGGAJG-UHFFFAOYSA-L cobalt dichloride Chemical compound [Cl-].[Cl-].[Co+2] GVPFVAHMJGGAJG-UHFFFAOYSA-L 0.000 description 2
- 229940044175 cobalt sulfate Drugs 0.000 description 2
- 229910000361 cobalt sulfate Inorganic materials 0.000 description 2
- KTVIXTQDYHMGHF-UHFFFAOYSA-L cobalt(2+) sulfate Chemical compound [Co+2].[O-]S([O-])(=O)=O KTVIXTQDYHMGHF-UHFFFAOYSA-L 0.000 description 2
- QAHREYKOYSIQPH-UHFFFAOYSA-L cobalt(II) acetate Chemical compound [Co+2].CC([O-])=O.CC([O-])=O QAHREYKOYSIQPH-UHFFFAOYSA-L 0.000 description 2
- BZRRQSJJPUGBAA-UHFFFAOYSA-L cobalt(ii) bromide Chemical compound Br[Co]Br BZRRQSJJPUGBAA-UHFFFAOYSA-L 0.000 description 2
- JZGWEIPJUAIDHM-QURGRASLSA-N cochineal red a Chemical compound C1=CC=C2C(/N=N/C3=C4C(=CC(=CC4=CC=C3O)S(O)(=O)=O)S(O)(=O)=O)=CC=C(S(O)(=O)=O)C2=C1 JZGWEIPJUAIDHM-QURGRASLSA-N 0.000 description 2
- 229960004126 codeine Drugs 0.000 description 2
- OROGSEYTTFOCAN-DNJOTXNNSA-N codeine Natural products C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC OROGSEYTTFOCAN-DNJOTXNNSA-N 0.000 description 2
- 238000007906 compression Methods 0.000 description 2
- 230000006835 compression Effects 0.000 description 2
- LAAPRQODJPXAHC-AATRIKPKSA-N coniferyl benzoate Chemical compound C1=C(O)C(OC)=CC(\C=C\COC(=O)C=2C=CC=CC=2)=C1 LAAPRQODJPXAHC-AATRIKPKSA-N 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 239000004121 copper complexes of chlorophylls and chlorophyllins Substances 0.000 description 2
- 235000012700 copper complexes of chlorophylls and chlorophyllins Nutrition 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- 235000019244 cryptoxanthin Nutrition 0.000 description 2
- VFLDPWHFBUODDF-FCXRPNKRSA-N curcumin Chemical compound C1=C(O)C(OC)=CC(\C=C\C(=O)CC(=O)\C=C\C=2C=C(OC)C(O)=CC=2)=C1 VFLDPWHFBUODDF-FCXRPNKRSA-N 0.000 description 2
- 238000005520 cutting process Methods 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- GHVNFZFCNZKVNT-UHFFFAOYSA-M decanoate Chemical compound CCCCCCCCCC([O-])=O GHVNFZFCNZKVNT-UHFFFAOYSA-M 0.000 description 2
- 235000010389 delta-tocopherol Nutrition 0.000 description 2
- 238000004925 denaturation Methods 0.000 description 2
- 230000036425 denaturation Effects 0.000 description 2
- 229960001271 desloratadine Drugs 0.000 description 2
- RJYMRRJVDRJMJW-UHFFFAOYSA-L dibromomanganese Chemical compound Br[Mn]Br RJYMRRJVDRJMJW-UHFFFAOYSA-L 0.000 description 2
- XYYVYLMBEZUESM-UHFFFAOYSA-N dihydrocodeine Natural products C1C(N(CCC234)C)C2C=CC(=O)C3OC2=C4C1=CC=C2OC XYYVYLMBEZUESM-UHFFFAOYSA-N 0.000 description 2
- 229960000520 diphenhydramine Drugs 0.000 description 2
- BCQFRUIIFOQGFI-LGVAUZIVSA-L dipotassium guanylate Chemical compound [K+].[K+].C1=2NC(N)=NC(=O)C=2N=CN1[C@@H]1O[C@H](COP([O-])([O-])=O)[C@@H](O)[C@H]1O BCQFRUIIFOQGFI-LGVAUZIVSA-L 0.000 description 2
- DLDSRSUKRMPQKB-IDIVVRGQSA-L dipotassium;[(2r,3s,4r,5r)-3,4-dihydroxy-5-(6-oxo-3h-purin-9-yl)oxolan-2-yl]methyl phosphate Chemical compound [K+].[K+].O[C@@H]1[C@H](O)[C@@H](COP([O-])([O-])=O)O[C@H]1N1C(NC=NC2=O)=C2N=C1 DLDSRSUKRMPQKB-IDIVVRGQSA-L 0.000 description 2
- 150000002016 disaccharides Chemical group 0.000 description 2
- 238000002845 discoloration Methods 0.000 description 2
- PVBRXXAAPNGWGE-LGVAUZIVSA-L disodium 5'-guanylate Chemical compound [Na+].[Na+].C1=2NC(N)=NC(=O)C=2N=CN1[C@@H]1O[C@H](COP([O-])([O-])=O)[C@@H](O)[C@H]1O PVBRXXAAPNGWGE-LGVAUZIVSA-L 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-M dodecanoate Chemical compound CCCCCCCCCCCC([O-])=O POULHZVOKOAJMA-UHFFFAOYSA-M 0.000 description 2
- 229940080643 dodecyl gallate Drugs 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 239000004318 erythorbic acid Substances 0.000 description 2
- 239000004174 erythrosine Substances 0.000 description 2
- 235000012732 erythrosine Nutrition 0.000 description 2
- GFJVXXWOPWLRNU-UHFFFAOYSA-N ethenyl formate Chemical compound C=COC=O GFJVXXWOPWLRNU-UHFFFAOYSA-N 0.000 description 2
- DQYBDCGIPTYXML-UHFFFAOYSA-N ethoxyethane;hydrate Chemical compound O.CCOCC DQYBDCGIPTYXML-UHFFFAOYSA-N 0.000 description 2
- 235000012656 ethyl ester of beta-apo-8'-carotenic acid Nutrition 0.000 description 2
- 239000001684 ethyl ester of beta-apo-8'-carotenic acid (C30) Substances 0.000 description 2
- VKOBVWXKNCXXDE-UHFFFAOYSA-N ethyl stearic acid Natural products CCCCCCCCCCCCCCCCCCCC(O)=O VKOBVWXKNCXXDE-UHFFFAOYSA-N 0.000 description 2
- 239000005038 ethylene vinyl acetate Substances 0.000 description 2
- 229940071106 ethylenediaminetetraacetate Drugs 0.000 description 2
- 239000002360 explosive Substances 0.000 description 2
- 239000000542 fatty acid esters of ascorbic acid Substances 0.000 description 2
- 229950010451 ferroquine Drugs 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 235000013373 food additive Nutrition 0.000 description 2
- 239000002778 food additive Substances 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 239000001530 fumaric acid Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 235000010382 gamma-tocopherol Nutrition 0.000 description 2
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 238000005227 gel permeation chromatography Methods 0.000 description 2
- 229960003180 glutathione Drugs 0.000 description 2
- KWIUHFFTVRNATP-UHFFFAOYSA-N glycine betaine Chemical compound C[N+](C)(C)CC([O-])=O KWIUHFFTVRNATP-UHFFFAOYSA-N 0.000 description 2
- WDPIZEKLJKBSOZ-UHFFFAOYSA-M green s Chemical compound [Na+].C1=CC(N(C)C)=CC=C1C(C=1C2=CC=C(C=C2C=C(C=1O)S([O-])(=O)=O)S([O-])(=O)=O)=C1C=CC(=[N+](C)C)C=C1 WDPIZEKLJKBSOZ-UHFFFAOYSA-M 0.000 description 2
- 239000004226 guanylic acid Substances 0.000 description 2
- 235000013928 guanylic acid Nutrition 0.000 description 2
- 239000011874 heated mixture Substances 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-M hexadecanoate Chemical compound CCCCCCCCCCCCCCCC([O-])=O IPCSVZSSVZVIGE-UHFFFAOYSA-M 0.000 description 2
- 229960003258 hexylresorcinol Drugs 0.000 description 2
- LLPOLZWFYMWNKH-CMKMFDCUSA-N hydrocodone Chemical compound C([C@H]1[C@H](N(CC[C@@]112)C)C3)CC(=O)[C@@H]1OC1=C2C3=CC=C1OC LLPOLZWFYMWNKH-CMKMFDCUSA-N 0.000 description 2
- 229960000240 hydrocodone Drugs 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- KHLVKKOJDHCJMG-QDBORUFSSA-L indigo carmine Chemical compound [Na+].[Na+].N/1C2=CC=C(S([O-])(=O)=O)C=C2C(=O)C\1=C1/NC2=CC=C(S(=O)(=O)[O-])C=C2C1=O KHLVKKOJDHCJMG-QDBORUFSSA-L 0.000 description 2
- 229960003988 indigo carmine Drugs 0.000 description 2
- 229940028843 inosinic acid Drugs 0.000 description 2
- RBTARNINKXHZNM-UHFFFAOYSA-K iron trichloride Chemical compound Cl[Fe](Cl)Cl RBTARNINKXHZNM-UHFFFAOYSA-K 0.000 description 2
- 229940026239 isoascorbic acid Drugs 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 229940070765 laurate Drugs 0.000 description 2
- 239000004335 litholrubine BK Substances 0.000 description 2
- 235000010187 litholrubine BK Nutrition 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 229960004999 lycopene Drugs 0.000 description 2
- 229940049920 malate Drugs 0.000 description 2
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 2
- 229940071125 manganese acetate Drugs 0.000 description 2
- 239000011565 manganese chloride Substances 0.000 description 2
- 235000002867 manganese chloride Nutrition 0.000 description 2
- 229940099607 manganese chloride Drugs 0.000 description 2
- 229940099596 manganese sulfate Drugs 0.000 description 2
- 239000011702 manganese sulphate Substances 0.000 description 2
- 235000007079 manganese sulphate Nutrition 0.000 description 2
- UOGMEBQRZBEZQT-UHFFFAOYSA-L manganese(2+);diacetate Chemical compound [Mn+2].CC([O-])=O.CC([O-])=O UOGMEBQRZBEZQT-UHFFFAOYSA-L 0.000 description 2
- SQQMAOCOWKFBNP-UHFFFAOYSA-L manganese(II) sulfate Chemical compound [Mn+2].[O-]S([O-])(=O)=O SQQMAOCOWKFBNP-UHFFFAOYSA-L 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 235000019426 modified starch Nutrition 0.000 description 2
- 229940105132 myristate Drugs 0.000 description 2
- 229960002009 naproxen Drugs 0.000 description 2
- CMWTZPSULFXXJA-VIFPVBQESA-M naproxen(1-) Chemical compound C1=C([C@H](C)C([O-])=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-M 0.000 description 2
- 229920005615 natural polymer Polymers 0.000 description 2
- 239000000879 neohesperidine DC Substances 0.000 description 2
- 229940078494 nickel acetate Drugs 0.000 description 2
- QMMRZOWCJAIUJA-UHFFFAOYSA-L nickel dichloride Chemical compound Cl[Ni]Cl QMMRZOWCJAIUJA-UHFFFAOYSA-L 0.000 description 2
- LGQLOGILCSXPEA-UHFFFAOYSA-L nickel sulfate Chemical compound [Ni+2].[O-]S([O-])(=O)=O LGQLOGILCSXPEA-UHFFFAOYSA-L 0.000 description 2
- UQPSGBZICXWIAG-UHFFFAOYSA-L nickel(2+);dibromide;trihydrate Chemical compound O.O.O.Br[Ni]Br UQPSGBZICXWIAG-UHFFFAOYSA-L 0.000 description 2
- 229910000363 nickel(II) sulfate Inorganic materials 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- NRPKURNSADTHLJ-UHFFFAOYSA-N octyl gallate Chemical compound CCCCCCCCOC(=O)C1=CC(O)=C(O)C(O)=C1 NRPKURNSADTHLJ-UHFFFAOYSA-N 0.000 description 2
- 229940049964 oleate Drugs 0.000 description 2
- ZQPPMHVWECSIRJ-KTKRTIGZSA-M oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC([O-])=O ZQPPMHVWECSIRJ-KTKRTIGZSA-M 0.000 description 2
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 2
- 239000008188 pellet Substances 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- 239000000825 pharmaceutical preparation Substances 0.000 description 2
- 229940127557 pharmaceutical product Drugs 0.000 description 2
- 230000035479 physiological effects, processes and functions Effects 0.000 description 2
- 239000002574 poison Substances 0.000 description 2
- 231100000614 poison Toxicity 0.000 description 2
- 229920001200 poly(ethylene-vinyl acetate) Polymers 0.000 description 2
- 229920000747 poly(lactic acid) Polymers 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 229940017794 potassium ascorbate Drugs 0.000 description 2
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 2
- 229940103091 potassium benzoate Drugs 0.000 description 2
- 239000004293 potassium hydrogen sulphite Substances 0.000 description 2
- RWPGFSMJFRPDDP-UHFFFAOYSA-L potassium metabisulfite Chemical compound [K+].[K+].[O-]S(=O)S([O-])(=O)=O RWPGFSMJFRPDDP-UHFFFAOYSA-L 0.000 description 2
- BHZRJJOHZFYXTO-UHFFFAOYSA-L potassium sulfite Chemical compound [K+].[K+].[O-]S([O-])=O BHZRJJOHZFYXTO-UHFFFAOYSA-L 0.000 description 2
- CONVKSGEGAVTMB-RXSVEWSESA-M potassium-L-ascorbate Chemical compound [K+].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-] CONVKSGEGAVTMB-RXSVEWSESA-M 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 235000019260 propionic acid Nutrition 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 2
- 239000003237 recreational drug Substances 0.000 description 2
- 229960002477 riboflavin Drugs 0.000 description 2
- 235000019231 riboflavin-5'-phosphate Nutrition 0.000 description 2
- 239000002336 ribonucleotide Substances 0.000 description 2
- 238000007493 shaping process Methods 0.000 description 2
- 229960005055 sodium ascorbate Drugs 0.000 description 2
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 2
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 2
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 2
- FDRCDNZGSXJAFP-UHFFFAOYSA-M sodium chloroacetate Chemical compound [Na+].[O-]C(=O)CCl FDRCDNZGSXJAFP-UHFFFAOYSA-M 0.000 description 2
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 2
- 239000004320 sodium erythorbate Substances 0.000 description 2
- 235000010352 sodium erythorbate Nutrition 0.000 description 2
- 239000004402 sodium ethyl p-hydroxybenzoate Substances 0.000 description 2
- 235000010226 sodium ethyl p-hydroxybenzoate Nutrition 0.000 description 2
- 239000004289 sodium hydrogen sulphite Substances 0.000 description 2
- 239000004290 sodium methyl p-hydroxybenzoate Substances 0.000 description 2
- 239000004404 sodium propyl p-hydroxybenzoate Substances 0.000 description 2
- 235000010230 sodium propyl p-hydroxybenzoate Nutrition 0.000 description 2
- PPASLZSBLFJQEF-RXSVEWSESA-M sodium-L-ascorbate Chemical compound [Na+].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RXSVEWSESA-M 0.000 description 2
- PESXGULMKCKJCC-UHFFFAOYSA-M sodium;4-methoxycarbonylphenolate Chemical compound [Na+].COC(=O)C1=CC=C([O-])C=C1 PESXGULMKCKJCC-UHFFFAOYSA-M 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 238000000638 solvent extraction Methods 0.000 description 2
- 229940075554 sorbate Drugs 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 229940086735 succinate Drugs 0.000 description 2
- 150000005846 sugar alcohols Chemical class 0.000 description 2
- 239000004173 sunset yellow FCF Substances 0.000 description 2
- 235000012751 sunset yellow FCF Nutrition 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 229920001059 synthetic polymer Polymers 0.000 description 2
- 229940095064 tartrate Drugs 0.000 description 2
- UJMBCXLDXJUMFB-GLCFPVLVSA-K tartrazine Chemical compound [Na+].[Na+].[Na+].[O-]C(=O)C1=NN(C=2C=CC(=CC=2)S([O-])(=O)=O)C(=O)C1\N=N\C1=CC=C(S([O-])(=O)=O)C=C1 UJMBCXLDXJUMFB-GLCFPVLVSA-K 0.000 description 2
- 229960000943 tartrazine Drugs 0.000 description 2
- 239000004250 tert-Butylhydroquinone Substances 0.000 description 2
- ISIJQEHRDSCQIU-UHFFFAOYSA-N tert-butyl 2,7-diazaspiro[4.5]decane-7-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CCCC11CNCC1 ISIJQEHRDSCQIU-UHFFFAOYSA-N 0.000 description 2
- 235000019281 tert-butylhydroquinone Nutrition 0.000 description 2
- TUNFSRHWOTWDNC-UHFFFAOYSA-N tetradecanoic acid Chemical compound CCCCCCCCCCCCCC(O)=O TUNFSRHWOTWDNC-UHFFFAOYSA-N 0.000 description 2
- 239000000541 tocopherol-rich extract Substances 0.000 description 2
- LLPOLZWFYMWNKH-UHFFFAOYSA-N trans-dihydrocodeinone Natural products C1C(N(CCC234)C)C2CCC(=O)C3OC2=C4C1=CC=C2OC LLPOLZWFYMWNKH-UHFFFAOYSA-N 0.000 description 2
- ZCIHMQAPACOQHT-ZGMPDRQDSA-N trans-isorenieratene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/c1c(C)ccc(C)c1C)C=CC=C(/C)C=Cc2c(C)ccc(C)c2C ZCIHMQAPACOQHT-ZGMPDRQDSA-N 0.000 description 2
- URAYPUMNDPQOKB-UHFFFAOYSA-N triacetin Chemical compound CC(=O)OCC(OC(C)=O)COC(C)=O URAYPUMNDPQOKB-UHFFFAOYSA-N 0.000 description 2
- UBOXGVDOUJQMTN-UHFFFAOYSA-N trichloroethylene Natural products ClCC(Cl)Cl UBOXGVDOUJQMTN-UHFFFAOYSA-N 0.000 description 2
- IAEGWXHKWJGQAZ-UHFFFAOYSA-N trimethylpyrazine Chemical compound CC1=CN=C(C)C(C)=N1 IAEGWXHKWJGQAZ-UHFFFAOYSA-N 0.000 description 2
- 150000003672 ureas Chemical class 0.000 description 2
- NCYCYZXNIZJOKI-UHFFFAOYSA-N vitamin A aldehyde Natural products O=CC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C NCYCYZXNIZJOKI-UHFFFAOYSA-N 0.000 description 2
- 125000001020 α-tocopherol group Chemical group 0.000 description 2
- OENHQHLEOONYIE-JLTXGRSLSA-N β-Carotene Chemical compound CC=1CCCC(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C OENHQHLEOONYIE-JLTXGRSLSA-N 0.000 description 2
- 239000011590 β-tocopherol Substances 0.000 description 2
- 235000007680 β-tocopherol Nutrition 0.000 description 2
- 239000002478 γ-tocopherol Substances 0.000 description 2
- QUEDXNHFTDJVIY-DQCZWYHMSA-N γ-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1 QUEDXNHFTDJVIY-DQCZWYHMSA-N 0.000 description 2
- 239000002446 δ-tocopherol Substances 0.000 description 2
- VDPLLINNMXFNQX-UHFFFAOYSA-N (1-aminocyclohexyl)methanol Chemical compound OCC1(N)CCCCC1 VDPLLINNMXFNQX-UHFFFAOYSA-N 0.000 description 1
- YQSHYGCCYVPRDI-UHFFFAOYSA-N (4-propan-2-ylphenyl)methanamine Chemical compound CC(C)C1=CC=C(CN)C=C1 YQSHYGCCYVPRDI-UHFFFAOYSA-N 0.000 description 1
- OJHZNMVJJKMFGX-BWCYBWMMSA-N (4r,4ar,7ar,12bs)-9-methoxy-3-methyl-1,2,4,4a,5,6,7a,13-octahydro-4,12-methanobenzofuro[3,2-e]isoquinoline-7-one;(2r,3r)-2,3-dihydroxybutanedioic acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)CC(=O)[C@@H]1OC1=C2C3=CC=C1OC OJHZNMVJJKMFGX-BWCYBWMMSA-N 0.000 description 1
- RKDVKSZUMVYZHH-UHFFFAOYSA-N 1,4-dioxane-2,5-dione Chemical compound O=C1COC(=O)CO1 RKDVKSZUMVYZHH-UHFFFAOYSA-N 0.000 description 1
- ZUOBAVDBHRETHH-UHFFFAOYSA-N 2,3,3,4,4-pentamethylchromen-2-ol Chemical compound C1=CC=C2C(C)(C)C(C)(C)C(C)(O)OC2=C1 ZUOBAVDBHRETHH-UHFFFAOYSA-N 0.000 description 1
- GNENVASJJIUNER-UHFFFAOYSA-N 2,4,6-tricyclohexyloxy-1,3,5,2,4,6-trioxatriborinane Chemical compound C1CCCCC1OB1OB(OC2CCCCC2)OB(OC2CCCCC2)O1 GNENVASJJIUNER-UHFFFAOYSA-N 0.000 description 1
- XBLZVFYOCZVABA-UHFFFAOYSA-N 2-Ethoxy-6-methylpyrazine Chemical compound CCOC1=CN=CC(C)=N1 XBLZVFYOCZVABA-UHFFFAOYSA-N 0.000 description 1
- JIKCUGHIEOGWTB-UHFFFAOYSA-N 2-ethoxy-6-methylpyridine Chemical compound CCOC1=CC=CC(C)=N1 JIKCUGHIEOGWTB-UHFFFAOYSA-N 0.000 description 1
- GJJVAFUKOBZPCB-UHFFFAOYSA-N 2-methyl-2-(4,8,12-trimethyltrideca-3,7,11-trienyl)-3,4-dihydrochromen-6-ol Chemical compound OC1=CC=C2OC(CCC=C(C)CCC=C(C)CCC=C(C)C)(C)CCC2=C1 GJJVAFUKOBZPCB-UHFFFAOYSA-N 0.000 description 1
- IUPHTVOTTBREAV-UHFFFAOYSA-N 3-hydroxybutanoic acid;3-hydroxypentanoic acid Chemical compound CC(O)CC(O)=O.CCC(O)CC(O)=O IUPHTVOTTBREAV-UHFFFAOYSA-N 0.000 description 1
- JVYNJRBSXBYXQB-UHFFFAOYSA-N 4-[3-(4-carboxyphenoxy)propoxy]benzoic acid;decanedioic acid Chemical compound OC(=O)CCCCCCCCC(O)=O.C1=CC(C(=O)O)=CC=C1OCCCOC1=CC=C(C(O)=O)C=C1 JVYNJRBSXBYXQB-UHFFFAOYSA-N 0.000 description 1
- 208000007848 Alcoholism Diseases 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 235000021357 Behenic acid Nutrition 0.000 description 1
- UKMSUNONTOPOIO-UHFFFAOYSA-N Behenic acid Natural products CCCCCCCCCCCCCCCCCCCCCC(O)=O UKMSUNONTOPOIO-UHFFFAOYSA-N 0.000 description 1
- DHHFDKNIEVKVKS-FMOSSLLZSA-N Betanin Chemical group O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC(C(=C1)O)=CC(C[C@H]2C([O-])=O)=C1[N+]2=C\C=C\1C=C(C(O)=O)N[C@H](C(O)=O)C/1 DHHFDKNIEVKVKS-FMOSSLLZSA-N 0.000 description 1
- DHHFDKNIEVKVKS-MVUYWVKGSA-N Betanin Natural products O=C(O)[C@@H]1NC(C(=O)O)=C/C(=C\C=[N+]/2\[C@@H](C(=O)[O-])Cc3c\2cc(O)c(O[C@H]2[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O2)c3)/C1 DHHFDKNIEVKVKS-MVUYWVKGSA-N 0.000 description 1
- 229920013642 Biopol™ Polymers 0.000 description 1
- XIVIFXANPXDWSV-UHFFFAOYSA-N C(C(CC(C)=O)=O)[Fe](CC(CC(C)=O)=O)CC(CC(C)=O)=O Chemical compound C(C(CC(C)=O)=O)[Fe](CC(CC(C)=O)=O)CC(CC(C)=O)=O XIVIFXANPXDWSV-UHFFFAOYSA-N 0.000 description 1
- JZDLGAZDHCFICL-UHFFFAOYSA-N C(C)(=O)O.C(CCC(=O)O)(=O)OCCCCO Chemical compound C(C)(=O)O.C(CCC(=O)O)(=O)OCCCCO JZDLGAZDHCFICL-UHFFFAOYSA-N 0.000 description 1
- 101100494266 Caenorhabditis elegans best-17 gene Proteins 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- 235000012766 Cannabis sativa ssp. sativa var. sativa Nutrition 0.000 description 1
- 235000012765 Cannabis sativa ssp. sativa var. spontanea Nutrition 0.000 description 1
- DBAKFASWICGISY-BTJKTKAUSA-N Chlorpheniramine maleate Chemical compound OC(=O)\C=C/C(O)=O.C=1C=CC=NC=1C(CCN(C)C)C1=CC=C(Cl)C=C1 DBAKFASWICGISY-BTJKTKAUSA-N 0.000 description 1
- 244000304337 Cuminum cyminum Species 0.000 description 1
- 235000007129 Cuminum cyminum Nutrition 0.000 description 1
- YTBSYETUWUMLBZ-UHFFFAOYSA-N D-Erythrose Natural products OCC(O)C(O)C=O YTBSYETUWUMLBZ-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-CBPJZXOFSA-N D-Gulose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@H](O)[C@H]1O WQZGKKKJIJFFOK-CBPJZXOFSA-N 0.000 description 1
- WQZGKKKJIJFFOK-WHZQZERISA-N D-aldose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-WHZQZERISA-N 0.000 description 1
- WQZGKKKJIJFFOK-IVMDWMLBSA-N D-allopyranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@H](O)[C@@H]1O WQZGKKKJIJFFOK-IVMDWMLBSA-N 0.000 description 1
- YTBSYETUWUMLBZ-IUYQGCFVSA-N D-erythrose Chemical compound OC[C@@H](O)[C@@H](O)C=O YTBSYETUWUMLBZ-IUYQGCFVSA-N 0.000 description 1
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 1
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 1
- YTBSYETUWUMLBZ-QWWZWVQMSA-N D-threose Chemical compound OC[C@@H](O)[C@H](O)C=O YTBSYETUWUMLBZ-QWWZWVQMSA-N 0.000 description 1
- 241000202296 Delphinium Species 0.000 description 1
- 206010013082 Discomfort Diseases 0.000 description 1
- 239000001692 EU approved anti-caking agent Substances 0.000 description 1
- 206010056474 Erythrosis Diseases 0.000 description 1
- 229920003134 Eudragit® polymer Polymers 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 240000001549 Ipomoea eriocarpa Species 0.000 description 1
- 235000005146 Ipomoea eriocarpa Nutrition 0.000 description 1
- 229910021577 Iron(II) chloride Inorganic materials 0.000 description 1
- WQZGKKKJIJFFOK-VSOAQEOCSA-N L-altropyranose Chemical compound OC[C@@H]1OC(O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-VSOAQEOCSA-N 0.000 description 1
- QAQJMLQRFWZOBN-LAUBAEHRSA-N L-ascorbyl-6-palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](O)[C@H]1OC(=O)C(O)=C1O QAQJMLQRFWZOBN-LAUBAEHRSA-N 0.000 description 1
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical group [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical group [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 1
- AQLLBJAXUCIJSR-UHFFFAOYSA-N OC(=O)C[Na] Chemical compound OC(=O)C[Na] AQLLBJAXUCIJSR-UHFFFAOYSA-N 0.000 description 1
- 239000008896 Opium Substances 0.000 description 1
- 229940123973 Oxygen scavenger Drugs 0.000 description 1
- 239000008118 PEG 6000 Substances 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229930182556 Polyacetal Natural products 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 229920002584 Polyethylene Glycol 6000 Polymers 0.000 description 1
- 229920001710 Polyorthoester Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 1
- 238000006828 Rosenmund reduction reaction Methods 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- YGCFIWIQZPHFLU-UHFFFAOYSA-N acesulfame Chemical compound CC1=CC(=O)NS(=O)(=O)O1 YGCFIWIQZPHFLU-UHFFFAOYSA-N 0.000 description 1
- 229960005164 acesulfame Drugs 0.000 description 1
- 125000005396 acrylic acid ester group Chemical group 0.000 description 1
- 238000006657 acyloin condensation reaction Methods 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 201000007930 alcohol dependence Diseases 0.000 description 1
- 150000001320 aldopentoses Chemical class 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 229910001420 alkaline earth metal ion Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 1
- SRBFZHDQGSBBOR-STGXQOJASA-N alpha-D-lyxopyranose Chemical compound O[C@@H]1CO[C@H](O)[C@@H](O)[C@H]1O SRBFZHDQGSBBOR-STGXQOJASA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 229920003144 amino alkyl methacrylate copolymer Polymers 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- DFMMVLFMMAQXHZ-CMGSAFQJSA-N apocarotenal Chemical compound O=CC(/C)=C/C=C/C(/C)=C/C=C/C=C(\C)/C=C/C=C(\C)C=CC1=C(C)CCCC1(C)C DFMMVLFMMAQXHZ-CMGSAFQJSA-N 0.000 description 1
- 229940019834 apocarotenal Drugs 0.000 description 1
- 239000012062 aqueous buffer Substances 0.000 description 1
- PYMYPHUHKUWMLA-WDCZJNDASA-N arabinose Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-WDCZJNDASA-N 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 239000012752 auxiliary agent Substances 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- UKMSUNONTOPOIO-UHFFFAOYSA-M behenate Chemical compound CCCCCCCCCCCCCCCCCCCCCC([O-])=O UKMSUNONTOPOIO-UHFFFAOYSA-M 0.000 description 1
- 229940116224 behenate Drugs 0.000 description 1
- 229940116226 behenic acid Drugs 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 229960003237 betaine Drugs 0.000 description 1
- 235000002185 betanin Nutrition 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- SRGKFVAASLQVBO-BTJKTKAUSA-N brompheniramine maleate Chemical compound OC(=O)\C=C/C(O)=O.C=1C=CC=NC=1C(CCN(C)C)C1=CC=C(Br)C=C1 SRGKFVAASLQVBO-BTJKTKAUSA-N 0.000 description 1
- 229940095259 butylated hydroxytoluene Drugs 0.000 description 1
- 235000009120 camo Nutrition 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 229960001803 cetirizine Drugs 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 235000005607 chanvre indien Nutrition 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 239000007806 chemical reaction intermediate Substances 0.000 description 1
- SOYKEARSMXGVTM-UHFFFAOYSA-N chlorphenamine Chemical compound C=1C=CC=NC=1C(CCN(C)C)C1=CC=C(Cl)C=C1 SOYKEARSMXGVTM-UHFFFAOYSA-N 0.000 description 1
- 229960003291 chlorphenamine Drugs 0.000 description 1
- 239000008199 coating composition Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical group [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 201000003740 cowpox Diseases 0.000 description 1
- 238000005336 cracking Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 229940109262 curcumin Drugs 0.000 description 1
- 239000000850 decongestant Substances 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 229960003782 dextromethorphan hydrobromide Drugs 0.000 description 1
- 235000015872 dietary supplement Nutrition 0.000 description 1
- VFLDPWHFBUODDF-UHFFFAOYSA-N diferuloylmethane Natural products C1=C(O)C(OC)=CC(C=CC(=O)CC(=O)C=CC=2C=C(OC)C(O)=CC=2)=C1 VFLDPWHFBUODDF-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 206010013663 drug dependence Diseases 0.000 description 1
- 239000013583 drug formulation Substances 0.000 description 1
- 238000007905 drug manufacturing Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 210000002388 eustachian tube Anatomy 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000004880 explosion Methods 0.000 description 1
- 229960003592 fexofenadine Drugs 0.000 description 1
- RWTNPBWLLIMQHL-UHFFFAOYSA-N fexofenadine Chemical compound C1=CC(C(C)(C(O)=O)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 RWTNPBWLLIMQHL-UHFFFAOYSA-N 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000013467 fragmentation Methods 0.000 description 1
- 238000006062 fragmentation reaction Methods 0.000 description 1
- 150000002240 furans Chemical class 0.000 description 1
- 229930182830 galactose Natural products 0.000 description 1
- 229940098330 gamma linoleic acid Drugs 0.000 description 1
- VZCCETWTMQHEPK-UHFFFAOYSA-N gamma-Linolensaeure Natural products CCCCCC=CCC=CCC=CCCCCC(O)=O VZCCETWTMQHEPK-UHFFFAOYSA-N 0.000 description 1
- FOYKKGHVWRFIBD-UHFFFAOYSA-N gamma-tocopherol acetate Natural products CC(=O)OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1 FOYKKGHVWRFIBD-UHFFFAOYSA-N 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 239000001087 glyceryl triacetate Substances 0.000 description 1
- 235000013773 glyceryl triacetate Nutrition 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 239000003979 granulating agent Substances 0.000 description 1
- 150000008282 halocarbons Chemical class 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 239000011487 hemp Substances 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- JMBRWJAVUIITGV-LNNMZZBZSA-N hydrocodone bitartrate Chemical compound [H+].[H+].[H+].[H+].O.O.O.O.O.[O-]C(=O)[C@H](O)[C@@H](O)C([O-])=O.[O-]C(=O)[C@H](O)[C@@H](O)C([O-])=O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)CC(=O)[C@@H]1OC1=C2C3=CC=C1OC.C([C@H]1[C@H](N(CC[C@@]112)C)C3)CC(=O)[C@@H]1OC1=C2C3=CC=C1OC JMBRWJAVUIITGV-LNNMZZBZSA-N 0.000 description 1
- 229960002764 hydrocodone bitartrate Drugs 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 229920000639 hydroxypropylmethylcellulose acetate succinate Polymers 0.000 description 1
- 125000002951 idosyl group Chemical class C1([C@@H](O)[C@H](O)[C@@H](O)[C@H](O1)CO)* 0.000 description 1
- 239000002117 illicit drug Substances 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000007373 indentation Methods 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- NMCUIPGRVMDVDB-UHFFFAOYSA-L iron dichloride Chemical compound Cl[Fe]Cl NMCUIPGRVMDVDB-UHFFFAOYSA-L 0.000 description 1
- AQBLLJNPHDIAPN-LNTINUHCSA-K iron(3+);(z)-4-oxopent-2-en-2-olate Chemical compound [Fe+3].C\C([O-])=C\C(C)=O.C\C([O-])=C\C(C)=O.C\C([O-])=C\C(C)=O AQBLLJNPHDIAPN-LNTINUHCSA-K 0.000 description 1
- 229940049918 linoleate Drugs 0.000 description 1
- 235000020778 linoleic acid Nutrition 0.000 description 1
- OYHQOLUKZRVURQ-IXWMQOLASA-N linoleic acid Natural products CCCCC\C=C/C\C=C\CCCCCCCC(O)=O OYHQOLUKZRVURQ-IXWMQOLASA-N 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 229940063557 methacrylate Drugs 0.000 description 1
- XMCDLLRJGFYERB-UHFFFAOYSA-N methyl formate prop-2-enoic acid Chemical compound COC=O.OC(=O)C=C XMCDLLRJGFYERB-UHFFFAOYSA-N 0.000 description 1
- 239000004200 microcrystalline wax Substances 0.000 description 1
- 235000019808 microcrystalline wax Nutrition 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- ARGKVCXINMKCAZ-UZRWAPQLSA-N neohesperidin Chemical compound C1=C(O)C(OC)=CC=C1[C@H]1OC2=CC(O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O3)O[C@H]3[C@@H]([C@H](O)[C@@H](O)[C@H](C)O3)O)=CC(O)=C2C(=O)C1 ARGKVCXINMKCAZ-UZRWAPQLSA-N 0.000 description 1
- ARGKVCXINMKCAZ-UHFFFAOYSA-N neohesperidine Natural products C1=C(O)C(OC)=CC=C1C1OC2=CC(OC3C(C(O)C(O)C(CO)O3)OC3C(C(O)C(O)C(C)O3)O)=CC(O)=C2C(=O)C1 ARGKVCXINMKCAZ-UHFFFAOYSA-N 0.000 description 1
- 229940030223 nexafed Drugs 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 229960001027 opium Drugs 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 150000002918 oxazolines Chemical class 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 229930015717 petunidin Natural products 0.000 description 1
- 235000006384 petunidin Nutrition 0.000 description 1
- QULMBDNPZCFSPR-UHFFFAOYSA-N petunidin chloride Chemical compound [Cl-].OC1=C(O)C(OC)=CC(C=2C(=CC=3C(O)=CC(O)=CC=3[O+]=2)O)=C1 QULMBDNPZCFSPR-UHFFFAOYSA-N 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- XNGIFLGASWRNHJ-UHFFFAOYSA-L phthalate(2-) Chemical compound [O-]C(=O)C1=CC=CC=C1C([O-])=O XNGIFLGASWRNHJ-UHFFFAOYSA-L 0.000 description 1
- 150000003021 phthalic acid derivatives Chemical class 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 229950004403 polifeprosan Drugs 0.000 description 1
- 238000005498 polishing Methods 0.000 description 1
- 229920000520 poly(3-hydroxybutyrate-co-3-hydroxyvalerate) Polymers 0.000 description 1
- 229920000218 poly(hydroxyvalerate) Polymers 0.000 description 1
- 239000002745 poly(ortho ester) Substances 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920001707 polybutylene terephthalate Polymers 0.000 description 1
- 229920001610 polycaprolactone Polymers 0.000 description 1
- 239000004632 polycaprolactone Substances 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 229920000867 polyelectrolyte Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229940050929 polyethylene glycol 3350 Drugs 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920006324 polyoxymethylene Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 229940100467 polyvinyl acetate phthalate Drugs 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 229920006316 polyvinylpyrrolidine Polymers 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- DJEHXEMURTVAOE-UHFFFAOYSA-M potassium bisulfite Chemical compound [K+].OS([O-])=O DJEHXEMURTVAOE-UHFFFAOYSA-M 0.000 description 1
- 229940099427 potassium bisulfite Drugs 0.000 description 1
- LWWSTSLFIIVTIS-UHFFFAOYSA-M potassium hydrogen sulfite sulfurous acid Chemical compound [K+].OS(O)=O.OS([O-])=O LWWSTSLFIIVTIS-UHFFFAOYSA-M 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 150000003230 pyrimidines Chemical class 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 239000002683 reaction inhibitor Substances 0.000 description 1
- 238000011946 reduction process Methods 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- WBHHMMIMDMUBKC-QJWNTBNXSA-M ricinoleate Chemical compound CCCCCC[C@@H](O)C\C=C/CCCCCCCC([O-])=O WBHHMMIMDMUBKC-QJWNTBNXSA-M 0.000 description 1
- 229940066675 ricinoleate Drugs 0.000 description 1
- 229960003656 ricinoleic acid Drugs 0.000 description 1
- FEUQNCSVHBHROZ-UHFFFAOYSA-N ricinoleic acid Natural products CCCCCCC(O[Si](C)(C)C)CC=CCCCCCCCC(=O)OC FEUQNCSVHBHROZ-UHFFFAOYSA-N 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 239000012748 slip agent Substances 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 235000002639 sodium chloride Nutrition 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 229920003109 sodium starch glycolate Polymers 0.000 description 1
- 239000008109 sodium starch glycolate Substances 0.000 description 1
- 229940079832 sodium starch glycolate Drugs 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 208000011117 substance-related disease Diseases 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- GMMAPXRGRVJYJY-UHFFFAOYSA-J tetrasodium 4-acetamido-5-hydroxy-6-[[7-sulfonato-4-[(4-sulfonatophenyl)diazenyl]naphthalen-1-yl]diazenyl]naphthalene-1,7-disulfonate Chemical compound [Na+].[Na+].[Na+].[Na+].OC1=C2C(NC(=O)C)=CC=C(S([O-])(=O)=O)C2=CC(S([O-])(=O)=O)=C1N=NC(C1=CC(=CC=C11)S([O-])(=O)=O)=CC=C1N=NC1=CC=C(S([O-])(=O)=O)C=C1 GMMAPXRGRVJYJY-UHFFFAOYSA-J 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 229920001169 thermoplastic Polymers 0.000 description 1
- 150000003557 thiazoles Chemical class 0.000 description 1
- 150000003548 thiazolidines Chemical class 0.000 description 1
- 150000003577 thiophenes Chemical class 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- 229930003802 tocotrienol Natural products 0.000 description 1
- 239000011731 tocotrienol Substances 0.000 description 1
- 235000019148 tocotrienols Nutrition 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 229960002622 triacetin Drugs 0.000 description 1
- 229960001128 triprolidine Drugs 0.000 description 1
- CBEQULMOCCWAQT-WOJGMQOQSA-N triprolidine Chemical compound C1=CC(C)=CC=C1C(\C=1N=CC=CC=1)=C/CN1CCCC1 CBEQULMOCCWAQT-WOJGMQOQSA-N 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 229940054882 zephrex-d Drugs 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/137—Arylalkylamines, e.g. amphetamine, epinephrine, salbutamol, ephedrine or methadone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Inorganic Chemistry (AREA)
- Emergency Medicine (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
本發明係關於一種醫藥劑型,其斷裂強度為至少300N且包含:(i)麻黃素組分,該麻黃素組分係選自由以下組成之群:麻黃素、偽麻黃素及其生理學上可接受之鹽,其中較佳該麻黃素組分之重量含量相對於該醫藥劑型之總重量在0.1至60wt.-%範圍內;及(ii)生理學上可接受之轉化抑制劑,該生理學上可接受之轉化抑制劑能夠抑制該麻黃素組分離體化學轉化為甲基安非他命。
Description
本發明係關於一種醫藥劑型,其斷裂強度為至少300N且包含:(i)麻黃素組分,該麻黃素組分選自由以下組成之群:麻黃素、偽麻黃素及其生理學上可接受之鹽,其中相對於醫藥劑型之總重量,麻黃素組分之重量含量較佳在0.1至60wt.-%範圍內;及(ii)生理學上可接受之轉化抑制劑,該生理學上可接受之轉化抑制劑能夠抑制麻黃素組分離體化學轉化為甲基安非他命(methamphetamine)。根據本發明之醫藥劑型提供針對損壞之抗性,特定而言針對麻黃素組分轉化為甲基安非他命(亦稱為例如「結晶甲安(Crystal Meth)」、「甲安(Meth)」、「水晶(Crystal)」、「亞霸(Yaba)」、「曲柄(Crank)」或「冰毒(Ice)」)。
偽麻黃素為刺激劑及去充血劑。其減輕組織充血、水腫及通常與感冒或過敏相關之鼻塞。其他有益作用可包括使鼻竇分泌物排出增加,及打開阻塞之耳咽管。
歸因於偽麻黃素在甲基安非他命之非法製造中的普遍濫用,已嚴格限制及控制偽麻黃素之分配,由此對罹患鼻塞及其他相關不適之個體構成過度的負擔,使其不能輕易獲得此高度有效之藥物。
不幸地,此類自麻黃素或偽麻黃素非法製造甲基安非他命亦對受害者造成嚴重身體傷害或死亡。因此,研發一種包含偽麻黃素且實質上抑制或阻止偽麻黃素或麻黃素化學轉化為甲基安非他命之有效防濫用組合物仍為緊急的未滿足的需求。
甲基安非他命(N-甲基安非他命、(R/S)-N-甲基-1-苯基丙-2-胺)亦以兩種具有單一立體中心之對映異構體的形式存在。
已藉由許多方法實現自偽麻黃素及麻黃素非法製造甲基安非他命,該等方法涉及用包括鋰、鋅、氫碘酸及磷之各種還原劑來還原偽麻黃素或麻黃素。
兩種不同方法可大致彼此區分開。在一鍋法中,視情況在粉碎之後,劑型在含有適合之化學品的適合之溶劑中經歷化學轉化。在兩鍋法中,視情況在粉碎之後,首先自劑型萃取偽麻黃素/麻黃素,且隨後使由此獲得之萃取物在 含有適合之化學品的適合之溶劑中經歷化學轉化。
流行的一鍋法為使用鋰及硝酸銨之所謂的「蘇打瓶振盪及焙燒(soda-bottle shake and bake)」程序(出於說明之目的亦稱為「振盪及焙燒一鍋程序(shake and bake one pot procedure)」)。該反應可被認為是「偽伯奇還原(pseudo-Birch reduction)」,其中硝酸銨與氫氧化鈉之反應產生氨,接著氨與鋰反應。
諸如醚、甲苯、輕質石油、氨、鹽酸、氫碘酸、氫氧化鈉及類似物之試劑及常用溶劑為非法製造商可獲得的(亦參見R.Turkington,Chemicals Used For Illegal Purposes,A Guide for First responders to Identify Explosives,Recreational Drugs,and Poisons,John Wiley & Sons 2010,第247頁)。
Skinner,Forensic Science International 1990,48(2),123-134係關於經由麻黃素之氫碘酸/紅磷還原來合成甲基安非他命。
Ely等人,Journal of Forensic Sciences 1990,35(3),720-723係關於麻黃素髮生鋰-氨還原變為甲基安非他命。
Person等人,J Forensic Sci.2005年1月;50(1):87-95係關於甲基安非他命製造之鋰-氨還原法(常常稱為「鋰-氨還原法」或「伯奇還原法」)之主要副產物的結構測定。
Lee等人,Forensic Sci Int.2006年9月12日;161(2-3):209-15係關於藉由埃姆德(Emde)、納加伊(Nagai)及莫斯科(Moscow)三種不同製造方法自麻黃素及偽麻黃素合成之甲基安非他命中之雜質的分析。
Salouros等人,J Forensic Sci.2010年5月;55(3):605-15係關於在藉由埃姆德途徑合成之甲基安非他命中發現之三種副產物的分離及鑑定,埃姆德途徑涉及分別自麻黃素或偽麻黃素製備中間物氯代偽麻黃素或氯代麻黃素。接著在壓力下在存在觸媒之情況下用氫將中間物還原為甲基安非他命。
Kunalan等人,Anal Chem.2012年7月3日;84(13):5744-52係關於與使用納加伊法合成之甲基安非他命相關之反應雜質的研究。
Romach等人,Drug and Alcohol Dependence,130(2013)13-23提供關於抗損壞藥物調配物之更新。
已引入各種固體醫藥劑量調配物,該等固體醫藥劑量調配物據稱在物理上阻礙自此類調配物(例如Tarex®及Nexafed®)萃取偽麻黃素。Zephrex-D®為抗甲基化形式之偽麻黃素,其在加熱時變得具膠黏性。
US 2004 0049079係關於一種抑制或防止在溶解金屬還原製程中使用無水氨作為溶劑之方法,其包括向無水氨中添加能夠清除當鹼金屬或鹼土金屬溶解於無水氨中時產生之溶劑化電子的化學試劑,該化學試劑添加至無水氨中使得當鹼金屬溶解於含有該化學試劑之無水氨中且此後將麻黃素、偽麻黃素或其組合引入無水氨以產生反應產物時,反應產物中之甲基安非他命產率低於50%,較佳低於10%,且更佳低於1%。
US 2008 0260836揭示包含第一聚合物及溶解溫度低於第一聚合物之第二聚合物的薄膜;其中薄膜之斷裂強度大於約750psi(5,171kPa)。
US 2008 0311187係關於如下醫藥劑型,其包含生理學有效量之生理活性物質(A);合成、半合成或天然聚合物(C);視情況存在之一或多種生理學上可接受之助劑物質(B)及視情況存在之合成、半合成或天然蠟(D),其中該醫藥劑型展現至少400N之抗壓碎性且其中在生理條件下生理活性物質(A)自該醫藥劑型之釋放為至少部分延遲的。
US 2009 0004267揭示一種經調配以使得更難誤用之多微粒醫藥劑型,其含有至少一種有可能誤用之活性物質(A);至少一種合成或天然聚合物(C);視情況存在之至少一種天然、半合成或合成蠟(D);至少一種崩解劑(E)及視情況存在之一或多種其他生理學相容之賦形劑(B),其中該醫藥劑型之個別粒 子展示至少500N之斷裂強度及在45分鐘之後至少75%之活性物質釋放,此釋放係根據歐洲藥典(Ph.Eur.)在具有沈錘之漿式混合器中在37℃及75rpm下在600ml之pH值為1.2的水性緩衝溶液中量測。
US 2009 0202634及WO 2009/092601係關於一種較佳具有其中所含之藥理學活性化合物(A)之控制釋放的醫藥劑型,該醫藥劑型極佳為抗損壞的且最佳沿延伸方向E1具有至少500N之斷裂強度B1且沿延伸方向E2具有小於500N之斷裂強度B2。
US 2011 077238揭示用於防止包括但不限於發生濫用之藥物之即刻釋放、持續或延長釋放及延遲釋放調配物的藥物產品(例如經口投與之藥物產品)的濫用之方法及組合物,其包含至少10重量%之羥丙基纖維素;聚氧化乙烯;及選自由交聯聚維酮、澱粉乙醇酸鈉及交聯羧甲基纖維素鈉組成之群的崩解劑;其中以重量計羥丙基纖維素與聚氧化乙烯之比率在約10:1與1:10之間。
US 2013 225625係關於如下醫藥劑型,其斷裂強度為至少500N且包含藥理學活性化合物、平均分子量為至少200,000g/mol之聚氧化烯及非離子表面活性劑;其中以醫藥劑型之總重量計聚氧化烯之含量在20至75wt.-%範圍內。
US 2014 0010874在某些實施例中揭示一種固體口服醫藥劑型,其包含:(a)惰性抗損壞核心;及(b)包圍核心之包衣,該包衣包含活性劑。
US 2014 034885係關於用於諸如藉由減小甲基安非他命實驗室之爆炸可能性來穩定甲基安非他命實驗室的方法及組合物。
US 2014 356426係關於一種包含一或多個粒子之抗損壞醫藥劑型,其中該一或多個粒子中之每一者包含藥理學活性成分及生理學上可接受之聚合物;具有至少300N之斷裂強度;具有至少2mg之重量;且視情況,包含薄膜包衣;其中該醫藥劑型之總重量大於該一或多個粒子之總重量。
US 2015 064250提供如下抗損壞劑型,其包括包埋於熱可成形基質中之治療劑-基質複合物;使得該複合物包括結合於至少一種基質以形成治療劑-基質複合物的至少一種治療劑。該至少一種基質係選自由以下組成之群:聚電解質、有機相對離子、藥理學惰性之有機前藥組分、包藏化合物及無機吸附劑;且該熱可成形基質包括一或多種熱塑性聚合物及視情況存在之至少一種醫藥添加劑。
US 2016 0089439係關於含有生物相容性感官(食品調味)賦形劑之麻黃素或偽麻黃素組合物,其可防止自麻黃素或偽麻黃素非法製造甲基安非他命。
WO 00/15261旨在使得在非法藥物製備中使用擬交感神經作用胺組合物為不切實際的。更特定而言,自所揭示之偽麻黃素鹽酸鹽調配物製備甲基安非他命受到抑制。WO 00/15261定義了包含擬交感神經作用胺鹽及至少一種組合抑制劑之醫藥組合物,該組合抑制劑起到既妨礙擬交感神經作用胺與組合物分離又妨礙擬交感神經作用胺轉化為另一藥理學活性化合物的作用。所涵蓋之組合物亦可在任何混合物中包括反應及分離抑制劑,以確保最大程度地防止使用含擬交感神經作用胺之組合物進行非法藥物製造。該組合抑制劑、該反應抑制劑及該分離抑制劑之存在不顯著改變擬交感神經作用胺自組合物之釋放。
WO 2015/048597大體係關於含有生物相容性感官賦形劑之麻黃素或偽麻黃素組合物,其將防止自麻黃素或偽麻黃素非法製造甲基安非他命。典型地用作食品調味劑之感官藥劑為基於吡嗪之賦形劑,該等基於吡嗪之賦形劑在與麻黃素或偽麻黃素共調配時阻止純甲基安非他命之分離及轉化。
先前技術中用於防止自麻黃素或偽麻黃素非法製造甲基安非他命之構思在各方面均不令人滿意且需要改良。
本發明之目標為提供如下醫藥劑型,該等醫藥劑型含有麻黃素、偽麻黃素或其生理學上可接受之鹽且特定而言,關於防止非法製造甲基安非他 命,該等醫藥劑型與先前技術相比具有優勢。
此目標已由專利申請範圍之主題達成。
已令人驚訝地發現,可提供如下醫藥劑型,該等醫藥劑型含有麻黃素、偽麻黃素或其生理學上可接受之鹽且尤其是在遵循特別流行之「振盪及焙燒一鍋」程序時,實質上阻礙(若非完全阻止)麻黃素或偽麻黃素化學轉化為甲基安非他命。另外,已令人驚訝地發現,可提供如下醫藥劑型,該等醫藥劑型含有麻黃素、偽麻黃素或其生理學上可接受之鹽且在萃取麻黃素或偽麻黃素之後實質上阻礙麻黃素或偽麻黃素化學轉化為甲基安非他命。
另外,已令人驚訝地發現,儘管醫藥劑型之機械強度增加,但即使至少在一定程度上可達成對醫藥劑型之機械破壞,例如即使意欲非法誤用之人可以使用適合之設備,以上阻礙作用仍保留。
另外,已令人驚訝地發現,適合之轉化抑制劑可抑制麻黃素或偽麻黃素離體化學轉化為甲基安非他命,例如藉由消耗化學品(還原劑),使得其不能與麻黃素或偽麻黃素反應,或者藉由與麻黃素或偽麻黃素或其反應中間物中之一者反應,由此使得副產物不同於甲基安非他命。
此外,已令人驚訝地發現,聚乙烯吡咯啶酮(PVP)及交聯羧甲基纖維素,特定而言當彼此組合時,則提供在研磨後產生粗粒子之醫藥劑型(若醫藥劑型完全可研磨)。另外,當設法用水及二乙醚自此類粗粒子萃取麻黃素或偽麻黃素時,形成穩定乳液,亦即乙醚相不與水相分離,使得根本不能或至少幾乎不能藉助於分液漏斗萃取。
此外,指示聚乙烯吡咯啶酮(PVP)在濫用者嘗試自醫藥劑型萃取麻黃素或偽麻黃素或嘗試將麻黃素或偽麻黃素化學轉化為甲基安非他命時習知使用之彼等溶劑中展現一定溶解度。此在所獲得之中間萃取物或所產生之產物中產生所需雜質,因此污染中間萃取物或最終產物且分別阻礙其進一步濫用及投與。
本發明之第一態樣係關於一種醫藥劑型,其斷裂強度為至少300N且包含:(i)麻黃素組分,該麻黃素組分選自由以下組成之群:麻黃素、偽麻黃素及其生理學上可接受之鹽,較佳為偽麻黃素鹽酸鹽或偽麻黃素硫酸鹽,其中相對於醫藥劑型之總重量,麻黃素組分之重量含量較佳在0.1至60wt.-%範圍內;及(ii)生理學上可接受之轉化抑制劑,該生理學上可接受之轉化抑制劑能夠抑制麻黃素組分離體化學轉化為甲基安非他命。
除非另外明確陳述,否則出於描述之目的,所有百分比為重量百分比(wt.-%)。
除非另外明確陳述,否則出於描述之目的,術語「衍生物」包括但不限於(適當時):- 具有較佳選自以下之陽離子的鹽:鹼金屬離子、鹼土金屬離子、銨離子及類似離子;- 具有較佳選自以下之陰離子的鹽:鹵素離子、硫酸根、磷酸根、乙酸根、硝酸根及類似離子;- 與較佳選自以下之醇的酯:甲醇、乙醇、丙醇、丁醇及類似物;- 與較佳選自以下之羧酸的酯:甲酸、乙酸、丙酸、脂肪酸及類似物;- 與較佳選自以下之羧酸的醯胺:甲酸、乙酸、丙酸、脂肪酸及類似物;及- 前述各項之任何組合。
除非另外明確陳述,否則出於描述之目的,關於麻黃素組分含量(例如以mg計或以wt.-%計)及任何組合之藥理學活性成分(若有)之所有值係分別以關於麻黃素組分之游離鹼(亦即分別為麻黃素游離鹼及偽麻黃素游離鹼)以及組合之藥理學活性成分的重量當量表示。
出於描述之目的,提供於括號中之E編號係指根據食品添加劑國際編號系統(INS)允許用作供在歐盟及EFTA使用之食品添加劑的物質的各別編 碼。
根據本發明之醫藥劑型包含選自由麻黃素、偽麻黃素及其生理學上可接受之鹽組成之群的麻黃素組分。
在一較佳實施例中,醫藥劑型含有麻黃素組分作為唯一藥理學活性成分。
在另一較佳實施例中,醫藥劑型含有麻黃素組分與一或多種藥理學活性成分之組合。
麻黃素組分可以生理學上可接受之鹽(例如生理學上可接受之酸加成鹽)的形式存在。較佳之鹽包括但不限於鹽酸鹽及硫酸鹽。較佳地,麻黃素組分包含偽麻黃素鹽酸鹽或偽麻黃素硫酸鹽或基本上由其組成。
生理學上可接受之鹽包含酸加成鹽形式,其可適宜地藉由用適當有機及無機酸處理鹼形式之麻黃素組分來獲得。該鹽亦包含水合物及麻黃素組分能夠形成之溶劑加成形式(solvent addition form)。此類形式之實例為例如水合物、醇合物及類似物。
麻黃素組分以治療有效量存在於醫藥劑型中。構成治療有效量之量根據所用活性成分、所治療之病狀、該病狀之嚴重程度、所治療之患者及醫藥劑型經設計用於即刻釋放抑或遲滯釋放而變化。
相對於醫藥劑型之總重量,麻黃素組分之重量含量較佳在0.1至60wt.-%範圍內。較佳地,相對於醫藥劑型之總重量,麻黃素組分之重量含量在15至45wt.-%範圍內。
較佳地,以醫藥劑型之總重量計,麻黃素組分之重量含量在30±18wt.-%、更佳30±15wt.-%、更佳30±12wt.-%、更佳30±9wt.-%、甚至更佳30±6wt.-%且最佳30±3wt.-%範圍內。
醫藥劑型中之麻黃素組分之絕對劑量不受限制。適合於投與之麻黃 素組分的劑量較佳在0.1mg至500mg範圍內,更佳在1.0mg至400mg範圍內,甚至更佳在5.0mg至300mg範圍內,且最佳在10mg至250mg範圍內。
在一較佳實施例中,麻黃素組分以以下量含於醫藥劑型中:7.5±5mg,10±5mg,20±5mg,30±5mg,40±5mg,50±5mg,60±5mg,70±5mg,80±5mg,90±5mg,100±5mg,110±5mg,120±5mg,130±5,140±5mg,150±5mg,160±5mg,170±5mg,180±5mg,190±5mg,200±5mg,210±5mg,220±5mg,230±5mg,240±5mg,250±5mg,260±5mg,270±5mg,280±5mg,290±5mg,或300±5mg。
麻黃素組分與一或多種其他藥理學活性成分之較佳組合包括但不限於偽麻黃素或其生理學上可接受之鹽與以下物質之組合:阿伐司汀(acrivastine)、阿紮他定順丁烯二酸鹽(azatadine maleate)、溴菲安明順丁烯二酸鹽(brompheniramine maleate)、氯菲安明(chlorpheniramine)、氯菲安明順丁烯二酸鹽、西替利嗪鹽酸鹽(cetirizine hydrochloride)、氯馬斯汀反丁烯二酸鹽(clemastine fumarate)、可待因磷酸鹽(codeine phosphate)、地洛他定(desloratadine)、右溴菲安明順丁烯二酸鹽(dexbromopheniramine maleate)、右美沙芬氫溴酸鹽(dextromethorphan hydrobromide)、苯海拉明鹽酸鹽(diphenhydramine hydrochloride)、非索非那定鹽酸鹽(fexofenadine hydrochloride)、愈創甘油醚(guaifenesin)、氫可酮酒石酸氫鹽(hydrocodone bitartrate)、布洛芬(ibuprofen)、氯雷他定(loratadine)、萘普生鈉(naproxen sodium)、對乙醯胺基酚及/或曲普利啶鹽酸鹽(triprolidine hydrochloride)。此類二元或三元組合可作為調配物以習知醫藥劑型形式商購獲得。
麻黃素組分及一或多種其他藥理學活性成分可藉由相同或不同之釋放動力學自根據本發明之醫藥劑型釋放。
在一較佳實施例中,麻黃素組分以及一或多種其他藥理學活性成分 係根據即刻釋放型態自醫藥劑型釋放。
在另一較佳實施例中,麻黃素組分以及一或多種其他藥理學活性成分係根據延期釋放型態自醫藥劑型釋放。
在另一較佳實施例中,麻黃素組分係根據延期釋放型態自醫藥劑型釋放,而一或多種其他藥理學活性成分係根據即刻釋放型態自醫藥劑型釋放。
在另一較佳實施例中,麻黃素組分係根據即刻釋放型態自醫藥劑型釋放,而一或多種其他藥理學活性成分係根據延期釋放型態自醫藥劑型釋放。
根據本發明之偽麻黃素或其生理學上可接受之鹽與曲普利啶或其生理學上可接受之鹽(較佳為曲普利啶鹽酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約2.5mg之劑量下的曲普利啶或其生理學上可接受之鹽(較佳為曲普利啶鹽酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與萘普生或其生理學上可接受之鹽(較佳為萘普生鈉)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約240mg之劑量下的萘普生或其生理學上可接受之鹽(較佳為萘普生鈉)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與非索非那定或其生理學上可接受之鹽(較佳為非索非那定鹽酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約60mg之劑量下的非索非那定或其生理學上可接受之鹽(較佳為非索非那定鹽酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與氯雷他定或其生理學上可接受之鹽的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳 在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約5mg或約10mg之劑量下的氯雷他定或其生理學上可接受之鹽的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與阿伐司汀或其生理學上可接受之鹽的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約8mg之劑量下的阿伐司汀或其生理學上可接受之鹽的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與西替利嗪或其生理學上可接受之鹽(較佳為西替利嗪鹽酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約5mg之劑量下的西替利嗪或其生理學上可接受之鹽(較佳為西替利嗪鹽酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與氯菲安明或其生理學上可接受之鹽(較佳為氯菲安明順丁烯二酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與氯菲安明或其生理學上可接受之鹽(較佳為氯菲安明順丁烯二酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與愈創甘油醚或其生理學上可接受之鹽的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約1200mg之劑量下的愈創甘油醚或其生理學上可接受之鹽的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與布洛芬或其生理學上可接受之鹽的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約100mg、約200mg或約400mg之劑量下的布洛芬或其生理學上可接受 之鹽的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與對乙醯胺基酚(乙醯胺酚)或其生理學上可接受之鹽的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與較佳在例如約250mg、約300mg、約450mg、約500mg、約550mg、約600mg或約650mg之劑量下的對乙醯胺基酚或其生理學上可接受之鹽的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與阿紮他定或其生理學上可接受之鹽(較佳為阿紮他定順丁烯二酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與阿紮他定或其生理學上可接受之鹽(較佳為阿紮他定順丁烯二酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與溴菲安明或其生理學上可接受之鹽(較佳為溴菲安明順丁烯二酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與溴菲安明或其生理學上可接受之鹽(較佳為溴菲安明順丁烯二酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與地洛他定或其生理學上可接受之鹽的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與地洛他定或其生理學上可接受之鹽的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與右溴菲安明或其生理學上可接受之鹽(較佳為右溴菲安明順丁烯二酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或 約240mg之劑量下的偽麻黃素與右溴菲安明或其生理學上可接受之鹽(較佳為右溴菲安明順丁烯二酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與苯海拉明或其生理學上可接受之鹽(較佳為苯海拉明鹽酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與苯海拉明或其生理學上可接受之鹽(較佳為苯海拉明鹽酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與氫可酮或其生理學上可接受之鹽(較佳為氫可酮酒石酸氫鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與氫可酮或其生理學上可接受之鹽(較佳為氫可酮酒石酸氫鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與可待因或其生理學上可接受之鹽(較佳為可待因磷酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與可待因或其生理學上可接受之鹽(較佳為可待因磷酸鹽)的組合。
根據本發明之偽麻黃素或其生理學上可接受之鹽與氯馬斯汀或其生理學上可接受之鹽(較佳為氯馬斯汀反丁烯二酸鹽)的較佳組合包括但不限於較佳呈鹽酸鹽或硫酸鹽形式、較佳在例如約30mg、約60mg、約120mg或約240mg之劑量下的偽麻黃素與氯馬斯汀或其生理學上可接受之鹽(較佳為氯馬斯汀反丁烯二酸鹽)的組合。
根據本發明之醫藥劑型包含生理學上可接受之轉化抑制劑,其能夠抑制麻黃素組分離體化學轉化為甲基安非他命。
根據本發明之醫藥劑型可含有兩種或更多種轉化抑制劑之組合。除 非另外明確陳述,否則提及轉化抑制劑之所有數值係指醫藥劑型中所含之所有轉化抑制劑的總量。
在一較佳實施例中,醫藥劑型含有單一轉化抑制劑。
該轉化抑制劑能夠抑制麻黃素組分離體化學轉化為甲基安非他命。因此,當例如在嘗試自麻黃素組分非法合成甲基安非他命之情況下損壞醫藥劑型時,轉化抑制劑抑制、阻礙、減少或阻抑預期化學轉化。熟練人員承認可經由涉及不同機制且需要不同化學品(典型地為還原劑)之各種合成途徑自麻黃素組分合成甲基安非他命。
較佳地,轉化抑制劑將麻黃素組分離體化學轉化為甲基安非他命抑制至少10%,較佳至少20%,更佳至少30%,更佳至少50%,甚至更佳至少75%,最佳至少90%,且特定而言為至少95%,在各情況下係與如下情況相對比較:其中對應比較醫藥劑型係在相同離體化學轉化條件下但在不存在轉化抑制劑之情況下進行處理且暴露於相同量之相同化學品。較佳地,該等離體化學轉化條件係選自由以下組成之群:- 振盪及焙燒一鍋程序條件(Li+NH4NO3);- 伯奇還原條件(含鹼金屬(典型地為Li或Na)之液體NH3);- 布沃-布朗還原(Bouveault-Blanc reduction)條件(含鹼金屬(典型地為Li或Na)之惰性溶劑);- 酮醇縮合(acyloin condensation)條件(含鹼金屬(典型地為Li或Na)之惰性溶劑);- 埃姆德途徑(Emde route)條件(SOCl2+Pd-BaSO4/H2),其在第二步中涉及羅森門還原(Rosenmund reduction);- 納加伊途徑(Nagai route)條件(HI+紅P);- 海波途徑(hypo route)條件(H3PO2+I2);及 - 莫斯科途徑(Moscow route)條件(I2+紅P+H2O)。
關於振盪及焙燒一鍋程序之條件,參考R.Turkington,Chemicals Used For Illegal Purposes,A Guide for First responders to Identify Explosives,Recreational Drugs,and Poisons,John Wiley & Sons 2010,第247頁。關於伯奇還原之條件,參考Person等人,J Forensic Sci.2005年1月;50(1):87-95。關於埃姆德途徑、納加伊途徑、海波途徑及莫斯科途徑之條件,參考Salouros等人,J Forensic Sci.2010年5月;55(3):605-15。
轉化抑制劑可通過與競爭性基質不同之機制起作用。舉例而言,當醫藥劑型經歷伯奇還原條件或偽伯奇還原條件(例如根據振盪及焙燒一鍋程序)時,轉化抑制劑可例如藉由布沃-布朗還原消耗還原劑,使得還原劑不可再用於將麻黃素組分還原為甲基安非他命(犧牲基質)。或者,在相同條件下,轉化抑制劑可例如在酮醇縮合中消耗麻黃素組分,使得麻黃素組分不再可用於轉化為甲基安非他命(副反應基質)。
因此,在一較佳實施例中,轉化抑制劑為犧牲基質,其在離體化學轉化條件下替代至少一部分麻黃素組分發生轉化。
在另一較佳實施例中,轉化抑制劑為副反應基質,其在離體化學轉化條件下與至少一部分麻黃素組分反應以形成不同於N-甲基安非他命之副產物。
在根據本發明之醫藥劑型之一較佳實施例中,轉化抑制劑為自由基清除劑或離子清除劑。
在根據本發明之醫藥劑型之一較佳實施例中,轉化抑制劑催化自經溶劑化之鹼金屬及氨形成鹼金屬醯胺(例如LiNH2或NaNH2)(例如Li+NH3->LiNH2+1/2 H2或Na+NH3->NaNH2+1/2 H2)。
在根據本發明之醫藥劑型之一較佳實施例中,轉化抑制劑影響變性。
在根據本發明之醫藥劑型之一較佳實施例中,轉化抑制劑包含選自由以下組成之群的自由基清除劑或離子清除劑(下文中亦稱為「轉化抑制劑I型」)或基本上由其組成:(i)抗氧化劑,其較佳選自由以下組成之群:抗壞血酸及抗壞血酸衍生物、赤藻糖酸及赤藻糖酸衍生物、生育酚及生育酚衍生物、沒食子酸酯、亞硫酸鹽、硫醇、類胡蘿蔔素及葉黃素、視黃醇及視黃醇衍生物及酚類或其任何組合;(ii)其他自由基捕獲劑或陰離子捕獲劑,其較佳選自由以下組成之群:烷基鹵化物、異腈及其他捕獲劑或其任何組合;(iii)複合劑,其較佳選自由以下組成之群:乙二胺四乙酸、環糊精、冠醚(例如12-冠-4)及穴狀配位子或其任何組合;(iv)沈澱劑,其較佳選自由以下組成之群:鹼金屬磷酸鹽及鹼金屬碳酸鹽或其任何組合;及(v)前述各項之任何組合。
當抗氧化劑為抗壞血酸或抗壞血酸衍生物時,其較佳係選自由以下組成之群:抗壞血酸(E300)、抗壞血酸鈉(E301)、抗壞血酸鉀(E303)、抗壞血酸鈣(E302)、抗壞血酸棕櫚酸酯(E304a)及硬脂酸抗壞血酸酯(E305)或其任何組合。當抗氧化劑為抗壞血酸赤藻糖酸或赤藻糖酸衍生物時,其較佳係選自由以下組成之群:赤藻糖酸(異抗壞血酸)(E315)及赤藻糖酸鈉(E316)或其任何組合。當抗氧化劑為生育酚或生育酚衍生物時,其較佳係選自由以下組成之群:α-生育酚、β-生育酚、γ-生育酚(E306、E307、E309)、a-生育酚乙酸酯及生育三烯酚(tocotrienole)或其任何組合。當抗氧化劑為沒食子酸酯時,其較佳係選自由以下組成之群:沒食子酸乙酯(E313)、沒食子酸丙酯(E310)、沒食子酸辛酯(E311)及沒食子酸十二酯(沒食子酸月桂酯)(E312)或其任何組合。當抗氧化劑為亞硫酸鹽時,其較佳係選自由以下組成之群:亞硫酸鈉(E221)、亞硫酸氫鈉(E222)、偏亞 硫酸鈉(E223)、亞硫酸鉀(E225)、亞硫酸氫鉀(E228)、偏亞硫酸氫鉀(E224)、亞硫酸鈣(E226)、亞硫酸氫鈣(E227)及雙(環己基)二硫化物或其任何組合。當抗氧化劑為硫醇時,其較佳係選自由以下組成之群:麩胱甘肽、半胱胺酸(E920)及單硫代甘油或其任何組合。當抗氧化劑為類胡蘿蔔素或葉黃素時,其較佳係選自由以下組成之群:β-胡蘿蔔素(E160a)、阿樸胡蘿蔔醛(apocarotenal)(E160e)、β-阿樸(apo)-8'-胡蘿蔔酸乙酯(E160f)、番茄素(E160d)、隱黃質(E161c)、辣椒紅素(E161c)、黃體素(E161b)及角黃素(E161g)或其任何組合。當抗氧化劑為視黃醇或視黃醇衍生物時,其較佳為視黃醇。當抗氧化劑為酚類時,其較佳係選自由以下組成之群:丁基化羥基茴香醚[=丁基羥基茴香醚(BHA)](E320)、丁基化羥基甲苯[=丁基羥基甲苯(BHT)](E321)、第三丁基氫醌(E319)、己基間苯二酚(E856)及降二氫愈創木酸。
當其他自由基捕獲劑或陰離子捕獲劑為烷基鹵化物時,其較佳係選自由以下組成之群:三氯乙烯、1,1,1,2-四氟乙烷、2-氯-6-(三氯-甲基)吡啶及1-氯甲基萘或其任何組合。當其他自由基捕獲劑或陰離子捕獲劑為其他捕獲劑時,其較佳係選自由以下組成之群:脲及脲衍生物(E927b)及乙醯舒泛(acesulfam)(E950)或其任何組合。
在根據本發明之醫藥劑型之一較佳實施例中,轉化抑制劑包含選自由以下組成之群的競爭性基質(下文中亦稱為「轉化抑制劑II型」)或基本上由其組成:(i)食品調味賦形劑(感官),其較佳選自由以下組成之群:吡嗪、嘧啶、呋喃、噁唑啉、噻吩、噻唑啶、噻唑、核苷酸及其他食品調味賦形劑或其任何組合;(ii)甜味劑,其較佳選自由以下組成之群:糖精(E954)、阿斯巴甜(aspartame)(E951)、新橘皮苷二氫查酮(neohesperidin dihydrochalcone)(E959)、紐甜(neotam)(E961)及愛德萬甜(advantame)或其任何組合; (iii)食品著色劑,其較佳選自由以下組成之群:類胡蘿蔔素及葉黃素、偶氮染料、酚類、葉綠素、花青素及其他食品著色劑或其任何組合;(iv)其他競爭性基質,其較佳選自由以下組成之群:苯甲酸鹽、鄰苯二甲酸酯及其他化合物或其任何組合;及(v)前述各項之任何組合。
各種嘧啶、呋喃、噁唑啉、噻吩、噻唑啶、噻唑及類似物及其感官特性詳細描述於Piatauro,N.D.「Food Flavoring Processes」Noyes Data Corporation:Park Ridge,1976中,該文獻以全文引用之方式併入本文中。
當食品調味賦形劑為吡嗪時,其較佳係選自由以下組成之群:乙醯吡嗪、2-乙氧基-5-甲基吡嗪、2-乙氧基-6-甲基吡嗪、2-異丁基-3-甲氧基吡嗪、2-甲氧基-3-甲基吡嗪及2,3.5-三甲基吡嗪或其任何組合。當食品調味賦形劑為噻唑時,其較佳為2-乙醯基噻唑。當食品調味賦形劑為核苷酸時,其較佳係選自由以下組成之群:鳥苷酸(E626)、鳥苷酸二鈉(E627)、鳥苷酸二鉀(E628)、鳥苷酸鈣(E629)、肌苷酸(E630)、肌苷酸二鈉(E631)、肌苷酸二鉀(E632)、肌苷酸鈣(E633)、5'-核糖核苷酸二鈉(E634)及5'-核糖核苷酸鈣(E635)或其任何組合。當食品調味賦形劑為其他食品調味賦形劑時,其較佳係選自由以下組成之群:鄰胺基苯甲酸異丁酯及香草醛或其任何組合。香草醛為尤其較佳的。
當食品著色劑為偶氮染料時,其較佳係選自由以下組成之群:酒石黃(E102)、晚霞黃fcf(E110)、偶氮玉紅(E122)、胭脂蟲紅a(E124)、阿洛拉紅ac(allura red ac)及其鹽(E129)、莧紅(E123)、立索玉紅bk(lithol rubin bk)(E180)、亮黑bn(brilliant black bn)(E151)、棕色fk(brown fk)(E154)及褐色ht(brown ht)(E155)或其任何組合。當食品著色劑為酚類時,其較佳為甜菜苷(E162)。當食品著色劑為葉綠素時,其較佳係選自由以下組成之群:葉綠素(E140)及葉綠素銅錯合物(E141)或其任何組合。當時食品著色劑為花青素,其較佳係選自由以下組成 之群:天竺葵色素及其糖苷(E163a)、矢車菊色素及其糖苷(E163b)、芍藥色素及其糖苷(E163c)、飛燕草色素及其糖苷(E163d)、牽牛花素及其糖苷(E163e)及錦葵色素(E163f)或其任何組合。當食品著色劑為其他食品著色劑時,其較佳係選自由以下組成之群:薑黃素(cucumin)(E100)、核黃素(E101)、核黃素-5-磷酸鹽(E101a)、喹啉黃ws(E104)、胭脂紅(E120)、赤藻紅(E127)、專利藍v(E131)、靛藍胭脂紅(E132)、亮藍fcf(E133)及綠色s(E142)或其任何組合。
當其他競爭性基質為苯甲酸鹽時,其較佳係選自由以下組成之群:苯甲酸(E210)、苯甲酸鈉(E211)、苯甲酸鉀(E212)及苯甲酸鈣(E213)或其任何組合。當其他競爭性基質為鄰苯二甲酸酯時,其較佳係選自由以下組成之群:鄰苯二甲酸二乙酯、鄰苯二甲酸羥丙基甲基纖維素及聚乙酸鄰苯二甲酸乙烯酯酯或其任何組合。當其他競爭性基質為其他化合物時,其較佳係選自由以下組成之群:苯甲醇(E1519)、2-氯-6-(三氯甲基)吡啶及五甲基色原醇或其任何組合。
在根據本發明之醫藥劑型之一較佳實施例中,轉化抑制劑包含選自由以下組成之群的競爭性基質(下文中亦稱為「轉化抑制劑III型」)或基本上由其組成:(i)羧酸酯,其較佳選自由以下組成之群:醫藥學上可接受之酸的酯、聚合物之酯及脂肪酸之酯或其任何組合;(ii)醛,其較佳選自由以下組成之群:醫藥學上可接受之醛及醛醣或其任何組合;及(iii)前述各項之任何組合。
當羧酸酯為醫藥學上可接受之酸的酯時,其較佳係選自由以下組成之群:抗壞血酸酯(E304)、乙酸酯、苯甲酸酯、對羥基苯甲酸酯、乙基對羥基苯甲酸酯(對羥基苯甲酸乙酯)(E214)、乙基對羥基苯甲酸鈉(E215)、丙基對羥基苯甲酸酯(E216)、丙基對羥基苯甲酸鈉(E217)、甲基對羥基苯甲酸酯(E218)、甲基 對羥基苯甲酸鈉(E219)、檸檬酸酯、反丁烯二酸酯、乳酸酯、順丁烯二酸酯、蘋果酸酯、甲基丙烯酸酯、山梨酸酯、丁二酸酯、酒石酸酯、胺基酸酯、乙二胺四乙酸酯、赤藻糖酸酯、聚半乳糖醛酸酯、海藻酸酯或其任何組合。當羧酸酯為聚合物之酯時,其較佳係選自由以下組成之群:乙烯-乙酸乙烯酯-共聚物、聚乙酸乙烯酯、乙酸纖維素及乙酸丁二酸羥丙基甲基纖維素或其任何組合。當羧酸酯為脂肪酸之酯時,其較佳係選自由以下組成之群:癸酸酯、月桂酸酯、肉豆蔻酸酯、棕櫚酸酯、硬脂酸酯、油酸酯、亞油酸酯、γ-亞油酸酯、蓖麻油酸酯、花生酸酯及山俞酸酯或其任何組合。
當醛為醫藥學上可接受之醛時,其較佳係選自由以下組成之群:苯甲醛、肉桂醛及香草醛或其任何組合。香草醛為尤其較佳的。當醛為醛醣時,其較佳係選自由以下組成之群:甘油醛、醛丁醣(赤藻糖或蘇糖)、醛戊醣(核糖、阿拉伯糖、木糖或來蘇糖(lyxose))及醛己醣(阿洛糖(allose)、阿卓糖(altrose)、葡萄糖、甘露糖、古洛糖(gulose)、艾杜糖(idose)、半乳糖或塔羅糖(talose))或其任何組合。
在根據本發明之醫藥劑型之一較佳實施例中,轉化抑制劑包含觸媒(下文中亦稱為「轉化抑制劑IV型」)或基本上由其組成,其中該觸媒為(i)金屬觸媒,其較佳選自由以下組成之群:Fe(II)鹽、Fe(III)鹽、氧化鐵、鈷鹽、鎳鹽及錳鹽或其任何組合;或者(ii)有機觸媒,其較佳選自由以下組成之群:異戊二烯、丁二烯、間戊二烯、二甲基丁二烯、己二烯、苯乙烯、甲基苯乙烯、萘及蒽或其任何組合;或者(iii)前述各項之任何組合;其中在任一情況下,觸媒能夠催化自經溶劑化之鹼金屬及氨形成鹼金屬醯胺(M+NH3->MNH2+1/2 H2,其中M=Li、Na、K)。
當金屬觸媒為Fe(II)鹽時,其較佳係選自由以下組成之群:FeCl2、 二茂鐵、二茂鐵衍生物二茂鐵喹(ferroquine)及反丁烯二酸Fe(II)或其任何組合。當金屬觸媒為Fe(III)鹽時,其較佳係選自由以下組成之群:FeCl3、檸檬酸Fe(III)、三(乙醯基丙酮基(acetylacetonato))鐵(III)及硝酸Fe(III)或其任何組合。當金屬觸媒為鈷鹽時,其較佳係選自由以下組成之群:氯化鈷、溴化鈷、乙酸鈷及硫酸鈷或其任何組合。當金屬觸媒為鎳鹽時,其較佳係選自由以下組成之群:氯化鎳、溴化鎳、乙酸鎳及硫酸鎳或其任何組合。當金屬觸媒為錳鹽時,其較佳係選自由以下組成之群:氯化錳、溴化錳、乙酸錳及硫酸錳或其任何組合。
預期根據本發明之醫藥劑型可不只包含單一轉化抑制劑。如上文指出,醫藥劑型可例如含有均為I型或均為II型或均為III型或均為IV型之兩種不同的轉化抑制劑。
亦預期不同類型之轉化抑制劑可組合彼此。舉例而言,轉化抑制劑I型可與轉化抑制劑II型組合(縮寫為「I+II」);或者轉化抑制劑I型可與轉化抑制劑III型組合(縮寫為「I+III」)。因此,根據此縮寫系統,根據本發明之醫藥劑型較佳包含兩種轉化抑制劑之組合,其中該組合係選自由以下組成之群:I+II、I+III、I+IV、II+III、II+IV及III+IV。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑之重量含量大於0.50wt.-%,更佳大於1.25wt.-%,更佳為至少1.50wt.-%,甚至更佳為至少3.00wt.-%,在各情況下均係相對於醫藥劑型之總重量。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑之重量含量為至少0.1mg,或至少0.5mg,或至少1.0mg,或至少2.5mg,或至少5.0mg,或至少7.5mg,或至少10mg,或至少15mg,或至少20mg,或至少25mg,或至少50mg,或至少75mg,或至少100mg。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑之重量含量不超過500mg,或不超過400mg,或不超過300mg,或不超過250mg,或不 超過200mg,或不超過150mg,或不超過100mg,或不超過75mg,或不超過50mg,或不超過25mg,或不超過20mg,或不超過15mg,或不超過10mg。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑之重量含量在以下範圍內:1.0±0.5mg,或2.5±2mg,或5.0±2mg,或7.5±2mg,或10±2mg,或7.5±5mg,或10±5mg,或12.5±5mg,或15±5mg,或17.5±5mg,或20±5mg,或12.5±10mg,或15±10mg,或17.5±10mg,或20±10mg,或22.5±10mg,或25±10mg,或27.5±10mg,或30±10mg,或30±25mg,或40±25mg,或50±25mg,或60±25mg,或70±25mg,或80±25mg,或90±25mg,或100±25mg,或60±50mg,或80±50mg,或100±50mg,或120±50mg,或140±50mg,或160±50mg,或180±50mg,或200±50mg。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑之重量含量為至少0.1wt.-%,或至少0.5wt.-%,或至少1.0wt.-%,或至少2.0wt.-%,或至少3.0wt.-%,或至少4.0wt.-%,或至少5.0wt.-%,或至少6.0wt.-%,或至少7.0wt.-%,或至少8.0wt.-%,或至少9.0wt.-%,或至少10wt.-%,在各情況下均係相對於劑型之總重量。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑之重量含量不超過50wt.-%,或不超過40wt.-%,或不超過30wt.-%,或不超過20wt.-%,或不超過10wt.-%,或不超過7.5wt.-%,或不超過5.0wt.-%,或不超過2.50wt.-%,或不超過1.0wt.-%,在各情況下均係相對於劑型之總重量。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑之重量含量在以下範圍內:1.0±0.5wt.-%,或2.5±2wt.-%,或5.0±2wt.-%,或7.5±2wt.-%,或10±2wt.-%,或7.5±5wt.-%,或10±5wt.-%,或12.5±5wt.-%,或15±5wt.-%,或17.5±5wt.-%,或20±5wt.-%,或10±7.5wt.-%,或12.5±10wt.-%,或15±10wt.-%,或17.5±10wt.-%,或20±10wt.-%,或22.5±10wt.-%,或25±10wt.-%, 或27.5±10wt.-%,或30±10wt.-%,或30±25wt.-%,或40±25wt.-%,或50±25wt.-%,或60±25wt.-%,或70±25wt.-%,在各情況下均係相對於劑型之總重量。
在根據本發明之醫藥劑型之較佳實施例中,麻黃素組分與轉化抑制劑之相對重量比在以下範圍內:1:100至100:1,或1:75至75:1,或1:50至50:1,或1:25至25:1,或1:10至10:1,或1:7.5至7.5:1,或1:5至5:1,或1:3至3:1,或1:2至2:1,或1:1.5至1.5:1。
在根據本發明之醫藥劑型之較佳實施例中,麻黃素組分與轉化抑制劑之相對重量比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1,或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑與麻黃素組分之相對重量比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1,或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
在根據本發明之醫藥劑型之較佳實施例中,麻黃素組分與轉化抑制劑之相對莫耳比在以下範圍內:1:100至100:1,或1:75至75:1,或1:50至50:1,或1:25至25:1,或1:10至10:1,或1:7.5至7.5:1,或1:5至5:1,或1:3至3:1,或1:2至2:1,或1:1.5至1.5:1。
在根據本發明之醫藥劑型之較佳實施例中,麻黃素組分與轉化抑制劑之相對莫耳比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1,或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
在根據本發明之醫藥劑型之較佳實施例中,轉化抑制劑與麻黃素組分之相對莫耳比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1, 或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
麻黃素組分較佳存在於控制釋放基質中,該控制釋放基質包含聚氧化烯,且視情況另外包含纖維素醚,較佳為羥丙基甲基纖維素;交聯聚合物,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉;及/或黏合劑,較佳為聚乙烯吡咯啶酮。
較佳地,根據本發明之醫藥劑型包含重量平均分子量為至少200,000g/mol之聚氧化烯。
在一較佳實施例中,聚氧化烯之重量平均分子量(MW)或黏度平均分子量(Mη)為至少500,000g/mol,較佳為至少1,000,000g/mol或至少2,500,000g/mol,更佳在約1,000,000g/mol至約15,000,000g/mol範圍內,且最佳在約5,000,000g/mol至約10,000,000g/mol範圍內。適合用於測定MW及Mη之方法為熟習此項技術者已知的。Mη較佳藉由流變量測來測定,而MW可藉由凝膠滲透層析(GPC)來測定。
較佳地,聚氧化烯之分子量分散性Mw/Mn在2.5±2.0、更佳2.5±1.5、更佳2.5±1.0、更佳2.5±0.8、最佳2.5±0.6且特定而言2.5±0.4範圍內。
較佳地,聚氧化烯在25℃下之黏度使用RVF型號布絡克菲爾德黏度計(Brookfield viscosimeter)(2號轉軸/轉速2rpm)在5wt.-%水溶液中量測,為30至17,600cP,更佳為55至17,600cP,更佳為600至17,600cP且最佳為4,500至17,600cP;使用所述黏度計(1號或3號轉軸/轉速10rpm)基於2wt.-%水溶液量測,為400至4,000cP,更佳為400至800cP或2,000至4,000cP;或者使用所述黏度計(2號轉軸/轉速2rpm)基於1wt.-%水溶液量測,為1,650至10,000cP,更佳為1,650至5,500cP,5,500至7,500cP或7,500至10,000eP。
較佳地,聚氧化烯係選自聚氧化甲烯(polymethylene oxide)、聚氧化 乙烯及聚氧化丙烯或其共聚物。較佳地,聚氧化烯為聚氧化乙烯。
較佳地,相對於醫藥劑型之總重量,聚氧化烯之重量含量為至少30wt.-%。
以醫藥劑型之總重量計,聚氧化烯之重量含量較佳在30至80wt.-%範圍內。較佳地,以醫藥劑型之總重量計,聚氧化烯之重量含量在50±20wt.-%範圍內。較佳地,以醫藥劑型之總重量計,聚氧化烯之重量含量在50±30wt.-%、更佳50±27wt.-%、更佳50±24wt.-%、更佳50±21wt.-%、甚至更佳50±18wt.-%且最佳50±15wt.-%範圍內。
聚氧化烯可包含具有特定平均分子量之單一聚氧化烯,或不同聚合物(諸如兩種、三種、四種或五種聚合物,例如化學性質相同但平均分子量不同之聚合物、化學性質不同但平均分子量相同之聚合物或化學性質不同並且分子量不同之聚合物)之混合物(摻混物)。
出於說明之目的,聚二醇具有至多20,000g/mol之分子量,而聚氧化烯具有超過20,000g/mol之分子量。在一較佳實施例中,醫藥劑型中所含之所有聚氧化烯之所有分子量的加權平均值為至少200,000g/mol。因此,當測定聚氧化烯之重量平均分子量時較佳不將聚二醇(若有)考慮在內。
在一較佳實施例中,聚氧化烯均勻分佈於根據本發明之醫藥劑型中。較佳地,麻黃素組分與聚氧化烯密切地均勻分佈於醫藥劑型中,使得醫藥劑型不含任何任一麻黃素組分存在而聚氧化烯不存在或聚氧化烯存在而麻黃素組分不存在的區段。
當醫藥劑型包覆有薄膜包衣時,聚氧化烯較佳均勻分佈於醫藥劑型之核心中,亦即薄膜包衣較佳不含聚氧化烯。不過,薄膜包衣本身當然可含有一或多種聚合物,然而其較佳不同於核心中所含之聚氧化烯。
較佳地,聚氧化烯與麻黃素組分之相對重量比在5:1至1:4、更佳4.5:1 至1:3.5、更佳4:1至1:3、更佳3.5:1至1:2.5、甚至更佳3:1至1:2、最佳2.5:1至1:1.5且特定而言2:1至1:1範圍內。
聚氧化烯可與一或多種選自由以下組成之群的不同聚合物組合:聚乙烯、聚丙烯、聚氯乙烯、聚碳酸酯、聚苯乙烯、聚乙烯吡咯啶酮、聚(烷基)丙烯酸酯、聚(羥基脂肪酸),諸如聚(3-羥基丁酸酯-共-3-羥基戊酸酯)(Biopol®)、聚(羥基戊酸);聚己內酯、聚乙烯醇、聚酯醯胺、聚丁二酸伸乙酯、聚內酯、聚乙交酯、聚胺基甲酸脂、聚醯胺、聚丙交酯、聚縮醛(例如視情況具有經修飾之側鏈的多醣)、聚丙交酯/乙交酯、聚內酯、聚乙交酯、聚原酸酯、聚酸酐、聚乙二醇及聚對苯二甲酸伸丁酯之嵌段聚合物(Polyactive®)、聚酸酐(Polifeprosan)、其共聚物、其嵌段共聚物及至少兩種所述聚合物之混合物或具有以上特徵之其他聚合物。
在一較佳實施例中,根據本發明之醫藥劑型不包含抗氧化劑。
在另一較佳實施例中,根據本發明之醫藥劑型包含抗氧化劑。較佳地,抗氧化劑係選自由以下組成之群:抗壞血酸、抗壞血酸鹽、丁基羥基茴香醚(BHA)、丁基羥基甲苯(BHT)、單硫代甘油、亞磷酸、α-生育酚、α-生育酚乙酸酯、苯甲酸松柏酯、降二氫愈創木酸、沒食子酸酯及亞硫酸氫鈉。尤其較佳之抗氧化劑為α-生育酚。
較佳地,較佳為α-生育酚之抗氧化劑的重量含量大於0.2wt.-%,更佳為至少0.3wt.-%或至少0.4wt.-%,更佳為至少0.5wt.-%或至少0.6wt.-%,更佳為至少0.7wt.-%或至少0.8wt.-%,甚至更佳為至少0.9wt.-%或至少1.0wt.-%,最佳為至少1.1wt.-%或至少1.2wt.-%,且特定而言為至少1.3wt.-%或至少1.4wt.-%,在各情況下均係相對於醫藥劑型之總重量。
較佳地,以醫藥劑型之總重量計,抗氧化劑之重量含量在1.00±0.95wt.-%範圍內。較佳地,抗氧化劑之重量含量在1.5±0.6wt.-%、更佳1.5±0.5 wt.-%、更較佳1.5±0.4wt.-%、更佳1.5±0.3wt.-%、甚至更佳1.5±0.2wt.-%且最佳1.5±0.1wt.-%範圍內,在各情況下均係以醫藥劑型之總重量計。
較佳地,麻黃素組分與較佳為α-生育酚之抗氧化劑的相對重量比在5:1至35:1範圍內或在7:1至33:1、更佳9:1至31:1、更佳11:1至29:1、更佳13:1至27:1、甚至更佳15:1至25:1、最佳17:1至23:1且特定而言19:1至21:1範圍內。
已令人驚訝地發現,相對高重量含量之抗氧化劑(尤其為α-生育酚)提供優勢。已發現包含較高含量之抗氧化劑(尤其α-生育酚)之醫藥劑型抑制麻黃素或偽麻黃素化學轉化為甲基安非他命。此外,當設法藉助於二氯甲烷自劑型萃取麻黃素或偽麻黃素時,抗氧化劑(尤其α-生育酚)之存在分別使麻黃素及偽麻黃素之可萃取量減少。
較佳地,根據本發明之醫藥劑型包含纖維素醚,較佳為羥丙基甲基纖維素。較佳為羥丙基甲基纖維素之纖維素醚不同於可視情況亦含於根據本發明之醫藥劑型中的交聯聚合物,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉;及黏合劑,較佳為聚乙烯吡咯啶酮。較佳地,較佳為羥丙基甲基纖維素之纖維素醚為實質上線性的,亦即不交聯。較佳地,較佳為羥丙基甲基纖維素之纖維素醚為實質上非離子的,亦即既不為陽離子亦不為陰離子。在一較佳實施例中,根據本發明之醫藥劑型包含交聯羧甲基纖維素,其由化學觀點來看亦可被視為纖維素醚。然而,當交聯羧甲基纖維素為交聯的時,出於說明之目的交聯羧甲基纖維素為「交聯聚合物」(參見下文),不為「纖維素醚」。
較佳地,纖維素醚係選自由以下組成之群:甲基纖維素、乙基纖維素、丙基纖維素、羥乙基纖維素、羥丙基纖維素(HPC)、羥丙基甲基纖維素(HPMC)、羧甲基纖維素、羧甲基纖維素之鹽及任何前述物質之混合物。羥丙基甲基纖維素為尤其較佳的。
較佳地,相對於醫藥劑型之總重量,較佳為羥丙基甲基纖維素之纖維素醚的重量含量在0.5至20wt.-%範圍內或在1.0至15wt.-%範圍內。
較佳地,較佳為羥丙基甲基纖維素之纖維素醚的重量含量在7.0±6.0wt.-%、更佳7.0±5.0wt.-%、更佳7.0±4.0wt.-%、更佳7.0±3.0wt.-%、甚至更佳7.0±2.0wt.-%且最佳7.0±1.0wt.-%範圍內,在各情況下均係以醫藥劑型之總重量計。
在另一較佳實施例中,根據本發明之醫藥劑型不含此類較佳為羥丙基甲基纖維素之纖維素醚。
較佳地,麻黃素組分與較佳為羥丙基甲基纖維素之纖維素醚的相對重量比在1:1至7.5:1、更佳1.5:1至7:1、更佳2:1至6.5:1、更佳2.5:1至6:1、甚至更佳3:1至5.5:1、最佳3.5:1至5:1且特定而言4:1至4.5:1範圍內。
在一較佳實施例中,聚氧化烯與較佳為羥丙基甲基纖維素之纖維素醚的相對重量比在2.0:1至12:1、更佳3.0:1至11:1、更佳3.5:1至10:1、更佳4.0:1至9.5:1、最佳4.5:1至8.0:1且特定而言5.0:1至7.5:1範圍內。
當根據本發明之醫藥劑型亦含有較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物時,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物與較佳為羥丙基甲基纖維素之纖維素醚的相對重量比較佳在4:1至1:4、更佳3.5:1至1:3.5、更佳3:1至1:3、更佳2.5:1至1:2.5、最佳2:1至1:2且特定而言1.5:1至1:1.5範圍內。
當根據本發明之醫藥劑型亦含有較佳為聚乙烯吡咯啶酮之黏合劑時,較佳為聚乙烯吡咯啶酮之黏合劑與較佳為羥丙基甲基纖維素之纖維素醚的相對重量比較佳在4:1至1:4、更佳3.5:1至1:3.5、更佳3:1至1:3、更佳2.5:1至1:2.5、最佳2:1至1:2且特定而言1.5:1至1:1.5範圍內。
在一較佳實施例中,較佳為羥丙基甲基纖維素之纖維素醚均勻分佈 於根據本發明之醫藥劑型中。較佳地,麻黃素組分與較佳為羥丙基甲基纖維素之纖維素醚密切地均勻分佈於醫藥劑型中,使得醫藥劑型不含任何任一麻黃素組分存在而較佳為羥丙基甲基纖維素之纖維素醚不存在或較佳為羥丙基甲基纖維素之纖維素醚存在而麻黃素組分不存在的區段。
當醫藥劑型包覆有薄膜包衣時,較佳為羥丙基甲基纖維素之纖維素醚較佳均勻分佈於醫藥劑型之核心中。薄膜包衣本身亦可含有包括纖維素醚之一或多種聚合物,該等纖維素醚可不同於核心中所含之較佳為羥丙基甲基纖維素之纖維素醚或可為相同的。
較佳地,根據本發明之醫藥劑型包含交聯聚合物,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉。較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物不同於可視情況亦含於根據本發明之醫藥劑型中的纖維素醚,較佳為羥丙基甲基纖維素;及黏合劑,較佳為聚乙烯吡咯啶酮。交聯纖維素醚較佳被視為「交聯聚合物」,而不為根據本發明之「纖維素醚」。
較佳地,交聯聚合物係選自由以下組成之群:交聯羧甲基纖維素、交聯羧甲基纖維素之鹽、交聯聚維酮及任何前述物質之混合物。
較佳地,相對於醫藥劑型之總重量,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的重量含量在1.0至15wt.-%範圍內。
當交聯聚合物為陰離子型,例如交聯羧甲基纖維素時,較佳地,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之陰離子交聯聚合物中所含之陰離子官能基(例如羧酸根及/或磺酸根陰離子)中之至少一些以中和形式存在,亦即其不以其質子化形式存在,而是替代地與成鹽陽離子一起為鹽。適合之成鹽陽離子包括鹼金屬、銨、經取代之銨及胺。更佳地,陰離子官能基(例如羧酸根及/或磺酸根陰離子)中之至少一些為鈉陽離子或鉀陽離子之鹽。
在一尤其較佳實施例中,交聯聚合物為交聯羧甲基纖維素或其生理 學上可接受之鹽。較佳地,交聯聚合物為交聯羧甲基纖維素鈉。較佳地,交聯羧甲基纖維素鈉符合USP之較佳於2016年之版本中之專題論文E-09 Croscarmellose Sodium。
交聯羧甲基纖維素鈉為內部交聯之羧甲基纖維素鈉,其典型地在醫藥調配物中用作超級崩解劑。交聯降低水溶性,同時仍允許材料在水中膨脹且吸收其重量之許多倍。其在大多數錠劑(包括膳食補充物)中之目的為幫助錠劑在胃腸道中迅速崩解。交聯羧甲基纖維素可藉由首先將粗纖維素浸泡於氫氧化鈉中,且接著使纖維素與單氯乙酸鈉反應以形成羧甲基纖維素鈉來製備。過量單氯乙酸鈉緩慢水解為乙醇酸且乙醇酸催化交聯以形成交聯羧甲基纖維素鈉。在化學上,交聯羧甲基纖維素鈉為交聯之部分O-(羧甲基化)纖維素的鈉鹽。
以醫藥劑型之總重量計,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的重量含量較佳在1.0至35wt.-%、更佳5.0至35wt.-%、更佳1.0至15wt.-%範圍內。
較佳地,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的重量含量在7.0±6.0wt.-%、更佳7.0±5.0wt.-%、更較佳7.0±4.0wt.-%、更佳7.0±3.0wt.-%、甚至更佳7.0±2.0wt.-%且最佳7.0±1.0wt.-%範圍內,在各情況下均係以醫藥劑型之總重量計。
交聯之交聯羧甲基纖維素與線性羥丙基甲基纖維素(根據本發明之纖維素醚)的比較表明其他條件均相同,在二氯甲烷、二乙醚及乙酸乙酯中添加及不添加氫氧化鈉之情況下,交聯之交聯羧甲基纖維素與線性羥丙基甲基纖維素相比針對溶劑萃取均提供更佳之抗性。
在另一較佳實施例中,根據本發明之醫藥劑型不含此類較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物。
在一較佳實施例中,聚氧化烯與較佳為交聯羧甲基纖維素或交聯羧 甲基纖維素鈉之交聯聚合物的相對重量比在2.0:1至12:1、更佳3.0:1至11:1、更佳3.5:1至10:1、更佳4.0:1至9.5:1、最佳4.5:1至8.0:1且特定而言5.0:1至7.5:1範圍內。
當根據本發明之醫藥劑型亦含有較佳為羥丙基甲基纖維素之纖維素醚時,較佳為羥丙基甲基纖維素之纖維素醚與較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的相對重量比較佳在4:1至1:4、更佳3.5:1至1:3.5、更佳3:1至1:3、更佳2.5:1至1:2.5、最佳2:1至1:2且特定而言1.5:1至1:1.5範圍內。
當根據本發明之醫藥劑型亦含有較佳為聚乙烯吡咯啶酮之黏合劑時,較佳為聚乙烯吡咯啶酮之黏合劑與較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的相對重量比較佳在4:1至1:4、更佳3.5:1至1:3.5、更佳3:1至1:3、更佳2.5:1至1:2.5、最佳2:1至1:2且特定而言1.5:1至1:1.5範圍內。
在一較佳實施例中,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物均勻分佈於根據本發明之醫藥劑型中。較佳地,麻黃素組分與較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物密切地均勻分佈於醫藥劑型中,使得醫藥劑型不含任何任一麻黃素組分存在而交聯聚合物不存在或交聯聚合物存在而麻黃素組分不存在的區段。
當醫藥劑型包覆有薄膜包衣時,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物較佳均勻分佈於醫藥劑型之核心中,亦即薄膜包衣較佳不含交聯聚合物。不過,薄膜包衣本身當然可含有一或多種聚合物,然而其較佳不同於核心中所含之交聯聚合物。
較佳地,根據本發明之醫藥劑型包含黏合劑,較佳為聚乙烯吡咯啶酮。較佳為聚乙烯吡咯啶酮之黏合劑不同於可視情況亦含於根據本發明之醫藥 劑型中的纖維素醚,較佳為羥丙基甲基纖維素;及交聯聚合物,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉。
較佳地,黏合劑係選自由以下組成之群:二醣、澱粉、經改質之澱粉、糖醇、聚乙烯吡咯啶酮及任何前述物質之混合物。聚乙烯吡咯啶酮為尤其較佳的。
較佳地,相對於醫藥劑型之總重量,較佳為聚乙烯吡咯啶酮之黏合劑的重量含量在1.0至15wt.-%範圍內。
較佳地,較佳為聚乙烯吡咯啶酮之黏合劑的重量含量在7.0±6.0wt.-%、更佳7.0±5.0wt.-%、更佳7.0±4.0wt.-%、更佳7.0±3.0wt.-%、甚至更佳7.0±2.0wt.-%且最佳7.0±1.0wt.-%範圍內,在各情況下均係以醫藥劑型之總重量計。
較佳地,麻黃素組分與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比在1:1至7.5:1、更佳1.5:1至7:1、更佳2:1至6.5:1、更佳2.5:1至6:1、甚至更佳3:1至5.5:1、最佳3.5:1至5:1且特定而言4:1至4.5:1範圍內。
在另一較佳實施例中,根據本發明之醫藥劑型不含此類黏合劑。
在一較佳實施例中,聚氧化烯與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比在2.0:1至12:1、更佳3.0:1至11:1、更佳3.5:1至10:1、更佳4.0:1至9.5:1、最佳4.5:1至8.0:1且特定而言5.0:1至7.5:1範圍內。
當根據本發明之醫藥劑型亦含有較佳為羥丙基甲基纖維素之纖維素醚時,較佳為羥丙基甲基纖維素之纖維素醚與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比較佳在4:1至1:4、更佳3.5:1至1:3.5、更佳3:1至1:3、更佳2.5:1至1:2.5、最佳2:1至1:2且特定而言1.5:1至1:1.5範圍內。
當根據本發明之醫藥劑型亦含有較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物時,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素 鈉之交聯聚合物與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比較佳在4:1至1:4、更佳3.5:1至1:3.5、更佳3:1至1:3、更佳2.5:1至1:2.5、最佳2:1至1:2且特定而言1.5:1至1:1.5範圍內。
在一較佳實施例中,較佳為聚乙烯吡咯啶酮之黏合劑均勻分佈於根據本發明之醫藥劑型中。較佳地,麻黃素組分與較佳為聚乙烯吡咯啶酮之黏合劑密切地均勻分佈於醫藥劑型中,使得醫藥劑型不含任何任一麻黃素組分存在而較佳為聚乙烯吡咯啶酮之黏合劑不存在或較佳為聚乙烯吡咯啶酮之黏合劑存在而麻黃素組分不存在的區段。
當醫藥劑型包覆有薄膜包衣時,較佳為聚乙烯吡咯啶酮之黏合劑較佳均勻分佈於醫藥劑型之核心中,亦即薄膜包衣較佳不含較佳為聚乙烯吡咯啶酮之黏合劑。不過,薄膜包衣本身當然可含有一或多種聚合物,然而其較佳不同於核心中所含之較佳為聚乙烯吡咯啶酮的黏合劑。
在一較佳實施例中,根據本發明之醫藥劑型包含如上文所定義之較佳為羥丙基甲基纖維素之纖維素醚,但較佳既不含如上文所定義之較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物亦不含如上文所定義之黏合劑。
在另一較佳實施例中,根據本發明之醫藥劑型包含如上文所定義之較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物,但較佳既不含如上文所定義之較佳為羥丙基甲基纖維素之纖維素醚亦不含如上文所定義之黏合劑。
在另一較佳實施例中,根據本發明之醫藥劑型包含如上文所定義之較佳為聚乙烯吡咯啶酮之黏合劑,但較佳既不含如上文所定義之較佳為羥丙基甲基纖維素之纖維素醚亦不含如上文所定義之較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物。
在另一較佳實施例中,根據本發明之醫藥劑型包含如上文所定義之較佳為羥丙基甲基纖維素之纖維素醚與如上文所定義之較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的組合,但較佳不含如上文所定義之黏合劑。
在另一較佳實施例中,根據本發明之醫藥劑型包含較佳為羥丙基甲基纖維素之如上文所定義之纖維素醚與較佳為聚乙烯吡咯啶酮之如上文所定義之黏合劑的組合,但較佳不含如上文所定義之交聯聚合物。較佳地,醫藥劑型另外包含升高量之抗氧化劑,較佳為α-生育酚。已令人驚訝地發現,在標準化條件下與其他調配物相比,此尤其較佳之根據本發明之醫藥劑型- 在苛刻條件下研磨後提供粗粒子(88wt.-%之粒度>1mm的材料,而其他調配物僅提供至多55wt.-%之粒度>1mm的材料);- 提供低量之藉由化學轉化產生之甲基安非他命;- 提供低量之可在伏特加(Vodka)中萃取之偽麻黃素;且- 在事先用氫氧化鈉處理或未用氫氧化鈉處理之情況下提供低量之可用二乙醚或乙酸乙酯萃取之偽麻黃素。
在另一較佳實施例中,根據本發明之醫藥劑型包含較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之如上文所定義之交聯聚合物與較佳為聚乙烯吡咯啶酮之如上文所定義之黏合劑的組合,但較佳不含如上文所定義之較佳為羥丙基甲基纖維素之纖維素醚。較佳地,醫藥劑型另外包含升高量之抗氧化劑,較佳為α-生育酚。已令人驚訝地發現,在標準化條件下與其他調配物相比,此尤其較佳之根據本發明之醫藥劑型- 在苛刻條件下研磨後提供粗粒子(88wt.-%之粒度>1mm的材料,而其他調配物僅提供至多55wt.-%之粒度>1mm的材料);- 提供低量之藉由化學轉化產生之甲基安非他命; - 提供低量之可在伏特加中萃取之偽麻黃素;且- 在事先用氫氧化鈉處理或未用氫氧化鈉處理之情況下提供低量之可用二乙醚或乙酸乙酯萃取之偽麻黃素。
在另一較佳實施例中,根據本發明之醫藥劑型包含如上文所定義之較佳為羥丙基甲基纖維素之纖維素醚與如上文所定義之較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物且與如上文所定義之較佳為聚乙烯吡咯啶酮之黏合劑的組合。
較佳地,根據本發明之醫藥劑型包含較佳為聚乙烯吡咯啶酮之如上文所定義之黏合劑與以下各項的組合:- 較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之如上文所定義之交聯聚合物;- 或較佳為羥丙基甲基纖維素之如上文所定義之纖維素醚;且在任一情況下較佳另外包含升高量之抗氧化劑,較佳為α-生育酚。
已令人驚訝地發現,聚乙烯吡咯啶酮(PVP)及交聯羧甲基纖維素特定而言在彼此組合時提供在研磨後產生粗粒子之醫藥劑型(若醫藥劑型完全可研磨)。另外,當設法用水及二乙醚自此類粗粒子萃取麻黃素或偽麻黃素時,形成穩定乳液,亦即乙醚相不與水相分離,使得根本不能或至少幾乎不能藉助於分液漏斗萃取。
另外,指示聚乙烯吡咯啶酮(PVP)在濫用者嘗試自醫藥劑型萃取麻黃素或偽麻黃素或嘗試將麻黃素或偽麻黃素化學轉化為甲基安非他命時習知使用之彼等溶劑中展現一定溶解度。此在所獲得之中間萃取物或所產生之產物中產生所需雜質,因此污染中間萃取物或最終產物且分別阻礙其進一步濫用及投與。
在一較佳實施例中,根據本發明之醫藥劑型另外包含塑化劑,其較佳選自由以下組成之群:聚二醇、三乙酸甘油酯、脂肪酸、脂肪酸酯、蠟及微 晶蠟。尤其較佳之塑化劑為聚乙二醇,諸如PEG 6000。
較佳地,以醫藥劑型之總重量計,塑化劑之重量含量較佳在10±9wt.-%範圍內。較佳地,以醫藥劑型之總重量計,塑化劑之重量含量在10±8wt.-%、更佳10±7wt.-%、更佳10±6wt.-%、更佳10±5wt.-%、甚至更佳10±4wt.-%且最佳10±3wt.-%範圍內。
除麻黃素組分、視情況存在之聚氧化烯、視情況存在之抗氧化劑、視情況存在之塑化劑、視情況存在之較佳為羥丙基甲基纖維素之纖維素醚、視情況存在之較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物及視情況存在之較佳為聚乙烯吡咯啶酮之黏合劑之外,根據本發明之醫藥劑型亦可含有其他成分,例如一或多種習知醫藥賦形劑,例如填料、助流劑、成粒劑、抗結塊劑、潤滑劑、調味劑、染料及/或防腐劑。
根據本發明之醫藥劑型較佳為口服醫藥劑型,特定而言為錠劑。
然而,亦可經由不同途徑投與醫藥劑型且因此,醫藥劑型或者可適合於經頰、經舌、經直腸或經陰道投與。植入物亦為可能的。
在一較佳實施例中,醫藥劑型為多微粒的,較佳為膠囊。在此等情況下,並非膠囊本身,而是膠囊中所含之粒子中之至少一部分具有至少300N之斷裂強度。
在另一較佳實施例中,醫藥劑型為整塊的。較佳地,醫藥劑型既不呈薄膜形式,亦不為多微粒的。
在一較佳實施例中,根據本發明之醫藥劑型為圓形錠劑。較佳地,此實施例之錠劑的直徑在約1mm至約30mm範圍內,特定而言在約2mm至約25mm範圍內,更特定而言為約5mm至約23mm,甚至更特定而言為7mm至約13mm;且厚度在約1.0mm至約12mm範圍內,特定而言在約2.0mm至約10mm範圍內,甚至更特定而言為3.0mm至約9.0mm,甚至進一步特定而言為 約4.0mm至約8.0mm。
在另一較佳實施例中,根據本發明之醫藥劑型為長方形錠劑。較佳地,此實施例之錠劑的縱長延伸(縱向延伸)為約1mm至約30mm,特定而言在約2mm至約25mm範圍內,更特定而言為約5mm至約23mm,甚至更特定而言為約7mm至約20mm;且厚度在約1.0mm至約12mm範圍內,特定而言在約2.0mm至約10mm範圍內,甚至更特定而言為3.0mm至約9.0mm,甚至進一步特定而言為約4.0mm至約8.0mm。
根據本發明之醫藥劑型較佳具有在0.01至1.5g範圍內、更佳在0.05至1.2g範圍內、更佳在0.1g至1.0g範圍內、更佳在0.2g至0.9g範圍內且最佳在0.25g至0.8g範圍內之重量。
可視情況部分或完全為本發明之醫藥劑型提供習知包衣。較佳用習知薄膜包衣組合物為本發明之醫藥劑型包覆薄膜包衣。
適合之包衣材料為可例如以商標Opadry®及Eudragit®商購獲得的。
適合之材料的實例包括纖維素酯及纖維素醚,諸如甲基纖維素(MC)、羥丙基甲基纖維素(HPMC)、羥丙基纖維素(HPC)、羥乙基纖維素(HEC)、羧甲基纖維素鈉(Na-CMC)、乙基纖維素(EC)、乙酸鄰苯二甲酸纖維素(CAP)、鄰苯二甲酸羥丙基甲基纖維素(HPMCP);聚(甲基)丙烯酸酯,諸如胺基烷基甲基丙烯酸酯共聚物、丙烯酸乙酯甲基丙烯酸甲酯共聚物、甲基丙烯酸甲基丙烯酸甲酯共聚物、甲基丙烯酸甲基丙烯酸甲酯共聚物;乙烯基聚合物,諸如聚乙烯吡咯啶酮、聚乙酸鄰苯二甲酸乙烯酯、聚乙烯醇、聚乙酸乙烯酯;及天然成膜劑,諸如蟲膠。
在一尤其較佳實施例中,包衣為水溶性的。在一較佳實施例中,包衣係基於聚乙烯醇,諸如部分水解之聚乙烯醇,且可另外含有聚乙二醇(諸如聚乙烯二醇3350)及/或顏料。在另一較佳實施例中,包衣係基於羥丙基甲基纖維 素,較佳為黏度為3至15mPa.s之羥丙基甲基纖維素2910型。
包衣可對胃液具抗性且根據釋放環境之pH值而溶解。藉助於此包衣,可確保根據本發明之醫藥劑型穿過胃而不溶解且使活性成分僅在腸道中釋放。對胃液具抗性之包衣較佳在5與7.5之間的pH值下溶解。用於延遲釋放活性成分及用於塗覆對胃液具抗性之包衣的對應材料及方法為熟習此項技術者例如由「Coated Pharmaceutical dosage forms-Fundamentals,Manufacturing Techniques,Biopharmaceutical Aspects,Test Methods and Raw Materials」,Kurt H.Bauer,K.Lehmann,Hermann P.Osterwald,Rothgang,Gerhart,第1版,1998,Medpharm Scientific Publishers已知的。
亦可塗覆包衣例如以改良醫藥劑型之美觀印象及/或味道及其吞咽容易性。為本發明之醫藥劑型包覆包衣亦可服務其他目的,例如改良穩定性及保質期。適合之包衣調配物包含成膜聚合物,諸如聚乙烯醇或羥丙基甲基纖維素,例如羥丙基甲基纖維素;塑化劑,諸如二醇,例如丙二醇或聚乙二醇;不透明劑,諸如二氧化鈦;及薄膜增滑劑,諸如滑石。適合之包衣溶劑為水以及有機溶劑。有機溶劑之實例為醇,例如乙醇或異丙醇;酮,例如丙酮;或鹵代烴,例如二氯甲烷。視情況,包衣可含有治療有效量之一或多種活性成分,以提供該麻黃素組分之即刻釋放且由此提供由麻黃素組分治療之症狀的即刻緩解。包覆包衣之本發明之醫藥劑型較佳係藉由首先製備核心且隨後使用習知技術為該等核心包覆包衣(諸如在包衣盤中包覆包衣)來製備。
根據本發明,麻黃素組分較佳包埋在包含聚氧化烯之控制釋放基質中。
活性成分自口服醫藥劑型控制釋放為熟習此項技術者已知的。出於說明之目的,控制釋放涵蓋延遲釋放、阻滯釋放、持續釋放、延期釋放及類似釋放。
根據本發明,控制或延期釋放較佳理解為意謂如下釋放型態,其中麻黃素組分以降低之攝入頻率歷經相對長之時間釋放,目的為延長治療作用。較佳地,術語「延期釋放」之含義符合歐洲醫藥劑型釋放型態命名準則(CHMP)。此係特定而言以經口投與來達成。表述「至少部分延遲或延期之釋放」根據本發明覆蓋確保其中所含之類鴉片(A)的經修改釋放之任何醫藥劑型。醫藥劑型較佳包含包覆包衣或未包覆包衣之醫藥劑型,其係使用特定助劑物質、藉由特定方法或藉由兩種可能之選擇的組合來製備,以有目的地改變釋放速率或釋放位置。
在根據本發明之醫藥劑型之情況下,控制釋放形式之釋放時間型態可例如如下進行修改:延長釋放、重複作用釋放、延期釋放及持續釋放。
出於說明之目的,「控制釋放」較佳意謂產物中活性成分隨時間推移之釋放受調配物之類型及組成的控制。出於說明之目的,「延長釋放」較佳意謂產物中活性成分之釋放延遲了有限的滯後時間,此後釋放不受阻礙。出於說明之目的,「重複作用釋放」較佳意謂產物中最初釋放了第一部分之活性成分,隨後後續釋放了至少另一部分之活性成分。出於說明之目的,「延期釋放」較佳意謂產物中在投與之後活性成分自調配物釋放之速率隨時間推移降低,以維持治療活性、降低毒性作用或用於一些其他治療目的。出於說明之目的,「持續釋放」較佳意謂將藥物調配成使得其歷經較長之一段時間穩定地釋放至體內,由此降低給藥頻率的方式。對於其他細節,可參考例如K.H.Bauer,Lehrbuch der Pharmazeutischen Technologie,第6版,WVG Stuttgart,1999;及歐洲藥典。
較佳地,在醫藥學上醫藥劑型在1小時之後提供較佳至多60%、更佳至多40%、更佳至多30%、更佳至多20%且最佳至多17%之麻黃素組分釋放。在2小時之後較佳至多80%,更佳至多60%,更佳至多50%,更佳至多40%且最佳至多32%。在3小時之後較佳至多85%,更佳至多65%,更佳至多55%, 更佳至多48%且最佳至多42%。在4小時之後較佳至多90%,更佳至多75%,更佳至多65%,更佳至多55%且最佳至多49%。在7小時之後較佳至多95%,更佳至多85%,更佳至多80%,更佳至多70%且最佳至多68%。在10小時之後較佳至多99%,更佳至多90%,更佳至多88%,更佳至多83%且最佳至多80%。在13小時之後較佳至多99%,更佳至多95%,更佳至多93%,更佳至多91%且最佳至多89%。
在一較佳實施例中,根據本發明之醫藥劑型在活體外條件下在1h之後已釋放醫藥劑型中最初所含麻黃素組分之總含量的至多40wt.-%,在2h之後已釋放至多55wt.-%,在3h之後已釋放至多70wt.-%,且在4h之後已釋放至多85wt.-%。
在另一較佳實施例中,根據本發明之醫藥劑型提供麻黃素組分之即刻釋放。出於說明之目的,即刻釋放較佳意謂在活體外條件下在30分鐘之後已釋放醫藥劑型中最初所含之麻黃素組分的至少80wt.-%。
即刻釋放較佳係藉助於較佳呈膠囊形式之多微粒醫藥劑型或MUPS調配物來達成,其中含有麻黃素之個別粒子中之至少一部分、較佳所有此類粒子具有至少300N之斷裂強度。
提供藥理學活性成分之即刻釋放的抗斷裂多微粒醫藥劑型由先前技術(例如由WO 2008/107149、US 2013 0028970及US 2013 0028972,該等專利以引用之方式併入本文中)為已知的。
適合之活體外條件為熟練技工已知的。在此方面,可參考例如歐洲藥典。較佳地,在以下條件下量測釋放型態:配備有沈錘之槳式設備,75rpm,37±5℃,900mL模擬腸液(pH 6.8)(磷酸鹽緩衝液)或pH 4.5。在一較佳實施例中,槳之轉速增加至100rpm。
較佳地,用於根據本發明之用途的醫藥劑型係每天一次、每天兩次或每天三次投與。較佳地,根據本發明之醫藥劑型係用於每天一次或每天兩次或每天三次投與醫藥劑型之療法中。因此,在一較佳實施例中,根據本發明之醫藥劑型適合於每天一次進行投與。在另一較佳實施例中,根據本發明之醫藥劑型適合於每天兩次進行投與。在另一較佳實施例中,根據本發明之醫藥劑型適合於每天三次進行投與。
出於說明之目的,「每天兩次」意謂在個別投與之間,時間間隔相等或幾乎相等,亦即,約每12小時;或者時間間隔不同,例如8及16小時或10及14小時。
出於說明之目的,「每天三次」意謂在個別投與之間時間間隔相等或幾乎相等,亦即,約每8小時;或者時間間隔不同,例如6、6及12小時,或者7、7及10小時。
根據本發明之醫藥劑型具有至少300N、較佳至少500N之斷裂強度。當醫藥劑型為整塊(例如錠劑)時,整塊醫藥劑型本身具有至少300N之斷裂強度。當醫藥劑型為多微粒(例如膠囊)時,較佳並非膠囊材料而是膠囊中所含粒子中之至少一部分具有至少300N之斷裂強度。
根據本發明之醫藥劑型較佳為抗損壞的。較佳地,抗損壞性係基於醫藥劑型之機械特性來達成,使得破碎得以避免或至少實質上被阻礙。根據本發明,術語破碎意謂使用濫用者通常可獲得之習知手段(例如杵棒及研缽、錘子、棒槌或其他用於在力之作用下進行粉碎之習知手段)將醫藥劑型粉碎。因此,抗損壞性較佳意謂避免或至少實質上阻礙使用習知手段將醫藥劑型粉碎。
較佳地,根據本發明之醫藥劑型之機械特性(特定而言其斷裂強度)實質上依賴於聚氧化烯之存在及空間分佈,不過其僅僅存在典型地不足以達成該等特性。藉由藉助於用於製備醫藥劑型之習知方法簡單地加工麻黃素組分、 聚氧化烯及視情況存在之其他賦形劑可能不會自動達成根據本發明之醫藥劑型的有利機械特性。事實上,通常必須選擇適合用於製備之設備且必須調節關鍵加工參數,特定而言為壓力/力、溫度及時間。因此,即使使用習知設備,通常亦必須對方法方案加以修改以滿足所需準則。
一般而言,只有在製備醫藥劑型期間適合之組分以適當量在足夠之溫度下暴露於足夠之壓力持續足夠之時間段時,才可獲得展現所需特性之醫藥劑型。
因此,與所用設備無關,必須對方法方案加以修改以滿足所需準則。因此,斷裂強度與組成為可分開的。
根據本發明之醫藥劑型之斷裂強度為至少300N,較佳至少500N,較佳至少600N,更佳至少700N,更佳至少800N,更佳至少1000N,最佳至少1250N且特定而言為至少1500N。
醫藥劑型之「斷裂強度」(抗壓碎性)為熟練人員已知的。在此方面,可參考例如W.A.Ritschel,Die Tablette,2.Auflage,Editio Cantor Verlag Aulendorf,2002;H Liebermann等人,Pharmaceutical dosage forms:Tablets,第2卷,Informa Healthcare;第2版,1990;及Encyclopedia of Pharmaceutical Technology,Informa Healthcare;第1版。
出於說明之目的,斷裂強度較佳定義為使醫藥劑型破裂必需之力(=斷裂力)的量。因此,出於說明之目的,醫藥劑型較佳在其斷裂時不展現所需斷裂強度,亦即,破裂為至少兩個彼此分離之獨立部分。然而,在另一較佳實施 例中,若力降低了在量測(參見下文)期間所量測之最高力的25%(臨限值),則認為醫藥劑型斷裂。
根據本發明之醫藥劑型不同於習知醫藥劑型,因為歸因於其斷裂強度,其不會因以習知手段(諸如杵棒及研缽、錘子、棒槌或其他通常用於粉碎之手段,特定而言出於此目的而研發之裝置(錠劑壓碎機))施加力而粉碎。在此方面,「粉碎」意謂碎裂成小粒子,該等小粒子在適合之介質中將即刻釋放麻黃素組分。
習知錠劑典型地沿任何延伸方向具有遠低於200N之斷裂強度。習知圓形錠劑之斷裂強度可根據以下經驗公式來估計:斷裂強度[N]=10 x 錠劑直徑[mm]。因此,根據該經驗公式,具有至少300N之斷裂強度的圓形錠劑將需要至少30mm之直徑)。然而,此類錠劑不能吞咽。以上經驗公式較佳不適用於本發明之醫藥劑型,其不為習知的而為專用的。
另外,有效平均咀嚼力為約220N(參看例如P.A.Proeschel等人,J Dent Res,2002,81(7),464-468)。此意謂斷裂強度遠低於200N之習知錠劑在自發咀嚼後可能被壓碎,而根據本發明之醫藥劑型不會被壓碎。
另外,當施加約9.81m/s2之重力加速度時,500N對應於超過50kg之重力,亦即根據本發明之醫藥劑型較佳可承受超過50kg之重量而不會粉碎。
用於量測醫藥劑型斷裂強度之方法為熟練技工已知的。適合之裝置為可商購獲得的。
舉例而言,斷裂強度(抗壓碎性)可根據歐洲藥典5.0,2.9.8或6.0,2.09.08「Resistance to Crushing of Tablets」來量測。該測試意在測定在所定義之條件下錠劑之抗壓碎性,其係由藉由壓碎使其破碎所需要之力來度量。設備由面向彼此之2個鉗口組成,其中之一者朝向另一者移動。鉗口之平面表面垂直於移動方向。鉗口之壓碎表面為平面的且大於與錠劑之接觸區。使用具有1牛 頓精確性之系統來校準設備。將錠劑放置於鉗口之間,在適當時將形狀、疵點(break-mark)及刻痕(inscription)考慮在內;在每次量測時,相對於施加力之方向(及要量測斷裂強度之延伸方向)以相同方式使錠劑定向。對10個錠劑進行量測,注意在每次測定之前移除錠劑之所有碎片。結果以所量測之力的平均值、最小值及最大值表示,所有值均以牛頓表示。
斷裂強度(斷裂力)之類似描述可見於USP中。或者可根據其中所描述之方法來量測斷裂強度,其中將斷裂強度陳述為在特定平面中使錠劑未通過測試(亦即,斷裂)所需的力。通常將錠劑放置於兩個壓板之間,其中之一者移動以對錠劑施加足夠之力從而引起破裂。對於習知圓形(圓形截面)錠劑,在其直徑上進行加載(有時稱為直徑加載),且在平面內發生破裂。錠劑之斷裂力在醫藥文獻中通常稱為硬度;然而,此術語之使用為有誤導性的。在材料科學中,術語硬度係指表面對由小探針穿透或壓凹之抗性。術語壓碎強度亦頻繁地用於描述錠劑對施加壓縮負荷之抗性。雖然此術語比硬度更準確地描述了該測試之真實性質,但其暗示錠劑在測試期間實際上被壓碎,常常並非此種情況。
或者,可根據WO 2005/016313、WO 2005/016314及WO 2006/082099量測斷裂強度(抗壓碎性),其可被視為歐洲藥典中所描述之方法的改良。用於量測之設備較佳為「Zwick Z 2.5」材料測試儀,Fmax=2.5kN,最大牽引為1150mm,其應經設置具有一個柱子及一個轉軸、100mm後之間隙及在0.1與800mm/min之間的可調節測試速度以及testControl軟體。使用以下設備進行量測:具有旋入式插入件及汽缸(直徑10mm)之壓力活塞、力轉換器(Fmax.1kN,直徑=8mm,根據ISO 7500-1之10N的類別0.5、2N的類別1)(具有製造商根據DIN 55350-18之測試證書M)(Zwick總力Fmax=1.45kN)(所有設備均來自Zwick GmbH & Co.KG,Ulm,Germany),測試儀訂單編號BTC-FR 2.5 TH.D09,力轉換器訂單編號BTC-LC 0050N.P01,定心裝置(centering device)訂單編號BO 70000 S06。
在本發明之一較佳實施例中,藉助於斷裂強度測試儀(例如Sotax® HT100型或HT1型(Allschwil,Switzerland))來量測斷裂強度。Sotax® HT100與Sotax® HT1可根據兩種不同量測原理量測斷裂強度:恆定速度(其中測試鉗口以5-200mm/min之可調節的恆定速度移動)或恆定力(其中測試鉗口使5-100N/sec之線性可調節的力增加)。原則上,兩種量測原理均適合用於量測根據本發明之醫藥劑型之斷裂強度。較佳地,以恆定速度量測斷裂強度,較佳以120mm/min之恆定速度量測。
在一較佳實施例中,若醫藥劑型破裂成至少兩個單獨碎塊,則將其視為斷裂。
根據本發明之醫藥劑型較佳在廣泛溫度範圍內展現機械強度,除斷裂強度(抗壓碎性)之外,視情況亦展現足夠之硬度、耐衝擊性、衝擊彈性、拉伸強度及/或彈性模量,視情況亦在低溫下(例如低於-24℃、低於-40℃或於液氮中)如此,以使得實際上不可能因自發咀嚼、在研缽中研磨、重擊等而粉碎。因此,較佳地,甚至在低溫或極低溫度下,例如當最初將醫藥劑型冰凍至例如低於-25℃、低於-40℃之溫度或甚至冰凍於液氮中以增加其脆性時,沿延伸方向E1,根據本發明之醫藥劑型之相對高斷裂強度亦得以維持。
根據本發明之醫藥劑型之特徵為一定程度之斷裂強度。此不意謂醫藥劑型必須亦展現一定程度之硬度。硬度與斷裂強度為不同之物理特性。因此,醫藥劑型之抗損壞性不一定取決於醫藥劑型之硬度。舉例而言,分別歸因於醫藥劑型之斷裂強度、衝擊強度、彈性模量及拉伸強度,其可較佳當例如使用錘子施加外力時發生例如塑性變形,但不會粉碎,亦即,碎裂成高數目之碎片。換言之,根據本發明之醫藥劑型之特徵為一定程度之斷裂強度,但不一定亦具有一定程度之形式穩定性。
因此,在本說明書之含義中,當暴露於沿特定延伸方向之力時發生 變形但不斷裂(塑性變形或塑性流動)之醫藥劑型較佳被視為沿該延伸方向具有所需斷裂強度。
較佳地,根據本發明之醫藥劑型較佳在「振盪及焙燒一鍋」程序之條件下、較佳在如實驗部分中進一步詳述之特定條件下提供針對麻黃素組分化學轉化為甲基安非他命的抗性,使得所產生甲基安非他命之量不超過醫藥劑型中最初所含麻黃素組分之總莫耳量的20莫耳-%,更佳不超過15莫耳-%,更佳不超過10莫耳-%,更佳不超過5.0莫耳-%,甚至更佳不超過2.5莫耳-%,且最佳不超過1.0莫耳-%。
在一較佳實施例中,尤其當試圖藉由「振盪及焙燒一鍋」程序將麻黃素組分直接化學轉化為甲基安非他命(亦即事先未進行萃取麻黃素組分之任何償試)時,所產生之甲基安非他命的量不超過醫藥劑型中最初所含麻黃素組分之總莫耳量的2.0莫耳-%,更佳不超過1.8莫耳-%,更佳不超過1.6莫耳-%,更佳不超過1.4莫耳-%,甚至更佳不超過1.2莫耳-%,且最佳不超過1.0莫耳-%。
較佳地,根據本發明之醫藥劑型亦提供針對在藉助於水性或有機溶劑(例如二乙醚、乙酸乙酯、二氯甲烷)自醫藥劑型萃取麻黃素組分之後將麻黃素組分化學轉化為甲基安非他命之抗性,使得所產生之甲基安非他命的量不超過醫藥劑型中最初所含麻黃素組分之總莫耳量的20莫耳-%,更佳不超過15莫耳-%,更佳不超過10莫耳-%,更佳不超過5.0莫耳-%,甚至更佳不超過2.5莫耳-%,且最佳不超過1.0莫耳-%。
在一較佳實施例中,尤其當可自醫藥劑型萃取大量麻黃素組分(例如多至80wt.-%)時,當試圖將由此萃取之麻黃素組分化學轉化為甲基安非他命時,歸因於存在共萃取之賦形劑,所產生之甲基安非他命的量不超過醫藥劑型中最初所含麻黃素組分之總莫耳量的5.0莫耳-%,更佳不超過4.5莫耳-%,更佳不超過4.0莫耳-%,更佳不超過3.5莫耳-%,甚至更佳不超過3.0莫耳-%,且最 佳不超過2.5莫耳-%。
在根據本發明之醫藥劑型之較佳實施例中,- 相對於醫藥劑型之總重量,麻黃素組分之重量含量在10至50wt.-%、更佳20至40wt.-%範圍內;及/或- 醫藥劑型包含聚氧化烯,其中- 相對於醫藥劑型之總重量,聚氧化烯之重量含量在25至65wt.-%、更佳30至60wt.-%、更佳35至55wt.-%、更佳40至50wt.-%範圍內;及/或- 聚氧化烯與麻黃素組分之相對重量比在3:1至1:2、更佳2.5:1至1:1.5、更佳2:1至1:1範圍內;及/或- 聚氧化烯之重量平均分子量為至少500,000g/mol,更佳至少750,000g/mol,更佳至少1,000,000g/mol;及/或- 醫藥劑型包含抗氧化劑,較佳為α-生育酚,其中- 相對於醫藥劑型之總重量,較佳為α-生育酚之抗氧化劑的重量含量為至少0.5wt.-%,更佳至少0.75wt.-%,更佳至少1.0wt.-%,更佳至少1.25wt.-%;及/或- 麻黃素組分與較佳為α-生育酚之抗氧化劑的相對重量比在35:1至5:1、更佳30:1至10:1、更佳25:1至15:1、更佳21:1至19:1範圍內;及/或- 醫藥劑型包含纖維素醚,較佳為羥丙基甲基纖維素,其中- 相對於醫藥劑型之總重量,較佳為羥丙基甲基纖維素之纖維素醚的重量含量在0.5至20wt.-%、更佳1.0至15wt.-%、更佳2.5至12.5wt.-%、更佳5.0至10wt.-%範圍內;及/或- 麻黃素組分與較佳為羥丙基甲基纖維素之纖維素醚的相對重量比在5.5:1至3:1、更佳5:1至3.5:1、更佳4.5:1至4:1範圍內;及/或- 醫藥劑型包含黏合劑,較佳為聚乙烯吡咯啶酮,其中 - 相對於醫藥劑型之總重量,較佳為聚乙烯吡咯啶酮之黏合劑的重量含量在0.5至20wt.-%、更佳1.0至15wt.-%、更佳2.5至12.5wt.-%、更佳5.0至10wt.-%範圍內;及/或- 麻黃素組分與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比在5.5:1至3:1、更佳5:1至3.5:1、更佳4.5:1至4:1範圍內;及/或- 較佳為羥丙基甲基纖維素之纖維素醚與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比在2.5:1至1:2.5、更佳2:1至1:2、更佳1.5:1至1:1.5範圍內。
在根據本發明之醫藥劑型之較佳實施例中,- 相對於醫藥劑型之總重量,麻黃素組分之重量含量在10至50wt.-%、更佳20至40wt.-%範圍內;及/或- 醫藥劑型包含聚氧化烯,其中- 相對於醫藥劑型之總重量,聚氧化烯之重量含量在25至65wt.-%、更佳30至60wt.-%、更佳35至55wt.-%、更佳40至50wt.-%範圍內;及/或- 聚氧化烯與麻黃素組分之相對重量比在3:1至1:2、更佳2.5:1至1:1.5、更佳2:1至1:1範圍內;及/或- 聚氧化烯之重量平均分子量為至少500,000g/mol,更佳至少750,000g/mol,更佳至少1,000,000g/mol;及/或- 醫藥劑型包含抗氧化劑,較佳為α-生育酚,其中- 相對於醫藥劑型之總重量,較佳為α-生育酚之抗氧化劑的重量含量為至少0.5wt.-%,更佳至少0.75wt.-%,更佳至少1.0wt.-%,更佳至少1.25wt.-%;及/或- 麻黃素組分與較佳為α-生育酚之抗氧化劑的相對重量比在35:1至5:1、更佳30:1至10:1、更佳25:1至15:1、更佳21:1至19:1範圍內;及/或- 醫藥劑型包含交聯聚合物,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素 鈉,其中- 相對於醫藥劑型之總重量,較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的重量含量在0.5至20wt.-%、更佳1.0至15wt.-%、更佳2.5至12.5wt.-%、更佳5.0至10wt.-%範圍內;及/或- 麻黃素組分與較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物的相對重量比在5.5:1至3:1、更佳5:1至3.5:1、更佳4.5:1至4:1範圍內;及/或- 醫藥劑型包含黏合劑,較佳為聚乙烯吡咯啶酮,其中- 相對於醫藥劑型之總重量,較佳為聚乙烯吡咯啶酮之黏合劑的重量含量在0.5至20wt.-%、更佳1.0至15wt.-%、更佳2.5至12.5wt.-%、更佳5.0至10wt.-%範圍內;及/或- 麻黃素組分與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比在5.5:1至3:1、更佳5:1至3.5:1、更佳4.5:1至4:1範圍內;及/或- 較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之交聯聚合物與較佳為聚乙烯吡咯啶酮之黏合劑的相對重量比在2.5:1至1:2.5、更佳2:1至1:2、更佳1.5:1至1:1.5範圍內。
在上表中,所有百分比為相對於醫藥劑型總重量之重量百分比。
較佳地,根據本發明之醫藥劑型係藉由熱熔擠出來製備。
較佳地,根據本發明之醫藥劑型係藉由熱成形來製備,不過為製造根據本發明之醫藥劑型亦可使用其他熱成形方法,諸如在高溫下壓力模製或加熱在第一步中藉由習知壓製所製造的錠劑且接著在第二步中加熱至超過錠劑中之聚合物的軟化溫度以形成硬錠劑。在此方面,熱成形意謂在施加熱量之後使團塊成形或對其進行模製。在一較佳實施例中,醫藥劑型係藉由熱熔擠出而熱成形的。
在一較佳實施例中,將成分之混合物加熱且隨後在足以達成所需機械特性(例如就斷裂強度及類似特性而言)之條件(時間、溫度及壓力)下進行壓製。此技術可例如藉助於製錠工具來達成,該製錠工具經加熱及/或填充有經加熱之混合物,隨後在不進一步供應熱量之情況下或在同時額外供應熱量之情況下對經加熱之混合物進行壓製。
在另一較佳實施例中,將成分之混合物加熱且同時在足以達成所需機械特性(例如就斷裂強度及類似特性而言)之條件下(時間、溫度及壓力)進行壓製。此技術可例如藉助於具有一或多個加熱區之擠出機來達成,其中混合物經加熱且同時經受擠出力,最後引起對經加熱混合物之壓製。
在其他實施例中,在周圍條件下在足夠之壓力下對成分之混合物進行壓製且隨後在足以達成所需機械特性(例如就斷裂強度及類似特性而言)之條件(時間、溫度)下加熱(固化)。此技術可例如藉助於固化爐來達成,其中經壓製之物品較佳未施加任何其他壓力之情況下在足夠之溫度下固化足夠之時間。此類方法進一步描述於例如US 2009/0081290中。
用於製造根據本發明之粒子的尤其較佳之方法涉及熱熔擠出。在此方法中,根據本發明之粒子係在擠出機之幫助下藉由熱成形來製備,較佳不存在任何可觀測之隨之發生的擠出物變色。
在一較佳實施例中,醫藥劑型係藉由熱熔擠出、較佳藉助於雙螺桿擠出機來製備。熔體擠出較佳提供熔融擠出股線,較佳將該熔融擠出股線切割成諸多個整塊,接著將整塊壓製且成形為錠劑。在此方面,術語「錠劑」較佳不應理解為藉由壓製粉末或顆粒而製備之醫藥劑型(壓製物(compressi)),而應理解為成型之擠出物。較佳地,較佳由藉由熔體擠出所獲得之整塊團塊藉助於模具及衝頭來達成壓製。若經由熔體擠出獲得,則壓製步驟較佳係使用展現周圍溫度(亦即在20至25℃範圍內之溫度)之整塊團塊來進行。通過擠出所獲得之股線可本身經歷壓製步驟或可在壓製步驟之前經切割。此切割可藉由普通技術例如使用旋轉刀或壓縮空氣來進行。或者,可如EP-A 240 906中所描述藉由將擠出物在兩個反向旋轉研光輥之間傳送且直接成型為錠劑來進行成型。當然亦可在仍溫熱時(亦即在擠出步驟之後近乎即刻)使擠出之股線經歷壓製步驟或切割步驟。較佳藉助於雙螺桿擠出機來進行擠出。
根據本發明之醫藥劑型可藉由不同方法來製備,以下更詳細解釋其中尤其較佳之方法。若干適合之方法已描述於先前技術中。在此方面,可參考例如WO 2005/016313、WO 2005/016314、WO 2005/063214、WO 2005/102286、WO 2006/002883、WO 2006/002884、WO 2006/002886、WO 2006/082097及WO 2006/082099。
本發明亦係關於可藉由本文以下所描述之方法中之任一者獲得的醫藥劑型。
一般而言,用於製備根據本發明之醫藥劑型的方法較佳包括以下步驟:混合所有成分;視情況較佳藉由對自步驟(a)獲得之混合物施加熱量及/或力將自步驟(a)獲得之混合物預成形,所供應熱量之量較佳不足以將聚氧化烯加熱至其軟化點;藉由施加熱量及力使混合物變硬,且在該製程之後將熱量及力減小,可在施加力期間及/或之前供應熱量且所供應熱量之量足以至少將聚氧化烯加熱至其軟化點;視情況將變硬之混合物切成單粒;視情況使醫藥劑型成型;及視情況提供薄膜包衣。
熱量可例如藉由接觸熱氣體(諸如熱空氣)或藉助於熱氣體(諸如熱空氣)或在超音波之幫助下直接供應;或者藉由摩擦及/或剪切力間接供應。可施加力及/或可例如藉由直接製錠或在適合之擠出機之幫助下,特定而言藉助於配備有兩個螺桿之螺桿擠出機(雙螺桿擠出機)或藉助於行星齒輪擠出機使醫藥劑型成型。
可在藉由施加熱量及力使混合物變硬(步驟(c))期間或在後續步驟(步驟(e))中提供醫藥劑型之最終形狀。在兩種情況下,所有組分之混合物較佳呈增塑狀態,亦即較佳地,在至少超過聚氧化烯軟化點之溫度下進行成型。然而,在較低溫度(例如周圍溫度)下擠出亦可且可為較佳的。
可例如藉助於包含模具及適當形狀之衝頭的製錠壓力機進行成型。
用於製造本發明之醫藥劑型之尤其較佳之方法涉及熱熔擠出。在此方法中,根據本發明之醫藥劑型係在擠出機之幫助下藉由熱成形來製備,較佳不存在任何可觀測之隨之發生的擠出物變色。
此方法之特徵在於a)將所有組分混合,b)在擠出機中將所得混合物至少加熱至聚氧化烯之軟化點且藉由施加力通過擠出機之出口孔擠出,c)將仍具塑性之擠出物切成單粒且成形為醫藥劑型或d)將經冷卻且視情況再加熱之切成單粒之擠出物成形為醫藥劑型。
根據方法步驟a)混合組分亦可在擠出機中進行。
亦可在熟習此項技術者已知之混合器中混合組分。混合器可例如為輥式混合器、振盪混合器、剪切混合器或強制混合器。
已在擠出機中至少加熱至聚氧化烯軟化點之較佳熔融之混合物通過具有至少一個孔洞之模具自擠出機擠出。
根據本發明之方法需要使用適合之擠出機,較佳為螺桿擠出機。配備有兩個螺桿之螺桿擠出機(雙螺桿擠出機)為尤其較佳的。
較佳進行擠出,使得股線歸因於擠出之擴展不超過30%,亦即當使用具有直徑為例如6mm之孔洞的模具時,擠出之股線應具有不超過8mm之直徑。更佳地,股線之擴展不超過25%,更佳不超過20%,最佳不超過15%且特定而言不超過10%。
較佳地,在不存在水之情況下進行擠出,亦即,不添加水。然而,可存在痕量之水(例如由大氣濕度引起)。
擠出機較佳包含至少兩個溫度區,其中在第一區中將混合物至少加熱至聚氧化烯之軟化點,該第一區在饋料區及視情況存在之混合區的下游。混 合物之通量較佳為每小時1.0kg至15kg。在一較佳實施例中,通量為每小時1至3.5kg。在另一較佳實施例中,通量為每小時4至15kg。
在一較佳實施例中,模具頭壓力在25至100bar範圍內。模具頭壓力可尤其根據模具幾何形狀、溫度型態及擠出速度加以調節。
模具幾何形狀或孔洞之幾何形狀為可自由選擇的。模具或孔洞可相應地展現圓形、長方形或橢圓形截面,其中圓形截面較佳具有0.1mm至15mm之直徑且長方形截面較佳具有21mm之最大縱長延伸及10mm之橫向延伸。較佳地,模具或孔洞具有圓形截面。根據本發明使用之擠出機之套管可經加熱或冷卻。將對應溫度控制(亦即加熱或冷卻)佈置成使得要擠出之混合物至少展現對應於聚氧化烯軟化溫度之平均溫度(產物溫度)且不升高至超過使所要加工之麻黃素組分可能被破壞的溫度。較佳地,將要擠出之混合物的溫度調節至低於180℃,較佳低於150℃,但至少達至聚氧化烯之軟化溫度。典型擠出溫度為120℃及130℃。
在一較佳實施例中,擠出機扭矩在30至95%範圍內。擠出機扭矩可尤其根據模具幾何形狀、溫度型態及擠出速度來調節。
在擠出熔融混合物且視情況冷卻所擠出之股線或所擠出之諸多條股線之後,較佳將擠出物切成單粒。此切成單粒可較佳藉由藉助於迴轉或旋轉刀、噴水切割機、絲線、刀片或在雷射切割機之幫助下將擠出物切碎來進行。
較佳地,視情況切成單粒之擠出物之中間或最終儲存或根據本發明之醫藥劑型之最終成形係在無氧氛圍下進行,無氧氛圍可例如藉助於氧清除劑來達成。
可將切成單粒之擠出物壓力成形為錠劑以賦予醫藥劑型最終形狀。
在擠出機中對至少塑化之混合物施加力係藉由控制擠出機中之傳送裝置的轉速及其幾何形狀及藉由以使得在擠出機中較佳在擠出之前即刻形成擠 出塑化混合物所必需之壓力的方式調節出口孔之尺寸來調節。產生具有所需機械特性之醫藥劑型所必需的各特定組合物之擠出參數可藉由簡單初步測試來確定。
舉例而言但不限於,可藉助於雙螺桿擠出機ZSE 18或ZSE27型(Leistritz,Nürnberg,Germany)進行擠出,螺桿直徑為18或27mm。可使用具有偏心末端之螺桿。可使用具有直徑為7、8或9mm之圓形孔洞的可加熱模具。可例如將擠出參數調節至以下值:螺桿轉速:120Upm;對於ZSE 18傳送速率為2kg/h或對於ZSE27則為8kg/h;產物溫度:模具前125℃且模具後135℃;且夾套溫度:110℃。
較佳地,藉助於雙螺桿擠出機或行星齒輪擠出機進行擠出,雙螺桿擠出機(共轉或對轉)為尤其較佳的。
用於製備根據本發明之醫藥劑型的方法較佳為連續進行的。較佳地,該方法涉及擠出所有組分之均勻混合物。若由此獲得之中間物(例如藉由擠出獲得之股線)展現均勻特性,則特別有利。特別理想的是均勻密度、均勻活性成分分佈、均勻機械特性、均勻孔隙率、均勻表面外觀等。僅僅在此等條件下,方可確保藥理學特性之均勻性,諸如釋放型態之穩定性,且可使次品量保持較低。
本發明之另一態樣係關於一種根據本發明之醫藥劑型,其用於治療較佳選自由組織充血、水腫及鼻塞組成之群的疾病、病症或病狀。
本發明之另一態樣係關於麻黃素組分之用途,其用於製造用於治療較佳選自由組織充血、水腫及鼻塞組成之群的疾病、病症或病狀的根據本發明之醫藥劑型。
本發明之另一態樣係關於一種用於治療較佳選自由組織充血、水腫及鼻塞組成之群的疾病、病症或病狀的方法,其包括向有需要之個體投與根據 本發明之醫藥劑型。
較佳地,用於根據本發明之用途的醫藥劑型係投與經口。較佳地,個體為人類。
另外,本發明係關於一種用於預防及/或治療較佳選自由組織充血、水腫及鼻塞組成之群的疾病、病症或病狀的方法,該方法包括提供或投與根據本發明之醫藥劑型,由此防止麻黃素組分化學轉化為甲基安非他命,該麻黃素組分化學轉化為甲基安非他命特定而言涉及藉由機械作用及/或溶劑萃取使醫藥劑型破碎。較佳地,機械作用係選自由以下組成之群:在研缽中研磨、重擊及使用用於粉碎習知醫藥劑型之設備。
本發明之另一態樣係關於上文所描述之根據本發明之醫藥劑型之用途,其用於阻礙或防止麻黃素組分化學轉化為甲基安非他命或其生理學上可接受之鹽。
下文將較佳實施例概述為條目1至133:
1.一種醫藥劑型,其斷裂強度為至少300N且包含:(i)麻黃素組分,其選自由以下組成之群:麻黃素、偽麻黃素及其生理學上可接受之鹽;及(ii)生理學上可接受之轉化抑制劑,其能夠抑制該麻黃素組分離體化學轉化為甲基安非他命。
2.根據條目1之醫藥劑型,其中相對於該醫藥劑型之總重量,該轉化抑制劑之重量含量為至少3.00wt.-%。
3.根據條目1或2之醫藥劑型,其中該離體化學轉化之條件係選自由以下組成之群:(a)振盪及焙燒一鍋程序條件(Li+NH4NO3),(b)埃姆德途徑條件(SOCl2+Pd-BaSO4/H2), (c)納加伊途徑條件(HI+紅P),(d)海波途徑條件(H3PO2+I2),(e)莫斯科途徑條件(I2+红P+H2O),(f)伯奇還原條件(含鹼金屬之液體NH3),(g)布沃-布朗還原條件(含鹼金屬之惰性溶劑),及(h)酮醇縮合條件(含鹼金屬之惰性溶劑)。
4.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑為競爭性基質。
5.根據條目4之醫藥劑型,其中該競爭性基質為犧牲基質,其在該等離體化學轉化條件下替代至少一部分該麻黃素組分發生轉化。
6.根據條目4之醫藥劑型,其中該競爭性基質為副反應基質,其在該等離體化學轉化條件下與至少一部分該麻黃素組分反應以形成不同於N-甲基安非他命之副產物。
7.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑為自由基清除劑或離子清除劑。
8.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑催化醯胺形成。
9.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑影響變性。
10.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑包含選自由以下組成之群的自由基清除劑或離子清除劑或基本上由其組成:抗氧化劑、其他自由基捕獲劑或陰離子捕獲劑、複合劑及沈澱劑或其任何組合。
11.根據條目10之醫藥劑型,其中該抗氧化劑係選自由以下組成之群:抗壞血酸及抗壞血酸衍生物、赤藻糖酸及赤藻糖酸衍生物、生育酚及生育酚衍生物、沒食子酸酯、亞硫酸鹽、硫醇、類胡蘿蔔素及葉黃素、視黃醇及視黃醇衍生物及酚類或其任何組合。
12.根據條目11之醫藥劑型,其中該抗壞血酸或抗壞血酸衍生物係選自由以下 組成之群:抗壞血酸(E300)、抗壞血酸鈉(E301)、抗壞血酸鉀(E303)、抗壞血酸鈣(E302)、抗壞血酸棕櫚酸酯(E304a)及硬脂酸抗壞血酸酯(E305)或其任何組合。
13.根據條目11之醫藥劑型,其中該赤藻糖酸或赤藻糖酸衍生物係選自由以下組成之群:赤藻糖酸(異抗壞血酸)(E315)及赤藻糖酸鈉(E316)或其任何組合。
14.根據條目11之醫藥劑型,其中該生育酚或生育酚衍生物係選自由以下組成之群:α-生育酚、β-生育酚、γ-生育酚(E306、E307、E309)、a-生育酚乙酸酯及生育三烯酚或其任何組合。
15.根據條目11之醫藥劑型,其中該沒食子酸酯係選自由以下組成之群:沒食子酸乙酯(E313)、沒食子酸丙酯(E310)、沒食子酸辛酯(E311)及沒食子酸十二酯(沒食子酸月桂酯)(E312)或其任何組合。
16.根據條目11之醫藥劑型,其中該亞硫酸鹽係選自由以下組成之群:亞硫酸鈉(E221)、亞硫酸氫鈉(E222)、偏亞硫酸鈉(E223)、亞硫酸鉀(E225)、亞硫酸氫鉀(E228)、偏亞硫酸氫鉀(E224)、亞硫酸鈣(E226)、亞硫酸氫鈣(E227)及雙(環己基)二硫化物或其任何組合。
17.根據條目11之醫藥劑型,其中該硫醇係選自由以下組成之群:麩胱甘肽、半胱胺酸(E920)及單硫代甘油或其任何組合。
18.根據條目11之醫藥劑型,其中該類胡蘿蔔素或葉黃素係選自由以下組成之群:β-胡蘿蔔素(E160a)、阿樸胡蘿蔔醛(E160e)、β-阿樸-8'-胡蘿蔔酸乙酯(E160f)、番茄素(E160d)、隱黃質(E161c)、辣椒紅素(E161c)、黃體素(E161b)及角黃素(E161g)或其任何組合。
19.根據條目11之醫藥劑型,其中該視黃醇或視黃醇衍生物為視黃醇。
20.根據條目11之醫藥劑型,其中該酚類係選自由以下組成之群:丁基化羥基茴香醚(E320)、丁基化羥基甲苯(E321)、第三丁基氫醌(E319)、己基間苯二酚(E856)及降二氫愈創木酸或其任何組合。
21.根據條目10之醫藥劑型,其中該其他自由基捕獲劑或陰離子捕獲劑係選自由以下組成之群:烷基鹵化物、異腈及其他捕獲劑或其任何組合。
22.根據條目21之醫藥劑型,其中該烷基鹵化物係選自由以下組成之群:三氯乙烯、1,1,1,2-四氟乙烷、2-氯-6-(三氯-甲基)吡啶及1-氯甲基萘或其任何組合。
23.根據條目21之醫藥劑型,其中該其他捕獲劑係選自由以下組成之群:脲及脲衍生物(E927b)及乙醯舒泛(E950)或其任何組合。
24.根據條目10之醫藥劑型,其中該複合劑係選自由以下組成之群:乙二胺四乙酸、環糊精、冠醚(例如12-冠-4)及穴狀配位子或其任何組合。
25.根據條目10之醫藥劑型,其中該沈澱劑係選自由以下組成之群:鹼金屬磷酸鹽及鹼金屬碳酸鹽或其任何組合。
26.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑包含選自由以下組成之群的競爭性基質或基本上由其組成:食品調味賦形劑(感官)、甜味劑、食品著色劑及其他競爭性基質或其任何組合。
27.根據條目26之醫藥劑型,其中該食品調味賦形劑(感官)係選自由以下組成之群:吡嗪、嘧啶、呋喃、噁唑啉、噻吩、噻唑啶、噻唑、核苷酸及其他食品調味賦形劑或其任何組合。
28.根據條目27之醫藥劑型,其中該吡嗪係選自由以下組成之群:乙醯吡嗪、2-乙氧基-5-甲基吡嗪、2-乙氧基-6-甲基吡嗪、2-異丁基-3-甲氧基吡嗪、2-甲氧基-3-甲基吡嗪及2,3.5-三甲基吡嗪或其任何組合。
29.根據條目27之醫藥劑型,其中該噻唑為2-乙醯基噻唑。
30.根據條目27之醫藥劑型,其中該核苷酸係選自由以下組成之群:鳥苷酸(E626)、鳥苷酸二鈉(E627)、鳥苷酸二鉀(E628)、鳥苷酸鈣(E629)、肌苷酸(E630)、肌苷酸二鈉(E631)、肌苷酸二鉀(E632)、肌苷酸鈣(E633)、5'-核糖核苷酸二鈉(E634)及5'-核糖核苷酸鈣(E635)或其任何組合。
31.根據條目27之醫藥劑型,其中該其他食品調味賦形劑係選自由以下組成之群:鄰胺基苯甲酸異丁酯及香草醛或其任何組合。
32.根據條目26之醫藥劑型,其中該甜味劑係選自由以下組成之群:糖精(E954)、阿斯巴甜(E951)、新橘皮苷二氫查酮(E959)、紐甜(E961)及愛德萬甜或其任何組合。
33.根據條目26之醫藥劑型,其中該食品著色劑係選自由以下組成之群:類胡蘿蔔素及葉黃素、偶氮染料、酚類、葉綠素、花青素及其他食品著色劑或其任何組合。
34.根據條目33之醫藥劑型,其中該偶氮染料係選自由以下組成之群:酒石黃(E102)、晚霞黃fcf(E110)、偶氮玉紅(E122)、胭脂蟲紅a(E124)、阿洛拉紅ac及其鹽(E129)、莧紅(E123)、立索玉紅bk(E180)、亮黑bn(E151)、棕色fk(E154)及褐色ht(E155)或其任何組合。
35.根據條目33之醫藥劑型,其中該酚類為甜菜苷(E162)或其任何組合。
36.根據條目33之醫藥劑型,其中該葉綠素係選自由以下組成之群:葉綠素(E140)及葉綠素銅錯合物(E141)或其任何組合。
37.根據條目33之醫藥劑型,其中該花青素係選自由以下組成之群:天竺葵色素及其糖苷(E163a)、矢車菊色素及其糖苷(E163b)、芍藥色素及其糖苷(E163c)、飛燕草色素及其糖苷(E163d)、牽牛花素及其糖苷(E163e)及錦葵色素(E163f)或其任何組合。
38.根據條目33之醫藥劑型,其中該其他食品著色劑係選自由以下組成之群:薑黃素(E100)、核黃素(E101)、核黃素-5-磷酸鹽(E101a)、喹啉黃ws(E104)、胭脂紅(E120)、赤藻紅(E127)、專利藍v(E131)、靛藍胭脂紅(E132)、亮藍fcf(E133)及綠色s(E142)或其任何組合。
39.根據條目26之醫藥劑型,其中該其他競爭性基質係選自由以下組成之群: 苯甲酸鹽、鄰苯二甲酸酯及其他化合物或其任何組合。
40.根據條目39之醫藥劑型,其中該苯甲酸鹽係選自由以下組成之群:苯甲酸(E210)、苯甲酸鈉(E211)、苯甲酸鉀(E212)及苯甲酸鈣(E213)或其任何組合。
41.根據條目39之醫藥劑型,其中該鄰苯二甲酸酯係選自由以下組成之群:鄰苯二甲酸二乙酯、鄰苯二甲酸羥丙基甲基纖維素及聚乙酸鄰苯二甲酸乙烯酯或其任何組合。
42.根據條目39之醫藥劑型,其中該其他化合物係選自由以下組成之群:苯甲醇(E1519)、2-氯-6-(三氯甲基)吡啶及五甲基-色原烷醇或其任何組合。
43.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑包含選自由羧酸酯及醛或其任何組合組成之群的競爭性基質或基本上由其組成。
44.根據條目43之醫藥劑型,其中該羧酸酯係選自由以下組成之群:醫藥學上可接受之酸的酯、聚合物之酯及脂肪酸之酯或其任何組合。
45.根據條目44之醫藥劑型,其中該醫藥學上可接受之酸的酯係選自由以下組成之群:抗壞血酸酯(E304)、乙酸酯、苯甲酸酯、對羥基苯甲酸酯、乙基對羥基苯甲酸酯(對羥基苯甲酸乙酯)(E214)、乙基對羥基苯甲酸鈉(E215)、丙基對羥基苯甲酸酯(E216)、丙基對羥基苯甲酸鈉(E217)、甲基對羥基苯甲酸酯(E218)、甲基對羥基苯甲酸鈉(E219)、檸檬酸酯、反丁烯二酸酯、乳酸酯、順丁烯二酸酯、蘋果酸酯、甲基丙烯酸酯、山梨酸酯、丁二酸酯、酒石酸酯、胺基酸酯、乙二胺四乙酸酯、赤藻糖酸酯、聚半乳糖醛酸酯、海藻酸酯或其任何組合。
46.根據條目44之醫藥劑型,其中該聚合物之酯係選自由以下組成之群:乙烯-乙酸乙烯酯-共聚物、聚乙酸乙烯酯、乙酸纖維素及乙酸丁二酸羥丙基甲基纖維素或其任何組合。
47.根據條目44之醫藥劑型,其中該脂肪酸之酯係選自由以下組成之群:癸酸酯、月桂酸酯、肉豆蔻酸酯、棕櫚酸酯、硬脂酸酯、油酸酯、亞油酸酯、γ-亞油 酸酯、蓖麻油酸酯、花生酸酯及山俞酸酯或其任何組合。
48.根據條目43之醫藥劑型,其中該醛係選自由以下組成之群:醫藥學上可接受之醛及醛醣或其任何組合。
49.根據條目48之醫藥劑型,其中該醫藥學上可接受之醛係選自由以下組成之群:苯甲醛、肉桂醛及香草醛或其任何組合。
50.根據條目48之醫藥劑型,其中該醛醣係選自由以下組成之群:甘油醛、醛丁醣、醛戊醣及醛己醣或其任何組合。
51.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑包含能夠催化自經溶劑化之鹼金屬及氨形成鹼金屬醯胺之金屬觸媒或有機觸媒或其任何組合或基本上由其組成。
52.根據條目51之醫藥劑型,其中該金屬觸媒係選自由以下組成之群:Fe(II)鹽、Fe(III)鹽、氧化鐵、鈷鹽、鎳鹽及錳鹽或其任何組合。
53.根據條目52之醫藥劑型,其中該Fe(II)鹽係選自由以下組成之群:FeCl2、二茂鐵、二茂鐵衍生物二茂鐵喹及反丁烯二酸Fe(II)或其任何組合。
54.根據條目52之醫藥劑型,其中該Fe(III)鹽係選自由以下組成之群:FeCl3、檸檬酸Fe(III)、三(乙醯基丙酮基)鐵(III)及硝酸Fe(III)或其任何組合。
55.根據條目52之醫藥劑型,其中該鈷鹽係選自由以下組成之群:氯化鈷、溴化鈷、乙酸鈷及硫酸鈷或其任何組合。
56.根據條目52之醫藥劑型,其中該鎳鹽係選自由以下組成之群:氯化鎳、溴化鎳、乙酸鎳及硫酸鎳或其任何組合。
57.根據條目52之醫藥劑型,其中該錳鹽係選自由以下組成之群:氯化錳、溴化錳、乙酸錳及硫酸錳或其任何組合。
58.根據條目51之醫藥劑型,其中該有機觸媒係選自由以下組成之群:異戊二烯、丁二烯、間戊二烯、二甲基丁二烯、己二烯、苯乙烯、甲基苯乙烯、萘及 蒽或其任何組合。
59.根據條目1或3至58中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該轉化抑制劑之重量含量大於0.50wt.-%。
60.根據條目59之醫藥劑型,其中相對於該醫藥劑型之總重量,該轉化抑制劑之重量含量大於1.25wt.-%。
61.根據條目60之醫藥劑型,其中相對於該醫藥劑型之總重量,該轉化抑制劑之重量含量為至少1.50wt.-%。
62.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑之重量含量為至少0.1mg,或至少0.5mg,或至少1.0mg,或至少2.5mg,或至少5.0mg,或至少7.5mg,或至少10mg,或至少15mg,或至少20mg,或至少25mg,或至少50mg,或至少75mg,或至少100mg。
63.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑之重量含量不超過500mg,或不超過400mg,或不超過300mg,或不超過250mg,或不超過200mg,或不超過150mg,或不超過100mg,或不超過75mg,或不超過50mg,或不超過25mg,或不超過20mg,或不超過15mg,或不超過10mg。
64.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑之重量含量在以下範圍內:1.0±0.5mg,或2.5±2mg,或5.0±2mg,或7.5±2mg,或10±2mg,或7.5±5mg,或10±5mg,或12.5±5mg,或15±5mg,或17.5±5mg,或20±5mg,或12.5±10mg,或15±10mg,或17.5±10mg,或20±10mg,或22.5±10mg,或25±10mg,或27.5±10mg,或30±10mg,或30±25mg,或40±25mg,或50±25mg,或60±25mg,或70±25mg,或80±25mg,或90±25mg,或100±25mg,或60±50mg,或80±50mg,或100±50mg,或120±50mg,或140±50mg,或160±50mg,或180±50mg,或200±50mg。
65.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑之重量含量為至少 0.1wt.-%,或至少0.5wt.-%,或至少1.0wt.-%,或至少2.0wt.-%,或至少3.0wt.-%,或至少4.0wt.-%,或至少5.0wt.-%,或至少6.0wt.-%,或至少7.0wt.-%,或至少8.0wt.-%,或至少9.0wt.-%,或至少10wt.-%,在各情況下均係相對於該劑型之總重量。
66.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑之重量含量不超過50wt.-%,或不超過40wt.-%,或不超過30wt.-%,或不超過20wt.-%,或不超過10wt.-%,或不超過7.5wt.-%,或不超過5.0wt.-%,或不超過2.50wt.-%,或不超過1.0wt.-%,在各情況下均係相對於該劑型之總重量。
67.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑之重量含量在以下範圍內:1.0±0.5wt.-%,或2.5±2wt.-%,或5.0±2wt.-%,或7.5±2wt.-%,或10±2wt.-%,或7.5±5wt.-%,或10±5wt.-%,或12.5±5wt.-%,或15±5wt.-%,或17.5±5wt.-%,或20±5wt.-%,或10±7.5wt.-%,或12.5±10wt.-%,或15±10wt.-%,或17.5±10wt.-%,或20±10wt.-%,或22.5±10wt.-%,或25±10wt.-%,或27.5±10wt.-%,或30±10wt.-%,或30±25wt.-%,或40±25wt.-%,或50±25wt.-%,或60±25wt.-%,或70±25wt.-%,在各情況下均係相對於該劑型之總重量。
68.根據前述條目中任一項之醫藥劑型,其中該麻黃素組分與該轉化抑制劑之相對重量比在以下範圍內:1:100至100:1,或1:75至75:1,或1:50至50:1,或1:25至25:1,或1:10至10:1,或1:7.5至7.5:1,或1:5至5:1,或1:3至3:1,或1:2至2:1,或1:1.5至1.5:1。
69.根據前述條目中任一項之醫藥劑型,其中該麻黃素組分與該轉化抑制劑之相對重量比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1,或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
70.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑與該麻黃素組分之相 對重量比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1,或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
71.根據前述條目中任一項之醫藥劑型,其中該麻黃素組分與該轉化抑制劑之相對莫耳比在以下範圍內:1:100至100:1,或1:75至75:1,或1:50至50:1,或1:25至25:1,或1:10至10:1,或1:7.5至7.5:1,或1:5至5:1,或1:3至3:1,或1:2至2:1,或1:1.5至1.5:1。
72.根據前述條目中任一項之醫藥劑型,其中該麻黃素組分與該轉化抑制劑之相對莫耳比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1,或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
73.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑與該麻黃素組分之相對莫耳比在以下範圍內:1:100至1:1.1,或1:75至1:1.1,或1:50至1:1.1,或1:25至1:1.1,或1:10至1:1.1,或1:7.5至1:1.1,或1:5至1:1.1,或1:3至1:1.1,或1:2至1:1.1,或1:1.5至1:1.1。
74.根據前述條目中任一項之醫藥劑型,其中該麻黃素組分包含偽麻黃素鹽酸鹽或偽麻黃素硫酸鹽。
75.根據前述條目中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該麻黃素組分之重量含量在0.1至60wt.-%範圍內。
76.根據前述條目中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該麻黃素組分之重量含量在10至50wt.-%範圍內。
77.根據前述條目中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該麻黃素組分之重量含量在15至45wt.-%範圍內。
78.根據前述條目中任一項之醫藥劑型,其包含聚氧化烯。
79.根據條目78之醫藥劑型,其中該聚氧化烯為聚氧化乙烯。
80.根據條目78或79之醫藥劑型,其中該聚氧化烯具有至少200,000g/mol之重量平均分子量。
81.根據條目78至80中任一項之醫藥劑型,其中該聚氧化烯具有至少500,000g/mol之重量平均分子量。
82.根據條目78至81中任一項之醫藥劑型,其中該聚氧化烯具有在1,000,000g/mol至15,000,000g/mol範圍內之重量平均分子量。
83.根據條目78至82中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該聚氧化烯之重量含量為至少25wt.-%。
84.根據條目78至83中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該聚氧化烯之重量含量在25至65wt.-%範圍內。
85.根據條目78至84中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該聚氧化烯之重量含量為至少30wt.-%。
86.根據條目78至85中任一項之醫藥劑型,其中以該醫藥劑型之總重量計,該聚氧化烯之重量含量在50±20wt.-%範圍內。
87.根據條目78至84中任一項之醫藥劑型,其中該聚氧化烯與該麻黃素組分之相對重量比在5:1至1:4範圍內。
88.根據條目78至87中任一項之醫藥劑型,其中該聚氧化烯與該麻黃素組分之相對重量比在3:1至1:2範圍內。
89.根據前述條目中任一項之醫藥劑型,其不包含抗氧化劑。
90.根據條目1至88中任一項之醫藥劑型,其包含抗氧化劑。
91.根據條目90之醫藥劑型,其中該抗氧化劑係選自由以下組成之群:抗壞血酸、抗壞血酸鹽、丁基羥基茴香醚、丁基羥基甲苯、單硫代甘油、亞磷酸、α-生育酚、α-生育酚乙酸酯、苯甲酸松柏酯、降二氫愈創木酸、沒食子酸酯及亞硫 酸氫鈉。
92.根據條目91之醫藥劑型,其中該抗氧化劑為α-生育酚。
93.根據條目90至92中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該抗氧化劑之重量含量大於0.2wt.-%。
94.根據條目90至93中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該抗氧化劑之重量含量為至少0.5wt.-%。
95.根據條目90至94中任一項之醫藥劑型,其中該麻黃素組分與該抗氧化劑之相對重量比在5:1至35:1範圍內。
96.根據前述條目中任一項之醫藥劑型,其包含纖維素醚。
97.根據條目96之醫藥劑型,其中該纖維素醚係選自由以下組成之群:甲基纖維素、乙基纖維素、丙基纖維素、羥乙基纖維素、羥丙基纖維素、羥丙基甲基纖維素、羧甲基纖維素、羧甲基纖維素之鹽及任何前述物質之混合物。
98.根據條目97之醫藥劑型,其中該纖維素醚為羥丙基甲基纖維素。
99.根據條目96至98中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該纖維素醚之重量含量在0.5至20wt.-%範圍內。
100.根據條目96至99中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該纖維素醚之重量含量在1.0至15wt.-%範圍內。
101.根據條目965至100中任一項之醫藥劑型,其中該麻黃素組分與該纖維素醚之相對重量比在1:1至7.5:1範圍內。
102.根據條目96至101中任一項之醫藥劑型,其中該麻黃素組分與該纖維素醚之相對重量比在3:1至5.5:1範圍內。
103.根據條目96至102中任一項之醫藥劑型,其包含聚氧化烯及纖維素醚,其中該聚氧化烯與該纖維素醚之相對重量比在2.0:1至12:1範圍內。
104.根據條目96至103中任一項之醫藥劑型,其包含聚氧化烯及纖維素醚, 其中該聚氧化烯與該纖維素醚之相對重量比在5.0:1至7.5:1範圍內。
105.根據前述條目中任一項之醫藥劑型,其包含黏合劑。
106.根據條目105之醫藥劑型,其中該黏合劑係選自由以下組成之群:二醣、澱粉、經改質之澱粉、糖醇、聚乙烯吡咯啶酮及任何前述物質之混合物。
107.根據條目105或106之醫藥劑型,其中該黏合劑為聚乙烯吡咯啶酮。
108.根據條目105至107中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該黏合劑之重量含量在0.5至20wt.-%範圍內。
109.根據條目105至108中任一項之醫藥劑型,其中相對於該醫藥劑型之總重量,該黏合劑之重量含量在1.0至15wt.-%範圍內。
110.根據條目105至109中任一項之醫藥劑型,其中該麻黃素組分與該黏合劑之相對重量比在1:1至7.5:1範圍內。
111.根據條目105至110中任一項之醫藥劑型,其中該麻黃素組分與該黏合劑之相對重量比在3:1至5.5:1範圍內。
112.根據條目105至111中任一項之醫藥劑型,其包含聚氧化烯及黏合劑,其中該聚氧化烯與該黏合劑之相對重量比在2.0:1至12:1範圍內。
113.根據條目105至112中任一項之醫藥劑型,其包含聚氧化烯及黏合劑,其中該聚氧化烯與該黏合劑之相對重量比在5.0:1至7.5:1範圍內。
114.根據前述條目中任一項之醫藥劑型,其包含交聯聚合物。
115.根據條目114之醫藥劑型,其中該交聯聚合物係選自由以下組成之群:交聯羧甲基纖維素、交聯羧甲基纖維素之鹽、交聯聚維酮及任何前述物質之混合物。
116.根據條目114或115之醫藥劑型,其中相對於該醫藥劑型之總重量,該交聯聚合物之重量含量在1.0至35wt.-%範圍內。
117.根據條目114至116中任一項之醫藥劑型,其中相對於該醫藥劑型之總 重量,該交聯聚合物之重量含量在1.0至15wt.-%範圍內。
118.根據條目114至117中任一項之醫藥劑型,其包含聚氧化烯及交聯聚合物,其中該聚氧化烯與較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之該交聯聚合物之相對重量比在2.0:1至12:1範圍內。
119.根據條目114至118中任一項之醫藥劑型,其包含聚氧化烯及交聯聚合物,其中該聚氧化烯與較佳為交聯羧甲基纖維素或交聯羧甲基纖維素鈉之該交聯聚合物之相對重量比在5.0:1至7.5:1範圍內。
120.根據前述條目中任一項之醫藥劑型,其包含纖維素醚及黏合劑,其中該纖維素醚與該黏合劑之相對重量比在2.5:1至1:2.5範圍內。
121.根據前述條目中任一項之醫藥劑型,其包含纖維素醚及黏合劑,其中該纖維素醚與該黏合劑之相對重量比在2:1至1:2範圍內。
122.根據前述條目中任一項之醫藥劑型,其包含纖維素醚及黏合劑,其中該纖維素醚與該黏合劑之相對重量比在1.5:1至1:1.5範圍內。
123.根據前述條目中任一項之醫藥劑型,其包含交聯聚合物及黏合劑,其中該交聯聚合物與該黏合劑之相對重量比在2.5:1至1:2.5範圍內。
124.根據前述條目中任一項之醫藥劑型,其包含交聯聚合物及黏合劑,其中該交聯聚合物與該黏合劑之相對重量比在2:1至1:2範圍內。
125.根據前述條目中任一項之醫藥劑型,其包含交聯聚合物及黏合劑,其中該交聯聚合物與該黏合劑之相對重量比在1.5:1至1:1.5範圍內。
126.根據前述條目中任一項之醫藥劑型,其包含交聯聚合物及纖維素醚,其中該纖維素醚與該交聯聚合物之相對重量比較佳在2.5:1至1:2.5範圍內。
127.根據前述條目中任一項之醫藥劑型,其包含交聯聚合物及纖維素醚,其中該纖維素醚與該交聯聚合物之相對重量比較佳在2:1至1:2範圍內。
128.根據前述條目中任一項之醫藥劑型,其包含交聯聚合物及纖維素醚,其 中該纖維素醚與該交聯聚合物之相對重量比較佳在1.5:1至1:1.5範圍內。
129.根據前述條目中任一項之醫藥劑型,其提供針對藉助於水性或有機溶劑自該醫藥劑型萃取該麻黃素組分的抗性。
130.根據前述條目中任一項之醫藥劑型,其中該轉化抑制劑包含香草醛或基本上由其組成。
131.根據前述條目中任一項之醫藥劑型,其用於治療選自由以下組成之群的疾病、病症或病狀:組織充血、水腫及鼻塞。
132.用於根據條目131之用途的醫藥劑型,其中該醫藥劑型係投與經口。
133.用於根據條目131或132之用途的醫藥劑型,其中該醫藥劑型係每天一次、每天兩次或每天三次投與。
Claims (15)
- 一種醫藥劑型,其斷裂強度為至少300N且包含:- 麻黃素組分,其選自由以下組成之群:麻黃素、偽麻黃素及其生理學上可接受之鹽;及- 生理學上可接受之轉化抑制劑,其能夠抑制該麻黃素組分離體化學轉化為甲基安非他命(methamphetamine)。
- 如申請專利範圍第1項之醫藥劑型,其中相對於該醫藥劑型之總重量,該轉化抑制劑之重量含量為至少3.00wt.-%。
- 如申請專利範圍第1項或第2項之醫藥劑型,其中該離體化學轉化之條件係選自由以下組成之群:- 振盪及焙燒一鍋程序(shake and bake one pot procedure)條件,其涉及Li+NH 4NO 3;- 愛姆德途徑( Emde route)條件,其涉及SOCl 2+Pd-BaSO 4/H 2;- 納加伊途徑( Nagai route)條件,其涉及HI+紅P;- 海波途徑(hypo route)條件,其涉及H 3PO 2+I 2;- 莫斯科途徑(Moscow route)條件,其涉及I 2+紅P+H 2O;- 伯奇還原( Birch reduction)條件,其涉及含鹼金屬之液體NH 3;- 布沃-布朗還原( Bouveault-Blanc reduction)條件,其涉及含鹼金屬之惰性溶劑;及- 酮醇縮合條件,其涉及含鹼金屬之惰性溶劑。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該轉化抑制劑包含選自由以下組成之群的自由基清除劑或離子清除劑或基本上由其組成:複合劑、沈澱劑、抗氧化劑及其他自由基捕獲劑或陰離子捕獲劑或其任何組合。
- 如申請專利範圍第4項之醫藥劑型,其中 - 該複合劑係選自由以下組成之群:乙二胺四乙酸、環糊精、冠醚及穴狀配位子或其任何組合;或者- 該沈澱劑係選自由以下組成之群:鹼金屬磷酸鹽及鹼金屬碳酸鹽或其任何組合;或者- 該抗氧化劑係選自由以下組成之群:抗壞血酸及抗壞血酸衍生物、赤藻糖酸及赤藻糖酸衍生物、生育酚及生育酚衍生物、沒食子酸酯、亞硫酸鹽、硫醇、類胡蘿蔔素及葉黃素、視黃醇及視黃醇衍生物以及酚類或其任何組合;或者- 該其他自由基捕獲劑或陰離子捕獲劑係選自由以下組成之群:烷基鹵化物、異腈及其他捕獲劑或其任何組合。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該轉化抑制劑包含選自由以下組成之群的競爭性基質或基本上由其組成:食品調味賦形劑、甜味劑、食品著色劑及其他競爭性基質或其任何組合。
- 如申請專利範圍第6項之醫藥劑型,其中- 該食品調味賦形劑係選自由以下組成之群:吡嗪、嘧啶、呋喃、噁唑啉、噻吩、噻唑啶、噻唑、核苷酸及其他食品調味賦形劑或其任何組合;較佳為香草醛;或者- 該甜味劑係選自由以下組成之群:糖精、阿斯巴甜、新橘皮苷二氫查酮、紐甜(neotam)及愛德萬甜(advantame)或其任何組合;或者- 該食品著色劑係選自由以下組成之群:類胡蘿蔔素及葉黃素、偶氮染料、酚類、葉綠素、花青素及其他食品著色劑或其任何組合;或者- 該其他競爭性基質係選自由以下組成之群:苯甲酸鹽、鄰苯二甲酸酯及其他化合物或其任何組合。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該轉化抑制劑包含選自由羧酸酯及醛或其任何組合組成之群的競爭性基質或基本上由其組成。
- 如申請專利範圍第8項之醫藥劑型,其中- 該羧酸酯係選自由以下組成之群:醫藥學上可接受之酸的酯、聚合物之酯及脂肪酸之酯或其任何組合;或者- 該醛係選自由以下組成之群:醫藥學上可接受之醛及醛醣或其任何組合;較佳為香草醛。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該轉化抑制劑包含金屬觸媒或有機觸媒或其任何組合或基本上由其組成,用於催化自經溶劑化之鹼金屬及氨形成鹼金屬醯胺。
- 如申請專利範圍第10項之醫藥劑型,其中- 該金屬觸媒係選自由以下組成之群:Fe(II)鹽、Fe(III)鹽、氧化鐵、鈷鹽、鎳鹽及錳鹽或其任何組合;或者- 該有機觸媒係選自由以下組成之群:異戊二烯、丁二烯、间戊二烯、二甲基丁二烯、己二烯、苯乙烯、甲基苯乙烯、萘及蒽或其任何組合;其中在任一情況下,該觸媒能夠催化自經溶劑化之鹼金屬及氨形成鹼金屬醯胺。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該轉化抑制劑之重量含量為至少0.1wt.-%,或至少0.5wt.-%,或至少1.0wt.-%,或至少2.0wt.-%,或至少3.0wt.-%,或至少4.0wt.-%,或至少5.0wt.-%,或至少6.0wt.-%,或至少7.0wt.-%,或至少8.0wt.-%,或至少9.0wt.-%,或至少10wt.-%,在各情況下均係相對於該劑型之總重量。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該轉化抑制劑之重量含量不超過50wt.-%,或不超過40wt.-%,或不超過30wt.-%,或不超 過20wt.-%,或不超過10wt.-%,或不超過7.5wt.-%,或不超過5.0wt.-%,或不超過2.5wt.-%,或不超過1.0wt.-%,在各情況下均係相對於該劑型之總重量。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該轉化抑制劑之重量含量在以下範圍內:1.0±0.5wt.-%,或2.5±2wt.-%,或5.0±2wt.-%,或7.5±2wt.-%,或10±2wt.-%,或7.5±5wt.-%,或10±5wt.-%,或12.5±5wt.-%,或15±5wt.-%,或17.5±5wt.-%,或20±5wt.-%,或10±7.5wt.-%,或12.5±10wt.-%,或15±10wt.-%,或17.5±10wt.-%,或20±10wt.-%,或22.5±10wt.-%,或25±10wt.-%,或27.5±10wt.-%,或30±10wt.-%,或30±25wt.-%,或40±25wt.-%,或50±25wt.-%,或60±25wt.-%,或70±25wt.-%,在各情況下均係相對於該劑型之總重量。
- 如前述申請專利範圍中任一項之醫藥劑型,其中該麻黃素組分與該轉化抑制劑之相對莫耳比在以下範圍內:1:100至100:1,或1:75至75:1,或1:50至50:1,或1:25至25:1,或1:10至10:1,或1:7.5至7.5:1,或1:5至5:1,或1:3至3:1,或1:2至2:1,或1:1.5至1.5:1。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EPEP18156016.0 | 2018-02-09 | ||
| EP18156016 | 2018-02-09 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202002957A true TW202002957A (zh) | 2020-01-16 |
Family
ID=61189310
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW108103594A TW202002957A (zh) | 2018-02-09 | 2019-01-30 | 包含轉化抑制劑之麻黃素及其衍生物之抗損壞調配物 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US20190247332A1 (zh) |
| TW (1) | TW202002957A (zh) |
| WO (1) | WO2019154948A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN119500410A (zh) * | 2024-11-22 | 2025-02-25 | 昆明理工大学 | 一种闪锌矿的组合抑制剂及其应用 |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3612211A1 (de) | 1986-04-11 | 1987-10-15 | Basf Ag | Kontinuierliches verfahren zum tablettieren |
| GT199900148A (es) | 1998-09-10 | 2001-02-28 | Desnaturalizantes para las sales aminas simpaticomimeticas. | |
| US6852891B2 (en) | 2001-05-08 | 2005-02-08 | The Johns Hopkins University | Method of inhibiting methaphetamine synthesis |
| DE10336400A1 (de) | 2003-08-06 | 2005-03-24 | Grünenthal GmbH | Gegen Missbrauch gesicherte Darreichungsform |
| PL1658054T3 (pl) | 2003-08-06 | 2007-11-30 | Gruenenthal Gmbh | Postać aplikacyjna zabezpieczona przed nadużyciem |
| DE10361596A1 (de) | 2003-12-24 | 2005-09-29 | Grünenthal GmbH | Verfahren zur Herstellung einer gegen Missbrauch gesicherten Darreichungsform |
| DE102005005446A1 (de) | 2005-02-04 | 2006-08-10 | Grünenthal GmbH | Bruchfeste Darreichungsformen mit retardierter Freisetzung |
| PL1740156T3 (pl) | 2004-04-22 | 2011-12-30 | Gruenenthal Gmbh | Sposób wytwarzania zabezpieczonej przed nadużyciem, stałej postaci aplikacyjnej |
| WO2006002884A1 (de) | 2004-07-01 | 2006-01-12 | Grünenthal GmbH | Gegen missbrauch gesicherte, orale darreichtungsform |
| CA2572352A1 (en) | 2004-07-01 | 2006-01-12 | Gruenenthal Gmbh | Oral dosage form safeguarded against abuse containing (1r,2r)-3-(3-dimethylamino-1-ethyl-2-methyl-propyl)phenol |
| EP1765298B1 (de) | 2004-07-01 | 2012-10-24 | Gruenenthal Gmbh | Verfahren zur herstellung einer gegen missbrauch gesicherten, festen darreichungsform unter verwendung eines planetwalzenextruders |
| DE102005005449A1 (de) | 2005-02-04 | 2006-08-10 | Grünenthal GmbH | Verfahren zur Herstellung einer gegen Missbrauch gesicherten Darreichungsform |
| SA07280459B1 (ar) | 2006-08-25 | 2011-07-20 | بيورديو فارما إل. بي. | أشكال جرعة صيدلانية للتناول عن طريق الفم مقاومة للعبث تشتمل على مسكن شبه أفيوني |
| DE102007011485A1 (de) | 2007-03-07 | 2008-09-11 | Grünenthal GmbH | Darreichungsform mit erschwertem Missbrauch |
| US20080260836A1 (en) | 2007-04-18 | 2008-10-23 | Thomas James Boyd | Films Comprising a Plurality of Polymers |
| AU2009207796B2 (en) | 2008-01-25 | 2014-03-27 | Grunenthal Gmbh | Pharmaceutical dosage form |
| EP3064064A1 (en) | 2009-09-30 | 2016-09-07 | Acura Pharmaceuticals, Inc. | Methods and compositions for deterring abuse |
| PH12013501345A1 (en) | 2010-12-23 | 2022-10-24 | Purdue Pharma Lp | Tamper resistant solid oral dosage forms |
| HRP20171458T1 (hr) | 2011-07-29 | 2017-11-17 | Grünenthal GmbH | Tableta otporna na mijenjanje koja pruža neposredno oslobađanje lijeka |
| KR20140053159A (ko) | 2011-07-29 | 2014-05-07 | 그뤼넨탈 게엠베하 | 즉시 약물 방출을 제공하는 탬퍼-저항성 정제 |
| EP2819657A1 (en) | 2012-02-28 | 2015-01-07 | Grünenthal GmbH | Tamper-resistant pharmaceutical dosage form comprising nonionic surfactant |
| WO2014022541A1 (en) | 2012-08-01 | 2014-02-06 | Acura Pharmaceuticals, Inc. | Stabilization of one-pot methamphetamine synthesis systems |
| BR112015026549A2 (pt) | 2013-05-29 | 2017-07-25 | Gruenenthal Gmbh | forma de dosagem à prova de violação contendo uma ou mais partículas |
| US9770514B2 (en) | 2013-09-03 | 2017-09-26 | ExxPharma Therapeutics LLC | Tamper-resistant pharmaceutical dosage forms |
| WO2015048597A1 (en) | 2013-09-30 | 2015-04-02 | Daya Drug Discoveries, Inc. | Prevention of illicit methamphetamine manufacture from pseudoephedrine using food flavor excipients |
| US20160089439A1 (en) | 2014-09-28 | 2016-03-31 | Satara Pharmaceuticals, LLC | Prevention of Illicit Manufacutre of Methamphetamine from Pseudoephedrine Using Food Flavor Excipients |
-
2019
- 2019-01-30 TW TW108103594A patent/TW202002957A/zh unknown
- 2019-02-08 WO PCT/EP2019/053071 patent/WO2019154948A1/en not_active Ceased
- 2019-02-08 US US16/270,641 patent/US20190247332A1/en not_active Abandoned
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN119500410A (zh) * | 2024-11-22 | 2025-02-25 | 昆明理工大学 | 一种闪锌矿的组合抑制剂及其应用 |
| CN119500410B (zh) * | 2024-11-22 | 2025-09-23 | 昆明理工大学 | 一种闪锌矿的组合抑制剂及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2019154948A1 (en) | 2019-08-15 |
| US20190247332A1 (en) | 2019-08-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN104394851B (zh) | 抗篡改和抗剂量‑倾泻药物剂型 | |
| EP2611428B1 (en) | Tamper resistant dosage form comprising an anionic polymer | |
| CN104428002A (zh) | 热成形的抗篡改含锌药物剂型 | |
| JP2019513768A (ja) | 調節放出乱用抑制剤形 | |
| KR20130137627A (ko) | 음이온성 중합체를 포함하는 내변조성 투여형 | |
| KR20160031526A (ko) | 에틸렌-비닐 아세테이트 중합체를 함유하는 템퍼 내성 투여형 | |
| CN104066426A (zh) | 包含药理学活性成分、阿片样物质拮抗剂和/或厌恶剂、聚环氧烷和阴离子聚合物的抗损坏口服药物剂型 | |
| CN107889459A (zh) | 具有立即释放和对溶剂萃取的抗性的抗篡改剂型 | |
| JP2018513872A (ja) | 異なる粒子から2種の薬物の急速放出をもたらすタンパレジスタントな固定用量組合せ | |
| TW202002957A (zh) | 包含轉化抑制劑之麻黃素及其衍生物之抗損壞調配物 | |
| JP2018513864A (ja) | 粒子及びマトリックスから2種の薬物の急速放出をもたらすタンパレジスタントな固定用量組合せ | |
| JP2018515456A (ja) | 粒子及び粉末から2種の薬物の急速放出をもたらすタンパレジスタントな固定用量組合せ | |
| JP2018515455A (ja) | 粒子から2種の薬物の急速放出をもたらすタンパレジスタントな固定用量組合せ | |
| US20180028670A1 (en) | Tamper resistant dosage form comprising an anionic polysaccharide | |
| CN111465390A (zh) | 调释防滥用剂型 | |
| TW201811313A (zh) | 麻黃鹼和其衍生物的防損壞製劑 | |
| CN120693151A (zh) | 包括奈妥匹坦和帕洛诺司琼的固定剂量组合 | |
| HK1184389B (zh) | 包含阴离子聚合物的抗破碎剂型 |