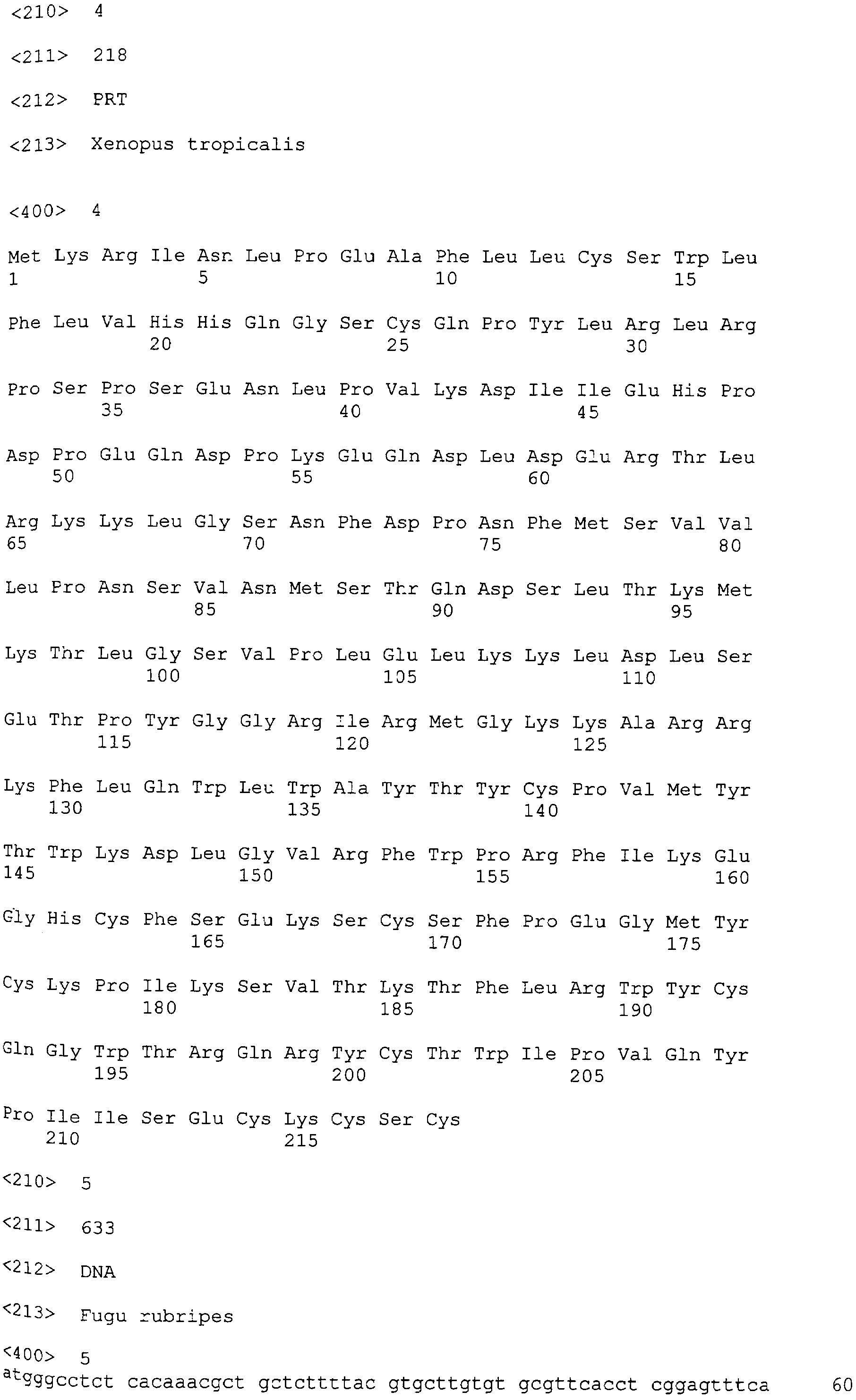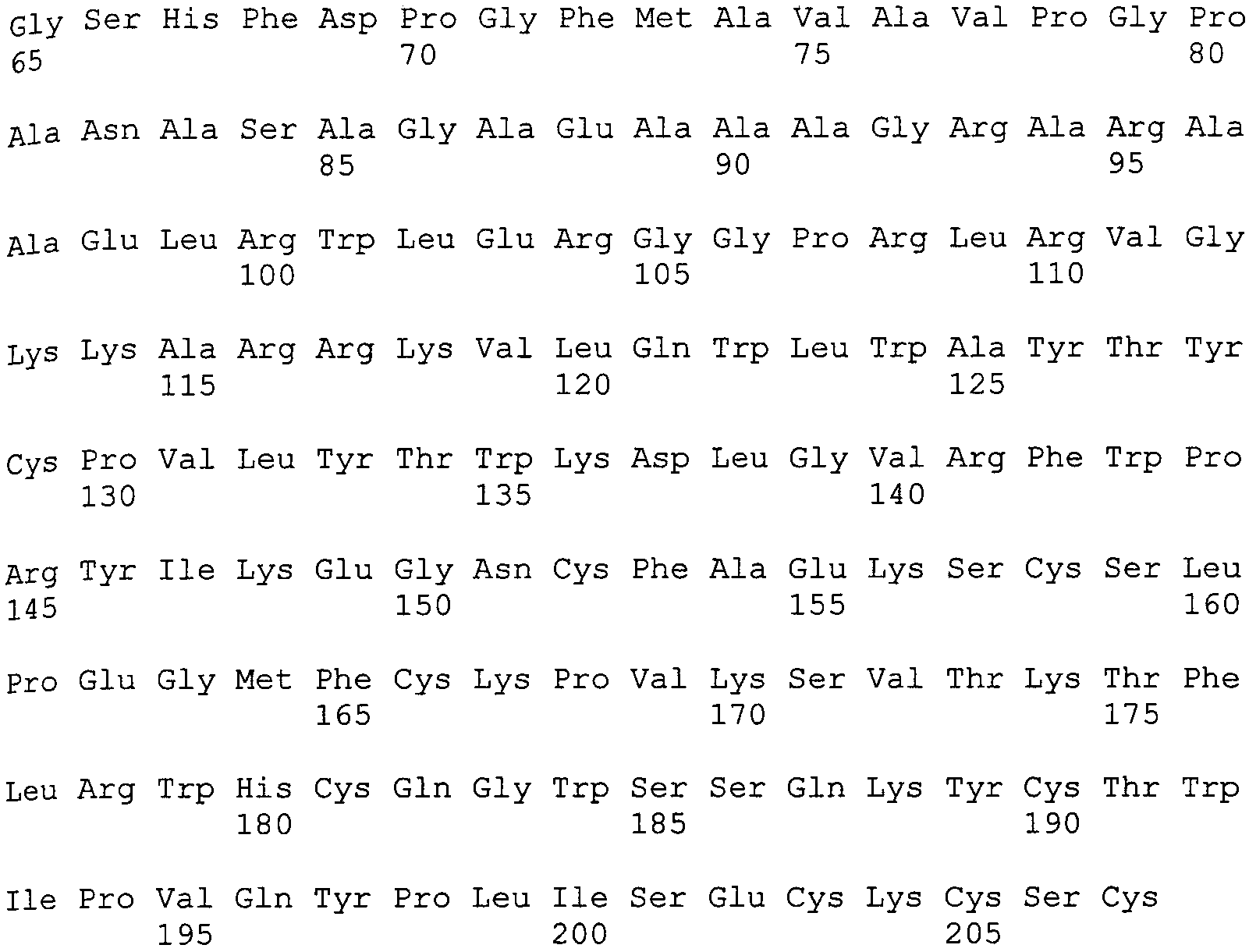RU2354662C2 - Noggin2-based activin activity blocking method - Google Patents
Noggin2-based activin activity blocking method Download PDFInfo
- Publication number
- RU2354662C2 RU2354662C2 RU2005123287/13A RU2005123287A RU2354662C2 RU 2354662 C2 RU2354662 C2 RU 2354662C2 RU 2005123287/13 A RU2005123287/13 A RU 2005123287/13A RU 2005123287 A RU2005123287 A RU 2005123287A RU 2354662 C2 RU2354662 C2 RU 2354662C2
- Authority
- RU
- Russia
- Prior art keywords
- noggin2
- protein
- activin
- mrna
- noggin1
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1875—Bone morphogenic factor; Osteogenins; Osteogenic factor; Bone-inducing factor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/495—Transforming growth factor [TGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Toxicology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
Область изобретенияField of Invention
Данное изобретение относится к белкам, регулирующим клеточную дифференцировку путем ингибирования белков надсемейства TGF-β.This invention relates to proteins that regulate cell differentiation by inhibiting TGF-β superfamily proteins.
Предшествующий уровень техникиState of the art
Надсемейство трансформирующего фактора роста Р (TGF-P) включает в себя множество факторов роста, обладающих общими структурными мотивами. Данные белки вовлечены в широкий спектр биологических процессов, таких как процессы клеточной и тканевой дифференцировки в ходе эмбрионального развития и заживления ран, восстановление и реконструкции костной ткани во взрослом организме. Идентифицирован ряд белков межклеточного матрикса, являющихся антагонистами различных представителей надсемейства TGF-β (например, белков костного морфогенеза, BMP) и играющих важную роль в процессах клеточной дифференцировки и развития (Balemans and Van Hul, Dev Biol. (2002) 250 (2):231-250; Avsian-Kretchmer and Hsueh, Mol Endocrinol. (2004) 18(I):1-12). К антагонистам BMP относятся, например, белки хордин, вентроптин, ноггин, церберус и фоллистатин.The superfamily of transforming growth factor P (TGF-P) includes many growth factors that share common structural motifs. These proteins are involved in a wide range of biological processes, such as the processes of cell and tissue differentiation during embryonic development and wound healing, restoration and reconstruction of bone tissue in the adult body. A number of intercellular matrix proteins have been identified that are antagonists of various representatives of the TGF-β superfamily (e.g., bone morphogenesis proteins, BMP) and play an important role in the processes of cell differentiation and development (Balemans and Van Hul, Dev Biol. (2002) 250 (2): 231-250; Avsian-Kretchmer and Hsueh, Mol Endocrinol. (2004) 18 (I): 1-12). BMP antagonists include, for example, chordin, ventroptin, noggin, cerberus and follistatin proteins.
Например, белки церберус и ноггин позвоночных индуцируют формирование структур головы в передней эктодерме эмбрионов позвоночных. Белок ноггин способен также изменять дифференцировку мезодермальных зачатков из вентральных зачатков, таких как кровь и мезенхима, в дорзальные зачатки, такие как мышца или хорда, или дифференцировку эпидермальных зачатков в нейральные зачатки. Функции хордина сходны с функциями ноггин1, отражая сходный механизм действия этих белков как антагонистов BMP.For example, the proteins cerberus and noggin vertebrates induce the formation of head structures in the anterior ectoderm of vertebrate embryos. The noggin protein is also able to change the differentiation of mesoderm primordia from ventral primordia, such as blood and mesenchyme, into dorsal primordia, such as muscle or chorda, or differentiation of epidermal primordia into neural rudiments. The functions of chordin are similar to those of noggin1, reflecting a similar mechanism of action of these proteins as antagonists of BMP.
Антагонисты факторов роста из надсемейства TGF-β являются важными фармацевтическими, клиническими и лабораторными инструментами для регуляции клеточной дифференцировки и терапевтического вмешательства.TGF-β superfamily growth factor antagonists are important pharmaceutical, clinical, and laboratory tools for regulating cell differentiation and therapeutic intervention.
Недавно у позвоночных был описан новый гомолог белка ноггин, названный ноггин2 (Fletcher et al., Gene Expr Patterns. 2004, v. 5(2), pp.225-230). Было показано, что ген ноггин2 имеет дифференциальный характер экспрессии в ходе развития Xenopus. Однако функция ноггин2 не исследована. Настоящее изобретение относится к функции ноггин2.Recently, a new protein noggin homologue, called noggin2, has been described in vertebrates (Fletcher et al., Gene Expr Patterns. 2004, v. 5 (2), pp. 225-230). The noggin2 gene has been shown to have a differential expression pattern during the development of Xenopus. However, the function of noggin2 has not been investigated. The present invention relates to the function of noggin2.
Сущность изобретенияSUMMARY OF THE INVENTION
Авторы настоящего изобретения открыли, что ноггин2 играет роль в регуляции клеточной дифференцировки и является антагонистом некоторых представителей надсемейства TGF-P. При этом спектр и характер действия ноггин2 отличны от таковых ноггин1 (ранее "ноггин"). В частности, в отличие от ноггин1, ноггин2 не индуцирует развитие мышечной ткани из эмбриональной вентральной мезодермы. Кроме того, он может препятствовать хорошо известной активности ноггин1 в отношении индукции развития мышц. В то же время, подобно ноггин1, ноггин2 может индуцировать развитие нервной ткани из эмбриональной эктодермы. Таким образом, ноггин2 обладает уникальной избирательной активностью в отношении индукции развития нервной ткани.The authors of the present invention discovered that noggin2 plays a role in the regulation of cell differentiation and is an antagonist of some members of the TGF-P superfamily. Moreover, the spectrum and nature of the action of noggin2 are different from those of noggin1 (formerly “noggin”). In particular, unlike noggin1, noggin2 does not induce the development of muscle tissue from embryonic ventral mesoderm. In addition, it may interfere with the well-known activity of noggin1 in relation to the induction of muscle development. At the same time, like noggin1, noggin2 can induce the development of nervous tissue from the embryonic ectoderm. Thus, noggin2 has unique selective activity in relation to the induction of the development of nervous tissue.
Выявленная способность ноггин2 препятствовать дифференцировке мышечной ткани объясняется его способностью ингибировать общую дифференцировку эмбриональной мезодермы благодаря взаимодействию с иным (более широким) спектром факторов из надсемейства TGF-β. Наряду с ингибированием эпидермализующей активности ВМР2, ВМР4 или ВМР7, которая, как известно, также ингибируется ноггин1, ноггин2 обладает способностью ингибировать активность такого индуктора эмбриональной мезодермы, как activin.The revealed ability of noggin2 to inhibit differentiation of muscle tissue is explained by its ability to inhibit the general differentiation of embryonic mesoderm due to its interaction with a different (wider) spectrum of factors from the TGF-β superfamily. In addition to inhibiting the epidermal activity of BMP2, BMP4 or BMP7, which is also known to be inhibited by noggin1, noggin2 has the ability to inhibit the activity of an embryonic mesoderm inducer such as activin.
Настоящее изобретение относится к способам и композициям, в которых используется ноггин2 или кодирующая его нуклеиновая кислота.The present invention relates to methods and compositions that use noggin2 or a nucleic acid encoding it.
В предпочтительном осуществлении настоящее изобретение относится к способу снижения или блокирования активности специфичных для ноггин2 мишеней (например, ВМР2, ВМР4, ВМР7, activin или их сочетания) в организме, ткани или клетке, предусматривающему введение ноггин2 в указанный организм, ткань или клетку в количестве, эффективном для ингибирования или снижения активности специфичных для ноггин2 мишеней посредством препятствования связыванию указанных мишеней или их фрагментов со специфическими белковыми рецепторами.In a preferred embodiment, the present invention relates to a method for reducing or blocking the activity of specific Noggin2 targets (e.g. BMP2, BMP4, BMP7, activin, or a combination thereof) in an organism, tissue or cell, comprising administering nailgin2 to the specified organism, tissue or cell in an amount effective to inhibit or reduce the activity of specific noggin2 targets by inhibiting the binding of these targets or fragments thereof to specific protein receptors.
В предпочтительном осуществлении указанный способ и композиции используются для модификации клеточной дифференцировки, где указанный способ предусматривает приведение клетки или окружающей клетку среды в контакт с белком ноггин2 в таких условиях, когда ноггин2 специфически взаимодействует со своими мишенями - компонентами среды и/или клеточной поверхности, для модификации клеточной дифференцировки.In a preferred embodiment, the method and compositions are used to modify cell differentiation, where the method involves bringing the cell or the surrounding medium into contact with the noggin2 protein under conditions where the noggin2 specifically interacts with its target components of the medium and / or cell surface, to modify cell differentiation.
В одном предпочтительном осуществлении используется экзогенный белок ноггин2; в другом предпочтительном осуществлении используется экспрессирующая конструкция, содержащая кодирующую ноггин2 нуклеиновую кислоту под контролем подходящего промотора. В этом осуществлении способ изменения клеточной дифференцировки предусматривает создание экспрессирующей конструкции, содержащей кодирующую ноггин2 нуклеиновую кислоту под контролем подходящего промотора; введение указанной экспрессирующей конструкции в клетку для экспрессии ноггин2 или функционального химерного белка, содержащего ноггин2, где экспрессия ноггин2 или указанного химерного белка приводит к изменению клеточной дифференцировки.In one preferred embodiment, the exogenous protein noggin2 is used; in another preferred embodiment, an expression construct is used comprising the Noggin2 encoding nucleic acid under the control of a suitable promoter. In this embodiment, a method for altering cell differentiation involves the creation of an expression construct comprising a nucleic acid encoding leggin2 under the control of a suitable promoter; introducing said expression construct into a cell for expressing noggin2 or a functional chimeric protein containing noggin2, where the expression of noggin2 or said chimeric protein leads to a change in cell differentiation.
Краткое описание фигурBrief Description of the Figures
На фиг.1 представлено различие между эффектами ноггин1 и ноггин2 на дифференцировку нервной и мышечной тканей в эмбрионах Xenopus laevis и их тканевых эксплантатах. (В-И) сигнал гибридизации 1 л situ показан черным.Figure 1 shows the difference between the effects of noggin1 and noggin2 on the differentiation of nervous and muscle tissue in Xenopus laevis embryos and their tissue explants. (VI) a 1 L situ hybridization signal is shown in black.
(А, Б). Вентральные микроинъекции 40 пг синтетической мРНК гена ноггин1 в зародыши X. laevis на ранних стадиях развития приводят к формированию дополнительной оси тела (черная стрелка указывает основную ось тела, серая стрелка указывает дополнительную ось тела), в то время, как микроинъекции такого же количества синтетической мРНК ноггин2 приводит к формированию грибообразного фенотипа (А: 80%, всего - 68 зародышей из 85; Б: 90%, всего - 68 зародышей из 75).(A, B). Ventral microinjections of 40 pg of synthetic noggin1 gene mRNA in X. laevis embryos at the early stages of development lead to the formation of an additional body axis (black arrow indicates the main body axis, gray arrow indicates the additional body axis), while microinjections of the same amount of synthetic mRNA noggin2 leads to the formation of a mushroom-like phenotype (A: 80%, 68 out of 85 embryos in total; B: 90%, 68 out of 75 embryos in total).
(В-Ж). In situ гибридизация контрольных зародышей (слева на каждой их фотографий) и зародышей, микроинъецированых мРНК ноггин2 с пробами мРНК приведенных генетических маркеров показывает усиление нейральной (В, Г) и подавление эпидермальной (Д) и мезодермальной (Е, Ж) дифференцировок. Сигнал показан черным.(VJ). In situ hybridization of control embryos (to the left of each of their photographs) and embryos microinjected with noggin2 mRNA with mRNA samples of the given genetic markers shows an increase in neural (B, D) and inhibition of epidermal (D) and mesoderm (E, G) differentiations. The signal is shown in black.
(З). Эксплантаты вентральной маргинальной зоны (VMZ) зародышей, микроинъецированных вентрально РНК ноггин1 удлиняются к концу нейруляции благодаря дифференцировке скелетной мускулатуры.(H). Explants of the ventral marginal zone (VMZ) of embryos micro-injected with ventral RNA of noggin1 are extended towards the end of neurulation due to differentiation of skeletal muscles.
(И). Эксплантаты вентральной маргинальной зоны (VMZ) зародышей, микроинъецированных вентрально РНК ноггин2 к концу нейруляции сохраняют округлую форму.(AND). The explants of the ventral marginal zone (VMZ) of embryos microinjected ventrally with Noggin2 RNA retain a rounded shape at the end of neurulation.
(К). Схема экспериментов с эксплантатами эктодермы анимальной области зародышей (анимальные шапочки - АС) и эксплантатов вентральной маргинальной зоны зародышей (VMZ).(TO). Scheme of experiments with ectoderm explants of the animal region of the embryo (animal caps - AS) and explants of the ventral marginal zone of the embryo (VMZ).
(Л). Обратная транскрипция - ПЦР анализ проб тотальной РНК эксплантатов эктодермы анимальной области зародышей и эксплантатов вентральной маргинальной зоны зародышей, микроинъецированных мРНК ноггин1 и ноггин2 с праймерами к нейроэктодермальным (NCAM, Xanf-1), эпидермальным (keratin), мышечным (α-actin), постериорному мезодермальному (brachyury) и эндомезодермальному (cerjberus) молекулярным маркерам и Ef-1α в качестве контроля количества мРНК. Ноггин1 и ноггин2 активируют экспрессию нейральных маркеров (NCAM, Xanf-1) и подавляют экспрессию эпидермального (keratin), в то время только мРНК ноггин1 обнаруживает способность активировать экспрессию мышечного молекулярного маркера α-actin в эксплантатах вентральной маргинальной зоны.(L). Reverse transcription - PCR analysis of total RNA samples of ectoderm explants of the animal region of the embryos and explants of the ventral marginal zone of the embryos, microinjected mRNAs of noggin1 and noggin2 with primers for neuroectodermal (NCAM, Xanf-1), epidermal (keratin-arterial) muscle mesoderm (brachyury) and endo mesoderm (cerjberus) molecular markers and Ef-1α as a control for the amount of mRNA. Noggin1 and noggin2 activate the expression of neural markers (NCAM, Xanf-1) and inhibit the expression of epidermal (keratin), while only moggin1 mRNA displays the ability to activate the expression of the muscle molecular marker α-actin in explants of the ventral marginal zone.
На фиг.2 представлено различие между эффектами ноггин1 и ноггин2 на экспрессию генов jbrachyury, BF-1 и Pax-6 и приведены анализы способности белка ноггин2 связываться с ВМР-4 и activin. (А-Е) - результаты гибридизации in situ тотальных препаратов эмбрионов Xenopus laevis с зондами к соответствующим генам (сигнал гибридизации in situ показан черным); (А'-Е') - те же эмбрионы показаны под ультрафиолетовым освещением, что позволяет визуализировать микроинъецированные клетки, содержащие помимо мРНК метку - флюоресцеин-лизин-декстран (FLD).Figure 2 shows the difference between the effects of noggin1 and noggin2 on the expression of the jbrachyury, BF-1, and Pax-6 genes and analyzes the ability of the noggin2 protein to bind to BMP-4 and activin. (AE) - results of in situ hybridization of total preparations of Xenopus laevis embryos with probes for the corresponding genes (the in situ hybridization signal is shown in black); (A'-E ') - the same embryos are shown under ultraviolet light, which allows you to visualize microinjected cells containing in addition to the mRNA tag - fluorescein-lysine-dextran (FLD).
(А, А'). Подавление экспрессии мезодермального молекулярного маркера (brachyury) у зародышей, микроинъецированных мРНК ноггин2. А' - зеленый флуоресцентный краситель показывает распределение микроинъецированного материала.(A, A '). Suppression of expression of a mesoderm molecular marker (brachyury) in embryos microinjected with noggin2 mRNA. A '- green fluorescent dye shows the distribution of microinjected material.
(Б, Б'). Экспрессия мезодермального молекулярного маркера (brachyury) у зародышей, микроинъецированных мРНК ноггин1 не обнаруживают изменений по сравнению с контрольным зародышем (стрелка).(B, B '). Expression of a mesoderm molecular marker (brachyury) in the embryos microinjected with noggin1 mRNA does not show changes compared to the control embryo (arrow).
(В, В', Д, Д'). Формирование дополнительной оси тела у зародышей, микроинъецированных 2-5 нг мРНК ноггин2 в один из вентральных бластомеров. Наличие экспрессии молекулярных маркеров BF-1 и Pax-6 указывает на наличие в дополнительных осях переднеголовных и глазных структур.(B, B ', D, D'). The formation of the additional axis of the body in embryos microinjected with 2-5 ng noggin2 mRNA into one of the ventral blastomeres. The presence of the expression of molecular markers BF-1 and Pax-6 indicates the presence of anterior-head and ocular structures in the additional axes.
(Г, Г', Е, Е'). Дополнительные оси тела, формирующиеся при микроинъекциях 40 нг мРНК ноггин1 в один из вентральных бластомеров зародыша не содержат переднеголовных и глазных структур.(G, G ', E, E'). Additional body axes formed upon microinjection of 40 ng moggin1 mRNA into one of the embryo ventral blastomeres of the embryo do not contain forehead and ocular structures.
(Ж). Белок ноггин2 проявляет способность связывать молекулы костного морфогенетического белка (BMP) и молекулы activin. Подробное описание экспериментов приведено в тексте примеров 4 и 5.(G). Noggin2 protein exhibits the ability to bind bone morphogenetic protein (BMP) molecules and activin molecules. A detailed description of the experiments is given in the text of examples 4 and 5.
(З). Белок ноггин2 проявляет способность ингибировать фосфорилирование внутриклеточных передатчиков сигналов BMP activin - белков Smad1 и Smad2 соответственно. Подробное описание экспериментов приведено в тексте примеров 4 и 5.(H). The noggin2 protein shows the ability to inhibit the phosphorylation of intracellular BMP activin signal transmitters, the Smad1 and Smad2 proteins, respectively. A detailed description of the experiments is given in the text of examples 4 and 5.
Подробное описание изобретенияDETAILED DESCRIPTION OF THE INVENTION
Используемый здесь термин "ортолог" обозначает полипептид или белок, полученный из одного вида, являющийся функциональной копией полипептида или белка другого вида. Различия последовательностей ортологов являются результатом видообразования.As used herein, the term "ortholog" refers to a polypeptide or protein derived from one species that is a functional copy of a polypeptide or protein of another species. Differences in ortholog sequences are the result of speciation.
Используемый здесь термин "гомолог" или "гомология" представляет собой термин, применяющийся в данной области для описания родства нуклеотидной или белковой последовательности другой нуклеотидной или белковой последовательности, определяемого посредством степени идентичности и/или подобия между указанными сравниваемыми последовательностями.As used herein, the term “homologue” or “homology” is a term used in the art to describe the affinity of a nucleotide or protein sequence of another nucleotide or protein sequence, determined by the degree of identity and / or similarity between said compared sequences.
Как обобщено выше, раскрыты способы изменения активности определенных представителей надсемейства TGF-J3, а также композиции, содержащие белок ноггин2, кодирующую его нуклеиновую кислоту или антитела против ноггин2 для применения в них. Указанные способы и композиции для их практического применения могут быть использованы в ряде исследовательских, диагностических или терапевтических приложений, включающих в себя в качестве неограничивающих примеров ингибирование или уменьшение воспаления; регуляцию реконструкции кости во взрослом скелете; профилактику и лечение связанных с BMP и activin нарушений у животных, в частности людей; исследование и лечение сердечных заболеваний и неврологических нарушений.As summarized above, methods for changing the activity of certain members of the TGF-J3 superfamily are disclosed, as well as compositions containing a noggin2 protein, a nucleic acid encoding it, or anti-noggin2 antibodies for use in them. These methods and compositions for their practical use can be used in a number of research, diagnostic or therapeutic applications, including, but not limited to, inhibition or reduction of inflammation; regulation of bone reconstruction in the adult skeleton; the prevention and treatment of BMP and activin-related disorders in animals, in particular humans; research and treatment of heart diseases and neurological disorders.
Настоящее изобретение относится к применению конкретной функции ноггин2. На примере белка ноггин2 из Xenopus laevis с аминокислотной последовательностью, приведенной в SEQ ID NO: 2, авторы открыли, что ноггин2 играет роль в регуляции дифференцировки клеток и по действию и особым мишеням для связывания отличен от ноггин1 и других известных антагонистов факторов роста, принадлежащего к надсемейству TGF-P. В отличие от ноггин1 ноггин2 подавляет общую дифференцировку эмбриональной мезодермы, ингибируя действие индуктора мезодермы - activin.The present invention relates to the use of the specific function of noggin2. Using the example of the noggin2 protein from Xenopus laevis with the amino acid sequence given in SEQ ID NO: 2, the authors discovered that nuggin2 plays a role in regulating cell differentiation and is different from noggin1 and other known growth factor antagonists belonging to superfamily TGF-P. Unlike noggin1, noggin2 suppresses the general differentiation of the embryonic mesoderm, inhibiting the action of the mesoderm inducer, activin.
В то же время, подобно ноггин1, ноггин2 индуцирует развитие нервной ткани из эмбриональной эктодермы. Таким образом, ноггин2 обладает уникальной избирательной активностью в отношении индукции развития нервной ткани. Выявленная способность ноггин2 препятствовать дорзализующей активности ноггин1 является результатом его способности связываться с некоторыми отличными от ВМР2, ВМР4 или ВМР7, достоверно связывающимися с ноггин1, представителями надсемейства TGF-β. В частности, дополнительными факторами TGF-β, связывающимися с ноггин2, являются activin и родственные ему белки, необходимые для индукции мышц из эмбриональной мезодермы.At the same time, like noggin1, noggin2 induces the development of nervous tissue from the embryonic ectoderm. Thus, noggin2 has unique selective activity in relation to the induction of the development of nervous tissue. The revealed ability of noggin2 to inhibit dorsalizing activity of noggin1 is the result of its ability to bind to some members of the TGF-β superfamily other than BMP2, BMP4 or BMP7. In particular, activin and its related proteins, necessary for muscle induction from embryonic mesoderm, are additional TGF-β factors that bind to noggin2.
Используемый здесь термин "ноггин2" означает белок, обладающий единственной и избирательной активностью в отношении индукции развития нервной ткани, связывающийся со специфичными для ноггин2 мишенями для связывания выбранными из группы, состоящей из ВМР2, ВМР4, ВМР7 и activin или их сочетания, и являющийся гомологом и ортологом белков ноггин2, выбранных из группы, состоящей из ноггин2 Xenopus laevis; ноггин2 Xenopus tropicalis; ноггин2 Fugu rubripes; ноггин2 Gallus gallus (SEQ ID NO: 2, 4, 6, 8). Ноггин2 млекопитающих, включая человеческий ноггин2, представляет собой особый интерес.The term “noggin2” as used herein means a protein having unique and selective activity for inducing the development of neural tissue, binding to noggin2-specific binding targets selected from the group consisting of BMP2, BMP4, BMP7 and activin, or a combination thereof, and a homologue and an ortholog of protein noggin2 selected from the group consisting of Xenopus laevis noggin2; Noggin2 Xenopus tropicalis; Noggin2 Fugu rubripes; Noggin2 Gallus gallus (SEQ ID NO: 2, 4, 6, 8). Mammal noggin2, including human noggin2, is of particular interest.
Специфичную для ноггин2 активность или функцию можно определить посредством известных подходов клеточной биологии в системах in vitro или in vivo, например, анализы связывания in vitro, анализы в клеточной культуре, у животных (например, иммунный ответ, генная терапия, трансгенные животные и т.д.) и т.п. Анализы связывания включают в себя любой анализ, где оценивают специфическое молекулярное взаимодействие ноггин2 с мишенью для связывания. Мишень для связывания может представлять собой природную мишень для связывания или неприродную мишень для связывания, такую как специфичный иммунный белок, например антитело. Как правило, специфичность связывания оценивают посредством биологического анализа (например, способность к индукции нервной ткани из инъецированной эмбриональной эктодермы) или определения константы связывания ноггин2 с его мишенями из надсемейства TGF-β и т.д.Noggin2-specific activity or function can be determined by known cell biology approaches in vitro or in vivo systems, e.g. in vitro binding assays, cell culture assays, in animals (e.g. immune response, gene therapy, transgenic animals, etc.) .) etc. Binding assays include any assay that assesses the specific molecular interaction of noggin2 with a binding target. The target for binding may be a natural target for binding or non-natural target for binding, such as a specific immune protein, such as an antibody. Typically, binding specificity is assessed by biological analysis (for example, the ability to induce nerve tissue from an injected embryonic ectoderm) or by determining the binding constant of noggin2 to its targets from the TGF-β superfamily, etc.
Под гомологом белка подразумевают белок, аминокислотная последовательность которого по меньшей мере приблизительно на 68%, как правило, по меньшей мере приблизительно на 75% и наиболее часто по меньшей мере приблизительно на 85% идентичен известным аминокислотным последовательностям ноггин2, приведенным в SEQ ID NO: 2, 4, 6, 8, как определено с применением алгоритма MegAlign, DNAstar clustal algorithm, как описано в D.G. Higgins and P.M. Sharp, "Fast and Sensitive multiple Sequence Alignments on a Microcomputer", CABIOS, 5 pp.151-3 (1989) (с применением параметров кратности 1, штрафа за пропуск 3, окна 5 и сохраненными диагоналями 5). Во многих осуществлениях представляющие интерес гомологи обладают гораздо большей идентичностью последовательности, например, 90% (например, 92%, 93%, 94%) или выше, например, 95%, 96%, 97%, 98%, 99%, 99,5%, особенно для последовательности аминокислот, формирующей функциональные области белка.By protein homologue is meant a protein whose amino acid sequence is at least about 68%, typically at least about 75%, and most often at least about 85%, is identical to the known amino acid sequences of noggin2 given in SEQ ID NO: 2 , 4, 6, 8, as determined using the MegAlign algorithm, DNAstar clustal algorithm, as described in DG Higgins and P.M. Sharp, "Fast and Sensitive multiple Sequence Alignments on a Microcomputer", CABIOS, 5 pp. 151-3 (1989) (using
Также представляют интерес белки, в значительной степени идентичные белкам ноггин2, с аминокислотными последовательностями SEQ ID №№2, 4, 6, 8, где под значительной идентичностью подразумевают то, что аминокислотная последовательность белка идентична с последовательностью указанного белка по меньшей мере приблизительно на 68%, как правило, по меньшей мере приблизительно на 75% и наиболее часто по меньшей мере приблизительно на 80%, где в некоторых случаях идентичность может составлять более чем, например, 85%, 90%, 95% или более.Also of interest are proteins that are substantially identical to noggin2 proteins with the amino acid sequences of SEQ ID Nos. 2, 4, 6, 8, where significant identity means that the amino acid sequence of the protein is at least about 68% identical to that of the protein typically at least about 75% and most often at least about 80%, where in some cases the identity may be more than, for example, 85%, 90%, 95% or more.
Представляющие интерес белки включают в себя встречающиеся в природе белки и рекомбинантные белки, содержащие аминокислотную последовательность ноггин2 или его функциональные белковые домены, обладающие определимой анализом специфической активностью ноггин2. Таким образом, белки могут представлять собой делеционные мутанты природных белков ноггин2, и их можно получать в виде гибридных продуктов, содержащих полипептиды ноггин2 или его функциональные белковые домены. Представляющие интерес фрагменты являются полипептидами, как правило, длиной по меньшей мере приблизительно 30 аминокислот, как правило, длиной по меньшей мере приблизительно 50 аминокислот, предпочтительно длиной по меньшей мере приблизительно от 75 до 100 аминокислот и могут составлять в длину до 300 аминокислот или более, но, как правило, не превосходят длины 250 аминокислот, где фрагмент содержит участок аминокислотной последовательности, идентичный рассматриваемому белку, длиной по меньшей мере приблизительно 25 аминокислот, а как правило, по меньшей мере 45 аминокислот, а во многих осуществлениях по меньшей мере 50 аминокислот. В некоторых осуществлениях рассматриваемые полипептиды составляют в длину приблизительно 25 аминокислот, приблизительно 50, приблизительно 75, приблизительно 100, приблизительно 125, приблизительно 150, приблизительно 200 или приблизительно 250 аминокислот, вплоть до полноразмерного белка. Представляющие интерес фрагменты сохраняют все или по существу все специфические функции белка дикого типа.Proteins of interest include naturally occurring proteins and recombinant proteins containing the amino acid sequence of noggin2 or its functional protein domains having definable analysis of the specific activity of noggin2. Thus, proteins can be deletion mutants of natural noggin2 proteins, and they can be obtained in the form of hybrid products containing noggin2 polypeptides or its functional protein domains. The fragments of interest are polypeptides, typically at least about 30 amino acids long, typically at least about 50 amino acids long, preferably at least about 75 to 100 amino acids long, and can be up to 300 amino acids or more in length, but, as a rule, do not exceed 250 amino acids in length, where the fragment contains a portion of the amino acid sequence identical to the protein in question, at least about 25 amino acids in length, and, as a rule, at least 45 amino acids, and in many embodiments, at least 50 amino acids. In some embodiments, the subject polypeptides are approximately 25 amino acids, approximately 50, approximately 75, approximately 100, approximately 125, approximately 150, approximately 200, or approximately 250 amino acids in length, up to a full length protein. The fragments of interest retain all or substantially all of the specific functions of the wild-type protein.
Также представляют интерес белки, являющиеся производными или мутантами встречающихся в природе белков со специфической активностью ноггин2. Мутанты и производные могут сохранять биологические свойства белков дикого типа (например, встречающихся в природе) или могут обладать биологическими свойствами, отличными от таковых белков дикого типа. Термин "биологическое свойство" белков по настоящему изобретению относится к биохимическим свойствам, таким как стабильность in vivo и/или in vitro (например, период полураспада); скорость созревания, способность к агрегации или к формированию олигомеров и другим таким свойствам, но не ограничен ими. Мутации включают в себя замены отдельных аминокислот, делеции или вставки одной или нескольких аминокислот, укорочения или удлинения на N-конце, укорочения или удлинения на С-конце и т.п.Also of interest are proteins that are derivatives or mutants of naturally occurring proteins with specific noggin2 activity. Mutants and derivatives may retain the biological properties of wild-type proteins (eg, those found in nature) or may possess biological properties different from those of wild-type proteins. The term “biological property” of the proteins of the present invention refers to biochemical properties, such as in vivo and / or in vitro stability (eg, half-life); ripening speed, ability to aggregate or to form oligomers and other such properties, but is not limited to them. Mutations include substitutions of individual amino acids, deletions or insertions of one or more amino acids, shortening or lengthening at the N-terminus, shortening or lengthening at the C-terminus, and the like.
Также интерес представляет кодирующая ноггин2 нуклеиновая кислота, содержащая нуклеиновую кислоту, выбранную из группы, состоящей из SEQ ID NO: I, 3, 5, 7; нукленовых кислот, в значительной степени идентичных указанным нуклеиновым кислотам и их мутантам, производным и гомологам. Нуклеиновые кислоты, кодирующие белки ноггин2 млекопитающих (например, человеческий ноггин2), представляют собой особый интерес.Also of interest is the nucleic acid encoding leggin2 comprising a nucleic acid selected from the group consisting of SEQ ID NO: I, 3, 5, 7; nucleic acids, substantially identical to these nucleic acids and their mutants, derivatives and homologs. Nucleic acids encoding mammalian noggin2 proteins (e.g., human noggin2) are of particular interest.
Под гомологом нуклеиновой кислоты подразумевают нуклеиновую кислоту, идентичную соответствующей нуклеотидной последовательности по меньшей мере приблизительно на 30%, а предпочтительно - приблизительно на 40%, 50%, 55%, 60%, 65%, 70% или выше, в т.ч. на 75%, 80%, 85%, 90% и 95% или выше. Контрольная последовательность составляет в длину, как правило, по меньшей мере приблизительно 30 нуклеотидов, более часто - по меньшей мере приблизительно 60 нуклеотидов и может достигать длины полной последовательности, подлежащей сравнению. Сходство последовательностей рассчитывают, основываясь на контрольной последовательности. В данной области известны такие алгоритмы для анализа последовательности, как BLAST, описанный в Altschul et al., J. Mol. Biol., 215, pp.403-10 (1990) (например, с применением значений по умолчанию, т.е., параметров w=4 и Т=17).By a nucleic acid homologue is meant a nucleic acid identical to the corresponding nucleotide sequence by at least about 30%, and preferably by about 40%, 50%, 55%, 60%, 65%, 70% or higher, including 75%, 80%, 85%, 90% and 95% or higher. The control sequence is typically at least about 30 nucleotides long, more often at least about 60 nucleotides in length, and can reach the length of the complete sequence to be compared. Sequence similarity is calculated based on the control sequence. Algorithms for sequence analysis such as BLAST described in Altschul et al., J. Mol. Are known in the art. Biol., 215, pp. 403-10 (1990) (for example, using default values, i.e., parameters w = 4 and T = 17).
Источником гомологичных нуклеиновых кислот и белка может являться любой вид растений или животных, или последовательность можно целиком или частично синтезировать, включая в нее аналоги нуклеиновых кислот.The source of homologous nucleic acids and protein can be any type of plant or animal, or the sequence can be fully or partially synthesized, including nucleic acid analogs.
Мутанты или производные белков и нуклеиновых кислот ноггин2 можно образовывать с применением стандартных способов молекулярной биологии к матричной нуклеиновой кислоте, кодирующей белок ноггин2, посредством изменения, делеции или добавления одного или нескольких нуклеотидов матричной последовательности или их сочетания, для образования варианта матричной нуклеиновой кислоты. Замены, добавления или делеции можно вносить любым известным в данной области способом (см., например, Gustin et al., Biotechniques (1993) 14: 22; Barany, Gene (1985) 37: 111-123 и Colicelli et al., Mol. Gen. Genet. (1985) 199:537-539, Sambrook et al., Molecular Cloning: A Laboratory Manual, (1989), CSH Press, pp.15.3-15.108), представляющим собой ПЦР с ошибками, перестановку, олигонуклеотид-направленный мутагенез, сборочный ПЦР, мутагенез посредством половой ПЦР, мутагенез in vivo, кассетный мутагенез, рекурсивный групповой мутагенез, экспоненциальный групповой мутагенез, сайт-направленный мутагенез, случайный мутагенез, перестановку генов, насыщающий мутагенез генных участков (GSSM), перестановку искусственным лигированием (SLR) или их сочетание.Mutants or derivatives of noggin2 proteins and nucleic acids can be formed using standard molecular biology methods to a matrix nucleic acid encoding a noggin2 protein by modifying, deleting, or adding one or more nucleotides of a template sequence or combination thereof to form a template nucleic acid variant. Substitutions, additions or deletions can be made by any method known in the art (see, for example, Gustin et al., Biotechniques (1993) 14: 22; Barany, Gene (1985) 37: 111-123 and Colicelli et al., Mol Gen. Genet. (1985) 199: 537-539, Sambrook et al., Molecular Cloning: A Laboratory Manual, (1989), CSH Press, pp. 15.3-15.108), which is a PCR with errors, permutation, oligonucleotide- directed mutagenesis, assembly PCR, mutagenesis through sexual PCR, in vivo mutagenesis, cassette mutagenesis, recursive group mutagenesis, exponential group mutagenesis, site-directed mutagenesis, random mutagenesis, gene rearrangement in, saturation mutagenesis of gene portions (GSSM), synthetic ligation permutation (SLR) or a combination thereof.
Замены, добавления или делеции также можно вводить способом, предусматривающим рекомбинацию, рекурсивную рекомбинацию последовательностей, мутагенез с применением модифицированной фосфотиоатом ДНК, мутагенез с применением содержащей урацил матрицы, мутагенез с применением разрыва дуплекса, мутагенез с применением восстановления точечных несоответствий, мутагенез с применением штамма-хозяина с недостаточностью системы восстановления, химический мутагенез, радиогенный мутагенез, мутагенез посредством делеции, мутагенез с применением рестрикции-отбора, мутагенез с применением рестрикции-очистки, синтез искусственных генов, групповой мутагенез, создание мультимеров химерной нуклеиновой кислоты и их сочетание.Substitutions, additions or deletions can also be introduced by a method involving recombination, recursive recombination of sequences, mutagenesis using a modified DNA phosphothioate, mutagenesis using a uracil matrix, mutagenesis using a duplex gap, mutagenesis using the recovery of point mismatches, mutagenesis using a host strain with a deficiency in the recovery system, chemical mutagenesis, radiogenic mutagenesis, deletion mutagenesis, mutagenesis has been applied restriction-selection, mutagenesis using restriction-purification, synthesis of artificial genes, group mutagenesis, the creation of multimers of chimeric nucleic acids and their combination.
Кроме того, могут быть получены вырожденные варианты кодирующих белки ноггин2 нуклеиновых кислот. Вырожденные варианты нуклеиновых кислот содержат замены кодонов нуклеиновой кислоты на другие кодоны, кодирующие те же аминокислоты. Конкретно, вырожденные варианты нуклеиновых кислот получают для усиления их экспрессии в клетке-хозяине. В данном осуществлении кодоны нуклеиновой кислоты, не являющиеся предпочтительными или менее предпочтительные в генах клетки-хозяина замещают наиболее представленными в кодирующих последовательностях клетки-хозяина кодонами, где указанные замещенные кодоны кодируют ту же аминокислоту.In addition, degenerate variants of the protein-encoding noggin2 nucleic acids can be obtained. Degenerate nucleic acid variants contain substitutions of nucleic acid codons for other codons encoding the same amino acids. Specifically, degenerate nucleic acid variants are prepared to enhance their expression in the host cell. In this embodiment, nucleic acid codons that are not preferred or less preferred in the host cell genes are replaced by the codons most represented in the host cell coding sequences, wherein said substituted codons encode the same amino acid.
Производные также можно получать с применением стандартных способов, включающих в себя изменение РНК, химические модификации, посттрансляционные и посттранскрипционные модификации и т.п. Например, производные можно получать с применением таких способов как изменение профиля фосфорилирования или гликозилирования или ацетилирования или липидизации или с применением различных типов расщепления зрелых форм и т.п.Derivatives can also be obtained using standard methods, including RNA modification, chemical modifications, post-translational and post-transcriptional modifications, etc. For example, derivatives can be obtained using methods such as changing the profile of phosphorylation or glycosylation or acetylation or lipidization, or using various types of cleavage of mature forms and the like.
Представляющие интерес белки и фрагменты являются выделенными, т.е. существуют вне природной среды. Рассматриваемые белки и белковые домены можно синтезировать или получать посредством рекомбинантных технологий или выделять из их природной среды. Для биохимического синтеза, молекулярной экспрессии и очистки указанных композиций существует множество молекулярных и биохимических способов, см., например Molecular Cloning, A Laboratory Manual (Sambrook, et al., Cold Spring Harbor Laboratory), Current Protocols in Molecular Biology (Eds. Ausubel, et al., Greene Publ. Assoc., Wiley-Interscience, NY).Proteins and fragments of interest are isolated, i.e. exist outside the natural environment. The considered proteins and protein domains can be synthesized or obtained by recombinant technologies or isolated from their natural environment. There are many molecular and biochemical methods for the biochemical synthesis, molecular expression, and purification of these compositions, see, e.g., Molecular Cloning, A Laboratory Manual (Sambrook, et al., Cold Spring Harbor Laboratory), Current Protocols in Molecular Biology (Eds. Ausubel, et al., Greene Publ. Assoc., Wiley-Interscience, NY).
В предпочтительных осуществлениях белки по настоящему изобретению представляют собой рекомбинантные белки, полученные с помощью стандартных подходов с применением кодирующей ноггин2 нуклеиновой кислоты, например, нуклеиновой кислоты, выбранной из группы, состоящей из SEQ ID NO: I, 3, 5 или 7.In preferred embodiments, the proteins of the present invention are recombinant proteins obtained using standard approaches using a Noggin2-encoding nucleic acid, for example, a nucleic acid selected from the group consisting of SEQ ID NO: I, 3, 5, or 7.
Упоминаемая здесь молекула нуклеиновой кислоты представляет собой молекулы ДНК, такие как молекулы геномной ДНК или молекулы кДНК или молекулы РНК, такие как молекулы мРНК. Конкретно, указанные молекулы нуклеиновой кислоты представляют собой молекулы кДНК с открытой рамкой считывания, кодирующие белок ноггин2 по настоящему изобретению или его функциональный фрагмент и способны в подходящих условиях экспрессироваться в качестве активного ноггин2 или функционального домена ноггин2 по настоящему изобретению.The nucleic acid molecule referred to herein is a DNA molecule, such as a genomic DNA molecule or a cDNA molecule, or an RNA molecule, such as an mRNA molecule. Specifically, said nucleic acid molecules are open reading frame cDNA molecules encoding the noggin2 protein of the present invention or a functional fragment thereof and are capable of being expressed under suitable conditions as the active noggin2 or functional domain of the noggin2 of the present invention.
Представляющая интерес геномная последовательность может содержать нуклеиновую кислоту, находящуюся между инициирующим кодоном и стоп-кодоном, как определено в перечисленных последовательностях, включающую в себя все интроны, в норме присутствующие в исходной хромосоме. Представляющая интерес геномная последовательность может включать в себя 5'- и 3'-нетранслируемые области, находящиеся в зрелой мРНК, а также специфические транскрипционные и трансляционные регуляторные последовательности, такие как промоторы, энхансеры и т.д., включая в себя приблизительно 1 т.п.н., но возможно больше, фланкирующей геномной ДНК или на 5'- или на 3'-конце транскрибируемой области.The genomic sequence of interest may contain a nucleic acid located between the initiating codon and the stop codon, as defined in the listed sequences, including all introns normally present in the original chromosome. The genomic sequence of interest may include 5'- and 3'-untranslated regions located in mature mRNA, as well as specific transcriptional and translational regulatory sequences, such as promoters, enhancers, etc., including about 1 t. bp, but possibly more, flanking genomic DNA at either the 5 ′ or 3 ′ end of the transcribed region.
Рассматриваемые нуклеиновые кислоты можно выделять и получать в существенно очищенной форме. Термин "существенно очищенная форма" означает, что нуклеиновые кислоты являются по меньшей мере приблизительно на 50% чистыми, как правило - по меньшей мере на 90% чистыми и, как правило, являются "рекомбинантными", т.е. фланкированы одним или несколькими нуклеотидами, с которыми они в норме не ассоциированы в природной хромосоме в их природном организме-хозяине.The nucleic acids of interest can be isolated and obtained in substantially purified form. The term "substantially purified form" means that the nucleic acids are at least about 50% pure, typically at least 90% pure and, as a rule, are "recombinant", i.e. flanked by one or more nucleotides with which they are normally not associated in the natural chromosome in their natural host organism.
Нуклеиновые кислоты по настоящему изобретению, соответствующие кДНК, полноразмерные гены и конструкции можно получать искусственно посредством различных протоколов, известных специалистам в данной области. Соответствующие конструкции нуклеиновых кислот очищают с применением стандартных способов рекомбинантных ДНК, например, как описано в Sambrook et al., Molecular Cloning: A Laboratory Manual, 2nd Ed., (1989) Cold Spring Harbor Press, Cold Spring Harbor, NY, и по правилам, описанным, например, в United States Dept. of HHS, National Institute of Health (NIH) Guidelines for Recombinant DNA Research.Nucleic acids of the present invention, corresponding cDNAs, full-length genes and constructs can be artificially produced using various protocols known to those skilled in the art. Appropriate nucleic acid constructs are purified using standard recombinant DNA methods, for example, as described in Sambrook et al., Molecular Cloning: A Laboratory Manual, 2 nd Ed., (1989) Cold Spring Harbor Press, Cold Spring Harbor, NY, and rules described, for example, in United States Dept. of HHS, National Institute of Health (NIH) Guidelines for Recombinant DNA Research.
Также интерес представляют химерные белки, содержащие ноггин2 или его фрагменты, слитые, например, с последовательностью деградации, сигнальным белком или любым белком или полипептидом, представляющим интерес. Слитые белки могут содержать, например, белок ноггин2 и второй полипептид ("партнер по слиянию"), объединенные в одну рамку считывания на N-конце и/или С-конце полипептида ноггин2. Партнеры по слиянию включают в себя в качестве неограничивающих примеров полипептиды, способные связывать антитела, специфичные к партнеру по слиянию (например, эпитопные метки), антитела или их связывающие домены, полипептиды, обеспечивающие каталитическую функцию или индукцию клеточного ответа, лиганды или рецепторы или их миметики и т.п. В таких слитых белках партнер по слиянию, как правило, ассоциирован с частью гибридного белка, являющейся белком ноггин2, неприродным способом и, как правило, не является белком ноггин2 по настоящему изобретению или их производным/фрагментом. Также интерес представляют нуклеиновые кислоты, кодирующие описанные выше гибридные белки.Also of interest are chimeric proteins containing noggin2 or fragments thereof, fused, for example, with a degradation sequence, a signal protein, or any protein or polypeptide of interest. Fusion proteins may contain, for example, the noggin2 protein and the second polypeptide (“fusion partner”), combined into a single reading frame at the N-terminus and / or C-terminus of the noggin2 polypeptide. Fusion partners include, but are not limited to, polypeptides capable of binding antibodies specific to the fusion partner (e.g., epitope tags), antibodies or their binding domains, polypeptides providing catalytic function or induction of a cellular response, ligands or receptors, or mimetics thereof etc. In such fusion proteins, the fusion partner is generally associated with a portion of the fusion protein, which is the noggin2 protein, a non-natural method and, as a rule, is not the noggin2 protein of the present invention or its derivative / fragment. Nucleic acids encoding the fusion proteins described above are also of interest.
Также раскрыты вектор и другие конструкции нуклеиновых кислот, содержащие кодирующую ноггин2 нуклеиновую кислоту. Применимые векторы включают в себя вирусные и невирусные векторы, плазмиды, космиды, фаги и т.д., предпочтительно плазмиды, и их применяют для клонирования, амплификации, экспрессии, переноса и т.д. последовательности нуклеиновой кислоты по настоящему изобретению в подходящем хозяине. Выбор подходящего вектора хорошо известен специалисту в данной области, а многие такие векторы имеются в продаже. Для получения конструкций частичную или полноразмерную нуклеиновую кислоту встраивают в вектор, обычно посредством присоединения ДНК-лигазой к расщепленному ферментом рестрикции участку в векторе. Альтернативно, желательную нуклеотидную последовательность можно встраивать посредством гомологичной рекомбинации in vivo, как правило, посредством присоединения к вектору по бокам желаемой нуклеотидной последовательности областей гомологии. Например, области гомологии добавляют посредством лигирования нуклеотидов или посредством полимеразной цепной реакции с применением праймеров, содержащих область гомологии и часть желаемой нуклеотидной последовательности.Also disclosed are a vector and other nucleic acid constructs comprising a Nuggin2 encoding nucleic acid. Applicable vectors include viral and non-viral vectors, plasmids, cosmids, phages, etc., preferably plasmids, and are used for cloning, amplification, expression, transfer, etc. the nucleic acid sequences of the present invention in a suitable host. The selection of a suitable vector is well known to the person skilled in the art, and many such vectors are commercially available. To obtain constructs, a partial or full-length nucleic acid is inserted into a vector, usually by attaching a DNA ligase to a restriction enzyme digested region in a vector. Alternatively, the desired nucleotide sequence can be inserted by homologous in vivo recombination, typically by attaching homology regions to the vector on the sides of the desired nucleotide sequence. For example, homology regions are added by ligation of nucleotides or by polymerase chain reaction using primers containing a homology region and part of a desired nucleotide sequence.
Также раскрыты экспрессирующие кассеты или системы, в числе прочего применяемые для получения белка ноггин2 или его гибридного белка или для репликации молекул нуклеиновой кислоты по настоящему изобретению. Экспрессирующая кассета может существовать в качестве внехромосомного элемента или ее можно интегрировать в геном клетки как результат введения указанной кассеты в клетку. Для экспрессии продукт гена, кодируемого нуклеиновой кислотой по изобретению, экспрессируют в любой подходящей экспрессирующей системе, включая, например, бактериальные, дрожжевые системы, системы насекомых, амфибий или млекопитающих. В экспрессирующем векторе нуклеиновую кислоту по изобретению функционально связывают с регуляторной последовательностью, которая может содержать промоторы, энхансеры, терминаторы, операторы, репрессоры и индукторы. Способы получения экспрессирующих кассет или систем, способных экспрессировать желаемый продукт, хорошо известны специалистам в данной области.Expressing cassettes or systems are also disclosed, inter alia, used to produce the noggin2 protein or its fusion protein, or to replicate nucleic acid molecules of the present invention. The expression cassette can exist as an extrachromosomal element, or it can be integrated into the genome of a cell as a result of introducing said cassette into the cell. For expression, the product of the gene encoded by the nucleic acid of the invention is expressed in any suitable expression system, including, for example, bacterial, yeast, insect, amphibian or mammalian systems. In the expression vector, the nucleic acid of the invention is operably linked to a regulatory sequence, which may contain promoters, enhancers, terminators, operators, repressors and inducers. Methods for preparing expression cassettes or systems capable of expressing a desired product are well known to those skilled in the art.
Клеточные линии, стабильно экспрессирующие ноггин2, можно отобрать посредством хорошо известных в данной области способов (например, совместной трансфекцией с селективным маркером, таким как dhfr, gpt, неомицин, гигромицин, обеспечивающим идентификацию и выделение трансфицированных клеток, содержащих интегрированный в геном ген).Cell lines stably expressing noggin2 can be selected by methods well known in the art (e.g., co-transfection with a selectable marker, such as dhfr, gpt, neomycin, hygromycin, which allows identification and isolation of transfected cells containing a gene integrated into the genome).
Описанные выше экспрессирующие системы можно применять у прокариотических или эукариотических хозяев. Для получения белка можно использовать такие клетки-хозяева как Е. coli, В. subtilis, S. cerevisiae, клетки насекомых в сочетании с бакуловирусными векторами или клетки высших организмов, таких как позвоночные, например клетки COS7, НЕК293, СНО, ооциты Xenopus и т.д.The expression systems described above can be used in prokaryotic or eukaryotic hosts. To obtain the protein, such host cells as E. coli, B. subtilis, S. cerevisiae, insect cells in combination with baculovirus vectors, or cells of higher organisms such as vertebrates, for example, COS7, HEK293, CHO cells, Xenopus oocytes, etc. can be used. .d.
Когда для репликации и/или экспрессии нуклеиновых кислот по изобретению применяют любые из указанных выше клеток-хозяев или другие применимые клетки-хозяева или организмы-хозяева, образующиеся в результате реплицированная нуклеиновая кислота, экспрессированный белок или полипептид подпадают под объем изобретения как продукт клетки-хозяина или организма-хозяина. Продукт можно выделить любыми известными в данной области подходящими способами.When any of the above host cells or other applicable host cells or host organisms are used to replicate and / or express the nucleic acids of the invention, the resulting replicated nucleic acid, expressed protein or polypeptide fall within the scope of the invention as a host cell product or the host organism. The product can be isolated by any suitable methods known in the art.
Также раскрыты антитела, специфично связывающиеся с ноггин2 по настоящему изобретению. Применимые антитела можно получать с применением известных в данной области способов. Например, поликлональные антитела можно получать, как описано в Harlow and Lane Antibodies: A Laboratory Manual, (1988) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, а моноклональные антитела можно получать, как описано в Coding Monoclonal Antibodies: Principles and Practice: Production and Application of Monoclonal Antibodies in Cell Biology, Biochemistry and Immunology; 3rd edition, (1996) Academic Press. Также представляют интерес гибридные антитела, включающие в себя гуманизированные антитела, а также одноцепочечные антитела и такие фрагменты антител как Fv, F(ab')2 и Fab.Also disclosed are antibodies specifically binding to noggin2 of the present invention. Applicable antibodies can be prepared using methods known in the art. For example, polyclonal antibodies can be prepared as described in Harlow and Lane Antibodies: A Laboratory Manual, (1988) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, and monoclonal antibodies can be prepared as described in Coding Monoclonal Antibodies: Principles and Practice: Production and Application of Monoclonal Antibodies in Cell Biology, Biochemistry and Immunology; 3rd edition, (1996) Academic Press. Hybrid antibodies are also of interest, including humanized antibodies, as well as single chain antibodies and antibody fragments such as Fv, F (ab ') 2 and Fab.
Ноггин2, а также другие описанные выше компоненты настоящего изобретения находят применение во множестве различных приложений, включающие в себя применение в качестве иммуногенов, мишеней в скринирующих анализах, биологически активных веществ для модуляции клеточного роста, дифференцировки и/или функционирования и т.д.Noggin2, as well as the other components of the present invention described above, are used in many different applications, including the use of immunogens, targets in screening assays, biologically active substances for modulating cell growth, differentiation and / or functioning, etc.
В предпочтительном осуществлении настоящее изобретение относится к способу снижения или ингибирования активности специфичных для ноггин2 мишеней (например, ВМР2, ВМР4, ВМР7, activin, nodal или их сочетания), предусматривающему введение ноггин2 в указанный организм, ткань или клетку в количестве достаточном для ингибировании или снижения активности специфичных для ноггин2 мишеней посредством препятствия связыванию указанных мишеней или их фрагментов со специфическими белковыми рецепторами.In a preferred embodiment, the present invention relates to a method for reducing or inhibiting the activity of specific noggin2 targets (e.g. BMP2, BMP4, BMP7, activin, nodal, or a combination thereof), comprising administering the noggin2 into the specified organism, tissue or cell in an amount sufficient to inhibit or reduce activity of noggin2-specific targets by inhibiting the binding of these targets or fragments thereof to specific protein receptors.
В предпочтительном осуществлении представленные способы и композиции используются для модификации клеточной дифференцировки. В частности, способ модификации клеточной дифференцировки предусматривает приведение клетки или окружающей клетку среды в контакт с белком ноггин2 в таких в условиях, когда ноггин2 специфически взаимодействует со своими мишенями - компонентами среды и/или клеточной поверхности, для осуществления изменения клеточной дифференцировки.In a preferred embodiment, the methods and compositions provided are used to modify cell differentiation. In particular, a method for modifying cell differentiation involves bringing the cell or the environment surrounding the cell into contact with the noggin2 protein under conditions where the noggin2 specifically interacts with its targets, the components of the medium and / or cell surface, to effect a change in cell differentiation.
В одном предпочтительном осуществлении используется экзогенный белок ноггин2; в другом предпочтительном осуществлении используется экспрессирующая конструкция, содержащая кодирующую ноггин2 нуклеиновую кислоту под контролем подходящего промотора. Белок ноггин2 может быть добавлен в среду культивирования in vitro и физиологические жидкости, такие как кровь, синовиальная жидкость и т.д. Белок можно также вводить или экспрессировать в конкретных популяциях клеток любым подходящим способом, таким как микроинъекция, зависимая от промотора экспрессия рекомбинантного фермента, целенаправленная доставка липидных частиц и т.д. Данные способы можно применять для снижения нежелательного остеогенеза, ингибирования роста клеток, требующего морфогенетического белка (например, зависимые от BMP нейробластомы и глиомы), регулирования образования и роста хряща, изменения зависимых от морфогена направления развития/дифференцировки клеток в культуре, таких как клетки для трансплантации или инфузии и т.д. Так как ноггин2 обуславливает активность в отношении индукции нервной ткани, он может быть применим для лечения периферических нейропатий при росте спинного мозга и отростков чувствительных нейронов, например, его можно включать в терапевтическое лечение для регенерации отростков нейронов после инсультов, повреждения головного мозга, вызванного травмами головы, и паралича, вызванного травмами спинного мозга. Применение также может состоять в лечении нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона и рассеянный склероз, посредством стимуляции отростков нейронов. Дополнительные применения могут включать в себя восстановление рассеченных аксонов, что часто происходит в очагах повреждения при рассеянном склерозе.In one preferred embodiment, the exogenous protein noggin2 is used; in another preferred embodiment, an expression construct is used comprising the Noggin2 encoding nucleic acid under the control of a suitable promoter. Noggin2 protein can be added to in vitro culture media and body fluids such as blood, synovial fluid, etc. The protein can also be introduced or expressed in specific cell populations by any suitable method, such as microinjection, promoter-dependent expression of the recombinant enzyme, targeted delivery of lipid particles, etc. These methods can be used to reduce unwanted osteogenesis, inhibit cell growth requiring morphogenetic protein (e.g. BMP-dependent neuroblastomas and gliomas), regulate cartilage formation and growth, change morphogen-dependent cell development / differentiation directions in culture, such as cells for transplantation or infusion, etc. Since noggin2 causes activity in relation to the induction of nerve tissue, it can be used to treat peripheral neuropathies in the growth of the spinal cord and processes of sensitive neurons, for example, it can be included in therapeutic treatment for the regeneration of processes of neurons after strokes, brain damage caused by head injuries , and paralysis caused by spinal cord injuries. The use may also be in the treatment of neurodegenerative diseases such as Alzheimer's disease, Parkinson's disease and multiple sclerosis, by stimulating the processes of neurons. Additional applications may include restoration of dissected axons, which often occurs in foci of damage in multiple sclerosis.
Как антагонист ряда факторов роста (например, ВМР2, ВМР4, ВМР7, activin или их сочетания) ноггин2 или его фрагмент находит применение в качестве супрессора активности этих факторов, например морфогенетического костного белка (BMP), activin или их ортологов. Предпочтительно, изобретение относится к способу противодействия функционированию указанной специфической мишени, предусматривающему приведение указанной мишени в контакт с белком ноггин2 или его фрагментом. Способ по изобретению осуществляют в условиях, когда ноггин2 или его фрагмент связываются со специфической мишенью. В качестве антагониста BMP ноггин2 может быть применим для профилактики или лечения связанных с BMP нарушений у животных, в частности у людей. Например, ноггин2 может быть использован для лечения заболеваний или нарушений, которые включают в себя в качестве неограничивающих примеров прогрессирующую оссифицирующую фибродисплазию (FOP), а также для лечения аномального роста кости, такого как патологический рост кости после операции замещения тазобедренного сустава, травмы, ожогов или повреждения спинного мозга. Кроме того, ноггин2 может быть применим для лечения или профилактики нежелательных воздействий BMP, ассоциированных с аномальным ростом кости, наблюдаемым в связи с метастазирующим раком простаты или остеосаркомой. Так как известно, что содержание лиганды ВМР2 и ВМР4 значительно увеличивается при астме (Rosendahl et al., Am J Respir Cell Mol Biol. 2002 Aug; 27(2):160-9) и при некоторых других воспалительных заболеваниях, в частности при ревматоидном артрите (Lories et al., Arthritis Rheum. 2003 Oct; 48 (10):2807-18.), то ноггин2 можно также применять для связывания BMP и, таким образом, для лечения воспалительных синдромов.As an antagonist of a number of growth factors (for example, BMP2, BMP4, BMP7, activin, or a combination thereof), leggin2 or a fragment thereof is used as a suppressor of the activity of these factors, for example, morphogenetic bone protein (BMP), activin, or their orthologs. Preferably, the invention relates to a method for counteracting the functioning of said specific target, comprising bringing said target into contact with the noggin2 protein or fragment thereof. The method according to the invention is carried out under conditions when noggin2 or a fragment thereof binds to a specific target. As an antagonist of BMP, noggin2 may be useful for the prophylaxis or treatment of BMP-related disorders in animals, in particular humans. For example, noggin2 can be used to treat diseases or disorders that include, but are not limited to, progressive ossifying fibrodysplasia (FOP), and also to treat abnormal bone growth, such as abnormal bone growth after hip replacement surgery, trauma, burns, or spinal cord injuries. In addition, noggin2 may be useful in treating or preventing the undesirable effects of BMP associated with abnormal bone growth observed in association with metastatic prostate cancer or osteosarcoma. Since it is known that the content of the BMP2 and BMP4 ligands increases significantly with asthma (Rosendahl et al., Am J Respir Cell Mol Biol. 2002 Aug; 27 (2): 160-9) and with some other inflammatory diseases, in particular with rheumatoid arthritis (Lories et al., Arthritis Rheum. 2003 Oct; 48 (10): 2807-18.), then noggin2 can also be used to bind BMP and, thus, to treat inflammatory syndromes.
Так как ноггин2 может связывать activin, он также находит применение для профилактики и лечения связанных с activin заболеваний, например для ингибирования прогрессирования хронической почечной недостаточности, острой почечной недостаточности, панкреатита и бронхолегочной дисплазии новорожденных и т.д. Также его можно применять при повреждениях глаза, таких как травма роговицы при ожогах или попадании чужеродного тела или воспалительных заболеваний глаза, таких как увеит.Since noggin2 can bind activin, it also finds use in the prevention and treatment of activin-related diseases, for example, inhibition of the progression of chronic renal failure, acute renal failure, pancreatitis and neonatal bronchopulmonary dysplasia, etc. It can also be used for eye injuries, such as trauma to the cornea due to burns or contact with a foreign body or inflammatory eye diseases such as uveitis.
Кроме того, нуклеиновые кислоты, белки, и фрагменты ноггин2 по изобретению можно применять для изменения активности специфичных для ноггин2 мишеней у животных, в частности у людей.In addition, the nucleic acids, proteins, and fragments of noggin2 of the invention can be used to alter the activity of specific noggin2 targets in animals, in particular humans.
Представляющие интерес композиции могут включать белок ноггин2, например рекомбинантный очищенный белок, или химерный белок, содержащий ноггин2, или функциональный фрагмент ноггин2. Указанные композиции могут также включать нуклеиновую кислоту, кодирующую белок ноггин2, способную экспрессировать белок ноггин2 в представляющих интерес клетках, тканях, органах или организмах. Указанные композиции также могут содержать пригодный фармацевтический носитель для системного или локального введения in vivo любым пригодным способом, включающим в себя в качестве неограничивающих примеров инъекцию (например, внутривенную, интраперитонеальную, внутримышечную, подкожную, эндоневральную, периневральную, интраспинальную, внутрижелудочковую, интравитреально, интратекально и т.д.), всасыванием через эпителиальные или слизисто-кожные выстилки (например, через слизистую ротовой полости, ректальную или кишечную слизистую и т.д.) или имплантантов с замедленным высвобождением, включающих в себя клеточные или тканевые имплантанты. В зависимости от способов введения композиция может содержать жидкий носитель, такой как физиологический раствор, являться заключенной в липосомы, микрокапсулы, полимерные или основанные на парафине препараты с контролируемым высвобождением, или являться сформулированным в формы таблетки, пилюли или капсулы. Концентрация применяемого активного ингредиента(ов) зависит от типа заболевания или признаков, которые подвергаются воздействию, от применяемого способа введения, а также от особенностей биологической системы. Эффективные дозы можно получить экстраполяцией кривых "доза-ответ", полученных в тестовых системах in vitro или на животных моделях.Compositions of interest may include a noggin2 protein, for example, a recombinant purified protein, or a chimeric protein containing noggin2, or a functional fragment of noggin2. These compositions may also include nucleic acid encoding a noggin2 protein capable of expressing noggin2 protein in cells, tissues, organs or organisms of interest. These compositions may also contain a suitable pharmaceutical carrier for systemic or local administration in vivo by any suitable method including, but not limited to, injection (e.g., intravenous, intraperitoneal, intramuscular, subcutaneous, endoneural, perineural, intraspinal, intraventricular, intravitreal, intrathecal and etc.) by absorption through the epithelial or mucocutaneous lining (e.g., through the mucosa of the oral cavity, rectal or intestinal mucosa, etc. e.) or delayed release implants, including cellular or tissue implants. Depending on the route of administration, the composition may contain a liquid carrier, such as saline, be enclosed in liposomes, microcapsules, polymer or paraffin-based controlled-release formulations, or be formulated in the form of a tablet, pill or capsule. The concentration of the active ingredient (s) used depends on the type of disease or signs that are affected, the method of administration used, and also the characteristics of the biological system. Effective doses can be obtained by extrapolating dose-response curves obtained in in vitro test systems or in animal models.
Используемый здесь термин "эффективная доза" обозначает количество белка, необходимое для достижения биологического эффекта, т.е. подавления функции указанных выше представителей суперсемейства TGF-бета. Биологический эффект может выражаться в уменьшении признаков, симптомов или устранении причин заболевания или любых иных изменениях биологической системы. Обычно эффективная доза находится в пределах от 0.1-100 мг/кг субъекта.As used herein, the term "effective dose" refers to the amount of protein required to achieve a biological effect, i.e. suppressing the function of the above representatives of the TGF-beta superfamily. The biological effect can be expressed in reducing signs, symptoms or eliminating the causes of the disease or any other changes in the biological system. Typically, an effective dose is in the range of 0.1-100 mg / kg of the subject.
Введение может приводить к распределению ноггин2 в организме или в локализованной области. Например, при многих состояниях, вовлекающих дистальные области нервной системы, можно применять внутривенное или интратекальное введение ноггин2. Альтернативно, и не в качестве ограничения, когда вовлечены локализованные области нервной системы, можно применять локальное введение. В таких ситуациях в конкретную область или рядом с ней можно поместить содержащий ноггин2 имплантант. Пригодные имплантанты включают в себя в качестве неограничивающих примеров желатиновую губку, воск или имплантанты, основанные на микрочастицах.Administration may result in the distribution of noggin2 in the body or in a localized area. For example, in many conditions involving the distal regions of the nervous system, intravenous or intrathecal administration of noggin2 can be used. Alternatively, and not by way of limitation, when localized regions of the nervous system are involved, local administration may be used. In such situations, an implant containing a nuggin2 can be placed in or near a specific area. Suitable implants include, but are not limited to, a gelatin sponge, wax, or microparticle based implants.
Следующие ниже примеры предложены для иллюстрации, а не с целью ограничения.The following examples are provided for illustration and not limitation.
Пример 1Example 1
Клонирование кДНК ноггин2Noggin2 cDNA cloning
кДНК ноггин2 клонировали во время поиска генов Xenopus laevis, вовлеченных в регуляторную сеть гомеобокс-содержащего гена Xanf-1 (Zaraisky et al. Developmental Biology 1992, v.152, pp.373-382; Ermakova et al., Development 1999, v. 126, pp.4513-4523). Для выявления генетических мишеней Xanf-1 авторы провели вычитающую гибридизацию образцов кДНК, полученных из эксплантатов передней эктодермы двух групп эмбрионов Xenopus: в одной группе трансляцию Xanf-1 и его псевдоаллеля у Xenopus laevis, Xanf-2 снизили с применением микроинъекций 1 мМ морфолиновых олигонуклеотидов против Xanf-1 (5'-ATCCTTTCTGAAGAGCAGGAGACAT и 5'-ATCCTTTCTGGAGACCAGTAGACAT, Gene Tools); в другой группе в эмбрионы посредством микроинъекции вводили контрольные морфолиновые олигонуклеотиды (МО), предоставленные Gene Tools Co. В эмбрионы Xenopus laevis на стадии двух бластомеров в анимальные полюса обоих бластомеров проводили микроинъекции МО против Xanf или контрольных МО, смешанных с витальным красителем флюоресцеинлизиндекстраном (FLD). Для каждого из двух типов эмбрионов на стадии средней нейрулы, как описано в Zaraisky et al. Developmental Biology 1992, v.152, pp.373-382, вырезали приблизительно 30 эксплантатов передней нейроэктодермы, взятых вместе с подлежащей энтомезодермой. Для операции выбирали только те эмбрионы, которые обладали равномерным сигналом FLD в передней области. Вычитающую гибридизацию и дифференциальный скрининг проводили с использованием набора реактивов PCR Select kit (BD Clontech). Вставки кДНК всех дифференцированно распределенных клонов (всего приблизительно 50) секвенировали и анализировали в режиме онлайн с применением программ BLAST по базам данных GeneBank и JGI. В результате идентифицировали клон, содержащий полную кодирующую область белка ноггин2. кДНК, содержащую полную кодирующую область ноггин2, реамплифицировали в ПЦР с использованием праймеров 5'-ATTACCGGTGGGAGAACCTTGTTCTTCATT-3' и 5'-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3' и субклонировали в вектор р35Т. Нуклеотидная и аминокислотные последовательности ноггин2 показаны в SEQ ID NO: 1 и 2.Noggin2 cDNA was cloned during a search for Xenopus laevis genes involved in the regulatory network of the homeobox-containing Xanf-1 gene (Zaraisky et al. Developmental Biology 1992, v.152, pp.373-382; Ermakova et al., Development 1999, v. 126, pp. 4513-4523). To identify Xanf-1 genetic targets, the authors carried out subtractive hybridization of cDNA samples obtained from anterior ectoderm explants of two groups of Xenopus embryos: in one group, translation of Xanf-1 and its pseudo-allele in Xenopus laevis, Xanf-2 was reduced using microinjections of 1 mM morpholine oligon Xanf-1 (5'-ATCCTTTCTGAAGAGCAGGAGACAT and 5'-ATCCTTTCTGGAGACCAGTAGACAT, Gene Tools); in another group, control morpholine oligonucleotides (MOs) provided by Gene Tools Co. were introduced into the embryos by microinjection In the embryos of Xenopus laevis, at the stage of two blastomeres, microinjections of MOs against Xanf or control MOs mixed with vital dye fluorescein lysine dextran (FLD) were performed at the animal poles of both blastomeres. For each of the two types of embryos in the middle neurula stage, as described in Zaraisky et al. Developmental Biology 1992, v. 152, pp. 373-382, excised approximately 30 anterior neuroectoderm explants, taken together with the underlying enthemesoderm. For the operation, only those embryos were selected that possessed a uniform FLD signal in the anterior region. Subtractive hybridization and differential screening was performed using the PCR Select kit (BD Clontech). The cDNA inserts of all differentially distributed clones (approximately 50 total) were sequenced and analyzed online using BLAST programs using the GeneBank and JGI databases. As a result, a clone was identified containing the complete coding region of the noggin2 protein. cDNA containing the complete coding region of noggin2 was reamplified in PCR using primers 5′-ATTACCGGTGGGAGAACCTTGTTCTTCATT-3 ′ and 5′-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3 ′ and subcloned into the p35T vector. The nucleotide and amino acid sequences of noggin2 are shown in SEQ ID NO: 1 and 2.
Пример 2Example 2
Воздействие ноггин2 на направление развития клетокThe effect of noggin2 on the direction of cell development
Вектор р35Т, содержащий полную кодирующую часть кДНК ноггин2 (вектор р35Т-ноггин2), был получен, как описано в примере 1.The p35T vector containing the complete coding part of the noggin2 cDNA (p35T-noggin2 vector) was obtained as described in Example 1.
Полную кодирующую последовательность ноггин1 получали путем ПЦР-амплификации с образца кДНК Xenopus laevis с использованием ноггин1 - специфичных праймеров 5'-TATCCATGGCAAGAAATCGGGAGCA-3' и 5'-ATTCTCGAGTCTCAGCATGAGCATTTGCA-3' и клонировали в вектор р35Т (вектор р35Т - ноггин1).The complete coding sequence of noggin1 was obtained by PCR amplification from a Xenopus laevis cDNA sample using noggin1-specific primers 5'-TATCCATGGCAAGAAATCGGGAGCA-3 'and 5'-ATTCTCGAGTCTCAGCATGAGCATTTGCA-3' and cloned into vector p35 (vector).
Синтетические мРНК ноггин2 и ноггин1 получали с применением набора реактивов mMESSAGE MASHINE Kit (Ambion) из векторов р35Т - ноггин2 и вектора р35Т - ноггин1 соответственно, линеаризованных рестрикционной эндонуклеазой EcoRI (Fermentas). Воздействия микроинъекций мРНК ноггин2 на развитие Xenopus laevis сравнивали с ранее описанными воздействиями инъекций мРНК ноггин1 (Smith and Harland, Cell 1992, v.70, pp.829-840; Lamb et al., Science 1993, v.262, pp.713-718; Smith et al. Nature 1993, v.361, pp.547-549). В ходе данных экспериментов мРНК ноггин1 и ноггин2 инъецировали в указанные ниже бластомеры с применением микроинъектора Eppendorf.Synthetic mRNAs of noggin2 and noggin1 were obtained using the mMESSAGE MASHINE Kit (Ambion) reagent kit from p35T vectors - noggin2 and p35T vector - noggin1, respectively, linearized with EcoRI restriction endonuclease (Fermentas). The effects of noggin2 mRNA microinjections on the development of Xenopus laevis were compared with the previously described effects of noggin1 mRNA injections (Smith and Harland, Cell 1992, v.70, pp. 829-840; Lamb et al., Science 1993, v.262, pp.713- 718; Smith et al. Nature 1993, v. 361, pp. 547-549). During these experiments, the mRNA of noggin1 and noggin2 were injected into the following blastomeres using an Eppendorf microinjector.
Вентральные инъекции 40 пг мРНК ноггин1 в ранние эмбрионы индуцировали вторичную ось тела (фиг. 1А, черная стрелка - первичная ось; серая стрелка - вторичная ось, эффект наблюдали в 68 из 85 подвергнутых микроинъекции эмбрионах), тогда как подобные инъекции мРНК ноггин2 (40 пкг) приводили к развитию грибовидных эмбрионов (фиг. 1Б, эффект наблюдали в 68 из 75 эмбрионах). Таким образом, в отличие от ноггин1 (Dale and Slack, Development 1987, v.100, pp.279-295; Cell 1992, v.70, pp.829-840; Smith et al., Nature 1993, v.361, pp.547-549), ноггин2, несмотря на его предполагаемую способность связывать BMP, не индуцировал вторичной оси тела при инъекции его мРНК в оба вентральных бластомера 8-клеточных эмбрионов. Вместо этого возникали аномальные грибовидные эмбрионы.Ventral injections of 40 pg of noggin1 mRNA into early embryos induced the secondary axis of the body (Fig. 1A, black arrow indicates the primary axis; gray arrow indicates the secondary axis, the effect was observed in 68 of 85 embryos subjected to microinjection), whereas similar injections of noggin2 mRNA (40 pkg) ) led to the development of mushroom-shaped embryos (Fig. 1B, the effect was observed in 68 of 75 embryos). Thus, unlike noggin1 (Dale and Slack, Development 1987, v. 100, pp. 279-295; Cell 1992, v. 70, pp. 829-840; Smith et al., Nature 1993, v. 361, pp.547-549), noggin2, despite its alleged ability to bind BMP, did not induce the secondary axis of the body when its mRNA was injected into both ventral blastomeres of 8-cell embryos. Instead, abnormal mushroom-shaped embryos arose.
Гибридизация in situ на тотальном препарате эмбрионов с инъекцией мРНК ноггин2 с зондами к мРНК нейральных (NCAM, Xanf-1), эпидермальных (ген кератина), мышечных (ген α-актина) генетических маркеров и генетических маркеров поздней мезодермы (brachyury) выявили гигантскую нейрализацию эктодермы и уменьшение мышечной и эпидермальной дифференцировки (фиг. 1В-Ж). Все вместе данные результаты указывают на то, что ноггин2 может нейрализовать эмбриональную эктодерму, но ингибирует дифференцировку дорзальной мезодермы и, таким образом, может препятствовать дорзализующему действию эндогенного ноггин1.In situ hybridization on a total preparation of embryos with injection of noggin2 mRNA with probes for mRNA of neural (NCAM, Xanf-1), epidermal (keratin gene), muscle (α-actin gene) genetic markers and genetic markers of late mesoderm (brachyury) revealed giant neuralization ectoderm and a decrease in muscle and epidermal differentiation (Fig. 1B-G). Taken together, these results indicate that noggin2 can neutralize the embryonic ectoderm, but inhibits the differentiation of the dorsal mesoderm and, thus, can inhibit the dorsalizing effect of endogenous noggin1.
Авторы также применяли эксплантаты, полученные из вентральной краевой зоны (VMZ) эмбрионов на стадии ранней гаструлы, для анализа эффектов ноггин2 на дифференцировку мезодермы. Микроинъекция мРНК ноггин1 вызывает сильное удлинение данных эксплантантов, преобразуя характер их вентральной мезодермы в мышечную мезодерму (дорзализация) (Dale and Slack, Development 1987, v.100, pp.279-295; Cell 1992, v.70, pp.829-840; Smith et al., Nature 1993, v.361, pp.547-549; Фиг. 1З). В отличие от этого, подобно эксплантатам VMZ без инъекции, экспрессирующие ноггин2 или и ноггин1, и ноггин2 эксплантаты остаются округлыми (фиг. 1И).The authors also used explants obtained from the ventral marginal zone (VMZ) of embryos at the stage of early gastrula to analyze the effects of noggin2 on the differentiation of the mesoderm. Microinjection of noggin1 mRNA causes a strong elongation of these explants, transforming the nature of their ventral mesoderm into muscle mesoderm (dorsalization) (Dale and Slack, Development 1987, v. 100, pp. 279-295; Cell 1992, v. 70, pp. 829-840 ; Smith et al., Nature 1993, v. 361, pp. 547-549; Fig. 1H). In contrast, like VMZ non-injection explants, expressing noggin2 or both noggin1 and noggin2 explants remain rounded (Fig. 1I).
Для независимого тестирования воздействий ноггин2 на дифференцировку эктодермальных клеток авторы использовали обратную транскрипцию-ПЦР (ОТ-ПЦР) и сравнили экспрессию различных генетических маркеров в эксплантатах "наивной" эктодермы (анимальные шапочки - АС), извлеченных из эмбрионов на стадии ранней гаструлы, в которые посредством микроинъекции ввели мРНК ноггин1 или ноггин2 (фиг. 1К, Л). Авторы также использовали эксплантаты, извлеченные из вентральной краевой зоны (VMZ) эмбрионов на стадии ранней гаструлы, для анализа воздействий ноггин2 на дифференцировку мезодермы (фиг. 1К, Л).For independent testing of the effects of noggin2 on the differentiation of ectodermal cells, the authors used reverse transcription-PCR (RT-PCR) and compared the expression of various genetic markers in explants of the "naive" ectoderm (animal caps - AS) extracted from embryos at the stage of early gastrula, into which microinjections introduced mRNA noggin1 or noggin2 (Fig. 1K, L). The authors also used explants extracted from the ventral marginal zone (VMZ) of the embryos at the stage of early gastrula to analyze the effects of noggin2 on the differentiation of the mesoderm (Fig. 1K, L).
Эксплантаты АС извлекали из эмбрионов, подвергнутых инъекции, с применением микроножа и стеклянной палочки, как ранее описано в Zaraisky et al. Developmental Biology 1992, v.152, pp.373-382. Все эксплантаты инкубировали в течение ночи в растворе 0,5×MMR. Из десяти эксплантатов каждого типа выделяли общую РНК и проводили ОТ-ПЦР, как описано в Zaraisky et al. Developmental Biology 1992, v.152, pp.373-382. Использовали следующие праймеры: ген α-актина: 5'-GCTGACAGAATGCAGAAG и 5'-TTGCTTGGAGGAGTGTGT; brachyury: 5'-GCTGGAAGTATGTGAATGGAG и 5'-TTAAGTGCTGTAATCTCTTCA; церберус: 5'-GCTTTGGTAAATGCATCTCTCTCC и 5'-GGTGACCAGTAAATCATACCTGCT; ген кератина ХК81: 5'-CTGAATAACATGAGAGCTG и 5'-TGGTTCTAGTTGTGGATGT; NCAM: 5'-CCTGCTTATGTGTATCGC и 5'-TTCACAGTACTGGGCTGTGCTT; Xanf-1: описаны в Groppe et al., 2002.AS explants were removed from the embryos subjected to injection using a micro-knife and a glass rod, as previously described in Zaraisky et al. Developmental Biology 1992, v. 152, pp. 373-382. All explants were incubated overnight in a 0.5 × MMR solution. Of the ten explants of each type, total RNA was isolated and RT-PCR was performed as described in Zaraisky et al. Developmental Biology 1992, v. 152, pp. 373-382. The following primers were used: α-actin gene: 5'-GCTGACAGAATGCAGAAG and 5'-TTGCTTGGAGGAGTGTGT; brachyury: 5'-GCTGGAAGTATGTGAATGGAG and 5'-TTAAGTGCTGTAATCTCTTCA; Cerberus: 5'-GCTTTGGTAAATGCATCTCTCTCC and 5'-GGTGACCAGTAAATCATACCTGCT; keratin gene XK81: 5'-CTGAATAACATGAGAGCTG and 5'-TGGTTCTAGTTGTGGATGT; NCAM: 5'-CCTGCTTATGTGTATCGC and 5'-TTCACAGTACTGGGCTGTGCTT; Xanf-1: described in Groppe et al., 2002.
ОТ-ПЦР на основе тотальной РНК из эксплантатов АС и VMZ эмбрионов, подвергнутых инъекции мРНК ноггин1 или ноггин2, осуществляли с праймерами к маркерам нейроэктодермы (NCAM, Xanf-1), эпидермиса (кератин), мышц (α-актин), поздней мезодермы (brachyury) и энтомезодермы (церберус) и Ef-1-α в качестве контроля (фиг. 1Л). Было показано, что ноггин1 и ноггин2 активируют экспрессию нейральных маркеров (NCAM, Xanf-1) и ингибируют эпидермальный маркер (кератин), тогда как только ноггин1 активирует экспрессию мышечного маркера (α-актин) в эксплантатах VMZ. Таким образом, в данном анализе ноггин2 показал сильную нейрализующую активность, подобную активности ноггин1 (Smith and Harland, Cell 1992, v.70, pp.829-840; Lamb et al., Science 1993, v.262, pp.713-718), индуцируя экспрессию маркеров передней части нервной системы, но ингибируя эпидермальный маркер. Способность ноггин2 нейрализовать эктодерму вкупе с его способностью подавлять дорзализующую активность ноггин1 выглядит очень необычно и означает то, что ноггин2, кроме BMP, может связывать некоторые другие факторы, необходимые для дифференцировки мышц.RT-PCR based on total RNA from AS and VMZ explants of embryos injected with moggin1 or noggin2 mRNA was performed with primers for markers of neuroectoderm (NCAM, Xanf-1), epidermis (keratin), muscle (α-actin), late mesoderm ( brachyury) and entomesoderm (cerberus) and Ef-1-α as a control (Fig. 1L). Noggin1 and noggin2 have been shown to activate the expression of neural markers (NCAM, Xanf-1) and inhibit the epidermal marker (keratin), while only noggin1 activates the expression of muscle marker (α-actin) in VMZ explants. Thus, in this analysis, noggin2 showed strong neuralizing activity similar to that of noggin1 (Smith and Harland, Cell 1992, v.70, pp. 829-840; Lamb et al., Science 1993, v.262, pp.713-718 ), inducing the expression of markers of the anterior part of the nervous system, but inhibiting the epidermal marker. The ability of noggin2 to neutralize the ectoderm, together with its ability to suppress the dorsalizing activity of noggin1, looks very unusual and means that noggin2, in addition to BMP, can bind some other factors necessary for muscle differentiation.
Пример 3Example 3
Подавление дифференцировки эмбриональной мезодермы с использованием ноггин2Inhibition of differentiation of embryonic mesoderm using noggin2
Влияние микроинъекций мРНК ноггин2 на дифференцировку эмбриональной мезодермы оценивали, анализируя экспрессию универсального маркера ранних стадий развития мезодермы - гена brachyury - на стадии ранней гаструлы Xenopus laevis. В ходе данных экспериментов мРНК ноггин1 либо ноггин2, полученные как описано в примере 2, инъецировали в экваториальную область одного из вентральных бластомеров на стадии 8 бластомеров в количестве 40 пг с применением микроинъектора Eppendorf.The effect of microinjections of noggin2 mRNA on the differentiation of the embryonic mesoderm was evaluated by analyzing the expression of the universal marker of the early stages of the development of the mesoderm - the brachyury gene - at the stage of the early gastrula Xenopus laevis. In the course of these experiments, moggin1 or noggin2 mRNA obtained as described in example 2 was injected into the equatorial region of one of the ventral blastomeres at the stage of 8 blastomeres in an amount of 40 pg using an Eppendorf microinjector.
Результаты эксперимента приведены на фиг. 2. Как видно из фиг. 2А и А', микроинъекции ноггин2 мРНК вызывают ингибирование экспрессии гена brachyury в области микроинъекции, что свидетельствует о подавлении в этом месте дифференцировки эмбриональной мезодермы. В то же время аналогичные микроинъекции мРНК ноггин1 не вызывают ингибирование экспрессии brachyury и, соответственно, подавления развития мезодермы (фиг.2Б и Б').The experimental results are shown in FIG. 2. As can be seen from FIG. 2A and A ', microinjections of noggin2 mRNA cause inhibition of the expression of the brachyury gene in the area of microinjection, which indicates the suppression of differentiation of embryonic mesoderm at this point. At the same time, similar microinjections of noggin1 mRNA do not cause inhibition of brachyury expression and, accordingly, inhibition of the development of mesoderm (Fig.2B and B ').
Результаты этих экспериментов ясно свидетельствуют о том, что в отличие от ноггин1 ноггин2 обладает уникальной способностью подавлять дифференцировку эмбриональной мезодермы.The results of these experiments clearly indicate that, unlike noggin1, noggin2 has a unique ability to suppress the differentiation of embryonic mesoderm.
Пример 4Example 4
Ингибирование сигнального каскада BMP с помощью ноггин2Inhibition of the BMP signaling cascade using noggin2
Способность ноггин2 ингибировать сигнальный каскад BMP оценивали по способности ноггин2 подавлять экспрессию основной генетической мишени этого каскада - гомеобоксного гена Vent2 - в эксплантатах эмбриональной эктодермы зародышей (АС эксплантаты), микроинъецированных смесью мРНК ноггин2 и мРНК ВМР2, ВМР4 либо ВМР7. Учитывая литературные данные о том, что разные BMP способны проявлять повышенную активность, образуя гетеродимеры, в специальной серии опытов мРНК ноггин2 смешивали для микроинъекций с мРНК всех вышеуказанных BMP одновременно. В качестве контроля аналогичные опыты проводили с мРНК и ноггин1.The ability of noggin2 to inhibit the BMP signaling cascade was assessed by the ability of noggin2 to suppress the expression of the main genetic target of this cascade - the Vent2 homeobox gene - in explants of embryonic ectoderm embryos (AS explants) microinjected with a mixture of noggin2 mRNA and BMP2, BMP4, or BMP4 mRNA. Considering the literature data that different BMPs are able to exhibit increased activity by forming heterodimers, in a special series of experiments, moggin2 mRNA was mixed for microinjections with mRNA of all of the above BMPs simultaneously. As a control, similar experiments were performed with mRNA and noggin1.
Экспрессию гена Vent2 анализировали с помощью ОТ-ПЦР основе тотальной РНК из АС эксплантатов, как описано в Примере 2. Использовали следующие Vent2-специфические праймеры: 5'-ACTGAACACAAGGACTAATACA и 5'-AGAGGCCAGAGACTGCCCAA.Vent2 gene expression was analyzed by RT-PCR based on total RNA from AS explants as described in Example 2. The following Vent2-specific primers were used: 5'-ACTGAACACAAGGACTAATACA and 5'-AGAGGCCAGAGACTGCCCAA.
Было установлено, что ноггин2 способен подавлять активацию экспрессии Vent2, индуцируемую любым из указанных BMP, а также их смесью. При этом ингибирование Vent2 наблюдалось даже в том случае, если концентрация микроинъецированной мРНК BMP превышала таковую ноггин2 в 30 раз. Напротив, ингибирование BMP каскада ноггин1 наблюдалось только в том случае, если концентрация мРНК BMP не превышала концентрацию мРНК ноггин1. Эти данные показывают, что ноггин2 является гораздо более эффективным ингибитором BMP каскада, чем ноггин1.It has been found that noggin2 is able to suppress activation of Vent2 expression induced by any of these BMPs, as well as mixtures thereof. Moreover, Vent2 inhibition was observed even if the concentration of microinjected BMP mRNA exceeded that of noggin2 by 30 times. In contrast, inhibition of BMP cascade of noggin1 was observed only if the concentration of BMP mRNA did not exceed the concentration of noggin1 mRNA. These data indicate that noggin2 is a much more effective inhibitor of the BMP cascade than noggin1.
Для прямого исследования способности белка ноггин2 связывать молекулы BMP в зародышах X.laevis были экспрессированы активные формы ноггин2 и ВМР4 в составе экспрессионных векторов pCS2-3Myc-noggin2 и pCS2-3Flag-BMP4, соответственно.To directly study the ability of the noggin2 protein to bind BMP molecules in X.laevis embryos, the active forms of noggin2 and BMP4 were expressed in the expression vectors pCS2-3Myc-noggin2 and pCS2-3Flag-BMP4, respectively.
Для получения pCS2-3Myc-noggin2 вектора нуклеотидная последовательность, кодирующая три аминокислотных последовательности эпитопа белка Мус (EQKLISEEDLEQKLISEEDLEQKLISEEDL), была вставлена с помощью ПЦР в кДНК ноггин2 непосредственно на 3' конец последовательности, кодирующей сигнальный пептид ноггин2. Для этого на первой стадии клонирования были получены соответственно 5' и 3' перекрывающиеся части кДНК ноггин2 в ПЦР с праймерами 5'-AATTGGATCCGCCACCATGAAGAGGATAAATCTGC-3' и 5'-GAGGTCTTCCTCCGATATCAGCTTCTGTTCCAGATCCTCTTCAGAGATGAGTTTCTGCTCATAAGGCTGACAGCACCCCTGA-3', 5'-GAACAGAAGCTGATATCGGAGGAAGACCTC GAGCAGAAACTCATCTCTGAAGAGGATCTGCTCAGGCTTAGACCCTCT-3' и 5'-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3' соответственно. На второй стадии эти фрагменты кДНК были очищены от не включившихся праймеров, смешаны друг с другом, денатурированы нагреванием, отожжены и подвергнуты второму раунду ПЦР с концевыми праймерами 5'-AATTGGATCCGCCACCATGAAGAGGATAAATCTGC-3' и 5'-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3'. Полученная полноразмерная кДНК ноггин2, содержащая последовательность, кодирующую три аминокислотных последовательности Мус, была клонирована в вектор pCS2 по рестриктным сайгам NcoI(тупой)/AgeI(тупой) и XhoI/XhoI. Для получения pCS2-3Flag-BMP4 вектора нуклеотидная последовательность, кодирующая три аминокислотных последовательности Flag (DYKDDDDKDYKDDDDKDYKDDDDK), была вставлена с помощью ПЦР в кДНК ВМР4 непосредственно на 3' конец последовательности, кодирующей прорегион белка ВМР4 Xenopus laevis. На первой стадии клонирования были получены 5' и 3' перекрывающиеся части кДНК ВМР4 в ПЦР с праймерами 5'-AATTGGATCCGCCACCATGATTCCTGGTAACCGAATG-3' и 5'-TTTGTCATCATCGTCTTTGTAGTCCTTATCGTCGTCATCCTTGTAATCCTGTTTTGGACT TCTTTTTGAC-3', 5'-GACTACAAAGACGATGATGACAAAGATTACAAGGATGACGACGATA AGCAGAGACCCCGTAAAAAAAAC-3' и 5'-AATCTCGAGTCAACGGCACCCACACCCTTCCA-3' соответственно. На второй стадии эти фрагменты кДНК были очищены от не включившихся праймеров, смешаны друг с другом, денатурированы нагреванием, отожжены и подвергнуты второму раунду ПЦР с концевыми праймерами 5'-AATTGGATCCGCCACCATGATTCCTGGTAACCGAATG-3' и 5'-AATCTCGAGTCAACGGCACCCACACCCTTCCA-3'. Полученная полноразмерная кДНК ВМР4, содержащая последовательность, кодирующую три аминокислотных последовательности эпитопа Flag, была клонирована в вектор pCS2 по рестриктным сайтам NcoI(тупой)/AgeI(тупой) и XhoI/XhoI.To obtain the pCS2-3Myc-noggin2 vector, the nucleotide sequence encoding the three amino acid sequences of the Myc protein epitope (EQKLISEEDLEQKLISEEDLEQKLISEEDL) was inserted by PCR into the noggin2 cDNA directly at the 3 'end of the sequence encoding the noggin2 signal peptide. For this purpose the first cloning step were obtained, respectively 5 'and 3' overlapping part noggin2 cDNA by PCR with the primers 5'-AATTGGATCCGCCACCATGAAGAGGATAAATCTGC-3 'and 5'-GAGGTCTTCCTCCGATATCAGCTTCTGTTCCAGATCCTCTTCAGAGATGAGTTTCTGCTCATAAGGCTGACAGCACCCCTGA-3', 5'-GAACAGAAGCTGATATCGGAGGAAGACCTC GAGCAGAAACTCATCTCTGAAGAGGATCTGCTCAGGCTTAGACCCTCT-3 'and 5'- ATTCTCGAGTTAGCATGAACACTTACACTCTG-3 ', respectively. In the second stage, these cDNA fragments were purified from unincorporated primers, mixed with each other, denatured by heating, annealed and subjected to a second round of PCR with end primers 5'-AATTGGATCCGCCACCATGAAGAGGATAAATCTGC-3 'and 5'-ATTCTCGTT-3. The resulting full-length noggin2 cDNA containing a sequence encoding the three amino acid sequences of Myc was cloned into the pCS2 vector at the restriction saigas NcoI (dull) / AgeI (dull) and XhoI / XhoI. To obtain the pCS2-3Flag-BMP4 vector, the nucleotide sequence encoding the Flag three amino acid sequences (DYKDDDDKDYKDDDDKDYKDDDDK) was inserted by PCR into BMP4 cDNA directly at the 3 'end of the sequence encoding the proregion of Xenopus laev BMP4 protein. In the first step were prepared by cloning the 5 'and 3' overlapping part BMP4 cDNA by PCR with the primers 5'-AATTGGATCCGCCACCATGATTCCTGGTAACCGAATG-3 'and 5'-TTTGTCATCATCGTCTTTGTAGTCCTTATCGTCGTCATCCTTGTAATCCTGTTTTGGACT TCTTTTTGAC-3', 5'-GACTACAAAGACGATGATGACAAAGATTACAAGGATGACGACGATA AGCAGAGACCCCGTAAAAAAAAC-3 'and 5'-AATCTCGAGTCAACGGCACCCACACCCTTCCA- 3 ', respectively. In the second stage, these cDNA fragments were purified from unincorporated primers, mixed with each other, denatured by heating, annealed and subjected to a second round of PCR with end primers 5'-AATTGGATCCGCCACCATGATTCCTGGTAACCGAATG-3 'and 5'-AATCGTAC-3A. The resulting full-length BMP4 cDNA containing a sequence encoding the three amino acid sequences of the Flag epitope was cloned into the pCS2 vector at the restriction sites NcoI (dull) / AgeI (dull) and XhoI / XhoI.
600 пг синтетической мРНК 3Myc-noggin2 и 600 pg синтетической мРНК 3Flag-BMP4 были микроинъецированы в развивающиеся зародыши X. laevis на стадии 2-х бластомеров. В дальнейшем эти зародыши были инкубированы в растворе 0.1 MMR до стадии ранней гаструлы.600 pg of synthetic 3Myc-noggin2 mRNA and 600 pg of synthetic 3Flag-BMP4 mRNA were microinjected into developing embryos of X. laevis at the stage of 2 blastomeres. Subsequently, these embryos were incubated in a 0.1 MMR solution until the early gastrula stage.
Выделение экспрессированных белков проводилось путем лизирования зародышей на стадии ранней гаструлы по методике, описанной в Tanegashima et al., Int.J.Dev.Biol (2004) 48:275-283.The expression of expressed proteins was carried out by lysing the embryos at the stage of early gastrula according to the method described in Tanegashima et al., Int.J.Dev. Biol (2004) 48: 275-283.
После выделения проводилась абсорбция экспрессированного белка 3Flag-BMP4 на смоле Flag-Agarose (Sigma) согласно протоколу производителя. После промывки смолы в соответствии с протоколом производителя наличие на этой смоле связавшегося белка 3Myc-noggin2 анализировалось методом белкового блоттинга с помощью Мус-специфических моноклональных антител (Sigma).After isolation, the expressed 3Flag-BMP4 protein was absorbed on Flag-Agarose resin (Sigma) according to the manufacturer's protocol. After washing the resin in accordance with the manufacturer's protocol, the presence of 3Myc-noggin2 protein bound on this resin was analyzed by protein blotting using Myc-specific monoclonal antibodies (Sigma).
Данный эксперимент выявил способность молекул белка ноггин2 связывать молекулы белка ВМР4 (фиг. 2Ж).This experiment revealed the ability of the noggin2 protein molecules to bind BMP4 protein molecules (Fig. 2G).
Для исследования способности белка ноггин2 ингибировать в клетках эмбрионов сигнальный путь BMP, индуцированный BMP, было проанализировано влияние ноггин2 на фосфорилирование внутриклеточного передатчика этого сигнального пути - белка Smadl. Для этого эмбрионы шпорцевой лягушки инъецировали на стадии 2-4 клеток либо мРНК ВМР4 (100 pg/эмбрион), либо смесью мРНК ВМР4 (10 пг/эмбрион) и ноггин2 (1 пг/эмбрион). Анализ фосфорилирования Smadl в инъецированных эмбрионах проводили на стадии начала гаструляции (стадия 10) методом вестерн-блоттинга при помощи коммерческих моноклональных антител к Phospho-Smadl (Cell Signalling Technology). В результате было показано, что ноггин2 способен блокировать повышение концентрации Phospho-Smadl, вызванное ВМР4 (фиг. 2, З).To study the ability of the noggin2 protein to inhibit BMP-induced BMP signaling in embryonic cells, the effect of noggin2 on the phosphorylation of the intracellular transmitter of this signaling pathway, Smadl, was analyzed. For this, embryos of the Spur frog were injected at the stage of 2-4 cells with either BMP4 mRNA (100 pg / embryo) or a mixture of BMP4 mRNA (10 pg / embryo) and noggin2 (1 pg / embryo). The analysis of Smadl phosphorylation in the injected embryos was carried out at the stage of the beginning of gastrulation (stage 10) by Western blotting using commercial monoclonal antibodies to Phospho-Smadl (Cell Signaling Technology). As a result, it was shown that noggin2 is able to block the increase in the concentration of Phospho-Smadl caused by BMP4 (Fig. 2, C).
Пример 5Example 5
Ингибирование сигнального каскада activin/nodal с помощью ноггин2Inhibition of the activin / nodal signaling cascade with noggin2
Способность ноггин2 ингибировать сигнальный каскад activin/nodal оценивали по способности ноггин2 подавлять экспрессию основной генетической мишени этого каскада - гена brachyury - в эксплантатах эмбриональной эктодермы зародышей (АС эксплантаты), микроинъецированных смесью мРНК ноггин2 и мРНК Xnr1, Xnr2, либо Xnr4 (гомологи гена nodal млекопитающих). В качестве контроля, аналогичные опыты проводили с мРНК и ноггин1.The ability of noggin2 to inhibit the activin / nodal signaling cascade was assessed by the ability of noggin2 to suppress the expression of the main genetic target of this cascade, the brachyury gene, in explants of embryonic ectoderm of embryos (AS explants) microinjected with a mixture of noggin2 mRNA and mammalian Xnr1, Xnr2, or nnr2, mice ) As a control, similar experiments were performed with mRNA and noggin1.
Экспрессию гена brachyury анализировали с помощью ОТ-ПЦР по общей РНК из АС эксплантатов, как описано в Примере 2.Brachyury gene expression was analyzed by RT-PCR for total RNA from AS explants as described in Example 2.
Было установлено, что ноггин2 способен подавлять активацию экспрессии brachyury, индуцируемую любым из указанных Xnr. При этом ингибирование brachyury наблюдалось только в том случае, если концентрация микроинъецированной мРНК Xnr не превышала таковую ноггин2. В отличие от этого ноггин1 не способен ингибировать активацию гена brachyury в аналогичных тестах. Эти данные демонстрируют, что в отличие от ноггин1 ноггин2 способен ингибировать не только сигнальный каскад BMP, но и каскад, активируемый членами другого большого надсемейства TGF-β факторов - activin/nodal.Noggin2 has been found to be able to suppress activation of brachyury expression induced by any of these Xnr. Moreover, inhibition of brachyury was observed only if the concentration of microinjected Xnr mRNA did not exceed that of noggin2. In contrast, noggin1 is not able to inhibit the activation of the brachyury gene in similar tests. These data demonstrate that, unlike noggin1, noggin2 is able to inhibit not only the BMP signaling cascade, but also the cascade activated by members of the other large superfamily of TGF-β factors - activin / nodal.
Для исследования способности белка ноггин2 связывать молекулы белка activin в зародышах X.laevis были экспрессированы активные формы ноггин2 и activin-B в составе экспрессионных векторов pCS2-3Myc-noggin2 и pCS2-3Flag-activin-B, соответственно.To study the ability of the noggin2 protein to bind activin protein molecules in X.laevis embryos, the active forms of noggin2 and activin-B were expressed in the expression vectors pCS2-3Myc-noggin2 and pCS2-3Flag-activin-B, respectively.
Получение pCS2-3Myc-noggin2 вектора было осуществлено как описано в Примере 4.Obtaining pCS2-3Myc-noggin2 vector was carried out as described in Example 4.
Для получения pSP64T-3Flag-activin-B вектора нуклеотидная последовательность, кодирующая три аминокислотных последовательности Flag (DYKDDDDKDYKDDDDKDYKDDDDK), была вставлена с помощью ПЦР в кДНК activin-B непосредственно позади последовательности, кодирующей прорегион белка activin-B Xenopus laevis. На первой стадии клонирования были получены 5' и 3' перекрывающиеся части кДНК activin-B в ПЦР с праймерами 5'-AATTGGATCCGCCACCATGGCTCTCCTGTTACTGCCTCTG-3' и 5'-TTTGTCATCATCGTCTTTGTAGTCCTTATCGTCGTCATCCTTGTAATCCTCGAGGCCTCTCTTACGGA-3', 5'-GACTACAAAGACGATGATGACAAAGATTACAAGGATGACGACGATAAG TGCGATGGACACACAAATT-3' и 5'-AATGAATTCATGCACAGCCGCACTCGTCCA-3' соответственно. На второй стадии эти фрагменты кДНК были очищены от не включившихся праймеров, смешаны друг с другом, денатурированы нагреванием, отожжены и подвергнуты второму раунду ПЦР с концевыми праймерами 5'-AATTGGATCCGCCACCATGGCTCTCCTGTTACTGCCTCTG-3' и 5'-AATGAATTCATGCACAGCCGCACTCGTCCA-3'. Полученная полноразмерная кДНК activin-B, содержащая последовательность, кодирующую три аминокислотных последовательности эпитопа Flag, была клонирована в вектор pSP64T по рестриктным сайтам HindIII(тупой)/Agel(тупой) и EcoRI/EcoRI.To obtain the pSP64T-3Flag-activin-B vector, the nucleotide sequence encoding the Flag three amino acid sequences (DYKDDDDKDYKDDDDKDYKDDDDK) was inserted by PCR into the activin-B cDNA immediately behind the sequence encoding the proregion of the Xenopus laevis activin-B protein. In the first step of cloning were obtained 5 'and 3' overlapping part of activin-B cDNA by PCR with the primers 5'-AATTGGATCCGCCACCATGGCTCTCCTGTTACTGCCTCTG-3 'and 5'-TTTGTCATCATCGTCTTTGTAGTCCTTATCGTCGTCATCCTTGTAATCCTCGAGGCCTCTCTTACGGA-3', 5'-GACTACAAAGACGATGATGACAAAGATTACAAGGATGACGACGATAAG TGCGATGGACACACAAATT-3 'and 5'-AATGAATTCATGCACAGCCGCACTCGTCCA -3 'respectively. In the second stage, these cDNA fragments were purified from unincorporated primers, mixed with each other, denatured by heating, annealed, and subjected to a second round of PCR with end primers 5'-AATTGGATCCGCCACCATGGCTCTCCTGTTACTGCCTCTG-3 'and 5'-ACG-ATGATCATGATCATGATCATGCCTG-3AT. The resulting full-length activin-B cDNA containing a sequence encoding the three amino acid sequences of the Flag epitope was cloned into the pSP64T vector at the restriction sites HindIII (dull) / Agel (dull) and EcoRI / EcoRI.
Анализ способности экспрессированного белка 3Myc-noggin2 связывать молекулы белка 3Flag-activin-B был проведен с помощью специфических антител по методике, описанной в Примере 4.Analysis of the ability of the expressed 3Myc-noggin2 protein to bind 3Flag-activin-B protein molecules was carried out using specific antibodies according to the procedure described in Example 4.
Данный эксперимент выявил способность молекул белка ноггин2 связывать молекулы белка activin-B (фиг. 2 Ж).This experiment revealed the ability of the noggin2 protein molecules to bind activin-B protein molecules (Fig. 2 G).
Для исследования способности белка ноггин2 ингибировать в клетках эмбрионов сигнальный путь activin/nodal, индуцированный activin, было проанализировано влияние ноггин2 на фосфорилирование внутриклеточного передатчика этого сигнального пути - белка Smad2. Для этого эмбрионы шпорцевой лягушки инъецировали на стадии 2-4 клеток либо мРНК activinB (100 pg/эмбрион), либо смесью мРНК activinB (10 pg/эмбрион) и Noggin2 (1 ng/эмбрион). Анализ фосфорилирования Smad2 в инъецированных эмбрионах проводили на стадии начала гаструляции (стадия 10) методом вестерн-блоттинга при помощи коммерческих моноклональных антител к Phospho-Smad2 (Cell Signalling Technology). В результате было показано, что ноггин2 способен блокировать повышение концентрации Phospho-Smad2, вызванное activinB (фиг. 2, З).To study the ability of the noggin2 protein to inhibit activin-induced activin / nodal signaling in embryonic cells, the effect of noggin2 on the phosphorylation of the intracellular transmitter of this signaling pathway, Smad2 protein, was analyzed. For this purpose, the frog embryos were injected at the stage of 2-4 cells with either activinB mRNA (100 pg / embryo) or a mixture of activinB mRNA (10 pg / embryo) and Noggin2 (1 ng / embryo). The analysis of Smad2 phosphorylation in the injected embryos was carried out at the stage of the beginning of gastrulation (stage 10) by Western blotting using commercial monoclonal antibodies to Phospho-Smad2 (Cell Signaling Technology). As a result, it was shown that noggin2 is able to block the increase in the concentration of Phospho-Smad2 caused by activinB (Fig. 2, C).
Пример 6Example 6
Одновременное ингибирование сигнальных каскадов BMP и activin/nodal и индукция головных структур с использованием ноггин2Simultaneous inhibition of BMP and activin / nodal signaling cascades and induction of head structures using noggin2
Как известно, дифференцировка структур главной оси тела позвоночных ингибируется на брюшной стороне эмбриона в результате перманентной активации двух основных TGF-β-каскадов: BMP и activin/nodal. При этом селективное ингибирование BMP каскада приводит "по умолчанию" к развитию структур, характерных для туловищной и заднеголовной части оси тела, в частности к развитию спинного мозга и мышц. В то же время одновременное ингибирование как BMP, так и activin/nodal каскадов вызывает индукцию переднеголовных структур, в том числе глаз и переднего мозга.As is known, the differentiation of the structures of the main axis of the vertebral body is inhibited on the ventral side of the embryo as a result of the permanent activation of two main TGF-β cascades: BMP and activin / nodal. Moreover, selective inhibition of the BMP cascade leads by default to the development of structures characteristic of the trunk and posterior part of the body axis, in particular, the development of the spinal cord and muscles. At the same time, the simultaneous inhibition of both BMP and activin / nodal cascades induces the anterior-head structures, including the eye and forebrain.
В нормальном развитии подавление BMP каскада на спинной стороне эмбриона осуществляется специфическими белковыми факторами, секретируемыми клетками шпемановского организатора и способными связывать BMP. Наиболее известным из них является ноггин1. Микроинъекции мРНК ноггин1 в вентральные вегетативные бластомеры эмбриона Xenopus способны вызывать развитие дополнительных туловищных структур на брюшной стороне тела эмбриона. При этом вторые оси тела, индуцируемые экзогенным ноггин1, никогда не содержат переднеголовных структур, для развития которых необходимо одновременное ингибирование как BMP, так и activin/nodal каскадов. В нормальном развитии ингибирование activin/nodal каскада, а также тесно связанного с ним положительной обратной связью Wnt-сигнального каскада осуществляется другими факторами, секретируемыми клетками головной части шпемановского организатора. Наиболее известными из них являются Dikkopf и церберус. Причем последний белок способен связывать сразу три фактора: BMP, nodal и Wnt. В результате в ростральной части эмбриона снимается запрет на активацию программы переднеголовной дифференцировки и происходит развитие переднеголовных структур.In normal development, the suppression of the BMP cascade on the dorsal side of the embryo is carried out by specific protein factors secreted by the cells of the Shperman organizer and able to bind BMP. The most famous of them is noggin1. Microinjections of noggin1 mRNA into the ventral vegetative blastomeres of the Xenopus embryo can cause the development of additional trunk structures on the ventral side of the embryo body. Moreover, the second body axes induced by exogenous noggin1 never contain anterior-headed structures, the development of which requires simultaneous inhibition of both BMP and activin / nodal cascades. In normal development, inhibition of the activin / nodal cascade, as well as the closely related positive feedback of the Wnt signaling cascade, is carried out by other factors secreted by the cells of the head part of the Shperman organizer. The most famous of these are Dikkopf and Cerberus. Moreover, the last protein is able to bind three factors at once: BMP, nodal and Wnt. As a result, in the rostral part of the embryo, the ban on activation of the anterior-head differentiation program is lifted and the anterior-head structures develop.
Способность ноггин2 ингибировать одновременно как каскад BMP, так и каскад activin/nodal, указывает на потенциальную способность этого фактора индуцировать переднеголовные структуры. Однако в опытах, описанных в Примере 2, подобный эффект мог быть маскирован сильным нейрализующим действием ноггин2, вызванным относительно высокими концентрациями микроинъецируемой мРНК.The ability of noggin2 to simultaneously inhibit both the BMP cascade and the activin / nodal cascade indicates a potential ability of this factor to induce anterior-headed structures. However, in the experiments described in Example 2, a similar effect could be masked by the strong neuralizing effect of noggin2, caused by relatively high concentrations of microinjectable mRNA.
В связи с этим была изучена способность низких концентраций ноггин2 индуцировать развитие дополнительных переднеголовных структур в целых эмбрионах. В данной серии опытов синтетическую мРНК ноггин2, полученную также, как описано в Примере 2, микроинъецировали в один из вентральных вегетативных бластомеров эмбрионов Xenopus laevis на стадии 8-16 бластомеров в количестве 2-5 пг. В результате, у 25% эмбрионов наблюдалось развитие дополнительного переднеголовного отдела. Как было показано с помощью метода гибридизации in situ со специфическими зондами к мРНК переднеголовных маркеров BF-1 и Рах-6, такие дополнительные головные структуры включали конечный мозг и глаза (Фиг.2, В и В'; Д и Д'). Аналогичные структуры отсутствовали в составе дополнительных осей тела, индуцированных микроинъекциями мРНК ноггин1 (фиг. 2, Г и Г'; Е и Е'). Эти данные демонстрируют качественное отличие эффектов ноггин2 от эффектов ноггин1, связанное со способностью ноггин2 ингибировать как BMP, так и activin/nodal сигнальный каскад.In this regard, the ability of low concentrations of noggin2 to induce the development of additional anterior-headed structures in whole embryos was studied. In this series of experiments, synthetic noggin2 mRNA, also obtained as described in Example 2, was microinjected into one of the ventral vegetative blastomeres of Xenopus laevis embryos at the stage of 8-16 blastomeres in the amount of 2-5 pg. As a result, in 25% of embryos, the development of an additional anterior-head section was observed. As shown by the in situ hybridization method with specific probes for mRNA of the forehead markers BF-1 and Pax-6, such additional brain structures included the end brain and eyes (Figure 2, B and B '; D and D'). Similar structures were absent in the additional body axes induced by microinjections of noggin1 mRNA (Fig. 2, D and G '; E and E'). These data demonstrate a qualitative difference between the effects of noggin2 and the effects of noggin1, associated with the ability of noggin2 to inhibit both BMP and the activin / nodal signaling cascade.
Пример 7Example 7
Получение рекомбинантного белка ноггин2Obtaining recombinant protein noggin2
Для получения активного гомодимера ноггин2 осуществляли экспрессию ноггин2 в культуре эпителиальных клеток зеленой мартышки CV-1 в составе экспрессирующего вектора pcDNA3-6His-noggin2. Для получения pcDNA3-6His-noggin2 вектора, нуклеотидная последовательность, кодирующая 6 аминокислотных остатков гистидина, была встроена с помощью ПЦР в кДНК ноггин2 непосредственно позади последовательности, кодирующей сигнальный пептид ноггин2. На первой стадии клонирования были получены соответственно 5' и 3' перекрывающиеся части кДНК ноггин2 в ПЦР с праймерами 5'-ATTACCGGTGGGAGAACCTTGTTCTTCATT-3' и 5'-GTGATGGTGATGGTGATGCCCGGGATAAGGCTGACAGCACCCCT-3', и 5'-CATCACCATCACCATCACGGGCCCTATCTCAGGCTTAGACCCTC-3'' и 5'-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3'. На второй стадии эти фрагменты кДНК были очищены от не включившихся праймеров, смешаны друг с другом, денатурированы нагреванием, отожжены и подвергнуты второму раунду ПЦР с праймерами 5'-ATTACCGGTGGGAGAACCTTGTTCTTCATT-3' и 5'-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3'. Полученная полноразмерная кДНК ноггин2, содержащая последовательность, кодирующую 6 гистидинов, была клонирована в вектор pcDNA3 по рестриктным сайгам NcoI (тупой) и XhoI.To obtain the active homodimer noggin2, expression of noggin2 was carried out in a culture of green monkey monkey CV-1 epithelial cells as part of the pcDNA3-6His-noggin2 expression vector. To obtain the pcDNA3-6His-noggin2 vector, a
Эпителиальные клетки зеленой мартышки (CV-1) культивировали в DMEM среде (Sigma) с 10% сывороткой (Biolot), 100 Ед/мл пенициллина и 100 мг/мл стрептомицина при 37°С и 1 атм. Для получения постоянной клеточной линии, продуцирующей 6His-noggin2, эти клетки были трансфицированы pcDNA3-6His-noggin2 вектором. Последующую селекцию проводили в среде, содержащей 1 мкг/мл генетицина (Gibco BRL). Секретируемый рекомбинантный 6His-Noggin2 получали из культуральной среды при помощи аффинной хроматографии на Ni-NTA агарозе (Qiagen). Выход белка был оценен как 50 мкг/миллион клеток в день. Активность белка подтверждали по его способности активировать нейрогенез в эксплантатах эмбриональной эктодермы.Green monkey epithelial cells (CV-1) were cultured in DMEM medium (Sigma) with 10% serum (Biolot), 100 U / ml penicillin and 100 mg / ml streptomycin at 37 ° C and 1 atm. To obtain a constant cell line producing 6His-noggin2, these cells were transfected with pcDNA3-6His-noggin2 vector. Subsequent selection was performed in a medium containing 1 μg / ml geneticin (Gibco BRL). Secreted recombinant 6His-Noggin2 was obtained from the culture medium by affinity chromatography on Ni-NTA agarose (Qiagen). Protein yield was estimated as 50 μg / million cells per day. Protein activity was confirmed by its ability to activate neurogenesis in explants of embryonic ectoderm.
Пример 8Example 8
Получение поликлональных антител против ноггин2 кДНК, содержащую полную кодирующую область ноггин2, реамплифицировали как описано в примере 1, субклонировали в вектор pQE30 и использовали для трансформации Escherichia coli. Рекомбинантный белок, содержащий шесть гистидиновых остатков, очищали с использованием аффинной хроматографии на Talon Resin (Clontech Laboratories, Inc.) в денатурирующих условиях и использовали для иммунизации кроликов по стандартной технологии. Поликлональную сыворотку тестировали против рекомбинантного белка с помощью методов ELISA и Вестерн-блота.Obtaining polyclonal antibodies against noggin2 cDNA containing the complete coding region of noggin2 was reamplified as described in Example 1, subcloned into the pQE30 vector and used to transform Escherichia coli. A recombinant protein containing six histidine residues was purified using Talon Resin affinity chromatography (Clontech Laboratories, Inc.) under denaturing conditions and used to immunize rabbits using standard technology. Polyclonal serum was tested against recombinant protein using ELISA and Western blot methods.
Claims (1)
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2005123287/13A RU2354662C2 (en) | 2005-07-21 | 2005-07-21 | Noggin2-based activin activity blocking method |
| PCT/RU2006/000382 WO2007011265A1 (en) | 2005-07-21 | 2006-07-18 | Method for blocking noggin2 target specific activities |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2005123287/13A RU2354662C2 (en) | 2005-07-21 | 2005-07-21 | Noggin2-based activin activity blocking method |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2005123287A RU2005123287A (en) | 2007-01-27 |
| RU2354662C2 true RU2354662C2 (en) | 2009-05-10 |
Family
ID=37669061
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2005123287/13A RU2354662C2 (en) | 2005-07-21 | 2005-07-21 | Noggin2-based activin activity blocking method |
Country Status (2)
| Country | Link |
|---|---|
| RU (1) | RU2354662C2 (en) |
| WO (1) | WO2007011265A1 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2407799C1 (en) * | 2009-06-18 | 2010-12-27 | Учреждение Российской академии наук Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН | METHOD OF BLOCKING SINGALLING PATHWAY ACTIVATED BY TGF-beta FACTOR DERRIERE IN ANIMAL CELLS |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2391352C1 (en) * | 2008-10-24 | 2010-06-10 | Учреждение Российской академии наук Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН | METHOD OF BLOCKING SIGNAL PATH ACTIVATED BY TGF-beta FACTOR OF VgI IN ANIMAL CELLS |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2194714C2 (en) * | 1995-02-20 | 2002-12-20 | Санкио Компани Лимитед | Novel proteins and methods of their preparing |
| WO2004064612A2 (en) * | 2003-01-21 | 2004-08-05 | The Rockefeller University | Regulation of tgf-b signaling by tomoregulin |
-
2005
- 2005-07-21 RU RU2005123287/13A patent/RU2354662C2/en not_active IP Right Cessation
-
2006
- 2006-07-18 WO PCT/RU2006/000382 patent/WO2007011265A1/en not_active Ceased
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2194714C2 (en) * | 1995-02-20 | 2002-12-20 | Санкио Компани Лимитед | Novel proteins and methods of their preparing |
| WO2004064612A2 (en) * | 2003-01-21 | 2004-08-05 | The Rockefeller University | Regulation of tgf-b signaling by tomoregulin |
Non-Patent Citations (1)
| Title |
|---|
| TAREK A.S. et al., DRAGON, A Bone Morphogenetic Protein Coreceptor, J. Biol. Chem, v.280, n.14, p.14124-14125. FURTHAUER M. et al., Three different noggin genes antagonize the activity of bone morphogenetic proteins in the zebrafish embryo, Dev. Biol., 1999, v.214, n.1, p.181-196. FLETCHER R.B. et al., Expression of Xenopus tropicalis noggini and noggin2 in early development: two noggin genes in a tetrapod, Gene Expr. Patterns, 2004, v.5, n.2, p.225-230. LANGENFELD E.M. et al., The mature bone morphogenetic protein-2 is aberrantly expressed in non-small cell lung carcinomas and stimulates tumor growth of A549 cells, Carcinogenesis, 2003, v.24, n.9, p.1445-1454. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2407799C1 (en) * | 2009-06-18 | 2010-12-27 | Учреждение Российской академии наук Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН | METHOD OF BLOCKING SINGALLING PATHWAY ACTIVATED BY TGF-beta FACTOR DERRIERE IN ANIMAL CELLS |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007011265A8 (en) | 2007-10-18 |
| WO2007011265A1 (en) | 2007-01-25 |
| RU2005123287A (en) | 2007-01-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Thomsen et al. | Processed Vg1 protein is an axial mesoderm inducer in Xenopus | |
| Rosenthal et al. | Primary structure and biological activity of a novel human neurotrophic factor | |
| EP1553182B1 (en) | Regulated genes and uses thereof | |
| JPH11512928A (en) | Neurturin and related growth factors | |
| JPH07250688A (en) | New human c-dna coding tgf-beta superfamily protein | |
| JP2010187691A (en) | MAMMALIAN TRANSFORMING GROWTH FACTOR beta-9 | |
| JP5748223B2 (en) | Neuron survival factor and use thereof | |
| JP2000517179A (en) | DON-1 genes and polypeptides, and uses thereof | |
| RU2354662C2 (en) | Noggin2-based activin activity blocking method | |
| US5679783A (en) | DNA encoding a tissue differentiation affecting factor | |
| CN101287747A (en) | GDNF-derived peptide | |
| WO2017032216A1 (en) | Acvr1-fc fusion protein, preparation method therefor, and application thereof | |
| US20040132136A1 (en) | Mammalian Transforming growth factor beta-9 | |
| CA2352495A1 (en) | Human semaphorin 6a-1 (sema6a-a), a gene involved in neuronal development and regeneration mechanisms during apoptosis, and its use as a potential drug target | |
| RU2407799C1 (en) | METHOD OF BLOCKING SINGALLING PATHWAY ACTIVATED BY TGF-beta FACTOR DERRIERE IN ANIMAL CELLS | |
| JP2002508666A (en) | Neural stem cell gene | |
| RU2391352C1 (en) | METHOD OF BLOCKING SIGNAL PATH ACTIVATED BY TGF-beta FACTOR OF VgI IN ANIMAL CELLS | |
| US7939635B2 (en) | Autotaxin: motility stimulating protein useful in cancer diagnosis and therapy | |
| CA2360530C (en) | A human nuclear protein having a ww domain and a polynucleotide encoding the protein | |
| US7285532B2 (en) | Therapeutic method for treating bone formation diseases | |
| WO2004035627A1 (en) | Modulation of tgfbeta-like signalling pathways | |
| US20020127594A1 (en) | Don-1 gene and polypeptides and uses therefor | |
| CA2419851A1 (en) | Genetic demonstration of requirement for nkx6.1, nkx2.2 and nkx6.2 in ventral neuron generation | |
| US7312081B2 (en) | Genetic demonstration of requirement for nkx6.1, nkx2.2 and nkx6.2 in ventral neuron generation | |
| JP2007006701A (en) | BMP-4 neutralizing factor protein |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20120722 |