RU2243221C2 - Производные 4-фенилпиримидина и фармацевтическая композиция - Google Patents
Производные 4-фенилпиримидина и фармацевтическая композиция Download PDFInfo
- Publication number
- RU2243221C2 RU2243221C2 RU2001133458/04A RU2001133458A RU2243221C2 RU 2243221 C2 RU2243221 C2 RU 2243221C2 RU 2001133458/04 A RU2001133458/04 A RU 2001133458/04A RU 2001133458 A RU2001133458 A RU 2001133458A RU 2243221 C2 RU2243221 C2 RU 2243221C2
- Authority
- RU
- Russia
- Prior art keywords
- carboxylic acid
- bis
- trifluoromethylbenzyl
- methylamide
- pyrimidine
- Prior art date
Links
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 7
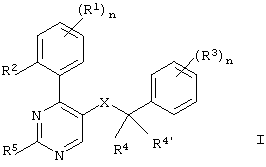
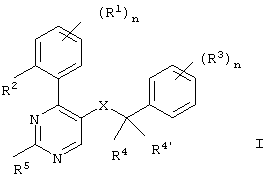
- MKLQPIYLZMLAER-UHFFFAOYSA-N 4-phenylpyrimidine Chemical class C1=CC=CC=C1C1=CC=NC=N1 MKLQPIYLZMLAER-UHFFFAOYSA-N 0.000 title abstract 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 52
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 35
- 150000003839 salts Chemical class 0.000 claims abstract description 17
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 12
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 10
- 239000001257 hydrogen Substances 0.000 claims abstract description 10
- 108010040718 Neurokinin-1 Receptors Proteins 0.000 claims abstract description 8
- 102000002002 Neurokinin-1 Receptors Human genes 0.000 claims abstract description 8
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims abstract description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 6
- 125000005322 morpholin-1-yl group Chemical group 0.000 claims abstract description 5
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 claims abstract description 5
- 238000011282 treatment Methods 0.000 claims abstract description 4
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims abstract description 3
- 125000004414 alkyl thio group Chemical group 0.000 claims abstract description 3
- 125000004429 atom Chemical group 0.000 claims abstract description 3
- 125000000440 benzylamino group Chemical group [H]N(*)C([H])([H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 claims abstract description 3
- 238000004177 carbon cycle Methods 0.000 claims abstract description 3
- 201000010099 disease Diseases 0.000 claims abstract description 3
- 125000004076 pyridyl group Chemical group 0.000 claims abstract description 3
- 125000000714 pyrimidinyl group Chemical group 0.000 claims abstract description 3
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims abstract description 3
- 230000001404 mediated effect Effects 0.000 claims abstract 2
- -1 amino, phenyl Chemical group 0.000 claims description 157
- ADTNSTHKMIPKIJ-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 ADTNSTHKMIPKIJ-UHFFFAOYSA-N 0.000 claims description 57
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 13
- 239000002253 acid Substances 0.000 claims description 11
- 229910052736 halogen Inorganic materials 0.000 claims description 9
- 150000002367 halogens Chemical class 0.000 claims description 9
- 125000002757 morpholinyl group Chemical group 0.000 claims description 7
- 125000004193 piperazinyl group Chemical group 0.000 claims description 7
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 6
- QLHLFYLRIYRMFY-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-chlorophenyl)-2-(4-methylpiperazin-1-yl)pyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1 QLHLFYLRIYRMFY-UHFFFAOYSA-N 0.000 claims description 5
- IENMCCVDCMICSD-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-chlorophenyl)-2-piperazin-1-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCNCC2)N=C1C(C=CC=C1)=C1Cl)=O IENMCCVDCMICSD-UHFFFAOYSA-N 0.000 claims description 4
- PJVDJTRBJXRLEH-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-methylphenyl)-2-(4-methylpiperazin-1-yl)pyrimidine-5-carboxylic acid Chemical compound CC(C=CC=C1)=C1C1=NC(N2CCN(C)CC2)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PJVDJTRBJXRLEH-UHFFFAOYSA-N 0.000 claims description 4
- UFHOAZWMVHBERI-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-methylphenyl)-2-piperazin-1-ylpyrimidine-5-carboxylic acid Chemical compound CC(C=CC=C1)=C1C1=NC(N2CCNCC2)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 UFHOAZWMVHBERI-UHFFFAOYSA-N 0.000 claims description 4
- BVJHCIDFWJRFPP-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(4-fluorophenyl)-2-(4-methylpiperazin-1-yl)pyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=C2)=CC=C2F)=N1 BVJHCIDFWJRFPP-UHFFFAOYSA-N 0.000 claims description 4
- IIOJQNGORCNUOX-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(4-fluorophenyl)-2-piperazin-1-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCNCC2)N=C1C(C=C1)=CC=C1F)=O IIOJQNGORCNUOX-UHFFFAOYSA-N 0.000 claims description 4
- DTVLBPGGPRVSCW-UHFFFAOYSA-N CC(C=C(C=C1)F)=C1C1=NC(N2CCN(C)CC2)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 Chemical compound CC(C=C(C=C1)F)=C1C1=NC(N2CCN(C)CC2)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 DTVLBPGGPRVSCW-UHFFFAOYSA-N 0.000 claims description 4
- JNMROCUGLWGMIW-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C(C(C(C=CC=C1)=C1Cl)=N1)=CN=C1OCCN1CCOCC1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C(C(C(C=CC=C1)=C1Cl)=N1)=CN=C1OCCN1CCOCC1)=O JNMROCUGLWGMIW-UHFFFAOYSA-N 0.000 claims description 4
- PSSFAHZSJPCROM-NJJJQDLFSA-N C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Br)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Br)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PSSFAHZSJPCROM-NJJJQDLFSA-N 0.000 claims description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 4
- MKCGSOVKTLWSKE-OEEJBDNKSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 2-[(3S,5R)-3,5-dimethylpiperazin-1-yl]-4-(2-methylphenyl)pyrimidine-5-carboxylic acid Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C2=C(C)C=CC=C2)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 MKCGSOVKTLWSKE-OEEJBDNKSA-N 0.000 claims description 3
- ZDYLPLRAVFLWMR-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-bromophenyl)-2-(4-methylpiperazin-1-yl)pyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Br)=N1 ZDYLPLRAVFLWMR-UHFFFAOYSA-N 0.000 claims description 3
- BGYJRRLRFQPIFM-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-chlorophenyl)-2-morpholin-4-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C(C=CC=C1)=C1Cl)=O BGYJRRLRFQPIFM-UHFFFAOYSA-N 0.000 claims description 3
- JKVYAARROHIHGR-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(4-fluoro-2-methylphenyl)-2-piperazin-1-ylpyrimidine-5-carboxylic acid Chemical compound CC(C=C(C=C1)F)=C1C1=NC(N2CCNCC2)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 JKVYAARROHIHGR-UHFFFAOYSA-N 0.000 claims description 3
- PIXZRHCAIVDFPD-UHFFFAOYSA-N 4-[2-[3,5-bis(trifluoromethyl)phenyl]ethyl]-2-[2-(dimethylamino)ethoxy]-6-(2-methylphenyl)pyrimidine-5-carboxylic acid Chemical compound FC(C=1C=C(CCC2=C(C(=NC(=N2)OCCN(C)C)C2=C(C=CC=C2)C)C(=O)O)C=C(C1)C(F)(F)F)(F)F PIXZRHCAIVDFPD-UHFFFAOYSA-N 0.000 claims description 3
- JECRSKVHMLNHRD-UHFFFAOYSA-N 4-[2-[3,5-bis(trifluoromethyl)phenyl]ethyl]-2-[3-(dimethylamino)propoxy]-6-(2-methylphenyl)pyrimidine-5-carboxylic acid Chemical compound FC(C=1C=C(CCC2=C(C(=NC(=N2)OCCCN(C)C)C2=C(C=CC=C2)C)C(=O)O)C=C(C1)C(F)(F)F)(F)F JECRSKVHMLNHRD-UHFFFAOYSA-N 0.000 claims description 3
- JTDULDYQHVULRE-UHFFFAOYSA-N 4-[[3,5-bis(trifluoromethyl)phenyl]methyl]-N-methyl-6-naphthalen-1-yl-2-piperazin-1-ylpyrimidine-5-carboxamide Chemical compound CNC(=O)C=1C(=NC(=NC1CC1=CC(=CC(=C1)C(F)(F)F)C(F)(F)F)N1CCNCC1)C1=CC=CC2=CC=CC=C12 JTDULDYQHVULRE-UHFFFAOYSA-N 0.000 claims description 3
- JDYRMDOJQIJKRP-UHFFFAOYSA-N CC(C=C(C=C1)F)=C1C1=NC(N2CCOCC2)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 Chemical compound CC(C=C(C=C1)F)=C1C1=NC(N2CCOCC2)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 JDYRMDOJQIJKRP-UHFFFAOYSA-N 0.000 claims description 3
- DWZGOJYERXFWSL-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCCOC1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCCOC1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1 DWZGOJYERXFWSL-UHFFFAOYSA-N 0.000 claims description 3
- BZHFMQLNRSPEOP-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCOC1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCOC1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1 BZHFMQLNRSPEOP-UHFFFAOYSA-N 0.000 claims description 3
- KJHAMPAKMHWSKC-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2OC)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2OC)=N1 KJHAMPAKMHWSKC-UHFFFAOYSA-N 0.000 claims description 3
- VMYZUCIVLSPCRR-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C2=CC=CC3=CC=CC=C23)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C2=CC=CC3=CC=CC=C23)=N1 VMYZUCIVLSPCRR-UHFFFAOYSA-N 0.000 claims description 3
- IZXHFBMOXVPZRJ-NJJJQDLFSA-N C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 IZXHFBMOXVPZRJ-NJJJQDLFSA-N 0.000 claims description 3
- LQALIWNGSMSJJA-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-bromophenyl)-2-piperazin-1-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCNCC2)N=C1C(C=CC=C1)=C1Br)=O LQALIWNGSMSJJA-UHFFFAOYSA-N 0.000 claims description 2
- FHUBFGFFZJDYOW-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-chlorophenyl)-2-[2-(dimethylamino)ethylamino]pyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCNC1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1 FHUBFGFFZJDYOW-UHFFFAOYSA-N 0.000 claims description 2
- TYYWRDWBUZAXGW-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-fluorophenyl)-2-(4-methylpiperazin-1-yl)pyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2F)=N1 TYYWRDWBUZAXGW-UHFFFAOYSA-N 0.000 claims description 2
- XBFMATCYYBERSR-UHFFFAOYSA-N 2-[3,5-bis(trifluoromethyl)phenyl]-n,2-dimethyl-n-[4-(2-methylphenyl)-2-(4-methylpiperazin-1-yl)pyrimidin-5-yl]propanamide Chemical compound C=1N=C(N2CCN(C)CC2)N=C(C=2C(=CC=CC=2)C)C=1N(C)C(=O)C(C)(C)C1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XBFMATCYYBERSR-UHFFFAOYSA-N 0.000 claims description 2
- JBXSWUZDCVXEOU-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC(C=CC=C1)=C1C1=NC(N2CCNCC2)=NC=C1C(O)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC(C=CC=C1)=C1C1=NC(N2CCNCC2)=NC=C1C(O)=O JBXSWUZDCVXEOU-UHFFFAOYSA-N 0.000 claims description 2
- ZALFKJBMSFZSRC-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC(C=CC=C1)=C1C1=NC(N2CCOCC2)=NC=C1C(O)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC(C=CC=C1)=C1C1=NC(N2CCOCC2)=NC=C1C(O)=O ZALFKJBMSFZSRC-UHFFFAOYSA-N 0.000 claims description 2
- QCTVHFNOHZEZNV-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C(C=CC=C1)=C1Br)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C(C=CC=C1)=C1Br)=O QCTVHFNOHZEZNV-UHFFFAOYSA-N 0.000 claims description 2
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims description 2
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 2
- 150000002431 hydrogen Chemical class 0.000 claims description 2
- 125000004312 morpholin-2-yl group Chemical group [H]N1C([H])([H])C([H])([H])OC([H])(*)C1([H])[H] 0.000 claims description 2
- 239000002464 receptor antagonist Substances 0.000 claims description 2
- 229940044551 receptor antagonist Drugs 0.000 claims description 2
- 229940126601 medicinal product Drugs 0.000 claims 1
- 239000003814 drug Substances 0.000 abstract description 6
- 102000005962 receptors Human genes 0.000 abstract description 6
- 108020003175 receptors Proteins 0.000 abstract description 6
- 125000003277 amino group Chemical group 0.000 abstract description 4
- 239000005557 antagonist Substances 0.000 abstract description 4
- 206010030113 Oedema Diseases 0.000 abstract description 3
- 239000000126 substance Substances 0.000 abstract description 3
- 208000024827 Alzheimer disease Diseases 0.000 abstract description 2
- 206010019233 Headaches Diseases 0.000 abstract description 2
- 208000037976 chronic inflammation Diseases 0.000 abstract description 2
- 208000037893 chronic inflammatory disorder Diseases 0.000 abstract description 2
- 230000000694 effects Effects 0.000 abstract description 2
- 231100000869 headache Toxicity 0.000 abstract description 2
- 125000005843 halogen group Chemical group 0.000 abstract 3
- 125000004435 hydrogen atom Chemical class [H]* 0.000 abstract 3
- 208000024172 Cardiovascular disease Diseases 0.000 abstract 1
- 208000034189 Sclerosis Diseases 0.000 abstract 1
- 239000000654 additive Substances 0.000 abstract 1
- 125000005189 alkyl hydroxy group Chemical group 0.000 abstract 1
- 230000007721 medicinal effect Effects 0.000 abstract 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 abstract 1
- 239000000460 chlorine Substances 0.000 description 137
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 96
- 239000006260 foam Substances 0.000 description 68
- 239000000243 solution Substances 0.000 description 64
- 239000011541 reaction mixture Substances 0.000 description 57
- 229910004298 SiO 2 Inorganic materials 0.000 description 45
- 238000004587 chromatography analysis Methods 0.000 description 45
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 42
- 239000000284 extract Substances 0.000 description 42
- 239000007787 solid Substances 0.000 description 41
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 40
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 34
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 26
- 239000002904 solvent Substances 0.000 description 26
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 26
- MGJXBDMLVWIYOQ-UHFFFAOYSA-N methylazanide Chemical compound [NH-]C MGJXBDMLVWIYOQ-UHFFFAOYSA-N 0.000 description 25
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 24
- 238000000034 method Methods 0.000 description 24
- 239000012230 colorless oil Substances 0.000 description 21
- 238000001704 evaporation Methods 0.000 description 20
- 230000008020 evaporation Effects 0.000 description 20
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 18
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 18
- 239000007858 starting material Substances 0.000 description 16
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 15
- 239000001530 fumaric acid Substances 0.000 description 15
- PVOAHINGSUIXLS-UHFFFAOYSA-N 1-Methylpiperazine Chemical compound CN1CCNCC1 PVOAHINGSUIXLS-UHFFFAOYSA-N 0.000 description 14
- 239000000203 mixture Substances 0.000 description 14
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 13
- 230000007062 hydrolysis Effects 0.000 description 13
- 238000006460 hydrolysis reaction Methods 0.000 description 13
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 12
- 239000003921 oil Substances 0.000 description 12
- 235000019198 oils Nutrition 0.000 description 12
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 11
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 11
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 10
- 239000011734 sodium Substances 0.000 description 10
- IFNWESYYDINUHV-OLQVQODUSA-N (2s,6r)-2,6-dimethylpiperazine Chemical compound C[C@H]1CNC[C@@H](C)N1 IFNWESYYDINUHV-OLQVQODUSA-N 0.000 description 9
- GSRJDEKCRIHKCJ-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-chlorophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Cl)=N1)(=O)=O GSRJDEKCRIHKCJ-UHFFFAOYSA-N 0.000 description 9
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 8
- 229920006395 saturated elastomer Polymers 0.000 description 8
- 239000000829 suppository Substances 0.000 description 8
- NKSUKPZGUDDPAH-UHFFFAOYSA-N 4-(2-methylphenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)C)=N1 NKSUKPZGUDDPAH-UHFFFAOYSA-N 0.000 description 7
- DHVHORCFFOSRBP-UHFFFAOYSA-N [3,5-bis(trifluoromethyl)phenyl]methanamine Chemical compound NCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 DHVHORCFFOSRBP-UHFFFAOYSA-N 0.000 description 7
- 239000008346 aqueous phase Substances 0.000 description 7
- 238000000605 extraction Methods 0.000 description 7
- QDZOEBFLNHCSSF-PFFBOGFISA-N (2S)-2-[[(2R)-2-[[(2S)-1-[(2S)-6-amino-2-[[(2S)-1-[(2R)-2-amino-5-carbamimidamidopentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-N-[(2R)-1-[[(2S)-1-[[(2R)-1-[[(2S)-1-[[(2S)-1-amino-4-methyl-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]pentanediamide Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](N)CCCNC(N)=N)C1=CC=CC=C1 QDZOEBFLNHCSSF-PFFBOGFISA-N 0.000 description 6
- AZUYLZMQTIKGSC-UHFFFAOYSA-N 1-[6-[4-(5-chloro-6-methyl-1H-indazol-4-yl)-5-methyl-3-(1-methylindazol-5-yl)pyrazol-1-yl]-2-azaspiro[3.3]heptan-2-yl]prop-2-en-1-one Chemical compound ClC=1C(=C2C=NNC2=CC=1C)C=1C(=NN(C=1C)C1CC2(CN(C2)C(C=C)=O)C1)C=1C=C2C=NN(C2=CC=1)C AZUYLZMQTIKGSC-UHFFFAOYSA-N 0.000 description 6
- SHQNWDPLIZGIEH-UHFFFAOYSA-N 2-[3,5-bis(trifluoromethyl)phenyl]-n,2-dimethyl-n-[4-(2-methylphenyl)-2-methylsulfonylpyrimidin-5-yl]propanamide Chemical compound C=1N=C(S(C)(=O)=O)N=C(C=2C(=CC=CC=2)C)C=1N(C)C(=O)C(C)(C)C1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 SHQNWDPLIZGIEH-UHFFFAOYSA-N 0.000 description 6
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 6
- 102100024304 Protachykinin-1 Human genes 0.000 description 6
- 101800003906 Substance P Proteins 0.000 description 6
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- WGQKYBSKWIADBV-UHFFFAOYSA-N benzylamine Chemical compound NCC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 description 6
- 239000002775 capsule Substances 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- NNBBQNFHCVVQHZ-UHFFFAOYSA-N methyl carbamimidothioate;sulfuric acid Chemical compound CSC(N)=N.OS(O)(=O)=O NNBBQNFHCVVQHZ-UHFFFAOYSA-N 0.000 description 6
- AZLYFFWKOFXIRJ-UHFFFAOYSA-N 1-(3,5-dimethoxyphenyl)-n-methylmethanamine Chemical compound CNCC1=CC(OC)=CC(OC)=C1 AZLYFFWKOFXIRJ-UHFFFAOYSA-N 0.000 description 5
- YOVLXKWFFDOLNW-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 2-methylsulfonyl-4-phenylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1)(=O)=O YOVLXKWFFDOLNW-UHFFFAOYSA-N 0.000 description 5
- UTQUBHPEQKBVBH-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-methylphenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CC(C=CC=C1)=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 UTQUBHPEQKBVBH-UHFFFAOYSA-N 0.000 description 5
- BNOPWFKTVOBQOS-UHFFFAOYSA-N 4-(2-bromophenyl)-2-methylpyrimidine-5-carboxylic acid Chemical compound CC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)Br)=N1 BNOPWFKTVOBQOS-UHFFFAOYSA-N 0.000 description 5
- BZJBDVRNEZTSAD-UHFFFAOYSA-N CC1=CC(CNC)=CC(C)=C1.CC(C=CC=C1)=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O Chemical compound CC1=CC(CNC)=CC(C)=C1.CC(C=CC=C1)=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O BZJBDVRNEZTSAD-UHFFFAOYSA-N 0.000 description 5
- 239000012071 phase Substances 0.000 description 5
- 125000001424 substituent group Chemical group 0.000 description 5
- SPEUIVXLLWOEMJ-UHFFFAOYSA-N 1,1-dimethoxyethane Chemical compound COC(C)OC SPEUIVXLLWOEMJ-UHFFFAOYSA-N 0.000 description 4
- VMQKIUGZHROWEY-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-bromophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Br)=N1 VMQKIUGZHROWEY-UHFFFAOYSA-N 0.000 description 4
- IIGAYNJDPHYYBI-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-fluorophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2F)=N1)(=O)=O IIGAYNJDPHYYBI-UHFFFAOYSA-N 0.000 description 4
- BSBLAEPWEJSURU-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-methoxyphenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC(C=CC=C1)=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O BSBLAEPWEJSURU-UHFFFAOYSA-N 0.000 description 4
- 125000006276 2-bromophenyl group Chemical group [H]C1=C([H])C(Br)=C(*)C([H])=C1[H] 0.000 description 4
- NVVTVOBHULVUCV-UHFFFAOYSA-N 4-(2-bromophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)Br)=N1 NVVTVOBHULVUCV-UHFFFAOYSA-N 0.000 description 4
- FEAPOOBZZBTHRU-UHFFFAOYSA-N 4-(2-methoxyphenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound COC1=CC=CC=C1C1=NC(SC)=NC=C1C(O)=O FEAPOOBZZBTHRU-UHFFFAOYSA-N 0.000 description 4
- HJQPYBFDSLUMMT-UHFFFAOYSA-N 4-(4-fluoro-2-methylphenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C(=CC(F)=CC=2)C)=N1 HJQPYBFDSLUMMT-UHFFFAOYSA-N 0.000 description 4
- HIYWULYJQJFPJZ-UHFFFAOYSA-N 4-phenyl-2-propylpyrimidine-5-carboxylic acid Chemical compound CCCC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 HIYWULYJQJFPJZ-UHFFFAOYSA-N 0.000 description 4
- HNMSDDRXJPPUBG-UHFFFAOYSA-N CC(C=CC=C1)=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O.CNCC1=CC(OC)=CC(OC)=C1 Chemical compound CC(C=CC=C1)=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O.CNCC1=CC(OC)=CC(OC)=C1 HNMSDDRXJPPUBG-UHFFFAOYSA-N 0.000 description 4
- HUNYRPRXAHODNE-UHFFFAOYSA-N CCC(N(C)C)=C(C(O)=O)C(=O)C1=CC=CC=C1 Chemical compound CCC(N(C)C)=C(C(O)=O)C(=O)C1=CC=CC=C1 HUNYRPRXAHODNE-UHFFFAOYSA-N 0.000 description 4
- UGKHYIQFHOZMSE-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C(C=C2)=CC=C2F)=N1)(=O)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C(C=C2)=CC=C2F)=N1)(=O)=O UGKHYIQFHOZMSE-UHFFFAOYSA-N 0.000 description 4
- 229920002261 Corn starch Polymers 0.000 description 4
- 239000001828 Gelatine Substances 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- 206010047700 Vomiting Diseases 0.000 description 4
- 239000008120 corn starch Substances 0.000 description 4
- NPRYIRPXKLDSKM-UHFFFAOYSA-N ethyl 2-(2-bromobenzoyl)-3-(dimethylamino)prop-2-enoate Chemical compound CCOC(=O)C(=CN(C)C)C(=O)C1=CC=CC=C1Br NPRYIRPXKLDSKM-UHFFFAOYSA-N 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 229920000159 gelatin Polymers 0.000 description 4
- 235000019322 gelatine Nutrition 0.000 description 4
- WFKAJVHLWXSISD-UHFFFAOYSA-N isobutyramide Chemical compound CC(C)C(N)=O WFKAJVHLWXSISD-UHFFFAOYSA-N 0.000 description 4
- 239000008101 lactose Substances 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- DILRJUIACXKSQE-UHFFFAOYSA-N n',n'-dimethylethane-1,2-diamine Chemical compound CN(C)CCN DILRJUIACXKSQE-UHFFFAOYSA-N 0.000 description 4
- 239000012074 organic phase Substances 0.000 description 4
- 229920005862 polyol Polymers 0.000 description 4
- 150000003077 polyols Chemical class 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- CEYUUWOJAANHPT-IWKKHLOMSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 2-[(3S,5R)-3,5-dimethylpiperazin-1-yl]-4-(4-fluoro-2-methylphenyl)pyrimidine-5-carboxylic acid Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=C2)=C(C)C=C2F)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 CEYUUWOJAANHPT-IWKKHLOMSA-N 0.000 description 3
- UHYRUIDFKYAJKZ-KAECKJJSSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 2-[(3S,5R)-3,5-dimethylpiperazin-1-yl]-4-naphthalen-1-ylpyrimidine-5-carboxylic acid Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C2=CC=CC3=CC=CC=C23)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 UHYRUIDFKYAJKZ-KAECKJJSSA-N 0.000 description 3
- NNCXVDJITFRSRU-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-chloro-4-fluorophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C(C=CC(F)=C2)=C2Cl)=N1)(=O)=O NNCXVDJITFRSRU-UHFFFAOYSA-N 0.000 description 3
- BYASWSKHYBWSPT-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(2-chloro-4-fluorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C=2C(=CC(F)=CC=2)Cl)=N1 BYASWSKHYBWSPT-UHFFFAOYSA-N 0.000 description 3
- COVZWBRTRRMGOB-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(2-fluorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)F)=N1 COVZWBRTRRMGOB-UHFFFAOYSA-N 0.000 description 3
- ASXKJNKHKBXWJD-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(4-fluorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C=2C=CC(F)=CC=2)=N1 ASXKJNKHKBXWJD-UHFFFAOYSA-N 0.000 description 3
- IQTXQTMYWOVILY-UHFFFAOYSA-N 2-(2-amino-2-oxoethyl)-4-phenylpyrimidine-5-carboxylic acid Chemical compound NC(=O)CC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 IQTXQTMYWOVILY-UHFFFAOYSA-N 0.000 description 3
- PBKGYWLWIJLDGZ-UHFFFAOYSA-N 2-(dimethylamino)propan-1-ol Chemical compound OCC(C)N(C)C PBKGYWLWIJLDGZ-UHFFFAOYSA-N 0.000 description 3
- TUSWRNPBPRJMRI-UHFFFAOYSA-N 2-(hydroxymethyl)-4-phenylpyrimidine-5-carboxylic acid Chemical compound OCC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 TUSWRNPBPRJMRI-UHFFFAOYSA-N 0.000 description 3
- KKFDCBRMNNSAAW-UHFFFAOYSA-N 2-(morpholin-4-yl)ethanol Chemical compound OCCN1CCOCC1 KKFDCBRMNNSAAW-UHFFFAOYSA-N 0.000 description 3
- VEQHDUGFRKAKLY-UHFFFAOYSA-N 2-methyl-4-naphthalen-1-ylpyrimidine-5-carboxylic acid Chemical compound CC1=NC=C(C(O)=O)C(C=2C3=CC=CC=C3C=CC=2)=N1 VEQHDUGFRKAKLY-UHFFFAOYSA-N 0.000 description 3
- XKJAQESOTNACHT-UHFFFAOYSA-N 2-methyl-4-phenylpyrimidine-5-carboxylic acid Chemical compound CC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 XKJAQESOTNACHT-UHFFFAOYSA-N 0.000 description 3
- MFOXORMYLUTTHZ-UHFFFAOYSA-N 2-methylsulfanyl-4-naphthalen-1-ylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C3=CC=CC=C3C=CC=2)=N1 MFOXORMYLUTTHZ-UHFFFAOYSA-N 0.000 description 3
- ZMVSTBFHLHZTBU-UHFFFAOYSA-N 4-(2-chloro-4-fluorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C(=CC(F)=CC=2)Cl)=N1 ZMVSTBFHLHZTBU-UHFFFAOYSA-N 0.000 description 3
- RTRULEZMOXHVGN-UHFFFAOYSA-N 4-(2-chloro-4-fluorophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CS(=O)(=O)C1=NC=C(C(O)=O)C(C=2C(=CC(F)=CC=2)Cl)=N1 RTRULEZMOXHVGN-UHFFFAOYSA-N 0.000 description 3
- VUSOFDSPDSYDII-UHFFFAOYSA-N 4-(2-chlorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)Cl)=N1 VUSOFDSPDSYDII-UHFFFAOYSA-N 0.000 description 3
- ZCNFTQVBUYFKHA-UHFFFAOYSA-N 4-(2-fluorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)F)=N1 ZCNFTQVBUYFKHA-UHFFFAOYSA-N 0.000 description 3
- LEBDEKQXWYXPEM-UHFFFAOYSA-N 4-phenyl-2-pyridin-3-ylpyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=C(C=2C=NC=CC=2)N=C1C1=CC=CC=C1 LEBDEKQXWYXPEM-UHFFFAOYSA-N 0.000 description 3
- PUEIKOCKEZXCRS-UHFFFAOYSA-N 4-phenyl-2-pyridin-4-ylpyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=C(C=2C=CN=CC=2)N=C1C1=CC=CC=C1 PUEIKOCKEZXCRS-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- VHPHBZPBFDNCPN-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C2=CC=CC3=CC=CC=C23)=N1)(=O)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C2=CC=CC3=CC=CC=C23)=N1)(=O)=O VHPHBZPBFDNCPN-UHFFFAOYSA-N 0.000 description 3
- QRRFOFBRNVLWRI-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 QRRFOFBRNVLWRI-UHFFFAOYSA-N 0.000 description 3
- NSMDICPFNSIUFP-NJJJQDLFSA-N C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2F)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2F)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 NSMDICPFNSIUFP-NJJJQDLFSA-N 0.000 description 3
- YVKIVDUZGQEHIT-IWKKHLOMSA-N C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2OC)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2OC)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 YVKIVDUZGQEHIT-IWKKHLOMSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- 102100021260 Galactosylgalactosylxylosylprotein 3-beta-glucuronosyltransferase 1 Human genes 0.000 description 3
- 101000894906 Homo sapiens Galactosylgalactosylxylosylprotein 3-beta-glucuronosyltransferase 1 Proteins 0.000 description 3
- 102000003141 Tachykinin Human genes 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 208000006673 asthma Diseases 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000008298 dragée Substances 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- KUPUOWGVCQOFJD-UHFFFAOYSA-N ethyl 4-(2-bromophenyl)-2-methylsulfanylpyrimidine-5-carboxylate Chemical compound CCOC(=O)C1=CN=C(SC)N=C1C1=CC=CC=C1Br KUPUOWGVCQOFJD-UHFFFAOYSA-N 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 125000002883 imidazolyl group Chemical group 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 125000003386 piperidinyl group Chemical group 0.000 description 3
- 108060008037 tachykinin Proteins 0.000 description 3
- 239000002462 tachykinin receptor antagonist Substances 0.000 description 3
- 239000000454 talc Substances 0.000 description 3
- 229910052623 talc Inorganic materials 0.000 description 3
- 230000008673 vomiting Effects 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 239000001993 wax Substances 0.000 description 3
- ICIJWOWQUHHETJ-UHFFFAOYSA-N (3,5-dichlorophenyl)methanamine Chemical compound NCC1=CC(Cl)=CC(Cl)=C1 ICIJWOWQUHHETJ-UHFFFAOYSA-N 0.000 description 2
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 2
- CTPLAFFXICBXRD-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-bromophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CS(C1=NC=C(C(O)=O)C(C(C=CC=C2)=C2Br)=N1)(=O)=O CTPLAFFXICBXRD-UHFFFAOYSA-N 0.000 description 2
- RXPIPSKVLSTPFS-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;2-methylsulfanyl-4-naphthalen-1-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C=2C3=CC=CC=C3C=CC=2)=N1 RXPIPSKVLSTPFS-UHFFFAOYSA-N 0.000 description 2
- QZJHVDYEFWCAPE-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(2-methoxyphenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC1=CC=CC=C1C1=NC(SC)=NC=C1C(O)=O QZJHVDYEFWCAPE-UHFFFAOYSA-N 0.000 description 2
- JQWMKWALTYVHQA-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(2-methylphenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)C)=N1 JQWMKWALTYVHQA-UHFFFAOYSA-N 0.000 description 2
- KCSVRDQYSXWGCF-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-phenyl-2-pyridin-3-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(=O)C1=CN=C(C=2C=NC=CC=2)N=C1C1=CC=CC=C1 KCSVRDQYSXWGCF-UHFFFAOYSA-N 0.000 description 2
- RSTIZKRDWDDGFJ-UHFFFAOYSA-N 2,4-diphenylpyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=C(C=2C=CC=CC=2)N=C1C1=CC=CC=C1 RSTIZKRDWDDGFJ-UHFFFAOYSA-N 0.000 description 2
- BZCYSRXYPDDTCX-UHFFFAOYSA-N 2-(2-amino-2-oxoethyl)-4-phenylpyrimidine-5-carboxylic acid;1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.NC(=O)CC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 BZCYSRXYPDDTCX-UHFFFAOYSA-N 0.000 description 2
- SFEVQUPISPQHOG-UHFFFAOYSA-N 2-[3,5-bis(trifluoromethyl)phenyl]-2-methylpropanoyl chloride Chemical compound ClC(=O)C(C)(C)C1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 SFEVQUPISPQHOG-UHFFFAOYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- 125000003635 2-dimethylaminoethoxy group Chemical group [H]C([H])([H])N(C([H])([H])[H])C([H])([H])C([H])([H])O* 0.000 description 2
- PLFZSJNZKWDUAO-UHFFFAOYSA-N 4-(2-methoxyphenyl)-2-methylpyrimidine-5-carboxylic acid Chemical compound COC1=CC=CC=C1C1=NC(C)=NC=C1C(O)=O PLFZSJNZKWDUAO-UHFFFAOYSA-N 0.000 description 2
- BIEKVVDMVHVHBM-UHFFFAOYSA-N 4-(2-methoxyphenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound COC1=CC=CC=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O BIEKVVDMVHVHBM-UHFFFAOYSA-N 0.000 description 2
- 125000004195 4-methylpiperazin-1-yl group Chemical group [H]C([H])([H])N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 description 2
- 208000019901 Anxiety disease Diseases 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- ZORNPIYFJMQQAS-UHFFFAOYSA-N CC(C=CC=C1)=C1C1=NC(SC)=NC=C1C(O)=O.CNCC1=CC(OC)=CC(OC)=C1 Chemical compound CC(C=CC=C1)=C1C1=NC(SC)=NC=C1C(O)=O.CNCC1=CC(OC)=CC(OC)=C1 ZORNPIYFJMQQAS-UHFFFAOYSA-N 0.000 description 2
- BEABGZKKIVOHBN-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.N#CCC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.N#CCC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 BEABGZKKIVOHBN-UHFFFAOYSA-N 0.000 description 2
- QMGSPECNDHJHPL-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCNCC2)N=C1C(C=CC(F)=C1)=C1Cl)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCNCC2)N=C1C(C=CC(F)=C1)=C1Cl)=O QMGSPECNDHJHPL-UHFFFAOYSA-N 0.000 description 2
- ZCVQOJFCWYINMM-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C(C=C1)=CC=C1F)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C(C=C1)=CC=C1F)=O ZCVQOJFCWYINMM-UHFFFAOYSA-N 0.000 description 2
- SFYCXNRGKZZOAK-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(NCC2=CC=CC=C2)N=C1C1=CC=CC=C1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(NCC2=CC=CC=C2)N=C1C1=CC=CC=C1)=O SFYCXNRGKZZOAK-UHFFFAOYSA-N 0.000 description 2
- XWKXVLPMKUNTKT-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=CN=C1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=CN=C1)=O XWKXVLPMKUNTKT-UHFFFAOYSA-N 0.000 description 2
- YWKOPRWZSSBHFR-NJJJQDLFSA-N C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=C2)=CC=C2F)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 Chemical compound C[C@H](C1)N[C@@H](C)CN1C1=NC=C(C(O)=O)C(C(C=C2)=CC=C2F)=N1.CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 YWKOPRWZSSBHFR-NJJJQDLFSA-N 0.000 description 2
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- 208000019695 Migraine disease Diseases 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 230000036506 anxiety Effects 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- YBFKACALUIUGHN-BENRWUELSA-N ethyl (z)-2-benzoyl-3-(dimethylamino)prop-2-enoate Chemical compound CCOC(=O)C(=C/N(C)C)\C(=O)C1=CC=CC=C1 YBFKACALUIUGHN-BENRWUELSA-N 0.000 description 2
- KQUNJRBKUQPTPM-UHFFFAOYSA-N ethyl 4-(2-bromophenyl)-2-methylpyrimidine-5-carboxylate Chemical compound CCOC(=O)C1=CN=C(C)N=C1C1=CC=CC=C1Br KQUNJRBKUQPTPM-UHFFFAOYSA-N 0.000 description 2
- 239000003925 fat Substances 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 229940047889 isobutyramide Drugs 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 229940098779 methanesulfonic acid Drugs 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- CPLPFKDTCYDKNE-UHFFFAOYSA-N methylthiourea;sulfuric acid Chemical compound CNC(S)=N.OS(O)(=O)=O CPLPFKDTCYDKNE-UHFFFAOYSA-N 0.000 description 2
- 206010027599 migraine Diseases 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- BQJCRHHNABKAKU-KBQPJGBKSA-N morphine Chemical compound O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O BQJCRHHNABKAKU-KBQPJGBKSA-N 0.000 description 2
- KPXYQZCELNPZDP-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-2-methyl-4-phenylpyrimidine-5-carboxamide Chemical compound C=1C=CC=CC=1C1=NC(C)=NC=C1C(=O)NCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 KPXYQZCELNPZDP-UHFFFAOYSA-N 0.000 description 2
- SOAYVVGHTCQLDR-UHFFFAOYSA-N n-methyl-4-(2-methylphenyl)-2-methylsulfanylpyrimidin-5-amine Chemical compound CNC1=CN=C(SC)N=C1C1=CC=CC=C1C SOAYVVGHTCQLDR-UHFFFAOYSA-N 0.000 description 2
- 239000002742 neurokinin 1 receptor antagonist Substances 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 230000002093 peripheral effect Effects 0.000 description 2
- 238000011321 prophylaxis Methods 0.000 description 2
- 206010039073 rheumatoid arthritis Diseases 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000012312 sodium hydride Substances 0.000 description 2
- 229910000104 sodium hydride Inorganic materials 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- ADNPLDHMAVUMIW-CUZNLEPHSA-N substance P Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 ADNPLDHMAVUMIW-CUZNLEPHSA-N 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- UKFIWKOQJGKTTQ-UHFFFAOYSA-N tert-butyl n-methyl-n-[4-(2-methylphenyl)-2-methylsulfanylpyrimidin-5-yl]carbamate Chemical compound CSC1=NC=C(N(C)C(=O)OC(C)(C)C)C(C=2C(=CC=CC=2)C)=N1 UKFIWKOQJGKTTQ-UHFFFAOYSA-N 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- QAEDZJGFFMLHHQ-UHFFFAOYSA-N trifluoroacetic anhydride Chemical compound FC(F)(F)C(=O)OC(=O)C(F)(F)F QAEDZJGFFMLHHQ-UHFFFAOYSA-N 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000008158 vegetable oil Substances 0.000 description 2
- VCGRFBXVSFAGGA-UHFFFAOYSA-N (1,1-dioxo-1,4-thiazinan-4-yl)-[6-[[3-(4-fluorophenyl)-5-methyl-1,2-oxazol-4-yl]methoxy]pyridin-3-yl]methanone Chemical compound CC=1ON=C(C=2C=CC(F)=CC=2)C=1COC(N=C1)=CC=C1C(=O)N1CCS(=O)(=O)CC1 VCGRFBXVSFAGGA-UHFFFAOYSA-N 0.000 description 1
- OXRSCXFOUBLJAR-TYYBGVCCSA-N (e)-but-2-enedioic acid;methanamine Chemical compound NC.OC(=O)\C=C\C(O)=O OXRSCXFOUBLJAR-TYYBGVCCSA-N 0.000 description 1
- FPCVTUWORJJFMX-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 2-[(dimethylamino)methyl]-4-phenylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 FPCVTUWORJJFMX-UHFFFAOYSA-N 0.000 description 1
- YRGCIHJSEOIAEY-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 2-[2-(dimethylamino)ethylamino]-4-phenylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCNC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 YRGCIHJSEOIAEY-UHFFFAOYSA-N 0.000 description 1
- MIPGYMHJXMQVEN-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 2-morpholin-4-yl-4-naphthalen-1-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C1=CC=CC2=CC=CC=C12)=O MIPGYMHJXMQVEN-UHFFFAOYSA-N 0.000 description 1
- DECYEHLXEWALPW-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-(2-chloro-4-fluorophenyl)-2-[2-(dimethylamino)ethoxy]pyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCOC1=NC=C(C(O)=O)C(C(C=CC(F)=C2)=C2Cl)=N1 DECYEHLXEWALPW-UHFFFAOYSA-N 0.000 description 1
- OFPNYZVNRFSGJN-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-N-methylmethanamine 4-phenyl-2-piperidin-1-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCCCC2)N=C1C1=CC=CC=C1)=O OFPNYZVNRFSGJN-UHFFFAOYSA-N 0.000 description 1
- GWCWGJHOSMRPAP-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;2-(hydroxymethyl)-4-phenylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OCC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 GWCWGJHOSMRPAP-UHFFFAOYSA-N 0.000 description 1
- RUKCRHZQVHHWRX-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(2-chlorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)Cl)=N1 RUKCRHZQVHHWRX-UHFFFAOYSA-N 0.000 description 1
- ZOMAVYWVKSOQST-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(2-methoxyphenyl)-2-methylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC1=CC=CC=C1C1=NC(C)=NC=C1C(O)=O ZOMAVYWVKSOQST-UHFFFAOYSA-N 0.000 description 1
- VVIRHEXQYZMVTD-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-(4-fluoro-2-methylphenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CSC1=NC=C(C(O)=O)C(C=2C(=CC(F)=CC=2)C)=N1 VVIRHEXQYZMVTD-UHFFFAOYSA-N 0.000 description 1
- QJGBSOXOADFHEJ-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-methylmethanamine;4-phenyl-2-pyridin-4-ylpyrimidine-5-carboxylic acid Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(=O)C1=CN=C(C=2C=CN=CC=2)N=C1C1=CC=CC=C1 QJGBSOXOADFHEJ-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- JWFZHQMWTFORNI-UHFFFAOYSA-N 2-(dimethylamino)ethanol;2-[2-(dimethylamino)ethoxy]-4-(2-methylphenyl)pyrimidine-5-carboxylic acid Chemical compound CN(C)CCO.CN(C)CCOC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)C)=N1 JWFZHQMWTFORNI-UHFFFAOYSA-N 0.000 description 1
- LXNPBFUTFDHVRV-UHFFFAOYSA-N 2-(dimethylamino)propan-1-ol;2-[3-(dimethylamino)propoxy]-4-(2-methylphenyl)pyrimidine-5-carboxylic acid Chemical compound OCC(C)N(C)C.CN(C)CCCOC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)C)=N1 LXNPBFUTFDHVRV-UHFFFAOYSA-N 0.000 description 1
- KZTWONRVIPPDKH-UHFFFAOYSA-N 2-(piperidin-1-yl)ethanol Chemical compound OCCN1CCCCC1 KZTWONRVIPPDKH-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- PMJHOUROTORNDR-UHFFFAOYSA-N 2-[(dimethylamino)methyl]-4-phenylpyrimidine-5-carboxylic acid Chemical compound CN(C)CC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 PMJHOUROTORNDR-UHFFFAOYSA-N 0.000 description 1
- XOENZEJNBMXAPM-UHFFFAOYSA-N 2-[3,5-bis(trifluoromethyl)phenyl]-n,2-dimethyl-n-[4-(2-methylphenyl)-2-methylsulfanylpyrimidin-5-yl]propanamide Chemical compound C=1C=CC=C(C)C=1C1=NC(SC)=NC=C1N(C)C(=O)C(C)(C)C1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XOENZEJNBMXAPM-UHFFFAOYSA-N 0.000 description 1
- XAOMDUJHVILFDB-UHFFFAOYSA-N 2-[3,5-bis(trifluoromethyl)phenyl]-n-[2-[2-(dimethylamino)ethylamino]-4-(2-methylphenyl)pyrimidin-5-yl]-n,2-dimethylpropanamide Chemical compound C=1C=CC=C(C)C=1C1=NC(NCCN(C)C)=NC=C1N(C)C(=O)C(C)(C)C1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XAOMDUJHVILFDB-UHFFFAOYSA-N 0.000 description 1
- QJNMFINEIFVNMK-UHFFFAOYSA-N 2-[3,5-bis(trifluoromethyl)phenyl]ethanamine Chemical compound NCCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 QJNMFINEIFVNMK-UHFFFAOYSA-N 0.000 description 1
- 125000004198 2-fluorophenyl group Chemical group [H]C1=C([H])C(F)=C(*)C([H])=C1[H] 0.000 description 1
- YEDUAINPPJYDJZ-UHFFFAOYSA-N 2-hydroxybenzothiazole Chemical compound C1=CC=C2SC(O)=NC2=C1 YEDUAINPPJYDJZ-UHFFFAOYSA-N 0.000 description 1
- DRWDZFNIPARKSG-UHFFFAOYSA-N 2-hydroxyethanimidamide;hydrochloride Chemical compound Cl.NC(=N)CO DRWDZFNIPARKSG-UHFFFAOYSA-N 0.000 description 1
- 125000004204 2-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C(OC([H])([H])[H])C([H])=C1[H] 0.000 description 1
- QBVCXBXAXVWKKZ-UHFFFAOYSA-N 2-methylsulfanyl-4-phenylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 QBVCXBXAXVWKKZ-UHFFFAOYSA-N 0.000 description 1
- HPZQYOJNWLCIQP-UHFFFAOYSA-N 2-methylsulfonyl-4-phenylpyrimidine-5-carboxylic acid Chemical compound CS(=O)(=O)C1=NC=C(C(O)=O)C(C=2C=CC=CC=2)=N1 HPZQYOJNWLCIQP-UHFFFAOYSA-N 0.000 description 1
- LSRCXDOPTMZQRR-UHFFFAOYSA-N 4-(2-bromophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CS(=O)(=O)C1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)Br)=N1 LSRCXDOPTMZQRR-UHFFFAOYSA-N 0.000 description 1
- OENBEWLBGISTRI-UHFFFAOYSA-N 4-(2-chloro-4-fluorophenyl)-2-(4-methylpiperazin-1-yl)pyrimidine-5-carboxylic acid Chemical compound C1CN(C)CCN1C1=NC=C(C(O)=O)C(C=2C(=CC(F)=CC=2)Cl)=N1 OENBEWLBGISTRI-UHFFFAOYSA-N 0.000 description 1
- IZIQTOBBTITUHJ-UHFFFAOYSA-N 4-(2-chlorophenyl)-2-[2-(dimethylamino)ethylamino]pyrimidine-5-carboxylic acid Chemical compound CN(C)CCNC1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)Cl)=N1 IZIQTOBBTITUHJ-UHFFFAOYSA-N 0.000 description 1
- MCPMVPVFYKSFHF-UHFFFAOYSA-N 4-(2-chlorophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CS(=O)(=O)C1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)Cl)=N1 MCPMVPVFYKSFHF-UHFFFAOYSA-N 0.000 description 1
- PVBFPINSJDMBHV-UHFFFAOYSA-N 4-(2-fluorophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CS(=O)(=O)C1=NC=C(C(O)=O)C(C=2C(=CC=CC=2)F)=N1 PVBFPINSJDMBHV-UHFFFAOYSA-N 0.000 description 1
- OKSBIBBAZUCZGS-UHFFFAOYSA-N 4-(2-fluorophenyl)-2-morpholin-4-ylpyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=C(N2CCOCC2)N=C1C1=CC=CC=C1F OKSBIBBAZUCZGS-UHFFFAOYSA-N 0.000 description 1
- KMZVWSCOOIXIMS-UHFFFAOYSA-N 4-(2-fluorophenyl)-2-piperazin-1-ylpyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=C(N2CCNCC2)N=C1C1=CC=CC=C1F KMZVWSCOOIXIMS-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- LYSKWGZOMBCGPQ-UHFFFAOYSA-N 4-(4-fluoro-2-methylphenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CC1=CC(F)=CC=C1C1=NC(S(C)(=O)=O)=NC=C1C(O)=O LYSKWGZOMBCGPQ-UHFFFAOYSA-N 0.000 description 1
- JJKUMNJTGBEJPK-UHFFFAOYSA-N 4-(4-fluorophenyl)-2-methylsulfanylpyrimidine-5-carboxylic acid Chemical compound CSC1=NC=C(C(O)=O)C(C=2C=CC(F)=CC=2)=N1 JJKUMNJTGBEJPK-UHFFFAOYSA-N 0.000 description 1
- WFCGZPUHKBLROQ-UHFFFAOYSA-N 4-(4-fluorophenyl)-2-methylsulfonylpyrimidine-5-carboxylic acid Chemical compound CS(=O)(=O)C1=NC=C(C(O)=O)C(C=2C=CC(F)=CC=2)=N1 WFCGZPUHKBLROQ-UHFFFAOYSA-N 0.000 description 1
- NIFNWTIFGASECQ-UHFFFAOYSA-N 4-(4-fluorophenyl)-2-piperazin-1-ylpyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=C(N2CCNCC2)N=C1C1=CC=C(F)C=C1 NIFNWTIFGASECQ-UHFFFAOYSA-N 0.000 description 1
- KVCQTKNUUQOELD-UHFFFAOYSA-N 4-amino-n-[1-(3-chloro-2-fluoroanilino)-6-methylisoquinolin-5-yl]thieno[3,2-d]pyrimidine-7-carboxamide Chemical compound N=1C=CC2=C(NC(=O)C=3C4=NC=NC(N)=C4SC=3)C(C)=CC=C2C=1NC1=CC=CC(Cl)=C1F KVCQTKNUUQOELD-UHFFFAOYSA-N 0.000 description 1
- PBIYDKXPPWPEPQ-UHFFFAOYSA-N 4-phenyl-2-(2-piperidin-1-ylethoxy)pyrimidine-5-carboxylic acid Chemical compound N1=C(C=2C=CC=CC=2)C(C(=O)O)=CN=C1OCCN1CCCCC1 PBIYDKXPPWPEPQ-UHFFFAOYSA-N 0.000 description 1
- HBWQATCLRHHZOS-UHFFFAOYSA-N 4-phenyl-2-piperidin-1-ylpyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=C(N2CCCCC2)N=C1C1=CC=CC=C1 HBWQATCLRHHZOS-UHFFFAOYSA-N 0.000 description 1
- XVMSFILGAMDHEY-UHFFFAOYSA-N 6-(4-aminophenyl)sulfonylpyridin-3-amine Chemical compound C1=CC(N)=CC=C1S(=O)(=O)C1=CC=C(N)C=N1 XVMSFILGAMDHEY-UHFFFAOYSA-N 0.000 description 1
- CYJRNFFLTBEQSQ-UHFFFAOYSA-N 8-(3-methyl-1-benzothiophen-5-yl)-N-(4-methylsulfonylpyridin-3-yl)quinoxalin-6-amine Chemical compound CS(=O)(=O)C1=C(C=NC=C1)NC=1C=C2N=CC=NC2=C(C=1)C=1C=CC2=C(C(=CS2)C)C=1 CYJRNFFLTBEQSQ-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 206010066091 Bronchial Hyperreactivity Diseases 0.000 description 1
- FMJOMRHRJOHFFC-UHFFFAOYSA-N CC(C=CC=C1)=C1C1=NC(OCCN(C)C)=NC=C1C(O)=O.CNCC1=CC(OC)=CC(OC)=C1 Chemical compound CC(C=CC=C1)=C1C1=NC(OCCN(C)C)=NC=C1C(O)=O.CNCC1=CC(OC)=CC(OC)=C1 FMJOMRHRJOHFFC-UHFFFAOYSA-N 0.000 description 1
- ZIIPEOKTYZSMAW-UHFFFAOYSA-N CC1=CC(CNC)=CC(C)=C1.CC(C=CC=C1)=C1C1=NC(OCCN(C)C)=NC=C1C(O)=O Chemical compound CC1=CC(CNC)=CC(C)=C1.CC(C=CC=C1)=C1C1=NC(OCCN(C)C)=NC=C1C(O)=O ZIIPEOKTYZSMAW-UHFFFAOYSA-N 0.000 description 1
- OKGXFLFAQWOKOI-UHFFFAOYSA-N CCCC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1.CNCC1=CC(Cl)=CC(Cl)=C1 Chemical compound CCCC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1.CNCC1=CC(Cl)=CC(Cl)=C1 OKGXFLFAQWOKOI-UHFFFAOYSA-N 0.000 description 1
- YDBISUQFKZQDOQ-UHFFFAOYSA-N CNC(=O)C=1C(=NC(=NC1)C)C1=CC=CC=C1 Chemical compound CNC(=O)C=1C(=NC(=NC1)C)C1=CC=CC=C1 YDBISUQFKZQDOQ-UHFFFAOYSA-N 0.000 description 1
- WODVBNZUILDKLV-UHFFFAOYSA-N CNC(=O)C=1C(=NC(=NC1)S(=O)(=O)C)C1=C(C=CC=C1)Br Chemical compound CNC(=O)C=1C(=NC(=NC1)S(=O)(=O)C)C1=C(C=CC=C1)Br WODVBNZUILDKLV-UHFFFAOYSA-N 0.000 description 1
- USZGVXXQJRVRMS-UHFFFAOYSA-N CNC(=O)C=1C(=NC(=NC1)S(=O)(=O)C)C1=C(C=CC=C1)F Chemical compound CNC(=O)C=1C(=NC(=NC1)S(=O)(=O)C)C1=C(C=CC=C1)F USZGVXXQJRVRMS-UHFFFAOYSA-N 0.000 description 1
- GLINXTIDWHRGIO-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCCOC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCCOC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 GLINXTIDWHRGIO-UHFFFAOYSA-N 0.000 description 1
- NISHPAWVJZMVEB-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCOC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(C)CCOC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 NISHPAWVJZMVEB-UHFFFAOYSA-N 0.000 description 1
- ZDYSFCNIQDTGRD-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=CC(F)=C2)=C2Cl)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CN(CC1)CCN1C1=NC=C(C(O)=O)C(C(C=CC(F)=C2)=C2Cl)=N1 ZDYSFCNIQDTGRD-UHFFFAOYSA-N 0.000 description 1
- HHUWBGNMXKSYFM-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.COC1=NC=C(C(O)=O)C(C2=CC=CC=C2)=N1 HHUWBGNMXKSYFM-UHFFFAOYSA-N 0.000 description 1
- NDBBAHWZQDDFCK-WLHGVMLRSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(/C=C/C(O)=O)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(/C=C/C(O)=O)=O NDBBAHWZQDDFCK-WLHGVMLRSA-N 0.000 description 1
- PZXJTVLHIQMSCK-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C(C(C1=CC=CC=C1)=N1)=CN=C1OCCN1CCCCC1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C(C(C1=CC=CC=C1)=N1)=CN=C1OCCN1CCCCC1)=O PZXJTVLHIQMSCK-UHFFFAOYSA-N 0.000 description 1
- ZSNXUDKPTLUPAF-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C(C(C1=CC=CC=C1)=N1)=CN=C1OCCN1CCOCC1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C(C(C1=CC=CC=C1)=N1)=CN=C1OCCN1CCOCC1)=O ZSNXUDKPTLUPAF-UHFFFAOYSA-N 0.000 description 1
- JJHWJOOLFKVEIV-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(C2=CC=CC=C2)N=C1C1=CC=CC=C1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(C2=CC=CC=C2)N=C1C1=CC=CC=C1)=O JJHWJOOLFKVEIV-UHFFFAOYSA-N 0.000 description 1
- KAMOVYPDVOPEPM-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(CN2C=NC=C2)N=C1C1=CC=CC=C1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(CN2C=NC=C2)N=C1C1=CC=CC=C1)=O KAMOVYPDVOPEPM-UHFFFAOYSA-N 0.000 description 1
- MRTJLHHGZRVYDJ-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(CN2CCOCC2)N=C1C1=CC=CC=C1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(CN2CCOCC2)N=C1C1=CC=CC=C1)=O MRTJLHHGZRVYDJ-UHFFFAOYSA-N 0.000 description 1
- POTNQHDFIUHKBQ-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCNCC2)N=C1C1=CC=CC=C1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCNCC2)N=C1C1=CC=CC=C1)=O POTNQHDFIUHKBQ-UHFFFAOYSA-N 0.000 description 1
- ZKBOLCPLGBPKEO-UHFFFAOYSA-N CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C1=CC=CC=C1)=O Chemical compound CNCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.OC(C1=CN=C(N2CCOCC2)N=C1C1=CC=CC=C1)=O ZKBOLCPLGBPKEO-UHFFFAOYSA-N 0.000 description 1
- PNGSXPGKCABVAB-UHFFFAOYSA-N CNCC1=CC(Cl)=CC(Cl)=C1.OC(C1=CN=C(C2=CC=CC=C2)N=C1C1=CC=CC=C1)=O Chemical compound CNCC1=CC(Cl)=CC(Cl)=C1.OC(C1=CN=C(C2=CC=CC=C2)N=C1C1=CC=CC=C1)=O PNGSXPGKCABVAB-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- 206010011971 Decreased interest Diseases 0.000 description 1
- 206010012374 Depressed mood Diseases 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 208000020564 Eye injury Diseases 0.000 description 1
- CFCWEKYPSDVMSW-UHFFFAOYSA-N FC(C=1C=C(CNC(=O)C=2C(=NC(=NC2)CCC)C2=CC=CC=C2)C=C(C1)C(F)(F)F)(F)F Chemical compound FC(C=1C=C(CNC(=O)C=2C(=NC(=NC2)CCC)C2=CC=CC=C2)C=C(C1)C(F)(F)F)(F)F CFCWEKYPSDVMSW-UHFFFAOYSA-N 0.000 description 1
- PCRLGNJSHOQOQV-UHFFFAOYSA-N FC(C=1C=C(CNC(=O)C=2C(=NC(=NC=2)C2=CC=CC=C2)C2=CC=CC=C2)C=C(C=1)C(F)(F)F)(F)F Chemical compound FC(C=1C=C(CNC(=O)C=2C(=NC(=NC=2)C2=CC=CC=C2)C2=CC=CC=C2)C=C(C=1)C(F)(F)F)(F)F PCRLGNJSHOQOQV-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 101000600903 Homo sapiens Substance-P receptor Proteins 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical class Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- GDBQQVLCIARPGH-UHFFFAOYSA-N Leupeptin Natural products CC(C)CC(NC(C)=O)C(=O)NC(CC(C)C)C(=O)NC(C=O)CCCN=C(N)N GDBQQVLCIARPGH-UHFFFAOYSA-N 0.000 description 1
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- ZSXGLVDWWRXATF-UHFFFAOYSA-N N,N-dimethylformamide dimethyl acetal Chemical compound COC(OC)N(C)C ZSXGLVDWWRXATF-UHFFFAOYSA-N 0.000 description 1
- AYCPARAPKDAOEN-LJQANCHMSA-N N-[(1S)-2-(dimethylamino)-1-phenylethyl]-6,6-dimethyl-3-[(2-methyl-4-thieno[3,2-d]pyrimidinyl)amino]-1,4-dihydropyrrolo[3,4-c]pyrazole-5-carboxamide Chemical compound C1([C@H](NC(=O)N2C(C=3NN=C(NC=4C=5SC=CC=5N=C(C)N=4)C=3C2)(C)C)CN(C)C)=CC=CC=C1 AYCPARAPKDAOEN-LJQANCHMSA-N 0.000 description 1
- SEIFPCNFFVOGLI-UHFFFAOYSA-N NCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CC1=NC=C(C(O)=O)C(C=2C3=CC=CC=C3C=CC=2)=N1 Chemical compound NCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1.CC1=NC=C(C(O)=O)C(C=2C3=CC=CC=C3C=CC=2)=N1 SEIFPCNFFVOGLI-UHFFFAOYSA-N 0.000 description 1
- 102000028517 Neuropeptide receptor Human genes 0.000 description 1
- 108070000018 Neuropeptide receptor Proteins 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- YTBDTSBAXDBPEI-UHFFFAOYSA-N OCCN1CCNCC1.O1CCOCC1 Chemical compound OCCN1CCNCC1.O1CCOCC1 YTBDTSBAXDBPEI-UHFFFAOYSA-N 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 208000012545 Psychophysiologic disease Diseases 0.000 description 1
- 208000028017 Psychotic disease Diseases 0.000 description 1
- 206010039085 Rhinitis allergic Diseases 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- 102100037346 Substance-P receptor Human genes 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 108010072901 Tachykinin Receptors Proteins 0.000 description 1
- 102000007124 Tachykinin Receptors Human genes 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- PBDNADPCPFXSTD-UHFFFAOYSA-N [4-(2-methylphenyl)-2-methylsulfanylpyrimidin-5-yl]carbamic acid Chemical compound CSC1=NC=C(NC(O)=O)C(C=2C(=CC=CC=2)C)=N1 PBDNADPCPFXSTD-UHFFFAOYSA-N 0.000 description 1
- MKJPBOVLAZADQJ-UHFFFAOYSA-N [amino(pyridin-3-yl)methylidene]azanium;chloride Chemical compound Cl.NC(=N)C1=CC=CN=C1 MKJPBOVLAZADQJ-UHFFFAOYSA-N 0.000 description 1
- IONKMFGAXKCLMI-UHFFFAOYSA-N [amino(pyridin-4-yl)methylidene]azanium;chloride Chemical compound [Cl-].NC(=[NH2+])C1=CC=NC=C1 IONKMFGAXKCLMI-UHFFFAOYSA-N 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 230000036427 bronchial hyperreactivity Effects 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- STYCVEYASXULRN-UHFFFAOYSA-N butanimidamide;hydrochloride Chemical compound [Cl-].CCCC(N)=[NH2+] STYCVEYASXULRN-UHFFFAOYSA-N 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N carbonic acid monoamide Natural products NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 150000001860 citric acid derivatives Chemical class 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000001595 contractor effect Effects 0.000 description 1
- 230000002354 daily effect Effects 0.000 description 1
- 230000003001 depressive effect Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- UXGNZZKBCMGWAZ-UHFFFAOYSA-N dimethylformamide dmf Chemical compound CN(C)C=O.CN(C)C=O UXGNZZKBCMGWAZ-UHFFFAOYSA-N 0.000 description 1
- MKRTXPORKIRPDG-UHFFFAOYSA-N diphenylphosphoryl azide Chemical compound C=1C=CC=CC=1P(=O)(N=[N+]=[N-])C1=CC=CC=C1 MKRTXPORKIRPDG-UHFFFAOYSA-N 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 210000001198 duodenum Anatomy 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- WCQOBLXWLRDEQA-UHFFFAOYSA-N ethanimidamide;hydrochloride Chemical compound Cl.CC(N)=N WCQOBLXWLRDEQA-UHFFFAOYSA-N 0.000 description 1
- YIIQLUXXLPAUOY-UHFFFAOYSA-N ethyl 2-(2-chlorobenzoyl)-3-(dimethylamino)prop-2-enoate Chemical compound CCOC(=O)C(=CN(C)C)C(=O)C1=CC=CC=C1Cl YIIQLUXXLPAUOY-UHFFFAOYSA-N 0.000 description 1
- IFSMFGOJDWUHEW-UHFFFAOYSA-N ethyl 3-(2-bromophenyl)-3-oxopropanoate Chemical compound CCOC(=O)CC(=O)C1=CC=CC=C1Br IFSMFGOJDWUHEW-UHFFFAOYSA-N 0.000 description 1
- KROPYAVVJDXRPH-UHFFFAOYSA-N ethyl 3-(2-methoxyphenyl)-3-oxopropanoate Chemical compound CCOC(=O)CC(=O)C1=CC=CC=C1OC KROPYAVVJDXRPH-UHFFFAOYSA-N 0.000 description 1
- ZDFVUGQHNJIXMZ-UHFFFAOYSA-N ethyl 3-(dimethylamino)-2-(2-methoxybenzoyl)prop-2-enoate Chemical compound CCOC(=O)C(=CN(C)C)C(=O)C1=CC=CC=C1OC ZDFVUGQHNJIXMZ-UHFFFAOYSA-N 0.000 description 1
- WZAWOXRPXQJZTK-UHFFFAOYSA-N ethyl 3-(dimethylamino)-2-(2-methylbenzoyl)prop-2-enoate Chemical compound CCOC(=O)C(=CN(C)C)C(=O)C1=CC=CC=C1C WZAWOXRPXQJZTK-UHFFFAOYSA-N 0.000 description 1
- JFWSFANXHXCJOY-UHFFFAOYSA-N ethyl 3-naphthalen-1-yl-3-oxopropanoate Chemical compound C1=CC=C2C(C(=O)CC(=O)OCC)=CC=CC2=C1 JFWSFANXHXCJOY-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 230000004968 inflammatory condition Effects 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 239000008011 inorganic excipient Substances 0.000 description 1
- 229960004903 invert sugar Drugs 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 210000001630 jejunum Anatomy 0.000 description 1
- GDBQQVLCIARPGH-ULQDDVLXSA-N leupeptin Chemical compound CC(C)C[C@H](NC(C)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C=O)CCCN=C(N)N GDBQQVLCIARPGH-ULQDDVLXSA-N 0.000 description 1
- 108010052968 leupeptin Proteins 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 150000002688 maleic acid derivatives Chemical class 0.000 description 1
- 230000000873 masking effect Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- LULAYUGMBFYYEX-UHFFFAOYSA-N metachloroperbenzoic acid Natural products OC(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-N 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M methanesulfonate group Chemical class CS(=O)(=O)[O-] AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 1
- CWWARWOPSKGELM-SARDKLJWSA-N methyl (2s)-2-[[(2s)-2-[[2-[[(2s)-2-[[(2s)-2-[[(2s)-5-amino-2-[[(2s)-5-amino-2-[[(2s)-1-[(2s)-6-amino-2-[[(2s)-1-[(2s)-2-amino-5-(diaminomethylideneamino)pentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-5 Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)OC)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 CWWARWOPSKGELM-SARDKLJWSA-N 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 229960005181 morphine Drugs 0.000 description 1
- 201000003152 motion sickness Diseases 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- ZSGFHWHAMJFWJO-UHFFFAOYSA-N n-[(3,5-dichlorophenyl)methyl]-2,4-diphenylpyrimidine-5-carboxamide Chemical compound ClC1=CC(Cl)=CC(CNC(=O)C=2C(=NC(=NC=2)C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 ZSGFHWHAMJFWJO-UHFFFAOYSA-N 0.000 description 1
- KYKXQGBXHZMBLD-UHFFFAOYSA-N n-[(3,5-dichlorophenyl)methyl]-2-methyl-4-phenylpyrimidine-5-carboxamide Chemical compound C=1C=CC=CC=1C1=NC(C)=NC=C1C(=O)NCC1=CC(Cl)=CC(Cl)=C1 KYKXQGBXHZMBLD-UHFFFAOYSA-N 0.000 description 1
- WQJKQWVLNIVXGL-UHFFFAOYSA-N n-[(3,5-dichlorophenyl)methyl]-4-phenyl-2-propylpyrimidine-5-carboxamide Chemical compound C=1C=CC=CC=1C1=NC(CCC)=NC=C1C(=O)NCC1=CC(Cl)=CC(Cl)=C1 WQJKQWVLNIVXGL-UHFFFAOYSA-N 0.000 description 1
- VYGVJCRONKWNKR-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-4-(2-bromophenyl)-2-methylpyrimidine-5-carboxamide Chemical compound C=1C=CC=C(Br)C=1C1=NC(C)=NC=C1C(=O)NCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 VYGVJCRONKWNKR-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- WOOWBQQQJXZGIE-UHFFFAOYSA-N n-ethyl-n-propan-2-ylpropan-2-amine Chemical compound CCN(C(C)C)C(C)C.CCN(C(C)C)C(C)C WOOWBQQQJXZGIE-UHFFFAOYSA-N 0.000 description 1
- 210000000653 nervous system Anatomy 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000008012 organic excipient Substances 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- GEAQYIBQNNMPEH-UHFFFAOYSA-N propanediimidamide;hydrochloride Chemical compound Cl.NC(=N)CC(N)=N GEAQYIBQNNMPEH-UHFFFAOYSA-N 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- LZIYBABLVXXFGZ-UHFFFAOYSA-N pyrimidine-2-carboximidamide;hydrochloride Chemical compound Cl.NC(=N)C1=NC=CC=N1 LZIYBABLVXXFGZ-UHFFFAOYSA-N 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- XGVXKJKTISMIOW-ZDUSSCGKSA-N simurosertib Chemical compound N1N=CC(C=2SC=3C(=O)NC(=NC=3C=2)[C@H]2N3CCC(CC3)C2)=C1C XGVXKJKTISMIOW-ZDUSSCGKSA-N 0.000 description 1
- 210000002460 smooth muscle Anatomy 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 210000003594 spinal ganglia Anatomy 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
- 150000003890 succinate salts Chemical class 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000002466 tachykinin receptor agonist Substances 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- LMBFAGIMSUYTBN-MPZNNTNKSA-N teixobactin Chemical compound C([C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H](CCC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H]1C(N[C@@H](C)C(=O)N[C@@H](C[C@@H]2NC(=N)NC2)C(=O)N[C@H](C(=O)O[C@H]1C)[C@@H](C)CC)=O)NC)C1=CC=CC=C1 LMBFAGIMSUYTBN-MPZNNTNKSA-N 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- AFPIPRGLDSYLCE-UHFFFAOYSA-N tert-butyl n-[4-(2-methylphenyl)-2-methylsulfanylpyrimidin-5-yl]carbamate Chemical compound CSC1=NC=C(NC(=O)OC(C)(C)C)C(C=2C(=CC=CC=2)C)=N1 AFPIPRGLDSYLCE-UHFFFAOYSA-N 0.000 description 1
- WYURNTSHIVDZCO-UHFFFAOYSA-N tetrahydrofuran Substances C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 1
- WHRNULOCNSKMGB-UHFFFAOYSA-N tetrahydrofuran thf Chemical compound C1CCOC1.C1CCOC1 WHRNULOCNSKMGB-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 230000003685 thermal hair damage Effects 0.000 description 1
- KJAMZCVTJDTESW-UHFFFAOYSA-N tiracizine Chemical compound C1CC2=CC=CC=C2N(C(=O)CN(C)C)C2=CC(NC(=O)OCC)=CC=C21 KJAMZCVTJDTESW-UHFFFAOYSA-N 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/08—Drugs for disorders of the alimentary tract or the digestive system for nausea, cinetosis or vertigo; Antiemetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/36—Opioid-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/34—One oxygen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/38—One sulfur atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/42—One nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/46—Two or more oxygen, sulphur or nitrogen atoms
- C07D239/48—Two nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Pain & Pain Management (AREA)
- Psychiatry (AREA)
- Pulmonology (AREA)
- Rheumatology (AREA)
- Hospice & Palliative Care (AREA)
- Addiction (AREA)
- Immunology (AREA)
- Ophthalmology & Optometry (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Psychology (AREA)
- Dermatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Otolaryngology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Изобретение относится к новым производным 4-фенилпиримидина и их фармацевтически приемлемым кислотно-аддитивным солям, которые обладают свойствами антагонистов рецептора нейрокинина(NK-1), и могут быть использованы для лечения заболеваний, опосредствованных NK-1 рецептором, например, головная боль, болезнь Альцгеймера, рассеянный склероз, сердечно-сосудистых изменений, отека, хронических воспалительных заболеваний и т.д. Соединения изобретения соответствуют общей формуле
где R1 означает водород или галоген, R2 означает водород, галоген, низший алкил или низший алкокси, R1 и R2 вместе с двумя атомами углеродного цикла могут означать группу -СН=СН-СН=СН-, R3 означает галоген, трифторметил, низший алкил или низший алкокси, R4/R4’ независимо друг от друга каждый означает водород или низший алкил, R5 означает низший алкил, низший алкокси, амино, фенил, гидрокси(низший)алкил, циано(низший)алкил, карбамоил(низший)алкил, пиридил, пиримидил, -(CH2)n-пиперазинил, необязательно замещенный одной или двумя низшими алкильными группами или гидрокси(низшим)алкилом,-(CH2)n-морфолинил, -(CH2)n-пиперидинил, -(CH2)n+1-имидазолил, низший алкилсульфанил, низший алкилсульфонил, бензиламино, -NH-(CH2)n+1N(R4’’)2, -(CH2)n+1N(R4’’)2, -O-(CH2)n+1-морфолинил, -O-(CH2)n+1-пиперидинил или -O-(СН2)n+1N(R4’’)2, где R4’’ означает водород или низший алкил, и n означает 0-2,Х означает -C(O)N(R4’’)- или -N(R4’’)C(O)-. Изобретение также относится к фармацевтической композиции. 2 н. и 9 з.п. ф-лы.
Description
Настоящее изобретение относится к соединениям общей формулы
где
R1 означает водород или галоген,
R2 означает водород, галоген, низший алкил или низший алкокси,
R1 и R2 вместе с двумя атомами углеродного цикла могут означать группу -СН=СН-СН=СН-,
R3 означает галоген, трифторметил, низший алкил или низший алкокси,
R4/R4’ независимо друг от друга каждый означает водород или низший алкил,
R5 означает низший алкил, низший алкокси, амино, фенил, гидрокси(низш.)алкил, циано(низш.)алкил, карбамоил(низш.)алкил, пиридил, пиримидил, -(СН2)n-пиперазинил, необязательно замещенный одной или двумя низшими алкильными группами или гидрокси(низш.)алкилом, -(СН2)n-морфолинил, -(СН2)n-пиперидинил, -(СН2)n+1-имидазолил, (низш.)алкилсульфанил, (низш.)алкилсульфонил, бензиламино, -NH-(СН2)n+1N(R4’’)2 -(СH2)n+1N(R4’’)2, -O-(СН2)n+1-морфолинил, -O-(СН2)n+1-пиперидинил или -O-(СН2)n+1N(R4’’)2, где R4’’ означает водород или (низш.)алкил, и
n означает 0-2,
Х означает -C(O)N(R4’’)- или -N(R4’’)C(O)-;
и к их фармацевтически приемлемым кислотно-аддитивным солям.
Соединения формулы I и их соли отличаются ценными терапевтическими свойствами. При создании изобретения неожиданно было установлено, что соединения по настоящему изобретению являются антагонистами рецептора нейрокинина 1 (NK-1, вещество Р). Вещество Р представляет собой встречающийся в естественных условиях ундекапептид, принадлежащий к пептидам из семейства тахикининов, последние так называются из-за быстрого сократительного действия на внесосудистую ткань гладкой мускулатуры.
Рецептор вещества Р является представителем надсемейства связанных с протеином G рецепторов.
Нейропептидные рецепторы вещества Р (NK-1) широко распространены в нервной системе млекопитающих (прежде всего в головном мозге и спинальных ганглиях), кровеносной системе и периферических тканях (прежде всего в двенадцатиперстной кишке и тощей кишке), и они участвуют в регуляции многочисленных разнообразных биологических процессов.
Установлено, что центральное и периферическое действие тахикинина млекопитающих, т.е. вещества Р, связано с многочисленными воспалительными состояниям, включая мигрень, ревматоидный артрит, астму и воспалительное заболевание кишечника, а также выявлена его роль в качестве медиатора рвотного рефлекса и модулятора нарушений центральной нервной системы (ЦНС), таких как болезнь Паркинсона (Neurosci. Res. 7, 187-214, 1996), состояние тревоги (Can. J. Phys., 75, 612-621, 1997) и депрессия (Science, 281, 1640-1645,1998).
Данные о возможности применения антагонистов рецептора тахикинина для лечения боли, головной боли, прежде всего мигрени, болезни Альцгеймера, рассеянного склероза, ослабления синдрома отказа от морфина, сердечно-сосудистых изменений, отека, такого как отек, вызванный термическим повреждением, хронических воспалительных заболеваний, таких как ревматоидный артрит, астма/бронхиальная гиперреактивность и другие респираторные заболевания, включая аллергический ринит, воспалительные заболевания кишечника, включая язвенный колит и болезнь Крона, повреждения глаза и глазных воспалительных заболеваний, обобщены в статье "Tachykinin Receptor and Tachykinin Receptor Antagonists" J. Auton. Pharmacol., 13, 23-93, 1993.
Кроме того, антагонисты рецептора нейрокинина 1 разрабатывают с целью лечения многочисленных физиологических нарушений, связанных с избытком или с нарушением баланса тахикининов, в частности вещества Р. Примеры состояний, которые связаны с веществом Р, включают нарушения центральной нервной системы, такие как состояние тревоги, депрессия и психоз (WO 95/16679, WO 95/18124 и WO 95/23798).
Антагонисты рецептора нейрокинина-1, кроме того, могут применяться для лечения состояния укачивания и индуцированной лекарственным средством рвоты.
Кроме того, в журнале The New England Journal of Medicine, том 34, №3, 190-195, 1999 описано уменьшение индуцированной цисплатином рвоты с помощью избирательных антагонистов рецептора нейрокинина-1.
В патенте US 5972938 также описан способ лечения психоиммунологического или психосоматического нарушения путем введения антагониста рецептора тахикинина, такого как рецептор NK-1.
Объектами настоящего изобретения являются соединения формулы I и их фармацевтически приемлемые соли, способ получения вышеупомянутых соединений, содержащие их лекарственные средства и способ их изготовления, а также применение вышеупомянутых соединений для лечения и профилактики заболеваний, прежде всего заболеваний и расстройств типа приведенных выше, или для производства соответствующих лекарственных средств.
Наиболее предпочтительными показаниями по настоящему изобретению являются такие, которые включают расстройства центральной нервной системы, например необходимость терапии или профилактики некоторых депрессивных состояний или рвоты при введении антагонистов NK-1 рецептора. Основной приступ депрессии определяют как период по крайней мере в течение двух недель, во время которого, в течение большинства дней или почти каждый день, наблюдается подавленное настроение или потеря интереса или отсутствие удовлетворения от любого или почти от любого вида активной деятельности.
Общие термины, используемые в контексте настоящего изобретения, имеют следующие значения, независимо от того, применяются эти термины индивидуально или в различных сочетаниях.
Используемый в описании термин "(низш.)алкил" означает линейную или разветвленную алкильную группу, содержащую от 1 до 7 атомов углерода, например, метил, этил, пропил, изопропил, н-бутил, изобутил, трет-бутил и т.п. Предпочтительны (низш.)алкильные группы, содержащие от 1 до 4 углеродных атомов.
Термин "(низш.)алкокси" означает группу, в которой алкильные остатки имеют значения, указанные выше, причем алкил присоединен через атом кислорода.
Термин "галоген" означает хлор, йод, фтор и бром. Термин "фармацевтически приемлемые кислотно-аддитивные соли" означает соли неорганических и органических кислот, таких как хлористоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, паратолуолсульфоновая кислота и т.п.
Предпочтительными являются соединения, у которых Х означает -C(O)N(R4’’)-, где R4’’ означает метил, a R5 означает пиперазинил, необязательно замещенный одной или двумя метильными группами, например, нижеуказанные соединения:
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-димeтилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-триф)торметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты и
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты.
Кроме того, предпочтительны соединения, у которых Х означает -C(O)N(R4’’)-, где R4’’ означает метил, a R5 означает морфолинил или -O(СН2)2-морфолинил.
Примерами таких соединений являются:
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты.
Кроме того, предпочтительны соединения, у которых Х означает
-C(O)N(R4’’)-, R4’’ означает метил, a R5 означает –NH(CH2)2N(CH3)2, -O(СН2)2N(СН3)2 или –O(CH2)3N(CH3)2, например следующие соединения:
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты или
(3,5-бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты.
Кроме того, предпочтительны соединения, у которых Х означает
-N(R4’’)C(O)-, R4’’ означает метил, а R5 означает морфолинил или пиперазинил, необязательно замещенный группой низший алкил, например, следующие соединения:
2-(3,5-бис-трифторметилфенил)-N-метил-N-[2-(4-метилпиперазан-1-ил)-4-о-толилпиримидин-5-ил] изобутирамид и
2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил) изобутирамид.
Настоящие соединения формулы I и их фармацевтически приемлемые соли могут быть получены по известным в данной области техники методам, например описанным ниже способом, который включает
а) взаимодействие соединения формулы
с соединением формулы
с образованием соединения формулы
где R1-R5 и n имеют значения, указанные выше, или б) взаимодействие соединения формулы
с соединением формулы
с образованием соединения формулы
где R1-R5 и n имеют значения, указанные выше, или
в) модификацию одного или более заместителей R1-R5, имеющих значения, указанные выше, и, если необходимо, перевод полученного соединения в его фармацевтически приемлемую кислотно-аддитивную соль.
По способу а) к смеси соединения формулы II, например метил [6-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-3-ил] амина и соединения формулы III, например, 2-(3,5-бис-трифторметилфенил)-2-метилпропионил-хлорида, добавляют DIPEA (N-этилдиизопропиламин) и смесь перемешивают при температуре от 35 до 40°С. Требуемое соединение формулы I-1 получают после очистки с высоким выходом.
Способ б) описывает взаимодействие соединения формулы IV с соединением формулы V с образованием соединения формулы I-2. Реакцию проводят в обычных условиях, например, в растворителе, таком как дихлорметан, в присутствии триэтиламина, EDCI (гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида) и НОВТ (1-гидроксибензотриазола). Полученную смесь перемешивают при 20°С в течение 12 ч.
Получение соли проводят при комнатной температуре по известным в данной области техники методам. При этом имеются ввиду соли как с неорганическими, так и органическими кислотами. Примерами таких солей являются гидрохлориды, гидробромиды, сульфаты, нитраты, цитраты, ацетаты, малеаты, сукцинаты, метансульфонаты, пара-толуолсульфонаты и т.п.
Нижеуказанные схемы 1-6 более подробно иллюстрируют способы получения соединений формулы I. Исходные материалы формул V, VIII, X, XIV и XVIII являются известными соединениями и могут быть получены по известным в данной области техники методам.
На схемах используются следующие сокращения:
ТГФ - тетрагидрофуран
DIPEA - N-этилдиизопропиламин
НОВТ - 1-гидроксибензотриазол
EDCI - гидрохлорид N-(3-диметиламинопропил)-N’-этилкарбодиимида
м-ХНБК - мета-хлорнадбензойная кислота
ДФФА - дифенилфосфорилазид
ДМФ - диметилформамид
ТЭА - триэтиламин
Схема 1
Заместители имеют значения, указанные выше.
Схема 2
Y=галоген
R4”(низш.)алкил
Заместители имеют значения, указанные выше.
Схема 3
R’ означает (низш.)алкил, Y означает галоген, А означает аминогруппу, такую, как -N(R4)2, пиперазинил, морфолинил, пиперидинил или имидазолил. Остальные заместители имеют значения, указанные выше.
Схема 4
Заместители имеют значения, указанные выше.
Схема 5
Тип реакции описан в журнале Bioorg. and Med. Chem., vol.5, №2, 437-444 (1997).
R1-R4 и n имеют значения, указанные выше, В означает (низш.)алкокси, -O-(CH2)n+1N(R4)2, -O-(СН2)n+1-морфолинил или -O-(СН2)n+1-пиперидинил, а А’ означает аминогруппу, такую как -N(R4)2, необязательно замещенный пиперазинил, морфолинил, пиперидинил, имидазолил, бензиламин или -NH-(CH)n+1N(R4)2.
Схема 6
R1-R4 и n имеют значения, указанные выше, В означает (низш.)алкокси, -O-(CH2)n+1N(R4)2 -O-(СН2)n+1-морфолинил или -O-(СН2)n+1-пиперидинил, а А’ означает аминогруппу, такую как -N(R4)2, необязательно замещенный пиперазинил, морфолинил, пиперидинил, имидазолил, бензиламин или -NH-(CH2)n+1N(R4)2.
Как отмечалось ранее, соединения формулы I и их фармацевтически приемлемые аддитивные соли обладают ценными фармакологическими свойствами. Установлено, что соединения по настоящему изобретению являются антагонистами рецептора нейрокинина 1 (NK-1, вещество Р).
Соединения формулы I были изучены с помощью приведенных ниже тестов.
Сродство тестируемых соединений к NK1-рецептору оценивали с использованием человеческих NK1-рецепторов в СНО-клетках, инфицированных человеческим NК1-рецептором (с использованием экспрессионной системы вируса Semliki) и в присутствии радиоактивно меченного с помощью [3Н]-вещества Р (конечная концентрация 0,6 нМ). Опыты по связыванию проводили в HEPES-буфере (50 мМ, рН 7,4), содержащим БСА (бычий сывороточный альбумин) (0,04%), леупептин (8 мкг/мл), MnCl2 (3 мМ) и фосфорамидон (2 мкМ). В опытах по связыванию использовали 250 мкл суспензии мембран (1,25×105 клеток/пробирку для анализа), 0,125 мкл буфера, включающего замещающий агент, и 125 мкл [3Н]-вещества Р. Для получения кривых замещения использовали по меньшей мере 7 концентраций соединения. Пробирки для анализа инкубировали в течение 60 мин при комнатной температуре, после чего содержимое пробирки быстро фильтровали под вакуумом через фильтры типа GF/C, которые предварительно в течение 60 мин пропитывали PEI (0,3%) с двумя промывками, для каждой из которых использовали по 2 мл HEPES-буфера (50 мМ, рН 7,4). Радиоактивность, сохранившуюся на фильтрах, оценивали с помощью сцинцилляционного счетчика. Все опыты проводили в трех повторностях по меньшей мере в двух различных экспериментах.
Для предпочтительных соединений их сродство к NК1-рецептору, выраженное в виде значения рКi, составляло 8,00-9,20. Примерами таких соединений являются:
Соединения формулы I, а также их фармацевтически приемлемые кислотно-аддитивные соли могут применяться в качестве лекарственных средств, например, в форме фармацевтических композиций. Фармацевтические композиции могут вводиться перорально, например, в форме таблеток, филмтаблеток, драже, желатиновых капсул с твердым или мягким покрытием, растворов, эмульсий или суспензий. Однако введение также может быть осуществлено ректально, например, в форме суппозиториев, или парентерально, например, в форме инъецируемых растворов.
Соединения формулы I и их фармацевтически приемлемые кислотно-аддитивные соли могут быть подвергнуты обработке вместе с фармацевтически инертными неорганическими или органическими эксципиентами для приготовления таблеток, филмтаблеток, драже и желатиновых капсул с твердым покрытием. В качестве таких эксципиентов для приготовления, например, таблеток, драже и желатиновых капсул с твердым покрытием могут использоваться лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.д.
Приемлемыми эксципиентами для приготовления желатиновых капсул с мягким покрытием являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.д.
Приемлемыми эксципиентами для приготовления растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.д.
Приемлемыми эксципиентами для инъецируемых растворов являются, например, вода, спирты, полиолы, глицерин, растительные масла и т.д.
Приемлемыми эксципиентами для суппозиториев являются, например, природные или гидрогенизированные масла, воски, жиры, полутвердые или жидкие полиолы.
Кроме того, фармацевтические композиции могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подслащивающие вещества, красители, корригенты, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать и другие терапевтически ценные вещества.
Дозы могут варьироваться в широких пределах и, естественно, должны быть подобраны в зависимости от индивидуальных требований в каждом конкретном случае. В целом, в случае перорального введения суточная доза для пациента может находиться в диапазоне примерно от 10 до 1000 мг соединения формулы I, однако при необходимости верхний предел может быть превышен.
Ниже настоящее изобретение проиллюстрировано примерами, не ограничивающими его объем.
Пример 1
(3,5-бис-трифторметилбензил)метиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты
а) 3,5-бис-трифторметилбензиламид 2-метид-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,50 г (2,33 ммоля) 2-метил-4-фенилпиримидин-5-карбоновой кислоты, 0,65 мл (4,47 ммоля) триэтиламина, 0,44 г (2,33 ммоля) 1-гидроксибензотриазола и 0,44 г (2,33 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 40 мл CH2Cl2 добавляли 0,68 г (2,8 ммоля) 3,5-бис-трифторметилбензиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 20 мл CH2Cl2, промывали 50 мл 0,5 н. НСl, 50 мл Н2О и проводили обратную экстракцию водных слоев 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, этилацетат), при этом получали 0,80 г (78%) 3,5-бис-трифторметилбензиламида 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 188,5-189,5°С.
б) (3,5-Бис-трифторметидбензил)метиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,67 г (1,52 ммоля) 3,5-бис-трифторметилбензиламида 2-метил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл N,N-диметилформамида добавляли 0,08 г (1,98 ммоля) гидрида натрия (60%-ная дисперсия в минеральном масле) и реакционную смесь перемешивали в течение 1 ч. Затем при 0°С добавляли 0,15 мл (2,4 ммоля) метилиодида и реакционную смесь перемешивали при комнатной температуре (КТ) в течение 3 ч. Реакционную смесь распределяли между 50 мл Н2О, 50 мл солевого раствора и 50 мл СН2Сl2. Фазы разделяли и водный слой дважды промывали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, этилацетат/гексан, 4:1), при этом получали 0,50 г (72%) (3,5-бис-трифторметилбензил)метиламида 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(EI):453 (М+).
Пример 2
(3,5-Дихлорбензил)метиламид 2-метид-4-фенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2-метил-4-фенилпиримидин-5-карбоновой кислоты и 3,5-дихлорбензиламина получали 3,5-дихлорбензиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 194-195°С, который метилировали аналогично тому, как описано в примере 1б), при этом получали (3,5-дихлорбензил)метиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(EI):385 (M+).
Пример 3
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-метидпиримидин-5-карбоновой кислоты
а) Этиловый эфир 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты
К раствору 25,9 г (95,5 ммоля) этилового эфира 3-(2-бромфенил)-3-оксопропионовой кислоты в 200 мл толуола в течение 1 ч добавляли 18,21 г (152 ммоля) диметилацеталя N,N-диметилформамида, растворенного в 100 мл толуола, и реакционную смесь перемешивали при 100°С в течение 1,5 ч. Растворитель выпаривали, полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 25 г (80%) этилового эфира 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты в виде твердого вещества светло-коричневого цвета.
б) Этиловый эфир 4-(2-бромфенил)-2-метидпиримидин-5-карбоновой кислоты
К свежеприготовленному раствору алкоголята натрия [полученному из 0,77 г (33,7 ммоля) натрия, добавленного к 100 мл этанола] добавляли 3,18 г (33,7 ммоля) гидрохлорида ацетамидина. Через 10 мин добавляли раствор 10,0 г (30,6 ммоля) этилового эфира 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты в 120 мл этанола и реакционную смесь нагревали при 80°С в течение 16 ч. Растворитель выпаривали, остаток распределяли между 100 мл Н2О и 100 мл СН2Сl2. Водную фазу дважды экстрагировали 100 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 8,3 г (84%) этилового эфира 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде масла светло-коричневого цвета.
в) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновая кислота
К раствору 8,3 г (25,8 ммоля) этилового эфира 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в 10 мл этанола добавляли 1,55 г (38,6 ммоля) NaOH в 20 мл Н2О. После перемешивания в течение 1 ч реакционную смесь промывали 100 мл диэтилового эфира. Водную фазу подкисляли 25%-ной НСl до рН 1 и дважды экстрагировали 200 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали, при этом получали 7,0 г (92%) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде пены светло-желтого цвета.
г) (3,5-Бис-трифторметилбензид)метиламид 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (1,71 ммоля) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты, 0,47 мл (3,41 ммоля) триэтиламина, 0,26 г (1,71 ммоля) 1-гидроксибензотриазола и 0,32 г (1,71 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 40 мл СН2Сl2 добавляли 0,52 г (2,0 ммоля) (3,5-бис-трифторметилбензил)метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 20 мл СН2Сl2, промывали 50 мл 0,5н. НСl, 50 мл Н2О и проводили обратную экстракцию водных слоев 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, этилацетат), при этом получали 0,7 г (77%) (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 121,5-122,5°С.
Пример 4
3,5-Бис-трифторметилбензиламид
4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (1,71 ммоля) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты, 0,47 мл (3,41 ммоля) триэтиламина, 0,26 г (1,71 ммоля) 1-гидроксибензотриазола и 0,32 г (1,71 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 40 мл CH2Cl2 добавляли 0,49 г (2,05 ммоля) 3,5-бис-трифторметилбензиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 20 мл СН2Сl2, промывали 50 мл 0,5н. НСl, 50 мл Н2О и проводили обратную экстракцию водных слоев 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH), при этом получали 0,4 г (45%) 3,5-бис-трифторметилбензиламида 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 137,5-138,5°С.
Пример 5
(3,5-Бис-трифторметилбензил)метиламид 2,4-дифенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2,4-дифенилпиримидин-5-карбоновой кислоты и 3,5-бис-трифторметилбензиламина получали 3,5-бис-трифторметилбензиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл>220°C, который метилировали, как описано в примере 1б), при этом получали (3,5-бис-трифторметилбензил)метиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):516,2 (M+H+).
Пример 6
(3,5-Дихлорбензил)метиламид 2,4-дифенидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2,4-дифенилпиримидин-5-карбоновой кислоты и 3,5-дихлорбензиламина получали 3,5-дихлорбензиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл>220°С, который метилировали, как описано в примере 1б), при этом получали (3,5-дихлорбензил)метиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):448 (M+H+).
Пример 7
(3,5-Дихлорбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 4-фенил-2-пропилпиримидин-5-карбоновой кислоты и 3,5-дихлорбензиламина получали 3,5-дихлорбензиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 183°С, который метилировали, как описано в примере 1б), при этом получали (3,5-дихлорбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного масла, МС(ЕI):413 (М+).
Исходное соединение, 4-фенил-2-пропилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида бутирамидина, с последующим гидролизом, как описано в примере 3в), до 4-фенил-2-пропилпиримидин-5-карбоновой кислоты.
Пример 8
(3,5-Бис-трифторметилбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 4-фенил-2-пропилпиримидин-5-карбоновой кислоты и 3,5-бис-трифторметилбензиламина получали 3,5-бис-трифторметилбензиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 194-195°С, который метилировали, как описано в примере 1б), при этом получали (3,5-бис-трифторметилбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):482,3 (M+H+).
Пример 9
(3,5-Бис-трифторметилбензил)метидамид 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 143-144°С.
Исходное соединение, 4-фенил-2-пиридин-4-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида изоникотинамидина, с последующим гидролизом, как описано в примере 3в), до 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты.
Пример 10
(3,5-Бис-трифторметилбензил)метиламид 4-фенил [2,2’] бипиримидинид-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-фенил-[2,2’] бипиримидинил-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-фенил- [2,2’]бипиримидинил-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 172-173°С.
Исходное соединение, 4-фенил[2,2’]бипиримидинил-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида пиримидин-2-карбоксамидина, с последующим гидролизом, как описано в примере 3в), до 4-фенил[2,2’]бипиримидинил-5-карбоновой кислоты.
Пример 11
3,5-Бис-трифторметидбензидамид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и 3,5-бис-трифторметилбензиламина получали 3,5-бис-трифторметилбензиламид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 146,7-146,9°С.
Исходное соединение, 2-метил-4-нафталин-1-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3а)-3в), из этилового эфира 3-нафталин-1-ил-3-оксопропионовой кислоты и диметилацеталя N,N-диметилформамида.
Пример 12
(3,5-Бис-трифторметилбензил)метиламид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1б), из 3,5-бис-трифторметилбензиламида 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и метилиодида получали (3,5-бис-трифторметилбензил)метиламид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 164,9-165,2°С.
Пример 13
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 140-141°С.
Исходное соединение, 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3а)-3в), из этилового эфира 3-(2-метоксифенил)-3-оксопропионовой кислоты и диметилацеталя N,N-диметилформамида.
Пример 14
(3,5-Бис-трифторметидбензил)метиламид 2-метилсудьфанил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 3 г (12,18 ммоля) 2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты, 3,32 мл (24,36 ммоля) триэтиламина, 1,84 г (12,18 ммоля) 1-гидроксибензотриазола и 2,33 г (12,81 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 170 мл СН2Сl2 добавляли 3,76 г (14,62 ммоля) (3,5-бис-трифторметилбензил) метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 100 мл СН2Сl2, промывали 100 мл 0,5н. НСl, 100 мл Н2О и проводили обратную экстракцию водных слоев 100 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат), при этом получали 4,15 г (67%) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 119,1-119,8°С.
Пример 15
(3,5-Бис-трифторметилбензил)метиламид 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 4,15 г (85,5 ммоля) (3,5-бис-трифторметилбензил)метиламида2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты в 170 мл CH2Cl2 при 5°С добавляли 5,27 г (21,4 ммоля) 3-хлорнадбензойной кислоты (70%) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли 150 мл насыщенного раствора NаНСО3, слои разделяли, органическую фазу промывали насыщенным раствором NaHCO3, сушили (Nа2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/метанол, 40:1), при этом получали 4,20 г (95%) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, MC(EI):517 (M+).
Пример 16
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,97 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,27 мл (2,42 ммоля) 1-метилпиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 9:1), при этом получали 0,4 г (77%) (3,5-бис-трифторметилбензил)метиламида 2-(4-метилпиперазин-1-ил)-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):538,3 (М+Н+).
Пример 17
(3,5-Бис-трифторметилбензил)метиламид 2-бензиламино-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,21 мл (1,923 ммоля) бензиламина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,2 г (47%) (3,5-бис-трифторметил-бензил)метиламида 2-бензиламино-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 117,2-118,1°С.
Пример 18
(3,5-Бис-трифторметилбензид)метиламид 2-морфолин-4-ил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,17 мл (1,93 ммоля) морфолина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,21 г (52%) (3,5-бис-трифторметилбензил)метиламида 2-морфолин-4-ил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 168,1-168,4°С.
Пример 19
(3,5-Бис-трифторметилбензил)метиламид 4-фенид-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,208 г (2,15 ммоля) пиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,42 г (83%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):524,1 (M+H+).
Пример 20
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-фенидпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,276 г (2,15 ммоля) цис-2,6-диметилпиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,51 г (96%) (3,5-бис-трифторметилбензил)метиламида (2R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):552,1 (M+H+).
Пример 21
(3,5-Бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтиламино)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,211 мл (1,93 ммоля) 2-диметиламиноэтиламина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/метанол/NH4OH, 140:10:1), при этом получали 0,22 г (54%) (3,5-бис-трифторметилбензил)метиламида 2-(2-диметиламиноэтиламино)-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 109,5-110,3°С.
Пример 22
(3,5-Бис-трифтоометилбензил)метиламид 4-фенил-2-пиперидин-1-илпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,183 г (2,15 ммоля) пиперидина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSО4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат, 20:1), при этом получали 0,48 г (95%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-пиперидин-1-илпиримидин-5-карбоновой кислоты в виде воскообразного вещества светло-желтого цвета, MC(ISP):523,2 (M+H+).
Пример 23
(3,5-Бис-трифторметилбензил)метиламид 2-[4-(2-гидроксиэтил)пиперазин-1-ил]-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,28 г (2,15 ммоля) N-(2-гидроксиэтил)пиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 6:1), при этом получали 0,43 г (78%) (3,5-бис-трифторметил-бензил)метиламида2-[4-(2-гидроксиэтил)пиперазин-1-ил]-4-фенилпиримидин-5-карбоновой кислоты в виде воскообразного вещества светло-желтого цвета. MC(ISP):568,2 (M+H+).
Пример 24
(3,5-Бис-трифторметилбензил)метиламид 2-(2-морфолин-4-илэтокси)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,15 г (1,16 ммоля) N-(2-гидроксиэтил)морфолина, 1,57 г (4,83 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 0,39 г (68%) (3,5-бис-трифторметилбензил)метиламида 2-(2-морфолин-4-илэтокси)-4-фенилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):569,2 (M+H+).
Пример 25
(3,5-Бис-трифторметилбензид)метиламид 4-фенил-2-(2-пиперидин-1-илэтокси)пиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,15 г (1,16 ммоля) N-(2-гидроксиэтил)пиперидина, 1,57 г (4,83 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 200:10:1), при этом получали 0,47 г (85%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-(2-пиперидин-1-илэтокси)пиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):567,2 (М+Н+).
Пример 26
(3,5-Бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,10 г (1,16 ммоля) 2-диметиламиноэтанола, 1,57 г (4,83 ммоля) Сs2СО3, и реакционную смесь перемешивали в течение 16 ч.
После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,43 г (82%) (3,5-бис-трифторметилбензил)метиламида2-(2-диметиламиноэтокси)-4-фенилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):527,2 (М+Н+).
Пример 27
(3,5-Бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,14 мл (1,16 ммоля) 2-диметиламинопропанола, 1,57 г (4,83 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч.
После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,50 г (95%) (3,5-бис-трифторметилбензил)метиламида 2-(3-диметиламинопропокси)-4-фенилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):541,2 (M+H+).
Пример 28
(3,5-Бис-трифторметилбензил)метиламид 2-метокси-4-фенилпиримидин-5-карбоновой кислоты
К суспензии 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл метанола добавляли 0,10 г (1,93 ммоля) метанолята натрия (95%) и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 0.23 г (63%) (3,5-бис-трифторметилбензил)метиламида 2-метокси-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 101,2-102°С.
Пример 29
(3,5-Бис-трифторметидбензил)метиламид 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 161-163°С.
Исходное соединение, 2-карбамоилметил-4-фенилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида малонамидина, с последующим гидролизом, как описано в примере 3в), до 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты.
Пример 30
(3,5-Бис-трифторметилбензил)метиламид 2-цианометил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,50 г (1,01 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты и 0,17 мл пиридина в 10 мл диоксана добавляли 0,15 мл (1,06 ммоля) ангидрида трифторуксусной кислоты и полученную реакционную смесь перемешивали при 50°С в течение 1 ч. Затем реакционную смесь выливали в смесь льда с водой и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSО4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 30:1), при этом получали 0,25 г (51%) (3,5-Бис-трифторметилбензил)метиламида2-цианометил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 114-116°С.
Пример 31
(3,5-Бис-трифторметилбензид)метиламид 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, МС(ЕI):469 (M+).
Исходное соединение, 2-гидроксиметил-4-фенилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида 2-гидроксиацетамидина, с последующим гидролизом, как описано в примере 3в), до 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты.
Пример 32
(3,5-Бис-трифторметилбензид)метидамид 2-диметиламинометил-4-фенилпиримидин-5-карбоновой кислоты
а) 5-[(3,5-Бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметиловый эфир метансульфоновой кислоты
К раствору 2,64 г (5,62 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты и 1,17 мл (8,44 ммоля) триэтиламина в 30 мл CH2Cl2 при 0°С добавляли 0,479 мл (6,19 ммоля) метансульфонилхлорида и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь выливали в насыщенный раствор NаНСО3 и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат, 8:1), при этом получали 2,30 г (74%) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметиловый эфир метансульфоновой кислоты в виде вязкого бесцветного масла, MC(ISP):548,1 (М+Н+).
б) (3,5-Бис-трифторметилбензил)метиламид 2-диметидаминометил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл СН2Сl2 добавляли 1 мл 5,6М раствора диметиламина в этаноле и реакционную смесь перемешивали при КТ в течение 16 ч. Затем реакционную смесь выливали в Н2О и трижды экстрагировали 50 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 20:1), при этом получали 0,33 г (90%) (3,5-бис-трифторметилбензил)метиламида2-диметиламинометил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):497,2 (М+Н+).
Пример 33
(3,5-Бис-трифторметилбензил)метиламид 2-морфолин-4-илметид-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл СН2Сl2 добавляли 0,095 мл (1,10 ммоля) морфолина и реакционную смесь перемешивали при КТ в течение 16 ч. Затем реакционную смесь выливали в Н2О и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,33 г (88%) (3,5-бис-трифторметилбензил)метиламида 2-морфолин-4-илметил-4-фенилпиримидин-5-карбоновой кислоты в виде воскообразного твердого вещества светло-желтого цвета, MC(ISP):539,3 (M+H+).
Пример 34
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-илметил)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл CH2Cl2 добавляли 0,12 мл (1,1 ммоля) N-метилпиперазина. Реакционную смесь перемешивали при КТ в течение 16 ч, затем выливали в Н2О и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,31 г (77%) (3,5-бис-трифторметилбензил)метиламида 2-(4-метилпиперазин-1-илметил)-4-фенилпиримидин-5-карбоновой кислоты в виде воскообразного твердого вещества светло-желтого цвета, MC(ISP):552,2 (M+H+).
Пример 35
(3,5-Бис-трифторметилбензил)метидамид 4-фенил-2-пиперидин-1-илметилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл CH2Cl2 добавляли 0,11 мл (1,1 ммоля) пиперидина. Реакционную смесь перемешивали при КТ в течение 16 ч, затем выливали в Н2О и трижды экстрагировали 50 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,32 г (81%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-пиперидин-1-илметилпиримидин-5-карбоновой кислоты в виде воскообразного твердого вещества светло-желтого цвета, MC(ISP):537,2 (M+H+).
Пример 36
(3,5-Бис-трифторметилбензил)метиламид 2-имидазол-1-илметил-4-фенилпиоимидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты и 0,04 г (0,80 ммоля) метанолята натрия в 15 мл N,N-диметилформамида добавляли 0,59 г (0,88 ммоля) имидазола и реакционную смесь перемешивали при КТ в течение 16 ч. Затем реакционную смесь упаривали и остаток распределяли между Н2О и СН2Сl2. Водный слой дважды экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,24 г (63%) (3,5-бис-трифторметилбензил)метиламида 2-имидазол-1-илметил-4-фенилпиримидин-5-карбоновой кислоты в виде твердого вещества светло-желтого цвета, MC(ISP):520.2 (М+Н+).
Пример 37
(3,5-Бис-трифторметилбензид)метиламид 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
а) Этиловый эфир 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
К суспензии 3,81 г (46,54 ммоля) ацетата натрия и 6,47 г (23,27 ммоля) сульфата S-метилизотиомочевины в 100 мл N,N-диметилформамида одной порцией добавляли раствор 6,90 г (21,15 ммоля) этилового эфира 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты в 20 мл N,N-диметилформамида и реакционную смесь перемешивали при 90°С в течение 16 ч. Затем растворитель выпаривали, остаток распределяли между 100 мл CH2Cl2 и 100 мл Н2О. Водную фазу дважды экстрагировали 100 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали.
Полученный остаток очищали хроматографией (SiO2, СН2Сl2), при этом получали 5,20 г (69%) этилового эфира 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде масла светло-зеленого цвета.
б) 4-(2-Бромфенил)-2-метилсульфанилпиримидин-5-карбоновая кислота
К раствору 5,10 г (14,4 ммоля) этилового эфира 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в 10 мл этанола добавляли 10 мл 2 н. раствора NaOH. После перемешивания в течение 1 ч к раствору желтого цвета добавляли 50 мл Н2О и 50 мл CH2Cl2, водную фазу подкисляли 25%-ной НСl до рН 1. Фазы разделяли и водную фазу дважды экстрагировали 200 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали, при этом получали 4,60 г (98%) 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде твердого вещества грязно-белого цвета.
в) (3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
К раствору 2 г (6,15 ммоля) 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, 1,71 мл (12,3 ммоля) триэтиламина, 0,94 г (6,15 ммоля) 1-гидроксибензотриазола и 1,17 г (6,15 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 70 мл СН2Сl2 добавляли 1,63 г (6,34 ммоля) (3,5-бис-трифторметилбензил) метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 50 мл СН2Сl2, промывали 50 мл 0,5 н. НСl, 50 мл Н2О, и проводили обратную экстракцию водных слоев 75 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 3,0 г (86%) (3,5-бис-трифторметилбензил) метиламида 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):566, 564 (М+Н+).
Пример 38
(3,5-Бис-трифторметилбензил)метидамид 4-(2-бромфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил) метиламида 4-(2-бромфенил)-2- метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):598, 596 (М+Н+).
Пример 39
(3,5-Бис-трифторметилбензил)метиламид 2-амино-4-(2-бромфенил)пиримидин-5-карбоновой кислоты
Через раствор 0,42 г (0,7 ммоля) (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в 30 мл N,N-диметилформамида пропускали NH3 в течение 10 мин и реакционную смесь перемешивали в течение 4 ч. Затем растворитель выпаривали, остаток распределяли между 20 мл CH2Cl2 и 20 мл Н2О. Водную фазу дважды экстрагировали 30 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4ОH, 140:10:1), при этом получали 0,29 г (77%) (3,5-бис-трифторметилбензил)метиламида 2-амино-4-(2-бромфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):535,1, 533,1 (М+Н+).
Пример 40
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метидпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):618,1, 616,1 (М+Н+), из которого после взаимодействия по известному способу с фумаровой кислотой получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты (1:1), tпл 179-180°С.
Пример 41
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):632,0, 630,0 (М+Н+).
Пример 42
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенид)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):603,9, 601,9 (М+Н+).
Пример 43
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-идпиримидин-5-кароновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):605, 603 (М+Н+).
Пример 44
(3,5-Бис-трифторметилбензилметиламид 4-(2-хдорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил)метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):519 (М+).
Исходное соединение, 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-хлорбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины, с последующим гидролизом до 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 45
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):552,0 (М+Н+).
Пример 46
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):572,1 (M+H+), из которого после взаимодействия по известному способу с фумаровой кислотой получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты (1:1), tпл 174,8-175,8°С.
Пример 47
(3,5-Бис-трифторметидбензил)метиламид (3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):586,1 (М+Н+).
Пример 48
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):558,2 (М+Н+), из которого после взаимодействия по известному способу с фумаровой кислотой получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 123-126°С.
Пример 49
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):559,1 (M+H+).
Пример 50
(3,5-Бис-трифторметидбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 21, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):560,2 (M+H+).
Пример 51
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 24, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и N-(2-гидроксиэтил) морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):603,0 (M+H+).
Пример 52
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):561,2 (M+H+).
Пример 53
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 27, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламинопропанола получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):575,1 (M+H+).
Пример 54
(3,5-Бис-трифторметилбензил)метиламид 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметил-бензил)метиламид 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):499 (M+).
Исходное соединение, 2-метилсульфанил-4-о-толилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-метилбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины, с последующим гидролизом до 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 55
(3,5-Бис-трифторметилбензил)метиламид 2-метилсудьфонил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):532,1 (M+H+).
Пример 56
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толил-пиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):552,1 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты (1:1), tпл 151,5-152,5°C.
Пример 57
(3,5-Бис-трифторметидбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):566,3 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты (1:0,5), tпл 203,5-204,5°С.
Пример 58
(3,5-Бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-тодидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP): 538,3 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты (1:1), tпл 149,5-151,5°С.
Пример 59
(3,5-Бис-трифторметилбензил)метидамид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):538 (M+).
Пример 60
(3,5-Бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):541,2 (M+H+).
Пример 61
(3,5-Бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 27, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламинопропанола получали (3,5-бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):555,2 (М+Н+).
Пример 62
(3,5-Бис-трифторметилбензил)метидамид 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):515 (M+).
Исходное соединение, 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-метоксибензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 63
(3,5-Бис-трифторметидбензил)метиламид 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)-метиламид 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):548,1 (M+H+).
Пример 64
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):568,5(M+H+).
Пример 65
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)-метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):582,2 (M+H+).
Пример 66
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-идпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):554,2(М+Н+).
Пример 67
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, tпл 190,8-192,0°С.
Пример 68
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):503 (M+).
Пример 69
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):535 (M+).
Пример 70
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил) пиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(Е1):555 (M+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты (1:1), tпл 144,5-145,5°C.
Пример 71
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фторфенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фторфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фторфенил)пиримидин-5-карбоновой кислоты (1:0,5), tпл 220-223°C.
Пример 72
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-метилсульфонил-пиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС (ISP):542,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 155-158°С.
Пример 73
(3,5-Бис-трифторметидбензил)метиламид 4-(4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):543,2 (М+Н+).
Пример 74
(3,5-Бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде твердого вещества белого цвета, tпл 109,5-110°С.
Исходное соединение, 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали, как описано в примере 37а), б), из этилового эфира 2-(2-фторбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 75
(3,5-Бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):536,2 (М+Н+).
Пример 76
(3,5-Бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-(4-метидпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил) метиламид 4-(2-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):556,1 (М+Н+).
Пример 77
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,2 (M+H+).
Пример 78
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4- (2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС (ISP):542,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 124,8-125,1°С.
Пример 79
(3,5-Бис-трифторметидбензид)метидамид 4-(2-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):542 (М+).
Пример 80
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде твердого вещества белого цвета, МС(ЕI):517 (М+). Исходное соединение, 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(4-фтор-2-метилбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 81
(3,5-Бис-трифторметилбензил)метидамид 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)-метиламид 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):549 (М+).
Пример 82
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,2 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 185,0-186,5°С.
Пример 83
(3,5-Бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)-метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):548,1 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты (1:0,5), tпл 228-230°С.
Пример 84
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метидфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):556,1 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 143-145°C.
Пример 85
(3,5-Бис-трифторметилбензил) метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):557,1 (M+H+).
Пример 86
(3,5-бис-трифторметилбензил)метиламид 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):535 (М+).
Исходное соединение, 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 3-диметиламино-2-(нафталин-1-карбонил)акриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 87
(3,5-Бис-трифторметилбензил)метиламид 2-метилсульфонид-4- нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):568,1 (M+H+).
Пример 88
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил) метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде твердого вещества белого цвета, tпл 170,6-170,9°С.
Пример 89
(3,5-Бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил) метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):602,1 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты (1:0,5), tпл 247-249°С.
Пример 90
(3,5-Бис-трифторметилбензил)метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил) метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС (ISP):574,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 176-178°С.
Пример 91
(3,5-Бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафтадин-1 -илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):575,1 (М+Н+).
Пример 92
(3,5-Бис-трифторметилбензил)метиламид 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 127-128°C.
Исходное соединение, 4-фенил-2-пиридин-3-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида 3-амидинопиридина с последующим гидролизом, как описано в примере 3в), до 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты, МС(Е1):277 (М+).
Пример 93
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):538,1 (M+H+).
Исходное соединение, 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-хлор-4-фторбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 94
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенид)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)-метиламид 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,1 (M+H+).
Пример 95
(3,5-Бис-трифторметидбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):590,1 (M+H+).
Пример 96
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):577,0 (M+H+).
Пример 97
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2- пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):576,0 (М+Н+).
Пример 98
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):579,1 (M+H+).
Пример 99
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 27, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламинопропанола получали (3,5-бис-трифторметилбензил) метиламид 4-(2-хлор-4-фторфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):593,1 (M+H+).
Пример 100
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 24, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и N-(2-гидроксиэтил)-морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):621,0 (М+Н+).
Пример 101
(3,5-Диметоксибензил)метиламид 2-метидсульфанил-4-о-толилпиримидин-5-карбоновой кислоты
К раствору 3,00 г (11,52 ммоля) 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в 70 мл СН2Сl2 добавляли 3,21 мл (23,05 ммоля) триэтиламина, 1,55 г (11,52 ммоля) 1-гидроксибензотриазола, 2,20 г (11,52 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида, 2,29 г (12,68 ммоля) (3,5-диметоксибензил) метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 100 мл СН2Сl2. промывали 100 мл 0,5н. НСl, 100 мл Н2О и проводили обратную экстракцию водных слоев 100 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH), при этом получали 4,20 г (86%) (3,5-диметоксибензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):424,1 (M+H+).
Пример 102
(3,5-Диметоксибензил)метиламид 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты
К раствору 4,00 г (9,44 ммоля) (3,5-диметоксибензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в 100 мл СН2Сl2 при 5°С добавляли 5,82 г (23,61 ммоля) 3-хлорнадбензойной кислоты (70%) 30 и реакционную смесь перемешивали при КТ в течение 3 ч. После добавления 100 мл насыщенного раствора NаНСО3 слои разделяли, органическую фазу промывали насыщенным раствором NаНСО3, сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат, 4:1), при этом получали 2,00 г (46%) (3,5-диметоксибензил)метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(ISP):456,5 (M+H+).
Пример 103
(3,5-Диметоксибензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-диметоксибензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-10 карбоновой кислоты и 1-метилпиперазина получали (3,5-диметоксибензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):476,3 (M+H+).
Пример 104
(3,5-Диметоксибензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-диметоксибензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-диметоксибензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде 20 бесцветной пены, MC(ISP):463,3 (M+H+).
Пример 105
(3,5-Диметоксибензил)метиламид 2-(2-диметиламиноэтиламино)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 21, из (3,5-диметоксибензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтиламина получали (3,5-диметоксибензил)метиламид 2-(2-диметиламиноэтиламино)-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):464,4 (M+H+).
Пример 106
(3,5-Диметоксибензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-диметоксибензил)метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-диметоксибензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, МС(ЕI):465,3 (M+H+).
Пример 107
(3,5-Диметилбензил)метиламид 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты
К раствору 2,60 г (9,99 ммоля) 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты, 2,78 мл (19,98 ммоля) триэтиламина, 1,34 г (9,99 ммоля) 1-гидроксибензотриазола и 1,91 г (9,99 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 70 мл CH2Cl2 добавляли 1,78 г (11,99 ммоля) (3,5-диметоксибензил) метиламина, и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 100 мл CH2Cl2, промывали 100 мл 0,5н. НСl, 100 мл Н2О и проводили обратную экстракцию водных слоев 100 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 3,20 г (82%) (3,5-диметилбензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(EI):391 (M+).
Пример 108
(3,5-Диметилбензил)метиламид 2-метансульфонил-4-о-толил-пиримидин -5-карбоновой кислоты
К раствору 3,20 г (8,17 ммоля) (3,5-диметилбензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в 70 мл CH2Cl2 при 5°С добавляли 3,52 г (20,43 ммоля) 3-хлорнадбензойной кислоты (70%) и реакционную смесь перемешивали при КТ в течение 3 ч. После добавления 100 мл насыщенного раствора NаНСО3 слои разделяли, органическую фазу промывали насыщенным раствором NаНСО3, сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 4:1), при этом получали 2,55 г (73%) (3,5-диметилбензил)метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(EI):423 (М+).
Пример 109
(3,5-Диметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-диметилбензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-диметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толил-пиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(ISP):444,5 (М+Н+).
Пример 110
(3,5-Диметил6ензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-диметилбензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-диметилбензил)-метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(EI):430 (M+).
Пример 111
(3,5-Диметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-диметилбензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-диметилбензил) метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):433,5 (М+Н+).
Пример 112
2-(3,5-Бис-трифторметилфенил)-N-метил-N-(2-метилсульфанил-4-о-толилпиримидин-5-ил)изобутиоамид
а) Трет-бутидовый эфир (2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты
К раствору 2,33 г (8,95 ммоля) 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты, 1,25 мл триэтиламина (8,95 ммоля) и 1,68 мл (17,9 ммоля) трет-бутанола в 30 мл ТГФ добавляли 1,97 мл (8,95 ммоля) дифенилфосфорилазида и полученный раствор кипятили с обратным холодильником в течение 12 ч. После выпаривания растворителя остаток распределяли между CH2Cl2 и Н2О. Водную фазу дважды экстрагировали CH2Cl2, объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 15:1), при этом получали 1,95 г (65%) трет-бутилового эфира (2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в виде бесцветного твердого вещества, MC(TSP):331 (M+).
б) Трет-бутиловый эфир метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты
К раствору 1,9 г (5,73 ммоля) трет-бутилового эфира (2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в 15 мл N,N-диметилформамида добавляли 0,29 г (7,45 ммоля) гидрида натрия (60%-ная дисперсия в минеральном масле) и реакционную смесь перемешивали в течение 1 ч. После добавления при 0°С 0,57 мл (9,17 ммоля) метилиодида реакционную смесь перемешивали в течение 3 ч. Затем реакционную смесь распределяли между 75 мл Н2О, 75 мл солевого раствора и 75 мл CH2Cl2. Фазы разделяли и водный слой дважды промывали 75 мл CH2Cl2. Объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 15:1), при этом получали 1,95 г (98%) трет-бутилового эфира метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в виде бесцветного масла, MC(TSP):345 (M+).
в) Метил(2-метилсульфанил-4-о-толидпиримидин-5-ил)амин
Раствор 1,95 г (5,64 ммоля) трет-бутилового эфира метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в 30 мл 30 МеОН/2 н. НСl перемешивали при 50°С в течение 3 ч. После выпаривания растворителя остаток распределяли между 40 мл 1 н. NaOH и 40 мл CH2Cl2. Фазы разделяли, водный слой дважды промывали 50 мл CH2Cl2. Объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 10:1), при этом получали 1,30 г (94%) метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)амина в виде твердого вещества белого цвета, МС(ЕI):245 (М+).
г) 2-(3.5-Бис-трифторметилфенил)-N-метил-N-(2-метилсульфанил-4-о-толилпиримидин-5-ил)изобутирамид
К раствору 1,30 г (5,3 ммоля) метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)амина и 1,36 мл (7,95 ммоля) N-этилдиизопропиламина в 15 мл CH2Cl2 добавляли раствор 1,30 г (5,3 ммоля) 2-(3,5-бис-трифторметилфенил)-2-метилпропионилхлорида в 5 мл CH2Cl2 и реакционную смесь перемешивали при КТ в течение 24 ч. Затем реакционную смесь выливали в 50 мл 0,5 н. NаОН. Фазы разделяли и водный слой дважды промывали 50 мл CH2Cl2. Объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 10:1), при этом получали 2,30 г (82%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-метилсульфанил-4-о-толилпиримидин-5-ил)изобутирамида в виде твердого вещества белого цвета, tпл 124-125°С, MC(TSP):528,2 (M+H+).
Пример 113
2-(3,5-Бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толидпиримидин-5-ил)-N-метилизобутирамид
К раствору 2,20 г (4,17 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты в 50 мл CH2Cl2 при 5°С добавляли 2,57 г (10,43 ммоля) 3-хлорнадбензойной кислоты (70%) и реакционную смесь перемешивали при КТ в течение 3 ч. После добавления 100 мл насыщенного раствора NаНСО3 слои разделяли, органичекую фазу промывали насыщенным раствором NaHCO3, сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 10:1), при этом получали 2,30 г (98%) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в виде бесцветной пены, MC(ISP):560,2 (M+H+).
Пример 114
2-(3,5-Бис-трифторметилфенил)-N-метил-N-[2-(4-метилпиперазин-1-ил)-4-о-тодидпиримидин-5-ид]изобутирамид
К раствору 0,5 г (0,89 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 10 мл диоксана добавляли 0,25 мл (2,23 ммоля) 1-метилпиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,37 г (71%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-ил]изобутирамида в виде бесцветного твердого вещества, tпл 149-151°С, MC(ISP):580,1 (M+H+).
Пример 115
2-(3,5-Бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил)изобутирамид
К раствору 0,4 г (0,71 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метил-изобутирамида в 10 мл диоксана добавляли 0,19 мл (2,14 ммоля) морфолина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат), при этом получали 0,34 г (84%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил)изобутирамида в виде бесцветного твердого вещества, tпл 151-152°C, MC(ISP):567,1 (M+H+).
Пример 116
2-(3,5-Бис-триФторметидфенил)-N-[2-(2-диметидаминоэтиламино)-4-о-толилпиримидин-5-ил]-N-метидизобутирамид
К раствору 0,35 г (0,63 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 10 мл диоксана добавляли 0,20 мл (1,88 ммоля) 2-диметиламиноэтиламина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH), при этом получали 0,23 г (64%) 2-(3,5-бис-трифторметилфенил)-N-[2-(2-диметиламиноэтиламино)-4-о-толилпиримидин-5-ил]-N-метилизобутирамида в виде бесцветного твердого вещества, tпл 143-144°C, MC(ISP):568,3 (M+H+).
Пример 117
2-(3,5-Бис-трифторметилфенил)-N-[2-(2-диметиламиноэтокси)-4-о-толидпиримидин-5-ил]-N-метилизобутирамид
К раствору 0,4 г (0,71 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 15 мл ацетонитрила добавляли 0,09 мл (0,93 ммоля) 2-диметиламиноэтанола, 1,17 г (3,57 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 40 мл CH2Cl2 и 40 мл Н2О. Водный слой экстрагировали 40 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,36 г (88%) 2-(3,5-бис-трифторметилфенил)-N-[2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-ил]-N-метилизобутирамида в виде бесцветного твердого вещества, tпл 140-141°С, MC(ISP):569,2 (M+H+).
Пример 118
2-(3,5-Бис-трифторметилфенил)-N-метил-N-[2-(2-морфолин-4-илэтокси)-4-о-толилпиримидин-5-ил] изобутирамид
К раствору 0,4 г (0,71 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 15 мл ацетонитрила добавляли 0,12 г (0,93 ммоля) N-(2-гидроксиметил)морфолина, 1,17 г (3,57 ммоля) Сs2СО3 и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 40 мл СН2Сl2 и 40 мл Н2О. Водный слой экстрагировали 40 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,35 г (80%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-[2-(2-морфолин-4-илэтокси)-4-о-толилпиримидин-5-ил]изобутирамида в виде бесцветной пены, MC(ISP):611,1 (M+H+).
Пример А
Таблетки следующего состава приготавливают обычным методом, мг/табл.:
Действующее вещество 5
Лактоза 45
Кукурузный крахмал 15
Микрокристаллическая целлюлоза 34
Стеарат магния 1
Масса таблетки 100
Пример Б
Приготавливают капсулы следующего состава, мг/капс.:
Действующее вещество 10
Лактоза 155
Кукурузный крахмал 30
Тальк 5
Масса содержимого капсулы 200
Действующее вещество, лактозу и кукурузный крахмал сначала перемешивают в смесителе, а затем обрабатывают в измельчающей машине. Смесь возвращают в смеситель, добавляют тальк и тщательно перемешивают. Смесью с помощью машины заполняют желатиновые капсулы с твердым покрытием.
Пример В
Приготавливают суппозитории следующего состава, мг/суппоз.:
Действующее вещество 15
Масса наполнителя суппозитория 1285
Всего 1300
Массу наполнителя суппозитория расплавляют в стеклянном или стальном резервуаре, тщательно перемешивают и охлаждают до 45°С. Затем к ней добавляют тонкоизмельченное действующее вещество и перемешивают до полного диспергирования. Смесью заполняют пресс-формы для суппозиториев требуемого размера, дают остыть, затем суппозитории удаляют из пресс-форм и упаковывают по отдельности в вощеную бумагу или металлическую фольгу.
Claims (11)
1. Соединения общей формулы
где R1 означает водород или галоген;
R2 означает водород, галоген, низший алкил или низший алкокси;
R1 и R2 вместе с двумя атомами углеродного цикла могут означать группу -СН=СН-СН=СН-;
R3 означает галоген, трифторметил, низший алкил или низший алкокси;
R4, R4’ независимо друг от друга каждый означает водород или низший алкил,
R5 означает низший алкил, низший алкокси, амино, фенил, гидрокси(низший)алкил, циано(низший)алкил, карбамоил(низший)алкил, пиридил, пиримидил, -(СH2)n-пиперазинил, необязательно замещенный одной или двумя низшими алкильными группами или гидрокси(низшим)алкилом, -(СH2)n-морфолинил, -(СH2)n-пиперидинил, -(СH2)n+1-имидазолил, низший алкилсульфанил, низший алкилсульфонил,бензиламино,-NH-(CH2)n+1 N(R4’’)2, -(CH2)n+1N(R4’’)2, -O-(CH2)n+1-морфолинил, -O-(CH2)n+1-пиперидинил или -O-(СН2)n+1N(R4’’)2,где R4’’ означает водород или низший алкил, где n = 0-2;
Х означает -C(O)N(R4’’)- или -N(R4’’)C(O)-,
и их фармацевтически приемлемые кислотно-аддитивные соли.
2. Соединение по п.1, в котором Х означает -C(O)N(R4’’)-; R4’’ означает метил, а R5 означает пиперазинил, необязательно замещенный одной или двумя метильными группами.
3. Соединение по п.2, которое означает
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-пиперазин-1 -илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5R)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил) пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5R)-2-(3,5-диметилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил) метиламид (3R,5R)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпи-перазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты и
(3,5-бис-трифторметилбензил)метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты.
4. Соединение по п.1, в котором Х означает -C(O)N(R4’’)-, R4’’ означает метил, а R5 означает морфолинил или –O(CH2)2-морфолинил.
5. Соединение по п.4, которое означает:
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты и
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафталин-1-илпиримидин-5-карбоновой кислоты.
6. Соединение по п.1, в котором Х означает -C(O)N(R4’’)-, R4’’ означает метил, а R5 означает -NН(СН2)2N(СН3)2, -O(СН2)2N(СН3)2 или -O(СН2)3N(СН3)2
7. Соединение по п.6, которое означает
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты или
(3,5-бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты.
8. Соединение по п.1, в котором Х означает -N(R4’’)C(O)-, R4’’ означает метил, а R5 означает морфолинил или пиперазинил, необязательно замещенный низшим алкилом.
9. Соединение по п.8, которое означает
2-(3,5-бис-трифторметилфенил)-N-метил-N-[2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-ил]изобутирамид и
2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил)изобутирамид.
10. Фармацевтическая композиция, обладающая свойствами антагонистов рецептора NK-1, содержащая одно или несколько соединений по любому из пп.1-9 и фармацевтически приемлемые эксципиенты.
11. Фармацевтическая композиция по п.10 для лекарственного средства для лечения заболеваний, опосредованных NK-1 рецептором.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP99110483.7 | 1999-05-31 | ||
| EP99110483 | 1999-05-31 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2001133458A RU2001133458A (ru) | 2003-06-27 |
| RU2243221C2 true RU2243221C2 (ru) | 2004-12-27 |
Family
ID=8238271
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2001133458/04A RU2243221C2 (ru) | 1999-05-31 | 2000-05-24 | Производные 4-фенилпиримидина и фармацевтическая композиция |
Country Status (36)
| Country | Link |
|---|---|
| US (1) | US6274588B1 (ru) |
| EP (1) | EP1187815B1 (ru) |
| JP (1) | JP3590592B2 (ru) |
| KR (1) | KR100440106B1 (ru) |
| CN (1) | CN1166643C (ru) |
| AR (1) | AR024146A1 (ru) |
| AT (1) | ATE317389T1 (ru) |
| AU (1) | AU770786B2 (ru) |
| BR (1) | BR0011127A (ru) |
| CA (1) | CA2375671C (ru) |
| CO (1) | CO5170520A1 (ru) |
| CZ (1) | CZ20014271A3 (ru) |
| DE (1) | DE60025918T2 (ru) |
| DK (1) | DK1187815T3 (ru) |
| ES (1) | ES2257294T3 (ru) |
| GC (1) | GC0000191A (ru) |
| HK (1) | HK1046528B (ru) |
| HR (1) | HRP20010871A2 (ru) |
| HU (1) | HUP0201315A3 (ru) |
| IL (2) | IL146460A0 (ru) |
| JO (1) | JO2261B1 (ru) |
| MA (1) | MA26793A1 (ru) |
| MX (1) | MXPA01012089A (ru) |
| MY (1) | MY122731A (ru) |
| NO (1) | NO321354B1 (ru) |
| NZ (1) | NZ515407A (ru) |
| PE (1) | PE20010153A1 (ru) |
| PL (1) | PL353441A1 (ru) |
| PT (1) | PT1187815E (ru) |
| RU (1) | RU2243221C2 (ru) |
| SI (1) | SI1187815T1 (ru) |
| TR (1) | TR200103457T2 (ru) |
| TW (1) | TW550258B (ru) |
| WO (1) | WO2000073279A1 (ru) |
| YU (1) | YU84901A (ru) |
| ZA (1) | ZA200109163B (ru) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8372849B2 (en) | 2008-04-21 | 2013-02-12 | Taigen Biotechnology Co., Ltd. | Heterocyclic compounds |
| RU2756055C2 (ru) * | 2017-01-10 | 2021-09-24 | Нэшнл Хелт Рисерч Инститьютс | Гетероциклические соединения и их применение |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AUPQ514600A0 (en) | 2000-01-18 | 2000-02-10 | James Cook University | Brain injury treatment |
| EP1318147A1 (en) * | 2000-09-14 | 2003-06-11 | Ajinomoto Co., Inc. | Novel pyrimidine derivative and novel pyridine derivative |
| WO2002066036A1 (en) * | 2001-02-20 | 2002-08-29 | Bristol-Myers Squibb Company | 2,4-disubstituted pyrimidine-5-carboxamide derivatives as kcnq potassium channel modulators |
| GB0201882D0 (en) * | 2002-01-28 | 2002-03-13 | Novartis Ag | Organic compounds |
| US20070099938A1 (en) * | 2003-10-24 | 2007-05-03 | Ono Pharmaceutical Co., Ltd. | Antistress drug and medical use thereof |
| HUP0400405A3 (en) * | 2004-02-10 | 2009-03-30 | Sanofi Synthelabo | Pyrimidine derivatives, process for producing them, their use, pharmaceutical compositions containing them and their intermediates |
| US7767680B2 (en) | 2004-11-03 | 2010-08-03 | Vertex Pharmaceuticals Incorporated | Ion channel modulators and methods of use |
| CA2601935C (en) * | 2005-02-22 | 2013-04-09 | F. Hoffmann-La Roche Ag | Nk1 antagonists |
| WO2006089674A2 (en) | 2005-02-25 | 2006-08-31 | F.Hoffmann-La Roche Ag | Tablets with improved drug substance dispersibility |
| CA2612227C (en) * | 2005-06-14 | 2014-04-22 | Taigen Biotechnology Co., Ltd. | Pyrimidine compounds |
| US8580805B2 (en) * | 2010-08-31 | 2013-11-12 | Hubert Maehr | Pyrimidine carboxamide derivatives |
| US10420341B2 (en) * | 2015-01-30 | 2019-09-24 | Basf Se | Herbicidal phenylpyrimidines |
| KR102006547B1 (ko) * | 2017-11-16 | 2019-08-01 | 서울대학교산학협력단 | 벤즈아미드 유도체 화합물, 이의 제조방법 및 이를 유효성분으로 함유하는 염증질환의 치료 또는 예방용 약학적 조성물 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3940394A (en) * | 1972-03-31 | 1976-02-24 | Santilli Arthur A | 2-pyrimidinylthio)alkanoic acids, esters, amides and hydrazides |
| US4015000A (en) * | 1972-09-29 | 1977-03-29 | Ciba-Geigy Corporation | 6-Acylamino-penam-3-carboxylic and 7-acylamino-3-cephem-4-carboxylic acids |
| WO1997009315A1 (en) * | 1995-09-01 | 1997-03-13 | Signal Pharmaceuticals, Inc. | Pyrimidine carboxamides and related compounds and methods for treating inflammatory conditions |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4698340A (en) | 1984-07-19 | 1987-10-06 | Fujisawa Pharmaceutical Co., Ltd. | Pyrimidine derivatives, processes for preparation thereof and composition containing the same |
| DE3614060A1 (de) * | 1986-04-23 | 1987-10-29 | Schering Ag | Pyrimidin-derivate, verfahren zu ihrer herstellung und ihre verwendung als fungizide |
| US5516775A (en) * | 1992-08-31 | 1996-05-14 | Ciba-Geigy Corporation | Further use of pyrimidine derivatives |
| CN1067683C (zh) | 1993-12-29 | 2001-06-27 | 默克·夏普-道姆公司 | 取代的吗啉衍生物及其作为治疗剂的用途 |
| US5972938A (en) | 1997-12-01 | 1999-10-26 | Merck & Co., Inc. | Method for treating or preventing psychoimmunological disorders |
-
2000
- 2000-05-22 US US09/575,382 patent/US6274588B1/en not_active Expired - Fee Related
- 2000-05-22 TW TW089109829A patent/TW550258B/zh not_active IP Right Cessation
- 2000-05-24 DK DK00927234T patent/DK1187815T3/da active
- 2000-05-24 BR BR0011127-9A patent/BR0011127A/pt not_active Application Discontinuation
- 2000-05-24 YU YU84901A patent/YU84901A/sh unknown
- 2000-05-24 JP JP2000621345A patent/JP3590592B2/ja not_active Expired - Fee Related
- 2000-05-24 AT AT00927234T patent/ATE317389T1/de not_active IP Right Cessation
- 2000-05-24 SI SI200030813T patent/SI1187815T1/sl unknown
- 2000-05-24 CA CA002375671A patent/CA2375671C/en not_active Expired - Fee Related
- 2000-05-24 MX MXPA01012089A patent/MXPA01012089A/es active IP Right Grant
- 2000-05-24 HU HU0201315A patent/HUP0201315A3/hu unknown
- 2000-05-24 RU RU2001133458/04A patent/RU2243221C2/ru not_active IP Right Cessation
- 2000-05-24 EP EP00927234A patent/EP1187815B1/en not_active Expired - Lifetime
- 2000-05-24 HR HR20010871A patent/HRP20010871A2/hr not_active Application Discontinuation
- 2000-05-24 TR TR2001/03457T patent/TR200103457T2/xx unknown
- 2000-05-24 PL PL00353441A patent/PL353441A1/xx unknown
- 2000-05-24 NZ NZ515407A patent/NZ515407A/xx unknown
- 2000-05-24 KR KR10-2001-7015393A patent/KR100440106B1/ko not_active Expired - Fee Related
- 2000-05-24 CZ CZ20014271A patent/CZ20014271A3/cs unknown
- 2000-05-24 AU AU45677/00A patent/AU770786B2/en not_active Ceased
- 2000-05-24 WO PCT/EP2000/004701 patent/WO2000073279A1/en not_active Ceased
- 2000-05-24 HK HK02107643.4A patent/HK1046528B/zh not_active IP Right Cessation
- 2000-05-24 CN CNB008082758A patent/CN1166643C/zh not_active Expired - Fee Related
- 2000-05-24 IL IL14646000A patent/IL146460A0/xx active IP Right Grant
- 2000-05-24 DE DE60025918T patent/DE60025918T2/de not_active Expired - Fee Related
- 2000-05-24 ES ES00927234T patent/ES2257294T3/es not_active Expired - Lifetime
- 2000-05-24 PT PT00927234T patent/PT1187815E/pt unknown
- 2000-05-26 PE PE2000000508A patent/PE20010153A1/es not_active Application Discontinuation
- 2000-05-28 JO JO200083A patent/JO2261B1/en active
- 2000-05-29 CO CO00039590A patent/CO5170520A1/es not_active Application Discontinuation
- 2000-05-29 AR ARP000102643A patent/AR024146A1/es not_active Application Discontinuation
- 2000-05-29 MY MYPI20002384A patent/MY122731A/en unknown
- 2000-05-30 GC GCP2000684 patent/GC0000191A/en active
-
2001
- 2001-11-06 ZA ZA200109163A patent/ZA200109163B/en unknown
- 2001-11-12 IL IL146460A patent/IL146460A/en not_active IP Right Cessation
- 2001-11-22 NO NO20015700A patent/NO321354B1/no unknown
- 2001-11-26 MA MA26424A patent/MA26793A1/fr unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3940394A (en) * | 1972-03-31 | 1976-02-24 | Santilli Arthur A | 2-pyrimidinylthio)alkanoic acids, esters, amides and hydrazides |
| US4015000A (en) * | 1972-09-29 | 1977-03-29 | Ciba-Geigy Corporation | 6-Acylamino-penam-3-carboxylic and 7-acylamino-3-cephem-4-carboxylic acids |
| WO1997009315A1 (en) * | 1995-09-01 | 1997-03-13 | Signal Pharmaceuticals, Inc. | Pyrimidine carboxamides and related compounds and methods for treating inflammatory conditions |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8372849B2 (en) | 2008-04-21 | 2013-02-12 | Taigen Biotechnology Co., Ltd. | Heterocyclic compounds |
| RU2756055C2 (ru) * | 2017-01-10 | 2021-09-24 | Нэшнл Хелт Рисерч Инститьютс | Гетероциклические соединения и их применение |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2244710C2 (ru) | Производные 5-фенилпиримидина и фармацевтическая композиция | |
| RU2236402C2 (ru) | Производные 3-фенилпиридина и фармацевтическая композиция на их основе | |
| RU2238264C2 (ru) | Производные бензола или пиридина и фармацевтическая композиция на их основе | |
| RU2243221C2 (ru) | Производные 4-фенилпиримидина и фармацевтическая композиция | |
| JP3399900B2 (ja) | 4−フェニル−ピリジン誘導体 | |
| JP4118673B2 (ja) | ニューロキニン1受容体アンタゴニストとしての4−フェニル−ピリジン誘導体 | |
| RU2284997C2 (ru) | Производные пиримидина и фармацевтическая композиция | |
| MXPA01008559A (en) | Phenyl- and pyridinyl derivatives |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20080525 |