RU2089543C1 - Method of preparing piperidone-4 (variants) derivatives and lower alkyl ester derivatives of 3-(n-lower alkyl-n- 3-2-carbolower alkoxy lower alkyl) (amino) 2,3-ene acids - Google Patents
Method of preparing piperidone-4 (variants) derivatives and lower alkyl ester derivatives of 3-(n-lower alkyl-n- 3-2-carbolower alkoxy lower alkyl) (amino) 2,3-ene acids Download PDFInfo
- Publication number
- RU2089543C1 RU2089543C1 RU94014982A RU94014982A RU2089543C1 RU 2089543 C1 RU2089543 C1 RU 2089543C1 RU 94014982 A RU94014982 A RU 94014982A RU 94014982 A RU94014982 A RU 94014982A RU 2089543 C1 RU2089543 C1 RU 2089543C1
- Authority
- RU
- Russia
- Prior art keywords
- lower alkyl
- derivatives
- phenyl
- alkoxy
- amino
- Prior art date
Links
- 125000000217 alkyl group Chemical group 0.000 title claims abstract description 23
- 125000003545 alkoxy group Chemical group 0.000 title claims abstract description 22
- 238000000034 method Methods 0.000 title claims abstract description 20
- 239000002253 acid Substances 0.000 title claims abstract 5
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 title claims description 13
- 125000005907 alkyl ester group Chemical group 0.000 title claims description 5
- 150000007513 acids Chemical class 0.000 title claims 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 18
- 239000001257 hydrogen Substances 0.000 claims abstract description 12
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 12
- 238000007363 ring formation reaction Methods 0.000 claims abstract description 9
- 150000001735 carboxylic acids Chemical class 0.000 claims abstract description 3
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims abstract 6
- -1 alkali metal alkoxides Chemical class 0.000 claims description 7
- 230000002378 acidificating effect Effects 0.000 claims description 6
- 229910052783 alkali metal Inorganic materials 0.000 claims description 4
- 238000010438 heat treatment Methods 0.000 claims description 4
- 238000005984 hydrogenation reaction Methods 0.000 claims description 4
- 150000002148 esters Chemical class 0.000 claims description 3
- 239000012442 inert solvent Substances 0.000 claims description 2
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical class NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 claims 1
- 150000005215 alkyl ethers Chemical class 0.000 claims 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims 1
- 150000002763 monocarboxylic acids Chemical class 0.000 claims 1
- 150000001875 compounds Chemical class 0.000 abstract description 9
- 238000006476 reductive cyclization reaction Methods 0.000 abstract description 4
- 239000000126 substance Substances 0.000 abstract description 4
- XUWHAWMETYGRKB-UHFFFAOYSA-N piperidin-2-one Chemical class O=C1CCCCN1 XUWHAWMETYGRKB-UHFFFAOYSA-N 0.000 abstract description 2
- 238000002360 preparation method Methods 0.000 abstract description 2
- 230000000694 effects Effects 0.000 abstract 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- VQHHMWWQNKUPKH-UHFFFAOYSA-N 1,2,5-trimethylpiperidin-4-one Chemical compound CC1CC(=O)C(C)CN1C VQHHMWWQNKUPKH-UHFFFAOYSA-N 0.000 description 4
- ZFDIRQKJPRINOQ-HWKANZROSA-N Ethyl crotonate Chemical compound CCOC(=O)\C=C\C ZFDIRQKJPRINOQ-HWKANZROSA-N 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- 235000019441 ethanol Nutrition 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- ZFDIRQKJPRINOQ-UHFFFAOYSA-N transbutenic acid ethyl ester Natural products CCOC(=O)C=CC ZFDIRQKJPRINOQ-UHFFFAOYSA-N 0.000 description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- FFUAGWLWBBFQJT-UHFFFAOYSA-N hexamethyldisilazane Chemical compound C[Si](C)(C)N[Si](C)(C)C FFUAGWLWBBFQJT-UHFFFAOYSA-N 0.000 description 3
- 150000002431 hydrogen Chemical class 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 238000006114 decarboxylation reaction Methods 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 238000000921 elemental analysis Methods 0.000 description 2
- 239000001307 helium Substances 0.000 description 2
- 229910052734 helium Inorganic materials 0.000 description 2
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 238000002329 infrared spectrum Methods 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- UCUUFSAXZMGPGH-UHFFFAOYSA-N penta-1,4-dien-3-one Chemical class C=CC(=O)C=C UCUUFSAXZMGPGH-UHFFFAOYSA-N 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- PPASLZSBLFJQEF-RKJRWTFHSA-M sodium ascorbate Substances [Na+].OC[C@@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RKJRWTFHSA-M 0.000 description 2
- 238000004611 spectroscopical analysis Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- OXTNCQMOKLOUAM-UHFFFAOYSA-N 3-Oxoglutaric acid Chemical compound OC(=O)CC(=O)CC(O)=O OXTNCQMOKLOUAM-UHFFFAOYSA-N 0.000 description 1
- 229910021578 Iron(III) chloride Inorganic materials 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 239000002360 explosive Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- RBTARNINKXHZNM-UHFFFAOYSA-K iron trichloride Chemical compound Cl[Fe](Cl)Cl RBTARNINKXHZNM-UHFFFAOYSA-K 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- 150000007934 α,β-unsaturated carboxylic acids Chemical class 0.000 description 1
Images
Landscapes
- Hydrogenated Pyridines (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
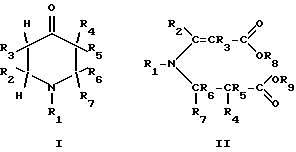
Изобретение относится к общей органической химии, конкретно, к способам получения производных пиперидона-4 (I), содержащих заместители в различных положениях [1-6] а также к новым производным алкиловых эфиров три-(N-алкил-N(3-(2-карбоалкоксиалкил)-2,3-непредельных карбоновых кислот (II), которые могут быть использованы для синтеза производных пиперидона-4. Производные пиперидона-4 широко используются для синтеза лекарственных препаратов в промышленности [1,3,4]
где R1-R7 представляют собой водород, фенил, низший алкокси, или низший алкил, возможно замещенный финилом или низшим алкокси, R8, R9 низший алкил.The invention relates to general organic chemistry, in particular, to methods for producing piperidone-4 (I) derivatives containing substituents in various positions [1-6] and also to new derivatives of tri- (N-alkyl-N (3- (2) alkyl esters -carboalkoxyalkyl) -2,3-unsaturated carboxylic acids (II), which can be used to synthesize piperidone-4 derivatives. piperidone-4 derivatives are widely used for the synthesis of drugs in industry [1,3,4]
where R 1 -R 7 are hydrogen, phenyl, lower alkoxy, or lower alkyl, optionally substituted with phenyl or lower alkoxy, R 8 , R 9 lower alkyl.
Известны следующие способы синтеза пиперидонов-4:
1. Конденсацией альдегидов с эфирами ацетондикарбоновой кислоты в присутствии первичных аминов или аммиака [2,3]
где R, R1, R2 и R6 представляют собой H, алкил, арил и др.The following methods for the synthesis of piperidones-4 are known:
1. The condensation of aldehydes with esters of acetone dicarboxylic acid in the presence of primary amines or ammonia [2,3]
where R, R 1 , R 2 and R 6 represent H, alkyl, aryl, etc.
Недостатком этого способа является возможность получать только 1,2,6-замещенные пиперидоны-4. The disadvantage of this method is the ability to obtain only 1,2,6-substituted piperidones-4.
2. Взаимодействием дивинилкетонов и первичных аминов [1,4,5,6]
Недостатком этого способа является сложность синтеза исходных дивенилкетонов и их нестойкость (большое количество отходов, использование взрывоопасных производных ацетилена).2. The interaction of divinyl ketones and primary amines [1,4,5,6]
The disadvantage of this method is the complexity of the synthesis of the starting divinyl ketones and their instability (a large amount of waste, the use of explosive derivatives of acetylene).
Наиболее близким является способ получения присоединением первичных аминов к эфирам α, β-ненасыщенных карбоновых кислот с последующей циклизацией по Дикману [8] по следующей схеме:
где R, R' представляет собой H, алкил, арил и др.The closest is the method of obtaining the addition of primary amines to esters of α, β-unsaturated carboxylic acids with subsequent cyclization according to Dickman [8] according to the following scheme:
where R, R 'represents H, alkyl, aryl, etc.
Циклизация (IIIa) осуществляется под действием алконолята щелочного металла, последующий гидролиз и декарбоксилирование осуществляются путем нагревания (IVa) в кислой среде. Cyclization (IIIa) is carried out under the action of an alkali metal alkonolate, subsequent hydrolysis and decarboxylation are carried out by heating (IVa) in an acidic medium.
Этот способ выбран в качестве прототипа. This method is selected as a prototype.
Недостатком способа является возможность получения с хорошим выходом только 1-замещенных производных пиперидона-4, а структуры с заместителями в кольце получаются с очень низким выходом до 10%
Целью изобретения является разработка простого и технологичного способа получения производных пиперидона-4 с высоким выходом, которые могут содержать различные заместители в кольце.The disadvantage of this method is the possibility of obtaining in good yield only 1-substituted derivatives of piperidone-4, and structures with substituents in the ring are obtained with a very low yield of up to 10%
The aim of the invention is to develop a simple and technologically advanced method for producing piperidone-4 derivatives in high yield, which may contain various substituents in the ring.
Способ заключается в восстановительной циклизации производных алкиловых эфиров 3-(N-алкил-N(3-(2-карбоалкоксиалкил))амино)-2,3-непредельных карбоновых кислот (II) с последующей обработкой полученного соединения (V) в кислой среде. Процесс протекает по следующей схеме:
где R1-R7 представляет собой водород, фенил, низший алкокси, или низший алкил, возможно замещенный фенилом или низшим алкокси; R8, R9 низший алкил.The method consists in reductive cyclization of 3- (N-alkyl-N (3- (2-carboalkoxyalkyl)) amino) -2,3-unsaturated carboxylic acid alkyl ester derivatives, followed by treatment of the resulting compound (V) in an acidic medium. The process proceeds as follows:
where R 1 -R 7 represents hydrogen, phenyl, lower alkoxy, or lower alkyl, possibly substituted by phenyl or lower alkoxy; R 8 , R 9 lower alkyl.
Процесс восстановительной циклизации осуществляется при обработке соединений формулы (II) щелочным металлом в среде растворителя, являющегося донором протона реакции, например, низшего спирта или его смеси с инертным в данной реакции растворителем. Выход на данной стадии составляет 80-90% Гидролиз и декарбоксилирование проводят при нагревании в кислой среде (выход 90-95% ). Общая методика синтеза (I) по вариантам восстановительной циклизации приведена в примере 1. The reductive cyclization process is carried out by treating the compounds of formula (II) with an alkali metal in a solvent which is a donor of the proton of the reaction, for example, a lower alcohol or a mixture thereof with an inert solvent in this reaction. The yield at this stage is 80-90%. Hydrolysis and decarboxylation are carried out by heating in an acidic medium (yield 90-95%). The general synthesis procedure (I) for reductive cyclization variants is given in Example 1.
Соединения формулы (I) в соответствии с изобретением могут быть получены и двухстадийным способом путем гидрирования соединений формулы (II), циклизацией полученных гидрированных производных III с последующей обработкой полученных соединений (IV) в кислой среде по следующей схеме:
где R1-R7 представляют собой водород, фенил, низший алкокси, или низший алкил, возможно замещенный фенилом или низшим алкокси; R8, R9 низший алкил.The compounds of formula (I) in accordance with the invention can be obtained in a two-stage way by hydrogenation of compounds of formula (II), cyclization of the obtained hydrogenated derivatives III, followed by treatment of the obtained compounds (IV) in an acidic medium according to the following scheme:
where R 1 -R 7 represent hydrogen, phenyl, lower alkoxy, or lower alkyl, possibly substituted by phenyl or lower alkoxy; R 8 , R 9 lower alkyl.
Процесс гидрирования осуществляется методом каталитического гидрирования, например, водородом в присутствии палладиевого катализатора. Могут быть использованы и другие катализаторы гидрирования. The hydrogenation process is carried out by catalytic hydrogenation, for example, with hydrogen in the presence of a palladium catalyst. Other hydrogenation catalysts may be used.
Общая методика синтеза (I) по варианту постадийного восстановления и циклизации приведена в примере 2. The general synthesis procedure (I) for the stepwise recovery and cyclization option is shown in Example 2.
Исходные соединения общей формулы (II) для получения производных пиперидона по способу, варианты которого описаны выше, являются новыми соединениями и легко могут быть получены известными методами. The starting compounds of the general formula (II) for the preparation of piperidone derivatives according to the method described above are novel compounds and can easily be prepared by known methods.
Пример 1. (+)-1,2,5-триметилпиперидин-4-он. Example 1. (+) - 1,2,5-trimethylpiperidin-4-one.
К смеси 122 г (0,5 моль) этилового эфира 3-(N-метил-N(3-(2-карбометоксипропил))амино) кротоновой кислоты и 400 мл этилового спирта при перемешивании прибавляют 25,3 г (1,1 моль) металлического натрия, отгоняют спирт, после чего к реакционной смеси прибавляют 450 мл 20%-ного раствора соляной кислоты и кипятят до отрицательной реакции на кетоэфир (IV) c хлоридом железа. Реакционную смесь охлаждают, нейтрализуют раствором щелочи и многократно экстрагируют эфиром. После перегонки получают 110 г (+)-1,2,5-триметилпиперидин-4-она с Tкип.=80-83oC при 11 мм рт.ст. Выход 86%
ИК спектр (CHCl3, ν, см-1); 1720(C=0), 2800(CH3-N).To a mixture of 122 g (0.5 mol) of 3- (N-methyl-N (3- (2-carbomethoxypropyl)) amino) crotonic acid ethyl ester and 400 ml of ethyl alcohol, 25.3 g (1.1 mol) are added with stirring ) of sodium metal, the alcohol is distilled off, after which 450 ml of a 20% hydrochloric acid solution are added to the reaction mixture and boiled until a negative reaction to the ketoester (IV) with ferric chloride is obtained. The reaction mixture is cooled, neutralized with an alkali solution and extracted repeatedly with ether. After distillation, 110 g of (+) - 1,2,5-trimethylpiperidin-4-one with T bales are obtained . = 80-83 o C at 11
IR spectrum (CHCl 3 , ν, cm -1 ); 1720 (C = 0), 2800 (CH 3 -N).
Спектр ПМР (ГМДС, d, м.д.): 2,93 кВ (1H, C2-C1H3, J 6 Гц), 2,46 кВ(1H-C5-CH3, J 6 Гц), 2616 C(3H, CH3-N), 2,06 м (4H, CH2), 1,00 д (3H, -C2H= J 6 Гц), 0,80 д (3H, -C5H= J 6 Гц).PMR spectrum (HMDS, d, ppm): 2.93 kV (1H, C 2 -C 1 H3,
Найдено,C 68.65; H 10.02; N 9.97. C8H15NO.Found, C, 68.65; H 10.02; N, 9.97. C 8 H 15 NO.
Вычислено,C 68.09; H 10,83; N 9.93. Calculated, C 68.09; H 10.83; N, 9.93.
n
Пример 2. (+)-1,2,5-триметилпиперидин-4-он. Example 2. (+) - 1,2,5-trimethylpiperidin-4-one.
К смеси 122 г (0,5 моль) этилового эфира 3-(N-метил-N(3-(2-карбометоксипропил))амино) кротоновой кислоты и 400 мл этилового спирта добавляют 30 г палладия на активированном угле, полученного из 25 г хлористого палладия. Далее через реакционную массу в течение нескольких часов барботируют водород при интенсивном перемешивании фильтруют. К фильтру прибавляют 12.68 г (0,55 моль) металлического натрия. Далее обработку реакционной массы ведут аналогично примеру 1. Получают 103,5 г (+)-1,2,5-триметилпиперидин-4-она. Выход 81% n
Найдено,C 68.50; H 10.10; N 9.87. C8H15NO.Found C, 68.50; H 10.10; N, 9.87. C 8 H 15 NO.
Вычислено,C 68.09; H 10.63; N 9.93. Calculated, C 68.09; H 10.63; N, 9.93.
ГЖХ: 1' 30'' (условия хроматографирования см. в примере 1). Совместный вкол продуктов, полученных в примерах 1 и 2, показал их идентичность. GLC: 1 '30' '(for chromatographic conditions, see Example 1). A joint injection of the products obtained in examples 1 and 2, showed their identity.
Аналогично примерам 1 и 2 получены соединения, приведенные в табл. 1. Similarly to examples 1 and 2, the compounds obtained are given in table. one.
Чистота и строение веществ, приведенных в табл. 1, подтверждены данными элементного анализа, ГЖХ, ПМР-спектроскопии и масс-спектрометрии. The purity and structure of the substances given in table. 1, confirmed by data of elemental analysis, GLC, PMR spectroscopy and mass spectrometry.
Пример 12. Этиловый эфир 3-(N-метил-N(3-(2-карбометоксипропил))амино) кротоновой кислоты. Example 12. 3- (N-methyl-N (3- (2-carbomethoxypropyl)) amino) crotonic acid ethyl ester.
Смесь 35,2 г (0,2 моль) этилового эфира 3,3-диметоксибутановой кислоты и 28,8 г (0,2 моль) этилового эфира 3-(N-метил)-2-метилпропановой кислоты, 5 мл эфирата трехфтористого бора и 200 мл абсолютного метанола кипятят в течение 10 ч. Отгоняют метиловый спирт и перегоняют при 1 мм рт.ст. собирая фракцию 90-95oC.A mixture of 35.2 g (0.2 mol) of
Выход 47.47 г (92,0% от теории), n
ИК спектр (CHCT3, ν, см-1): 1720, 1730(C=0):1570Б 2900Б 3445 (CH3N); 1670, 3010(C=C).IR spectrum (CHCT 3 , ν, cm -1 ): 1720, 1730 (C = 0): 1570B 2900B 3445 (CH 3 N); 1670, 3010 (C = C).
Спектр ПМР (ГМДС, d, м.д.): 4.30 c(1H,CH-), 3,82 д(2H, CH2-, J 7 Гц), 3.71 c(3H, CH3-C= ). 3.30 кВ(2H. -CH2-CH3), 2,73 c(3H, CH3O), 2.31 c(3H, CH3-N), 1.10 d(3H, CH3-CH2-, J 6 Гц), 1.10 кВ (3H, CH3-CH, J 7 Гц).1 H-NMR spectrum (HMDS, d, ppm): 4.30 s (1H, CH-), 3.82 d (2H, CH 2 -,
Найдено, C 55.70; H 8.70; N 6.39; C12H2NO4.Found, C, 55.70; H 8.70; N, 6.39; C 12 H 2 NO 4 .
Вычислено, C 55.50; H 8.72; N 6.42. Calculated, C 55.50; H 8.72; N, 6.42.
ГЖХ: 6' 15'' (Инертон 5% E301, E 220oC, l=2 м, d=2 мм, 25 мл/мин, гелий).GLC: 6 '15''(
Аналогично получены соединения, приведенные в табл. 2. Similarly obtained compounds are shown in table. 2.
Чистота и строение веществ, приведенных в табл. 1 и 2, подтверждены данными элементного анализа, ГЖХ и ПМР-спектроскопии. The purity and structure of the substances given in table. 1 and 2, confirmed by elemental analysis, GLC and PMR spectroscopy.
Пример 21. Получение метилового эфира 3(-N-метил-N-(3-(2-этоксикарбонил-1-метилэтил))амино-2-метилпропионовой кислоты. Example 21. Obtaining methyl ester of 3 (-N-methyl-N- (3- (2-ethoxycarbonyl-1-methylethyl)) amino-2-methylpropionic acid.
Раствор 24,30 г (0,1 моль) этилового эфира 3-(N-метил-N(3-(2-карбометоксипропил))амино) кротоновой кислоты в 100 мл метилового спирта гидрируют водородом при 50 ати и комнатной температуре в течение 4 ч. Раствор фильтруют, жидкую фазу отделяют, отгоняют метанол и перегоняют при 1 мм рт.ст. собирая фракцию 110-125oC. Повторная перегонка дает продукт с Tкип.=115-117oC/1 мм рт.ст. в количестве 22,81 г. Выход 93,1%
Спектр ПМР (ГМДС, d, м. д. ): 3.98 кВ(2H, -OCH2-, 15 Гц), 3.53 c(3H, CH3N), 3.00 м (1H, -CH-), 2.2 м (5H, N-CH''-, -CH''-C), 2.10 c(3H, CH3O-), 1.0 м (9H, -CH3-C).A solution of 24.30 g (0.1 mol) of 3- (N-methyl-N (3- (2-carbomethoxypropyl)) amino) crotonic acid ethyl ester in 100 ml of methyl alcohol is hydrogenated with hydrogen at 50 atm and room temperature for 4 hours. The solution is filtered, the liquid phase is separated, methanol is distilled off and distilled at 1 mm Hg. collecting a fraction of 110-125 o C. Re-distillation gives a product with T bales. = 115-117 o C / 1 mm RT.article in the amount of 22.81 g. Yield 93.1%
1 H-NMR spectrum (HMDS, d, ppm): 3.98 kV (2H, -OCH 2 -, 15 Hz), 3.53 s (3H, CH 3 N), 3.00 m (1H, -CH-), 2.2 m ( 5H, N-CH '-, -CH' - C), 2.10 s (3H, CH 3 O-), 1.0 m (9H, -CH 3 -C).
Найдено, C 58,92; H 9,15; N 5,85; C12H23NO4.Found C, 58.92; H 9.15; N, 5.85; C 12 H 23 NO 4 .
Вычислено, C 58,78; H 9,32; N 5,7. Calculated, C 58.78; H 9.32; N, 5.7.
n
Источники информации
1. М. В. Рубцов, А.Г. Бейчиков "Синтетические химико-теравпевтические препараты", М. Медицина, 1971, с.195-198.Sources of information
1. M.V. Rubtsov, A.G. Beichikov "Synthetic chemical and therapeutic drugs", M. Medicine, 1971, S. 195-198.
2. Robinson r. Soc. v.111/112, p.762 (1917). 2. Robinson r. Soc. v. 1111/112, p. 762 (1917).
3. Hall H.K. J. Am. Chem. v.79, N 20, p.5444 (1957). 3. Hall H.K. J. Am. Chem. v. 79, No. 20, p. 5444 (1957).
4. И. Н. Назаров, Н.С. Простаков, Н.И. Швецов ЖОХ, т.26, N 10, с. 2798 (1956). 4. I.N. Nazarov, N.S. Prostakov, N.I. Shvetsov OX, t.26,
5. И.Н. Назаров, В.А. Руденко, Изв. АН СССР ОХН, 1948, N 6, с.610. 5. I.N. Nazarov, V.A. Rudenko, Izv. USSR Academy of Sciences, 1948,
6. И.Н. Назаров и др. Изв. АН СССР ОХН, 1949, N 2, с.493. 6. I.N. Nazarov et al. Izv. USSR Academy of Sciences, 1949,
7. Ziering A. Berger L. J.Org.Chem. v.12, p.895 (1947). 7. Ziering A. Berger L. J. Org. Chem. v. 12, p. 895 (1947).
8. Mc Elvain S.M. Roring K. J.Am.Chem.Soc. v.70, Nj 5, p.1820 (1948). 8. Mc Elvain S.M. Roring K. J. Am. Chem. Soc. v. 70,
Claims (3)
где R1 R7 каждый независимо обозначает водород, фенил, низший алкокси или низший алкил, возможно замещенный фенилом или низшим алкокси,
включающий циклизацию производных эфиров аминокарбоновых кислот в присутствии алкоголятов щелочных металлов с последующей обработкой продуктов циклизации нагреванием в кислой среде, отличающийся тем, что в качестве производных эфиров аминокарбоновых кислот используют производные низших алкиловых эфиров 3-[N-низший алкил-N-[3-(2 карбонизший алкокси низший алкил)]амино]-2,3-еновых кислот общей формулы II
где R1 R7 каждый независимо обозначает водород, фенил, низший алкокси или низший алкил, возможно замещенный фенилом или низшим алкокси;
R8 и R9 обозначают низший алкил.1. The method of obtaining derivatives of piperidone-4 of General formula I
where R 1 R 7 each independently represents hydrogen, phenyl, lower alkoxy or lower alkyl, possibly substituted by phenyl or lower alkoxy,
comprising cyclization of derivatives of aminocarboxylic acid esters in the presence of alkali metal alkoxides followed by treatment of cyclization products by heating in an acidic medium, characterized in that derivatives of lower alkyl ethers 3- [N-lower alkyl-N- [3- ( 2 carbonized alkoxy lower alkyl)] amino] -2,3-enoic acids of the general formula II
where R 1 R 7 each independently represents hydrogen, phenyl, lower alkoxy or lower alkyl, possibly substituted by phenyl or lower alkoxy;
R 8 and R 9 are lower alkyl.
где R1 R7 каждый независимо обозначает водород, фенил, низший алкокси или низший алкил, возможно замещенный фенилом или низшим алкокси,
включающий циклизацию производных эфиров монокарбоновых кислот в присутствии алкоголятов щелочных металлов с последующей обработкой продуктов циклизации нагреванием в кислой среде, отличающийся тем, что в качестве производных эфиров аминокарбоновых кислот используют производные низших алкиловых эфиров 3-[N-низший алкил-N-[3-(2 карбонизший алкокси низший алкил)]амино] карбоновых кислот общей формулы III
где R1 R7 каждый независимо обозначает водород, фенил, низший алкокси или низший алкил, возможно замещенный фенилом или низшим алкокси;
R8 и R9 обозначает низший алкил, полученные гидрированием производных низших алкиловых эфиров 3-[N-низший алкил-N-[3-(2-карбонизший алкоксинизший алкил)]амино]-2, 3-еновых кислот общей формулы II
4. Производные низших алкиловых эфиров 3-[N-низший алкил-N-3-(2 карбнизший алкоксинизший алкил)]амино]-2,3-еновых кислот общей формулы II
где R1 R7 каждый независимо обозначает водород, фенил, низший алкокси или низший алкил, возможно замещенный фенилом или низшим алкокси;
R8 и R9 обозначают низший алкил.3. A method of obtaining derivatives of piperidone-4 of General formula I
where R 1 R 7 each independently represents hydrogen, phenyl, lower alkoxy or lower alkyl, possibly substituted by phenyl or lower alkoxy,
comprising cyclization of derivatives of esters of monocarboxylic acids in the presence of alkali metal alkoxides followed by treatment of cyclization products by heating in an acidic medium, characterized in that derivatives of lower alkyl esters 3- [N-lower alkyl-N- [3- ( 2 carbonized alkoxy lower alkyl)] amino] carboxylic acids of the general formula III
where R 1 R 7 each independently represents hydrogen, phenyl, lower alkoxy or lower alkyl, possibly substituted by phenyl or lower alkoxy;
R 8 and R 9 are lower alkyl obtained by hydrogenation of derivatives of lower alkyl esters of 3- [N-lower alkyl-N- [3- (2-carbonized alkoxysilane alkyl)] amino] -2, 3-enoic acids of the general formula II
4. Derivatives of lower alkyl esters of 3- [N-lower alkyl-N-3- (2 carboxy lower alkoxysilane alkyl)] amino] -2,3-enoic acids of General formula II
where R 1 R 7 each independently represents hydrogen, phenyl, lower alkoxy or lower alkyl, possibly substituted by phenyl or lower alkoxy;
R 8 and R 9 are lower alkyl.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU94014982A RU2089543C1 (en) | 1994-04-22 | 1994-04-22 | Method of preparing piperidone-4 (variants) derivatives and lower alkyl ester derivatives of 3-(n-lower alkyl-n- 3-2-carbolower alkoxy lower alkyl) (amino) 2,3-ene acids |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU94014982A RU2089543C1 (en) | 1994-04-22 | 1994-04-22 | Method of preparing piperidone-4 (variants) derivatives and lower alkyl ester derivatives of 3-(n-lower alkyl-n- 3-2-carbolower alkoxy lower alkyl) (amino) 2,3-ene acids |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU94014982A RU94014982A (en) | 1995-12-20 |
| RU2089543C1 true RU2089543C1 (en) | 1997-09-10 |
Family
ID=20155114
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU94014982A RU2089543C1 (en) | 1994-04-22 | 1994-04-22 | Method of preparing piperidone-4 (variants) derivatives and lower alkyl ester derivatives of 3-(n-lower alkyl-n- 3-2-carbolower alkoxy lower alkyl) (amino) 2,3-ene acids |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2089543C1 (en) |
-
1994
- 1994-04-22 RU RU94014982A patent/RU2089543C1/en not_active IP Right Cessation
Non-Patent Citations (1)
| Title |
|---|
| Рубцов М.В., Бейчиков А.Г. Синтетические химико-терапевтические препараты. - М.: Медицина, 1971, с. 195 - 198. Robinson R, Soc., v. 111/112, 1917, p. 762. Hall H. C., J.Am.Chem.Soc, v. 79, N 20, 1957, p. 5444. Назаров И.Н. и др. - ЖОХ, т. 26, N 10, 1956, с. 2798. Назаров И.Н. и др. - Изв. АН СССР, ОХН, N 6, 1948, с. 610. Назаров И.Н. и др. - Изв. АН СССР, ОХН, N 2, 1949, с. 493. Liering A., Beger L., J.Org.Chem, v. 12, 1947, p. 895. Mc Elvain SM., Roring K., J.Am.Chem.Soc., v. 70, N 5, 1948, r. 1820. Kuettel G.M., Mc Elvain, J.Am.Chem.Soc., v. 53, 1931, p. 2692. Howton N, J.Org.Chem, v. 10, 1945, p. 279. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US5959161A (en) | Method for producing para-menthane-3,8-diol | |
| US5840992A (en) | Process for producing 6-methylheptan-2-one | |
| Maehr et al. | A new approach to 4-substituted indoles | |
| JP3504960B2 (en) | Preparation of tertiary butyl (3R, 5S) -6-hydroxy-3,5-O-isopropylidene-3,5-dihydroxyhexanoate | |
| Pietruszka et al. | Diastereo‐and Enantiomerically Pure Allylboronates: Their Synthesis and Scope | |
| Maruyama et al. | A short and stereoselective synthesis of the (±) Prelog-Djerassi lactonic acid | |
| Bailey et al. | Pyrrolidinones derived from (S)-pyroglutamic acid. Part 1. Conformationally constrained glutamate | |
| KR102261108B1 (en) | Highly enantioselective bifunctional chiral organocatalytic compound, method for preparing the same, and method for preparing non-natural gamma-amino acid from nitrocompound using thereof | |
| RU2089543C1 (en) | Method of preparing piperidone-4 (variants) derivatives and lower alkyl ester derivatives of 3-(n-lower alkyl-n- 3-2-carbolower alkoxy lower alkyl) (amino) 2,3-ene acids | |
| CN115340482B (en) | Synthesis method of brivaracetam | |
| JPH0246590B2 (en) | ||
| Yao et al. | A practical approach to stereodefined cyclopropyl-substituted heteroarenes using a Suzuki-type reaction | |
| JPS6023345A (en) | Manufacture of glyoxylic acid ester | |
| JPS649316B2 (en) | ||
| RU2146246C1 (en) | METHOD OF PREPARING γ-амино-β--AMINO-γPHENYLBUTYRIC ACID HYDROCHLORIDE | |
| KR100625649B1 (en) | Method for preparing β-hydroxybutyl acid alkyl ester | |
| EP0872463A1 (en) | Chlorination of substituted alkenes using trichloroisocyanuric acid | |
| JPH06503328A (en) | Preparation method of α-alkyl lactone | |
| JP2004505071A (en) | Continuous production method of optically pure (S) -β-hydroxy-γ-butyrolactone | |
| HU213374B (en) | Process for producing 4-amino-5-hexenoic acid | |
| RU2283301C2 (en) | Method for preparing fluorinated benzonitrile | |
| JP3529876B2 (en) | 3-methyl-3-methoxybutanoic acid. | |
| Hochstetler et al. | Hydrochlorination of thujopsene | |
| JPH08277256A (en) | Optically active (s)-2-benzyloxycarbonylamino-1-(4-methoxyphenyl)ethanol and its production | |
| JP4266408B2 (en) | Method for producing optically active glycol |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20070423 |