KR20250099770A - 코로나바이러스에 대한 백신 - Google Patents
코로나바이러스에 대한 백신 Download PDFInfo
- Publication number
- KR20250099770A KR20250099770A KR1020257009272A KR20257009272A KR20250099770A KR 20250099770 A KR20250099770 A KR 20250099770A KR 1020257009272 A KR1020257009272 A KR 1020257009272A KR 20257009272 A KR20257009272 A KR 20257009272A KR 20250099770 A KR20250099770 A KR 20250099770A
- Authority
- KR
- South Korea
- Prior art keywords
- coronavirus
- cov
- antigenic
- sars
- peptide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/215—Coronaviridae, e.g. avian infectious bronchitis virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/5123—Organic compounds, e.g. fats, sugars
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
- C12N15/88—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation using microencapsulation, e.g. using amphiphile liposome vesicle
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/53—DNA (RNA) vaccination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55555—Liposomes; Vesicles, e.g. nanoparticles; Spheres, e.g. nanospheres; Polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6031—Proteins
- A61K2039/6068—Other bacterial proteins, e.g. OMP
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/64—Medicinal preparations containing antigens or antibodies characterised by the architecture of the carrier-antigen complex, e.g. repetition of carrier-antigen units
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/70—Multivalent vaccine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/20011—Coronaviridae
- C12N2770/20022—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/20011—Coronaviridae
- C12N2770/20034—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Virology (AREA)
- Molecular Biology (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Epidemiology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Communicable Diseases (AREA)
- Mycology (AREA)
- Immunology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Oncology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pulmonology (AREA)
- General Chemical & Material Sciences (AREA)
- Optics & Photonics (AREA)
- Nanotechnology (AREA)
- Dermatology (AREA)
- Peptides Or Proteins (AREA)
Abstract
본 개시 내용은 백신 및 결합 분자의 분야, 및 질환의 치료 및/또는 예방에 사용하는 제제 및 방법에 관한 것이다. 다가 mRNA 및 나노입자 백신을 포함하여, 코로나바이러스 감염을 치료 또는 예방하기 위한 백신 및 결합 분자, 이를 함유하는 조성물, 및 이의 용도를 기술한다.
Description
관련 출원에 대한 상호 참조
본 출원은 2022년 8월 22일에 출원된 미국 가출원 제63/399,990호, 2022년 8월 23일에 출원된 미국 가출원 제63/400,334호, 2022년 12월 8일에 출원된 미국 가출원 제63/431,286호, 및 2023년 8월 17일에 출원된 유럽 출원 제23315318.8호에 대한 우선권을 주장하며, 이들 각각의 전체 내용은 본원에 참조로 포함된다.
발명 분야
본 개시 내용은 백신 분야, 및 질환의 치료 및/또는 예방에 사용하는 제제 및 방법에 관한 것이다. 백신, 이를 함유하는 약학 조성물(본원에서 면역원성 조성물이라고도 함), 및 코로나바이러스 감염 및 관련 바이러스 감염, 예컨대 사르베코바이러스 및 메르베코바이러스에 의해 유발되는 감염을 치료 또는 예방하기 위한 이의 용도를 기술한다.
정부 지원 조항
본 발명은 미국 육군 의료 연구 개발 사령부에서 수여한 W81XWH-18-2-0040, 및 군 감염병 연구 프로그램에서 수여한 MI220230에 따른 정부 지원으로 만들어졌다. 정부는 본 발명에 대한 특정 권리를 가지고 있다.
배경
다음 논의는 독자가 개시 내용을 이해하는 데 도움을 주기 위해 제공될 뿐이며, 이에 대한 선행 기술을 설명하거나 구성하는 것으로 인정되지 않는다.
SARS-CoV-2(COVID-19로도 명명되며, 때로는 본원에서 SARS2 또는 SARS-2라고도 함)의 출현은 인간으로부터 단리된 일곱 번째 코로나바이러스이며, 중증 급성 호흡기 증후군(SARS)과 중동 호흡기 증후군(MERS) 이후 세 번째로 중증 질환을 유발한다. SARS-CoV-2의 빠른 확산과 비교적 높은 치사율은 전 세계 수백만 명의 상당한 인명 손실과 장기적 이환율을 초래하였다. SARS-CoV-2 팬데믹의 빠르게 진화하는 역학은 특히 병원성과 전염성 수준이 상이한 새로운 바이러스 변종이 계속 확산됨에 따라 이 새로운 코로나바이러스의 분자 생물학을 규명할 필요성을 강조하였다.
계속해서 진화하고 새로운 발병을 유발하는 우려되는 SARS-CoV-2 변종에 대한 방역을 확실히 하기 위해 SARS-CoV-2 및 사르베코바이러스 아속의 다른 구성원에 대한 효과적인 예방 백신이 시급히 필요하다. SARS-CoV-2에 대한 현재 사용 가능한 백신에는 부모, 베타- 및/또는 오미크론 균주의 SARS-CoV-2 스파이크 단백질에 대한 mRNA, 벡터화, 및 재조합 단백질 백신이 포함된다. 이러한 사용 가능한 백신에도 불구하고, SARS-CoV-2 변종은 백신 접종자와 미접종자 모두에게 계속 유행되고 있다. 이는 현재 및 향후 유행 SARS-CoV-2 변종에 효과적인 백신에 대한 공중 보건의 필요성을 강조한다. 사르베코바이러스에 대한 광범위한 보호 면역 반응을 유발하는 백신의 개발은 차세대 예방 백신의 기반을 형성할 수 있었다. MERS-CoV 및 기타 메르베코바이러스에 대한 백신도 팬데믹 예방 노력에 필요하다. MERS-CoV는 아라비아 반도에서 상당한 사망률과 이환율을 계속 유발하고 있으며, 현재 낮은 재생산율에도 불구하고 대규모 팬데믹 발병 가능성은 여전히 높다. 향후 다른 코로나바이러스 인수공통감염 사건에 대한 팬데믹 대비를 위해 몇몇 또는 모든 베타-코로나바이러스, 결국 몇몇 또는 모든 베타-코로나바이러스, 및/또는 광범위한 사르베코바이러스에 대한 광범위한 보호 면역 반응을 유발할 수 있는 백신이 관심의 대상이 되고 있다. 본 개시 내용은 코로나바이러스 감염 및 기타 관련 바이러스 감염을 치료 또는 예방하는 데 사용할 수 있는 mRNA 및 나노입자 백신을 제공한다.
요약
본원에서는 메르베코바이러스, 및 사르베코바이러스를 포함하는 코로나바이러스에 의해 유발되는 감염의 치료 및/또는 예방을 위한 면역원성 조성물 및 백신, 및 상기의 방법 및 용도에 대해 기술한다.
한 측면에 따라, 적어도 제1 항원성 코로나바이러스 펩티드와 제2 항원성 코로나바이러스 펩티드를 포함하는 적어도 두 개의 항원성 코로나바이러스 펩티드, 또는 이를 코딩하는 하나 이상의 메신저 RNA(mRNA) 분자를 포함하는 면역원성 조성물을 제공하며, 여기서 각 항원성 코로나바이러스 펩티드는 코로나바이러스의 수용체 결합 도메인(RBD 또는 R), 또는 이의 단편 또는 변이체, 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체, 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 및 코로나바이러스의 안정화된 스파이크 S-삼량체, 또는 이의 단편 또는 변이체로부터 독립적으로 선택되며, 여기서 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함한다: (i) 둘 이상의 선택된 클레이드 1b; (ii) 클레이드 1b로부터 선택된 하나 이상 및 클레이드 1a로부터 선택된 하나 이상 (iii) 클레이드 1b로부터 선택된 하나 이상, 및 클레이드 1a로부터 선택된 하나 이상, 및 클레이드 2로부터 선택된 하나 이상; (iv) 클레이드 1b로부터 선택된 하나 이상, 및 클레이드 1a로부터 선택된 하나 이상, 및 클레이드 3으로부터 선택된 하나 이상; (v) 클레이드 1b로부터 선택된 하나 이상, 클레이드 2로부터 선택된 하나 이상, 및 클레이드 3으로부터 선택된 하나 이상; 및 (v) 클레이드 1a로부터 선택된 하나 이상, 클레이드 2로부터 선택된 하나 이상, 및 클레이드 3으로부터 선택된 하나 이상. 일부 실시양태에서, 항원성 코로나바이러스 펩티드 중 적어도 하나는 S-2P 펩티드이며, 선택적으로 S-2P 펩티드는 서열 번호 536-543 중 어느 하나의 아미노산 서열, 또는 이에 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 또는 적어도 99%의 상동성 또는 동일성을 갖는 서열을 포함한다. 추가적으로 또는 대안적으로, 일부 실시양태에서, 항원성 코로나바이러스 펩티드 중 하나 이상은 항원성 코로나바이러스 펩티드와 나노입자 형성 단백질을 포함하는 융합 단백질에 포함되며, 여기서 상기 항원성 코로나바이러스 펩티드 중 둘 이상은 나노입자 형성 단백질과의 동일하거나 상이한 융합 단백질에 포함될 수 있다.
다른 측면에 따라, 적어도 제1 항원성 코로나바이러스 펩티드와 제2 항원성 코로나바이러스 펩티드를 포함하는 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 나노입자, 또는 적어도 두 개의 항원성 코로나바이러스 펩티드를 코딩하는 하나 이상의 메신저 RNA(mRNA) 분자를 포함하는 면역원성 조성물을 제공하며, 여기서 각 항원성 코로나바이러스 펩티드는 코로나바이러스의 수용체 결합 도메인(RBD 또는 R), 또는 이의 단편 또는 변이체, 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체, 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 및 코로나바이러스의 안정화된 세포외 스파이크 S-삼량체, 또는 이의 단편 또는 변이체로부터 독립적으로 선택되며, 여기서 각 항원성 코로나바이러스 펩티드는 항원성 코로나바이러스 펩티드와 나노입자 형성 단백질을 포함하는 융합 단백질에 포함되며, 여기서 항원성 코로나바이러스 펩티드는 동일하거나 상이한 융합 단백질에 포함될 수 있고, 여기서 조성물은 적어도 두 가지 상이한 코로나바이러스 균주의 항원성 코로나바이러스 펩티드, 또는 이를 코딩하는 하나 이상의 mRNA 분자를 포함한다. 일부 실시양태에서, 각 항원성 코로나바이러스 펩티드는 클레이드 1a, 클레이드 1b, 클레이드 2, 클레이드 3, 및 중동 호흡기 증후군 관련 코로나바이러스(MERS-CoV)로부터 독립적으로 선택된 코로나바이러스 균주로부터 유래되고, 선택적으로 적어도 제1 및 제2 항원성 코로나바이러스 펩티드는 상이한 클레이드의 코로나바이러스 균주로부터 유래된다. 일부 실시양태에서, 적어도 제1 및 제2 항원성 코로나바이러스 펩티드는 WA-1, 베타, 오미크론 BQ.1.1, 오미크론 XBB.1.5, SARS-CoV-1 균주, BANAL20-247, Khosta-2, 및 MERS-CoV로부터 독립적으로 선택된 상이한 코로나바이러스 균주로부터 유래된다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함한다: (i) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1로부터 선택된 둘 이상; (ii) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주; (iii) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 하나 이상; (iv) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 하나 이상, 및 MERS-CoV; 및 (v) SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 둘 이상.
전술한 임의의 측면의 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함한다: WA-1, 베타, 및 오미크론 BQ1.1; WA-1, 오미크론 BQ.1.1, 및 SARS-CoV-1; WA-1, SARS-CoV-1, 및 Khosta2; WA-1, SARS-CoV-1, 및 BANAL20-247; WA-1, SARS-CoV-1, 및 MERS-CoV; 및 SAR-CoV-1, Khosta-2, 및 BANAL20-247.
전술한 임의의 측면의 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함한다:
(i) WA-1, 베타, 및 오미크론 BQ.1.1(또는 XBB.1.5), 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(베타)FN, 및 R(BQ1.1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(베타)-2P, 및 S(BQ1.1)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(베타)FN, 및 Sp(BQ1.1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(ii) WA-1, 오미크론 BQ.1.1(또는 XBB1.5), 및 SARS-CoV-1, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(BQ 1.1)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(BQ 1.1)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(BQ 1.1)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(iii) WA-1, SARS-CoV-1, 및 Khosta2, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(Khosta2)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(Khosta2)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(Khosta2)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(iv) WA-1, SARS-CoV-1, 및 BANAL20-247, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(BANAL20-247)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(BANAL20-247)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(BANAL20-247)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(v) WA-1, SARS-CoV-1, 및 MERS-CoV, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(MERS-CoV)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(MERS-CoV)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(MERS-CoV)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(vi) SARS-CoV-1, Khosta-2, 및 BANAL20-247, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(SARS-CoV-1)FN, R(Khosta2)FN, 및 R(BANAL20-247)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(SARS-CoV-1)-2P, S(Khosta2)-2P, 및 S(BANAL20-247)-2P) 또는 SpFN 융합 단백질 Sp(SARS-CoV-1)FN, Sp(Khosta2)FN, 및 Sp(BANAL20-247)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(vii) 베타, 오미크론 BQ.1.1(또는 XBB1.5), 및 SARS-CoV-1, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(베타)FN, R(BQ 1.1)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(베타)-2P, S(BQ 1.1)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(베타)FN, Sp(BQ 1.1)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(viii) 베타, 오미크론 XBB.1.5, 및 SARS-CoV-1, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(베타)FN, R(XBB.1.5)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(베타)-2P, S(XBB.1.5)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(베타)FN, Sp(XBB.1.5)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(ix) 오미크론 BQ.1.1, SARS-CoV-1, 및 Khosta2, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(오미크론 BQ.1.1)FN, R(SARS-CoV-1)FN, 및 R(Khosta2)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(오미크론 BQ.1.1)-2P, S(SARS-CoV-1)-2P, 및 S(Khosta2)-2P) 또는 SpFN 융합 단백질 Sp(오미크론 BQ.1.1)FN, Sp(SARS-CoV-1)FN, 및 Sp(Khosta2)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임. ***
전술한 임의의 측면의 일부 실시양태에서, 나노입자 형성 펩티드는 페리틴 단백질 또는 이의 단편 또는 변이체이거나 이를 포함한다. 일부 실시양태에서, 나노입자 형성 펩티드는 헬리코박터 파일로리(Helicobacter pylori) 페리틴(Hpf) 또는 이의 단편 또는 변이체이거나 이를 포함한다. 일부 실시양태에서, 나노입자 형성 펩티드는 다음으로부터 선택된 아미노산 서열을 포함한다:
다른 측면에서, 본 개시 내용은 나노입자 형성 펩티드 및 다음으로부터 선택된 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 융합 단백질을 포함하는 나노입자를 제공한다: 코로나바이러스의 수용체 결합 도메인(RBD), 또는 이의 단편 또는 변이체, 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체, 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S-삼량체, 또는 이의 단편 또는 변이체, 및 모자이크 코로나바이러스 스파이크 단백질, 여기서 모자이크 코로나바이러스 스파이크 단백질의 적어도 하나의 도메인은 이종 코로나바이러스 균주 또는 종으로부터 치환되거나 추가됨.
일부 실시양태에서, 나노입자 형성 펩티드는 페리틴 단백질 또는 이의 단편 또는 변이체이거나 이를 포함한다. 일부 실시양태에서, 나노입자 형성 펩티드는 헬리코박터 파일로리 페리틴(Hpf) 또는 이의 단편 또는 변이체이거나 이를 포함한다. 일부 실시양태에서, 나노입자 형성 펩티드는 다음으로부터 선택된 아미노산 서열을 포함한다:
상기 임의의 측면의 일부 실시양태에서, 상기 항원성 코로나바이러스 펩티드 중 적어도 두 개는 링커를 통해 연결된 융합 단백질에 포함된다. 일부 실시양태에서, 상기 항원성 코로나바이러스 펩티드 중 2-10개는 융합 단백질에 직렬로 포함되며, 선택적으로 항원성 코로나바이러스 펩티드는 링커를 통해 연결된다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 나노입자 형성 펩티드와의 융합 단백질에 포함되며, 여기서 항원성 코로나바이러스 펩티드는 링커를 통해 나노입자 형성 펩티드에 연결된다. 링커를 포함하는 임의의 실시양태에서, 링커는 다음으로부터 선택된 아미노산 서열을 포함할 수 있다: GGGSGGSG(서열 번호 583), GSGGGG(서열 번호 11), GGGG(서열 번호 15), GSGG(서열 번호 5), GGG(서열 번호 16), 및 SGG(서열 번호 17).
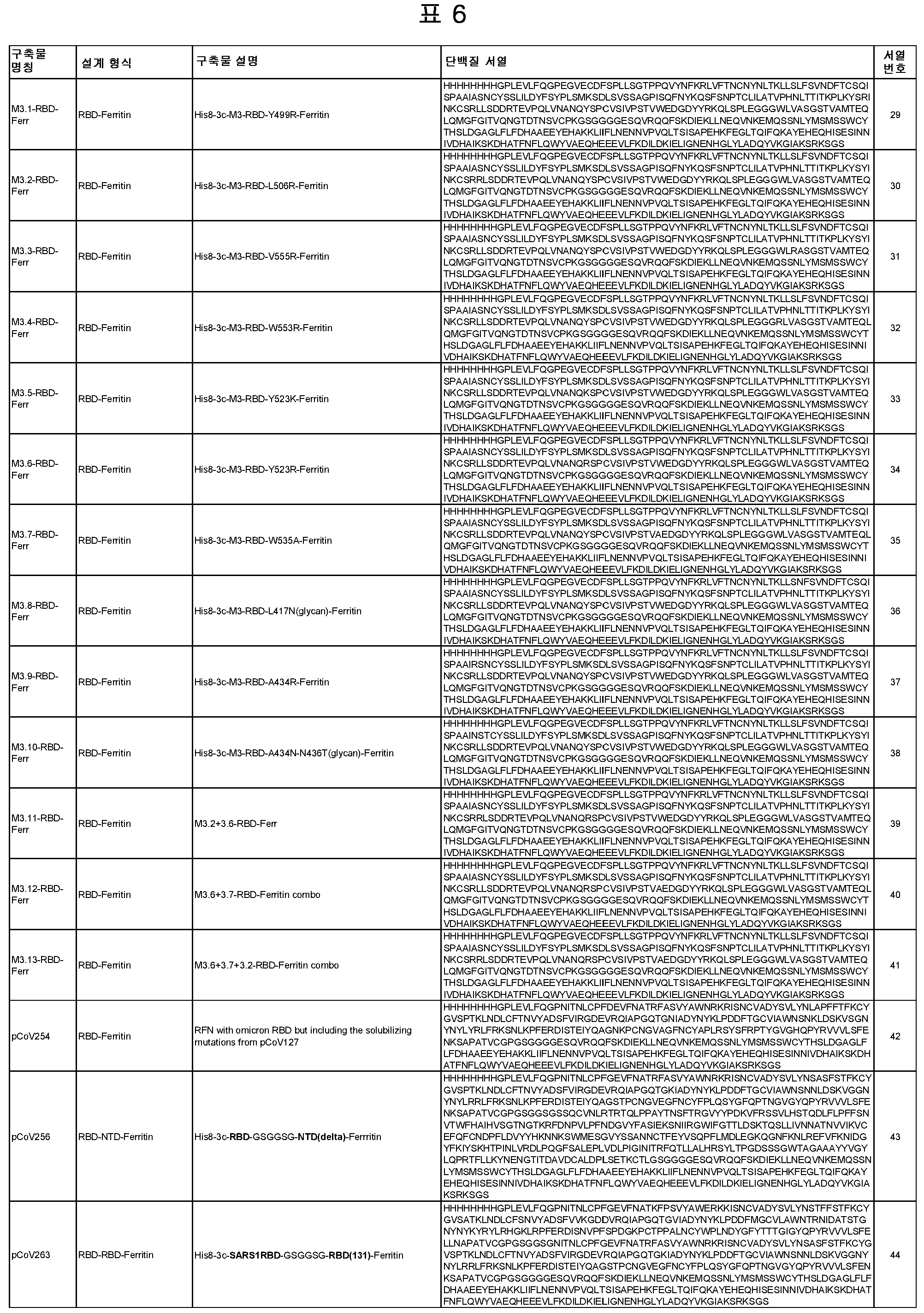
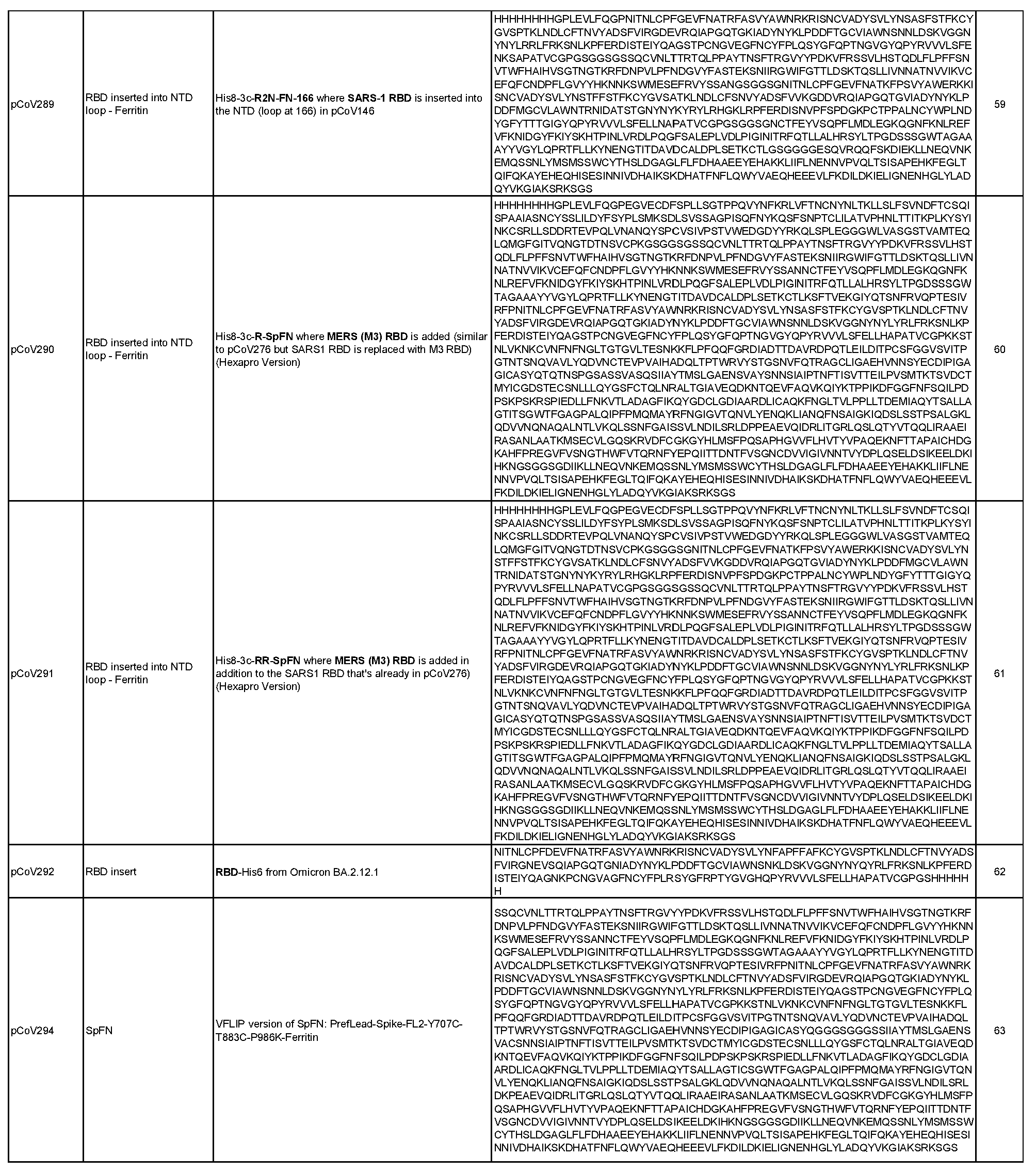
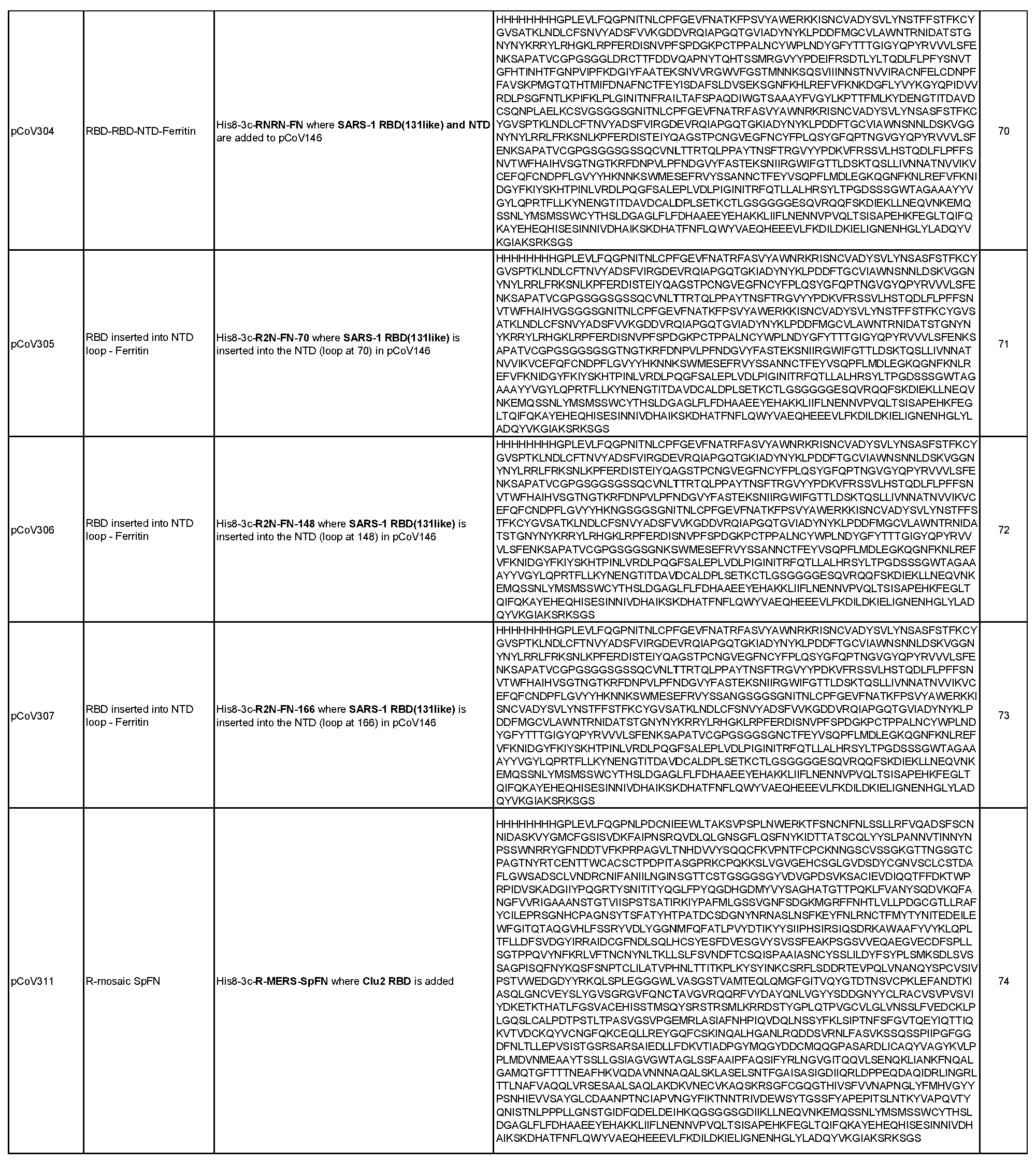
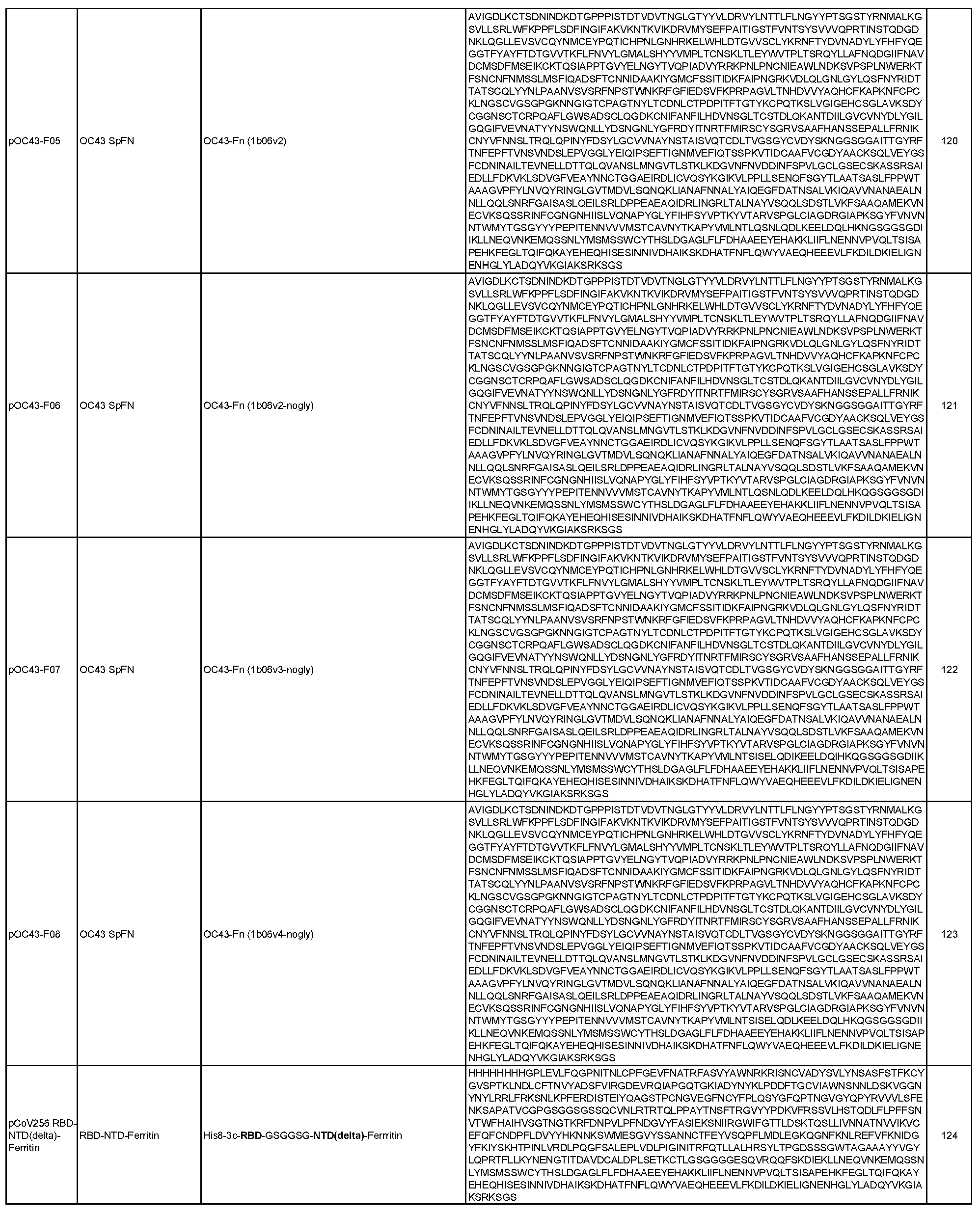
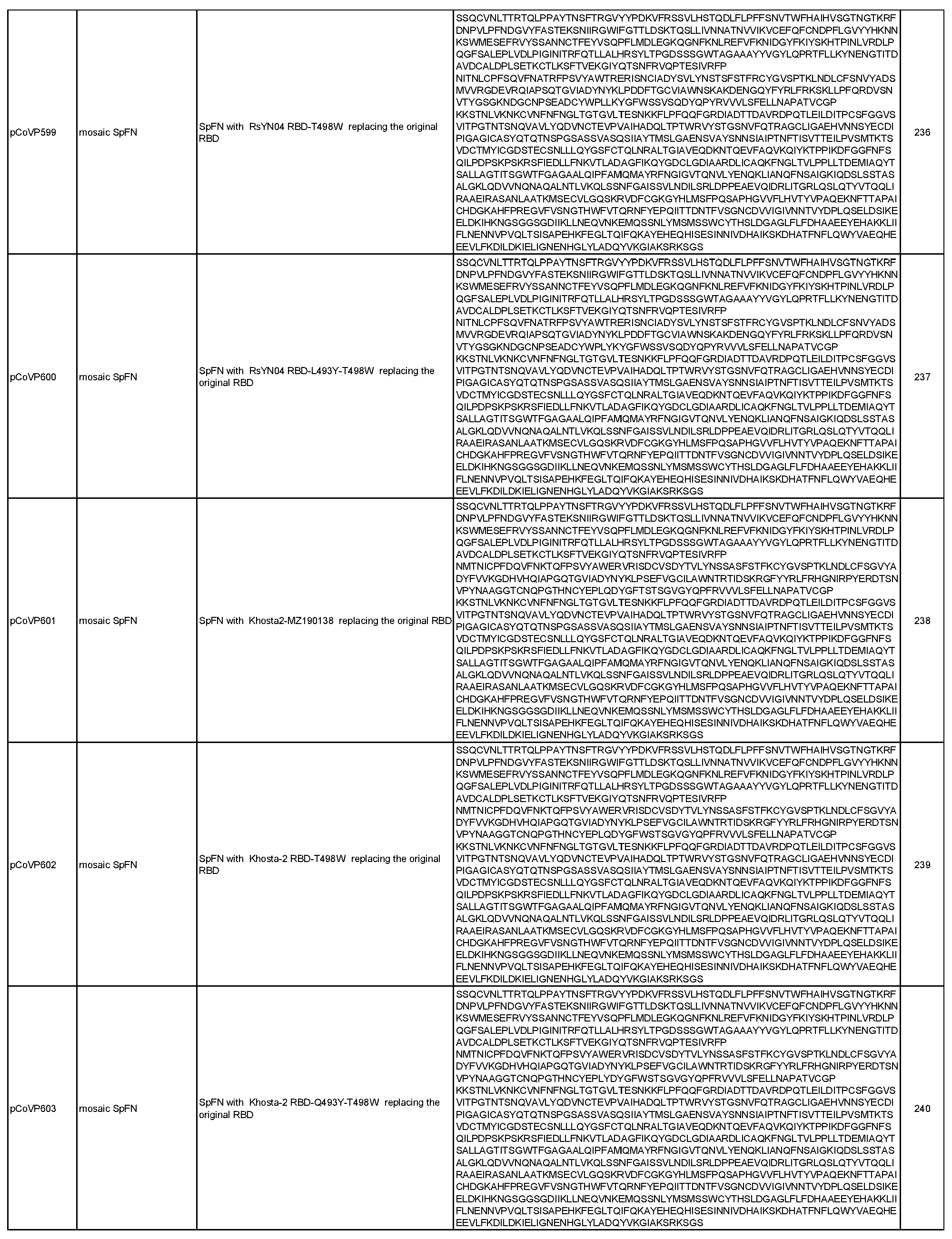
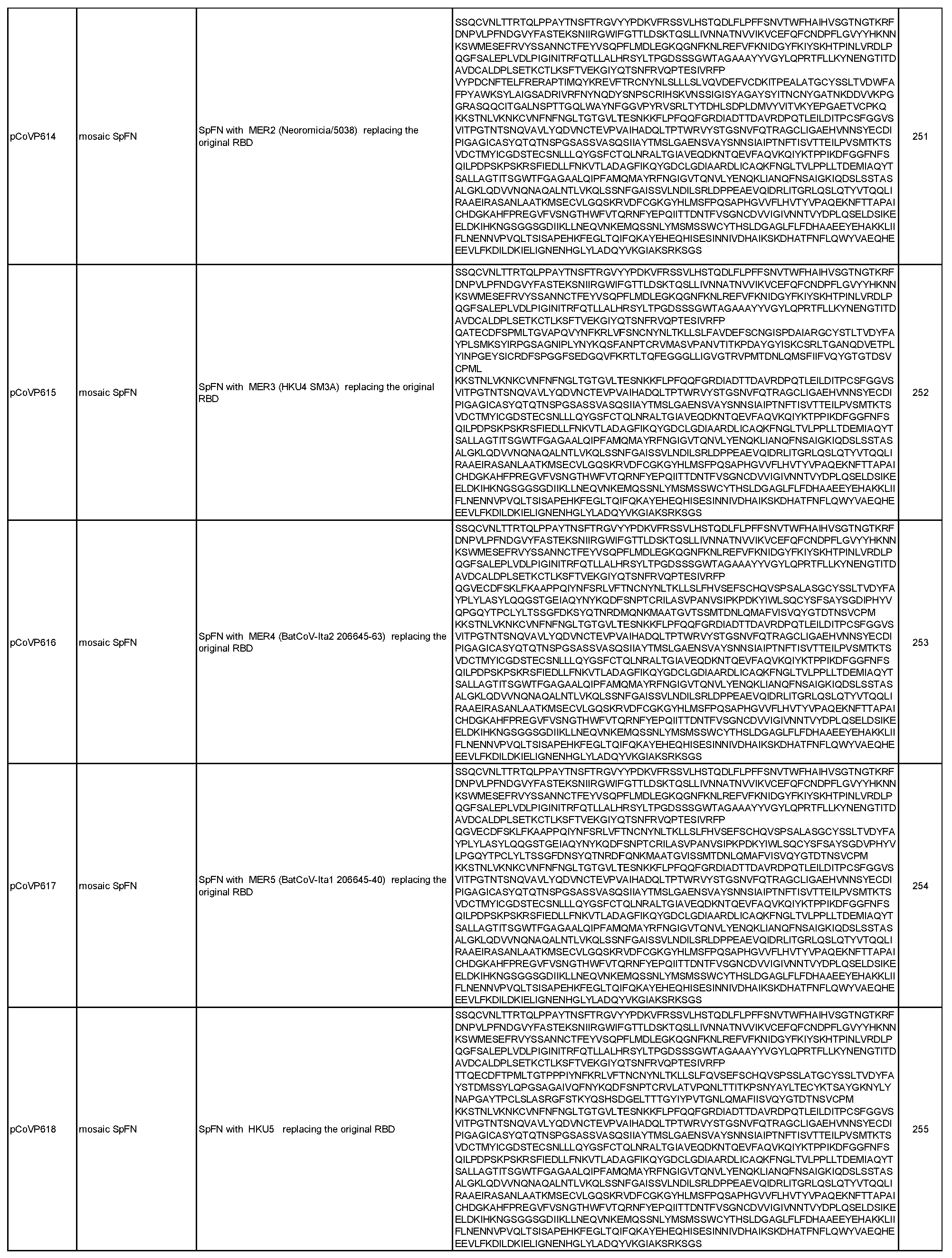
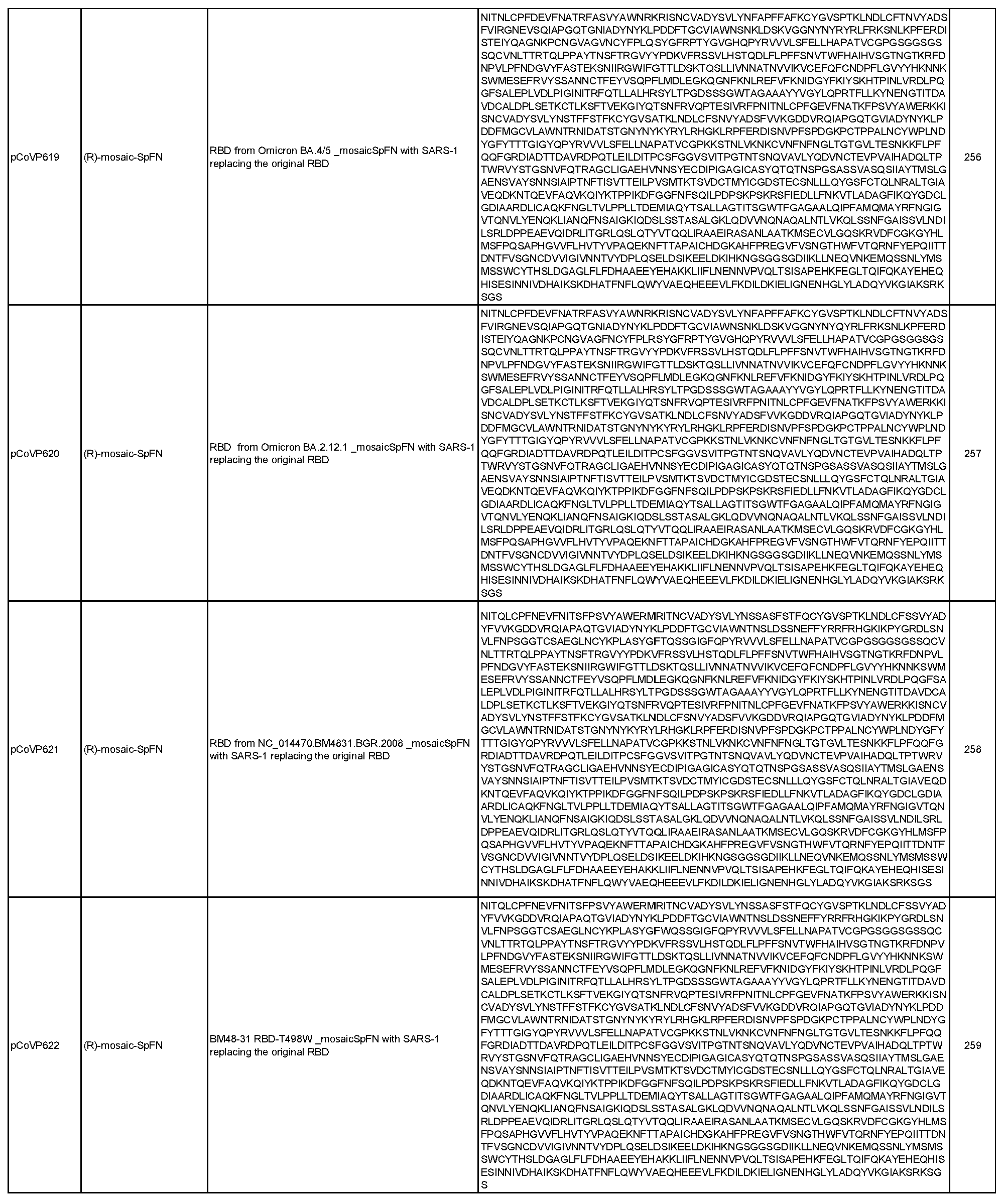
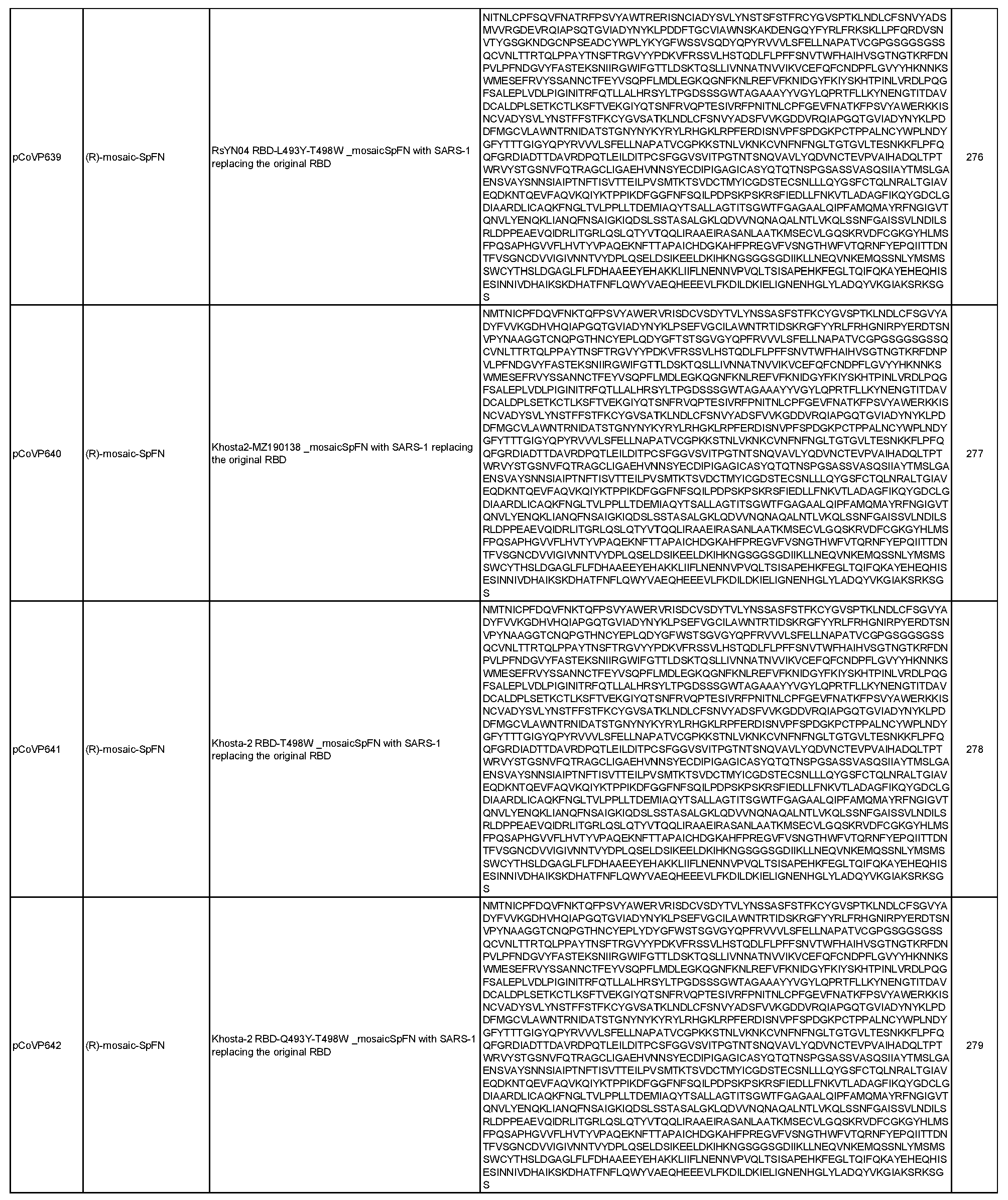
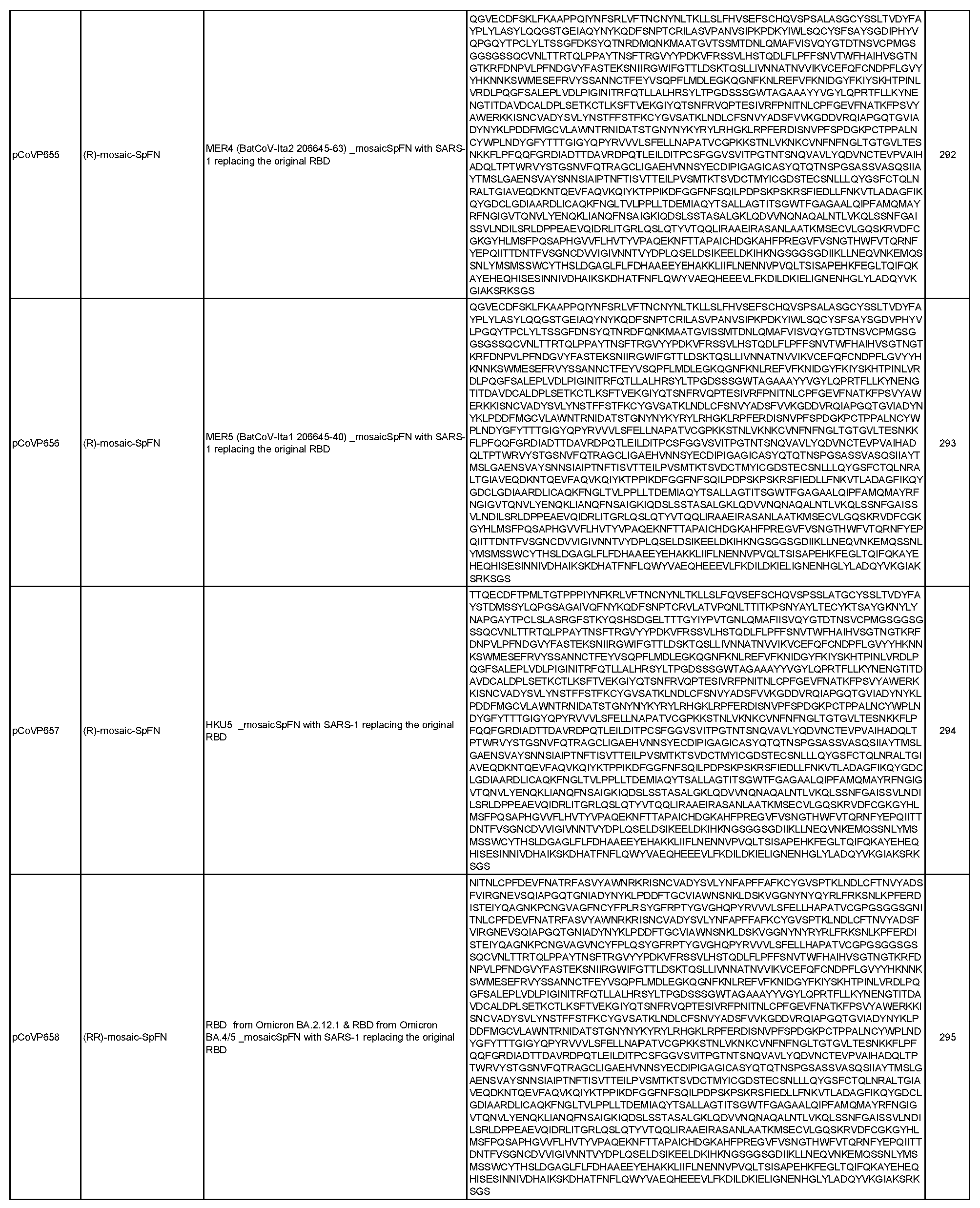
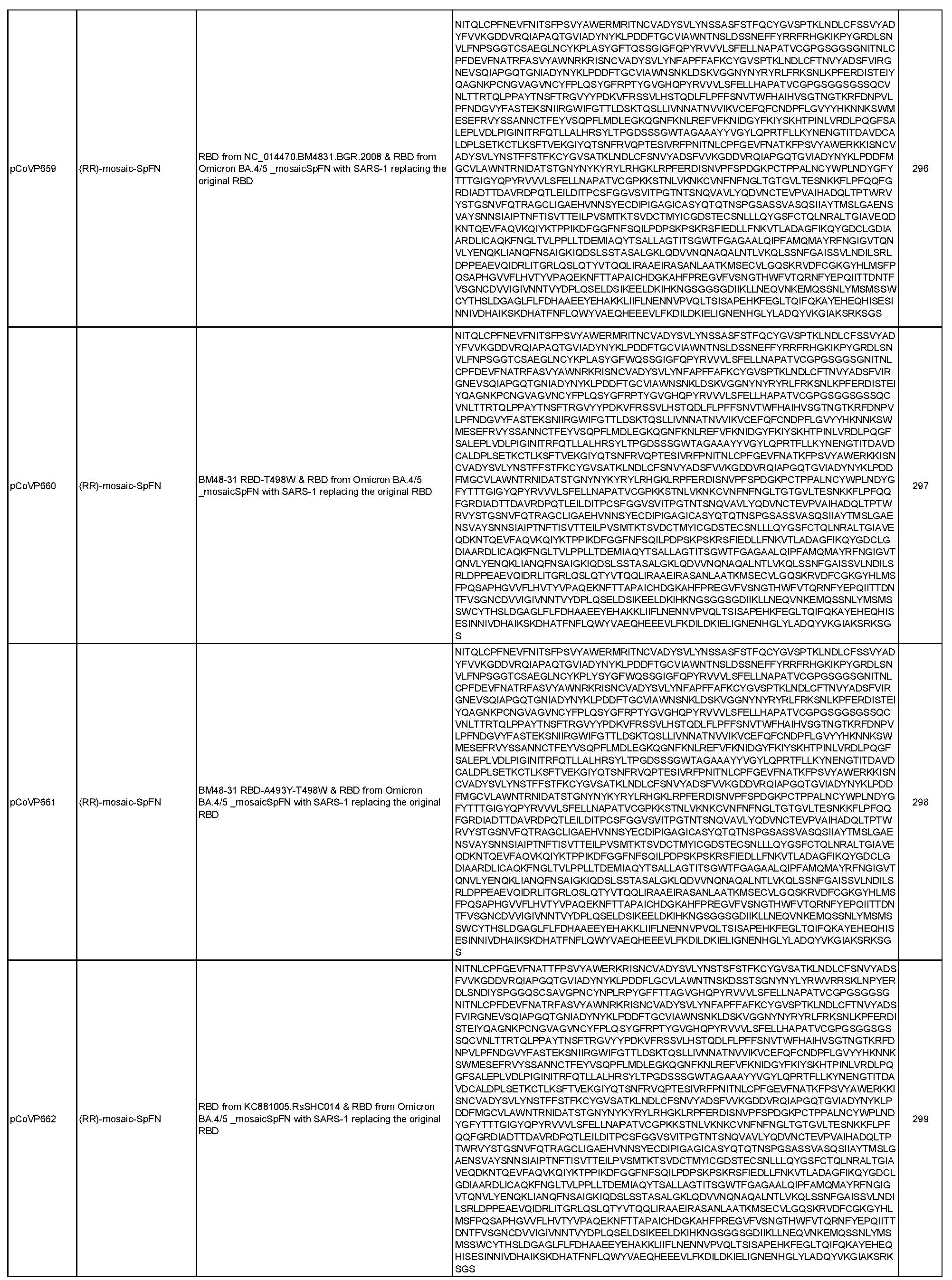
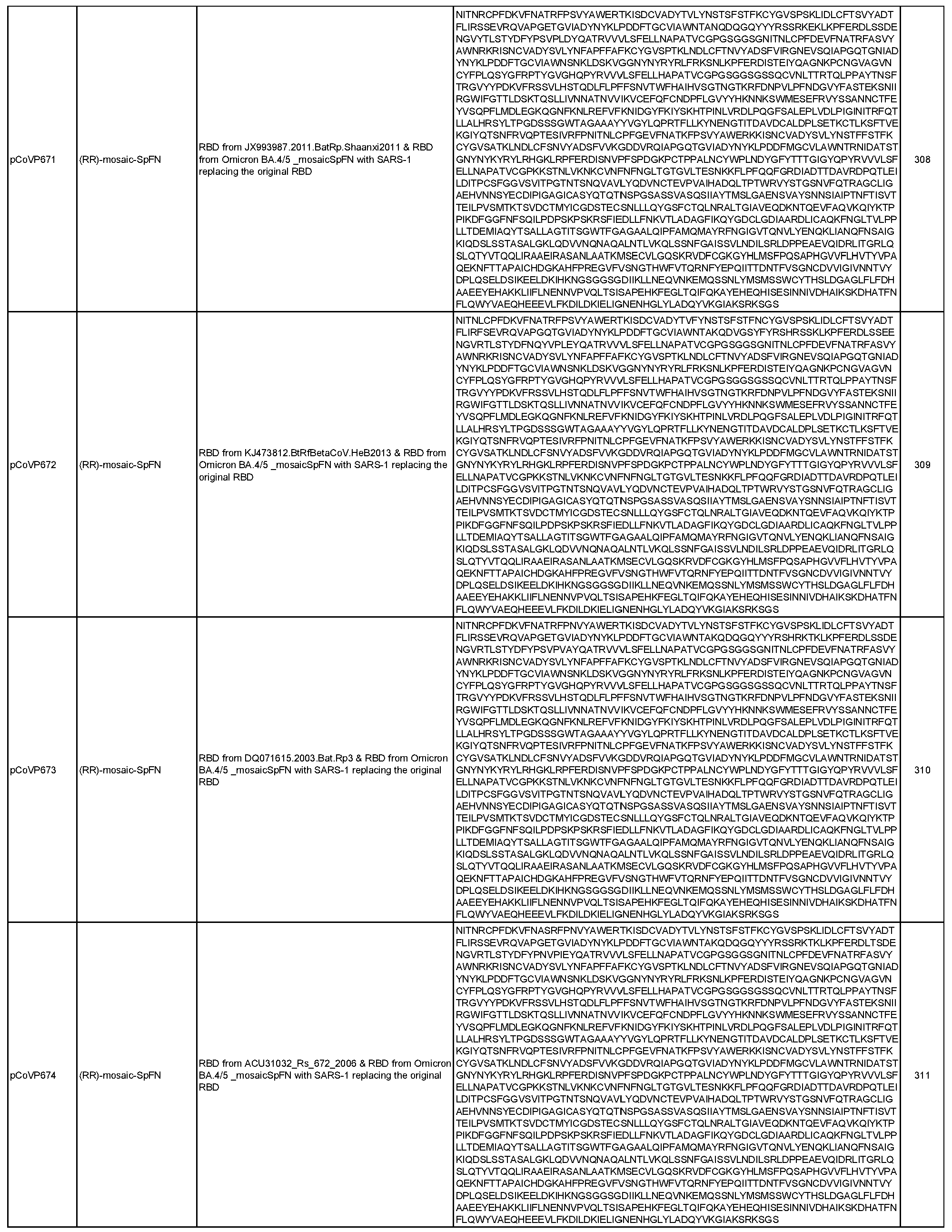
상기 임의의 측면의 일부 실시양태에서, 제1 및 제2 항원성 코로나바이러스 펩티드는 모자이크 코로나바이러스 스파이크 단백질에 포함되며, 여기서 모자이크 코로나바이러스 스파이크 단백질의 적어도 하나의 도메인은 이종 코로나바이러스 균주로부터 치환되거나 추가된다. 항원성 코로나바이러스 펩티드가 나노입자 형성 펩티드와의 융합 단백질에 포함되는 임의의 실시양태에서, 융합 단백질은 SpFN, 실에 꿰어진 구슬(beads on a string), 도메인 융합, 도메인 스왑, 루프 삽입, 및 도메인 삽입으로부터 선택된 형식을 포함할 수 있다. 이러한 일부 실시양태에서, 융합 단백질은 도 2-7에 도시된 형식으로부터 선택된 형식을 포함한다. 이러한 임의의 실시양태에서, 제1 및 제2 항원성 코로나바이러스 펩티드는 동일한 융합 단백질(예를 들어, R1R2FN)에 포함된 상이한 코로나바이러스 균주의 상이한 RBD 펩티드(예를 들어, R1, R2)일 수 있으며, 선택적으로 융합 단백질은 스파이크 단백질을 추가로 포함하고(예를 들어, R1R2mosSpFN), 추가로 선택적으로 조성물은 융합 단백질의 상이한 위치에 동일한 두 개 이상의 상이한 RBD 펩티드를 포함하는 두 개 이상의 상이한 융합 단백질(예를 들어, R1R2FN, R2R1FN 또는 R1R2mosSpFN, R2R1mosSpFN), 또는 상기 두 개 이상의 상이한 융합 단백질을 코딩하는 mRNA 분자, 또는 상기 두 개 이상의 상이한 융합 단백질을 표시하는 나노입자를 포함한다. 이러한 임의의 실시양태에서, 융합 단백질은 표 6 및 표 7에 개시된 서열(서열 번호 29-551)로부터 선택된 아미노산 서열, 또는 이에 적어도 80%(예를 들어, 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 또는 적어도 99%)의 서열 동일성을 갖는 서열을 포함할 수 있다.
일부 실시양태에서, 조성물은 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 나노입자를 포함한다.
일부 실시양태에서, 조성물은 적어도 두 개의 항원성 코로나바이러스 펩티드를 코딩하는 하나 이상의 mRNA 분자를 포함하며, 선택적으로 하나 이상의 mRNA 분자는 하나 이상의 지질 나노입자(LNP)에 캡슐화되거나 공동 캡슐화된다. 일부 실시양태에서, 조성물은 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 하나의 융합 단백질을 코딩하는 하나의 mRNA 분자를 포함하며, 선택적으로 융합 단백질은 나노입자 형성 펩티드를 추가로 포함하고, mRNA 분자는 지질 나노입자(LNP)에 캡슐화되고; 일부 실시양태에서, 조성물은 선택적으로 나노입자 형성 펩티드와의 융합 단백질에 있는, 적어도 두 개의 항원성 코로나바이러스 펩티드 중 적어도 하나를 각각 코딩하는 두 개 이상의 mRNA 분자를 포함하며, 각 mRNA 분자는 별도의 지질 나노입자(LNP)에 캡슐화되고; 일부 실시양태에서, 조성물은 선택적으로 나노입자 형성 펩티드와의 융합 단백질에 있는, 적어도 두 개의 항원성 코로나바이러스 펩티드 중 적어도 하나를 각각 코딩하는 두 개 이상의 mRNA 분자를 포함하며, 두 개 이상의 mRNA 분자는 동일한 지질 나노입자(LNP)에 공동 캡슐화된다.
상기 임의의 측면 또는 실시양태에 따라, 조성물이 하나 이상의 mRNA 분자를 포함하는 경우, mRNA 분자는 5' 비번역 영역(5' UTR), 3' 비번역 영역(3' UTR), 폴리아데닐화(폴리(A)) 서열, 화학적 변형, 선택적으로 화학적 변형은 N1-메틸슈도우리딘을 포함함, 및 자가 복제 mRNA 또는 비복제 mRNA인 mRNA로부터 선택된 하나 이상의 특징을 가질 수 있으며, 선택적으로 여기서 mRNA 분자는 지질 나노입자(LNP)에 캡슐화된다.
상기 임의의 실시양태에 따라, 면역원성 조성물은 추가로 보조제를 포함할 수 있다. 항원 또는 나노입자를 포함하는 일부 실시양태에서, 보조제는 ALFQ, 알히드로겔, 및 이들의 조합으로부터 선택된 하나 이상을 포함한다.
추가 측면에서, 본 개시 내용은 나노입자 형성 펩티드 및 다음으로부터 독립적으로 선택된 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 융합 단백질을 포함하는 나노입자를 제공한다: 코로나바이러스의 수용체 결합 도메인(RBD), 또는 이의 단편 또는 변이체, 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체, 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S-삼량체, 또는 이의 단편 또는 변이체, 및 모자이크 코로나바이러스 스파이크 단백질, 여기서 모자이크 코로나바이러스 스파이크 단백질의 적어도 하나의 도메인은 이종 코로나바이러스 균주로부터 치환되거나 추가됨.
추가의 측면에서, 본 개시 내용은 본원에 개시된 나노입자(예를 들어, 상기 측면의 나노입자)를 코딩하는 서열을 포함하는 DNA 분자, 또는 상기 DNA 분자를 포함하는 플라스미드를 제공하며, 선택적으로 여기서 플라스미드는 생체 내에서 DNA 분자를 발현할 수 있다.
추가의 측면에서, 본 개시 내용은 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하는 방법으로서, 이를 필요로 하는 대상체에게 본원에 개시된 바와 같은 면역원성 조성물(예를 들어, 상기 임의의 측면 또는 실시양태의 면역원성 조성물)을 투여하는 단계를 포함하는 방법을 제공한다. 또한, 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하는 데 사용하기 위한 본원에 기술된 바와 같은 면역원성 조성물을 제공한다. 또한, 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하기 위한 의약을 제조하는 데 있어서의 본원에 기술된 바와 같은 면역원성 조성물의 용도를 제공한다. 일부 실시양태에서, 대상체는 코로나바이러스 감염 위험에 있다.
일부 실시양태에서, 대상체는 이미 코로나바이러스에 감염되었다. 일부 실시양태에서, 대상체는 이전에 코로나바이러스 감염 예방을 위한 백신을 투여받은 적이 없다. 일부 실시양태에서, 대상체는 이전에 코로나바이러스 감염 예방을 위한 백신을 투여받은 적이 있다. 일부 실시양태에서, 방법, 사용하기 위한 조성물, 또는 용도는 대상체에서 코로나바이러스에 대한 면역 반응을 유발하고, 선택적으로 면역 반응은 중화 항체를 포함하고, 추가로 선택적으로 중화 항체는 두 가지 이상의 코로나바이러스 균주를 교차 중화하고, 추가로 선택적으로 중화 항체는 면역원성 조성물의 구성 균주가 아닌 하나 이상의 코로나바이러스 균주를 교차 중화한다.
다른 측면에서, 본 개시 내용은 서열 번호 552-582 중 어느 하나로부터 선택된 서열 또는 이에 적어도 80% 상동성인 서열을 포함하거나 이로 이루어진 mRNA 분자를 제공한다. 일부 실시양태에서, mRNA 분자는 서열 번호 552-582 중 어느 하나에 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 또는 적어도 99%의 상동성 또는 동일성을 갖는 서열을 포함하거나 이로 이루어진 서열을 갖는다. 일부 실시양태에서, mRNA 분자는 서열 번호 552-582 중 어느 하나를 포함하는 서열을 갖는다. 일부 실시양태에서, mRNA 분자는 서열 번호 552-582 중 어느 하나로 이루어진 서열을 갖는다.
상기 일반적인 설명 및 이하의 상세한 설명은 예시적이고 설명적이며 청구된 바와 같은 개시 내용에 대한 추가 설명을 제공하고자 한다. 다른 목적, 이점, 및 새로운 특징은 도면에 대한 다음의 간략한 설명 및 개시 내용에 대한 상세한 설명으로부터 당업자에게 자명할 것이다.
도 1은 코로나바이러스 계통수의 개략도를 보여준다. 인간을 감염시키고 심각한 질병을 유발하는 것으로 알려진 바이러스 종이 명명되고 밝은 회색으로 표시되어 있다(예를 들어, HCoV-229E).
도 2는 범(pan)-CoV 나노입자 설계 형식의 선형 개략도를 보여준다. 10가지 설계 형식이 표시되어 있으며, 여기에는 직렬로 연결된 이종 수용체 결합 도메인(RBD)이 선행된 C-말단 H. 파일로리 페리틴, 직렬의 RBD와 N-말단 도메인(NTD), S1 폴리펩티드의 천연 하위 도메인(SD)을 보유하면서 NTD를 대체하는 RBD, 및 NTD의 루프에 삽입된 RBD가 포함된다. 이종 RBD 분자가 천연 RBD 또는 NTD 도메인을 대체하기 위해 도입되거나, N-말단에서 연결된 추가 RBD 도메인으로서 도입되는 스파이크 페리틴 나노입자(SpFN)의 세 가지 예가 있다. 이러한 설계 형식 중 다수는 직교적이며 결합될 수 있다. 구체적으로, NTD의 루프에 RBD를 삽입하는 것은 NTD를 함유하는 구축물과 결합될 수 있다. 페리틴으로 예시되었지만, 페리틴은 본원에 논의된 바와 같이 다른 나노입자 운반체 분자로 대체될 수 있다.
도 3은 선택된 "실에 꿴 구슬" 형식을 그래픽 표현으로 보여주며, (A) RR-FN, (B) RN-FN, (C) RRN-FN, (D) RNRN-FN, (E) R-FN, (F) RR-FN, 및 (G) RR-FN에 대한 예가 제공된다. 예를 들어, 임의의 조합의 하나 이상의 RBD는 페리틴에 직렬로 연결될 수 있고("R-FN" 또는 "RR-FN"); 임의의 코로나바이러스 균주의 하나의 RBD는 임의의 코로나바이러스 균주의 NTD와 페리틴에 연결될 수 있고("RN-FN"); 상이한 코로나바이러스 균주의 두 RBD는 상이한 코로나바이러스 균주의 NTD와 페리틴에 직렬로 연결될 수 있으며("RRN-FN"); RBD-NTD-RBD-NTD 시리즈는 임의의 코로나바이러스 균주의 RBD 또는 NTD가 직렬로 연결되고 페리틴에 연결된다("RNRN-FN").
도 4는 선택된 "도메인 융합" 형식을 그래픽 표현으로 보여주며, (A) R2-SD-FN, (B) R-S1-FN, (C) R2-SD-S2-FN, (D) (R)-R-SpFN, (E) R-SpFN, (F) RR-SpFN, 및 (G) RR-SpFN에 대한 예와 도메인 표기가 제공되어 있다.
도 5는 선택된 "루프 삽입" 형식을 그래픽 표현으로 보여주며, 이종 RBD 분자가 (A) R2N-FN-70, (B) R2N-FN-148, 및 (C) R2N-FN-164에 삽입되는 키메라 융합 페리틴 나노입자 면역원 세트에 대한 예와 도메인 표기가 제공되어 있다.
도 6은 선택된 "도메인 스왑" 형식(이하 "모자이크" 형식으로도 지칭함)을 그래픽 표현으로 보여주며, 이종 RBD 분자가 (A) CoV SpFN 분자에 삽입되고(모자이크 SpFN) (B) 추가 이종 RBD 분자가 SpFN 분자의 N-말단에 추가되는(모자이크 R-모자이크 SpFN) 키메라 융합 스파이크 페리틴 나노입자 면역원 세트에 대한 예와 도메인 표기가 제공되어 있다. 키메라 융합 스파이크는 만화 표현으로 보여주며, 추가 이종 RBD가 표시되어 있다.
도 7a 및 7b는 이종 RBD 또는 NTD 분자가 모자이크 SpFN 설계의 N-말단에 추가되는 키메라 융합 스파이크 페리틴 나노입자(SpFN) 면역원 세트(예를 들어, 모자이크 형식)에 대한 선택된 설계를 그래픽 표현으로 보여준다: 도 7a: 다양한 R-R-모자이크 SpFN; 도 7b: RNR-모자이크 SpFN. 추가 RBD 또는 NTD 분자를 모자이크 SpFN의 N-말단에 추가할 수 있다.
도 8은 (A) MERS-CoV RBD-페리틴 나노입자의 음성 염색 전자 현미경, 및 (B) M3 RBD 페리틴 및 M4RBD-페리틴 나노입자의 2D 분류를 보여준다. 간단히 말해서, 정제된 단백질은 탄소 코팅 구리 격자에 0.02-0.08 mg/ml로 침적되고 0.75% 우라닐 포르메이트로 염색되었다. 격자는 SerialEM을 사용하는 Eagle 4K CCD가 장착된 200 kV에서 작동하는 FEI T20을 사용하거나 EPU를 사용하는 Thermo Scientific Ceta가 장착된 120 kV에서 작동하는 Thermo Scientific Talos L120C를 사용하여 이미지화되었다.
도 9는 스파이크 단백질 수용체 결합 도메인(RBD)의 아미노산 서열의 서열 유사성을 기반으로 선택된 사르베코바이러스 균주의 계통학적 그룹화를 반영하는 분기도를 보여준다.
도 10은 두 가지 형식으로 MERS-CoV 중화 인간 단클론 항체 CDC-C2에 대한 결합을 평가한 MERS RBD-페리틴 나노입자 면역원(M.1-M3.6)의 octet 생물층 간섭 결합 분석 결과를 보여준다.
도 11은 MERS RBD-페리틴 나노입자 면역원의 음성 염색 전자 현미경 및 결합 연구를 보여준다. 패널 A는 SARS2-RBD-MERS-RBD CoV-페리틴 구축물이 음성 염색 EM에서 나타난 바와 같이 나노입자를 형성함을 보여주고, 패널 B는 SARS2-RBD-MERS-RBD CoV-페리틴 구축물을 MERS-CoV 중화 인간 단클론 항체 및 SARS-CoV-2 중화 mAb에 대한 결합에 대해 평가한 것을 보여준다. pCoV247 및 pCoV248에 대한 구축물 설계는 표 3에 나와 있다.
도 12는 패널 A에서 코로나바이러스 스파이크 페리틴 나노입자 구축물의 음성 염색 전자 현미경이 음성 염색 EM에서 나타난 바와 같이 나노입자를 형성함을 보여주고; 패널 B에서 SARS-1(SARS-CoV-1), MERS, HKU-1, 및 229E 스파이크 페리틴 나노입자의 2D 분류를 보여주고, 패널 C에서 HKU-1 및 229E 스파이크 페리틴 나노입자의 3D 재구성을 보여준다.
도 13은 중화 항체 ShAb01(SARS-CoV-1 및 SARS-CoV-2를 중화), ShAb02(SARS-CoV-2를 중화), 및 인간 ACE2 수용체에 대한 결합을 생물층 간섭법으로 평가한 R-SpFN 설계 pCoV316 및 pCoV317의 결과를 보고하는 그래프를 보여준다. 180초 동안 결합이 발생하도록 한 다음 60초 동안 해리되도록 하였다.
도 14는 구축물 pCoV323(RR-SpFN, 여기서 MZ081380_bat_Yunnan_RsYN04_2020의 RBD, 및 SARS-1 RBD가 WA-1 SpFN 분자에 연결됨)의 생산 및 특성화를 보여준다. 왼쪽 패널: pCoV323(RR-SpFN)의 크기 배제 크로마토그래피는 일시적으로 형질감염된 단백질이 예상된 크기의 큰 나노입자를 형성함을 보여준다. 오른쪽 패널: 크기 배제 크로마토그래피 후 NiNTA 친화성 정제에 의한 정제 후 pCoV323의 SDS-PAGE.
도 15는 스파이크 단백질 수용체 결합 도메인(RBD)의 아미노산 서열의 서열 유사성을 기반으로 선택된 사르베코바이러스 균주의 계통학적 그룹화를 반영하는 분기도를 보여준다.
도 16은 패널 A에서 항원 거리 세트의 그림을 보여준다. 비례적으로 더 가까운 사르베코바이러스 균주는 더 멀리 떨어진 균주에 비해 면역학적 유사성이 더 크다. 도 16은 또한 패널 B에서 항원 거리 세트의 세 가지 상이한 균주의 항원을 포함하는 다가 RFN의 그림을 보여준다. 상이한 RBD(즉, "RFN"의 "R")는 상이한 기원 균주를 반영하기 위해 상이한 패턴으로 도시되어 있다.
도 17은 상이한 항원 제시 형식에서 테스트된 항원 거리 세트의 요약을 보여준다. (+)는 공동 캡슐화된 mRNA 분자에서 발현된 구축물을 나타내고; (++)는 별도로 캡슐화된 mRNA 분자의 혼합물에서 발현된 구축물을 나타내고; +/- FN은 빈 페리틴 입자가 있거나 없이 테스트한 형식을 나타낸다.
도 18은 HeLa 세포에서 mRNA 구축물을 발현시킨 후의 웨스턴 블롯 결과(패널 A)와 단가 구축물의 정확한 밴딩(MW)을 보여주는 블롯(패널 B) 결과를 보여준다.
도 19는 HeLa 세포에서 mRNA 구축물을 발현시킨 후의 웨스턴 블롯과 전자 현미경 결과를 보여준다. 패널 A는 세포 용해물의 단백질을 보여주고; 패널 B는 배양 상층액의 단백질을 보여주고; 패널 C는 상층액에서 정제된 SARS-CoV-2 베타 SpFN 분자의 음성 염색 전자 현미경 격자를 보여준다. 입자의 조립은 검은색 화살표로 표시되어 있으며, 스파이크는 페리틴 나노입자의 표면에서 보인다. 패널 D는 스파이크와 페리틴 입자를 포함한 SpFN 입자의 클래스 평균을 보여준다
도 20은 단가 RFN(그룹 1-7)(패널 A), SpFN(그룹 18-24)(패널 B), 또는 안정화된 막관통 스파이크(S2P, 그룹 15-17, 37-40)(패널 C)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 WA-1, 델타, 베타, BA5, BQ.1.1, 또는 XBB.1.5, 코로나바이러스 클레이드 1a의 SARS-COV-1 균주, 및 메르비코바이러스에 대해 유발된 가성 중화 역가의 기하 평균을 보여준다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 21은 다가 믹스 A-E RFN(그룹 8-12)(패널 A), SpFN(그룹 25-29)(패널 B), 또는 안정화된 막관통 스파이크(S2P, 그룹 41-44)(패널 C)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 WA-1, 델타, 베타, BA5, BQ.1.1, 또는 XBB.1.5, 코로나바이러스 클레이드 1a의 SARS-COV-1 균주, 및 메르비코바이러스에 대해 유발된 가성 중화 역가의 기하 평균을 보여준다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 22는 단가 RFN 또는 RFN 항원 거리 믹스 A-E(그룹 1-12)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 (A) WA-1, (B) 델타, (C) 베타, (D) BA5, (E) BQ.1.1, 또는 (F) XBB.1.5에 대해 유발된 가성 중화 역가의 기하 평균을 보여준다. 각 마우스 그룹의 역가와 판독값은 평균(수평선), 제1 표준 편차(박스), 및 제2 표준 편차(수직선)를 보여주는 박스 수염 플롯으로 표현된다. 평균에서 2 표준 편차 넘게 떨어진 임의의 개별 역가(즉, 이상치)는 원으로 표현된다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 23은 단가 SpFN 또는 SpFN 항원 거리 믹스 A-E(그룹 18-29)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 (A) WA-1, (B) 델타, (C) 베타, (D) BA5, (E) BQ.1.1, 또는 (F) XBB.1.5에 대해 유발된 가성 중화 역가를 보여준다. 각 마우스 그룹의 역가와 판독값은 평균(수평선), 제1 표준 편차(박스), 및 제2 표준 편차(수직선)를 보여주는 박스 수염 플롯으로 표현된다. 평균에서 2 표준 편차 넘게 떨어진 임의의 개별 역가(즉, 이상치)는 원으로 표현된다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 24는 단가 S2P 또는 S2P 항원 거리 믹스 A-E(그룹 15-17, 31, 38-44)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 (A) WA-1, (B) 델타, (C) 베타, (D) BA5, (E) BQ.1.1, 또는 (F) XBB.1.5에 대해 유발된 가성 중화 역가를 보여준다. 각 마우스 그룹의 역가와 판독값은 평균(수평선), 제1 표준 편차(박스), 및 제2 표준 편차(수직선)를 보여주는 박스 수염 플롯으로 표현된다. 평균에서 2 표준 편차 넘게 떨어진 임의의 개별 역가(즉, 이상치)는 원으로 표현된다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 25는 단가 또는 다가 안정화된 막관통 항원(S-2P, 단가 그룹 15-17, 37-40; 다가 그룹 31, 41-44)으로서 제시된 스파이크 항원 및 페리틴에 접합된 단가 또는 다가 스파이크(SpFN, 단가 그룹 18-24; 다가 그룹 25-29)로 면역화된 마우스의 혈청에서 코로나바이러스 균주 WA-1, 델타, 베타, BA5, BQ.1.1, XBB.1.5, SARS1, 또는 MERS에 대해 유발된 기하 평균 가성 중화 역가를 보여준다. 그룹은 구성 균주를 기준으로 일치시키고, 안정화된 막관통 스파이크 그룹이 x축 좌표를 형성하고, 페리틴 그룹에 접합된 스파이크가 y축 좌표를 형성하는 산점도에 플로팅하였다. 단가 역가(채워지지 않은 원)는 x = y 선(점선) 주위에 분포되어 있어 각 그룹마다 대략 동일한 역가를 시사한다. 개별 그룹 역가 및 역가 분포는 도 20 및 21을 참조한다.
도 26은 믹스 C SpFN(그룹 #), 믹스 D RFN(그룹 #), 및 빈 페리틴이 포함된 믹스 D RFN(RFN+FN, 그룹 #)으로 면역화된 마우스의 혈청에서 코로나바이러스 균주 (A) WA-1, (B) 델타, (C) 베타, (D) SARS-1에 대해 유발된 가성 중화 역가를 보여준다. mRNA는 각 구축물을 코딩하는 mRNA 분자를 별도로 캡슐화하는 LNP 혼합물의 공동 투여(투여) 또는 mRNA 분자를 공동 캡슐화하는 LNP(캡슐화)로 투여하였다.
도 27은 빈 페리틴이 포함 또는 미포함된 RFN으로 면역화된 마우스의 혈청에 의해 코로나바이러스 균주 유사바이러스 (A) WA-1, (B) 델타, (C) 베타, (D) SARS-1에 대해 유발된 가성 중화 역가를 보여준다: WA-1(그룹 1, 34), SARS-1(그룹 4, 36), 또는 BANAL20-247(그룹 7, 35). 또한, 다가 믹스 D(WA-1 + SARS-1 + BANAL20-247) RFN을 4가지 제제로 테스트하였다: 각 단가 성분(빈 FN 미포함)을 공동 투여(ca -, 그룹 33), 각 단가 성분을 빈 FN과 공동 캡슐화하여 공동 투여(ca ce +, 그룹 14), 빈 FN 없이 공동 캡슐화(그룹 13), 및 공동 캡슐화(그룹 8).
도 28은 다가 입자가 각각 상이한 융합 단백질(상이한 균주의 RFN으로 도시됨)을 발현하는 여러 mRNA를 단일 LNP에 공동 캡슐화하거나(상단 패널에 표시됨), 각각 상이한 mRNA를 캡슐화하는 여러 LNP를 투여하여 생산될 수 있음을 보여준다.
도 29는 실험에 사용된 균주의 다양한 믹스(믹스 A-E)와 균주의 상대적 항원 거리, 및 생성된 나노입자의 개략도를 보여준다.
도 30은 다가 입자의 다양한 예를 보여준다. 도시된 예에는 두 가지 상이한 RFN 융합 단백질(A)과 네 가지 상이한 RFN 융합 단백질(B)로 구성된 입자가 포함되지만, 다른 입자는 3, 5 또는 6개 이상의 상이한 RFN 융합 단백질로부터 형성될 수 있다. 도시된 예에는 또한 각 RBD(즉, "RRFN"의 각 "R")가 상이한 균주에서 유래된 단일 RRFN 융합 단백질을 포함하는 다가 입자(C), 및 RBD 도메인의 순서가 두 개의 상이한 RRFN 융합 단백질 사이에서 스위칭된 두 개의 RRFN 융합 단백질을 포함하는 입자가 포함된다. 상이한 순서의, 그리고 상이한 균주의 다양한 RBD 도메인을 갖는 RRFN 융합 단백질을 포함하는 다른 RRFN 입자도 형성될 수 있다.
도 31은 부스터 백신으로서 본원에 기술된 바와 같은 다가 항원에 대한 연구를 위한 투여 요법을 보여준다.
도 2는 범(pan)-CoV 나노입자 설계 형식의 선형 개략도를 보여준다. 10가지 설계 형식이 표시되어 있으며, 여기에는 직렬로 연결된 이종 수용체 결합 도메인(RBD)이 선행된 C-말단 H. 파일로리 페리틴, 직렬의 RBD와 N-말단 도메인(NTD), S1 폴리펩티드의 천연 하위 도메인(SD)을 보유하면서 NTD를 대체하는 RBD, 및 NTD의 루프에 삽입된 RBD가 포함된다. 이종 RBD 분자가 천연 RBD 또는 NTD 도메인을 대체하기 위해 도입되거나, N-말단에서 연결된 추가 RBD 도메인으로서 도입되는 스파이크 페리틴 나노입자(SpFN)의 세 가지 예가 있다. 이러한 설계 형식 중 다수는 직교적이며 결합될 수 있다. 구체적으로, NTD의 루프에 RBD를 삽입하는 것은 NTD를 함유하는 구축물과 결합될 수 있다. 페리틴으로 예시되었지만, 페리틴은 본원에 논의된 바와 같이 다른 나노입자 운반체 분자로 대체될 수 있다.
도 3은 선택된 "실에 꿴 구슬" 형식을 그래픽 표현으로 보여주며, (A) RR-FN, (B) RN-FN, (C) RRN-FN, (D) RNRN-FN, (E) R-FN, (F) RR-FN, 및 (G) RR-FN에 대한 예가 제공된다. 예를 들어, 임의의 조합의 하나 이상의 RBD는 페리틴에 직렬로 연결될 수 있고("R-FN" 또는 "RR-FN"); 임의의 코로나바이러스 균주의 하나의 RBD는 임의의 코로나바이러스 균주의 NTD와 페리틴에 연결될 수 있고("RN-FN"); 상이한 코로나바이러스 균주의 두 RBD는 상이한 코로나바이러스 균주의 NTD와 페리틴에 직렬로 연결될 수 있으며("RRN-FN"); RBD-NTD-RBD-NTD 시리즈는 임의의 코로나바이러스 균주의 RBD 또는 NTD가 직렬로 연결되고 페리틴에 연결된다("RNRN-FN").
도 4는 선택된 "도메인 융합" 형식을 그래픽 표현으로 보여주며, (A) R2-SD-FN, (B) R-S1-FN, (C) R2-SD-S2-FN, (D) (R)-R-SpFN, (E) R-SpFN, (F) RR-SpFN, 및 (G) RR-SpFN에 대한 예와 도메인 표기가 제공되어 있다.
도 5는 선택된 "루프 삽입" 형식을 그래픽 표현으로 보여주며, 이종 RBD 분자가 (A) R2N-FN-70, (B) R2N-FN-148, 및 (C) R2N-FN-164에 삽입되는 키메라 융합 페리틴 나노입자 면역원 세트에 대한 예와 도메인 표기가 제공되어 있다.
도 6은 선택된 "도메인 스왑" 형식(이하 "모자이크" 형식으로도 지칭함)을 그래픽 표현으로 보여주며, 이종 RBD 분자가 (A) CoV SpFN 분자에 삽입되고(모자이크 SpFN) (B) 추가 이종 RBD 분자가 SpFN 분자의 N-말단에 추가되는(모자이크 R-모자이크 SpFN) 키메라 융합 스파이크 페리틴 나노입자 면역원 세트에 대한 예와 도메인 표기가 제공되어 있다. 키메라 융합 스파이크는 만화 표현으로 보여주며, 추가 이종 RBD가 표시되어 있다.
도 7a 및 7b는 이종 RBD 또는 NTD 분자가 모자이크 SpFN 설계의 N-말단에 추가되는 키메라 융합 스파이크 페리틴 나노입자(SpFN) 면역원 세트(예를 들어, 모자이크 형식)에 대한 선택된 설계를 그래픽 표현으로 보여준다: 도 7a: 다양한 R-R-모자이크 SpFN; 도 7b: RNR-모자이크 SpFN. 추가 RBD 또는 NTD 분자를 모자이크 SpFN의 N-말단에 추가할 수 있다.
도 8은 (A) MERS-CoV RBD-페리틴 나노입자의 음성 염색 전자 현미경, 및 (B) M3 RBD 페리틴 및 M4RBD-페리틴 나노입자의 2D 분류를 보여준다. 간단히 말해서, 정제된 단백질은 탄소 코팅 구리 격자에 0.02-0.08 mg/ml로 침적되고 0.75% 우라닐 포르메이트로 염색되었다. 격자는 SerialEM을 사용하는 Eagle 4K CCD가 장착된 200 kV에서 작동하는 FEI T20을 사용하거나 EPU를 사용하는 Thermo Scientific Ceta가 장착된 120 kV에서 작동하는 Thermo Scientific Talos L120C를 사용하여 이미지화되었다.
도 9는 스파이크 단백질 수용체 결합 도메인(RBD)의 아미노산 서열의 서열 유사성을 기반으로 선택된 사르베코바이러스 균주의 계통학적 그룹화를 반영하는 분기도를 보여준다.
도 10은 두 가지 형식으로 MERS-CoV 중화 인간 단클론 항체 CDC-C2에 대한 결합을 평가한 MERS RBD-페리틴 나노입자 면역원(M.1-M3.6)의 octet 생물층 간섭 결합 분석 결과를 보여준다.
도 11은 MERS RBD-페리틴 나노입자 면역원의 음성 염색 전자 현미경 및 결합 연구를 보여준다. 패널 A는 SARS2-RBD-MERS-RBD CoV-페리틴 구축물이 음성 염색 EM에서 나타난 바와 같이 나노입자를 형성함을 보여주고, 패널 B는 SARS2-RBD-MERS-RBD CoV-페리틴 구축물을 MERS-CoV 중화 인간 단클론 항체 및 SARS-CoV-2 중화 mAb에 대한 결합에 대해 평가한 것을 보여준다. pCoV247 및 pCoV248에 대한 구축물 설계는 표 3에 나와 있다.
도 12는 패널 A에서 코로나바이러스 스파이크 페리틴 나노입자 구축물의 음성 염색 전자 현미경이 음성 염색 EM에서 나타난 바와 같이 나노입자를 형성함을 보여주고; 패널 B에서 SARS-1(SARS-CoV-1), MERS, HKU-1, 및 229E 스파이크 페리틴 나노입자의 2D 분류를 보여주고, 패널 C에서 HKU-1 및 229E 스파이크 페리틴 나노입자의 3D 재구성을 보여준다.
도 13은 중화 항체 ShAb01(SARS-CoV-1 및 SARS-CoV-2를 중화), ShAb02(SARS-CoV-2를 중화), 및 인간 ACE2 수용체에 대한 결합을 생물층 간섭법으로 평가한 R-SpFN 설계 pCoV316 및 pCoV317의 결과를 보고하는 그래프를 보여준다. 180초 동안 결합이 발생하도록 한 다음 60초 동안 해리되도록 하였다.
도 14는 구축물 pCoV323(RR-SpFN, 여기서 MZ081380_bat_Yunnan_RsYN04_2020의 RBD, 및 SARS-1 RBD가 WA-1 SpFN 분자에 연결됨)의 생산 및 특성화를 보여준다. 왼쪽 패널: pCoV323(RR-SpFN)의 크기 배제 크로마토그래피는 일시적으로 형질감염된 단백질이 예상된 크기의 큰 나노입자를 형성함을 보여준다. 오른쪽 패널: 크기 배제 크로마토그래피 후 NiNTA 친화성 정제에 의한 정제 후 pCoV323의 SDS-PAGE.
도 15는 스파이크 단백질 수용체 결합 도메인(RBD)의 아미노산 서열의 서열 유사성을 기반으로 선택된 사르베코바이러스 균주의 계통학적 그룹화를 반영하는 분기도를 보여준다.
도 16은 패널 A에서 항원 거리 세트의 그림을 보여준다. 비례적으로 더 가까운 사르베코바이러스 균주는 더 멀리 떨어진 균주에 비해 면역학적 유사성이 더 크다. 도 16은 또한 패널 B에서 항원 거리 세트의 세 가지 상이한 균주의 항원을 포함하는 다가 RFN의 그림을 보여준다. 상이한 RBD(즉, "RFN"의 "R")는 상이한 기원 균주를 반영하기 위해 상이한 패턴으로 도시되어 있다.
도 17은 상이한 항원 제시 형식에서 테스트된 항원 거리 세트의 요약을 보여준다. (+)는 공동 캡슐화된 mRNA 분자에서 발현된 구축물을 나타내고; (++)는 별도로 캡슐화된 mRNA 분자의 혼합물에서 발현된 구축물을 나타내고; +/- FN은 빈 페리틴 입자가 있거나 없이 테스트한 형식을 나타낸다.
도 18은 HeLa 세포에서 mRNA 구축물을 발현시킨 후의 웨스턴 블롯 결과(패널 A)와 단가 구축물의 정확한 밴딩(MW)을 보여주는 블롯(패널 B) 결과를 보여준다.
도 19는 HeLa 세포에서 mRNA 구축물을 발현시킨 후의 웨스턴 블롯과 전자 현미경 결과를 보여준다. 패널 A는 세포 용해물의 단백질을 보여주고; 패널 B는 배양 상층액의 단백질을 보여주고; 패널 C는 상층액에서 정제된 SARS-CoV-2 베타 SpFN 분자의 음성 염색 전자 현미경 격자를 보여준다. 입자의 조립은 검은색 화살표로 표시되어 있으며, 스파이크는 페리틴 나노입자의 표면에서 보인다. 패널 D는 스파이크와 페리틴 입자를 포함한 SpFN 입자의 클래스 평균을 보여준다
도 20은 단가 RFN(그룹 1-7)(패널 A), SpFN(그룹 18-24)(패널 B), 또는 안정화된 막관통 스파이크(S2P, 그룹 15-17, 37-40)(패널 C)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 WA-1, 델타, 베타, BA5, BQ.1.1, 또는 XBB.1.5, 코로나바이러스 클레이드 1a의 SARS-COV-1 균주, 및 메르비코바이러스에 대해 유발된 가성 중화 역가의 기하 평균을 보여준다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 21은 다가 믹스 A-E RFN(그룹 8-12)(패널 A), SpFN(그룹 25-29)(패널 B), 또는 안정화된 막관통 스파이크(S2P, 그룹 41-44)(패널 C)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 WA-1, 델타, 베타, BA5, BQ.1.1, 또는 XBB.1.5, 코로나바이러스 클레이드 1a의 SARS-COV-1 균주, 및 메르비코바이러스에 대해 유발된 가성 중화 역가의 기하 평균을 보여준다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 22는 단가 RFN 또는 RFN 항원 거리 믹스 A-E(그룹 1-12)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 (A) WA-1, (B) 델타, (C) 베타, (D) BA5, (E) BQ.1.1, 또는 (F) XBB.1.5에 대해 유발된 가성 중화 역가의 기하 평균을 보여준다. 각 마우스 그룹의 역가와 판독값은 평균(수평선), 제1 표준 편차(박스), 및 제2 표준 편차(수직선)를 보여주는 박스 수염 플롯으로 표현된다. 평균에서 2 표준 편차 넘게 떨어진 임의의 개별 역가(즉, 이상치)는 원으로 표현된다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 23은 단가 SpFN 또는 SpFN 항원 거리 믹스 A-E(그룹 18-29)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 (A) WA-1, (B) 델타, (C) 베타, (D) BA5, (E) BQ.1.1, 또는 (F) XBB.1.5에 대해 유발된 가성 중화 역가를 보여준다. 각 마우스 그룹의 역가와 판독값은 평균(수평선), 제1 표준 편차(박스), 및 제2 표준 편차(수직선)를 보여주는 박스 수염 플롯으로 표현된다. 평균에서 2 표준 편차 넘게 떨어진 임의의 개별 역가(즉, 이상치)는 원으로 표현된다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 24는 단가 S2P 또는 S2P 항원 거리 믹스 A-E(그룹 15-17, 31, 38-44)로 면역화된 마우스의 혈청에서 코로나바이러스 클레이드 1b 균주 (A) WA-1, (B) 델타, (C) 베타, (D) BA5, (E) BQ.1.1, 또는 (F) XBB.1.5에 대해 유발된 가성 중화 역가를 보여준다. 각 마우스 그룹의 역가와 판독값은 평균(수평선), 제1 표준 편차(박스), 및 제2 표준 편차(수직선)를 보여주는 박스 수염 플롯으로 표현된다. 평균에서 2 표준 편차 넘게 떨어진 임의의 개별 역가(즉, 이상치)는 원으로 표현된다. 각 그룹의 추가 세부 정보는 표 8에서 찾을 수 있다.
도 25는 단가 또는 다가 안정화된 막관통 항원(S-2P, 단가 그룹 15-17, 37-40; 다가 그룹 31, 41-44)으로서 제시된 스파이크 항원 및 페리틴에 접합된 단가 또는 다가 스파이크(SpFN, 단가 그룹 18-24; 다가 그룹 25-29)로 면역화된 마우스의 혈청에서 코로나바이러스 균주 WA-1, 델타, 베타, BA5, BQ.1.1, XBB.1.5, SARS1, 또는 MERS에 대해 유발된 기하 평균 가성 중화 역가를 보여준다. 그룹은 구성 균주를 기준으로 일치시키고, 안정화된 막관통 스파이크 그룹이 x축 좌표를 형성하고, 페리틴 그룹에 접합된 스파이크가 y축 좌표를 형성하는 산점도에 플로팅하였다. 단가 역가(채워지지 않은 원)는 x = y 선(점선) 주위에 분포되어 있어 각 그룹마다 대략 동일한 역가를 시사한다. 개별 그룹 역가 및 역가 분포는 도 20 및 21을 참조한다.
도 26은 믹스 C SpFN(그룹 #), 믹스 D RFN(그룹 #), 및 빈 페리틴이 포함된 믹스 D RFN(RFN+FN, 그룹 #)으로 면역화된 마우스의 혈청에서 코로나바이러스 균주 (A) WA-1, (B) 델타, (C) 베타, (D) SARS-1에 대해 유발된 가성 중화 역가를 보여준다. mRNA는 각 구축물을 코딩하는 mRNA 분자를 별도로 캡슐화하는 LNP 혼합물의 공동 투여(투여) 또는 mRNA 분자를 공동 캡슐화하는 LNP(캡슐화)로 투여하였다.
도 27은 빈 페리틴이 포함 또는 미포함된 RFN으로 면역화된 마우스의 혈청에 의해 코로나바이러스 균주 유사바이러스 (A) WA-1, (B) 델타, (C) 베타, (D) SARS-1에 대해 유발된 가성 중화 역가를 보여준다: WA-1(그룹 1, 34), SARS-1(그룹 4, 36), 또는 BANAL20-247(그룹 7, 35). 또한, 다가 믹스 D(WA-1 + SARS-1 + BANAL20-247) RFN을 4가지 제제로 테스트하였다: 각 단가 성분(빈 FN 미포함)을 공동 투여(ca -, 그룹 33), 각 단가 성분을 빈 FN과 공동 캡슐화하여 공동 투여(ca ce +, 그룹 14), 빈 FN 없이 공동 캡슐화(그룹 13), 및 공동 캡슐화(그룹 8).
도 28은 다가 입자가 각각 상이한 융합 단백질(상이한 균주의 RFN으로 도시됨)을 발현하는 여러 mRNA를 단일 LNP에 공동 캡슐화하거나(상단 패널에 표시됨), 각각 상이한 mRNA를 캡슐화하는 여러 LNP를 투여하여 생산될 수 있음을 보여준다.
도 29는 실험에 사용된 균주의 다양한 믹스(믹스 A-E)와 균주의 상대적 항원 거리, 및 생성된 나노입자의 개략도를 보여준다.
도 30은 다가 입자의 다양한 예를 보여준다. 도시된 예에는 두 가지 상이한 RFN 융합 단백질(A)과 네 가지 상이한 RFN 융합 단백질(B)로 구성된 입자가 포함되지만, 다른 입자는 3, 5 또는 6개 이상의 상이한 RFN 융합 단백질로부터 형성될 수 있다. 도시된 예에는 또한 각 RBD(즉, "RRFN"의 각 "R")가 상이한 균주에서 유래된 단일 RRFN 융합 단백질을 포함하는 다가 입자(C), 및 RBD 도메인의 순서가 두 개의 상이한 RRFN 융합 단백질 사이에서 스위칭된 두 개의 RRFN 융합 단백질을 포함하는 입자가 포함된다. 상이한 순서의, 그리고 상이한 균주의 다양한 RBD 도메인을 갖는 RRFN 융합 단백질을 포함하는 다른 RRFN 입자도 형성될 수 있다.
도 31은 부스터 백신으로서 본원에 기술된 바와 같은 다가 항원에 대한 연구를 위한 투여 요법을 보여준다.
본 개시 내용은 코로나바이러스 감염 및 코로나바이러스 감염성 질환, 그리고 사르베코바이러스 및 메르베코바이러스에 의해 유발되는 관련 감염 및 질환을 치료 또는 예방하기 위한 나노입자 백신 및 이를 코딩하는 mRNA 분자를 포함하는 면역원성 조성물을 제공한다. 개시된 면역원성 조성물은 적어도 제1 항원성 코로나바이러스 펩티드와 제2 항원성 코로나바이러스 펩티드를 포함하는 적어도 두 개의 항원성 코로나바이러스 펩티드, 또는 이를 코딩하는 하나 이상의 메신저 RNA(mRNA) 분자를 포함하는 면역원성 조성물을 포함한다. 일부 실시양태에 따라, 본원에서는 상이한 균주의 두 개 이상의 항원성 코로나바이러스 펩티드, 또는 이를 코딩하는 mRNA 분자를 포함하는 다가 면역원성 조성물을 기술한다. 이종 항원은 면역 반응을 집중시켜 인식된 항원의 추가 폭을 생성할 수 있다. 또한, 여러 이종 균주, 심지어 클레이드에 걸친 균주에 의한 면역화는 면역 반응의 추가 폭을 제공할 수 있다.
본원에서 개시된 나노입자는 나노입자 형성 펩티드와 항원성 코로나바이러스 펩티드(예를 들어, 적어도 두 개의 항원성 코로나바이러스 펩티드, 선택적으로 상이한 코로나바이러스 균주에서 유래)를 포함하는 융합 단백질로 구성되며, 이는 링커를 통해 선택적으로 결합될 수 있다. 융합 단백질은 용액에서 안정하고 대상체에게 투여될 때 보호적 중화 면역 반응(즉, 중화 항체 및/또는 방어적 사이토카인 생성)을 생성할 수 있는 나노입자로 자가 조립될 수 있다. 마찬가지로, 개시된 mRNA 분자는 생체 내에 투여되고 발현될 때 보호적 중화 면역 반응을 생성하는 항원을 생성한다. 일부 실시양태에서, 면역원성 조성물은 나노입자 형성 펩티드와 항원성 코로나바이러스 펩티드를 포함하는 하나 이상의 융합 단백질을 코딩하는 하나 이상의 mRNA 분자를 포함하고, 생체 내에 투여되고 발현될 때 보호적 중화 면역 반응을 생성하는 본원에서 개시된 바와 같은 나노입자를 생성한다. 임의의 실시양태에서, 본원에 개시된 바와 같은 면역원성 조성물은 또한 보조제를 포함할 수 있다
개시된 면역원성 조성물(예를 들어, mRNA 분자 또는 나노입자를 포함함)은 SARS-CoV-2 및 기타 사르베코바이러스, MERS-CoV 및 기타 메르베코바이러스, 및 기타 코로나바이러스와 같은 코로나바이러스 감염에 대한 보호를 제공할 것이다. 개시된 면역원성 조성물은 또한 코로나바이러스로 인한 질병을 줄일 수 있다. 개시된 면역원성 조성물은 백신을 접종한 개인에게 보호 면역 반응을 유발할 수 있다.
I. 정의
본원에 사용된 용어는 특정 실시양태를 설명하기 위한 목적일 뿐, 제한하려는 의도가 아님을 이해해야 한다.
본원에 사용된 기술 및 과학 용어는 달리 정의되지 않는 한 해당 분야의 통상의 기술자가 일반적으로 이해하는 의미를 갖는다. 달리 명시되지 않는 한, 해당 분야의 통상의 기술자에게 알려진 재료 및/또는 방법은 본원에 제공된 지침에 따라 본원에 기술된 방법을 수행하는 데 활용할 수 있다.
본원에 사용되는 바와 같이, 단수 용어 "a", "an", 및 "the"는 문맥상 명확히 달리 지시되지 않는 한 복수 지시 대상을 포함한다. 단수형으로 대상을 지칭하는 것은 명시적으로 그렇게 언급되지 않는 한 "하나이자 유일한 하나"를 의미하는 것이 아니라 "하나 이상"을 의미하는 것이다.
본원에 사용되는 바와 같이, "약"은 수치 값과 함께 사용될 때 명시된 수치 값과 수치 값의 플러스 또는 마이너스 10%를 의미한다. 예를 들어, "약 10"은 "10"과 "9 내지 11" 둘 다로 이해되어야 한다.
본원에서 사용되는 바와 같이, "A/B" 형태 또는 "A 및/또는 B" 형태의 문구는 (A), (B), 또는 (A 및 B)를 의미하고; "A, B, 및 C 중 적어도 하나" 형태의 문구는 (A), (B), (C), (A 및 B), (A 및 C), (B 및 C), 또는 (A, B, 및 C)를 의미한다.
본원에서 사용되는 바와 같이, "포함하는"이라는 용어는 조성물 및 방법이 언급된 요소를 포함하지만 다른 요소를 배제하지 않는다는 것을 의미하는 것으로 의도된다.
본원에서 사용되는 바와 같이, "변이체"는 펩티드를 지칭하는 맥락에서 사용될 때 치환, 결실, 또는 삽입을 포함할 수 있는 하나 이상의 아미노산 변화를 통합하여 부모 서열로부터 유래되는 펩티드 서열을 의미한다. 본 개시 내용의 목적을 위해, 변이체는 참조(또는 "부모") 서열과 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 약 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있다. 본 개시 내용의 목적을 위해, 펩티드를 지칭하는 맥락에서 사용될 때 "변이체" 및 "유도체"라는 용어는 상호교환 가능하게 사용된다.
본원에서 사용되는 바와 같이, 바이러스(예를 들어, SARS-CoV-2)를 지칭하는 맥락에서 사용될 때 "변종"은 게놈(예를 들어, RNA 게놈)에 하나 이상의 변화를 갖는 참조(또는 "부모") 바이러스의 자손인 바이러스, 또는 참조(또는 "부모") 바이러스에 비해 게놈에 하나 이상의 변화를 갖도록 유전적으로 조작된 바이러스를 의미하며, 이는 RNA 서열에 의해 코딩된 단백질에 변화를 초래할 수도 있고 초래하지 않을 수도 있다(예를 들어, 변종 바이러스의 하나 이상의 단백질은 부모 균주에 비해 치환, 결실, 또는 삽입을 포함할 수 있음). 예를 들어, SARS-CoV-2의 알려진 변종에는 B.1.1.7(영국에서 처음 확인됨), B.1.351(남아프리카에서 처음 확인됨), 및 P.1(브라질에서 처음 확인됨), 및 XBB.1.5, EG.5.1, BA.1, BA.2, 및 BA.5를 포함하는 오미크론 변종이 포함되지만 이에 제한되지 않는다. 본 개시 내용의 목적을 위해, 바이러스 변종은 참조(또는 "부모") 게놈 서열과 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 약 100%의 서열 동일성 또는 상동성을 공유하는 게놈 서열을 포함할 수 있다.
본원에서 사용되는 바와 같이, "유효량", "치료 유효량" 및 "치료 수준"이라는 문구는 백신이 상기 치료가 필요한, 즉 코로나바이러스 감염(예를 들어, MERS, SARS, 또는 COVID-19)의 치료 또는 예방을 위해 치료가 필요한 대상체에게 투여되는 특정 약리학적 효과를 제공하는 개시된 백신의 투여량 또는 농도를 의미한다. 백신의 치료 유효량 또는 치료 수준은 상기 투여량이 해당 분야의 기술자에게 치료 유효량으로 간주되더라도 본원에서 기술하는 감염을 치료 또는 예방하는 데 항상 효과적인 것은 아니라는 점을 강조한다. 단지 편의상, 예시적 투여량, 약물 전달량, 치료 유효량, 및 치료 수준이 본원에서 제공된다. 치료 유효량은 투여 경로 및 제형, 대상체의 연령 및 체중, 및/또는 코로나바이러스 감염의 유형 및 중증도를 포함한 대상체의 상태에 따라 달라질 수 있다.
코로나바이러스 감염과 관련하여 본원에서 사용되는 바와 같이 용어 "치료하다", "치료" 또는 "치료하는"은 바이러스 부하를 감소시키거나 제거하거나 기도 또는 폐에서 조직병리 또는 바이러스 존재를 제거하는 것을 말한다.
코로나바이러스 감염과 관련하여 본원에서 사용되는 바와 같이 용어 "예방하다", "예방하는" 또는 "예방"은 코로나바이러스에 노출된 대상체에서 감염이 발생할 위험을 방지하거나 감소시키거나, 코로나바이러스의 높은 바이러스 부하가 발생할 위험을 예방하거나 감소시키거나, 기도 또는 폐에서 조직병리 또는 바이러스 존재를 감소시키거나 제거하는 것을 말한다. 예방은 또한 초기 감염이 치료되거나 치유된 후 후속 감염을 예방하는 것을 말할 수 있다. 예방은 또한 한 대상체 숙주에서 다른 대상체 숙주로 바이러스가 전파되는 위험을 예방하거나 감소시키는 것을 말할 수 있다.
용어 "개인", "대상체", 및 "환자"는 본원에서 상호교환 가능하게 사용되며, 소, 개, 고양이, 말, 또는 인간과 같은 모든 개별 포유류 대상체를 지칭한다. 특정 실시양태에서, 대상체, 개인, 또는 환자는 인간이다.
본원에서 사용되는 바와 같이, 개시된 융합 단백질의 맥락에서 약어 "SD"는 코로나바이러스 스파이크 단백질의 하위 도메인을 지칭한다. 스파이크 단백질에는 하위 도메인 1과 하위 도메인 2가 있다(예를 들어, 문헌 [Wrapp et al., Science 367, 1260-1263(2020)] 참조). 따라서 "SD"는 스파이크 단백질의 SD1과 SD2(즉, 하위 도메인 1과 2) 중 하나 또는 둘 다를 지칭할 수 있다.
II. 코로나바이러스
코로나바이러스는 포유류에서 호흡기 감염을 유발하고 길이가 약 30킬로베이스인 게놈을 포함하는 바이러스 과(즉, 코로나바이러스과(Coronaviridae family))이다. 코로나바이러스과는 4개 속으로 나뉘며, 게놈은 다중 오픈 리딩 프레임에 걸쳐 28개의 단백질을 코딩하는데, 여기에는 폴리프로테인으로부터 번역 후 절단되는 16개의 비구조 단백질(nsp)이 포함된다. 예를 들어 문헌 [Letko et al., Nature Microbiology, 2020, 5(4):562-569]을 참조한다.
코로나바이러스과에는 α-코로나바이러스 또는 β-코로나바이러스가 모두 포함되며, 둘 다 주로 박쥐를 감염시키지만 인간, 낙타, 및 토끼와 같은 다른 포유류도 감염시킬 수 있다. β-코로나바이러스는 지금까지 임상적으로 더 중요했으며, 중증 급성 호흡기 증후군(SARS-CoV-1), 중동 호흡기 증후군(MERS-CoV), 및 COVID-19(SARS-CoV-2)와 같이 사망률이 높은 질환의 전염병을 유발하였다. 질환을 유발하는 다른 β-코로나바이러스에는 OC43, 및 HKU1이 포함된다. 질환을 유발하는 α-코로나바이러스의 비제한적인 예로는 229E 및 NL63이 포함되지만 이에 제한되지 않는다.
SARS-CoV-2는 새롭게 확인된 바이러스이지만, 코로나바이러스과의 다른 바이러스, 특히 β-코로나바이러스 속의 바이러스와 유전 및 형태적 특징을 공유한다. 최근 단리된 SARS-CoV-2의 게놈은 인간 SARS-CoV(SARS-CoV-1)와 82%의 뉴클레오티드 동일성을 공유하고 박쥐 SARS-유사-CoVZXC21과 89%의 뉴클레오티드 동일성을 공유한다(Lu et al., 2020). 특히 스파이크(S) 당단백질은 MERS-CoV와 같은 다른 코로나바이러스에 비해 SARS-CoV-1과 상당한 구조적 상동성을 보인다. SARS-CoV-1과 마찬가지로, SARS-CoV-2의 표면 스파이크(S) 당단백질은 동일한 숙주 수용체인 ACE-2에 결합하여 세포 진입을 매개한다(Letko et al., 2020; Yan et al., 2020a). 클래스 I 융합 단백질인 S는 또한 바이러스 숙주 범위와 조직 향성의 중요한 결정 요인이며 숙주 면역 반응의 주요 표적이다(Li, 2016). 따라서, 지금까지 개발된 대부분의 코로나바이러스 백신 후보는 S 또는 그 하위 구성 요소 중 하나를 기반으로 한다. 코로나바이러스 S 당단백질은 큰 엑토도메인, 단일 통과 막관통 앵커 및 짧은 세포 내 꼬리의 3개의 세그먼트를 포함한다. 엑토도메인은 수용체 결합 서브유닛인 S1로 이루어지며, 이는 2개의 하위 도메인 N-말단에 하나와 C-말단에 다른 하나를 함유한다. 후자는 수용체 결합 도메인(RBD)을 포함하며, 이는 바이러스를 숙주 수용체에 부착하고 단백질의 구조적 변화를 유발하여 S2 서브유닛을 통해 숙주 세포막과 융합하는 중요한 기능을 한다. 항체는 스파이크 단백질의 RBD에 결합하여 바이러스 진입을 중화하는 것으로 나타났다. 이 영역은 또한 단백질의 가장 가변적인 부분으로 알려져 있으며 재감염이나 백신 효능 저하로 이어지는 면역 회피의 원인이 될 가능성이 있다.
아래에서 더 자세히 논하겠지만, 페리틴은 많은 유기체에서 발현되는 작은 단백질로, 동형 24-머 "나노입자"를 형성할 수 있다. 이전 연구에서는 관심 항원으로 N-말단 영역을 장식하여 항원 제시 시스템으로서 역할을 하는 것으로 나타났다. 항원은 나노입자 형성을 방해하지 않고 페리틴 모이어티에 접합될 수 있다. 충분히 긴 링커를 통해 항원이 접합된 페리틴은 (8개의) CoV 삼량체와 같은 4차 구조를 형성할 수 있다.
핵산 백신, 전체 바이러스 백신, 재조합 단백질 서브유닛 백신 및 나노입자 백신을 포함하여 현재 여러 기술 플랫폼이 SARS-CoV-2 백신 개발을 진행하고 있다. 이러한 백신 플랫폼 유형 중 나노입자 기술은 이전에 항원 구조와 안정성뿐만 아니라, 백신 표적화 전달, 면역원성, 및 안전성을 개선하는 것으로 나타났다. 스파이크 단백질 또는 스파이크 단백질의 RBD 영역에 접합된 페리틴 나노입자를 함유한 백신은 동물 모델에서 후속 공격에 대해 보호적인 면역 반응을 유발하는 것으로 입증되었다. 문헌 [Joyce, et al., Science Translational Med., 14 (632) (DOI: 10.1126scitranslmed.abi5735)(2021년 12월 16일)]; 문헌 [Joyce et al., Cell Reports, 37: 110143 (2021년 12월 21일)]. 다중 항원(다가)을 사용한 항원 디스플레이 시스템은 코로나바이러스(예를 들어, 문헌 [Cohen at al., Science, 371: 735-741 (2021년 2월)]; 문헌 [Cohen at al., Science 377, eabq0839(2022) (DOI:10.1126/science.abq0839)] 참조) 및 인플루엔자(예를 들어, 문헌 [Kanekiyo et al., Nat. Immunol., 20: 367-72 (2019년 4월)] 참조)에 대한 반응 폭을 늘리는 것으로 입증되었다. 이종 균주로 추가 접종(또는 순차적 백신접종)을 하면 원래 균주의 이종 균주에 대한 커버리지 효과가 향상되는 것으로 나타났다. 예를 들어, 문헌 [Tan et al., N. Eng. J. Med., 385: 1401-06 (2021년 8월)]을 참조한다.
본 개시 내용의 일부 실시양태에서, 개시된 면역원성 조성물(예를 들어, 백신)에 의해 치료 또는 예방되는 코로나바이러스는 β-코로나바이러스이다. 일부 실시양태에서, β-코로나바이러스는 중증 급성 호흡기 증후군 코로나바이러스 2(SARS-CoV-2)(임시 명칭 2019 신종 코로나바이러스, 또는 2019-nCoV 또는 COVID-19로도 알려짐), 인간 코로나바이러스 OC43(hCoV-OC43), 중동 호흡기 증후군 관련 코로나바이러스(MERS-CoV, 임시 명칭 2012 신종 코로나바이러스, 또는 2012-nCoV로도 알려짐), 중증 급성 호흡기 증후군 관련 코로나바이러스(SARS-CoV, SARS-CoV-1로도 알려짐), HKU-1, 229E, 및 NL63으로 이루어진 군으로부터 선택된다. 일부 실시양태에서, β-코로나바이러스는 COVID-19의 원인체인 SARS-CoV-2이다. 일부 실시양태에서, 개시된 백신은 MERS-CoV, SARS-CoV-1, 및/또는 SARS-CoV-2, 및/또는 기타와 같은 여러 상이한 유형의 코로나바이러스에 대한 광범위한 치료 및/또는 예방을 제공할 수 있다.
III. 면역원성 조성물
본원에서는 코로나바이러스 감염을 치료 또는 예방하는 데 사용할 수 있는 면역원성 조성물(예를 들어, 백신)을 개시한다. 일부 측면에서, 개시된 면역원성 조성물은 나노입자 형성 펩티드와 항원성 코로나바이러스 펩티드를 포함하는 융합 단백질을 포함하며, 이는 선택적으로 링커(즉, "링커 도메인")에 의해 연결될 수 있다. 항원성 코로나바이러스 펩티드는 아래에서 더 자세히 기술되는 바와 같이 코로나바이러스(예를 들어, SARS-CoV-2 또는 SARS-CoV-1 또는 MERS-CoV)로부터 유래된 하나 이상의 단편 또는 전장 단백질을 포함할 수 있다.
A. 나노입자 형성 펩티드
본원에서 개시된 바와 같은 면역원성 조성물의 나노입자 형성 펩티드는 임의의 적합한 나노입자 형성 펩티드일 수 있다. H. 파일로리 페리틴 및 이의 단편 및 변이체는 본원에서 개시된 바와 같은 백신을 위한 나노입자 형성 펩티드로서 사용하기에 특히 적합하다. 따라서, 본원에 개시된 바와 같은 백신의 나노입자 형성 펩티드는 헬리코박터 파일로리 페리틴 단백질(HpF) 또는 이의 단편 또는 변이체를 포함할 수 있다. 예를 들어, 나노입자 구성 요소는 H. 파일로리 페리틴으로부터 유래된 다음 아미노산 서열을 포함할 수 있다:
따라서, 백신의 나노입자 형성 펩티드는 상기 H. 파일로리 페리틴 서열(서열 번호 1) 또는 이의 변이체를 포함할 수 있으며, 이는 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있다. 예를 들어, 나노입자 형성 펩티드는 서열 번호 1의 N-말단 도메인에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개 이상의 아미노산의 결실을 포함할 수 있는 서열 번호 1의 변이체를 포함할 수 있다. 일부 실시양태에서, 해당 나노입자 형성 펩티드는 서열 번호 1의 위치 13에서 글루탐산 잔기(E)의 치환을 포함할 수 있다. 일부 실시양태에서, 해당 나노입자 형성 펩티드는 다음 서열에서와 같이 서열 번호 1의 위치 13에서 글루탐산 잔기(E)의 치환과 서열 번호 1의 N-말단 도메인에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개 이상의 아미노산의 결실을 포함할 수 있다:
일부 실시양태에서, 나노입자 형성 펩티드는 서열 번호 1, 서열 번호 2, 또는 서열 번호 3 중 어느 하나의 변이체를 포함할 수 있으며, 이는 서열 번호 1, 서열 번호 2, 또는 서열 번호 3 중 어느 하나와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있다.
위에서 언급한 바와 같이, 일부 실시양태에서, 나노입자 형성 펩티드는 비-페리틴 기반 펩티드, 예컨대 다음 서열을 포함하는 펩티드 또는 이의 단편 또는 변이체일 수 있다:
일부 실시양태에서, 나노입자 형성 펩티드는 서열 번호 4의 변이체를 포함할 수 있으며, 이는 서열 번호 4에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있다. 일부 실시양태에서, 나노입자 형성 펩티드는 서열 번호 4와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있는 서열 번호 4의 변이체를 포함할 수 있다.
B. 링커 도메인
개시된 융합 단백질은 일반적으로 가요성 아미노산 링커를 포함하지만, 링커 도메인(즉, 링커)은 선택적이며, 일부 실시양태에서 나노입자 형성 펩티드는 항원성 코로나바이러스 펩티드와 직접 연결될 수 있다. 링커는 약 3 내지 약 50개 아미노산 길이이거나, 보다 구체적으로 약 4 내지 약 42개 아미노산 길이일 수 있다. 일부 실시양태에서, 링커는 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 또는 42개 아미노산 길이일 수 있다. 링커 도메인은 글리신(G) 반복체 및/또는 글리신(G)과 세린(S) 잔기의 조합을 포함할 수 있다. 여러 예시적인 링커 서열이 아래 표 1에 개시되어 있다.
링커 도메인은 서열 번호 5-17 또는 583 중 어느 하나의 1, 2, 또는 3개의 반복체를 포함할 수 있다. 일부 실시양태에서, 링커 도메인은 서열 번호 5-17 또는 583 중 어느 하나의 변이체를 포함하며, 이는 서열 번호 5-17 또는 583 중 어느 하나와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있다.
상기 링커 서열은 제한적인 것으로 의도되지 않으며, 당업자는 다른 가요성 펩티드 링커도 본원에 제공된 지침에 따라 나노입자 형성 펩티드와 항원성 코로나바이러스 펩티드를 연결하는 데 적합할 수 있음을 이해할 것이다.
C. 항원성 코로나바이러스 펩티드
일반적으로, 개시된 면역원성 조성물 및 융합 단백질의 항원성 코로나바이러스 펩티드는 일반적으로 숙주 세포로의 바이러스 진입을 담당하는 코로나바이러스 스파이크 단백질("S 단백질" 또는 "당단백질 S"로도 알려짐), 또는 이의 단편 또는 변이체(예컨대 RBD 도메인 또는 이의 단편 또는 변이체)를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 순서대로 함께 연결된 코로나바이러스 스파이크 단백질의 1, 2, 또는 3개 이상의 별개의 도메인을 포함할 수 있으며, 이러한 실시양태에서 링커는 선택적으로 별개의 도메인을 분리할 수 있다.
스파이크 단백질은 본원에 개시된 바와 같은 백신의 항원성 코로나바이러스 펩티드로서 선택되는데, 그 이유는 이 펩티드에 대해 개발된 항체가 중화적일 가능성이 높기 때문이다. 스파이크 단백질은 숙주 세포 수용체(S1 서브유닛)와의 결합 및 바이러스와 세포막의 융합(S2 서브유닛)을 담당하는 두 개의 기능적 서브유닛을 포함한다. 본 개시 내용의 융합 단백질은 전체 스파이크 단백질, S1 서브유닛 단독, S2 서브유닛 단독, 또는 이의 임의의 항원성/면역원성 단편 또는 변이체를 포함할 수 있다. 일부 실시양태에서, 융합 단백질은 전체 길이의 코로나바이러스 스파이크 단백질 서열을 포함한다. 일부 실시양태에서, 융합 단백질은 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 코로나바이러스 스파이크 단백질(예를 들어, 서열 번호 18)의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 변이체를 포함한다.
이론에 얽매이고 싶지는 않지만, SARS-CoV-2의 스파이크 단백질은 인간 안지오텐신 전환 효소 (ACE)-2 세포 표면 수용체에 부착하여 인간 감염을 촉진하는 것으로 이해된다. 따라서, 스파이크 당단백질에 결합하고 ACE2 수용체와의 상호작용을 방지할 수 있는 항체는 감염으로부터의 보호를 촉진할 수 있다. SARS-CoV-2 스파이크 단백질(NCBI 참조 서열: YP_009724390.1)은 1273개의 아미노산으로 구성되어 있으며 N-말단에 위치한 신호 펩티드(아미노산 1-13), S1 서브유닛(14-685개의 잔기), 및 S2 서브유닛(686-1273개의 잔기)으로 이루어지며, 마지막 두 영역은 각각 수용체 결합과 막 융합을 담당한다. 아미노산 서열은 아래에 나타낸다:
본 개시 내용의 맥락에서 항원성 코로나바이러스 펩티드로서 특히 유용한 코로나바이러스 스파이크 단백질의 구체적인 도메인에는 다음이 포함된다:
● 코로나바이러스의 수용체 결합 도메인(RBD), 또는 이의 단편 또는 변이체,
● 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체,
● 코로나바이러스의 수용체 결합 도메인(RBD)-N-말단 도메인 키메라, 또는 이의 단편 또는 변이체,
● 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체,
● 코로나바이러스의 안정화된 스파이크 S-2P 도메인 또는 안정화된 세포외 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체,
● 코로나바이러스의 안정화된 스파이크 S 도메인 또는 안정화된 세포외 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 또는
● 코로나바이러스의 안정화된 스파이크 S-삼량체 또는 안정화된 세포외 스파이크 S-삼량체, 또는 이의 단편 또는 변이체.
따라서, 본 개시 내용의 항원성 코로나바이러스 펩티드는 RBD를 포함할 수 있다. RBD는 아래에 제시된 SARS-CoV-2 RBD 아미노산 서열을 포함할 수 있다:
일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 19에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있는 서열 번호 19의 변이체를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 19와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있는 서열 번호 19의 변이체를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 서열 번호 19의 길이의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 서열 번호 19의 단편일 수 있는 RBD의 단편을 포함한다.
항원성 코로나바이러스 펩티드는 발현 및/또는 나노입자를 형성하는 능력을 증가시킬 수 있는, "접착성" 소수성 영역을 줄이기 위해 만들어진 하나 이상의 특정 변형, 예를 들어, 다음 변형 중 하나 이상을 갖는 RBD(예를 들어, 서열 번호 19)의 변이체를 포함할 수 있다.
상기 변형은 이러한 변형을 갖는 RBD를 포함하는 융합 단백질의 발현 및/또는 나노입자 형성을 증가시킬 수 있다.
추가적으로 또는 대안적으로, 항원성 코로나바이러스 펩티드는 SARS-CoV-2가 아닌 코로나바이러스의 RBD일 수 있거나 이를 포함할 수 있다. 예를 들어, RBD 도메인은 MERS 또는 SARS-CoV-1(본원에서 SARS1 및 SARS-1이라고도 함)에서 유래될 수 있다. 예시적인 RBD 서열은 첨부된 표 6 및 표 7에 제공된 전체 길이의 구축물에서 찾을 수 있다. 더욱이, 일부 실시양태에서, 입자는 아래에서 더 자세히 논의되는 것과 같이 동일하거나 상이한 코로나바이러스의 여러 RBD를 포함할 수 있다.
추가적으로 또는 대안적으로, 본 개시 내용의 항원성 코로나바이러스 펩티드는 NTD를 포함할 수 있다. NTD는 SARS-CoV-2 NTD 아미노산 서열
을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 20에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있는 서열 번호 20의 변이체를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 20과 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있는 서열 번호 20의 변이체를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 서열 번호 20의 길이의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 서열 번호 20의 단편일 수 있는 NTD의 단편을 포함한다.
추가적으로 또는 대안적으로, 본 개시 내용의 항원성 코로나바이러스 펩티드는 SARS-CoV-2가 아닌 코로나바이러스의 NTD일 수 있거나 이를 포함할 수 있다. 예를 들어, NTD 도메인은 MERS 또는 SARS-CoV-1로부터 유래될 수 있다. 예시적인 NTD 서열은 첨부된 표 6 및 표 7에 제공된 전체 길이의 구축물에서 찾을 수 있다. 더욱이, 일부 실시양태에서, 입자는 동일하거나 상이한 코로나바이러스의 여러 NTD를 포함할 수 있다.
일부 실시양태에서, 입자는 하나 이상의 RBD(들) 및 하나 이상의 NTD(들)의 조합을 포함할 수 있으며, RBD(들) 및 NTD(들)는 동일하거나 상이한 코로나바이러스 또는 균주로부터 유래될 수 있다.
추가적으로 또는 대안적으로, 본 개시 내용의 항원성 코로나바이러스 펩티드는 S1 단백질 서열을 포함할 수 있다. S1 단백질 서열은 다음의 SARS-CoV-2 S1 단백질 아미노산 서열을 포함할 수 있다:
일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 21, 서열 번호 22, 또는 서열 번호 23에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있는 서열 번호 21, 서열 번호 22, 또는 서열 번호 23의 변이체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 21, 서열 번호 22, 또는 서열 번호 23과 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있는 서열 번호 21, 서열 번호 22, 또는 서열 번호 23의 변이체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 서열 번호 21, 서열 번호 22, 또는 서열 번호 23의 길이의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 서열 번호 21, 서열 번호 22, 또는 서열 번호 23의 단편일 수 있는 S1의 단편을 포함할 수 있다.
추가적으로 또는 대안적으로, 본 개시 내용의 항원성 코로나바이러스 펩티드는 S-2P 서열 또는 이의 단편 또는 변이체를 포함할 수 있다. S-2P 서열은 2개의 프롤린 치환을 포함하고 융합 전 형태를 안정화하는 스파이크 엑토도메인의 안정화된 버전이다. 대안적으로, S-2P 도메인은 막관통 도메인을 포함한다. 구체적으로, S-2P는 프롤린 변형 K986P 및 V987P, 게다가 푸린 절단 부위의 제거(RRAS에서 GSAS로)를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 S-2P 서열에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있는 S-2P 서열의 변이체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 안정화된 S-2P와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있는 S-2P 서열의 변이체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 안정화된 S-2P의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 S-2P의 단편을 포함할 수 있다.
추가적으로 또는 대안적으로, 본 개시 내용의 항원성 코로나바이러스 펩티드는 스파이크 S 도메인 또는 세포외 스파이크 S 도메인(예를 들어, 안정화된 스파이크 S 도메인 또는 안정화된 세포외 스파이크 S 도메인) 또는 이의 단편 또는 변이체를 포함할 수 있다. 안정화된 세포외 스파이크 S 도메인은 도메인 또는 세포외 도메인의 재융합 형태를 안정화하는 하나 이상의 변형을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 세포외 스파이크 S 도메인에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함하는 안정화된 세포외 스파이크 S 도메인을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 세포외 스파이크 S 도메인과 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함하는 안정화된 세포외 스파이크 S 도메인을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 세포외 스파이크 S 도메인(예를 들어, 안정화된 세포외 스파이크 S 도메인)의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 세포외 스파이크 S 도메인의 단편(예를 들어, 안정화된 세포외 스파이크 S 도메인의 단편)을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 스파이크 S 도메인에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함하는 안정화된 스파이크 S 도메인을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 스파이크 S 도메인과 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함하는 안정화된 스파이크 S 도메인을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 스파이크 S 도메인(예를 들어, 안정화된 스파이크 S 도메인)의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 스파이크 S 도메인의 단편(예를 들어, 안정화된 스파이크 S 도메인의 단편)을 포함할 수 있다.
추가적으로 또는 대안적으로, 본원에 기술된 바와 같은 항원성 코로나바이러스 펩티드는 스파이크 S 삼량체 또는 세포외 스파이크 S 삼량체(예를 들어, 안정화된 스파이크 S 삼량체 또는 안정화된 세포외 스파이크 S 삼량체) 또는 이의 단편 또는 변이체를 포함할 수 있다. 안정화된 세포외 스파이크 S 삼량체는 세포외 삼량체의 재융합 형태를 안정화하는 하나 이상의 변형을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 세포외 스파이크 S 삼량체에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함하는 안정화된 세포외 스파이크 S 삼량체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 세포외 스파이크 S 삼량체와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함하는 안정화된 세포외 스파이크 S 삼량체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 세포외 스파이크 S 삼량체(예를 들어 안정화된 세포외 스파이크 S 삼량체)의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 세포외 스파이크 S 삼량체의 단편(예를 들어 안정화된 세포외 스파이크 S 삼량체의 단편)을 포함할 수 있다. 안정화된 스파이크 S 삼량체는 삼량체의 융합 전 형태(예를 들어, 삼량체화 도메인)를 안정화하는 하나 이상의 변형을 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 스파이크 S 삼량체에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함하는 안정화된 스파이크 S 삼량체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 스파이크 S 삼량체와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함하는 안정화된 스파이크 S 삼량체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 스파이크 S 삼량체(예를 들어 안정화된 스파이크 S 삼량체)의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 스파이크 S 삼량체의 단편(예를 들어 안정화된 세포외 스파이크 S 삼량체의 단편)을 포함할 수 있다.
추가적으로 또는 대안적으로, 본원에 기술된 바와 같은 항원성 코로나바이러스 펩티드는 6개의 프롤린을 갖는 안정화된 변이체(즉, "헥사프로")를 포함할 수 있으며, 이는 S-2P의 2개의 프롤린 치환에 더하여 F817P, A892P, A899P, 및 A942P 치환을 포함하는 스파이크 단백질의 또 다른 변이체이다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 헥사프로에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있는 헥사프로의 변이체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 헥사프로와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있는 헥사프로의 변이체를 포함할 수 있다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 헥사프로의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 헥사프로의 단편을 포함할 수 있다.
추가적으로 또는 대안적으로, 본원에 기술된 바와 같은 항원성 코로나바이러스 펩티드는 SARS-CoV-1 스파이크 단백질(S 단백질) 또는 이의 단편 또는 변이체를 포함할 수 있다. SARS-CoV-1 스파이크 단백질은 아래에 제시된 아미노산 서열을 포함할 수 있다:
일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 24에서 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15개 이상의 치환, 결실, 또는 삽입 돌연변이를 포함할 수 있는 서열 번호 24의 변이체를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 서열 번호 24와 약 80%, 약 81%, 약 82%, 약 83%, 약 84%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99%, 또는 최대 100%의 서열 동일성 또는 상동성을 공유하는 아미노산 서열을 포함할 수 있는 서열 번호 24의 변이체를 포함한다. 일부 실시양태에서, 항원성 코로나바이러스 펩티드는 단편이 면역 반응을 유발할 수 있는 한(즉, 항원성 단편인 한) 서열 번호 24의 길이의 약 20%, 약 25%, 약 30%, 약 35%, 약 40%, 약 45%, 약 50%, 약 55%, 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99%를 포함하는 서열 번호 24의 단편일 수 있는 SARS-CoV-1 스파이크 단백질의 단편을 포함한다.
D. 융합 단백질 및 백신 나노입자
개시된 백신 나노입자는 나노입자로 자가 조립되는 복수의 융합 당단백질 도메인으로 구성된다. 상기 언급된 바와 같이, 융합 단백질은 나노입자 형성 펩티드를 포함하는데, 이는 H. 파일로리 페리틴 단백질 또는 이의 단편 또는 변이체일 수 있다. 페리틴은 24개 구성원의 구형 입자로 자가 조립되는 자연 발생 단백질로, 다수의 3-폴드, 4-폴드 및/또는 2-폴드 축으로 구성된다. 따라서, 나노입자는 3-폴드 축, 4-폴드 축, 또는 2-폴드 축을 포함할 수 있다. 3-폴드 축을 사용하면, 8개의 항원성 삼량체 코로나바이러스 펩티드가 자가 조립 단백질 나노입자 표면의 표면에 제시될 수 있다. RBD와 같은 단량체 항원의 경우, 24개의 코로나바이러스 펩티드가 자가 조립 단백질 나노입자 표면의 표면에 제시될 수 있다.
E. 다가 면역원성 조성물
위에서 언급했듯이, SARS-CoV-2 변종의 진화는 백신 효능에 대한 문제를 제시하였다. 바이러스가 진화함에 따라, 단백질 항원의 에피토프 내의 아미노산이 돌연변이될 수 있다. 이 과정으로 인해, 숙주가 한 단백질에 대해 생성한 항체(예를 들어, 바이러스에 노출되거나 단백질로 면역화된 후)는 진화적으로 관련된 단백질의 동일한 에피토프에 강하게 결합하거나, 약하게 결합하거나, 전혀 결합하지 않을 수 있다. 두 가지 이상의 연관된(그러나 동일하지 않은) 균주에서 유사한 위치에서 결합이 관찰되는 경우, 결합 위치를 "공통" 에피토프라고 할 수 있으며, 이는 일반적으로 중화 에피토프이다. 중화 에피토프인 공통 에피토프는 진화적 압력을 받을 수 있으며 단기 진화(예를 들어, 아미노산 서열의 변화)를 보일 수 있다. 정의에 따르면, 공통 에피토프는 돌연변이될 가능성이 있지만, 지금까지는 중복되는 항체 집단의 결합을 소멸시킬 만큼 충분히 돌연변이되지 않았기 때문에 균주에 공통으로 남아 있다. 공통 에피토프의 가변성으로 인해, 더 멀리 연관된 균주에서는 결합이 관찰될 가능성이 낮다. 공통 에피토프의 가변성에 내성이 큰(예를 들어, 공통 에피토프에 걸쳐 결합을 나타내는) 항체를 생성하는 것은 현재 및 향후 유행 코로나바이러스 균주에 대한 보호를 제공할 수 있는 광범위한 항원 반응을 생성하는 한 가지 접근 방식을 나타낸다. 덜 일반적으로 알려진 에피토프(즉, 준우성 에피토프)는 진화적 압력 부재로 인해 짧은 시간 척도(즉, 계절 간)에서는 변하지 않을 수 있지만, 진화적 표류로 인해 더 긴 시간 척도(즉, 수십 년/세기)에서는 여전히 변할 수 있다. 일부 경우에, 단백질의 기능 영역과 일치하는 준우성 에피토프에 대한 돌연변이가 덜 허용될 수 있다. 항체가 멀리 연관된 항원의 그러한 한 에피토프에 지속적으로 결합하는 경우, 그 결합 위치를 "보존된" 에피토프라고 지칭할 수 있다. 덜 일반적으로 알려진 보존된 에피토프에 대한 항체를 생성하는 것은 현재 및 향후 유행 코로나바이러스 균주에 대한 보호를 제공할 수 있는 광범위한 항원 반응을 생성하는 또 다른 접근 방식을 나타낸다. 본원에 기술된 다가 실시양태는 공통 및/또는 보존된 에피토프에 대한 항체를 유도함으로써 이러한 접근 방식 중 하나 또는 둘 다를 활용할 수 있다.
일부 측면에서, 본 개시 내용은 나노입자(예를 들어, mRNA 코딩 페리틴 나노입자) 상에 항원성 코로나바이러스 펩티드의 최적화된 다가 제시에 관한 것이며, 이는 투여 시 광범위한 코로나바이러스에 대한 중화 면역 반응을 생성한다(도 15). 본원에 기술된 바와 같이, 면역계에 대한 여러 항원의 동시적이고 국소화된 제시를 통해 면역 반응의 항원 폭을 향상시킨다. 이러한 다가 백신 접종은 하나 이상의 항원성 코로나바이러스 펩티드와 페리틴과 같은 나노입자 형성 단백질을 포함하는 융합 단백질을 코딩하는 mRNA 분자 또는 나노입자를 투여한 후 생체 내에서 형성될 수 있는 것과 같은 모자이크 항원을 통해 달성할 수 있다. 상이한 융합 단백질(상이한 항원성 코로나바이러스 펩티드를 함유함)을 코딩하는 mRNA 분자는 하나의 지질 나노입자(LNP)에 공동 캡슐화되거나 면역원성 조성물에 함께 제제화되는 별도의 LNP에 캡슐화되어 동시 전달을 달성할 수 있다. 일단 투여되면, mRNA 분자(들)를 생체 내 발현하여 상이한 균주의 항원성 코로나바이러스 펩티드를 표시하는 다가 나노입자를 형성한다. 이러한 항원은 가까운, 먼 또는 다양한 사르베코바이러스 균주로부터 유래될 수 있다. (도 16, 패널 A). 다양한 코로나바이러스 균주로부터의 여러 항원의 에피토프에 결합할 수 있는 항체의 성숙을 촉진하기 위해, 선택된 항원 거리를 갖는 균주로부터의 여러 항원의 공동 국소화된 제시(도 16, 패널 B에 도시됨)를 설계한다. 이는 현재 및 향후 유행 코로나바이러스 균주에 대한 보호의 폭을 증가시킬 가능성이 높다.
따라서, 본 개시 내용의 일부 측면은 선택된 항원 거리를 갖는 상이한 균주의 여러 항원의 공동 국소화된 제시에 관한 것이다(도 17에 도시됨). 이 맥락에서, 항원 거리는 분석(예를 들어, 가성 중화 분석)에서 판독값의 유사성으로 측정되는 바와 같이 두 가지 상이한 항원에 노출되어 생성된 혈청의 항체 결합 프로파일의 면역원성 유사성을 말한다. 항원 거리가 작을수록 면역원성 유사성이 더 크다는 것(예를 들어, 여러 균주에 걸친 중화 역가의 더 높은 유사성)을 의미하고, 거리가 클수록 면역원성 차이가 크다는 것(예를 들어, 여러 균주에 걸친 중화 역가의 더 낮은 유사성)을 의미한다. 생물학적으로, 항원성 유사성은 겹치고/겹치거나 동일한 에피토프에 결합하는 항체를 갖는 두 가지 상이한 항원에 의해 생성된 혈청을 말한다. 따라서, 항원 거리가 작은 항원은 물리화학적 특성을 공유하여 유사한 항체의 결합을 촉진하는 공통 에피토프를 가질 것으로 예상되는 반면, 더 먼 거리에 있는 항원은 공통 에피토프가 부재하여 겹치지 않는 항체 세트의 결합을 촉진할 것이다. 일부 경우에, 항원은 멀리 연관된 균주에 대한 반응을 유도할 수 있는데; 이는 아마도 준우성 보존 에피토프에 결합하는 항체에 의해 매개될 가능성이 높다.
일부 다가 실시양태에 따라, 본 개시 내용은 항원 거리 세트의 항원을 기반으로 설계된 면역원성 조성물로서, 물리적으로 가까운 거리에 제시될 때 광범위하게 결합하는 항체의 생성을 촉진하는 조성물을 제공한다. 항원을 동일한 나노입자 상에서와 같이 물리적으로 가까운 거리에 제시함으로써 면역계는 상이하지만 진화적으로 연관된 두 에피토프에 동시에 결합하는 항체를 유발할 가능성이 높다. 이는 두 개의 가변 공통 에피토프에 결합하는 항체가 더 광범위한 폭의 항원에 결합하기 때문에 면역 반응의 추가적인 폭을 제공한다. 면역계는 또한 두 개의 준우성 보존 에피토프에 결합하는 항체를 유도할 수 있는데, 이는 예를 들어 두 에피토프의 돌연변이에 대한 내성 및/또는 항체의 항원 결합 부위에 의한 더 강한 결합으로 인해 항체-항원 상호작용을 안정화하기 때문이다. 따라서, 위에서 언급한 바와 같이, 본원에 기술된 다가 실시양태는 공통 및/또는 보존 에피토프에 대한 항체를 유도한다. 도 15는 코로나바이러스가 RBD 단백질의 서열 유사성에 따라 계통학적으로 클레이드로 그룹화되는 방식을 보여준다. 도 16, 패널 A는 여러 균주에 대한 항원 거리 맵을 제공한다. 도 17은 항원 거리 세트를 기반으로 하는 다양한 다가 실시양태(믹스 A-믹스 F)를 보여준다.
개시된 면역원성 조성물 또는 여기에 포함된 융합 단백질의 항원성 코로나바이러스 펩티드 성분 또는 이를 코딩하는 mRNA는 1, 2, 또는 3개 이상의 별개의 도메인 또는 부분을 포함할 수 있으며, 이는 위에서 논의된 예시적인 항원성 펩티드로부터 선택될 수 있다. 예를 들어, 일부 실시양태에서 항원성 코로나바이러스 펩티드(들)는 RBD, NTD, 전체 스파이크 단백질, 안정화된 세포외 스파이크 S-2P 도메인, 안정화된 세포외 스파이크 S 도메인, 안정화된 세포외 스파이크 S-삼량체(선택적으로 막관통 성분 포함), 및 이의 변이체 또는 단편으로부터 선택된 하나 이상의 도메인을 포함할 수 있다. 예를 들어, 본원에 개시된 바와 같은 면역원성 조성물의 항원성 코로나바이러스 펩티드(들)는 RBD, NTD, 전체 스파이크 단백질, 안정화된 세포외 스파이크 S-2P 도메인, 안정화된 세포외 스파이크 S 도메인, 안정화된 세포외 스파이크 S-삼량체, 헥사프로, 및 이의 변이체 또는 단편으로부터 독립적으로 선택된 두 개의 도메인과 같은 두 개의 도메인의 조합을 포함할 수 있다. 대안적으로, 항원성 코로나바이러스 펩티드는 RBD, NTD, 전체 스파이크 단백질, S1 서브유닛, S2 서브유닛, 안정화된 세포외 스파이크 S-2P 도메인, 안정화된 세포외 스파이크 S 도메인, 안정화된 세포외 스파이크 S-삼량체, 헥사프로, 및 이의 변이체 또는 단편으로부터 독립적으로 선택된 세 개의 도메인과 같은 세 개의 도메인의 조합을 포함할 수 있다. 나노입자 실시양태의 경우, 항원성 코로나바이러스 펩티드(들)는 추가적으로 또는 대안적으로 안정화된 스파이크 S-2P 도메인, 안정화된 스파이크 S 도메인, 안정화된 스파이크 S-삼량체, 및 이의 변이체 또는 단편으로부터 선택된 하나 이상의 도메인을 포함할 수 있다. 개시된 면역원성 조성물(예를 들어, 백신)은 여러 유형의 코로나바이러스(즉, SARS, MERS 등)로부터 면역 반응을 유발할 수 있으므로, 항원성 코로나바이러스 펩티드(들)의 다양한 도메인은 상이한 코로나바이러스, 동일한 코로나바이러스의 상이한 균주, 또는 이들의 조합으로부터 유래될 수 있으며, 이는 위에서 언급하고 아래에서 보다 자세히 설명한다.
예시적 융합 단백질 형식에는 다음을 포함하는 융합 단백질이 포함되지만 이에 제한되지 않는다: (1) RBD 및 페리틴("R-FN"), (2) 코로나바이러스 균주의 스파이크 단백질 및 페리틴("SpFN"), 선택적으로 여기서 스파이크 단백질은 상이한 균주의 RBD를 가짐("모자이크 SpFN"), (3) RBD-RBD 및 페리틴, 여기서 두 RBD는 두 가지 상이한 코로나바이러스 균주로부터 유래될 수 있음("RR-FN"), (4) RBD-NTD 및 페리틴("RN-FN"), (5) RBD-RBD-NTD 및 페리틴("RRN-FN"), (6) RBD-NTD-RBD-NTD 및 페리틴("RNRN-FN"), (7) RBD-SD-RBD-SD("R2-SD-FN") 및 페리틴, (8) RBD-NTD-SD-RBD-SD 및 페리틴("R-S1-FN") (9) NTD가 제2 RBD로 대체된 스파이크 단백질 및 페리틴("R2-SD-S2-FN"), (10) RBD가 상이한 코로나바이러스 균주로부터 유래된 RBD-스파이크 단백질 및 페리틴("RmosSpFN"), (11) RBD가 상이한 코로나바이러스 균주로부터 유래된 RBD-RBD-스파이크 단백질 및 페리틴("RR-mos-SpFN"), (12) 추가 RBD가 있는 스파이크 단백질 및 페리틴("(R)-SpFN"), (13) 두 개의 추가 RBD가 있는 스파이크 단백질 및 페리틴, 여기서 두 RBD는 두 가지 상이한 코로나바이러스 균주로부터 유래될 수 있음("RR-SpFN"), 및 (14) 제2 RBD가 NTD 루프에 삽입된 RBD-NTD/RBD/NTD, 및 페리틴("R2N-FN"). 이러한 융합 단백질 구축물 중 다수의 선형 다이어그램이 도 2 내지 도 7에 도시되어 있다. 개시된 융합 단백질에서 사용되는 RBD, NTD, 및 SD의 다양한 조합은 동일한 코로나바이러스 균주 또는 상이한 코로나바이러스 균주로부터 유래될 수 있지만, 다가 실시양태에서는 적어도 두 가지 상이한 균주로부터 유래된다.
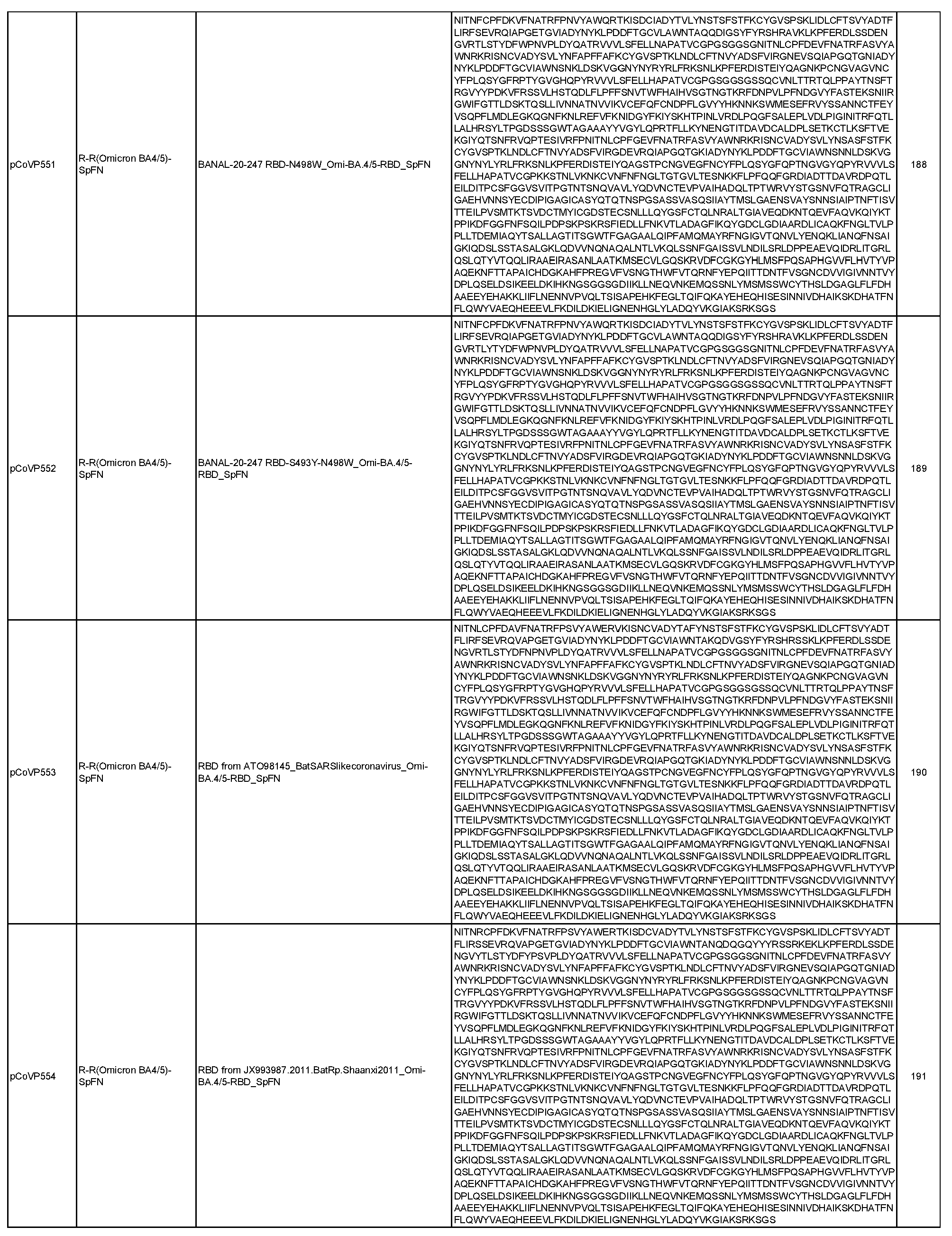
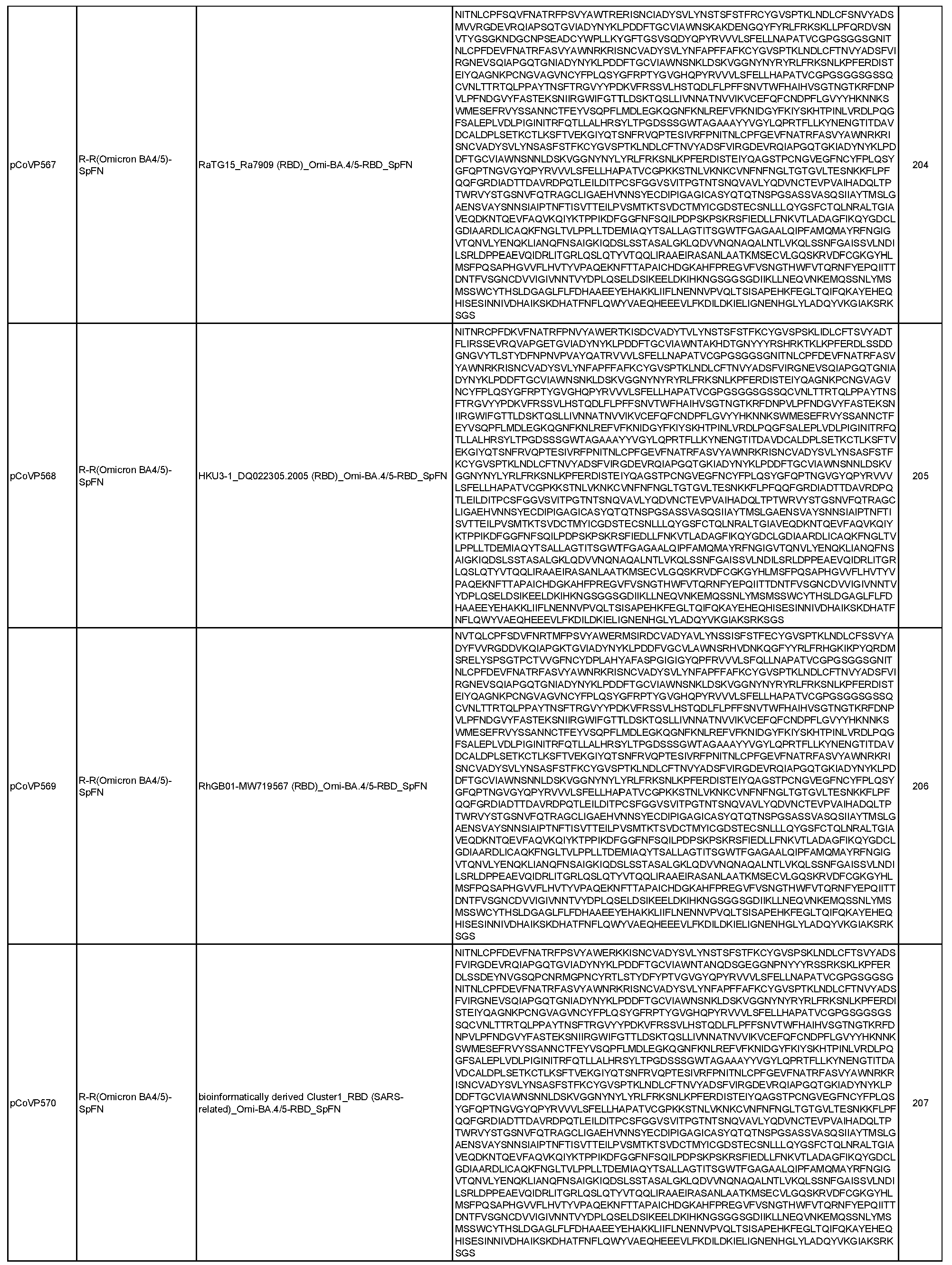
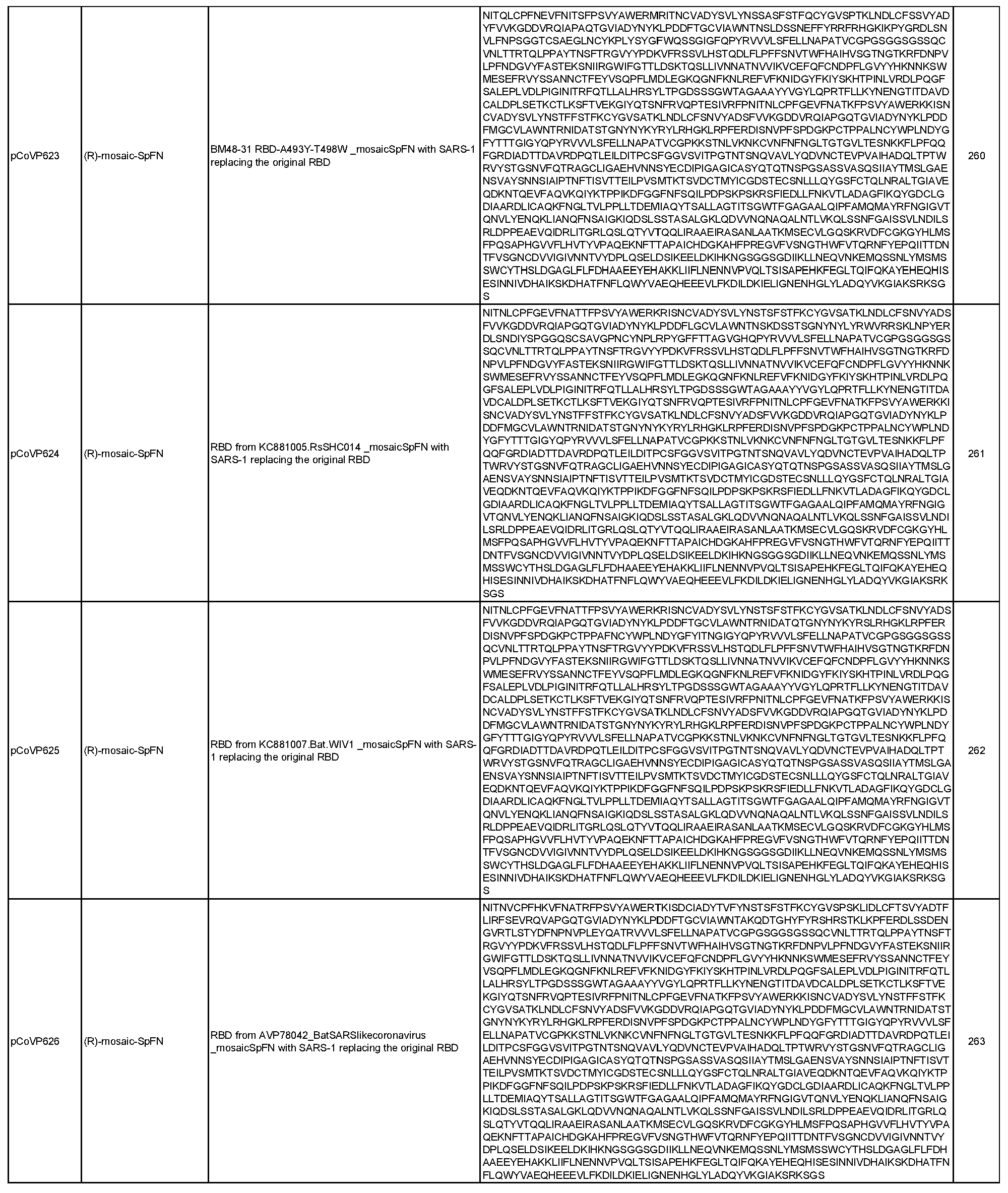
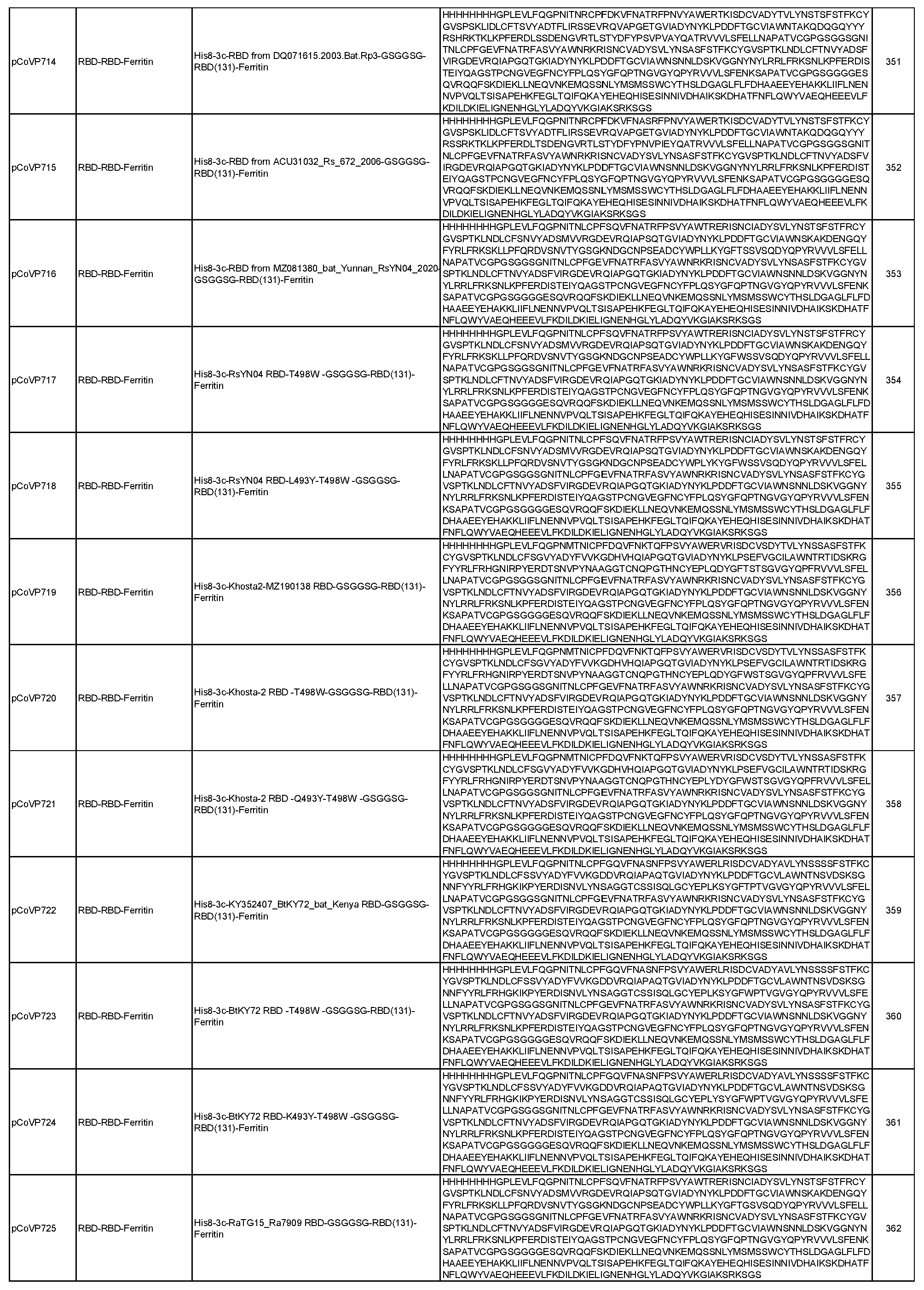
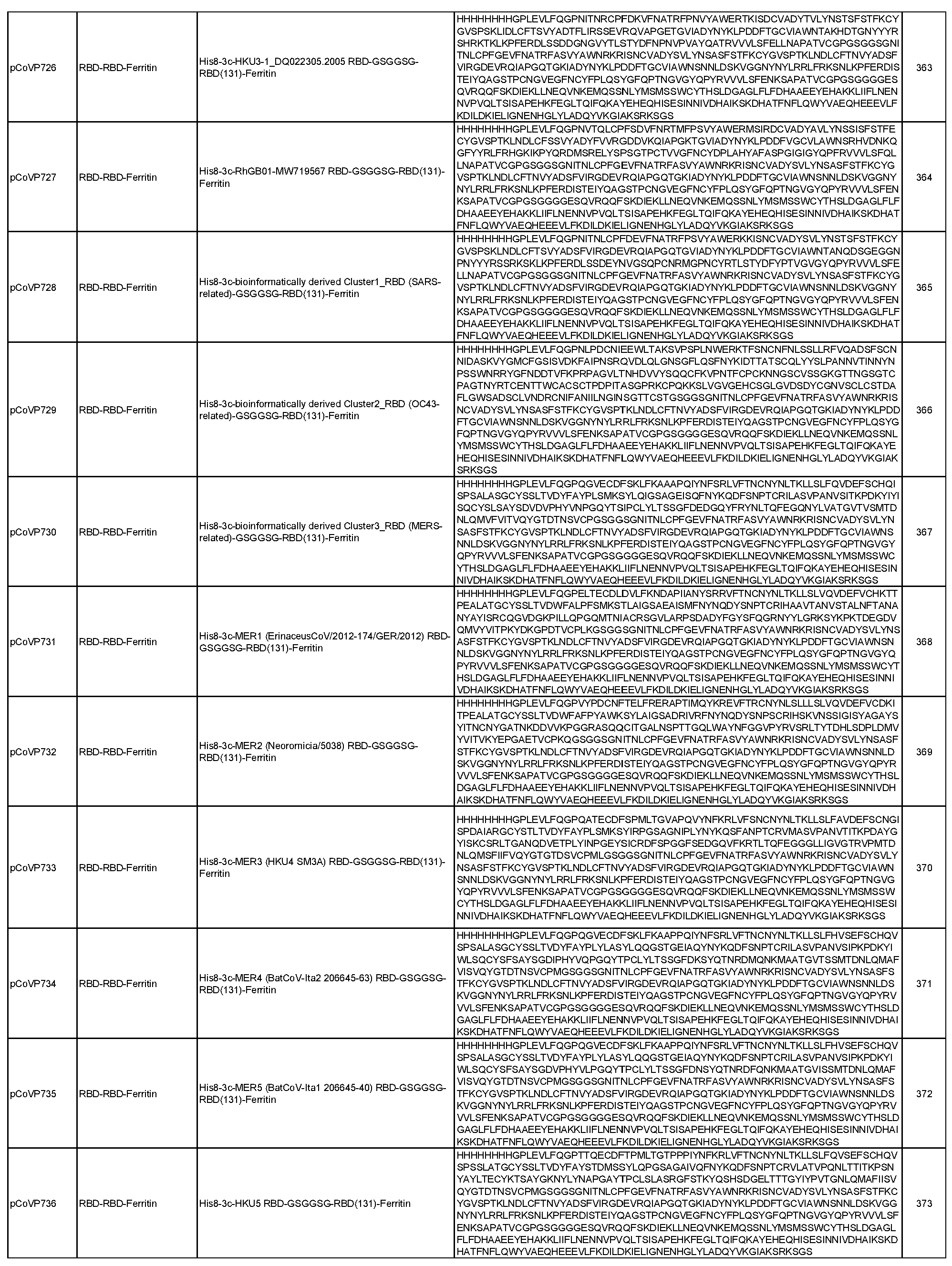
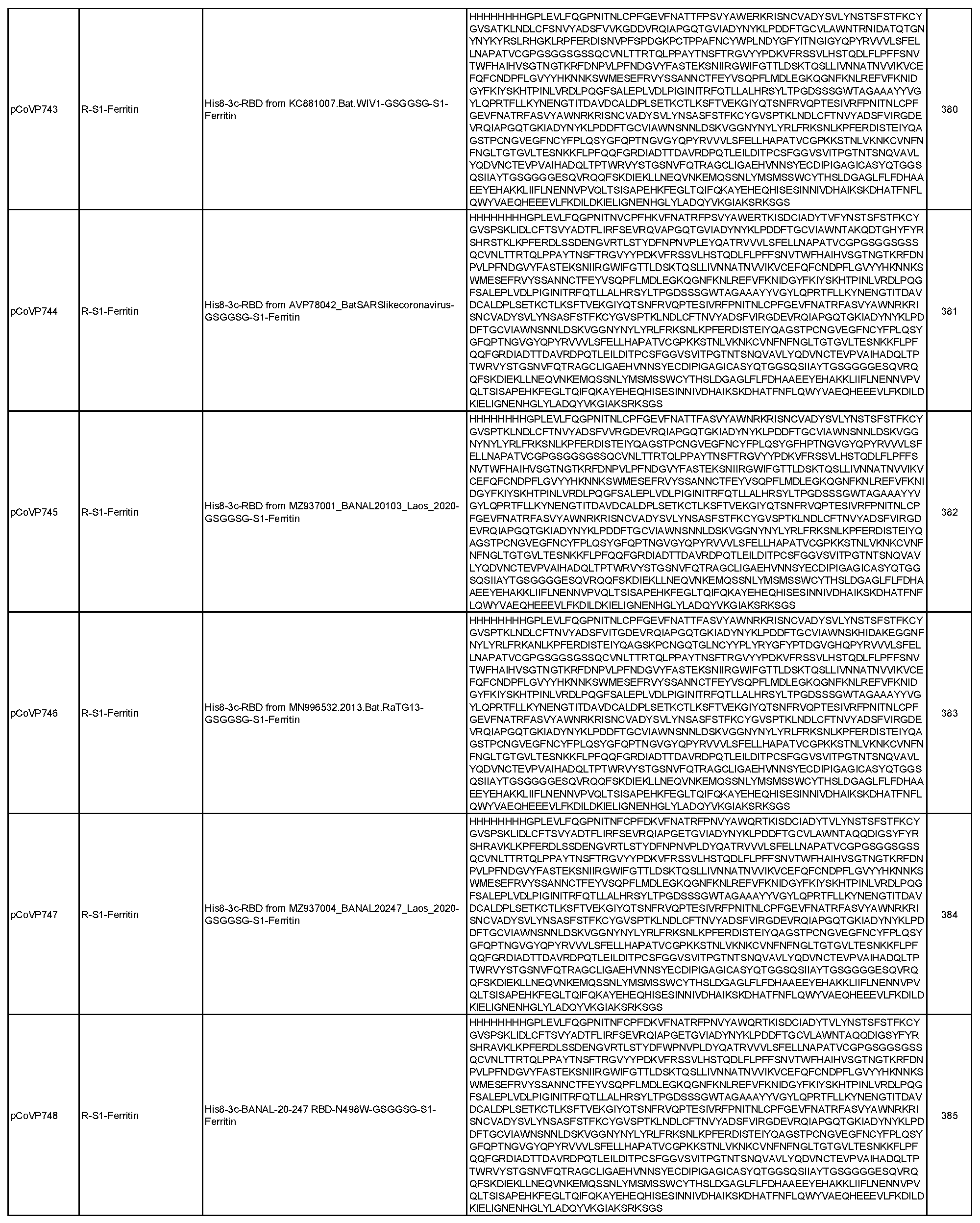
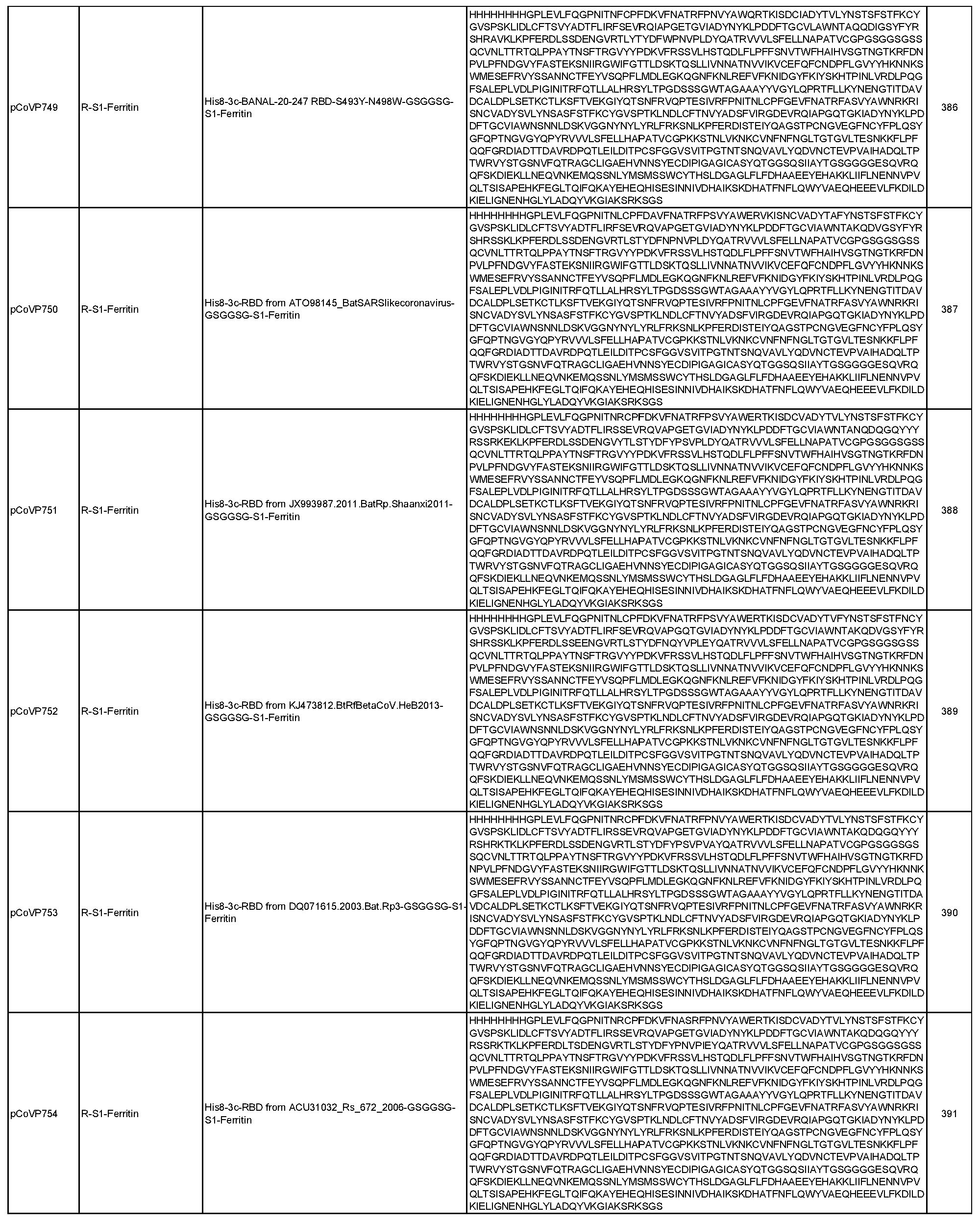
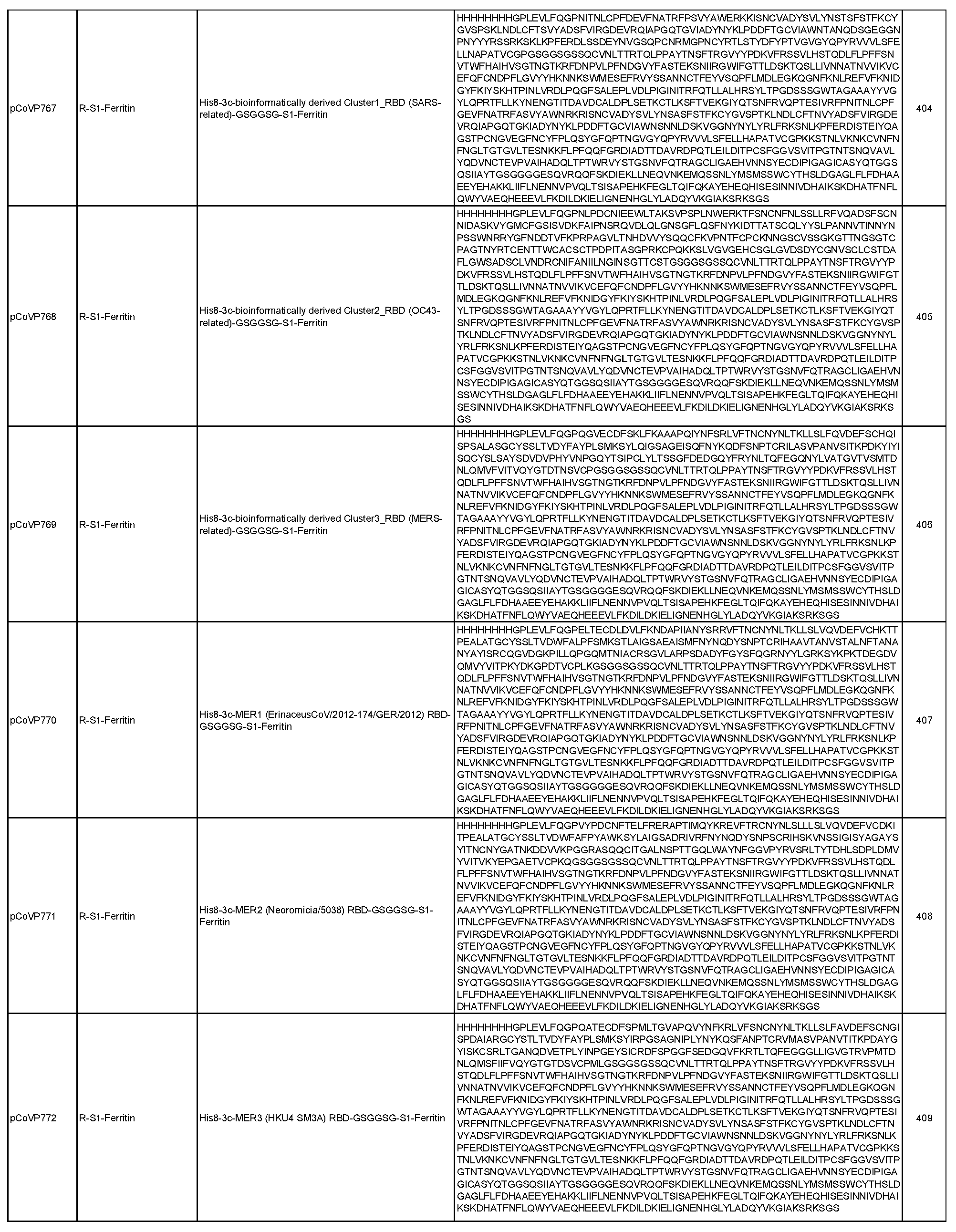
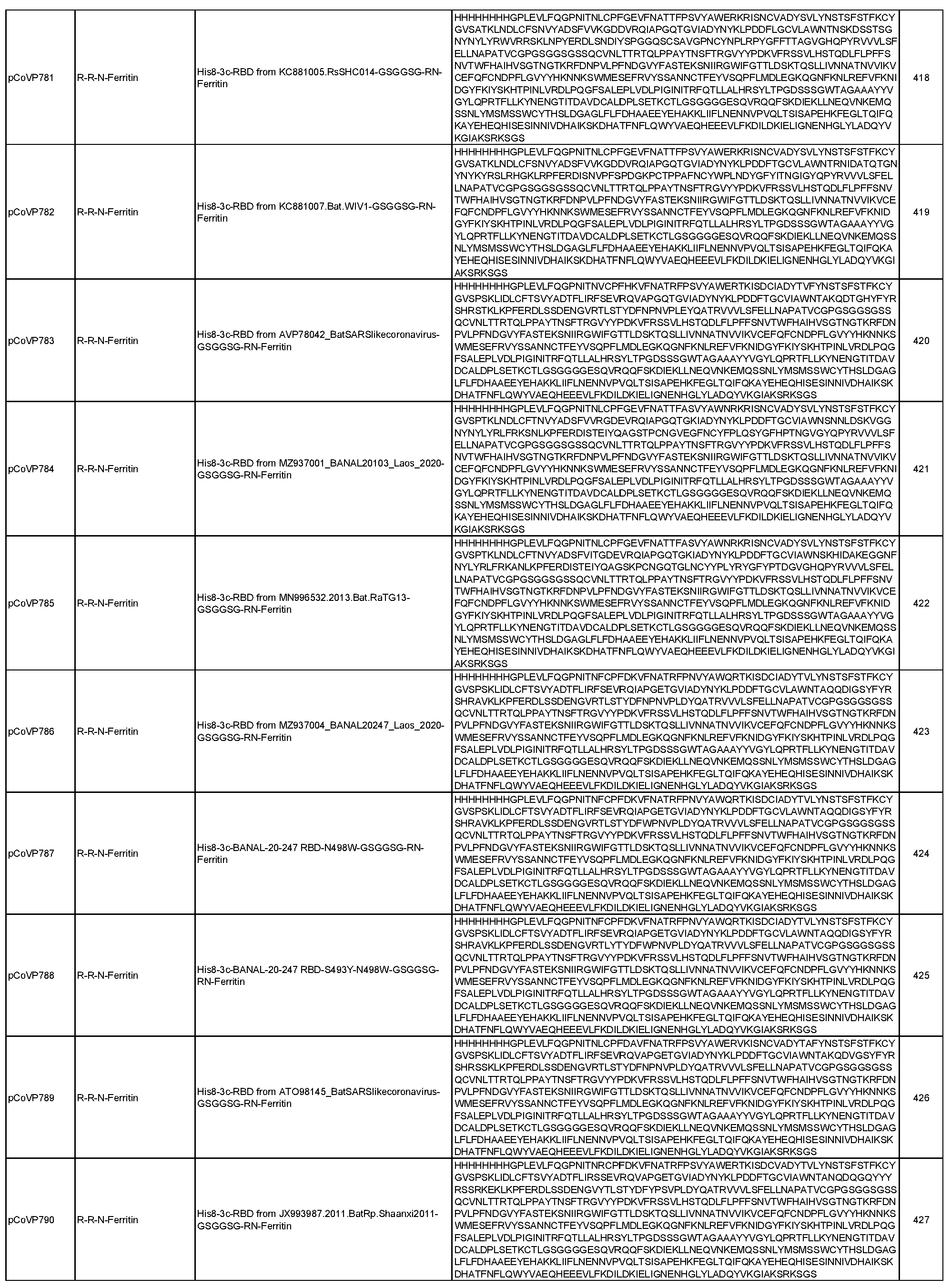
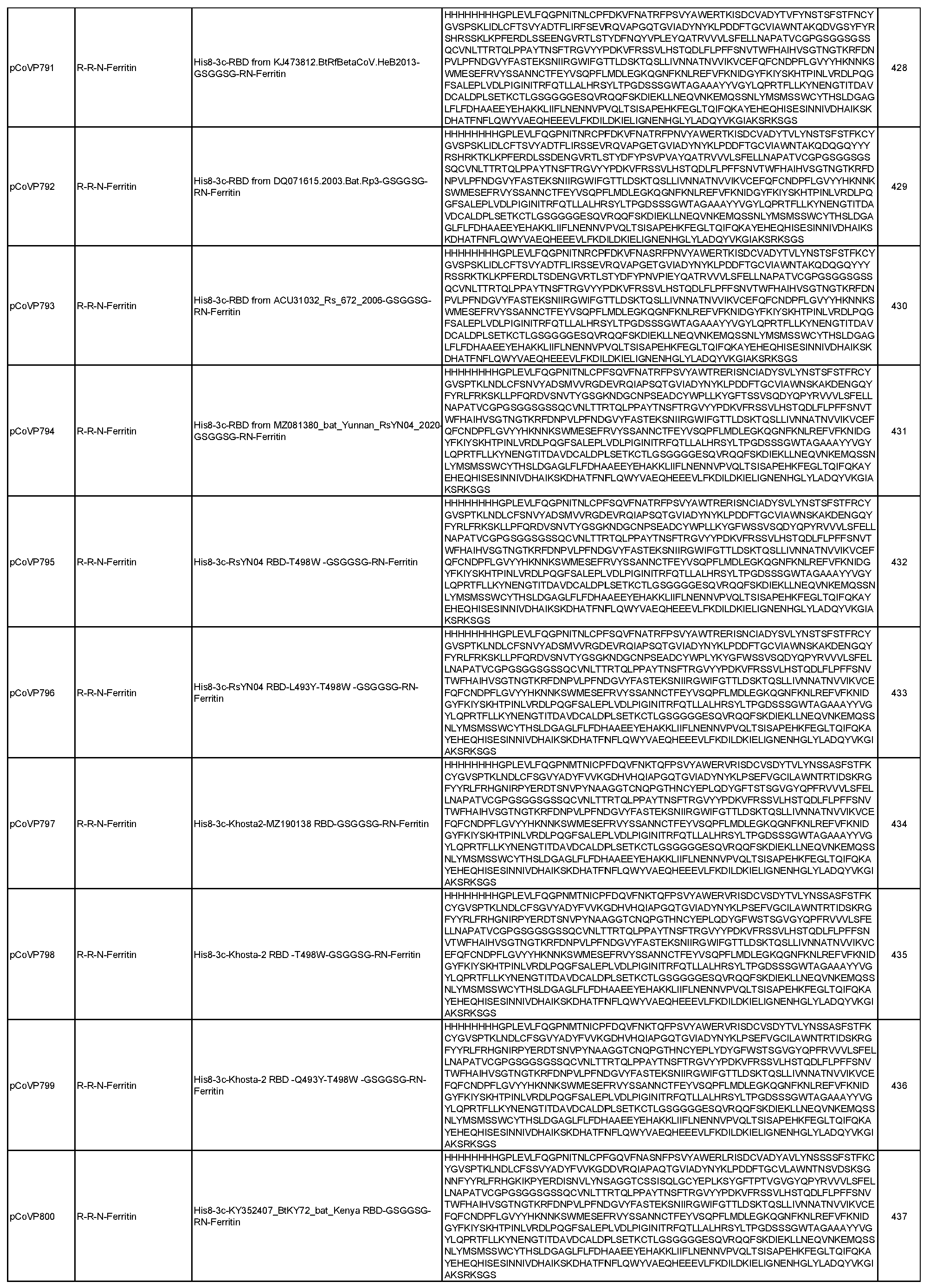
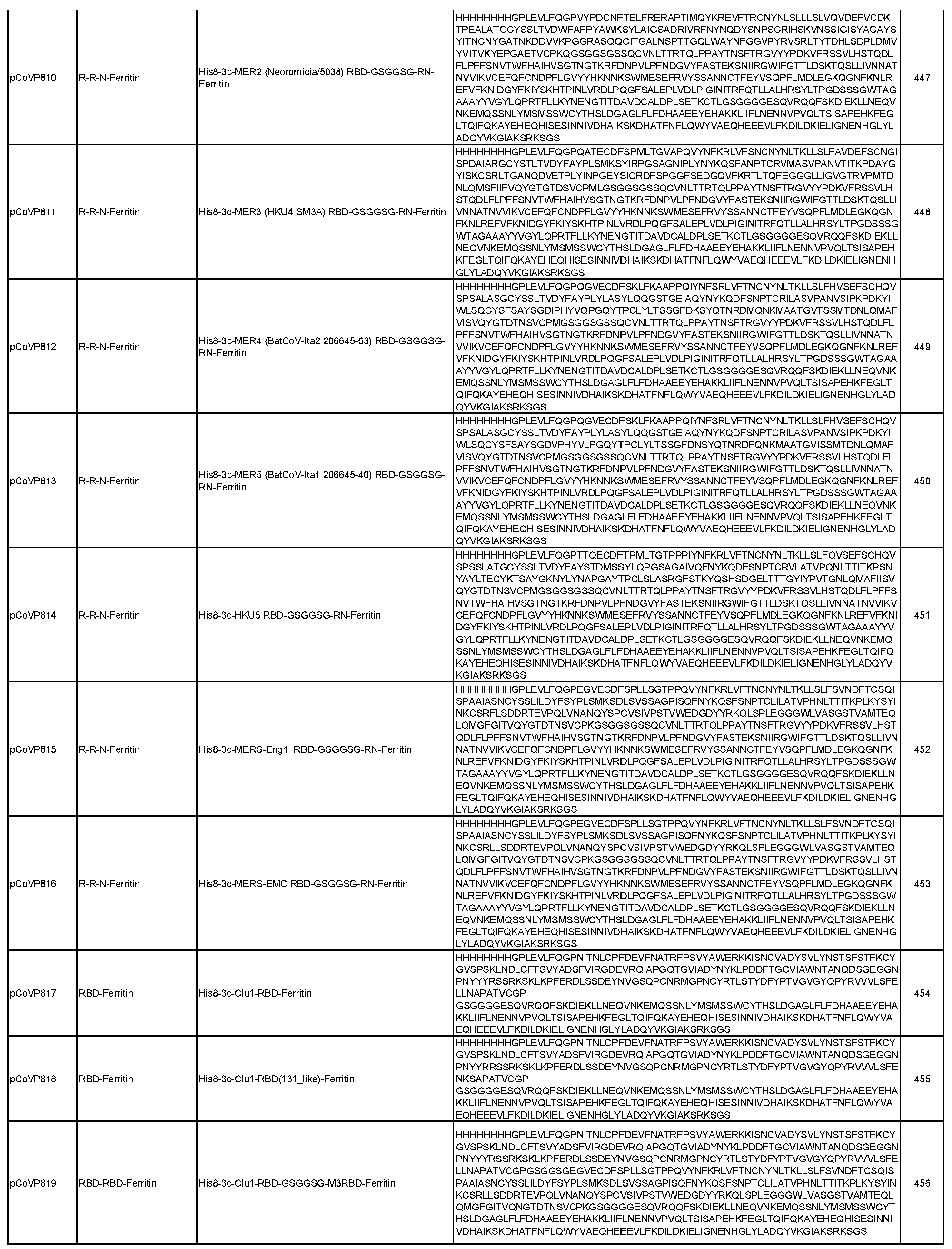
일반적으로, 본원에서 개시된 융합 단백질은 4가지 주요 설계 형식 중 하나에 속한다: 실에 꿴 구슬(예를 들어, RN-FN, RRN-FN, RNRN-FN, R-FN, 및 RR-FN; 도 3 참조), 도메인 융합(R-S1-FN, R2-SD-S2-FN, 및 (R)-R-SpFN 또는 RR-SpFN; 도 4 참조), 루프 삽입(R2N-FN; 도 5 참조), 및 도메인 스왑(모자이크 SpFN; 도 6 참조). 또한, SpFN 형식이 포함된다. 예시적 융합 단백질 서열은 표 6 및 표 7에 개시되어 있다. 표 7의 예시적 융합 단백질 서열을 코딩하는 예시적 mRNA 서열도 표 7에 제시되어 있다(서열 번호 552-566 및 575-582).
선택된 나노입자에 대한 음성 염색 전자 현미경 3차원 재구성은 도 8, 11, 및 12에 도시되어 있다.
예시적 나노입자 및 그것의 각각의 설계는 아래 표 3에 개시되어 있다.
본원에 개시된 바와 같은 나노입자(직접 투여되거나 구성 단백질을 코딩하는 mRNA 투여 후 형성됨)는 인간 ACE-2 수용체에 결합할 수 있다. 추가적으로 또는 대안적으로, 본원에 개시된 바와 같은 나노입자는 박쥐 ACE2 단백질, 예컨대 중국 적갈색 관박쥐(R. 시니쿠스(R. sinicus) 3364), 중국 적갈색 관박쥐(R. 시니쿠스 1434), 중간 관박쥐(R. 아피니스(R. affinis) 787), 중간 관박쥐(R 아피니스 9479), 사하라 이남 아프리카(케냐 포함) 랜더 관박쥐 (R. 랜더리(R. landeri)), 서부 및 중부 아프리카 할시온 관박쥐(R. 알시온(R. alcyone) ), 아시아, 그러나 또한 유럽 및 북아프리카 큰 관박쥐(리놀로푸스 페루메키눔(Rhinolophus ferrumequinum)), 및 작은 관박쥐(리놀로푸스 푸실루스(Rhinolophus pusillus))의 단백질에 결합할 수 있다. 추가적으로 또는 대안적으로, 본원에 개시된 바와 같은 나노입자는 인간 DPP4 수용체에 결합할 수 있다.
상기 표 3에 기술된 나노입자 및 하기 표 6 및 표 7에 개시된 융합 단백질을 포함하여, 개시된 나노입자로 자가 조립되는 개시된 융합 단백질은 포유류 또는 진핵 생물 발현 시스템을 포함할 수 있는 적합한 발현 시스템에서 단독으로 발현되거나 공동 발현될 수 있다(예를 들어, 두 개의 상이한 플라스미드에서). 표 6 및 표 7에 개시된 일부 융합 단백질은 5-10개의 히스티딘(H) 잔기의 반복체 또는 기타 태그 서열을 포함하는 히스티딘 태그(즉, His 태그)를 포함할 수 있으며, 이는 단백질을 처리 또는 정제하는 데 유용할 수 있지만 궁극적으로 나노입자 조립 전에 활성 단백질로부터 절단될 수 있다. 대안적으로, 위에서 언급하고 아래에서 더 자세히 논의하는 바와 같이, 상기 표 3에 기술된 나노입자를 포함하여 개시된 나노입자로 자가 조립되는 개시된 융합 단백질 및 아래 표 6 및 표 7에 개시된 융합 단백질은 mRNA 분자에 의해 코딩될 수 있으며, 이는 생체 내에 투여되고 발현될 때 본원에 개시된 바와 같은 나노입자를 형성한다.
표 6에 개시된 모든 단백질과 표 7에 개시된 일부 단백질은 RBD-페리틴 또는 스파이크-페리틴 나노입자를 형성할 수 있는 예시적인 나노입자 형성 단백질이다. 이러한 서열은 RBD-페리틴 또는 스파이크-페리틴 구축물의 안정성과 면역원성을 개선하기 위한 일련의 대체 서열을 포함한다. 여기에는 안정화 디설파이드 결합, D614G 돌연변이, RBD가 더 자유롭게 움직일 수 있도록 하고 RBD가 "위쪽"에 더 노출된 형태로 있을 수 있도록 스파이크의 N165에서 글리칸을 제거하는 돌연변이, 및 RBD가 더 닫힌 형태로 있을 수 있도록 스파이크의 234에서 글리칸을 제거하는 N234Q 돌연변이가 포함된다. 추가적으로 또는 대안적으로, 페리틴 서열의 N146 또는 N77에서 글리칸은 페리틴 분자를 개선하고 안정화할 수 있다.
"실에 꿴 구슬" 융합 단백질 형식은 SARS-CoV-2, SARS-CoV-1, Khosta-2, BANAL-20-247, HKU-1, MERS-CoV, 229E, NL63, OC43, 또는 박쥐, 낙타, 또는 천산갑에서 식별된 것을 포함한 연관 코로나바이러스와 같은 여러 코로나바이러스의 항원성 성분을 갖는 나노입자를 생성하는 데 사용될 수 있다. 이러한 실시양태는 범-사르베코바이러스 백신, 범-메르베코바이러스 백신, 범-사르베코바이러스-메르베코바이러스 백신, 범-β-코로나바이러스 백신, 또는 범-코로나바이러스 백신을 생성하는 데 사용될 수 있다. 예를 들어, 상이한 항원성 서열로 구성된 다중 RBD, NTD, 또는 이들의 조합 "구슬"은 단일 "실"(즉, 단일 구축물)에 함께 제공되어 코로나바이러스에 대한 광범위한 면역 반응을 유발할 수 있다. 예를 들어, SARS-CoV-2-RBD-SARS-CoV-1-RBD-Khosta-2-RBD-BANAL-20-247-RBD 또는 SARS-CoV-2-RBD-SARS-CoV-1-RBD-HKU-1-RBD-MERS-CoV-RBD-229E-RBD-NL63-RBD와 같은 항원의 "실"을 SARS-CoV-2-오미크론-BQ.1.1-RBD-SARS-CoV-1-RBD 또는 SARS-CoV-2-RBD-천상갑SARS-CoV-1-RBD-OC43-RBD-낙타MERS-CoV-RBD-229E-RBD-NL63-RBD와 같은 항원의 "실"과 함께 사용하여 특정 범-반응성 또는 범-보호성 면역에 대한 면역 반응을 증가시키거나 집중시킬 수 있다. "실에 꿴 구슬"은 예를 들어, 1-10개의 RBD, NTD, 또는 RBD와 NTD 도메인 모두에 대한 서열을 직렬로 포함할 수 있거나, 다시 말해 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의 RBD, NTD, 또는 둘 다를 포함할 수 있다. 표 1에 개시된 링커 서열을 포함하되 이에 제한되지 않는 링커 서열은 RBD 및/또는 NTD 서열의 하나 이상 또는 각각을 직렬로 연결할 수 있다.
"실에 꿴 구슬"은 또한 추가 1-10개의 RBD, NTD, 또는 둘 다를 직렬로 포함하는 SpFN 또는 mos-SpFN 분자에 추가될 수 있거나, 다시 말해 SpFN 또는 mos-SpFN 분자에 연결된 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의 RBD를 포함할 수 있다. 표 1에 개시된 링커 서열로부터 선택된 링커를 포함하되 이에 제한되지 않는 링커 서열은 RBD 및/또는 NTD 서열의 하나 이상 또는 각각을 직렬로 연결할 수 있다.
융합 단백질의 "도메인 융합" 형식은 관심 받는 것(예를 들어, 알파, 베타, 델타, 오미크론)을 포함한, SARS-CoV-2 및 이의 변종 및 하위 변종, SARS-CoV-1, Khosta-2, BANAL-20-247, HKU-1, MERS-CoV, 229E, NL63, OC43, 또는 박쥐, 낙타, 또는 천산갑에서 식별된 것을 포함한 연관 코로나바이러스와 같은 여러 코로나바이러스의 항원성 성분을 갖는 나노입자를 생성하는 데 사용될 수 있다. 이러한 실시양태는 범-β-코로나바이러스 백신, 또는 범-코로나바이러스 백신을 생성하는 데 사용될 수 있다. 이 형식에서, 이종 RBD는 이전에 기술된 구축물의 N-말단에 추가될 수 있다. 예시적 구축물은 NTD, SD1, SD2, S-2P, 또는 헥사프로 도메인과 같은 다른 항원성 도메인과 함께 상이한 코로나바이러스 균주의 여러(즉, 적어도 2개의) RBD 도메인을 포함할 수 있다.
융합 단백질의 "루프 삽입" 형식은 SARS-CoV-2, SARS-CoV-1, HKU-1, MERS-CoV, 229E, NL63, OC43, 또는 박쥐, 낙타, 또는 천산갑에서 식별된 것을 포함한 연관 코로나바이러스와 같은 여러 코로나바이러스의 항원성 성분을 갖는 나노입자를 생성하는 데 사용될 수 있다. 이러한 실시양태는 범-β-코로나바이러스 백신, 또는 범-코로나바이러스 백신을 생성하는 데 사용될 수 있다. 이 형식에서, 하나 이상의 RBD가 링커(예를 들어, 표 1의 링커)를 통해 NTD의 루프 도메인에 부착되거나 삽입된다. 일부 실시양태에서, 적어도 두 개의 RBD가 NTD의 동일한 루프 또는 상이한 루프에 삽입될 것이다. RBD는 상이한 코로나바이러스 균주 또는 변종으로부터 유래될 수 있다. NTD는 RBD 중 하나 또는 둘 다와 동일한 균주 또는 변종으로부터 유래될 수 있거나, NTD는 RBD 중 하나 또는 둘 다와 관련하여 상이한 코로나바이러스 균주 또는 변종으로부터 유래될 수도 있다.
융합 단백질의 "도메인 삽입" 또는 "모자이크" 형식은 관심 받는 것(예를 들어, 알파, 베타, 델타, 오미크론)을 포함한, SARS-CoV-2 및 이의 변종 및 하위 변종, SARS-CoV-1, Khosta-2, BANAL-20-247, HKU-1, MERS-CoV, 229E, NL63, OC43, 또는 박쥐, 낙타, 또는 천산갑에서 식별된 것을 포함한 연관 코로나바이러스와 같은 여러 코로나바이러스의 항원성 성분을 갖는 나노입자를 생성하는 데 사용될 수 있다. 유용한 코로나바이러스의 예로는 사르베코바이러스(예를 들어, ZXC21, BANAL-20-247, Rf4092, Shaanxi2011, HeB2013, Rp3, Rs_672, HKU3-1, Rs4081, RmYN02, Rf1, Yun11, BM48-31, BB9904, Khosta-1, Khosta-2, RhGB01, BtKY72, RsYN04, RatG15 (Ra7909), SHC014, WIV1, LyRa3, Rs4084, Rs4231, BANAL-20-103, RaTG13, BANAL-20-52, Pang17(GX-P5L), 또는 RshSTT182/200), 메르코바이러스(예를 들어, MER1(에리나세우스(Erinaceus)CoV/2012-174/GER/2012), MER2(네오로미시아(Neoromicia)/5038), MER3(HKU4 SM3A), MER4 (BatCoV-Ita2 206645-63), MER5(BatCoV-Ita1 206645-40), 또는 HKU5), 또는 이들의 조합이 포함되지만 이에 제한되지 않는다. 이러한 실시양태는 범-β-코로나바이러스 백신, 또는 범-코로나바이러스 백신을 생성하는 데 사용될 수 있다. 이 형식에서, 스파이크 단백질 또는 이의 세그먼트는 페리틴 펩티드에 부착되고, 하나 이상의 이종 도메인(예를 들어, RBD, NTD, 또는 이들의 임의의 조합)이 천연 도메인 대신 대체되거나 추가 도메인으로서 추가된다. 예를 들어, 한 균주의 이종 RBD로 주어진 스파이크 단백질의 천연 RBD를 대체하여 "모자이크"를 형성할 수 있다. 추가적으로 또는 대안적으로, 이종 종이나 균주의 RBD를 스파이크 단백질의 천연 NTD 대신 대체하여 "모자이크"를 형성할 수 있다. 추가적으로 또는 대안적으로, 이종 균주의 하나 이상의 RBD를 천연 스파이크 단백질의 한쪽 끝(즉, C-말단 또는 N-말단)에 추가하여 모자이크를 형성할 수 있다. 여러 구축물을 공동 발현을 통해 단일 나노입자에 함께 결합하여 안정된 단백질 나노입자를 생성할 수 있으며, 여기서 나노입자 표면의 스파이크 삼량체는 이종 혼합물, 예를 들어, WA-1 균주의 프로토머, BA.4/5의 프로토머, 및 베타의 프로토머가 될 수 있다. 이러한 이종 나노입자는 또한 mRNA 구축물로서 코딩될 수 있으며, 여기서 상이한 스파이크-페리틴 분자를 코딩하는 mRNA 분자를 단일 지질 나노입자에 캡슐화하여 백신 접종자 내에서 이종 나노입자 형성을 용이하게 할 수 있다. 이종 나노입자는 또한 F2A와 같은 주어진 구축물 사이에 예시적인 절단 부위가 코딩되는 단일 구축물 내에 코딩될 수도 있다(예를 들어, ncbi.nlm.nih.gov/pmc/articles/PMC4622431/ 참조).
일부 실시양태에서, 본원에서 기술된 면역원성 조성물은 클레이드 1a, 클레이드 1b, 클레이드 2, 클레이드 3, 및 중동 호흡기 증후군 관련 코로나바이러스(MERS-CoV)(또는 이를 코딩하는 mRNA 분자(들))로부터 독립적으로 선택된 두 가지 이상의 코로나바이러스 균주의 항원성 코로나바이러스 펩티드를 포함한다. 일부 실시양태에서, 본원에서 기술된 면역원성 조성물은 WA-1, 베타, 오미크론 BQ.1.1, 및 XBB.1.5; SARS-CoV-1 균주, BANAL20-247, Khosta2, 및 MERS-CoV(또는 이를 코딩하는 mRNA 분자(들))로부터 독립적으로 선택된 상이한 코로나바이러스 균주의 항원성 코로나바이러스 펩티드를 포함한다. 일부 실시양태에서, 본원에서 기술된 바와 같은 면역원성 조성물은 다음의 균주 조합(또는 이를 코딩하는 mRNA 분자(들))으로부터 선택된 항원성 코로나바이러스 펩티드를 포함한다: (i) WA-1, 베타, 및 오미크론 BQ1.1 또는 XBB.1.5로부터 선택된 둘 이상; (ii) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주; (iii) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 하나 이상; (iv) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 하나 이상, 및 MERS-CoV; 및 (v) SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 둘 이상.
융합 단백질은 상이한 항원 제시 형식으로 설계될 수 있다. 융합 단백질은, 대안적으로 페리틴 모이어티에 접합된, 단일 항원성 코로나바이러스 펩티드(예를 들어, 스파이크 단백질 및/또는 RBD 항원)를 포함하거나, 나노입자 형성 단백질(예를 들어, 페리틴 모이어티)에 접합된 두 개 이상의 항원성 코로나바이러스 펩티드를 직렬로 포함할 수 있다(본원에서 "다중 도메인" 융합 단백질이라고도 함). 여러 항원성 코로나바이러스 펩티드를 포함하는 융합 단백질의 경우, (예를 들어, 단일 나노입자를 형성하기 위해) 단일 면역원성 조성물에 사용되는 융합 단백질은 항원성 코로나바이러스 펩티드의 구성이 상이하여(예를 들어, A-B 및 B-A) 나노입자 상에 주변 및 측면으로 제시된 항원을 제공할 수 있다. 이 맥락에서 "주변"은 나노입자 상의 인접한 융합 단백질에 있는 에피토프를 말하며, "측면"은 동일한 융합 단백질 내의 에피토프를 말한다. 예를 들어, 다중 도메인 융합 단백질(예를 들어, RBD-RBD 또는 RBD-RBD-스파이크 등)은 주변 및 측면으로 항체 결합을 허용한다. 예를 들어, 도 30을 참조한다. 따라서, 주변 및 측면 항체 결합을 모두 허용하기 위해, 에피토프 조합이 측면 및 주변 모두에서 인접하도록 구성 균주의 항원(예를 들어, RBD)의 순서를 변경하여 나노입자 표면을 "패턴화"하도록 융합 단백질을 제조할 수 있다. 스파이크 단백질을 포함하는 실시양태의 경우, 스파이크 단백질이 한 균주로부터 유래되고 스파이크 단백질의 RBD 도메인 또는 추가 RBD 도메인이 상이한 코로나바이러스부터 유래되는 "모자이크" 형식(mosSp, RmosSp)을 설계할 수 있다. 예로서, 항원성 펩티드 시리즈가 상이한 사르베코바이러스 균주로부터 취한 RBD-RBD-스파이크(스파이크는 RBD 도메인을 포함함)인 융합 단백질(각각 A, B 및 C, 균주 C의 스파이크 포함)을 고려해보자; 추가 융합 단백질은 RBD-RBD-mosSpike일 수 있는데, 여기서 RBD는 (각각 B, C, A, 균주 C의 스파이크 포함) 및 (각각 C, A, B, 균주 C의 스파이크 포함)이어서 각 균주의 항원성 도메인이 융합 단백질의 각 가능한 위치에 제시될 수 있다.
이 접근 방식을 구현하여, 다양한 항원 거리 세트에 걸쳐 다음 항원 접합 프레임워크("항원 제시")에 따라 융합 단백질을 설계하여, 공통 및 보존 에피토프가 B 세포 수용체에 의해 최적으로 인식되고 가교될 수 있도록 선택된 항원 거리의 항원을 표시하는 다가 나노입자를 제공하였다. 구체적으로, 우리는 표 8 및 도 17 및 29에 나타낸 바와 같이, 항원 제시 형식(RFN, SpFN, RRFN, RR-SpFN)에 해당하는 항원 거리 세트의 구성 균주를 각각 코딩하는 최대 5개의 별도 mRNA 구축물을 함유하는 제제를 만들었다(아래의 도 16, 패널 A 및 표 8 참조).
동일한 LNP에 공동 캡슐화되거나 별도의 LNP에 별도로 캡슐화한 후 동일한 조성물로 투여되는 여러 상이한 mRNA 분자(예를 들어, 상이한 융합 단백질을 코딩함)를 포함하는 본원에 기술된 바와 같은 면역원성 조성물을 투여하면 각 코딩된 융합 단백질(예를 들어, 페리틴-접합 항원을 포함함)이 공동 발현된다. 동일한 세포에서 생성된 페리틴-접합 항원은 동일한 나노입자 상에 발현된 융합 단백질을 표시하는 페리틴 나노입자로 자가조립되어, 본원에서 "모자이크 나노입자" 또는 "다가 나노입자"라고 하는 것을 생성한다.
본 개시 내용의 예시를 위해, 사르베코바이러스의 항원 공간에 걸쳐있는 항원(즉, 서열) 거리 수준이 상이한 7개의 균주가 선택되었다. 균주에는 항원적으로 구별되는 3개의 SARS-CoV-2(클레이드 1b) 균주: 부모 WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ.1.1; SARS-CoV-1(클레이드 1a) 균주(프랑크푸르트); 점점 멀어지는 2가지 박쥐 인수공통감염 코로나바이러스(클레이드 2 및 3): 각각 BANAL20-247 및 Khosta2; 및 이상치로서 비-ACE2 결합 균주를 나타내는 메르코바이러스(MERS-CoV) 균주(도 16, 패널 A)가 포함된다. 이러한 균주 세트로부터, 선택된 항원 거리 패러다임을 기반으로 다음과 같은 균주 세트가 설계되었다: 낮음: 부모 WA-1, 베타, 오미크론 BQ.1.1 (믹스 A); 중간: 부모 WA-1, 오미크론 BQ.1.1, SARS-CoV-1 (믹스 B); 중간-높음: 부모 WA-1, SARS-CoV-1, Khosta-2 (믹스 C); 중간-높음: 부모 WA-1, SARS-CoV-1, BANAL20-247 (믹스 D); 높음: 부모 WA-1, SARS-CoV-1, MERS-CoV (믹스 E); 높음: SARS-CoV-1, Khosta-2, BANAL20-247 (믹스 F).
실시예에서 기술된 바와 같이, 이러한 항원 거리 세트(페리틴 모이어티가 있거나 없음)의 균주로부터 항원성 코로나바이러스 펩티드(예를 들어, 스파이크 및/또는 RBD 항원)를 코딩하는 mRNA 분자를 구성하여 다양한 항원 거리 패러다임을 반영하는 항원의 다가 제시를 제공하는 면역원성 조성물을 얻었다. 따라서, 일부 실시양태에서, 본원에 기술된 바와 같은 면역원성 조성물은 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드(또는 이를 코딩하는 mRNA 분자(들))를 포함한다: (i) WA-1, 베타, 및 오미크론 BQ.1.1(또는 XBB.1.5), 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(베타)FN, 및 R(BQ1.1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(베타)-2P, 및 S(BQ1.1)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(베타)FN, 및 Sp(BQ1.1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; 및 (ii) WA-1, 오미크론 BQ.1.1(또는 XBB1.5), 및 SARS-CoV-1, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(BQ 1.1)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(BQ 1.1)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(BQ 1.1)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; (iii) WA-1, SARS-CoV-1, 및 Khosta2, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(Khosta2)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(Khosta2)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(Khosta2)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; (iv) WA-1, SARS-CoV-1, 및 BANAL20-247, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(BANAL20-247)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(BANAL20-247)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(BANAL20-247)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; (v) WA-1, SARS-CoV-1, 및 MERS-CoV, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(MERS-CoV)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(MERS-CoV)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(MERS-CoV)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; 및 (vi) SARS-CoV-1, Khosta-2, 및 BANAL20-247, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(SARS-CoV-1)FN, R(Khosta2)FN, 및 R(BANAL20-247)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(SARS-CoV-1)-2P, S(Khosta2)-2P, 및 S(BANAL20-247)-2P) 또는 SpFN 융합 단백질 Sp(SARS-CoV-1)FN, Sp(Khosta2)FN, 및 Sp(BANAL20-247)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; (vii) 베타, 오미크론 BQ.1.1(또는 XBB1.5), 및 SARS-CoV-1, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(베타)FN, R(BQ 1.1)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(베타)-2P, S(BQ 1.1)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(베타)FN, Sp(BQ 1.1)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; (viii) 베타, 오미크론 XBB.1.5, 및 SARS-CoV-1, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(베타)FN, R(XBB.1.5)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(베타)-2P, S(XBB.1.5)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(베타)FN, Sp(XBB.1.5)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임; (ix) 오미크론 BQ.1.1, SARS-CoV-1, 및 Khosta2, 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(오미크론 BQ.1.1)FN, R(SARS-CoV-1)FN, 및 R(Khosta2)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(오미크론 BQ.1.1)-2P, S(SARS-CoV-1)-2P, 및 S(Khosta2)-2P) 또는 SpFN 융합 단백질 Sp(오미크론 BQ.1.1)FN, Sp(SARS-CoV-1)FN, 및 Sp(Khosta2)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임.
본원에 개시된 융합 단백질, 나노입자, mRNA 분자 및 면역원성 조성물(예를 들어, 백신)은 코로나바이러스 감염을 치료하거나 예방하는 데 사용될 수 있다. 최적의 용량 및 투여 경로는 면역원성 조성물의 특성(예를 들어, mRNA 대 나노입자), 표적이 되는 바이러스(들), 및 치료되는 대상체에 따라 달라질 수 있다.
F. 항원 및 나노입자를 코딩하는 핵산
앞서 논의한 내용은 항원, 융합 단백질, 및 나노입자에 초점을 맞추었지만, 본 개시 내용은 본원에 기술된 바와 같은 항원성 코로나바이러스 항원을 코딩하는 mRNA 분자 및 본원에 기술된 바와 같은 항원성 코로나바이러스 항원을 코딩하는 하나 이상의 mRNA 분자를 포함하는 면역원성 조성물을 포함하며, 선택적으로 mRNA 분자(들)는 아래에서 더 자세히 기술되는 바와 같이 지질 나노입자(LNP)에 캡슐화되거나 공동 캡슐화되는 것으로 이해해야 한다. 따라서, 본원에서는 SARS-CoV-2에 의해 유발되는 COVID-19와 같은 코로나바이러스 감염을 치료 또는 예방하거나, SARS-CoV-1 감염을 치료 또는 예방하는 데 사용될 수 있는 핵산 기반 백신(예를 들어, mRNA 백신), 프라이밍제(예를 들어, 백신 프라이머), 및 부스터를 추가로 개시한다. 예를 들어, 개시된 핵산은 본원에 기술된 바와 같은 임의의 항원성 코로나바이러스 펩티드(들) 또는 융합 단백질(즉, 나노입자 형성 펩티드와 항원성 코로나바이러스 펩티드를 포함하는 융합 단백질, 이는 선택적으로 링커에 의해 연결될 수 있음)을 코딩하는 DNA 또는 mRNA를 포함할 수 있다. 핵산에 의해 코딩된 항원성 코로나바이러스 펩티드는 코로나바이러스(예를 들어, SARS-CoV-2 또는 SARS-CoV-1)로부터 유래된 하나 이상의 단편 또는 전장 단백질, 예컨대 S 단백질, 그리고 특히 S 단백질의 RBD, 또는 본원에 기술된 바와 같은 임의의 항원성 코로나바이러스 펩티드(들)을 포함할 수 있다.
본원에서 논의는 mRNA에 초점을 맞추지만, 본 개시 내용의 핵산은 RNA(mRNA 포함) 또는 DNA일 수 있음을 이해해야 한다. 본 개시 내용의 핵산은 단일 가닥 또는 이중 가닥일 수 있다. 특정 실시양태에서, 핵산은 RNA, 예를 들어 mRNA이다.
일부 측면에 따르면, 본 개시 내용은 서열 번호 552-582 중 어느 하나로부터 선택된 서열 또는 이에 적어도 80% 상동성인 서열을 포함하거나 이로 이루어진 mRNA 분자를 제공한다. 일부 실시양태에서, mRNA 분자는 서열 번호 552-582 중 어느 하나에 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 또는 적어도 99%의 상동성 또는 동일성을 갖는 서열을 포함하거나 이로 이루어진 서열을 갖는다. 일부 실시양태에서, mRNA 분자는 서열 번호 552-582 중 어느 하나를 포함하는 서열을 갖는다. 일부 실시양태에서, mRNA 분자는 서열 번호 552-582 중 어느 하나로 이루어진 서열을 갖는다.
i, DNA 백신, 프라이머, 및 부스터
본원에 개시된 바와 같은 융합 단백질 또는 본원에 개시된 바와 같은 항원성 코로나바이러스 펩티드(예를 들어, 코로나바이러스 S 단백질 또는 이의 단편 또는 변이체)를 코딩하는 DNA는 백신으로, 본원에 개시된 바와 같은 나노입자 또는 mRNA 백신을 투여하기 전에 투여할 수 있는 프라이머로, 또는 본원에 개시된 바와 같은 나노입자 또는 mRNA 백신을 투여한 후 부스터로 사용될 수 있다. 예를 들어, DNA는 코로나바이러스 S 단백질(예를 들어, SARS-CoV-2 또는 SARS-CoV-1의 S 단백질)의 RBD(또는 다른 항원성 펩티드)의 전체, 이의 단편, 또는 변이체를 코딩할 수 있다. DNA는 플라스미드에 통합될 수 있으며, 이는 대상체에게 투여된 후 생체 내에서 DNA를 발현하는 데 필요한 구성 요소(예를 들어, 프로모터)를 포함할 수 있으며, 플라스미드는 인간과 같은 포유류에서 발현되도록 작동적으로 구성될 수 있다.
(1) 벡터
한 측면에서, 본원에서는 본원에 개시된 핵산을 포함하는 벡터를 개시한다. 일부 실시양태에서, 본원에 기술된 바와 같은 mRNA는 벡터로 클로닝될 수 있다. 벡터에는 플라스미드, 파지미드, 파지 유도체, 동물 바이러스, 및 코스미드가 포함되지만 이에 제한되지 않는다. 벡터에는 또한 발현 벡터, 복제 벡터, 프로브 생성 벡터, 시퀀싱 벡터, 및 시험관 내 전사(IVT)에 최적화된 벡터가 포함된다.
특정 실시양태에서, 벡터는 숙주 세포에서 mRNA를 발현하는 데 사용될 수 있다. 다양한 실시양태에서, 벡터는 IVT에 대한 주형으로 사용될 수 있다. 치료적 용도에 적합한 최적으로 번역된 IVT mRNA의 구축은 문헌 [Sahin, et al. (2014). Nat. Rev. Drug Discov. 13, 759-780; Weissman (2015). Expert Rev. Vaccines 14, 265-281]에 자세히 개시되어 있다.
일부 실시양태에서, 본원에 개시된 벡터는 5'에서 3'으로 적어도 다음을 포함할 수 있다: RNA 중합효소 프로모터; 5' UTR을 코딩하는 폴리뉴클레오티드 서열; ORF를 코딩하는 폴리뉴클레오티드 서열; 3' UTR을 코딩하는 폴리뉴클레오티드 서열; 및 적어도 하나의 RNA 앱타머를 코딩하는 폴리뉴클레오티드 서열. 일부 실시양태에서, 본원에 개시된 벡터는 폴리(A) 서열 및/또는 폴리아데닐화 신호를 코딩하는 폴리뉴클레오티드 서열을 포함할 수 있다.
다양한 RNA 중합효소 프로모터가 알려져 있다. 일부 실시양태에서, 프로모터는 T7 RNA 중합효소 프로모터일 수 있다. 다른 유용한 프로모터는 T3 및 SP6 RNA 중합효소 프로모터를 포함할 수 있지만 이에 제한되지 않는다. T7, T3, 및 SP6 프로모터에 대한 공통 뉴클레오티드 서열은 알려져 있다.
또한, 본원에서는 본원에 개시된 벡터 또는 핵산을 포함하는 숙주 세포(예를 들어, 포유류 세포, 예를 들어, 인간 세포)를 개시한다. "숙주 세포"에는 외인성 핵산의 수용자일 수 있거나 수용자였던 개별 세포 또는 세포 배양물이 포함된다. 숙주 세포는 단일 숙주 세포의 자손을 포함하며, 자손은 자연적, 우연적, 또는 의도적인 돌연변이 및/또는 변화로 인해 (형태 또는 전체 DNA 상보체에서) 원래 부모 세포와 반드시 완전히 동일한 것은 아닐 수 있다. 숙주 세포는 본원에 개시된 핵산 또는 벡터로 생체 내 또는 시험관 내에서 형질감염되거나 감염된 세포를 포함한다.
벡터는 여러 상이한 방법, 예를 들어, 전기천공법(Amaxa Nucleofector-II(Amaxa Biosystems, 독일 쾰른 소재)), (ECM 830(BTX)(Harvard Instruments, 미국 매사추세츠주 보스턴 소재) 또는 Gene Pulser II(BioRad, 미국 콜로라도주 덴버 소재), Multiporator(Eppendort, 독일 함부르크 소재), 리포펙션을 이용한 양이온성 리포솜 매개 형질감염, 중합체 캡슐화, 펩티드 매개 형질감염, 또는 "유전자총"과 같은 바이올리스틱 입자 전달 시스템(예를 들어, 문헌 [Nishikawa, et al. (2001). Hum Gene Ther. 12(8):861-70] 참조), 또는 TransIT-RNA 형질감염 키트(Mirus, 미국 위스콘신 매디슨 소재)를 포함하지만, 이에 제한되지 않는 상업적으로 이용 가능한 방법 중 임의의 방법을 사용하여 표적 세포에 도입될 수 있다.
숙주 세포 내로 벡터를 도입하기 위한 화학적 수단에는 콜로이드성 분산 시스템, 예컨대 거대분자 복합체, 나노캡슐, 미소구체, 비드, 및 수중유 에멀젼, 미셀, 혼합된 미셀, 및 리포솜을 비롯한 지질 기반 시스템이 포함된다. 시험관 내 및 생체 내 전달 비히클로서 사용하기 위한 예시적 콜로이드성 시스템은 리포솜(예를 들어, 인공 막 소포)이다.
외인성 핵산을 숙주 세포 내로 도입하거나 세포를 본 개시 내용의 억제제에 노출시키는 데 사용되는 방법에 관계없이, 숙주 세포 내 mRNA 서열의 존재를 확인하기 위해 다양한 분석이 수행될 수 있다.
ii. mRNA 백신
일부 실시양태에서, 본 개시 내용의 핵산은 메신저 RNA(mRNA)이다. mRNA는 변형되거나 변형되지 않을 수 있다. mRNA는 하나 이상의 코딩 및 비코딩 영역을 함유할 수 있다. 코딩 영역은 대안적으로 오픈 리딩 프레임(ORF)이라고도 한다. mRNA의 비코딩 영역에는 5' 캡, 5' 비번역 영역(UTR), 3' UTR, 및 폴리 A 꼬리가 포함된다. mRNA는 천연 공급원으로부터 정제되거나, 재조합 발현 시스템(예를 들어, 시험관 내 전사)을 사용하여 생산되고 선택적으로 정제되거나, 화학적으로 합성될 수 있다.
특정 실시양태에서, mRNA는 관심 항원을 코딩하는 ORF를 포함한다. 특정 실시양태에서, RNA(예를 들어, mRNA)는 또한 적어도 하나의 5' UTR, 3' UTR, 폴리(A) 꼬리, 및/또는 5' 캡을 포함한다.
본원에 개시된 항원성 코로나바이러스 펩티드(들) 또는 융합 단백질 중 하나 이상을 코딩하는 mRNA 분자를 제조하여 mRNA 백신을 제조할 수 있다. 개시된 나노입자의 자가 조립 특성의 결과로서, 대상체에게 투여된 후 이러한 mRNA의 발현으로 생체 내에서 나노입자가 형성될 것이고, 이러한 나노입자는 대상체로부터 면역원성 반응을 유도할 수 있어 대상체는 코로나바이러스 특이적 항체를 생산할 것이다. 따라서 본 개시 내용은 본원에 개시된 항원성 코로나바이러스 펩티드(들) 또는 융합 단백질 중 하나 이상을 코딩하는 백신으로 사용될 수 있는 mRNA를 제공한다.
본원에 개시된 바와 같은 mRNA는 표 6 또는 표 7에 나열된 임의의 단백질을 코딩할 수 있다. mRNA는 선형 mRNA 또는 원형 mRNA일 수 있다.
일부 실시양태에서, 본원에 기술된 바와 같은 면역원성 조성물은 상이한 균주로부터의 적어도 두 개의 항원성 코로나바이러스 펩티드를 코딩하는 하나 이상의 mRNA 분자를 포함하며, 선택적으로 하나 이상의 mRNA 분자는 하나 이상의 지질 나노입자(LNP)에 캡슐화되거나 공동 캡슐화된다. 일부 실시양태에서, 조성물은 상이한 균주로부터의 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 하나의 융합 단백질을 코딩하는 하나의 mRNA 분자를 포함하며, 선택적으로 융합 단백질은 나노입자 형성 펩티드를 추가로 포함하고, mRNA 분자는 지질 나노입자(LNP)에 캡슐화된다. 일부 실시양태에서, 조성물은 선택적으로 나노입자 형성 펩티드와의 융합 단백질에 있는, 적어도 하나의 항원성 코로나바이러스 펩티드를 각각 코딩하는 두 개 이상의 mRNA 분자를 포함하며, 각 mRNA 분자는 별도의 지질 나노입자(LNP)에 캡슐화된다. 일부 실시양태에서, 조성물은 선택적으로 나노입자 형성 펩티드와의 융합 단백질에 있는, 적어도 하나의 항원성 코로나바이러스 펩티드를 각각 코딩하는 두 개 이상의 mRNA 분자를 포함하며, 두 개 이상의 mRNA 분자는 동일한 지질 나노입자(LNP)에 공동 캡슐화된다.
임의의 mRNA 실시양태에서, mRNA 분자는 5' 비번역 영역(5' UTR); 3' 비번역 영역(3' UTR); 폴리아데닐화(폴리(A)) 서열; 화학적 변형, 선택적으로 화학적 변형은 N1-메틸슈도우리딘을 포함함으로부터 선택된 하나 이상의 특징을 가질 수 있다. 추가적으로 또는 대안적으로, mRNA는 자가 복제 mRNA 또는 비복제 mRNA일 수 있다. 한 측면에서 본 개시 내용은 본원에 기술된 바와 같은 항원(예를 들어, 스파이크 단백질, RBD 도메인, 및 이들의 조합 등) 또는 본원에 기술된 바와 같은 융합 단백질(예를 들어, RFN, RRFN, SpFN, mosSpFN, R-SpFN, R-mosSpFN, RR-SpFN, RR-mosSpFN 등)을 코딩하는 뉴클레오티드 서열(예를 들어, mRNA)을 포함하는 본원에 기술된 바와 같은 핵산을 포함하는 조성물을 제공한다.
따라서, 본 개시 내용은, 선택적으로 페리틴 모이어티와 같은 나노입자 형성 단백질을 포함하는 융합 단백질로, 본원에 기술된 바와 같은 항원성 코로나바이러스 펩티드(예를 들어, 본원에 기술된 바와 같은 사르베코바이러스 스파이크 항원 또는 이의 단편)를 코딩하는 뉴클레오티드 서열을 포함하는 1개, 2개, 3개 또는 4개 이상의 핵산(들)(예를 들어, mRNA 분자)을 포함하는 조성물을 제공한다. 단일 mRNA 분자는, 선택적으로 페리틴 모이어티와 같은 나노입자 형성 단백질을 포함하는 융합 단백질로, 본원에서 기술된 바와 같은 2개 이상의 항원성 코로나바이러스 펩티드를 코딩할 수 있다. 대안적으로, 단일 mRNA 분자는, 선택적으로 페리틴 모이어티와 같은 나노입자 형성 단백질을 포함하는 융합 단백질로, 본원에서 기술된 바와 같은 단 하나의 항원성 코로나바이러스 펩티드를 코딩할 수 있다. 본원에서 고려되는 실시양태에는 모든 구성 항원이 상이한 mRNA 분자에 의해 코딩되는 실시양태, 두 개 이상 또는 모든 구성 항원이 동일한 mRNA 분자에 의해 코딩되는 실시양태, 및 이들의 모든 순열 및 조합이 포함된다.
본원에 개시된 바와 같은 면역원성 조성물은 단일 유형의 mRNA 분자(예를 들어, 동일한 항원성 코로나바이러스 펩티드(들)를 코딩하는 mRNA 분자) 또는 동일한 조성물로 제제화되는 mRNA 분자의 조합(예를 들어, 상이한 코로나바이러스 펩티드(들)를 코딩하는 mRNA 분자)을 포함할 수 있다. 추가적으로 또는 대안적으로, 본원에 기재된 바와 같은 조성물은 단 하나의 항원성 코로나바이러스 펩티드를 코딩하는 mRNA 분자를 포함할 수 있으며, 이는 선택적으로 또 다른 그러한 단가 조성물과 조합하여 사용하거나, 본원에 기술된 바와 같은 다가 조성물과 조합(예를 들어, 동시, 별도, 또는 순차적 투여를 위한 조성물의 조합)하여 사용하기 위한 것이다. 본원에서 고려되는 실시양태에는 2개 이상 또는 모든 mRNA 분자가 동일한 조성물로 제제화되는(선택적으로 동일하거나 별도의 LNP에 캡슐화되거나 공동 캡슐화됨) 실시양태와 2개 이상 또는 모든 mRNA 분자가 별도의 조성물로 제제화되는 실시양태가 포함된다. 일부 실시양태에서, 모든 mRNA 분자는 동일한 조성물(선택적으로 별도의 LNP에 캡슐화되거나 동일한 LNP에 공동 캡슐화됨)로 제제화된다. 다른 실시양태에서, 각 mRNA 분자는 별도의 조성물로 제제화된다. 일부 실시양태에서, 두 개 이상의 mRNA 분자는 하나의 조성물(선택적으로 별도의 LNP에 캡슐화되거나 동일한 LNP에 공동 캡슐화됨)로 제제화되고, 하나 이상의 추가 mRNA 분자는 제2 조성물(선택적으로 별도의 LNP에 캡슐화되거나 동일한 LNP에 공동 캡슐화됨)로 제제화된다. 일부 실시양태에서, 본원에서 기술된 바와 같은 1, 2, 3, 4개 이상의 mRNA 분자는 하나의 조성물로 제제화되거나, 각각이 임의의 조합 또는 하위 조합을 갖는 2, 3, 4개 이상의 조성물로 제제화된다.
본원에서 기술된 바와 같은 mRNA 조성물은 선택적으로 하나 이상의 추가 성분, 예컨대 하나 이상의 소분자 면역 증강제(예를 들어, TLR 아고니스트)를 포함할 수 있다.
본원에서 기술된 바와 같은 mRNA 조성물은 선택적으로 리포솜, 수중유 에멀전, 또는 마이크로입자와 같은 핵산(예를 들어, mRNA)을 위한 전달 시스템을 포함할 수 있다. 일부 실시양태에서, mRNA를 포함하는 본원에서 기술된 바와 같은 조성물에서, mRNA는 지질 나노입자(LNP) 제제와 같은 LNP에 캡슐화된다.
(1) 5' Cap
mRNA 5' 캡은 대부분의 진핵 세포에서 발견되는 뉴클레아제에 대한 저항성을 제공하고 번역 효율을 증진시킬 수 있다. 여러 유형의 5' 캡이 알려져 있다. 7-메틸구아노신 캡(또한 "m7G" 또는 "Cap-0"이라고도 함)은 5' - 5' - 삼인산 결합을 통해 첫 번째 전사된 뉴클레오티드에 연결된 구아노신을 포함한다.
5' 캡은 일반적으로 다음과 같이 추가된다. 먼저, RNA 말단 포스파타제가 5' 뉴클레오티드에서 말단 인산기 중 하나를 제거하여 두 개의 말단 인산을 남기고; 그런 다음 구아노신 삼인산(GTP)이 구아닐릴 트랜스퍼라제를 통해 말단 인산에 추가되어 5'5'5 삼인산 결합을 생성하고; 그런 다음 구아닌의 7-질소가 메틸트랜스퍼라제에 의해 메틸화된다. 캡 구조의 예로는 m7G(5')ppp, (5'(A,G(5')ppp(5')A, 및 G(5')ppp(5')G가 포함되지만 이에 제한되지 않는다. 추가 캡 구조는 미국 공개 번호 US 2016/0032356 및 미국 공개 번호 US 2018/0125989에 기술되어 있으며, 이는 본원에 참조로 포함된다.
폴리뉴클레오티드의 5'-캡핑은 제조업체 프로토콜에 따라 5'-구아노신 캡 구조를 생성하기 위해 다음의 화학적 RNA 캡 유사체를 사용하여 시험관 내 전사 반응 동안 동시에 완료할 수 있다: 3'-O-Me-m7G(5')ppp(5')G (the ARCA cap); G(5')ppp(5')A; G(5')ppp(5')G; m7G(5')ppp(5')A; m7G(5')ppp(5')G; m7G(5')ppp(5')(2'OMeA)pG; m7G(5')ppp(5')(2'OMeA)pU; m7G(5')ppp(5')(2'OMeG)pG (New England BioLabs, 미국 매사추세츠주 입스위치 소재; TriLink Biotechnologies). 변형된 RNA의 5'-캡핑은 백시니아 바이러스 캡핑 효소를 사용하여 전사 후에 완료하여 캡 0 구조인 m7G(5')ppp(5')G를 생성할 수 있다. 백시니아 바이러스 캡핑 효소와 2'-O 메틸 트랜스퍼라제를 모두 사용하여 m7G(5')ppp(5')G-2'-O-메틸을 생성하여 캡 1 구조를 생성할 수 있다. 이어서 캡 1 구조로부터 2'-O 메틸 트랜스퍼라제를 사용하여 5'-말단에서 세 번째 뉴클레오티드를 2'-O-메틸화하여 캡 2 구조를 생성할 수 있다. 이어서 캡 2 구조로부터 2'-O 메틸 트랜스퍼라제를 사용하여 5'-말단에서 네 번째 뉴클레오티드를 2'-O-메틸화하여 캡 3 구조를 생성할 수 있다.
특정 실시양태에서, 본 개시 내용의 mRNA는 3'-O-Me-m7G(5')ppp(5')G (the ARCA cap), G(5')ppp(5')A, G(5')ppp(5')G, m7G(5')ppp(5')A, m7G(5')ppp(5')G, m7G(5')ppp(5')(2'OMeA)pG, m7G(5')ppp(5')(2'OMeA)pU, 및 m7G(5')ppp(5')(2'OMeG)pG로 이루어진 군으로부터 선택된 5' 캡을 포함한다.
특정 실시양태에서, 본 개시 내용의 mRNA는 다음의 5' 캡을 포함한다:
(2) 비번역 영역(UTR)
일부 실시양태에서, 본 개시 내용의 mRNA는 5' 및/또는 3' 비번역 영역(UTR)을 포함한다. mRNA에서, 5' UTR은 전사 시작 부위에서 시작하여 시작 코돈까지 이어지지만 시작 코돈은 포함하지 않는다. 3' UTR은 정지 코돈 바로 다음에 시작하여 전사 종결 신호까지 이어진다.
일부 실시양태에서, 본원에 개시된 mRNA는 mRNA의 안정성 또는 번역에 영향을 미치는 하나 이상의 요소를 포함하는 5' UTR을 포함할 수 있다. 일부 실시양태에서, 5' UTR은 약 10 내지 5,000개 뉴클레오티드 길이일 수 있다. 일부 실시양태에서, 5' UTR은 약 50 내지 500개 뉴클레오티드 길이일 수 있다. 일부 실시양태에서, 5' UTR은 적어도 약 10개 뉴클레오티드 길이, 약 20개 뉴클레오티드 길이, 약 30개 뉴클레오티드 길이, 약 40개 뉴클레오티드 길이, 약 50개 뉴클레오티드 길이, 약 100개 뉴클레오티드 길이, 약 150개 뉴클레오티드 길이, 약 200개 뉴클레오티드 길이, 약 250개 뉴클레오티드 길이, 약 300개 뉴클레오티드 길이, 약 350개 뉴클레오티드 길이, 약 400개 뉴클레오티드 길이, 약 450개 뉴클레오티드 길이, 약 500개 뉴클레오티드 길이, 약 550개 뉴클레오티드 길이, 약 600개 뉴클레오티드 길이, 약 650개 뉴클레오티드 길이, 약 700개 뉴클레오티드 길이, 약 750개 뉴클레오티드 길이, 약 800개 뉴클레오티드 길이, 약 850개 뉴클레오티드 길이, 약 900개 뉴클레오티드 길이, 약 950개 뉴클레오티드 길이, 약 1,000개 뉴클레오티드 길이, 약 1,500개 뉴클레오티드 길이, 약 2,000개 뉴클레오티드 길이, 약 2,500개 뉴클레오티드 길이, 약 3,000개 뉴클레오티드 길이, 약 3,500개 뉴클레오티드 길이, 약 4,000개 뉴클레오티드 길이, 약 4,500개 뉴클레오티드 길이 또는 약 5,000개 뉴클레오티드 길이이다.
일부 실시양태에서, 본원에 개시된 mRNA는 폴리아데닐화 신호, 세포에서 mRNA의 위치 안정성에 영향을 미치는 단백질에 대한 결합 부위, 또는 miRNA에 대한 하나 이상의 결합 부위 중 하나 이상을 포함하는 3' UTR을 포함할 수 있다. 일부 실시양태에서, 3' UTR은 50 내지 5,000개 이상의 뉴클레오티드 길이일 수 있다. 일부 실시양태에서, 3' UTR은 50 내지 1,000개 이상의 뉴클레오티드 길이일 수 있다. 일부 실시 양태에서, 3' UTR은 적어도 약 50개 뉴클레오티드 길이, 약 100개 뉴클레오티드 길이, 약 150개 뉴클레오티드 길이, 약 200개 뉴클레오티드 길이, 약 250개 뉴클레오티드 길이, 약 300개 뉴클레오티드 길이, 약 350개 뉴클레오티드 길이, 약 400개 뉴클레오티드 길이, 약 450개 뉴클레오티드 길이, 약 500개 뉴클레오티드 길이, 약 550개 뉴클레오티드 길이, 약 600개 뉴클레오티드 길이, 약 650개 뉴클레오티드 길이, 약 700개 뉴클레오티드 길이, 약 750개 뉴클레오티드 길이, 약 800개 뉴클레오티드 길이, 약 850개 뉴클레오티드 길이, 약 900개 뉴클레오티드 길이, 약 950개 뉴클레오티드 길이, 약 1,000개 뉴클레오티드 길이, 약 1,500개 뉴클레오티드 길이, 약 2,000개 뉴클레오티드 길이, 약 2,500개 뉴클레오티드 길이, 약 3,000개 뉴클레오티드 길이, 약 3,500개 뉴클레오티드 길이, 약 4,000개 뉴클레오티드 길이, 약 4,500개 뉴클레오티드 길이, 또는 약 5,000개 뉴클레오티드 길이이다.
일부 실시양태에서, 본원에 개시된 mRNA는 mRNA 전사체에 의해 코딩된 것과 다른 유전자로부터 유래된 5' 또는 3' UTR을 포함할 수 있다(즉, UTR은 이종 UTR임).
특정 실시양태에서, 5' 및/또는 3' UTR 서열은 mRNA의 안정성을 증가시키기 위해 안정적인 mRNA(예를 들어, 글로빈, 액틴, GAPDH, 튜불린, 히스톤, 또는 구연산 회로 효소)로부터 유래될 수 있다. 예를 들어, 5' UTR 서열은 뉴클레아제 저항성을 개선하고/하거나 mRNA의 반감기를 개선하기 위해 CMV 즉시 초기 1(IE1) 유전자의 부분 서열 또는 이의 단편을 포함할 수 있다. 또한, 인간 성장 호르몬(hGH)을 코딩하는 서열, 또는 이의 단편을 mRNA의 3' 말단 또는 비번역 영역에 포함시키는 것도 고려된다. 일반적으로, 이러한 변형은 변형되지 않은 대응물에 비해 mRNA의 안정성 및/또는 약동학적 특성(예를 들어, 반감기)을 개선하고, 예를 들어 생체 내 뉴클레아제 소화에 대한 이러한 mRNA 저항성을 개선하기 위해 만들어진 변형을 포함한다.
예시적 5' UTR에는 CMV 즉시 초기 1(IE1) 유전자로부터 유래된 서열(미국 공개 번호 2014/0206753 및 2015/0157565, 각각 본원에 참조로 포함됨) 또는 서열 GGGAUCCUACC(서열 번호 25)(미국 공개 번호 2016/0151409, 본원에 참조로 포함됨)이 포함된다.
다양한 실시양태에서, 5' UTR은 TOP 유전자의 5' UTR로부터 유래될 수 있다. TOP 유전자는 일반적으로 5'-말단 올리고피리미딘(TOP) 트랙트의 존재를 특징으로 한다. 더욱이, 대부분의 TOP 유전자는 성장 관련 번역 조절을 특징으로 한다. 그러나 조직 특이적으로 번역이 조절되는 TOP 유전자도 알려져 있다. 특정 실시양태에서, TOP 유전자의 5' UTR로부터 유래된 5' UTR은 5' TOP 모티프(올리고피리미딘 트랙트)가 없다(예를 들어, 미국 공개 번호 2017/0029847, 2016/0304883, 2016/0235864, 및 2016/0166710, 각각 본원에 참조로 포함됨).
특정 실시양태에서, 5' UTR은 리보솜 단백질 Large 32(L32) 유전자로부터 유래된다(미국 공개 번호 2017/0029847, 상기).
특정 실시양태에서, 5' UTR은 하이드록시스테로이드(17-b) 탈수소효소 4 유전자(HSD17B4)의 5' UTR로부터 유래된다(미국 공개 번호 2016/0166710, 상기).
특정 실시양태에서, 5' UTR은 ATP5A1 유전자의 5' UTR로부터 유래된다(미국 공개 번호 2016/0166710, 상기).
일부 실시양태에서, 5' UTR 대신 내부 리보솜 진입 부위(IRES)가 사용된다.
일부 실시양태에서, 5'UTR은 서열 번호 26에 제시되고 아래에 재생산된 핵산 서열을 포함한다:
일부 실시양태에서, 3'UTR은 서열 번호 27에 제시되고 아래에 재생산된 핵산 서열을 포함한다:
5'UTR 및 3'UTR은 본원에 참조로 포함된 WO2012/075040에 더 자세히 기술되어 있다.
(3) 폴리아데닐화 꼬리
본원에서 사용되는 바와 같이, 용어 "폴리(A) 서열", "폴리(A) 꼬리" 및 "폴리(A) 영역"은 mRNA 분자의 3' 말단에 있는 아데노신 뉴클레오티드의 서열을 지칭한다. 폴리(A) 꼬리는 mRNA에 안정성을 부여하고 엑소뉴클레아제 분해로부터 mRNA를 보호할 수 있다. 폴리(A) 꼬리는 번역을 향상시킬 수 있다. 일부 실시양태에서, 폴리(A) 꼬리는 본질적으로 동종중합체이다. 예를 들어, 100개의 아데노신 뉴클레오티드의 폴리(A) 꼬리는 본질적으로 100개의 뉴클레오티드의 길이를 가질 수 있다. 특정 실시양태에서, 폴리(A) 꼬리는 아데노신 뉴클레오티드와 상이한 적어도 하나의 뉴클레오티드(예를 들어, 아데노신 뉴클레오티드가 아닌 뉴클레오티드)에 의해 중단될 수 있다. 예를 들어, 100개의 아데노신 뉴클레오티드로의 폴리(A) 꼬리는 100개 초과의 뉴클레오티드 길이(100개의 아데노신 뉴클레오티드와 아데노신 뉴클레오티드와 상이한 적어도 하나의 뉴클레오티드, 또는 뉴클레오티드 스트레치를 포함함)를 가질 수 있다. 특정 실시양태에서, 폴리(A) 꼬리는 서열
(서열 번호 28)를 포함한다.
본원에서 사용되는 바와 같이 "폴리(A) 꼬리"는 일반적으로 RNA와 관련이 있다. 그러나, 본 개시 내용의 맥락에서, 이 용어는 마찬가지로 DNA 분자의 해당 서열(예를 들어, "폴리(T) 서열")과도 관련이 있다.
폴리(A) 꼬리는 약 10 내지 약 500개의 아데노신 뉴클레오티드, 약 10 내지 약 200개의 아데노신 뉴클레오티드, 약 40 내지 약 200개의 아데노신 뉴클레오티드, 또는 약 40 내지 약 150개의 아데노신 뉴클레오티드를 포함할 수 있다. 폴리(A) 꼬리의 길이는 적어도 약 10, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 또는 500개의 아데노신 뉴클레오티드일 수 있다.
핵산이 RNA인 일부 실시양태에서, 핵산의 폴리(A) 꼬리는 RNA 시험관 내 전사 동안 DNA 주형으로부터 얻는다. 특정 실시양태에서, 폴리(A) 꼬리는 DNA 주형으로부터 전사되지 않고 일반적인 화학 합성 방법에 의해 시험관 내에서 얻는다. 다양한 실시양태에서, 폴리(A) 꼬리는 상업적으로 이용 가능한 폴리아데닐화 키트 및 해당 프로토콜을 사용하여 (RNA 시험관 내 전사 후에) RNA의 효소적 폴리아데닐화에 의해 생성되거나, 대안적으로 고정화된 폴리(A)중합효소를 사용하여, 예를 들어, WO2016/174271에 기술된 방법 및 수단을 사용하여 생성된다.
핵산은 효소적 폴리아데닐화에 의해 얻어진 폴리(A) 꼬리를 포함할 수 있으며, 여기서 대부분의 핵산 분자는 약 100(±20) 내지 약 500(±50)개 또는 약 250(±20)개의 아데노신 뉴클레오티드를 포함한다.
일부 실시양태에서, 핵산은 주형 DNA로부터 유래된 폴리(A) 꼬리를 포함할 수 있으며, 예를 들어 WO2016/091391에 기술된 바와 같이, 효소적 폴리아데닐화에 의해 생성된 적어도 하나의 추가 폴리(A) 꼬리를 추가로 포함할 수 있다.
특정 실시양태에서, 핵산은 적어도 하나의 폴리아데닐화 신호를 포함한다.
다양한 실시양태에서, 핵산은 적어도 하나의 폴리(C) 서열을 포함할 수 있다.
본원에서 사용되는 바와 같이, 용어 "폴리(C) 서열"은 최대 약 200개의 시토신 뉴클레오티드의 시토신 뉴클레오티드 서열을 의미한다. 일부 실시양태에서, 폴리(C) 서열은 약 10 내지 약 200개의 시토신 뉴클레오티드, 약 10 내지 약 100개의 시토신 뉴클레오티드, 약 20 내지 약 70개의 시토신 뉴클레오티드, 약 20 내지 약 60개의 시토신 뉴클레오티드, 또는 약 10 내지 약 40개의 시토신 뉴클레오티드를 포함한다. 일부 실시양태에서, 폴리(C) 서열은 약 30개의 시토신 뉴클레오티드를 포함한다.
(4) 화학적 변형
본원에 개시된 mRNA는 변형되거나 변형되지 않을 수 있다. 전형적으로, mRNA는 적어도 하나의 화학적 변형을 포함한다. 일부 실시양태에서, 본원에 개시된 mRNA는 전형적으로 RNA 안정성을 향상시키는 하나 이상의 변형을 함유할 수 있다. 예시적인 변형에는 백본 변형, 당 변형, 또는 염기 변형이 포함될 수 있다. 일부 실시양태에서, 개시된 mRNA는 퓨린(아데닌(A) 및 구아닌(G)) 또는 피리미딘(티민(T), 시토신(C), 및 우라실(U))을 포함하지만 이에 제한되지 않는 자연 발생 뉴클레오티드 및/또는 뉴클레오티드 유사체(변형된 뉴클레오티드)로부터 합성될 수 있다. 특정 실시양태에서, 개시된 mRNA는 퓨린 및 피리미딘의 변형된 뉴클레오티드 유사체 또는 유도체, 예를 들어, 1-메틸-아데닌, 2-메틸-아데닌, 2-메틸티오-N-6-이소펜테닐-아데닌, N6-메틸-아데닌, N6-이소펜테닐-아데닌, 2-티오-시토신, 3-메틸-시토신, 4-아세틸-시토신, 5-메틸-시토신, 2,6-디아미노퓨린, 1-메틸-구아닌, 2-메틸-구아닌, 2,2-디메틸-구아닌, 7-메틸-구아닌, 이노신, 1-메틸-이노신, 슈도우라실(5-우라실), 디하이드로-우라실, 2-티오-우라실, 4-티오-우라실, 5-카복시메틸아미노메틸-2-티오-우라실, 5-(카복시하이드록시메틸)-우라실, 5-플루오로-우라실, 5-브로모-우라실, 5-카복시메틸아미노메틸-우라실, 5-메틸-2-티오-우라실, 5-메틸-우라실, N-우라실-5-옥시아세트산 메틸 에스테르, 5-메틸아미노메틸-우라실, 5-메톡시아미노메틸-2-티오-우라실, 5'-메톡시카보닐메틸-우라실, 5-메톡시-우라실, 우라실-5-옥시아세트산 메틸 에스테르, 우라실-5-옥시아세트산(v), 1-메틸-슈도우라실, 퀘오신, β-D-만노실-퀘오신, 포스포라미데이트, 포스포로티오에이트, 펩티드 뉴클레오티드, 메틸포스포네이트, 7-데아자구아노신, 5-메틸시토신, 및 이노신으로부터 합성될 수 있다.
일부 실시양태에서, 개시된 mRNA는 슈도우리딘, N1-메틸슈도우리딘, 2-티오우리딘, 4'-티오우리딘, 5-메틸시토신, 2-티오-1-메틸-1-데아자-슈도우리딘, 2-티오-1-메틸-슈도우리딘, 2-티오-5-아자-우리딘, 2-티오-디하이드로슈도우리딘, 2-티오-디하이드로우리딘, 2-티오-슈도우리딘, 4-메톡시-2-티오-슈도우리딘, 4-메톡시-슈도우리딘, 4-티오-1-메틸-슈도우리딘, 4-티오-슈도우리딘, 5-아자-우리딘, 디하이드로슈도우리딘, 5-메틸우리딘, 5-메틸우리딘, 5-메톡시우리딘, 및 2'-O-메틸우리딘을 포함하지만 이에 제한되지 않는 적어도 하나의 화학적 변형을 포함할 수 있다.
일부 실시양태에서, 화학적 변형은 슈도우리딘, N1-메틸슈도우리딘, 5-메틸시토신, 5-메톡시우리딘, 및 이들의 조합으로 이루어진 군으로부터 선택된다.
일부 실시양태에서, 화학적 변형은 N1-메틸슈도우리딘을 포함한다.
일부 실시양태에서, mRNA의 우라실 뉴클레오티드의 적어도 20%, 적어도 30%, 적어도 40%, 적어도 50%, 적어도 60%, 적어도 70%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 또는 100%가 화학적으로 변형된다.
일부 실시양태에서, ORF의 우라실 뉴클레오티드의 적어도 20%, 적어도 30%, 적어도 40%, 적어도 50%, 적어도 60%, 적어도 70%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 또는 100%가 화학적으로 변형된다.
상기 유사체의 제조는 예를 들어 미국 특허 제4,373,071호, 미국 특허 제4,401,796호, 미국 특허 제4,415,732호, 미국 특허 제4,458,066호, 미국 특허 제4,500,707호, 미국 특허 제4,668,777호, 미국 특허 제4,973,679호, 미국 특허 제5,047,524호, 미국 특허 제5,132,418호, 미국 특허 제5,153,319호, 미국 특허 제5,262,530호, 및 미국 특허 제5,700,642호에 기술되어 있다.
(5) mRNA 합성
본원에 개시된 mRNA는 임의의 다양한 방법에 따라 합성될 수 있다. 예를 들어, 본 개시 내용에 따른 mRNA는 시험관 내 전사(IVT)를 통해 합성될 수 있다. 시험관 내 전사를 위한 일부 방법은 예를 들어 문헌 [Geall et al. (2013) Semin. Immunol. 25(2): 152-159; Brunelle et al. (2013) Methods Enzymol. 530:101-14]에 기술되어 있다. 간략하게, IVT는 일반적으로 프로모터를 함유하는 선형 또는 원형 DNA 주형, 리보뉴클레오티드 삼인산 풀, DTT 및 마그네슘 이온을 포함할 수 있는 완충 시스템, 적절한 RNA 중합효소(예를 들어, T3, T7, 또는 SP6 rNA 중합효소), DNase I, 피로포스파타제, 및/또는 RNase 억제제로 수행된다. 정확한 조건은 구체적인 응용 분야에 따라 다를 수 있다. 이러한 시약의 존재는 일반적으로 최종 mRNA 생성물에서 바람직하지 않으며 이러한 시약은 불순물 또는 오염 물질로 간주될 수 있으며, 이를 정제하거나 제거하여 치료 용도에 적합한 깨끗하고/하거나 균질한 mRNA를 제공할 수 있다. 시험관 내 전사 반응으로부터 제공된 mRNA가 일부 실시양태에서 바람직할 수 있지만, 박테리아, 진균류, 식물, 및/또는 동물로부터 생성된 야생형 mRNA를 포함하여 본 개시 내용에 따라 다른 mRNA 공급원을 사용할 수 있다.
iii. 기타 RNA 백신
(1) 자가 복제 RNA, 트랜스 복제 RNA 및 비복제 RNA
일반적으로, 본원에 기술된 핵산 분자는 비복제 RNA이다. 그러나, 본원에 기술된 핵산 분자는 대안적으로 자가 복제 RNA 또는 트랜스 복제 RNA일 수 있다.
(2) 자가 복제 RNA
자가 복제(또는 자가 증폭) RNA는 예를 들어 알파바이러스로부터 유래된 복제 요소를 사용하고, 구조적 바이러스 단백질을 관심 단백질(예를 들어, 사르베코바이러스 스파이크 항원)을 코딩하는 뉴클레오티드 서열로 대체하여 생산할 수 있다. 자가 복제 RNA는 일반적으로 세포에 전달된 후 직접 번역될 수 있는 양성 가닥 분자이며, 이 번역은 RNA 의존성 RNA 중합효소를 제공하고, 이는 그 후 전달된 RNA로부터 안티센스 및 센스 전사체를 모두 생성하는 한다. 따라서, 전달된 RNA는 여러 개의 딸 RNA의 생산으로 이어진다. 이러한 딸 RNA와 공선성 하위게놈 전사체는 스스로 번역되어 코딩된 항원의 원위치 발현을 제공할 수 있거나, 번역되어 항원의 원위치 발현을 제공하는 전달된 RNA와 동일한 의미를 갖는 추가 전사체를 제공하도록 전사될 수 있다. 이러한 전사 서열의 전체적인 결과는 도입된 레플리콘 RNA 수가 크게 증폭되는 것이고 따라서 코딩된 항원이 세포의 주요 폴리펩티드 생성물이 된다.
이러한 방식으로 자가 복제를 달성하기 위한 하나의 적합한 시스템은 알파바이러스 기반 레플리콘을 사용하는 것이다. 이러한 레플리콘은 세포에 전달된 후 복제효소(또는 복제효소-전사효소)의 번역으로 이어지는 양성 가닥(양성 센스 가닥) RNA이다. 복제효소는 자가 절단되어 양성 가닥의 전달된 RNA의 게놈 가닥 복사본을 생성하는 복제 복합체를 제공하는 폴리프로테인으로 번역된다. 이러한 음성(-) 가닥 전사체는 스스로 전사되어 양성 가닥 부모 RNA의 추가 복사본을 제공하고 항원을 코딩하는 하위게놈 전사체도 제공할 수 있다. 따라서 하위게놈 전사체의 번역은 감염된 세포에 의한 항원의 원위치 발현으로 이어진다. 적합한 알파바이러스 레플리콘은 신드비스 바이러스, 셈리키 삼림 바이러스, 동부 말 뇌염 바이러스, 베네수엘라 말 뇌염 바이러스 등의 복제효소를 사용할 수 있다. 돌연변이 또는 야생형 바이러스 서열을 사용할 수 있는데, 예를 들어, VEEV의 약독화된 TC83 돌연변이체가 레플리콘에서 사용되었다. 다음 참고문헌을 참조한다: 본원에 참조로 포함된 WO2005/113782.
한 실시양태에서, 본원에 기술된 각각의 자가 복제 RNA는 (i) 자가 복제 RNA 분자로부터 RNA를 전사할 수 있는 RNA 의존성 RNA 중합효소 및 (ii) 본원에서 개시된 바와 같은 스파이크 폴리펩티드 항원을 코딩한다. 중합효소는 알파바이러스 복제효소, 예를 들어 알파바이러스 단백질 nsP1, nsP2, nsP3, 및 nsP4 중 하나 이상을 포함하는 것일 수 있다. 천연 알파바이러스 게놈은 비구조적 복제효소 폴리프로테인 외에도 구조적 비리온 단백질을 코딩하는 반면, 특정 실시양태에서, 자가 복제 RNA 분자는 알파바이러스 구조적 단백질을 코딩하지 않는다. 따라서, 자가 복제 RNA는 세포에서 자체의 게놈 RNA 복사본을 생산할 수 있지만 RNA를 함유하는 비리온을 생산할 수는 없다. 이러한 비리온을 생산할 수 없다는 것은 야생형 알파바이러스와 달리 자가 복제 RNA 분자가 감염성 형태로 자체를 영속시킬 수 없다는 것을 의미한다. 야생형 바이러스에서 영속화에 필요한 알파바이러스 구조적 단백질은 본 개시 내용의 자가 복제 RNA에는 없으며, 그 자리는 관심 면역원을 코딩하는 유전자(들)에 의해 차지되어, 하위게놈 전사체가 구조적 알파바이러스 비리온 단백질이 아닌 면역원을 코딩한다. 자가 복제 RNA는 본원에 참조로 포함된 WO2011005799에 더 자세히 기술되어 있다.
(3) 트랜스 복제 RNA
트랜스 복제(또는 트랜스 증폭) RNA는 상기 기술된 자가 복제 RNA와 유사한 요소를 가지고 있다. 그러나 트랜스 복제 RNA의 경우 두 개의 별도 RNA 분자가 사용된다. 제1 RNA 분자는 상기 기술된 RNA 복제효소(예를 들어, 알파바이러스 복제효소)를 코딩하고 제2 RNA 분자는 관심 단백질(예를 들어, 본원에 기술된 스파이크 단백질)을 코딩한다. RNA 복제효소는 제1 및 제2 RNA 분자 중 하나 또는 둘 다를 복제하여 관심 단백질을 코딩하는 RNA 분자의 복사본 수를 크게 증가시킬 수 있다. 트랜스 복제 RNA는 본원에 참조로 포함된 WO2017162265에 더 자세히 설명되어 있다.
(4) 비복제 RNA
비복제(또는 비증폭) RNA는 자체 복제 능력이 없는 RNA이다.
G. LNP
특정 실시양태에서, 본원에 기술된 바와 같은 면역원 조성물은 본원에 기술된 바와 같은 하나 이상의 mRNA 분자를 캡슐화한 지질 나노입자(LNP)를 포함한다. mRNA는 변형된 에탄올-적하 나노침전 공정과 같은 당업계에 알려진 방법을 통해 지질 나노입자(LNP)에 캡슐화될 수 있다. 간략하게, 이온화 가능한 구조적, 헬퍼 및 폴리에틸렌 글리콜 지질은 지질:mRNA의 주어진 비율로 아세트산 완충액 pH 5.0에서 mRNA와 혼합될 수 있다. 혼합물은 Tris-Cl pH 7.5로 중화시키고, 동결 보호제로 수크로스를 첨가하고, 멸균 여과하고, 추가 사용까지 -70℃에서 냉동 보관할 수 있다. mRNA와 LNP는 다음과 같을 수 있다: 지질 나노입자는 RNA, 이온화 가능한 지질, ((4-하이드록시부틸)아잔디일)비스(헥산-6,1-디일)비스(2-헥실데카노에이트)), PEG화된 지질, 2-[(폴리에틸렌 글리콜)-2000]-N,N-디테트라데실아세트아미드 및 두 가지 구조적 지질(1,2-디스테아로일-sn-글리세로-3-포스포콜린(DSPC) 및 콜레스테롤)을 함유한다. 당업자는 이것이 mRNA를 제제화하는 단지 하나의 예시적인 방법일 뿐이며, 당업계에서 사용되는 다른 방법 및 제제화제(예를 들어, 다른 지질)도 적합할 수 있음을 이해할 것이다. 병렬 방법론은 본원에서 고려되는 mRNA 백신의 다른 실시양태를 실시하는 데 사용될 수 있다.
특정 실시양태에서, 본 개시 내용의 조성물(예를 들어, 본 개시 내용의 핵산을 포함하는 조성물)은 추가로 지질 나노입자(LNP)를 포함한다. 특정 실시양태에서, 본 개시 내용의 핵산은 LNP에 캡슐화된다.
본 개시 내용의 LNP는 네 가지 지질 범주를 포함할 수 있다: (i) 이온화 가능한 지질(예를 들어, 양이온성 지질); (ii) PEG화된 지질; (iii) 콜레스테롤 기반 지질, 및 (iv) 헬퍼 지질.
i. 이온화 가능한 지질
이온화 가능한 지질은 mRNA 캡슐화를 용이하게 하며 양이온성 지질일 수 있다. 양이온성 지질은 낮은 pH에서 양전하 환경을 제공하여 음전하 mRNA 약물 물질의 효율적인 캡슐화를 용이하게 한다.
일부 실시양태에서, 양이온성 지질은 OF-02이다:
OF-02는 OF-Deg-Lin의 비분해성 구조적 유사체이다. OF-Deg-Lin은 디케토피페라진 코어와 이중 불포화 꼬리를 부착하기 위한 분해성 에스테르 결합을 함유하는 반면, OF-02는 동일한 디케토피페라진 코어와 이중 불포화 꼬리를 부착하기 위한 비분해성 1,2-아미노-알코올 결합을 함유한다(Fenton et al., Adv Mater. (2016) 28:2939; 미국 특허 제10,201,618호). 본원의 예시적인 LNP 제제인 지질 A는 OF-2를 함유한다.
일부 실시양태에서, 양이온성 지질은 cKK-E10이다(Dong et al., PNAS (2014) 111(11):3955-60 미국 특허 제9,512,073호):
본원의 예시적인 LNP 제제인 지질 B는 cKK-E10를 함유한다.
일부 실시양태에서, 양이온성 지질은 GL-HEPES-E3-E10-DS-3-E18-1(2-(4-(2-((3-(비스((Z)-2-하이드록시옥타데크-9-엔-1-일)아미노)프로필)디설파네일)에틸)피페라진-1-일)에틸 4-(비스(2-하이드록시데실)아미노)부타노에이트)(WO2022/221688)이며, 이는 피페라진 코어를 갖는 HEPES 기반 디설파이드 양이온성 지질이며, 화학식 III을 갖는다:
본원의 예시적인 LNP 제제인 지질 C는 GL-HEPES-E3-E10-DS-3-E18-1을 함유한다. 지질 C는 지질 A 또는 지질 B와 동일한 구성을 갖지만 양이온성 지질에 차이가 있다.
일부 실시양태에서, 양이온성 지질은 GL-HEPES-E3-E12-DS-4-E10(2-(4-(2-((3-(비스(2-하이드록시데실)아미노)부틸)디설파네일)에틸)피페라진-1-일)에틸 4-(비스(2-하이드록시도데실)아미노)부타노에이트)(WO2022/221688)이며, 이는 피페라진 코어를 갖는 HEPES 기반 디설파이드 양이온성 지질이며, 화학식 IV를 갖는다:
본원의 예시적인 LNP 제제인 지질 D는 GL-HEPES-E3-E12-DS-4-E10을 함유한다. 지질 D는 지질 A 또는 지질 B와 동일한 구성을 갖지만 양이온성 지질에 차이가 있다.
일부 실시양태에서, 양이온성 지질은 GL-HEPES-E3-E12-DS-3-E14(2-(4-(2-((3-(비스(2-하이드록시테트라데실)아미노)프로필)디설파네일)에틸)피페라진-1-일)에틸 4-(비스(2-하이드록시도데실)아미노)부타노에이트)(WO2022/221688)이며, 이는 피페라진 코어를 갖는 HEPES 기반 디설파이드 양이온성 지질이며, 화학식 V를 갖는다:
본원의 예시적인 LNP 제제인 지질 E는 GL-HEPES-E3-E12-DS-3-E14를 함유한다. 지질 E는 지질 A 또는 지질 B와 동일한 구성을 갖지만 양이온성 지질에 차이가 있다.
양이온성 지질 GL-HEPES-E3-E10-DS-3-E18-1(III), GL-HEPES-E3-E12-DS-4-E10(IV), 및 GL-HEPES-E3-E12-DS-3-E14(V)는 반응식 1에 제시된 일반적인 절차에 따라 합성될 수 있다:
반응식 1: 화학식 (III), (IV), 및 (V)에 대한 일반적인 합성 반응식
일부 실시양태에서, 양이온성 지질은 화학식 VI를 갖는 MC3이다:
일부 실시양태에서, 양이온성 지질은 하기 화학식 VII을 갖는 SM-102(9-헵타데카닐 8-{(2-하이드록시에틸)[6-옥소-6-(운데실옥시)헥실]아미노}옥타노에이트)이다:
일부 실시양태에서, 양이온성 지질은 화학식 VIII을 갖는 ALC-0315[(4-하이드록시부틸)아잔디일]디(헥산-6,1-디일)비스(2-헥실데카노에이트)이다:
일부 실시양태에서, 양이온성 지질은 화학식 IX를 갖는 cOrn-EE1이다:
일부 실시양태에서, 양이온성 지질은 cKK-E10; OF-02; [(6Z,9Z,28Z,31Z)-헵타트리아콘타-6,9,28,31-테트라엔-19-일] 4-(디메틸아미노)부타노에이트(D-Lin-MC3-DMA); 2,2-디리놀레일-4-디메틸아미노에틸-[1,3]-디옥솔란(DLin-KC2-DMA); 1,2-디리놀레일옥시-N,N-디메틸-3-아미노프로판(DLin-DMA); 디((Z)-논-2-엔-1-일) 9-((4-(디메틸아미노)부타노일)옥시)헵타데칸디오에이트(L319); 9-헵타데카닐 8-{(2-하이드록시에틸)[6-옥소-6-(운데실옥시)헥실]아미노}옥타노에이트(SM-102); [(4-하이드록시부틸)아잔디일]디(헥산-6,1-디일) 비스(2-헥실데카노에이트)(ALC-0315); [3-(디메틸아미노)-2-[(Z)-옥타데크-9-에노일]옥시프로필] (Z)-옥타데크-9-에노에이트(DODAP); 2,5-비스(3-아미노프로필아미노)-N-[2-[디(헵타데실)아미노]-2-옥소에틸]펜탄아미드(DOGS); [(3S,8S,9S,10R,13R,14S,17R)-10,13-디메틸-17-[(2R)-6-메틸헵탄-2-일]-2,3,4,7,8,9,11,12,14,15,16,17-도데카하이드로-1H-사이클로펜타[a]페난트렌-3-일] N-[2-(디메틸아미노)에틸]카바메이트(DC-Chol); 테트라키스(8-메틸노닐) 3,3',3",3"'-(((메틸아잔디일) 비스(프로판-3,1디일))비스(아잔트리일))테트라프로피오네이트(306Oi10); 데실(2-(디옥틸암모니오)에틸)포스페이트(9A1P9); 에틸 5,5-디((Z)-헵타데크-8-엔-1-일)-1-(3-(피롤리딘-1-일)프로필)-2,5-디하이드로-1H-이미다졸-2-카복실레이트(A2-Iso5-2DC18); 비스(2-(도데실디설파닐)에틸) 3,3'-((3-메틸-9-옥소-10-옥사-13,14-디티아-3,6-디아자헥사코실)아잔디일)디프로피오네이트(BAME-O16B); 1,1'-((2-(4-(2-((2-(비스(2-하이드록시도데실)아미노)에틸) (2-하이드록시도데실)아미노)에틸) 피페라진-1-일)에틸)아잔디일) 비스(도데칸-2-올)(C12-200); 3,6-비스(4-(비스(2-하이드록시도데실)아미노)부틸)피페라진-2,5-디온(cKK-E12); 헥사(옥탄-3-일) 9,9',9",9"',9"",9"'"-((((벤젠-1,3,5-트리카보닐)이리스(아잔디일)) 트리스(프로판-3,1-디일)) 트리스(아잔트리일))헥사노나노에이트(FTT5); (((3,6-디옥소피페라진-2,5-디일)비스(부탄-4,1-디일))비스(아잔트리일))테트라키스(에탄-2,1-디일) (9Z,9'Z,9"Z,9"'Z,12Z,12'Z,12"Z,12"'Z)-테트라키스(옥타데카-9,12-디에노에이트)(OF-Deg-Lin); TT3; N1,N3,N5-트리스(3-(디도데실아미노)프로필)벤젠-1,3,5-트리카복사미드; N1-[2-((1S)-1-[(3-아미노프로필)아미노]-4-[디(3-아미노프로필)아미노]부틸카복사미도)에틸]-3,4-디[올레일옥시]-벤자미드(MVL5); 헵타데칸-9-일 8-((2-하이드록시에틸)(8-(노닐옥시)-8-옥소옥틸)아미노)옥타노에이트(지질 5); GL-HEPES-E3-E10-DS-3-E18-1; GL-HEPES-E3-E12-DS-4-E10; GL-HEPES-E3-E12-DS-3-E14; 및 이들의 조합을 포함하는 군으로부터 선택될 수 있다.
일부 실시양태에서, 양이온성 지질은 화학식 X(EP23306049.0)을 갖는 IM-001이다:
일부 실시양태에서, 양이온성 지질은 화학식 XI(EP23306049.0)을 갖는 IS-001이다:
일부 실시양태에서, 양이온성 지질은 생분해성이다.
일부 실시양태에서, 양이온성 지질은 생분해성이 아니다.
일부 실시양태에서, 양이온성 지질은 절단 가능하다.
일부 실시양태에서, 양이온성 지질은 절단 가능하지 않다.
양이온성 지질은 문헌 [Dong et al. (PNAS. 111(11):3955-60. 2014)]; 문헌 [Fenton et al. (Adv Mater. 28:2939. 2016)]; 미국 특허 제9,512,073호; 및 미국 특허 제10,201,618호에 더 자세히 기술되어 있으며, 이들 각각은 본원에 참조로 포함된다.
ii. PEG화된 지질
PEG화된 지질 성분은 나노입자의 입자 크기와 안정성을 제어한다. 이러한 성분을 추가하면 복합체 응집을 방지하고, 순환 수명을 늘리고 표적 조직에 지질-핵산 약학 조성물을 전달하는 수단을 제공할 수 있다(Klibanov et al. FEBS Letters 268(1):235-7. 1990). 이러한 성분은 생체 내에서 약학 조성물 밖으로 빠르게 교환되도록 선택될 수 있다(예를 들어, 미국 특허 제5,885,613호 참조).
고려되는 PEG화된 지질은 C6-C20(예를 들어, C8, C10, C12, C14, C16, 또는 C18) 길이의 알킬 사슬(들)을 갖는 지질에 공유적으로 부착된 최대 5 kDa 길이의 폴리에틸렌 글리콜(PEG) 사슬, 예컨대 유도체화된 세라마이드(예를 들어, N-옥타노일-스핑고신-1-[숙시닐(메톡시폴리에틸렌 글리콜)](C8 PEG 세라마이드))를 포함하지만, 이에 제한되지 않는다. 일부 실시양태에서, PEG화된 지질은 1,2-디미리스토일-rac-글리세로-3-메톡시폴리에틸렌 글리콜(DMG-PEG); 1,2-디스테아로일-sn-글리세로-3-포스포에탄올아민-폴리에틸렌 글리콜(DSPE-PEG); 1,2-디라우로일-sn-글리세로-3-포스포에탄올아민-폴리에틸렌 글리콜(DLPE-PEG); 또는 1,2-디스테아로일-rac-글리세로-폴리에틸렌 글리콜(DSG-PEG), PEG-DAG; PEG-PE; PEG-S-DAG; PEG-S-DMG; PEG-cer; PEG-디알키옥시프로필카바메이트; 2-[(폴리에틸렌 글리콜)-2000]-N,N-디테트라데실아세트아미드(ALC-0159); 및 이들의 조합이다.
특정 실시양태에서, PEG는 고분자량, 예를 들어 2000-2400 g/mol을 갖는다. 특정 실시양태에서, PEG는 PEG2000(또는 PEG-2K)이다. 특정 실시양태에서, 본원의 PEG화된 지질은 DMG-PEG2000, DSPE-PEG2000, DLPE-PEG2000, DSG-PEG2000, C8 PEG2000, 또는 ALC-0159(2-[(폴리에틸렌 글리콜)-2000]-N,N-디테트라데실아세트아미드)이다. 특정 실시양태에서, 본원의 PEG화된 지질은 DMG-PEG2000이다.
iii. 콜레스테롤 기반 지질
콜레스테롤 성분은 나노입자 내의 지질 이중층 구조에 안정성을 제공한다. 일부 실시양태에서, LNP는 하나 이상의 콜레스테롤 기반 지질을 포함한다. 적합한 콜레스테롤 기반 지질은 예를 들어 다음을 포함한다: DC-Choi(N,N-디메틸-N-에틸카복사미도콜레스테롤), 1,4-비스(3-N-올레일아미노-프로필)피페라진(Gao et al., Biochem Biophys Res Comm. (1991) 179:280; Wolf et al., BioTechniques (1997) 23:139; 미국 특허 제5,744,335호), 이미다졸 콜레스테롤 에스테르("ICE"; WO2011/068810), 시토스테롤(22,23-디하이드로스티그마스테롤), β-시토스테롤, 시토스타놀, 푸코스테롤, 스티그마스테롤(스티그마스타-5,22-디엔-3-올), 에르고스테롤; 데스모스테롤(3β-하이드록시-5,24-콜레스타디엔); 라노스테롤(8,24-라노스타디엔-3b-올); 7-디하이드로콜레스테롤(Δ5,7-콜레스테롤); 디하이드로라노스테롤(24,25-디하이드로라노스테롤); 지모스테롤(5α-콜레스타-8,24-디엔-3β-올); 라토스테롤(5α-콜레스트-7-엔-3β-올); 디오스게닌((3β,25R)-스피로스트-5-엔-3-올); 캄페스테롤(캄페스트-5-엔-3β-올); 캄페스타놀(5a-캄페스탄-3b-올); 24-메틸렌 콜레스테롤(5,24(28)-콜레스타디엔-24-메틸렌-3β-올); 콜레스테릴 마가레이트(콜레스트-5-엔-3β-일 헵타데카노에이트); 콜레스테릴 올레에이트; 콜레스테릴 스테아레이트 및 기타 변형된 형태의 콜레스테롤. 일부 실시양태에서, LNP에 사용된 콜레스테롤 기반 지질은 콜레스테롤이다.
iv. 헬퍼 지질
헬퍼 지질은 LNP의 구조적 안정성을 향상시키고 엔도솜 탈출 시 LNP를 돕는다. 이는 mRNA 약물 페이로드의 흡수 및 방출을 개선한다. 일부 실시양태에서, 헬퍼 지질은 약물 페이로드의 흡수 및 방출을 향상시키기 위한 융합생성 특성을 갖는 양쪽이온성 지질이다. 헬퍼 지질의 예는 1,2-디올레오일-SN-글리세로-3-포스포에탄올아민(DOPE); 1,2-디스테아로일-sn-글리세로-3-포스포콜린(DSPC); 1,2-디올레오일-sn-글리세로-3-포스포-L-세린(DOPS); 1,2-디엘라이도일-sn-글리세로-3-포스포에탄올아민(DEPE); 및 1,2-디올레오일-sn-글리세로-3-포스포콜린(DPOC), 디팔미토일포스파티딜콜린(DPPC), DMPC, 1,2-디라우로일-sn-글리세로-3-포스포콜린(DLPC), 1,2-디스테아로일포스파티딜에탄올아민(DSPE), 및 1,2-디라우로일-sn-글리세로-3-포스포에탄올아민(DLPE)이다.
다른 예시적인 헬퍼 지질은 디올레오일포스파티딜콜린(DOPC), 디올레오일포스파티딜글리세롤(DOPG), 디팔미토일포스파티딜글리세롤(DPPG), 팔미토일올레오일포스파티딜콜린(POPC), 팔미토일올레오일-포스파티딜에탄올아민(POPE), 디올레오일-포스파티딜에탄올아민 4-(N-말레이미도메틸)-사이클로헥산-1-카복실레이트(DOPE-mal), 디팔미토일 포스파티딜 에탄올아민(DPPE), 디미리스토일포스포에탄올아민(DMPE), 포스파티딜세린, 스핑고지질, 스핑고미엘린, 세라마이드, 세레브로사이드, 갱글리오사이드, 16-O-모노메틸 PE, 16-O-디메틸 PE, 18-1-트랜스 PE, l-스테아로일-2-올레오일-포스파티딜에탄올아민(SOPE), 또는 이들의 조합이다. 특정 실시양태에서, 헬퍼 지질은 DOPE이다. 특정 실시양태에서, 헬퍼 지질은 DSPC이다.
다양한 실시양태에서, 본 LNP는 (i) OF-02, cKK-E10, GL-HEPES-E3-E10-DS-3-E18-1, GL-HEPES-E3-E12-DS-4-E10, 또는 GL-HEPES-E3-E12-DS-3-E14로부터 선택된 양이온성 지질; (ii) DMG-PEG2000; (iii) 콜레스테롤; 및 (iv) DOPE를 포함한다.
다른 실시양태에서, 본 LNP는 (i) SM-102; (ii) DMG-PEG2000; (iii) 콜레스테롤; 및 (iv) DSPC를 포함한다.
또 다른 실시양태에서, 본 LNP는 (i) ALC-0315; (ii) ALC-0159; (iii) 콜레스테롤; 및 (iv) DSPC를 포함한다.
v. 지질 성분의 몰 비율
상기 성분의 몰 비율은 mRNA를 전달하는 데에 있어 LNP의 효과에 중요하다. 양이온성 지질, PEG화된 지질, 콜레스테롤 기반 지질, 및 헬퍼 지질의 몰 비율은 A: B: C: D이고, 여기서 A + B + C + D = 100%이다. 일부 실시양태에서, 총 지질에 대한 LNP의 양이온성 지질의 몰 비율(즉, A)은 35-55%, 예컨대 35-50%(예를 들어, 38-42%, 예컨대 40%, 또는 45-50%)이다. 일부 실시양태에서, 총 지질에 대한 PEG화된 지질 성분의 몰 비율(즉, B)은 0.25-2.75%(예를 들어, 1-2%, 예컨대 1.5%)이다. 일부 실시양태에서, 총 지질에 대한 콜레스테롤 기반 지질의 몰 비율(즉, C)은 20-50%(예를 들어, 27-30%, 예컨대 28.5%, 또는 38-43%)이다. 일부 실시양태에서, 총 지질에 대한 헬퍼 지질의 몰 비율(즉, D)은 5-35%(예를 들어, 28-32%, 예컨대 30%, 또는 8-12%, 예컨대 10%)이다. 일부 실시양태에서, (PEG화 지질 + 콜레스테롤) 성분은 헬퍼 지질과 동일한 몰량을 갖는다. 일부 실시양태에서, LNP는 1 초과의 양이온성 지질 대 헬퍼 지질의 몰 비율을 함유한다.
특정 실시양태에서, 본 개시 내용의 LNP는 다음을 포함한다: 35% 내지 55% 또는 40% 내지 50%의 몰 비율의 양이온성 지질(예를 들어, 35%, 36%, 37%, 38%, 39%, 40%, 41% 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 또는 55%의 몰 비율의 양이온성 지질); 0.25% 내지 2.75% 또는 1.00% 내지 2.00%의 몰 비율의 폴리에틸렌 글리콜(PEG)이 접합된(PEG화된) 지질(예를 들어, 0.25%, 0.50%, 0.75%, 1.00%, 1.25%, 1.50%, 1.75%, 2.00%, 2.25%, 2.50%, 또는 2.75%의 몰 비율의 PEG화된 지질); 20% 내지 50%, 25% 내지 45%, 또는 28.5% 내지 43%의 콜레스테롤 기반 지질(예를 들어, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41% 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 또는 50%의 몰 비율의 콜레스테롤 기반 지질); 및 5% 내지 35%, 8% 내지 30%, 또는 10% 내지 30%의 몰 비율의 헬퍼 지질(예를 들어, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 또는 35%의 몰 비율의 헬퍼 지질), 여기서 모든 몰 비율은 LNP의 총 지질 함량에 상대적인 것임.
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 양이온성 지질; 1.5%의 몰 비율의 PEG화된 지질; 28.5%의 몰 비율의 콜레스테롤 기반 지질; 및 30%의 몰 비율의 헬퍼 지질.
특정 실시양태에서, 본 개시 내용의 LNP는 다음을 포함한다: 45% 내지 50%의 몰 비율의 양이온성 지질; 1.5% 내지 1.7%의 몰 비율의 PEG화된 지질; 38% 내지 43%의 몰 비율의 콜레스테롤 기반 지질; 및 9% 내지 10%의 몰 비율의 헬퍼 지질.
특정 실시양태에서, PEG화된 지질은 디미리스토일-PEG2000(DMG-PEG2000)이다.
다양한 실시양태에서, 콜레스테롤 기반 지질은 콜레스테롤이다.
일부 실시양태에서, 헬퍼 지질은 1,2-디올레오일-SN-글리세로-3-포스포에탄올아민(DOPE)이다.
특정 실시양태에서, LNP는 다음을 포함한다: 35% 내지 55%의 몰 비율의 OF-02; 0.25% 내지 2.75%의 몰 비율의 DMG-PEG2000; 20% 내지 50%의 몰 비율의 콜레스테롤; 및 5% 내지 35%의 몰 비율의 DOPE.
특정 실시양태에서, LNP는 다음을 포함한다: 35% 내지 55%의 몰 비율의 cKK-E10; 0.25% 내지 2.75%의 몰 비율의 DMG-PEG2000; 20% 내지 50%의 몰 비율의 콜레스테롤; 및 5% 내지 35%의 몰 비율의 DOPE.
특정 실시양태에서, LNP는 다음을 포함한다: 35% 내지 55%의 몰 비율의 GL-HEPES-E3-E10-DS-3-E18-1; 0.25% 내지 2.75%의 몰 비율의 DMG-PEG2000; 20% 내지 50%의 몰 비율의 콜레스테롤; 및 5% 내지 35%의 몰 비율의 DOPE.
특정 실시양태에서, LNP는 다음을 포함한다: 35% 내지 55%의 몰 비율의 GL-HEPES-E3-E12-DS-4-E10; 0.25% 내지 2.75%의 몰 비율의 DMG-PEG2000; 20% 내지 50%의 몰 비율의 콜레스테롤; 및 5% 내지 35%의 몰 비율의 DOPE.
특정 실시양태에서, LNP는 다음을 포함한다: 35% 내지 55%의 몰 비율의 GL-HEPES-E3-E12-DS-3-E14; 0.25% 내지 2.75%의 몰 비율의 DMG-PEG2000; 20% 내지 50%의 몰 비율의 콜레스테롤; 및 5% 내지 35%의 몰 비율의 DOPE.
특정 실시양태에서, LNP는 다음을 포함한다: 35% 내지 55%의 몰 비율의 SM-102; 0.25% 내지 2.75%의 몰 비율의 DMG-PEG2000; 20% 내지 50%의 몰 비율의 콜레스테롤; 및 5% 내지 35%의 몰 비율의 DSPC.
특정 실시양태에서, LNP는 다음을 포함한다: 35% 내지 55%의 몰 비율의 ALC-0315; 0.25% 내지 2.75%의 몰 비율의 ALC-0159; 20% 내지 50%의 몰 비율의 콜레스테롤; 및 5% 내지 35%의 몰 비율의 DSPC.
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 OF-02; 1.5%의 몰 비율의 DMG-PEG2000; 28.5%의 몰 비율의 콜레스테롤; 및 30%의 몰 비율의 DOPE. 이 LNP 제제는 본원에서 "지질 A"로 명명된다.
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 cKK-E10; 1.5%의 몰 비율의 DMG-PEG2000; 28.5%의 몰 비율의 콜레스테롤; 및 30%의 몰 비율의 DOPE. 이 LNP 제제는 본원에서 "지질 B"로 명명된다.
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 GL-HEPES-E3-E10-DS-3-E18-1; 1.5%의 몰 비율의 DMG-PEG2000; 28.5%의 몰 비율의 콜레스테롤; 및 30%의 몰 비율의 DOPE. 이 LNP 제제는 본원에서 "지질 C"로 명명된다.
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 GL-HEPES-E3-E12-DS-4-E10; 1.5%의 몰 비율의 DMG-PEG2000; 28.5%의 몰 비율의 콜레스테롤; 및 30%의 몰 비율의 DOPE. 이 LNP 제제는 본원에서 "지질 D"로 명명된다.
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 GL-HEPES-E3-E12-DS-3-E14; 1.5%의 몰 비율의 DMG-PEG2000; 28.5%의 몰 비율의 콜레스테롤; 및 30%의 몰 비율의 DOPE. 이 LNP 제제는 본원에서 "지질 E"로 명명된다.
특정 실시양태에서, LNP는 다음을 포함한다: 50%의 몰 비율의 DLin-MC3-DMA(MC3); 1.5%의 몰 비율의 DMG-PEG2000; 38.5%의 몰 비율의 콜레스테롤; 및 10%의 몰 비율의 DSPC. 이 LNP 제제는 본원에서 "지질 F"로 명명된다.
특정 실시양태에서, LNP는 다음을 포함한다: 50%의 몰 비율의 9-헵타데카닐 8-{(2-하이드록시에틸)[6-옥소-6-(운데실옥시)헥실]아미노}옥타노에이트(SM-102); 10%의 몰 비율의 1,2-디스테아로일-sn-글리세로-3-포스포콜린(DSPC); 38.5%의 몰 비율의 콜레스테롤; 및 1.5%의 몰 비율의 1,2-디미리스토일-rac-글리세로-3-메톡시폴리에틸렌 글리콜-2000(DMG-PEG2000).
특정 실시양태에서, LNP는 다음을 포함한다: 46.3%의 몰 비율의 (4-하이드록시부틸)아잔디일]디(헥산-6,1-디일) 비스(2-헥실데카노에이트)(ALC-0315); 9.4%의 몰 비율의 1,2-디스테아로일-sn-글리세로-3-포스포콜린(DSPC); 42.7%의 몰 비율의 콜레스테롤; 및 1.6%의 몰 비율의 2-[(폴리에틸렌 글리콜)-2000]-N,N-디테트라데실아세트아미드(ALC-0159).
특정 실시양태에서, LNP는 다음을 포함한다: 47.4%의 몰 비율의 (4-하이드록시부틸)아잔디일]디(헥산-6,1-디일) 비스(2-헥실데카노에이트)(ALC-0315); 10%의 몰 비율의 1,2-디스테아로일-sn-글리세로-3-포스포콜린(DSPC); 40.9%의 몰 비율의 콜레스테롤; 및 1.7%의 몰 비율의 2-[(폴리에틸렌 글리콜)-2000]-N,N-디테트라데실아세트아미드(ALC-0159).
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 IM-001; 1.5%의 몰 비율의 DMG-PEG2000; 28.5%의 몰 비율의 콜레스테롤; 및 30%의 몰 비율의 DOPE.
특정 실시양태에서, LNP는 다음을 포함한다: 40%의 몰 비율의 IS-001; 1.5%의 몰 비율의 DMG-PEG2000; 28.5%의 몰 비율의 콜레스테롤; 및 30%의 몰 비율의 DOPE.
일부 실시양태에서, LNP 제제는 "지질 A", "지질 B" 또는 "지질 D"에 대해 정의된 바와 같다.
LNP 제제에 넣을 각 지질의 실제 양을 계산하기 위해, 먼저 양이온성 지질의 몰량을 원하는 N/P 비율에 따라 결정하며, 여기서 N은 양이온성 지질의 질소 원자 수이고 P는 LNP에 의해 운반될 mRNA의 인산기 수이다. 다음으로, 다른 각 지질의 몰량을 양이온성 지질의 몰량과 선택된 몰 비율을 기반으로 계산한다. 그런 다음 이러한 몰량을 각 지질의 분자량을 사용하여 중량으로 변환한다.
vi. LNP 내의 핵산
본원에서 기술된 LNP 조성물은 본 개시 내용의 핵산(예를 들어, mRNA)을 포함할 수 있다.
원하는 경우, LNP는 다가일 수 있다. 일부 실시양태에서, LNP는 본 개시 내용의 하나 초과의 폴리펩티드, 예컨대 2, 3, 4, 5, 6, 7, 또는 8개의 폴리펩티드를 코딩하는 핵산(예컨대 mRNA)을 운반할 수 있다. 예를 들어, LNP는 각각이 본 개시 내용의 상이한 폴리펩티드를 코딩하는 본 개시 내용의 여러 핵산(예를 들어, mRNA)을 운반할 수 있거나; 하나 초과의 본 개시 내용의 폴리펩티드로 번역될 수 있는 폴리시스트론 mRNA를 운반할 수 있다(예를 들어, 각 항원-코딩 서열은 2A 펩티드와 같은 자가 절단 펩티드를 코딩하는 뉴클레오티드 링커에 의해 분리됨). 상이한 핵산(예를 들어, mRNA)을 운반하는 LNP는 일반적으로 각 핵산의 여러 복사본을 포함(캡슐화)한다. 예를 들어, 두 개의 상이한 핵산을 운반하거나 캡슐화하는 LNP는 일반적으로 두 개의 상이한 핵산 각각의 여러 복사본을 운반한다.
일부 실시양태에서, 단일 LNP 제제는 여러 종류(예를 들어, 2, 3, 4, 5, 6, 7, 8, 9, 10개 이상)의 LNP를 포함할 수 있으며, 각 종류는 상이한 핵산(예를 들어, mRNA)을 운반한다.
핵산이 mRNA인 경우, mRNA는 변형되지 않을 수 있거나(즉, 인산디에스테르 결합으로 연결된 천연 리보뉴클레오티드 A, U, C, 및/또는 G만 함유), 화학적으로 변형될 수 있다(예를 들어, 슈도우리딘(예를 들어, N-1-메틸 슈도우리딘), 2'-플루오로 리보뉴클레오티드, 및 2'-메톡시 리보뉴클레오티드와 같은 뉴클레오티드 유사체, 및/또는 포스포로티오에이트 결합 포함). mRNA 분자는 5' 캡과 폴리A 꼬리를 포함할 수 있다.
vii. 완충액 및 기타 성분
핵산 및/또는 LNP를 안정화하기 위해(예를 들어, 백신 제품의 유통기한을 연장하기 위해), LNP 약학 조성물의 투여를 용이하게 하기 위해, 및/또는 핵산의 생체 내 발현을 향상시키기 위해, 핵산 및/또는 LNP는 하나 이상의 담체, 표적화 리간드, 안정화 시약(예를 들어, 방부제 및 산화방지제), 및/또는 기타 약학적으로 허용 가능한 부형제와 조합하여 제제화될 수 있다. 이러한 부형제의 예로는 파라벤, 티메로살, 티오머살, 클로로부탄올, 벤잘코늄 클로라이드, 및 킬레이트제(예를 들어, EDTA)가 있다.
본 개시 내용의 LNP 조성물은 동결된 액체 형태 또는 동결건조 형태로 제공될 수 있다. 다양한 냉동 보호제를 사용할 수 있으며, 여기에는 제한 없이, 수크로스, 트레할로스, 글루코스, 만니톨, 만노스, 덱스트로스 등이 포함된다. 냉동 보호제는 LNP 조성물의 5-30%(w/v)를 구성할 수 있다. 일부 실시양태에서, LNP 조성물은 트레할로스를 예를 들어, 5-30%(예를 들어, 10%)(w/v) 포함한다. 냉동 보호제로 제제화된 후, LNP 조성물은 -20℃ 내지 -80℃에서 동결(또는 동결 건조 및 동결 보존)될 수 있다.
LNP 조성물은 환자에게 수성 완충 용액으로 제공될 수 있다(이전에 동결된 경우 해동하거나, 이전에 동결 건조된 경우 병실에서 수성 완충 용액으로 재구성). 완충 용액은 바람직하게는 등장성이고 예를 들어 근육 내 또는 피내 주사에 적합하다. 일부 실시양태에서, 완충 용액은 인산 완충 식염수(PBS)이다.
viii. 본 발명의 LNP 조성물의 제조 방법
본 발명의 LNP는 현재 기술 분야에 공지된 다양한 기술에 의해 제조될 수 있다. 예를 들어, 다층 소포(MLV)는 적절한 용매에 지질을 용해시켜 적합한 용기 또는 통의 내벽에 선택된 지질을 침적시킨 다음 용매를 증발시켜 용기의 내부에 얇은 필름을 남기거나 분무 건조시키는 것과 같은 통상적인 기술에 따라 제조될 수 있다. 그런 다음 수성 상을 와류 운동과 함께 용기에 첨가하여 MLV를 형성할 수 있다. 그런 다음 다층 소포의 균질화, 초음파 처리, 또는 압출을 통해 단층 소포(ULV)를 형성할 수 있다. 또한, 단층 소포는 세제 제거 기술에 의해 형성할 수 있다.
다양한 방법이 US 2011/0244026, US 2016/0038432, US 2018/0153822, US 2018/0125989, 및 PCT/US2020/043223(2020년 7월 23일 출원)에 기술되어 있으며, 본 개시 내용을 실시하는 데 사용될 수 있다. 한 가지 예시적인 공정은 US 2016/0038432에 기술된 바와 같이 먼저 지질을 지질 나노입자로 미리 형성하지 않고, mRNA를 지질 혼합물과 혼합하여 mRNA를 캡슐화하는 단계를 수반한다. 또 다른 예시적인 공정은 US 2018/0153822에 기술된 바와 같이 미리 형성된 LNP를 mRNA와 혼합하여 mRNA를 캡슐화하는 단계를 수반한다.
일부 실시양태에서, mRNA가 로딩된 LNP를 제조하는 공정은 하나 이상의 용액을 주변 온도보다 높은 온도로 가열하는 단계를 포함하며, 하나 이상의 용액은 미리 형성된 지질 나노입자를 포함하는 용액, mRNA를 포함하는 용액 및 LNP-캡슐화된 mRNA를 포함하는 혼합 용액이다. 일부 실시양태에서, 공정은 혼합 단계 전에 mRNA 용액과 미리 형성된 LNP 용액 중 하나 또는 둘 다를 가열하는 단계를 포함한다. 일부 실시양태에서, 공정은 혼합 단계 동안 미리 형성된 LNP를 포함하는 용액, mRNA를 포함하는 용액 및 LNP-캡슐화된 mRNA를 포함하는 용액 중 하나 이상을 가열하는 단계를 포함한다. 일부 실시양태에서, 공정은 혼합 단계 후에 LNP-캡슐화된 mRNA를 가열하는 단계를 포함한다. 일부 실시양태에서, 하나 이상의 용액이 가열되는 온도는 약 30℃, 37℃, 40℃, 45℃, 50℃, 55℃, 60℃, 65℃, 또는 70℃이거나 그보다 높다. 일부 실시양태에서, 하나 이상의 용액이 가열되는 온도는 약 25-70℃, 약 30-70℃, 약 35-70℃, 약 40-70℃, 약 45-70℃, 약 50-70℃, 또는 약 60-70℃의 범위이다. 일부 실시양태에서, 온도는 약 65℃이다.
다양한 방법을 사용하여 본 개시 내용에 적합한 mRNA 용액을 제조할 수 있다. 일부 실시양태에서, mRNA는 본원에서 기술된 완충 용액에 직접 용해할 수 있다. 일부 실시양태에서, mRNA 용액은 캡슐화를 위해 지질 용액과 혼합하기 전에 mRNA 스톡 용액을 완충 용액과 혼합하여 생성할 수 있다. 일부 실시양태에서, mRNA 용액은 캡슐화를 위해 지질 용액과 혼합하기 직전에 mRNA 스톡 용액을 완충 용액과 혼합하여 생성할 수 있다. 일부 실시양태에서, 적합한 mRNA 스톡 용액은 약 0.2 mg/ml, 0.4 mg/ml, 0.5 mg/ml, 0.6 mg/ml, 0.8 mg/ml, 1.0 mg/ml, 1.2 mg/ml, 1.4 mg/ml, 1.5 mg/ml, 또는 1.6 mg/ml, 2.0 mg/ml, 2.5 mg/ml, 3.0 mg/ml, 3.5 mg/ml, 4.0 mg/ml, 4.5 mg/ml, 또는 5.0 mg/ml 이상의 농도로 물 또는 완충액에 mRNA를 함유할 수 있다.
일부 실시양태에서, mRNA 스톡 용액은 펌프를 사용하여 완충 용액과 혼합한다. 예시적인 펌프는 기어 펌프, 연동 펌프 및 원심 펌프를 포함하지만 이에 제한되지 않는다. 일반적으로, 완충 용액은 mRNA 스톡 용액의 속도보다 더 빠른 속도로 혼합된다. 예를 들어, 완충 용액은 mRNA 스톡 용액의 속도보다 적어도 1x, 2x, 3x, 4x, 5x, 6x, 7x, 8x, 9x, 10x, 15x, 또는 20x 더 빠른 속도로 혼합될 수 있다. 일부 실시양태에서, 완충 용액은 약 100-6000 ml/분(예를 들어, 약 100-300 ml/분, 300-600 ml/분, 600-1200 ml/분, 1200-2400 ml/분, 2400-3600 ml/분, 3600-4800 ml/분, 4800-6000 ml/분, 또는 60-420 ml/분)의 범위의 유속으로 혼합된다. 일부 실시양태에서, 완충액은 약 60 ml/분, 100 ml/분, 140 ml/분, 180 ml/분, 220 ml/분, 260 ml/분, 300 ml/분, 340 ml/분, 380 ml/분, 420 ml/분, 480 ml/분, 540 ml/분, 600 ml/분, 1200 ml/분, 2400 ml/분, 3600 ml/분, 4800 ml/분, 또는 6000 ml/분 이상의 유속으로 혼합된다.
일부 실시양태에서, mRNA 스톡 용액은 약 10-600 ml/분(예를 들어, 약 5-50 ml/분, 약 10-30 ml/분, 약 30-60 ml/분, 약 60-120 ml/분, 약 120-240 ml/분, 약 240-360 ml/분, 약 360-480 ml/분, 또는 약 480-600 ml/분)의 범위의 유속으로 혼합된다. 일부 실시양태에서, mRNA 스톡 용액은 약 5 ml/분, 10 ml/분, 15 ml/분, 20 ml/분, 25 ml/분, 30 ml/분, 35 ml/분, 40 ml/분, 45 ml/분, 50 ml/분, 60 ml/분, 80 ml/분, 100 ml/분, 200 ml/분, 300 ml/분, 400 ml/분, 500 ml/분, 또는 600ml/분 이상의 유속으로 혼합된다.
원하는 mRNA를 지질 나노입자에 통합하는 과정을 "로딩"이라고 한다. 예시적 방법은 문헌 [Lasic et al., FEBS Lett . (1992) 312:255-8]에 기술되어 있다. LNP 통합된 핵산은 지질 나노입자의 내부 공간, 지질 나노입자의 이중층 막 내에 완전히 또는 부분적으로 위치하거나, 지질 나노입자 막의 외부 표면과 연관될 수 있다. mRNA를 지질 나노입자에 통합하는 것은 또한 본원에서 "캡슐화"로 지칭되며, 여기서 핵산은 지질 나노입자의 내부 공간 내에 완전히 또는 실질적으로 함유된다.
적합한 LNP는 다양한 크기로 만들어질 수 있다. 일부 실시양태에서, 지질 나노입자의 크기가 감소하면 mRNA가 더 효율적으로 전달된다. 적절한 LNP 크기를 선택할 때는 표적 세포 또는 조직의 위치와 어느 정도 지질 나노입자가 만들어지는 용도를 고려할 수 있다.
지질 나노입자 집단의 크기를 측정하기 위해 해당 기술 분야에 알려진 다양한 방법을 사용할 수 있다. 본원에서 선호하는 방법은 LNP 입자 크기를 측정하기 위해 Zetasizer Nano ZS(Malvern Panalytical)를 사용한다. 한 프로토콜에서, 10 ㎕의 LNP 샘플을 990 ㎕의 10% 트레할로스와 혼합한다. 이 용액을 큐벳에 넣은 다음 Zetasizer 기계에 넣는다. z-평균 직경(nm), 또는 누적 평균을 샘플의 LNP에 대한 평균 크기로 간주한다. Zetasizer 기계는 동적 광산란(DLS) 및 자기상관 함수의 누적 분석을 사용하여 다분산 지수(PDI)를 측정하는 데에도 사용할 수 있다. 평균 LNP 직경은 형성된 LNP의 초음파 처리로 줄일 수 있다. 간헐적 초음파 처리 주기를 준탄성 광산란(QELS) 평가와 번갈아 가며 효율적인 지질 나노입자 합성을 안내할 수 있다.
일부 실시양태에서, 정제된 LNP의 대부분, 즉 LNP의 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 또는 99% 초과는 약 70-150 nm(예를 들어, 약 145 nm, 약 140 nm, 약 135 nm, 약 130 nm, 약 125 nm, 약 120 nm, 약 115 nm, 약 110 nm, 약 105 nm, 약 100 nm, 약 95 nm, 약 90 nm, 약 85 nm, 또는 약 80 nm)의 크기를 갖는다. 일부 실시양태에서, 정제된 지질 나노입자의 실질적으로 전부(예를 들어, 80% 또는 90% 초과)는 약 70-150 nm(예를 들어, 약 145 nm, 약 140 nm, 약 135 nm, 약 130 nm, 약 125 nm, 약 120 nm, 약 115 nm, 약 110 nm, 약 105 nm, 약 100 nm, 약 95 nm, 약 90 nm, 약 85 nm, 또는 약 80 nm)의 크기를 갖는다.
일부 실시양태에서, 본 조성물 내 LNP는 150 nm 미만, 120 nm 미만, 100 nm 미만, 90 nm 미만, 80 nm 미만, 70 nm 미만, 60 nm 미만, 50 nm 미만, 30 nm 미만, 또는 20 nm 미만의 평균 크기를 갖는다.
일부 실시양태에서, 본 조성물 내 LNP 중 약 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% 초과가 약 40-90 nm(예를 들어, 약 45-85 nm, 약 50-80 nm, 약 55-75 nm, 약 60-70 nm) 또는 약 50-70 nm(예를 들어, 55-65 nm)의 범위의 크기를 갖는 것이 분무를 통한 폐 전달에 특히 적합하다.
일부 실시양태에서, 본 개시 내용에 의해 제공되는 약학 조성물 내 LNP의 분산도, 또는 분자 크기의 이질성의 척도(PDI)는 약 0.5 미만이다. 일부 실시양태에서, LNP는 약 0.5 미만, 약 0.4 미만, 약 0.3 미만, 약 0.28 미만, 약 0.25 미만, 약 0.23 미만, 약 0.20 미만, 약 0.18 미만, 약 0.16 미만, 약 0.14 미만, 약 0.12 미만, 약 0.10 미만, 또는 약 0.08 미만의 PDI를 갖는다. PDI는 상기 기술된 바와 같이 Zetasizer 기계로 측정할 수 있다.
일부 실시양태에서, 본원에서 제공되는 약학 조성물 내 정제된 LNP의 약 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 또는 99% 초과가 각 개별 입자 내에 mRNA를 캡슐화한다. 일부 실시양태에서, 약학 조성물 내 정제된 지질 나노입자의 실질적으로 전부(예를 들어, 80% 또는 90% 초과)가 각 개별 입자 내에 mRNA를 캡슐화한다. 일부 실시양태에서, 지질 나노입자는 50% 내지 99%; 또는 약 60, 65, 70, 75, 80, 85, 90, 92, 95, 98, 또는 99% 초과의 캡슐화 효율을 갖는다. 일반적으로, 본원에서 사용하기 위한 지질 나노입자는 적어도 90%(예를 들어, 적어도 91, 92, 93, 94, 또는 95%)의 캡슐화 효율을 갖는다.
일부 실시양태에서, LNP는 1과 10 사이의 N/P 비율을 갖는다. 일부 실시양태에서, 지질 나노입자는 1, 약 1, 약 2, 약 3, 약 4, 약 5, 약 6, 약 7, 또는 약 8보다 큰 N/P 비율을 갖는다. 추가 실시양태에서, 본원에서 전형적인 LNP는 4의 N/P 비율을 갖는다.
일부 실시양태에서, 본 개시 내용에 따른 약학 조성물은 적어도 약 0.5 ㎍, 1 ㎍, 5 ㎍, 10 ㎍, 100 ㎍, 500 ㎍, 또는 1000 ㎍의 캡슐화된 mRNA를 함유한다. 일부 실시양태에서, 약학 조성물은 약 0.1 ㎍ 내지 1000 ㎍, 적어도 약 0.5 ㎍, 적어도 약 0.8 ㎍, 적어도 약 1 ㎍, 적어도 약 5 ㎍, 적어도 약 8 ㎍, 적어도 약 10 ㎍, 적어도 약 50 ㎍, 적어도 약 100 ㎍, 적어도 약 500 ㎍, 또는 적어도 약 1000 ㎍의 캡슐화된 mRNA를 함유한다.
일부 실시양태에서, mRNA는 화학 합성 또는 DNA 주형의 시험관 내 전사(IVT)에 의해 만들 수 있다. mRNA를 만들고 정제하는 예시적인 공정은 실시예 1에 기술되어 있다. 이 공정에서, IVT 공정에서, cDNA 주형을 사용하여 mRNA 전사체를 생성하고 DNA 주형은 DNase에 의해 분해한다. 전사체는 심층 여과 및 접선 유동 여과(TFF)에 의해 정제한다. 정제된 전사체는 캡과 꼬리를 추가하여 더 변형시키고, 변형된 RNA는 심층 여과 및 TFF에 의해 다시 정제한다.
그런 다음 mRNA는 수성 완충액에 제조하고 LNP의 지질 성분을 함유하는 양친매성 용액과 혼합한다. LNP의 네 가지 지질 성분을 용해시키기 위한 양친매성 용액은 알코올 용액일 수 있다. 일부 실시양태에서, 알코올은 에탄올이다. 수성 완충액은 예를 들어, 시트르산염, 인산염, 아세트산염, 또는 숙신산염 완충액일 수 있으며, 약 3.0-7.0, 예를 들어, 약 3.5, 약 4.0, 약 4.5, 약 5.0, 약 5.5, 약 6.0, 또는 약 6.5의 pH를 가질 수 있다. 완충액은 염(예를 들어, 나트륨, 칼륨, 및/또는 칼슘 염)과 같은 다른 성분을 함유할 수 있다. 특정 실시양태에서, 수성 완충액은 1 mM 시트르산염, 150 mM NaCl, pH 3.5 또는 4.5를 갖는다.
mRNA-LNP 조성물을 제조하는 예시적이고 비제한적인 공정은 실시예 1에 기술되어 있다. 이 공정은 완충된 mRNA 용액을 에탄올 중 지질 용액과 제어된 균질 방식으로 혼합하는 단계를 포함하며, 여기서 지질:mRNA의 비율은 혼합 공정 전체에 걸쳐 유지된다. 이 설명적 예에서, mRNA는 시트르산 일수화물, 시트르산 삼나트륨 이수화물, 및 염화나트륨을 함유하는 수성 완충액에 제공된다. mRNA 용액을 용액(1 mM 시트르산 완충액, 150 mM NaCl, pH 4.5)에 첨가한다. 4가지 지질(예를 들어, 양이온성 지질, PEG화 지질, 콜레스테롤 기반 지질, 및 헬퍼 지질)의 지질 혼합물을 에탄올에 용해시킨다. 수성 mRNA 용액과 에탄올 지질 용액을 거의 "펄스 없는" 펌프 시스템이 구비된 "T" 믹서에서 4:1의 부피 비율로 혼합한다. 그 후 생성된 혼합물은 하류 정제 및 완충액 교환을 거친다. 완충액 교환은 투석 카세트 또는 TFF 시스템을 사용하여 달성할 수 있다. TFF를 이용하여 T-mix 공정을 통해 형성된 직후 생성된 신생 LNP를 농축하고 완충액 교환할 수 있다. 투석여과 공정은 연속적인 작업으로, 투과액 흐름과 동일한 속도로 적절한 완충액을 추가하여 부피를 일정하게 유지한다.
H. 핵산 제제 및 보조제
본원에 개시된 핵산 백신, 프라이머, 및 부스터는 비경구 투여를 통한 전신 투여를 위해 제제화될 수 있다. 비경구 투여에는 정맥 내, 동맥 내, 피하, 피내, 복강 내, 또는 근육 내 주사 또는 주입이 포함된다. 비경구 투여를 위한 제제에는 멸균 수용액이 포함될 수 있으며, 여기에는 완충제, 희석제 및 숙련된 기술자에게 알려진 기타 약학적으로 허용 가능한 첨가제도 함유될 수 있다. 정맥 내 용도의 경우, 제제를 등장성으로 만들기 위해 용질의 총 농도를 조절할 수 있다. 정맥 내, 동맥 내, 피하, 또는 근육 내 주사가 바람직한 투여 경로이다. 추가적으로 또는 대안적으로, 개시된 백신은 비강 내 투여 또는 다른 점막과의 접촉을 위해 제제화될 수 있다.
주사용 핵산 제제는 단위 투여 형태, 예를 들어 앰플, 또는, 선택적으로 방부제가 첨가된, 다회 투여 용기에 제공될 수 있다. 제제는 유성 또는 수성 비히클에 현탁액, 용액 또는 에멀전과 같은 형태를 취할 수 있으며, 현탁화제, 안정화제 및/또는 분산제와 같은 제제화제를 함유할 수 있다. 제제는 임의의 적합한 약학적으로 허용 가능한 부형제를 포함할 수 있다.
일반적으로, 대상체에게 투여되는 핵산은 위에서 논의한 바와 같이 지질 나노입자와 같은 지질 조성물에 제제화된다.
I. 백신 보조제
개시된 면역원성 조성물(예를 들어, 본원에서 기술된 바와 같은 융합 단백질, 나노입자 또는 mRNA 분자(들)를 포함함)은 면역 반응을 개선하고 보호 반응을 촉진하기 위한 보조제를 포함할 수 있다. 보조제는 일부 백신에 사용되는 성분으로 백신을 접종받는 사람들에게 더 강력한 면역 반응을 생성하는 데 도움이 된다. 보조제는 신체가 백신 접종을 받고 있는 질병으로부터 개인을 보호할 수 있을 만큼 강력한 면역 반응을 생성하도록 돕는다.
본 개시 내용은 임의의 개시된 항원 및/또는 나노입자(또는 이들의 조합)와 ALFQ, 알히드로겔, 및 이들의 조합으로 이루어진 군으로부터 선택된 적어도 하나의 보조제를 함유하는 백신 제제를 제공한다.
보조제 ALFQ는 미국 육군에서 개발되었으며, QS21 사포닌(ALFQ)과 함께 높은 양의 콜레스테롤을 함유하는 ALF(Army-Liposome-Formulation)이다. ALFQ는 수많은 동물 연구에서 다양한 면역원과 함께 사용되었으며, 강력한 면역 반응을 유발하는 데 효과를 나타냈다. 일부 보조제와 달리, ALFQ는 백신 관련 호흡기 질환 강화증(VAERD)과 관련된 왜곡된 면역 반응을 피하면서 균형 잡힌 Th1/Th2 면역 반응을 유발하는 경향이 있다. 일부 실시양태에서, ALFQ 보조제는 모노포스포릴 지질 A(MPLA) 및 QS-21 사포닌을 함유하는 리포솜 제제이다. 일부 실시양태에서, ALFQ 리포솜은 약 600 ㎍/mL 모노포스포릴 3-데아실 지질 A(3D-PHAD) 및 약 300 ㎍/mL QS-21을 함유할 수 있다. ALFQ를 제조하기 위해, 한 가지 예시적인 실시양태에서, 14.7 mL의 ALF55(1.236 mg/ml 3D-PHAD 함유)를 멸균 유리 바이알에 6.5 mL의 등장성 Sorensen PBS pH 6.15로 희석할 수 있고, 희석된 ALF55에 9.08 mL의 QS-21(1 mg/ml)을 천천히 교반하면서 첨가할 수 있다.
알히드로겔은 인간 및 수의학 백신의 보조제로 사용하기 위해 특별히 개발된 다양한 수산화알루미늄 겔 제품을 지칭한다. 이 겔은 느슨한 응집물 내 보헤마이트 유사(옥시수산화 알루미늄) 수화된 나노/마이크론 크기 결정의 현탁액이다. 이 제품은 완충 이온이 없기 때문에 전도도가 매우 낮다. 이는 중성 pH에서 양전하를 띠고 음전하 항원을 효과적으로 흡착한다. 백신 내 보조제의 주요 목적은 항원에 대한 항체 매개(Th2) 면역 반응을 증가시키는 것이다. 알히드로겔 제품을 다른 보조제 유형(예를 들어, 모노포스포릴 지질)과 조합하여 균형 잡힌 Th1/Th2 면역 반응을 달성할 수 있다. 개시된 백신을 제제화하기 위해, 알히드로겔 스톡을 개시된 나노입자와 결합하기 전에 알루미늄의 농도가 약 500 ㎍/ml, 약 550 ㎍/ml, 약 600 ㎍/ml, 약 650 ㎍/ml, 약 700 ㎍/ml, 약 750 ㎍/ml, 약 800 ㎍/ml, 약 850 ㎍/ml, 약 900 ㎍/ml, 약 950 ㎍/ml, 약 1000 ㎍/ml, 약 1050 ㎍/ml, 약 1100 ㎍/ml, 약 1150 ㎍/ml, 약 1200 ㎍/ml, 약 1250 ㎍/ml, 약 1300 ㎍/ml, 약 1350 ㎍/ml, 약 1400 ㎍/ml, 약 1450 ㎍/ml, 또는 약 1500 ㎍/ml 이상이 되도록 희석할 수 있다.
다른 백신 보조제가 해당 기술 분야에 알려져 있으며, ALFQ 및 알히드로겔과 관련하여 본원에 보고된 결과를 기반으로, 해당 기술 분야의 숙련자는 다른 보조제도 개시된 항원 및 나노입자의 기능과 함께 사용되어 이를 보완할 수 있음을 이해할 것이다. 개시된 항원 및 나노입자와 함께 사용하기에 적합한 다른 보조제로는 모노포스포릴 지질 A(MPLA), 수중유 에멀전, ADJUPLEX™(레시틴 및 카보머 동종 중합체), ADDAVAX™(스쿠알렌 기반 수중유 나노 에멀전), CARBOPOL® 중합체(가교 폴리아크릴산 중합체), Poly IC:LC(카복시메틸셀룰로오스, 폴리이노신-폴리시티딜산, 및 폴리-L-리신 이중 가닥 RNA의 합성 복합체), PolyI:C(폴리이노신:폴리시티딜산), CpG 올리고데옥시뉴클레오티드, 플라젤린, 이스코매트릭스(사포닌, 콜레스테롤, 및 디팔미토일포스파티딜콜린으로 구성됨), 비로솜, MF59(스쿠알렌 기반 수중유 에멀전), AS03(스쿠알렌 기반의 수중유 에멀전), 및 AS04(명반(alum) 흡수된 3-O-데스아실-4'-모노포스포릴 지질 A)가 포함되지만 이에 제한되지는 않는다.
J. 약학 조성물
본 개시 내용의 약학 조성물에는 본원에 개시된 바와 같은 mRNA 분자 또는 나노입자를 포함하는 면역원성 조성물(예를 들어, 백신)이 포함된다.
일부 실시양태에서, 약학 조성물은 또한 보조제(예를 들어, ALFQ, 알히드로겔, 또는 이들의 조합, 또는 mRNA 백신과 함께 사용하기에 적합한 보조제)를 포함할 것이다. 나노입자(들) 또는 mRNA 분자(들)는 단독으로 또는 하나 이상의 보조제와 함께 적합한 담체에 제제화되어 의도된 투여 경로에 적합한 약학 조성물을 형성할 수 있다. 또한 본원에 기술된 바와 같은 면역원성 조성물은 그 자체가 약학 조성물일 수 있으며, 예를 들어 의도된 투여 경로를 위한 보조제 및/또는 적합한 담체를 포함할 수 있음을 이해해야 한다. 따라서, 이어지는 논의에서 "약학 조성물"에 대한 언급은 본원에 기술된 바와 같은 면역원성 조성물의 실시양태를 포함하는 것으로 이해해야 한다.
일부 실시양태에서, 약학 조성물은 비경구 투여를 통한 전신 투여를 위해 제제화된다. 비경구 투여에는 정맥 내, 동맥 내, 피하, 피내, 복강 내, 또는 근육 내 주사 또는 주입이 포함된다. 비경구 투여를 위한 제제에는 멸균 수용액이 포함될 수 있으며, 여기에는 완충제, 희석제 및 숙련된 기술자에게 알려진 기타 약학적으로 허용 가능한 첨가제도 함유될 수 있다. 정맥 내 용도의 경우, 제제를 등장성으로 만들기 위해 용질의 총 농도를 제어할 수 있다. 정맥 내, 동맥 내, 피하, 또는 근육 내 주사가 바람직한 투여 경로이다. 추가적으로 또는 대안적으로, 개시된 백신은 비강 내 투여 또는 다른 점막과의 접촉을 통한 투여를 위해 제제화될 수 있다.
주사용 약학 조성물은 단위 투여 형태, 예를 들어 앰플, 또는, 선택적으로 방부제가 첨가된, 다회 투여 용기에 제공될 수 있다. 조성물은 유성 또는 수성 비히클에 현탁액, 용액 또는 에멀전과 같은 형태를 취할 수 있으며, 현탁화제, 안정화제 및/또는 분산제와 같은 제제화제를 함유할 수 있다. 개시된 백신은 임의의 적합한 약학적으로 허용 가능한 부형제를 사용하여 제제화될 수 있다.
비강 투여용 약학 조성물은 액체 분산액, 현탁액, 용액, 또는 에멀전의 형태를 취할 수 있으며 비강 에어로졸 또는 비강 스프레이에 통합될 수 있다. 이러한 조성물은 현탁화제, 안정화제 및/또는 분산제와 같은 제제화제를 함유할 수 있으며, 임의의 적합한 약학적으로 허용 가능한 부형제를 사용하여 제제화될 수 있다. 비강 내 투여에는 투여 중 흡입을 동반하거나 동반하지 않는 코를 통한 투여가 포함된다. 이러한 투여는 일반적으로 개시된 백신을 비강 점막, 비강 비갑개, 또는 부비동과 접촉시켜 이루어진다. 흡입에 의한 투여는 비강 내 투여를 포함할 수 있거나, 경구 흡입을 포함할 수 있다. 이러한 투여에는 또한 구강 점막, 기관지 점막, 및 기타 상피와의 접촉이 포함될 수 있다.
개시된 면역원성 조성물은 다른 치료제와 동시에 투여되도록 제제화될 수 있다. 면역원성 조성물은 다른 치료제와 순서대로 투여되도록 제제화될 수 있다. 예를 들어, 면역원성 조성물은 대상체가 항바이러스 치료 요법을 받기 전 또는 후에 투여될 수 있다.
본원에 개시된 임의의 면역원성 조성물 및 약학 조성물은 예를 들어 SARS-CoV-2 감염(예를 들어, COVID-19) 또는 SARS-CoV-1 감염과 같은 코로나바이러스 감염을 치료하거나 예방하는 데 사용될 수 있다. 특정 코로나바이러스 감염(예컨대 SARS-CoV-2)에 대한 사용을 위한 약학 조성물 또는 면역원성 조성물은 일반적으로 표적 코로나바이러스(예를 들어, SARS-CoV-2)의 항원성 펩티드(또는 이를 코딩하는 mRNA)를 포함할 것이지만, 선택적으로 추가적으로 또는 대안적으로 밀접하게 연관된 코로나바이러스(예를 들어, SARS-CoV-1)의 항원성 펩티드(또는 이를 코딩하는 mRNA)를 포함할 수 있다. 최적의 용량 및 투여 경로는 면역원성 조성물의 특성(예를 들어, mRNA 대 나노입자), 표적이 되는 바이러스(들), 및 치료되는 대상체에 따라 달라질 수 있다.
IV. 코로나바이러스의 치료 및 예방
본 개시 내용은 본원에 개시된 나노입자 또는 mRNA 분자 중 하나 이상을 포함하는 본원에 기술된 바와 같은 면역원성 조성물(예를 들어, 백신)을 투여함으로써 사르베코바이러스 감염 및 메르베코바이러스 감염을 포함하지만 이에 제한되지 않는 코로나바이러스 감염의 치료 및 예방 방법을 제공한다. 본 개시 내용은 또한 코로나바이러스 감염, 예컨대 SARS-CoV-2 감염(예를 들어, COVID-19), SARS 감염, 및 MERS 감염을 치료 또는 예방하기 위한 개시된 면역원성 조성물 및 약학 조성물의 용도를 제공한다. 본원에 개시된 임의의 방법 및 용도에 따라, 대상체는 코로나바이러스 감염의 위험에 있을 수 있거나 이미 코로나바이러스에 감염될 수 있다. 추가적으로 또는 대안적으로, 대상체는 이전에 코로나바이러스 감염의 예방을 위한 백신을 투여받은 적이 없을 수 있거나 이전에 코로나바이러스 감염의 예방을 위한 백신을 투여받은 적이 있을 수 있다. 특정 코로나바이러스 감염(예컨대 SARS-CoV-2)을 표적화하는 방법은 일반적으로 표적 코로나바이러스(예를 들어, SARS-CoV-2)의 항원성 펩티드(또는 이를 코딩하는 mRNA)를 포함하는 면역원성 조성물 또는 약학 조성물을 사용할 것이지만, 선택적으로 추가적으로 또는 대안적으로 밀접하게 연관된 코로나바이러스(예컨대 SARS-CoV-1)의 항원성 펩티드(또는 이를 코딩하는 mRNA)를 포함할 수 있다.
개시된 방법은 본원에 개시된 면역원성 조성물(예를 들어, 백신) 또는 약학 조성물 중 하나 이상의 유효량을 대상체에게 투여하는 단계를 포함한다. 투여는 정맥 내, 동맥 내, 근육 내, 피하, 또는 피내 주사를 통해 수행될 수 있다. 일부 실시양태에서, 대상체는 예를 들어 SARS-CoV-2, MERS, 또는 SARS-CoV-1과 같은 코로나바이러스에 노출될 위험에 있을 수 있다. 일부 실시양태에서, 대상체는 이전에 SARS-CoV-2, MERS, 또는 SARS-CoV-1과 같은 코로나바이러스에 노출된 적이 있을 수 있다. 일부 실시양태에서, 대상체는 이전에 코로나바이러스 감염 예방을 위한 백신을 투여받은 적이 없다. 일부 실시양태에서, 대상체는 이전에 코로나바이러스 감염 예방을 위한 백신을 투여받은 적이 있다. 일부 실시양태에서, 대상체는 투여의 결과로 치료될 수 있는 활성 감염을 가질 수 있다. 일부 실시양태에서, 백신의 투여는 대상체에게 코로나바이러스 감염이 발생하는 것을 예방한다. 일부 실시양태에서, 상기 방법은 대상체에서 코로나바이러스에 대한 면역 반응을 유발하며, 선택적으로 면역 반응은 중화 항체를 포함하고, 추가로 선택적으로 중화 항체는 두 가지 이상의 코로나바이러스 균주를 교차 중화하고, 추가로 선택적으로 중화 항체는 면역원성 조성물의 구성 균주가 아닌 하나 이상의 코로나바이러스 균주를 교차 중화한다.
상기 방법은 본원에서 기술된 바와 같은 나노입자 백신 또는 면역원성 조성물에 대한 프라이밍제(즉, "프라이머")의 투여를 추가로 포함할 수 있다. 프라이머는 나노입자 백신 투여 전(예를 들어, 1주, 2주, 3주, 4주, 5주, 또는 6주 이상 전)에 투여될 수 있다. 프라이머는 코로나바이러스 S 단백질(예를 들어, SARS-CoV-2 또는 SARS-CoV-1의 S 단백질)의 RBD의 융합 단백질 또는 전체, 단편, 또는 변이체를 코딩하는 핵산(즉, DNA 또는 mRNA)을 포함할 수 있다.
개시된 방법 및 용도의 목적을 위해, 다양한 SARS-CoV-2 균주의 치료 및/또는 예방을 포함하여 모든 코로나바이러스에 의한 감염의 치료 및/또는 예방이 특히 고려된다. 또한, SARS-CoV-1, SARS-CoV-2, 및 MERS-CoV의 모든 균주 및 변종뿐만 아니라 본원에 개시된 다른 코로나바이러스의 모든 균주 및 변종에 의한 감염의 치료 및/또는 예방을 위한 방법 및 용도가 고려된다.
투여 요법은 최적의 원하는 반응(예를 들어, 코로나바이러스에 대한 항체 및/또는 사이토카인 생성)을 제공하도록 조정될 수 있다. 예를 들어, 일부 실시양태에서, 단일 볼러스의 백신(예를 들어, 본원에 기술된 바와 같은 면역원성 조성물)이 투여될 수 있는 반면, 일부 실시양태에서, 시간에 걸쳐 여러 용량이 투여될 수 있거나, 용량은 상황에 따라 비례적으로 감소되거나 증가될 수 있다. 예를 들어, 일부 실시양태에서, 개시된 백신은 주 1회 또는 2회, 월 1회 또는 2회, 매주 1회, 2주에 1회, 3주에 1회, 4주에 1회, 2개월에 1회, 3개월에 1회, 4개월에 1회, 5개월에 1회, 6개월에 1회, 7주에 1회, 8주에 1회, 3개월에 1회, 4개월에 1회, 5개월에 1회, 6개월에 1회, 또는 1년에 1회 투여될 수 있다. 일부 실시양태에서, 대상체는 초기 용량을 투여받은 다음, 각 용량 사이에 미리 정해진 시간 간격(예를 들어, 1, 2, 3, 또는 4주, 또는 1, 2, 3, 4, 5, 6, 9, 또는 12개월)을 두고 1회 이상의 부스터 용량을 투여받을 수 있다. 일부 실시양태에서, 대상체는 단회 용량만 받을 수 있다. 일부 실시양태에서, 대상체는 초기 용량을 투여받은 후 초기 용량 후 설정된 시간, 예컨대 1주, 2주, 3주, 4주, 5주, 6주, 7주, 8주, 9주, 10주, 11주, 12주, 13주, 14주, 15주, 16주, 17주, 18주, 19주 또는 20주 이상, 예컨대 24주, 52주, 104주, 260주, 또는 520주에 동일하거나 더 낮은 농도의 후속 용량을 1회 이상 투여받을 수 있다.
용량은 마찬가지로 최적의 원하는 반응을 제공하도록 조정될 수 있다. 예를 들어, 일부 실시양태에서, 개시된 백신의 용량은 1 ㎍ 내지 50 mg의 백신을 포함할 수 있다. 단회 용량은 약 1 ㎍, 약 5 ㎍, 약 10 ㎍, 약 15 ㎍, 약 20 ㎍, 약 25 ㎍, 약 30 ㎍, 약 35 ㎍, 약 40 ㎍, 약 45 ㎍, 약 50 ㎍, 약 55 ㎍, 약 60 ㎍, 약 65 ㎍, 약 70 ㎍, 약 75 ㎍, 약 80 ㎍, 약 85 ㎍, 약 90 ㎍, 약 95 ㎍, 약 100 ㎍, 약 125 ㎍, 약 150 ㎍, 약 175 ㎍, 약 200 ㎍, 약 225 ㎍, 약 250 ㎍, 약 275 ㎍, 약 300 ㎍, 약 325 ㎍, 약 350 ㎍, 약 375 ㎍, 약 400 ㎍, 약 425 ㎍, 약 450 ㎍, 약 475 ㎍, 약 500 ㎍, 약 525 ㎍, 약 550 ㎍, 약 575 ㎍, 약 600 ㎍, 약 625 ㎍, 약 650 ㎍, 약 675 ㎍, 약 700 ㎍, 약 725 ㎍, 약 750 ㎍, 약 775 ㎍, 약 100 ㎍, 약 825 ㎍, 약 850 ㎍, 약 875 ㎍, 약 900 ㎍, 약 925 ㎍, 약 950 ㎍, 약 975 ㎍, 약 1 mg, 약 1.25 mg, 약 1.5 mg, 약 1.75 mg, 약 2 mg, 약 2.25 mg, 약 2.5 mg, 약 2.75 mg, 약 3 mg, 약 3.25 mg, 약 3.5 mg, 약 3.75 mg, 약 4 mg, 약 4.25 mg, 약 4.5 mg, 약 5.75 mg, 약 5 mg, 약 10 mg, 약 15 mg, 약 20 mg, 약 25 mg, 약 30 mg, 약 35 mg, 약 45 mg, 또는 약 50 mg을 포함할 수 있다. 일부 실시양태에서, 단회 용량은 4 mg 이하의 백신 또는 나노입자를 포함할 수 있다.
대안적으로, 투여는 대상체에게 투여된 나노입자 수에 기초할 수 있다. 예를 들어, 일부 실시양태에서, 개시된 백신의 용량은 1.0 x 108 내지 1.0 x 1012개의 나노입자를 포함할 수 있다. 예를 들어, 단회 용량은 1.0 x 108, 1.5 x 108, 2.0 x 108, 2.5 x 108, 3.0 x 108, 3.5 x 108, 4.0 x 108, 4.5 x 108, 5.0 x 108, 5.5 x 108, 6.0 x 108, 6.5 x 108, 7.0 x 108, 7.5 x 108, 8.0 x 108, 8.5 x 108, 9.0 x 108, 9.5 x 108, 1.0 x 109, 1.5 x 109, 2.0 x 109, 2.5 x 109, 3.0 x 109, 3.5 x 109, 4.0 x 109, 4.5 x 109, 5.0 x 109, 5.5 x 109, 6.0 x 109, 6.5 x 109, 7.0 x 109, 7.5 x 109, 8.0 x 109, 8.5 x 109, 9.0 x 109, 9.5 x 109, 1.0 x 1010, 1.5 x 1010, 2.0 x 1010, 2.5 x 1010, 3.0 x 1010, 3.5 x 1010, 4.0 x 1010, 4.5 x 1010, 5.0 x 1010, 5.5 x 1010, 6.0 x 1010, 6.5 x 1010, 7.0 x 1010, 7.5 x 1010, 8.0 x 1010, 8.5 x 1010, 9.0 x 1010, 9.5 x 1010, 1.0 x 1011, 1.5 x 1011, 2.0 x 1011, 2.5 x 1011, 3.0 x 1011, 3.5 x 1011, 4.0 x 1011, 4.5 x 1011, 5.0 x 1011, 5.5 x 1011, 6.0 x 1011, 6.5 x 1011, 7.0 x 1011, 7.5 x 1011, 8.0 x 1011, 8.5 x 1011, 9.0 x 1011, 9.5 x 1011, 또는 1.0 x 1012개의 나노입자를 포함할 수 있다. 일부 실시양태에서, 용량은 약 9.5 x 108, 약 9.75 x 108, 약 9.85 x 108, 약 9.95 x 108, 약 1.0 x 109, 약 1.1 x 109, 약 1.15 x 109, 약 1.2 x 109, 약 1.25 x 109, 약 1.3 x 109, 약 1.35 x 109, 약 1.4 x 109, 약 1.45 x 109, 또는 약 1.5 x 109개의 나노입자일 수 있다.
일부 실시양태에서, 대상체는 포유류이다. 일부 실시양태에서, 대상체는 인간이다. 대상체가 인간인 실시양태에서, 대상체는 적어도 18세, 40세, 적어도 45세, 적어도 50세, 적어도 55세, 적어도 60세, 적어도 65세, 적어도 70세, 적어도 75세, 또는 적어도 80세 이상일 수 있다. 일부 실시양태에서, 대상체는 소아 대상체(즉, 18세 미만)이다.
V. 결합
분자에 대한 스크리닝
치료에 사용되는 것 외에도, 개시된 나노입자 및 융합 단백질은 코로나바이러스(예를 들어, SARS-CoV-1 또는 SARS-CoV-2)에 결합하고 이를 중화하는 능력에 대해 항체와 같은 결합 분자를 스크리닝하는 데 사용될 수 있다. 본원에 개시된 임의의 융합 단백질은 추정된 코로나바이러스 결합 분자(예컨대 추정된 항-코로나바이러스 항체)와 접촉시키고, 융합 단백질 또는 나노입자에 대한 결합을 평가할 수 있다. 본원에 개시된 융합 단백질에 결합하는 항체(또는 다른 결합 분자)는 중화적인 것으로 예상된다.
VI. 결합 분자를 이용한 수동 면역요법 및 치료
결합 분자(예를 들어, 본원에 개시된 바와 같이 SARS-CoV-2 또는 다른 코로나바이러스에 결합하는 항체)는 코로나바이러스 감염의 발병을 예방하기 위한 수동 면역 요법 또는 이미 코로나바이러스 감염이 있는 대상체의 치료에 사용될 수 있다. 일반적으로, 코로나바이러스 특이 항체는 본원에 개시된 바와 같은 면역원성 조성물을 투여받은 대상체로부터 얻을 수 있거나, 코로나바이러스 특이 항체는 스크리닝 분석을 위한 미끼로서 개시된 융합 단백질 및 나노입자를 사용하여 코로나바이러스 감염(예를 들어, COVID-19)에서 회복된 대상체로부터 확인할 수 있다. 이러한 항체는 예를 들어 COVID-19 또는 SARS-CoV-1 감염과 같은 코로나바이러스 감염의 발병을 예방하기 위해 코로나바이러스에 노출되었거나 노출될 위험이 있는 대상체에게 투여될 수 있다(즉, 항체는 "수동 면역 요법"으로 사용될 수 있음). 추가적으로 또는 대안적으로, 이러한 항체는 SARS-CoV-1 또는 SARS-CoV-2와 같은 코로나바이러스에 감염된 대상체에게 투여되어, 예를 들어 바이러스 부하를 줄이거나 제거함으로써, 감염을 치료할 수 있다.
개시된 결합 단백질은 인간 IgG1 항체, 인간 IgG2 항체, 인간 IgG3 항체, 또는 인간 IgG4 항체이거나 이로부터 유래될 수 있다. 일부 실시양태에서, 결합 단백질은 IgG, IgM, IgA, IgE, 및 IgD로부터 선택된 항체 클래스이거나 이로부터 유래될 수 있다. 즉, 개시된 결합 단백질은 IgG, IgM, IgA, IgE, 또는 IgD 항체의 불변 영역, 프레임워크 영역, 또는 이들의 조합의 전부 또는 일부를 포함할 수 있다. 예를 들어, IgG1 면역글로불린 구조를 포함하는 개시된 결합 단백질은 IgG1 구조를 또 다른 IgG-클래스 면역글로불린 또는 IgM, IgA, IgE, 또는 IgD 면역글로불린의 해당 구조로 대체(또는 "스위치")하도록 변형될 수 있다. 이러한 유형의 변형 또는 스위칭은 항체 의존성 세포 독성(ADCC) 및 보체 고정(CDC)과 같은 펩티드의 중화 기능을 증강시키기 위해 수행될 수 있다. 당업자는 예를 들어, 재조합 IgG1 면역글로불린 구조가 예를 들어 점막 표면에 국소 적용하는 데 유용할 수 있는 재조합 분비 IgA1 또는 재조합 분비 IgA2와 같은 다른 면역글로불린 클래스의 면역글로불린 구조의 해당 영역으로 "스위칭"될 수 있다는 것을 이해할 것이다. 예를 들어, 면역글로불린 IgA 구조는 감염성 질환의 침입에 대항하는 보호 면역 감시에 적용되는 것으로 알려져 있으며, 이로써 상기 구조가 이러한 맥락에서, 예를 들어 코로나바이러스 감염(예를 들어, COVID-19 또는 SARS-CoV-1 감염) 또는 한 개인에서 다른 개인으로의 코로나바이러스 전파를 치료 또는 예방하는 데에 있어서 개시된 결합 단백질을 사용하는 방법에 적합하게 된다.
개시된 면역원성 조성물로 접종되거나 개시된 융합 단백질을 사용하여 스크리닝/선택된 대상체로부터 얻은 코로나바이러스 특이적 결합 단백질 또는 항체는 예를 들어 COVID-19 또는 SARS-CoV-1 감염과 같은 코로나바이러스 감염을 치료 및/또는 예방하는 데 사용될 수 있다. 최적의 용량 및 투여 경로는 예를 들어 투여 경로 및 제형, 대상체의 연령 및 체중, 및/또는 코로나바이러스 감염의 유형 및 중증도를 포함한 대상체의 상태를 기초로 하여 달라질 수 있으며, 숙련된 실무자에 의해 결정될 수 있다. 결합 단백질은 임의의 의도된 투여 경로를 통해 대상체에게 투여하기에 적합한 약학 조성물로 제제화될 수 있다.
VII. 예시적인 실시양태
본 개시 내용은 개시 내용과 관련하여 비제한적인 다음의 예시적인 실시양태를 제공한다:
실시양태 1: 나노입자 형성 펩티드와 다음으로부터 선택된 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 융합 단백질을 포함하는 나노입자: 코로나바이러스의 수용체 결합 도메인(RBD), 또는 이의 단편 또는 변이체, 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체, 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 코로나바이러스의 안정화된 세포외 스파이크 S-삼량체, 또는 이의 단편 또는 변이체, 및 모자이크 코로나바이러스 스파이크 단백질, 여기서 모자이크 코로나바이러스 스파이크 단백질의 적어도 하나의 도메인은 이종으로부터 치환되거나 추가됨.
실시양태 2: 실시양태 1에 있어서, 나노입자 형성 펩티드는 페리틴 단백질 또는 이의 단편 또는 변이체이거나 이를 포함하는 것인 나노입자.
실시양태 3: 실시양태 1 또는 2에 있어서, 나노입자 형성 펩티드는 헬리코박터 파일로리 페리틴(Hpf) 또는 이의 단편 또는 변이체이거나 이를 포함하는 것인 나노입자.
실시양태 4: 실시양태 1 내지 3 중 어느 하나에 있어서, 나노입자 형성 펩티드는 다음으로부터 선택된 아미노산 서열을 포함하는 것인 나노입자:
실시양태 5: 실시양태 1-4 중 어느 하나에 있어서, 적어도 두 개의 항원성 코로나바이러스 펩티드는 링커를 통해 연결되는 것인 나노입자.
실시양태 6: 실시양태 1-5 중 어느 하나에 있어서, 적어도 두 개의 항원성 코로나바이러스 펩티드는 링커를 통해 나노입자 형성 펩티드에 연결된 것인 나노입자.
실시양태 7: 실시양태 5 또는 6에 있어서, 링커는 다음으로부터 선택된 아미노산 서열을 포함하는 것인 나노입자: GSGGGG(서열 번호 11), GGGG(서열 번호 15), GSGG(서열 번호 5), GGG(서열 번호 16), 및 SGG(서열 번호 17).
실시양태 8: 실시양태 1-7 중 어느 하나에 있어서, 융합 단백질은 직렬로 연결된 3-10개의 항원성 코로나바이러스 펩티드를 포함하고, 선택적으로 항원성 코로나바이러스 펩티드는 펩티드 링커를 통해 연결되는 것인 나노입자.
실시양태 9: 실시양태 1-8 중 어느 하나에 있어서, 적어도 두 개의 항원성 코로나바이러스 펩티드는 SARS-CoV-2, 인간 코로나바이러스 OC43(hCoV-OC43), 중동 호흡기 증후군 관련 코로나바이러스(MERS-CoV), 중증 급성 호흡기 증후군 관련 코로나바이러스(SARS-CoV-1), HKU-1, 229E, 또는 NL63으로부터 선택된 하나 이상의 코로나바이러스로부터 단리되거나 유래된 것인 나노입자.
실시양태 10: 실시양태 1-9 중 어느 하나에 있어서, 융합 단백질은 실에 꿴 구슬, 도메인 융합, 루프 삽입, 또는 도메인 삽입으로부터 선택된 형식을 포함하는 것인 나노입자.
실시양태 11: 실시양태 1-10 중 어느 하나에 있어서, 융합 단백질은 도 2에 도시된 형식을 포함하는 것인 나노입자.
실시양태 12: 실시양태 1 내지 11 중 어느 하나에 있어서, 융합 단백질은 표 6에 개시된 아미노산 서열을 포함하는 것인 나노입자.
실시양태 13: 실시양태 1-12 중 어느 하나의 나노입자를 포함하는 백신.
실시양태 14: 실시양태 13에 있어서, ALFQ, 알히드로겔, 및 이들의 조합으로부터 선택된 하나 이상의 보조제를 추가로 포함하는 백신.
실시양태 15: 실시양태 1 내지 12 중 어느 하나에 따른 나노입자를 코딩하는 메신저 RNA(mRNA).
실시양태 16: 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하는 방법으로, 이를 필요로 하는 대상체에게 실시양태 1 내지 12 중 어느 하나에 따른 나노입자, 실시양태 13 또는 14에 따른 백신 또는 실시양태 15에 따른 mRNA를 투여하는 단계를 포함하는 방법.
실시양태 17: 실시양태 16에 있어서, 대상체는 코로나바이러스 감염 위험에 있는 것인 방법.
실시양태 18: 실시양태 16에 있어서, 대상체는 이미 코로나바이러스에 감염된 것인 방법.
실시양태 19: 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하는 데 사용하기 위한 실시양태 1-12 중 어느 하나에 따른 나노입자, 실시양태 13 또는 14에 따른 백신, 또는 실시양태 15에 따른 mRNA.
실시양태 20: 실시양태 19에 있어서, 대상체는 코로나바이러스 감염 위험에 있는 것인 나노입자, 백신 또는 mRNA.
실시양태 21: 실시양태 19에 있어서, 대상체는 이미 코로나바이러스에 감염된 것인 나노입자, 백신, 또는 mRNA.
실시양태 22: 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하기 위한 의약의 제조에 있어서 실시양태 1-12 중 어느 하나에 따른 나노입자, 실시양태 13 또는 14 중 어느 하나에 따른 백신, 또는 실시양태 16에 따른 mRNA의 용도.
실시양태 23: 실시양태 1-12 중 어느 하나에 따른 나노입자를 코딩하는 서열을 포함하는 DNA 분자.
실시양태 24: 실시양태 23의 DNA 분자를 포함하는 플라스미드.
실시양태 25: 실시양태 24에 있어서, 생체 내에서 DNA 분자를 발현할 수 있는 플라스미드.
다음 실시예는 본 개시 내용을 설명하기 위해 제공된다. 본 발명은 이 실시예에서 기술된 구체적인 조건 또는 세부 사항에 제한되지 않는다는 것을 이해해야 한다.
실시예
실시예
1 - 개시된 융합 단백질의 스크리닝
MERS-CoV RBD-페리틴 나노입자 면역원의 결합 연구를 수행하여, 두 가지 형식으로 MERS-CoV 중화 인간 단클론 항체 CDC-C2에 대한 결합에 대해 MERS-CoV RBD-페리틴 구축물을 평가하였다. 간략하게, 바이오센서를 사용 전에 PBS에서 수화한다. Octet RED96 기기(FortBio)에서 1,000 crpm으로 설정하여 교반하면서 30℃에서 분석 단계를 수행한다. 바이오센서를 분석 완충액(PBS)에서 15초 동안 평형화한 후 IgG 항체(30 ㎍/ml로 PBS에 희석)를 로딩한다. 사용된 스파이크 RBD를 표적화하는 MERS-CoV 중화 항체에는 D12, F11, CDC2-C2, 및 JC57-11이 포함되고, SARS-CoV-2 중화 항체에는 WRAIR-2125, WRAIR-5001, 및 ShAb02가 포함된다. MERS-CoV 및 SARS-CoV-2 항체를 AHC 바이오센서(FortBio)에 100초 동안 고정시킨 다음, 분석 완충액에서 15초 동안 짧은 기준선을 두었다. 그 다음 고정된 항체를 다양한 항원에 180초 동안 담갔다. 결합 단계 종료 시 반응 값을 측정하였다. 구축물 M.1-M3.6에 대한 결과는 도 10에 나타낸다.
MERS RBD 함유 면역원 M3.7, M3.12 및 M3.13과 이중 RBD 구축물 SARS-CoV-2-MERS-CoV RR-FN 면역원 248-250 및 267-270의 유사한 항원 특성화는 중화 항체 세트를 사용하여 octet 생물층 간섭법을 통해 수행하였다. 결과(결합 180초 후 결합 반응)는 아래 표 4에 나타낸다.
SARS-CoV-1 RBD 함유 면역원인 CoV263, CoV277, CoV278, CoV316, 및 CoV317 면역원의 항원 특성화는 중화 항체 세트를 사용하여 octet 생물층 간섭법을 통해 평가하였다. 결과는 아래 표 5에 나타낸다.
실시예
2 - 융합 단백질의 생성 및 크기 평가
RR-SpFN 구축물을 설계하고 발현, 수율, 및 나노입자 형성에 대해 테스트하였다. 구축물 pCoV323(RR-SpFN MR14-SARS1-SpFN)을 Expi293F 세포에서 37℃에서 5일 동안 발현시키고 갈란투스 니발리스(Galanthus nivalis) 렉틴(GNA) 친화성 크로마토그래피로 정제하였다. 이 구축물은 0.4 mg/L 배지 상층액의 적정한 발현 수준을 보였다. 정제된 단백질을 SDS-PAGE 및 크기 배제 크로마토그래피에 의해 분석하여 발현을 평가하고 크기를 확인하였다. 결과는 도 14에 나타내며, RR-SpFN 구축물은 SDS-PAGE로 적절한 크기를 보였고 크기 배제 크로마토그래피로 나노입자 형성을 보였다.
실시예
3
mRNA
구축물 발현
스파이크 항원을 코딩하는 mRNA 구축물을 제공하고 HeLa 세포에서 발현시켰다. 또한, 발현된 융합 단백질은 중화 항체 세트를 사용하여 octet 생물층 간섭법을 통해 평가하였다.
방법
HeLa 세포를 0.5 mL EMEM + 10% FBS에 7만5천개 세포/웰로 24웰 플레이트에 도말하였다. 세포는 다음날 리포펙타민 2000을 사용하여 백만개 세포당 1 ㎍ mRNA 구축물로 형질감염시켰다. 다양한 mRNA 구축물은 형질감염 후 HeLa 세포에서 시험관 내 발현 및 분비에 대해 테스트하였다. 형질감염 24시간 후, 세포 용해물과 상층액(분비를 평가하기 위함)을 도트 블롯에서 형태적 중화 에피토프를 표적화하는 항-RBD 단클론 항체(mAb)(예를 들어, SA55) 및/또는 항-페리틴 mAb로 스파이크 또는 RBD를 프로빙하여 분석하였다.
octet 결합 연구의 경우, 총 대략 12 ㎍의 mRNA를 사용하여 25 ml의 Expi 293F 세포를 형질감염시켰다. 2-4일 후에 상층액을 수거하고, 생물층 간섭법을 통해 CoV 특이적 항체 세트, 인간 ACE2, 및 음성 대조군 인플루엔자 항체에 대한 결합에 대해 평가하였다.
용해물의
제조
22-24시간 후에 세포를 수거하여 웰당 225 ㎕의 CelLytic M +1x HALT에서 용해시켰다. 용해물을 얼음 위에서 10분간 인큐베이션한 다음, 4℃에서 최대 속도로 10분간 마이크로 원심분리기에서 청징하였다. 용해물을 하류 분석을 위해 PBS로 2배 및 4배 희석하였다.
상층액
샘플의 제조
형질감염 후 22-24시간 후에 세포 배양 상층액을 수거하였다. 상층액 샘플은 하류 분석을 위해 PBS로 2배 및 4배 희석하였다.
발현 분석
순수, 2배, 및 4배 희석된 용해물 또는 상층액 샘플을 건조 니트로셀룰로오스 막에 1 ㎕ 도트로 점적하였다. 그런 다음 막을 완전히 건조시킨 후 추가 처리하였다. 블롯을 Intercept 차단 완충액으로 실온에서 1시간 동안 차단하였다. 블롯을 인간 항-스파이크 항체 또는 인간 항-페리틴 항체로 염색하였다. 항체 염색은 Intercept 차단 완충액 + 0.2% 트윈 20에서 4℃에서 하룻밤 동안 수행하였다. 블롯은 TBST로 5분씩 3회 세척하였다. 그런 다음 블롯을 Intercept 차단 완충액 + 0.2% 트윈 20에서 당나귀 항-인간 IR800 2차 항체로 실온에서 1시간 동안 염색하였다. 블롯을 TBST로 5분씩 4회 세척하고 Licor odyssey에서 스캔하였다.
발현 결과
다음 구축물은 표 10에 표시된 대로 용해물 및/또는 상층액에서 발현되고 검출되었다. 상층액에서의 발현은 단백질이 분비되었음을 나타냈다. 모든 mRNA는 세포 용해물에서 예상 항원을 발현하였고; S-2P 항원은 막관통 단백질에 대해 예상한 대로 상층액에서는 검출되지 않았고; 더 복잡한 다중 균주 구축물(R-SpFN 및 RR-SpFN) 중 일부는 상층액에서 검출되지 않아 분비가 적거나 결함이 있음을 나타냈다. 결과는 아래 표 10에 요약한다.
서열 번호가 제공되지 않은 특정 구축물에 대해 현재로서는 생체 내 연구를 진행하지 않았다.
Octet 결합 결과
octet 결합 연구 결과는 아래 표 11에 요약한다.
실시예
4: 모자이크 나노입자 조립
천연 상태 겔 전기영동(PAGE)을 사용하여 다양한 균주로부터의 RFN 또는 SpFN의 겉보기 크기에서 관찰된 차이에 따라, 단가 및 다가 RFN(또는 SpFN)의 겉보기 크기를 비교하여 한 페리틴 나노입자에서 다양한 균주로부터의 RBD 또는 스파이크 삼량체의 조립을 평가하였다. 또한, RFN과 빈 FN의 공발현이 조립 및 분비 효율에 대한 잠재적인 이점이 있는지, 예를 들어, FN에서 RBD 간 입체 장애 위험을 감소시키는지 평가하였다.
방법
HeLa 세포를 0.5 mL EMEM + 10% FBS에 7만 5천개 세포/웰로 24웰 플레이트에 도말하였다. 세포는 다음날 리포펙타민 2000을 사용하여 백만개 세포당 1 ㎍ mRNA 구축물로 형질감염시켰다. 형질감염 24시간 후, 세포 용해물과 상층액(분비를 평가하기 위함)을 천연 상태 PAGE 웨스턴 블롯에서 항-페리틴 mAb로 프로빙하여 분석하였다.
용해물의 제조
22-24시간 후에 세포를 수거하여 웰당 125 ㎕의 CelLytic M +1x HALT에 용해시켰다. 용해물을 얼음에서 10분 동안 인큐베이션한 다음 4℃에서 최대 속도로 10분 동안 미세 원심분리기에서 청징하였다. 15 ㎕의 용해물을 환원제 없는 5 ㎕의 천연 상태 트리스-글리신 샘플 완충액과 합하였다.
상층액 샘플의 제조
형질감염 후 22-24시간 후에 세포 배양 상층액을 수거하였다. 상층액 15 ㎕를 환원제 없는 천연 상태 트리스-글리신 샘플 완충액 5 ㎕와 합하였다.
분석
생성된 용해물 또는 상층액 샘플을 4-12% 구배 천연 상태 PAGE에서 185V에서 75분 동안 이동시켰다. 단백질을 니트로셀룰로오스 막으로 옮겼다. 블롯을 Intercept 차단 완충액으로 실온에서 1시간 동안 차단하였다. 블롯을 인간 항-페리틴 항체로 염색하였다. 항체 염색을 Intercept 차단 완충액 + 0.2% 트윈 20에서 4℃에서 하룻밤 동안 수행하였다. 블롯은 TBST로 5분씩 3회 세척하였다. 그런 다음 블롯을 Intercept 차단 완충액 + 0.2% 트윈 20에서 염소 항-인간 IR800 2차 항체로 실온에서 1시간 동안 염색하였다. 블롯을 TBST로 5분씩 4회 세척하고 Licor odyssey에서 스캔하였다.
결과
이 연구의 결과는 도 18 및 19에 나타낸다. 데이터는 SARS-1 RFN(더 높은 이동)과 BANAL-20-247 RFN(더 낮은 이동)을 공동 발현할 때 밴딩 패턴이 단일 RFN에서 관찰된 패턴에 비해 중간 패턴으로 이동한다는 것을 보여준다. 이는 각 구축물이 상이한 비율로 구성되어 있을 가능성이 높은 여러 종이 있음을 나타낸다. 각 RFN이 빈 FN(페리틴 단독)과 결합될 때에도 동일한 현상이 관찰된다. 이 효과는 이동 차이가 훨씬 더 크고 복합체의 여러 종을 명확히 나타나기 때문에 더욱 극적이다. 또한, 가장 낮은 이동 다가 복합체는 빈 FN보다 높아서 검출 가능한 모든 빈 FN이 최소한 1개의 RFN 구성 요소가 있는 복합체에 있음을 나타낸다. 세 가지 구성 요소를 모두 결합하면 자신의 고유한 밴딩 패턴이 생성되어 세 가지 구성 요소를 모두 함유하는 복합체가 형성됨을 뒷받침한다. 상층액 샘플은 유사한 밴딩 패턴을 보여 다중 구성원 복합체가 분비될 수 있음을 나타낸다. 흥미롭게도, 더 낮은 이동 복합체는 더 높은 이동 복합체에 비해 훨씬 더 효율적으로 분비되는 것으로 보인다. 이는 빈 FN의 비율이 더 높은 더 작은 복합체가 더 효율적으로 분비될 수 있음을 나타낸다.
실시예 5 -나이브 마우스에서의 면역원성 연구
이 마우스 연구는 다양한 항원 거리에서 RFN 및 SpFN 항원 디스플레이 패러다임에 걸친 mRNA 설계에 초점을 맞추었다(아래 표 8). 백신 조성물은 지질 D LNP에 제제화하였고 근육 내 경로를 통해 4주 간격의 2회 투여 일차 면역화 일정을 사용하여 나이브 수컷 및 암컷 C57BL/6 마우스에서 면역원성을 평가하였다. 다가 혼합물의 각 구성 균주 항원의 단가 버전으로 비교 제제를 제조하여 개별 균주의 기여도를 비교하고 다가 제시의 영향을 평가하였다. 또한, 단가 및 다가 제제의 모든 균주에 대한 안정화된 막관통 스파이크 단백질(S-2P)을 생성하여 페리틴 나노입자에 의한 항원 디스플레이의 기여도를 평가하였다.
한 세트의 제제에서, RFN 제제에는 페리틴 단량체(접합된 항원 없음)를 코딩하는 구축물도 포함되었으며, 이를 "빈 FN"이라고 한다. 제제의 한 하위 집합에 대해, 개별 mRNA 구축물을 동일한 조성물로 투여되는 별도의 LNP에 별도로 캡슐화하고 동일한 LNP에 공동 캡슐화된 일치하는 mRNA로 제조된 제제로 달성한 결과와 비교하였다.
제제
각 면역화 그룹(표 8 참조)에 대해, 투여되는 조성물을 제제화하고 50 ㎕당 구축물당 1 ㎍ 용량에 적합한 농도로 희석하였다. 빈 페리틴만 코딩하는 mRNA가 포함된 경우, 해당 mRNA를 50 ㎕당 구축물당 0.3 ㎕로 첨가하였다. "공동 투여"로 나열된 대조 제제를 투여받은 마우스는 각각이 1 ㎍ 용량(총 용량 3 ㎍)으로 LNP에 캡슐화된 나열된 하나의 구축물을 함유하는 세 개의 별도 주사로 접종하였다.
2차 면역화 2주 후에 수집한 혈청을 임상 관련성에 대해 선택된 균주 패널에 대한 중화 능력에 대해 테스트하였다. 이 패널에는 SARS-CoV-2(클레이드 1b) 변종(WA-1, 델타, 베타, BA.5, BQ.1.1, XBB.1.5)과 SARS-CoV-1의 대표 균주가 포함되었다. 메르비코바이러스 판독값도 포함되었다.
유사바이러스 중화 분석
SARS-CoV-2 및 SARS-CoV-1에 대한 스파이크 단백질(S) 발현 플라스미드 서열을 코돈 최적화 및 변형하여 SARS-CoV-2의 경우 세포질 꼬리에서 18개 아미노산 소포체 유지 신호를 제거하고, SARS-CoV의 경우 세포질 꼬리에서 28개 아미노산을 결실시켰다. 이를 통해 유사비리온(PSV)에 S 통합이 증가하여 감염성을 개선할 수 있었다. 수포구내염 바이러스(VSV) G 단백질로 위형화된 비리온을 비특이적 대조군으로 사용하였다. SARS-CoV-2 유사바이러스(PSV)는 HEK293T/17 세포에 SARS-CoV-2 S 플라스미드(pcDNA3.4)와 HIV-1 NL4-3 루시퍼라제 리포터 플라스미드를 공동 형질감염시켜 생산하였다(시약은 NIH HIV 시약 프로그램(AIDS 부서, NIAID, NIH)을 통해 얻었으며: 인간 면역결핍 바이러스 1(HIV-1) NL4-3 ΔEnv Vpr 루시퍼라제 리포터 벡터(pNL4-3.Luc.R-E-), ARP-3418은 Nathaniel Landau 박사와 Aaron Diamond 박사에게서 제공받음).
감염성 및 중화 역가는 ACE2-발현 HEK293 표적 세포(Integral Molecular)를 사용하여 로봇 액체 취급기(Biomek NXp Beckman Coulter)를 사용하여 반자동 분석 형식으로 결정하였다. 테스트 혈청은 성장 배지에 1:40으로 희석하고 연속 희석한 다음, 25 ㎕/웰을 흰색 96웰 플레이트에 첨가하였다. 동일한 부피의 희석된 SARS-CoV-2 PSV를 각 웰에 첨가하고 플레이트를 37℃에서 1시간 동안 인큐베이션하였다. 표적 세포를 각 웰에 첨가하고(40,000개 세포/웰) 플레이트를 추가 48시간 동안 인큐베이션하였다. RLU는 Bright-Glo Luciferase Assay System(Promega Corporation, 미국 위스콘신주 매디슨 소재)을 사용하여 EnVision Multimode Plate Reader(Perkin Elmer, 미국 매사추세츠주 월섬 소재)로 측정하였다. 중화 용량-반응 곡선은 LabKey Server®를 사용하여 5-매개변수 곡선 피팅을 사용한 비선형 회귀를 통해 피팅하였으며, 최종 역가는 50% 중화(ID50, 50% 억제 희석) 및 80% 중화(ID80, 80% 억제 희석)를 달성하는 데 필요한 혈청 희석의 역수로 보고하였다.
RFN, SpFN, 또는 S2P 항원 제시 형식의 단가 구축물 및 다가 믹스 A 내지 E 제제에 대한 결과는 도 20 및 21에 요약한다. RFN, SpFN, 또는 S2P 항원 제시 형식의 단가 또는 다가 믹스 A 내지 E로 접종한 마우스의 마우스 그룹 역가에 대한 통계적 표현은 도 22, 23, 및 24에 제공한다. 일반적으로, 항원 제시 형식 전반에 걸쳐 단가 균주는 유사한 균주에 대해 상당한 중화 역가를 제공하였다(도 20). WA-1(그룹 1, 15, 19)은 WA-1, 델타, 및 베타를 중화한다. 단가 대조군의 경우, 클레이드 1a와 1b에서 가장 큰 폭이 베타 면역화(그룹 2, 22, 37)에서 관찰되었으며, 이로부터 혈청이 WA-1, 델타, 및 베타를 중화하는 것으로 관찰되었다. 또한, 일부 마우스는 서열적으로 먼 두 오미크론 균주인 BA.5 및 BQ.1.1, 그리고 클레이드 1a SARS-CoV-1 유사바이러스에 대해 상당한 역가를 보였다. BQ.1.1 면역화된 마우스(그룹 3, 16, 21)의 혈청은 테스트된 오미크론 균주인 BA.5 및 BQ.1.1에 대해 높은 역가를 유발했지만 베타, 델타, 및 WA-1에 대한 역가는 감소하였다. 이 세 가지 단가 대조군은 선택된 클레이드 1b 균주가 원래 균주에서 최근 오미크론 균주까지 SARS-CoV-2 팬데믹의 항원적 환경을 포괄한다는 것을 입증한다. SARS-CoV-1, Khosta-2, BANAL20-247, 및 MERS를 포함한 다른 항원의 경우, 면역 마우스 혈청은 테스트된 클레이드 1b 유사바이러스에 대한 임의의 중화 역가를 유발하지 않았다. SARS-CoV-1(그룹 4, 17, 20) 및 MERS(6, 24, 39) 균주는 동종 유사바이러스에 대해서만 높은 역가를 유발하였다(도 20).
3가지 구성 단가 균주를 포함하는 믹스 A(WA-1, 베타, BQ.1.1)(그룹 10, 27, 41) 다가 제제는 테스트된 모든 클레이드 1b 사르베코바이러스에 대한 고역가 관찰을 통해 입증된 클레이드 1b에 걸친 폭을 생성하였으며, 특히 SpFN 및 S-2P 항원 디스플레이 방법(각각 그룹 27 및 41)에 대해 그랬다. 믹스 B(WA-1, BQ.1.1, SARS-CoV-1)(그룹 11, 25, 31)는 모든 클레이드 1b 사르베코바이러스에 걸쳐 고역가를 생성하였을 뿐만 아니라 클레이드 1a 내에서 최소한 동종 커버리지를 제공하였다. WA-1, SARS-CoV-1 및 다음 중 하나를 포함하는 믹스: Khosta-2(믹스 C; 그룹 9, 26, 44), BANAL20-247(믹스 D; 그룹 8, 28, 42), 또는 MERS(믹스 E; 그룹 12, 29, 43)는 클레이드 1b에 대해 WA-1과 유사한 역가를 보였고 클레이드 1a에 대해 SARS-CoV-1과 유사한 역가를 보였으며 추가 균주의 간섭은 거의 없었다(도 21-24).
믹스
B 면역화로 향상된
클레이드
1b 중화
역가
본원에 개시된 항원 설계 및 면역화 전략을 사용하여 생성된 혈청은 백신 성분으로 포함되지 않은 하나 이상의 사르베코바이러스 균주에 대한 중화 역가(가성 중화 분석으로 측정)를 증가시킨 경우 면역 반응의 폭이 향상된 것으로 간주할 수 있다. 본원에 기술된 바와 같은 다가 항원 제시의 효과 향상은 다가 제제로 접종된 마우스 그룹과 동일한 항원 제시에서 일치하는 단가 제제 간의 가성 중화 역가를 비교하여 평가할 수 있다.
공동 캡슐화된 SpFN 항원 제시 형식(그룹 25)에서 WA-1, BQ.1.1, 및 SARS-CoV-1(믹스 B)을 함유하는 중간 항원 거리 세트에 의해 유발된 베타 균주에 대한 중화 역가는 WA-1, BQ.1.1, 또는 SARS-1 단가 SpFN(그룹 19-21)에 의해 유발된 것과 비교하여 향상되었다(도 23, 패널 C). 믹스 B SpFN의 경우 베타 유사바이러스에 대한 역가도 모든 항원 제시에 걸쳐 베타 균주를 함유하지 않는 임의의 다른 다가 또는 단가에 비해 개선되었다(마우스 그룹당 GMT 역가 및 최소 역가 기준).
이론에 얽매이지 않고, 베타 유사바이러스에 대한 이러한 역가 향상은 더 광범위한 공통 에피토프(예를 들어, 균주 간 누적된 돌연변이에 대한 내성이 있는 항체)에 결합하는 항체의 생성에 의해 매개될 수 있어 동일한 나노입자에 표시된 WA-1, BQ.1.1, 및 SARS-CoV-1 SpFN 구축물 중 두 가지에 동시에 결합할 수 있다. 이 결과는 믹스 B의 구성 균주가 베타 균주 항원을 함유하지 않지만 여전히 1:2560 초과의 중화 역가를 유발했기 때문에 향상된 면역 반응 폭의 증거이다. 마찬가지로, 공동 캡슐화된 SpFN 또는 공동 투여된 S-2P 믹스 B를 사용한 면역화도 XBB.1.5 균주의 교차 중화가 향상되는 경향이 있다(도 23f 및 24f). 공동 캡슐화된 SpFN 믹스 B를 사용한 면역화도 BQ.1.1에 대한 동종 역가가 향상하는 경향이 있다(도 23, 패널 E).
다른 연구자들은 8가지 SARS-CoV-1 및 SARS CoV-2 균주를 제시하는 다가 디스플레이 시스템으로 접종하여 여러 SARS-CoV-1 균주에 대한 역가 증가를 보고했지만, 해당 보고서에서 관찰된 모든 역가는 구성 항원에 의한 백신접종과 일치하였다. 다시 말해, 임의의 폭 증가는 항원 간 교차 결합이 아니라 단순히 존재하는 각 개별 항원에 의해 매개되었다. 이와 대조적으로, 본원의 결과는 하나 이상의 다가 항원 간의 주변 결합에 의해 반드시 매개되는 폭 증가를 보여준다.
다가
SpFN
항원 제시 형식은 다가 S-2P 형식보다 더 높은 중화
역가를
유발한다
안정화된 막관통 단백질(S-2P) 및 SpFN으로 제시된 믹스 B 항원 거리 세트를 접종한 마우스 그룹 간의 가성 중화 역가를 비교하여 페리틴 항원 제시 시스템의 이점을 입증한다. 도 25는 단가 및 다가 SpFN 그룹과 S-2P 그룹 간의 가성 중화 역가를 비교한다. 단가 그룹(열린 원; S-2P, 단가 그룹 15-17, 37-40; SpFN, 단가 그룹 18-24)의 경우, x=y 선(파선)을 따라 추세를 보이는 중화 역가가 관찰되었으며, 이는 역가가 항원 제시 전반에 걸쳐 거의 동일함을 시사한다. 그러나 다가 그룹(채워진 원; S-2P, 그룹 31, 41-44; SpFN, 그룹 25-29)은 SpFN 항원 제시에 대한 개선된 가성 중화 역가를 보였으며, 이는 테스트된 6가지 균주 중 4가지에서 x = y 선(파선) 위의 역가로 밝혀졌다(도 25에 표시되지 않은 SARS-CoV-1 및 XBB.1.5는 제외).
공동 캡슐화 및 공동 투여된 다가 항원
공동 캡슐화된 mRNA의 LNP 제제 대 별도로 캡슐화된 mRNA의 혼합물의 LNP 제제(예를 들어, 각 mRNA 분자를 LNP에 별도로 캡슐화하고 공동 투여)로 접종한 마우스 그룹에서 얻은 결과를 비교하여 공동 캡슐화와 별도의 캡슐화 간에 유의미한 차이가 나타나지 않았다. 가성 중화 역가는 세 가지 모두 공동 투여된 혼합물과 그것의 공동 캡슐화된 대응물 간에 매우 유사하였다. 이는 각 유형의 개별 mRNA/LNP 제제가 각 세포에 의해 흡수되어 유사한 발현 패턴과 나노입자 형성을 초래한다는 것을 시사한다(도 26a-26d).
RFN
,
SpFN
및
S2P
항원 제시 형식에 의해 유발된 중화
역가
이들 RFN, SpFN, 및 S-2P 항원 디스플레이 형식 간에 일치하는 균주 세트를 비교했을 때, SpFN 제제는 모든 클레이드 1a 및 1b 판독값에서 개선된 역가를 보였다(도 20-23). 예외적으로 MERS 판독값은 RFN 및 SpFN 구축물과, MERS 구축물을 함유하는 제제 모두에 대해 강력한 면역원성을 보였다.
실시예
6: 부스터
백신으로서 다가
항원
0일차 및 21일차에 WA-1을 코딩하는 mRNA로 프라이밍하고, 3개월 후에 표 9에 표시된 제제 및 용량 수준으로 부스트(1차 부스트)한 BALB/C 암컷 마우스(n=8)에서 다가 조성물이 부스터 백신 접종 시 교차 중화 항체를 유발하는 능력을 평가한다. 마우스는 부스트 1일 전에 채혈하여 모든 그룹의 부스트 전 역가를 평가한다. 그런 다음 동물은 부스트 2주 후에 채혈하여 그룹 간 부스트 후 역가를 결정하고 비교한다. 이 연구에는 제안된 신규 부스터 제제에 대한 대조구로서 상업용 S2-P XBB.1.5 SARS CoV-2(SoC) 백신이 포함된다.
선택된 S-2P 및 SpFN 다가 제제(베타, BQ.1.1, SARS-CoV-1)와 단가 대조군 WA-1 S-2P 및 SpFN에 대해 중화 항체의 폭에서의 잠재적인 추가의 증가에 대한 2차 부스트의 효과를 테스트한다. 1차 부스트 1개월 후에 2차 부스트를 도입한다. 마우스는 2차 부스트를 투여하기 1일 전에 채혈한 다음 2차 부스트 2주 후에 다시 채혈하여 2차 부스트 전과 후 역가를 평가한다. 이 연구의 모든 채혈은 임상 관련성에 대해 선택된 클레이드 1a, 1b, 3 및 4에 걸친 정의된 균주 패널에 대한 가성 중화 역가에 대해 테스트한다.
구체적인 투여 요법은 다음과 같다: 프라이밍: 0일차 및 21일차; 채혈: 35일차; 부스트 전 채혈: 1차 부스트 약 1일 전; 1차 부스트: 21일차 3개월 후(119일차); 채혈: 1차 부스트 2주 후(133일차); 2차 부스트 전 채혈: 2차 부스트 약 1일 전(150일차); 2차 부스트: 1차 부스트 1개월 후(151일차). 각 그룹에는 8마리의 마우스가 있다. 투여 요법은 도 31에 도시한다.
이 연구의 경우, 다가 조성물은 주어진 항원을 코딩하는 mRNA 분자를 별도로 캡슐화하는 LNP의 혼합물을 포함하지만, 다른 연구에서는 단일 LNP에 공동 캡슐화된 여러 mRNA 분자를 포함하는 다가 조성물을 사용할 수 있다.
서열목록 전자파일 첨부
Claims (38)
- 적어도 제1 항원성 코로나바이러스 펩티드와 제2 항원성 코로나바이러스 펩티드를 포함하는 적어도 두 개의 항원성 코로나바이러스 펩티드, 또는 이를 코딩하는 하나 이상의 메신저 RNA(mRNA) 분자를 포함하는 면역원성 조성물로서, 각 항원성 코로나바이러스 펩티드는
a. 코로나바이러스의 수용체 결합 도메인(RBD 또는 R), 또는 이의 단편 또는 변이체,
b. 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체,
c. 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체,
d. 코로나바이러스의 안정화된 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체,
e. 코로나바이러스의 안정화된 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 및
f. 코로나바이러스의 안정화된 스파이크 S-삼량체, 또는 이의 단편 또는 변이체
로부터 독립적으로 선택되며,
g. 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함하는 것인 조성물:
(i) 둘 이상의 선택된 클레이드 1b;
(ii) 클레이드 1b로부터 선택된 하나 이상 및 클레이드 1a SARS-CoV-1로부터 선택된 하나 이상;
(iii) 클레이드 1b로부터 선택된 하나 이상, 및 클레이드 1a로부터 선택된 하나 이상, 및 클레이드 2로부터 선택된 하나 이상;
(iv) 클레이드 1b로부터 선택된 하나 이상, 및 클레이드 1a로부터 선택된 하나 이상, 및 클레이드 3으로부터 선택된 하나 이상;
(v) 클레이드 1b로부터 선택된 하나 이상, 클레이드 2로부터 선택된 하나 이상, 및 클레이드 3으로부터 선택된 하나 이상; 및
(v) 클레이드 1a로부터 선택된 하나 이상, 클레이드 2로부터 선택된 하나 이상, 및 클레이드 3으로부터 선택된 하나 이상. - 제1항에 있어서, 상기 항원성 코로나바이러스 펩티드 중 적어도 하나는 S-2P 펩티드이며, 선택적으로 S-2P 펩티드는 서열 번호 536-543 중 어느 하나의 아미노산 서열, 또는 이에 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 또는 적어도 99%의 상동성 또는 동일성을 갖는 서열을 포함하는 것인 조성물.
- 제1항 또는 제2항에 있어서, 상기 항원성 코로나바이러스 펩티드 중 적어도 하나는 항원성 코로나바이러스 펩티드와 나노입자 형성 단백질을 포함하는 융합 단백질에 포함되며, 상기 항원성 코로나바이러스 펩티드 중 둘 이상은 나노입자 형성 단백질과의 동일하거나 상이한 융합 단백질에 포함될 수 있는 것인 조성물.
- 적어도 제1 항원성 코로나바이러스 펩티드와 제2 항원성 코로나바이러스 펩티드를 포함하는 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 나노입자, 또는 적어도 두 개의 항원성 코로나바이러스 펩티드를 코딩하는 하나 이상의 메신저 RNA(mRNA) 분자를 포함하는 면역원성 조성물로서,
각 항원성 코로나바이러스 펩티드는
a. 코로나바이러스의 수용체 결합 도메인(RBD 또는 R), 또는 이의 단편 또는 변이체,
b. 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체,
c. 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체,
d. 코로나바이러스의 안정화된 세포외 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체,
e. 코로나바이러스의 안정화된 세포외 스파이크 S 도메인, 또는 이의 단편 또는 변이체, 및
f. 코로나바이러스의 안정화된 세포외 스파이크 S-삼량체, 또는 이의 단편 또는 변이체
로부터 독립적으로 선택되며,
각 항원성 코로나바이러스 펩티드는 항원성 코로나바이러스 펩티드와 나노입자 형성 단백질을 포함하는 융합 단백질에 포함되며, 항원성 코로나바이러스 펩티드는 동일하거나 상이한 융합 단백질에 포함될 수 있고,
조성물은 적어도 두 가지 상이한 코로나바이러스 균주의 항원성 코로나바이러스 펩티드, 또는 이를 코딩하는 하나 이상의 mRNA 분자를 포함하는 것인 조성물. - 제4항에 있어서, 각 항원성 코로나바이러스 펩티드는 클레이드 1a, 클레이드 1b, 클레이드 2, 클레이드 3, 및 중동 호흡기 증후군 관련 코로나바이러스(MERS-CoV)로부터 독립적으로 선택된 코로나바이러스 균주로부터 유래되고, 선택적으로 적어도 제1 및 제2 항원성 코로나바이러스 펩티드는 상이한 클레이드의 코로나바이러스 균주로부터 유래되는 것인 조성물.
- 제4항 또는 제5항에 있어서, 적어도 제1 및 제2 항원성 코로나바이러스 펩티드는 WA-1, 베타, 오미크론 BQ.1.1, 오미크론 XBB.1.5, SARS-CoV-1 균주, BANAL20-247, Khosta2, 및 MERS-CoV로부터 독립적으로 선택된 상이한 코로나바이러스 균주로부터 유래되는 것인 조성물.
- 제1항 내지 제6항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함하는 것인 조성물:
(i) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ1.1로부터 선택된 둘 이상;
(ii) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주;
(iii) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 하나 이상;
(iv) WA-1, 베타, 오미크론 XBB.1.5, 및 오미크론 BQ1.1로부터 선택된 하나 이상, 및 SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 하나 이상, 및 MERS-CoV; 및
(v) SARS-CoV-1 균주, BANAL20-247, 및 Khosta-2로부터 선택된 둘 이상. - 제1항 내지 제7항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함하는 것인 조성물:
a. WA-1, 베타, 및 오미크론 BQ1.1;
b. WA-1, 오미크론 BQ.1.1, 및 SARS-CoV-1;
c. WA-1, SARS-CoV-1, 및 Khosta2;
d. WA-1, SARS-CoV-1, 및 BANAL20-247;
e. WA-1, SARS-CoV-1, 및 MERS-CoV; 및
f. SAR-CoV-1, Khosta-2, 및 BANAL20-247. - 제1항 내지 제8항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 다음의 균주 조합으로부터 선택된 항원성 코로나바이러스 펩티드를 포함하는 것인 조성물:
(i) WA-1, 베타, 및 오미크론 BQ.1.1(또는 XBB.1.5), 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(베타)FN, 및 R(BQ1.1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(베타)-2P, 및 S(BQ1.1)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(베타)FN, 및 Sp(BQ1.1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(ii) WA-1, 오미크론 BQ.1.1(또는 XBB1.5), 및 SARS-CoV-1, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(BQ 1.1)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(BQ 1.1)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(BQ 1.1)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(iii) WA-1, SARS-CoV-1, 및 Khosta2, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(Khosta2)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(Khosta2)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(Khosta2)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(iv) WA-1, SARS-CoV-1, 및 BANAL20-247, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(BANAL20-247)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(BANAL20-247)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(BANAL20-247)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(v) WA-1, SARS-CoV-1, 및 MERS-CoV, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(WA-1)FN, R(SARS-CoV-1)FN, 및 R(MERS-CoV)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(WA-1)-2P, S(SARS-CoV-1)-2P, 및 S(MERS-CoV)-2P) 또는 SpFN 융합 단백질 Sp(WA-1)FN, Sp(SARS-CoV-1)FN, 및 Sp(MERS-CoV)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(vi) SARS-CoV-1, Khosta-2, 및 BANAL20-247, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(SARS-CoV-1)FN, R(Khosta2)FN, 및 R(BANAL20-247)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(SARS-CoV-1)-2P, S(Khosta2)-2P, 및 S(BANAL20-247)-2P) 또는 SpFN 융합 단백질 Sp(SARS-CoV-1)FN, Sp(Khosta2)FN, 및 Sp(BANAL20-247)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(vii) 베타, 오미크론 BQ.1.1(또는 XBB1.5), 및 SARS-CoV-1, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(베타)FN, R(BQ 1.1)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(베타)-2P, S(BQ 1.1)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(베타)FN, Sp(BQ 1.1)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(viii) 베타, 오미크론 XBB.1.5, 및 SARS-CoV-1, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(베타)FN, R(XBB 1.5)FN, 및 R(SARS-CoV-1)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(베타)-2P, S(XBB 1.5)-2P, 및 S(SARS-CoV-1)-2P) 또는 SpFN 융합 단백질 Sp(베타)FN, Sp(XBB1.5)FN, 및 Sp(SARS-CoV-1)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임;
(ix) 오미크론 BQ.1.1, SARS-CoV-1, 및 Khosta2, 선택적으로 여기서 항원성 코로나바이러스 펩티드는 RFN 융합 단백질 R(오미크론 BQ.1.1)FN, R(SARS-CoV-1)FN, 및 R(Khosta2)FN에 포함된 RBD 항원이거나, S-2P(예를 들어, S(오미크론 BQ.1.1)-2P, S(SARS-CoV-1)-2P, 및 S(Khosta2)-2P) 또는 SpFN 융합 단백질 Sp(오미크론 BQ.1.1)FN, Sp(SARS-CoV-1)FN, 및 Sp(Khosta2)FN에 포함된 스파이크 항원이거나, RmosSpFN 또는 RRmosSpFN 융합 단백질에 포함된 모자이크 항원이거나, 이들의 임의의 조합임. - 제3항 내지 제9항 중 어느 한 항에 있어서, 나노입자 형성 펩티드는 페리틴 단백질 또는 이의 단편 또는 변이체이거나 이를 포함하는 것인 조성물.
- 제3항 내지 제9항 중 어느 한 항에 있어서, 나노입자 형성 펩티드는 헬리코박터 파일로리(Helicobacter pylori) 페리틴(Hpf) 또는 이의 단편 또는 변이체이거나 이를 포함하는 것인 조성물.
- 제3항 내지 제9항 중 어느 한 항에 있어서, 나노입자 형성 펩티드는 다음으로부터 선택된 아미노산 서열을 포함하는 것인 조성물:
- 제1항 내지 제12항 중 어느 한 항에 있어서, 적어도 두 개의 상기 항원성 코로나바이러스 펩티드는 융합 단백질에 포함되며, 항원성 코로나바이러스 펩티드는 링커를 통해 연결되는 것인 조성물.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 2-10개의 상기 항원성 코로나바이러스 펩티드는 융합 단백질에 직렬로 포함되며, 선택적으로 항원성 코로나바이러스 펩티드는 링커를 통해 연결되는 것인 조성물.
- 제3항 내지 제14항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 나노입자 형성 펩티드와의 융합 단백질에 포함되며, 항원성 코로나바이러스 펩티드는 링커를 통해 나노입자 형성 펩티드에 연결되는 것인 조성물.
- 제13항 내지 제15항 중 어느 한 항에 있어서, 링커는 다음으로부터 선택된 아미노산 서열을 포함하는 것인 조성물: GGGSGGSG(서열 번호 583), GSGGGG(서열 번호 11), GGGG(서열 번호 15), GSGG(서열 번호 5), GGG(서열 번호 16), 및 SGG(서열 번호 17).
- 제1항 내지 제16항 중 어느 한 항에 있어서, 제1 및 제2 항원성 코로나바이러스 펩티드는 모자이크 코로나바이러스 스파이크 단백질에 포함되며, 모자이크 코로나바이러스 스파이크 단백질의 적어도 하나의 도메인은 이종 코로나바이러스 균주로부터 치환되거나 추가되는 것인 조성물.
- 제3항 내지 제17항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 나노입자 형성 펩티드와의 융합 단백질에 포함되며, 융합 단백질(들)은 SpFn, 실에 꿰어진 구슬(beads on a string), 도메인 융합, 도메인 스왑, 루프 삽입, 및 도메인 삽입으로부터 선택된 하나 이상의 형식을 포함하는 것인 조성물.
- 제3항 내지 제18항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 나노입자 형성 펩티드와의 융합 단백질에 포함되며, 융합 단백질은 도 2 내지 7 중 어느 하나에 도시된 형식으로부터 선택된 형식을 갖는 것인 조성물.
- 제3항 내지 제19항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 나노입자 형성 펩티드와의 융합 단백질에 포함되고, 적어도 제1 및 제2 항원성 코로나바이러스 펩티드는 동일한 융합 단백질(예를 들어, R1R2FN)에 포함된 상이한 코로나바이러스 균주의 상이한 RBD 펩티드(예를 들어, R1, R2)이며, 선택적으로 융합 단백질은 스파이크 단백질(예를 들어, R1R2mosSpFN)을 추가로 포함하고, 추가로 선택적으로 조성물은 융합 단백질의 상이한 위치에 동일한 두 개 이상의 상이한 RBD 펩티드를 포함하는 두 개 이상의 상이한 융합 단백질(예를 들어, R1R2FN, R2R1FN 또는 R1R2mosSpFN, R2R1mosSpFN), 또는 상기 두 개 이상의 상이한 융합 단백질을 코딩하는 mRNA 분자, 또는 상기 두 개 이상의 상이한 융합 단백질을 표시하는 나노입자를 포함하는 것인 조성물.
- 제1항 내지 제20항 중 어느 한 항에 있어서, 항원성 코로나바이러스 펩티드는 표 6 또는 표 7에 개시된 서열(서열 번호 29-551)로부터 선택된 아미노산 서열, 또는 이에 적어도 80%의 서열 동일성을 갖는 서열을 포함하는 하나 이상의 융합 단백질에 포함되는 것인 조성물.
- 제3항 내지 제21항 중 어느 한 항에 있어서, 조성물은 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 나노입자를 포함하는 것인 조성물.
- 제1항 내지 제21항 중 어느 한 항에 있어서, 조성물은 적어도 두 개의 항원성 코로나바이러스 펩티드를 코딩하는 하나 이상의 mRNA 분자를 포함하며, 선택적으로 하나 이상의 mRNA 분자는 하나 이상의 지질 나노입자(LNP)에 캡슐화되거나 공동 캡슐화되는 것인 조성물.
- 제23항에 있어서, 다음으로부터 선택된 조성물:
a. 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 하나의 융합 단백질을 코딩하는 하나의 mRNA 분자를 포함하는 조성물로서, 선택적으로 융합 단백질은 나노입자 형성 펩티드를 추가로 포함하고, mRNA 분자는 지질 나노입자(LNP)에 캡슐화되는 것인 조성물;
b. 선택적으로 나노입자 형성 펩티드와의 융합 단백질에 있는, 적어도 두 개의 항원성 코로나바이러스 펩티드 중 적어도 하나를 각각 코딩하는 두 개 이상의 mRNA 분자를 포함하는 조성물로서, 각 mRNA 분자는 별도의 지질 나노입자(LNP)에 캡슐화되는 것인 조성물;
c. 선택적으로 나노입자 형성 펩티드와의 융합 단백질에 있는, 적어도 두 개의 항원성 코로나바이러스 펩티드 중 적어도 하나를 각각 코딩하는 두 개 이상의 mRNA 분자를 포함하는 조성물로서, 두 개 이상의 mRNA 분자는 동일한 지질 나노입자(LNP)에 공동 캡슐화되는 것인 조성물. - 제1항 내지 제24항 중 어느 한 항에 있어서, mRNA 분자를 포함하는 조성물로서, mRNA 분자는
a. 5' 비번역 영역(5' UTR);
b. 3' 비번역 영역(3' UTR);
c. 폴리아데닐화(폴리(A)) 서열;
d. 화학적 변형, 선택적으로 화학적 변형은 N1-메틸슈도우리딘을 포함함; 및
e. 자가 복제 mRNA 또는 비복제 mRNA인 mRNA
로부터 선택된 하나 이상의 특징을 가지며,
선택적으로 mRNA 분자는 지질 나노입자(LNP)에 캡슐화되는 것인 조성물. - 제1항 내지 제25항 중 어느 한 항에 있어서, 보조제를 추가로 포함하는 조성물.
- 제26항에 있어서, 조성물은 항원 또는 나노입자를 포함하고, 보조제는 ALFQ, 알히드로겔, 및 이들의 조합으로부터 선택된 하나 이상을 포함하는 것인 조성물.
- 나노입자 형성 펩티드 및 다음으로부터 독립적으로 선택된 적어도 두 개의 항원성 코로나바이러스 펩티드를 포함하는 융합 단백질을 포함하는 나노입자:
a. 코로나바이러스의 수용체 결합 도메인(RBD), 또는 이의 단편 또는 변이체,
b. 코로나바이러스의 N-말단 도메인(NTD), 또는 이의 단편 또는 변이체,
c. 코로나바이러스의 S1 도메인, 또는 이의 단편 또는 변이체,
d. 코로나바이러스의 안정화된 세포외 스파이크 S-2P 도메인, 또는 이의 단편 또는 변이체,
e. 코로나바이러스의 안정화된 세포외 스파이크 S 도메인, 또는 이의 단편 또는 변이체,
f. 코로나바이러스의 안정화된 세포외 스파이크 S-삼량체, 또는 이의 단편 또는 변이체, 및
g. 모자이크 코로나바이러스 스파이크 단백질, 여기서 모자이크 코로나바이러스 스파이크 단백질의 적어도 하나의 도메인은 이종 코로나바이러스 균주로부터 치환되거나 추가됨. - 제28항에 따른 나노입자를 코딩하는 서열을 포함하는 DNA 분자, 또는 상기 DNA 분자를 포함하는 플라스미드, 선택적으로 생체 내에서 DNA 분자를 발현할 수 있는 플라스미드.
- 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하는 방법으로서, 이를 필요로 하는 대상체에게 제1항 내지 제29항 중 어느 한 항의 면역원성 조성물을 투여하는 단계를 포함하는 방법.
- 제1항 내지 제29항 중 어느 한 항에 있어서, 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하는 데 사용하기 위한 면역원성 조성물.
- 코로나바이러스 감염의 치료 또는 예방을 필요로 하는 대상체에서 이를 치료 또는 예방하기 위한 의약을 제조하는 데 있어서의 제1항 내지 제29항 중 어느 한 항의 면역원성 조성물의 용도.
- 제30항 내지 제32항 중 어느 한 항에 있어서, 대상체는 코로나바이러스 감염 위험에 있는 것인 방법, 조성물, 또는 용도.
- 제30항 내지 제32항 중 어느 한 항에 있어서, 대상체는 이미 코로나바이러스에 감염된 것인 방법, 조성물, 또는 용도.
- 제30항 내지 제34항 중 어느 한 항에 있어서, 대상체는 이전에 코로나바이러스 감염 예방을 위한 백신을 투여받은 적이 없는 것인 방법, 조성물, 또는 용도.
- 제30항 내지 제34항 중 어느 한 항에 있어서, 대상체는 이전에 코로나바이러스 감염 예방을 위한 하나 이상의 백신을 투여받은 적이 있는 것인 방법, 조성물, 또는 용도.
- 제30항 내지 제36항 중 어느 한 항에 있어서, 상기 방법은 대상체에서 코로나바이러스에 대한 면역 반응을 유발하고, 선택적으로 면역 반응은 중화 항체를 포함하고, 추가로 선택적으로 중화 항체는 두 가지 이상의 코로나바이러스 균주를 교차 중화하고, 추가로 선택적으로 중화 항체는 면역원성 조성물의 구성 균주가 아닌 하나 이상의 코로나바이러스 균주를 교차 중화하는 것인 방법, 조성물, 또는 용도.
- 서열 번호 552-582 중 어느 하나로부터 선택된 서열 또는 이에 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 또는 적어도 99%의 상동성 또는 동일성을 갖는 서열을 포함하거나 이로 이루어진 mRNA 분자.
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202263399990P | 2022-08-22 | 2022-08-22 | |
| US63/399,990 | 2022-08-22 | ||
| US202263400334P | 2022-08-23 | 2022-08-23 | |
| US63/400,334 | 2022-08-23 | ||
| US202263431286P | 2022-12-08 | 2022-12-08 | |
| US63/431,286 | 2022-12-08 | ||
| EP23315318.8 | 2023-08-17 | ||
| EP23315318 | 2023-08-17 | ||
| PCT/US2023/030602 WO2024044108A1 (en) | 2022-08-22 | 2023-08-18 | Vaccines against coronaviruses |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20250099770A true KR20250099770A (ko) | 2025-07-02 |
Family
ID=88016638
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020257009272A Pending KR20250099770A (ko) | 2022-08-22 | 2023-08-18 | 코로나바이러스에 대한 백신 |
Country Status (7)
| Country | Link |
|---|---|
| EP (1) | EP4577236A1 (ko) |
| JP (1) | JP2025529906A (ko) |
| KR (1) | KR20250099770A (ko) |
| CN (1) | CN120813372A (ko) |
| AU (1) | AU2023330867A1 (ko) |
| CA (1) | CA3265295A1 (ko) |
| WO (1) | WO2024044108A1 (ko) |
Family Cites Families (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5132418A (en) | 1980-02-29 | 1992-07-21 | University Patents, Inc. | Process for preparing polynucleotides |
| US4458066A (en) | 1980-02-29 | 1984-07-03 | University Patents, Inc. | Process for preparing polynucleotides |
| US4500707A (en) | 1980-02-29 | 1985-02-19 | University Patents, Inc. | Nucleosides useful in the preparation of polynucleotides |
| US4668777A (en) | 1981-03-27 | 1987-05-26 | University Patents, Inc. | Phosphoramidite nucleoside compounds |
| US4415732A (en) | 1981-03-27 | 1983-11-15 | University Patents, Inc. | Phosphoramidite compounds and processes |
| US4973679A (en) | 1981-03-27 | 1990-11-27 | University Patents, Inc. | Process for oligonucleo tide synthesis using phosphormidite intermediates |
| US4373071A (en) | 1981-04-30 | 1983-02-08 | City Of Hope Research Institute | Solid-phase synthesis of polynucleotides |
| US4401796A (en) | 1981-04-30 | 1983-08-30 | City Of Hope Research Institute | Solid-phase synthesis of polynucleotides |
| US5153319A (en) | 1986-03-31 | 1992-10-06 | University Patents, Inc. | Process for preparing polynucleotides |
| US5047524A (en) | 1988-12-21 | 1991-09-10 | Applied Biosystems, Inc. | Automated system for polynucleotide synthesis and purification |
| US5262530A (en) | 1988-12-21 | 1993-11-16 | Applied Biosystems, Inc. | Automated system for polynucleotide synthesis and purification |
| US5885613A (en) | 1994-09-30 | 1999-03-23 | The University Of British Columbia | Bilayer stabilizing components and their use in forming programmable fusogenic liposomes |
| US5700642A (en) | 1995-05-22 | 1997-12-23 | Sri International | Oligonucleotide sizing using immobilized cleavable primers |
| US5744335A (en) | 1995-09-19 | 1998-04-28 | Mirus Corporation | Process of transfecting a cell with a polynucleotide mixed with an amphipathic compound and a DNA-binding protein |
| DE602005012382D1 (de) | 2004-05-18 | 2009-03-05 | Alphavax Inc | Von tc-83 abgeleitete alphavirus-vektoren, partikel und verfahren |
| CA2766907A1 (en) | 2009-07-06 | 2011-01-13 | Novartis Ag | Self replicating rna molecules and uses thereof |
| ES2666559T3 (es) | 2009-12-01 | 2018-05-07 | Translate Bio, Inc. | Entrega del mrna para la aumentación de proteínas y enzimas en enfermedades genéticas humanas |
| WO2012075040A2 (en) | 2010-11-30 | 2012-06-07 | Shire Human Genetic Therapies, Inc. | mRNA FOR USE IN TREATMENT OF HUMAN GENETIC DISEASES |
| BR112013031553A2 (pt) | 2011-06-08 | 2020-11-10 | Shire Human Genetic Therapies, Inc. | composições, mrna que codifica para uma hgla e seu uso, uso de pelo menos uma molécula de mrna e um veículo de transferência e uso de um mrna que codifica para proteína exógena |
| NZ747501A (en) | 2011-10-27 | 2020-05-29 | Massachusetts Inst Technology | Amino acid derivatives functionalized on the n-terminal capable of forming drug encapsulating microspheres |
| CA2876155C (en) | 2012-06-08 | 2022-12-13 | Ethris Gmbh | Pulmonary delivery of mrna to non-lung target cells |
| CA2903487A1 (en) | 2013-03-14 | 2014-09-25 | Shire Human Genetic Therapies, Inc. | Quantitative assessment for cap efficiency of messenger rna |
| ES2795249T3 (es) | 2013-03-15 | 2020-11-23 | Translate Bio Inc | Mejora sinérgica de la administración de ácidos nucleicos a través de formulaciones mezcladas |
| CN105451779A (zh) | 2013-08-21 | 2016-03-30 | 库瑞瓦格股份公司 | 增加rna编码蛋白表达的方法 |
| WO2015062738A1 (en) | 2013-11-01 | 2015-05-07 | Curevac Gmbh | Modified rna with decreased immunostimulatory properties |
| CA2927254C (en) | 2013-12-30 | 2023-10-24 | Curevac Ag | Artificial nucleic acid molecules |
| KR102399799B1 (ko) | 2013-12-30 | 2022-05-18 | 큐어백 아게 | 인공 핵산 분자 |
| US9668980B2 (en) | 2014-07-02 | 2017-06-06 | Rana Therapeutics, Inc. | Encapsulation of messenger RNA |
| DE202015009961U1 (de) | 2014-12-12 | 2022-01-25 | Curevac Ag | Artifizielle Nukleinsäuremoleküle für eine verbesserte Proteinexpression |
| EP3289101B1 (en) | 2015-04-30 | 2021-06-23 | CureVac AG | Immobilized poly(n)polymerase |
| HRP20230494T1 (hr) | 2015-06-19 | 2023-08-04 | Massachusetts Institute Of Technology | Alkenil supstituirani 2,5-piperazindioni i njihova upotreba u pripravcima za isporuku sredstva subjektu ili stanici |
| WO2017162265A1 (en) | 2016-03-21 | 2017-09-28 | Biontech Rna Pharmaceuticals Gmbh | Trans-replicating rna |
| MX2019005470A (es) | 2016-11-10 | 2019-11-21 | Translate Bio Inc | Formulación de nanopartículas lipídicas basadas en ice mejorada para el suministro de arnm. |
| AU2017357758B2 (en) | 2016-11-10 | 2023-11-16 | Translate Bio, Inc. | Improved process of preparing mRNA-loaded lipid nanoparticles |
| CN117098553A (zh) * | 2020-11-11 | 2023-11-21 | 加州理工学院 | 多价载体和相关疫苗组合物 |
| AU2022207495A1 (en) * | 2021-01-15 | 2023-08-03 | Modernatx, Inc. | Variant strain-based coronavirus vaccines |
| AU2022208057A1 (en) * | 2021-01-15 | 2023-08-03 | Modernatx, Inc. | Variant strain-based coronavirus vaccines |
| TW202309002A (zh) | 2021-04-15 | 2023-03-01 | 美商轉譯生技公司 | 基於「古德」緩衝液的陽離子脂質 |
| CN113861278B (zh) * | 2021-06-18 | 2022-08-05 | 国药中生生物技术研究院有限公司 | 一种产生广谱交叉中和活性的重组新型冠状病毒rbd三聚体蛋白疫苗、其制备方法和应用 |
| WO2023283645A1 (en) * | 2021-07-09 | 2023-01-12 | Modernatx, Inc. | Pan-human coronavirus domain vaccines |
| US20250134987A1 (en) * | 2021-10-15 | 2025-05-01 | Yale University | Compositions and methods for vaccination against pathogenic coronavirus species and variants |
-
2023
- 2023-08-18 CA CA3265295A patent/CA3265295A1/en active Pending
- 2023-08-18 JP JP2025511847A patent/JP2025529906A/ja active Pending
- 2023-08-18 KR KR1020257009272A patent/KR20250099770A/ko active Pending
- 2023-08-18 EP EP23768415.4A patent/EP4577236A1/en active Pending
- 2023-08-18 AU AU2023330867A patent/AU2023330867A1/en active Pending
- 2023-08-18 WO PCT/US2023/030602 patent/WO2024044108A1/en not_active Ceased
- 2023-08-18 CN CN202380073582.3A patent/CN120813372A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU2023330867A1 (en) | 2025-03-06 |
| WO2024044108A1 (en) | 2024-02-29 |
| CA3265295A1 (en) | 2024-02-29 |
| JP2025529906A (ja) | 2025-09-09 |
| CN120813372A (zh) | 2025-10-17 |
| EP4577236A1 (en) | 2025-07-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20230302112A1 (en) | Respiratory synctial virus rna vaccine | |
| US20230310571A1 (en) | Human metapneumovirus vaccines | |
| KR20240022610A (ko) | 다가 인플루엔자 백신 | |
| JP2025503994A (ja) | コロナウイルスワクチン | |
| US20250009863A1 (en) | Lyme disease rna vaccine | |
| JP2024530047A (ja) | ワクチン抗原 | |
| KR20250155051A (ko) | 클라미디아의 치료에 사용하기 위한 조성물 | |
| US12397051B2 (en) | Vaccine for use against coronavirus and variants thereof | |
| KR20250099770A (ko) | 코로나바이러스에 대한 백신 | |
| US20250009865A1 (en) | Combination respiratory mrna vaccines | |
| US20240374698A1 (en) | Compositions for use in treatment of acne | |
| KR20260010728A (ko) | 조합 호흡기 mrna 백신 | |
| WO2025017202A2 (en) | Porphyromonas gingivalis antigenic constructs | |
| JP2026504629A (ja) | 安定化ワクチン | |
| JP2026504797A (ja) | クラミジア(Chlamydia)の治療に使用するための組成物 | |
| CN118159287A (zh) | 呼吸道合胞病毒rna疫苗 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20250320 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application |