KR20230097043A - Method for producing modified lithium nickel manganese cobalt composite oxide particles - Google Patents
Method for producing modified lithium nickel manganese cobalt composite oxide particles Download PDFInfo
- Publication number
- KR20230097043A KR20230097043A KR1020237014914A KR20237014914A KR20230097043A KR 20230097043 A KR20230097043 A KR 20230097043A KR 1020237014914 A KR1020237014914 A KR 1020237014914A KR 20237014914 A KR20237014914 A KR 20237014914A KR 20230097043 A KR20230097043 A KR 20230097043A
- Authority
- KR
- South Korea
- Prior art keywords
- composite oxide
- cobalt composite
- lithium nickel
- nickel manganese
- oxide particles
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000002245 particle Substances 0.000 title claims abstract description 308
- 239000002131 composite material Substances 0.000 title claims abstract description 237
- SOXUFMZTHZXOGC-UHFFFAOYSA-N [Li].[Mn].[Co].[Ni] Chemical class [Li].[Mn].[Co].[Ni] SOXUFMZTHZXOGC-UHFFFAOYSA-N 0.000 title claims abstract description 214
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 53
- 239000010936 titanium Substances 0.000 claims abstract description 176
- 229910052719 titanium Inorganic materials 0.000 claims abstract description 92
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 claims abstract description 79
- 239000013522 chelant Substances 0.000 claims abstract description 79
- 150000001875 compounds Chemical class 0.000 claims abstract description 62
- 229910052744 lithium Inorganic materials 0.000 claims abstract description 41
- 238000004381 surface treatment Methods 0.000 claims abstract description 41
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims abstract description 39
- 238000010438 heat treatment Methods 0.000 claims abstract description 27
- 239000007774 positive electrode material Substances 0.000 claims abstract description 21
- 238000012986 modification Methods 0.000 claims abstract description 10
- 230000004048 modification Effects 0.000 claims abstract description 10
- 150000003863 ammonium salts Chemical class 0.000 claims abstract description 9
- 125000004429 atom Chemical group 0.000 claims description 35
- 239000007788 liquid Substances 0.000 claims description 34
- 239000003513 alkali Substances 0.000 claims description 24
- 238000000034 method Methods 0.000 claims description 24
- 238000002156 mixing Methods 0.000 claims description 24
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 claims description 15
- 229910052751 metal Inorganic materials 0.000 claims description 12
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 claims description 8
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 claims description 8
- 230000008569 process Effects 0.000 claims description 7
- 229910052782 aluminium Inorganic materials 0.000 claims description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 6
- 125000003545 alkoxy group Chemical group 0.000 claims description 5
- 125000005843 halogen group Chemical group 0.000 claims description 5
- 125000003277 amino group Chemical group 0.000 claims description 4
- 150000001735 carboxylic acids Chemical class 0.000 claims description 4
- 229910052802 copper Inorganic materials 0.000 claims description 4
- 229910052733 gallium Inorganic materials 0.000 claims description 4
- 229910052732 germanium Inorganic materials 0.000 claims description 4
- 229910052742 iron Inorganic materials 0.000 claims description 4
- 239000004310 lactic acid Substances 0.000 claims description 4
- 235000014655 lactic acid Nutrition 0.000 claims description 4
- 229910052749 magnesium Inorganic materials 0.000 claims description 4
- 229910052758 niobium Inorganic materials 0.000 claims description 4
- 229910000073 phosphorus hydride Inorganic materials 0.000 claims description 4
- 229910052700 potassium Inorganic materials 0.000 claims description 4
- 229910052710 silicon Inorganic materials 0.000 claims description 4
- 229910052708 sodium Inorganic materials 0.000 claims description 4
- 229910052712 strontium Inorganic materials 0.000 claims description 4
- 229910052718 tin Inorganic materials 0.000 claims description 4
- 229910052725 zinc Inorganic materials 0.000 claims description 4
- 229910052726 zirconium Inorganic materials 0.000 claims description 4
- 238000002407 reforming Methods 0.000 claims description 3
- MZZUATUOLXMCEY-UHFFFAOYSA-N cobalt manganese Chemical compound [Mn].[Co] MZZUATUOLXMCEY-UHFFFAOYSA-N 0.000 claims 1
- 229910013200 LiNiMnCo Inorganic materials 0.000 abstract 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 44
- 239000000243 solution Substances 0.000 description 36
- 239000011572 manganese Substances 0.000 description 29
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 25
- 229910052759 nickel Inorganic materials 0.000 description 24
- 239000000203 mixture Substances 0.000 description 23
- 239000002994 raw material Substances 0.000 description 23
- 229910052748 manganese Inorganic materials 0.000 description 22
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 20
- 238000010304 firing Methods 0.000 description 20
- 229910017052 cobalt Inorganic materials 0.000 description 18
- 239000010941 cobalt Substances 0.000 description 18
- 239000000047 product Substances 0.000 description 13
- 238000011156 evaluation Methods 0.000 description 12
- 239000011248 coating agent Substances 0.000 description 11
- 238000000576 coating method Methods 0.000 description 11
- BFZPBUKRYWOWDV-UHFFFAOYSA-N lithium;oxido(oxo)cobalt Chemical compound [Li+].[O-][Co]=O BFZPBUKRYWOWDV-UHFFFAOYSA-N 0.000 description 10
- 239000002184 metal Substances 0.000 description 9
- -1 oxides Chemical class 0.000 description 9
- 238000000550 scanning electron microscopy energy dispersive X-ray spectroscopy Methods 0.000 description 9
- 239000002002 slurry Substances 0.000 description 9
- 239000011149 active material Substances 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 8
- 230000014759 maintenance of location Effects 0.000 description 8
- 238000013507 mapping Methods 0.000 description 8
- KFDQGLPGKXUTMZ-UHFFFAOYSA-N [Mn].[Co].[Ni] Chemical compound [Mn].[Co].[Ni] KFDQGLPGKXUTMZ-UHFFFAOYSA-N 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 7
- 238000001035 drying Methods 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 7
- 229910000625 lithium cobalt oxide Inorganic materials 0.000 description 7
- 230000009257 reactivity Effects 0.000 description 7
- 239000002904 solvent Substances 0.000 description 7
- 238000005979 thermal decomposition reaction Methods 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- 125000004430 oxygen atom Chemical group O* 0.000 description 6
- 239000006072 paste Substances 0.000 description 6
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 5
- 150000002815 nickel Chemical group 0.000 description 5
- 239000006104 solid solution Substances 0.000 description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 4
- 239000006185 dispersion Substances 0.000 description 4
- 239000011888 foil Substances 0.000 description 4
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 description 4
- 229910052808 lithium carbonate Inorganic materials 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 238000000790 scattering method Methods 0.000 description 4
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 4
- AIFLGMNWQFPTAJ-UHFFFAOYSA-J 2-hydroxypropanoate;titanium(4+) Chemical compound [Ti+4].CC(O)C([O-])=O.CC(O)C([O-])=O.CC(O)C([O-])=O.CC(O)C([O-])=O AIFLGMNWQFPTAJ-UHFFFAOYSA-J 0.000 description 3
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 239000002033 PVDF binder Substances 0.000 description 3
- ZYXUQEDFWHDILZ-UHFFFAOYSA-N [Ni].[Mn].[Li] Chemical class [Ni].[Mn].[Li] ZYXUQEDFWHDILZ-UHFFFAOYSA-N 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 230000006866 deterioration Effects 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 229940126062 Compound A Drugs 0.000 description 2
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 2
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 2
- 229910011322 LiNi0.6Mn0.2Co0.2O2 Inorganic materials 0.000 description 2
- 229910013870 LiPF 6 Inorganic materials 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- YRKCREAYFQTBPV-UHFFFAOYSA-N acetylacetone Chemical compound CC(=O)CC(C)=O YRKCREAYFQTBPV-UHFFFAOYSA-N 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- XRASGLNHKOPXQL-UHFFFAOYSA-L azane 2-oxidopropanoate titanium(4+) dihydrate Chemical compound N.N.O.O.[Ti+4].CC([O-])C([O-])=O.CC([O-])C([O-])=O XRASGLNHKOPXQL-UHFFFAOYSA-L 0.000 description 2
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 description 2
- 125000006309 butyl amino group Chemical group 0.000 description 2
- 238000007600 charging Methods 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 150000001868 cobalt Chemical class 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 229910001882 dioxygen Inorganic materials 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 238000007580 dry-mixing Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 239000003792 electrolyte Substances 0.000 description 2
- 239000008151 electrolyte solution Substances 0.000 description 2
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 2
- 125000000031 ethylamino group Chemical group [H]C([H])([H])C([H])([H])N([H])[*] 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 150000004679 hydroxides Chemical class 0.000 description 2
- ROBFUDYVXSDBQM-UHFFFAOYSA-N hydroxymalonic acid Chemical compound OC(=O)C(O)C(O)=O ROBFUDYVXSDBQM-UHFFFAOYSA-N 0.000 description 2
- 125000006316 iso-butyl amino group Chemical group [H]N(*)C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 238000007561 laser diffraction method Methods 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 150000002641 lithium Chemical class 0.000 description 2
- 238000003760 magnetic stirring Methods 0.000 description 2
- 150000002696 manganese Chemical class 0.000 description 2
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 2
- 230000001590 oxidative effect Effects 0.000 description 2
- 125000004894 pentylamino group Chemical group C(CCCC)N* 0.000 description 2
- 150000003003 phosphines Chemical class 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000011164 primary particle Substances 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 125000006308 propyl amino group Chemical group 0.000 description 2
- 238000005245 sintering Methods 0.000 description 2
- 238000001694 spray drying Methods 0.000 description 2
- 238000004448 titration Methods 0.000 description 2
- TUQOTMZNTHZOKS-UHFFFAOYSA-N tributylphosphine Chemical compound CCCCP(CCCC)CCCC TUQOTMZNTHZOKS-UHFFFAOYSA-N 0.000 description 2
- RXJKFRMDXUJTEX-UHFFFAOYSA-N triethylphosphine Chemical compound CCP(CC)CC RXJKFRMDXUJTEX-UHFFFAOYSA-N 0.000 description 2
- YWWDBCBWQNCYNR-UHFFFAOYSA-N trimethylphosphine Chemical compound CP(C)C YWWDBCBWQNCYNR-UHFFFAOYSA-N 0.000 description 2
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 2
- 238000005303 weighing Methods 0.000 description 2
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- RBNPOMFGQQGHHO-UHFFFAOYSA-N -2,3-Dihydroxypropanoic acid Natural products OCC(O)C(O)=O RBNPOMFGQQGHHO-UHFFFAOYSA-N 0.000 description 1
- SJZRECIVHVDYJC-UHFFFAOYSA-N 4-hydroxybutyric acid Chemical compound OCCCC(O)=O SJZRECIVHVDYJC-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- RBNPOMFGQQGHHO-UWTATZPHSA-N D-glyceric acid Chemical compound OC[C@@H](O)C(O)=O RBNPOMFGQQGHHO-UWTATZPHSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 229910012851 LiCoO 2 Inorganic materials 0.000 description 1
- VEQPNABPJHWNSG-UHFFFAOYSA-N Nickel(2+) Chemical compound [Ni+2] VEQPNABPJHWNSG-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- NXPZICSHDHGMGT-UHFFFAOYSA-N [Co].[Mn].[Li] Chemical compound [Co].[Mn].[Li] NXPZICSHDHGMGT-UHFFFAOYSA-N 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000004703 alkoxides Chemical class 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- FPCJKVGGYOAWIZ-UHFFFAOYSA-N butan-1-ol;titanium Chemical compound [Ti].CCCCO.CCCCO.CCCCO.CCCCO FPCJKVGGYOAWIZ-UHFFFAOYSA-N 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 229910001429 cobalt ion Inorganic materials 0.000 description 1
- XLJKHNWPARRRJB-UHFFFAOYSA-N cobalt(2+) Chemical compound [Co+2] XLJKHNWPARRRJB-UHFFFAOYSA-N 0.000 description 1
- 239000008139 complexing agent Substances 0.000 description 1
- 238000010280 constant potential charging Methods 0.000 description 1
- 238000010277 constant-current charging Methods 0.000 description 1
- 238000010281 constant-current constant-voltage charging Methods 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000010419 fine particle Substances 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- ODBLHEXUDAPZAU-UHFFFAOYSA-N isocitric acid Chemical compound OC(=O)C(O)C(C(O)=O)CC(O)=O ODBLHEXUDAPZAU-UHFFFAOYSA-N 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 229910001437 manganese ion Inorganic materials 0.000 description 1
- ZEIWWVGGEOHESL-UHFFFAOYSA-N methanol;titanium Chemical compound [Ti].OC.OC.OC.OC ZEIWWVGGEOHESL-UHFFFAOYSA-N 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 229910001453 nickel ion Inorganic materials 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 238000009828 non-uniform distribution Methods 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000003973 paint Substances 0.000 description 1
- 238000011056 performance test Methods 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000011163 secondary particle Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 125000006318 tert-butyl amino group Chemical group [H]N(*)C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- JMXKSZRRTHPKDL-UHFFFAOYSA-N titanium ethoxide Chemical compound [Ti+4].CC[O-].CC[O-].CC[O-].CC[O-] JMXKSZRRTHPKDL-UHFFFAOYSA-N 0.000 description 1
- VXUYXOFXAQZZMF-UHFFFAOYSA-N titanium(IV) isopropoxide Chemical compound CC(C)O[Ti](OC(C)C)(OC(C)C)OC(C)C VXUYXOFXAQZZMF-UHFFFAOYSA-N 0.000 description 1
- 229910021642 ultra pure water Inorganic materials 0.000 description 1
- 239000012498 ultrapure water Substances 0.000 description 1
- 238000009827 uniform distribution Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G51/00—Compounds of cobalt
- C01G51/40—Complex oxides containing cobalt and at least one other metal element
- C01G51/42—Complex oxides containing cobalt and at least one other metal element containing alkali metals, e.g. LiCoO2
- C01G51/44—Complex oxides containing cobalt and at least one other metal element containing alkali metals, e.g. LiCoO2 containing manganese
- C01G51/50—Complex oxides containing cobalt and at least one other metal element containing alkali metals, e.g. LiCoO2 containing manganese of the type (MnO2)n-, e.g. Li(CoxMn1-x)O2 or Li(MyCoxMn1-x-y)O2
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/362—Composites
- H01M4/366—Composites as layered products
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/80—Particles consisting of a mixture of two or more inorganic phases
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/028—Positive electrodes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Composite Materials (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
Abstract
리튬 2차 전지의 정극 활물질로서 사용했을 때에, 사이클 특성을 높게 할 수 있는 LiNiMnCo 복합 산화물 입자를 제공하는 것. 하기 일반식 (1):
(식 중, x는 0.98≤x≤1.20, y는 0.30≤y<1.00, z는 0<z≤0.50, t는 0<t≤0.50, p는 0≤p≤0.05를 나타내고, y+z+t+p=1.00임)
로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 티타늄킬레이트 화합물을 포함하는 표면 처리액에 접촉시켜서, 해당 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 티타늄킬레이트 화합물이 부착된 피복 입자를 얻고, 이어서 해당 피복 입자를 가열 처리함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 얻는 개질 공정을 갖고,
상기 티타늄킬레이트 화합물이, 하기 일반식 (2):
로 표시되는 티타늄킬레이트 또는 그의 암모늄염인 것을 특징으로 하는 개질 LiNiMnCo 복합 산화물 입자의 제조 방법.To provide a LiNiMnCo composite oxide particle capable of improving cycle characteristics when used as a positive electrode active material for a lithium secondary battery. The following general formula (1):
(In the formula, x represents 0.98≤x≤1.20, y represents 0.30≤y<1.00, z represents 0<z≤0.50, t represents 0<t≤0.50, p represents 0≤p≤0.05, and y+z+ t+p=1.00)
The lithium nickel manganese cobalt composite oxide particles represented by are brought into contact with a surface treatment solution containing a titanium chelate compound to obtain coated particles in which the titanium chelate compound adheres to the particle surfaces of the lithium nickel manganese cobalt composite oxide particles. a modification step of obtaining modified lithium nickel manganese cobalt composite oxide particles by heating the coated particles;
The titanium chelate compound has the following general formula (2):
A method for producing modified LiNiMnCo composite oxide particles, which is a titanium chelate represented by or an ammonium salt thereof.
Description
본 발명은 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 관한 것이다.The present invention relates to a method for producing modified lithium nickel manganese cobalt composite oxide particles.
종래, 리튬 2차 전지의 정극 활물질로서는, 코발트산 리튬이 사용되어 왔다. 그러나, 코발트는 희소 금속이기 때문에, 코발트의 함유율이 낮은 리튬 니켈 망간 코발트 복합 산화물이 개발되고 있다(예를 들어, 특허문헌 1 내지 2 참조).Conventionally, lithium cobaltate has been used as a positive electrode active material for lithium secondary batteries. However, since cobalt is a rare metal, lithium nickel manganese cobalt composite oxides having a low content of cobalt have been developed (see Patent Documents 1 and 2, for example).
리튬 니켈 망간 코발트 복합 산화물을 정극 활물질로서 사용하는 리튬 2차 전지는, 복합 산화물 중에 포함되는 니켈, 망간, 코발트의 원자비를 조정함으로써, 저비용화가 가능하게 되고, 또한 코발트산 리튬에 비하여 고용량이 되는 것이 알려져 있다(예를 들어, 특허문헌 3 참조).A lithium secondary battery using a lithium nickel manganese cobalt composite oxide as a positive electrode active material can be reduced in cost and has a higher capacity than lithium cobaltate by adjusting the atomic ratio of nickel, manganese, and cobalt contained in the composite oxide. It is known (for example, refer to Patent Document 3).
그러나, 이들 종래 기술의 방법에서도, 리튬 니켈 망간 코발트 복합 산화물을 정극 활물질로서 사용한 리튬 2차 전지는, 사이클 특성의 열화라고 하는 문제가 남아 있었다.However, even with these prior art methods, a lithium secondary battery using a lithium nickel manganese cobalt composite oxide as a positive electrode active material still has a problem of deterioration in cycle characteristics.
리튬 니켈 망간 코발트 복합 산화물을 정극 활물질로서 사용한 리튬 2차 전지의 사이클 특성을 개선하는 방법으로서, 리튬 니켈 망간 코발트 복합 산화물의 입자 표면을 Ti 함유 화합물로 피복하는 방법이 제안되어 있다(예를 들어, 특허문헌 4, 특허문헌 5 등 참조).As a method for improving cycle characteristics of a lithium secondary battery using a lithium nickel manganese cobalt composite oxide as a positive electrode active material, a method of coating the particle surface of a lithium nickel manganese cobalt composite oxide with a Ti-containing compound has been proposed (for example, See Patent Document 4, Patent Document 5, etc.).
리튬 니켈 망간 코발트 복합 산화물의 입자 표면을 Ti 함유 화합물로 피복하는 방법으로서는, 특허문헌 4, 5에는, Ti 등의 유기 금속 화합물을 포함하는 알콕시드 모노머 혹은 올리고머와, 2-프로판올 등의 알코올을 혼합한 후, 아세틸아세톤 등의 킬레이트제를 첨가하고, 물을 더 첨가하여, 평균 입자가 1 내지 20㎚의 Ti를 포함하는 미립자의 전구체가 분산된 분산액을 조제하고, 해당 분산액에 의해 리튬 니켈 망간 코발트 복합 산화물의 입자 표면을 피복 처리하고, 이어서 열처리를 행하는 방법이 제안되어 있다.As a method for coating the particle surface of lithium nickel manganese cobalt composite oxide with a Ti-containing compound, Patent Documents 4 and 5 mix an alkoxide monomer or oligomer containing an organometallic compound such as Ti with an alcohol such as 2-propanol. After that, a chelating agent such as acetylacetone is added, and water is further added to prepare a dispersion in which precursors of fine particles having an average particle size of 1 to 20 nm containing Ti are dispersed, and lithium nickel manganese cobalt A method of coating the surface of a composite oxide particle and then performing a heat treatment has been proposed.
최근, 리튬 2차 전지는 전기 자동차, 하이브리드 자동차, 플러그인 하이브리드 자동차 등의 자동차 분야에서의 사용이 검토되고 있다. 이 때문에 리튬 니켈 망간 코발트 복합 산화물을 정극 활물질로 하는 리튬 2차 전지에 있어서, 사이클 특성의 더한층의 향상이 요구되고 있다.Recently, lithium secondary batteries are being reviewed for use in automobile fields such as electric vehicles, hybrid vehicles, and plug-in hybrid vehicles. For this reason, in a lithium secondary battery using a lithium nickel manganese cobalt composite oxide as a positive electrode active material, further improvement in cycle characteristics is required.
따라서, 본 발명의 목적은, 리튬 2차 전지의 정극 활물질로서 사용했을 때에, 사이클 특성을 높게 할 수 있는 리튬 니켈 망간 코발트 복합 산화물 입자를 제공하는 데 있다.Accordingly, an object of the present invention is to provide lithium nickel manganese cobalt composite oxide particles capable of improving cycle characteristics when used as a positive electrode active material for a lithium secondary battery.
본 발명자들은, 상기 실정을 감안하여 예의 연구를 거듭한 결과, 일반식 (1)로 표시되는 리튬망간 코발트 복합 산화물 입자를, 특정의 일반식으로 표시되는 티타늄킬레이트 또는 그의 암모늄염을 포함하는 표면 처리액에 접촉시킨 후, 가열 처리함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자가 얻어지고, 해당 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 정극 활물질로 하는 리튬 2차 전지는, 사이클 특성이 우수하다는 것을 알아내어, 본 발명을 완성하기에 이르렀다.The inventors of the present invention, as a result of intensive research in view of the above circumstances, found that lithium manganese cobalt composite oxide particles represented by the general formula (1) are a surface treatment solution containing a titanium chelate represented by a specific general formula or an ammonium salt thereof. and heat treatment to obtain modified lithium nickel manganese cobalt composite oxide particles, and a lithium secondary battery using the modified lithium nickel manganese cobalt composite oxide particles as a positive electrode active material has excellent cycle characteristics, The present invention has been completed.
즉, 본 발명 (1)은 하기 일반식 (1):That is, the present invention (1) is the following general formula (1):
(식 중, M은, Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na 및 K로부터 선택되는 1종 또는 2종 이상의 금속 원소를 나타낸다. x는 0.98≤x≤1.20, y는 0.30≤y<1.00, z는 0<z≤0.50, t는 0<t≤0.50, p는 0≤p≤0.05를 나타내고, y+z+t+p=1.00임)(Wherein, M is selected from Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na and K Represents one or more metal elements that are x is 0.98≤x≤1.20, y is 0.30≤y<1.00, z is 0<z≤0.50, t is 0<t≤0.50, p is 0≤p≤ represents 0.05, and y+z+t+p=1.00)
로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 티타늄킬레이트 화합물을 포함하는 표면 처리액에 접촉시켜서, 해당 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 티타늄킬레이트 화합물이 부착된 피복 입자를 얻고, 이어서 해당 피복 입자를 가열 처리함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 얻는 개질 공정을 갖고,The lithium nickel manganese cobalt composite oxide particles represented by are brought into contact with a surface treatment solution containing a titanium chelate compound to obtain coated particles in which the titanium chelate compound adheres to the particle surfaces of the lithium nickel manganese cobalt composite oxide particles. a modification step of obtaining modified lithium nickel manganese cobalt composite oxide particles by heating the coated particles;
상기 티타늄킬레이트 화합물이, 하기 일반식 (2):The titanium chelate compound has the following general formula (2):
(식 중, R1은, 알콕시기, 수산기, 할로겐 원자, 아미노기 또는 포스핀류를 나타내고, 복수 존재하는 경우, 동일해도 되며 달라도 된다. L은 히드록시카르복실산에서 유래되는 기를 나타내고, 복수 존재하는 경우, 동일해도 되며 달라도 된다. m은 0 이상 3 이하의 수를 나타내고, n은 1 이상 3 이하의 수를 나타내며, m+n은 3 내지 6임)(In the formula, R 1 represents an alkoxy group, a hydroxyl group, a halogen atom, an amino group or a phosphine, and when present in a plurality thereof, may be the same or different. L represents a group derived from hydroxycarboxylic acid, and a plurality of In this case, it may be the same or different. m represents a number of 0 or more and 3 or less, n represents a number of 1 or more and 3 or less, and m+n is 3 to 6)
로 표시되는 티타늄킬레이트 또는 그의 암모늄염인 것A titanium chelate represented by or an ammonium salt thereof
을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.It is to provide a method for producing modified lithium nickel manganese cobalt composite oxide particles characterized by.
또한, 본 발명 (2)는 상기 가열 처리의 온도가 400 내지 1000℃인 것을 특징으로 하는 (1)의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.In addition, the present invention (2) provides the method for producing modified lithium nickel manganese cobalt composite oxide particles of (1) characterized in that the temperature of the heat treatment is 400 to 1000°C.
또한, 본 발명 (3)은 상기 일반식 (2) 중의 L이 1가의 카르복실산인 것을 특징으로 하는 (1) 또는 (2)의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.In addition, the present invention (3) provides the method for producing modified lithium nickel manganese cobalt composite oxide particles according to (1) or (2), characterized in that L in the general formula (2) is a monovalent carboxylic acid.
또한, 본 발명 (4)는 상기 일반식 (2) 중의 L이 락트산인 것을 특징으로 하는 (1) 또는 (2)의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.Further, the present invention (4) provides the method for producing modified lithium nickel manganese cobalt composite oxide particles according to (1) or (2), characterized in that L in the general formula (2) is lactic acid.
또한, 본 발명 (5)는 상기 표면 처리액의 pH가 7 이상인 것을 특징으로 하는 (1) 내지 (4) 중 어느 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.In addition, the present invention (5) provides the method for producing modified lithium nickel manganese cobalt composite oxide particles according to any one of (1) to (4), characterized in that the surface treatment liquid has a pH of 7 or higher.
또한, 본 발명 (6)은 상기 피복 입자에 있어서의 상기 티타늄킬레이트 화합물의 부착량이, 상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당, Ti 원자 환산으로 0.1 내지 150㎎인 것을 특징으로 하는 (1) 내지 (5) 중 어느 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.Further, in the present invention (6), the amount of adhesion of the titanium chelate compound on the coated particles is 0.1 to 150 mg in terms of Ti atom per 1 m 2 of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1). It is to provide a method for producing a modified lithium nickel manganese cobalt composite oxide particle according to any one of (1) to (5), characterized in that.
또한, 본 발명 (7)은 상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자 중의 잔존 알칼리양이 1.2질량% 이하인 것을 특징으로 하는 (1) 내지 (6) 중 어느 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.Further, the present invention (7) is any of the modified lithium nickel manganese of (1) to (6), characterized in that the amount of residual alkali in the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) is 1.2% by mass or less. It is to provide a method for producing cobalt composite oxide particles.
또한, 본 발명 (8)은 상기 개질 리튬 니켈 망간 코발트 복합 산화물 입자 중의 잔존 알칼리양이 1.2질량% 이하인 것을 특징으로 하는 (1) 내지 (7) 중 어느 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.Further, the present invention (8) is a method for producing modified lithium nickel manganese cobalt composite oxide particles according to any one of (1) to (7), characterized in that the amount of residual alkali in the modified lithium nickel manganese cobalt composite oxide particles is 1.2% by mass or less. is to provide
또한, 본 발명 (9)는 상기 개질 공정에 있어서,In addition, in the reforming step of the present invention (9),
상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당 Ti 함유량이, Ti 원자 환산으로 0.1 내지 150㎎이 되는 첨가량이고, 상기 표면 개질액을, 상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자에 첨가하여 혼합하고, 전량 건조시키는 것The Ti content per 1 m 2 of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) is an addition amount of 0.1 to 150 mg in terms of Ti atoms, and the surface modification liquid is represented by the general formula (1) Adding to the lithium nickel manganese cobalt composite oxide particles to be mixed, and drying the entire amount
을 특징으로 하는 (1) 내지 (8) 중 어느 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 제공하는 것이다.It is to provide a method for producing modified lithium nickel manganese cobalt composite oxide particles according to any one of (1) to (8), characterized by:
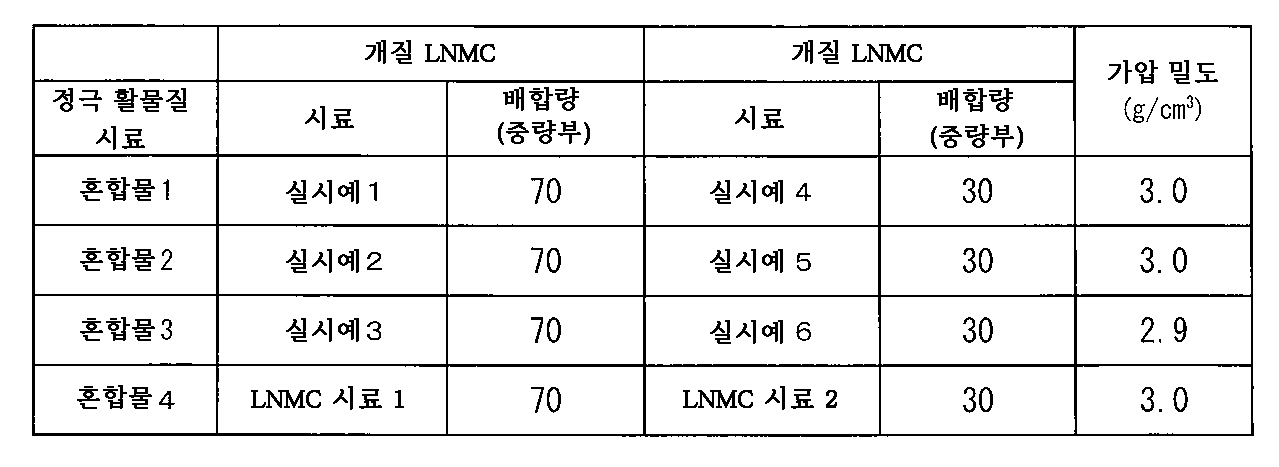
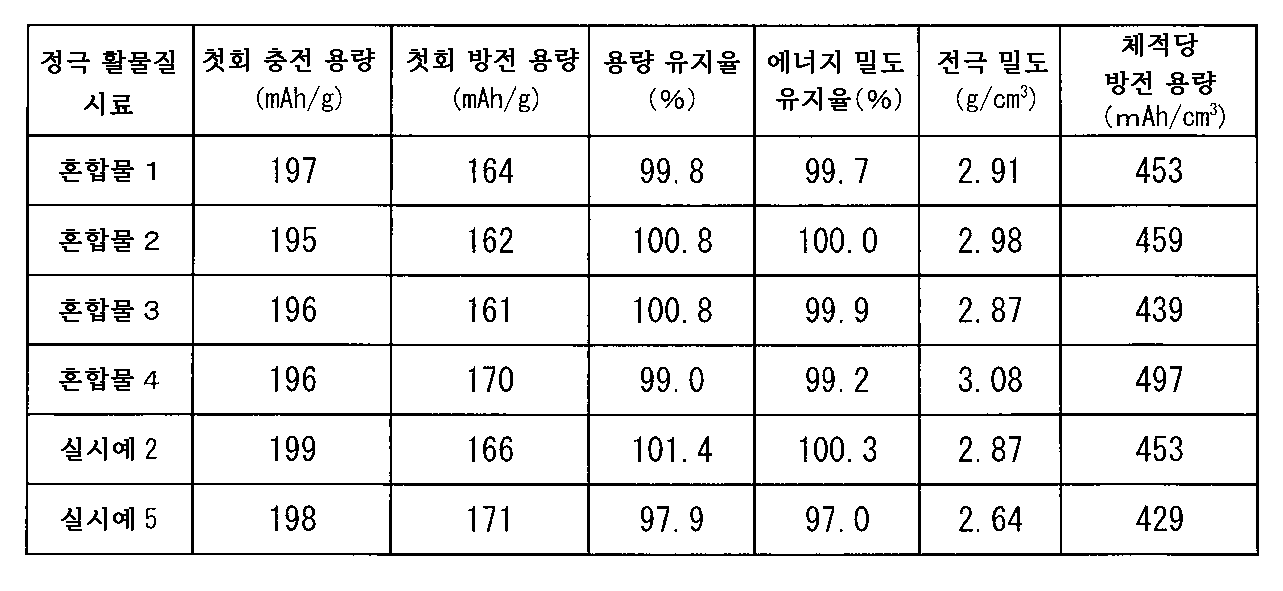
또한, 본 발명 (10)은, (1) 내지 (9) 중 어느 한 항에 기재된 제조 방법에 의해 얻어지는 평균 입자경이 7.5 내지 30.0㎛인 큰 입자와, (1) 내지 (9) 중 어느 한 항에 기재된 제조 방법에 의해 얻어지는 평균 입자경이 0.5 내지 7.5㎛인 작은 입자를 혼합하는 공정을 포함하는 것을 특징으로 하는 리튬 2차 전지용 정극 활물질의 제조 방법을 제공하는 것이다.Further, the present invention (10) provides large particles having an average particle diameter of 7.5 to 30.0 µm obtained by the production method according to any one of (1) to (9), and any one of (1) to (9). It is to provide a method for producing a positive electrode active material for a lithium secondary battery characterized by including a step of mixing small particles having an average particle diameter of 0.5 to 7.5 μm obtained by the production method described in .
본 발명에 따르면, 리튬 2차 전지의 정극 활물질로서 사용했을 때에, 사이클 특성을 높게 할 수 있는 리튬 니켈 망간 코발트 복합 산화물 입자를 제공할 수 있다.ADVANTAGE OF THE INVENTION According to this invention, when used as a positive electrode active material of a lithium secondary battery, the lithium nickel manganese cobalt composite oxide particle which can improve cycling characteristics can be provided.
이하, 본 발명을 바람직한 실시 형태에 기초하여 설명한다.Hereinafter, the present invention will be described based on preferred embodiments.
본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법은, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 일반식 (2)로 표시되는 티타늄킬레이트 또는 일반식 (2)로 표시되는 티타늄킬레이트의 암모늄염을 포함하는 표면 처리액에 접촉시켜서, 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에, 이들 티타늄킬레이트 화합물이 부착된 피복 입자를 얻고, 이어서 얻어진 피복 입자를 가열 처리함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 얻는 개질 공정을 갖는다. 이하, 일반식 (2)로 표시되는 티타늄킬레이트 및 일반식 (2)로 표시되는 티타늄킬레이트의 암모늄염을 총칭하여, 「티타늄킬레이트 화합물」이라고 하는 경우가 있다.In the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention, the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) are converted into a titanium chelate represented by the general formula (2) or the general formula (2). By contacting the surface treatment solution containing the ammonium salt of the indicated titanium chelate to obtain coated particles having these titanium chelate compounds adhered to the particle surfaces of the lithium nickel manganese cobalt composite oxide particles, and then heat-treating the obtained coated particles to modify It has a reforming process to obtain lithium nickel manganese cobalt composite oxide particles. Hereinafter, the titanium chelate represented by the general formula (2) and the ammonium salt of the titanium chelate represented by the general formula (2) are collectively referred to as "titanium chelate compounds" in some cases.
본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물의 제조 방법은, 기본적으로는 하기의 (A) 공정 내지 (B) 공정을 갖는 것이다.The method for producing the modified lithium nickel manganese cobalt composite oxide of the present invention basically has the following steps (A) to (B).
(A) 공정: 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자, 즉, 개질 대상의 리튬 니켈 망간 코발트 복합 산화물을, 본 발명에 따른 티타늄킬레이트 화합물을 포함하는 표면 처리액에 접촉시켜서, 리튬 니켈 망간 코발트 복합 산화물 입자의 표면에 티타늄킬레이트 화합물이 부착된 피복 입자를 얻는 공정.Step (A): The lithium nickel manganese cobalt composite oxide particles represented by the general formula (1), that is, the lithium nickel manganese cobalt composite oxide to be modified are brought into contact with a surface treatment solution containing a titanium chelate compound according to the present invention. , A step of obtaining coated particles in which a titanium chelate compound is adhered to the surface of lithium nickel manganese cobalt composite oxide particles.
(B) 공정: (A) 공정을 행하여 얻어진 피복 입자를 가열 처리하여, 후술하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A), 또는 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)를 얻는 공정.Step (B): A step of heating the coated particles obtained in step (A) to obtain modified lithium nickel manganese cobalt composite oxide particles (A) or modified lithium nickel manganese cobalt composite oxide particles (B) described later.
또한, 이하에서는, 「개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)」 및 「개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)」를 총칭하여, 「개질 리튬 니켈 망간 코발트 복합 산화물 입자」라고 기재하는 경우가 있다.In the following, "modified lithium nickel manganese cobalt composite oxide particles (A)" and "modified lithium nickel manganese cobalt composite oxide particles (B)" are collectively referred to as "modified lithium nickel manganese cobalt composite oxide particles". there is
(B) 공정에 있어서, 피복 입자를 가열 처리함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A) 및 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)가 얻어진다.In step (B), the coated particles are subjected to heat treatment to obtain modified lithium nickel manganese cobalt composite oxide particles (A) and modified lithium nickel manganese cobalt composite oxide particles (B).
개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)는 Ti를 포함하는 산화물이 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 부착되어 존재하는 것이다. 해당 Ti를 포함하는 산화물이 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 부착되어 존재하는 것은, 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면을, 10,000 내지 30,000배의 확대 배율로 SEM-EDX에 의한 Ti의 원소 매핑 분석으로 분석했을 때에, 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 Ti가 편재 등의 불균일하게 분포된 상태에서 관찰됨으로써 확인된다.The modified lithium nickel manganese cobalt composite oxide particles (A) are those in which an oxide containing Ti adheres to the particle surface of the lithium nickel manganese cobalt composite oxide particles. The fact that the Ti-containing oxide adheres to the particle surface of the lithium nickel manganese cobalt composite oxide particle indicates that the particle surface of the modified lithium nickel manganese cobalt composite oxide particle is examined by SEM-EDX at a magnification of 10,000 to 30,000 times. When analyzed by elemental mapping analysis of Ti, it is confirmed by observing that Ti is unevenly distributed on the particle surface of the lithium nickel manganese cobalt composite oxide particles.
한편, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)에서는, 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면을, 10,000 내지 30,000배의 확대 배율로 SEM-EDX에 의한 Ti의 원소 매핑 분석으로 분석했을 때에, Ti가 Co, Ni, Mn 등과 마찬가지로 균일하게 분포된 상태에서 관찰된다. 본 발명자들은, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)는 Ti의 고용 반응이 우선적으로 진행되고, 리튬 니켈 망간 코발트 복합 산화물 입자에 Ti가 고용하여 함유되기 때문에, Ti가 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에서 Co, Ni, Mn 등과 마찬가지로 균일하게 분포될 것으로 추측하고 있다.On the other hand, in the modified lithium nickel manganese cobalt composite oxide particles (B), when the particle surface of the modified lithium nickel manganese cobalt composite oxide particles is analyzed by elemental mapping analysis of Ti by SEM-EDX at a magnification of 10,000 to 30,000 times , Ti is observed in a uniformly distributed state like Co, Ni, Mn, etc. The inventors of the present invention found that the solid solution reaction of Ti proceeds preferentially in the modified lithium nickel manganese cobalt composite oxide particles (B), and since Ti is contained in solid solution in the lithium nickel manganese cobalt composite oxide particles, Ti is lithium nickel manganese cobalt composite oxide. It is assumed that Co, Ni, Mn, etc. are uniformly distributed on the particle surface of the particles.
(A) 공정은, 개질 대상인 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 본 발명에 따른 티타늄킬레이트 화합물을 포함하는 표면 처리액에 접촉시켜서, 리튬 니켈 망간 코발트 복합 산화물 입자의 표면에 티타늄킬레이트 화합물이 부착된 피복 입자를 얻는 공정이다. 또한, 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면의 티타늄킬레이트 화합물은, 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면의 전체를 피복하는 것이어도 되고 또는 일부를 피복하는 것이어도 된다. 입자 표면의 일부를 피복한다라고 함은, 입자 표면에, 티타늄킬레이트 화합물 이외에 피복 대상물의 표면이 노출되는 부분을 갖는 상태를 말한다.In the step (A), lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) to be modified are brought into contact with a surface treatment solution containing a titanium chelate compound according to the present invention to form lithium nickel manganese cobalt composite oxide particles. This is a step of obtaining coated particles with a titanium chelate compound attached to the surface. In addition, the titanium chelate compound on the particle surface of the lithium nickel manganese cobalt composite oxide particle may cover the entire particle surface of the lithium nickel manganese cobalt composite oxide particle or a part thereof. Covering a part of the particle surface means a state in which the particle surface has a portion where the surface of the object to be coated is exposed other than the titanium chelate compound.
(A) 공정에 있어서, 개질 대상이 되는 리튬 니켈 망간 코발트 복합 산화물 입자는, 하기 일반식 (1):In step (A), the lithium nickel manganese cobalt composite oxide particles to be modified have the following general formula (1):
(식 중, M은, Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na 및 K로부터 선택되는 1종 또는 2종 이상의 금속 원소를 나타낸다. x는 0.98≤x≤1.20, y는 0.30≤y<1.00, z는 0<z≤0.50, t는 0<t≤0.50, p는 0≤p≤0.05를 나타내고, y+z+t+p=1.00임)(Wherein, M is selected from Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na and K Represents one or more metal elements that are x is 0.98≤x≤1.20, y is 0.30≤y<1.00, z is 0<z≤0.50, t is 0<t≤0.50, p is 0≤p≤ represents 0.05, and y+z+t+p=1.00)
로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자이다.It is a lithium nickel manganese cobalt composite oxide particle represented by
일반식 (1)의 식 중의 x는, 0.98≤x≤1.20이다. x는, 초기 용량이 높아진다는 점에서, 1.00≤x≤1.10인 것이 바람직하다. 또한, 일반식 (1)의 식 중의 y는, 0.30≤y<1.00이다. y는, 초기 용량과 사이클 특성을 양립할 수 있다는 점에서, 0.50≤y≤0.95인 것이 바람직하고, 0.60≤y≤0.90인 것이 특히 바람직하다. 또한, 일반식 (1)의 식 중의 z는, 0<z≤0.50이다. z는, 안전성이 우수하다는 점에서, 0.025≤z≤0.45인 것이 바람직하다. 또한, t는, 0<t≤0.50이다. t는, 안전성이 우수하다는 점에서, 0.025≤t≤0.45인 것이 바람직하다. y+z+t+p=1.00이다. y/z는, 바람직하게는 (y/z)>1, 특히 바람직하게는 (y/z)≥1.5, 보다 바람직하게는 3≤(y/z)≤38이다.x in the formula of General Formula (1) is 0.98≤x≤1.20. It is preferable that x is 1.00 ≤ x ≤ 1.10 from the viewpoint of increasing the initial capacity. In addition, y in the formula of General Formula (1) is 0.30≤y<1.00. y is preferably 0.50 ≤ y ≤ 0.95, particularly preferably 0.60 ≤ y ≤ 0.90, from the viewpoint of achieving both initial capacity and cycle characteristics. In addition, z in the formula of General Formula (1) is 0<z≤0.50. z is preferably 0.025 ≤ z ≤ 0.45 from the viewpoint of excellent safety. Also, t is 0<t≤0.50. t is preferably 0.025≤t≤0.45 from the viewpoint of excellent safety. y+z+t+p=1.00. y/z is preferably (y/z)>1, particularly preferably (y/z)≥1.5, more preferably 3≤(y/z)≤38.
또한, 식 중의 M은, 사이클 특성, 안전성 등의 전지 성능을 향상시킬 것을 목적으로 하여, 필요에 따라서, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자에 함유시키는 금속 원소이며, M으로서는, Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na 및 K로부터 선택되는 1종 또는 2종 이상의 금속 원소를 들 수 있다. 일반식 (1)의 식 중의 p는, 0≤p≤0.05, 바람직하게는 0.0001≤p≤0.045이다.In addition, M in the formula is a metal element to be incorporated into the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) as necessary for the purpose of improving battery performance such as cycle characteristics and safety, M As, one or two selected from Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na and K More than one kind of metal element can be mentioned. In formula (1), p is 0 ≤ p ≤ 0.05, preferably 0.0001 ≤ p ≤ 0.045.
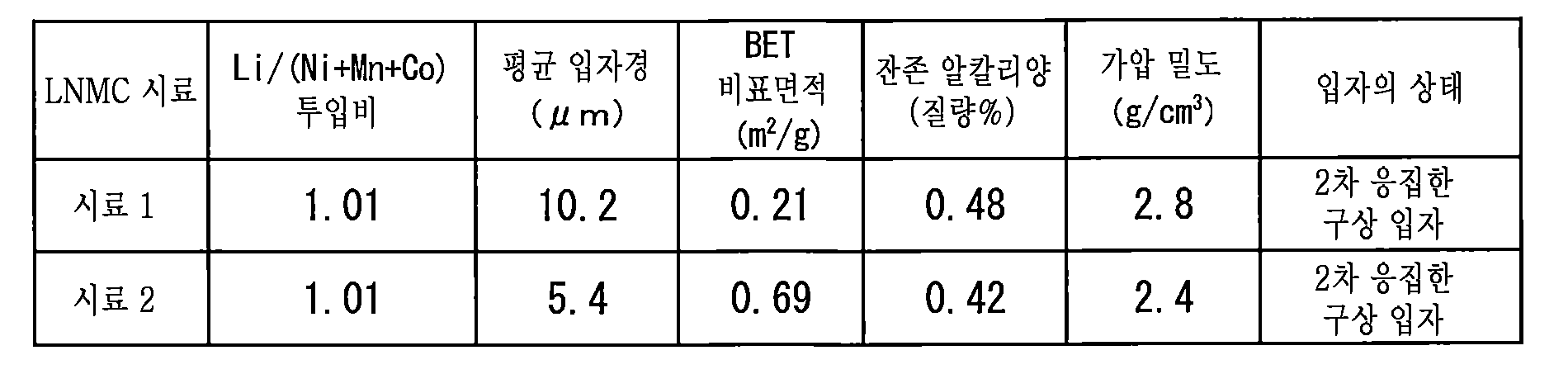
또한, 개질 대상인 리튬 니켈 망간 코발트 복합 산화물 입자는, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물의 입상물이다. 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자는, 1차 입자가 단분산된 단립자여도, 1차 입자가 집합하여 2차 입자를 형성한 응집 입자여도 된다. 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경은, 레이저 회절·산란법에 의해 구해지는 입도 분포에 있어서의 체적 환산 50%의 입자경(D50)이고, 바람직하게는 1.0 내지 30.0㎛, 특히 바람직하게는 3.0 내지 25.0㎛이다. 또한, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자의 BET 비표면적은, 바람직하게는 0.05 내지 2.00㎡/g, 특히 바람직하게는 0.15 내지 1.00㎡/g이다. 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경 또는 BET 비표면적이 상기 범위에 있음으로써, 정극 합제의 조제나 도공성이 용이해지고, 나아가 충전성이 높은 전극이 얻어진다.In addition, the lithium nickel manganese cobalt composite oxide particle to be modified is a granular material of a lithium nickel manganese cobalt composite oxide represented by the general formula (1). The lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) may be single particles in which primary particles are monodispersed, or may be aggregated particles in which primary particles aggregate to form secondary particles. The average particle diameter of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) is the 50% volume conversion particle diameter (D50) in the particle size distribution determined by the laser diffraction/scattering method, and is preferably 1.0 to 1.0. 30.0 μm, particularly preferably 3.0 to 25.0 μm. The BET specific surface area of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) is preferably 0.05 to 2.00 m 2 /g, particularly preferably 0.15 to 1.00 m 2 /g. When the average particle diameter or BET specific surface area of the lithium nickel manganese cobalt composite oxide particles is within the above range, the preparation and coating properties of the positive electrode mixture are facilitated, and an electrode with high fillability can be obtained.
또한, 개질 대상인 일반식 (1)인 리튬 니켈 망간 코발트 복합 산화물 입자 중의 잔존 알칼리양은, 바람직하게는 1.2질량% 이하, 특히 바람직하게는 1.0질량% 이하이다. 리튬 니켈 망간 코발트 복합 산화물 입자 중의 잔존 알칼리양이 상기 범위에 있음으로써, 잔존 알칼리에 기인하는 가스 발생에 의해 발생하는 전지의 팽창이나 열화를 억제할 수 있다.The amount of residual alkali in the lithium nickel manganese cobalt composite oxide particles of the general formula (1) to be modified is preferably 1.2% by mass or less, particularly preferably 1.0% by mass or less. When the amount of residual alkali in the particles of the lithium nickel manganese cobalt composite oxide is within the above range, expansion and deterioration of the battery caused by gas generation due to the residual alkali can be suppressed.
또한, 본 발명에 있어서, 잔존 알칼리는, 리튬 니켈 망간 코발트 복합 산화물 입자를 25℃의 물에 교반 분산시켰을 때에, 물에 용출되는 알칼리 성분을 나타낸다. 그리고, 잔존 알칼리양은, 리튬 니켈 망간 코발트 복합 산화물 입자 5g 및 순수 100g을 비이커에 칭량하고, 25℃에서, 자기 교반 막대로 5분간 분산시켜서, 이어서 이 분산액을 여과하고, 얻어지는 여액 중에 존재하는 알칼리의 양을 중화 적정함으로써 구해진다. 또한, 해당 잔존 알칼리양은, 적정에 의해 리튬양을 측정하여 탄산리튬으로 환산한 값이다.In the present invention, residual alkali refers to an alkali component that is eluted into water when lithium nickel manganese cobalt composite oxide particles are stirred and dispersed in water at 25°C. Then, the amount of residual alkali was determined by weighing 5 g of lithium nickel manganese cobalt composite oxide particles and 100 g of pure water in a beaker, dispersing them at 25° C. for 5 minutes with a magnetic stirring bar, filtering the dispersion, and measuring the amount of alkali present in the obtained filtrate. It is obtained by neutralizing titration of the amount. In addition, the amount of the remaining alkali is a value obtained by measuring the amount of lithium by titration and converting it into lithium carbonate.
개질 대상인 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자는, 예를 들어 리튬원, 니켈원, 망간원, 코발트원 및 필요에 따라서 첨가하는 M원을 혼합하여 원료 혼합물을 조제하는 원료 혼합 공정과, 이어서 얻어지는 원료 혼합물을 소성하는 소성 공정을 행함으로써 제조된다.The lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) to be modified are, for example, a raw material for preparing a raw material mixture by mixing a lithium source, a nickel source, a manganese source, a cobalt source, and an M source added as needed It is manufactured by performing a mixing process and a sintering process of sintering the raw material mixture obtained subsequently.
원료 혼합 공정에 따른 리튬원, 니켈원, 망간원, 코발트원 및 M원으로서는, 예를 들어 이들 수산화물, 산화물, 탄산염, 질산염, 황산염, 유기산염 등이 사용된다. 리튬원, 니켈원, 망간원, 코발트원 및 M원의 평균 입자경은, 레이저·산란법에 의해 구해지는 평균 입자경이 1.0 내지 30.0㎛, 바람직하게는 2.0 내지 25.0㎛인 것이 바람직하다.As the lithium source, nickel source, manganese source, cobalt source, and M source according to the raw material mixing step, for example, these hydroxides, oxides, carbonates, nitrates, sulfates, organic acid salts, etc. are used. It is preferable that the average particle diameter of the lithium source, nickel source, manganese source, cobalt source, and M source is 1.0 to 30.0 μm, preferably 2.0 to 25.0 μm, as determined by a laser scattering method.
원료 혼합 공정에 따른 니켈원, 망간원 및 코발트원은, 니켈 원자, 망간 원자 및 코발트 원자를 함유하는 화합물이어도 된다. 니켈 원자, 망간 원자 및 코발트 원자를 함유하는 화합물로서는, 예를 들어 이들 원자를 함유하는 복합 산화물, 복합 수산화물, 복합 옥시수산화물, 복합 탄산염 등을 들 수 있다.The nickel source, manganese source, and cobalt source according to the raw material mixing step may be compounds containing nickel atoms, manganese atoms, and cobalt atoms. As a compound containing a nickel atom, a manganese atom, and a cobalt atom, the composite oxide, composite hydroxide, composite oxyhydroxide, composite carbonate etc. which contain these atoms are mentioned, for example.
또한, 니켈 원자, 망간 원자 및 코발트 원자를 함유하는 화합물을 조제하는 방법으로서는, 공지된 방법이 이용된다. 예를 들어, 복합 수산화물의 경우, 공침법에 의해 조제할 수 있다. 구체적으로는, 소정량의 니켈 원자, 코발트 원자 및 망간 원자를 포함하는 수용액과, 착화제의 수용액과, 알칼리의 수용액을 혼합함으로써, 복합 수산화물을 공침시킬 수 있다(일본 특허 공개 평10-81521호 공보, 일본 특허 공개 평10-81520호 공보, 일본 특허 공개 평10-29820호 공보, 일본 특허 공개 제2002-201028호 공보 등 참조). 또한, 복합 탄산염의 경우에는, 니켈 이온, 망간 이온 및 코발트 이온을 포함하는 용액(A액)과, 탄산 이온 또는 탄산수소 이온을 포함하는 용액(B액)을 반응 용기에 첨가하여 반응을 행하는 방법(일본 특허 공개 제2009-179545호 공보), 혹은 니켈염, 망간염 및 코발트염을 포함하는 용액(A액)과, 금속 탄산염 또는 금속 탄산수소염을 포함하는 용액(B액)을 해당 A액 중의 해당 니켈염, 해당 망간염 및 해당 코발트염의 음이온과 동일한 음이온과, 해당 B액 중의 해당 금속 탄산염 또는 해당 금속 탄산수소염의 음이온과 동일한 음이온을 포함하는 용액(C액)에 첨가하여, 반응을 행하는 방법(일본 특허 공개 제2009-179544호 공보) 등을 들 수 있다. 또한, 니켈 원자, 망간 원자 및 코발트 원자를 함유하는 화합물은, 시판품이어도 된다.In addition, as a method for preparing a compound containing a nickel atom, a manganese atom, and a cobalt atom, a known method is used. For example, in the case of a composite hydroxide, it can be prepared by a coprecipitation method. Specifically, a composite hydroxide can be coprecipitated by mixing an aqueous solution containing predetermined amounts of nickel atoms, cobalt atoms, and manganese atoms, an aqueous solution of a complexing agent, and an aqueous alkali solution (Japanese Unexamined Patent Publication No. 10-81521). Japanese Patent Laid-Open No. 10-81520, Japanese Patent Laid-Open No. 10-29820, Japanese Patent Laid-Open No. 2002-201028, etc.). Further, in the case of a complex carbonate, a method in which a solution containing nickel ions, manganese ions, and cobalt ions (liquid A) and a solution containing carbonate ions or hydrogen carbonate ions (liquid B) are added to a reaction vessel to perform the reaction. (Japanese Unexamined Patent Publication No. 2009-179545), or a solution (liquid A) containing nickel salt, manganese salt and cobalt salt and a solution (liquid B) containing metal carbonate or metal hydrogen carbonate in the liquid A A method of reacting by adding to a solution (liquid C) containing the same anion as that of the nickel salt, manganese salt, and cobalt salt, and the same anion as that of the metal carbonate or metal hydrogencarbonate in the liquid B (Japanese Unexamined Patent Publication No. 2009-179544), etc. are mentioned. In addition, commercial items may be sufficient as the compound containing a nickel atom, a manganese atom, and a cobalt atom.
니켈 원자, 코발트 원자 및 망간 원자를 함유하는 화합물의 평균 입자경은, 레이저·산란법에 의해 구해지는 평균 입자경이 1.0 내지 100㎛, 바람직하게는 2.0 내지 80.0㎛이다.The average particle diameter of the compound containing nickel atoms, cobalt atoms and manganese atoms, determined by a laser scattering method, is 1.0 to 100 µm, preferably 2.0 to 80.0 µm.
일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자의 제조에 있어서, 니켈원, 망간원 및 코발트원으로서, 니켈 원자, 코발트 원자 및 망간 원자를 함유하는 복합 수산화물을 사용하는 것이, 반응성이 양호해진다는 점에서 바람직하다.In the production of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1), it is preferable to use composite hydroxides containing nickel atoms, cobalt atoms and manganese atoms as the nickel source, manganese source and cobalt source because the reactivity is It is desirable in that it becomes good.
원료 혼합 공정에 있어서, 리튬원과, 니켈원, 망간원, 코발트원 및 필요에 따라서 첨가하는 M원의 혼합 비율은, 방전 용량이 높아진다는 점에서, 니켈원, 망간원 및 코발트원 중의 Ni 원자, Mn 원자, Co 원자 및 M 원자의 총 몰수(Ni+Mn+Co+M)에 대한 Li 원자의 몰비(Li/(Ni+Mn+Co+M))는 0.98 내지 1.20, 바람직하게는 1.00 내지 1.10이다.In the raw material mixing step, the mixing ratio of the lithium source, the nickel source, the manganese source, the cobalt source, and the M source added as needed increases the discharge capacity, so the Ni atoms in the nickel source, manganese source, and cobalt source , the molar ratio of Li atoms (Li/(Ni+Mn+Co+M)) to the total number of moles of Mn atoms, Co atoms and M atoms (Ni+Mn+Co+M) is from 0.98 to 1.20, preferably from 1.00 to 1.20. It is 1.10.
또한, 원료 혼합 공정에 있어서, 니켈원, 망간원, 코발트원 및 필요에 따라서 첨가하는 M원의 각 원료의 혼합 비율에 대해서는, 상기 일반식 (1)로 표시되는 니켈, 망간, 코발트 및 M의 원자 몰비가 되도록 조정하면 된다.In addition, in the raw material mixing step, the mixing ratio of each raw material of the nickel source, the manganese source, the cobalt source, and the M source added as needed is the nickel, manganese, cobalt, and M represented by the general formula (1) above. What is necessary is just to adjust it so that it may become an atomic molar ratio.
또한, 원료의 리튬원, 니켈원, 망간원, 코발트원 및 M원의 제조 이력은 불문이지만, 고순도의 리튬 니켈 망간 코발트 복합 산화물 입자를 제조하기 위해서, 가급적으로 불순물 함유량이 적은 것이면 바람직하다.In addition, the manufacturing history of the lithium source, nickel source, manganese source, cobalt source, and M source as a raw material is irrelevant, but in order to produce high-purity lithium nickel manganese cobalt composite oxide particles, it is preferable that the impurity content is as low as possible.
원료 혼합 공정에 있어서, 리튬원, 니켈원, 망간원, 코발트원 및 필요에 따라서 첨가하는 M원을 혼합하는 수단으로서는, 건식이어도 습식이어도 어느 방법이어도 되지만, 제조가 용이하기 때문에 건식에 의한 혼합이 바람직하다.In the raw material mixing step, as means for mixing the lithium source, nickel source, manganese source, cobalt source, and M source added as needed, either dry or wet method may be used, but dry mixing is preferable because production is easy. desirable.
건식 혼합의 경우에는, 원료가 균일하게 혼합하도록 기계적 수단으로 행하는 것이 바람직하다. 혼합 장치로서는, 예를 들어 하이 스피드 믹서, 슈퍼 믹서, 터보 스페어 믹서, 아이리히 믹서, 헨쉘 믹서, 나우타 믹서, 리본 블렌더, V형 혼합기, 코니컬 블렌더, 제트 밀, 코스모마이저, 페인트 셰이커, 비즈 밀, 볼 밀 등을 들 수 있다. 또한, 실험실 레벨에서는, 가정용 믹서로 충분하다.In the case of dry mixing, it is preferable to perform by mechanical means so that raw materials may be mixed uniformly. As a mixing device, for example, a high-speed mixer, a super mixer, a turbo spare mixer, an Irish mixer, a Henschel mixer, a Nauta mixer, a ribbon blender, a V-type mixer, a conical blender, a jet mill, a cosmizer, a paint shaker, and a bead mill , a ball mill, and the like. Also, at the laboratory level, a household mixer is sufficient.
습식 혼합의 경우, 혼합 장치로서는, 미디어 밀을 사용하는 것이, 각 원료가 균일하게 분산된 슬러리를 조제할 수 있다는 점에서 바람직하다. 또한, 혼합 처리 후의 슬러리는, 반응성이 우수하고 각 원료가 균일하게 분산된 원료 혼합물이 얻어진다는 관점에서 분무 건조를 행하는 것이 바람직하다.In the case of wet mixing, it is preferable to use a media mill as a mixing device in that a slurry in which each raw material is uniformly dispersed can be prepared. Further, the slurry after the mixing treatment is preferably spray-dried from the viewpoint of obtaining a raw material mixture having excellent reactivity and in which each raw material is uniformly dispersed.
소성 공정은, 원료 혼합 공정을 행하여 얻어지는 원료 혼합물을, 소성함으로써, 리튬 니켈 망간 코발트 복합 산화물을 얻는 공정이다.The firing step is a step of obtaining a lithium nickel manganese cobalt composite oxide by firing the raw material mixture obtained by performing the raw material mixing step.
소성 공정에 있어서, 원료 혼합물을 소성하고, 원료를 반응시킬 때의 소성 온도는 600 내지 1000℃, 바람직하게는 700 내지 950℃이다. 이 이유는 소성 온도가 600℃ 미만이면 반응이 불충분하여 미반응된 리튬이 다량으로 잔류하는 경향이 있고, 한편, 1000℃를 초과하면 한번 생성된 리튬 니켈 망간 코발트 복합 산화물이 분해되어버리는 경향이 있기 때문이다.In the firing step, the firing temperature for firing the raw material mixture and reacting the raw materials is 600 to 1000°C, preferably 700 to 950°C. The reason for this is that when the firing temperature is less than 600 ° C, the reaction is insufficient and unreacted lithium tends to remain in a large amount. Because.
소성 공정에 있어서의 소성 시간은 3시간 이상, 바람직하게는 5 내지 30시간다. 또한, 소성 공정에 있어서의 소성 분위기는 공기, 산소 가스의 산화 분위기이다.The firing time in the firing step is 3 hours or more, preferably 5 to 30 hours. In addition, the firing atmosphere in the firing process is an oxidizing atmosphere of air and oxygen gas.
또한, 소성 공정에 있어서, 소성은 다단식으로 행해도 된다. 다단식으로 소성을 행함으로써, 한층 더 사이클 특성이 우수한 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 얻을 수 있다. 다단으로 소성을 행하는 경우, 650 내지 800℃의 범위에서 1 내지 10시간 소성한 후, 또한 해당 소성 온도보다 높은 온도가 되도록 800 내지 950℃에서 승온하고, 그대로 5 내지 30시간 소성하는 것이 바람직하다.In addition, in the firing step, firing may be performed in a multi-stage manner. By firing in a multi-stage manner, modified lithium nickel manganese cobalt composite oxide particles having further excellent cycle characteristics can be obtained. When firing in multiple stages, it is preferable to fire in the range of 650 to 800 ° C. for 1 to 10 hours, then raise the temperature to 800 to 950 ° C. so that the temperature is higher than the firing temperature, and then fire as it is for 5 to 30 hours.
이와 같이 얻어지는 리튬 니켈 망간 코발트 복합 산화물을, 필요에 따라 복수회의 소성 공정에 회부해도 된다.The lithium nickel manganese cobalt composite oxide obtained in this way may be subjected to a plurality of firing steps as needed.
또한, 잔존 알칼리양이 상기 범위인 리튬니켈 망간 복합 산화물 입자는, 리튬원, 니켈원, 망간원, 코발트원 및 필요에 따라서 첨가하는 M원의 원료 혼합 공정에 있어서, 니켈원, 망간원, 코발트원 및 M원 중의 Ni 원자, Mn 원자, Co 원자 및 M 원자의 총 몰수(Ni+Mn+Co+M)에 대한 Li 원자의 몰비(Li/(Ni+Mn+Co+M))가 0.98 내지 1.20이 되는 혼합 비율로 하고, 700℃ 이상, 바람직하게는 750 내지 1000℃에서, 3시간 이상, 바람직하게는 5 내지 30시간 소성 반응에 회부하여, 충분히 리튬원, 니켈원, 망간원, 코발트원 및 필요에 따라서 첨가하는 M원을 반응시킴으로써 제조할 수 있다. 본 제조 방법에 있어서, 상기 소성은, 전술한 다단식으로 행함으로써, 잔존 알칼리양이 한층 더 저감된 리튬니켈 망간 복합 산화물 입자를 제조할 수 있다.In addition, the lithium nickel manganese composite oxide particles having a residual alkali amount in the above range are a lithium source, a nickel source, a manganese source, a cobalt source, and an M source added as needed in the raw material mixing step, the nickel source, manganese source, and cobalt The molar ratio of Li atoms (Li/(Ni+Mn+Co+M)) to the total number of moles (Ni+Mn+Co+M) of Ni atoms, Mn atoms, Co atoms and M atoms in the circle and M circle is from 0.98 to 0.98. At a mixing ratio of 1.20, subject to a firing reaction at 700 ° C. or higher, preferably 750 to 1000 ° C. for 3 hours or more, preferably 5 to 30 hours, and a sufficient lithium source, nickel source, manganese source, cobalt source And it can be manufactured by reacting M source added as needed. In this production method, the firing is carried out in the above-described multi-stage manner, whereby lithium nickel manganese composite oxide particles in which the amount of residual alkali is further reduced can be produced.
(A) 공정에 따른 표면 처리액은, 티타늄킬레이트 화합물, 즉, 일반식 (2)로 표시되는 티타늄킬레이트 또는 일반식 (2)로 표시되는 티타늄킬레이트의 암모늄염을, 물 및/또는 유기 용매에 용해 또는 분산시킨 것이다.(A) The surface treatment liquid according to the step dissolves a titanium chelate compound, that is, a titanium chelate represented by the general formula (2) or an ammonium salt of the titanium chelate represented by the general formula (2) in water and/or an organic solvent. or dispersed.
(A) 공정에 따른 티타늄킬레이트는, 하기 일반식 (2):(A) Titanium chelate according to the process, the following general formula (2):
(식 중, R1은, 알콕시기, 수산기, 할로겐 원자, 아미노기 또는 포스핀류를 나타내고, 복수 존재하는 경우, 동일해도 되며 달라도 된다. L은 히드록시카르복실산에서 유래되는 기를 나타내고, 복수 존재하는 경우, 동일해도 되며 달라도 된다. m은 0 이상 3 이하의 수를 나타내고, n은 1 이상 3 이하의 수를 나타내며, m+n은 3 내지 6임)(In the formula, R 1 represents an alkoxy group, a hydroxyl group, a halogen atom, an amino group or a phosphine, and when present in a plurality thereof, may be the same or different. L represents a group derived from hydroxycarboxylic acid, and a plurality of In this case, it may be the same or different. m represents a number of 0 or more and 3 or less, n represents a number of 1 or more and 3 or less, and m+n is 3 to 6)
로 표시되는 티타늄킬레이트이다.It is a titanium chelate represented by
R1에 관련된 알콕시기로서는, 탄소수 1 내지 4의 직쇄상 또는 분지상의 알콕시기가 바람직하다. R1에 관련된 할로겐 원자로서는, 불소 원자, 염소 원자, 브롬 원자, 요오드 원자를 들 수 있다. R1에 관련된 아미노기로서는, 예를 들어 메틸아미노기, 에틸아미노기, 프로필아미노기, 이소프로필아미노기, 부틸아미노기, 이소부틸아미노기, tert-부틸아미노기, 펜틸아미노기 등을 들 수 있다. R1에 관련된 포스핀류로서는, 예를 들어 트리메틸포스핀, 트리에틸포스핀, 트리부틸포스핀, 트리스-tert-부틸포스핀, 트리페닐포스핀 등을 들 수 있다.As the alkoxy group related to R 1 , a linear or branched alkoxy group having 1 to 4 carbon atoms is preferable. As a halogen atom related to R 1 , a fluorine atom, a chlorine atom, a bromine atom, and an iodine atom are exemplified. Examples of the amino group related to R 1 include a methylamino group, an ethylamino group, a propylamino group, an isopropylamino group, a butylamino group, an isobutylamino group, a tert-butylamino group, and a pentylamino group. Examples of the phosphines related to R 1 include trimethylphosphine, triethylphosphine, tributylphosphine, tris-tert-butylphosphine, and triphenylphosphine.
L에 관련된 히드록시카르복실산에서 유래되는 기로서는, 히드록시카르복실산에 있어서의 히드록실기의 산소 원자 또는 히드록시카르복실산에 있어서의 카르복실기의 산소 원자가, 티타늄 원자에 배위하여 이루어지는 기를 들 수 있다. 또한, L에 관련된 히드록시카르복실산에서 유래되는 기로서는, 히드록시카르복실산에 있어서의 히드록실기의 산소 원자 및 히드록실 카르복실산에 있어서의 카르복실기의 산소 원자가, 티타늄 원자에 2좌로 배위하여 이루어지는 기를 들 수 있다. 이들 중, 히드록시카르복실산에 있어서의 히드록실기의 산소 원자 및 히드록시카르복실산에 있어서의 카르복실기의 산소 원자가, 티타늄 원자에 2좌로 배위하여 이루어지는 기인 것이 바람직하다. m이 0인 경우에는 m+n은 3인 것이 바람직하고, m이 1 이상 3 이하인 경우에는 m+n은 4 또는 5인 것이 바람직하다.As the group derived from the hydroxycarboxylic acid related to L, a group formed by coordinating the oxygen atom of the hydroxyl group in the hydroxycarboxylic acid or the oxygen atom of the carboxyl group in the hydroxycarboxylic acid to the titanium atom is exemplified. can In addition, as a group derived from the hydroxycarboxylic acid related to L, the oxygen atom of the hydroxyl group in the hydroxycarboxylic acid and the oxygen atom of the carboxyl group in the hydroxyl carboxylic acid are doubled on the titanium atom. A group made for this can be mentioned. Among these, it is preferable that the oxygen atom of the hydroxyl group in hydroxycarboxylic acid and the oxygen atom of the carboxyl group in hydroxycarboxylic acid are a group formed by coordinating with a titanium atom in a bidentate manner. When m is 0, it is preferable that m+n is 3, and when m is 1 or more and 3 or less, it is preferable that m+n is 4 or 5.
티타늄킬레이트의 제조 방법이지만, 예를 들어 티타늄알콕시드를 용매로 희석하여 희석액을 얻고, 해당 희석액과 히드록시카르복실산을 혼합함으로써, 티타늄킬레이트를 포함하는 용액이 얻어진다(WO2019/138989호 팸플릿 참조). 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에서는, 상기 티타늄킬레이트의 제조 방법에 의해 얻어지는 티타늄킬레이트를 포함하는 용액을, 그대로 (A) 공정에서 표면 처리액으로서 사용할 수 있다. 또한, 티타늄킬레이트를 포함하는 용액에 물을 첨가하여, 표면 처리액으로서 사용해도 된다. 이에 의해, 표면 처리액으로서, 티타늄킬레이트의 물 함유 용매의 분산액 또는 용해액을 얻을 수 있다.Although it is a method for producing titanium chelate, for example, a solution containing titanium chelate is obtained by diluting titanium alkoxide with a solvent to obtain a diluted solution and mixing the diluted solution with hydroxycarboxylic acid (see pamphlet WO2019/138989). ). In the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention, the solution containing the titanium chelate obtained by the method for producing titanium chelate can be used as a surface treatment liquid in step (A). In addition, water may be added to a solution containing titanium chelate and used as a surface treatment liquid. As a result, a dispersion or solution of titanium chelate in a water-containing solvent can be obtained as a surface treatment solution.
또한, 상기 티타늄알콕시드로서는, 예를 들어 테트라메톡시티타늄(Ⅳ), 테트라에톡시티타늄(Ⅳ), 테트라-n-프로폭시티타늄(Ⅳ), 테트라이소프로폭시티타늄(Ⅳ), 테트라-n-부톡시티타늄(Ⅳ) 및 테트라이소부톡시 티타늄(Ⅳ) 등을 들 수 있다.Examples of the titanium alkoxide include tetramethoxytitanium (IV), tetraethoxytitanium (IV), tetra-n-propoxytitanium (IV), tetraisopropoxytitanium (IV), tetra-n -butoxytitanium (IV) and tetraisobutoxytitanium (IV); and the like.
또한, 상기 히드록시카르복실산으로서는, 예를 들어 락트산, 글리콜산, 글리세린산, 히드록시부티르산 등의 1가의 카르복실산, 타르트론산, 말산, 타르타르산 등의 2가의 카르복실산, 시트르산, 이소시트르산 등의 3가의 카르복실산 등을 들 수 있다. 이들 중, 락트산이, 실온에서 용이하게 용액으로 되어, 티타늄알콕시드 희석액과 혼합하기 쉽고, 용이하게 티타늄킬레이트를 제조할 수 있다는 관점에서 바람직하다.Examples of the hydroxycarboxylic acid include monovalent carboxylic acids such as lactic acid, glycolic acid, glyceric acid, and hydroxybutyric acid, divalent carboxylic acids such as tartronic acid, malic acid, and tartaric acid, citric acid, and isocitrate Trivalent carboxylic acids, such as these, etc. are mentioned. Among these, lactic acid is preferred from the viewpoint that it easily becomes a solution at room temperature, is easily mixed with a diluted titanium alkoxide solution, and can easily produce a titanium chelate.
또한, 희석액으로서 사용하는 용매로서는, 메탄올, 에탄올, 이소프로판올, n-프로판올, n-부탄올, sec-부탄올, tert-부탄올, n- 펜탄 등의 알코올을 바람직하게 사용할 수 있다.As the solvent used as the diluent, alcohols such as methanol, ethanol, isopropanol, n-propanol, n-butanol, sec-butanol, tert-butanol, and n-pentane can be preferably used.
또한, 희석액과 히드록시카르복실산을 혼합할 때, 또는 티타늄킬레이트를 포함하는 용액에, 높은 생산성에 의해 효율적으로 티타늄킬레이트를 얻을 것을 목적으로 하여, 히드록시카르복실산 이외에, 티타늄에 배위 가능한 배위자 화합물을 첨가해도 된다. 그와 같은 배위자 화합물로서는, 예를 들어 할로겐 원자 함유 화합물, 메틸아미노기, 에틸아미노기, 프로필아미노기, 이소프로필아미노기, 부틸아미노기, 이소부틸아미노기, t-부틸아미노기, 펜틸아미노 등의 관능기를 갖는 아민류, 트리메틸포스핀, 트리에틸포스핀, 트리부틸포스핀, 트리스-tert-부틸포스핀, 트리페닐포스핀 등의 포스핀류를 들 수 있다.In addition, for the purpose of obtaining titanium chelate efficiently with high productivity when mixing the diluted solution and hydroxycarboxylic acid or in a solution containing titanium chelate, a ligand capable of coordinating to titanium in addition to hydroxycarboxylic acid A compound may be added. Examples of such ligand compounds include halogen atom-containing compounds, amines having functional groups such as methylamino group, ethylamino group, propylamino group, isopropylamino group, butylamino group, isobutylamino group, t-butylamino group, and pentylamino group, trimethyl and phosphines such as phosphine, triethylphosphine, tributylphosphine, tris-tert-butylphosphine, and triphenylphosphine.
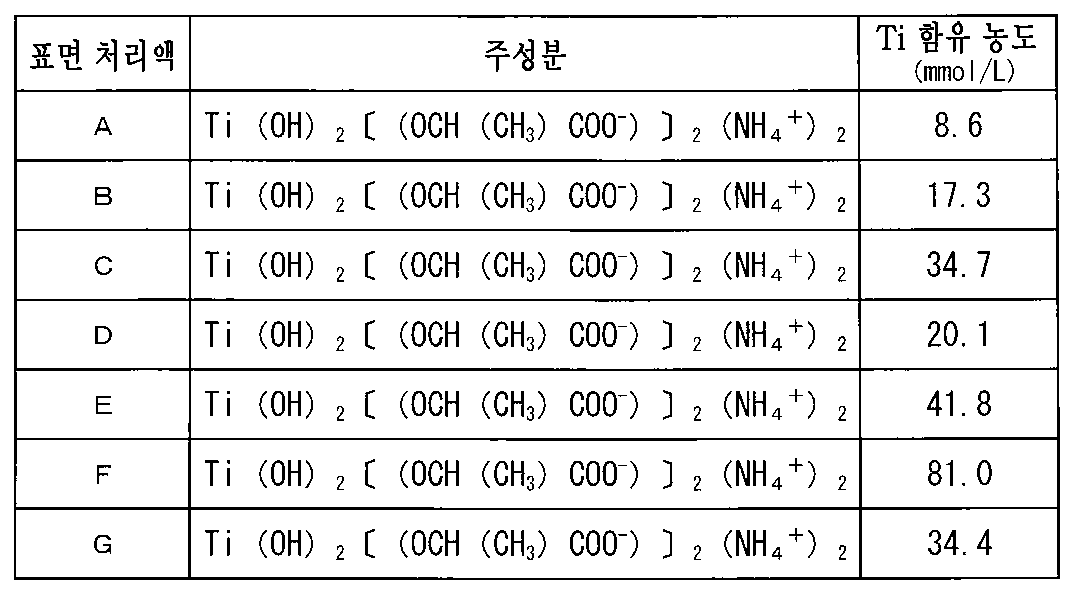
티타늄킬레이트의 암모늄염으로서는, 티타늄락테이트암모늄염(Ti(OH)2〔(OCH(CH3)COO-)2(NH4 +)2)이 바람직하다.As the ammonium salt of titanium chelate, titanium lactate ammonium salt (Ti(OH) 2 [(OCH(CH 3 )COO - ) 2 (NH 4 + ) 2 ) is preferable.
또한, 티타늄킬레이트 및 그의 암모늄염은, 마츠모토파인케미컬사에서 일부 시판 중이며, 시판품을 사용해도 된다.In addition, some titanium chelates and their ammonium salts are commercially available from Matsumoto Fine Chemical Co., Ltd., and commercial products may be used.
또한, (A) 공정에 따른 표면 처리액 중의 Ti 농도는, Ti 원자로서, 0.1 내지 1500mmol/L, 바람직하게는 0.2 내지 1000mmol/L인 것이, Ti 용액의 안정성과 피복 처리의 조작성이 용이해진다는 관점에서 바람직하다.In addition, the Ti concentration in the surface treatment solution according to the step (A), in terms of Ti atoms, is 0.1 to 1500 mmol/L, preferably 0.2 to 1000 mmol/L, so that the stability of the Ti solution and the operability of the coating treatment become easy. desirable from the point of view
(A) 공정에 따른 표면 처리액의 pH는 7 이상, 바람직하게는 8 이상 11 이하, 특히 바람직하게는 8보다 크고 10 이하인 것이, 리튬 니켈 망간 코발트 복합 산화물 입자와, 표면 처리액이 접촉했을 때에, 리튬 니켈 망간 코발트 복합 산화물 입자로부터의 Li의 용출이 억제된다는 점에서 바람직하다. 또한, 표면 처리액의 pH에 대해서는, 상기 범위의 pH가 되도록, 표면 처리액에 산이나 알칼리를 첨가하여 pH를 조정할 수 있다.(A) The pH of the surface treatment solution according to the step is 7 or more, preferably 8 or more and 11 or less, particularly preferably more than 8 and 10 or less, when the lithium nickel manganese cobalt composite oxide particles and the surface treatment solution come into contact. , which is preferable in that elution of Li from lithium nickel manganese cobalt composite oxide particles is suppressed. In addition, about the pH of the surface treatment liquid, the pH can be adjusted by adding acid or alkali to the surface treatment liquid so that it becomes a pH within the above range.
(A) 공정에 있어서, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와, 티타늄킬레이트 화합물을 포함하는 표면 처리액을 접촉시키는 방법은, 특별히 제한되는 것은 아니지만, 예를 들어 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와 티타늄킬레이트 화합물을 포함하는 표면 처리액을 혼합 처리하는 방법 등을 들 수 있다. 또한, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와 티타늄킬레이트 화합물을 포함하는 표면 처리액의 혼합물은 분말상이어도, 페이스트상이어도 되며 또는 슬러리상이어도 된다. 해당 혼합물이, 분말상, 페이스트상 또는 슬러리상의 것은, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자에 대한 티타늄킬레이트 화합물을 포함하는 표면 처리액의 첨가량을 조제함으로써, 어떠한 형태의 것도 얻을 수 있다. 예를 들어, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와 티타늄킬레이트 화합물을 포함하는 표면 처리액의 혼합물이 분말상의 것은, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자에 대하여 액의 체적이 소량의 티타늄킬레이트 화합물을 포함하는 표면 처리액을 첨가함으로써 얻어지고, 또한 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와 티타늄킬레이트 화합물을 포함하는 표면 처리액의 혼합물이 슬러리상의 것은, 액의 체적이 다량의 티타늄킬레이트 화합물을 포함하는 표면 처리액에 대하여 소량의 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를 첨가함으로써 얻어진다.In the step (A), the method of contacting the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) with the surface treatment liquid containing the titanium chelate compound is not particularly limited, but, for example, the general formula A method of mixing the lithium nickel manganese cobalt composite oxide particles represented by (1) with a surface treatment solution containing a titanium chelate compound, and the like are exemplified. The mixture of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) and the surface treatment liquid containing the titanium chelate compound may be in the form of powder, paste or slurry. Whether the mixture is in powder form, paste form or slurry form, any form can be obtained by adjusting the addition amount of the surface treatment liquid containing the titanium chelate compound to the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1). can For example, the powdery mixture of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) and the surface treatment liquid containing the titanium chelate compound is the lithium nickel manganese cobalt composite oxide represented by the general formula (1) A surface treatment liquid obtained by adding a surface treatment liquid containing a titanium chelate compound in a small volume to particles, and containing lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) and a titanium chelate compound A mixture of in the form of a slurry is obtained by adding a small amount of lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) to a surface treatment liquid containing a large amount of titanium chelate compound by volume of the liquid.
또한, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와, 티타늄킬레이트 화합물을 포함하는 용액의 접촉은, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 티타늄킬레이트 화합물을 포함하는 용액에 침지하는 방법이어도 된다.Further, the contact of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) with the solution containing the titanium chelate compound results in the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1), the titanium chelate compound A method of immersing in a solution containing
이들 중, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 있어서, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와, 티타늄킬레이트 화합물을 포함하는 표면 처리액을 접촉시키는 방법으로서는, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자의 표면 전체에 티타늄킬레이트 화합물을 용이하게 부착시킬 수 있다는 점에서, 혼합물이 슬러리상이 되는 방법이 바람직하다.Among these, in the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention, a method in which lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) are brought into contact with a surface treatment liquid containing a titanium chelate compound. As a method, a method in which the mixture is in a slurry form is preferable in that the titanium chelate compound can be easily adhered to the entire surface of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1).
일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 티타늄킬레이트 화합물을 포함하는 표면 처리액에 접촉시킨 후, 그대로 용매를 전량 건조시킴으로써, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면이 티타늄킬레이트 화합물로 피복된 피복 입자를 얻는 것이 바람직하다. 건조 시의 건조 온도는, 용매가 증발하는 온도이면, 특별히 제한되지는 않지만, 바람직하게는 60 내지 180℃ 특히 바람직하게는 90 내지 150℃이다.Lithium nickel manganese cobalt represented by general formula (1) is obtained by bringing lithium nickel manganese cobalt composite oxide particles represented by general formula (1) into contact with a surface treatment solution containing a titanium chelate compound, and then drying the entire amount of the solvent as it is. It is preferable to obtain coated particles in which the particle surfaces of composite oxide particles are coated with a titanium chelate compound. The drying temperature at the time of drying is not particularly limited as long as the solvent evaporates, but is preferably 60 to 180°C and particularly preferably 90 to 150°C.
또한, 건조에 대해서는, 분무 건조 장치, 로터리 증발기, 유동층 건조 코팅 장치, 진동 건조 장치 등에 의해 전량 건조를 행해도 된다.In addition, regarding drying, you may perform whole-quantity drying by a spray drying apparatus, a rotary evaporator, a fluid bed dry-coating apparatus, a vibration drying apparatus, etc.
(A) 공정에 있어서, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자와, 티타늄킬레이트 화합물을 포함하는 표면 처리액을 함유하는 슬러리를, 분무 건조 장치로 용매를 전량 건조시키는 것이 티타늄킬레이트 화합물의 피복량을 컨트롤하는 것이 용이해진다는 점에서 바람직하다.In the step (A), the slurry containing the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) and the surface treatment liquid containing the titanium chelate compound is dried by a spray drying device to remove the entire amount of the solvent. It is preferable in that it becomes easy to control the coating amount of the chelate compound.
(B) 공정은, (A) 공정에서 얻어진 피복 입자를 가열 처리함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 (A) 혹은 개질 리튬 니켈 망간 코발트 복합 산화물 (B)를 얻는 공정이다.Step (B) is a step of obtaining a modified lithium nickel manganese cobalt composite oxide (A) or a modified lithium nickel manganese cobalt composite oxide (B) by heating the coated particles obtained in step (A).
개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)에 있어서, Ti 원자는, 주로, 리튬 니켈 망간 코발트 복합 산화물 입자에 고용되지 않고, Ti를 포함하는 산화물의 상태에서, 리튬 니켈 망간 코발트 복합 산화물 입자의 표면에 존재하고 있다. 또한, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)에 있어서는, 소량의 일부 Ti 원자가, 리튬 니켈 망간 코발트 복합 산화물 입자의 내부에 고용되어 있어도 된다.In the modified lithium nickel manganese cobalt composite oxide particles (A), Ti atoms are mainly not dissolved in the lithium nickel manganese cobalt composite oxide particles, and in the state of an oxide containing Ti, the surface of the lithium nickel manganese cobalt composite oxide particles exists in In addition, in the modified lithium nickel manganese cobalt composite oxide particles (A), a small amount of some Ti atoms may be dissolved inside the lithium nickel manganese cobalt composite oxide particles.
개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)에 있어서, Ti 원자는, 주로, 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 내부에 고용된 상태로 존재하고 있다고 생각된다. 또한, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)에 있어서는, 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면을 SEM-EDX로 Ti의 원소 매핑 분석으로 분석했을 때에, Ti가 Co, Ni, Mn 등과 마찬가지로 균일하게 분포된 상태에서 관찰되는 범위이면, Ti 원자가, 리튬 니켈 망간 코발트 복합 산화물 입자의 표면에 Ti를 포함하는 산화물이 상태로 존재하고 있어도 된다.In the modified lithium nickel manganese cobalt composite oxide particles (B), Ti atoms are considered to exist mainly in a solid solution state inside the particles of the lithium nickel manganese cobalt composite oxide particles. Further, in the modified lithium nickel manganese cobalt composite oxide particles (B), when the particle surface of the modified lithium nickel manganese cobalt composite oxide particles was analyzed by elemental mapping analysis of Ti by SEM-EDX, Ti was found to be Co, Ni, Mn, etc. Similarly, as long as it is within the range observed in a uniformly distributed state, Ti atoms may exist in a Ti-containing oxide state on the surface of the lithium nickel manganese cobalt composite oxide particle.
따라서, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)인지, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)인지는, SEM-EDX로 샘플 입자의 입자 표면을 Ti의 원소 매핑 분석으로 분석함으로써 확인된다. 즉, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)인 경우에는, 샘플 입자의 입자 표면을 10,000 내지 30,000배의 확대 배율로 SEM-EDX에 의한 Ti의 원소 매핑 분석으로 분석했을 때에, 샘플 입자 표면에 Ti가 편재 등의 불균일하게 분포하여 존재하는 것이 관찰된다. 또한, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)인 경우에는, 샘플 입자의 입자 표면을 10,000 내지 30,000배의 확대 배율로 SEM-EDX에 의한 Ti의 원소 매핑 분석으로 분석했을 때에, 샘플 입자 표면에 Ti가 균일하게 분포하여 존재하는 것이 관찰된다.Therefore, whether the particle is a modified lithium nickel manganese cobalt composite oxide particle (A) or a modified lithium nickel manganese cobalt composite oxide particle (B) is confirmed by analyzing the particle surface of the sample particle by elemental mapping analysis of Ti with SEM-EDX. That is, in the case of the modified lithium nickel manganese cobalt composite oxide particles (A), when the particle surfaces of the sample particles are analyzed by elemental mapping analysis of Ti by SEM-EDX at a magnification of 10,000 to 30,000 times, the surface of the sample particles It is observed that Ti exists in a non-uniform distribution such as uneven distribution. In addition, in the case of the modified lithium nickel manganese cobalt composite oxide particles (B), when the particle surfaces of the sample particles are analyzed by elemental mapping analysis of Ti by SEM-EDX at a magnification of 10,000 to 30,000 times, the surface of the sample particles It is observed that Ti exists in a uniform distribution.
또한, 본 발명에 있어서, 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면을 피복하는 Ti를 포함하는 산화물이란, Ti의 산화물, Ti와, Li, Ni, Mn, Co 및 M으로부터 선택되는 1종 또는 2종 이상을 포함하는 복합 산화물 등을 나타내는 것이다.In the present invention, the oxide containing Ti that coats the particle surface of the lithium nickel manganese cobalt composite oxide particles is an oxide of Ti, Ti, and one or two selected from Li, Ni, Mn, Co, and M. It represents a composite oxide containing more than one species.
(B) 공정에 따른 가열 처리에 있어서, 가열 처리 온도는 400 내지 1000℃, 바람직하게는 450 내지 950℃이다. 이 이유는, 가열 처리 온도가 400℃ 미만이면 피복 처리용 티타늄킬레이트의 충분한 분해 및 산화 반응이 행해지지 않아 충분한 효과를 얻지 못하고, 한편, 가열 처리 온도가 1000℃를 초과하면 Ti와 리튬 니켈 망간 코발트 복합 산화물 입자의 고용 반응이 과도하게 진행되어, 입자 표면 근교뿐만 아니라 안쪽까지 Ti의 고용이 진행되기 때문에 입자 표면 근방의 Ti양이 부족해서 본 발명의 개질 효과가 얻어지기 어렵기 때문이다.In the heat treatment according to step (B), the heat treatment temperature is 400 to 1000°C, preferably 450 to 950°C. The reason for this is that when the heat treatment temperature is less than 400°C, sufficient decomposition and oxidation reaction of the titanium chelate for coating treatment are not performed, and sufficient effects cannot be obtained. This is because the solid solution reaction of the composite oxide particles proceeds excessively, and the solid solution of Ti proceeds not only in the vicinity of the particle surface but also in the depth, so that the amount of Ti in the vicinity of the particle surface is insufficient, making it difficult to obtain the modification effect of the present invention.
(B) 공정에 따른 가열 처리에 있어서, 가열 처리의 시간은, 본 제조 방법에 있어서 임계적이 아니라, 통상은 1시간 이상, 바람직하게는 2 내지 10시간으로, 만족스러운 성능의 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 얻을 수 있다.In the heat treatment according to step (B), the time of the heat treatment is not critical in the present production method, but is usually 1 hour or more, preferably 2 to 10 hours, and the modified lithium nickel manganese cobalt with satisfactory performance. Complex oxide particles can be obtained.
(B) 공정에 따른 가열 처리에 있어서, 가열 처리의 분위기는 공기, 산소 가스 등의 산화 분위기인 것이 바람직하다.In the heat treatment according to step (B), the atmosphere of the heat treatment is preferably an oxidizing atmosphere such as air or oxygen gas.
또한, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 있어서, 바람직한 실시 형태에서는, 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 티타늄킬레이트 화합물을 포함하는 표면 처리액에 접촉시킨 후, 그대로 용매를 전량 건조시킨다는 점에서, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)에서의 리튬 니켈 망간 코발트 복합 산화물 입자에 대한 Ti를 포함하는 산화물의 피복량(부착량) 및 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)에서의 리튬 니켈 망간 코발트 복합 산화물 입자에 대한 Ti의 고용량(함유량)은 리튬 니켈 망간 코발트 복합 산화물 입자의 양과 사용한 티타늄킬레이트 화합물을 포함하는 표면 처리액 중 Ti 함유량으로부터 구해지는 이론상의 피복량(부착량) 및 고용량(함유량)으로서 나타낼 수 있다.Further, in the method for producing the modified lithium nickel manganese cobalt composite oxide particles of the present invention, in a preferred embodiment, the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) are prepared in a surface treatment solution containing a titanium chelate compound. in that the entire amount of the solvent is dried as it is after contact with the lithium nickel manganese cobalt composite oxide particle (A), the coating amount (adhesion amount) of the oxide containing Ti on the lithium nickel manganese cobalt composite oxide particle and the modified lithium The high amount (content) of Ti relative to the lithium nickel manganese cobalt composite oxide particles in the nickel manganese cobalt composite oxide particles (B) was determined from the amount of the lithium nickel manganese cobalt composite oxide particles and the Ti content in the surface treatment solution containing the titanium chelate compound used. It can be expressed as a theoretical coating amount (adhesion amount) and a high amount (content amount) obtained.
개질 공정의 (A) 공정에서는, 후술하는 Ti를 포함하는 산화물의 부착량의 범위가 되도록, 상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당 Ti 함유량이, Ti 원자 환산으로 0.1 내지 150㎎, 바람직하게는 0.5 내지 120㎎이 되는 첨가량으로 상기 표면 개질액을, 상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자에 첨가하여 혼합하고, 전량 건조시키는 것이, 티타늄킬레이트 화합물의 피복량 및 고용량을 컨트롤하는 것이 용이해진다는 점에서, 바람직하다.In the step (A) of the modification step, the Ti content per 1 m 2 of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) is calculated in terms of Ti atoms so as to fall within the range of the amount of oxide containing Ti that is deposited, which will be described later. The above surface modification liquid is added in an amount of 0.1 to 150 mg, preferably 0.5 to 120 mg, to the lithium nickel manganese cobalt composite oxide particles represented by the above general formula (1), mixed, and dried. It is preferable in that it becomes easy to control the amount of coating and high amount of the chelate compound.
또한, 본 발명에 있어서 「리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당 Ti 원자 환산 Ti 함유량」은 하기의 계산식에 의해 구해지는 것이다.In the present invention, the "Ti content in terms of Ti atoms per 1 m 2 of lithium nickel manganese cobalt composite oxide particles" is obtained by the following formula.
k: 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당 Ti 원자 환산 Ti 함유량(㎎)k: Ti content (mg) in terms of Ti atoms per 1 m2 of lithium nickel manganese cobalt composite oxide particles
x: 리튬 니켈 망간 코발트 복합 산화물 1g에 대한 Ti 원자 환산 Ti 함유량(㎎)x: Ti content (mg) in terms of Ti atoms relative to 1 g of lithium nickel manganese cobalt composite oxide
t: 리튬 니켈 망간 코발트 복합 산화물 입자의 BET 비표면적(㎡/g)t: BET specific surface area of lithium nickel manganese cobalt composite oxide particles (m 2 / g)
본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 있어서, 얻어지는 개질 리튬 니켈 망간 코발트 복합 산화물 입자 중의 Ti를 포함하는 산화물의 부착량 및 Ti의 고용량(함유량)은 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당, Ti 원자 환산으로 0.1 내지 150㎎, 바람직하게는 0.5 내지 120㎎이다. 개질 리튬 니켈 망간 코발트 복합 산화물 입자 중의 Ti를 포함하는 산화물의 부착량 및 Ti의 고용량(함유량)이 상기 범위에 있음으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A) 및/또는 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)를 리튬 2차 전지의 정극 활물질로서 사용했을 때에, 사이클 특성이 한층 더 높아진다는 점에서 바람직하다. 즉, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물의 제조 방법에서는, 얻어지는 개질 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당, Ti 원자 환산으로 0.1 내지 150㎎, 바람직하게는 0.5 내지 120㎎이 되도록, (A) 공정에 있어서, 접촉시키는 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자의 양과, 표면 처리액 중 티타늄킬레이트 화합물의 농도 및 표면 처리액의 양을 조제하는 것이 바람직하다.In the method for producing the modified lithium nickel manganese cobalt composite oxide particles of the present invention, the amount of oxide deposited with Ti and the high amount (content) of Ti in the obtained modified lithium nickel manganese cobalt composite oxide particles are lithium nickel manganese cobalt composite oxide particles 1 It is 0.1 to 150 mg, preferably 0.5 to 120 mg in terms of Ti atom per m 2 . The amount of oxide attached to Ti and the high amount (content) of Ti in the modified lithium nickel manganese cobalt composite oxide particles are within the above ranges, so that the modified lithium nickel manganese cobalt composite oxide particles (A) and/or the modified lithium nickel manganese cobalt composite When the oxide particle (B) is used as a positive electrode active material of a lithium secondary battery, it is preferable in that the cycle characteristics are further improved. That is, in the method for producing the modified lithium nickel manganese cobalt composite oxide of the present invention, the amount of the obtained modified lithium nickel manganese cobalt composite oxide particle is 0.1 to 150 mg, preferably 0.5 to 120 mg in terms of Ti atoms per 1 m 2 ( In step A), it is preferable to prepare the amount of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) to be brought into contact, the concentration of the titanium chelate compound in the surface treatment solution, and the amount of the surface treatment solution.
또한, 본 발명에 있어서 「Ti를 포함하는 산화물의 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당 Ti 원자 환산의 부착량」은, 하기의 계산식에 의해 구해지는 것이다.In the present invention, the "attachment amount in terms of Ti atoms per 1 m 2 of the lithium nickel manganese cobalt composite oxide particles of the oxide containing Ti" is obtained by the following formula.
k': Ti를 포함하는 산화물의 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당 Ti 원자 환산의 부착량(㎎)k': Attachment amount (mg) in terms of Ti atoms per 1 m2 of lithium nickel manganese cobalt composite oxide particles of Ti-containing oxide
x: 리튬 니켈 망간 코발트 복합 산화물 1g에 대한 Ti 원자 환산 Ti 함유량(㎎)x: Ti content (mg) in terms of Ti atoms relative to 1 g of lithium nickel manganese cobalt composite oxide
t: 리튬 니켈 망간 코발트 복합 산화물 입자의 BET 비표면적(㎡/g)t: BET specific surface area of lithium nickel manganese cobalt composite oxide particles (m 2 / g)
또한, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 행하여 얻어지는 개질 리튬 니켈 망간 코발트 복합 산화물 입자 중의 잔존 알칼리양은 1.2질량% 이하, 바람직하게는 1.0질량% 이하인 것이, 잔존 알칼리에 기인하는 가스 발생에 의해 발생하는 전지의 팽창이나 열화를 억제할 수 있다는 점에서 바람직하다.Further, the amount of residual alkali in the modified lithium nickel manganese cobalt composite oxide particles obtained by performing the method for producing the modified lithium nickel manganese cobalt composite oxide particles of the present invention is 1.2% by mass or less, preferably 1.0% by mass or less, attributable to the residual alkali. It is preferable in that expansion or deterioration of the battery caused by gas generation can be suppressed.
본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 행하여 얻어지는 개질 리튬 니켈 망간 코발트 복합 산화물 입자는, 리튬 2차 전지의 정극 활물질로서 적합하게 사용되고 또한 해당 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 정극 활물질로서 사용한 리튬 2차 전지는, 개질 되어 있지 않은 Li, Ni, Mn 및 Co가 동 조성의 리튬 니켈 망간 코발트 복합 산화물 입자를 사용한 경우에 비하여, 사이클 특성이 높아진다.The modified lithium nickel manganese cobalt composite oxide particles obtained by performing the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention are suitably used as a positive electrode active material of a lithium secondary battery, and the modified lithium nickel manganese cobalt composite oxide particles are used as a positive electrode. A lithium secondary battery used as an active material has higher cycle characteristics than a case where lithium nickel manganese cobalt composite oxide particles having the same composition as unmodified Li, Ni, Mn, and Co are used.
또한, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 행하여 얻어지는 개질 리튬 니켈 망간 코발트 복합 산화물의 큰 입자와, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법을 행하여 얻어지는 개질 리튬 니켈 망간 코발트 복합 산화물의 작은 입자를 혼합함으로써, 체적당 용량을 향상시킬 수 있다. 이 경우, 큰 입자의 평균 입자경이 7.5 내지 30.0㎛, 바람직하게는 8.0 내지 25.0㎛이며, 작은 입자의 평균 입자경이 0.5 내지 7.5㎛, 바람직하게는 1.0 내지 7.0㎛인 것이, 체적당 용량을 향상시킨다는 관점에서 바람직하다. 또한, 혼합물을 0.65tonf/㎠로 압축 처리했을 때의 가압 밀도가 2.7g/㎤ 이상, 바람직하게는 2.8 내지 3.3g/㎤인 것이, 체적당 용량이 한층 더 높아진다는 점에서 바람직하다.Further, large particles of the modified lithium nickel manganese cobalt composite oxide obtained by performing the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention, and modified lithium obtained by performing the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention By mixing small particles of nickel manganese cobalt composite oxide, the capacity per volume can be improved. In this case, when the average particle diameter of the large particles is 7.5 to 30.0 μm, preferably 8.0 to 25.0 μm, and the average particle diameter of the small particles is 0.5 to 7.5 μm, preferably 1.0 to 7.0 μm, the capacity per volume is improved. desirable from the point of view In addition, the press density when the mixture is compressed at 0.65 tonf/cm 2 is 2.7 g/cm 3 or more, preferably 2.8 to 3.3 g/cm 3 , from the standpoint of further increasing the capacity per volume.
본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 있어서, 개질 리튬 니켈 망간 코발트 복합 산화물의 큰 입자는, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)가 바람직하고, 개질 리튬 니켈 망간 코발트 복합 산화물의 작은 입자는, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)인 것이, 사이클 특성이 한층 더 높아진다는 점에서 바람직하다.In the method for producing the modified lithium nickel manganese cobalt composite oxide particles of the present invention, the modified lithium nickel manganese cobalt composite oxide particles (A) are preferably the large particles of the modified lithium nickel manganese cobalt composite oxide, and the modified lithium nickel manganese cobalt composite oxide particles (A) are preferred. The small particles of the oxide are preferably modified lithium nickel manganese cobalt composite oxide particles (B) in terms of further improving cycle characteristics.
본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 있어서는, (A) 공정에서 티타늄킬레이트 화합물을 부착시키는 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경이 작은 쪽이, 부착된 티타늄킬레이트 화합물이나 그 가열 분해 생성물인 Ti를 포함하는 산화물이 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 균일하게 부피가 커지지 않아 고분산되기 쉽고, 고분산되어 부착된 티타늄킬레이트 화합물의 가열 분해 생성물인 Ti를 포함하는 산화물과 리튬 니켈 망간 코발트 복합 산화물 입자와의 반응성이 리튬 니켈 망간 코발트 복합 산화물 입자 표면상에서 높아진다. 그 때문에, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 있어서는, (A) 공정에서 티타늄킬레이트 화합물을 부착시키는 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경이 작은 쪽이, 부착된 티타늄킬레이트 화합물이나 그 가열 분해 생성물인 Ti를 포함하는 산화물이 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 균일하게 한층 더 고분산되기 쉽고, 고분산되어 부착된 티타늄킬레이트 화합물의 가열 분해 생성물인 Ti를 포함하는 산화물은, 리튬 니켈 망간 코발트 복합 산화물 입자와의 반응성이 리튬 니켈 망간 코발트 복합 산화물 입자 표면상에서 높아지므로, (B) 공정에서의 가열 처리 온도가 동일하여도, (A) 공정에서 티타늄킬레이트 화합물을 부착시키는 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경이 작은 쪽이, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)가 생성되기 쉬워진다. 또한, (B) 공정에서의 가열 처리 온도가 높은 쪽이, 부착된 티타늄킬레이트 화합물의 가열 분해 생성물인 Ti를 포함하는 산화물과 리튬 니켈 망간 코발트 복합 산화물 입자와의 반응성이 리튬 니켈 망간 코발트 복합 산화물 입자 표면상에서 높아지므로, (B) 공정에서의 가열 처리 온도가 높은 쪽이, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)가 생성되기 쉬워진다.In the method for producing the modified lithium nickel manganese cobalt composite oxide particles of the present invention, the smaller the average particle diameter of the lithium nickel manganese cobalt composite oxide particles to which the titanium chelate compound is deposited in step (A), the adhering titanium chelate compound or its The oxide containing Ti, which is a thermal decomposition product, does not uniformly increase in volume on the particle surface of the lithium nickel manganese cobalt composite oxide particles and is easily highly dispersed, and the oxide containing Ti, which is a thermal decomposition product of the titanium chelate compound adhered in a highly dispersed manner. The reactivity between the lithium nickel manganese cobalt composite oxide particles and the lithium nickel manganese cobalt composite oxide particles is increased on the surface of the lithium nickel manganese cobalt composite oxide particles. Therefore, in the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention, the smaller the average particle diameter of the lithium nickel manganese cobalt composite oxide particles to which the titanium chelate compound is deposited in step (A), the smaller the adhering titanium chelate. A compound or an oxide containing Ti, which is a thermal decomposition product thereof, is more easily dispersed uniformly and highly dispersed on the particle surface of lithium nickel manganese cobalt composite oxide particles, and Ti, which is a thermal decomposition product of a titanium chelate compound adhered in a highly dispersed manner, Since the oxide has a higher reactivity with the lithium nickel manganese cobalt composite oxide particles on the surface of the lithium nickel manganese cobalt composite oxide particles, the titanium chelate compound is attached in the step (A) even if the heat treatment temperature in the step (B) is the same. The smaller the average particle diameter of the lithium nickel manganese cobalt composite oxide particles, the easier the modified lithium nickel manganese cobalt composite oxide particles (B) are to be formed. In addition, the higher the heat treatment temperature in the step (B), the higher the reactivity between the lithium nickel manganese cobalt composite oxide particles and the Ti-containing oxide, which is a thermal decomposition product of the attached titanium chelate compound, the lithium nickel manganese cobalt composite oxide particles Since it is higher on the surface, the higher the heat treatment temperature in the step (B), the easier it is to generate the modified lithium nickel manganese cobalt composite oxide particles (B).
다시 말해, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에 있어서는, (A) 공정에서 티타늄킬레이트 화합물을 부착시키는 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경이 큰 쪽이, 부착된 티타늄킬레이트 화합물이나 그 가열 분해 생성물인 Ti를 포함하는 산화물이 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 불균일하게 부피가 커져 분산되기 쉽고, 부피가 커져 부착된 티타늄킬레이트 화합물의 가열 분해 생성물인 Ti를 포함하는 산화물은, 리튬 니켈 망간 코발트 복합 산화물 입자와의 반응성이 리튬 니켈 망간 코발트 복합 산화물 입자 표면상에서 낮아지므로, (B) 공정에서의 가열 처리 온도가 동일하여도, (A) 공정에서 티타늄킬레이트 화합물을 부착시키는 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경이 큰 쪽이, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)가 생성되기 쉬워진다. 또한, (B) 공정에서의 가열 처리 온도가 낮을수록, 부착된 티타늄킬레이트 화합물과 리튬 니켈 망간 코발트 복합 산화물 입자와의 반응성이 리튬 니켈 망간 코발트 복합 산화물 입자 표면상에서 낮아지므로, (B) 공정에서의 가열 처리 온도가 낮을수록, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)가 생성되기 쉬워진다.In other words, in the method for producing the modified lithium nickel manganese cobalt composite oxide particles of the present invention, the larger the average particle diameter of the lithium nickel manganese cobalt composite oxide particles to which the titanium chelate compound is deposited in step (A), the larger the titanium chelate adhering. A compound or an oxide containing Ti, which is a thermal decomposition product of the compound, is non-uniformly bulky and easily dispersed on the particle surface of the lithium nickel manganese cobalt composite oxide particles, and Ti, which is a thermal decomposition product of the titanium chelate compound attached to the particle surface, Since the oxide has a lower reactivity with the lithium nickel manganese cobalt composite oxide particles on the surface of the lithium nickel manganese cobalt composite oxide particles, the titanium chelate compound is attached in the step (A) even if the heat treatment temperature in the step (B) is the same. The larger the average particle diameter of the lithium nickel manganese cobalt composite oxide particles, the more easily the modified lithium nickel manganese cobalt composite oxide particles (A) are formed. In addition, as the heat treatment temperature in step (B) is lowered, the reactivity between the adhering titanium chelate compound and the lithium nickel manganese cobalt composite oxide particles is lowered on the surface of the lithium nickel manganese cobalt composite oxide particles, so in step (B) The lower the heat treatment temperature, the easier the formation of the modified lithium nickel manganese cobalt composite oxide particles (A).
그 때문에, 본 발명의 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법에서는, (A) 공정에서 사용하는 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자의 평균 입자경과 (B) 공정에서의 가열 처리 온도의 조합을, 적절히 선택함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)와 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)를 구분하여 제조할 수 있다.Therefore, in the method for producing modified lithium nickel manganese cobalt composite oxide particles of the present invention, the average particle diameter of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) used in step (A) in step (B) The modified lithium nickel manganese cobalt composite oxide particles (A) and the modified lithium nickel manganese cobalt composite oxide particles (B) can be produced separately by appropriately selecting a combination of heat treatment temperatures.
예를 들어, 본 발명의 바람직한 실시 형태에 있어서, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)는, (A) 공정에 있어서 일반식 (1)인 리튬 니켈 망간 코발트 복합 산화물 입자로서, 평균 입자경이 7.5 내지 30.0㎛, 바람직하게는 8.0 내지 25.0㎛의 입자를 사용하고, (B) 공정의 가열 처리 온도를 750℃ 이상 1000℃ 이하, 바람직하게는 750℃ 이상 900℃ 이하로 하여 상기 (A) 공정 및 (B) 공정을 행함으로써 제조할 수 있다.For example, in a preferred embodiment of the present invention, the modified lithium nickel manganese cobalt composite oxide particles (A) are lithium nickel manganese cobalt composite oxide particles of the general formula (1) in step (A), and have an average particle diameter Step (A) using particles of 7.5 to 30.0 μm, preferably 8.0 to 25.0 μm, and setting the heat treatment temperature in step (B) to 750° C. or more and 1000° C. or less, preferably 750° C. to 900° C. And (B) It can manufacture by performing a process.
또한, 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)는 (A) 공정에 있어서 일반식 (1)인 리튬 니켈 망간 코발트 복합 산화물 입자로서, 평균 입자경이 0.5 내지 7.5㎛, 바람직하게는 1.0 내지 7.0㎛의 입자를 사용하고, (B) 공정의 가열 처리 온도를 750℃ 이상 1000℃ 이하, 바람직하게는 750℃ 이상 900℃ 이하로 하여 상기 (A) 공정 및 (B) 공정을 행함으로써 제조할 수 있다.In addition, the modified lithium nickel manganese cobalt composite oxide particles (B) are lithium nickel manganese cobalt composite oxide particles of the general formula (1) in step (A), and have an average particle diameter of 0.5 to 7.5 μm, preferably 1.0 to 7.0 μm. It can be produced by performing the above steps (A) and (B) using particles of, and setting the heat treatment temperature in the step (B) to 750 ° C. or more and 1000 ° C. or less, preferably 750 ° C. or more to 900 ° C. or less. .
실시예Example
이하, 본 발명을 실시예에 의해 설명하지만, 본 발명은 이들로 한정되는 것은 아니다.Hereinafter, the present invention will be described by examples, but the present invention is not limited thereto.
<리튬 니켈 망간 코발트 복합 산화물 입자(LNMC) 시료의 조제><Preparation of Lithium Nickel Manganese Cobalt Composite Oxide Particles (LNMC) Sample>
<LNMC 시료 1><LNMC sample 1>
탄산리튬(평균 입자경 5.7㎛) 및 니켈 망간 코발트 복합 수산화물(Ni:Mn:Co=6:2:2(몰비), 평균 입자경 9.8㎛)을 칭량하고, 가정용 믹서로 충분히 혼합 처리하고, Li/(Ni+Mn+Co)의 몰비가 1.01인 원료 혼합물을 얻었다. 또한, 니켈 망간 코발트 복합 수산화물은 시판 중인 것을 사용하였다.Lithium carbonate (average particle diameter 5.7 μm) and nickel manganese cobalt composite hydroxide (Ni: Mn: Co = 6: 2: 2 (molar ratio), average particle diameter 9.8 μm) were weighed, thoroughly mixed with a household mixer, and Li / ( A raw material mixture having a molar ratio of Ni+Mn+Co) of 1.01 was obtained. In addition, a commercially available nickel-manganese-cobalt composite hydroxide was used.
이어서, 얻어진 원료 혼합물을, 알루미나제의 사발로 700℃에서 2시간, 계속하여 850℃에서 10시간, 대기 분위기 중에서 소성하였다. 소성 종료 후, 해당 소성품을 분쇄, 분급하였다. 얻어진 소성품을 XRD로 측정한 결과, 단상의 리튬 니켈 망간 코발트 복합 산화물임을 확인하였다. 또한, 얻어진 것은, 평균 입자경이 10.2㎛이고, BET 비표면적이 0.21㎡/g이며, 2차 응집한 구상의 리튬 니켈 망간 코발트 복합 산화물 입자(LiNi0.6Mn0.2Co0.2O2)였다.Next, the obtained raw material mixture was fired in an air atmosphere at 700°C for 2 hours and then at 850°C for 10 hours in an alumina bowl. After completion of firing, the fired product was pulverized and classified. As a result of measuring the obtained fired product by XRD, it was confirmed that it was a single-phase lithium nickel manganese cobalt composite oxide. What was obtained was secondary agglomerated spherical lithium nickel manganese cobalt composite oxide particles (LiNi 0.6 Mn 0.2 Co 0.2 O 2 ) with an average particle diameter of 10.2 μm and a BET specific surface area of 0.21 m 2 /g.
<LNMC 시료 2><LNMC sample 2>
탄산리튬(평균 입자경 5.7㎛) 및 니켈 망간 코발트 복합 수산화물(Ni:Mn:Co=6:2:2(몰비), 평균 입자경 3.7㎛)을 칭량하고, 가정용 믹서로 충분히 혼합 처리하여, Li/(Ni+Mn+Co)의 몰비가 1.01인 원료 혼합물을 얻었다. 또한, 니켈 망간 코발트 복합 수산화물은 시판 중인 것을 사용하였다.Lithium carbonate (average particle diameter 5.7 μm) and nickel manganese cobalt composite hydroxide (Ni: Mn: Co = 6: 2: 2 (molar ratio), average particle diameter 3.7 μm) were weighed and sufficiently mixed with a household mixer to obtain Li / ( A raw material mixture having a molar ratio of Ni+Mn+Co) of 1.01 was obtained. In addition, a commercially available nickel-manganese-cobalt composite hydroxide was used.
이어서, 얻어진 원료 혼합물을, 알루미나제의 사발로 700℃에서 2시간, 계속하여 850℃에서 10시간, 대기 분위기 중에서 소성하였다. 소성 종료 후, 해당 소성품을 분쇄, 분급하였다. 얻어진 소성품을 XRD로 측정한 결과, 단상의 리튬 니켈 망간 코발트 복합 산화물임을 확인하였다. 또한, 얻어진 것은, 평균 입자경이 5.4㎛이고, BET 비표면적이 0.69㎡/g이며, 2차 응집한 구상의 리튬 니켈 망간 코발트 복합 산화물 입자(LiNi0.6Mn0.2Co0.2O2)였다.Next, the obtained raw material mixture was fired in an air atmosphere at 700°C for 2 hours and then at 850°C for 10 hours in an alumina bowl. After completion of firing, the fired product was pulverized and classified. As a result of measuring the obtained fired product by XRD, it was confirmed that it was a single-phase lithium nickel manganese cobalt composite oxide. What was obtained was secondary agglomerated spherical lithium nickel manganese cobalt composite oxide particles (LiNi 0.6 Mn 0.2 Co 0.2 O 2 ) with an average particle diameter of 5.4 μm and a BET specific surface area of 0.69 m 2 /g.
상기에서 얻어진 리튬 니켈 망간 코발트 복합 산화물 시료(LNMC 시료)의 제물성을 표 1에 나타낸다.Table 1 shows the physical properties of the lithium nickel manganese cobalt composite oxide sample (LNMC sample) obtained above.
또한, LNMC 시료의 평균 입자경, 잔존 알칼리양 및 가압 밀도는 하기와 같이 하여 측정하였다.In addition, the average particle diameter of the LNMC sample, the amount of residual alkali, and the pressed density were measured as follows.
<평균 입자경><Average Particle Size>
평균 입자경은 레이저 회절·산란법에 의해 구하였다.The average particle diameter was determined by a laser diffraction/scattering method.
<잔존 알칼리양의 측정><Measurement of Residual Alkali Amount>
LNMC 시료의 잔존 알칼리양에 대해서는, 시료 5g, 초순수 100g을 비이커로 측량하고 자기 교반 막대를 사용하여 25℃에서 5분간 분산시켰다. 이어서, 이 분산액을 여과하고, 그 여액 70ml를 자동 적정 장치(모델 COMTITE-2500)로 0.1N-HCl로 적정하고, 시료 중에 존재하고 있는 잔존 알칼리양(리튬양을 측정하여 탄산리튬으로 환산한 값)을 산출하였다.Regarding the amount of residual alkali in the LNMC sample, 5 g of the sample and 100 g of ultrapure water were weighed in a beaker and dispersed at 25° C. for 5 minutes using a magnetic stirring bar. Next, this dispersion liquid was filtered, and 70 ml of the filtrate was titrated with 0.1 N-HCl with an automatic titrator (model COMTITE-2500), and the amount of remaining alkali present in the sample (value obtained by measuring the amount of lithium and converting it to lithium carbonate) ) was calculated.
<가압 밀도><Pressed Density>
시료 2.25g을 칭량 직경 1.5㎝의 양축 성형기 내에 투입하고, 프레스기를 사용하여 0.65tonf/㎠의 압력을 1분간 가한 상태에서, 압축물의 높이를 측정하고, 그 높이로부터 계산되는 압축물의 겉보기 체적으로 측량한 시료의 질량으로부터, 시료의 가압 밀도를 산출하였다.2.25 g of the sample was put into a twin-shaft molding machine with a weighing diameter of 1.5 cm, and the height of the compressed material was measured in a state where a pressure of 0.65 tonf / cm 2 was applied for 1 minute using a press machine, and the apparent volume of the compressed material calculated from the height was measured. From the mass of one sample, the pressed density of the sample was calculated.
<표면 처리액의 조제><Preparation of surface treatment solution>
<락트산티타늄킬레이트 함유 표면 처리액의 조제><Preparation of Surface Treatment Liquid Containing Titanium Lactate Chelate>
마츠모토파인케미컬사제 티타늄락테이트암모늄염(Ti(OH)2〔(OCH(CH3)COO-)2(NH4 +)2) 수용액(제품명 TC-335, pH 4.4)에 암모니아수를 첨가하여 pH를 8.5가 되도록 조정하여, 하기의 표 2에 나타내는 농도의 락트산티타늄킬레이트 함유 표면 처리액을 제조하였다.Ammonia water was added to an aqueous solution of titanium lactate ammonium salt (Ti(OH) 2 [(OCH(CH 3 )COO - ) 2 (NH 4 + ) 2 ) manufactured by Matsumoto Fine Chemical Co., Ltd. (product name: TC-335, pH 4.4) to adjust the pH to 8.5. was adjusted so as to prepare a titanium lactate chelate-containing surface treatment solution having a concentration shown in Table 2 below.
(실시예 1 내지 6)(Examples 1 to 6)
LNMC 시료 및 표면 처리액을 사용하고, 표 3에 나타내는 비율이 되도록 칭량하여, 고형분 농도가 25질량%의 슬러리가 되도록 조제하였다.Using the LNMC sample and surface treatment liquid, it was weighed so as to have the ratio shown in Table 3, and it was prepared so that it might become a slurry with a solid content concentration of 25 mass %.
이어서, 출구의 온도를 120℃로 설정한 스프레이 드라이어에 슬러리의 공급 속도가 65g/분으로 공급하고, 락트산티타늄킬레이트가 LNMC 시료의 입자 표면에 부착된 피복 입자를 얻었다.Subsequently, the slurry was supplied at a feed rate of 65 g/min to a spray dryer with an outlet temperature set at 120° C. to obtain coated particles in which titanium lactate chelate adhered to the particle surfaces of the LNMC sample.
이어서, 피복 입자를 800℃에서 5시간, 가열 처리를 행하여 LNMC 시료의 입자 표면에 Ti의 산화물이 부착된 개질 LNMC 시료(A) 및 LNMC 시료에 Ti를 고용시켜서 함유시킨 개질 LNMC 시료 (B)를 얻었다.Subsequently, the coated particles were subjected to heat treatment at 800°C for 5 hours to obtain a modified LNMC sample (A) in which oxides of Ti adhered to the surface of the particles of the LNMC sample and a modified LNMC sample (B) in which Ti was dissolved and contained in the LNMC sample. got it
또한, Ti의 산화물이 부착된 개질 LNMC 시료 및 LNMC 시료에 Ti를 고용시켜서 함유시킨 개질 LNMC 시료인지는, 20,000배의 확대 배율로 샘플 입자의 입자 표면을 SEM-EDX(히타치하이테크놀러지즈사제 전계 방출형 주사 전자 현미경 SU-8220 및 BRUKER사제 에너지 분산형 X선 분석 장치 XFlash5060FlatQUAD)로 Ti의 원소 매핑 분석을 행하여 확인하였다. LNMC 시료로서 LNMC 시료 1을 사용한 것은 SEM-EDX에 의해, 샘플 입자의 입자 표면을 Ti의 원소 매핑 분석한 결과, Ti가 편재되어 불균일하게 분포되어 있는 것이라는 점에서 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (A)임이 확인되었다. 한편, LNMC 시료로서 LNMC 시료 2를 사용한 것은 SEM-EDX에 의해, 샘플 입자의 입자 표면을 Ti의 원소 매핑 분석한 결과, Co, Ni 및 Mn과 마찬가지로 Ti가 균일하게 분포되어 있는 것이라는 점에서 개질 리튬 니켈 망간 코발트 복합 산화물 입자 (B)임이 확인되었다.In addition, to determine whether the modified LNMC sample to which oxides of Ti are adhered or the modified LNMC sample in which Ti is dissolved and contained in the LNMC sample, the particle surfaces of the sample particles are examined by SEM-EDX (field emission manufactured by Hitachi High-Technologies Co., Ltd.) at a magnification of 20,000 times. It was confirmed by performing elemental mapping analysis of Ti using a scanning electron microscope SU-8220 and an energy dispersive X-ray analyzer XFlash5060FlatQUAD manufactured by BRUKER. The use of LNMC sample 1 as the LNMC sample is a modified lithium nickel manganese cobalt composite oxide particle ( A) has been confirmed. On the other hand, when LNMC sample 2 was used as the LNMC sample, as a result of elemental mapping analysis of Ti on the particle surface of the sample particle by SEM-EDX, Ti was uniformly distributed in the same way as Co, Ni, and Mn. It was confirmed that it was the nickel-manganese-cobalt composite oxide particle (B).
또한, SEM-EDX의 측정 조건은 하기와 같다.In addition, the measurement conditions of SEM-EDX are as follows.
가속 전압: 15㎸, 확대 배율: 20,000배, 워킹 디스턴스: 9.5 내지 11.5㎜, 측정시간: 6분간Acceleration voltage: 15 kV, magnification: 20,000 times, walking distance: 9.5 to 11.5 mm, measurement time: 6 minutes
또한, 개질 LNMC 시료에 대해서도, LNMC 시료와 마찬가지의 방법으로, 잔존 알칼리양을 측정하였다.In addition, the amount of residual alkali was also measured for the modified LNMC sample in the same manner as for the LNMC sample.
또한, 표 3 중의 표면 처리액의 첨가량은, 해당 표면 처리액을 첨가했을 때에, LNMC 시료 1㎡당 Ti 원자 환산 Ti 함유량이 되는 계산값이며, 하기 계산식에 의해 구하였다.In addition, the addition amount of the surface treatment liquid in Table 3 is a calculated value that becomes the Ti content in terms of Ti atoms per 1 m 2 of the LNMC sample when the surface treatment liquid is added, and was obtained by the following formula.
k: LNMC 시료 1㎡당 Ti 원자 환산 Ti 함유량(㎎)k: Ti content (mg) in terms of Ti atoms per 1 m2 of LNMC sample
x: LNMC 시료 1g에 대한 Ti 원자 환산 Ti 함유량(㎎)x: Ti content in terms of Ti atom with respect to 1 g of LNMC sample (mg)
t: LNMC 시료의 BET 비표면적(㎡/g)t: BET specific surface area of LNMC sample (m2/g)
(참고예 1)(Reference Example 1)
시판 중인 코발트산 리튬(LiCoO2: 평균 입자경 9.5㎛, BET 비표면적 0.37㎡/g)을 사용하고, 실시예 1 내지 3과 마찬가지로 하여, 코발트산 리튬(LCO) 시료의 입자 표면에 Ti의 산화물이 부착된 개질 LCO 시료를 얻었다.Commercially available lithium cobalt oxide (LiCoO 2 : average particle diameter: 9.5 μm, BET specific surface area: 0.37 m/g) was used, and in the same manner as in Examples 1 to 3, oxides of Ti were formed on the particle surfaces of lithium cobalt oxide (LCO) samples. An attached modified LCO sample was obtained.
또한, 개질 LCO에 대해서도, LNMC 시료와 마찬가지의 방법으로, 잔존 알칼리양을 측정하였다.In addition, for the modified LCO, the amount of residual alkali was measured in the same manner as for the LNMC sample.
또한, 표 3 중의 표면 처리액의 첨가량은, 해당 표면 처리액을 첨가했을 때에, LCO 시료 1㎡당 Ti 원자 환산 Ti 함유량이 되는 계산값이며, 하기 계산식에 의해 구하였다.In addition, the addition amount of the surface treatment liquid in Table 3 is a calculated value that becomes the Ti content in terms of Ti atoms per 1 m 2 of the LCO sample when the surface treatment liquid is added, and was obtained by the following formula.
k": LCO 시료 1㎡당 Ti 원자 환산 Ti 함유량(㎎)k": Ti content (mg) in terms of Ti atoms per 1 m2 of LCO sample
x": LCO 시료 1g에 대한 Ti 원자 환산 Ti 함유량(㎎)x": Ti content (mg) in terms of Ti atom with respect to 1 g of LCO sample
t": LCO 시료의 BET 비표면적(㎡/g)t": BET specific surface area of LCO sample (m 2 / g)
이하와 같이 하여, 전지 성능 시험을 행하였다.A battery performance test was conducted as follows.
<리튬 2차 전지의 제작 1><Production of Lithium Secondary Battery 1>
실시예에서 얻어진 개질 LNMC 시료 95질량%, 흑연 분말 2.5질량%, 폴리불화비닐리덴 2.5질량%를 혼합하여 정극제로 하고, 이것을 N-메틸-2-피롤리디논으로 분산시켜서 혼련 페이스트를 조제하였다. 해당 혼련 페이스트를 알루미늄박에 도포한 후 건조, 프레스하여 직경 15㎜의 원반에 펀칭하여 정극판을 얻었다.95% by mass of the modified LNMC samples obtained in Examples, 2.5% by mass of graphite powder, and 2.5% by mass of polyvinylidene fluoride were mixed to make a positive electrode agent, which was dispersed in N-methyl-2-pyrrolidinone to prepare a kneaded paste. The kneaded paste was applied to an aluminum foil, dried and pressed, and then punched into a disc having a diameter of 15 mm to obtain a positive electrode plate.
이 정극판을 사용하여, 세퍼레이터, 부극, 정극, 집전판, 설치 금속 부재, 외부 단자, 전해액 등의 각 부재를 사용하여 코인형 리튬 2차 전지를 제작하였다. 이 중, 부극은 금속 리튬박을 사용하고, 전해액에는 에틸렌카르보네이트와 메틸에틸카르보네이트의 1:1 혼합액 1리터에 LiPF6 1몰을 용해한 것을 사용하였다.Using this positive electrode plate, a coin-type lithium secondary battery was produced using each member such as a separator, negative electrode, positive electrode, current collector plate, mounting metal member, external terminal, and electrolyte solution. Among them, a metallic lithium foil was used as the negative electrode, and as the electrolyte, one obtained by dissolving 1 mole of LiPF 6 in 1 liter of a 1:1 mixture of ethylene carbonate and methyl ethyl carbonate was used.
이어서, 얻어진 리튬 2차 전지의 성능 평가를 행하였다. 그 결과를, 표 4에 나타낸다. 또한, 참고예 1에서 조제한 개질 LCO 시료, 개질을 행하지 않는 LNMC 시료 1(비교예 1) 및 LNMC 시료 2(비교예 2)에 대해서도 마찬가지의 방법으로 리튬 2차 전지를 작성하고, 마찬가지의 평가를 행하였다. 그 결과를, 표 4에 병기하였다.Subsequently, performance evaluation of the obtained lithium secondary battery was conducted. The results are shown in Table 4. In addition, lithium secondary batteries were prepared in the same manner for the modified LCO sample prepared in Reference Example 1, LNMC sample 1 (Comparative Example 1) and LNMC sample 2 (Comparative Example 2) without modification, and the same evaluation was performed. did The results are listed together in Table 4.
<전지의 성능 평가 1><Battery performance evaluation 1>
제작한 코인형 리튬 2차 전지를 실온에서 하기 시험 조건으로 작동시켜서, 하기의 전지 성능을 평가하였다.The produced coin-type lithium secondary battery was operated at room temperature under the following test conditions, and the following battery performance was evaluated.
(1) 사이클 특성 평가의 시험 조건(1) Test conditions for evaluation of cycle characteristics
우선, 0.5C에서 4.3V까지 2시간에 걸쳐 충전을 행하고, 또한 4.3V로 3시간 전압을 유지시키는 정전류·정전압 충전(CCCV 충전)을 행하였다. 그 후, 0.2C에서 2.7V까지 정전류 방전(CC 방전)시키는 충방전을 행하고, 이들 조작을 1사이클로 하여 20사이클 반복하였다.First, charging was performed from 0.5 C to 4.3 V over 2 hours, and constant current/constant voltage charging (CCCV charging) was performed in which the voltage was maintained at 4.3 V for 3 hours. Thereafter, charge/discharge was performed by constant current discharge (CC discharge) at 0.2 C to 2.7 V, and these operations were repeated 20 cycles as one cycle.
(2) 첫회 충전 용량, 첫회 방전 용량(활물질 중량당)(2) Initial charge capacity, initial discharge capacity (per weight of active material)
사이클 특성 평가에 있어서의 1사이클째의 충전 용량 및 방전 용량을 첫회 충전 용량, 첫회 방전 용량으로 하였다.The first cycle charge capacity and discharge capacity in the evaluation of cycle characteristics were defined as the first charge capacity and the first discharge capacity.
(3) 20사이클째 방전 용량(활물질 중량당)(3) Discharge capacity at 20th cycle (per weight of active material)
사이클 특성 평가에 있어서의 20사이클째의 방전 용량을 20사이클째 방전 용량으로 하였다.The discharge capacity at the 20th cycle in the evaluation of cycle characteristics was taken as the discharge capacity at the 20th cycle.
(4) 용량 유지율(4) Capacity retention rate
사이클 특성 평가에 있어서의 1사이클째와 20사이클째의 각각의 방전 용량(활물질 중량당)으로부터, 하기 식에 의해 용량 유지율을 산출하였다.From each discharge capacity (per active material weight) of the 1st cycle and the 20th cycle in evaluation of cycle characteristics, the capacity retention rate was calculated by the following formula.
용량 유지율(%)=(20사이클째의 방전 용량/1사이클째의 방전 용량)×100Capacity retention rate (%) = (discharge capacity at the 20th cycle/discharge capacity at the 1st cycle) x 100
(5) 에너지 밀도 유지율(5) Energy density retention rate
사이클 특성 평가에 있어서의 1사이클째와 20사이클째의 각각의 방전 시의 Wh 용량(활물질 중량당)으로부터, 하기 식에 의해 에너지 밀도 유지율을 산출하였다.The energy density retention rate was calculated from the Wh capacity (per weight of active material) at each discharge of the 1st cycle and the 20th cycle in the evaluation of cycle characteristics by the following formula.
에너지 밀도 유지율(%)=(20사이클째의 방전 Wh 용량/1사이클째의 방전 Wh 용량)×100Energy density retention rate (%) = (discharge Wh capacity at the 20th cycle/discharge Wh capacity at the 1st cycle) x 100
<리튬 2차 전지의 제작 2><Production of lithium secondary battery 2>
실시예 1 내지 6에서 얻어진 개질 LNMC 시료 및 개질 전의 LNMC 시료를 사용하여, 가정용 믹서로 충분히 혼합하여 표 5에 나타내는 조성의 혼합물을 조제하고, 정극 활물질 시료로 하였다. 또한, 상기 LNMC 시료와 마찬가지로 하여 정극 활물질 시료의 가압 밀도를 측정하고, 그 결과를 표 5에 병기하였다.Using the modified LNMC samples obtained in Examples 1 to 6 and the LNMC samples before modification, they were thoroughly mixed with a household mixer to prepare a mixture having the composition shown in Table 5, and used as a positive electrode active material sample. In addition, the pressed density of the positive electrode active material sample was measured in the same manner as in the above LNMC sample, and the results are shown in Table 5 together.
정극 활물질 시료 95질량%, 흑연 분말 2.5질량%, 폴리불화비닐리덴 2.5질량%를 혼합하여 정극제로 하고, 이것을 N-메틸-2-피롤리디논에 분산시켜서 혼련 페이스트를 조제하였다. 해당 혼련 페이스트를 알루미늄박에 도포한 후 건조, 프레스하여 직경 15㎜의 원반에 펀칭하여 정극판을 얻었다.95% by mass of the positive electrode active material sample, 2.5% by mass of graphite powder, and 2.5% by mass of polyvinylidene fluoride were mixed to make a positive electrode agent, which was dispersed in N-methyl-2-pyrrolidinone to prepare a kneaded paste. The kneaded paste was applied to an aluminum foil, dried and pressed, and then punched into a disc having a diameter of 15 mm to obtain a positive electrode plate.
이 정극판을 사용하여, 세퍼레이터, 부극, 정극, 집전판, 설치 금속 부재, 외부 단자, 전해액 등의 각 부재를 사용하여 코인형 리튬 2차 전지를 제작하였다. 이 중, 부극은 금속 리튬박을 사용하고, 전해액에는 에틸렌카르보네이트와 메틸에틸카르보네이트의 1:1 혼합액 1리터에 LiPF6 1몰을 용해한 것을 사용하였다.Using this positive electrode plate, a coin-type lithium secondary battery was produced using each member such as a separator, negative electrode, positive electrode, current collector plate, mounting metal member, external terminal, and electrolyte solution. Among them, a metallic lithium foil was used as the negative electrode, and as the electrolyte, one obtained by dissolving 1 mole of LiPF 6 in 1 liter of a 1:1 mixture of ethylene carbonate and methyl ethyl carbonate was used.
이어서, 얻어진 리튬 2차 전지의 성능 평가를 행하였다. 그 결과를, 표 6에 병기하였다.Subsequently, performance evaluation of the obtained lithium secondary battery was conducted. The results are listed together in Table 6.
<전지의 성능 평가 2><Battery performance evaluation 2>
제작한 코인형 리튬 2차 전지를 실온에서 하기 시험 조건으로 작동시켜서, 사이클 특성 평가, 첫회 충전 용량, 첫회 방전 용량(활물질 중량당), 첫회 충전 용량, 첫회 방전 용량(활물질 중량당), 용량 유지율, 에너지 밀도 유지율을 상기 전지의 성능 평가 1과 마찬가지의 방법으로 평가하였다. 또한, 또한 체적당 방전 용량도 평가하고, 그 결과를 표 6에 나타낸다. 또한, 실시예 2, 실시예 5의 개질 LNMC 시료를 정극 활물질 시료로 하고, 마찬가지의 방법으로 평가를 행하였다. 그 결과를, 표 6에 병기하였다.The fabricated coin-type lithium secondary battery was operated at room temperature under the following test conditions, cycle characteristics evaluation, initial charge capacity, initial discharge capacity (per weight of active material), initial charge capacity, initial discharge capacity (per weight of active material), capacity retention rate , energy density retention was evaluated in the same manner as in Performance Evaluation 1 of the battery. Further, the discharge capacity per volume was also evaluated, and the results are shown in Table 6. In addition, the modified LNMC samples of Examples 2 and 5 were used as positive electrode active material samples and evaluated in the same manner. The results are listed together in Table 6.
(6) 체적당 방전 용량(6) Discharge capacity per volume
체적당 방전 용량은, 초기 방전 용량과, 전극 밀도에 의해 하기 계산식으로 구하였다.The discharge capacity per volume was determined by the following formula based on the initial discharge capacity and the electrode density.
체적당 방전 용량(mAh/㎤)=1사이클째의 방전 용량(mAh/g)×전극 밀도(g/㎤)×0.95(정극재 중의 활물질량의 비율)Discharge capacity per volume (mAh/cm3) = discharge capacity at the first cycle (mAh/g) x electrode density (g/cm3) x 0.95 (ratio of active material amount in positive electrode material)
또한, 전극 밀도는, 측정 대상 시료로 제작한 전극의 질량과 두께를 측정하고, 여기에서, 집전체의 두께와 질량을 차감하여, 정극재의 밀도로서 산출하였다. 또한, 정극재는, 정극 활물질 시료 95질량%, 흑연 분말 2.5질량%, 폴리불화비닐리덴 2.5질량%의 혼합물이며, 전극 제작 시의 프레스압은 선압이고 0.38ton/㎝로 하였다.In addition, the electrode density was calculated as the density of the positive electrode material by measuring the mass and thickness of the electrode fabricated from the sample to be measured, subtracting the thickness and mass of the current collector from this. In addition, the positive electrode material was a mixture of 95% by mass of the positive electrode active material sample, 2.5% by mass of graphite powder, and 2.5% by mass of polyvinylidene fluoride.
Claims (10)
(식 중, M은, Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na 및 K로부터 선택되는 1종 또는 2종 이상의 금속 원소를 나타낸다. x는 0.98≤x≤1.20, y는 0.30≤y<1.00, z는 0<z≤0.50, t는 0<t≤0.50, p는 0≤p≤0.05를 나타내고, y+z+t+p=1.00임)
로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자를, 티타늄킬레이트 화합물을 포함하는 표면 처리액에 접촉시켜서, 해당 리튬 니켈 망간 코발트 복합 산화물 입자의 입자 표면에 티타늄킬레이트 화합물이 부착된 피복 입자를 얻고, 이어서 해당 피복 입자를 가열 처리함으로써, 개질 리튬 니켈 망간 코발트 복합 산화물 입자를 얻는 개질 공정을 갖고,
상기 티타늄킬레이트 화합물이, 하기 일반식 (2):
(식 중, R1은, 알콕시기, 수산기, 할로겐 원자, 아미노기 또는 포스핀류를 나타내고, 복수 존재하는 경우, 동일해도 되며 달라도 된다. L은 히드록시카르복실산에서 유래되는 기를 나타내고, 복수 존재하는 경우, 동일해도 되며 달라도 된다. m은 0 이상 3 이하의 수를 나타내고, n은 1 이상 3 이하의 수를 나타내며, m+n은 3 내지 6임)
로 표시되는 티타늄킬레이트 또는 그의 암모늄염인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.The following general formula (1):
(Wherein, M is selected from Mg, Al, Ti, Zr, Cu, Fe, Sr, Ca, V, Mo, Bi, Nb, Si, Zn, Ga, Ge, Sn, Ba, W, Na and K Represents one or more metal elements that are x is 0.98≤x≤1.20, y is 0.30≤y<1.00, z is 0<z≤0.50, t is 0<t≤0.50, p is 0≤p≤ represents 0.05, and y+z+t+p=1.00)
The lithium nickel manganese cobalt composite oxide particles represented by are brought into contact with a surface treatment solution containing a titanium chelate compound to obtain coated particles in which the titanium chelate compound adheres to the particle surfaces of the lithium nickel manganese cobalt composite oxide particles. a modification step of obtaining modified lithium nickel manganese cobalt composite oxide particles by heating the coated particles;
The titanium chelate compound has the following general formula (2):
(In the formula, R 1 represents an alkoxy group, a hydroxyl group, a halogen atom, an amino group or a phosphine, and when present in a plurality thereof, may be the same or different. L represents a group derived from hydroxycarboxylic acid, and a plurality of In this case, it may be the same or different. m represents a number of 0 or more and 3 or less, n represents a number of 1 or more and 3 or less, and m+n is 3 to 6)
Method for producing a modified lithium nickel manganese cobalt composite oxide particle, characterized in that the titanium chelate represented by or its ammonium salt.
상기 가열 처리의 온도가 400 내지 1000℃인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to claim 1,
A method for producing modified lithium nickel manganese cobalt composite oxide particles, characterized in that the temperature of the heat treatment is 400 to 1000 ° C.
상기 일반식 (2) 중의 L이 1가의 카르복실산인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to claim 1 or 2,
A method for producing modified lithium nickel manganese cobalt composite oxide particles, characterized in that L in the general formula (2) is a monovalent carboxylic acid.
상기 일반식 (2) 중의 L이 락트산인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to claim 1 or 2,
A method for producing modified lithium nickel manganese cobalt composite oxide particles, wherein L in the general formula (2) is lactic acid.
상기 표면 처리액의 pH가 7 이상인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to any one of claims 1 to 4,
Method for producing modified lithium nickel manganese cobalt composite oxide particles, characterized in that the pH of the surface treatment liquid is 7 or more.
상기 피복 입자에 있어서의 상기 티타늄킬레이트 화합물의 부착량이, 상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당, Ti 원자 환산으로 0.1 내지 150㎎인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to any one of claims 1 to 5,
The amount of the titanium chelate compound attached to the coated particles is 0.1 to 150 mg in terms of Ti atoms per 1 m of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1), Method for producing manganese-cobalt composite oxide particles.
상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자 중의 잔존 알칼리양이 1.2질량% 이하인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to any one of claims 1 to 6,
A method for producing modified lithium nickel manganese cobalt composite oxide particles, characterized in that the amount of residual alkali in the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) is 1.2% by mass or less.
상기 개질 리튬 니켈 망간 코발트 복합 산화물 입자 중의 잔존 알칼리양이 1.2질량% 이하인 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to any one of claims 1 to 7,
A method for producing modified lithium nickel manganese cobalt composite oxide particles, wherein the amount of residual alkali in the modified lithium nickel manganese cobalt composite oxide particles is 1.2% by mass or less.
상기 개질 공정에 있어서,
상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자 1㎡당 Ti 함유량이, Ti 원자 환산으로 0.1 내지 150㎎이 되는 첨가량이고, 상기 표면 개질액을, 상기 일반식 (1)로 표시되는 리튬 니켈 망간 코발트 복합 산화물 입자에 첨가하여 혼합하고, 전량 건조시키는 것을 특징으로 하는 개질 리튬 니켈 망간 코발트 복합 산화물 입자의 제조 방법.According to any one of claims 1 to 8,
In the reforming process,
The Ti content per 1 m 2 of the lithium nickel manganese cobalt composite oxide particles represented by the general formula (1) is an addition amount of 0.1 to 150 mg in terms of Ti atoms, and the surface modification liquid is represented by the general formula (1) A method for producing modified lithium nickel manganese cobalt composite oxide particles, characterized in that the particles are added to the lithium nickel manganese cobalt composite oxide particles, mixed, and dried.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2020-185031 | 2020-11-05 | ||
| JP2020185031 | 2020-11-05 | ||
| JP2021177454A JP7252298B2 (en) | 2020-11-05 | 2021-10-29 | Method for producing modified lithium-nickel-manganese-cobalt composite oxide particles |
| JPJP-P-2021-177454 | 2021-10-29 | ||
| PCT/JP2021/040449 WO2022097653A1 (en) | 2020-11-05 | 2021-11-02 | Method of producing modified lithium nickel manganese cobalt composite oxide particles |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20230097043A true KR20230097043A (en) | 2023-06-30 |
Family
ID=81457013
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237014914A Pending KR20230097043A (en) | 2020-11-05 | 2021-11-02 | Method for producing modified lithium nickel manganese cobalt composite oxide particles |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR20230097043A (en) |
| WO (1) | WO2022097653A1 (en) |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004092073A1 (en) | 2003-04-17 | 2004-10-28 | Seimi Chemical Co. Ltd. | Lithium-nickel-cobalt-manganese containing composite oxide, material for positive electrode active material for lithium secondary battery, and methods for producing these |
| JP2005025975A (en) | 2003-06-30 | 2005-01-27 | Mitsubishi Chemicals Corp | Lithium nickel manganese cobalt based composite oxide for lithium secondary battery positive electrode material, positive electrode for lithium secondary battery using the same, and lithium secondary battery |
| JP2011023120A (en) | 2009-07-13 | 2011-02-03 | Nippon Chem Ind Co Ltd | Positive active material for lithium secondary battery, method of manufacturing the same, and lithium secondary battery |
| JP2016024968A (en) | 2014-07-22 | 2016-02-08 | 住友金属鉱山株式会社 | Cathode active material for non-aqueous electrolyte secondary battery and method for producing the same |
| JP2016072071A (en) | 2014-09-30 | 2016-05-09 | 住友金属鉱山株式会社 | Cathode active material for non-aqueous electrolyte secondary battery, dispersion used for production thereof, and production method thereof |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FI20060951L (en) * | 2004-04-30 | 2006-10-27 | Seimi Chem Kk | A method of preparing a lithium-containing composite oxide for a positive electrode for a lithium battery |
| WO2008013208A1 (en) * | 2006-07-26 | 2008-01-31 | Agc Seimi Chemical Co., Ltd. | Positive electrode active material for nonaqueous electrolyte secondary battery and method for producing the same |
| JP5193189B2 (en) * | 2007-11-01 | 2013-05-08 | Agcセイミケミカル株式会社 | Method for producing positive electrode active material for lithium ion secondary battery |
| JP5584456B2 (en) * | 2009-12-10 | 2014-09-03 | 日本化学工業株式会社 | Positive electrode active material for lithium secondary battery, method for producing the same, and lithium secondary battery |
| JP2014075177A (en) * | 2011-01-27 | 2014-04-24 | Asahi Glass Co Ltd | Positive electrode active material for lithium ion secondary battery and method for manufacturing the same |
| KR102101006B1 (en) * | 2015-12-10 | 2020-04-14 | 주식회사 엘지화학 | Positive electrode for secondary battery and secondary battery comprising the same |
-
2021
- 2021-11-02 KR KR1020237014914A patent/KR20230097043A/en active Pending
- 2021-11-02 WO PCT/JP2021/040449 patent/WO2022097653A1/en not_active Ceased
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004092073A1 (en) | 2003-04-17 | 2004-10-28 | Seimi Chemical Co. Ltd. | Lithium-nickel-cobalt-manganese containing composite oxide, material for positive electrode active material for lithium secondary battery, and methods for producing these |
| JP2005025975A (en) | 2003-06-30 | 2005-01-27 | Mitsubishi Chemicals Corp | Lithium nickel manganese cobalt based composite oxide for lithium secondary battery positive electrode material, positive electrode for lithium secondary battery using the same, and lithium secondary battery |
| JP2011023120A (en) | 2009-07-13 | 2011-02-03 | Nippon Chem Ind Co Ltd | Positive active material for lithium secondary battery, method of manufacturing the same, and lithium secondary battery |
| JP2016024968A (en) | 2014-07-22 | 2016-02-08 | 住友金属鉱山株式会社 | Cathode active material for non-aqueous electrolyte secondary battery and method for producing the same |
| JP2016072071A (en) | 2014-09-30 | 2016-05-09 | 住友金属鉱山株式会社 | Cathode active material for non-aqueous electrolyte secondary battery, dispersion used for production thereof, and production method thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2022097653A1 (en) | 2022-05-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110416525B (en) | Composite material containing lithium manganese iron phosphate with core-shell structure and preparation method thereof | |
| JP4475941B2 (en) | Method for producing lithium manganese nickel composite oxide | |
| TWI583623B (en) | Metal phosphate and method of manufacturing the same | |
| TWI576312B (en) | Manganese-bearing metal phosphates and process for the production thereof | |
| EP0806397A1 (en) | Lithium-nickel composite oxide, process for preparing the same, and positive active material for secondary battery | |
| JP6544579B2 (en) | Method for producing lithium tungstate, and method for producing positive electrode active material for non-aqueous electrolyte secondary battery using lithium tungstate | |
| JP7397409B2 (en) | Li-Ni composite oxide particles and non-aqueous electrolyte secondary battery | |
| AU2011290195A1 (en) | Production method for a composite compound comprising nickel and cobalt | |
| US9412486B2 (en) | Composite oxide powder for solid oxide fuel cell and its production method | |
| US12308426B2 (en) | Methods for the production of cathode materials for lithium ion batteries | |
| JP2020055735A (en) | Method for producing titanium pyrophosphate, method for producing titanium phosphate, and method for producing proton conductor | |
| KR20240141786A (en) | Single crystal sodium ion battery cathode active material and its manufacturing method and use | |
| JP2025506136A (en) | High Entropy Oxide | |
| JP7252298B2 (en) | Method for producing modified lithium-nickel-manganese-cobalt composite oxide particles | |
| JP2002068750A (en) | Method of producing tricobalt tetraoxide | |
| TWI580100B (en) | Nickel lithium metal composite oxide, and a nickel-lithium metal composite oxide obtained by the production method and a positive electrode active material composed of a nickel-lithium metal composite oxide | |
| JP2021048120A (en) | Positive electrode active material for lithium secondary battery and lithium secondary battery | |
| CN112204775A (en) | Method for preparing particle precursors and cathode active particles and particle precursors prepared therefrom | |
| KR20230097043A (en) | Method for producing modified lithium nickel manganese cobalt composite oxide particles | |
| CN116490997A (en) | Manufacturing method of modified lithium nickel manganese cobalt composite oxide particles | |
| EP4407713A1 (en) | Positive electrode active material for lithium ion secondary battery, and lithium ion secondary battery | |
| JPH10279315A (en) | Method for producing lithium cobalt composite oxide | |
| JP2010044890A (en) | Method for manufacturing positive electrode active material for lithium secondary battery, positive electrode active material, and lithium secondary battery | |
| JP2025032997A (en) | Positive electrode active material for lithium secondary battery, its manufacturing method and lithium secondary battery | |
| JP2023162136A (en) | Method for producing positive electrode active material for lithium secondary battery |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20230502 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20240814 Comment text: Request for Examination of Application |