KR20180035973A - Sulfur Dioxide Redox flow Secondary Battery and Electrolyte including the same - Google Patents
Sulfur Dioxide Redox flow Secondary Battery and Electrolyte including the same Download PDFInfo
- Publication number
- KR20180035973A KR20180035973A KR1020160125469A KR20160125469A KR20180035973A KR 20180035973 A KR20180035973 A KR 20180035973A KR 1020160125469 A KR1020160125469 A KR 1020160125469A KR 20160125469 A KR20160125469 A KR 20160125469A KR 20180035973 A KR20180035973 A KR 20180035973A
- Authority
- KR
- South Korea
- Prior art keywords
- electrolyte
- redox flow
- flow secondary
- sulfur dioxide
- secondary battery
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/18—Regenerative fuel cells, e.g. redox flow batteries or secondary fuel cells
- H01M8/184—Regeneration by electrochemical means
- H01M8/188—Regeneration by electrochemical means by recharging of redox couples containing fluids; Redox flow type batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/134—Electrodes based on metals, Si or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/96—Carbon-based electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/18—Regenerative fuel cells, e.g. redox flow batteries or secondary fuel cells
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/20—Indirect fuel cells, e.g. fuel cells with redox couple being irreversible
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/002—Inorganic electrolyte
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
-
- Y02E60/528—
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Sustainable Development (AREA)
- Sustainable Energy (AREA)
- Materials Engineering (AREA)
- Fuel Cell (AREA)
Abstract
본 발명은 이산화황계 레독스 흐름 이차 전지에 관한 것으로, 전해액이 주입된 스택, 스택 내에 배치된 정극 및 부극, 전해액을 저장하고 스택에 주입된 전해액을 교체하는 전해액 저장조, 전해액 저장조에 저장된 전해액을 스택에 주입하는데 이용되는 펌프를 포함하고, 전해액은 이산화황과 리튬염 또는 나트륨염으로 구성된 무기 액체 전해질을 포함하는 이산화황계 레독스 흐름 이차 전지를 개시한다.The present invention relates to a sulfur dioxide based redox flow secondary cell, which comprises a stack in which an electrolyte is injected, a positive electrode and a negative electrode disposed in the stack, an electrolyte storage tank for storing the electrolyte solution and replacing the electrolyte solution injected into the stack, A sulfur dioxide based redox flow secondary cell comprising an inorganic liquid electrolyte comprising a sulfur dioxide and a lithium salt or a sodium salt.
Description
본 발명은 레독스 흐름 이차 전지에 관한 것으로, 더욱 상세하게는 이산화황 기반 무기 전해질을 포함한 이산화황계 레독스 흐름 이차 전지에 관한 것이다.The present invention relates to a redox flow secondary cell, and more particularly to a sulfur dioxide redox flow secondary cell including a sulfur dioxide based inorganic electrolyte.
최근 온실 가스 방출에 대한 관심이 높아지고 있다. 이에 온실 가스 방출을 줄이면서 안정적인 전기 에너지 공급이 가능한 해결 방안이 요구되고 있다. 상술한 방안에 대한 해결책으로, 신재생 에너지와 스마트 그리드가 융합된 대용량 에너지 저장 시스템이 제안되고 있다. 상술한 대용량 에너지 저장 시스템 중에서 레독스 흐름 이차 전지는 실현 가능성이 가장 높은 기술 중 하나이다. Recently, interest in greenhouse gas emissions is increasing. Therefore, there is a need for a solution capable of supplying stable electric energy while reducing greenhouse gas emissions. As a solution to the above-mentioned problem, a large-capacity energy storage system in which a renewable energy and a smart grid are fused is proposed. Of the above-mentioned large-capacity energy storage systems, redox flow secondary batteries are one of the most feasible technologies.
종래의 레독스 흐름 이차 전지는 정극 및 부극 활물질이 전해액에 용해되어 있고, 활물질이 정극 및 부극 전극 표면에서 산화 및 환원 반응을 하며, 이온들은 분리막을 통해 이동하는 형태로 설계되었다. V/V redox couple, Zn/Br redox couple을 적용한 레독스 흐름 이차 전지가 널리 이용되고 있지만, 셀 전압이 낮고 에너지밀도가 낮은 단점이 있다. 이에, 고전압 구현을 위해 유기용매를 이용한 redox couple 개발이 진행되고 있으나 유기용매를 사용함으로써 전해액의 가연성 문제가 존재한다. In the conventional redox flow secondary battery, the positive electrode and negative electrode active material are dissolved in the electrolyte, and the active material is oxidized and reduced on the surface of the positive electrode and the negative electrode, and ions are designed to move through the separator. The redox flow secondary battery using the V / V redox couple and the Zn / Br redox couple is widely used, but has a disadvantage in that the cell voltage is low and the energy density is low. Therefore, development of a redox couple using an organic solvent is underway to realize a high voltage, but there is a problem of flammability of an electrolyte by using an organic solvent.
기존의 레독스 흐름 이차 전지에서는 자가 방전에 의한 효율 저하를 억제하고 이온이 전달 가능한 분리막의 역할이 매우 중요하며, anolyte와 catholyte가 분리되어 있어야 하므로 2개의 전해액 저장조가 채택된 시스템이 적용되고 있다. 이에 따라, 종래 레독스 흐름 이차 전지는 부피를 원하는 만큼 축소하기가 어렵고, 설계가 복잡한 문제가 있었다.In the existing redox flow secondary battery, the efficiency of the self - discharge is suppressed and the role of separator capable of transferring ions is very important. Since anolyte and catholyte should be separated, a system adopting two electrolyte reservoirs is being applied. As a result, the conventional redox flow secondary battery has difficulty in reducing the volume as much as desired and has a problem of complicated design.
이에 따라, 본 발명의 목적은 고전압 구현이 가능하고 불연성인 리튬(또는 나트륨)을 기반으로 하는 이산화황 무기액체전해질을 사용하는 전지를 지정된 형태의 용량 및 출력 형태로 설계가 가능한 레독스 흐름 이차 전지 및 이에 포함되는 전해액을 제공하는데 있다.Accordingly, an object of the present invention is to provide a redox flow secondary battery capable of designing a battery using a sulfur dioxide inorganic liquid electrolyte based on lithium (or sodium) which is capable of realizing a high voltage and is nonflammable in a specified form of capacity and output form, And an electrolytic solution contained therein.
또한, 본 발명의 목적은 리튬(또는 나트륨) 이산화황 이차 전지의 방전산물인 NaCl 석출로 인한 전극 표면의 제한으로 인한 용량 감소를 개선하기 위하여 2종의 전해질 첨가제를 포함하는 레독스 흐름 이차 전지 및 이에 포함되는 전해액을 제공하는데 있다. It is another object of the present invention to provide a redox flow secondary battery comprising two kinds of electrolyte additives for improving the capacity reduction due to limitation of the electrode surface due to NaCl precipitation as a discharge product of a lithium (or sodium) sulfur dioxide secondary battery, And to provide an electrolytic solution contained therein.
상술한 바와 같은 목적을 달성하기 위한 본 발명의 레독스 흐름 이차 전지는 전해액이 주입된 스택, 상기 스택 내에 배치된 정극 및 부극, 전해액을 저장하고 상기 스택에 주입된 전해액을 교체하는 전해액 저장조, 상기 전해액 저장조에 저장된 전해액을 상기 스택에 주입하는데 이용되는 펌프를 포함하고, 상기 전해액은 이산화황과 리튬염 또는 나트륨염으로 구성된 무기 액체 전해질을 포함하는 것을 특징으로 한다.According to an aspect of the present invention, there is provided a redox flow secondary battery comprising: a stack in which an electrolyte is injected; a positive electrode and a negative electrode disposed in the stack; an electrolyte reservoir for storing an electrolyte solution and replacing the electrolyte solution injected into the stack; And a pump used for injecting an electrolyte solution stored in the electrolyte reservoir into the stack, wherein the electrolyte solution comprises an inorganic liquid electrolyte composed of sulfur dioxide and a lithium salt or a sodium salt.
상기 전해액은 NaAlCl4 대비 SO2 몰비 함량이 0.5~10인 것을 특징으로 한다.The electrolytic solution has an SO 2 molar ratio of 0.5 to 10 with respect to NaAlCl 4 .
상기 전해액은 NaAlCl4 대비 SO2 몰비 함량이 1.5~3.0인 것을 특징으로 한다.The electrolytic solution has an SO 2 molar ratio of 1.5 to 3.0 with respect to NaAlCl 4 .
상기 전해액은 무기 액체 전해질에 니트로컴파운드 또는 염화알루미늄 염을 무게비율로 0.1~5 배 첨가한 것을 특징으로 한다.The electrolytic solution is characterized in that a nitro compound or an aluminum chloride salt is added to the inorganic liquid electrolyte in an amount of 0.1 to 5 times by weight.
상기 전해액은 무기 액체 전해질에 2종 이상의 염을 첨가한 것을 특징으로 한다.The electrolytic solution is characterized in that two or more kinds of salts are added to the inorganic liquid electrolyte.
상기 정극은 탄소재로 이루어진 것을 특징으로 한다.The positive electrode is made of a carbon material.
상기 부극은 리튬 또는 나트륨 금속, 리튬 또는 나트륨을 함유한 합금, 리튬 또는 나트륨을 함유하는 금속간화합물, 리튬 또는 나트륨을 함유하는 무기계 재료 중 적어도 하나로 이루어진 것을 특징으로 한다.The negative electrode is characterized in that it is made of at least one of lithium or a sodium metal, an alloy containing lithium or sodium, an intermetallic compound containing lithium or sodium, or an inorganic material containing lithium or sodium.
본 발명의 레독스 흐름 이차 전지에 포함되는 전해액은 무기 액체 전해질, 상기 무기 액체 전해질에 무게비율로 0.1~5 배 첨가된 2종 이상의 염을 포함하는 것을 특징으로 한다.The electrolytic solution contained in the redox flow secondary battery of the present invention is characterized by containing an inorganic liquid electrolyte and two or more kinds of salts added to the inorganic liquid electrolyte in an amount of 0.1 to 5 times by weight.
상기 2종 이상의 염은 니트로컴파운드 및 염화알루미늄 염을 포함하는 것을 특징으로 한다.The at least two salts are characterized in that they contain a nitro compound and an aluminum chloride salt.
상술한 바와 같이 본 발명의 실시 예에 따르면 본 발명의 레독스 흐름 이차 전지는 상대적으로 간단한 구성이 가능하며, 고전압에 불연성을 가지고, 높은 전원 용량을 제공할 수 있다. As described above, according to the embodiment of the present invention, the redox flow secondary battery of the present invention can be relatively simple in configuration, and can provide a high power capacity with high voltage and incombustibility.
도 1은 본 발명의 실시 예에 따른 레독스 흐름 이차 전지 구성을 개략적으로 나타낸 도면,
도 2는 본 발명의 실시 예에 따른 리튬 이산화황 이차 전지 정극 전극 표면의 방전 전과 후의 SEM image를 나타낸 도면,
도 3은 본 발명의 실시 예에 따른 비수계 용매들의 안정성 실험 결과를 나타낸 도면,
도 4는 본 발명의 실시 예에 따른 첨가제가 포함된 전해액에 따른 용해 정도를 나타낸 도면,
도 5는 본 발명의 실시 예에 따른 레독스 흐름 이차 전지 특성 비교를 위한 비이커 셀의 한 예를 나타낸 도면,
도 6은 본 발명의 실시 예에 따른 표 1에서 언급된 비교 예1, 실시 예1, 실시 예2에 대한 방전 용량을 나타낸 도면이다.1 is a schematic view of a redox flow secondary battery according to an embodiment of the present invention,
2 is a SEM image of a surface of a positive electrode of a lithium sulfur dioxide secondary battery according to an embodiment of the present invention before and after discharge,
3 is a graph showing the stability test results of nonaqueous solvents according to an embodiment of the present invention,
FIG. 4 is a graph showing the degree of dissolution according to an electrolyte solution containing an additive according to an embodiment of the present invention,
5 is a view illustrating an example of a beaker cell for comparing characteristics of a redox flow secondary battery according to an embodiment of the present invention;
6 is a graph showing discharge capacities for Comparative Example 1, Example 1, and Example 2 mentioned in Table 1 according to an embodiment of the present invention.
본 발명의 상세한 설명에 앞서, 이하에서 설명되는 본 명세서 및 청구범위에 사용된 용어나 단어는 통상적이거나 사전적인 의미로 한정해서 해석되어서는 아니 되며, 발명자는 그 자신의 발명을 가장 최선의 방법으로 설명하기 위해 용어의 개념으로 적절하게 정의할 수 있다는 원칙에 입각하여 본 발명의 기술적 사상에 부합하는 의미와 개념으로 해석되어야만 한다. 따라서 본 명세서에 기재된 실시 예와 도면에 도시된 구성은 본 발명의 가장 바람직한 실시 예에 불과할 뿐, 본 발명의 기술적 사상을 모두 대변하는 것은 아니므로, 본 출원시점에 있어서 이들을 대체할 수 있는 다양한 균등물과 변형 예들이 있을 수 있음을 이해하여야 한다. Prior to the detailed description of the present invention, the terms or words used in the present specification and claims should not be construed as limited to ordinary or preliminary meaning, and the inventor may designate his own invention in the best way It should be construed in accordance with the technical idea of the present invention based on the principle that it can be appropriately defined as a concept of a term to describe it. Therefore, the embodiments described in the present specification and the configurations shown in the drawings are merely the most preferred embodiments of the present invention, and are not intended to represent all of the technical ideas of the present invention. Therefore, various equivalents It should be understood that water and variations may be present.
이하, 첨부된 도면을 참조하여 본 발명의 바람직한 실시 예들을 상세히 설명한다. 이때, 첨부된 도면에서 동일한 구성 요소는 가능한 동일한 부호로 나타내고 있음을 유의해야 한다. 또한, 본 발명의 요지를 흐리게 할 수 있는 공지 기능 및 구성에 대한 상세한 설명은 생략할 것이다. 마찬가지의 이유로 첨부 도면에 있어서 일부 구성요소는 과장되거나 생략되거나 또는 개략적으로 도시되었으며, 각 구성요소의 크기는 실제 크기를 전적으로 반영하는 것이 아니다. Hereinafter, preferred embodiments of the present invention will be described in detail with reference to the accompanying drawings. Note that, in the drawings, the same components are denoted by the same reference symbols as possible. Further, the detailed description of known functions and configurations that may obscure the gist of the present invention will be omitted. For the same reason, some of the elements in the accompanying drawings are exaggerated, omitted, or schematically shown, and the size of each element does not entirely reflect the actual size.
도 1은 본 발명의 실시 예에 따른 레독스 흐름 이차 전지 구성을 개략적으로 나타낸 도면이다.1 is a schematic view of a redox flow secondary battery according to an embodiment of the present invention.
도 1을 참조하면, 본 발명의 레독스 흐름 이차 전지(100)는 스택(110), 전해액 저장조(120), 펌프(130)를 포함할 수 있다. 추가적으로, 상기 레독스 흐름 이차 전지(100)는 상기 전해액 저장조(120)와 스택(110)을 연결하는 제1 연결로, 상기 전해액 저장조(120)와 상기 펌프(130)를 연결하는 제2 연결로, 상기 펌프(130)와 상기 스택(110)을 연결하는 제3 연결로 중 적어도 하나를 더 포함할 수 있다. 또한, 상기 레독스 흐름 이차 전지(100)는 상기 스택(110) 내부에 배치된 정극과 부극에 각각 연결되는 전극부들을 더 포함할 수 있다. 상기 전극부들의 적어도 일부는 상기 스택(110) 외부에 노출되도록 배치될 수 있다. 상술한 본 발명의 레독스 흐름 이차 전지(100)는 정극(Cathode)으로는 탄소재를 사용하며, 부극(Anode)으로는 리튬 또는 나트륨 및 이를 포함하는 금속 또는 무기재료를 포함하고 분리막이 없는 단일 저장조를 사용할 수 있는 하이브리드형 타입이며, 2종 첨가제가 포함된 무기전해질을 포함하는 구조를 채용할 수 있다.Referring to FIG. 1, the redox flow
상기 스택(110)은 적용될 제품의 형상이나 제품이 배치될 위치 등에 따라 다양한 형태로 마련될 수 있다. 한 실시 예에 따르면, 상기 스택(110)은 직사각형의 박스 형태로 마련될 수 있다. 그러나, 본 발명이 이에 한정되는 것은 아니며, 상기 스택(110)은 배치될 위치의 형상에 따라 다양하게 변형 가공될 수 있다. 상기 스택(110)은 부극(111)(anode), 정극(112)(cathode), 전해액(113)이 내측에 배치될 수 있다. 특히, 본 발명의 레독스 흐름 이차 전지(100)는 부극(111)과 정극(112) 사이에 분리막이 존재하지 않는 형태를 가질 수 있다.The
상기 정극(112)은 다공성의 탄소재로 이루어질 수 있다. 상기 정극(112)은 스택(110) 내부에 충진된 전해액이 종류에 따라 LiAlCl4-xSO2 또는 NaAlCl4-xSO2의 산화-환원 반응이 일어나는 장소를 제공한다. 한 예시로서, 정극(112)은 Ketjenblack 600JD에 PTFE 바인더 10%를 사용하여 제작될 수 있다. 다른 예시로서, 상기 정극(112)은 상기 탄소재에 하나 또는 둘 이상의 이종원소가 0~20 at% 포함될 수 있으며, 이종원소는 질소(N), 산소(O), 붕소(B), 불소(F), 인(P), 황(S), 규소(Si)를 포함할 수 있다.The
상기 부극(111)은 리튬 금속 시트(sheet)를 이용하여 마련될 수 있다. 다른 예시로서, 부극(111)은 리튬을 함유한 합금, 또는 리튬을 함유하는 금속간화합물, 또는 리튬을 함유하는 무기계 재료 중 적어도 하나로 구성될 수 있다. 상기 무기계 재료는 탄소, 산화물, 황화물, 인화물, 질화물, 불화물 중 적어도 하나를 포함할 수 있다.The
상기 전해액(113)은 이산화황계열의 금속 화합물을 포함할 수 있다. 예컨대, 전해액(113)은 Li(or Na)AlCl4-xSO2 이 이용될 수 있다. 상기 전해액(113)은 전해액 저장조(120)에 저장되고, 펌프(130)에 의해 스택(110)에 공급될 수 있다. The
상기 전해액 저장조(120)는 상기 전해액(113)을 저장하는 저장조일 수 있다. 본 발명의 전해액 저장조(120)는 펌프(130) 동작에 따라, 저장된 전해액(113)을 스택(110)에 공급할 수 있다. The
상기 펌프(130)는 제어기의 제어에 대응하여 펌핑 동작을 수행할 수 있다. 펌프(130)의 펌핑 동작에 따라 스택(110)에 공급되는 전해액(113)의 양이 달라지며, 결과적으로 스택(110)에서의 전해액(113)의 반응에 의하여 생산되는 전원의 양이 달라진다. 이에 따라 펌프(130)의 펌핑 동작 제어는 부하에 공급되는 전원의 양에 따라 달라질 수 있다. 본 발명의 펌프(130)는 하나의 전해액 저장조(120)를 사용함으로써, 하나의 펌프를 포함할 수 있다.The
추가적으로, 본 발명의 레독스 흐름 이차 전지(100)는 펌프(130)의 펌핑 속도 제어를 수행하는 제어기에 연결되고, 또한 레독스 흐름 이차 전지(100)에서 발생하는 전력을 공급하는 부하와 연결될 수 있다. 또한, 전해액 저장조(120)에 저장된 전해액(113)을 스택(110)에 이동시켜 전원을 생성하도록 반응시키는 과정에서 열이 발생할 수 있으며, 이러한 열은 전해액 저장조(120)의 온도를 증가시키게 된다. 이에 따라, 레독스 흐름 이차 전지(100)는 전력 생산 및 제공 과정에서 발생하는 열을 발열시키기 위한 냉각 시스템을 더 포함할 수 있다. 냉각 시스템은 전해액 저장조(120)의 온도를 검출하고, 전해액 저장조(120)가 사전 정의된 온도를 가지도록 냉각시키는 구성이다. 이를 위하여 냉각 시스템은 전해액 저장조(120)의 온도를 검측하는 센서를 포함하고, 상기 센서가 수집한 센서 신호를 기반으로 상기 전해액 저장조(120)의 냉각 제어를 수행할 수 있다. In addition, the redox flow
상술한 바와 같이, 본 발명의 레독스 흐름 이차 전지(100)는 이산화황 기반 리튬계 무기액체 전해질을 이온전도체 및 활물질로 적용하며, 분리막이 없는 한 개의 전해액 저장조(120)를 적용한 레독스 흐름 이차 전지이다. 이러한 레독스 흐름 이차 전지(100)는 기존의 레독스 흐름 이차 전지 대비 구성이 간단하고 이산화황 기반 리튬계 이차 전지의 용량 및 출력 설계를 자유롭게 할 수 있어, 고전압 및 불연성 레독스 흐름 이차 전지를 제공할 수 있다. 상술한 바와 같이 리튬(또는 나트륨) 이산화황 레독스 흐름 이차 전지는 고전압 구현이 가능하고 불연성인 액체 전해질을 사용함으로써 안전성을 확보할 수 있는 장점이 있다. As described above, the redox flow
추가적으로, 본 발명의 레독스 흐름 이차 전지(100)는 2종의 전해액 첨가제를 이용하여 방전산물을 제거함으로써, 방전산물로 인한 용량제한 문제를 해결할 수 있다. In addition, the redox flow
도 2는 리튬 이산화황 이차 전지 정극 전극 표면의 방전 전과 후의 SEM image를 나타낸 도면이다. 도시된 바와 같이, 방전 전(201)에는 정극 전극의 표면에 LiCl 결정이 형성되지 않은 반면, 방전 후(203) LiCl 결정이 정극 전극의 표면에 형성된 것을 뚜렷하게 관찰 할 수 있다. 2 is a SEM image before and after discharging the surface of the positive electrode of a lithium sulfur dioxide secondary battery. As shown in the drawing, it can be clearly observed that LiCl crystals are not formed on the surface of the positive electrode in the
따라서, 방전 후 생성된 방전산물인 LiCl(or NaCl)을 용해 또는 정극에서 탈착시켜 레독스 흐름 이차 전지의 구동 및 성능 향상을 위해 전해액 저장조(120)에는 전해액(113) 외에 방전산물 제거를 위한 첨가제 또는 용매를 더 포함할 수 있다. Therefore, in order to improve the driving and performance of the redox flow secondary battery by dissolving or discharging LiCl (or NaCl), which is a discharge product generated after discharging, the
도 3은 본 발명의 실시 예에 따른 비수계 용매들의 안정성 실험 결과를 나타낸 도면이다.3 is a graph showing the stability test results of nonaqueous solvents according to an embodiment of the present invention.
도 3을 참조하면, LiCl을 용해할 수 있는 비수계 용매들로는 Pyridine 계열(301), 니트로컴파운드(303), 알콜계열(305) 등이 사용될 수 있으나, 초기 전해액과 안정성 실험에서 니트로컴파운드 중 하나인 니트로벤젠(303)만이 전해액과 안정한 결과를 나타내고 있다. 그러나, 니트로컴파운드 등의 단수 용매를 사용할 경우, 방전산물인 LiCl(or NaCl)의 용해의 한계를 나타내는 문제가 있다. 이에 따라, 본 발명의 레독스 흐름 이차 전지(100)는 LiCl (or NaCl)을 다량으로 용해시킬 수 있는 2종(Co-additive) 전해액 첨가제를 이용하고 있다. 예컨대, 본 발명에서는 SO2 전해액의 니트로컴파운드에 새로운 염을 추가하여 LiCl(or NaCl) 용해도 평가를 진행하였다. Referring to FIG. 3, non-aqueous solvents capable of dissolving LiCl include
도 4는 본 발명의 실시 예에 따른 첨가제가 포함된 전해액에 따른 용해 정도를 나타낸 도면이다.4 is a graph showing the degree of dissolution according to an electrolyte solution containing an additive according to an embodiment of the present invention.
도 4의 401 상태는 SO2 전해액에 니트로컴파운드와 염화알루미늄 염이 동시에 용해된 상태를 나타낸 것이며, 403 상태는 SO2 전해액에 0.5M LiCl 2종 염(니트로컴파운드 및 염화알루미늄 염)이 용해된 상태를 나타낸 것이다. 도시된 바와 같이, SO2 전해액에 니트로컴파운드와 염화알루미늄 염을 동시 용해시킬 수 있으며, 일정 몰비로 SO2 전해액에 상기 2종의 염(니트로컴파운드 및 염화알루미늄)을 첨가제로 사용할 경우 레독스 흐름 이차 전지의 방전 시 정극 표면에 발생하는 방전 산물을 용해시켜 전극 표면을 refresh 할 수 있다. 상기 SO2 전해액에는 무기 액체 전해질에 니트로컴파운드 또는 염화알루미늄 염을 무게비율로 0.1~5 배 첨가될 수 있다.Will showing a state of FIG. 401 is a 4-nitro compound and the aluminum chloride salt at the same time dissolved SO 2 in the electrolyte solution state,
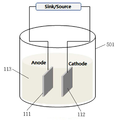
도 5는 본 발명의 실시 예에 따른 레독스 흐름 이차 전지 특성 비교를 위한 비이커 셀의 한 예를 나타낸 도면이다.5 is a view illustrating an example of a beaker cell for comparing characteristics of a redox flow secondary battery according to an embodiment of the present invention.
상술한 본 발명의 리튬 이산화항 레독스 흐름 이차 전지의 특성 비교를 위하여 도 5에 나타낸 바와 같이 분리막이 없고 전해액의 흐름이 없지만 레독스 흐름 이차 전지와 유사한 조건의 비이커 셀(Beaker cell)을 제작하여 전지특성을 비교하였다. 비이커 셀은 도시된 바와 같이 비이커(501), 전해액(113), 부극(111), 정극(112), 부하를 포함할 수 있다. 상기 전해액(113)은 앞서 언급한 바와 같이 LiAlCl4-xSO2 또는 NaAlCl4-xSO2 중 어느 하나가 될 수 있다. 정극(112)은 탄소재로 이루어지며, 부극(111)은 리튬계 금속 시트가 될 수 있다. 전해질 및 정극반응 활물질로 사용되는 이산화황 기반 무기액체 전해질은 LiAlCl4(용질)과 SO2(용매)로 구성되어 있으며, LiAlCl4 대비 SO2의 함량 몰비는 0.5 ~ 10에 해당하는 것으로 바람직하게는 1.5~3에 해당한다. In order to compare the characteristics of the lithium secondary batteries according to the present invention, as shown in FIG. 5, a beaker cell having no separation membrane and no electrolyte flow, but having similar conditions to the redox flow secondary battery, was fabricated The battery characteristics were compared. The beaker cell may include a
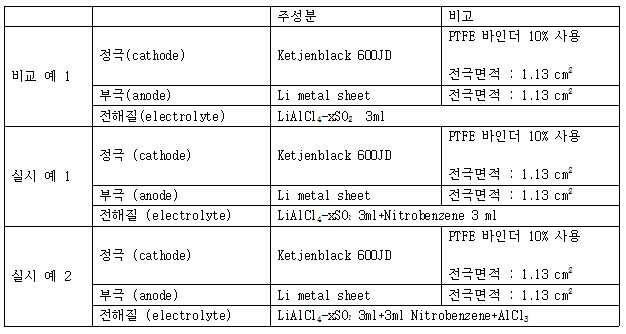
실시 예 및 비교 예의 전지구성 및 전극/전해질 조건은 다음의 표 1과 같다.The cell configurations and electrode / electrolyte conditions of Examples and Comparative Examples are shown in Table 1 below.
도 6은 본 발명의 실시 예에 따른 표 1에서 언급된 비교 예1, 실시 예1, 실시 예2에 대한 방전 용량을 나타낸 도면이다.6 is a graph showing discharge capacities for Comparative Example 1, Example 1, and Example 2 mentioned in Table 1 according to an embodiment of the present invention.
도 6에 나타낸 바와 같이 실시 예와 비교 예의 결과를 면적당 방전용량을 비교해 보면 동일한 활물질인 LiAlCl4-xSO2 전해액을 사용하였음에도 불구하고 Nitrobenzene 첨가제가 적용된 전해액은 방전용량이 약 2배 정도 증가한 결과할 확인하였다. 또한, Nitrobenzene과 염화알루미늄 2종의 co-additive를 적용한 전해액은 면적당 방전용량이 비교 예 대비 약 7배의 용량 증대 효과를 확인할 수 있었다. 이는 앞서 언급한 것처럼 방전 산물인 다량의 LiCl 결정을 용해하여 전극 반응이 일어날 수 있는 정극 전극의 표면을 보다 많이 확보하였기 때문으로 판단된다. As shown in FIG. 6, when the discharge capacity per area is compared with the results of the examples and the comparative examples, it is found that although the same active material LiAlCl 4 -xSO 2 electrolyte was used, the electrolytic solution to which the Nitrobenzene additive was applied exhibited about twice the discharge capacity Respectively. In addition, it was confirmed that the electrolytic solution to which the co-additive of Nitrobenzene and aluminum chloride was applied showed a capacity increase of about 7 times as compared with the comparative example. As described above, it is considered that the surface of the positive electrode capable of electrode reaction can be secured by dissolving a large amount of LiCl crystal as a discharge product.
이상 본 발명을 몇 가지 바람직한 실시 예를 사용하여 설명하였으나, 이들 실시 예는 예시적인 것이며 한정적인 것이 아니다. 이와 같이, 본 발명이 속하는 기술 분야에서 통상의 지식을 지닌 자라면 본 발명의 사상과 첨부된 특허청구범위에 제시된 권리범위에서 벗어나지 않으면서 균등론에 따라 다양한 변화와 수정을 가할 수 있음을 이해할 것이다.While the present invention has been described with reference to several preferred embodiments, these embodiments are illustrative and not restrictive. It will be understood by those skilled in the art that various changes and modifications may be made without departing from the spirit of the invention and the scope of the appended claims.
100 : 레독스 흐름 이차 전지
110 : 스택
120 : 전해액 저장조
130 : 펌프100: redox flow secondary battery
110: Stack
120: Electrolyte storage tank
130: pump
Claims (8)
상기 스택 내에 배치된 정극 및 부극;
전해액을 저장하고 상기 스택에 주입된 전해액을 교체하는 전해액 저장조;
상기 전해액 저장조에 저장된 전해액을 상기 스택에 주입하는데 이용되는 펌프;를 포함하고,
상기 전해액은
이산화황과 리튬염 또는 나트륨염으로 구성된 무기 액체 전해질을 포함하는 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지.A stack in which electrolyte is injected;
A positive electrode and a negative electrode disposed in the stack;
An electrolyte reservoir for storing the electrolyte solution and replacing the electrolyte solution injected into the stack;
And a pump used to inject the electrolyte stored in the electrolyte reservoir into the stack,
The electrolyte solution
Wherein the sulfur dioxide-based redox flow secondary cell comprises an inorganic liquid electrolyte composed of sulfur dioxide and a lithium salt or a sodium salt.
상기 전해액은
NaAlCl4 대비 SO2 몰비 함량이 0.5~10인 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지.The method according to claim 1,
The electrolyte solution
Wherein the SO 2 molar ratio based on NaAlCl 4 is 0.5 to 10.
상기 전해액은
NaAlCl4 대비 SO2 몰비 함량이 1.5~3.0인 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지.3. The method of claim 2,
The electrolyte solution
Wherein the SO 2 molar ratio based on NaAlCl 4 is 1.5 to 3.0.
상기 전해액은
무기 액체 전해질에 니트로컴파운드 또는 염화알루미늄 염을 무게비율로 0.1~5 배 첨가한 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지.The method according to claim 1,
The electrolyte solution
A sulfur dioxide based redox flow secondary cell characterized in that a nitro compound or an aluminum chloride salt is added to the inorganic liquid electrolyte in a weight ratio of 0.1 to 5 times.
상기 전해액은
무기 액체 전해질에 2종 이상의 염을 첨가한 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지.The method according to claim 1,
The electrolyte solution
A sulfur dioxide-based redox flow secondary cell characterized in that two or more salts are added to the inorganic liquid electrolyte.
상기 정극은 탄소재로 이루어지고,
상기 부극은 리튬 또는 나트륨 금속, 리튬 또는 나트륨을 함유한 합금, 리튬 또는 나트륨을 함유하는 금속간화합물, 리튬 또는 나트륨을 함유하는 무기계 재료 중 적어도 하나로 이루어진 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지.The method according to claim 1,
Wherein the positive electrode is made of a carbon material,
Wherein the negative electrode is made of at least one of lithium or a sodium metal, an alloy containing lithium or sodium, an intermetallic compound containing lithium or sodium, or an inorganic material containing lithium or sodium.
무기 액체 전해질;
상기 무기 액체 전해질에 무게비율로 0.1~5 배 첨가된 2종 이상의 염;
을 포함하는 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지에 사용되는 전해액.In the electrolytic solution used in the redox flow secondary battery,
An inorganic liquid electrolyte;
Two or more salts added to the inorganic liquid electrolyte in an amount of 0.1 to 5 times by weight;
Wherein the electrolyte is used in a sulfur dioxide-based redox flow secondary battery.
상기 2종 이상의 염은
니트로컴파운드 및 염화알루미늄 염을 포함하는 것을 특징으로 하는 이산화황계 레독스 흐름 이차 전지에 사용되는 전해액.8. The method of claim 7,
The two or more salts
Wherein the electrolytic solution is used in a sulfur dioxide-based redox flow secondary cell, which comprises a nitro compound and an aluminum chloride salt.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160125469A KR20180035973A (en) | 2016-09-29 | 2016-09-29 | Sulfur Dioxide Redox flow Secondary Battery and Electrolyte including the same |
| PCT/KR2016/013767 WO2018062619A1 (en) | 2016-09-29 | 2016-11-28 | Sulfur dioxide-based redox flow secondary battery and electrolyte solution included therein |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160125469A KR20180035973A (en) | 2016-09-29 | 2016-09-29 | Sulfur Dioxide Redox flow Secondary Battery and Electrolyte including the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180035973A true KR20180035973A (en) | 2018-04-09 |
Family
ID=61759878
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160125469A Withdrawn KR20180035973A (en) | 2016-09-29 | 2016-09-29 | Sulfur Dioxide Redox flow Secondary Battery and Electrolyte including the same |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR20180035973A (en) |
| WO (1) | WO2018062619A1 (en) |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7358012B2 (en) * | 2004-01-06 | 2008-04-15 | Sion Power Corporation | Electrolytes for lithium sulfur cells |
| US20140178735A1 (en) * | 2011-07-21 | 2014-06-26 | National University Of Singapore | Redox flow battery system |
| KR101480771B1 (en) * | 2013-01-30 | 2015-01-29 | 전자부품연구원 | Anode active material comprising phosphorus, lithium secondary battery having the anode active material and manufacturing method thereof |
| KR102276169B1 (en) * | 2014-04-04 | 2021-07-12 | 에스케이이노베이션 주식회사 | Electrolyte for Sodium Secondary Battery and Sodium Secondary Battery using thereof |
| KR20160082372A (en) * | 2014-12-26 | 2016-07-08 | 전자부품연구원 | Redox flow battery that do not contain physically seperation the electrolyte layer part and stacked redox flow secondary battery |
-
2016
- 2016-09-29 KR KR1020160125469A patent/KR20180035973A/en not_active Withdrawn
- 2016-11-28 WO PCT/KR2016/013767 patent/WO2018062619A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| WO2018062619A1 (en) | 2018-04-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5796417B2 (en) | Non-aqueous electrolyte battery electrolyte and non-aqueous electrolyte battery | |
| KR101353363B1 (en) | Improvements relating to electrolyte compositions for batteries using sulphur or sulphur compounds | |
| JP6436874B2 (en) | Lithium air electrochemical cell, battery including lithium air electrochemical cell, and vehicle including the battery | |
| US9214695B2 (en) | Hybrid anodes for redox flow batteries | |
| KR20120095949A (en) | Solid-state sodium-based secondary cell having a sodium ion conductive ceramic separator | |
| WO2019245461A1 (en) | An aqueous redox flow battery | |
| JPWO2006129635A1 (en) | Secondary battery, power supply system using the same, and method of using the power supply system | |
| JP5157107B2 (en) | Non-aqueous electrolyte battery | |
| KR20150131019A (en) | Lithium ion capacitor and method for charging and discharging same | |
| WO2010135283A2 (en) | Improved sodium-sulfur batteries | |
| US12199282B2 (en) | Halogenated battery comprising a greenhouse gas | |
| KR20150049588A (en) | Sodium Secondary Battery having Graphite Felt | |
| CN108933293B (en) | Phosphonium-based ionic liquids for lithium metal-based batteries | |
| CN106415909A (en) | Electrolyte solution comprising sulfur dioxide-based ionic liquid electrolyte, and sodium-sulfur dioxide secondary battery having same | |
| JP4868350B2 (en) | Non-aqueous electrolyte battery | |
| KR20170096641A (en) | Method of preparing Anolyte for vanadium redox flow battery including additives and vanadium redox flow battery comprising the same | |
| KR101118862B1 (en) | Electrolyte solution composition and energy storage device with the same | |
| KR20170027141A (en) | Sulfone containing organic electrolyte for lithium-air battery having good energy efficiency and oxygen efficiency and lithium-air battery using the same | |
| WO2020121015A1 (en) | Electrochemical device for storing energy | |
| KR20180035975A (en) | Sulfur Dioxide Redox flow Secondary Battery | |
| KR20180035973A (en) | Sulfur Dioxide Redox flow Secondary Battery and Electrolyte including the same | |
| KR101693576B1 (en) | Sulfur dioxide based inorganic electrolyte solution and sulfur dioxide based redox flow secondary battery using the same | |
| CN113728477A (en) | Negative electrode electrolyte for redox flow battery and redox flow battery | |
| JP5062505B2 (en) | Non-aqueous electrolyte battery | |
| JP2014072078A (en) | Selection method of solvent for electrolyte |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20160929 |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination |