KR20140009819A - Pharmaceutical composition for topical administration comprising vancomycin or its salt and dexamethasone phosphate or its salt - Google Patents
Pharmaceutical composition for topical administration comprising vancomycin or its salt and dexamethasone phosphate or its salt Download PDFInfo
- Publication number
- KR20140009819A KR20140009819A KR1020120076674A KR20120076674A KR20140009819A KR 20140009819 A KR20140009819 A KR 20140009819A KR 1020120076674 A KR1020120076674 A KR 1020120076674A KR 20120076674 A KR20120076674 A KR 20120076674A KR 20140009819 A KR20140009819 A KR 20140009819A
- Authority
- KR
- South Korea
- Prior art keywords
- pharmaceutical composition
- topical administration
- vancomycin
- acceptable salt
- pharmaceutically acceptable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/14—Peptides containing saccharide radicals; Derivatives thereof, e.g. bleomycin, phleomycin, muramylpeptides or vancomycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/14—Esters of carboxylic acids, e.g. fatty acid monoglycerides, medium-chain triglycerides, parabens or PEG fatty acid esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Gastroenterology & Hepatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Dermatology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
Abstract
본 발명은 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염을 포함하는 국소투여용 약학 조성물로서, 반코마이신 또는 그의 약학적으로 허용가능한 염과 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염을 특정 중량비로 함유하는 국소투여용 약학 조성물을 제공한다. 본 발명에 따른 약학 조성물은 재구성 제제(reconstitutable formulation)의 형태로 제제화될 수 있으며, 신속한 재구성(reconstitution)을 통하여 침전이나 겔화 발생 없이 투명한 용액을 얻을 수 있다. 또한, 재구성된 용액은 실온에서도 장기간(예를 들어, 약 1개월) 동안 침전이나 겔화가 발생하지 않고 또한 유연물질의 발생이 최소화됨으로써, 우수한 물리적 및 화학적 안정성을 갖는다.The present invention relates to a pharmaceutical composition for topical administration comprising vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof, wherein vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof. It provides a pharmaceutical composition for topical administration containing an acceptable salt in a specific weight ratio. The pharmaceutical composition according to the present invention may be formulated in the form of a reconstitutable formulation, and a rapid solution may be obtained to obtain a clear solution without precipitation or gelation through rapid reconstitution. In addition, the reconstituted solution has good physical and chemical stability by not causing precipitation or gelation for a long time (eg, about 1 month) even at room temperature, and minimizing the generation of the flexible material.
Description
본 발명은 반코마이신 또는 그의 염 및 덱사메타손 포스페이트 또는 그의 염을 포함하는 국소투여용 약학 조성물에 관한 것이다.The present invention relates to a pharmaceutical composition for topical administration comprising vancomycin or a salt thereof and dexamethasone phosphate or a salt thereof.
반코마이신(vancomycin)은 메티실린-내성 스타필로코쿠스 에피더미디스(Staphylococcus epidemidis)를 포함한 메티실린-내성 균주에 대한 치료에 유용하게 사용되는 항생제이다. 현재, 반코마이신은 안정성을 담보하기 위하여 동결건조 주사제 혹은 냉동 링거액 제제로서 시판되고 있다. 상기 동결건조 주사제는 주사용수, 생리식염수 등에 용해시켜 사용되며, 냉장 조건에서 96시간 이내에 사용할 것을 필요로 한다. 상기 냉동 링거액은 -20℃에서의 냉동보관을 필요로 한다. 덱사메타손 포스페이트(dexamethasone phosphate)는 코르티코스테로이드로서 강력한 항염증작용을 가지며, 특히 알레르기성 질환, 피부질환, 염증성 안질환 및 외이/중이염 등의 치료에 유용하게 사용된다. Vancomycin is an antibiotic that is useful for the treatment of methicillin-resistant strains, including methicillin-resistant Staphylococcus epidemidis . Currently, vancomycin is marketed as a lyophilized injection or frozen Ringer's solution to ensure stability. The lyophilized injection is used after being dissolved in water for injection, physiological saline, etc., and needs to be used within 96 hours under refrigerated conditions. The freezing ringer solution requires freezing storage at -20 ℃. Dexamethasone phosphate (dexamethasone phosphate) is a corticosteroid and has a strong anti-inflammatory action, and is particularly useful for the treatment of allergic diseases, skin diseases, inflammatory eye diseases, and ear / otitis media.
항생제와 스테로이드의 조합치료는 다양한 연구에서 치료학적 개선을 야기하는 것으로 보고된 바 있다(Baum JL, et al., Am J Ophthalmol 1974;80:513-7; Barza M. et al., Infect Dis Clin North Am 1989;3:533-49; Schulman JA, et al., Retina 1992; 12:336-40; Meredith TA, et al., Ophthalmology 1990;108:857-60; Maxwell DP Jr, et al., Ophthalmology 1990;98:1370-5 등). 또한, Smith MA 등은 반코마이신과 덱사메타손의 조합 치료가 반코마이신 단독 투여 시 보다 염증치료에 있어서 우수한 효과를 달성할 수 있음을 개시한 바 있다(Smith MA, et al., J Infect Dis. 1997 Feb;175(2):462-6). 따라서 반코마이신과 덱사메타손을 유효성분으로서 함유한 약학적 제제는 눈, 귀, 코, 피부에 적용하기 위한 국소 투여용 제제로서 유용하게 사용될 수 있을 것으로 기대된다.The combination therapy of antibiotics and steroids has been reported to cause therapeutic improvement in various studies (Baum JL, et al., Am J Ophthalmol 1974; 80: 513-7; Barza M. et al., Infect Dis Clin Merelith TA, et al., Ophthalmology 1990; 108: 857-60; Maxwell DP Jr, et al., ≪ RTI ID = 0.0 > Ophthalmology 1990; 98: 1370-5, etc.). In addition, Smith MA et al. Have disclosed that the combination treatment of vancomycin and dexamethasone can achieve better effects in the treatment of inflammation than vancomycin alone (Smith MA, et al., J Infect Dis. 1997 Feb; 175; (2): 462-6). Therefore, pharmaceutical preparations containing vancomycin and dexamethasone as active ingredients are expected to be usefully used as preparations for topical administration for application to the eyes, ears, nose and skin.
한편, 반코마이신과 덱사메타손을 동시에 포함하는 국소투여용 약학적 제제를 설계하기 위해서는, 주사용수 등의 수성 매질 중에서 침전이나 미립자의 형성 없이 물리적 안정성을 가질 것이 요구된다. 그러나, 반코마이신과 덱사메타손을 수성 매질 중에서 서로 혼합할 경우, 침전물이 형성되어 물리적 안정성을 기대하기 곤란하다. Smith MA 등의 논문에서도, 침전을 회피하기 위하여 반코마이신과 덱사메타손을 별도의 시린지(syringe)를 사용하여 투여한 바 있다. On the other hand, in order to design a pharmaceutical formulation for topical administration containing vancomycin and dexamethasone simultaneously, it is required to have physical stability without precipitation or formation of fine particles in an aqueous medium such as water for injection. However, when vancomycin and dexamethasone are mixed with each other in an aqueous medium, precipitates form and it is difficult to expect physical stability. In the paper by Smith MA et al., Vancomycin and dexamethasone were administered using separate syringes to avoid precipitation.
본 발명자들은 반코마이신과 덱사메타손을 포함하는 국소투여용 약학적 제제로서, 침전이나 미립자의 형성 없이 우수한 안정성을 갖는 약학적 제제를 개발하기 위하여 다양한 연구를 수행하였다. 본 발명자들은 다양한 연구를 통하여 반코마이신과 덱사메타손이 중량비에 따라 안정성에 크게 영향을 미친다는 것을 발견하였다. 특히, 본 발명자들은 반코마이신과 덱사메타손을 특정 중량비로 사용하여, 두개의 컴파트먼트(예를 들어, 바이알 또는 플라스틱 용기)로 구성된 재구성 제제(reconstitutable formulation)의 형태로 제제화할 경우, 신속한 재구성(reconstitution)을 달성함으로써 침전이나 겔화 발생 없이 투명한 용액을 얻을 수 있다는 것을 발견하였다. 또한, 재구성된 용액이 실온에서도 장기간(예를 들어, 약 1개월) 동안 침전이나 겔화가 발생하지 않고 또한 유연물질의 발생이 최소화됨으로써, 우수한 물리적 및 화학적 안정성을 갖는다는 것을 발견하였다. 이는 -20℃에서 냉동 보관해야 하는 반코마이신-함유 냉동 제제에 비하여 특히 우수한 편리성을 제공한다. The present inventors have conducted various studies to develop a pharmaceutical formulation having topical administration as a pharmaceutical formulation containing vancomycin and dexamethasone, without precipitation or formation of fine particles. The inventors have found through the various studies that vancomycin and dexamethasone greatly affect the stability according to the weight ratio. In particular, the present inventors, when using vancomycin and dexamethasone in specific weight ratios, formulated in the form of a reconstitutable formulation consisting of two compartments (eg, vials or plastic containers), rapid reconstitution It was found that a clear solution can be obtained without achieving precipitation or gelation by achieving. It has also been found that the reconstituted solution has good physical and chemical stability by not causing precipitation or gelation for long periods of time even at room temperature (eg, about 1 month) and minimizing the generation of analogues. This provides particularly good convenience compared to vancomycin-containing frozen formulations that must be frozen at −20 ° C.
따라서, 본 발명은 반코마이신과 덱사메타손 포스페이트를 특정 중량비로 포함하는 국소투여용 약학 조성물을 제공하는 것을 목적으로 한다.Accordingly, an object of the present invention is to provide a pharmaceutical composition for topical administration containing vancomycin and dexamethasone phosphate in a specific weight ratio.
본 발명의 일 태양에 따라, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염을 포함하는 국소투여용 약학 조성물로서, (i) 반코마이신 또는 그의 약학적으로 허용가능한 염의 농도가 총 조성물에 대하여 1.0 %(w/v) 이상일 때, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 중량비가 1 : 0.02 ∼ 0.1이고; (ii) 반코마이신 또는 그의 약학적으로 허용가능한 염의 농도가 총 조성물에 대하여 1.0 %(w/v) 미만일 때, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 중량비가 1 : 0.05 ∼ 0.4인 국소투여용 약학 조성물이 제공된다.According to one aspect of the invention, a pharmaceutical composition for topical administration comprising vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof, comprising: (i) vancomycin or a pharmaceutically acceptable salt thereof When the concentration is at least 1.0% (w / v) relative to the total composition, the weight ratio of vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof is 1: 0.02 to 0.1; (ii) when the concentration of vancomycin or its pharmaceutically acceptable salt is less than 1.0% (w / v) relative to the total composition, the weight ratio of vancomycin or its pharmaceutically acceptable salt and dexamethasone phosphate or its pharmaceutically acceptable salt is 1: The pharmaceutical composition for topical administration which is 0.05-0.4 is provided.
본 발명의 일 구현예에서, 상기 약학 조성물은 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염을 포함하는 제1 컴파트먼트; 및 물을 포함하는 제2 컴파트먼트로 구성된 단위 투여 형태를 가질 수 있다. In one embodiment of the invention, the pharmaceutical composition comprises a first compartment comprising vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof; And a second compartment containing water.
본 발명의 다른 구현예에서, 상기 제2 컴파트먼트는 글리세린을 추가로 포함할 수 있으며, 그 농도는 총 조성물에 대하여 20.0 %(w/v)이하일 수 있다. 또한, 상기 제2 컴파트먼트는 총 조성물에 대하여 0.001 내지 0.1 %(w/w)의 킬레이트화제 및/또는 0.001 내지 0.18 %(w/v)의 보존제를 추가로 포함할 수 있다.In another embodiment of the present invention, the second compartment may further comprise glycerin, the concentration of which may be 20.0% (w / v) or less based on the total composition. In addition, the second compartment may further comprise 0.001 to 0.1% (w / w) chelating agent and / or 0.001 to 0.18% (w / v) preservative relative to the total composition.
반코마이신과 덱사메타손이 중량비에 따라 안정성에 크게 영향을 받는다는 것이 본 발명에 의해 밝혀졌다. 특히, 반코마이신과 덱사메타손을 특정 중량비로 사용하여, 두개의 컴파트먼트(예를 들어, 바이알 또는 플라스틱 용기)로 구성된 재구성 제제(reconstitutable formulation)의 형태로 제제화할 경우, 신속한 재구성(reconstitution)을 달성함으로써 침전이나 겔화 발생 없이 투명한 용액을 얻을 수 있다는 것이 본 발명에 의해 밝혀졌다. It has been found by the present invention that vancomycin and dexamethasone are significantly affected by stability by weight ratio. In particular, when using vancomycin and dexamethasone in specific weight ratios to formulate in the form of a reconstitutable formulation consisting of two compartments (e.g., vials or plastic containers), a rapid reconstitution is achieved. It has been found by the present invention that a clear solution can be obtained without precipitation or gelation occurring.
또한, 재구성된 용액이 실온에서도 장기간(예를 들어, 약 1개월) 동안 침전이나 겔화가 발생하지 않고 또한 유연물질의 발생이 최소화됨으로써, 우수한 물리적 및 화학적 안정성을 갖는다는 것이 본 발명에 의해 밝혀졌다. 따라서, 본 발명에 따른 약학 조성물은 단회 사용뿐만 아니라, 실온(약 25℃)에서 보관하면서 장기간 동안 복수회로 유용하게 사용될 수 있는 장점을 갖는다.In addition, it has been found by the present invention that the reconstituted solution has excellent physical and chemical stability by not causing precipitation or gelation for a long time (eg, about 1 month) even at room temperature and minimizing the generation of soft substances. . Therefore, the pharmaceutical composition according to the present invention has the advantage that it can be usefully used in multiple times for a long time while storing at room temperature (about 25 ° C.) as well as single use.
본 발명은 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염을 포함하는 국소투여용 약학 조성물로서, (i) 반코마이신 또는 그의 약학적으로 허용가능한 염의 농도가 총 조성물에 대하여 1.0 %(w/v) 이상일 때, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 중량비가 1 : 0.02 ∼ 0.1이고; (ii) 반코마이신 또는 그의 약학적으로 허용가능한 염의 농도가 총 조성물에 대하여 1.0 %(w/v) 미만일 때, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 중량비가 1 : 0.05 ∼ 0.4인 국소투여용 약학 조성물을 제공한다.The present invention provides a pharmaceutical composition for topical administration comprising vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof, wherein (i) the concentration of vancomycin or a pharmaceutically acceptable salt thereof is added to the total composition. When the ratio is 1.0% (w / v) or more, the weight ratio of vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof is 1: 0.02 to 0.1; (ii) when the concentration of vancomycin or its pharmaceutically acceptable salt is less than 1.0% (w / v) relative to the total composition, the weight ratio of vancomycin or its pharmaceutically acceptable salt and dexamethasone phosphate or its pharmaceutically acceptable salt is 1: The pharmaceutical composition for topical administration which is 0.05-0.4 is provided.
반코마이신과 덱사메타손이 중량비에 따라 안정성에 크게 영향을 받는다는 것이 본 발명에 의해 밝혀졌다. 즉, 반코마이신과 덱사메타손을 상기한 바와 같은 특정 중량비로 함유할 경우, 수성 매질에서 침전이나 겔화 등이 발생하지 않는다. 본 발명에 따른 국소 투여용 약학 조성물은 눈, 귀, 코, 피부 등에 적용될 수 있으며, 바람직하게는 귀에 적용되는 이과용 제제(otic formulation)의 형태일 수 있다.It has been found by the present invention that vancomycin and dexamethasone are significantly affected by stability by weight ratio. That is, when vancomycin and dexamethasone are contained in the specific weight ratios described above, precipitation or gelation does not occur in the aqueous medium. The pharmaceutical composition for topical administration according to the present invention may be applied to eyes, ears, nose, skin, and the like, preferably in the form of an otic formulation applied to the ear.
본 발명에 따른 국소투여용 약학 조성물에 있어서, 상기 반코마이신의 약학적으로 허용가능한 염은 염산염, 황산염 등을 포함한 통상의 산부가염일 수 있으며, 바람직하게는 반코마이신 염산염일 수 있다. 상기 반코마이신 또는 그의 약학적으로 허용가능한 염의 농도는 치료학적으로 유효한 함량범위일 수 있으며, 바람직하게는 총 조성물에 대하여 0.3 ∼ 4.0 %(w/v)의 범위일 수 있다. In the pharmaceutical composition for topical administration according to the present invention, the pharmaceutically acceptable salt of vancomycin may be a conventional acid addition salt including hydrochloride, sulfate, and the like, and preferably vancomycin hydrochloride. The concentration of vancomycin or a pharmaceutically acceptable salt thereof may be in a therapeutically effective content range, preferably 0.3 to 4.0% (w / v) relative to the total composition.
또한, 상기 덱사메타손 포스페이트의 약학적으로 허용가능한 염은 덱사메타손 모노소디움 포스페이트, 덱사메타손 디소디움 포스페이트 등의 통상의 금속염일 수 있으며, 바람직하게는 덱사메타손 디소디움 포스페이트일 수 있다. 상기 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염은 상기한 중량비 내에서 치료학적으로 유효한 함량으로 사용될 수 있다. 일 예로서, 반코마이신 또는 그의 염의 농도가 1 %(w/v) 이상일 때에는, 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염은 0.02 ∼ 0.4 %(w/v) 의 농도로 사용될 수 있고; 반코마이신 또는 그의 염의 농도가 1 %(w/v) 미만일 때에는 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염은 0.025 ∼ 0.2 %(w/v)의 농도로 사용될 수 있다. 물론, 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 농도는 상기한 반코마이신 또는 그의 염과의 중량비 범위내에서 결정되어야 한다.In addition, the pharmaceutically acceptable salt of dexamethasone phosphate may be a conventional metal salt such as dexamethasone monosodium phosphate, dexamethasone disodium phosphate and the like, preferably dexamethasone disodium phosphate. The dexamethasone phosphate or a pharmaceutically acceptable salt thereof may be used in a therapeutically effective amount within the above weight ratios. As an example, when the concentration of vancomycin or a salt thereof is at least 1% (w / v), dexamethasone phosphate or a pharmaceutically acceptable salt thereof may be used at a concentration of 0.02 to 0.4% (w / v); When the concentration of vancomycin or its salt is less than 1% (w / v), dexamethasone phosphate or its pharmaceutically acceptable salt may be used at a concentration of 0.025 to 0.2% (w / v). Of course, the concentration of dexamethasone phosphate or a pharmaceutically acceptable salt thereof should be determined within the weight ratio range with vancomycin or salt thereof.
반코마이신과 덱사메타손을 상기한 바와 같이 특정 중량비로 사용하여, 두개의 컴파트먼트로 구성된 재구성 제제(reconstitutable formulation)의 형태로 제제화할 경우, 신속한 재구성(reconstitution)을 달성함으로써 침전이나 겔화 발생 없이 투명한 용액을 얻을 수 있다는 것이 본 발명에 의해 밝혀졌다. 또한, 재구성된 용액이 실온에서도 장기간(예를 들어, 약 1개월) 동안 침전이나 겔화가 발생하지 않고 또한 유연물질의 발생이 최소화됨으로써, 우수한 물리적 및 화학적 안정성을 갖는다는 것이 본 발명에 의해 밝혀졌다. 따라서, 본 발명의 일 구현예에서, 상기 약학 조성물은 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염을 포함하는 제1 컴파트먼트; 및 물(예를 들어, 주사용수)을 포함하는 제2 컴파트먼트로 구성된 단위 투여 형태를 가질 수 있다.When vancomycin and dexamethasone are formulated in the form of a two-compartment reconstitutable formulation using specific weight ratios as described above, a rapid reconstitution is achieved to achieve a clear solution without precipitation or gelation. It has been found by the present invention that it can be obtained. In addition, it has been found by the present invention that the reconstituted solution has excellent physical and chemical stability by not causing precipitation or gelation for a long time (eg, about 1 month) even at room temperature and minimizing the generation of soft substances. . Accordingly, in one embodiment of the present invention, the pharmaceutical composition comprises a first compartment comprising vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof; And a second compartment comprising water (eg water for injection).
상기 제1 컴파트먼트 및 제2 컴파트먼트가 바이알(vial) 또는 플라스틱 용기의 형태를 가질 수 있다. The first compartment and the second compartment may have the form of a vial or plastic container.
상기 제1 컴파트먼트는 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 단순 혼합물(simple mixture)을 함유할 수 있다. 또한, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 함량을 정확히 조절할 수 있도록, 상기 제1 컴파트먼트는 이들의 동결건조물 형태를 함유할 수 있다. 즉, 상기 제1 컴파트먼트는 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염을 포함하는 수용액을 동결건조하여 얻어진 고형물을 포함할 수 있다.The first compartment may contain a simple mixture of vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof. In addition, the first compartment may contain their lyophilized form so that the content of vancomycin or its pharmaceutically acceptable salts and dexamethasone phosphate or its pharmaceutically acceptable salts can be precisely controlled. That is, the first compartment may include a solid obtained by lyophilizing an aqueous solution including vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof.
상기 제2 컴파트먼트는 물(예를 들어, 주사용수)에 추가하여 안정화제로서 글리세린을 추가로 포함할 수 있다. 글리세린은 귀, 눈 또는 코 점막에 사용될 수 있는 비수성 용매이다. 상기 제2 컴파트먼트는 글리세린을 안정화제로서 함유할 수 있으며, 화학적 안정성 및 자극성의 측면에서, 상기 글리세린의 농도는 총 조성물에 대하여 20 %(w/v) 이하, 바람직하게는 0.5 내지 10 %(w/v)의 범위로 사용될 수 있다. The second compartment may further comprise glycerin as a stabilizer in addition to water (eg water for injection). Glycerin is a non-aqueous solvent that can be used on the ear, eye or nasal mucosa. The second compartment may contain glycerin as a stabilizer, and in terms of chemical stability and irritation, the concentration of glycerin is 20% (w / v) or less, preferably 0.5 to 10%, based on the total composition. It can be used in the range of (w / v).
또한, 상기 제2 컴파트먼트는 총 조성물에 대하여 0.001 내지 0.1 %(w/w)의 킬레이트화제 및/또는 0.001 내지 0.18 %(w/v)의 보존제를 추가로 포함할 수 있다. 상기 킬레이트화제가 에데테이트 염[예를 들어, 에데테이트 디소듐(수화물 포함), 에데테이트 트리소듐(수화물 포함), 에데테이트 테트라소듐(수화물 포함) 등] 또는 디에틸렌아민 펜타아세테이트(diethyleneamine pentaacetate)일 수 있으나, 이에 제한되는 것은 아니다. 또한, 상기 보존제는 메틸파라벤, 에틸파라벤, 프로필파라벤(이소프로필파라벤 포함), 이소부틸파라벤 등으로부터 1종 이상 선택될 수 있다.In addition, the second compartment may further comprise 0.001 to 0.1% (w / w) chelating agent and / or 0.001 to 0.18% (w / v) preservative relative to the total composition. The chelating agent may be an edetate salt [for example, edetate disodium (including hydrate), edetate trisodium (including hydrate), edetate tetrasodium (including hydrate), etc.] Or diethyleneamine pentaacetate, but is not limited thereto. In addition, the preservative may be selected from one or more from methyl paraben, ethyl paraben, propyl paraben (including isopropyl paraben), isobutyl paraben and the like.
본 발명의 일 구현예에서, 총 조성물에 대한 하기 함량으로 구성된 국소투여용 약학 조성물이 제공되며, 바람직하게는 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트를 포함하는 바이알과; 글리세린, 에데테이트 디소듐, 메틸파라벤, 프로필파라벤, 및 주사용수를 포함하는 플라스틱 용기로 구성된 국소투여용 약학 조성물이 제공된다:In one embodiment of the invention, there is provided a pharmaceutical composition for topical administration consisting of the following contents relative to the total composition, preferably a vial comprising vancomycin hydrochloride and dexamethasone disodium phosphate; There is provided a pharmaceutical composition for topical administration consisting of a plastic container comprising glycerin, edetate disodium, methylparaben, propylparaben, and water for injection:
본 발명의 다른 구현예에서, 총 조성물에 대한 하기 함량으로 구성된 국소투여용 약학 조성물이 제공되며, 바람직하게는 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트를 포함하는 바이알과; 글리세린, 에데테이트 디소듐, 메틸파라벤, 프로필파라벤, 및 주사용수를 포함하는 플라스틱 용기로 구성된 국소투여용 약학 조성물이 제공된다:In another embodiment of the present invention, there is provided a pharmaceutical composition for topical administration consisting of the following contents relative to the total composition, preferably a vial comprising vancomycin hydrochloride and dexamethasone disodium phosphate; There is provided a pharmaceutical composition for topical administration consisting of a plastic container comprising glycerin, edetate disodium, methylparaben, propylparaben, and water for injection:
본 발명의 또다른 구현예에서, 총 조성물에 대한 하기 함량으로 구성된 국소투여용 약학 조성물이 제공되며, 바람직하게는 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트를 포함하는 바이알과; 글리세린, 에데테이트 디소듐, 메틸파라벤, 프로필파라벤, 및 주사용수를 포함하는 플라스틱 용기로 구성된 국소투여용 약학 조성물이 제공된다:In another embodiment of the invention, there is provided a pharmaceutical composition for topical administration consisting of the following contents relative to the total composition, preferably a vial comprising vancomycin hydrochloride and dexamethasone disodium phosphate; There is provided a pharmaceutical composition for topical administration consisting of a plastic container comprising glycerin, edetate disodium, methylparaben, propylparaben, and water for injection:
본 발명의 또다른 구현예에서, 총 조성물에 대한 하기 함량으로 구성된 국소투여용 약학 조성물이 제공되며, 바람직하게는 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트를 포함하는 바이알과; 글리세린, 에데테이트 디소듐, 메틸파라벤, 프로필파라벤, 및 주사용수를 포함하는 플라스틱 용기로 구성된 국소투여용 약학 조성물이 제공된다:In another embodiment of the invention, there is provided a pharmaceutical composition for topical administration consisting of the following contents relative to the total composition, preferably a vial comprising vancomycin hydrochloride and dexamethasone disodium phosphate; There is provided a pharmaceutical composition for topical administration consisting of a plastic container comprising glycerin, edetate disodium, methylparaben, propylparaben, and water for injection:
이하, 본 발명을 실시예를 통하여 더욱 상세히 설명한다. 그러나, 이들 실시예는 본 발명을 예시하기 위한 것으로, 본 발명이 이들 실시예에 한정되는 것은 아니다.
Hereinafter, the present invention will be described in more detail with reference to examples. However, these examples are for illustrating the present invention, and the present invention is not limited to these examples.
실시예Example 1. 약학 조성물의 제조 1. Preparation of Pharmaceutical Composition
하기 표 1의 성분 및 함량에 따라 반코마이신 염산염과 덱사메타손 디소듐 포스페이트를 포함하는 국소투여용 제제를 제조하였다. 하기 표 1의 함량은 제1 컴파트먼트 및 제2 컴파트먼트를 혼합하여 얻어진 용액을 기준으로 한 함량[%(w/v)]을 의미한다.According to the ingredients and contents of Table 1, a formulation for topical administration containing vancomycin hydrochloride and dexamethasone disodium phosphate was prepared. The content in Table 1 below means the content [% (w / v)] based on the solution obtained by mixing the first compartment and the second compartment.
<제1 컴파트먼트의 제조>≪ Preparation of first compartment >
주사용수 900 mL에 반코마이신 염산염을 완전히 용해시켰다. 얻어진 용액을 교반하면서, 덱사메타손 디소디움 포스페이트를 넣고 완전히 용해시켰다. 주사용수로 1,000 mL이 되도록 조절한 다음, 약 30분간 교반하였다. 얻어진 용액을 무균 여과한 후, 멸균된 바이알에 분주한 후 동결건조하였다. 각각의 바이알을 고무 마개(Rubber stopper)로 밀봉하였다.Vancomycin hydrochloride was completely dissolved in 900 mL of water for injection. While stirring the obtained solution, dexamethasone disodium phosphate was added and completely dissolved. The solution was adjusted to 1,000 mL with the injection water, and stirred for about 30 minutes. The resulting solution was aseptically filtered, dispensed into sterile vials, and lyophilized. Each vial was sealed with a rubber stopper.
<제2 바이알의 제조><Production of Second Vial>
주사용수 900 mL를 약 90℃로 가온한 후, 프로필파라벤 및 메틸파라벤을 용해시켰다. 얻어진 용액을 실온으로 냉각한 후, 에데트산 나트륨 수화물 및 글리세린을 용해시켰다. 주사용수로 1,000 mL이 되도록 조절한 다음, 약 30분간 교반하였다. 얻어진 용액을 무균 여과한 후, 멸균된 바이알에 분주한 후, 플리스틱 용기에 분주한 후, 멸균된 Sealing cap으로 닫았다.
After 900 mL of water for injection was heated to about 90 캜, propylparaben and methylparaben were dissolved. After cooling the obtained solution to room temperature, sodium edetate hydrate and glycerin were dissolved. The solution was adjusted to 1,000 mL with the injection water, and stirred for about 30 minutes. The resulting solution was sterile filtered, then dispensed into sterilized vials, then dispensed into a plastic container and then closed with a sterile sealing cap.
실시예Example 2. 물리적 안정성 평가 2. Physical stability assessment
주사용수에 하기 표 2에서와 같이 소정의 농도로 반코마이신 염산염을 용해시켰다. 얻어진 각각의 용액을 교반하면서, 덱사메타손 디소디움 포스페이트를 다양한 농도(표 2 참조)로 첨가한 다음, 침전물의 발생을 측정하였다. 그 결과는 하기 표 2와 같다. 표 2에서 '반코마이신'은 반코마이신 염산염을 지칭하며, '덱사메타손'은 덱사메타손 디소디움 포스페이트를 지칭한다. 또한, '%'는 %(w/v)을 의미하며, O는 투명한 용액, X는 침전물 발생을 의미한다.Vancomycin hydrochloride was dissolved in water for injection at a predetermined concentration as shown in Table 2 below. While each solution obtained was stirred, dexamethasone disodium phosphate was added at various concentrations (see Table 2), and then the occurrence of precipitate was measured. The results are shown in Table 2 below. In Table 2 'vancomycin' refers to vancomycin hydrochloride and 'dexamethason' refers to dexamethasone disodium phosphate. In addition, '%' means% (w / v), O means a transparent solution, X means sediment generation.
상기 표 2의 결과로부터, 반코마이신 염산염의 농도가 0.5 %(w/v) 이상일 경우, 덱사메타손 디소디움 포스페이트의 농도에 따라 침전물이 발생하였음을 알 수 있다. 또한, 반코마이신 염산염의 농도가 치료학적으로 유효한 농도 범위인 약 4.0 %(w/v) 이하, 예를 들어 1.0 내지 4.0 %(w/v)일 경우, 물리적 안정성은 반코마이신 염산염과 덱사메타손 디소디움 포스페이트의 중량비가 1 : 0.02 ∼ 0.1 의 범위에서 확보될 수 있음을 알 수 있다. 또한, 반코마이신 염산염의 농도가 1.0 %(w/v) 미만일 경우, 물리적 안정성은 반코마이신 염산염과 덱사메타손 디소디움 포스페이트의 중량비가 1 : 0.05 ∼ 0.4 의 범위에서 확보될 수 있음을 알 수 있다.
From the results of Table 2, when the concentration of vancomycin hydrochloride is 0.5% (w / v) or more, it can be seen that the precipitate occurred according to the concentration of dexamethasone disodium phosphate. In addition, when the concentration of vancomycin hydrochloride is less than or equal to about 4.0% (w / v) in the therapeutically effective concentration range, for example 1.0 to 4.0% (w / v), the physical stability of vancomycin hydrochloride and dexamethasone disodium phosphate It can be seen that the weight ratio can be ensured in the range of 1: 0.02 to 0.1. In addition, when the concentration of vancomycin hydrochloride is less than 1.0% (w / v), it can be seen that the physical stability can be ensured in the weight ratio of vancomycin hydrochloride and dexamethasone disodium phosphate in the range of 1: 0.05 to 0.4.
실시예Example 3. 화학적 안정성 평가 3. Chemical Stability Assessment
(1) 화학적 안정성 평가 [반코마이신 염산염의 농도: 1.0 %(w/v)](1) Chemical stability evaluation [concentration of vancomycin hydrochloride: 1.0% (w / v)]
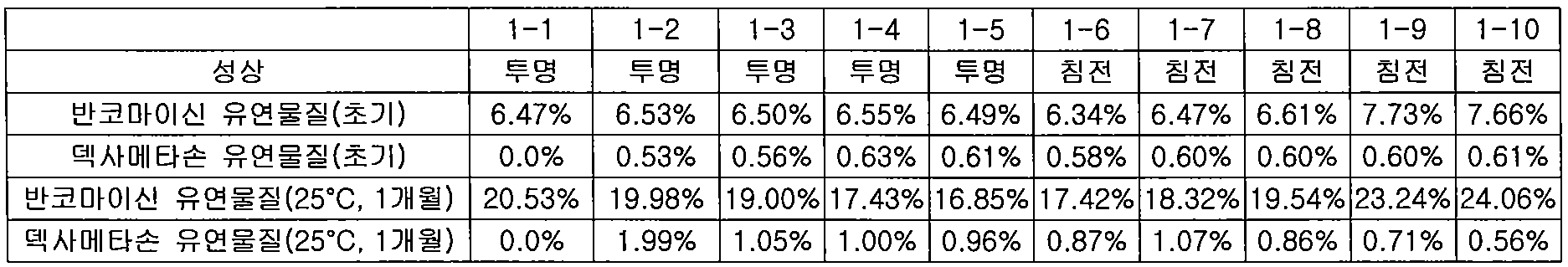
하기 표 3에 나타낸 바와 같이, 반코마이신 염산염의 농도를 1.0 %(w/v)로 고정하고, 덱사메타손 디소디움 포스페이트의 함량을 조절하여, 실시예 1과 동일한 방법으로 제1 컴파트먼트를 제조하였다. 얻어진 각각의 제1 컴파트먼트에 주사용수를 가하여 용해시켰다. 표 3에서 각각의 농도는 주사용수를 가했을 때 얻어진 최종 제제의 농도를 나타낸다. 각각의 용액의 초기 유연물질의 함량을 측정한 다음, 실온(25℃)에서 1개월 동안 보관 후 유연물질의 함량을 다시 측정하였다. 그 결과는 하기 표 4와 같다. As shown in Table 3 below, the concentration of vancomycin hydrochloride was fixed at 1.0% (w / v), and the content of dexamethasone disodium phosphate was adjusted to prepare a first compartment in the same manner as in Example 1. Each of the obtained first compartments was dissolved by adding water for injection. Each concentration in Table 3 represents the concentration of the final formulation obtained when water for injection is added. The content of the initial flexible material of each solution was measured, and then stored for 1 month at room temperature (25 ° C.), and the content of the flexible material was measured again. The results are shown in Table 4 below.
(2) 화학적 안정성 평가 [반코마이신 염산염의 농도: 2.5 %(w/v)](2) chemical stability evaluation [concentration of vancomycin hydrochloride: 2.5% (w / v)]
하기 표 5에 나타낸 바와 같이, 반코마이신 염산염의 농도를 2.5 %(w/v)로 고정하고, 덱사메타손 디소디움 포스페이트의 함량을 조절하여, 실시예 1과 동일한 방법으로 제1 컴파트먼트를 제조하였다. 표 5에서 각각의 농도는 주사용수를 가했을 때 얻어진 최종 제제의 농도를 나타낸다. 각각의 용액에 대하여 상기 (1)과 동일한 방법으로 화학적 안정성을 평가하였다. 그 결과는 하기 표 6과 같다. As shown in Table 5 below, the concentration of vancomycin hydrochloride was fixed at 2.5% (w / v), and the content of dexamethasone disodium phosphate was adjusted to prepare a first compartment in the same manner as in Example 1. Each concentration in Table 5 represents the concentration of the final formulation obtained when water for injection is added. For each solution, chemical stability was evaluated in the same manner as in (1) above. The results are shown in Table 6 below.
(3) 화학적 안정성 평가 [반코마이신 염산염의 농도: 4.0 %(w/v)](3) Chemical stability evaluation [concentration of vancomycin hydrochloride: 4.0% (w / v)]
하기 표 7에 나타낸 바와 같이, 반코마이신 염산염의 농도를 4.0 %(w/v)로 고정하고, 덱사메타손 디소디움 포스페이트의 함량을 조절하여, 실시예 1과 동일한 방법으로 제1 컴파트먼트를 제조하였다. 표 7에서 각각의 농도는 주사용수를 가했을 때 얻어진 최종 제제의 농도를 나타낸다. 각각의 용액에 대하여 상기 (1)과 동일한 방법으로 화학적 안정성을 평가하였다. 그 결과는 하기 표 8과 같다. As shown in Table 7 below, the concentration of vancomycin hydrochloride was fixed at 4.0% (w / v), and the content of dexamethasone disodium phosphate was adjusted to prepare a first compartment in the same manner as in Example 1. Each concentration in Table 7 represents the concentration of the final formulation obtained when water for injection is added. For each solution, chemical stability was evaluated in the same manner as in (1) above. The results are shown in Table 8 below.
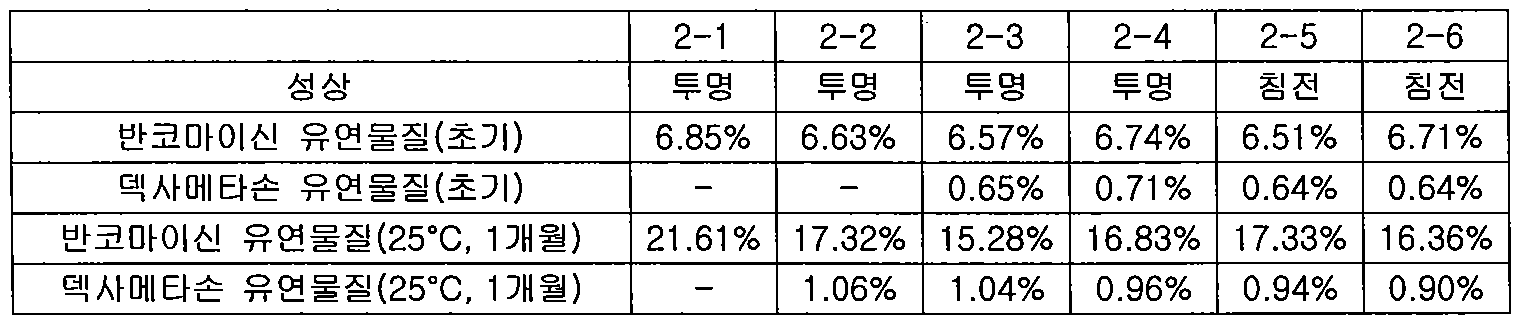
(4) 화학적 안정성 평가 [반코마이신 염산염의 농도: 0.3 %(w/v)](4) Chemical stability evaluation [concentration of vancomycin hydrochloride: 0.3% (w / v)]
하기 표 9에 나타낸 바와 같이, 반코마이신 염산염의 농도를 4.0 %(w/v)로 고정하고, 덱사메타손 디소디움 포스페이트의 함량을 조절하여, 실시예 1과 동일한 방법으로 제1 컴파트먼트를 제조하였다. 표 9에서 각각의 농도는 주사용수를 가했을 때 얻어진 최종 제제의 농도를 나타낸다. 각각의 용액에 대하여 상기 (1)과 동일한 방법으로 화학적 안정성을 평가하였다. 그 결과는 하기 표 10과 같다. As shown in Table 9 below, the concentration of vancomycin hydrochloride was fixed at 4.0% (w / v), and the content of dexamethasone disodium phosphate was adjusted to prepare a first compartment in the same manner as in Example 1. Each concentration in Table 9 represents the concentration of the final formulation obtained when water for injection is added. For each solution, chemical stability was evaluated in the same manner as in (1) above. The results are shown in Table 10 below.
(5) 화학적 안정성 평가 [반코마이신 염산염의 농도: 0.5 %(w/v)](5) Chemical stability evaluation [concentration of vancomycin hydrochloride: 0.5% (w / v)]
하기 표 11에 나타낸 바와 같이, 반코마이신 염산염의 농도를 0.5 %(w/v)로 고정하고, 덱사메타손 디소디움 포스페이트의 함량을 조절하여, 실시예 1과 동일한 방법으로 제1 컴파트먼트를 제조하였다. 표 11에서 각각의 농도는 주사용수를 가했을 때 얻어진 최종 제제의 농도를 나타낸다. 각각의 용액에 대하여 상기 (1)과 동일한 방법으로 화학적 안정성을 평가하였다. 그 결과는 하기 표 12와 같다. As shown in Table 11 below, the concentration of vancomycin hydrochloride was fixed at 0.5% (w / v), and the content of dexamethasone disodium phosphate was adjusted to prepare a first compartment in the same manner as in Example 1. Each concentration in Table 11 represents the concentration of the final formulation obtained when water for injection is added. For each solution, chemical stability was evaluated in the same manner as in (1) above. The results are shown in Table 12 below.
상기 표 4, 표 6, 및 표 8의 결과로부터, 반코마이신 염산염의 농도가 1.0 %(w/v) 이상일 경우, 덱사메타손 디소디움 포스페이트의 농도를 0.1 %(w/v) 까지 증가시켰을 때, 반코마이신 염산염의 유연물질 발생이 감소하였음을 알 수 있다. 특히, 반코마이신 염산염을 단독으로 사용한 경우에는 허용되는 유연물질 기준에 부적합하였으나, 덱사메타손 디소디움 포스페이트를 특정 범위로 첨가할 경우 반코마이신 염산염의 유연물질 발생이 감소한다는 것은 매우 놀라운 것이다. 반코마이신 및 덱사메타손에 대하여 허용되는 유연물질의 기준은 각각 20.0% 및 2.0% 이다. 따라서, 상기 결과로부터 알 수 있는 바와 같이, 반코마이신 염산염의 농도가 1.0 %(w/v) 이상일 때, 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트의 중량비는 1 : 0.02 ∼ 0.1 의 범위가 물리적 및 화학적 안정성 측면에서 적합하다.From the results of Tables 4, 6, and 8, when the concentration of vancomycin hydrochloride is 1.0% (w / v) or more, when the concentration of dexamethasone disodium phosphate is increased to 0.1% (w / v), vancomycin hydrochloride It can be seen that the occurrence of the flexible substance of. Particularly, when vancomycin hydrochloride alone was used, it was unsuitable to the acceptable softener standard. However, it is surprising that the addition of dexamethasone disodium phosphate reduces the formation of the softener of vancomycin hydrochloride. Acceptable baselines for vancomycin and dexamethasone are 20.0% and 2.0%, respectively. Therefore, as can be seen from the above results, when the concentration of vancomycin hydrochloride is 1.0% (w / v) or more, the weight ratio of vancomycin hydrochloride and dexamethasone disodium phosphate ranges from 1: 0.02 to 0.1 in terms of physical and chemical stability. Suitable.
또한, 상기 표 10 및 표 12의 결과로부터, 덱사메타손 디소디움 포스페이트의 농도를 특정 범위로 증가시켰을 때, 반코마이신 염산염의 유연물질 발생이 감소하였음을 알 수 있다. 또한, 상기 결과로부터 알 수 있는 바와 같이, 반코마이신 염산염의 농도가 1.0 %(w/v) 미만일 때, 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트의 중량비는 1 : 0.05 ∼ 0.4 의 범위가 물리적 및 화학적 안정성 측면에서 적합하다.
In addition, it can be seen from the results of Tables 10 and 12 that when the concentration of dexamethasone disodium phosphate was increased to a specific range, the generation of analogues of vancomycin hydrochloride decreased. In addition, as can be seen from the above results, when the concentration of vancomycin hydrochloride is less than 1.0% (w / v), the weight ratio of vancomycin hydrochloride and dexamethasone disodium phosphate ranges from 1: 0.05 to 0.4 in terms of physical and chemical stability. Suitable.
실시예Example 4. 안정화제(글리세린)의 평가 4. Evaluation of Stabilizers (Glycerin)
(1) 안정화제의 효능 및 재구성(reconstituion) 평가(1) Evaluation of efficacy and reconstituion of stabilizers
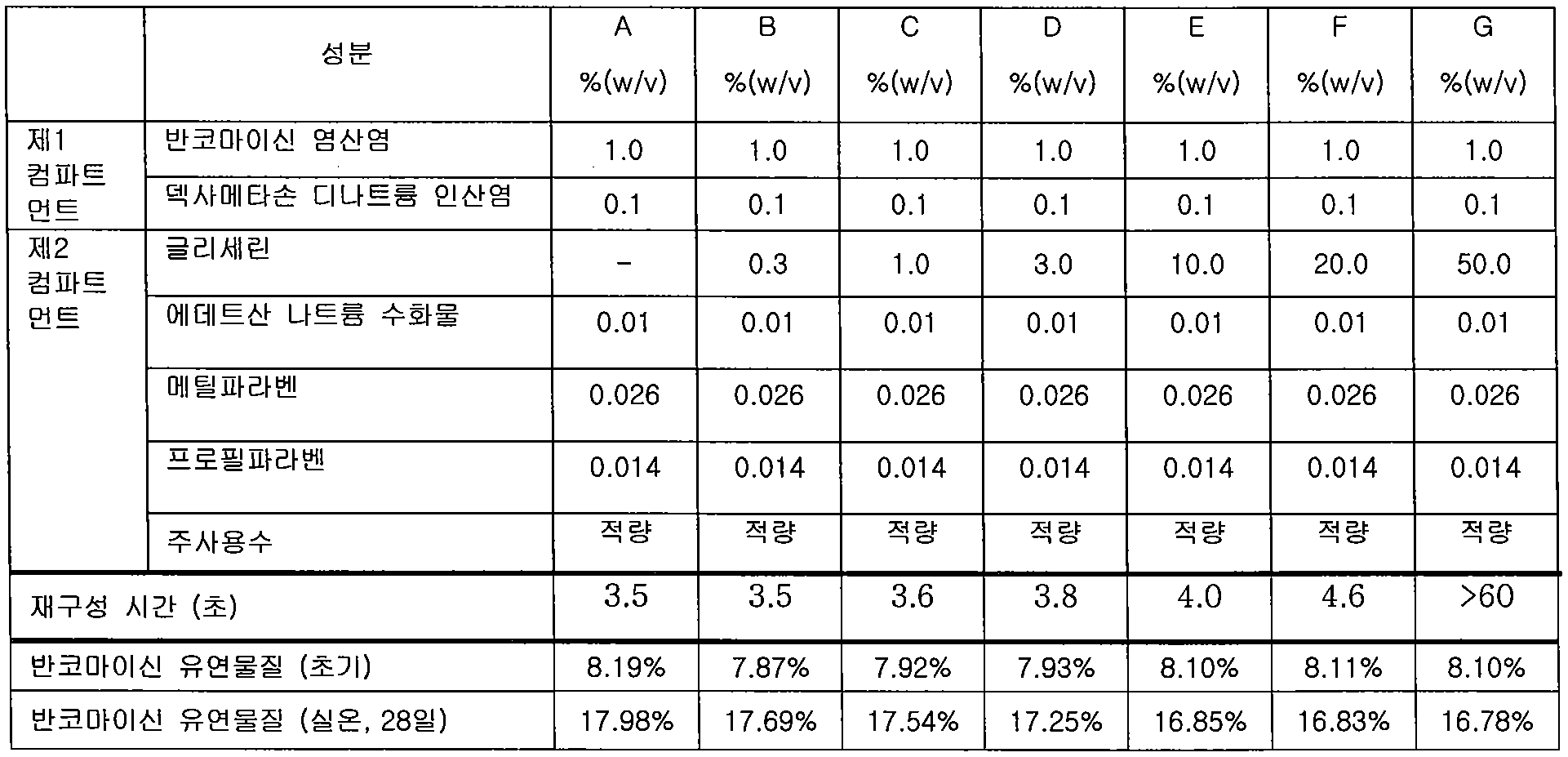
하기 표 13에 따라 글리세린의 농도를 변화시킨 것을 제외하고는, 실시예 1과 동일한 방법으로 제1 컴파트먼트 및 제2 컴파트먼트를 제조하였다. 각각의 제1 컴파트먼트 및 제2 컴파트먼트를 서로 혼합하여 용액으로 재구성하는데 소요되는 시간 즉, 재구성 시간(reconstitution time)을 측정하였으며, 얻어진 각각의 용액에 대하여 반코마이신의 유연물질 변화를 측정하였다. 그 결과는 하기 표 13과 같다.A first compartment and a second compartment were manufactured in the same manner as in Example 1, except that the concentration of glycerin was changed according to Table 13 below. The time taken to reconstitute each of the first and second compartments into a solution, ie, the reconstitution time, was measured, and the change in the soft matter of vancomycin was measured for each of the obtained solutions. . The results are shown in Table 13 below.
상기 표 13의 결과로부터 알 수 있는 바와 같이, 글리세린의 농도가 높아질수록 화학적 안정성은 향상되었다(A∼F). 그러나, 글리세린의 농도가 20 %(w/v)를 초과할 경우, 화학적 안정성에 유의성 있는 영향을 미치지 못한 반면, 재구성 시간은 현저하게 증가하였다. As can be seen from the results in Table 13, the higher the concentration of glycerin, the better the chemical stability (A to F). However, when the concentration of glycerin exceeded 20% (w / v), the reconstruction time increased markedly while not having a significant effect on chemical stability.
(2) 자극성 평가(2) stimulus evaluation
하기 표 14에 따라, 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트 농도를 각각 1.0 %(w/v) 및 0.1 %(w/v)으로 고정하고, 글리세린의 농도에 따른 자극성을 평가하였다. 각각의 농도는 주사용수 중의 농도를 나타낸다. 단, G8은 주사용수를 사용하지 않고, 글리세린을 용매로 사용하여 반코마이신 염산염 및 덱사메타손 디소디움 포스페이트를 각각 1.0 %(w/v) 및 0.1 %(w/v)로 용해시켰다. 상기 자극성은 비글독의 안구를 이용하여 평가하였으며, 시험군 당 마리수는 3마리씩 사용하였다. 투여는 좌안 및 우안 각각 0.1 mL씩 투여하였다. 좌안에는 비교군으로 주사용수를 점적하였고, 우안에는 시험물질을 점적하였다. 안구 자극의 정도에 따라 눈의 깜빡임 횟수로 점수화하였으며, 점수가 높을수록 자극이 높은 것을 의미한다. 그 결과는 표 15와 같다.According to Table 14 below, the vancomycin hydrochloride and dexamethasone disodium phosphate concentrations were fixed at 1.0% (w / v) and 0.1% (w / v), respectively, and the stimulation according to the concentration of glycerin was evaluated. Each concentration represents a concentration in water for injection. However, G8 was dissolved in vancomycin hydrochloride and dexamethasone disodium phosphate at 1.0% (w / v) and 0.1% (w / v), respectively, using glycerin as a solvent without using water for injection. The irritation was evaluated using eye of Beagledog, and the number of animals per test group was used three. Administration was performed by 0.1 mL each of the left eye and the right eye. In the left eye, water for injection was added to the control group, and for the right eye, test substance was instilled. The number of eye blinks was scored according to the degree of eye irritation, and the higher the score, the higher the stimulus. The results are shown in Table 15.
상기 표 15의 결과로부터 알 수 있는 바와 같이, 글리세린의 자극성이 증가하였으며, 글리세린의 농도가 20 %(w/v)를 초과할 경우에는 자극성이 급격히 증가하였다. As can be seen from the results of Table 15, the stimulation of glycerin was increased, and when the concentration of glycerin exceeds 20% (w / v), the irritation was rapidly increased.
따라서, 상기 결과로부터 글리세린의 농도는 20 %(w/v) 이하가 적합함을 알 수 있다.
Therefore, it can be seen from the above results that the concentration of glycerin is suitably 20% (w / v) or less.
Claims (21)
(i) 반코마이신 또는 그의 약학적으로 허용가능한 염의 농도가 총 조성물에 대하여 1.0 %(w/v) 이상일 때, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 중량비가 1 : 0.02 ∼ 0.1이고;
(ii) 반코마이신 또는 그의 약학적으로 허용가능한 염의 농도가 총 조성물에 대하여 1.0 %(w/v) 미만일 때, 반코마이신 또는 그의 약학적으로 허용가능한 염 및 덱사메타손 포스페이트 또는 그의 약학적으로 허용가능한 염의 중량비가 1 : 0.05 ∼ 0.4인
국소투여용 약학 조성물.A pharmaceutical composition for topical administration comprising vancomycin or a pharmaceutically acceptable salt thereof and dexamethasone phosphate or a pharmaceutically acceptable salt thereof,
(i) when the concentration of vancomycin or its pharmaceutically acceptable salt is at least 1.0% (w / v) relative to the total composition, the weight ratio of vancomycin or its pharmaceutically acceptable salt and dexamethasone phosphate or its pharmaceutically acceptable salt is 1: 0.02 to 0.1;
(ii) when the concentration of vancomycin or its pharmaceutically acceptable salt is less than 1.0% (w / v) relative to the total composition, the weight ratio of vancomycin or its pharmaceutically acceptable salt and dexamethasone phosphate or its pharmaceutically acceptable salt is 1: 0.05 to 0.4
Pharmaceutical composition for topical administration.
A pharmaceutical composition for topical administration consisting of the following contents relative to the total composition:
A pharmaceutical composition for topical administration consisting of the following contents relative to the total composition:
A pharmaceutical composition for topical administration consisting of the following contents relative to the total composition:
A pharmaceutical composition for topical administration consisting of the following contents relative to the total composition:
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120076674A KR20140009819A (en) | 2012-07-13 | 2012-07-13 | Pharmaceutical composition for topical administration comprising vancomycin or its salt and dexamethasone phosphate or its salt |
| PCT/KR2013/006111 WO2014010924A1 (en) | 2012-07-13 | 2013-07-10 | Pharmaceutical composition for topical administration comprising vancomycin or its salt and dexamethasone phosphate or its salt |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120076674A KR20140009819A (en) | 2012-07-13 | 2012-07-13 | Pharmaceutical composition for topical administration comprising vancomycin or its salt and dexamethasone phosphate or its salt |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140009819A true KR20140009819A (en) | 2014-01-23 |
Family
ID=49916300
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020120076674A Withdrawn KR20140009819A (en) | 2012-07-13 | 2012-07-13 | Pharmaceutical composition for topical administration comprising vancomycin or its salt and dexamethasone phosphate or its salt |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR20140009819A (en) |
| WO (1) | WO2014010924A1 (en) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015138983A1 (en) | 2014-03-14 | 2015-09-17 | Cutispharma, Inc. | Composition and method for vancomycin oral liquid |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6239113B1 (en) * | 1999-03-31 | 2001-05-29 | Insite Vision, Incorporated | Topical treatment or prevention of ocular infections |
| US20040151765A1 (en) * | 2001-09-18 | 2004-08-05 | Ritchie Branson W. | Methods and compositions for wound management |
| US8216609B2 (en) * | 2002-08-05 | 2012-07-10 | Torrent Pharmaceuticals Limited | Modified release composition of highly soluble drugs |
| US8784852B2 (en) * | 2009-02-27 | 2014-07-22 | Audrey Kunin | Topical skin care composition |
-
2012
- 2012-07-13 KR KR1020120076674A patent/KR20140009819A/en not_active Withdrawn
-
2013
- 2013-07-10 WO PCT/KR2013/006111 patent/WO2014010924A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| WO2014010924A1 (en) | 2014-01-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2929368T3 (en) | Aqueous composition containing atropine | |
| AU2009223649B2 (en) | Low viscosity, highly flocculated triamcinolone acetonide suspensions for intravitreal injection | |
| DE2708152A1 (en) | PHARMACEUTICAL CARRIERS AND THEIR USE | |
| KR20180004164A (en) | Aqueous suspensions containing nanoparticles of glucocorticosteroids | |
| JP2025170781A (en) | Stable peptide compositions | |
| US9682099B2 (en) | Compositions and methods for treating joints | |
| KR20170008252A (en) | Formulations of cyclophosphamide liquid concentrate | |
| TW202122094A (en) | Diquafosol or salt thereof, and aqueous ophthalmic composition containing polyvinylpyrrolidone | |
| DE60305687T2 (en) | Aqueous injectable suspensions for animals containing florfenicol | |
| KR20170103974A (en) | Pharmaceutical formulation | |
| CN104814924A (en) | Brinzolamide liposome eye preparation and preparation method thereof | |
| CN101969926A (en) | Topotecan ready to use solutions | |
| ES3031815T3 (en) | Antimicrobial compositions containing polyquaternium | |
| CN108601730A (en) | The preparation of vancomycin | |
| BRPI0721255B1 (en) | olopatadine compositions for topical nasal administration | |
| KR20140009819A (en) | Pharmaceutical composition for topical administration comprising vancomycin or its salt and dexamethasone phosphate or its salt | |
| JPH11302197A (en) | Hyaluronic acid-stabilizing composition | |
| ES2617235T3 (en) | Use of pidotimod to treat psoriasis | |
| CN108136036A (en) | Novel ophthalmic composition comprising Rebamipide and preparation method thereof | |
| ES3034195T3 (en) | Xanthan-based ophthalmic topical formulations with a reduced dosage regimen | |
| ES2731754T3 (en) | Ophthalmic pharmaceutical composition containing a carbonic anhydrase inhibitor and method for preparing it | |
| KR101816798B1 (en) | Pharmaceutical composition for topical administration comprising piperacillin or its salt, tazobactam or its salt and dexamethasone phosphate or its salt | |
| BRPI0616449A2 (en) | ophthalmic composition, combined preparation, use of said composition and use of a film-forming agent | |
| SA90110074B1 (en) | Pharmaceutical compositions containing an aqueous solution of a pyranoquinoline derivative | |
| EP0893990A1 (en) | Ophthalmological composition of the type which undergoes liquid-gel phase transition |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20120713 |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |