KR20110091777A - 폴리펩티드, 항체 가변 도메인 및 길항제 - Google Patents
폴리펩티드, 항체 가변 도메인 및 길항제 Download PDFInfo
- Publication number
- KR20110091777A KR20110091777A KR1020117014479A KR20117014479A KR20110091777A KR 20110091777 A KR20110091777 A KR 20110091777A KR 1020117014479 A KR1020117014479 A KR 1020117014479A KR 20117014479 A KR20117014479 A KR 20117014479A KR 20110091777 A KR20110091777 A KR 20110091777A
- Authority
- KR
- South Korea
- Prior art keywords
- seq
- amino acid
- acid sequence
- composition
- variable domain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/241—Tumor Necrosis Factors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
- C07K16/245—IL-1
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/569—Single domain, e.g. dAb, sdAb, VHH, VNAR or nanobody®
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Ophthalmology & Optometry (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Epidemiology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
본 발명은 면역글로불린 단일 가변 도메인(dAb), 예를 들어, 프로테아제 내성인 dAb, 및 안구 전달을 위한 상기 dAb를 포함하는 제형, 및 조성물, 및 안구 질병 및 질환을 치료하기 위한 이들의 용도에 관한 것이다.
Description
본 발명은 면역글로불린 단일 가변 도메인(dAb), 예를 들어, 프로테아제 내성인 dAb, 및 상기 dAb를 포함하는 안구 전달용 제형 및 조성물, 및 안구 질병 및 질환을 치료하기 위한 이들의 용도에 관한 것이다.
발명의 배경
치료제의 안구로의 전달의 비효율성으로 인해 안구 질병 및 질환을 치료하는 것은 어렵다. 약물이 안구로 전달되는 경우, 이는 매우 빈번히 안구 조직으로부터 극도로 신속히 청소된다. 또한, 치료제가 안구로 국소적으로 전달되는 경우, 이들은 안구의 후부 세그먼트(망막, 유리체막 및 맥락막)에 도달하지 않을 수 있는 문제점이 존재한다. 그러므로, 많은 후부 세그먼트 안구 질환은 정맥내 또는 유리체내 투여에 의해 약물을 투여함으로써 치료되었다. AMD, 녹내장, 당뇨망막병증과 같은 많은 상기 질병은 최적으로 치료될 수 없다. 따라서, 안구 전달에 적합할 수 있고, 안구 질병 및 질환을 치료하거나 예방할 수 있는 추가 작용제를 제공할 필요가 존재한다.
폴리펩티드 및 펩티드는 점차 약제, 치료제 및 진단제로 사용하기 위한 중요한 작용제가 되고 있다. 그러나, 특정한 생체내 환경, 예를 들어, 안구, 및 특정한 생리학적 상태, 예를 들어, 암 및 염증 상태에서, 조직, 기관 또는 동물에 존재하는 프로테아제의 양이 증가할 수 있다. 이러한 프로테아제의 증가는 내생 단백질, 및 질병을 치료하기 위해 투여되는 치료 펩티드, 폴리펩티드 및 단백질의 분해 및 불활성화를 촉진시킬 수 있다. 따라서, 생체내 용도(예를 들어, 질병 치료, 진단 또는 예방에서의 용도)에 잠재성을 갖는 일부 작용제가 단지 제한된 효능을 가지는데, 이는 이들이 프로테아제에 의해 신속히 분해되고 비활성화되기 때문이다.
프로테아제 내성 폴리펩티드는 여러 이점을 제공한다. 예를 들어, 프로테아제 내성 폴리펩티드는 프로테아제 민감성 작용제보다 길게 생체내에서 활성으로 유지되고, 이에 따라 생물학적 효과를 발생시키기에 충분한 기간 동안 기능성인 채로 유지된다.
VEGF는 이의 일차 전사의 대안적 스플라이싱(splicing)으로 인해 여러 대안적 형태로 존재하는 분비성의 헤파린-결합 동종이합체 당단백질이다(Leung et al., 1989, Science 246: 1306). VEGF는 또한 염증에서의 중요한 과정인 혈관 누출을 유도하는 능력으로 인해 혈관 투과 인자(VPF)로 공지되어 있다.
안구에서, VEGF 및 VEGF-수용체는 맥락막 및 망막 혈관신생 둘 모두를 자극하고, 상기 혈관의 혈관 투과성을 조절하는 것으로 공지되어 있다. 상기 두 특징은 다수의 망막 염증 질환, 혈관병증 및 황반병증으로부터 발생하는 망막 손상 및 이에 수반하는 시각적인 예민함의 악화에 기여한다. 기존의 VEGF 활성 또는 VEGF-수용체 활성을 조절하려는 시도는 동물 모델 및 인간 질병 둘 모두에서 혈관 투과성을 효과적으로 조절하는 것으로 밝혀졌다(Gragoudas et al., 2004: N. Engl. J. Med 351:2805).
현재 이용가능한 치료제를 이용하여 VEGF를 표적화하는 것은 모든 환자에서 효과적이진 않다. 따라서, VEGF에 의해 매개되는 병리학적 질환, 예를 들어, 혈관 증식 질병(예를 들어, 연령 관련 황반 변성(AMD))을 치료하기 위한 개선된 작용제가 여전히 필요하다.
TNF-α(종양 괴사 인자-α)는 다수의 안과 염증 질환, 예를 들어, 포도막염 및 AMD, 및 염증 성분이 존재하는 망막 혈관병증의 발생과 관련된 전염증성 사이토카인이다. 연령 관련 황반 질병과 관련된 맥락막 신생혈관 병변의 발생은 관련 염증 성분을 갖는 것으로 입증되었다. 상기 관련 염증 성분의 효과적인 조절이 인간 질병에 영향을 줄 수 있는 맥락막 신생혈관 병변 및 혈관 투과성의 발달에 직접적으로 영향을 주는 것으로 입증되었다. 인간 AMD 환자의 최근의 증거는 항-TNFα 치료제의 사용이 항-VEGF 요법에 반응하지 않는 환자의 질병에 영향을 미칠 수 있는 것을 암시하였다(Theodossiadis et al., 2009: Am. J. Ophthalmol. 147: 825-830).
인터루킨 1(IL-1)은 여러 유형의 세포에 대해 생물학적 효과를 갖는 면역 반응의 중요한 매개체이다. 인터루킨 1은 2개의 수용체, IL-1에 결합시 세포로 신호를 전달하는 인터루킨 1 수용체 타입 1(IL-1R1, CD121a, p80), 및 IL-1에 결합시 신호를 전달하지 않는 인터루킨 1 수용체 타입 2(IL-1R1, CDw121b)에 결합하고, IL-1의 내생 조절인자로 작용한다. IL-1과 IL-1R1의 상호작용을 조절하는 또 다른 내생 단백질은 인터루킨 1 수용체 길항제(IL-1ra)이다. IL-1ra는 IL-1R1에 결합하나, IL-1R1이 신호를 전달하도록 활성화시키지는 않는다.
IL-1(예를 들어, IL-1α 또는 IL-1β) 결합시의 IL-1R1을 통해 전달된 신호는 병원성일 수 있는 광범위한 생물학적 활성을 유도한다. 예를 들어, IL-1의 결합시의 IL-1R1을 통해 전달된 신호는 국소 또는 전신 염증, 및 추가 염증 매개체(예를 들어, IL-6, IL-8, TNF)의 동화를 발생시킬 수 있다. 따라서, IL-1과 IL-1R1의 상호작용은 안구 질병의 발병기전과 관련이 있다.
인터루킨 1 수용체 타입 1(IL-1R1)에 결합하고, 이의 활성을 중화시키는 특정 작용제(예를 들어, IL-1ra)가 특정 염증 질환에 대한 효과적인 치료제인 것으로 증명되었다.
발명의 개요
제 1 양태에서, 본 발명은, 예를 들어, 전달 부위에서 요망되는 표적 분자(예를 들어, VEGF, IL-1, 또는 TNF-α)에 결합할 수 있는 면역글로불린 단일 가변 도메인(또는 dAb)을 포함하거나 이로 구성되는 안구 투여용의 조성물을 제공한다.
본 발명은 또한 안구 질병 또는 질환, 예를 들어, 연령 관련 황반 변성(AMD), 포도막염, 녹내장, 안구 건조, 당뇨망막병증, 및 당뇨 황반 부종을 치료하거나, 예방하거나, 진단하는데 사용하기 위한, 요망되는 표적 분자(예를 들어, VEGF, IL-1, 또는 TNF-α, TNFR1, TNFR2, IL-1r)에 결합할 수 있는 면역글로불린 단일 가변 도메인(또는 dAb)를 포함하거나 이로 구성되는 조성물을 제공한다.
한 구체예에서, 면역글로불린 단일 가변 도메인은 프로테아제 내성, 예를 들어, 하기 중 하나 이상에 대해 내성일 수 있다: 세린 프로테아제, 시스테인 프로테아제, 아스파테이트 프로테아제, 티올 프로테아제, 기질 금속단백분해효소, 카르복시펩티다제(예를 들어, 카르복시펩티다제 A, 카르복시펩티다제 B), 트립신, 키모트립신, 펩신, 파파인, 엘라스타제, 류코자임, 판크레아틴, 트롬빈, 플라스민, 카텝신(예를 들어, 카텝신 G), 프로테이나제(예를 들어, 프로테이나제 1, 프로테이나제 2, 프로테이나제 3), 써몰리신(thermolysin), 키모신, 엔테로펩티다제, 카스파제(예를 들어, 카스파제 1, 카스파제 2, 카스파제 4, 카스파제 5, 카스파제 9, 카스파제 12, 카스파제 13), 칼파인, 피카인, 클로스트리파인, 악티니다인, 브로멜라인, 및 세파라제. 특정 구체예에서, 프로테아제는 트립신, 엘라스타제 또는 류코자임이다. 이러한 프로테아제 내성 폴리펩티드는 안구와 같은 생체내 프로테아제 풍부 환경으로의 전달에 특히 적합하다. 프로테아제는 또한 생물학적 추출물, 생물학적 균질화물 또는 생물학적 제조물에 의해 제공될 수 있다. 한 구체예에서, 프로테아제는 안구 및/또는 눈물에서 발견된 것이다. 안구에서 발견되는 상기 프로테아제의 예는 카스파제, 칼파인, 기질 금속단백분해효소, 디스인테그린, 금속단백분해효소(ADAM) 및 트롬보스폰딘 모티프를 갖는 ADAM, 프로테오좀, 조직 플라스미노겐 활성인자, 세크레타제, 카텝신 B 및 D, 시스타틴 C, 세린 프로테아제 PRSS1, 유비퀴틴 프로테오좀 경로(UPP)를 포함한다. 한 구체예에서, 프로테아제는 비-박테리아성 프로테아제이다. 한 구체예에서, 프로테아제는 동물, 예를 들어, 포유동물, 예를 들어, 인간 프로테아제이다.
조성물은 안구의 다양한 영역, 예를 들어, 안구의 표면, 각막, 또는 누관 또는 누선으로 전달될 수 있거나, 안구내 전달(예를 들어, 안구의 전방 또는 후방, 예를 들어, 유리체액)될 수 있고, 안구 구조, 예를 들어, 홍채, 섬모체, 누선으로 전달될 수 있고, 조성물은 상기 안구 부분에서 표적 분자(예를 들어, VEGF, IL-1, 또는 TNF-α)에 결합할 수 있다. 조성물은 또한 안구의 안구 주위 영역으로 전달될 수 있다.
표적 분자는, 예를 들어, VEGF, IL-1, 또는 TNF-α일 수 있거나, 이는 임의의 다른 요망되는 표적, 예를 들어, 안구, 예를 들어, 안구의 표면 상, 안구 내, 또는 누관 또는 누선에 존재하는 표적 분자일 수 있고, 예를 들어, 표적은 IL-1, IL-17 또는 TNF 수용체, 예를 들어, TNFR1, TGF베타, IL-6, IL-8, IL-21, IL-23, CD20, Nogo-a, 미엘린 결합 당단백질(MAG) 또는 베타 아밀로이드일 수 있다.
한 구체예에서, 본 발명은, 안구 점적 형태, 또는 젤, 또는, 예를 들어, 이식물 형태의 안구에 투여하기 위한 프로테아제 내성 면역글로불린 단일 가변 도메인(또는 dAb)을 제공한다. dAb는, 예를 들어, 안구에 존재하는 표적 분자, 예를 들어, VEGF, IL-1, 또는 TNF-α에 결합할 수 있다.
안구로의 투여는, 예를 들어, 국소 투여, 예를 들어, 안구 점적 형태의 국소 투여에 의해 이루어질 수 있거나, 대안적으로 이는 안구로의 주사에 의해 이루어질 수 있다.
안구의 특정 영역, 예를 들어, 안구의 표면, 또는 누관 또는 누선으로의 면역글로불린 단일 가변 도메인의 전달을 표적으로 하는 것이 유용할 수 있거나, 안구내 전달(예를 들어, 안구의 전방 또는 후방, 예를 들어, 유리체액)될 수 있다. 그러므로, 본 발명은 안구내 주사, 국소 전달, 안구 점적, 안구 주변 투여 및 서방형 제형의 사용(예를 들어, 중합 나노 또는 미세입자 또는 젤) 또는 이온삼투요법을 사용하는 전달 장치의 이용으로부터 선택되는 방법에 의해 안구로 조성물을 투여하는 것을 포함하는, 안구로 조성물을 직접 전달하는 방법을 추가로 제공한다.
이는 또한 면역글로불린 단일 가변 도메인이, 예를 들어, 국소 전달, 예를 들어, 안구 침투 향상제, 예를 들어, 소듐 카프레이트, 또는 점성도 향상제, 예를 들어, 히드록시프로필메틸셀룰로오스(HPMC)와 함께 안구 점적으로 안구에 투여되는 경우에 유용할 수 있다. 따라서, 본 발명은, (a) 예를 들어, 안구 내에서 표적 분자(예를 들어, VEGF, IL-1, 또는 TNF-α)에 결합하는 면역글로불린 단일 가변 도메인, 및 또한 (b) 안구 침투 향상제 및/또는 (c) 점성도 향상제, 예를 들어, 안구로의 국소 전달을 위한 점성도 향상제를 포함하는 조성물을 추가로 제공한다.
한 양태에서, 안구로 전달되는 면역글로불린 단일 가변 도메인은 VEGF에 결합하는 WO 2008/149146호, WO 2008/149147호, 또는 WO 2008/149150호에 기재된 VEGF dAb 중 어느 하나일 수 있다. 예를 들어, 이는 DOM15-26-593의 아미노산 서열(도 1a의 SEQ ID NO 1에 제시됨)과 80% 이상 동일한 아미노산 서열에 의해 엔코딩되는 폴리펩티드일 수 있다. 한 구체예에서, 동일성 %는 70, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 이상 또는 100%이다. 한 구체예에서, 프로테아제 내성 폴리펩티드는 프로테아제 내성 폴리펩티드를 분리시키기 위한 본원에 기재된 방법에 의해 수득된다. 안구로의 전달을 위한 DOM15-26-593은 또한 항체 불변 영역의 도메인을 추가로 포함할 수 있다. 예를 들어, 이는 DOM15-26-593-Fc 융합체의 아미노산 서열(도 1b의 SEQ ID NO 2에 제시됨)과 동일한 아미노산 서열을 가질 수 있거나, 동일성 %는 도 1b의 SEQ ID NO 2에 제시된 서열과 70, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 이상일 수 있다.
한 양태에서, DOM15-26-593의 아미노산 서열과 80% 이상 동일한 아미노산 서열(예를 들어, 97% 이상인 것)에 의해 엔코딩되는 VEGF dAb는 WO 2008/149150호 및 WO 2008/149147호(이의 내용은 참조로서 본원에 포함됨)에 기재된 바와 같이 위치 6에 발린, 및/또는 위치 99에 루신, 및/또는 위치 30에 리신(케이뱃(Kabat) 넘버링)을 포함할 수 있다.
한 추가 양태에서, 안구로 전달되는 면역글로불린 단일 가변 도메인은 WO 2008/149144호, 또는 WO 2008/149148호에 기재된 항 TNFR1 dAb 중 어느 하나일 수 있다.
한 구체예에서, α-TNF-αR1에 결합하는 면역글로불린 단일 가변 도메인은 Dom1h-131-206의 아미노산 서열(도 4의 SEQ ID NO 6에 제시됨)과 97% 이상 동일(예를 들어, 98%, 99% 또는 100% 동일)한 아미노산 서열을 포함할 수 있다. Dom1h-131-206의 제조 및 선택은 WO 2008/149148호에 기재되어 있다.
한 추가 양태에서, 안구로 전달되는 면역글로불린 단일 가변 도메인은 WO 2008/149149호에 기재된 항-IL-1R1 dAb 중 어느 하나일 수 있다.
한 구체예에서, IL-1에 결합하는 면역글로불린 단일 가변 도메인은 (a) DOM4-130-54의 아미노산 서열(도 3의 SEQ ID NO 5에 제시됨), 또는 (b) DOM0400 PEG의 아미노산 서열(도 2의 SEQ ID NO 4에 제시됨)과 97% 이상 동일(예를 들어, 98%, 99% 또는 100% 동일)한 아미노산 서열을 포함할 수 있다.
DOM4-130-54의 제조 및 선택은 WO 2007/063311호 및 또한 WO 2008/149149호에 기재되어 있다. Dom0400을 제조하기 위해, DOM4-130-54 dAb 서열이 수득되고, 위치 80의 시스테인이 DOM4-130-54에 존재하는 프롤린으로 대체되도록 돌연변이되어, 이후 상기 dAb가 dAb의 위치 80에서의 자유 시스테인으로의 표준 말레이미드 커플링에 의해 40KDa 선형 PEG 분자(NOF Corporation, Europe으로부터 구입)에 부착된다.
본 발명은 또한 안구 질환 또는 질병의 치료, 예방 또는 진단을 위한 약제의 제조에 있어서 면역글로불린 단일 가변 도메인을 포함하거나 이로 구성되는 임의의 조성물의 용도를 제공하며, 예를 들어, 여기서 상기 안구 질병은 연령 관련 황반 변성(AMD), 포도막염 녹내장, 안구 건조, 당뇨망막병증, 또는 당뇨 황반 부종이다.
본 발명은 또한 안구 질환 또는 질병, 예를 들어, AMD, 포도막염 녹내장, 안구 건조, 당뇨망막병증, 또는 당뇨 황반 부종의 치료, 예방 또는 진단에 사용하기 위한, 면역글로불린 단일 가변 도메인, 예를 들어, VEGF, IL-1, 또는 TNF-α dAb를 포함하거나 이로 구성되는 조성물을 제공한다.
한 대안적 구체예에서, 안구로의 전달을 위한 면역글로불린 단일 가변 도메인은 DOM15-26-593의 아미노산 서열(도 1a의 SEQ ID NO 1에 제시됨)이 아니거나, DOM15-26-593-Fc 융합체의 아미노산 서열(도 1b의 SEQ ID NO 2에 제시됨)이 아닌 것일 수 있다.
또 다른 대안적 구체예에서, 안구로의 전달을 위한 면역글로불린 단일 가변 도메인은 PCT/GB2008/050399호, PCT/GB2008/050400호, PCT/GB2008/050406호, PCT/GB2008/050405호, PCT/GB2008/050403호, PCT/GB2008/050404호, PCT/GB2008/050407호에 기재된 임의의 분자를 포함하거나 이로 구성되는 분자가 아닌 것일 수 있다.
또 다른 대안적 구체예에서, 안구로의 전달을 위한 면역글로불린 단일 가변 도메인은 PCT/GB2008/050400호에 기재된 Dom1h-131-511, Dom1h-131-201, Dom1h-131-202, Dom1h-131-203, Dom1h-131-204, Dom1h-131-205의 아미노산 서열이 아닌 것일 수 있다.
또 다른 대안적 구체예에서, 안구로의 전달을 위한 면역글로불린 단일 가변 도메인은 PCT/GB2008/050406호에 기재된 Dom4-130-202의 아미노산 서열이 아닌 것일 수 있다.
또 다른 대안적 구체예에서, 안구로의 전달을 위한 면역글로불린 단일 가변 도메인은 PCT/GB2008/050405호에 기재된 Dom1h-131-206의 아미노산 서열이 아닌 것일 수 있다.
면역글로불린 단일 가변 도메인과 조합하거나 회합하여 안구로 다른 작용제를 전달하는 것이 또한 유용할 수 있고, 예를 들어, 침투 향상제, 예를 들어, 소듐 카프레이트 또는 점성도 작용제, 예를 들어, 히드록시프로필메틸셀룰로오스(HPMC)를 전달하는 것이 유용할 수 있다.
안구 전달을 위한 단일 면역글로불린 가변 도메인(dAb)(예를 들어, VEGF, IL-1, 또는 TNF-α에 결합함)은, 예를 들어, PEG 기, 혈청 알부민, 트랜스페린, 트랜스페린 수용체 또는 적어도 이의 트랜스페린 결합 부분, 항체 Fc 영역의 부착, 또는 항체 도메인으로의 컨쥬게이션에 의해 보다 큰 유체역학적 크기를 갖도록 포맷화될 수 있다. 예를 들어, dAb 단량체(예를 들어, VEGF dAb)는 항체의 보다 큰 항원 결합 단편으로 포맷화(예를 들어, Fab, Fab', F(ab)2, F(ab')2, IgG, scFv로 포맷화됨)될 수 있다. dAb의 유체역학 크기 및 이의 혈청 반감기는 또한 본원에 기재(예를 들어, 참조로서 본원에 포함되는 WO 2006/038027호의 부록 1)된 바와 같이 dAb를 생체내 반감기를 증가시키는 항원 또는 에피토프에 결합하는 결합 도메인(예를 들어, 항체 또는 항체 단편)에 컨쥬게이션시키거나 연결시킴으로써 증가될 수 있다. 예를 들어, VEGF dAb는 항-혈청 알부민 또는 항-신생아 Fc 수용체 항체 또는 항체 단편, 예를 들어, 항-SA 또는 항-신생아 Fc 수용체 dAb, Fab, Fab' 또는 scFv, 또는 항-SA 어피바디(affibody) 또는 항-신생아 Fc 수용체 어피바디에 컨쥬게이션되거나 연결될 수 있다.
예를 들어, VEGF-결합 dAb와 연결된 본원에 기재된 조성물에 사용하기에 적합한 알부민, 알부민 단편 또는 알부민 변이체의 예는 전체내용이 참조로서 본원에 포함되는 WO 2005/077042 A2호 및 WO 2006/038027호에 기재되어 있다.
포맷화된 dAb(예를 들어, 페길화에 의해 포맷화된 dAb)는, 예를 들어, 30 KDa 내지 100 KDa, 예를 들어, 약 50-60 KDa인 분자량을 가질 수 있고, 이는 망막 및/또는 맥락막 및/또는 누액으로의 전달에 유용할 수 있다.
약 15 KDa의 분자량을 갖는 네이키드(포맷화되지 않은) dAb는 유리체액 및/또는 방수 및/또는 망막 및/또는 맥락막으로의 전달에 유용할 수 있다.
본 명세서 전체에 걸쳐 기재된 본 발명의 다른 구체예에서, 본 발명의 길항제 또는 리간드에서 단일 면역글로불린 가변 도메인 또는 "dAb"의 사용 대신, 당업자가, 예를 들어, VEGF, IL-I, 또는 TNF-α(예를 들어, 적합한 단백질 스캐폴드 또는 골격에 이식된 CDR, 예를 들어, 어피바디, SpA 스캐폴드, LDL 수용체 부류 A 도메인 또는 EGF 도메인)에 결합하는 dAb의 CDR을 포함하는 도메인을 사용할 수 있거나, 이는 VEGF, IL-I, 또는 TNF-α에 대한 결합 부위를 포함하는 단백질 도메인로서, 예를 들어, 상기 도메인이 어피바디, SpA 도메인, LDL 수용체 부류 A 도메인 또는 EGF 도메인으로부터 선택되는 단백질 도메인일 수 있음이 고려된다. 따라서, 전체적으로 상기 기재는 dAb 대신에 상기 도메인을 이용하는 길항제, 리간드 및 방법의 기재를 제공하는 것으로 해석되어야 한다.
본원에 기재된 프로테아제 내성 dAb는 전체내용이 참조로서 본원에 포함되는 WO 2008/149143호에 기재된 방법 및 교시내용을 이용하여 선택될 수 있다.
한 양태에서, 본 발명은, 예를 들어, VEGF, IL-I, 또는 TNF-α 결합 부위를 포함하는 프로테아제 내성 면역글로불린 단일 가변 도메인을 제공하며, 여기서 상기 가변 도메인은, (ⅰ) 1시간 이상의 시간(t) 동안 37℃에서 10 마이크로그램/ml 프로테아제 이상의 농도(c), 또는 (ⅱ) 1시간 이상의 시간(t) 동안 30℃에서 40 마이크로그램/ml 프로테아제 이상의 농도(c')로 인큐베이션되는 경우에 프로테아제에 대해 내성이다. 한 구체예에서, 프로테아제, 예를 들어, 트립신 대 가변 도메인의 비(몰/몰 기준)는 8,000 대 80,000의 프로테아제:가변 도메인이거나, 예를 들어, C가 10 마이크로그램/ml인 경우, 상기 비는 800 대 80,000의 프로테아제:가변 도메인이거나, C 또는 C'가 100 마이크로그램/ml인 경우, 상기 비는 8,000 대 80,000의 프로테아제:가변 도메인이다. 한 구체예에서, 프로테아제(예를 들어, 트립신) 대 가변 도메인의 비(중량/중량, 예를 들어, 마이크로그램/마이크로그램 기준)는 16,000 대 160,000의 프로테아제:가변 도메인이거나, 예를 들어, C가 10 마이크로그램/ml인 경우, 상기 비는 1,600 대 160,000의 프로테아제:가변 도메인이거나, C 또는 C'이 100 마이크로그램/ml인 경우, 상기 비는 16,000 대 160,000의 프로테아제:가변 도메인이다. 한 구체예에서, 농도(c 또는 c')는 100 또는 1000 마이크로그램/ml 프로테아제 이상이다. 한 구체예에서, 농도(c 또는 c')는 100 또는 1000 마이크로그램/ml 프로테아제 이상이다. 펩티드 또는 폴리펩티드의 레퍼토리 또는 라이브러리로 작업하는 경우에 사용하기 위한 프로테아제의 단백질분해 활성에 적합한 조건(예를 들어, w/w 파라미터)의 본원의 기재를 참조로 할 수 있다. 이러한 조건은 특정 면역글로불린 단일 가변 도메인의 프로테아제 내성을 결정하기 위한 조건에 사용될 수 있다. 한 구체예에서, 시간(t)은 약 1시간, 3시간 또는 24시간 또는 밤새(예를 들어, 약 12-16시간)이다. 한 구체예에서, 가변 도메인은 조건 (ⅰ)하에서 내성이고, 농도(c)는 약 10 또는 100 마이크로그램/ml 프로테아제이고, 시간(t)은 1시간이다. 한 구체예에서, 가변 도메인은 조건 (ⅱ)하에서 내성이고, 농도(c')는 약 40 마이크로그램/ml 프로테아제이고, 시간(t)은 약 3시간이다. 한 구체예에서, 프로테아제는 트립신, 엘라스타제, 류코자임 및 판크레아틴으로부터 선택된다. 한 구체예에서, 프로테아제는 트립신이다. 한 구체예에서, 프로테아제는 담, 점액(예를 들어, 위 점액, 비 점액, 기관지 점액), 기관지폐포 세척액, 폐 균질액, 폐 추출물, 췌장 추출액, 위액, 타액 또는 눈물 또는 안구에서 발견되는 프로테아제이다. 한 구체예에서, 프로테아제는 안구 및/또는 눈물에서 발견되는 것이다. 한 구체예에서, 프로테아제는 비-박테리아성 프로테아제이다. 한 구체예에서, 프로테아제는 동물, 포유동물, 예를 들어, 인간 프로테아제이다.
한 구체예에서, 가변 도메인은 트립신 및/또는 엘라스타제, 류코자임 및 판크레아틴으로부터 선택된 하나 이상의 다른 프로테아제에 대해 내성이다. 예를 들어, 내성은 트립신 및 엘라스타제; 트립신 및 류코자임; 트립신 및 판크레아틴; 트립신, 엘라스타제 및 류코자임; 트립신, 엘라스타제 및 판크레아틴; 트립신, 엘라스타제, 판크레아틴 및 류코자임; 또는 트립신, 판크레아틴 및 류코자임에 대한 것이다.
한 구체예에서, 가변 도메인은, 예를 들어, 106 내지 1013의 파아지 라이브러리 크기, 예를 들어, 108 내지 1012의 복제 단위(감염성 비리온)로 조건 (ⅰ) 또는 (ⅱ)하에서 인큐베이션되는 경우에 박테리오파지 상에 전시된다.
한 구체예에서, 가변 도메인은, 예를 들어, BiaCore TM 또는 ELISA, 예를 들어, 파아지 ELISA 또는 모노클로날 파아지 ELISA를 이용하여 평가시 조건 (ⅰ) 또는 (ⅱ) 하에서의 인큐베이션 후에 VEGF, IL-1, 또는 TNF-α에 특이적으로 결합한다.
한 구체예에서, 가변 도메인은 단백질 A 또는 단백질 L에 특이적으로 결합한다. 한 구체예에서, 단백질 A 또는 L로의 특이적 결합은 조건 (ⅰ) 또는 (ⅱ) 하에서의 인큐베이션 후에 존재하다.
한 구체예에서, 가변 도메인은, 예를 들어, 조건 (ⅰ) 또는 (ⅱ) 하에서의 인큐베이션 후에 0.404 이상의 ELISA, 예를 들어, 파아지 ELISA 또는 모노클로날 파아지 ELISA에서의 OD450 판독값을 가질 수 있다.
한 구체예에서, 가변 도메인은, 예를 들어, 조건 (ⅰ) 또는 (ⅱ) 하에서의 인큐베이션 후에 젤 전기영동에서 (실질적으로) 단일한 밴드를 나타낸다.
또 다른 구체예에서, 작용제(dAb)는 삽입형 전달 장치를 통해 안구에 국소적으로 투여될 수 있다. 따라서, 한 구체예에서, 본 발명은 안구 전달을 위한, 예를 들어, VEGF, IL-1, 또는 TNF-α dAb를 함유하는 삽입형 전달 장치를 제공한다.
한 추가 양태에서, 본 발명은 면역글로불린 단일 가변 도메인(예를 들어, VEGF, IL-1, 또는 TNF-α dAb), 및 약학적 또는 생리학적으로 허용되는 담체, 부형제 또는 희석제를 포함하는 안구 전달용 약제 조성물을 제공한다.
도면의 간단한 설명
도 1a는 DOM15-26-593의 아미노산 서열을 도시한다.
도 1b는 DOM15-26-593-Fc 융합체의 아미노산 서열을 도시한다.
도 1c는 항체 Fc의 아미노산 서열을 도시한다.
도 2는 DOM0400 PEG(페길화된 항-IL1 dAb, 분자량 약 52 KDa)의 아미노산 서열을 도시한다.
도 3은 DOM4-130-54(항-IL1 dAb)의 아미노산 서열을 도시한다.
도 4는 Dom1h-131-206(항 TNF 알파 R1 dAb)의 아미노산 서열을 도시한다.
발명의 상세한 설명
본 명세서에서, 본 발명은 명세서가 명확하고 간결하게 기재되는 것을 가능케 하는 방식의 구체예를 참조로 하여 기재되었다. 구체예는 본 발명을 벗어남이 없이 다양하게 조합되거나 구별될 수 있으며, 이러한 사실이 인지되어야 한다.
달리 정의되지 않는 경우, 본원에서 사용된 모든 기술 및 과학 용어는 당업자(예를 들어, 세포 배양, 분자유전학, 핵산 화학, 하이브리드화 기술 및 생화학)에 의해 통상적으로 이해되는 것과 동일한 의미를 갖는다. 분자, 유전학 및 생화학적 방법(일반적으로, 참조로서 본원에 포함되는 문헌[Sambrook et al ., Molecular Cloning: A Laboratory Manual, 2d ed. (1989) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. and Ausubel et al ., Short Protocols in Molecular Biology (1999) 4th Ed, John Wiley & Sons, Inc.] 참조) 및 화학 방법에 대해 표준 기술이 사용된다.
본원에서 사용되는 용어 "혈관 내피세포 성장인자(VEGF)의 길항제" 또는 "항-VEGF 길항제" 등은 VEGF에 결합하고, VEGF의 기능(즉, 하나 이상의 기능)을 억제할 수 있는 작용제(예를 들어, 분자, 화합물)를 의미한다.
본원에서 사용되는 "펩티드"는 펩티드 결합을 통해 함께 연결되는 약 2개 내지 약 50개의 아미노산을 의미한다.
본원에서 사용되는 "폴리펩티드"는 펩티드 결합에 의해 함께 연결되는 약 50개 이상의 아미노산을 의미한다. 폴리펩티드는 일반적으로 3차 구조를 포함하고, 기능적 도메인으로 폴딩된다.
본원에서 사용되는 "프로테아제 분해에 내성"인 펩티드 또는 폴리펩티드(예를 들어, 도메인 항체(dAb))는 프로테아제 활성에 적합한 조건하에서 프로테아제와 함께 인큐베이션되는 경우에 프로테아제에 의해 실질적으로 분해되지 않는다. 폴리펩티드(예를 들어, dAb)는 프로테아제 활성에 적합한 온도에서 약 1시간 동안 프로테아제와의 인큐베이션 후에 약 25% 이하, 약 20% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하의 단백질이 프로테아제에 의해 분해되거나, 실질적으로 단백질이 프로테아제에 의해 분해되지 않는다. 예를 들어, 37 또는 50℃에서, 단백질 분해가 본원에 기재된 바와 같이 임의의 적합한 방법, 예를 들어, SDS-PAGE 또는 기능 검정(예를 들어, 리간드 결합)에 의해 평가될 수 있다.
본원에서 사용되는 "표적 리간드"는 폴리펩티드 또는 펩티드에 의해 특이적 또는 선택적으로 결합되는 리간드를 의미한다. 예를 들어, 폴리펩티드가 항체 또는 이의 항원 결합 단편인 경우, 표적 리간드는 임의의 요망되는 항원 또는 에피토프일 수 있다. 표적 항원으로의 결합은 작용성인 폴리펩티드 또는 펩티드에 좌우된다.
본원에서 사용되는 항체는 항체를 자연 생성하는 임의의 종으로부터 유래되거나, 재조합 DNA 기술에 의해 생성되는지, 혈청, B 세포, 하이브리도마, 트랜스펙토마(transfectoma), 효모 또는 박테리아로부터 분리되었는지 아닌지 간에 IgG, IgM, IgA, IgD 또는 IgE 또는 단편(예를 들어, Fab, F(ab')2, Fv, 이황화 연결된 Fv, scFv, 닫힌 형태의 다중특이적 항체, 이황화 연결된 scFv, 디아바디(diabody))를 의미한다.
본원에서 사용되는 "항체 포맷"은 하나 이상의 항체 가변 도메인이 통합되어, 구조 상의 항원에 대한 결합 특이성을 부여할 수 있는 임의의 적합한 폴리펩티드 구조를 의미한다. 다양한 적합한 항체 포맷, 예를 들어, 키메라 항체, 인간화된 항체, 인간 항체, 단쇄 항체, 이특이적 항체, 항체 중쇄, 항체 경쇄, 항체 중쇄 및/또는 경쇄의 동종이합체 및 이종이합체, 이들의 임의의 항원 결합 단편(예를 들어, Fv 단편(예를 들어, 단쇄 Fv(scFv), 이황화 결합된 Fv), Fab 단편, Fab' 단편, F(ab')2 단편), 단일 항체 가변 도메인(예를 들어, dAb, VH, VHH, VL), 및 이들의 임의의 변형된 형태(예를 들어, 폴리에틸렌 글리콜 또는 다른 적합한 중합체의 공유적 부착에 의한 변형 또는 인간화된 VHH)가 당 분야에 공지되어 있다.
구 "면역글로불린 단일 가변 도메인"은 독립적으로 다른 V 영역 또는 도메인의 항원 또는 에피토프에 특이적으로 결합하는 항체 가변 도메인(VH, VHH, VL)을 의미한다. 면역글로불린 단일 가변 도메인은 다른 영역 또는 도메인이 단일 면역글로불린 가변 도메인에 의한 항원 결합에 필요하지 않은 경우(즉, 면역글로불린 단일 가변 도메인이 추가 가변 도메인과는 독립적으로 항원에 결합하는 경우)에 다른 가변 영역 또는 가변 도메인을 갖는 포맷(예를 들어, 동종다합체 또는 이종다합체)로 존재할 수 있다. "도메인 항체" 또는 "dAb"는 "면역글로불린 단일 가변 도메인"과 동일하고, 이러한 용어가 본원에서 사용된다. "단일 면역글로불린 가변 도메인"은 "면역글로불린 단일 가변 도메인"과 동일하고, 이러한 용어가 본원에서 사용된다. "단일 항체 가변 도메인"은 "면역글로불린 단일 가변 도메인"과 동일하고, 이러한 용어가 본원에서 사용된다. 면역글로불린 단일 가변 도메인은 한 구체예에서 인간 항체 가변 도메인이나, 이는 또한 설치류(예를 들어, 전체내용이 참조로서 본원에 포함되는 WO 00/29004호에 기재되어 있음), 너스 샤크(nurse shark) 및 카멜리드 VHH dAb와 같은 다른 종으로부터의 단일 항체 가변 도메인을 포함한다. 카멜리드 VHH는 경쇄가 자연적으로 결여된 중쇄 항체를 생성시키는 낙타, 라마, 알파카, 단봉 낙타, 및 과나코를 포함하는 종으로부터 유래되는 면역글로불린 단일 가변 도메인 폴리펩티드이다. VHH는 인간화될 수 있다.
"도메인"은 단백질의 나머지와는 독립적인 3차 구조를 갖는 폴딩된 단백질 구조이다. 일반적으로, 도메인은 단백질의 별개의 기능적 특성을 책임지고, 많은 경우에 단백질 및/또는 도메인의 나머지의 기능의 손실 없이 첨가되거나, 제거되거나, 다른 단백질로 옮겨질 수 있다. "단일 항체 가변 도메인"은 항체 가변 도메인의 서열 특성을 포함하는 폴딩된 폴리펩티드 도메인이다. 따라서, 이는 완전한 항체 가변 도메인 및 변형된 가변 도메인, 예를 들어, 하나 이상의 루프가 항체 가변 도메인에 특징을 이루지 않는 서열로 대체된 변형된 가변 도메인, 또는 트렁케이션되거나 N-말단 또는 C-말단 신장부를 포함하는 항체 가변 도메인, 뿐만 아니라 전장 도메인의 적어도 결합 활성 및 특이성을 보유하는 가변 도메인의 폴딩된 단편을 포함한다.
본원에서 사용되는 용어 "용량"은 한번에(단위 용량), 또는 소정의 기간 동안 2회 이상의 투여로 모든 피검체에 투여되는 리간드의 양을 의미한다. 예를 들어, 용량은 1일(24시간)(일일 용량), 2일, 1주, 2주, 3주 또는 1개월 이상(예를 들어, 단일 투여, 또는 2회 이상의 투여에 의함)의 과정에 걸쳐 피검체에 투여되는 리간드(예를 들어, 표적 항원에 결합하는 면역글로불린 단일 가변 도메인을 포함하는 리간드)의 양을 의미할 수 있다. 용량 사이의 간격은 임의의 요망되는 시간일 수 있다.
구 "반감기"는, 예를 들어, 리간드의 분해 및/또는 자연 메커니즘에 의한 리간드의 청소 또는 격리로 인해 생체내에서 리간드(예를 들어, dAb, 폴리펩티드 또는 길항제)의 혈청 농도가 50%까지 감소하는데 걸리는 시간을 의미한다. 본 발명의 리간드는 생체내에서 안정화될 수 있고, 이의 반감기는 분해 및/또는 청소 또는 격리에 견디는 분자로의 결합에 의해 증가된다. 통상적으로, 이러한 분자는 생체내에서 본래 긴 반감기를 갖는 자연 발생 단백질이다. 리간드의 반감기는, 이의 기능적 활성이 생체내에서 반감기를 증가시키는 분자에 특이적이지 않은 유사한 리간드보다 긴 기간 동안 지속되는 경우에 증가된다. 예를 들어, 인간 혈청 알부민(HSA) 및 표적 분자에 특이적인 리간드는, HSA에 대한 특이성이 존재하지 않아, HSA에 결합하지 않지만 다른 분자에는 결합하는 동일 리간드와 비교된다. 예를 들어, 이는 세포 상의 제 3의 표적에 결합할 수 있다. 통상적으로, 반감기는 10%, 20%, 30%, 40%, 50% 또는 이 이상 증가된다. 반감기의 2x, 3x, 4x, 5x, 10x, 20x, 30x, 40x, 50x 또는 이 이상의 범위의 증가가 가능하다. 대안적으로, 또는 추가로, 반감기의 30x, 40x, 50x, 60x, 70x, 80x, 90x, 100x, 150x 이하의 범위의 증가가 가능하다.
본원에서 사용되는 "유체역학적 크기"는 수용액을 통한 분자의 확산을 기초로 하는 분자(예를 들어, 단백질 분자, 리간드)의 외견상의 크기를 의미한다. 용액을 통한 단백질의 확산 또는 이동은 단백질의 외견상의 크기를 유도하도록 처리될 수 있고, 여기서 상기 크기는 단백질 입자의 "스토크스 반경(Stokes radius)" 또는 "유체역학적 반경"에 의해 제공된다. 단백질의 "유체역학적 크기"는 질량 및 형상(형태) 둘 모두에 좌우되어, 동일한 분자량을 갖는 두개의 단백질이 단백질의 전체적인 형태에 기초하여 상이한 유체역학적 크기를 가질 수 있다.
본원에서 언급되는 용어 "경쟁하다"는 제 1 표적의 이의 인지체(cognate) 표적 결합 도메인으로의 결합이 상기 인지체 표적에 특이적인 제 2의 결합 도메인의 존재로 억제되는 것을 의미한다. 예를 들어, 결합은, 예를 들어, 결합 도메인의 물리적 차단 또는 결합 도메인의 구조 또는 환경의 변경에 의해 입체구조적으로 방해되어, 이의 표적에 대한 친화성 또는 결합력이 감소될 수 있다. 제 1 및 제 2 결합 도메인 사이의 경쟁을 결정하기 위한 경쟁 ELISA 및 경쟁 BiaCore 실험을 수행하는 방법의 세부사항은 WO 2006/038027호를 참조하라.
두 서열 사이의 "동종성" 또는 "동일성" 또는 "유사성"(이들 용어는 본원에서 상호교환적으로 사용됨)의 계산은 하기와 같이 수행된다. 서열은 최적 비교 목적을 위해 정렬된다(예를 들어, 최적 정렬을 위해 제 1 및 제 2 아미노산 또는 핵산 서열 중 하나 또는 둘 모두에 갭이 도입될 수 있고, 비교 목적을 위해 비상동성 서열이 무시될 수 있음). 한 구체예에서, 비교 목적을 위해 정렬된 참조 서열의 길이는 참조 서열 길이의 30% 이상, 또는 40% 이상, 또는 50% 이상, 또는 60% 이상, 또는 70% 이상, 80%, 90%, 100%이다. 이후, 상응하는 아미노산 위치 또는 누클레오티드 위치에서 아미노산 잔기 또는 누클레오티드가 비교된다. 제 1 서열 내의 위치가 제 2 서열 내의 상응한 위치와 동일한 아미노산 잔기 또는 누클레오티드에 의해 점유되는 경우, 분자는 상기 위치에서 동일하다(본원에서 사용되는 바와 같은 아미노산 또는 핵산 "상동성"은 아미노산 또는 핵산 "동일성"과 동등함). 두 서열 사이의 동일성 %는 두 서열의 최적 정렬을 위해 도입될 필요가 있는 갭의 수, 및 각각의 갭의 길이를 고려한 서열에 의해 공유되는 동일한 위치의 수의 함수이다. 본원에 정의된 바와 같은 아미노산 및 누클레오티드 서열 정렬 및 상동성, 유사성 또는 동일성은 디폴트 파라미터를 이용하는 알고리즘 BLAST 2 시퀀스(BLAST 2 Sequence)를 이용하여 준비되고 결정될 수 있다(Tatusova, T.A. et al , FEMS Microbiol Lett, 174:187-188 (1999)).
프로테아제 내성:
한 구체예에서, 본 발명은 요망되는 생물학적 활성, 예를 들어, VEGF, TNFR1 또는 IL-1으로의 결합을 갖는 프로테아제 내성 dAb의 선택 방법에 의해 선택된, 안구 전달용의 dAb, 예를 들어, 항-VEGF dAb, TNFR1 dAb, IL-1 dAb에 관한 것이다. 고도로 안정적이고 프로테아제 분해에 내성이고, 요망되는 생물학적 활성을 갖는 폴리펩티드를 선택하기 위한 효과적인 과정을 발생시키기 위한 방법에서 2개의 선택압이 사용된다. 본원에 기재된 바와 같이, 프로테아제 내성 펩티드 및 폴리펩티드는 일반적으로 생물학적 활성을 보유한다. 대조적으로, 프로테아제 민감성 펩티드 및 폴리펩티드는 본원에 기재된 방법에서 프로테아제에 의해 절단되거나 분해되고, 이에 따라 이의 생물학적 활성을 상실한다. 따라서, 프로테아제 내성 펩티드 또는 폴리펩티드는 일반적으로 이의 생물학적 활성, 예를 들어, 결합 활성을 기초로 하여 선택된다.
안구 환경은 프로테아제가 풍부하므로, 본원에 기재된 바와 같은 안구 전달용 프로테아제 내성 dAb의 사용이 여러 이점을 제공하는 환경이다. 예를 들어, 하나의 프로테아제(예를 들어, 트립신)에 의한 단백질분해성 분해에 대한 내성에 대해 선택되는 가변 도메인은 다른 프로테아제(예를 들어, 엘라스타제, 류코자임)에 의한 분해에도 내성이다. 프로테아제 내성은 펩티드 또는 폴리펩티드의 보다 높은 융해 온도(Tm)와 관련이 있을 수 있다. 보다 높은 융해 온도는 보다 안정한 가변 도메인, 길항제, 펩티드 및 폴리펩티드를 나타낸다. 프로테아제 분해에 대한 내성은 또한 표적 리간드로의 높은 친화성 결합과 관련이 있을 수 있다. 따라서, 본원에 기재되고 본원에서 참조(WO 2008/149143호)된 방법은 요망되는 생물학적 활성을 갖고, 프로테아제 내성이고 안정적이어서 안구의 생체내 치료 및/또는 진단 용도에 매우 적합한 dAb를 선택하고/하거나, 분리하고/하거나, 회수하는 효과적인 방법을 제공한다. 한 구체예에서, 프로테아제 내성은 개선된 PK, 예를 들어, 프로테아제 내성이 아닌 가변 도메인, 길항제, 펩티드 또는 폴리펩티드에 비해 개선된 PK와 관련이 있을 수 있다. 개선된 PK는 개선된 AUC(곡선하영역) 및/또는 개선된 반감기일 수 있다. 프로테아제 내성은 또한 전단 및/또는 열 스트레스 및/또는 분무 동안의 감소된 응집 경향에 대한 가변 도메인, 길항제, 펩티드 또는 폴리펩티드의 개선된 안정성, 예를 들어, 프로테아제 내성이 아닌 가변 도메인, 길항제, 펩티드 또는 폴리펩티드에 비한 개선된 안정성과 관련이 있을 수 있다. 한 구체예에서, 프로테아제 내성은 개선된 저장 안정성, 예를 들어, 프로테아제 내성이 아닌 가변 도메인, 길항제, 펩티드 또는 폴리펩티드에 비해 개선된 저장 안정성과 관련이 있다. 한 양태에서, 1개, 2개, 3개, 4개 또는 모두의 이점이 제공되며, 상기 이점은 프로테아제 분해에 대한 내성, 보다 높은 Tm 및 표적 리간드로의 높은 친화성의 결합이다.
본원에 기재되고 참조(WO 2008/149143호)된 방법은 요망시 다른 적합한 선택 방법을 포함할 수 있는 프로테아제 내성 펩티드 또는 폴리펩티드, 예를 들어, dAb를 분리시키기 위한 프로그램의 일부로 사용될 수 있다. 이러한 상황에서, 본원에 기재된 방법은 상기 프로그램의 임의의 요망되는 지점, 예를 들어, 다른 선택 방법이 이용되기 전 또는 후에 이용될 수 있다.
특정 구체예에서, 안구 전달용 dAb는 트립신, 엘라스타제 또는 류코자임에 의한 분해에 대한 내성에 대해 선택되고, 이는 VEGF에 특이적으로 결합한다. 이러한 구체예에서, dAb를 포함하는 라이브러리 또는 레퍼토리가 제공되고, 단백질분해성 분해에 적합한 조건하에서 트립신, 엘라스타제 또는 류코자임(또는 트립신을 포함하는 생물학적 제조물, 추출물 또는 균질화물)과 조합된다. VEGF에 결합하는 트립신, 엘라스타제 또는 류코자임 내성 dAb가 선택된다. 예를 들어, 프로테아제 내성 dAb는 약 2시간 이상의 기간 동안 37℃에서 0.04% (w/w)의 프로테아제 용액 중에서 인큐베이션되는 경우에 실질적으로 분해되지 않는다. 또 다른 구체예에서, 프로테아제 내성 dAb는 약 3시간 이상의 기간 동안 37℃에서 0.04% (w/w)의 프로테아제 용액 중에서 인큐베이션되는 경우에 실질적으로 분해되지 않는다. 또 다른 예에서, 프로테아제 내성 dAb는 약 4시간 이상, 약 5시간 이상, 약 6시간 이상, 약 7시간 이상, 약 8시간 이상, 약 9시간 이상, 약 10시간 이상, 약 11시간 이상, 또는 약 12시간 이상의 기간 동안 37℃에서 0.04% (w/w)의 프로테아제 용액 중에서 인큐베이션되는 경우에 실질적으로 분해되지 않는다.
또 다른 양태에서, 프로테아제 내성 펩티드 또는 폴리펩티드(예를 들어, dAb)의 레퍼토리를 생성시키는 방법이 제공된다. 상기 방법은 프로테아제 활성에 적합한 조건하에서 펩티드 또는 폴리펩티드 및 프로테아제의 레퍼토리를 조합시키고, VEGF에 특이적으로 결합하는 다수의 펩티드 또는 폴리펩티드를 회수함으로써, 프로테아제 내성 펩티드 또는 폴리펩티드의 레퍼토리가 생성되어, 펩티드 또는 폴리펩티드의 레퍼토리를 제공하는 것을 포함한다. 상기 방법에 사용하기에 적합한 프로테아제, 디스플레이 시스템, 프로테아제 활성을 위한 조건, 및 펩티드 또는 폴리펩티드를 선택하는 방법은 다른 방법과 관련하여 본원에 기재되어 있다.
일부 구체예에서, 펩티드 또는 폴리펩티드의 레퍼토리를 포함하는 디스플레이 시스템(예를 들어, 핵산의 코딩 작용과 상기 핵산에 의해 엔코딩되는 펩티드 또는 폴리펩티드의 기능적 특성을 연결시키는 디스플레이 시스템)이 사용되고, 상기 방법은 선택된 펩티드 또는 폴리펩티드의 다수를 엔코딩하는 핵산의 카피수를 증폭시키거나 증가시키는 것을 추가로 포함한다. 핵산은 임의의 적합한 방법, 예를 들어, 파아지 증폭, 세포 성장 또는 중합효소 연쇄 반응을 이용하여 증폭될 수 있다.
특정 구체예에서, 항-VEGF dAb를 포함하는 프로테아제 내성 폴리펩티드의 레퍼토리를 생성시키는 방법이 제공된다. 상기 방법은 프로테아제 활성에 적합한 조건하에서 펩티드 또는 폴리펩티드 및 프로테아제(예를 들어, 트립신, 엘라스타제, 류코자임)의 레퍼토리를 조합시키고, VEGF에 대한 결합 특이성을 갖는 dAb를 포함하는 다수의 폴리펩티드를 회수하여, 항-VEGF dAb를 포함하는 폴리펩티드의 레퍼토리를 제공하는 것을 포함한다. 상기 방법은 나이브 레퍼토리, 또는 요망되는 결합 특이성으로 편향되는 레퍼토리, 예를 들어, VEGF에 대한 결합 특이성을 갖는 모(parental) dAb를 기초로 하는 친화성 성숙 레퍼토리를 생성시키는데 사용될 수 있다.
선택/분리/회수
프로테아제 내성 펩티드 또는 폴리펩티드(예를 들어, 프로테아제 내성 폴리펩티드의 집단)은 임의의 적합한 방법을 이용하여 레퍼토리 또는 라이브러리(예를 들어, 디스플레이 시스템)로부터 선택되고/되거나, 분리되고/되거나, 회수될 수 있다. 한 구체예에서, 프로테아제 내성 폴리펩티드는 선택가능한 특성(예를 들어, 물리적 특성, 화학적 특성, 기능적 특성)을 기초로 하여 선택되거나 분리된다. 적합한 선택가능한 기능적 특성은 레퍼토리 내의 펩티드 또는 폴리펩티드의 생물학적 활성, 예를 들어, 포괄 리간드(예를 들어, 초항원)으로의 결합, 표적 리간드(예를 들어, 항원, 에피토프, 기질)로의 결합, 항체로의 결합(예를 들어, 펩티드 또는 폴리펩티드에서 발현되는 에피토프를 통함), 및 촉매 활성(예를 들어, Tomlinson et al., WO 99/20749; WO 01/57065; WO 99/58655 참조)을 포함한다. 한 구체예에서, 선택은 VEGF로의 특이적 결합을 기초로 한다. 또 다른 구체예에서, 선택은 일원이 프로테아제 내성인 제 2의 레퍼토리를 생성시키는 선택된 기능적 특성, 이후 VEGF에 특이적으로 결합하는 제 2의 레퍼토리로부터의 일원의 선택을 기초로 한다.
일부 구체예에서, 프로테아제 내성 펩티드 또는 폴리펩티드는, 실질적으로 모든 프로테아제 내성 펩티드 또는 폴리펩티드가 공통의 선택가능한 특징을 공유하는 펩티드 또는 폴리펩티드의 라이브러리 또는 레퍼토리로부터 선택되고/되거나 분리된다. 예를 들어, 실질적으로 모든 프로테아제 내성 펩티드 또는 폴리펩티드가 공통의 포괄 리간드에 결합하거나, 공통의 표적 리간드에 결합하거나, 공통의 항체에 결합(또는 이에 의해 결합됨)되거나, 공통의 촉매 활성을 갖는 라이브러리 또는 레퍼토리로부터 프로테아제 내성 펩티드 또는 폴리펩티드가 선택될 수 있다. 이러한 유형의 선택은, 예를 들어, 면역글로불린 단일 가변 도메인의 친화성 성숙을 수행하는 경우에 요망되는 생물학적 활성을 갖는 모 펩티드 또는 폴리펩티드를 기초로 하는 프로테아제 내성 펩티드 또는 폴리펩티드의 레퍼토리를 제조하는데 특히 유용하다.
공통의 포괄 리간드로의 결합을 기초로 하는 선택은 본래의 라이브러리 또는 레퍼토리의 성분인 모든 또는 실질적으로 모든 프로테아제 내성 펩티드 또는 폴리펩티드를 함유하는 펩티드 또는 폴리펩티드의 집합물 또는 집단을 생성시킬 수 있다. 예를 들어, 표적 리간드 또는 포괄 리간드에 결합하는 펩티드 또는 폴리펩티드, 예를 들어, 단백질 A, 단백질 L 또는 항체는, 패닝(panning)에 의하거나 적합한 친화성 매트릭스를 이용하여 선택되고/되거나, 분리되고/되거나, 회수될 수 있다. 패닝은 적합한 용기(예를 들어, 튜브, 페트리 접신)에 리간드(예를 들어, 포괄 리간드, 표적 리간드)의 용액을 첨가하고, 리간드가 용기의 벽에 침착되거나 코팅되도록 함으로써 달성될 수 있다. 과량의 리간드는 세척될 수 있고, 펩티드 또는 폴리펩티드(예를 들어, 프로테아제와 인큐베이션된 레퍼토리)가 용기에 첨가될 수 있고, 용기는 펩티드 또는 폴리펩티드가 고정된 리간드에 결합하기에 적합한 조건하에서 유지된다. 결합되지 않은 펩티드 또는 폴리펩티드는 세척될 수 있고, 결합된 펩티들 또는 폴리펩티드는 임의의 적합한 방법, 예를 들어, 스크래핑(scraping) 또는 pH의 저하를 이용하여 회수될 수 있다.
적합한 리간드 친화성 매트릭스는 일반적으로 고체 지지체 또는 비드(예를 들어, 아가로오스)를 함유하고, 여기에 리간드가 공유적 또는 비공유적으로 부착된다. 친화성 매트릭스는 매트릭스 상의 리간드로의 펩티드 또는 폴리펩티드의 결합에 적합한 조건하에서 배치(batch) 방법, 컬럼 방법 또는 임의의 다른 적합한 방법을 이용하여 펩티드 또는 폴리펩티드(예를 들어, 프로테아제와 인큐베이션된 레퍼토리)와 조합될 수 있다. 친화성 매트릭스에 결합하지 않은 펩티드 또는 폴리펩티드는 세척될 수 있고, 결합된 펩티드 또는 폴리펩티드는 임의의 적합한 방법, 예를 들어, 낮은 pH의 완충액, 순한 변성제(예를 들어, 우레아) 또는 리간드로의 결합에 대해 경쟁하는 펩티드를 이용한 용리를 이용하여 용리되고 회수될 수 있다. 한 구체예에서, 비오티닐화된 표적 리간드는 레터포리 내의 펩티드 또는 폴리펩티드가 표적 리간드(VEGF)에 결합하기에 적합한 조건하에서 레퍼토리와 조합된다. 결합된 펩티드 또는 폴리펩티드는 고정된 아비딘 또는 스트렙타비딘(예를 들어, 비드 상)을 이용하여 회수된다.
일부 구체예에서, 포괄 리간드는 항체 또는 이의 항원 결합 단편이다. 라이브러리 또는 레퍼토리의 펩티드 또는 폴리펩티드에서 실질적으로 보존된 펩티드 또는 폴리펩티드의 구조적 특징부에 결합하는 항체 또는 항원 결합 단편이 포괄 리간드로서 특히 유용하다. 프로테아제 내성 펩티드 또는 폴리펩티드를 분리시키고/시키거나, 선택하고/하거나, 회수하기 위한 리간드로 사용하기에 적합한 항체 및 항원 결합 단편은 모노클로날 또는 폴리클로날일 수 있고, 임의의 적합한 방법을 이용하여 제조될 수 있다.
프로테아제 내성 폴리펩티드를 생성시키기 위한 핵산, 숙주 세포 및 방법:
본원에 기재된 방법에 의해 선택된 프로테아제 내성 펩티드 또는 폴리펩티드는 또한 적합한 시험관내 발현 시스템, 예를 들어, E. 콜리(E.coli) 또는 피키아(Pichia) 종, 예를 들어, P. 파스토리스(P. pastoris)에서 생성되거나, 화학적 합성 또는 임의의 다른 적합한 방법에 의해 생성될 수 있다.
폴리펩티드, dAb & 길항제:
본원에 기재된 바와 같이, 프로테아제 내성 dAb는 일반적으로 높은 친화성으로 이의 표적에 결합한다.
예를 들어, VEGF dAb는 표면 플라즈몬 공명에 의해 결정시 300 nM 내지 1 pM (즉, 3 x 10-7 내지 5 x 10-12M), 예를 들어, 50 nM 내지 1 pM, 예를 들어, 5 nM 내지 1 pM, 예를 들어, 1 nM 내지 1 pM의 친화성(KD; KD=Koff (kd)/Kon (ka), 표면 플라즈몬 공명에 의해 결정); 예를 들어, 1 x 10-7M 이하, 예를 들어, 1 x 10-8M 이하, 예를 들어, 1 x 10-9M 이하, 예를 들어, 1 x 10-10M 이하, 예를 들어, 1 x 10-11M 이하의 KD; 및/또는 5 x 10-1 s-1 내지 1 x 10-7 s-1, 예를 들어, 1 x 10-2 s-1 내지 1 x 10-6 s-1, 예를 들어, 5 x 10-3 s-1 내지 1 x 10-5 s-1, 예를 들어, 5 x 10-1 s-1 이하, 예를 들어, 1 x 10-2 s-1 이하, 예를 들어, 1 x 10-3 s-1 이하, 예를 들어, 1 x 10-4 s-1 이하, 예를 들어, 1 x 10-5 s-1 이하, 예를 들어, 1 x 10-6 s-1 이하의 Koff 속도 상수로 VEGF에 결합할 수 있다.
임의의 특정 이론으로 제한하고자 하는 바는 아니지만, 프로테아제에 대해 내성인 펩티드 및 폴리펩티드는 낮은 엔트로피 및/또는 높은 안정화 에너지를 갖는 것으로 생각된다. 따라서, 프로테아제 내성과 높은 친화성의 결합 사이의 상관관계는 본원에 기재된 방법에 의해 선택된 펩티드 및 폴리펩티드 및 dAb의 표면의 치밀함(compactness) 및 안정성과 관련이 있을 수 있다.
한 구체예에서, VEGF dAb는 약 1 μM 이하, 약 500 nM 이하, 약 100 nM 이하, 약 75 nM 이하, 약 50 nM 이하, 약 10 nM 이하 또는 약 1 nM 이하의 IC50의 농도 50(IC50)에서 VEGF의 결합을 억제한다.
특정 구체예에서, VEGF dAb는 VEGF, 예를 들어, 인간 VEGF에 특이적으로 결합하고, 표면 플라즈몬 공명에 의해 결정시 300 nM 내지 1 pM 또는 300nM 내지 5 pM 또는 50 nM 내지 1 pM 또는 50 nM 내지 5 pM 또는 50 nM 내지 20 pM 또는 약 10 pM 또는 약 15pM 또는 약 20 pM의 해리 상수(KD)로 인간 VEGF로부터 해리된다. 특정 구체예에서, 폴리펩티드, dAb 또는 길항제는 VEGF, 예를 들어, 인간 VEGF에 특이적으로 결합하고, 표면 플라즈몬 공명에 의해 결정시 5 x 10-1 s-1 내지 1 x 10-7 s-1, 예를 들어, 1 x 10-2 s-1 내지 1 x 10-6 s-1, 예를 들어, 5 x 10-3 s-1 내지 1 x 10-5 s-1, 예를 들어, 5 x 10-1 s-1 이하, 예를 들어, 1 x 10-2 s-1 이하, 예를 들어, 1 x 10-3 s-1 이하, 예를 들어, 1 x 10-4 s-1 이하, 예를 들어, 1 x 10-5 s-1 이하, 예를 들어, 1 x 10-6 s-1 이하의 Koff 속도 상수로 인간 VEGF로부터 해리된다.
특정 구체예에서, VEGF dAb는 1 x 10-3 M-1s-1 내지 1 x 10-7 M-1s-1 또는 1 x 10-3 M-1s-1 내지 1 x 10-6 M-1s-1 또는 약 1 x 10-4 M-1s-1 또는 약 1 x 10-5 M-1s-1의 Kon으로 VEGF, 예를 들어, 인간 VEGF에 특이적으로 결합한다. 한 구체예에서, 폴리펩티드, dAb 또는 길항제는 VEGF, 예를 들어, 인간 VEGF에 특이적으로 결합하고, 본 단락에 정의된 해리 상수(KD) 및 Koff로 인간 VEGF로부터 해리된다. 한 구체예에서, 폴리펩티드, dAb 또는 길항제는 VEGF, 예를 들어, 인간 VEGF에 특이적으로 결합하고, 본 단락에 정의된 해리 상수(KD) 및 Kon으로 인간 VEGF로부터 해리된다. 일부 구체예에서, 폴리펩티드 또는 dAb는 본 단락에 열거된 KD 및/또는 Koff 및/또는 Kon으로 VEGF(예를 들어, 인간 VEGF)에 특이적으로 결합하고, 이는 DOM15-26-593의 아미노산 서열을 갖는 dAb의 아미노산 서열과 약 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99% 이상 동일한 아미노산 서열을 포함한다.
dAb는 E. 콜리 또는 피키아 종(예를 들어, P. 파스토리스)에서 발현될 수 있다. 한 구체예에서, 리간드 또는 dAb 단량체는 E. 콜리 또는 피키아 종(예를 들어, P. 파스토리스)에서 발현되는 경우 약 0.5 mg/L 이상의 양으로 분비된다. 본원에 기재된 리간드 및 dAb 단량체는 E. 콜리 또는 피키아 종(예를 들어, P. 파스 토리스)에서 발현되는 경우에 분비될 수 있으나, 이들은 임의의 적합한 방법, 예를 들어, E. 콜리 또는 피키아 종을 이용하지 않는 합성 화학 방법 또는 생물학적 생성 방법을 이용하여 생성될 수 있다.
일부 구체예에서, 폴리펩티드, dAb 또는 길항제는 카멜리드 면역글로불린 가변 도메인, 또는, 예를 들어, 위치 108, 37, 44, 45 및/또는 47의 카멜리드 점라인(germline) 항체 유전자 세그먼트에 의해 엔코딩되는 면역글로불린 가변 도메인에 대해 독특한 하나 이상의 프레임워크 아미노산을 포함하지 않는다.
VEGF의 길항제는 1가 또는 다가일 수 있다. 일부 구체예에서, 길항제는 1가이고, VEGF와 상호작용하는 하나의 결합 부위를 함유하고, 이러한 결합 부위는 본 발명의 폴리펩티드 또는 dAb에 의해 제공된다. 1가 길항제는 하나의 VEGF에 결합하고, 수용체의 활성화 및 신호전달을 발생시킬 수 있는 세포의 표면 상의 VEGF의 가교 또는 집락화(clustering)를 유도하지 않을 수 있다.
대안적으로, VEGF의 길항제는 다가이다. VEGF의 다가 길항제는 VEGF에 대한 특정 결합 부위의 2개 이상의 카피를 함유할 수 있거나, VEGF에 결합하는 2개 이상의 상이한 결합 부위를 함유할 수 있고, 이러한 결합 부위 중 적어도 하나는 본 발명의 dAb에 의해 제공된다. 예를 들어, 본원에 기재된 바와 같이, VEGF의 길항제는 VEGF에 결합하는 dAb의 2개 이상의 카피, 또는 VEGF에 결합하는 2개 이상의 상이한 dAb를 포함하는 이합체, 삼합체 또는 다합체일 수 있다.
다른 구체예에서, dAb는 본원에 기재된 KD로 VEGF에 특이적으로 결합하고, 표준 뮤린 이종이식 모델에서 종양 성장을 억제(예를 들어, 적합한 대조군에 비해 약 10% 이상 종양 성장 억제)한다. 한 구체예에서, 폴리펩티드, dAb 또는 길항제는 약 1 mg/kg 이상, 예를 들어, 약 5 또는 10 mg/kg으로 투여되는 경우에 표준 뮤린 이종이식 모델에서 적합한 대조군에 비해 약 10% 이상, 또는 약 25% 이상, 또는 약 50% 이상 종양 성장을 억제한다.
다른 구체예에서, 폴리펩티드, dAb 또는 길항제는 VEGF에 결합하고, ≤100 nM의 ND50으로 표준 세포 검정에서 VEGF의 활성을 길항시킨다.
특정 구체예에서, dAb는 유효량이 투여되는 경우에 안구 질병의 동물 모델에서 유효하다. 일반적으로, 유효량은 약 1 mg/kg 내지 약 10 mg/kg(예를 들어, 약 1 mg/kg, 약 2 mg/kg, 약 3 mg/kg, 약 4 mg/kg, 약 5 mg/kg, 약 6 mg/kg, 약 7 mg/kg, 약 8 mg/kg, 약 9 mg/kg, 또는 약 10 mg/kg)이다. dAb는, 예를 들어, 하루에 1회 또는 2회, 1 주일에 1회 또는 2회, 1개월에 1회 또는 2회로 투여될 수 있다.
일반적으로, dAb는 안구 전달을 위해 약리학적으로 적절한 담체와 함께 정제된 형태로 이용될 것이다. 통상적으로, 이러한 담체는 임의의 염수 및/또는 완충 매질을 포함하는 수성 용액 또는 알코올/수성 용액, 에멀젼 또는 현탁액을 포함할 수 있다. 필요시 현탁액 중에 폴리펩티드 복합체를 유지시키기 위해 적합한 생리학적으로 허용되는 애쥬번트가 증점제, 예를 들어, 카르복시메틸셀룰로오스, 폴리비닐피롤리돈, 젤라틴 및 알기네이트로부터 선택될 수 있다. 보존제 및 다른 첨가제, 예를 들어, 항균제, 항산화제, 킬레이트 작용제 및 비활성 가스가 또한 존재할 수 있다(Mack (1982) Remington's Pharmaceutical Sciences, 16th Edition). 연장 방출 제형을 포함하는 다양한 적합한 제형이 사용될 수 있다. 이는 이식물, 젤, 나노입자 및 미세입자를 포함할 것이다. 제형의 결막하 전달 후에 안구의 후안부로 약물을 전달하기 위해 약물이 적하된 PLA 나노입자 및 미세입자가 사용되었다(Kompella et al IOVS 2003 44(3) 1192-1201). 특히, 전달 부위에 미세구가 유지되고, 이는 보다 용이하게 청소될 수 있는 나노입자에 비해 망막 약물 전달에 더욱 적절한 것으로 보인다(Amrite et al ARVO abstract #5067/B391 2003).
본 발명의 리간드(예를 들어, 길항제)는 별개로 투여되는 조성물로 사용될수 있거나, 다른 작용제와 함께 사용될 수 있다. 이들은 안구로의 안구 전달을 위한 다양한 약물 및/또는 안구 침투 향상제 및/또는 점성도 향상제를 포함할 수 있다.
약제 조성물은 본 발명의 리간드와 함께 다양한 다른 작용제의 "칵테일", 또는 다양한 특이성을 갖는 본 발명에 따른 리간드, 예를 들어, 투여 전에 풀링(pooling)되거나 풀링되지 않건 간에 다양한 표적 항원 또는 에피토프를 이용하여 선택된 리간드의 조합물을 포함할 수 있다.
안구로의 dAb의 정확한 투여량 및 투여 빈도는 환자의 연령, 성별 및 상태, 다른 약물의 동반 투여, 임상의에 의해 고려되어야 하는 금기 및 다른 파라미터에 좌우될 것이다.
본 발명의 dAb는 저장을 위해 동결건조될 수 있고, 사용 전에 적합한 담체에서 재구성될 수 있다. 이러한 기술은 통상적인 면역글로불린을 이용하여 효과적인 것으로 밝혀졌고, 당 분야에 공지된 동결건조 및 재구성 기술이 사용될 수 있다. 동결건조 및 재구성이 다양한 정도의 항체 활성 손실(예를 들어, 통상적인 면역글로불린과 함께 IgM 항체는 IgG 항체보다 큰 활성 손실을 갖는 경향이 있음)을 발생시킬 수 있고, 사용 수준이 벌충을 위해 조정되어야 함이 당업자에 의해 인지될 것이다.
본 발명의 dAb를 함유하는 조성물 또는 이의 칵테일은 예방적 및/또는 치료적 치료를 위해 투여될 수 있다. 특정 치료 적용에서, 선택된 세포의 집단의 적어도 부분적인 저해, 억제, 조절, 사멸, 또는 일부 다른 측정가능한 파라미터를 달성하기에 충분한 양은 "치료적 유효량"으로 정의될 수 있다. 상기 투여량을 달성하는데 필요한 양은 질병의 중증도 및 환자 본인의 면역계의 일반적인 상태에 좌우될 것이다. 숙련된 임상의는 질병을 치료하거나, 억제하거나, 예방하기 위한 적절한 투여 간격을 결정할 수 있을 것이다.
본원에 기재된 조성물을 이용하여 수행되는 치료 또는 요법은, 하나 이상의 증상이 치료 전에 존재하는 상기 증상 또는 상기 조성물로 치료되지 않은 개체(인간 또는 모델 동물) 또는 다른 적합한 대조군에서의 상기 증상에 비해 감소(예를 들어, 10% 이상의 감소, 또는 임상 평가 스케일에서의 하나 이상의 포인트의 감소)되는 경우에 "유효"한 것으로 간주된다. 증상은 표적이 되는 질병 또는 장애에 따라 명백히 다양할 것이나, 이는 숙련된 임상의 또는 기술자에 의해 측정될 수 있다. 이러한 증상은, 예를 들어, 질병 또는 장애의 하나 이상의 생화학적 지표의 수준(예를 들어, 질병, 병에 걸린 세포 수 등과 관련이 있는 효소 또는 대사산물의 수준)을 모니터하거나, 물리적 표시를 모니터하거나, 허용되는 임상 평가 스케일에 의해 측정될 수 있다.
유사하게, 본원에 기재된 조성물을 이용하여 수행된 예방은 하나 이상의 증상의 발생 또는 중증도가 조성물로 치료되지 않은 유사한 개체(인간 또는 동물 모델)에서의 상기 증상에 비해 지연되거나, 감소되거나, 제거되는 경우에 "유효"하다.
한 구체예에서, 본 발명은 치료학적 유효 용량 또는 유효량의 폴리펩티드, 본 발명에 따른 VEGF 또는 VEGF의 길항제 또는 IL-1 또는 TNF-α 또는 TNF-αR에 결합하는 dAb를 이를 필요로 하는 포유동물에 투여하는 것을 포함하는, 예를 들어, 암(예를 들어, 고형암), 염증 질병, 자가면역 질병, 혈관 증식 질병(예를 들어, AMD(연령 관련 황반 변성))으로부터 선택된 안구 질병 또는 질환을 치료하거나, 억제하거나, 예방하는 방법이다. 이러한 안구 질병 또는 질환의 예는 AMD, 포도막염, 안구 건조, 당뇨망막병증 및 당뇨 황반 부종을 포함한다.
포맷:
증가된 반감기는 면역글로불린, 특히 항체, 더욱 특히 작은 크기의 항체 단편의 생체내 적용에 유용하다. 이러한 단편(Fv, 이황화 결합된 Fv, Fab, scFv, dAb)은 신체로부터의 신속하게 청소되고, 이에 따라, 이들은 신체의 대부분의 부분에 신속하게 도달할 수 있고, 생성시키는데 신속하고, 다루기에 용이하나, 이들의 생체내에서의 짧은 지속에 의해 생체내 적용이 제한되었다. 그러므로, 본원에 기재된 dAb는 생체내에서 증가된 반감기를 제공하고, 결과적으로 신체에서의 보다 긴 지속 기간을 제공하도록 변형될 수 있다.
약동학 분석 및 리간드 반감기 결정을 위한 방법은 당업자에게 친숙할 것이다. 세부사항은 문헌[Kenneth , A et al: Chemical Stability of Pharmaceuticals: A Handbook for Pharmacists and in Peters et al, Pharmacokinetic analysis: A Practical Approach (1996)]에서 발견될 수 있다. 또한, t 알파 및 t 베타 반김기 및 곡선하 영역(AUC)와 같은 약동학 파라미터를 기재하는 문헌["Pharmacokinetics", M Gibaldi & D Perron, published by Marcel Dekker, 2nd Rev. ex edition (1982)]을 참조하라.
반감기(t1/2 알파 및 t1/2 베타) 및 AUC는 시간에 대한 리간드의 혈청 농도의 곡선으로부터 결정될 수 있다. 예를 들어, 곡선을 모델링하기 위해 윈놀린(WinNonlin) 분석 패키지(Pharsight Corp., Mountain View, CA94040, USA에서 이용가능함)가 사용될 수 있다. 첫번째 단계(알파 단계)에서, 리간드는 주로 약간의 제거와 함께 환자 내의 분포를 겪는다. 두번째 단계(베타 단계)는, 리간드가 분포된 경우의 말단 단계로, 리간드가 환자로부터 청소됨에 따라 혈청 농도가 감소한다. t 알파 반감기는 첫번째 단계의 반감기이고, t 베타 반감기는 두번째 단계의 반감기이다. 따라서, 한 구체예에서, 본 발명은 15분 이상의 범위의 tα 반감기를 갖는 본 발명에 따른 리간드 또는 리간드를 포함하는 조성물을 제공한다. 한 구체예에서, 상기 범위의 하한은 30분, 45분, 1시간, 2시간, 3시간, 4시간, 5시간, 6시간, 7시간, 10시간, 11시간 또는 12시간이다. 또한, 또는 대안적으로, 본 발명에 따른 리간드 또는 조성물은 12시간 이하의 범위의 tα 반감기를 가질 것이다. 한 구체예에서, 상기 범위의 상한은 11, 10, 9, 8, 7, 6 또는 5시간이다. 적절한 범위의 예는 1 내지 6시간, 2 내지 5시간 또는 3 내지 4시간이다.
한 구체예에서, 본 발명에 따른 dAb 또는 dAb를 포함하는 조성물은 30분 이상의 범위의 tβ 반감기를 갖는다. 한 구체예에서, 상기 범위의 하한은 45분, 1시간, 2시간, 3시간, 4시간, 5시간, 6시간, 7시간, 10시간, 11시간, 또는 12시간이다. 또한, 또는 대안적으로, 본 발명에 따른 리간드 또는 조성물은 21일 이하의 범위의 tβ 반감기를 갖는다. 한 구체예에서, 상기 범위의 상한은 12시간, 24시간, 2일, 3일, 5일, 10일, 15일 또는 20일이다. 한 구체예에서, 본 발명에 다른 리간드 또는 조성물은 12 내지 60시간 범위의 tβ 반감기를 가질 것이다. 한 추가 구체예에서, 이는 12 내지 48시간 범위일 것이다. 한 추가 구체예에서, 이는 12 내지 26시간 범위일 것이다.
상기 기준 외에, 또는 상기 기준에 대해 대안적으로, 본 발명은 1 mg.분/ml 이상의 범위의 AUC 값(곡선하 영역)을 갖는 본 발명에 따른 dAb 또는 리간드를 포함하는 조성물을 제공한다. 한 구체예에서, 상기 범위의 하한은 5, 10, 15, 20, 30, 100, 200 또는 300 mg.분/ml이다. 또한, 또는 대안적으로, 본 발명에 따른 리간드 또는 조성물은 600 mg.분/ml 이하의 범위의 AUC를 갖는다. 한 구체예에서, 상기 범위의 상한은 500, 400, 300, 200, 150, 100, 75 또는 50 mg.분/ml이다. 한 구체예에서, 본 발명에 따른 리간드는 하기로 구성된 군으로부터 선택된 범위의 AUC를 가질 것이다: 15 내지 150 mg.분/ml, 15 내지 100 mg.분/ml, 15 내지 75 mg.분/ml, 및 15 내지 50mg.분/ml.
본 발명의 dAb는, 예를 들어, PEG 기, 혈청 알부민, 트랜스페린, 트랜스페린 수용체 또는 적어도 이의 트랜스페린 결합 부분, 항체 Fc 영역의 부착, 또는 항체 도메인으로의 컨쥬게이션에 의해 보다 큰 유체역학 크기를 갖도록 포맷화될 수 있다. 예를 들어, dAb는 항체의 보다 큰 항원 결합 단편, 또는 항체(예를 들어, Fab, Fab', F(ab)2, F(ab')2, IgG, scFv로 포맷화됨)로 포맷화될 수 있다. 또 다른 구체예에서, 본 발명에 따른 dAb는 또 다른 폴리펩티드 또는 펩티드와의 융합체 또는 컨쥬게이트로 포맷화될 수 있다.
본 발명의 리간드(예를 들어, dAb 단량체 및 다합체)의 유체역학 크기는 당 분야에 널리 공지된 방법을 이용하여 결정될 수 있다. 예를 들어, 리간드의 유체역학 크기를 결정하기 위해 젤 여과 크로마토그래피가 사용될 수 있다. 리간드의 유체역학 크기를 결정하기에 적합한 젤 투과 매트릭스, 예를 들어, 가교된 아가로오스 매트릭스가 널리 공지되어 있고, 용이하게 이용가능하다.
리간드, 즉 dAb 포맷의 크기(예를 들어, dAb 단량체에 부착된 PEG 모이어티의 크기)는 요망되는 적용, 예를 들어, dAb가 체순환에서 보다 오랜 기간 동안 남거나, 예를 들어, Ig 유사 단백질로서 포맷화시킴으로써 이의 크기가 증가될 수 있는 것이 요망되는 경우에 따라 다양할 수 있다.
생체내에서
반감기를 증가시키는 항원 또는
에피토프의
표적화에
의한 반감기 연장
리간드의 유체역학 크기 및 이의 혈청 반감기는 또한 dAb를 본원에 기재된 바와 같이 생체내에서 반감기를 증가시키는 항원 또는 에피토프에 결합하는 결합 도메인(예를 들어, 항체 또는 항체 단편)에 컨쥬게이션시키거나 회합시킴으로써 증가될 수 있다. 예를 들어, VEGF dAb는 항-혈청 알부민 또는 항-신생아 Fc 수용체 항체 또는 항체 단편, 예를 들어, 항-SA 또는 항-신생아 Fc 수용체 dAb, Fab, Fab' 또는 scFv, 또는 항-SA 어피바디 또는 항-신생아 Fc 수용체 어피바디 또는 항-SA 아비머(avimer), 또는 CTLA-4, 리포칼린, SpA, 어피바디, 아비머, GroEl 및 피브로넥틴으로 구성된 군으로부터 선택되나 이에 제한되지는 않는 스캐폴드를 포함하는 항-SA 결합 도메인에 컨쥬게이션되거나 연결될 수 있다(예를 들어, 상기 결합 도메인의 개시에 대해 2008년 2월 8일에 출원된 PCT/GB2008/000453 참조, 여기서 상기 도메인 및 이의 서열은 참조로서 본원에 포함되고, 본 발명의 본문의 개시의 일부를 형성함). 컨쥬게이션은 혈청 알부민에 결합하는 결합 도메인에 결합(공유 또는 비공유)된 본 발명의 폴리펩티드, dAb 또는 길항제를 포함하는 조성물을 의미한다.
생체내에서 혈청 반감기를 향상시키는 적합한 폴리펩티드는, 예를 들어, 트랜스페린 수용체 특이적 리간드-신경제약 융합 단백질(교시내용이 참조로서 본원에 포함되는 미국 특허 제5,977,307호 참조), 뇌 모세혈관 내피 세포 수용체, 트랜스페린, 트랜스페린 수용체(예를 들어, 가용성 트랜스페린 수용체), 인슐린, 인슐린 유사 성장 인자 1(IGF 1) 수용체, 인슐린-유사 성장 인자 2(IGF 2) 수용체, 인슐린 수용체, 혈액 응고 인자 X, α1-항트립신 및 HNF 1α를 포함한다. 반감기를 향상시키는 적합한 폴리펩티드는 또한 알파-1 당단백질(오로소뮤코이드; AAG), 알파-1 항키모트립신(ACT), 알파-1 마이크로글로불린(단백질 HC; AIM), 항트롬빈 Ⅲ (AT Ⅲ), 아포지질단백질 A-1(Apo A-1), 아포지질단백질 B(Apo B), 세룰로플라스민(Cp), 보체 성분 C3(C3), 보체 성분 C4(C4), C1 에스테라제 억제제(C1 INH), C-반응성 단백질(CRP), 페리틴(FER), 헤모펙신(HPX), 지질단백질(a) (Lp(a)), 만노오스 결합 단백질(MBP), 미오글로빈(Myo), 전알부민(트랜스타이레틴; PAL), 레티놀 결합 단백질(RBP), 및 류머티스 인자(RF)를 포함한다.
세포외 기질로부터의 적합한 단백질은, 예를 들어, 콜라겐, 라미닌, 인테그린 및 피브로넥틴을 포함한다. 콜라겐은 세포외 기질의 주요 단백질이다. 약 15개 유형의 콜라겐 분자가 현재 공지되어 있고, 신체의 다양한 부분에서 발견되고, 예를 들어, 타입 Ⅰ 콜라겐(체내 콜라겐의 90%에 해당함)은 뼈, 피부, 힘줄, 인대, 각막, 내부 장기에서 발견되거나, 타입 Ⅱ 콜라겐은 연골, 추간판(vertebral disc), 척삭, 및 안구의 유리체액에서 발견된다.
혈액으로부터의 적합한 단백질은, 예를 들어, 혈장 단백질(예를 들어, 피브린, α-2 마크로글로불린, 혈청 알부민, 피브리노겐(예를 들어, 피브리노겐 A, 피브리노겐 B), 혈청 아밀로이드 단백질 A, 합토글로빈, 프로필린, 유비퀴틴, 우테로글로불린(uteroglobulin) 및 β-2-마이크로글로불린), 효소 및 효소 억제제(예를 들어, 플라스미노겐, 리소자임, 시스타틴 C, 알파-1-항트립신 및 췌장 트립신 억제제), 면역계의 단백질, 예를 들어, 면역글로불린 단백질(예를 들어, IgA, IgD, IgE, IgG, IgM, 면역글로불린 경쇄(카파/람다)), 수송 단백질(예를 들어, 레티놀 결합 단백질, α-1 마이크로글로불린), 디펜신(defensin)(예를 들어, 베타-디펜신 1, 호중구 디펜신 1, 호중구 디펜신 2 및 호중구 디펜신 3) 등을 포함한다.
혈액뇌장벽 및 신경 조직에서 발견되는 적합한 단백질은, 예를 들어, 멜라노코르틴 수용체, 미엘린, 아스코르베이트 수송체 등을 포함한다.
생체내에서 혈청 반감기를 향상시키는 적합한 폴리펩티드는 또한 신장에 국소화되는 단백질(예를 들어, 폴리시스틴, 타입 Ⅳ 콜라겐, 유기 음이온 수송체 K1, 헤이만 항원(Heymann's antigen)), 간에 국소화되는 단백질(예를 들어, 알코올 탈수소효소, G250), 폐에 국소화되는 단백질(예를 들어, IgA에 결합하는 분비 성분), 심장에 국소화되는 단백질(예를 들어, 확장심근병증과 관련된 HSP 27), 피부에 국소화되는 단백질(예를 들어, 케라틴), 뼈 특이적 단백질, 예를 들어, 골형성 활성을 나타내는 단백질의 전환성장인자 β 상과의 서브셋인 형태형성 단백질(BMP)(예를 들어, BMP-2, BMP-4, BMP-5, BMP-6, BMP-7, BMP-8), 종양 특이적 단백질(예를 들어, 영양막 항원, 허셉틴 수용체, 에스트로겐 수용체, 카텝신(예를 들어, 간 및 비장에서 발견될 수 있는 카텝신 B))을 포함한다.
적합한 질병 특이적 단백질은, 예를 들어, 활성화된 T 세포에서만 발현되는 항원, 예를 들어, LAG-3(림프구 활성화 유전자), 오스테오프로테게린(osteoprotegerin) 리간드(OPGL; Nature 402, 304-309 (1999) 참조), OX40(활성화된 T 세포에서 발현되고, 인간 T 세포 백혈병 바이러스 타입-Ⅰ(HTLV-I) 생성 세포에서 특이적으로 상향조절되는 TNF 수용체 과의 일원; Immunol. 165 (1):263-70 (2000) 참조)을 포함한다. 적합한 질병 특이적 단백질은 또한, 예를 들어, 금속단백분해효소(관절염/암과 관련됨), 예를 들어, CG6512 드로소필라(Drosophila), 인간 파라플레긴(paraplegin), 인간 FtsH, 인간 AFG3L2, 뮤린 ftsH; 및 혈관신생 성장인자, 예를 들어, 산성 섬유모세포 성장인자(FGF-1), 염기성 섬유모세포 성장인자(FGF-2), 혈관 내피 성장 인자/혈관 투과 인자(VEGF/VPF), 전환성장인자-α(TGF α), 종양 괴사 인자-알파(TNF-α), 안지오제닌, 인터루킨-3(IL-3), 인터루킨-8(IL-8), 혈소판 유래 내피 성장 인자(PD-ECGF), 태반 성장인자(P1GF), 미드카인(midkine) 혈소판 유래 성장 인자-BB (PDGF), 및 프랙탈카인을 포함한다.
생체내에서 혈청 반감기를 향상시키는 적합한 폴리펩티드는 또한 스트레스 단백질, 예를 들어, 열 쇼크 단백질(HSP)를 포함한다. HSP는 보통 세포내에서 발견된다. 이들이 세포외에서 발견되는 경우, 이는 세포가 사멸되고, 이의 내용물이 유출된 것을 나타낸다. 이러한 프로그램화되지 않은 세포 사멸(괴사)은 외상, 질병 또는 손상의 결과로서 세포외 HSP가 면역계로부터의 반응을 촉발시키는 경우에 발생한다. 세포외 HSP로의 결합은 본 발명의 조성물을 질병 부위로 국소화시킬 수 있다.
Fc 수송과 관련된 적합한 단백질은, 예를 들어, 브람벨(Brambell) 수용체(FcRB로도 공지되어 있음)을 포함한다. 이러한 Fc 수용체는 두개의 기능을 갖고, 이러한 두 기능 모두는 전달에 잠재적으로 유용하다. 상기 기능은, (1) 태반을 통한 모체로부터 아이로의 IgG의 수송, 및 (2) 분해로부터 IgG의 보호에 의한 이의 혈청 반감기의 연장이다. 상기 수용체는 엔도솜으로부터 IgG를 재생시키는 것으로 생각된다(Holliger et al , Nat Biotechnol 15(7):632-6 (1997) 참조).
혈청 알부민에 결합하는
dAb
본 발명은 한 구체예에서 안구 표적 분자, 예를 들어, VEGF, IL-1 또는 TNF-α에 결합하는 제 1 dAb, 및 혈청 알부민(SA)에 결합하는 제 2의 dAb에 관한 것으로, 상기 제 2 dAb는 표면 플라즈몬 공명에 의해 결정시 1 nM 내지 1, 2, 3, 4, 5, 10, 20, 30, 40, 50, 60, 70, 100, 200, 300, 400 또는 500 μM(즉, 1 x 10-9 내지 5 x 10-4), 또는 100 nM 내지 10 μM, 또는 1 내지 5 μM 또는 3 내지 70 nM 또는 10 nM 내지 1, 2, 3, 4 또는 5μM의 KD로 SA에 결합한다. 예를 들어, 표면 플라즈몬 공명에 의해 결정시 30 내지 70 nM. 한 구체예에서, 제 1 dAb(또는 dAb 단량체)는 표면 플라즈몬 공명에 의해 결정시 약 1, 50, 70, 100, 150, 200, 300 nM 또는 1, 2 또는 3 μM의 KD로 SA(예를 들어, HSA)에 결합한다. 한 구체예에서, 제 1 항-SA dAb 및 VEGF에 대한 제 2 dAb를 포함하는 이중 특이적 리간드에 대해, 표적에 대한 제 2 dAb의 친화성(예를 들어, 비아코어(BiaCore)를 이용한 표면 플라즈몬 공명에 의해 측정되는 KD 및/또는 Koff)은 SA에 대한 제 1 dAb의 친화성의 1 내지 100000배(예를 들어, 100 내지 100000배, 또는 1000 내지 100000배, 또는 10000 내지 100000배)이다. 한 구체예에서, 혈청 알부민은 인간 혈청 알부민(HSA)이다. 예를 들어, 제 1 dAb는 약 10 μM의 친화성으로 SA에 결합하고, 제 2 dAb는 이의 표적에 100 pM의 친화성으로 결합한다. 한 구체예에서, 혈청 알부민은 인간 혈청 알부민(HSA)이다. 한 구체예에서, 제 1 dAb는 약 50, 예를 들어, 70, 100, 150 또는 200 nM의 KD로 SA(예를 들어, HSA)에 결합한다. 이중 특이적 리간드의 세부사항은 WO 03/002609호, WO 04/003019호 및 WO 04/058821호에서 발견된다.
한 구체예에서, 본 발명의 dAb는 표면 플라즈몬 공명에 의해 결정시 1 nM 내지 1, 2, 3, 4, 5, 10, 20, 30, 40, 50, 60, 70, 100, 200, 300, 400 또는 500 μM(즉, 1 x 10-9 내지 5 x 10-4), 또는 100 nM 내지 10 μM, 또는 1 내지 5 μM 또는 3 내지 70 nM 또는 10 nM 내지 1, 2, 3, 4 또는 5μM의 KD로 혈청 알부민(SA)에 결합하는 dAb를 포함할 수 있다. 예를 들어, 표면 플라즈몬 공명에 의해 결정시 30 내지 70 nM. 한 구체예에서, 제 1 dAb(또는 dAb 단량체)는 표면 플라즈몬 공명에 의해 결정시 약 1, 50, 70, 100, 150, 200, 300 nM 또는 1, 2 또는 3 μM의 KD로 SA(예를 들어, HSA)에 결합한다. 한 구체예에서, 제 1 및 제 2 dAb는 링커, 예를 들어, 1 내지 4개의 아미노산 또는 1 내지 3개의 아미노산, 또는 3개를 초과하는 아미노산 또는 4, 5, 6, 7, 8, 9, 10, 15 또는 20개를 초과하는 아미노산의 링커에 의해 연결된다. 한 구체예에서, 보다 긴 링커(3개를 초과하는 아미노산)가 효능(길항제 내의 dAb 중 하나 또는 둘 모두의 KD)을 향상시키기 위해 사용된다.
특정 구체예에서, dAb는 인간 혈청 알부민에 결합하고, 알부민으로의 결합에 대해,
MSA-16, MSA-26(상기 서열의 개시에 대해 WO 04/003019호 참조, 이의 서열 및 이의 핵산 대응부는 참조로서 본원에 포함되고, 본 발명의 본문의 개시의 일부를 형성함),
DOM7m-16 (SEQ ID NO: 473), DOM7m-12 (SEQ ID NO: 474), DOM7m-26 (SEQ ID NO: 475), DOM7r-1 (SEQ ID NO: 476), DOM7r-3 (SEQ ID NO: 477), DOM7r-4 (SEQ ID NO: 478), DOM7r-5 (SEQ ID NO: 479), DOM7r-7 (SEQ ID NO: 480), DOM7r-8 (SEQ ID NO: 481), DOM7h-2 (SEQ ID NO: 482), DOM7h-3 (SEQ ID NO: 483), DOM7h-4 (SEQ ID NO: 484), DOM7h-6 (SEQ ID NO: 485), DOM7h-1 (SEQ ID NO: 486), DOM7h-7 (SEQ ID NO: 487), DOM7h-22 (SEQ ID NO: 489), DOM7h-23 (SEQ ID NO: 490), DOM7h-24 (SEQ ID NO: 491), DOM7h-25 (SEQ ID NO: 492), DOM7h-26 (SEQ ID NO: 493), DOM7h-21 (SEQ ID NO: 494), DOM7h-27 (SEQ ID NO: 495), DOM7h-8 (SEQ ID NO: 496), DOM7r-13 (SEQ ID NO: 497), DOM7r-14 (SEQ ID NO: 498), DOM7r-15 (SEQ ID NO: 499), DOM7r-16 (SEQ ID NO: 500), DOM7r-17 (SEQ ID NO: 501), DOM7r-18 (SEQ ID NO: 502), DOM7r-19 (SEQ ID NO: 503), DOM7r-20 (SEQ ID NO: 504), DOM7r-21 (SEQ ID NO: 505), DOM7r-22 (SEQ ID NO: 506), DOM7r-23 (SEQ ID NO: 507), DOM7r-24 (SEQ ID NO: 508), DOM7r-25 (SEQ ID NO: 509), DOM7r-26 (SEQ ID NO: 510), DOM7r-27 (SEQ ID NO: 511), DOM7r-28 (SEQ ID NO: 512), DOM7r-29 (SEQ ID NO: 513), DOM7r-30 (SEQ ID NO: 514), DOM7r-31 (SEQ ID NO: 515), DOM7r-32 (SEQ ID NO: 516), DOM7r-33 (SEQ ID NO: 517)(상기 서열의 개시에 대해 WO 2007/080392호 참조, 이의 서열 및 이의 핵산 대응부는 참조로서 본원에 포함되고, 본 발명의 본문의 개시의 일부를 형성함; 본 단락의 SEQ ID NO는 WO 2007/080392호에 기재된 것임),
dAb8 (dAb10), dAb10, dAb36, dAb7r20 (DOM7r20), dAb7r21 (DOM7r21), dAb7r22 (DOM7r22), dAb7r23 (DOM7r23), dAb7r24 (DOM7r24), dAb7r25 (DOM7r25), dAb7r26 (DOM7r26), dAb7r27 (DOM7r27), dAb7r28 (DOM7r28), dAb7r29 (DOM7r29), dAb7r29 (DOM7r29), dAb7r31 (DOM7r31), dAb7r32 (DOM7r32), dAb7r33 (DOM7r33), dAb7r33 (DOM7r33), dAb7h22 (DOM7h22), dAb7h23 (DOM7h23), dAb7h24 (DOM7h24), dAb7h25 (DOM7h25), dAb7h26 (DOM7h26), dAb7h27 (DOM7h27), dAb7h30 (DOM7h30), dAb7h31 (DOM7h31), dAb2 (dAbs 4,7,41), dAb4, dAb7, dAb11, dAb12 (dAb7m12), dAb13 (dAb 15), dAb15, dAb16 (dAb21, dAb7m16) , dAb17, dAb18, dAb19, dAb21, dAb22, dAb23, dAb24, dAb25 (dAb26, dAb7m26), dAb27, dAb30 (dAb35), dAb31, dAb33, dAb34, dAb35, dAb38 (dAb54), dAb41, dAb46 (dAbs 47, 52 및 56), dAb47, dAb52, dAb53, dAb54, dAb55, dAb56, dAb7m12, dAb7m16, dAb7m26, dAb7r1 (DOM7r1), dAb7r3 (DOM7r3), dAb7r4 (DOM7r4), dAb7r5 (DOM7r5), dAb7r7 (DOM7r7), dAb7r8 (DOM7r8), dAb7r13 (DOM7r13), dAb7r14 (DOM7r14), dAb7r15 (DOM7r15), dAb7r16 (DOM7r16), dAb7r17 (DOM7r17), dAb7r18 (DOM7r18), dAb7r19 (DOM7r19), dAb7h1 (DOM7h1), dAb7h2 (DOM7h2), dAb7h6 (DOM7h6), dAb7h7 (DOM7h7), dAb7h8 (DOM7h8), dAb7h9 (DOM7h9), dAb7h10 (DOM7h10), dAb7h11 (DOM7h11), dAb7h12 (DOM7h12), dAb7h13 (DOM7h13), dAb7h14 (DOM7h14), dAb7p1 (DOM7p1), 및 dAb7p2 (DOM7p2)(상기 서열의 개시에 대해 2008년 2월 8일에 출원되고 WO 2008/096158호로 공개된 PCT/GB2008/000453호 참조, 이의 서열 및 이의 핵산 대응부는 참조로서 본원에 포함되고, 본 발명의 본문의 개시의 일부를 형성함)로 구성된 군으로부터 선택된 dAb와 경쟁한다. 대안적 명칭이 dAb 뒤의 괄호에 제시되어 있고, 예를 들어, dAb8은 dAb10의 대안적 명칭, 즉 dAb8 (dAb10)을 갖는다.
특정 구체예에서, dAb는 인간 혈청 알부민에 결합하고,
MSA-16, MSA-26,
D0M7m-16 (SEQ ID NO: 473), D0M7m-12 (SEQ ID NO: 474), DOM7m-26 (SEQ ID NO: 475), DOM7r-1 (SEQ ID NO: 476), DOM7r-3 (SEQ ID NO: 477), DOM7r-4 (SEQ ID NO: 478), DOM7r-5 (SEQ ID NO: 479), DOM7r-7 (SEQ ID NO: 480), DOM7r-8 (SEQ ID NO: 481), DOM7h-2 (SEQ ID NO: 482), DOM7h-3 (SEQ ID NO: 483), DOM7h-4 (SEQ ID NO: 484), DOM7h-6 (SEQ ID NO: 485), DOM7h-1 (SEQ ID NO: 486), DOM7h-7 (SEQ ID NO: 487), DOM7h-22 (SEQ ID NO: 489), DOM7h-23 (SEQ ID NO: 490), DOM7h-24 (SEQ ID NO: 491), DOM7h-25 (SEQ ID NO: 492), DOM7h-26 (SEQ ID NO: 493), DOM7h-21 (SEQ ID NO: 494), DOM7h-27 (SEQ ID NO: 495), DOM7h-8 (SEQ ID NO: 496), DOM7r-13 (SEQ ID NO: 497), DOM7r-14 (SEQ ID NO: 498), DOM7r-15 (SEQ ID NO: 499), DOM7r-16 (SEQ ID NO: 500), DOM7r-17 (SEQ ID NO: 501), DOM7r-18 (SEQ ID NO: 502), DOM7r-19 (SEQ ID NO: 503), DOM7r-20 (SEQ ID NO: 504), DOM7r-21 (SEQ ID NO: 505), DOM7r-22 (SEQ ID NO: 506), DOM7r-23 (SEQ ID NO: 507), DOM7r-24 (SEQ ID NO: 508), DOM7r-25 (SEQ ID NO: 509), DOM7r-26 (SEQ ID NO: 510), DOM7r-27 (SEQ ID NO: 511), DOM7r-28 (SEQ ID NO: 512), DOM7r-29 (SEQ ID NO: 513), DOM7r-30 (SEQ ID NO: 514), DOM7r-31 (SEQ ID NO: 515), DOM7r-32 (SEQ ID NO: 516), DOM7r-33 (SEQ ID NO: 517)(본 단락의 SEQ ID NO는 WO 2007/080392호에 기재된 것임),
dAb8, dAb10, dAb36, dAb7r20, dAb7r21, dAb7r22, dAb7r23, dAb7r24, dAb7r25, dAb7r26, dAb7r27, dAb7r28, dAb7r29, dAb7r30, dAb7r31, dAb7r32, dAb7r33, dAb7h21, dAb7h22, dAb7h23, Ab7h24, Ab7h25, Ab7h26, dAb7h27, dAb7h30, dAb7h31, dAb2, dAb4, dAb7, dAb11, dAb12, dAb13, dAb15, dAb16, dAb17, dAb18, dAb19, dAb21, dAb22, dAb23, dAb24, dAb25, dAb26, dAb27, dAb30, dAb31, dAb33, dAb34, dAb35, dAb38, dAb41, dAb46, dAb47, dAb52, dAb53, dAb54, dAb55, dAb56, dAb7m12, dAb7m16, dAb7m26, dAb7r1, dAb7r3, dAb7r4, dAb7r5, dAb7r7, dAb7r8, dAb7r13, dAb7r14, dAb7r15, dAb7r16, dAb7r17, dAb7r18, dAb7r19, dAb7h1, dAb7h2, dAb7h6, dAb7h7, dAb7h8, dAb7h9, dAb7h10, dAb7h11, dAb7h12, dAb7h13, dAb7h14, dAb7p1, 및 dAb7p2로 구성된 군으로부터 선택된 dAb의 아미노산 서열과 약 80% 이상, 또는 약 85% 이상, 또는 약 90% 이상, 또는 약 95% 이상, 또는 약 96% 이상, 또는 약 97% 이상, 또는 약 98% 이상, 또는 약 99% 이상의 아미노산 서열 동일성을 갖는 아미노산 서열을 포함한다.
예를 들어, 인간 혈청 알부민에 결합하는 dAb는,
DOM7h-2 (SEQ ID NO:482), DOM7h-3 (SEQ ID NO:483), DOM7h-4 (SEQ ID NO:484), DOM7h-6 (SEQ ID NO:485), DOM7h-1 (SEQ ID NO:486), DOM7h-7 (SEQ ID NO:487), DOM7h-8 (SEQ ID NO:496), DOM7r-13 (SEQ ID NO:497), DOM7r-14 (SEQ ID NO:498), DOM7h-22 (SEQ ID NO:489), DOM7h-23 (SEQ ID NO:490), DOM7h-24 (SEQ ID NO:491), DOM7h-25 (SEQ ID NO:492), DOM7h-26 (SEQ ID NO :493), DOM7h-21 (SEQ ID NO:494), DOM7h-27 (SEQ ID NO:495)(본 단락의 SEQ ID NO는 WO 2007/080392호에 기재된 것임),
dAb8, dAb10, dAb36, dAb7h21, dAb7h22, dAb7h23, Ab7h24, Ab7h25, Ab7h26, dAb7h27, dAb7h30, dAb7h31, dAb2, dAb4, dAb7, dAb11, dAb12, dAb13, dAb15, dAb16, dAb17, dAb18, dAb19, dAb21, dAb22, dAb23, dAb24, dAb25, dAb26, dAb27, dAb30, dAb31, dAb33, dAb34, dAb35, dAb38, dAb41, dAb46, dAb47, dAb52, dAb53, dAb54, dAb55, dAb56, dAb7h1, dAb7h2, dAb7h6, dAb7h7, dAb7h8, dAb7h9, dAb7h10, dAb7h11, dAb7h12, dAb7h13 및 dAb7h14와 약 90% 이상, 또는 약 95% 이상, 또는 약 96% 이상, 또는 약 97% 이상, 또는 약 98% 이상, 또는 약 99% 이상의 아미노산 서열 동일성을 갖는 아미노산 서열을 포함할 수 있다.
특정 구체예에서, dAb는 인간 혈청 알부민에 결합하고,
DOM7h-2 (SEQ ID NO:482), DOM7h-6 (SEQ ID NO:485), DOM7h-1 (SEQ ID NO:486), DOM7h-7 (SEQ ID NO:487), DOM7h-8 (SEQ ID NO:496), DOM7h-22 (SEQ ID NO:489), DOM7h-23 (SEQ ID NO:490), DOM7h-24 (SEQ ID NO:491), DOM7h-25 (SEQ ID NO:492), DOM7h-26 (SEQ ID NO:493), DOM7h-21 (SEQ ID NO:494), DOM7h-27 (SEQ ID NO:495)(본 단락의 SEQ ID NO는 WO 2007/080392호에 기재된 것임),
dAb7h21, dAb7h22, dAb7h23, Ab7h24, Ab7h25, Ab7h26, dAb7h27, dAb7h30, dAb7h31, dAb2, dAb4, dAb7, dAb38, dAb41, dAb7h1, dAb7h2, dAb7h6, dAb7h7, dAb7h8, dAb7h9, dAb7h10, dAb7h11, dAb7h12, dAb7h13 및 dAb7h14로 구성된 군으로부터 선택된 dAb의 아미노산 서열과 약 80% 이상, 또는 약 85% 이상, 또는 약 90% 이상, 또는 약 95% 이상, 또는 약 96% 이상, 또는 약 97% 이상, 또는 약 98% 이상, 또는 약 99% 이상의 아미노산 서열 동일성을 갖는 아미노산 서열을 포함한다.
더욱 특정한 구체예에서, dAb는 인간 혈청 알부민에 결합하는 Vκ dAb이고, 이는,
DOM7h-2 (SEQ ID NO:482), DOM7h-6 (SEQ ID NO:485), DOM7h-1 (SEQ ID NO:486), DOM7h-7 (SEQ ID NO:487), DOM7h-8 (SEQ ID NO:496)(본 단락의 SEQ ID NO는 WO 2007/080392호에 기재된 것임),
dAb2, dAb4, dAb7, dAb38, dAb41, dAb54, dAb7h1, dAb7h2, dAb7h6, dAb7h7, dAb7h8, dAb7h9, dAb7h10, dAb7h11, dAb7h12, dAb7h13 및 dAb7h14로 구성된 군으로부터 선택된 아미노산 서열을 가진다.
더욱 특정한 구체예에서, dAb는 인간 혈청 알부민에 결합하는 VH dAb이고, 이는 dAb7h30 및 dAb7h31로부터 선택된 아미노산 서열을 갖는다.
더욱 특정한 구체예에서, dAb는 dAb7h11 또는 dAb7hl4이다.
다른 구체예에서, dAb, 리간드 또는 길항제는 인간 혈청 알부민에 결합하고, 전술된 아미노산 서열 중 임의의 서열의 CDR 중 1개, 2개 또는 3개, 예를 들어, dAb7h11 또는 dAb7h14의 CDR 중 1개, 2개 또는 3개를 포함한다.
혈청 알부민에 결합하는 적합한 카멜리드 VHH는 WO 2004/041862호(Ablynx N.V.) 및 WO 2007/080392호(이의 VHH 서열 및 이의 핵산 대응부는 참조로서 본원에 포함되고, 본 발명의 본문의 개시의 일부를 형성함)에 기재된 것, 예를 들어, 서열 A(SEQ ID NO:518), 서열 B(SEQ ID NO:519), 서열 C(SEQ ID NO:520), 서열 D(SEQ ID NO:521), 서열 E(SEQ ID NO:522), 서열 F(SEQ ID NO:523), 서열 G(SEQ ID NO:524), 서열 H(SEQ ID NO:525), 서열 I(SEQ ID NO:526), 서열 J(SEQ ID NO:527), 서열 K(SEQ ID NO:528), 서열 L(SEQ ID NO:529), 서열 M(SEQ ID NO:530), 서열 N(SEQ ID NO:531), 서열 O(SEQ ID NO:532), 서열 P(SEQ ID NO:533), 서열 Q(SEQ ID NO:534)를 포함하며, 이러한 서열 번호는 WO 2007/080392호 또는 WO 2004/041862호(Ablynx N.V.)에 언급된 것에 해당한다. 특정 구체예에서, 카멜리드 VHH는 인간 혈청 알부민에 결합하고, WO 2007/080392호에 기재된 ALB1 또는 SEQ ID NOS:518-534 중 어느 하나와 약 80% 이상, 또는 약 85% 이상, 또는 약 90% 이상, 또는 약 95% 이상, 또는 약 96% 이상, 또는 약 97% 이상, 또는 약 98% 이상, 또는 약 99% 이상의 아미노산 서열 동일성을 갖는 아미노산 서열을 포함하며, 이러한 서열 번호는 WO 2007/080392호 또는 WO 2004/041862호에 언급된 것에 해당한다.
일부 구체예에서, dAb 조성물은 혈청 알부민(예를 들어, 인간 혈청 알부민)으로의 결합에 대해 본원에 기재된 임의의 항-혈청 알부민 dAb와 경쟁하는 항-혈청 알부민 dAb를 포함한다.
반감기 연장
모이어티(예를 들어, 알부민)으로의
컨쥬게이션
한 구체예에서, (하나 이상의) 반감기 연장 모이어티(예를 들어, 알부민, 트랜스페린 및 이의 단편 및 유사체)가 VEGF 결합(또는 IL-1, 또는 TNF-α 결합 또는 TNF-αR 결합) dAb에 컨쥬게이션되거나 이와 회합된다. VEGF(또는 IL-1, 또는 TNF-α 또는 TNF-αR) 결합 포맷에 사용하기에 적합한 알부민, 알부민 단편 또는 알부민 변이체의 예는 개시내용이 본원에 참조로서 포함되고, 본 발명의 본문의 기재의 일부를 형성하는 WO 2005/077042호에 기재되어 있다. 특히, 하기 알부민, 알부민 단편 또는 알부민 변이체가 본 발명에 사용될 수 있다:
● SEQ ID NO: 1(WO 2005/077042호에 개시됨, 이 서열은 명백히 참조로서 본 발명의 개시에 포함됨);
● WO 2005/077042호의 SEQ ID NO:1의 아미노산 1-387을 포함하거나 이로 구성되는 알부민 단편 또는 변이체;
● (a) WO 2005/077042호의 SEQ ID NO:1의 아미노산 54 내지 61; (b) WO 2005/077042호의 SEQ ID NO:1의 아미노산 76 내지 89; (c) WO 2005/077042호의 SEQ ID NO:1의 아미노산 92 내지 100; (d) WO 2005/077042호의 SEQ ID NO:1의 아미노산 170 내지 176; (e) WO 2005/077042호의 SEQ ID NO:1의 아미노산 247 내지 252; (f) WO 2005/077042호의 SEQ ID NO:1의 아미노산 266 내지 277; (g) WO 2005/077042호의 SEQ ID NO:1의 아미노산 280 내지 288; (h) WO 2005/077042호의 SEQ ID NO:1의 아미노산 362 내지 368; (i) WO 2005/077042호의 SEQ ID NO:1의 아미노산 439 내지 447; (j) WO 2005/077042호의 SEQ ID NO:1의 아미노산 462 내지 475; (k) WO 2005/077042호의 SEQ ID NO:1의 아미노산 478 내지 486; 및 (l) WO 2005/077042호의 SEQ ID NO:1의 아미노산 560 내지 566으로 구성된 군으로부터 선택된 아미노산 서열을 포함하는 알부민, 또는 이의 단편 또는 변이체.
VEGF 결합 포맷에 사용하기에 적합한 알부민, 단편 및 유사체의 추가 예는 개시내용이 참조로서 본원에 포함되고, 본 발명의 본문의 일부를 형성하는 WO 03/076567호에 기재되어 있다. 특히, 하기 알부민, 단편 또는 변이체가 본 발명에 사용될 수 있다:
● WO 03/076567호, 예를 들어, 도 3에 기재된 인간 혈청 알부민(이의 서열 정보는 명백히 참조로서 본 발명의 개시에 포함됨);
● 66,500의 화학식 분자량을 갖는 585개의 아미노산의 단일한 당화되지 않은 폴리펩티드 사슬로 구성된 인간 혈청 알부민(HA)(Meloun, et al , FEBS Letters 58:136 (1975); Behrens, et al ., Fed . Proc . 34:591 (1975); Lawn, et al ., Nucleic Acids Research 9:6102-6114 (1981); Minghetti, et al ., J. Biol . Chem . 261:6747 (1986) 참조);
● 문헌[Weitkamp, et al ., Ann . Hum . Genet . 37:219 (1973)]에 기재된 알부민의 다형 변이체 또는 유사체 또는 단편;
● EP 322094호에 기재된 알부민 단편 또는 변이체, 예를 들어, HA(1-373), HA(1-388), HA(1-389), HA(1-369), 및 HA(1-419) 및 1-369와 1-419 사이의 단편;
● EP 399666호에 기재된 알부민 단편 또는 변이체, 예를 들어, HA(1-177) 및 HA(1-200) 및 HA(1-X) 사이의 단편, 여기서 X는 178에서 199 중 임의의 수임.
본 발명의 dAb를 포맷화시키는데 (하나 이상의) 반감기 연장 모이어티(예를 들어, 알부민, 트랜스페린 및 이의 단편 및 유사체)가 사용되는 경우, 이는 임의의 적합한 방법, 예를 들어, 직접 융합, 예를 들어, 융합 단백질을 엔코딩하는 단일한 누클레오티드 작제물을 이용하여 컨쥬게이션될 수 있고, 상기 융합 단백질은 dAb에 대해 N- 또는 C-말단으로 위치된 반감기 연장 모이어티를 갖는 단일한 폴리펩티드 사슬로 엔코딩된다. 대안적으로, 컨쥬게이션은 모이어티 사이에 펩티드 링커, 예를 들어, WO 03/076567호 또는 WO 2004/003019호에 기재된 펩티드 링커를 이용함으로써 달성될 수 있다(상기 링커의 개시내용은 본 발명에서 사용하기 위한 예를 제공하기 위해 본 발명의 개시내용에 참조로서 포함됨). 통상적으로, 생체내에서 혈청 반감기를 향상시키는 폴리펩티드는 생체내에서 자연 발생하고, 유기체(예를 들어, 인간)으로부터 원치 않는 물질을 제거하는 내생 메커니즘에 의한 분해 또는 제거에 내성이 있는 폴리펩티드이다. 예를 들어, 생체내에서 혈청 반감기를 향상시키는 폴리펩티드는 세포외 기질로부터의 단백질, 혈액에서 발견되는 단백질, 혈액뇌장벽 또는 신경 조직에서 발견되는 단백질, 신장, 간, 폐, 심장, 피부 또는 뼈에 국소화되는 단백질, 스트레스 단백질, 질병 특이적 단백질, 또는 Fc 수송과 관련된 단백질로부터 선택될 수 있다.
본 발명의 dAb는 제 2 면역글로불린 단일 가변 도메인에 직접 융합되는 제 1 면역글로불린 단일 가변 도메인을 함유하는 융합 단백질로 포맷화될 수 있다. 요망시, 이러한 포맷은 반감기 연장 모이어티를 추가로 포함할 수 있다. 예를 들어, 리간드는 혈청 알부민에 결합하는 면역글로불린 단일 가변 도메인에 직접 융합되는 제 2 면역글로불린 단일 가변 도메인에 직접 융합되는 제 1 면역글로불린 단일 가변 도메인을 포함할 수 있다.
일반적으로, 표적에 대한 결합 특이성을 갖는 결합 부위를 갖는 폴리펩티드 도메인의 배향, 및 리간드가 링커를 포함하는지의 여부는 설계 선택 사항이다. 그러나, 링커를 갖거나 갖지 않는 일부 배향은 다른 배향보다 나은 결합 특성을 제공할 수 있다. 모든 배향(예를 들어, dAb1-링커-dAb2; dAb2-링커-dAb1)은 본 발명에 포함되고, 요망되는 결합 특성을 제공하는 배향을 함유하는 리간드는 스크리닝에 의해 용이하게 확인될 수 있다.
dAb 단량체, 이합체 및 삼합체를 포함하는 본 발명에 따른 dAb는 CH2 및 CH3 도메인 중 하나 또는 둘 모두, 및 임의로 힌지 영역을 포함하는 항체 Fc 영역에 연결될 수 있다. 예를 들어, 상기 폴리펩티드를 제조하기 위해 Fc 영역에 단일 누클레오티드 서열로서 연결된 리간드를 엔코딩하는 벡터가 사용될 수 있다.
본 발명의 구체예에서, dAb는, 예를 들어, WO 2008/149147호에 기재된 바와 같이 피키아 파스토리스 또는 E. 콜리 E.G.에 의한 발현에 최적화된, 코돈 최적화된 누클레오티드 서열에 의해 엔코딩될 수 있다.
예시
실시예 1:
래빗의 안구로의 DOM15-26-593(myc 태깅된(tagged) 항-VEGF dAb)의 국소 전달:
DOM15-26-593은 WO 2008/149147호에 기재된 바와 같이 선택되고, 제조될 수 있으며, 이는 도 1a에 기재된 아미노산 서열(SEQ ID NO 1)을 갖는다.
Myc 태깅된 DOM15-26-593(도 1a에 도시된 아미노산 서열(SEQ ID NO 1)을 갖는 Dom15-26-593 dAb를 제조하고, 본 실험에서 c-myc-태깅된 항-VEGF dAb로 사용하였음)을 104 mM 염화나트륨, 0.02% (w/v) Tween 80, 0.5% (w/v) 소듐 카프레이트 및 0.3% 또는 1.5% (w/v) 히드록시프로필 메틸셀룰로오스(HPMC)가 보충된 50 mM 아세트산 나트륨 완충액(pH 7.0)에서 2 mg/ml 농도로 제형화된 내독소 비함유 제조물로 제조하였다. 성체 친칠라 바스타드(Chinchilla Bastard) 래빗을 찰스 리버사(Charles River, Germany)에서 구입하였다. 동물을 사용 전에 새 환경에 순응하도록 두었다. 6마리의 암컷 래빗의 좌측 안구에 50 마이크로리터의 항-VEGF dAb의 2 mg/ml 용액을 4시간의 기간 동안 20분 마다 투여하였다. 각각의 투여는 결막하낭에서 이루어졌다. 3마리의 래빗에 0.3% HPMC에 제형화된 항-VEGF dAb를 투여하고, 3마리의 래빗에 1.5% HPMC에 제형화된 약물을 투여하였다. 마지막 투여 2시간 후, 동물을 선별하였다. 안락사 시기에 최대한 가깝게 각각의 동물로부터의 두 안구를 적출하여 확인하였다. 각각의 안구를 PBS에서 세척하여 표면으로부터 임의의 과량의 약물을 제거하였다. 방수 및 유리체액의 샘플을 수집하고, 분석 전에 동결(-20℃)시켜 저장하였다. dAb가 재조합 인간 VEGF 단백질이 코팅된 플레이트에서 포획되고, c-myc 태그에 대한 특이성을 갖는 항체를 이용하여 검출되는 샌드위치 ELISA 검정을 이용하여 존재하는 DOM15-26-593(항-VEGF-dAb)의 농도에 대해 방수 및 유리체액의 샘플을 시험하였다.
상기 기재된 VEGF dAb ELISA 검정을 다음과 같이 수행하였다:
상기 검정에서 VEGF dAb를 포획하기 위해 이뮤노솔브(Immunsorb) 플레이트(Nunc로부터 구입됨)의 표면에 코팅된 재조합 인간 VEGF(rVEGF, R&D Systems에서 구입)를 사용하였다. 플레이트를 세척하여 임의의 결합되지 않은 dAb를 제거하였다, 이후, 결합된 dAb를 VEGF dab의 Myc 태그에 대한 항체(Sigm에서 구입)를 이용하여 검출하였다. 과량의 항체를 세척하여 제거하고, 결합된 항-myc 항체를 항-마우스 IgG 퍼옥시다제 컨쥬게이트(Sigma)를 이용하여 검출하였다. 검정을 TMB 용액을 이용하여 발달시키고, 산을 이용하여 중지시켰다. 상기 검정으로부터의 신호는 dAb의 양에 비례하였다. 상기 검정의 단계는 하기와 같이 요약된다:
플레이트 코팅:
1. 플레이트를 코팅하기 위해 0.25μg/mL의 충분한 rVEGF를 제조하였다(각 ELISA 플레이트에 대해 5 ml). 이를, 5 mL의 카보네이트 코팅 완충액(0.2M 탄산나트륨-중탄산나트륨 코팅 완충액 용액 pH 9.4(Pierce, Cat No: 28382))에 25 μL의 스톡 VEGF를 첨가하고, 역위에 의해 혼합하여 각각의 플레이트에 대해 수행하였다.
2. 50μL의 rVEGF(0.25μg/mL) 용액을 다채널 피펫을 이용하여 이뮤노소브(Immunsorb) 96-웰 ELISA 플레이트의 각각의 웰에 첨가하였다.
3. 플레이트에 플라스틱 뚜껑을 덮고, 약 42시간 동안 4℃에 저장하였다.
세척 및 블로킹 플레이트:
4. 플레이트를 4℃의 저장으로부터 분리시켰다.
5. 각각의 플레이트를 PBS+0.1% Tween 20으로 6회 세척하였다.
6. 100μL의 검정 블로킹 완충액(1% BSA/PBS)을 각각의 플레이트의 모든 웰에 첨가하였다.
7. 플레이트를 1시간 동안 진탕과 함께 실온에서 인큐베이션하였다.
샘플 및 기준의 제조:
8. 플레이트를 블로킹시키면서, 기준 및 샘플을 검정 희석액(0.1% BSA/0.05% Tween20/PBS)에 희석시켰다. 기준(참고 물질, 즉, Dom15-26-593)을 연속적으로 희석(10배)시켜 log 희석 곡선을 생성시켰다.
샘플의 첨가:
9. 블로킹된 플레이트를 세척(상기 6에서와 같음)하였다.
10. 50μl의 희석된 샘플 또는 기준을 적절한 웰에 첨가하였다. 50 μl/웰 검정 희석액을 웰에 첨가하여 음성 대조군으로 작용하도록 하였다.
11. 플레이트를 진탕과 함께 실온에서 2시간 동안 인큐베이션하였다.
12. 플레이트를 6회 세척하고, 블로팅(blotting)하여 건조시켰다(상기 6에서와 같음).
13. 50μL의 항-myc 항체(9E10 Sigma M5546)를 모든 웰에 첨가하여 1:500으로 희석(검정 희석액 : 0.1% BSA/0.05% Tween20/PBS 중)시켰다(즉, 각각의 플레이트에 대해 5 ml의 검정 희석액에 10μL의 항-myc 항체(9E10)를 첨가함).
14. 플레이트를 실온에서 1시간 이상 동안 로커(rocker)에서 인큐베이션하였다.
15. 플레이트를 6회 세척하고, 블로팅하여 건조시켰다(상기 6에서와 같음).
16. 1:10000의 50μL의 항-마우스 Ig HRP(Sigma A9309)를 모든 웰에 첨가하였다(즉, 45 μL의 검정 희석액(0.1% BSA/0.05% Tween20/PBS)에 5μL의 항-마우스 Ig HRP 항체를 첨가하여 스톡 항체를 1:10 희석시킴). 각각의 플레이트에 대해, 5 μL의 1:10 희석된 스톡을 5 ml 검정 희석액에 첨가하였다.
17. 플레이트를 실온에서 1시간 이상 동안 로커에서 인큐베이션하였다.
18. 플레이트를 6회 세척하고, 블로팅하여 건조시켰다(상기 6에서와 같음).
19. 50μL의 TMB 기질을 모든 웰에 첨가하였다. 상기 검정의 발달이 매우 신속하므로, 한번에 3개 이하의 플레이트에 TMB를 첨가하는 것이 적당하다. TMB는 냉장고로부터 직접 사용되거나 실온에서 사용될 수 있다.
20. 각 웰에 50μL의 1M HCl을 첨가함으로써 반응을 중지(충분히 색이 발달된 후)시켰다.
21. 플레이트를 450nm에서 96웰 플레이트 판독기에서 판독하였다.
결과:
결과는 표 1에 제시된다.
투여 스케줄은 발적, 초조 또는 이상 동물 행동의 증후가 관찰되지 않고 잘 용인되었다. 처리된 안구 및 대측(비처리) 안구로부터 수득된 유리체액 및 방수 샘플에 존재하는 항-VEGF dAb(DOM15-26-593)의 수준을 연구하기 위해 수행된 ELISA 검정의 결과는 검출된 dAb의 대부분이 처리된 안구의 유리체액에 존재하는 것을 나타내었다. 유리체액에서 가장 높은 농도를 갖는 래빗(동물 3)은 또한 처리된 안구의 방수에 존재하는 검출가능한 수준의 항-VEGF dAb를 가졌다.
1.5% HPMC(이는 좀더 점성의 용액임)에 제형화된 dAb는 보다 유동적인 0.3% HPMC 함유 제형보다 효과적으로 각각의 투여 후에 안구에서 유지되는 것으로 관찰되었다. 보다 낮은 HPMC 농도로 투여된 래빗은 눈을 깜빡임에 따라 이후의 투여 물질의 일부를 상실한 것으로 보였다.
표 1: 국소적으로 처리된 안구 및 대측 안구로부터의 유리체액 및 방수에 존재하는 항-VEGF dAb(DOM15-26-593)의 농도. 처리는 결막하낭에 투여(4시간의 기간 동안 20분 마다 투여)되는 12회 용량(각각 50 μL 부피의 2 mg/ml 용액으로 구성됨)으로 구성되었다.
결론:
항-VEGF dAb의 투여는 결막하낭에서 이루어졌다. dAb의 일부가 각막을 통해 침투하여, 이후에 방수에서 검출될 것이 예상되었다. 놀랍게도, 검출된 항-VEGF dAb의 대부분이 유리체액에 존재하였고, 이러한 관찰은 후방으로 진입하기 위해 공막 및 맥락막을 가로지르는 안와로부터의 확산에 의해 항-VEGF dAb가 안구로 진입하는 것과 일치하였다.
점성도 향상제로서 히드록시프로필셀룰로오스(HPMC)를 제형에 포함시켰다. 1.5%의 제형은 처리된 안구에서 보다 효과적으로 유지되는 것으로 보였다. 보다 유동성인 0.3%의 제형은 보다 덜 유지되었고, 이는 본 그룹의 3마리의 래빗 중 2마리에서 관찰된 대측 안구로의 항-VEGF dAb의 이동으로부터 기인될 수 있다.
실시예 2:
래빗의 안구로의 유리체내 투여 후의 DOM15-26-593의 약물동력학:
유리체액으로의 DOM15-26-593의 직접적인 주사 후 항-VEGF 면역글로불린 단일 가변 도메인 항체(항-VEGF dAb) DOM15-26-593이 안구에서 유지되는 기간을 연구하기 위한 실험을 수행하였다. 도 1a에 도시된 아미노산 서열(SEQ ID NO 1)을 갖는 Dom15-26-593 dAb를 제조(104 mM 염화나트륨, 0.02% (w/v) Tween 80이 보충된 50 mM 아세트산 나트륨 완충액(pH 7.0)에 2 mg/ml 농도로 제형화됨)하고, 본 실험에서 c-myc-태깅된 항-VEGF dAb로 사용하였다. 성체 친칠라 바스타드 래빗을 찰스 리버사(Charles River, Germany)에서 구입하였다. 동물을 사용 전에 새 환경에 순응하도록 하였다. 각각의 래빗을 마취시키고, 10 마이크로리터의 c-myc 태깅된 항-VEGF dAb(DOM15-26-593)(전체 20 μg)의 2 mg/ml 용액(실시예 1에 기재된 바와 같이 제조된 용액)을 좌측 안구의 유리체액에 적접 주사하였다. 주사 후 다양한 시점(2, 24 및 30시간)에서 래빗을 안락사시키고, 둘 모두의 안구를 적출하고, 방수 및 유리체액의 샘플을 수집하였다. 이러한 샘플을 분석 전에 동결(-20℃)하여 저장하였다. dAb가 재조합 VEGF 단백질이 코팅된 플레이트에서 포획되고, c-myc 태그에 대한 특이성을 갖는 항체를 이용하여 검출되는 샌드위치 ELISA 검정을 이용하여 존재하는 DOM15-26-593의 농도에 대해 방수 및 유리체액의 샘플을 시험하였다.
결과:
DOM15-26-593(항-VEGF dAb)의 농도는 하기 표 2에 제시된다:
표 2: 유리체내 투여된 안구 및 대측 안구로부터의 유리체액 및 방수에 존재하는 항-VEGF dAb(DOM15-26-593)의 농도. 처리는 좌측 안구로의 1회의 유리체내 주사(10 μL의 2 mg/ml 용액)로 이루어졌고, 래빗을 마취로부터 회복되도록 두고, 투여 2, 24 및 30시간 후에 선별하였다.
농도는 2개의 소수 자리로 반올림하였다.
결론:
실험 결과는 DOM15-26-593의 농도가 투여 24시간 후에 주사 농도와 비슷한 수준으로 유지된 것을 나타내었다. 도메인 항체는 투여 24 및 30시간 후에 유리체액에 존재하였다.
처리된 안구의 일부의 방수에서 낮은 농도의 DOM15-26-593(항-VEGF dAb)이 검출되었다. 그러나, 대측의 미처리된 안구에서는 최소한의 DOM15-26-593의 전달이 있었다.
실시예 3:
래트 레이저 유발성 맥락막 혈관신생(CNV) 모델:
실험용 맥락막 혈관신생(CNV)을 5마리의 2-4개월령의 암컷 다크 아구티(Dark Agouti, DA) 래트 군에서 일방적으로 유발시켰다. 마취된 래트의 바닥복합층(Bruch's membrane)을 파열시키기 위해 레이저 광응고술(PC)을 이용하였다. 시력(ocular power)을 중화시키기 위해 각막에 적용되는, 슬릿(slit) 램프 검안경, 및 핸드헬드(handheld) 평면오목 컨택트 렌즈(Moorfields Eye hospital, London, UK)에 부착된 다이오드-펌핑되는(diode-pumped), 532 nm 아르곤 레이저(Novus Omni, Coherent Inc., Santa Clara, CA)를 이용하여 색소 레이저 PC를 수행하였다. 각각의 실험 동물의 하나의 안구에 5개의 병변(532 nm, 150 mW, 0.2초, 200 μm 직경)을 만들었다. 500μm 반경으로 시신경에 집중되고, 주요 혈관을 피하여, 유두주위 분포되고 표준화된 방식으로 병변을 만들었다. 레이저 손상의 형태적 종점을 바닥복합층의 파열과 관련된 신호인 공동화 기포의 일시적 출현으로 확인하였다. 기포를 형성하지 않은 레이저 스폿을 분석으로부터 제외시켰다. 레이저 CNV 유도 직후, 각각의 동물에 5μL 부피(시신경유두에 집중됨)를 유리체내 투여하였다(이러한 부피는 병변이 만들어진 망막 영역을 포함하기에 충분한 부피일 것으로 계산하여 선택됨). dAb를 104 mM 염화나트륨, 0.02% (w/v) Tween 80이 보충된 50 mM 아세트산 나트륨 완충액(pH 5.5) 중에 2 mg/ml 농도로 제형화시켰다. 5 μL 부피는 50 μg의 항-VEGF dAb(DOM15-26-593; 도 1a에 도시된 아미노산 서열(SEQ ID NO 1)을 가짐), 또는 50 μg의 항-VEGF DOM15-26-593-Fc 융합체(도 1b에 도시된 아미노산 서열(SEQ ID NO 2)을 가짐)를 갖거나, 화합물을 포함하지 않았다(비히클 단독, 음성 대조군). 병변 발생 및 주사 7 및 14일 후에 공초점 고해상도 SLO 플루오레신 혈관조영술(0.2ml 10% 복강내 주사되는 플루오레신 나트륨, FS) 및 OCT(Heidelberg Spectralis, Heidelberg, Germany)를 이용하여 CNV 및 관련 누출의 생체내 이미지 데이터를 생성시켰다. 플루오레신 혈관조영술 이미지에 병변의 위치를 정하는 것을 돕기 위해 FS의 주입 전에 기준선 반사율(488nm 및 790nm) 및 자가형광(예를 들어, 488nm, em. >498nm) 이미지를 작성하였다. FS 주입 직후 동맥-정맥 상을 기록하였다. 주입 1분 후에 플루오레신 혈관조영도를 기록하고, 주입 4분 후에 다시 기록하였다. 후기 플루오레신 혈관조영법의 반정량 평가에 의해 약물 처리의 효과를 평가하였다. 누출을 후기 혈관조영도에서 시간이 지남에 따라 크기가 증가된 초형광(hyperfluorescent) 병변의 존재로 정의하였다. 후기 플루오레신 혈관조영법에서의 염색의 강도 및 영역이 차폐된 방식으로 2명의 검사관에 의해 등급이 매겨졌다. 특정 병변에 제공된 2 스코어가 일치되지 않은 경우, 보다 높은 스코어를 분석에 이용하였다. 이러한 상위되는 스코어는 분석된 병변의 10% 미만에서 관찰되었고, 불일치는 1 등급을 초과하지 않았다. 연구를 차폐된 방식으로 수행하였고, 모든 데이터가 수집된 후에만 내용을 차폐하지 않았다.
결과:
결과는 하기 표 3에 제시된다.
래트 망막에 대한 레이저 화상을 이용한 맥락막 혈관신생(CNV)의 유도 7 및 14일 후에, 각각의 병변을 관찰하기 위해 플루오레신 혈관조영법을 이용하였다. 병변을 다음과 같이 등급화시켰다: 등급 0 = 누출 없음, 등급 1 = 적은 누출, 등급 2 = 중간 누출, 및 등급 3 = 많은 누출. 항-혈관 내피세포 성장인자 도메인 항체(항-VEGF dAb, DOM15-26-593) 및 DOM15-26-593-FC 융합체로 유리체내 처리된 래트의 군, 및 음성 대조군 비히클이 투여된 군에 대한 결과가 하기에 표로 제작되어 있다. 결과는 항-VEGF dAb(DOM15-26-593) 또는 DOM15-26-593-FC 융합체를 이용한 처리가 대조군(모의(sham)-처리) 래트에 비해 혈관신생 및 누출의 정도를 감소시킨 것을 나타내었다.
표 3: 광응고에 의한 유도 7 및 14일 후의 래트 안구에서의 CNV 병변 스코어.
결론:
결과는 DOM15-26-593-Fc 융합체, (항-VEGF dAb-Fc)가 RPE-막락막의 레이저 광응고에 의해 유도된 실험적 맥락막 혈관신생(CNV)이 플루오레신 혈관조영법에 의해 특성규명된 래트 모델에서 효능이 있는 것을 나타내었다. DOM15-26-593-Fc 융합체에 대한 결과는 7 및 14일 둘 모두에서 대조군 비히클이 투여된 군보다 현저히 나았다. 이러한 군은 항-VEGF dAb(DOM15-26-593) 군보다 약간 더 활성을 유지하는 것을 나타내었다. 그러나, 항-VEGF dAb(DOM15-26-593)가 또한 효능이 있었다(레이저 유발 손상 7 및 14일 후 둘 모두에서 대조군에 비해 현저히 나음).
이러한 결과는 항-VEGF dAb(DOM15-26-593) 및 항-VEGF dAb-Fc가 실험 래트 CNV 모델에서 효능이 있는 것을 나타낸다. 이러한 안과 질병의 생체내 설치류 모델에서의 효능의 입증은 도메인 항체가 연령 관련 황반 변성(AMD)에서 맥락막 혈관신생의 치료에 유익할 수 있음을 나타낸다.
실시예 4:
래빗으로의
항-
TNF
-α 항체,
Fc
-
포맷화된
항-
VEGF
dAb
,
페길화된
항-
IL
-1 dAb 및 항-
IL
-1
dAb
의 국소 전달:
방법
성체 암컷 친칠라 바스타드 래빗을 찰스 리버사(Charles River, Germany)에서 구입하였다. 동물을 사용 전에 새 환경에 순응되도록 두었다. 투여 개시 5일 전에 모든 래빗의 귀 가장자리 정맥으로부터 혈액 샘플을 수집하였다. 혈액을 실온에서 응도되도록 두고, 원심분리(12000 rpm/2분)하여 혈청을 분리시켰다. 혈청을 새로운 튜브로 옮기고, 동결(-20℃) 저장하였다.
DOM4-130-54의 제조 및 선택은 WO 2007/063311호 및 WO 2008/149149호에 기재되어 있다. Dom0400을 제조하기 위해, DOM4-130-54 dAb 서열을 취하고, 위치 80의 시스테인을 DOM4-130-54에 존재하는 프롤린으로 대체하도록 돌연변이시켰고, 이러한 dAb는 이후 dAb의 위치 80의 자유 시스테인으로의 표준 말레이미드 커플링에 의해 40KDa의 선형 PEG 분자(NOF Corp., Europe에서 구입)에 부착된다.
네이키드(naked) 포맷(D0M4-130-54; IL-1 네이키드 dAb, 12.026 kDa; 도 3에 도시된 아미노산 서열(SEQ ID NO 5)을 가짐) 또는 페길화된 포맷(DOM0400PEG; IL-1 페길화된 dAb, 52.032 kDa; 도 2에 도시된 아미노산 서열(SEQ ID NO 4)을 가짐)의 IL-1에 대한 특이성을 갖는 도메인 항체(dAb)를 20 mM 숙시네이트, 5% 소르비톨, pH 6.0 중에서 각각 8.5 및 10.4 mg/ml로 제형화시켰다.
Fc-포맷화된 α-VEGF dAb(도 1b에 도시된 아미노산 서열(SEQ ID NO 2)을 갖는 VEGF15-26-593)를 50 mM 포스페이트, 1% L-아르기닌, 0.05 mM EDTA.0.02% 폴리소르베이트 및 0.3% NaCl pH 7.0 중에서 9.1 mg/ml로 제형화시켰다. TNF-α에 대한 특이성을 갖는 모노클로날 항체(시판됨)를 멸균 증류수를 이용하여 10 mg/ml로 동결건조된 제조물로부터 재구성시켰다. 4마리의 래트의 군의 좌측 안구에 4.2일의 기간에 걸쳐 매일 5회(3시간 간격) 투여하였다. 동물을 각각의 투여일 사이에 12시간(밤새)의 휴식 기간을 두었다. 각각의 투여는 윗눈꺼풀 하에 배치되는 25 마이크로리터의 관련 화합물의 용액으로 이루어졌다. 동물을 투여 후 적어도 30초 동안 고정된 상태로 두었다. 투여 스케줄 전과 투여 스케줄 동안의 여러 시점에서, 약간의 유체를 흡수하도록 눈꺼풀 하에 작은 흡수성 종이 조각을 두어 누액(눈물)의 샘플을 수집하였다. 누액이 스며든 종이의 영역을 200 μL의 포스페이트 완충 염수를 함유하는 튜브에 두었다. 튜브를 원심분리(12000 rpm/2분)하고, 종이를 제거하고, 회수된 샘플을 분석 전에 동결(-20℃) 저장하였다.
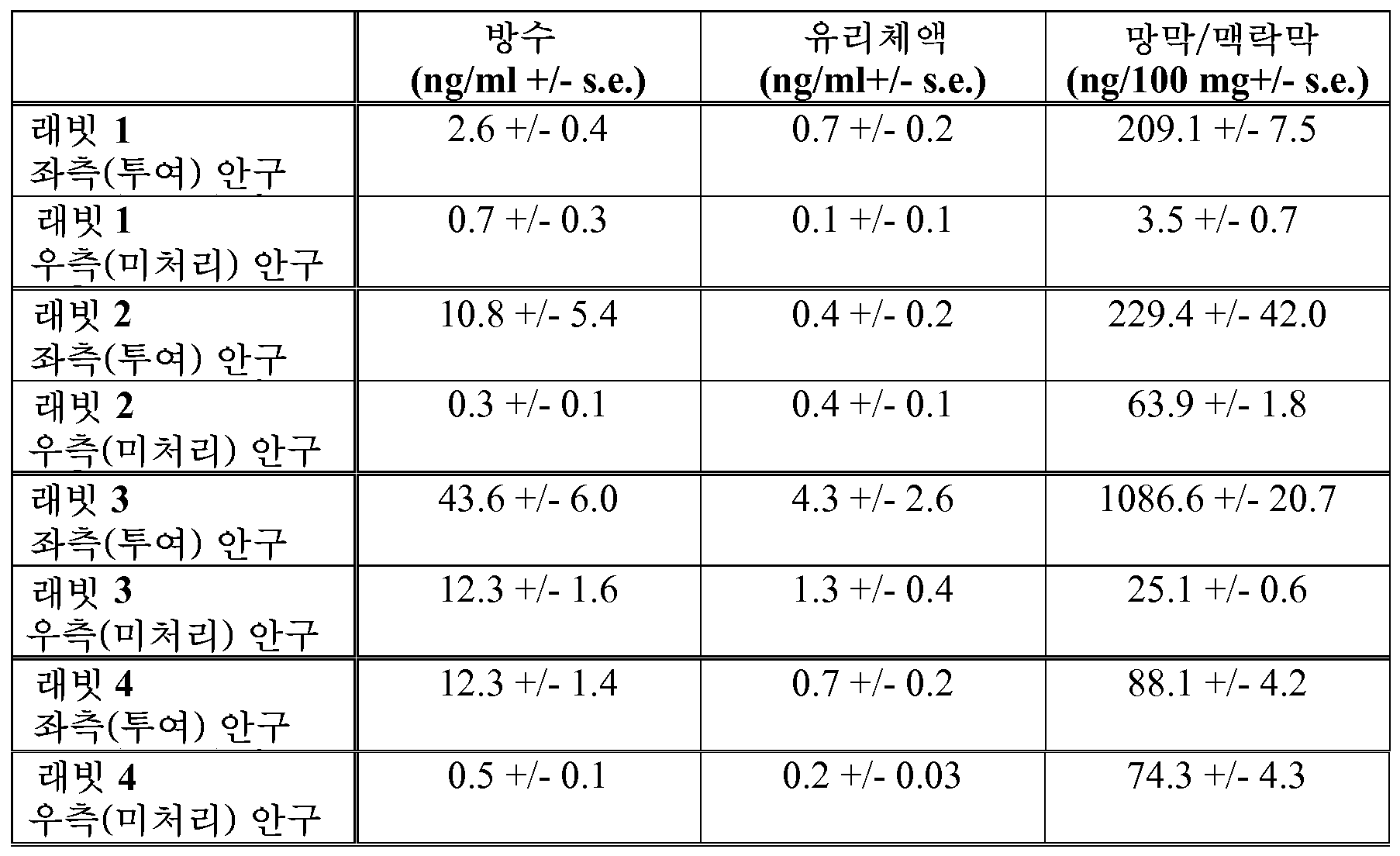
마지막 투여 1시간 후에 각각의 래빗의 귀 가장자리 정맥으로부터 혈액 샘플을 수집하였다. 혈액을 응고되도록 두어 혈청을 분리시키고, 상기 기재된 방법에 의해 저장하였다. 이후 즉시 동물을 안락사시켰다. 안락사 시기에 최대한 가깝게 각각의 동물로부터의 두 안구를 적출하여 확인하였다. 각각의 안구를 PBS에서 세척하여 표면으로부터 임의의 과량의 약물을 제거하였다. 방수 및 유리체액의 샘플을 수집하고, 분석 전에 동결(-20℃)시켜 저장하였다. 유리체액을 분석에서 시험하기 전에 1회의 동결/해동 주기에 적용시켰다. 안구를 절개하고, 망막/맥락막을 수집하였다. 망막/맥락막 샘플을 칭량하고, 100 마이크로리터의 용해 완충액(10 mM Tris pH 7.4; 0.1% SDS; 프로테이나제 억제제 칵테일을 가짐, (Roche))을 각각의 15 mg의 망막/맥락막 조직에 첨가하였다. 샘플을 반복된 고주파 및 저주파 파열의 2분의 주기를 이용하는 초음파 분해(Covaris S2 Sonolab Single)를 이용하여 균질화시켰다. 망막/맥락막의 샘플을 마이크로퓨즈(microfuge)(Heraeus)에서 원심분리(12000 rpm/2분)시켰다. 상층액을 새로운 튜브로 옮기고, 동결(-20℃) 저장시켰다.
각각의 샘플의 약물 함량을 샌드위치 포맷의 ELISA 검정을 이용하여 시험하고, 측정하였다. 재조합 인간 TNF-α 단백질(Peprotech)로 코팅된 플레이트를 이용하여 α-TNF-α 항체를 포획하고, 이를 알카리성 포스파타제가 컨쥬게이션된 항-인간 IgG (Fc 특이적) 항체(Sigma)를 이용하여 검출하였다. 재조합 인간 IL-1 수용체 타입 1 Fc(Axxora)로 코팅된 플레이트를 이용하여 IL-1 및 페길화된 IL-1 dAb를 포획하고, 이를 단백질 L-퍼옥시다제(Sigma)를 이용하여 검출하였다. 재조합 VEGF 단백질의 사내(in-house) 제조물을 이용하여 VEGF-Fc 포맷화된 dAb를 포획하고, 이를 항-인간 IgG (Fc 특이적) 알칼리성 포스파타제 컨쥬게이션된 항체(Sigma)로 검출하였다.
결과
모든 경우에서 약물 투여는 발적, 초조 또는 이상 동물 행동의 증후가 관찰되지 않고 잘 용인되었다.
방수 및 유리체액, 및 망막/맥락막에서의 다양한 포맷의 도메인 항체 및 α-TNF-α 항체에 대한 결과가 하기 표에 제시된다. 결과는 평균 농도(각각의 샘플이 삼중으로 시험된 3개의 독립적 검정으로부터의 평균 농도) +/- 표준 편차(괄호에 제시됨)로 제시된다.
표 4: 국소 투여 후의 방수에서의 농도(
ng
/
ml
)
본 표에서 결과는 1개의 소수 자리로 반올림하였다.
표 5: 국소 투여 후의 유리체액에서의 농도(
ng
/
ml
):
본 표에서 결과는 1개의 소수 자리로 반올림하였다.
표 6: 국소 투여 후의 망막/맥락막에서의 농도(100μL 용해
완충액이
15
mg
의 조직에 첨가된 샘플 중에서의
ng
/
ml
):
본 표에서 결과는 1개의 소수 자리로 반올림하였다.
누액(눈물) 샘플을 투여 20 및 21 직전에 래빗으로부터 수집하였고, 존재하는 약물의 농도에 대한 결과가 표 4 및 5에 각각 제시된다. 투여된 물질이 좌측(투여된 측) 안구 모두에서 검출되었고(개별적 래빗 사이에서 검출된 농도에서 많은 변동이 있었음), 대측(투여되지 않은 우측)의 대부분으로의 투여 물질 일부의 이동이 또한 발생하였다. 투여 물질은 투여 20 12시간 후에 여전히 안구에 존재하였다. DOM0400PEG(페길화된 IL-1 dAb) 및 VEGF-Fc(15-26-593)가 네이키드 IL-1 dAb(D0M4-130-54)에 비해 투여 20과 21 사이의 12시간의 기간 동안 높은 농도로 눈물에서 유지되는 것으로 나타났다.
다양한 포맷의 도메인 항체의 농도 및 누액(눈물) 내의 상기 항체에 대한 결과가 하기 표에 제시된다(좌측 안구에만 투여됨):
표 7: 투여 20 전에 수집된
누액
샘플에서의 농도(이전의 투여 3시간 후)(μg/ml). 표준 편차가 괄호 내에 제공된다:
본 표에서 결과는 1개의 소수 자리로 반올림하였다.
표 8: 투여 21 전에 수집된
누액
샘플에서의 농도(이전의 투여 12시간 후): 농도 (μg/
ml
). 표준 편차가 괄호 내에 제공된다:
본 표에서 결과는 1개의 소수 자리로 반올림하였다.
다양한 포맷의 도메인 항체의 농도 및 처리전 혈액(prebleed) 및 혈청 내의 항체에 대한 결과는 하기 표에 제시된다:
표 9: 괄호 내에 표준 편차가 제공된, 안락사 직전에 수집된
처리전
혈액 및 혈청에서의 농도(
ng
/
ml
):
본 표에서 결과는 1개의 소수 자리로 반올림하였다.
* α-TNF-α 항체 처리 군의 래빗 3은 용해로 인해 색이 적색인 처리전 혈액을 가졌고, 이는 명백히 높은 결과에 기여했을 수 있다.
실시예
5:
α-
TNF
-α
R1
dAb
의 국소 전달
방법
성체 수컷 친칠라 바스타드 래빗을 찰스 리버사(Charles River, Germany)에서 구입하였다. 동물을 사용 전에 새 환경에 순응하도록 두었다. 투여 개시 7일 전에 각각의 래빗의 귀 가장자리 정맥으로부터 혈액 샘플을 수집하였다. 혈액을 실온에서 응고되도록 하고, 원심분리(12000 rpm/2분)하여 혈청을 분리시켰다. 혈청을 새로운 튜브로 옮기고, 동결(-20℃) 저장하였다.
TNF-αR1에 대한 특이성을 갖는 도메인 항체(dAb)(즉, 도 4에 도시된 아미노산 서열(SEQ ID NO 6)을 갖는 Dom1h-131-206인 항-TNFα 수용체 타입 1 dAb; Dom1h-131-206의 제조 및 선택은 WO 2008/149148호에 기재되어 있음)를 10 mg/ml로 포스페이트 완충 염수에서 제형화시켰다. 4마리의 래빗의 군의 좌측 안구에 하루에 10회(1시간 간격)회 투여하였다. 각각의 투여는 윗눈꺼풀 하에 배치되는 50 마이크로리터의 10 mg/ml의 α-TNF-αR1 dAb 용액으로 이루어졌다. 동물을 투여 후 적어도 30초 동안 고정된 채로 두었다. 투여 스케줄 전과 투여 스케줄 동안의 여러 시점에서, 약간의 유체를 흡수하도록 눈꺼풀 하에 작은 흡수성 종이 조각을 두어 누액(눈물)의 샘플을 수집하였다. 누액이 스며든 종이의 영역을 200 μL의 포스페이트 완충 염수를 함유하는 튜브에 두었다. 튜브를 원심분리(12000 rpm/2분)하고, 종이를 제거하고, 회수된 샘플을 분석 전에 동결(-20℃) 저장하였다.
마지막 투여 1시간 후에 각각의 래빗의 귀 가장자리 정맥으로부터 혈액 샘플을 수집하였다. 혈액을 응고되도록 두고, 상기 기재된 방법에 의해 혈청을 분리시켰다. 이후 즉시 동물을 안락사시켰다. 안락사 시기에 최대한 가깝게 각각의 동물로부터의 두 안구를 적출하여 확인하였다. 각각의 안구를 PBS에서 세척하여 표면으로부터 임의의 과량의 약물을 제거하였다. 방수 및 유리체액의 샘플을 수집하고, 분석 전에 동결(-20℃)시켜 저장하였다. 유리체액을 검정에서 시험하기 전에 1회의 동결/해동 주기에 적용시켰다. 안구를 절개하고, 망막/맥락막을 수집하였다. 망막/맥락막 샘플을 칭량하고, 900 마이크로리터의 용해 완충액(10 mM Tris pH 7.4; 0.1% SDS; 프로테이나제 억제제 칵테일을 가짐, (Roche))을 각각의 샘플에 첨가하였다. 샘플을 반복된 고주파 및 저주파 파열의 2분의 주기를 이용하는 초음파 분해(Covaris S2 Sonolab Single)를 이용하여 균질화시켰다. 망막/맥락막의 샘플을 마이크로퓨즈(microfuge)(Heraeus)에서 원심분리(12000 rpm/2분)시켰다. 상층액을 새로운 튜브로 옮기고, 동결(-20℃) 저장시켰다. dAb가 재조합 인간 TNF R1/TNFRSF 1A/Fc 키메라(R+D Systems)로 코팅된 플레이트를 이용하여 포획되고, 인간 IgG(F(ab)2) 단편(Thermo)에 대한 특이성으로 검출되는 샌드위치 ELISA에 의해 α-TNF-αR1 dAb의 농도에 대해 샘플을 시험하였다. 이러한 항체는 컨쥬게이션되지 않았으므로, 결합된 항체를 검출하기 위해 항-염소/양-HRP 시약(Sigma)을 사용하였다.
결과
약물 투여는 발적, 초조 또는 이상 동물 행동의 증후가 관찰되지 않고 잘 용인되었다.
안구 유체 및 혈청 내의 α-TNF-αR1 dAb의 농도는 삼중으로 시험된 샘플에 대해 제시된다. α-TNF-αR1 dAb가 시험된 안구 샘플 모두에서 검출되었다.
표 10: 안구 샘플에서의 α-
TNF
-α
R1
dAb
의 농도:
표 10의 결과는 1개의 소수 자리로 반올림하였다.
S.E. = 표준 오차
누액(눈물) 샘플을 투여 2, 6, 10 직전, 및 최종 투여 1시간 후에 래빗으로부터 수집하였으며, 샘플에서 검출된 α-TNF-αR1 dAb의 농도가 표 8에 제시된다. α-TNF-αR1 dAb는 좌측(투여) 안구의 모두에서 검출되었고, 대측(투여되지 않은 우측)의 대부분으로의 일부 이동이 또한 발생하였다.
표 11:
누액
(눈물) 샘플에서의 α-
TNF
-α
R1
dAb
의 농도:
표 11의 결과는 2개의 소수 자리로 반올림하였다.
S.E. = 표준 오차
혈액을 첫번째 투여 전 및 안락사 시에 혈청에 대해 수집하였다. 생성된 데이터는 표 9에 제시된다. 최종 투여 1시간 후에 4마리의 래빗의 각각으로부터 수득된 혈청에서 낮은 농도의 α-TNF-αR1 dAb가 검출되었다.
표 12: 혈청 샘플 중의 α-
TNF
-α
R1
dAb
의 농도:
표 12의 결과는 2개의 소수 자리로 반올림하였다.
ND = 검출되지 않음
S.E. = 표준 오차
SEQUENCE LISTING
<110> Gough, Gerald
Cook, Fiona
Jespers, Laurent
Steward, Michael
Glaxo Group Limited
<120> polypeptides, antibody variable domains
and antagonists
<130> DB00063
<150> USSN 12/323,632
<151> 2009-06-11
<160> 6
<170> FastSEQ for Windows Version 4.0
<210> 1
<211> 116
<212> PRT
<213> Artificial Sequence
<220>
<223> artficial sequence derived from homo sapiens
sequence
<400> 1
Glu Val Gln Leu Leu Val Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Lys Ala Tyr
20 25 30
Pro Met Met Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Glu Ile Ser Pro Ser Gly Ser Tyr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Pro Arg Lys Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 2
<211> 343
<212> PRT
<213> Artificial Sequence
<220>
<223> artficial sequence derived from homo sapiens
sequence
<400> 2
Glu Val Gln Leu Leu Val Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Lys Ala Tyr
20 25 30
Pro Met Met Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Glu Ile Ser Pro Ser Gly Ser Tyr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Pro Arg Lys Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr His Thr Cys Pro Pro Cys Pro Ala Pro
115 120 125
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
130 135 140
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
145 150 155 160
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
165 170 175
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
180 185 190
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
195 200 205
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
210 215 220
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
225 230 235 240
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
245 250 255
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
260 265 270
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
275 280 285
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
290 295 300
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
305 310 315 320
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
325 330 335
Leu Ser Leu Ser Pro Gly Lys
340
<210> 3
<211> 225
<212> PRT
<213> homo sapiens
<400> 3
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
1 5 10 15
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
20 25 30
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
35 40 45
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
50 55 60
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
65 70 75 80
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
85 90 95
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
100 105 110
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
115 120 125
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
130 135 140
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
145 150 155 160
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
165 170 175
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
180 185 190
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
195 200 205
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
210 215 220
Lys
225
<210> 4
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<223> artficial sequence derived from homo sapiens
sequence
<400> 4
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Tyr Leu Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Asn Phe Gly Ser Glu Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Cys
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Pro Ser Phe Tyr Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 5
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<223> artficial sequence derived from homo sapiens
sequence
<400> 5
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Tyr Leu Asn
20 25 30
Leu Asp Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Asn Phe Gly Ser Glu Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Pro Ser Phe Tyr Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 6
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> artficial sequence derived from homo sapiens
sequence
<400> 6
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ala His Glu
20 25 30
Thr Met Val Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser His Ile Pro Pro Asp Gly Gln Asp Pro Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr His Cys
85 90 95
Ala Leu Leu Pro Lys Arg Gly Pro Trp Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
Claims (35)
- 표적 분자에 결합하는 면역글로불린 단일 가변 도메인을 포함하는 안구 전달용 조성물.
- 제 1항에 있어서, 상기 면역글로불린 단일 가변 도메인이 프로테아제에 대해 내성이고, 상기 프로테아제가 안구 프로테아제, 카스파제(caspases), 칼파인(calpains), 기질 금속단백분해효소(matric metalloproteases), 디스인테그린(disintegrins), 금속단백분해효소(ADAMs) 및 트롬보스폰딘 모티프를 갖는 ADAM, 프로테오좀, 조직 플라스미노겐 활성인자, 세크레타제(secretases), 카텝신 B, 카텝신 D, 시스타틴 C, 세린 프로테아제 PRSS1, 및 유비퀴틴 프로테오좀 경로(UPP)로 구성된 군으로부터 선택되는 안구 전달용 조성물.
- 제 1항 또는 제 2항에 있어서, VEGF, TNFα, TNFαR, IL-1, IL-1r, TNFαR1, TGF베타, IL-6, IL-8, IL-17, IL-21, IL-23, CD20, Nogo-a, 미엘린 결합 당단백질(MAG) 및 베타 아밀로이드의 군으로부터 선택된 표적 분자에 결합하는 면역글로불린 단일 가변 도메인을 포함하는 안구 전달용 조성물.
- 제 3항에 있어서, VEGF에 결합하는 상기 면역글로불린 단일 가변 도메인이 (a) DOM15-26-593의 아미노산 서열(SEQ ID NO 1에 제시됨) 또는 (b) DOM15-26-593-Fc의 아미노산 서열(SEQ ID NO 2에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 조성물.
- 제 4항에 있어서, 상기 면역글로불린 단일 가변 도메인이 위치 6(여기서, 넘버링(numbering)은 케이뱃(Kabat)에 따름)에 발린을 포함하는 조성물.
- 제 4항에 있어서, 상기 면역글로불린 단일 가변 도메인이 위치 99(여기서, 넘버링은 케이뱃에 따름)에 루신을 포함하는 조성물.
- 제 4항에 있어서, 상기 면역글로불린 단일 가변 도메인이 위치 30(여기서, 넘버링은 케이뱃에 따름)에 리신을 포함하는 조성물.
- 제 4항에 있어서, 상기 면역글로불린 단일 가변 도메인이 (a) DOM15-26-593의 아미노산 서열(SEQ ID NO 1에 제시됨), 또는 (b)DOM15-26-593-Fc의 아미노산 서열(SEQ ID NO 2에 제시됨)로부터 선택된 서열과 동일한 아미노산 서열을 포함하는 조성물.
- 제 3항에 있어서, IL-1에 결합하는 상기 면역글로불린 단일 가변 도메인이 (a) DOM4-130-54의 아미노산 서열(SEQ ID NO 5에 제시됨), 또는 (b) DOM0400 PEG의 아미노산 서열(SEQ ID NO 4에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 조성물.
- 제 9항에 있어서, IL-1에 결합하는 상기 면역글로불린 단일 가변 도메인이 (a) DOM4-130-54의 아미노산 서열(SEQ ID NO 5에 제시됨), 또는 (b) DOM0400 PEG의 아미노산 서열(SEQ ID NO 4에 제시됨)과 동일한 아미노산 서열을 포함하는 조성물.
- 제 3항에 있어서, α-TNF-αR1에 결합하는 상기 면역글로불린 단일 가변 도메인이 Dom1h-131-206의 아미노산 서열(SEQ ID NO 6에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 조성물.
- 제 3항에 있어서, 상기 α-TNF-αR1에 결합하는 상기 면역글로불린 단일 가변 도메인이 Dom1h-131-206의 아미노산 서열(SEQ ID NO 6에 제시됨)과 동일한 아미노산 서열을 포함하는 조성물.
- 제 1항 내지 제 12항 중 어느 한 항에 있어서, 항체 불변 영역의 도메인을 추가로 포함하고, 상기 항체 불변 영역이 항체 Fc 영역인 조성물.
- 제 9항에 있어서, 상기 항체 Fc 영역이 SEQ ID NO 3에 제시된 아미노산 Fc 서열을 갖는 조성물.
- 제 9항에 있어서, 상기 면역글로불린 단일 가변 도메인이 Fc와의 융합체로 존재하고, DOM15-26-593-Fc 융합체의 아미노산 서열(SEQ ID NO 2에 제시됨)과 동일한 아미노산 서열을 갖는 조성물.
- 유리체액, 방수(aqueous humour), 망막 및 맥락막으로부터 선택된 안구 영역 중 하나 이상으로의 전달을 위한, 표적 분자에 결합하는 네이키드(naked) 면역글로불린 단일 가변 도메인을 포함하는 조성물.
- 제 16항에 있어서, 상기 표적 분자가 VEGF, VEGF 길항제, TNFα, TNFα 수용체, IL-1, α-TNF-αR1, IL-6, IL-8, IL-17, IL-21, IL-23, Nogo-a, 미엘린 결합 당단백질(MAG) 및 베타 아밀로이드로부터 선택되는 조성물.
- 제 16항 또는 제 17항에 있어서, 상기 면역글로불린 단일 가변 도메인이 프로테아제에 대해 내성이고, 상기 프로테아제가 안구 프로테아제, 카스파제, 칼파인, 기질 금속단백분해효소, 디스인테그린, 금속단백분해효소(ADAM) 및 트롬보스폰딘 모티프를 갖는 ADAM, 프로테오좀, 조직 플라스미노겐 활성인자, 세크레타제, 카텝신 B, 카텝신 D, 시스타틴 C, 세린 프로테아제 PRSS1, 및 유비퀴틴 프로테오좀 경로(UPP)로 구성된 군으로부터 선택되는 조성물.
- 제 16항 또는 제 17항에 있어서, 상기 면역글로불린 단일 가변 도메인이, (a) VEGF에 결합하고, (ⅰ) DOM15-26-593의 아미노산 서열(SEQ ID NO 1에 제시됨) 또는 (ⅱ) DOM15-26-593-Fc의 아미노산 서열(SEQ ID NO 2에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 면역글로불린 단일 가변 도메인, (b) IL-1에 결합하고, (ⅰ) DOM4-130-54의 아미노산 서열(SEQ ID NO 5에 제시됨) 또는 (ⅱ) DOM0400 PEG의 아미노산 서열(SEQ ID NO 4에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 면역글로불린 단일 가변 도메인, 및 (c) α-TNF-αR1에 결합하고, Dom1h-131-206의 아미노산 서열(SEQ ID NO 6에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 면역글로불린 단일 가변 도메인으로 구성된 군으로부터 선택되는 조성물.
- 망막, 맥락막 및 누액(lachrymal fluid)으로부터 선택된 안구 영역 중 하나 이상으로의 전달을 위한, 표적 분자에 결합하는 포맷화된(formatted) 면역글로불린 단일 가변 도메인을 포함하는 조성물.
- 제 20항에 있어서, 상기 표적 분자가 VEGF, VEGF 길항제, TNFα, TNFα 수용체, IL-1, α-TNF-αR1, IL-17, IL-21, IL-23, Nogo-a, 미엘린 결합 당단백질(MAG) 및 베타 아밀로이드로부터 선택되는 조성물.
- 제 20항 또는 제 21항에 있어서, 상기 면역글로불린 단일 가변 도메인이 프로테아제에 대해 내성이고, 상기 프로테아제가 안구 프로테아제, 카스파제, 칼파인, 기질 금속단백분해효소, 디스인테그린, 금속단백분해효소(ADAM) 및 트롬보스폰딘 모티프를 갖는 ADAM, 프로테오좀, 조직 플라스미노겐 활성인자, 세크레타제, 카텝신 B, 카텝신 D, 시스타틴 C, 세린 프로테아제 PRSS1, 및 유비퀴틴 프로테오좀 경로(UPP)로 구성된 군으로부터 선택되는 조성물.
- 제 16항 또는 제 17항에 있어서, 상기 면역글로불린 단일 가변 도메인이, (a) VEGF에 결합하고, (ⅰ) DOM15-26-593의 아미노산 서열(SEQ ID NO 1에 제시됨) 또는 (ⅱ) DOM15-26-593-Fc의 아미노산 서열(SEQ ID NO 2에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 면역글로불린 단일 가변 도메인, (b) IL-1에 결합하고, (ⅰ) DOM4-130-54의 아미노산 서열(SEQ ID NO 5에 제시됨) 또는 (ⅱ) DOM0400 PEG의 아미노산 서열(SEQ ID NO 4에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 면역글로불린 단일 가변 도메인, 및 (c) α-TNF-αR1에 결합하고, Dom1h-131-206의 아미노산 서열(SEQ ID NO 6에 제시됨)과 97% 이상 동일한 아미노산 서열을 포함하는 면역글로불린 단일 가변 도메인으로 구성된 군으로부터 선택되는 조성물.
- 제 20항 내지 제 23항 중 어느 한 항에 있어서, 상기 면역글로불린 단일 가변 도메인이 약 50 KDa의 분자량을 갖는 조성물.
- 제 20항 내지 제 24항 중 어느 한 항에 있어서, 상기 면역글로불린 단일 가변 도메인이 페길화(pegylation) 또는 항체 Fc로의 융합에 의해 포맷화되는 조성물.
- 제 1항 내지 제 25항 중 어느 한 항에 있어서, 안구 침투 향상제 및 점성도 향상제로부터 선택된 하나 이상의 향상제를 추가로 포함하는 조성물.
- 제 1항 내지 제 26항 중 어느 한 항에 있어서, 약학적 또는 생리학적으로 허용되는 담체, 희석제 또는 부형제를 추가로 포함하는 조성물.
- 안구로의 국소 전달, 예를 들어, 안구 점적에 의한 안구로의 국소 전달 또는 안구내 주사, 안구주위 투여, 또는 서방형 제형의 군으로부터 선택된 방법에 의해 안구로 조성물을 투여하는 것을 포함하는, 제 1항 내지 제 27항 중 어느 한 항에 따른 조성물을 안구에 직접 전달하는 방법.
- 안구내 주사, 유리체내 주사, 안구로의 국소 전달, 예를 들어, 안구 점적에 의한 안구로의 국소 전달, 안구주위 투여, 및 서방형 제형으로 구성된 군으로부터 선택된 방법에 의해 제 1항 내지 제 27항 중 어느 한 항에 따른 조성물을 안구에 직접 투여하는 것을 포함하는, 안구 질환을 치료하거나, 예방하거나, 진단하는 방법.
- 제 28항 또는 제 29항에 있어서, 상기 조성물이 안구의 표면, 누관, 누선, 안구내 영역, 전방(anterior chamber), 후방(posterior chamber) 및 유리체액의 군으로부터 선택된 안구의 하나 이상의 영역으로 투여되는 방법.
- 국소 전달, 예를 들어, 안구 점적을 이용한 국소 전달에 의해 안구로 조성물을 투여하는 것을 포함하는, 유리체액, 방수, 망막, 및 맥락막의 군으로부터 선택된 안구의 하나 이상의 영역으로 제 16항 내지 제 19항, 제 26항 또는 제 27항 중 어느 한 항에 따른 조성물을 전달하는 방법.
- 국소 전달, 예를 들어, 안구 점적을 이용한 국소 전달에 의해 안구로 조성물을 투여하는 것을 포함하는, 망막, 맥락막, 및 누액의 군으로부터 선택된 안구의 하나 이상의 영역으로 제 20항 내지 제 27항 중 어느 한 항에 따른 조성물을 전달하는 방법.
- (a) 제 1항 내지 제 27항 중 어느 한 항의 조성물과, (b) 약학적으로 허용되는 담체, 희석제 또는 부형제를 혼합하는 것을 포함하는, 약제 조성물을 생성시키는 방법.
- 제 33항에 있어서, 상기 약제 조성물이 안구 질환 또는 질병을 치료하거나, 예방하거나, 진단하기 위한 것인 방법.
- 제 34항에 있어서, 상기 안구 질환 또는 질병이 AMD, 포도막염, 녹내장, 안구 건조, 당뇨망막병증, 당뇨병성 황반부종 및 포도막염의 군으로부터 선택되는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/323,632 US20090148437A1 (en) | 2007-06-06 | 2008-11-26 | Polypeptides, antibody variable domains & antagonists |
| US12/323,632 | 2008-11-26 | ||
| PCT/EP2009/064654 WO2010060768A1 (en) | 2008-11-26 | 2009-11-04 | Polypeptides, antibody variable domains & antagonists |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20110091777A true KR20110091777A (ko) | 2011-08-12 |
Family
ID=41507943
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020117014479A Withdrawn KR20110091777A (ko) | 2008-11-26 | 2009-11-04 | 폴리펩티드, 항체 가변 도메인 및 길항제 |
Country Status (11)
| Country | Link |
|---|---|
| EP (1) | EP2356147A1 (ko) |
| JP (1) | JP2012509852A (ko) |
| KR (1) | KR20110091777A (ko) |
| CN (1) | CN102224169A (ko) |
| AU (1) | AU2009319175A1 (ko) |
| BR (1) | BRPI0921319A2 (ko) |
| CA (1) | CA2744055A1 (ko) |
| IL (1) | IL212333A0 (ko) |
| MX (1) | MX2011005540A (ko) |
| WO (1) | WO2010060768A1 (ko) |
| ZA (1) | ZA201103588B (ko) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2403873A1 (en) | 2009-03-05 | 2012-01-11 | Ablynx N.V. | Novel antigen binding dimer-complexes, methods of making/avoiding and uses thereof |
| US9265834B2 (en) | 2009-03-05 | 2016-02-23 | Ablynx N.V. | Stable formulations of polypeptides and uses thereof |
| US20120244158A1 (en) * | 2009-09-03 | 2012-09-27 | Ablynx N.V. | Stable formulations of polypeptides and uses thereof |
| US9011861B2 (en) | 2010-02-25 | 2015-04-21 | Schepens Eye Research Institute | Therapeutic compositions for the treatment of dry eye disease |
| AU2011333738A1 (en) * | 2010-11-24 | 2013-07-11 | Glaxo Group Limited | Multispecific antigen binding proteins targeting HGF |
| MX2015005831A (es) | 2012-11-08 | 2015-09-24 | Eleven Biotherapeutics Inc | Antagonistas de il-6 y usos de los mismos. |
| US10568951B2 (en) | 2013-11-18 | 2020-02-25 | Formycon Ag | Pharmaceutical composition of an anti-VEGF antibody |
| PH12017500809B1 (en) | 2014-11-07 | 2023-09-20 | F Hoffmann La Roche Ltd | Improved il-6 antibodies |
| AR103173A1 (es) | 2014-12-22 | 2017-04-19 | Novarits Ag | Productos farmacéuticos y composiciones líquidas estables de anticuerpos il-17 |
| JP2019510078A (ja) | 2016-02-23 | 2019-04-11 | セセン バイオ, インコーポレイテッド | Il−6アンタゴニスト製剤およびその使用 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060073141A1 (en) * | 2001-06-28 | 2006-04-06 | Domantis Limited | Compositions and methods for treating inflammatory disorders |
| GB0521621D0 (en) * | 2005-10-24 | 2005-11-30 | Domantis Ltd | Tumor necrosis factor receptor 1 antagonists for treating respiratory diseases |
| JP2009519011A (ja) * | 2005-12-01 | 2009-05-14 | ドマンティス リミテッド | インターロイキン1受容体1型に結合する非競合ドメイン抗体フォーマット |
| EP1966242A1 (en) * | 2005-12-06 | 2008-09-10 | Domantis Limited | Ligands that have binding specificity for egfr and/or vegf and methods of use therefor |
| JP5259423B2 (ja) * | 2006-02-01 | 2013-08-07 | セファロン・オーストラリア・ピーティーワイ・リミテッド | ドメイン抗体構築物 |
| MX2009013137A (es) * | 2007-06-06 | 2010-04-30 | Domantis Ltd | Metodos para seleccionar polipeptidos resistentes a la proteasa. |
| JP2010528647A (ja) * | 2007-06-06 | 2010-08-26 | ドマンティス リミテッド | ポリペプチド、抗体可変ドメインおよびアンタゴニスト |
| GB0724331D0 (en) * | 2007-12-13 | 2008-01-23 | Domantis Ltd | Compositions for pulmonary delivery |
-
2009
- 2009-11-04 KR KR1020117014479A patent/KR20110091777A/ko not_active Withdrawn
- 2009-11-04 AU AU2009319175A patent/AU2009319175A1/en not_active Abandoned
- 2009-11-04 EP EP09748778A patent/EP2356147A1/en not_active Withdrawn
- 2009-11-04 WO PCT/EP2009/064654 patent/WO2010060768A1/en not_active Ceased
- 2009-11-04 BR BRPI0921319A patent/BRPI0921319A2/pt not_active Application Discontinuation
- 2009-11-04 CN CN2009801469998A patent/CN102224169A/zh active Pending
- 2009-11-04 MX MX2011005540A patent/MX2011005540A/es not_active Application Discontinuation
- 2009-11-04 CA CA2744055A patent/CA2744055A1/en not_active Abandoned
- 2009-11-04 JP JP2011536817A patent/JP2012509852A/ja active Pending
-
2011
- 2011-04-14 IL IL212333A patent/IL212333A0/en unknown
- 2011-05-16 ZA ZA2011/03588A patent/ZA201103588B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| WO2010060768A1 (en) | 2010-06-03 |
| JP2012509852A (ja) | 2012-04-26 |
| CA2744055A1 (en) | 2010-06-03 |
| IL212333A0 (en) | 2011-06-30 |
| MX2011005540A (es) | 2011-06-21 |
| EP2356147A1 (en) | 2011-08-17 |
| CN102224169A (zh) | 2011-10-19 |
| BRPI0921319A2 (pt) | 2018-10-16 |
| AU2009319175A1 (en) | 2010-06-03 |
| ZA201103588B (en) | 2012-01-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20110256122A1 (en) | Polypeptides, antibody variable domains & antagonists | |
| KR20110091777A (ko) | 폴리펩티드, 항체 가변 도메인 및 길항제 | |
| US20200231703A1 (en) | Treatment of ocular disease | |
| JP2023029557A (ja) | 糖尿病黄斑浮腫の治療のための組成物および方法 | |
| US20120076787A1 (en) | Combination of a tnf-alpha antagonist and a vegf antagonist for use in the treatment or prevention of diseases of the eye | |
| AU2007272224B2 (en) | scFv antibodies which pass epithelial and/or endothelial layers | |
| JP6062375B2 (ja) | Tgf−ベータ受容体iiに結合するリガンド | |
| JP2020062036A (ja) | 二重特異性抗vegf/抗ang−2抗体及び眼血管疾患の処置におけるそれらの使用 | |
| AU2011200544A1 (en) | Anti-IL-1R1 single domain antibodies and therapeutic uses | |
| US20250051459A1 (en) | Wnt-surrogate agents and methods for lacrimal gland regeneration | |
| US8092800B2 (en) | Antibodies against Candida antigens | |
| JP7189878B2 (ja) | ヒトcd160を結合する結合物及びその使用 | |
| CN101260156A (zh) | 免疫球蛋白单个变体抗原结合区及其特异性构建体 | |
| WO2024114641A1 (en) | C5/vegf bispecific binding molecules | |
| HK40126782A (zh) | C5/vegf双特异性结合分子 | |
| KR20220029343A (ko) | 항-vegf 육량체 항체, 및 이를 포함하는 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20110623 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |