KR20060026426A - 4'-아지도 뉴클레오사이드 유도체의 제조 방법 - Google Patents
4'-아지도 뉴클레오사이드 유도체의 제조 방법 Download PDFInfo
- Publication number
- KR20060026426A KR20060026426A KR1020057024240A KR20057024240A KR20060026426A KR 20060026426 A KR20060026426 A KR 20060026426A KR 1020057024240 A KR1020057024240 A KR 1020057024240A KR 20057024240 A KR20057024240 A KR 20057024240A KR 20060026426 A KR20060026426 A KR 20060026426A
- Authority
- KR
- South Korea
- Prior art keywords
- formula
- compound
- contacting
- solution
- nucleoside
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 238000004519 manufacturing process Methods 0.000 title claims description 17
- 150000001875 compounds Chemical class 0.000 claims abstract description 144
- 239000002777 nucleoside Substances 0.000 claims abstract description 68
- 238000000034 method Methods 0.000 claims abstract description 38
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 26
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 25
- 229910052736 halogen Inorganic materials 0.000 claims abstract description 21
- 150000002367 halogens Chemical group 0.000 claims abstract description 21
- 239000001257 hydrogen Substances 0.000 claims abstract description 21
- 150000003839 salts Chemical class 0.000 claims abstract description 20
- 239000003444 phase transfer catalyst Substances 0.000 claims abstract description 18
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 17
- DRTQHJPVMGBUCF-XVFCMESISA-N Uridine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-XVFCMESISA-N 0.000 claims abstract description 16
- 239000002253 acid Substances 0.000 claims abstract description 16
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims abstract description 13
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims abstract description 11
- 125000001424 substituent group Chemical group 0.000 claims abstract description 11
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 10
- 125000004093 cyano group Chemical group *C#N 0.000 claims abstract description 10
- DRTQHJPVMGBUCF-PSQAKQOGSA-N beta-L-uridine Natural products O[C@H]1[C@@H](O)[C@H](CO)O[C@@H]1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-PSQAKQOGSA-N 0.000 claims abstract description 9
- DRTQHJPVMGBUCF-UHFFFAOYSA-N uracil arabinoside Natural products OC1C(O)C(CO)OC1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-UHFFFAOYSA-N 0.000 claims abstract description 9
- 229940045145 uridine Drugs 0.000 claims abstract description 9
- 150000002431 hydrogen Chemical class 0.000 claims abstract description 7
- 150000004965 peroxy acids Chemical class 0.000 claims abstract description 6
- 125000001188 haloalkyl group Chemical group 0.000 claims abstract description 5
- 239000000243 solution Substances 0.000 claims description 73
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims description 71
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 69
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 60
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 57
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 claims description 51
- -1 nucleoside compound Chemical class 0.000 claims description 49
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical group CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 claims description 45
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 claims description 40
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 claims description 32
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 30
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 claims description 29
- 239000003795 chemical substances by application Substances 0.000 claims description 29
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims description 25
- 239000011630 iodine Substances 0.000 claims description 25
- 229910052740 iodine Inorganic materials 0.000 claims description 25
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 25
- 239000002585 base Substances 0.000 claims description 24
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 claims description 24
- ODLGMSQBFONGNG-JVZYCSMKSA-N 4-amino-1-[(2r,3r,4s,5r)-5-azido-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]pyrimidin-2-one Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@H](O)[C@H](O)[C@](CO)(N=[N+]=[N-])O1 ODLGMSQBFONGNG-JVZYCSMKSA-N 0.000 claims description 23
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 claims description 20
- 239000000203 mixture Substances 0.000 claims description 19
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 claims description 18
- 239000002904 solvent Substances 0.000 claims description 17
- YPWNNTBDMSIJIR-UHFFFAOYSA-N 14696-82-3 Chemical compound IN=[N+]=[N-] YPWNNTBDMSIJIR-UHFFFAOYSA-N 0.000 claims description 16
- LULAYUGMBFYYEX-UHFFFAOYSA-N 3-chlorobenzoic acid Chemical compound OC(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-N 0.000 claims description 16
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 claims description 16
- 150000003833 nucleoside derivatives Chemical class 0.000 claims description 15
- 229910021529 ammonia Inorganic materials 0.000 claims description 14
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 13
- MWQNEHXISGLUDQ-UHFFFAOYSA-N benzyl(triethyl)azanium;azide Chemical group [N-]=[N+]=[N-].CC[N+](CC)(CC)CC1=CC=CC=C1 MWQNEHXISGLUDQ-UHFFFAOYSA-N 0.000 claims description 13
- 150000003852 triazoles Chemical class 0.000 claims description 13
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical group ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 claims description 11
- 150000002148 esters Chemical class 0.000 claims description 11
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 claims description 10
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 claims description 10
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 claims description 10
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 9
- 239000000908 ammonium hydroxide Substances 0.000 claims description 9
- 150000005690 diesters Chemical class 0.000 claims description 8
- 239000000460 chlorine Substances 0.000 claims description 7
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 claims description 7
- 239000007864 aqueous solution Substances 0.000 claims description 6
- 230000002140 halogenating effect Effects 0.000 claims description 6
- SHFJWMWCIHQNCP-UHFFFAOYSA-M hydron;tetrabutylazanium;sulfate Chemical compound OS([O-])(=O)=O.CCCC[N+](CCCC)(CCCC)CCCC SHFJWMWCIHQNCP-UHFFFAOYSA-M 0.000 claims description 6
- XLOLWBTYFFTMCW-UHFFFAOYSA-N 1,2,3,5,6,7-hexahydroimidazo[1,5-a]pyridine Chemical compound C1CCN2CNCC2=C1 XLOLWBTYFFTMCW-UHFFFAOYSA-N 0.000 claims description 5
- 239000003960 organic solvent Substances 0.000 claims description 5
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 claims description 4
- 229910000396 dipotassium phosphate Inorganic materials 0.000 claims description 4
- 235000019797 dipotassium phosphate Nutrition 0.000 claims description 4
- 125000001453 quaternary ammonium group Chemical group 0.000 claims description 4
- 239000011734 sodium Substances 0.000 claims description 4
- LMBFAGIMSUYTBN-MPZNNTNKSA-N teixobactin Chemical compound C([C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H](CCC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H]1C(N[C@@H](C)C(=O)N[C@@H](C[C@@H]2NC(=N)NC2)C(=O)N[C@H](C(=O)O[C@H]1C)[C@@H](C)CC)=O)NC)C1=CC=CC=C1 LMBFAGIMSUYTBN-MPZNNTNKSA-N 0.000 claims description 4
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical group C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 claims description 3
- 239000012062 aqueous buffer Substances 0.000 claims description 3
- 229910052799 carbon Inorganic materials 0.000 claims description 3
- 229910052708 sodium Inorganic materials 0.000 claims description 3
- 239000000126 substance Substances 0.000 claims description 3
- 238000005406 washing Methods 0.000 claims description 3
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims description 2
- 239000012458 free base Substances 0.000 claims description 2
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 2
- 125000005207 tetraalkylammonium group Chemical group 0.000 claims description 2
- 125000005270 trialkylamine group Chemical group 0.000 claims description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 abstract description 4
- 229940104302 cytosine Drugs 0.000 abstract description 2
- 238000006243 chemical reaction Methods 0.000 description 29
- 239000011541 reaction mixture Substances 0.000 description 19
- 239000002002 slurry Substances 0.000 description 15
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 13
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 13
- 239000000047 product Substances 0.000 description 13
- 125000003835 nucleoside group Chemical group 0.000 description 11
- 230000008569 process Effects 0.000 description 11
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 10
- 235000011114 ammonium hydroxide Nutrition 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 8
- HTZCNXWZYVXIMZ-UHFFFAOYSA-M benzyl(triethyl)azanium;chloride Chemical compound [Cl-].CC[N+](CC)(CC)CC1=CC=CC=C1 HTZCNXWZYVXIMZ-UHFFFAOYSA-M 0.000 description 8
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 8
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical group CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 8
- SCKXCAADGDQQCS-UHFFFAOYSA-N Performic acid Chemical compound OOC=O SCKXCAADGDQQCS-UHFFFAOYSA-N 0.000 description 7
- 150000001540 azides Chemical class 0.000 description 7
- UHDGCWIWMRVCDJ-UHFFFAOYSA-N 1-beta-D-Xylofuranosyl-NH-Cytosine Natural products O=C1N=C(N)C=CN1C1C(O)C(O)C(CO)O1 UHDGCWIWMRVCDJ-UHFFFAOYSA-N 0.000 description 6
- UHDGCWIWMRVCDJ-PSQAKQOGSA-N Cytidine Natural products O=C1N=C(N)C=CN1[C@@H]1[C@@H](O)[C@@H](O)[C@H](CO)O1 UHDGCWIWMRVCDJ-PSQAKQOGSA-N 0.000 description 6
- 241000711549 Hepacivirus C Species 0.000 description 6
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical group O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 6
- 235000019439 ethyl acetate Nutrition 0.000 description 6
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical group O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 6
- 238000001914 filtration Methods 0.000 description 5
- 239000012074 organic phase Substances 0.000 description 5
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 5
- 0 *C[C@](*)(CC1)O[C@]1*(C=CC(*=*)=*1)C1=O Chemical compound *C[C@](*)(CC1)O[C@]1*(C=CC(*=*)=*1)C1=O 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- 229930024421 Adenine Chemical group 0.000 description 4
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical group NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 125000002252 acyl group Chemical group 0.000 description 4
- 229960000643 adenine Drugs 0.000 description 4
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- UHDGCWIWMRVCDJ-ZAKLUEHWSA-N cytidine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O1 UHDGCWIWMRVCDJ-ZAKLUEHWSA-N 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 239000012071 phase Substances 0.000 description 4
- 239000003880 polar aprotic solvent Substances 0.000 description 4
- 235000000346 sugar Nutrition 0.000 description 4
- 229940113082 thymine Drugs 0.000 description 4
- 150000005691 triesters Chemical class 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- QWOJMRHUQHTCJG-UHFFFAOYSA-N CC([CH2-])=O Chemical compound CC([CH2-])=O QWOJMRHUQHTCJG-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 241000700605 Viruses Species 0.000 description 3
- WGZCUXZFISUUPR-UHFFFAOYSA-N acetonitrile;oxolane Chemical compound CC#N.C1CCOC1 WGZCUXZFISUUPR-UHFFFAOYSA-N 0.000 description 3
- 150000001336 alkenes Chemical class 0.000 description 3
- 125000003710 aryl alkyl group Chemical group 0.000 description 3
- 125000000852 azido group Chemical group *N=[N+]=[N-] 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- GNOIPBMMFNIUFM-UHFFFAOYSA-N hexamethylphosphoric triamide Chemical compound CN(C)P(=O)(N(C)C)N(C)C GNOIPBMMFNIUFM-UHFFFAOYSA-N 0.000 description 3
- 238000005984 hydrogenation reaction Methods 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 239000003495 polar organic solvent Substances 0.000 description 3
- 239000002718 pyrimidine nucleoside Substances 0.000 description 3
- 229910052938 sodium sulfate Inorganic materials 0.000 description 3
- 235000011152 sodium sulphate Nutrition 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- NHGXDBSUJJNIRV-UHFFFAOYSA-M tetrabutylammonium chloride Chemical compound [Cl-].CCCC[N+](CCCC)(CCCC)CCCC NHGXDBSUJJNIRV-UHFFFAOYSA-M 0.000 description 3
- IMNIMPAHZVJRPE-UHFFFAOYSA-N triethylenediamine Chemical compound C1CN2CCN1CC2 IMNIMPAHZVJRPE-UHFFFAOYSA-N 0.000 description 3
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 description 2
- 239000005711 Benzoic acid Substances 0.000 description 2
- NYHBQMYGNKIUIF-UUOKFMHZSA-N Guanosine Chemical group C1=NC=2C(=O)NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O NYHBQMYGNKIUIF-UUOKFMHZSA-N 0.000 description 2
- PWKSKIMOESPYIA-BYPYZUCNSA-N L-N-acetyl-Cysteine Chemical compound CC(=O)N[C@@H](CS)C(O)=O PWKSKIMOESPYIA-BYPYZUCNSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 229960004308 acetylcysteine Drugs 0.000 description 2
- 150000001266 acyl halides Chemical class 0.000 description 2
- 238000005917 acylation reaction Methods 0.000 description 2
- 150000001350 alkyl halides Chemical class 0.000 description 2
- 238000005915 ammonolysis reaction Methods 0.000 description 2
- 125000005129 aryl carbonyl group Chemical group 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 235000010233 benzoic acid Nutrition 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 150000001734 carboxylic acid salts Chemical class 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 238000005695 dehalogenation reaction Methods 0.000 description 2
- 238000006356 dehydrogenation reaction Methods 0.000 description 2
- 239000012973 diazabicyclooctane Substances 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 238000007337 electrophilic addition reaction Methods 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- FDGQSTZJBFJUBT-UHFFFAOYSA-N hypoxanthine Chemical group O=C1NC=NC2=C1NC=N2 FDGQSTZJBFJUBT-UHFFFAOYSA-N 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- NKBSRXQDIXSDFH-UHFFFAOYSA-N methanesulfonic acid;4-methylmorpholine Chemical compound CS([O-])(=O)=O.C[NH+]1CCOCC1 NKBSRXQDIXSDFH-UHFFFAOYSA-N 0.000 description 2
- QPJVMBTYPHYUOC-UHFFFAOYSA-N methyl benzoate Chemical compound COC(=O)C1=CC=CC=C1 QPJVMBTYPHYUOC-UHFFFAOYSA-N 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000012038 nucleophile Substances 0.000 description 2
- 230000000269 nucleophilic effect Effects 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 239000002798 polar solvent Substances 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 2
- 150000003254 radicals Chemical class 0.000 description 2
- 239000000376 reactant Substances 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 229940035893 uracil Drugs 0.000 description 2
- FHPJZSIIXUQGQE-JVZYCSMKSA-N 1-[(2r,3r,4s,5r)-5-azido-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]pyrimidine-2,4-dione Chemical class O[C@@H]1[C@H](O)[C@](CO)(N=[N+]=[N-])O[C@H]1N1C(=O)NC(=O)C=C1 FHPJZSIIXUQGQE-JVZYCSMKSA-N 0.000 description 1
- NEMNIUYGXIQPPK-XVFCMESISA-N 1-[(2r,3r,4s,5s)-3,4-dihydroxy-5-(iodomethyl)oxolan-2-yl]pyrimidine-2,4-dione Chemical compound O1[C@H](CI)[C@@H](O)[C@@H](O)[C@@H]1N1C(=O)NC(=O)C=C1 NEMNIUYGXIQPPK-XVFCMESISA-N 0.000 description 1
- 125000006083 1-bromoethyl group Chemical group 0.000 description 1
- CCZMQYGSXWZFKI-UHFFFAOYSA-N 1-chloro-4-dichlorophosphoryloxybenzene Chemical compound ClC1=CC=C(OP(Cl)(Cl)=O)C=C1 CCZMQYGSXWZFKI-UHFFFAOYSA-N 0.000 description 1
- 125000001478 1-chloroethyl group Chemical group [H]C([H])([H])C([H])(Cl)* 0.000 description 1
- PCYYYAWPQFJTJF-UHFFFAOYSA-M 1-ethyl-2-hexyl-n,n-dimethylpyridin-1-ium-4-amine;bromide Chemical compound [Br-].CCCCCCC1=CC(N(C)C)=CC=[N+]1CC PCYYYAWPQFJTJF-UHFFFAOYSA-M 0.000 description 1
- 125000004776 1-fluoroethyl group Chemical group [H]C([H])([H])C([H])(F)* 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 1
- ICHLNDWMYWZUTG-UHFFFAOYSA-N 2-azido-7h-purine Chemical class [N-]=[N+]=NC1=NC=C2NC=NC2=N1 ICHLNDWMYWZUTG-UHFFFAOYSA-N 0.000 description 1
- 125000005999 2-bromoethyl group Chemical group 0.000 description 1
- 125000001340 2-chloroethyl group Chemical group [H]C([H])(Cl)C([H])([H])* 0.000 description 1
- ASJSAQIRZKANQN-CRCLSJGQSA-N 2-deoxy-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)CC=O ASJSAQIRZKANQN-CRCLSJGQSA-N 0.000 description 1
- 125000004777 2-fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- LULAYUGMBFYYEX-UHFFFAOYSA-M 3-chlorobenzoate Chemical compound [O-]C(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-M 0.000 description 1
- 125000004179 3-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(Cl)=C1[H] 0.000 description 1
- 125000006201 3-phenylpropyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical group [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 206010008909 Chronic Hepatitis Diseases 0.000 description 1
- MIKUYHXYGGJMLM-GIMIYPNGSA-N Crotonoside Chemical group C1=NC2=C(N)NC(=O)N=C2N1[C@H]1O[C@@H](CO)[C@H](O)[C@@H]1O MIKUYHXYGGJMLM-GIMIYPNGSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- NYHBQMYGNKIUIF-UHFFFAOYSA-N D-guanosine Chemical group C1=2NC(N)=NC(=O)C=2N=CN1C1OC(CO)C(O)C1O NYHBQMYGNKIUIF-UHFFFAOYSA-N 0.000 description 1
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- UGQMRVRMYYASKQ-UHFFFAOYSA-N Hypoxanthine nucleoside Natural products OC1C(O)C(CO)OC1N1C(NC=NC2=O)=C2N=C1 UGQMRVRMYYASKQ-UHFFFAOYSA-N 0.000 description 1
- QZRGKCOWNLSUDK-UHFFFAOYSA-N Iodochlorine Chemical compound ICl QZRGKCOWNLSUDK-UHFFFAOYSA-N 0.000 description 1
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000010939 advanced reactive system screening zool Methods 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 239000000010 aprotic solvent Substances 0.000 description 1
- 150000005840 aryl radicals Chemical class 0.000 description 1
- IVRMZWNICZWHMI-UHFFFAOYSA-N azide group Chemical group [N-]=[N+]=[N-] IVRMZWNICZWHMI-UHFFFAOYSA-N 0.000 description 1
- 229940068606 benzoxonium Drugs 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 238000006480 benzoylation reaction Methods 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Chemical group BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 150000001244 carboxylic acid anhydrides Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 150000003983 crown ethers Chemical class 0.000 description 1
- 125000004966 cyanoalkyl group Chemical group 0.000 description 1
- 230000006196 deacetylation Effects 0.000 description 1
- 238000003381 deacetylation reaction Methods 0.000 description 1
- 230000020176 deacylation Effects 0.000 description 1
- 238000005947 deacylation reaction Methods 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- RCJVRSBWZCNNQT-UHFFFAOYSA-N dichloridooxygen Chemical compound ClOCl RCJVRSBWZCNNQT-UHFFFAOYSA-N 0.000 description 1
- 238000000113 differential scanning calorimetry Methods 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000004880 explosion Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 229930182470 glycoside Natural products 0.000 description 1
- 229940029575 guanosine Drugs 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 239000012770 industrial material Substances 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000005650 intramolecular substitution reaction Methods 0.000 description 1
- 150000004694 iodide salts Chemical class 0.000 description 1
- 239000012336 iodinating agent Substances 0.000 description 1
- 230000002083 iodinating effect Effects 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000011005 laboratory method Methods 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 229940095102 methyl benzoate Drugs 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 229940127073 nucleoside analogue Drugs 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- TVMXDCGIABBOFY-UHFFFAOYSA-N octane Chemical compound CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 150000002972 pentoses Chemical class 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- XCRBXWCUXJNEFX-UHFFFAOYSA-N peroxybenzoic acid Chemical class OOC(=O)C1=CC=CC=C1 XCRBXWCUXJNEFX-UHFFFAOYSA-N 0.000 description 1
- 125000000286 phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- RLOWWWKZYUNIDI-UHFFFAOYSA-N phosphinic chloride Chemical compound ClP=O RLOWWWKZYUNIDI-UHFFFAOYSA-N 0.000 description 1
- 150000004714 phosphonium salts Chemical class 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 235000007686 potassium Nutrition 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- JRMUNVKIHCOMHV-UHFFFAOYSA-M tetrabutylammonium bromide Chemical compound [Br-].CCCC[N+](CCCC)(CCCC)CCCC JRMUNVKIHCOMHV-UHFFFAOYSA-M 0.000 description 1
- IBWGNZVCJVLSHB-UHFFFAOYSA-M tetrabutylphosphanium;chloride Chemical compound [Cl-].CCCC[P+](CCCC)(CCCC)CCCC IBWGNZVCJVLSHB-UHFFFAOYSA-M 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 125000003866 trichloromethyl group Chemical group ClC(Cl)(Cl)* 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- 238000005292 vacuum distillation Methods 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
- C07H19/067—Pyrimidine radicals with ribosyl as the saccharide radical
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Virology (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Saccharide Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
본 발명은 화학식 II의 5'-아이오도 화합물을 과산 R2aC(O)OOH, 산 R2aC(O)OH 및 상전이촉매와 접촉시키고 화학식 B1의 우리딘을 화학식 B2의 시토신으로 상호 전환시킴을 포함하는, 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물(화학식 I; B=B1; R1은 R1aCO-이고, R2는 R2aCO-임) 또는 4'-아지도뉴클레오사이드 화합물(화학식 I; B는 B1 또는 B2이고, R1 및 R2는 수소임) 및 그의 산부가염을 제조하는 방법에 관한 것이다:
상기 식에서,
R1a 및 R2a는 독립적으로 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1-10 알킬 또는 페닐이고,
R3은 수소, C1 -6 알킬, C1 -3 할로알킬 및 할로겐으로 이루어진 군으로부터 선택된다.
본 발명은 4'-아지도뉴클레오사이드를 더욱 높은 효율로 고순도로 안전하고 도 선택적으로 제공한다.
Description
본 발명은 바이러스 매개되는 질환을 치료하는데 유용한 4-아지도뉴클레오사이드 유도체의 신규 제조 방법에 관한 것이다. 더욱 구체적으로, 본 발명은 4-아미노-1-((2R,3R,4S,5R)-5-아지도-3,4-다이하이드록시-5-하이드록시메틸-테트라하이드로-퓨란-2-일)-1H-피리미딘-2-온 및 그의 약학적으로 허용가능한 산부가염, 특히 헤미설페이트 염의 제조 방법에 관한 것이다.
본 발명은 바이러스-매개되는 질환을 치료하는데 유용한 아지도 치환된 뉴클레오사이드 유도체의 제조 방법에 관한 것이다. 특히, 본 발명은 C형 간염 바이러스(HCV) RNA 복제의 유용한 저해제인 4-아지도 피리미딘 뉴클레오사이드 유도체의 제조 방법에 관한 것이다.
C형 간염 바이러스(HCV)는 전세계적으로 만성 간 질환의 큰 부분을 차지하며, 산업화된 국가에서의 만성 간염의 70%에 달한다. C형 간염의 전체적인 비율은 평균 3%(0.1 내지 5%)로 추정되며, 전세계적으로 1억 7천만명의 만성 보균자가 있 는 것으로 추산된다. HCV에 대해 효과적인 치료제 및 이러한 약제를 제조하는 방법이 지속적으로 요구되고 있다.
모팻(J. G. Moffatt)[Chemical Transformation of the Sugar Moiety of Nucleosides, in Nucleoside Analogues, 워커, 클러크 및 엑스타인 편집, Plenum Publishing Corp., 뉴욕, 1979, p. 144]은 아지드화요오드의 N-[1-((2R,3R,4S)-3,4-다이하이드록시-5-메틸렌-테트라하이드로-퓨란-2-일)-2-옥소-1,2-다이하이드로-피리미딘-4-일]-벤즈아마이드(X)로의 친전자성 부가에 의해 4'-아지도시티딘(VIIIb)을 제조함을 기재하고 있다.
맥(Maag) 등[J. Med . Chem . 1992 35:1440-1451]은 아지드화요오드의 5-메틸렌-테트라하이드로-퓨란-2-일 뉴클레오사이드(XI)(여기에서, B는 티민, 우라실, 아데닌 또는 구아노신임)로의 부가에 의해 4'-아지도 뉴클레오사이드를 제조함을 개시하고 있다.
맥 등(상기 문헌)은 4'-위치에서의 전자-회수 기에 의해 5'-아이오도의 치환이 지연되기는 하지만 화합물(XIIa)를 퍼벤조산 유도체와 접촉시킴으로써 아이오다이드를 산화시켜 과원자가(hypervalent) 상태로 만들고, 이를 치환시켜 화합물(XIIb)과 화합물(XIIc)을 포함하는 생성물의 혼합물을 제공함을 추가로 개시한다. 이 반응은 3'-5'-환상 벤즈옥소늄 이온을 통해 진행되는 것으로 암시되었다. 3'-위치에서 에스터화되지 않은 뉴클레오사이드 또는 3'-데옥시-뉴클레오사이드를 사용하여서는 반응시키지 못하였을 때, 근위 3'-아실옥시 잔기의 중요성이 명백해졌다.
WO 02/100415 호[드보(R. Devos) 등]에는 바이러스의 DNA 폴리머라제를 저해하는 4'-치환된 뉴클레오사이드 유도체가 개시되어 있다. 맥 등(상기 문헌)에 의해 기재된 방법에 의해 4'-아지도뉴클레오사이드를 제조하였다. TPP, 요오드 및 피리딘의 혼합물을 사용하여 우리딘의 아세토나이드(IVd)를 요오드화시켜, 상응하는 5'-아이오도 유도체(IVe)를 제공하였다. 버헤이든(J. P. Verheyden) 등의 문헌[J. Org. Chem., 1970, 35(7): 2319]에 기재되어 있는 바와 같이, 산, 예컨대 아세트산으로 처리함으로써 아세토나이드 보호기를 제거하여, 화학식 IVf의 뉴클레오사이드를 제공하였으며, 이를 메톡시화나트륨으로 탈요오드화수소화시켜 화합물(Va)을 제공하였다. DMF중 염화요오드와 아지드화나트륨의 혼합물로 화합물(Va)을 처리하여 화학식 IIa의 아이오도아지드 뉴클레오사이드를 제공하였다. 화합물(IIa)의 하이드록시기를 피리딘중 벤조일 클로라이드로 처리함으로써 보호하여, 화학식 IId의 다이아실 뉴클레오사이드를 제공하고, 다이에스터를 다이클로로메테인중 MCPBA로 처리함으로써 화학식 IIIb의 5'-벤조일 뉴클레오사이드로 전화시켰다. Ac2O 및 피리딘으로 3'-하이드록시를 보호하고, 보쓰윅(A. D. Borthwick) 등의 문헌[J. Med . Chem . 1990, 33(1): 179]에 기재된 방법{또한 디바카(K. J. Divakar) 및 리즈(C. B. Reese)의 문헌[J. Chem . Soc ., Perkin Trans, I 1982 1171-1176]도 참조함}을 이용함으로써 우리딘(IIIb)을 시티딘으로 전환시켰다. 화합물(IIIc)을 4-클로로페닐 다이클로로포스페이트 및 1,2,4-트라이아졸로 처리하여, 화학식 XIII의 4-트라이아졸릴 뉴클레오사이드를 제공하고, 이를 암모니아 수용액으로 치환시켜 화학식 VIII의 4'-치환된 시티딘을 제공하였다.
본 발명은 또한 4'-아지도-우리딘 유도체(I) 또는 4'-아지도-시티딘(VIII) 또는 이의 산부가염을 제조하는 방법에 관한 것이다.
최근, 4'-아지도시티딘이 HCV 폴리머라제에 대해 탁월한 활성을 갖는 것으로 밝혀졌다. 공정 단계를 최소화시키고 비효율적인 보호 전략에 대한 의존성이 감소된, 화합물(VIII) 및 그의 산부가염을 제조하는 새로운 효과적인 방법이 필요하다. 또한, 공정 단계는 열불안정성 아지드 잔기와 상용성이어야 한다. 본 발명은 4'-아지도뉴클레오사이드 화합물 및 4'-아지도-2',3',5'-트라이-아실뉴클레오사이드 화합물을 제조하는 신규 방법에 관한 것이다.
본 발명의 하나의 목적은 (i) 단계 a)에서 하기 화학식 IVa의 뉴클레오사이드 화합물을 하기 화학식 II의 화합물로 변환시키고, 단계 b)에서 적합한 용매중 화학식 II의 5'-아이오도 화합물의 용액을 과산 R2aC(O)OOH, 산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜 하기 화학식 I의 4-'아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 생성시키며, 단계 c)에서 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 변환시켜 화학식 VIII의 4'-아지도-시티딘 화합물 및 필요한 경우 그의 약학적으로 허용가능한 부가염을 제공함을 특징으로 하는, 하기 화학식 VIII의 4'-아지도-시티딘 화합물 및 그의 약학적으로 허용가능한 부가염을 제조하는 방법이다:
상기 식에서,
R3은 H, C1 -6-알킬, C1 -3-할로알킬 또는 할로겐이고,
R1은 R1aCO-이고,
R1a는 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택 되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1 -10-알킬 또는 페닐이며,
R2는 R2aCO-이고,
R2a는 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1 -10-알킬 또는 페닐이다.
본 발명의 다른 목적은 다음과 같다:
(ii) 적합한 용매중 화학식 II의 5'-아이오도 화합물의 용액을 과산 R2aC(O)OOH, 산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜, 하기 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 생성시킴을 포함하는, 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드를 제조하는 방법:
화학식 I
상기 식에서,
R1은 R1aCO-이고,
R2는 R2aCO-이고,
R1a 및 R2a는 독립적으로 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1 -10-알킬 또는 페닐이며,
R3은 H, C1 -6-알킬, C1 -3-할로알킬 또는 할로겐이다.
(iii) 화학식 IV의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 제 1 염기와 접촉시켜 하기 화학식 Ia의 4'-아지도-뉴클레오사이드 화합물을 제공하는 것을 추가로 포함함을 특징으로 하는, 화학식 Ia의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 제조하는, (i)에 따른 방법:
상기 식에서, R3은 (i)에서 정의된 바와 같다.
(iv) a) 화학식 IVa의 뉴클레오사이드를 할로겐화제와 접촉시켜, 하기 화학식 IVb의 5'-할로 뉴클레오사이드 화합물을 생성시키는 단계; b) 화학식 IVb의 화합물을 탈할로겐화수소화제와 접촉시켜, 하기 화학식 Va의 5'-메틸렌 뉴클레오사이드 화합물을 생성시키는 단계; c) 화학식 Va의 화합물을 테트라하이드로퓨란(THF) 및 아세토나이트릴(MeCN)에 용해된 아지드화 4급 암모늄 및 요오드와 접촉시켜, 하기 화학식 IIa의 아이오도 아지드 화합물을 생성시키는 단계; d) 하기 화학식 IIa의 화합물을 하나 이상의 제 2 염기 및 제 1 아실화제와 접촉시켜, 하기 화학식 II 의 다이에스터 화합물을 생성시키는 단계를 포함함을 특징으로 하는, 화학식 II의 5'-아이오도 화합물을 제조하는, (i)에 따른 방법:
화학식 II
상기 식에서, X는 할로겐이고, R1 및 R3은 (i)에서 정의된 바와 같다.
(v) a) 하기 화학식 I의 화합물을 CH2Cl2중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드, 트라이에틸아민(TEA)과 접촉시켜, 하기 화학식 VI의 트라이아졸 화합물을 제공하는 단계, b) 화학식 VI의 화합물을 수산화암모늄과 테트라하이드로퓨란(THF)의 용액과 접촉시켜 트라이아졸을 치환시킴으로써, 하기 화학식 VII의 4'-아지도-2',3',5'-트라이아실시티딘 화합물을 제공하는 단계, c) 화학식 VII의 화합물을 암모니아와 알콜의 용액과 접촉시켜 에스터를 절단함으로써, 하기 화학식 VIII의 화합물을 제공하는 단계를 포함함을 특징으로 하는, (i)에 따른 화학식 VIII의 4'-아지도시티딘 화합물을 제조하는 방법:
화학식 I
화학식 VIII
상기 식에서, R1 및 R2는 (i)에서 정의된 바와 같고, R3은 수소이다.
(vi) a) 하기 화학식 Va의 화합물을 제 2 아실화제 및 임의적으로는 트라이알킬아민 염기와 접촉시켜, 하기 화학식 Vb의 다이아실 화합물을 제공하고, 화학식 Vb의 화합물의 유기 용액을 NaHCO3 수용액으로 세척하며, 이 때 pH를 약 7.5로 유지시키는 단계; 및 b) 화학식 Vb의 상기 다이아실 화합물을 암모니아와 메탄올의 용액과 접촉시켜 화학식 Va의 화합물을 재생시키는 단계를 포함함을 특징으로 하는, (iv)에 따른 방법:
화학식 Va
상기 식에서, R1 및 R3은 (iv)에서 정의된 바와 같다.
(vii) 화학식 VIII의 화합물을 아이소프로판올, 물 및 황산으로부터 결정화시키는 것을 추가로 포함함을 특징으로 하는, 하기 화학식 VIIIa의 4'-아지도시티딘의 헤미설페이트 산부가염을 제조하는, (i)에 따른 방법:
상기 식에서, R3은 (i)에서 정의된 바와 같다.
(viii) 상기 상전이촉매가 테트라알킬 암모늄 하이드로젠 설페이트이고; 상기 용매가 수성 완충액과 비극성 유기 용매의 혼합물이며; 상기 요오드화제가 트라이페닐포스핀(TPP), 요오드 및 이미다졸이고; 상기 탈할로겐화수소화제가 메톡시화나트륨 또는 1,8-다이아자바이사이클로[4.3.0]논-5-엔(DBN)이며; 상기 아지드화 4급 암모늄이 벤질 트라이에틸암모늄 아지드이고; 상기 아실화제가 벤조일 클로라이드이며; 상기 제 1 염기가 암모니아이고; 상기 제 2 염기가 N-메틸모폴린(NMM) 및 4-다이메틸아미노피리딘(DMAP)이고; 상기 알콜이 메탄올인, R3이 수소이고, R1이 PhCO이고, R2가 R2aCO이고, R2a가 임의적으로 치환되는 페닐인 화학식 VIIIa의 4'-아지도-시티딘의 헤미설페이트 산부가염을 제조하는, (vii)에 따른 방법.
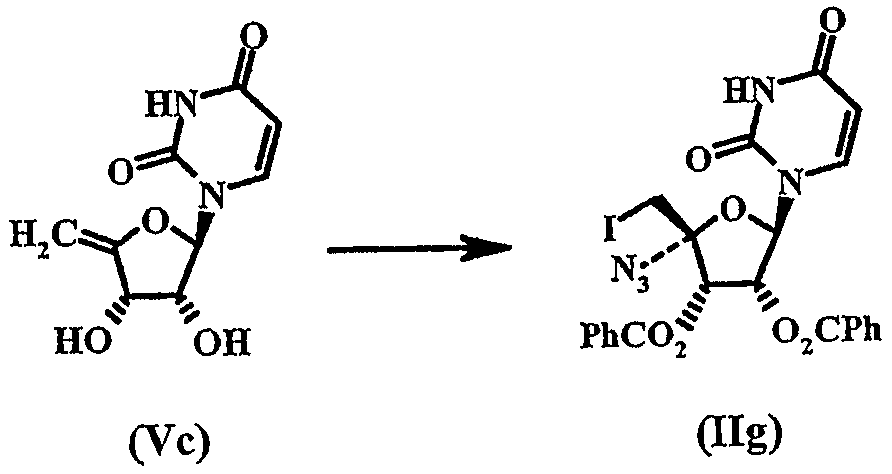
(ix) a) 하기 화학식 IVg의 우리딘 화합물의 테트라하이드로퓨란(THF) 용액을 트라이페닐포스핀(TPP), 요오드 및 이미다졸과 접촉시켜, 하기 화학식 IVh의 1-(3,4-다이하이드록시-5-할로메틸-테트라하이드로-퓨란-2-일)-1H-피리미딘-2,4-다이온을 생성시키는 단계; b) 화학식 IVh의 화합물을 메톡시화나트륨의 메탄올 용액과 접촉시켜, 하기 화학식 Vc의 1-(3,4-다이하이드록시-5-메틸렌-테트라하이드로-퓨란-2-일)-1H-피리미딘-2,4-다이온을 생성시키는 단계; c) 화학식 Vc의 화합물을 테트라하이드로퓨란(THF) 및 아세토나이트릴(MeCN)중 벤질 트라이에틸암모늄 아지드 및 요오드의 용액과 접촉시켜 하기 화학식 IIe의 아이오도 아지드를 제공하는 단계; d) 화학식 IIe의 화합물을 벤조일 클로라이드, N-메틸모폴린(NMM) 및 아세토나이트릴(MeCN)의 용액과 접촉시켜, 하기 화학식 IIg의 다이벤조에이트 화합물을 제공하는 단계; e) 화학식 IIg의 화합물을 다이클로로메테인(DCM)과 인산수소칼륨의 수용액의 2-상 용액중에서 m-클로로퍼벤조산, m-클로로벤조산 및 테트라뷰틸암모늄 하이드로젠 설페이트와 접촉시켜, 하기 화학식 IIId의 화합물을 제공하는 단계; f) 화학식 IIId의 화합물을 다이클로로메테인(DCM)중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드, 트라이에틸아민(TEA)의 용액과 접촉시켜, 하기 화학식 IIIe의 화합물을 제공하는 단계; g) 화학식 IIIe의 화합물을 암모니아의 메탄올 용액과 접촉시켜 에스터를 절단하고 하기 화학식 VIIIb의 화합물의 유리 염기를 제공하는 단계; h) 화학식 VIIIb의 화합물을 아이소프로판올 및 H2SO4 함유 물로부터 결정화시켜, 하기 화학식 VIIIc의 헤미설페이트 염을 제공하는 단계를 포함함을 특징으로 하는, 하기 화학식 VIIIc의 4-'아지도시티딘 헤미설페이트를 제조하는 방법:
(x) 하기 화학식 Ic의 화합물:
상기 식에서, R은 할로겐, C1 -10-알킬, C1 -10-알콕시, 나이트로, 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 페닐이다.
본 발명의 한 실시태양에서는, 적합한 용매중 5'-아이오도메틸-2',3'-다이아실 뉴클레오사이드 화합물(II)의 용액을 과카복실산 R2aC(O)OOH, 카복실산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시킴을 포함하는, 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 제조하는 방법이 제공된다:
상기 식에서,
R1은 R1aCO-이고,
R2는 R2aCO-이고,
R1a 및 R2a는 독립적으로 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1 -10 알킬 또는 페닐이며,
R3은 수소, C1 -6 알킬, C1 -3 할로알킬 및 할로겐으로 이루어진 군으로부터 선택된다.
놀랍게도, 이탈기를 산화제(MCPBA)로 활성화시킴으로써 아이오도-다이벤조에이트(II)를 치환시키고, 상전이촉매를 함유하는 적합한 용매중에서 외부 친핵체(MCBA)를 사용하여 치환시키면, 맥 등(상기 문헌)에 의해 기재된 치환 반응보다 상당히 더 높은 트라이에스터 수율이 달성되었다. 반응은 직접적으로 트라이에스터를 제공하고, 외부 친핵체의 부재하에 생성된 3'-하이드록실기를 에스터화시키기 위한 별도의 반응 단계가 필요 없다. 이탈기를 활성화시키기 위하여, 아이오다이드를 산화시켜 과카복실산에 의한 과원자가 상태로 만든다. 4'-위치에 전자-회수기가 존재함으로써 과산 활성화가 필요해진다. 이전의 연구 결과, 3'-하이드록실상의 아실 잔기가 5'-하이드록실로 분자내 전달됨으로써 불안정한 과원자가 아이오다이드를 치환시키는 것으로 밝혀졌다. 대조적으로, 본 반응은 3-아실 잔기의 분자내 전달보다는 카복실산 염(예: m-클로로벤조산칼륨, 벤조산나트륨, 아세트산나 트륨)에 의한 분자내 치환을 통해 진행된다. 다양한 용매 중에서 반응을 수행할 수 있다. 친핵성 카복실산의 염을 용해시키기에 충분히 극성인 임의의 유기 용매가 허용되지만, 친핵성 카복실산 염, 상전이촉매 및 비-극성 유기 용매를 제공하기 위하여 완충된 수용액을 포함하는 2상 매질이 특히 적합하다. 물 및 다이클로로메테인을 포함하는 2상 매질이 유기 용매의 불연성 때문에 바람직하다. 적합한 완충액은 약 2 내지 약 10의 pH를 제공하고, 인산칼륨, 인산수소칼륨, 이수소 칼륨, 탄산나트륨 및 중탄산나트륨을 포함하지만 이들로 한정되지는 않는다. 본 방법에 의해 특이적인 5-아실옥시 잔기를 우수한 수율 및 높은 순도로 도입할 수 있다.
본 발명의 다른 실시태양에서는, (i) 적합한 용매중 5'-아이오도메틸-2',3'-다이아실 뉴클레오사이드 화합물의 용액을 과카복실산 R2aC(O)OOH, 카복실산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜, R1, R2 및 R3이 상기 기재된 바와 같은 화학식 I의 화합물을 제공하고; (ii) 생성된 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 염기와 접촉시켜, 화학식 Ia의 피리미딘 뉴클레오사이드 화합물을 제공함으로써, 4'-아지도 피리미딘 뉴클레오사이드를 제조하는 효과적인 신규 방법을 제공한다.
본 발명의 다른 실시태양에서는, 아지도 잔기가 혼입될 때까지 아데닌의 6- 아미노 또는 구아닌의 2-아미노를 N-보호기에 의해 마스킹하는, B가 하이포잔틴, 아데닌 또는 구아닌인 화학식 Ia의 4'-아지도퓨린 유도체를 제조하는 방법을 제공한다.
본 발명의 다른 실시태양에서는, (i) 화학식 IVa의 화합물을 할로겐화제와 접촉시켜, 화학식 IVb의 화합물을 제공하고; (ii) 화학식 IVb의 화합물을 탈할로겐화수소화제와 접촉시켜 화학식 Va의 5-메틸렌 뉴클레오사이드 화합물을 생성시키고; (iii) 화학식 Va의 화합물을 극성 비양성자성 용매에 용해된 아지드화 4급 암모늄 및 요오드와 접촉시켜, 화학식 IIa의 아이오도 아지드를 생성시키고; (iv) 화학식 IIa의 화합물을 아실화제와 접촉시켜 화학식 IIb의 다이에스터를 제공하고; (v) 적합한 용매중 화학식 IIb의 5'-아이오도메틸-2',3'-다이아실 뉴클레오사이드 화합물의 용액을 과카복실산 R2aC(O)OOH, 카복실산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜 화학식 I의 화합물을 제공함을 포함하는, 화학식 IVa의 뉴클레 오사이드로부터 R1, R2 및 R3이 상기 정의된 바와 같은 화학식 I의 4'-아지도-2',3'-5'-트라이아실-뉴클레오사이드 화합물을 제조하는 방법(반응식 2)을 제공한다.
통상 공정의 개별 단계의 수를 최소화시키기 위하여 보호/탈보호 단계를 없애는 것이 바람직하다. 츠지(T. Tsuji) 및 다케나카(K. Takenaka)[Nucleosides & Nucleotides 1987 6(3): 575-80]는 DMF 또는 HMPA 중에서 사할로겐화탄소 및 TPP를 사용하여 보호되지 않은 뉴클레오사이드의 5-하이드록시메틸을 브롬화 또는 요오드화시킴을 개시하고 있다. 맥 등(상기 문헌)은 피리딘 또는 이미다졸의 존재하에 뉴클레오사이드의 다이옥세인 용액을 요오드 및 TPP와 접촉시킴으로써 보호되지 않은 뉴클레오사이드를 선택적으로 요오드화시키는 절차를 개시하고 있다. 29 내지 59%의 수율이 보고되었다. 알콜을 아이오다이드로 전환시키는 다른 방법은 널리 공지되어 있다. 예를 들어 마치(J. March)의 문헌[Advanced Organic Chemistry, John Wiley & Sons, 제4판, 1992, pp. 431-433] 참조. 본 발명의 방법의 단계 (a)에서는, 다이옥세인을 THF로 대체하고 반응 온도를 조심스럽게 제어함으로써 반응 조건을 개선 및 최적화시켜, 화학식 IVb의 화합물 84%의 수율을 나타내었다.
5'-할로뉴클레오사이드의 탈할로겐화수소화는 개시된 바 있다{우에다(T. Ueda)의 문헌[Chemistry of Nuclotides and Nucleosides, 타운센드 편집, Plenum Press, 뉴욕, 1988, pp. 83-88]}. 탈할로겐화수소화제의 다른 예는 마치의 문헌 및 그에 인용된 참조문헌(마치, 상기 문헌, pp. 1023-1025)에 기재되어 있다. 맥 등(상기 문헌)은 DBN 또는 메톡시화나트륨을 사용한 관련 뉴클레오사이드 유도체의 탈요오드화수소화를 개시하였다. 본 발명에 따른 방법의 단계 (b)에서는, 메톡시화나트륨을 사용한 탈수소화가 최상의 결과를 제공하였다. N-메틸모폴리늄 메실레이트를 첨가함으로써 과량의 메톡시화나트륨을 급랭시켰다.
본 발명에 따른 방법의 단계 (e)는 외향 고리 올레핀으로의 아지드화요오드의 공식적인 친전자성 부가이다. 유기 아지드화물{예컨대 비핀(M.E.C. Biffin) 등의 문헌[Chemistry of the Azido Group, 파타이 편집, Wiley-Interscience, 뉴욕, 1971, pp 61-63] 참조} 및 아지드화요오드{색스(N. I. Sax) 및 루이스(R. J. Lewis)의 문헌[Dangerous Properties of Industrial Materials, van Nostrand, 뉴욕, 1989, p. 1993]}의 알려져 있는 폭발 및 독성 위험에 비추어, 유기 아지드화물을 사용한 합성 반응은 위험을 최소화시킬 뿐만 아니라 효율을 증가시키도록 조심스럽게 디자인되어야 한다. 이는, 목적이 상업적인 규모의 제조인 경우에 특히 그러하다. 맥 등(상기 문헌) 및 모팻(상기 문헌)은 5-메틸렌 뉴클레오사이드로의 아지드화요오드의 부가를 개시하고 있다. 놀랍게도, 최근 시차 주사 열계량법 및 ARSST[진보된 반응 시스템 주사 도구; Advanced Reaction System Screening Tool]에서는 아지드화 4급 암모늄과 요오드의 혼합물이 아지드화요오드보다 격렬하게 분해될 가능성이 적고 5-메틸렌 뉴클레오사이드에 효율적으로 부가되어 요오도 아지드를 제공하는 것으로 밝혀졌다. 바람직하게는, 4급 암모늄 염은 상전이촉매, 특히 벤질 트라이에틸암모늄 아지드이다. 따라서, 벤질 트라이에틸 암모늄 클로라이드 및 아지드화나트륨을 아세토나이트릴에 슬러리화시키고, 벤질 트라이에틸암모늄 아지드(BTEAA)를 침전된 염화나트륨으로부터 여과한다. BTEAA, 화학식 Va의 화합물 및 NMM의 MeCN 용액을 0 내지 5℃로 냉각시키고 요오드 및 THF의 용액을 첨가하여, 목적하는 화학식 IIa의 요오도 아지드 및 화학식 IX의 그의 부분입체 이성질체를 약 9:1(IIa:IX) 이상의 비로 생성시켰다. 요오드에 의한 아지드의 산화를 촉진시키는 소량의 N-아세틸시스테인을 첨가함으로써 과량의 아지드를 제거하고, 내부 온도를 약 5℃로 유지시키면서 하나 이상의 염기 및 벤조일 클로라이드를 첨가함으로써 동일 반응계 내에서 반응 생성물을 화학식 IIb의 다이벤조에이트(R1a=Ph)로 전환시킨다. 이렇게 수득된 다이벤조에이트에 대해 퍼카복실레이트/카복실레이트(예컨대, MCPBA/MCBA) 매개되는 치환을 수행하여 화학식 I의 화합물을 제공한다.
본 발명의 다른 실시태양에서는, (i) 화학식 IVa의 뉴클레오사이드를 할로겐화제와 접촉시켜 화학식 IVb의 5'-할로 뉴클레오사이드 화합물을 생성시키는 단계; (ii) 화학식 IVb의 화합물을 탈할로겐화수소화제와 접촉시켜 화학식 Va의 5-메틸렌 뉴클레오사이드 화합물을 생성시키는 단계; (iii) 화학식 Va의 화합물을 비양성자성 극성 매질에 용해된 아지드화 4급 암모늄 및 요오드와 접촉시켜 화학식 IIa의 아이오도 아지드를 생성시키는 단계; (iv) 화학식 IIa의 화합물을 아실화제와 접촉시켜 R1, R2 및 R3이 상기 기재된 바와 같은 화학식 IIb의 다이에스터를 제공하는 단계; (v) 적합한 용매중 화학식 II의 5'-아이오도메틸-2',3'-다이아실 뉴클레오사이드 화합물의 용액을 과카복실산 R2aC(O)OOH, 카복실산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜 화학식 I의 화합물을 제공하는 단계; (vi) 화학식 I의 화합물을 CH2Cl2중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드 및 TEA와 접촉시켜 화학식 VI의 트라이아졸을 제공하는 단계; (vii) 화학식 VI의 화합물을 비양성자성 용매(예: MeCN, THF 또는 DMF)중 수산화암모늄의 용액과 접촉시켜 트라이아졸을 치환시킴으로써 화학식 VII의 4'-아지도-2',3',5'-트라이아실시티딘을 제공하는 단계; (viii) 화학식 VII의 화합물을 암모니아와 알콜의 용액과 접촉시켜 에스터를 절단함으로써 화학식 VIII의 화합물을 제공하는 단계를 포함하는, R3이 상기 정의된 바와 같은 화학식 VIII의 4'-아지도-시티딘을 제조하는 방법(반응식 2 및 3)을 제공한다. 2단계 가암모니아분해에 의해 허용가능한 순도를 갖는 최종 생성물을 제공하는데 칼럼 크로마토그래피가 필요하지 않을 정도로 충분한 순도를 갖는 생성물이 제공된다.
본 발명의 또 다른 실시태양에서는, (i) 화학식 IVa의 화합물을 할로겐화제와 접촉시켜 R1이 수소인 화학식 IVb의 5'-할로 뉴클레오사이드 화합물을 생성시키고; (ii) 화학식 IVb의 화합물을 탈할로겐화수소화제와 접촉시켜, 화학식 Va의 5- 메틸렌 뉴클레오사이드 화합물을 생성시키며; (iii) 화학식 Va의 화합물을 아실화제로 처리하여 화학식 Vb의 화합물을 제공하고, 화학식 Vb의 화합물과 및 수-비혼화성 용매의 용액을 약 7.5 이상의 pH를 갖는 NaHCO3 수용액으로 추출하며; (iv) 아실기를 제거하여 화학식 Va의 화합물을 재생시키고; (v) 화학식 Va의 화합물을 THF 및 MeCN에 용해된 아지드화 4급 암모늄 및 요오드와 접촉시켜, 화학식 IIa의 아이오도 아지드를 생성시키고; (vi) 화학식 IIa의 화합물을 아실화제와 접촉시켜 화학식 IIb의 다이에스터를 제공하고; (vii) 적합한 용매중 화학식 II의 5'-아이오도메틸-2',3'-다이아실 뉴클레오사이드 화합물의 용액을 과카복실산 R2aC(O)OOH, 카복실산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜, 화학식 I의 화합물을 제공하고; (viii) 화학식 I의 화합물을 CH2Cl2중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드 및 TEA와 접촉시켜 화학식 VI의 트라이아졸을 제공하며; (ix) 화학식 VI의 화합물을 극성 비양성자성 용매중 수산화암모늄의 용액과 접촉시켜 트라이아졸을 치환시킴으로써, 화학식 VII의 4'-아지도-2',3',5'-트라이아실시티딘을 제공하고; (x) 화학식 VII의 화합물을 암모니아와 알콜의 용액과 접촉시켜 에스터를 절단함으로써 화학식 VIII의 화합물을 제공함을 포함하는, 화학식 (IVa)의 뉴클레오사이드로부터 R1, R2 및 R3이 상기 정의된 바와 같은 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 제조하는 방법(반응식 2)을 제공한다.
본 발명의 다른 실시태양에서는, 반응식 2 및 3에 기재되어 있는 바와 같이 화학식 VIII의 화합물을 제조함을 포함하고, 화학식 VIII의 화합물을 결정화시키는데 사용되는 아이소프로판올/물 혼합물에 황산을 첨가하는 단계를 추가로 포함하는, 화학식 VIIIa의 4'-아지도시티딘의 헤미설페이트 산부가염을 제조하는 방법을 제공한다.
칼럼 크로마토그래피에 의한 정제는 통상적인 실험실 기법이지만, 대규모 공정에서는 비싸고 손이 많이 간다. 또한, 크로마토그래피는 비싸고 폐기 또는 재순환되어야 하는 용매를 다량 생성시킨다. 따라서, 크로마토그래피를 없애는 변형법이 유리하다. 앞 실시태양의 단계 (iii) 및 (iv)는 화학식 Va의 5-메틸렌 뉴클레오사이드 중간체를 추가로 정제해야 할 필요가 있을 때 임의적으로 공정 내로 혼입되어 염기 수용액 세척을 부가할 수 있다. 뿐만 아니라, 탈요오드화수소화, 아실화, 세척 및 탈아실화를 단일 용기에서 수행할 수 있다.
본 발명의 다른 실시태양에서는 (i) 화학식 IVa의 뉴클레오사이드를 TPP, 요오드 및 이미다졸과 접촉시켜 화학식 IVb의 5'-아이오도 뉴클레오사이드 화합물(X=I)을 생성시키는 단계; (ii) 화학식 IVb의 화합물(X=I)을 DBN 또는 메톡시화나트륨과 접촉시켜 화학식 Va의 5-메틸렌 뉴클레오사이드 화합물을 생성시키는 단계; (iii) 화학식 Va의 화합물을 THF 및 MeCN에 용해된 벤질 트라이에틸암모늄 아지드 및 요오드와 접촉시켜 화학식 IIa의 아이오도 아지드를 생성시키는 단계; (iv) 화학식 IIa의 화합물을 벤조일 클로라이드와 접촉시켜 화학식 IIb의 다이에스터(R1=PhCO)를 제공하는 단계; (v) 수성 완충액 및 비극성 유기 용매중 화학식 IIb의 5'-아이오도메틸-2',3'-다이아실 뉴클레오사이드 화합물(R1=PhCO)의 용액을 과카복실산 R2aC(O)OOH, 카복실산 R2aC(O)OH 및 상전이촉매와 접촉시켜, 화학식 Ib의 화합물(R1a는 Ph이고, R2a는 임의적으로 치환되는 Ph임)을 제공하는 단계; (vi) 화학식 Ib의 화합물(R1a는 Ph이고, R2a는 임의적으로 치환되는 Ph이며, R3은 수소임)을 CH2Cl2중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드 및 TEA와 접촉시켜, 화학식 VI의 트라이아졸(R1a는 Ph이고, R2a는 임의적으로 치환되는 Ph이며, R3은 수소임)을 제공하는 단계; (vii) 화학식 VI의 화합물(R1a는 Ph이고, R2a는 임의적으로 치환되는 Ph이고, R3은 수소임)을 수산화암모늄 및 아세토나이트릴의 용액과 접촉시켜 트라이아졸을 치환시키고 화학식 VII의 4'-아지도-2',3',5'-트라이아실시티딘(R1a는 Ph이고, R2a는 임의적으로 치환되는 Ph이며, R3은 수소임)을 제공하는 단계; (viii) 화학식 VII의 화합물(R1a는 Ph이고, R2a는 임의적으로 치환되는 Ph이고, R3은 수소임)을 수산화암모늄과 알콜의 용액과 접촉시켜 에스터를 절단함으로써 화학식 VIIIb의 화합물을 제공하고, 이를 아이소프로판올/물/황산으로부터 결정화시켜 화학식 VIIIc의 헤미설페이트 염을 제공하는 단계를 포함하는, R3이 수소인 화학식 VIIIa의 4'-아지도-시티딘을 제조하는 방법(반응식 2 및 3)을 제공한다.
모팻(상기 문헌)은 5'-메틸렌 N-벤조일 시티딘(X)으로의 아지드화요오드의 부가를 개시하였다. 최근, 뉴클레오사이드 염기가 1H-피리미딘-2,4-다이온인 경우 전체 공정이 더욱 효과적인 것으로 밝혀졌다. 본 실시태양은 뉴클레오사이드에 연결된 염기를 상호-전환시킴으로써 우리딘 및 시티딘 뉴클레오사이드를 생성시킬 수 있다. 본 발명에 따른 방법에서는 우리딘 또는 티민을 시티딘으로 전환시키는 방법을 제공한다. 트라이아졸의 첨가에 의해 티민을 우리딘으로 전환시키는 것은 맥(상기 문헌), 보쓰윅(상기 문헌) 및 디바카와 리즈(상기 문헌)에 의해 기재된 바 있다. 연속해서 극성 비양성자성 용매중에서 화학식 VI의 화합물(R1은 R1aCO이고, R2는 R2aCO이고, R3은 수소임)을 수소화암모늄과 반응시켜 화학식 VII의 시티딘을 생성시키고, 화학식 VII의 트라이에스터를 약 45℃에서 암모니아 및 메탄올과 반응시켜 벤조일 에스터를 절단함으로써 메틸 벤조에이트 및 벤즈아마이드와 함께 화학식 VIII의 화합물을 제공함으로써, 암모니아를 사용한 트라이아졸의 치환 및 트라이에스터의 절단을 가장 우수하게 선택적으로 달성하였다.
본 발명의 다른 실시태양에서는, (i) 화학식 IVg의 뉴클레오사이드를 TPP, 요오드 및 이미다졸과 접촉시켜 화학식 IVh의 5'-아이오도 뉴클레오사이드 화합물을 생성시키는 단계; (ii) 화학식 IVh의 화합물을 메톡시화나트륨의 메탄올 용액과 접촉시켜 화학식 Vc의 5-메틸렌 뉴클레오사이드 화합물을 생성시키는 단계; (iii) 화학식 Vc의 화합물을 THF 및 MeCN에 용해된 벤질 트라이에틸암모늄 아지드 및 요오드와 접촉시켜 화학식 IIe의 아이오도 아지드를 생성시키는 단계; (iv) 화학식 IIe의 화합물을 벤조일 클로라이드와 접촉시켜 화학식 IIg의 다이에스터를 제공하는 단계; (v) 화학식 IIg의 5'-아이오도메틸-2',3'-다이아실 뉴클레오사이드 화합물을 DCM과 인산수소칼륨 수용액(MCPBA에 대해 K2HPO4 2몰당량)으로 이루어진 2상 매질중 MCPBA, MCBA, 테트라뷰틸암모늄 헤미설페이트와 접촉시켜 화학식 IIId의 화합물을 제공하는 단계; (vi) 화학식 IIId의 화합물을 CH2Cl2중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드 및 TEA와 접촉시켜 화학식 IIIe의 트라이아졸을 제공하는 단계; (vii) 화학식 IIIe의 화합물을 비양성자성 극성 용매중 수산화암모늄의 용액과 접촉시켜 트라이아졸을 치환시키고 화학식 VII의 4'-아지도-2',3',5'-트라이아실시티딘(R1a는 Ph이고, R2a는 3-Cl-Ph이고, R3은 수소임)을 제공하는 단계; (viii) 화학식 VII의 화합물(R1a는 Ph이고, R2a는 3-Cl-Ph이며, R3은 수소임)을 암모니아와 메탄올의 용액과 접촉시켜 에스터를 절단함으로써 화학식 VIIIb의 화합물을 생성시키고, MeOH를 제거한 후 이를 아이소프로판올/물/황산으로부터 결정화시켜 화학식 VIIIc의 헤미설페이트 염을 제공하는 단계를 포함하는, 화학식 VIIIc의 4'-아지도-시티딘의 헤미설페이트 염(R1은 PhCO이고, X는 m-클로로-벤조일옥시이고, R2는 m-클로로벤조일이며, R2a는 m-클로로페닐이고, R3은 수소임)을 제조하는 방법(반응식 2 및 3)을 제공한다.
본 발명의 다른 실시태양에서는, 화학식 VIIIc의 화합물을 제조하는데 유용한 중간체인 하기 화학식 Ic의 신규 화합물이 제공된다:
화학식 Ic
상기 식에서, R은 할로겐, C1 -10 알킬, C1 -10 알콕시, 나이트로, 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 페닐이다.
달리 언급되지 않는 한, 상세한 설명 및 청구의 범위를 비롯한 본원에 사용되는 하기 용어는 아래 기재된 정의를 갖는다. 본원에 사용되는 단수형은 하나 이상을 일컫는데, 예를 들어 화합물은 하나 이상 또는 적어도 하나의 화합물을 말한다. 이러한 단수형 표현, "하나 이상" 및 "적어도 하나"는 본원에서 호환성있게 사용될 수 있다.
일반적으로, 본원에 사용되는 분류상의 명칭은 IUPAC 분류상의 명칭을 만들기 위한 바일스타인 인스티튜트(Beilstein Institute) 전산화 시스템인 오토놈(AUTONOM™ v. 4.0)에 기초한다.
"상기 정의된 바와 같은"이란 구는 발명의 상세한 설명에 제공된 첫번째 정의를 일컫는다.
본원에 사용되는 용어 "알킬"은 1 내지 10개의 탄소 원자를 함유하는 비-분지쇄 또는 분지쇄 포화 1가 탄화수소 잔기를 일컫는다. 본원에 사용되는 "C1 -10 알 킬"은 1 내지 10개의 탄소로 구성된 알킬을 말한다. 알킬기의 예는 메틸, 에틸, 프로필, i-프로필, n-뷰틸, i-뷰틸, t-뷰틸(이상 저급 알킬기), 또는 펜틸, 아이소펜틸, 네오펜틸, 헥실, 헵틸 및 옥틸을 포함하지만, 이들로 한정되지는 않는다.
본원에 사용되는 "알콕시기"라는 용어는 알킬이 상기 정의된 바와 같은 -O-알킬기, 예컨대 메톡시, 에톡시, n-프로필옥시, i-프로필옥시, n-뷰틸옥시, i-뷰틸옥시, t-뷰틸옥시, 펜틸옥시, 헥실옥시(이들의 이성질체 포함)를 의미한다. 본원에 사용되는 "C1 -10 알콕시"는 알킬이 C1 -10 알킬인 -O-알킬을 말한다.
본원에 사용되는 용어 "아실"은 R이 수소, 본원에 정의된 바와 같은 알킬 또는 페닐인 화학식 -C(=O)R의 기를 나타낸다. 본원에 사용되는 용어 "알킬카본일"은 R이 본원에 정의된 바와 같은 알킬인 화학식 C(=O)R의 기를 말한다. 본원에 사용되는 용어 "아릴카본일"은 R이 아릴기인 화학식 C(=O)R의 기를 의미하고; 본원에 사용되는 용어 "벤조일"은 R이 페닐인 "아릴카본일기"를 의미한다.
본원에 사용되는 용어 "아실화제"는 상기 정의된 바와 같은 아실기를 분자 내로 도입할 수 있는 화합물을 말한다. 통상 하이드록실, 아민 또는 황 치환기와 반응하는 아실화제는 카복실산 무수물 또는 아실 할라이드이다. 본원에 사용되는 용어 "무수물"은 R이 앞 단락에 정의된 바와 같은 일반식 RC(O)-O-C(O)R의 화합물을 일컫는다. 본원에 사용되는 용어 "아실 할라이드"는 X가 브로모 또는 클로로인 기 RC(O)X를 일컫는다. 당해 분야의 숙련자는 카복실산의 다른 "활성화된 유도체"가 당해 분야에 공지되어 있고 이들도 사용할 수 있음을 알 것이다. 본원에 사용 되는 화합물의 "활성화된 유도체"란 용어는 어느 정도로만 반응성이거나 비-반응성인 원래 화합물을 목적하는 화학 반응에 반응성이 되도록 하는, 원래 화합물의 일시적인 반응성 형태를 일컫는다.
본원에 사용되는 용어 "아릴알킬" 또는 "아르알킬"은 라디칼 R'R"-을 말하며, 이 때 R'은 아릴 라디칼이고 R"은 알킬렌 라디칼이며, 아릴알킬 잔기의 부착 지점은 알킬렌 라디칼에 있다. 본원에 사용되는 용어 "알킬렌"은 1 내지 6개의 탄소를 갖는 2가 선형 또는 분지된 포화 탄화수소 라디칼을 지칭한다. 본원에 사용되는 용어 아릴은 페닐, 1-나프틸 또는 2-나프틸 잔기를 말한다. 알킬렌 라디칼의 예는 메틸렌, 에틸렌, 프로필렌, 2-메틸-프로필렌, 뷰틸렌, 2-에틸뷰틸렌을 포함하지만 이들로 한정되지는 않는다. 아릴알킬 라디칼의 예는 벤질, 페닐에틸 및 3-페닐프로필을 포함하지만 이들로 한정되는 것은 아니다.
본원에 사용되는 용어 "할로알킬"은 1, 2, 3개 이상의 수소 원자가 할로겐으로 치환된 상기 정의된 바와 같은 비-분지쇄 또는 분지쇄 알킬기를 말한다. 예로는 1-플루오로메틸, 1-클로로메틸, 1-브로모메틸, 1-아이오도메틸, 트라이플루오로메틸, 트라이클로로메틸, 트라이브로모메틸, 트라이아이오도메틸, 1-플루오로에틸, 1-클로로에틸, 1-브로모에틸, 1-아이오도에틸, 2-플루오로에틸, 2-클로로에틸, 2-브로모에틸, 2-아이오도에틸, 2,2-다이클로로에틸, 3-브로모프로필 또는 2,2,2-트라이플루오로에틸이 있다.
본원에 사용되는 용어 "할로겐" 또는 "할로"는 플루오르, 염소, 브롬 또는 요오드를 말한다.
본원에 사용되는 용어 "상전이촉매"는 음이온 또는 중성 화합물이 유기 상에 이미 위치된 유기 반응물과 자유롭게 반응할 수 있는, 유기 상과의 계면을 가로지르는 수용성 반응물의 전달 속도를 변화시키는 촉매를 말한다. 통상적으로 사용되는 상전이 촉매는 4급 암모늄 염, 포스포늄 염 및 크라운 에터 또는 폴리에틸렌 글라이콜이다. 적합한 촉매는 예를 들어 테트라뷰틸암모늄 클로라이드, 테트라뷰틸암모늅 브로마이드, 테트라뷰틸포스포늄 클로라이드, 벤질 트라이에틸암모늄 클로라이드 및 N-2-에틸헥실-4-다이메틸아미노 피리디늄 브로마이드이다. 용어 "아지드화 4급 암모늄"은 R1 내지 R4가 독립적으로 알킬 또는 아르알킬인 화합물 R1R2R3R4N+N3 -를 일컫는다.
본원에 사용되는 구 "극성 비양성자성 용매"는 뉴클레오사이드 유도체를 용해시키기에 충분히 극성이지만 교환가능한 양성자는 갖지 않는 극성 용매, 예를 들어 아세토나이트릴, DMF, 다이옥세인, 테트라하이드로퓨란 등을 말한다.
본원에 사용되는 "비극성 유기 용매"란 구는 리그로인, 펜테인, 헥세인, 사이클로헥세인, 헵테인, 옥테인, 벤젠, 톨루엔, 다이에틸 에터, 다이옥세인, 테트라하이드로퓨란, 다이클로로메테인, 사염화탄소 등과 같은 유기 용매를 의미한다.
본원에 사용되는 용어 "할로겐화제"는 알콜을 알킬 할라이드로 전환시킬 수 있는 시약을 일컫는다. 본원에 사용되는 용어 "탈할로겐화수소화제"는 할로알케인으로부터 할로겐화수소산 HX를 제거하여 알켄을 제공할 수 있는 화합물을 말한다.
본원에 사용되는 용어 "아이오도 아지드"는 아이오다이드 및 아지드에 의해 치환된 2개의 인접한 탄소 원자, 즉 I-CH2C(N3)=를 말한다.
용어 "제 1 염기"는 에스터와 반응하여 상응하는 알콜 및 카복실산을 제공할 수 있는 염기를 일컫는다. 적합한 제 1 염기는 암모니아, 1급 및 2급 아민, NaHCO3, Na2CO3, KOH 및 NaOMe 등을 포함한다. 용어 "제 2 염기"는 촉매로서 아실화 반응에 사용되는 염기 및 변환동안 방출되는 산을 제거하는 시약을 일컫는다. 전형적인 제 2 염기는 TEA, 피리딘, DMAP, NMM, DABCO 등을 포함한다.
본원에 사용되는 용어 "뉴클레오사이드"는 C-1에서의 배당체 결합에 의해 펜토즈 당에 연결된 질소성 헤테로환상 염기를 일컫는다. 천연 발생 염기는 우라실, 티민, 시토신, 아데닌 및 구아닌을 포함하고, 천연 발생 당은 리보즈 및 2-데옥시리보즈이다. 용어 뉴클레오사이드는 당 및/또는 질소성 염기가 화학적으로 개질된 화합물을 추가로 포함한다.
화학 반응을 일컬을 때 본원에서 사용되는 용어 "처리", "접촉" 또는 "반응"은 적절한 조건하에서 둘 이상의 시약을 첨가 또는 혼합하여 표시되고/되거나 목적하는 생성물을 생성시킴을 의미한다. 표시되고/되거나 목적하는 생성물을 생성시키는 반응이 반드시 최초로 첨가된 두 시약의 조합으로부터 직접 결과되어야 하는 것은 아닐 수 있음을 알아야 한다. 즉, 궁극적으로는 표시되고/되거나 목적하는 생성물을 생성시키는 혼합물중에 생성된 하나 이상의 중간체가 있을 수 있다.
약어
BTEAA: 벤질 트라이에틸암모늄 아지드
DABCO: 1,4-다이아자바이사이클로[2.2.2]옥테인
DBN: 1,8-다이아자바이사이클로[4.3.0]논-5-엔
DCM: 다이클로로메테인
DMF: N,N-다이메틸폼아마이드
DMAP: 4-다이메틸아미노피리딘
Gc: 기체 크로마토그래피
HMPA: 헥사메틸포스포라마이드
Hplc: 고성능 액체 크로마토그래피
MCPBA: m-클로로퍼벤조산
MCBA: m-클로로벤조산
MeCN: 아세토나이트릴
NMM: N-메틸모폴린
Ph: 페닐
TEA: 트라이에틸아민
THF: 테트라하이드로퓨란
TPP: 트라이페닐포스핀
4'-아지도뉴클레오사이드 유도체를 생성시키는 특이적인 방법이 아래에 기재되지만, 당해 분야의 숙련자는 다수의 변형 및 다른 공정 단계를 쉽게 알 것이다. 따라서, 이들 기재내용 및 이들 실시예는 예시하기 위한 것으로 간주되어야 하며, 당해 분야의 숙련자에게 4'-아지도뉴클레오사이드 유도체를 제조하는 신규 방법을 교시하기 위한 것이다. 이들 방법은 본 발명의 원리를 벗어나지 않으면서 실질적으로 변화될 수 있고, 첨부된 청구의 범위의 영역에 속하는 모든 변형의 독점적인 사용이 가능하다.
실시예 1
1-((2R,3R,4S,5S)-3,4-
다이하이드록시
-5-
아이오도메틸
-
테트라하이드로
-
퓨란
-2-일)-1H-피리미딘-2,4-다이온(
IVh
)
우리딘(IVg; 30.0kg), TPP(46.8kg) 및 이미다졸(12.2kg)을 THF(267kg)에 슬러리화시켰다. 반응 온도를 28℃ 미만으로 유지시키면서 THF(87kg)중 요오드(33.2kg)의 용액을 슬러리에 서서히 첨가하였다. 반응 혼합물을 약 25℃에서 하룻밤동안(약 18시간) 교반하여 완전히 전환시켰다. 반응 혼합물을 소량(2.3L)의 물로 급랭시켰다. 증류물의 IPA 함량(gc에 의해)이 87%(v/v)보다 클 때까지 아이소프로판올(최대 내부 온도: 50℃)을 첨가하면서 반응 혼합물을 온화한 진공하에 증류시켰다. 생성된 슬러리를 실온(약 22℃)으로 냉각시키고 하룻밤동안 숙성시켰다. 침전된 생성물을 여과하고 아이소프로판올(2×50kg)로 세척한 다음 진공하에 약 50℃에서 느린 질소 스트림으로 건조시켜, 화학식 IVh의 화합물(36.5kg; 이론치의 83.9%)을 수득하였다.
실시예 2
1-((2R,3R,4S)-3,4-
다이하이드록시
-5-메틸렌-
테트라하이드로
-
퓨란
-2-일)-1H-피리미딘-2,4-다이온(
Vc
)
MeOH(20kg)중 화학식 IVh의 화합물(4.0kg)의 현탁액을 25% 메톡시화나트륨 용액(6.1kg)으로 처리하여 투명한 용액을 수득하고, 이를 약 60℃에서 약 2시간동안 유지시켰다. 진공 증류를 통해 메탄올을 제거하고, 메탄올 함량(gc에 의해)이 약 0.5% v/v로 떨어질 때까지 MeCN으로 대체하였다. 생성된 슬러리의 부피를 아세토나이트릴로 약 30L로 조정한 다음 아세트산 무수물 3.5kg으로 처리하고 약 60℃에서 약 5시간동안 가열하였다. 반응 혼합물을 진공에서 농축시켜 약 18L로 만들고 에틸 아세테이트로 희석시켰다. 반응 혼합물을 약 20℃로 냉각시키고, 용액의 pH가 약 7.5가 될 때까지 포화 NaHCO3를 서서히 첨가함으로써 과량의 Ac2O를 급랭시켰다. 상을 분리하고 유기 상을 물 및 염수로 세척하였다. 유기 상을 진공에서 농축시키고 MeOH(19kg)로 희석시킨 후 진한 NH4OH 1.08kg으로 처리하였다. 반응 혼합물을 약 20℃에서 하룻밤동안(약 18시간) 정치시켜 탈아세틸화를 종결시켰다. 반응 혼합물을 진공에서 농축시키고(내부 온도 <40℃) 잔류물을 아이소프로판올과 아세토나이트릴의 혼합물로 희석시켰다. 치환 증류 후 용매의 최종 조성은 전형적으로 아세토나이트릴 65%, IPA 30%, 메탄올 5%였다. 침전된 화학식 Vc의 올레핀 및 생성된 슬러리를 약 15℃로 냉각시키고 여과한 다음, 차가운 아세토나이트릴로 세척하고 20 내지 25℃의 진공하에 건조시켜, 화학식 Vc의 화합물(1.92kg; 이론치의 75.1%)을 수득하였다.
실시예 3
벤조산 (2S,3S,4R,5R)-4-
벤조일옥시
-2-
아지도
-5-(2,4-
다이옥소
-3,4-다이하이드로-2H-피리미딘-1-일)-2-아이오도메틸-테트라하이드로-퓨란-3-일 에스터(
IIg
)
MeOH(68kg)중 화학식 IVh의 화합물(12.0kg)의 현탁액을 25% 메톡시화나트륨 용액(18.4kg)으로 처리하여 투명한 용액을 수득하고, 이를 약 60℃에서 2시간동안 정치시켜 완전히 전환시켰다. 반응 혼합물을 메탄올중 N-메틸모폴리늄 메실레이트의 용액(MeOH 19kg중 메테인설폰산 8.1kg의 용액에 NMM 8.9kg을 첨가함으로써 동일 반응계 내에서 제조함)에 첨가하였다. 반응 혼합물을 진공에서 농축시키고(내부 온도 <40℃), 증발된 MeOH를 잔류 메탄올 수준이 약 1 내지 2%(gc에 의해)로 될 때 까지 THF(배치 부피 약 50L)로 대체하였다. 화학식 Vc의 조질 화합물의 생성된 슬러리를 아세토나이트릴(20kg)로 희석시키고 NMM(1.2kg)으로 약간 염기성으로 만들었다. 벤질 트라이에틸암모늄 클로라이드(10.0kg) 및 아지드화나트륨(2.87kg)을 아세토나이트릴(45kg)에 함께 슬러리화시켜, 아지드를 아지드화 4급 암모늄으로서 아세토나이트릴 중으로 추출시켰다. 슬러리를 여과하고 4급 아지드 용액을 화학식 Vc의 조질 화합물의 슬러리에 첨가하였다. 배치 온도를 0 내지 5℃로 유지시키면서 THF(40kg)중 요오드(11.2kg)의 용액을 생성된 슬러리에 서서히 첨가하였다. 다 첨가한 후, 반응 혼합물을 5 내지 10℃에서 18 내지 24시간동안 정치시켜 완전히 전환시켰다. 생성된 혼합물에 TEA(17.2kg) 및 DMAP(0.41kg)를 첨가하고, 혼합물을 약 -10℃로 냉각시킨 다음, 내부 온도를 -5℃ 미만으로 유지시키면서 벤조일 클로라이드(14.3kg)로 처리하였다. 다 첨가한 후, 벤조일화가 종결될 때까지 반응 혼합물을 약 -5℃에서 정치시켰다. 반응 혼합물을 물 및 황산나트륨(잔류 요오드를 분해시키기 위해) 수용액으로 급랭시키고 EtOAc(44kg)로 처리하였다. 유기 상을 물로 세척하고, 물을 EtOAc(44kg)으로 다시 추출한 다음, 모아진 유기 추출물을 감압하에 농축시키고(최대 재킷 온도: 65℃) 증발된 용매를 아이소프로판올로 대체한 결과, 화학식 IIg의 화합물이 결정화되었다. 생성된 슬러리를 약 20℃로 냉각시키고 2시간 이상동안 정치시켰다. 침전된 생성물을 여과에 의해 단리하고 아이소프로판올로 세척한 다음, 질소 스트림 중에서 진공하에 25 내지 50℃에서 건조시켜 화학식 IIg의 화합물(15.9kg; 총 수율 이론치의 77.6%)을 수득하였다.
실시예 4
벤조산 (2S,3S,4R,5R)-4-
벤조일옥시
-2-
아지도
-5-(2,4-
다이옥소
-3,4-다이하이드로-2H-피리미딘-1-일)-2-아이오도메틸-테트라하이드로-퓨란-3-일 에스터(
IIg
)
단계 1
벤질 트라이에틸암모늄 클로라이드(2.0kg) 및 아지드화나트륨(0.69kg)의 혼합물을 함께 MeCN(12kg)에 슬러리화시켰다. 불용성 염화나트륨을 여과에 의해 제거하고 여액을 MeCN으로 세척하였다. 화학식 Vc의 화합물(1.9kg), 4-NMM(0.26kg) 및 THF(7.6L)의 균질한 혼합물에 벤질 트라이에틸암모늄 아지드의 MeCN 용액을 첨가하여 투명한 용액을 생성시켰다. 내부 온도를 0 내지 5℃로 유지하면서 THF(10L)중 요오드(2.45kg)의 용액을 서서히 첨가하였다. 다 첨가한 후, 반응 혼합물을 5 내지 10℃에서 약 2시간동안 숙성시켰다. 진행시키기 전에 소량의 N-아세틸 시스테인(40g)을 첨가함으로써 과량의 아지드를 분해시켰다.
단계 2
이전 단계로부터의 조질 반응 혼합물을 NMM(4.3kg) 및 DMAP(100g)로 처리하고 약 0℃로 냉각시킨 다음, 내부 온도를 약 5℃로 유지하면서 벤조일 클로라이드 (2.6kg)를 첨가하였다. 다 첨가한 후, 반응 혼합물을 약 5℃에서 약 30분간 교반하였다. 물을 조심스럽게 첨가하여 과량의 벤조일 클로라이드를 분해시키고, 황산나트륨을 첨가하여 잔류 요오드를 분해시키며, EtOAc를 첨가하여 목적하는 생성물을 추출하였다. EtOAc 용액을 물로 세척하고 진공에서 농축시켰다. 이렇게 제거된 EtOAc를 아이소프로판올로 대체하여(최대 재킷 온도: 65℃) 목적하는 생성물을 결정화시켰다. 생성된 슬러리를 약 22℃로 냉각시키고 하룻밤동안 정치시켰다. 침전물을 여과하고 아이소프로판올로 세척한 다음, 질소 스트림 하에 진공 및 실온에서 건조시켜 화학식 IIg의 화합물(3.80kg; 이론치의 74.2%)을 수득하였다.
실시예 5
3-
클로로
-벤조산 (2R,3S,4R,5R)-2-
아지도
-3,4-
비스
-
벤조일옥시
-5-(2,4-다이옥소-3,4-다이하이드로-2H-피리미딘-1-일)-테트라하이드로-퓨란-2-일메틸 에스터(
IIId
)
화학식 IIg의 화합물(14.2kg), 테트라뷰틸 암모늄 하이드로젠 설페이트(8.5kg), 인산수소나트륨(8.5kg), m-클로로벤조산(4.0kg), DCM(70kg) 및 물(28kg)의 혼합물을 DCM(70kg)중 m-클로로퍼벤조산(22.4kg)의 슬러리에 넣었다. 반응이 종결될 때까지(HPLC에 의해) 혼합물을 실온에서 교반하였다. 반응물을 급랭시키기 위하여, 온도를 25℃ 미만으로 유지시키면서 반응 혼합물을 물(70kg)중 황산나트륨(19kg)의 용액에 첨가하였다. 단시간동안 교반한 다음, 물(51kg)중 탄산칼륨(28kg)의 용액을 첨가하였다. 하부 유기 층을 분리하고 대기압에서 농축시켰다. DCM을 아이소프로판올로 대체하였다. 생성된 용액(부피 40 내지 50L)을 온수(70L)로 처리함으로써, 목적하는 생성물을 침전시켰다. 생성된 슬러리를 2시간동안 약 65℃까지 가온한 다음 실온으로 냉각시켰다. 침전된 생성물을 여과에 의해 단리하고 아이소프로판올과 물의 혼합물로 세척한 후, 진공하에 약 50℃에서 건조시켜 화학식 IIId의 화합물(10.6kg; 이론치의 71.3%)을 수득하였다.
실시예 6
3-
클로로
-벤조산 (2R,3S,4R,5R)-2-
아지도
-3,4-
비스
-
벤조일옥시
-5-(2-옥소-4-[1,2,4]
트라이아졸
-1-일-3,4-
다이하이드로
-2H-피리미딘-1-일)-
테트라하이드
로-퓨란-2-일메틸 에스터(
IIIe
)
반응 온도를 25℃ 미만으로 유지시키면서 화학식 IIId의 화합물(34.1kg), 1,2,4-트라이아졸(42.1kg), TEA(63.1kg) 및 DCM(270kg)의 냉각된 혼합물에 포스포러스 옥시클로라이드(21.5kg)를 첨가하였다. 반응 혼합물을 실온에서 교반하고 반 응의 진행을 hplc에 의해 모니터링하였다. 반응이 종결되면, 반응 온도를 30℃ 미만으로 유지하면서 냉수(280kg)를 조심스럽게 첨가하여 과량의 POCl3를 급랭시켰다. 하부 유기 층을 분리하고 대기압에서 증류시켜 농축시켰다. DCM이 증류됨에 따라, 이를 MeCN으로 대체하여 부피를 거의 일정하게 유지하였다. 생성된 슬러리(약 70L)를 물(70L)로 희석시킨 결과, 화학식 IIIe의 화합물이 침전되었다. 생성된 슬러리를 약 15℃에서 16시간 이하동안 교반하였다. 침전물을 여과에 의해 단리하고 아세토나이트릴과 물의 혼합물로 세척한 다음, 약 50℃에서 진공하에 건조시켜 화학식 IIIe의 화합물(32.7kg; 이론치의 88.8%)을 수득하였다.
실시예 7
1-((2R,3R,4S,5R)-5-
아지도
-3,4-
다이하이드록시
-5-
하이드록시메틸
-
테트라하이드로
-퓨란-2-일)-2-옥소-1,2-다이하이드로-피리미딘-4-일-암모늄; 황산수소(
VIIIc
)
화학식 IIIe의 트라이아졸(32.2kg)을 THF(152kg)에 현탁시키고 진한 수산화암모늄 수용액(15kg)으로 처리하였다. 가암모니아분해 반응이 종결된 후, 반응 혼합물을 진공에서 농축시키고, 메탄올을 첨가하여 부피를 약 180L로 만들었다. 생성된 용액에 진한 수산화암모늄 수용액(15kg)을 첨가하여 보호성 에스터 작용기를 절단하였다. 목적하는 반응을 종결시킨 후, 용액을 여과하고 진공에서 농축시킨 다음, 반응 혼합물을 아이소프로판올로 약 80L까지 희석시켰다. 생성된 용액을 아이소프로판올(64kg) 및 물(습윤시키기 위해)(82kg)로 희석시켜 투명한 용액을 생성시켰다. 용액을 약 70℃까지 가온시키면서 용액을 묽은 황산 수용액-아이소프로판올 혼합물(진한 황산 2.4kg을 물 10kg과 혼합한 후 아이소프로판올 68kg을 첨가함으로써 제조함)로 처리하였다. 생성된 슬러리를 약 70℃에서 0.5시간동안 숙성시킨 다음 2시간동안에 걸쳐 주위온도로 냉각시켰다. 침전된 생성물을 여과에 의해 단리하고 아이소프로판올로 세척한 후 50℃ 및 진공에서 질소 스트림으로 건조시켜, 화학식 VIIIa의 화합물(15.3kg; 이론치의 95.8%)을 수득하였다.
청구범위 8항에 기재된 단계는 본 발명자들에게 알려져 있는 방법을 수행하는 최선의 방식을 나타낸다. 이들은 각각 실시예 1, 3, 5 내지 7에 기재되어 있다. 이들 단계는 본 발명을 실행하기 위한 가장 편리하고 경제적인 방식을 제공한다.
구체적인 형태 또는 개시된 기능을 수행하기 위한 수단, 또는 적절한 경우 개시된 결과를 획득하기 위한 방법 또는 공정으로 표현되는, 상기 상세한 설명 또는 하기 청구의 범위, 또는 첨부된 도면에 개시되는 특징은, 별도로 또는 이들 특징의 임의의 조합으로, 본 발명을 그의 다양한 형태로 달성하는데 이용될 수 있다.
상기 발명은 명료함과 이해를 위해 예시 및 실시예에 의해 다소 상세하게 기재되었다. 당해 분야의 숙련자는 첨부된 청구의 범위의 영역 내에서 변화 및 변형을 수행할 수 있음을 쉽게 알 것이다. 따라서, 상기 상세한 설명은 예시하기 위한 것이지 제한하기 위한 것이 아님을 알아야 한다. 그러므로, 본 발명의 영역은 상기 상세한 설명을 참조하여 결정되는 대신 하기 첨부된 청구의 범위의 모든 등가 영역과 함께 이들 청구의 범위를 참조하여 결정되어야 한다.
본원에 인용된 모든 특허, 특허원 및 문헌은 각 개별 특허, 특허원 또는 문헌이 그렇게 개별적으로 표시되는 것과 동일한 정도로 본원에 참고로 인용된다.
Claims (10)
- 단계 a)에서 하기 화학식 IVa의 뉴클레오사이드 화합물을 하기 화학식 II의 화합물로 변환시키고,단계 b)에서 적합한 용매중 화학식 II의 5'-아이오도 화합물의 용액을 과산 R2aC(O)OOH, 산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜 하기 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 생성시키며,단계 c)에서 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 변환시켜 화학식 VIII의 4'-아지도-시티딘 화합물 및 필요한 경우 그의 약학적으로 허용가능한 부가염을 제공함을 특징으로 하는,하기 화학식 VIII의 4'-아지도-시티딘 화합물 및 그의 약학적으로 허용가능한 부가염을 제조하는 방법:화학식 VIII화학식 IVa화학식 II화학식 I상기 식에서,R3은 H, C1 -6-알킬, C1 -3-할로알킬 또는 할로겐이고,R1은 R1aCO-이고,R1a는 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1 -10-알킬 또는 페닐이며,R2는 R2aCO-이고,R2a는 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1 -10-알킬 또는 페닐이다.
- 적합한 용매중 화학식 II의 5'-아이오도 화합물의 용액을 과산 R2aC(O)OOH, 산 R2aC(O)OH 및 임의적으로는 상전이촉매와 접촉시켜, 하기 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드 화합물을 생성시킴을 포함하는, 화학식 I의 4'-아지도-2',3',5'-트라이아실-뉴클레오사이드를 제조하는 방법:화학식 I상기 식에서,R1은 R1aCO-이고,R2는 R2aCO-이고,R1a 및 R2a는 독립적으로 알킬, 알콕시, 할로겐, 나이트로 또는 사이아노로 이루어진 군으로부터 선택되는 1 내지 3개의 치환기로 임의적으로 치환되는 C1 -10-알킬 또는 페닐이며,R3은 H, C1 -6-알킬, C1 -3-할로알킬 또는 할로겐이다.
- 제 1 항에 있어서,a) 화학식 IVa의 뉴클레오사이드를 할로겐화제와 접촉시켜, 하기 화학식 IVb의 5'-할로 뉴클레오사이드 화합물을 생성시키는 단계;b) 화학식 IVb의 화합물을 탈할로겐화수소화제와 접촉시켜, 하기 화학식 Va의 5-메틸렌 뉴클레오사이드 화합물을 생성시키는 단계;c) 화학식 Va의 화합물을 테트라하이드로퓨란(THF) 및 아세토나이트릴(MeCN)에 용해된 아지드화 4급 암모늄 및 요오드와 접촉시켜, 하기 화학식 IIa의 아이오도 아지드 화합물을 생성시키는 단계;d) 하기 화학식 IIa의 화합물을 하나 이상의 제 2 염기 및 제 1 아실화제와 접촉시켜, 하기 화학식 II의 다이에스터 화합물을 생성시키는 단계를 포함함을 특징으로 하는,화학식 II의 5'-아이오도 화합물을 제조하는 방법:화학식 IVb화학식 Va화학식 IIa화학식 II상기 식에서, X는 할로겐이고, R1 및 R3은 제 1 항에 정의된 바와 같다.
- 제 1 항에 있어서,a) 하기 화학식 I의 화합물을 CH2Cl2중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드, 트라이에틸아민(TEA)과 접촉시켜, 하기 화학식 VI의 트라이아졸 화합물을 제공하는 단계,b) 화학식 VI의 화합물을 수산화암모늄과 테트라하이드로퓨란(THF)의 용액과 접촉시켜 트라이아졸을 치환시킴으로써, 하기 화학식 VII의 4'-아지도-2',3',5'-트라이아실시티딘 화합물을 제공하는 단계,c) 화학식 VII의 화합물을 암모니아와 알콜의 용액과 접촉시켜 에스터를 절단함으로써, 하기 화학식 VIII의 화합물을 제공하는 단계를 포함함을 특징으로 하는,화학식 VIII의 4'-아지도시티딘 화합물을 제조하는 방법:화학식 I화학식 VI화학식 VII화학식 VIII상기 식에서, R1 및 R2는 제 1 항에 정의된 바와 같고, R3은 수소이다.
- 제 7 항에 있어서,상전이촉매가 테트라알킬 암모늄 하이드로젠 설페이트이고; 용매가 수성 완충액과 비극성 유기 용매의 혼합물이며; 요오드화제가 트라이페닐포스핀(TPP), 요오드 및 이미다졸이고; 탈할로겐화수소화제가 메톡시화나트륨 또는 1,8-다이아자바이사이클로[4.3.0]논-5-엔(DBN)이며; 아지드화 4급 암모늄이 벤질 트라이에틸암모늄 아지드이고; 아실화제가 벤조일 클로라이드이며; 제 1 염기가 암모니아이고; 제 2 염기가 N-메틸모폴린(NMM) 및 4-다이메틸아미노피리딘(DMAP)이고; 상기 알콜이 메탄올인,R3이 수소이고, R1이 PhCO이고, R2가 R2aCO이고, R2a가 임의적으로 치환되는 페닐인 화학식 VIIIa의 4'-아지도-시티딘의 헤미설페이트 산부가염을 제조하는 방법.
- a) 하기 화학식 IVg의 우리딘 화합물의 테트라하이드로퓨란(THF) 용액을 트라이페닐포스핀(TPP), 요오드 및 이미다졸과 접촉시켜, 하기 화학식 IVh의 1-(3,4-다이하이드록시-5-할로메틸-테트라하이드로-퓨란-2-일)-1H-피리미딘-2,4-다이온을 생성시키는 단계;b) 화학식 IVh의 화합물을 메톡시화나트륨의 메탄올 용액과 접촉시켜, 하기 화학식 Vc의 1-(3,4-다이하이드록시-5-메틸렌-테트라하이드로-퓨란-2-일)-1H-피리미딘-2,4-다이온을 생성시키는 단계;c) 화학식 Vc의 화합물을 테트라하이드로퓨란(THF) 및 아세토나이트릴(MeCN)중 벤질 트라이에틸암모늄 아지드 및 요오드의 용액과 접촉시켜 하기 화학식 IIe의 아이 오도 아지드를 제공하는 단계;d) 화학식 IIe의 화합물을 벤조일 클로라이드, N-메틸모폴린(NMM) 및 아세토나이트릴(MeCN)의 용액과 접촉시켜, 하기 화학식 IIg의 다이벤조에이트 화합물을 제공하는 단계;e) 화학식 IIg의 화합물을 다이클로로메테인(DCM)과 인산수소칼륨의 수용액의 2-상 용액중에서 m-클로로퍼벤조산, m-클로로벤조산 및 테트라뷰틸암모늄 하이드로젠 설페이트와 접촉시켜, 하기 화학식 IIId의 화합물을 제공하는 단계;f) 화학식 IIId의 화합물을 다이클로로메테인(DCM)중 1,2,4-트라이아졸, 포스포러스 옥시클로라이드, 트라이에틸아민(TEA)의 용액과 접촉시켜, 하기 화학식 IIIe의 화합물을 제공하는 단계;g) 화학식 IIIe의 화합물을 암모니아의 메탄올 용액과 접촉시켜 에스터를 절단하고 하기 화학식 VIIIb의 화합물의 유리 염기를 제공하는 단계;h) 화학식 VIIIb의 화합물을 아이소프로판올 및 H2SO4 함유 물로부터 결정화시켜, 하기 화학식 VIIIc의 헤미설페이트 염을 제공하는 단계를 포함함을 특징으로 하는,하기 화학식 VIIIc의 4'-아지도시티딘 헤미설페이트를 제조하는 방법:화학식 VIIIc화학식 IVg화학식 IVh화학식 Vc화학식 IIe화학식 IIg화학식 IIId화학식 IIIe화학식 VIIIb
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US47979603P | 2003-06-19 | 2003-06-19 | |
| US60/479,796 | 2003-06-19 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20060026426A true KR20060026426A (ko) | 2006-03-23 |
Family
ID=33551901
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020057024240A Withdrawn KR20060026426A (ko) | 2003-06-19 | 2004-06-11 | 4'-아지도 뉴클레오사이드 유도체의 제조 방법 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US20050038240A1 (ko) |
| EP (1) | EP1644395B1 (ko) |
| JP (1) | JP2006527719A (ko) |
| KR (1) | KR20060026426A (ko) |
| CN (1) | CN1809582A (ko) |
| AT (1) | ATE346078T1 (ko) |
| CA (1) | CA2528294A1 (ko) |
| DE (1) | DE602004003389T2 (ko) |
| DK (1) | DK1644395T3 (ko) |
| ES (1) | ES2276311T3 (ko) |
| IL (1) | IL172275A0 (ko) |
| MX (1) | MXPA05013452A (ko) |
| TW (1) | TW200519122A (ko) |
| WO (1) | WO2005000864A1 (ko) |
Families Citing this family (90)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MY164523A (en) | 2000-05-23 | 2017-12-29 | Univ Degli Studi Cagliari | Methods and compositions for treating hepatitis c virus |
| MXPA02011691A (es) | 2000-05-26 | 2004-05-17 | Idenix Cayman Ltd | Metodos y composiciones para el tratamiento de flavivirus y pestivirus. |
| US7608600B2 (en) | 2002-06-28 | 2009-10-27 | Idenix Pharmaceuticals, Inc. | Modified 2′ and 3′-nucleoside prodrugs for treating Flaviviridae infections |
| CN101172993A (zh) * | 2002-06-28 | 2008-05-07 | 埃迪尼克斯(开曼)有限公司 | 用于治疗黄病毒感染的2′-c-甲基-3′-o-l-缬氨酸酯核糖呋喃基胞苷 |
| JP2005533824A (ja) * | 2002-06-28 | 2005-11-10 | イデニクス(ケイマン)リミテツド | フラビウイルス科感染の治療のための2’−c−メチル−3’−o−l−バリンエステルリボフラノシルシチジン |
| PL377342A1 (pl) * | 2002-11-15 | 2006-01-23 | Idenix (Cayman) Limited | Nukleozydy rozgałęzione w pozycji 2' oraz mutacja Flaviviridae |
| AU2003300901A1 (en) * | 2002-12-12 | 2004-06-30 | Idenix (Cayman) Limited | Process for the production of 2'-branched nucleosides |
| EP1879607B1 (en) * | 2005-05-02 | 2014-11-12 | Merck Sharp & Dohme Corp. | Hcv ns3 protease inhibitors |
| AR057456A1 (es) * | 2005-07-20 | 2007-12-05 | Merck & Co Inc | Inhibidores de la proteasa ns3 del vhc |
| WO2007016441A1 (en) * | 2005-08-01 | 2007-02-08 | Merck & Co., Inc. | Macrocyclic peptides as hcv ns3 protease inhibitors |
| EP1976382B1 (en) * | 2005-12-23 | 2013-04-24 | IDENIX Pharmaceuticals, Inc. | Process for preparing a synthetic intermediate for preparation of branched nucleosides |
| GB0609492D0 (en) * | 2006-05-15 | 2006-06-21 | Angeletti P Ist Richerche Bio | Therapeutic agents |
| GB0612423D0 (en) * | 2006-06-23 | 2006-08-02 | Angeletti P Ist Richerche Bio | Therapeutic agents |
| ATE493428T1 (de) | 2006-10-10 | 2011-01-15 | Medivir Ab | Hcv-nukleosidinhibitor |
| JP2010507656A (ja) * | 2006-10-24 | 2010-03-11 | メルク エンド カムパニー インコーポレーテッド | Hcvns3プロテアーゼ阻害剤 |
| WO2008051475A2 (en) * | 2006-10-24 | 2008-05-02 | Merck & Co., Inc. | Hcv ns3 protease inhibitors |
| CA2667266C (en) * | 2006-10-24 | 2015-11-24 | Merck & Co., Inc. | Hcv ns3 protease inhibitors |
| EP2083844B1 (en) * | 2006-10-27 | 2013-11-27 | Merck Sharp & Dohme Corp. | Hcv ns3 protease inhibitors |
| CA2667031C (en) | 2006-10-27 | 2013-01-22 | Merck & Co., Inc. | Hcv ns3 protease inhibitors |
| EP2102221B1 (en) * | 2006-12-11 | 2010-08-18 | F. Hoffmann-La Roche AG | Process for preparation of 4'-azido cytidine derivatives |
| GB0625349D0 (en) * | 2006-12-20 | 2007-01-31 | Angeletti P Ist Richerche Bio | Therapeutic compounds |
| GB0625345D0 (en) * | 2006-12-20 | 2007-01-31 | Angeletti P Ist Richerche Bio | Therapeutic compounds |
| CN103224506A (zh) * | 2006-12-20 | 2013-07-31 | P.安杰莱蒂分子生物学研究所 | 抗病毒的吲哚 |
| US7951789B2 (en) | 2006-12-28 | 2011-05-31 | Idenix Pharmaceuticals, Inc. | Compounds and pharmaceutical compositions for the treatment of viral infections |
| WO2008106167A1 (en) * | 2007-02-28 | 2008-09-04 | Conatus Pharmaceuticals, Inc. | Combination therapy comprising matrix metalloproteinase inhibitors and caspase inhibitors for the treatment of liver diseases |
| HRP20110713T1 (hr) * | 2007-02-28 | 2011-11-30 | Conatus Pharmaceuticals | Postupci liječenja kroničnog virusnog hepatitisa c uz upotrebu ro 113-0830 |
| JP2010533698A (ja) * | 2007-07-17 | 2010-10-28 | イステイチユート・デイ・リチエルケ・デイ・ビオロジア・モレコラーレ・ピ・アンジエレツテイ・エツセ・ピー・アー | C型肝炎感染症の治療のための大環状インドール誘導体 |
| JP5433573B2 (ja) * | 2007-07-19 | 2014-03-05 | イステイチユート・デイ・リチエルケ・デイ・ビオロジア・モレコラーレ・ピ・アンジエレツテイ・エツセ・エルレ・エルレ | 抗ウイルス剤としての大環状化合物 |
| CA2720850A1 (en) * | 2008-04-28 | 2009-11-05 | Merck Sharp & Dohme Corp. | Hcv ns3 protease inhibitors |
| EP2476690A1 (en) * | 2008-07-02 | 2012-07-18 | IDENIX Pharmaceuticals, Inc. | Compounds and pharmaceutical compositions for the treatment of viral infections |
| EP2540350B1 (en) * | 2008-07-22 | 2014-05-21 | Merck Sharp & Dohme Corp. | Combinations of a macrocyclic quinoxaline compound which is an hcv ns3 protease inhibitor with other hcv agents |
| US8815829B2 (en) | 2008-12-09 | 2014-08-26 | Rfs Pharma, Llc | 3′-azido purine nucleotide prodrugs for treatment of viral infections |
| EA019341B1 (ru) | 2008-12-23 | 2014-02-28 | Джилид Фармассет, Ллс. | Фосфорамидаты нуклеозидов |
| EA201100851A1 (ru) | 2008-12-23 | 2012-04-30 | Фармассет, Инк. | Аналоги нуклеозидов |
| US8716263B2 (en) | 2008-12-23 | 2014-05-06 | Gilead Pharmasset Llc | Synthesis of purine nucleosides |
| WO2010082050A1 (en) | 2009-01-16 | 2010-07-22 | Istituto Di Ricerche Di Biologia Molecolare P. Angeletti S.P.A. | Macrocyclic and 7-aminoalkyl-substituted benzoxazocines for treatment of hepatitis c infections |
| CN102395590A (zh) | 2009-02-06 | 2012-03-28 | Rfs制药公司 | 用于治疗癌症和病毒感染的嘌呤核苷单磷酸酯前药 |
| EP2403860B1 (en) | 2009-03-04 | 2015-11-04 | IDENIX Pharmaceuticals, Inc. | Phosphothiophene and phosphothiazole as hcv polymerase inhibitors |
| EP2459582B1 (en) | 2009-07-30 | 2015-05-27 | Merck Sharp & Dohme Corp. | Hepatitis c virus ns3 protease inhibitors |
| US20110027229A1 (en) | 2009-07-31 | 2011-02-03 | Medtronic, Inc. | Continuous subcutaneous administration of interferon-alpha to hepatitis c infected patients |
| TW201117812A (en) | 2009-08-05 | 2011-06-01 | Idenix Pharmaceuticals Inc | Macrocyclic serine protease inhibitors |
| WO2011063076A1 (en) | 2009-11-19 | 2011-05-26 | Itherx Pharmaceuticals, Inc. | Methods of treating hepatitis c virus with oxoacetamide compounds |
| KR20120118008A (ko) | 2009-12-18 | 2012-10-25 | 아이데닉스 파마슈티칼스, 인코포레이티드 | 5,5-융합 아릴렌 또는 헤테로아릴렌 간염 c 바이러스 억제제 |
| MX2012011171A (es) | 2010-03-31 | 2013-02-01 | Gilead Pharmasset Llc | Fosforamidatos de nucleosido. |
| AR094621A1 (es) | 2010-04-01 | 2015-08-19 | Idenix Pharmaceuticals Inc | Compuestos y composiciones farmacéuticas para el tratamiento de infecciones virales |
| CA2812962C (en) | 2010-09-22 | 2020-03-31 | Alios Biopharma, Inc. | Azido nucleosides and nucleotide analogs |
| WO2012080050A1 (en) | 2010-12-14 | 2012-06-21 | F. Hoffmann-La Roche Ag | Solid forms of a phenoxybenzenesulfonyl compound |
| TW201309690A (zh) | 2011-02-10 | 2013-03-01 | Idenix Pharmaceuticals Inc | 巨環絲胺酸蛋白酶抑制劑,其醫藥組合物及其於治療hcv感染之用途 |
| CN103842369A (zh) | 2011-03-31 | 2014-06-04 | 埃迪尼克斯医药公司 | 用于治疗病毒感染的化合物和药物组合物 |
| US20120252721A1 (en) | 2011-03-31 | 2012-10-04 | Idenix Pharmaceuticals, Inc. | Methods for treating drug-resistant hepatitis c virus infection with a 5,5-fused arylene or heteroarylene hepatitis c virus inhibitor |
| CA2847892A1 (en) | 2011-09-12 | 2013-03-21 | Idenix Pharmaceuticals, Inc. | Compounds and pharmaceutical compositions for the treatment of viral infections |
| US9403863B2 (en) | 2011-09-12 | 2016-08-02 | Idenix Pharmaceuticals Llc | Substituted carbonyloxymethylphosphoramidate compounds and pharmaceutical compositions for the treatment of viral infections |
| US8507460B2 (en) | 2011-10-14 | 2013-08-13 | Idenix Pharmaceuticals, Inc. | Substituted 3′,5′-cyclic phosphates of purine nucleotide compounds and pharmaceutical compositions for the treatment of viral infections |
| EP2780026B1 (en) | 2011-11-15 | 2019-10-23 | Merck Sharp & Dohme Corp. | Hcv ns3 protease inhibitors |
| WO2013082476A1 (en) | 2011-11-30 | 2013-06-06 | Emory University | Antiviral jak inhibitors useful in treating or preventing retroviral and other viral infections |
| WO2013133927A1 (en) | 2012-02-13 | 2013-09-12 | Idenix Pharmaceuticals, Inc. | Pharmaceutical compositions of 2'-c-methyl-guanosine, 5'-[2-[(3-hydroxy-2,2-dimethyl-1-oxopropyl)thio]ethyl n-(phenylmethyl)phosphoramidate] |
| WO2013177188A1 (en) | 2012-05-22 | 2013-11-28 | Idenix Pharmaceuticals, Inc. | 3',5'-cyclic phosphoramidate prodrugs for hcv infection |
| US9296778B2 (en) | 2012-05-22 | 2016-03-29 | Idenix Pharmaceuticals, Inc. | 3′,5′-cyclic phosphate prodrugs for HCV infection |
| CN104470939B (zh) | 2012-05-22 | 2017-04-26 | 埃迪尼克斯医药有限责任公司 | 用于肝脏疾病的d型氨基酸化合物 |
| CA2871547C (en) | 2012-05-25 | 2021-05-25 | Janssen R&D Ireland | Uracyl spirooxetane nucleosides |
| US9192621B2 (en) | 2012-09-27 | 2015-11-24 | Idenix Pharmaceuticals Llc | Esters and malonates of SATE prodrugs |
| EA030189B8 (ru) | 2012-10-08 | 2018-10-31 | Иденикс Фармасьютикалз Ллс | Аналоги 2'-хлоронуклеозидов для инфекции вгс |
| WO2014063019A1 (en) | 2012-10-19 | 2014-04-24 | Idenix Pharmaceuticals, Inc. | Dinucleotide compounds for hcv infection |
| EP2909222B1 (en) | 2012-10-22 | 2021-05-26 | Idenix Pharmaceuticals LLC | 2',4'-bridged nucleosides for hcv infection |
| WO2014078427A1 (en) | 2012-11-14 | 2014-05-22 | Idenix Pharmaceuticals, Inc. | D-alanine ester of rp-nucleoside analog |
| WO2014078436A1 (en) | 2012-11-14 | 2014-05-22 | Idenix Pharmaceuticals, Inc. | D-alanine ester of sp-nucleoside analog |
| WO2014099941A1 (en) | 2012-12-19 | 2014-06-26 | Idenix Pharmaceuticals, Inc. | 4'-fluoro nucleosides for the treatment of hcv |
| WO2014121418A1 (en) | 2013-02-07 | 2014-08-14 | Merck Sharp & Dohme Corp. | Tetracyclic heterocycle compounds and methods of use thereof for the treatment of hepatitis c |
| WO2014121417A1 (en) | 2013-02-07 | 2014-08-14 | Merck Sharp & Dohme Corp. | Tetracyclic heterocycle compounds and methods of use thereof for the treatment of hepatitis c |
| WO2014137926A1 (en) | 2013-03-04 | 2014-09-12 | Idenix Pharmaceuticals, Inc. | 3'-deoxy nucleosides for the treatment of hcv |
| US9339541B2 (en) | 2013-03-04 | 2016-05-17 | Merck Sharp & Dohme Corp. | Thiophosphate nucleosides for the treatment of HCV |
| US20140271547A1 (en) | 2013-03-13 | 2014-09-18 | Idenix Pharmaceuticals, Inc. | Amino acid phosphoramidate pronucleotides of 2'-cyano, azido and amino nucleosides for the treatment of hcv |
| EP2981542B1 (en) | 2013-04-01 | 2021-09-15 | Idenix Pharmaceuticals LLC | 2',4'-fluoro nucleosides for the treatment of hcv |
| EP3004130B1 (en) | 2013-06-05 | 2019-08-07 | Idenix Pharmaceuticals LLC. | 1',4'-thio nucleosides for the treatment of hcv |
| EP3027636B1 (en) | 2013-08-01 | 2022-01-05 | Idenix Pharmaceuticals LLC | D-amino acid phosphoramidate pronucleotides of halogeno pyrimidine compounds for liver disease |
| EP3046924A1 (en) | 2013-09-20 | 2016-07-27 | IDENIX Pharmaceuticals, Inc. | Hepatitis c virus inhibitors |
| WO2015061683A1 (en) | 2013-10-25 | 2015-04-30 | Idenix Pharmaceuticals, Inc. | D-amino acid phosphoramidate and d-alanine thiophosphoramidate pronucleotides of nucleoside compounds useful for the treatment of hcv |
| EP3063165A1 (en) | 2013-11-01 | 2016-09-07 | Idenix Pharmaceuticals LLC | D-alanine phosphoramidate pronucleotides of 2'-methyl 2'-fluoro guanosine nucleoside compounds for the treatment of hcv |
| US20170198005A1 (en) | 2013-11-27 | 2017-07-13 | Idenix Pharmaceuticals Llc | 2'-dichloro and 2'-fluoro-2'-chloro nucleoside analogues for hcv infection |
| EP3083654A1 (en) | 2013-12-18 | 2016-10-26 | Idenix Pharmaceuticals LLC | 4'-or nucleosides for the treatment of hcv |
| WO2015134560A1 (en) | 2014-03-05 | 2015-09-11 | Idenix Pharmaceuticals, Inc. | Solid forms of a flaviviridae virus inhibitor compound and salts thereof |
| WO2015134561A1 (en) | 2014-03-05 | 2015-09-11 | Idenix Pharmaceuticals, Inc. | Pharmaceutical compositions comprising a 5,5-fused heteroarylene flaviviridae inhibitor and their use for treating or preventing flaviviridae infection |
| EP3131914B1 (en) | 2014-04-16 | 2023-05-10 | Idenix Pharmaceuticals LLC | 3'-substituted methyl or alkynyl nucleosides for the treatment of hcv |
| DK3265102T3 (da) | 2015-03-06 | 2025-10-13 | Atea Pharmaceuticals Inc | Beta-d-2'-deoxy-2'alpha-fluoro-2'-beta-c-substituerede-2-modificerede-n6-substituerede purinnukleotider til hcv-behandling |
| BR112019004297A2 (pt) | 2016-09-07 | 2019-05-28 | Atea Pharmaceuticals Inc | método, uso de uma quantidade eficaz de um composto, composto, e, composição farmacêutica. |
| HRP20250266T1 (hr) | 2017-02-01 | 2025-04-25 | Atea Pharmaceuticals, Inc. | Nukleotid hemi-sulfat sol za liječenje virusa hepatitisa c |
| EP3773753A4 (en) | 2018-04-10 | 2021-12-22 | ATEA Pharmaceuticals, Inc. | TREATMENT OF PATIENTS INFECTED WITH THE HEPATITIS C VIRUS WITH CIRRHOSIS |
| US10874687B1 (en) | 2020-02-27 | 2020-12-29 | Atea Pharmaceuticals, Inc. | Highly active compounds against COVID-19 |
| EP4355319A4 (en) | 2021-06-17 | 2025-01-22 | ATEA Pharmaceuticals, Inc. | BENEFICIAL ANTI-HCV COMBINATION THERAPY |
| CN117509571B (zh) * | 2023-11-01 | 2025-12-05 | 乐威医药(江苏)股份有限公司 | 一种连续化制备叠氮化碘的方法及其应用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6363668A (ja) * | 1986-09-04 | 1988-03-22 | Yuki Gosei Yakuhin Kogyo Kk | 5−メチルピリミジン誘導体の製造法 |
| MXPA00012237A (es) * | 1998-06-10 | 2002-11-15 | Glycodesign Inc | Biblioteca de compuestos combinatorios derigidos y ensayos de alto rendimiento para seleccionar los mismos. |
| NZ546060A (en) * | 2001-04-30 | 2006-11-30 | Trommsdorff Gmbh & Co | Pharmaceutically active drug combination comprising a fatty acid and a uridine compound, and use thereof |
| GB0114286D0 (en) * | 2001-06-12 | 2001-08-01 | Hoffmann La Roche | Nucleoside Derivatives |
| TWI332507B (en) * | 2002-11-19 | 2010-11-01 | Hoffmann La Roche | Antiviral nucleoside derivatives |
| EP1794172B1 (en) * | 2004-08-23 | 2009-07-15 | F.Hoffmann-La Roche Ag | Antiviral 4'-azido-nucleosides |
-
2004
- 2004-06-11 KR KR1020057024240A patent/KR20060026426A/ko not_active Withdrawn
- 2004-06-11 ES ES04739843T patent/ES2276311T3/es not_active Expired - Lifetime
- 2004-06-11 CN CNA2004800171531A patent/CN1809582A/zh active Pending
- 2004-06-11 JP JP2006515914A patent/JP2006527719A/ja active Pending
- 2004-06-11 DK DK04739843T patent/DK1644395T3/da active
- 2004-06-11 MX MXPA05013452A patent/MXPA05013452A/es unknown
- 2004-06-11 CA CA002528294A patent/CA2528294A1/en not_active Abandoned
- 2004-06-11 WO PCT/EP2004/006357 patent/WO2005000864A1/en not_active Ceased
- 2004-06-11 EP EP04739843A patent/EP1644395B1/en not_active Expired - Lifetime
- 2004-06-11 AT AT04739843T patent/ATE346078T1/de not_active IP Right Cessation
- 2004-06-11 DE DE602004003389T patent/DE602004003389T2/de not_active Expired - Fee Related
- 2004-06-15 TW TW093117231A patent/TW200519122A/zh unknown
- 2004-06-18 US US10/871,917 patent/US20050038240A1/en not_active Abandoned
-
2005
- 2005-11-30 IL IL172275A patent/IL172275A0/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP1644395B1 (en) | 2006-11-22 |
| DK1644395T3 (da) | 2007-04-02 |
| DE602004003389T2 (de) | 2007-09-13 |
| CN1809582A (zh) | 2006-07-26 |
| IL172275A0 (en) | 2006-04-10 |
| WO2005000864A1 (en) | 2005-01-06 |
| JP2006527719A (ja) | 2006-12-07 |
| EP1644395A1 (en) | 2006-04-12 |
| ES2276311T3 (es) | 2007-06-16 |
| DE602004003389D1 (de) | 2007-01-04 |
| MXPA05013452A (es) | 2006-03-09 |
| US20050038240A1 (en) | 2005-02-17 |
| CA2528294A1 (en) | 2005-01-06 |
| ATE346078T1 (de) | 2006-12-15 |
| TW200519122A (en) | 2005-06-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20060026426A (ko) | 4'-아지도 뉴클레오사이드 유도체의 제조 방법 | |
| US6090932A (en) | Method of preparation of known and novel 2'-modified nucleosides by intramolecular nucleophilic displacement | |
| CA2098881C (en) | Stereoselective glycosylation process | |
| JP2012097095A (ja) | フルオロシチジン誘導体ための方法 | |
| EP0653436B1 (en) | 5-Methyluridine process for large-scale preparation of 2',3'-didehydro-3'-deoxythymidine (d4T) | |
| IE883406L (en) | 2',3'-Dideoxy-2'-fluoronucleosides | |
| JP2017522387A (ja) | ゲムシタビン−[フェニル(ベンゾキシ−l−アラニニル)]ホスフェートの製造方法リン酸誘導体を製造する方法 | |
| JP7554279B2 (ja) | 3’-o-アミノ-2’-デオキシリボヌクレオシド-5’-三リン酸を調製する方法 | |
| US5466787A (en) | Process for preparing AZT | |
| JP4802712B2 (ja) | リボ核酸化合物及びオリゴ核酸化合物の液相合成法 | |
| JPH08269081A (ja) | 2位が置換されている3,3−ジフルオロフランの製造方法 | |
| SK278598B6 (en) | Method for preparation of deoxynucleosides | |
| CA2266089A1 (en) | Methods for producing nucleoside derivatives and intermediates therefor | |
| JP2006022009A (ja) | 3−フルオロ−2,3−ジデオキシ−β−D−リボフラノシル型ヌクレオシド誘導体の製造方法 | |
| WO2000039144A1 (fr) | Procede de preparation de derives fluores de nucleosides et de sucres | |
| Pedersen et al. | The first example of a new type of acyclic, achiral nucleoside analogue: 1-[3-hydroxy-2-(hydroxymethyl) prop-1-enyl] thymine | |
| EP1186612A1 (en) | Process for the preparation of cytidine derivatives | |
| CA2318277A1 (en) | Process for producing nucleoside derivatives | |
| JPWO1999038879A1 (ja) | ヌクレオシド誘導体の製造方法 | |
| JPH072846A (ja) | テトラヒドロフルフリルアルコール誘導体 | |
| JPWO2000039144A1 (ja) | ヌクレオシド又は糖のフッ素化誘導体の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20051216 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |