KR20060018752A - Collagen Conduit Coated with Synthetic Biodegradable Polymer and Manufacturing Method - Google Patents
Collagen Conduit Coated with Synthetic Biodegradable Polymer and Manufacturing Method Download PDFInfo
- Publication number
- KR20060018752A KR20060018752A KR1020040067269A KR20040067269A KR20060018752A KR 20060018752 A KR20060018752 A KR 20060018752A KR 1020040067269 A KR1020040067269 A KR 1020040067269A KR 20040067269 A KR20040067269 A KR 20040067269A KR 20060018752 A KR20060018752 A KR 20060018752A
- Authority
- KR
- South Korea
- Prior art keywords
- collagen
- conduit
- biodegradable polymer
- coated
- synthetic biodegradable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/22—Polypeptides or derivatives thereof, e.g. degradation products
- A61L27/24—Collagen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/04—Hollow or tubular parts of organs, e.g. bladders, tracheae, bronchi or bile ducts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/28—Materials for coating prostheses
- A61L27/34—Macromolecular materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2210/00—Particular material properties of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2210/0004—Particular material properties of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof bioabsorbable
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Transplantation (AREA)
- Animal Behavior & Ethology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Dermatology (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Vascular Medicine (AREA)
- Gastroenterology & Hepatology (AREA)
- Heart & Thoracic Surgery (AREA)
- Biomedical Technology (AREA)
- Engineering & Computer Science (AREA)
- Pulmonology (AREA)
- Cardiology (AREA)
- Biophysics (AREA)
- Materials For Medical Uses (AREA)
Abstract
본 발명은 콜라젠 도관의 외부가 합성 생분해성 고분자로 코팅된 콜라젠 도관 및 이의 제조방법에 관한 것이다.The present invention relates to a collagen conduit coated with a synthetic biodegradable polymer on the outside of the collagen conduit and a method for producing the same.
신경도관, 생분해성 고분자, 신경재생, 코팅, 콜라젠, 신경세포, PLGA, PLANeural conduit, biodegradable polymer, nerve regeneration, coating, collagen, nerve cell, PLGA, PLA
Description
도 1은 신경도관을 만들기 위해서 사용된 콜라젠 필름이다.1 is a collagen film used to make neural conduits.
도 2는 콜라젠 도관에 합성 생분해성 고분자를 코팅하기 위해서 사용된 분사기이다.2 is an injector used to coat synthetic biodegradable polymers into collagen conduits.
도 3은 생분해성 폴리머인 생분해성 고분자로 분사 코팅된 신경도관이다.3 is a neural conduit spray coated with a biodegradable polymer that is a biodegradable polymer.
도 4는 (1) 코팅전 콜라젠 필름의 표면사진, (2) 0.1% PLGA로 코팅된 콜라젠 필름의 표면사진, (3) 0.3% PLGA로 코팅된 콜라젠 필름의 표면사진, (4) 0.5% PLGA로 코팅된 콜라젠 필름의 표면사진, (5) 0.1% PLA로 코팅된 콜라젠 필름의 표면사진, (6) 0.3% PLA로 코팅된 콜라젠 필름의 표면사진, (7) 0.5% PLA로 코팅된 콜라젠 필름의 표면사진, (8) 0.25% GA로 가교된 콜라젠 필름의 표면사진, (9) 0.5% GA로 콜라젠 필름의 표면사진이다.Figure 4 is (1) the surface photograph of the collagen film before coating, (2) the surface photograph of the collagen film coated with 0.1% PLGA, (3) the surface photograph of the collagen film coated with 0.3% PLGA, (4) 0.5% PLGA Surface photo of the collagen film coated with (5) surface photo of the collagen film coated with 0.1% PLA, (6) surface photo of the collagen film coated with 0.3% PLA, (7) collagen film coated with 0.5% PLA Surface photograph of (8) surface photograph of collagen film crosslinked with 0.25% GA, (9) surface photograph of collagen film with 0.5% GA.
도 5는 (1) 코팅전 콜라젠 필름의 단면사진, (2) (1)의 ○ 부분을 확대한 단면사진, (3) 0.3% 폴리락틱코글리콜릭산으로 코팅된 콜라젠 필름의 단면사진, (4) (3)의 ○ 부분을 확대한 단면사진이다.5 is a cross-sectional photograph of (1) a pre-coated collagen film, (2) an enlarged cross-sectional photograph of a ○ part of (1), (3) a cross-sectional photograph of a collagen film coated with 0.3% polylacticcoglycolic acid, (4 ) It is cross-sectional photograph which enlarged ○ part of (3).
도 6은 농도에 따른 생분해성 고분자가 코팅된 신경도관의 생분해성 실험 결 과로 (a)는 콜라게네즈 첨가하였을 때 (b)는 콜라게네즈를 첨가하지 않았을 때의 결과이다. C는 생분해성 고분자 무처리, G는 PLGA, L은 PLA, GA는 글루타르알데하이드를 의미한다. Figure 6 shows the results of the biodegradability test results of the neural conduit coated with the biodegradable polymer according to the concentration (a) when collagenase was added (b) was not added collagenase. C means no biodegradable polymer, G means PLGA, L means PLA, GA means glutaraldehyde.
도 7은 농도에 따른 생분해성 고분자가 코팅된 신경도관의 탄성계수를 나타낸다.Figure 7 shows the elastic modulus of the neural conduit coated with the biodegradable polymer according to the concentration.
도 8은 농도에 따른 생분해성 고분자가 코팅된 신경도관의 인장강도를 나타낸다.8 shows the tensile strength of the neural conduit coated with the biodegradable polymer according to the concentration.
도 9는 농도에 따른 생분해성 고분자가 코팅된 신경도관의 세포독성을 나타낸다.9 shows the cytotoxicity of neural conduits coated with biodegradable polymers at different concentrations.
도 10은 (1) 토끼 대퇴부 좌측좌골신경에 0.3% PLGA 코팅된 신경도관을 매식후 사진과 (2) 매식 후 12주가 지난 신경도관을 통하여 재생된 신경사진이다.Figure 10 is a (1) picture of the nerve conduit coated 0.3% PLGA on the left sciatic nerve of the rabbit fetus and (2) a neurophotograph regenerated through the
도 11은 (1) 0.3% PLGA 코팅된 신경도관을 토끼 대퇴부 좌측좌골신경에 매식 후 12주가 지난 신경도관을 통하여 재생된 신경의 저배율의 조직학적 사진이고 (2) 고배율의 조직학적 사진이다.FIG. 11 is (1) histological picture of low magnification of nerves regenerated through the
본 발명은 도관 내부는 콜라젠으로 구성되고 도관의 외부는 생분해성 고분자로 코팅된 콜라젠 도관 및 이의 제조방법에 관한 것이다. The present invention relates to a collagen conduit coated with a biodegradable polymer and a method for producing the same, wherein the conduit is composed of collagen.
말초신경이 절단되면 신경조직은 특이한 과정을 거쳐 재생을 하게 된다. 절단 부위의 근위부의 축삭은 절단 직후에는 위축되지만 수일 후에는 자라기 시작하면서 말단 부위에는 성장 원추가 형성되어 사방으로 성장해 나아간다. 일단 어느 하나의 성장 원추가 적절한 위치에 도달하게 되면 다른 성장 원추는 제거되고 도달에 성공한 축삭만 계속 목표 조직으로 향하게 된다. 그러나 절단 부위가 너무 광범위한 경우에는 재생이 이렇게 순조롭게 이루어지지는 않는다. 이 경우 기능이 별로 중요하지 않는 말초 신경을 부분적으로 절제하고, 이것을 신경 절단 부위에 자가 이식을 행할 때도 있다. 그러나, 이 방법으로는 신경 기능이 충분히 회복되지 않으며 이식 신경을 채취한 부분에서도 기능의 저하가 일어날 수 있다. When the peripheral nerves are cut, the nerve tissue regenerates through a unique process. The axon at the proximal portion of the cut site contracts shortly after the cut but begins to grow a few days later, with growth cones formed at the distal end that grow in all directions. Once one growth cone is reached, the other growth cone is removed and only successful axons continue to the target tissue. However, if the cleavage site is too extensive, the regeneration is not so smooth. In this case, the peripheral nerves, of which function is not important, are partially excised and autologous transplantation is sometimes performed at the nerve cutting sites. However, this method does not fully restore nerve function, and a decrease in function may occur even in the area where the transplanted nerve is collected.
따라서, 신경 결손 부위가 클 경우 그 기능을 회복하기 위한 방법의 하나로 신경도관이 있다. 신경도관이란 절단된 신경의 양쪽 끝을 인공으로 만든 튜브 안에 고정하고 그 튜브 안으로 신경의 연결을 유도하는 관을 의미한다. 이러한 신경도관은 신경재생을 방해하는 반흔조직의 침투를 막을 수 있고, 올바른 방향으로 축삭의 성장을 유도할 수 있으며, 신경자체에서 분비되는 재생촉진 물질들이 관 내에 유지되는 반면 재생을 방해하는 물질은 외부로부터 차단되는 이점을 가지고 있다.Therefore, there is a neural conduit as a method for restoring its function when the nerve defect is large. Neural conduit refers to a tube that fixes both ends of a cut nerve in an artificial tube and induces nerve connections into the tube. These nerve conduits can prevent the penetration of scar tissue that interferes with nerve regeneration, induce the growth of axons in the right direction, and the substances that interfere with regeneration while maintaining the regeneration materials secreted by the nerve itself It has the advantage of being cut off from the outside.
현재까지 가장 많이 사용되고 있는 신경도관은 콜라젠 도관이다. 콜라젠은 뛰어난 생체적합성과 약한 항원성으로 인하여 생체재료 분야에서 많이 사용되고 있는 물질로 신경재생을 위한 신경도관의 재료로서도 기존 여러 발명에서 사용되었다. 그러나, 콜라젠은 분해 속도가 매우 빠르고 기계적 강도가 약하다는 단점이 있다. 이런 단점을 보완하기 위하여 가교된 콜라젠을 사용하기도 하였으나 가교된 콜라젠은 가교제로 인한 독성과 낮은 친수성으로 인해 생체적합성이 낮다는 한계가 있다. The most commonly used nerve conduit to date is the collagen conduit. Collagen is a material widely used in the field of biomaterials because of its excellent biocompatibility and weak antigenicity, and has been used in various inventions as a material of neural conduits for nerve regeneration. However, collagen has the disadvantage that the decomposition rate is very fast and the mechanical strength is weak. Although cross-linked collagen was used to compensate for this drawback, cross-linked collagen has a limitation of low biocompatibility due to toxicity and low hydrophilicity due to the cross-linking agent.
이에 본 발명자는 콜라젠 도관 외부를 생분해성 고분자로 코팅할 경우, 코팅된 생분해성 고분자 용액의 농도에 따라 도관의 기계적 성질과 생분해성을 조절할 수 있어 목적하는 기계적 강도 및 분해 속도를 가지면서 독성이 없이 말초신경 결손 부위의 회복에 유용하게 사용 될 수 있다는 것을 밝히고 본 발명을 완성하였다. Therefore, the present inventors can control the mechanical properties and biodegradability of the conduit according to the concentration of the coated biodegradable polymer solution when coating the outside of the collagen conduit with the biodegradable polymer, so that the desired mechanical strength and decomposition rate are not toxic. The present invention has been completed and found that it can be usefully used for the repair of peripheral nerve defects.
본 발명의 하나의 목적은 콜라젠 도관 외부가 합성 생분해성 고분자로 코팅된 콜라젠 도관을 제공하는 것이다.One object of the present invention is to provide a collagen conduit in which the outside of the collagen conduit is coated with a synthetic biodegradable polymer.
본 발명의 또 다른 목적은 다공성 콜라젠 필름을 말아(rolling) 건조시키는 단계 및 합성 생분해성 고분자 용액을 콜라젠 필름 외부에 분사하여 코팅하는 단계로 이루어지는 생분해성 고분자 코팅된 콜라젠 도관 제조과정을 제공하는 것이다.
Still another object of the present invention is to provide a biodegradable polymer-coated collagen conduit manufacturing process comprising rolling and drying a porous collagen film and spraying and coating a synthetic biodegradable polymer solution on the outside of the collagen film.
하나의 양태로서, 본 발명은 콜라젠 도관 외부가 합성 생분해성 고분자로 코팅된 콜라젠 도관에 관한 것이다. In one embodiment, the present invention relates to a collagen conduit wherein the outside of the collagen conduit is coated with a synthetic biodegradable polymer.
본 발명에서 "도관"은 생체이식, 보다 자세히는 신경 재생을 위한 신경도관(neural conduit)으로 사용되는 튜브 모양의 물체이다. 생체 이식용 도관이므로 생체적합성이 높은 물질을 사용하여야 하는데, 본 발명에서는 콜라젠을 사용하였다."Conduit" in the present invention is a tubular object that is used as a neural conduit for biotransplantation, more specifically for nerve regeneration. Since a conduit for living transplantation, a material having high biocompatibility should be used. In the present invention, collagen was used.
본 발명에서 "콜라젠"은 천연에서 추출하거나 또는 재조합적으로 생성된 모든 형태의 콜라젠을 포함한다. 콜라젠은 생체 친화성 및 조직 접합성이 우수하고, 항원성이 낮으며 숙주세포의 분화 및 증식을 촉진시키는 작용을 하고 생체내에서 완전히 분해 흡수되는 특징을 가지므로 의료용 재료로 바람직하다. 천연의 콜라젠은 동물의 피부, 뼈, 연골, 힘줄, 장기 등 각종 기관의 결합 조직으로부터 산 가용화법, 알칼리 가용화법, 중성 가용화법, 효소 가용화법 등으로 추출 및 정제하여 사용할 수 있다. 현재까지 타입I 내지 XIX이 발견되었는데 그 중에서 타입I 내지 V형 콜라젠이 가장 많이 사용되고 있다. 본 발명에서는 모든 타입의 콜라젠을 단독 또는 한 성분 이상 혼합하여 사용 가능하나 바람직하게는 천연의 타입Ⅰ, Ⅱ, Ⅲ, Ⅳ, V 콜라젠이고, 가장 바람직하게는 소 유래 타입Ⅰ콜라젠이다. In the present invention, "collagen" includes all forms of collagen extracted from nature or produced recombinantly. Collagen is preferred as a medical material because it has excellent biocompatibility and tissue adhesion, low antigenicity, functions to promote differentiation and proliferation of host cells, and has a characteristic of being completely degraded and absorbed in vivo. Natural collagen can be extracted and used from connective tissues of various organs such as skin, bone, cartilage, tendons and organs of animals by acid solubilization, alkali solubilization, neutral solubilization and enzyme solubilization. To date, Type I to XIX have been discovered, and Type I to V type collagen is the most used. In the present invention, all types of collagen may be used alone or in combination of one or more components. Preferably, they are natural type I, II, III, IV and V collagen, and most preferably bovine-derived type I collagen.
그러나, 콜라젠은 강도가 약하여 물, 체액 또는 혈액 등과 접촉하였을 때 일정 기간동안 강도를 유지시키기가 힘들고 분해 속도가 빠르다는 단점이 있다. 이런 점을 해결하기 위하여 글루타르알데하이드(GA), 에폭시 등의 가교제로 가교시킬 경우, 가교제 자체가 가지는 독성이 생체에 문제가 될 뿐 아니라 콜라겐이 원래 갖는 생화학적 특성, 특히 세포 증식에 대한 촉진 효과가 손실되게 된다. 또한, 가교제 처리된 콜라젠은 생분해가 거의 일어나지 않고 기계적 강도가 지나치게 강하다는 단점도 있다. 가교제 처리 대신 방사선, 전자선, 자외선 또는 열 등으로 물리적 가교 처리를 할 경우에는 가교율이 불안정하고, 충분한 물성이 부여되지 않고 생체내에서의 흡수 속도를 제어할 수 있도록 가교 처리하는 것이 곤란하다. However, collagen has a disadvantage in that it is difficult to maintain the strength for a period of time when the collagen is in contact with water, body fluid or blood and the decomposition rate is fast. In order to solve this problem, when crosslinking with a crosslinking agent such as glutaraldehyde (GA) or epoxy, the toxicity of the crosslinking agent itself is not only a problem for the living body, but also a promoting effect on the biochemical properties of collagen, in particular, cell proliferation. Will be lost. In addition, the crosslinking agent-treated collagen has the disadvantage that the biodegradation hardly occurs and the mechanical strength is too strong. In the case of performing physical crosslinking treatment with radiation, electron beam, ultraviolet rays or heat instead of the crosslinking agent treatment, the crosslinking rate is unstable, and it is difficult to perform crosslinking treatment so that the absorption rate in vivo can be controlled without providing sufficient physical properties.
본 발명의 콜라젠은 비가교된 콜라젠인 것을 특징으로 한다. 대신 종래의 가교된 콜라젠이 가지는 기술적 단점을 보완하면서 콜라젠 도관의 기계적 강도는 높이고 분해속도는 감소시키기 위하여 본 발명에서는 콜라젠 도관의 외부를 합성 생분해성 고분자로 코팅하였다. Collagen of the present invention is characterized in that the non-crosslinked collagen. Instead, to improve the mechanical strength of the collagen conduit while reducing the decomposition rate of the conventional crosslinked collagen in the present invention, the outside of the collagen conduit was coated with a synthetic biodegradable polymer.
본 발명에서 "생분해성 고분자"란 생체내에서 일정 시간이 지나면 자연적으로 무독성 분해 산물로 서서히 전환되는 고분자를 의미한다. 본 발명에서는 합성 생분해성 고분자를 콜라젠 도관의 기계적 강도를 높이기 위한 도관 외피 코팅제로 사용하였으며, 합성 생분해성 고분자로 코팅된 콜라젠 도관은 신경이 재생될 때까지 존재하는 것이 바람직하다.As used herein, the term "biodegradable polymer" refers to a polymer that is gradually converted into a non-toxic decomposition product after a certain time in vivo. In the present invention, the synthetic biodegradable polymer was used as a conduit jacket coating to increase the mechanical strength of the collagen conduit, and the collagen conduit coated with the synthetic biodegradable polymer is preferably present until the nerve is regenerated.
본 발명에서 외피 코팅제로 사용될 수 있는 합성 생분해성 고분자는 콜라젠 도관의 기계적 강도를 강화시키고 신경재생을 방해하지 않으며 분해되는 성질을 가지는 모든 생분해성 고분자를 포함한다. 예를 들어, 폴리락트산 (Polylactic acid: PLA), 폴리글라이콜산 (Polyglycolic acid: PGA), 이들의 공중합체인 폴리(락틱-코-글라이콜산) (Poly(lactic-co-glycolic acid): PLGA), 이의 성형중합체(star polymer)인 폴리(락틱-코-글라이콜산)-글루코스 (PLGA-glucose) 등의 폴리에스테르, 폴리오르토에스테르 (Polyorthoester), 폴리안하이드라이드 (Polyanhydride), 폴리디옥사논(polydioxanone), 폴리아미노산 (Polyamino acid), 폴리하이드록시부티르산 (Polyhydroxybutyric acid), 폴리카프로락톤 (Polycaprolactone), 폴리알킬카보네이트 (Polyalkylcarbonate) 등과 같은 생분해 성 고분자가 있으나 이로 제한되지는 않는다. 상기 생분해성 고분자는 이들의 유도체들도 사용 가능하며, 또한 단독 또는 2 성분 이상의 혼합 사용도 가능하다. 바람직하게는 PLA, PGA, PLGA 또는 이들의 혼합물이며, 보다 바람직하게는 PLA, PLGA이다. Synthetic biodegradable polymers that can be used as skin coatings in the present invention include all biodegradable polymers that have properties that enhance the mechanical strength of collagen conduits and do not interfere with neuronal regeneration. For example, polylactic acid (PLA), polyglycolic acid (PGA), and copolymers thereof poly (lactic-co-glycolic acid) (PLGA) ), Polyesters such as poly (lactic-co-glycolic acid) -glucose (PLGA-glucose), star polymers thereof, polyorthoesters, polyanhydrides, and polydioxa Biodegradable polymers such as, but not limited to, polydioxanone, polyamino acid, polyhydroxybutyric acid, polycaprolactone, polyalkylcarbonate, and the like. The biodegradable polymers may be used as derivatives thereof, or may be used alone or in combination of two or more components. Preferably it is PLA, PGA, PLGA, or a mixture thereof, More preferably, it is PLA, PLGA.
본 발명의 도관의 내부는 콜라젠이고 외부는 합성 생분해성 고분자로 코팅된 콜라젠층을 갖는 비균일층이다. 콜라젠으로만 이루어진 도관 내부는 콜라젠의 장점, 즉 세포 유착성이 우수하여 신경 세포의 성장에 유리하다. 종래의 합성 생분해성 고분자를 이용한 도관의 경우 친수성이 낮아 세포 유착이 어려웠다 (D. J. Mooney., Biomaterials, 17:115-124, 1996). 본 발명은 천연 생분해성 고분자인 콜라젠의 특성을 이용하면서도 합성 생분해성 고분자를 도관 외부에 코팅시켜 기계적 강도를 증진시켰다. The inside of the conduit of the invention is a collagen and the outside is a non-uniform layer having a collagen layer coated with a synthetic biodegradable polymer. The inside of the conduit consisting of collagen alone has the advantages of collagen, ie, cell adhesion, which is advantageous for the growth of nerve cells. Conduits using conventional synthetic biodegradable polymers have low hydrophilicity, making cell adhesion difficult (DJ Mooney., Biomaterials , 17: 115-124, 1996). The present invention improves the mechanical strength by coating the synthetic biodegradable polymer on the outside of the conduit while using the properties of collagen, a natural biodegradable polymer.
도관 외부에 코팅되는 합성 생분해성 고분자는 1회 이상, 예를 들어, 2회 또는 3회 코팅될 수도 있다. Synthetic biodegradable polymers coated outside the conduit may be coated one or more times, for example two or three times.
본 발명의 도관은 내경과 길이를 자유롭게 조절 가능하다. 신경도관으로 사용할 경우 결손된 신경의 크기에 따라 내경과 길이를 조절하여 제작한다. 내경은 바람직하게는 0.5mm 내지 5mm, 보다 바람직하게는 0.8mm 내지 1.2mm이고, 길이는 바람직하게는 5mm 내지 200mm, 보다 바람직하게는 10mm 내지 20mm이다.The conduit of the present invention is freely adjustable the inner diameter and length. When used as a nerve conduit, the inner diameter and length are adjusted according to the size of the missing nerve. The inner diameter is preferably 0.5 mm to 5 mm, more preferably 0.8 mm to 1.2 mm, and the length is preferably 5 mm to 200 mm, more preferably 10 mm to 20 mm.
본 발명의 합성 생분해성 고분자로 코팅된 콜라젠 도관은 의료용 대체관, 예를들어 인공 신경도관, 인공 척수. 인공 식도, 인공 기관. 인공 혈관, 인공 밸브 등에 사용 가능하며 이로 제한되지는 않는다. 신경 재생에 사용되는 인공 신경도 관에의 적용이 바람직하다. Collagen conduits coated with synthetic biodegradable polymers of the present invention are medical alternatives, such as artificial neural conduits, artificial spinal cord. Artificial esophagus, artificial organs. It can be used for artificial blood vessels, artificial valves, etc., but is not limited thereto. Application to artificial nerve channels also used for nerve regeneration.
구체적 실험 양태에서, 기존의 GA 가교된 콜라젠 신경도관이 생분해가 거의 일어나지 않고 세포독성이 높아 매우 낮은 세포 생존률을 보이는 것에 비하여 본 발명의 콜라젠 도관은 본 발명의 도관은 일정 기간 동안 그 형상을 유지할 수 있는 생체 이식 생분해성 고분자 코팅이 되어 적절한 기계적 강도를 가지지만 생체내 독성이 없이 안전하고 세포 증식에 대한 촉진 효과가 손실되지 않았으며 분해 속도도 코팅되지 않은 콜라젠에 비해 적절하게 감소되었다. 또한, 합성 생분해성 고분자로 코팅된 콜라젠 도관의 강도와 분해 속도는 코팅제로 사용하는 고분자의 종류, 농도 및 코팅층의 수에 따라 자유롭게 조절 가능하였다. 생체내 실험 결과, 토끼 좌측좌골신경을 수술로 15mm 길이 정도 절단하고 본 발명의 0.3% PLGA이 코팅된 콜라젠 도관을 이식한 뒤 12주 경과 후 봉합 부위를 개복하여 관찰 하였을 때, 신경은 완전히 재생되고 이식한 신경도관은 완전 생분해되었다. In a specific experimental embodiment, the collagen conduit of the present invention can maintain its shape for a period of time, compared with the conventional GA crosslinked collagen neural conduit shows little biodegradation and high cytotoxicity. Biodegradable biodegradable polymer coatings have adequate mechanical strength, but are safe without in vivo toxicity, have no loss of promoting effect on cell proliferation, and degradation rates are adequately reduced compared to uncoated collagen. In addition, the strength and decomposition rate of the collagen conduit coated with a synthetic biodegradable polymer was freely adjustable according to the type, concentration and number of coating layers of the polymer used as a coating agent. As a result of in vivo experiments, when the rabbit left sciatic nerve was surgically cut about 15 mm in length and the collagen conduit coated with 0.3% PLGA of the present invention was implanted and the suture was opened after 12 weeks, the nerve was completely regenerated. The implanted neural conduit was fully biodegradable.
또 다른 양태로서, 본 발명은 다공성 콜라젠 필름을 말아(rolling) 건조시키는 단계 및 합성 생분해성 고분자 용액을 콜라젠 필름 외부에 분사하여 코팅하는 단계를 포함하는 합성 생분해성 고분자로 코팅된 콜라젠 도관의 제조방법에 관한 것이다.In still another aspect, the present invention provides a method for producing a collagen conduit coated with a synthetic biodegradable polymer comprising rolling and drying a porous collagen film and spraying and coating the synthetic biodegradable polymer solution outside the collagen film. It is about.
다공의 크기는 도관 외부의 영양분이 도관내부로 유입되고 또한 도관내부에서 재생되는 신경이 외부의 반흔 조직의 침투를 막는데 매우 중요하다. 분사한 코팅 용액에 농도가 높을수록 도관의 다공의 크기가 작아지게 된다. The size of the pores is very important for the nutrients from outside the catheter to enter the catheter and the nerves regenerated inside the catheter to prevent the penetration of external scar tissue. The higher the concentration in the sprayed coating solution, the smaller the size of the pores in the conduit.
코팅 용액의 농도가 증가할수록 도관의 생분해 속도가 느리게 되는데 신경이 재생될 때까지 생체내에 잔존하도록 분해 속도를 조절하는 것이 중요하다. As the concentration of the coating solution increases, the rate of biodegradation of the conduit is slowed. It is important to control the rate of decomposition so that it remains in vivo until the nerve is regenerated.
바람직하게는 4주 내지 20주 내에 분해되도록 하고, 보다 바람직하게는 8주 내지 16주 내에 분해되도록 한다. Preferably it is to be degraded within 4 to 20 weeks, more preferably 8 to 16 weeks.
또한, 코팅 용액의 농도가 증가할수록 도관의 기계적 강도가 증가하게 되며 생체에서 일정 기간 동안 형상을 유지하도록, 바람직하게는 0.1 내지 0.6 MPa의 인장강도와 0.2 내지 1.2 MPa의 탄성계수를 가진다. In addition, as the concentration of the coating solution increases, the mechanical strength of the conduit increases, and in order to maintain the shape for a certain period in the living body, it preferably has a tensile strength of 0.1 to 0.6 MPa and an elastic modulus of 0.2 to 1.2 MPa.
절단된 신경의 크기에 따라 상기 사항을 모두 고려하여 적절한 농도의 코팅 용액을 사용해야 한다. 생분해성 고분자 농도는 바람직하게는 0.05% 내지 1.0%이고, 보다 바람직하게는 0.1% 내지 0.5%이다.Depending on the size of the cut nerves, all of the above considerations should be used to use a coating solution of the appropriate concentration. The biodegradable polymer concentration is preferably 0.05% to 1.0%, more preferably 0.1% to 0.5%.
코팅층이 너무 두꺼우면 박리현상이 발생하기 싶고 너무 얇으면 분균질한 코팅층이 형성되기 싶다. 코팅 두께는 코팅액의 농도, 분사시 압력, 분사량 및 분사 노즐과 도관과의 거리등에 따라 두께가 결정되는 바, 목적에 맞게 이를 적절히 조절하도록 한다. 구체적 실시 양태에서는 분사 노즐과 도관과의 거리가 3㎝가 되도록 하고 분사 코팅하였다. 코팅층의 두께는 바람직하게는 1μm 내지 50μm 이고, 보다 바람직하게는 5μm 내지 20μm이고, 가장 바람직하게는 8μm 내지 12μm이다.If the coating layer is too thick, peeling phenomenon will occur, and if too thin, a homogeneous coating layer will be formed. The thickness of the coating is determined according to the concentration of the coating liquid, the pressure at the time of injection, the amount of injection, and the distance between the injection nozzle and the conduit. In a specific embodiment, the distance between the spray nozzle and the conduit is 3 cm and spray coated. The thickness of the coating layer is preferably 1 μm to 50 μm, more preferably 5 μm to 20 μm, and most preferably 8 μm to 12 μm.
구체적 양태로서 도관 제조 과정을 예시하면 다음과 같다. 수화된 콜라젠 필름을 테프론 봉을 이용하여 도관 모양을 만든 뒤 이를 30℃ 건조기에서 건조시킨다. 테프론 봉을 제거하고 증류수로 1회 이상 세척한다. 콜라젠 도관을 원하는 길이로 절단한다. 메틸클로라이드(MC)에 생분해성 고분자, 바람직하게는 PLGA 또 는 PLA를 0.01% 내지 1%, 바람직하게는 0.1% 내지 0.5%의 농도로 녹여 제조된 고분자 용액을 절단된 도관에 분무 코팅한다. 생분해성 고분자 코팅된 도관을 1회 이상 증류수로 세척 후 진공 건조기에서 약 24시간 동안 건조한다. 이온개스로 멸균하고 포장하여 보관한다.Illustrating the conduit manufacturing process as a specific embodiment is as follows. The hydrated collagen film is conduit shaped using Teflon rods and then dried in a 30 ° C. dryer. Remove the Teflon rods and wash at least once with distilled water. The collagen conduit is cut to the desired length. The polymer solution prepared by dissolving the biodegradable polymer, preferably PLGA or PLA in methyl chloride (MC) at a concentration of 0.01% to 1%, preferably 0.1% to 0.5%, is spray coated on the cut conduit. The biodegradable polymer coated conduit is washed one or more times with distilled water and then dried in a vacuum dryer for about 24 hours. Sterilize with ion gas and pack and store.
이하, 본 발명을 실험예에 의해 상세히 설명한다. 그러나, 하기 실시예는 본 발명을 예시하는 것일 뿐, 본 발명이 하기 실시예에 한정되는 것은 아니다.Hereinafter, the present invention will be described in detail by experimental examples. However, the following examples are merely to illustrate the invention, the present invention is not limited to the following examples.
실시예 1: 생분해성 고분자가 코팅된 생분해성 콜라젠 도관 제조 Example 1 Preparation of Biodegradable Collagen Conduit Coated with Biodegradable Polymer
시판되는 치과용 다공성 콜라젠 필름(CollaTape®: Integra LifeSciences Coporation, Plainsboro, NJ, USA)을 신경도관을 만들기 위한 기본 재료로 사용하였다(도 1). 이 콜라젠 필름을 증류수에 적신 후 테프론 봉을 이용하여 도관 모양을 만들었다. 이것을 30℃ 건조기에서 건조시킨 후 테프론 봉을 제거하고 다시 증류수를 이용하여 세척하였다. 이렇게 만들어진 콜라젠 신경도관을 필요한 길이로 자른 후 생분해성 고분자로 분사 코팅 하였다. 분사 코팅은 팁 지름 0.3mm인 분사기(Richpen, Tokyo, Japan)를 사용하였다 (도 2). 메틸클로라이드(MC; Duksan, Kyoungkido, South Korea)에 생분해성 고분자 PLGA(Sigma, St. Louis, MO, USA) 또는 PLA(Sigma, St. Louis, MO, USA)를 0.1%, 0.3% 0.5%의 농도로 녹여 제조하였다. 스프레이 코팅은 회전기를 이용하여 상기 만들어진 콜라젠 신경도관을 회전시키면서 분무기를 이용하여 도관 모든 면에 골고루 코팅 될 수 있도록 약 5초 동안 스프레이 코팅 하였다. 생분해성 고분자가 코팅된 신경도관을 세척 후 진공 건조기에서 약 24시간 동안 건조하였다. 그 후 다시 이온개스로 멸균하고 멸균한 신경도관을 포장하여 보관하여 사용하였다 (도 3).It was used as a basic material for making a: (Integra LifeSciences Coporation, Plainsboro, NJ, USA CollaTape ®) nerve conduit (1) a commercially available dental porous collagen film. The collagen film was soaked in distilled water and then made a conduit shape using a Teflon rod. This was dried in a 30 ℃ drier, the Teflon rod was removed and washed again with distilled water. The collagen neural conduit thus made was cut to the required length and spray coated with a biodegradable polymer. The spray coating used an injector (Richpen, Tokyo, Japan) having a tip diameter of 0.3 mm (FIG. 2). Methyl chloride (MC; Duksan, Kyoungkido, South Korea) contains 0.1%, 0.3% 0.5% of biodegradable polymer PLGA (Sigma, St. Louis, MO, USA) or PLA (Sigma, St. Louis, MO, USA). It was prepared by melting to concentration. Spray coating was spray-coated for about 5 seconds to be evenly coated on all sides of the conduit using a sprayer while rotating the collagen neural conduit made using a rotator. The neural conduit coated with the biodegradable polymer was washed and dried in a vacuum dryer for about 24 hours. Then sterilized with ion gas again, sterilized neural conduit was packaged and used (Fig. 3).
또한, 코팅된 콜라젠 신경도관의 특성을 기존의 콜라젠 신경도관의 특성과 비교하기 위하여 글루타르알데하이드(GA: Sigma, St. Louis, MO, USA)를 사용하여 가교된 콜라젠 신경도관을 제조하였다. 위에서 제시된 방법으로 만들어진 코팅전 콜라젠 도관을 0.25%와 0.5% GA 용액에서 약 24시간동안 4℃에서 보관한 후 꺼내어 증류수를 이용하여 세척하였다. 세척 후 가교된 신경도관을 가교된 특성을 보존하기 위하여 동결건조 하였다. 그 후 다시 이온 개스로 멸균하고 멸균한 신경도관을 포장하여 보관하여 사용하였다.In addition, crosslinked collagen neural conduits were prepared using glutaraldehyde (GA: Sigma, St. Louis, Mo., USA) in order to compare the properties of the coated collagen neural conduits with those of existing collagen neural conduits. The pre-coated collagen conduit made by the method presented above was stored at 0.25 ° C. and 0.5% GA solution at 4 ° C. for about 24 hours, and then taken out and washed with distilled water. After washing, the crosslinked neural conduit was lyophilized to preserve the crosslinked properties. Then, sterilized with ion gas again, the sterilized neural conduit was packaged and used.
본 발명의 신경도관은 결손된 신경의 크기에 따라 내경과 길이를 조절하여 제조될 수 있다. 본 실험에 사용한 토끼 신경 재건에서는 내경 1 mm, 길이 20 mm의 도관이 바람직하므로 이에 맞게 크기를 제작하여 사용하였다.The neural conduit of the present invention can be prepared by adjusting the inner diameter and the length according to the size of the missing nerve. In the rabbit nerve reconstruction used in this experiment, a conduit with a diameter of 1 mm and a length of 20 mm is preferable, and thus the size of the rabbit nerve reconstruction was used.
실시예 2: 코팅 후 전자현미경에 의한 표면 관찰 Example 2 Surface Observation by Electron Microscopy After Coating
생분해성 폴리머로 코팅하지 않은 콜라젠 필름, 생분해성 폴리머로 코팅된 콜라젠 필름, 가교된 콜라젠 필름을 SEM (scanning electron microscopy: Hitachi, Tokyo, Japan)으로 관찰하였다. Collagen films not coated with biodegradable polymers, collagen films coated with biodegradable polymers, crosslinked collagen films were observed by scanning electron microscopy (Hitachi, Tokyo, Japan).
도 4에서 확인 할 수 있듯이 PLGA과 PLA 모두 코팅 용액에 농도가 높을수록 다공의 크기도 작아졌다. 이러한 다공의 크기는 도관 외부의 영양분이 도관내부로 유입되고 또한 도관 내부에서 재생되는 신경이 외부의 반흔 조직의 침투를 막는데 매우 중요하며 여러 가지 사항을 고려해 볼 때 0.3%의 농도로 코팅된 신경도관이 가장 적절하다. 또한, 이런 0.3% PLGA로 코팅된 신경도관의 단면을 보면 코팅 전과는 달리 약 10 μm의 두께로 생분해성 고분자가 코팅되어 있음을 알 수 있었다 (도 5). 두께는 코팅액의 농도와 스프레이 코팅시 압력과 시편과의 거리를 조절함으로써 조절가능 하였다.As can be seen in Figure 4 both the PLGA and PLA, the higher the concentration in the coating solution, the smaller the size of the pores. The size of these pores is very important for the nutrients from outside the catheter to enter the catheter and the nerves regenerated inside the catheter to prevent external scar tissue from infiltrating. Conduit is most appropriate. In addition, the cross section of the neural conduit coated with 0.3% PLGA showed that the biodegradable polymer was coated with a thickness of about 10 μm, unlike before the coating (FIG. 5). The thickness was adjustable by adjusting the concentration of the coating solution and the distance between the pressure and the specimen during spray coating.
실시예 3: 생분해성 실험 Example 3 : Biodegradability Experiment
생분해성 실험은 10 μg/ml 콜라게네즈 타입 Ⅰ(collagenase type Ⅰ; Sigma, St. Louis, MO, USA)가 첨가된 또는 첨가되지 않은 pH 7.4인 PBS 용액에서 8주 동안 신경도관을 담아 놓고 각각의 시점에서 신경도관을 꺼내 건조시킨후 질량 변화를 특정함으로써 실시하였다. 질량변화는 다음과 같은 수학식 1로 계산된다.Biodegradability experiments were carried out with neuroconduits for 8 weeks in PBS solution at pH 7.4 with or without 10 μg / ml collagenase type I (Sigma, St. Louis, MO, USA). The neural conduit was taken out and dried at the point of time, followed by specifying the mass change. The mass change is calculated by the following equation (1).
여기서, Wf는 생분해된 후 도관의 무게이고 Wi는 생분해전 도관의 초기 무게이다. Where Wf is the weight of the conduit after biodegradation and Wi is the initial weight of the conduit before biodegradation.
도 6에 나타난 결과로부터 신경도관을 코팅하는 코팅액의 농도가 증가할수록 생분해 속도가 적어짐을 알 수 있었다. 그러나 가교된 신경도관은 코팅된 신경도관과 비교하여 생분해가 거의 일어나지 않았다.From the results shown in FIG. 6, it can be seen that the biodegradation rate decreases as the concentration of the coating solution coating the neural conduit increases. However, the crosslinked neural conduit showed little biodegradation compared to the coated neural conduit.
실시예 4: 기계적 성질 실험 Example 4 Mechanical Properties Experiment
기계적 성질은 만능시험기를 이용하여 코팅전 콜라젠 필름, 코팅후 콜라젠 필름, 가교된 콜라젠 필름을 1mm/min 속도로 끊어질 때까지 지그를 당겨 측정하였다. 코팅된 도관과 유사하게 실험하기 위하여 20 mm × 8 mm 콜라젠 필름 두개를 코팅된 부분이 바깥쪽 하여 겹쳐서 인장실험을 실시하였다. 코팅전 필름과 가교된 필름은 앞뒤 상관없이 두개를 겹쳐서 인장실험을 실시하였다. 기계적 성질은 탄성계수와 인장강도로 나타난다. 또한 신경도관이 건조한 상태와 습한 상태 모두에서 기계적 성질을 살펴보았다. Mechanical properties were measured by pulling the jig until the collagen film before coating, the collagen film after coating, the cross-linked collagen film was cut at a rate of 1mm / min using a universal testing machine. In order to experiment similarly to the coated conduit, two 20 mm × 8 mm collagen films were subjected to a tensile test by overlapping the coated parts to the outside. The pre-coated film and the crosslinked film were subjected to a tensile test by overlapping the two before and after. Mechanical properties are manifested by modulus of elasticity and tensile strength. We also examined the mechanical properties of both neural conduits in both dry and wet conditions.
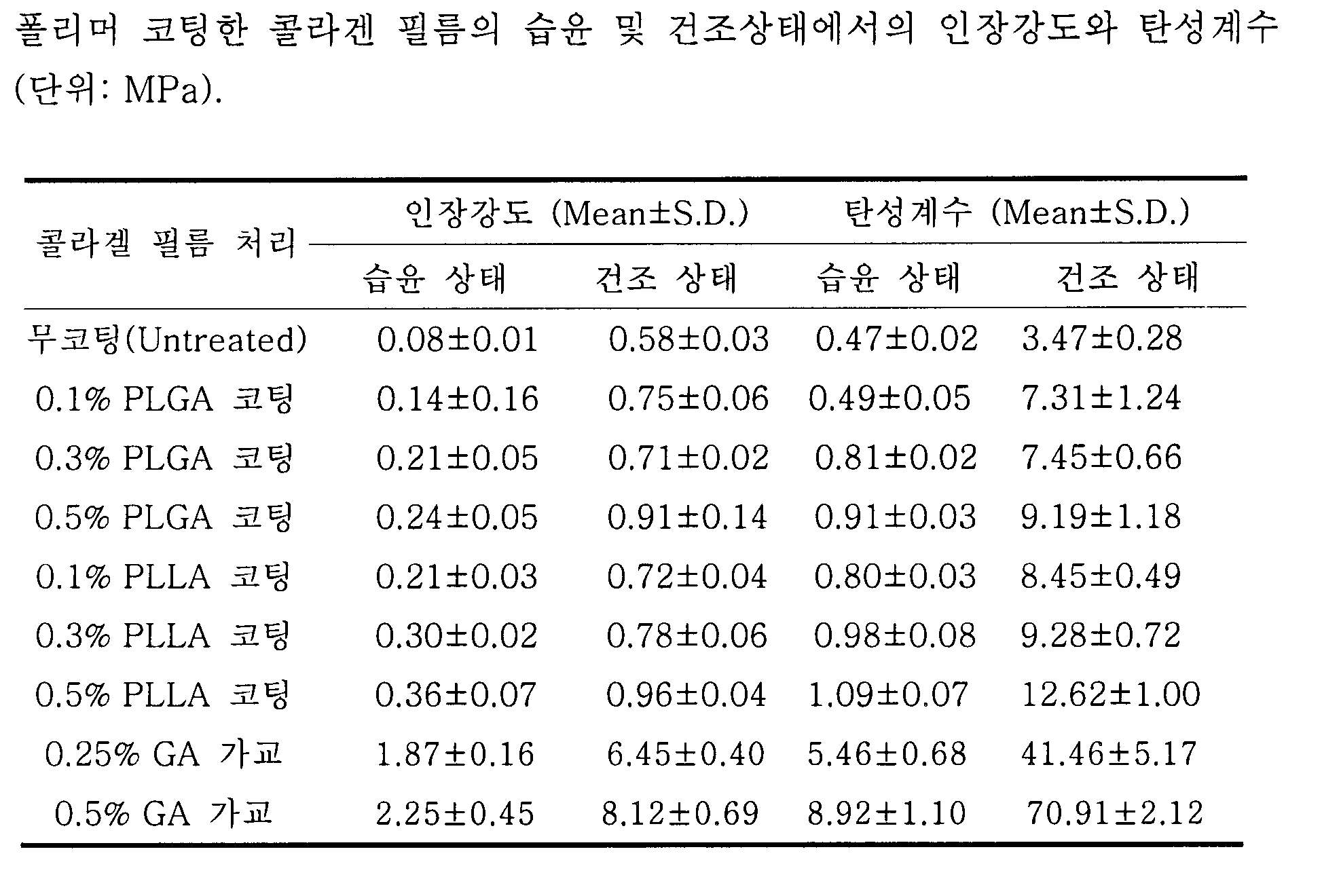
표 1, 도 7 및 도 8에 나타난 결과에서 알 수 있듯이 신경도관을 코팅하는 코팅액의 농도가 증가할수록 건조하거나 습한 상태에 상관없이 탄성계수와 인장강도가 증가하였다. 또한, 가교된 콜라젠 필름은 코팅된 콜라젠 필름보다 매우 큰 기계적 성질은 보여주었다. 그러나, 이렇게 큰 기계적 성질은 신경조직의 기계적 성질과 유사하지 않기 때문에 손상된 신경조직과 도관의 연결시 연결된 신경조직에 큰 응력을 주므로 신경재생에 좋지 않은 영향을 줄 것으로 생각되어 진다.As can be seen from the results shown in Table 1, 7 and 8, the elastic modulus and tensile strength increased as the concentration of the coating liquid coating the nerve conduit increased regardless of the dry or wet condition. In addition, the crosslinked collagen film showed much greater mechanical properties than the coated collagen film. However, such a large mechanical property is not similar to the mechanical properties of the neural tissue, so it is thought that it will adversely affect the nerve regeneration because it gives a great stress on the connected neural tissue when connecting the damaged and conduit.
상기 값은 평균 ± 표준편차(n=3)로 나타냄The values are expressed as mean ± standard deviation (n = 3).
실시예 5: 세포독성 실험 Example 5 : Cytotoxicity Experiment
세포독성 실험은 WST-1 분석법을 통하여 실시하였다. WST-1 분석법은 세포증식 능력이나 세포생존 능력을 발색 측정으로 정량화하여 세포 생존률을 측정하는 분석법으로 생세포 내의 미토콘드리아 탈수소효소에 의한 테트라졸리움 (tetrazolium)염 (WST-1)을 포르마잔(formazan) 색소로 변환시키는 정도에 따른 배지의 흡광도로 측정되어진다. 배지에 첨가한 테트라졸리움염은 미토콘드리아의 호흡사슬에 존재하며 생존세포에만 활성이 있는 쑤시네이트-테트라졸리옴-리덕테즈(succinate-tetrazolium-reductase: EC 1.3.99.1)에 의해 포르마잔 색소로 변환된다. 생세포수가 증가하면 시료 중의 미토콘드리아 탈수소효소의 전체의 활성이 증가하여 이 효소활성의 증가가 포르마잔 색소의 생성증가를 유도하기 때문에, 포르마잔 색소와 배지중의 대사활성이 있는 세포의 수와는 직선적인 상관관계를 나타내게 된다. 이 측정법은 세포를 세정하거나 결합할 필요가 없고, 미량배양의 개시에서 ELISA 리더에 의한 데이터 해석까지 동일한 마이크로필터 플레이드에서 시행할 수 있는 장점이 있다. 또 증식능력이나 약제감수성 측정법에서 세포증식과 생존능력을 non-RI로 분광광도계로 정량할 수도 있다.Cytotoxicity experiments were carried out through the WST-1 assay. WST-1 assay is a method of measuring cell viability by quantifying cell proliferation ability or cell viability by colorimetric measurement. Tetrazolium salt (WST-1) by mitochondrial dehydrogenase in living cells is transformed into formazan pigment. The absorbance of the medium depends on the degree of conversion. The tetrazolium salt added to the medium is converted into formazan pigment by succinate-tetrazolium-reductase (EC 1.3.99.1), which is present in the respiratory chain of mitochondria and is active only in living cells. . As the number of live cells increases, the activity of the entire mitochondrial dehydrogenase in the sample increases, which increases the production of formazan pigment, which is linear with the number of formazan pigment and metabolic cells in the medium. The correlation is This assay does not require washing or binding of cells, and has the advantage that it can be performed in the same microfilter plate from initiation of microculture to data interpretation by an ELISA reader. Cell proliferation and viability can also be quantified non-RI spectrophotometrically in proliferative or drug sensitivity assays.
코팅전 콜라젠 신경도관, 코팅된 콜라젠 신경도관, 가교된 콜라젠 신경도관을 증류수에 37℃에서 3일동안 용출한 후 이 용출액을 세포독성 실험을 위해서 사용하였다. 세포독성 실험에는 섬유모세포(L929)와 신경세포(PC12)를 사용하였다. L929 및 PC12는 KCLC (한국세포주은행)에서 구입하였으며, 10% Fetal Bovine Serum (FBS; Gibco, Grand Island, NY, USA) 과 1% 페니실리-스트렙토마이신 (PS; Gibco, Grand Island, NY, USA)이 첨가된 RPMI Medium 1640 (Gibco, Grand Island, NY, USA) 배지를 사용하여 37℃ 5% CO2 농도의 배양기 안에서 세포 배양하였다. 1×105 세포/ml의 농도를 가진 각각의 세포를 96 웰에서 하루동안 배양한 후 앞에서 준비 한 각각의 신경도관에 대한 용출액을 첨가하였다. 첨가 3일 후 WST-1 용액을 첨가하여 용액을 염색시킨 후 용액의 흡광도를 측정하였다. 각각의 신경도관에 대한 세포독성 실험은 5번씩 실시하고 평균을 냈다. 도 9에 의하면 코팅된 콜라젠 신경도관은 세포에 상관없이 코팅 전과 거의 같은 세포생존률을 보이므로 코팅된 생분해성 고분자에 의한 독성은 거의 없는 것으로 나타났다. 그러나 GA 가교된 콜라젠 신경도관은 코팅된 콜라젠 신경도관과 비교하여 매우 낮은 세포생존률을 보임에 따라 가교제로 사용된 GA에 의해 세포독성을 가지고 있음을 알 수 있었다. The collagen neural conduit, the coated collagen neural conduit, and the crosslinked collagen neural conduit before elution were eluted in distilled water at 37 ° C. for 3 days, and the eluate was used for cytotoxicity experiments. Fibroblasts (L929) and neurons (PC12) were used for cytotoxicity experiments. L929 and PC12 were purchased from KCLC (Korea Cell Line Bank), 10% Fetal Bovine Serum (FBS; Gibco, Grand Island, NY, USA) and 1% Penicilis-streptomycin (PS; Gibco, Grand Island, NY, USA) Cells were cultured in an incubator at 37 ° C. 5
실시예 6: 동물매식실험 Example 6 Animal Feeding Experiment
3 kg의 토끼 5마리를 염산케타민을 실험동물의 복강내로 주입하여 깊은 마취상태로 유도한 후, 수술 주위를 면도하고 요오드 스폰지를 이용하여 소독을 실시하였다. 실험동물을 엎드린 상태로 위치시킨 후, 뒤쪽 대퇴골에 평행하게 3cm 의 절개선을 주었다. 좌측좌골신경을 좌골절흔(sciatic notch)으로부터 오금부위까지 노출 시킨 후 약 15mm 길이의 신경을 절단하였다. 근심과 원심측의 신경 절단부를 17 mm 길이의 본 발명의 0.3% PLGA이 코팅된 신경도관에 연결하였다. 각 신경 절단부의 신경 1mm 정도가 도관앞으로 들어가도록 10-0 나일론을 이용하여 3 내지 4 부위에 봉합을 실시하였다. 봉합 후 준비되어진 콜라젠 젤을 도관내부에 주사기를 사용하여 삽입하였다. 모든 시술 후 삽입된 신경도관의 사진이 도 10(1)이다. 시술 부위를 잘 소독한 후 절대부위를 완전히 봉합한 후 12주 동안 토끼를 그대로 두 었다.Five rabbits of 3 kg were injected with ketamine hydrochloride into the intraperitoneal cavity of the experimental animals to induce deep anesthesia, and then the area around the surgery was shaved and sterilized using an iodine sponge. After placing the animal lying down, a 3 cm incision was made parallel to the posterior femur. The left sciatic nerve was exposed from the sciatic notch to the popliteal site, and the nerve of about 15 mm in length was cut. Nerve and distal nerve cuts were connected to a 17 mm long 0.3% PLGA coated neural conduit. Sutures were performed at 3 to 4 sites using 10-0 nylon so that about 1 mm of nerves in each nerve cutting portion entered the conduit. The collagen gel prepared after closure was inserted into the conduit using a syringe. A photograph of the neural conduit inserted after all procedures is shown in FIG. 10 (1). After disinfecting the site, the rabbit was left intact for 12 weeks after the absolute site was completely sealed.
6-1: 육안적 소견 6-1 : Visual findings
도 10(2)에서와 같이 신경도관을 이식한 수 12주가 경과한 뒤에 봉합부위를 재절개하여 개복하여 관찰한 결과 신경이 완전히 재생되었고 또한 매식되었던 신경도관은 완전히 생분해되어 육안으로 관찰되지 않았다.As shown in FIG. 10 (2), after 12 weeks after transplantation of the nerve conduits, the sutures were re-dissected and opened. The nerves were completely regenerated, and the nerve conduits that had been implanted were completely biodegraded and not visually observed.
6-2: 조직학적 검사 6-2 : Histological Examination
조직학적 검사를 실시하기 위하여 재생된 좌골신경을 박리하여 채취한 후, 2.5% G에 고정하였고, Epon에 포매시키고 마이크로절단기를 이용하여 0.5 μm 두께로 단면을 절단하였다. 각 조직편을 톨루이딘 블루를 이용하여 염색하였다. 준비된 슬라이드를 광학현미경과 전자현미경하에서 각각 관찰하였다. 도 11에서 보여지는 바와 같이 재생된 신경의 단면사진에서 잘 분포된 두꺼운 말이집으로 둘러싸인 축삭들이 많이 관찰되어졌다. 이러한 결과는 신경재생이 효과적으로 되었음을 의미한다.In order to perform histological examination, the regenerated sciatic nerve was removed and collected, fixed at 2.5% G, embedded in Epon, and cut into 0.5 μm thickness using a microcutter. Each tissue piece was stained using toluidine blue. The prepared slides were observed under an optical microscope and an electron microscope, respectively. As shown in FIG. 11, axons surrounded by a well-distributed thick horseshoe were observed in the cross-sectional view of the regenerated nerve. These results indicate that nerve regeneration was effective.
본 발명의 생분해성 고분자로 코팅된 콜라젠 도관은 가교제로 인한 독성을 가지고 않기 때문에 안전하고 분해 속도와 기계적 강도를 조절할 수 있는 생체적합한 도관으로써 수술, 종양 및 외상에 의하여 손상을 받은 신경의 재생에 효과적으로 사용 가능하다.Since the collagen conduit coated with the biodegradable polymer of the present invention has no toxicity due to the crosslinking agent, it is a safe and biocompatible conduit that can control the rate of decomposition and mechanical strength, and thus is effective for regeneration of nerves damaged by surgery, tumors and trauma. Can be used
Claims (14)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020040067269A KR100700674B1 (en) | 2004-08-25 | 2004-08-25 | Collagen Conduit Coated with Synthetic Biodegradable Polymer and Manufacturing Method |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020040067269A KR100700674B1 (en) | 2004-08-25 | 2004-08-25 | Collagen Conduit Coated with Synthetic Biodegradable Polymer and Manufacturing Method |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20060018752A true KR20060018752A (en) | 2006-03-02 |
| KR100700674B1 KR100700674B1 (en) | 2007-03-30 |
Family
ID=37126330
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020040067269A Expired - Fee Related KR100700674B1 (en) | 2004-08-25 | 2004-08-25 | Collagen Conduit Coated with Synthetic Biodegradable Polymer and Manufacturing Method |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR100700674B1 (en) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8758374B2 (en) | 2010-09-15 | 2014-06-24 | University Of Utah Research Foundation | Method for connecting nerves via a side-to-side epineurial window using artificial conduits |
| KR20150007576A (en) * | 2013-07-11 | 2015-01-21 | 단국대학교 천안캠퍼스 산학협력단 | Multi-channel nerve conduit comprising carbon nanotube coated phosphate glass fiber and preparation method thereof |
| US9931121B2 (en) | 2011-10-17 | 2018-04-03 | University Of Utah Research Foundation | Methods and devices for connecting nerves |
| US10842494B2 (en) | 2011-10-17 | 2020-11-24 | University Of Utah Research Foundation | Methods and devices for connecting nerves |
| CN117258043A (en) * | 2023-09-21 | 2023-12-22 | 苏州大学 | Preparation method of composite nerve conduit with outer braiding layer and inner layer penetrating through micro-channel structure |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100926678B1 (en) | 2007-12-17 | 2009-11-17 | 재단법인대구경북과학기술원 | Biodegradable plastic / nano fiber composite support neural conduit manufacturing method. |
| KR101671399B1 (en) * | 2014-12-31 | 2016-11-01 | 인하대학교 산학협력단 | Electrically conducting nerve regeneration-inducing tube coated with natural conductive material |
| KR101987783B1 (en) * | 2015-12-22 | 2019-06-13 | 주식회사 삼양바이오팜 | Biodegradable polymeric microparticle and method for preparing the same, and biodegradable polymeric filler comprising the same |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2280850B (en) | 1993-07-28 | 1997-07-30 | Johnson & Johnson Medical | Absorbable composite materials for use in the treatment of periodontal disease |
| US6001895A (en) | 1993-03-22 | 1999-12-14 | Johnson & Johnson Medical, Inc. | Composite surgical material |
| CA2334688A1 (en) * | 1998-06-10 | 1999-12-16 | Yasuhiko Shimizu | Artificial tube for nerve |
| KR100496354B1 (en) * | 2002-03-27 | 2005-06-20 | 서울산업대학교 산학협력단 | Hybrid Grafts Including Biodegradable Polymer Supporting Layer And Manufacturing Process Thereof |
| KR100488405B1 (en) * | 2002-05-07 | 2005-05-11 | 정필훈 | Bio-resorbable nerve conduit and method for preparing the same |
| JP2005525911A (en) * | 2002-05-20 | 2005-09-02 | オーバス メディカル テクノロジーズ インク. | Implantable drug eluting medical device |
-
2004
- 2004-08-25 KR KR1020040067269A patent/KR100700674B1/en not_active Expired - Fee Related
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8758374B2 (en) | 2010-09-15 | 2014-06-24 | University Of Utah Research Foundation | Method for connecting nerves via a side-to-side epineurial window using artificial conduits |
| US9931121B2 (en) | 2011-10-17 | 2018-04-03 | University Of Utah Research Foundation | Methods and devices for connecting nerves |
| US10772633B2 (en) | 2011-10-17 | 2020-09-15 | University Of Utah Research Foundation | Methods and devices for connecting nerves |
| US10842494B2 (en) | 2011-10-17 | 2020-11-24 | University Of Utah Research Foundation | Methods and devices for connecting nerves |
| KR20150007576A (en) * | 2013-07-11 | 2015-01-21 | 단국대학교 천안캠퍼스 산학협력단 | Multi-channel nerve conduit comprising carbon nanotube coated phosphate glass fiber and preparation method thereof |
| CN117258043A (en) * | 2023-09-21 | 2023-12-22 | 苏州大学 | Preparation method of composite nerve conduit with outer braiding layer and inner layer penetrating through micro-channel structure |
Also Published As
| Publication number | Publication date |
|---|---|
| KR100700674B1 (en) | 2007-03-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7550152B2 (en) | Tissue graft scaffold made from cholecyst-derived extracellular matrix | |
| US7084082B1 (en) | Collagen material and its production process | |
| US6761736B1 (en) | Medical article with a diamond-like carbon coated polymer | |
| EP0943346B1 (en) | Collagen laminate material and process for producing the same | |
| JP4526487B2 (en) | Implantable tubular prosthesis made of polytetrafluoroethylene | |
| Ahmed et al. | Multilayered peptide incorporated collagen tubules for peripheral nerve repair | |
| ES2325675T3 (en) | MEDICAL DEVICES WITH METAL / POLYMER COMPOSITE MATERIALS. | |
| JP5702515B2 (en) | Nerve regeneration induction tube | |
| JP2009515620A (en) | Nerve guide | |
| JP5518288B2 (en) | Anti-adhesion medical material | |
| KR100700674B1 (en) | Collagen Conduit Coated with Synthetic Biodegradable Polymer and Manufacturing Method | |
| US20090169593A1 (en) | Method of using and producing tropoelastin and tropoelastin biomaterials | |
| JP2022523406A (en) | Biodegradable mesh grafts for soft tissue repair, especially hernia repair | |
| CN102781490A (en) | Composite matrix | |
| JP2008100038A (en) | Laminin modified conduit for nerve regeneration, method for producing this conduit, and nerve regeneration method using this conduit | |
| Rizvi et al. | Peripheral nerve regeneration in the presence of collagen fibers: Effect of removal of the distal nerve stump | |
| KR102549899B1 (en) | Method for adjusting adhesive force of animal cartilage-derived extracellular matrix membrane and animal cartilage-derived extracellular matrix membrane having adjustable adhesive force by using the same | |
| Zhong et al. | The degradation of glycolic acid/lactic acid copolymer in vivo | |
| US20220387662A1 (en) | Biological tissue adhesive sheet, biological tissue reinforcement material kit, and method for producing biological tissue adhesive sheet | |
| Yang et al. | Surface modification and fibrovascular ingrowth of porous polyethylene anophthalmic implants | |
| Wasserman et al. | Clinical applications of electron microscopy in the analysis of collagenous biomaterials | |
| Bird et al. | In vivo degradation of collagen-vicryl materials in rabbit ear chambers | |
| AU724790B2 (en) | Tubular polytetrafluoroethylene implantable prostheses | |
| Jee et al. | Heparinized tissue matrices as novel biomaterials | |
| TWM451975U (en) | Neurorrhaphy catheter for amputated peripheral nerve |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| N231 | Notification of change of applicant | ||
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| FPAY | Annual fee payment |
Payment date: 20130322 Year of fee payment: 7 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| FPAY | Annual fee payment |
Payment date: 20140321 Year of fee payment: 8 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 8 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| LAPS | Lapse due to unpaid annual fee | ||
| PC1903 | Unpaid annual fee |
St.27 status event code: A-4-4-U10-U13-oth-PC1903 Not in force date: 20150322 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20150322 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |