KR102787034B1 - Organic optoelectronic device and display device - Google Patents
Organic optoelectronic device and display device Download PDFInfo
- Publication number
- KR102787034B1 KR102787034B1 KR1020230063961A KR20230063961A KR102787034B1 KR 102787034 B1 KR102787034 B1 KR 102787034B1 KR 1020230063961 A KR1020230063961 A KR 1020230063961A KR 20230063961 A KR20230063961 A KR 20230063961A KR 102787034 B1 KR102787034 B1 KR 102787034B1
- Authority
- KR
- South Korea
- Prior art keywords
- group
- substituted
- unsubstituted
- chemical formula
- independently
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/12—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
Landscapes
- Physics & Mathematics (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Organic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
서로 마주하는 양극과 음극, 상기 양극과 상기 음극 사이에 위치하는 발광층, 상기 양극과 상기 발광층 사이에 위치하는 정공수송층, 그리고 상기 발광층과 상기 정공수송층 사이에 위치하는 정공수송보조층을 포함하고,
상기 발광층은 화학식 1로 표현되는 제1 화합물 및 화학식 2로 표현되는 제2 화합물을 포함하는 조성물을 포함하고, 상기 정공수송보조층은 화학식 3으로 표현되는 제3 화합물을 포함하는 유기 광전자 소자 및 표시 장치에 관한 것이다.
상기 화학식 1 내지 화학식 3의 상세 내용은 명세서에서 정의한 바와 같다.It comprises an anode and a cathode facing each other, a light-emitting layer positioned between the anode and the cathode, a hole transport layer positioned between the anode and the light-emitting layer, and a hole transport auxiliary layer positioned between the light-emitting layer and the hole transport layer.
The present invention relates to an organic optoelectronic device and display device, wherein the light-emitting layer comprises a composition including a first compound represented by chemical formula 1 and a second compound represented by chemical formula 2, and the hole transport auxiliary layer comprises a third compound represented by chemical formula 3.
The details of the above chemical formulas 1 to 3 are as defined in the specification.
Description
유기 광전자 소자 및 표시 장치에 관한 것이다.It relates to organic optoelectronic devices and display devices.
유기 광전자 소자(organic optoelectronic diode)는 전기 에너지와 광 에너지를 상호 전환할 수 있는 소자이다.Organic optoelectronic diodes are devices that can convert electrical energy and light energy into each other.
유기 광전자 소자는 동작 원리에 따라 크게 두 가지로 나눌 수 있다. 하나는 광 에너지에 의해 형성된 엑시톤(exciton)이 전자와 정공으로 분리되고 전자와 정공이 각각 다른 전극으로 전달되면서 전기 에너지를 발생하는 광전 소자이고, 다른 하나는 전극에 전압 또는 전류를 공급하여 전기 에너지로부터 광 에너지를 발생하는 발광 소자이다. Organic optoelectronic devices can be broadly divided into two types based on their operating principles. One is a photoelectric device in which excitons formed by light energy are separated into electrons and holes, and the electrons and holes are transferred to different electrodes to generate electrical energy, and the other is a light-emitting device in which light energy is generated from electrical energy by supplying voltage or current to the electrode.
유기 광전자 소자의 예로는 유기 광전 소자, 유기 발광 소자, 유기 태양 전지 및 유기 감광체 드럼(organic photo conductor drum) 등을 들 수 있다. Examples of organic optoelectronic devices include organic photovoltaic devices, organic light-emitting devices, organic solar cells, and organic photo conductor drums.
이 중, 유기 발광 소자(organic light emitting diode, OLED)는 근래 평판 표시 장치(flat panel display device)의 수요 증가에 따라 크게 주목받고 있다. 유기 발광 소자는 전기 에너지를 빛으로 전환시키는 소자로서, 유기 발광 소자의 성능은 전극 사이에 위치하는 유기 재료에 의해 많은 영향을 받는다.Among these, organic light emitting diodes (OLEDs) have recently attracted significant attention due to the increasing demand for flat panel display devices. Organic light emitting diodes are devices that convert electrical energy into light, and the performance of organic light emitting diodes is greatly affected by the organic materials located between the electrodes.
일 구현예는 고효율 및 장수명 유기 광전자 소자를 제공한다.One embodiment provides a high-efficiency and long-life organic optoelectronic device.
다른 구현예는 상기 유기 광전자 소자를 포함하는 표시 장치를 제공한다.Another embodiment provides a display device including the organic optoelectronic device.
일 구현예에 따르면, 서로 마주하는 양극과 음극, 상기 양극과 상기 음극 사이에 위치하는 발광층, 상기 양극과 상기 발광층 사이에 위치하는 정공수송층, 그리고 상기 발광층과 상기 정공수송층 사이에 위치하는 정공수송보조층을 포함하고, 상기 발광층은 하기 화학식 1로 표현되는 제1 화합물 및 하기 화학식 2로 표현되는 제2 화합물을 포함하는 조성물을 포함하고, 상기 정공수송보조층은 하기 화학식 3으로 표현되는 제3 화합물을 포함하는 유기 광전자 소자를 제공한다.According to one embodiment, an organic optoelectronic device is provided, including an anode and a cathode facing each other, a light-emitting layer positioned between the anode and the cathode, a hole transport layer positioned between the anode and the light-emitting layer, and a hole transport auxiliary layer positioned between the light-emitting layer and the hole transport layer, wherein the light-emitting layer includes a composition including a first compound represented by the following chemical formula 1 and a second compound represented by the following chemical formula 2, and the hole transport auxiliary layer includes a third compound represented by the following chemical formula 3.
[화학식 1][Chemical Formula 1]
상기 화학식 1에서,In the above chemical formula 1,
L1 내지 L5는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,L 1 to L 5 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
Ar1은 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이고,Ar 1 is a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof,
R1 내지 R4는 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 할로겐, 시아노기 또는 이들의 조합이고,R 1 to R 4 are each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C30 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, a substituted or unsubstituted silyl group, a substituted or unsubstituted amine group, halogen, a cyano group or a combination thereof,
R1 내지 R4는 각각 독립적으로 존재하거나 인접한 기가 연결되어 치환 또는 비치환된 방향족의 단환식 또는 다환식 고리를 형성하고,R 1 to R 4 are each independently present or adjacent groups are connected to form a substituted or unsubstituted aromatic monocyclic or polycyclic ring,
Ar1 및 R1 내지 R4 중 적어도 하나는 하기 화학식 A로 표현되는 기이고,At least one of Ar 1 and R 1 to R 4 is a group represented by the following chemical formula A,
[화학식 A][Chemical Formula A]
상기 화학식 A에서,In the above chemical formula A,
Z1 내지 Z5는 각각 독립적으로 N 또는 C-La-Ra이고, Z 1 to Z 5 are each independently N or CL a -R a ,
Z1 내지 Z5 중 적어도 하나는 N이고,At least one of Z 1 to Z 5 is N,
여기서 La는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고, Here, L a is each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
Ra는 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 할로겐, 시아노기 또는 이들의 조합이고,R a is each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C30 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, a substituted or unsubstituted silyl group, a substituted or unsubstituted amine group, halogen, cyano group or a combination thereof,
Ra는 각각 독립적으로 존재하거나 인접한 기가 연결되어 치환 또는 비치환된 방향족의 단환식 또는 다환식 고리, 또는 치환 또는 비치환된 방향족의 단환식 또는 다환식 헤테로고리를 형성하고,R a each independently exists or is connected to an adjacent group to form a substituted or unsubstituted aromatic monocyclic or polycyclic ring, or a substituted or unsubstituted aromatic monocyclic or polycyclic heterocycle,
*는 L1 내지 L5와의 연결 지점이고;* is the connection point with L 1 to L 5 ;
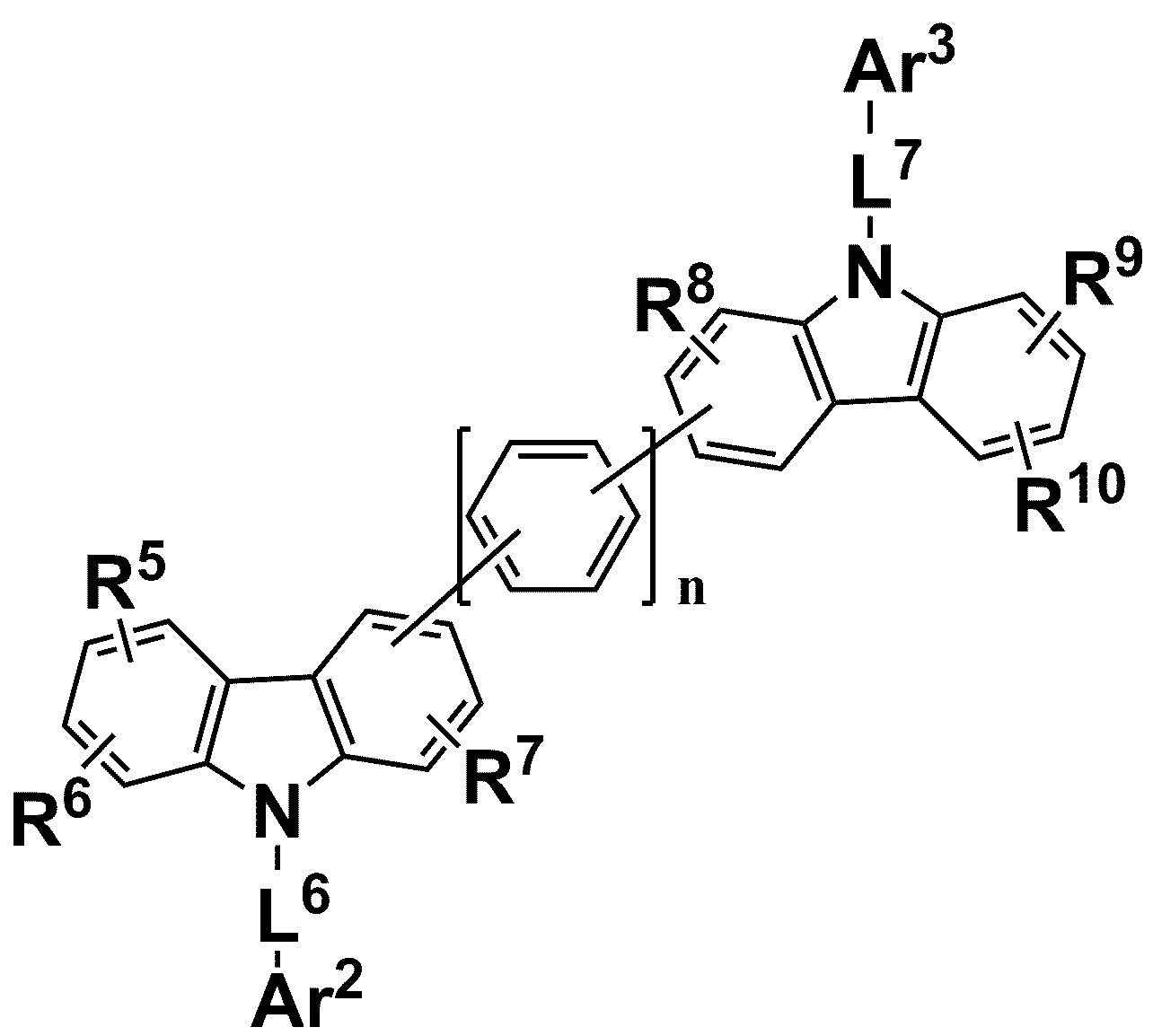
[화학식 2][Chemical formula 2]
상기 화학식 2에서,In the above chemical formula 2,
Ar2 및 Ar3은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기 또는 이들의 조합이고,Ar 2 and Ar 3 are each independently a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heteroaryl group, or a combination thereof,
L6 및 L7은 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,L 6 and L 7 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
R5 내지 R10은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 또는 이들의 조합이고,R 5 to R 10 are each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted C1 to C30 alkyl group, substituted or unsubstituted C6 to C30 aryl group or a combination thereof,
n은 0 내지 2의 정수 중 하나이고;n is an integer between 0 and 2;
[화학식 3][Chemical Formula 3]
상기 화학식 3에서,In the above chemical formula 3,
L8 및 L9는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,L 8 and L 9 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
R11 내지 R14는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 또는 이들의 조합이고,R 11 to R 14 are each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted C1 to C30 alkyl group, substituted or unsubstituted C6 to C30 aryl group, or a combination thereof,
Ar4 내지 Ar7은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이다.Ar 4 to Ar 7 are each independently a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof.
다른 구현예에 따르면, 상기 유기 광전자 소자를 포함하는 표시 장치를 제공한다.According to another embodiment, a display device including the organic optoelectronic device is provided.
고효율 장수명 유기 광전자 소자를 구현할 수 있다.High-efficiency, long-life organic optoelectronic devices can be realized.
도 1은 일 구현예에 따른 유기 광전자 소자를 개략적으로 도시한 단면도이다.FIG. 1 is a cross-sectional view schematically illustrating an organic optoelectronic device according to one embodiment.
이하, 본 발명의 구현예를 상세히 설명하기로 한다. 다만, 이는 예시로서 제시되는 것으로, 이에 의해 본 발명이 제한되지는 않으며 본 발명은 후술할 청구범위의 범주에 의해 정의될 뿐이다.Hereinafter, embodiments of the present invention will be described in detail. However, these are presented as examples, and the present invention is not limited thereby, and the present invention is defined only by the scope of the claims described below.
본 명세서에서 "치환"이란 별도의 정의가 없는 한, 치환기 또는 화합물 중의 적어도 하나의 수소가 중수소, 할로겐기, 히드록실기, 아미노기, 치환 또는 비치환된 C1 내지 C30 아민기, 니트로기, 치환 또는 비치환된 C1 내지 C40 실릴기, C1 내지 C30 알킬기, C1 내지 C10 알킬실릴기, C6 내지 C30 아릴실릴기, C3 내지 C30 시클로알킬기, C3 내지 C30 헤테로시클로알킬기, C6 내지 C30 아릴기, C2 내지 C30 헤테로아릴기, C1 내지 C20 알콕시기, C1 내지 C10 트리플루오로알킬기, 시아노기, 또는 이들의 조합으로 치환된 것을 의미한다. As used herein, unless otherwise defined, the term "substituted" means that at least one hydrogen in a substituent or compound is substituted with deuterium, a halogen group, a hydroxyl group, an amino group, a substituted or unsubstituted C1 to C30 amine group, a nitro group, a substituted or unsubstituted C1 to C40 silyl group, a C1 to C30 alkyl group, a C1 to C10 alkylsilyl group, a C6 to C30 arylsilyl group, a C3 to C30 cycloalkyl group, a C3 to C30 heterocycloalkyl group, a C6 to C30 aryl group, a C2 to C30 heteroaryl group, a C1 to C20 alkoxy group, a C1 to C10 trifluoroalkyl group, a cyano group, or a combination thereof.
본 발명의 일 예에서, "치환"은 치환기 또는 화합물 중의 적어도 하나의 수소가 중수소, C1 내지 C30 알킬기, C1 내지 C10 알킬실릴기, C6 내지 C30 아릴실릴기, C3 내지 C30 시클로알킬기, C3 내지 C30 헤테로시클로알킬기, C6 내지 C30 아릴기, C2 내지 C30 헤테로아릴기로 치환된 것을 의미한다. 또한, 본 발명의 구체적인 일 예에서, "치환"은 치환기 또는 화합물 중의 적어도 하나의 수소가 중수소, C1 내지 C20 알킬기, C6 내지 C30 아릴기, 또는 C2 내지 C30 헤테로아릴기로 치환된 것을 의미한다. 또한, 본 발명의 구체적인 일 예에서, "치환"은 치환기 또는 화합물 중의 적어도 하나의 수소가 중수소, C1 내지 C5 알킬기, C6 내지 C18 아릴기, 피리디닐기, 퀴놀리닐기, 이소퀴놀리닐기, 디벤조퓨란일기, 디벤조티오펜일기 또는 카바졸일기로 치환된 것을 의미한다. 또한, 본 발명의 구체적인 일 예에서, "치환"은 치환기 또는 화합물 중의 적어도 하나의 수소가 중수소, C1 내지 C5 알킬기, C6 내지 C18 아릴기, 디벤조퓨란일기 또는 디벤조티오펜일기로 치환된 것을 의미한다. 또한, 본 발명의 구체적인 일 예에서, "치환"은 치환기 또는 화합물 중의 적어도 하나의 수소가 중수소, 메틸기, 에틸기, 프로판일기, 부틸기, 페닐기, 바이페닐기, 터페닐기, 나프틸기, 트리페닐기, 디벤조퓨란일기 또는 디벤조티오펜일기로 치환된 것을 의미한다. In one embodiment of the present invention, "substitution" means that at least one hydrogen in a substituent or a compound is substituted with deuterium, a C1 to C30 alkyl group, a C1 to C10 alkylsilyl group, a C6 to C30 arylsilyl group, a C3 to C30 cycloalkyl group, a C3 to C30 heterocycloalkyl group, a C6 to C30 aryl group, or a C2 to C30 heteroaryl group. In addition, in one specific embodiment of the present invention, "substitution" means that at least one hydrogen in a substituent or a compound is substituted with deuterium, a C1 to C20 alkyl group, a C6 to C30 aryl group, or a C2 to C30 heteroaryl group. In addition, in a specific example of the present invention, "substitution" means that at least one hydrogen in a substituent or a compound is substituted with deuterium, a C1 to C5 alkyl group, a C6 to C18 aryl group, a pyridinyl group, a quinolinyl group, an isoquinolinyl group, a dibenzofuranyl group, a dibenzothiophenyl group, or a carbazolyl group. In addition, in a specific example of the present invention, "substitution" means that at least one hydrogen in a substituent or a compound is substituted with deuterium, a C1 to C5 alkyl group, a C6 to C18 aryl group, a dibenzofuranyl group, or a dibenzothiophenyl group. Also, in a specific example of the present invention, "substitution" means that at least one hydrogen in a substituent or compound is replaced with deuterium, a methyl group, an ethyl group, a propanyl group, a butyl group, a phenyl group, a biphenyl group, a terphenyl group, a naphthyl group, a triphenyl group, a dibenzofuranyl group, or a dibenzothiophenyl group.
본 명세서에서 "헤테로"란 별도의 정의가 없는 한, 하나의 작용기 내에 N, O, S, P 및 Si로 이루어진 군에서 선택되는 헤테로 원자를 1 내지 3개 함유하고, 나머지는 탄소인 것을 의미한다.As used herein, unless otherwise defined, "hetero" means containing 1 to 3 heteroatoms selected from the group consisting of N, O, S, P, and Si in one functional group, and the remainder being carbon.
본 명세서에서 "아릴(aryl)기"는 탄화수소 방향족 모이어티를 하나 이상 갖는 그룹을 총괄하는 개념으로서, 탄화수소 방향족 모이어티의 모든 원소가 p-오비탈을 가지면서, 이들 p-오비탈이 공액(conjugation)을 형성하고 있는 형태, 예컨대 페닐기, 나프틸기 등을 포함하고, 2 이상의 탄화수소 방향족 모이어티들이 시그마 결합을 통하여 연결된 형태, 예컨대 바이페닐기, 터페닐기, 쿼터페닐기 등을 포함하며, 2 이상의 탄화수소 방향족 모이어티들이 직접 또는 간접적으로 융합된 비방향족 융합 고리, 예컨대 플루오레닐기 등을 포함할 수 있다.In this specification, "aryl group" is a concept that encompasses a group having one or more hydrocarbon aromatic moieties, and includes a form in which all elements of the hydrocarbon aromatic moieties have p-orbitals and these p-orbitals form conjugation, such as a phenyl group, a naphthyl group, etc., a form in which two or more hydrocarbon aromatic moieties are connected via a sigma bond, such as a biphenyl group, a terphenyl group, a quarterphenyl group, etc., and a non-aromatic fused ring in which two or more hydrocarbon aromatic moieties are directly or indirectly fused, such as a fluorenyl group, etc.
아릴기는 모노시클릭, 폴리시클릭 또는 융합 고리 폴리시클릭(즉, 탄소원자들의 인접한 쌍들을 나눠 가지는 고리) 작용기를 포함한다.Aryl groups include monocyclic, polycyclic, or fused ring polycyclic (i.e., rings that share adjacent pairs of carbon atoms) functional groups.
본 명세서에서 "헤테로고리기(heterocyclic group)"는 헤테로아릴기를 포함하는 상위 개념으로서, 아릴기, 시클로알킬기, 이들의 융합고리 또는 이들의 조합과 같은 고리 화합물 내에 탄소 (C) 대신 N, O, S, P 및 Si로 이루어진 군에서 선택되는 헤테로 원자를 적어도 한 개를 함유하는 것을 의미한다. 상기 헤테로고리기가 융합고리인 경우, 상기 헤테로고리기 전체 또는 각각의 고리마다 헤테로 원자를 한 개 이상 포함할 수 있다.In this specification, the "heterocyclic group" is a superior concept including a heteroaryl group, and means a group containing at least one heteroatom selected from the group consisting of N, O, S, P, and Si instead of carbon (C) in a ring compound such as an aryl group, a cycloalkyl group, a fused ring thereof, or a combination thereof. When the heterocyclic group is a fused ring, the heterocyclic group as a whole or each ring may contain one or more heteroatoms.
일 예로 "헤테로아릴(heteroaryl)기"는 아릴기 내에 N, O, S, P 및 Si로 이루어진 군에서 선택되는 헤테로 원자를 적어도 한 개를 함유하는 것을 의미한다. 2 이상의 헤테로아릴기는 시그마 결합을 통하여 직접 연결되거나, 상기 헤테로아릴기가 2 이상의 고리를 포함할 경우, 2 이상의 고리들은 서로 융합될 수 있다. 상기 헤테로아릴기가 융합고리인 경우, 각각의 고리마다 상기 헤테로 원자를 1 내지 3개 포함할 수 있다.For example, a "heteroaryl group" means an aryl group containing at least one heteroatom selected from the group consisting of N, O, S, P, and Si. Two or more heteroaryl groups may be directly connected via a sigma bond, or, when the heteroaryl group includes two or more rings, the two or more rings may be fused to each other. When the heteroaryl group is a fused ring, each ring may contain 1 to 3 of the heteroatoms.
보다 구체적으로, 치환 또는 비치환된 C6 내지 C30 아릴기는, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트레닐기, 치환 또는 비치환된 나프타세닐기, 치환 또는 비치환된 피레닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 p-터페닐기, 치환 또는 비치환된 m-터페닐기, 치환 또는 비치환된 o-터페닐기, 치환 또는 비치환된 크리세닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 페릴레닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 인데닐기, 또는 이들의 조합일 수 있으나, 이에 제한되지는 않는다.More specifically, the substituted or unsubstituted C6 to C30 aryl group may be, but is not limited to, a substituted or unsubstituted phenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted anthracenyl group, a substituted or unsubstituted phenanthrenyl group, a substituted or unsubstituted naphthacenyl group, a substituted or unsubstituted pyrenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted p-terphenyl group, a substituted or unsubstituted m-terphenyl group, a substituted or unsubstituted o-terphenyl group, a substituted or unsubstituted chrysenyl group, a substituted or unsubstituted triphenylene group, a substituted or unsubstituted perylenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted indenyl group, or a combination thereof.
보다 구체적으로, 치환 또는 비치환된 C2 내지 C30 헤테로고리기는, 치환 또는 비치환된 퓨라닐기, 치환 또는 비치환된 티오페닐기, 치환 또는 비치환된 피롤릴기, 치환 또는 비치환된 피라졸릴기, 치환 또는 비치환된 이미다졸일기, 치환 또는 비치환된 트리아졸일기, 치환 또는 비치환된 옥사졸일기, 치환 또는 비치환된 티아졸일기, 치환 또는 비치환된 옥사디아졸일기, 치환 또는 비치환된 티아디아졸일기, 치환 또는 비치환된 피리딜기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 벤조퓨라닐기, 치환 또는 비치환된 벤조티오페닐기, 치환 또는 비치환된 벤즈이미다졸일기, 치환 또는 비치환된 인돌일기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 나프티리디닐기, 치환 또는 비치환된 벤즈옥사진일기, 치환 또는 비치환된 벤즈티아진일기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페나진일기, 치환 또는 비치환된 페노티아진일기, 치환 또는 비치환된 페녹사진일기, 치환 또는 비치환된 디벤조퓨란일기, 또는 치환 또는 비치환된 디벤조티오펜일기, 또는 이들의 조합일 수 있으나, 이에 제한되지는 않는다.More specifically, the substituted or unsubstituted C2 to C30 heterocyclic group is selected from the group consisting of a substituted or unsubstituted furanyl group, a substituted or unsubstituted thiophenyl group, a substituted or unsubstituted pyrrolyl group, a substituted or unsubstituted pyrazolyl group, a substituted or unsubstituted imidazolyl group, a substituted or unsubstituted triazolyl group, a substituted or unsubstituted oxazolyl group, a substituted or unsubstituted thiazolyl group, a substituted or unsubstituted oxadiazolyl group, a substituted or unsubstituted thiadiazolyl group, a substituted or unsubstituted pyridyl group, a substituted or unsubstituted pyrimidinyl group, a substituted or unsubstituted pyrazinyl group, a substituted or unsubstituted triazinyl group, a substituted or unsubstituted benzofuranyl group, a substituted or unsubstituted benzothiophenyl group, a substituted or unsubstituted benzimidazolyl group, a substituted or unsubstituted indolyl group, a substituted or unsubstituted quinolinyl group, a substituted or unsubstituted An isoquinolinyl group, a substituted or unsubstituted quinazolinyl group, a substituted or unsubstituted quinoxalinyl group, a substituted or unsubstituted naphthyridinyl group, a substituted or unsubstituted benzoxazinyl group, a substituted or unsubstituted benzthiazinyl group, a substituted or unsubstituted acridinyl group, a substituted or unsubstituted phenazinyl group, a substituted or unsubstituted phenothiazinyl group, a substituted or unsubstituted phenoxazinyl group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group, or a combination thereof, may be, but is not limited thereto.
본 명세서에서, 정공 특성이란, 전기장(electric field)을 가했을 때 전자를 공여하여 정공을 형성할 수 있는 특성을 말하는 것으로, HOMO 준위를 따라 전도 특성을 가져 양극에서 형성된 정공의 발광층으로의 주입, 발광층에서 형성된 정공의 양극으로의 이동 및 발광층에서의 이동을 용이하게 하는 특성을 의미한다. In this specification, the hole characteristic refers to a characteristic that can form holes by donating electrons when an electric field is applied, and has a conductive characteristic along the HOMO level, which means a characteristic that facilitates the injection of holes formed at the anode into the light-emitting layer, the movement of holes formed in the light-emitting layer to the anode, and the movement in the light-emitting layer.
또한 전자 특성이란, 전기장을 가했을 때 전자를 받을 수 있는 특성을 말하는 것으로, LUMO 준위를 따라 전도 특성을 가져 음극에서 형성된 전자의 발광층으로의 주입, 발광층에서 형성된 전자의 음극으로의 이동 및 발광층에서의 이동을 용이하게 하는 특성을 의미한다. In addition, electronic properties refer to the property of being able to receive electrons when an electric field is applied, and have conductive properties along the LUMO level, which means the property of facilitating the injection of electrons formed at the cathode into the light-emitting layer, the movement of electrons formed in the light-emitting layer to the cathode, and the movement in the light-emitting layer.
이하 일 구현예에 따른 유기 광전자 소자에 대하여 설명한다.An organic optoelectronic device according to an embodiment of the present invention is described below.
상기 유기 광전자 소자는 전기 에너지와 광 에너지를 상호 전환할 수 있는 소자이면 특별히 한정되지 않으며, 예컨대 유기 광전 소자, 유기 발광 소자, 유기 태양 전지 및 유기 감광체 드럼 등을 들 수 있다.The above organic optoelectronic device is not particularly limited as long as it is a device capable of converting electrical energy and optical energy into each other, and examples thereof include organic photoelectric devices, organic light-emitting devices, organic solar cells, and organic photosensitive drums.
여기서는 유기 광전자 소자의 일 예인 유기 발광 소자를 예시적으로 설명하지만, 이에 한정되지 않고 다른 유기 광전자 소자에도 동일하게 적용될 수 있다.Here, an organic light-emitting device, which is an example of an organic optoelectronic device, is described as an example, but it is not limited thereto and can be equally applied to other organic optoelectronic devices.
도면에서 여러 층 및 영역을 명확하게 표현하기 위하여 두께를 확대하여 나타내었다. 명세서 전체를 통하여 유사한 부분에 대해서는 동일한 도면 부호를 붙였다. 층, 막, 영역, 판 등의 부분이 다른 부분 "위에" 있다고 할 때, 이는 다른 부분 "바로 위에" 있는 경우 뿐만 아니라 그 중간에 또 다른 부분이 있는 경우도 포함한다. 반대로 어떤 부분이 다른 부분 "바로 위에" 있다고 할 때에는 중간에 다른 부분이 없는 것을 뜻한다.In order to clearly express various layers and regions in the drawings, the thickness is enlarged and shown. Similar parts are designated by the same drawing reference numerals throughout the specification. When a part such as a layer, film, region, or plate is said to be "on" another part, this includes not only the case where it is "directly on" the other part, but also the case where there is another part in between. Conversely, when a part is said to be "directly on" another part, it means that there is no other part in between.
도 1은 일 구현예에 따른 유기 발광 소자를 개략적으로 도시한 단면도이다.FIG. 1 is a cross-sectional view schematically illustrating an organic light-emitting device according to one embodiment.
도 1을 참고하면, 일 구현예에 따른 유기 발광 소자(300)는 서로 마주하는 양극(110)과 음극(120), 그리고 양극(110)과 음극(120) 사이에 위치하는 유기층(105)을 포함하고, 유기층(105)은 발광층(130), 정공수송보조층(142) 및 정공수송층(141)을 포함한다.Referring to FIG. 1, an organic light-emitting device (300) according to one embodiment includes an anode (110) and a cathode (120) facing each other, and an organic layer (105) positioned between the anode (110) and the cathode (120), and the organic layer (105) includes a light-emitting layer (130), a hole transport auxiliary layer (142), and a hole transport layer (141).
양극(110)은 예컨대 정공 주입이 원활하도록 일 함수가 높은 도전체로 만들어질 수 있으며, 예컨대 금속, 금속 산화물 및/또는 도전성 고분자로 만들어질 수 있다. 애노드(110)는 예컨대 니켈, 백금, 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금; 아연산화물, 인듐산화물, 인듐주석산화물(ITO), 인듐아연산화물(IZO)과 같은 금속 산화물; ZnO와 Al 또는 SnO2와 Sb와 같은 금속과 산화물의 조합; 폴리(3-메틸티오펜), 폴리(3,4-(에틸렌-1,2-디옥시)티오펜)(polyehtylenedioxythiophene: PEDOT), 폴리피롤 및 폴리아닐린과 같은 도전성 고분자 등을 들 수 있으나, 이에 한정되는 것은 아니다. The anode (110) can be made of a conductor having a high work function, for example, to facilitate hole injection, and can be made of, for example, a metal, a metal oxide, and/or a conductive polymer. The anode (110) may include, but is not limited to, a metal such as nickel, platinum, vanadium, chromium, copper, zinc, or gold, or an alloy thereof; a metal oxide such as zinc oxide, indium oxide, indium tin oxide (ITO), or indium zinc oxide (IZO); a combination of a metal and an oxide such as ZnO and Al or SnO 2 and Sb; a conductive polymer such as poly(3-methylthiophene), poly(3,4-(ethylene-1,2-dioxy)thiophene) (polyehtylenedioxythiophene: PEDOT), polypyrrole, and polyaniline.
음극(120)은 예컨대 전자 주입이 원활하도록 일 함수가 낮은 도전체로 만들어질 수 있으며, 예컨대 금속, 금속 산화물 및/또는 도전성 고분자로 만들어질 수 있다. 음극(120)은 예컨대 마그네슘, 칼슘, 나트륨, 칼륨, 타이타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석, 납, 세슘, 바륨 등과 같은 금속 또는 이들의 합금; LiF/Al, LiO2/Al, LiF/Ca, LiF/Al 및 BaF2/Ca과 같은 다층 구조 물질을 들 수 있으나, 이에 한정되는 것은 아니다. The cathode (120) can be made of a conductor having a low work function, for example, to facilitate electron injection, and can be made of, for example, a metal, a metal oxide, and/or a conductive polymer. The cathode (120) can be, for example, a metal such as magnesium, calcium, sodium, potassium, titanium, indium, yttrium, lithium, gadolinium, aluminum, silver, tin, lead, cesium, barium, or an alloy thereof; a multilayer structure material such as LiF/Al, LiO 2 /Al, LiF/Ca, LiF/Al, and BaF 2 /Ca, but is not limited thereto.
발광층(130)은 양극(110)과 음극(120) 사이에 위치하며, 복수의 호스트(host)와 적어도 한 종류의 도펀트(dopant)를 포함한다.The light-emitting layer (130) is located between the anode (110) and the cathode (120) and includes a plurality of hosts and at least one type of dopant.
발광층(130)은 호스트로서 전자 특성이 상대적으로 강한 제1 화합물과 정공 특성이 상대적으로 강한 제2 화합물을 함께 포함할 수 있으며, 상기 호스트는 제1 화합물과 제2 화합물을 포함하는 조성물일 수 있다.The light-emitting layer (130) may include a first compound having relatively strong electron properties as a host and a second compound having relatively strong hole properties, and the host may be a composition including the first compound and the second compound.
정공수송보조층(142)은 발광층(130)과 후술하는 정공수송층(141) 사이에 위치하고 발광층(130)에 접하여 위치함으로써 발광층(130)과 정공 수송층(141)의 계면에서 정공의 이동도를 세밀하게 제어할 수 있다. 정공수송보조층(142)은 제3 화합물을 포함할 수 있으며, 복수 층을 포함할 수도 있다.The hole transport auxiliary layer (142) is positioned between the light-emitting layer (130) and the hole transport layer (141) described below and is positioned in contact with the light-emitting layer (130), thereby enabling fine control of hole mobility at the interface between the light-emitting layer (130) and the hole transport layer (141). The hole transport auxiliary layer (142) may include a third compound and may also include multiple layers.
제1 화합물은 전자 특성이 상대적으로 강한 화합물로, 하기 화학식 1로 표현될 수 있다.The first compound is a compound with relatively strong electronic properties and can be expressed by the following chemical formula 1.
[화학식 1][Chemical Formula 1]
상기 화학식 1에서,In the above chemical formula 1,
L1 내지 L5는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,L 1 to L 5 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
Ar1은 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이고,Ar 1 is a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof,
R1 내지 R4는 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 할로겐, 시아노기 또는 이들의 조합이고,R 1 to R 4 are each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C30 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, a substituted or unsubstituted silyl group, a substituted or unsubstituted amine group, halogen, a cyano group or a combination thereof,
R1 내지 R4는 각각 독립적으로 존재하거나 인접한 기가 연결되어 치환 또는 비치환된 방향족의 단환식 또는 다환식 고리를 형성하고,R 1 to R 4 are each independently present or adjacent groups are connected to form a substituted or unsubstituted aromatic monocyclic or polycyclic ring,
Ar1 및 R1 내지 R4 중 적어도 하나는 하기 화학식 A로 표현되는 기이고,At least one of Ar 1 and R 1 to R 4 is a group represented by the following chemical formula A,
[화학식 A][Chemical Formula A]
상기 화학식 A에서,In the above chemical formula A,
Z1 내지 Z5는 각각 독립적으로 N 또는 C-La-Ra이고, Z 1 to Z 5 are each independently N or CL a -R a ,
Z1 내지 Z5 중 적어도 하나는 N이고,At least one of Z 1 to Z 5 is N,
여기서 La는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고, Here, L a is each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
Ra는 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 할로겐, 시아노기 또는 이들의 조합이고,R a is each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C30 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, a substituted or unsubstituted silyl group, a substituted or unsubstituted amine group, halogen, cyano group or a combination thereof,
Ra는 각각 독립적으로 존재하거나 인접한 기가 연결되어 치환 또는 비치환된 방향족의 단환식 또는 다환식 고리, 또는 치환 또는 비치환된 방향족의 단환식 또는 다환식 헤테로고리를 형성하고,R a each independently exists or is connected to an adjacent group to form a substituted or unsubstituted aromatic monocyclic or polycyclic ring, or a substituted or unsubstituted aromatic monocyclic or polycyclic heterocycle,
*는 L1 내지 L5와의 연결 지점이다.* is the connection point with L 1 to L 5 .
제2 화합물은 정공 특성이 상대적으로 강한 화합물로, 하기 화학식 2로 표현될 수 있다.The second compound is a compound with relatively strong hole properties and can be expressed by the following chemical formula 2.
[화학식 2][Chemical formula 2]
상기 화학식 2에서,In the above chemical formula 2,
Ar2 및 Ar3은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기 또는 이들의 조합이고,Ar 2 and Ar 3 are each independently a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heteroaryl group, or a combination thereof,
L6 및 L7은 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,L 6 and L 7 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
R5 내지 R10은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 또는 이들의 조합이고,R 5 to R 10 are each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted C1 to C30 alkyl group, substituted or unsubstituted C6 to C30 aryl group or a combination thereof,
n은 0 내지 2의 정수 중 하나이다.n is an integer between 0 and 2.
제3 화합물은 정공수송보조층(142)에 포함되어 발광층(130)과 정공 수송층(141)의 계면에서 정공의 이동도를 세밀하게 제어하는 화합물로, 하기 화학식 3으로 표현될 수 있다.The third compound is a compound that is included in the hole transport auxiliary layer (142) and precisely controls the mobility of holes at the interface between the light-emitting layer (130) and the hole transport layer (141), and can be expressed by the following chemical formula 3.
[화학식 3][Chemical Formula 3]
상기 화학식 3에서,In the above chemical formula 3,
L8 및 L9는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,L 8 and L 9 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
R11 내지 R14는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 또는 이들의 조합이고,R 11 to R 14 are each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted C1 to C30 alkyl group, substituted or unsubstituted C6 to C30 aryl group, or a combination thereof,
Ar4 내지 Ar7은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이다.Ar 4 to Ar 7 are each independently a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof.
제1 화합물은 전기장을 걸었을 때 정공과 전자를 모두 받을 수 있는 특성, 즉 바이폴라 특성을 가지는 화합물로, 구체적으로 카바졸 코어에 질소를 함유하는 고리, 예컨대 피리미딘, 트리아진 등이 치환됨으로써 분자량 대비 유리 전이 온도가 향상되는 효과가 있으므로, 내열성이 확보될 수 있다. 이와 함께, 제2 호스트로서 바이카바졸 화합물을 조합함으로써, 빠르고 안정한 전자 전달 특성을 갖는 제1 호스트 재료와 빠르고 안정한 정공 전달 특성을 갖는 제2 호스트 재료로써 소자 내 정공과 전자의 균형을 맞출 수 있다.The first compound is a compound having a property of accepting both holes and electrons when an electric field is applied, that is, a bipolar property. Specifically, since a nitrogen-containing ring, such as pyrimidine or triazine, is substituted in the carbazole core, the glass transition temperature is improved relative to the molecular weight, so that heat resistance can be secured. In addition, by combining a bicarbazole compound as the second host, the first host material having fast and stable electron transfer properties and the second host material having fast and stable hole transfer properties can be used to balance holes and electrons in the device.
뿐만 아니라 정공수송보조층에 제3 화합물과 같은 화합물을 적용함으로써 정공수송층과 발광층 사이의 계면에 정공 또는 전자가 축적되는 것을 방지하고 전하의 밸런스를 높일 수 있다. 따라서 유기 광전자 소자의 구동 전압 및 수명 특성을 현저히 개선시킬 수 있다. In addition, by applying a compound such as the third compound to the hole transport auxiliary layer, it is possible to prevent holes or electrons from accumulating at the interface between the hole transport layer and the light-emitting layer and to improve charge balance. Accordingly, the driving voltage and life characteristics of the organic optoelectronic device can be significantly improved.
일 예로, 상기 화학식 1에서, L1 내지 L5는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기 또는 치환 또는 비치환된 C2 내지 C20 헤테로고리기일 수 있다.For example, in the chemical formula 1, L 1 to L 5 can each independently be a single bond, a substituted or unsubstituted C6 to C20 arylene group, or a substituted or unsubstituted C2 to C20 heterocyclic group.
일 예로, L1 내지 L5는 각각 독립적으로 단일 결합, 치환 또는 비치환된 페닐렌기, 치환 또는 비치환된 바이페닐렌기, 치환 또는 비치환된 터페닐렌기, 치환 또는 비치환된 나프틸렌기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기일 수 있다.For example, L 1 to L 5 can each independently be a single bond, a substituted or unsubstituted phenylene group, a substituted or unsubstituted biphenylene group, a substituted or unsubstituted terphenylene group, a substituted or unsubstituted naphthylene group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group.
예컨대 L1 내지 L5는 각각 독립적으로 단일 결합, 치환 또는 비치환된 m-페닐렌기, 치환 또는 비치환된 p-페닐렌기, 치환 또는 비치환된 o-페닐렌기, 또는 치환 또는 비치환된 바이페닐렌기일 수 있다. 여기서 치환은 예컨대 적어도 하나의 수소가 중수소, C1 내지 C20 알킬기, C6 내지 C20 아릴기, C2 내지 C20 헤테로고리기, 할로겐, 시아노기 또는 이들의 조합으로 치환된 것일 수 있으나, 이에 한정되는 것은 아니다. For example, L 1 to L 5 can each independently be a single bond, a substituted or unsubstituted m-phenylene group, a substituted or unsubstituted p-phenylene group, a substituted or unsubstituted o-phenylene group, or a substituted or unsubstituted biphenylene group. Here, the substitution may be, for example, but is not limited to, substitution of at least one hydrogen with deuterium, a C1 to C20 alkyl group, a C6 to C20 aryl group, a C2 to C20 heterocyclic group, halogen, a cyano group, or a combination thereof.
일 예로, Ar1은 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트레닐기, 치환 또는 비치환된 트리페닐레닐기, 치환 또는 비치환된 플루오레닐기, 상기 화학식 A로 표현되는 기 또는 이들의 조합일 수 있다.For example, Ar 1 may be a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted anthracenyl group, a substituted or unsubstituted phenanthrenyl group, a substituted or unsubstituted triphenylenyl group, a substituted or unsubstituted fluorenyl group, a group represented by the above chemical formula A, or a combination thereof.
예컨대 Ar1은 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 나프틸기, 또는 상기 화학식 A로 표현되는 기일 수 있으나, 이에 한정되는 것은 아니다. For example, Ar 1 may be, but is not limited to, a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted naphthyl group, or a group represented by the above chemical formula A.
일 예로, R1 내지 R4는 각각 독립적으로 수소, 중수소, 시아노기, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트레닐기, 치환 또는 비치환된 트리페닐레닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기, 상기 화학식 A로 표현되는 기 또는 이들의 조합일 수 있다.For example, R 1 to R 4 can each independently be hydrogen, deuterium, a cyano group, a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted anthracenyl group, a substituted or unsubstituted phenanthrenyl group, a substituted or unsubstituted triphenylenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted dibenzofuranyl group, a substituted or unsubstituted dibenzothiophenyl group, a group represented by the above chemical formula A, or a combination thereof.
예컨대 R1 내지 R4는 각각 독립적으로 수소, 중수소, 시아노기, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기 또는 상기 화학식 A로 표현되는 기일 수 있으나, 이에 한정되는 것은 아니다.For example, R 1 to R 4 may each independently be hydrogen, deuterium, a cyano group, a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted dibenzofuranyl group, a substituted or unsubstituted dibenzothiophenyl group, or a group represented by the above chemical formula A, but is not limited thereto.
일 예로, 제1 화합물은 상기 화학식 A로 표현되는 기의 결합 위치에 따라 예컨대 하기 화학식 1A 내지 화학식 1L 중 어느 하나로 표현될 수 있다.For example, the first compound can be expressed by any one of the following chemical formulas 1A to 1L, depending on the bonding position of the group represented by the chemical formula A.
[화학식 1A] [화학식 1B] [화학식 1C][Chemical Formula 1A] [Chemical Formula 1B] [Chemical Formula 1C]
[화학식 1D] [화학식 1E] [화학식 1F][Formula 1D] [Formula 1E] [Formula 1F]
[화학식 1G] [화학식 1H] [화학식 1I][Chemical Formula 1G] [Chemical Formula 1H] [Chemical Formula 1I]
[화학식 1J] [화학식 1K] [화학식 1L][Chemical Formula 1J] [Chemical Formula 1K] [Chemical Formula 1L]
상기 화학식 1A 내지 화학식 1L에서, L1 내지 L5, Ar1 및 R1 내지 R4, Z1 내지 Z5는 전술한 바와 같고,In the chemical formulas 1A to 1L above, L 1 to L 5 , Ar 1 and R 1 to R 4 , Z 1 to Z 5 are as described above,
Rc, Rd, Re, Rf, Rg 및 Rh는 전술한 R1 내지 R4의 정의와 같고,R c , R d , R e , R f , R g and R h are as defined for R 1 to R 4 described above,
Z1a 내지 Z5a는 전술한 Z1 내지 Z5의 정의와 같으며, Z 1a to Z 5a are as defined for Z 1 to Z 5 described above,
Z1b 내지 Z5b도 전술한 Z1 내지 Z5의 정의와 같다.Z 1b to Z 5b are also defined as Z 1 to Z 5 described above.
일 예로 상기 La는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고, For example, each of the above L a is independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
예컨대 La는 각각 독립적으로 단일 결합, 치환 또는 비치환된 페닐렌기, 치환 또는 비치환된 바이페닐렌기, 치환 또는 비치환된 터페닐렌기, 치환 또는 비치환된 플루오레닐렌기, 치환 또는 비치환된 디벤조퓨란일렌기 또는 치환 또는 비치환된 디벤조티오펜일렌기일 수 있다.For example, L a can each independently be a single bond, a substituted or unsubstituted phenylene group, a substituted or unsubstituted biphenylene group, a substituted or unsubstituted terphenylene group, a substituted or unsubstituted fluorenylene group, a substituted or unsubstituted dibenzofuranylene group, or a substituted or unsubstituted dibenzothiophenylene group.
예컨대 La는 각각 독립적으로 단일 결합, 치환 또는 비치환된 m-페닐렌기 또는 치환 또는 비치환된 p-페닐렌기일 수 있으나, 이에 한정되는 것은 아니다. For example, L a can each independently be a single bond, a substituted or unsubstituted m-phenylene group, or a substituted or unsubstituted p-phenylene group, but is not limited thereto.
일 예로 Ra는 각각 독립적으로 수소, 중수소, 시아노기, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C20 아릴기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,For example, R a is each independently hydrogen, deuterium, a cyano group, a substituted or unsubstituted C1 to C20 alkyl group, a substituted or unsubstituted C6 to C20 aryl group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
예컨대 Ra는 각각 독립적으로 수소, 중수소, 시아노기, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트렌기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 카바졸일기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기일 수 있다.For example, R a can each independently be hydrogen, deuterium, a cyano group, a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted anthracenyl group, a substituted or unsubstituted phenanthrene group, a substituted or unsubstituted triphenylene group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted carbazolyl group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group.
예컨대 Ra는 각각 독립적으로 수소, 중수소, 시아노기, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 m-바이페닐기, 치환 또는 비치환된 p-바이페닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기일 수 있으나, 이에 한정되는 것은 아니다.For example, R a may each independently be hydrogen, deuterium, a cyano group, a substituted or unsubstituted phenyl group, a substituted or unsubstituted m-biphenyl group, a substituted or unsubstituted p-biphenyl group, a substituted or unsubstituted triphenylene group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group, but is not limited thereto.
Ra는 각각 독립적으로 존재하거나 인접한 기가 서로 연결되어 치환 또는 비치환된 방향족의 단환식 또는 다환식 고리, 또는 치환 또는 비치환된 방향족의 단환식 또는 다환식 헤테로고리를 형성할 수 있다.R a may exist independently, or adjacent groups may be linked to each other to form a substituted or unsubstituted aromatic monocyclic or polycyclic ring, or a substituted or unsubstituted aromatic monocyclic or polycyclic heterocycle.
일 예로, 상기 화학식 A로 표현되는 기에서 Z1 내지 Z5 중 적어도 둘은 N이고, Ra는 각각 독립적으로 존재할 수 있다.For example, in the group represented by the chemical formula A, at least two of Z 1 to Z 5 are N, and each R a can exist independently.
일 예로, 상기 화학식 A로 표현되는 기는 치환 또는 비치환된 피리미디닐기 또는 치환 또는 비치환된 트리아지닐기일 수 있다.For example, the group represented by the chemical formula A may be a substituted or unsubstituted pyrimidinyl group or a substituted or unsubstituted triazinyl group.
예컨대, Z1 및 Z3이 N이고, Z2, Z4 및 Z5가 각각 독립적으로 C-La-Ra이거나; Z3 및 Z5가 N이고, Z1, Z2 및 Z4가 각각 독립적으로 C-La-Ra이거나; 또는 Z2 및 Z4가 N이고, Z1, Z3 및 Z5가 각각 독립적으로 C-La-Ra 일 수 있다. 이 경우, La 및 Ra는 전술한 바와 같다.For example, Z 1 and Z 3 may be N, and Z 2 , Z 4 , and Z 5 may each independently be CL a -R a ; Z 3 and Z 5 may be N, and Z 1 , Z 2 , and Z 4 may each independently be CL a -R a ; or Z 2 and Z 4 may be N, and Z 1 , Z 3 , and Z 5 may each independently be CL a -R a . In this case, L a and R a are as described above.
예컨대, Z1, Z3 및 Z5가 N이고, Z2 및 Z4는 각각 독립적으로 C-La-Ra 일 수 있다. 이 경우, La 및 Ra는 전술한 바와 같다.For example, Z 1 , Z 3 and Z 5 can be N, and Z 2 and Z 4 can be independently CL a -R a . In this case, L a and R a are as described above.
일 예로, 화학식 A로 표현되는 기에서 Z1 내지 Z5 중 적어도 하나는 N이고, 인접한 Ra가 서로 연결되어 치환 또는 비치환된 방향족의 단환식 고리, 또는 치환 또는 비치환된 방향족의 단환식 헤테로고리를 형성할 수 있다.For example, in a group represented by chemical formula A, at least one of Z 1 to Z 5 is N, and adjacent R a can be connected to each other to form a substituted or unsubstituted aromatic monocyclic ring, or a substituted or unsubstituted aromatic monocyclic heterocycle.
이 경우, 화학식 A로 표현되는 기는 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기 또는 치환 또는 비치환된 나프티리디닐기일 수 있다.In this case, the group represented by chemical formula A may be a substituted or unsubstituted quinolinyl group, a substituted or unsubstituted isoquinolinyl group, a substituted or unsubstituted quinoxalinyl group, a substituted or unsubstituted quinazolinyl group, or a substituted or unsubstituted naphthyridinyl group.
예컨대, Z3 및 Z4는 각각 C-Ra이고 인접한 Ra가 서로 연결되어 벤젠 고리를 형성하고 Z1, Z2 및 Z5 중 어느 하나가 N일 수 있다. For example, Z 3 and Z 4 are each CR a , adjacent R a are connected to each other to form a benzene ring, and any one of Z 1 , Z 2 , and Z 5 can be N.
예컨대, Z3 및 Z4는 C-Ra이고 인접한 Ra가 서로 연결되어 벤젠 고리를 형성하고 Z1, Z2 및 Z5 중 어느 둘이 N일 수 있다.For example, Z 3 and Z 4 are CR a and adjacent R a are connected to each other to form a benzene ring, and any two of Z 1 , Z 2 , and Z 5 can be N.
예컨대, Z3 및 Z4는 C-Ra이고 인접한 Ra가 서로 연결되어 벤젠 고리를 형성하고 Z1, Z2 및 Z5이 각각 N일 수 있다.For example, Z 3 and Z 4 may be CR a , adjacent R a may be connected to each other to form a benzene ring, and Z 1 , Z 2 , and Z 5 may each be N.
예컨대, 상기 화학식 A는 하기 화학식 A-1 내지 A-7 중 어느 하나로 표현될 수 있으나, 이에 한정되는 것은 아니다.For example, the chemical formula A may be expressed by any one of the following chemical formulas A-1 to A-7, but is not limited thereto.
[화학식 A-1] [화학식 A-2] [화학식 A-3][Chemical Formula A-1] [Chemical Formula A-2] [Chemical Formula A-3]
[화학식 A-4] [화학식 A-5] [화학식 A-6] [화학식 A-7][Chemical Formula A-4] [Chemical Formula A-5] [Chemical Formula A-6] [Chemical Formula A-7]
상기 화학식 A-1 내지 화학식 A-7에서, In the above chemical formulas A-1 to A-7,
La1 내지 La5, 그리고 Lb1 및 Lb2는 전술한 La의 정의와 같고,L a1 to L a5 , and L b1 and L b2 are as defined for L a above,
Ra1 내지 Ra5, Rb1 및 Rb2는 전술한 Ra의 정의와 같다.R a1 to R a5 , R b1 and R b2 are as defined for R a above.
구체적인 일 예로 상기 화학식 A로 표현되는 기는 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기 또는 치환 또는 비치환된 나프티리디닐기일 수 있다.As a specific example, the group represented by the chemical formula A may be a substituted or unsubstituted pyrimidinyl group, a substituted or unsubstituted triazinyl group, a substituted or unsubstituted quinoxalinyl group, a substituted or unsubstituted quinazolinyl group, or a substituted or unsubstituted naphthyridinyl group.
더욱 구체적인 일 예로 상기 화학식 A는 하기 그룹 Ⅰ에 나열된 기 중 어느 하나로 표현될 수 있다.As a more specific example, the chemical formula A can be expressed by any one of the groups listed in Group I below.
[그룹 Ⅰ][Group I]
일 예로, 상기 화학식 1A는 상기 화학식 A로 표현되는 기의 구체적인 결합 위치에 따라 하기 화학식 1A-1 내지 화학식 1A-4 중 어느 하나로 표현될 수 있다.For example, the chemical formula 1A can be expressed as any one of the following chemical formulas 1A-1 to 1A-4 depending on the specific bonding position of the group expressed by the chemical formula A.
[화학식 1A-1] [화학식 1A-2][Chemical Formula 1A-1] [Chemical Formula 1A-2]
[화학식 1A-3] [화학식 1A-4][Chemical Formula 1A-3] [Chemical Formula 1A-4]
상기 화학식 1A-1 내지 화학식 1A-4에서, L1 내지 L5, Ar1, R2 내지 R4 및 Z1 내지 Z5는 전술한 바와 같다.In the above chemical formulas 1A-1 to 1A-4, L 1 to L 5 , Ar 1 , R 2 to R 4 and Z 1 to Z 5 are as described above.
예컨대 화학식 1A는 상기 화학식 1A-2 또는 화학식 1A-4로 표현될 수 있다. For example, chemical formula 1A can be expressed as chemical formula 1A-2 or chemical formula 1A-4.
일 예로, 상기 화학식 1C는 상기 화학식 A로 표현되는 기의 구체적인 결합 위치에 따라 하기 화학식 1C-1 내지 화학식 1C-4 중 어느 하나로 표현될 수 있다.For example, the chemical formula 1C above can be expressed by any one of the following chemical formulas 1C-1 to 1C-4 depending on the specific bonding position of the group represented by the chemical formula A.
[화학식 1C-1] [화학식 1C-2] [화학식 1C-3] [화학식 1C-4][Chemical Formula 1C-1] [Chemical Formula 1C-2] [Chemical Formula 1C-3] [Chemical Formula 1C-4]
상기 화학식 1C-1 내지 화학식 1C-4에서, L1 내지 L5, R2 내지 R4, Z1 내지 Z5, Z1a 내지 Z5a, 및 Z1b 내지 Z5b는 전술한 바와 같다.In the chemical formulas 1C-1 to 1C-4, L 1 to L 5 , R 2 to R 4 , Z 1 to Z 5 , Z 1a to Z 5a , and Z 1b to Z 5b are as described above.
예컨대 화학식 1C는 상기 화학식 1C-2 또는 화학식 1C-4로 표현될 수 있다. For example, chemical formula 1C can be expressed as chemical formula 1C-2 or chemical formula 1C-4.
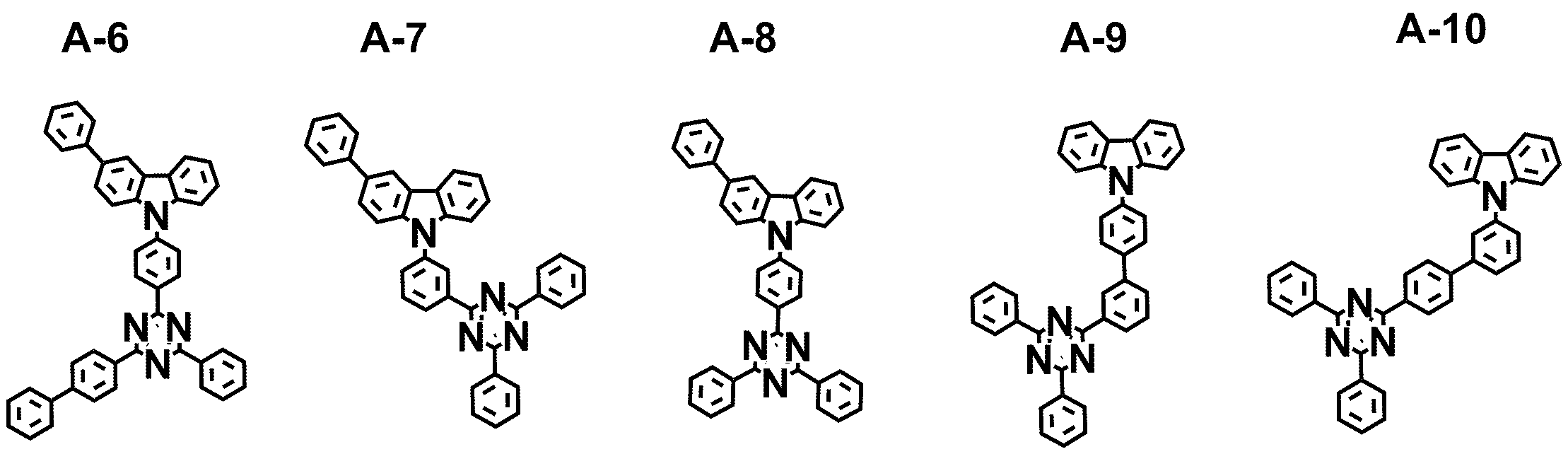
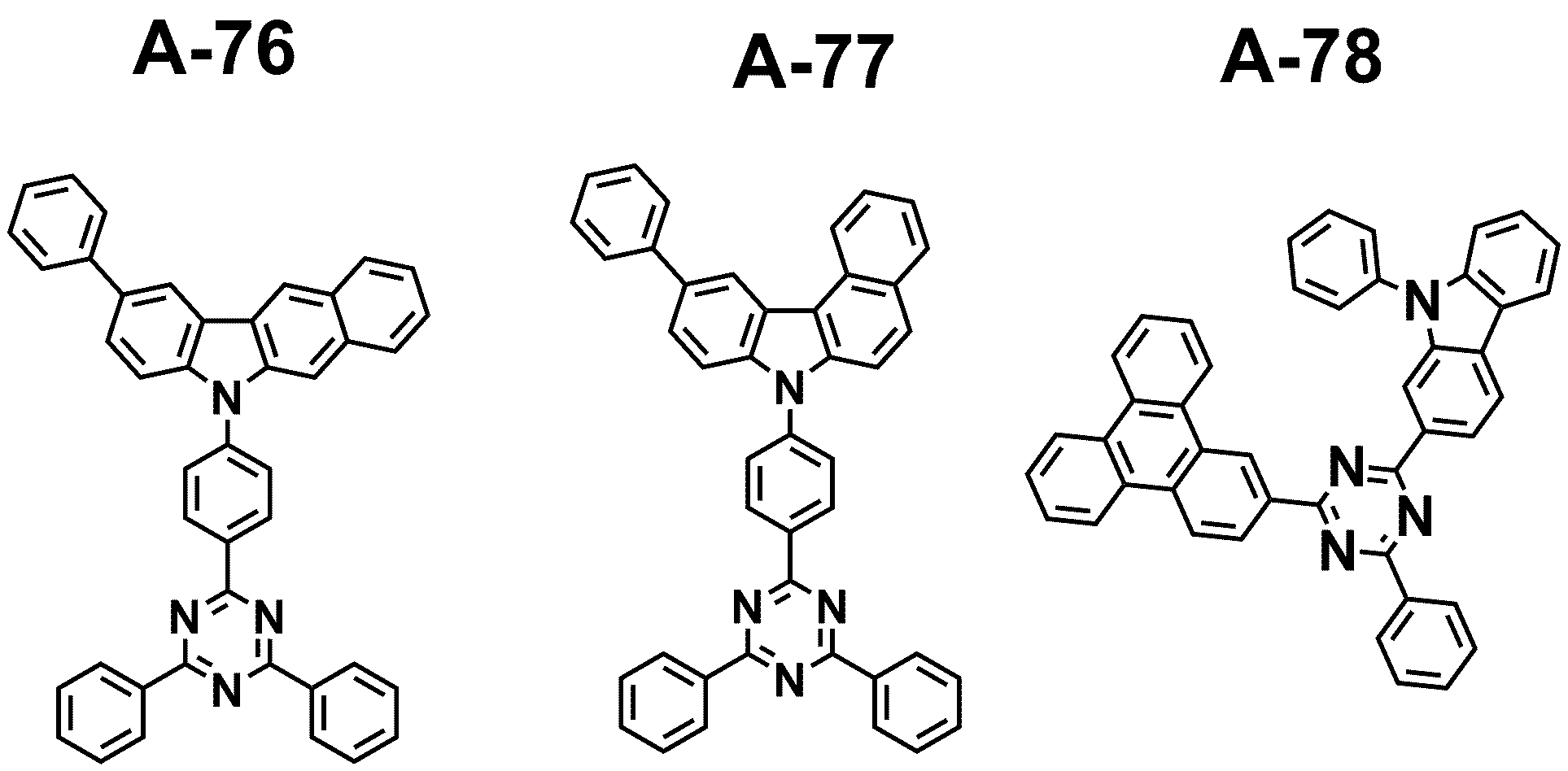
제1 화합물은 예컨대 하기 그룹 1에 나열된 화합물에서 선택된 하나일 수 있으나, 이에 한정되는 것은 아니다.The first compound may be, for example, but is not limited to, one selected from the compounds listed in Group 1 below.
[그룹 1][Group 1]
제1 화합물과 함께 제2 화합물을 포함함으로써 정공과 전자의 밸런스를 높여 이를 적용한 소자의 구동 또는 수명 특성을 크게 개선할 수 있다.By including the second compound together with the first compound, the balance between holes and electrons can be increased, thereby significantly improving the driving or life characteristics of a device to which it is applied.
일 예로, 상기 화학식 2는 하기 화학식 2-1로 표현될 수 있다.For example, the chemical formula 2 can be expressed as the following chemical formula 2-1.
[화학식 2-1][Chemical Formula 2-1]
상기 화학식 2-1에서, Ar2, Ar3, L6, L7, R5 내지 R10의 정의는 전술한 바와 같다. In the above chemical formula 2-1, the definitions of Ar 2 , Ar 3 , L 6 , L 7 , R 5 to R 10 are as described above.
일 실시예에서, 제2 화합물은 상기 화학식 2-1로 표현될 수 있고, 상기 화학식 2-1의 R5 내지 R10은 모두 수소이며, *-L6-Ar2 및 *-L7-Ar3는 각각 독립적으로 하기 그룹 Ⅱ에 나열된 치환기 중 하나일 수 있다.In one embodiment, the second compound can be represented by the chemical formula 2-1, wherein R 5 to R 10 of the chemical formula 2-1 are all hydrogen, and *-L 6 -Ar 2 and *-L 7 -Ar 3 can each independently be one of the substituents listed in Group II below.
[그룹 Ⅱ][Group II]
상기 그룹 Ⅱ에서, *은 연결지점이다.In the above group II, * is a connection point.
예컨대, Ar2 및 Ar3은 각각 독립적으로 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기 또는 치환 또는 비치환된 터페닐기일 수 있다.For example, Ar 2 and Ar 3 can each independently be a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, or a substituted or unsubstituted terphenyl group.
또한, L6 및 L7은 각각 독립적으로 단일결합 또는 치환 또는 비치환된 페닐렌기일 수 있다.Additionally, L 6 and L 7 can each independently be a single bond or a substituted or unsubstituted phenylene group.
또한, R5 내지 R10은 각각 독립적으로 수소 또는 C6 아릴기일 수 있다.Additionally, R 5 to R 10 can each independently be hydrogen or a C6 aryl group.
제2 화합물은 예컨대 하기 그룹 2에 나열된 화합물에서 선택된 하나일 수 있으나, 이에 한정되는 것은 아니다.The second compound may be, for example, but is not limited to, one selected from the compounds listed in Group 2 below.
[그룹 2][Group 2]
[C-1] [C-2] [C-3] [C-4] [C-5][C-1] [C-2] [C-3] [C-4] [C-5]
[C-6] [C-7] [C-8] [C-9] [C-10][C-6] [C-7] [C-8] [C-9] [C-10]
[C-11] [C-12] [C-13] [C-14] [C-15][C-11] [C-12] [C-13] [C-14] [C-15]
[C-16] [C-17] [C-18] [C-19] [C-20][C-16] [C-17] [C-18] [C-19] [C-20]
[C-21] [C-22] [C-23] [C-24] [C-25][C-21] [C-22] [C-23] [C-24] [C-25]
[C-26] [C-27] [C-28] [C-29] [C-30][C-26] [C-27] [C-28] [C-29] [C-30]
[C-31] [C-32] [C-33] [C-34] [C-35][C-31] [C-32] [C-33] [C-34] [C-35]
[C-36] [C-37] [C-38] [C-39] [C-40][C-36] [C-37] [C-38] [C-39] [C-40]
[C-41] [C-42] [C-43] [C-44] [C-45][C-41] [C-42] [C-43] [C-44] [C-45]
[C-46] [C-47] [C-48] [C-49] [C-50][C-46] [C-47] [C-48] [C-49] [C-50]
[C-51] [C-52] [C-53] [C-54] [C-55][C-51] [C-52] [C-53] [C-54] [C-55]
[C-56] [C-57] [C-58] [C-59] [C-60][C-56] [C-57] [C-58] [C-59] [C-60]
[C-61] [C-62] [C-63] [C-64] [C-65][C-61] [C-62] [C-63] [C-64] [C-65]
[C-66] [C-67] [C-68] [C-69] [C-70][C-66] [C-67] [C-68] [C-69] [C-70]
[C-71] [C-72] [C-73] [C-74] [C-75][C-71] [C-72] [C-73] [C-74] [C-75]
[C-76] [C-77] [C-78] [C-79] [C-80][C-76] [C-77] [C-78] [C-79] [C-80]
[C-81] [C-82] [C-83] [C-84] [C-85][C-81] [C-82] [C-83] [C-84] [C-85]
[C-86] [C-87] [C-88] [C-89] [C-90][C-86] [C-87] [C-88] [C-89] [C-90]
[C-91] [C-92] [C-93] [C-94] [C-95][C-91] [C-92] [C-93] [C-94] [C-95]
[C-96] [C-97] [C-98] [C-99] [C-100][C-96] [C-97] [C-98] [C-99] [C-100]
[C-101] [C-102] [C-103] [C-104] [C-105][C-101] [C-102] [C-103] [C-104] [C-105]
[C-106] [C-107] [C-108] [C-109] [C-110][C-106] [C-107] [C-108] [C-109] [C-110]
[C-111] [C-112] [C-113][C-111] [C-112] [C-113]
상기 제1 화합물과 상기 제2 화합물은 예컨대 1:99 내지 99:1의 중량비로 포함될 수 있다. 상기 범위로 포함됨으로써 제1 화합물의 전자 수송 능력과 제2 화합물의 정공 수송 능력을 이용해 적절한 중량비를 맞추어 바이폴라 특성을 구현하여 효율과 수명을 개선할 수 있다. 상기 범위 내에서 예컨대 약 10:90 내지 90:10, 약 20:80 내지 80:20, 약 20:80 내지 70:30, 약 20:80 내지 60:40의 중량비로 포함될 수 있다. 일 예로, 30:70 내지 50:50의 중량비로 포함될 수 있으며, 예컨대, 30:70의 중량비로 포함될 수 있다. The first compound and the second compound may be included in a weight ratio of, for example, 1:99 to 99:1. By being included in the above range, the electron transport ability of the first compound and the hole transport ability of the second compound can be used to achieve an appropriate weight ratio to implement bipolar characteristics, thereby improving efficiency and lifespan. Within the above range, the weight ratio may be, for example, about 10:90 to 90:10, about 20:80 to 80:20, about 20:80 to 70:30, about 20:80 to 60:40. For example, the weight ratio may be 30:70 to 50:50, and for example, the weight ratio may be 30:70.
발광층은 전술한 호스트 외에 1종 이상의 화합물을 더 포함할 수 있다. The emitting layer may further include one or more compounds in addition to the aforementioned host.
발광층은 도펀트를 더 포함할 수 있다. 도펀트는 예컨대 인광 도펀트일 수 있고, 예컨대 적색, 녹색 또는 청색의 인광 도펀트일 수 있고, 예컨대 적색 인광 도펀트일 수 있다.The emissive layer may further comprise a dopant. The dopant may be, for example, a phosphorescent dopant, for example, a red, green or blue phosphorescent dopant, for example, a red phosphorescent dopant.
도펀트는 전술한 호스트에 미량 혼합되어 발광을 일으키는 물질로, 일반적으로 삼중항 상태 이상으로 여기시키는 다중항 여기(multiple excitation)에 의해 발광하는 금속 착체(metal complex)와 같은 물질이 사용될 수 있다. 도펀트는 예컨대 무기, 유기, 유무기 화합물일 수 있으며, 1종 또는 2종 이상 포함될 수 있다.A dopant is a substance that causes light emission when mixed in a small amount with the aforementioned host. Generally, a substance such as a metal complex that causes light emission by multiple excitation that excites to a triplet state or higher can be used. The dopant can be, for example, an inorganic, organic, or organic-inorganic compound, and can be included in one or more types.
도펀트의 일 예로 인광 도펀트를 들 수 있으며, 인광 도펀트의 예로는 Ir, Pt, Os, Ti, Zr, Hf, Eu, Tb, Tm, Fe, Co, Ni, Ru, Rh, Pd 또는 이들의 조합을 포함하는 유기 금속화합물을 들 수 있다. 인광 도펀트는 예컨대 하기 화학식 Z로 표현되는 화합물을 사용할 수 있으나, 이에 한정되는 것은 아니다.An example of a dopant is a phosphorescent dopant, and examples of a phosphorescent dopant include an organometallic compound containing Ir, Pt, Os, Ti, Zr, Hf, Eu, Tb, Tm, Fe, Co, Ni, Ru, Rh, Pd or a combination thereof. The phosphorescent dopant may be, for example, a compound represented by the following chemical formula Z, but is not limited thereto.
[화학식 Z][chemical formula Z]
L10MXL 10 MX
상기 화학식 Z에서, M은 금속이고, L10 및 X는 서로 같거나 다르며 M과 착화합물을 형성하는 리간드이다. In the above chemical formula Z, M is a metal, L 10 and X are the same or different and are ligands that form a complex with M.
상기 M은 예컨대 Ir, Pt, Os, Ti, Zr, Hf, Eu, Tb, Tm, Fe, Co, Ni, Ru, Rh, Pd 또는 이들의 조합일 수 있고, 상기 L10 및 X는 예컨대 바이덴테이트 리간드일 수 있다.The above M can be, for example, Ir, Pt, Os, Ti, Zr, Hf, Eu, Tb, Tm, Fe, Co, Ni, Ru, Rh, Pd or a combination thereof, and the above L 10 and X can be, for example, a bidentate ligand.
정공수송보조층(142)은 제3 화합물을 포함할 수 있다.The positive hole transport auxiliary layer (142) may include a third compound.
제3 화합물은 높은 HOMO 에너지 준위를 가지는 화합물로 양호한 정공 주입 특성을 가질 수 있다. 이에 따라 제3 화합물은 정공수송보조층(142)에 적용되어 발광층(130)과 정공수송층(141)의 계면에서 정공의 이동도를 효과적으로 개선하여 유기 광전자 소자의 구동 전압을 효과적으로 낮출 수 있다.The third compound is a compound having a high HOMO energy level and can have good hole injection properties. Accordingly, the third compound can be applied to the hole transport auxiliary layer (142) to effectively improve the mobility of holes at the interface between the light-emitting layer (130) and the hole transport layer (141), thereby effectively lowering the operating voltage of the organic optoelectronic device.
일 예로 상기 화학식 3의 Ar4 내지 Ar7은 각각 독립적으로 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기 또는 이들의 조합일 수 있다.For example, Ar 4 to Ar 7 in the chemical formula 3 may each independently be a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted dibenzofuranyl group, a substituted or unsubstituted dibenzothiophenyl group, or a combination thereof.
예컨대 제3 화합물은 하기 화학식 3-1로 표현될 수 있다.For example, the third compound can be expressed by the following chemical formula 3-1.
[화학식 3-1][Chemical Formula 3-1]
상기 화학식 3-1에서, L8, L9, R11 내지 R14, 및 Ar4 내지 Ar6은 전술한 바와 같고,In the chemical formula 3-1 above, L 8 , L 9 , R 11 to R 14 , and Ar 4 to Ar 6 are as described above,
X는 O, S 또는 CRiRj 이며,X is O, S, or CR i R j ,
Ri, Rj 및 R15 내지 R17은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 또는 이들의 조합이다.R i , R j and R 15 to R 17 are each independently hydrogen, deuterium, halogen, cyano group, a substituted or unsubstituted C1 to C30 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, or a combination thereof.
더욱 구체적인 일 예로 상기 화학식 3-1의 L8 및 L9는 각각 독립적으로 meta-페닐렌기 또는 para-페닐렌기이고,As a more specific example, L 8 and L 9 in the chemical formula 3-1 are each independently a meta-phenylene group or a para-phenylene group,
Ar4는 페닐기이고,Ar 4 is a phenyl group,
Ar5 및 Ar6은 각각 독립적으로 치환 또는 비치환된 페닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기이며,Ar 5 and Ar 6 are each independently a substituted or unsubstituted phenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group,
R11 내지 R17은 각각 독립적으로 수소 또는 페닐기일 수 있다.R 11 to R 17 can each independently be hydrogen or a phenyl group.
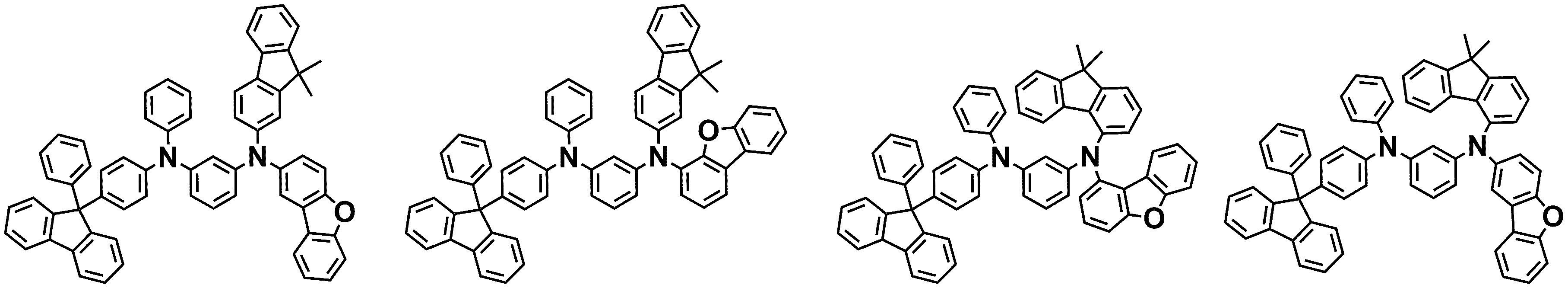
상기 제3 화합물은 예컨대 하기 그룹 3에 나열된 화합물에서 선택된 하나일 수 있으나, 이에 한정되는 것은 아니다.The third compound may be, for example, one selected from the compounds listed in Group 3 below, but is not limited thereto.
[그룹 3] [Group 3]
[D-1] [D-2] [D-3] [D-4][D-1] [D-2] [D-2] [D-3] [D-4]
[D-5] [D-6] [D-7] [D-8][D-5] [D-6] [D-6] [D-7] [D-8]
[D-9] [D-10] [D-11] [D-12][D-9] [D-10] [D-10] [D-10] [D-11] [D-12]
[D-13] [D-14] [D-15] [D-16][D-13] [D-14] [D-15] [D-15] [D-16]
[D-17] [D-18] [D-19] [D-20][D-17] [D-18] [D-19] [D-19] [D-20]
[D-21] [D-22] [D-23] [D-24][D-21] [D-22] [D-23] [D-24]
[D-25] [D-26] [D-27] [D-28][D-25] [D-26] [D-26] [D-27] [D-28]
[D-29] [D-30] [D-31] [D-32][D-29] [D-30] [D-30] [D-31] [D-31] [D-32]
[D-33] [D-34] [D-35] [D-36][D-33] [D-34] [D-34] [D-34] [D-35] [D-35] [D-36]
[D-37] [D-38] [D-39] [D-40][D-37] [D-38] [D-38] [D-38] [D-39] [D-39] [D-40]
[D-41] [D-42] [D-43] [D-44][D-41] [D-42] [D-43] [D-44]
[D-45] [D-46] [D-47] [D-48][D-45] [D-46] [D-46] [D-46] [D-47] [D-48]
[D-49] [D-50] [D-51] [D-52][D-49] [D-50] [D-50] [D-51] [D-51] [D-52]
[D-53] [D-54] [D-55] [D-56][D-53] [D-54] [D-54] [D-55] [D-56]
[D-57] [D-58] [D-59] [D-60][D-57] [D-58] [D-59] [D-60]
[D-61] [D-62] [D-63] [D-64][D-61] [D-62] [D-63] [D-64]
[D-65] [D-66] [D-67] [D-68][D-65] [D-66] [D-67] [D-68]
더욱 구체적인 일 실시예에서, 상기 제1 화합물은 상기 화학식 1B로 표현되고, 상기 제2 화합물은 상기 화학식 2-1로 표현되고, 상기 제3 화합물은 하기 화학식 3-1로 표현될 수 있다.In a more specific embodiment, the first compound may be represented by the chemical formula 1B, the second compound may be represented by the chemical formula 2-1, and the third compound may be represented by the chemical formula 3-1 below.
이 경우 상기 화학식 1B에서, In this case, in the chemical formula 1B above,
Z1, Z3 및 Z5는 각각 N이고,Z 1 , Z 3 and Z 5 are each N,
Z2 및 Z4는 각각 독립적으로 C-La-Ra 이고,Z 2 and Z 4 are each independently CL a -R a ,
La 및 L1 내지 L4는 각각 단일 결합이고,L a and L 1 to L 4 are each a single bond,
L5는 페닐렌기 또는 바이페닐렌기이고,L 5 is a phenylene group or a biphenylene group,
Ra는 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 터페닐기 또는 치환 또는 비치환된 트리페닐렌기이고,R a is a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted terphenyl group, or a substituted or unsubstituted triphenylene group,
R1 내지 R4는 각각 독립적으로 수소, 치환 또는 비치환된 C1 내지 C10 알킬기, 또는 치환 또는 비치환된 C6 내지 C12 아릴기일 수 있다.R 1 to R 4 can each independently be hydrogen, a substituted or unsubstituted C1 to C10 alkyl group, or a substituted or unsubstituted C6 to C12 aryl group.
이 경우 상기 화학식 2-1에서,In this case, in the chemical formula 2-1 above,
*-L6-Ar2 및 *-L7-Ar3는 각각 독립적으로 상기 그룹 Ⅱ에 나열된 치환기 중 B-1 내지 B-4 중 어느 하나이고,*-L 6 -Ar 2 and *-L 7 -Ar 3 are each independently any one of the substituents B-1 to B-4 listed in the above Group II,
R5 내지 R10은 각각 독립적으로 수소, 치환 또는 비치환된 C1 내지 C10 알킬기, 또는 치환 또는 비치환된 C6 내지 C12 아릴기일 수 있다.R 5 to R 10 can each independently be hydrogen, a substituted or unsubstituted C1 to C10 alkyl group, or a substituted or unsubstituted C6 to C12 aryl group.
이 경우 상기 화학식 3-1에서, In this case, in the chemical formula 3-1 above,
L8 및 L9는 각각 독립적으로 meta-페닐렌기 또는 para-페닐렌기이고,L 8 and L 9 are each independently a meta-phenylene group or a para-phenylene group,
Ar4는 페닐기이고,Ar 4 is a phenyl group,
Ar5 및 Ar6은 각각 독립적으로 치환 또는 비치환된 페닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기이며,Ar 5 and Ar 6 are each independently a substituted or unsubstituted phenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group,
R11 내지 R17은 각각 독립적으로 수소 또는 페닐기일 수 있다.R 11 to R 17 can each independently be hydrogen or a phenyl group.
정공수송층(141)은 양극(110)과 발광층(130) 사이에 위치하며, 양극(110)으로부터 발광층(130)으로 정공 수송을 용이하게 할 수 있다. 일 예로, 정공수송층(141)은 양극(110)을 이루는 도전체의 일 함수(work function)와 발광층(130)을 이루는 물질의 HOMO 에너지 레벨 사이의 HOMO 에너지 레벨을 가지는 물질을 포함할 수 있다. The hole transport layer (141) is positioned between the anode (110) and the light-emitting layer (130) and can facilitate hole transport from the anode (110) to the light-emitting layer (130). For example, the hole transport layer (141) may include a material having a HOMO energy level between the work function of a conductor forming the anode (110) and the HOMO energy level of a material forming the light-emitting layer (130).
정공수송층(141)은 예컨대 아민 유도체를 포함할 수 있다.The hole transport layer (141) may include, for example, an amine derivative.
정공수송층(141)은 예컨대 하기 화학식 4로 표현되는 화합물을 포함할 수 있으나, 이에 한정되는 것은 아니다.The hole transport layer (141) may include, for example, a compound represented by the following chemical formula 4, but is not limited thereto.
[화학식 4][Chemical Formula 4]
상기 화학식 4에서, In the above chemical formula 4,
R18 내지 R21은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C10 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이며, R 18 to R 21 are each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C10 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof,
R18 및 R19는 각각 독립적으로 존재하거나 서로 결합하여 고리를 형성하고,R 18 and R 19 exist independently or combine with each other to form a ring,
R20 및 R21은 각각 독립적으로 존재하거나 서로 결합하여 고리를 형성하고,R 20 and R 21 exist independently or combine with each other to form a ring,
R22 내지 R24는 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기 또는 치환 또는 비치환된 C2 내지 C30 헤테로고리기이고, R 22 to R 24 are each independently a substituted or unsubstituted C6 to C30 aryl group or a substituted or unsubstituted C2 to C30 heterocyclic group,
L11 내지 L14는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C30 아릴렌기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이다. L 11 to L 14 are each independently a single bond, a substituted or unsubstituted C6 to C30 arylene group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof.
일 예로, R22는 치환 또는 비치환된 C6 내지 C30 아릴기일 수 있고, 예컨대 R22는 치환 또는 비치환된 페닐기 또는 치환 또는 비치환된 바이페닐기일 수 있다.For example, R 22 can be a substituted or unsubstituted C6 to C30 aryl group, for example, R 22 can be a substituted or unsubstituted phenyl group or a substituted or unsubstituted biphenyl group.
일 예로, R23 및 R24는 각각 독립적으로 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 비스플루오렌기, 치환 또는 비치환된 트리페닐레닐기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기 또는 이들의 조합일 수 있다.For example, R 23 and R 24 can each independently be a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted bisfluorene group, a substituted or unsubstituted triphenylenyl group, a substituted or unsubstituted anthracenyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted dibenzofuranyl group, a substituted or unsubstituted dibenzothiophenyl group, or a combination thereof.
상기 화학식 4로 표현되는 화합물은 예컨대 하기 그룹 4에 나열된 화합물 중 하나일 수 있으나, 이에 한정되는 것은 아니다.The compound represented by the above chemical formula 4 may be, for example, one of the compounds listed in Group 4 below, but is not limited thereto.
[그룹 4][Group 4]
유기층(105)은 전술한 발광층(130), 정공수송보조층(142) 및 정공수송층(141) 외에 정공 주입층, 전자 차단층, 전자 수송층, 전자 주입층 및/또는 정공 차단층(도시하지 않음)을 더 포함할 수 있다.The organic layer (105) may further include a hole injection layer, an electron blocking layer, an electron transport layer, an electron injection layer, and/or a hole blocking layer (not shown) in addition to the aforementioned light-emitting layer (130), hole transport auxiliary layer (142), and hole transport layer (141).
유기 발광 소자(300)는 기판 위에 양극 또는 음극을 형성한 후, 진공증착법(evaporation), 스퍼터링(sputtering), 플라즈마 도금 및 이온도금과 같은 건식성막법 또는 용액 공정 등으로 유기층을 형성한 후, 그 위에 음극 또는 양극을 형성하여 제조할 수 있다.The organic light-emitting device (300) can be manufactured by forming an anode or cathode on a substrate, forming an organic layer using a dry film method such as evaporation, sputtering, plasma plating, and ion plating, or a solution process, and then forming a cathode or anode thereon.
상술한 유기 광전자 소자는 표시 장치에 적용될 수 있다. 예컨대 유기 발광 소자는 유기 발광 표시 장치에 적용될 수 있다.The above-described organic optoelectronic device can be applied to a display device. For example, the organic light-emitting device can be applied to an organic light-emitting display device.
이하 실시예를 통하여 상술한 구현예를 보다 상세하게 설명한다. 다만 하기의 실시예는 단지 설명의 목적을 위한 것이며 권리범위를 제한하는 것은 아니다.The above-described implementation examples are described in more detail through the following examples. However, the following examples are for the purpose of explanation only and do not limit the scope of rights.
(제1 화합물의 합성)(Synthesis of the first compound)
합성예Synthetic example 1: 화합물 A-27의 합성1: Synthesis of compound A-27
[반응식 1][Reaction Formula 1]
KR10-1947747B1에 공지된 방법을 참고하여 화합물 A-27을 합성하였다.Compound A-27 was synthesized by referring to the method disclosed in KR10-1947747B1.
합성예Synthetic example 2: 화합물 A-13의 합성2: Synthesis of compound A-13
[반응식 2][Reaction Formula 2]
KR10-2019-0090204A에 공지된 방법을 참고하여 화합물 A-13을 합성하였다.Compound A-13 was synthesized by referring to the method disclosed in KR10-2019-0090204A.
(제2 화합물의 합성)(Synthesis of the second compound)
합성예Synthetic example 3: 화합물 C-74의 합성3: Synthesis of compound C-74
KR10-1773363B1에 공지된 방법을 참고하여 화합물 C-74를 합성하였다.Compound C-74 was synthesized by referring to the method disclosed in KR10-1773363B1.
LC Mass M+H+ = 637.33LC Mass M + H + = 637.33
(제3 화합물의 합성)(Synthesis of the third compound)
합성예Synthetic example 4: 화합물 D-53의 합성4: Synthesis of compound D-53
[반응식 3][Reaction Formula 3]
KR10-2019-0038303A에 공지된 방법을 참고하여 화합물 D-53을 합성하였다.Compound D-53 was synthesized by referring to the method disclosed in KR10-2019-0038303A.
합성예Synthetic example 5: 화합물 D-55의 합성5: Synthesis of compound D-55
[반응식 4][Reaction Formula 4]
KR10-2019-0038303A에 공지된 방법을 참고하여 화합물 D-55를 합성하였다.Compound D-55 was synthesized by referring to the method disclosed in KR10-2019-0038303A.
(비교화합물 합성)(Comparative compound synthesis)
참고합성예Reference synthesis example 1: 화합물 R-1의 합성1: Synthesis of compound R-1
KR10-2019-0038303A에 공지된 방법을 참고하여 화합물 R-1을 합성하였다.Compound R-1 was synthesized by referring to the method disclosed in KR10-2019-0038303A.
참고합성예Reference synthesis example 2: 화합물 R-2의 합성2: Synthesis of compound R-2
[반응식 5][Reaction Formula 5]
둥근 바닥 플라스크에 비스(4-비페닐-일)아민 7.6g(23.6mmol), 중간체 M-2 9.4g(23.6mmol), 및 소디윰 t-부톡사이드 3.4g(35.4mmol)을 넣고 톨루엔 240ml을 가하여 용해시켰다. 여기에 Pd(dba)2 0.14g(0.24mmol)과 트리-터셔리-부틸포스핀 0.12g(0.60mmol)을 차례로 넣은 후 질소 분위기 하에서 4시간 동안 환류 교반시킨다. 반응 종료 후 톨루엔과 증류수로 추출 후 유기층을 마그네슘 설페이트로 건조, 여과하고 여과액을 감압 농축하였다. 생성물을 n-헥산/디클로로메탄(7:3 부피비)으로 실리카 겔 컬럼 크로마토그래피로 정제하여 화합물 R-2를 13.5g(수율 90%) 수득하였다.In a round-bottomed flask were added 7.6 g (23.6 mmol) of bis (4-biphenyl-yl) amine, 9.4 g (23.6 mmol) of intermediate M-2, and 3.4 g (35.4 mmol) of sodium t-butoxide, and 240 ml of toluene was added to dissolve. To this, 0.14 g (0.24 mmol) of Pd (dba) 2 and 0.12 g (0.60 mmol) of tri-tert-butylphosphine were sequentially added, and the mixture was refluxed and stirred for 4 hours under a nitrogen atmosphere. After completion of the reaction, the mixture was extracted with toluene and distilled water, and the organic layer was dried over magnesium sulfate and filtered, and the filtrate was concentrated under reduced pressure. The product was purified by silica gel column chromatography with n-hexane/dichloromethane (7:3 by volume) to obtain 13.5 g (yield 90%) of compound R-2.
(유기 발광 소자의 제작)(Fabrication of organic light-emitting devices)
실시예Example 1 1
ITO(Indium tin oxide)가 1,500Å 두께로 박막 코팅된 유리 기판을 증류수로 세척하였다. 증류수 세척이 끝나면 이소프로필 알코올, 아세톤, 메탄올 등의 용제로 초음파 세척을 하고 건조시킨 후 플라즈마 세정기로 이송시킨 다음 산소 플라즈마를 이용하여 상기 기판을 10분간 세정한 후 진공 층착기로 기판을 이송하였다. 이렇게 준비된 ITO 투명 전극을 양극으로 사용하여 ITO 기판 상부에 N4,N4'-디페닐-N4,N4'-비스(9-페닐-9H-카바졸-3-일)바이페닐-4,4'디아민(N4,N4'-diphenyl-N4,N4'-bis(9-phenyl-9H-carbazol-3-yl)biphenyl-4,4'-diamine)(화합물 A)을 진공 증착하여 700Å 두께의 정공 주입층을 형성하고 상기 정공 주입층 상부에 1,4,5,8,9,11-헥사아자트리페닐렌-헥사카보니트릴(1,4,5,8,9,11-hexaazatriphenylene-hexacarbonitrile, HATCN)(화합물 B)을 50Å의 두께로 증착한 후, N-(바이페닐-4-일)-9,9-디메틸-N-(4-(9-페닐-9H-카바졸-3-일)페닐)-9H-플루오렌-2-아민(N-(biphenyl-4-yl)-9,9-dimethyl-N-(4-(9-phenyl-9H-carbazol-3-yl)phenyl)-9Hfluoren-2-amine)(화합물 C)을 700Å의 두께로 증착하여 정공수송층을 형성하였다. 정공수송층 상부에 합성예 4에서 얻어진 화합물 D-53을 진공 증착으로 320Å 두께의 정공수송보조층을 형성하였다. 이어서 상기 정공수송보조층 상부에 합성예 1에서 얻어진 화합물 A-27 및 합성예 3에서 얻어진 화합물 C-74를 호스트로 동시에 사용하고 도펀트로 트리스(4-메틸-2,5-디페닐피리딘)이리듐(III)(화합물 D)를 10wt%로 도핑하여 진공 증착으로 400Å 두께의 발광층을 형성하였다. 여기서 화합물 A-27과 화합물 C-74는 3:7 중량비로 사용되었다. 이어서 상기 발광층 상부에 8-(4-(4-(나프탈렌-2-일)-6-(나프탈렌-3-일)-1,3,5-[0677] 트리아진-2-일)페닐)퀴놀린(8-(4-(4-(naphthalen-2-yl)-6-(naphthalen-3-yl)-1,3,5-triazin-2-yl)phenyl)quinoline)(화합물E)와 Liq를 동시에 1:1 비율로 진공 증착하여 300Å 두께의 전자수송층을 형성하고 상기 전자수송층 상부에 Liq 15Å과 Al 1,200Å을 순차적으로 진공 증착하여 음극을 형성함으로써 유기발광소자를 제작하였다.A glass substrate coated with a 1,500Å thick ITO (Indium Tin Oxide) film was washed with distilled water. After washing with distilled water, the substrate was ultrasonically washed with a solvent such as isopropyl alcohol, acetone, or methanol, dried, and then transferred to a plasma cleaner. The substrate was then cleaned for 10 minutes using oxygen plasma and then transferred to a vacuum layer depositor. Using the ITO transparent electrode prepared in this way as an anode, N4,N4'-diphenyl-N4,N4'-bis(9-phenyl-9H-carbazol-3-yl)biphenyl-4,4'-diamine (Compound A) was vacuum-deposited on the ITO substrate to form a hole injection layer with a thickness of 700 Å, and 1,4,5,8,9,11-hexaazatriphenylene-hexacarbonitrile (HATCN) (Compound B) was deposited on the hole injection layer with a thickness of 50 Å. A hole transport layer was formed by depositing N-(biphenyl-4-yl)-9,9-dimethyl-N-(4-(9-phenyl-9H-carbazol-3-yl)phenyl)-9H-fluoren-2-amine (Compound C) to a thickness of 700 Å. A hole transport auxiliary layer was formed on the hole transport layer by vacuum deposition of Compound D-53 obtained in Synthesis Example 4 to a thickness of 320 Å. Next, compound A-27 obtained in Synthesis Example 1 and compound C-74 obtained in Synthesis Example 3 were simultaneously used as hosts on the hole transport auxiliary layer, and tris(4-methyl-2,5-diphenylpyridine)iridium(III) (compound D) was doped at 10 wt% as a dopant to form a 400 Å thick light-emitting layer by vacuum deposition. Here, compound A-27 and compound C-74 were used at a weight ratio of 3:7. Next, 8-(4-(4-(naphthalen-2-yl)-6-(naphthalen-3-yl)-1,3,5-[0677] triazin-2-yl)phenyl)quinoline (8-(4-(4-(naphthalen-2-yl)-6-(naphthalen-3-yl)-1,3,5-triazin-2-yl)phenyl)quinoline) (Compound E) and Liq were simultaneously vacuum-deposited at a 1:1 ratio on the light-emitting layer to form a 300Å thick electron transport layer, and 15Å of Liq and 1,200Å of Al were sequentially vacuum-deposited on the electron transport layer to form a cathode, thereby fabricating an organic light-emitting device.
상기 유기발광소자는 6층의 유기 박막층을 가지는 구조로 되어 있으며, 구체적으로 ITO/A(700Å)/B(50Å)/C(700Å)/정공수송보조층[D-53(320Å)]/EML[A-27:C-74:D=3:7:10%](400Å)/E:Liq(300Å)/Liq(15Å)/Al(1,200Å)의 구조로 제작하였다.The above organic light-emitting device has a structure with six organic thin film layers, and is specifically manufactured with a structure of ITO/A(700Å)/B(50Å)/C(700Å)/hole transport auxiliary layer[D-53(320Å)]/EML[A-27:C-74:D=3:7:10%](400Å)/E:Liq(300Å)/Liq(15Å)/Al(1,200Å).
실시예Example 2, 2, 비교예Comparative example 1 및 1 and 비교예Comparative example 22
표 1 및 표 2에 기재한 바와 같이 정공수송보조층, 발광층에 각각의 화합물을 적용하여 실시예 1과 동일한 방법으로 유기발광소자를 제작하였다.An organic light-emitting device was manufactured using the same method as Example 1 by applying each compound to the hole transport auxiliary layer and the light-emitting layer as described in Tables 1 and 2.
평가: 구동 전압 개선 또는 수명 특성 Evaluation: Improvement of driving voltage or life characteristics 상승 효과Rising effect 확인 check
실시예 1 및 2와 비교예 1 및 2에 따른 유기발광소자의 구동전압 및 수명 특성을 평가하였다. 구체적인 측정방법은 하기와 같고, 그 결과는 표 1 및 표 2와 같다.The driving voltage and life characteristics of the organic light-emitting devices according to Examples 1 and 2 and Comparative Examples 1 and 2 were evaluated. The specific measurement methods are as follows, and the results are as shown in Tables 1 and 2.
(1) 수명 측정(1) Life span measurement
제조된 유기발광소자에 대해 폴라로닉스 수명측정 시스템을 사용하여 실시예 1 및 실시예 2, 그리고 비교예 1 및 비교예 2의 소자를 초기휘도(cd/m2) 24,000cd/m2로 발광시키고 시간경과에 따른 휘도의 감소를 측정하여 초기 휘도 대비 90%로 휘도가 감소된 시점을 T90 수명으로 측정하였다.Using a polaronics life measurement system for the manufactured organic light-emitting devices, the devices of Examples 1 and 2, and Comparative Examples 1 and 2 were made to emit light at an initial luminance (cd/m 2 ) of 24,000 cd/m 2 , and the decrease in luminance over time was measured. The point in time when the luminance decreased by 90% compared to the initial luminance was measured as the T90 lifespan.
(2) 구동전압 측정(2) Driving voltage measurement
전류-전압계(Keithley 2400)를 이용하여 15mA/cm2에서 각 소자의 구동전압을 측정하여 결과를 얻었다.The results were obtained by measuring the driving voltage of each device at 15 mA/cm 2 using a current-voltage meter (Keithley 2400).
(3) T90 수명비(%) 계산(3) Calculation of T90 life ratio (%)
표 1에서 비교예 1의 T90 수명을 기준으로 평가하였다.The evaluation was conducted based on the T90 life of Comparative Example 1 in Table 1.
(4) 구동전압비(%) 계산(4) Calculation of driving voltage ratio (%)
표 2에서 비교예 2의 구동전압 값을 기준으로 평가하였다.The evaluation was conducted based on the driving voltage value of Comparative Example 2 in Table 2.
보조층Public transport
Auxiliary layer
제2호스트
(wt%:wt%)1st host:
2nd host
(wt%:wt%)
(wt%)Dopant ratio
(wt%)
보조층Public transport
Auxiliary layer
제2호스트
(wt%:wt%)1st host:
2nd host
(wt%:wt%)
비율
(wt%)Dopant
ratio
(wt%)
표 1 및 2를 참고하면, 본 발명에 따른 유기 광전자 소자용 화합물은 비교예에 따른 유기 광전자 소자용 화합물 대비 구동 전압이 떨어지고, 수명 특성이 향상된 것을 확인할 수 있다.Referring to Tables 1 and 2, it can be confirmed that the compound for an organic optoelectronic device according to the present invention has a lower operating voltage and improved life characteristics compared to the compound for an organic optoelectronic device according to a comparative example.
이상에서 본 발명의 바람직한 실시예들에 대하여 상세하게 설명하였지만 본 발명의 권리범위는 이에 한정되는 것은 아니고 다음의 청구 범위에서 정의하고 있는 본 발명의 기본 개념을 이용한 당업자의 여러 변형 및 개량 형태 또한 본 발명의 권리범위에 속하는 것이다.Although the preferred embodiments of the present invention have been described in detail above, the scope of the present invention is not limited thereto, and various modifications and improvements made by those skilled in the art using the basic concept of the present invention defined in the following claims also fall within the scope of the present invention.
300: 유기 발광 소자
110: 양극
120: 음극
130: 발광층
141: 정공수송층
142: 정공수송보조층
105: 유기층300: Organic light emitting diode
110: Bipolar
120: Negative
130: Emissive layer
141: Hole transport layer
142: Auxiliary layer for positive transport
105: Organic layer
Claims (8)
상기 양극과 상기 음극 사이에 위치하는 발광층,
상기 양극과 상기 발광층 사이에 위치하는 정공수송층, 그리고
상기 발광층과 상기 정공수송층 사이에 위치하는 정공수송보조층
을 포함하고,
상기 발광층은 하기 화학식 1A 내지 화학식 1C 중 어느 하나로 표현되는 제1 화합물 및 하기 화학식 2로 표현되는 제2 화합물을 포함하는 조성물을 포함하고,
상기 정공수송보조층은 하기 화학식 3으로 표현되는 제3 화합물을 포함하는 유기 광전자 소자:
[화학식 1A] [화학식 1B] [화학식 1C]
상기 화학식 1A 내지 화학식 1C에서,
L1 내지 L5는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 또는 이들의 조합이고,
Ar1은 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이고,
R1 내지 R4는 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 아민기, 할로겐, 시아노기 또는 이들의 조합이고,
La2 및 La4는 각각 단일 결합이고,
Ra2는 치환 또는 비치환된 para-바이페닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기이고,
Ra4는 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트렌기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 플루오레닐기, 또는 치환 또는 비치환된 카바졸일기이고;
[화학식 2]
상기 화학식 2에서,
Ar2 및 Ar3은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기 또는 이들의 조합이고,
L6 및 L7은 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,
R5 내지 R10은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 또는 이들의 조합이고,
n은 0 내지 2의 정수 중 하나이고;
[화학식 3]
상기 화학식 3에서,
L8 및 L9는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C20 아릴렌기, 치환 또는 비치환된 C2 내지 C20 헤테로고리기 또는 이들의 조합이고,
R11 내지 R14는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 또는 이들의 조합이고,
Ar4 내지 Ar7은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기 또는 이들의 조합이다.Positive and negative poles facing each other,
A light-emitting layer positioned between the anode and the cathode,
A hole transport layer positioned between the anode and the light-emitting layer, and
A hole transport auxiliary layer located between the above light-emitting layer and the above hole transport layer
Including,
The above-mentioned light-emitting layer comprises a composition including a first compound represented by any one of the following chemical formulas 1A to 1C and a second compound represented by the following chemical formula 2,
The above-mentioned hole transport auxiliary layer is an organic optoelectronic device including a third compound represented by the following chemical formula 3:
[Chemical Formula 1A] [Chemical Formula 1B] [Chemical Formula 1C]
In the above chemical formulas 1A to 1C,
L 1 to L 5 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, or a combination thereof,
Ar 1 is a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof,
R 1 to R 4 are each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C30 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted amine group, halogen, cyano group or a combination thereof,
L a2 and L a4 are each single bonds,
R a2 is a substituted or unsubstituted para-biphenyl group, a substituted or unsubstituted triphenylene group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group,
R a4 is a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted anthracenyl group, a substituted or unsubstituted phenanthrene group, a substituted or unsubstituted triphenylene group, a substituted or unsubstituted fluorenyl group, or a substituted or unsubstituted carbazolyl group;
[Chemical formula 2]
In the above chemical formula 2,
Ar 2 and Ar 3 are each independently a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heteroaryl group, or a combination thereof,
L 6 and L 7 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
R 5 to R 10 are each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted C1 to C30 alkyl group, substituted or unsubstituted C6 to C30 aryl group or a combination thereof,
n is an integer between 0 and 2;
[Chemical Formula 3]
In the above chemical formula 3,
L 8 and L 9 are each independently a single bond, a substituted or unsubstituted C6 to C20 arylene group, a substituted or unsubstituted C2 to C20 heterocyclic group, or a combination thereof,
R 11 to R 14 are each independently hydrogen, deuterium, halogen, cyano group, substituted or unsubstituted C1 to C30 alkyl group, substituted or unsubstituted C6 to C30 aryl group, or a combination thereof,
Ar 4 to Ar 7 are each independently a substituted or unsubstituted C6 to C30 aryl group, a substituted or unsubstituted C2 to C30 heterocyclic group, or a combination thereof.
상기 제1 화합물은 상기 화학식 1B로 표현되는 유기 광전자 소자.In the first paragraph,
The above first compound is an organic optoelectronic device represented by the above chemical formula 1B.
상기 화학식 2는 하기 화학식 2-1로 표현되는 유기 광전자 소자:
[화학식 2-1]
상기 화학식 2-1에서,
R5 내지 R10은 제1항에서 정의한 바와 같고,
*-L6-Ar2 및 *-L7-Ar3은 각각 독립적으로 하기 그룹 Ⅱ에 나열된 치환기 중 하나이며,
[그룹 Ⅱ]
상기 그룹 Ⅱ에서, *은 연결지점이다.In the first paragraph,
The above chemical formula 2 is an organic optoelectronic device represented by the following chemical formula 2-1:
[Chemical Formula 2-1]
In the above chemical formula 2-1,
R 5 to R 10 are as defined in paragraph 1,
*-L 6 -Ar 2 and *-L 7 -Ar 3 are each independently one of the substituents listed in Group II below,
[Group II]
In the above group II, * is a connection point.
상기 화학식 3의 Ar5 내지 Ar7은 각각 독립적으로 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기 또는 이들의 조합인, 유기 광전자 소자.In paragraph 1,
An organic optoelectronic device, wherein Ar 5 to Ar 7 in the chemical formula 3 are each independently a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted dibenzofuranyl group, a substituted or unsubstituted dibenzothiophenyl group, or a combination thereof.
상기 화학식 3은 하기 화학식 3-1로 표현되는 유기 광전자 소자:
[화학식 3-1]
상기 화학식 3-1에서,
L8, L9, R11 내지 R14, 및 Ar4 내지 Ar6은 제1항에서 정의한 바와 같고,
X는 O, S 또는 CRiRj 이며,
Ri, Rj 및 R15 내지 R17은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 치환 또는 비치환된 C1 내지 C30 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 또는 이들의 조합이다.In paragraph 1,
The above chemical formula 3 is an organic optoelectronic device represented by the following chemical formula 3-1:
[Chemical Formula 3-1]
In the above chemical formula 3-1,
L 8 , L 9 , R 11 to R 14 , and Ar 4 to Ar 6 are as defined in paragraph 1,
X is O, S, or CR i R j ,
R i , R j and R 15 to R 17 are each independently hydrogen, deuterium, halogen, cyano group, a substituted or unsubstituted C1 to C30 alkyl group, a substituted or unsubstituted C6 to C30 aryl group, or a combination thereof.
상기 제1 화합물은 하기 화학식 1B로 표현되고,
상기 제2 화합물은 하기 화학식 2-1로 표현되고,
상기 제3 화합물은 하기 화학식 3-1로 표현되는 것인, 유기 광전자 소자:
[화학식 1B] [화학식 2-1] [화학식 3-1]
상기 화학식 1B에서,
La2, La4 및 L1 내지 L4는 각각 단일 결합이고,
L5는 페닐렌기 또는 바이페닐렌기이고,
Ra2는 치환 또는 비치환된 para-바이페닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기이고,
Ra4는 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트렌기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 플루오레닐기, 또는 치환 또는 비치환된 카바졸일기이고,
R1 내지 R4는 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C10 알킬기, 또는 치환 또는 비치환된 C6 내지 C12 아릴기이고;
상기 화학식 2-1에서,
*-L6-Ar2 및 *-L7-Ar3는 각각 독립적으로 하기 그룹 Ⅱ-1에 나열된 치환기 중 B-1 내지 B-4 중 어느 하나이고,
[그룹 Ⅱ-1]
R5 내지 R10은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C10 알킬기, 또는 치환 또는 비치환된 C6 내지 C12 아릴기이며;
상기 화학식 3-1에서,
L8 및 L9는 각각 독립적으로 meta-페닐렌기 또는 para-페닐렌기이고,
Ar4는 페닐기이고,
Ar5 및 Ar6은 각각 독립적으로 치환 또는 비치환된 페닐기, 치환 또는 비치환된 플루오레닐기, 치환 또는 비치환된 디벤조퓨란일기 또는 치환 또는 비치환된 디벤조티오펜일기이며,
R11 내지 R17은 각각 독립적으로 수소, 중수소 또는 페닐기이다.In the first paragraph,
The above first compound is represented by the following chemical formula 1B,
The above second compound is represented by the following chemical formula 2-1,
The third compound is an organic optoelectronic device represented by the following chemical formula 3-1:
[Chemical Formula 1B] [Chemical Formula 2-1] [Chemical Formula 3-1]
In the above chemical formula 1B,
L a2 , L a4 and L 1 to L 4 are each a single bond,
L 5 is a phenylene group or a biphenylene group,
R a2 is a substituted or unsubstituted para-biphenyl group, a substituted or unsubstituted triphenylene group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group,
R a4 is a substituted or unsubstituted phenyl group, a substituted or unsubstituted biphenyl group, a substituted or unsubstituted naphthyl group, a substituted or unsubstituted terphenyl group, a substituted or unsubstituted anthracenyl group, a substituted or unsubstituted phenanthrene group, a substituted or unsubstituted triphenylene group, a substituted or unsubstituted fluorenyl group, or a substituted or unsubstituted carbazolyl group,
R 1 to R 4 are each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C10 alkyl group, or a substituted or unsubstituted C6 to C12 aryl group;
In the above chemical formula 2-1,
*-L 6 -Ar 2 and *-L 7 -Ar 3 are each independently any one of the substituents B-1 to B-4 listed in Group II-1 below,
[Group II-1]
R 5 to R 10 are each independently hydrogen, deuterium, a substituted or unsubstituted C1 to C10 alkyl group, or a substituted or unsubstituted C6 to C12 aryl group;
In the above chemical formula 3-1,
L 8 and L 9 are each independently a meta-phenylene group or a para-phenylene group,
Ar 4 is a phenyl group,
Ar 5 and Ar 6 are each independently a substituted or unsubstituted phenyl group, a substituted or unsubstituted fluorenyl group, a substituted or unsubstituted dibenzofuranyl group, or a substituted or unsubstituted dibenzothiophenyl group,
R 11 to R 17 are each independently hydrogen, deuterium, or a phenyl group.
상기 발광층은 도펀트를 더 포함하는 유기 광전자 소자.In the first paragraph,
An organic optoelectronic device wherein the light-emitting layer further comprises a dopant.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020230063961A KR102787034B1 (en) | 2019-11-20 | 2023-05-17 | Organic optoelectronic device and display device |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020190149623A KR20210061734A (en) | 2019-11-20 | 2019-11-20 | Organic optoelectronic device and display device |
| KR1020230063961A KR102787034B1 (en) | 2019-11-20 | 2023-05-17 | Organic optoelectronic device and display device |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020190149623A Division KR20210061734A (en) | 2019-11-20 | 2019-11-20 | Organic optoelectronic device and display device |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20230074445A KR20230074445A (en) | 2023-05-30 |
| KR102787034B1 true KR102787034B1 (en) | 2025-03-25 |
Family
ID=75907874
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020190149623A Ceased KR20210061734A (en) | 2019-11-20 | 2019-11-20 | Organic optoelectronic device and display device |
| KR1020230063961A Active KR102787034B1 (en) | 2019-11-20 | 2023-05-17 | Organic optoelectronic device and display device |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020190149623A Ceased KR20210061734A (en) | 2019-11-20 | 2019-11-20 | Organic optoelectronic device and display device |
Country Status (2)
| Country | Link |
|---|---|
| KR (2) | KR20210061734A (en) |
| CN (1) | CN112825344B (en) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20250036560A (en) * | 2023-09-07 | 2025-03-14 | 삼성에스디아이 주식회사 | Organic optoelectronic device and display device |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101754715B1 (en) * | 2014-04-08 | 2017-07-10 | 롬엔드하스전자재료코리아유한회사 | Multi-component host material and organic electroluminescence device comprising the same |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20190038254A (en) * | 2017-09-29 | 2019-04-08 | 덕산네오룩스 주식회사 | Compound for organic electronic element, organic electronic element using the same, and an electronic device thereof |
| KR102138823B1 (en) * | 2017-12-27 | 2020-07-28 | 삼성에스디아이 주식회사 | Organic optoelectric device and display device |
-
2019
- 2019-11-20 KR KR1020190149623A patent/KR20210061734A/en not_active Ceased
-
2020
- 2020-11-12 CN CN202011260588.6A patent/CN112825344B/en active Active
-
2023
- 2023-05-17 KR KR1020230063961A patent/KR102787034B1/en active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101754715B1 (en) * | 2014-04-08 | 2017-07-10 | 롬엔드하스전자재료코리아유한회사 | Multi-component host material and organic electroluminescence device comprising the same |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20210061734A (en) | 2021-05-28 |
| CN112825344A (en) | 2021-05-21 |
| KR20230074445A (en) | 2023-05-30 |
| CN112825344B (en) | 2024-09-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102162402B1 (en) | Organic optoelectronic device and display device | |
| CN107849000B (en) | Organic compound, organic photoelectric device and display device | |
| KR102008897B1 (en) | Organic optoelectronic device and display device | |
| CN107623073B (en) | Composition for organic photoelectric device and organic photoelectric device and display device | |
| KR101912107B1 (en) | Organic compound and composition and organic optoelectric device and display device | |
| KR102645136B1 (en) | Compound for organic optoelectronic device, composition for organic optoelectronic device, organic optoelectronic device and display device | |
| EP2182039A2 (en) | Aromatic electroluminescent compounds and organic electroluminescent device using the same | |
| WO2014104535A1 (en) | Compound for organic optoelectronic device, organic light-emitting diode including same, and display apparatus including said organic light-emitting diode | |
| CN103608429A (en) | Novel compounds and organic electronic devices using said compounds | |
| KR102162404B1 (en) | Compound for organic optoelectric device, composition for organic optoelectric device, organic optoelectric device and display device | |
| WO2012165256A1 (en) | Organic electroluminescent element | |
| KR20140100447A (en) | New compounds and organic electronic device using the same | |
| CN117003716A (en) | Triarylamine derivative based on fluorenyl heterocycle and organic electroluminescent device thereof | |
| JP2015526393A (en) | Polycyclic compound and organic electronic device containing the same | |
| KR102864766B1 (en) | Compound for organic optoelectronic device, composition for organic optoelectronic device, organic optoelectronic device and display device | |
| WO2018128255A1 (en) | Compound for organic optoelectronic element, composition for organic optoelectronic element, organic optoelectronic element, and display device | |
| KR102586097B1 (en) | Compound for organic optoelectronic device, organic optoelectronic device and display device | |
| KR102787034B1 (en) | Organic optoelectronic device and display device | |
| KR20220165699A (en) | Compound for organic optoelectronic device and organic optoelectronic device and display device | |
| KR20180035076A (en) | Compound for organic optoelectric device, composition for organic optoelectric device and organic optoelectric device and display device | |
| KR20190031781A (en) | Composition for organic optoelectronic device and organic optoelectronic device and display device | |
| CN107880045A (en) | Compound for organic photoelectric device, the composition for organic photoelectric device and organic photoelectric device and display device | |
| CN112802969A (en) | Organic optoelectronic device and display device | |
| KR102146791B1 (en) | Compound for organic optoelectronic device, and organic optoelectronic device and display device | |
| KR101926022B1 (en) | Organic compound and organic optoelectronic device and display device |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| PA0107 | Divisional application |
Comment text: Divisional Application of Patent Patent event date: 20230517 Patent event code: PA01071R01D Filing date: 20191120 Application number text: 1020190149623 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20230530 Comment text: Request for Examination of Application Patent event code: PA02011R04I Patent event date: 20230517 Comment text: Divisional Application of Patent |
|
| PG1501 | Laying open of application | ||
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20240110 Patent event code: PE09021S01D |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20240805 Comment text: Decision to Refuse Application Patent event code: PE06012S01D |
|
| PX0701 | Decision of registration after re-examination |
Patent event date: 20241230 Comment text: Decision to Grant Registration Patent event code: PX07013S01D |
|
| X701 | Decision to grant (after re-examination) | ||
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20250321 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20250321 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration |