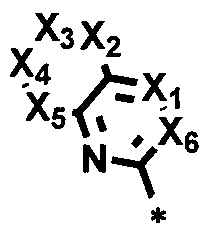KR102529341B1 - 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 - Google Patents
유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 Download PDFInfo
- Publication number
- KR102529341B1 KR102529341B1 KR1020170098913A KR20170098913A KR102529341B1 KR 102529341 B1 KR102529341 B1 KR 102529341B1 KR 1020170098913 A KR1020170098913 A KR 1020170098913A KR 20170098913 A KR20170098913 A KR 20170098913A KR 102529341 B1 KR102529341 B1 KR 102529341B1
- Authority
- KR
- South Korea
- Prior art keywords
- substituted
- unsubstituted
- organic electroluminescent
- formula
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 148
- 239000000463 material Substances 0.000 claims description 62
- 125000003118 aryl group Chemical group 0.000 claims description 51
- 125000000923 (C1-C30) alkyl group Chemical group 0.000 claims description 32
- 125000001072 heteroaryl group Chemical group 0.000 claims description 32
- 229910052739 hydrogen Inorganic materials 0.000 claims description 23
- 239000001257 hydrogen Substances 0.000 claims description 23
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 17
- 229910052805 deuterium Inorganic materials 0.000 claims description 17
- 150000002431 hydrogen Chemical class 0.000 claims description 17
- 229910052736 halogen Inorganic materials 0.000 claims description 15
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 14
- 150000002367 halogens Chemical class 0.000 claims description 14
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 14
- 229910052760 oxygen Inorganic materials 0.000 claims description 11
- 229910052717 sulfur Chemical group 0.000 claims description 11
- 125000005842 heteroatom Chemical group 0.000 claims description 10
- 229910052757 nitrogen Inorganic materials 0.000 claims description 10
- 125000001424 substituent group Chemical group 0.000 claims description 10
- 125000000732 arylene group Chemical group 0.000 claims description 7
- 125000005549 heteroarylene group Chemical group 0.000 claims description 7
- 125000002950 monocyclic group Chemical group 0.000 claims description 7
- 125000005104 aryl silyl group Chemical group 0.000 claims description 6
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 6
- 229910052710 silicon Inorganic materials 0.000 claims description 6
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 5
- 229910052796 boron Inorganic materials 0.000 claims description 5
- 238000000034 method Methods 0.000 claims description 5
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 5
- 229910052698 phosphorus Inorganic materials 0.000 claims description 5
- 125000001769 aryl amino group Chemical group 0.000 claims description 4
- 230000004927 fusion Effects 0.000 claims description 4
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 3
- 125000002723 alicyclic group Chemical group 0.000 claims description 3
- 125000003545 alkoxy group Chemical group 0.000 claims description 3
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 3
- 125000005843 halogen group Chemical group 0.000 claims description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 3
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 claims description 3
- 239000001301 oxygen Chemical group 0.000 claims description 3
- 239000011593 sulfur Chemical group 0.000 claims description 3
- 125000000739 C2-C30 alkenyl group Chemical group 0.000 claims description 2
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims description 2
- 125000003282 alkyl amino group Chemical group 0.000 claims description 2
- 125000004448 alkyl carbonyl group Chemical group 0.000 claims description 2
- 125000004414 alkyl thio group Chemical group 0.000 claims description 2
- 125000000304 alkynyl group Chemical group 0.000 claims description 2
- 125000005129 aryl carbonyl group Chemical group 0.000 claims description 2
- 125000005110 aryl thio group Chemical group 0.000 claims description 2
- 125000004104 aryloxy group Chemical group 0.000 claims description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 2
- 125000000392 cycloalkenyl group Chemical group 0.000 claims description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 2
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 2
- 125000003107 substituted aryl group Chemical group 0.000 claims description 2
- 125000005346 substituted cycloalkyl group Chemical group 0.000 claims description 2
- 125000006822 tri(C1-C30) alkylsilyl group Chemical group 0.000 claims description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims 2
- 239000010410 layer Substances 0.000 description 110
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 72
- 238000002360 preparation method Methods 0.000 description 36
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 30
- 238000002347 injection Methods 0.000 description 25
- 239000007924 injection Substances 0.000 description 25
- -1 pyridopyrimidinyl Chemical group 0.000 description 25
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 24
- 238000004440 column chromatography Methods 0.000 description 23
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 18
- 230000005525 hole transport Effects 0.000 description 18
- 239000002019 doping agent Substances 0.000 description 17
- 238000004519 manufacturing process Methods 0.000 description 17
- 238000006243 chemical reaction Methods 0.000 description 16
- 239000012044 organic layer Substances 0.000 description 15
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 14
- 230000000903 blocking effect Effects 0.000 description 13
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 12
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- 125000000217 alkyl group Chemical group 0.000 description 11
- 239000012153 distilled water Substances 0.000 description 11
- 239000000203 mixture Substances 0.000 description 11
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 10
- 239000007787 solid Substances 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- 230000005684 electric field Effects 0.000 description 9
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 9
- 235000019341 magnesium sulphate Nutrition 0.000 description 9
- 238000001771 vacuum deposition Methods 0.000 description 8
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 7
- 125000004432 carbon atom Chemical group C* 0.000 description 7
- 239000011368 organic material Substances 0.000 description 7
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- AMSJIGYDHCSSRE-UHFFFAOYSA-N 3,14-diazahexacyclo[11.11.0.02,10.04,9.015,24.016,21]tetracosa-1(24),2,4,6,8,10,12,14,16,18,20,22-dodecaene Chemical group C1=CC=C2C=CC3=C4C5=NC6=CC=CC=C6C5=CC=C4N=C3C2=C1 AMSJIGYDHCSSRE-UHFFFAOYSA-N 0.000 description 6
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 6
- 125000004429 atom Chemical group 0.000 description 6
- 229910052751 metal Inorganic materials 0.000 description 6
- 239000002184 metal Substances 0.000 description 6
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 6
- 238000010992 reflux Methods 0.000 description 6
- MZSAMHOCTRNOIZ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-phenylaniline Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(NC2=CC=CC=C2)C=CC=1 MZSAMHOCTRNOIZ-UHFFFAOYSA-N 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 238000000151 deposition Methods 0.000 description 5
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical group C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 5
- 238000000605 extraction Methods 0.000 description 5
- 239000010408 film Substances 0.000 description 5
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 5
- 125000001624 naphthyl group Chemical group 0.000 description 5
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 5
- KPGPIQKEKAEAHM-UHFFFAOYSA-N 2-chloro-3-phenylquinoxaline Chemical compound ClC1=NC2=CC=CC=C2N=C1C1=CC=CC=C1 KPGPIQKEKAEAHM-UHFFFAOYSA-N 0.000 description 4
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical group CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical class C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 238000004770 highest occupied molecular orbital Methods 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- ZEEBGORNQSEQBE-UHFFFAOYSA-N [2-(3-phenylphenoxy)-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound C1(=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)C1=CC=CC=C1 ZEEBGORNQSEQBE-UHFFFAOYSA-N 0.000 description 3
- ABRVLXLNVJHDRQ-UHFFFAOYSA-N [2-pyridin-3-yl-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound FC(C1=CC(=CC(=N1)C=1C=NC=CC=1)CN)(F)F ABRVLXLNVJHDRQ-UHFFFAOYSA-N 0.000 description 3
- YCOXTKKNXUZSKD-UHFFFAOYSA-N as-o-xylenol Natural products CC1=CC=C(O)C=C1C YCOXTKKNXUZSKD-UHFFFAOYSA-N 0.000 description 3
- 150000004770 chalcogenides Chemical class 0.000 description 3
- IYYZUPMFVPLQIF-ALWQSETLSA-N dibenzothiophene Chemical group C1=CC=CC=2[34S]C3=C(C=21)C=CC=C3 IYYZUPMFVPLQIF-ALWQSETLSA-N 0.000 description 3
- IYYZUPMFVPLQIF-UHFFFAOYSA-N dibenzothiophene sulfoxide Chemical group C1=CC=C2C3=CC=CC=C3SC2=C1 IYYZUPMFVPLQIF-UHFFFAOYSA-N 0.000 description 3
- 238000004821 distillation Methods 0.000 description 3
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 3
- SNHMUERNLJLMHN-UHFFFAOYSA-N iodobenzene Chemical compound IC1=CC=CC=C1 SNHMUERNLJLMHN-UHFFFAOYSA-N 0.000 description 3
- 229910052741 iridium Inorganic materials 0.000 description 3
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 3
- 229910001507 metal halide Inorganic materials 0.000 description 3
- 150000005309 metal halides Chemical class 0.000 description 3
- 229910044991 metal oxide Inorganic materials 0.000 description 3
- 150000004706 metal oxides Chemical class 0.000 description 3
- 150000002739 metals Chemical class 0.000 description 3
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 3
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 3
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 3
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 2
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- PJRGCJBBXGNEGD-UHFFFAOYSA-N 2-bromo-9h-carbazole Chemical compound C1=CC=C2C3=CC=C(Br)C=C3NC2=C1 PJRGCJBBXGNEGD-UHFFFAOYSA-N 0.000 description 2
- AELILXBWWJSIMK-UHFFFAOYSA-N 2-chloro-4-naphthalen-2-ylquinazoline Chemical compound C1=CC=CC2=NC(Cl)=NC(C=3C=C4C=CC=CC4=CC=3)=C21 AELILXBWWJSIMK-UHFFFAOYSA-N 0.000 description 2
- ISWSFPQWSDIVGH-UHFFFAOYSA-N 3-chloronaphthalen-2-amine Chemical compound C1=CC=C2C=C(Cl)C(N)=CC2=C1 ISWSFPQWSDIVGH-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- SAHIZENKTPRYSN-UHFFFAOYSA-N [2-[3-(phenoxymethyl)phenoxy]-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound O(C1=CC=CC=C1)CC=1C=C(OC2=NC(=CC(=C2)CN)C(F)(F)F)C=CC=1 SAHIZENKTPRYSN-UHFFFAOYSA-N 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 235000010290 biphenyl Nutrition 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- SSJXIUAHEKJCMH-UHFFFAOYSA-N cyclohexane-1,2-diamine Chemical compound NC1CCCCC1N SSJXIUAHEKJCMH-UHFFFAOYSA-N 0.000 description 2
- 230000005281 excited state Effects 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- VVVPGLRKXQSQSZ-UHFFFAOYSA-N indolo[3,2-c]carbazole Chemical class C1=CC=CC2=NC3=C4C5=CC=CC=C5N=C4C=CC3=C21 VVVPGLRKXQSQSZ-UHFFFAOYSA-N 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 2
- 229940078552 o-xylene Drugs 0.000 description 2
- 229910052762 osmium Inorganic materials 0.000 description 2
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 2
- 230000001590 oxidative effect Effects 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 229910052697 platinum Inorganic materials 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- 229910052761 rare earth metal Inorganic materials 0.000 description 2
- 150000002910 rare earth metals Chemical class 0.000 description 2
- 230000027756 respiratory electron transport chain Effects 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 125000003003 spiro group Chemical group 0.000 description 2
- 239000002344 surface layer Substances 0.000 description 2
- 125000001935 tetracenyl group Chemical group C1(=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C12)* 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- 239000010409 thin film Substances 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 150000003624 transition metals Chemical class 0.000 description 2
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- WRGKKASJBOREMB-UHFFFAOYSA-N 1,4-dibromo-2-nitrobenzene Chemical compound [O-][N+](=O)C1=CC(Br)=CC=C1Br WRGKKASJBOREMB-UHFFFAOYSA-N 0.000 description 1
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 description 1
- HQHHKYXPFKHLBF-UHFFFAOYSA-N 1-bromo-4-iodonaphthalene Chemical compound C1=CC=C2C(Br)=CC=C(I)C2=C1 HQHHKYXPFKHLBF-UHFFFAOYSA-N 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- HIYWOHBEPVGIQN-UHFFFAOYSA-N 1h-benzo[g]indole Chemical compound C1=CC=CC2=C(NC=C3)C3=CC=C21 HIYWOHBEPVGIQN-UHFFFAOYSA-N 0.000 description 1
- NUQHGLAGHWFIMW-UHFFFAOYSA-N 2-chloro-3-naphthalen-2-ylquinoxaline Chemical compound C1=CC=CC2=CC(C3=NC4=CC=CC=C4N=C3Cl)=CC=C21 NUQHGLAGHWFIMW-UHFFFAOYSA-N 0.000 description 1
- SFKMVPQJJGJCMI-UHFFFAOYSA-N 2-chloro-4-phenylquinazoline Chemical compound C=12C=CC=CC2=NC(Cl)=NC=1C1=CC=CC=C1 SFKMVPQJJGJCMI-UHFFFAOYSA-N 0.000 description 1
- FRNLBIWVMVNNAZ-UHFFFAOYSA-N 2-iodonaphthalene Chemical compound C1=CC=CC2=CC(I)=CC=C21 FRNLBIWVMVNNAZ-UHFFFAOYSA-N 0.000 description 1
- 229910004261 CaF 2 Inorganic materials 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 229910018068 Li 2 O Inorganic materials 0.000 description 1
- 101150003085 Pdcl gene Proteins 0.000 description 1
- 229910003564 SiAlON Inorganic materials 0.000 description 1
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 description 1
- XSTXAVWGXDQKEL-UHFFFAOYSA-N Trichloroethylene Chemical group ClC=C(Cl)Cl XSTXAVWGXDQKEL-UHFFFAOYSA-N 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001339 alkali metal compounds Chemical class 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- SMWDFEZZVXVKRB-UHFFFAOYSA-N anhydrous quinoline Natural products N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 150000004984 aromatic diamines Chemical class 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 125000002047 benzodioxolyl group Chemical group O1OC(C2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000005872 benzooxazolyl group Chemical group 0.000 description 1
- 125000005874 benzothiadiazolyl group Chemical group 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- PJVZQNVOUCOJGE-CALCHBBNSA-N chembl289853 Chemical compound N1([C@H]2CC[C@H](O2)N2[C]3C=CC=CC3=C3C2=C11)C2=CC=C[CH]C2=C1C1=C3C(=O)N(C)C1=O PJVZQNVOUCOJGE-CALCHBBNSA-N 0.000 description 1
- 239000007810 chemical reaction solvent Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 125000002676 chrysenyl group Chemical group C1(=CC=CC=2C3=CC=C4C=CC=CC4=C3C=CC12)* 0.000 description 1
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- ONCCWDRMOZMNSM-FBCQKBJTSA-N compound Z Chemical compound N1=C2C(=O)NC(N)=NC2=NC=C1C(=O)[C@H]1OP(O)(=O)OC[C@H]1O ONCCWDRMOZMNSM-FBCQKBJTSA-N 0.000 description 1
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000005137 deposition process Methods 0.000 description 1
- 125000005299 dibenzofluorenyl group Chemical group C1(=CC=CC2=C3C(=C4C=5C=CC=CC5CC4=C21)C=CC=C3)* 0.000 description 1
- 150000004826 dibenzofurans Chemical class 0.000 description 1
- 125000005509 dibenzothiophenyl group Chemical group 0.000 description 1
- 229940117389 dichlorobenzene Drugs 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000005611 electricity Effects 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 125000003914 fluoranthenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC=C4C1=C23)* 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 125000003838 furazanyl group Chemical group 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 229960005544 indolocarbazole Drugs 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 239000011229 interlayer Substances 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 238000007733 ion plating Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 125000001977 isobenzofuranyl group Chemical group C=1(OC=C2C=CC=CC12)* 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- KUDPGZONDFORKU-UHFFFAOYSA-N n-chloroaniline Chemical compound ClNC1=CC=CC=C1 KUDPGZONDFORKU-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- KPTRDYONBVUWPD-UHFFFAOYSA-N naphthalen-2-ylboronic acid Chemical compound C1=CC=CC2=CC(B(O)O)=CC=C21 KPTRDYONBVUWPD-UHFFFAOYSA-N 0.000 description 1
- 125000004957 naphthylene group Chemical group 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- 125000004934 phenanthridinyl group Chemical group C1(=CC=CC2=NC=C3C=CC=CC3=C12)* 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000001725 pyrenyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000005551 pyridylene group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052814 silicon oxide Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical compound C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 description 1
- 125000005247 tetrazinyl group Chemical group N1=NN=NC(=C1)* 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- BDZBKCUKTQZUTL-UHFFFAOYSA-N triethyl phosphite Chemical compound CCOP(OCC)OCC BDZBKCUKTQZUTL-UHFFFAOYSA-N 0.000 description 1
- 125000003960 triphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C3=CC=CC=C3C12)* 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/90—Multiple hosts in the emissive layer
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
Claims (8)
- 하기 화학식 1로 표시되는 유기 전계 발광 화합물.
[화학식 1]
[화학식 1-a]
상기 화학식 1에서,
x와 y, y 와 z, p와 q, q와 r 중 하나 이상은 화학식 1-a의 * 위치와 융합하고, 이 경우, x와 y, y와 z가 동시에 화학식 1-a의 * 위치와 융합하는 것은 제외되고, p와 q, q와 r이 동시에 화학식 1-a의 * 위치와 융합하는 것은 제외되며;
L은 단일 결합, 치환 또는 비치환된 (C6-C30)아릴렌, 또는 치환 또는 비치환된 (5-30원)헤테로아릴렌이고;
X1은 N이고;
X2 내지 X5는 각각 독립적으로 CR4이며, 여기서 R4는 수소 또는 중수소이고;
X6은 CR4이며, 여기서 R4는 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이며;
Ar1은 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이고;
R1 내지 R3은 각각 독립적으로 수소, 중수소, 할로겐, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 치환 또는 비치환된 (5-30원)헤테로아릴, 치환 또는 비치환된 (C3-C30)시클로알킬, 치환 또는 비치환된 (3-7원)헤테로시클로알킬, 치환 또는 비치환된 (C6-C30)아르(C1-C30)알킬, -NR11R12, -SiR13R14R15, -SR16, -OR17, 시아노, 니트로, 또는 하이드록시이며;
R11 내지 R17은 각각 독립적으로 수소, 중수소, 할로겐, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 치환 또는 비치환된 (5-30원)헤테로아릴, 치환 또는 비치환된 (3-7원)헤테로시클로알킬, 또는 치환 또는 비치환된 (C3-C30)시클로알킬이거나; 인접한 치환체와 연결되어 치환 또는 비치환된 (3-30원)의 단일환 또는 다환의 지환족, 방향족, 또는 이들의 조합의 고리를 형성할 수 있으며, 상기 형성된 지환족, 방향족, 또는 이들의 조합의 고리는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자를 포함할 수 있으며;
a 내지 c는 각각 독립적으로 1 내지 4의 정수이고, a 내지 c가 각각 2 이상의 정수인 경우, 각각의 R1 내지 R3은 동일하거나 상이할 수 있으며;
상기 헤테로아릴(렌) 또는 상기 헤테로시클로알킬은 B, N, O, S, Si 및 P로부터 선택된 하나 이상의 헤테로원자를 포함한다. - 제1항에 있어서, L, Ar1, R1 내지 R4, 및 R11 내지 R17에서, 치환된 알킬, 치환된 아릴(렌), 치환된 헤테로아릴(렌), 치환된 시클로알킬, 치환된 헤테로시클로알킬, 치환된 아르알킬, 및 치환된 단일환 또는 다환의 지환족, 방향족, 또는 이들의 조합의 고리의 치환체는 각각 독립적으로 중수소; 할로겐; 시아노; 카르복실; 니트로; 히드록시; (C1-C30)알킬; 할로(C1-C30)알킬; (C2-C30)알케닐; (C2-C30)알키닐; (C1-C30)알콕시; (C1-C30)알킬티오; (C3-C30)시클로알킬; (C3-C30)시클로알케닐; (3-7원)헤테로시클로알킬; (C6-C30)아릴옥시; (C6-C30)아릴티오; (C6-C30)아릴; (5-30원)헤테로아릴; 트리(C1-C30)알킬실릴; 트리(C6-C30)아릴실릴; 디(C1-C30)알킬(C6-C30)아릴실릴; (C1-C30)알킬디(C6-C30)아릴실릴; 아미노; 모노- 또는 디- (C1-C30)알킬아미노; 모노- 또는 디- (C6-C30)아릴아미노; (C1-C30)알킬(C6-C30)아릴아미노; (C1-C30)알킬카보닐; (C1-C30)알콕시카보닐; (C6-C30)아릴카보닐; 디(C6-C30)아릴보로닐; 디(C1-C30)알킬보로닐; (C1-C30)알킬(C6-C30)아릴보로닐; (C6-C30)아르(C1-C30)알킬; 및 (C1-C30)알킬(C6-C30)아릴로 이루어진 군으로부터 선택되는 하나 이상인, 유기 전계 발광 화합물.
- 제1항에 기재된 유기 전계 발광 화합물을 포함하는, 유기 전계 발광 소자.
- 제6항에 있어서, 상기 유기 전계 발광 화합물을 호스트로서 포함하는, 유기 전계 발광 소자.
- 제1항에 기재된 유기 전계 발광 화합물을 포함하는, 디스플레이 장치.
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US16/331,543 US11283028B2 (en) | 2016-10-05 | 2017-08-22 | Organic electroluminescent compound and organic electroluminescent device comprising the same |
| CN201780057564.0A CN109790455B (zh) | 2016-10-05 | 2017-08-22 | 有机电致发光化合物和包括其的有机电致发光装置 |
| PCT/KR2017/009141 WO2018066812A1 (en) | 2016-10-05 | 2017-08-22 | Organic electroluminescent compound and organic electroluminescent device comprising the same |
| TW106132478A TWI745435B (zh) | 2016-10-05 | 2017-09-21 | 有機電致發光化合物及包括其之有機電致發光裝置 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20160128230 | 2016-10-05 | ||
| KR1020160128230 | 2016-10-05 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20180037881A KR20180037881A (ko) | 2018-04-13 |
| KR102529341B1 true KR102529341B1 (ko) | 2023-05-09 |
Family
ID=61974156
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020170098913A Active KR102529341B1 (ko) | 2016-10-05 | 2017-08-04 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR102529341B1 (ko) |
| CN (1) | CN109790455B (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111057014A (zh) * | 2019-12-27 | 2020-04-24 | 吉林奥来德光电材料股份有限公司 | 一种有机电致发光化合物及其制备方法与电致发光器件 |
| KR102745170B1 (ko) * | 2020-03-03 | 2024-12-19 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101511072B1 (ko) * | 2009-03-20 | 2015-04-10 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 전계 발광소자 |
| TWI429650B (zh) | 2010-02-12 | 2014-03-11 | Nippon Steel & Sumikin Chem Co | Organic electroluminescent elements |
| KR102158000B1 (ko) * | 2013-09-26 | 2020-09-22 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 소자 |
| KR102214622B1 (ko) | 2013-12-27 | 2021-02-15 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR102291492B1 (ko) * | 2015-01-16 | 2021-08-20 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR102110983B1 (ko) * | 2016-04-14 | 2020-05-14 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102479135B1 (ko) * | 2016-04-18 | 2022-12-21 | 롬엔드하스전자재료코리아유한회사 | 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
| KR102211337B1 (ko) * | 2016-05-19 | 2021-02-03 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102018685B1 (ko) * | 2016-07-29 | 2019-09-04 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102170190B1 (ko) * | 2016-08-24 | 2020-10-26 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102863646B1 (ko) * | 2016-09-30 | 2025-09-24 | 듀폰스페셜티머터리얼스코리아 유한회사 | 유기 전계 발광 재료 및 이를 포함하는 유기 전계 발광 소자 |
-
2017
- 2017-08-04 KR KR1020170098913A patent/KR102529341B1/ko active Active
- 2017-08-22 CN CN201780057564.0A patent/CN109790455B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN109790455B (zh) | 2023-05-26 |
| KR20180037881A (ko) | 2018-04-13 |
| CN109790455A (zh) | 2019-05-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102533792B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102129236B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102792006B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102112786B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| CN110078742B (zh) | 新颖有机电致发光化合物、和包含其的多组分主体材料与有机电致发光装置 | |
| KR102372950B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102666615B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102430648B1 (ko) | 정공 전달 재료 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102516317B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20230029748A (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102455660B1 (ko) | 유기 전계 발광 소자 | |
| KR102794564B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102728866B1 (ko) | 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102552768B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| TWI745435B (zh) | 有機電致發光化合物及包括其之有機電致發光裝置 | |
| KR102820821B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20160037107A (ko) | 유기 전계 발광 화합물, 및 이를 포함하는 유기 전계 발광 재료 및 유기 전계 발광 소자 | |
| KR20170129599A (ko) | 유기 전계 발광 화합물, 유기 전계 발광 재료, 및 이를 포함하는 유기 전계 발광 소자 | |
| JP2021093526A (ja) | 有機エレクトロルミネセント化合物及びこれを含む有機エレクトロルミネセントデバイス | |
| KR102683908B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20240132232A (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102158472B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102432976B1 (ko) | 복수종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102062022B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102530113B1 (ko) | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20170804 |
|
| PG1501 | Laying open of application | ||
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20200721 Comment text: Request for Examination of Application Patent event code: PA02011R01I Patent event date: 20170804 Comment text: Patent Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20220817 Patent event code: PE09021S01D |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20230206 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20230502 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20230503 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration |