KR101867399B1 - Perylene-based compounds, method of producing the same, and fluorescent dye including the same - Google Patents
Perylene-based compounds, method of producing the same, and fluorescent dye including the same Download PDFInfo
- Publication number
- KR101867399B1 KR101867399B1 KR1020160109172A KR20160109172A KR101867399B1 KR 101867399 B1 KR101867399 B1 KR 101867399B1 KR 1020160109172 A KR1020160109172 A KR 1020160109172A KR 20160109172 A KR20160109172 A KR 20160109172A KR 101867399 B1 KR101867399 B1 KR 101867399B1
- Authority
- KR
- South Korea
- Prior art keywords
- group
- compound
- ring
- mmol
- perylene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 title claims abstract description 32
- 239000007850 fluorescent dye Substances 0.000 title claims abstract description 23
- 238000000034 method Methods 0.000 title claims abstract description 11
- 150000001875 compounds Chemical class 0.000 title claims description 59
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 title claims description 21
- -1 perylene compound Chemical class 0.000 claims abstract description 134
- 238000006243 chemical reaction Methods 0.000 claims description 17
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 claims description 14
- 239000003960 organic solvent Substances 0.000 claims description 14
- LLEMOWNGBBNAJR-UHFFFAOYSA-N biphenyl-2-ol Chemical compound OC1=CC=CC=C1C1=CC=CC=C1 LLEMOWNGBBNAJR-UHFFFAOYSA-N 0.000 claims description 13
- 229910052736 halogen Inorganic materials 0.000 claims description 11
- 150000002367 halogens Chemical class 0.000 claims description 10
- 125000005157 alkyl carboxy group Chemical group 0.000 claims description 9
- 229910052739 hydrogen Inorganic materials 0.000 claims description 9
- 239000001257 hydrogen Substances 0.000 claims description 9
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 7
- 125000001624 naphthyl group Chemical group 0.000 claims description 6
- SKDGWNHUETZZCS-UHFFFAOYSA-N 2,3-ditert-butylphenol Chemical compound CC(C)(C)C1=CC=CC(O)=C1C(C)(C)C SKDGWNHUETZZCS-UHFFFAOYSA-N 0.000 claims description 5
- 239000002253 acid Substances 0.000 claims description 5
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 claims description 4
- 238000001914 filtration Methods 0.000 claims description 4
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 150000002825 nitriles Chemical class 0.000 claims description 4
- QXZBVXIQHVQHNX-UHFFFAOYSA-N 2-tert-butyl-3-methoxyphenol Chemical compound COC1=CC=CC(O)=C1C(C)(C)C QXZBVXIQHVQHNX-UHFFFAOYSA-N 0.000 claims description 3
- 150000005323 carbonate salts Chemical class 0.000 claims description 3
- 239000000463 material Substances 0.000 claims description 3
- KJCVRFUGPWSIIH-UHFFFAOYSA-N 1-naphthol Chemical compound C1=CC=C2C(O)=CC=CC2=C1 KJCVRFUGPWSIIH-UHFFFAOYSA-N 0.000 claims description 2
- DSCJETUEDFKYGN-UHFFFAOYSA-N 2-Methoxybenzenethiol Chemical compound COC1=CC=CC=C1S DSCJETUEDFKYGN-UHFFFAOYSA-N 0.000 claims description 2
- WJQOZHYUIDYNHM-UHFFFAOYSA-N 2-tert-Butylphenol Chemical compound CC(C)(C)C1=CC=CC=C1O WJQOZHYUIDYNHM-UHFFFAOYSA-N 0.000 claims description 2
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 claims description 2
- 230000001376 precipitating effect Effects 0.000 claims description 2
- 239000000376 reactant Substances 0.000 claims description 2
- 150000002431 hydrogen Chemical class 0.000 claims 2
- 125000004802 cyanophenyl group Chemical group 0.000 claims 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 63
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 60
- 238000004458 analytical method Methods 0.000 description 60
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 40
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 34
- 125000003118 aryl group Chemical group 0.000 description 31
- 238000005033 Fourier transform infrared spectroscopy Methods 0.000 description 30
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 30
- 238000002844 melting Methods 0.000 description 30
- 230000008018 melting Effects 0.000 description 30
- 239000007787 solid Substances 0.000 description 30
- 238000003756 stirring Methods 0.000 description 26
- 230000015572 biosynthetic process Effects 0.000 description 25
- 238000003786 synthesis reaction Methods 0.000 description 25
- 239000013078 crystal Substances 0.000 description 22
- 125000000217 alkyl group Chemical group 0.000 description 20
- 239000002244 precipitate Substances 0.000 description 20
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 18
- 235000019270 ammonium chloride Nutrition 0.000 description 17
- 239000007864 aqueous solution Substances 0.000 description 16
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 15
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 14
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 14
- 125000000623 heterocyclic group Chemical group 0.000 description 14
- 125000004432 carbon atom Chemical group C* 0.000 description 13
- 229940125773 compound 10 Drugs 0.000 description 13
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 13
- 239000011259 mixed solution Substances 0.000 description 12
- 125000003545 alkoxy group Chemical group 0.000 description 11
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 11
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 10
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 9
- 229910000024 caesium carbonate Inorganic materials 0.000 description 9
- 125000000753 cycloalkyl group Chemical group 0.000 description 9
- 239000000543 intermediate Substances 0.000 description 9
- 229910000027 potassium carbonate Inorganic materials 0.000 description 9
- 125000004054 acenaphthylenyl group Chemical group C1(=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 8
- 125000005578 chrysene group Chemical group 0.000 description 8
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 8
- 125000004104 aryloxy group Chemical group 0.000 description 7
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 7
- 229940125904 compound 1 Drugs 0.000 description 7
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 7
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 7
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 7
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 7
- 229910000029 sodium carbonate Inorganic materials 0.000 description 7
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 7
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 6
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 125000003277 amino group Chemical group 0.000 description 6
- 229910052794 bromium Inorganic materials 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- 125000004093 cyano group Chemical group *C#N 0.000 description 6
- 125000001424 substituent group Chemical group 0.000 description 6
- 125000005579 tetracene group Chemical group 0.000 description 6
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 5
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 5
- 125000006414 CCl Chemical group ClC* 0.000 description 5
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 5
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 5
- 239000007795 chemical reaction product Substances 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 229940126543 compound 14 Drugs 0.000 description 5
- 125000000000 cycloalkoxy group Chemical group 0.000 description 5
- 239000000975 dye Substances 0.000 description 5
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 5
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 5
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical group C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 5
- 239000000049 pigment Substances 0.000 description 5
- 125000005548 pyrenylene group Chemical group 0.000 description 5
- 125000001935 tetracenyl group Chemical group C1(=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C12)* 0.000 description 5
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 4
- 229940061334 2-phenylphenol Drugs 0.000 description 4
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical group CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 4
- 125000000748 anthracen-2-yl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C([H])=C([*])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 4
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 4
- 125000005264 aryl amine group Chemical group 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 125000005583 coronene group Chemical group 0.000 description 4
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 4
- 125000005843 halogen group Chemical group 0.000 description 4
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 4
- 235000010292 orthophenyl phenol Nutrition 0.000 description 4
- 229910052760 oxygen Inorganic materials 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 4
- LLHKCFNBLRBOGN-UHFFFAOYSA-N propylene glycol methyl ether acetate Chemical compound COCC(C)OC(C)=O LLHKCFNBLRBOGN-UHFFFAOYSA-N 0.000 description 4
- LNKHTYQPVMAJSF-UHFFFAOYSA-N pyranthrene Chemical group C1=C2C3=CC=CC=C3C=C(C=C3)C2=C2C3=CC3=C(C=CC=C4)C4=CC4=CC=C1C2=C34 LNKHTYQPVMAJSF-UHFFFAOYSA-N 0.000 description 4
- PGXOVVAJURGPLL-UHFFFAOYSA-N trinaphthylene Chemical group C1=CC=C2C=C3C4=CC5=CC=CC=C5C=C4C4=CC5=CC=CC=C5C=C4C3=CC2=C1 PGXOVVAJURGPLL-UHFFFAOYSA-N 0.000 description 4
- 125000005580 triphenylene group Chemical group 0.000 description 4
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 3
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 3
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 3
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 description 3
- TWOSGOLFNJPHJX-UHFFFAOYSA-N 1-ethylchrysene Chemical group C1=CC2=C3C=CC=CC3=CC=C2C2=C1C(CC)=CC=C2 TWOSGOLFNJPHJX-UHFFFAOYSA-N 0.000 description 3
- QHPQWRBYOIRBIT-UHFFFAOYSA-N 4-tert-butylphenol Chemical compound CC(C)(C)C1=CC=C(O)C=C1 QHPQWRBYOIRBIT-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 125000006519 CCH3 Chemical group 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- YFNONBGXNFCTMM-UHFFFAOYSA-N butoxybenzene Chemical group CCCCOC1=CC=CC=C1 YFNONBGXNFCTMM-UHFFFAOYSA-N 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 229940125797 compound 12 Drugs 0.000 description 3
- DOBRDRYODQBAMW-UHFFFAOYSA-N copper(i) cyanide Chemical compound [Cu+].N#[C-] DOBRDRYODQBAMW-UHFFFAOYSA-N 0.000 description 3
- 239000002270 dispersing agent Substances 0.000 description 3
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 3
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 239000000976 ink Substances 0.000 description 3
- HUMMCEUVDBVXTQ-UHFFFAOYSA-N naphthalen-1-ylboronic acid Chemical compound C1=CC=C2C(B(O)O)=CC=CC2=C1 HUMMCEUVDBVXTQ-UHFFFAOYSA-N 0.000 description 3
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- JQQSUOJIMKJQHS-UHFFFAOYSA-N pentaphenyl group Chemical group C1=CC=CC2=CC3=CC=C4C=C5C=CC=CC5=CC4=C3C=C12 JQQSUOJIMKJQHS-UHFFFAOYSA-N 0.000 description 3
- 125000001388 picenyl group Chemical group C1(=CC=CC2=CC=C3C4=CC=C5C=CC=CC5=C4C=CC3=C21)* 0.000 description 3
- 125000005581 pyrene group Chemical group 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- UAOUIVVJBYDFKD-XKCDOFEDSA-N (1R,9R,10S,11R,12R,15S,18S,21R)-10,11,21-trihydroxy-8,8-dimethyl-14-methylidene-4-(prop-2-enylamino)-20-oxa-5-thia-3-azahexacyclo[9.7.2.112,15.01,9.02,6.012,18]henicosa-2(6),3-dien-13-one Chemical compound C([C@@H]1[C@@H](O)[C@@]23C(C1=C)=O)C[C@H]2[C@]12C(N=C(NCC=C)S4)=C4CC(C)(C)[C@H]1[C@H](O)[C@]3(O)OC2 UAOUIVVJBYDFKD-XKCDOFEDSA-N 0.000 description 2
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 2
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 2
- CEBAHYWORUOILU-UHFFFAOYSA-N (4-cyanophenyl)boronic acid Chemical compound OB(O)C1=CC=C(C#N)C=C1 CEBAHYWORUOILU-UHFFFAOYSA-N 0.000 description 2
- 125000000027 (C1-C10) alkoxy group Chemical group 0.000 description 2
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 2
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 2
- ADOBXTDBFNCOBN-UHFFFAOYSA-N 1-heptadecene Chemical group CCCCCCCCCCCCCCCC=C ADOBXTDBFNCOBN-UHFFFAOYSA-N 0.000 description 2
- BMVXCPBXGZKUPN-UHFFFAOYSA-N 1-hexanamine Chemical compound CCCCCCN BMVXCPBXGZKUPN-UHFFFAOYSA-N 0.000 description 2
- PAMIQIKDUOTOBW-UHFFFAOYSA-N 1-methylpiperidine Chemical compound CN1CCCCC1 PAMIQIKDUOTOBW-UHFFFAOYSA-N 0.000 description 2
- ICKWICRCANNIBI-UHFFFAOYSA-N 2,4-di-tert-butylphenol Chemical compound CC(C)(C)C1=CC=C(O)C(C(C)(C)C)=C1 ICKWICRCANNIBI-UHFFFAOYSA-N 0.000 description 2
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 2
- ZAZPDOYUCVFPOI-UHFFFAOYSA-N 2-methylpropylboronic acid Chemical compound CC(C)CB(O)O ZAZPDOYUCVFPOI-UHFFFAOYSA-N 0.000 description 2
- JWAZRIHNYRIHIV-UHFFFAOYSA-N 2-naphthol Chemical compound C1=CC=CC2=CC(O)=CC=C21 JWAZRIHNYRIHIV-UHFFFAOYSA-N 0.000 description 2
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 2
- NIFAOMSJMGEFTQ-UHFFFAOYSA-N 4-methoxybenzenethiol Chemical compound COC1=CC=C(S)C=C1 NIFAOMSJMGEFTQ-UHFFFAOYSA-N 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- 125000003860 C1-C20 alkoxy group Chemical group 0.000 description 2
- KCBAMQOKOLXLOX-BSZYMOERSA-N CC1=C(SC=N1)C2=CC=C(C=C2)[C@H](C)NC(=O)[C@@H]3C[C@H](CN3C(=O)[C@H](C(C)(C)C)NC(=O)CCCCCCCCCCNCCCONC(=O)C4=C(C(=C(C=C4)F)F)NC5=C(C=C(C=C5)I)F)O Chemical compound CC1=C(SC=N1)C2=CC=C(C=C2)[C@H](C)NC(=O)[C@@H]3C[C@H](CN3C(=O)[C@H](C(C)(C)C)NC(=O)CCCCCCCCCCNCCCONC(=O)C4=C(C(=C(C=C4)F)F)NC5=C(C=C(C=C5)I)F)O KCBAMQOKOLXLOX-BSZYMOERSA-N 0.000 description 2
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 2
- 229940126657 Compound 17 Drugs 0.000 description 2
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 2
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 2
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- 150000001335 aliphatic alkanes Chemical class 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 2
- 230000008033 biological extinction Effects 0.000 description 2
- YLNJGHNUXCVDIX-UHFFFAOYSA-N bis(2-methylpropyl) perylene-3,9-dicarboxylate Chemical compound C=12C3=CC=CC2=C(C(=O)OCC(C)C)C=CC=1C1=CC=CC2=C1C3=CC=C2C(=O)OCC(C)C YLNJGHNUXCVDIX-UHFFFAOYSA-N 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 239000006103 coloring component Substances 0.000 description 2
- 229940126142 compound 16 Drugs 0.000 description 2
- 229940125810 compound 20 Drugs 0.000 description 2
- 229940126086 compound 21 Drugs 0.000 description 2
- 229940126208 compound 22 Drugs 0.000 description 2
- 229940125833 compound 23 Drugs 0.000 description 2
- 229940125961 compound 24 Drugs 0.000 description 2
- 229940125846 compound 25 Drugs 0.000 description 2
- 229940125851 compound 27 Drugs 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 description 2
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 2
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 2
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000004185 ester group Chemical group 0.000 description 2
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 2
- 125000003824 heptacenyl group Chemical group C1(=CC=CC2=CC3=CC4=CC5=CC6=CC7=CC=CC=C7C=C6C=C5C=C4C=C3C=C12)* 0.000 description 2
- ACJRMEVDTSKFDP-UHFFFAOYSA-N heptaphene Chemical group C1=CC=C2C=C(C=C3C4=CC5=CC6=CC=CC=C6C=C5C=C4C=CC3=C3)C3=CC2=C1 ACJRMEVDTSKFDP-UHFFFAOYSA-N 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- PKIFBGYEEVFWTJ-UHFFFAOYSA-N hexaphene Chemical group C1=CC=C2C=C3C4=CC5=CC6=CC=CC=C6C=C5C=C4C=CC3=CC2=C1 PKIFBGYEEVFWTJ-UHFFFAOYSA-N 0.000 description 2
- 229910010272 inorganic material Inorganic materials 0.000 description 2
- 239000011147 inorganic material Substances 0.000 description 2
- ZXEKIIBDNHEJCQ-UHFFFAOYSA-N isobutanol Chemical compound CC(C)CO ZXEKIIBDNHEJCQ-UHFFFAOYSA-N 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 239000010977 jade Substances 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical group CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 239000011368 organic material Substances 0.000 description 2
- 239000003973 paint Substances 0.000 description 2
- 125000001828 phenalenyl group Chemical group C1(C=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- DSNYFFJTZPIKFZ-UHFFFAOYSA-N propoxybenzene Chemical group CCCOC1=CC=CC=C1 DSNYFFJTZPIKFZ-UHFFFAOYSA-N 0.000 description 2
- SMUQFGGVLNAIOZ-UHFFFAOYSA-N quinaldine Chemical compound C1=CC=CC2=NC(C)=CC=C21 SMUQFGGVLNAIOZ-UHFFFAOYSA-N 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- KZNICNPSHKQLFF-UHFFFAOYSA-N succinimide Chemical compound O=C1CCC(=O)N1 KZNICNPSHKQLFF-UHFFFAOYSA-N 0.000 description 2
- 150000003462 sulfoxides Chemical class 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- 125000005425 toluyl group Chemical group 0.000 description 2
- 125000003944 tolyl group Chemical group 0.000 description 2
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 description 1
- 125000006651 (C3-C20) cycloalkyl group Chemical group 0.000 description 1
- UVNPEUJXKZFWSJ-LMTQTHQJSA-N (R)-N-[(4S)-8-[6-amino-5-[(3,3-difluoro-2-oxo-1H-pyrrolo[2,3-b]pyridin-4-yl)sulfanyl]pyrazin-2-yl]-2-oxa-8-azaspiro[4.5]decan-4-yl]-2-methylpropane-2-sulfinamide Chemical compound CC(C)(C)[S@@](=O)N[C@@H]1COCC11CCN(CC1)c1cnc(Sc2ccnc3NC(=O)C(F)(F)c23)c(N)n1 UVNPEUJXKZFWSJ-LMTQTHQJSA-N 0.000 description 1
- AVQQQNCBBIEMEU-UHFFFAOYSA-N 1,1,3,3-tetramethylurea Chemical compound CN(C)C(=O)N(C)C AVQQQNCBBIEMEU-UHFFFAOYSA-N 0.000 description 1
- GGYVTHJIUNGKFZ-UHFFFAOYSA-N 1-methylpiperidin-2-one Chemical compound CN1CCCCC1=O GGYVTHJIUNGKFZ-UHFFFAOYSA-N 0.000 description 1
- HYVXFSHEINIWJP-UHFFFAOYSA-N 2-(5-methyl-2-propan-2-ylhexyl)phenol Chemical compound C(C)(C)C(CC1=C(C=CC=C1)O)CCC(C)C HYVXFSHEINIWJP-UHFFFAOYSA-N 0.000 description 1
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 1
- WDBQJSCPCGTAFG-QHCPKHFHSA-N 4,4-difluoro-N-[(1S)-3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-pyridin-3-ylpropyl]cyclohexane-1-carboxamide Chemical compound FC1(CCC(CC1)C(=O)N[C@@H](CCN1CCC(CC1)N1C(=NN=C1C)C(C)C)C=1C=NC=CC=1)F WDBQJSCPCGTAFG-QHCPKHFHSA-N 0.000 description 1
- BWGRDBSNKQABCB-UHFFFAOYSA-N 4,4-difluoro-N-[3-[3-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)-8-azabicyclo[3.2.1]octan-8-yl]-1-thiophen-2-ylpropyl]cyclohexane-1-carboxamide Chemical compound CC(C)C1=NN=C(C)N1C1CC2CCC(C1)N2CCC(NC(=O)C1CCC(F)(F)CC1)C1=CC=CS1 BWGRDBSNKQABCB-UHFFFAOYSA-N 0.000 description 1
- OJRUSAPKCPIVBY-KQYNXXCUSA-N C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N Chemical compound C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N OJRUSAPKCPIVBY-KQYNXXCUSA-N 0.000 description 1
- 125000006416 CBr Chemical group BrC* 0.000 description 1
- 0 CC(C)COC(c1ccc(-c(cc2)c34)c5c1c(-c(cc1)ccc1[Zn])ccc5-c3ccc(C(O)OCC(C)N)c4c2-c1ccc(*)cc1)=O Chemical compound CC(C)COC(c1ccc(-c(cc2)c34)c5c1c(-c(cc1)ccc1[Zn])ccc5-c3ccc(C(O)OCC(C)N)c4c2-c1ccc(*)cc1)=O 0.000 description 1
- NUGPIZCTELGDOS-QHCPKHFHSA-N N-[(1S)-3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-pyridin-3-ylpropyl]cyclopentanecarboxamide Chemical compound C(C)(C)C1=NN=C(N1C1CCN(CC1)CC[C@@H](C=1C=NC=CC=1)NC(=O)C1CCCC1)C NUGPIZCTELGDOS-QHCPKHFHSA-N 0.000 description 1
- LFZAGIJXANFPFN-UHFFFAOYSA-N N-[3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-thiophen-2-ylpropyl]acetamide Chemical compound C(C)(C)C1=NN=C(N1C1CCN(CC1)CCC(C=1SC=CC=1)NC(C)=O)C LFZAGIJXANFPFN-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 1
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical group C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 1
- LJOOWESTVASNOG-UFJKPHDISA-N [(1s,3r,4ar,7s,8s,8as)-3-hydroxy-8-[2-[(4r)-4-hydroxy-6-oxooxan-2-yl]ethyl]-7-methyl-1,2,3,4,4a,7,8,8a-octahydronaphthalen-1-yl] (2s)-2-methylbutanoate Chemical compound C([C@H]1[C@@H](C)C=C[C@H]2C[C@@H](O)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)CC1C[C@@H](O)CC(=O)O1 LJOOWESTVASNOG-UFJKPHDISA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 229910000288 alkali metal carbonate Inorganic materials 0.000 description 1
- 150000008041 alkali metal carbonates Chemical class 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000005577 anthracene group Chemical group 0.000 description 1
- 125000001204 arachidyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 229910000063 azene Inorganic materials 0.000 description 1
- 229950011260 betanaphthol Drugs 0.000 description 1
- 125000006267 biphenyl group Chemical group 0.000 description 1
- 230000000740 bleeding effect Effects 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 229940125758 compound 15 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940127204 compound 29 Drugs 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- ZXZBMGGWHWRHPS-UHFFFAOYSA-N cyanato(phenyl)borinic acid Chemical compound N#COB(O)C1=CC=CC=C1 ZXZBMGGWHWRHPS-UHFFFAOYSA-N 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000005805 dimethoxy phenyl group Chemical group 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- 125000004914 dipropylamino group Chemical group C(CC)N(CCC)* 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000004815 dispersion polymer Substances 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 125000000031 ethylamino group Chemical group [H]C([H])([H])C([H])([H])N([H])[*] 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- YLQWCDOCJODRMT-UHFFFAOYSA-N fluoren-9-one Chemical group C1=CC=C2C(=O)C3=CC=CC=C3C2=C1 YLQWCDOCJODRMT-UHFFFAOYSA-N 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001475 halogen functional group Chemical group 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- GNOIPBMMFNIUFM-UHFFFAOYSA-N hexamethylphosphoric triamide Chemical compound CN(C)P(=O)(N(C)C)N(C)C GNOIPBMMFNIUFM-UHFFFAOYSA-N 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000000990 laser dye Substances 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000012860 organic pigment Substances 0.000 description 1
- 125000000913 palmityl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000005582 pentacene group Chemical group 0.000 description 1
- 125000002958 pentadecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- 125000005575 polycyclic aromatic hydrocarbon group Chemical group 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 125000006308 propyl amino group Chemical group 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000012453 solvate Substances 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000003107 substituted aryl group Chemical group 0.000 description 1
- 125000005346 substituted cycloalkyl group Chemical group 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 229960002317 succinimide Drugs 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000000000 tetracarboxylic acids Chemical class 0.000 description 1
- KTQYWNARBMKMCX-UHFFFAOYSA-N tetraphenylene Chemical group C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C3=CC=CC=C3C2=C1 KTQYWNARBMKMCX-UHFFFAOYSA-N 0.000 description 1
- 125000005556 thienylene group Chemical group 0.000 description 1
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001680 trimethoxyphenyl group Chemical group 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/20—Polycyclic condensed hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/40—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts substituted by unsaturated carbon radicals
- C07C15/56—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts substituted by unsaturated carbon radicals polycyclic condensed
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B3/00—Dyes with an anthracene nucleus condensed with one or more carbocyclic rings
- C09B3/14—Perylene derivatives
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
본원은 신규한 페릴렌계 화합물, 이의 제조 방법 및 이를 포함하는 형광 염료에 관한 것이다.The present invention relates to a novel perylene compound, a process for producing the same, and a fluorescent dye containing the same.
Description
본원은 신규한 페릴렌계 화합물, 이의 제조 방법, 및 이를 포함하는 형광 염료에 관한 것이다.The present invention relates to a novel perylene-based compound, a process for producing the same, and a fluorescent dye containing the same.
페릴렌계 화합물은 다환 방향족 탄화수소 화합물로서 액상의 형광 염료로 사용되고 있으며, 특히 우수한 광안전성 안료와 배트염료로서 각광받고 있다. 페릴렌계 화합물을 포함하는 안료 및 염료는 확장된 공명성으로 인하여 장파장에서 발광파장을 보이며, 매우 강한 형광성으로 다양한 분야에서 사용되고 있으며, 최근에는 디스플레이 분야에 화학 발광 물질로서 사용이 크게 증가하고 있다(미국 특허 공개번호 US2011/0251393). The perylene-based compound is a polycyclic aromatic hydrocarbon compound and is used as a liquid fluorescent dye, and has been particularly popular as an excellent light-safe pigment and a bat dye. Pigments and dyes including a perylene group compound exhibit emission wavelengths in a long wavelength due to their extended vacancy and are used in various fields because of their very strong fluorescence. Recently, their use as a chemiluminescent material in a display field has been greatly increased Patent Publication No. US2011 / 0251393).
본원은, 신규한 페릴렌계 화합물, 이의 제조 방법 및 이를 포함하는 형광 염료를 제공하고자 한다.The present invention is to provide a novel perylene compound, a process for producing the same, and a fluorescent dye containing the same.
그러나, 본원이 해결하고자 하는 과제는 이상에서 기술한 과제로 제한되지 않으며, 기술되지 않은 또 다른 과제들은 아래의 기재로부터 당업자에게 명확하게 이해될 수 있을 것이다.However, the problems to be solved by the present invention are not limited to the problems described above, and other problems not described can be clearly understood by those skilled in the art from the following description.
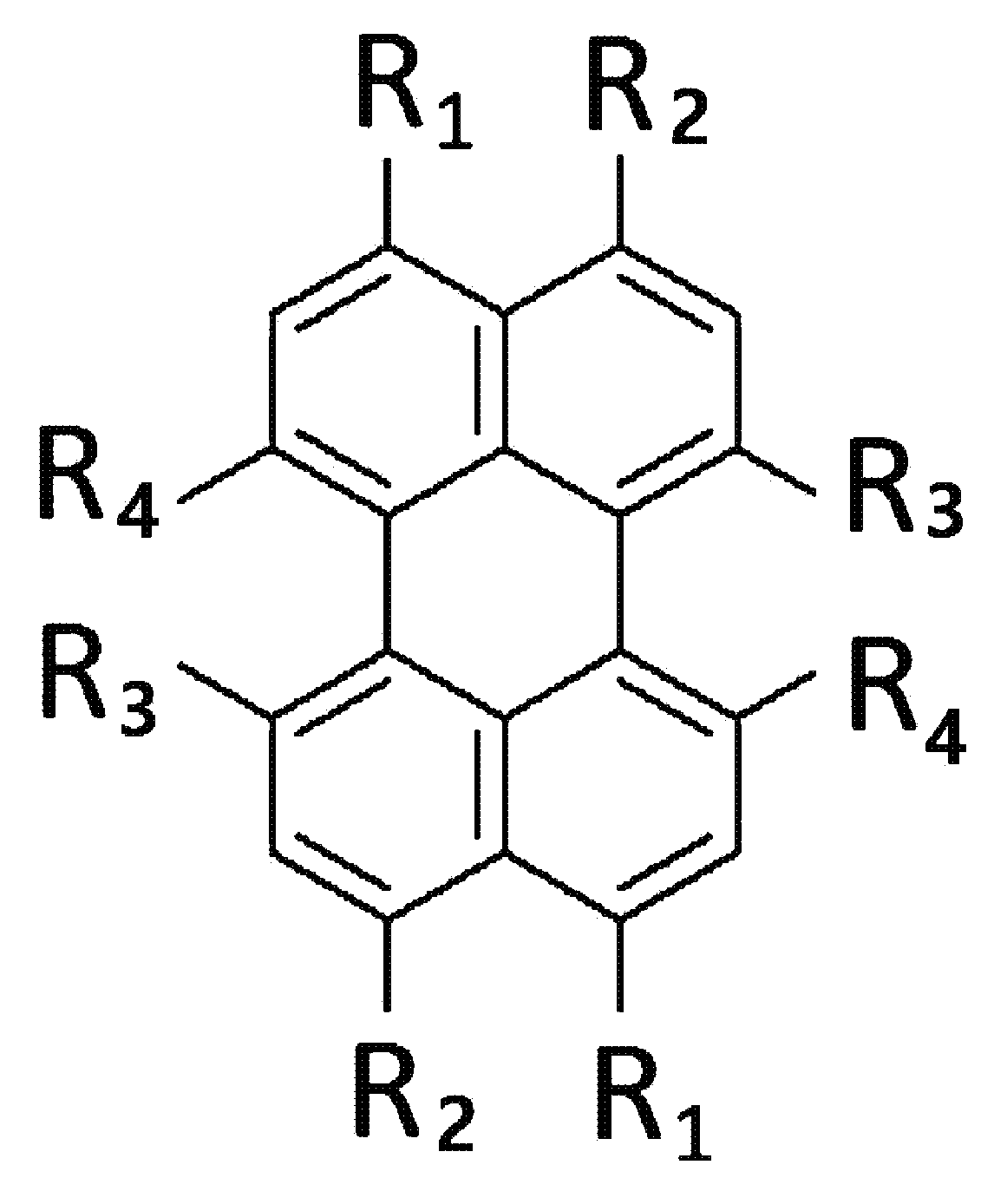
본원의 제 1 측면은, 하기 화학식 1로서 표시되는, 페릴렌계 화합물을 제공한다:A first aspect of the present invention provides a perylene-based compound represented by the following Formula 1:
[화학식 1][Chemical Formula 1]
상기 화학식 1에서, 상기 R1 및 상기 R2는, 각각 독립적으로, 수소, 할로겐기, 시아노기, 치환될 수 있는 선형 또는 분지형의 C1-20 알킬기, 치환될 수 있는 C3-30 시클로알킬기, 치환될 수 있는 C6-30 아릴기, 치환될 수 있는 선형 또는 분지형의 C1-20 알킬아민기, 치환될 수 있는 C3-30 시클로알킬아민기, 치환될 수 있는 C6-30 아릴아민기, 치환될 수 있는 선형 또는 분지형의 C1-20 알콕시기, 치환될 수 있는 C3-30 시클로알콕시기, 치환될 수 있는 C6-30 아릴옥시기, 치환될 수 있는 선형 또는 분지형의 C2-10 알킬카르복실기, 치환될 수 있는 C6-30 아릴카르복실기, 또는 치환될 수 있는 C6-30 아릴머캅토기이고, 상기 R3 및 상기 R4는, 각각 독립적으로, 수소, 할로겐기, 시아노기, 치환될 수 있는 선형 또는 분지형의 C1-20 알킬기, 치환될 수 있는 C3-30 시클로알킬기, 치환될 수 있는 C6-30 아릴기, 치환될 수 있는 선형 또는 분지형의 C1-20 알콕시기, 치환될 수 있는 C3-30 시클로알콕시기, 또는 치환될 수 있는 C6-30 아릴옥시기임.In the formula 1, wherein R 1 and said R 2 are, each independently, hydrogen, halogen, cyano, C 1-20 alkyl group which may be substituted with a linear or branched, optionally substituted C 3-30 cycloalkyl alkyl, optionally substituted C 6-30 aryl group, which may be C 1-20 alkyl which may be substituted with a linear or branched amine group, a substituted C 3-30 cycloalkyl amine groups, which may be substituted with C 6- 30 arylamine group, a linear or branched C 1-20 alkoxy group which may be substituted, a C 3-30 cycloalkoxy group which may be substituted, a C 6-30 aryloxy group which may be substituted, a linear Or a branched C 2-10 alkylcarboxyl group, a C 6-30 arylcarboxyl group which may be substituted, or a C 6-30 arylmercapto group which may be substituted, and R 3 and R 4 are each independently hydrogen , A halogen group, a cyano group, a linear or branched C 1-20 alkyl group which may be substituted, a C 3-30 cycloalkyl group which may be substituted , A C 6-30 aryl group which may be substituted, a linear or branched C 1-20 alkoxy group which may be substituted, a C 3-30 cycloalkoxy group which may be substituted, or C 6-30 aryl It is jade.
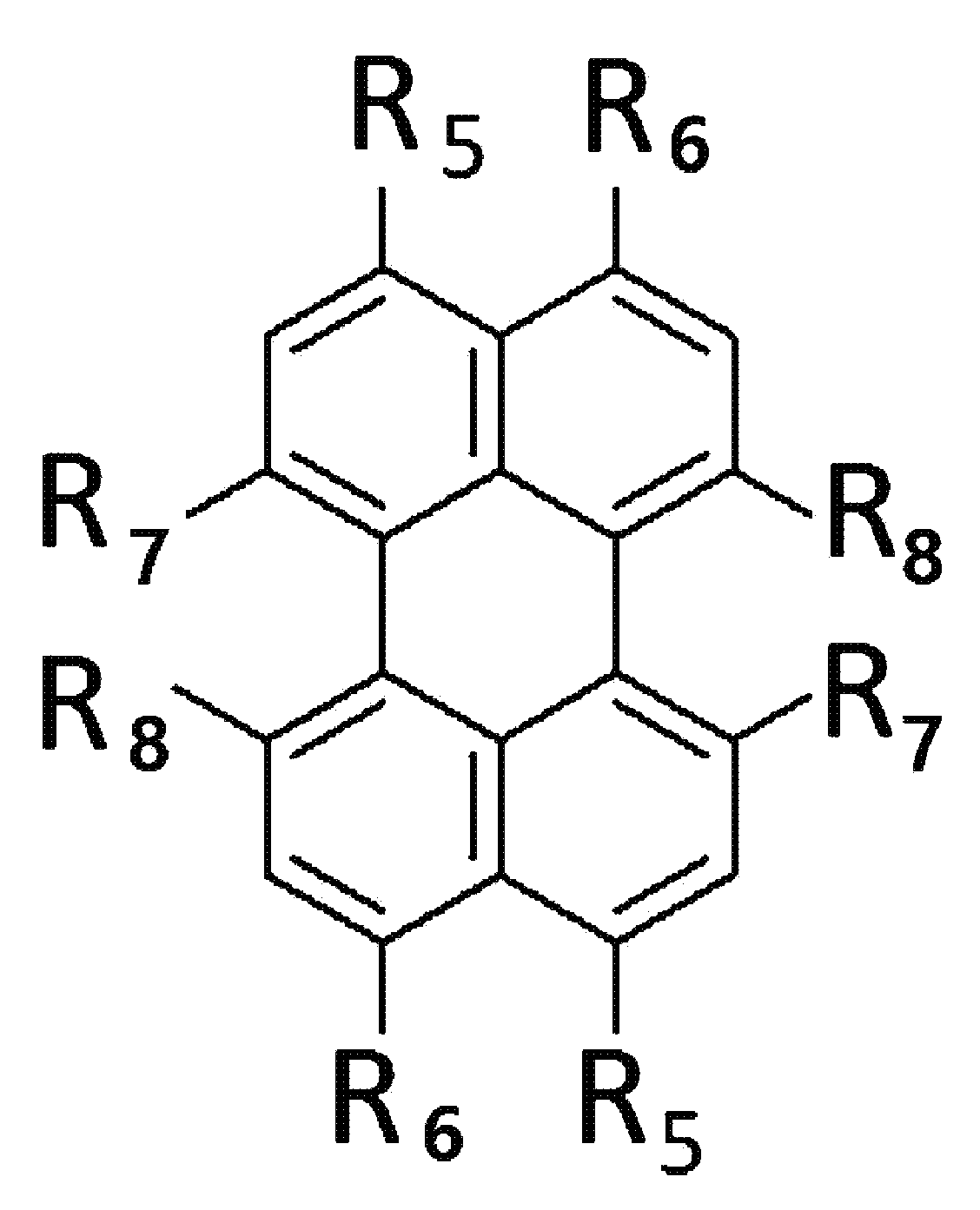
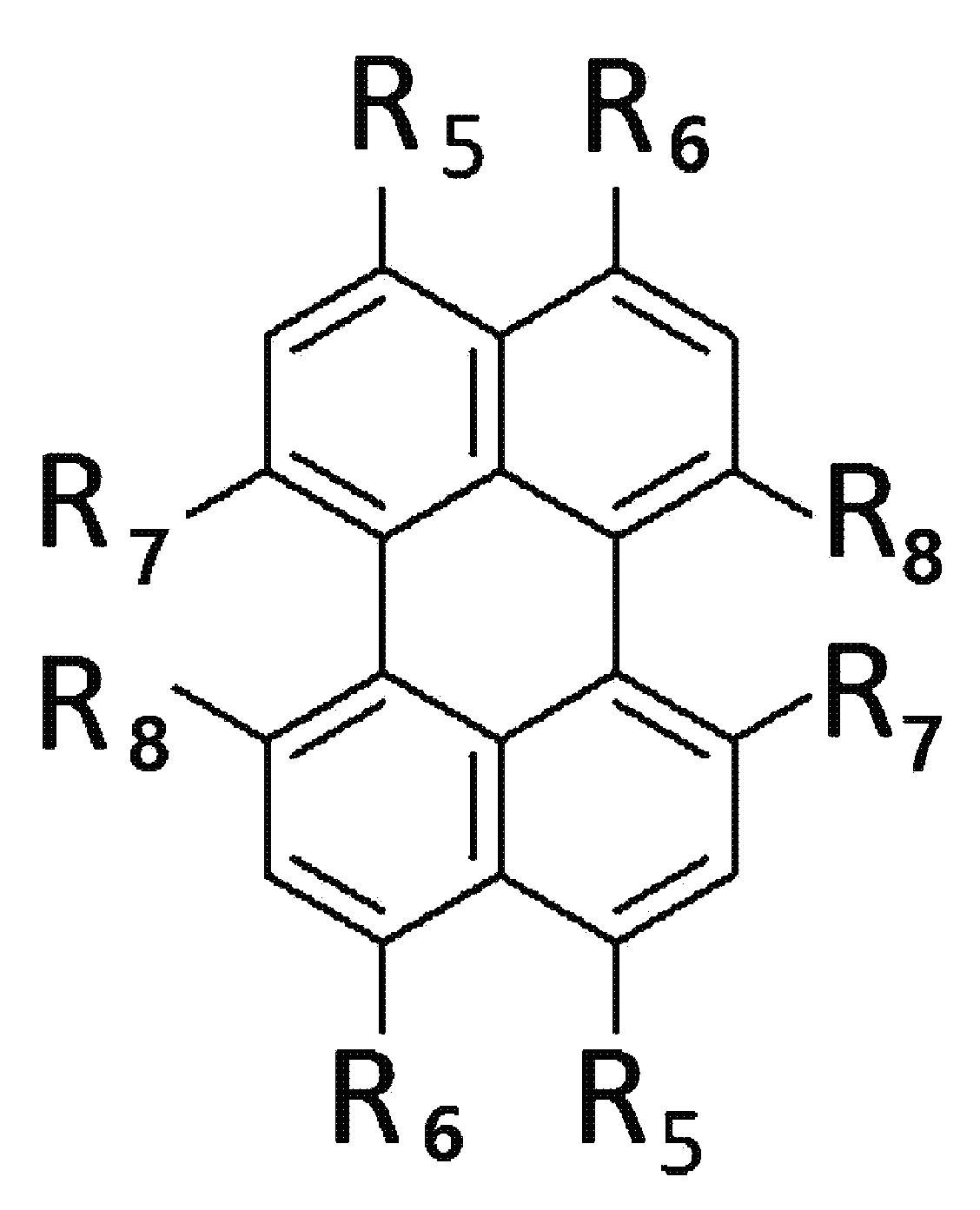
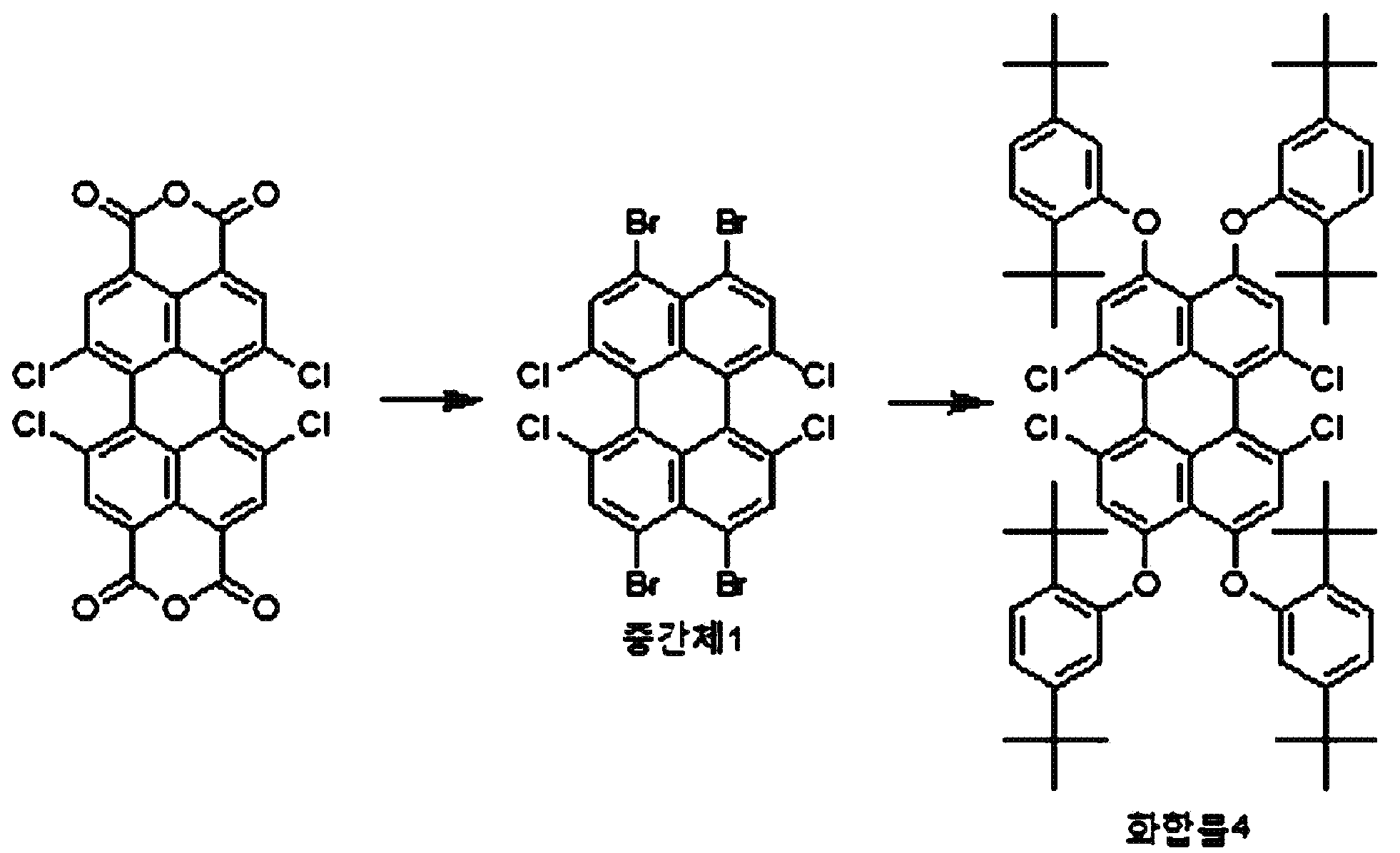
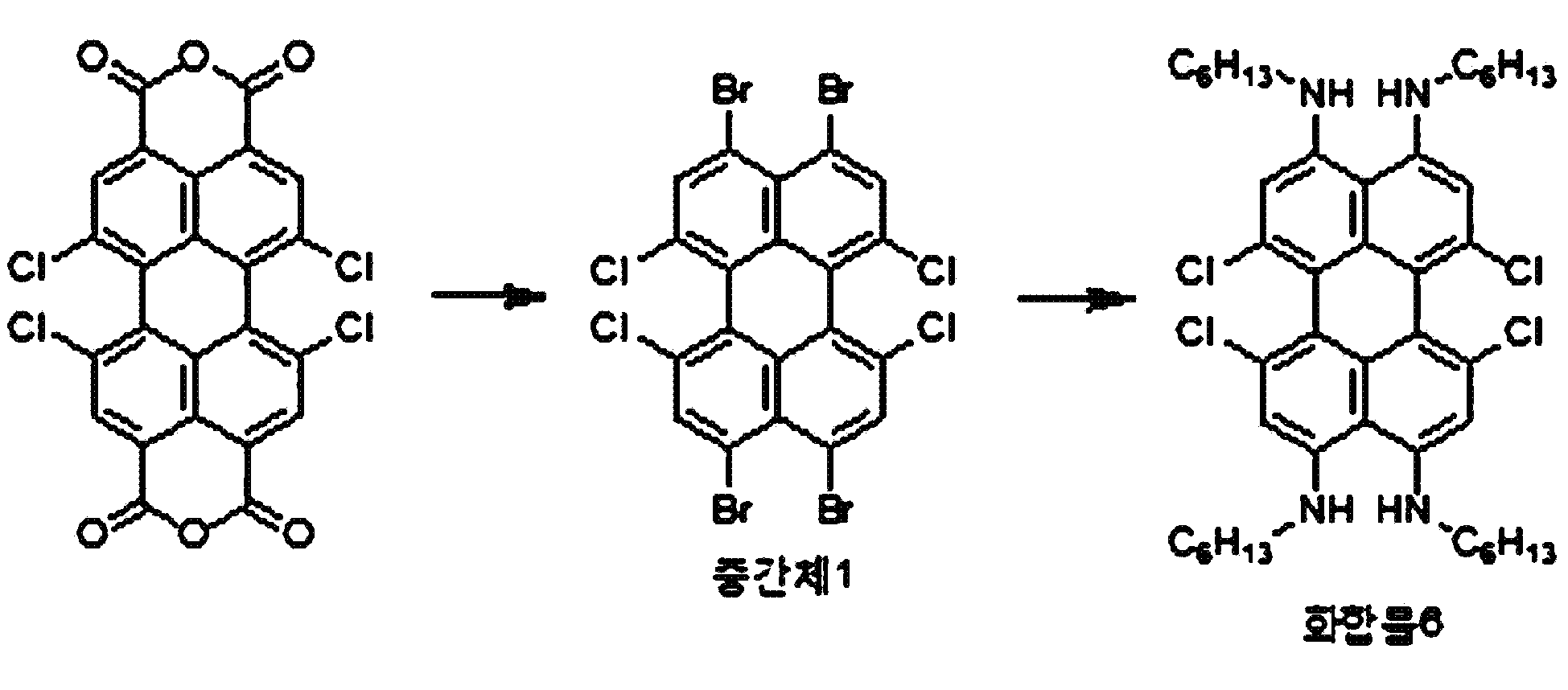
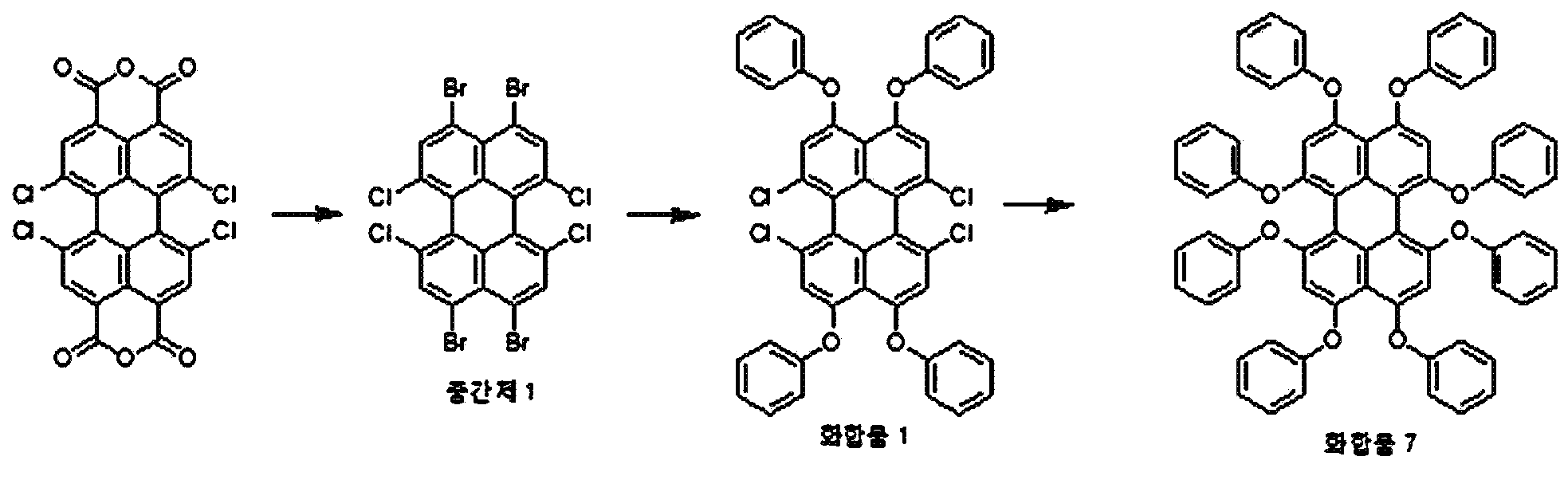
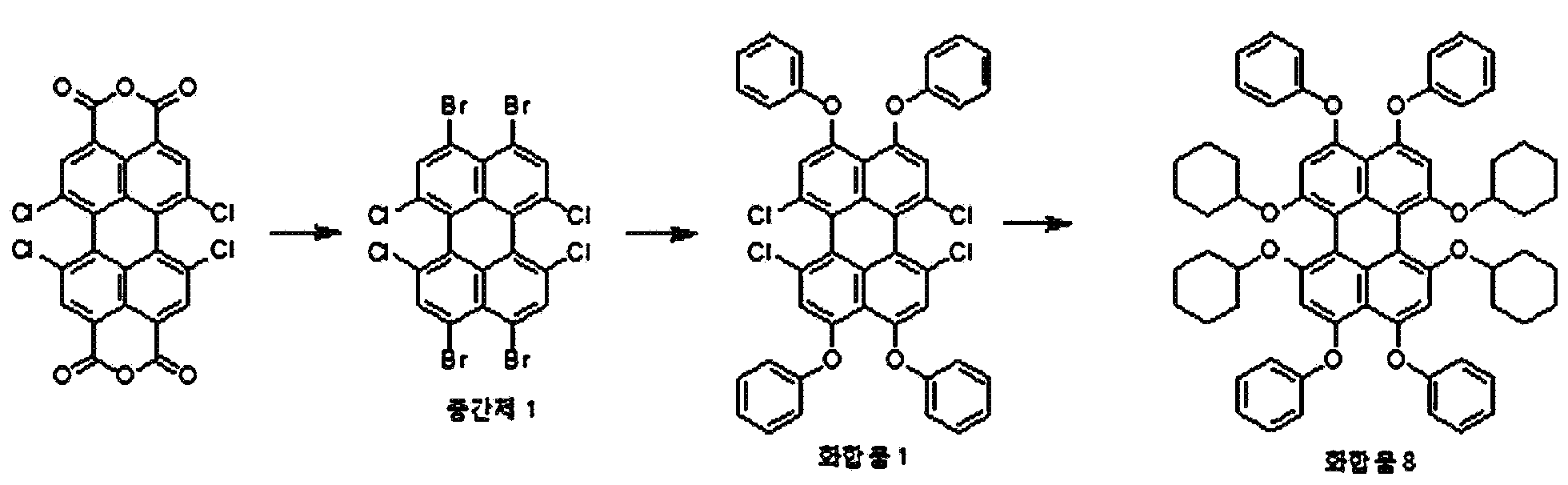
본원의 제 2 측면은, 하기 화학식 2로 표시되는 화합물을, 치환될 수 있는 선형 또는 분지형의 C1-20 알칸 화합물, 치환될 수 있는 C3-30 시클로알칸 화합물, 치환될 수 있는 C6-30 아릴 화합물, 치환될 수 있는 C6-30 페놀계 화합물, 치환될 수 있는 선형 또는 분지형의 C1-20 알코올계 화합물, 치환될 수 있는 선형 또는 분지형의 C1-20 알킬아민 화합물, 치환될 수 있는 C3-30 시클로알킬아민 화합물, 치환될 수 있는 C6-30 아릴아민 화합물, 또는 N-할로석신이미드와 반응시키는 것을 포함하는, 제 1 항에 따른 페릴렌계 화합물의 제조 방법을 제공한다:Present the second side, to C 6 in the compound represented by the formula 2, C 1-20 alkanes which may be substituted with a compound of linear or branched, C 3-30 cycloalkane compound which may be substituted, may be substituted -30 aryl compound, a C 6-30 phenol compound which may be substituted, a linear or branched C 1-20 alcohol compound which may be substituted, a linear or branched C 1-20 alkylamine compound which may be substituted , A C 3-30 cycloalkylamine compound that may be substituted, a C 6-30 arylamine compound that may be substituted, or N-halosuccinimide. The method provides:
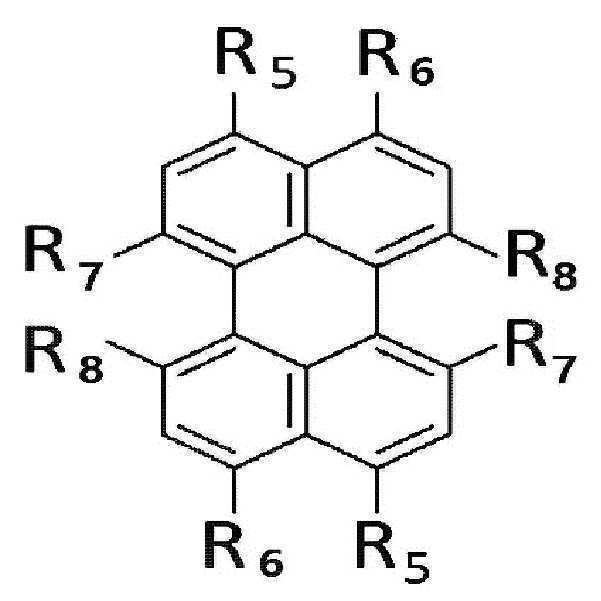
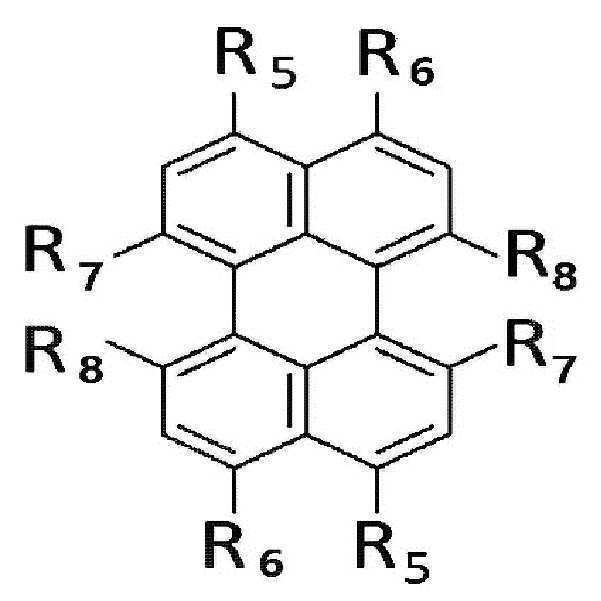
[화학식 2](2)
상기 화학식 2에서, R5 내지 R8은, 각각 독립적으로 수소, 할로겐 또는 치환될 수 있는 선형 또는 분지형의 C2-10 알킬카르복실기임.In Formula 2, R 5 to R 8 are each independently hydrogen, halogen, or a linear or branched C 2-10 alkylcarboxyl group which may be substituted.
본원의 제 3 측면은, 본원에 따른 페릴린계 화합물을 포함하는, 형광염료를 제공한다. A third aspect of the present invention provides a fluorescent dye comprising a perylenic compound according to the present invention.
본원의 페릴렌계 화합물은 페릴렌을 모핵구조로 하는, 녹색 형광 염료로서 사용가능한 신규한 화합물로서, 우수한 용해도, 특히, 유기 용매에 대한 우수한 용해도, 내구성, 열 안정성, 발광 특성을 나타낸다. The perylene-based compound of the present invention is a novel compound that can be used as a green fluorescent dye having perylene as a perinuclear structure, and exhibits excellent solubility, particularly excellent solubility, durability, thermal stability, and luminescent property with respect to an organic solvent.
도 1은 본원의 일 실시예에 따른 페릴린계 화합물의 UV/PL 결과를 나타낸 스펙트럼이다.BRIEF DESCRIPTION OF THE DRAWINGS FIG. 1 is a spectrum showing UV / PL results of a perillin compound according to one embodiment of the present invention. FIG.
이하, 첨부한 도면을 참조하여 본 발명이 속하는 기술 분야에서 통상의 지식을 가진 자가 용이하게 실시할 수 있도록 본원의 구현예 및 실시예를 상세히 설명한다.Hereinafter, embodiments and examples of the present invention will be described in detail with reference to the accompanying drawings, which will be readily apparent to those skilled in the art to which the present invention pertains.
그러나 본원은 여러 가지 상이한 형태로 구현될 수 있으며 여기에서 설명하는 구현예 및 실시예에 한정되지 않는다. 그리고 도면에서 본 발명을 명확하게 설명하기 위해서 설명과 관계없는 부분은 생략하였으며, 명세서 전체를 통하여 유사한 부분에 대해서는 유사한 도면 부호를 붙였다.It should be understood, however, that the present invention may be embodied in many different forms and is not limited to the embodiments and examples described herein. In order to clearly illustrate the present invention, parts not related to the description are omitted, and similar parts are denoted by like reference characters throughout the specification.
본원 명세서 전체에서, 어떤 부재가 다른 부재 "상에" 위치하고 있다고 할 때, 이는 어떤 부재가 다른 부재에 접해 있는 경우뿐 아니라 두 부재 사이에 또 다른 부재가 존재하는 경우도 포함한다.Throughout this specification, when a member is "on " another member, it includes not only when the member is in contact with the other member, but also when there is another member between the two members.
본원 명세서 전체에서, 어떤 부분이 어떤 구성 요소를 "포함" 한다고 할 때, 이는 특별히 반대되는 기재가 없는 한 다른 구성 요소를 제외하는 것이 아니라 다른 구성 요소를 더 포함할 수 있는 것을 의미한다. 본원 명세서 전체에서 사용되는 정도의 용어 "약", "실질적으로" 등은 언급된 의미에 고유한 제조 및 물질 허용오차가 제시될 때 그 수치에서 또는 그 수치에 근접한 의미로 사용되고, 본원의 이해를 돕기 위해 정확하거나 절대적인 수치가 언급된 개시 내용을 비양심적인 침해자가 부당하게 이용하는 것을 방지하기 위해 사용된다. 본원 명세서 전체에서 사용되는 정도의 용어 "~(하는) 단계" 또는 "~의 단계"는 "~ 를 위한 단계"를 의미하지 않는다.Throughout this specification, when an element is referred to as "including " an element, it is understood that the element may include other elements as well, without departing from the other elements unless specifically stated otherwise. The terms "about "," substantially ", etc. used to the extent that they are used throughout the specification are intended to be taken to mean the approximation of the manufacturing and material tolerances inherent in the stated sense, Accurate or absolute numbers are used to help prevent unauthorized exploitation by unauthorized intruders of the referenced disclosure. The word " step (or step) "or" step "used to the extent that it is used throughout the specification does not mean" step for.
본원 명세서 전체에서, 마쿠시 형식의 표현에 포함된 "이들의 조합"의 용어는 마쿠시 형식의 표현에 기재된 구성 요소들로 이루어진 군에서 선택되는 하나 이상의 혼합 또는 조합을 의미하는 것으로서, 상기 구성 요소들로 이루어진 군에서 선택되는 하나 이상을 포함하는 것을 의미한다.Throughout this specification, the term "combination thereof" included in the expression of the machine form means one or more combinations or combinations selected from the group consisting of the constituents described in the expression of the machine form, And the like.
본원 명세서 전체에서, "A 및/또는 B"의 기재는, "A 또는 B, 또는 A 및 B"를 의미한다. Throughout this specification, the description of "A and / or B" means "A or B, or A and B".
본원 명세서 전체에서, 단독 또는 다른 치환기와 함께 기재되는 용어 "알킬"은 치환될 수 있는 선형 또는 분지형의, C1-C20 알킬, C1-C15 알킬, C1-C10 알킬, 또는 C1-C6 알킬을 포함하는 것일 수 있으며, 예를 들어, 메틸, 에틸, 프로필, 부틸, 펜틸, 헥실, 헵틸, 옥틸, 노닐, 데실, 운데실, 도데실 또는 이들의 가능한 모든 이성질체들을 포함하는 것일 수 있으나, 이에 제한되지 않을 수 있다.Throughout the present specification, alone or in the term "alkyl" described in combination with other substituents are linear or branched, optionally substituted, C 1 -C 20 alkyl, C 1 -C 15 alkyl, C 1 -C 10 alkyl, or C 1 -C 6 alkyl and include, for example, methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl, octyl, nonyl, decyl, undecyl, dodecyl or all possible isomers thereof , But may not be limited thereto.
본원 명세서 전체에서, 단독 또는 다른 치환기와 함께 기재되는 용어 "시클로알킬"은 치환될 수 있는 C3-30 시클로알킬, C3-20 시클로알킬, 또는 C3-10 시클로알킬을 포함하는 것일 수 있으며, 모노- 또는 비시클로지방족을 의미할 수 있다. 예를 들어, 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헥세닐, 시클로헵틸, 시클로헵테닐, 시클로옥틸, 시클로옥테닐, 2,5-시클로헥사디에닐, 비시클로[2.2.2]옥틸, 아다만트-1-일, 데카히드로나프틸, 옥소시클로헥실, 디옥소시클로헥실, 티오시클로헥실, 2-옥소비시클로[2.2.1]헵트-1-일, 또는 이들의 가능한 모든 이성질체들을 포함할 수 있으나, 이에 제한되지 않을 수 있다.Throughout the specification, the term "cycloalkyl ", alone or in combination with other substituents, may include C 3-30 cycloalkyl, C 3-20 cycloalkyl, or C 3-10 cycloalkyl which may be substituted , Mono- or bicycloaliphatic. Cyclobutyl, cyclopentyl, cyclohexyl, cyclohexenyl, cycloheptyl, cycloheptenyl, cyclooctyl, cyclooctenyl, 2,5-cyclohexadienyl, bicyclo [2.2.2] 2-oxocyclo [2.2.1] hept-1-yl, or any of the possible isomers thereof, or a pharmaceutically acceptable salt, solvate or prodrug thereof. But are not limited thereto.
본원 명세서 전체에서, 단독 또는 다른 치환기와 함께 기재되는 용어 "아릴"은 치환될 수 있는 C6-30 아릴, C6-20 아릴, 또는 C6-10 아릴을 포함하는 것일 수 있으며, 인접하는 탄소 원자 또는 적합한 이형 원자들 사이에서 이중 결합이 교대(공명)한다. 예를 들어, 페닐 고리, 톨루일 고리, 나프탈레닐 고리, 안트라세닐 고리, 페난트렌 고리, 펜타렌 고리, 인덴 고리, 비페닐렌 고리, 페날렌 고리, 아즈렌 고리, 헵타렌 고리, 아세나프틸렌 고리, 플루오렌 고리, 테트라센 고리, 트리페닐렌 고리, 피렌 고리, 크리센 고리, 에틸-크리센 고리, 피센 고리, 페릴렌 고리, 펜타펜 고리, 펜타센 고리, 테트라페닐렌 고리, 헥사펜 고리, 헥사센고리, 루비센 고리, 코로넨 고리, 트리나프틸렌 고리, 헵타펜 고리, 헵타센 고리, 피란트렌 고리, 오바렌 고리, 플로란센 고리, 벤조플로란센 고리, 9-안트릴기, 2-안트릴기, 9-페난트릴기, 2-페난트릴기, 1-피렌일기, 크라이센일기, 나프타센일기, 코로닐기 및 이들의 유도체로 이루어진 군으로부터 선택될 수 있으나, 이에 제한되지 않을 수 있다.Throughout this specification, the term "aryl ", alone or in combination with other substituents, may include C 6-30 aryl, C 6-20 aryl, or C 6-10 aryl which may be substituted, The double bonds alternate (resonate) between the atoms or the appropriate heteroatoms. Examples of the hetero ring include a phenyl ring, a tolyl ring, a naphthalenyl ring, an anthracenyl ring, a phenanthrene ring, a pentaren ring, an indene ring, a biphenylene ring, a phenalene ring, A heterocyclic ring, a thiophene ring, a thienylene ring, a fluorene ring, a tetracene ring, a triphenylene ring, a pyrene ring, a chrysene ring, an ethyl-chrysene ring, a picene ring, a perylene ring, a pentaphene ring, A phenanthrene ring, a hexane ring, a rubisen ring, a coronene ring, a trinaphthylene ring, a heptaphene ring, a heptacene ring, a pyranthrene ring, an obaren ring, a fluoransen ring, A phenanthryl group, a 1-pyrenyl group, a chrysene group, a naphthacene group, a coronyl group, and derivatives thereof, But may not be limited.
본원 명세서 전체에서, 용어 "알콕시"는 산소와 단일 결합된 알킬기를 의미하는 것으로, 예를 들어, 치환될 수 있는 선형 또는 분지형의 C1-C20 알콕시, C1-C15 알콕시, C1-C10 알콕시, 또는 C1-C6 알콕시를 포함하는 것일 수 있으며, 예를 들어, 메톡시, 에톡시, 프로폭시, 부톡시, 펜틸옥시, 헵틸옥시 등 및 이들의 모든 가능한 이성질체를 포함할 수 있으나, 이에 제한되지 않을 수 있다.For the purposes of the present specification, the term "alkoxy" means an alkyl group mono-bonded to oxygen, for example, linear or branched C 1 -C 20 alkoxy which may be substituted, C 1 -C 15 alkoxy, C 1 -C 10 alkoxy, or C 1 -C 6 alkoxy may be one containing, for example, methoxy, ethoxy, propoxy, butoxy, pentyloxy, heptyloxy, and the like thereof to include all possible isomers But may not be limited thereto.
본원 명세서 전체에서, 용어 "아릴옥시"는 산소와 단일 결합된 아릴기를 의미하는 것으로, 산소와 단일 결합된 아릴기는 치환될 수 있는 C6-30 아릴, C6-20 아릴, 또는 C6-10 아릴을 포함하는 것일 수 있으며, 예를 들어, 페닐 고리, 톨루일 고리, 나프탈레닐 고리, 안트라세닐 고리, 페난트렌 고리, 펜타렌 고리, 인덴 고리, 비페닐렌 고리, 페날렌 고리, 아즈렌 고리, 헵타렌 고리, 아세나프틸렌 고리, 플루오렌 고리, 테트라센 고리, 트리페닐렌 고리, 피렌 고리, 크리센 고리, 에틸-크리센 고리, 피센 고리, 페릴렌 고리, 펜타펜 고리, 펜타센 고리, 테트라페닐렌 고리, 헥사펜 고리, 헥사센고리, 루비센 고리, 코로넨 고리, 트리나프틸렌 고리, 헵타펜 고리, 헵타센 고리, 피란트렌 고리, 오바렌 고리, 플로란센 고리, 벤조플로란센 고리, 9-안트릴기, 2-안트릴기, 9-페난트릴기, 2-페난트릴기, 1-피렌일기, 크라이센일기, 나프타센일기, 코로닐기, 및 이들의 유도체로 이루어진 군으로부터 선택될 수 있으나, 이에 제한되지 않을 수 있다.Throughout the present specification, the term "aryloxy" is to mean a group of a single bond and oxygen, aryl, C 6-30 aryl which may be substituted aryl groups with a single bond and oxygen, C 6-20 aryl, or C 6-10 And examples thereof include a phenyl ring, a tolyl ring, a naphthalenyl ring, an anthracenyl ring, a phenanthrene ring, a pentaren ring, an indene ring, a biphenylene ring, a phenalene ring, azene A heterocyclic ring, a heterocyclic ring, a heterocyclic ring, an acenaphthylene ring, an acenaphthylene ring, a fluorene ring, a tetracene ring, a triphenylene ring, a pyrene ring, a chrysene ring, A heterocyclic ring, a heterocyclic ring, a heterocyclic ring, a heterocyclic ring, a heterocyclic ring, a heterocyclic ring, a heterocyclic ring, a tetraphenyl ring, a hexaphen ring, a hexasene ring, a rubisene ring, a coronene ring, a trinaphthylene ring, Fluoransene ring, 9-anthryl group, 2-anthryl group, 9-phen May be selected from the group consisting of a trityl group, a 2-phenanthryl group, a 1-pyrenyl group, a chrysene group, a naphthacene group, a coronyl group, and derivatives thereof.
본원 명세서 전체에서, 용어 "알킬카르복실기"는 에스테르기에 있어서 카보닐기의 탄소와 단일결합된 알콕시기를 포함하는 것으로, 상기 알킬카르복실기에 포함되는 알콕시기는 예를 들어, 치환될 수 있는 선형 또는 분지형의 C1-C20 알콕시, C1-C15 알콕시, C1-C10 알콕시, 또는 C1-C6 알콕시를 포함하는 것일 수 있으며, 예를 들어, 메톡시, 에톡시, 프로폭시, 부톡시, 펜틸옥시, 헵틸옥시 등 및 이들의 모든 가능한 이성질체를 포함할 수 있으나, 이에 제한되지 않을 수 있다. Throughout the specification, the term "alkylcarboxyl group" includes an alkoxy group that is single bonded to the carbon of the carbonyl group in the ester group, and the alkoxy group contained in the alkylcarboxyl group includes, for example, a linear or branched C 1 -C 20 alkoxy, C 1 -C 15 alkoxy, C 1 -C 10 alkoxy, or C 1 may be one containing a -C 6 alkoxy, e.g., methoxy, ethoxy, propoxy, butoxy, Pentyloxy, heptyloxy, and the like, as well as all possible isomers thereof.
본원 명세서 전체에서, 용어 "아릴카르복실기"는 에스테르기에 있어서 카보닐기의 탄소와 단일결합된 아릴옥시기를 포함하는 것으로, 상기 아릴카르복실기에 포함되는 아릴옥시기에서 산소와 단일 결합된 아릴기는 치환될 수 있는 C6-30 아릴, C6-20 아릴, 또는 C6-10 아릴을 포함하는 것일 수 있으며, 예를 들어, 페닐 고리, 톨루일 고리, 나프탈레닐 고리, 안트라세닐 고리, 페난트렌 고리, 펜타렌 고리, 인덴 고리, 비페닐렌 고리, 페날렌 고리, 아즈렌 고리, 헵타렌 고리, 아세나프틸렌 고리, 플루오렌 고리, 테트라센 고리, 트리페닐렌 고리, 피렌 고리, 크리센 고리, 에틸-크리센 고리, 피센 고리, 페릴렌 고리, 펜타펜 고리, 펜타센 고리, 테트라페닐렌 고리, 헥사펜 고리, 헥사센고리, 루비센 고리, 코로넨 고리, 트리나프틸렌 고리, 헵타펜 고리, 헵타센 고리, 피란트렌 고리, 오바렌 고리, 플로란센 고리, 벤조플로란센 고리, 9-안트릴기, 2-안트릴기, 9-페난트릴기, 2-페난트릴기, 1-피렌일기, 크라이센일기, 나프타센일기, 코로닐기, 및 이들의 유도체로 이루어진 군으로부터 선택될 수 있으나, 이에 제한되지 않을 수 있다.Throughout this specification, the term "arylcarboxyl group" includes an aryloxy group which is mono-bonded to the carbon of the carbonyl group in the ester group, and the aryl group mono-bonded to oxygen in the aryloxy group contained in the arylcarboxyl group may be substituted C 6-30 aryl, C 6-20 aryl, or may be one containing a C 6-10 aryl group, for example, a phenyl ring, toluyl ring, naphthalenyl ring, anthracenyl ring, a phenanthrene ring, a cyclopenta An acenaphthylene ring, an acenaphthylene ring, a fluorenone ring, a tetracene ring, a triphenylene ring, a pyrenylene ring, a chrysene ring, an ethylenic ring, an acenaphthylene ring, an indene ring, a biphenylene ring, a phenylene ring, A hexene ring, a hexane ring, a rubisene ring, a coronene ring, a trinaphthylene ring, a heptane ring, a heptane ring, a heptane ring, a heptane ring, Tassen Gori , A pyranthrene ring, an obaren ring, a fluoransen ring, a benzofluoransen ring, a 9-anthryl group, a 2-anthryl group, a 9-phenanthryl group, a 2-phenanthryl group, A naphthacene group, a naphthacene group, a coronyl group, and derivatives thereof, but the present invention is not limited thereto.
본원 명세서 전체에서, 용어 "아릴머캅토기"는 황과 단일 결합된 아릴기를 의미하는 것으로, 상기 황과 단일 결합된 아릴기는 치환될 수 있는 C6-30 아릴, C6-20 아릴, 또는 C6-10 아릴을 포함하는 것일 수 있으며, 예를 들어, 페닐 고리, 톨루일 고리, 나프탈레닐 고리, 안트라세닐 고리, 페난트렌 고리, 펜타렌 고리, 인덴 고리, 비페닐렌 고리, 페날렌 고리, 아즈렌 고리, 헵타렌 고리, 아세나프틸렌 고리, 플루오렌 고리, 테트라센 고리, 트리페닐렌 고리, 피렌 고리, 크리센 고리, 에틸-크리센 고리, 피센 고리, 페릴렌 고리, 펜타펜 고리, 펜타센 고리, 테트라페닐렌 고리, 헥사펜 고리, 헥사센고리, 루비센 고리, 코로넨 고리, 트리나프틸렌 고리, 헵타펜 고리, 헵타센 고리, 피란트렌 고리, 오바렌 고리, 플로란센 고리, 벤조플로란센 고리, 9-안트릴기, 2-안트릴기, 9-페난트릴기, 2-페난트릴기, 1-피렌일기, 크라이센일기, 나프타센일기, 코로닐기, 및 이들의 유도체로 이루어진 군으로부터 선택될 수 있으나, 이에 제한되지 않을 수 있다.Throughout the present specification, the term "aryl mercapto group" is sulfur and a single bond to mean an aryl, wherein the sulfur single bond and the aryl group is C 6-30 aryl, C 6-20 aryl, or C 6 which may be substituted be one that includes a -10 aryl, and, for example, a phenyl ring, a toluyl ring, a naphthalenyl ring, anthracenyl ring, a phenanthrene ring, a cyclopenta alkylene ring, indene ring, a biphenylene ring, a page nalren ring, A pyrenylene ring, a pyrenylene ring, a pyrenylene ring, a pyrenylene ring, a chrysene ring, an ethyl-chrysene ring, a picene ring, a perylene ring, a pentaphene ring, A pentacene ring, a tetraphenylene ring, a hexaphen ring, a hexasene ring, a rubisene ring, a coronene ring, a trinaphthylene ring, a heptaphene ring, a heptacene ring, a pyranthrene ring, , Benzofluoransene ring, 9-anthryl group, 2-anthryl group , A 9-phenanthryl group, a 2-phenanthryl group, a 1-pyrenyl group, a chrysene group, a naphthacene group, a coronyl group, and derivatives thereof.
본원의 명세서 전체에서, 용어 "할로겐"은 주기율표의 17족 원소로서, 예를 들어, F, Cl, Br, 또는 I를 포함할 수 있으나, 이에 제한되지 않을 수 있다.Throughout the specification of the present application, the term "halogen" may include, but is not limited to, Group 17 elements of the periodic table, for example, F, Cl, Br,
본원의 제 1 측면은, 하기 화학식 1로서 표시되는, 페릴렌계 화합물을 제공한다:A first aspect of the present invention provides a perylene-based compound represented by the following Formula 1:
[화학식 1][Chemical Formula 1]
상기 화학식 1에서, 상기 R1 및 상기 R2는, 각각 독립적으로, 수소, 할로겐기, 시아노기, 치환될 수 있는 선형 또는 분지형의 C1-20 알킬기, 치환될 수 있는 C3-30 시클로알킬기, 치환될 수 있는 C6-30 아릴기, 치환될 수 있는 선형 또는 분지형의 C1-20 알킬아민기, 치환될 수 있는 C3-30 시클로알킬아민기, 치환될 수 있는 C6-30 아릴아민기, 치환될 수 있는 선형 또는 분지형의 C1-20 알콕시기, 치환될 수 있는 C3-30 시클로알콕시기, 치환될 수 있는 C6-30 아릴옥시기, 치환될 수 있는 선형 또는 분지형의 C2-10 알킬카르복실기, 치환될 수 있는 C6-30 아릴카르복실기, 또는 치환될 수 있는 C6-30 아릴머캅토기이고, 상기 R3 및 상기 R4는, 각각 독립적으로, 수소, 할로겐기, 시아노기, 치환될 수 있는 선형 또는 분지형의 C1-20 알킬기, 치환될 수 있는 C3-30 시클로알킬기, 치환될 수 있는 C6-30 아릴기, 치환될 수 있는 선형 또는 분지형의 C1-20 알콕시기, 치환될 수 있는 C3-30 시클로알콕시기, 또는 치환될 수 있는 C6-30 아릴옥시기임.In the formula 1, wherein R 1 and said R 2 are, each independently, hydrogen, halogen, cyano, C 1-20 alkyl group which may be substituted with a linear or branched, optionally substituted C 3-30 cycloalkyl alkyl, optionally substituted C 6-30 aryl group, which may be C 1-20 alkyl which may be substituted with a linear or branched amine group, a substituted C 3-30 cycloalkyl amine groups, which may be substituted with C 6- 30 arylamine group, a linear or branched C 1-20 alkoxy group which may be substituted, a C 3-30 cycloalkoxy group which may be substituted, a C 6-30 aryloxy group which may be substituted, a linear Or a branched C 2-10 alkylcarboxyl group, a C 6-30 arylcarboxyl group which may be substituted, or a C 6-30 arylmercapto group which may be substituted, and R 3 and R 4 are each independently hydrogen , A halogen group, a cyano group, a linear or branched C 1-20 alkyl group which may be substituted, a C 3-30 cycloalkyl group which may be substituted , A C 6-30 aryl group which may be substituted, a linear or branched C 1-20 alkoxy group which may be substituted, a C 3-30 cycloalkoxy group which may be substituted, or C 6-30 aryl It is jade.
본원의 일 구현예에 있어서, 상기 R1 내지 R4 각각에 독립적으로 포함되는 상기 알킬기, 상기 알킬아민기, 상기 알콕시기, 및 상기 알킬카르복실기는 탄소 수 약 1 내지 약 20인 치환될 수 있는 선형 또는 분지형의 알킬기를 포함할 수 있다. 본원에서 사용되는 선형 또는 분지형의 알킬기는, 탄소 수 약 1 내지 약 20, 약 1 내지 약 15, 약 1 내지 약 10, 또는 약 1 내지 6의 알킬기를 포함하는 것일 수 있으며, 메틸, 에틸, 프로필, 부틸, 펜틸, 헥실, 헵틸, 옥틸, 노닐, 데실, 운데실, 도데실, 트리데실, 테트라데실, 펜타데실, 헥사데실, 옥타데실, 노나데실, 에이코사닐, 또는 이들의 가능한 모든 이성질체를 포함한다. 예를 들어, 탄소수가 1 내지 12인 알킬기, 즉, 메틸기, 에틸기, 프로필기, 부틸기, 펜틸기, 헥실기, 헵틸기, 옥틸기, 노닐기, 데실, 운데실, 도데실기일 수 있고, 또는 탄소수가 1 내지 6인 알킬기, 즉, 메틸기, 에틸기, 프로필기, 부틸기, 펜틸기, 또는 헥실기일 수 있으며, 또는 탄소수가 1 내지 4인 알킬기, 즉, 메틸기, 에틸기, i-프로필기, n-프로필기, t-부틸기, s-부틸기, 또는 n-부틸기일 수 있다.In one embodiment of the invention, the alkyl, amine, alkoxy, and alkyl carboxyl groups independently included in each of R 1 to R 4 are substituted linear groups having from about 1 to about 20 carbon atoms Or a branched alkyl group. As used herein, a linear or branched alkyl group can have from about 1 to about 20 carbon atoms, from about 1 to about 15, from about 1 to about 10, or from about 1 to about 6 Alkyl group and may be an alkyl group such as methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl, octyl, nonyl, decyl, undecyl, dodecyl, tridecyl, tetradecyl, pentadecyl, hexadecyl, octadecyl, Decyl, eicosanyl, or all possible isomers thereof. For example, an alkyl group having 1 to 12 carbon atoms, that is, a methyl group, an ethyl group, a propyl group, a butyl group, a pentyl group, a hexyl group, a heptyl group, an octyl group, a nonyl group, a decyl group, Or an alkyl group having 1 to 6 carbon atoms, that is, a methyl group, an ethyl group, a propyl group, a butyl group, a pentyl group, or a hexyl group, or an alkyl group having 1 to 4 carbon atoms, , n-propyl group, t-butyl group, s-butyl group, or n-butyl group.
본원의 일 구현예에 있어서, 상기 R1 내지 R4 각각에 독립적으로 포함되는 상기 시클로알킬기, 상기 시클로알킬아민기, 및 상기 시클로알콕시기는 탄소수 약 3 내지 약 30인 치환될 수 있는 시클로알킬기를 포함할 수 있으며, 이는 단일의 시클릭 고리 또는 단일의 시클릭 고리가 연결되거나 융합된 다환 고리를 포함할 수 있다. 본원에서 사용되는 시클로알킬기는, 탄소 수 약 3 내지 약 30, 약 3 내지 약 25, 약 3 내지 약 20, 약 3 내지 약 15, 약 3 내지 약 10, 약 5 내지 약 30, 약 5 내지 약 25, 약 5 내지 약 20, 약 5 내지 약 15, 약 5 내지 10, 약 6 내지 약 30, 약 6 내지 약 25, 약 6 내지 약 20, 약 6 내지 약 15, 또는 약 6 내지 약 10의 시클로알킬기를 포함하는 것일 수 있으며, 예를 들면, 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헥세닐, 시클로헵틸, 시클로헵테닐, 시클로옥틸, 시클로옥테닐, 2,5-시클로헥사디에닐, 비시클로[2.2.2]옥틸, 아다만트-1-일, 데카히드로나프틸, 옥소시클로헥실, 디옥소시클로헥실, 티오시클로헥실, 2-옥소비시클로[2.2.1]헵트-1-일, 또는 이들의 가능한 모든 이성질체일 수 있으나, 이에 제한되지 않을 수 있다.In one embodiment of the present invention, the cycloalkyl group, the cycloalkylamine group, and the cycloalkoxy group independently included in each of R 1 to R 4 include an optionally substituted cycloalkyl group having about 3 to about 30 carbon atoms , Which may comprise a single cyclic ring or a polycyclic ring fused or fused with a single cyclic ring. As used herein, cycloalkyl groups may have from about 3 to about 30 carbon atoms, from about 3 to about 25, from about 3 to about 20, from about 3 to about 15, from about 3 to about 10, from about 5 to about 30, from about 5 to about 25, about 5 to about 20, about 5 to about 15, about 5 to 10, about 6 to about 30, about 6 to about 25, about 6 to about 20, about 6 to about 15, or about 6 to about 10 And may include a cycloalkyl group. Examples thereof include cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cyclohexenyl, cycloheptyl, cycloheptenyl, cyclooctyl, cyclooctenyl, 2,5-cyclohexadiyl 2-oxocyclo [2.2.1] hept-1-yl, and the like are preferable, and the heterocyclic ring may be substituted with at least one substituent selected from the group consisting of hydrogen, -, or all possible isomers thereof.
본원의 일 구현예에 있어서, 상기 R1 내지 상기 R4 각각에 독립적으로 포함되는 상기 아릴기, 상기 아릴아민기, 상기 아릴옥시기, 상기 아릴카르복실기, 및 상기 아릴머캅토기에 포함되는 치환될 수 있는 아릴기는 탄소 수 약 6 내지 약 30인 치환될 수 있는 아릴기를 포함할 수 있으며, 이는 페닐기이거나 또는 두 개 이상의 페닐기가 연결되거나 융합된 다환고리를 포함할 수 있다. 상기 아릴기는, 탄소 수 약 6 내지 약 30, 약 6 내지 약 25, 약 6 내지 약 20, 약 6 내지 약 15, 또는 약 6 내지 약 10의 아릴기를 포함하는 것일 수 있으며, 예를 들어, 페닐 고리, 톨루일 고리, 나프탈레닐 고리, 안트라세닐 고리, 페난트렌 고리, 펜타렌 고리, 인덴 고리, 비페닐렌 고리, 페날렌 고리, 아즈렌 고리, 헵타렌 고리, 아세나프틸렌 고리, 플루오렌 고리, 테트라센 고리, 트리페닐렌 고리, 피렌 고리, 크리센 고리, 에틸-크리센 고리, 피센 고리, 페릴렌 고리, 펜타펜 고리, 펜타센 고리, 테트라페닐렌 고리, 헥사펜 고리, 헥사센고리, 루비센 고리, 코로넨 고리, 트리나프틸렌 고리, 헵타펜 고리, 헵타센 고리, 피란트렌 고리, 오바렌 고리, 플로란센 고리, 벤조플로란센 고리, 9-안트릴기, 2-안트릴기, 9-페난트릴기, 2-페난트릴기, 1-피렌일기, 크라이센일기, 나프타센일기, 코로닐기, 및 이들의 유도체로 이루어진 군으로부터 선택될 수 있으나, 이에 제한되지 않을 수 있다.In one embodiment of the present invention, the aryl group, the arylamine group, the aryloxyl group, the arylcarboxyl group, and the arylmercapto group contained in the aryl mercapto group, which are independently included in each of R 1 to R 4 , The aryl group may comprise an aryl group that may be substituted having from about 6 to about 30 carbon atoms, which may be a phenyl group or may comprise a polycyclic ring fused with two or more phenyl groups. The aryl group may be an aryl group containing from about 6 to about 30 carbon atoms, from about 6 to about 25, from about 6 to about 20, from about 6 to about 15, or from about 6 to about 10, A heterocyclic ring, an acenaphthylene ring, an acenaphthylene ring, a fluorene ring, a phenylene ring, a biphenylene ring, a phenylene ring, a phenylene ring, an azrene ring, a heptarenylene ring, an acenaphthylene ring, A heterocyclic ring, a tetracene ring, a tetracene ring, a tetracene ring, a triphenylene ring, a pyrene ring, a chrysene ring, an ethyl-chrysene ring, a picene ring, a perylene ring, a pentaphene ring, Anthracene ring, heptadecene ring, heptadecene ring, pyranthrene ring, obaren ring, fluoransen ring, benzofluoransen ring, 9-anthryl group, 2- Anthryl group, 9-phenanthryl group, 2-phenanthryl group, 1-pyreneyl group, Line group, nose group, and may be selected from the group consisting of their derivatives, may not be limited thereto.
본원의 일 구현예에 있어서, 상기 R1 내지 상기 R4 각각에 독립적으로 포함되는 상기 아릴기, 상기 아릴아민기, 상기 아릴옥시기, 상기 아릴카르복실기 또는 상기 아릴머캅토기에 포함되는 아릴기는 페닐기, 비페닐기, 또는 나프틸기를 포함하는 것일 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, the aryl group, the arylamine group, the aryloxy group, the arylcarboxyl group or the aryl group contained in the arylmercapto group, which are independently included in each of R 1 to R 4 , A biphenyl group, or a naphthyl group, but the present invention is not limited thereto.
본원의 일 구현예에 있어서, 상기 R1 및 상기 R2에 치환될 수 있는 치환기는, 각각 독립적으로 할로겐기, 시아노기, 선형 또는 분지형의 C1-8 알킬기, 또는 선형 또는 분지형의 C1-8 알콕시기인 것을 포함하는 것일 수 있으나, 이에 제한되는 것은 아니다.In one embodiment of the present invention, the substituents which may be substituted for R 1 and R 2 are each independently a halogen group, a cyano group, a linear or branched C 1-8 alkyl group, or a linear or branched C Lt; / RTI > alkoxy group, but is not limited thereto.
본원의 일 구현예에 있어서, 상기 R3 및 상기 R4 각각에 독립적으로 치환될 수 있는 치환기는, 각각 독립적으로 할로겐기, 시아노기, 선형 또는 분지형의 C1-8 알킬기, 또는 선형 또는 분지형의 C1-8 알콕시기인 것을 포함하는 것일 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, the substituent which can be independently substituted for each of R 3 and R 4 is, each independently, a halogen group, a cyano group, a linear or branched C 1-8 alkyl group, Lt; RTI ID = 0.0 > C 1-8 < / RTI > alkoxy group of the terrestrial form.
본원의 일 구현예에 있어서, 상기 R1 내지 R4에 치환될 수 있는 상기 선형 또는 분지형의 C1-8 알킬기 또는 상기 선형 또는 분지형의 C1-8 알콕시기는 탄소 수 약 1 내지 약 8의 선형 또는 분지형의 알킬기를 포함할 수 있으나, 이에 제한되는 것은 아니다. 상기 선형 또는 분지형의 알킬기는, 탄소 수 약 1 내지 약 8, 약 1 내지 약 7, 약 1 내지 약 6, 약 1 내지 약 5, 약 1 내지 약 4, 약 1 내지 약 3, 또는 약 1 내지 약 2의 알킬기를 포함하는 것일 수 있으며, 메틸, 에틸, 프로필, 부틸, 펜틸, 헥실, 헵틸, 옥틸, 또는 이들의 가능한 모든 이성질체를 포함한다. 예를 들어, 탄소수가 1 내지 8인 알킬기, 즉, 메틸기, 에틸기, 프로필기, 부틸기, 펜틸기, 헥실기, 헵틸기, 옥틸기일 수 있고, 또는 탄소수가 1 내지 6인 알킬기, 즉, 메틸기, 에틸기, 프로필기, 부틸기, 펜틸기, 또는 헥실기일 수 있으며, 또는 탄소수가 1 내지 4인 알킬기, 즉, 메틸기, 에틸기, i-프로필기, n-프로필기, t-부틸기, s-부틸기, 또는 n-부틸기일 수 있으나, 이에 제한되는 것은 아니다.In one embodiment of the present invention, the linear or branched C 1-8 alkyl group or the linear or branched C 1-8 alkoxy group which may be substituted for R 1 to R 4 has a carbon number of about 1 to about 8 But are not limited to, linear or branched alkyl groups. Wherein the linear or branched alkyl group has from about 1 to about 8 carbon atoms, from about 1 to about 7, from about 1 to about 6, from about 1 to about 5, from about 1 to about 4, from about 1 to about 3, To about 2 alkyl groups, and includes methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl, octyl, or all possible isomers thereof. For example, the alkyl group having 1 to 8 carbon atoms, that is, a methyl group, an ethyl group, a propyl group, a butyl group, a pentyl group, a hexyl group, a heptyl group, an octyl group, or an alkyl group having 1 to 6 carbon atoms, , An ethyl group, a propyl group, a butyl group, a pentyl group or a hexyl group, or an alkyl group having 1 to 4 carbon atoms such as a methyl group, an ethyl group, an i-propyl group, -Butyl group, or n-butyl group, but is not limited thereto.
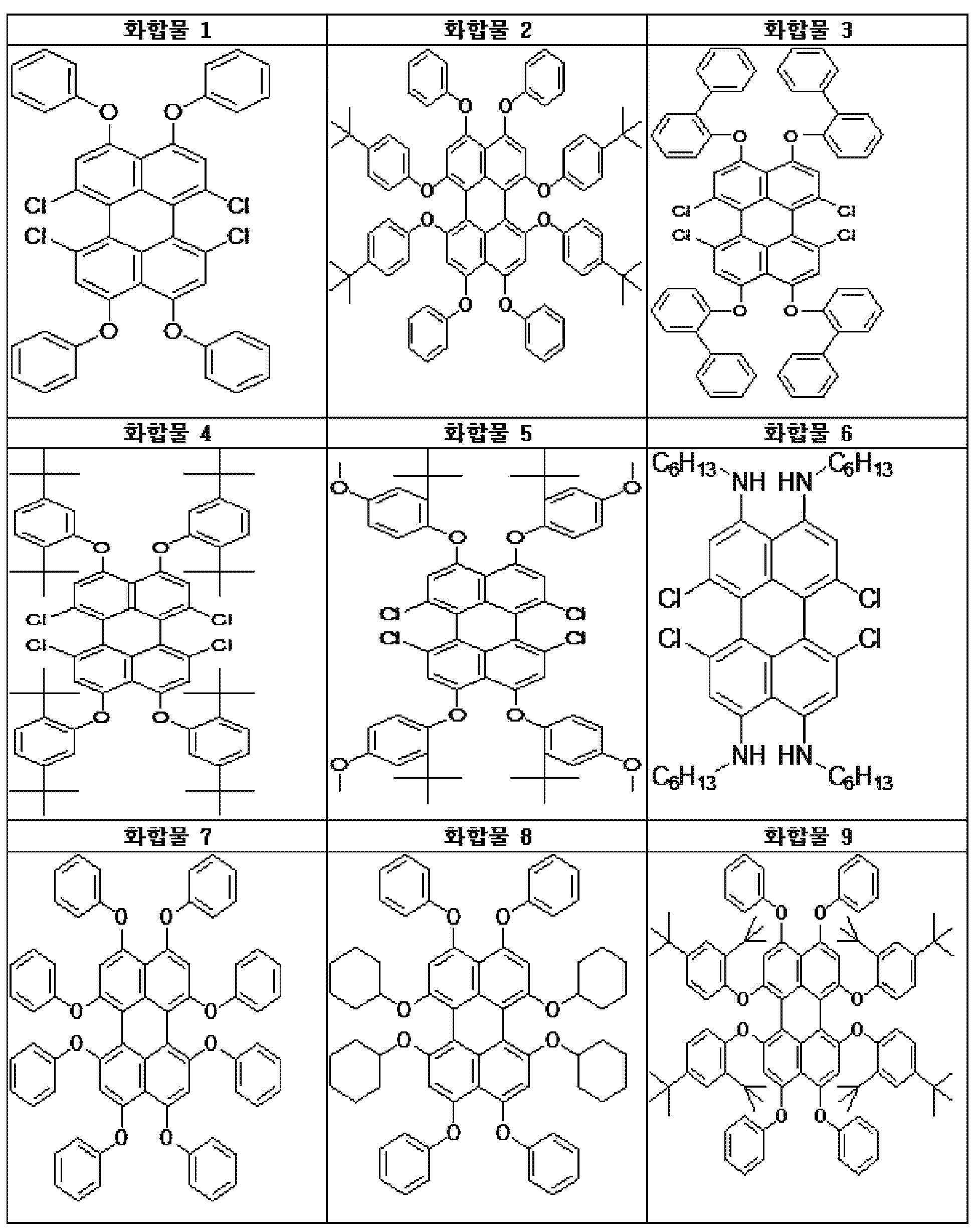
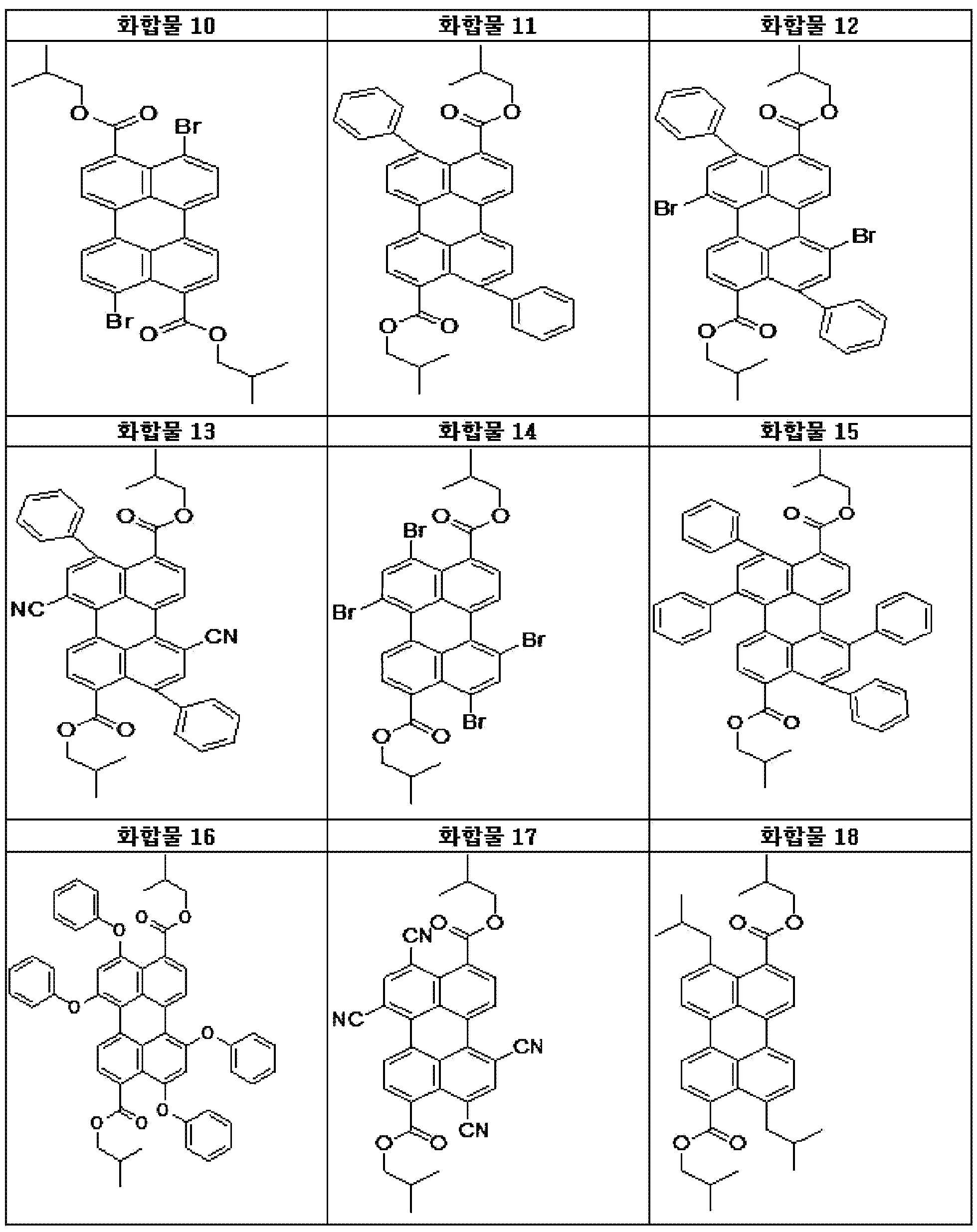
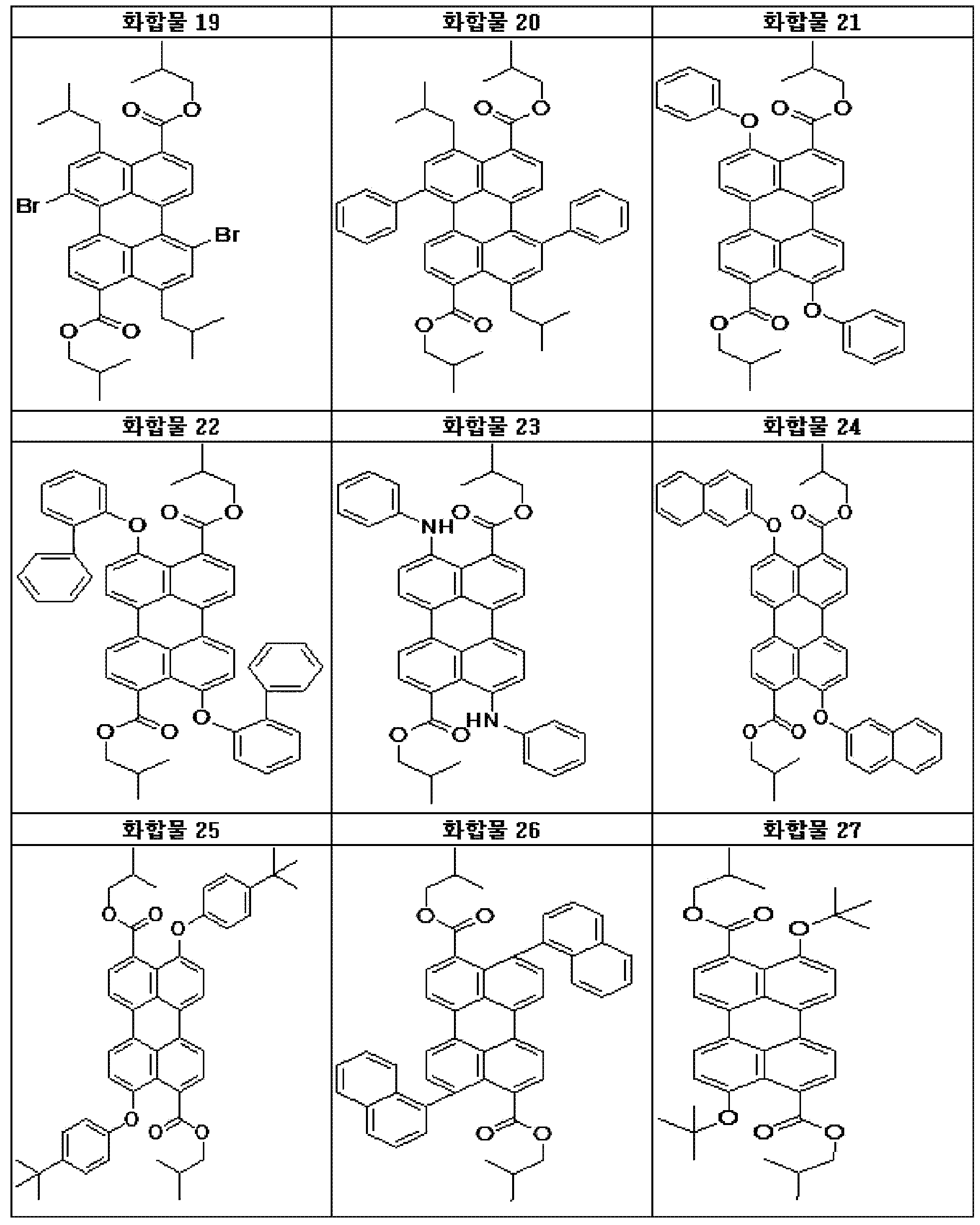
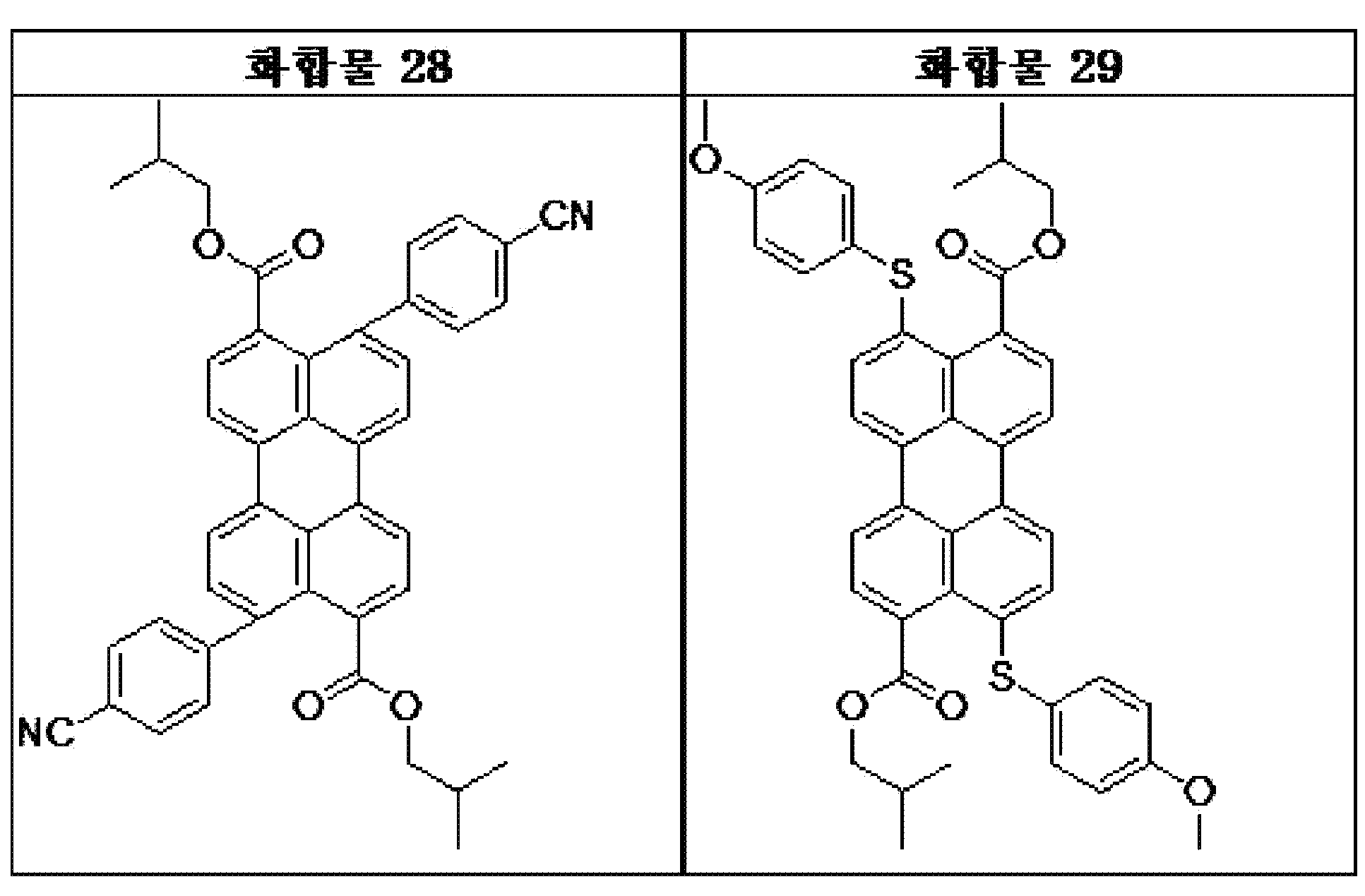
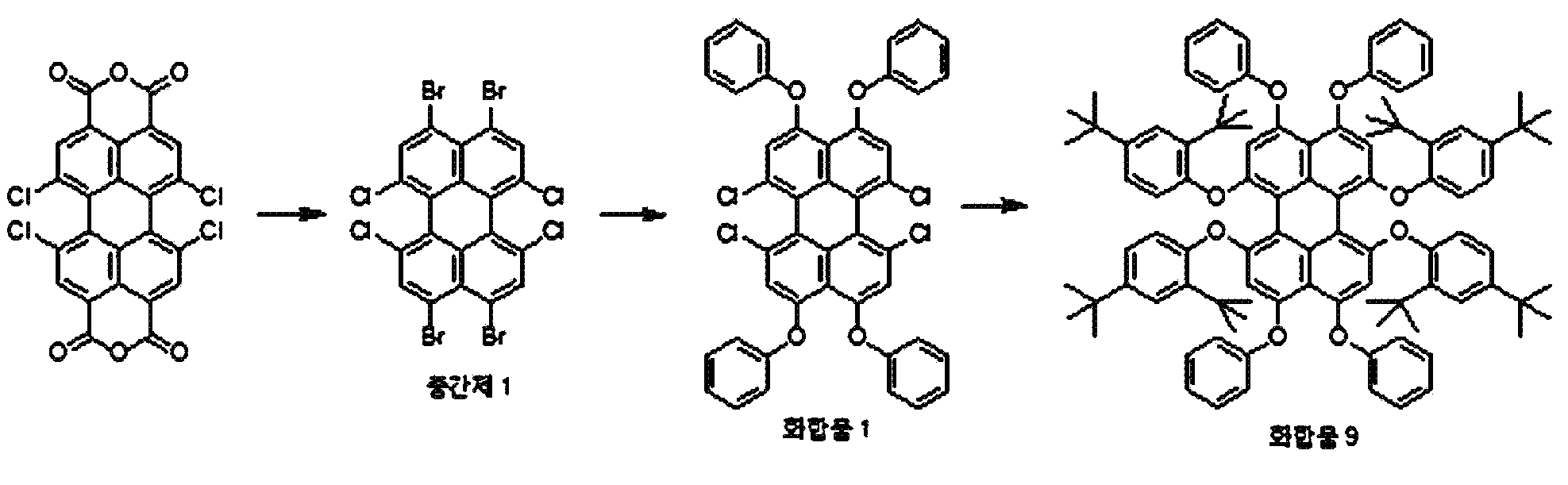
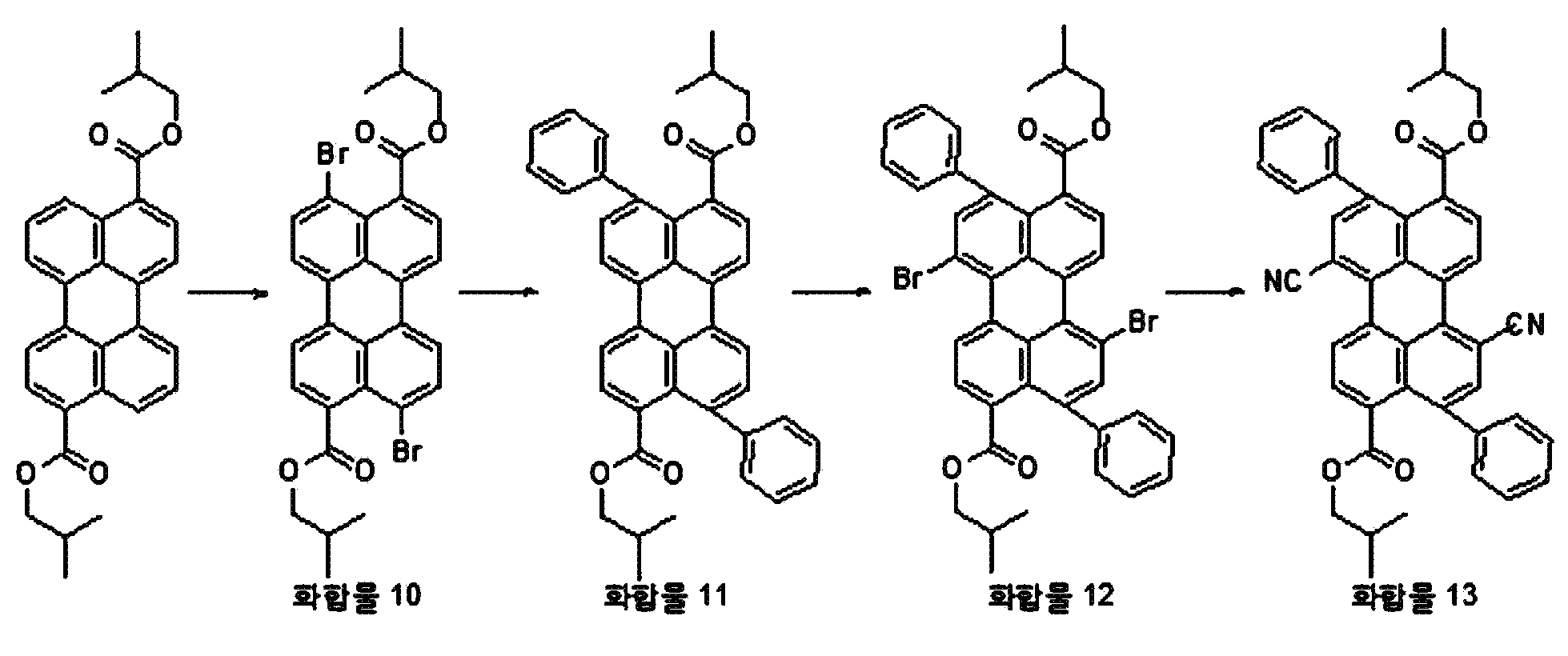
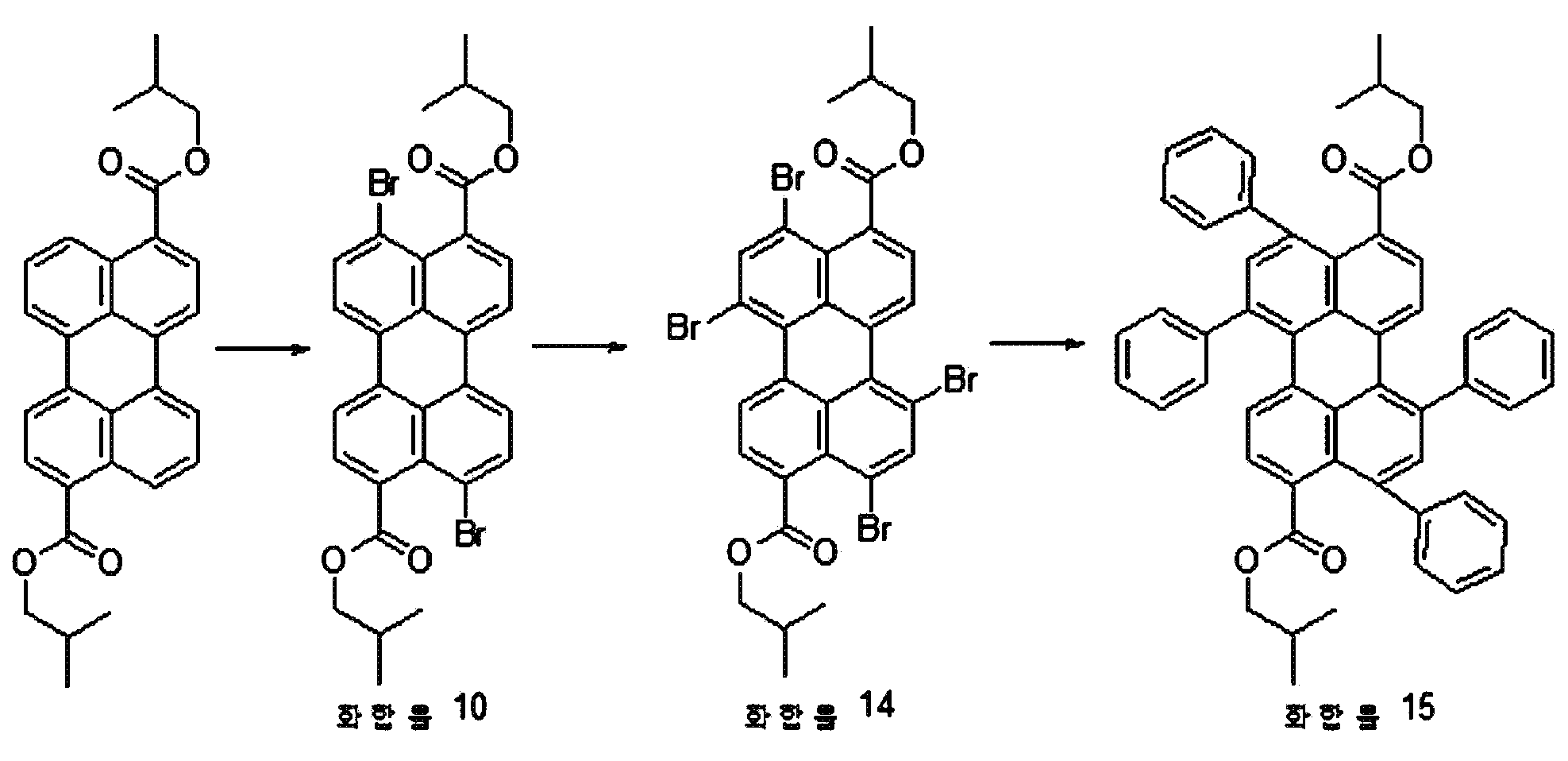
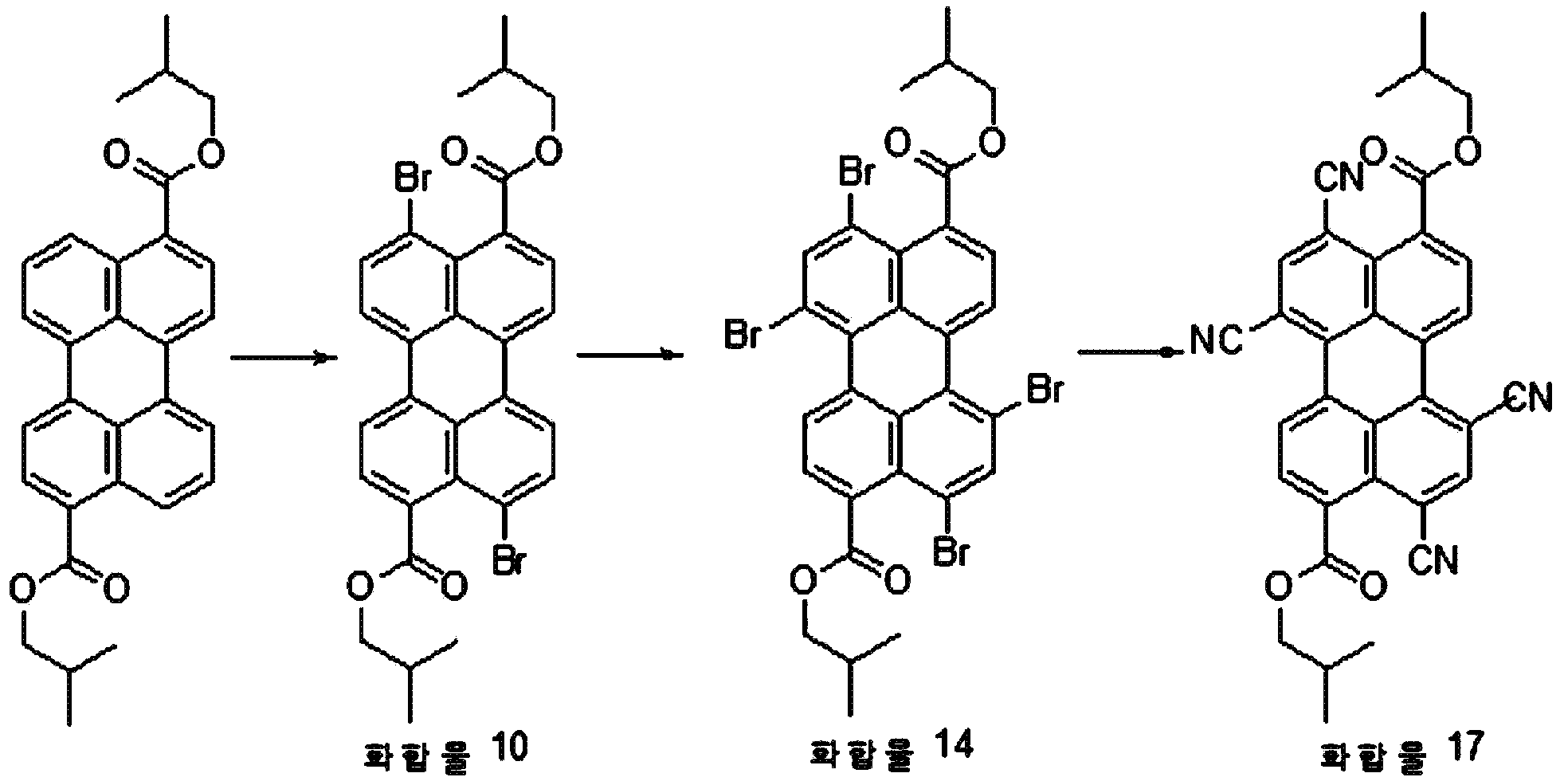
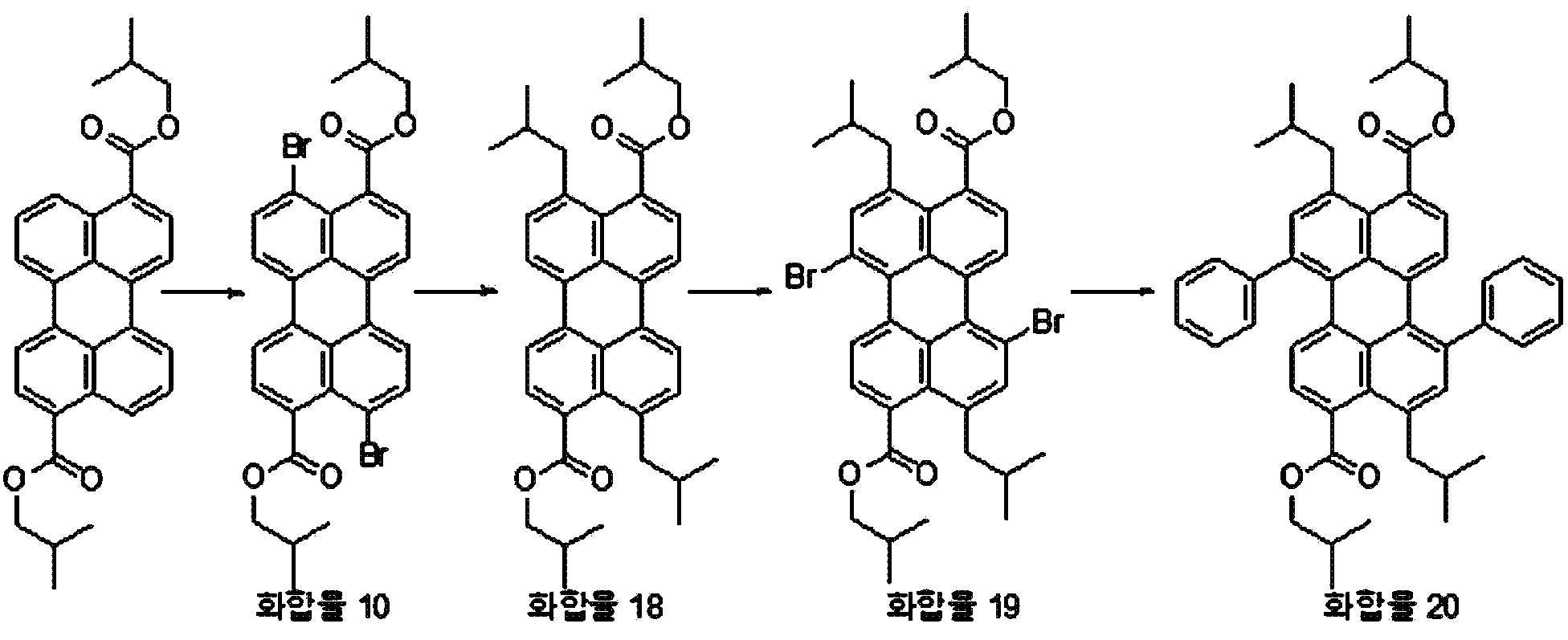
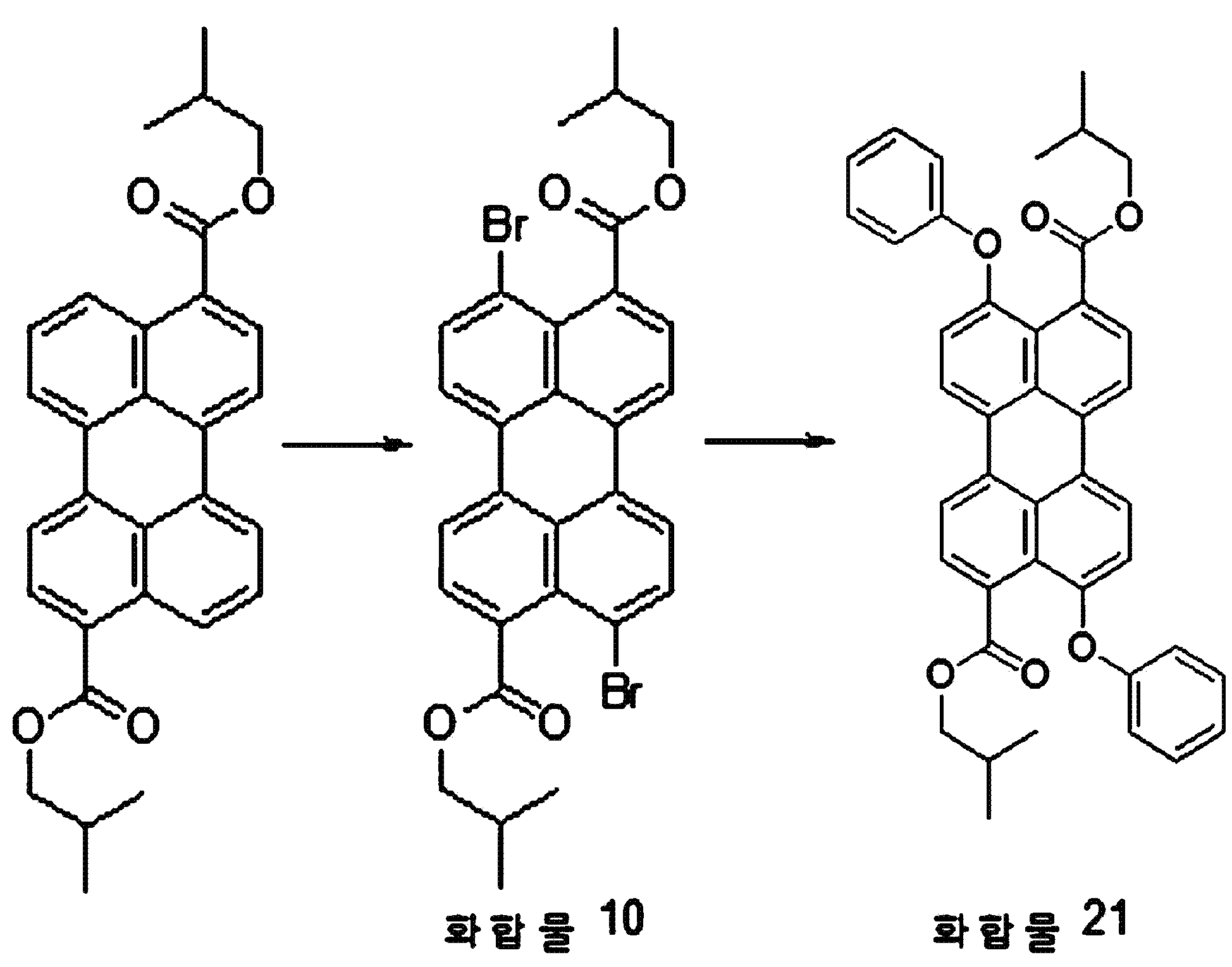
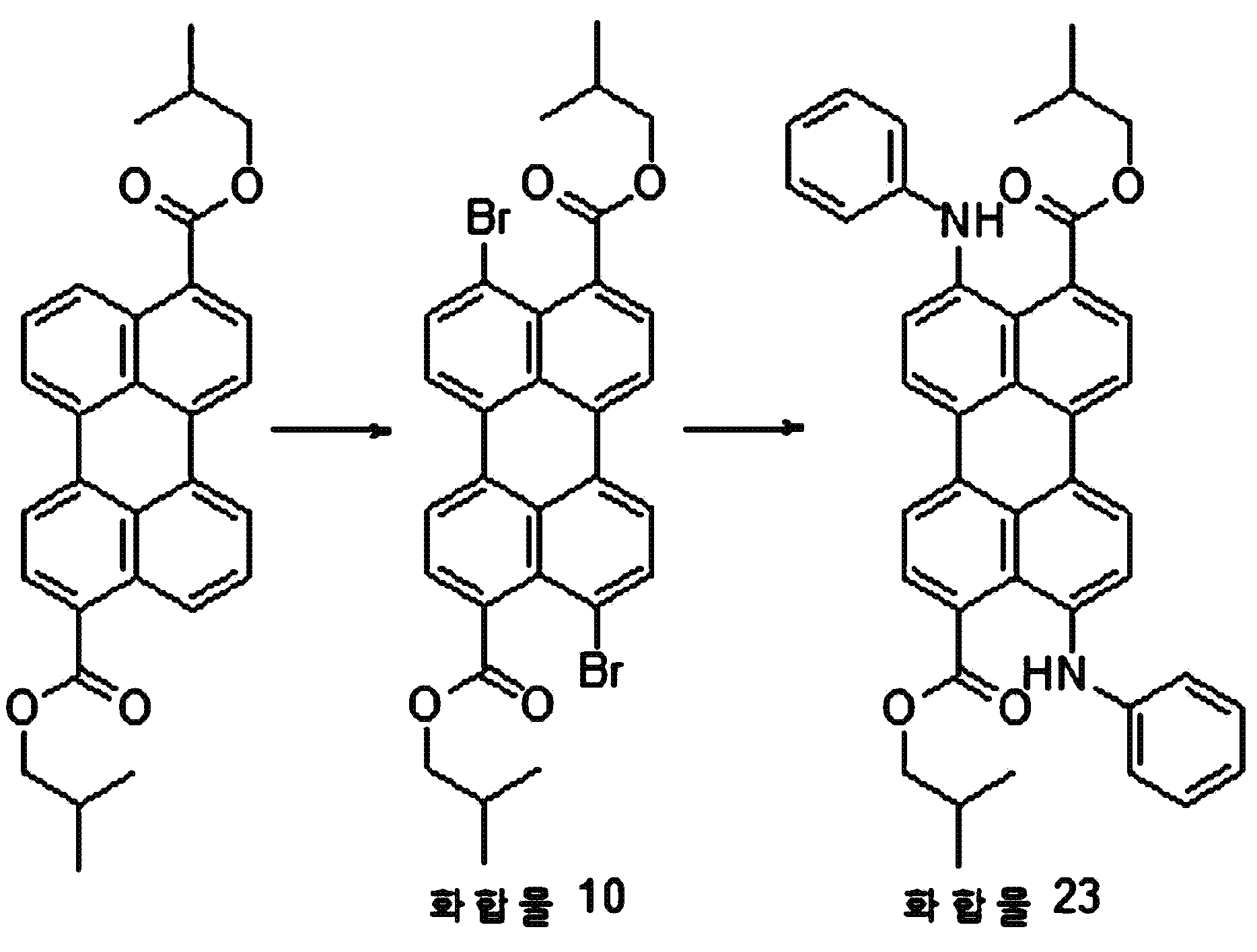
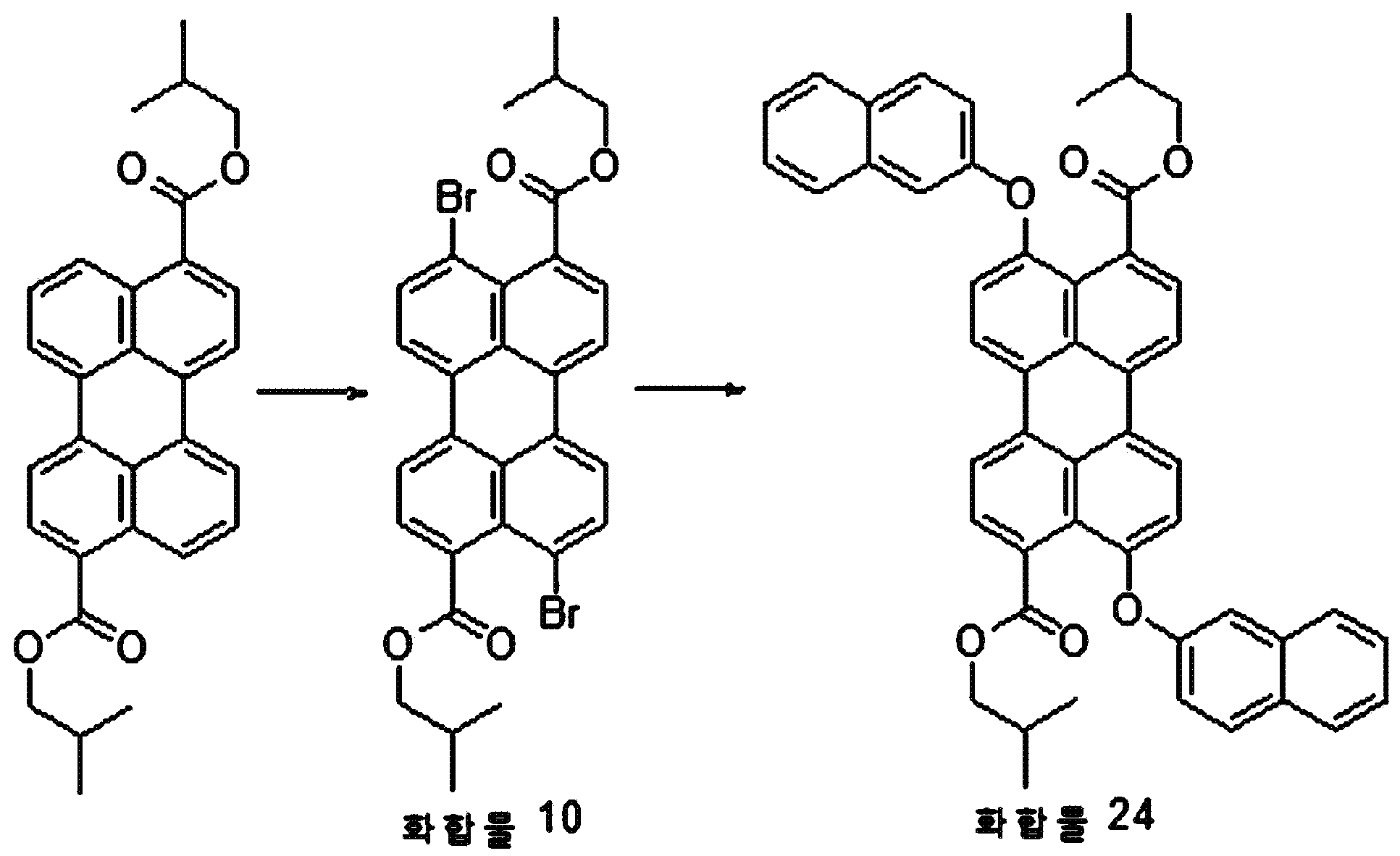
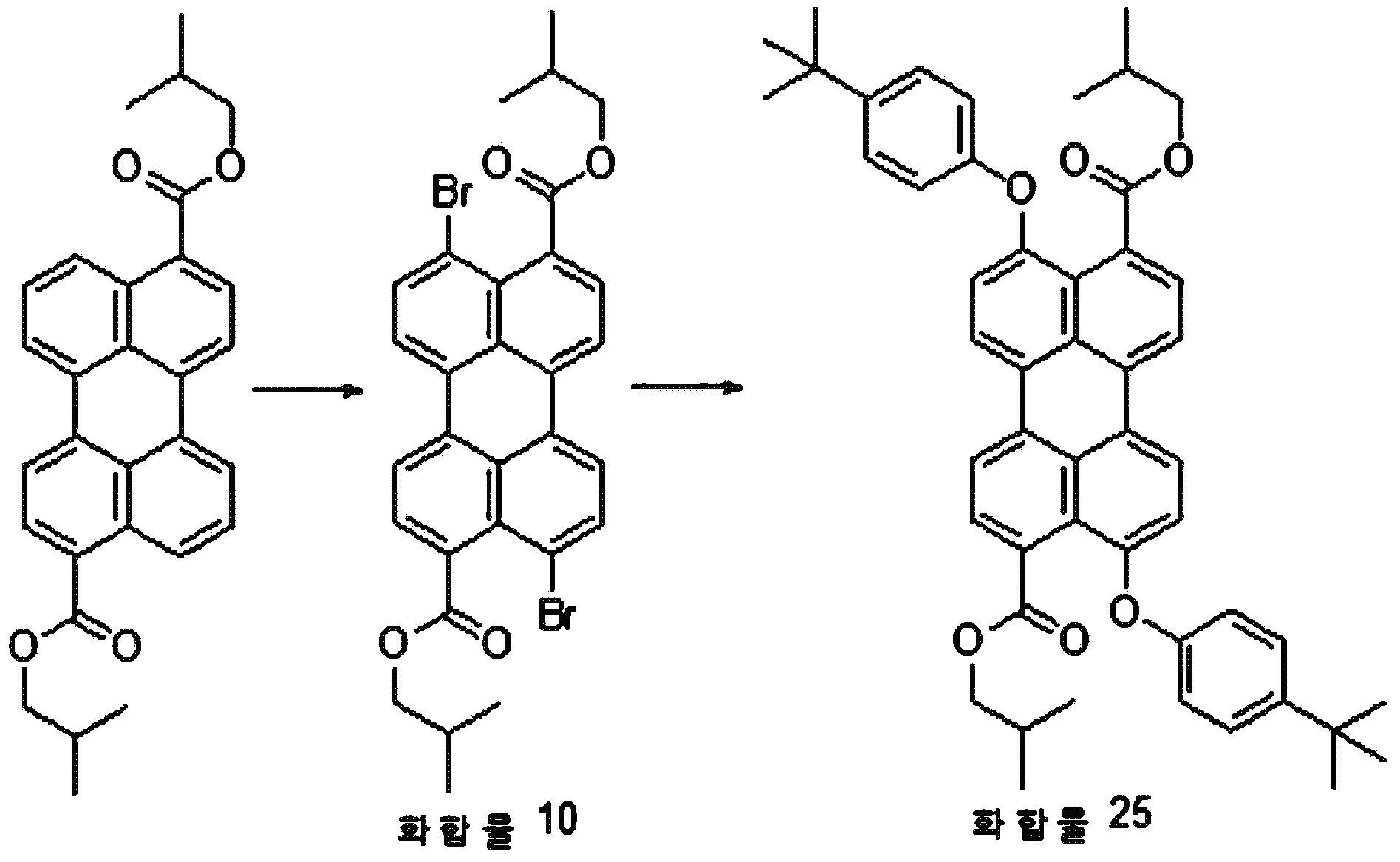
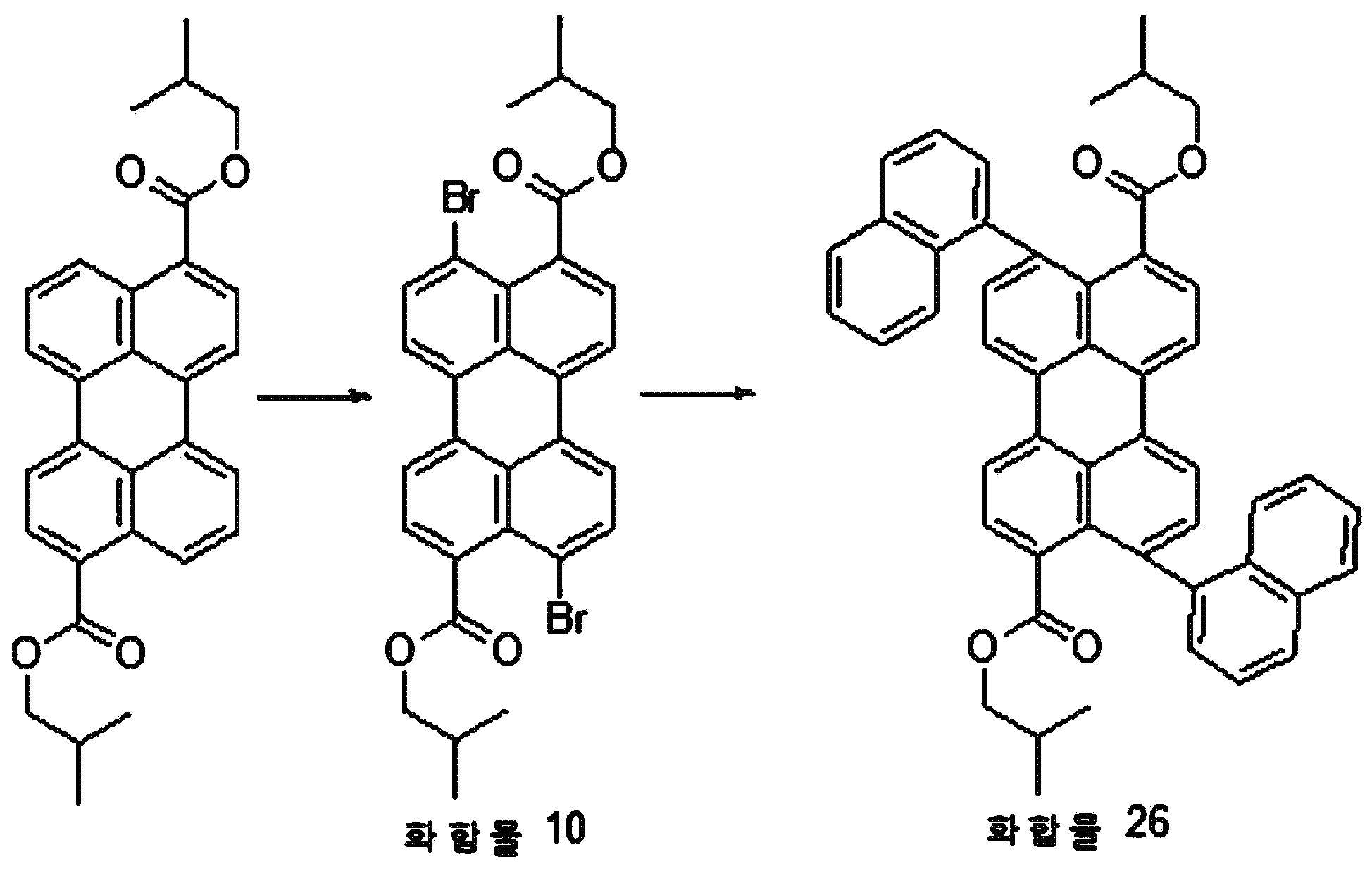
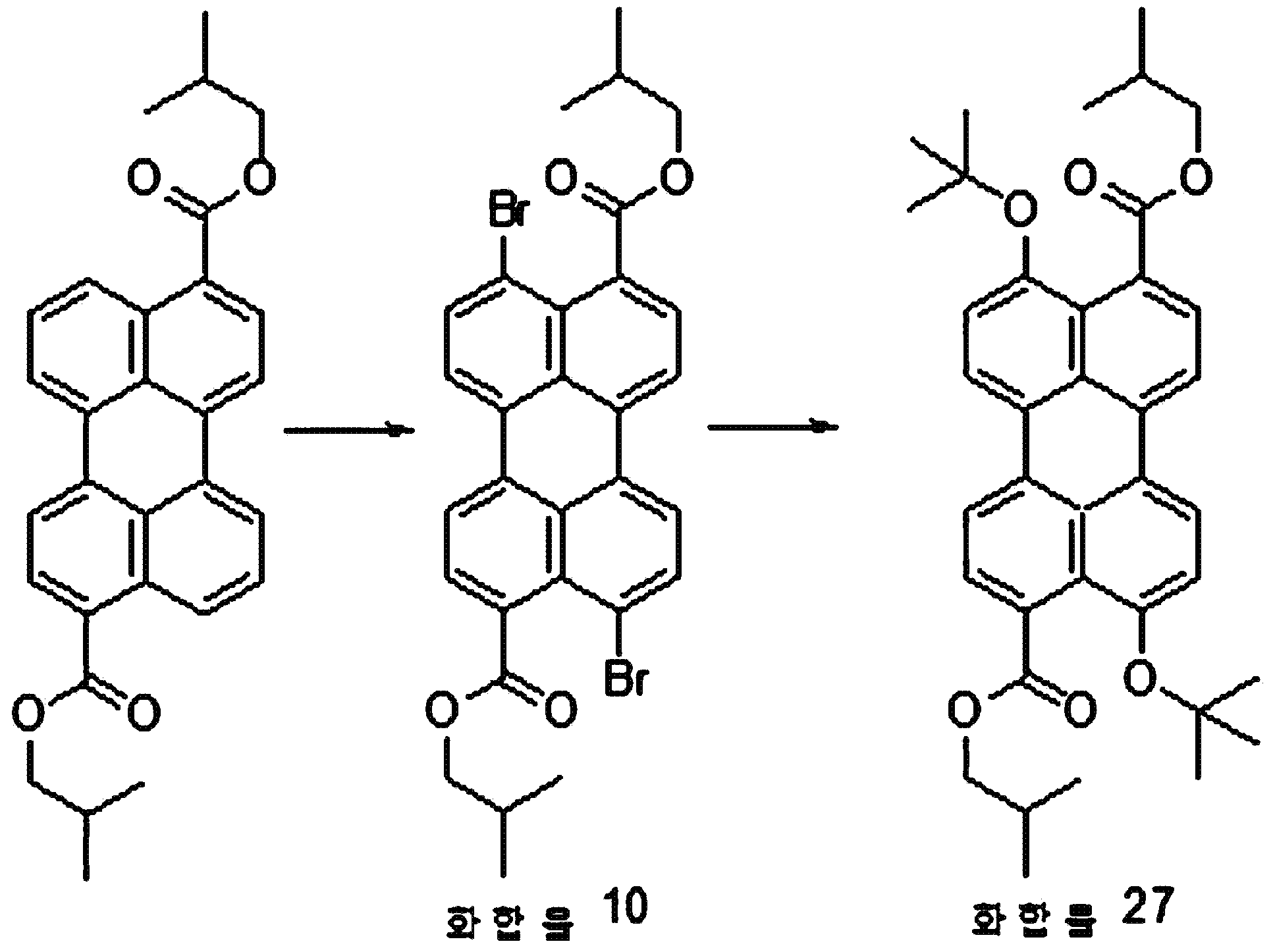
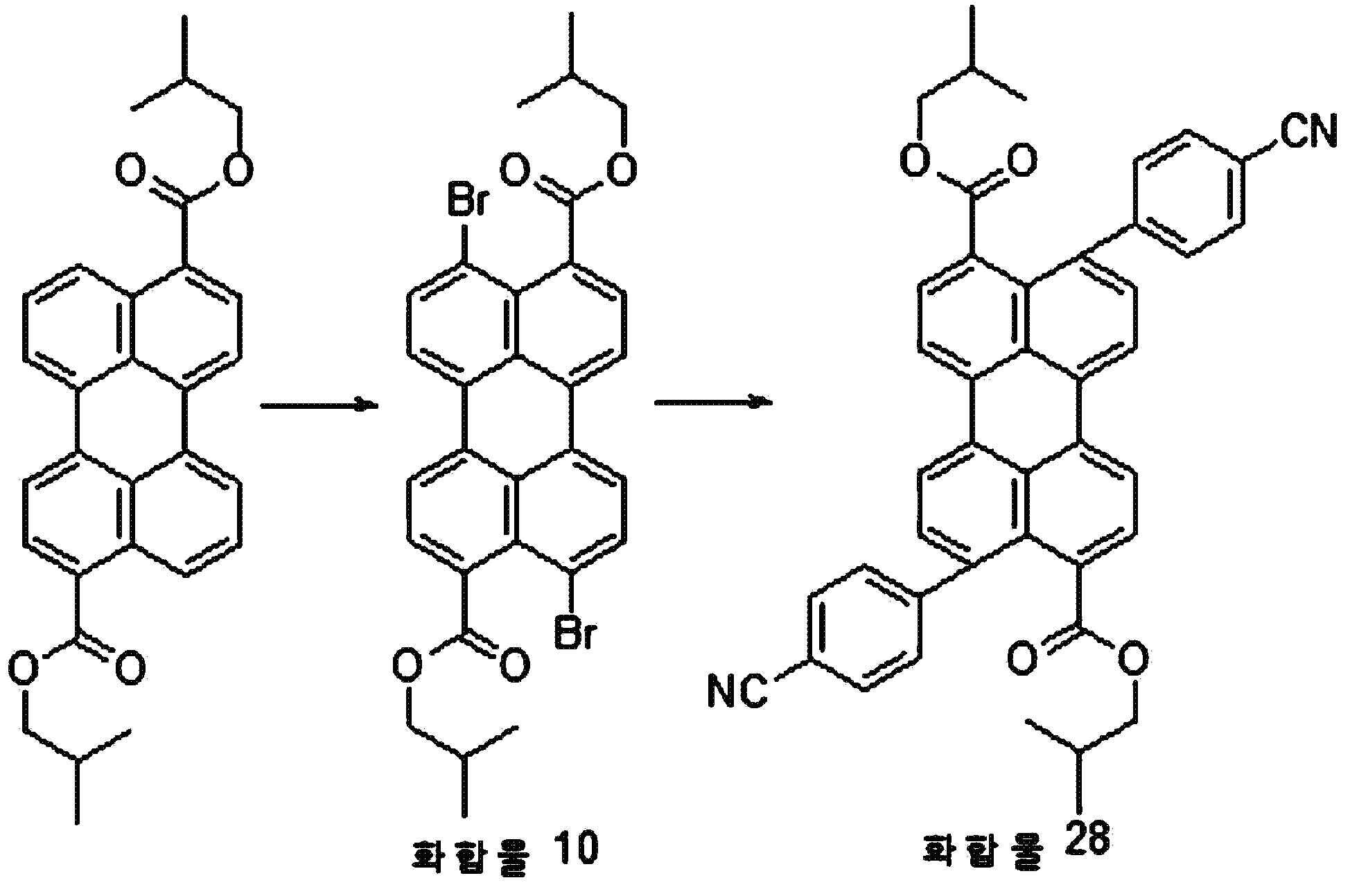
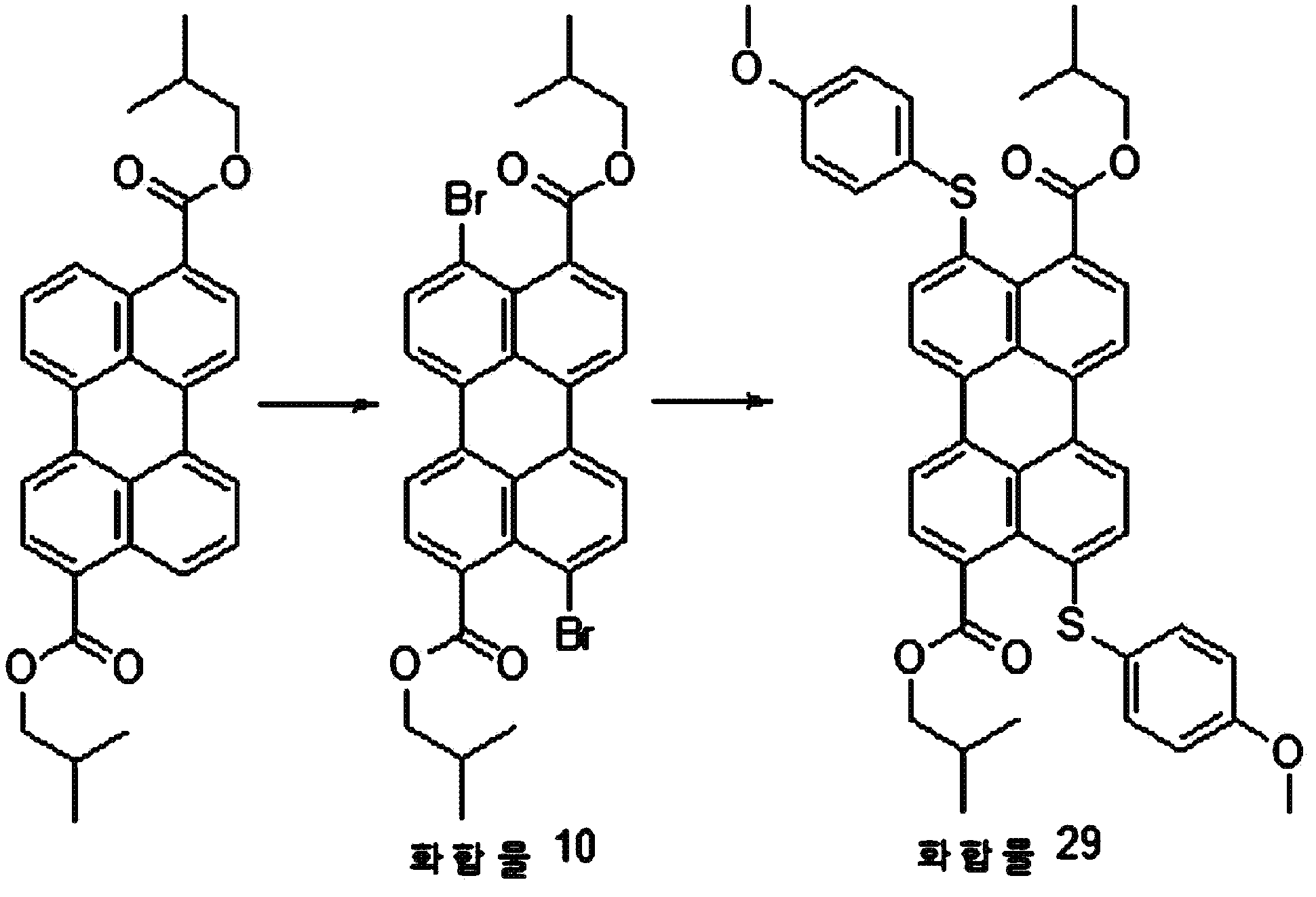
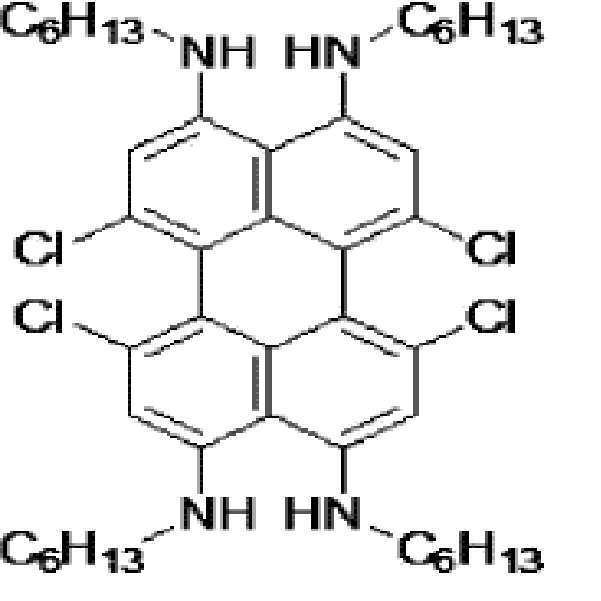
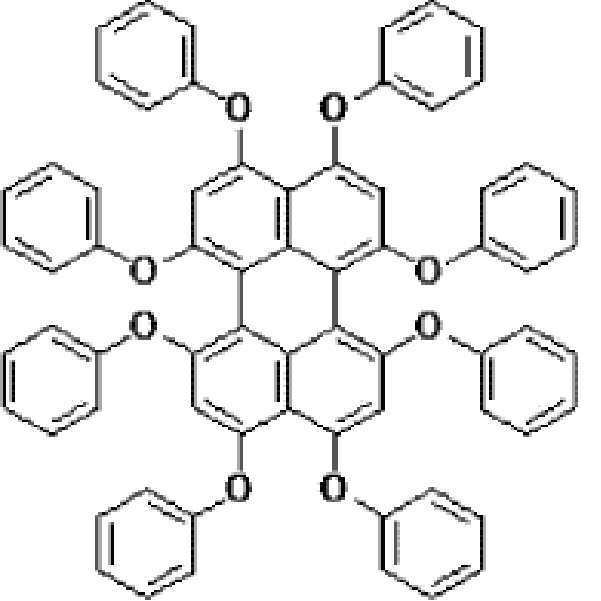
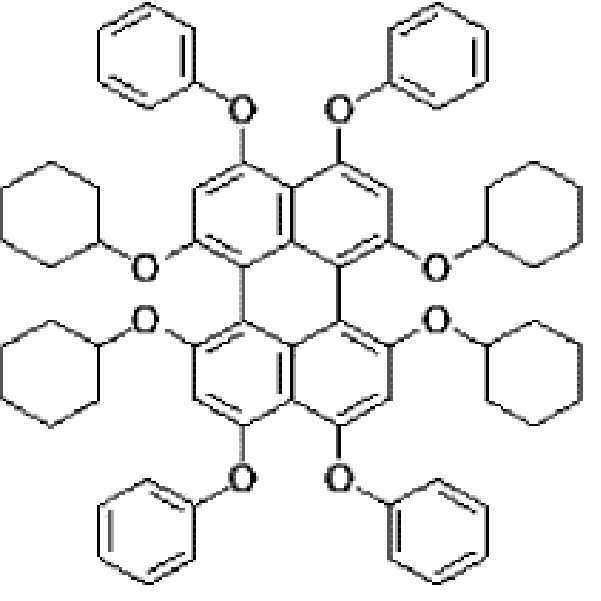
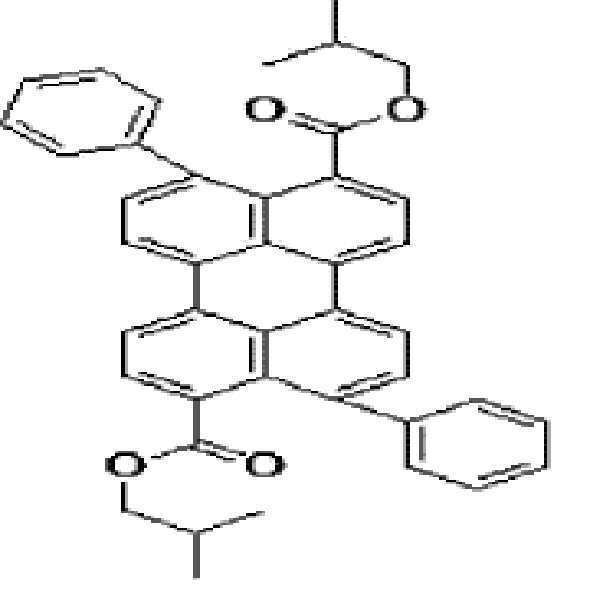
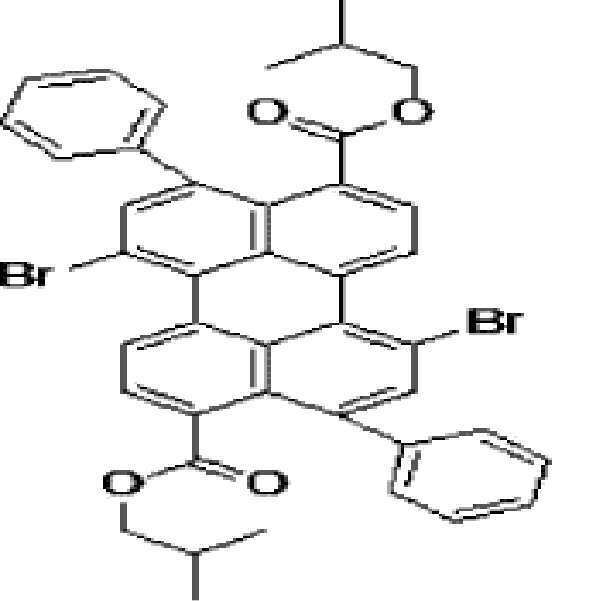
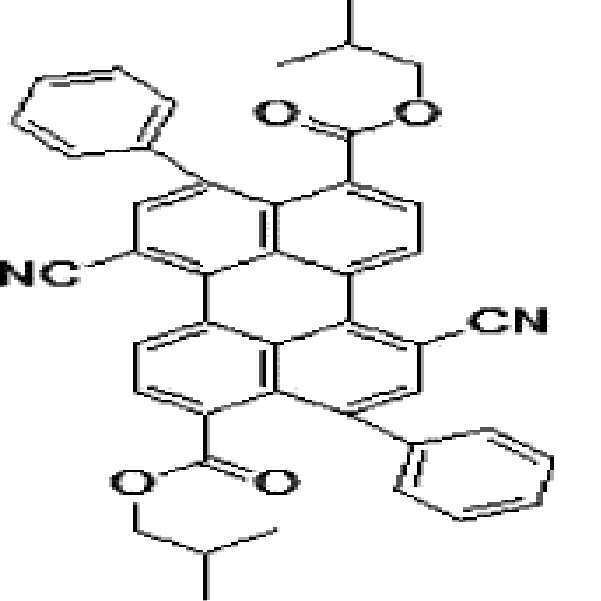
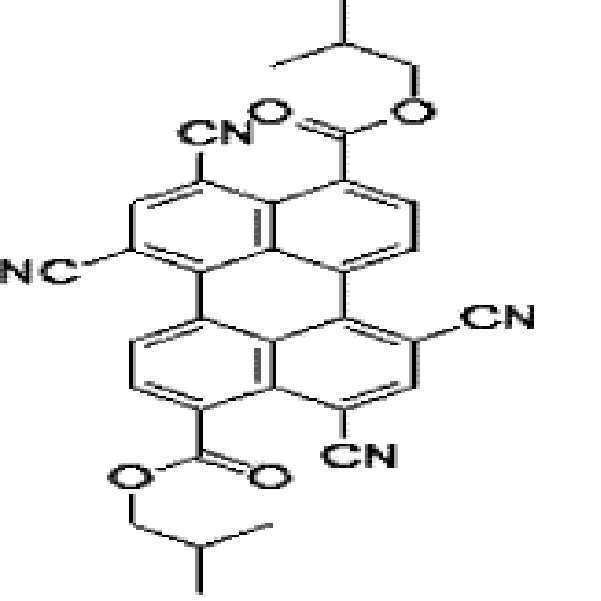
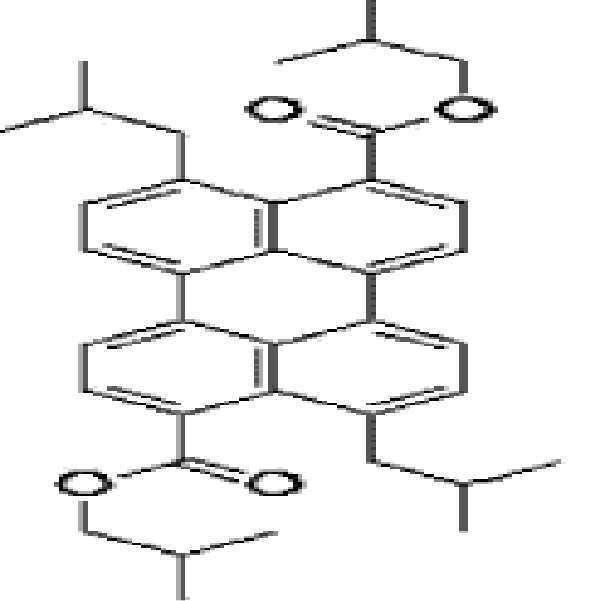
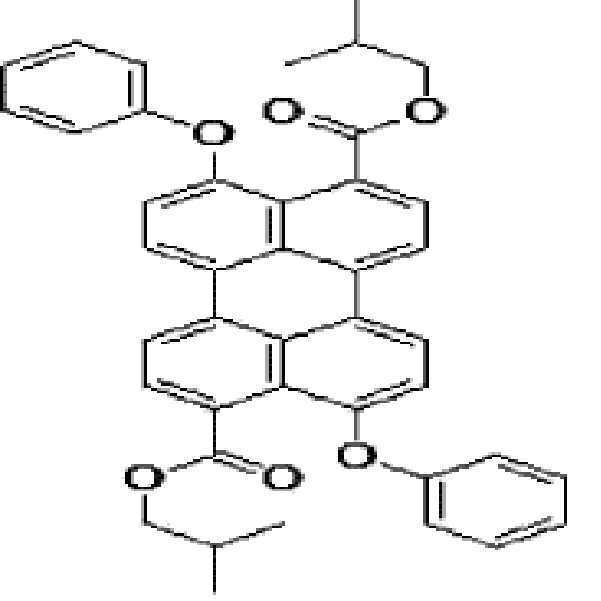
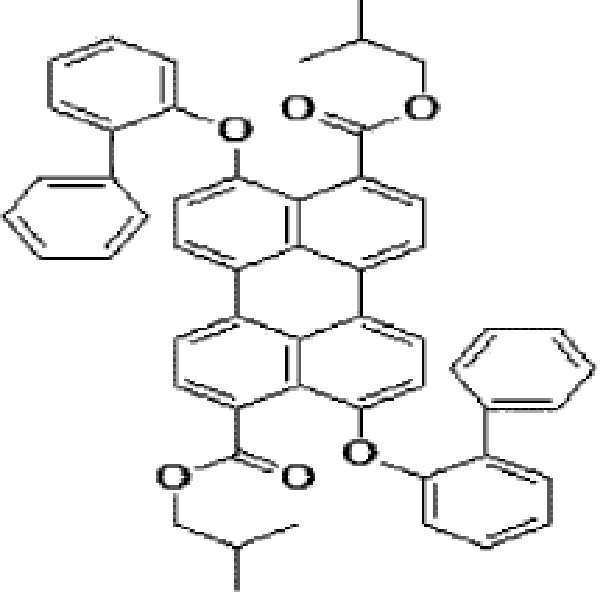
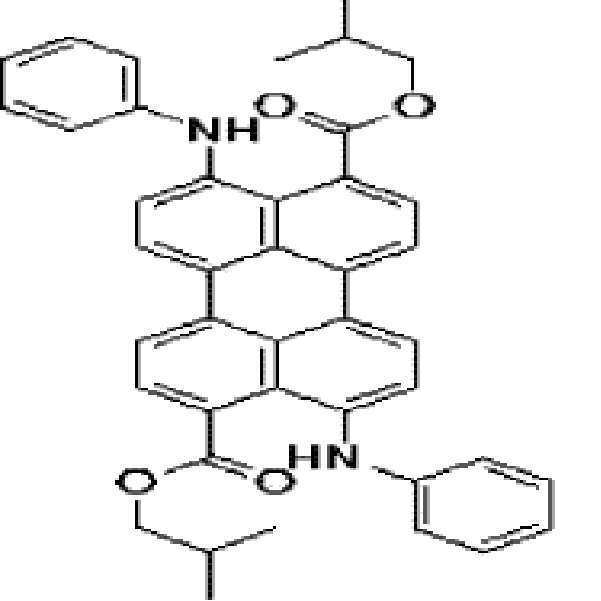
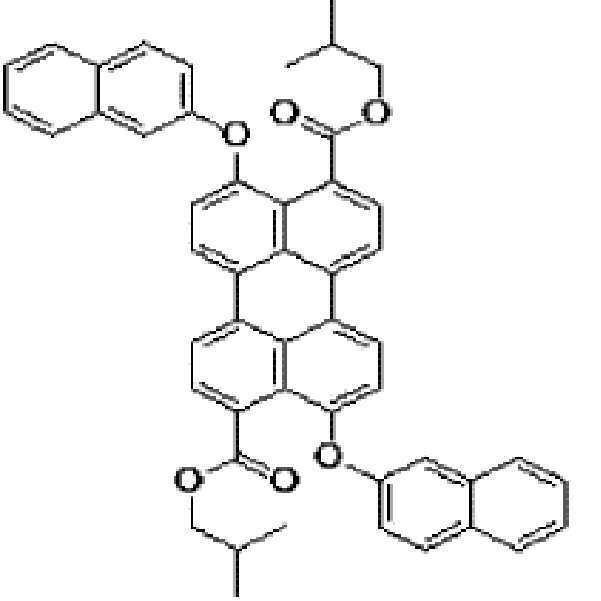
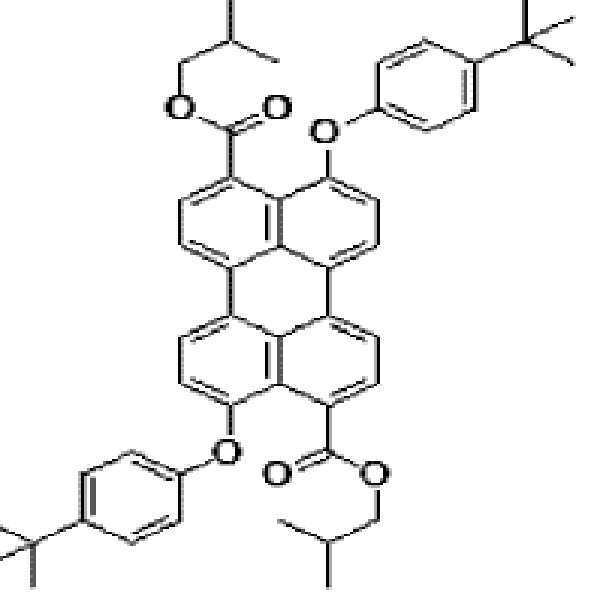
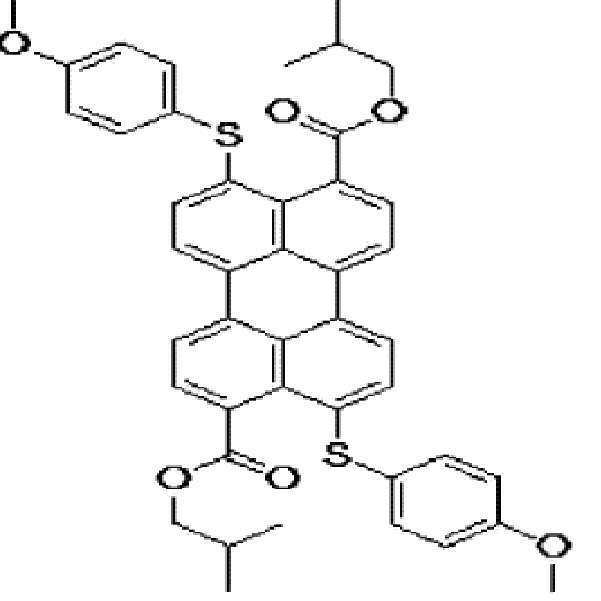
본원의 일 구현예에 있어서, 상기 페릴렌계 화합물은 하기 화합물을 포함할 수 있으나, 이에 제한되지 않을 수 있다:In one embodiment herein, the perylene compound may include, but is not limited to, the following compounds:
본원의 제 2 측면은, 하기 화학식 2로 표시되는 화합물을 치환될 수 있는 C1-20 알칸 화합물, 치환될 수 있는 C6-30 시클로알칸 화합물, 치환될 수 있는 C6-30 아릴 화합물, 치환될 수 있는 C6-30 페놀계 화합물, 치환될 수 있는 C1-20 알코올계 화합물, 치환될 수 있는 C1-20 알킬아민 화합물, 치환될 수 있는 C6-30 시클로알킬아민 화합물, 치환될 수 있는 C6-30 아릴아민 화합물, 또는 N-할로석신이미드와 반응시키는 것을 포함하는, 제 1 측면에 따른 페릴렌계 화합물의 제조 방법을 제공한다:Second aspect of the present application is to C 6-30 aryl compound, which may substituted C 6-30 cycloalkane compound, optionally substituted C 1-20 alkanes which may be the compounds, which may be substituted with a substituted a compound represented by the formula (2) be C 6-30 phenol-based compound, which may be substituted with C 1-20 alcohol-based compound, a C 1-20 alkyl amine compound which may be substituted, may be substituted with a C 6-30 cycloalkyl amine compound, which may be optionally substituted , it provides a process for the preparation of a perylene compound of the first aspect, which comprises a C 6-30 aryl amine, or N- halo succinimide which can be reacted with imide:
[화학식 2](2)
상기 화학식 2에서, R5 내지 R8은, 각각 독립적으로 수소, 할로겐 또는 치환될 수 있는 선형 또는 분지형의 C2-10 알킬카르복실기임.In Formula 2, R 5 to R 8 are each independently hydrogen, halogen, or a linear or branched C 2-10 alkylcarboxyl group which may be substituted.
본원의 일 구현예에 있어서, 상기 화학식 2로 표시되는 화합물과 반응시킬 수 있는 치환될 수 있는 C6-30 페놀계 화합물은, 예를 들면, 각각 독립적으로 히드록시페닐, 디히드록시페닐, 메톡시페닐, 디메톡시페닐, 트리메톡시페닐, 에톡시페닐, 디에톡시페닐, 트리에톡시페닐, 프로폭시페닐, 디프로폭시페닐, 이소프로폭시페닐, 디이소프로폭시페닐, 부톡시페닐, 히드록시페닐, 디히드록시페닐, 시아노페닐, 카르복시페닐, 카르복사미도페닐, N-메틸카르복사미도페닐, 아세틸아미노페닐, 프로피오닐아미노페닐, 부티릴아미노페닐, N-페닐아미노페닐, N-(o-톨릴)아미노페닐, N-(m-톨릴)아미노페닐, N-(p-톨릴)아미노페닐, (2-피리딜)아미노페닐, (3-피리딜)아미노페닐, (4-피리딜)아미노페닐, (2-피리미딜)아미노페닐, 4-(4-피리미딜)아미노페닐, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 포함할 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, the C 6-30 phenol-based compound that can be reacted with the compound represented by Formula 2 is, for example, independently selected from the group consisting of hydroxyphenyl, dihydroxyphenyl, Propoxyphenyl, dipropoxyphenyl, diisopropoxyphenyl, diisopropoxyphenyl, butoxyphenyl, heptoxyphenyl, diethoxyphenyl, trimethoxyphenyl, ethoxyphenyl, diethoxyphenyl, triethoxyphenyl, N-methylcarbamidophenyl, acetylaminophenyl, propionylaminophenyl, butyrylaminophenyl, N-phenylaminophenyl, N-phenylaminophenyl, N-phenylaminophenyl, (o-tolyl) aminophenyl, N- (m-tolyl) aminophenyl, N- (p- tolyl) aminophenyl, Dilaminophenyl, (2-pyrimidyl) aminophenyl, 4- (4-pyrimidyl) aminophenyl, It may include those selected from the group consisting of chedeul However, without being limited thereto.
본원의 일 구현예에 있어서, 상기 화학식 2로 표시되는 화합물과 반응시킬 수 있는 치환될 수 있는 C1-20 알코올계 화합물은, 예를 들면, 각각 독립적으로 히드록시에틸, 히드록시프로필, 디히드록시프로필, 히드록시부틸, 디히드록시부틸, 히드록시펜틸, 디히드록시펜틸, 히드록시헥실, 디히드록시헥실, 히드록시헵틸, 디히드록시헵틸, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 포함할 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, the C 1-20 alcohol compound which can be reacted with the compound represented by Formula 2 is, for example, independently selected from the group consisting of hydroxyethyl, hydroxypropyl, dihydro Is selected from the group consisting of hydroxypropyl, hydroxypropyl, hydroxybutyl, dihydroxybutyl, hydroxypentyl, dihydroxypentyl, hydroxyhexyl, dihydroxyhexyl, hydroxyheptyl, dihydroxyheptyl, and all isomers thereof , But is not limited thereto.
본원의 일 구현예에 있어서, 상기 화학식 2로 표시되는 화합물과 반응시킬 수 있는 치환될 수 있는 선형 또는 분지형의 C1-20 알킬아민 화합물, 치환될 수 있는 C3-30 시클로알킬아민 화합물, 및 치환될 수 있는 C6-30 아릴아민 화합물은, 예를 들면, 각각 독립적으로 아미노기, 메틸아미노, 디메틸아미노, 에틸아미노, 디에틸아미노, 프로필아미노, 디프로필아미노, 디이소프로필아미노, 디부틸아미노, 디이소부틸아미노, 디-tert-부틸아미노, 디펜틸아미노, 디헥실아미노, 디페닐아미노, 디-o-톨릴아미노, 디-m-톨릴아미노, 디-p-톨릴아미노, 디(4-시아노페닐)아미노, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 포함할 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, a linear or branched C 1-20 alkylamine compound which may be substituted, which may be reacted with the compound represented by Formula 2, a C 3-30 cycloalkylamine compound that may be substituted, And C 6-30 arylamine compounds which may be substituted are, for example, each independently selected from the group consisting of an amino group, a methylamino group, a dimethylamino group, an ethylamino group, a diethylamino group, a propylamino group, a dipropylamino group, a diisopropylamino group, Amino, diisobutylamino, di-tert-butylamino, dipentylamino, dihexylamino, diphenylamino, di-o- tolylamino, di- -Cyanophenyl) amino, and all isomers thereof, but is not limited thereto.
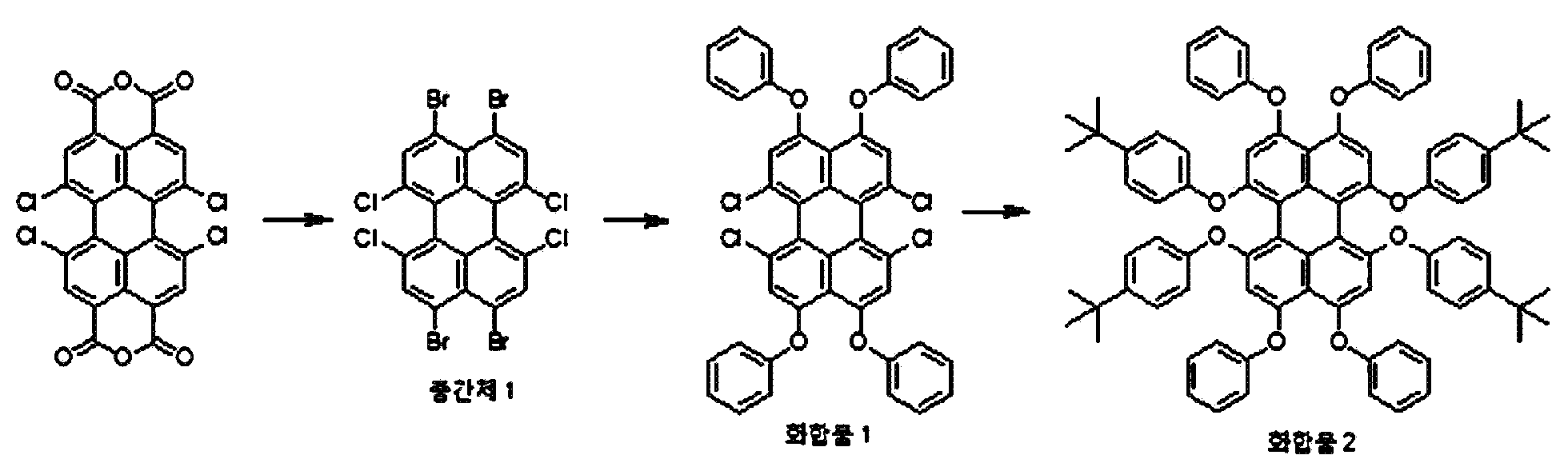
본원의 일 구현예에 있어서, 상기 화학식 2로 표시되는 화합물을, 페놀, 페닐 페놀, 디-tert-부틸 페놀, 하이드록시 tert-부틸 아니솔, N-할로 석신이미드, 헥실 아민, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것과 반응시키는 것을 포함하는 것일 수 있다. In one embodiment of the present invention, the compound represented by the general formula (2) is used in combination with at least one compound selected from the group consisting of phenol, phenylphenol, di-tert-butylphenol, hydroxy tert- butyl anisole, N-halosuccinimide, All of the isomers, and all of the isomers.
본원의 일 구현예에 있어서, 상기 화학식 2로 표시되는 화합물을, 페놀, 2-페닐페놀, 2,4-다이-tert-부틸페놀, 4-하이드록시-3-tert-부틸아니솔, N-브로모석신이미드, 헥실아민, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것과 반응시키는 것을 포함하는 것일 수 있다. In one embodiment herein, the compound of Formula 2 is reacted with a compound selected from the group consisting of phenol, 2-phenylphenol, 2,4-di-tert-butylphenol, 4-hydroxy- Bromosuccinimide, hexylamine, and all of the isomers thereof.
본원의 일 구현예에 있어서, 상기 제조된 페릴렌계 화합물에 할로겐, 시안화 염, 페놀계 화합물, 나프톨계 화합물, 알코올계 화합물, 티올계 화합물, 아민계 화합물 및 치환될 수 있는 보로닉엑시드로 이루어진 군으로부터 선택되는 물질을 첨가하여서 반응시키는 단계를 1회 내지 3회 수행하는 것을 추가 포함할 수 있다. In one embodiment of the present invention, the perylene-based compound prepared by the above-mentioned process comprises a compound consisting of a halogen, a cyanide salt, a phenol compound, a naphthol compound, an alcohol compound, a thiol compound, And then performing the reaction one to three times.
본원의 일 구현예에 있어서, 상기 제조된 페릴렌계 반응시킬 수 있는 페놀계 화합물 및 나프톨계 화합물은, 예를 들면, 각각 독립적으로 히드록시페닐, 디히드록시페닐, 메톡시페닐, 디메톡시페닐, 트리메톡시페닐, 에톡시페닐, 디에톡시페닐, 트리에톡시페닐, 프로폭시페닐, 디프로폭시페닐, 이소프로폭시페닐, 디이소프로폭시페닐, 부톡시페닐, 히드록시페닐, 디히드록시페닐, 시아노페닐, 카르복시페닐, 카르복사미도페닐, N-메틸카르복사미도페닐, 아세틸아미노페닐, 프로피오닐아미노페닐, 부티릴아미노페닐, N-페닐아미노페닐, N-(o-톨릴)아미노페닐, N-(m-톨릴)아미노페닐, N-(p-톨릴)아미노페닐, (2-피리딜)아미노페닐, (3-피리딜)아미노페닐, (4-피리딜)아미노페닐, (2-피리미딜)아미노페닐, 4-(4-피리미딜)아미노페닐, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 포함할 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, the phenol compound and the naphthol compound that can be reacted with the perylene compound are each independently selected from the group consisting of hydroxyphenyl, dihydroxyphenyl, methoxyphenyl, dimethoxyphenyl, Butoxyphenyl, diethoxyphenyl, diethoxyphenyl, triethoxyphenyl, propoxyphenyl, dipropoxyphenyl, isopropoxyphenyl, diisopropoxyphenyl, butoxyphenyl, hydroxyphenyl, dihydroxyphenyl , Naphthylaminophenyl, N-phenylaminophenyl, N- (o-tolyl) aminophenyl, N-phenylcarbamoylphenyl, N-methylcarboxamidophenyl, acetylaminophenyl, , (2-pyridyl) aminophenyl, (4-pyridyl) aminophenyl, (2-pyridyl) aminophenyl, -Pyrimidyl) aminophenyl, 4- (4-pyrimidyl) aminophenyl, and all isomers thereof. Gin may include is selected from the group, but is not limited to this.
본원의 일 구현예에 있어서, 상기 제조된 페릴렌계 반응시킬 수 있는 알코올계 화합물은, 예를 들면, 각각 독립적으로 히드록시에틸, 히드록시프로필, 디히드록시프로필, 히드록시부틸, 디히드록시부틸, 히드록시펜틸, 디히드록시펜틸, 히드록시헥실, 디히드록시헥실, 히드록시헵틸, 디히드록시헵틸, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 포함할 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, the produced perylene-based reactive alcohol-based compound is, for example, independently selected from the group consisting of hydroxyethyl, hydroxypropyl, dihydroxypropyl, hydroxybutyl, dihydroxybutyl Dihydroxypentyl, dihydroxypentyl, hydroxyhexyl, dihydroxyhexyl, hydroxyheptyl, dihydroxyheptyl, and all isomers thereof, but is not limited thereto no.
본원의 일 구현예에 있어서, 상기 제조된 페릴렌계 반응시킬 수 있는 아민계 화합물은, 예를 들면, 각각 독립적으로 아미노기, 메틸아미노, 디메틸아미노, 에틸아미노, 디에틸아미노, 프로필아미노, 디프로필아미노, 디이소프로필아미노, 디부틸아미노, 디이소부틸아미노, 디-tert-부틸아미노, 디펜틸아미노, 디헥실아미노, 디페닐아미노, 디-o-톨릴아미노, 디-m-톨릴아미노, 디-p-톨릴아미노, 디(4-시아노페닐)아미노, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 포함할 수 있으나, 이에 제한되는 것은 아니다.In one embodiment of the present invention, the produced perylene-based reactive amine compound is, for example, each independently an amino group, methylamino, dimethylamino, ethylamino, diethylamino, Di-tert-butylamino, di-tert-butylamino, dipentylamino, dihexylamino, diphenylamino, di- p-tolylamino, di (4-cyanophenyl) amino, and all isomers thereof, but is not limited thereto.
본원의 일 구현예에 있어서, 상기 제조된 페릴렌계 화합물에 할로겐, 시안화 염, 페놀, 페닐페놀, tert-부틸 페놀, 디-tert-부틸 페놀, 나프톨, 메틸 프로판올, 사이클로헥산올, 메톡시 티오페놀, 아닐린, 페닐 보로닉엑시드, 사이아노페닐보로닉엑시드, 나프틸 보로닉엑시드, 및 2-메틸프로필 보로닉엑시드, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 첨가하여서 반응시키는 단계를 1회 내지 3회 수행하는 것을 추가 포함할 수 있다. In one embodiment of the present invention, the perylene compound thus prepared is reacted with a halogenated cyanide salt, phenol, phenylphenol, tert-butylphenol, di-tert-butylphenol, naphthol, methylpropanol, cyclohexanol, methoxythiophenol , Aniline, phenylboronic acid, cyanophenylboronic acid, naphthylboronic acid, and 2-methylpropylboronic acid, and all isomers thereof. One to three times.
본원의 일 구현예에 있어서, 상기 제조된 페릴렌계 화합물에 브로민, 시안화구리, 페놀, 2-페닐페놀, 4-tert-부틸페놀, 2,4-다이-tert-부틸페놀, 2-나프톨, 2-메틸-2-프로판올, 사이클로헥산올, 4-메톡시티오페놀, 아닐린, 페닐보로닉엑시드, 4-사이아노페닐보로닉엑시드, 1-나프틸보로닉엑시드, 및 2-메틸프로필보로닉엑시드, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되는 것을 첨가하여서 반응시키는 단계를 1회 내지 3회 수행하는 것을 추가 포함할 수 있다. In one embodiment of the present invention, the perylene-based compound prepared above is mixed with a compound selected from the group consisting of bromine, copper cyanide, phenol, 2-phenylphenol, 4-tert- butylphenol, 2-methylpropanol, cyclohexanol, 4-methoxythiophenol, aniline, phenylboronic acid, 4-cyanophenylboronic acid, 1-naphthylboronic acid, The addition of one selected from the group consisting of an isomer, a boronic acid, a boronic acid, a boronic acid, a boronic acid, a boronic acid, a boronic acid, a boronic acid, a boronic acid, a boronic acid, a boronic acid, a boronic acid, and all isomers thereof.
본원의 일 구현예에 있어서, 상기 각 반응 단계의 일부 또는 전부에 있어서 카보네이트 염을 첨가하는 것을 추가 포함할 수 있으나, 이에 제한되는 것은 아니다. 상기 카보네이트 염은 각 반응 단계에서 염기성 분위기를 형성하는 것으로, 예를 들면, 탄산나트륨, 탄산칼륨, 및 탄산세슘 등의 알칼리 금속 탄산염또는 동일한 목적으로 수산화나트륨 또는 수산화칼륨 등의 알칼리 금속 수산화물도 이용될 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the invention, the addition of a carbonate salt in some or all of the above reaction steps may additionally include, but is not limited to. The carbonate salt forms a basic atmosphere in each reaction step, for example an alkali metal carbonate such as sodium carbonate, potassium carbonate and cesium carbonate or an alkali metal hydroxide such as sodium hydroxide or potassium hydroxide for the same purpose But is not limited thereto.
본원의 일 구현예에 있어서, 상기 반응들은 유기 용매에 반응물을 용해시켜 반응시킨 후 상온에서 침전 및 여과하는 것을 포함하는 것일 수 있으나, 이에 제한되는 것은 아니다. In one embodiment herein, the reactions may include, but are not limited to, dissolving the reactants in an organic solvent, reacting, and then precipitating and filtering at room temperature.
본원의 일 구현예에 있어서, 상기 반응들은 상온 내지 약 200℃ 범위, 예를 들어, 상온 내지 약 200℃, 상온 내지 약 180℃, 상온 내지 약 160℃, 상온 내지 약 140℃, 상온 내지 약 120℃, 상온 내지 약 100℃, 상온 내지 약 80℃, 약 70℃ 내지 약 200℃, 약 70℃ 내지 약 180℃, 약 70℃ 내지 약 160℃, 약 70℃ 내지 약 140℃, 약 80℃ 내지 약 130℃, 약 100℃ 내지 약 130℃, 약 110℃ 내지 약 130℃, 또는 약 120℃ 내지 약 130℃의 온도에서 수행되는 것일 수 있으나, 이에 제한되는 것은 아니다. In one embodiment herein, the reactions are conducted at ambient temperature to about 200 ° C, such as ambient temperature to about 200 ° C, ambient temperature to about 180 ° C, ambient temperature to about 160 ° C, ambient temperature to about 140 ° C, From about 70 ° C to about 180 ° C, from about 70 ° C to about 160 ° C, from about 70 ° C to about 140 ° C, from about 80 ° C to about 100 ° C, from ambient temperature to about 80 ° C, But is not limited to, at a temperature of about 130 캜, about 100 캜 to about 130 캜, about 110 캜 to about 130 캜, or about 120 캜 to about 130 캜.
본원의 일 구현예에 있어서, 상기 제조 방법은, 유기 용매에 용해된 상기 화학식 2의 화합물에 상기 화합물을 치환될 수 있는 C1-20 알칸 화합물, 치환될 수 있는 C6-30 시클로알칸 화합물, 치환될 수 있는 C6-30 아릴 화합물, 치환될 수 있는 C6-30 페놀계 화합물, 치환될 수 있는 C1-20 알코올계 화합물, 치환될 수 있는 C1-20 알킬아민 화합물, 치환될 수 있는 C6-30 시클로알킬아민 화합물, 치환될 수 있는 C6-30 아릴아민 화합물, 또는 N-할로석신이미드을 첨가한 후 상온 내지 약 200℃의 온도에서 반응시킨 후 상온에서 침전 및 여과하는 것을 포함하는 것일 수 있으나, 이에 제한되는 것은 아니다.In one embodiment of the present invention, the production method comprises a step of preparing a C 1-20 alkane compound, an optionally substituted C 6-30 cycloalkane compound, A C 6-30 aryl compound which may be substituted, a C 6-30 phenol compound which may be substituted, a C 1-20 alcohol compound which may be substituted, a C 1-20 alkylamine compound which may be substituted, A C 6-30 cycloalkylamine compound, a C 6-30 arylamine compound which may be substituted, or N-halosuccinimide, followed by reaction at a temperature of room temperature to about 200 캜, followed by precipitation and filtration at room temperature But are not limited thereto.
본원의 일 구현예에 있어서, 상기 제조 방법은, 유기 용매에 용해된 상기 제조된 페릴렌계 화합물에 할로겐, 시안화 염, 페놀계 화합물, 나프톨계 화합물, 알코올계 화합물, 티올계 화합물, 아민계 화합물 및 치환될 수 있는 보로닉엑시드로 이루어진 군으로부터 선택되는 물질을 첨가하여서 상온 내지 약 200℃의 온도에서 반응시킨 후 상온에서 침전 및 여과하는 것을 포함하는 것일 수 있으나, 이에 제한되는 것은 아니다.In one embodiment of the present invention, the production method is characterized in that a halogen, a cyanide salt, a phenol compound, a naphthol compound, an alcohol compound, a thiol compound, an amine compound and / or a salt thereof is added to the prepared perylene compound dissolved in an organic solvent Substitution of a substance selected from the group consisting of voronic acids, and the like, followed by reaction at a temperature ranging from room temperature to about 200 ° C., followed by precipitation and filtration at room temperature. However, the present invention is not limited thereto.
본원의 일 구현예에 있어서, 상기 유기 용매는, 본 분야에서 사용 가능한 유기 용매라면 제한 없이 사용될 수 있으며, 예를 들어, 디메틸포름아마이드, 테트라하이드로퓨란, 메틸렌클로라이드, 아세톤, 아세토나이트릴, 다이메틸설폭사이드, 헥사메틸포스포아마이드, 피리딘, 피리미딘, 이미다졸, 퀴놀린, 이소퀴놀린, 퀴날딘, N-메틸피페리딘, N-메틸피페리돈, N-메틸피롤리돈, 디메틸포름아미드, 디메틸아세트아미드, 또는 테트라메틸우레아를포함하는 것일 수 있으나, 이에 제한되는 것은 아니다. 상기 유기 용매는 페릴렌 원료 1 g당 약 5 g 내지 약 120 g 사용할 수 있으나, 이에 제한되는 것은 아니다. In one embodiment of the present invention, the organic solvent may be any organic solvent usable in the art without limitation, and examples thereof include dimethylformamide, tetrahydrofuran, methylene chloride, acetone, acetonitrile, dimethyl But are not limited to, sulfoxide, sulfoxide, hexamethylphosphoramide, pyridine, pyrimidine, imidazole, quinoline, isoquinoline, quinaldine, N-methylpiperidine, N-methylpiperidone, Acetamide, or tetramethylurea, but the present invention is not limited thereto. The organic solvent may be used in an amount of about 5 g to about 120 g per g of the perylene raw material, but is not limited thereto.
본원의 제 3 측면은, 본원에 따른 페릴렌계 화합물을 포함하는 형광 염료를 제공한다.The third aspect of the present invention provides a fluorescent dye comprising a perylene-based compound according to the present invention.
본원의 일 구현예에 있어서, 상기 형광 염료는 녹색 형광 염료일수 있으나, 이에 제한되지 않을 수 있다. In one embodiment of the present invention, the fluorescent dye may be a green fluorescent dye, but may not be limited thereto.
본원의 일 구현예에 있어서, 상기 형광 염료는 고분자량 유기 및 무기 재료, 특히 플라스틱, 페인트, 인쇄 잉크, 무기-유기 복합체, 및 산화물 층 시스템을 착색시키기 위한 형광 염료로서 사용될 수 있으나, 이에 제한되지 않을 수 있다. 상기 형광 염료는 분산제, 유기 안료용 안료 첨가제 및 형광 염료 및 안료 첨가제를 제조하기 위한 중간체로서 사용될 수 있으며, 또는 전자기 스펙트럼의 황색 영역에서 흡수 및/또는 방출하는 잉크젯 잉크 및 수성 중합체 분산액를 제조하기 위한 분산제, 안료 첨가제 및 중간체로서 사용될 수 있으나, 이에 제한되지 않을 수 있다. 상기 형광염료는 분산제, 전자사진술의 광전도체로서, 발광성 칼라 필터 및 반투과성 칼라 필터와 재귀반사성 소자의 착색 성분 또는 색보정 성분으로서, 또는 전계발광 장치 및 화학발광 장치의 전자 방출원으로서 사용될 수 있으나, 이에 제한되지 않을 수 있다. 또한, 상기 형광 염료는 형광 변환, 형광 태양광 집열기, 생물발광 어레이, 및 태양광발전의 활성 성분으로서, 또는 레이저 염료로서 사용될 수 있으나, 이에 제한되지 않을 수 있다. In one embodiment of the invention, the fluorescent dye may be used as a fluorescent dye for coloring high molecular weight organic and inorganic materials, especially plastic, paint, printing ink, inorganic-organic complexes, and oxide layer systems, . The fluorescent dyes can be used as intermediates for preparing dispersants, pigment additives for organic pigments and fluorescent dyes and pigment additives, or they can be used as ink-jet inks absorbing and / or releasing in the yellow region of the electromagnetic spectrum and dispersants for producing aqueous polymer dispersions , Pigment additives, and intermediates. The fluorescent dye can be used as a coloring component or a color correcting component of a luminescent color filter and a semipermeable color filter and a retroreflective element or as an electron emitting source of an electroluminescent device and a chemiluminescent device as a dispersant, But may not be limited thereto. In addition, the fluorescent dye may be used as an active component of a fluorescent conversion, a fluorescent photovoltaic collector, a bioluminescent array, and a photovoltaic generation, or as a laser dye, but may not be limited thereto.
본원의 일 구현예에 있어서, 상기 형광 염료는 고분자량 유기 및 무기 재료, 특히 플라스틱, 페인트, 인쇄 잉크, 무기-유기 복합체의 반응성 착색을 위한 형광 염료로서, 또는 전자기 스펙트럼의 황색 영역에서 흡수 및/또는 방출하는 내번짐성(bleeding-resistant) 수성 중합체 분산액를 제조하기 위한 형광 염료로서 사용될 수 있으나, 이에 제한되지 않을 수 있다. 또한, 상기 형광 염료는 발광성 칼라 필터 및 반투과성 칼라 필터와 재귀반사성 소자의 착색 성분 또는 색보정 성분으로서, 또는 전계발광 장치 및 화학발광 장치의 이동 안정성(migration-stable) 전자 방출원으로서 사용될 수 있으나, 이에 제한되지 않을 수 있다In one embodiment of this application, the fluorescent dyes are used as fluorescent dyes for reactive coloration of high molecular weight organic and inorganic materials, especially plastics, paints, printing inks, inorganic-organic complexes, or as absorbing and / But not limited to, a fluorescent dye for producing a bleeding-resistant aqueous polymer dispersion. In addition, the fluorescent dye can be used as a coloring component or a color correcting component of a luminescent color filter and a semipermeable color filter and a retroreflective element, or as a migration-stable electron emitter of an electroluminescent device and a chemiluminescent device, But may not be limited thereto
본 측면에 따른 형광 염료에 대하여 본원의 제 1 측면 내지 제 2 측면에 대하여 기재된 내용이 모두 적용될 수 있으나, 이에 제한되지 않을 수 있다.The fluorescent dye according to the present aspect may be applied to all of the first and second aspects of the present invention, but the present invention is not limited thereto.
이하, 본원의 실시예를 통하여 보다 구체적으로 설명하며, 본 실시예에 의하여 본원의 범위가 제한되는 것은 아니다.Hereinafter, the present invention will be described in more detail with reference to Examples, but the scope of the present invention is not limited by these Examples.
[실시예][Example]
실시예 1Example 1
중간체 1의 합성Synthesis of Intermediate 1
1,6,7,12-테트라클로로퍼릴렌 테트라카르복실릭엑시드디안하이드라이드 (2.00 mmol)와 물 20 mL의 현탁액에 10 mL의 1 M NaOH 수용액을 첨가한 후 55℃에서 30 분동안 교반하였다. 브로민(1.0 mL)를 첨가한 후 24 시간동안 교반하고 침전물을 여과한 후 건조하여 중간체 1의 화합물(주황색 고체, 수율 : 87%)을 수득하였다.To a suspension of 1,6,7,12-tetrachlorophorylene tetracarboxylic acid dihydroidide (2.00 mmol) and 20 mL of water was added 10 mL of 1 M aqueous NaOH solution and stirred at 55 DEG C for 30 minutes . Bromine (1.0 mL) was added, and the mixture was stirred for 24 hours. The precipitate was filtered off and dried to give Intermediate Compound 1 (orange solid, yield: 87%).
- MALDI-TOF 분석 : 계산 분자량 705, 측정 분자량 704 - MALDI-TOF analysis: calculated molecular weight 705, measured molecular weight 704
- 녹는점 : 226℃- Melting point: 226 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3165, 3016, (Ar C=C) 1667, 1547, (C-Cl) 743, (C-Br) 651. FTIR analysis (cm -1 ): (Ar CH) 3165, 3016, (Ar C = C) 1667, 1547, (C-Cl) 743, (C-Br) 651.
화합물 1의 합성Synthesis of Compound 1
상기 중간체 1(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 페놀(5.00 mmol)과 포타슘카보네이트(5.00 mmol)를 첨가하였다. 130℃에서 6 시간 동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 반응물을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 1(노란색 고체, 수율 : 68%)을 수득하였다.Intermediate 1 (1.00 mmol) was dissolved in 10 mL of dimethylformamide, followed by addition of phenol (5.00 mmol) and potassium carbonate (5.00 mmol). After stirring at 130 DEG C for 6 hours, the temperature was lowered to room temperature. The reaction product was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 1 (yellow solid, yield: 68%).
- MALDI-TOF 분석 : 계산 분자량 758, 측정 분자량 756- MALDI-TOF analysis: calculated molecular weight 758, measured molecular weight 756
- 녹는점 : > 350℃- Melting point:> 350 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3060, 2957, (Ar C=C) 1569, 1484, 1431, (C-O-C) 1212, 1149, (C-Cl) 752, 713.- FTIR analysis (cm -1 ): (Ar CH) 3060, 2957, (Ar C = C) 1569, 1484, 1431, (COC) 1212, 1149, (C-Cl) 752, 713.
화합물 2의 합성Synthesis of Compound 2
상기 화합물 1(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 4-터셔리부틸페놀(5.00 mmol)과 세슘카보네이트(5.00 mmol)를 첨가하였다. 130℃에서 12 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 반응물을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 2(노란색 고체, 수율 : 38%)를 수득하였다.Compound 1 (1.00 mmol) was dissolved in 10 mL of dimethylformamide, followed by addition of 4-tert-butylphenol (5.00 mmol) and cesium carbonate (5.00 mmol). After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. The reaction product was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 2 (yellow solid, yield: 38%).
- MALDI-TOF 분석 : 계산 분자량 1213, 측정 분자량 1212- MALDI-TOF analysis: calculated molecular weight 1213, measured molecular weight 1212
- 녹는점 : 311℃- Melting point: 311 ℃
- FTIR 분석(cm-1) : (Ar C-H) 2935, 2821, (Ar C=C) 1565, 1546, 1485, (C-CH3) 1367, (C-O-C) 1255, 1216, 1167.FTIR analysis (cm -1 ): (Ar CH) 2935, 2821, (Ar C = C) 1565, 1546, 1485, (C-CH 3 ) 1367, (COC) 1255, 1216, 1167.
실시예 2Example 2
화합물 3의 합성Synthesis of Compound 3
상기 실시예 1에서와 같이 제조한 중간체 1(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 2-페닐페놀(5.00 mmol)과 포타슘카보네이트(5.00 mmol)을 첨가하였다. 130℃에서 8 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 혼합액을 넣어 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 3(노란색 고체, 수율 : 78%)를 수득하였다.Intermediate 1 (1.00 mmol) prepared as in Example 1 was dissolved in 10 mL of dimethylformamide, and then 2-phenylphenol (5.00 mmol) and potassium carbonate (5.00 mmol) were added. After stirring at 130 DEG C for 8 hours, the temperature was lowered to room temperature. The mixed solution was put into 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 3 (yellow solid, yield: 78%).
- MALDI-TOF 분석 : 계산 분자량 1063, 측정 분자량 1064- MALDI-TOF analysis: calculated molecular weight 1063, measured molecular weight 1064
- 녹는점: > 350℃- Melting point:> 350 ℃
- FTIR 분석(cm-1) (Ar C-H) 3052, 2995, (Ar C=C) 1572, 1521, 1491, (C-O-C) 1256, 1205, (C-Cl) 769, 753.- FTIR analysis (cm -1 ) (Ar CH) 3052, 2995, (Ar C = C) 1572, 1521, 1491, (COC) 1256, 1205, (C-Cl) 769, 753.
실시예 3Example 3
화합물 4의 합성Synthesis of Compound 4
상기 실시예 1에서와 같이 제조한 중간체 1(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 2,4-다이테트라부틸페놀(5.00 mmol)과 포타슘카보네이트(5.00 mmol)을 첨가하였다. 130℃에서 12 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 넣어 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 4(노란색 고체, 수율 : 63%)을 수득하였다.Intermediate 1 (1.00 mmol) prepared as in Example 1 was dissolved in 10 mL of dimethylformamide, and 2,4-ditetrabutylphenol (5.00 mmol) and potassium carbonate (5.00 mmol) were added. After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. The mixed solution was put into 20 mL of 5% aqueous ammonium chloride solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 4 (yellow solid, yield: 63%).
- MALDI-TOF 분석 : 계산 분자량 1207, 측정 분자량 1206- MALDI-TOF analysis: calculated molecular weight 1207, measured molecular weight 1206
- 녹는점: > 350℃- Melting point:> 350 ℃
- FTIR 분석(cm-1) : (Ar C-H) 2954, 2865, (Ar C=C) 1569, 1482, (C-CH3) 1394, 1359, (C-O-C) 1211, 1155, 1120, (C-Cl) 769, 693.- FTIR analysis (cm -1): (Ar CH ) 2954, 2865, (Ar C = C) 1569, 1482, (C-CH 3) 1394, 1359, (COC) 1211, 1155, 1120, (C-Cl ) 769, 693.
실시예 4Example 4
화합물 5의 합성Synthesis of Compound 5
상기 실시예 1에서와 같이 제조한 중간체 1(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 4-하이드록시-3-테트라부틸아니솔(5.00 mmol)과 포타슘카보네이트(5.00 mmol)을 첨가하였다. 130℃에서 12 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 혼합액을 넣어 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 5(노란색 고체, 수율 : 42%)을 수득하였다Intermediate 1 (1.00 mmol) prepared as in Example 1 was dissolved in 10 mL of dimethylformamide, followed by addition of 4-hydroxy-3-tetrabutyl anisole (5.00 mmol) and potassium carbonate (5.00 mmol) Respectively. After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. The mixed solution was put into 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 5 (yellow solid, yield: 42%)
- MALDI-TOF 분석 : 계산 분자량 1103, 측정 분자량 1103- MALDI-TOF analysis: calculated molecular weight 1103, measured molecular weight 1103
- 녹는점: > 350℃- Melting point:> 350 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3012, 2965, (Ar C=C) 1502, 1499, (C-CH3) 1386, 1348, (C-O-C) 1202, 1185, 1166, 1058 (C-Cl) 715.- FTIR analysis (cm -1): (Ar CH ) 3012, 2965, (Ar C = C) 1502, 1499, (C-CH 3) 1386, 1348, (COC) 1202, 1185, 1166, 1058 (C- Cl) 715.
실시예 5Example 5
화합물 6의 합성Synthesis of Compound 6
상기 실시예 1에서와 같이 제조한 중간체 1(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 헥실아민(5.00 mmol)과 트리에틸아민(5.00 mmol)을 첨가하였다. 130℃에서 12 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 혼합액을 넣어 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 6(주황색 고체, 수율 : 76%)를 수득하였다.Intermediate 1 (1.00 mmol) prepared as in Example 1 was dissolved in 10 mL of dimethylformamide, and then hexylamine (5.00 mmol) and triethylamine (5.00 mmol) were added. After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. The mixed solution was put into 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 6 (orange solid, yield: 76%).
- MALDI-TOF 분석 : 계산 분자량 786, 측정 분자량 785- MALDI-TOF analysis: calculated molecular weight 786, measured molecular weight 785
- 녹는점: > 350℃- Melting point:> 350 ℃
- FTIR 분석(cm-1) : (N-H) 3233, (C-H2) 3211, (Ar C-H) 3021, 2915, (Ar C=C) 1565, 1501, 1486 (C-CH3) 1415, 1392, 1331, (C-O-C) 185 1138 (C-Cl) 775.FTIR analysis (cm -1 ): (NH) 3233, (CH 2 ) 3211, (Ar CH) 3021, 2915, (Ar C = C) 1565, 1501, 1486 (C-CH 3 ) 1415, 1392, 1331 , (COC) 185 1138 (C-Cl) 775.
실시예 6Example 6
화합물 7의 합성Synthesis of Compound 7
상기 실시예 1의 화합물 1(1.00 mmol)를 10 mL의 디메틸포름아마이드에 녹인 후, 페놀(5.00 mmol)과 포타슘카보네이트(5.00 mmol)를 첨가하였다. 130℃에서 8 동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 반응물을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 7(노란색 고체, 수율 : 42%)를 수득하였다.Compound 1 (1.00 mmol) of Example 1 was dissolved in 10 mL of dimethylformamide, and phenol (5.00 mmol) and potassium carbonate (5.00 mmol) were added. After stirring at 130 ° C for 8 hours, the temperature was lowered to room temperature. The reaction product was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 7 (yellow solid, yield: 42%).
- MALDI-TOF 분석 : 계산 분자량 989, 측정 분자량 989- MALDI-TOF analysis: calculated molecular weight 989, measured molecular weight 989
- 녹는점 : 263℃- Melting point: 263 ℃
- FTIR 분석(cm-1) : (Ar C-H) 2975, 2844, (Ar C=C) 1577, 1465, (C-CH3) 1301, 1287, (C-O-C) 1212, 1192.- FTIR analysis (cm -1): (Ar CH ) 2975, 2844, (Ar C = C) 1577, 1465, (C-CH 3) 1301, 1287, (COC) 1212, 1192.
실시예 7Example 7
화합물 8의 합성Synthesis of Compound 8
상기 실시예 1에서의 화합물 1(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 사이클로헥산올(5.00 mmol)과 세슘카보네이트(5.00 mmol)를 첨가하였다. 130℃에서 12 동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 8(노란색 고체, 수율 : 42%)을 수득하였다.Compound 1 (1.00 mmol) in Example 1 was dissolved in 10 mL of dimethylformamide, followed by addition of cyclohexanol (5.00 mmol) and cesium carbonate (5.00 mmol). After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 8 (yellow solid, yield: 42%).
- MALDI-TOF 분석 : 계산 분자량 1013, 측정 분자량 1012- MALDI-TOF analysis: calculated molecular weight 1013, measured molecular weight 1012
- 녹는점 : 212℃- Melting point: 212 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3061, 2931, (Ar C=C) 1575, 1485, (C-O-C) 1206, 1162, (-CH2) 812, 747.- FTIR analysis (cm -1): (Ar CH ) 3061, 2931, (Ar C = C) 1575, 1485, (COC) 1206, 1162, (-CH 2) 812, 747.
실시예 8Example 8
화합물 9의 합성Synthesis of Compound 9
상기 실시예 1의 화합물 1(1.00 mmol)를 10 mL의 디메틸포름아마이드에 녹인 후, 2,4-다이터셔리부틸페놀(5.00 mmol)과 세슘카보네이트(5.00 mmol)를 첨가하였다. 130℃에서 12 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 반응물을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 9(노란색 고체, 수율 : 24%)를 수득하였다.Compound 1 (1.00 mmol) of Example 1 was dissolved in 10 mL of dimethylformamide, and then 2,4-diisopropylbutylphenol (5.00 mmol) and cesium carbonate (5.00 mmol) were added. After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. The reaction product was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 9 (yellow solid, yield: 24%).
- MALDI-TOF 분석 : 계산 분자량 1437, 측정 분자량 1436- MALDI-TOF analysis: calculated molecular weight 1437, measured molecular weight 1436
- 녹는점 : 285℃- Melting point: 285 ℃
- FTIR 분석(cm-1) : (Ar C-H) 2954, 2866, (Ar C=C) 1584, 1487, (C-CH3) 1372, 1303, (C-O-C) 1209, 1121.- FTIR analysis (cm -1): (Ar CH ) 2954, 2866, (Ar C = C) 1584, 1487, (C-CH 3) 1372, 1303, (COC) 1209, 1121.
실시예 9Example 9
화합물 10의 합성.Synthesis of compound 10.
다이이소부틸 퍼릴렌-3,9-다이카르복실레이트 (2.00 mmol)를 10 mL의 디메틸포름아마이드에 녹인 뒤 N-브로모석신이미드 (4.20 mmol)를 첨가한 후 80℃에서 6 시간동안 교반한 후 온도를 상온으로 낮췄다. 30 mL의 메탄올에 혼합액을 부은 뒤 30 분간 교반한다. 생성된 결정을 필터 후 물과 메탄올 각각 20 mL로 수세 진행 후 건조 진행 후 화합물 10(옅은 주황색 고체, 수율 : 83%)을 수득하였다.Diisobutyl perylene-3,9-dicarboxylate (2.00 mmol) was dissolved in 10 mL of dimethylformamide, N-bromosuccinimide (4.20 mmol) was added, and the mixture was stirred at 80 ° C for 6 hours The temperature was then lowered to room temperature. Pour the mixture into 30 mL of methanol and stir for 30 minutes. The resulting crystals were filtered and washed with water and 20 mL of methanol, respectively. After drying, Compound 10 (pale orange solid, yield: 83%) was obtained.
- MALDI-TOF 분석 : 계산 분자량 610, 측정 분자량 610 - MALDI-TOF analysis: calculated molecular weight 610, measured molecular weight 610
- 녹는점 : 351℃- Melting point: 351 ℃
- FTIR 분석(cm-1) : (Ar C-H) 2967, (C=O) 1717, (Ar C=C) 1581, 1502, 1465, (C-CH3) 1393, 1302, (C-O-C)1155, 1132, (C-H) 760.- FTIR analysis (cm -1 ): (Ar CH) 2967, (C = O) 1717, (ArC = C) 1581,1502,1465, (C-CH3) 1393,1302, (COC) 1155,1132, (CH) 760.
화합물 11의 합성Synthesis of Compound 11
상기 화합물 10(1.00 mmol)을 5 mL의 테트라하이드로퓨란에 녹인 뒤, 물 3 mL와 페닐보로닉엑시드(4.00 mmol), 소듐카보네이트(4.00 mmol)와 함께 교반하였다. 촉매로 Pd(PPh3)4 (0.01 mmol)를 첨가하여 70℃에서 12 시간동안 환류 반응 진행 하였다. 온도를 낮춘 뒤 분별 깔때기로 물 층을 제거한 뒤, 10 mL의 메탄올에 부어서 결정을 생성시켰다. 생성된 결정을 필터 한 뒤, 물과 메탄올 각각 20 mL씩으로 세척하여 화합물 11(밝은 노란색 고체, 수율 : 30%)를 수득하였다.The compound 10 (1.00 mmol) was dissolved in 5 mL of tetrahydrofuran, followed by stirring with 3 mL of water, phenylboronic acid (4.00 mmol) and sodium carbonate (4.00 mmol). Pd (PPh 3 ) 4 (0.01 mmol) was added as a catalyst, and the reaction was carried out at 70 ° C for 12 hours. After lowering the temperature, the water layer was removed with a separating funnel and poured into 10 mL of methanol to produce crystals. The resulting crystals were filtered and washed with 20 mL of water and methanol, respectively, to obtain Compound 11 (light yellow solid, yield: 30%).
- MALDI-TOF 분석 : 계산 분자량 604, 측정 분자량 604- MALDI-TOF analysis: calculated molecular weight 604, measured molecular weight 604
- 녹는점 : 395℃- Melting point: 395 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3050, 2959, (C=O) 1708, (Ar C=C) 1584, 1515, (C-CH3) 1373, (C-O-C)1149, 1123, (C-H) 759, 700. - FTIR analysis (cm -1 ): (Ar CH) 3050, 2959, (C = O) 1708, (Ar C = C) 1584, 1515, (C- ) 759, 700.
화합물 12의 합성Synthesis of Compound 12
상기 화합물 11(1.00 mmol)을 10 mL의 메틸렌클로라이드에 녹인 후, 브로민 (2.5 mmol)을 첨가하였다. 상온에서 6 시간동안 교반한 후 30 ml의 메탄올에 혼합액을 부어 1 시간동안 교반하여 결정을 생성하였다. 생성된 결정을 필터 한 뒤, 50 mL의 메탄올로 세척하여 화합물 12(주황색 고체, 수율 : 70%)를 수득하였다.Compound 11 (1.00 mmol) was dissolved in 10 mL of methylene chloride, followed by addition of bromine (2.5 mmol). After stirring at room temperature for 6 hours, the mixture was poured into 30 ml of methanol and stirred for 1 hour to produce crystals. The resulting crystals were filtered and washed with 50 mL of methanol to give compound 12 (orange solid, yield: 70%).
- MALDI-TOF 분석 : 계산 분자량 762, 측정 분자량 761- MALDI-TOF analysis: calculated molecular weight 762, measured molecular weight 761
- 녹는점 : 345℃- Melting point: 345 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3052, 2955, (C=O) 1718, (Ar C=C) 1543, 1487, (C-CH3) 1368, (C-O-C)1194, 1139, (C-H) 760, 700. - FTIR analysis (cm -1 ): (Ar CH) 3052, 2955, (C = O) 1718, (Ar C = C) 1543, 1487, (C-CH 3) 1368, (COC) 1194, ) 760, 700.
화합물 13의 합성Synthesis of Compound 13
상기 화합물 12(1.00 mmol)을 10 mL의 메틸렌클로라이드에 녹인 후, 시안화 구리 (4 mmol)을 첨가하였다. 150℃에서 5 시간동안 교반한 후 온도를 낮추고, 30 mL의 물에 부어서 결정을 생성하였다. 생성된 결정을 필터 한 뒤, 50 mL의 메탄올로 세척하여 화합물 13(붉은색 고체, 수율 : 65%)를 수득하였다.Compound 12 (1.00 mmol) was dissolved in 10 mL of methylene chloride, followed by addition of copper cyanide (4 mmol). After stirring at 150 ° C for 5 hours, the temperature was lowered and poured into 30 mL of water to produce crystals. The resulting crystals were filtered and washed with 50 mL of methanol to obtain Compound 13 (red solid, yield: 65%).
- MALDI-TOF 분석 : 계산 분자량 654, 측정 분자량 654- MALDI-TOF analysis: calculated molecular weight 654, measured molecular weight 654
- 녹는점 : 420℃- Melting point: 420 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3056, 2957, (C≡N) 2214, (C=O) 1720, (Ar C=C) 1589, 1489, 1468, (C-CH3) 1370, (C-O-C)1192, 1151, (C-H) 763, 703. - FTIR analysis (cm -1 ): (Ar CH) 3056, 2957, (C = N) 2214, (C = O) 1720, (Ar C = C) 1589, 1489, 1468, (C- (COC) 1192, 1151, (CH) 763, 703.
실시예 10Example 10
화합물 14의 합성Synthesis of Compound 14
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL 메틸렌클로라이드에 녹인 후 브로민(3 mmol)을 첨가하여 상온에 교반하였다. 6 시간 뒤 50 mL의 메탄올에 부어서 결정을 생성시킨 뒤, 필터 및 50 mL의 물로 3회 세척하여 화합물 14(밝은 노란색 고체, 수율 : 76%)를 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of methylene chloride, followed by addition of bromine (3 mmol), and the mixture was stirred at room temperature. After 6 hours, it was poured into 50 mL of methanol to form crystals, which were then washed three times with a filter and 50 mL of water to obtain Compound 14 (light yellow solid, yield: 76%).
- MALDI-TOF 분석 : 계산 분자량 768, 측정 분자량 768- MALDI-TOF analysis: calculated molecular weight 768, measured molecular weight 768
- 녹는점: 321℃- Melting point: 321 ℃
- FTIR 분석(cm-1) : (Ar C-H) 2966, (C=O) 1717, (Ar C=C) 1579, 1513, 1452, (C-CH3) 1381, 1331, (C-O-C)1157, 1136, (C-H) 758.- FTIR analysis (cm -1 ): (Ar CH) 2966, (C = O) 1717, (Ar C = C) 1579, 1513, 1452, (C- (CH) 758.
화합물 15의 합성Synthesis of Compound (15)
상기 화합물 14 (1.00 mmol)를 5 mL의 테트라하이드로퓨란에 녹인 뒤, 물 3 mL와 페닐보로닉엑시드(6.00 mmol), 소듐카보네이트(6.00 mmol)와 함께 교반하였다. 촉매로 Pd(PPh3)4 (0.01 mmol)를 첨가하여 70℃에서 12 시간동안 환류 반응 진행하였다. 온도를 낮춘 뒤 분별 깔때기로 물 층을 제거한 뒤, 10 mL의 메탄올에 부어서 결정을 생성시켰다. 생성된 결정을 필터 한 뒤, 물과 메탄올 각각 20 mL씩으로 세척하여 화합물 15(밝은 주황색 고체, 수율 : 22%)를 수득하였다.The compound 14 (1.00 mmol) was dissolved in 5 mL of tetrahydrofuran, followed by stirring with 3 mL of water, phenylboronic acid (6.00 mmol) and sodium carbonate (6.00 mmol). Pd (PPh 3 ) 4 (0.01 mmol) was added as a catalyst, and the reaction was carried out at 70 ° C for 12 hours. After lowering the temperature, the water layer was removed with a separating funnel and poured into 10 mL of methanol to produce crystals. The resulting crystals were filtered and washed with 20 mL of water and methanol, respectively, to obtain Compound 15 (light orange solid, yield: 22%).
- MALDI-TOF 분석 : 계산 분자량 756, 측정 분자량 756- MALDI-TOF analysis: calculated molecular weight 756, measured molecular weight 756
- 녹는점 : 363℃- Melting point: 363 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3055, 2958, (C=O) 1717, (Ar C=C) 1598, (C-CH3) 1368, 1256, (C-O-C) 1190, 1145, (C-H) 756, 698. - FTIR analysis (cm -1 ): (Ar CH) 3055, 2958, (C = O) 1717, (ArC.dbd.C) 1598, (C-CH3) 1368, 1256, (COC) 1190, ) 756, 698.
실시예 11Example 11
화합물 16의 합성Synthesis of Compound 16
상기 실시예 10에서의 화합물 14(1.00 mmol)를 10 mL 디메틸포름아마이드에 녹인 후, 페놀 (6.00 mmol)과 포타슘카보네이트 (6.00 mmol)를 첨가하였다. 130℃에서 12 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 16 (노란색 고체, 수율 : 63%)을 수득하였다.Compound 14 (1.00 mmol) in Example 10 was dissolved in 10 mL of dimethylformamide, and phenol (6.00 mmol) and potassium carbonate (6.00 mmol) were added. After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 16 (yellow solid, yield: 63%).
- MALDI-TOF 분석 : 계산 분자량 820, 측정 분자량 820- MALDI-TOF analysis: calculated molecular weight 820, measured molecular weight 820
- 녹는점: 353℃- Melting point: 353 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3050, 2960, (C=O) 1717, (Ar C=C) 1583, 1502, (C-CH3) 1368, 1301, (C-O-C)1155, 1102, (C-H) 760. - FTIR analysis (cm -1 ): (Ar CH) 3050, 2960, (C = O) 1717, (ArC = C) 1583, 1502, (C- (CH) 760.
실시예 12Example 12
화합물 17의 합성Synthesis of Compound 17
상기 실시예 10에서의 화합물 14(1.00 mmol)를 10 mL의 디메틸포름아마이드에 녹인 후, 시안화 구리(6 mmol)을 첨가하였다. 150℃에서 8 시간동안 교반한 후 온도를 낮추고, 30 mL의 물에 부어서 결정을 생성하였다. 생성된 결정을 필터한 뒤, 50 mL의 메탄올로 세척하여 화합물 17(붉은색 고체, 수율 : 72%)를 수득하였다.Compound 14 (1.00 mmol) in Example 10 was dissolved in 10 mL of dimethylformamide, followed by addition of copper cyanide (6 mmol). After stirring at 150 DEG C for 8 hours, the temperature was lowered and poured into 30 mL of water to produce crystals. The resulting crystals were filtered and washed with 50 mL of methanol to obtain Compound 17 (red solid, yield: 72%).
- MALDI-TOF 분석 : 계산 분자량 554, 측정 분자량 554- MALDI-TOF analysis: calculated molecular weight 554, measured molecular weight 554
- 녹는점: 332℃- Melting point: 332 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3050, 2963, (C≡N) 2211 (C=O) 1715, (Ar C=C) 1611, 1593, (C-CH3) 1336, 1289, (C-O-C) 1152, 1129, (C-H) 760, 681. FTIR analysis (cm -1 ): (Ar CH) 3050, 2963, (C = N) 2211 (C = O) 1715, (Ar C = C) 1611, 1593, (C- COC) 1152, 1129, (CH) 760,681.
실시예 13Example 13
화합물 18의 합성Synthesis of compound 18
상기 실시예 9에서의 화합물 10(1.00 mmol)을 5 mL의 테트라하이드로퓨란에 녹인 뒤, 물 3 mL와 2-메틸프로필보로닉엑시드(4.00 mmol), 소듐카보네이트(4.00 mmol)와 함께 교반하였다. 촉매로 Pd(PPh3)4 (0.01 mmol)를 첨가하여 70℃에서 24 시간동안 환류 반응 진행하였다. 온도를 낮춘 뒤 분별 깔때기로 물 층을 제거한 뒤, 10 mL의 메탄올에 부어서 결정을 생성시켰다. 생성된 결정을 필터 한 뒤, 물과 메탄올 각각 20 mL씩으로 세척하여 화합물 18(밝은 노란색 고체, 수율 : 20%)를 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 5 mL of tetrahydrofuran, and then stirred with 3 mL of water, 2-methylpropylboronic acid (4.00 mmol) and sodium carbonate (4.00 mmol) . Pd (PPh 3 ) 4 (0.01 mmol) was added as a catalyst, and the reaction was carried out at 70 ° C for 24 hours. After lowering the temperature, the water layer was removed with a separating funnel and poured into 10 mL of methanol to produce crystals. The resulting crystals were filtered and washed with 20 mL of water and methanol, respectively, to obtain Compound 18 (light yellow solid, yield: 20%).
- MALDI-TOF 분석 : 계산 분자량 564, 측정 분자량 564- MALDI-TOF analysis: calculated molecular weight 564, measured molecular weight 564
- 녹는점 : 395℃ - Melting point: 395 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3050, 2972, (C=O) 1717, (Ar C=C) 1603, 1578, (C-CH3) 1302, 1288, (C-O-C) 1189, 1129, (C-H) 760, 700. - FTIR analysis (cm -1 ): (Ar CH) 3050, 2972, (C = O) 1717, (Ar C = C) 1603, 1578, (C- (CH) 760, 700.
화합물 19의 합성Synthesis of Compound 19
상기 화합물 18 (1.00 mmol)을 10 mL의 메틸렌클로라이드에 녹인 후, 브로민 (3 mmol)을 첨가하였다. 상온에서 6 시간동안 교반한 후 30 mL의 메탄올에 혼합액을 부어 1시간 동안 교반하여 결정을 생성하였다. 생성된 결정을 필터 한 뒤, 50 mL의 메탄올로 세척하여 화합물 19(짙은 노란색 고체, 수율 : 59%)를 수득하였다.Compound 18 (1.00 mmol) was dissolved in 10 mL of methylene chloride, and bromine (3 mmol) was added. After stirring at room temperature for 6 hours, the mixture was poured into 30 mL of methanol and stirred for 1 hour to produce crystals. The resulting crystals were filtered and washed with 50 mL of methanol to obtain Compound 19 (dark yellow solid, yield: 59%).
- MALDI-TOF 분석 : 계산 분자량 722, 측정 분자량 721- MALDI-TOF analysis: calculated molecular weight 722, measured molecular weight 721
- 녹는점 : 345℃- Melting point: 345 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3057, 2959, (C=O) 1714, (Ar C=C) 1640, 1598, (C-CH3) 1369, 1255, (C-O-C) 1190, 1145, (C-H) 755, 698. - FTIR analysis (cm -1 ): (Ar CH) 3057, 2959, (C = O) 1714, (Ar C = C) 1640, 1598, (C-CH 3) 1369, 1255, (COC) 1190, (CH) 755, 698.
화합물 20의 합성Synthesis of Compound 20
상기 화합물 19(1.00 mmol)을 5 mL의 테트라하이드로퓨란에 녹인 뒤, 물 3 mL와 페닐보로닉엑시드 (4.00 mmol), 소듐카보네이트(4.00 mmol)와 함께 교반하였다. 촉매로 Pd(PPh3)4 (0.01 mmol)를 첨가하여 70℃에서 12 시간동안 환류 반응 진행하였다. 온도를 낮춘 뒤 분별 깔때기로 물 층을 제거한 뒤, 10 mL의 메탄올에 부어서 결정을 생성시켰다. 생성된 결정을 필터 한 뒤, 물과 메탄올 각각 20 mL씩으로 세척하여 화합물 20(주황색 고체, 수율 : 23%)를 수득하였다.The compound 19 (1.00 mmol) was dissolved in 5 mL of tetrahydrofuran, followed by stirring with 3 mL of water, phenylboronic acid (4.00 mmol) and sodium carbonate (4.00 mmol). Pd (PPh 3 ) 4 (0.01 mmol) was added as a catalyst, and the reaction was carried out at 70 ° C for 12 hours. After lowering the temperature, the water layer was removed with a separating funnel and poured into 10 mL of methanol to produce crystals. The resulting crystals were filtered and washed with 20 mL of water and methanol, respectively, to obtain Compound 20 (orange solid, yield: 23%).
- MALDI-TOF 분석 : 계산 분자량 716, 측정 분자량 716- MALDI-TOF analysis: calculated molecular weight 716, measured molecular weight 716
- 녹는점 : 377℃- Melting point: 377 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3060, 2979, (C=O) 1717, (Ar C=C) 1652, 1597, (C-CH3) 1355, 1305, (C-O-C) 1178, 1135, (C-H) 761, 698. - FTIR analysis (cm -1 ): (Ar CH) 3060, 2979, (C = O) 1717, (Ar C = C) 1652, 1597, (C- (CH) 761, 698.
실시예 14 Example 14
화합물 21의 합성Synthesis of Compound 21
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 페놀 (3.00 mmol)과 포타슘카보네이트 (3.00mmol)과 함께 130℃에서 6시간 동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 상기 반응물을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 21(노란색 고체, 수율 : 68%)을 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of dimethylformamide, stirred with phenol (3.00 mmol) and potassium carbonate (3.00 mmol) at 130 ° C for 6 hours, Lowered. The reaction product was added to 20 mL of a 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain a compound 21 (yellow solid, yield: 68%).
- MALDI-TOF 분석 : 계산 분자량 636, 측정 분자량 638- MALDI-TOF analysis: calculated molecular weight 636, measured molecular weight 638
- 녹는점 : 373℃- Melting point: 373 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3049, 2959, (C=O) 1717, (Ar C=C) 1583, 1502, 1489, (C-CH3) 1367, 1302, (C-O-C)1155, 1132, (C-H) 794, 760. - FTIR analysis (cm -1 ): (Ar CH) 3049, 2959, (C = O) 1717, (Ar C = C) 1583, 1502, 1489, (C- 1132, (CH) 794, 760.
실시예 15 Example 15
화합물 22의 합성Synthesis of Compound 22
상기 실시예 9에서의 화합물 10 (1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 2-페닐페놀 (5.00 mmol)과 세슘카보네이트(5.00 mmol)를 첨가하였다. 130℃에서 8시간 동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 22 (노란색 고체, 수율 : 52%)을 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of dimethylformamide, followed by addition of 2-phenylphenol (5.00 mmol) and cesium carbonate (5.00 mmol). After stirring at 130 DEG C for 8 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 22 (yellow solid, yield: 52%).
- MALDI-TOF 분석 : 계산 분자량 788, 측정 분자량 790- MALDI-TOF analysis: calculated molecular weight 788, measured molecular weight 790
- 녹는점 : 369℃- Melting point: 369 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3054, 2958, (C=O) 1717, (Ar C=C) 1581, 1502, 1467, (C-CH3) 1366, 1302, (C-O-C)1155, 1132, (C-H) 759, 698. - FTIR analysis (cm -1 ): (Ar CH) 3054, 2958, (C = O) 1717, (Ar C = C) 1581, 1502, 1467, (C- 1132, (CH) 759, 698.
실시예 16Example 16
화합물 23의 합성Synthesis of Compound 23
상기 실시예 9에서의 화합물 10 (1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 아닐린 (3.00 mmol)과 세슘카보네이트 (3.00 mmol)을 첨가하였다. 130℃에서 12 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 23(노란색 고체, 수율 : 48%)을 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of dimethylformamide, and aniline (3.00 mmol) and cesium carbonate (3.00 mmol) were added. After stirring at 130 DEG C for 12 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of a 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain a compound 23 (yellow solid, yield: 48%).
- MALDI-TOF 분석 : 계산 분자량 636, 측정 분자량 636- MALDI-TOF analysis: calculated molecular weight 636, measured molecular weight 636
- 녹는점: 359℃- Melting point: 359 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3050, 2959, 2873 (C=O) 1717, (Ar C=C) 1581, 1502, 1466, (C-CH3) 1365,1264, (C-O-C)1156, 1132, (C-H) 760. FTIR analysis (cm -1 ): (Ar CH) 3050, 2959, 2873 (C = O) 1717, (Ar C = C) 1581, 1502, 1466, (C- , 1132, (CH) 760.
실시예 17 Example 17
화합물 24의 합성Synthesis of Compound 24
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 2-나프톨 (3.00 mmol)과 세슘카보네이트 (3.00 mmol)를 첨가하였다. 130℃에서 10 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 24(짙은 노란색 고체, 수율 : 62%)을 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of dimethylformamide, and then 2-naphthol (3.00 mmol) and cesium carbonate (3.00 mmol) were added. After stirring at 130 DEG C for 10 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 24 (a dark yellow solid, yield: 62%).
- MALDI-TOF 분석 : 계산 분자량 736, 측정 분자량 737- MALDI-TOF analysis: calculated molecular weight 736, measured molecular weight 737
- 녹는점 : 351℃- Melting point: 351 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3050, 2956, (C=O) 1707, (Ar C=C) 1584, 1515, 1463, (C-CH3) 1373, (C-O-C) 1166, 1152, (C-H) 758, 700. - FTIR analysis (cm -1 ): (Ar CH) 3050, 2956, (C = O) 1707, (Ar C = C) 1584, 1515, 1463, (C- (CH) 758, 700.
실시예 18Example 18
화합물 25의 합성Synthesis of Compound 25
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 4-터셔리부틸페놀 (3.00 mmol)과 포타슘카보네이트 (3.00 mmol)를 첨가하였다. 130℃에서 6 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 25(노란색 고체, 수율 : 63%)을 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of dimethylformamide, and then 4-tert-butylphenol (3.00 mmol) and potassium carbonate (3.00 mmol) were added. After stirring at 130 DEG C for 6 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 25 (yellow solid, yield: 63%).
- MALDI-TOF 분석 : 계산 분자량 748, 측정 분자량 747- MALDI-TOF analysis: calculated molecular weight 748, measured molecular weight 747
- 녹는점 : 373℃- Melting point: 373 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3054, 2958, (C=O) 1716, (Ar C=C) 1584, 1537, 1495, (C-CH3) 1370, 1353, (C-O-C) 1158, (C-H) 748, 692. - FTIR analysis (cm -1 ): (Ar CH) 3054, 2958, (C = O) 1716, (Ar C = C) 1584, 1537, 1495, (C- (CH) 748, 692.
실시예 19Example 19
화합물 26의 합성Synthesis of Compound 26
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL 테트라하이드로퓨란에 녹인 뒤 물 3 mL와 1-나프틸보로닉엑시드(4.00 mmol), 소듐카보네이트(4.00 mmol)와 함께 교반하였다. 촉매로 Pd(PPh3)4 (0.01 mmol)를 첨가하여 70℃에서 8 시간동안 환류 반응 진행하였다. 온도를 낮추고 분별 깔때기로 물 층을 제거 한 뒤, 10 mL의 메탄올에 부어서 결정을 생성시켰다. 생성된 결정을 필터 한 뒤, 물과 메탄올 각각 20 mL씩으로 세척하여 화합물 26 (밝은 노란색 고체, 수율 : 24%)를 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of tetrahydrofuran, followed by stirring with 3 mL of water, 1-naphthylboronic acid (4.00 mmol) and sodium carbonate (4.00 mmol). Pd (PPh 3 ) 4 (0.01 mmol) was added as a catalyst, and the reaction was carried out at 70 ° C for 8 hours. The temperature was lowered, the water layer was removed with a separating funnel, and the solution was poured into 10 mL of methanol to form crystals. The resulting crystals were filtered and washed with 20 mL of water and methanol, respectively, to obtain 26 (light yellow solid, yield: 24%).
- MALDI-TOF 분석 : 계산 분자량 704, 측정 분자량 704- MALDI-TOF analysis: calculated molecular weight 704, measured molecular weight 704
- 녹는점: 382℃- melting point: 382 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3052, (C=O) 1715, (Ar C=C) 1593, 1522, 1502, (C-CH3) 1381, 1372, (C-O-C) 1157, 1102, (C-H) 760, 699. - FTIR analysis (cm -1 ): (Ar CH) 3052, (C = O) 1715, (Ar C = C) 1593, 1522, 1502, (C- (CH) 760, 699.
실시예 20Example 20
화합물 27의 합성Synthesis of Compound 27
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 2-메틸-2-프로판올 (5.00 mmol)과 세슘카보네이트 (5.00 mmol)를 첨가하였다. 130℃에서 24 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 27 (노란색 고체, 수율 : 38%)을 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of dimethylformamide, followed by addition of 2-methyl-2-propanol (5.00 mmol) and cesium carbonate (5.00 mmol). After stirring at 130 DEG C for 24 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain Compound 27 (yellow solid, yield: 38%).
- MALDI-TOF 분석 : 계산 분자량 596, 측정 분자량 596- MALDI-TOF analysis: calculated molecular weight 596, measured molecular weight 596
- 녹는점 : 348℃- Melting point: 348 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3050, 2959, (C=O) 1717, (Ar C=C) 1581, 1502, (C-CH3) 1365, 1302, (C-O-C) 1155, 1132, (C-H) 817, 760, 696.- FTIR analysis (cm -1 ): (Ar CH) 3050, 2959, (C = O) 1717, (ArC = C) 1581, 1502, (C-CH3) 1365,1302, (COC) 1155, 1132, (CH) 817, 760, 696.
실시예 21Example 21
화합물 28의 합성Synthesis of Compound 28
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL 테트라하이드로퓨란에 녹인 뒤 물 3 mL와 4-사이아노페닐보로닉엑시드(4.00 mmol), 소듐카보네이트(4.00 mmol)와 함께 교반하였다. 촉매로 Pd(PPh3)4 (0.01 mmol)를 첨가하여 70℃에서 12 시간 동안 환류 반응 진행하였다. 온도를 낮춘 뒤 분별 깔때기로 물 층을 제거한 뒤, 10 mL의 메탄올에 부어서 결정을 생성시킨다. 생성된 결정을 필터 한 뒤, 물과 메탄올 각각 20 mL씩으로 세척하여 화합물 28 (밝은 노란색 고체, 수율 : 25%)를 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of tetrahydrofuran, followed by stirring with 3 mL of water, 4-cyanophenylboronic acid (4.00 mmol) and sodium carbonate (4.00 mmol). Pd (PPh 3 ) 4 (0.01 mmol) was added as a catalyst, and the reaction was carried out at 70 ° C for 12 hours. After lowering the temperature, remove the water layer with a separating funnel and pour into 10 mL of methanol to form crystals. The resulting crystals were filtered and washed with 20 mL of water and methanol, respectively, to obtain Compound 28 (light yellow solid, yield: 25%).
- MALDI-TOF 분석 : 계산 분자량 654, 측정 분자량 654- MALDI-TOF analysis: calculated molecular weight 654, measured molecular weight 654
- 녹는점 : 383℃- Melting point: 383 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3042, 2961, 2880, (C≡N) 2221 (C=O) 1707, (Ar C=C) 1602, 1589, (C-CH3) 1306, 1279, (C-O-C) 1181, 1152, 1129, (C-H) 767, 671. FTIR analysis (cm -1 ): (Ar CH) 3042, 2961, 2880, (C = N) 2221 (C = O) 1707, (Ar C = C) 1602, 1589, (C- , (COC) 1181, 1152, 1129, (CH) 767, 671.
실시예 22Example 22
화합물 29의 합성Synthesis of Compound 29
상기 실시예 9에서의 화합물 10(1.00 mmol)을 10 mL의 디메틸포름아마이드에 녹인 후, 4-메톡시티오페놀 (4.00 mmol)과 세슘카보네이트 (4.00 mmol)를 첨가하였다. 130℃에서 24 시간동안 교반한 후 온도를 상온으로 낮췄다. 20 mL의 5% 암모늄클로라이드 수용액에 혼합액을 첨가하여 생성된 침전물을 여과한 후 30 mL의 물로 세척하여 화합물 29 (주황색 고체, 수율 : 63%)을 수득하였다.Compound 10 (1.00 mmol) in Example 9 was dissolved in 10 mL of dimethylformamide, followed by addition of 4-methoxythiophenol (4.00 mmol) and cesium carbonate (4.00 mmol). After stirring at 130 DEG C for 24 hours, the temperature was lowered to room temperature. A mixed solution was added to 20 mL of 5% ammonium chloride aqueous solution, and the resulting precipitate was filtered and washed with 30 mL of water to obtain 29 (orange solid, yield: 63%).
- MALDI-TOF 분석 : 계산 분자량 728, 측정 분자량 728- MALDI-TOF analysis: calculated molecular weight 728, measured molecular weight 728
- 녹는점: 328℃- Melting point: 328 ℃
- FTIR 분석(cm-1) : (Ar C-H) 3065, 2983, (C=O) 1717, (Ar C=C) 1601, 1581, (C-CH3) 1316, 1298, (C-O-C) 1129, (C-H) 758. - FTIR analysis (cm -1 ): (Ar CH) 3065, 2983, (C = O) 1717, (Ar C = C) 1601, 1581, (C-CH 3) 1316, 758.
실험예Experimental Example 1 One
상기 실시예에서와 같이 합성한 페릴렌계 화합물 1 내지 29에 대한 흡수 및 형광의 광학특성을 확인하기 위해 각 페릴렌계 화합물에 프로필렌글리콜모노메틸에테르아세테이트를 넣고(1000 ppm) 10 분간 교반시켰다. 그 후, 프로필렌글리콜모노메틸에테르아세테이트를 추가로 넣고 농도를 20 ppm으로 희석시킨 후, UV/Vis/NIR 분광 광도계(UV3600-shimadzu) 및 분광형광 광도계(RF-5301PC-shimadzu)를 사용하여 흡수 및 형광을 측정하고 그 결과를 하기 표 1에 나타냈다. 비교예로서 시판되는 Lumogen F Yellow 083(BASF)를 사용하였다. 표 1은 상기 실시예들에서와 같이 제조한 염료 화합물들 및 비교예로서 Lumogen 083에 대한 최대 흡수 파장(Λmax), 최대 방출 파장(Λemission) 및 몰 흡광 계수(ε)를 나타낸 것이다. 하기 표 1에서, Lumogen 083은 용해가 되지 않아 몰 흡광 계수 값을 나타낼 수 없었다. 하기 표 1에서 볼 수 있는 바와 같이, 비교예인 Lumogen 083은 용해도가 낮아 용매에 용해가 되지 않는 반면, 본원의 실시예에 따른 염료 화합물들은 우수한 용해도를 보임을 확인할 수 있었다. 상기 실험으로, 본 실시예에 따른 화합물들이 비교예의 화합물과 유사한 분광 특성을 나타내면서도 비교예에 비해 매우 개선된 용해도를 가짐을 확인할 수 있었다.Propylene glycol monomethyl ether acetate was added to each of the perylene-based compounds to confirm absorption and fluorescence of the synthesized perylene-based compounds 1 to 29, and the mixture was stirred for 10 minutes. Thereafter, propylene glycol monomethyl ether acetate was further added, and the concentration was diluted to 20 ppm. Then, a UV / Vis / NIR spectrophotometer (UV3600-shimadzu) and a spectrofluorophotometer (RF-5301PC-shimadzu) Fluorescence was measured and the results are shown in Table 1 below. As a comparative example, commercially available Lumogen F Yellow 083 (BASF) was used. Table 1 shows the maximum absorption wavelength (Λmax), the maximum emission wavelength (Λ emission) and the molar extinction coefficient (ε) for the dye compounds prepared as in the above Examples and Comparative Example as Lumogen 083. In Table 1 below, Lumogen 083 was not dissolved and could not exhibit molar extinction coefficient values. As can be seen from the following Table 1, Lumogen 083, which is a comparative example, is low in solubility and does not dissolve in a solvent. On the other hand, it is confirmed that the dye compounds according to the present examples show excellent solubility. In the above experiment, it was confirmed that the compounds according to the present invention exhibit spectral characteristics similar to those of the comparative examples and have a much improved solubility as compared with the comparative examples.
[표 1] [Table 1]
도 1은 본원 실시예에 따른 염료 화합물 중 유기 용제에 대한 용해도가 높으면서 몰 계수가 높은 화합물인 화합물 2, 7 및 9의 최대 흡수 파장(실선)과 최대 방출 파장(점선)을 나타낸 것이다.FIG. 1 shows the maximum absorption wavelength (solid line) and the maximum emission wavelength (dotted line) of the compounds 2, 7 and 9, which are compounds having high molarities and high solubility in organic solvents among the dye compounds according to the present example.
실험예Experimental Example 2 2
상기 실시예와 같이 제조된 페릴렌계 화합물 1 내지 12에 대해 프로필렌글리콜모노메틸에테르아세테이트(PGMEA) 및 메틸에틸케톤(methyl ethyl ketone, MEK)에서의 용해도를 평가하였다.The solubility of propylene glycol monomethyl ether acetate (PGMEA) and methyl ethyl ketone (MEK) was evaluated for the perylene-based compounds 1 to 12 prepared as in the above examples.
25 mL 바이알 병에 화합물과 용제를 약 3% 내지 약 5%의 농도로 혼합하고 바이알 병을 완전히 밀봉하여 15 분간 흔들어 준 뒤 30 분 후에 액상의 침전물 유무를 육안으로 관찰하였다. 침전물이 확인될 경우 용해성이 불량하다고 판단하였다. 용해도 판정 기준으로서, 3% 이상 완전 용해되는 경우에는 ◎, 3% 이하 완전히 용해되는 경우에는 O, 일부 용해되는 경우 및 용해되지 않는 경우에는 X로 표시하였다(표 2). 하기 표 2에서 확인할 수 있는 바와 같이, 본원의 페릴렌계 화합물의 용해성이 기존의 형광 염료에 비해 우수한 것을 확인할 수 있었다.The compound and solvent were mixed at a concentration of about 3% to about 5% in a 25 mL vial bottle, the vial bottle was completely sealed, and shaken for 15 minutes. After 30 minutes, the presence or absence of the liquid precipitate was visually observed. When the precipitate was confirmed, it was judged that the solubility was poor. As a criterion of solubility,?,?,?, And? Were shown as?,?, And?, Respectively, when the solubility was 3% or less and 3% or less, respectively. As can be seen from the following Table 2, it was confirmed that the solubility of the perylene compound of the present invention is superior to that of the conventional fluorescent dye.
[표 2] [Table 2]
전술한 본원의 설명은 예시를 위한 것이며, 본원이 속하는 기술분야의 통상의 지식을 가진 자는 본원의 기술적 사상이나 필수적인 특징을 변경하지 않고서 다른 구체적인 형태로 쉽게 변형이 가능하다는 것을 이해할 수 있을 것이다. 그러므로 이상에서 기술한 실시예들은 모든 면에서 예시적인 것이며 한정적이 아닌 것으로 이해해야만 한다. 예를 들어, 단일형으로 설명되어 있는 각 구성 요소는 분산되어 실시될 수도 있으며, 마찬가지로 분산된 것으로 설명되어 있는 구성 요소들도 결합된 형태로 실시될 수 있다.It will be understood by those of ordinary skill in the art that the foregoing description of the embodiments is for illustrative purposes and that those skilled in the art can easily modify the invention without departing from the spirit or essential characteristics thereof. It is therefore to be understood that the above-described embodiments are illustrative in all aspects and not restrictive. For example, each component described as a single entity may be distributed and implemented, and components described as being distributed may also be implemented in a combined form.
본원의 범위는 상기 상세한 설명보다는 후술하는 특허청구범위에 의하여 나타내어지며, 특허청구범위의 의미 및 범위, 그리고 그 균등 개념으로부터 도출되는 모든 변경 또는 변형된 형태가 본원의 범위에 포함되는 것으로 해석되어야 한다. The scope of the present invention is defined by the appended claims rather than the detailed description, and all changes or modifications derived from the meaning and scope of the claims and their equivalents should be interpreted as being included in the scope of the present invention .
Claims (12)
, , , , , , , , , , , , , , , , , , , , , , , , , , , 및 A perylene compound comprising any one of the following compounds:
, , , , , , , , , , , , , , , , , , , , , , , , , , , And
을 포함하는, 제 1 항에 따른 페릴렌계 화합물의 제조 방법:
[화학식 2]
상기 화학식 2에서,
R5 내지 R8은, 각각 독립적으로 수소, 할로겐 또는 선형 또는 분지형의 C2-10 알킬카르복실기임.The compound represented by the following formula 2 is dissolved in an organic solvent and then reacted with an organic solvent such as phenol, phenyl phenol, di-tert-butyl phenol, hydroxy tert-butyl anisole, N-halosuccinimide, ≪ RTI ID = 0.0 >
A process for producing the perylene compound according to claim 1, comprising:
(2)
In Formula 2,
R 5 to R 8 are each independently hydrogen, halogen or a linear or branched C 2-10 alkylcarboxyl group.
[화학식 2]
상기 화학식 2에서,
R5 내지 R8은, 각각 독립적으로 수소, 할로겐 또는 선형 또는 분지형의 C2-10 알킬카르복실기임;
상기 제조되는 페릴렌계 화합물을 유기 용매에 녹인 후, 할로겐, 시안화 염, 페놀, 페닐페놀, tert-부틸 페놀, 디-tert-부틸 페놀, 나프톨, 메틸 프로판올, 사이클로헥산올, 메톡시 티오페놀, 아닐린, 페닐 보로닉엑시드, 사이아노페닐보로닉엑시드, 나프틸 보로닉엑시드, 및 2-메틸프로필 보로닉엑시드, 및 이들의 모든 이성질체들로 이루어진 군으로부터 선택되 는 물질을 첨가하여서 반응시키는 단계를 1회 내지 3회 수행하는 것
을 포함하는, 제 1 항에 따른 페릴렌계 화합물의 제조 방법.The compound represented by the following formula 2 is dissolved in an organic solvent and then reacted with an organic solvent such as phenol, phenyl phenol, di-tert-butyl phenol, hydroxy tert-butyl anisole, N-halosuccinimide, With a compound selected from the group consisting of:
(2)
In Formula 2,
R 5 to R 8 are each independently hydrogen, halogen or a linear or branched C 2-10 alkylcarboxyl group;
The perylene compound thus prepared is dissolved in an organic solvent and then reacted with an organic solvent such as halogen, cyanide salt, phenol, phenylphenol, tert-butylphenol, di-tert-butylphenol, naphthol, methylpropanol, cyclohexanol, methoxythiophenol, , the step of phenyl Boro Nick Acid, cyanophenyl beam Nick Acid, naphthyl Boro Nick Acid, and 2-methylpropyl Boro Nick Acid, and their addition hayeoseo the reaction being selected is a material from the group consisting of all isomers Performing one to three times
Wherein the perylene-based compound is a perylene-based compound.
상기 각 반응 단계의 일부 또는 전부에 있어서 카보네이트 염을 첨가하는 것을 추가 포함하는, 제 1 항에 따른 페릴렌계 화합물의 제조 방법. 10. The method according to claim 8 or 9,
The method of producing a perylene compound according to Claim 1, further comprising adding a carbonate salt in some or all of the above reaction steps.
상기 반응들은 유기 용매에 반응물을 용해시켜 반응시킨 후 상온에서 침전 및 여과하는 것을 포함하는 것인, 제 1 항에 따른 페릴렌계 화합물의 제조 방법. 10. The method according to claim 8 or 9,
The method for producing a perylene compound according to claim 1, wherein the reactions include dissolving the reactants in an organic solvent, reacting them, and then precipitating and filtering at room temperature.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20150119971 | 2015-08-26 | ||
| KR1020150119971 | 2015-08-26 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20170026245A KR20170026245A (en) | 2017-03-08 |
| KR101867399B1 true KR101867399B1 (en) | 2018-06-21 |
Family
ID=58100587
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160109172A Active KR101867399B1 (en) | 2015-08-26 | 2016-08-26 | Perylene-based compounds, method of producing the same, and fluorescent dye including the same |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR101867399B1 (en) |
| WO (1) | WO2017034370A1 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210121752A (en) | 2020-03-31 | 2021-10-08 | 동우 화인켐 주식회사 | Self emission type photosensitive resin composition, color conversion layer manufactured by using thereof and a display device |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102253839B1 (en) | 2017-11-16 | 2021-05-20 | 에스에프씨 주식회사 | Labeling dye and kit comprising the same |
| KR102539870B1 (en) | 2018-09-12 | 2023-06-05 | 동우 화인켐 주식회사 | Self emission type photosensitive resin composition, color filter comprising color conversion layer using the same and display device |
| JP2020083982A (en) * | 2018-11-21 | 2020-06-04 | 住友化学株式会社 | Colored curable resin composition, color filter, display device and compound |
| KR102607871B1 (en) | 2019-03-29 | 2023-11-29 | 동우 화인켐 주식회사 | Self emission type photosensitive resin composition, color filter comprising color conversion layer using the same and display device |
| KR102204532B1 (en) | 2019-05-28 | 2021-01-19 | 동우 화인켐 주식회사 | A self emission type photosensitive resin composition, a color conversion layer manufactured by using thereof and a color fiilter comprising the color conversion layer and display device |
| KR102760849B1 (en) | 2020-02-20 | 2025-02-03 | 동우 화인켐 주식회사 | Self emission type photosensitive resin composition, color filter comprising color conversion layer using the same and display device |
| KR20210106170A (en) | 2020-02-20 | 2021-08-30 | 동우 화인켐 주식회사 | Self emission type photosensitive resin composition, color filter comprising color conversion layer using the same and display device |
| KR20210121648A (en) | 2020-03-31 | 2021-10-08 | 동우 화인켐 주식회사 | A self emission type photosensitive resin composition, a color conversion layer manufactured by using thereof and a color fiilter comprising the color conversion layer and display device |
| KR102772174B1 (en) | 2020-03-31 | 2025-02-25 | 동우 화인켐 주식회사 | A self emission type photosensitive resin composition, a color conversion layer manufactured by using thereof and a color fiilter comprising the color conversion layer and display device |
| WO2022191485A1 (en) | 2021-03-10 | 2022-09-15 | 에스에프씨 주식회사 | Reporter and use thereof |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003292758A (en) * | 2002-03-29 | 2003-10-15 | Fine Rubber Kenkyusho:Kk | Fluorescent member and light-generating device by using the same |
| US20130100048A1 (en) * | 2011-08-05 | 2013-04-25 | Brett T. Harding | Optical Element for Correcting Color Blindness |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103380192B (en) * | 2011-02-24 | 2016-04-20 | 巴斯夫欧洲公司 | Novel lighting device |
| US9382264B2 (en) * | 2012-08-30 | 2016-07-05 | Basf Se | Conveniently prepared naphthalene and perylene derivatives as building blocks for organic electronic materials and dyestuff |
-
2016
- 2016-08-26 KR KR1020160109172A patent/KR101867399B1/en active Active
- 2016-08-26 WO PCT/KR2016/009517 patent/WO2017034370A1/en not_active Ceased
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003292758A (en) * | 2002-03-29 | 2003-10-15 | Fine Rubber Kenkyusho:Kk | Fluorescent member and light-generating device by using the same |
| US20130100048A1 (en) * | 2011-08-05 | 2013-04-25 | Brett T. Harding | Optical Element for Correcting Color Blindness |
Non-Patent Citations (2)
| Title |
|---|
| The Journal of Organic Chemistry, Vol. 79, pp.6655-6662, 2014 |
| Thin Solid Films, Vol. 516, pp.8834-8838, 2008 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210121752A (en) | 2020-03-31 | 2021-10-08 | 동우 화인켐 주식회사 | Self emission type photosensitive resin composition, color conversion layer manufactured by using thereof and a display device |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20170026245A (en) | 2017-03-08 |
| WO2017034370A1 (en) | 2017-03-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101867399B1 (en) | Perylene-based compounds, method of producing the same, and fluorescent dye including the same | |
| Phadtare et al. | Halogenation reactions in biodegradable solvent: Efficient bromination of substituted 1-aminoanthra-9, 10-quinone in deep eutectic solvent (choline chloride: urea) | |
| Geerts et al. | Quaterrylenebis (dicarboximide) s: near infrared absorbing and emitting dyes | |
| JP6916769B2 (en) | Platinum (II) emitter for OLED applications | |
| KR102070833B1 (en) | Pyromethene boron complex, color conversion composition, color conversion film, and light source unit including it, display and illumination | |
| CN110386930B (en) | Aggregation-induced luminescence compound, preparation method and application thereof | |
| EP3789464B1 (en) | Ink composition for organic light emitting device | |
| EP3336077B1 (en) | Amine-based compound and organic light-emitting element comprising same | |
| KR20040029478A (en) | Process for the preparation of diketopyrrolopyrroles | |
| EP1741756A1 (en) | Tetraazaporphyrin compound | |
| KR20160038310A (en) | fused fluoranthene derivatives and organic electroluminescent device including the same | |
| JP6796749B2 (en) | New fluorescent compound and fluorescent composition containing it | |
| US12173212B2 (en) | Design, synthesis, and photophysical properties of a novel NIR II dye for biological imaging and optoelectronic devices | |
| Zhang et al. | Reaction of tetrachlorinated perylene bisimide in a strong base to form an asymmetric compound with charge transfer optical properties | |
| KR101570449B1 (en) | Novel BODIPY derivative for green organic light-emitting diode dopant and method for preparing the same | |
| JP6226363B2 (en) | Bis-boron dipyrromethene dye | |
| CN102516171A (en) | N-alkyl-4-aryl aldehyde hydrazone hydrazine-1,8-naphthalimide compound and preparation method thereof | |
| CN111423450A (en) | Compound, display panel and display device | |
| CN105384679B (en) | N, N ' diphenyl N, N ' two (base of 9,9 dimethyl fluorene 2) N hexyls (4,4 ' two aminocarbonyl phenyl) carbazole and its synthetic method | |
| CN107057054B (en) | Quinacridone polyether derivatives and preparation method and application thereof | |
| KR101751784B1 (en) | Novel phenylanthracene derivatives and organic electroluminescent device using the same | |
| WO2005078024A1 (en) | Heteropolycyclic compound and dye | |
| CN103930403B (en) | A kind of bisquinaldine compound and a kind of method for preparing this compound | |
| KR20190043743A (en) | Dicyanstyryl benzene derivatives and fluorescent material comprising the same | |
| Damit et al. | Synthesis, characterization, and systematic structure–property investigation of a series of carbazole–thiophene derivatives |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20160826 |
|
| PA0201 | Request for examination | ||
| PG1501 | Laying open of application | ||
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20180119 Patent event code: PE09021S01D |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20180530 |
|
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20180607 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20180608 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration | ||
| PR1001 | Payment of annual fee |
Payment date: 20210608 Start annual number: 4 End annual number: 4 |
|
| PR1001 | Payment of annual fee |
Payment date: 20220527 Start annual number: 5 End annual number: 7 |