KR101400064B1 - Dry direct compression fast disintegrating tablet - Google Patents
Dry direct compression fast disintegrating tablet Download PDFInfo
- Publication number
- KR101400064B1 KR101400064B1 KR1020087027556A KR20087027556A KR101400064B1 KR 101400064 B1 KR101400064 B1 KR 101400064B1 KR 1020087027556 A KR1020087027556 A KR 1020087027556A KR 20087027556 A KR20087027556 A KR 20087027556A KR 101400064 B1 KR101400064 B1 KR 101400064B1
- Authority
- KR
- South Korea
- Prior art keywords
- weight
- hydrochloride
- tablet
- mixing
- excipient
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
- A61K31/5415—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame ortho- or peri-condensed with carbocyclic ring systems, e.g. phenothiazine, chlorpromazine, piroxicam
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Organic Chemistry (AREA)
- Neurology (AREA)
- Pain & Pain Management (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Rheumatology (AREA)
- Neurosurgery (AREA)
- Zoology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Anesthesiology (AREA)
- Medicinal Preparation (AREA)
Abstract
함유시키는 유효 성분의 종류에 관계 없이, 또 배합하는 다른 성분의 종류에 관계 없이, 목적으로 하는 속붕괴성 정제를 높은 타정 효율로 제조할 수 있는 방법, 그리고 그 제조 방법에 의해 얻어지는 속붕괴성 정제를 제공함에 있어서, 에리트리톨, 자일리톨, 만니톨, 유당, 자당으로 이루어지는 군에서 선택되는 1 종 이상의 교미제와, 결정 셀룰로오스, 결정 셀룰로오스·카르멜로오스나트륨, 카르멜로오스칼륨으로 이루어지는 군에서 선택되는 1 종 이상의 결합제의 분체를 혼합하고, 환원 맥아당 물엿의 수용액을 분무하면서 유동층 조립기를 사용하여 조립함으로써 얻어지는 조립물과, 유효 성분, 부형제, 붕괴제, 유동화제 및 활택제를 혼합하여 얻어진 혼합물을 직접 타정하여 얻은 건식 직타 속붕괴성 정제이며, 특히 타르타르산졸피뎀은 멜록시캄을 함유하는 건식 직타 속붕괴성 정제이다. Irrespective of the kind of the active ingredient to be contained and regardless of the kind of the other ingredients to be blended, a method for producing a desired fast disintegrating tablet at a high tableting efficiency, and a method for producing a fast disintegrating tablet The present invention provides a method for producing a microcapsule comprising the steps of mixing at least one matting agent selected from the group consisting of erythritol, xylitol, mannitol, lactose, and sucrose, and 1 or 2 selected from the group consisting of crystalline cellulose, crystalline cellulose, carmellose sodium, A mixture obtained by mixing powders of a binder of at least two types and a granule obtained by granulating an aqueous solution of reduced maltose starch syrup with a fluidized bed granulator while mixing the obtained mixture with an effective ingredient, an excipient, a disintegrant, a fluidizing agent and a lubricant, It is a dried tablets disintegrating tablet obtained by the method of the present invention. Especially, zolpidem tartrate is meloxicam Dry jikta in a degradable tablets containing.
Description
본 발명은 유효 성분과 그 밖의 배합 성분, 특히 특정한 교미제(矯味劑)와 특정한 결합제의 분체를 혼합하고, 환원 맥아당 물엿의 수용액을 분무하면서 얻은 조립물(造粒物)의 조합을 고려함으로써, 속붕괴성을 유지하면서, 실용적인 정제의 경도를 갖는 건식 직타 속붕괴성 정제 및 그 제조 방법에 관한 것이다. The present invention is based on the consideration that a combination of an active ingredient and other ingredients, particularly a powder of a specific taste modifier and a specific binder, and a combination of granules obtained by spraying an aqueous solution of reduced maltose syrup is taken into consideration, The present invention relates to a disintegrating tablets having a disintegrable nature and having practical tablet hardness and a process for producing the same.
최근, 의료용 고형 제제에 있어서, 복용의 용이성 등의 이유로 구강 내 속붕괴정의 개발의 요망이 높아지고 있다. 구강 내 속붕괴정으로서의 정제에 요구되는 요건으로는, (1) 일본 약국방의 붕괴 시험법에 의해 30 초 이내에 붕괴될 것, (2) 구강 내에서 60 초 이내에 붕괴될 것이라는 붕괴성과, (3) 마손도 시험 200 회전에서 눈에 띈 파손이 확인되지 않을 것이라는 경도 등을 들 수 있다. BACKGROUND ART [0002] In recent years, there has been a growing demand for the development of a rapid decay in oral cavity for reasons of ease of administration and the like in medical solid preparations. (1) disintegration within 30 seconds by the Japanese Pharmacopoeia collapse test; (2) disintegration within the oral cavity within 60 seconds; (3) disintegration within 60 seconds of oral disintegration; And the hardness that visible damage is not observed at 200 rotation of the test.
이와 같은 구강 내 속붕괴정의 제조 방법으로서 종래부터, 습식 조립법과 건식 조립법이 제안되어 있다. 습식 조립법으로는 예를 들어, (1) 약효 성분과 부형제로서의 당류를 함유하는 정제 성분에 대해, 0.3 ∼ 7 중량% 의 수분을 사용하여 상기 당류의 입자 표면을 습기차게 하고, 상기 약효 성분과 당류와 수분을 함유하는 혼합물을 타정한 후 건조시키는 것에 의한 일본 약국방 제 12 개정에 기재 되어 있는 붕괴 시험법에 의한 붕괴 시간이 0.05 ∼ 3.0 분인 구강 내 붕괴형 정제를 제조하는 방법 (특허 문헌 1) 이 보고되어 있다. Conventionally, as a method for producing such a rapid decay in the oral cavity, a wet assembly method and a dry assembly method have been proposed. As the wet granulation method, for example, (1) moisturizing the surface of the saccharide particles using water of 0.3 to 7% by weight with respect to the tablet component containing the active ingredient and the saccharide as an excipient, And a method for producing an intraoral disintegrating tablet having a disintegration time of 0.05 to 3.0 minutes according to the disintegration test method described in Japanese Pharmacopoeia 12th edition by drying the tablet after mixing the mixture with water (Patent Document 1) Reported.
또, 건식 조립법으로는, 예를 들어, (2) 투여 전에 수중에 분산시키지 않고 경구 투여하는 정제로서, 미각을 마스크하도록 피복된 미결정 또는 미립자 형태의 유효 물질과, 부형제를 함유하는 혼합물의 혼합 재료를 직접 압축하여 얻어진 급속 붕괴성 다입자 정제가 제안되어 있다 (특허 문헌 2). 이 경우, 상기 부형제를 함유하는 혼합물로는, 적어도 1 개의 붕괴제, 및 전분, 가공 전분, 혹은 미결정 셀룰로오스에서 선택되고, 물과 접촉하여 고점도를 발생시키지 않는 적어도 1 개의 팽창제, 또는 적어도 1 개의 가용제를 함유하는 것이고, 정제는 발포제 및 유리된 유기산을 함유하지 않고, 구강 내에서 타액의 존재 하에서 저작없이 60 초보다 짧은 시간에 붕괴하는 급속 붕괴성 다입자 정제이다. The dry granulation method includes, for example, (2) a method for preparing tablets, which are orally administered without being dispersed in water before administration, as tablets containing a mixture of an effective substance in the form of microcrystalline or fine particles coated to mask the taste, (Japanese Patent Application Laid-Open No. 2001-325819). In this case, the mixture containing the excipient includes at least one disintegrant and at least one swelling agent selected from starch, modified starch or microcrystalline cellulose, which does not generate high viscosity upon contact with water, Wherein the tablet is a rapidly disintegrable multiparticulate tablet that does not contain a foaming agent and free organic acid and disintegrates in less than 60 seconds without chewing in the presence of saliva in the oral cavity.
또 동일하게 건식 타정법으로서 예를 들어, (3) 물에 대한 용해성이 높은 당류와 팽윤성의 부형제를 습식 조립하여 조제한 과립과, 결정 셀룰로오스를 타정하여 얻어지는 구강 내 속붕정 (특허 문헌 3) 등이 보고되어 있다. (3) granules prepared by wet-granulating a saccharide having high solubility in water and a swelling excipient, and an inner buccal buccal cavity obtained by tableting crystalline cellulose (Patent Document 3), etc. Reported.
또, 본 발명자들도 앞서 (a) 유효 성분, (b) 용해 보조제로서의 시트르산, 타르타르산, 말산, 락트산 및 아스코르브산에서 선택되는 산류 또는 그 알칼리 금속염 ; 알칼리 금속 탄산수소염 ; 및 알칼리 금속 탄산염으로 이루어지는 군에서 선택되는 적어도 1 종을 함유하고, 또한 (c) 부형제, (d) 결합제, (e) 붕괴제, (f) 유동화제 및 (g) 활택제로서의 스테아르산마그네슘 및 자당 지방산 에스테르의 조합으로 이루어지는 활택제를 함유하는 것을 특징으로 하는 건식 직타 속붕괴성 정 제 및 그 제조 방법 (특허 문헌 4) 을 출원중이다. The present inventors have also found that (a) an active ingredient, (b) an acid or an alkali metal salt thereof selected from citric acid, tartaric acid, malic acid, lactic acid and ascorbic acid as a solubilizing agent; Alkali metal hydrogencarbonate; (C) an excipient, (d) a binder, (e) a disintegrant, (f) a fluidizing agent, and (g) magnesium stearate as a lubricant, and (Patent Document 4), which is characterized in that it contains a lubricant composed of a combination of sucrose fatty acid ester and a sucrose fatty acid ester.
특허 문헌 1 : 일본특허공보 제3069458호 Patent Document 1: Japanese Patent Publication No. 3069458
특허 문헌 2 : 일본특허공보 제2820319호 Patent Document 2: Japanese Patent Publication No. 2820319
특호 문헌 3 : 일본 공개특허공보 2000-16930호 Japanese Patent Laid-Open Publication No. 2000-16930
특허 문헌4 : 일본 특허출원 2006-17401호Patent Document 4: Japanese Patent Application No. 2006-17401
그러나, 이들의 종래의 방법은 예를 들어, 상기 (1) 의 습식 조립법에서는, 약효 성분과 당류를 함유하는 정제 성분에 대해, 0.3 ∼ 7 중량% 의 수분을 사용하고, 상기 당류의 입자의 표면을 습기차게 하고, 건조시킨다는 번잡한 처리가 필요하다. 또 상기 (2) 의 건식 조립법은 활성 성분 (유효 성분) 이 피복되어 미결정 상태에 있을 때는, 미결정을 피복하는 것이고, 또 유효 성분이 피복되지 않은 미과립 상태에 있는 경우에는, 유효 성분을 예를 들어 압출 조립화, 팬 내에서의 가공, 공기 유동층 등과 같은 방법에 의해 미과립 형상으로 하는 것으로서, 번잡한 조작을 필요로 하는 것이었다. 또 (3) 의 건식 타정법에서는, 과립 외에 결정 셀룰로오스를 배합하지 않는 것으로는, 밀어 올리는 레일치가 높아, 타정 장해가 일어나는 경향이 있는 것이 보고되어 있다. 또, (4) 의 건식 직타 속붕괴성 정제에서는, 멜록시캄 원말 (原末) 의 입자형이 약 12㎛ 이하가 되면 혼합품의 유동성이 급격하게 저하되어, 타정 효율이 저하되는 것을 알 수 있었다. However, in these conventional methods, for example, in the wet granulation method of (1), 0.3 to 7% by weight of water is used for the tablet component containing the active ingredient and the saccharide, It is necessary to carry out troublesome treatment such as wetting and drying. The dry granulation method of (2) above covers the microcrystalline when the active component (effective component) is coated and is in the microcrystalline state, and when the microcrystalline state is not coated with the active component, It has been required to carry out troublesome operations because it is made into a non-granular shape by a method such as extrusion granulation, processing in a fan, air fluidized bed, and the like. In the dry tableting method of (3), it has been reported that when the crystalline cellulose other than granules is not blended, the rail value to be pushed up is high, and tableting trouble tends to occur. Further, in the dry type disintegrating tablet (4), when the particle size of the meloxicam raw material is about 12 μm or less, the fluidity of the mixed product is drastically lowered and the tableting efficiency is lowered .
건식 타정법은 유효 성분인 약물과 그 밖의 부형제 등의 성분을 혼합한 후, 당해 혼합물을 직접 타정 (직타) 하여 정제를 형성하는 방법으로서, 혼합, 타정의 2공정으로 정제를 조제할 수 있는 간편한 조제 방법이다. 그러나, 약물의 종류 에 따라, 혹은 혼합 성분 등과의 조합에 따라서는, 직타법으로는 목적으로 하는 정제를 제조할 수 없는 문제가 있다. The dry tabletting method is a method of mixing tablets with a drug such as an active ingredient and other excipients and then directly tableting the mixture to form tablets, It is a preparation method. However, there is a problem in that it is not possible to produce a desired tablet by the direct method depending on the kind of the drug, or the combination with the mixed component or the like.
예를 들어, 약물 및 첨가하는 성분의 분체 혼합물의 유동성이 낮은 경우에는, 타정기의 호퍼로부터 분체 혼합물이 유출되지 않아, 타정 불가능해지거나, 캡핑에 의한 수율의 저하, 정제의 중량 편차가 현저하게 커지는 것이 관찰된다. 또, 정제의 붕괴성을 개선하면 정제의 경도를 유지할 수 없게 되는 등의 문제가 있었다. For example, when the fluidity of the powder mixture of the drug and the ingredients to be added is low, the powder mixture does not flow out from the hopper of the tableting machine and becomes unable to be tableted, or the yield is decreased due to capping and the weight deviation of the tablet is remarkably increased Is observed. Further, there has been a problem that if the disintegration property of the tablet is improved, the hardness of the tablet can not be maintained.
사실, 본 발명자들은 유효 성분으로서 타르타르산졸피뎀 또는 멜록시캄을 사용하여 직접 타정법에 의한 속붕괴성 정제의 제조를 검토하고 있는 가운데, 혼합 성분의 조합에 따라서는 타정 전의 분체 혼합물의 유동성이 저하됨으로써 타정 효율이 저하되는 것, 또, 타르타르산졸피뎀 또는 멜록시캄의 입자직경이 작을수록 얻어지는 정제로부터의 타르타르산졸피뎀 또는 멜록시캄의 용출 속도는 빨라지지만, 절굿공이에 부착되는 등의 타정 장해가 일어나기 쉬워지는 것을 경험하고 있다.In fact, the present inventors have studied the preparation of fast disintegrating tablets by a direct tableting method using zolpidem tartrate or meloxicam as an active ingredient, and depending on the combination of the ingredients, the fluidity of the powder mixture before tableting is lowered The dissolution rate of tartaric acid solpipem or meloxicam from tablets obtained with a smaller particle diameter of tartaric acid solpipem or meloxicam is accelerated, but a tableting disadvantage such as adherence to a jellyfish And it is becoming easy to happen.
발명의 개시DISCLOSURE OF INVENTION
발명이 해결하고자 하는 과제Problems to be solved by the invention
따라서 본 발명은 직접 타정법에 의한 속붕괴성 정제를 제조함에 있어서, 함유시키는 유효 성분의 종류에 관계없이, 또 배합하는 다른 성분의 종류에 관계없이, 목적으로 하는 속붕괴성 정제를 높은 타정 효율로 제조할 수 있는 방법, 그리고 그 제조 방법에 의해 얻어지는 속붕괴성 정제를 제공하는 것을 과제로 한다. Accordingly, the present invention relates to a method for producing a fast disintegrating tablet by a direct tableting method, wherein the desired disintegrating tablet has a high tableting efficiency regardless of the kind of the active ingredient to be contained, And a method of producing the same. The present invention also provides a rapid disintegrating tablet obtained by the method.
본 발명자들은 상기 과제를 해결하기 위하여 예의 검토한 결과, 첨가하는 각 성분 중에서, 타정 전의 분체 혼합물의 유동성을 저하시키는 원인이 되는 성분을 미리 과립화함으로써 유동성을 갖게하면 분체 혼합물의 타정기의 호퍼로부터의 유출성이 좋아져, 캡핑의 발생을 억제함과 함께, 결과적으로 정제의 중량 편차를 작게 할 수 있는 것, 나아가서는, 정제의 붕괴성을 유지하면서, 실용적인 정제의 경도를 갖는 속붕괴성 정제를 제조할 수 있을 것으로 생각하였다. The present inventors have intensively studied in order to solve the above problems. As a result of intensive studies, it has been found that, among the components to be added, the components causing the deterioration of the fluidity of the powder mixture before crushing are previously granulated, It is possible to prevent the occurrence of capping and consequently to reduce the weight deviation of the tablet. In addition, it is possible to produce a fast disintegrating tablet having practical tablet hardness while maintaining the disintegration property of tablets I thought that I could do it.
이러한 생각을 기초로 검토한 결과, 특히 혼합 분체물의 유동성을 저하시키는 원인이 되는 성분은 교미제로서 배합하는 에리트리톨, 자일리톨, 만니톨 등에서 기인하는 것을 확인하고, 이러한 성분을 결합제, 예를 들어 결정 셀룰로오스와 함께 과립화하고, 이 조립물과, 유효 성분 그리고 다른 배합 성분을 혼합한 혼합 분체물은 그 유동성이 양호한 것으로서, 상기한 문제점을 단번에 해결할 수 있는 것을 알아내어, 본 발명을 완성시키기에 이르렀다. As a result of the study based on this idea, it has been found that the components causing the deterioration of the fluidity of the mixed powder are found to be caused by erythritol, xylitol, mannitol and the like to be mixed as a mating agent and these components are mixed with a binder such as crystalline cellulose And that the mixed powder obtained by mixing the granulated product with the granulated product, the active ingredient and other blending ingredients has good fluidity and can solve the above problems at once. Thus, the present invention has been accomplished.
과제를 해결하기 위한 수단Means for solving the problem
그리고, 본 발명의 하나의 기본적 양태인 청구항 1 에 기재된 발명은 에리트리톨, 자일리톨, 만니톨, 유당, 자당으로 이루어지는 군에서 선택되는 1 종 이상의 교미제와, 결정 셀룰로오스, 결정 셀룰로오스·카르멜로오스나트륨, 카르멜로오스칼륨으로 이루어지는 군에서 선택되는 1 종 이상의 결합제의 분체를 혼합하고, 환원 맥아당 물엿의 수용액을 분무하여 얻은 조립물을 사용하는 것을 특징으로 하는 건식 직타 속붕괴성 정제이다. The invention according to claim 1 as one basic aspect of the present invention relates to a pharmaceutical composition comprising at least one compounding agent selected from the group consisting of erythritol, xylitol, mannitol, lactose, and sucrose, and at least one kind selected from the group consisting of crystalline cellulose, crystalline cellulose, carmellose sodium, Disintegrating tablet which is obtained by mixing powders of at least one binder selected from the group consisting of carnauba wax and carmellose potassium and spraying an aqueous solution of reduced maltose syrup.
보다 구체적인 청구항 2 에 기재된 본 발명은 청구항 1 에 기재된 발명에 있어서, 조립을 유동층 조립기에 의해 실시하는 것인 건식 직타 속붕괴성 정제이다.More specifically, the present invention described in claim 2 is the dry-laid collapse-resistant tablet according to claim 1, wherein the granulation is carried out by a fluidized-bed granulator.
따라서, 본 발명의 다른 기본적 양태는 상기에서 얻은 조립물과, 유효 성분, 부형제, 붕괴제, 유동화제, 활택제 및 착색제를 혼합하고, 얻어진 혼합물을 직접 타정하는 것을 특징으로 하는 건식 직타 속붕괴성 정제이다. Therefore, another basic aspect of the present invention is to provide a dry-laid collapse-resistant granular material which is obtained by mixing the granules obtained above with an effective ingredient, an excipient, a disintegrant, a fluidizing agent, a lubricant and a colorant, It is tablets.
가장 구체적인 본 발명은 유효 성분으로서 타르타르산졸피뎀 또는 멜록시캄을 사용한 상기의 건식 직타 속붕괴성 정제이다. The most specific invention of the present invention is the aforementioned dry type disintegrating tablets using zolpidem tartrate or meloxicam as an active ingredient.
또한 본 발명의 다른 양태인 청구항 5 에 기재된 발명은 에리트리톨, 자일리톨, 만니톨, 유당, 자당으로 이루어지는 군에서 선택되는 1 종 이상의 교미제와, 결정 셀룰로오스, 결정 셀룰로오스·카르멜로오스나트륨, 카르멜로오스칼륨으로 이루어지는 군에서 선택되는 1 종 이상의 결합제의 분체를 혼합하고, 환원 맥아당 물엿의 수용액을 분무하면서 유동층 조립기를 사용하여 조립함으로써 얻어진 조립물과, 유효 성분, 부형제, 붕괴제, 유동화제, 활택제 및 착색제를 혼합하고, 당해 혼합물을 직접 타정하는 것을 특징으로 하는 건식 직타 속붕괴성 정제의 제조 방법이다. 또, 가장 구체적인 청구항 6 에 기재된 발명은 유효 성분으로서 타르타르산졸피뎀 또는 멜록시캄을 사용한 상기의 건식 직타 속붕괴성 정제의 제조 방법이다. According to a fifth aspect of the present invention, there is also provided a method for producing a microcapsule comprising the steps of mixing at least one matting agent selected from the group consisting of erythritol, xylitol, mannitol, lactose, and sucrose and a microcrystalline cellulose selected from the group consisting of crystalline cellulose, crystalline cellulose, carmellose sodium, Potassium, and granules obtained by mixing powder of an aqueous solution of reduced maltose starch syrup using a fluidized bed granulator while spraying an active ingredient, an excipient, a disintegrant, a fluidizing agent, a lubricant And a colorant are mixed and directly kneaded with the mixture. The most specific invention according to claim 6 is a process for producing the above dry-type disintegrating tablets using zolpidem tartrate or meloxicam as an active ingredient.
발명의 효과Effects of the Invention
본 발명에 의해, 직접 타정 전의 유효 성분을 함유하는 분말상의 혼합물에 대해, 그 유동성이 양호한 것이며, 따라서, 타정기의 호퍼로부터의 혼합 분체물의 유출성이 좋고, 캡핑의 발생을 억제하고, 결과적으로 정제의 중량 편차가 거의 없는 속붕괴성 정제, 및 그 건식 직타법에 의한 속붕괴성 정제의 제조 방법이 제공된다. According to the present invention, the fluidity of the powdery mixture containing the active ingredient directly before tableting is good, and therefore, the flowability of the powdery mixture from the hopper of the tableting machine is good, the occurrence of capping is suppressed, , And a method for producing a rapidly disintegrating tablet by the dry cutting method.
또, 본 발명에 의해 얻어진 속붕괴성 정제는 원하는 붕괴 속도를 가지며, 실용적인 정제의 경도를 갖는 것이고, 또한 그 제조 방법은 저가이고, 간편한 제조 방법이다. 따라서, 각종 유효 성분에 대해, 목적으로 하는 속붕괴성 정제를 조제할 수 있는 이점을 갖고 있다. In addition, the fast disintegrating tablet obtained by the present invention has a desired disintegration rate, has practical tablet hardness, and its manufacturing method is inexpensive and easy to manufacture. Therefore, it has an advantage that it is possible to prepare a targeted disintegrating tablet for various active ingredients.
발명을 실시하기 위한 최선의 형태BEST MODE FOR CARRYING OUT THE INVENTION
본 발명의 기본은 상기한 바와 같이, 직접 타정 전의 혼합 분체물의 유동성을 저하시키는 원인이 되는 성분을 미리 과립화함으로써 유동성을 갖게 하고, 이러한 조립물을 사용하여, 유효 성분, 다른 성분을 혼합하고, 얻어진 그 혼합 분체물을 직접 타정하여 얻은 직타 속붕괴성 정제이다. The basic of the present invention is to provide a method for making a granular material having a fluidity in advance by granulating a component which causes a decrease in fluidity of a powdery mixture directly before tableting, And is obtained by directly kneading the obtained mixed powder.
본 발명자들의 검토에 의하면, 직접 타정 전의 혼합 분체의 유동성을 저하시키는 성분은 교미제로서 배합되는 성분인 것이 판명되었다. According to the investigations of the present inventors, it has been found that the component that lowers the fluidity of the powdery powder directly before tableting is a component to be compounded as a mating agent.
이와 같은 교미제로는 에리트리톨, 자일리톨, 만니톨, 유당, 자당이다. These mating agents are erythritol, xylitol, mannitol, lactose, and sucrose.
또한, 이러한 교미제는 어느 일면에 있어서는 부형제로서 사용되는 성분이며, 부형제로서 첨가하는 경우에 있어서도 이것과 다른 성분, 예로는 유효 성분 혹은 결합제 등을 미리 조립해 두는 것은 바람직한 것이다. In addition, such a mating agent is a component used as an excipient on any one of the surfaces, and when it is added as an excipient, it is preferable to previously assemble other components such as an active ingredient or a binder.
본 발명에 있어서는, 이러한 유동성을 저하시키는 교미제를 미리 과립화 (조립) 하고, 그 유동성을 향상시키는 것이지만, 과립화를 실시함에 있어서는, 결합제와 함께 과립화하는 것이 좋다. In the present invention, such a mating agent for lowering the fluidity is previously granulated (granulated) to improve its fluidity, but granulation is preferably carried out together with the binder.
그러한 결합제로는, 결정 셀룰로오스, 결정 셀룰로오스·카르멜로오스나트륨, 카르멜로오스칼륨 등을 들 수 있다. 그 중에서도 특히 결정 셀룰로오스가 바람직하게 사용된다. 이 결정 셀룰로오스로는 예를 들어, 세오라스 PH101, 세오라스 PH302 [아사히 화성 케미컬즈 (주) 제조] 이다. Such binders include crystalline cellulose, crystalline cellulose, carmellose sodium, and carmellose potassium. Among them, crystalline cellulose is preferably used. The crystalline cellulose includes, for example, Seoras PH101 and Seoras PH302 (manufactured by Asahi Chemical Industry Co., Ltd.).
사용하는 결합제의 배합량은 최종 정제의 중량을 기준으로 하여 5 ∼ 20 중량% 이며, 바람직하게는 약 10 중량% 인 것이 좋다. The blending amount of the binder to be used is 5 to 20% by weight, preferably about 10% by weight, based on the weight of the final tablet.
본 발명에 있어서는, 상기한 교미제와 결합제의 양자를 특히 환원 맥아당 물엿의 수용액을 분무하면서 조립함으로써 과립화하는 것이 좋다. In the present invention, it is preferable to granulate both of the above-described mating agent and binder by granulating while spraying an aqueous solution of reduced maltose starch syrup.
사용하는 환원 맥아당 물엿은 분말 환원 맥아당 물엿, 환원 맥아당 물엿 (별명 멀티톨) 이며, 전분류를 물에 첨가하여 가열하여, 풀(糊)화하고, 이것에 아밀라아제를 첨가하여, 가수분해하고, 정제한 것을 환원하여 더욱 정제 농축한 것이다. 냄새가 없고, 맛이 달아, 지금까지 감미제, 기제, 교미제 등으로서 각종 제제의 첨가물로서 널리 사용되어 온 성분이다. The reduced maltose syrup used is a powdered maltose syrup, a reduced maltose syrup (nick name is multitol), and the whole fraction is added to water to be heated to paste, to which amylase is added for hydrolysis, Which is further purified and concentrated. It has no odor and flavor, and has been widely used as an additive for various preparations as sweeteners, base agents, mating agents and the like.
본 발명에 있어서는, 이러한 환원 맥아당 물엿은 상기한 교미제와 결합제의 조립물의 조제시에 사용하는 액제용의 부형제로서 사용된다. In the present invention, such reduced maltose starch syrup is used as an excipient for a liquid preparation used for preparing the above-described matting agent and a granulation product of the binder.
본 발명에 있어서는, 교미제와 결합제의 분체를 혼합하고, 부형제로서의 환원 맥아당 물엿의 수용액을 분무하면서 조립하지만, 이 조립은 예를 들어, 유동층 조립기를 사용하여 실시할 수 있고, 그 조립 자체는 다른 자체 공지된 방법으로 실시할 수도 있다. In the present invention, the powder is mixed with a powder of a mating agent and a binder, and an aqueous solution of reduced maltose syrup as an excipient is sprayed. The granulation can be carried out, for example, by using a fluidized bed granulator. Or may be carried out by a method known per se.
본 발명은 그 기본적 양태로는 분체 혼합물의 유동성을 저하시키는 원인 성분인 교미제를 결합제와 함께 특정한 부형제인 환원 맥아당 물엿의 수용액을 사용하여 조립하고, 그 유동성을 향상시키고, 그 후에, 이러한 조립물과, 유효 성분, 부형제, 붕괴제, 유동화제 및 활택제를 혼합하고, 얻어진 혼합물을 직접 타정하는 것을 특징으로 하는 건식 직타 속붕괴성 정제이다. In the basic mode of the present invention, a basic agent for lowering the fluidity of a powder mixture is prepared by combining a binder with a binding agent using an aqueous solution of reduced maltose starch syrup, which is a specific excipient, to improve its fluidity, And an active ingredient, an excipient, a disintegrant, a fluidizing agent and a lubricant, and directly kneading the resulting mixture.
이로써, 원하는 속붕괴성과 적당한 경도를 갖는 건식 직타 속붕괴성 정제를 얻는 것이 가능해진다. This makes it possible to obtain a disintegrating tablet in the dry type with a desired decay rate and an appropriate hardness.
이 경우의 본 발명의 건식 직타 속붕괴성 정제에 사용하는 약효 성분으로는, 특별히 제한되는 것은 아니다. 예를 들어, 항균약, 항결핵약, 항진균, 항바이러스제, 항암제, 비타민제, 부신 피질 호르몬 제제, 항알레르기약, 비스테로이드성 항염증약, 마약, 편두통용약, 당뇨병약, 고지혈증 치료제, 통풍·고요산혈증용약, 대사이상증용약, 진정·최면약, 항불안약, 항간질약, 항우울증약, 항정신병약, 정신자극약, 강심약, β 수용체 차단약, 칼슘채널길항약, 항부정맥약, 이뇨약, 강압약, 승압약, 뇌순환·대사장해용약, 진해약, 거담약, 기관지 확장약, 기관지천식용약, 호흡 촉진약, 건위약·소화제, 위염용약, 제토약, 소화성궤양약, 지사약·정장약·장질환용약, 사하제 (하제), 이담제, 파킨슨병 (증후군) 용약, 골대사질환·골다공증용제 (골흡수억제약) 및 류머티즘·관절증용약 (항류머티즘약) 등을 들 수 있다. The pharmaceutical active ingredient to be used in the dry compact powder of the present invention in this case is not particularly limited. For example, there is provided a pharmaceutical composition comprising an antimicrobial drug, an anti-TB drug, an antifungal agent, an antiviral agent, an anticancer agent, a vitamin agent, a corticosteroid agent, an antiallergic drug, a non- steroidal antiinflammatory drug, a drug, a migraine drug, , Antidepressant drugs, sedative hypnotics, anxiolytics, antiepileptics, antidepressants, antipsychotics, mental stimulants, anticholinergic agents, β-receptor blockers, calcium channel antagonists, antiarrhythmic drugs, diuretics, Medicines, hypertensive drugs, cerebral circulation · metabolic disorder drugs, chinhae medicines, gadam drugs, bronchodilators, bronchial asthma medicines, respiratory stimulants, placebo medicines, gastritis medicines, pharmacological agents, peptic ulcer drugs, · Drugs for intestinal diseases, depressants (laxatives), medicines, Parkinson's disease (syndrome) drugs, bone metabolism diseases · Osteoporosis drugs (bone resorption inhibitors) and rheumatism and arthritic drugs (antirheumatic drugs).
항생 물질로는, 예를 들어 세파렉신, 세파클로르, 아목시실린, 염산피브메실리남, 염산세포티암헥세틸, 세파드록실, 세픽심, 세프디토렌피복실, 세프테람피복실, 세프포독심프록세틸, 염산세포티암, 염산세파조프란, 염산세프메녹심, 세프술로딘나트륨 등의 세펨계, 암피실린, 시클라실린, 술베니실린나트륨, 날리딕스산, 에녹사신 등의 합성 항균제, 카루모남나트륨 등의 모노박탐계, 페넴계 및 카르바페넴계 항생 물질, 황산 파로모마이신, 아목시실린, 세파클로르, 세파렉신, 아세틸스피라마이신, 염산미노사이클린을 들 수 있다. Examples of antibiotics include, but are not limited to, cephalexin, cephalocor, amoxicillin, pbemethicillin hydrochloride, cytochromeethelic acid hydrochloride, cephadoxyl, cephicim, cefditorenecrosil, Synthetic antimicrobial agents such as cetyl chloride, cetyltrimethylammonium chloride, cetyltrimethylammonium chloride, cetyltrimethylammonium chloride, cetyltrimethylammonium chloride, cetyltrimethylammonium chloride, cetyltrimethylammonium chloride, cetyltrimethylammonium chloride, Antibiotics such as phenobarbital and carbapenem antibiotics, paromomycin sulfate, amoxicillin, cepharchlor, cepharaxine, acetyl spiramycin, and minocycline hydrochloride.
항결핵약으로는, 예를 들어 이소니아지드, 염산에탄부톨 등을 들 수 있다. Examples of anti-tuberculosis drugs include isoniazid, and thanabutol hydrochloride.
항진균약으로는, 예를 들어 미코나졸, 염산테르비나핀 등을 들 수 있다.Examples of antifungal drugs include mycotriazole and terbinafine hydrochloride.
또, 항바이러스제로는, 예를 들어 라미부딘, 리바비린, 아시클로비르 등을 들 수 있다. Examples of antiviral agents include lamivudine, ribavirin, and acyclovir.
항암제로는, 예를 들어 5-플루오로우라실, 우라실, 마이토마이신, 카르모푸르, 염산아클라루비신, 시클로포스파미드, 티오테파 등을 들 수 있다. Examples of the anticancer agent include 5-fluorouracil, uracil, mitomycin, carmopur, aclarubicin hydrochloride, cyclophosphamide, thiotepa, and the like.
비타민약으로는, 예를 들어 염산티아민, 질산티아민, 아세트산토코페놀, 시코티아민, 인산피리독살, 코바마미드, 아스코르브산, 니코틴산아미드, 알파칼시돌, 코바마이드, 비타록신, 부티르산리보플라빈, 아스코르브산 등을 들 수 있다. Examples of the vitamin medicine include thiamine hydrochloride, thiamine nitrate, tocopherol acetate, cicotiamine, pyridoxal phosphate, cobamamide, ascorbic acid, nicotinic acid amide, alphalcidol, cobamide, vitaoxin, riboflavin butyrate, And the like.
부신 피질 호르몬 제제로는, 예를 들어 프레드니조론, 트리암시놀론, 베타메타존 등을 들 수 있다. Examples of adrenocortical hormone preparations include, for example, prednisolone, triamcinolone, betamethasone, and the like.
항알레르기약으로는, 예를 들어, 염산디펜히드라민, 타닌산디펜히드라민, 염산트리프롤리딘, 염산프로메타진, 타르타르산알리메마진, 메퀴타진, 테오클산디페닐피랄린, d-말레산클로르페니라민, 염산시프로헵타딘, 푸마르산클레마스틴, 푸마르산케토티펜, 염산아젤라스틴, 옥사토미드, 푸마르산에메다스틴, 에바스틴, 염산세티리진, 염산펙소페나딘, 로라타딘, 염산올로파타딘, 트라니라스트, 암렉사녹스, 타자노라스트, 프란루카스트 수화물, 염산오자그렐 등을 들 수 있다. Antiallergic drugs include, for example, diphenhydramine hydrochloride, diphenhydramine tannate, triprolidine hydrochloride, prometazine hydrochloride, tartaric acid alimemazin, mequitazine, diphenhydramine theophylline, d-maleic acid A drug such as cholestyramine, chlorpheniramine hydrochloride, cipherin hydrochloride, clemastine fumarate, ketotifen fumarate, azelastine hydrochloride, oxathomide, methadestin fumarate, evastin, cetirizine hydrochloride, fexofenadine hydrochloride, loratadine hydrochloride, , Tranilast, Amelexacox, Tazanorast, Pranlukast hydrate, Ozagrel hydrochloride and the like.
비스테로이드성 항염증약으로는, 예를 들어, 아스피린, 메페남산, 톨페남산, 인도메타신, 인도메타신파르네실, 아세메타신, 디클로페낙, 디클로페낙나트륨, 암페낙나트륨, 에토돌락, 모페졸락, 술린닥, 나브메톤이브프로펜, 케토프로펜, 록소프로펜나트륨, 피록시캄, 안피록시캄, 멜록시캄 등을 들 수 있다. Non-steroidal antiinflammation agents include, for example, aspirin, mefenamic acid, tolpennamic acid, indomethacin, indomethacinparinace, acetemethine, diclofenac, diclofenac sodium, amfenac sodium, etodolac, Lyxac, nalbumetone ibuprofen, ketoprofen, losoprofen sodium, piroxycam, amphoxocam, meloxicam, and the like.
마약으로는, 예를 들어, 염산모르핀, 염산옥시코돈, 염산코카인 등을 들 수 있다. Examples of the drug include morphine hydrochloride, oxycodone hydrochloride, cocaine hydrochloride, and the like.
편두통용약으로는, 예를 들어, 타르타르산에르고타민, 숙신산스마트립탄, 졸미트립탄, 염산로메디린, 메실산디메토티아진, 카페인 등을 들 수 있다. Examples of the migraine drug include, for example, tartaric acid ergotamine, succinic acid smartlitane, zolmitriptan, hydrochloric acid medillin, mesylate dimethothiazine, caffeine and the like.
당뇨병용제로는, 예를 들어, 톨부타미드, 아세토헥사미드, 클로르프로파미드, 글리클로피라미드, 글리부졸, 글리벤클라미드, 글리메피리드, 염산부포르민, 염산메트포르민, 나테글리니드, 아카르보오스, 보글리보오스, 염산피오글리타존, 에팔레스타트 등을 들 수 있다. Examples of the diabetic agent include, for example, tolbutamide, acetohexamide, chlorpropamide, glycopyrimide, glybuzole, glibenclamide, glimepiride, hydrochlorofluoride, metformin hydrochloride, nateglinide, Osse, boglibose, pioglitazone hydrochloride, and epelastat.
고지혈증 치료제로는, 예를 들어, 프라바스타틴나트륨, 심바스타틴, 로바스타틴, 플루바스타틴, 아토르바스타틴 등을 들 수 있다. Examples of therapeutic agents for hyperlipidemia include pravastatin sodium, simvastatin, lovastatin, fluvastatin, atorvastatin and the like.
통풍 치료약으로는, 예를 들어, 알로프리놀, 콜히친, 벤즈브로마론, 프로베네시드 등을 들 수 있다. Examples of the gout remedy include alloprenol, colchicine, benzbromarone, proveneside, and the like.
진정·최면약으로는, 예를 들어, 트리아졸람, 미다졸람, 브로티졸람, 염산릴마자폰, 롤메타파젬, 니메타파젬, 플루니트라제팜, 에스타졸람, 니트라제팜, 타르타르산졸피뎀, 조피클론 등을 들 수 있다. Examples of sedative and hypnotic medicines include, for example, triazolam, midazolam, bromothalam, hydrochlorothiazide, rilmazapone hydrochloride, roll metaprazim, nitmetapagem, flunitrazepam, esthazolam, nitrazepam, Clones, and the like.
항불안약으로는, 예를 들어, 플루타졸람, 클로티아제팜, 에티졸람, 알프라졸람, 로라제팜, 브로마제팜 등을 들 수 있다. Anti-anxiety drugs include, for example, flutazolam, clothiazepam, ethiazolam, alprazolam, lorazepam, and bromamphetamine.
항간질약으로는, 예를 들어, 페니토인, 에토토인, 프리미돈, 발프로산나트륨, 카르마제핀, 클로나제팜, 에토숙시미드, 트리메타디온, 술티암, 아세틸페네투라이드 등을 들 수 있다. Examples of anti-epileptic drugs include phenytoin, etotone, primidone, sodium valproate, carmajepine, clonazepam, ethosuccimide, trimethadione, sultiam, acetylpeneturide and the like .
항우울증약으로는, 예를 들어, 염산이미프라민, 염산아미트리프틸린, 염산클로미프라민, 염산노르트리프틸린, 염산로페프라민, 염산도술레핀, 아목사핀, 염산마프로틸린, 염산미안세린, 염산트라조돈, 말레산플루복사민, 염산밀나시프란 등을 들 수 있다. Examples of the antidepressant drugs include, for example, imipramine hydrochloride, amitriptyline hydrochloride, clomipramine hydrochloride, norptrythrine hydrochloride, lopepramine hydrochloride, docosapine hydrochloride, amosulfine hydrochloride, Miracenin hydrochloride, trazodone hydrochloride, fluvoxamine maleate, milnacipran hydrochloride, and the like.
항정신병약으로는, 예를 들어, 클로르프로마진, 염산티오리다진, 프로페리시아진, 플루페나진, 염산클로카프라민, 염산티아프리드 등을 들 수 있다. The antipsychotic drugs include, for example, chlorpromazine, thioridazine hydrochloride, propriacyine, fluphenazine, clocapramine hydrochloride, thiaplore hydrochloride, and the like.
정신 자극약으로는, 예를 들어, 염산메틸페니데이트, 페몰린 등을 들 수 있다. Mental stimulants include, for example, methylphenidate hydrochloride, pemoline, and the like.
강심제로는, 예를 들어, 암리논, 염산올프리논, 피모벤단 등을 들 수 있다. As a cardiotonic agent, for example, aminonone, olifrone hydrochloride, and fomobenzone may be mentioned.
β 수용체 차단약으로는, 예를 들어, 염산라베타롤, 카르베디롤, 염산아모술라롤, 염산아로티놀롤, 염산베반톨롤, 핀도롤, 염산카르테올롤, 염산부페톨롤, 염산프로프라놀롤, 나돌롤, 니프라딜롤, 염산아미오다론, 염산베탁솔롤 등을 들 수 있다. beta receptor blockers include, for example, rhamnose hydrochloride, carvedilol, amosulolol hydrochloride, arothinolol hydrochloride, bevantolol hydrochloride, fimodrol, fructooluron hydrochloride, bupitol hydrochloride, propranolol hydrochloride, Nipradolol hydrochloride, amiodarone hydrochloride, and betaxolol hydrochloride.
칼슘채널길항약으로는, 예를 들어, 염산베라파밀, 염산딜티아젬, 니페디핀, 염산니카르디핀, 닐바디핀, 염산마니디핀, 염산베프리딜 등을 들 수 있다.Examples of the calcium channel antagonist include verapamil hydrochloride, diltiazem hydrochloride, nifedipine, nicardipine hydrochloride, neilbodipine, manidipine hydrochloride, bepredil hydrochloride, and the like.
항부정맥약으로는, 예를 들어, 황산 프로카인아미드, 인산디소피라미드 등을 들 수 있다. Anti-arrhythmic drugs include, for example, sulfuric acid procainamide, diphosphoric acid phosphate, and the like.
이뇨약으로는 클로르탈리돈, 트리파미드 등을 들 수 있다. Diuretics include chlortalidone and tripamid.
강압약으로는, 예를 들어, 염산프라조신, 염산부나조신, 염산테라조신, 우라피딜, 카드랄라진 등을 들 수 있다. Examples of the depressant include prazosin hydrochloride, buccal acid hydrochloride, terazosin hydrochloride, urafidil, and cardralazine.
승압약으로는, 예를 들어, 캡토프릴, 알라세프릴, 리시노프릴, 염산이미다프릴, 말레산에날라프릴, 염산퀴나프릴, 실라자프릴, 염산델라프릴, 염산테모카프릴, 염산베나제프릴 등을 들 수 있다. Examples of the boosting agent include caprofuryl, allacril, ricinopril, iminapril hydrochloride, enalapril maleate, quinapril hydrochloride, silazapril, delapril hydrochloride, temocapril hydrochloride, And frills.
뇌순환·대사 장해용약으로는, 예를 들어, 니세르골린, 타르타르산이펜프로딜, 염산파수딜, 오자그렐나트륨 등을 들 수 있다. Examples of the brain circulatory / metabolic disorder drug include nisergoline, fenpropyl tartrate, fasudil hydrochloride, and ozagrel sodium.
진해약으로는, 예를 들어, 브롬화수소산덱스트로메토르판, 클로페라스틴, 염산포미노벤 등을 들 수 있다. Examples of the chelating agent include dextromethorphan hydrobromide, cloferastine, and pominoben hydrochloride.
거담약으로는, 예를 들어 염산브롬헥신, 염산암브록솔 등을 들 수 있다. Examples of the godad drugs include bromhexine hydrochloride, ambroxol hydrochloride, and the like.
기관지 확장약으로는, 예를 들어, 염산에페드린, 황산살부타몰, 황산테르부탈린, 염산프로카테롤 등을 들 수 있다. Examples of the bronchodilator include ephedrine hydrochloride, salbutamol sulfate, terbutaline sulfate, and procertol hydrochloride.
기관지 천식용약으로는, 예를 들어, 프로피온산베클로메타손, 프로피온산플루티카손, 부데소니드 등을 들 수 있다. Examples of bronchial asthma drugs include beclomethasone propionate, fluticasone propionate, budesonide, and the like.
호흡 촉진제로는, 예를 들어, 디모르폴라민, 염산독사프람 등을 들 수 있다. The respiratory stimulants include, for example, dimorpholamine, hydrochloric acid viperpram, and the like.
소화관용약으로는, 예를 들어, 파모티딘, 염산라니티딘, 시메티딘, 수크랄페이트, 술피리드, 테프레논, 플라우노톨, 5-아미노살리실산, 술파살라진, 오메프라졸, 란소프라졸 등을 들 수 있다. Examples of digestive tract drugs include famotidine, ranitidine hydrochloride, cimetidine, sucralfate, sulpiride, teprenone, flavolol, 5-aminosalicylic acid, sulfasalazine, omeprazole and lansoprazole.
위염용약으로는, 예를 들어, 염산메토클로프라미드, 돔페리돈, 염산이토프리드, 시트르산모사프리드, 말레산트리메부틴, 염산아자세트론, 염산온단세트론, 염산그라니세트론, 염산트로피세트론, 염산라모세트론 등을 들 수 있다. Examples of the gastritis drug include, for example, methoclofamide hydrochloride, domperidone, hydrochloric acid itopride, citric acid mothafride, maleic acid trimesbutin, azacetrone hydrochloride, ondansetron hydrochloride, , And ramosetron hydrochloride.
제토제로는, 예를 들어 메토클로프라미드, 염산라모세트론, 염산그라니세트론, 염산온단세트론, 염산아자세트론 등을 들 수 있다. Examples of the aerosol agent include methoclopramide, ramosetron hydrochloride, granisetron hydrochloride, ondansetron hydrochloride, and azasituron hydrochloride.
소화성궤양약으로는, 예를 들어 오메프라졸, 라베프라졸나트륨, 란소프라졸, 시메티딘, 니자티딘, 파모티딘, 염산라니티딘, 염산록사딘아세테이트, 수크랄페이트 등을 들 수 있다. Examples of peptic ulcer drugs include omeprazole, rabeprazole sodium, lansoprazole, cimetidine, nizatidine, famotidine, ranitidine hydrochloride, roxadine hydrochloride acetate, sucralfate and the like.
지사약·정장약·장질환용약으로는, 예를 들어 염산로페라미드, 메살라진, 베타메타손 등을 들 수 있다. Examples of the medicines for the branch, the rectal, and intestinal diseases include ferric amide hydrochloride, mesalazine, betamethasone, and the like.
지하제 (하제) 로는, 예를 들어 비사코딜 등을 들 수 있다. As an underground agent (laxative agent), for example, bisacodyl and the like can be mentioned.
이담제로는, 예를 들어 디하이드로콜산, 트레피부톤 등을 들 수 있다. Examples of the dyestuff include dihydrocholic acid, tretachin, and the like.
파킨슨병약으로는, 예를 들어 레보도파, 레포도파, 염산아만타딘, 염산트리헥시페니딜, 염산피로헵틴 등을 들 수 있다. Examples of the Parkinson's disease include levodopa, lepodopa, amantadine hydrochloride, trihexyphenidyl hydrochloride, pyroheptin hydrochloride, and the like.
골다공증용제로는, 예를 들어 이프리플라본 등을 들 수 있다. Examples of the agent for osteoporosis include ipriflavone.
항류머티즘약으로는, 예를 들어 메토트렉세이트, 부시라민, 악타리트 등을 들 수 있다. Examples of antirheumatic drugs include methotrexate, bushiramine, and actarit.
이하에, 본 발명의 건식 직타 속붕괴성 정제의 상세함을, 유효 성분으로써 예를 들어, 타르타르산졸피뎀 또는 멜록시캄을 대표예로 하여 설명해 간다. Hereinafter, the details of the dry-type disintegrating tablet of the present invention will be described as a representative example of the active ingredient, for example, zolpidem tartrate or meloxicam.
타르타르산졸피뎀은 백색의 결정성의 분말로 냄새는 없고, 맛은 쓰고, 물 또는 에탄올 (95%) 에 다소 잘 녹지 않는 것이다. 이것은 광에 의해 서서히 착색 (황색) 되는 성질을 갖고, 임상적으로는 불면증 (통합 실조증 및 조울증에 따르는 불면증은 제외한다) 에 사용되고 있는 약물이다. 투여량으로는, 통상적으로 성인에게는 타르타르산졸피뎀으로서 1 회 5 ∼ 10㎎ 을 취침 직전에 경구 투여한다. 또한, 고령자에게는 1 회 5㎎부터 투여를 개시하여, 연령, 증상, 질환에 따라 적절히 증감할 수 있지만, 1 일 10㎎ 을 초과하지 않는 것으로 되어 있다. Tartaric acid zolpidem is a white crystalline powder with no odor, taste, and slightly soluble in water or ethanol (95%). It is a drug that has the property of gradually coloring (yellow) by light, clinically used for insomnia (except for insomnia according to integrated ataxia and manic depression). As a dose, usually 5 to 10 mg of tartrate tablets are administered orally to an adult just before bed. In addition, the elderly are started to administer the medicament at a dose of 5 mg once per day, and can be appropriately increased or decreased according to age, symptoms, or disease, but do not exceed 10 mg per day.
본 발명의 건식 직타 속붕괴성 정제에 사용하는 타르타르산졸피뎀의 의약 원체의 입자직경은 작을수록 그 취급이 어렵지만 용출은 빨라진다. 따라서, 정제로 했을 경우의 용해성이 향상될 것을 고려하여, 적절한 입경의 것을 사용할 수 있고, 바람직하게는, 평균 입자직경이 100㎛ 이하인 것을 사용하는 것이 좋다. The smaller the particle diameter of the drug substance used in the dry-type disintegrating tablet of the present invention, the more difficult it is to handle, but the faster the dissolution. Therefore, in consideration of improvement in solubility in the case of tablets, it is possible to use a powder having an appropriate particle size, and preferably an average particle diameter of 100 탆 or less.
또, 멜록시캄은 관절 류머티즘, 변형성 관절증, 요통증, 견관절주위염, 경견완증후군의 치료에 사용되는 비스테로이드성 소염·진통약이며, 임상적으로 1 회 10㎎/일의 양으로 경구적으로 투여되는 약물이다. Meloxicam is a non-steroidal anti-inflammatory and analgesic drug used for the treatment of arthritic rheumatism, deformity arthropathy, urinary incontinence, shoulder joint inflammation, and cervicitis syndrome. It is clinically administered orally at a dose of 10 mg / .
본 발명의 건식 직타 속붕괴성 정제에 사용하는 멜록시캄의 의약 원체의 입자직경은 작을수록 그 취급이 어렵지만 용출은 빨라진다. 따라서, 정제로 했을 경우의 용해성이 향상될 것을 고려하여, 적절한 입경의 것을 사용할 수 있고, 바람직하게는, 평균 입자직경 11㎛ 이하이며, 보다 바람직하게는 평균 입자직경이 1 ∼ 11㎛, 특히 바람직하게는 평균 입자직경이 6 ∼ 11㎛ 인 것을 사용하는 것이 좋다. The smaller the particle diameter of the medicinal drug of meloxicam used in the dry-type disintegrating tablet of the present invention, the more difficult it is to handle, but the faster the dissolution. Therefore, in consideration of the improvement in solubility in the case of tablets, an appropriate particle diameter can be used, and preferably an average particle diameter of 11 mu m or less, more preferably an average particle diameter of 1 to 11 mu m, , It is preferable to use one having an average particle diameter of 6 to 11 mu m.
이 타르타르산졸피뎀 또는 멜록시캄을 대표예로 하는 약물과 함께 사용되는 부형제로는, 유당, 에리트리톨, D-만니톨, 자일리톨, 멀티톨 등의 당류, 히드록시프로필스타치나트륨, 결정 셀룰로오스, 히드록시프로필스타치, 무수 인산수소칼슘, 합성 규산알루미늄, 환원 맥아당 물엿 등을 들 수 있다. Examples of the excipient to be used in combination with the drug exemplified by zolpidem tartrate or meloxicam include sugars such as lactose, erythritol, D-mannitol, xylitol and multitol, sodium hydroxypropyl starch, crystalline cellulose, Hydroxypropyl starch, anhydrous calcium hydrogen phosphate, synthetic aluminum silicate, reduced maltose syrup, and the like.
배합하는 부형제는 최종 정제의 중량을 기준으로 하여 20 ∼ 70 중량%, 바람직하게는 30 ∼ 70 중량% 이며, 보다 바람직하게는 약 60 중량% 인 것이 좋다. The excipient to be incorporated is 20 to 70% by weight, preferably 30 to 70% by weight, more preferably about 60% by weight, based on the weight of the final tablet.
붕괴제로는, 크로스포비돈, 카르멜로오스, 카르멜로오스칼슘, 카르복시메틸스타치나트륨으로 이루어지는 군에서 선택되는 1 종 이상을 들 수 있다. 바람직하게는, 크로스포비돈, 카르멜로오스의 병용이다. Examples of the disintegrator include at least one selected from the group consisting of crospovidone, carmellose, carmellose calcium, and carboxymethylstarch sodium. Preferably, the combination of crospovidone and carmellose is used.
붕괴제의 배합량은 최종 정제의 중량을 기준으로 하여 5 ∼ 20 중량% 이며, 바람직하게는 약 15 중량% 인 것이 좋다. The blending amount of the disintegrant is 5 to 20% by weight, preferably about 15% by weight, based on the weight of the final tablet.
유동화제로는, 경질 무수 규산 (이산화규소) 등의 무수 규산류를 들 수 있다. 바람직하게는, 아드솔리더 101 [상품명, 프로인트 산업 (주) 제조] 을 들 수 있다. 유동화제의 배합량은 최종 정제의 중량을 기준으로 하여 0.5 ∼ 3 중량% 이며, 바람직하게는 약 0.5 ∼ 1.5 중량% 인 것이 좋다. Examples of the fluidizing agent include anhydrous silicic acid such as light anhydrous silicic acid (silicon dioxide). Adsorsole 101 (trade name, manufactured by Freight Industries Co., Ltd.) is preferably used. The blending amount of the fluidizing agent is 0.5 to 3% by weight, preferably about 0.5 to 1.5% by weight based on the weight of the final tablet.
본 발명이 제공하는 속붕괴성 정제에 있어서, 활택제로는 스테아르산마그네슘 및 자당 지방산 에스테르, 예를 들어, 슈가에스테르 B-370F, 혹은 사프 호프 J-2203F [자당 베헨산에스테르를 활택제용으로 하여 B-370 을 미분쇄한 것 ; 미츠비시 화학 푸즈 (주) 제조] 의 양자를 병용하여 사용하는 것이 바람직하다. In the fast disintegrating tablet provided by the present invention, as the lubricant, magnesium stearate and sucrose fatty acid esters such as sucroester B-370F, or SAFFOFF J-2203F [sucrose behenic acid ester as a lubricant and B Finely ground -370; (Manufactured by Mitsubishi Chemical Corporation) are preferably used in combination.
스테아르산마그네슘 및 자당 지방산 에스테르의 배합비는 중량비로 1:1 ∼ 3 정도, 바람직하게는 1:1 ∼ 2 정도인 것이 좋다. The blending ratio of magnesium stearate and sucrose fatty acid ester is preferably about 1: 1 to 3, and more preferably about 1: 1 to 2, by weight.
또, 활택제의 배합량은, 최종 정제의 중량을 기준으로 하여 1.0 ∼ 3 중량%, 바람직하게는 약 1.0 ∼ 2.0 중량% 이다. The blending amount of the lubricant is 1.0 to 3% by weight, preferably about 1.0 to 2.0% by weight based on the weight of the final tablet.
또한, 유효 성분이 쓴맛을 갖는 경우에는, 통상적인 방법에 따라, 이러한 쓴맛을 마스킹하는 마스킹제를 배합할 수 있다. 그러한 마스킹제로는, 아스파르템, 타우마틴 등의 감미제, 혹은 1-멘톨, 드라이 코트 바닐라, 흑당 플레이버, 드라이 코트 페퍼민트, 그레이프후르츠 코트 등의 향료를 들 수 있다. 바람직하게는 아스파르템이다. When the active ingredient has a bitter taste, a masking agent capable of masking such a bitter taste can be formulated according to a conventional method. Examples of such masking agents include sweeteners such as aspartame and tauromine, and flavoring agents such as 1-menthol, dry-coat vanilla, black sugar flavor, dry coat peppermint and grapefruit coat. It is preferably an aspartame.
이들 마스킹제의 배합량은 함유시키는 유효 성분에 따라, 그 사용량을 적절히 증감할 수 있다. The blending amount of these masking agents can be appropriately increased or decreased depending on the active ingredient to be contained.
착색제로는, 황색3이산화철, 3이산화철, 흑산화철 (혹은 산화철류), 알루미늄킬레이트제를 들 수 있다. Examples of the colorant include yellow 3 iron dioxide, 3 iron dioxide, black iron oxide (or iron oxide), and aluminum chelating agent.
본 발명이 제공하는 건식 직타 속붕괴성 정제는 예를 들어, 이하의 공정에 의한 제조 방법으로 조제할 수 있다. The dry-type disintegrating tablet provided by the present invention can be prepared, for example, by the following process.
이러한 방법은 개략, 먼저 교미제와 결합제로 이루어지는 조립물을 조제하는 제 1 공정, 각 성분을 혼합하는 제 2 공정, 이어서 타정하는 제 3 공정의 3 공정으로 이루어지고, 각 공정 자체는 통상적인 방법에 따라 실시할 수 있는 간편하고 효율적인 정제의 조제 방법이다. This method roughly comprises a first step of preparing a granule composed of a mating agent and a binder, a second step of mixing the respective components, and a third step of subsequent sequencing, and each step itself is carried out by a conventional method , Which is a simple and efficient method for preparing tablets.
그 상세한 것에 대하여 서술하면 이하와 같이 된다. The details will be described below.
[제 1 공정] [First Step]
미리, 부형제 (예를 들어, 분말 환원 맥아당 물엿) 의 수용액을 조제하고, 교미제 (예를 들어, 에리트리톨) 와 결합제 (예를 들어, 결정 셀룰로오스) 를 혼합하고, 유동층 조립기를 사용하여 조립함으로써 조립물을 얻는다. 상기의 부형제의 수용액의 농도는 사용하는 교미제의 종류, 사용량 등에 따라, 또 사용하는 결합제의 종류, 사용량 등에 따라 상이하고, 특별히 제한되지 않지만 바람직하게는 10 ∼ 20%, 보다 바람직하지는 15% 부근이다. (For example, erythritol) and a binder (for example, crystalline cellulose) are mixed in advance and assembled using a fluidized bed granulator to prepare an aqueous solution of an excipient (e.g., powdered maltose syrup) Obtain the assembly. The concentration of the aqueous solution of the excipient varies depending on the type and amount of the used mating agent to be used, the type and amount of the binder to be used, and the like, and is not particularly limited, but is preferably about 10 to 20%, more preferably about 15% to be.
부형제와 결합제의 배합비는 특별히 한정되지 않지만, 바람직하게는 교미제의 1 중량당, 결합제의 양이 0.15 ∼ 3.2 의 범위이다. 결합제의 양이 많아질수록, 유동성은 개선되지만, 붕괴성이 저하된다. 또, 교미제의 배합비가 많아지면 유동성이 저하되는 경향이 보였다. The mixing ratio of the excipient and the binder is not particularly limited, but the amount of the binder is preferably in the range of 0.15 to 3.2 per 1 weight of the mating agent. The greater the amount of binder, the better the fluidity, but the lower the collapsibility. In addition, when the compounding ratio of the mating agent increased, the fluidity tended to decrease.
[제 2 공정] [Second Step]
상기 제 1 공정에서 얻어진 조립물과, 유효 성분 (예를 들어, 타르타르산졸피뎀 또는 멜록시캄), 부형제 (예를 들어, 유당), 붕괴제 (예를 들어, 크로스포비돈, 카르멜로오스), 유동화제 (예를 들어, 경질 무수 규산), 활택제 (예를 들어, 스테아르산마그네슘, 자당 지방산 에스테르), 향료 (예를 들어, 1-멘톨), 착색제 (예를 들어, 황색3이산화철, 알루미늄킬레이트제) 를 혼합하고, 분체 혼합물을 얻는다. (For example, lactose), a disintegrant (for example, crospovidone, carmellose), a disintegrant (for example, (E.g., magnesium stearate, sucrose fatty acid esters), perfumes (e.g., 1-menthol), colorants (e.g., yellow 3 iron dioxide, Aluminum chelating agent) are mixed to obtain a powder mixture.
이 제 2 공정의 혼합은 소정량의 각 성분, 유효 성분을 통상적인 방법에 따라, 예를 들어, 혼합기 [상품명, 보레콘테이너믹서 ; 코토부키 기술 연구소 공업 (주) 제조] 를 사용하여 혼합함으로써 실시할 수 있다. 이 혼합 시간은 사용하는 첨가제의 종류, 사용량 등에 따라 상이하고 특별히 한정되는 것은 아니지만, 바람직하게는 5 ∼ 40 분간, 보다 바람직하게는 5 ∼ 30 분간 혼합한다. The mixing of the second step is carried out by mixing a predetermined amount of each component and the active ingredient in accordance with a conventional method, for example, in a mixer (trade name: Vore Container Mixer; (Manufactured by Kotobuki Kogyo Kagaku Kogyo Co., Ltd.). The mixing time varies depending on the type and amount of the additive to be used, and is not particularly limited, but is preferably 5 to 40 minutes, and more preferably 5 to 30 minutes.
또한, 활택제에 대해서는 상기 혼합물에 후에 첨가하여 혼합할 수도 있다. 이 경우의 혼합 시간은 활택제가 충분히 혼합될 수 있는 시간이면 되고, 상기 혼합물의 사용량 등에 따라 특별히 한정되는 것은 아니지만, 통상적으로 2 ∼ 10 분간, 바람직하게는 2 ∼ 4 분간이다. Further, the lubricant may be added to the mixture after mixing. In this case, the mixing time is not particularly limited depending on the amount of the mixture to be used, and is usually 2 to 10 minutes, preferably 2 to 4 minutes.
[제 3 공정] [Third Step]
이렇게 하여 제조된 상기의 제 2 공정에서 얻어진 분체 혼합물을 사용하여, 직접 타정함으로써, 목적으로 하는 본 발명의 속붕괴성 정제를 얻을 수 있다. The desired disintegrating tablet of the present invention can be obtained by direct tableting using the powder mixture obtained in the second step thus produced.
본 발명이 제공하는 속붕괴성 정제에 사용하는 향료는 상기 제 1 공정부터 제 2 공정까지의 어디에나 첨가할 수 있지만, 바람직하게는 제 2 공정에서 첨가하는 것이 좋다. The fragrance to be used in the fast disintegrating tablet provided by the present invention can be added anywhere from the first step to the second step, but is preferably added in the second step.
또, 본 발명의 정제에, 원하는 바에 따라 추가로 아스파르템 등의 통상적으로 사용되는 감미제, 용해 보조제 (예를 들어 시트르산나트륨, 탄산수소나트륨) 를 첨가할 수 있지만, 상기 제 1 공정부터 제 2 공정의 어디에나 첨가할 수 있다. To the tablets of the present invention, conventionally used sweetening agents and solubilizing agents such as sodium citrate, sodium hydrogen carbonate, etc., such as aspartame, may be further added as desired. However, It can be added anywhere in the process.
이상에 의해, 본 발명이 목적으로 하는 건식 직타 속붕괴성 정제가 제공되지만, 얻어진 정제는 원하는 속붕괴성을 유지하면서, 실용적인 정제의 경도를 갖는 것이다. Although the present invention provides the disintegrating tablets of the dry type in the present invention, the tablets obtained have practical tablet hardness while maintaining the desired decidual disintegration property.
또한, 정제의 형태로는, 특별히 제한은 없고, 통상적인 방법에 따라, 예를 들어, 원하는 직경을 갖는 할선을 넣은 혈구형 원형 나정 등의 속붕괴성 정제를 간편하게 조제할 수 있다 There are no particular restrictions on the form of the tablet, and it is possible to easily prepare, for example, a rapidly disintegrating tablet such as a hemocyte-shaped tablet liner with a cuticle having a desired diameter according to a conventional method
이하에, 실시예를 들어 본 발명을 상세하게 설명하지만, 이들은 본 발명을 한정하는 것은 아니다. Hereinafter, the present invention will be described in detail with reference to Examples, but the present invention is not limited thereto.
실시예 1 ∼ 8 :Examples 1 to 8:
하기 표 1 에 기재된 배합 (배합량 :g) 에 의해, 상기한 각 공정에 준하여 조립, 혼합하고, 목적으로 하는 정제의 경도를 설정하여, 분체 혼합물을 타정함으로써 타르타르산졸피뎀이 함유된 속붕괴성 정제를 얻었다. The tablets were granulated and mixed according to the above-mentioned respective steps according to the compounding amount (g) shown in the following Table 1, and the hardness of the intended tablet was set. The powder mixture was tableted to obtain a disintegrating tablet containing tartaric acid zofetil .
얻어진 정제에 대해, 정제의 경도, 일본 약국방의 붕괴 시험법에 의한 붕괴 시간 (초), 마손도 시험 200 회전에서의 마손도 (%) 를 측정하였다. The hardness of the tablets, the disintegration time (second) according to the Japanese Pharmacopoeia collapse test method, and the degree of abrasion (%) at 200 rounds of the abrasion test were measured for the obtained tablets.
또, 구강 내의 붕괴 시간 (초) 을 측정하였다. In addition, the collapse time (seconds) in the oral cavity was measured.
그 결과를 함께 표 1 중에 나타냈다. The results are shown in Table 1.
대표적인 정제의 제조 조작예를 실시예 6 의 배합 처방으로 나타낸다. A representative example of the preparation of tablets is shown in the formulation of Example 6.
[공정 1] [Step 1]
에리트리톨 [교미제, 미분, 닛켄 화성 (주) 제조] 95.0g, 결정 셀룰로오스 [결합제, 세오라스 PH-101, 아사히 화성 케미컬즈 (주) 제조] 30.0g 의 혼합 분체를 유동층 조립기 [상품명 MP-01 ; (주) 파우레크 제조] 를 사용하고, 미리 분말 환원 맥아당 물엿 [부형제, 아말티, 토와 화성 공업 (주) 제조] 을 정제수에 용해시켜 얻은 15% 수용액을 사용하여 조립함으로써 조립물을 얻었다. 95.0 g of erythritol (trade name, fine powder, manufactured by Nikkiso Co., Ltd.) and 30.0 g of crystalline cellulose (binder, Seoras PH-101, manufactured by Asahi Kasei Chemicals Corporation) were placed in a fluidized bed granulator 01; (Manufactured by Powrex Co., Ltd.) was used and assembled using a 15% aqueous solution obtained by previously dissolving powdered maltose syrup syrup (excipient, manufactured by Amalti, Toowar Chemical Industries, Ltd.) in purified water to obtain a granulation product.
상기 제법에서 얻어진 조립물의 분석치는 이하와 같았다. The analytical values of the granules obtained by the above production method were as follows.
안식각 (˚) 51.5 ; 비용적 (루즈) 2.45㎖/g ; 비용적 (탭) 2.27㎖/g ; 수분 (%) 0.6 ; 평균 입자직경 (㎛) 88.75 Angle of repose (˚) 51.5; Cost (loose) 2.45 ml / g; Cost (tab) 2.27 ml / g; Moisture (%) 0.6; Average particle diameter (占 퐉) 88.75
[공정 2] [Step 2]
상기 조립물과 타르타르산졸피뎀 (유효 성분) 5.0g, 유당 (부형제) 105.3g, 크로스포비돈 (붕괴제, 크로스포비돈 XL, ISP 제조) 33.0g, 카르멜로오스 [붕괴제, NS-300, 고토쿠 약품 (주) 제조] 12.0g, 경질 무수 규산 [유동화제, 프로인트 산업 (주) 제조] 3.90g, 스테아르산마그네슘 (활택제) 1.50g, 자당 지방산 에스테르 [활택제, 슈가에스테르 B-370F, 미츠비시 화성 푸즈 (주) 제조] 3.0g, 아스파르템 [감미제, 아스파르템, 아지노모토 (주) 제조] 6.00g, 1-멘톨 [향료, 코바야시 케이 (주) 제조] 0.15g, 황색3이산화철 [착색제, 아오미 화성 (주) 제조] 0.15g 을 첨가하고, 3분간 혼합하였다. 5.0 g of the above granule, zofetil tartrate (active ingredient), 105.3 g of lactose (excipient), 33.0 g of crospovidone (disintegrant, crospovidone XL, ISP), carmelose [disintegrant, NS- (Liquid lubricant, manufactured by Freight Industries, Ltd.), 1.50 g of magnesium stearate (lubricant), 12.0 g of sucrose fatty acid ester (lubricant, sucroester B-370F, 3.0 g of aspartame [sweetener, aspartame, manufactured by Ajinomoto Co., Ltd.], 0.15 g of 1-menthol (perfume, manufactured by Kobayashi K.K.), 3 yellow iron oxide (Manufactured by Aomi Chemical Industry Co., Ltd.) was added and mixed for 3 minutes.
상기 혼합법으로 얻어진 분체 혼합물의 분석치는 이하와 같았다. The analytical values of the powder mixture obtained by the above mixing method were as follows.
안식각 (˚) 39.0 ; 비용적 (루즈) 2.45㎖/g ; 비용적 (탭) 1.86㎖/g ; 압축비 (%) 24.1 ; 수분(%) 0.8 Angle of repose (˚) 39.0; Cost (loose) 2.45 ml / g; Cost (taps) 1.86 ml / g; Compression ratio (%) 24.1; Moisture (%) 0.8
[공정 3] [Step 3]
상기 공정 2 에서 얻어진 분체 혼합물을 사용하고, 설정 경도 5kp 로 타정함으로써 건식 직타 속붕괴성 정제를 얻었다 (유효 성분을 5㎎ 함유하는 300㎎ 정). The powder mixture obtained in the above Step 2 was used and tableted at a setting hardness of 5 kp to obtain a dry type tablet disintegrating tablet (300 mg tablets containing 5 mg of the active ingredient).
상기 각 실시예에 있어서, 향료로서 1-멘톨을 첨가하여 정제를 조제한 것은 불쾌한 쓴맛이 완화되었다. In each of the above Examples, 1-menthol was added as a perfume to prepare tablets, which resulted in less unpleasant bitter taste.
정제의 직경은 통상적으로 약 5㎜ ∼ 약 20㎜, 바람직하게는 약 7㎜ ∼ 약 15㎜ 의 사이로, 복용에 적절한 크기를 선택할 수 있다. The diameter of the tablet is typically between about 5 mm and about 20 mm, preferably between about 7 mm and about 15 mm, and a size suitable for dosing can be selected.
실시예 9 :Example 9:
에리트리톨 [교미제, 미분, 닛켄 화성 (주) 제조] 107.5g, 결정 셀룰로오스 [결합제, 세오라스 PH-101, 아사히 화성 케미컬즈 (주) 제조] 17.5g 의 혼합 분체를 유동층 조립기 [상품명 MP-01 ; (주) 파우레크 제조] 를 사용하고, 미리 분말 환원 맥아당 물엿 [부형제, 아말티, 토와 화성 공업 (주) 제조] 을 정제수에 용해시켜 얻은 15% 수용액을 사용하여 조립함으로써 조립물을 얻었다. 107.5 g of erythritol (microcrystalline powder, fine powder, manufactured by Nikkiso Co., Ltd.) and 17.5 g of crystalline cellulose (binder, SEORAS PH-101, manufactured by Asahi Chemical Industry Co., Ltd.) 01; (Manufactured by Powrex Co., Ltd.) was used and assembled using a 15% aqueous solution obtained by previously dissolving powdered maltose syrup syrup (excipient, manufactured by Amalti, Toowar Chemical Industries, Ltd.) in purified water to obtain a granulation product.
상기에서 얻어진 조립물은 실시예 1 의 공정 1 에서 얻어진 것과 동등한 성질을 나타냈다.The granules thus obtained exhibited properties equivalent to those obtained in Step 1 of Example 1. [
실시예 10 :Example 10:
에리트리톨 [교미제, 미분, 닛켄 화성 (주) 제조] 30.0g, 결정 셀룰로오스[결합제, 세오라스 PH-101, 아사히 화성 케미컬즈 (주) 제조] 95.0g 의 혼합 분체를 유동층 조립기 [상품명 MP-01 ; (주) 파우레크 제조] 를 사용하고, 미리 분말 환원 맥아당 물엿 [부형제, 아말티, 토와 화성 공업 (주) 제조] 을 정제수에 용해 시켜 얻은 15% 수용액을 사용하여 조립함으로써 조립물을 얻었다. 30.0 g of erythritol (microcrystalline powder, fine powder, manufactured by Nikkiso Co., Ltd.) and 95.0 g of crystalline cellulose (binder, Seoras PH-101, manufactured by Asahi Chemical Industry Co., Ltd.) 01; (Manufactured by Powrex Co., Ltd.) was used and assembled using a 15% aqueous solution obtained by previously dissolving powdered maltose syrup syrup (excipient, manufactured by Amalti, Toowar Chemical Industries, Ltd.) in purified water to obtain a granulation product.
상기에서 얻어진 조립물은 실시예 1 의 공정 1 에서 얻은 것과 동등한 물성 치를 나타냈다. The granules thus obtained exhibited the same physical properties as those obtained in Step 1 of Example 1.
비교예 1 :Comparative Example 1:
하기의 각 성분을 통상적인 방법에 따라, 혼합하고, 직타함으로써 건식 직타 속붕괴성 정제의 조제를 시도하였다. Each of the following components was mixed according to a conventional method, and an attempt was made to prepare a dry-type collapsible tablet by grinding.
배합 목적 성분명 중량 (g) Compounding purpose Ingredient name Weight (g)
유효 성분 타르타르산졸피뎀 5.00Active ingredient Tartaric acid zolpidem 5.00
부형제 유당 105.60 Excipient lactose 105.60
결합제 결정 셀룰로오스 30.00Binder Crystalline Cellulose 30.00
교미제 에리트리톨 100.00Mating agent Erythritol 100.00
붕괴제 크로스포비돈 45.00 Collapse Crospovidone 45.00
유동화제 경질 무수 규산 3.90Fluidizer Light Silicic anhydride 3.90
교미제 아스파르템 6.00Mating agent Aspartame 6.00
활택제 자당 지방산 에스테르 3.00 Glutathione Sucrose Fatty Acid Esters 3.00
활택제 스테아르산마그네슘 1.50Magnesium stearate 1.50
나정 (합계) 300.00 No (total) 300.00
상기의 각 배합 성분의 혼합물의 시험 분석치 (수분, 비용적, 안식각) 를 이하에 나타낸다. Test analytical values (moisture, cost, and angle of repose) of the mixture of each of the above ingredients are shown below.
안식각 (˚) 39.5˚ ; 비용적 (루즈) 2.03㎖/g ; 비용적 (탭) 1.47㎖/g ; 압축비 (%) 27.6 ; Carr 의 지수 (%) 38.1 ; 수분 (%) 1.0 Angle of repose (˚) 39.5˚; Cost (loose) 2.03 ml / g; Cost (taps) 1.47 ml / g; Compression ratio (%) 27.6; Carr's index (%) 38.1; Moisture (%) 1.0
결과적으로, 얻어진 혼합물의 유동성이 불량이어서, 타정 효율이 저하되었다. As a result, the fluidity of the obtained mixture was poor, and the tableting efficiency was lowered.
비교예 2 :Comparative Example 2:
상기 비교예 1 의 조제법에 있어서, 활택제 (자당 지방산 에스테르와 스테아르산마그네슘) 를 탤크 (활택제·유동화제) 로 바꿔 혼합물을 조제하고, 타정을 시도하였다. In the preparation method of Comparative Example 1, the lubricant (sucrose fatty acid ester and magnesium stearate) was changed to talc (lubricant / fluidizing agent) to prepare a mixture, and the tablet was tried.
배합 목적 성분명 중량 (g) Compounding purpose Ingredient name Weight (g)
유효 성분 타르타르산졸피뎀 5.00Active ingredient Tartaric acid zolpidem 5.00
부형제 유당 100.10 Excipient lactose 100.10
결합제 결정 셀룰로오스 30.00Binder Crystalline Cellulose 30.00
교미제 에리트리톨 95.00Mating agent Erythritol 95.00
붕괴제 크로스포비돈 45.00 Collapse Crospovidone 45.00
유동화제 경질무수 규산 3.90Fluidizer Light Silicic anhydride 3.90
교미제 아스파르템 6.00Mating agent Aspartame 6.00
유동화·활택제 탤크 15.00Securitization · Lubricant talc 15.00
나정 (합계) 300.00 No (total) 300.00
상기 각 배합 성분의 혼합물의 시험 분석치 (수분, 비용적, 안식각) 를 이하에 나타낸다. 안식각 (˚) 45.5˚ ; 비용적 (루즈) 1.94㎖/g ; 비용적 (탭) 1.36㎖/g ; 압축비 (%) 29.9 ; Carr 의 지수 (%) 42.6 ; 수분 (%) 0.8 Test analytical values (moisture, cost, and angle of repose) of the mixture of the respective ingredients are shown below. Angle of repose (˚) 45.5˚; Cost (loose) 1.94 ml / g; Cost (taps) 1.36 ml / g; Compression ratio (%) 29.9; Carr's index (%) 42.6; Moisture (%) 0.8
결과적으로, 얻어진 혼합물의 유동성은 불량이어서, 타정 효율이 저하되었다. As a result, the fluidity of the obtained mixture was poor, and the tableting efficiency was lowered.
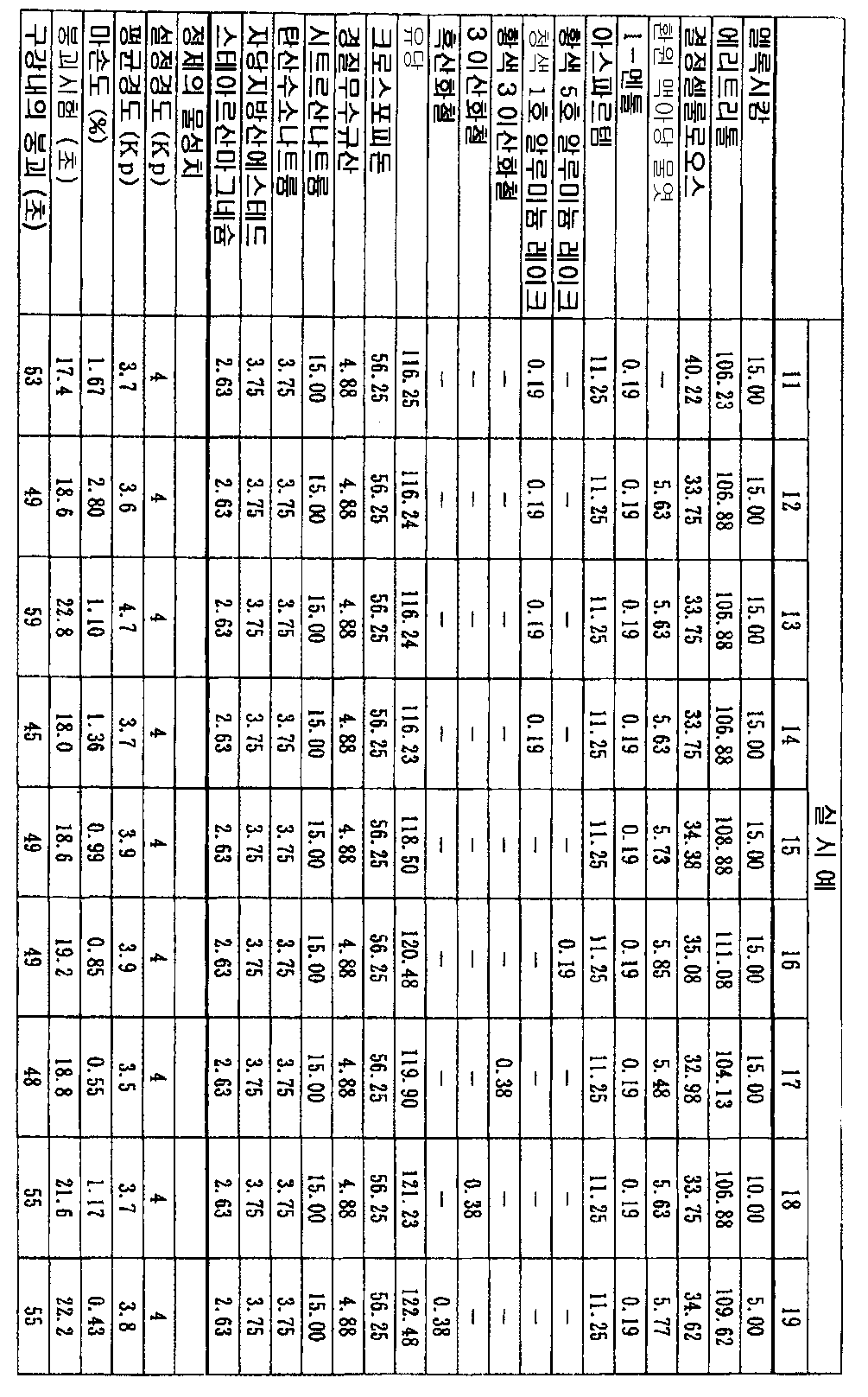
실시예 11 ∼19 :Examples 11-19:
하기 표 2 에 기재된 배합 (배합량 : g) 에 의해, 상기한 각 공정에 준하여 조립, 혼합하고, 목적으로 하는 정제의 경도를 설정하여 분체 혼합물을 타정함으로써 멜록시캄이 함유된 속붕괴성 정제를 얻었다. Granulated tablets containing meloxicam were prepared by mixing and mixing according to the respective steps described above according to the blend (mixing amount: g) shown in Table 2 below, and setting the hardness of the tablets to be desired, .
얻어진 정제에 대해, 정제의 경도, 일본 약국방의 붕괴 시험법에 의한 붕괴 시간 (초), 마손도 시험 200 회전에서의 마손도를 측정하였다. The hardness of the tablets, the disintegration time (second) according to the Japanese Pharmacopoeia collapse test method, and the degree of abrasion at 200 revolutions of the abrasion test were measured for the obtained tablets.
또, 구강 내의 붕괴 시간 (초) 을 측정하였다. In addition, the collapse time (seconds) in the oral cavity was measured.
그 결과를 함께 표 2 중에 나타냈다. The results are shown in Table 2.
대표적인 정제의 제조 조작법을 실시예 18 에 준거한 배합 처방으로 나타낸다. Representative tablet preparation operations are shown in the formulation according to Example 18.
[공정 1][Step 1]
에리트리톨 [교미제, 미분, 닛켄 화성 (주) 제조] 95.0g, 결정 셀룰로오스 [결합제, 세오라스 PH-101, 아사히 화성 케미컬즈 (주) 제조] 30.0g 의 혼합 분체를 유동층 조립기 [상품명 MP-01 ; (주) 파우레크 제조] 를 사용하고, 미리 분말 환원 맥아당 물엿 [부형제, 아말티, 토와 화성 공업 (주) 제조] 을 정제수에 용해시켜 얻은 15% 수용액을 사용하여 조립함으로써 조립물을 얻었다. 95.0 g of erythritol (trade name, fine powder, manufactured by Nikkiso Co., Ltd.) and 30.0 g of crystalline cellulose (binder, Seoras PH-101, manufactured by Asahi Kasei Chemicals Corporation) were placed in a fluidized bed granulator 01; (Manufactured by Powrex Co., Ltd.) was used and assembled using a 15% aqueous solution obtained by previously dissolving powdered maltose syrup syrup (excipient, manufactured by Amalti, Toowar Chemical Industries, Ltd.) in purified water to obtain a granulation product.
상기 제법으로 얻어진 조립물의 분석치는 이하와 같았다. The analytical values of the granules obtained by the above production method were as follows.
안식각 (˚) 51.5 ; 비용적 (루즈) 2.45㎖/g ; 비용적 (탭) 2.27㎖/g ; 수분 (%) 0.6 ; 평균 입자직경 (㎛) 88.75 Angle of repose (˚) 51.5; Cost (loose) 2.45 ml / g; Cost (tab) 2.27 ml / g; Moisture (%) 0.6; Average particle diameter (占 퐉) 88.75
[공정 2] [Step 2]
상기 조립물과 멜록시캄 (유효 성분, 입자직경 약 8㎛) 13.33g, 유당 (부형제) 161.64g, 크로스포비돈 (붕괴제, 크로스포비돈 XL, ISP 제조) 75.00g, 시트르산나트륨 [용해 보조제, 코마츠야 화학 (주) 제조], 탄산수소나트륨 [용해 보조제, 아사히 화성 케미컬즈 (주) 제조], 경질 무수 규산 [유동화제, 프로인트 산업 (주) 제조] 6.51g, 스테아르산마그네슘 (활택제) 3.51g, 자당 지방산 에스테르 [활택제, 사프 호프 J2203-F, 미츠비시 화성 푸즈 (주) 제조] 5.00g, 아스파르템 [감미제, 아스파르템, 아지노모토 (주) 제조] 15.00g, 1-멘톨 [향료, 코바야시케이 (주) 제조] 0.25g, 3이산화철 [착색제, 아오미 화성 (주) 제조] 0.51g 을 첨가하고, 30 분간 혼합하였다. The above granulated product was mixed with 13.33 g meloxicam (active ingredient, particle diameter about 8 탆), 161.64 g lactose (excipient), 75.00 g crospovidone (disintegrant, crospovidone XL, ISP), sodium citrate 6.51 g of light silicic anhydride (fluidizing agent, manufactured by Freight Industries, Ltd.), magnesium stearate (lubricant), sodium hydrogen carbonate (solubility aiding agent, manufactured by Asahi Chemical Industry Co., Ltd.) 5.00 g of sucrose fatty acid ester (liquid lubricant, SAHOPH J2203-F, manufactured by Mitsubishi Foods Corporation), 15.00 g of aspartame [sweetener, aspartame, manufactured by Ajinomoto Co., 0.25 g of ferric oxide (manufactured by Kobayashi K.K.), and 0.51 g of ferric oxide (coloring agent, manufactured by Aomi Kasei Kogyo Co., Ltd.) were added and mixed for 30 minutes.
상기 혼합법으로 얻어진 분체 혼합물의 분석치는 이하와 같았다. The analytical values of the powder mixture obtained by the above mixing method were as follows.
안식각 (˚) 37.5 ; 비용적 (루즈) 2.01㎖/g ; 비용적 (탭) 1.61㎖/g ; 압축비 (%) 24.96 ; 수분 (%) 0.8 Angle of repose (˚) 37.5; Cost (loose) 2.01 ml / g; Cost (taps) 1.61 ml / g; Compression ratio (%) 24.96; Moisture (%) 0.8
[공정 3] [Step 3]
상기 공정 2 에서 얻어진 분체 혼합물을 사용하여 설정 경도 4kp 로 타정함으로써 건식 직타 속붕괴성 정제를 얻었다 (유효 성분을 10㎎ 함유하는 375㎎ 정). Using the powder mixture obtained in the above step 2, the tablets were tableted at a set hardness of 4 kp to obtain a dry, directly disintegrating tablets (375 mg tablets containing 10 mg of the active ingredient).
상기 각 실시예에 있어서, 향료로서 1-멘톨을 첨가하여 정제를 조제한 것은 불쾌한 쓴맛이 완화되었다. In each of the above Examples, 1-menthol was added as a perfume to prepare tablets, which resulted in less unpleasant bitter taste.
정제의 직경은 통상적으로 약 5㎜ ∼ 약 20㎜, 바람직하게는 약 7㎜ ∼ 약 15㎜ 의 사이로, 복용에 적절한 크기를 선택할 수 있다. The diameter of the tablet is typically between about 5 mm and about 20 mm, preferably between about 7 mm and about 15 mm, and a size suitable for dosing can be selected.
비교예 3 :Comparative Example 3:
하기의 각 성분을 통상적인 방법에 따라, 혼합하고, 직타함으로써 건식 직타 속붕괴성 정제의 조제를 시도하였다. Each of the following components was mixed according to a conventional method, and an attempt was made to prepare a dry-type collapsible tablet by grinding.
배합 목적 성분명 중량 (g) Compounding purpose Ingredient name Weight (g)
유효 성분 멜록시캄(입자직경 약 8㎛) 15.00Active Ingredient Meloxicam (particle diameter approx. 8 μm) 15.00
부형제 유당 116.25 Excipient lactose 116.25
결합제 결정 셀룰로오스 37.50Binder Crystalline Cellulose 37.50
교미제 에리트리톨 108.75Mating agent erythritol 108.75
붕괴제 크로스포비돈 56.25 Disintegrant crospovidone 56.25
용해 보조제 시트르산나트륨 15.00Solubility Supplement Sodium Citrate 15.00
용해 보조제 탄산수소나트륨 3.75Solubilizer Sodium Hydrogenate 3.75
유동화제 경질 무수 규산 4.88Fluidizing agent Density Anhydrous silicic acid 4.88
교미제 아스파르템 11.25Mating agent Aspardem 11.25
활택제 자당 지방산 에스테르 3.75 Lactose Sucrose Fatty Acid Esters 3.75
활택제 스테아르산마그네슘 2.63Magnesium stearate 2.63
향료 1-멘톨 0.19Perfume 1-menthol 0.19
착색료 청색 1 호 알루미늄레이크 0.19Coloring Blue No. 1 Aluminum Lake 0.19
나정 (합계) 375.39 No (Total) 375.39
상기의 각 배합 성분의 혼합물의 시험 분석치 (수분, 비용적, 안식각) 를 이하에 나타낸다.Test analytical values (moisture, cost, and angle of repose) of the mixture of each of the above ingredients are shown below.
안식각 (˚) 39.5˚ ; 비용적 (루즈) 1.83㎖/g ; 비용적 (탭) 1.37㎖/g ; Carr 의 지수 (%) 33.85 ; 수분 (%) 0.8 Angle of repose (˚) 39.5˚; Cost (loose) 1.83 ml / g; Cost (taps) 1.37 ml / g; Carr's index (%) 33.85; Moisture (%) 0.8
결과적으로, 얻어진 혼합물의 유동성이 불량이어서, 타정 효율이 저하되었다. As a result, the fluidity of the obtained mixture was poor, and the tableting efficiency was lowered.
비교예 4 :Comparative Example 4:
하기의 각 성분을 통상적인 방법에 따라 혼합하고, 직타함으로써 건식 직타 속붕괴성 정제의 조제를 시도하였다. 단 멜록시캄은 경질 무수 규산으로 미리 표면 개질한 것을 사용하였다. Each of the following components was mixed according to a conventional method, and an attempt was made to prepare a dry, collapsible tablet by dry grinding. Danseloxycam was previously surface-modified with light silicic anhydride.
배합 목적 성분명 중량 (g) Compounding purpose Ingredient name Weight (g)
유효 성분 멜록시캄 (입자직경 약 8㎛) 15.00Active Ingredient Meloxicam (particle diameter approx. 8 μm) 15.00
부형제 유당 116.25 Excipient lactose 116.25
결합제 결정 셀룰로오스 37.50Binder Crystalline Cellulose 37.50
교미제 에리트리톨 108.75Mating agent erythritol 108.75
붕괴제 크로스포비돈 56.25 Disintegrant crospovidone 56.25
용해 보조제 시트르산나트륨 15.00Solubility Supplement Sodium Citrate 15.00
용해 보조제 탄산수소나트륨 3.75Solubilizer Sodium Hydrogenate 3.75
유동화제 경질 무수 규산 4.88Fluidizing agent Density Anhydrous silicic acid 4.88
교미제 아스파르템 11.25Mating agent Aspardem 11.25
활택제 자당 지방산 에스테르 3.75 Lactose Sucrose Fatty Acid Esters 3.75
활택제 스테아르산마그네슘 2.63Magnesium stearate 2.63
향료 1-멘톨 0.19Perfume 1-menthol 0.19
착색료 청색 1 호 알루미늄레이크 0.19Coloring Blue No. 1 Aluminum Lake 0.19
나정 (합계) 375.39 No (Total) 375.39
상기의 각 배합 성분의 혼합물의 시험 분석치 (수분, 비용적, 안식각) 를 이하에 나타낸다.Test analytical values (moisture, cost, and angle of repose) of the mixture of each of the above ingredients are shown below.
안식각 (˚) 40.0˚ ; 비용적 (루즈) 1.80㎖/g ; 비용적 (탭) 1.34㎖/g ; Carr 의 지수 (%) 34.61 ; 수분 (%) 0.8 Angle of repose (˚) 40.0˚; Cost (loose) 1.80 ml / g; Cost (taps) 1.34 ml / g; Carr's index (%) 34.61; Moisture (%) 0.8
결과적으로, 얻어진 혼합물의 유동성이 불량이어서, 타정 효율이 저하되었다. As a result, the fluidity of the obtained mixture was poor, and the tableting efficiency was lowered.
이상의 각 표에 나타낸 결과로부터도 판명되듯이, 본 발명의 직타 속붕괴성 정제는 양호한 경도를 갖는 한편, 구강 내에서의 붕괴성이 우수하다는 것을 이해시킨다. As is apparent from the results shown in the above Tables, it is understood that the disintegrating tablet of the present invention has good hardness and excellent disintegration property in the oral cavity.
또한, 상기 실시예는 유효 성분으로서 타르타르산졸피뎀 또는 멜록시캄을 사용한 구체예를 나타냈지만, 다른 유효 성분이라도 동일하게 직타 속붕괴성 정제를 제조할 수 있는 것은 말할 필요도 없다. In addition, although the above example shows a specific example using salmetidomatetram or meloxicam as an active ingredient, needless to say, it is also possible to produce disintegrating tablets in the same manner with other effective ingredients.
이상 기재와 같이, 본 발명에 의해 속붕괴성을 유지하면서 실용적인 정제의 경도를 갖는 건식 직타 속붕괴성 정제, 특히 타르타르산졸피뎀 또는 멜록시캄이 함유된 직타 속붕괴성 정제가 제공되고, 그 용출 거동도 양호한 것인 점에서 의료상의 가치는 큰 것이다. As described above, according to the present invention, there is provided a disintegrating tablets having a disintegrable property while having a practical tablet disintegration property, in particular, disintegrating tablets containing disintegrating tablets of dry tablets containing disintegrating tablets or meloxicam, The medical value is big because it is in good condition.
Claims (18)
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006110753 | 2006-04-13 | ||
| JPJP-P-2006-110753 | 2006-04-13 | ||
| PCT/JP2007/058095 WO2007119792A1 (en) | 2006-04-13 | 2007-04-12 | Dry direct compression fast disintegrating tablet |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20090010978A KR20090010978A (en) | 2009-01-30 |
| KR101400064B1 true KR101400064B1 (en) | 2014-05-27 |
Family
ID=38609552
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020087027556A Expired - Fee Related KR101400064B1 (en) | 2006-04-13 | 2007-04-12 | Dry direct compression fast disintegrating tablet |
Country Status (4)
| Country | Link |
|---|---|
| JP (1) | JP5215172B2 (en) |
| KR (1) | KR101400064B1 (en) |
| CN (1) | CN101420982B (en) |
| WO (1) | WO2007119792A1 (en) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101543480A (en) * | 2008-03-28 | 2009-09-30 | 兴和株式会社 | Tablets |
| WO2010061846A1 (en) * | 2008-11-25 | 2010-06-03 | 田辺三菱製薬株式会社 | Orally rapidly disintegrating tablet, and process for producing same |
| JP5517327B2 (en) * | 2008-12-16 | 2014-06-11 | 日医工株式会社 | Composition for orally disintegrating tablets |
| CN101618026B (en) * | 2009-07-06 | 2011-03-16 | 江苏飞马药业有限公司 | Meloxicam tablet, production technology and purposes thereof |
| CN101869236A (en) * | 2010-06-09 | 2010-10-27 | 山东福田药业有限公司 | Xylitol particles capable of being directly pressed into tablets and preparation method thereof |
| KR101226271B1 (en) | 2011-01-14 | 2013-01-25 | 에스케이하이닉스 주식회사 | Programing circuit using antifuse |
| BR112014026292B1 (en) * | 2012-04-24 | 2022-09-27 | Daiichi Sankyo Company, Limited | ORALLY DISINTEGRABLE PILL, AND, PROCESS FOR THE PRODUCTION OF AN ORRALLY DISINTEGRABLE PILL |
| US8431155B1 (en) | 2012-04-30 | 2013-04-30 | Veroscience Llc | Bromocriptine formulations |
| CN103202817B (en) * | 2013-04-28 | 2014-10-08 | 山东天力药业有限公司 | Preparation method for mannitol grains capable of being directly pressed |
| CN103494821B (en) * | 2013-10-01 | 2018-09-25 | 迪沙药业集团有限公司 | A kind of cefixime composition |
| JP2023019149A (en) * | 2021-07-28 | 2023-02-09 | エスエス製薬株式会社 | tablet |
| JP2023019148A (en) * | 2021-07-28 | 2023-02-09 | エスエス製薬株式会社 | General pharmaceutical |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3122141B2 (en) * | 1994-01-31 | 2001-01-09 | 山之内製薬株式会社 | Oral dissolution type compression molded product and method for producing the same |
| JP2001058944A (en) * | 1999-06-18 | 2001-03-06 | Takeda Chem Ind Ltd | Rapidly disintegrating solid formulation |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2174538A1 (en) * | 1993-10-22 | 1995-04-27 | Michio Nagasawa | Base for sustained-release preparation, sustained-release preparation, and process for producing the preparation |
| JP4438121B2 (en) * | 1998-04-27 | 2010-03-24 | 大正製薬株式会社 | Intraoral rapidly disintegrating tablet and method for producing the same |
| AU5248900A (en) * | 1999-06-18 | 2001-01-09 | Takeda Chemical Industries Ltd. | Quickly disintegrating solid preparations |
-
2007
- 2007-04-12 JP JP2008510987A patent/JP5215172B2/en not_active Expired - Fee Related
- 2007-04-12 KR KR1020087027556A patent/KR101400064B1/en not_active Expired - Fee Related
- 2007-04-12 WO PCT/JP2007/058095 patent/WO2007119792A1/en not_active Ceased
- 2007-04-12 CN CN2007800132649A patent/CN101420982B/en not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3122141B2 (en) * | 1994-01-31 | 2001-01-09 | 山之内製薬株式会社 | Oral dissolution type compression molded product and method for producing the same |
| JP2001058944A (en) * | 1999-06-18 | 2001-03-06 | Takeda Chem Ind Ltd | Rapidly disintegrating solid formulation |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5215172B2 (en) | 2013-06-19 |
| CN101420982A (en) | 2009-04-29 |
| CN101420982B (en) | 2011-11-09 |
| WO2007119792A1 (en) | 2007-10-25 |
| JPWO2007119792A1 (en) | 2009-08-27 |
| KR20090010978A (en) | 2009-01-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101400064B1 (en) | Dry direct compression fast disintegrating tablet | |
| KR101612137B1 (en) | Orally disintegrating tablets | |
| ES2813859T3 (en) | Rapidly dispersing granules, orally disintegrating tablets and methods | |
| JP5296456B2 (en) | Irbesartan-containing pharmaceutical composition with good dissolution and orally disintegrating tablet | |
| JP5637624B2 (en) | Disintegrating particle composition and fast disintegrating compression molding using the same | |
| JP5674667B2 (en) | Disintegrating particle composition and intraoral quick disintegrating tablet | |
| JP2009114113A (en) | Orally disintegrating tablet and method for producing the same | |
| WO2011019043A1 (en) | Tablet that disintegrates rapidly in the mouth and that contains two or more types of particles | |
| KR20050096941A (en) | Tablet quickly melting in oral cavity | |
| JP5074190B2 (en) | Orally rapidly disintegrating tablets | |
| CN102355890A (en) | Orally disintegrating tablet | |
| JP2003034655A (en) | Fast disintegrating solid preparation | |
| JP2017141299A (en) | Irbesartan-containing pharmaceutical composition showing excellent elution, and orally disintegrable tablet | |
| JP2010270110A (en) | Oral formulation containing neotame | |
| JP2003176242A (en) | Quickly disintegrable compression-molded material and method for producing the same | |
| JP2015098470A (en) | Tablet containing loxoprofen or salt thereof | |
| TWI762450B (en) | Ultra-high-speed disintegrating tablet and its manufacturing method | |
| JP5978335B2 (en) | Irbesartan-containing pharmaceutical composition with good dissolution and orally disintegrating tablet | |
| JP5080856B2 (en) | Tablets for oral administration | |
| JP6151413B2 (en) | Irbesartan-containing pharmaceutical composition with good dissolution and orally disintegrating tablet | |
| JP5714652B2 (en) | Irbesartan-containing pharmaceutical composition with good dissolution and orally disintegrating tablet | |
| JP2021113237A (en) | Irbesartan-containing pharmaceutical composition showing excellent elution, and orally disintegrable tablet | |
| JP2018168185A (en) | Irbesartan-containing pharmaceutical composition and orally disintegrable tablet with excellent elution | |
| KR20080048923A (en) | Oral solid composition with reduced irritation to the digestive tract | |
| HK1155978B (en) | Orally disintegrating tablets |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| N231 | Notification of change of applicant | ||
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| N231 | Notification of change of applicant | ||
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| A201 | Request for examination | ||
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| FPAY | Annual fee payment |
Payment date: 20170512 Year of fee payment: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| LAPS | Lapse due to unpaid annual fee | ||
| PC1903 | Unpaid annual fee |
St.27 status event code: A-4-4-U10-U13-oth-PC1903 Not in force date: 20180522 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20180522 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |