KR101326367B1 - Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent - Google Patents
Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent Download PDFInfo
- Publication number
- KR101326367B1 KR101326367B1 KR1020060062231A KR20060062231A KR101326367B1 KR 101326367 B1 KR101326367 B1 KR 101326367B1 KR 1020060062231 A KR1020060062231 A KR 1020060062231A KR 20060062231 A KR20060062231 A KR 20060062231A KR 101326367 B1 KR101326367 B1 KR 101326367B1
- Authority
- KR
- South Korea
- Prior art keywords
- seq
- gene
- resistance
- drug resistance
- imatinib
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/686—Polymerase chain reaction [PCR]
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Immunology (AREA)
- Analytical Chemistry (AREA)
- Genetics & Genomics (AREA)
- Physics & Mathematics (AREA)
- Pathology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Health & Medical Sciences (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Oncology (AREA)
- Hospice & Palliative Care (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
본 발명은 항암제 저항성의 진단 방법 및 진단 키트에 관한 것으로서, 보다 상세하게는 만성 골수성 백혈성 (chronic myelogenous leukemia; CML)을 치료하는 약제에 대한 저항성 (drug resistance)을 예측하는 유전자, 이를 이용하는 항암제 저항성의 진단 방법 및 진단 키트에 관한 것이다. 본 발명의 진단 방법 및 진단 키트는 항암제인 이마티닙 (imatinib)에 대한 저항성을 부여하는 유전자 발현 신호를 다양한 저항성 유전자군을 사용하여 감지하는 과정으로, 만성 골수성 백혈병을 포함한 각종 암을 효과적으로 진단하고 치료하며 더 나아가 글리벡에 대한 저항성 기작을 연구하는 데 널리 사용될 수 있다.
항암제 저항성, 이마티닙 (imatinib), 저항성 유전자군, 만성 골수성 백혈병 (CML), 진단 키트
The present invention relates to a diagnostic method and a diagnostic kit for anticancer drug resistance, and more particularly, a gene for predicting drug resistance to drugs for treating chronic myelogenous leukemia (CML), and anticancer drug resistance using the same. Relates to diagnostic methods and diagnostic kits. The diagnostic method and diagnostic kit of the present invention detects gene expression signals that impart resistance to imatinib, an anticancer agent, using various resistance gene groups, and effectively diagnoses and treats various cancers including chronic myelogenous leukemia. Furthermore, it can be widely used to study the mechanism of resistance to Gleevec.
Anticancer drug resistance, imatinib, resistance gene family, chronic myelogenous leukemia (CML), diagnostic kit
Description
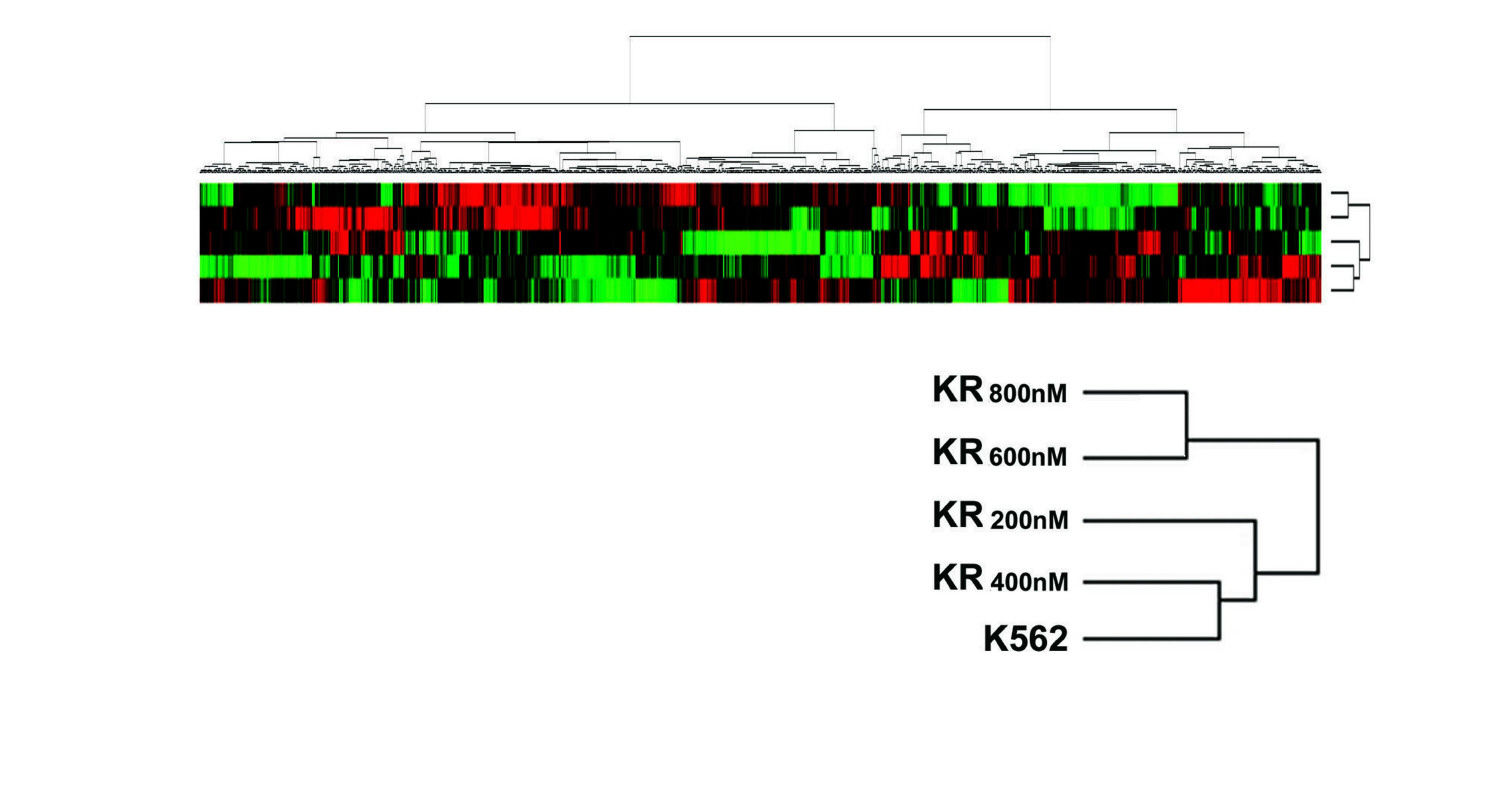
도 1 은 이마티닙-저항성 유전자군의 배열 순서를 유전자 발현 프로파일에 따라 나타낸 것이다.1 shows the sequence of imatinib-resistant gene groups according to gene expression profiles.
도 2a 는 이마티닙의 투여량에 따라 포지티브하게 상관된 유전자의 발현 변화를 이마티닙-저항성 유전자군을 사용하여 분석한 것이다.FIG. 2A analyzes the expression change of positively correlated genes according to the dose of imatinib using imatinib-resistant gene group.
도 2b 는 이마티닙의 투여량에 따라 네가티브하게 상관된 유전자의 발현 변화를 이마티닙-저항성 유전자군을 사용하여 분석한 것이다.FIG. 2B analyzes the expression changes of negatively correlated genes according to the dose of imatinib using imatinib-resistant gene group.
도 3a 은 만성 골수성 백혈병 (CML)의 이마티닙 저항성을 6가지 후보 유전자 중에서 CASP4 및 TNFRSF21 유전자의 발현 변화로 분석한 것이다.FIG. 3A shows CASP4 resistance among six candidate genes for imatinib resistance in chronic myelogenous leukemia (CML). And TNFRSF21 It is analyzed by the change of expression of gene.
도 3b 은 만성 골수성 백혈병 (CML)의 이마티닙 저항성을 6가지 후보 유전자 중에서 RAB11A 및 IGF1 유전자의 발현 변화로 분석한 것이다.도 3c 은 만성 골수성 백혈병 (CML)의 이마티닙 저항성을 6가지 후보 유전자 중에서 LYN 및 RHOA 유전자의 발현 변화로 분석한 것이다.3B shows RAB11A resistance among imatinib resistance of six candidate genes in chronic myelogenous leukemia (CML) And IGF1 Figure 3c shows the LYN of imatinib resistance in chronic myeloid leukemia (CML) among six candidate genes. And RHOA It is analyzed by the change of expression of gene.
본 발명은 항암제 저항성의 진단 방법 및 진단 키트에 관한 것으로서, 보다 상세하게는 만성 골수성 백혈성 (chronic myelogenous leukemia; 이하, ?CML?라고 약칭함)을 치료하는 약제에 대한 저항성을 예측하는 유전자, 이를 이용하는 항암제 저항성의 진단 방법 및 진단 키트에 관한 것이다. The present invention relates to a diagnostic method and a diagnostic kit for anticancer drug resistance, and more particularly, a gene for predicting resistance to an agent for treating chronic myelogenous leukemia (hereinafter, abbreviated as? CML?). The present invention relates to a diagnostic method and a diagnostic kit for anticancer drug resistance.
항암제 이마티닙 (imatinib)은 이마티닙 메실레이트 (imatinib mesylate), STI-571 및 글리벡 (Gleevec) 등으로 불리는 타이로신 키나제 (tyrosine kinase)에 대한 선택적인 저해제로서, 만성 골수성 백혈병 (chronic myelogenous leukemia; 이하, ?CML?이라고 약칭함)을 치료하는 데 주로 사용되고 있다. BCR-ABL 융합 키나제를 겨낭하여 치료하는 일차적인 약제인 이마티닙은 특히 만성 골수성 백혈병의 초기 단계에서 80% 이상 증상을 완화시키는 것으로 알려져 있다 (O'Dwyer, M. E. 및 Druker, B. J. J. Intern. Med . 250: 3-9, 2001). 그러나, 초기 혈액 및 세포 반응 후에 증상이 재발되는 현상이 자주 발생한다 (Druker, B. J. et al., N. Engl . J. Med ., 344: 1038-1042, 2001). 따라서, BCR-ABL 키나제을 겨낭한 치료법은 약제 저항성으로 인해 방해를 받고 이마티닙의 임상적 효능을 심각하게 감소시킨다.The anticancer agent imatinib is a selective inhibitor of tyrosine kinase, called imatinib mesylate, STI-571, and Gleevec, and is known as chronic myelogenous leukemia; Abbreviated? Imatinib, the primary drug for treating BCR-ABL fusion kinase, is known to alleviate more than 80% of symptoms, especially in the early stages of chronic myeloid leukemia (O'Dwyer, ME and Druker, BJ J. Intern. Med . 250: 3-9, 2001) . However, symptoms recur frequently after initial blood and cellular responses (Druker, BJ et al ., N. Engl . J. Med . , 344: 1038-1042, 2001). Thus, therapies targeting BCR-ABL kinase are hampered by drug resistance and severely reduce the clinical efficacy of imatinib.
또한, BCR-ABL 타이로신 키나제의 일정 도메인에 전사 증폭 (transcription amplification) 또는 점 돌연변이가 종종 저항성의 임상 사례들 또는 생체 외 (in vitro) 세포 모델에서 관찰되어 왔다 (Hochhaus, A. et al., Science, 293: 876-880, 2001; Shah, N. P. et al., Cancer Cell, 2: 117-125, 2002; Gorre, M. E. et al., Science, 293: 876-880, 2001). 이러한 변화가 이마티닙-저항성을 획득하는 가장 그럴듯한 원인이라고 할지라도, 선행 연구들은 이 저항성이 증폭 또는 돌연변이 없이 생길 수 있다고 보여주기도 한다 (Donato, N. J. et al., Blood, 101: 690-698, 2003; Hofmann, W. K. et al., Lancet, 359: 481-486, 2002; Mahon, F. X. et al., Blood, 96: 1070-1079, 2000). 또한, 다제 저항성유전자의 과발현이 이마티닙에 대한 저항성을 부여하기도 한다. 이러한 연구들은 이마티닙-저항성이 서로 다른 기작들에 의해 야기될 수 있는 점을 제시한다. 따라서 이마티닙-저항성을 유발하는 주요 인자를 확인하기 위하여 마이크로어레이 (microarray)를 사용한 범용 유전자 발현 분석과 같은 다양한 접근법이 도입되어 왔다 (Tipping, A. J. et al., Exp . Hematol ., 31: 1073-1080, 2003; Ohmine, K. et al., Stem Cells, 21: 315-321, 2003). In addition, BCR-ABL amplification transcription (transcription amplification) or point mutations in the constant domain of a tyrosine kinase is often been observed in other clinical cases of resistance or in vivo (in vitro) cell model (Hochhaus, A. et al., Science , 293: 876-880, 2001; Shah, NP et al. , Cancer Cell , 2: 117-125, 2002; Gorre, ME et al ., Science , 293: 876-880, 2001). Although this change is the most likely cause of obtaining imatinib-resistance, previous studies have shown that this resistance can occur without amplification or mutation (Donato, NJ et al ., Blood , 101: 690-698, 2003; Hofmann, WK et al ., Lancet, 359: 481-486, 2002; Mahon, FX et al ., Blood, 96: 1070-1079, 2000). In addition, overexpression of a multidrug resistant gene also confers resistance to imatinib. These studies suggest that imatinib-resistance can be caused by different mechanisms. Thus, a variety of approaches have been introduced, such as general purpose gene expression analysis using microarrays to identify the major factors causing imatinib-resistance (Tipping, AJ et al. , Exp . Hematol . , 31: 1073-1080 , 2003; Ohmine, K. et al. , Stem Cells , 21: 315-321, 2003).
본 발명자들은 이마티닙-저항성 유전자군을 다양한 이마티닙 투여량 및 CML 사례들을 참고하여 확립하고 이마티닙-저항성의 발현 프로파일을 조사하여 생물학적으로 적절히 발현 변화를 보이는 전사체 (transcript)들에 초점을 맞추어 이마티닙-저항성과 관련된 유전자 발현 서명 (gene expression signature)을 밝혔다. 또한, 유전자 세트 증폭 분석 (gene set enrichment analysis)과 같은 생물정보학적 접근법을 통하여 이마티닙-저항성과 관련된 발현 프로파일 및 후보 신호전달과정을 설명하려고 하였다. We established an imatinib-resistant gene family with reference to various imatinib doses and CML cases and examined imatinib-resistant expression profiles to focus on imatinib-resistant transcripts showing biologically appropriate expression changes. The gene expression signature associated with the gene was identified. In addition, bioinformatics approaches such as gene set enrichment analysis attempted to describe the expression profiles and candidate signaling processes associated with imatinib-resistance.
이에 본 발명자들은 새로운 항암제 저항성을 검사하는 진단 방법을 개발하기 위하여 노력을 계속한 결과, 만성 골수성 백혈성 (chronic myelogenous leukemia; CML) 을 치료하는 항암제인 이마티닙 (imatinib)에 대한 저항성을 부여하는 유전자 신호를 선별하여 저항성 유전자 6종을 분리하고 다양한 유전자 프로브들을 제작하여 진단 키트를 개발한 다음 CML을 포함한 각종 암의 약제 저항성을 검사하는 데 유용한 점을 확인함으로써 본 발명을 성공적으로 완성하였다.Therefore, the present inventors have continued to develop a diagnostic method for testing new anticancer drug resistance, and as a result, the gene signal conferring resistance to imatinib, an anticancer drug treating chronic myelogenous leukemia (CML) The present invention was successfully completed by selecting 6 isolates of resistance genes, producing various gene probes, and developing a diagnostic kit, and then confirming the usefulness of testing drug resistance of various cancers including CML.
본 발명은 항암제 저항성 유전자, 이를 이용한 항암제 저항성의 진단 방법 및 진단 키트를 제공하는 것을 목적으로 한다.An object of the present invention is to provide an anticancer drug resistance gene, a method for diagnosing anticancer drug resistance and a diagnostic kit using the same.
상기 목적을 달성하기 위하여, 본 발명은 In order to achieve the above object,
(1) 항암제 저항성 유전자들 선택하고; 및 (1) selecting anticancer drug resistance genes; And
(2) 상기 유전자의 발현 정도를 측정하여 결과를 분석하는; 과정으로 이루어진 항암제에 대한 저항성을 검사하는 진단 방법을 제공한다. (2) analyzing the results by measuring the expression level of the gene; It provides a diagnostic method for testing resistance to the anticancer drug.
상기 (1) 과정에서 항암제 저항성 유전자는 아폽토시스 (apoptosis), 세포 신호 전달, 세포 주기 조절, GTP 결합 단백질, 세포 증식 및 전사 관련 유전자 중에서 선택된 하나 이상인 것이 바람직하다.In the process (1), the anticancer drug resistance gene is preferably at least one selected from apoptosis, cell signal transduction, cell cycle regulation, GTP binding protein, cell proliferation and transcription related genes.
상기 항암제 저항성 유전자는 CASP4, TNFRSF21, TNFRSF9, NOTCH2, SQSTM1, TGIF, PLCD1, CCNB1P1, RAB11A, IGF1, LYN, RHOA, NMI, FOXO3A, ZNF226, ZNF140, LTBP1 및 ABCA8 유전자 중에서 선택된 하나 이상인 것이 바람직하고, CASP4, TNFRSF21, RAB11A, IGF1, LYN 및 RHOA 유전자 중에서 선택된 하나 이상인 것은 더욱 바람직하다.The anticancer agent resistance gene is CASP4, TNFRSF21, TNFRSF9, NOTCH2, SQSTM1, TGIF, PLCD1, CCNB1P1, RAB11A, IGF1, LYN, RHOA, NMI, FOXO3A, ZNF226, ZNF140, LTBP1 and ABCA8 gene preferably at least one selected from a, and CASP4 More preferably, at least one selected from among TNFRSF21, RAB11A, IGF1, LYN and RHOA genes.
상기 (2) 과정에서 상기 항암제 저항성 유전자의 발현 정도는 상승 또는 감소 조절되고, 이 때 CASP4, TNFRSF21, LYN 및/또는 RHOA 유전자는 상승 발현되고 RAB11A 및/또는 IGF1 유전자는 감소 발현되는 것이 바람직하다.In the process (2), the expression level of the anticancer drug resistance gene is increased or decreased, and at this time, the CASP4, TNFRSF21, LYN and / or RHOA genes are up-expressed and the RAB11A and / or IGF1 genes are decreased.
상기 (2) 과정에서 상기 항암제 저항성 유전자의 발현 정도는 중합효소 연쇄반응 (PCR) 및/또는 마이크로어레이 (microarray) 등을 수행하여 분석하는 것이 바람직하다.In the step (2), the expression level of the anticancer drug resistance gene is preferably analyzed by performing polymerase chain reaction (PCR) and / or microarray.
본 발명의 진단 방법은 만성 골수성 백혈병 (CML)을 치료하는 데 사용되는 것이 바람직하다.The diagnostic method of the present invention is preferably used to treat chronic myeloid leukemia (CML).
또한, 본 발명은 아폽토시스 (apoptosis), 세포 신호 전달, 세포 주기 조절, GTP 결합 단백질, 세포 증식 및 전사 관련 유전자 중에서 선택되는 항암제 저항성 유전자 및 그의 전부 또는 일부 서열로 구성된 상기 유전자에 대한 표지자를 제공한다. 상기 항암제 저항성 유전자는 CASP4, TNFRSF21, TNFRSF9, NOTCH2, SQSTM1, TGIF, PLCD1, CCNB1P1, RAB11A, IGF1, LYN, RHOA, NMI, FOXO3A, ZNF226, ZNF140, LTBP1 및 ABCA8 유전자 중에서 선택된 하나 이상인 것이 바람직하고, CASP4, TNFRSF21, RAB11A, IGF1, LYN 및 RHOA 유전자 중에서 선택된 하나 이상인 것은 더욱 바람직하며, 만성 골수성 백혈병 (CML)을 치료하는 데 사용되는 것이 바람직하다.In addition, the present invention provides a marker for an anticancer agent resistance gene selected from apoptosis, cell signal transduction, cell cycle regulation, GTP binding protein, cell proliferation and transcription related genes and all or a portion thereof. . The anticancer agent resistance gene is CASP4, TNFRSF21, TNFRSF9, NOTCH2, SQSTM1, TGIF, PLCD1, CCNB1P1, RAB11A, IGF1, LYN, RHOA, NMI, FOXO3A, ZNF226, ZNF140, LTBP1 and ABCA8 gene preferably at least one selected from a, and CASP4 More preferably, at least one selected from among TNFRSF21, RAB11A, IGF1, LYN, and RHOA genes, and is preferably used to treat chronic myeloid leukemia (CML).
이하, 본 발명을 상세히 설명하면 다음과 같다.Hereinafter, the present invention will be described in detail.
본 발명은 항암제 저항성 유전자에 대한 프로브를 이용하여 항암제에 대한 저항성 을 검사하는 진단 방법을 제공한다. The present invention provides a diagnostic method for testing resistance to anticancer drugs using a probe for anticancer drug resistance genes.
상기 항암제로는 이마티닙 (imatinib), 글리벡 (Gleevec) 및 STI-571 등이 포함된다. 또한, 상기 항암제 저항성 유전자로는 CASP4, TNFRSF21, RAB11A, IGF1, LYN 및 RHOA 유전자 중에서 선택된 하나 이상이 포함된다.The anticancer agents include imatinib, Gleevec and STI-571. In addition, the anticancer drug resistance gene includes one or more selected from the CASP4, TNFRSF21, RAB11A, IGF1, LYN and RHOA gene.
본 발명의 진단 방법에는 항암제 저항성 유전자에 대한 프로브를 사용하는 모든 검사 방법이 포함될 수 있고, 바람직하게는 상기 저항성 유전자에 대한 프로브를 사용하여 수행하는 중합효소 연쇄반응 등이 포함될 수 있다. 보다 바람직하게는 항암제 저항성 유전자 CASP4 에 대한 서열번호 1 과 서열번호 2의 염기 서열을 가지는 프라이머 세트;The diagnostic method of the present invention may include any test method using a probe for an anticancer drug resistance gene, and preferably include a polymerase chain reaction performed using the probe for the resistance gene. More preferably the anticancer drug resistance gene CASP4 A primer set having a nucleotide sequence of SEQ ID NO: 1 and SEQ ID NO: 2 for;
항암제 저항성 유전자 TNFRSF21 에 대한 서열번호 3 과 서열번호 4의 염기 서열을 가지는 프라이머 세트; Anticancer drug resistance gene TNFRSF21 A primer set having a nucleotide sequence of SEQ ID NO: 3 and SEQ ID NO: 4 for a;
항암제 저항성 유전자 RAB11A 에 대한 서열번호 5 과 서열번호 6의 염기 서열을 가지는 프라이머 세트; Anticancer drug resistance gene RAB11A A primer set having a nucleotide sequence of SEQ ID NO: 5 and SEQ ID NO: 6 for a;
항암제 저항성 유전자 IGF1 에 대한 서열번호 7 과 서열번호 8의 염기 서열을 가지는 프라이머 세트; Anticancer drug resistance gene IGF1 A primer set having the nucleotide sequences of SEQ ID NO: 7 and SEQ ID NO: 8 for the;
항암제 저항성 유전자 LYN 에 대한 서열번호 9 또는 서열번호 10의 염기 서열을 가지는 프라이머 세트; 및A primer set having a nucleotide sequence of SEQ ID NO: 9 or SEQ ID NO: 10 for an anticancer drug resistance gene LYN ; And
항암제 저항성 유전자 RHOA에 대한 서열번호 11 과 서열번호 12의 염기서열을 가지는 프라이머 세트로 이루어진 그룹에서 하나 이상 선택되는 것을 특징으로 하는 항암제 저항성 진단 프라이머 세트를 제공한다. 또한 상기 프라이머 세트를 이용하 여 중합효소 연쇄반응(PCR)를 하는 것을 특징으로 하는 항암제 저항성 진단방법을 제공한다. 본 발명의 진단 방법은 만성 골수성 백혈병 (CML)을 포함하는 각종 암 질환을 치료하는 데 사용하는 것이 바람직하다.Provided is a set of anti-cancer drug resistance diagnostic primers, characterized in that at least one selected from the group consisting of a primer set having the nucleotide sequences of SEQ ID NO: 11 and SEQ ID NO: 12 for the anti-cancer drug resistance gene RHOA. In addition, the present invention provides a method for diagnosing resistance to cancer, wherein the polymerase chain reaction (PCR) is performed using the primer set. The diagnostic method of the present invention is preferably used to treat various cancer diseases including chronic myeloid leukemia (CML).
본 발명은 항암제 저항성 유전자에 대한 프로브를 이용하여 항암제에 대한 저항성을 검사하는 진단 키트를 제공한다. 바람직하게는 항암제 저항성 유전자 CASP4, TNFRSF21, RAB11A, IGF1, LYN 및 RHOA 중에서 선택된 하나 이상의 유전자를 암호화 하는 핵산서열을 포함하는 항암제에 대한 저항성을 검사하는 진단 키트를 제공한다. 보다 바람직하게는 상기 항암제 저항성 유전자에 더하여 TNFRSF9, NOTCH2, SQSTM1, TGIF, PLCD1, CCNB1P1, NMI, FOXO3A, ZNF226, ZNF140, LTBP1 및 ABCA8 유전자 중에서 선택된 하나 이상의 유전자를 암호화 하는 핵산서열을 추가로 포함하는 것을 특징으로 하는 항암제에 대한 저항성을 검사하는 진단 키트를 제공한다. 상기 항암제 저항성 진단키트는 만성 골수성 백혈병 (CML)을 치료하는 데 사용될 수 있다. 상기 항암제로는 이마티닙 (imatinib), 글리벡 (Gleevec) 및 STI-571 등이 포함된다. 또한, 상기 항암제 저항성 유전자로는 CASP4, TNFRSF21, RAB11A, IGF1, LYN 및 RHOA 유전자 중에서 선택된 하나 이상이 포함된다. 본 발명의 진단 키트는 만성 골수성 백혈병 (CML)을 포함하는 각종 암 질환을 치료하는 데 사용하는 것이 바람직하다. The present invention provides a diagnostic kit for testing resistance to an anticancer agent using a probe for an anticancer agent resistance gene. Preferably, a diagnostic kit for testing resistance to an anticancer agent comprising a nucleic acid sequence encoding at least one gene selected from an anticancer agent resistance gene CASP4, TNFRSF21 , RAB11A, IGF1, LYN, and RHOA is provided. More preferably, it further comprises a nucleic acid sequence encoding at least one gene selected from TNFRSF9 , NOTCH2 , SQSTM1 , TGIF , PLCD1 , CCNB1P1 , NMI , FOXO3A , ZNF226 , ZNF140 , LTBP1 and ABCA8 genes in addition to the anticancer drug resistance gene. A diagnostic kit for testing resistance to an anticancer agent is provided. The anticancer drug resistance diagnostic kit can be used to treat chronic myeloid leukemia (CML). The anticancer agents include imatinib, Gleevec and STI-571. In addition, the anticancer drug resistance gene includes one or more selected from the CASP4, TNFRSF21, RAB11A, IGF1, LYN and RHOA gene. The diagnostic kit of the present invention is preferably used to treat various cancer diseases including chronic myeloid leukemia (CML).
본 발명의 진단 키트에는 항암제 저항성 유전자에 대한 프로브를 사용하는 모든 검사용 시약 및 장치 등이 포함될 수 있고, 바람직하게는 상기 저항성 유전자에 대한 프로브를 사용하여 중합효소 연쇄반응 등을 수행하는 데 필요한 시약 및 장치 등이 포함될 수 있다. The diagnostic kit of the present invention may include all test reagents and devices using probes for anticancer drug resistance genes, and preferably reagents for performing polymerase chain reaction using the probes for the resistance genes. And devices.
이하, 실시예에 의하여 본 발명을 더욱 상세히 설명하고자 한다.Hereinafter, the present invention will be described in more detail with reference to Examples.
단, 하기 실시예는 본 발명을 예시하는 것일 뿐, 본 발명의 내용이 하기 실시예에 한정되는 것은 아니다. However, the following examples are illustrative of the present invention, and the present invention is not limited to the following examples.
<< 실시예Example 1> 1> 이마티닙Imatinib -저항성 - Resistance K562K562 세포주들의 발현 프로파일 조사 Examining Expression Profiles of Cell Lines
먼저, 본 발명에서는 이마티닙-저항성 세포주를 확립하기 위하여, 이마티닙에 대한 저항성을 적혈구가 되는 백혈병성 K562 세포주에 이마티닙을 2주마다 50 mM 씩 농도를 증가시키면서 노출하여 유도하였다. 이마티닙을 처리하여 세포를 배양하는 동안 다양한 이마티닙 농도 200 nM, 400 nM, 600 nM 및 800 nM에 각각 노출된 4가지 저항성 세포주 계열, KR200nM, KR400nM, KR600nM 및 KR800nM 을 확립하였다. 이 때 BCR-ABL 키나제 도메인에 생긴 돌연변이는 이미 기술되어 있는 바와 같이 검색하였다 (Shah, N. P. et al., Cancer Cell, 2: 117-125, 2002). 또한, BCR-ABL 키나제 도메인의 발현 수준은 돌연변이 분석에 사용되는 프라이머들을 사용한 실시간 (real time) 역전사효소-중합효소 연쇄반응 (RT-PCR)을 수행하여 측정하였다. 이 때 대조군으로는 인간 GAPDH 를 사용하였다.First, in the present invention, in order to establish an imatinib-resistant cell line, resistance to imatinib was induced by increasing the concentration of imatinib by 50 mM every two weeks in a leukemia K562 cell line that becomes a red blood cell. During the process the imatinib culturing cells imatinib
먼저, 상기 세포주들의 이마티닙 저항성이 선행 연구에서 이미 보고된 바와 같이 증가된 전사 활성 때문인지 또는 BCR-ABL 키나제 도메인의 점 돌연변이로부터 유발되는지 여부를 조사하였다 (Shah, N. P. et al., Cancer Cell, 2: 117-125, 2002). 그러나 상기 키나제 도메인의 특정 영역에 점 돌연변이와 BCR-ABL 유전자의 상승적 전사 조절 모두가 4가지 저항성 세포주에서는 관찰되지 않았다. K562 세포주 및 이마티닙 저항성 세포주의 발현 프로파일은 30,000개 정도의 인간 유전자를 포함하는 올리고-마이크로어레이를 사용하여 측정되었다. 3,000개의 가장 다양한 전사체들의 집단이 저항성을 유도하는 이마티닙 투여량에 의한 세포주들을 서로 구별되게 하였다 (도 1 참조). 이러한 집단 구성에 따라, 고투여량 그룹, 즉 KR600nM 및 KR800nM 은 저투여량 그룹, 즉 KR200nM 및 KR400nM 그리고 K562 모세포와는 분명히 구별되는 것을 확인하였다.First, it was investigated whether the imatinib resistance of these cell lines was due to increased transcriptional activity, as previously reported in previous studies, or whether it was caused by point mutations in the BCR-ABL kinase domain (Shah, NP et al ., Cancer Cell , 2). : 117-125, 2002). However, neither point mutations in the specific region of the kinase domain nor synergistic transcriptional regulation of the BCR-ABL gene were observed in four resistant cell lines. Expression profiles of K562 cell lines and imatinib resistant cell lines were measured using oligo-microarrays containing as many as 30,000 human genes. The population of 3,000 most diverse transcripts allowed cell lines to be distinguished from each other by imatinib doses that induce resistance (see FIG. 1). According to such grouping, struggled yeoryang group, i.e. KR KR 600nM and 800nM are low dose group, i.e. KR KR 200nM and 400nM And it was confirmed that it is clearly distinguished from K562 parental cells.
실시예Example 2. 항암제 저항성 세포주에서 2. In anticancer drug resistant cell lines 전사체들의Transcripts 변화 분석 Change analysis
(1) RNA 분리 및 (1) RNA isolation and 하이브리디제이션Hybridization
먼저, 전체 RNAs 가 K562 모세포 및 이마티닙-저항성 세포주로부터 트리졸 (Trizol; Invitrogen사 제품)을 사용하여 제조자의 매뉴얼에 따라 분리하였다. 분리된 RNAs 의 양과 질은 바이오애널라이저 (Bioanalyzer 2100; 애질런트 테크놀로지사 제품)를 사용하여 평가하였다. 30,000개 정도의 인간 유전자 세트를 포함하는 인간 게놈 조사 마이크로어레이 (Human Genome Survey Microarray; 어플라이드 바이오시스템사 제품) 버전 2.0을 사용하여 5가지 세포주들, 즉 민감성 K562 세포 및 4가지 저항성 세포주들의 발현 프로파일을 분석하였다. 디옥시제닌-UTP 로 표 지된 cRNA 를 만들고 화학형광 RT-IVT 라벨링 키트 버전 2.0 (어플라이드 바이오시스템사 제품)을 사용하여 5 μg 전체 RNAs 로부터 차례대로 증폭시켰다. 어레이 하이브리디제이션, 화학형광 검사 및 이미지 촬영 및 분석이 화학형광 검사 키트 및 화학형광 마이크로어레이 애널라이저 1700 (어플라이드 바이오시스템사 제품)를 사용하여 제조자의 프로토콜에 따라 진행되었다. 하이브리디제이션 반응은 각 시료마다 3번 반복 수행되었다.First, total RNAs were isolated from K562 parental and imatinib-resistant cell lines using Trizol (Invitrogen) according to the manufacturer's manual. The quantity and quality of the isolated RNAs were assessed using a Bioanalyzer (Bioanalyzer 2100; manufactured by Agilent Technologies). Human Genome Survey Microarray (applied by Applied Biosystems) version 2.0 containing about 30,000 human gene sets was used to express the expression profiles of five cell lines, namely sensitive K562 cells and four resistant cell lines. Analyzed. CRNA labeled with deoxygenin-UTP was made and in turn amplified from 5 μg total RNAs using the chemifluorescence RT-IVT labeling kit version 2.0 (Applied Biosystems). Array hybridization, chemifluorescence testing and imaging and analysis were performed according to the manufacturer's protocol using a chemifluorescence kit and a chemifluorescence microarray analyzer 1700 (Applied Biosystems). The hybridization reaction was repeated three times for each sample.
(2) (2) 데이타Data 프로세싱 Processing
각 어레이-하이브리디제이션의 이미지들은 고해상도 광포맷 CCD 카메라가 장착된 1700 애널라이저를 사용하여 모았다. 여기에는 유전자 발현을 분석하기 위해 5초 동안 노출시킨 2개의 화학형광 이미지들, 특징 연구 및 스폿 정상화를 위한 2개의 형광 이미지들 및 스펙트럼 교정을 위한 2개의 QC 이미지들이 포함된다. 이들 이미지는 자동으로 입력되어 (gridded) 화학형광 신호가 정량되었다. 백그라운드를 감안하여, 스폿의 강도 데이터가 편차 안정화 및 정상화 (VSN) 방법을 사용하여 조정되었다 (Huber, W. et al., Bioinformatics, 18: S96-104, 2002).Images of each array-hybridization were collected using a 1700 analyzer equipped with a high-resolution optical format CCD camera. This includes two chemifluorescent images exposed for 5 seconds to analyze gene expression, two fluorescent images for feature studies and spot normalization, and two QC images for spectral correction. These images were automatically entered (gridded) to quantify the chemifluorescent signal. In light of the background, the intensity data of the spots were adjusted using the deviation stabilization and normalization (VSN) method (Huber, W. et al. , Bioinformatics , 18: S96-104, 2002).
(3) 차별적으로 발현된 (3) differentially expressed 전사체들의Transcripts 분석 analysis
K562 모세포를 포함하는 5가지 세포주들에서 나온 29,098개 유전자의 평균적인 발현이 One-way ANOVA 분석으로 평가되었다. 가장 변화가 많은 3,000개의 전사체들이 선택되고, 평균적 연관성을 통한 집단이 클러스터 및 트리뷰 (Cluster and Treeview; http://rana.lbl.gov/EisenSoftware.htm) 소프트웨어를 사용하여 형성되 었다. 상기 전사체들이 저항성 세포주들에서 상승적 또는 감소적으로 조절되는지 여부를 조사하기 위하여, 발현 변화를 민감성 모세포 대조군과 비교하고 상대적인 차이를 계산하여 평가하였다.Average expression of 29,098 genes from five cell lines, including K562 blasts, was assessed by one-way ANOVA analysis. The 3,000 mutants with the most variation were selected, and populations with average associations were formed using Cluster and Treeview ( http://rana.lbl.gov/EisenSoftware.htm ) software. To investigate whether the transcripts are synergistically or diminishedly regulated in resistant cell lines, expression changes were evaluated by comparing the relative blast control and calculating relative differences.
(4) 투여량-의존적인 발현 변화의 조사(4) Investigation of Dose-dependent Expression Changes
저항성 세포주들에서 투여량에 의존적으로 발현이 변화하는 유전자를 확인하기 위하여, 2가지 통계적 접근법을 조합하였다 (Tseng, Y. H. et al., Nat. Cell Biol ., 7: 601-611, 2005). 먼저, 5개의 평균 발현 수준이 대조군 및 4가지 저항성 세포주들에서 이마티닙 투여량이 200 nM 로부터 800 nM 범위까지 연속적으로 고려되었다. 상승적 및 감소적 진행 상태의 중요도가 하기 수학식 1의 가설 또는 수학식 2의 역가설에 따라 결정되었다.In order to identify genes whose expression changes in dose-resistant cell lines, two statistical approaches were combined (Tseng, YH et al. , Nat. Cell Biol . , 7: 601-611, 2005). First, five average expression levels were considered consecutively in the control and four resistant cell lines, with imatinib doses ranging from 200 nM to 800 nM. The importance of synergistic and declining progression was determined according to the hypothesis of
먼저, 대조군으로 사용된 K562 세포와 비교하여 저항성을 보이는 4개 세포주 모두에서 상승적 또는 감소적으로 조절되는 전사체들 조사한 결과, 공통적으로 변화되는 전사체들은 과다 또는 과소 발현되는 것으로 관찰되었다 (표 1 참조). 구체적으로, 아폽토시스 (apoptosis) 관련 유전자, 즉 CASP4, TNFRSF21 및 TNFRSF9 는 저 항성 세포주들에서 공통적으로 상승 조절되고, 또한 전사 및 신호전달과 연관된 유전자, 즉 NOTCH2, SQSTM1 및 TGIF 는 감소적으로 조절되었다.First, as a result of investigating synergistically or diminishingly regulated transcripts in all four cell lines resistant to K562 cells used as a control, it was observed that commonly changed transcripts are over or underexpressed (Table 1). Reference). Specifically, apoptosis related genes, namely CASP4 , TNFRSF21 and TNFRSF9, are commonly upregulated in resistant cell lines, and also genes associated with transcription and signaling, such as NOTCH2 , SQSTM1 and TGIF, are reduced.
특히 NOTCH2 유전자는 그 산물이 백혈병 유발 과정 (leukemogenesis)에서 RAS 신호 전달에 포지티브 조절자이고, 미토젠-활성화 단백질 (MAP) 키나제와 함께 분자적 상호 연결에 관여하는 것으로 알려져 있다 (Aster, J. C. 및 Pear, W. S. Curr . Opin . Hematol ., 8: 237-244, 2001; Zeng, Q. et al., Cancer Cell, 8: 13-23, 2005). 또한, TGIF 는 TGF-β 신호 전달에 네가티브 피드백을 형성하는 전사 억제인자 (co-repressor)이다. 상기 발현 감소되는 유전자들 중에서, IGF1 및 PLCD1 유전자는 신호 전달과 관련되고, IGF1 는 발암화 뿐만 아니라 체세포 성장 및 발생을 조절하는 성장인자를 인코딩하는 것으로 보고되어 있다 (Zumkeller, W., Mol . Pathol ., 54: 285-288, 2001). 또한, PLCD1 유전자는 신호전달물질 (second messenger molecule)인 디아실글리세롤 및 이노시톨-1,4,5-트리포스페이트를 생산하여 신호 전달에 관여하였다 (Stallings, J. D. et al., J. Biol . Chem ., 280: 22060-22069, 2005). 또한, CCNB1P1과 같은 세포 주기와 관련된 분자들이 확인되어, G2/M 기를 통한 세포 주기의 진행 과정에 작용하는 것으로 보고되었다 (Toby, G. G. et al., Mol . Cell. Biol ., 23: 2109-2122, 2003).Especially NOTCH2 The gene is known to be a positive regulator of RAS signal transduction in its product, and is involved in molecular interconnection with mitogen-activated protein (MAP) kinases (Aster, JC and Pear, WS). . Curr Opin Hematol, 8: 237-244 , 2001; Zeng, Q. et al, Cancer Cell, 8:... 13-23, 2005). TGIF is also a co-repressor that forms negative feedback in TGF-β signaling. Among the expression decreasing genes, IGF1 and PLCD1 genes are involved in signal transduction, and IGF1 has been reported to encode growth factors that regulate somatic growth and development as well as carcinogenesis (Zumkeller, W., Mol . Pathol ., 54: 285-288, 2001). In addition, the PLCD1 gene produced the second messenger molecules diacylglycerol and inositol-1,4,5-triphosphate and was involved in signal transduction (Stallings, JD et al. , J. Biol . Chem . , 280: 22060-22069, 2005). In addition, molecules related to the cell cycle such as CCNB1P1 have been identified and reported to act on the progression of the cell cycle through the G 2 / M phase (Toby, GG et al. , Mol . Cell. Biol . , 23: 2109- 2122, 2003).
실시예Example 3. 3. 이마티닙Imatinib -저항성 세포주에서 In resistant cell lines 이마티닙Imatinib 투여량과 관련된 발현 변화 조사 Investigate changes in expression related to dosage
4가지 저항성 세포주들에서 유전자 발현 및 이마티닙 투여량 간의 반응 양상 (dose-response)을 보이는 유전자들이 조사되었다 (표 2 참조). 도 2 는 이마티닙의 투여량에 따른 유전자의 발현 변화를 이마티닙-저항성 유전자군을 사용하여 분석한 것이다. 이마티닙 투여량의 증가와 상호연관된 22개 유전자들 중에서, 전사와 관련된 4개의 유전자, 즉 NMI , FOXO3A , ZNF226 및 ZNF140 가 확인되었다.Genes showing dose-response between gene expression and imatinib doses were examined in four resistant cell lines (see Table 2). Figure 2 is a change analysis of gene expression according to the dose of imatinib using imatinib-resistant gene group. Of the 22 genes correlated with an increase in imatinib dosage, four genes involved in transcription, NMI , FOXO3A , ZNF226 And ZNF140 Was confirmed.
구체적으로, NMI 유전자로부터 인코드되는 단백질은 N-MYC, C-MYC 및 신호전달인자 (signal transducer)와 같은 전자조절인자 및 전자활성인자 (STAT)와 반응한다. 또한, NMI 유전자로부터 인코딩되는 단백질은 골수성 백혈병에서 높게 발현되는 것이 밝혀졌다 (Bao, J. 및 Zervos, A. S., Oncogene, 12: 2171-2176, 1996). 또한 신호 전달과 관련된 전사체인 LTBP1 은 TGF-β 신호전달 과정에 관련되어 TGF-β 분자와 반응하는 단백질을 생산한다. ATP 의존성 약제 전달체 (drug transporter)인 ABCA8 도 역시 이마티닙 투여량과 포지티브하게 관련된 발현 변화를 보이는 유전자들 중에서 확인되었다 (Tsuruoka, S. et al., Biochem . Biophys . Res. Commun ., 298: 41-45, 2002). 세포증식과 연관된 유전자는 이마티닙 투여량과 네가티브하게 상관된 전사체들 중에서 확인되었다. 또한, MLF1 의 전위 (translocation) 도 종종 골수형성이상 증후군 및 급성 골수성 백혈병에서 관찰되어 왔다 (Matsumoto, N. et al., Leukemia, 14: 1757-1765, 2000). 대사와 신호 전달과 관련된 유전자들 중에서, RAB11A 는 발암화 과정에 작용하는 RAS와 관련된 GTP 결합 단백질이다.Specifically, proteins encoded from the NMI gene react with electron regulators and electron activators (STATs), such as N-MYC, C-MYC and signal transducers. In addition, proteins encoded from the NMI gene were found to be highly expressed in myeloid leukemia (Bao, J. and Zervos, AS, Oncogene , 12: 2171-2176, 1996). LTBP1, a transcript involved in signal transduction, is also involved in the TGF-β signaling process and produces proteins that react with TGF-β molecules. ABCA8, an ATP-dependent drug transporter, has also been identified among genes with positive expression changes associated with imatinib doses (Tsuruoka, S. et al., Biochem . Biophys . Res. Commun . , 298: 41- 45, 2002). Genes associated with cell proliferation have been identified among transcripts that negatively correlated with imatinib dose. In addition, translocation of MLF1 has often been observed in myelodysplastic syndromes and acute myeloid leukemia (Matsumoto, N. et al. , Leukemia , 14: 1757-1765, 2000). Among the genes involved in metabolism and signal transduction, RAB11A is a GTP binding protein associated with RAS that acts on carcinogenesis.
실시예Example 4. 유전자 세트 증폭 분석 4. Gene Set Amplification Analysis
기능적으로 관련된 유전자: GO (Gene Ontology), BioCarta (http://www.biocarta.com) 및 KEGG (Kyoto Encyclopedia of Genes and Genomes), 및 GenMAPP (Gene MicroArray Pathway Profiler)가 일반 유전자 데이터베이스로부터 수집되었다 (Harris, M. A. et al., Nucleic Acids Res., 32: D258-D261, 2004; Kanehisa, M. et al., Nucleic Acids Res., 30: 42-46, 2002; Dahlquist, K. D. et al., Nat. Genet., 31: 19-20, 2002). 유전자를 매치하여 특정 표시가 된 유전자 세트로 분류하고, 공통의 기능적 표시가 있지만 서로 배타적이지는 않은 3,774개 유전자 세트들이 수집되었다. 유전자의 증폭 분석은 Z-통계에 기초한 중요도를 직접 계산하는 지수 분석 (PAGE)을 사용하여 이루어졌다. 상기 분석을 수행하기 위하여, 최소 유전자 세트에 해당하는 적어도 10개의 유전자를 포함하는 721 세트들로 초기 유전자 세트들을 제한하였다. 여기서는 Z-통계학에 기초한 중요도를 산정하기 위하여 2종류의 지수값, 즉 상대적 차이 r.d. 및 Fk 를 사용하였다. Functionally related genes: GO (Gene Ontology), BioCarta ( http://www.biocarta.com ) and KEGTO (Kyoto Encyclopedia of Genes and Genomes), and Gene MicroArray Pathway Profiler (GenMAPP) were collected from the general genetic database ( Harris, MA et al. , Nucleic Acids Res. , 32: D258-D261, 2004; Kanehisa, M. et al ., Nucleic Acids Res. , 30: 42-46, 2002; Dahlquist, KD et al ., Nat. Genet. , 31: 19-20, 2002). Genes were matched and sorted into sets of genes with specific markers, and 3,774 sets of genes with common functional markers but not mutually exclusive were collected. Amplification analysis of genes was done using exponential analysis (PAGE), which directly calculates importance based on Z-statistics. To perform the analysis, initial gene sets were limited to 721 sets containing at least 10 genes corresponding to the minimum gene set. In this case, two kinds of index values, ie, relative differences rd and F k, are used to calculate the importance based on Z-statistics.
이마티닙 저항성 유전자 세트들에서 700개 정도의 기능이 알려진 유전자 세트들에 대한 증폭의 통계적 중요도를 측정하여 분석한 결과, 표 3에 보는 바와 같이 활성화 또는 억제된 유전자 세트가 밝혀졌다.As a result of measuring and analyzing the statistical significance of amplification for gene sets of about 700 known functions in imatinib-resistant gene sets, the gene sets activated or suppressed were identified as shown in Table 3.
15개의 활성화된 유전자 세트는 다음과 같다: 전사 조절과 관련된 4개의 유전자 세트; DNA 결합, 핵산 결합, 아연 이온 결합과 같은 전사와 관련이 있는 듯한 3개의 유전자 세트; 아폽토시스와 연관된 2개의 유전자 세트; 및 TGF-β 신호전달 과정과 관련된 유전자 세트. 또한, 7개의 억제된 유전자 세트는 다음과 같다: 생합성, 운반 및 접힘 그리고 단백질 대사에 관련된 유전자 세트; 및 작은 GTPase 신호전달과 관련된 3개의 유전자 세트. The 15 activated gene sets are as follows: four gene sets involved in transcriptional regulation; Three sets of genes that appear to be involved in transcription such as DNA binding, nucleic acid binding, and zinc ion binding; Two sets of genes associated with apoptosis; And a set of genes associated with the TGF-β signaling process. In addition, the seven suppressed gene sets are: gene sets involved in biosynthesis, transport and folding and protein metabolism; And three gene sets associated with small GTPase signaling.
실시예Example 5. 골수성 백혈병 5. Myeloid Leukemia 환자에서In patients 유전자 발현 프로파일 조사 Gene Expression Profile Investigation
본 발명은 CML 환자의 유전자 발현 프로파일을 조사하기 위하여, 실시간 정량적 PCR 분석을 다음과 같이 실시하였다. 이마티닙 저항성이 획득된 전후로 6명의 CML 환자들의 혈액 시료로부터 얻은 전체 RNA 가 6가지 후보 유전자: CASP4, TNFRSF21, RAB11A, IGF1, LYN 및 RHOA 에 대한 실시간 QPCR 분석에 사용되었다. 그 결과, 환자들 중 3명은 BCR-ABL 돌연변이를 가지고 있고, 나머지 3명에서는 돌연변이가 발견되지 않았다. 첫 번째 cDNA 가닥은 M-MLV 역전사효소 (Invitrogen사 제품)를 사용하여 합성되어 PCR 에 사용되었다. 실시간 QPCR 은 MxPro 버전 3.00 소프트웨어 (Stratagene사 제품)과 함께 Mx300P QPCR 시스템을 사용하여 수행되었다. 20 μL의 실시간 QPCR 반응물에는 10 ng cDNA, 1X SYBR Green Tbr 폴리머라제 혼합물, 0.5X ROX 및 20 pmole 프라이머를 첨가하였다. 본 발명에서는 서열번호 1 내지 서열번호 14의 염기 서열을 포함하는 프라이머를 합성하여 사용하였다. 이 때 GAPDH가 각 과정의 대조군으로 사용되었다. In order to investigate the gene expression profile of CML patients, the present invention was performed in real time quantitative PCR analysis as follows. Total RNA from blood samples from six CML patients before and after imatinib resistance was obtained was used for real-time QPCR analysis for six candidate genes: CASP4, TNFRSF21, RAB11A, IGF1, LYN and RHOA . As a result, three of the patients had a BCR-ABL mutation and no mutations were found in the other three. The first cDNA strand was synthesized using M-MLV reverse transcriptase (Invitrogen) and used for PCR. Real-time QPCR was performed using the Mx300P QPCR system with MxPro version 3.00 software from Stratagene. 20 μL of real time QPCR reaction was added with 10 ng cDNA, 1 × SYBR Green Tbr polymerase mixture, 0.5 × ROX and 20 pmole primer. In the present invention, a primer comprising a nucleotide sequence of SEQ ID NO: 1 to SEQ ID NO: 14 was synthesized and used. GAPDH was used as a control for each process.
상기 QPCR 과정은: 95℃, 10분; 94℃, 10초, 40회 반복; 55 - 60℃, 30초; 및 72℃, 30초로 진행되었다. 특정 증폭 여부를 확인하기 위하여, 곡선 (melting curve) 분석이 55 - 95℃, 0.5℃/sec로 수행되었다. 상대적 정량은 △Ct 방법으로 수행하였다. The QPCR procedure was: 95 ° C., 10 minutes; 94 ° C., 10 seconds, 40 repetitions; 55-60 ° C., 30 seconds; And 72 ° C., 30 seconds. In order to confirm the specific amplification, the melting (melting curve) analysis was performed at 55-95 ℃, 0.5 ℃ / sec. Relative quantification was performed by the ΔC t method.
생체 외 모델에서 이마티닙 저항성을 획득하여 생긴 발현 변화가 실제로 백혈병 (CML) 환자들에게도 적절한지 여부를 확인하기 위하여, 이마티닙 저항성을 보이는 6명의 CML 환자들을 대상으로 실험하였다. 상기 저항성을 획득하기 전 및 후에 발현 변화의 로그 비율 (Log2 ratio)이 BCR-ABL 돌연변이 (n = 3)가 있는지에 따라 각 환자에 대해 계산되었다 (도 3 참조). 도 3a, 도 3b 및 도 3c 는 만성 골수성 백혈병 (CML)의 이마티닙 저항성을 6가지 후보 유전자의 발현 변화로 분석한 것이다. 이 때 K562 대 KR800nM 간의 발현 비율이 기준이 되었다. Six CML patients with imatinib resistance were tested to determine whether the expression changes resulting from obtaining imatinib resistance in an in vitro model were actually appropriate for leukemia (CML) patients. The log ratio of expression change (Log 2 ratio) before and after obtaining the resistance was calculated for each patient depending on the presence of the BCR-ABL mutation (n = 3) (see FIG. 3). 3A, 3B and 3C show the imatinib resistance of chronic myeloid leukemia (CML) as a change in expression of six candidate genes. At this time, the expression ratio between K562 and KR 800nM was the reference.
구체적으로 CASP4 및 TNFRSF21 은 이마티닙 저항성을 획득한 후에 각각 4명과 3명에서 상승적으로 조절되었다, 그러나 이 발현 비율이 BCR-ABL 돌연변이에 대한 포지티브 및 네가티브 환자들 간에는 명확하게 구분되지 않았다. 한편, RAB11A 및 IGF1 은 BCR-ABL 돌연변이 네가티브 환자들에서 일관되게 감소되었으며, BCR-ABL 돌연변이 포지티브 환자들 3명 중 2명에서는 상승되었다. 또한, 이미 이마티닙 저항성과 관련되어 상승되는 것으로 보고된 LYN 및 RHOA 에 대해서도 조사되었다. 이들이 BCR-ABL 돌연변이가 없는 세포주에서 증가된다고 하더라도, 본 연구에서는 상기 돌연변이 네가티브 환자 3명 중 2명에서 과소발현되는 것으로 밝혀졌다. 또한, LYN 및 RHOA 의 발현은 오히려 돌연변이 포지티브 환자 3명 중 2명에서 유의하게 상승되었다.Specifically, CASP4 and TNFRSF21 were synergistically regulated in four and three patients after obtaining imatinib resistance, but this expression rate was not clearly distinguished between positive and negative patients for BCR-ABL mutations. On the other hand, RAB11A and IGF1 were consistently reduced in BCR-ABL mutant negative patients and elevated in 2 of 3 BCR-ABL mutant positive patients. In addition, LYN and RHOA which have already been reported to be elevated in relation to imatinib resistance Was also investigated. Although they are increased in cell lines without BCR-ABL mutations, this study was found to be underexpressed in two of the three mutant negative patients. In addition, expression of LYN and RHOA was significantly elevated in two out of three mutant positive patients.
상술한 바와 같이, 본 발명은 만성 골수성 백혈성 (chronic myelogenous leukemia; CML)을 치료하는 약제 저항성 (drug resistance)을 예측하는 유전자, 이를 이용하는 항암제 저항성의 진단 방법 및 진단 키트에 관한 것으로서, 항암제인 이마티닙 (imatinib)에 대한 저항성을 부여하는 유전자 발현 신호를 다양한 저항성 유전자군을 사용하여 감지하는 과정으로, 만성 골수성 백혈병을 포함한 각종 암을 효과적으로 진단하고 치료하며 더 나아가 글리벡에 대한 저항성 기작을 연구하는 데 널리 사용될 수 있다.As described above, the present invention relates to a gene for predicting drug resistance for treating chronic myelogenous leukemia (CML), a diagnostic method and a diagnostic kit for anticancer drug resistance using the same, and an anticancer agent imatinib A gene expression signal that confers resistance to imatinib is detected using various groups of resistance genes, and is widely used to effectively diagnose and treat various cancers including chronic myelogenous leukemia and further study the mechanism of resistance to Gleevec. Can be used.
<110> CATHOLIC UNIVERSITY INDUSTRY ACADEMIC COOPERATION FOUNDATION <120> Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent <130> PN060075 <160> 14 <170> KopatentIn 1.71 <210> 1 <211> 21 <212> DNA <213> Artificial Sequence <220> <223> CASP4-Forward primer <400> 1 acacgcctgg ctctcatcat a 21 <210> 2 <211> 19 <212> DNA <213> Artificial Sequence <220> <223> CASP-4 Reverse primer <400> 2 cacagttccc cacggtttg 19 <210> 3 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> TNFRSF21 Foward Primer <400> 3 caaggccccc accacagaca catc 24 <210> 4 <211> 22 <212> DNA <213> Artificial Sequence <220> <223> TNFRSF21 Reverse Primer <400> 4 gccggggccc ctttttcaga gt 22 <210> 5 <211> 17 <212> DNA <213> Artificial Sequence <220> <223> RAB11A Forward primer <400> 5 acccgcgacg acgagta 17 <210> 6 <211> 21 <212> DNA <213> Artificial Sequence <220> <223> RAB11A Revers Primer <400> 6 gcccacaagc atgataacaa t 21 <210> 7 <211> 20 <212> DNA <213> Artificial Sequence <220> <223> IGF1 Forward Primer <400> 7 gcggggctga gctggtggat 20 <210> 8 <211> 22 <212> DNA <213> Artificial Sequence <220> <223> IGF1 Reverse Primer <400> 8 ggtcttgggc atgtcggtgt gg 22 <210> 9 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> LYN Forward Primer <400> 9 atacatcgag cggaagaact acat 24 <210> 10 <211> 17 <212> DNA <213> Artificial Sequence <220> <223> LYN Reverse Primer <400> 10 acagggcggt catcacg 17 <210> 11 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> RHOA Forward Primer <400> 11 acagctgggc aggaagatta tgat 24 <210> 12 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> RHOA Reverse Primer <400> 12 acaagacaag gcacccagat tttt 24 <210> 13 <211> 22 <212> DNA <213> Artificial Sequence <220> <223> GAPDH Forward Primer <400> 13 gcggggctct ccagaacatc at 22 <210> 14 <211> 21 <212> DNA <213> Artificial Sequence <220> <223> GAPDH Reverse Primer <400> 14 ccagccccag cgtcaaaggt g 21 <110> CATHOLIC UNIVERSITY INDUSTRY ACADEMIC COOPERATION FOUNDATION <120> Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent <130> PN060075 <160> 14 <170> Kopatentin 1.71 <210> 1 <211> 21 <212> DNA <213> Artificial Sequence <220> <223> CASP4-Forward primer <400> 1 acacgcctgg ctctcatcat a 21 <210> 2 <211> 19 <212> DNA <213> Artificial Sequence <220> <223> CASP-4 Reverse primer <400> 2 cacagttccc cacggtttg 19 <210> 3 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> TNFRSF21 Foward Primer <400> 3 caaggccccc accacagaca catc 24 <210> 4 <211> 22 <212> DNA <213> Artificial Sequence <220> <223> TNFRSF21 Reverse Primer <400> 4 gccggggccc ctttttcaga gt 22 <210> 5 <211> 17 <212> DNA <213> Artificial Sequence <220> <223> RAB11A Forward primer <400> 5 acccgcgacg acgagta 17 <210> 6 <211> 21 <212> DNA <213> Artificial Sequence <220> <223> RAB11A Revers Primer <400> 6 gcccacaagc atgataacaa t 21 <210> 7 <211> 20 <212> DNA <213> Artificial Sequence <220> <223> IGF1 Forward Primer <400> 7 gcggggctga gctggtggat 20 <210> 8 <211> 22 <212> DNA <213> Artificial Sequence <220> <223> IGF1 Reverse Primer <400> 8 ggtcttgggc atgtcggtgt gg 22 <210> 9 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> LYN Forward Primer <400> 9 atacatcgag cggaagaact acat 24 <210> 10 <211> 17 <212> DNA <213> Artificial Sequence <220> <223> LYN Reverse Primer <400> 10 acagggcggt catcacg 17 <210> 11 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> RHOA Forward Primer <400> 11 acagctgggc aggaagatta tgat 24 <210> 12 <211> 24 <212> DNA <213> Artificial Sequence <220> <223> RHOA Reverse Primer <400> 12 acaagacaag gcacccagat tttt 24 <210> 13 <211> 22 <212> DNA <213> Artificial Sequence <220> <223> GAPDH Forward Primer <400> 13 gcggggctct ccagaacatc at 22 <210> 14 <211> 21 <212> DNA <213> Artificial Sequence <220> <223> GAPDH Reverse Primer <400> 14 ccagccccag cgtcaaaggt g 21
Claims (9)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020060062231A KR101326367B1 (en) | 2006-07-03 | 2006-07-03 | Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020060062231A KR101326367B1 (en) | 2006-07-03 | 2006-07-03 | Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20080003692A KR20080003692A (en) | 2008-01-08 |
| KR101326367B1 true KR101326367B1 (en) | 2013-11-11 |
Family
ID=39214819
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020060062231A Expired - Fee Related KR101326367B1 (en) | 2006-07-03 | 2006-07-03 | Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101326367B1 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107427552A (en) * | 2014-08-22 | 2017-12-01 | 中国科学院生物物理研究所 | Methods and compositions for treating and/or preventing diseases or disorders associated with abnormal levels and/or activity of the IFP35 protein family |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101994821B1 (en) * | 2016-11-23 | 2019-07-01 | 연세대학교 산학협력단 | Use of forkhead box o 3 protein |
-
2006
- 2006-07-03 KR KR1020060062231A patent/KR101326367B1/en not_active Expired - Fee Related
Non-Patent Citations (1)
| Title |
|---|
| Stem Cells, Vol. 21, No. 3, pp315-321(2003.05.01.) * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107427552A (en) * | 2014-08-22 | 2017-12-01 | 中国科学院生物物理研究所 | Methods and compositions for treating and/or preventing diseases or disorders associated with abnormal levels and/or activity of the IFP35 protein family |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20080003692A (en) | 2008-01-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Durrand et al. | Variations in the sequence and expression of the Plasmodium falciparum chloroquine resistance transporter (Pfcrt) and their relationship to chloroquine resistance in vitro | |
| JP6404208B2 (en) | Methods of prognosis, diagnosis and treatment of idiopathic pulmonary fibrosis | |
| JP6280206B2 (en) | Prognosis prediction system for locally advanced gastric cancer | |
| US20140005070A1 (en) | Markers associated with cyclin-dependent kinase inhibitors | |
| CN109837340B (en) | Peripheral blood gene marker for noninvasive diagnosis of lung cancer | |
| KR20180054829A (en) | Method for evaluating immunity repertoire steadiness and its use | |
| JPWO2015093557A1 (en) | A novel fusion gene as a responsible factor for gastric cancer | |
| Abramzon et al. | Investigating RFC1 expansions in sporadic amyotrophic lateral sclerosis | |
| JP5161091B2 (en) | Markers for predicting anti-cancer drug response in patients with acute myeloid leukemia | |
| Jensen et al. | A distinctive gene expression fingerprint in mentally retarded male patients reflects disease-causing defects in the histone demethylase KDM5C | |
| CN112921091B (en) | Use of FLT3 gene mutation in predicting sensitivity of non-small cell lung cancer patient to immune checkpoint inhibitor therapy | |
| KR101326367B1 (en) | Diagnostic methods and kits for monitoring resistance to therapeutic chemoagent | |
| KR20170055435A (en) | Methods and compositions for determining resistance of cancer treatment | |
| KR102280463B1 (en) | Primers for diagnosis of Leukemia, and method for diagnosis of Leukemia using the same | |
| KR20230028619A (en) | Biomarker for diagnosing atopic dermatitis and use thereof | |
| Peuckert et al. | Adaptive changes in gene expression patterns in the somatosensory cortex after deletion of ephrinA5 | |
| US20100221738A1 (en) | Method of diagnosis of a predisposition to develop thrombotic disease and its uses | |
| JP7665526B2 (en) | Method for predicting sensitivity of cancer cells to helicase inhibitors | |
| KR100962209B1 (en) | Biomarker for Checking Malachite Green Exposure and Confirmation Method Using the Same | |
| JPWO2006013862A1 (en) | Method for predicting drug sensitivity to CDK4 inhibitor | |
| KR102781057B1 (en) | Novel Biomarker for Diagnosing Charcot-Marie-Tooth Disease Comprising Mutation of MPZ Gene and Uses Thereof | |
| US9512484B2 (en) | Methods for determining a prognosis for survival for a patient with breast cancer | |
| EP3489364A1 (en) | Method for assisting determination of hematological stage of childhood acute lymphoblastic leukemia | |
| KR20250143182A (en) | Analytical method for classification of non-small cell lung cancer patients showing prognosis of responsiveness to cisplatin | |
| WO2025041146A1 (en) | Markers of resistance and systemic inflammation and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| FPAY | Annual fee payment |
Payment date: 20161027 Year of fee payment: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20170927 Year of fee payment: 5 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| FPAY | Annual fee payment |
Payment date: 20181001 Year of fee payment: 6 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: A-4-4-U10-U13-oth-PC1903 Not in force date: 20191101 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20191101 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |