발명의 설명
이하 본 발명에 사용된 용어를 정의하였다.
정의
결합분자
본 발명에 사용되는 용어 "결합 분자"는 키메릭, 인간화 또는 인간 모노클로날 항체와 같은 모노클로날 항체를 포함하는 완전한 면역글로불린, 또는 항원-결합 및/또는 면역글로불린의 결합 파트너, 즉 SARS-CoV에 특이적으로 결합하기 위해 완전한 면역글로불린과 경쟁하는 면역글로불린의 단편을 포함하는 가변 도메인을 말한다. 구조와 상관없이, 항원-결합 단편은 완전한 면역글로불린에 의해 인식되는 동일한 항원과 결합된다. 항원-결합 단편은 결합 분자의 아미노산 서열의 적어도 2개의 연속 아미노산 잔기, 적어도 5개의 연속 아미노산 잔기, 적어도 10개의 연속 아미노산 잔기, 적어도 15개의 연속 아미노산 잔기, 적어도 20개의 연속 아미노산 잔기, 적어도 25개의 연속 아미노산 잔기, 적어도 30개의 연속 아미노산 잔기, 적어도 35개의 연속 아미노산 잔기, 적어도 40개의 연속 아미노산 잔기, 적어도 50개의 연속 아미노산 잔기, 적어도 60개의 연속 아미노산 잔기, 적어도 70개의 연속 아미노산 잔기, 적어도 80개의 연속 아미노산 잔기, 적어도 90개의 연속 아미노산 잔기, 적어도 100개의 연속 아미노산 잔기, 적어도 125개의 연속 아미노산 잔기, 적어도 150개의 연속 아미노산 잔기, 적어도 175개의 연속 아미노산 잔기, 적어도 200개의 연속 아미노산 잔기, 적어도 250개의 연속 아미노산 잔기의 아미노산 서열을 포함하는 펩티드 또는 폴리펩티드를 포함할 수 있다.
본 명세서에 사용되는 바와 같이, 용어 "결합 분자"는 본 분야에 알려진 모든 면역글로불린류 및 아류를 포함한다. 그들의 중쇄의 불변 도메인의 아미노산 서열에 따라, 결합 분자는 완전 항체의 5가지의 주류로 나눌 수 있다:IgA, IgD, IgE, IgG 및 IgM. 그리고 이들 중 여럿은 아류(이소타입)로 더욱 나눌 수 있다:예를 들면, IgA1, IgA2, IgG1, IgG2, IgG3 및 IgG4.
항원-결합 단편은, 무엇보다도, Fab, F(ab'), F(ab')2, Fv, dAb, Fd, 상보성 결정영역(CDR) 단편, 단일-사슬 항체(ScFv), 이가의 단일-사슬 항체, 단일-사슬 파아지 항체, diabodies, triabodies, tetrabodies, 폴리펩티드에 결합된 특이 항원을 제공하기에 충분한 면역글로불린의 적어도 단편을 함유하는 (폴리)펩티드를 포함한다. 상기 단편들은 합성적으로 또는 효소적으로 또는 완전한 면역글로불린의 화학적 분열에 의해 생산될 수 있고 또는 재조합 DNA 기술에 의해 유전적으로 설계될 수 있다. 생산의 방법은 본 분야에 잘 알려져 있고 예를 들면, Antibodies: A Laboratory Manual, Edited By: E. Harlow 및 D. Lane(1988), Cold Spring Harbor Laboratory, Cold Spring Harbor, New York에 기재되어 있고, 여기에 참조로 병합되어 있다. 결합분자 또는 그들의 항원-결합 단편은 하나 이상의 결합 부위를 가질 수 있다. 하나보다 많은 결합부위를 갖는 경우, 결합 부위들은 서로 동일하거나 또는 다를 수 있다.
결합분자는 네이크(nake)된 또는 비컨쥬게이트된 결합 분자일 수 있지만, 또한 면역컨쥬게이트의 일부일 수 있다. 네이크된 또는 비컨쥬게이트된 결합분자는, 컨쥬게이트되고, 효과적으로 연결되고, 또는 한편으로 물리적으로 또는 무엇보다도, 독성 물질, 방사성 물질, 리포좀, 효소와 같은 기능적으로 작동체(effector) 부분 또는 테그와 연결되지 않는 결합분자를 말하는 의도이다. 네이크된 또는 비컨쥬게이트된 결합 분자는 작동체 부분 또는 태그의 결합에 의한 것 이외의, 안정화되고, 멀티머화되고, 인간화되거나 또는 다른 방법으로 조작된 결합분자를 배척하지 않는다. 따라서, 모든 후-번역적으로 변형된 네이크된 및 비컨쥬게이트된 결합 분자들은 여기에 포함되고, 변형이 재조합 결합 분자-생산 세포에 의해, 천연 결합 분자-생산 세포 환경에서 이루어지고, 초기 결합 분자 제조 후 인간의 손에 의해 도입되는 것을 포함한다. 물론, 용어 네이크된, 또는 비컨쥬게이트된 결합분자는 작동체세포 및/또는 분자와 기능적 관련을 형성하는 결합분자의 가능성을 배척하지 않고, 이와 같은 상호작용의 몇몇은 생리적 효과를 발휘하기 위해 필요하기 때문이다.
생리적 샘플
여기서 사용되는 바에 따라, 용어 "생리적 샘플"은 혈액 및 생리적 기원의 다른 액체 샘플, 생검 시편 또는 조직 배양물과 같은 고형 조직 샘플, 또는 그로부터 유래된 세포 및 그들의 자손을 포함하여, 샘플 타입의 다양성을 망라한다. 또한, 용어는 그들의 획득 후, 예를 들면 시약으로 처리, 고형화, 또는 단백질 또는 폴리뉴클레오티드와 같은 특정 성분의 풍부에 의한 바와 같이, 여러 방법으로 조작된 샘플을 포함한다. 용어는 어느 종류로부터 얻은 임상적 샘플의 여러 종류를 포함하고, 또한 배양물 중의 세포, 세포 상징액 및 세포 용출물을 포함한다.
상보적 결정 영역(
CDR
)
본 명세서에서 사용되는 용어 "상보적 결정 영역"은 면역글로불린과 같은 결합 분자의 가변영역 내의 서열을 의미하고, 보통 형태와 전하 분포에서 항원에서 인식되는 에피토프와 상보적인 항원 결합 부위에 대부분 기여한다. CDR 영역은 선형 에피토프, 불연속 에피토프, 또는 단백질의 천연 형태로 단백질 상에 존재하거나 또는 몇몇 경우, 예를 들면, SDS에서 안정화됨에 의해 변형된 단백질 상에 존재하는 바와 같이, 단백질 또는 단백질 단편의 구조적(conformational) 에피토프에 특이적일 수 있다. 에피토프는 또한 단백질의 후번역 변형으로 이루어진다.
발현-조절 핵산 서열
여기서 사용되는 용어 "발현-조절 핵산 서열"은 특정 숙주 유기물에서 사용가능하게 연결된 암호화 서열의 발현에 필요하거나 및/또는 영향을 미치는 폴리뉴클레오티드 서열을 말한다. 발현-조절 핵산 서열, 무엇보다도 적절한 전사 개시, 종료, 프로모터, 인핸서 서열; 스플라이싱(splicing)과 같은 효과적인 RNA 처리 시그널 및 폴리아데닐화 시그널; 세포질 mRNA를 안정화시키는 서열; 번역 효율을 강화하는 서열(예를 들면, 리보솜 결합부위); 단백질 안정성을 강화하는 서열; 및 필요한 경우, 단백질 분비를 강화하는 서열은 선택된 숙주 유기체에서 활성을 나타내는 어느 핵산 서열일 수 있고 그리고 단백질을 암호화하는 유전자에서 유래될 수 있고, 이것은 숙주 유기체와 상동 또는 비상동이다. 발현-조절 서열의 동정 및 작용은 본 분야의 당업자들에게는 정례적인 것이다.
기능적
변이체
여기서 사용되는 용어 "기능적 변이체"는 부모 결합 분자의 뉴클레오티드 및/또는 아미노산 서열과 비교하여 하나 이상의 뉴클레오티드 및/또는 아미노산에 의해 변형되고 여전히 결합 파트너, 예를 들면, SARS-CoV에 결합하기 위해, 부모 결합 분자와 경쟁할 수 있는 뉴클레오티드 및/또는 아미노산 서열을 포함하는 결합분자를 말한다. 다시 말하면, 부모 결합 분자의 아미노산 및/또는 뉴클레오티드 서열에서의 변형은 뉴클레오티드 서열에 의해 암호화되거나 아미노산 서열을 함유하는 결합 분자의 결합 특성에 상당한 영향을 미치거나 변형시키지 않고, 즉 결합 분자는 여전히 그것의 표적을 인식하고 결합할 수 있다. 기능적 변이체는 뉴클레오티드와 아미노산 치환, 첨가 및 결실을 포함하는 보수적인 서열 변형을 가질 것이다. 이들 변형은 부위-지향 돌연변이 생성 및 랜덤 PCR- 조절 돌연변이 생성과 같은 본 분야에 알려진 표준 기술에 의해 유도될 수 있고, 비-천연 뉴클레오티드와 아미노산 뿐 아니라 천연 뉴클레오티드를 포함할 것이다.
보존적(conservative) 아미노산 치환체는 아미노산 잔기가 유사한 구조적 또는 화학적 특성을 갖는 아미노산 잔기로 대체된 것을 포함한다. 유사한 부사슬을 갖는 아미노산 잔기의 종류들이 본 분야에 정의되어 있다. 이들 종류들은 염기성 부사슬(예를 들면, 라이신, 아르기닌, 히스티딘), 산성 부사슬(예를 들면, 아스파르트산, 글루타민산), 비하전된 극성 부사슬(예를 들면, 글리신, 아스파라긴, 글루타민, 세린, 트레오닌, 티로신, 시스틴, 트립토판), 비극성 부사슬(예를 들면, 알라닌, 발린, 로이신, 이소로이신, 프롤린, 페닐알라닌, 메티오닌), 베타-분지된 부사슬(예를 들면, 트레오닌, 발린, 이소로이신) 및 방향족 부사슬(예를 들면, 티로신, 페닐알라닌, 트립토판, 히스티딘)을 갖는 아미노산을 포함한다. 위에서 사용된 것 이외의 아미노산 잔기 종류의 분류가 또한 적용될 수 있다는 것은 당업자에게 명백할 것이다. 더우기, 변이체는 비-보전적 아미노산 치환물, 예를 들면, 다른 구조 및 화학적 특성을 갖는 아미노산 잔기에 의한 아미노산의 대체물을 가질 수 있다. 유사한 사소한 변이는 또한 아미노산 결실 또는 삽입, 또는 둘 다를 포함할 수 있다. 면역학적 활성의 파기없이 어느 아미노산 잔기가 치환되고, 삽입되고 또는 결실되는가를 결정하는 안내는 본 분야에 잘 알려진 컴퓨터 프로그램을 사용하여 발견될 수 있다.
뉴클레오티드 서열의 돌연변이는 전이 또는 전위 돌연변이와 같은 유전자자리에서 이루어지는 단일 변형(1점 돌연변이)일 수 있고, 또는 선택적으로, 복수개의 뉴클레오티드가 단일 유전자자리에서 삽입, 결실 또는 변화될 수 있다. 이에 더하여, 하나 이상의 변형이 뉴클레오티드 서열 내의 어느 수의 유전자 자리에서 이루어질 수 있다. 돌연변이는 본 분야에 알려진 어느 알맞은 방법으로 실시될 수 있다.
숙주
여기서 사용되는 용어 "숙주"는 그곳으로 클로닝 벡터 또는 발현 벡터와 같은 벡터가 도입되어진 유기체 또는 세포를 말하는 것을 의도한다. 유기체 또는 세포는 원핵 또는 진핵일 수 있다. 이 용어는 특정 개체 유기물 또는 세포만을 언급하는 것이 아니며 또한 유기체와 세포의 자손도 언급하는 의미이다. 어느 변형은 돌연변이 또는 환경적 영향에 의해 연속적인 세대에서 발생할 수 있기 때문에, 이와 같은 자손은, 실제로, 부모 유기체 또는 세포와 동일하지 않을 수 있지만, 여기서 사용되는 용어 "숙주"의 범위에는 여전히 포함된다.
인간
용어 "인간'은, 여기서 정의된 바와 같이 결합분자에 적용될 때, 인간으로부터 직접 유래되거나 또는 인간 서열을 기재로 하는 분자를 말한다. 결합 분자가 인간서열로부터 유래되거나 기재로 하고 이어서 변형되면, 이것은 여전히 본 명세서에 전반적으로 사용된 바와 같이 인간으로 간주된다. 다시 말하면, 용어 인간은 결합 분자에 적용될 때, 가변 또는 불변 영역 어느 것을 기준으로 하거나, 인간 또는 인간 림프구에서 또는 변형된 형태에서 발생하지 않는 인간 생식계 면역글로불린 서열로부터 유래된 가변 및 불변 영역을 갖는 결합분자를 포함하는 것을 의도한다. 그러므로, 인간 결합 분자는 인간 생식계 면역글로불린 서열에 의해 암호화되지 않는 아미노산 잔기를 포함할 수 있고, 치환 및/또는 결실을 포함한다(예를 들면, 인비트로 임의 또는 부위-특이 돌연변이 또는 인비보 체세포 돌연변이에 의해 도입되는 돌연변이). 여기서 사용되는 "기재로 하는 (based on)"은 핵산 서열이 주형으로부터 정확히 복사되거나, 또는 에러가 많은(error-pronc) PCT법에서와 같이 사소한 돌연변이를 갖거나, 또는 주형과 정확히 매치되도록 인공적으로 제조되거나 또는 사소한 변형을 갖는 상황을 말한다. 인간 서열을 기재로 하는 반합성 분자는 또한 여기서 사용되는 인간으로 간주된다.
단리
용어 "단리"는, 여기서 정의된 바와 같이 결합분자에 적용될 때, 실질적으로 다른 단백질 또는 폴리펩티드가 없는, 특히 다른 항원 특이성을 갖는 다른 결합 분자가 없고, 또한 실질적으로 다른 세포형 재료 및/또는 화학약품이 없는 결합분자를 말한다. 예를 들면, 결합 분자가 재조합적으로 생산되면, 이들은 바람직하기는 실질적으로 배지가 없고, 결합분자가 화학적 합성에 의해 생산되면, 이들은 바람직하기는 실질적으로 화학적 전구체 또는 다른 화학약품이 없고, 즉 이들은 단백질의 합성에 참여한 화학적 전구체 또는 다른 화학약품으로부터 분리된다. 용어 "단리"는, 여기에 정의된 바와 같이 결합 분자를 암호화하는 핵산 분자에 적용될 때, 결합분자를 암호화하는 뉴클레오티드 서열이, 다른 서열, 특히 SARS-CoV 이외의 결합분자에 결합하는 결합분자를 암호화하는 뉴클레오티드 서열이 없는 핵산분자를 말하는 의도이다. 또한, 용어 "단리된"은 천연숙주에서 천연 핵산 분자를 천연적으로 수바나는 다른 세포형 성분으로부터 실질적으로 분리된 핵산분자를 말한다. 더우기, cDNA와 같은 "단리된" 핵산 분자는 다른 세포물질 또는 재조합 기술에 의해 생산될 때는 배지가 실질적으로 없을 수 있고 또는 화학적으로 합성될 때에는 화학적 전구체 또는 다른 화학약품이 실질적으로 없을 수 있다.
모노클로날
항체
여기서 사용되는 용어 "모노클로날 항체"는 단일 분자 조성물의 항체 분자의 제제를 말한다. 모노클로날 항체는 특정 에피토프에 대해 단일 결합 특이성 및 친화성을 나타낸다. 따라서, 용어 "인간 모노클로날 항체"는 인간 생식계 면역글로불린 서열로부터 유래되거나 또는 기재로 하는 또는 완전히 합성 서열로부터 유래된 가변 및 불변영역을 갖는 단일 결합 특이성을 나타내는 항체를 말한다. 모노클로날 항체의 제조방법은 중요하지 않다.
핵산분자
본 발명에 사용되는 용어 "핵산분자"는 뉴클레오티드의 중합형태를 말하고 RNA, cDNA, 게놈성 DNA 및 합성 형태 및 상기의 혼합된 폴리머의 센스 및 안티센스모두를 포함한다. 뉴클레오티드는 리보뉴클레오티드, 데옥시뉴클레오티드 또는 뉴클레오티드의 어느 타입의 변형된 형태를 말한다. 용어는 또한 DNA의 단일- 및 이중-스트랜드 형태를 포함한다. 이에 더하여, 폴리뉴클레오티드는 천연적으로-발생하는 및 천연적으로-발생하는 및/또는 비-천연적으로 발생하는 뉴클레오티드 연결에 의해 함께 연결된 변형된 뉴클레오티드 중 어느 것 또는 모두를 포함할 수 있다. 핵산 분자는 화학적으로 또는 생화학적으로 변형될 수 있거나 또는 비-천연적 또는 유도된 뉴클레오티드 염기를 함유할 수 있고, 본 분야의 당업자들에 의해 쉽게 이해될 것이다. 이와 같은 변형은, 예를 들면, 라벨, 메틸화, 하나 이상의 천연적으로 발생한 뉴클레오티드의 동족체에 의한 치환, 비하전된 연결과 같은 뉴클레오티드간 변형(예를 들면, 메틸 포스포네이트, 포스포트리에스테르, 포스포라미데이트, 카바메이트 등), 하전된 연결(예를 들면, 포스포로티오에이트, 포스포로디티오에이트, 등), 펜던트 모이어티(예를 들면, 폴리펩티드), 삽입물(예를 들면, 아크리딘, 소랄렌, 등), 킬레이터, 알킬레이터, 및 변형된 연쇄를 포함한다. 상기 용어는 또한, 단일-스트랜드, 이중-스트랜드, 특히 이중체, 삼중체, 머리핀형, 환형 및 패드록(padlock) 배치를 포함하는 어느 위상 배치를 포함하는 의도이기도 하다. 또한, 수소결합 및 다른 화학적 상호작용을 통해 고안된 서열에 결합할 수 있는 그들의 능력에서 폴리뉴클레오티드를 모방하는 합성 분자를 포함한다. 이와 같은 분자는 본 분야에 잘 알려져 있고 예를 들면, 펩티드 연쇄가 분자의 골격에서 인산염 연쇄를 대체하는 것을 포함한다. 핵산 서열에 대한 참조는 다르게 명시되지 않는 한 그것의 상보체를 포함한다. 그러므로, 특정 서열을 갖는 핵산 분자에 대한 참조는 그것의 상보체 서열을 갖는, 그것의 상보체 스트랜드를 포함하는 것으로 이해되어야한다. 상보체 스트랜드는 또한, 예를 들면, 안티센스 치료법, 혼성화 프로브 및 PCR 프라이머에 유용하다.
작동적으로
연결된
용어 "작동적으로 연결된"은 보통 물리적으로 연결되고 서로 기능적 관계에 있는 2개 이상의 핵산 서열을 말한다. 예를 들면, 프로모터가 암호화 서열의 전사 또는 발현을 개시 또는 조절할 수 있다면, 프로모터는 암호화 서열과 작동적으로 연결되고, 여기서 암호화 서열은 프로모터의 "조절하에 있다"고 이해되어야 한다.
약제학적으로 허용가능한 부형제
"약제학적으로 허용가능한 부형제"는 약물, 약제와 같은 활성물질과 결합된 어느 불활성 물질 또는 허용가능한 편리한 투여형태를 제조하기 위한 결합 물질을 의미한다. "약제학적으로 허용가능한 부형제"는 투여량 및 적용된 농도에서 수용체에 비-독성이고, 약물, 약제 또는 결합분자를 포함하는 제형의 다른 구성성분과 양립할 수 있는 부형제이다.
특이적으로 결합하는
여기서 사용되는 용어 "특이적으로 결합하는"은, 결합분자, 예를 들면 항체 및 그것의 결합 파트너, 예를 들면 항원의 상호작용을 참조로 하여, 상호작용이 결합 파트너 상의 특정 구조체, 예를 들면 항원성 결정체 또는 에피토프의 존재에 의존한다는 것을 의미한다. 다시 말하면, 항체는 결합 파트너가 다른 분자들 또는 유기체의 혼합물 중에 존재할 때에도 결합 파트너와 우선적으로 결합하거나 인식한다. 결합은 공유 또는 비-공유 결합에 의해 또는 둘 다의 조합에 의해 이루어질 것이다. 또 다시 말하면, 용어 "특이적으로 결합하는"은 항원 또는 그것의 단편에 대해 면역특이적으로 결합하고 다른 항원에는 면역특이적으로 결합하지 않는 것을 의미한다. 항원에 면역특이적으로 결합한 결합분자는, 예를 들면, 방사선면역조사(RIA), 효소-연결 면역흡수 조사(ELISA), BIACORE, 또는 본 분야에 알려진 다른 조사에 의해 측정된 바와 같이, 다른 펩티드 또는 폴리펩티드와는 낮은 친화력으로 결합할 수 있다. 항원에 면역특이적으로 결합하는 결합분자 또는 단편은 관련 항원과 교차-반응될 수 있다. 바람직하기는, 항원과 면역특이적으로 결합하는 결합분자 또는 단편은 다른 항원과 교차-반응하지 않는다.
치료적으로
효과적인 양
용어 "치료적으로 효과적인 양"은 SARS-CoV에 의한 감염에 의해 생기는 질환의 예방, 개선 및/또는 치료에 효과적인 것으로 여기에 정의된 바에 따른 결합분자의 양을 말한다.
치료
용어 "치료"는 예방 뿐 아니라 치료적 처리 또는 치유 또는 정지 또는 적어도 질병의 진행의 지연을 위한 예방적 조치를 말한다. 치료가 필요하다는 것은 SARS-CoV에 의한 감염이 예방되어져야 하는 것 뿐 아니라 SARS-CoV에 의한 감염으로 인한 질환이 이미 가해지 것을 포함한다. SARS-CoV의 감염으로부터 부분적으로 또는 완전히 회복된 개체도 역시 치료가 필요할 수 있다. 예방은 SARS-CoV의 억제 또는 감소 또는 하나 이상의 SARS-CoV에 의한 감염과 관련된 증후근의 개시, 전개 또는 진행의 억제 및 감소를 포함한다.
벡터
용어 "벡터"는 복제되어질, 그리고 몇몇 경우에는 발현되어질 숙주에 도입되도록 하기 위해 제2 핵산 분자가 삽입될 수 있는 핵산분자를 말한다. 다시 말하면, 벡터는 그것이; 연결되어 있는 핵산 분자를 이송할 수 있다. 발현벡터 뿐만 아니라 클로닝 벡터는 여기서 사용되는 바와 같이 용어 "벡터"에 의해 의도된다. 벡터는 플라즈미드, 코스미드, 세균성 인공염색체(BAC) 및 이스트 인조염색체(YAC), 및 박테리오파아지 또는 식물 또는 동물(인간 포함)로부터 유래된 벡터를 포함하지만, 이것으로 한정되는 것은 아니다. 벡터는 제안된 숙주에 의해 인식된 복제물의 기원 및 발현 벡터의 경우, 프로모터와 숙주에 의해 인식된 다른 조절 영역을 포함한다. 제2 핵산 분자를 함유하는 벡터는 변형, 트란스펙션, 또는 바이러스성 도입 메카니즘의 사용에 의해 세포에 도입된다. 어느 벡터는 그들이 도입되는 숙주 세포에서 독립적인 복제를 할 수 있다(예를 들면, 복제의 세균성 기원을 갖는 벡터는 세균에 복제될 수 있다). 다른 벡터는 숙주에 도입된 후 숙주의 게놈으로 통합될 수 있고, 그것에 의해 숙주 게놈에 따라 복제된다.
발명의 요약
본 발명은 SARS-CoV에 특이적으로 결합할 수 있고 SARS-CoV 중화활성을 갖는 결합분자들의 조성물을 제공한다. 바람직한 구현예에서, 상기 결합분자는 인간 결합분자이다. 본 발명은 추가로, SARS-CoV로 인한 질환을 갖거나 또는 진행 위험이 있는 개체의 예방 및/또는 치료에 본 발명의 조성물을 사용하는 것을 제공한다. 그 밖에, 본 발명은 SARS-CoV의 진단/검출에 본 발명의 조성물을 사용하는 것을 포함한다.
발명의 상세한 설명
제 1면에서, 본 발명은 2 이상의 결합분자를 포함하는 조성물을 포함한다. 구현예에서, 결합분자들은 면역글로불린이다. 또한, 완전한 면역글로불린의 원하는 기능 및/또는 활성을 여전히 갖는 면역글로불린 단편들은 본 발명에 따른 면역글로불린으로 간주된다. 바람직하기는, 2 이상의 (두 가지 이상의) 결합분자들, 즉, 면역글로불린들은 코로나바이러스에 특이적으로 결합할 수 있다. 코로나바이러스는 조류 감염성 기관지염 바이러스, 조류 감염성 후두기관 바이러스, 장 코로나바이러스, 말 코로나바이러스, 예를 들면 인간 코로나바이러스 229E 또는 인간 코로나바이러스 NL63과 같은 코로나바이러스 군 1 종, 인간 코로나바이러스 OC43 또는 닭 장 바이러스와 같은 코로나바이러스 군 2 종, 코로나바이러스 군 3 종, 인간 장 코로나바이러스 4408, 및 SARS-CoV를 포함하지만, 이것으로 제한되는 것은 아니다. 본 조성물은 코로나 바이러스와 관련된 하나 이상의 증상을 치료, 예방 또는 개선하기 위해 포유동물에 투여될 수 있다.
구현예에서, 본 발명은 상승작용 조성물, 즉 상승작용 코로나바이러스 중화 활성을 나타내는 조성물에 관한 것이다. 다시 말하면, 본 조성물은 코로나바이러스에 특이적으로 결합할 수 있고 코로나바이러스 중화활성을 갖는, 적어도 2개의 (두 가지의) 결합분자들, 즉, 면역글로불린을 포함하고, 결합분자는 코로나바이러스들은 상승작용적(시너지적; synergistic)으로 중화하는 작용을 하는 것을 특징으로 한다. 여기서 사용되는 바에 따르면, 용어 "상승작용"은 결합하여 사용하였을 때 결합 분자들의 결합된 효과가 개별적으로 사용하였을 때 그들의 부가적 효과보다 큰 것을 의미한다. 한 구현예에서, 상승작용 코로나바이러스 중화 활성을 나타내는 조성물에 존재하는 결합분자, 즉 면역글로불린 어느 것도 개별적인 결합분자로서 사용되었을 때 코로나바이러스 중화활성을 갖지 않았다. 선택적으로, 상상작용 코로나바이러스 중화활성을 나타내는 조성물에서 적어도 2개의 결합분자중 하나의 결합분자는 개별적으로 사용될 때 코로나바이러스 중화활성을 가질 수 있다. 바람직한 구현예에서, 적어도 2개의 결합분자, 즉 면역글로불린 모두는 개별적으로 사용될 때 코로나바이러스 중화활성을 갖는다. 한 구현예에서, 상승작용적 코로나바이러스 중화활성을 나타내는 조성물 중 적어도 2개의 결합분자 중 하나는 코로나바이러스에 결합할 수 있고 다른 하나는 코로나바이러스의 세포 관련 수용체에 결합될 수 있다. 선택적으로, 두 결합분자는 코로나바이러스 또는 세포 관련 수용체에 결합할 수 있다.
본 발명의 바람직한 구현예에서, 코로나바이러스는 동물 또는 인간 SARS-CoV를 포함하는 SARS-CoV이다. 바람직하기는, SARS-CoV는 인간 SARS-CoV이다. 다른 면에서, 본 발명은 따라서 SARS-CoV에 특이적으로 결합할 수 있고 바람직하기는 SARS-CoV 중화 활성을 갖는 2 이상의 결합분자, 즉 면역글로불린을 포함하는 조성물을 제공한다. 본 조성물은 바람직하기는 상승작용적 SARS-CoV 중화활성을 나타낸다. 다시 말하면, 본 조성물은 SARS-CoV 중화활성을 갖는 2 이상의 결합분자, 즉 면역글로불린을 포함하고, 상기 결합분자는 SARS-CoV를 중화하는데 상승작용적으로 작용하는 것을 특징으로 한다. 본 조성물의 SARS-CoV 중화활성은 각 면역글로불린 단독의 중화활성의 합보다 크다. 본 발명의 바람직한 구현예에서, 본 조성물 중의 결합 분자들은 다수의 SARS-CoV 균주를 중화하는데 상승적으로 작용한다(여러 공지의 SARS-CoV 게놈서열과 S 단백질 유전자의 리스트에 관하여 표 1을 참조). 또 다른 구현예에서, 조성물의 각각의 면역글로불린은 다수의(다른) SARS-CoV 균주, 바람직하기는 인간 SARS-CoV 균주를 중화시킬 수 있다. 또 다른 구현예에서, 본 발명의 조성물의 적어도 하나의 결합분자, 즉 면역글로불린은 동물 SARS-CoV를 중화시킬 수 있다. 본 발명의 조성물 중 결합분자들은 숙주세포의 가능한 수용체에 코로나바이러스의 부착을 막거나, 세포의 세포질로의 RNA의 방출을 억제하거나, RNA 전사 또는 번역을 막거나, 또는 코로나바이러스 복제를 억제 또는 하향조절하는 것을 포함하는 여러 방법의 작용에 의해 SARS-CoV 전염성과 같은 코로나바이러스 전염성을 중화시킬 수 있지만, 이것으로 제한되는 것은 아니다. 더우기, 결합분자들은 상보체를 고정시켜 작용하거나 피복된 코로나바이러스의 세포용해를 도울 수 있다. 이들은 옵소닌으로 작용할 수 있고, Fc 또는 C3b 수용체를 통해 섭취를 촉진시키거나 또는 코로나바이러스의 식균작용을 더욱 쉽게 하기 위해 코로나바이러스를 교착시켜 코로나 바이러스의 식균작용을 증대시킨다. 조성물 중의 결합분자들은 유사한 작용 형태를 갖거나 또는 다른 작용 형태를 가질 수 있다. 특정 구현예에서, 조성물은, 상기 조성물의 부재시 코로나바이러스에 의한 숙주세포의 감염과 비교하여 적어도 10%, 적어도 20%, 적어도 30%, 적어도 40%, 적어도 50%, 적어도 60%, 적어도 70%, 적어도 80%, 적어도 90%, 적어도 95% 또는 적어도 99%까지 SARS-CoV와 같은 코로나바이러스 전염성을 중화시킨다. 바이러스 중화 작용을 측정하기 위한 조사는 당업자에게 알려져 있다. 이와 같은 조사법의 예를 아래에 기재한다.
본 발명의 조성물 중의 결합분자들, 즉 면역글로불린은 활성화된 또는 불활성화된/감쇄된 형태로 SARS-CoV와 같은 코로나바이러스에 특이적으로 결합할 수 있다. 바이러스를 불활성화/감쇄하기 위한 방법은 본 분야에 잘 알려져 있고 열불활성화, UV 방사에 의한 불활성화, 감마방사에 의한 불활성화를 포함하지만, 이것으로 한정되는 것은 아니다. 결합분자는 또한 무엇보다도 코로나바이러스로부터 유도된 하나 이상의 단백질 및/또는 (폴리)펩티드의 제제를 포함하는 코로나바이러스의 하나 이상의 단편에 특이적으로 결합할 수 있다. 바람직하기는, 단편들은 적어도 본 발명의 결합분자에 의해 인식되는 항원성 결정기를 포함한다. 여기서 사용되는 "항원성 결정기"는 코로나바이러스(SARS-CoV와 같은), (폴리)펩티드, 단백질, 당단백질, 동족체 또는 단편과 같은 모이어티이고, 이것은 본 발명이 결합분자에 검출가능한 항원-결합 분자 복합체를 형성하기에 충분히 고친화적으로 결합할 수 있다.
한 구현예에서, 결합분자, 즉 면역글로불린은 코로나바이러스의 표면접근성 단백질에 특이적으로 결합할 수 있고, 이것은 내부 및 외부 막 단백질, 세포벽에 고착하는 단백질 및 전위 분비 단백질을 포함하지만, 이것으로 한정되는 것은 아니다. 이와 관련하여 SARS-CoV의 접근성 단백질은 무엇보다도 스파이크(S) 단백질, 막(매트릭스) 단백질, (소)외포 단백질, Orf 3, Orf 4, Orf 7, Orf 8, Orf 9, Orf 10 및 Orf 14이다. SARS-CoV와 같은 코노나바이러스의 여러 공지된 균주의 단백질과 유력한 단백질의 아미노산 서열은 EMBL-데이타베이스 및/또는 다른 데이타베이스에서 발견할 수 있다. 예를 들면, 코로나바이러스 Urbani의 완전게놈은 EMBL-데이타베이스에서 수탁번호 AY278741로 발견되고, SARS 코로나바이러스 HSR 1의 완전한 게놈은 수탁번호 AY323977로 발견되고, SARS 코로나바이러스 Frankfurt 1의 완전게놈은 수탁번호 AY291315에서 발견되고 그리고 SARS 코로나바이러스 TOR2의 완전 게놈은 수탁번호 AY274119로 발견될 수 있다.
한 구현예에서 본 발명의 조성물 중의 적어도 하나의 결합분자, 즉 면역글로불린은 SARS-CoV의 S 단백질에 특이적으로 결합할 수 있다. 다른 결합분자는 표적 세포에 또는 그와 연합되어 SARS-CoV 단백질의 수용체에 결합될 수 있다. 이와 같은 수용체의 예는 ACE-2 수용체이다(Li et al., 2003 참조). 다른 구현예에서, 본 발명의 조성물 중의 모든 결합분자는 SARS-CoV의 단백질에 특이적으로 결합할 수 있다.
또 다른 구현예에서, 본 발명의 조성물 중의 적어도 하나의 결합분자는 SARS-CoV의 S 단백질의 세포외 도메인에 특이적으로 결합할 수 있다. 이 도메인은 S 단백질의 아미노산 15-1195으로 구성된다. 특이적 구현예에서, 본 발명의 조성물 중 적어도 하나의 결합분자는 SARS-CoV의 S 단백질의 아미노산 318-510에 특이적으로 결합할 수 있다. 본 발명의 조성물 중 중화 결합분자, 즉 면역글로불린은 오버래핑, 경쟁 에피토프와 반응할 수 있지만, 바람직하기는 SARS-CoV와 같은 코로나바이러스의 다른/구별되는, 비-경쟁 에피토프와 반응할 수 있다.
본 발명의 다른 면은 SARS-CoV와 같은 코로나바이러스와 특이적으로 결합할 수 있는 적어도 2개의 결합분자를 포함하는 조성물에 관한 것으로, 여기서 상기 결합분자는 코로나바이러스의 다양한, 비-경쟁적 에피토프와 반응할 수 있다. 바람직하기는, 코로나바이러스는 인간 코로나바이러스이고, 더욱 바람직하기는 SARS-CoV 이다. 각 결합분자가 바이러스 상의 다른 에피트프 또는 부위에 결합하는, 적어도 2개의 결합분자들을 포함하는 조성물은, 각 결합분자가 바이러스 상의 오버래핑 에피토프 또는 부위에 결합하는 적어도 2개의 결합분자를 포함하는 조성물과 비교하여 바이러스의 내성 변이체의 탈출을 막는데 더욱 알맞다.
특정 구현예에서, 본 발명의 조성물 중에서 결합분자, 즉 면역글로불린에 의해 인식되는 다양한, 비-경쟁적 에피토프는 SARS-CoV의 S 단백질, 특히 S 단백질의 세포외 도메인, 더욱 특별히는 S 단백질의 아미노산 318-510 내에 위치한다. 다른 면에서, 본 발명의 조성물의 적어도 하나의 결합분자, 즉 면역글로불린은 인간 또는 동물 SARS-CoV의 S 단백질의 아미노산 318-510과 반응할 수 있다. 또 다른 구현예에서, 본 발명의 조성물의 적어도 하나의 결합분자, 즉 면역글로불린은 SEQ ID.NO:128의 아미노산 서열을 포함하는 에피토프와 반응한다. 에피토프는 11, 11~15, 11~20, 11~25, 11~30, 11~35, 11~40, 11~45 또는 그 이상의 아미노산으로 이루어질 수 있다. 또 다른 면에서, 본 발명의 조성물의 적어도 하나의 결합분자, 즉 면역글로불린은 SARS-CoV의 S 단백질의 아미노산 318-510 (여기서 위치 479에서 아미노산은 아스파라긴과 다른 아미노산이다)과, SARS-CoV의 S 단백질의 아미노산 318-510(여기서 위치 479에서 아미노산은 아스파라긴산이다)과의 반응과 유사한 정도로 반응할 수 있다. 다시 말하면, 위치 479에서 아미노산의 치환은 SARS-CoV의 S 단백질의 아미노산 318-510에 대한 본 발명의 조성물 중 적어도 하나의 면역글로불린의 결합에 극적으로 영향을 미치지 않는다. 상기의 "유사한 정도"는 결합분자가 위치 479에서 아미노산이 아스파라긴산과 다른 아미노산인 SARS-CoV의 S 단백질의 아미노산 318-510에, 위치 479에서 아미노산이 아스파라긴인 SARS-CoV의 S 단백질의 아미노산 318~510에 대한 결합분자의 결합과 비교하여, 적어도 60%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 바람직하기는 적어도 100%의 양으로 결합하는 것을 의미한다.
본 발명에 따른 조성물 중의 결합분자는 바람직하기는 인간 결합분자, 즉 면역글로불린이다. 이들은 폴리클로날 또는 모노클로날 항체, 특히 인간 모노클로날 항체와 같은 완전한 면역글로불린 분자일 수 있고, 또는 결합분자는 Fab, F(ab') F(ab')2, Fv, dAb, Fd, 상보적 결정영역(CDR) 단편, 단일-사슬 항체(scFv), 2가 단일-사슬 항체, 단일-사슬 파아지 항체, 다이아바디(diabodies), 트리아바디(triabodies), 테트라바디(tetrabodies) 및 적어도 SARS-Cov 또는 그것의 단편에 특이적 항원을 제공하기에 충분한 면역글로불린의 단편을 함유하는 (폴리)펩티드를 포함하는 항원-결합 단편일 수 있지만, 이것으로 제한되는 것은 아니다. 인간 결합분자는 바람직하기는 인간 모노클로날 항체이다. 본 조성물 중의 결합분자는 비-단리된 또는 단리된 형태일 수 있다. 본 발명의 조성물은 추가로 적어도 하나의 다른 치료제를 포함할 수 있다. 바람직하기는 치료제는 예를 들면 SARS-CoV와 같은 코로나바이러스로부터 생긴 질환의 예방 및/또는 치료에 유용하다.
통상적으로, 결합분자는 그들의 결합 파트너, 즉 코로나바이러스 또는 그것의 단편에 0.2×10-4M, 1.0×10-5M, 1.0×10-6M, 1.0×10-7 M 미만, 바람직하기는 1.0×10-8M 미만, 더욱 바람직하기는 1.0×10-9M 미만, 더욱 바람직하기는 1.0×10-10M 미만, 더욱 바람직하기는 1.0×10-11M 미만, 및 가장 바람직하기는 1.0×10-12M 미만의 친화력 상수(Kd-값)로 결합할 수 있다. 친화력 상수는 항체 이소타입에 따라 변할 수 있다. 예를 들면, IgM 이소타입의 결합친화력은 적어도 1.0×10-7M 의 결합 친화력을 말한다. 결합 친화력은 예를 들면, 표면 플라즈몬 공명, 즉, 예를 들면 BIACORE 시스템(Pharmacia Biosensor AB, Uppsala, Sweden)을 사용하여 생체 센서 매트릭스 내의 단백질 농도의 변화의 검출에 의해 실시간 생체특이적 상호작용의 분석을 허용하는 광학 현상을 이용하여 측정될 수 있다.
결합 분자는 예를 들면, 샘플에서와 같이 가용성 형태로 SARS-CoV에 결합될 수 있고, 또는 예를 들면, 미세 역가 플레이트, 막 및 비드 등과 같은 담체 또는 기질에 결합 또는 부착된 SARS-CoV에 결합될 수 있다. 담체 또는 기질은 유리, 플라스틱(예를 들면 폴리스티렌), 다당류, 나일론, 니트로셀룰로스, 또는 테프론 등으로 이루어질 수 있다. 이와 같은 지지체의 표면은 고형 또는 다공성일 수 있고 어느 통상의 형태일 수 있다. 또한, 결합분자는 순수/단리 또는 비-순수/비-단리된 형태로 SARS-CoV에 결합될 수 있다.
바람직한 구현예에서, 본 발명에 따른 조성물의 결합분자, 즉 면역글로불린은 SEQ ID NO:1 또는 SEQ ID NO:2의 아미노서열을 포함하는, 적어도 CDR3 영역, 바람직하기는 중쇄 CDR3 영역을 포함한다. 또 다른 구현예에서, SEQ ID NO:1의 중쇄 CDR3 영역을 포함하는 결합분자는 추가로 SEQ ID NO:129의 아미노산 서열을 포함하는 경쇄 CDR3 영역을 포함한다. 또 다른 구현예에서, SEQ ID NO:1의 중쇄 CDR3 영역을 포함하는 결합분자는 추가로 각각 SEQ ID NO:130, SEQ ID NO:131, SEQ ID NO:132, 및 SEQ ID NO:133의 아미노산 서열을 포함하는 중쇄 CDR1, 중쇄 CDR2, 경쇄 CDR1 및 경쇄 CDR2 영역을 포함한다. 또 다른 구현예에서, SEQ ID NO:2의 중쇄 CDR3 영역을 포함하는 결합분자는 추가로 각각 SEQ ID NO:135, SEQ ID NO:136, SEQ ID NO:137, 및 SEQ ID NO:138의 아미노산 서열을 포함하는 중쇄 CDR1, 중쇄 CDR2, 경쇄 CDR1 및 경쇄 CDR2 영역을 포함한다. 또 다른 구현예에서, 본 발명에 따른 결합분자는 SEQ ID NO:4 또는 SEQ ID NO:6의 아미노산 서열을 포함하는 중쇄 가변영역을 포함한다. 한 구현예에서, 본 발명의 조성물 중의 결합분자, 즉 면역글로불린은 SEQ ID NO:4 또는 SEQ ID NO:6의 아미노산 서열을 포함하는 중쇄 가변영역을 포함하는 결합분자의 CDR 영역을 적어도 하나 포함한다. 또 다른 구현예에서, 그들은 2, 3, 4, 5 또는 6개 모두의 CDR 영역을 포함한다.
추가의 구현예에서, 본 발명에 따른 결합분자는 SEQ ID NO:4의 아미노산 서열을 포함하는 중쇄 가변영역과 SEQ ID NO:8의 아미노산 서열을 포함하는 경쇄 가변영역, 또는 SEQ ID NO:6의 아미노산 서열을 포함하는 중쇄 가변영역과 SEQ ID NO:10의 아미노산 서열을 포함하는 경쇄 가변영역을 포함한다.
바람직한 구현예에서, 활성을 중화시키는 SARS-CoV와 같은 코로나바이러스를 갖는 결합분자들이 IgG1 또는 IgA 포맷에 투여된다.
본 발명의 또 다른 면에서 본 발명의 조성물은 여기에 정의된 바와 같이 결합 분자의 기능적 변이체를 적어도 하나 포함한다. 본 조성물은 여기서 정의된 바와 같은 결합분자의 기능적 변이체들로만 이루어질 수 있다. 분자들은, 상기 변이체들이 SARS-CoV와 같은 코로나 바이러스 또는 그것의 단편에 특이적으로 결합하기 위해 부모 결합분자와 경쟁할 수 있다면, 결합 분자의 기능적 변이체라고 간주된다. 다시 말하면, 기능적 변이체가 SARS-CoV와 같은 코로나바이러스 또는 그것의 단편에 여전히 결합할 수 있다. 바람직하기는, 기능적 변이체는 SARS-CoV와 같은 코로나바이러스 전염성을 중화시킬 수 있고 다른 결합분자(또는 다른 기능적 변이체) 또는 다른 결합분자들(또는 다른 기능적 변이체들)와 상승적인 SARS-CoV와 같은 코로나바이러스 중화활성을 나타내는 조성물을 형성해야만 한다. 기능적 변이체의 중화활성은 부모 결합분자와 비교하여 더 높거나 또는 더 낮을 수 있다.
기능적 변이체는 실질적으로 1차 구조적 서열이 실질적으로 유사한 유도체들을 포함하지만, 이것으로 제한되는 것은 아니고, 그러나 예를 들면 인 비트로 또는 인 비보 변형, 화학약품 및/또는 생화학 약품을 포함하며, 이들은 부모 결합분자에서는 발견되지 않는다. 이와 같은 변형은 당업자에게 잘 알려져 있고, 무엇보다도, 아세틸화, 아실화, 뉴클레오티드 또는 뉴클레오티드 유도체의 공유결합, 지질 또는 지질 유도체의 공유결합, 글리코실화, 메틸화, 페길화, 단백질분해, 인산화 등을 포함한다.
선택적으로, 기능적 변이체는 부모 결합분자의 아미노산 서열과 비교하여 하나 이상의 아미노산의 치환, 삽입, 결실 또는 그들의 조합을 함유하는 아미노산 서열을 포함하는 본 발명에 정의된 바와 같은 결합분자일 수 있다. 더우기, 기능적 변이체는 아미노 또는 카르복시 말단 어느 것 또는 모두에서 아미노산 서열의 절단체(truncation)를 포함할 수 있다. 기능적 변이체는 부모 결합분자와 비교하여 동일하거나 다른, 더 높거나 낮은 결합 친화력을 가질 수 있지만, 여전히 SARS-CoV와 같은 코로나바이러스 또는 그것의 단편에 결합할 수 있고 바람직하기는 여전히 SARS-CoV와 같은 코로나바이러스 전염성을 중화시킬 수 있다. 예를 들면, 기능적 변이체는 부모 결합 분자와 비교하여 SARS-CoV와 같은 코로나바이러스 또는 그것의 단편에 대해 증가된 또는 감소된 결합 친화력을 가질 수 있다. 바람직하기는 골격구조, 초가변(hypervariable) 영역, 특히 CDR3 영역을 포함하지만, 이것으로 제한되는 것은 아닌 가변 영역의 아미노산 서열이 변형된다. 일반적으로, 경쇄 및 중쇄 가변 영역은 3개의 CDR을 포함하는, 3개의 초가변 영역 및 더욱 보존된 영역, 소위 골격 영역(FR)을 포함한다. 초가변 영역은 CDR로부터의 아미노산 잔기와 초가변 루프로부터의 아미노산 잔기를 포함한다. 본 발명의 범위에 속하기 위한 기능적 변이체는 본 명세서에 정의된 바와 같은 부모 결합 분자와, 적어도 약 50%~약 99%, 바람직하기는 적어도 약 60% ~ 약 99%, 더욱 바람직하기는 적어도 약 70% ~ 약 99%, 더욱 바람직하기는 적어도 약 80% ~ 약 99%, 더욱 바람직하기는 약 90% ~ 약 99%, 특히 적어도 약 95% ~ 99%, 및 특히 적어도 약 97% ~ 약 99% 아미노산 서열 상동성(동질성)을 갖는다. 컴퓨터 알고리즘, 무엇보다도 본 분야의 당업자들에게 알려진 Gap 또는 Bestfit를, 비교되어질 아미노산 서열을 최적으로 배열하고 유사하거나 또는 동일한 아미노산 잔기를 정의하기 위해 사용할 수 있다. 기능적 변이체는 부모 결합분자 또는 그것의 일부를, 에러가 많은 PCR, 올리고머뉴클레오티드-지향 돌연변이생성 및 부위-지향 돌연변이생성을 포함하는 공지의 일반 분자생물학적 방법에 의해 변화시킴으로써 얻을 수 있지만, 이것으로 제한되는 것은 아니다.
또 다른 면에서, 본 발명은 적어도 하나의 면역컨쥬게이트, 즉 여기서 정의된 바와 같은 적어도 하나의 결합 분자 또는 그것의 기능적 변이체를 포함하고 그리고 추가로, 적어도 하나의 태그를 포함하는 조성물을 포함한다. 또한, 본 발명에서 고려되는 것은 면역컨쥬게이트로 이루어진 조성물이다. 본 조성물은 추가로 치료적 약제와 같은 다른 분자 또는 다른 특이성을 갖는 면역컨쥬게이트를 포함할 수있다. 추가의 구현예에서, 본 발명의 면역컨쥬게이트는 하나 이상의 태그를 포함할 수 있다. 이들 태그들은 동일하거나 또는 서로 구별할 수 있고 결합분자에 비-공유적으로 연결/컨쥬게이트 될 수 있다. 태그는 또한 공유결합을 통해 결합분자에 직접적으로 연결/컨쥬게이트 될 수 있다. 선택적으로, 태그(들)은 하나 이상의 연결화합물에 의해 결합분자에 연결/컨쥬게이트 될 수 있다. 태그를 결합분자에 컨쥬게이트하는 기술은 당업자들에게 잘 알려져 있다.
본 발명의 면역컨쥬게이트의 태그는 치료적 약제일 수 있지만, 바람직하기는 이들은 검출가능한 모이어티/약제이다. 검출가능한 약제를 포함하는 면역컨쥬게이트를 포함하는 조성물은 예를 들면, 개체가 SARS-CoV와 같은 코로나바이러스에 의해 감염되었는지를 평가하거나 또는 임상적 시험과정의 일부로서 SARS-CoV와 같은 코로나바이러스 감염의 전개 또는 진행을 모니터하기 위해, 예를 들면 제공된 치료 처방계획의 효율성을 결정하기 위해, 진단적으로 사용될 수 있다. 그러나, 이들은 또한 다른 검출 및/또는 분석 및/또는 진단목적을 위해 사용될 수 있다. 검출가능한 모이어티/약제는 효소, 보결분자단, 형광물질, 발광물질, 생물발광물질, 방사성 물질, 양전자 방출금속, 및 비방사성 파라마그네틱 금속이온을 포함하지만, 이것으로 제한되는 것은 아니다. 검출 및/또는 분석 및/또는 진단 목적을 위해 결합분자를 라벨링 하는데 사용되는 태그는 특정 검출/분석/진단 기술 및/또는 사용되는 방법, 그중에서도 (조직)샘플의 면역조직화학적 염색, 유동세포계측법, 주사레이저세포계측법, 형광면역분석, 효소-연결 면역흡착제 분석(ELISA's), 방사면역분석(RIA's), 생검 (예를 들면, 중화분석), 웨스턴 블로팅 응용법 등에 의존한다. 조직 샘플의 면역조직화학적 염색을 위해 바람직한 태그는 검출가능한 산물의 생산 및 국소침착을 촉매화하는 효소이다. 또한, 본 발명의 조성물은 고형 지지체에 부착될 수 있고, 이것은 특히 코로나바이러스 또는 그것의 단편의 인 비트로 면역조사 또는 정제에 유용하다. 이와 같은 고형 담체는 다공성 또는 비다공성, 평면 또는 비평면일 수 있다. 본 발명의 결합분자 또는 그것의 기능적 단편은 정화를 용이하게 하기 위해 펩티드와 같은 마커 서열에 융합될 수 있다. 선택적으로, 항체는 항체 헤테로컨쥬게이트를 형성하기 위해 제2 항체에 컨쥬게이트될 수 있다. 또 다른 면에서, 본 발명의 결합분자는 하나 이상의 항원에 컨쥬게이트/부착될 수 있다. 바람직하기는, 이들 항원은 결합분자-항원 컨쥬게이트가 투여되는 개체의 면역시스템에 의해 인식되는 항원이다.
예를 들면 링커를 직접 또는 간접적으로 통해 컨쥬게이트에 의해 화학적으로 면역컨쥬게이트를 생산한 후, 면역컨쥬게이트는 본 발명의 결합분자와 알맞은 태그를 포함하는 융합 단백질로서 생산될 수 있다. 융합단백질은 본 분야에 알려진 방법 예를 들면, 알맞은 태그를 암호화하는 뉴클레오티드 서열을 포함하는 핵산 분자를 갖는 프레임에서 결합분자를 암호화하는 핵산 서열을 포함하는 핵산을 구조화하고 그리고 나서 핵산분자를 발현함으로써 재조합적으로 생산될 수 있다.
본 발명의 또 다른 면은 적어도 본 발명에 따른 조성물에 존재하는 적어도 결합분자 또는 그것의 단편을 암호화하는 핵산분자를 제공하는 것이다. 이와 같은 핵산 분자는 클로닝 목적을 위한 중간체로서, 예를 들면 상기 친화성 성숙의 과정에 사용될 수 있다. 바람직한 구현예에서, 핵산분자는 단리되거나 또는 정제된다.
당업자는 이들 핵산분자의 기능적 변이체가 본 발명의 일부로서 의도된다는 것을 이해할 것이다. 기능적 변이체는, 부모 핵산분자로부터 번역된 것과 동일한 아미노산 서열을 제공하기 위해, 표준 유전자코드를 사용하여 직접적으로 번역될 수 있는 핵산서열이다.
바람직하기는, 핵산분자는 CDR3 영역, 바람직하기는 SEQ ID NO:1 또는 SEQ ID NO:2의 아미노산 서열을 포함하는 중쇄 CDR3 영역을 포함하는 결합분자를 암호화한다. 또 다른 구현예에서, 본 발명의 핵산분자는 SEQ ID NO:129 또는 SEQ ID NO:134의 아미노산 서열을 포함하는 경쇄 CDR3 영역을 포함하는 결합분자를 암호화한다. 또 다른 구현예에서, 본 발명의 핵산분자는 SEQ ID NO:130 또는 SEQ ID NO:135의 아미노산을 포함하는 중쇄 CDR1 영역; SEQ ID NO: 131 또는 SEQ ID NO:136의 아미노산을 포함하는 중쇄 CDR2 영역; SEQ ID NO: 132 또는 SEQ ID NO:137의 아미노산을 포함하는 경쇄 CDR1 영역; 및/또는 SEQ ID NO:133 또는 SEQ ID NO:138의 아미노산을 포함하는 경쇄 CDR2 영역을 포함하는 결합분자를 암호화한다.
더욱 바람직하기는, 핵산분자는 SEQ ID NO:4 또는 SEQ ID NO:6의 아미노산을 포함하는 중쇄 가변영역을 포함하는 결합분자를 암호화한다.
또 다른 구현예에서, 핵산분자는 SEQ ID NO:4의 아미노산을 포함하는 중쇄 가변영역과 SEQ ID NO:8의 아미노산을 포함하는 경쇄 가변영역을 포함하는 결합분자를 암호화하거나 또는 그들은 SEQ ID NO:6의 아미노산을 포함하는 중쇄 가변영역과 SEQ ID NO:10의 아미노산을 포함하는 경쇄 가변영역을 암호화한다.
본 발명의 특정 구현예에서, 본 발명의 결합분자의 중쇄 가변영역을 암호화하는 핵산분자는 SEQ ID NO:3 또는 SEQ ID NO:5의 핵산서열을 포함한다.
본 발명의 또 다른 특정 구현예에서, 본 발명의 결합분자의 경쇄 가변역역을 암호화하는 핵산분자는 SEQ ID NO:7 또는 SEQ ID NO:9의 핵산서열을 포함한다. 본 발명의 핵산분자는 본 발명의 조성물 중에 존재하는 적어도 2개의 결합분자의 뉴클레오티드 서열 또는 그것의 일부를 함유할 수 있다.
본 발명의 다른 면은 벡터, 즉 본 발명에 따른 하나 이상의 핵산 분자를 포함하는 핵산 구조체를 제공하는 것이다. 벡터는 플라즈미드, 그중에서도 F, R1, RP1, Co1, pBR322, TOL, Ti 등; 코스미드; 람다, 람도이드(lambdoid), M13, Mu, P1 P22, Qβ, T-even, T-odd, T2, T4, T7 등과 같은 파아지; 식물 바이러스; 또는 동물 바이러스 등으로부터 유래될 수 있다. 벡터는 본 발명의 결합분자의 클로닝 및/또는 발현에 사용될 수 있고 그리고 유전자 치료목적으로도 사용될 것이다. 하나 이상의 발현-조절 핵산분자에 작동적으로 연결된 본 발명에 따른 핵산분자를 하나 이상 포함하는 벡터는 또한 본 발명의 범위이다. 본 발명의 조성물 중에 존재하는 결합분자는 개별적인 벡터 상에 발현될 수 있거나 또는 동일한 벡타 상에 발현될 수 있다. 벡터의 선택은 다음의 재조합 과정과 사용되는 숙주에 따른다. 숙주세포로의 벡터의 도입은 무엇보다도, 인산칼슘 트란스펙션, 바이러스 감염, DEAE-덱스트란 조절 트란스펙션, 리포펙타민 트란스펙션 또는 전기영동법에 의해 수행될 수 있다. 벡터는 자율적으로 복제되거나 또는 그들이 집적되어져 있는 염색체와 함께 복제될 수 있다. 바람직하기는, 벡터는 하나 이상의 선택 마커를 함유한다. 마커의 선택은 선택된 숙주세포에 의존하며, 이것이 본 분야의 당업자에게 알려진 바와 같이 본 발명에 결정적인 것은 아니다. 그들은 카나마이신, 네오마이신, 퓨로마이신, 히그로마이신, 제오신, 헤르페스 단순 바이러스로부터의 티미딘 키나제 유전자(HSV-TK), 마우스로부터의 디히드로폴레이트 리덕타제 유전자(dhfr)을 포함하지만, 이것으로 제한되는 것은 아니다. 결합분자를 단리하는데 사용될 수 있는 단백질 또는 펩티드를 암호화하는 하나 이상의 핵산분자에 작동적으로 연결된 상기와 같은 결합분자를 암호화하는 하나 이상의 핵산분자를 포함하는 벡터는 또한 본 발명에 속한다. 이들 단백질 또는 펩티드는 글루타티온-S-트란스퍼라제, 말토스 결합 단백질, 금속-결합 폴리히스티딘, 녹색형광 단백질, 루시퍼라제 및 베타-갈락토시다제를 포함하지만, 이것으로 제한되는 것은 아니다.
상기 벡터의 하나 이상의 사본을 함유하는 숙주는 본 발명의 추가의 대상이다. 바람직하기는, 숙주는 숙주세포이다. 숙주세포는 포유동물, 식물, 곤충, 균류 또는 세균성 기원의 세포를 포함하지만, 이것으로 제한되는 것은 아니다. 세균성 세포는 Bacillus, Streptomyces 및 Staphylococcus 속의 여러 종과 같은 그람양성 세균으로부터의 세포 또는 E. Coli 및 Pseudomonas와 같은 genera Escherichia 속의 여러 종과 같은 그람 음성 세균으로부터의 세포를 포함하지만, 이것으로 한정되는 것은 아니다. 균류 세포의 군에서 바람직하기는 이스트 세포가 사용된다. 이스트에서의 발현은 무엇보다도 Pichia pastoris, Saccharomyces cerevisiae 및 Hansenula polymorpha와 같은 이스트 균주를 사용하여 얻어질 수 있다.
더우기, Drosophilla 및 Sf9로부터의 세포와 같은 곤충 세포가 숙주세포로 사용될 수 있다. 더우기, 숙주세포는 식물 세포일 수 있다. 중국 햄스터 난소(CHO) 세포, COS 세포, BHK 세포 또는 바우스(Bowes) 흑색종 세포를 사용한 발현 시스템이 본 발명에 바람직하다. 포유동물 세포는 발현된 단백질에 포유동물 기원의 천연 분자와 거의 유사한 후번역 변형을 제공한다. 본 발명은 인간에게 투여될 수 있는 분자를 다루기 때문에, 완전 인간 발현 시스템이 특히 바람직할 것이다. 그러므로, 더욱 바람직하기는, 숙주 세포는 인간세포이다. 인간 세포의 예는 무엇보다도 HeLa, 911, AT1080, A549, 293 및 HEK293T 세포이다. 바람직한 포유동물 세포는 European Collection of Cell Cultures(EACC), CAMR, Salisbury, Wiltshire SP4 OJG, Great Britain 에 기탁번호 96022940으로 1996년 2월 29일자로 기탁되고 상표명 PER.C6?(PER.C6는 크루셀 홀란드 비.브이.의 등록상표이다)로 시판중인 911 세포 또는 세포계와 같은 인간 망막세포이다. 이 출원의 목적을 위해, "PER.C6"는 제96022940으로 기탁된 세포 또는 원형종, 기탁된 세포의 원형종으로부터의 자손 뿐 아니라, 계대 상류 또는 하류 뿐 아니라, 상기의 유도체를 말한다. 바람직한 구현예에서, 인간 프로듀서 세포는 발현가능 포맷에서 적어도 아데노바이러스 E1 영역을 암호화하는 핵산 서열의 기능적 일부를 포함한다. 더욱 바람직한 구현예에서, 상기 숙주세포는 인간 망막으로부터 유래되고 European Collection of Cell Cultures(EACC), CAMR, Salisbury, Wiltshire SP4 OJG, Great Britain에 기탁번호 96022940으로 1996년 2월 29일자로 기탁되고 상표명 PER.C6TM(PER.C6는 크루셀 홀란드 비.브이.의 등록상표이다)로 시판중인 세포계 및 그것의 유도체와 같은 아데노바이러스 E1 서열을 포함하는 핵산으로 고정화된다. 숙주세포에서 재조합 단백질의 생산은 본 분야에 잘 알려진 방법에 따라 실시될 수 있다. 관심있는 단백질의 생산 플랫폼으로서 상표명 PER.C6TM으로 시판중인 세포의 사용은 그 전체가 본 명세서에 참조로서 병합되어 있는 WO 00/63403에 기재되어 있다.
결합분자 또는 기능적 변이체의 생산방법은 본 분야의 당업자들에게 잘 알려져 있다. 하나의 방법은 a)상기 정의에 따른 숙주를 결합분자 또는 기능적 변이체의 발현을 가져오는 조건하에서 배양하는 단계, 및 b) 임의로, 발현된 결합 분자 또는 기능적 변이체를 회수하는 단계를 포함한다. 발현된 결합분자 또는 그것의 기능적 단편은 세포 프리 추출물로부터 회수될 수 있지만, 바람직하기는 배지로부터 회수된다. 세포 프리 추출물 또는 배지로부터 결합분자와 같은 단백질을 회수하는 방법은 본 분야의 당업자에게 잘 알려져 있다. 상기 방법으로 얻을 수 있는 결합분자 또는 그들의 기능적 유도체들은 또한 본 발명의 일부이다. 선택적으로, 숙주 세포와 같은, 숙주에서의 발현에 이어서, 본 발명의 결합분자 또는 그들의 기능적 변이체는 통상의 펩티드 합성기에 의해 또는 본 발명에 따른 DNA 분자로부터 유래된 RNA 핵산분자를 사용한 세포-프리 번역 시스템에서 생산될 수 있다. 상기 합성생산법 또는 세포-프리 번역 시스템에 의해 얻을 수 있는 바와 같은 결합분자 또는 그것의 기능적 유도체는 또한 본 발명의 일부이다.
본 발명의 또 다른 구현예에서, 본 발명에 따른 결합분자, 바람직하기는 SARS-CoV 또는 단편에 특이적으로 결합되는 인간 결합분자는 인간 면역글로불린 유전자를 발현하는, 예를 들면 유전자 변이 마이스 또는 토끼와 같은 유전자 변이 비-인간 포유동물에 의해 생성될 수 있다. 바람직하기는, 유전자 변이 비-인간 포유동물은 상기 인간 결합 분자의 전체 또는 일부를 암호화하는 인간 중쇄 트란스유전자와 인간 경쇄 트란스유전자를 포함하는 게놈을 갖는다. 유전자 변이 비-인간 포유동물은 SARS-CoV와 같은 코로나바이러스 또는 그것의 단편의 정제된 또는 풍부한 제제로 면역화될 수 있다. 비-인간 포유동물을 면역화하기 위한 프로토콜은 본 분야에 잘 알려져 있다. 그 내용이 여기에 참조로서 기재된 Using Antibodies: A Laboratory Manual, Edited by :E.Harlow, D. Lane(1998), Cold Spring Harbor Laboratory, Cold Spring Harbor, New York 및 Current Protocols in Immunology, Edited By:J.E. Coligan, A.M. Kruisbeek, D.H. Margulies, E.M. Shevach, W. Strober(2001), John Wiley & Sons Inc., New York을 참조하라. 면역프로토콜은 종종 프로인트 완전 보조액과 프로인트 불완전 보조액과 같은 보조액을 갖거나 또는 갖지 않는 다중 면역을 포함하지만, 또한 네이크된 DNA 면역을 포함한다. 또 다른 구현예에서, 인간 결합분자는 유전자도입 동물로부터 유래된 B 세포 또는 플라즈마 세포에 의해 생성된다. 또 다른 구현예에서, 인간 결합분자는 상기 유전자 변이 비-인간 동물 또는 불멸화된 인간 세포에서부터 얻어진 B 세포의 고정화된 세포에의 융합에 의해 제조되는 하이브리도마에 의해 생산된다. 상기 유전자 변이 비-인간 포유동물로부터 얻을 수 있는 B 세포, 플라즈마 세포 및 하이브리도마와 상기 유전자 변이 비-인간 포유동물, 또는 인간 개체로부터 얻을 수 있는 인간 결합분자는 또한 본 발명의 일부이다.
결합분자, 바람직하기는 인간 모노클로날 항체 또는 그것의 단편과 같은 인간 결합분자 또는 결합분자를 암호화하는 핵산분자를 동정하는 방법은 a)결합분자, 바람직하기는 인간 결합분자의 파아지 라이브러리를 SARS-CoV와 같은 코로나바이러스 또는 그것의 단편과 접촉시키는 단계, b) 코로나바이러스 또는 그것의 단편에 결합된 파아지에 대해 적어도 1회 선택하는 단계, 그리고 c) 코로나바이러스 또는 그것의 단편에 결합된 파아지를 분리 및 회수하는 단계를 포함한다. 선택단계는 파아지 라이브러리를 불활성화된 코로나바이러스와 접촉시키는 것을 수행될 수 있다. 코로나바이러스는 단리되거나 비단리될 수 있고, 예를 들면 감염 개체의 혈청 및/또는 혈액 중에 존재할 수 있다. 선택적으로, 선택단계는 (SARS-CoV와 같은) 코로나바이러스의 세포외 부분, 코로나바이러스로부터 유래된 하나 이상의 단백질 또는 (폴리)펩티드, 이들 단백질 또는 (폴리)펩티드를 포함하는 융합 단백질 등과 같은 SARS-CoV의 단편의 존재하에 실시될 수 있다. 결합분자, 예를 들면 항체를 동정하고 얻기 위한 파아지 디스플레이방법은 본 분야의 당업자에게 잘 알려져 있다. 그들은 예를 들면, 미국특허 제5,696,108호; Burton and Barbas, 1994; de Kruif et al., 1995b; 및 Phage Display: A Laboratory Manual. Edited by: CF Barbas, DR Burton, JK Scott and GJ Silverman(2001), Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York에 기재되어 있다. 이들 모든 참조들은 본 명세서에 전체적으로 병합되어 있다. 파아지 디스플레이 라이브러리의 구성을 위해, 인간 모노클로날 항체 중 및 경쇄 가시 영역 유전자의 수집은 박테리오파아지, 바람직하기는 필라멘트성 박테리오파아지, 입자들, 예를 들면 단일-사슬 Fv(scFv) 또는 Fab 포멧(de Kruif et al., 1995b 참조)의 표면에 발현된다. 항체 단편-발현 파아지의 큰 라이브러리는 통상적으로 1.0×109 항체 특이성을 함유하고 면역화된- 또는 비-면역화된 개인의 B 림프구에서 발현되는 면역글로불린 V 영역으로부터 조립될 수 있다. 특정 구현예에서, 결합분자의 파아지 라이브러리, 바람직하기는 scFv 파아지 라이브러리는 백신화된 또는 SARS-CoV와 같은 코로나바이러스에 노출된 개체로부터 얻어진 세포로부터 단리된 RNA로부터 제조된다. RNA는 골수 또는 말초혈액으로부터, 바람직하기는 말초혈액 림프구로부터 단리될 수 있다. 개체는 백신화되거나 또는 코로나바이러스에 노출된 동물일 수 있지만, 바람직하기는 백신화된 또는 코로나바이러스에 노출된 인간 환자이다. 바람직하기는 인간 환자는 코로나바이러스로부터 회복된다.
선택적으로, 파아지 디스플레이 라이브러리는 라이브러리에 추가의 항체 다양성을 도입하기 위해 부분적으로 인 비트로 조립되어진 면역글로불린 가변 영역으로부터 구성될 수 있다(세미-합성 라이브러리). 예를 들면, 인 비트로 조립된 가변 영역은 항체 특이성에 중요한 분자의 이들 영역, 예를 들면 CDR 영역에서 합성적으로 생산된, 무작위의 또는 부분적으로 무작위의 DNA의 확장을 함유한다. 코로나비이러스 특이 파아지 항체는, 코로나바이러스(불활성 또는 활성 형태로) 또는 코로나바이러스로부터의 항원과 같은 표적 항원을 고형상에 고정화시키고, 이어서, 고형상-결합된 항원에 특이적인 항체 단편을 발현하는 파아지의 결합을 허용하도록 코로나바이러스 또는 표적 항원을 파아지의 라이브러리에 노출시킴에 의해 라이브러리로부터 선택될 수 있다. 비-결합된 파아지는 세척에 의해 제거되고 결합된 파아지는 Escherichia coli (E. coli) 세균의 감염에 대해 고체상으로부터 용출되고 이어서 번식된다. 코로나바이러스(불활성 또는 활성 형태로) 또는 표적 항원(들)에 특이적으로 결합하는 파아지가 충분히 풍부해지기 위해서는 통상적으로 선택과 번식의 복수의 운행(round)이 요구된다. 필요하다면, 파아지 라이브러리를 코로나바이러스(불활성 또는 활성 형태로) 또는 표적 항원에 노출시키기 전에, 우선 파아지 라이브러리를 고형 상에 결합된 비-표적 항원에 노출시킴에 의해 파아지 라이브러리를 제거한다. 파아지는 코로나바이러스 단백질 또는 (폴리)펩티드, 코로나바이러스의 하나 이상의 단백질 또는 (폴리)펩티드를 발현하는 숙주세포의 복합체 혼합물과 같은 복합물 항원에 결합되도록 선택될 수 있다. 항원 특이 파아지 항체는, 예를 들면 파아지의 scFv 또는 Fab 부분을 코로나바이러스 제제의 단백질/폴리펩티드에 결합되도록 하기 위해 항체 라이브러리로 불활성화된 코로나바이러스의 제제를 그 위에 결합시켜 고체상을 배양함에 의해 라이브러리로부터 선택될 수 있다. 배양 및 비결합된 그리고 느슨히 부착된 파아지를 제거하기 위한 여러 번의 세척 후, 그들의 scFv 또는 Fab 부분으로 제제에 결합되어 있는 파아지가 용출되고 새로운 특이성의 증폭을 허용하도록 Escherichia coli를 감염시키는데 사용된다. 일반적으로, 대량의 비-결합 파아지로부터 관심있는 파아지를 분리하기 위해 1회 이상의 선택 운행이 요구된다. 선택적으로, 코로나바이러스의 공지의 단백질 또는 (폴리)펩티드가 숙주 세포에서 발현될 수 있고 이들 세포들은 단백질 또는 (폴리)펩티드에 특이적인 파아지 항체의 선택에 사용될 수 있다. 이들 숙주세포를 사용한 파아지 디스플레이법은, 표적 분자 또는 표적과 유사하지만 동일하지 않은 비-표적 분자를 함유하지 않는 다량의 숙주세포의 첨가에 의해 스크리닝 동안 비-관련 바인더를 제거하고, 그것에 의해 관련 결합 분자를 찾는 확률을 크게 강화함으로써 확장되고 개선될 수 있다(이 과정을 MabstractTM 법이라 부른다. MabstractTM법은 크루셀 홀란드 비.브이.의 계류중인 상표명이다. 또한, 여기에 참조로서 병합된 미국특허 제6,265,150를 참조하라). 상기 동정법을 사용하여 발견될 수 있는 결합분자에 대한 코로나바이러스의 예는 SARS-CoV이다.
결합분자, 바람직하기는 인간 결합분자 또는 결합분자를 암호화하는 핵산분자를 얻는 방법은 a)결합분자, 바람직하기는 인간 모노클로날 항체 또는 그것의 단편, 또는 결합분자를 암호화하는 핵산분자와 같은 인간 결합분자를 동정하는 상기의 방법을 실시하는 단계, 및 b)회수된 파아지로부터 인간 결합분자 및/또는 인간결합분자를 암호화하는 핵산을 단리하는 단계를 포함한다. 결합 분자 또는 결합분자를 암호화하는 핵산분자의 상기 방법으로 일단 새로운 모노클로날 파아지 항체가 확립되거나 동정되면, scFv 또는 Fab를 암호화하는 DNA는 세균 또는 파아지로부터 단리될 수 있고 표준 분자생물법과 결합하여 2가 scFv를 암호화하는 구조체를 제조하거나 원하는 특이성의 인간 면역글로불린(예를 들면, IgG, IgA 또는 IgM)을 완성할 수 있다. 이들 구조체들은 알맞은 세포계로 트란스펙션될 수 있고 완전 인간 모노클로날 항체가 생산될 수 있다(Huls, et al., 1999; Boel et al., 2000 참조).
적어도 2개의 결합분자 이외에, 본 발명의 조성물은 알부민 또는 폴리에틸렌 글리콜과 같은 안정화분자 또는 염을 포함할 수 있다. 바람직하기는, 사용된 염은 결합분자의 원하는 생리활성을 유지하고 원하지않는 독물학적 효과를 주지않는 염이다. 이와 같은 염의 예로는 산 부가염과 염기 부가염을 포함하지만, 이것으로 제한되는 것은 아니다. 산 부가염은 염화수소산, 질산, 인산, 황산, 브롬화수소산, 요오드화수소산, 인산염산과 같은 비독성 무기산으로부터 유래되는 것을 포함할 뿐 아니라, 지방족 모노- 및 디카르복실산, 페닐-치환된 알카논산, 히드록시알카논산, 방향족산, 지방족 및 방향족 황산 등과 같은 비독성 유기산을 포함하지만, 이것으로 제한되는 것은 아니다. 염기 부가염은 나트륨, 칼륨, 마그네슘, 칼슘 등과 같은 알칼리토금속, 뿐 아니라 N,N'-디벤질에틸렌디아민, N-메틸글루카민, 클로로프로카인, 콜린, 디에탄올아민, 에틸렌디아민, 프로카인 등과 같은 비독성 유기아민으로부터 유래된 것을 포함하지만, 이것으로 제한되는 것은 아니다. 필요에 따라, 본 발명의 결합분자는 결합분자를 불활성화할 수 있는 산의 작용 또는 다른 천연 또는 비천연 조건으로부터 그들을 보호하기 위해 결합분자에 또는 그 위에 코팅될 수 있다.
또 다른 추가의 면에서, 본 발명은 본 발명에 정의된 바와 같은 결합분자를 암호화하는 적어도 2개의 핵산분자를 포함하는 조성물을 제공한다. 조성물은 염(예를 들면, NaCl 또는 상기와 같은 염들), 세척제(예를 들면, SDS) 및/또는 다른 적절한 성분을 함유하는 수용액과 같은 수용액을 포함할 수 있다.
더우기, 본 발명은 본 발명에 따른 조성물을 포함하는 약제학적 조성물에 관한 것이다. 본 발명의 약제학적 조성물은 추가로 적어도 하나의 약제학적으로 허용가능한 부형제를 포함한다.
본 발명에 따른 약제학적 조성물은 적어도 하나의 다른 치료, 예방 및/또는 진단 약제를 추가로 포함할 수 있다. 바람직하기는, 약제학적 조성물은 적어도 하나의 예방 및/또는 치료 약제를 포함한다. 바람직하기는, 상기 추가의 치료 및/또는 예방 약제는 SARS-CoV와 같은 코로나바이러스로 인한 감염 및/또는 질환을 예방 및/또는 치료할 수 있는 약제이다. 치료 및/또는 예방 약제는 항바이러스 약제를 포함하지만, 이것으로 제한되는 것은 아니다. 이와 같은 약제는 결합분자, 소분자, 유기 또는 무기 화합물, 효소, 폴리뉴클레오티드 서열 등 일 수 있다.
항-바이러스제의 예는 당업자에게 알려져 있다. 예를 들면 SARS-CoV에 감염된 환자를 치료하는데 현재 사용되는 약제는 인터페론-알파, 스테로이드 및 유력한 리플리카제 억제제이다. 더우기, SARS-CoV에 감염된 환자는 현재, 바이러스에 노출되어진 후 항체를 생산하고 회복중인/회복된 SARS 환자로부터 기부된 혈액으로 생산된 혈청의 수혈로 치료된다. 실험단계에 있는 SARS-CoV 또는 다른 코로나바이러스의 감염 및 SARS-CoV 또는 다른 코로나바이러스로 인한 질환을 예방 및/또는 치료할 수 있는 약제는 본 발명에 유용한 다른 치료적 및/또는 예방적 약제로서 또한 사용될 수 있다.
본 발명의 결합분자 또는 본 발명의 약제학적 조성물은 인간에 사용되기에 앞서 알맞은 동물 모델 시스템에서 시험될 수 있다. 이와 같은 동물 모델 시스템은 흰담비, 마이스, 래트, 닭, 소, 원숭이, 돼지, 개, 토끼 등을 포함할 수 있지만, 이것으로 제한되는 것은 아니다.
통상적으로, 약제학적 조성물은 제조 및 저장조건하에서 무균이며 안정하다. 본 발명의 조성물은 전달시 또는 전달 전에 적절한 약제학적으로 허용가능한 부형제 중에 재구성을 위해 분말 형태로 존재할 수 있다. 살균성 주사용액의 제조를 위한 살균분말의 경우, 바람직한 제조방법은 활성 구성성분의 분말과 그것의 미리 살균-여과된 용액으로부터의 추가의 원하는 구성성분을 생산하는 진공건조 및 냉동-건조(냉동건조)이다.
선택적으로, 본 발명의 조성물은 용액상태일 수 있고, 적절한 약제학적으로 허용가능한 부형제가 단위 투여량 주사형을 제공하기 위해 전달되기 전 또는 전달시에 첨가 및/또는 혼합될 수 있다. 바람직하기는, 본 발명에 사용되는 약제학적으로 허용가능한 부형제는 고 약물농도에 알맞고, 알맞은 흐름성을 유지할 수 있고, 필요에 따라 흡수가 지연될 수 있다.
약제학적 조성물의 투여의 최적 경로의 선택은 조성물 내의 활성 분자들의 물리-화학적 특성, 임상적 상황의 긴급성 및 원하는 치료적 효과에 대한 활성분자의 플라즈마 농도의 관계를 포함하는 여러 인자들에 의해 영향을 받는다. 예를 들면, 본 발명의 결합분자는 필요에 따라, 임플란트, 피부에 바르는 패치, 및 마이크로캡슐화 전달시스템을 포함하는 조절된 방출 제형과 같은, 그들의 신속한 방출을 막는 담체와 함께 제조될 수 있다. 에틸렌 비닐 아세테이트, 다가무수물, 폴리글리콜산, 콜라겐, 폴리오르쏘에스테르, 및 폴리락트산과 같은 생분해성, 생체적합성 폴리머가 사용될 수 있다. 또한, 결합분자는 결합분자의 불활성화를 막는 물질 또는 화합물로 코팅되거나 또는 함께 투여되는 것이 필요할 수 있다. 예를 들면, 결합분자는 적절한 담체, 예를 들면 리포좀 또는 희석제에서 개체로 투여될 수 있다.
투여경로는 2개의 주요 카테고리, 경구 및 비경구로 나뉠 수 있다. 이들 2개의 카테고리는 당업자에게 잘 알려져 있다. 바람직한 투여경로는 정맥 내이고, 특히 바람직한 것은 근육 내이다.
경구 제형은 여러 형태로 제제화될 수 있고, 불활성 희석제, 과립화 또는 붕해제, 결합제, 광택제, 보존제, 착색제, 풍미제 또는 감미제, 식물성유, 미네랄유, 습윤제, 및 점증제를 포함하지만 제한되는 것은 아닌, 약제학적으로 허용가능한 부형제를 포함할 수 있다.
본 발명의 약제학적 조성물은 비경구적 투여용으로 제형화될 수 있다. 비경구 투여용 제형은 그중에서도, 수성 또는 비-수성 등장성 살균 비-독성 주사 또는 주입 용액 또는 현탁액의 형태일 수 있다. 바람직한 비경구 투여 경로는 정맥내, 복막내, 경막외, 근육내 및 종양내 주사 또는 주입을 포함한다. 용액 또는 현탁액은 적용된 투여량 및 농도에서 수용체에 비독성인 약제를 포함할 수 있다. 이와 같은 약제는 당업자에게 알려져 있고, 1,3-부탄디올, 링거스 용액, 행크스 용액, 등장성 염화나트륨 용액과 같은 약제, 오일 또는 지방산, 국소마취제, 보존제, 완충액, 점도 또는 용해도 증가제, 수용성 항산화제, 유용성 항산화제, 및 금속 킬레이트화제를 포함한다.
추가의 면에서, 본 발명의 약제학적 조성물은 의약으로 사용될 수 있다. 따라서, 본 발명의 약제학적 조성물을 사용한 코로나바이러스 감염의 치료 및/또는 예방법은 본 발명의 또 다른 부분이다. 본 발명의 (약제학적) 조성물은 코로나바이러스로 인한, 하나 이상의 질환의 진단, 예방, 치료 또는 그것의 조합을 위해 사용될 수 있다. 이들은 코로나바이러스로 인한 질환을 겪는 비치료 환자 및 코로나바이러스로 인한 질환의 또는 질환으로부터 치료된 환자의 치료에 알맞다. 이들은 코로나바이러스에 의한 추가의 감염에 대해 보호하고 및/또는 코로나바이러스 관련 증상의 개시 또는 전진을 저지시킨다. 이들은 용의선상의 환자를 돌보는 병원 관계자와 같이 코로나바이러스에 노출된 사람들의 코로나바이러스로 인한 질환 예방에 사용될 수 있다. 바람직하기는 (약제학적) 조성물은 SARS-CoV와 같은 인간 코로나바이러스 감염의 검출, 예방 및/또는 치료 방법에 사용될 수 있다.
상기 조성물과 약제학적 조성물은 코로나바이러스의 진단, 예방 및/또는 치료에 유용한 다른 분자들과 함께 적용될 수 있다. 이들은 인비트로, 엑스비트로 또는 인비보에서 사용될 수 있다. 예를 들면, 본 발명의 약제학적 조성물은 SARS-CoV와 같은 코로나바이러스에 대한 백신과 함께 투여될 수 있다. 선택적으로, 백신은 또한 본 발명의 약제학적 조성물을 투여하기 전 또는 후에 투여될 수 있다. 백신과 함께 본 발명의 약제학적 조성물의 투여는 노출 후 예방에 알맞을 수 있고 면역력이 약화된 수용체에서 생-감쇄된 백신의 부작용 가능성을 감소시킬 수 있다.
결합 분자는 통상적으로 치료적 또는 진단학적 유효량으로 본 발명의 조성물과 약제학적 조성물에서 제형화된다. 투여량 처방계획은 원하는 최적의 반응(예를 들면 치료적 반응)을 제공하도록 조절될 수 있다. 알맞은 투여량 범위는 예를 들면, 0.05~100 mg/kg(체중)이고, 바람직하기는 0.1~15 mg/kg(체중)일 수 있다.
통상적으로, 본 발명의 조성물과 약제학적 조성물 중 2개의 결합분자들의 몰비는 1:100 내지 100:1, 바람직하기는 1:50 내지 50:1, 더욱 바람직하기는 1:25 내지 25:1, 특히 바람직하기는 1:10 내지 10:1, 및 더욱 특히 바람직하기는 1:5 내지 5:1이다. 더우기, 예를 들면, 단일 큰 알약이 제공되는 경우 시간에 걸쳐 투여량을 몇 개로 나누어 투여될 수 있고 또는 투여량은 치료적 상황의 긴급사태에 의해 나타나는 바에 따라 비례적으로 감소되거나 또는 증가될 수 있다. 본 발명에 따른 분자 및 조성물은 바람직하기는 살균된다. 이들 분자들과 조성물을 살균하는 방법은 본 분야에 잘 알려져 있다. 진단, 예방 및/또는 치료에 유용한 다른 분자는 본 발명의 결합분자에 제안되는 유사한 투여량 처방계획으로 투여될 수 있다. 다른 분자들이 개별적으로 투여된다면, 이들은 개체에게 하나 이상의 본 발명의 결합 분자 또는 약제학적 조성물의 투여 전(예를 들면, 2분, 5분, 10분, 15분, 30분, 45분, 60분, 2시간, 4시간, 6시간, 8시간, 10시간, 12시간, 14시간, 16시간, 18시간, 20시간, 22시간, 24시간, 2일, 3일, 4일, 5일, 7일, 2주, 4주 또는 6주), 동시에, 또는 이후에 (예를 들면, 2분, 5분, 10분, 15분, 30분, 45분, 60분, 2시간, 4시간, 6시간, 8시간, 10시간, 12시간, 14시간, 16시간, 18시간, 20시간, 22시간, 24시간, 2일, 3일, 4일, 5일, 7일, 2주, 4주 또는 6주 후)에 투여될 수 있다. 정확한 투여량 처방계획은 보통 인간 환자에서의 임상시험 동안 가려진다.
인간결합분자와 인간결합분자를 포함하는 약제학적 조성물은, 투여된 항체에 대한 수용체 면역반응이 실질적으로 모노클로날 뮤린(murine), 키메릭 또는 인간화된 결합분자의 투여에 의해 발생하는 것보다 실질적으로 덜하므로, 인간에게 인비보 치료제로서 투여될 때 특히 유용하고, 종종 바람직하다.
다른 면에서, 본 발명은 코로나바이러스로 인한 질환의 진단, 예방, 치료 또는 그들의 조합을 위한 의약의 제조에 본 발명에 따른 (약제학적) 조성물의 사용에 관한 것이다. 바람직하기는, 코로나바이러스는 SARS-CoV와 같은 인간 코로나바이러스이다.
그 다음, 본 발명에 따른 적어도 하나의 조성물 또는 적어도 하나의 본 발명에 따른 약제학적 조성물을 포함하는 키트는 또한 본 발명의 일부이다. 임의로, 본 발명의 키트의 상기 성분들은 표시된 질환의 진단, 예방 및/또는 치료를 위해 알맞은 용기에 포장되고 라벨을 붙여 분리될 수 있다. (약제학적) 조성물 중의 결합분자들은 개별적으로 포장될 수 있다. 상기 성분들은 유니트 또는 다중-투여량 용기, 예를 들면, 밀봉된 앰플, 바이알, 병, 주사기, 및 시험관에, 바람직하기는 멸균된 수용액으로서 또는 재구성을 위해 냉동건조된, 바람직하기는 멸균된 제형으로 저장될 수 있다. 용기는 다양한 재료로 형성될 수 있고 멸균제 투입 구멍을 가질 수 있다(예를 들면, 용기는 피하주사기용 바늘이 꽂힐 수 있는 마개를 갖는 정맥 용액 주머니 또는 바이알 일 수 있다). 키트는 추가로, 약제학적으로 허용가능한 완충액을 포함하는 용기를 포함한다. 이것은 추가로 다른 완충액, 희석제, 필터, 바늘, 주사기, 하나 이상의 알맞은 숙주용 배지를 포함하는 시판 및 사용자 관점에서 바람직한 다른 재료를 포함할 수 있다. 키트와 관련된 것은 치료, 예방, 또는 진단 제품의 시판 패키지에 관습적으로 포함된 사용설명서일 수 있고, 즉, 예를 들면, 이와 같은 치료, 예방, 또는 진단 제품의 사용과 관련된 증상, 사용법, 투여량, 제조, 투여, 모순 및/또는 경고를 포함한다.
본 발명은 추가로, 샘플 중의 SARS-CoV를 검출하는 방법에 관한 것이고, 여기서 상기 방법은 a)샘플과 본 발명에 따른 조성물 또는 약제학적 조성물의 진단적으로 효과적인 양을 접촉시키는 단계, 및 b)조성물 또는 약제학적 조성물이 샘플의 분자와 특이적으로 결합하는 단계를 포함한다. 샘플은 혈액, 혈청, 소변, 조직 또는 다른 (잠재적으로)감염된 개체의 생리적 물질을 포함하는 생리적 샘플, 또는 물, 음료 등과 같은 비생리적 샘플일 수 있지만, 이것으로 제한되는 것은 아니다. (잠재적으로)감염된 개체는 인간 환자일 수 있지만, 또한 SARS-CoV와 같은 코로나바이러스의 담체로서 추측되는 동물이 본 발명의 조성물 또는 약제학적 조성물을 사용하여 코로나바이러스의 존재에 대해 시험될 수 있다. 샘플은 우선 검출방법에 더욱 알맞게 되도록 조작될 수 있다. 조작은 코로나바이러스를 함유하고 있다고 추측되는 및/또는 함유하는 샘플을, 코로나바이러스가 단백질, (폴리)펩티드 또는 다른 항원 단편과 같은 항원성 성분들로 분해되도록 하는 방법으로 처리하는 것을 의미한다. 바람직하기는, 본 조성물 또는 약제학적 조성물은, 본 조성물 또는 약제학적 조성물과 샘플에 존재할 수 있는 코로나바이러스 또는 그들의 항원성 성분들 간의 면역 복합체의 형성을 허용하는 조건하에서, 샘플과 접촉된다. 샘플 중의 코로나바이러스의 존재를 나타내는 면역학상의 복합체의 형성은 알맞은 방법에 의해 검출되고 측정된다. 이와 같은 방법은, 무엇보다도, 방사면역측정법(RIA), ELISA, 면역형광법, 면역세포화학, FACS, BIACORE 및 웨스턴 블롯 분석과 같은 균질 및 이종성 결합면역분석을 포함한다.
바람직한 분석법, 특히 개체 혈청 및 혈액과 혈액-유도 산물의 대규모 임상 스크리닝을 위한 분석법은 ELISA 및 웨스턴 블롯법이다. ELISA 시험이 특히 바람직하고 본 분야의 당업자에게 잘 알려져 있다.
또 다른 면에서, 본 발명은 본 발명의 결합분자 또는 기능적 변이체에 의해 결합된 에피토프로서 SARA-CoV와 같은 코로나바이러스의 다양하고 비-오버래핑하는 에피토프에의 특이 결합을 위한 결합분자 또는 결합분자의 기능적 변이체를 스크리닝하는 방법을 제공하고, 여기서 상기 방법은 a) 스크리닝될 결합분자 또는 기능적 변이체, 본 발명의 결합분자 또는 기능적 변이체와 코로나바이러스 또는 그것의 단편을 접촉시키는 단계, b) 스크리닝될 결합분자 또는 기능적 변이체가 본 발명의 결합분자 또는 기능적 변이체와 코로나바이러스 또는 그것의 단편과의 특이적 결합에 대해 경쟁할 수 있는지를 측정하는 단계를 포함한다. 스크리닝될 결합분자 또는 기능적 변이체가 본 발명의 결합분자 또는 기능적 변이체를 갖는 코로나바이러스 또는 그들의 단편에 특이적으로 결합하기 위해 경쟁하는 능력이 없다면, 이것은 주로 다른, 비-오버래핑 에피토프에 결합할 것이다. 추가의 단계에서, 본 발명의 결합분자에 비하여 다른, 비-오버래핑 에피토프에 결합하는 스크린된 결합분자가 코로나바이러스 중화활성을 갖는가를 측정할 수 있다. 또 다른 추가의 단계에서, 본 발명의 결합분자에 비해 다른, 비-오버래핑 에피토프에 결합하고 코로나바이러스 중화활성을 갖는 스크리닝된 결합분자가 본 발명의 결합분자와 함께 상승작용하는 코로나바이러스 중화활성을 나타내는 조성물을 형성하는지를 측정할 수 있다. 비-경쟁적 결합분자에 대한 스크리닝과 (상승작용적) 중화활성을 측정하기 위한 방법은 당업자에게 잘 알려져 있다.
다음의 예들은 본 발명을 설명하기 위해 제공된다. 이 실시예들은 본 발명의 범위를 어느 경우로도 제한하려는 의도는 아니다.
실시예
1
SARS
-
CoV
에 노출된 환자의 말초 혈액 림프구를 사용한
scFv
파아지
디스플레이 라이브러리의 구성
SARS-CoV로부터 회복된 환자로부터 림프구를 얻었고(Rickerts et al., 2003 참조) 액체 질소 중에 냉동시켰다. 림프구를 37℃ 수조에서 신속히 해동하고 습식-냉동을 위해 옮겼다. 림프구를 50㎖ 튜브에서 냉각된 DMEM 배양액으로 최종 부피 50㎖으로 희석시키고 350×g에서 5분 동안 원심분리하였다. 얻은 세포 펠렛을 5㎖ DMEM 중에 현탁시키고 사멸세포를 가시화하기 위해 트립판-블루 배제를 사용하여 세포밀도를 현미경적으로 측정하였다. 모든 세포(~5×106)를 350×g에서 5분 동안 다시 회전시키고, 가만히 따라버리고 잔류 유체(DMEM) 중에 현탁시켰다. 이들 세포로부터 유기 상분리법(TRIZOLTM) 및 이어서 에탄올 침전법을 사용하여 전체적인 RNA를 제조하였다. 얻어진 RNA를 DEPC 처리된 초순도 물에 용해시키고 농도를 OD 260nm 측정법으로 측정하였다. 그리고 나서, RNA를 100ng/㎕의 농도로 희석시켰다. 그리고 나서, RNA 1㎍을 다음과 같이 cDNA로 전환하였다: 전체 RNA 10㎕에 DEPC 처리된 초순도 물 13㎕과 임의의 헥사머(500ng/㎕) 1㎕를 첨가하고, 얻어진 혼합물을 65℃에서 5분 동안 가열하고 습식-얼음 중에서 신속히 냉각시켰다. 그리고 나서, 5× 첫번째-스트랜드 완충액 8㎕, dNTP 2㎕(각각 10 mM), DTT 2㎕(0.1M), Rnase-억제제(40U/㎕) 2㎕ 및 SuperscriptTMⅢ MMLV 역 트란스크립타제(200U/㎕) 2㎕를 혼합물에 첨가하고, 실온에서 5분 동안 배양하고 그리고 50℃에서 1시간 동안 배양하였 다. 반응을 열 불활성화에 의해, 즉 혼합물을 15분 동안 75℃에서 배양함으로써 종료시켰다.
얻어진 cDNA 생성물을 DEPC 처리된 초순도 물로 최종부피 200㎕로 희석하였다. 얻어진 cDNA 생성물의 희석물의 50배 희석용액(10 mM Tris 완충액 중)의 OD 260nm는 0.1의 값을 가졌다.
희석된 cDNA 생성물 5~10㎕를, 특이 올리고뉴클레오티드 프라이머를 사용한 면역글로불린 감마 중쇄류 및 카파 또는 람다 경쇄 서열의 PCR 증폭용 주형으로서 사용하였다(표 2~9 참조). PCR 반응 혼합물은 20mM Tris-HCl(pH 8.4), 50mM KCl, 2.5mM MgCl2, 250μM dNTPs 및 1.25 유니트 Taq 폴리머라제로 이루어진 최종부피 50㎕ 중에, 희석된 cDNA 생성물 이외에, 25pmol 센스 프라이머와 25pmol 안티-센스 프라이머를 함유하였다. 96℃의 온도로 가열된-뚜껑을 갖는 열 순환기에서, 얻어진 혼합물을 2분 동안 신속히 녹이고, 96℃에서 30초, 60℃에서 30초 및 72℃에서 60초로 이루어진 증폭순환을 30회 실시하였다. 첫번째 증폭에서, 센스 검출된 프라이머 9개 (표 2 참조, 중쇄 가변영역의 모든 류를 포함) 각각을 HuCIgG 5'-GTC CAC CTT GGT GTT GCT GGG CTT-3'(SEQ ID NO:87)로 불리는, IgG 특이 상수 영역 안티-센스 프라이머와 결합시켜 약 650 염기쌍의 9개 생성물을 생성하였다.
이들 생성물을 2% 아가로스 겔 상에서 정제하였고 Qiagen 겔-추출 칼럼을 사용하여 겔로부터 단리하였다. 단리된 생성물 각각의 1/10을 동일한 9 센스 프라이머(중쇄 가변영역의 모든 종류를 포함)를 사용하여 상기와 같은 동일한 PCR 반응에 사용하였고, 그것에 의해 각 센스 프라이머는 4개의 J-영역 특이 안티-센스 프라이머 중 하나와 결합하였다(표 3 참조). 이것은 약 350 염기쌍의 36 생성물을 가져왔다. 얻어진 생성물을 2% 아가로스 겔 상에서 정제하고 Qiagen 겔-추출 칼럼을 사용하여 분리하였다. 3번째 라운드에서, 사용된 프라이머를 제한부위들로 연장하여(표 4 참조) 파아지 디스플레이 벡터 pDV-C05(SEQ ID NO:88 참조)에서 지향된 클로닝이 가능하도록 하는 조건으로, 분리된 생성물 각각의 1/10을 두번째 라운드에서와 동일한 프라이머 세트로 재-증폭시켰다. 이것은 다시 36개의 생성물을 가져왔다. 이들 생성물을 사용된(VH) 센스 프라이머 당 9개의 분획으로 울혈(pool)시켰다. 다음 단계에서, 울혈된 분획 2.5㎍과 pDV-C05 벡터 100㎍을 NcoI 및 XhoI로 소화시키고 겔로 정제하였다. 그리고 나서, 다음과 같이 16℃에서 밤새도록 결찰을 수행하였다. pDV-CO5 벡터 500ng에, 풀된 분획 70ng을 50mM Tris-HCl(pH 7.5), 10mM MgCl2, 10mM DTT, 1mM ATP, 25㎍/㎖ BSA 및 T4 DNA 리가아제 2.5㎕ (400u/㎕)를 함유하는 총 부피 50㎕ 결찰 혼합물에 첨가하였다. 이 과정을 각각의 풀된 분획에 대해 수행하였다. 결찰 혼합물은 당업자에게 잘 알려진, 페놀/클로로포름, 이어서 클로로포름 추출 및 에탄올 침전에 의해 정제되었다. 얻어진 DNA를 초순수 물 50㎕에 용해시키고 결찰 혼합물 당 2회씩 분취량(aliquots) 2.5㎕를 제조자 지침에 따라 TG1 반응성 E. coli 세균 40㎕로 전기영동하였다(Stratagene). 형질전환체를 밤새도록 37℃에서 앰피실린 50㎍/㎖과 4.5% 글루코스가 공급된 2TY 아가를 함유하는 총 27개의 디쉬(풀된 분획당 3개의 디쉬; 디쉬의 디멘젼 240 mm×240 mm)에서 성장시켰 다. 가변 중쇄 영역의 (서브)라이브러리는 아가 플레이트로부터의 형질전환체를 긁어서(scraping) 얻었다. 이 (서브)라이브러리를 QiagenTM 키트를 사용한 플라즈미드 DNA 제조를 위해 직접적으로 사용하였다.
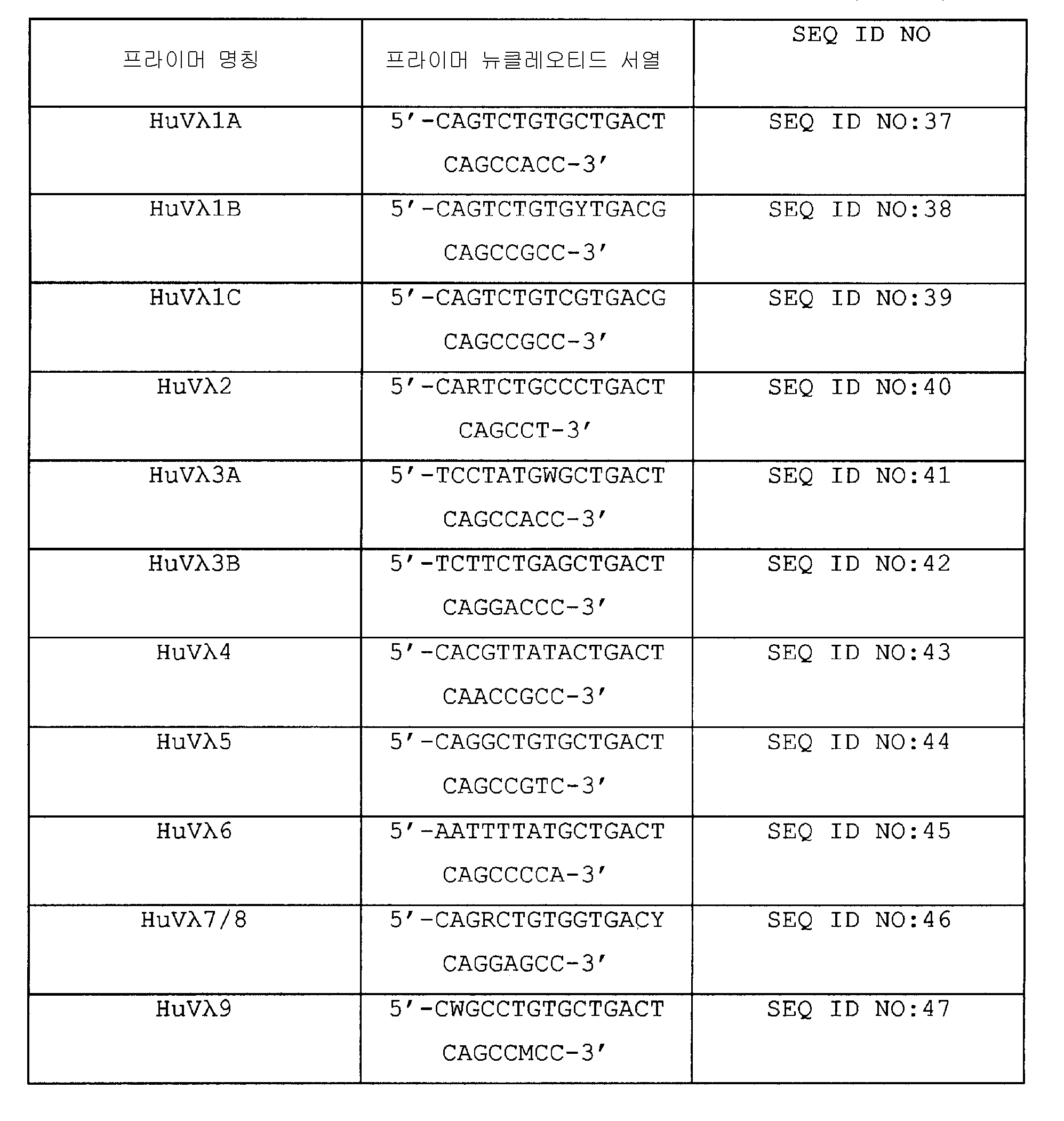
경쇄 면역글로불린 서열을, 표 5~9에 나타낸 프라이머를 사용하는 조건으로 상기 중쇄 영역에 대해 기재된 바와 같은 유사한 3회의 PCR 과정 및 동일한 반응 계수로 동일한 cDNA 제제로부터 증폭하였다. 첫번째 증폭은 각각 HuCk 5'-ACACTCTCCCCTGTTGAAGCTCTT-3'(SEQ ID NO:89)로 불리우는 C-카파 또는 C-람다 불변 영역 HuCλ2 5'-TGAACATTCTGTAGGGGCCACTG-3'(SEQ ID NO: 90) 또는 HuCλ7 5'-AGAGCATTCTGCAGGGGCCACTG-3'(SEQ ID NO: 91) (HuCλ2 및 HuCλ7 안티-센스 프라이머는 사용하기 전에 등몰량으로 혼합되었다)로 혼합된 17개 경쇄 가변 영역 센스 파라이머들(람다 경쇄용 11개(표 5 참조) 및 카파 경쇄용 6개(표 6 참조)의 세트를 사용하여 수행하였고 약 600 염기쌍의 생성물 17개를 수득하였다. 이들 생성물을 2% 아가로스 겔 상에서 정제하고 Qiagen 겔-추출 칼럼을 사용하여 겔로부터 분리하였다. 분리된 생성물들 각각의 1/10을 동일한 17개 센스 프라이머들을 상기와 같은 동일한 PCR 반응에 사용하였고, 그것에 의해 각 람다 경쇄 센스 프라이머를 3개의 J람다-영역 특이 안티-센스 프라이머 중 하나(표 7 참조)와 결합시키고 그리고 각 카파 경쇄 센스 프라이머를 5개의 J 카파-영역 특이 안티-센스 프라이머의 하나와 결합시켰다(표 8 참조). 이것으로 약 350 염기쌍의 생성물 63개가 생겼다. 얻어진 생성물을 2% 아가로스 겔에서 정제하였고 Quagen 겔-추출 칼럼을 사용하여 겔로부 터 분리하였다. 세번째 라운드에서, 분리된 생성물 각각의 1/10을, 사용된 프라이머를 중쇄(서브)라이브러리 벡터에서 유도된 클로닝이 가능하도록 제한 부위(표 9 참조)로 연장되는 것을 조건으로 두번째 라운드와 같이 동일한 프라이머 세트로 재-증폭하였다. 그 결과 다시 63개의 생성물을 얻었다. 이들 생성물을 10 분획으로 풀(pool)하였다. 분획의 이 갯수는 다양한 경쇄류의 천연 분포를 라이브러리 내에서 유지하고 특정 류보다 많이 또는 적게 나타내기 위해 선택하였다. 하나의 류(family) 내의 대립형질의 수를 사용하여 라이브러리 내의 표현의 백분률을 결정하였다(표 10 참조). 다음, 분획을 SalI 및 NotI로 소화시키고 중쇄 (서브)라이브러리 벡터에서 결찰시키고, 이것을 중쇄 (서브)라이브러리에 대하여 위에서 기재한 바와 동일한 결찰 과정 및 부피를 사용하여, 동일한 제한 효소를 이용하여 절단하였다. 결찰 정제 및 이후의 생성된 최종적인 라이브러리의 변형을 또한 중쇄 (서브)라이브러리에 대한 상기와 같이 수행하였다. 변형물을 50㎍/㎖ 암피실린과 4.5% 글루코스가 보충된 2TY 아가를 함유하는 30개의 디쉬(풀된 분획당 3개의 디쉬; 디쉬의 디멘젼: 240 mm×240 mm)에서 성장시켰다. 모든 세균들을 50㎍/㎖ 암피실린과 4.5% 글루코스를 함유하는 2TY 배양 매질에서 15%(v/v)로 글리세롤과 혼합하고, 80℃에서 1.5㎖ 부분 중에 냉동시켰다.
실시예
2
특이적으로
SARS
-
CoV
를 인식하는 단일-사슬
Fv
단편을 운반하는
파아지의
선택
항체 단편들을, 특히 미국 특허 6,265,150 및 WO 98/15833에 기재된 바와 같 이, 항체 파아지 디스플레이 라이브러리 및 기술을 사용하여 선택하였고, 이 둘은 모두 전체적으로 본 명세서에 병합된다. 모든 과정을 다른 언급이 없는 한 실온에서 수행하였다. 불활성화된 SARS-CoV 제제(Frankfurt 1 균주)를 다음과 같이 제조하였다. SARS-CoV 균주 Frnakfurt 1을 감염된 베로 세포로부터의 매질을 세포변성 효과(CPE)가 관찰되자마자 수확하였다. 수확매질을 15분 동안 3000rpm에서 원심분리하여 세포 부스러기를 제거하였다. 얻어진 상등액을 수확하고, 또 다시 15분 동안 3000rpm에서 회전시키고 깨끗한 튜브로 옮겼다. 이어서, 초원심분리 튜브에 PBS 중의 살균 25% 글리세롤 10㎖를 채웠다. 맑아진 상등액 20㎖를 글리세롤 쿠션에 부드럽게 따르고 튜브를 2시간 동안 4℃, 20,000 rpm에서 회전시켰다. 상등액을 따라버리고 바이러스 펠렛을 TNE 완충액(10mM Tris-HCl pH 7.4, 1mM EDTA, 200 mM NaCl) 1㎖ 중에 재현탁하고 -80℃에서 보관하였다. 그리고 나서, 재현탁된 바이러스 펠렛을 드라이 아이스 상에서 45kGy에서 감마-조사시켰다. 이어서, 그들을 세포 배지에서 감염성의 부재에 관하여 시험하였다. 감염성의 부재가 확립되면, 이와 같이 얻은 불활성화 SARS-CoV 제제는 SARS-CoV에 특이적으로 결합하는 단일-사슬 파아지 항체의 선택을 위해 사용되었다.
불활성화 바이러스 제제 및 열-불활성화된 송아지 태아 혈청(FBS)을 4℃에서 밤새도록 별개의 MaxisorpTM 플라스틱 튜브(Nunc)의 표면에 코팅하였다. 튜브를 2% FBS와 2% 무지방 우유 분말을 함유하는 PBS 2㎖(2% PBS-FM)에 대하여 블록하였다. 2시간 후, FBS-코팅 튜브를 비우고 PBS로 3회 세척하였다. 이 튜브에, 본질적으로 De Kruif et al.(1995a) 및 여기의 참조(그들 전체가 본 명세서에 병합된)에 의해 기재된 바와 같이 제조된 단일-사슬 Fv 단편(scFvs)를 발현하는 파아지 디스플레이 라이브러리 500㎕ (약 1013 cfu), 4% PBS-FM 500㎕ 및 2% PBS-FM 2㎖를 첨가하였다. 튜브를 밀봉하고 실온에서 2시간 동안 천천히 회전시켰다. 이어서, 얻어진 블록된 파아지 라이브러리(3㎖)를 PBS로 3회 세척해놓은 SARS-CoV 제제-코팅 튜브로 옮겼다. Tween-20을 0.05%의 최종 농도까지 첨가하고 실온에서 또는 37℃에서 느린 회전 휠 상에서 2시간 동안 결합을 진행시켰다. 튜브를 비우고 0.05% Tween-20을 함유하는 PBS로 10회 세척하고, 이어서 PBS로 10회 세척하였다. 글리세린-HCl(0.05M, pH 2.2) 1㎖를 첨가하여 결합된 파아지를 용출시키고, 튜브를 10분 동안 천천히 회전시켰다. 중화를 위해, 용출된 파아지를 1M Tris-HCl pH 7.4 500㎕에 첨가하였다. 이 혼합물에, 지수적으로 증가하는 XL-1 블루 박테리아 배지 5㎖를 첨가하였다. 얻어진 배양물을 흔들지 않고 37℃에서 30분 동안 배양하였다. 그리고 나서, 박테리아를 앰피실린, 테트라실린 및 글루코스를 함유하는 TYE 아가 플레이트에 놓았다. 플레이트를 37℃에서 밤새도록 배양한 후, 콜로니들을 플레이크로부터 긁어 De Kruif et al.(1995a) 및 WO 02/103012(둘 다 본 명세서에 병합된)에 의해 기재된 바와 같이 풍부한 파아지 라이브러리를 제조하는데 사용하였다. 즉, 긁어놓은 박테리아를 앰피실린, 테트라실린 및 글루코스를 함유하는 2TY 매질을 접종하는데 사용하였고 37℃의 온도에서 ~0.3의 OD 600 nm에서 성장시켰다. CT 또는 VCSM13 헬퍼 파아지를 첨가하고 매질을 앰피실린, 테트라실린 및 카나마이신을 함유하는 2TY로 교환한 후 박테리아로 감염시켰다. 배양을 30℃에서 밤새도록 계속하였다. 다음 날, 박테리아를 원심분리에 의해 2TY 매질로부터 제거하고 그 후 얻어진 상등액 중의 파아지를 폴리에틸렌 글리콜 6000/NaCl을 이용하여 침전시켰다. 마지막으로, 파아지를 1% BSA를 함유하는 소용량의 PBS에 용해시키고, 필터-살균하고 선택을 위한 다음 라운드에 사용하였다. 선택/재-감염 공정을 2회 또는 3회 수행하였다. 선택의 각 라운드 후, 개별적인 E. coli 콜로니들을 사용하여 모노클로날 파아지 항체를 제조하였다. 본질적으로, 개별적인 콜로니들을 로그-파아지로 성장시키고 VCSM13 헬퍼 파아지로 감염시킨 후, 파아지 항체 생산을 밤새도록 진행시켰다. 상등액을 함유하는 파아지 항체를 96-웰 플레이트에 코팅된 SARS-CoV 제제에 대한 결합 활성에 관하여 ELISA로 시험하였다. 상기 선택에서, SC03-014로 불리는 파아지 항체를 얻었다. 파아지 항체 SC03-014의 ScFvs를 De Kruif et al.(1995a 및 1995b) 및 참조문헌에 기재된 바와 같이 생성하였다. scFvs의 완충액을 1×PBS로 조절하였다.
추가적으로, 항체 단편들을 본질적으로 위에 기재된 바와 같은 단일 사슬 Fv 단편(scFvs)를 발현하는 면역 파아지 디스플레이 라이브러리(이 라이브러리를 구성하기 위해 실시예 1을 참조)로부터 선택하였다. 하기의 선택을 위해, UV-불활성화된 SARS-CoV 제제를 제조하였다. UV-불활성화된 SARS-CoV(Frankfurt 1 균주)를 다음과 같이 제조하였다. O.I. moi(감염의 다중도) SARS-CoV 균주 Frankfurt 1으로 감염된 베라 세포로부터 매질을 세포변성 효과(CPE)가 관찰되자마자 수확하였다. 세포를 일단 -20℃로 냉각시키고 해동시켰다. 수확된 매질을 15분 동안 3000rpm에서 원심분리하여 세포 부스러기들을 제거하였다. 얻어진 상등액을 수집하고, 15분 동안 3000 rpm에서 다시 회전시키고 깨끗한 튜브로 옮겼다. 이어서, 초원심분리 튜브에 PBS 중의 살균 25% v/v 글리세롤 10㎖를 채웠다. 깨끗해진 상등액 20㎖를 글리세롤 쿠션에 부드럽게 적용시키고 튜브를 2시간 동안 4℃, 20,000 rpm에서 Beckman SW28 회전자 중에서 회전시켰다. 상등액을 따라버리고 바이러스 펠렛들을 TNE 완충액(10mM Tris-HCl pH 7.4, 1mM EDTA, 200 mM NaCl) 1㎖ 중에 재현탁시키고 -80℃에서 저장하였다. 그 다음, 재현탁된 바이러스 펠렛에 4℃에서 15분간 UV를 조사하였다(UV-B 조사 280~350nm; λmax 306nm). 이어서, 이들을 세포 배양물 중에서 감염성의 부재에 관하여 조사하였다. 감염성이 없다고 확립되면, 이와 같이 얻은 불활성화된 SARS-CoV 제제를 추가의 실험에 사용하였다.
상기의 선택과 반대로, 열-불활성화 송아지 태아 혈청 코팅된 MaxisorpTM 튜브(Nunc)를 사용한 비 예비-공제(pre-subtraction)를 수행하였다. SARS-CoV 코팅된 튜브에, 단일 사슬 Fv 단편(scFvs)을 발현하는 면역 파아지 디스플레이 라이브러리 500㎕(약 1013 cfu), 4% PBS-FM의 1 부피 및 Tween-20를 최종 농도가 0.05%가 되도록 첨가하였다.
단일 선택 라운드만으로 이루어진 면역 파아지 디스플레이 라이브러리 선택의 경우, 결합은 37℃ 또는 실온에서 느린 회전 휠 상에서 실시되도록 허용되었고 이어서 교반없이 30분 동안 배양되었다. 다음의 선택과 세척이 실시되었다: 37℃에서 배양, 0.05% Tween-20을 함유하는 PBS(PBST)로 5회 및 PBS로 5회 세척; 37℃에서 배양, PBST로 10회 및 PBS로 10회 세척; 실온에서 배양, PBST로 10회 및 PBS로 10회 세척. 결합된 파아지를 용출시키고 상기와 같이 처리하였다. 개개의 콜로니로부터 유도된 파아지들을 96-웰 플레이트에 코팅된 SARS-CoV에 대한 결합 활성에 관하여 ELISA로 시험하였다. 면역 파아지 디스플레이 라이브러리로부터의 선택에서 SC03-022로 불리는 파아지 항체를 얻었다.
실시예
3
SARS-
CoV
특이 단일-사슬
파아지
항체의 확인
상기 스크린에서 얻어진 선택된 단일-사슬 파아지 항체들을 특이성, 즉 상기와 같이 제조된 UV-불활성화된 SARS-CoV 제제에 대한 결합에 관하여 ELISA로 확인하였다. 이에 더하여, 단일-사슬 파아지 항체를 또한 10% FBS에 대한 결합에 관하여 시험하였다. 이 목적을 위해, UV-불활성화된 SARS-CoV 제제 또는 10% FBS 제제를 MaxisorpTM ELISA 플레이트에 코팅하였다. 코팅 후, 플레이트를 2% PBS-FM으로 블록하였다. 선택된 단일-사슬 파아지 항체들을 4% PBS-FM의 동일 부피 중에서 배양시켜 블록된 파아지 항체들을 얻었다. 플레이트들을 비우고, PBS로 3회 세척하고 나서 블록된 파아지 항체를 첨가하였다. 배양은 1시간 동안 진행되었고, 플레이트를 0.05% Tween-20을 함유하는 PBS로 세척하고, 결합된 파아지 항체를 퍼옥시다제에 컨쥬게이트된 안티-M13 항체를 사용하여 검출하였다(OD 492 nm 측정기 사용). 대조로서, 단일-사슬 파아지 항체 없이 또는 티로글로불린(SC02-006)에 대해 지향된 대조 단일-사슬 파아지 항체를 사용하여 동시에 과정을 실시하였다(De Kruif et al. 1995a 및 1995b 참조). 두 대조는 모두 음성 대조로서 작용하였다. 도 1에 나 타낸 바와 같이, SC03-014 및 SC03-022로 불리는 선택된 파아지 항체들은 고정화된 UV-불활성화 SARS-CoV 제제에 상당한 결합을 나타내었고, 반면 FBS에 대한 결합은 관찰되지 않았다.
실시예
4
SARS
-
CoV
에 특이한
scFvs
의 특성화
선택된 특이적 단일 사슬 파아지 항체(scFv) 클론으로부터 플라즈미드 DNA를 얻었고 뉴클레오티드 서열을 표준 기술법에 따라 결정하였다. SC03-014 및 SC03-022로 불리는 scFvs의 뉴클레오티드 서열(암호화를 위한 제한부위 포함)을 각각 SEQ ID NO:92와 SEQ ID NO:94에 나타내었다. SC03-014 및 SC03-022로 불리는 scFvs의 아미노산 서열을 각각 SEQ ID NO: 93과 SEQ ID NO: 9에 나타내었다. HV와 VL 유전자 동정(Tomlinson IM, Williams SC, Ignatovitch O, Corbett SJ, Winter G. V-BASE Sequence Dictionary. Cambridge United Kingdom: MRC Centre for Protein Engineering (1997) 참조) 및 SARS-CoV 제제에 특이적으로 결합하는 scFvs의 중쇄 CDR3 조성을 표 11에 나타내었다.
실시예
5
선택된
안티
-
SARS
-
CoV
단일 사슬
Fvs
로부터 완전한 인간 면역글로불린 분자(인간
모노클로날
안티
-SARS-
CoV
항체)의 구성
SC03-014 및 SC03-022로 불리는 scFvs의 중쇄 및 경쇄 가변 영역을 올리고뉴클레오티드를 사용하여 PCR-증폭시켜, 각각 IgG 발현 벡터 pSyn-C03-HCγ1(SEQ ID NO:96) 및 pSyn-C05-Cκ(SEQ ID NO: 97)에 발현을 위한 제한부위 및/또는 서열을 부착시켰다. scFv SC03-014의 VL 유전자를 올리고뉴클레오티드 5K-I acctgtctcgagttttccatggctgacatccagatgacccagtctccatcctcc (SEQ ID NO:98) 및 sy3K-C gctgggggcggccacggtccgtttgatctccaccttggtccc (SEQ ID NO:99)를 사용하여 증폭하였고 PCR 산물을 벡터 pSyn-C05-Cκ로 암호화하였다. scFv SC03-022의 VL 유전자를 올리고뉴클레오티드 5K-J acctgtctcgagttttccatggctgacatcgtgatgacccagtctc cag (SEQ ID NO:100) 및 sy3K-F gctgggggcggccacggtccgcttgatctccaccttggtccc (SEQ ID NO:101)을 사용하여 증폭하였고 PCR 산물을 벡터 pSyn-C05-Cκ로 암호화하였다. 모든 구조체에 대한 뉴클레오티드 서열을 본 발명의 당업자에게 알려진 표준 기술에 따라 확인하였다. scFv SC03-014의 VH 유전자를 올리고뉴클레오티드 5H-B acctgtcttgaattctccatggccgaggtgcagctggtggagtctg (SEQ ID NO: 102) 및 sy3H-A gcccttggtgctagcgctggagacggtcaccagggtgccctggcccc (SEQ ID NO:103)을 사용하여 증폭시켰다. scFv SC03-022의 VH 유전자를 올리고뉴클레오티드 세트 5H-H acctgtcttgaattctccatggccgaggtgcagctggtgcagtctgg (SEQ ID NO. 104) 및 sy3H-C gcccttggtgctagcgctggagacggtcacggtggtgccctggcccc (SEQ ID NO:105)를 사용하여 증폭하였다. 그리고나서, PCR 산물을 벡터 pSyn-C03-HCγ1으로 암호화하고 뉴클레오티드 서열을 본 분야의 당업자에게 알려진 표준 방법에 따라 확인하였다.
항-SARS-CoV 인간 IgG1 중쇄를 암호화하는 생성된 발현 구조체 pgG103-014C03 및 pgG103-022C03는 pSyn-C05-VkI (VL SC03-014) 및 pgG103-022C05(VL SC03-022)와 조합하여 각각 HEK293T 또는 PER.C6? 세포에서 일시적으로 발현되었 고 IgG1 항체를 함유하는 상등액을 얻었다. CR03-014 및 CR03-022로 불리는 항체의 중쇄의 뉴클레오티드 서열은 각각 SEQ ID NO:106 및 SEQ ID NO:108에 나타내었다. 항체 CR03-014 및 CR03-022의 중쇄의 아미노산 서열은 각각 SEQ ID NO:107 및 SEQ ID NO:109에 나타내었다.
항체 CR03-014 및 CR03-022의 경쇄의 뉴클레오티드 서열은 각각 SEQ ID NO:110 및 SEQ ID NO:112에 나타내었다. 항체 CR03-014 및 CR03-022의 경쇄의 아미노산 서열은 SEQ ID NO: 111 및 SEQ ID NO:113에 나타내었다. 그 후에, 재조합 인간 모노클로날 항체는 일반적으로 면역글로불린에 대해 사용되는 표준 정제방법을 사용하여 단백질-A 칼럼 및 크기-배제 칼럼을 통해 정제되었다(참고로 본 명세서에 병합되어 있는 WO 00/63403을 참조).
실시예
6
재조합 인간 항-SARS-
CoV
항체의 SARS-
CoV
중화활성에 대한 스크리닝 조사
SARS-CoV 중화조사를 베로 세포에서 수행하였다(ATCC CCL 81). 중화 조사에 사용된 SARS-CoV 균주는 Frankfurt 1 균주(이 균주의 완전 게놈에 대해서는 EMBL-데이타베이스 접수번호 AY291315를 참조)였다(Rickerts et al. 2003). 이 균주의 바이러스 스톡을 당업자에게 알려진 방법인 Spearman and Kaeber법에 따라 산출된 역가로, 4×103 TCID50/㎖(㎖ 당 50% 조직 배양 감염성 투여량)의 역가로 사용하였다. 상기와 같이 생산된 재조합 인간 항-SARS-CoV 항체를 1:4로 시작하여 PBS 중에서 비희석된 재료(2.5mg/㎖)의 연속적인 2-배 희석물로 스크리닝하였다 (희석범위 1:4~1:512) . ≥1:4의 특이적 중화역가를 스크리닝 방법에서 SARS-CoV에 대한 항체의 반응성의 특이적 증거로 간주하였다. SARS-환자로부터의 회복기 혈청을 중화 조사에 대한 양성 대조로 사용하였다.
일반적으로, 중화조사는 다음과 같이 실시된다. 각각의 항체 희석물 25㎕를 바이러스 현탁액 25㎕(약 100 TCID50/25㎕)와 혼합하고 37℃에서 1시간 동안 배양하였다. 그리고 나서, 현탁물을 96-웰 플레이트로 3중으로 피펫으로 옮겼다. 그 다음, 10% w/v FCS와 항체를 함유하는 DMEM에 재현탁된 베로세포의 신선하게 트립신화되고 균질화된 현탁액 50㎕(T75-플라스크의 합류 세포 단일층의 1: 3 분열)를 첨가하였다. 접종된 세포를 37℃에서 3~4일 동안 배양하였고 세포병리학적 효과(CPE)의 전개에 대해 매일 관찰하였다. CPE를 양성 대조(바이러스 접종된 세포) 및 음성 대조(모조-감염된 세포)와 비교하였다. 개개의 세포 배양물에서 CPE의 완전한 부재는 보호(=100% 역가 감소)로 정의된다. 웰의 66%의 보호를 제공하는 가장 높은 항원/혈청 희석은 중화항체 역가로 정의된다. 실험은 3중으로 3회 실시되었다(표 12A, B 및 C 참조). IgG CR03-014, CR03-022, 음성 대조 IgG1 및 SARS 환자로부터의 양성 대조 혈청을 SARS-CoV 중화 활성에 대해 시험하였다. 표 12A, B 및 C로부터 IgG CR03-014와 CR03-022가 상당한 중화 활성을 나타낸다는 것이 분명하다. CR03-014 IgG는 상기 조사에서 128(n=1) 또는 256(n=2)의 역가에서 Frankfurt 1 균주를 중화시켰다. CR03-022 IgG는 32(n=1) 또는 64(n=2)의 역가에서 Frankfurt 1 균주를 중화시켰다. 이들 역가는 CR03-014에 대한 2.4μg/㎖(n=2) 및 4.9 μg/ ㎖(n=2) 및 CR03-022에 대한 9.8μg/㎖(n=2) 및 19.5μg/㎖(n=1)의 조직 배양액에서의 최종 항체 중화 농도에 대응한다. 이들 농도에 비추어, 둘 다의 중화항체 모두 SARS-CoV 감염에 의한 질환의 예방 및/또는 치료에 적당하다.
이에 더하여, 다른 SARS-CoV 균주를 항-SARS-CoV 항체의 보호의 능력 및 폭을 평가하는데 사용하였다. SARS-CoV 균주를 HKU-36, HKU-39849, HKU-66, HKU-61567, GZ43 및 GZ50을 시험 전에 2회 또는 3회 FRhK-4 세포에서 계대배양하였다(표 13 참조). 균주 HKU-61644를 베로 세포에서 계대배양시키고 계대배양 1과 15 이후에 시험하였다. SARS-CoV 중화조사를 다음과 같이 FRhK-4 세포에서 수행하였다. 항체의 스톡 용액 500㎕ (100μg/㎖)를 보존 매질(1% w/v FCS가 보충된 MM, MEM) 중에서 제조하였다. 이 스톡 용액으로부터 2-배 연속적 희석액을 제조하였다. 220㎕ 스톡 용액(100μg/㎖)을 96-웰 플레이트에 이중으로 첨가하고 그것으로부터 110㎕를 취하고 9개의 순차적인 웰 각각에 110 ㎕ MM과 혼합하였다. 10번째 웰의 110㎕을 따라버렸다. 이것은 0.2~100 μg/㎖ 항체를 함유하는 10개의 웰을 가져왔다. 항체 희석액 110㎕를 본 분야의 당업자에게 알려진 Reed and Muench 법에 따라 산출된 역가로 2000 TCID50/㎖의 농도에서 다양한 SARS-CoV 분리물 110㎕와 혼합하였다. 이 단계에서, 220㎕의 부피에서, 항체 농도는 SARS-CoV 1000 TCID50/㎖의 존재하에 0.1~50μg/㎖로 변하였다. 항체/바이러스 혼합물을 함유하는 96-웰 플레이트를 37℃에서 1~2시간 동안 예비배양시켰다. 항체/바이러스 혼합물 100㎕를 100㎕ MM 중의 합류물 FRhK-4 세포를 함유하는 제2 96-웰 조직 배양 플레이트로부터의 웰 에 4중으로 첨가하였다. 이 최종 단계 동안, SARS-CoV의 100 TCID50이 0.05에서 25μg/㎖으로 변하는 항체 농도 하에서 존재하였다. 세포를 37℃에서 배양시켰고 72 및 96시간에서 CPE의 전개에 관하여 관찰하였다. CPE를 양성 대조(SARS-CoV 예방접종된 세포) 및 음성 대조(MM 만으로 배양된 세포)와 비교하였다. 항체 중화 역가를 4중 세포 배양물의 100% 보호를 제공하는 항체의 농도로서 측정하였다. 모노클로날 항-SARS-CoV 항체 CR03-014는 농도 12.5μg/㎖에서 모든 시험된 SARS-CoV 분리물의 100 TCID50을 완전히 중화시켰다(표 13 참조). 이것은 항체 CR03-014가 다양한 SARS-CoV 분리물을 중화시킬 수 있다는 것을 나타낸다.
추가의 실험에서, SARS-CoV 중화 조사는 SARS-CoV 중화 항체 CR03-014과 CR03-022 사이의 시너지를 측정하기에 앞서, Frankfurt 1 균주에 대해 기재된 바와 같이 수행되었다. 거의 유사한 잠재력의 항체 CR03-014와 CR03-022의 스톡 용액을 다양한 비율로 혼합하였다. CR03-022와 비교하여 CR03-014의 4배 더 높게 평가된 잠재력을 보상하기 위해, 2.5mg/㎖의 CR03-014 항체 스톡 용액을 625μg/㎖로 4배 희석하였다. 이어서, 항체 CR03-014와 CR03-022를 다음의 비율로 혼합하였다(혼합물 A: CR03-014 0%, CR03-022 100%; 혼합물 B: CR03-014 10%, CR03-022 90%; 혼합물 C: CR03-014 50%, CR03-022 50%; 혼합물 D: CR03-014 90%, CR03-022 10%; 그리고 혼합물 E: CR03-014 100%, CR03-022 0%). 혼합물 중의 항체가 추가의 효과를 가질 때, 혼합물은 본 혼합물에 존재하는 개별적인 항체와 동일한 역가로 SARS-CoV를 중화시켜야 한다. 혼합물 중의 항체가 시너지 효과를 가지면, 혼합물은 본 발명에 존재하는 개개의 항체보다 더 높은 역가에서 SARS-CoV를 중화시켜야 한다. 중화 조사는 상기와 같이 3중 웰에서 2회 수행하였다. 두 조사 결과를 조합하였다. 웰의 적어도 66%의(시험된 6개의 웰 중 4) 보호는 중화 항체 역가로 정의되었다. 개별적인 혼합물의 중화역가를 표 14에 나타내었다. 표 14로부터 혼합물들이 다음의 역가를 갖는다는 것을 추론할 수 있다: 혼합물 A, 64; 혼합물 B, 256; 혼합물 C, >1024; 혼합물 D, 265; 및 혼합물 E, 16. 이것으로부터 두개의 항체를 조합하여 시험하였을 때(혼합물 B~D), 중화 역가는 개별적인 항체 CR03-014 및 CR03-022의 역가보다 높다고 결론지을 수 있다. 이와 함께, 이들 자료들은 항체 CR03-014 및 CR03-022가 시너지성 SARS-CoV 중화활성을 보인다는 것을 나타낸다.
또 다른 구현예에서, 항-SARS-CoV 항체들 간에 시너지를 나타내는 SARS-CoV 중화 조사는 다음과 같이 FRhK-4 세포(ATCC CRL-1688)에서 수행되었다. HK-39849로 불리는 SARS-CoV 균주(GenBank 수탁번호 AY278491)를 일반적인 당업자에게 알려진 Reed and Muench의 방법에 따라 산출된 역가 2×103 TCID50/㎖에서 사용하였다. 인간 항-SARS-CoV 항체를 이중으로 200μg/㎖의 농도에서 시작하여 보존 매질(MM)(항체를 갖는 MEM 중 1% w/v) 중에서 연속 1.46-배 희석으로 스크린하였다(희석범위 200~6.7μg/㎖). 4개의 다른 조성물을 시험하였다: 항체 CR03-014 개별적으로, 항체 CR03-022 개별적으로, 대조 IgG1 항체, 및 항체 CR03-014 및 CR03-022 조합하여(각 항체의 시작 농도 200μg/㎖ ). 바이러스 현탁액 110㎕를 대표적인 재조합 인간 항-SARS-CoV 항체 희석물 110㎕와 혼합하고 1시간 동안 37℃에서 배양하였다. 이 현탁액 100㎕를 100㎕ MM 중에 FRhK-4 세포의 80% 합류 단일층을 함유하는 96-웰 플레이트로 이중으로 2회 피펫으로 계량하였다. FRhK-4 세포를 37℃에서 배양하고 3~4일 후에 CPE의 진행에 대해 관찰하였다. CPE를 양성대조(바이러스 접종된 세포) 및 음성대조(모조-감염된 세포 또는 재조합 항체만으로 배양된 세포)와 비교하였다. 개개의 세포 배양물에서의 CPE의 완전한 부재는 보호(=100% 역가 감소)로 정의되었다. 조합 인덱스(CI)의 개념은 상기와 같은 정량적 시너지 효과에 사용되었다(Chou and Talalay, 1984). 추가적 효과를 생성하는 약제의 조합 개념에 따르면, 혼합물에서 개별적으로 혼합물과 동일한 효과를 갖는 약제의 농도(ceffect)에 대한 혼합물에서 그들의 농도(cmixt)의 비의 합은 1이다. 이 합은 CI이다. 이 합이 1보다 작으면, 약제는 시너지로 작용한다.
이-성분 시스템에서, 현재 연구에서, CI는 다음과 같이 산출된다:
C1mixt는 특정 수준의 억제(f)를 가져오는 혼합물의 첫번째 성분의 농도이고, C1effect는 단독으로 (두번째 성분의 부재시) 두번째 성분의 혼합물과 동일한 억제 효과를 가져오는 첫번째 성분의 농도이고, c2mixt와 c2effect는 두번째 성분에 대한 대응하는 농도이다.
항체 CR03-014와 CR03-022에 대한 CI를 측정하기 위해, 중화조사가 상기와 같이 수행된다. 균주 HKU39849의 100 TCID50의 완전 중화는 CR03-014의 경우 7.6μg/㎖, CR03-022의 경우 50.0μg/㎖ 및 조합물로 첨가되었을 때는 각 항체의 2.4μ g/㎖에 도달하였다. 이 결과는 2.4/7.6 + 2.4/50.0= 0.36의 CI를 가져왔다. 50% 중화는 CR03-014의 경우 5.9μg/㎖, CR03-022의 경우 30.2μg/㎖ 및 조합물로 첨가되었을 때는 각 항체의 1.7μg/㎖에 도달하였다. 이 결과는 1.7/5.9 + 1.7/30.2= 0.34의 CI를 가져왔다. 그러므로, 50 및 100% 중화에서 1 미만의 CI값이 CR03-014와 CR03-022의 혼합물에 대해 관찰되었고, 이것은 두 항체가 모두 SARS-CoV에 대해 시너지 작용을 한다는 것을 나타낸다.
실시예
7
항-
SARs
-
CoV
항체의 SARS-
CoV
, SARS-
CoV
스파이크 단백질 및 그것의 단편에의 결합
SARS-CoV에 대한 항-SARS-CoV 항체의 결합을 검출하기 위한 ELISA는 다음과 같이 수행되었다. ELISA 플레이트의 웰을 밤새도록 탄산수소염 완충액 50mM pH 9.6중에서 UV-불활성화된 SARS-CoV 제제로 코팅하였다. 이 플레이트의 웰을 0.05% Tween을 함유하는 PBS로 3회 세척하고 1% BSA를 함유하는 PBS로 37℃에서 2시간 동안 블록하였다. 그리고나서, 1% BSA를 함유하는 PBS 중에 희석된 항체를 실온에서 1시간 동안 배양하였다. 웰을 0.05% Tween을 함유하는 PBS로 3회 세척하였고 뮤린 항-Hu-IgG HRP 컨쥬게이트를 사용하여 실온에서 1시간 동안 배양하였다. O-페닐렌디아민 기질에서 전개를 행하였고, 1M H2SO4를 첨가하여 반응을 멈추고 흡광도를 492 nm에서 측정하였다. 도 2에 나타낸 바와 같이, 항체 CR03-014 및 CR03-022 모두는 관련없는 항원에 대해 지향된 음성 대조 IgG와 반대로 ELISA에서 불활성화된 SARS-CoV 제제를 결합시킬 수 있다.
항체 CR03-014와 CR03-022의 표적을 검출하기 위해, 또 다른 결합조사가 사용되었다. 단일사슬 파아지 항체 CR03-014와 SC03-022를 SARS-CoV의 단백질을 재조합적으로 발현시키는 HEK293T 세포를 결합시키기 위한 그들의 능력에 대해 분석하였다. 이것을 위해, 마지막 HEK293T 세포를 SARS-CoV 균주 Frankfurt 1으로부터의 스파이크 단백질을 암호화하는 cDNA 서열을 수반하는 플라스미드로 또는 대조 벡터로 트란스펙션시켰다. 유동세포분석법의 경우, 단일사슬 파아지 항체들을 트란스펙션된 HEK293T 세포의 염색에 앞서 우선 4℃에서 15분 동안 4% PBS-M의 동일 부피로 블록시켰다. 블록된 파아지 항체들을 모조 트란스펙션된 HEK293T 세포와 SARS-CoV S 단백질로 트란스펙션된 HEK293T 세포에 첨가하였다. 세포에 대한 단일 사슬 파아지 항체의 결합은 비오티닐화된 항-M13 항체(Santa Cruz Biotechnology) 및 이어서 스트렙타비딘-피코에리트린(Caltag)를 사용하여 가시화하였다. 도 3에 나타낸 바와 같이, 단일사슬 파아지 항체 SC03-014와 SC03-022는 결합 스파이크 트란스펙션된 HEK293T 세포를 결합시킬 수 있는 반면, 모조 트란스펙션된 HEK293T 세포에 대한 결합은 관찰되지 않았다. 대조 단일 사슬 파아지 항체는 스파이크 트란스펙션된 HER293T 세포 또는 모조 트란스펙션된 HER293T 세포를 모두 인식하지 못했다. 이들 자료는 두 항체 모두가 SARS-CoV의 S 단백질을 지향한다는 것을 제안한다.
S 단백질 내에 항체의 결합 부위를 더욱 배치시키기 위해, 조사를 수행하였고, 여기서 항체는 SARS-CoV의 S 단백질의 일부에 결합하는 그들의 능력에 관하여 분석되었다. S 단백질의 뉴클레오티드와 아미노산 서열은 각각 SEQ ID NO:114와 SEQ ID NO: 115에 나타내었다. N-터미날 565 아미노산(S565로 불리는 단백질)에 대한 DNA 코딩은 pcDNA3.1/mycHis C(Invitrogen)으로 불리는 벡터(pAdapt/myc-His C로 불리는 벡터)의 폴리링커의 삽입에 의해 변형되는 pAdapt에서의 KpnI-BamHI 단편(Havenga et al., 2001)으로서 클론되었다. S 단백질의 아미노산 잔기 318-510에 대응하는 단편(S318-510으로 불리는 부분)은 올리고뉴클레오티드 프라이머: EcoRIspikeFor318 5'-cctggaattctccatggccaacatcaccaacc-3'(SEQ ID NO:116) 및 XbaIspikeRev510 5'-gaagggccctctagacacggtggcagg-3'(SEQ ID NO:117)을 사용하여 S 유전자 cDNA 상에서 증폭되었다. 생성된 단편은 EcoRI-XbasI로 소화시켰고 pHAVT20/myc His A로 클론시켜 pHAVT20/myc-His AS318-510을 수득하였다. 이 벡터에서 HAVT20 리더서열로 융합된 단편 S318-510의 발현은 인간, 전장, 즉시-초기 CMV 프로모터의 조절하에 있었다. DNA 트란스펙션을 표준기술을 사용하는 일시적 발현을 위해 HEK293T 세포에서 수행하였다. S 단백질 유래 단편은 배양 상등액으로부터 직접 사용되거나 배양 상등액으로부터 Ni-NTA(Qiagen)을 사용하여 정제되었다. S 단백질 유래 단편에 대한 항체의 결합을 평가하기 위한 ELISA를 다음과 같이 실시하였다. ELISA 플레이트의 웰을 탄산수소염 완충액 pH 9.6 50mM 중의 항-myc 항체 5μg/㎖으로 밤새도록 코팅하였다. 플레이트의 웰을 0.05% Tween을 함유하는 PBS로 3회 세척하고 1% BSA를 함유하는 PBS로 37℃에서 2시간 동안 블록하였다. 항-myc 항체로 코팅된 웰을 myc-태그된 단편 S565 또는 1% BSA를 함유하는 PBS 중에 희석된 S318-510으로 1시간 동안 실온에서 배양하였다. 웰을 0.05% Tween을 함유하는 PBS로 3회 세척하였다. 그리고 나서, 항체 CR03-014, CR03-022 또는 1% BSA를 함유하는 PBS에 희석된 대조항체를 실온에서 1시간 동안 배양하였다. 결합된 항체의 검출은 상기와 같이 수행되었다. 도 4에 나타낸 바와 같이, 항체 CR03-014와 CR03-022는 모두 S565와 S318-510 단편에 결합할 수 있었지만, 관련없는 대조 myc-태그된 항원에는 결합할 수 없었다.
S565 단편에의 결합에 대한 항체의 친화도를 평가하기 위해, (항체를 1% ELK를 함유하는 PBS에 용해시킴으로써) IgG 농도의 적정을 수행하고, 이어서 상기와 같이 ELISA를 수행하였다. 모노클로날 항체의 적정은 CR03-014와 CR03-022가 거의 유사한 친화력으로 S565에 결합한다는 것을 나타낸다(도 5 참조). 가능한 시너지 메카니즘으로서 친화력의 변화를 조사하기 위해, 재조합 수용체 결합 도메인 단편 S318-510에 순차적으로 또는 동시에 결합하는 CR03-014와 CR03-022에 대한 KD를 BIAcore 분석으로 조사하였다. 표면 플라즈몬 공명 분석법을 25℃에서 BIAcore3000TM에서 수행하였다. CM5 센서칩과 이동 완충액 HBS-EP는 Biacore AB(Uppsala Sweden)사 제품이었다. 재조합 S318-510 단편을 아민 결합공정을 사용하여 CM5 칩에 고정시켜 약 1,000 공명 단위(RU)의 반응 수준을 얻었다. 반응속도론 분석으로 모노클로날 항체들의 조합속도(ka), 해리속도(kd) 상수 및 친화도(KD)를 측정하였다. 그러므로, 0.4~250 nM IgG의 농도 시리즈를 HBS-EP 중의 2-배 희석물을 사용하여 제조하였다. 샘플을 30㎕/분의 유속으로 이중으로 주입하였다(주입 시간 = 2분, 해리 시간 = 5분). 센서 칩 표면을 5nM NaOH 5㎕의 펄스로 재생하였다. 주입된 모든 농도의 조합 및 해리 곡선을 맞추기 위해 Biacore evlauation software(BIAevalution, July 2001)를 사용하였다. CR03-014와 CR03-022의 개개의 KD는 각각 16.3nM과 0.125nM로 측정되었고, 동시에 결합하는 항체들에 대한 KD는 5.71nM, CR03-014의 CR03-022 포화된 S318-510에 대한 결합의 KD는 14.8nM로 측정되었다. 각각 CR03-014와 CR03-022에 대한 3과 20의 투여량 감소 지수와 비교하여, 모노클로날 항체들에 대한 동시 또는 순차적 결합 모두 KD의 변화를 가져오지 않았고 이것은 협조적 결합을 통한 그들의 시너지성 중화 작용을 설명한다.
S 단백질 내의 항체 결합 부위를 더욱 조사하기 위해, 고정화된 S318-510 단편에서 경쟁 ELISA를 실시하였다. 캡쳐된 S318-510을 경쟁 항체 없이, 또는 경쟁항체(항체 CR03-014, CR03-022 또는 대조 항체) 1, 5, 및 25μg/㎖의 존재하에, 비오티닐화된 항체의 비-포화량으로 배양시켰다. 결합된 비오틴화된 항체를 스트렙타비딘-컨쥬게이트된-HRP(BD Pharmingen)으로 검출하였고 상기와 같이 전개시켰다. 도 6A는 모노클로날 항체 CR03-014의 결합은 과량의 비라벨된 모노클로날 항체 대조 또는 항체 CR03-022의 존재하에 영향을 받지 않는다는 것을 나타낸다. 도 6B는 항체 CR03-022의 결합은 과량의 비라벨된 모노클로날 항체 대조 또는 항체 CR03-014의 존재에 영향을 받지 않는다는 것을 나타낸다. 예상과 같이, 비오티닐화된 CR03-014와 CR03-022의 결합은 그들의 비라벨된 대응물에 의해 효과적으로 감소된다(도 6A와 6B 참조). 이들 결과는 항체 CR03-014와 CR03-022는 S318-510 단편에 대한 결합에서 서로 경쟁하지 않고 다른/구별된, 비-경쟁 에피토프를 인식한다는 것을 설명한다.
이 결과를 확인하기 위해, 항체 샌드위치 ELISA를 수행하였다. 항체 CR03-014와 CR03-022를 pH 9.6의 탄산수소염 완충액 50mM 중 5μg/㎖으로 미세역가 웰에밤새도록 코팅하였다. S318-510 단편의 캡쳐, 비오티닐화된 항체의 결합 및 ELISA 반응의 이후의 전개를 상기와 같이 수행하였다. 도 7은 CR03-014-캡쳐된 S318-510은 비오티닐화된 CR03-022에 의해서는 결합될 수 있지만, CR03-014에 의해서는 결합되지 않는다는 것을 나타낸다. CR03-022-캡쳐된 S318-510은 오직 비오티닐화된 CR03-014에 의해서만 결합되고 CR03-022에 의해서는 결합되지 않는다. 이것은 CR03-014와 CR03-022가 S 유래된 단편 S318-510내의 다른 에페토프에 동시에 결합될 수 있다는 것을 나타내고 추가로 두 항체들이 다른 비-경쟁 에피토프에 결합된다는 것을 나타낸다.
실시예
8
모노클로날
항-SARS-
CoV
항체들의
변이체
S318
-510 단편에 대한 결합의 구성 및 평가
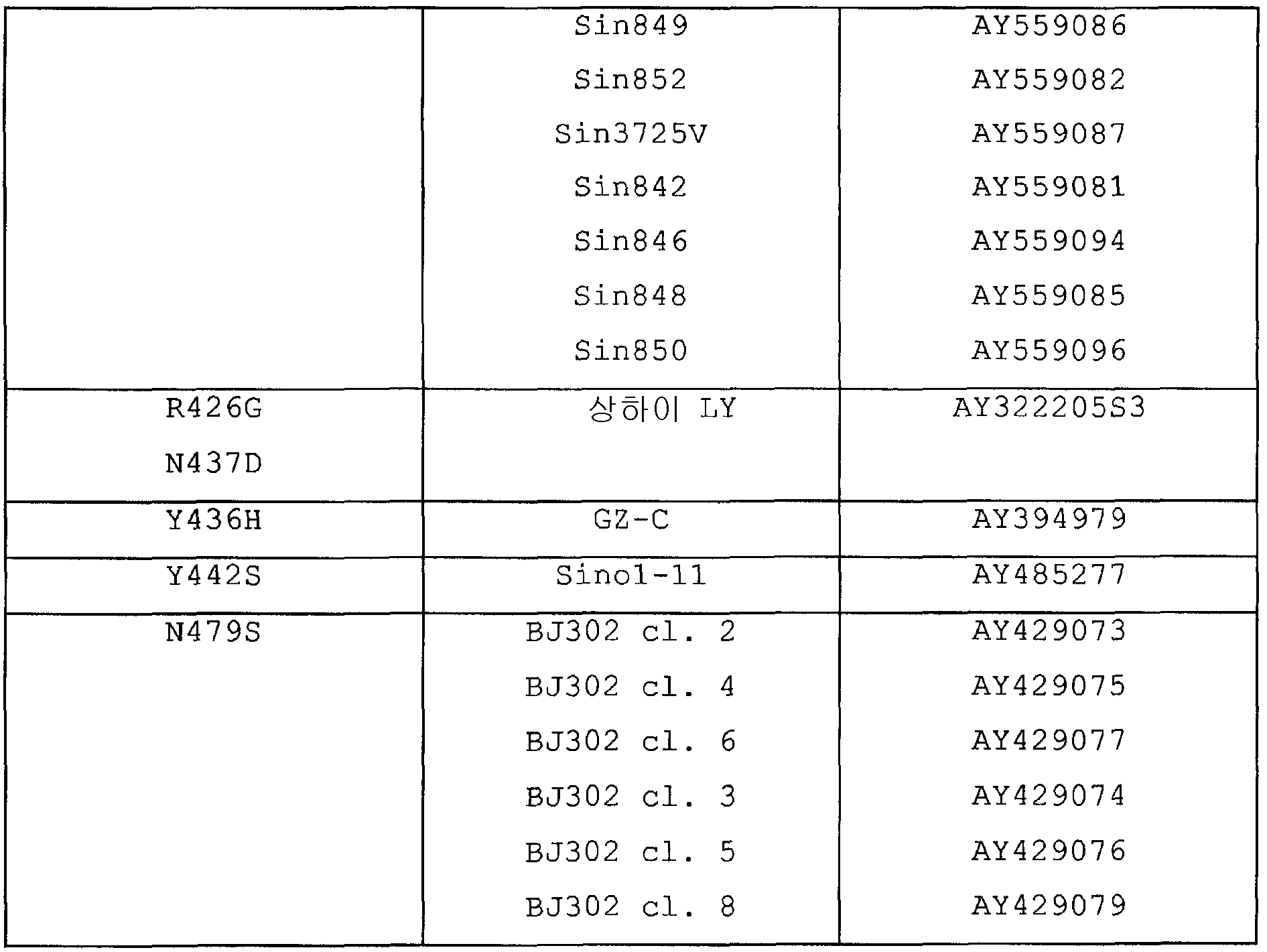
S 단백질의 영역 318-510 내의 다양성을 다음과 같이 측정하였다. 146을 넘는 게놈 또는 완전 인간 SARS-CoV 또는 그것의 단편을 암호화하는 유전자를 함유하는 리스트를 편집하였다. 114개의 경우, 전장 스파이크 (S) 단백질을 암호화하는 개방형 해독틀을 동정하였다. 스파이크 아미노산 잔기 318-510의 정렬은 30개 스파이크 단백질들을 드러내었고, 여기서 영역 310-510은 여기서 야생형으로 사용되었던 균주 Frankfurt 1의 스파이크 단백질의 영역(Genbank 수탁번호 AY291315 참조)과 동일하지 않았다. 돌연변이체, 균주 및 GeneBank 번호를 표 15에 나타내었다. CR03-014와 CR03-022가 현재 알려진 인간 SARS-CoV 단리물의 모든 S 단백질에 결합하는가를 조사하기 위해, 표 15에 나타낸 바와 같은 다양한 아미노산 치환체를 품는(harbouring) 8개 재조합 스파이크 318-510 단편(변이체 A-F와 변이체 H 및 I)를생성하였다. 이에 더하여, 4개의 동물 SARS-유사 CoV의 서열(Genbank 수탁번호 AY304486-AY304489; 또한 표 1 참조, 각각, SARS-CoV SZ3, SZ13, SZ16 및 SZ1)에 해당하는 318-510 단편(변이체 G)가 발생되었다. 너구리와 사향고양이로부터 단리된 4개의 SARS-유사 CoV는 아미노산 치환체 K344R, F360S, N479K 및 T487을 함유한다(Guan et al. 2003 참조). 마지막에, 상기 치환체들을 Stratagene's QuikChangeⅡ 부위-지향된 돌연변이생성 키트를 제조자 지침에 따라 사용하여 pHAVT20/myc-His A S318-510 벡터에 도입하였다. 다중 아미노산 치환체가 함유된 서열의 경우, 돌연변이 생성의 과정, 서열 분석 및 확인을 매 단일 치환에 대해 반복하였다. 관심있는 유전자 이외에 플라즈미드에 추가의 돌연변이체의 도입을 배제하기 위해, 돌연변이된(592 bp EcoRI-XbaI) 단편을 EcoRI-XbaI cut pHAVT20/myc-His A에서 재클로닝하였다. 생성된 플라스미드를 HEK293T 세포에 트란스펙션시키고, CR03-14와 CR03-022의 결합을 상기의 ELISA에 의해 평가하였다. 도 8에 나타낸 바와 같이, CR03-014는 야생형 단편에 대해서와 유사한 정도로 변이체 A-E 및 변이체 H와 I에 결합할 수 있었다. CR03-014의 변이체 F(N479S 치환체)에 대한 결합은 다른 단편에 대한 결합보다 상당히 낮았다. CR03-14의 변이체 G(K344R, F360S, N479K 및 T487S 치환체)에 대한 결합은 관찰되지 않았다. 항체 CR03-022는 야생형(비-돌연변이) S318-510 단편에 대해서와 유사한 정도로 모든 변이체 S318-510 단편에 결합할 수 있었다. 이것은 잔기 N479가 CR03-014의 결합에, CR03-014의 결합부위의 일부가 됨에 의해 직접적으로 또는 S 단백질 내의 CR03-014의 결합부위의 정확한 배치의 중요성 때문에 간접적으로 포함된다는 것을 나타낸다. 따라서, 항체 CR03-022는 (표 15에 기재된 바와 같은) 모든 인간 SARS-CoV 단리물의 아미노산 잔기 318-510으로 이루어진 재조합 단편에 결합할 수 있고, 이에 더하여 동물 SARS-유사 CoV에 결합할 수 있고, CR03-022는 일반적인 SARS-CoV 단리물에 대한 치료 및/또는 보호에 적당하다.
인간 SARS-CoV 단리물에 대한 치료 및/또는 보호에 특히 적절한 것은 두 항체, CR03-014와 CR03-022를 포함하는 조합물/칵테일이고, 이들 두 항체들은 인간 SARS-CoV에 특이적으로 결합할 수 있고 인간 SARS-CoV의 중화에 시너지적으로 작용하기 때문이다. 다시 말하면, CR03-014와 CR03-022의 조합물/칵테일은 시너지적인 인간 SARS-CoV 중화 활성을 포함한다. 이와 같은 조합물/칵테일의 추가의 장점은 동물 SARS-CoV 뿐 아니라 인간 SARS-CoV를 중화시킬 수 있는 그것의 능력이다.
실시예
9
SARS-
CoV
의
CR03
-014와
CR03
-022 도피 바이러스의 생성
인간 모노클로날 항체 CR03-014와 CR03-022에 의해 인식되는 에피토프를 더욱 설명하기 위해, CR03-014와 CR03-022의 도피 바이러스를 생성하였다. CR03-014의 도피 바이러스의 생성과정은 다음과 같다. CR03-022의 도피 바이러스의 생성과정은 모든 개개의 과정에서 항체 20μg/㎖ 대신 60 μg/㎖ 를 사용하는 조건에서 동일하다. SARS-CoV 균주 HKU 39849의 연속적인 희석물(0.5㎖)(희석 범위 10-1~10-8)을, 1시간 동안 37℃/5% CO2에서 FRhK-4 세포를 함유하는 웰에 첨가하기 전에, 항체 CR03-015(0.5㎖)의 일정량(TCID50/㎖의 ~3 로그 감소를 제공하는 20 μg/㎖)으로 배양하였다. 바이러스가 1시간 동안 37℃/5% CO2에서 세포에 부착되도록 하고, 그리고 나서 제거하고 세포를 매질로 2회 세척하였다. 마지막으로, 세포들을 0.5㎖ 매질 중 20μg/㎖로 선택된 항체 CR03-014의 존재하에 2일 동안 배양하였다. 그리고 나서, 잠재적인 도피 바이러스를 함유하는 CPE(cytopathic effect)를 나타내는 최고의 바이러스 희석물을 갖는 웰의 매질을 수확하고 4℃에서 추가 사용할 때까지 저장하였다. 그리고 나서, 바이러스 샘플을 1회 냉동/해동시키고 일련의 희석물들을 매질에서 제조하였다. 바이러스 희석물을 FRhK-4 세포를 함유하는 웰에 첨가시키고 20μg/㎖의 CR03-014의 존재하에 37℃/5% CO2에서 1~2시간 배양하였다. 그리고 나서 웰을 20μg/㎖의 CR03-014를 함유하는 아가로스로 덮고 37℃/5% CO2에서 3~5일 동안 배양하였다. 개개의 도피 바이러스 플라그를 파스퇴르 피펫을 사용하여 취하고, 1회 냉동/해동시키고, 그리고 나서 도피 바이러스를 FRhK-4 세포 상에서 증폭시켰다. 도피 바이러스를 분석하기 위해 다음의 실험을 수행하였다.
우선, 도피 바이러스 각각의 SARS-CoV 스파이크 단백질에서 가능한 돌연변이를 동정하기 위해, SARS-CoV 스파이크 개방형 해독틀(ORF)의 뉴클레오티드 서열을 결정하였다. 도피 바이러스들과 야생형 SARS-CoV 바이러스 각각의 바이러스성 RNA 를 단리하고 표준 RT-PCR에 의해 cDNA로 전환시켰다. 이어서, 돌연변이체를 동정하기 위해 SARS-CoV 스파이크 ORF의 뉴클레오티드 서열화를 위해 cDNA를 사용하였다. 도 9는 얻어진 5개 E014 도피 바이러스들에 대한 서열화 자료의 결과를 나타낸다. 모든 바이러스들은 위치 1385(C 내지 T)에 뉴클레오티드 돌연변이체를 함유하였고, 이것은 스파이크 단백질에서 위치 462에서 아미노산 돌연변이체 P 내지 L을 가져온다. 외관상, P462L은 에피토프 인식의 손실, 및 그 결과, CR03-014에 의한 SARS-CoV의 중화의 손실을 가져온다. 이것은 아미노산 479에 가까운, 또한 아미노산 462는 SARS-CoV의 S 단백질에 대한 CR03-014의 결합에 포함된다는 것을 나타낸다. 얻어진 5개의 E022 도피 서열에 대한 서열 데이타의 결과는 다음과 같다. 5개 중 4개의 도피 서열은 위치 2588(C 에서 T)에서 뉴클레오티드 돌연변이체를 함유하고, 이것은 스파이크 단백질의 위치 863에서 아미노산 돌연변이체 T 내지 I를 가져온다.
두번째로, E014와 E022 도피 바이러스의 각각에 대해 중화 인덱스(NI)를 측정하였다. 중화 인덱스가 <2.5 logs이면, 바이러스를 도피 돌연변이로 정의한다. NI를 측정하는 과정은 아래에 E014에 관하여 제공하였다. 과정은 모노클로날 항체 60μg/㎖ 대신 20μg/㎖을 모든 개개의 단계에서 사용하는 조건으로 E022 도피 바이러스와 동일하였다. 중화 인덱스는 바이러스 단독으로 감염된 FRhK-4 세포에서 생산된 염증성 바이러스 입자들의 수 (TCID50/㎖)([모노클로날 항체의 부재시 log TCID50/㎖ 바이러스 - 모노클로날 항체의 존재시 log TCID50/㎖ 바이러스])에서 바이러스 더하기 모노클로날 항체로 감염된 FRhK-4 세포 배양물 중에 생산된 염증성 바 이러스 입자의 수(TCID50/㎖)를 빼서 측정하였다. 2.5 log보다 작은 인덱스는 도피의 증거로 간주되었다. 그러므로, 각각의 도피 바이러스와 야생형 바이러스 SARS-CoV(100 (TCID50)를 FRhK-4 세포에 첨가하기 전에 CR03-014 20μg/㎖으로 1시간 동안 37℃/5% CO2에서 배양하였다. 바이러스를 접종원이 제거된 후 37℃/5% CO2에서 1시간 동안 세포에 부착되도록 하고 세포를 CR03-014 20μg/㎖을 함유하는 매질로 대체하기 전에 매질로 2회 세척하였다. 37℃/5% CO2에서 접종 2일 후, 매질을 수확하고 각 바이러스의 TCID50를 측정하였다. 표 16에 나타낸 바와 같이, NI를 측정하기 위해 사용된 항체의 농도는 야생형 SARS-CoV 바이러스에서 실시되었을 때 바이러스 역가의 ~3 log 감소를 가져왔다. 그러므로, 야생형 SARs-CoV는 NI 3.3에 의해 판정된 바에 따르면 CR03-014에 의해 중화되었다. 반대로, 각 도피 바이러스에 대한 NI는 <2.5였고, 따라서 도피 바이러스의 각각은 CR03-014에 의해 더 오래 중화되지 않았다. NI 3.3에 의해 판정된 바에 따르면, 야생형 SARS-CoV 바이러스는 또한 CR03-022에 의해서도 중화되었다(표 17 참조). 각 E022 도피 바이러스의 경우 NI는 >2.5였고 그러므로 도피 바이러스 각각은 여전히 CR03-022에 의해 중화된다고 결론된다. 5개의 E022 도피 바이러스 중 4개에서 아미노산 치환체는 외관상 CR03-022에 의한 SARS-CoV의 중화에 역할을 하지 않는다. 이것은 실험 코스 중에 비-특이적으로 유도될 수 있다. 이것은 SARS-CoV가 FRhK-4 세포에서 수회 계대배양될 때 위치 863(T에서 I) 돌연변이체를 발견한 Poon et al.의 발견과 일치한다(2005). CR03-022의 중화 에피토프는 도피 바이러스들의 발생에 의해 측정될 수 없다. 이것은 S 단백질에서 결합 영역의 기능적 제한에 기인할 것이다. 이 영역에서 발생하는 돌연변이는 바이러스의 안정성에 불리할 것이고 그러므로 상기 실험에서 단리될 수 없었다.
도피 변이체에 대한 항체 CR03-014의 결합의 부족을 확인하기 위해, 위치 462에서 P에서 L 치환체를 품는 재조합 S318-510 단편은 본질적으로 상기와 같이 구성된다. 생성된 플라스미드의 DNA 트란스펙션은 일시적인 발현을 위해 HEK293T 세포에서 실시되었고 단편들은 배양 상등액으로부터 직접적으로 사용되었다. ELISA는 상기와 같이 실시되었다. 즉, 단편들은 항-myc 코팅된 미세역가 웰에서 캡쳐되었다. 이어서, 항체 CR03-014와 CR03-022가 첨가되었고 항체의 결합은 항-인간 IgG HRP-컨쥬게이트를 사용하여 검출되었다. 도 10에 나타낸 바와 같이, 항체 CR03-014는 위치 462에서 P에서 L 치환체를 이동시키는 S318-510 단편에 결합할 수 없었다. 이것은 항체 CR03-022가 다른/구별되는, 비경쟁적인 S 단백질 상의 에피토프에 결합할 수 있다는 것을 더욱 나타내고 CR03-022가 CR03-104에 의한 SARS-CoV 변이체의 중화의 잠재적 결핍을 보상하는데 사용될 수 있다는 것을 제안한다.
더우기, 교차-중화 조사는 E14 도피 바이러스 상에서 수행되었다. 표 18은 CR03-022가 야생형 바이러스와 유사한 수준으로 E14 도피 바이러스를 중화시키고, 더이상 E14 도피 바이러스를 중화시키지 않는 CR03-014와 비교하여 다른 에피토프에 결합된다는 것을 더욱 나타낸다. 이것은 도 10의 ELISA 자료와 일치한다. 역 실험은 CR03-022의 도피 바이러스가 생성되지 않음으로써 실시될 수 없었다. 상기로 부터 칵테일 중의 CR03-014와 CR03-022의 조합은 중화-내성 SARS-CoV 변이체의 도피를 막고 그러므로 SARS-CoV 예방 및 치료법을 위한 이상적인 면역글로불린 제제이다.
실시예
10
인간 항-SARS-
CoV
모노클로날
항체
CR03
-014에 의한 인간
마크로파아지에서의
SARS-
CoV
감염의 잠재적 강화의 평가
면역 또는 불활성화 전 코로나바이러스에 의한 특정 질병에서 항체는 질병의 심각성을 증가시킨다고 알려진다. 고양이 염증성 복막염에서, 마크로파아지는 바이러스 복제의 주요 표적 세포이고 항-바이러스성 항체는 인 비트로 마크로파아지 배지에서 바이러스의 복제를 강화시킨다. 마크로파아지는 또한 SARS-CoV로 사망한 환자의 폐의 세포 침윤물에서 보이는 주목을 끄는 세포이다(Nicholls et al. 2003). 이것은 항체 의존 강화가 SARS-CoV 진단에 관련이 있는가의 관심을 일으킨다. 이것을 조사하기 위해, 중화 항-SARS-CoV 모노클로날 항체 CR03-014, 비-중화 항-SARS-CoV 모노클로날 항체 CR03-015, CR-JA(여기서 대조 항체로 사용되는 광견병에 대한 모노클로날 항체)로 불리는 모노클로날 항체, SARS-CoV에 노출된 개인으로부터의 회복기 혈청 및 건강한 개인의 혈청의 존재에서 마크로파지가 SARS-CoV로 감염되었을 때 ADE가 발생하는가를 시험하였다.
인간 말초혈액 단핵세포(PBMC)를 건강한 혈액 공여자의 백혈구-풍부 연층(buffy coat)으로부터 얻었다(홍콩 적십자 혈액원, 홍콩). PBMC를 Ficoll-Paque 구배 원심분리기로 분리하였다(Pharmacia Biotech, Uppsala, Sweden). 분리된 단핵 세포에 2×107 PBMC를 페트리디쉬(Greiner, Frickenhausen, Germany)에서 1시간 동안 20mM HEPES, 2mM 글루타민, 0.6μg/㎖ 페니실린, 그리고 60μg/㎖ 스트렙토마이신과 5% 열-불활성화된 자가 플라스마가 공급된 RPMI 1640 매질 중에서 부착되도록 하였다. 매질로 세척 후, 점착성 단핵세포를 피펫으로 떨어뜨리고 24-웰 플레이트에 RPMI 1640이 보충된 매질에서 웰당 2×105 세포의 밀도로 재-시드 하였다.
단핵세포 제제의 순도를 확인하기 위해, 단핵백혈구를 또한 시드하고 유리 커버슬릿에 부착되도록 하였다. 유리 커버슬릿 상의 단핵세포의 순도를 CD14 R-피코에리트린 (R-PE)-컨쥬게이트된 마우스 항-인간 모노클로날 항체(BD Biosciences, San Diego, U.S.A.)로 염색하여 확인하였다
단핵세포 배지의 매질을 2~3일 마다 교환하고 세포를 인 비트로에서 14일 동안 분화시켰다. 단핵세포의 마크로파아지로의 분화는 마크로파아지의 통상의 형태에 의해 확인하였다. 얻어진 일차 인간 단핵세포-유래 마크로파아지를 추가의 실험에 사용하였다. ADE 실험 이틀 전에, 보충된 RPMI 1640 매질을 마크로파아지 무혈청 배지(SFM)(Invitrogen, Carlsbad, CA, U.S.A)로 교환하였다.
마크로파아지에서의 바이러스 감염에 대한 항체의 서브-중화 투여량의 효과를 조사하기 위해, 모노클로날 항체 CR03-014, CR03-015 및 CR-JA, SARS-CoV에 노출된 개인의 회복기 혈청 및 건강한 개인의 혈청의 MM 매질(1% FCS와 0.6μg/㎖ 페니실린, 그리고 60μg/㎖ 스트렙토마이신을 포함하는 MEM)의 일련의 10배 희석물 300㎕를 SARS-CoV 300㎕와 혼합하였다. SARS-CoV와 혼합된 MM 매질은 바이러스 대 조로 작용하였다. 바이러스/모노클로날 항체 혼합물과 바이러스/혈청 혼합물을 1시간 동안 37℃에서 배양하였다. 그리고 나서, 혼합물 250㎕을 마크로파아지를 함유하는 웰에 이중으로 첨가하였다. 37℃에서 바이러스의 흡착 1시간 후, 바이러스 접종원을 제거하고, 감염된 세포들을 마크로파아지 SFM 배양 매질로 세척하고 그리고 0.6μg/㎖ 페니실린, 그리고 60μg/㎖ 스트렙토마이신이 보충된 마크로파아지 SFM 매질에서 배양하였다. 배양 상등액의 샘플들을 감염 후 제 0, 1, 2, 3, 5 및 7일에 수확하고 바이러스 역가 실험을 위해 -70℃에서 보관하였다. SARS-CoV를 적정하고 TCID50을 본질적으로 상기와 같이 측정하였다.
마크로파아지 내의 바이러스를 검출하고(무산된 감염으로 인해) 그리고 마크로파아지 내의 SARS-CoV RNA의 잠재적 전사를 검출하기 위해, RNA를 RNeasy Mini kit(Qiagen)을 제조자 지침에 따라 사용하여 감염 후 3, 6 및 24시간에 감염된 마크로파아지로부터 단리하였다. 올리고-dT 프라이머에 의한 역전사를 Superscript Ⅱ 역전사제(Invitrogen)을 제조자 지침에 따라 사용하여 수행하였다. 상보적 DNA를 RNA 10㎕로 발생시키고, 올리고-dT12 -18 프라이머 25ng, 디티오트레이톨 10mM 및 데옥시뉴크레오티드 트리포스페이트 0.5mM을 함유하는 반응물 20 ㎕ 중의 Superscript Ⅱ 역전사제(Invitrogen) 200U로 역전사시켰다. 반응물을 42℃에서 50분 동안 배양시키고, 열 불활성화 시켰다(72℃ 15분). 반응 혼합물을 완충액 AE(Qiagen) 180㎕을 첨가하여 10배 희석하고 -20℃에서 저장하였다.
실시간 정량적 PCR을 FastStart DNA Master SYBR Green I 형광반응(Roche)을 사용하여 실시하였다. 희석된 상보적 DNA 5㎕를 MgCl2 4mM, 포워드 프라이머 0.5mM(액틴-LF: CCCAAGGCCAACCGCGAGAAGAT (SEQ ID NO:122)) 및 리버스 프라이머 0.5mM(액틴-LR: GTCCCGGCCAGCCAGGTCCAG (SEQ ID NO: 123))을 함유하는 반응물 20㎕ 중에서 증폭시켰다. 반응물을 다음의 조건으로 LightCyclel(Roche) 중에서 수행하였다: 95℃에서 10분, 이어서 95℃에서 0초, 66℃에서 5초 그리고 72℃에서 9초의 순환 40회. 표적 서열을 함유하는 플라스미드를 양성 대조로서 사용하였다. 이들 반응물로부터의 형광 신호를 각 순환의 연장 단계의 마지막에 캡쳐하였다(87℃). 조사의 특이성을 결정하기 위해, PCR 산물을 조사 마지막에(65~95℃; 2℃/초) 녹는점 곡선 분석하였다. 센스(음성 스트랜드 검출) 또는 안티-센스(양성 스트랜드 검출)프라이머에 의한 SARS-CoV의 폴리머라제 유전자에 대한 역전사를 Superscript Ⅱ 역전사제(Invitrogen)를 제조자 지침에 따라 사용하여 달성하였다. 상보적 DNA를 RNA 5㎕로 발생시키고, 유전자 특이 프라이머 0.1μM, 디티오트레이톨 10mM, 및 데녹시뉴클레오티드 트리포스페이트 0.5mM을 함유하는 반응물 20㎕ 중에서 Superscript Ⅱ 역전사제(Invitrogen) 200U에 의해 역-전사시켰다. 반응물을 42℃에서 50분 동안 배양하고, 열-불활성화 시켰다(72℃ 15분). 반응 혼합물을 완충액 AE(Qiagen) 180㎕을 첨가하여 10배 희석하고 -20℃에서 저장하였다. 희석된 상보적 DNA 2㎕를 MgCl2 3.5mM, 포워드 프라이머 (coro3: 5'-TACACACCTCAGCGTTG-3' (SEQ ID NO: 124)) 0.25μM, 및 리버스 프라이머 (coro4: 5'-CACGAACGTGACGAAT-3' (SEQ ID NO:125)) 0.25μM을 함유하는 20㎕ 중에서 증폭시켰다. 반응물을 다음의 조건으로 LightCycler(Roche) 중에서 수행하였다: 95℃에서 10분, 이어서 95℃에서 0초, 60℃에서 5초 그리고 72℃에서 9초의 순환 50회. 표적 서열을 함유하는 플라스미드를 양성 대조로서 사용하였다. 이들 반응물로부터의 형광 신호를 각 순환의 연장 단계의 마지막에 캡쳐하였다. 조사의 특이성을 결정하기 위해, PCR 산물을 조사 마지막에(65~95℃; 0.1℃/초) 녹는점 곡선 분석하였다. 바이러스성 RNA에 대한 자료를 β-액틴 관리유전자(housekeeping gene)의 RNA 수준에 대해 표준화하였다
마크로파아지를 SARS-CoV로 감염시킨 후, 세포를 현미경으로 매일 모니터하였다. SARS-CoV로 감염되고 10일 후 검출가능한 세포병변효과는 검출되지 않았고 증식성 염증으로 전환된 마크로파아지의 불발 감염은 없었다. 마크로파아지의 감염 전에, 다양한 농도의 모노클로날 항체 CR03-014, CR03-015, CR-JA, 회복기 혈청 또는 건강한 개인의 혈청으로 SARS-CoV의 예비-배양은 이 결과를 바꾸지 않는다.
FRhK-4 세포상에서의 감염 후 제 0, 1, 2, 3, 5 및 7일에서 감염된 마크로파아지 배양물로부터 취한 상등액의 일정부분의 적정은 모노클로날 항체 및 시험된 혈청들에 의한 마크로파아지에서의 SARS-CoV 복제의 상당한 강화의 증거를 나타내지 않는다(데이타는 나타내지 않음).
이에 더하여, SARS-CoV에 의한 마크로파아지의 (증식성)염증 및 상기 마크로파아지 내의 SARS-CoV 유전자의 전사에 대한 항체의 효과는 분자 수준에서 측정되었다. 마지막에, 전체 RNA를 상기와 같이 여러 후-감염 시간 지점에서 감염된 마크로파아지로부터 추출하였다. 이어서, 전체 RNA를 실시간 RT-PCR을 사용하여 SARS-CoV 바이러스 양성 스트랜드 RNA와 바이러스성 음성 스트랜드 RNA 전사에 대해 분 석하였다. SARS-CoV RNA 수준을 β-액틴 mRNA의 수준으로 정상화시켰다. 결과는 양성 스트랜드 SARS-CoV RNA는 SARS-CoV로 배양된 모든 마크로파아지 배양물에서 검출되었음을 나타내고, 이것은 SARS-CoV에 의한 마크로파아지의 증식성 염증을 확인한다. 항-SARS-CoV 모노클로날 항체들 CR03-014 또는 CR03-015 또는 회복기 혈청의 존재에서 SARS-CoV 항체로 감염된 마크로파아지 배양물에서 관찰된 양성 스트랜드 RNA의 수준은 대조 모노클로날 항체 CR-JA 또는 건강한 개인으로부터의 혈청의 존재하에 또는 모노클로날 항체 또는 혈청의 부재하에 SARS-CoV에 의해 감염된 마크로파아지 배양물에서보다 상당히 높지 않았다.
더우기, SARS-CoV에 의한 마크로파아지의 감염 후 SARS-CoV 유전자 전사 활성에 대해 나타내는 음성 스트랜드 RNA의 존재가 관찰되었다. 또한, 음성 스트랜드 RNA의 수준과 항-SARS-CoV 항체의 존재 또는 부재 사이의 관계는 관찰되지 않았다(자료는 도시하지 않음).
이와 함께, 염증성 바이러스 수득률과 마크로파아지 내의 바이러스 관련 RNA 수준을 조사하는 실험은 항-SARS-CoV 모노클로날 항체 CR03-014와 CR03-015 및 SARS 환자로부터의 회복기 혈청에 존재하는 항-SARS-CoV 항체에 의한 인간 마크로파아지에서의 SARS-CoV 복제의 항체 의존 강화가 없다는 것을 나타낸다.
실시예
11
PEPSCAN
-ELISA에 의한 재조합 인간 항-SARS-
CoV
에 의해 인식된
에피토프의
동정
15-mer 선형 및 루프형/원형 펩티드를 SARS-CoV의 단백질로부터 합성하고 상 기와 같은 신용카트-포맷의 미니-PEPSCAN 카드(455 펩티드 포맷/카드)를 사용하여 스크린하였다(WO 84/03564, WO 93/09872, Slootstra et al. 1996). 모든 펩티드를 아미노 말단에서 아세틸화하였다. 즉, SARS-CoV Urbani(EMBL-데이타베이스에서 표면 스파이크 당단백질의 단백질-id는 AAAP13441이다) 스파이크 당백질의 일련의 오버래핑 펩티드(이들은 선형 또는 루프형/환형이다)를 생산하고 PEPSCAN 분석법에 따라 본 발명의 재조합 인간 항-SARS-CoV 항체에 대한 결합을 시험하였다.
상기 나타낸 Urbani 스파이크 단백질은 또한 다른 SARS-CoV 균주에서 동일한 또는 더 균질한 형태로 발견되므로, 분석법에서 발견된 항원성 펩티드는 SARS-CoV 균주 Urbani의 검출 및 SARS-CoV 균주 Urbani로부터 생긴 질병의 예방 및/또는 치료를 위해서 사용될 뿐 아니라, 일반적인 SARS-Cov의 검출 및 일반적인 SARS-CoV로부터 생긴 질병의 예방 및/또는 치료에도 유용하다. 예를 들면, EMBL-데이타베이스에서 SARS-CoV 균주 TOR2, Frankfurt 1 및 HSR 1의 표면 스파이크 당단백질의 단백질-id는 AAP41037, AAP33697 및 AAP72986이다. 균주 TOR2, Frankfurt 1 및 HSR 1의 완전 게놈의 EMBL-데이타베이스에서 수탁번호는 각각 AY274119, AY291315 및 AY323977이다. 이 수탁번호에서, 이들 균주의 다른 (잠재적)단백질의 아미노산 서열이 발견될 수 있다.
모든 루프형 펩티드에서 위치-2와 위치-4는 시스테인에 의해 대체되었다(아세틸-XCXXXXXXXXXXX-미니카드). 위치-2 및 위치-14에서 시스테인 이외의 다른 시스테인이 제조된 펩티드에 존재한다면, 다른 시스테인은 알라닌에 의해 대체되었다. 루프형 펩티드들을 표준 Fmoc-화학에 의해 합성하고 스캐빈저를 갖는 트리플루오르 산을 이용하여 탈보호하였다. 이어서, 탈보호된 펩티드를 카드상에서 암모늄 바이카보네이트(20 mM, pH 7.9/아세토니크릴 (1:1 (v/v)) 중의 1.3-비스(브로모메틸)벤젠 0.5mM과 반응시켰다. 카드를 용액에 완전히 담그어, 용액 중에서 30분 ~ 60분 동안 부드럽게 흔들었다. 마지막으로, 카드를 과량의 H2O로 완전히 씻고 PBS (pH 7.2) 중에서 1% SDS/0.1% 베타-메르캅토에탄올을 함유하는 분쇄된-완충액 중에서 30분 동안 고주파분해시키고, 또 다른 45분 동안 H2O 중에서 고주파분해하였다.
재조합 인간 항-SARS-CoV 항체 CR03-014 및 CR03-022를 PEPSCAN-기재 효소-링크 면역조사법(ELISA)에서 선형 및 루프형 펩티드 각각에 대한 결합에 관하여 시험하였다. 공유결합적으로 결합된 펩티드를 함유하는 455-웰 신용카드-포맷 폴리프로필렌 카드를 항체(1~10μg/㎖; 5% 말-혈청(v/v)와 5% 오브알부민(w/v)을 함유하는 블로킹 용액에 희석)로 배양하였다. 세척 후, 펩티드를 항-인간 항체 퍼옥시다제(1/1000 희석)로 배양시키고(1시간, 25℃), 이어서, 퍼옥시다제 기질을 세척 후 2,2'-아지노-디-3-에틸벤즈티아졸린 술포네이트(ABTS)과 3% H2O2 2㎕/㎖를 첨가하였다. (선형 및 루프형에 대해) 대조물을 항-인간 항체 퍼옥시다제 만으로 배양하였다. 1시간 후, 색 전개를 측정하였다. ELISA의 색 전개를 CCD-카메라와 상 처리시스템으로 정량화하였다. 장치는 CCD-카메라와 55mm 렌즈(Sony CCD Video Camera XC-77RR, Nikon micro-nikkir 55mm f/2.8 렌즈), 카메라 어뎁터(Sony Camera adaptor DC-77RR) 및 상처리 소프트웨어 패키지 옵티머스, 버전 6.5 (Media Cybernetics, Silver Spring, MD 20910, U.S.A.)로 이루어진다. 옵티머스는 펜티엄 Ⅱ 컴퓨터 시스템에서 작동한다.
재조합 인간 항-SARS-CoV 항체 CR03-014와 CR03-022를 상기와 같이 합성된 15-mer 선형 및 루프형/환형 펩티드에 대한 결합에 관하여 시험하였다. 재조합 인간 항-SARS-CoV 항체에 대한 펩티드의 적절한 결합을 다음과 같이 산출하였다. 각각의 항체에 대한 평균 OD-값은 관련 단백질에 대해 산출하였다(모든 펩티드의 OD-값의 합/총 펩티드의 수). 그리고 나서, 이 평균의 표준 편차에 2를 곱하고, 얻어진 값을 평균치에 더하여 보정인자를 얻었다. 그리고 나서 각 펩티드의 OD-값을 이 보정인자로 나누었다. 0.9보다 높은 값이 발견되면, 관련 결합은 특정 펩티드와 각 항체사이에 존재한다고 간주되었다. 특히 흥미로운 것은 여러 반응성 펩티드를 포함하는 영역으로 보이는데, 여기서 영역의 대부분의 펩티드는 항체와 반응한다.
모노클로날 항체 CR03-014는 특별히 CR03-014가 불연속적인 비-선형 에피토프를 인식한다는 것은 나타내는 SARS-CoV 스파이크 단백질 내의 펩티드 또는 여러 펩티드를 포함하는 영역과 반응하는 것으로 보이지 않는다(자료는 나타내지 않음). 그 영역들은 SARS-CoV 스파이크 단백질의 아미노산 잔기 430-449 및 484-503으로 이루어지고 각각 아미노산 서열 ATSTGNYNYKYRYLRHGKLR (SEQ ID NO: 126)과 YTTTGIGYQPYRVVVLSFEL (SEQ ID NO:127)을 갖는다. 놀랍기는, 두 영역은 통상적으로 모티프 TXTGXXXXXYR (SEQ ID NO: 128)을 갖고, 이 모티프는 항체 CR03-022가 SARS-CoV 스파이크 단백질에의 결합에 결정적이라는 것을 나타낸다.
표 1. 현재 알려진 SARS-CoV 게놈서열과 스파이크 유전자의 리스트
(표 1 계속)
(표 1 계속)
(표 1 계속)
표 2. 인간 IgG 중쇄 가변영역 프라이머(센스)
표 3. 인간 IgG 중쇄 J-영역 프라이머 (안티-센스)
표 4. SfiI/NcoI 제한 부위를 갖는 연장된 인간 IgG 중쇄 가변영역 프라이머(센스) 및 XhoI/BstEII 제한 부위를 갖는 연장된 인간 IgG 중쇄 J-영역 프라이머(안티-센스)
(표 4 계속)
표 5. 인간 람다 사슬 가변영역 프라이머(센스)
표 6. 인간 카파 사슬 가변영역 프라이머 (센스)
표 7. 인간 람다 사슬 J-영역 프라이머 (안티-센스)
표 8. 인간 람다 사슬 J-영역 프라이머 (안티-센스)
표 9. SalI 제한 부위를 갖는 연장된 인간 카파 사슬 가변영역 프라이머 (센스), NotI 제한 부위를 갖는 연장된 인간 카파 사슬 J-영역 프라이머 (안티-센스), SalI 제한 부위를 갖는 연장된 인간 람다 가변 사슬 영역 프라이머 (센스) 및 NotI 제한 부위를 갖는 연장된 인간 람다 사슬 J-영역 프라이머
(표 9 계속)
(표 9 계속)
표 10. 10개의 분획을 넘는 다양한 경쇄 산물의 분포
표 11. SARS-CoV와 결합 가능한 단일-사슬 Fvs의 자료
표 12A. SARS-CoV 중화 실험 I
표 12B. SARS-CoV 중화 실험 Ⅱ
표 12C. SARS-CoV 중화 실험 Ⅲ
-: CPE 없음, +: CPE
표 13. 인 비트로 중화시험에서 나타난 다양한 SARS-CoV 단리물 100 TCID50에 대해 완전 보호를 제공하는 모노클로날 항-SARS-CoV 항체 CR03-014의 농도
* 괄호 안에 각각의 균주의 계대배양 수를 나타냄.
1 균주 GZ43과 GZ50에 대해서는 계대배양 히스토리가 알려지지 않음
표 14. CR03-014와 CR03-022의 여러 혼합물의 SARS-CoV 중화 실험
표 15. SARS-CoV Frankfurt 1 균주의 S 단백질의 영역 318-510과 동일하지 않은 S 단백질의 영역 318-510을 갖는 SARS-CoV 균주의 리스트.
(표 15 계속)
Frankfurt 1 S 단백질과 비교한 아미노산 치환을 좌측 칼럼에 표시하였다. 균주와 GenBank 기탁 번호는 제2 및 제3 칼럼에 표시하였다.
표 16. E014도피 바이러스의 중화 인덱스
표 17. 추정의 E022 도피바이러스의 중화 인덱스
표 18. CR03-014의 두 대표적인 도피 바이러스에 대한 CR03-022 중화 역가
a 각 바이러스에 대한 CR03-022의 50% 중화역가를 μg/㎖로 나타내었다.
b 각 바이러스에 대한 CR03-022의 100% 중화역가를 μg/㎖로 나타내었다.
참조문헌