KR100909786B1 - Novel cationic lipids modified with oligopeptides, preparation methods thereof, and carriers comprising the same - Google Patents
Novel cationic lipids modified with oligopeptides, preparation methods thereof, and carriers comprising the same Download PDFInfo
- Publication number
- KR100909786B1 KR100909786B1 KR1020080111275A KR20080111275A KR100909786B1 KR 100909786 B1 KR100909786 B1 KR 100909786B1 KR 1020080111275 A KR1020080111275 A KR 1020080111275A KR 20080111275 A KR20080111275 A KR 20080111275A KR 100909786 B1 KR100909786 B1 KR 100909786B1
- Authority
- KR
- South Korea
- Prior art keywords
- cationic
- acid
- nucleic acid
- carrier
- oligonucleic acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C237/00—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups
- C07C237/02—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atoms of the carboxamide groups bound to acyclic carbon atoms of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C237/00—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups
- C07C237/02—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atoms of the carboxamide groups bound to acyclic carbon atoms of the carbon skeleton
- C07C237/04—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atoms of the carboxamide groups bound to acyclic carbon atoms of the carbon skeleton the carbon skeleton being acyclic and saturated
- C07C237/12—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atoms of the carboxamide groups bound to acyclic carbon atoms of the carbon skeleton the carbon skeleton being acyclic and saturated having the nitrogen atom of at least one of the carboxamide groups bound to an acyclic carbon atom of a hydrocarbon radical substituted by carboxyl groups
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82B—NANOSTRUCTURES FORMED BY MANIPULATION OF INDIVIDUAL ATOMS, MOLECULES, OR LIMITED COLLECTIONS OF ATOMS OR MOLECULES AS DISCRETE UNITS; MANUFACTURE OR TREATMENT THEREOF
- B82B1/00—Nanostructures formed by manipulation of individual atoms or molecules, or limited collections of atoms or molecules as discrete units
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Nanotechnology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Saccharide Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
본 발명은 올리고 펩티드를 수식한 신규한 양이온성 지질, 그의 제조 방법 및 그를 포함하는 핵산 전달체를 제공한다. 본 발명의 양이온성 지질은 핵산 전달체의 제조를 위해 사용된다. 본 발명의 양이온성 지질은 제조 및 정제 공정이 간편하여 대량 생산시의 경제성이 높다. 또한, 본 발명의 양이온성 지질을 포함한 핵산 전달체는 세포 내로 전달하고자 하는 리보핵산, 작은 간섭 리보핵산, 안티센스 올리고핵산, 핵산 앱타머(aptamer) 등의 올리고 핵산 의약을 세포 내로 수송하는 효율을 현저히 증강시킬 뿐만 아니라, 세포 독성을 감소시켜 핵산 의약의 치료 효능을 증강시키는 용도로 유용하게 사용된다.The present invention provides novel cationic lipids modified with oligopeptides, methods for their preparation and nucleic acid carriers comprising the same. Cationic lipids of the present invention are used for the preparation of nucleic acid carriers. The cationic lipids of the present invention have high economical efficiency in mass production due to the simple manufacturing and purification process. In addition, the nucleic acid carrier including the cationic lipid of the present invention significantly enhances the efficiency of transporting oligonucleotide medicines such as ribonucleic acid, small interfering ribonucleic acid, antisense oligonucleic acid, nucleic acid aptamer, etc. to be delivered into the cell. In addition to reducing the cytotoxicity, it is useful for the purpose of enhancing the therapeutic efficacy of nucleic acid medicine.
Description
본 발명은 올리고 펩티드를 수식한 신규한 양이온성 지질, 그의 제조 방법 및 그를 포함하는 전달체에 관한 것이다The present invention relates to novel cationic lipids modified with oligopeptides, methods for their preparation, and carriers comprising the same.
1960년대 중반에 불완전한 유전자 서열을 가지는 유전성 질환자들의 세포 내로 정상적인 유전자 서열을 삽입해서 유전성 질병을 처치하는데 사용할 수 있는 기술이 제안된 이후로 유전자 처치에 의한 다양한 유전적 장애를 치료하려는 시도들이 있어 왔다. 또한 최근에는 플라스미드 데옥시리보핵산 (plasmid DNA), 작은 간섭 이중나선 리보핵산(siRNA), 마이크로 리보핵산(micro RNA), 안티센스 올리고 핵산(antisense oligonucleotide) 등 각종 핵산 물질의 의약적 용도가 규명됨에 따라서 이들 핵산 물질들을 세포 내로 효율적으로 전달하는 핵산 전달 물질의 중요성도 증대되고 있다. In the mid-1960s, attempts have been made to treat various genetic disorders caused by gene therapy since a technique has been proposed that can be used to treat hereditary diseases by inserting normal gene sequences into cells of hereditary patients with incomplete gene sequences. Recently, as medicinal uses of various nucleic acid materials such as plasmid deoxyribonucleic acid (small DNA), small interfering double-stranded ribonucleic acid (siRNA), microribonucleic acid (micro RNA), antisense oligonucleotide, etc. have been identified, The importance of nucleic acid delivery materials for efficiently delivering these nucleic acid materials into cells has also increased.
각종 세포내로 유전자를 전달하기 위하여 다양한 기술 및 운반체, 특히 벡터들이 제안되어 왔으나, 핵산의 전달 또는 발현을 위해 사용되는 기술은 크게 바이 러스성 벡터와 비바이러스성 벡터를 이용한 방법으로 구분할 수 있다. 특히, 상기 비바이러스성 벡터 중 양이온성 리포좀 또는 양이온성 고분자들은 구조적인 특징에 의한 양하전으로 유전자의 음이온성 하전과 결합하여 복합체를 형성하는 특징이 있어 유전자 전달체로서 연구되어 왔다.Various techniques and carriers, particularly vectors, have been proposed to transfer genes into various cells, but techniques used for delivery or expression of nucleic acids can be largely divided into methods using viral and non-viral vectors. In particular, cationic liposomes or cationic polymers in the non-viral vector have been studied as gene carriers because they have a characteristic of forming a complex by binding to the anionic charge of a gene by positive charges due to structural features.
이러한 합성 물질을 이용한 유전자 전달 방법은 렌티바이러스나 아데노 바이러스 등을 사용한 바이러스성 유전자 수송체에 비하여 제조방법이 간편하고, 전달하려는 유전자의 크기가 제한을 받지 않으며, 바이러스 캡시드 단백질에 의한 반복투여시의 면역부작용이 적고, 바이러스 자체가 소유하는 유전자에 의한 체내 안전성 문제가 제기되지 않으며, 제조비용이나 시간에 있어서도 상업적으로 유리한 장점이 있다.Gene delivery methods using such synthetic materials are simpler to manufacture than viral gene transporters using lentiviruses or adenoviruses, and are not limited in size to the genes to be delivered, and are repeatedly administered by viral capsid proteins. There is little immune side effect, no safety problems caused by the genes owned by the virus itself, and there is a commercially advantageous advantage in terms of manufacturing cost or time.
양이온성 물질을 이용한 유전자 전달방법 중 양이온성 고분자 수송체의 경우 DEAE 덱스트란(dextran), 라이신 아미노산이 반복되는 구조의 폴리라이신, 에틸렌이민이 반복되는 구조의 폴리에틸렌이민, 폴리아미도아민(polyamidoamine) (미국특허 제6,020,457호) 등이 유전자의 수송체로 연구되어 왔다. 그러나 이들 양이온성 고분자를 이용한 수송체 경우에는 세포 표면의 수용체를 통하여 효과적으로 수송되는 바이러스성 수송체에 비하여 체내 세포 내로의 수송 효율이 낮다는 문제점이 지적되어 왔다. 한편 양이온성 인지질 수송체의 경우 인지질 조성에 양하전의 지질을 일정 비율로 혼합하여 양이온성 리포좀 (cationic liposome)과 같은 나노 크기의 입자를 제조하고 이 입자를 유전자와 혼합하여 양하전 인지질 입자와 유전자의 복합체를 세포주들에 처리하여 유전자의 발현을 증강시키는 방법이 사용되어 왔다(미 국특허 제5,858,784호).Cationic polymer transporter in the gene transfer method using a cationic material, DEAE dextran, polylysine of repeating lysine amino acid, polyethyleneimine of repeating ethyleneimine, polyamidoamine (polyamidoamine) ( US Patent No. 6,020,457) has been studied as a transporter of genes. However, it has been pointed out that in the case of transporters using these cationic polymers, transport efficiency into cells in the body is lower than that in viral transporters that are effectively transported through receptors on the cell surface. On the other hand, in the case of cationic phospholipid transporters, nanocharged particles such as cationic liposomes are prepared by mixing positively charged lipids in a phospholipid composition and mixing these particles with genes to complex positively charged phospholipid particles with genes. Has been used to enhance the expression of genes by treating the cell lines (US Pat. No. 5,858,784).
종래에 개발된 양이온성 지질들은 중성의 지방산 사슬에 1차 아민 (primary amine), 2차 아민(secondary amine), 3차 아민(tertiary amine), 또는 4급 암모늄염(quarternary ammonium salt) 등의 아민 보유 화합물을 결합시켜 양이온성을 부여하는 방법을 사용하였다. 초기 단계의 핵산 전달용 양이온성 지질로서는 1987년 Felgner 박사 연구진이 합성한 양이온성 4급 아미노 지질인 N-[1-(2,3-디올레일옥시)프로필]-N,N,N-트리에틸암모늄 클로라이드 (N-[1-(2,3-dioleyloxy) propyl]-N,N,Ntriethylammonium chloride; DOTMA)가 있다. DOTMA는 세포막 융합 활성을 가진 것으로 알려진 디올레오일 포스파티딜 에탄올아민(dioleoylphosphatidylethanolamine; DOPE)과 양이온성 리포좀을 형성하여 유전자 전달에 이용되고 있다. DOTMA의 소수성기는 이중결합을 갖는 탄소수 18개의 지방족 화합물 그룹 (aliphatic group)이며, 스페이서 아암(spacer arm)과 에테르 결합(ether linker bond)을 통하여 화학적으로 연결된 소수성기의 반대쪽에 4차 암모늄염이 결합되어 있다. DOTMA의 경우 유전자 전달효율은 비교적 높지만 세포 독성을 지니고 있으며, 여러 공정의 합성과정을 거쳐야 한다는 단점을 가지고 있다.Conventionally developed cationic lipids have amines such as primary amine, secondary amine, tertiary amine, or quarternary ammonium salt in neutral fatty acid chains. The method of combining compounds to impart cationicity was used. Early cationic lipids for nucleic acid delivery include N- [1- (2,3-dioleyloxy) propyl] -N, N, N-triethyl, a cationic quaternary amino lipid synthesized by Dr. Felgner's team in 1987. Ammonium chloride (N- [1- (2,3-dioleyloxy) propyl] -N, N, Ntriethylammonium chloride; DOTMA). DOTMA is used for gene delivery by forming cationic liposomes with dioleoylphosphatidylethanolamine (DOPE), which is known to have cell membrane fusion activity. The hydrophobic group of DOTMA is an aliphatic group of 18 carbon atoms having a double bond, and a quaternary ammonium salt is bonded to the opposite side of the hydrophobic group chemically linked through a spacer arm and an ether linker bond. . In the case of DOTMA, gene transfer efficiency is relatively high, but it is cytotoxic and has the disadvantage of having to go through the synthesis process of various processes.
DOTMA의 높은 독성을 해결하고 세포 내 핵산 전달 효율을 보다 높이기 위해 DOTMA의 다른 형태의 유도체인 1,2-디미리스틸옥시프로필-3-디메틸하이드록시에틸 암모늄 브로마이드(1,2-dimyristyloxypropyl-3- dimethylhydroxyethyl ammonium bromide; DM RIE), N-[1-(2,3-디올레일옥시)프로필]-N,N,N-트리메틸암모늄 메틸 설페이트(N-[1-(2,3- dioleyloxy)propyl]-N,N,N- trimethylammonium methyl sulfate; DOTAP), 2,3-디올레일옥시-N-[2-(스퍼마인카복시아미드)에틸]-N,N-디메틸-1-프로판 암모늄 트리플루오로아세테이트 (2,3-dioleyloxy-N-[2- sperminecarboxyamide)ethyl]-N,N-dimethyl-1-propane ammonium trifluoroacetate; DOSPA) 등이 개발되었다.In order to solve the high toxicity of DOTMA and increase the efficiency of intracellular nucleic acid delivery, 1,2-dimyristyloxypropyl-3-dimethylhydroxyethyl ammonium bromide (1,2-dimyristyloxypropyl-3-), another form of DOTMA derivative dimethylhydroxyethyl ammonium bromide; DM RIE), N- [1- (2,3-dioleyloxy) propyl] -N, N, N-trimethylammonium methyl sulfate (N- [1- (2,3-dioleyloxy) propyl] -N, N, N-trimethylammonium methyl sulfate; DOTAP), 2,3-dioleyloxy-N- [2- (sperminecarboxyamide) ethyl] -N, N-dimethyl-1-propane ammonium trifluoro Acetate (2,3-dioleyloxy-N- [2-sperminecarboxyamide) ethyl] -N, N-dimethyl-1-propane ammonium trifluoroacetate; DOSPA).
또한, 콜레스테롤(cholesterol) 유도체인 3β-[N-(N',N'-디메틸아미노에탄)카바모일]콜레스테롤(3β-[N-(N',N'-dimethylaminoethane)carbamoyl] cholesterol; DC-Chol), 디메틸-디옥타데실 암모늄 브로마이드(dimethyl- dioctadecyl ammonium bromide; DDAB), N-(α-트리메틸암모니오아세틸)-디도데실-D-글루타메이트 클로라이드(N-(α-trimethylammonioacetyl)- didodecyl-D-glutamate chloride; TMAC), 디옥타데실 아미도글리실스퍼민(dioctadecylamidoglycylspermine; DOGS) 등이 합성되어 데옥시리보핵산 등의 핵산 물질 전달을 목적으로 이용되고 있다. 이들 양이온성 지질들은 4차 아민, 3차 아민, 또는 하이드록시 에틸화 4차 아민 등이 지질의 헤드 부분에 연결되어 한 개의 양전하를 제공하는 종류 (DC-Chol, DDAB, TMAC 등)와 스퍼민(spermine) 등의 다중 아민(polyamine) 물질이 연결되어 여러 개의 양전하를 제공하는 종류 (DOGS) 로 구분될 수도 있다.In addition, 3β- [N- (N ', N'-dimethylaminoethane) carbamoyl] cholesterol (cholesterol derivative) (3β- [N- (N', N'-dimethylaminoethane) carbamoyl] cholesterol; DC-Chol ), Dimethyl-dioctadecyl ammonium bromide (DDAB), N- (α-trimethylammonioacetyl) -didodecyl-D-glutamate chloride (N- (α-trimethylammonioacetyl)-didodecyl-D- Glutamate chloride (TMAC) and dioctadecyl amidoglysylspermine (DOGS) have been synthesized and used for the delivery of nucleic acid substances such as deoxyribonucleic acid. These cationic lipids are categorized by quaternary amines, tertiary amines, or hydroxyethylated quaternary amines (such as DC-Chol, DDAB, TMAC, etc.) and spermine (such as DC-Chol, DDAB, TMAC, etc.) connected to the head portion of the lipid. Polyamines, such as spermine, can be classified into different types (DOGS), which provide several positive charges.
핵산 전달에 사용되는 양이온성 지질의 또 다른 예는 4급 암모늄염(quarternary ammonium salt)인 계면활성제(detergent)이다. 이들은 단일사슬, 예를 들어, 세트리 메틸 암모늄 브로마이드(cetrimethylammonium bromide) 또는 이중사슬, 예를 들어, 디메틸 디옥타데실 암모늄 브로마이드(dimethyldioctadecyl ammonium bromide) 등의 계면 활성제이고, 모두 동물세포에 핵산 전달이 가능하다. 이들 4급 암모늄염 양이온성 지질의 경우 양친매성(amphiphile)에 속하는 아민기(amine group)는 4차이고, 스페이서 아암(spacer arm)이나 연결 결합(linker bond) 없이 지질의 단일사슬이 1차 아민기에 붙어있다. 그러나 이들 양친매성 계면활성제를 이용한 제형들 또한 일반적으로 세포 독성이 심각한 문제점을 가지고 있다. 또 다른 양친매성 물질들로는 DOTMA와 구조가 유사한 1,2-디올레오일-3-(4'-트리메틸암모니오)부타노일-글리세롤(1,2-dioleoyl-3-(4'-trimethylammonio)butanoyl- sn-glycerol), 콜레스테릴(4'-트리메틸암모니오)부타노에이트 (cholesteryl (4'-trimethylammonino)butanoate), 1,2-디올레오일-3-숙시닐-글리세롤 콜린 에스테르(1,2-dioleoyl-3-succinylsn-glycerol choline ester) 등이 있는데, 이들 양친매성 물질들은 세포내 핵산 전달효율(delivery efficiency)이 일반적으로 낮다.Another example of a cationic lipid used for nucleic acid delivery is a surfactant, which is a quarternary ammonium salt. These are surfactants such as single chains such as cetrimethylammonium bromide or double chains such as dimethyldioctadecyl ammonium bromide, all of which are capable of delivering nucleic acids to animal cells. Do. For these quaternary ammonium salt cationic lipids, the amine groups belonging to the amphiphile are quaternary, with a single chain of lipids attached to the primary amine groups without spacer arms or linker bonds. have. However, formulations using these amphipathic surfactants also generally have serious problems with cytotoxicity. Other amphiphiles include 1,2-dioleoyl-3- (4'-trimethylammonio) butanoyl-glycerol similar in structure to DOTMA (1,2-dioleoyl-3- (4'-trimethylammonio) butanoyl- sn-glycerol), cholesteryl (4'-trimethylammonino) butanoate, 1,2-dioleoyl-3-succinyl-glycerol choline ester (1,2 -dioleoyl-3-succinylsn-glycerol choline esters. These amphiphiles generally have low intracellular nucleic acid delivery efficiency.
비바이러스성 벡터 중 양이온성 지질은 렌티바이러스나 아데노 바이러스 등의 바이러스성 핵산 수송체에 비하여 제조방법이 간편하고, 바이러스 캡시드 단백질에 의한 반복투여시의 면역부작용이 적고, 바이러스 자체가 소유하는 유전자에 의한 체내 안전성 문제가 제기되지 않으며, 제조비용 또는 제조 공정에 있어서도 산업적으로 유리한 장점이 있다. 그러나, 종래에 개시된 여러 핵산 전달용 양이온성 지질들은 합성 방법, 세포 독성 및 세포내 핵산 전달 효율 면에서 아직 보완되어야 할 점이 많다. 그러므로 합성 공정이 짧고, 세포 독성이 작으면서도 세포 내로 효율적으로 핵산 물질들을 전달하는 기술의 개발이 요구된다.Cationic lipids in non-viral vectors are simpler to manufacture than viral nucleic acid transporters such as lentiviruses and adenoviruses, have less immune side effects upon repeated doses by viral capsid proteins, and the genes owned by the virus itself. It does not pose a safety problem due to the body, there is an industrially advantageous advantage in the manufacturing cost or manufacturing process. However, many of the previously disclosed cationic lipids for nucleic acid delivery still need to be complemented in terms of synthetic methods, cytotoxicity and intracellular nucleic acid delivery efficiency. Therefore, there is a need for the development of a technology that delivers nucleic acid materials efficiently into cells while having a short synthetic process and low cytotoxicity.
이에 본 발명자들은 핵산 등의 세포 내 전달 효율을 증가시키기 위하여 양전 하를 가지는 올리고 펩티드를 이용하여 신규한 양이온성 지질을 합성하였으며 이 양이온성 지질을 포함한 핵산 전달체의 경우 사람의 암 세포주에서 핵산의 전달 효율을 현저히 증가시킬 뿐만 아니라 세포 독성도 현저하게 감소시키는 것을 확인함으로써, 본 발명을 완성하였다.Therefore, the present inventors synthesized a new cationic lipid using an oligopeptide having a positive charge to increase the intracellular delivery efficiency of nucleic acid and the like. In the case of a nucleic acid carrier including the cationic lipid, the delivery of nucleic acid in human cancer cell lines The present invention was completed by confirming that not only significantly increased the efficiency but also significantly reduced the cytotoxicity.
본 발명의 목적은 올리고 펩티드를 수식한 신규한 양이온성 지질, 그의 제조 방법 및 그를 포함하는 전달체를 제공하는 것이다. 본 발명의 양이온성 지질은 다양한 형태의 핵산 전달체로 제제화되어 세포 내로 목적하는 물질의 전달을 증강시키는데 사용될 수 있다.It is an object of the present invention to provide novel cationic lipids modified with oligopeptides, methods for their preparation and transporters comprising the same. Cationic lipids of the present invention can be formulated into various forms of nucleic acid carriers and used to enhance delivery of the desired material into cells.
본 발명은 하기 일반식 (I)의 양이온성 지질을 제공한다.The present invention provides cationic lipids of the general formula (I).
상기 식에서, n은 3내지 6의 정수이고, Wherein n is an integer of 3 to 6,
R은 탄소수 12 내지 20인 포화 또는 불포화 탄화수소 라디칼로, 바람직하게는 올레일(oleyl), 미리스틸(myristyl), 팔미틸(palmityl), 스테아릴(stearyl), 라우릴(lauryl), 리놀레일(linoleyl), 및 아라키딜(arachidyl)로 구성된 군으로부터 선택된다. R is a saturated or unsaturated hydrocarbon radical having 12 to 20 carbon atoms, preferably oleyl, myristyl, palmityl, stearyl, lauryl, linoleyl ( linoleyl), and arachidyl.
상기 일반식 (I)으로 표시되는 본 발명의 양이온성 지질은 양이온성을 띠는 아미노산 그룹, 바람직하게는 올리고라이신 그룹과, 소수성인 탄소수 12 내지 20의 포화 또는 불포화 지방산 아민 유도체가 결합되어 이루어진다. 본 발명의 양이온성 지질은 친수성인 아미노산 그룹과 소수성인 지방산 부위로 구성된 양친매성 화합물로서 아미노산의 카르복실 그룹(-COOH) 과 지방산 아민 유도체의 아민그룹(-NH2)간의 아미드(amide) 결합으로 이루어진다. 본 발명의 양이온성 지질을 구성하는 아미노산 그룹으로는 양하전을 가지는 아미노산 중 라이신(Lysine, K)이 3개 내지 6개로 이루어진 올리고라이신이 바람직하다.The cationic lipid of the present invention represented by general formula (I) is formed by combining a cationic amino acid group, preferably an oligolysine group, with a saturated or unsaturated fatty acid amine derivative having 12 to 20 carbon atoms. The cationic lipid of the present invention is an amphiphilic compound composed of a hydrophilic amino acid group and a hydrophobic fatty acid moiety, and is an amide bond between a carboxyl group (-COOH) of an amino acid and an amine group (-NH 2 ) of a fatty acid amine derivative. Is done. As the amino acid group constituting the cationic lipid of the present invention, oligolysine having 3 to 6 lysine (Lysine, K) among amino acids having a positive charge is preferable.
본 발명은 또한 하기 화학식 (II)로 표시되는 올리고라이신의 카르복실 그룹(-COOH)과 The present invention also relates to a carboxyl group (-COOH) of oligolysine represented by the following general formula (II)
하기 화학식 (III)으로 표시되는 지방산 아민 유도체의 아민 그룹(-NH2)을 The amine group (-NH2) of the fatty acid amine derivative represented by the following general formula (III)
H2N-R (III)H 2 NR (III)
아마이드 결합(amide bond)으로 연결하는 단계를 포함하는 화학식(I)의 양이온성 지질의 제조방법을 제공하는 데, 상기 식에서 m은 1 내지 4의 정수, R은 탄소수 12 내지 20인 포화 또는 불포화 탄화수소 라디칼이다.It provides a method for producing a cationic lipid of formula (I) comprising the step of connecting by an amide bond, wherein m is an integer of 1 to 4, R is a saturated or unsaturated hydrocarbon having 12 to 20 carbon atoms It is a radical.
상기 화학식 (III)으로 표시되는 지방산 아민 유도체는 올레일아민(oleylamine), 미리스틸아민(myristylamine), 팔미틸아민(palmitylamine), 스테아릴아민(stearylamine), 라우릴아민(laurylamine), 리놀레일아민(linoleylamine), 및 아라키딜아민(arachidylamine)으로 구성된 군으로부터 선택될 수 있다. The fatty acid amine derivative represented by the formula (III) is oleylamine, oleylamine, myristylamine, palmitylamine, stearylamine, laurylamine, linoleylamine linoleylamine, and arachidylamine.
본 발명은 또한 상기 방법에 의해 제조된 양이온성 지질을 제공한다. The present invention also provides cationic lipids prepared by the above method.
본 발명의 양이온성 지질은 생체 단백질의 구성성분인 아미노산을 사용하여 간단한 공정으로 높은 수율의 합성이 가능하다. 본 발명의 양이온성 지질의 경우, 정상적인 생체내 환경의 중성영역 pH에서 올리고 라이신의 아민기가 양하전의 형태로 존재하게 되므로 상기 일반식 (I)의 양이온성 지질은 전체적으로 세포내에서 양전하의 하전상태를 보유하게 된다. 상기 양이온성 지질의 양이온 하전은 중성영역 pH에서 음전하를 띠고 있는 각종 핵산 물질과 복합체를 형성하는 것을 가능하게 하고 또한 생체내에서 상대적으로 음전하를 보유하고 있는 표적 세포막과의 접촉을 증가시키는데 도움을 준다. Cationic lipids of the present invention can be synthesized in high yield by a simple process using amino acids that are components of biological proteins. In the case of the cationic lipid of the present invention, since the amine group of the oligo lysine is present in the form of a positive charge in the neutral region pH of a normal in vivo environment, the cationic lipid of the general formula (I) generally has a positively charged state in the cell. Will have. The cationic charge of the cationic lipids makes it possible to form complexes with various nucleic acid materials that are negatively charged at neutral pH and also increase contact with target cell membranes having relatively negative charges in vivo. .
따라서 본 발명은 또한 상기 화학식 (I)의 양이온성 지질을 포함하는 세포내로의 핵산 전달체(nucleic acid delivery system), 바람직하게는 올리고핵산 전달체(oligonucleic acid delivery system)를 제공한다. 본 발명에 있어서, 핵산 전달체는, 음전하를 띤 핵산 서열과의 상호작용에 의해 통상적으로 핵산과 결합하여 세포 내로 유입될 수 있는 복합체를 형성할 수 있는 핵산 운반 매개체를 말한다.The present invention therefore also provides a nucleic acid delivery system, preferably an oligonucleic acid delivery system, into a cell comprising said cationic lipid of formula (I). In the present invention, a nucleic acid carrier refers to a nucleic acid carrier medium capable of forming a complex that can normally enter a cell by binding to the nucleic acid by interaction with a negatively charged nucleic acid sequence.
본 발명에 있어서, 핵산은 리보핵산(RNA), 작은 간섭 리보핵산(small interfering RNA), 안티센스 올리고핵산(antisense oligonucleotide), 핵산 앱타 머(aptamer) 등을 포함한다.In the present invention, nucleic acids include ribonucleic acid (RNA), small interfering RNA (small interfering RNA), antisense oligonucleotide, nucleic acid aptamer and the like.
본 발명의 양이온성 지질은 세포내로의 핵산 전달을 위해 리포좀, 미셀, 에멀젼, 나노입자 등 다양한 형태의 핵산 전달체 제형(delivery formulation)으로 사용될 수 있다.Cationic lipids of the present invention can be used in various forms of nucleic acid delivery formulations such as liposomes, micelles, emulsions, nanoparticles, etc. for nucleic acid delivery into cells.
본 발명의 구체 예에서, 본 발명의 양이온성 지질을 포함하는 핵산 전달체는 리보핵산(RNA), 작은 간섭 리보핵산(small interfering RNA), 안티센스 올리고핵산(antisense oligonucleotide), 핵산 앱타머(aptamer) 등을 포함하는 올리고 핵산의 세포 내로의 운반을 매개한다.In embodiments of the invention, nucleic acid carriers comprising cationic lipids of the invention are ribonucleic acid (RNA), small interfering RNA, antisense oligonucleotides, nucleic acid aptamers, and the like. Mediates delivery of oligonucleotides comprising cells into cells.
또한 상기 핵산 전달체는 본 발명의 양이온성 지질 성분 외에도 갈락토오스 지질 유도체, 만노오스 지질 유도체, 엽산 지질 유도체, 폴리틸렌 글리콜 지질 유도체, 바이오틴 지질 유도체로 이루어진 군으로부터 선택된 1종 이상의 것을 추가로 포함할 수 있다.In addition to the cationic lipid component of the present invention, the nucleic acid carrier may further include one or more selected from the group consisting of galactose lipid derivatives, mannose lipid derivatives, folate lipid derivatives, polystyrene glycol lipid derivatives, and biotin lipid derivatives.
본 발명의 한 구체 예에서, 상기 핵산 전달체는 상기 양이온성 지질 및 세포 융합성 인지질을 함유하는 리포좀 제형으로 이루어진 것일 수 있다. 상기 세포 융합성 인지질은 예를 들어 디올레오일 포스파티딜에탄올 아민(dioleoylphosphatidylethanolamine; DOPE), 또는 1,2-디피타노일-sn-글리세로-3-포스포에탄올아민 (1,2-diphytanoyl-sn-glycero-3-phospho ethanolamine) 등을 포함한다.In one embodiment of the invention, the nucleic acid carrier may be made of a liposome formulation containing the cationic lipids and cell fusion phospholipids. Such cell fusion phospholipids can be, for example, dioleoylphosphatidylethanolamine (DOPE), or 1,2-diphytanoyl-sn-glycero-3-phosphoethanolamine (1,2-diphytanoyl-sn- glycero-3-phospho ethanolamine).
본 발명의 다른 구체 예에서, 상기 핵산 전달체는 상기 양이온성 지질에 계면활성제를 추가적으로 함유하는 미셀 제형으로 이루어진 것일 수 있다. 상기 미셀 제형에서 사용될 수 있는 계면활성제는 예를 들어 트윈 20 (Tween 20), 폴리에틸렌글리콜 모노올레일 에테르(polyethylene glycol monooleyl ether), 에틸렌글리콜 모노도데실 에테르 (ethylene glycol monododecyl ether), 디에틸렌글리콜 모노헥실 에테르 (diethylene glycol monohexyl ether), 트리메틸헥사데실 암모늄 클로라이드 (trimethylhexadecyl ammonium chloride), 도데실트리메틸 암모늄 클로라이드 (dodecyltrimethyl ammonium bromide), 사이클로헥실 베타 말토사이드 (cyclohexylmethyl β-D-maltoside), 펜타에리스리틸 팔미테이트 (pentaerythrityl palmitate), 라우릴에메틸아민옥사이드 (lauryldimethylamine-oxide), 또는 라우로살코신 소듐염(N-lauroylsarcosine sodium salt) 등을 포함한다.In another embodiment of the present invention, the nucleic acid carrier may be composed of a micelle formulation additionally containing a surfactant in the cationic lipid. Surfactants that can be used in the micelle formulation are, for example,
본 발명의 다른 구체 예에서, 상기 핵산 전달체는 상기 양이온성 지질에 계면활성제를 추가적으로 함유하는 에멀젼 제형으로 이루어진 것일 수 있다. 에멀젼 제형에서 사용할 수 있는 계면활성제는 양이온성(cationic), 양쪽성(zwitterionic), 비이온성(nonionic) 등으로 분류된다. 양이온성 계면활성제로는 예를 들어 세틸 브롬화 트리메틸암모늄염(cetyl trimethylammonium bromide), 헥사데실 브롬화 암모늄염(hexadecyl trimethyl ammonium bromide) 등을 사용할 수 있으며, 양쪽성 계면활성제로는 예를 들어 도데실 베타인(dodecyl betaine), 도데실 디메틸아민 산화물(dodecyl dimethylamine oxide), 디메틸팔미토일암모니오프로판 설포네이트(3-(N,N-dimethylpalmitylammonio)propane sulfonate) 등을 사용할 수 있으며, 비이온성 계면활성제로는 예를 들어 트윈-20 (Tween 20), 트윈-80(Tween 80), 트리톤 X-100 (Triton-X-100), 폴리에틸렌글리콜 모노올레일 에테 르(polyethylene glycol monooleyl ether), 트리에틸렌 글리콜 모노도데실 에테르 (triethylene glycol monododecyl ether), 옥틸 글루코사이드(octyl glucoside), 노나노일메틸글루카민 (N-nonanoyl-N-methyl glucamine)등을 사용할 수 있다.In another embodiment of the present invention, the nucleic acid carrier may be composed of an emulsion formulation additionally containing a surfactant in the cationic lipid. Surfactants that can be used in emulsion formulations are classified into cationic, zwitterionic, nonionic, and the like. As the cationic surfactant, for example, cetyl trimethylammonium bromide, hexadecyl trimethyl ammonium bromide, etc. may be used, and as amphoteric surfactant, for example, dodecyl betaine betaine), dodecyl dimethylamine oxide, dimethylpalmitoylammonoprovane sulfonate (3- (N, N-dimethylpalmitylammonio) propane sulfonate) and the like can be used.
본 발명에 의한 양이온성 리포좀, 미셀, 에멀젼, 나노입자 등의 제형으로 이루어진 핵산 전달체는 동물 세포 내에 목적하는 핵산의 수송 효율을 현저히 증강시킬 수 있으며 세포에 대한 독성 역시 감소시킨다.Nucleic acid carriers consisting of formulations of cationic liposomes, micelles, emulsions, nanoparticles and the like according to the invention can significantly enhance the transport efficiency of the desired nucleic acid in animal cells and also reduce the toxicity to the cells.
본 발명의 양이온성 지질을 함유한 핵산 전달체는 전달하고자 하는 핵산의 사용 목적에 따라 어떤 동물 세포로도 핵산 전달이 가능하다. 하기 실시예에서는 그 대표적인 예로 상기 핵산 전달체의 종양세포(사람의 자궁경부암 상피 세포인 HeLa 세포주, 폐암 세포인 A549 세포주, 간암 세포주인 Huh-7, 흑색종인 WM266.4, A375 세포주, 신경교종인 U87 세포주)로의 핵산 전달 효율을 평가하였다.Nucleic acid carriers containing cationic lipids of the present invention can be delivered to any animal cell, depending on the intended use of the nucleic acid to be delivered. In the following examples, the tumor cells of the nucleic acid carrier (HeLa cell line, which is a human cervical cancer epithelial cell, A549 cell line, which is a lung cancer cell, Huh-7, a hepatic cancer cell line, WM266.4, a melanoma, and a U87 cell line, which are glioma) Nucleic acid delivery efficiency).
형광 표식이 붙어있는 Block IT (Invitrogen, USA) 이중 나선 리보핵산을 사용하여 양이온성 지질을 함유하는 다양한 제형과 복합체를 형성시켜 세포 내에 전달하고 이를 형광 현미경으로 관찰하면 상기 양이온성 지질의 세포 내로 전달되는 핵산 수송 능력을 구체적으로 측정할 수 있다. 또한 본 발명의 핵산 전달체의 세포 독성은 tetrazolium 3-(4,5-dimethylthiazol -2-yl)-2,5-diphenyltetrazolium bromide을 이용한 발색 방법(MTT)을 사용하여 평가할 수 있다.Block IT (Invitrogen, USA) double-stranded ribonucleic acid with fluorescent labeling forms complexes with various formulations containing cationic lipids and delivers them into cells, and when observed under a fluorescence microscope, delivers the cationic lipids into cells. Specifically, the nucleic acid transport ability can be measured. In addition, the cytotoxicity of the nucleic acid carrier of the present invention can be evaluated using the color development method (MTT) using tetrazolium 3- (4,5-dimethylthiazol-2-yl) -2,5-diphenyltetrazolium bromide.
본 발명에서 기술된 양이온성 지질을 포함하는 리포좀, 미셀, 에멀젼, 나노입자 등의 핵산 전달체는 다양한 세포들에서 핵산의 세포내 수송도를 증가시킬 뿐만 아니라 세포 독성도 현저하게 감소시키는 바, 리보핵산, 작은 간섭 리보핵산, 안티센스 올리고핵산, 핵산 앱타머 (aptamer) 등의 올리고 핵산 의약을 이용한 치료요법 등에 효과적으로 사용 가능하다.Nucleic acid carriers such as liposomes, micelles, emulsions, nanoparticles, and the like comprising the cationic lipids described in the present invention not only increase the intracellular transport of nucleic acids in various cells but also significantly reduce cytotoxicity. In addition, the present invention can be effectively used for treatment with oligonucleotide medicines such as small interfering ribonucleic acid, antisense oligonucleotide, and nucleic acid aptamer.
또한 본 발명은 상기 핵산 전달체와 핵산의 복합체를, 바람직하게는 올리고핵산 전달체와 올리고 핵산의 복합체를 제공한다. 리포좀, 미셀, 에멀젼 등의 제형을 갖는 본 발명의 핵산 전달체는 양이온성 지질로 인해 양하전을 띠게 되므로, 핵산 전달체의 양하전과 핵산의 음이온성 하전에 의해 단순한 혼합(mix)에 의해 정전기 결합을 통해 핵산 전달체와 핵산 간의 복합체를 효율적으로 형성할 수 있다.The present invention also provides a complex of the nucleic acid carrier and the nucleic acid, preferably a complex of the oligonucleotide carrier and the oligo nucleic acid. Nucleic acid carriers of the present invention having a formulation of liposomes, micelles, emulsions, etc. are positively charged due to cationic lipids, and thus, nucleic acid through electrostatic bonding by a simple mix by positive charge of nucleic acid carriers and anionic charge of nucleic acid. Complexes between the carrier and the nucleic acid can be efficiently formed.
상기 핵산 전달체와 핵산의 복합체는 종양, 관절염, 심혈관계, 내분비계 질환 등을 포함하는 병인성 단백질의 과다발현으로 야기되는 각종 질환들의 치료를 위해 세포 내로 도입될 수 있다. 본 발명의 핵산 전달체는 핵산전달 효율이 우수할 뿐만 아니라 세포 독성이 낮으므로 병인성 단백질의 세포내 과다 발현을 억제하여 우수한 질환 치료 효과를 거둘 수 있다.The complex of nucleic acid carrier and nucleic acid may be introduced into cells for the treatment of various diseases caused by overexpression of pathogenic proteins including tumors, arthritis, cardiovascular, endocrine diseases and the like. The nucleic acid carrier of the present invention is excellent in nucleic acid delivery efficiency and low in cytotoxicity, thereby inhibiting overexpression of pathogenic proteins in cells, thereby achieving an excellent disease treatment effect.
따라서 본 발명은 또한 상기 핵산 전달체와 핵산의 복합체를 유효성분으로 포함하는 핵산 의약 치료제, 핵산 의약 치료제의 제조를 위한 상기 핵산 전달체와 핵산의 복합체의 용도 및 치료상 유효량의 상기 핵산 전달체와 핵산의 복합체를 대상체의 세포 내로 도입하는 것을 포함하는 종양, 관절염, 심혈관계, 내분비계 질환 등을 포함하는 병인성 단백질의 과다발현으로 야기되는 각종 질환들의 치료 방법을 제공한다.Accordingly, the present invention also provides a nucleic acid medicament therapeutic agent comprising the complex of the nucleic acid carrier and the nucleic acid as an active ingredient, the use of the nucleic acid carrier and the complex of the nucleic acid for the manufacture of a nucleic acid medicament therapeutic agent and a therapeutically effective amount of the complex of the nucleic acid carrier and the nucleic acid. It provides a method for the treatment of various diseases caused by overexpression of pathogenic proteins, including tumors, arthritis, cardiovascular, endocrine diseases, and the like, comprising introducing into a cell of a subject.
본 발명의 핵산 의약 치료제를 통해 in vivo 또는 ex vivo 상에서 세포 내부로 목적하는 핵산을 도입하게 되면 표적 단백질의 발현을 선택적으로 감소시키거나 표적 유전자에 생긴 변이를 수정하는 역할을 하여 병인성 단백질의 과다 발현으로 발생되는 질환이나 표적 유전자로 인해 발생한 질환 등을 치료할 수 있게 된다. 본 발명에 있어서, 상기 핵산 전달체와 핵산의 복합체의 치료상 유효량은 질환 치료 효과를 기대하기 위하여 투여에 요구되는 양을 의미한다. 따라서, 질환의 종류, 질환의 중증도, 투여되는 핵산의 종류, 제형의 종류, 환자의 연령, 체중, 일반 건강 상태, 성별 및 식이, 투여 시간, 투여 경로 및 치료 기간, 동시 사용되는 화학 항암제 등의 약물을 비롯한 다양한 인자에 따라 조절될 수 있다. 성인에게 상기 핵산 의약 치료제를 예컨대 1일 1회투여시 0.001 mg/kg ~ 100 ㎎/kg의 용량으로 투여하는 것이 바람직하다.The introduction of a desired nucleic acid into a cell in vivo or ex vivo through the nucleic acid medicament treatment of the present invention serves to selectively reduce the expression of the target protein or to correct for mutations in the target gene. It is possible to treat diseases caused by expression or diseases caused by target genes. In the present invention, the therapeutically effective amount of the complex of the nucleic acid carrier and the nucleic acid means an amount required for administration in order to expect a therapeutic effect of the disease. Therefore, the type of disease, the severity of the disease, the type of nucleic acid to be administered, the type of formulation, the age, weight, general health, sex and diet of the patient, the time of administration, the route of administration and the duration of treatment, the chemotherapy drug used simultaneously, etc. It can be adjusted according to various factors including a drug. It is preferable to administer the nucleic acid medicament therapeutic agent to an adult at a dose of 0.001 mg / kg to 100 mg / kg once daily.
또한 본 발명의 양이온성 지질은 체외에서 핵산 앱타머를 이용한 진단 키트의 구성 성분으로서도 이용가능하다. 예를 들면 진단용 플레이트의 표면을 양이온성 지질로 코팅하고 이 코팅 면 위에 앱타머를 결합시킬 경우 시료 중 앱타머와 선택적으로 반응하는 물질의 존재를 진단하는데 이용 가능하다. 따라서 본 발명은 본 발명의 양이온성 지질로 코팅된 플레이트를 포함하는 진단 키트를 제공한다. 상기 진단 키트의 양이온성 지질 코팅 면에는 앱타머가 결합되어 있을 수 있다.The cationic lipids of the present invention can also be used as components of diagnostic kits using nucleic acid aptamers in vitro. For example, coating the surface of a diagnostic plate with cationic lipids and binding aptamers on these coating surfaces can be used to diagnose the presence of substances that selectively react with aptamers in a sample. The present invention therefore provides a diagnostic kit comprising a plate coated with the cationic lipid of the present invention. An aptamer may be bound to the cationic lipid coating side of the diagnostic kit.
상술한 바와 같이, 본 발명의 양이온성 지질은 제조 및 정제 공정이 간편하여 대량 생산시의 경제성이 높다. 또한, 본 발명의 양이온성 지질을 포함하는 핵산 전달체는 목적하는 리보핵산, 작은 간섭 리보핵산, 안티센스 올리고핵산, 핵산 앱 타머 (aptamer) 등의 올리고 핵산 의약을 세포 내로 수송하는 효율을 현저히 증강시킬 뿐만 아니라, 세포 독성을 감소시켜 핵산 또는 단백질 소재 의약의 치료 효능을 증강시키는 용도로 유용하게 사용된다.As described above, the cationic lipid of the present invention is easy to manufacture and purify, and thus economical in mass production. In addition, the nucleic acid carrier comprising the cationic lipid of the present invention not only significantly enhances the efficiency of transporting oligonucleotide medicines such as desired ribonucleic acid, small interfering ribonucleic acid, antisense oligonucleic acid, nucleic acid aptamer, etc. into cells. In addition, it is useful for the purpose of reducing the cytotoxicity to enhance the therapeutic efficacy of the drug based nucleic acid or protein.
본 발명의 이점 및 특징, 그리고 그것들을 달성하는 방법은 상세하게 후술되어 있는 실시예들을 참조하면 명확해질 것이다. 그러나 본 발명은 이하에서 개시되는 실시예들에 한정되는 것이 아니라 서로 다른 다양한 형태로 구현될 것이며, 단지 본 실시예들은 본 발명의 개시가 완전하도록 하고, 본 발명이 속하는 기술 분야에서 통상의 지식을 가진 자에게 발명의 범주를 완전하게 알려주기 위해 제공되는 것이며, 본 발명은 청구항의 범주에 의해 정의될 뿐이다.Advantages and features of the present invention and methods for achieving them will be apparent with reference to the embodiments described below in detail. However, the present invention is not limited to the embodiments disclosed below, but will be implemented in various forms, and only the embodiments are intended to complete the disclosure of the present invention, and the general knowledge in the technical field to which the present invention pertains. It is provided to fully convey the scope of the invention to those skilled in the art, and the present invention is defined only by the scope of the claims.
<신규 양이온성 지질의 합성>Synthesis of New Cationic Lipids
실시예 1. 올레일 트리라이신아미드 (oleyl trilysinamide)의 합성 Example 1 Synthesis of Oleyl Trilysinamide
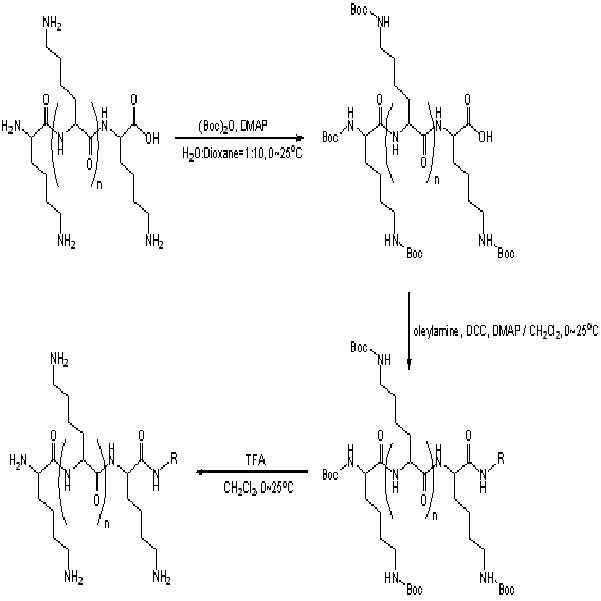
1-1). 트리라이신(1g, 2.48mmole, PEPTRON, Inc., Korea)을 H2O:p-Dioxane(Sigma-Aldrich, USA)=1:10의 비율로 얼음물 중탕하에서 녹인 후 DMAP(4-(Dimethylamino)pyridine)(0.91g, 7.45mmole, FLUKA, USA), (Boc)2O(Di-tert-butyl pyrocarbonate)(1.62g, 7.45mmole, FLUKA, USA)를 첨가한 후 12시간정도 교반한다. 반응 후 얻어진 생성물을 감압 농축하여 에틸아세테이트(ethylacetate, Sigma- Aldrich, USA)에 녹여 과포화 중탄산나트륨용액, 과포화 염화나트륨용액으로 각각 3회씩 세척하여 미반응 물질을 제거시키고, 여분의 수분을 무수황화마그네슘(Sigma-Aldrich, USA)으로 제거한 후 건조하여 흰색 고체생성물을 얻었다. 반응 여부는 박막층 크로마토그래피법 (TLC, thin layer chromatograpy, Merck & Co., Inc. USA)로 확인하였다. 1-1). Trilysine (1g, 2.48mmole, PEPTRON, Inc., Korea) was dissolved in ice water in a ratio of H 2 O: p -Dioxane (Sigma-Aldrich, USA) = 1: 10, followed by DMAP (4- (Dimethylamino) pyridine ) (0.91g, 7.45mmole, FLUKA, USA), (Boc) 2 O (Di-tert-butyl pyrocarbonate) (1.62g, 7.45mmole, FLUKA, USA) is added and stirred for 12 hours. The product obtained after the reaction was concentrated under reduced pressure, dissolved in ethyl acetate (ethylacetate, Sigma-Aldrich, USA), washed three times each with a supersaturated sodium bicarbonate solution and a supersaturated sodium chloride solution to remove unreacted substances. Sigma-Aldrich, USA) and dried to obtain a white solid product. The reaction was confirmed by thin layer chromatography (TLC, thin layer chromatograpy, Merck & Co., Inc. USA).
1-2). 실시예 1-1에서 얻어진 반응 생성물을 디클로로메탄에 녹인 후, DCC(N,N′-Dicyclohexylcarbodiimide, FLUKA, USA), DMAP(4-(Dimethylamino) pyridine)를 각각 3당량씩 얼음물 중탕에서 1시간 정도 교반한다. 올레일아민(oleylamine, FLUKA, USA) 1.5당량을 무수디클로로메탄(Dichloromethane, Sigma-Aldrich, USA)에 녹여 천천히 적하한 후 상온에서 12시간 반응시킨다. 반응 후 디클로로메탄을 감압 농축하여 제거시킨 후, 얻어진 생성물을 에틸아세테이트(ethylacetate)에 녹여 과포화 중탄산나트륨용액, 과포화 염화나트륨용액으로 각각 3회씩 세척하여 미반응 물질을 제거시키고, 여분의 수분을 무수황화마그네슘으로 제거한 후 건조하여 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.1-2). The reaction product obtained in Example 1-1 was dissolved in dichloromethane, and then 3 equivalents of DCC (N, N′-Dicyclohexylcarbodiimide, FLUKA, USA) and DMAP (4- (Dimethylamino) pyridine), respectively, were used in an ice water bath for about 1 hour. Stir. 1.5 equivalents of oleylamine (oleukamine, FLUKA, USA) are dissolved in anhydrous dichloromethane (Sigma-Aldrich, USA), slowly added dropwise and reacted at room temperature for 12 hours. After the reaction, dichloromethane was concentrated under reduced pressure to remove the obtained product, and the obtained product was dissolved in ethylacetate, and washed three times with supersaturated sodium bicarbonate solution and supersaturated sodium chloride solution to remove unreacted substances. After removal, the mixture was dried to obtain a colorless liquid product. The reaction was confirmed by TLC.
1-3). 실시예 1-2에서 얻어진 반응 생성물을 얼음물 중탕하에서 트라이플루오르아세트산(TFA, Trifluoreacetic acid, Sigma-Aldrich, USA):디클로로메탄=1:1을 천천히 적하한 후 약1시간 정도 교반한다. 반응 후 에틸아세테이트(ethylacetate)로 TFA를 제거한 후 건조하여 약간 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.1-3). Trifluoroacetic acid (TFA, Trifluoreacetic acid, Sigma-Aldrich, USA): dichloromethane = 1: 1 was slowly added dropwise to the reaction product obtained in Example 1-2 under ice water, followed by stirring for about 1 hour. After the reaction, the TFA was removed with ethylacetate, and dried to obtain a slightly yellow liquid product. The reaction was confirmed by TLC.
[반응식1][Scheme 1]
상기 반응식 1의 R은 탄소수 18의 불포화 탄화수소 라디칼로 올레일이다.R in
실시예 2. 팔미틸 테트라라이신아미드 (palmityl tetralysinamide)의 합성Example 2 Synthesis of palmityl tetralysinamide
2-1) 테트라라이신(1g, 1.88mmole, PEPTRON, Inc., Korea)과 (Boc)2O(3.08g, 14.13mmole) 실시예 1-1과 동일한 방법으로 반응시켜 라이신 유도체 생성물을 얻었다.2-1) Tetralysine (1 g, 1.88 mmol, PEPTRON, Inc., Korea) and (Boc) 2 O (3.08 g, 14.13 mmol) were reacted in the same manner as in Example 1-1 to obtain a lysine derivative product.
2-2) 실시예 2-1에서 얻어진 반응 생성물을 무수디클로로메탄에 녹인 후, 팔미틸아민(palmitylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.2-2) The reaction product obtained in Example 2-1 was dissolved in anhydrous dichloromethane, and then reacted in the same manner as in Example 1-2 using 1.5 equivalents of palmitylamine to obtain a colorless liquid product. . The reaction was confirmed by TLC.
2-3) 실시예 2-2에서 얻어진 반응 생성물을 실시예 1-3과 동일한 방법으로 반응후, 약간 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.2-3) After the reaction product obtained in Example 2-2 was reacted in the same manner as in Example 1-3, a slightly yellow liquid product was obtained. The reaction was confirmed by TLC.
[반응식 2]
상기 반응식 2의 R은 탄소수 16의 포화 탄화수소 라디칼로 팔미틸이다.R in
실시예 3. 리놀레일 펜타라이신아미드(linoleyl pentalysinamide)Example 3 linoleyl pentalysinamide
3-1) 펜타라이신(1g, 1.5mmole, Sigma-Aldrich, USA)과 (Boc)2O(2.98g, 13.66mmole) 실시예 1-1과 동일한 방법으로 반응시켜 라이신 유도체 생성물을 얻었다.3-1) Pentalysine (1 g, 1.5 mmol, Sigma-Aldrich, USA) and (Boc) 2 O (2.98 g, 13.66 mmol) were reacted in the same manner as in Example 1-1 to obtain a lysine derivative product.
3-2) 실시예 3-1에서 얻어진 반응 생성물을 무수디클로로메탄에 녹인 후, 리놀레일아민(linoleylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.3-2) The reaction product obtained in Example 3-1 was dissolved in anhydrous dichloromethane, and then reacted in the same manner as in Example 1-2 using 1.5 equivalents of linoleylamine, whereby a colorless liquid product was obtained. . The reaction was confirmed by TLC.
3-3) 실시예 3-2에서 얻어진 반응 생성물을 실시예 1-3과 동일한 방법으로 반응후, 약간 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.3-3) After the reaction product obtained in Example 3-2 was reacted in the same manner as in Example 1-3, a slightly yellow liquid product was obtained. The reaction was confirmed by TLC.
[반응식 3]
상기 반응식 3의 R은 탄소수 18의 이중 불포화 탄화수소 라디칼로 리놀레일이다.R in
실시예 4. 라우릴 헥사라이신아미드(lauryl hexalysinamide)Example 4. Lauryl hexalysinamide
4-1) 헥사라이신(1g, 1.27mmole, PEPTRON, Inc., Korea)과 (Boc)2O(2.77g, 12.7mmole) 실시예 1-1과 동일한 방법으로 반응시켜 라이신 유도체 생성물을 얻었다.4-1) Reaction with hexalysine (1 g, 1.27 mmol, PEPTRON, Inc., Korea) and (Boc) 2 O (2.77 g, 12.7 mmol) in the same manner as in Example 1-1 to obtain a lysine derivative product.
4-2) 실시예 4-1에서 얻어진 반응 생성물을 무수디클로로메탄에 녹인 후, 라우릴아민(laurylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.4-2) The reaction product obtained in Example 4-1 was dissolved in anhydrous dichloromethane, and then reacted in the same manner as in Example 1-2 using 1.5 equivalents of laurylamine, to thereby give a colorless liquid product. . The reaction was confirmed by TLC.
4-3) 실시예 4-2에서 얻어진 반응 생성물을 실시예 1-3과 동일한 방법으로 반응후, 약간 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다. 4-3) After reacting the reaction product obtained in Example 4-2 in the same manner as in Example 1-3, a slightly yellow liquid product was obtained. The reaction was confirmed by TLC.
[반응식 4]
상기 반응식 4의 R은 탄소수 12의 포화탄화수소 라디칼로 라우릴이다.R in
비교예 1. 라우릴 라이신아미드(lauryl lysinamide)Comparative Example 1. Lauryl lysinamide
1-1) 라이신(1g, 6.84mmole, Sigma-Aldrich, USA)과 (Boc)2O(4.48g, 20.5mmole) 실시예 1-1과 동일한 방법으로 반응시켜 라이신 유도체 생성물을 얻었다.1-1) Lysine (1 g, 6.84 mmol, Sigma-Aldrich, USA) and (Boc) 2 O (4.48 g, 20.5 mmol) were reacted in the same manner as in Example 1-1 to obtain a lysine derivative product.
1-2) 비교예 1-1에서 얻어진 반응 생성물을 무수디클로로메탄에 녹인 후, 라우릴아민(laurylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.1-2) The reaction product obtained in Comparative Example 1-1 was dissolved in anhydrous dichloromethane, and then reacted in the same manner as in Example 1-2 using 1.5 equivalents of laurylamine, to thereby give a colorless liquid product. . The reaction was confirmed by TLC.
1-3) 비교예 1-2에서 얻어진 반응 생성물을 실시예 1-3과 동일한 방법으로 반응후, 약간 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.1-3) The reaction product obtained in Comparative Example 1-2 was reacted in the same manner as in Example 1-3, to give a slightly yellow liquid product. The reaction was confirmed by TLC.
비교예 2. 올레일 노나라이신아미드(oleyl nonalysinamide)Comparative Example 2. Oleyl Nonalysinamide
2-1) 노나라이신(1g, 0.85mmole, PEPTRON, Inc., Korea)과 (Boc)2O(2.79g, 12.8mmole) 실시예 1-1과 동일한 방법으로 반응시켜 라이신 유도체 생성물을 얻었다.2-1) Nonlysine (1 g, 0.85 mmol, PEPTRON, Inc., Korea) and (Boc) 2 O (2.79 g, 12.8 mmol) were reacted in the same manner as in Example 1-1 to obtain a lysine derivative product.
2-2) 비교예 2-1에서 얻어진 반응 생성물을 무수디클로로메탄에 녹인 후, 올레일아민(oleylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.2-2) The reaction product obtained in Comparative Example 2-1 was dissolved in anhydrous dichloromethane, and then reacted in the same manner as in Example 1-2 using 1.5 equivalents of oleylamine to obtain a colorless liquid product. . The reaction was confirmed by TLC.
2-3) 비교예 2-2에서 얻어진 반응 생성물을 실시예 1-3과 동일한 방법으로 반응후, 약간 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.2-3) After reacting the reaction product obtained in Comparative Example 2-2 in the same manner as in Example 1-3, a slightly yellow liquid product was obtained. The reaction was confirmed by TLC.
비교예 3. 스테아릴 데카라이신아미드(stearyl decalysinamide)Comparative Example 3 stearyl decalysinamide
3-1) 데카라이신(1g, 0.77mmole, PEPTRON, Inc., Korea)과 (Boc)2O(3.56g, 15.3mmole) 실시예 1-1과 동일한 방법으로 반응시켜 라이신 유도체 생성물을 얻었다.3-1) Decalysin (1 g, 0.77 mmol, PEPTRON, Inc., Korea) and (Boc) 2 O (3.56 g, 15.3 mmol) were reacted in the same manner as in Example 1-1 to obtain a lysine derivative product.
3-2) 비교예 3-1에서 얻어진 반응 생성물을 디클로로메탄에 녹인 후, 스테아릴아민(stearylamine, Sigma-Aldrich, USA) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.3-2) The reaction product obtained in Comparative Example 3-1 was dissolved in dichloromethane, and then reacted in the same manner as in Example 1-2 using 1.5 equivalents of stearylamine (stearylamine, Sigma-Aldrich, USA), and then colorless. The liquid product of was obtained. The reaction was confirmed by TLC.
3-3) 비교예 3-2에서 얻어진 반응 생성물을 실시예 1-3과 동일한 방법으로 반응후, 약간 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.3-3) After reacting the reaction product obtained in Comparative Example 3-2 in the same manner as in Example 1-3, a slightly yellow liquid product was obtained. The reaction was confirmed by TLC.
비교예 4. 리놀레일 아르기닌아미드(linoleyl argininamide)Comparative Example 4. linoleyl argininamide
4-1) Boc-Arg(Pbf)-OH(1g, 1.89mmole, PEPTRON, Inc., Korea)를 무수디클로로메탄에 녹인 후, 리놀레일아민(linoleylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.4-1) After dissolving Boc-Arg (Pbf) -OH (1 g, 1.89 mmol, PEPTRON, Inc., Korea) in anhydrous dichloromethane, Example 1-2 and 1.5 equivalents of linoleylamine were used. After the reaction in the same manner, a colorless liquid product was obtained. The reaction was confirmed by TLC.
4-2) 비교예 4-1에서 얻어진 반응 생성물에 TFA:H2O:TIS(triisopropyl silane, Sigma-Aldrich, USA)=90:5:5를 첨가 후, 2시간 동안 교반한다. 반응 후, 건조시켜 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.4-2) After adding TFA: H 2 O: TIS (triisopropyl silane, Sigma-Aldrich, USA) = 90: 5: 5 to the reaction product obtained in Comparative Example 4-1, the mixture was stirred for 2 hours. After the reaction, it was dried to give a yellow liquid product. The reaction was confirmed by TLC.
[반응식 5]Scheme 5
상기 반응식 5의 R은 탄소수 18의 이중 불포화 탄화수소 라디칼로 리놀레일이다.R in Scheme 5 is linoleyl as a C18 double unsaturated hydrocarbon radical.
비교예 5. 미리스틸 펜타아르기닌아미드(myristyl pentaargininamide)Comparative Example 5. myristyl pentaargininamide
5-1) 비교예 4-1과 같은 보호기가 있는 펜타아르기닌(1g, 0.46mmole, PEPTRON, Inc., Korea)을 무수디클로로메탄에 녹인 후, 미리스틸아민(myristylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무 색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.5-1) A penta arginine (1 g, 0.46 mmol, PEPTRON, Inc., Korea) having the same protecting group as in Comparative Example 4-1 was dissolved in anhydrous dichloromethane, followed by using 1.5 equivalents of myristylamine. After the reaction in the same manner as in 1-2, a colorless liquid product was obtained. The reaction was confirmed by TLC.
5-2) 비교예 5-1에서 얻어진 반응 생성물에 TFA:H2O:TIS(triisopropyl silane)=90:5:5를 첨가 후, 2시간 동안 교반한다. 반응 후, 건조시켜 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.5-2) TFA: H 2 O: TIS (triisopropyl silane) = 90: 5: 5 was added to the reaction product obtained in Comparative Example 5-1, followed by stirring for 2 hours. After the reaction, it was dried to give a yellow liquid product. The reaction was confirmed by TLC.
비교예 6. 스테아릴 옥타아르기닌아미드(stearyl octaargininamide)Comparative Example 6. stearyl octaargininamide
6-1) 비교예 4-1과 같은 보호기가 있는 옥타아르기닌(1g, 0.29mmole, PEPTRON, Inc., Korea)을 무수디클로로메탄에 녹인 후, 스테아릴아민(stearylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.6-1) Example 1-1, dissolving octaarginine (1 g, 0.29 mmol, PEPTRON, Inc., Korea) having the same protecting group in anhydrous dichloromethane, and then using 1.5 equivalents of stearylamine. After the reaction in the same manner as in 1-2, a colorless liquid product was obtained. The reaction was confirmed by TLC.
6-2) 비교예 6-1에서 얻어진 반응 생성물에 TFA:H2O:TIS(triisopropyl silane)=90:5:5를 첨가 후, 2시간 동안 교반한다. 반응 후, 건조시켜 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.6-2) TFA: H 2 O: TIS (triisopropyl silane) = 90: 5: 5 was added to the reaction product obtained in Comparative Example 6-1, followed by stirring for 2 hours. After the reaction, it was dried to give a yellow liquid product. The reaction was confirmed by TLC.
비교예 7. 아라키딜 노나아르기닌아미드(arachidyl nonaargininamide)Comparative Example 7. arachidyl nonaargininamide
7-1) 비교예 4-1과 같은 보호기가 있는 노나아르기닌(1g, 0.26mmole, PEPTRON, Inc., Korea)을 무수디클로로메탄에 녹인 후, 아라키딜아민(arachidylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.7-1) Non-arginine (1 g, 0.26 mmol, PEPTRON, Inc., Korea) having the same protective group as Comparative Example 4-1 was dissolved in anhydrous dichloromethane, followed by using 1.5 equivalents of arachidylamine. After the reaction in the same manner as in 1-2, a colorless liquid product was obtained. The reaction was confirmed by TLC.
7-2) 비교예 7-1에서 얻어진 반응 생성물에 TFA:H2O:TIS(triisopropyl silane)=90:5:5를 첨가 후, 2시간 동안 교반한다. 반응 후, 건조시켜 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.7-2) TFA: H 2 O: TIS (triisopropyl silane) = 90: 5: 5 was added to the reaction product obtained in Comparative Example 7-1, followed by stirring for 2 hours. After the reaction, it was dried to give a yellow liquid product. The reaction was confirmed by TLC.
비교예 8. 올레일 데카아르기닌아미드(oleyl dacaargininamide)Comparative Example 8. oleyl dacaargininamide
8-1) 비교예 4-1과 같은 보호기가 있는 데카아르기닌(1g, 0.24mmole, PEPTRON, Inc., Korea)을 무수디클로로메탄에 녹인 후, 올레일아민(oleylamine) 1.5당량을 사용하여 실시예 1-2와 동일한 방법으로 반응 후, 무색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.8-1) A decaarginine (1 g, 0.24 mmol, PEPTRON, Inc., Korea) having the same protecting group as in Comparative Example 4-1 was dissolved in anhydrous dichloromethane, followed by using 1.5 equivalents of oleylamine. After the reaction in the same manner as in 1-2, a colorless liquid product was obtained. The reaction was confirmed by TLC.
8-2) 비교예 8-1에서 얻어진 반응 생성물에 TFA:H2O:TIS(triisopropyl silane)=90:5:5를 첨가 후, 2시간 동안 교반한다. 반응 후, 건조시켜 노란색의 액체생성물을 얻었다. 반응 여부는 TLC로 확인하였다.8-2) TFA: H 2 O: TIS (triisopropyl silane) = 90: 5: 5 was added to the reaction product obtained in Comparative Example 8-1, followed by stirring for 2 hours. After the reaction, it was dried to give a yellow liquid product. The reaction was confirmed by TLC.
<양이온성 지질을 함유하는 핵산 전달체의 제조><Production of Nucleic Acid Carrier Containing Cationic Lipids>
실시예 5. 실시예1의 올레일 트리라이신아미드 (oleyl trilysinamide)를 함유하는 양이온성 리포좀 제조Example 5 Preparation of Cationic Liposomes Containing Oleyl Trilysinamide of Example 1
실시예 1에서 제조한 양이온성 지질인 올레일 트리라이신아미드 (oleyl trilysinamide)와 세포 융합성 인지질인 DOPE(Avanti Polar Lipid Inc., USA)를 각각 1ml의 클로로포름에 녹인 후 몰비 1:1의 비율로 취해 파이렉스 10ml 유리 격막 바이알에 넣어 혼합한 후 질소 환경에서 모든 클로로포름이 증발될 때까지 낮은 속도로 회전 증발시켜 지질 박막 필름으로 제조하였다. 지질 다층형 소구체 (multilamella vesicle)를 제조하기 위하여 이 박막필름에 인산완충용액 1ml을 첨가하고 바이알을 37℃로 하여 밀봉 후 3분간 교반(vortexing)하였다. 균일한 크기를 만들기 위해 이를 입자 균질화 제조기 (extruder, Northern Lipid Inc., Canada)를 사용하여 0.2㎛폴리카보네이트 막을 3번 통과시켜 제조하였다. 얻어진 양이온성 리포좀은 사용하기 전까지 4℃에서 보관하였다.Oleyl trilysinamide, a cationic lipid prepared in Example 1, and DOPE (Avanti Polar Lipid Inc., USA), a cell-compatible phospholipid, were dissolved in 1 ml of chloroform, respectively, at a molar ratio of 1: 1. The mixture was taken into a
실시예 6. 실시예3의 리놀레일 펜타라이신아미드(linoleyl pentalysinamide)를 함유하는 양이온성 리포좀 제조Example 6 Preparation of Cationic Liposomes Containing Linoleyl Pentalysinamide of Example 3
실시예 3에서 제조한 양이온성 지질인 리놀레오일 펜타라이신아미드(linoleyl pentalysinamide)와 세포 융합성 인지질인 DPhPE(Avanti Polar Lipid Inc., USA)를 각각 1ml의 클로로포름에 녹인 후 몰비 1:1의 비율로 취해 파이렉스 10ml 유리 격막 바이알에 넣어 혼합한 후 실시예 5와 동일한 방법으로 양이온성 리포좀을 제조하였다.A molar ratio of 1: 1 after dissolving linoleyl pentalysinamide, a cationic lipid prepared in Example 3, and DPhPE (Avanti Polar Lipid Inc., USA), a cell phospholipid, were dissolved in 1 ml of chloroform, respectively. After taking into a Pyrex 10ml glass septum vial and mixing, a cationic liposome was prepared in the same manner as in Example 5.
실시예 7. 실시예3의 리놀레일 펜타라이신아미드(linoloeyl pentalysinamide)를 함유하는 양이온성 미셀 제조Example 7 Preparation of Cationic Micelles Containing Linoloeyl Pentalysinamide of Example 3
실시예 3에서 제조한 양이온성 지질인 리놀레오일 펜타라이신아미드(linoleyl pentalysinamide)와 계면활성제인 폴리에틸렌글리콜 모노올레일 에테 르를 1:1의 몰 비율로 취하여 혼합한 다음, 혼합액 대 인산완충용액을 1:10의 부피 비율로 혼합하고 수회 진탕혼합 (vortexing)한 다음 약 1분 동안 초음파 발생기를 사용하여 양이온성 미셀을 제조하였다.Linoleyl pentalysinamide, a cationic lipid prepared in Example 3, and polyethyleneglycol monooleyl ether, a surfactant, were mixed in a molar ratio of 1: 1, and then the mixed solution and the phosphate buffer solution were mixed. Cationic micelles were prepared by mixing in a volume ratio of 1:10, vortexing several times and using an ultrasonic generator for about 1 minute.
실시예 8. 실시예2의 팔미틸 테트라라이신아미드 (palmityl tetralysinamide)를 함유하는 양이온성 미셀 제조Example 8 Preparation of Cationic Micelles Containing Palmityl Tetralysinamide of Example 2
실시예 2에서 제조한 양이온성 지질인 팔미틸 테트라라이신아미드 (palmityl tetralysinamide)와 계면활성제인 트윈 20을 1:1의 몰 비율로 취하여 혼합한 다음, 실시예 7과 동일한 방법으로 양이온성 미셀을 제조하였다.A cationic lipid prepared in Example 2, palmithyl tetralysinamide and a surfactant,
실시예 9. 실시예4의 라우릴 헥사라이신아미드(lauryl hexalysinamide)를 함유하는 양이온성 에멀젼 제조Example 9 Preparation of Cationic Emulsion Containing Lauryl hexalysinamide of Example 4
실시예 4에서 제조한 양이온성 지질인 라우릴 헥사라이신아미드(lauryl hexalysinamide)와 트윈 80을 1: 0.1의 몰 비율로 혼합하고 혼합물을 인산 완충용액에 1:10의 부피 비율로 가한 다음, 균질기(homogenizer)를 이용하여 약 2분간 균질화 시켜 유상이 수상 내에 분산된 수중유형 (o/w형) 양이온성 에멀젼을 제조하였다.The cationic lipid lauryl hexalysinamide prepared in Example 4 and
실시예 10. 실시예2의 팔미틸 테트라라이신아미드 (palmityl tetralysinamide)를 함유하는 양이온성 에멀젼 제조Example 10 Preparation of Cationic Emulsions Containing Palmityl Tetralysinamide of Example 2
실시예 2에서 제조한 양이온성 지질인 팔미틸 테트라라이신아미드 (palmityl tetralysinamide)와 트윈 20을 1: 0.1의 몰 비율로 혼합하고 혼합물을 인산 완충용액에 1:10의 부피 비율로 가한 다음, 실시예 9와 동일한 방법으로 양이온성 에멀젼을 제조하였다.Palmityl tetralysinamide, a cationic lipid prepared in Example 2, and
실시예 11. 실시예2의 팔미틸 테트라라이신아미드 (palmityl tetralysinamide) 및 엽산 지질 유도체를 함유하는 양이온성 리포좀 제조Example 11 Preparation of Cationic Liposomes Containing Palmityl Tetralysinamide and Folic Acid Lipid Derivatives of Example 2
실시예 2에서 제조한 양이온성 지질인 팔미틸 테트라라이신아미드 (palmityl tetralysinamide), 세포 융합성 인지질인 DOPE 및 엽산 지질 유도체인 1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-[folate (polyethylene glycol)-2000(Avanti Polar Lipid Inc., USA)을 각각 1ml의 클로로포름에 녹인 후 1:1:0.05의 몰 비율로 취하여 실시예 5와 동일한 방법으로 표면에 엽산 잔기 (folate moiety)가 존재하는 양이온성 리포좀을 제조하였다.Palmityl tetralysinamide, a cationic lipid prepared in Example 2, DOPE, a cell-compatible phospholipid, and 1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N- [folate ( After dissolving polyethylene glycol) -2000 (Avanti Polar Lipid Inc., USA) in 1 ml of chloroform, the molar ratio of 1: 1: 0.05 was taken and the folate moiety was present on the surface in the same manner as in Example 5. Cationic liposomes were prepared.
실시예 12. 실시예4의 라우릴 헥사라이신아미드(lauryl hexalysinamide) 및 폴리에틸렌글리콜 지질 유도체를 함유하는 양이온성 리포좀 제조Example 12 Preparation of Cationic Liposomes Containing Lauryl Hexalysinamide and Polyethylene Glycol Lipid Derivatives of Example 4
실시예 4에서 제조한 양이온성 지질인 라우릴 헥사라이신아미드(lauryl hexalysinamide), 세포 융합성 인지질인 DPhPE 및 폴리에틸렌글리콜 지질 유도체인 1,2-diacyl-sn-glycero- 3-phosphoethanolamine-N- [methoxy(polyethylene glycol)-3000(Avanti Polar Lipid Inc., USA)을 각각 1ml의 클로로포름에 녹인 후 1:1:0.05의 몰 비율로 취하여 실시예 5와 동일한 방법으로 표면에 폴리에틸렌글리콜 그룹이 존재하는 양이온성 리포좀을 제조하였다.Lauryl hexalysinamide, a cationic lipid prepared in Example 4, DPhPE, a cell-fusion phospholipid, and 1,2-diacyl-sn-glycero-3, phosphoethanolamine-N- [methoxy (polyethylene glycol) -3000 (Avanti Polar Lipid Inc., USA) was dissolved in 1 ml of chloroform, and then taken at a molar ratio of 1: 1: 0.05, and cationic cationic glycol groups exist on the surface in the same manner as in Example 5. Liposomes were prepared.
실시예 13. 실시예1의 올레일 트리라이신아미드 (oleyl trilysinamide) 및 갈락토오스 지질 유도체를 함유하는 양이온성 미셀 제조Example 13 Preparation of Cationic Micelles Containing Oleyl Trilysinamide and Galactose Lipid Derivatives of Example 1
실시예 1에서 제조한 양이온성 지질인 올레일 트리라이신아미드 (oleyl trilysinamide)와 갈락토오스 지질 유도체인 세리브로사이드(cerebroside) (Avanti Polar Lipid Inc., USA) 및 계면활성제인 트리톤 X-100을 각각 1:0.05:1의 몰 비율로 취하여 혼합한 다음, 실시예 7과 동일한 방법으로 표면에 갈락토오즈 잔기 (galactose moiety)가 존재하는 양이온성 미셀을 제조하였다.Oleyl trilysinamide, a cationic lipid prepared in Example 1, cerebroside, a galactose lipid derivative (Avanti Polar Lipid Inc., USA), and a surfactant, Triton X-100, were respectively prepared. Cationic micelles containing galactose moiety on the surface were prepared in the same manner as in Example 7, after mixing in a molar ratio of: 0.05: 1.
실시예 14. 실시예3의 리놀레일 펜타라이신아미드(linoleyl pentalysinamide)를 함유하는 양이온성 에멀젼 제조Example 14 Preparation of Cationic Emulsion Containing Linoleyl Pentalysinamide of Example 3
실시예 3에서 제조한 양이온성 지질인 리놀레일 펜타라이신아미드(linoleyl pentalysinamide)와 트윈 20을 1: 0.1의 몰 비율로 혼합하고 혼합물을 인산 완충용액에 1:10의 부피 비율로 가한 다음, 실시예 9와 동일한 방법으로 양이온성 에멀젼을 제조하였다.Linoleyl pentalysinamide, a cationic lipid prepared in Example 3, and
실시예 15. 실시예1의 올레일 트리라이신아미드 (oleyl trilysinamide) 및 폴리에틸렌글리콜 지질 유도체를 함유하는 양이온성 리포좀 제조Example 15 Preparation of Cationic Liposomes Containing Oleyl Trilysinamide and Polyethylene Glycol Lipid Derivatives of Example 1
실시예 1에서 제조한 양이온성 지질인 올레일 트리라이신아미드 (oleyl trilysinamide), 세포 융합성 인지질인 DPhPE 및 폴리에틸렌글리콜 지질 유도체인 1,2-diacyl-sn-glycero- 3-phosphoethanolamine-N- [methoxy(polyethylene glycol)-3000(Avanti Polar Lipid Inc., USA)을 각각 1ml의 클로로포름에 녹인 후 1:1:0.05의 몰 비율로 취하여 실시예 5와 동일한 방법으로 표면에 폴리에틸렌글리콜 그룹이 존재하는 양이온성 리포좀을 제조하였다.Oleyl trilysinamide, a cationic lipid prepared in Example 1, DPhPE, a cell soluble phospholipid, and 1,2-diacyl-sn-glycero-3, phosphoethanolamine-N- [methoxy (polyethylene glycol) -3000 (Avanti Polar Lipid Inc., USA) was dissolved in 1 ml of chloroform, and then taken at a molar ratio of 1: 1: 0.05, and cationic cationic glycol groups exist on the surface in the same manner as in Example 5. Liposomes were prepared.
비교예 9. 기존에 판매되고 있는 양이온성 리포좀 Comparative Example 9. Existing Cationic Liposomes
기존의 핵산 전달 실험용으로 시판되고 있는 양이온성 리포좀인 리포펙타민(LipofectAMINE)TM 2000(Invitrogen, USA)을 구입하여 사용하였다.Lipofectamine (2000) (Invitrogen, USA), a cationic liposome that is commercially available for conventional nucleic acid delivery experiments, was purchased and used.
비교예 10. 비교예1의 라우릴 라이신아미드(lauryl lysinamide)를 함유하는 양이온성 리포좀 제조 Comparative Example 10 Preparation of Cationic Liposomes Containing Lauryl Lysamide In Comparative Example 1
비교예 1에서 제조한 양이온성 지질인 라우릴 라이신아미드(lauryl lysinamide)와 세포 융합성 인지질인 DOPE(Avanti Polar Lipid Inc., USA)를 각각 1ml의 클로로포름에 녹인 후 몰비 1:1의 비율로 취해 파이렉스 10ml 유리 격막 바이알에 넣어 혼합한 후 실시예 5와 동일한 방법으로 양이온성 리포좀을 제조하였다.Lauryl lysinamide, a cationic lipid prepared in Comparative Example 1, and DOPE (Avanti Polar Lipid Inc., USA), a cell-compatible phospholipid, were dissolved in 1 ml of chloroform, and then taken in a ratio of 1: 1. Cationic liposomes were prepared in the same manner as in Example 5 after mixing into a
비교예 11. 비교예 5의 미리스틸 펜타아르기닌아미드(myristyl pentaargininamide) 를 함유하는 양이온성 리포좀 제조 Comparative Example 11. Cationic liposome preparation containing myristyl pentaargininamide of Comparative Example 5
비교예 5에서 제조한 양이온성 지질인 미리스틸 펜타아르기닌아미드(myristyl pentaargininamide)와 세포 융합성 인지질인 DPhPE(Avanti Polar Lipid Inc., USA)를 각각 1ml의 클로로포름에 녹인 후 몰비 1:1의 비율로 취해 파이렉스 10ml 유리 격막 바이알에 넣어 혼합한 후 실시예 5와 동일한 방법으로 양이온성 리포좀을 제조하였다.Myristyl pentaargininamide, a cationic lipid prepared in Comparative Example 5, and DPhPE (Avanti Polar Lipid Inc., USA), a cell-compatible phospholipid, were dissolved in 1 ml of chloroform, respectively, in a ratio of 1: 1. Cationic liposomes were prepared in the same manner as in Example 5 after mixing into a Pyrex 10ml glass septum vial and mixing.
비교예 12. 비교예 6의 스테아릴 옥타아르기닌아미드(stearyl octaargininamide)를 함유하는 양이온성 리포좀 제조 Comparative Example 12. Preparation of Cationic Liposomes Containing Stearyl octaargininamide of Comparative Example 6
비교예 6에서 제조한 양이온성 지질인 스테아릴 옥타아르기닌아미드(stearyl octaargininamide)와 세포 융합성 인지질인 DPhPE(Avanti Polar Lipid Inc., USA)를 각각 1ml의 클로로포름에 녹인 후 몰비 1:1의 비율로 취해 파이렉스 10ml 유리 격막 바이알에 넣어 혼합한 후 실시예 5와 동일한 방법으로 양이온성 리포좀을 제조하였다.Stearyl octaargininamide, a cationic lipid prepared in Comparative Example 6, and DPhPE (Avanti Polar Lipid Inc., USA), a cell-fusion phospholipid, were dissolved in 1 ml of chloroform, respectively, at a molar ratio of 1: 1. Cationic liposomes were prepared in the same manner as in Example 5 after mixing into a Pyrex 10ml glass septum vial and mixing.
비교예 13. 비교예 2의 올레일 노나라이신아미드(oleyl nonalysinamide)를 함유하는 양이온성 리포좀 제조 Comparative Example 13 Preparation of Cationic Liposomes Containing Oleyl Nonalysinamide of Comparative Example 2
비교예 2에서 제조한 양이온성 지질인 올레일 노나라이신아미드(oleyl nonalysinamide)와 세포 융합성 인지질인 DPhPE(Avanti Polar Lipid Inc., USA)를 각각 1ml의 클로로포름에 녹인 후 몰비 1:1의 비율로 취해 파이렉스 10ml 유리 격 막 바이알에 넣어 혼합한 후 실시예 5와 동일한 방법으로 양이온성 리포좀을 제조하였다.Oleyl nonalysinamide, a cationic lipid prepared in Comparative Example 2, and DPhPE (Avanti Polar Lipid Inc., USA), a cell-compatible phospholipid, were dissolved in 1 ml of chloroform, respectively, in a ratio of 1: 1. Cationic liposomes were prepared in the same manner as in Example 5 after mixing into a Pyrex 10ml glass septum vial and mixing.
비교예 14. 비교예 4의 리놀레일 아르기닌아미드(linoleyl argininamide) 을 함유하는 양이온성 리포좀 제조 Comparative Example 14. Cationic liposome preparation containing linoleyl argininamide of Comparative Example 4
비교예 4에서 제조한 양이온성 지질인 리놀레일 아르기닌아미드(linoleyl argininamide) 와 세포 융합성 인지질인 DOPE(Avanti Polar Lipid Inc., USA)를 각각 1ml의 클로로포름에 녹인 후 몰비 1:1의 비율로 취해 파이렉스 10ml 유리 격막 바이알에 넣어 혼합한 후 실시예 5와 동일한 방법으로 양이온성 리포좀을 제조하였다.Linoleyl argininamide, a cationic lipid prepared in Comparative Example 4, and DOPE (Avanti Polar Lipid Inc., USA), a cell-compatible phospholipid, were dissolved in 1 ml of chloroform, respectively, and were taken at a molar ratio of 1: 1. Cationic liposomes were prepared in the same manner as in Example 5 after mixing into a
비교예 15. 비교예 3의 스테아릴 데카라이신아미드(stearyl decalysinamide)를 함유하는 양이온성 미셀 제조 Comparative Example 15 Preparation of Cationic Micelle Containing Stearyl Decalysinamide of Comparative Example 3
비교예 3에서 제조한 양이온성 지질인 스테아릴 데카라이신아미드(stearyl decalysinamide)와 계면활성제인 트윈 20을 1:1의 몰 비율로 취하여 혼합한 다음, 실시예 7과 동일한 방법으로 양이온성 미셀을 제조하였다.Stearyl decalysinamide, a cationic lipid prepared in Comparative Example 3, and
비교예 16. 비교예 7의 아라키딜 노나아르기닌아미드(arachidyl nonaargininamide)를 함유하는 양이온성 에멀젼 제조 Comparative Example 16 Preparation of Cationic Emulsion Containing Arachidyl Nonaargininamide of Comparative Example 7
비교예 7에서 제조한 양이온성 지질인 아라키딜 노나아르기닌아미 드(arachidyl nonaargininamide)와 트윈 80을 1: 0.1의 몰 비율로 혼합하고 혼합물을 인산 완충용액에 1:10의 부피 비율로 가한 다음, 실시예 9와 동일한 방법으로 양이온성 에멀젼을 제조하였다.Arachidyl nonaargininamide, a cationic lipid prepared in Comparative Example 7, and
비교예 17. 비교예 8의 올레일 데카아르기닌아미드(oleyl dacaargininamide)를 함유하는 양이온성 에멀젼 제조 Comparative Example 17 Preparation of Cationic Emulsion Containing Oleyl Dacaargininamide of Comparative Example 8
비교예 8에서 제조한 양이온성 지질인 올레일 데카아르기닌아미드(oleyl dacaargininamide)와 트윈 20을 1: 0.1의 몰 비율로 혼합하고 혼합물을 인산 완충용액에 1:10의 부피 비율로 가한 다음, 실시예 9와 동일한 방법으로 양이온성 에멀젼을 제조하였다.Oleyl dacaargininamide, a cationic lipid prepared in Comparative Example 8, and
비교예 18. 비교예 4의 리놀레일 아르기닌아미드(linoleyl argininamide) 및 엽산 지질 유도체를 함유하는 양이온성 리포좀 제조 Comparative Example 18 Preparation of Cationic Liposomes Containing Linoleyl Argininamide and Folic Acid Lipid Derivatives of Comparative Example 4
비교예 4에서 제조한 양이온성 지질인 리놀레일 아르기닌아미드(linoleoyl argininamide), 세포 융합성 인지질인 DOPE 및 엽산 지질 유도체인 1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-[folate(polyethylene glycol)-2000(Avanti Polar Lipid Inc., USA)을 각각 1ml의 클로로포름에 녹인 후 1:1:0.05의 몰 비율로 취하여 실시예 5와 동일한 방법으로 표면에 엽산 잔기 (folate moiety)가 존재하는 양이온성 리포좀을 제조하였다.Linoleoyl argininamide, a cationic lipid prepared in Comparative Example 4, DOPE, a cell-fusion phospholipid, and 1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N- [folate (polyethylene Cation dissolving glycol) -2000 (Avanti Polar Lipid Inc., USA) in 1 ml of chloroform and taking a molar ratio of 1: 1: 0.05, and a folate moiety is present on the surface in the same manner as in Example 5. Sex liposomes were prepared.
비교예 19. 비교예 1의 라우릴 라이신아미드(lauryl lysinamide) 및 갈락토오스 지질 유도체를 함유하는 양이온성 미셀 제조Comparative Example 19 Preparation of Cationic Micelle Containing Lauryl lysinamide and Galactose Lipid Derivative of Comparative Example 1
비교예 1에서 제조한 양이온성 지질인 라우릴 라이신아미드(lauryl lysinamide)와 갈락토오스 지질 유도체인 세리브로사이드(cerebroside) (Avanti Polar Lipid Inc., USA) 및 계면활성제인 트리톤 X-100을 각각 1:0.05:1의 몰 비율로 취하여 혼합한 다음, 실시예 7과 동일한 방법으로 표면에 갈락토오즈 잔기 (galactose moiety)가 존재하는 양이온성 미셀을 제조하였다.Lauryl lysinamide, a cationic lipid prepared in Comparative Example 1, cerebroside, a galactose lipid derivative (Avanti Polar Lipid Inc., USA) and Triton X-100, a surfactant, were each 1: After mixing in a molar ratio of 0.05: 1, cationic micelles having a galactose moiety on their surface were prepared in the same manner as in Example 7.
[실험예]Experimental Example
세포 배양Cell culture
사람의 자궁경부암 상피 세포인 HeLa 세포주, 폐암 세포인 A549 세포주, 간암 세포주인 Huh-7, 흑색종인 WM266.4와 A375 세포주, 신경교종인 U87 세포주는 ATCC (American Type Culture Collection, USA)로부터 구입하여 사용하였다. HeLa, A549 세포주는 RPMI(Gibco, USA), Huh-7, A375, U87 세포주는 DMEM(Dulbecco's modified eagles medium, Gibco, USA), WM266.4 세포주는 MEM(Minimum Essential Medium, Gibco, USA)에 10% 우태아 혈청 w/v (HyClone laboratories Inc, USA)와 100 unit/ml 페니실린 또는 100㎍/ml 스트렙토마이신을 포함하여 배양하였다. Human cervical carcinoma epithelial cell HeLa cell line, lung cancer cell A549 cell line, liver cancer cell line Huh-7, melanoma WM266.4 and A375 cell line, glioma U87 cell line are purchased from ATCC (American Type Culture Collection, USA) It was. HeLa, A549 cell lines RPMI (Gibco, USA), Huh-7, A375, U87 cell lines DMEM (Dulbecco's modified eagles medium, Gibco, USA), WM266.4 cell lines to MEM (Minimum Essential Medium, Gibco, USA) Incubated with% fetal calf serum w / v (HyClone laboratories Inc, USA) and 100 unit / ml penicillin or 100 μg / ml streptomycin.
[실험예 I] 형광마커로 표지된 작은 간섭 리보핵산을 이용한 핵산 전달 효율 평가Experimental Example I Evaluation of Nucleic Acid Delivery Efficiency Using Small Interfering Ribonucleic Acid Labeled with Fluorescent Markers
I-1. WM266.4 세포주에서의 작은 간섭 리보핵산의 전달 효율 평가 I-1. Evaluation of Delivery Efficiency of Small Interfering Ribonucleic Acids in WM266.4 Cell Line
WM266.4 세포주를 실험 전날 48 웰 플레이트에 웰 당 3×10⁴개씩 분주(seeding)하고 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 50 ㎕씩을 넣고 형광 마커로 표지된 작은 간섭 리보핵산 물질인 BlockiT(Invitrogen, USA) 5pmole씩과 비교예 10, 14와 실시예 5에서 제조된 양이온성 리포좀 2㎕를 각각 첨가하였다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하였다. 이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37℃의 CO₂배양기에서 24시간 동안 배양하였다. 배양된 세포의 미디어를 웰 당 200㎕씩 새 미디어로 교체하여 준 후 형광 현미경으로 리보핵산 전달 효율을 관찰하였다. 50 μl of serum-free medium was added to the Eppendorf tubes when the WM266.4 cell line was seeded in 48 well plates at the day before the experiment and seeded at 3 × 10 μL per well and cells of each plate were grown uniformly by 60-70%. 5 μl of BlockiT (Invitrogen, USA), a small interfering ribonucleic acid substance labeled with a fluorescent marker, and 2 μl of cationic liposomes prepared in Comparative Examples 10, 14 and 5 were added. These were slowly pipetted and mixed and left at room temperature for 20 minutes. The complex thus prepared was added to a well plate and incubated in a
도1은 비교예 10, 14와 실시예 5로부터 제조된 양이온성 리포좀의 핵산 전달 효율을 위상차와 형광 현미경(DM IL, Leica, Germany)으로 관찰한 것으로 도1A와 C는 비교예 10, 14 처리시의 위상차 현미경 사진이고, 도1E는 실시예 5의 조성 처리시의 위상차 현미경 사진이다. 또한 도1B와 D는 비교예 10, 14 처리시의 형광 마커로 표지된 작은 간섭 리보핵산의 세포내 전달을 보여주는 형광 현미경 사진이고, 도1F는 실시예 5의 조성 처리시의 형광 현미경 사진이다. 본 도면으로부터 실시예 5에서 본 발명의 양이온성 지질을 함유하여 제조된 양이온성 리포좀이 비교예 10 및 14에서 제조된 공지 조성의 리포좀보다 WM266.4 세포내에서 작은 간섭 리보핵산의 전달 효율을 증가시킨다는 사실을 알 수 있다.Figure 1 shows the nucleic acid transfer efficiency of the cationic liposomes prepared from Comparative Examples 10, 14 and Example 5 with a phase difference and a fluorescence microscope (DM IL, Leica, Germany), Figures 1A and C treated Comparative Examples 10, 14 It is a phase contrast microscope photograph at the time, and FIG. 1E is a phase difference microscope photograph at the time of the composition process of Example 5. FIG. 1B and D are fluorescence micrographs showing intracellular delivery of small interfering ribonucleic acid labeled with fluorescent markers in Comparative Examples 10 and 14, and FIG. 1F is fluorescence micrographs in the composition treatment of Example 5. FIG. From this figure, the cationic liposomes prepared by containing the cationic lipids of the present invention in Example 5 increased the delivery efficiency of small interfering ribonucleic acid in WM266.4 cells than the liposomes of the known composition prepared in Comparative Examples 10 and 14. It can be seen that.
I-2. HeLa 세포주에서의 작은 간섭 리보핵산의 전달 효율 평가 I-2. Evaluation of Delivery Efficiency of Small Interfering Ribonucleic Acids in HeLa Cell Lines
HeLa 세포주를 실험 전날 48 웰 플레이트에 웰 당 3×10⁴개씩 분주(seeding)하고 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 50 ㎕씩을 넣고 형광 마커로 표지된 작은 간섭 리보핵산 물질인 BlockiT 5pmole씩과 비교예 11, 13과 실시예 6에서 제조된 양이온성 리포좀 2㎕를 각각 첨가하였다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하였다. 이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37℃의 CO₂배양기에서 24시간 동안 배양하였다. 배양된 세포의 미디어를 웰 당 200㎕씩 새 미디어로 교체하여 준 후 형광 현미경으로 리보핵산의 전달 효율을 관찰하였다. HeLa cell lines were seeded in 3 wells per 48 well plates on the day before the experiment, and when the cells of each plate were evenly grown by 60-70%, 50 μl of serum-free medium was added to the Eppendorf tube. BlockiT 5 pmole, a small interfering ribonucleic acid substance labeled with a fluorescent marker, and 2 μl of cationic liposomes prepared in Comparative Examples 11, 13 and 6 were added, respectively. These were slowly pipetted and mixed and left at room temperature for 20 minutes. The complex thus prepared was added to a well plate and incubated in a
도2는 비교예 11, 13과 실시예 6으로부터 제조된 양이온성 리포좀의 핵산 전달 효율을 위상차 현미경과 형광 현미경으로 관찰한 것으로 도2A와 C는 비교예 11, 13 처리시의 위상차 현미경 사진이고, 도2E는 실시예 6의 조성 처리시의 위상차 현미경 사진이다. 또한 도2B와 D는 비교예 11, 13 처리시의 형광 마커로 표지된 작은 간섭 리보핵산의 세포내 전달을 보여주는 형광 현미경 사진이고, 도2F는 실시예 6의 조성 처리시의 형광 현미경 사진이다. 본 도면으로부터 실시예 6에서 본 발명의 양이온성 지질을 함유하여 제조된 양이온성 리포좀이 비교예 11, 13에서 제조된 공지 조성의 리포좀보다 HeLa 세포내에서 작은 간섭 리보핵산의 전달 효율을 증가시킨다는 사실을 알 수 있다.FIG. 2 shows the nucleic acid transfer efficiency of the cationic liposomes prepared from Comparative Examples 11 and 13 and Example 6 using a phase contrast microscope and a fluorescence microscope. FIGS. 2A and C are phase contrast micrographs when the Comparative Examples 11 and 13 were treated. 2E is a phase contrast micrograph at the time of the composition treatment of Example 6. FIG. 2B and D are fluorescence micrographs showing intracellular delivery of small interfering ribonucleic acid labeled with fluorescent markers in Comparative Examples 11 and 13, and FIG. 2F is fluorescence micrographs in the composition treatment of Example 6. FIG. The fact that cationic liposomes prepared with the cationic lipids of the present invention in Example 6 from this figure increases the delivery efficiency of small interfering ribonucleic acid in HeLa cells than liposomes of known composition prepared in Comparative Examples 11 and 13 It can be seen.
I-3. U87 세포주에서의 작은 간섭 리보핵산의 전달 효율 평가I-3. Evaluation of Delivery Efficiency of Small Interfering Ribonucleic Acids in U87 Cell Line
U87 세포주를 실험 전날 48 웰 플레이트에 웰 당 3×10⁴개씩 분주(seeding)하고 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 50 ㎕씩을 넣고 형광 마커로 표지된 작은 간섭 리보핵산 물질인 BlockiT 5pmole씩과 비교예 12, 19와 실시예 13에서 제조된 양이온성 리포좀 및 미셀 2㎕를 각각 첨가하였다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하였다. 이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37℃의 CO₂배양기에서 24시간 동안 배양하였다. 배양된 세포의 미디어를 웰 당 200㎕씩 새 미디어로 교체하여 준 후 형광 현미경으로 리보핵산 전달 효율을 관찰하였다. When the U87 cell line was seeded at 3 × 10 mm / well in a 48 well plate on the day before the experiment, and the cells of each plate were uniformly grown by 60-70%, 50 μl of serum-free medium was added to the Eppendorf tube. BlockiT 5 pmole, a small interfering ribonucleic acid substance labeled with a fluorescent marker, and 2 μl of cationic liposomes and micelles prepared in Comparative Examples 12, 19 and 13 were added, respectively. These were slowly pipetted and mixed and left at room temperature for 20 minutes. The complex thus prepared was added to a well plate and incubated in a
도3은 비교예 12, 19와 실시예 13로부터 제조된 양이온성 리포좀 및 미셀의 핵산 전달 효율을 위상차 현미경과 형광 현미경으로 관찰한 것으로 도3A와 C는 비교예 12, 19 처리시의 위상차 현미경 사진이고, 도3E는 실시예 13의 조성 처리시의 위상차 현미경 사진이다. 또한 도3B와 D는 비교예 12, 19 처리시의 형광 마커로 표지된 작은 간섭 리보핵산의 세포내 전달을 보여주는 형광 현미경 사진이고, 도3F는 실시예 13의 조성 처리시의 형광 현미경 사진이다. 본 도면으로부터 실시예 13에서 본 발명의 양이온성 지질을 함유하여 제조된 양이온성 미셀이 비교예 12, 19에서 제조된 공지 조성의 리포좀 및 미셀보다 U87 세포내에서 작은 간섭 리보핵산의 전달 효율을 증가시킨다는 사실을 알 수 있다.3 is a phase contrast microscope and a fluorescence microscope of the nucleic acid transfer efficiency of the cationic liposomes and micelles prepared from Comparative Examples 12, 19 and 13, and FIGS. 3A and C are phase contrast micrographs of Comparative Examples 12 and 19. 3E is a phase contrast micrograph at the time of the composition treatment of Example 13. FIG. 3B and D are fluorescence micrographs showing intracellular delivery of small interfering ribonucleic acid labeled with fluorescent markers in Comparative Examples 12 and 19, and FIG. 3F is fluorescence micrographs in the composition treatment of Example 13. FIG. From this figure, the cationic micelle prepared with the cationic lipid of the present invention in Example 13 increased the delivery efficiency of the interfering ribonucleic acid in U87 cells smaller than the liposomes and micelles of known composition prepared in Comparative Examples 12 and 19. It can be seen that.
[실험예 II] 형광 유세포 분석법 (Fluorescence Activated Cell Sorting, FACS)을 이용한 작은 간섭 리보핵산의 전달 효율 측정 Experimental Example II Measurement of Delivery Efficiency of Small Interfering Ribonucleic Acid Using Fluorescence Activated Cell Sorting (FACS)
II-1. A549 세포주에서의 형광 유세포 분석법 (Fluorescence Activated Cell Sorting, FACS)을 이용한 작은 간섭 리보핵산의 전달 효율 측정 II-1. Measurement of Delivery Efficiency of Small Interfering Ribonucleic Acid Using Fluorescence Activated Cell Sorting (FACS) in A549 Cell Line
A549 세포주를 실험 전날 6 웰 플레이트에 웰 당 3×105개씩 분주(seeding)하였다. 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 100㎕씩을 넣고 형광표지된 이중나선 리보핵산인 BlockiT 20pmole씩과 비교예 12, 15와 실시예 8에서 제조된 양이온성 미셀 또는 리포좀 6 ㎕를 각각 첨가하였다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하였다.A549 cell lines were seeded 3 × 10 5 per well in 6 well plates the day before the experiment. When the cells of each plate grew uniformly by 60-70%, 100 μl of serum-free medium was added to the Eppendorf tube, and 20 pmole of BlockiT, a fluorescently labeled double-stranded ribonucleic acid, and Comparative Examples 12 and 15, respectively. 6 μl of cationic micelles or liposomes prepared in 8 were added, respectively. These were slowly pipetted and mixed and left at room temperature for 20 minutes.
이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37 ℃의 CO₂배양기에서 24시간 동안 배양하였다. 배양된 세포를 수집한 후 PBS로 2번 세척하였다. 형광표지된 이중나선 리보핵산이 들어간 세포들을 형광 유세포 분석기인 BD FACS CALIBUR(BD Bioscience, USA)를 사용하여 형광 강도 피크의 이동에 의한 세포내 전달 효율을 분석하였다. 이를 도4에 나타내었다. 도4A의 세포에 아무 처리하지 않은 미처리군은 대조군으로 리보핵산이 세포 내로 전달되지 않아 피크가 거의 이동하지 않았고, 도4B는 비교예 12에서 제조된 리포좀, 도4C는 비교예 15에서 제조된 공지 조성의 미셀로 처리한 세포군으로 도4B는 리보핵산이 44.79%, 도4C는 58.93% 전달되었다. 반면, 본 발명의 실시예 8 처리군의 경우 84.78% 을 나타내어 비교예 12, 15 처리군에 비하여 세포내 전달효율이 증가되었다.The complex thus prepared was added to a well plate and incubated for 24 hours in a
따라서 본 발명의 실시예 8에서 제조된 양이온성 미셀이 비교예 12, 15에서 제조된 리포좀 또는 미셀보다 A549세포 내에서 리보핵산 전달 효율이 증가되었음을 알 수 있었다.Therefore, it was found that the cationic micelles prepared in Example 8 of the present invention had increased ribonucleic acid transfer efficiency in A549 cells than liposomes or micelles prepared in Comparative Examples 12 and 15.
II-2. A375 세포주에서의 형광 유세포 분석법 (Fluorescence Activated Cell Sorting, FACS)을 이용한 작은 간섭 리보핵산의 전달 효율 측정 II-2. Measurement of Delivery Efficiency of Small Interfering Ribonucleic Acid Using Fluorescence Activated Cell Sorting (FACS) in A375 Cell Line
A375 세포주를 실험 전날 6 웰 플레이트에 웰 당 3×105개씩 분주(seeding)하였다. 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 100㎕씩을 넣고 형광표지된 이중나선 리보핵산인 BlockiT 20pmole씩과 비교예 14, 16과 실시예 9에서 제조된 양이온성 리포좀 또는 에멀젼 6 ㎕를 각각 첨가하였다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하였다.A375 cell lines were seeded 3 × 10 5 per well in 6 well plates the day before the experiment. When the cells of each plate grew uniformly about 60-70%, 100 μl of medium without serum was added to the Eppendorf tube and 20 pmole of BlockiT, a fluorescently labeled double-stranded ribonucleic acid, and Comparative Examples 14 and 16, respectively. 6 μl of cationic liposomes or emulsion prepared in 9 were added respectively. These were slowly pipetted and mixed and left at room temperature for 20 minutes.
이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37 ℃의 CO₂배양기에서 24시간 동안 배양하였다. 배양된 세포를 수집한 후 PBS로 2번 세척하였다. 형광표지된 이중나선 리보핵산이 들어간 세포들을 형광 유세포 분석기인 BD FACS CALIBUR를 사용하여 형광 강도 피크의 이동에 의한 세포내 전달 효율을 분석하였다. 이를 도5에 나타내었다. 도5A의 세포에 아무 처리하지 않은 미처리군은 대조군으로 리보핵산이 세포 내로 전달되지 않아 피크가 거의 이동하지 않았고, 도5B는 비교예 14에서 제조된 공지조성의 리포좀으로 처리한 세포군이고, 도5C는 비교예 16에서 제조 된 공지 조성의 에멀젼으로 처리한 세포군으로 도5B는 유전자가 55.59%, 도5C 는 51.89% 전달되었다. 반면, 본 발명의 실시예 9 처리군의 경우 89.69% 을 나타내어 비교예 14, 16 처리군에 비하여 세포내 전달효율이 증가되었다.The complex thus prepared was added to a well plate and incubated for 24 hours in a
따라서 본 발명의 실시예 9에서 제조된 양이온성 에멀젼이 비교예 14, 16에서 제조된 리포좀 및 에멀젼보다 A375세포 내에서 리보핵산 전달 효율이 증가되었음을 알 수 있었다.Therefore, it was found that the cationic emulsion prepared in Example 9 of the present invention had increased ribonucleic acid transfer efficiency in A375 cells than the liposomes and emulsion prepared in Comparative Examples 14 and 16.
II-3. Huh-7 세포주에서의 형광 유세포 분석법 (Fluorescence Activated Cell Sorting, FACS)을 이용한 작은 간섭 리보핵산의 전달 효율 측정 II-3. Measurement of Delivery Efficiency of Small Interfering Ribonucleic Acid Using Fluorescence Activated Cell Sorting (FACS) in Huh-7 Cell Line
Huh-7 세포주를 실험 전날 6 웰 플레이트에 웰 당 3×105개씩 분주(seeding)하였다. 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 100㎕씩을 넣고 형광표지된 핵산 앱타머와 비교예 10, 18과 실시예 15에서 제조된 양이온성 리포좀 6 ㎕를 각각 첨가하였다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하였다.Huh-7 cell lines were seeded 3 × 10 5 per well in 6 well plates the day before the experiment. When the cells of each plate were grown uniformly by 60-70%, 100 μl of the medium containing no serum was added to the Eppendorf tube and the fluorescently labeled nucleic acid aptamer and the cations prepared in Comparative Examples 10, 18 and Example 15. 6 μl of sex liposomes were added respectively. These were slowly pipetted and mixed and left at room temperature for 20 minutes.
이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37 ℃의 CO₂배양기에서 24시간 동안 배양하였다. 배양된 세포를 수집한 후 PBS로 2번 세척하였다. 형광표지된 이중나선 리보핵산이 들어간 세포들을 형광 유세포 분석기인 BD FACS CALIBUR를 사용하여 형광 강도 피크의 이동에 의한 세포내 전달 효율을 분석하였다. 이를 도 6에 나타내었다. 도6A의 세포에 아무 처리하지 않은 미처리군은 대조군으로 유전자 가 세포 내로 전달되지 않아 피크가 거의 이동하지 않았고, 도6B는 비교예 10, 도6C는 비교예 18에서 제조된 공지 조성의 리포좀으로 처리한 세포군으로 도6B는 리보핵산이 42.08%, 도6C는 38.16% 전달되었다. 반면, 본 발명의 실시예 15 처리군의 경우 85.53% 을 나타내어 비교예 10, 18 처리군에 비하여 세포내 전달효율이 증가되었다.The complex thus prepared was added to a well plate and incubated for 24 hours in a
따라서 본 발명의 실시예 15에서 제조된 양이온성 리포좀이 비교예 10, 18에서 제조된 리포좀보다 Huh-7세포 내에서 리보핵산 전달 효율이 증가되었음을 알 수 있었다.Therefore, it was found that the cationic liposomes prepared in Example 15 of the present invention had increased ribonucleic acid delivery efficiency in Huh-7 cells than the liposomes prepared in Comparative Examples 10 and 18.
[실험예 III] 역전사 중합효소 연쇄반응을 이용한 작은간섭 리보핵산 전달 효능 평가Experimental Example III Evaluation of Small Interfering Ribonucleic Acid Delivery Efficacy Using Reverse Transcriptase Polymerase Chain Reaction
III-1. A375 세포주에서의 역전사 중합효소 연쇄반응을 이용한 작은간섭 리보핵산 전달 효능 평가III-1. Evaluation of Small Interfering Ribonucleic Acid Delivery Efficacy by Reverse Transcription Polymerase Chain Reaction in A375 Cell Line
A375 세포주를 실험 전날 24 웰 플레이트에 웰 당 세포를 8×10⁴씩 분주(seeding)하였다. 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 25㎕씩을 넣고, siRNA와 비교예 9, 13, 16과 실시예 6에서 제조된 양이온성 리포좀 또는 에멀젼을 각각 4㎕씩 첨가하였다. 서바이빈 (survivin) 유전자(Gene bank accession number: NM_001168)의 발현 억제를 유도하기 위한 siRNA는 삼천리제약 (Samchully Pharmaceuticals, Seoul, Korea)에서 구입하여 사용하였다. 미디어에 포함된 siRNA의 최종 농도는 100nM이 되게 맞 추었다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하고 이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37 ℃의 CO₂세포배양기에서 24시간 동안 배양하였다. 24시간 후 Trizol 시약(Invitrogen, Carlsbad, CA, USA)을 사용하여 세포내에 존재하는 전체 리보핵산 (RNA)을 분리하였으며, 이 RNA는 AccuPowerRT PreMix (Bioneer, Daejeon, Korea)를 사용하여 cDNA로 역전사 하였다. 서바이빈(survivin)에 특이적인 프라이머의 서열은 5'-GGACCACCGCATCTCTACAT-3'(정방향), 5'-CTTTCTCCGCAGTTTCCTCA-3'(역방향)이며 중합효소연쇄반응은 95℃에서 5분 반응 후, 95℃에서 1분, 59℃에서 1분, 72℃에서 30초를 30번 반복한 후 72℃에서 5분 더 반응시켜주었다. 생성물의 크기는 347 염기쌍이었다. 서바이빈(survivin) 유전자 발현의 정도는 서바이빈 특이적인 연쇄반응 생성물의 밴드 밀도를 GAPDH(glyceraldehyde-3-phosphate dehydrogenase) 유전자를 증폭하여 나타나는 밴드 밀도로 보정하여 정량적인 발현의 변화를 측정하였다.A375 cell lines were seeded 8 × 10 μs of cells per well into 24 well plates the day before the experiment. When the cells of each plate were grown uniformly by about 60-70%, 25 μl of medium without serum was added to the eppendorf tube, and the siRNA and the cationic liposomes prepared in Comparative Examples 9, 13, 16 and Example 6 Or 4 μl of emulsion each. SiRNA for inducing expression of survivin gene (Gene bank accession number: NM_001168) was purchased from Samchully Pharmaceuticals, Seoul, Korea. The final concentration of siRNA included in the media was adjusted to 100 nM. After slowly pipetting and mixing, the mixture was allowed to stand at room temperature for 20 minutes, and the complex thus prepared was added to a well plate and incubated in a
도7은 각각의 조성을 처리한 경우 A375 세포내에서 타겟 유전자인 서바이빈의 전사체 발현을 비교한 것이다. 대조군은 유전자가 세포 내로 전달되지 않아 서바이빈 유전자의 발현에 변화가 없었고, 비교예 13에서 제조된 양이온성 리포좀, 비교예 16에서 제조된 양이온성 에멀젼과 시판품인 비교예 9는 실시예 6에서 제조된 양이온성 리포좀보다 서바이빈 유전자의 발현 감소 효능이 낮은 것으로 관찰되었다. 이와 같은 결과에서 알 수 있듯이, 실시예 6에서 제조된 양이온성 리포좀이 흑색종 세포 내로 작은간섭 리보핵산물질을 전달하여 표적유전자의 발현을 선택적으로 억제시킴을 알 수 있었다.Figure 7 compares the expression of transcripts of survivin, a target gene, in A375 cells when each composition was treated. In the control group, the gene was not delivered into the cell, and there was no change in the expression of the survivin gene. The cationic liposome prepared in Comparative Example 13, the cationic emulsion prepared in Comparative Example 16, and Comparative Example 9, which are commercially available, were used in Example 6. It was observed that the expression reduction effect of survivin gene was lower than the prepared cationic liposomes. As can be seen from these results, the cationic liposome prepared in Example 6 was found to deliver a small interfering ribonucleate into the melanoma cells to selectively inhibit the expression of the target gene.
III-2. HeLa 세포주에서의 역전사 중합효소 연쇄반응을 이용한 안티센스 올리고 핵산 전달 효능 평가III-2. Evaluation of Antisense Oligonucleotide Delivery Efficacy by Reverse Transcription Polymerase Chain Reaction in HeLa Cell Line
HeLa 세포주를 실험 전날 24 웰 플레이트에 웰 당 세포를 8×10⁴씩 분주(seeding)하였다. 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 25㎕씩을 넣고, 안티센스 올리고핵산과 비교예 9, 11, 16에서 제조된 양이온성 리포좀 또는 에멀젼과 실시예 12에서 제조된 양이온성 리포좀을 각각 4㎕씩 첨가하였다. 비씨엘2(Bcl2) 유전자(Gene bank accession number: NM_000633)의 발현 억제를 유도하기 위한 안티센스 올리고핵산으로는 바이오니아(Bioneer, Deajeon, Korea)에서 합성 주문한 것(5'-TCT CCC AGC GTG CGC CAT-3')을 사용하였다. 미디어에 포함된 안티센스 올리고핵산의 최종 농도는 100nM이 되게 맞추었다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하고 이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37 ℃의 CO₂세포배양기에서 24시간 동안 배양하였다. 24시간 후 Trizol 시약(Invitrogen, Carlsbad, CA, USA)을 사용하여 세포내에 존재하는 전체 리보핵산 (RNA)을 분리하였으며, 이 RNA는 AccuPowerRT PreMix (Bioneer, Daejeon, Korea)를 사용하여 cDNA로 역전사 하였다. 비씨엘2 (Bcl2)에 특이적인 프라이머의 서열은 5'-ATG GCG CAC GCT GGG AGA AC-3'(왼쪽), 5'-GCG GTA GCG GCG GGA GAA GT-3'(오른쪽)이며 중합효소연쇄반응은 95℃에서 5분 반응 후, 95℃에서 1분, 53℃에서 1분, 72℃에서 50초를 32번 반복한 후 72℃에서 5분 더 반응시켜주었다. 생성물의 크기는 327염기쌍 이었다. 비씨엘2 (Bcl2) 전사체 발현의 정도는 비씨엘2 특이적인 연쇄반응 생성물의 밴드 밀도를 glyceraldehyde-3-phosphate dehydrogenase (GAPDH) 유전자를 증폭하여 나타나는 밴드 밀도로 보정하여 정량적인 발현의 변화를 측정하였다.HeLa cell lines were seeded 8 × 10 μs of cells per well in 24 well plates the day before the experiment. When the cells of each plate were grown uniformly by 60-70%, 25 μl of the medium containing no serum was added to the Eppendorf tube, and the antisense oligonucleic acid and the cationic liposomes or emulsions prepared in Comparative Examples 9, 11 and 16 were used. And 4 µl of the cationic liposomes prepared in Example 12 were added. Antisense oligonucleotides for inducing the expression inhibition of Bcl2 gene (Gcl bank accession number: NM_000633) were synthesized and ordered from Bioneer (Bioneer, Deajeon, Korea) (5'-TCT CCC AGC GTG CGC CAT- 3 ') was used. The final concentration of antisense oligonucleotide included in the media was set to 100 nM. After slowly pipetting and mixing, the mixture was allowed to stand at room temperature for 20 minutes, and the complex thus prepared was added to a well plate and incubated in a
도8은 각각의 조성을 처리한 경우 HeLa 세포내에서 타겟 유전자인 비씨엘2의 전사체 발현을 비교한 것이다. 대조군은 유전자가 세포 내로 전달되지 않아 비씨엘2 유전자의 발현에 변화가 없었고, 비교예 11에서 제조된 양이온성 리포좀, 비교예 16에서 제조된 양이온성 에멀젼과 시판품인 비교예 9는 실시예 12에서 제조된 양이온성 리포좀보다 비씨엘2 유전자의 발현억제 효능이 유의적으로 낮은 것이 관찰되었다. 이와 같은 결과에서 알 수 있듯이, 실시예 12에서 제조된 양이온성 리포좀이 자궁경부암 세포주 내로 안티센스 올리고핵산 물질을 전달하여 표적유전자의 발현을 선택적으로 억제시킴을 알 수 있었다.Figure 8 compares the expression of transcripts of BC2, a target gene, in HeLa cells after treatment with each composition. In the control group, there was no change in the expression of the BC2 gene because the gene was not transferred into the cell, and the cationic liposome prepared in Comparative Example 11, the cationic emulsion prepared in Comparative Example 16 and the commercially available Comparative Example 9 were used in Example 12. It was observed that the expression inhibitory effect of BCL2 gene was significantly lower than the prepared cationic liposomes. As can be seen from these results, the cationic liposome prepared in Example 12 was found to deliver the antisense oligonucleotide material into the cervical cancer cell line to selectively inhibit the expression of the target gene.
III-3. A549 세포주에서의 역전사 중합효소 연쇄반응을 이용한 작은간섭 리보핵산 전달 효능 평가III-3. Evaluation of Small Interfering Ribonucleic Acid Delivery Efficacy by Reverse Transcription Polymerase Chain Reaction in A549 Cell Line
A549 세포주를 실험 전날 24 웰 플레이트에 웰 당 세포를 8×10⁴씩 분주(seeding)하였다. 각 플레이트의 세포가 60-70%정도 균일하게 성장했을 때, 에펜도르프 튜브에 혈청이 포함되지 않은 배지 25㎕씩을 넣고, 서바이빈 siRNA와 비교예 9, 15, 19와 실시예 11에서 제조된 양이온성 리포좀 또는 미셀을 각각 4㎕씩 첨가하였다. 미디어에 포함된 siRNA의 최종 농도는 100nM이 되게 맞추었다. 이들을 서서히 피펫팅(pipetting)하여 혼합한 후 실온에서 20분간 방치하고 이렇게 제조된 복합체를 웰 플레이트에 첨가하여 37 ℃의 CO₂세포배양기에서 24시간 동안 배양하였다. 24시간 후 Trizol 시약(Invitrogen, Carlsbad, CA, USA)을 사용하여 세포내에 존재하는 전체 리보핵산 (RNA)을 분리하였으며, 이 RNA는 AccuPowerRT PreMix (Bioneer, Daejeon, Korea)를 사용하여 cDNA로 역전사 하였다. 서바이빈(survivin) 유전자 발현의 정도는 서바이빈 특이적인 연쇄반응 생성물의 밴드 밀도를 GAPDH(glyceraldehyde-3-phosphate dehydrogenase) 유전자를 증폭하여 나타나는 밴드 밀도로 보정하여 정량적인 발현의 변화를 측정하였다.The A549 cell line was seeded 8 × 10 μs of cells per well in a 24-well plate the day before the experiment. When the cells of each plate were grown uniformly by 60-70%, 25 μl of serum-free medium was added to the Eppendorf tube, and the survivin siRNA prepared in Comparative Examples 9, 15, 19 and Example 11 were prepared. 4 μl of cationic liposomes or micelles were added respectively. The final concentration of siRNA included in the media was set to 100 nM. After slowly pipetting and mixing, the mixture was allowed to stand at room temperature for 20 minutes, and the complex thus prepared was added to a well plate and incubated in a
도9는 각각의 조성을 처리한 경우 A549 세포내에서 타겟 유전자인 서바이빈의 전사체 발현을 비교한 것이다. 대조군은 유전자가 세포 내로 전달되지 않아 서바이빈 유전자의 발현에 변화가 없었고, 비교예 15, 19에서 제조된 양이온성 미셀과 시판품 양이온성 리포좀인 비교예 9는 실시예 11에서 제조된 양이온성 리포좀보다 서바이빈 유전자의 발현 억제 효능이 유의적으로 낮은 것으로 나타났다. 이와 같은 결과에서 알 수 있듯이, 실시예 11에서 제조된 양이온성 리포좀이 폐암 세포주 내로 작은간섭 리보핵산물질을 전달하여 표적유전자의 발현을 보다 효과적으로 억제시킴을 알 수 있었다.9 compares the expression of transcripts of survivin, a target gene, in A549 cells after treatment with each composition. The control group had no change in the expression of survivin gene because the gene was not delivered into cells, and Comparative Example 9, which is a cationic micelle prepared in Comparative Examples 15 and 19 and a commercially available cationic liposome, was used as a cationic liposome prepared in Example 11. It was shown that the suppression effect of survivin gene was significantly lower. As can be seen from the results, it was found that the cationic liposome prepared in Example 11 delivers a small interfering ribonucleate into the lung cancer cell line to more effectively suppress the expression of the target gene.
[실험예 IV] 3-(4,5-dimethylthiazole-2-yl)-2,5-diphenyl tetrazolium bromide (MTT)을 사용한 세포독성 평가Experimental Example IV Cytotoxicity Evaluation Using 3- (4,5-dimethylthiazole-2-yl) -2,5-diphenyl tetrazolium bromide (MTT)
IV-1. WM266.4 세포주에서의 세포독성 평가IV-1. Cytotoxicity Assessment in WM266.4 Cell Line
본 발명의 신규 양이온성 지질을 포함하는 핵산 전달체의 세포 독성에 관한 평가를 하기 위하여 하기와 같은 과정으로 실험을 수행하였다. WM266.4 세포에 실시예 7의 양이온성 미셀과 비교예 9, 12, 16에서 제조한 양이온성 리포좀 또는 에멀젼과 작은간섭 리보핵산의 복합체 조성을 처리하고 세포 독성을 평가하였다. 핵산 전달체만의 세포 독성을 명확히 평가하기 위하여 siRNA는 세포내에서 활성이 없는 스크램블 서열을 사용하였다. 세포 독성은 3-(4,5-dimethylthiazole-2-yl)-2,5-diphenyl tetrazolium bromide (MTT) 시약에 의한 방법으로 평가하였다.In order to evaluate the cytotoxicity of the nucleic acid carrier containing a novel cationic lipid of the present invention, the experiment was carried out as follows. WM266.4 cells were treated with the complex composition of the cationic micelle of Example 7, the cationic liposomes or emulsions prepared in Comparative Examples 9, 12, and 16 and small interfering ribonucleic acids, and the cytotoxicity was evaluated. In order to clearly assess the cytotoxicity of the nucleic acid carrier only, siRNA used an inert scrambled sequence in the cell. Cytotoxicity was assessed by the method with 3- (4,5-dimethylthiazole-2-yl) -2,5-diphenyl tetrazolium bromide (MTT) reagent.
세포를 웰 당 2×104 세포가 되도록 48 웰(well)에 분주 (seeding)하고 12시간 배양한 후 실시예 7의 양이온성 미셀과 비교예 9, 12, 16에서 제조한 양이온성 리포좀 또는 에멀젼과 siRNA의 복합체 조성을 처리하였다. 24시간 경과 후 각각 MTT 용액을 배지의 10%가 되도록 가하고, 4시간 더 배양한 다음 상층액을 제거하고 0.04 N 염산 이소프로판올 용액을 첨가한 후에 엘라이져 리더 (ELISA reader, Sunrise-Basic TECAN, M, Switzerland)를 이용하여 570 nm에서 그 흡광도를 측정하였다. 대조군으로는 아무것도 처리하지 않은 세포가 사용되었다. 도10은 실시예 7에서 제조된 양이온성 미셀과 siRNA 복합체의 세포독성 실험을 수행한 결과로 실시예 7의 양이온성 미셀과 siRNA의 복합체는 비교예 9, 12, 16의 양이온성 제형들과 비교하여 큰 세포 독성을 나타내지 않았고 따라서 도 10으로부터 실시예 7에서 제조된 본 발명의 양이온성 미셀은 사람의 흑색종 세포주에 대해 심각한 독성을 나타내지 않는다는 사실을 알 수 있고 또한, 본 발명의 양이온성 지질보다 수식하는 양이온성 아미노산의 개수가 많은 지질로 제조된 비교예 12 및 비교예 16의 경우 독 성이 증가한다는 사실을 알 수 있다. The cells were seeded in 48 wells for 2 × 10 4 cells per well and incubated for 12 hours, followed by cationic micelles of Example 7 and cationic liposomes or emulsions prepared in Comparative Examples 9, 12, and 16. The complex composition of and siRNA was treated. After 24 hours, MTT solution was added to 10% of the medium, incubated for 4 hours more, the supernatant was removed, and 0.04 N isopropanol solution was added, followed by ELISA reader, Sunrise-Basic TECAN, M, Its absorbance was measured at 570 nm. As a control, no cells were used. 10 is a result of performing a cytotoxicity test of the cationic micelles and siRNA complexes prepared in Example 7 compared to the cationic formulations of Comparative Examples 9, 12 and 16 as a result of the synthesis of the cationic micelles and siRNA of Example 7 It was found that the cationic micelles of the present invention prepared in Example 7 did not show significant toxicity to human melanoma cell lines. It can be seen that the toxicity is increased in Comparative Example 12 and Comparative Example 16 made of a lipid having a large number of modified cationic amino acids.
IV-2. Huh-7 세포주에서의 세포독성 평가IV-2. Cytotoxicity Assessment in Huh-7 Cell Line
본 발명의 신규 양이온성 지질을 포함하는 핵산 전달체의 세포 독성에 관한 평가를 하기 위하여 하기와 같은 과정으로 실험을 수행하였다. Huh-7 세포에 실시예 10과 비교예 9, 13, 17에서 제조한 양이온성 에멀젼 또는 리포좀과 작은간섭 리보핵산의 복합체 조성을 처리하고 세포 독성을 평가하였다. 핵산 전달체만의 세포 독성을 명확히 평가하기 위하여 siRNA는 세포내에서 활성이 없는 스크램블 서열을 사용하였다. 세포 독성은 3-(4,5-dimethylthiazole-2-yl)-2,5-diphenyl tetrazolium bromide (MTT) 시약에 의한 방법으로 평가하였다.In order to evaluate the cytotoxicity of the nucleic acid carrier containing a novel cationic lipid of the present invention, the experiment was carried out as follows. Huh-7 cells were treated with a complex composition of cationic emulsions or liposomes prepared in Example 10, Comparative Examples 9, 13, and 17 and small interfering ribonucleic acids, and cytotoxicity was evaluated. In order to clearly assess the cytotoxicity of the nucleic acid carrier only, siRNA used an inert scrambled sequence in the cell. Cytotoxicity was assessed by the method with 3- (4,5-dimethylthiazole-2-yl) -2,5-diphenyl tetrazolium bromide (MTT) reagent.
세포를 웰 당 2×104 세포가 되도록 48 웰(well)에 분주 (seeding)하고 12시간 배양한 후 실시예 10, 비교예 9, 13, 17에서 제조한 양이온성 제형 (formulations)들과 siRNA의 복합체 조성을 처리하였다. 24시간 경과 후 각각 MTT 용액을 배지의 10%가 되도록 가하고, 4시간 더 배양한 다음 상층액을 제거하고 0.04 N 염산 이소프로판올 용액을 첨가한 후에 엘라이져 리더 (ELISA reader)를 이용하여 570 nm에서 그 흡광도를 측정하였다. 대조군으로는 아무것도 처리하지 않은 세포가 사용되었다. The cells were seeded in 48 wells for 2 × 10 4 cells per well and incubated for 12 hours, followed by cationic formulations prepared in Examples 10, Comparative Examples 9, 13, and 17 and siRNA. The composite composition of was processed. After 24 hours, each MTT solution was added to 10% of the medium, incubated for another 4 hours, the supernatant was removed, and 0.04 N isopropanol solution was added, and then the resultant was removed at 570 nm using an ELISA reader. Absorbance was measured. As a control, no cells were used.
도11은 실시예 10에서 제조된 양이온성 에멀젼과 siRNA 복합체의 세포독성 실험을 수행한 결과로 실시예 10의 양이온성 에멀젼과 siRNA의 복합체는 비교예 9, 13, 17의 전달체들과 비교하여 큰 세포 독성을 나타내지 않았고 따라서 도 11로부터 실시예 10에서 제조된 본 발명의 양이온성 에멀젼은 사람의 흑색종 세포주에 대해 심각한 독성을 나타내지 않는다는 사실을 알 수 있다. 또한, 본 발명의 양이온성 지질보다 수식하는 양이온성 아미노산의 개수가 많은 경우 독성이 증가한다는 것을 비교예 13, 17의 독성 결과에서 알 수 있다.11 is a result of performing the cytotoxicity test of the cationic emulsion and siRNA complex prepared in Example 10, the complex of the cationic emulsion and siRNA of Example 10 was larger than the carriers of Comparative Examples 9, 13, 17 It was seen that the cationic emulsions of the present invention prepared in Example 10 did not show cytotoxicity and therefore do not show severe toxicity to human melanoma cell lines. In addition, it can be seen from the toxicity results of Comparative Examples 13 and 17 that the toxicity increases when the number of cationic amino acids modified more than the cationic lipid of the present invention increases.
IV-3. U87 세포주에서의 세포독성 평가IV-3. Cytotoxicity Assessment in U87 Cell Line
본 발명의 신규 양이온성 지질을 포함하는 핵산 전달체의 세포 독성에 관한 평가를 하기 위하여 하기와 같은 과정으로 실험을 수행하였다. U87 세포에 실시예 14와 비교예 9, 13, 15에서 제조한 양이온성 에멀젼, 리포좀, 또는 미셀과 작은간섭 리보핵산의 복합체 조성을 처리하고 세포 독성을 평가하였다. 핵산 전달체만의 세포 독성을 명확히 평가하기 위하여 siRNA는 세포내에서 활성이 없는 스크램블 서열을 사용하였다. 세포 독성은 3-(4,5-dimethylthiazole-2-yl)-2,5-diphenyl tetrazolium bromide (MTT) 시약에 의한 방법으로 평가하였다.In order to evaluate the cytotoxicity of the nucleic acid carrier containing a novel cationic lipid of the present invention, the experiment was carried out as follows. U87 cells were treated with a complex composition of cationic emulsions, liposomes, or micelles and small interfering ribonucleic acids prepared in Example 14 and Comparative Examples 9, 13, and 15 and evaluated for cytotoxicity. In order to clearly assess the cytotoxicity of the nucleic acid carrier only, siRNA used an inert scrambled sequence in the cell. Cytotoxicity was assessed by the method with 3- (4,5-dimethylthiazole-2-yl) -2,5-diphenyl tetrazolium bromide (MTT) reagent.
세포를 웰 당 2×104 세포가 되도록 48 웰(well)에 분주 (seeding)하고 12시간 배양한 후 실시예 14과 비교예 9, 13, 15에서 제조한 양이온성 에멀젼, 미셀 또는 리포좀과 siRNA의 복합체 조성을 처리하였다. 24시간 경과 후 각각 MTT 용액을 배지의 10%가 되도록 가하고, 4시간 더 배양한 다음 상층액을 제거하고 0.04 N 염산 이소프로판올 용액을 첨가한 후에 엘라이져 리더 (ELISA reader)를 이용하여 570 nm에서 그 흡광도를 측정하였다. 대조군으로는 아무것도 처리하지 않은 세포가 사용되었다. The cells were seeded in 48 wells for 2 × 10 4 cells per well and incubated for 12 hours, and then cationic emulsions, micelles, or liposomes and siRNA prepared in Example 14 and Comparative Examples 9, 13, and 15 were used. The composite composition of was processed. After 24 hours, each MTT solution was added to 10% of the medium, incubated for another 4 hours, the supernatant was removed, and 0.04 N isopropanol solution was added, and then the resultant was removed at 570 nm using an ELISA reader. Absorbance was measured. As a control, no cells were used.
도12는 실시예 14에서 제조된 양이온성 에멀젼과 siRNA 복합체의 세포독성 실험을 수행한 결과로 실시예 14의 양이온성 에멀젼과 siRNA의 복합체는 비교예 9, 13, 15의 전달체와 siRNA의 복합체에 비교하여 큰 세포 독성을 나타내지 않았다. 따라서 도 12로부터 실시예 14에서 제조된 양이온성 에멀젼은 사람의 신경교종 세포주에 대해 심각한 독성을 나타내지 않는다는 사실을 알 수 있고 또한, 본 발명의 양이온성 지질보다 수식하는 양이온성 아미노산의 개수가 많은 지질로 제조된 비교예 13, 15의 경우 증가된 세포독성을 나타낸다는 것을 알 수 있다.12 shows the cytotoxicity test of the cationic emulsion prepared in Example 14 and the siRNA complex. As a result, the complex of the cationic emulsion and siRNA of Example 14 was added to the complex of the carrier and siRNA of Comparative Examples 9, 13, and 15. There was no significant cytotoxicity in comparison. Therefore, it can be seen that the cationic emulsion prepared in Example 14 from FIG. 12 does not show serious toxicity to human glioma cell lines, and also has a higher number of cationic amino acids modified than the cationic lipid of the present invention. It can be seen that in Comparative Examples 13 and 15 prepared with increased cytotoxicity.
도 1은 형광 표식이 붙어있는 이중나선 리보핵산을 사용하여 사람의 흑색종 세포인 WM266.4에서 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포내 핵산 전달 효율을 보여주는 사진이다.FIG. 1 is a photograph showing intracellular nucleic acid delivery efficiency of a nucleic acid carrier containing a cationic lipid of the present invention in human melanoma cells WM266.4 using double-stranded ribonucleic acid labeled with fluorescent labels.
도 2는 형광 표식이 붙어있는 이중나선 리보핵산을 사용하여 사람의 자궁경부암 세포인 HeLa에서 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포내 핵산 전달 효율을 보여주는 사진이다.Figure 2 is a photograph showing the intracellular nucleic acid delivery efficiency of the nucleic acid carrier containing a cationic lipid of the present invention in HeLa, a human cervical cancer cell using a double-stranded ribonucleic acid with a fluorescent label.
도 3은 형광 표식이 붙어있는 이중나선 리보핵산을 사용하여 사람의 신경교종 세포인 U87에서 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포내 핵산 전달 효율을 보여주는 사진이다.Figure 3 is a photograph showing the intracellular nucleic acid delivery efficiency of the nucleic acid carrier containing a cationic lipid of the present invention in human glioma cells U87 using a double-stranded ribonucleic acid with a fluorescent label.
도 4는 형광 표식이 붙어있는 이중나선 리보핵산을 사용하여 사람의 폐암 세포인 A549에서 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포내 핵산 전달 효율 정도를 형광 유세포분석기 (FACS)를 사용해 분석한 결과이다.Figure 4 is analyzed using a fluorescence flow cytometer (FACS) the degree of intracellular nucleic acid delivery efficiency of the nucleic acid carrier containing a cationic lipid of the present invention in human lung cancer cells A549 using a double-stranded ribonucleic acid with a fluorescent label One result.
도 5는 형광 표식이 붙어있는 이중나선 리보핵산을 사용하여 사람의 흑색종 세포인 A375에서 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포내 핵산 전달 효율 정도를 형광 유세포분석기 (FACS)를 사용해 분석한 결과이다.FIG. 5 shows the degree of intracellular nucleic acid delivery efficiency of a nucleic acid carrier containing a cationic lipid of the present invention in A375, a human melanoma cell, using a double-stranded ribonucleic acid labeled with a fluorescent flow cytometer (FACS). The result of the analysis.
도 6은 형광 표식이 붙어있는 이중나선 리보핵산을 사용하여 사람의 간암 세포인 Huh-7에서 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포내 핵산 전달 효율 정도를 형광 유세포분석기 (FACS)를 사용해 분석한 결과이다.FIG. 6 shows a fluorescence flow cytometer (FACS) of intracellular nucleic acid delivery efficiency of a nucleic acid carrier containing a cationic lipid of the present invention in Huh-7, a human liver cancer cell, using a double-stranded ribonucleic acid labeled with a fluorescent label. The result of the analysis.
도 7은 본 발명의 양이온성 지질을 포함하는 핵산 전달체를 이용하여 서바이 빈 발현 억제 siRNA에 의해 매개된 서바이빈 전사체 발현 억제 효능을 사람의 흑색종 세포주인 A375에서 역전사 중합효소 연쇄반응으로 확인한 결과를 보여준다.Figure 7 shows the effect of inhibiting the expression of survivin transcript mediated by survivin transcript siRNA using a nucleic acid carrier comprising a cationic lipid of the present invention in reverse transcriptase polymerase chain reaction in human melanoma cell line A375. Show the result.
도 8은 본 발명의 양이온성 지질을 포함하는 핵산 전달체를 이용하여 비씨엘2 발현 억제 안티센스 올리고핵산에 의해 매개된 비씨엘2 전사체 발현 억제 효능을 사람의 자궁경부암 세포주인 HeLa에서 역전사 중합효소 연쇄반응으로 확인한 결과를 보여준다.Figure 8 is a reverse transcriptase polymerase chain in HeLa, a cervical cancer cell line of human cervical cancer cell line using the nucleic acid carrier containing a cationic lipid of the present invention to inhibit the BCL2 transcript expression mediated by BCL2 expression inhibition antisense oligonucleotide Show the results confirmed by the reaction.
도 9는 본 발명의 양이온성 지질을 포함하는 핵산 전달체를 이용하여 서바이빈 발현 억제 siRNA에 의해 매개된 서바이빈 전사체 발현 억제 효능을 사람의 폐암 세포주인 A549에서 역전사 중합효소 연쇄반응으로 확인한 결과를 보여준다.Figure 9 shows the effect of inhibiting the expression of survivin transcript mediated by survivin expression siRNA using a nucleic acid carrier containing a cationic lipid of the present invention by reverse transcriptase polymerase chain reaction in human lung cancer cell line A549 Show results.
도 10은 MTT (tetrazolium 3-(4,5-dimethylthiazol-2-yl)-2,5- diphenyl tetrazolium bromide) 염색법을 사용하여 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포독성을 사람의 흑색종 세포주인 WM266.4에서 확인한 결과를 보여준다.Figure 10 shows the cytotoxicity of the nucleic acid carriers comprising the cationic lipids of the present invention using tetrazolium 3- (4,5-dimethylthiazol-2-yl) -2,5-diphenyl tetrazolium bromide (MTT) staining. The results confirmed in the species cell line WM266.4.
도 11은 MTT (tetrazolium 3-(4,5-dimethylthiazol-2-yl)-2,5- diphenyl tetrazolium bromide) 염색법을 사용하여 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포독성을 사람의 간암 세포주인 Huh-7에서 확인한 결과를 보여준다.Figure 11 shows the cytotoxicity of nucleic acid carriers comprising cationic lipids of the present invention using MTT (tetrazolium 3- (4,5-dimethylthiazol-2-yl) -2,5-diphenyl tetrazolium bromide) staining. The results confirmed in the cell line Huh-7 are shown.
도 12는 MTT (tetrazolium 3-(4,5-dimethylthiazol-2-yl)-2,5- diphenyl tetrazolium bromide) 염색법을 사용하여 본 발명의 양이온성 지질을 포함하는 핵산 전달체의 세포독성을 사람의 신경교종 세포주인 U87에서 확인한 결과를 보여준다.Figure 12 shows the cytotoxicity of nucleic acid carriers comprising cationic lipids of the present invention using tetrazolium 3- (4,5-dimethylthiazol-2-yl) -2,5-diphenyl tetrazolium bromide (MTT) staining. The results confirmed in glioma cell line U87 are shown.
Claims (29)
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020080111275A KR100909786B1 (en) | 2008-11-10 | 2008-11-10 | Novel cationic lipids modified with oligopeptides, preparation methods thereof, and carriers comprising the same |
| PCT/KR2009/006567 WO2010053329A2 (en) | 2008-11-10 | 2009-11-10 | Novel oligopeptide-derived cationic lipid, method for preparing same, and delivery system comprising same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020080111275A KR100909786B1 (en) | 2008-11-10 | 2008-11-10 | Novel cationic lipids modified with oligopeptides, preparation methods thereof, and carriers comprising the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR100909786B1 true KR100909786B1 (en) | 2009-07-29 |
Family
ID=41338037
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020080111275A Expired - Fee Related KR100909786B1 (en) | 2008-11-10 | 2008-11-10 | Novel cationic lipids modified with oligopeptides, preparation methods thereof, and carriers comprising the same |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR100909786B1 (en) |
| WO (1) | WO2010053329A2 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011116152A3 (en) * | 2010-03-16 | 2012-04-05 | Sanford -Burnham Medical Research Institute | Delivery of agents using interfering nanoparticles |
| US20220356303A1 (en) * | 2021-04-08 | 2022-11-10 | The Curators Of The University Of Missouri | Lipidated poly(amino acid) nanostructures |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103760428B (en) * | 2014-01-24 | 2016-01-27 | 上海同耀通信技术有限公司 | The simulated solution of tissue liquid |
| CN115919769A (en) * | 2016-05-16 | 2023-04-07 | 德克萨斯大学系统董事会 | Compositions for delivering tRNA as nanoparticles and methods of use thereof |
| US12357580B2 (en) | 2018-06-19 | 2025-07-15 | The Board Of Regents Of The University Of Texas System | Lipid nanoparticle compositions for delivery of mRNA and long nucleic acids |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4600526A (en) * | 1982-09-22 | 1986-07-15 | Centre National de la Recherche Schientifique (C N R S) | Lipopeptides, their preparation and their application as emulsifiers |
| KR100807060B1 (en) * | 2007-08-28 | 2008-02-25 | 고려대학교 산학협력단 | Novel cationic lipids, methods for their preparation and carriers comprising the same |
-
2008
- 2008-11-10 KR KR1020080111275A patent/KR100909786B1/en not_active Expired - Fee Related
-
2009
- 2009-11-10 WO PCT/KR2009/006567 patent/WO2010053329A2/en not_active Ceased
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4600526A (en) * | 1982-09-22 | 1986-07-15 | Centre National de la Recherche Schientifique (C N R S) | Lipopeptides, their preparation and their application as emulsifiers |
| KR100807060B1 (en) * | 2007-08-28 | 2008-02-25 | 고려대학교 산학협력단 | Novel cationic lipids, methods for their preparation and carriers comprising the same |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011116152A3 (en) * | 2010-03-16 | 2012-04-05 | Sanford -Burnham Medical Research Institute | Delivery of agents using interfering nanoparticles |
| US9526693B2 (en) | 2010-03-16 | 2016-12-27 | Sanford-Burnham Medical Research Inslilute | Delivery of agents using interfering nanoparticles |
| US9878050B2 (en) | 2010-03-16 | 2018-01-30 | Sanford-Burnham Medical Research Institute | Delivery of agents using interfering nanoparticles |
| US20220356303A1 (en) * | 2021-04-08 | 2022-11-10 | The Curators Of The University Of Missouri | Lipidated poly(amino acid) nanostructures |
| US12509552B2 (en) * | 2021-04-08 | 2025-12-30 | The Curators Of The University Of Missouri | Lipidated poly(amino acid) nanostructures |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2010053329A2 (en) | 2010-05-14 |
| WO2010053329A3 (en) | 2010-08-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100807060B1 (en) | Novel cationic lipids, methods for their preparation and carriers comprising the same | |
| US20240246898A1 (en) | Cationic lipids for nucleic acid delivery and preparation thereof | |
| US5705385A (en) | Lipid-nucleic acid particles prepared via a hydrophobic lipid-nucleic acid complex intermediate and use for gene transfer | |
| US11952351B2 (en) | Lipid particle, composition comprising lipid particle, and method for delivering activators to cell | |
| CN104922676B (en) | Polyamine derivatives | |
| CA2651389C (en) | Novel reagents for transfection of eukaryotic cells | |
| Byk et al. | Synthesis, activity, and structure− activity relationship studies of novel cationic lipids for DNA transfer | |
| JP6182457B2 (en) | Lipid nanoparticles for drug delivery systems containing cationic lipids | |
| Choi et al. | Dexamethasone conjugated poly (amidoamine) dendrimer as a gene carrier for efficient nuclear translocation | |
| JP4764426B2 (en) | Cationic lipids and methods of use | |
| JP4999784B2 (en) | Lipopolyamine as a transfection agent and its pharmaceutical use | |
| KR100953917B1 (en) | Lipopeptides with specific affinity to fc region of antibodies and antigen-recognizing lipid nanoparticles comprising the same | |
| MX2010012326A (en) | Methods and compositions comprising novel cationic lipids. | |
| TW201021852A (en) | Releasable fusogenic lipids for nucleic acids delivery systems | |
| KR100909786B1 (en) | Novel cationic lipids modified with oligopeptides, preparation methods thereof, and carriers comprising the same | |
| KR101343791B1 (en) | Lipopeptides with specific affinity to Fc region of antibodies and antigen-recognizing lipid nanoparticles comprising the same | |
| JP7411824B2 (en) | Aminolipid compounds, their preparation methods, and their uses | |
| KR101000358B1 (en) | Integrin α V β 3 Binding Lipid Derivatives and Lipid Nanoparticles Comprising the Same | |
| Gosangi et al. | Evolution of new “Bolaliposomes” using novel α-tocopheryl succinate based cationic lipid and 1, 12-disubstituted dodecane-based bolaamphiphile for efficient gene delivery | |
| EP2802556B1 (en) | Lipopolyamines of spermine type for construction of liposomal transfection systems | |
| US20050261214A1 (en) | Complexes for transferring substances of interest into a cell | |
| KR100953498B1 (en) | Novel compound, a preparation method of the same and a delivery system comprising the same | |
| Patel | Development of Amino Acid-Modified Drug Delivery Systems for RNA Delivery in Cancer Therapeutics | |
| AU2012268866B2 (en) | Novel reagents for transfection of eukaryotic cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| A302 | Request for accelerated examination | ||
| PA0302 | Request for accelerated examination |
St.27 status event code: A-1-2-D10-D16-exm-PA0302 St.27 status event code: A-1-2-D10-D17-exm-PA0302 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R11-asn-PN2301 St.27 status event code: A-3-3-R10-R13-asn-PN2301 |
|
| PE0801 | Dismissal of amendment |
St.27 status event code: A-2-2-P10-P12-nap-PE0801 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
Fee payment year number: 1 St.27 status event code: A-2-2-U10-U11-oth-PR1002 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 4 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| FPAY | Annual fee payment |
Payment date: 20130621 Year of fee payment: 5 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 5 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| FPAY | Annual fee payment |
Payment date: 20140630 Year of fee payment: 6 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 6 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| FPAY | Annual fee payment |
Payment date: 20151123 Year of fee payment: 7 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 7 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PC1903 | Unpaid annual fee |
Not in force date: 20160722 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE St.27 status event code: A-4-4-U10-U13-oth-PC1903 |
|
| FPAY | Annual fee payment |
Payment date: 20170321 Year of fee payment: 8 |
|
| K11-X000 | Ip right revival requested |
St.27 status event code: A-6-4-K10-K11-oth-X000 |
|
| PC1903 | Unpaid annual fee |
Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20160722 St.27 status event code: N-4-6-H10-H13-oth-PC1903 |
|
| PR0401 | Registration of restoration |
St.27 status event code: A-6-4-K10-K13-oth-PR0401 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 8 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| R401 | Registration of restoration | ||
| FPAY | Annual fee payment |
Payment date: 20170707 Year of fee payment: 9 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 9 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| FPAY | Annual fee payment |
Payment date: 20180702 Year of fee payment: 10 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 10 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| FPAY | Annual fee payment |
Payment date: 20190715 Year of fee payment: 11 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 11 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 12 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 13 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 14 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 15 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PC1903 | Unpaid annual fee |
Not in force date: 20240722 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE St.27 status event code: A-4-4-U10-U13-oth-PC1903 |
|
| PC1903 | Unpaid annual fee |
Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20240722 St.27 status event code: N-4-6-H10-H13-oth-PC1903 |